RU2563991C2 - Синергические комбинации каротиноидов и полифенолов - Google Patents
Синергические комбинации каротиноидов и полифенолов Download PDFInfo
- Publication number
- RU2563991C2 RU2563991C2 RU2011134652/15A RU2011134652A RU2563991C2 RU 2563991 C2 RU2563991 C2 RU 2563991C2 RU 2011134652/15 A RU2011134652/15 A RU 2011134652/15A RU 2011134652 A RU2011134652 A RU 2011134652A RU 2563991 C2 RU2563991 C2 RU 2563991C2
- Authority
- RU
- Russia
- Prior art keywords
- carnosic acid
- lycopene
- lutein
- carotene
- therapeutic composition
- Prior art date
Links
- 150000008442 polyphenolic compounds Chemical class 0.000 title claims abstract description 54
- 235000021466 carotenoid Nutrition 0.000 title claims abstract description 50
- 150000001747 carotenoids Chemical class 0.000 title claims abstract description 50
- 235000013824 polyphenols Nutrition 0.000 title claims abstract description 42
- 239000011885 synergistic combination Substances 0.000 title description 4
- QRYRORQUOLYVBU-VBKZILBWSA-N carnosic acid Chemical compound CC([C@@H]1CC2)(C)CCC[C@]1(C(O)=O)C1=C2C=C(C(C)C)C(O)=C1O QRYRORQUOLYVBU-VBKZILBWSA-N 0.000 claims abstract description 292
- 229960004999 lycopene Drugs 0.000 claims abstract description 116
- OAIJSZIZWZSQBC-GYZMGTAESA-N lycopene Chemical compound CC(C)=CCC\C(C)=C\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\C=C(/C)CCC=C(C)C OAIJSZIZWZSQBC-GYZMGTAESA-N 0.000 claims abstract description 115
- UPYKUZBSLRQECL-UKMVMLAPSA-N Lycopene Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1C(=C)CCCC1(C)C)C=CC=C(/C)C=CC2C(=C)CCCC2(C)C UPYKUZBSLRQECL-UKMVMLAPSA-N 0.000 claims abstract description 112
- JEVVKJMRZMXFBT-XWDZUXABSA-N Lycophyll Natural products OC/C(=C/CC/C(=C\C=C\C(=C/C=C/C(=C\C=C\C=C(/C=C/C=C(\C=C\C=C(/CC/C=C(/CO)\C)\C)/C)\C)/C)\C)/C)/C JEVVKJMRZMXFBT-XWDZUXABSA-N 0.000 claims abstract description 112
- 235000012661 lycopene Nutrition 0.000 claims abstract description 112
- 239000001751 lycopene Substances 0.000 claims abstract description 112
- ZCIHMQAPACOQHT-ZGMPDRQDSA-N trans-isorenieratene Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/c1c(C)ccc(C)c1C)C=CC=C(/C)C=Cc2c(C)ccc(C)c2C ZCIHMQAPACOQHT-ZGMPDRQDSA-N 0.000 claims abstract description 112
- KBPHJBAIARWVSC-XQIHNALSSA-N trans-lutein Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CC(O)CC1(C)C)C=CC=C(/C)C=CC2C(=CC(O)CC2(C)C)C KBPHJBAIARWVSC-XQIHNALSSA-N 0.000 claims abstract description 102
- 235000012680 lutein Nutrition 0.000 claims abstract description 101
- 229960005375 lutein Drugs 0.000 claims abstract description 101
- 239000001656 lutein Substances 0.000 claims abstract description 101
- KBPHJBAIARWVSC-RGZFRNHPSA-N lutein Chemical compound C([C@H](O)CC=1C)C(C)(C)C=1\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\[C@H]1C(C)=C[C@H](O)CC1(C)C KBPHJBAIARWVSC-RGZFRNHPSA-N 0.000 claims abstract description 101
- ORAKUVXRZWMARG-WZLJTJAWSA-N lutein Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CCCC1(C)C)C=CC=C(/C)C=CC2C(=CC(O)CC2(C)C)C ORAKUVXRZWMARG-WZLJTJAWSA-N 0.000 claims abstract description 101
- FJHBOVDFOQMZRV-XQIHNALSSA-N xanthophyll Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CC(O)CC1(C)C)C=CC=C(/C)C=CC2C=C(C)C(O)CC2(C)C FJHBOVDFOQMZRV-XQIHNALSSA-N 0.000 claims abstract description 101
- 230000015572 biosynthetic process Effects 0.000 claims abstract description 89
- OENHQHLEOONYIE-UKMVMLAPSA-N all-trans beta-carotene Natural products CC=1CCCC(C)(C)C=1/C=C/C(/C)=C/C=C/C(/C)=C/C=C/C=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C OENHQHLEOONYIE-UKMVMLAPSA-N 0.000 claims abstract description 88
- 235000013734 beta-carotene Nutrition 0.000 claims abstract description 88
- 239000011648 beta-carotene Substances 0.000 claims abstract description 88
- TUPZEYHYWIEDIH-WAIFQNFQSA-N beta-carotene Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CCCC1(C)C)C=CC=C(/C)C=CC2=CCCCC2(C)C TUPZEYHYWIEDIH-WAIFQNFQSA-N 0.000 claims abstract description 88
- 229960002747 betacarotene Drugs 0.000 claims abstract description 88
- OENHQHLEOONYIE-JLTXGRSLSA-N β-Carotene Chemical compound CC=1CCCC(C)(C)C=1\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C OENHQHLEOONYIE-JLTXGRSLSA-N 0.000 claims abstract description 88
- 230000005764 inhibitory process Effects 0.000 claims abstract description 83
- 239000000203 mixture Substances 0.000 claims abstract description 75
- REFJWTPEDVJJIY-UHFFFAOYSA-N Quercetin Chemical compound C=1C(O)=CC(O)=C(C(C=2O)=O)C=1OC=2C1=CC=C(O)C(O)=C1 REFJWTPEDVJJIY-UHFFFAOYSA-N 0.000 claims abstract description 32
- 108060008682 Tumor Necrosis Factor Proteins 0.000 claims abstract description 32
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 claims abstract description 32
- LNTHITQWFMADLM-UHFFFAOYSA-N gallic acid Chemical compound OC(=O)C1=CC(O)=C(O)C(O)=C1 LNTHITQWFMADLM-UHFFFAOYSA-N 0.000 claims abstract description 32
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 claims abstract description 31
- 230000001225 therapeutic effect Effects 0.000 claims abstract description 25
- 238000000034 method Methods 0.000 claims abstract description 24
- ZVOLCUVKHLEPEV-UHFFFAOYSA-N Quercetagetin Natural products C1=C(O)C(O)=CC=C1C1=C(O)C(=O)C2=C(O)C(O)=C(O)C=C2O1 ZVOLCUVKHLEPEV-UHFFFAOYSA-N 0.000 claims abstract description 16
- QNVSXXGDAPORNA-UHFFFAOYSA-N Resveratrol Natural products OC1=CC=CC(C=CC=2C=C(O)C(O)=CC=2)=C1 QNVSXXGDAPORNA-UHFFFAOYSA-N 0.000 claims abstract description 16
- HWTZYBCRDDUBJY-UHFFFAOYSA-N Rhynchosin Natural products C1=C(O)C(O)=CC=C1C1=C(O)C(=O)C2=CC(O)=C(O)C=C2O1 HWTZYBCRDDUBJY-UHFFFAOYSA-N 0.000 claims abstract description 16
- LUKBXSAWLPMMSZ-OWOJBTEDSA-N Trans-resveratrol Chemical compound C1=CC(O)=CC=C1\C=C\C1=CC(O)=CC(O)=C1 LUKBXSAWLPMMSZ-OWOJBTEDSA-N 0.000 claims abstract description 16
- 235000004515 gallic acid Nutrition 0.000 claims abstract description 16
- 229940074391 gallic acid Drugs 0.000 claims abstract description 16
- MWDZOUNAPSSOEL-UHFFFAOYSA-N kaempferol Natural products OC1=C(C(=O)c2cc(O)cc(O)c2O1)c3ccc(O)cc3 MWDZOUNAPSSOEL-UHFFFAOYSA-N 0.000 claims abstract description 16
- 235000005875 quercetin Nutrition 0.000 claims abstract description 16
- 229960001285 quercetin Drugs 0.000 claims abstract description 16
- 235000021283 resveratrol Nutrition 0.000 claims abstract description 16
- 229940016667 resveratrol Drugs 0.000 claims abstract description 16
- 230000004054 inflammatory process Effects 0.000 claims abstract description 14
- -1 polyphenol compounds Chemical class 0.000 claims abstract description 11
- 206010061218 Inflammation Diseases 0.000 claims abstract description 10
- 230000001575 pathological effect Effects 0.000 claims abstract description 4
- 230000003110 anti-inflammatory effect Effects 0.000 claims abstract description 3
- 239000003814 drug Substances 0.000 claims abstract description 3
- 230000002401 inhibitory effect Effects 0.000 claims description 17
- 230000004968 inflammatory condition Effects 0.000 claims description 10
- 238000004519 manufacturing process Methods 0.000 claims description 9
- 206010001052 Acute respiratory distress syndrome Diseases 0.000 claims description 8
- 208000013616 Respiratory Distress Syndrome Diseases 0.000 claims description 8
- 239000013543 active substance Substances 0.000 claims description 8
- 208000011341 adult acute respiratory distress syndrome Diseases 0.000 claims description 8
- 201000000028 adult respiratory distress syndrome Diseases 0.000 claims description 8
- 206010034674 peritonitis Diseases 0.000 claims description 7
- 208000024827 Alzheimer disease Diseases 0.000 claims description 6
- 208000006673 asthma Diseases 0.000 claims description 5
- 235000013305 food Nutrition 0.000 claims description 5
- 208000001072 type 2 diabetes mellitus Diseases 0.000 claims description 5
- 201000001320 Atherosclerosis Diseases 0.000 claims description 4
- 206010016654 Fibrosis Diseases 0.000 claims description 4
- 206010064147 Gastrointestinal inflammation Diseases 0.000 claims description 4
- 201000009794 Idiopathic Pulmonary Fibrosis Diseases 0.000 claims description 4
- 201000004681 Psoriasis Diseases 0.000 claims description 4
- 208000017442 Retinal disease Diseases 0.000 claims description 4
- 206010038923 Retinopathy Diseases 0.000 claims description 4
- 206010040047 Sepsis Diseases 0.000 claims description 4
- 230000007882 cirrhosis Effects 0.000 claims description 4
- 208000019425 cirrhosis of liver Diseases 0.000 claims description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 4
- 230000002526 effect on cardiovascular system Effects 0.000 claims description 4
- 208000014674 injury Diseases 0.000 claims description 4
- 208000036971 interstitial lung disease 2 Diseases 0.000 claims description 4
- 208000031225 myocardial ischemia Diseases 0.000 claims description 4
- 230000004770 neurodegeneration Effects 0.000 claims description 4
- 208000015122 neurodegenerative disease Diseases 0.000 claims description 4
- 230000010410 reperfusion Effects 0.000 claims description 4
- 206010039073 rheumatoid arthritis Diseases 0.000 claims description 4
- 206010039083 rhinitis Diseases 0.000 claims description 4
- 230000008733 trauma Effects 0.000 claims description 4
- 208000022559 Inflammatory bowel disease Diseases 0.000 claims description 3
- OVSVTCFNLSGAMM-UZFNGAIXSA-N di-cis-phytoene Natural products CC(C)=CCCC(C)=CCCC(C)=CCCC(C)=CC=C\C=C(/C)\C=C\C=C(C)CCC=C(C)CCC=C(C)C OVSVTCFNLSGAMM-UZFNGAIXSA-N 0.000 claims description 3
- 239000002552 dosage form Substances 0.000 claims description 3
- ZIUDAKDLOLDEGU-UHFFFAOYSA-N trans-Phytofluen Natural products CC(C)=CCCC(C)CCCC(C)CC=CC(C)=CC=CC=C(C)C=CCC(C)CCCC(C)CCC=C(C)C ZIUDAKDLOLDEGU-UHFFFAOYSA-N 0.000 claims description 3
- 241000124008 Mammalia Species 0.000 claims description 2
- PXJNUPOCGBDYJJ-UHFFFAOYSA-N Phytofluen Natural products CC(CCCC(=CC=CC(=CC=CC=C(C)/CCC=C(/C)CCC=C(/C)CCC=C(C)C)C)C)CCC=C(C)C PXJNUPOCGBDYJJ-UHFFFAOYSA-N 0.000 claims 2
- 208000035475 disorder Diseases 0.000 claims 2
- 230000002195 synergetic effect Effects 0.000 abstract description 50
- 230000000694 effects Effects 0.000 abstract description 19
- 239000000126 substance Substances 0.000 abstract description 4
- 230000009467 reduction Effects 0.000 abstract description 3
- XEYBRNLFEZDVAW-ARSRFYASSA-N dinoprostone Chemical compound CCCCC[C@H](O)\C=C\[C@H]1[C@H](O)CC(=O)[C@@H]1C\C=C/CCCC(O)=O XEYBRNLFEZDVAW-ARSRFYASSA-N 0.000 abstract description 2
- 230000003993 interaction Effects 0.000 abstract description 2
- 230000037361 pathway Effects 0.000 abstract description 2
- 125000002575 PGE2 group Chemical group 0.000 abstract 1
- MWUXSHHQAYIFBG-UHFFFAOYSA-N Nitric oxide Chemical compound O=[N] MWUXSHHQAYIFBG-UHFFFAOYSA-N 0.000 description 102
- FQYUMYWMJTYZTK-UHFFFAOYSA-N Phenyl glycidyl ether Chemical compound C1OC1COC1=CC=CC=C1 FQYUMYWMJTYZTK-UHFFFAOYSA-N 0.000 description 32
- 210000003024 peritoneal macrophage Anatomy 0.000 description 20
- 210000004027 cell Anatomy 0.000 description 18
- 238000010586 diagram Methods 0.000 description 17
- 239000000284 extract Substances 0.000 description 17
- 239000002158 endotoxin Substances 0.000 description 16
- 229920006008 lipopolysaccharide Polymers 0.000 description 16
- 230000009044 synergistic interaction Effects 0.000 description 16
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 15
- 210000002540 macrophage Anatomy 0.000 description 14
- 235000007688 Lycopersicon esculentum Nutrition 0.000 description 13
- 240000003768 Solanum lycopersicum Species 0.000 description 13
- OUUQCZGPVNCOIJ-UHFFFAOYSA-M Superoxide Chemical compound [O-][O] OUUQCZGPVNCOIJ-UHFFFAOYSA-M 0.000 description 13
- 230000000996 additive effect Effects 0.000 description 13
- 238000002474 experimental method Methods 0.000 description 12
- 102000011779 Nitric Oxide Synthase Type II Human genes 0.000 description 11
- 108010076864 Nitric Oxide Synthase Type II Proteins 0.000 description 11
- 108010037462 Cyclooxygenase 2 Proteins 0.000 description 10
- 102100038280 Prostaglandin G/H synthase 2 Human genes 0.000 description 10
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 9
- 108090000623 proteins and genes Proteins 0.000 description 9
- 239000000654 additive Substances 0.000 description 8
- 150000001875 compounds Chemical class 0.000 description 8
- 230000002757 inflammatory effect Effects 0.000 description 8
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 6
- 238000003119 immunoblot Methods 0.000 description 6
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 6
- 230000026731 phosphorylation Effects 0.000 description 6
- 238000006366 phosphorylation reaction Methods 0.000 description 6
- 230000034190 positive regulation of NF-kappaB transcription factor activity Effects 0.000 description 6
- 101000979342 Homo sapiens Nuclear factor NF-kappa-B p105 subunit Proteins 0.000 description 5
- 102100023050 Nuclear factor NF-kappa-B p105 subunit Human genes 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 102000008299 Nitric Oxide Synthase Human genes 0.000 description 4
- 108010021487 Nitric Oxide Synthase Proteins 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 4
- 238000004113 cell culture Methods 0.000 description 4
- VFLDPWHFBUODDF-FCXRPNKRSA-N curcumin Chemical compound C1=C(O)C(OC)=CC(\C=C\C(=O)CC(=O)\C=C\C=2C=C(OC)C(O)=CC=2)=C1 VFLDPWHFBUODDF-FCXRPNKRSA-N 0.000 description 4
- 238000002955 isolation Methods 0.000 description 4
- 239000006166 lysate Substances 0.000 description 4
- 235000015097 nutrients Nutrition 0.000 description 4
- YBYRMVIVWMBXKQ-UHFFFAOYSA-N phenylmethanesulfonyl fluoride Chemical compound FS(=O)(=O)CC1=CC=CC=C1 YBYRMVIVWMBXKQ-UHFFFAOYSA-N 0.000 description 4
- LPXPTNMVRIOKMN-UHFFFAOYSA-M sodium nitrite Chemical compound [Na+].[O-]N=O LPXPTNMVRIOKMN-UHFFFAOYSA-M 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 3
- 230000001154 acute effect Effects 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 238000001962 electrophoresis Methods 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- 230000006698 induction Effects 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 230000007246 mechanism Effects 0.000 description 3
- 230000001404 mediated effect Effects 0.000 description 3
- 239000002609 medium Substances 0.000 description 3
- 230000033116 oxidation-reduction process Effects 0.000 description 3
- 230000000770 proinflammatory effect Effects 0.000 description 3
- 239000011780 sodium chloride Substances 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- 239000012130 whole-cell lysate Substances 0.000 description 3
- YVLPJIGOMTXXLP-UHFFFAOYSA-N 15-cis-phytoene Chemical compound CC(C)=CCCC(C)=CCCC(C)=CCCC(C)=CC=CC=C(C)CCC=C(C)CCC=C(C)CCC=C(C)C YVLPJIGOMTXXLP-UHFFFAOYSA-N 0.000 description 2
- 108010075031 Cytochromes c Proteins 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- 229920002307 Dextran Polymers 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 2
- 102000000589 Interleukin-1 Human genes 0.000 description 2
- 108010002352 Interleukin-1 Proteins 0.000 description 2
- 108010057466 NF-kappa B Proteins 0.000 description 2
- 102000003945 NF-kappa B Human genes 0.000 description 2
- IOVCWXUNBOPUCH-UHFFFAOYSA-M Nitrite anion Chemical compound [O-]N=O IOVCWXUNBOPUCH-UHFFFAOYSA-M 0.000 description 2
- 208000035868 Vascular inflammations Diseases 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 229940124599 anti-inflammatory drug Drugs 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 230000001684 chronic effect Effects 0.000 description 2
- 208000037976 chronic inflammation Diseases 0.000 description 2
- 208000037893 chronic inflammatory disorder Diseases 0.000 description 2
- 239000003245 coal Substances 0.000 description 2
- 230000001276 controlling effect Effects 0.000 description 2
- 239000012228 culture supernatant Substances 0.000 description 2
- 235000012754 curcumin Nutrition 0.000 description 2
- 239000004148 curcumin Substances 0.000 description 2
- 229940109262 curcumin Drugs 0.000 description 2
- 238000000326 densiometry Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- VFLDPWHFBUODDF-UHFFFAOYSA-N diferuloylmethane Natural products C1=C(O)C(OC)=CC(C=CC(=O)CC(=O)C=CC=2C=C(OC)C(O)=CC=2)=C1 VFLDPWHFBUODDF-UHFFFAOYSA-N 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 231100000673 dose–response relationship Toxicity 0.000 description 2
- 238000001378 electrochemiluminescence detection Methods 0.000 description 2
- 235000002780 gingerol Nutrition 0.000 description 2
- NLDDIKRKFXEWBK-AWEZNQCLSA-N gingerol Chemical compound CCCCC[C@H](O)CC(=O)CCC1=CC=C(O)C(OC)=C1 NLDDIKRKFXEWBK-AWEZNQCLSA-N 0.000 description 2
- JZLXEKNVCWMYHI-UHFFFAOYSA-N gingerol Natural products CCCCC(O)CC(=O)CCC1=CC=C(O)C(OC)=C1 JZLXEKNVCWMYHI-UHFFFAOYSA-N 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 230000001771 impaired effect Effects 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 208000027866 inflammatory disease Diseases 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 229930014626 natural product Natural products 0.000 description 2
- 210000000440 neutrophil Anatomy 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 238000011002 quantification Methods 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 2
- 235000010288 sodium nitrite Nutrition 0.000 description 2
- 238000010183 spectrum analysis Methods 0.000 description 2
- 238000007619 statistical method Methods 0.000 description 2
- 239000011550 stock solution Substances 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 239000012085 test solution Substances 0.000 description 2
- 210000001519 tissue Anatomy 0.000 description 2
- JKQXZKUSFCKOGQ-JLGXGRJMSA-N (3R,3'R)-beta,beta-carotene-3,3'-diol Chemical compound C([C@H](O)CC=1C)C(C)(C)C=1/C=C/C(/C)=C/C=C/C(/C)=C/C=C/C=C(C)C=CC=C(C)C=CC1=C(C)C[C@@H](O)CC1(C)C JKQXZKUSFCKOGQ-JLGXGRJMSA-N 0.000 description 1
- YVLPJIGOMTXXLP-UUKUAVTLSA-N 15,15'-cis-Phytoene Natural products C(=C\C=C/C=C(\CC/C=C(\CC/C=C(\CC/C=C(\C)/C)/C)/C)/C)(\CC/C=C(\CC/C=C(\CC/C=C(\C)/C)/C)/C)/C YVLPJIGOMTXXLP-UUKUAVTLSA-N 0.000 description 1
- YVLPJIGOMTXXLP-BAHRDPFUSA-N 15Z-phytoene Natural products CC(=CCCC(=CCCC(=CCCC(=CC=C/C=C(C)/CCC=C(/C)CCC=C(/C)CCC=C(C)C)C)C)C)C YVLPJIGOMTXXLP-BAHRDPFUSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- FAWLNURBQMTKEB-URDPEVQOSA-N 213546-53-3 Chemical compound N([C@@H](C)C(=O)N[C@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N1CCC[C@H]1C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N1[C@@H](CCC1)C(O)=O)C(C)C)C(C)C)C(=O)[C@@H]1CCCN1C(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)N)C(C)C FAWLNURBQMTKEB-URDPEVQOSA-N 0.000 description 1
- AJBZENLMTKDAEK-UHFFFAOYSA-N 3a,5a,5b,8,8,11a-hexamethyl-1-prop-1-en-2-yl-1,2,3,4,5,6,7,7a,9,10,11,11b,12,13,13a,13b-hexadecahydrocyclopenta[a]chrysene-4,9-diol Chemical compound CC12CCC(O)C(C)(C)C1CCC(C1(C)CC3O)(C)C2CCC1C1C3(C)CCC1C(=C)C AJBZENLMTKDAEK-UHFFFAOYSA-N 0.000 description 1
- 102000007469 Actins Human genes 0.000 description 1
- 108010085238 Actins Proteins 0.000 description 1
- 101800004538 Bradykinin Proteins 0.000 description 1
- 235000003880 Calendula Nutrition 0.000 description 1
- 240000001432 Calendula officinalis Species 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 238000008157 ELISA kit Methods 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 208000018522 Gastrointestinal disease Diseases 0.000 description 1
- QXZGBUJJYSLZLT-UHFFFAOYSA-N H-Arg-Pro-Pro-Gly-Phe-Ser-Pro-Phe-Arg-OH Natural products NC(N)=NCCCC(N)C(=O)N1CCCC1C(=O)N1C(C(=O)NCC(=O)NC(CC=2C=CC=CC=2)C(=O)NC(CO)C(=O)N2C(CCC2)C(=O)NC(CC=2C=CC=CC=2)C(=O)NC(CCCN=C(N)N)C(O)=O)CCC1 QXZGBUJJYSLZLT-UHFFFAOYSA-N 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 102000008379 I-kappa B Proteins Human genes 0.000 description 1
- 108010021699 I-kappa B Proteins Proteins 0.000 description 1
- 102000001284 I-kappa-B kinase Human genes 0.000 description 1
- 108060006678 I-kappa-B kinase Proteins 0.000 description 1
- 102000008070 Interferon-gamma Human genes 0.000 description 1
- 108010074328 Interferon-gamma Proteins 0.000 description 1
- 102100035792 Kininogen-1 Human genes 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 241000699670 Mus sp. Species 0.000 description 1
- 239000000020 Nitrocellulose Substances 0.000 description 1
- 102000007999 Nuclear Proteins Human genes 0.000 description 1
- 108010089610 Nuclear Proteins Proteins 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 239000004115 Sodium Silicate Substances 0.000 description 1
- 102000019197 Superoxide Dismutase Human genes 0.000 description 1
- 108010012715 Superoxide dismutase Proteins 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- 239000013504 Triton X-100 Substances 0.000 description 1
- JKQXZKUSFCKOGQ-LQFQNGICSA-N Z-zeaxanthin Natural products C([C@H](O)CC=1C)C(C)(C)C=1C=CC(C)=CC=CC(C)=CC=CC=C(C)C=CC=C(C)C=CC1=C(C)C[C@@H](O)CC1(C)C JKQXZKUSFCKOGQ-LQFQNGICSA-N 0.000 description 1
- QOPRSMDTRDMBNK-RNUUUQFGSA-N Zeaxanthin Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CCC(O)C1(C)C)C=CC=C(/C)C=CC2=C(C)CC(O)CC2(C)C QOPRSMDTRDMBNK-RNUUUQFGSA-N 0.000 description 1
- 210000000683 abdominal cavity Anatomy 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 230000006978 adaptation Effects 0.000 description 1
- JKQXZKUSFCKOGQ-LOFNIBRQSA-N all-trans-Zeaxanthin Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CC(O)CC1(C)C)C=CC=C(/C)C=CC2=C(C)CC(O)CC2(C)C JKQXZKUSFCKOGQ-LOFNIBRQSA-N 0.000 description 1
- 238000000149 argon plasma sintering Methods 0.000 description 1
- 206010003246 arthritis Diseases 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 230000008033 biological extinction Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- QXZGBUJJYSLZLT-FDISYFBBSA-N bradykinin Chemical compound NC(=N)NCCC[C@H](N)C(=O)N1CCC[C@H]1C(=O)N1[C@H](C(=O)NCC(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CO)C(=O)N2[C@@H](CCC2)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)CCC1 QXZGBUJJYSLZLT-FDISYFBBSA-N 0.000 description 1
- 239000007894 caplet Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 230000005754 cellular signaling Effects 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- OVSVTCFNLSGAMM-KGBODLQUSA-N cis-phytofluene Natural products CC(=CCCC(=CCCC(=CCCC(=CC=C/C=C(C)/C=C/C=C(C)/CCC=C(/C)CCC=C(C)C)C)C)C)C OVSVTCFNLSGAMM-KGBODLQUSA-N 0.000 description 1
- 239000006071 cream Substances 0.000 description 1
- 230000009089 cytolysis Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 235000015872 dietary supplement Nutrition 0.000 description 1
- 150000002066 eicosanoids Chemical class 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- DEFVIWRASFVYLL-UHFFFAOYSA-N ethylene glycol bis(2-aminoethyl)tetraacetic acid Chemical compound OC(=O)CN(CC(O)=O)CCOCCOCCN(CC(O)=O)CC(O)=O DEFVIWRASFVYLL-UHFFFAOYSA-N 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- MHMNJMPURVTYEJ-UHFFFAOYSA-N fluorescein-5-isothiocyanate Chemical compound O1C(=O)C2=CC(N=C=S)=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 MHMNJMPURVTYEJ-UHFFFAOYSA-N 0.000 description 1
- 229940044627 gamma-interferon Drugs 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 230000004190 glucose uptake Effects 0.000 description 1
- 229960001340 histamine Drugs 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 208000028774 intestinal disease Diseases 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 150000002664 lycopenes Chemical class 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 244000000010 microbial pathogen Species 0.000 description 1
- 238000000386 microscopy Methods 0.000 description 1
- 239000008267 milk Substances 0.000 description 1
- 210000004080 milk Anatomy 0.000 description 1
- 235000013336 milk Nutrition 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 230000017128 negative regulation of NF-kappaB transcription factor activity Effects 0.000 description 1
- 229920001220 nitrocellulos Polymers 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 230000035764 nutrition Effects 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 239000006186 oral dosage form Substances 0.000 description 1
- 150000002927 oxygen compounds Chemical class 0.000 description 1
- 230000008506 pathogenesis Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 102000013415 peroxidase activity proteins Human genes 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 235000011765 phytoene Nutrition 0.000 description 1
- 235000002677 phytofluene Nutrition 0.000 description 1
- ZYSFBWMZMDHGOJ-SGKBLAECSA-N phytofluene Natural products CC(=CCCC(=CCCC(=CCCC(=CC=C/C=C(C)/CCC=C(/C)C=CC=C(/C)CCC=C(C)C)C)C)C)C ZYSFBWMZMDHGOJ-SGKBLAECSA-N 0.000 description 1
- 239000000419 plant extract Substances 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 230000004647 pro-inflammatory pathway Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000006337 proteolytic cleavage Effects 0.000 description 1
- 238000003127 radioimmunoassay Methods 0.000 description 1
- 230000000284 resting effect Effects 0.000 description 1
- 229940092258 rosemary extract Drugs 0.000 description 1
- 235000020748 rosemary extract Nutrition 0.000 description 1
- 239000001233 rosmarinus officinalis l. extract Substances 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 238000004611 spectroscopical analysis Methods 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 238000007910 systemic administration Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 229940126585 therapeutic drug Drugs 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 230000006433 tumor necrosis factor production Effects 0.000 description 1
- 238000010798 ubiquitination Methods 0.000 description 1
- 230000008728 vascular permeability Effects 0.000 description 1
- 229940124549 vasodilator Drugs 0.000 description 1
- 239000003071 vasodilator agent Substances 0.000 description 1
- 235000010930 zeaxanthin Nutrition 0.000 description 1
- 239000001775 zeaxanthin Substances 0.000 description 1
- 229940043269 zeaxanthin Drugs 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/01—Hydrocarbons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/01—Hydrocarbons
- A61K31/015—Hydrocarbons carbocyclic
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/047—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates having two or more hydroxy groups, e.g. sorbitol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/05—Phenols
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/07—Retinol compounds, e.g. vitamin A
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/12—Ketones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/22—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acyclic acids, e.g. pravastatin
- A61K31/225—Polycarboxylic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/35—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom
- A61K31/352—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having six-membered rings with one oxygen as the only ring hetero atom condensed with carbocyclic rings, e.g. methantheline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/02—Stomatological preparations, e.g. drugs for caries, aphtae, periodontitis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/02—Nasal agents, e.g. decongestants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Epidemiology (AREA)
- Pulmonology (AREA)
- Emergency Medicine (AREA)
- Diabetes (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Cardiology (AREA)
- Heart & Thoracic Surgery (AREA)
- Immunology (AREA)
- Rheumatology (AREA)
- Dermatology (AREA)
- Food Science & Technology (AREA)
- Nutrition Science (AREA)
- Mycology (AREA)
- Polymers & Plastics (AREA)
- Vascular Medicine (AREA)
- Psychiatry (AREA)
- Pain & Pain Management (AREA)
- Hospice & Palliative Care (AREA)
- Ophthalmology & Optometry (AREA)
- Otolaryngology (AREA)
- Oncology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
Abstract
Изобретение относится к фармацевтической промышленности, а именно к терапевтической противовоспалительной композиции, которая содержит один или несколько полифенолов и два или более каротиноидов, которые выбирают из группы, состоящей из лютеина, ликопена и β-каротина, где полифенолы выбирают из группы, состоящей из карнозной кислоты, кверцетина, резвератрола и галловой кислоты, в определенном количестве; к способу ингибирования или снижения образования супероксид-ионов, NO, TNF-α и/или PGE2 у субъекта-млекопитающего, которому вводят указанную выше композицию; к способу лечения патологических состояний, в которых супероксид-ионы, NO, TNF-α и/или PGE2 выполняют функцию модулятора или медиатора указанного состояния у субъекта-млекопитающего, которому вводят указанную выше композицию; к применению комбинации одного или нескольких полифенолов и двух или более каротиноидов, которые выбирают из группы, состоящей из лютеина, ликопена и β-каротина, где полифенолы выбирают из группы, состоящей из карнозной кислоты, кверцетина, резвератрола и галловой кислоты, в определенном количестве. Вышеописанные изобретения характеризуются синергетическим взаимодействием полифенольных соединений с каротиноидами при ингибировании путей воспаления. 4 н. и 24 з.п. ф-лы, 11 ил., 4 пр.
Description
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композиции, содержащей синергические комбинации полифенолов и каротиноидов. Более конкретно, настоящее изобретение относится к композиции, содержащей синергическую комбинацию указанных выше соединений, которые можно использовать inter alia для ингибирования образования различных медиаторов воспаления.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Воспалительный процесс, который образует важную часть неспецифической иммунной системы, характеризуется сложным набором химических и клеточных изменений, которые необходимы для защиты организма-хозяина перед лицом микробных агентов и других потенциально опасных факторов окружающей среды. Однако во многих случаях может происходить нецелесообразный запуск воспаления, и/или оно может сохраняться в той степени, которая становится опасной для организма-хозяина. В таких случаях может существовать необходимость ингибировать или предотвращать развитие одного или нескольких аспектов воспалительного процесса, в частности в оазисах неинфекционных воспалительных заболеваний.
Показано, что в развитие и контроль воспалительного процесса вовлечено очень большое число различных химических медиаторов. Недавние исследования во многих различных лабораториях связывают оксид азота (NO) в качестве важного модулятора различных острых и хронических воспалительных нарушений, включая различные типы артрита, желудочно-кишечных заболеваний, воспалительных состояний центральной нервной системы и определенные формы астмы. Таким образом, предполагают, что ингибирование образования NO может предоставить эффективный терапевтический механизм для лечения и/или контроля этих воспалительных нарушений. Кроме того, также показано, что ингибирование синтеза NO можно использовать при некоторых заболеваниях или состояниях, которые не обладают первичной воспалительной природой. Таким образом, например, обнаружено, что ингибирование синтеза NO снижает захват глюкозы в тканях конечностей у индивидуумов с диабетом 2-го типа во время физических нагрузок.
Образование NO in vivo опосредовано ферментами семейства синтазы оксида азота (NOS), включая индуцибельную синтазу оксида азота (iNOS), которую активируют многие различные иммунологические стимулы, включая липополисахарид (ЛПС), γ-интерферон и интерлейкин 1 (IL-1).
Ингибирование NOS можно осуществить как in vitro, так и in vivo путем использования L-NG-монометиларгининцитрата (L-NMMA). Кроме того, также показано, что некоторые другие соединения, включая множество натуральных продуктов, ингибируют образование NO. Последняя группа включает соединения, такие как лютеин [Rafi M. M. et al. Mol Nutr Food Res. 2007 Mar; 51 (3): 333-40; Choi, J. S. Nutrition. 2006 Jun; 22 (6):668-71] и ликопен [Rafi, M. M. et al. J Food Sci. 2007 Jan; 72 (1):S069-74]. Однако доказано, что эффективность и активность многих ингибиторов NO из натуральных продуктов не особенно высока. Следовательно существует необходимость в усовершенствованных ингибирующих образование NO композициях природного происхождения.
Другим крайне важным медиатором воспаления является фактор некроза опухоли α (TNF-α), который представляет собой цитокин, образуемый множеством типов клеток, включая макрофаги, нейтрофилы и лимфоциты. TNF-α занимает ключевое положение на ранней стадии воспалительного процесса и отвечает за стимуляцию образования других факторов, таких как ядерный фактор κB, который в свою очередь вызывает активацию широкого диапазона провоспалительных генов. Таким образом, принимая во внимание его ключевую роль, TNF-α, несомненно, является важной возможной терапевтической мишенью для противовоспалительных средств.
Третьим ключевым медиатором воспаления является простагландин E2 (PGE2), член семейства регулирующих молекул эйкозаноидов. Таким образом, PGE2 образуется в значительных количествах в местах воспаления, где он выполняет функцию вазодилататора, а также (вместе с другими медиаторами, такими как гистамин и брадикинин) вызывает повышение проницаемости сосудов, тем самым внося вклад в большинство классических признаков воспаления.
Наконец, другим провоспалительным медиатором, который высвобождают воспалительные клетки, такие как макрофаги и нейтрофилы, является супероксид-ион. Несмотря на то, что супероксид-ионы очень эффективно убивают микробных возбудителей, в других (в частности, неинфекционных) воспалительных состояниях, эти ионы могут вызывать обширное повреждение тканей организма-хозяина. Следовательно, образование супероксид-ионов является потенциально эффективной терапевтической мишенью при рассмотрении новых средств контроля воспалительных состояний.
Цель настоящего изобретения состоит в том, чтобы предоставить композицию, которую можно использовать для ингибирования образования одного или нескольких ключевых медиаторов воспаления, таких как супероксид-ионы, NO, TNF-α и/или PGE2, в качестве средства лечения или контроля патологических состояний и процессов, в которые вовлечены указанные медиаторы.
Другая цель изобретения состоит в том, чтобы предоставить композицию, которая может ингибировать образование указанных выше медиаторов воспаления с более высокой эффективностью и/или активностью, чем соединения и композиция, о которых сообщалось в предшествующем уровне техники.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Недавно авторы настоящего изобретения неожиданно обнаружили, что полифенольные соединения могут синергически взаимодействовать с каротиноидами при ингибировании некоторых провоспалительных путей. В частности, недавно обнаружено, что полифенольное соединение карнозная кислота вызывает синергическое усиление ингибирующего действия определенных каротиноидов, таких как ликопен, лютеин и β-каротин, на образование медиаторов воспаления NO, TNF-α и PGE2. Кроме того, несмотря на то, что это синергическое действие наблюдали в двойных комбинациях карнозной кислоты вместе с ликопеном, β-каротином или лютеином, синергизм значительно усиливается, когда карнозную кислоту комбинируют двумя указанными выше каротиноидами. Указанное выше синергическое противовоспалительное действие также наблюдают, когда каротиноиды представлены в сочетании с другими полифенолами, такими как кверцетин, резвератрол и галловая кислота.
Следовательно настоящее изобретение главным образом направлено на терапевтическую композицию, которая содержит один или несколько полифенолов и два или более каротиноидов, которые выбирают из группы, состоящей из лютеина, ликопена и β-каротина.
В одном из предпочтительных вариантов осуществления полифенолы, использованные в композициях по настоящему изобретению, выбирают из группы, состоящей из карнозной кислоты, кверцетина, резвератрола, галловой кислоты, цикориевой кислоты, гингерола и куркумина.
В одном особенно предпочтительном варианте осуществления композиции по настоящему изобретению содержат полифенольное соединение карнозную кислоту.
В другом особенно предпочтительном варианте осуществления композиции по настоящему изобретению содержат полифенольное соединение кверцетин.
В другом особенно предпочтительном варианте осуществления композиции по настоящему изобретению содержат полифенольное соединение резвератрол.
В другом особенно предпочтительном варианте осуществления композиции по настоящему изобретению содержат полифенольное соединение галловую кислоту.
В одном из вариантов осуществления указанная выше терапевтическая композиция содержит карнозную кислоту, ликопен и лютеин.
В другом предпочтительном варианте осуществления композиция содержит карнозную кислоту, лютеин и β-каротин.
В еще одном дополнительном предпочтительном варианте осуществления композиция содержит ликопен, β-каротин и карнозную кислоту.
В другом варианте осуществления композиция по существу состоит из ликопена, лютеина и карнозной кислоты.
В дополнительном предпочтительном варианте осуществления композиция по существу состоит из лютеина, β-каротина и карнозной кислоты.
В еще одном дополнительном предпочтительном варианте осуществления композиция по существу состоит из ликопена, β-каротина и карнозной кислоты.
Следует отметить, что термин «по существу состоит из», как используют на всем протяжении этого описания и приложенной формулы изобретения, относится к ситуации, где композиция по настоящему изобретению может содержать, в дополнение к названным компонентам (т.е. карнозная кислота вместе с ликопеном и/или лютеином), другие соединения, вещества и средства, которые существенно не влияют на основные и новые характеристики настоящего изобретения.
В других предпочтительных вариантах осуществления композиции по описанным выше предпочтительным вариантам осуществления могут дополнительно содержать один или несколько дополнительных каротиноидов. В одном особенно предпочтительном варианте осуществления дополнительные каротиноиды выбирают из группы, состоящей из фитоена и фитофлуена.
Активные компоненты описанных выше композиций (т.е. полифенол(ы) и каротиноиды) могут представлять собой очищенные соединения, синтетические соединения или могут быть представлены в смеси с другими компонентами, например, в растительных экстрактах, таких как экстракт розмарина (в случае карнозной кислоты), экстракт календулы (в случае лютеина) или экстракт томата (такой как Lycomato, который коммерчески доступен в компании LycoRed, Be'er Sheva, Israel - в случае ликопена и других каротиноидов).
Следует понимать, что термин «лютеин», как используют в настоящем описании, включает все сложные эфиры лютеина в пределах его объема. Кроме того, в объем термина «лютеин» может входить смесь лютеина и зеаксантина, поскольку указанный последним каротиноид часто присутствует вместе с лютеином (иногда составляет 0,1%-15% и более часто 4%-6% от содержания лютеина).
В другом аспекте настоящее изобретение относится к способу ингибирования или снижения образования супероксид-ионов, NO, TNF-α и/или PGE2 у субъекта-млекопитающего, который содержит введение указанному субъекту терапевтической композиции по любому варианту осуществления, описанному выше в настоящем документе.
Кроме того, настоящее изобретение также относится к способу лечения патологических состояний, в которых супероксид-ионы, NO, TNF-α и/или PGE2 выполняют функцию модулятора или медиатора указанного состояния у субъекта-млекопитающего, нуждающегося в таком лечении, где указанный способ включает в себя введение указанному субъекту терапевтической композиции согласно любому варианту осуществления, описанному выше в настоящем документе. В одном из предпочтительных вариантов осуществления этого способа состояние, подлежащее лечению, выбирают из группы, состоящей из острых воспалительных состояний, хронических воспалительных состояний, ревматоидного артрита, синдрома расстройства дыхания взрослых (СРДВ), астмы, ринита, идиопатического фиброза легких, перитонита, сердечно-сосудистого воспаления, ишемии миокарда, нарушения реперфузии, атеросклероза, сепсиса, травмы, диабета 2-го типа, ретинопатии, псориаза, желудочно-кишечного воспаления, цирроза, перитонита и воспалительного заболевания кишечника и нейродегенеративных заболеваний, таких как, например, болезнь Альцгеймера (БА).
В особенно предпочтительных вариантах осуществления способов, описанных выше в настоящем документе, субъектом-млекопитающим является человеческий субъект.
Несмотря на то, что в описанных выше способах терапевтическую композицию можно вводить любым удобным средством, в одном из предпочтительных вариантов осуществления указанную композицию вводят в фармацевтической лекарственной форме. Однако в другом предпочтительном варианте осуществления терапевтическую композицию включают в продукт питания или напиток.
В другом аспекте настоящее изобретение относится к использованию комбинации одного или нескольких полифенолов и двух или более каротиноидов, которые выбирают из группы, состоящей из ликопена, β-каротина и лютеина, в производстве лекарственного средства для лечения состояний, чувствительных к ингибированию образования NO, TNF-α и/или PGE2.
В одном из предпочтительных вариантов осуществления этого аспекта по изобретению один или несколько полифенолов выбирают из группы, состоящей из карнозной кислоты, кверцетина, резвератрола, галловой кислоты, цикориевой кислоты, гингерола и куркумина.
В одном особенно предпочтительном варианте осуществления этого аспекта по изобретению полифенолом является карнозная кислота.
В другом особенно предпочтительном варианте осуществления этого аспекта по изобретению полифенолом является кверцетин.
В еще одном другом особенно предпочтительном варианте осуществления этого аспекта по изобретению полифенолом является резвератрол.
В еще одном другом особенно предпочтительном варианте осуществления этого аспекта по изобретению полифенолом является галловая кислота.
В одном из предпочтительных вариантов осуществления состоянием, подлежащим лечению, является воспалительное состояние.
В одном из предпочтительных вариантов осуществления описанного выше использования состояние, подлежащее лечению, выбирают из группы, состоящей из острых воспалительных состояний, хронических воспалительных состояний, ревматоидного артрита, синдрома расстройства дыхания взрослых (СРДВ), астмы, ринита, идиопатического фиброза легких, перитонита, сердечно-сосудистого воспаления, ишемии миокарда, нарушения реперфузии, атеросклероза, сепсиса, травмы, диабета 2-го типа, ретинопатии, псориаза, желудочно-кишечного воспаления, цирроза, перитонита и воспалительного заболевания кишечника и нейродегенеративных заболеваний, таких как, например, болезнь Альцгеймера (БА).
В одном особенно предпочтительном варианте осуществления этого аспекта по изобретению, карнозную кислоту используют в сочетании как с ликопеном, так и с лютеином.
В другом особенно предпочтительном варианте осуществления этого аспекта по изобретению, карнозную кислоту используют в сочетании как с ликопеном, так и с β-каротином.
В еще одном дополнительном предпочтительном варианте осуществления этого аспекта по изобретению карнозную кислоту используют в сочетании как с лютеином, так и с β-каротином.
Все указанные выше и другие характеристики и преимущества настоящего изобретения можно глубже понять на основе следующих иллюстративных неограничивающих примеров его предпочтительных вариантов осуществления.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
На фиг. 1 графически представлено синергическое взаимодействие карнозной кислоты и ликопена при ингибировании образования NO перитонеальными макрофагами. На верхнем графике показаны результаты, полученные с использованием очищенного ликопена, тогда как на нижнем графике показаны результаты, полученные с использованием обогащенного ликопеном экстракта томата.
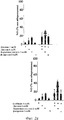
На фиг. 2a графически представлено синергическое взаимодействие между карнозной кислотой и очищенным ликопеном (верхний график) и между карнозной кислотой и обогащенным ликопеном экстрактом томата (нижний график) при ингибировании образования NO перитонеальными макрофагами.
На фиг. 2b графически представлено синергическое взаимодействие между ликопеном и различными комбинациями лютеина, карнозной кислоты и β-каротина при ингибировании образования NO перитонеальными макрофагами. На верхнем графике представлены результаты, полученные с использованием очищенного ликопена, тогда как на нижнем графике представлены результаты, полученные с использованием обогащенного ликопеном экстракта томата.
На фиг. 2c дополнительно показано синергическое взаимодействие между ликопеном и различными комбинациями лютеина, карнозной кислоты и β-каротина при ингибировании образования NO перитонеальными макрофагами. На верхнем графике представлены результаты, полученные с использованием очищенного ликопена, тогда как на нижнем графике представлены результаты, полученные с использованием обогащенного ликопеном экстракта томата.
На фиг. 3 графически представлено синергическое взаимодействие между ликопеном и различными комбинациями лютеина, карнозной кислоты и β-каротина при ингибировании образования TNF-α перитонеальными макрофагами. На верхнем графике представлены результаты, полученные с использованием очищенного ликопена, тогда как на нижнем графике представлены результаты, полученные с использованием обогащенного ликопеном экстракта томата.
На фиг. 4 графически представлено синергическое взаимодействие между ликопеном и различными комбинациями лютеина, карнозной кислоты и β-каротина при ингибировании образования PGE2 перитонеальными макрофагами, в сравнении с несинергическим действием комбинаций без ликопена.
На фиг. 5a графически представлено синергическое взаимодействие между очищенным ликопеном и различными комбинациями различных смесей лютеина, карнозной кислоты и β-каротина при ингибировании образования PGE2 перитонеальными макрофагами.
На фиг. 5b графически представлено синергическое взаимодействие между обогащенным ликопеном экстрактом томата и различными комбинациями различных смесей лютеина, карнозной кислоты и β-каротина при ингибировании образования PGE2 перитонеальными макрофагами.
На фиг. 6 графически представлено синергическое взаимодействие между лютеином, β-каротином и карнозной кислотой при ингибировании стимулированного липополисахаридом образования NO перитонеальными макрофагами.
На фиг. 7 графически представлено синергическое взаимодействие между лютеином, β-каротином и карнозной кислотой при ингибировании стимулированного липополисахаридом образования TNF-α перитонеальными макрофагами.
На фиг. 8 графически представлено синергическое взаимодействие между ликопеном, лютеином и различными полифенолами при ингибировании стимулированного липополисахаридом образования NO перитонеальными макрофагами. На диаграмме A представлены результаты использования очищенного ликопена, тогда как на диаграмме B представлены результаты, полученные при использовании содержащего ликопен экстракта томата (Lyc-O-Mato).
На фиг. 9 графически представлено синергическое взаимодействие между ликопеном, лютеином, β-каротином и карнозной кислотой при ингибировании образования супероксида макрофагами. На диаграмме A представлены результаты использования очищенного ликопена, тогда как на диаграмме B представлены результаты, полученные с использованием содержащего ликопен экстракта томата (Lyc-O-Mato).
На фиг. 10 представлено синергическое взаимодействие между ликопеном или Lyc-O-Mato с лютеином и карнозной кислотой при ингибировании фосфорилирования p65-NFκB по серину 536 в клеточных ядерных лизатах, после предварительной инкубации с ЛПС в течение 10 минут. На верхней части фигуры представлены результаты иммуноблоттинга, из которых получали графические данные.
На фиг. 11 графически представлено синергическое взаимодействие между ликопеном или Lyc-O-Mato с лютеином и карнозной кислотой при ингибировании экспрессии белка индуцируемой липополисахаридом синтазы оксида азота (iNOS) и циклооксигеназы-2 (ЦОГ-2) в цельноклеточных лизатах.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Как описано выше в настоящем документе, настоящее изобретение относится к композициям, которые содержат комбинации одного или нескольких полифенолов с одним или несколькими каротиноидами. В особенно предпочтительном варианте осуществления изобретения композиции содержат карнозную кислоту в качестве единственного полифенола и один или несколько каротиноидов, которые выбирают из группы, состоящей из ликопена (или очищенного или содержащегося в экстракте томата), лютеина и β-каротина. В других предпочтительных вариантах осуществления единственный полифенольный компонент выбирают из группы, состоящей из кверцетина, резвератрола и галловой кислоты.
Предпочтительные суточные количества каждого активного средства, присутствующего в композициях, которые вводят субъектам, нуждающимся в таком введении, имеют следующие значения:
| Карнозная кислота | от 0,5 до 30 мг |
| Ликопен | от 0,5 до 30 мг |
| Лютеин | от 0,5 до 30 мг |
| β-каротин | от 0,5 до 30 мг |
Более предпочтительно, суточное количество каждого указанного выше активного средства находится в диапазоне от 1 до 5 мг.
Количество каждого из различных активных компонентов можно выбрать так, чтобы массовые отношения между ними попадали в следующий широкий диапазон:
| Ликопен: | Лютеин: | β-каротин: | Карнозная кислота: |
| 0,1-5,0: | 0,1-5,0: | 0,1-5,0: | 0,1-5,0 |
В одной предпочтительной группе композиций активные компоненты можно комбинировать в следующих диапазонах массовых отношений:
| Ликопен: | Лютеин: | β-каротин: | Карнозная кислота: |
| 0,1-1,0: | 0,1-1,0: | 0,1-1,0: | 0,1-1,0 |
В одном из предпочтительных вариантов осуществления активные компоненты можно комбинировать при следующем отношении:
| Ликопен: | Лютеин: | β-каротин: | Карнозная кислота: |
| 1,0: | 1,0: | 1,0: | 0,5 |
В другом предпочтительном варианте осуществления активные компоненты можно комбинировать при следующем отношении:
| Ликопен: | Лютеин: | β-каротин: | Карнозная кислота: |
| 1,0: | 0,3: | 0,3: | 0,4 |
В еще одном дополнительном предпочтительном варианте осуществления активные компоненты можно комбинировать при следующем отношении:
| Ликопен: | Лютеин: | β-каротин: | Карнозная кислота: |
| 1,0: | 1,0: | 1,0: | 1,0 |
Следует отметить, что композиции, полученные в соответствии с предыдущими примерами предпочтительных массовых отношений не требуют обязательного присутствия всех четырех перечисленных компонентов. Точнее достаточно, чтобы композиция содержала карнозную кислоту (или другой полифенол) вместе с по меньшей мере двумя указанными каротиноидами, где относительное количество каждого из этих компонентов равно указанному с помощью фигур, приведенных непосредственно выше в настоящем документе.
В другой группе предпочтительных вариантов осуществления активные компоненты можно комбинировать в следующих диапазонах массовых отношений:
| Ликопен: | Лютеин: | β-каротин: | Карнозная кислота: |
| 0,1-1,0: | 0,1-5,0: | 0,1-1,0: | 0,1-1,0 |
Более предпочтительно активные компоненты можно комбинировать в следующих диапазонах массовых отношений:
| Ликопен: | Лютеин: | β-каротин: | Карнозная кислота: |
| 0,1-1,0: | 0,1-4,0: | 0,1-1,0: | 0,1-1,0 |
В конкретных предпочтительных вариантах осуществления активные компоненты можно комбинировать при следующих массовых отношениях:
| Ликопен: | Лютеин: | Карнозная кислота: |
| 0,1: | 1,73: | 0,13 |
| Ликопен: | Лютеин: | Карнозная кислота: |
| 0,1: | 1,8: | 0,26 |
| β-каротин: | Лютеин: | Карнозная кислота: |
| 0,29: | 1,29: | 0,1 |
| β-каротин: | Лютеин: | Карнозная кислота: |
| 0,39: | 1,29: | 0,1 |
| β-каротин: | Лютеин: | Карнозная кислота: |
| 0,32: | 3,42: | 0,1 |
| β-каротин: | Лютеин: | Карнозная кислота: |
| 0,16: | 1,71: | 0,1 |
| β-каротин: | Лютеин: | Карнозная кислота: |
| 0,29: | 1,29: | 0,1 |
| β-каротин: | Лютеин: | Карнозная кислота: |
| 0,39: | 1,29: | 0,1 |
Различные активные компоненты можно вводить в составы или для системного, или для местного использования. В случае системного введения полифенол(ы) и каротиноид(ы) можно включать в пероральные лекарственные формы, такие как таблетки, каплеты, капсулы, сиропы, эликсиры, жидкости и т.д.
В других предпочтительных вариантах осуществления композицию по настоящему изобретению можно вводить местно, например на кожу или слизистые оболочки (например, в виде кремов, лосьонов, мазей и т.д.). Дополнительные подробности относительно подходящих способов включения содержащих полифенолы и каротиноиды композиций по настоящему изобретению во многие различные лекарственные формы можно получить из любого стандартного справочника, известного специалистам, включая, например, Remington's Pharmaceutical Sciences, Mack Publishing Co, Easton, Па, USA (1980).
В других предпочтительных вариантах осуществления композицию по настоящему изобретению получают в виде пищевой добавки, которая подходит для непосредственного включения в продукт питания или напиток.
Карнозную кислоту, которую используют для получения композиций по настоящему изобретению, можно получать коммерческим путем от нескольких различных поставщиков, включая Alexis Biochemicals, Lausen, Switzerland. Каротиноиды получали от нескольких различных поставщиков, включая LycoRed Ltd., Be'er Sheva, Israel.
Альтернативно, некоторые компоненты композиции, такие как ликопен, можно включать в указанную композицию в форме обогащенного ликопеном экстракта томата. Один такой экстракт томата коммерчески доступен (например, в форме капсул) из LycoRed Ltd., Beer Sheva, Israel, под торговым названием «Lyc-O-Mato®». Подходящие процессы для получения этого экстракта и схожих экстрактов описаны в US 5837311, описание которого включено в настоящий документ в качестве ссылки в полном объеме. Однако следует учитывать, что любые другие типы процедур получения можно использовать для получения содержащей каротиноид композиции из множества растительных источников. Кроме того, композиции также можно получать из одного или нескольких синтетических каротиноидов.
Следующие примеры приведены в иллюстративных целях и для того, чтобы более конкретно объяснить и описать настоящее изобретение. Однако настоящее изобретение не ограничено конкретными вариантами осуществления, описанными в этих примерах.
ПРИМЕР 1
Ингибирование образования NO, TNF-α и PGE
2
в перитонеальных макрофагах различными комбинациями карнозной кислоты, лютеина, ликопена и β-каротина
Способы и материалы
Выделение и клеточная культура макрофагов. Перитонеальные макрофаги собирали из брюшных полостей самцов мышей ICR в возрасте 6-8 недель (Harlan, Israel), которым вводили интраперитонеальную инъекцию 1,5 мл тиогликолевой жидкой среды (4%) за 4 суток до сбора. Перитонеальные макрофаги отмывали три раза с PBS и, при необходимости, осуществляли гипотонический лизис эритроцитов, получали чистоту 90-95%. Макрофаги идентифицировали в анализе на клеточном сортере с возбуждением флуоресценции с использованием конъюгированных с ФИТЦ антител крысы против F4/80 мыши (MCA497F) (Serotec, Oxford, England) посредством проточной микрофлуорометрии на клеточном сортере с возбуждением флуоресценции (Becton Dickinson, Mountain View, CA). Для каждого образца анализировали 10000 отобранных по светорассеянию жизнеспособных клеток. Перитонеальные макрофаги и клеточную линию макрофагов мыши RAW264,7 культивировали в среде RPMI 1640, содержащей 10% FCS, 2 мМ L-глутамина; 100 Ед/мл пенициллина; 100 мкг/мл стрептомицина (Beit-Haemek, Israel) в 96-луночных плашках (1×106 клеток/лунка) при 37°C в атмосфере с 5% CO2. Клетки стимулировали липополисахаридом (0,1-1 мкг/мл) в присутствии или в отсутствие карнозной кислоты и/или одного или нескольких следующих каротиноидов: карнозная кислота, очищенные ликопен, обогащенный ликопеном экстракт томата (Lyc-O-Mato®; LycoRed Ltd., Be'er Sheva, Israel), лютеин и β-каротин.
Карнозную кислоту и различные каротиноиды растворяли в DMSO (до конечной концентрации 5 мМ). Смесь энергично перемешивали и инкубировали на водяной бане при 37°C (при встряхивании) в течение 10 мин, а затем обрабатывали звуком в ванне для обработки звуком три раза, каждый раз в течение 15 секунд. Используя этот основной раствор, желаемые концентрации получают добавлением соответствующих его объемов в теплую среду для культивирования.
Концентрацию ликопена в растворе определяли после экстракции следующим образом: 0,5 мл изопропанола + 1,5 гексана/дихлорметана (1:5 об./об.), содержащего 0,025% BHT, добавляли в 1 мл свежеприготовленного раствора ликопена с концентрацией 20 мкМ в предварительно нагретой среде. Раствор энергично перемешивали и разделяли фазы посредством центрифугирования на скорости 3000 об./мин в течение 10 мин.
Чтобы измерить содержание ликопена проводили спектральный анализ (пик поглощения 471 нм).
Соответствующие объемы DMSO (0,1-0,2%) добавляли в контроли и процент ингибирования в каждой пробирке вычисляли по отношению к его контролю.
Анализ образования NO. Уровни NO в супернатантах клеточных культур определяли посредством анализа уровней нитрита с использованием реактива Грисса и нитрита натрия в качестве стандарта, как описано в Green, L. C, Wagner, D. A., Glogowski, J., Skipper, P. L., Wishnok, J. S., и Tannenfaaum, S. R. (1982) Anal Biochem. 126: 131-138.
Измерение PGE 2 . Супернатанты покоящихся и стимулированных клеток собирали и незамедлительно сохраняли при -70°C. Уровни PGE2 определяли, используя протокол радиоиммунного анализа с угля, покрытого декстраном, как ранее описано (Dror N, Tveria L, Meniv I, Ben-Shmuel S, Filipovich T, Fleisher-Berkovich S., Regul Pept. 2008 150: 21-5).
В кратком изложении, 100 мкл образца или стандарта PGE2 (Sigma Israel, Rehovot, Israel) инкубировали в присутствии 500 мкл антисыворотки против PGE2 (Sigma Israel, Rehovot, Israel) в течение 30 мин. Затем добавляли [3H]PGE2 (Amersham Biosciences, NJ, USA) в течение 24 ч при температуре 4°C. Через 24 ч 200 мкл холодной суспензии угля, покрытого декстраном, добавляли в каждую пробирку и инкубировали в течение 10 мин на льду. Пробирки центрифугировали на скорости 3500 об/мин в течение 15 мин при температуре 4°C. В 500 мкл супернатантов, содержащих комплексы [3H]PGE2 и антител против PGE2, проводили подсчет (Packard Spectrometry 1900CA) и вычисляли количество PGE2.
Анализ образования TNF-α. Концентрации TNF-α количественно определяли с использованием наборов ELISA (Biolegend Inc., San Diego, CA).
Статистический анализ. Данные представляли в виде среднего значения ± стандартная ошибка среднего. Статистическую значимость для сравнений между группами определяли с использованием двустороннего парного критерия Стьюдента.
Результаты
Фиг. 1
Зависящее от дозы синергическое ингибирование образования NO комбинацией ликопена или Lycomato и карнозной кислоты.
С использованием карнозной кислоты или отдельных каротиноидов самих по себе получены следующие результаты: ликопен или Lycomato в диапазоне 1-5 мкМ вызывали низкий уровень ингибирования образования NO. Карнозная кислота (1 и 2 мкМ) вызывала 12% и 18% ингибирование образования NO, соответственно.
Добавление карнозной кислоты к ликопену или Lycomato вызывало синергическое ингибирование образования NO, которое зависело от дозы.
Более эффективна комбинация карнозной кислоты с Lycomato, чем с очищенным ликопеном.
Результаты, представленные на фиг. 1, представляют собой средние значения ± стандартная ошибка среднего 10 независимых экспериментов, каждый из которых проводили дважды.
Фиг. 2a
Ингибирование образования NO комбинацией оптимальных низких концентраций двух компонентов: ликопена или Lycomato с карнозной кислотой, лютеином и β-каротином.
Комбинация 1 мкМ ликопена или Lycomato с 2 мкМ карнозной кислоты вызывала значимое синергическое ингибирование образования NO, которое было более эффективным в присутствии Lycomato в сравнении с ликопеном.
Комбинация 1 мкМ ликопена или Lycomato с 1 мкМ лютеина или с 2 мкМ β-каротина вызывала аддитивное или не обладающее значимостью синергическое ингибирование образования NO, соответственно.
Комбинация ликопена или Lycomato с карнозной кислотой (т.е. комбинация каротиноида с полифенолом) более эффективна, чем комбинация двух каротиноидов.
Фиг. 2b
Ингибирование образования NO комбинацией оптимальных низких концентрации ликопена или Lycomato с двумя другими компонентами.
Комбинация ликопена или Lycomato с карнозной кислотой и лютеином или с карнозной кислотой и β-каротином (концентрации такие же, как использовали для получения результатов, представленных на фиг. 2a) вызывала значимое и схожее синергическое ингибирование образования NO, тогда как комбинация, не содержащая карнозную кислоту, оказывала только аддитивное действие (обозначено пунктирным эллипсом).
Комбинация четырех компонентов (т.е. ликопена или Lycomato вместе с карнозной кислотой, лютеином и β-каротином) не превосходила комбинацию трех компонентов.
Фиг. 2c
Комбинация карнозной кислоты и каротиноидов, исключая ликопен или Lycomato.
Комбинация или лютеина, или β-каротина с карнозной кислотой вызывала значимое и схожее синергическое ингибирование образования NO (которое схоже с комбинацией ликопена и карнозной кислоты, но ниже, чем наблюдали при использовании комбинации Lycomato и карнозной кислоты). Комбинация лютеина и β-каротина оказывала аддитивное (или более слабое) действие. Эти результаты дополнительно подтверждают то, что как каротиноид(ы), так и полифенол(ы) необходимы для того, чтобы добиться оптимального синергического действия.
Результаты представляют собой средние значения ± стандартная ошибка среднего 3 независимых экспериментов, каждый из которых проводили дважды.
Фиг. 3
Верхний график: Ингибирование образования TNF-α различными комбинациями оптимальных низких концентраций ликопена с карнозной кислотой, лютеином и β-каротином.
Образование TNF-α в том же наборе экспериментов, что и на фиг. 2, менее чувствительно, чем образование NO, поскольку ни одно из этих средств не вызывало какого-либо обнаружимого ингибирования образования TNF-α при использовании по отдельности (т.е. не в сочетании с другими средствами).
Комбинации ликопена с карнозной кислотой или с β-каротином вызывали низкий уровень синергического ингибирования образования TNF-α: 10% и 8% соответственно.
Сходно действию на образование NO, комбинации ликопена или с карнозной кислотой и лютеином или с карнозной кислотой и β-каротином вызывали значимое и схожее синергическое ингибирование образования TNF-α, которое превышало синергическое ингибирование, вызванное комбинацией, не содержащей карнозную кислоту.
Комбинация карнозной кислоты со всеми тремя каротиноидами не превосходила синергический результат, полученный с использованием указанной выше комбинации карнозной кислоты с двумя каротиноидами.
Нижний график: Ингибирование образования TNF-α различными комбинациями оптимальных низких концентраций Lycomato с карнозной кислотой, лютеином и β-каротином.
Образование TNF-α ингибировали (10%) в присутствии Lycomato (в отличие от отсутствия обнаружимого ингибирования в присутствии ликопена). Комбинации Lycomato с каждым другим каротиноидом вызывали синергическое ингибирование, которое было выше в присутствии карнозной кислоты.
Сходно с действием на образование NO, комбинации Lycomato с карнозной кислотой и лютеином или с карнозной кислотой и β-каротином вызывало значимое схожее синергическое ингибирование образования TNF-α, тогда как комбинации, не содержащие карнозную кислоту, оказывали меньшее синергическое действие.
Как и в случае очищенного ликопена, комбинация карнозной кислоты со всеми тремя каротиноидами не превосходила синергический результат, полученный при использовании указанной выше комбинации карнозной кислоты с двумя каротиноидами.
Результаты представляли собой средние значения ± стандартную ошибку среднего 3 независимых экспериментов, каждый из которых осуществляли дважды.
Следует отметить, что комбинации, которые содержали Lycomato, были более эффективны при ингибировании образования TNF-α, чем те, что содержали очищенный ликопен.
Фиг. 4
Ингибирование образования PGE
2
различными комбинациями оптимальных низких концентраций ликопена с карнозной кислотой, лютеином и β-каротином.
Образование PGE2 в том же наборе экспериментов, как представлено на фиг. 2, более чувствительно, чем образование NO, к карнозной кислоте или β-каротину при использовании по отдельности (ингибирование приблизительно 20% для каждого). Комбинации ликопена с лютеином, карнозной кислотой или β-каротином вызывали синергическое ингибирование образования PGE2.
Низкий уровень синергического ингибирования можно обнаружить с использованием комбинации Lycomato только с лютеином и карнозной кислотой, тогда как комбинация с карнозной кислотой и β-каротином вызывала только аддитивное действие. Комбинация с лютеином и β-каротином вызывала аддитивное ингибирование образования PGE2.
На фиг. 4 также вновь можно видеть, что комбинация четырех средств (карнозной кислоты плюс три каротиноида) не превосходила комбинацию карнозной кислоты с двумя каротиноидами.
Фиг. 5a
Ингибирование образования PGE
2
различными комбинациями оптимальных низких концентраций ликопена с карнозной кислотой, лютеином и β-каротином.
Как уже показано на фиг. 4, на верхней диаграмме на фиг. 5a показано, что карнозная кислота или β-каротин (каждое использовали раздельно) вызывали высокий уровень ингибирования образования PGE2 (ингибирование приблизительно 20% для каждого). Комбинации ликопена с лютеином, карнозной кислотой или β-каротином вызывали синергическое ингибирование образования PGE2.
Низкий уровень синергического ингибирования можно определить в случае комбинации ликопена только с лютеином и карнозной кислотой, тогда как комбинация с карнозной кислотой и β-каротином вызывала только аддитивное действие. Комбинация, содержащая лютеин и β-каротин, вызывала аддитивное ингибирование образования PGE2. Таким образом, изучали более низкие концентрации (как показано на нижней диаграмме на фиг. 5a, рассмотрено ниже).
Комбинация всех четырех активных средств (т.е. карнозной кислоты плюс три каротиноида) не превосходила комбинацию карнозной кислоты с двумя каротиноидами.
Синергическое ингибирование образования PGE
2
различными комбинациями оптимальных более низких концентраций карнозной кислоты, лютеина и β-каротина (нижняя диаграмма).
Ни лютеин (0,5 мкМ), ни β-каротин (1 мкМ) по отдельности не оказывали действие на образование PGE2, тогда как карнозная кислота (1 мкМ) вызывала 10% ингибирование. В этих условиях комбинации ликопена 1 мМ с более низкой концентрацией одного из двух других компонентов вызывали синергическое ингибирование.
Комбинация всех четырех активных средств не превосходила комбинацию трех активных средств.
Фиг. 5b
Ингибирование образования PGE
2
различными комбинациями оптимальных низких концентраций Lycomato с карнозной кислотой, лютеином и β-каротином.
На верхней диаграмме показано, что действие Lycomato на ингибирование образования PGE2 схоже с таковым чистого ликопена и схожие комбинации приводили к схожему действию, как показано для ликопена (верхняя диаграмма на фиг. 5a).
Синергическое ингибирование образования PGE
2
различными комбинациями оптимальных более низких концентраций карнозной кислоты, лютеина и β-каротина (нижняя диаграмма).
Как на фиг. 5a ни лютеин (0,5 мкМ), ни β-каротин (1 мкМ) по отдельности не оказывали влияние на образование PGE2, тогда как карнозная кислота (1 мкМ) вызывала 10% ингибирование. Комбинация с β-каротином была аддитивной, тогда как комбинации с лютеином или с карнозной кислотой были синергическими и более эффективными, чем полученные с использованием очищенного ликопена (фиг. 5a). Комбинация Lycomato с карнозной кислотой и лютеином или с карнозной кислотой и β-каротином вызывала значимое и схожее синергетическое ингибирование образования PGE2. Комбинация лютеина и β-каротина (не содержащая карнозную кислоту) вызывала более низкий уровень синергического ингибирования. При этих концентрациях комбинация Lycomato с лютеином и карнозной кислотой вызывала синергическое действие, которое значительно превосходило полученное в результате использования комбинаций с очищенным ликопеном.
Комбинация всех четырех активных средств (т.е. карнозной кислоты плюс три каротиноида) не превосходила комбинацию карнозной кислоты с двумя каротиноидами.
Фиг. 6
Синергическое ингибирование образования NO комбинациями лютеина, β-каротина и карнозной кислоты.
На двух верхних диаграммах (A и B) представлено синергическое взаимодействие между тремя компонентами тестируемой композиции на образование NO, где конечная концентрация β-каротина составляла 0,5 мкМ. Аналогичным образом, композиции, содержащие более высокую концентрацию β-каротина (1,0 мкМ; диаграммы C и D), также вызывали ингибирование образования NO синергическим образом.
На каждой диаграмме, представленной на фиг. 6, горизонтальная линия на столбце, представляющем трехкомпонентную композицию, указывает уровень ингибирования NO, который следовало ожидать, если бы действие каждого указанного компонента было аддитивным. Наблюдаемый значительно повышенный уровень ингибирования (область столбца над горизонтальной линией, обозначенная «S») указывает на то, что три компонента композиции действовали синергически.
Фиг. 7
Синергическое ингибирование образования TNF-α комбинациями лютеина, β-каротина и карнозной кислоты.
На двух верхних диаграммах (A и B) представлено влияние синергического взаимодействия между тремя компонентами тестируемой композиции на образование TNF-α, где конечная концентрация β-каротина составляла 0,5 мкМ. Аналогичным образом, композиции, содержащие более высокую концентрацию β-каротина (1,0 мкМ; диаграммы C и D) также вызывали ингибирование образования TNF-α синергическим образом.
На каждой диаграмме, представленной на фиг. 7, горизонтальная линия на столбце, соответствующем трехкомпонентной композиции, указывает уровень ингибирования TNF-α, который следовало ожидать, если бы действие каждого указанного компонента было аддитивным. Наблюдаемый значительно повышенный уровень ингибирования (область столбца над горизонтальной линией, обозначенной «S») указывает на то, что три компонента композиции действовали синергически.
ПРИМЕР 2
Ингибирование индуцированного липополисахаридом образования NO в перитонеальных макрофагах различными комбинациями лютеина, ликопена и полифенола, который выбирают из группы, состоящей из карнозной кислоты, галловой кислоты, резвератрола и кверцетина
Способы и материалы
Выделение и клеточная культура макрофагов. Перитонеальные макрофаги собирали и культивировали, как описано в примере 1 выше в настоящем документе.
Получение тестируемых средств. Ликопен и лютеин растворяли в DMSO (объем DMSO в тестируемом растворе не превышал 0,04%). Смесь энергично перемешивали и встряхивали при температуре 37°C в течение 10 мин и обрабатывали звуком в ванне для обработки звуком 3 раза по 15 с. Из этого основного раствора желаемые концентрации получали добавлением соответствующих объемов в теплую среду для культивирования. Концентрацию в растворе вычисляли для 1 мл самой высокой конечной концентрации 0,5 мл изопропанола + 1,5 мл гексана/дихлорметана (1:5 об./об.), содержащего 0,025% BHT. Раствор энергично перемешивали и фазы разделяли посредством центрифугирования на скорости 3000 об/мин в течение 10 мин. Для определения уровня питательных веществ проводили спектральный анализ. Карнозную кислоту, резвератрол, галловую кислоту или кверцетин растворяли в этаноле (объем этанола в тестируемом растворе не превышал 0,0025%).
В контроли добавляли соответствующие объемы DMSO и/или этанола и вычисляли процент ингибирования каждой пробирки по отношению к ее контрольной пробирке.
Анализ образования NO. Уровни NO в супернатантах клеточных культур определяли посредством анализа уровней нитрита с использованием реактива Грисса и нитрита натрия, как описано выше в настоящем документе в примере 1.
Статистический анализ. Данные представляли в виде среднего значения ± стандартная ошибка среднего. Статистическую значимость для сравнений между группами определяли с использованием двустороннего парного критерия Стьюдента.
Результаты
Фиг. 8
A. Синергическое ингибирование образования NO комбинациями низких концентраций ликопена, лютеина и каждого из различных полифенолов
Макрофаги инкубировали 1 мкМ ликопена, 1 мкМ лютеина и одним из 2 мкМ карнозной кислоты, 2 мкМ резвератрола, 2 мкМ галловой кислоты или 2 мкМ кверцетина и их комбинациями в течение 1 часа перед добавлением ЛПС на 16 ч при температуре 37°C. Измеряли образование NO и вычисляли процент ингибирования. В каждом эксперименте анализировали действие трех различных концентраций ЛПС, поскольку чувствительность клеток могла меняться в различных экспериментах.
Комбинации 1 мкМ ликопена, 1 мкМ лютеина и 2 мкМ одного из карнозной кислоты, резвератрола, галловой кислоты или кверцетина вызывали значимое синергическое ингибирование образования NO (обозначено буквой «S» на диаграмме, где горизонтальная линия, пересекающая каждый столбец, представляющий синергическую комбинацию, обозначает результаты, которые следовало ожидать, если бы взаимодействие было аддитивным, а не синергическим). Отсутствовали значимые различия между всеми этими различными комбинациями. Как показано на фигуре, действие каждого тестируемого каротиноида или полифенола при данной концентрации было очень слабым. Как показано горизонтальной линией на каждой диаграмме, синергическое действие было приблизительно в три раза сильнее, чем аддитивное действие.
B. Синергическое ингибирование образования NO комбинацией низких концентраций Lyc-O-Mato, лютеина и каждого из различных полифенолов.
Макрофаги обрабатывали как в п. A, но эксперименты проводили с использованием Lyc-O-Mato вместо ликопена.
Несмотря на то, что сам Lyc-O-Mato вызывал ингибирование образования NO, схожее с вызываемым ликопеном, комбинации с Lyc-O-Mato были более эффективными и приводили к более выраженному приблизительно четырехкратному синергизму по сравнению с аддитивным действием.
Результаты, приведенные на фиг. 8, приведены в виде среднего значения ± стандартная ошибка среднего трех различных экспериментов, каждый из которых выполняли трижды.
ПРИМЕР 3
Ингибирование индуцированного липополисахаридом образования супероксида в макрофагах различными комбинациями ликопена или Lyc-O-Mato, лютеина, β-каротина и карнозной кислоты
Способы и материалы
Выделение макрофагов. Перитонеальные макрофаги выделяли и обрабатывали, как описано выше в настоящем документе в примере 1.
Образование супероксида. Образование супероксид-аниона (O2 -) макрофагами измеряли в виде ингибируемого супероксиддисмутазой восстановления феррицитохрома способом с микротитровальным планшетом, как известно в существующем уровне техники. Аликвоту радиоактивно меченных макрофагов (5×105 клеток/лунка), использованных в анализе прилипания, брали и суспендировали в 100 мкл инкубационной среды, содержащей феррицитохром c (150 мМ). Стимуляцию индуцировали с использованием PMA (50 нг/мл). Восстановление феррицитохрома c вызывало изменение спектральной поглощательной способности, которую измеряли при 550 нм через интервалы 2 мин в течение 30 мин на Thermomax Microplate Reader (Molecular Devices, Melno Park, Calif., USA). Максимальные интенсивности образования супероксида определяли и выражали в виде наномолей O2 -/106 клеток/10 мин с использованием коэффициента экстинкции E550=21 мМ-1см-1.
Результаты
Фиг. 9
Верхняя диаграмма (A): Ингибирование образования супероксида различными комбинациями оптимальных низких концентраций очищенного ликопена с карнозной кислотой, лютеином или β-каротином.
Образование супероксида ингибировали в присутствии 2 мкМ β-каротина (10%).
Комбинации ликопена с карнозной кислотой или с β-каротином вызывали низкий уровень ингибирования образования супероксида, которое незначительно отличалось от действия β-каротина.
Схожее с действием на образование NO (см. пример 1 выше в настоящем документе), комбинации ликопена или с карнозной кислотой и лютеином или с карнозной кислотой и β-каротином, вызывали значимое и схожее синергическое ингибирование образования супероксида, которое превышало синергическое ингибирование, вызванное комбинацией, не содержащей карнозную кислоту.
Комбинация карнозной кислоты со всеми тремя каротиноидами не превосходила синергический результат, полученный с использованием указанной выше комбинации карнозной кислоты с двумя каротиноидами.
Нижняя диаграмма (B): Ингибирование образования супероксида различными комбинациями оптимальных низких концентраций Lyc-O-Mato с карнозной кислотой, лютеином или β-каротином.
Образование супероксида ингибировали (7%) в присутствии Lyc-O-Mato (в отличие от отсутствия обнаружимого ингибирования в присутствии ликопена). Комбинации Lyc-O-Mato с каждым из других каротиноидов вызывали низкий уровень ингибирования образования супероксида, которое незначительно отличалось от действия β-каротина или Lyc-O-Mato.
Схоже с действием на образование NO (см. пример 1 выше в настоящем документе), комбинации Lyc-O-Mato с карнозной кислотой и лютеином или с карнозной кислотой и β-каротином вызывали значимое и схожее синергическое ингибирование образования супероксида, тогда как комбинация, не содержащая карнозную кислоту, вызывала менее выраженное синергическое действие.
Как и в случае очищенного ликопена, комбинация карнозной кислоты со всеми тремя каротиноидами не превосходила синергический результат, полученный с использованием указанной выше комбинации карнозной кислоты с двумя каротиноидами.
Результаты представляли собой среднее значение ± стандартная ошибка среднего 3 независимых экспериментов, каждый из которых осуществляли дважды.
ПРИМЕР 4
Ингибирование индуцированного липополисахаридом фосфорилирования p65-NFkB по серину 536 в клеточных ядерных лизатах и активации iNOS и ЦОГ-2 различными комбинациями ликопена или Lyc-O-Mato с лютеином и карнозной кислотой
Введение
Экспрессию воспалительных цитокинов, а также экспрессию белков-ферментов можно регулировать посредством активации транскрипционного фактора ядерного фактора κB (NFκB), который выполняет ключевую роль в некоторых аспектах патогенеза хронических воспалительных заболеваний. NFκB активируется вследствие фосфорилирования, убиквитинилирования и последующего протеолитического расщепления белка IκB через активацию киназы IκB (IKK). Высвобожденный NFκB перемещается в ядра и связывается с мотивами в промоторах провоспалительных генов, таких как индуцибельная синтаза оксида азота (iNOS), и циклооксигеназы-2 (ЦОГ-2) TNF-α и IL-1β, что ведет к индукции экспрессии их мРНК. Показано, что большинство противовоспалительных лекарственных средств подавляют экспрессию этих генов посредством ингибирования пути активации NFκB. Таким образом, ингибитор NFκB можно использовать в качестве потенциального терапевтического лекарственного средства в клинических применениях для регулирования связанных с воспалением заболеваний человека.
p65 NFκB RelA можно фосфорилировать с помощью PKA по Ser-276 или с помощью чувствительного к окислению-восстановлению механизма по Ser-536. Показано, что реакционноспособные соединения кислорода (ROS) играют важную роль в активации NFκB и экспрессии воспалительных генов.
Цель этого исследования состояла в том, чтобы изучить, могут ли низкие концентрации комбинаций ликопена/Lyc-O-Mato + лютеина + карнозной кислоты вызывать синергическое ингибирование активации NFκB.
Активацию NFκB анализировали по его двум фосфорилированным формам: PKA-зависимая Ser-276 и чувствительная к окислению-восстановлению Ser-536.
Способы
Выделение макрофагов. Перитонеальные макрофаги выделяли и обрабатывали, как описано выше в настоящем документе в примере 1.
Для определения активации NFκB клетки обрабатывали липополисахаридом в течение 10 мин.
Получение ядерного белкового экстракта. 2×106 клеток суспендировали в 600 мкл ледяного буфера для лизиса NP-40 (0,1% NP-40, 10 мМ Tris-HCl, pH 7,4, 10 мМ NaCl, 3 мМ MgCl2, 1 мМ ЭДТА, 10 мкг/мл лейпептина, 10 мкг/мл апротонина и 1 мМ PMSF). Клетки энергично перемешивали в течение 15 с, держали на льду в течение 5 мин и центрифугировали на скорости 300 об в течение 10 мин при температуре 4°C. Затем полученные осадки (содержащие ядра фракции) немедленно растворяли в буфере для электрофореза образца. Целостность ядер подтверждали непосредственно световой микроскопией, которая также выявила, что редко наблюдались интактные клетки в содержащей ядра фракции (<2%).
Цельноклеточные лизаты получали, используя 1% Triton X-100, 50 мМ HEPES (pH 7,5), 150 мМ NaCl, 1 мМ ЭДТА, 1 мМ ЭГТА, 10% глицерин, 25 мМ NaF, 10 мкМ ZnCl2, 1 мМ PMSF и 100 мкМ лейпептин.
Иммуноблот-анализ. Белки лизата (35-50 мкг) разделяли электрофорезом на 7,5% полиакриламидных SDS гелях. Разрешенные белки электрофоретически переносили на нитроцеллюлозу, которую окрашивали Понсе красным для определения полос белков и затем блокировали в 5% молоке в TBS (10 мМ Tris, 135 мМ NaCl, pH 7,4). Определение иммуноблоттинга осуществляли, как описано выше (17), с использованием первичных антител p-P65, ЦОГ-2 и iNOS (Cell Signaling Technology, Beverly, MA) для инкубации в течение ночи при температуре 4°C и вторичного антитела, противокроличьего или противомышиного конъюгированного с пероксидазой антитела козы (Amersham Biosciences, Buckinghamshire, United Kingdom), в течение 1 часа при комнатной температуре и определяли, используя систему определения усиленной хемилюминесценции (ECL) (Amersham Biosciences).
Для определения иммуноблоттинга P-65 ядерные фракции 2×106 клеток незамедлительно растворяли в буфере для электрофореза образца и обрабатывали для разделения в 8% SDS электрофорезе в полиакриламидном геле (SDS-PAGE).
Результаты
Как показано на фиг. 10, в представительном иммуноблот-анализе добавление комбинации 1 мкМ ликопена или 1 мкМ Lyc-O-Mato с 1 мкМ лютеина и 2 мкМ карнозной кислоты к перитонеальным макрофагам на 1 ч перед добавлением ЛПС на 10 мин вызывало значимое синергическое ингибирование (приблизительно 80%) фосфорилирования p65-NFκB по серину 536 в клеточных ядерных лизатах, тогда как каждое питательное вещество по отдельности не оказывало действия вовсе. Интенсивность каждой полосы фосфорилированного p-65-NFκB делили на интенсивность каждой полосы ламина после количественного определения посредством денситометрии и выражали в произвольных единицах. Приведены средние значения ± стандартная ошибка среднего трех независимых экспериментов.
Как показано в иммуноблоте, фосфорилирование p65 NFκB по серину 276 отсутствовало.
Эти результаты демонстрируют, что тестируемая композиция каротиноида-полифенола вызывает значимое синергическое ингибирование активации NFκB, опосредованной фосфорилированием Ser-536, которое опосредовано чувствительным к окислению-восстановлению механизмом.
В аналогичных условиях добавление комбинаций питательных веществ (в концентрациях, подробно указанных выше) за 1 ч до добавления ЛПС на 24 ч вызывало значимое ингибирование экспрессии белков iNOS и ЦОГ-2 в цельноклеточных лизатах (фиг. 11). Каждое питательное вещество по отдельности не вызывало ингибирования индукции ни iNOS, ни ЦОГ-2.
Интенсивность каждой белковой полосы (iNOS или ЦОГ-2) делили на активность каждой полосы β-актина после количественного определения посредством денситометрии и выражали в произвольных единицах. Приведены средние значения ± стандартная ошибка среднего трех независимых экспериментов.
Эти результаты демонстрируют синергическое ингибирование индукции обоих воспалительных ферментов на уровне приблизительно 80% и приблизительно 60% для iNOS и ЦОГ-2 соответственно и обеспечивают поддержку для ингибирования как образования NO, так и высвобождения PGE2, о которых сообщалось выше в настоящем документе, а также молекулярное объяснение для этого.
Несмотря на то, что конкретные варианты осуществления изобретения описаны для иллюстративной цели, понятно, что специалисты могут осуществить изобретение на практике со многими модификациями, изменениями и адаптациями, не отступая от его сущности или не превышая объем формулы изобретения.
Claims (28)
1. Терапевтическая противовоспалительная композиция, которая содержит один или несколько полифенолов и два или более каротиноидов, которые выбирают из группы, состоящей из лютеина, ликопена и β-каротина, где полифенолы выбирают из группы, состоящей из карнозной кислоты, кверцетина, резвератрола и галловой кислоты, и
где суточное количество каждого из активных агентов находится в диапазоне 1-5 мг.
где суточное количество каждого из активных агентов находится в диапазоне 1-5 мг.
2. Терапевтическая композиция по п. 1, где полифенолом является карнозная кислота.
3. Терапевтическая композиция по п. 1, где полифенолом является кверцетин.
4. Терапевтическая композиция по п. 1, где полифенолом является резвератрол.
5. Терапевтическая композиция по п. 1, где полифенолом является галловая кислота.
6. Терапевтическая композиция по п. 1, которая по существу состоит из ликопена, лютеина и карнозной кислоты.
7. Терапевтическая композиция по п. 1, которая по существу состоит из лютеина, β-каротина и карнозной кислоты.
8. Терапевтическая композиция по п. 1, которая по существу состоит из ликопена, β-каротина и карнозной кислоты.
9. Терапевтическая композиция по любому из пп. 6-8, где указанная композиция дополнительно содержит фитоен.
10. Терапевтическая композиция по любому из пп. 6-8, где указанная композиция дополнительно содержит фитофлуен.
11. Терапевтическая композиция по любому из пп. 6-8, где указанная композиция дополнительно содержит фитоен и фитофлуен.
12. Способ ингибирования или снижения образования супероксид-ионов, NO, TNF-α и/или PGE2 у субъекта-млекопитающего, который содержит введение указанному субъекту терапевтической композиции по любому из пп. 1-11.
13. Способ лечения патологических состояний, в которых супероксид-ионы, NO, TNF-α и/или PGE2 выполняют функцию модулятора или медиатора указанного состояния, у субъекта-млекопитающего, нуждающегося в таком лечении, где указанный способ включает в себя введение указанному субъекту терапевтической композиции по любому из пп. 1-11.
14. Способ лечения по п. 13, где состоянием, подлежащим лечению, является воспалительное состояние.
15. Способ лечения по п. 13, где состояние, подлежащее лечению, выбирают из группы, состоящей из ревматоидного артрита, синдрома расстройства дыхания взрослых (СРДВ), астмы, ринита, идиопатического фиброза легких, перитонита, сердечно-сосудистого воспаления, ишемии миокарда, нарушения реперфузии, атеросклероза, сепсиса, травмы, диабета 2-го типа, ретинопатии, псориаза, желудочно-кишечного воспаления, цирроза, перитонита и воспалительного заболевания кишечника и нейродегенеративных заболеваний, включая болезнь Альцгеймера.
16. Способ по любому из пп. 12-15, где субъектом-млекопитающим является человеческий субъект.
17. Способ по любому из пп. 12-15, где терапевтическую композицию вводят в фармацевтической лекарственной форме.
18. Способ по любому из пп. 12-15, где терапевтическую композицию включают в продукт питания или напиток.
19. Применение комбинации одного или нескольких полифенолов и двух или более каротиноидов, которые выбирают из группы, состоящей из лютеина, ликопена и β-каротина, в производстве лекарственного средства для лечения состояний, чувствительных к ингибированию образования супероксид-ионов, NO, TNF-α и/или PGE2, где полифенолы выбирают из группы, состоящей из карнозной кислоты, кверцетина, резвератрола и галловой кислоты, и где суточное количество каждого из активных агентов находится в диапазоне 1-5 мг.
20. Применение по п. 19, где полифенолом является карнозная кислота.
21. Применение по п. 19, где полифенолом является кверцетин.
22. Применение по п. 19, где полифенолом является резвератрол.
23. Применение по п. 19, где полифенолом является галловая кислота.
24. Применение по п. 19, где состоянием является воспалительное состояние.
25. Применение по п. 19, где состояние, подлежащее лечению, выбирают из группы, состоящей из ревматоидного артрита, синдрома расстройства дыхания взрослых (СРДВ), астмы, ринита, идиопатического фиброза легких, перитонита, сердечно-сосудистого воспаления, ишемии миокарда, нарушения реперфузии, атеросклероза, сепсиса, травмы, диабета 2-го типа, ретинопатии, псориаза, желудочно-кишечного воспаления, цирроза, перитонита и воспалительного заболевания кишечника и нейродегенеративных заболеваний, включая болезнь Альцгеймера.
26. Применение по п. 19, где карнозную кислоту используют в сочетании с ликопеном и лютеином.
27. Применение по п. 19, где карнозную кислоту используют в сочетании с ликопеном и β-каротином.
28. Применение по п. 19, где карнозную кислоту используют в сочетании с лютеином и β-каротином.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US14559309P | 2009-01-19 | 2009-01-19 | |
| US61/145,593 | 2009-01-19 | ||
| US26651709P | 2009-12-04 | 2009-12-04 | |
| US61/266,517 | 2009-12-04 | ||
| PCT/IL2010/000045 WO2010082205A1 (en) | 2009-01-19 | 2010-01-19 | Synergistic combinations of carotenoids and polyphenols |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2011134652A RU2011134652A (ru) | 2013-02-27 |
| RU2563991C2 true RU2563991C2 (ru) | 2015-09-27 |
Family
ID=42339496
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2011134652/15A RU2563991C2 (ru) | 2009-01-19 | 2010-01-19 | Синергические комбинации каротиноидов и полифенолов |
Country Status (11)
| Country | Link |
|---|---|
| US (3) | US20120071550A1 (ru) |
| EP (2) | EP3085365A3 (ru) |
| JP (2) | JP5778584B2 (ru) |
| CN (2) | CN102355894B (ru) |
| AU (1) | AU2010205367B2 (ru) |
| BR (1) | BRPI1005154A2 (ru) |
| CA (1) | CA2749202C (ru) |
| ES (1) | ES2580173T3 (ru) |
| PL (1) | PL2381935T3 (ru) |
| RU (1) | RU2563991C2 (ru) |
| WO (1) | WO2010082205A1 (ru) |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL146496A0 (en) | 2001-11-14 | 2002-07-25 | Lycored Natural Prod Ind Ltd | Carotenoid composition and method for protecting skin |
| CA2749202C (en) * | 2009-01-19 | 2019-11-26 | Lycored Ltd. | The use of compositions comprising carnosic acid and two or more carotenoids in the treatment of inflammation |
| SG166688A1 (en) | 2009-05-14 | 2010-12-29 | Hsiehs Biotech Singapore Pte Ltd | Lycopene and resveratrol dietary supplement |
| US9107853B2 (en) | 2012-10-12 | 2015-08-18 | L'oreal S.A. | Compositions containing phenolic compounds and hydrotropes for cosmetic use |
| US9018177B2 (en) | 2012-10-12 | 2015-04-28 | L'oreal S.A. | Cosmetic compositions for increasing bioavailability of the active compounds baicalin and/or vitamin C |
| US9023826B2 (en) | 2012-10-12 | 2015-05-05 | L'oreal S.A. | Compositions containing adenosine and the hydrotropes caffeine and nicotinamide for cosmetic use |
| US9072919B2 (en) | 2012-10-12 | 2015-07-07 | L'oreal S.A. | Synergistic antioxidant cosmetic compositions containing at least one of baicalin and taxifolin, at least one of caffeine and nicotinamide, at least one of vitamin C and resveratrol and ferulic acid |
| WO2014082027A2 (en) | 2012-11-26 | 2014-05-30 | Access Business Group International Llc | Antioxidant dietary supplement and related method |
| CA2898284C (en) * | 2013-01-22 | 2023-03-28 | Lycored Ltd. | Compositions comprising heat-treated clear tomato concentrate |
| CN108245496B (zh) * | 2013-03-19 | 2021-07-16 | 乐康瑞德有限公司 | 虾青素抗炎增效组合 |
| US9901562B2 (en) | 2013-04-04 | 2018-02-27 | Lycored Ltd. | Anti-inflammatory omega-3 synergistic combinations |
| US9669242B2 (en) | 2013-07-01 | 2017-06-06 | L'oreal | Compositions containing at least two phenolic compounds, a lipid-soluble antioxidant and at least one hydrotrope for cosmetic use |
| CN104543983A (zh) * | 2013-10-15 | 2015-04-29 | 泰运生技有限公司 | 保健食品组合物 |
| CN104083345A (zh) * | 2014-06-13 | 2014-10-08 | 华中科技大学 | 番茄红素在制备防治老年痴呆药物中的应用 |
| AU2015351930B2 (en) * | 2014-11-25 | 2021-08-12 | Lycored Ltd. | Biologically-active tomato composition having reduced amount of lycopene |
| CN106998778A (zh) | 2014-11-25 | 2017-08-01 | 雅培制药有限公司 | 通过向婴儿施用包含RRR‑α‑生育酚和类胡萝卜素的组合物来改善视觉处理、视敏度或两者的方法 |
| KR101632839B1 (ko) * | 2015-07-10 | 2016-06-23 | 아주대학교산학협력단 | 레스베라트톨 유도체를 유효성분으로 포함하는 간경화 또는 간섬유화 예방 또는 치료용 약학 조성물 |
| EP3120842A1 (en) * | 2015-07-20 | 2017-01-25 | Opterion Health AG | Peritoneal therapeutic fluid |
| CN105476982A (zh) * | 2016-02-02 | 2016-04-13 | 张干 | 没食子酸的新用途 |
| CN105616439A (zh) * | 2016-03-11 | 2016-06-01 | 王巧玲 | 一种治疗酒精性心肌病的胶囊剂及其制备方法 |
| CA3097521C (en) | 2017-05-15 | 2023-10-17 | Axial Biotherapeutics, Inc. | Inhibitors of microbially induced amyloid |
| US20190070244A1 (en) * | 2017-06-30 | 2019-03-07 | The New Zealand Institute For Plant And Food Research Limited | Boysenberry compositions and methods of preparation and use thereof |
| TW202406562A (zh) | 2017-08-08 | 2024-02-16 | 奧德特M 蕭 | 波森莓、蘋果及黑醋栗組成物及其製備方法與用途 |
| WO2019087189A1 (en) * | 2017-11-01 | 2019-05-09 | Lycored Ltd. | A method for improving ocular blood flow |
| CN107823196A (zh) * | 2017-11-24 | 2018-03-23 | 广西医科大学 | 鼠尾草酸在制备治疗类风湿性关节炎药物方面的应用 |
| US11318136B2 (en) | 2018-04-13 | 2022-05-03 | Seung Hyun Yoo | Identification of granins as the pathogenic factor of alzheimer's disease and compositions and methods for inhibiting granin aggregation and treating alzheimer's disease |
| CA3136554A1 (en) * | 2018-04-19 | 2019-10-24 | Fff Bioworks Llp | Synergistic hepatoprotective composition |
| AU2019309497A1 (en) * | 2018-07-23 | 2021-03-11 | Lycored Ltd. | Lycopene compositions and methods for protecting skin against ultraviolet radiation |
| CN110200956B (zh) * | 2019-07-17 | 2021-07-27 | 吴广森 | 一种眼科外用药物组合物 |
| CN111588716A (zh) * | 2020-06-11 | 2020-08-28 | 中国医学科学院肿瘤医院 | 一种药物组合物及其在制备治疗前列腺炎产品应用 |
| JP7005043B2 (ja) * | 2020-07-08 | 2022-02-10 | 株式会社東洋新薬 | 網膜保護組成物 |
| WO2022128052A1 (en) | 2020-12-14 | 2022-06-23 | Symrise Ag | Medicament for fighting inflammatory conditions of human skin |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20060127505A1 (en) * | 2002-01-16 | 2006-06-15 | David Haines | Anti-inflammatory formulations |
| WO2007096886A2 (en) * | 2006-02-27 | 2007-08-30 | Lycored Ltd. | Composition and methods for treating and preventing age-related macular degeneration |
Family Cites Families (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE69033299T2 (de) * | 1990-10-06 | 2000-01-05 | Nestle Sa | Verwendung von Carnosolsäure wegen seiner anticarcinogenen und antiviralen Eigenschaften |
| US5837311A (en) | 1993-12-13 | 1998-11-17 | Makhteshim Chemical Works Ltd. | Industrial processing of tomatoes and product thereof |
| AU2001258237B8 (en) * | 2000-05-12 | 2006-02-09 | Bengt Krister Olson | Combined cartilage and plant extract compositions |
| WO2002047493A2 (en) * | 2000-12-16 | 2002-06-20 | Aventis Pharma Deutschland Gmbh | Health promoting compositions |
| IL141039A (en) * | 2001-01-23 | 2006-10-31 | Lycored Natural Prod Ind Ltd | The composition for the prevention of atherosclerosis containing carotenoids and use for the preparation of drugs to inhibit LDL oxidation |
| US20030008048A1 (en) * | 2001-06-08 | 2003-01-09 | David Winston | Methods and compositions for helping the body resist the effects of the aging process |
| IL146449A0 (en) * | 2001-11-12 | 2002-07-25 | Lycored Natural Prod Ind Ltd | Method and pharmaceutical preparations for reducing the activity of cells |
| EP1470817A4 (en) * | 2002-01-31 | 2006-03-22 | Kansai Tech Licensing Org Co | COMPOSITIONS FOR PREVENTING CANCER IN HUMANS AND METHOD FOR PREVENTING CANCER IN HUMANS |
| EP1476143A1 (en) * | 2002-02-15 | 2004-11-17 | DSM IP Assets B.V. | Compositions comprising lycopene for the treatment and prevention of angiogenesis associated pathologies |
| JP2004035550A (ja) * | 2002-05-07 | 2004-02-05 | Access Business Group Internatl Llc | 植物栄養素栄養サプリメント |
| US20040001817A1 (en) * | 2002-05-14 | 2004-01-01 | Giampapa Vincent C. | Anti-aging nutritional supplement |
| KR100739531B1 (ko) * | 2004-05-07 | 2007-07-13 | 주식회사 이오텍 | 리코펜과 피토에스트로겐을 포함하는 혼합 조성물 |
| US9579298B2 (en) * | 2004-12-02 | 2017-02-28 | Piotr Chomczynski | Antioxidant dietary supplement compositions and methods for maintaining healthy skin |
| US20070065396A1 (en) * | 2005-09-21 | 2007-03-22 | Tracie Martyn International, Llc | Topical macqui berry formulation |
| JP2009515821A (ja) * | 2005-10-16 | 2009-04-16 | リコレッド リミテッド | 眼疾患を治療するための組成物 |
| US20070141170A1 (en) * | 2005-12-20 | 2007-06-21 | Alcon Manufacturing, Ltd. | Composition and methods for inhibiting the progression macular degeneration and promoting healthy vision |
| SG10201700743PA (en) * | 2006-02-10 | 2017-03-30 | Mannatech Inc | All natural multivitamin and multimineral dietary supplement formulations for enhanced absorption and biological utilization |
| JP2007254427A (ja) * | 2006-03-24 | 2007-10-04 | Shimane Pref Gov | 抗酸化剤およびその用途 |
| US8841264B2 (en) * | 2006-07-14 | 2014-09-23 | Dsm Ip Assets B.V. | Compositions |
| IL184575A0 (en) * | 2007-07-12 | 2008-01-20 | Lycored Ltd | Synergistic combinations for treating hypertension |
| ITMI20080003A1 (it) * | 2008-01-02 | 2009-07-03 | Alfredo Pulpito | Composizioni per uso oftalmico |
| CA2749202C (en) * | 2009-01-19 | 2019-11-26 | Lycored Ltd. | The use of compositions comprising carnosic acid and two or more carotenoids in the treatment of inflammation |
-
2010
- 2010-01-19 CA CA2749202A patent/CA2749202C/en active Active
- 2010-01-19 JP JP2011545840A patent/JP5778584B2/ja not_active Expired - Fee Related
- 2010-01-19 PL PL10731120.1T patent/PL2381935T3/pl unknown
- 2010-01-19 EP EP16172113.9A patent/EP3085365A3/en not_active Withdrawn
- 2010-01-19 BR BRPI1005154A patent/BRPI1005154A2/pt not_active Application Discontinuation
- 2010-01-19 CN CN201080012356.7A patent/CN102355894B/zh active Active
- 2010-01-19 ES ES10731120.1T patent/ES2580173T3/es active Active
- 2010-01-19 WO PCT/IL2010/000045 patent/WO2010082205A1/en active Application Filing
- 2010-01-19 RU RU2011134652/15A patent/RU2563991C2/ru active
- 2010-01-19 AU AU2010205367A patent/AU2010205367B2/en active Active
- 2010-01-19 EP EP10731120.1A patent/EP2381935B1/en active Active
- 2010-01-19 CN CN201510486515.1A patent/CN105193777B/zh active Active
-
2011
- 2011-07-18 US US13/137,061 patent/US20120071550A1/en not_active Abandoned
-
2015
- 2015-05-12 JP JP2015097204A patent/JP2015205882A/ja active Pending
-
2016
- 2016-10-21 US US15/299,634 patent/US20170035713A1/en not_active Abandoned
-
2021
- 2021-11-23 US US17/533,637 patent/US20220079901A1/en active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20060127505A1 (en) * | 2002-01-16 | 2006-06-15 | David Haines | Anti-inflammatory formulations |
| WO2007096886A2 (en) * | 2006-02-27 | 2007-08-30 | Lycored Ltd. | Composition and methods for treating and preventing age-related macular degeneration |
Non-Patent Citations (1)
| Title |
|---|
| Майский В.В. Элементарная фармакология. М.: Фарма Диалог, 2009. С.363-377. * |
Also Published As
| Publication number | Publication date |
|---|---|
| PL2381935T3 (pl) | 2016-11-30 |
| JP2012515198A (ja) | 2012-07-05 |
| AU2010205367A1 (en) | 2011-08-11 |
| JP5778584B2 (ja) | 2015-09-16 |
| CN105193777A (zh) | 2015-12-30 |
| EP3085365A3 (en) | 2017-01-04 |
| EP3085365A2 (en) | 2016-10-26 |
| ES2580173T3 (es) | 2016-08-19 |
| JP2015205882A (ja) | 2015-11-19 |
| US20120071550A1 (en) | 2012-03-22 |
| CN105193777B (zh) | 2019-06-28 |
| BRPI1005154A2 (pt) | 2018-02-06 |
| EP2381935A1 (en) | 2011-11-02 |
| CA2749202A1 (en) | 2010-07-22 |
| CN102355894A (zh) | 2012-02-15 |
| EP2381935A4 (en) | 2013-03-13 |
| AU2010205367B2 (en) | 2015-06-18 |
| CN102355894B (zh) | 2016-06-15 |
| WO2010082205A1 (en) | 2010-07-22 |
| RU2011134652A (ru) | 2013-02-27 |
| EP2381935B1 (en) | 2016-06-01 |
| US20170035713A1 (en) | 2017-02-09 |
| CA2749202C (en) | 2019-11-26 |
| US20220079901A1 (en) | 2022-03-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2563991C2 (ru) | Синергические комбинации каротиноидов и полифенолов | |
| Zhao et al. | Black rice anthocyanin-rich extract and rosmarinic acid, alone and in combination, protect against DSS-induced colitis in mice | |
| JP6903594B2 (ja) | 食品、栄養補助食品、化粧品および医薬品に有用な複数の相乗的抗酸化活性を示すフィトコンプレックス | |
| KR20080109583A (ko) | 자가면역 질병을 치료하기 위한 안트로디아 캄포라타로부터얻은 시클로헥세논 화합물 | |
| Lee et al. | Medicinal effects of bromelain (Ananas comosus) targeting oral environment as an anti-oxidant and anti-inflammatory agent | |
| Zha et al. | A newly identified polyunsaturated macamide alleviates dextran sulfate sodium-induced colitis in mice | |
| Adeyi et al. | The anti-inflammatory effect of ferulic acid is via the modulation of NFκB-TNF-α-IL-6 and STAT1-PIAS1 signaling pathways in 2-methoxyethanol-induced testicular inflammation in rats | |
| JP6641180B2 (ja) | 熱処理した透明トマト濃縮物を含む組成物 | |
| TW201618802A (zh) | 用於調控pp2a甲基化反應並提供抗氧化及抗發炎活性之天然萃取物 | |
| US20210244786A1 (en) | Compositions and methods for nutritional supplements | |
| ES2678023T3 (es) | Factores extraídos de embriones de pez y uso de mezclas de los mismos en el control de la multiplicación y la diferenciación de células madre | |
| JP2007186431A (ja) | 抗酸化組成物及び脳神経細胞保護用医薬組成物、抗酸化剤及び脳神経細胞保護剤、並びにそれらの使用方法 | |
| KR20130046138A (ko) | 소회향 추출물을 포함하는 염증성 질환의 예방 또는 치료용 조성물 | |
| Landrier et al. | Tomatoes and lycopene: Inflammatory modulator effects | |
| Rajakumar | Psychoactive properties of microalgae | |
| EP4364730A1 (en) | Pharmaceutical composition comprising l-acetyl carnitine and beta-caryophyllene | |
| Rashid et al. | Kenyan purple tea anthocyanins ability to cross the blood brain barrier reinforcing brain antioxidant capacity in mice | |
| El-Khadragy et al. | Immunomodulatory effect of Eugenia caryophyllata against Vitamin D-induced Toxicity in Liver of Male Westar Rats | |
| Marina et al. | INFLUENCE OF AQUEOUS EXTRACT OF ANNONA SENEGALENSIS LEAVES ON SOME PARAMETERS OF INFLAMMATION ON RAT SPECIALLY THOSE OF ‘WISTAR’ORIGIN | |
| KR101171834B1 (ko) | 강활 추출물 또는 비사볼란겔론을 유효성분으로 함유하는 알레르기성 질환을 포함한 각 종 염증질환의 예방 및 치료용 약제학적 조성물 | |
| KR20170055792A (ko) | 해당화 꽃 추출물 또는 분획물을 유효성분으로 함유하는 염증 질환의 예방, 개선 또는 치료용 조성물 | |
| KR20160068055A (ko) | 페닐-β-D-글루코피라노사이드를 유효성분으로 함유하는 염증성 질환 예방 또는 치료용 조성물 |