RU2414239C2 - Белки, слитые с кошачьим аллергеном, и их применение - Google Patents
Белки, слитые с кошачьим аллергеном, и их применение Download PDFInfo
- Publication number
- RU2414239C2 RU2414239C2 RU2007138265/15A RU2007138265A RU2414239C2 RU 2414239 C2 RU2414239 C2 RU 2414239C2 RU 2007138265/15 A RU2007138265/15 A RU 2007138265/15A RU 2007138265 A RU2007138265 A RU 2007138265A RU 2414239 C2 RU2414239 C2 RU 2414239C2
- Authority
- RU
- Russia
- Prior art keywords
- seq
- chain
- protein
- composition according
- hpv
- Prior art date
Links
- 108090000623 proteins and genes Proteins 0.000 title claims abstract description 142
- 102000004169 proteins and genes Human genes 0.000 title claims abstract description 127
- 239000013566 allergen Substances 0.000 title abstract description 19
- 239000000203 mixture Substances 0.000 claims abstract description 105
- 239000000427 antigen Substances 0.000 claims abstract description 76
- 108091007433 antigens Proteins 0.000 claims abstract description 76
- 102000036639 antigens Human genes 0.000 claims abstract description 76
- 239000002245 particle Substances 0.000 claims abstract description 73
- 229960005486 vaccine Drugs 0.000 claims abstract description 43
- 241000282326 Felis catus Species 0.000 claims abstract description 39
- 206010020751 Hypersensitivity Diseases 0.000 claims abstract description 27
- 230000007815 allergy Effects 0.000 claims abstract description 24
- 208000026935 allergic disease Diseases 0.000 claims abstract description 12
- 235000018102 proteins Nutrition 0.000 claims description 125
- 238000000034 method Methods 0.000 claims description 52
- 102000037865 fusion proteins Human genes 0.000 claims description 44
- 108020001507 fusion proteins Proteins 0.000 claims description 44
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 41
- 125000003275 alpha amino acid group Chemical group 0.000 claims description 37
- 125000006850 spacer group Chemical group 0.000 claims description 32
- 239000002671 adjuvant Substances 0.000 claims description 30
- 239000007771 core particle Substances 0.000 claims description 24
- 238000002347 injection Methods 0.000 claims description 17
- 239000007924 injection Substances 0.000 claims description 17
- 125000003396 thiol group Chemical group [H]S* 0.000 claims description 17
- 241001515965 unidentified phage Species 0.000 claims description 17
- 125000003277 amino group Chemical group 0.000 claims description 16
- 125000000539 amino acid group Chemical group 0.000 claims description 14
- 241000124008 Mammalia Species 0.000 claims description 10
- 101710132601 Capsid protein Proteins 0.000 claims description 7
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 claims description 7
- 235000018417 cysteine Nutrition 0.000 claims description 7
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 claims description 7
- 239000008194 pharmaceutical composition Substances 0.000 claims description 6
- 239000004472 Lysine Substances 0.000 claims description 5
- 239000003937 drug carrier Substances 0.000 claims description 3
- 210000003462 vein Anatomy 0.000 claims 1
- 239000012634 fragment Substances 0.000 abstract description 66
- 239000000126 substance Substances 0.000 abstract description 33
- 230000003612 virological effect Effects 0.000 abstract description 22
- 238000011282 treatment Methods 0.000 abstract description 12
- 230000000694 effects Effects 0.000 abstract description 10
- 230000004044 response Effects 0.000 abstract description 9
- 239000003814 drug Substances 0.000 abstract description 5
- 230000002265 prevention Effects 0.000 abstract description 2
- 208000022361 Human papillomavirus infectious disease Diseases 0.000 description 148
- 230000008696 hypoxemic pulmonary vasoconstriction Effects 0.000 description 148
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 72
- 235000001014 amino acid Nutrition 0.000 description 50
- 229940024606 amino acid Drugs 0.000 description 49
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 45
- 101710091045 Envelope protein Proteins 0.000 description 42
- 101710188315 Protein X Proteins 0.000 description 42
- 102100021696 Syncytin-1 Human genes 0.000 description 42
- 150000001413 amino acids Chemical class 0.000 description 35
- 108020004707 nucleic acids Proteins 0.000 description 34
- 102000039446 nucleic acids Human genes 0.000 description 34
- 150000007523 nucleic acids Chemical class 0.000 description 34
- 230000003308 immunostimulating effect Effects 0.000 description 29
- 102000004196 processed proteins & peptides Human genes 0.000 description 29
- 210000000234 capsid Anatomy 0.000 description 27
- 241000700605 Viruses Species 0.000 description 24
- 230000000890 antigenic effect Effects 0.000 description 24
- 230000003993 interaction Effects 0.000 description 22
- 239000011780 sodium chloride Substances 0.000 description 22
- 229920002521 macromolecule Polymers 0.000 description 21
- 125000003588 lysine group Chemical group [H]N([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(N([H])[H])C(*)=O 0.000 description 20
- 229920001184 polypeptide Polymers 0.000 description 20
- 239000000872 buffer Substances 0.000 description 19
- 230000014509 gene expression Effects 0.000 description 18
- 239000003431 cross linking reagent Substances 0.000 description 17
- 208000015181 infectious disease Diseases 0.000 description 17
- 230000027455 binding Effects 0.000 description 16
- 238000006243 chemical reaction Methods 0.000 description 16
- 241000588724 Escherichia coli Species 0.000 description 15
- 239000000243 solution Substances 0.000 description 15
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 15
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 14
- 230000028993 immune response Effects 0.000 description 14
- 241000699670 Mus sp. Species 0.000 description 12
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 12
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 12
- 210000004027 cell Anatomy 0.000 description 12
- 230000002458 infectious effect Effects 0.000 description 12
- 230000003362 replicative effect Effects 0.000 description 12
- 238000012360 testing method Methods 0.000 description 12
- 210000002966 serum Anatomy 0.000 description 11
- 210000003491 skin Anatomy 0.000 description 11
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 10
- 208000024891 symptom Diseases 0.000 description 10
- 230000000172 allergic effect Effects 0.000 description 9
- 208000010668 atopic eczema Diseases 0.000 description 9
- 210000003651 basophil Anatomy 0.000 description 9
- 230000015572 biosynthetic process Effects 0.000 description 9
- 238000005119 centrifugation Methods 0.000 description 9
- 238000004519 manufacturing process Methods 0.000 description 9
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 8
- 238000002965 ELISA Methods 0.000 description 8
- VHJLVAABSRFDPM-QWWZWVQMSA-N dithiothreitol Chemical compound SC[C@@H](O)[C@H](O)CS VHJLVAABSRFDPM-QWWZWVQMSA-N 0.000 description 8
- RWSXRVCMGQZWBV-WDSKDSINSA-N glutathione Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O RWSXRVCMGQZWBV-WDSKDSINSA-N 0.000 description 8
- 230000028996 humoral immune response Effects 0.000 description 8
- 239000006228 supernatant Substances 0.000 description 8
- 206010001742 Allergy to animal Diseases 0.000 description 7
- 241000282324 Felis Species 0.000 description 7
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Natural products NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 7
- 238000000502 dialysis Methods 0.000 description 7
- 238000010790 dilution Methods 0.000 description 7
- 239000012895 dilution Substances 0.000 description 7
- 239000002773 nucleotide Substances 0.000 description 7
- 125000003729 nucleotide group Chemical group 0.000 description 7
- 239000012064 sodium phosphate buffer Substances 0.000 description 7
- 238000006467 substitution reaction Methods 0.000 description 7
- 241000709737 Enterobacteria phage GA Species 0.000 description 6
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 6
- 239000004471 Glycine Substances 0.000 description 6
- 229920001213 Polysorbate 20 Polymers 0.000 description 6
- 108091008874 T cell receptors Proteins 0.000 description 6
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 description 6
- 238000010521 absorption reaction Methods 0.000 description 6
- 229940037003 alum Drugs 0.000 description 6
- 210000004899 c-terminal region Anatomy 0.000 description 6
- 230000037430 deletion Effects 0.000 description 6
- 238000012217 deletion Methods 0.000 description 6
- 125000000524 functional group Chemical group 0.000 description 6
- 238000002523 gelfiltration Methods 0.000 description 6
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 6
- 230000003053 immunization Effects 0.000 description 6
- 238000001727 in vivo Methods 0.000 description 6
- 239000006166 lysate Substances 0.000 description 6
- -1 phospho ester Chemical class 0.000 description 6
- 229920002643 polyglutamic acid Polymers 0.000 description 6
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 6
- 238000000746 purification Methods 0.000 description 6
- 230000002829 reductive effect Effects 0.000 description 6
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 6
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 5
- 208000001840 Dandruff Diseases 0.000 description 5
- 102000002689 Toll-like receptor Human genes 0.000 description 5
- 108020000411 Toll-like receptor Proteins 0.000 description 5
- 125000000637 arginyl group Chemical group N[C@@H](CCCNC(N)=N)C(=O)* 0.000 description 5
- 239000004202 carbamide Substances 0.000 description 5
- 230000004927 fusion Effects 0.000 description 5
- 229910052739 hydrogen Inorganic materials 0.000 description 5
- 238000002649 immunization Methods 0.000 description 5
- 239000013612 plasmid Substances 0.000 description 5
- 238000002360 preparation method Methods 0.000 description 5
- 239000011541 reaction mixture Substances 0.000 description 5
- 241000701447 unidentified baculovirus Species 0.000 description 5
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 4
- LMDZBCPBFSXMTL-UHFFFAOYSA-N 1-ethyl-3-(3-dimethylaminopropyl)carbodiimide Chemical compound CCN=C=NCCCN(C)C LMDZBCPBFSXMTL-UHFFFAOYSA-N 0.000 description 4
- 102100025222 CD63 antigen Human genes 0.000 description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 4
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 4
- 241001534160 Escherichia virus Qbeta Species 0.000 description 4
- 108010053070 Glutathione Disulfide Proteins 0.000 description 4
- 241000282412 Homo Species 0.000 description 4
- 101000934368 Homo sapiens CD63 antigen Proteins 0.000 description 4
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 4
- 108091034117 Oligonucleotide Proteins 0.000 description 4
- 229920002684 Sepharose Polymers 0.000 description 4
- 230000005867 T cell response Effects 0.000 description 4
- 210000001744 T-lymphocyte Anatomy 0.000 description 4
- 108010067390 Viral Proteins Proteins 0.000 description 4
- FPIPGXGPPPQFEQ-OVSJKPMPSA-N all-trans-retinol Chemical compound OC\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-OVSJKPMPSA-N 0.000 description 4
- 230000002009 allergenic effect Effects 0.000 description 4
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 4
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 4
- 235000011130 ammonium sulphate Nutrition 0.000 description 4
- 230000001580 bacterial effect Effects 0.000 description 4
- 230000000903 blocking effect Effects 0.000 description 4
- 239000000284 extract Substances 0.000 description 4
- YPZRWBKMTBYPTK-BJDJZHNGSA-N glutathione disulfide Chemical compound OC(=O)[C@@H](N)CCC(=O)N[C@H](C(=O)NCC(O)=O)CSSC[C@@H](C(=O)NCC(O)=O)NC(=O)CC[C@H](N)C(O)=O YPZRWBKMTBYPTK-BJDJZHNGSA-N 0.000 description 4
- 230000002209 hydrophobic effect Effects 0.000 description 4
- 230000005847 immunogenicity Effects 0.000 description 4
- 238000000338 in vitro Methods 0.000 description 4
- 239000003446 ligand Substances 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 230000035772 mutation Effects 0.000 description 4
- 230000008520 organization Effects 0.000 description 4
- YBYRMVIVWMBXKQ-UHFFFAOYSA-N phenylmethanesulfonyl fluoride Chemical compound FS(=O)(=O)CC1=CC=CC=C1 YBYRMVIVWMBXKQ-UHFFFAOYSA-N 0.000 description 4
- 229930000044 secondary metabolite Natural products 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 241001672158 Acinetobacter phage AP205 Species 0.000 description 3
- 108090000565 Capsid Proteins Proteins 0.000 description 3
- 102100023321 Ceruloplasmin Human genes 0.000 description 3
- 241000709738 Enterobacteria phage fr Species 0.000 description 3
- 241000700721 Hepatitis B virus Species 0.000 description 3
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 3
- 108010020346 Polyglutamic Acid Proteins 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 101710132457 Protein A1 Proteins 0.000 description 3
- 229930006000 Sucrose Natural products 0.000 description 3
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 3
- 239000007983 Tris buffer Substances 0.000 description 3
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 3
- 229960004784 allergens Drugs 0.000 description 3
- 208000006673 asthma Diseases 0.000 description 3
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 238000010276 construction Methods 0.000 description 3
- 238000000586 desensitisation Methods 0.000 description 3
- 239000002158 endotoxin Substances 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 229960003180 glutathione Drugs 0.000 description 3
- 230000013595 glycosylation Effects 0.000 description 3
- 238000006206 glycosylation reaction Methods 0.000 description 3
- 238000004128 high performance liquid chromatography Methods 0.000 description 3
- 239000001257 hydrogen Substances 0.000 description 3
- 238000003780 insertion Methods 0.000 description 3
- 230000037431 insertion Effects 0.000 description 3
- 229920006008 lipopolysaccharide Polymers 0.000 description 3
- 239000012139 lysis buffer Substances 0.000 description 3
- 239000000178 monomer Substances 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 230000009257 reactivity Effects 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 210000003296 saliva Anatomy 0.000 description 3
- 239000000523 sample Substances 0.000 description 3
- 239000001488 sodium phosphate Substances 0.000 description 3
- 229910000162 sodium phosphate Inorganic materials 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 239000011550 stock solution Substances 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 239000005720 sucrose Substances 0.000 description 3
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 3
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 3
- 230000003827 upregulation Effects 0.000 description 3
- IOOMXPHYBWAZAQ-REOHCLBHSA-N (2r)-3-sulfanyl-2-(sulfanylamino)propanoic acid Chemical group OC(=O)[C@H](CS)NS IOOMXPHYBWAZAQ-REOHCLBHSA-N 0.000 description 2
- FPIPGXGPPPQFEQ-UHFFFAOYSA-N 13-cis retinol Natural products OCC=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-UHFFFAOYSA-N 0.000 description 2
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 2
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 2
- 229920000936 Agarose Polymers 0.000 description 2
- 206010002199 Anaphylactic shock Diseases 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- 108020004414 DNA Proteins 0.000 description 2
- 101000968532 Dictyocaulus viviparus DVA-1 polyprotein Proteins 0.000 description 2
- 108010024636 Glutathione Proteins 0.000 description 2
- 239000007995 HEPES buffer Substances 0.000 description 2
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 2
- 241000699666 Mus <mouse, genus> Species 0.000 description 2
- NQTADLQHYWFPDB-UHFFFAOYSA-N N-Hydroxysuccinimide Chemical compound ON1C(=O)CCC1=O NQTADLQHYWFPDB-UHFFFAOYSA-N 0.000 description 2
- 108091028043 Nucleic acid sequence Proteins 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 206010037660 Pyrexia Diseases 0.000 description 2
- 206010070834 Sensitisation Diseases 0.000 description 2
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 2
- 206010040914 Skin reaction Diseases 0.000 description 2
- 108010090804 Streptavidin Proteins 0.000 description 2
- PZBFGYYEXUXCOF-UHFFFAOYSA-N TCEP Chemical compound OC(=O)CCP(CCC(O)=O)CCC(O)=O PZBFGYYEXUXCOF-UHFFFAOYSA-N 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 238000005273 aeration Methods 0.000 description 2
- 229940074608 allergen extract Drugs 0.000 description 2
- 208000030961 allergic reaction Diseases 0.000 description 2
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 2
- 150000001408 amides Chemical class 0.000 description 2
- 208000003455 anaphylaxis Diseases 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 229960002685 biotin Drugs 0.000 description 2
- 235000020958 biotin Nutrition 0.000 description 2
- 239000011616 biotin Substances 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- AIYUHDOJVYHVIT-UHFFFAOYSA-M caesium chloride Chemical compound [Cl-].[Cs+] AIYUHDOJVYHVIT-UHFFFAOYSA-M 0.000 description 2
- 238000005277 cation exchange chromatography Methods 0.000 description 2
- 238000010382 chemical cross-linking Methods 0.000 description 2
- 239000003638 chemical reducing agent Substances 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- 238000004140 cleaning Methods 0.000 description 2
- 238000010367 cloning Methods 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 125000000753 cycloalkyl group Chemical group 0.000 description 2
- 238000001212 derivatisation Methods 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 230000008030 elimination Effects 0.000 description 2
- 238000003379 elimination reaction Methods 0.000 description 2
- 238000010828 elution Methods 0.000 description 2
- 239000012149 elution buffer Substances 0.000 description 2
- 238000000684 flow cytometry Methods 0.000 description 2
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 2
- 229960002143 fluorescein Drugs 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 208000002672 hepatitis B Diseases 0.000 description 2
- 125000001072 heteroaryl group Chemical group 0.000 description 2
- 210000003630 histaminocyte Anatomy 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- 210000000987 immune system Anatomy 0.000 description 2
- 230000002163 immunogen Effects 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- PGLTVOMIXTUURA-UHFFFAOYSA-N iodoacetamide Chemical compound NC(=O)CI PGLTVOMIXTUURA-UHFFFAOYSA-N 0.000 description 2
- BPHPUYQFMNQIOC-NXRLNHOXSA-N isopropyl beta-D-thiogalactopyranoside Chemical compound CC(C)S[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O BPHPUYQFMNQIOC-NXRLNHOXSA-N 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 229910021645 metal ion Inorganic materials 0.000 description 2
- 230000000877 morphologic effect Effects 0.000 description 2
- 239000012452 mother liquor Substances 0.000 description 2
- 238000002703 mutagenesis Methods 0.000 description 2
- 231100000350 mutagenesis Toxicity 0.000 description 2
- 229920005615 natural polymer Polymers 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- YPZRWBKMTBYPTK-UHFFFAOYSA-N oxidized gamma-L-glutamyl-L-cysteinylglycine Natural products OC(=O)C(N)CCC(=O)NC(C(=O)NCC(O)=O)CSSCC(C(=O)NCC(O)=O)NC(=O)CCC(N)C(O)=O YPZRWBKMTBYPTK-UHFFFAOYSA-N 0.000 description 2
- 230000036961 partial effect Effects 0.000 description 2
- 108091033319 polynucleotide Proteins 0.000 description 2
- 102000040430 polynucleotide Human genes 0.000 description 2
- 239000002157 polynucleotide Substances 0.000 description 2
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 2
- 230000004481 post-translational protein modification Effects 0.000 description 2
- 238000001556 precipitation Methods 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 230000009465 prokaryotic expression Effects 0.000 description 2
- 230000010076 replication Effects 0.000 description 2
- 229960003471 retinol Drugs 0.000 description 2
- 235000020944 retinol Nutrition 0.000 description 2
- 239000011607 retinol Substances 0.000 description 2
- 230000002441 reversible effect Effects 0.000 description 2
- 230000008313 sensitization Effects 0.000 description 2
- 230000035483 skin reaction Effects 0.000 description 2
- 231100000430 skin reaction Toxicity 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 239000000021 stimulant Substances 0.000 description 2
- 230000000638 stimulation Effects 0.000 description 2
- 239000012089 stop solution Substances 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 229920001059 synthetic polymer Polymers 0.000 description 2
- 230000001225 therapeutic effect Effects 0.000 description 2
- 238000005199 ultracentrifugation Methods 0.000 description 2
- 238000009281 ultraviolet germicidal irradiation Methods 0.000 description 2
- 238000000870 ultraviolet spectroscopy Methods 0.000 description 2
- 238000002255 vaccination Methods 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- JWDFQMWEFLOOED-UHFFFAOYSA-N (2,5-dioxopyrrolidin-1-yl) 3-(pyridin-2-yldisulfanyl)propanoate Chemical compound O=C1CCC(=O)N1OC(=O)CCSSC1=CC=CC=N1 JWDFQMWEFLOOED-UHFFFAOYSA-N 0.000 description 1
- ASWBNKHCZGQVJV-UHFFFAOYSA-N (3-hexadecanoyloxy-2-hydroxypropyl) 2-(trimethylazaniumyl)ethyl phosphate Chemical compound CCCCCCCCCCCCCCCC(=O)OCC(O)COP([O-])(=O)OCC[N+](C)(C)C ASWBNKHCZGQVJV-UHFFFAOYSA-N 0.000 description 1
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 1
- DIYPCWKHSODVAP-UHFFFAOYSA-N 1-[3-(2,5-dioxopyrrol-1-yl)benzoyl]oxy-2,5-dioxopyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)C1=CC=CC(N2C(C=CC2=O)=O)=C1 DIYPCWKHSODVAP-UHFFFAOYSA-N 0.000 description 1
- UFBJCMHMOXMLKC-UHFFFAOYSA-N 2,4-dinitrophenol Chemical compound OC1=CC=C([N+]([O-])=O)C=C1[N+]([O-])=O UFBJCMHMOXMLKC-UHFFFAOYSA-N 0.000 description 1
- ASNTZYQMIUCEBV-UHFFFAOYSA-N 2,5-dioxo-1-[6-[3-(pyridin-2-yldisulfanyl)propanoylamino]hexanoyloxy]pyrrolidine-3-sulfonic acid Chemical compound O=C1C(S(=O)(=O)O)CC(=O)N1OC(=O)CCCCCNC(=O)CCSSC1=CC=CC=N1 ASNTZYQMIUCEBV-UHFFFAOYSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- RHKWIGHJGOEUSM-UHFFFAOYSA-N 3h-imidazo[4,5-h]quinoline Chemical class C1=CN=C2C(N=CN3)=C3C=CC2=C1 RHKWIGHJGOEUSM-UHFFFAOYSA-N 0.000 description 1
- 206010067484 Adverse reaction Diseases 0.000 description 1
- 241000710929 Alphavirus Species 0.000 description 1
- ATRRKUHOCOJYRX-UHFFFAOYSA-N Ammonium bicarbonate Chemical compound [NH4+].OC([O-])=O ATRRKUHOCOJYRX-UHFFFAOYSA-N 0.000 description 1
- 229910000013 Ammonium bicarbonate Inorganic materials 0.000 description 1
- 241000193830 Bacillus <bacterium> Species 0.000 description 1
- 238000009010 Bradford assay Methods 0.000 description 1
- 101100494773 Caenorhabditis elegans ctl-2 gene Proteins 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 206010010741 Conjunctivitis Diseases 0.000 description 1
- 241000186216 Corynebacterium Species 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- 238000008157 ELISA kit Methods 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 241001261579 Enterobacteria phage M11 Species 0.000 description 1
- 241001278075 Enterobacteria phage MX1 Species 0.000 description 1
- 241001278054 Enterobacteria phage NL95 Species 0.000 description 1
- 241000709747 Enterobacteria phage R17 Species 0.000 description 1
- 241000709743 Enterobacteria phage SP Species 0.000 description 1
- 241000709739 Enterobacteria phage f2 Species 0.000 description 1
- 241000709744 Enterobacterio phage MS2 Species 0.000 description 1
- 101100112369 Fasciola hepatica Cat-1 gene Proteins 0.000 description 1
- 108010040721 Flagellin Proteins 0.000 description 1
- 241000723754 Flock house virus Species 0.000 description 1
- 241000710198 Foot-and-mouth disease virus Species 0.000 description 1
- 101710177291 Gag polyprotein Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- SXRSQZLOMIGNAQ-UHFFFAOYSA-N Glutaraldehyde Chemical compound O=CCCCC=O SXRSQZLOMIGNAQ-UHFFFAOYSA-N 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 241000701806 Human papillomavirus Species 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 101710125418 Major capsid protein Proteins 0.000 description 1
- 201000005505 Measles Diseases 0.000 description 1
- 241000712079 Measles morbillivirus Species 0.000 description 1
- 102000018697 Membrane Proteins Human genes 0.000 description 1
- 108010052285 Membrane Proteins Proteins 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 102000016943 Muramidase Human genes 0.000 description 1
- 108010014251 Muramidase Proteins 0.000 description 1
- 101100010166 Mus musculus Dok3 gene Proteins 0.000 description 1
- 241001148639 Mycoplasma haemofelis Species 0.000 description 1
- 108010062010 N-Acetylmuramoyl-L-alanine Amidase Proteins 0.000 description 1
- 101100005271 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) cat-1 gene Proteins 0.000 description 1
- 101100386053 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) cys-3 gene Proteins 0.000 description 1
- 241000714209 Norwalk virus Species 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 238000012408 PCR amplification Methods 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 229920002230 Pectic acid Polymers 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- 229920000805 Polyaspartic acid Polymers 0.000 description 1
- 241001505332 Polyomavirus sp. Species 0.000 description 1
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 1
- 241000709749 Pseudomonas phage PP7 Species 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 241000702670 Rotavirus Species 0.000 description 1
- 108700031620 S-acetylthiorphan Proteins 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 235000014680 Saccharomyces cerevisiae Nutrition 0.000 description 1
- 101100421708 Schistosoma mansoni SM20 gene Proteins 0.000 description 1
- 241000710960 Sindbis virus Species 0.000 description 1
- 239000012505 Superdex™ Substances 0.000 description 1
- 108700005078 Synthetic Genes Proteins 0.000 description 1
- 230000024932 T cell mediated immunity Effects 0.000 description 1
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 1
- 239000004473 Threonine Substances 0.000 description 1
- 241000723873 Tobacco mosaic virus Species 0.000 description 1
- YYQRGCZGSFRBAM-UHFFFAOYSA-N Triclofos Chemical compound OP(O)(=O)OCC(Cl)(Cl)Cl YYQRGCZGSFRBAM-UHFFFAOYSA-N 0.000 description 1
- 241000209140 Triticum Species 0.000 description 1
- 235000021307 Triticum Nutrition 0.000 description 1
- JXBAVRIYDKLCOE-UHFFFAOYSA-N [C].[P] Chemical compound [C].[P] JXBAVRIYDKLCOE-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 238000007792 addition Methods 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N adenyl group Chemical class N1=CN=C2N=CNC2=C1N GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 230000006838 adverse reaction Effects 0.000 description 1
- 238000001042 affinity chromatography Methods 0.000 description 1
- 235000004279 alanine Nutrition 0.000 description 1
- 238000012867 alanine scanning Methods 0.000 description 1
- 208000037884 allergic airway inflammation Diseases 0.000 description 1
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical class [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 1
- 230000009435 amidation Effects 0.000 description 1
- 238000007112 amidation reaction Methods 0.000 description 1
- 235000012538 ammonium bicarbonate Nutrition 0.000 description 1
- 239000001099 ammonium carbonate Substances 0.000 description 1
- 230000002052 anaphylactic effect Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- 229960005261 aspartic acid Drugs 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 238000009395 breeding Methods 0.000 description 1
- 230000001488 breeding effect Effects 0.000 description 1
- 229940041514 candida albicans extract Drugs 0.000 description 1
- 150000001718 carbodiimides Chemical class 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 239000011545 carbonate/bicarbonate buffer Substances 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000005018 casein Substances 0.000 description 1
- BECPQYXYKAMYBN-UHFFFAOYSA-N casein, tech. Chemical compound NCCCCC(C(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(CC(C)C)N=C(O)C(CCC(O)=O)N=C(O)C(CC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(C(C)O)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=N)N=C(O)C(CCC(O)=O)N=C(O)C(CCC(O)=O)N=C(O)C(COP(O)(O)=O)N=C(O)C(CCC(O)=N)N=C(O)C(N)CC1=CC=CC=C1 BECPQYXYKAMYBN-UHFFFAOYSA-N 0.000 description 1
- 235000021240 caseins Nutrition 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 238000005341 cation exchange Methods 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 238000011097 chromatography purification Methods 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 238000010835 comparative analysis Methods 0.000 description 1
- 238000004590 computer program Methods 0.000 description 1
- 239000000356 contaminant Substances 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 239000013256 coordination polymer Substances 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 230000009260 cross reactivity Effects 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 125000000392 cycloalkenyl group Chemical group 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000000779 depleting effect Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 229960000633 dextran sulfate Drugs 0.000 description 1
- 238000011026 diafiltration Methods 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 239000013024 dilution buffer Substances 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- 230000008034 disappearance Effects 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 125000002228 disulfide group Chemical group 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000000428 dust Substances 0.000 description 1
- 238000001962 electrophoresis Methods 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 238000011067 equilibration Methods 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 125000003630 glycyl group Chemical group [H]N([H])C([H])([H])C(*)=O 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- ZRALSGWEFCBTJO-UHFFFAOYSA-O guanidinium Chemical compound NC(N)=[NH2+] ZRALSGWEFCBTJO-UHFFFAOYSA-O 0.000 description 1
- 108060003552 hemocyanin Proteins 0.000 description 1
- 244000144980 herd Species 0.000 description 1
- 239000000833 heterodimer Substances 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- 239000000710 homodimer Substances 0.000 description 1
- 239000002955 immunomodulating agent Substances 0.000 description 1
- 230000002584 immunomodulator Effects 0.000 description 1
- 229940121354 immunomodulator Drugs 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 239000002198 insoluble material Substances 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 238000005304 joining Methods 0.000 description 1
- 210000004561 lacrimal apparatus Anatomy 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 229960000274 lysozyme Drugs 0.000 description 1
- 239000004325 lysozyme Substances 0.000 description 1
- 235000010335 lysozyme Nutrition 0.000 description 1
- 229910001629 magnesium chloride Inorganic materials 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 229940126601 medicinal product Drugs 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 108020004999 messenger RNA Proteins 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 210000004877 mucosa Anatomy 0.000 description 1
- BSOQXXWZTUDTEL-ZUYCGGNHSA-N muramyl dipeptide Chemical class OC(=O)CC[C@H](C(N)=O)NC(=O)[C@H](C)NC(=O)[C@@H](C)O[C@H]1[C@H](O)[C@@H](CO)O[C@@H](O)[C@@H]1NC(C)=O BSOQXXWZTUDTEL-ZUYCGGNHSA-N 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 230000009871 nonspecific binding Effects 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 229940046166 oligodeoxynucleotide Drugs 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 150000002895 organic esters Chemical class 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 238000012856 packing Methods 0.000 description 1
- 230000037368 penetrate the skin Effects 0.000 description 1
- 230000000149 penetrating effect Effects 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 238000000053 physical method Methods 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 239000000902 placebo Substances 0.000 description 1
- 229940068196 placebo Drugs 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 229920001983 poloxamer Polymers 0.000 description 1
- 229920000447 polyanionic polymer Polymers 0.000 description 1
- 108010064470 polyaspartate Proteins 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 239000010318 polygalacturonic acid Substances 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 125000001500 prolyl group Chemical group [H]N1C([H])(C(=O)[*])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 1
- 125000006239 protecting group Chemical group 0.000 description 1
- 230000005180 public health Effects 0.000 description 1
- 238000003259 recombinant expression Methods 0.000 description 1
- 230000003252 repetitive effect Effects 0.000 description 1
- 108091008146 restriction endonucleases Proteins 0.000 description 1
- 206010039083 rhinitis Diseases 0.000 description 1
- 210000003705 ribosome Anatomy 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 238000003118 sandwich ELISA Methods 0.000 description 1
- 238000013391 scatchard analysis Methods 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 238000004062 sedimentation Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- 238000004904 shortening Methods 0.000 description 1
- ULARYIUTHAWJMU-UHFFFAOYSA-M sodium;1-[4-(2,5-dioxopyrrol-1-yl)butanoyloxy]-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCCN1C(=O)C=CC1=O ULARYIUTHAWJMU-UHFFFAOYSA-M 0.000 description 1
- VUFNRPJNRFOTGK-UHFFFAOYSA-M sodium;1-[4-[(2,5-dioxopyrrol-1-yl)methyl]cyclohexanecarbonyl]oxy-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)C1CCC(CN2C(C=CC2=O)=O)CC1 VUFNRPJNRFOTGK-UHFFFAOYSA-M 0.000 description 1
- MIDXXTLMKGZDPV-UHFFFAOYSA-M sodium;1-[6-(2,5-dioxopyrrol-1-yl)hexanoyloxy]-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)CCCCCN1C(=O)C=CC1=O MIDXXTLMKGZDPV-UHFFFAOYSA-M 0.000 description 1
- 238000000527 sonication Methods 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- FRGKKTITADJNOE-UHFFFAOYSA-N sulfanyloxyethane Chemical compound CCOS FRGKKTITADJNOE-UHFFFAOYSA-N 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 230000008961 swelling Effects 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- CNHYKKNIIGEXAY-UHFFFAOYSA-N thiolan-2-imine Chemical compound N=C1CCCS1 CNHYKKNIIGEXAY-UHFFFAOYSA-N 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 229960001147 triclofos Drugs 0.000 description 1
- 239000012137 tryptone Substances 0.000 description 1
- 241001430294 unidentified retrovirus Species 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 239000012138 yeast extract Substances 0.000 description 1
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/35—Allergens
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6901—Conjugates being cells, cell fragments, viruses, ghosts, red blood cells or viral vectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/525—Virus
- A61K2039/5258—Virus-like particles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55505—Inorganic adjuvants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
Abstract
Изобретение относится к области медицины и касается белков, слитых с кошачьим аллергеном и их применения. Сущность изобретения включает композиции, содержащие вирусоподобную частицу (ВПЧ) или вирусную частицу и по меньшей мере один антиген, прежде всего по меньшей мере, один кошачий антиген, и более конкретно по меньшей мере один кошачий антиген, который является человеческим аллергеном. В конкретных вариантах осуществления изобретения антиген представляет собой кошачий антиген Fe1 d1 или его фрагмент, ковалентно связанный с ВПЧ. Изобретение можно применять для получения вакцин, предназначенных прежде всего для лечения и/или предупреждения аллергии на кошачью перхоть и другие кошачьи антигены и аллергены. 5 н. и 20 з.п. ф-лы, 5 табл., 4 ил.
Description
Предпосылки создания изобретения
Область техники, к которой относится изобретение
Настоящее изобретение относится к областям медицины, общественного здравоохранения, иммунологии, молекулярной биологии и вирусологии. В изобретении предложены композиции, содержащие вирусоподобную частицу (ВПЧ) или вирусную частицу и по меньшей мере один антиген, прежде всего по меньшей мере один кошачий антиген, и наиболее конкретно по меньшей мере один кошачий антиген, который является человеческим аллергеном. В конкретных вариантах осуществления изобретения антиген представляет собой антиген Fe1 d1 или его фрагмент, ковалентно связанный с ВПЧ. В изобретении предложены также способы получения композиций. Композиции, предлагаемые в изобретении, индуцируют эффективные иммунные ответы, прежде всего гуморальные иммунные ответы, у млекопитающих, прежде всего у человека. Композиции и способы, предлагаемые в изобретении, можно применять для получения вакцин, предназначенных прежде всего для лечения и/или профилактики аллергии на кошачью перхоть и другие кошачьи антигены и аллергены.
Ссылка на родственные заявки
Домашняя кошка (Felis domesticus) является важным источником аллергенов в помещениях (Lau S. и др., Lancet 356, 2000, cc.1392-1397). Так, кошек содержат примерно в 25% домов в западных странах, и аллергия на кошек обнаружена у значительной части популяции. Серьезность симптомов колеблется от относительно слабого ринита и конъюнктивита до потенциально опасного для жизни обострения астмы.
Хотя в некоторых случаях у пациентов наблюдается сенсибилизация некоторыми другими молекулами кошачьей перхоти и шкуры, основным аллергеном является Fe1 d1 (т.е. аллерген 1 Felis domesticus; ранее обозначали как Cat 1, т.е. кошачий аллерген 1). Важность этого аллергена доказана в многочисленных исследованиях. Фактически более чем у 80% пациентов, страдающих аллергией на кошек, вырабатываются антитела типа IgE на этот сильный аллерген (van Ree R. и др., J. Allergy Clin Immunol 104, 1999, cc.1223-1230).
Fe1 d1 представляет собой кислый гликопротеин с молекулярной массой 35-39 кДа, содержащий 10-20% N-связанных углеводов, и он обнаружен в шкуре, слюне и слезных железах кошек. Он состоит из двух нековалентно связанных гетеродимеров. Каждый гетеродимер состоит из одного пептида, содержащего 70 остатков (обозначен как «цепь 1»), и одного пептида, содержащего 78, 85, 90 или 92 остатка (обозначен как «цепь 2»), которые кодируются различными генами (см. Duffort О.А. и др., Mol Immunol 28, 1991, cc.301-309; Morgenstern J.P. и др., Proc Natl Acad Sci USA 88, 1991, cc.9690-9694 и Griffith I.J. и др., Gene 113, 1992, cc.263-268).
Лечение пациентов, страдающих аллергией на кошек, в настоящее время осуществляют посредством десенсибилизирующей терапии, которая включает повторные инъекции возрастающими дозами либо неочищенного экстракта кошачьей перхоти, либо коротких пептидов, полученных из Fe1 d1. У Lilja с соавторами и Hedlin с соавторами описана программа десенсибилизации, в процессе которой страдающим аллергией на кошек пациентам вводят неочищенные экстракты кошачьей перхоти (Lilja Q и др., J Allergy Clin Immunol 83, 1989, cc.37-44 и Hedlin и др., J Allergy Clin Immunol 87, 1991, cc.955-964). Для осуществления этой программы требуется по меньшей мере 2-3 года, и пациенты после трехлетнего лечения все еще сохраняют системные симптомы. Применение для десенсибилизации коротких пептидов, полученных из Fe1 d1, приводит к несущественным различиям между группой, обработанной пептидов, и группой, обработанной плацебо (Oldfield W.L. и др., Lancet 360, 2002, cc.47-53). Эффективность была обнаружена только тогда, когда пациентам вводили короткий пептид в большом количестве (750 мкг) (Norman P.S. и др., Am J Respir Crit Care Med 154, 1996, cc.1623-1628).
Связанные с аллергией побочные действия, такие как астматические реакции замедленного типа, обнаружены как при лечении неочищенным экстрактом кошачьей перхоти, так и при лечении короткими пептидами. Таким образом, анафилактический шок, вызываемый инъецируемым аллергеном, имеет очень большое значение для безопасности любой программы десенсибилизации. Однако устранение этого явления посредством снижения количества инъецируемого аллергена либо снижает эффективность лечения, либо удлиняет период лечения. Таким образом, в области лечения аллергии на кошек существует большая потребность в альтернативных режимах десенсибилизации и, прежде всего, в режимах десенсибилизации, которые позволяют снижать аллергические симптомы, но не стимулируют связанную с аллергией побочную реакцию.
Краткое изложение сущности изобретения
При создании изобретения неожиданно было установлено, что предлагаемые в изобретении композиции и вакцины соответственно, которые содержат по меньшей мере один антиген Fe1 d1 или его фрагмент, предлагаемый в изобретении, не только не обладают способностью индуцировать иммунные ответы на Fe1 d1 и прежде всего гуморальные иммунные ответы, но также могут оказывать десенсибилизирующее действие на пациента, страдающего аллергией на кошек, и, в частности, при кратковременном использовании, выявлена высокая эффективность предлагаемых в изобретении композиций и вакцин соответственно. Кроме того, при создании изобретения неожиданно было установлено, что Fe1 d1, предлагаемый в изобретении, когда его ковалентно связывают с ВПЧ, предлагаемой в изобретении, обладает резко пониженной анафилактической активностью по сравнению с Fe1 d1, предлагаемым в изобретении, не связанным ковалентно с ВПЧ, сохраняя при этом высокую степень антигенности и иммуногенности. Это является важным преимуществом по сравнению с известными из прототипов схемами лечения аллергии на кошек, поскольку предлагаемые в изобретении композиции и вакцины соответственно резко снижают риск возникновения анафилактического шока у иммунизированных животных и людей. Кроме того, предлагаемые в изобретении композиции и вакцины соответственно позволяют применять антиген в существенно более высоких дозах по сравнению с дозами, которые применяли в известных из прототипов схемах лечения аллергии на кошек, что, в свою очередь, может повышать эффективность и/или укорачивать всю программу десенсибилизации. Таким образом, предлагаемые в изобретении композиции и вакцины соответственно индуцируют сильные иммунные ответы против Fe1 d1, но не стимулируют аллергическую реакцию.
Таким образом, первым объектом настоящего изобретения является композиция, содержащая (а) коровую частицу, которая несет по меньшей мере один первый сайт присоединения, где коровая частица представляет собой вирусоподобную частицу (ВПЧ) или вирусную частицу; и (б) по меньшей мере один антиген, который несет по меньшей мере один второй сайт присоединения, где по меньшей мере один антиген представляет собой белок Fe1 d1 или фрагмент Fe1 d1, и где (а) и (б) ковалентно связаны через по меньшей мере один первый и по меньшей мере один второй сайт присоединения, предпочтительно с образованием упорядоченного и повторяющегося набора антигенов. Другим объектом настоящего изобретения является композиция вакцины. Кроме того, настоящее изобретение относится к способу введения композиции вакцины человеку или млекопитающему кроме человека, такому как собака, которые страдают аллергией на кошек, предпочтительно на кошачий Fe1 d1. В одном из предпочтительных вариантов осуществления изобретения в состав вакцины входит также по меньшей мере один адъювант. Однако композиция вакцины, предлагаемая в изобретении, обладает способностью индуцировать сильный иммунный ответ, прежде всего гуморальный иммунный ответ, и при отсутствии по меньшей мере одного адъюванта. Таким образом, в одном из предпочтительных вариантов осуществления изобретения в вакцине отсутствует адъювант. Отказ от применения адъюванта может снижать вероятность возникновения возможных побочных действий, связанных с применением адъювантов.
В одном из предпочтительных вариантов осуществления изобретения ВПЧ, входящую в состав композиции и композиции вакцины соответственно, получают рекомбинантно в хозяине, и ВПЧ практически свободна от РНК хозяина, предпочтительно свободна от нуклеиновых кислот хозяина. Снижение или предпочтительно элиминация нуклеиновых кислот хозяина, предпочтительно отсутствие нуклеиновых кислот хозяина, является важным устранения нежелательных Т-клеточных ответов, а также других нежелательных побочных действий, таких как лихорадка.
В одном из предпочтительных вариантов осуществления изобретения композиция, предлагаемая в изобретении, содержит также по меньшей мере одну иммуностимулирующую субстанцию, предпочтительно по меньшей мере одну иммуностимулирующую нуклеиновую кислоту. Еще в одном предпочтительном варианте осуществления изобретения иммуностимулирующую нуклеиновую кислоту упаковывают внутрь ВПЧ, предлагаемой в изобретении. Введение иммуностимулирующих субстанций, предпочтительно иммуностимулирующих нуклеиновых кислот, в композицию, предлагаемую в изобретении, может сдвигать иммунные ответы в сторону Th1-ответов и тем самым подавлять Th2-ответы и, как следствие, производство IgE.
Одним из объектов настоящего изобретения является способ лечения аллергии на кошек, заключающийся в том, что индивидууму, который страдает аллергией на кошек, предпочтительно человеку, вводят предлагаемую в изобретении композицию или вакцину соответственно.
Следующим объектом настоящего изобретения является фармацевтическая композиция, содержащая композицию, предлагаемую в изобретении, и приемлемый фармацевтический носитель.
И еще одним объектом настоящего изобретения является способ получения предлагаемой в изобретении композиции, заключающийся в том, что (а) получают коровую частицу, которая несет по меньшей мере один первый сайт присоединения, где коровая частица представляет собой вирусоподобную частицу (ВПЧ) или вирусную частицу; и (б) получают по меньшей мере один антиген, который несет по меньшей мере один второй сайт присоединения, где по меньшей мере один антиген представляет собой белок Fe1 d1 или фрагмент Fe1 d1, и (в) объединяют коровую частицу и по меньшей мере один антиген с получением композиции, где по меньшей мере один антиген и коровая частица связаны с помощью по меньшей мере одного первого и по меньшей мере одного второго сайтов присоединения.
Один из объектов изобретения является слитый белок Fe1 d1, который содержит цепь 1 Fe1 d1 и цепь 2 Fe1 d1, слитые через аминокислотный спейсер, который связывает N-конец одной цепи с С-концом другой цепи, где аминокислотный спейсер состоит из 10-30 аминокислотных остатков и где слитый белок получают в Е.coli или где слитый белок не является гликозилированным.
Краткое описание чертежей
На чертежах показано:
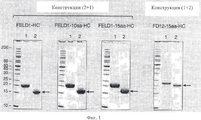
на фиг.1 - окрашенные кумасси очищенные и ренатурированные слитые белки Fe1 d1 при электрофорезе в ДСН-ПААГ при использовании невосстанавливающих гелей. В образцы, представленные в полосе 1, был добавлен дитиотреитол (ДТТ) в качестве восстановителя. В образцы, представленные в полосе 2, ДТТ не добавляли;
на фиг.2 - дегрануляция базофилов при использовании либо только слитых белков Fe1 d1, либо слитых белков Fe1 d1, связанных с Qβ. По оси абсцисс отложена концентрация соответствующего белка Fe1 d1. По оси ординат отложен процент базофилов, подвергшихся дегрануляции;
на фиг.3 - результаты инъекционной кожной пробы добровольца, страдающего аллергией на кошек, которому вводили Qβ-FELD1 в день 0, 7 и 14 и проводили также пробы в день 0, 14 и 21;
на фиг.4А - балл при использовании возрастающих назальных доз и общий назальный балл (фиг.4Б) для добровольца, страдающего аллергией на кошек, которому вводили Qβ-FELD1 в день 0, 7 и 14 и проводили также пробы в день 0, 14 и 21.
Подробное описание изобретения
Если не указано иное, все технические и научные понятия, употребляемые в настоящем описании, имеют общепринятые значения, очевидные специалисту в области, к которой относится настоящее изобретение.
Адъювант: Понятие «адъювант» в контексте настоящего описания относится к неспецифическим стимуляторам иммунного ответа или субстанциям, которые обеспечивают образование депо в хозяине, и при объединении с предлагаемыми в настоящем изобретении вакциной и фармацевтической композицией соответственно могут еще в большей степени усиливать иммунный ответ. Можно применять различные адъюванты. Их примерами являются полный и неполный адъювант Фрейнда, гидроксид алюминия и модифицированный мурамилдипептид. Кроме того, адъювантами являются минеральные гели, такие как гидроксид алюминия, поверхностно-активные вещества, такие как лизолецитин, плюроновые полиолы, полианионы, пептиды, масляные эмульсии, гемоцианины лимфы улитки, динитрофенол, и адъюванты, которые потенциально можно применять для введения человеку, такие как БЦЖ (бацилла Кальмета-Герена) и Corynebacterium parvum. Такие адъюванты также хорошо известны в данной области. Другие адъюванты, которые можно вводить в сочетании с композициями, предлагаемыми в изобретении, включают (но не ограничиваясь ими) монофосфорильный липидный иммуномодулятор, AdjuVax 100a, QS-21, QS-18, CRL1005, соли алюминия (квасцы), MF-59, ОМ-174, ОМ-197, ОМ-294 и адъювант, применяемый в Virosomal -технологии (вирус-липосомной вакцине). Адъюванты могут представлять собой также смеси этих соединений. Как правило, ВПЧ представляет собой адъювант. Однако, когда понятие «адъювант» упоминается в контексте настоящего описания, то оно относится к адъюванту, который не является ВПЧ, применяемой в композициях, предлагаемых в настоящем изобретении, но который добавлен к ВПЧ.
Антиген: В контексте настоящего описания понятие «антиген» относится к молекуле, которая обладает способностью связываться с антителом или Т-клеточным рецептором (ТКР), если презентируется с помощью молекул ГКГ. Понятие «антиген» в контексте настоящего описания включает также Т-клеточные эпитопы. Кроме того, антиген обладает способностью распознаваться иммунной системой и/или обладает способностью индуцировать гуморальный иммунный ответ и/или клеточный иммунный ответ, что приводит к активации В- и/или Т-лимфоцитов. Однако по меньшей мере в некоторых случаях, антиген может содержать или быть связанным с Th-клеточным эпитопом и использоваться в адъюванте. Антиген может нести один или несколько эпитопов (В- и Т-эпитопы). Описанная выше специфическая реакция подразумевает, что антиген должен предпочтительно реагировать, как правило, с высокой степенью избирательности, с соответствующим ему антителом или ТКР и не вступать в реакцию с множеством других антител или ТКР, которые могут вырабатываться в ответ на другие антигены. В контексте настоящего описания антигены могут представлять также смеси нескольких индивидуальных антигенов.
Антигенная детерминанта: Понятие «антигенная детерминанта» и «антигенный эпитоп», которые в контексте настоящего описания используются взаимозаменяемо, относится к непрерывным или прерывистым областям полипептида, которые могут иммуноспецифически связываться с антителом или Т-клеточным рецептором в контексте молекулы ГКГ. Иммуноспецифическое связывание исключает неспецифическое связывание, но не обязательно исключает перекрестную реактивность. Антигенная детерминанта, как правило, содержит 5-10 аминокислот в пространственной конформации, которая является уникальной для антигенной детерминанты.
Ассоциированный: Понятие «ассоциированный» (или соответствующее ему существительное ассоциация) в контексте настоящего описания относится ко всем возможным путям, предпочтительно химическим взаимодействиям, с помощью которых две молекулы соединяются друг с другом. Химические взаимодействия включают ковалентные и нековалентные взаимодействия Типичными примерами нековалентых взаимодействий являются ионные взаимодействия, гидрофобные взаимодействия или водородные связи, где основой ковалентных взаимодействий являются, например, ковалентные связи, такие как сложноэфирные связи, связи, образованные с помощью простого эфира, сложного фосфоэфира, амидные, пептидные связи, связи типа углерод-фосфор, связи типа углерод-сера, такие как тиоэфирные связи, или имидные связи.
Сайт присоединения, первый: в контексте настоящего описания понятие «первый сайт присоединения» относится к элементу, который встречается в естественных условиях в ВПЧ или который искусственно добавляют к ВПЧ, и с которым может связываться второй сайт присоединения. Первый сайт присоединения может представлять собой белок, полипептид, аминокислоту, пептид, сахар, полинуклеотид, природный или синтетический полимер, вторичный метаболит или соединение (биотин, флуоресцеин, ретинол, дигоксигенин, ионы металлов, фенилметилсульфонилфторид), или химически реактивную группу, такую как аминогруппа, карбоксильная группа, сульфгидрильная группа, гидроксильная группа, гуанидинильная группа, гистидинильная группа, или их комбинацию. В предпочтительном варианте осуществления изобретения химически реактивная группа в качестве первого сайта присоединения представляет собой аминогруппу аминокислоты, такой как лизин. Первый сайт присоединения локализован, как правило, на поверхности, и предпочтительно на наружной поверхности ВПЧ. Множество первых сайтов присоединения присутствует на поверхности, предпочтительно на наружной поверхности вирусоподобной частицы, как правило, они имеют повторяющуюся конфигурацию. В предпочтительном варианте осуществления изобретения первый сайт присоединения ассоциирован с ВПЧ с помощью по меньшей мере одной ковалентной связи, предпочтительно с помощью по меньшей мере одной пептидной связи. В другом предпочтительном варианте осуществления изобретения первый сайт присоединения представляет собой сайт, встречающийся в естественных условиях в ВПЧ. В другом варианте первый сайт присоединения искусственно добавляют к ВПЧ.
Сайт присоединения, второй: в контексте настоящего описания понятие «второй сайт присоединения» относится к элементу, который встречается в естественных условиях в сочетании с Fe1 d1, предлагаемым в настоящем изобретении, или который искусственно добавлен к нему, и с которым может связываться первый сайт присоединения. Второй сайт присоединения Fe1 d1, предлагаемого в изобретении, может представлять собой белок, полипептид, пептид, аминокислоту, сахар, полинуклеотид, природный или синтетический полимер, вторичный метаболит или соединение (биотин, флуоресцеин, ретинол, дигоксигенин, ионы металлов, фенилметилсульфонилфторид), или химически реактивную группу, такую как аминогруппа, карбоксильная группа, сульфгидрильная группа, гидроксильная группа, гуанидинильная группа, гистидинильная группа, или их комбинацию. В предпочтительном варианте осуществления изобретения химически реактивная группа в качестве второго сайта присоединения представляет собой сульфгидрильную группу аминокислоты, такой как цистеин. Таким образом, понятие «белок Fe1 d1, несущий по меньший мере один второй сайт присоединения» относится к конструкции, содержащей Fe1 d1, предлагаемый в изобретении, и по меньшей мере один второй сайт присоединения. Однако в случае второго сайта присоединения, который не встречается в естественных условиях в сочетании с Fe1 d1, такая конструкция, как правило и предпочтительно, дополнительно, содержит «линкер». В другом предпочтительном варианте осуществления изобретения второй сайт присоединения ассоциирован с Fe1 d1, предлагаемым в изобретении, с помощью по меньшей мере одной ковалентной связи, предпочтительно через с помощью по меньшей мере одной пептидной связи. В другом варианте осуществления изобретения второй сайт присоединения представляет собой сайт, встречающийся в естественных условиях в Fe1 d1, предлагаемом в изобретении. В другом предпочтительном варианте осуществления изобретения второй сайт присоединения искусственно добавляют к Fe1 d1, предлагаемому в изобретении, через аминокислотный линкер, предпочтительно содержащий цистеин. Предпочтительно линкер сливают с Fe1 d1, предлагаемым в изобретении, пептидной связью.
Оболочечный белок: В контексте настоящего описания понятие «оболочечный белок» и понятие «капсидный белок», которые используются взаимозаменяемо в контексте настоящего описания, относятся к вирусному белку, предпочтительно субъединице встречающегося в естественных условиях капсида вируса, предпочтительно РНК содержащего фага, который можно включать в вирусный капсид или ВПЧ.
Fe1 d1, предлагаемый в изобретении: Понятие «Fe1 d1, предлагаемый в изобретении» в контексте настоящего описания относится по меньшей мере к одному белку Fe1 d1 или по меньшей мере одному фрагменту Fe1 d.
Цепь 1 Fe1 d1: Понятие «цепь 1 Fe1 d1» в контексте настоящего описания относится к полипептиду, который содержит или в другом варианте состоит из аминокислотной последовательности, представленной в SEQ ID NO:22, или гомологичной ей последовательности. Понятие «последовательность, гомологичная SEQ ID NO:22» в контексте настоящего описания относится к полипептиду, который идентичен SEQ ID NO:22 более чем на 70%, предпочтительно более чем на 80%, более предпочтительно более чем на 90% и еще более предпочтительно более чем на 95%. Понятие «цепь 1 Fe1 d1» в контексте настоящего описания относится также к полипептиду, который несет по меньшей мере одну пост-трансляционную модификацию, включающую (но, не ограничиваясь ими) по меньшей мере одно гликозилирование цепи 1 Fe1 d1, как она определена в настоящем описании. Предпочтительно цепь 1 Fe1 d1, как она определена в настоящем описании, состоит в целом максимум из 130, еще более предпочтительно максимум из 100 аминокислот.
Цепь 2 Fe1 d1: Понятие «цепь 2 Fe1 d1» в контексте настоящего описания относится к полипептиду, который содержит или в другом варианте состоит из аминокислотных последовательностей, представленных в SEQ ID NO:23, SEQ ID NO:25 или SEQ ID NO:26, или гомологичной ей последовательности. Понятие «последовательность, гомологичная SEQ ID NO:23, SEQ ID NO:25 или SEQ ID NO:26» в контексте настоящего описания относится к полипептиду, который идентичен SEQ ID NO:23, SEQ ID NO:25 или SEQ ID NO:26 более чем на 70%, предпочтительно более чем на 80%, более предпочтительно более чем на 90% и еще более предпочтительно более чем на 95%. Понятие «цепь 2 Fe1 d1» в контексте настоящего описания относится также к полипептиду, который несет по меньшей мере одну пост-трансляционную модификацию, включающую (но, не ограничиваясь ими) по меньшей мере одно гликозилирование цепи 2 Fe1 d1, как она определена в настоящем описании. Предпочтительно цепь 2 Fe1 d1, как она определена в настоящем описании, состоит в целом максимум из 150, еще более предпочтительно максимум из 130 и еще более предпочтительно максимум из 100 аминокислот.
Белок Fe1 d1: Понятие «белок Fe1 d1» в контексте настоящего описания относится к белку, который содержит или в другом варианте состоит из цепи 1 Fe1 d1 и цепи 2 Fe1 d1. Предпочтительно цепь 1 Fe1 d1 и цепь 2 Fe1 d1 связаны ковалентно. В одном предпочтительном варианте осуществления изобретения цепь 1 Fe1 d1 и цепь 2 Fe1 d1 связаны с помощью по меньшей одной дисульфидной связи. В другом варианте осуществления изобретения цепь 1 и цепь 2 слиты непосредственно или с помощью спейсера, в этом случае белок Fe1 d1 дополнительно содержит или в другом варианте представляет собой спейсер. Предпочтительно белок Fe1 d1, как он определен в настоящем описании, состоит в целом максимум из 300, еще более предпочтительно максимум из 200 аминокислот. Как правило и предпочтительно, белок Fe1 d1, предлагаемый в изобретении, обладает способностью индуцировать in vivo производство антитела, которое специфически связывается либо с встречающимся в естественных условиях Fe1 d1, либо с рекомбинантным Fe1 d1, который получают согласно методу, описанному в примере 5 настоящего описания.
Фрагмент Fe1 d1: Понятие «фрагмент Fe1 d1» в контексте настоящего описания относится к полипептиду, который содержит или в другом варианте состоит по меньшей мере из одной антигенной детерминанты Fe1 d1. Как правило и предпочтительно, понятие «фрагмент Fe1 d1» в контексте настоящего описания относится к полипептиду, который содержит или в другом варианте состоит по меньшей мере из двух антигенных детерминант Fe1 d1. Предпочтительно антигенные детерминанты ковалентно связаны, предпочтительно также антигенные детерминанты связаны с помощью по меньшей мере одной пептидной связи, в этом случае может требоваться спейсер между антигенными детерминантами. Предпочтительно по меньшей мере две антигенные детерминанты обе получают из цепи 1 Fe1 d1 и из цепи 2 Fe1 d1. Предпочтительно фрагмент Fe1 d1, как он определен в настоящем описании, состоит в целом максимум из 130, еще более предпочтительно максимум из 100 и еще более предпочтительно из 60 аминокислот. Как правило и предпочтительно, фрагмент Fe1 d1, предлагаемый в изобретении, обладает способностью индуцировать in vivo производство антитела, которое специфически связывается либо с встречающимся в естественных условиях Fe1 d1, либо с рекомбинантным Fe1 d1, который получают согласно методу, описанному в примере 5 настоящего описания.
Связанный: Понятие «связанный» (или существительное: связь) в контексте настоящего описания относится ко всем возможным путям, предпочтительно химическим взаимодействиям, с помощью которых соединяют вместе по меньшей мере один первый сайт присоединения и по меньшей мере один второй сайт присоединения. Химические взаимодействия представляют собой ковалентные и нековалентные взаимодействия. Типичными примерами нековалентных взаимодействий являются ионные взаимодействия, гидрофобные взаимодействия или водородные связи, в то время как ковалентные взаимодействия базируются, например, на ковалентных связях, таких как сложноэфирные связи, связи, образованные с помощью простого эфира, сложного фосфоэфира, амидные, пептидные, связи типа углерод-фосфор, связи типа углерод-сера, такие как тиоэфирные связи, или имидные связи. В конкретных предпочтительных вариантах осуществления изобретения первый сайт присоединения и второй сайт присоединения связывают с помощью по меньшей мере одной ковалентной связи, предпочтительно с помощью по меньшей мере одной непептидной связи и еще более предпочтительно с помощью только непептидной(ых) связи(ей). Однако понятие «связанный» в контексте настоящего описания не относится только к непосредственному связыванию по меньшей мере одного первого сайта присоединения и по меньшей мере одного второго сайта присоединения, но в другом варианте и предпочтительно относится к опосредованному связыванию по меньшей мере одного первого сайта присоединения и по меньшей мере одного второго сайта присоединения через промежуточную(ые) молекулу(ы), и для их создания, как правило и предпочтительно, используют по меньшей мере один, предпочтительно один, гетеробифункциональный перекрестносшивающий агент.
Линкер: «Линкер» в контексте настоящего описания либо ассоциирует второй сайт присоединения с Fe1 d1, предлагаемым в изобретении, или уже содержит, практически состоит или состоит из второго сайта присоединения. Предпочтительно «линкер» в контексте настоящего описания уже содержит второй сайт присоединения, как правило, но не обязательно, в виде одного аминокислотного остатка, предпочтительно остатка цистеина. Понятие «линкер» в контексте настоящего описания обозначают также как «аминокислотный линкер», прежде всего, когда линкер, предлагаемый в изобретении, содержит по меньшей мере один аминокислотный остаток. Таким образом, понятия «линкер» и «аминокислотный линкер» в контексте настоящего описания используют взаимозаменяемо. Однако не предусматривается, что линкер состоит только из аминокислотных остатков, даже, если состоящий из аминокислотных остатков линкер является предпочтительным вариантом осуществления настоящего изобретения. Аминокислотные остатки линкера предпочтительно представляют собой встречающиеся в естественных условиях аминокислоты или не встречающиеся в естественных условиях аминокислоты, известные в данной области, включая их полностью L- или полностью D-изомеры и их смеси. Другими предпочтительными вариантами линкера, предлагаемого в настоящем изобретении, являются молекулы, содержащие сульфгидрильную группу или цистеиновый остаток, и, следовательно, такие молекулы также подпадают под объем изобретения. Другие линкеры, которые можно применять согласно настоящему изобретению, представляют собой молекулы, содержащие С1-С6алкильный, циклоалкильный, такой как циклопентильный или циклогексильный, циклоалкенильный, арильный или гетероарильный фрагмент. Однако линкеры, содержащие предпочтительно C1-С6алкильный, циклоалкильный (C5, C6), арильный или гетероарильный фрагмент и дополнительную(ые) аминокислоту(ы), можно применять также в качестве линкеров, предлагаемых в настоящем изобретении, и они подпадают под объем настоящего изобретения. Ассоциацию линкера с Fe1 d1, предлагаемым в изобретении, предпочтительно осуществляют с помощью по меньшей мере одной ковалентной связи, более предпочтительно по меньшей мере одной пептидной связи.
Упорядоченный и повторяющийся набор антигенов: В контексте настоящего описания понятие «упорядоченный и повторяющийся набор антигенов», в целом, относится к повторяющейся организации антигенов, как правило и предпочтительно, отличающейся единообразным пространственным расположением антигенов относительно вирусоподобной частицы. В одном из вариантов осуществления изобретения повторяющаяся организация может представлять собой геометрическую организацию. В некоторых вариантах осуществления изобретения такие антигены, сшитые с ВПЧ РНК содержащих фагов, являются типичными и предпочтительными примерами приемлемых упорядоченных и повторяющихся наборов антигенов, которые, кроме того, имеют точно повторяющиеся паракристаллические схемы расположения антигенов, предпочтительно с интервалами от 1 до 30 нм, предпочтительно от 2 до 15 нм, еще более предпочтительно от 2 до 10 нм и еще более предпочтительно от 2 до 8 нм, и наиболее предпочтительно от 1,6 до 7 нм.
Упакованная: Понятие «упакованная» в контексте настоящего описания относится к состоянию полианионной макромолекулы или иммуностимулирующих субстанций относительно ВПЧ. Понятие «упакованная» в контексте настоящего описания включает связывание, которое может быть ковалентным, например, путем химического сочетания, или нековалентным, например, путем ионных взаимодействий, гидрофобных взаимодействий, водородных связей и т.д. Понятие «упакованная» относится к включению или частичному включению полианионной макромолекулы. Так, полианионную макромолекулу или иммуностимулирующие субстанции можно включать в ВПЧ без осуществления фактического связывания, в частности с помощью ковалентной связи. В предпочтительных вариантах осуществления изобретения по меньшей мере одну полианионную макромолекулу или иммуностимулирующие субстанции упаковывают внутрь ВПЧ, наиболее предпочтительно нековалентно.
Спейсер: Понятие «спейсер», а также эквивалентное ему понятие «аминокислотный спейсер» в контексте настоящего описания относится к участку аминокислотной последовательности, который состоит не более чем из 30 аминокислот и который связывает N-конец одной цепи с С-концом другой цепи Fe1 d1.
Вирусная частица: Понятие «вирусная частица» в контексте настоящего описания относится к морфологической форме вируса. Для некоторых типов вирусов она представляет собой геном, окруженный белковым капсидом; другие типы вирусов имеют дополнительные структуры (например, оболочки, хвосты и т.д.).
Вирусоподобная частица (ВПЧ) в контексте настоящего описания относится к нерепликативной или неинфекционной, предпочтительно нерепликативной и неинфекционной, вирусной частице, или относится к нереплекативной или неинфекционной, предпочтительно нерепликативной и неинфекционной, структуре, напоминающей вирусную частицу, предпочтительно капсид вируса. Понятие «нерепликативный» в контексте настоящего описания обозначает отсутствие у генома, входящего в ВПЧ, способности к репликации. Понятие «неинфекционный» в контексте настоящего описания обозначает неспособность проникать в клетку-хозяина. Предпочтительно вирусоподобная частица, предлагаемая в изобретении, является нерепликативной и/или неинфекционной, поскольку у нее отсутствуют полностью или частично вирусный геном или функции генома. В одном из вариантов осуществления изобретения вирусоподобная частица представляет собой вирусную частицу, в которой вирусный геном инактивирован физически или химически. Как правило и более предпочтительно, у вирусоподобной частицы отсутствуют все или часть репликативных и инфекционных компонентов вирусного генома. Вирусоподобная частица, предлагаемая в изобретении, может содержать нуклеиновую кислоту из генома, отличного от ее генома. Обычным и предпочтительным вариантом вирусоподобной частицы, предлагаемой в настоящем изобретении, является вирусный капсид, такой как вирусный капсид соответствующего вируса, бактериофага, предпочтительно РНК содержащего фага. Понятия «вирусный капсид» или «капсид» означают макромолекулярную структуру, состоящую из субъединиц вирусного белка. Как правило, она состоит из 60, 120, 180, 240, 300, 360 и более субъединиц вирусного белка. Как правило и предпочтительно, взаимодействия этих субъединиц приводят к формированию вирусного капсида или напоминающей вирусной капсид структуры с присущей ей повторяющейся организацией, при этом структура, как правило, является сферической или трубчатой. Например, капсиды РНК содержащих фагов или HbcAg (внутренний (коровый) антиген вируса гепатита В) имеют сферическую форму, обладающую икосаэдральной симметрией. Понятие «капсидоподобная структура» в контексте настоящего описания относится к макромолекулярной структуре, состоящей из субъединиц вирусного белка, которая имеет морфологическое строение, сходное с капсидом, как он определен выше, но не имеет характерного симметричного строения, сохраняя при этом достаточную упорядоченность и частоту встречаемости.
Одним из общих признаков вирусной частицы и вирусоподобной частицы является высокий уровень упорядоченности и повторяющаяся структура их субъединиц.
Вирусоподобная частица РНК содержащего фага: В контексте настоящего описания понятие «вирусоподобная частица РНК содержащего фага» относится к вирусоподобной частице, содержащей или предпочтительно практически состоящей или состоящей из оболочечных белков, их мутантов или фрагментов РНК содержащего фага. Кроме того, вирусоподобная частица РНК содержащего фага, имея структуру РНК содержащего фага, является нерепликативной или неинфекционной, и, как правило, у нее отсутствуют ген или гены, кодирующие комплекс репликации РНК содержащего фага, и, как правило, она лишена также гена или генов, кодирующих белок или белки, которые ответственны за связывание вируса с хозяином или за проникновение в хозяина. Однако под это определение подпадают также вирусоподобные частицы РНКовых фагов, в которых вышеупомянутый(ые) ген или гены еще присутствуют, но являются неактивными, и вследствие этого такие частицы также представляют собой нерепликативные и неинфекционные вирусоподобные частицы РНК содержащего фага. Предпочтительные ВПЧ, полученные из РНКовых фагов, обладают икосаэдральной симметрией и состоят из 180 субъединиц. В контексте настоящего описания понятие «субъединица» и «мономер» используют взаимозаменяемо, и они являются эквивалентными. В контексте настоящего описания понятие «РНК содержащий фаг» и понятие «РНК содержащий бактериофаг» используют взаимозаменяемо. Предпочтительными методами, с помощью которых вирусоподобную частицу РНК содержащего фага можно сделать нерепликативной и/или неинфекционной являются физическая, химическая инактивация, такая как УФ-облучение или обработка формальдегидом, как правило и предпочтительно, методы генной инженерии.
Один или несколько: В контексте настоящего описания упоминание единственного числа может обозначать «по меньшей мере один» или «один или несколько», если не указано иное.
Идентичность аминокислотных последовательностей полипептидов можно определять общепринятым методом с помощью известных компьютерных программ, таких как программа Bestfit. При использовании программы Bestfit или любой другой программы для сравнительного анализа последовательностей, предпочтительно при использовании программы Bestfit, для решения вопроса о том, идентична ли конкретная последовательность, например, на 95%, аминокислотной последовательности, с которой проводят сравнение, параметры устанавливают так, чтобы процент идентичности рассчитывать для полноразмерной аминокислотной последовательности, с которой проводят сравнение, и при этом допускается наличие «брешей» в гомологии вплоть до 5% от общего количества аминокислотных остатков в последовательности, с которой проводят сравнение. Вышеуказанный метод определения процента идентичности полипептидов применим для всех белков, полипептидов или их фрагментов, описанных в настоящем изобретении.
Согласно изобретению считается, что антитела специфически связываются, если их связывание с антигеном характеризуется аффинностью связывания (Ka) 106 М-1 или более, предпочтительно 107 М-1 или более, более предпочтительно 108 М-1 или более, и наиболее предпочтительно 109 М-1 или более. Обычный специалист в данной области легко может определять аффинность антител (например, с помощью анализа Скэтчарда).
Настоящее изобретение относится к композициям, предлагаемым в изобретении, содержащим: (а) короную частицу, которая несет по меньшей мере один первый сайт присоединения, где коровая частица представляет собой вирусоподобную частицу (ВПЧ) или вирусную частицу и (б) по меньшей мере один антиген, который несет по меньшей мере один второй сайт присоединения, где по меньшей мере один антиген представляет собой белок Fe1 d1 или фрагмент Fe1 d1, и где (а) и (б) ковалентно связаны с помощью по меньшей мере одного первого и по меньшей мере одного второго сайта присоединения.
Предпочтительно белок Fe1 d1 или фрагмент Fe1 d1 связаны так, чтобы формировать упорядоченный и повторяющийся набор антиген-ВПЧ. В предпочтительных вариантах осуществления изобретения по меньшей мере 20, предпочтительно по меньшей мере 30, более предпочтительно по меньшей мере 60, еще более предпочтительно по меньшей мере 120 и еще более предпочтительно по меньшей мере 180 единиц белка Fe1 d1 или фрагмента Fe1 d1 связаны с коровой частицей.
В качестве ВПЧ или вирусной частицы, предлагаемой в изобретении, можно использовать любой вирус, известный в данной области, который обладает упорядоченной и повторяющейся структурой. Примеры ДНК содержащих или РНК содержащих вирусов, оболочечный или капсидный белок которых можно применять для получения ВПЧ, описаны в WO 2004/009124 на странице 25, строки 10-21, на странице 26, строки 11-28 и со страницы 28, строка 4, до страницы 31, строка 4. Указанный документ включен в настоящее описание в качестве ссылки.
Вирус или вирусоподобную частицу можно получать и очищать из зараженной вирусом клеточной культуры. Полученный в результате вирус или вирусоподобная частица, предназначенные для приготовления вакцины, должны предпочтительно быть нерепликативными или неинфекционными, более предпочтительно нерепликативными и неинфекционными. Общепринятыми методами для этой цели являются УФ-облучение, химическая обработка, например формальдегидом или хлороформом.
В одном из предпочтительных вариантов осуществления изобретения коровая частица представляет собой вирусную частицу, и предпочтительно вирусная частица представляет собой вирусную частицу бактериофага, и предпочтительно также бактериофаг представляет собой РНК содержащий фаг, и еще более предпочтительно РНК содержащий фаг представляет собой РНК содержащий фаг, выбранный из Qβ, fr, GA или АР205.
В предпочтительном варианте осуществления изобретения коровая частица представляет собой ВПЧ. В другом предпочтительном варианте осуществления изобретения ВПЧ представляет собой рекомбинантную ВПЧ. Почти все широко известные вирусы были секвенированы, и эти данные доступны научной общественности. Специалист в данной области легко может идентифицировать ген, кодирующий оболочечный белок, получение ВПЧ с помощью рекомбинантной экспрессии оболочечного белка в хозяине является общеизвестным для специалистов в данной области.
В одном из предпочтительных вариантов осуществления изобретения вирусоподобная частица содержит или в другом варианте состоит из рекомбинантных белков, их мутантов или фрагментов вируса, выбранного из группы, включающей: а) РНК содержащие фаги; б) бактериофаги; в) вирус гепатита В, предпочтительно его капсидный белок (Ulrich и др., Virus Res. 50, 1998, cc.141-182) или его поверхностный белок (WO 92/11291); г) вирус кори (Warnes и др., Gene 160, 1995, cc.173-178); д) вирус Синдбис; е) ротавирус (US 5071651 и US 5374426); ж) вирус ящура (Twomey и др., Vaccine 13, 1995, cc.1603-1610); з) вирус Норвалка (Jiang X. и др., Science 250, 1990, cc.1580-1583; Matsui S.M. и др., J. Clin. Invest. 87, 1991, cc.1456-1461) и) альфавирус; к) ретровирус, предпочтительно его белок GAG (WO 96/30523); л) ретротранспозон Ту, предпочтительно белок р1; м) вирус человеческой папилломы (WO 98/15631); н) вирус полиомы; о) вирус табачной мозаики; и п) вирус домашних стад (Flock House Virus).
В другом предпочтительном варианте осуществления изобретения ВПЧ содержит или состоит более чем из одной последовательности, предпочтительно из двух аминокислотных последовательностей рекомбинантных белков, их мутантов или фрагментов. ВПЧ, которая содержит или состоит более чем из одной аминокислотной последовательности, в контексте настоящего описания обозначают как мозаичная ВПЧ.
Понятие «фрагмент рекомбинантного белка» или понятие «фрагмент оболочечного белка» в контексте настоящего описания относится к полипептиду, длина которого составляет по меньшей мере 70%, предпочтительно по меньшей мере 80%, более предпочтительно по меньшей мере 90%, еще более предпочтительно по меньшей мере 95% от длины рекомбинантного белка или оболочечного белка дикого типа соответственно, и который предпочтительно сохраняет способность формировать ВПЧ. Предпочтительно фрагмент получают с помощью по меньшей мере одной внутренней делеции, по меньшей мере одного укорочения или по меньшей мере одной их комбинации. Понятие «фрагмент рекомбинантного белка» или «фрагмент оболочечного белка» относится также к полипептиду, аминокислотная последовательность которого идентична по меньшей мере на 80%, предпочтительно на 90%, еще более предпочтительно на 95% аминокислотной последовательности «фрагмента рекомбинантного белка» или «фрагмента оболочечного белка» соответственно, как они определены выше, и который предпочтительно обладает способностью к сборке с образованием вирусоподобной частицы.
Понятие «мутантный рекомбинантный белок» или понятие «мутант рекомбинантного белка», которые в настоящем описании используют взаимозаменяемо, или понятие «мутантный оболочечный белок» или понятие «мутант оболочечного белка», которые в настоящем описании используют взаимозаменяемо, относится к полипептиду, аминокислотная последовательность которого выведена из рекомбинантного белка или оболочечного белка дикого типа соответственно, аминокислотная последовательность которого по меньшей мере на 80%, предпочтительно по меньшей мере на 85%, 90%, 95%, 97% или 99% идентична последовательности дикого типа, и предпочтительно сохраняет способность к сборке с образованием ВПЧ.
В одном из предпочтительных вариантов осуществления изобретения вирусоподобная частица, предлагаемая в изобретении, представляет собой вирус гепатита В. Получение вирусоподобных частиц гепатита В описано среди прочего в WO 00/32227, WO 01/85208 и WO 01/056905. Все три документа специально включены в настоящее описание в качестве ссылки. Другие варианты HBcAg, пригодные для воплощения на практике настоящего изобретения, описаны на страницах 34-39 WO 01/056905.
Еще в одном предпочтительном варианте осуществления изобретения остаток лизина интродуцируют в полипептид HBcAg с целью опосредования связывания Fe1 d1, предлагаемого в изобретении, с ВПЧ HBcAg. В предпочтительных вариантах осуществления изобретения ВПЧ и композиции, предлагаемые в изобретении, получают с использованием HBcAg, который содержит или в другом варианте состоит из аминокислот 1-144 или 1-149, 1-185 SEQ ID NO:20, которая модифицирована, в результате чего аминокислоты в положениях 79 и 80 заменены пептидом, имеющим аминокислотную последовательность Gly-Gly-Lys-Gly-Gly. Эта модификация изменяет SEQ ID NO:20 на SEQ ID NO:21. В других предпочтительных вариантах осуществления изобретения остатки цистеина в положениях 48 и 110 SEQ ID NO:21 или ее соответствующих фрагментах, предпочтительно 1-144 или 1-149, заменены в результате мутации на серин. Изобретение относится также к композициям, содержащим мутанты коревого белка вируса гепатита В, которые имеют вышеуказанные аминокислотные замены. Изобретение относится также к композициям и вакцинам соответственно, содержащим полипептиды HBcAg, которые содержат или в другом варианте состоят из аминокислотных последовательностей, которые по меньшей мере на 80%, 85%, 90%, 95%, 97% или 99% идентичны SEQ ID NO:21.
В одном из предпочтительных вариантов осуществления изобретения вирусоподобная частица, предлагаемая в изобретении, содержит, практически состоит или в другом варианте состоит из рекомбинантных оболочечных белков, их мутантов или фрагментов РНК содержащего фага. Предпочтительно РНК содержащий фаг выбирают из группы, включающей а) бактериофаг Qд.; б) бактериофаг R17; в) бактериофаг fr; г) бактериофаг GA; д) бактериофаг SP; е) бактериофаг MS2; ж) бактериофаг М11; з) бактериофаг МХ1; и) бактериофаг NL95; к) бактериофаг f2; л) бактериофаг РР7 и м) бактериофаг АР205.
В одном из предпочтительных вариантов осуществления изобретения композиция содержит оболочечный белок, его мутанты или фрагменты РНК содержащих фагов, где оболочечный белок имеет аминокислотную последовательность, выбранную из группы, включающей: (a) SEQ ID NO:1, относящуюся к СР Qβ; (б) смесь SEQ ID NO:1 и SEQ ID NO:2 (относящуюся к белку А1 Qβ); (в) SEQ ID NO:3; (г) SEQ ID NO:4; (д) SEQ ID NO:5; (е) SEQ ID NO:6, (ж) смесь SEQ ID NO:6 и SEQ ID NO:7; (з) SEQ ID NO:8; (и) SEQ ID NO:9; (к) SEQ ID NO:10; (л) SEQ ID NO:11; (м) SEQ ID NO:12; (н) SEQ ID NO:13 и (о) SEQ ID NO:14.
В одном из предпочтительных вариантов осуществления изобретения ВПЧ представляет собой мозаичную ВПЧ, которая содержит или в другом варианте состоит более чем из одной аминокислотной последовательности, предпочтительно из двух аминокислотных последовательностей, оболочечных белков, их мутантов или фрагментов РНК содержащего фага.
В наиболее предпочтительном варианте осуществления изобретения ВПЧ содержит или в другом варианте состоит из двух различных оболочечных белков РНК содержащего фага, где эти два оболочечных белка имеют аминокислотную последовательность SEQ ID NO:1 и SEQ ID NO:2 или SEQ ID NO:6 и SEQ ID NO:7.
В других предпочтительных вариантах осуществления изобретения вирусоподобная частица, предлагаемая в изобретении, содержит или в другом варианте практически состоит или еще в одном варианте состоит из оболочечных белков, их фрагментов или мутантов РНК содержащего бактериофага Qβ, fr, AP205 или GA. В одном из предпочтительных вариантов осуществления изобретения ВПЧ представляет собой ВПЧ РНК содержащего бактериофага, предпочтительно РНК содержащего бактериофага Qβ, fr, AP205 или GA.
В одном из предпочтительных вариантов осуществления изобретения ВПЧ, предлагаемая в изобретении, представляет собой ВПЧ РНК содержащего фага Qβ. Капсид или вирусоподобная частица фага Qβ обладает икосаэдральной фагоподобной капсидной структурой с диаметром 25 нм и квазисимметрией Т=3. Капсид содержит 180 копий оболочечного белка, которые связаны в ковалентные пентамеры и гексамеры дисульфидными мостиками (Golmohammadi R. и др., Structure 4, 1996, cc.543-5554), что позволяет получать обладающий высокой стабильностью капсид Qβ. Однако капсиды или ВПЧ, полученные из рекомбинантного оболочечного белка Qβ, могут содержать субъединицы, не связанные или не полностью связанные дисульфидными мостиками с другими субъединицами капсида. Капсид или ВПЧ Qβ обладает также необычной устойчивостью к органическим растворителям и денатурирующим агентам. При создании изобретения неожиданно было установлено, что ДМСО и ацетонитрил при их применении в концентрациях порядка 30% и гуанидиний в концентрациях порядка 1М не оказывают воздействия на стабильность капсида. Высокая стабильность капсида или ВПЧ Qβ является имеющим преимущество признаком, в частности при их применении для иммунизации и вакцинации млекопитающих и человека согласно настоящему изобретению.
Другие предпочтительные согласно настоящему изобретению вирусоподобные частицы РНКовых фагов, в частности Qβ и fr, описаны в WO 02/056905, содержание которой полностью включено в настоящее описание в качестве ссылки. Конкретно в примере 18 WO 02/056905 дано подробное описание получения ВПЧ из Qβ.
В другом предпочтительном варианте осуществления изобретения ВПЧ, предлагаемая в изобретении, представляет собой ВПЧ РНК содержащего фага АР205. Компетентные в отношении сборки мутантные формы ВПЧ АР205, содержащие оболочечный белок АР205 с заменой пролина в положении 5 аминокислотной последовательности на треонин, можно применять также для воплощения на практике изобретения, и они являются предпочтительными дополнительными вариантами осуществления изобретения. В WO 2004/007538, в частности в примере 1 и в примере 2, описан метод получения ВПЧ, содержащих оболочечные белки АР205, и в частности их экспрессия и очистка. WO 2004/007538 включена в настоящее описание в качестве ссылки. ВПЧ АР205 обладают высокой иммуногенностью и их можно связывать с Fe1 d1, предлагаемым в изобретении, как правило и предпочтительно, для получения конструкций вакцины, презентирующих Fe1 d1, предлагаемый в изобретении, ориентированный упорядоченным образом. При такой презентации Fe1 d1, предлагаемого в изобретении, продуцируется высокий титр антител, что свидетельствует о том, что связанные Fe1 d1, предлагаемые в изобретении, доступны для взаимодействия с молекулами антитела и обладают иммуногенностью.
В одном из предпочтительных вариантов осуществления изобретения ВПЧ, предлагаемая в изобретении, содержит или состоит из мутантного оболочечного белка вируса, предпочтительно РНК содержащего фага, где мутантный оболочечный белок РНК содержащего фага модифицирован путем удаления по меньшей мере одного остатка лизина посредством замены и/или посредством делеции. В другом предпочтительном варианте осуществления изобретения ВПЧ, предлагаемая в изобретении, содержит или состоит из мутантного оболочечного белка вируса, предпочтительно РНК содержащего фага, где мутантный оболочечный белок РНК содержащего фага модифицирован посредством добавления по меньшей мере одного остатка лизина путем замены или путем инсерции. Делеция, замена или добавление по меньшей мере одного остатка лизина позволяет варьировать уровень сочетания, т.е. количество Fe1 d1, предлагаемого в изобретении, на одну субъединицу ВПЧ вируса, предпочтительно РНКовых фагов, в частности, для удовлетворения и соответствия требованиям, предъявляемым к вакцине.
В еще одном предпочтительном варианте осуществления изобретения композиции и вакцины, предлагаемые в изобретении, имеют антигенную плотность от 0,5 до 4,0. Понятие «антигенная плотность» в контексте настоящего описания относится к среднему количеству Fe1 d1, предлагаемого в изобретении, которое связано с субъединицей, и предпочтительно с оболочечным белком ВПЧ и предпочтительно ВПЧ РНК содержащего фага. Так, это значение рассчитывают как среднее для всех субъединиц или мономеров ВПЧ, предпочтительно ВПЧ РНК содержащего фага, в композиции или вакцинах, предлагаемых в изобретении.
ВПЧ или капсиды оболочечного белка Qβ имеют определенное количество остатков лизина на своей поверхности, характеризующихся определенной топологией, которая отличается тем, что три остатка лизина направлены внутрь капсида и взаимодействуют с РНК, а четыре других остатка лизина направлены кнаружи капсида. Предпочтительно по меньшей мере один первый сайт присоединения представляет собой остаток лизина, направленный кнаружи или расположенный снаружи ВПЧ.
Согласно настоящему изобретению можно применять мутанты Qβ, в которых находящиеся на поверхности (презентированные) остатки лизина заменены остатком аргинина. Таким образом, в еще одном предпочтительном варианте осуществления настоящего изобретения вирусоподобная частица содержит, практически состоит или в еще одном варианте состоит из мутантных оболочечных белков Qβ. Предпочтительно эти мутантные оболочечные белки содержат или в другом варианте состоят из аминокислотных последовательностей, выбранных из группы, включающей a) Qβ-240 (SEQ ID NO:15, Lys13-Arg SEQ ID NO:1); 6) Qβ-243 (SEQ ID NO:16, Asn10-Lys SEQ ID NO:1); в) Qβ-250 (SEQ ID NO:17, Lys2-Arg SEQ ID NO:1); г) Qβ-251 (SEQ ID NO:18, Lys16-Arg SEQ ID NO:1); и д) Qβ-259" (SEQ ID NO:19, Lys2-Arg, Lys16-Arg SEQ ID NO:1). Конструирование, экспрессия и очистка вышеуказанных мутантных оболочечных белков Qβ, ВПЧ и капсидов соответственно из мутантного оболочечного белка Qβ описаны в WO 02/056905, в частности в примере 18 вышеуказанной заявки.
В другом предпочтительном варианте осуществления настоящего изобретения вирусоподобная частица содержит или в другом варианте практически состоит, или еще в одном варианте состоит из мутантных оболочечных белков Qβ или их мутантов или фрагментов и соответствующего белка А1. В другом предпочтительном варианте осуществления изобретения вирусоподобная частица содержит или в другом варианте практически состоит, или еще в одном варианте состоит из мутантного оболочечного белка, который имеет аминокислотную последовательность, представленную в SEQ ID NO:15, 16, 17, 18 или 19, и соответствующего белка А1.
Кроме того, обнаружены другие оболочечные белки РНКовых фагов, которые также обладают способностью к самосборке при экспрессии в бактериальном хозяине (Kastelein R.A. и др., Gene 23, 1983, cc.245-254, Kozlovskaya T.M. и др., Dokl. Akad. Nauk SSSR 287, 1986, cc.452-455, Adhin M.R. и др., Virology 170, 1989, cc.238-242 (1989), Priano С. и др., J. Mol. Biol. 249, 1995, cc.283-297). Выявлены конкретные биологические и биохимические свойства GA (Ni CZ. и др., Protein Sci. 5, 1996, cc.2485-2493. Tars K. и др., J. Mol.Biol. 271, 1997, cc.759-773) и fr (Pushko P. и др., Prot. Eng. 6, 1993, cc.883-891; Liljas L. и др., J Mol. Biol. 244, 1994, cc.279-290). Определена кристаллическая структура некоторых РНКовых бактериофагов (Golmohammadi R. и др., Structure 4, 1996, cc.543-554). На основе этой информации можно идентифицировать находящиеся на поверхности остатки и благодаря этому оболочечные белки РНКовых фагов можно модифицировать таким образом, чтобы один или несколько реакционноспособных аминокислотных остатков можно было встраивать путем инсерции или замены. Другим преимуществом ВПЧ, выведенных из РНКовых фагов, является их высокий уровень экспрессии в бактериях, в частности в Е.coli, что позволяет получать большие количества материала с приемлемыми затратами.
В одном из предпочтительных вариантов осуществления изобретения композиция, предлагаемая в изобретении, содержит по меньшей мере один антиген, где указанный по меньшей мере один антиген представляет собой белок Fe1 d1.
В одном из предпочтительных вариантов осуществления изобретения белок Fe1 d1 содержит или в другом варианте состоит из встречающегося в естественных условиях Fe1 d1. Первичная структура цепи 1 представлена в последовательности SEQ ID NO:22. Известными из литературы вариантами цепи 1 являются Lys29-Arg или Asn, Val33-Ser, Val60-Leu. Первичная структура цепи 2 представлена в последовательности SEQ ID NO:23, 25 или 26. Известными из литературы вариантами цепи 2 являются варианты SEQ ID NO:23, 25 или 26 Cys7-Phe, Phe15-Thr, Asn19-Ser, Gly20-Leu, Ile55-Val, Arg57-Lys, Val58-Phe. Другими вариантами цепи 2 являются Glu69-Val, Tyr70-Asp, Met72-Thr, Gln-77-Glu и Asn86-Lys (вариант SEQ ID NO:25); Met74-Thr, Gln79-Glu и Asn88-Lys (вариант SEQ ID NO:23) (Griffith I.J. и др.. Gene 113, 1992, cc.263-268); Morgenstern J.P. и др., Proc. Natl. Acad. Sci. U.S.A. 88, 1991, cc.9690-9694); Duffort O.A. и др., 1 Mol. Immunol. 28, 1991, cc.301-309; Leitermann K. и др., J. Allergy Clin. Immunol. 74, 1984, cc.147-153; Kristensen А. K и др., Biol Chem 378, 1997, cc.899-908). Встречающийся в естественных условиях Fe1 d1 получают очисткой, например, из кошачьей слюны, кошачьей перхоти, домашней пыли жилищ, в которых обитают кошки, и т.д.
В одном из предпочтительных вариантов осуществления изобретения Fe1 d1, предлагаемый в изобретении, представляет собой рекомбинантный белок Fe1 d1 или рекомбинантный фрагмент Fe1 d1. Понятия «рекомбинантный белок Fe1 d1» или «рекомбинантный фрагмент Fe1 d1» в контексте настоящего описания относятся к белку Fe1 d1 или фрагменту Fe1 d1, полученному с помощью процесса, который включает по меньшей мере одну стадию применения технологии рекомбинантной ДНК. Понятия «рекомбинантный белок Fe1 d1 d1» или «рекомбинантный фрагмент Fe1 d1» и «полученный путем рекомбинации белок Fe1 d1 d1» или «полученный путем рекомбинации фрагмент Fe1 d1» в контексте настоящего описания используют взаимозаменяемо, и они имеют идентичное значение. Рекомбинантный белок Fe1 d1 d1 или его фрагмент можно получать в любых прокариотических системах экспрессии, таких как Е.coli (WO 2004/094639), или эукариотических системах экспрессии, таких как бакуловирус (WO 00/20032). Seppala с соавторами описали одновременную экспрессию цепи 1 и цепи 2 Fe1 d1 при использовании дицистройного промотора в бакуловирусе (J. Biol. Chem., ноябрь 2004 г.). Полученный рекомбинантно белок Fe1 d1 или его фрагмент может быть гликозилированным или негликозилированным в зависимости от применяемой для получения рекомбинантного белка клетки-хозяина.
В одном из вариантов осуществления изобретения рекомбинантный белок Fe1 d1 содержит или в другом варианте состоит из цепи 1 Fe1 d1 и цепи 2 Fe1 d1, где цепь 1 Fe1 d1 ассоциируют с цепью 2 Fe1 d1 только с помощью нековалентной связи, такой как гидрофобные взаимодействия.
В одном из предпочтительных из вариантов осуществления изобретения рекомбинантный белок Fe1 d1 содержит или в другом варианте состоит из цепи 1 Fe1 d1 и цепи 2 Fe1 d1, где цепь 1 Fe1 d1 ассоциируют с цепью 2 Fe1 d1 с помощью по меньшей мере одной ковалентной связи. В одном из предпочтительных вариантов осуществления изобретения по меньшей мере одна ковалентная связь представляет собой непептидную связь, где непептидная связь представляет собой дисульфидный мостик, или где предпочтительно непептидная связь представляет собой дисульфидный мостик. Например, цепь 1 Fe1 d1 и цепь 2 Fe1 d1 можно экспрессировать по отдельности и затем объединять в условиях, которые обеспечивают формирование правильного дисульфидного мостика, таких как метод решуффлинга (перестановки). В другом варианте цепь 1 Fe1 d1 и цепь 2 Fe1 d1 можно экспрессировать одновременно в одном хозяине, например путем клонирования генов, кодирующих цепь 1 Fe1 d1 и цепь 2 Fe1 d1 соответственно, под контролем двух промоторов в одной плазмиде. В эукариотической системе экспрессии цепь 1 Fe1 d1 и цепь 2 Fe1 d1 можно транскрибировать в одной мРНК и транслировать по отдельности с использованием внутреннего рибосомального сайта проникновения (IRES).
В одном из предпочтительных вариантов осуществления изобретения белок Fe1 d1 содержит или в другом варианте состоит из слитого белка, где слитый белок содержит цепь 1 Fe1 d1 и цепь 2 Fe1 d1. В одном из предпочтительных вариантов осуществления изобретения цепь 1 Fe1 d1 и цепь 2 Fe1 d1 сливают непосредственно с помощью одной пептидной связи, которая соединяет N-конец одной цепи с С-концом другой цепи. В другом предпочтительном варианте осуществления изобретения цепь 1 Fe1 d1 и цепь 2 Fe1 d1 сливают через спейсер, который связывает N-конец одной цепи с С-концом другой цепи. Предпочтительно спейсер состоит из 1-30, предпочтительно 1-25, предпочтительно 1-20, предпочтительно 1-15, предпочтительно 1-9, предпочтительно 1-5, предпочтительно 1-3 аминокислот. В другом варианте спейсер состоит из 10-30, предпочтительно 10-25, более предпочтительно 10-20, более предпочтительно 13-20, более предпочтительно 15-20, более предпочтительно 13-17, более предпочтительно 15-17 аминокислот. Предпочтительно спейсер имеет аминокислотную последовательность, состоящую из 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 аминокислотных остатков. В одном из предпочтительных вариантов осуществления изобретения спейсер содержит 15 аминокислот. В другом предпочтительном варианте осуществления изобретения спейсер представляет собой (GGGGS)3.
В одном из предпочтительных вариантов осуществления изобретения слитый белок содержит аминокислотную последовательность, выбранную из группы, включающей: (a) SEQ ID NO:24; (б) SEQ ID NO:54; (в) SEQ ID NO:55; (г) SEQ ID NO:56 и (д) SEQ ID NO:57.
В одном из предпочтительных вариантов осуществления изобретения цепь 2 Fe1 d1 сливают через ее С-конец с N-концом цепи 1 Fe1 d1 либо непосредственно, либо через спейсер. В одном из предпочтительных вариантов осуществления изобретения белок Fe1 d1 содержит или в другом варианте состоит из аминокислотной последовательности, представленной в SEQ ID NO:24.
В WO 2004/094639 описан рекомбинантный складчатый Fe1 d1, молекулярные и биологические свойства, которого аналогичны встречающейся в естественных условиях копии, и специфические синтетические гены, кодирующие непосредственное слияние N-конца цепи 2 Fe1 d1 с цепью 1. Экспрессия в Е.coli приводила к получению нековалентно ассоциированного гомодимера с кажущейся молекулярной массой 30 кДа, которую определяли с помощью гель-фильтрации, каждая субъединица с молекулярной массой 19177 Да, для которой характерна дисульфидная структура, идентична субъединице, присутствующей во встречающемся в естественных условиях Fe1 d1, и у встречающегося в естественных условиях и рекомбинантного Fe1 d1 обнаружена идентичная складчатость. Рекомбинантный Fe1 d1 взаимодействует с IgE из сыворотки пациентов, страдающих аллергией на кошек, аналогично встречающемуся в естественных условиях Fe1 d1. Таким образом, этот слитый белок Fe1 d1 имитирует антигенные свойства встречающегося в естественных условиях Fe1 d1.
В одном из предпочтительных вариантов осуществления изобретения цепь 1 Fe1 d1 сливают через ее С-конец с N-концом цепи 2 Fe1 d1 либо непосредственно, либо через спейсер.
В одном из предпочтительных вариантов осуществления изобретения цепь 1 Fe1 d1 содержит или в другом варианте состоит их последовательности SEQ ID NO:22 или гомологичной ей последовательности, где гомологичная последовательность идентична SEQ ID NO:22 более чем на 80%, предпочтительно более чем на 90% или еще более предпочтительно более чем на 95%.
В одном из предпочтительных вариантов осуществления изобретения цепь 2 Fe1 d1 содержит или в другом варианте состоит из последовательности SEQ ID NO:23, SEQ ID NO:25 или SEQ ID NO:26 или гомологичной ей последовательности, где гомологичная последовательность идентична SEQ ID NO:23, SEQ ID NO:25 или SEQ ID NO:26 более чем на 80%, предпочтительно более чем на 90% и еще более предпочтительно более чем на 95%.
В одном из предпочтительных вариантов осуществления изобретения белок Fe1 d1 представляет собой рекомбинантный белок Fe1 d1, в котором по меньшей мере одна дисульфидная связь разрушена, предпочтительно путем мутации, более предпочтительно путем консервативной замены, такой как Cys на Ser. Идентифицированы три находящихся внутри цепи дисульфидных мостика, связывающие два пептида во встречающемся в естественных условиях Fe1 d1, т.е. Cys3(1)-Cys73(2), Cys44(1)-48Cys(2) и Cys70(1)-Cys7(2), что позволяет предположить наличие антипараллельной ориентации пептидов Fe1 d1 (Kristensen А. К. и др., Biol Chem 378, 1997, cc.899-908). В одном из предпочтительных вариантов осуществления изобретения разрушают один такой дисульфидный мостик в белке Fe1 d1. В другом предпочтительном варианте осуществления изобретения разрушают два таких дисульфидных мостика в белке Fe1 d1. И еще в одном из предпочтительных вариантов осуществления разрушают все три таких дисульфидных мостика в белке Fe1 d1. В одном из предпочтительных вариантов осуществления изобретения Cys70 цепи 1 либо изымают путем делеции, либо подвергают мутации. В другом предпочтительном варианте осуществления изобретения Cys73 цепи изымают путем делеции или подвергают мутации. В одном из предпочтительных вариантов осуществления изобретения белок Fe1 d1 представляет собой слитый белок, который содержит цепь 1 Fe1 d1 и цепь 2 Fe1 d1, слитые либо непосредственно, либо через спейсер, в которых разрушены все три указанных дисульфидных мостика. В одном из предпочтительных вариантов осуществления изобретения белок Fe1 d1 содержит или в другом варианте состоит из аминокислотной последовательности, представленной в SEQ ID NO:24, 55 или 57, в которой по меньшей мере один, предпочтительно по меньшей мере три, еще более предпочтительно по меньшей мере пять остатков цистеина удалены в результате замены или делеции.
В одном из предпочтительных вариантов осуществления изобретения антиген, предлагаемый в изобретении, содержит или в другом варианте состоит из фрагмента Fe1 d1. Известно, что для проявления иммуногенности не всегда требуется полноразмерный белок и, как правило, белок содержит более одного антигенного эпитопа, т.е. антигенной детерминанты. Может оказаться достаточным, если фрагмент или короткий пептид содержит по меньшей мере одну антигенную детерминанту, которая может иммуноспецифически связываться с антителом или Т-клеточным рецептором в контексте молекулы ГКС. Антигенную детерминанту или детерминанты можно определять многочисленными методами, известными специалисту в данной области. Это можно осуществлять путем сравнительного анализа первичной структуры последовательности и предсказания структуры. Например, можно предсказывать возможные α-спирали, обороты спирали, меж- и внутрицепочечные дисульфидные мостики и т.д., с помощью программы, такой как Rasmol. Можно предсказывать также последовательности, погруженные в молекулу, или последовательности, находящиеся на поверхности молекулы. Последовательности, находящиеся на поверхности молекулы, наиболее вероятно содержат встречающуюся(иеся) в естественных условиях антигенную(ые) детерминанту(ы), и поэтому их можно применять для индукции терапевтических антител. После определения поверхностных пептидов антигенную детерминанту внутри этой последовательности можно определять также, например, методом истощающего мутагенеза (такого как аланинсканирующий мутагенез, Cunningham B.C., Wells J.A., Science 244(4908), 2 июня 1989 г., cc.1081-1085). В целом, метод состоит в следующем: аминокислоты в рассматриваемой последовательности одну за другой заменяют путем мутации на аналин и аминокислоты, замена которых на аланин привела к соответствующему уменьшению связывания с антителом (образовавшемся в ответ на обработку последовательностью дикого типа) или полной потери способности к связыванию, рассматривают как вероятный компонент антигенной детерминанты. Другой метод определения антигенных(ой) детерминант(ы) заключается в создании перекрывающихся пептидов, которые простираются на полноразмерную последовательность Fe1 d1 (Geysen, PNAS, 81, 1984, cc.3998-4002 и Slootstra J. W. и др., Mol. Divers. 1, 1996, cc.87-96).
В одном из предпочтительных вариантов осуществления изобретения антиген, предлагаемый в изобретении, содержит или в другом варианте состоит по меньшей мере из одного, предпочтительно по меньшей мере из двух эпитопов Fe1 d, предпочтительно также по меньшей мере один эпитоп получают из цепи 1 Fe1 d1 и по меньшей мере один эпитоп получают из цепи 2 Fe1 d1.
Реактивные в отношении Т-клеток эпитопы Fe1 d1 картировали в целом белке Fe1 d1, и они известны в данной области техники, например, описаны в US 6120769, четвертый параграф столбца 14, в столбце 130 и 131 US6025162, содержание этих документов включено в настоящее описание в качестве ссылки. В предпочтительном варианте осуществления изобретения Т-клеточный эпитоп Fe1 d1 выбирают из группы, включающей: SEQ ID NO:27-32.
Настоящее изобретение относится также к способу получения композиции, предлагаемой в изобретении, заключающемуся в том, что (а) получают ВПЧ, которая несет по меньшей мере один первый сайт присоединения; (б) получают по меньшей мере один антиген, где антиген представляет собой белок Fe1 d1 или фрагмент Fe1 d1, который несет по меньшей мере один второй сайт присоединения; и (в) объединяют ВПЧ и по меньшей мере один антиген с получением композиции, где по меньшей мере один антиген и ВПЧ связаны с помощью первого и второго сайтов присоединения. В предпочтительном варианте осуществления изобретения получение по меньшей мере одного антигена, т.е. белка Fe1 d1 или фрагмента Fe1 d1, который несет по меньшей мере один второй сайт присоединения, осуществляют с помощью экспрессии, предпочтительно экспрессии в бактериальной системе, предпочтительно в Е.coli. Общепринятые метки, такие как His-метку, Мус-метку, добавляют для облегчения процесса очистки. При применении другого подхода конкретные фрагменты Fe1 d1 длиной не более 50 аминокислот можно получать с помощью химического синтеза.
В одном из предпочтительных вариантах осуществления изобретения ВПЧ, которая несет по меньшей мере один первый сайт присоединения, связывают с Fe1 d1, предлагаемым в изобретении, с помощью по меньшей мере одного второго сайта присоединения по меньшей мере через одну пептидную связь. Ген, кодирующий Fe1 d1, предлагаемый в изобретении, предпочтительно фрагмент Fe1 d1, более предпочтительно фрагмент длиной не более 50 аминокислот, еще более предпочтительно длиной менее 30 аминокислот, лигируют в рамке считывания, либо путем встраивания внутрь, либо предпочтительно с N- или С-концом гена, который кодирует оболочечный белок ВПЧ. Варианты осуществления, касающиеся связывания антигена, предлагаемого в изобретении, с оболочечным белком, его мутантами или фрагментами, с оболочечным белком вируса, описаны в WO 2004/009124 со с.62, строка 20 до с.68, строка 17 и включены в настоящее описание в качестве ссылки.
В одном из предпочтительных вариантов осуществления изобретения фрагмент Fe1 d1 сливают либо с N-, либо с С-концом оболочечного белка, его мутантов или фрагментов РНК содержащего фага АР205. В другом предпочтительном варианте осуществления изобретения слитый белок содержит также спейсер, где спейсер слит с оболочечным белком, его фрагментами или мутантами фага АР205 и фрагментом Fe1 d1.
В одном из предпочтительных вариантов осуществления настоящего изобретения композиция содержит или в другом варианте практически состоит из вирусоподобной частицы, которая несет по меньшей мере один первый сайт присоединения, связанный по меньшей мере с одним Fe1 d1, предлагаемым в изобретении, который несет по меньшей мере один второй сайт присоединения, с помощью по меньшей мере одной ковалентной связи, предпочтительно ковалентной связи, и которая представляет собой непептидную связь. В предпочтительном варианте осуществления настоящего изобретения первый сайт присоединения содержит или предпочтительно представляет собой аминогруппу, предпочтительно аминогруппу остатка лизина. В другом предпочтительном варианте осуществления настоящего изобретения второй сайт присоединения содержит или предпочтительно представляет собой сульфгидрильную группу, предпочтительно сульфгидрильную группу цистеина.
В наиболее предпочтительном варианте осуществления настоящего изобретения по меньшей мере один первый сайт присоединения представляет собой аминогруппу, предпочтительно аминогруппу лизина, а по меньшей мере один второй сайт присоединения представляет собой сульфгидрильную группу, предпочтительно сульфгидрильную группу цистеина.
В одном из предпочтительных вариантов осуществления изобретения Fe1 d1, предлагаемый в изобретении, связывают с ВПЧ с помощью химического перекрестного сшивания, как правило и предпочтительно, с помощью гетеробифункционального перекрестносшивающего агента. В предпочтительных вариантах осуществления изобретения гетеробифункциональный перекрестносшивающий агент содержит функциональную группу, которая может вступать во взаимодействие с предпочтительными первыми сайтами присоединения, т.е. аминогруппой, предпочтительно с остатком(ами) лизина ВПЧ, и дополнительную функциональную группу, которая может вступать во взаимодействие с предпочтительным вторым сайтом присоединения, т.е. сульфгидрильной группой, предпочтительно присущей остатку(ам) цистеина или искусственно добавленной к Fe1 d1, предлагаемому в изобретении, и необязательно также обеспечивать его доступность для реакции путем восстановления. В данной области известно несколько гетеробифункциональных перекрестносшивающих агентов. Они представляют собой предпочтительные перекрестносшивающие агенты SMPH (сукцинимидил-6-[В-малеимидопропионамидо]гексаноат) (фирма Pierce), сульфо-MBS, сульфо-EMCS, сульфо-GMBS, судьфо-SIAB, сульфо-SMPB, сульфо-SMCC, SVSB, SIA и другие перекрестносшивающие агенты, которые выпускаются, например, фирмой Pierce Chemical Company, и они имеют одну функциональную группу, обладающую реакционной способностью в отношении аминогрупп, и одну функциональную группу, обладающую реакционной способностью в отношении сульфгидрильных групп. Все указанные выше перекрестносшивающие агенты приводят к образованию амидной связи после реакции с аминогруппой и тиоэфирной связи с сульфгидрильными группами. Другой класс перекрестносшивающих агентов, которые можно применять для воплощения изобретения на практике, отличается тем, что при сшивании происходит введение дисульфидного мостика между антигеном и ВПЧ. Предпочтительные перекрестносшивающие агенты, принадлежащие к этому классу, представляют собой, например, SPDP и сульфо-LC-SPDP (фирма Pierce).
В предпочтительном варианте осуществления изобретения композиция, предлагаемая в изобретении, дополнительно содержит линкер. Создание второго сайта присоединения в Fe1 d1, предлагаемом в изобретении, осуществляют путем ассоциации линкера, который предпочтительно содержит по меньшей мере одну аминокислоту, пригодную в качестве второго сайта присоединения, предлагаемого в изобретении. Таким образом, в предпочтительном варианте осуществления настоящего изобретения линкер ассоциируют с Fe1 d1, предлагаемым в изобретении, с помощью по меньшей мере одной ковалентной связи, предпочтительно с помощью по меньшей мере одной, как правило, одной пептидной связи. Предпочтительно линкер содержит или в альтернативном варианте состоит из второго сайта присоединения. Предпочтительно линкер содержит или в другом варианте представляет собой второй сайт присоединения. В другом предпочтительном варианте осуществления изобретения линкер содержит сульфгидрильную группу, предпочтительно остатка цистеина. В другом предпочтительном варианте осуществления изобретения аминокислотный линкер представляет собой остаток цистеина.
Выбор линкера должен зависеть от природы Fe1 d1, предлагаемого в изобретении, от его биохимических свойств, таких как pI, распределение заряда и гликозилирование. В целом, предпочтительными являются пластичные аминокислотные линкеры. В другом предпочтительном варианте осуществления настоящего изобретения линкер состоит из аминокислот, предпочтительно также линкер состоит максимум из 25, предпочтительно максимум из 20, более предпочтительно максимум из 15 аминокислот. В предпочтительных вариантах осуществления изобретения линкер выбирают из группы, включающей: (a) CGG; (б) N-концевой линкер гамма 1 (например, CGDKTHTSPP, SEQ ID NO:58); (в) N-концевой линкер гамма 3 (например, CGGPKPSTPPGSSGGAP, SEQ ID NO:69); (г) шарнирные области Ig; (д) N-концевые глициновые линкеры (например, GCGGGG, SEQ ID NO:59); (е) (G)kC(G)n, где n=0-12 и k=0-5; (ж) N-концевые глицин-сериновые линкеры ((GGGGS)n, n=1-3 с одним дополнительным остатком цистеина (например, SEQ ID NO:60, которая соответствует варианту, где n=1); (з) (G)kC(G)m(S)1(GGGGS)n, где n=0-3, k=0-5, m=0-10, l=0-2 (например, SEQ ID NO:61, которая соответствует варианту, где n=1, k=1, l=1 и m=1); (и) GGC; (к) GGC-NH2; (л) С-концевой линкер гамма 1 (например, DKTHTSPPCG, SEQ ID NO:62); (м) С-концевой линкер гамма 3 (например, PKPSTPPGSSGGAPGGCG, SEQ ID NO:63); (н) С-концевые глициновые линкеры (GGGGCG, SEQ ID NO:64); (о) (G)nC(G)k, где n=0-12 и k=0-5; (п) С-концевые глицин-сериновые линкеры ((SGGGG)n, n=1-3 с одним дополнительным остатком цистеина (например, SEQ ID NO:65, которая соответствует варианту, где n=1)); (p) (G)m(S)1(GGGGS)n(G)oC(G)k, где n=0-3, k=0-5, m=0-10, l=0-2 и о=0-8 (например, SEQ ID NO:66, которая соответствует варианту, где n=1, k=1, l=1, o=1 и m=1). В еще одном предпочтительном варианте осуществления изобретения линкер добавляют к N-концу Fe1 d1, предлагаемого в изобретении. В другом предпочтительном варианте осуществления изобретения линкер добавляют к С-концу Fe1 d1, предлагаемого в изобретении.
Предпочтительными линкерами, предлагаемыми в изобретении, являются глициновые линкеры (G)n, дополнительно содержащие остаток цистеина в качестве второго сайта присоединения, такие как N-концевой глициновый линкер (GCGGGG) и С-концевой глициновый линкер (GGGGCG). В других предпочтительных вариантах осуществления изобретения линкеры представляют собой С-концевой глицин-лизиновый линкер (GGKKGC, SEQ ID NO:67) и N-концевой глицин-лизиновый линкер (CGKKGG, SEQ ID NO:68), GGCG, GGC или GGC-NH2 («NH2» обозначает группу, предназначенную для амидирования) на С-конце пептида или CGG на его N-конце. Как правило, глициновые остатки должны быть встроены между имеющими большой объем аминокислотами, а остаток цистеин следует применять в качестве второго сайта присоединения, для того, чтобы избегать возможной стерической помехи, связанной с объемной аминокислотой при реакции сочетания.
В одном из предпочтительных вариантов осуществления изобретения линкер сливают с N-концом белка Fe1 d1 или фрагмента Fe1 d1. В другом предпочтительном варианте осуществления изобретения линкер представляет собой GCGG. В другом предпочтительном варианте осуществления изобретения линкер сливают с С-концом белка Fe1 d1 или фрагмента Fe1 d1. В следующем предпочтительном варианте осуществления изобретения линкер представляет собой GGC. В случае, когда белок Fe1 d1 или фрагмент Fe1 d1 состоит из двух полипептидных цепей, такой белок Fe1 d1 или фрагмент Fe1 d1 имеет два N-конца и два С-конца. Линкер можно сливать как с двумя N-концами, так и с двумя С-концами. Предпочтительно линкер сливают только с одним из двух N-концов или только с одним из двух С-концов.
Связывание Fe1 d1, предлагаемого в изобретении, с ВПЧ с помощью гетеробифункционального перекрестносшивающего агента согласно описанным выше предпочтительным методам позволяет осуществлять сочетание Fe1 d1, предлагаемого в изобретении, с ВПЧ в определенной ориентации. Другие методы связывания Fe1 d1, предлагаемого в изобретении, с ВПЧ, включают методы, при которых Fe1 d1, предлагаемый в изобретении, перекрестно сшивают с ВПЧ с использованием карбодиимида ЭДК (1-этил-3-(3-диметиламинопропил)карбодиимид) и NHS (N-гидроксисукцинимид). Fe1 d1, предлагаемый в изобретении, можно также сначала тиолировать с помощью реакции, например, с SATA, SATP или иминотиоланом. Fe1 d1, предлагаемый в изобретении, после удаления при необходимости защитной группы, затем можно сшивать с ВПЧ с помощью следующего метода. После отделения избытка тиолирующего реагента Fe1 d1, предлагаемый в изобретении, подвергают взаимодействию с ВПЧ, которую предварительно активируют с помощью гетеробифункционального перекрестносшивающего агента, который содержит реактивный остаток цистеина и поэтому несет по меньшей мере одну или несколько функциональных групп, обладающих реакционной способностью в отношении остатков цистеина, с которым тиолированный Fe1 d1, предлагаемый в изобретении, может вступать в указанное выше взаимодействие. Необязательно в реакционную смесь вносят небольшие количества восстановителя. Согласно другим методам Fe1 d1, предлагаемый в изобретении, присоединяют к ВПЧ с помощью гомобифункционального перекрестносшивающего агента, такого как глутаровый альдегид, DSG, ВМ[РЕО]4, BS3, (фирма Pierce) или других известных гомобифункциональных перекрестносшивающих агентов, несущих функциональные группы, которые обладают реакционной способностью в отношении аминогрупп или карбоксильных групп ВПЧ.
В других вариантах осуществления настоящего изобретения композиция содержит или в другом варианте практически состоит из вирусоподобной частицы, связанной с Fe1 d1, предлагаемым в изобретении, посредством химических взаимодействий, где по меньшей мере одно из этих взаимодействий не представляет собой ковалентную связь. Например, связывание ВПЧ с Fe1 d1, предлагаемым в изобретении, можно осуществлять путем биотинилирования ВПЧ и экспрессии Fe1 d1, предлагаемого в изобретении, в виде белка, слитого со стрептавидином.
Одну или несколько молекул антигена, т.е. Fe1 d1, предлагаемого в изобретении, можно присоединять к одной субъединице ВПЧ, предпочтительно из оболочечных белков РНК содержащего фага, предпочтительно через находящиеся на поверхности (презентируемые) остатки лизина ВПЧ из оболочечных белков РНК содержащего фага, если они истерически являются доступными. Специфической особенностью ВПЧ РНК содержащего фага и, в частности, ВПЧ из оболочечного белка фага Qβ, является способность к сочетанию с несколькими антигенами на единицу. Это позволяет получать набор с высокой антигенной плотностью.
В наиболее предпочтительных вариантах осуществления изобретения Fe1 d1, предлагаемый в изобретении, связывают через остаток цистеина, добавленный либо к N-концу, либо к С-концу Fe1 d1, предлагаемого в изобретении, или остаток цистеина, встречающийся в естественных условиях в Fe1 d1, предлагаемом в изобретении, с остатками лизина оболочечных белков ВПЧ РНК содержащего фага и, в частности, оболочечного белка Qβ.
Как описано выше, четыре остатка лизина презентируются на поверхности ВПЧ из оболочечного белка Qβ. Как правило и предпочтительно, эти остатки дериватизируют путем реакции с молекулой перекрестносшивающего агента. В случае, когда не все презентированные остатки лизина можно сшивать с антигеном, остатки лизина, которые прореагировали с перекрестносшивающим агентом, после стадии дериватизации сохраняются в виде, в котором молекула перекрестносшивающего агента присоединена к ε-аминогруппе. Этот приводит к исчезновению одного или нескольких положительных зарядов, что может оказывать отрицательное воздействие на растворимость и стабильность ВПЧ. При создании изобретения установлено, что путем замены некоторых остатков лизина на остатки аргинина, как это описано для мутантов оболочечных белков Qβ, можно препятствовать чрезмерному уменьшению положительных зарядов, поскольку остатки аргинина не вступают во взаимодействие с предпочтительными перекрестносшивающими агентами. Кроме того, замена остатков лизина на остатки аргинина может приводить к получению более правильных наборов антигенов, так как для реакции с антигеном доступно меньшее количество сайтов.
Так, презентированные остатки лизина заменяли остатками аргинина в следующих мутантах оболочечного белка Qβ: Qβ-240 (Lys13-Arg; SEQ ID NO:15), Qβ-250 (Lys 2-Arg, Lys13-Arg; SEQ ID NO:17), Qβ-259 (Lys 2-Arg, Lys16-Arg; SEQ ID NO:19) и Qβ-251; (Lys16-Arg, SEQ ID NO:18). Другим вариантом осуществления изобретения является мутант оболочечного белка Qβ с одним дополнительным остатком лизина, т.е. Qβ-243 (Asn 10-Lys; SEQ ID NO:16), который можно применять для получения набора с более высокой антигенной плотностью.
В одном из предпочтительных вариантов осуществления изобретения ВПЧ, предлагаемую в изобретении, получают рекомбинантно в хозяине, и при этом ВПЧ практически свободна от РНК хозяина, предпочтительно от нуклеиновых кислот хозяина. В следующем предпочтительном варианте осуществления настоящего изобретения композиция содержит также по меньшей мере одну полианионную макромолекулу, связанную, предпочтительно включенную или упакованную в ВПЧ. В еще одном предпочтительном варианте осуществления изобретения полианионная макромолекула представляет собой полиглутаминовую кислоту и/или полиаспарагиновую кислоту.
Практически свободный от РНК (или ДНК) хозяина, предпочтительно нуклеиновых кислот хозяина: Понятие «практически свободный от РНК хозяина, предпочтительно нуклеиновых кислот хозяина» в контексте настоящего описания относится к количеству РНК хозяина, предпочтительно нуклеиновых кислот хозяина, входящему в состав ВПЧ, которое, как правило и предпочтительно, составляет менее 30 мкг, предпочтительно менее 20 мкг, более предпочтительно менее 10 мкг, еще более предпочтительно менее 8 мкг, еще более предпочтительно менее 6 мкг, еще более предпочтительно менее 4 мкг, наиболее предпочтительно менее 2 мкг на 1 мг ВПЧ. Понятие «хозяин» в вышеуказанном контексте относится к хозяину, в котором ВПЧ получают рекомбинантным путем. Общепринятые методы определения количества РНК, предпочтительно нуклеиновых кислот, известны специалисту в данной области. Обычный и предпочтительный метод определения количества РНК, предпочтительно нуклеиновых кислот, предлагаемый в настоящем изобретении, описан в примере 17 РСТ/ЕР2005/055009, поданной 5 октября 2005 г. этим же агентством. Идентичные, сходные или аналогичные условия, как правило и предпочтительно, используют для определения количества РНК, предпочтительно нуклеиновых кислот, в предлагаемых в изобретении композициях, которые содержат ВПЧ, отличные от ВПЧ Qβ. Модификации условий, которые могут потребоваться, известны специалисту в данной области. Следует понимать, что численные значения определенных количеств, как правило и предпочтительно, представляют собой значения с отклонением ±10%, предпочтительно с отклонением ±5% от указанного численного значения.
Полианионная макромолекула: Понятие «полианионная макромолекула» в контексте настоящего описания относится к молекуле с относительно высокой молекулярной массой, которая содержит повторяющиеся отрицательно заряженные группы, структура которых практически состоит из множества повторов единиц, полученных, фактически или умозрительно, из молекул с относительно невысокой молекулярной массой. Полианионная макромолекула должна иметь молекулярную массу по меньшей мере 2000 Да, более предпочтительно по меньшей мере 3000 Да и еще более предпочтительно по меньшей мере 5000 Да. Понятие «полианионная макромолекула» в контексте настоящего описания, как правило и предпочтительно, относится к молекуле, которая не может активировать Толл-подобные рецепторы. Так, понятие «полианионная макромолекула», как правило и предпочтительно, не включает лиганды Толл-подобных рецепторов и еще более предпочтительно не включает иммуностимулирующие субстанции, такие как лиганды Толл-подобных рецепторов, иммуностимулирующие нуклеиновые кислоты и липополисахариды (LPS). Более предпочтительно понятие «полианионная макромолекула» в контексте настоящего описания относится к молекуле, которая может индуцировать производство цитокинов. Еще более предпочтительно понятие «полианионная макромолекула» исключает иммуностимулирующие субстанции. Понятие «иммуностимулирующая субстанция» в контексте настоящего описания относится к молекуле, которая обладает способностью индуцировать и/или усиливать специфический иммунный ответ против антигена, входящего в композицию, предлагаемую в настоящем изобретении.
РНК хозяина, предпочтительно нуклеиновые кислоты хозяина: Понятие «РНК хозяина, предпочтительно нуклеиновые кислоты хозяина» или понятие «РНК хозяина, предпочтительно нуклеиновые кислоты хозяина, имеющие вторичную структуру» в контексте настоящего описания относится к РНК или предпочтительно нуклеиновым кислотам, которые исходно синтезируются в хозяине. Однако РНК, предпочтительно нуклеиновые кислоты, могут подвергаться химическим и/или физическим изменениям в процессе снижения количества или элиминации РНК, предпочтительно нуклеиновых кислот, как правило и предпочтительно, с помощью способов, предлагаемых в изобретении, например размер РНК, предпочтительно нуклеиновых кислот, может быть укорочен или их вторичная структура может быть изменена. Однако полученные таким образом РНК или нуклеиновые кислоты все еще рассматриваются как РНК хозяина или нуклеиновые кислоты хозяина.
Методы определения количества РНК и снижения количества РНК, входящей в ВПЧ, описаны в РСТ/ЕР2005/055009, поданной этим же агентством 5 октября 2005 г., указанная заявка полностью включена в настоящее описание в качестве ссылки. Снижение количества или элиминация РНК хозяина, предпочтительно нуклеиновых кислот хозяина, минимизирует или снижает нежелательные Т-клеточные ответы, такие как воспалительный Т-клеточный ответ и цитотоксический Т-клеточный ответ, и другие нежелательные побочные действия, такие как лихорадка, сохраняя при этом сильный гуморальный иммунный ответ, специфический в отношении Fe1 d1.
Одним из предпочтительных вариантов осуществления изобретения является способ получения композиций, предлагаемых в изобретении, и конъюгата ВПЧ РНК содержащего бактериофага - Fe1 d1, предлагаемого в изобретении, где ВПЧ получают рекомбинантно в хозяине и где ВПЧ практически свободна от РНК хозяина, предпочтительно нуклеиновых кислот хозяина, заключающийся в том, что осуществляют следующие стадии: а) получают рекомбинантно в хозяине вирусоподобную частицу (ВПЧ), которая несет по меньшей мере один первый сайт присоединения, где ВПЧ содержит оболочечные белки, их варианты или фрагменты РНК содержащего бактериофага; (б) «разбирают» вирусоподобную частицу до оболочечных белков РНК содержащего бактериофага, их вариантов или фрагментов; (в) очищают оболочечные белки, их варианты или фрагменты; (г) осуществляют повторную сборку очищенных оболочечных белков РНК содержащего бактериофага, их вариантов или фрагментов с получением вирусоподобной частицы, где вирусоподобная частица практически свободна от РНК хозяина, предпочтительно нуклеиновых кислот хозяина; и (д) связывают по меньший мере один антиген, предлагаемый в изобретении, который несет по меньший мере один второй сайт присоединения, с ВПЧ, полученной на стадии (г). В предпочтительном варианте осуществления изобретения повторную сборку очищенных оболочечных белков, их вариантов или фрагментов осуществляют в присутствии по меньшей мере одной полианионной макромолекулы.
В одном из предпочтительных вариантов осуществления изобретения композиция, предлагаемая в изобретении, содержит также по меньшей мере одну иммуностимулирующую субстанцию, которая обладает способностью индуцировать и/или повышать иммунный ответ. Предпочтительно иммуностимулирующая субстанция представляет собой лиганд Толл-подобного рецептора, предпочтительно выбранный из группы, включающей: (а) иммуностимулирующие нуклеиновые кислоты; (б) пептидогликаны; (в) липополисахариды; (г) липотеихоевые кислоты; (д) имидазохинолиновые производные; (е) флагеллины; (ж) липопротеины; (з) иммуностимулирующие органические молекулы; (и) неметилированные содержащие CpG олигонуклеотиды; и (к) любые смеси субстанций, перечисленных в (а), (б), (в), (г), (д), (е), (ж), (з) и (и).
В еще одном предпочтительном варианте осуществления изобретения иммуностимулирующую нуклеиновую кислоту предпочтительно выбирают из группы, включающей: (а) нуклеиновую кислоту бактериального происхождения; (б) нуклеиновую кислоту вирусного происхождения; (в) нуклеиновую кислоту, содержащую неметилированный мотив CpG; (г) двухцепочечную РНК; (д) одноцепочечную РНК и (ж) нуклеиновую кислоту, не содержащую неметилированный мотив CpG. Иммуностимулирующие нуклеиновые кислоты, которые не содержат неметилированный мотив CpG, известны из существующего уровня техники, например, описаны в WO 01/22972. Понятие «нуклеиновая кислота» в контексте настоящего описания относится к молекуле, состоящей из линейно ковалентно связанных мономеров (нуклеотидов). Оно относится к молекулярной цепи нуклеотидов и не касается конкретной длины продукта. Так, олигонуклеотиды подпадают под понятие «нуклеиновая кислота». Связь между нуклеотидами, как правило и предпочтительно, представляет собой фосфодиэфирную связь. Под объем настоящего изобретения подпадают также нуклеиновые кислоты, содержащие модификации связей, например фосфотиоатную связь.
В одном из предпочтительных вариантов осуществления изобретения иммуностимулирующую субстанцию смешивают с рекомбинантной ВПЧ. В другом предпочтительном варианте осуществления изобретения иммуностимулирующую субстанцию связывают, предпочтительно упаковывают внутрь ВПЧ, предлагаемой в изобретении.
Подробные описания иммуностимулирующей субстанции, прежде всего иммуностимулирующей нуклеиновой кислоты, более конкретно олигонуклеотидов, содержащих неметилированный CpG, представлены в WO 03/024480, 03/024481 и РСТ/ЕР/04/003165. Методы смешения иммуностимулирующих субстанций с комплексом ВПЧ-антиген, описаны в WO 03/024480. Методы упаковки иммуностимулирующих субстанций внутрь ВПЧ описаны в WO 03/024481. Полное содержание заявок WO 03/024480, 03/024481 и РСТ/ЕР/04/003165 включено в настоящее описание в качестве ссылки. ВПЧ может, как правило, индуцировать и/или усиливать иммунную систему. Однако понятие «иммуностимулирующая субстанция» в контексте настоящего описания относится к иммуностимулирующей субстанции, которая не представляет собой ВПЧ, которую применяют в композициях, предлагаемых в изобретении, а относится к субстанции, добавляемой к ВПЧ.
Введение иммуностимулирующих субстанций, предпочтительно иммуностимулирующих нуклеиновых кислот, в композицию, предлагаемую в изобретении, может сдвигать иммунные ответы в сторону Th1-ответов и тем сам подавлять Th2-ответы.
Одним из объектов изобретения является вакцина, которая содержит композицию, предлагаемую в изобретении. Другим объектом изобретения является вакцина, которая содержит композицию, предлагаемую в изобретении, и приемлемый буфер. В одном из предпочтительных вариантов осуществления изобретения в состав вакцины входит также по меньшей мере один адъювант. Введение по меньшей мере одного адъюванта можно осуществлять до, одновременно или после введения композиции, предлагаемой в изобретении. Понятие «адъювант» в контексте настоящего описания относится к неспецифическим стимуляторам иммунного ответа или субстанциям, которые обеспечивают образование депо в хозяине, и при объединении с вакциной и фармацевтической композицией соответственно, предлагаемыми в настоящем изобретении, могут еще в большей степени усиливать иммунный ответ.
В другом предпочтительном варианте осуществления изобретения в состав вакцины не входит адъювант. Важной особенность настоящего изобретения является высокая иммуногенность композиции, даже в отсутствии адъювантов. Отсутствие адъювантов может снижать возможность возникновения побочных действий, связанных с применением адъювантов. Таким образом, введение вакцины, предлагаемой в изобретении, пациенту предпочтительно осуществляют без введения по меньшей мере одного адъюванта этому пациенту до, одновременно или после введения вакцины.
В изобретении предложен также способ иммунизации, заключающийся в том, что человеку или млекопитающему кроме человека, такому как собака или кошка, вводят вакцину, предлагаемую в настоящем изобретении. Не ограничивая объем настоящего изобретения какой-либо теорией, инъекция композиции вакцины, предлагаемой в изобретении, кошке может нейтрализовать Fe1 d1 и снизить тем самым количество Fe1 d1 в кошачьей слюне.
Вакцину можно вводить различными хорошо известными в данной области путями, но, как правило, ее вводят путем инъекции, инфузии, ингаляции, орально или с использованием других пригодных физических методов. Альтернативно этому конъюгаты можно вводить внутримышечно, внутривенно, через слизистую, чрескожно, интраназально, внутрибрюшинно или подкожно. Компонентами конъюгатов, предназначенных для введения, являются стерильные водные (например, физиологические растворы) или неводные растворы и суспензии. Примерами неводных растворителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, и пригодные для инъекции органические сложные эфиры, такие как этилолеат. Для повышения способности проникать через кожу и повышения абсорбции антигена можно применять носители или окклюзионные повязки.
Считается, что вакцины, предлагаемые в изобретении, являются «фармакологически приемлемыми», если при их введении они переносятся конкретным реципиентом. Кроме того, вакцины, предлагаемые в изобретении, следует вводить в «терапевтически эффективном количестве» (т.е. в количестве, которое вызывает требуемое терапевтическое действие). Природа или тип иммунного ответа не имеет решающего значения в контексте настоящего описания. Не ограничивая объем настоящего изобретения следующим механистическим объяснением, можно считать, что вакцина, предлагаемая в изобретении, может индуцировать антитела, преимущественно IgG-подтипов, которые связываются с Fe1 d1, и тем самым предупреждают распознавание Fe1 d1 в результате связывания IgE с тучными клетками и базофилами. Альтернативно или одновременно композиция, предлагаемая в настоящем изобретении, сдвигает иммунные ответы в сторону Th1-ответов, подавляя развитие Th2-ответов, и, как следствие, производство антител типа IgE, которые являются основным компонентом аллергических реакций.
Одним из объектов изобретения является фармацевтическая композиция, содержащая композицию, предлагаемую в настоящем изобретении, и приемлемый фармацевтический носитель. Когда вакцину, предлагаемую в изобретении, вводят индивидууму, она может находиться в форме, которая содержит соли, буферы, адъюванты или другие субстанции, которые требуются для повышения эффективности конъюгата. Примеры материалов, которые можно применять для приготовления фармацевтических композиций, даны в многочисленных справочниках, включая remington's pharmaceutical sciences (под ред. Osol А, изд-во Mack Publishing Co., 1990).
Изобретение относится к получению композиции, предлагаемой в изобретении, заключающемуся в том, что осуществляют следующие стадии: (а) получают коровую частицу, которая несет по меньшей мере один первый сайт присоединения, где коровая частица представляет собой вирусоподобную частицу или вирусную частицу; (б) получают по меньшей мере один антиген, который несет по меньшей мере один второй сайт присоединения, где по меньшей мере антиген представляет собой белок Fe1 d1 или фрагмент Fe1 d1, и (в) объединяют коровую частицу и по меньшей мере один антиген с получением композиции, где по меньшей мере один антиген и коровая частица связаны через первый и второй сайты присоединения.
В другом варианте осуществления изобретения стадия получения коровой частицы, которая несет по меньшей мере один первый сайт присоединения, предусматривает, что осуществляют следующие дополнительные стадии: (а) «разбирают на части» коровую частицу до оболочечных белков, их мутантов или фрагментов; (б) очищают оболочечные белки, их мутанты или фрагменты; (в) осуществляют повторную сборку очищенных оболочечных белков, их мутантов или фрагментов коровой частицы, где коровая частица практически свободна от РНК хозяина, предпочтительно нуклеиновых кислот хозяина. В еще одном предпочтительном варианте осуществления изобретения повторную сборку очищенных коровых белков осуществляют в присутствии по меньшей мере одной полианионной макромолекулы или по меньшей мере одной иммуностимулирующей нуклеиновой кислоты.
Одним из объектов изобретения является способ применения композиций, предлагаемых в изобретении, для предупреждения и/или лечения аллергии на кошек у млекопитающего, где предпочтительно млекопитающее представляет собой человека или собаку.
Еще одним объектом изобретения является применение композиции, предлагаемой в изобретении, в качестве лекарственного средства. Другим объектом изобретения является применение композиции, предлагаемой в изобретении, для приготовления лекарственного средства, предназначенного для лечения аллергии на кошек у млекопитающего, где предпочтительно млекопитающее представляет собой человека или собаку.
Следующим объектом изобретения является слитый белок Fe1 d1, который содержит цепь 1 Fe1 d1 и цепь 2 Fe1 d1, слитые через аминокислотный спейсер, который связывает N-конец одной цепи с С-концом другой цепи, где аминокислотный спейсер состоит из аминокислотной последовательности длиной 10-30, предпочтительно 10-25, предпочтительно 10-20, предпочтительно 13-20, предпочтительно 15-20, предпочтительно 13-17, предпочтительно 15-17 аминокислотных остатков, и где слитый белок не представляет собой слитый белок, который содержит цепь 1, имеющую последовательность SEQ ID NO:22, слитую через (GGGGS)3 с N-концом цепи 2, которая имеет последовательность SEQ ID NO:23, 25 или 26, и где этот слитый белок, не подпадающий под объем формулы изобретения, экспрессируют в бакуловирусной системе экспрессии.
В WO 2004/094639 описан слитый белок Fe1 d1, полученный в результате связывания цепи 1 и цепи 2 с помощью линкера, выбранного из связи типа углерод-азот и короткого пептида, т.е. имеющего от 1 до 9, предпочтительно от 1 до 5, особенно предпочтительно от 1 до 3 аминокислот. При создании изобретения также неожиданного установлено, что связь или короткий пептид не индуцирует заметное конформационное ограничение или отсутствие складчатости. Однако в WO 2004/094639 не описан линкер, состоящий более чем из 9 аминокислот.
В WO 00/20032 описан экспрессируемый в бакуловирусе рекомбинантный Fe1 d1, который содержит цепь 1 и цепь 2, экспрессируемые в виде серий и связанные друг с другом глицин/сериновым линкером (GGGGS)3. В WO 00/20032 описано также, что иммунореактивность rFe1 d1 в отношении антител типа IgG и IgE резко повышается при экспрессии аллергена в бакуловирусе по сравнению с экспрессией аллергена в Е.coli.
Слитый белок Fe1 d1, предлагаемый в изобретении, можно получать либо в прокариотической системе экспрессии, либо в эукариотической системе экспрессии, такой как бакуловирус. В одном из предпочтительных вариантов осуществления изобретения слитый белок Fe1 d1, предлагаемый в изобретении, получают в Е.coli.
В одном из предпочтительных вариантов осуществления изобретения спейсер, входящий в слитый белок Fe1 d1, предлагаемый в изобретении, состоит из аминокислотной последовательности, которая несет 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 или 20 аминокислотных остатков.
В одном из предпочтительных вариантов осуществления изобретения спейсер, входящий в слитый белок Fe1 d1, состоит из аминокислотной последовательности, несущей 2, 3 или 4 повтора GGGGS.
В одном из предпочтительных вариантов осуществления изобретения цепь 2 Fe1 d1 представляет собой N-концевой слитый белок, предлагаемый в изобретении.
В другом предпочтительном варианте осуществления изобретения цепь 1 Fe1 d1 представляет собой N-концевой слитый белок, предлагаемый в изобретении. В одном из предпочтительных вариантов осуществления изобретения слитый белок, предлагаемый в изобретении, получают в Е.coli. В одном из наиболее предпочтительных вариантов осуществления изобретения слитый белок Fe1 d1, предлагаемый в изобретении, содержит аминокислотную последовательность, выбранную из группы, включающей: (a) SEQ ID NO:54; (б) SEQ ID NO:55; и (в) SEQ ID NO:57. Изобретение относится также к нуклеотидной последовательности, которая кодирует слитый белок Fe1 d1, предлагаемый в изобретении. В одном из предпочтительных вариантов осуществления изобретения нуклеотидную последовательность, которая кодирует слитый белок, предлагаемый в изобретении, выбирают из группы, включающей: (a) SEQ ID NO:54; (б) SEQ ID NO:55; и (в) SEQ ID NO:57. В одном из предпочтительных вариантов осуществления изобретения слитый белок Fe1 d1, предлагаемый в изобретении, получают в Е.coli. В другом предпочтительном варианте осуществления изобретения слитый белок Fe1 d1, предлагаемый в изобретении, содержит или в другом варианте состоит из аминокислотной последовательности SEQ ID NO:57, где слитый белок, предлагаемый в изобретении, получают в Е.coli.
Одним из объектов изобретения является применения слитого белка Fe1 d1, предлагаемого в изобретении, для диагностики и лечения аллергии на кошек.
Примеры
Пример 1
Получение ВПЧ Qβ, предлагаемых в изобретении, путем разборки на части/повторной сборки в присутствии различных полианионных макромолекул, что приводит к повторной сборке ВПЧ Qβ
(А) Разборка на части известных из прототипов ВПЧ Qβ
45 мг известных из прототипов ВПЧ Qβ (2,5 мг/мл, как установлено методом Брэдфорда) в ЗФР (20 мМ фосфат, 150 мМ NaCl, pH 7,5), очищенных из лизата Е.coli, восстанавливали с использованием 10 мМ ДТТ в течение 15 мин при комнатной температуре в условиях перемешивания. Затем добавляли хлорид магния до конечной концентрации 0,7М и инкубирование продолжали в течение 15 мин при комнатной температуре в условиях перемешивания, что приводило к осаждению инкапсулированной РНК клеток-хозяев. Раствор центрифугировали в течение 10 мин при 4000 об/мин при 4°С (центрифугу Эппендорфа 5810 R с фиксированным углом ротора А-4-62 использовали на всех последующих стадиях) для удаления осажденной РНК из раствора. Супернатант, содержащий высвободившийся димерный оболочечный белок Qβ, применяли для хромато графической очистки.
(Б) Очистка оболочечного белка Qβ с помощью катионообменной хроматографии и гель-фильтрации
Супернатант, полученный в результате реакции разборки на части, который содержит димерный оболочечный белок, белки клетки-хозяина и оставшуюся РНК клетки-хозяина, разбавляли в соотношении 1:15 водой, доводя проводимость до уровня ниже 10 мС/см, и вносили на SP-сефарозную FF-колонку (xk16/20, 6 мл, фирма Amersham Bioscience). Предварительно колонку уравновешивали 20 мМ натрий-фосфатным буфером, рН 7. Элюирование связанного оболочечного белка осуществляли с помощью ступенчатого градиента до 20 мМ фосфата натрия/500 мМ хлорида натрия и белок собирали, получая фракцию, объемом примерно 25 мл. Хроматографию осуществляли при комнатной температуре со скоростью потока 5 мл/мин и абсорбцию оценивали при 260 нм и 280 нм.
На второй стадии выделенный оболочечный белок Qβ (фракция, элюированная из катионообменной колонки) вносили (два погона) на сефакриловую S-100 HR-колонку (xk26/60, 320 мл, фирма Amersham Bioscience), уравновешенную 20 мМ фосфатом натрия/250 мМ хлоридом натрия; рН 6,5. Хроматографию осуществляли при комнатной температуре при скорости потока 2,5 мл/мин и абсорбцию оценивали при 260 нм и 280 нм. Собирали фракции объемом 5 мл.
(B1) Повторная сборка ВПЧ Qβ путем диализа
Очищенный оболочечный белок Qβ (2,2 мг/мл в 20 мМ натрий-фосфатном буфере, рН 6,5), одну полианионную макромолекулу (2 мг/мл в воде), мочевину (7,2М в воде) и ДТТ (0,5М в воде) смешивали до конечных концентраций 1,4 мг/мл оболочечного белка, 0,14 мг/мл соответствующей полианионной макромолекулы, 1М мочевина и 2,5 мМ ДТТ. Смеси (по 1 мл каждой) подвергали диализу в течение 2 дней при 5°С в 20 мМ Трис×HCl, 150 мМ NaCl, рН 8, используя мембрану, отсекающую молекулярную массу 3,5 кДа. Полианионные макромолекулы представляли собой: полигалактуроновую кислоту (25000-50000, фирма Fluka), сульфат декстрана (ММ 5000 и 10000, фирма Sigma), поли-L-аспарагиновую кислоту (ММ 11000 и 33400, фирма Sigma), поли-L-глутаминовую кислоту (ММ 3000, 13600 и 84600, фирма Sigma) и тРНК из пекарских дрожжей и зародыша пшеницы.
(B2) Повторная сборка ВПЧ Qβ путем диафильтрации (сочетание диализа с фильтрацией)
33 мл очищенного оболочечного белка Qβ (1,5 мг/мл в 2 мМ натрий-фосфатной буфере, рН 6,5, 250 мМ NaCl) смешивали с водой и мочевиной (7,2М в воде), NaCl (5M в воде) и поли-L-глутаминовой кислотой (2 мг/мл в воде, ММ: 84600). Объем смеси составлял 50 мл, а конечные концентрации компонентов были следующие: 1 мг/мл оболочечного белка, 300 мМ NaCl, 1,0М мочевина и 0,2 мг/мл поли-L-глутаминовой кислоты. Затем смесь подвергали диафильтации при комнатной температуре в противотоке 500 мл 20 мМ Трис×HCl, рН 8, 50 мМ NaCl, применяя скорость поперечного потока 10 мл/мин и скорость проникающего потока 2,5 мл/мин, в устройстве для фильтрации с тангенциальным потоком с использованием мембранного картриджа Pellicon XL (Biomax 5K, фирма Millipore).
Пример 2
Сборка in vitro ВПЧ АР205
(А) Очистка оболочечного белка АР205
Разборка на части: 20 мл раствора ВПЧ АР205 (1,6 мг/мл в ЗФР, очищенных из экстракта Е.coli) смешивали с 0,2 мл 0,5М ДТТ и инкубировали в течение 30 мин при комнатной температуре. Добавляли 5 мл 5M NaCl и затем смесь инкубировали в течение 15 мин при 60°С, что приводило к осаждению восстановленных с помощью ДТТ оболочечных белков. Мутную смесь центрифугировали (ротор Sorvall SS34, 10000×g, 10 мин, 20°С) и супернатант отбрасывали, а дебрис диспергировали в 20 мл смеси 1М мочевина/20 мМ Na-цитрат, рН 3,2. После перемешивания в течение 30 мин при комнатной температуре значение рН дисперсии доводили до 6,5, добавляя 1,5М Na2HPO4, a затем центрифугировали (ротор Sorvall SS34, 10000×g, 10 мин, 20°С) для получения супернатанта, содержащего димерный оболочечный белок.
Катионообменная хроматография; Супернатант (см. выше) разбавляли 20 мл воды, доводя проводимость примерно до 5 мС/см. Образовавшийся раствор вносили на колонку, заполненную 6 мл SP сефарозы FF (фирма Amersham Bioscience), которую предварительно уравновешивали 20 мМ натрий-фосфатным буфером, рН 6,5. После внесения образцов колонку промывали 48 мл 20 мМ натрий-фосфатного буфера, рН 6,5, а затем элюировали связанный оболочечный белок с помощью линейного градиента до 1М NaCl, взятого в объеме, равном 20 объемам колонки. Фракции основного пика объединяли и анализировали с помощью ДСН-ПААГ и анализировали УФ-спектроскопией. Согласно данным ДСН-ПААГ выделенный оболочечный белок был практически очищенным от других белковых загрязнителей. Согласно данным УФ-спектроскопии концентрация белка составляла 0,6 мг/мл (общее количество 12 мг), принимая, что 1 единице А280 соответствует 1,01 мг/мл оболочечного белка АР205. Кроме того, соотношение уровня А280 (0,5999) и уровня А260 (0,291) составляет примерно 2, это свидетельствует о том, что препарат практически свободен от нуклеиновых кислот.
(Б) Сборка ВПЧ АР205
Сборка без какой-либо полианионной макромолекулы: Указанную выше элюированную белковую фракцию подвергали диафильтрации и концентрировали с помощью TFF до достижения концентрации белка 1 мг/мл в 20 мМ натрий-фосфатном буфере, рН 6,5. 500 мкл этого раствора смешивали с 50 мкл 5М раствора NaCl и инкубировали в течение 48 ч при комнатной температуре. Образование повторно собранных ВПЧ в смеси подтверждали с помощью невосстанавливающего ДСН-ПААГ и ЖХВР-гель-фильтрации. Для ЖХВР-анализа применяли колонку TSKgel G5000 PWXL (фирмы Tosoh Bioscience), уравновешенную 20 мМ фосфатом натрия, 150 мМ NaCl рН 7,2.
Сборка в присутствии полиглутаминовой кислоты; 375 мкл очищенного оболочечного белка АР205 (1 мг/мл в 20 мМ натрий-фосфатном буфере, рН 6,5) смешивали с 50 мкл маточного раствора NaCl (5M в воде), 50 мкл маточного раствора полиглутаминовой кислоты (2 мг/мл в воде, ММ: 86400, фирма Sigma) и 25 мкл воды. Смесь инкубировали в течение 48 ч при комнатной температуре. Образование повторно собранных ВПЧ в смеси подтверждали с помощью невосстанавливающего ДСН-ПААГ и ЖХВР-гель-фильтрации. Оболочечный белок, присутствующий в смеси, практически полностью был включен в ВПЧ, что свидетельствует о более высокой эффективности сборки по сравнению со сборкой оболочечного белка АР205 без какой-либо полианионной макромолекулы.
Пример 3
Клонирование слитых белков Fe1 d1
Гены, кодирующие цепь 1 и цепь 2 Fe1 d1 соответственно, получали путем ПЦР-амплификации с использованием перекрывающихся ПЦР-праймеров согласно описанному ниже методу. «Прямой» (F) и «обратный» (R) праймеры представлены ниже. Фрагменты встраивали путем лигирования в вектор pCRII-ТОРО (фирма Invitrogen) и трансформировали им штамм XL1-Blue.
Подтверждали последовательность вставок цепи 1 и цепи 2 Fe1 d1.
Последовательность праймера 1F: SEQ ID NO:34;
последовательность праймера 2R: SEQ ID NO:35;
последовательность праймера 3F: SEQ ID NO:36;
последовательность праймера 4R: SEQ ID NO:37;
последовательность праймера 5F: SEQ ID NO:38;
последовательность праймера 6R: SEQ ID NO:39;
последовательность праймера 7F: SEQ ID NO:40;
последовательность праймера 8R: SEQ ID NO:41;
последовательность праймера 9F: SEQ ID NO:42;
последовательность праймера 10R: SEQ ID NO:43.
Слитые конструкции Fe1 d1:
Обозначение «FELD1» относится к белку, цепь 2 которого на N-конце слита непосредственно с цепью 1. Нуклеотидные последовательности, кодирующие FELD1, создавали путем ПЦР с удлинением посредством сплайсингового перекрытия (SOE) с использованием праймерного линкера 11 (SEQ ID NO:44).
Обозначение «FD12» относится к белку, цепь 1 которого на N-конце непосредственно слита с цепью 2. Нуклеотидную последовательность, кодирующую FD12, создавали путем ПЦР с удлинением посредством сплайсингового перекрытия (SOE) с использованием праймеров 12-1 (SEQ ID NO:45), 12-3 (SEQ ID NO:46) и 12-2-1 (SEQ ID NO:47).
Обозначения «FELD1-10аа» и «FELD1-15aa» относятся к белкам, цепь 2 которых на N-концах слита через состоящий из 10 (GGGGS)2 или 15 аминокислот (GGGGS)3 аминокислотный спейсер соответственно с цепью 1 на С-конце. Плазмиду, содержащую нуклеотидную последовательность, которая кодирует FELD1, применяли в качестве матрицы для создания состоящего из 10 аминокислот или 15 аминокислот спейсера путем мутагенеза на основе обратной ПЦР (ОПЦРМ). Для спейсера 1-15 использовал два праймера (праймер 1-10аа, SEQ ID NO:48 и праймер 2-5аа, SEQ ID NO:49). Для спейсера 1-10 использовали два праймера (праймер 1-5аа, SEQ ID NO:50 и праймер 2-5аа). Образовавшийся ПЦР-фрагмент замыкали путем лигирования. Он обладает устойчивостью к расщеплению Dpn I, которая представляет собой единственную рестриктазу, распознающую последовательность, которая содержит метилированный аденин, в то время как плазмидная матрица расщепляется Dpn I.
Обозначения «FD12-10aa» и «FD12-15aa» относятся к белкам, цепь 1 которых на N-конце слита через состоящий из 10 (GGGGS)2 или 15 аминокислот (GGGGS)3 аминокислотный спейсер соответственно с цепью 2 на С-конце. Слияние FD12-10aa и FD12-15aa осуществляли аналогично описанному выше методу. Для состоящего из 15 аминокислот спейсера использовали праймер FD2-10аа (SEQ ID NO:51) и праймер FD1-5aa (SEQ ID NO:52). Для состоящего из 10 аминокислот спейсера использовали праймеры FD1-5aa и FD2-5aa (SEQ ID NO:53).
Пример 4
Экспрессия в бактериях и очистка меченных с помощью His слитых белков Fe1 d1
Нуклеотидные последовательности, которые кодируют различные слитые конструкции Fe1 d1, описанные в примере 3, субклонировали в основанной на Т7 экспрессионной системе рЕТ-42Т(+), которая является модификацией плазмиды рЕТ-42а(+) (фирма Novagen). С-конец слитых конструкций сливали с последовательностью His-метки, за которой был расположен GGC, т.е. аминокислотный линкер, содержащий цистеин в качестве второго сайта присоединения. Образовавшиеся конструкции обозначали, добавляя на конце «-НС».
FELD1-HC, FELD1-10aa-HC и FELD1-15aa-HC и FD12-15aa-HC экспрессировали и очищали следующим образом: Плазмидой трансформировали штамм BL21(DE3). Экспрессию индуцировали, добавляя к культуре 1 мМ ИПТГ (изопропилтиогалактозид) при ОП600, составляющей примерно 1. Культуру выращивали в течение еще 20 ч при 20°С, собирали и лизировали обработкой ультразвуком в нативном буфере для лизиса (50 мМ NaH2PO4, 300 мМ NaCl, 10 мМ имидазол, рН 8,0). Объем осветленного бактериального лизата доводили до 50 мл нативным буфером для лизиса. Добавляли 5 мл содержащей никель-нитрилоукусусную кислоту (Ni-NTA) агарозу (фирма Qiagen) и лизат инкубировали путем переворачивания в течение 1 ч при 4°С. Неспецифические связанные белки удаляли путем 4-кратной отмывки буфером для лизиса. Связанный белок элюировали путем ресуспендирования Ni-NTA-агарозой и 2 мл буфера для элюции (50 мМ NaH2PO4, 300 мМ NaCl, 250 мМ имидазол, рН 8,0).
Пример 5
Окислительная укладка дисульфидных мостиков в очищенных слитых белках Fe1 d1
Очищенный с помощью Ni2+-аффинной хроматографии FELD1-HC состоит из различных видов с молекулярной массой от 15 до 20 кДа. Для нативной укладки FELD1-HC использовали внутримолекулярную повторную перестановку (решуффлинг) дисульфидных связей окисленным глутатионом (GSSG, фирма Applichem) и восстановленным глутатионом (GSH, фирма Applichem) при молярном соотношении 1:1. Реакцию осуществляли в течение 24 ч сразу после элюции FELD1 в буфере для элюции путем добавления 2,5 мМ GSSG и 2,5 мМ GSH при комнатной температуре. После повторной укладки FELD1-HC характеризуется одной полосой, соответствующей молекулярной массе 15 кДа в невосстанавливающих условиях (фиг.1, первая панель, полоса 2). Потенциально свободные сульфгидрильные группы FELD1-HC алкилировали йодацетамидом (фирма Sigma). Зонды обрабатывали 5 мМ йодацетамидом в 20 мМ бикарбонате аммония при рН 8,0 в течение 15 мин при комнатной температуре.
Повторно уложенный FELD1-HC дополнительно очищали до гомогенного состояния с помощью гель-фильтрации (SEC) (Superdex 75 пг, фирма Amersham Pharmacia Biosciences) при уравновешивании в ЗФР.
FELD1-10аа-НС и FELD1-15аа-НС ренатурировали практически аналогично описанному выше методу (фиг.1, две средние панели).
Для нативной укладки FD12-15аа-НС также использовали повторную перестановку (решуффлинг) дисульфидных связей окисленным глутатионом и восстановленным глутатионом при молярном соотношении 1:1. После элюции FD12-15aa разводили двадцатикратно в буфере для повторной укладки FD12-15аа (50 мМ Tris-Cl рН 8,5, 240 мМ NaCl, 10 мМ KCl, 1 мМ ЭДТК, 0,05% ПЭГ-3550, 1 мМ GSH, 0,1 мМ GSSH) и инкубировали при 4°С в течение 24 ч. После повторной укладки FD12-15aa характеризуется одной полосой, соответствующей молекулярной массе 20 кДа, по сравнению с восстановленной формой, которой соответствует молекулярная масса 23 кДа (фиг.1, последняя панель).
Пример 6
Слитые белки Fe1 d1 распознаются эпитопспецифическими моноклональными антителами
Связывание слитых белков Fe1 d1 в сравнении с встречающимся в естественных условиях Fe1 d1 (nFe1 d1) с эпитопспецифическими моноклональными антителами (МАт) оценивали с помощью сэндвич-ELISA, используя набор Fe1 d1 ELISA (6F9/3E4) от фирмы Indoor biotechnologies (Кардифф, Великобритания).
В целом, метод состоял в следующем: МАт к Fe1 d1 6F9, поставляемое в виде маточного раствора с концентрацией 2 мг/мл, разводили в соотношении 1:1000 в 50 мМ карбонат-бикарбонатном буфере, рН 9,6. Титрационные микропланшеты сенсибилизировали 100 мкл разведенного МАт 6F9 на лунку при 4°С в течение ночи. Планшеты отмывали трижды ЗФР-0,05% Твин-20 (ЗФР-Т) и затем блокировали 100 мкл блокирующего буфера (1% БСА (фирма Sigma) в ЗФР-Т). Затем титрационные микропланшеты инкубировали в течение 1 ч с 100 мкл слитых белков Fe1 d1 или стандарта nFe1 d1 (фирма Indoors technologies; Великобритания), используя с дублированием разведения от 80 до 0,16 нг/мл. Стандартный (референс) образец nFe1 d1 создавали в качестве подстандарта из CBER-стандарта из перхоти кошек Е10, который содержал 13,47 ед./мл Fe1 d1 (1 единица = 4 мг белка).
Затем планшеты отмывали и добавляли по 100 мкл разведенного (1:1000 в 1% БСА/ЗФР-Т) биотинилированного МАт к Fe1 d1 3E4 и инкубировали в течение 1 ч при комнатной температуре. Планшеты отмывали трижды ЗФР-Т, используя по 100 мкл разведенного конъюгата (1:1000 в 1% БСА/ЗФР-Т) стрептавидин-пероксидаза (фирма Sigma, S5512, 0,25 мкг восстановленного в 1 мл дистиллированной воды). После инкубации в течение 30 мин при комнатной температуре лунки отмывали трижды ЗФР-Т. Обнаружение осуществляли с помощью раствора субстрата OPD и 5%-ной H2SO4 в качестве стоп-раствора. Абсорбцию оценивали с помощью ELISA-ридера (фирма BioRad) при 450 нм и для расчета среднеарифметических значений и стандартного отклонения среднего значения (СКО) использовали программу EXCEL (MS Office; фирма Microsoft). Результаты представлены в таблице 1. Таким образом, распознавание слитых белков Fe1 d1 и nFe1 d1 эпитопспецифическими МАт отражает высокое сходство антигенности обоих белков.
| Таблица 1 | ||||
| Изучаемые белки | FELD1-HC | FELD1-10aa-НС | FELD1-15aa-НС | Встречающийся в естественных условиях Fe1 d1 |
| Fe1 d1 (нг/мл) при ОП50% | 8,4 | 6,7 | 7,9 | 7,2 |
Пример 7
Сочетание слитых белков Fe1 d1 с ВПЧ из Qβ
Раствор, содержащий 143 мкМ ВПЧ Qβ в HEPES-буфере (20 мМ HEPES, 150 мМ NaCl, pH 7,2), подвергали взаимодействию с 5-кратным молярным избытком (715 мкМ) SMPH (фирма Pierce) в течение 30 мин при 25°С при встряхивании. SMPH получали из 50 мМ маточного раствора в диметилсульфоксиде. Продукты реакции подвергали диализу в противотоке ЗФР с двумя замена в устройстве для диализа с отсечением молекулярной массы 10000 Да (Slide-A-Lyzer, фирма Pierce). Диализ осуществляли при температуре от 4°С до комнатной температуры с использованием более чем 1000-кратного избытка буфера по отношению к реакционной смеси.
Перед сочетанием слитых белков Fe1 d1 с дериватизированной SMPH ВПЧ Qβ инкубировали FELD1, FELD1-10aa, FELD1-15aa и FD12-15aa соответственно, полученные согласно методу, описанному в примере 5, с ТСЕР (трихлорэтилфосфат) (фирма Pierce, Perbio Science) в эквимолярных количествах в течение 30 мин при комнатной температуре.
Добавляли слитые белки Fe1 d1 в 5-кратном молярном избытке к 143 мкМ раствору дериватизированных с помощью SMPH ВПЧ Qβ. Реакционный объем составлял 650 мкл и параллельно осуществляли несколько реакций. Реакционные смеси инкубировали в течение 4 ч при комнатной температуре при встряхивании. После сочетания аликвоты центрифугировали при 16000×g в течение 3 мин при 4° до получения дебриса нерастворенного материала. Супернатанты объединяли в чистые пробирки. Сочетание слитых белков Fe1 d1 с ВПЧ Qβ оценивали с помощью ДСН-ПААГ в восстанавливающих условиях.
Практически аналогично осуществляли сочетание слитых белков Fe1 d1 с повторно собранной ВПЧ Qβ (полученной согласно методу, описанному в примере 1).
Пример 8
Сочетание FELD1, FELD1-15aa и FD12-15aa с HBcAg1-185-Lys
Конструирование HBcAg1-185-Lys, его экспрессия и очистка описаны в целом в примерах 2-5 WO 03/040164. Раствор, содержащий 120 мМ ВПЧ HBcAg1-185-Lys в 20 мМ Hepes, 150 мМ NaCl, pH 7,2, подвергали взаимодействию в течение 30 мин при 25°С на качающемся шейкере с 25-кратным молярным избытком SMPH (фирма Pierce), который получали разведением маточного раствора в ДМСО. Затем реакционный раствор подвергали диализу дважды в течение 2 ч в противотоке 1 л 20 мМ Hepes, 150 мМ NaCl, pH 7,2 при 4°С. Затем полученную после диализа реакционную смесь HBcAg1-185-Lys подвергали взаимодействию с рекомбинантным Fe1 d1, полученным согласно методу, описанному в примере 5. Для реакции сочетания FELD1, FELD1-15aa и FD12-15aa соответственно использовали их двукратный молярный избыток относительно дериватизированной ВПЧ HBcAg1-185-Lys. Реакцию сочетания осуществляли в течение 4 ч при 25°С на качающемся шейкере.
Пример 9
Сочетание FELD1, FELD1-15aa и FD12-15aa с ВПЧ, полученными из АР205
Получение ВПЧ АР205 описано в примерах 1 и 2 WO 2004/007538. Дериватизацию ВПЧ АР205 осуществляли практически аналогично методу получения ВПЧ Qβ, описанному в примере 7. Перед сочетанием слитых белков Fe1 d1 с дериватизированной с помощью SMPH ВПЧ АР205, FELD1, FELD1-15aa и FD12-15aa соответственно, полученные согласно методу, описанному в примере 5, инкубировали с ТСЕР (фирма Pierce, Perbio Science) в эквимолярных количествах в течение 30 мин при комнатной температуре.
Слитые белки Fe1 d1 добавляли в 5-кратном молярном избытке к 143 мкМ раствору дериватизированновых с помощью SMPH ВПЧ АР205. Реакционные смеси инкубировали в течение 4 ч при комнатной температуре при встряхивании.
Сочетание слитых белков Fe1 d1 с повторно собранной ВПЧ АР205 (которую получали согласно методу, описанному в примере 2) осуществляли практически аналогично описанному выше методу.
Пример 10
Получение композиции, предлагаемой в изобретении, на основе бактериофага Qβ
60 л культуры штамма Е.coli AB259 (5×107 клеток/мл) выращивали в течение 2-3 ч при 37°С при интенсивной аэрации (1 объем воздуха/объем культуры/мин), получая культуру с плотностью клеток примерно 2-4×109 клеток/мл. Осуществляли инокуляцию очищенным лизатом фага Qβ с множественностью заражения 5 и добавляли CaCl2 до конечной концентрации 2,2 мМ. После 5-минутной фазы адсорбции аэрацию интенсифицировали (1,5 объема воздуха /объем культуры/ мин). Клетки выращивали в течение еще 3 ч до достижения стабильного значения ОП650 нм, получая 4-6×1012 фаговых частиц в культуре. Их очищали следующим образом. E.coli лизировали, добавляя 10 мл CHCl3 / 1 л культуры, 0,1 мг лизоцима / 1 л культуры и ЭДТК до конечной концентрации 20 мМ. Лизат осветляли путем центрифугирования в проточной центрифуге с охлаждением, для седиментации фаговых частиц использовали сульфат аммония (500 г/л, выход примерно 66% от насыщения). Суспензию сначала сливали и осадок выделяли путем центрифугирования в течение 30 мин на центрифуге типа Janetzki K26, ротор W.R. 6×500 мл при 6000 об/мин или на центрифуге типа Beckman J21 С, ротор JA-10. Дебрис повторно солюбилизировали в NT-буфере (0,15М NaCl, 0,1% триптона) и осветляли центрифугированием. Супернатант осаждали сульфатом аммония (добавляли 500 г/л, примерно 66% от насыщения). Осадок выделяли центрифугированием, повторно солюбилизировали в NT-буфере и осветляли вновь центрифугированием. Фаговые частицы выделяли из образовавшегося супернатанта путем ультрацентрифугирования в течение 3,5 ч, используя ротор типа Beckman 35 при 32000 об/мин. Осажденные фаги повторно суспендировали NT-буфере и очищали ультрацентрифугированием с использованием общепринятого непрерывного градиента CsCl. Центрифугирование осуществляли с использованием ротора типа Beckman Ti-70 (8×38,5) при 55000 об/мин в течение 20 ч. Затем фаговые частицы подвергали диализу в противотоке буфера, содержащего 20 мМ Hepes, 150 мМ NaCl, рН 7,4, который использовали на стадиях химического сшивания согласно методу, описанному в примере 7.
Пример 11
Получение композиции, предлагаемой в изобретении, на основе фага GA
12 л культуры штамма Е.coli Q 13 Hfr RNASse I- в среде М9, содержащей 2% гидролизата казеина, 0,5% дрожжевого экстракта, 0,2% глюкозы, выращивали до достижения значения ОП540 нм 0,6-0,7, что соответствовало примерно 2×108 клеток/мл, и заражали фагом GA с множественностью заражения 10-20. Культуру выращивали в течение еще 2,5-3 ч при 37°С, получая примерно 10 фаговых частиц во всей культуре. Клетки лизировали, добавляя 1-2% об% CHCl3, и инкубировали культуру в течение 15 мин. Лизат осветляли путем центрифугирования в течение 30 мин при 5000 об/мин с использованием ротора типа Janetzi K26. Фаговые частицы осаждали из культуральных сред сульфатом аммония (60% насыщения) в течение нескольких дней при 4°С. Суспензию сначала отбрасывали и осадок выделяли центрифугированием в течение 30 мин при 6000 об/мин с использованием ротора типа Janetzki K26. Дебрис повторно суспендировали в NET-буфере (20 мМ Трис, рН 7,8, 150 мМ NaCl, 5 мМ ЭДТК) и частицы экстрагировали путем нескольких циклов центрифугирования и ресуспендирования в небольших порциях NET-буфера. Объединяли группы, содержащие капсиды, и осаждали 60%-ным сульфатом аммония. Частицы, ресуспендированные в NET-буфере, очищали трижды на колонке, заполненной Сефарозой 4 В, с последующим использованием двух градиентов сахарозы. В целом, для создания градиента приготавливали в центрифужных пробирках 7 мл 50%-ной, 7 мл 43%-ной, 7 мл 36%-ной, 7 мл 29%-ной и 7 мл 22 мас.%-ной сахарозы в NET-буфере. Раствор фага (в NET-буфере) наслаивали на градиент и центрифугировали в течение 17 ч с использованием ротора типа Beckman SW 28 при 25000 об/мин. Содержащие капсиды фракции объединяли и отделяли от сахарозы гель-фильтрацией на колонке, заполненной Сефарозой 4 В. Затем фаговые частицы подвергали диализу в противотоке воды и лиофилизировали для дальнейшего применения.
Условия сочетания слитых белков Fe1 d1 с бактериофагом Qβ или GA практически аналогичны условиям реакции сочетания с ВПЧ Qβ, описанным в примере 7.
Пример 12
Слитые белки Qβ-Fe1 d1 обладают высокой иммуногенностью для мышей
Мышей линии BALB/c иммунизировали подкожно (sc) 50 мкг конъюгата Qβ-FELD1, который получали согласно методу, описанному в примере 7, или 50 мкг Qβ, смешанного с рекомбинантным Fe1 d1 (который получали согласно методу, описанному в примере 5) в дни 0, 14 и 21 и брали образцы крови в дни 0, 21 и 28. Специфические для Fe1 d1 антитела оценивали с помощью ELISA, используя для сенсибилизации FELD1 (10 мкг/мл). В целом метод состоял в следующем: использовали 96-луночный планшет типа F96, который предварительно сенсибилизировали при 4°С в течение ночи 10 мкг/мл FELD1 в 0,1М NaHCO3 рН 9,6. Планшеты отмывали четыре раза ЗФР-Твин 20 и основной уровень снижали путем инкубации планшетов в течение 2 ч при 37°С в блокирующем буфере (2% БСА (фирма Sigma) в ЗФР-Твин 20). Сыворотку разводили буфером для разведения сыворотки (2% БСА, 1% ФТС в ЗФР-Твин 20). Осуществляли последовательные двукратные разведения и инкубировали в течение 2 ч при комнатной температуре на шейкере для ELISA-планшетов. Планшеты отмывали 5 раз и инкубировали с разведенным в соотношении 1:1000 идентифицирующим антителом (антитело к мышиному IgG, конъюгированное с пероксидазой из хрена (HRPO) (фирма Sigma)) в течение 1 ч при комнатной температуре. Планшеты отмывали 5 раз ЗФР-Твин 20 и обнаружение осуществляли с использованием раствора субстрата OPD (0,066M Na2HPO4, 0,035М лимонная кислота, рН 5,0, содержащий 10 мг OPD (фирма Fluka) и 8 мкл 30%-ной Н2О2 (фирма Fluka) на 25 мл) и 5% H2SO4 в Н2О в качестве стоп-раствора. Абсорбцию оценивали с помощью ридера для ELISA при 450 нм и рассчитывали средние арифметические значения и стандартные отклонения (СКО) с помощью программы EXCEL (фирма Microsoft).
Для мышей, иммунизированных Qβ-FELD1, уровень абсорбции, составляющий половину от максимального, был равен 120000 и 75000 в день 21 и день 28 соответственно. В противоположность этому у мышей, иммунизированных не сшитой смесью Qβ/FELD 1, обнаружены более низкие титры, составляющие 7000 и 6000 в день 21 и день 28 соответственно.
Пример 13
Иммунизация мышей с использованием квасцов в качестве адъюванта
7-8-недельных самок мышей линии Balb/c вакцинировали трижды (в день 0, 14 и 28) 50 мкг вакцины, содержащей конъюгат: известная из прототипов ВПЧ Qβ - FELD1-HC. Вакцины разводили в 200 мкл стерильного ЗФР или 100 мкл ЗФР и 100 мкл AluGel-S (фирма Serva) соответственно и вводили подкожно в левую и правую паховую область.
Образцы сыворотки получали в день 14, 21, 28, 42, 56, 84 и 112. Антитела, специфические для встречающегося в естественных условиях Fe1 d1, FELD-HC и ВПЧ Qβ, определяли с помощью ELISA.
Титрационные планшеты сенсибилизировали в течение ночи 1 мкг/мл встречающегося в естественных условиях Fe1 d1 (nFe1 d1, фирма Indoors biotechnologies), 10 мг/мл FELD1-HC и 10 мг/мл ВПЧ Qβ соответственно. После отмывки (0,05% Твин 20/ЗФР) и блокирования 2% БСА в ЗФР, добавляли сыворотку с использованием различных разведении в 2% БСА/1% ФТС/ЗФР.
Затем осуществляли ELISA стандартным методом. Вакцины, содержащие конъюгат ВПЧ Qβ-FELD1-HC, индуцировали пролонгированный высокий специфический в отношении Fe1 d1 гуморальный иммунный ответ на встречающийся в естественных условиях белок и на FELD1. Титр антител оказался выше в присутствии квасцов по сравнению с вариантом без квасов (таблица 2).
| Таблица 2 | ||||
| С квасцами | Без квасцов | |||
| Даты | nFe1 d1 | FELD1-HC | nFe1 d1 | FELD1-HC |
| день 13 | 15984 | 53939 | 3394 | 7871 |
| день 20 | 100311 | 203636 | 38980 | 77323 |
| день 27 | 173190 | 368716 | 38177 | 56836 |
| день 42 | 240173 | 419072 | 88953 | 170377 |
| день 56 | 228500 | 492520 | 65370 | 163093 |
| день 84 | 157009 | 219834 | 59603 | 115049 |
| день 112 | 127745 | 203719 | 62290 | 116132 |
Пример 14
FELD1, сшитый с Qβ, резко снижает аллергенный потенциал in vitro
Для оценки способности Qβ-FELD1-HC запускать аллергическую реакцию in vitro, из крови трех доноров, страдающих аллергией на кошек, выделяли базофилы. У индивидуума, страдающего аллергией на кошек, эти базофилы сенсибилизированы специфическим для Fe1 d1 IgE и реагируют на стимуляцию аллергеном повышающей регуляцией CD63. В связи с вышесказанным базофилы страдающего аллергией индивидуума стимулировали определенными количествами Qβ-FELD1-HC или только FELD1-HC и оценивали с помощью проточной цитометрии повышающую регуляцию CD63. В то время как FELD1-HC (полученный согласно методу, описанному в примере 5) провоцировал повышающую регуляцию CD63 при использовании самого низкого из тестируемых разведении (примерно 0,2 нг/мл), Qβ-FELD1-HC (полученный согласно методу, описанному в примере 7) обладал резко сниженным аллергенным потенциалом и требовалось использовать в 100-1000 раз большие его количества (примерно 70 нг/мл) по сравнению с FELD1-HC для получения аналогичной реакции базофилов.
Тест, аналогичный описанному, повторяли с использованием слитых белков FELD-15aa-HC и FD12-15aa-HC либо индивидуально, либо сшитых с Qβ. Эти результаты представлены на фиг.2. Все указанные слитые белки Fe1 d1, когда они были сшиты с Qβ, обладали резко сниженным аллергенным потенциалом.
Пример 15
FELD1, сшитый с Qβ, не провоцирует инъекционную кожную пробу у страдающего аллергией добровольца
Если аллергены интродуцируют путем инъекции в кожу страдающего аллергией индивидуума, то возникает местный отек в течение примерно 20 мин из-за активации находящихся в коже тучных клеток. В настоящем описании кожную пробу применяли для определения аллергенного потенциала Qβ-FELD1-HC (полученного согласно методу, описанному в примере 7). Определенные количества Qβ-FELD1-HC или соответствующие количества FELD1-HC (полученного согласно методу, описанному в примере 5) интродуцировали в кожу страдающего аллергией на кошек индивидуума и оценивали кожную реакцию через 20 мин. Qβ-FELD1-HC не обладал способностью провоцировать кожную реакцию, в то время как FELD1-HC обладал активностью при использовании в 100 раз более низких концентраций (таблица 3)
| Таблица 3 | ||
| Соответствующие количества FELD1-HC, присутствующие в обоих препаратах | ||
| Разведение | FELD1-HC | Qβ-FELD1-HC |
| неразведенный | +++ | - |
| 1:10 | ++ | - |
| 1:100 | + | - |
| 1:1000 | - | - |
Пример 16
Иммунизация страдающего аллергией индивидуума Qβ-FELD1-HC снижает реактивность инъекционной кожной пробы
Для оценки способности Qβ-FELD-HC облегчать клинические симптомы у пациента, страдающего аллергией на кошек, вакцинировали 17 мкг Qβ-FELD1-НС (полученного согласно методу, описанному в примере 7) в день 0 (3 инъекции по 2, 5 и 10 мкг), 40 мкг в день 7 (3 инъекции по 10, 10 и 20 мкг) и 50 мкг в день 14 (2 инъекции по 10 и 40 мкг). Осуществляли инъекционные кожные пробы с использованием стандартизованного экстракта кошачьего аллергена в день 0, 14 и 21 и количественно оценивали реакцию по диаметру центральной припухлости (фиг.3). Через 3 недели требовались в 1000 раз более высокие концентрации аллергена для индукции клинических симптомов при инъекционной кожной пробе по сравнению с количеством, которое первоначально являлось достаточным для индукции симптома при инъекционной пробе.
Пример 17
Иммунизация страдающего аллергией индивидуума Qβ-FELD1-HC снижает симптомы назальной провокационной пробы
Для оценки способности Qβ-FELD-HC облегчать клинические симптомы пациента, страдающего аллергией на кошек, вакцинировали 17 мкг Qβ-FELD1-HC (полученного согласно методу, описанному в примере 7) в день 0 (3 инъекции по 2, 5 и 10 мкг), 40 мкг в день 7 (3 инъекции по 10, 10 и 20 мкг) и 50 мкг в день 14 (2 инъекции по 10 и 40 мкг). Осуществляли назальные провокационные пробы с использованием стандартизованного экстракта кошачьего аллергена в дни 0, 14 и 21 и клинические симптомы оценивали для каждой из возрастающих доз (фиг.4А) и определяли общий балл аллергии (как показано на фиг.4Б). Через 3 недели требовались в 100-1000 раз более высокие концентрации аллергена для индукции клинических симптомов, и общий балл заметно снижался.
Пример 18
Упаковка иммуностимулирующих нуклеиновых кислот в ВПЧ QB
Разобранный на части и очищенный оболочечный белок Qβ получали согласно методу, описанному в примере 1 (А) и (Б). Повторная сборка: (3-меркаптоэтанол добавляли к 10 мл содержащей димеры фракции до конечной концентрации 10% и добавляли 300 мкл раствора олигодезоксинуклеотида (CpG)20ОрА, содержащего 12,3 нмоля олигонуклеотида. Смесь для повторной сборки сначала подвергали диализу в противотоке 30 мл NET-буфера (20 мМ Трис-HCl, рН 7,8 с 5 мМ ЭДТК и 150 мМ NaCl), содержащему 10% β-меркаптоэтанола, в течение 2 ч при 4°С, а затем подвергали непрерывному диализу со скоростью потока NET-буфера 8 мл/ч в течение 4 дней при 4°С. Затем смесь для повторной сборки обессоливали в противотоке воды путем диализа с шестью заменами буфера (4×100 мл, 2×1 л).
Сочетание слитых белков Fe1 d1 с ВПЧ Qβ, внутри которой упакован CpG, осуществляли практически аналогично методу, описанном в примере 7.
Пример 19
Специфическая для Fe1 d1 сыворотка ингибирует индуцированную слитыми белками Fe1 d1 дегрануляцию базофилов in vitro
Для оценки способности специфических для Fe1 d1 антител типа IgG ингибировать дегрануляцию базофилы индивидуума, страдающего аллергией, стимулировали определенным количеством FELD1-HC или FELD1-15aa-HC, предварительно инкубированным с серийными разведениями понижающихся концентраций IgG, выделенных из кроликов, которые иммунизировали 0Qβ-FELD1-HC. Повышающую регуляцию CD63 оценивали с помощью проточной цитометрии. Антитела к Fe1 d1 типа IgG блокировали индуцируемую Fe1 d1 дегрануляцию во всех тестируемых концентрациях, в то время как контрольный IgG не оказывал никакого действия (таблица 4).
| Таблица 4 | ||
| Образцы | FELD1-HC Процент дегрануляции | FELD1-15aa-HC Процент дегрануляции |
| без IgG | 33 | 33 |
| специфический для Fe1 d1 IgG (200 нг/мл) | 1,9 | 1,6 |
| специфический для Fe1 d1 IgG (100 нг/мл) | 5,2 | 2,1 |
| специфический для Fe1 d1 IgG (50 нг/мл) | 8,2 | 2,3 |
| специфический для Fe1 | 10,6 | 4,2 |
| Образцы | FELD1-HC Процент дегрануляции | FELDl-15aa-HC Процент дегрануляции |
| d1 IgG (25 нг/мл) | ||
| неспецифический IgG | 35 | 29 |
| без стимуляции Fe1 d1 | 1,2 | 1,2 |
Пример 20
Иммунизация страдающих аллергией на Fe1 d1 мышей с помощью Qβ-FELD1-HC
Экспериментальную модель астмы в результате аллергического воспаления дыхательных путей у мышей использовали для оценки воздействия вакцинации против встречающегося в естественных условиях аллергена Fe1 d1 на гуморальный иммунный ответ в виде IgE в сыворотке и БАЛ (бронхоальвеолярный лаваж) на мышах линии BALB/c. По 5 мышей в группе сенсибилизировали путем внутрибрюшинной инъекции 1 мкг встречающегося в естественных условиях Fe1 d1 в AlumGel-S в день 0. Мышей подвергали подкожной вакцинации в день 35 и 49 либо 50 мкг только Qβ, либо 50 мкг Qβ-FELD1-HC перед осуществлением двух последовательных интраназальных контрольных заражений в день 63 и день 70. Через 5 дней после последнего интраназального контрольного заражения мышей умерщвляли и брали образцы сыворотки и БАЛЖ (жидкость бронхоальвеолярного лаважа) для анализа гуморального иммунного ответа (титры IgE-подкласса) с помощью ELISA.
Планшеты для ELISA сенсибилизировали крысиным МАт к IgE (2 мкг/мл), разведенным в карбонатном буфере, в течение ночи при 4°С. После блокирования планшетов с помощью ЗФР/5% БСА в течение 2 ч планшеты инкубировали в течение еще 2 ч либо с сывороткой (первая лунка, предварительное разведение 1:100, затем с использованием 8 стадий разведения 1:3) или БАЛ (первая лунка, чистое содержимое БАЛ, затем с использованием 8 стадий разведения 1:3) из организма сенсибилизированных, вакцинированных, подвергнутых контрольному заражения антигеном мышей. После инкубации образца в течение 2 ч IgE в сыворотке и БАЛ выявляли с помощью крысиного антитела к мышиному IgE, меченного пероксидазой из хрена (HRP), перед выявлением с помощью субстрата OPD.
| Таблица 5 | ||||
| Группа | Сыворотка (д75) | БАЛ (д75) | ||
| Титр при ОП50 | Снижение (в %) | Титр при ОП50 | Снижение (в %) | |
| Вакцинированная Qβ | 1036 | - | 15 | - |
| Вакцинированная Qβ-Fe1 d1 | 49 | 95 | 0 | 100 |
Claims (25)
1. Композиция, содержащая:
(а) коровую частицу, которая несет по меньшей мере один первый сайт присоединения, где коровая частица представляет собой вирусоподобную частицу (ВПЧ) РНК содержащего бактериофага,
(б) по меньшей мере один антиген, который несет по меньшей мере один второй сайт присоединения, где по меньшей мере один антиген представляет собой белок Fe1 d1, где указанный белок Fe1 d1 представляет собой слитый белок, который содержит цепь 1 Fe1 d1 и цепь 2 Fe1 d1, где указанная цепь 2 Fe1 d1 связана посредством ее С-конца с N-концом указанной цепи 1 Fe1 d1 непосредственно или через спейсер, и где (а) и (б) ковалентно связаны с помощью по меньшей мере одного первого и по меньшей мере одного второго сайта присоединения.
(а) коровую частицу, которая несет по меньшей мере один первый сайт присоединения, где коровая частица представляет собой вирусоподобную частицу (ВПЧ) РНК содержащего бактериофага,
(б) по меньшей мере один антиген, который несет по меньшей мере один второй сайт присоединения, где по меньшей мере один антиген представляет собой белок Fe1 d1, где указанный белок Fe1 d1 представляет собой слитый белок, который содержит цепь 1 Fe1 d1 и цепь 2 Fe1 d1, где указанная цепь 2 Fe1 d1 связана посредством ее С-конца с N-концом указанной цепи 1 Fe1 d1 непосредственно или через спейсер, и где (а) и (б) ковалентно связаны с помощью по меньшей мере одного первого и по меньшей мере одного второго сайта присоединения.
2. Композиция по п.1, в которой указанная цепь 2 Fe1 d1 связана посредством ее С-конца с N-концом указанной цепи 1 Fe1 d1 через спейсер, где спейсер состоит из аминокислотной последовательности, которая имеет 1-20 аминокислотных остатков.
3. Композиция по п.1, в которой указанная цепь 2 Fe1 d1 связана посредством ее С-конца с N-концом указанной цепи 1 Fe1 d1 через спейсер, где спейсер состоит из аминокислотной последовательности, которая имеет 10-20 аминокислотных остатков.
4. Композиция по п.1, в которой указанная цепь 2 Fe1 d1 связана посредством ее С-конца с N-концом указанной цепи 1 Fe1 d1 через спейсер, где спейсер состоит из аминокислотной последовательности, которая имеет 15 аминокислотных остатков.
5. Композиция по п.1, в которой указанная цепь 2 Fe1 d1 связана посредством ее С-конца с N-концом указанной цепи 1 Fe1 d1 через спейсер и где спейсером является (GGGGS)3.
6. Композиция по п.1, в которой слитый белок содержит аминокислотную последовательность, выбранную из группы, включающей:
(a)SEQ ID NO:24;
(б) SEQ ID NO:54; и
(в) SEQ ID NO:55.
(a)SEQ ID NO:24;
(б) SEQ ID NO:54; и
(в) SEQ ID NO:55.
7. Композиция по п.1, в которой по меньшей мере один антиген является белком Fe1 d1, и где белок Fe1 d1 выбирают из группы, включающей:
(а) SEQ ID NO:24;
(б) SEQ ID NO:54; и
(в) SEQ ID NO:55.
(а) SEQ ID NO:24;
(б) SEQ ID NO:54; и
(в) SEQ ID NO:55.
8. Композиция по п.1, в которой указанная цепь 2 Fe1 d1 связана посредством ее С-конца с N-концом указанной цепи 1 Fe1 d1 через спейсер и где белок Fe1 d1 является SEQ ID NO:55.
9. Композиция по п.1, в которой цепь 1 Fe1 d1 содержит последовательность SEQ ID NO:22 или гомологичную ей последовательность, где гомологичная последовательность идентична SEQ ID NO:22 более чем на 80%, предпочтительно более чем на 90% или еще более предпочтительно более чем на 95% и наиболее предпочтительно цепь 1 Fe1 d1 состоит из аминокислотной последовательности SEQ ID NO:22.
10. Композиция по п.1, в которой цепь 2 Fe1 d1 содержит последовательность SEQ ID NO:23, SEQ ID NO:25 или SEQ ID NO:26, или гомологичную им последовательность, где гомологичная последовательность идентична SEQ ID NO:23, SEQ ID NO:25 или SEQ ID NO:26 более чем на 80%, предпочтительно более чем на 90%, еще более предпочтительно более чем на 95% и наиболее предпочтительно цепь 2 Fe1 d1 состоит из аминокислотной последовательности SEQ ID NO:23.
11. Композиция по п.1, в которой РНК содержащий бактериофаг выбран из Qβ, fr, GA или АР205.
12. Композиция по п.1, в которой РНК содержащий бактериофаг представляет собой Qβ.
13. Композиция по п.1, в которой указанная вирусоподобная частица РНК содержащего бактериофага включает коровый протеин SEQ ID NO:1.
14. Композиция по п.1, в которой первый сайт присоединения содержит или предпочтительно представляет собой аминогруппу, предпочтительно аминогруппу лизина.
15. Композиция по п.1, в которой второй сайт присоединения содержит или предпочтительно представляет собой сульфгидрильную группу, предпочтительно сульфгидрильную группу цистеина.
16. Композиция по п.1, в которой первый сайт присоединения содержит собой аминогруппу и в которой второй сайт присоединения содержит сульфгидрильную группу, где предпочтительно аминогруппа является аминогруппой лизина и сульфгидрильная группа является сульфгидрильной группой цистеина.
17. Композиция по п.1, где указанная вирусоподобная частица, которая несет по меньшей мере один указанный первый сайт присоединения, связана с по меньшей мере одним белком Fe1 d1, который несет по меньшей мере один указанный второй сайт присоединения, с помощью по меньшей мере одной непептидной ковалентной связи.
18. Композиция по п.1, дополнительно содержащая линкер, в которой предпочтительно линкер слит с С-концом белка Fe1 d1.
19. Композиция по п.18, где указанный линкер включает указанный второй сайт присоединения.
20. Композиция по п.12, где указанный антиген является SEQ ID NO:55.
21. Композиция по п.20, в которой первый сайт присоединения является аминогруппой лизина, и второй сайт присоединения является сульфгидрильной группой цистеина.
22. Вакцина, содержащая композицию по пп.1-21, где предпочтительно вакцина дополнительно содержит по меньшей мере один адъювант.
23. Фармацевтическая композиция, содержащая:
(а) композицию по одному из пп.1-21; и
(б) приемлемый фармацевтический носитель.
(а) композицию по одному из пп.1-21; и
(б) приемлемый фармацевтический носитель.
24. Способ получения композиции по одному из пп.1-21, заключающийся в том, что:
(а) получают коровую частицу, которая несет по меньшей мере один первый сайт присоединения, где коровая частица представляет собой вирусоподобную частицу (ВПЧ) РНК содержащего бактериофага,
(б) получают по меньшей мере один антиген, который несет по меньшей мере один второй сайт присоединения, где антиген представляет собой белок Fe1 d1, где указанный белок Fe1 d1 представляет собой слитый белок, который содержит цепь 1 Fe1 d1 и цепь 2 Fe1 d1, где указанная цепь 2 Fe1 d1 связана посредством ее С-конца с N-концом указанной цепи 1 Fe1 d1 непосредственно или через спейсер, и
(в) связывают коровую частицу и по меньшей мере один антиген с получением композиции, в которой по меньшей мере один антиген и коровая частица связаны с помощью по меньшей мере одного первого и по меньшей мере одного второго сайта присоединения.
(а) получают коровую частицу, которая несет по меньшей мере один первый сайт присоединения, где коровая частица представляет собой вирусоподобную частицу (ВПЧ) РНК содержащего бактериофага,
(б) получают по меньшей мере один антиген, который несет по меньшей мере один второй сайт присоединения, где антиген представляет собой белок Fe1 d1, где указанный белок Fe1 d1 представляет собой слитый белок, который содержит цепь 1 Fe1 d1 и цепь 2 Fe1 d1, где указанная цепь 2 Fe1 d1 связана посредством ее С-конца с N-концом указанной цепи 1 Fe1 d1 непосредственно или через спейсер, и
(в) связывают коровую частицу и по меньшей мере один антиген с получением композиции, в которой по меньшей мере один антиген и коровая частица связаны с помощью по меньшей мере одного первого и по меньшей мере одного второго сайта присоединения.
25. Способ лечения аллергии на кошек, заключающийся в том, что вводят композицию по одному из пп.1-21 или вакцину по п.22 человеку или млекопитающему, кроме человека, где предпочтительно млекопитающее, кроме человека, представляет собой собаку или кошку, и где дополнительно предпочтительно указанная композиция вводится посредством инъекции, ингаляции, перорально, внутримышечно, через вену, трансдермально, через нос или подкожно.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US66291805P | 2005-03-18 | 2005-03-18 | |
| US60/662,918 | 2005-03-18 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2007138265A RU2007138265A (ru) | 2009-04-27 |
| RU2414239C2 true RU2414239C2 (ru) | 2011-03-20 |
Family
ID=36843236
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2007138265/15A RU2414239C2 (ru) | 2005-03-18 | 2006-03-17 | Белки, слитые с кошачьим аллергеном, и их применение |
Country Status (19)
| Country | Link |
|---|---|
| US (3) | US7767212B2 (ru) |
| EP (1) | EP1868642B1 (ru) |
| JP (2) | JP5302671B2 (ru) |
| KR (1) | KR20070112225A (ru) |
| CN (2) | CN103203016A (ru) |
| AU (1) | AU2006224529B2 (ru) |
| BR (1) | BRPI0608455A2 (ru) |
| CA (1) | CA2599218C (ru) |
| CY (1) | CY1114171T1 (ru) |
| DK (1) | DK1868642T3 (ru) |
| ES (1) | ES2424229T3 (ru) |
| IL (1) | IL185103A0 (ru) |
| MX (1) | MX2007011160A (ru) |
| NZ (1) | NZ561040A (ru) |
| PL (1) | PL1868642T3 (ru) |
| PT (1) | PT1868642E (ru) |
| RU (1) | RU2414239C2 (ru) |
| WO (1) | WO2006097530A2 (ru) |
| ZA (1) | ZA200707413B (ru) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2486206C2 (ru) * | 2006-06-09 | 2013-06-27 | Биомей Аг | Гипоаллергенный слитый белок, молекула нуклеиновой кислоты, кодирующая его, вектор экспрессии, клетка-хозяин, вакцинная композиция и его применение |
| RU2706206C1 (ru) * | 2013-12-19 | 2019-11-14 | Сосьете Де Продюи Нестле С.А. | Композиции и способы уменьшения кошачьих аллергенов в окружающей среде |
Families Citing this family (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7264810B2 (en) * | 2001-01-19 | 2007-09-04 | Cytos Biotechnology Ag | Molecular antigen array |
| AU2002339224B2 (en) | 2001-09-14 | 2008-10-09 | Kuros Us Llc | Packaging of immunostimulatory substances into virus-like particles: method of preparation and use |
| RU2324704C2 (ru) * | 2002-07-17 | 2008-05-20 | Цитос Байотекнолоджи Аг | Молекулярные массивы антигенов |
| EP2338510A1 (en) * | 2002-07-19 | 2011-06-29 | Novartis Pharma AG | Vaccine compositions containing amyloid beta1-6 antigen arrays |
| ES2424229T3 (es) * | 2005-03-18 | 2013-09-30 | Cytos Biotechnology Ag | Proteínas de fusión de alérgenos de gato y utilización de las mismas |
| US20070184068A1 (en) * | 2005-12-14 | 2007-08-09 | Cytos Biotechnology Ag | Immunostimulatory nucleic acid packaged particles for the treatment of hypersensitivity |
| WO2007113633A2 (en) * | 2006-04-03 | 2007-10-11 | Pfizer Products Inc. | Immunogenic compositions comprising cat allergen fel dl |
| PL2032592T3 (pl) | 2006-06-12 | 2013-11-29 | Kuros Biosciences Ag | Sposoby pakowania oligonukleotydów do cząstek wirusopodobnych z bakteriofagów RNA |
| DK2601969T3 (en) | 2006-09-29 | 2016-04-18 | Takeda Vaccines Inc | Norovirus vaccine formulations |
| RU2491937C2 (ru) * | 2007-07-09 | 2013-09-10 | Нестек С.А. | Способы уменьшения аллергических реакций, вызванных аллергенами окружающей среды |
| US9388236B2 (en) | 2007-07-09 | 2016-07-12 | Nestec Sa | Methods for reducing allergies caused by environmental allergens |
| US20100266636A1 (en) | 2007-09-18 | 2010-10-21 | Ligocyte Pharmaceuticals, Inc. | Method of conferring a protective immune response to norovirus |
| CN104740624B (zh) | 2007-09-18 | 2018-04-24 | 武田疫苗股份有限公司 | 赋予针对诺如病毒的保护性免疫应答的疫苗 |
| EP2042193A1 (en) * | 2007-09-28 | 2009-04-01 | Biomay AG | RNA Vaccines |
| PL2324113T3 (pl) | 2008-08-08 | 2018-08-31 | Takeda Vaccines, Inc. | Cząstki wirusopodobne zawierające złożone kapsydowe sekwencje aminokwasowe do zwiększonej reaktywności krzyżowej |
| BR112013011069A2 (pt) * | 2009-11-05 | 2017-03-28 | Padgett Hal | geração de partículas antigênicas semelhantes a virus através de ligações de proteína-proteína |
| US8321012B2 (en) * | 2009-12-22 | 2012-11-27 | The Invention Science Fund I, Llc | Device, method, and system for neural modulation as vaccine adjuvant in a vertebrate subject |
| PL3299030T3 (pl) | 2011-07-11 | 2022-12-05 | Takeda Vaccines, Inc. | Pozajelitowe preparaty szczepionek przeciw norowirusowi |
| BR112014013035A2 (pt) | 2011-12-22 | 2018-10-09 | Hoffmann La Roche | métodos de seleção de células, conjuntos de expressão bicistrônica, células eucarióticas, vetores lentivirais, uso de vetor lentiviral, bibliotecas de ventores lentivirais e de células eucarióticas, métodos de seleção de células, fluxos de trabalho e uso de célula |
| JO3820B1 (ar) | 2012-05-03 | 2021-01-31 | Regeneron Pharma | أجسام مضادة بشرية لـ fel d1وطرق لاستخدامها |
| EP2912069B1 (en) * | 2012-10-23 | 2019-07-31 | Emory University | Gm-csf and il-4 conjugates, compositions, and methods related thereto |
| EP3564671B1 (en) | 2013-08-23 | 2021-09-29 | Regeneron Pharmaceuticals, Inc. | Diagnostic tests and methods for assessing safety, efficacy or outcome of allergen-specific immunotherapy (sit) |
| MA40824A (fr) * | 2014-10-22 | 2017-08-29 | Saiba Gmbh | Particules de cmv de type virus modifié |
| EA035378B1 (ru) | 2015-01-15 | 2020-06-04 | Юниверсити Оф Копенгаген | Вирусоподобная частица с эффективным экспонированием эпитопов |
| WO2016192788A1 (en) * | 2015-06-03 | 2016-12-08 | Universität Zürich Prorektorat Mnw | Methods and compositions for preventing and treating cat or dog dander allergy |
| RU2018105007A (ru) | 2015-09-08 | 2019-10-10 | Университет Цюрих | Композиции против аллергии на кошек |
| US11129882B2 (en) | 2015-10-30 | 2021-09-28 | University Of Copenhagen | Virus like particle with efficient epitope display |
| CN105219742A (zh) * | 2015-11-10 | 2016-01-06 | 海南大学 | 一种展示重组猫致敏原rFel d 1蛋白的免疫增强型病毒样颗粒、其表达载体及其制备与应用 |
| WO2017179025A1 (en) | 2016-04-15 | 2017-10-19 | Alk-Abelló A/S | Epitope polypeptides of ragweed pollen allergens |
| FR3054547B1 (fr) * | 2016-07-29 | 2020-06-05 | Angany Inc. | Particules pseudo-virales et leurs utilisations |
| WO2018118713A1 (en) | 2016-12-22 | 2018-06-28 | Regeneron Pharmaceuticals, Inc. | Method of treating an allergy with allergen-specific monoclonal antibodies |
| US20220073946A1 (en) | 2018-12-20 | 2022-03-10 | Saiba AG | Virus-like particles of cmv modified by fusion |
| WO2023176206A1 (ja) * | 2022-03-18 | 2023-09-21 | デンカ株式会社 | リンカーにより連結されたカプシドタンパク質を含むウイルス様粒子 |
| CN114933639B (zh) * | 2022-05-05 | 2023-12-29 | 中国农业科学院兰州兽医研究所 | 非洲猪瘟病毒p72N抗原表位蛋白及其制备方法和用途 |
Family Cites Families (37)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4163778A (en) * | 1978-05-04 | 1979-08-07 | The Foundation for the Study of Asthma and Related Diseases | Asthma immunotherapy |
| US5374426A (en) | 1986-09-03 | 1994-12-20 | University Of Saskatchewan | Rotavirus nucleocapsid protein VP6 in vaccine compositions |
| EP0420913B1 (en) | 1988-06-14 | 1995-11-15 | Cell Med, Inc. | Heterofunctional cellular immunological reagents, vaccines containing same and methods for the use of same |
| US6120769A (en) | 1989-11-03 | 2000-09-19 | Immulogic Pharmaceutical Corporation | Human T cell reactive feline protein (TRFP) isolated from house dust and uses therefor |
| WO1992011291A1 (en) | 1990-12-20 | 1992-07-09 | Smithkline Beecham Biologicals (S.A.) | Vaccines based on hepatitis b surface antigen |
| GB9114003D0 (en) | 1991-06-28 | 1991-08-14 | Mastico Robert A | Chimaeric protein |
| GB9213601D0 (en) | 1992-06-26 | 1992-08-12 | Mastico Robert A | Protein based delivery system |
| JPH10505356A (ja) | 1994-09-02 | 1998-05-26 | イミユロジク・フアーマシユーチカル・コーポレーシヨン | ヒトへの投与のための組成物および方法、抗原特異的免疫応答のダウンレギュレーションを行うことが可能なペプチド |
| US6759234B1 (en) | 1994-09-02 | 2004-07-06 | Immulogic Pharmaceutical Corporation | Compositions and methods for administering to humans, peptides capable of down regulating an antigen specific immune response |
| WO1996030523A2 (en) | 1995-03-31 | 1996-10-03 | Hans Wolf | Antigen presentation system based on retrovirus-like particles |
| GB9621091D0 (en) | 1996-10-09 | 1996-11-27 | Fondation Pour Le Perfectionem | Attenuated microorganisms strains and their uses |
| US6054312A (en) | 1997-08-29 | 2000-04-25 | Selective Genetics, Inc. | Receptor-mediated gene delivery using bacteriophage vectors |
| EP1037663A2 (en) | 1997-12-16 | 2000-09-27 | Regents Of The University Of Minnesota | Methods to treat undesirable immune responses |
| AR020102A1 (es) | 1998-07-30 | 2002-04-10 | Ucb Sa | Compuesto para la prevencion y/o tratamiento de la alergia; composicion farmaceutica, composicion cosmetica, composicion en forma de bebida, alimento y/oalimento para animales domesticos que lo comprende y uso de dicho compuesto o dicha composicion farmaceutica para la fabricacion de un alimento |
| WO2000020032A1 (en) | 1998-10-06 | 2000-04-13 | Trustees Of Dartmouth College | RECOMBINANT CAT ALLERGEN, Fel dI, EXPRESSED IN BACULOVIRUS FOR DIAGNOSIS AND TREATMENT OF CAT ALLERGY |
| AU770802B2 (en) | 1998-10-21 | 2004-03-04 | Government Of The United States Of America, As Represented By The Secretary Of The Department Of Health And Human Services, The | Virus-like particles for the induction of autoantibodies |
| RU2245163C2 (ru) * | 1998-11-30 | 2005-01-27 | Сайтос Байотекнолэджи АГ | Композиция (варианты), способ получения не природной упорядоченной и содержащей повторы антигенной матрицы, способ терапевтического лечения и способ иммунизации |
| TR200503031T2 (tr) | 1999-09-25 | 2005-09-21 | University Of Iowa Research Foundation | İmmünostimülatör nükleik asitler |
| EP1278542A2 (en) * | 2000-05-05 | 2003-01-29 | Cytos Biotechnology AG | Molecular antigen arrays and vaccines |
| MXPA03004174A (es) | 2000-11-16 | 2004-12-02 | Alk Abello As | Alergenos mutantes novedosos. |
| EP1219300B1 (en) | 2000-12-28 | 2006-12-06 | BIOMAY Produktions- und Handels- Aktiengesellschaft | Treatment of allergies |
| EP1221317A1 (en) | 2000-12-28 | 2002-07-10 | SHAN-Beteiligungsgesellschaft m.b.H. | Vaccines containing hybrid polypeptides consisting of at least two different allergenic proteins |
| US7264810B2 (en) | 2001-01-19 | 2007-09-04 | Cytos Biotechnology Ag | Molecular antigen array |
| CA2441476A1 (en) | 2001-03-02 | 2002-09-12 | The Rockefeller University | Recombinant hybrid allergen constructs with reduced allergenicity that retain immunogenicity of the natural allergen |
| US20030091593A1 (en) | 2001-09-14 | 2003-05-15 | Cytos Biotechnology Ag | In vivo activation of antigen presenting cells for enhancement of immune responses induced by virus like particles |
| AU2002339224B2 (en) | 2001-09-14 | 2008-10-09 | Kuros Us Llc | Packaging of immunostimulatory substances into virus-like particles: method of preparation and use |
| BR0213950A (pt) * | 2001-11-07 | 2004-08-24 | Cytos Biotechnology Ag | Arranjos de antìgenos para o tratamento de doenças eosinofólicas alérgicas |
| CA2465981A1 (en) * | 2001-11-07 | 2003-05-15 | Cytos Biotechnology Ag | Antigen arrays comprising rankl for treatment of bone disease |
| RU2324704C2 (ru) * | 2002-07-17 | 2008-05-20 | Цитос Байотекнолоджи Аг | Молекулярные массивы антигенов |
| WO2004009124A2 (en) | 2002-07-19 | 2004-01-29 | Cytos Biotechnology Ag | Ghrelin-carrier conjugates |
| EP1530585A2 (en) | 2002-08-22 | 2005-05-18 | Cytos Biotechnology AG | Inducible alphaviral/orip based gene expression system |
| CA2503886A1 (en) | 2002-11-01 | 2004-05-13 | Alk-Abello A/S | Recombinant protein variants |
| WO2004047793A1 (en) | 2002-11-26 | 2004-06-10 | Alk-Abelló A/S | Pharmaceutical allergen product |
| EP1605973B1 (en) * | 2003-03-26 | 2012-09-26 | Cytos Biotechnology AG | Packaging of immunostimulatory oligonucleotides into virus-like particles: methods of preparation and uses |
| US20090117136A1 (en) * | 2003-04-24 | 2009-05-07 | Imvision Gmbh | Recombinant allergen |
| WO2005004907A1 (en) * | 2003-07-10 | 2005-01-20 | Cytos Biotechnology Ag | Packaged virus-like particles |
| ES2424229T3 (es) * | 2005-03-18 | 2013-09-30 | Cytos Biotechnology Ag | Proteínas de fusión de alérgenos de gato y utilización de las mismas |
-
2006
- 2006-03-17 ES ES06725140T patent/ES2424229T3/es active Active
- 2006-03-17 DK DK06725140.5T patent/DK1868642T3/da active
- 2006-03-17 KR KR1020077022225A patent/KR20070112225A/ko not_active Application Discontinuation
- 2006-03-17 MX MX2007011160A patent/MX2007011160A/es active IP Right Grant
- 2006-03-17 EP EP06725140.5A patent/EP1868642B1/en not_active Not-in-force
- 2006-03-17 RU RU2007138265/15A patent/RU2414239C2/ru not_active IP Right Cessation
- 2006-03-17 CN CN2013101152149A patent/CN103203016A/zh active Pending
- 2006-03-17 JP JP2008501331A patent/JP5302671B2/ja not_active Expired - Fee Related
- 2006-03-17 CN CN2006800088726A patent/CN101141979B/zh not_active Expired - Fee Related
- 2006-03-17 AU AU2006224529A patent/AU2006224529B2/en not_active Ceased
- 2006-03-17 US US11/886,577 patent/US7767212B2/en not_active Expired - Fee Related
- 2006-03-17 PL PL06725140T patent/PL1868642T3/pl unknown
- 2006-03-17 BR BRPI0608455-9A patent/BRPI0608455A2/pt active Search and Examination
- 2006-03-17 ZA ZA200707413A patent/ZA200707413B/xx unknown
- 2006-03-17 WO PCT/EP2006/060845 patent/WO2006097530A2/en active Application Filing
- 2006-03-17 CA CA2599218A patent/CA2599218C/en not_active Expired - Fee Related
- 2006-03-17 NZ NZ561040A patent/NZ561040A/en not_active IP Right Cessation
- 2006-03-17 PT PT67251405T patent/PT1868642E/pt unknown
-
2007
- 2007-08-07 IL IL185103A patent/IL185103A0/en not_active IP Right Cessation
-
2010
- 2010-05-21 US US12/785,174 patent/US20110045013A1/en not_active Abandoned
-
2012
- 2012-12-21 US US13/724,331 patent/US20130344098A1/en not_active Abandoned
-
2013
- 2013-03-12 JP JP2013048847A patent/JP2013155176A/ja active Pending
- 2013-07-26 CY CY20131100638T patent/CY1114171T1/el unknown
Non-Patent Citations (1)
| Title |
|---|
| Vailes L.D.et al., High level expression of immunoreactive recombinant cat allergen (Fel d): Targeting to antigen-presenting cells, Allergy Clin. Immunol, 2002, Nov., v.110, №5, pp.757-762. KAISER L. et al., The crystal structure of the major cat allergen Fe1 d1, a member of the secretoglobin family, J.Biol. Chem., 2003 Sep. v.278, №39, pp.37730-37735. * |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2486206C2 (ru) * | 2006-06-09 | 2013-06-27 | Биомей Аг | Гипоаллергенный слитый белок, молекула нуклеиновой кислоты, кодирующая его, вектор экспрессии, клетка-хозяин, вакцинная композиция и его применение |
| RU2706206C1 (ru) * | 2013-12-19 | 2019-11-14 | Сосьете Де Продюи Нестле С.А. | Композиции и способы уменьшения кошачьих аллергенов в окружающей среде |
| US10889785B2 (en) | 2013-12-19 | 2021-01-12 | Société des Produits Nestlé S.A. | Compositions and methods for reducing cat allergens in the environment |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2006097530A2 (en) | 2006-09-21 |
| CN103203016A (zh) | 2013-07-17 |
| PT1868642E (pt) | 2013-07-10 |
| RU2007138265A (ru) | 2009-04-27 |
| CN101141979A (zh) | 2008-03-12 |
| PL1868642T3 (pl) | 2013-10-31 |
| IL185103A0 (en) | 2007-12-03 |
| US20090175896A1 (en) | 2009-07-09 |
| JP2013155176A (ja) | 2013-08-15 |
| JP2008535800A (ja) | 2008-09-04 |
| US20110045013A1 (en) | 2011-02-24 |
| CY1114171T1 (el) | 2016-08-31 |
| US20130344098A1 (en) | 2013-12-26 |
| WO2006097530A3 (en) | 2007-06-21 |
| CA2599218A1 (en) | 2006-09-21 |
| AU2006224529B2 (en) | 2012-05-24 |
| EP1868642A2 (en) | 2007-12-26 |
| US7767212B2 (en) | 2010-08-03 |
| BRPI0608455A2 (pt) | 2010-01-05 |
| EP1868642B1 (en) | 2013-05-08 |
| ES2424229T3 (es) | 2013-09-30 |
| KR20070112225A (ko) | 2007-11-22 |
| CA2599218C (en) | 2015-08-11 |
| DK1868642T3 (da) | 2013-06-24 |
| ZA200707413B (en) | 2009-01-28 |
| CN101141979B (zh) | 2013-05-08 |
| AU2006224529A1 (en) | 2006-09-21 |
| NZ561040A (en) | 2009-04-30 |
| MX2007011160A (es) | 2007-11-13 |
| JP5302671B2 (ja) | 2013-10-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2414239C2 (ru) | Белки, слитые с кошачьим аллергеном, и их применение | |
| US20090123414A1 (en) | Il-15 Antigen Arrays And Uses Thereof | |
| RU2441067C2 (ru) | Конъюгаты интерлейкина-1 и их применение | |
| KR20100111273A (ko) | 신경성장인자 콘쥬게이트 및 그 용도 | |
| AU2006259057A1 (en) | Antigen conjugates and uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20150318 |