RU2201788C2 - Выделение и очистка паклитакселя и других родственных таксанов с помощью промышленной препаративной хроматографии низкого давления на колонне с полимерной смолой - Google Patents
Выделение и очистка паклитакселя и других родственных таксанов с помощью промышленной препаративной хроматографии низкого давления на колонне с полимерной смолой Download PDFInfo
- Publication number
- RU2201788C2 RU2201788C2 RU2000100420/12A RU2000100420A RU2201788C2 RU 2201788 C2 RU2201788 C2 RU 2201788C2 RU 2000100420/12 A RU2000100420/12 A RU 2000100420/12A RU 2000100420 A RU2000100420 A RU 2000100420A RU 2201788 C2 RU2201788 C2 RU 2201788C2
- Authority
- RU
- Russia
- Prior art keywords
- taxane
- taxanes
- source
- analogue
- fractions
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D305/00—Heterocyclic compounds containing four-membered rings having one oxygen atom as the only ring hetero atoms
- C07D305/14—Heterocyclic compounds containing four-membered rings having one oxygen atom as the only ring hetero atoms condensed with carbocyclic rings or ring systems
-
- E—FIXED CONSTRUCTIONS
- E06—DOORS, WINDOWS, SHUTTERS, OR ROLLER BLINDS IN GENERAL; LADDERS
- E06B—FIXED OR MOVABLE CLOSURES FOR OPENINGS IN BUILDINGS, VEHICLES, FENCES OR LIKE ENCLOSURES IN GENERAL, e.g. DOORS, WINDOWS, BLINDS, GATES
- E06B7/00—Special arrangements or measures in connection with doors or windows
- E06B7/16—Sealing arrangements on wings or parts co-operating with the wings
- E06B7/22—Sealing arrangements on wings or parts co-operating with the wings by means of elastic edgings, e.g. elastic rubber tubes; by means of resilient edgings, e.g. felt or plush strips, resilient metal strips
- E06B7/23—Plastic, sponge rubber, or like strips or tubes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- E—FIXED CONSTRUCTIONS
- E06—DOORS, WINDOWS, SHUTTERS, OR ROLLER BLINDS IN GENERAL; LADDERS
- E06B—FIXED OR MOVABLE CLOSURES FOR OPENINGS IN BUILDINGS, VEHICLES, FENCES OR LIKE ENCLOSURES IN GENERAL, e.g. DOORS, WINDOWS, BLINDS, GATES
- E06B3/00—Window sashes, door leaves, or like elements for closing wall or like openings; Layout of fixed or moving closures, e.g. windows in wall or like openings; Features of rigidly-mounted outer frames relating to the mounting of wing frames
- E06B3/66—Units comprising two or more parallel glass or like panes permanently secured together
- E06B3/67—Units comprising two or more parallel glass or like panes permanently secured together characterised by additional arrangements or devices for heat or sound insulation or for controlled passage of light
Abstract
Способ получения таксановых аналогов из источника, содержащего таксаны. Способ включает экстракцию таксанов, использование полимерной смолы для выделения таксанов при низком давлении без применения сложных и дорогостоящих стадий разделения/очистки, кристаллизацию фракций, содержащих таксановые соединения, концентрирование маточного раствора и использование полимерной смолы для выделения второго таксанового соединения из маточного раствора. Способ обеспечивает высокий выход и чистоту. 3 с. и 17 з.п. ф-лы.
Description
Изобретение относится к методике разделения, более конкретно к методике разделения паклитакселя и родственных таксанов.
Паклитаксель является хорошо известным хемотерапевтическим средством против различных метастатических видов рака. Он был испытан FDA и НРB для лечения рака молочной железы и рака яичников.
Данное соединение является природным продуктом, экстрагируемым главным образом из коры тихооокеанского тиса Taxus brevifolia, также он найден в Т. baccata, Т. walichiana, Т. vunnanensis и Т. canadensis.
Концентрация паклитакселя в различных видах сырья, как правило, является низкой, например в коре тихооокеанского тиса содержится порядка от 0,0004 до 0,01 мас.%. Такие низкие концентрации делают экстракцию соединения из сырья и его очистку до фармакопейной чистоты весьма спорной, а поэтому нецелесообразной в промышленном масштабе. Были разработаны различные методики нормально-фазной и обращенно-фазной хроматографии, равно как и колоночной хроматографии низкого и высокого давления для выделения паклитакселя из первичных экстрактов сырья.
Успех применения хроматографии низкого давления в большей мере зависит от устройства колонны. Различные проблемы связаны с использованием силикагеля и окиси алюминия, которые являются классическими носителями в системах разделения с неподвижной фазой. Они образуют неподвижную фазу с большинством систем растворителей, но она является сильным сорбентом и может участвовать в процессе разделения в такой степени, что затрагивает хроматографическое поведение и выход образцов.
Разработаны хроматографические методы определения и выделения паклитакселя из различных видов Taxus в аналитических и препаративных количествах. Эти способы выделения обычно проводятся в ограниченном лабораторном масштабе и обладают низкими селективностью и выходом, высокой себестоимостью производства, поэтому существует насущная и неудовлетворенная потребность в экономически приемлемом способе разделения противоракового соединения паклитакселя от его ближайших аналогов цефаломанина, а также других близкородственных таксанов.
Предшествующий уровень техники описывает использование различных типов хроматографических методик разделения паклитакселя и родственных таксанов, включающих нормально-фазную и обращенно-фазную хроматографию на колоннах с силикагелем или привитым силикагелем. Способы, известные из предшествующего уровня техники, отличаются низким выходом, высокой себестоимостью производства или включают многоступенчатое разделение, которое трудно интенсифицируется до масштабов промышленного производства.
Типичным примером предшествующего уровня техники является патент США 5620875, выданный Хоффману с сотр. 15 апреля 1997 г. В документе указано, что разделение паклитакселя и других таксанов производится многоступенчатой экстракцией гексаном и высокоэффективной жидкостной хроматографией (ВЭЖХ). Данный процесс применяется в лаборатории и дает умеренные выходы целевых соединений.
В патенте США 5670673, выданном Рао 23 сентября 1997 г., изложено разделение и очистка таксола и его аналогов. Способ включает использование обращенно-фазной жидкостной хроматографии на сорбенте C18 с элюированием сорбированных аналогов. Хотя данная методика имеет определенные преимущества, тем не менее существуют ограничения в отношении производительности и чистоты получаемых соединений.
Данное изобретение обеспечивает простой способ разделения, основанный на применении полимерной смолы, который устраняет ограничения существующей методологии.
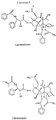
Объектом данного изобретения является простой и экономически более эффективный способ разделения и очистки важных таксанов, таких как 13-ацетил-9-дигидробаккатин III, 10-деацетилбаккатин III, баккатин III, цефаломанин и паклитаксель.
Обычные методы выделения таксанов, включая паклитаксель, 13-ацетил-9-дигидробаккатин III и баккатин III, обычно включают стадии экстракции таксанов из сырья спиртовым растворителем, обезжиривания экстракта и хроматографического разделения и очистки индивидуального таксана.
Первым объектом данного изобретения является обеспечение способа выделения и очистки таксановых аналогов из источника таксанов.
Способ включает
- экстракцию источника таксанов органическим экстрагентом;
- обработку рабочей сорбирующей среды экстрагентом и загрузку среды в колонну, содержащую сорбент;
- элюирование на первой стадии смесью органических растворителей под давлением от 68,948 до 137,90 кПа (от 10 до 20 psi) для получения фракций, содержащих таксановые соединения;
- кристаллизацию фракций для получения твердого таксанового соединения и маточного раствора, концентрирование маточного раствора;
- элюирование маточного раствора на второй стадии смесью полярных растворителей через полимерную смолу для выделения по меньшей мере второго таксанового соединения.
- экстракцию источника таксанов органическим экстрагентом;
- обработку рабочей сорбирующей среды экстрагентом и загрузку среды в колонну, содержащую сорбент;
- элюирование на первой стадии смесью органических растворителей под давлением от 68,948 до 137,90 кПа (от 10 до 20 psi) для получения фракций, содержащих таксановые соединения;
- кристаллизацию фракций для получения твердого таксанового соединения и маточного раствора, концентрирование маточного раствора;
- элюирование маточного раствора на второй стадии смесью полярных растворителей через полимерную смолу для выделения по меньшей мере второго таксанового соединения.
Другим объектом данного изобретения является способ выделения и очистки таксанов из источника таксанов.
Способ включает
- получение источника таксанов;
- экстракцию таксанов из источника в органическую экстракционную среду с получением органического слоя, содержащего таксановые соединения;
- обработку носителя органическим слоем;
- применение колонны низкого давления, содержащей сорбент;
- элюирование колонны органическим растворителем на первой стадии для получения очищенных таксановых фракций;
- кристаллизацию таксановых фракций для получения первого таксанового аналога и маточного раствора;
- элюирование маточного раствора на второй стадии через полимерную смолу на хроматографической колонне для очистки и выделения по меньшей мере второго таксанового аналога и третьего таксанового аналога;
- сбор разделенных таксановых аналогов.
- получение источника таксанов;
- экстракцию таксанов из источника в органическую экстракционную среду с получением органического слоя, содержащего таксановые соединения;
- обработку носителя органическим слоем;
- применение колонны низкого давления, содержащей сорбент;
- элюирование колонны органическим растворителем на первой стадии для получения очищенных таксановых фракций;
- кристаллизацию таксановых фракций для получения первого таксанового аналога и маточного раствора;
- элюирование маточного раствора на второй стадии через полимерную смолу на хроматографической колонне для очистки и выделения по меньшей мере второго таксанового аналога и третьего таксанового аналога;
- сбор разделенных таксановых аналогов.
Еще одним объектом данного изобретения является способ выделения и очистки таксанов из источника таксанов.
Способ включает
- получение источника таксанов;
- экстракцию таксанов из источника в органическую экстракционную среду с получением органического слоя, содержащего таксановые соединения;
- обработку носителя органическим слоем;
- применение колонны низкого давления, содержащей сорбент;
- элюирование колонны органическим растворителем на первой стадии под давлением 68,948-137,90 кПа (10-20 psi) для получения очищенных таксановых фракций и удаления флавоноидных и лигниновых примесей;
- кристаллизацию таксановых фракций для получения первого таксанового аналога и маточного раствора;
- элюирование маточного раствора на второй стадии через полистирол-ДВБ смолу на хроматографической колонне под давлением 206,84 кПа (30 psi) для очистки и выделения по меньшей мере второго и третьего таксановых аналогов;
- элюирование на третьей стадии второго таксанового аналога и третьего таксанового аналога через нормально-фазную колонну с силикагелем для очистки второго таксанового аналога и третьего таксанового аналога;
- сбор разделенных таксановых аналогов.
- получение источника таксанов;
- экстракцию таксанов из источника в органическую экстракционную среду с получением органического слоя, содержащего таксановые соединения;
- обработку носителя органическим слоем;
- применение колонны низкого давления, содержащей сорбент;
- элюирование колонны органическим растворителем на первой стадии под давлением 68,948-137,90 кПа (10-20 psi) для получения очищенных таксановых фракций и удаления флавоноидных и лигниновых примесей;
- кристаллизацию таксановых фракций для получения первого таксанового аналога и маточного раствора;
- элюирование маточного раствора на второй стадии через полистирол-ДВБ смолу на хроматографической колонне под давлением 206,84 кПа (30 psi) для очистки и выделения по меньшей мере второго и третьего таксановых аналогов;
- элюирование на третьей стадии второго таксанового аналога и третьего таксанового аналога через нормально-фазную колонну с силикагелем для очистки второго таксанового аналога и третьего таксанового аналога;
- сбор разделенных таксановых аналогов.
Исходным источником таксанов является растительный материал Taxus canadensis, которым изобилует восток Канады. Используются ветки и иглы Taxus canadensis или их смесь. Материал может быть свежим или сушеным.
Сырье замачивают и экстрагируют метанолом при 60oС в течение 5 час, затем фильтруют. Метанольный экстракт смешивают с активированным углем, оставляют на 1 час при комнатной температуре, затем отфильтровывают. Фильтрат концентрируют примерно до 15% от исходного объема путем выпаривания. К концентрату прибавляют смесь вода : дихлорметан 1:1 (v/v) для получения фракции, обогащенной паклитакселем (органический слой).
Органический слой концентрируют для уменьшения объема и наносят на носитель, в данном случае носителем является Celite 545.
Обработанный материал загружают наверху промышленной препаративной колонны, например, размером 150•1500 мм и набитой сорбентом Аl2О3. Колонну элюируют смесью гексан : ацетон (начало 100:0, окончание 45:55) под давлением 68,948- 137,90 кПа (от 10 до 20 psi). Собирают фракции, содержащие таксаны, анализируют тонкослойной хроматографией (ТСХ) с последующим объединением в соответствии с данными ТСХ.
Собранные фракции затем концентрируют в вакууме, полученные вещества растворяют в метаноле и выдерживают в течение суток. Образовавшиеся кристаллы отфильтровывают и промывают метанолом, а затем перекристаллизовывают из ацетона. Получают 13-ацетил-9-дигидробаккатин III в виде белых кристаллов.
Маточный раствор упаривают досуха, остаток растворяют в ацетоне. Ацетоновый раствор смешивают с полимерной смолой (смола DowexTM, полистирол-ДВБ). Смесь упаривают в вакууме для удаления ацетона. Полученный порошок подвергают хроматографии низкого давления. Промышленную хроматографическую колонну (150•1500 мм) набивают смолой DowexTM и элюируют смесью ацетон : вода (45:55, v/v) с расходом 150 мл/мин при рабочем давлении 206,84 кПа (30 psi). Собирают фракции объемом порядка 2 л каждая, которые анализируют ТСХ и ВЭЖХ. Фракции, содержащие баккатин III и 10-деацетилбаккатин III, объединяют и упаривают в вакууме до удаления практически всего органического растворителя, разбавляют водой и экстрагируют CH2Cl2. Экстракт упаривают досуха, полученный остаток растворяют в EtOAc и очищают на нормально-фазной колонне с силикагелем, используя в качестве растворителя систему гексан : EtOAc (начало 5: 5, окончание 35:65). Баккатин III и 10-деацетилбаккатин III получают в виде белого порошка со степенью чистоты выше 98%.
Фракции, содержащие паклитаксель и цефаломанин, объединяют и упаривают в вакууме до удаления практически всего ацетона, затем разделяют в системе вода : СН2Сl2. Органический слой отделяют и упаривают досуха в вакууме. Остаток растворяют в метаноле. К метанольному раствору прибавляют примерно 30% (w/v) воды, смесь нагревают до 60oС в течение 5 мин и оставляют на ночь при комнатной температуре. Неочищенный кристаллический осадок отфильтровывают от метанольного раствора и высушивают в вакууме при 70-75oС. Остаток анализируют с помощью ВЭЖХ. Он состоит приблизительно из 70% паклитакселя и 25% цефаломанина и некоторых других таксанов.
Неочищенный паклитаксель может подвергаться обработке в соответствии с тремя альтернативными способами. В первом случае его растворяют в ацетоне и очищают обращенно-фазной колоночной хроматографией. Колонну набивают полимерной смолой (смола Diaion HP2MG) и элюируют смесью ацетонитрил : вода (45: 55). Получают паклитаксель в виде белых кристаллов со степенью чистоты более 99%. Цефаломанин получают в виде белого порошка со степенью чистоты более 98%.
Альтернативно согласно второму способу очистку паклитакселя и цефаломанина проводят с помощью химического превращения, а затем очищают обращенно-фазной колоночной хроматографией на привитом силикагеле. Смесь неочищенных паклитакселя и цефаломанина растворяют в смеси СН2Сl2 : СНСl3 (1:10 w/v) и проводят реакцию с 10 эквивалентами брома в круглодонной колбе, помещенной на ледяную баню (при 0...5oС) в течение приблизительно 40 мин. Полученную смесь паклитакселя и 2",3"-бромоцефаломанина легко разделяют на обращенно-фазной хроматографической колонне (C18 или фенил), элюент СН3СN : Н2O (45:55). Паклитаксель получают в виде белых кристаллов со степенью чистоты более 99%. 2",3"-Бромоцефаломанин получают в виде смеси диастереомеров, которая реагирует с активированным цинком в уксусной кислоте при комнатной температуре, а затем подвергается очистке колоночной флэш-хроматографией. Получают цефаломанин со степенью чистоты более 95%.
Согласно третьему альтернативному способу паклитаксель и бромоцефаломанин очищают на нормально-фазной колонне с силикагелем. Элюирующие системы могут включать гексан : ЕtОАс (начало 6:4, окончание 4:6) или CH2Cl2 : Me2CO (начало 8:2, окончание 65:35) или CH2Cl2 : EtOAc (начало 75:25, окончание 6: 4). Этим способом паклитаксель получают в виде белых кристаллов со степенью чистоты, превосходящей 99%, с содержанием цефаломанина не более 0,2%.
После обсуждения изобретения далее следуют примеры для более точного понимания.
Пример 1
Приблизительно 200 кг сушеных игл и веток Taxus canadensis экстрагируют 1000 л метанола при 60oС в течение 5 ч в промышленном многоцелевом экстракторе и отфильтровывают. Сырье дополнительно экстрагируют 700 л метанола при температуре от 55 до 60oС в течение 5 ч и отфильтровывают. Фильтраты объединяют и смешивают с 10 кг активированного угля (5% w/w) и выдерживают при комнатной температуре 1 ч, отфильтровывают от активированного угля. Затем фильтрат концентрируют в вакууме приблизительно до 100 л и прибавляют 300 л смеси вода : дихлорметан (1:1). Отделяют органический слой, а водный слой еще дважды экстрагируют 200 л дихлорметана. Дихлорметановые растворы объединяют и упаривают в вакууме до образования суспензии, а затем разбавляют 20 л ацетона.
Приблизительно 200 кг сушеных игл и веток Taxus canadensis экстрагируют 1000 л метанола при 60oС в течение 5 ч в промышленном многоцелевом экстракторе и отфильтровывают. Сырье дополнительно экстрагируют 700 л метанола при температуре от 55 до 60oС в течение 5 ч и отфильтровывают. Фильтраты объединяют и смешивают с 10 кг активированного угля (5% w/w) и выдерживают при комнатной температуре 1 ч, отфильтровывают от активированного угля. Затем фильтрат концентрируют в вакууме приблизительно до 100 л и прибавляют 300 л смеси вода : дихлорметан (1:1). Отделяют органический слой, а водный слой еще дважды экстрагируют 200 л дихлорметана. Дихлорметановые растворы объединяют и упаривают в вакууме до образования суспензии, а затем разбавляют 20 л ацетона.
Ацетоновым раствором пропитывают 20 кг Celite 545. Пропитанный материал высушивают на воздухе, после чего загружают наверху трех промышленных хроматографических колонн низкого давления (размером 150•15 см). Каждая колонна набита 15 кг сорбента (окись алюминия, Аl2О3). Следует отметить, что точный размер колонн не имеет решающего значения, но колонны должны быть достаточно велики, чтобы вместить количество Аl2О3, требуемое для разделения. Использование окиси алюминия эффективно при сорбции флавоноидов и лигнинов, которые также экстрагируются из сырья. Их трудно удалить, поэтому возникает проблема чистоты выпускаемого товарного паклитакселя.
Колонну элюируют системой гексан : ацетон (начало 100:0, окончание 45: 55) под давлением 68,948-103,42 кПа (от 10 до 15 psi) с расходом приблизительно 150 мл/мин.
Фракции, содержащие таксаны, собирают и объединяют согласно результатам тонкослойной хроматографии (ТСХ), после чего концентрируют в вакууме для удаления всех растворителей. Полученное вещество растворяют в метаноле и оставляют на ночь при комнатной температуре до образования игольчатых кристаллов. Кристаллы отфильтровывают и перекристаллизовывают из ацетона. Получают 13-ацетил-9-дигидробаккатин III в виде игольчатых кристаллов со степенью чистоты более 96%, выход составляет 148 г (0,074% в пересчете на сырье).
Маточный раствор после кристаллизации 13-ацетил-9-дигидробаккатина III упаривают досуха в вакууме. Остаток растворяют в 3 л ацетона. Ацетоновый раствор смешивают с 1,5 кг сополимерной смолы полистирола-дивинилбензола. Смесь упаривают для удаления растворителя, полученный порошок загружают наверху промышленной хроматографической колонны низкого давления, набитой сополимерной смолой полистирола-дивинилбензола, и элюируют 45%-ным водным ацетоном с расходом 150 мл/мин при рабочем давлении ниже 206,84 кПа (30 psi). Фракции, объемом 2 л каждая, собирают и анализируют с применением ТСХ и ВЭЖХ.
Фракции, содержащие паклитаксель и цефаломанин, объединяют, упаривают в вакууме до удаления большей части ацетона, затем разбавляют деионизированной водой и трижды экстрагируют 2,5 л дихлорметана. Органический слой упаривают досуха в вакууме, остаток растворяют в 1 л метанола.
К метанольному раствору прибавляют приблизительно 30% воды (w/v), смесь нагревают до 60oС, выдерживают несколько минут, после чего оставляют на ночь при комнатной температуре. Неочищенный кристаллический твердый продукт отфильтровывают от метанола и высушивают в вакуумной сушилке при температуре от 70 до 75oС. Получают 31 г твердого вещества, состоящего приблизительно из 70% паклитакселя и 25% цефаломанина.
Неочищенный паклитаксель (30 г) растворяют в 200 мл ацетонитрила, разбавляют 250 мл деионизированной воды и перекачивают наверх хроматографической колонны низкого давления (размер 10•150 см), набитой полимерной смолой (Diaion, макропористая полиметакрилатная смола). После перекачивания образца колонну подвергают градиентному элюированию водным ацетонитрилом с шагом 35, 40, 45 и 50% ацетонитрила в воде. Изменение состава элюента отмечают по результатам ТСХ и ВЭЖХ фракций.
Фракции, объемом приблизительно 1 л каждая, собирают и анализируют с применением ТСХ и ВЭЖХ. Расход 75 мл/мин. Фракции с колонны, содержащие паклитаксель или цефаломанин, объединяют по отдельности. Два раствора, полученных объединением таких фракций, оставляют при температуре приблизительно 5oС до окончания кристаллизации индивидуальных соединений.
Кристаллы раздельно отфильтровывают, оба вещества перекристаллизовывают при 65oС из смеси метанол-вода.
Паклитаксель получают в виде белых игольчатых кристаллов со степенью чистоты выше 99%. Выход 18,5 г (0,009%).
Цефаломанин получают в виде белых игл с чистотой выше 98%. Выход 6,5 г (0,003%).
Фракции с предыдущей стадии, содержащие баккатин III и 10-деацетилбаккатин III, объединяют и упаривают в вакууме до по существу удаления ацетона, после чего экстрагируют 3 л смеси вода-дихлорметан (1:1 v/v). Органический слой упаривают досуха, остаток подвергают нормально-фазной хроматографии. Размеры применяемой колонны, набитой силикагелем (ситовый состав 200-300), равны 4"•4'. Состав элюента гексан : этилацетат (начало 50:50, окончание 35: 65) изменяют шаговым градиентным способом. Фракции, объемом приблизительно 1000 мл каждая, собирают и анализируют с применением ТСХ.
Фракции, содержащие баккатин III или 10-деацетилбаккатин III, собирают по отдельности и объединяют согласно результатам ТСХ, после чего упаривают досуха.
Часть продукта, содержащую баккатин III, растворяют в 200 мл метанола и оставляют на ночь в холодильнике. Образовавшиеся белые кристаллы отфильтровывают и перекристаллизовывают из метанола. Получают баккатин III в виде белых кристаллов. Выход 7,5 г (0,003%).
Неочищенный 10-деацетилбаккатин III растворяют в 150 мл ацетона, затем разбавляют 150 мл гексана. Смесь оставляют на ночь при комнатной температуре. Образовавшиеся белые кристаллы отфильтровывают и перекристаллизовывают из того же растворителя. Получают 10-деацетилбаккатин III в виде белых кристаллов. Выход 15 г (0,007%).
Пример 2
С использованием аппаратов и методики, подобных приведенным в примере 1, получают неочищенный паклитаксель. Неочищенный паклитаксель растворяют в 300 мл дихлорметана, раствор переносят в круглодонную трехгорлую колбу емкостью 1000 мл. Колбу помещают на ледяную баню, раствор перемешивают магнитной мешалкой. По достижении температуры около 5oС при перемешивании медленно добавляют раствор 10 эквивалентов брома в дихлорметане (1:1 v/v). Мольное соотношение цефаломанина и брома составляет 1:10.
С использованием аппаратов и методики, подобных приведенным в примере 1, получают неочищенный паклитаксель. Неочищенный паклитаксель растворяют в 300 мл дихлорметана, раствор переносят в круглодонную трехгорлую колбу емкостью 1000 мл. Колбу помещают на ледяную баню, раствор перемешивают магнитной мешалкой. По достижении температуры около 5oС при перемешивании медленно добавляют раствор 10 эквивалентов брома в дихлорметане (1:1 v/v). Мольное соотношение цефаломанина и брома составляет 1:10.
За ходом бромирования следят с помощью ТСХ, отбирая пробы с периодичностью от 5 до 10 мин. По окончании реакции реакционную массу разбавляют 300 мл дихлорметана и переносят в делительную воронку (для завершения реакции требуется от 40 до 50 мин). В реакционную смесь добавляют 350 мл 10%-ного водного раствора тиосульфата натрия для удаления избытка брома. Слой дихлорметана отделяют и промывают водой и насыщенным раствором поваренной соли, упаривают досуха в вакууме. Получают легкий коричневый порошок.
Пример 3
Неочищенный продукт из примера 2 растворяют в 120 мл ацетонитрила, разбавленного 150 мл деионизированной воды. Раствор перекачивают наверх обращенно-фазной хроматографической колонны (5•100 см), набитой силикагелем, привитым C18.
Неочищенный продукт из примера 2 растворяют в 120 мл ацетонитрила, разбавленного 150 мл деионизированной воды. Раствор перекачивают наверх обращенно-фазной хроматографической колонны (5•100 см), набитой силикагелем, привитым C18.
Колонну элюируют смесью ацетонитрил : вода (45:55) при рабочем давлении 206,84-275,79 кПа (от 30 до 40 psi). Расход 30 мл/мин. Собирают фракции по 250 мл каждая, которые затем анализируют с помощью ТСХ и объединяют.
Порцию, содержащую паклитаксель, оставляют в холодильнике на ночь, образовавшиеся кристаллы отфильтровывают и перекристаллизовывают из 70% метанола. Получают паклитаксель в виде белых игольчатых кристаллов со степенью чистоты выше 99%. Выход 6,1 г. Фракции, содержащие 2",3"-бромоцефаломанин, объединяют, экстрагируют смесью воды и дихлорметана. Органический слой отделяют и упаривают в вакууме досуха. Остаток растворяют в 150 мл метанола, разбавляют 50 мл воды для получения игольчатых кристаллов. Кристаллы грязно-белого цвета перекристаллизовывают из смеси метанол-вода. Получают 2", 3"-бромоцефаломанин в виде белых кристаллов.
В 30 мл АсОН растворяют 2 г 1",3"-бромоцефаломанина и прибавляют 2 г свежеактивированного цинка. Смесь перемешивают 3 ч при комнатной температуре, за ходом реакции следят с помощью ТСХ. После того как результаты ТСХ укажут на завершение реакции, смесь экстрагируют 300 мл смеси дихлорметана и 10% NaHCO3 (2:1). Органический слой промывают водой и упаривают досуха. Неочищенный продукт очищают флэш-хроматографией, получают цефаломанин в виде белого порошка.
Пример 4
Неочищенное вещество из примера 2 растворяют в 120 мл дихлорметана. Органический слой упаривают досуха, остаток подвергают нормально-фазной хроматографии. Размеры применяемой колонны, набитой силикагелем (ситовый состав между 200 и 300), равны 4"•4'. Проводят градиентное элюирование системой дихлорметан : этилацетат (начало 75:25, окончание 6:4), для выделения паклитакселя и 2",3"-бромоцефаломанина также могут быть использованы системы гексан : этилацетат (начало 6:4, окончание 4:6) и дихлорметан : ацетон (начало 8: 2, окончание 65:35). Фракции объемом 500 мл каждая собирают и анализируют с помощью ТСХ.
Неочищенное вещество из примера 2 растворяют в 120 мл дихлорметана. Органический слой упаривают досуха, остаток подвергают нормально-фазной хроматографии. Размеры применяемой колонны, набитой силикагелем (ситовый состав между 200 и 300), равны 4"•4'. Проводят градиентное элюирование системой дихлорметан : этилацетат (начало 75:25, окончание 6:4), для выделения паклитакселя и 2",3"-бромоцефаломанина также могут быть использованы системы гексан : этилацетат (начало 6:4, окончание 4:6) и дихлорметан : ацетон (начало 8: 2, окончание 65:35). Фракции объемом 500 мл каждая собирают и анализируют с помощью ТСХ.
Фракции, содержащие паклитаксель и 2",3"-бромоцефаломанин, собирают по отдельности и объединяют согласно результатам ТСХ, а затем упаривают досуха.
Часть, содержащую паклитаксель, растворяют в 100 мл метанола и разбавляют 35 мл воды, после чего выдерживают при охлаждении. Образовавшиеся белые кристаллы отфильтровывают и перекристаллизовывают из смеси метанол-вода. Получают 5,5 г паклитакселя в виде белых кристаллов.
Неочищенный 1", 3"-бромоцефаломанин растворяют в 50 мл ацетона, затем разбавляют 50 мл гексана. Смесь оставляют на ночь при комнатной температуре. Образовавшиеся белые кристаллы отфильтровывают и перекристаллизовывают из того же растворителя. Получают 2",3"-бромоцефаломанин в виде белых кристаллов.
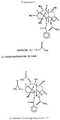
Структуры I и II иллюстрируют строение соединений.
Несмотря на то, что выше уже были описаны осуществления данного изобретения, это никак не ограничивает его, и любому специалисту в данной области очевидно, что многочисленные модификации являются частью данного изобретения, в той мере, в какой они не противоречат идее, содержанию и рамкам заявленного и описанного изобретения.
Claims (20)
1. Способ выделения и очистки таксановых аналогов из источника таксанов, отличающийся тем, что включает: экстракцию источника таксанов органическим экстрагентом; обработку слабо сорбирующей среды указанным экстрагентом и загрузку указанной среды в колонну, содержащую сорбент; элюирование на первой стадии смесью органических растворителей под давлением 68,948-137,90 кПа (от 10 до 20 psi) для получения фракций, содержащих таксановые соединения; кристаллизацию указанных фракций для получения твердого таксанового соединения и маточного раствора, концентрирование указанного маточного раствора; элюирование маточного раствора на второй стадии смесью полярных растворителей через полимерную смолу для выделения по меньшей мере второго таксанового соединения.
2. Способ по п.1, отличающийся тем, что дополнительно включает стадию удаления лигниновых и флавоноидных примесей на указанной первой стадии.
3. Способ по п. 1, отличающийся тем, что указанный источник таксанов включает растительный источник.
4. Способ по п. 3, отличающийся тем, что в нем указанный растительный источник выбирается из группы, состоящей из Taxus brevifolia, Taxus baccata, Taxus walichiana, Taxus yunnanensis и Taxus canadensis.
5. Способ по п.3, отличающийся тем, что указанные таксаны включают по меньшей мере 13-ацетил-9-дигидробаккатин III, 10-деацетилбаккатин III, баккатин III, цефаломанин, паклитаксель.
6. Способ по п.1, отличающийся тем, что указанный органический экстрагент включает дихлорметан.
7. Способ по п. 1, отличающийся тем, что указанная слабо сорбирующая среда включает Celite 545.
8. Способ по п.1, отличающийся тем, что указанный сорбент включает окись алюминия.
9. Способ по п.1, отличающийся тем, что указанный органический растворитель на первой стадии включает смесь гексана и ацетона.
10. Способ выделения и очистки таксанов из источника, содержащего таксаны, отличающийся тем, что включает: получение источника таксанов; экстракцию указанных таксанов из указанного источника в органическую экстракционную среду с получением органического слоя, содержащего таксановые соединения; обработку носителя указанным органическим слоем; применение колонны низкого давления, содержащей сорбент; элюирование указанной колонны органическим растворителем на первой стадии для получения очищенных таксановых фракций; кристаллизацию указанных таксановых фракций для получения первого из таксановых аналогов и маточного раствора; элюирование указанного маточного раствора на второй стадии через полимерную смолу на хроматографической колонне для очистки и выделения по меньшей мере второго таксанового аналога и третьего таксанового аналога; сбор разделенных таксановых аналогов.
11. Способ по п.10, отличающийся тем, что дополнительно включает стадию удаления лигниновых и флавоноидных примесей на указанной первой стадии.
12. Способ по п.10, отличающийся тем, что дополнительно включает стадию размола указанного источника таксанов и экстракцию метанолом.
13. Способ по п.12, отличающийся тем, что дополнительно включает стадию смешения экстракта с активированным углем, фильтрацию и выпаривание для получения концентрата.
14. Способ по п.13, отличающийся тем, что указанный носитель включает Сelite 545.
15. Способ по п.1, отличающийся тем, что указанный органический растворитель включает смесь ацетона и гексана.
16. Способ по п.15, отличающийся тем, что указанный органический растворитель пропускают через указанную колонну под давлением 68,948-137,90 кПа (от 10 до 20 рsi).
17. Способ по п.1, отличающийся тем, что дополнительно включает стадию сбора и анализа указанных таксановых фракций с помощью тонкослойной хроматографии.
18. Способ выделения и очистки таксанов из источника, содержащего таксаны, отличающийся тем, что включает: получение источника таксанов; экстракцию указанных таксанов из указанного источника в органическую экстракционную среду с получением органического слоя, содержащего таксановые соединения; обработку носителя указанным органическим слоем; применение колонны низкого давления, содержащей сорбент; элюирование указанной колонны органическим растворителем на первой стадии под давлением 68,948-137,90 кПа (от 10 до 20 psi) для получения очищенных таксановых фракций и удаления флавоноидных и лигниновых примесей; кристаллизацию указанных таксановых фракций для получения первого таксанового аналога и маточного раствора; элюирование указанного маточного раствора на второй стадии через смолу полистирол-дивинилбензол на хроматографической колонне под давлением 206,84 кПа (30 psi) для очистки и выделения по меньшей мере второго таксанового аналога и третьего таксанового аналога; элюирование на третьей стадии указанного второго таксанового аналога и третьего таксанового аналога через нормальнофазную колонну с силикагелем для очистки указанного второго таксанового аналога и указанного третьего таксанового аналога; сбор разделенных таксановых аналогов.
19. Способ по п.18, отличающийся тем, что указанный второй таксановый аналог включает баккатин III, а указанный третий таксановый аналог включает 10-деацетилбаккатин III.
20. Способ по п.18, отличающийся тем, что указанные аналоги имеют степень чистоты по меньшей мере 98%.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US09/226,192 | 1999-01-07 | ||
| US09/226,192 US5969165A (en) | 1999-01-07 | 1999-01-07 | Isolation and purification of paclitaxel and other related taxanes by industrial preparative low pressure chromatography on a polymeric resin column |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2000100420A RU2000100420A (ru) | 2001-11-27 |
| RU2201788C2 true RU2201788C2 (ru) | 2003-04-10 |
Family
ID=22847945
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2000100420/12A RU2201788C2 (ru) | 1999-01-07 | 2000-01-06 | Выделение и очистка паклитакселя и других родственных таксанов с помощью промышленной препаративной хроматографии низкого давления на колонне с полимерной смолой |
Country Status (22)
| Country | Link |
|---|---|
| US (1) | US5969165A (ru) |
| EP (1) | EP1018510B1 (ru) |
| JP (1) | JP2000204090A (ru) |
| KR (1) | KR20000062437A (ru) |
| CN (1) | CN1266059A (ru) |
| AR (1) | AR022218A1 (ru) |
| AT (1) | ATE260908T1 (ru) |
| AU (1) | AU768026B2 (ru) |
| BR (1) | BR0000884A (ru) |
| DE (1) | DE69915241T2 (ru) |
| DK (1) | DK1018510T3 (ru) |
| ES (1) | ES2216431T3 (ru) |
| IL (1) | IL133956A (ru) |
| IN (1) | IN186600B (ru) |
| NO (1) | NO321779B1 (ru) |
| NZ (1) | NZ502204A (ru) |
| PL (1) | PL337764A1 (ru) |
| PT (1) | PT1018510E (ru) |
| RU (1) | RU2201788C2 (ru) |
| SG (1) | SG87072A1 (ru) |
| SK (1) | SK292000A3 (ru) |
| ZA (1) | ZA200000036B (ru) |
Families Citing this family (38)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP1254128A2 (en) * | 2000-01-13 | 2002-11-06 | Purdue Research Foundation | Production of taxol and taxanes |
| US6452024B1 (en) | 2000-02-22 | 2002-09-17 | Chaichem Pharmaceuticals International | Process for extraction and purification of paclitaxel from natural sources |
| AU2006201733B2 (en) * | 2000-03-10 | 2007-05-24 | Ivax Research, Inc. | Process for manufacturing paclitaxel and 13-acetyl-9-dihydrobaccatin III |
| US6229027B1 (en) * | 2000-03-10 | 2001-05-08 | Jian Liu | Process for manufacturing paclitaxel and 13-acetyl-9-dihydrobaccatin IV |
| WO2002038556A2 (en) * | 2000-11-08 | 2002-05-16 | Actipharm, Inc. | Process for mass production of gmp paclitaxel and related taxanes |
| EP1335910A1 (en) * | 2000-11-13 | 2003-08-20 | Lahu Saiji | Isolation of taxanes |
| US6333419B1 (en) * | 2000-11-28 | 2001-12-25 | Indena Spa | Chromatographic separation method of paclitaxel and cephalomannin |
| AU2002344514A1 (en) * | 2002-10-17 | 2004-05-25 | Jingyu Liang | A natural compound useful for treating diabetes, its preparation and use |
| US6759539B1 (en) | 2003-02-27 | 2004-07-06 | Chaichem Pharmaceuticals International | Process for isolation and purification of paclitaxel from natural sources |
| CN100448859C (zh) * | 2003-03-17 | 2009-01-07 | 天然医药品公司 | 使用键合有聚乙烯亚胺的树脂提纯紫杉醇和紫杉醇混合物的方法 |
| US8703982B2 (en) | 2003-03-17 | 2014-04-22 | Phyton Holdings Llc | Purification of taxanes |
| US6956123B2 (en) * | 2003-03-17 | 2005-10-18 | Natural Pharmaccuticals, Inc. | Purification of taxanes and taxane mixtures using polyethyleneimine-bonded resins |
| FR2859996B1 (fr) * | 2003-09-19 | 2006-02-03 | Aventis Pharma Sa | Solvat acetonique du dimethoxy docetaxel et son procede de preparation |
| US7259268B2 (en) * | 2003-12-31 | 2007-08-21 | Samyang Genex Corporation | Method for purification of paclitaxel from paclitaxel-containing materials |
| ES2293129T3 (es) * | 2004-07-13 | 2008-03-16 | Indena Spa | Procedimiento para obtener paclitaxel de plantas de taxus. |
| US7169307B2 (en) * | 2004-09-02 | 2007-01-30 | Jian Liu | Process for the extraction of paclitaxel and 9-dihydro-13-acetylbaccatin III from Taxus |
| US20060074254A1 (en) * | 2004-09-30 | 2006-04-06 | Zisheng Zhang | Process for extracting taxanes |
| CN1331859C (zh) * | 2005-01-04 | 2007-08-15 | 四川华申科技开发有限公司 | 分离紫杉醇和三尖杉磷碱的方法 |
| EP1818328A1 (en) * | 2006-02-10 | 2007-08-15 | 6570763 Canada Inc. | Chromatographic method for the isolation and purification of taxane derivatives |
| ATE489375T1 (de) * | 2006-03-24 | 2010-12-15 | Postech Foundation | Stationäre phase und säule unter verwendung von cucurbiturilgebundenem kieselgel, und verfahren zur abtrennung von taxol unter verwendung der säule |
| CN101460473A (zh) | 2006-04-03 | 2009-06-17 | 药物热化学品公司 | 热提取方法和产物 |
| US7905990B2 (en) | 2007-11-20 | 2011-03-15 | Ensyn Renewables, Inc. | Rapid thermal conversion of biomass |
| KR101149600B1 (ko) * | 2009-12-31 | 2012-05-29 | 주식회사 삼양제넥스바이오 | 고순도 무수결정형 도세탁셀 제조방법 |
| US20110284359A1 (en) | 2010-05-20 | 2011-11-24 | Uop Llc | Processes for controlling afterburn in a reheater and for controlling loss of entrained solid particles in combustion product flue gas |
| US8499702B2 (en) | 2010-07-15 | 2013-08-06 | Ensyn Renewables, Inc. | Char-handling processes in a pyrolysis system |
| US9441887B2 (en) | 2011-02-22 | 2016-09-13 | Ensyn Renewables, Inc. | Heat removal and recovery in biomass pyrolysis |
| US9347005B2 (en) | 2011-09-13 | 2016-05-24 | Ensyn Renewables, Inc. | Methods and apparatuses for rapid thermal processing of carbonaceous material |
| US9044727B2 (en) | 2011-09-22 | 2015-06-02 | Ensyn Renewables, Inc. | Apparatuses and methods for controlling heat for rapid thermal processing of carbonaceous material |
| US10041667B2 (en) | 2011-09-22 | 2018-08-07 | Ensyn Renewables, Inc. | Apparatuses for controlling heat for rapid thermal processing of carbonaceous material and methods for the same |
| US10400175B2 (en) | 2011-09-22 | 2019-09-03 | Ensyn Renewables, Inc. | Apparatuses and methods for controlling heat for rapid thermal processing of carbonaceous material |
| US9109177B2 (en) | 2011-12-12 | 2015-08-18 | Ensyn Renewables, Inc. | Systems and methods for renewable fuel |
| US9670413B2 (en) | 2012-06-28 | 2017-06-06 | Ensyn Renewables, Inc. | Methods and apparatuses for thermally converting biomass |
| AR097135A1 (es) | 2013-06-26 | 2016-02-24 | Ensyn Renewables Inc | Sistemas y métodos para combustible renovable |
| CN104422749A (zh) * | 2013-09-04 | 2015-03-18 | 南京工业大学 | 一种分离、纯化紫杉醇与三尖杉宁碱的制备方法 |
| CN103588736B (zh) * | 2013-12-03 | 2015-06-03 | 云南汉德生物技术有限公司 | 13-乙酰基-9-羟基巴卡亭iii的提取分离方法 |
| US10337726B2 (en) | 2015-08-21 | 2019-07-02 | Ensyn Renewables, Inc. | Liquid biomass heating system |
| HUP1500603A2 (en) | 2015-12-11 | 2017-06-28 | Rotachrom Tech Kft | Process for the separation of 10-deacetyl baccatin iii |
| WO2018125753A1 (en) | 2016-12-29 | 2018-07-05 | Ensyn Renewables, Inc. | Demetallization of liquid biomass |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5475120A (en) * | 1990-11-02 | 1995-12-12 | University Of Florida | Method for the isolation and purification of taxol and its natural analogues |
| AU1888792A (en) * | 1991-04-19 | 1992-11-17 | University Of Mississippi, The | Methods and compositions for isolating taxanes |
| FR2696462B1 (fr) * | 1992-10-05 | 1994-11-25 | Rhone Poulenc Rorer Sa | Procédé d'obtention de la désacétyl-10 baccatine III. |
| US5281727A (en) * | 1992-11-27 | 1994-01-25 | Napro Biotherapeutics, Inc. | Method of using ion exchange media to increase taxane yields |
| US5620875A (en) * | 1995-02-17 | 1997-04-15 | University Of Portland | Transfer of taxol from yew tree cuttings into a culture medium over time |
| JPH08277280A (ja) * | 1995-04-06 | 1996-10-22 | Nippon Steel Corp | イチイ細胞からのタキサン化合物の抽出方法 |
| AU5516596A (en) * | 1995-04-29 | 1996-11-21 | Samyang Genex Co., Ltd. | A method for mass production of taxol from taxus genus plant |
| US5654448A (en) * | 1995-10-02 | 1997-08-05 | Xechem International, Inc. | Isolation and purification of paclitaxel from organic matter containing paclitaxel, cephalomannine and other related taxanes |
| JPH1052296A (ja) * | 1996-08-09 | 1998-02-24 | Nippon Oil Co Ltd | タキサン類化合物の製造方法(iii) |
-
1999
- 1999-01-07 US US09/226,192 patent/US5969165A/en not_active Expired - Fee Related
- 1999-12-27 PT PT99126036T patent/PT1018510E/pt unknown
- 1999-12-27 AT AT99126036T patent/ATE260908T1/de not_active IP Right Cessation
- 1999-12-27 DE DE69915241T patent/DE69915241T2/de not_active Expired - Fee Related
- 1999-12-27 DK DK99126036T patent/DK1018510T3/da active
- 1999-12-27 EP EP99126036A patent/EP1018510B1/en not_active Expired - Lifetime
- 1999-12-27 ES ES99126036T patent/ES2216431T3/es not_active Expired - Lifetime
-
2000
- 2000-01-06 NO NO20000070A patent/NO321779B1/no unknown
- 2000-01-06 IN IN7CA2000 patent/IN186600B/en unknown
- 2000-01-06 RU RU2000100420/12A patent/RU2201788C2/ru not_active IP Right Cessation
- 2000-01-06 JP JP2000000798A patent/JP2000204090A/ja active Pending
- 2000-01-07 AU AU10145/00A patent/AU768026B2/en not_active Ceased
- 2000-01-07 PL PL00337764A patent/PL337764A1/xx not_active Application Discontinuation
- 2000-01-07 AR ARP000100057A patent/AR022218A1/es active IP Right Grant
- 2000-01-07 BR BR0000884-2A patent/BR0000884A/pt not_active IP Right Cessation
- 2000-01-07 KR KR1020000000588A patent/KR20000062437A/ko not_active Application Discontinuation
- 2000-01-07 NZ NZ502204A patent/NZ502204A/en not_active IP Right Cessation
- 2000-01-07 ZA ZA200000036A patent/ZA200000036B/xx unknown
- 2000-01-07 CN CN00102118A patent/CN1266059A/zh active Pending
- 2000-01-07 SG SG200000086A patent/SG87072A1/en unknown
- 2000-01-07 SK SK29-2000A patent/SK292000A3/sk unknown
- 2000-01-09 IL IL13395600A patent/IL133956A/xx not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| PL337764A1 (en) | 2000-07-17 |
| EP1018510B1 (en) | 2004-03-03 |
| ZA200000036B (en) | 2000-07-12 |
| AR022218A1 (es) | 2002-09-04 |
| NZ502204A (en) | 2001-06-29 |
| NO20000070L (no) | 2000-07-10 |
| US5969165A (en) | 1999-10-19 |
| DE69915241D1 (de) | 2004-04-08 |
| ATE260908T1 (de) | 2004-03-15 |
| SK292000A3 (en) | 2000-10-09 |
| IL133956A (en) | 2003-10-31 |
| IL133956A0 (en) | 2001-04-30 |
| AU768026B2 (en) | 2003-11-27 |
| IN186600B (ru) | 2001-10-06 |
| ES2216431T3 (es) | 2004-10-16 |
| AU1014500A (en) | 2000-07-13 |
| PT1018510E (pt) | 2004-06-30 |
| CN1266059A (zh) | 2000-09-13 |
| EP1018510A1 (en) | 2000-07-12 |
| NO20000070D0 (no) | 2000-01-06 |
| DE69915241T2 (de) | 2004-12-30 |
| SG87072A1 (en) | 2002-03-19 |
| KR20000062437A (ko) | 2000-10-25 |
| BR0000884A (pt) | 2001-08-21 |
| DK1018510T3 (da) | 2004-07-05 |
| JP2000204090A (ja) | 2000-07-25 |
| NO321779B1 (no) | 2006-07-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2201788C2 (ru) | Выделение и очистка паклитакселя и других родственных таксанов с помощью промышленной препаративной хроматографии низкого давления на колонне с полимерной смолой | |
| RU2108330C1 (ru) | Способы получения 10-дезацетил-баккатина iii | |
| RU2000100420A (ru) | Выделение и очистка паклитакселя и других родственных таксанов с помощью промышленной препаративной хроматографии низкого давления на колонне с полимерной смолой | |
| EP0774010B1 (en) | A method for mass production of taxol from taxus genus plant | |
| US20030032820A1 (en) | Process for mass production of GMP paclitaxel and related taxanes | |
| US7169307B2 (en) | Process for the extraction of paclitaxel and 9-dihydro-13-acetylbaccatin III from Taxus | |
| EP1818328A1 (en) | Chromatographic method for the isolation and purification of taxane derivatives | |
| CA2402519C (en) | Process for manufacturing paclitaxel and 13-acetyl-9-dihydrobaccatin iii | |
| US6878832B2 (en) | Isolation of taxanes | |
| CA2258066C (en) | Isolation and purification of paclitaxel, and other related taxanes by industrial preparative low pressure chromatography on a polymeric resin column | |
| CZ200070A3 (cs) | Izolace a čištění paclitaxelu a dalších příbuzných taxanů průmyslovou preparativní nízkotlakou chromatografií na polymerních kolonách | |
| MXPA00000318A (en) | Isolation and purification of paclitaxel and other related taxanes by industrial preparative low pressure chromatography on a polymeric resin column | |
| RU2373198C2 (ru) | СПОСОБЫ ПОЛУЧЕНИЯ ПАКЛИТАКСЕЛА ИЗ РАСТЕНИЙ РОДА Taxus | |
| KR100259396B1 (ko) | 택서스속 식물체로부터 택솔의 대량 추출 정제방법 | |
| CA2536000C (en) | Process for the extraction of paclitaxel and 9-dihydro-13-acetylbaccatin iii from taxus | |
| KR100259395B1 (ko) | 택서스속 식물체로부터 택솔의 대량 추출 정제방법 | |
| UA68355C2 (en) | Method for isolating and purifying taxan analogues, in particular paclitaxel (variants) | |
| AU2006201733B2 (en) | Process for manufacturing paclitaxel and 13-acetyl-9-dihydrobaccatin III | |
| WO2003080587A1 (en) | Labelled taxanes | |
| WO1999036413A1 (en) | Novel crystalline complexes of baccatin iii with imidazole, 2-methylimidazole or isopropanol |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20080107 |