RU2188637C2 - Применение алкалоидов класса ламелларина в способах лечения - Google Patents
Применение алкалоидов класса ламелларина в способах лечения Download PDFInfo
- Publication number
- RU2188637C2 RU2188637C2 RU98101364/14A RU98101364A RU2188637C2 RU 2188637 C2 RU2188637 C2 RU 2188637C2 RU 98101364/14 A RU98101364/14 A RU 98101364/14A RU 98101364 A RU98101364 A RU 98101364A RU 2188637 C2 RU2188637 C2 RU 2188637C2
- Authority
- RU
- Russia
- Prior art keywords
- resistant
- lamellarin
- multidrug
- derivative
- group
- Prior art date
Links
- 0 CC(C(C(C12)C(**)(*I)C(*)(*3CC3)c3c1c(*)c(*)c(*)c3*)=C1C2c2c(**)c(**)c(C)c(*)c2*)Oc2c1c(C)c(C)c(C)c2** Chemical compound CC(C(C(C12)C(**)(*I)C(*)(*3CC3)c3c1c(*)c(*)c(*)c3*)=C1C2c2c(**)c(**)c(C)c(*)c2*)Oc2c1c(C)c(C)c(C)c2** 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/475—Quinolines; Isoquinolines having an indole ring, e.g. yohimbine, reserpine, strychnine, vinblastine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Steroid Compounds (AREA)
- Coating Apparatus (AREA)
Abstract
Изобретение относится к медицине, в частности к онкологии, и касается способа лечения мультилекарственно резистентных опухолей у млекопитающих, включающих введение пациенту, нуждающемуся в таком лечении, эффективного количества ингибирующего мультилекарственную резистентность антимультилекарственно резистентного производного ламелларина. Предложенный способ позволяет повысить эффективность лечения и устранить побочные токсические эффекты. 4 c. и 11 з.п.ф-лы, 5 табл.
Description
Доказано, что морские асцидианы являются ценными источниками алкалоидов различных структур, многие из которых проявляют биологическую активность широкого спектра действия. Представители семейства Didemnidae обычно являются организмами с насыщенной окраской, образующими сплошное покрытие и колониальными по образу жизни, и характеристически содержат химические составляющие, которые образуются из аминокислот. Например, полиароматические ламеллариновые алкалоиды, вероятно, являются производными трех тирозиновых остатков. Структура ламелларина была впервые идентифицирована при выделении из моллюска прозобранх вида Lamellaria spp., из Палау, но недавно соединения этих структур были обнаружены в дидемнидных асцидианах Didemnum chartaceum на Сейшелах. Предполагалось также, что ламелларины могут отдаленно относится к тунихромам (tunichrome), восстанавливающим пигменты крови и выделенным из асцидиана вида Ascidia nigra.
Anderson et al., J. Am. Chem Soc., 107: 5492-5495 (1985) описали выделение и характеристики четырех полиароматических метаболитов ламеллатинов A-D, полученных из морского моллюска прозобранха Lamellaria sp. Структура ламелларина А была определена путем рентгенокристаллографии, а структуры ламелларинов B-D были установлены посредством обработки данных спектрального анализа. Эта публикация включена здесь в качестве ссылки.
Lindquist et al., J. Org. Chem., 53: 4570-4574 (1988) описали выделение и характеристики четырех новых алкалоидов пластинообразной структуры из морского асцидиана Didemnum chartaceum из Индийского океана. Структура ламелларина Е была установлена методами спектроскопии и рентгенокристаллографии. Структуры ламелларинов F-H были описаны посредством обработки данных ЯМР-спектроскопии. Эта публикация включена здесь в качестве ссылки.
Carroll et al., Aust. J. Chem., 46: 489-501 (1993) описали шесть новых полиароматических алкалоидов, ламмеларины I, J, K, L, M и триацетат ламелларина N и четыре известных алкалоида этого типа, ламелларины А, В, С и триацетат ламелларина D, выделенные из морского асцидиана вида Didemnum sp. Эта публикация включена здесь в качестве ссылки.
Найдено, что ламеллариновые производные, описанные здесь, являются нетоксичными ингибиторами приобретенной мультилекарственной резистентности (МЛР), которая становится главной проблемой в лечении различных опухолевых заболеваний человека. Было также обнаружено, что ламеллариновые производные являются цитотоксичными по отношению к МЛР клеткам. Обе эти активности могут использоваться при лечении МЛР опухолей.
Лекарства, обладающие доказанной противоопухолевой химиотерапевтической активностью, у которых наблюдается мультилекарственная резистентность, включают винбластин, винкристин, этопозид, тенипозид, доксорубицин (адриамицин), даунорубицин, плизмацин (митрамицин) и актиномицин D. Многие опухоли являются наследственно мультилекарственно резистентными (например, аденокарциномы толстой кишки и почки), в то время как другие опухоли приобретают мультилекарственную резистентность в процессе лечения (например, нейробластома и детская лейкемия).
Не заостряя внимание на основополагающей теории, считают, что mdr ген кодирует гликопротеид (Р-170 или Р-гликопротеид). Этот белок является жестким, чтобы действовать в качестве энергетически независимого отсасывающего насоса, который используется в нормальных клетках, а также в раковых клетках для их детоксикации. Но когда последние способны преодолеть экспрессию гена, влияние противоопухолевого лекарства в таких клетках в значительной степени снижается и, следовательно, появляется МЛР фенотип. См., например, Deuchars et al. , Seminars in Oncology, 16:156-165(1989) и Gottesman et al., Ann. Rev. Biochem.,62:385-427(1993). Существуют два способа преодоления МЛР: (1) найти ингибиторы Р-170 или (2) найти лекарства, которые являются активными против МЛР линий раковых клеток, а также являются нормальной контрчастью для указанных линий клеток.
Ингибиторы МЛР представляют собой реагенты, которые используются для восстановления чувствительности к лекарствам некоторых опухолевых клеток с мультилекарственной резистентностью. Как известно, реагентами, обладающими такой способностью, являются некоторые вещества, блокирующие транспорт кальция (например, верапамил) и некоторые ингибиторы калмодилина (например, трифторпиразин). Однако клиническое применение этих соединений ограничивается их побочными токсическими действиями. Cм. Ozols et al., J. Clin.Oncol., 5: 541-547(1987), u Twentyman et al., Int. J. Radiat.Oncol.Biol.Phys.,12: 1355(1986). Поэтому сведение к минимуму (или удаление) таких побочных токсичных эффектов является важным фактором в отборе ингибитора МЛР.
Поскольку верапамил был описан первым, были описаны несколько соединений из природных продуктов, преодолевающих или ингибирующих МЛР. Примеры таких соединений включают растительный алкалоид таилбластин (см.Сhеn et al., Cancer Res., 53:2544-2547(1993)) и морской природный продукт пателламинд D (см. Williams et al.,Cancer Letters,71:97-102(1993)). Другими примерами соединений, активных против МЛР, являются пептидный циклоспорин А (см. Beck et al., Biochem. Pharmacol., 43: 89-93 (1992)), гетероциклическое соединение 5-N-ацетилардеемин (см. Karwowsky et al., J. Antibiotics, 46: 374-379 (1993)), геодиамолид А, джаспамид и гласиастерол A (glaciasterol A) (см. Stingi et al., Cancer Chemother. Pharmacol., 30: 401-406 (1992)). Таким образом, поиск новых ингибиторов МЛР и соединений, активных против МЛР клеток, продолжается.
Краткое описание изобретения
Обнаружено, что производные ламелларина, описанные здесь, являются нетоксичными ингибиторами приобретенной мультилекарственной резистентности (МЛР), к действию большого количества, которая стала главной проблемой при лечении различных опухолей человека. Обнаружено также, что производные ламелларина цитотоксичны по отношению к МЛР клеткам. Обе эти активности могут использоваться при лечении МЛР опухолей. Как описано выше, полагают, что МЛР связана с некоторыми изменениями в опухолевых клетках, включая сверхэкспрессию определенного высокомолекулярного мембранного гликопротеида и снижение способности опухолевой клетки аккумулировать и удерживать химиотерапевтические агенты.
Обнаружено, что производные ламелларина, описанные здесь, являются нетоксичными ингибиторами приобретенной мультилекарственной резистентности (МЛР), к действию большого количества, которая стала главной проблемой при лечении различных опухолей человека. Обнаружено также, что производные ламелларина цитотоксичны по отношению к МЛР клеткам. Обе эти активности могут использоваться при лечении МЛР опухолей. Как описано выше, полагают, что МЛР связана с некоторыми изменениями в опухолевых клетках, включая сверхэкспрессию определенного высокомолекулярного мембранного гликопротеида и снижение способности опухолевой клетки аккумулировать и удерживать химиотерапевтические агенты.
Таким образом, настоящее изобретение относится к способам лечения определенных опухолей эффективным анти-МЛР количеством, то есть количеством, которое либо эффективно ингибирует МЛР, либо оказывает эффективное цитотоксическое действие, либо и то, и другое, одного или нескольких производных ламелларина, которые, как установлено, являются эффективными противоопухолевыми агентами в отношении МЛР клеток.
Итак, в одном предпочтительном воплощении данного изобретения предлагается способ лечения (то есть замедлением или остановкой роста) МЛР опухолей, включающий введение соединения, имеющего одну (или обе) из следующих формул, в количестве, эффективно ингибирующем МЛР:
где R1-R17 (в формуле А) или R1-R15 (в формуле В) могут быть одинаковыми или могут отличаться и выбраны из группы, включающей -Н,-ОН,-Me,-Et,-Pro,-OМe,-CОMe u -ОСОМе.
где R1-R17 (в формуле А) или R1-R15 (в формуле В) могут быть одинаковыми или могут отличаться и выбраны из группы, включающей -Н,-ОН,-Me,-Et,-Pro,-OМe,-CОMe u -ОСОМе.
Таким образом, во втором предпочтительном воплощении настоящего изобретения предлагается способ лечения (т.е. замедления или остановки роста) МЛР опухолей, включающий введение эффективного в отношении МЛР клеток цитотоксического количества анти-МЛР производного ламелларина, а именно формулы А или В, которые представлены выше.
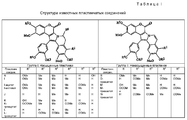
Следовательно, настоящее изобретение относится к способам лечения с использованием производных ламелларина, описываемых двумя общими формулами А и В, и более конкретно к способам лечения с использованием ламелларинов, представленных в табл. 1, в качестве особенно предпочтительных примеров соединений, используемых в настоящем изобретении. В табл. 1 приведено строение известных производных ламелларинов.
Подробное описание предпочтительных воплощений
Как описано выше, настоящее изобретение относится к новым способам лечения опухолей у млекопитающих, включающим введение пациенту, нуждающемуся в таком лечении, ламелларинов либо в качестве ингибиторов МЛР активности, либо в качестве МЛР-цитотоксичных соединений. Таким образом, ламелларины могут применяться против МЛР опухолей либо сами по себе, либо в сочетании с другими противоопухолевыми лекарственными средствами как эффективные способы лечения МЛР клеток.
Как описано выше, настоящее изобретение относится к новым способам лечения опухолей у млекопитающих, включающим введение пациенту, нуждающемуся в таком лечении, ламелларинов либо в качестве ингибиторов МЛР активности, либо в качестве МЛР-цитотоксичных соединений. Таким образом, ламелларины могут применяться против МЛР опухолей либо сами по себе, либо в сочетании с другими противоопухолевыми лекарственными средствами как эффективные способы лечения МЛР клеток.
Настоящее изобретение также относится к фармацевтическим композициям, содержащим одно или несколько производных ламелларина, которые могут использоваться, как здесь описано. Кроме того, такие фармацевтические композиции могут дополнительно содержать одно или несколько других противоопухолевых лекарственных средств, в частности таких, к которым наблюдалась мультилекарственная резистентность, включая, например, винбластин, винкристин, этопозид, тенипозид, доксарубицин (адриамицин), даунорубицин, пликамицин (митрамицин) и актиномицин D.
Таким образом, настоящее изобретение относится также к способу усиления противоопухолевого химиотерапевтического действия лекарственных средств, которые вызывают МЛР у пациентов, нуждающихся в таком лечении, который включает совместное введение (одновременно или последовательно) противоопухолевого лекарства, вызывающего МЛР, и эффективного анти-МЛР количества производного ламелларина.
Как здесь показано, было обнаружено, что соединения по данному изобретению проявляют МЛР противоопухолевую активность в опытах как in vitro, так и in vivo, поэтому полагают, что эти цитотоксические соединения могут быть использованы в качестве МЛР противоопухолевых соединений для животных и, предпочтительно, для людей.
При использовании в качестве цитотоксических агентов или противоопухолевых ингибиторов МЛР соединения по настоящему изобретению могут быть приготовлены и введены в виде различных стандартных лекарственных форм, особенно в виде стандартных лекарственных форм для парентерального введения. Специалисту понятно, что стандартные лекарственные формы могут содержать в качестве активного ингредиента одно или несколько соединений по данному изобретению. Специалисту, вероятно, понятно, что дозы и способы введения будут изменяться в соответствии с потребностями пациента и конкретной активностью активного(ных) ингредиента(тов). Определение этих параметров является обычной практикой лечащего врача.
В табл. 2 и 3 приводятся дополнительные сведения об активности ламелларинов. Эти данные были получены с помощью методов, описанных далее.
Определение МЛР активности
Чувствительные и МЛР клетки выдерживали в фазе логарифмического роста в минимально необходимом количестве среды Игла (Eagle's Minimum Essential Medium) со сбалансированными по Иглу солями (Earle's Balanced Salts), с несущественными аминокислотами, с 2,0 мМ L-глютамина, без бикарбоната натрия (ЕМЕМ/nеаа), с добавлением 5% фетальной телячьей сыворотки (FSC), 10-2 M бикарбоната натрия и 0,1 г/л пенициллина G+0,1 г/л стрептомицинсульфата.
Чувствительные и МЛР клетки выдерживали в фазе логарифмического роста в минимально необходимом количестве среды Игла (Eagle's Minimum Essential Medium) со сбалансированными по Иглу солями (Earle's Balanced Salts), с несущественными аминокислотами, с 2,0 мМ L-глютамина, без бикарбоната натрия (ЕМЕМ/nеаа), с добавлением 5% фетальной телячьей сыворотки (FSC), 10-2 M бикарбоната натрия и 0,1 г/л пенициллина G+0,1 г/л стрептомицинсульфата.
Клеточную цитотоксичность в опытах in vitro определяют с использованием бромида 3-[4,5-диметилтиазол-2-ил] -2,5-дифенилтетразола (МТТ) от фирмы Sigma, Ref. : 2128 для количественного измерения роста клеток и их жизнеспособности. См. публикацию Т. Massmann, Rapid Colorimetric Assay for Growth and Survival: Aoolication to Proliferation and Cytotoxicity Assays, Journal of Immunological Methods, 65: 55-63 (1983).
Используют следующие линии опухолевых клеток: Р-833 (АТТСС CCL 46), суспензионная культура лимфоидной неоплазмы из мыши DBA/2 и соответствующая линия MDR клеток Р-388/SHABEL; CHOB1 (ATCCCCL 16), монослойная культура яичника хомячка китайского и соответствующая линия MDR клеток - СНОС5. См.публикацию Rausher 111 et al., Characterization of Auromycin-Resistant Hamster Cell Mutants that Display a Multidrag Resistance Phernotype, Molecular Pharmacology, 38: 198-206 (1990).
В этом опыте применяют 96-ячеечные клеточные культуральные планшеты диаметром 99 мм. Клетки высевают в ячейки с концентрацией 1х103 клеток на ячейку в 100 мкл аликвотах ЕМЕМ c 5% FSC, содержащие различные концентрации соответствующих ламелларинов и другие соединения (контроль), которые подлежат испытанию. Высевают также две отдельные серии культур без лекарств, одну - в качестве контроля роста для подтверждения того, что клетки находятся в экспоненциальной фазе роста, другую - без клеток, в качестве контроля среды. Все определения проводят повторно.
После трех дней инкубирования при 37oС, 10% СО2 в атмосфере с влажностью 98% в каждую ячейку добавляют 150 мкл МТТ в 100 мкл аликвотах изопропанола. Широкий абсорбционный спектр для изопропанольного раствора кристаллов является оптимальным при 570 нм. Величины оптических плотностей получают с помощью микропланшетного читающего устройства Dynatech и результаты опыта используют для получения графиков, по которым вычисляют IС50, где IС50 представляет собой концентрацию в опыте, которая дает 50% ингибирование роста клеток.
Другие биологические свойства
Производные ламелларина также обладают иммуномодулирующей активностью и, таким образом, могут использоваться в качестве иммуномодуляторных соединений. Иммуномодуляторные соединения и композиции, как подразумевает их название, могут использоваться для модулирования или регулирования иммунорегуляторных функций у теплокровных животных. Иммуномодуляторы могут быть иммуностимуляторами для повышения иммунитета для инициирования лечения некоторых заболеваний и расстройств. И, наоборот, они могут быть иммуноингибиторами или иммуносуппрессорами для профилактики нежелательных иммунных реакций организма на инородные материалы и аутоиммунных заболеваний.
Производные ламелларина также обладают иммуномодулирующей активностью и, таким образом, могут использоваться в качестве иммуномодуляторных соединений. Иммуномодуляторные соединения и композиции, как подразумевает их название, могут использоваться для модулирования или регулирования иммунорегуляторных функций у теплокровных животных. Иммуномодуляторы могут быть иммуностимуляторами для повышения иммунитета для инициирования лечения некоторых заболеваний и расстройств. И, наоборот, они могут быть иммуноингибиторами или иммуносуппрессорами для профилактики нежелательных иммунных реакций организма на инородные материалы и аутоиммунных заболеваний.
Установлено, что иммуномодуляторы могут использоваться для лечения системных аутоиммунных заболеваний, таких как красная волчанка, а также заболеваний, связанных с ослаблением иммунитета. Кроме того, иммуномодуляторы могут использоваться в иммунотерапии рака или для профилактики отторжения чужеродных органов или других тканей трансплантата, например почки, сердца или костного мозга.
Ламелларины I,K u L проявляют сравнимую и значительную цитотоксичность в отношении клеток линий Р388 и А549 в культуре (IС50=0,25 мг/мл для каждой линии клеток). Ламелларины К u L также проявляют умеренную иммуномодуляторную активность (LeV:VLR 147 и 98 соответственно) и как таковые обладают специфическими свойствами, признаваемыми специалистами.
Как показано в табл.4, производные ламелларина M, J и триацетат N обладают, как было неожиданно обнаружено, антиопухолевыми активностями in vitro, которые существенно лучше, особенно в отношении клеток линии А549, чем ламелларины I, К u L.
Как показано в табл.5, противоопухолевая активность in vivo ламелларина К совпадает с активностью in vitro, представленной выше. На основе этих данных делают вывод о том, что производные ламелларина, описанные здесь, могут использоваться в качестве противоопухолевых соединений, в частности, в отношении следующих типов опухолевых клеток: клетки лейкемии (Р388), клетки карциномы легкого (А549), клетки карциномы толстой кишки человека (НТ-29), клетки меланомы человека (MEL-28).
Настоящее изобретение описано подробно, включая предпочтительные воплощения. Однако, следует учесть, что специалистом при рассмотрении данного изобретения могут быть предприняты изменения и/или усовершенствования данного изобретения, и эти изменения также включены в объем данного изобретения.
Claims (15)
1. Способ лечения мультилекарственно резистентных опухолей у млекопитающих, включающих введение пациенту, нуждающемуся в таком лечении, эффективного количества ингибирующего мультилекарственную резистентность антимультилекарственно резистентного производного ламелларина.
4. Способ лечения мультилекарственно резистентных опухолей у млекопитающих, включающих введение пациенту, нуждающемуся в таком лечении, антимультилекарственно резистентного производного ламелларина, в количестве, которое обеспечивает эффективное цитотоксическое действие в отношении мультилекарственно резистентных клеток.
7. Фармацевтическая композиция для лечения мультилекарственно резистентных опухолей, содержащая одно или несколько антимультилекарственно резистентные производные ламелларина в сочетании с одним или несколькими противоопухолевыми лекарственными средствами, вызывающими мультилекарственную резистентность.
8. Фармацевтическая композиция по п. 7, где противоопухолевое лекарственное средство, вызывающее мультилекарственную резистентность, выбирают из группы, включающей винбластин, винкристин, этопозид, тенипозид, доксарубицин (адримицин), даунорубицин, пликамицин (митрамицин) и актиномицин D.
11. Способ усиления противоопухолевого химиотерапевтического действия лекарственных средств, вызывающих у пациентов, нуждающихся в таком лечении, мультилекарстенную резистентность, который включает совместное введение противоопухолевого лекарственного средства, вызывающего мультилекарстенную резистентность, и эффективного количества антимультилекарственно резистентного производного ламелларина.
14. Способ по п. 11, где противоопухолевое лекарственное средство, вызывающее мультилекарственную резистентность, и антимультилекарственно резистентное производное ламелларина вводят одновременно.
15. Способ по п. 11, где противоопухолевое лекарственное средство, вызывающее мультилекарственную резистентность, и антимультилекарственно резистентное производное ламелларина вводят последовательно.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US08/496,465 US5852033A (en) | 1995-06-29 | 1995-06-29 | Methods of treatment using lamellarin-class alkaloids |
| US08/496,465 | 1995-06-29 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU98101364A RU98101364A (ru) | 2000-01-27 |
| RU2188637C2 true RU2188637C2 (ru) | 2002-09-10 |
Family
ID=23972747
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU98101364/14A RU2188637C2 (ru) | 1995-06-29 | 1996-06-26 | Применение алкалоидов класса ламелларина в способах лечения |
Country Status (15)
| Country | Link |
|---|---|
| US (2) | US5852033A (ru) |
| EP (1) | EP0835108B1 (ru) |
| JP (1) | JP4153992B2 (ru) |
| AT (1) | ATE208196T1 (ru) |
| AU (1) | AU700420B2 (ru) |
| CA (1) | CA2225807C (ru) |
| DE (1) | DE69616792T2 (ru) |
| DK (1) | DK0835108T3 (ru) |
| ES (1) | ES2164899T3 (ru) |
| HU (1) | HU225588B1 (ru) |
| MX (1) | MX9800248A (ru) |
| PL (1) | PL184667B1 (ru) |
| PT (1) | PT835108E (ru) |
| RU (1) | RU2188637C2 (ru) |
| WO (1) | WO1997001336A1 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2745401C1 (ru) * | 2020-07-13 | 2021-03-24 | Федеральное государственное бюджетное учреждение науки Федеральный исследовательский центр "Институт биологии южных морей имени А.О. Ковалевского РАН" (ФИЦ ИнБЮМ) | Способ индукции секреции биологически активных соединений у рапаны rapana venosa val. |
Families Citing this family (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5852033A (en) * | 1995-06-29 | 1998-12-22 | Pharma Mar, S.A. | Methods of treatment using lamellarin-class alkaloids |
| AUPO656597A0 (en) * | 1997-05-02 | 1997-05-29 | Australian National University, The | Preparation of therapeutic compounds |
| US6248752B1 (en) * | 1998-02-27 | 2001-06-19 | Charles Duane Smith | Azabicyclooctane compositions and methods for enhancing chemotherapy |
| AUPP433398A0 (en) * | 1998-06-25 | 1998-07-16 | Australian National University, The | Compounds and processes |
| GB9920912D0 (en) * | 1999-09-03 | 1999-11-10 | Indena Spa | Novel derivatives of flavones,xanthones and coumarins |
| CA2401673A1 (en) * | 2000-03-01 | 2001-09-07 | The Scripps Research Institute | Ningalin b analogs employable for reversing multidrug resistance |
| US6989396B2 (en) | 2001-04-12 | 2006-01-24 | The Board Of Trustees Of The University Of Illinois | Tropane alkaloid multidrug resistance inhibitors from Erythroxylum pervillei and use of the same |
| EP1451856A2 (en) * | 2001-11-07 | 2004-09-01 | Pharmacia Corporation | Methods of promoting uptake and nuclear accumulation of polyamides in eukaryotic cells |
| US20060040945A1 (en) * | 2002-05-17 | 2006-02-23 | Merckle Gmbh | Annellated pyrrole compounds as proton pump inhibitors for treating ulcer |
| RU2336872C2 (ru) * | 2002-05-17 | 2008-10-27 | Меркле Гмбх | Аннелированные пиррольные соединения как ингибиторы протонового насоса для лечения язвы |
| GB0218816D0 (en) | 2002-08-13 | 2002-09-18 | Pharma Mar Sa | Antitumoral analogs of lamellarins |
| US8138170B2 (en) * | 2004-08-27 | 2012-03-20 | Memorial Sloan-Kettering Cancer Center | Immunosuppressive Ningalin compounds |
| WO2012099129A1 (ja) * | 2011-01-17 | 2012-07-26 | 国立大学法人 長崎大学 | 抗癌活性化合物 |
| EP3604312B1 (en) * | 2017-03-29 | 2023-11-29 | Nagasaki University | Fourth-generation egfr tyrosine kinase inhibitor |
| JOP20190254A1 (ar) | 2017-04-27 | 2019-10-27 | Pharma Mar Sa | مركبات مضادة للأورام |
| CN112300232B (zh) * | 2020-11-03 | 2021-11-09 | 浙江大学 | Lamellarin D糖基化衍生物及其制备和应用 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5852033A (en) * | 1995-06-29 | 1998-12-22 | Pharma Mar, S.A. | Methods of treatment using lamellarin-class alkaloids |
-
1995
- 1995-06-29 US US08/496,465 patent/US5852033A/en not_active Expired - Fee Related
-
1996
- 1996-06-26 EP EP96922197A patent/EP0835108B1/en not_active Expired - Lifetime
- 1996-06-26 DK DK96922197T patent/DK0835108T3/da active
- 1996-06-26 WO PCT/IB1996/000742 patent/WO1997001336A1/en active IP Right Grant
- 1996-06-26 PL PL96324282A patent/PL184667B1/pl not_active IP Right Cessation
- 1996-06-26 PT PT96922197T patent/PT835108E/pt unknown
- 1996-06-26 RU RU98101364/14A patent/RU2188637C2/ru not_active IP Right Cessation
- 1996-06-26 ES ES96922197T patent/ES2164899T3/es not_active Expired - Lifetime
- 1996-06-26 HU HU9900186A patent/HU225588B1/hu not_active IP Right Cessation
- 1996-06-26 AT AT96922197T patent/ATE208196T1/de not_active IP Right Cessation
- 1996-06-26 JP JP50428597A patent/JP4153992B2/ja not_active Expired - Fee Related
- 1996-06-26 CA CA002225807A patent/CA2225807C/en not_active Expired - Fee Related
- 1996-06-26 DE DE69616792T patent/DE69616792T2/de not_active Expired - Fee Related
- 1996-06-26 AU AU63167/96A patent/AU700420B2/en not_active Ceased
-
1998
- 1998-01-07 MX MX9800248A patent/MX9800248A/es not_active IP Right Cessation
- 1998-12-18 US US09/216,406 patent/US6087370A/en not_active Expired - Fee Related
Non-Patent Citations (1)
| Title |
|---|
| GRANT S et al. Characterization of multidrug resistant human erythroleukemia cell line (K 562) exhibiting spontaneous resistance to 1-beta-D-arabinofuranosylcytosine, Leukemia, 1995, may, 9(5), 808-14. * |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2745401C1 (ru) * | 2020-07-13 | 2021-03-24 | Федеральное государственное бюджетное учреждение науки Федеральный исследовательский центр "Институт биологии южных морей имени А.О. Ковалевского РАН" (ФИЦ ИнБЮМ) | Способ индукции секреции биологически активных соединений у рапаны rapana venosa val. |
Also Published As
| Publication number | Publication date |
|---|---|
| JP4153992B2 (ja) | 2008-09-24 |
| JPH11508882A (ja) | 1999-08-03 |
| HUP9900186A2 (hu) | 1999-06-28 |
| HU225588B1 (en) | 2007-03-28 |
| PL184667B1 (pl) | 2002-11-29 |
| ES2164899T3 (es) | 2002-03-01 |
| CA2225807A1 (en) | 1997-01-16 |
| MX9800248A (es) | 1998-11-30 |
| PT835108E (pt) | 2002-03-28 |
| EP0835108A1 (en) | 1998-04-15 |
| EP0835108B1 (en) | 2001-11-07 |
| HUP9900186A3 (en) | 2001-08-28 |
| DE69616792D1 (de) | 2001-12-13 |
| CA2225807C (en) | 2008-04-22 |
| AU700420B2 (en) | 1999-01-07 |
| DK0835108T3 (da) | 2002-03-18 |
| PL324282A1 (en) | 1998-05-11 |
| US6087370A (en) | 2000-07-11 |
| ATE208196T1 (de) | 2001-11-15 |
| WO1997001336A1 (en) | 1997-01-16 |
| AU6316796A (en) | 1997-01-30 |
| US5852033A (en) | 1998-12-22 |
| DE69616792T2 (de) | 2002-06-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2188637C2 (ru) | Применение алкалоидов класса ламелларина в способах лечения | |
| KR102155588B1 (ko) | Notch 억제제로서의 비스(플루오로알킬)-1,4-벤조디아제피논 화합물 | |
| US20080076772A1 (en) | Anti-Inflammatory Agents | |
| HUE024568T2 (hu) | N-(4-((3-(2-amino-4-pirimidinil)-2-piridinil)oxi)fenil)-4-(4-metil-2-tienil)-1-ftalazinamin antimitotikus szerre rezisztens rák kezelésében történõ alkalmazásra | |
| KR20200083532A (ko) | 적어도 1종의 스플라이세오솜 조정제, 및 bcl2 억제제, bcl2/bclxl 억제제 및 bclxl 억제제로부터 선택된 적어도 1종의 억제제를 포함하는 조합물 및 사용 방법 | |
| JP2009543874A (ja) | チアゾリジノン誘導体 | |
| JPH10504014A (ja) | Ssiチルホスチンと薬剤組成物 | |
| RU2335294C2 (ru) | Аплидин для лечения множественной миеломы | |
| KR100468271B1 (ko) | 피페라진옥시란유도체를포함하는약제학적조성물 | |
| KR20160087037A (ko) | 혈관석회화 방지용 조성물 및 이를 포함하는 혈관 석회화 치료제 | |
| JP2003523383A (ja) | ジクチオスタチン化合物の新規な組成物及び使用 | |
| JP2000501118A (ja) | 2,2′−ビ−1h−ピロール化合物を含有する相乗作用性免疫抑制剤組成物 | |
| AU2020325143A1 (en) | Therapeutic agent for cancer having resistance to anti-CCR4 antibody | |
| KR20030019371A (ko) | 고수준의 글루타티온과 관련된 종양 치료에 있어서 치환된아크릴로일 디스타마이신 유도체의 용도 | |
| EP1753420A1 (en) | Indole derivatives useful for treating resistance to antitumour agents | |
| KR20050078743A (ko) | 로즈마린산의 하이드록실페닐 유도체를 유효성분으로 하는항암용 약학 조성물 | |
| Pettit et al. | Biosynthetic products for anticancer drug design and treatment: The Bryostatins | |
| US20200016118A1 (en) | Hdac inhibitor in combination with vegf/vegfr interaction for cancer therapy based on platelet count | |
| US20110077230A1 (en) | Copper organocomplexes, use thereof as antitumor means and for protecting healthy tissue from ionizing radiation | |
| KR100550356B1 (ko) | 매크로사이클릭 펩티드계 화합물과 미토콘드리아 해당과정 저해제를 포함하는 항암제 | |
| CN116942680A (zh) | 一种治疗耐药的非小细胞肺癌的药物组合物 | |
| WO2018142288A1 (en) | Mukaadial acetate isolated from warburgia salutaris and the use thereof as an antimalarial | |
| JP2007223962A (ja) | 抗バベシア剤および新規クアシノイド誘導体 | |
| KR20050020834A (ko) | 소염 조성물 및 이의 사용 방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20090627 |