RU2169742C2 - Гетеротелехелатный блок-сополимер и способ его получения - Google Patents
Гетеротелехелатный блок-сополимер и способ его получения Download PDFInfo
- Publication number
- RU2169742C2 RU2169742C2 RU97119062/04A RU97119062A RU2169742C2 RU 2169742 C2 RU2169742 C2 RU 2169742C2 RU 97119062/04 A RU97119062/04 A RU 97119062/04A RU 97119062 A RU97119062 A RU 97119062A RU 2169742 C2 RU2169742 C2 RU 2169742C2
- Authority
- RU
- Russia
- Prior art keywords
- group
- block copolymer
- integer
- alkyl
- hydrogen atom
- Prior art date
Links
- 0 *C(C(O)OC1*)OC1=O Chemical compound *C(C(O)OC1*)OC1=O 0.000 description 2
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/26—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring from cyclic ethers and other compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/107—Emulsions ; Emulsion preconcentrates; Micelles
- A61K9/1075—Microemulsions or submicron emulsions; Preconcentrates or solids thereof; Micelles, e.g. made of phospholipids or block copolymers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/56—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule
- A61K47/59—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes
- A61K47/60—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic macromolecular compound, e.g. an oligomeric, polymeric or dendrimeric molecule obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyureas or polyurethanes the organic macromolecular compound being a polyoxyalkylene oligomer, polymer or dendrimer, e.g. PEG, PPG, PEO or polyglycerol
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G63/00—Macromolecular compounds obtained by reactions forming a carboxylic ester link in the main chain of the macromolecule
- C08G63/02—Polyesters derived from hydroxycarboxylic acids or from polycarboxylic acids and polyhydroxy compounds
- C08G63/06—Polyesters derived from hydroxycarboxylic acids or from polycarboxylic acids and polyhydroxy compounds derived from hydroxycarboxylic acids
- C08G63/08—Lactones or lactides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G63/00—Macromolecular compounds obtained by reactions forming a carboxylic ester link in the main chain of the macromolecule
- C08G63/66—Polyesters containing oxygen in the form of ether groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G63/00—Macromolecular compounds obtained by reactions forming a carboxylic ester link in the main chain of the macromolecule
- C08G63/66—Polyesters containing oxygen in the form of ether groups
- C08G63/664—Polyesters containing oxygen in the form of ether groups derived from hydroxy carboxylic acids
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/26—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring from cyclic ethers and other compounds
- C08G65/2603—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring from cyclic ethers and other compounds the other compounds containing oxygen
- C08G65/2606—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring from cyclic ethers and other compounds the other compounds containing oxygen containing hydroxyl groups
- C08G65/2609—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring from cyclic ethers and other compounds the other compounds containing oxygen containing hydroxyl groups containing aliphatic hydroxyl groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/32—Polymers modified by chemical after-treatment
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/32—Polymers modified by chemical after-treatment
- C08G65/329—Polymers modified by chemical after-treatment with organic compounds
- C08G65/331—Polymers modified by chemical after-treatment with organic compounds containing oxygen
- C08G65/332—Polymers modified by chemical after-treatment with organic compounds containing oxygen containing carboxyl groups, or halides, or esters thereof
- C08G65/3324—Polymers modified by chemical after-treatment with organic compounds containing oxygen containing carboxyl groups, or halides, or esters thereof cyclic
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L71/00—Compositions of polyethers obtained by reactions forming an ether link in the main chain; Compositions of derivatives of such polymers
- C08L71/02—Polyalkylene oxides
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S525/00—Synthetic resins or natural rubbers -- part of the class 520 series
- Y10S525/922—Polyepoxide polymer having been reacted to yield terminal ethylenic unsaturation
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Organic Chemistry (AREA)
- Polymers & Plastics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- General Chemical & Material Sciences (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Dispersion Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Polyesters Or Polycarbonates (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Graft Or Block Polymers (AREA)
- Polymerisation Methods In General (AREA)
- Medicinal Preparation (AREA)
- Other Resins Obtained By Reactions Not Involving Carbon-To-Carbon Unsaturated Bonds (AREA)
- Polyethers (AREA)
- Materials For Medical Uses (AREA)
Abstract
Описывается новый гетеротелехелатный блок-сополимер, который представлен формулой I, в которой R1 и R2, соединенные вместе, означают этилендиоксигруппу (-O-CH(R')-СН2-О, в которой R' означает атом водорода или C1-6-алкил), которая может быть замещена C1-6-алкилом, или в сочетании друг с другом означают оксогруппу (=O), L означает группу (а), в которой R3 и R4 независимо означают атом водорода, С1-10-алкил, арил или арил-С1-3-алкил и r означает целое число от 2 до 5, m означает целое число от 2 до 10000, n означает целое число от 2 до 10000, p означает целое число от 1 до 5, q означает целое число от 0 до 20, Z означает, когда q равно нулю, атом водорода, щелочной металл, ацетил, акрилоил, метакрилоил, циннамоил, паратолуолсульфонил, 2-меркаптопропионил или 2-аминопропионил, или аллил, или винилбензил, в то время как, когда q является целым числом от 1 до 20, Z означает С1-6-алкоксикарбонил, карбокси-, меркапто- или аминогруппу. Описанные выше олигомер или полимер образуют высокомолекулярную мицеллу, которая стабильна в водном растворителе. Указанные олигомер или полимер могут быть полезными в качестве носителя при подаче лекарства. Описан также способ получения указанного олигомера или полимера методом полимеризации живых цепей. 3 с. и 9 з. п. ф-лы, 1 табл., 8 ил.
Description
Настоящее изобретение относится к гетеротелехелатному блок-сополимеру, который имеет различные функциональные группы на обоих концах молекулы, к способу его получения и к его применению для получения высокомолекулярной мицеллы. Более конкретно, в этом изобретении описан полимер, который имеет различные функциональные группы на обоих концах молекулы и в то же время содержит в основной цепи полиэтиленоксид в качестве гидрофильного сегмента и полиэфир в качестве гидрофобного сегмента.
В этом изобретении термин "полимер" включает в себя олигомер.
Уровень техники
В настоящее время высокомолекулярные мицеллы или наносферы, состоящие из блок-сополимера гидрофильно/гидрофобного типа, в котором гидрофильный полимер типа полиэтиленоксида сочетается с гидрофобным полимером на молекулярном уровне, привлекают внимание в качестве носителя при подаче лекарства или т. п. Такие высокомолекулярные мицеллы и наносферы были приготовлены из блок-сополимера гидрофильно/гидрофобного типа, в котором гидрофильный полимер типа полиэтиленоксида сочетается с гидрофобным полимером на молекулярном уровне.
В настоящее время высокомолекулярные мицеллы или наносферы, состоящие из блок-сополимера гидрофильно/гидрофобного типа, в котором гидрофильный полимер типа полиэтиленоксида сочетается с гидрофобным полимером на молекулярном уровне, привлекают внимание в качестве носителя при подаче лекарства или т. п. Такие высокомолекулярные мицеллы и наносферы были приготовлены из блок-сополимера гидрофильно/гидрофобного типа, в котором гидрофильный полимер типа полиэтиленоксида сочетается с гидрофобным полимером на молекулярном уровне.
Однако в традиционных способах получения блок-сополимера гидрофильно/гидрофобного типа существует ограничение на виды введенных концевых функциональных групп, причем были предложены только блок-сополимеры, в которых функциональные группы были ограничены метоксильной и гидроксильной группами. Если бы удалось осуществить введение необязательных функциональных групп на поверхность мицеллы в выбранном соотношении, то стало бы возможной разработка функциональной высокомолекулярной мицеллы, которая могла быть полезной при подаче лекарства в определенные органы.
Ближайшим аналогом настоящего изобретения является WO 95/03357, где описаны частицы, которые не выводятся быстро из кровяного потока макрофагами ретикулоендотелиальной системы и могут быть модифицированы для достижения различных скоростей высвобождения или для поступления к нужным определенным клеткам или органам. Частицы имеют биоразлагаемый твердый сердечник, содержащий биологически активный материал и поли(алкиленгликолевые) группы на поверхности.
В WO 95/03357 отмечается, что белок, например антитело, связан за счет концевой гидроксигруппы поли(алкиленгликоля), что образует поверхность частиц. В WO 95/03357, однако, не указано, не предполагается, такой блок-полимер, как в настоящем изобретении, который имеет альдегидную группу на конце поли(этиленгликоля) (отметим: ацетали легко превращаются в альдегиды в разбавленных водных кислотах).
Как хорошо понятно специалисту в данной области, альдегидная группа (-CHO) легко превращается в иминное соединение через основание Шиффа, как показано в следующем уравнении:
Таким образом, т. к. полимер по настоящему изобретению легко может образовывать полимер-протеиновые конъюгаты посредством аминогруппы, которая существует, например, в белке, указанный полимер по настоящему изобретению может использоваться намного более удобно, например, при модификации белка, чем полимер, указанный в WO 95/03357.
Таким образом, т. к. полимер по настоящему изобретению легко может образовывать полимер-протеиновые конъюгаты посредством аминогруппы, которая существует, например, в белке, указанный полимер по настоящему изобретению может использоваться намного более удобно, например, при модификации белка, чем полимер, указанный в WO 95/03357.
Таким образом, полимер по настоящему изобретению четко отличается от предшествующего уровня техники.
Целью настоящего изобретения является разработка блок-сополимера, который имеет различные функциональные группы на обоих концах молекулы, в качестве многофункционального полимера, способного образовывать высокомолекулярную мицеллу.
Описание изобретения
Авторы настоящего изобретения установили, что можно легко получить блок-сополимер, имеющий защищенную или незащищенную альдегидную группу на одном конце молекулы и различные функциональные группы на другом конце, когда алкиленовая производная, имеющая определенного вида альдегидную группу и гидроксильную группу, применяется как инициатор полимеризации в живой цепи и когда в качестве мономеров полимеризуются оксид этилена и лактид или лактон.
Авторы настоящего изобретения установили, что можно легко получить блок-сополимер, имеющий защищенную или незащищенную альдегидную группу на одном конце молекулы и различные функциональные группы на другом конце, когда алкиленовая производная, имеющая определенного вида альдегидную группу и гидроксильную группу, применяется как инициатор полимеризации в живой цепи и когда в качестве мономеров полимеризуются оксид этилена и лактид или лактон.
Они также подтвердили, что полученный таким образом блок-сополимер образует высокомолекулярную мицеллу, которая вполне стабильна в водном растворителе.
Это изобретение предлагает гетеротелехелатный блок-сополимер, который имеет различные функциональные группы на обоих концах молекулы и который представлен следующей формулой:
в которой R1 и R2 независимо означают C1-10-алкокси, арилокси или арил-C1-3-алкилокси или R1 и R2 в сочетании друг с другом означают этилендиоксигруппу (-O-CH(R')-CH2-O-, в которой R' означает атом водорода или C1-6-алкил), которая может быть замещена C1-6-алкилом, или в сочетании друг с другом означают оксогруппу (=O), L означает группу
в которой R3 и R4 независимо означают атом водорода, C1-10-алкил, арил или арил-C1-3-алкил и r означает целое число от 2 до 5, m означает целое число от 2 до 10000, n означает целое число от 2 до 10000, p означает целое число от 1 до 5, q означает целое число от 0 до 20,
Z означает, когда q равно нулю, атом водорода, щелочной металл, ацетил, акрилоил, метакрилоил, циннамоил, паратолуолсульфонил, 2-меркаптопропионил или 2-аминопропионил, или аллил, или винилбензил, означая, когда q является целым числом от 1 до 20, C1-6-алкоксикарбонил, карбоксил, меркапто- или аминогруппу.
в которой R1 и R2 независимо означают C1-10-алкокси, арилокси или арил-C1-3-алкилокси или R1 и R2 в сочетании друг с другом означают этилендиоксигруппу (-O-CH(R')-CH2-O-, в которой R' означает атом водорода или C1-6-алкил), которая может быть замещена C1-6-алкилом, или в сочетании друг с другом означают оксогруппу (=O), L означает группу
в которой R3 и R4 независимо означают атом водорода, C1-10-алкил, арил или арил-C1-3-алкил и r означает целое число от 2 до 5, m означает целое число от 2 до 10000, n означает целое число от 2 до 10000, p означает целое число от 1 до 5, q означает целое число от 0 до 20,
Z означает, когда q равно нулю, атом водорода, щелочной металл, ацетил, акрилоил, метакрилоил, циннамоил, паратолуолсульфонил, 2-меркаптопропионил или 2-аминопропионил, или аллил, или винилбензил, означая, когда q является целым числом от 1 до 20, C1-6-алкоксикарбонил, карбоксил, меркапто- или аминогруппу.
В другом аспекте это изобретение представляет способ получения блок-сополимера указанной выше формулы (I), причем этот способ включает следующие стадии:
Стадия 1)
Инициатор полимеризации, представленный следующей формулой (II)
в которой R1-1 и R2-1 независимо означают C1-10-алкоксигруппу или в сочетании друг с другом означают этилендиоксигруппу, которая может быть замещена C1-6-алкилом, p означает целое число от 1 до 5 и M означает шелочной металл,
заставляют взаимодействовать с этиленоксидом таким образом, чтобы можно было получить соединение, представленное следующей формулой (III):
в которой R1-1, R2-1, p и M - такие, как определено в формуле (II), и m означает целое число от 2 до 10000.
Стадия 1)
Инициатор полимеризации, представленный следующей формулой (II)
в которой R1-1 и R2-1 независимо означают C1-10-алкоксигруппу или в сочетании друг с другом означают этилендиоксигруппу, которая может быть замещена C1-6-алкилом, p означает целое число от 1 до 5 и M означает шелочной металл,
заставляют взаимодействовать с этиленоксидом таким образом, чтобы можно было получить соединение, представленное следующей формулой (III):
в которой R1-1, R2-1, p и M - такие, как определено в формуле (II), и m означает целое число от 2 до 10000.
Стадия 2)
Соединению формулы (II) дают прореагировать с лактидом или лактоном, который представлен следующей формулой (III-a) или (III-b):
или
в которой R3 и R4 независимо означают атом водорода, C1-10-алкил, арил или арил-C1-3-алкил и r означает целое число от 2 до 5,
таким образом, чтобы можно было получить соединение, представленное следующей формулой (IV):
в которой L означает группу
и R1-1, R2-1, p, m и M - такие, как определено выше.
Соединению формулы (II) дают прореагировать с лактидом или лактоном, который представлен следующей формулой (III-a) или (III-b):
или
в которой R3 и R4 независимо означают атом водорода, C1-10-алкил, арил или арил-C1-3-алкил и r означает целое число от 2 до 5,
таким образом, чтобы можно было получить соединение, представленное следующей формулой (IV):
в которой L означает группу
и R1-1, R2-1, p, m и M - такие, как определено выше.
Указанная выше стадия обеспечивает получение живой цепи полимера этого изобретения (который включен в полимер формулы (I)), которая применяется в качестве промежуточного соединения для дальнейшего наращивания некоторого количества полимерного сегмента и т.п.
Стадия 3)
i) Алкоксид щелочного металла формулы (IV) селективно гидролизуют, получая блок-сополимер следующей формулы (V):
в которой R1-1, R2-1, p, m, L и n - такие, как определено выше; или
ii) блок-сополимер формулы (IV) полностью гидролизуют, получая блок-сополимер следующей формулы (VI):
в которой p, m, L и n - такие, как определено выше.
i) Алкоксид щелочного металла формулы (IV) селективно гидролизуют, получая блок-сополимер следующей формулы (V):
в которой R1-1, R2-1, p, m, L и n - такие, как определено выше; или
ii) блок-сополимер формулы (IV) полностью гидролизуют, получая блок-сополимер следующей формулы (VI):
в которой p, m, L и n - такие, как определено выше.
Указанная выше стадия обеспечивает получение блок-сополимера этого изобретения, который имеет защищенную альдегидную группу или собственно альдегидную группу в начале полимерной цепи (α-терминальная группа) и гидроксильную группу в конце цепи (ω-терминальная группа).
Стадия 4)
Блок-сополимеру формулы (V), который имеет защищенную альдегидную группу в начале полимерной цепи, дают прореагировать с
i) уксусной кислотой, акриловой кислотой, метакриловой кислотой, коричной кислотой или паратолуолсульфоновой кислотой, или их реакционноспособными производными, или
ii) аллилгалогенидом, или винилбензилгалогенидом, или
iii) галогенидом, представленным следующей формулой (VII):
в которой X представляет собой атом хлора, брома или иода, q' является целым числом от 1 до 20 и Z' является C1-6-алкоксикарбонилом или защищенной аминогруппой;
с образованием блок-сополимеров этого изобретения, каждый из которых имеет соответствующие функциональные группы, отличающиеся от гидроксильной группы, в ω-конце цепи макромолекулы.
Блок-сополимеру формулы (V), который имеет защищенную альдегидную группу в начале полимерной цепи, дают прореагировать с
i) уксусной кислотой, акриловой кислотой, метакриловой кислотой, коричной кислотой или паратолуолсульфоновой кислотой, или их реакционноспособными производными, или
ii) аллилгалогенидом, или винилбензилгалогенидом, или
iii) галогенидом, представленным следующей формулой (VII):
в которой X представляет собой атом хлора, брома или иода, q' является целым числом от 1 до 20 и Z' является C1-6-алкоксикарбонилом или защищенной аминогруппой;
с образованием блок-сополимеров этого изобретения, каждый из которых имеет соответствующие функциональные группы, отличающиеся от гидроксильной группы, в ω-конце цепи макромолекулы.
Стадия 5)
Полученный на стадии 4)-i) эфир паратолуолсульфоновой кислоты может быть подвергнут дальнейшему превращению, посредством трансэтерификации, в блок-сополимер, имеющий другие функциональные группы (например, меркапто- или амино-) в конце полимерной цепи (ω). Блок-сополимер, который имеет альдегидзащищающую группу или карбоксилзащищающую группу и который был получен по указанным выше стадиям, может быть превращен посредством гидролиза в блок-сополимер этого изобретения, в котором одна из защищающих групп или все защищающие группы удалены.
Полученный на стадии 4)-i) эфир паратолуолсульфоновой кислоты может быть подвергнут дальнейшему превращению, посредством трансэтерификации, в блок-сополимер, имеющий другие функциональные группы (например, меркапто- или амино-) в конце полимерной цепи (ω). Блок-сополимер, который имеет альдегидзащищающую группу или карбоксилзащищающую группу и который был получен по указанным выше стадиям, может быть превращен посредством гидролиза в блок-сополимер этого изобретения, в котором одна из защищающих групп или все защищающие группы удалены.
В соответствии с другим замыслом это изобретение обеспечивает высокомолекулярную мицеллу на основе использования блок-сополимера формулы (I).
Часть полученного таким образом гетеротелехелатного полимера настоящего изобретения может применяться в качестве исходного вещества для получения другого полимера. Как будет видно из составляющих их компонентов, можно ожидать, что эти полимеры будут обладать биологическим сродством и высокой биологической пригодностью. Поэтому они могут использоваться для производства материалов, непосредственно вводимых в живые организмы, таких как носитель для подачи лекарств. Сверх того, в соответствии с третьим замыслом изобретения оно представляет высокомолекулярную мицеллу, которая вполне стабильна в водном растворителе. Поэтому полимер этого изобретения также является эффективным для подачи лекарств в определенные органы.
Краткое описание чертежей
На фиг. 1 приведена гель-проникающая хроматограмма для полиэфироксид/полилактидного блок-сополимера с ацетальной -терминальной группой и гидроксильной ω-терминальной группой (образец Примера 1).
На фиг. 1 приведена гель-проникающая хроматограмма для полиэфироксид/полилактидного блок-сополимера с ацетальной -терминальной группой и гидроксильной ω-терминальной группой (образец Примера 1).
Рабочие условия: Ти - Эс - Кей - Гель (G4000HXL, G3000HXL, G2500HXL)
Элюент: тетрагидрофуран, содержащий 2% триэтиламина
Скорость потока: 1 мл/мин
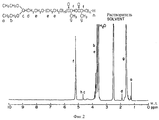
На фиг. 2 представлен спектр ядерного протонного магнитного резонанса (ПМР) полиэтиленоксид/полилактидного блок-сополимера с ацетальной α-терминальной группой и гидроксильной ω-терминальной группой (образец Примера 1).
Элюент: тетрагидрофуран, содержащий 2% триэтиламина
Скорость потока: 1 мл/мин
На фиг. 2 представлен спектр ядерного протонного магнитного резонанса (ПМР) полиэтиленоксид/полилактидного блок-сополимера с ацетальной α-терминальной группой и гидроксильной ω-терминальной группой (образец Примера 1).
На фиг. 3 представлен спектр протонного магнитного резонанса полиэтиленоксид/поли(δ-валеролактонового) блок-сополимера с ацетальной α-терминальной группой и гидроксильной ω-терминальной группой (образец Примера 3).
На фиг. 4 представлен спектр протонного магнитного резонанса полиэтиленоксид/полилактидного блок-сополимера с альдегидной α-терминальной группой и гидроксильной ω-терминальной группой (образец Примера 4).
На фиг. 5 представлен спектр протонного магнитного резонанса полиэтиленоксид/полилактидного блок-сополимера с ацетальной α-терминальной группой и метакрилоильной ω-терминальной группой (образец Примера 5).
На фиг. 6 представлен спектр протонного магнитного резонанса полиэтиленоксид/полилактидного блок-сополимера с ацетальной α-терминальной группой и аллильной ω-терминальной группой (образец Примера 6).
На фиг. 7 представлен спектр протонного магнитного резонанса полиэтиленоксид/полилактидного блок-сополимера с ацетальной α-терминальной группой и паратолуолсульфонильной ω-терминальной группой (образец Примера 7).
На фиг. 8 приведено распределение по размерам частиц высокомолекулярной мицеллы, найденное с использованием динамического лазерного рассеяния в водном растворе полиэтиленоксид/полилактидного блок-сополимера с альдегидной α\-терминальной группой и гидроксильной ω-терминальной группой (образец Примера 4).
Подробное описание изобретения
В этом изобретении алкильная часть алкоксигруппы и алкил означают алкильную группу с линейной или разветвленной цепочкой. Следовательно, алкильная часть C1-10-алкоксигруппы или C1-10-алкил в формулах (II) и (III-a) включают метил, этил, пропил, изопропил, бутил, втор-бутил, трет-бутил, пентил, изо-пентил, гексил, 2-метилпентил, 3-метилпентил, октил, 2-этилгексил, децил и 4-пропилпентил. Из них алкильная часть в алкоксигруппе R1 и R2 предпочтительно является алкилом C1-6, в частности алкилом C1-3.
В этом изобретении алкильная часть алкоксигруппы и алкил означают алкильную группу с линейной или разветвленной цепочкой. Следовательно, алкильная часть C1-10-алкоксигруппы или C1-10-алкил в формулах (II) и (III-a) включают метил, этил, пропил, изопропил, бутил, втор-бутил, трет-бутил, пентил, изо-пентил, гексил, 2-метилпентил, 3-метилпентил, октил, 2-этилгексил, децил и 4-пропилпентил. Из них алкильная часть в алкоксигруппе R1 и R2 предпочтительно является алкилом C1-6, в частности алкилом C1-3.
Следовательно, особенно предпочтительные примеры алкоксигруппы R1 и R2 включают метокси-, этокси-, пропокси- и изопропокси-. Примеры R1 и R2 включают арил, особенно фенил, и арил C1-3-алкил, особенно бензил или фенетил. Эти группы могут быть одинаковыми или различными, но предпочтительно они являются одинаковыми. Хотя R1 и R2 в сочетании друг с другом может означать этилендиоксигруппу (-O-CH(R')-CH2-O-, в которой R' означает атом водорода или C1-6-алкил), которая может быть замещена C1-6-алкилом, предпочтительно они представляют собой этилендиокси-, пропилендиокси- или 1,2-бутилендиоксигруппы.
При гидролизе заместители R1 и R2 удобно объединяются с образованием оксогруппы (= O), или иными словами, с образованием блок-сополимера этого изобретения, который имеет альдегидную группу в α-терминальной части молекулы.
Знак "p" в формуле (I) означает целое число от 1 до 5. В связи с тем, что сегмент
произведен из инициатора полимеризации (смотрите формулу (II)), в процессе этого изобретения R1, R2 и p предпочтительно выбирают таким образом, чтобы этот сегмент составлял блок ацетальной группы, такой как диметоксиметокси-, 2,2-диметоксиэтокси-, 3,3-диметоксипропокси-, 4,4-диметоксибутокси-, диэтоксиметокси-, 2,2-диэтоксиэтокси-, 3,3-диэтоксипропокси-, 4,4-диэтоксибутокси-, дипропоксиметокси-, 2,2-дипропоксиэтокси-, 3,3-дипропоксипропокси- или 4,4-дипропоксибутокси-.
произведен из инициатора полимеризации (смотрите формулу (II)), в процессе этого изобретения R1, R2 и p предпочтительно выбирают таким образом, чтобы этот сегмент составлял блок ацетальной группы, такой как диметоксиметокси-, 2,2-диметоксиэтокси-, 3,3-диметоксипропокси-, 4,4-диметоксибутокси-, диэтоксиметокси-, 2,2-диэтоксиэтокси-, 3,3-диэтоксипропокси-, 4,4-диэтоксибутокси-, дипропоксиметокси-, 2,2-дипропоксиэтокси-, 3,3-дипропоксипропокси- или 4,4-дипропоксибутокси-.
Радикалы R3 и R4 могут означать или атом водорода, или C1-10-алкил, или арил, или арил-C1-3-алкил, поскольку они пригодны для цели этого изобретения. Однако с точки зрения биологической пригодности предпочтительным является атом водорода (произведен из глутаровой кислоты) и метил (произведен из молочной кислоты).
В соответствии со способом получения с использованием полимеризации живых цепей этого изобретения знак "m" в формуле (I) теоретически может принимать любое значение, если устанавливается количественное соотношение между мономерным этиленоксидом и инициатором полимеризации. Однако для достижения цели этого изобретения, предпочтительно, m является целым числом от 2 до 10000. Для того, чтобы этот сегмент мог придать гидрофильность блок-сополимеру этого изобретения, предпочтительно, m является целым числом, равным по меньшей мере 10. С целью легкого достижения узкого молекулярно-весового распределения этого сегмента и обеспечения превосходной биологической пригодности блок-сополимера m является целым числом, равным по меньшей мере 500, предпочтительно по меньшей мере 200.
Что касается знака "n", который означает молекулярный вес полиэфирного сегмента формулы (I), его оптимальное значение изменяется в зависимости от свойств групп R3 и R4 как можно понять из того факта, что этот сегмент в основном придает гидрофобность блок-сополимеру этого изобретения. Следуя способу полимеризации этого изобретения, n может принимать любые значения, таким же образом, как в случае полиэтиленоксидного сегмента. Поэтому значение n не ограничено. Однако обычно оно составляет от 2 до 10000.
Более того, для поддержания хорошего баланса гидрофильности и гидрофобности относительно полиэтиленоксидного сегмента целое число m предпочтительно принимает значения от 10 до 200, в частности от 10 до 100.
Сегмент формулы (I) в основном оговаривает функциональные группы (или реакционноспособные группы) в ω-терминальной группе блок-сополимера этого изобретения. Когда q равно нулю (то есть в случае, когда Z непосредственно связан с атомом кислорода в ω-положении полиэфирного сегмента), Z может быть щелочным металлом. В этом случае полимер этого изобретения может быть "живым" полимером. Поскольку такой полимер этого изобретения может действовать как инициатор для дальнейшей полимеризации живых цепей, он применяется в качестве предшественника для полимеров различного типа. С этой точки зрения примеры щелочного металла включают натрий, калий и цезий.
Указанный выше живой полимер может легко обеспечить полимер, в котором Z означает атом водорода (или полимер, который имеет гидроксильную группу в ω-положении), так как алкоголятная часть живого полимера легко гидролизуется. Указанная гидроксильная группа может быть далее превращена в другие функциональные группы с использованием различных реакций, таких как этерификация кислотой или спиртом. Таким образом, когда q равно нулю, Z может быть ацетилом (-COCH3), акрилоилом (-COCH=CH2), метакрилоилом (-COC(CH3)=CH2), циннамоилом (-CHCH= CH-фенил) и паратолуолсульфонилом (-SO2-фенилен-CH3) и, кроме того, может быть аллилом (-CH2-CH=CH2) и винилбензилом (-CH2-фенилен-CH=CH2). Когда эти функциональные группы имеют этиленово ненасыщенную связь, с использованием указанной связи могут быть получены полимеры со свисающими цепями. Когда Z означает паратолуолсульфонильную группу, она может быть превращена в другую функциональную группу известным методом с использованием трансэтерификации. Поэтому Z может быть 2-меркаптопропионилом или 2-аминопропионилом.
Когда q является целым числом от 1 до 20, предпочтительно от 1 до 4, особенно предпочтительно 2, сегмент означает блок, например C1-6-алкокси- (например, метокси-, этокси- или пропокси-) карбонил-метил, -этил или -пропил, или 2-аминоэтил, карбокси-метил, -этил или -пропил.
В приведенной в конце описания таблице указаны примеры блок-сополимеров этого изобретения, которые включают указанные выше заместители (или сегменты) в различных взаимных сочетаниях.
Упомянутые выше гетеротелехелатные блок-сополимеры, которые могут быть представлены этим изобретением, эффективно получаются по способу этого изобретения, который иллюстрирован схемами реакции (см. в конце описания).
Получение (B) из (A)
Ацеталь - защищенный алкоксид щелочного металла (A) заставляют взаимодействовать с этиленоксидом с образованием соединения (B), к которому добавляется полиэтиленоксидный сегмент. Соединение (A) может быть приготовлено путем обработки ацеталь - защищенного спирта металлизирующим реагентом, таким как щелочной металл, подобный натрию или калию; металлоорганическим соединением, подобным нафталиннатрию, нафталинкалию, кумилкалию и кумил-цезию; или гидридом металла, таким как гидрид натрия или гидрид калия.
Ацеталь - защищенный алкоксид щелочного металла (A) заставляют взаимодействовать с этиленоксидом с образованием соединения (B), к которому добавляется полиэтиленоксидный сегмент. Соединение (A) может быть приготовлено путем обработки ацеталь - защищенного спирта металлизирующим реагентом, таким как щелочной металл, подобный натрию или калию; металлоорганическим соединением, подобным нафталиннатрию, нафталинкалию, кумилкалию и кумил-цезию; или гидридом металла, таким как гидрид натрия или гидрид калия.
Указанное выше превращение (A) в (B) должно протекать без растворителя или предпочтительно в безводном апротонном растворителе и в широком интервале температур, например от -50 до 300oC, предпочтительно 10-60oC, удобно при комнатной температуре (20-30oC). Эта реакция может быть проведена либо при повышенном, либо при пониженном давлении. Не ограничивающие примеры применяемых растворителей включают бензол, толуол, ксилол, тетрагидрофуран, диоксан и ацетонитрил. Не ограничивающие примеры реакторов включают круглодонную колбу, автоклав и запаянную под давлением трубку. Предпочтительно реактор запаивают герметично от воздуха и более предпочтительно его заполняют инертным газом. Концентрация реагирующей жидкости составляет от 0,1 до 95 вес.%, предпочтительно от 1 до 80 вес.%, наиболее предпочтительно от 3 до 10 вес.%.
Получение (C) из (B)
Реакционной смеси, содержащей (B), дают прореагировать с лактидом или лактоном с образованием живой цепи блок-сополимера (C), в котором полиэфирный сегмент добавляется по ω-терминальной гидроксильной группе полиэтиленоксида. Условия этой реакции могут быть практически такими же, как для предыдущего превращения (A) в (B). Применяемый лактид или лактон способен образовывать такую цепь, которая была определена в связи с радикалами R3 и R4 в группе L формулы (I). Не ограничивающие примеры лактидов включают лактид молочной кислоты и лактид гликолевой кислоты. С другой стороны, примеры подходящих лактонов включают бета-пропиолактон, гамма-бутиролактон, дельта-валеролактон и эпсилон-капролактон. Среди них предпочтительными, с точки зрения хорошей реакционной способности, являются гамма-бутиролактон и дельта-валеролактон.
Реакционной смеси, содержащей (B), дают прореагировать с лактидом или лактоном с образованием живой цепи блок-сополимера (C), в котором полиэфирный сегмент добавляется по ω-терминальной гидроксильной группе полиэтиленоксида. Условия этой реакции могут быть практически такими же, как для предыдущего превращения (A) в (B). Применяемый лактид или лактон способен образовывать такую цепь, которая была определена в связи с радикалами R3 и R4 в группе L формулы (I). Не ограничивающие примеры лактидов включают лактид молочной кислоты и лактид гликолевой кислоты. С другой стороны, примеры подходящих лактонов включают бета-пропиолактон, гамма-бутиролактон, дельта-валеролактон и эпсилон-капролактон. Среди них предпочтительными, с точки зрения хорошей реакционной способности, являются гамма-бутиролактон и дельта-валеролактон.
В приведенных выше стадиях молярное соотношение инициатора полимеризации к этиленоксиду, лактиду или лактону составляет от 1:1 до 1:10000, более предпочтительно от 1:5 до 1:10000, наиболее предпочтительно от 1:10-200 до 1:50-200.
Способ этого изобретения не только дает возможность регулировать молекулярный вес каждого сегмента в соответствии с соотношением инициатора полимеризации к использованному маномеру, но также обеспечивает монодисперсный или мономодальный блок-сополимер, в котором каждый из полученных сегментов имеет весьма узкое молекулярно-весовое распределение.
Полученный указанным выше способом живой полимер (C) входит в объем защиты полимера этого изобретения. Однако алкоголят (C) может быть превращен i) в полимер D посредством частичного гидролиза в мягких условиях (например, просто при добавлении воды) или ii) в полимер D', который имеет альдегидную группу в α-терминальном положении и гидроксильную группу в ω-терминальном положении, посредством обработки C в условиях, в которых ацетальная группа может одновременно гидролизоваться. Эта реакция гидролиза может быть осуществлена с использованием или кислот, таких как трифторуксусная кислота, хлористоводородная кислота, серная кислота, азотная кислота, муравьиная кислота и фтористоводородная кислота, или щелочей, таких как гидроксид натрия и гидроксид калия, и в случае необходимости при нагревании.
Получение (E)-(G) из (D)
Инициируют взаимодействие D с
i) уксусной кислотой, акриловой кислотой, метакриловой кислотой или паратолуолсульфоновой кислотой с образованием ω-терминального ацильного соединения с концевой группой в ω-положении, или
ii) галогенидом, представленным формулой (V)
галоид-E,
где галоид- и E в формуле (V) соответствуют группам, отличающимся от ацильной группы в блоке формулы (I), с образованием эфирного соединения с концевой группой в ω-положении.
Инициируют взаимодействие D с
i) уксусной кислотой, акриловой кислотой, метакриловой кислотой или паратолуолсульфоновой кислотой с образованием ω-терминального ацильного соединения с концевой группой в ω-положении, или
ii) галогенидом, представленным формулой (V)
галоид-E,
где галоид- и E в формуле (V) соответствуют группам, отличающимся от ацильной группы в блоке формулы (I), с образованием эфирного соединения с концевой группой в ω-положении.
Указанные выше реакции могут быть осуществлены с использованием известных процессов этерификации кислотой или спиртом. Что касается органической кислоты в указанной выше стадии i), удобно использовать реакционноспособную производную органической кислоты, такую как ангидрид кислоты и галогенид кислоты.
Когда необходимо ввести меркаптогруппу в ω-концевую часть, то эффективным является инициирование взаимодействия паратулолсульфированного соединения F с электрофильным реагентом, таким как тиоацетат натрия, тиоацетат калия или гидросульфид калия, таким образом, чтобы тиоэфирную группу можно было ввести в ω -концевую группу, и затем эту тиоэфирную группу обрабатывают кислотой или щелочью и после этого можно получить полимер, представленный формулой G.
Когда необходимо ввести аминогруппу в ω-концевую часть, то эффективным является инициирование гидролиза соединения D с использованием электрофильного реагента, такого как N-(2-бромэтил)фтальимид, N-(3-бромпропил)фтальимид, 1-бром-2-(аминобензол)этан или N-(2-бромэтил)бензилкарбамат, и после этого проводят обработку кислотой или щелочью, для того чтобы удалить группы R1 и R2 и одновременно гидролизовать ω-концевую имидную связь, и таким образом может быть получен полимер, который содержит ω-концевую аминогруппу.
Удаление групп R1 и R2 из полимеров D, E, F и G, с целью получения альдегида с концевой группой в α-положении, может быть осуществлено в результате упомянутого выше превращения C в D'. Что касается выделения полимера из жидкой реакционной смеси, оно может быть осуществлено посредством осаждения собственно полимера растворителем, гель-фильтрующей хроматографией, диализом, ультрафильтрацией или т.п.
Таким же способом были получены гетеротелехелатные блок-сополимеры различного типа, представленные формулой (I) этого изобретения. Полученные полимеры (за исключением живых полимеров) способны образовывать высокомолекулярные мицеллы, которые весьма стабильны в водном растворителе.
Эта высокомолекулярная мицелла может быть получена, например, в результате воздействия на раствор или суспензию полимера органического растворителя, термической и ультразвуковой обработки, отдельно или в сочетании. Термическую обработку осуществляют посредством диспергирования или растворения смеси одного или нескольких типов блок-сополимеров этого изобретения в воде при температуре, находящейся в интервале от 30 до 100oC, более предпочтительно от 30 до 50oC. Обработку ультразвуком осуществляют посредством диспергирования или растворения смеси одного или нескольких типов блок-сополимеров этого изобретения в воде при мощности, находящейся в интервале от 1 до 20 Вт в течение от 1 секунды до 24 ч, предпочтительно в интервале от 1 до 3 Вт в течение 3 ч.
Обработку органическим растворителем осуществляют посредством растворения смеси одного или нескольких типов блок-сополимеров в органическом растворителе, диспергирования полученного раствора в воде с последующим выпариванием органического растворителя. Примеры органических растворителей включают хлороформ, бензол, толуол, хлористый метилен и др.
Кроме того, возможно получение высокомолекулярной мицеллы этого изобретения посредством растворения упомянутой смеси в метаноле, этаноле, тетрагидрофуране, диоксане, диметилсульфоксиде, диметилформамиде или т. п. растворителе, и затем полученный раствор подвергают диализу относительно водного растворителя. Фракционный молекулярный вес мембраны, применяемой для диализа, не ограничен, поскольку его оптимальное значение изменяется в соответствии с молекулярным весом блок-сополимера, подлежащего обработке. Однако обычно фракционный молекулярный вес мембраны составляет не более 1000000, предпочтительно 5000 - 20000.
В качестве водного растворителя можно использовать воду и буферный раствор. Соотношение используемого водного раствора к указанному выше органическому растворителю при диализе обычно составляет от 1 до 1000 раз, предпочтительно от 10 до 100 раз. Температура конкретно не ограничивается. Обычно обработку проводят при 5 - 25oC.
Полученные таким образом высокомолекулярные мицеллы этого изобретения имеют критическую концентрацию мицелл не выше 4 - 12 мг/л, причем они гораздо более стабильны в водном растворе, чем низкомолекулярные мицеллы, такие как липосома, которая была детально рассмотрена в качестве носителя для подачи лекарств. Это означает, что при введении в кровь высокомолекулярной мицеллы этого изобретения можно ожидать, что она будет иметь значительно большее характерное время жизни в крови, и, таким образом, можно сказать, что полимер этого изобретения имеет превосходные свойства в качестве носителя для подачи лекарств.
Ниже это изобретение подробно поясняется рабочими примерами, однако эти рабочие примеры никоим образом не ограничивают объем защиты этого изобретения.
Пример 1
В реакционную емкость вводят 20 мл тетрагидрофурана, 0,15 г 3,3-диэтоксипропанола и 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и перемешивают 3 минуты в атмосфере аргона; получают 3,3-диэтоксипропаноксид калия.
В реакционную емкость вводят 20 мл тетрагидрофурана, 0,15 г 3,3-диэтоксипропанола и 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и перемешивают 3 минуты в атмосфере аргона; получают 3,3-диэтоксипропаноксид калия.
В этот раствор добавляют 8,8 г этиленоксида и перемешивают при комнатной температуре и атмосферном давлении. После взаимодействия в течение 2 суток добавляют в этот реакционный раствор лактид в количестве 7,2 г и затем перемешивают 1 час. Этот раствор выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок выделяют методом центрифугирования и очищают посредством лиофильной сушки из бензола. Выход продукта 15 г (94%). Полимер, выделенный методом гель-проникающей хроматографии, является мономодальным, его молекулярный вес равен 16000 (фиг. 1).
В соответствии со спектром протонного ядерного магнитного резонанса (ПМР) полученного полимера в дейтерохлороформе было установлено, что он является гетеротелехелатным олигомером, имеющим как полиэтиленоксидные, так и полилактидные блоки, и количественно содержит ацетальную группу в α-концевой части и гидроксильную группу в ω-концевой части (фиг. 2). Среднечисловой молекулярный вес каждого сегмента блок-полимера, найденный по интегральному отношению в спектре, равен 8800 для полиэтиленоксида и 7000 для полилактида.
Пример 2
В реакционную емкость вводят 20 мл тетрагидрофурана, 0,15 г 3,3-диэтоксипропанола и 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и перемешивают 3 минуты в атмосфере аргона; получают 3,3-диэтоксипропаноксид калия.
В реакционную емкость вводят 20 мл тетрагидрофурана, 0,15 г 3,3-диэтоксипропанола и 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и перемешивают 3 минуты в атмосфере аргона; получают 3,3-диэтоксипропаноксид калия.
В этот раствор добавляют 5,7 г этиленоксида и перемешивают при комнатной температуре и атмосферном давлении. После взаимодействия в течение 2 суток добавляют в этот реакционный раствор 7,2 г лактида и затем перемешивают 1 час. Этот раствор выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок выделяют методом центрифугирования и очищают посредством лиофильной сушки из бензола. Выход продукта 12,4 г (95%). Полимер, выделенный методом гель-проникающей хроматографии, является мономодальным, его молекулярный вес равен 12000.
В соответствии со спектром протонного ядерного магнитного резонанса полученного полимера в дейтерохлороформе было установлено, что он является гетеротелехелатным олигомером, имеющим как полиэтиленоксидные, так и полилактидные блоки, и количественно содержит ацетальную группу в α-концевой части и гидроксильную группу в ω-концевой части. Среднечисловой молекулярный вес каждого сегмента блок-полимера, найденный по интегральному отношению в спектре, равен 5400 для полиэтиленоксида (ПЭО) и 6600 для полилактида (ПЛ).
Пример 3
В реакционную емкость вводят 20 мл тетрагидрофурана, 0,15 г 3,3-диэтоксипропанола и 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и перемешивают 3 минуты в атмосфере аргона; получают 3,3-диэтоксипропаноксид калия.
В реакционную емкость вводят 20 мл тетрагидрофурана, 0,15 г 3,3-диэтоксипропанола и 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и перемешивают 3 минуты в атмосфере аргона; получают 3,3-диэтоксипропаноксид калия.
В этот раствор добавляют 8,8 г этиленоксида и перемешивают при комнатной температуре и атмосферном давлении. После взаимодействия в течение 2 суток добавляют в этот реакционный раствор 5,0 г дельта-валеролактона и перемешивают 1 час. Этот раствор выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок выделяют методом центрифугирования и очищают посредством лиофильной сушки из бензола. Выход продукта 13,5 г (97%). Полимер, выделенный методом гель-проникающей хроматографии, является мономодальным, его молекулярный вес равен 14000.
В соответствии со спектром протонного ядерного магнитного резонанса полученного полимера в дейтерохлороформе было установлено, что он является гетеротелехелатным олигомером, имеющим как полиэтиленоксидные, так и поли(дельта-валеролактонные) блоки, и количественно содержит ацетальную группу в α-концевой части и гидроксильную группу в ω-концевой части (фиг. 3). Среднечисловой молекулярный вес каждого сегмента блок-полимера, найденный по интегральному отношению в спектре, равен 8800 для полиэтиленоксида и 5200 для поли (дельта-валеролактона).
Пример 4
Добавляют 50 мл 2-молярного раствора соляной кислоты к 50 мл метанола, в котором растворен образец блок-сополимера, полученного в Примере 2, смесь перемешивают 1 час при комнатной температуре. После этого раствор нейтрализуют водным раствором гидроксида натрия и в течение 4 ч подвергают его диализу (фракционный молекулярный вес 1000) относительно 20-кратного количества воды и очищают посредством лиофильной сушки. Выход продукта 0,85 г (85%). Установлено, что молекулярный вес полимера, выделенного методом гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
Добавляют 50 мл 2-молярного раствора соляной кислоты к 50 мл метанола, в котором растворен образец блок-сополимера, полученного в Примере 2, смесь перемешивают 1 час при комнатной температуре. После этого раствор нейтрализуют водным раствором гидроксида натрия и в течение 4 ч подвергают его диализу (фракционный молекулярный вес 1000) относительно 20-кратного количества воды и очищают посредством лиофильной сушки. Выход продукта 0,85 г (85%). Установлено, что молекулярный вес полимера, выделенного методом гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
В соответствии со спектром протонного ядерного магнитного резонанса полученного полимера в дейтерохлороформе в нем отсутствует ацетальная группа в α-концевой части и вместо нее появляется пик, обусловленный альдегидом. Установлено, что продукт является гетеротелехелатным ПЭО/ПЛ олигомером, содержащим альдегидную группу в α-концевой части и гидроксильную группу в ω-концевой части (фиг. 4).
Пример 5
Добавляют 20 мл пиридина и 1 г ангидрида метакриловой кислоты к 20 мл хлороформа, в котором растворен 1 г образца блок-сополимера, полученного в Примере 2, и смесь перемешивают 24 часа при комнатной температуре. После этого раствор нейтрализуют и промывают водным раствором соляной кислоты. Хлороформовую фазу выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок, выделенный методом центрифугирования, очищают посредством лиофильной сушки из бензола. Выход продукта 0,8 г (80%). Установлено, что молекулярный вес полимера, выделенного методом гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
Добавляют 20 мл пиридина и 1 г ангидрида метакриловой кислоты к 20 мл хлороформа, в котором растворен 1 г образца блок-сополимера, полученного в Примере 2, и смесь перемешивают 24 часа при комнатной температуре. После этого раствор нейтрализуют и промывают водным раствором соляной кислоты. Хлороформовую фазу выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок, выделенный методом центрифугирования, очищают посредством лиофильной сушки из бензола. Выход продукта 0,8 г (80%). Установлено, что молекулярный вес полимера, выделенного методом гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
В соответствии со спектром ядерного (углеродного) магнитного резонанса полученного полимера в дейтерохлороформе в нем полностью отсутствует гидроксильная группа в ω-терминальной части и вместо нее появляется пик, обусловленный метакрилоильной группой. Установлено, что продукт является гетеротелехелатным ПЭО/ПЛ олигомером, содержащим ацетальную группу в α-терминальной части и метакрилоильную группу в ω-терминальной части (фиг. 5).
Пример 6
Добавляют 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и 5 мл бромистого аллила к 20 мл тетрагидрофурана, в котором растворен 1 г блок-сополимера, полученного в Примере 2, и смесь перемешивают 4 часа при комнатной температуре. Полученный продукт выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок, выделенный методом центрифугирования, очищают посредством лиофильной сушки из бензола. Выход продукта 0,98 г (98%). Установлено, что молекулярный вес полимера, выделенного методом гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
Добавляют 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и 5 мл бромистого аллила к 20 мл тетрагидрофурана, в котором растворен 1 г блок-сополимера, полученного в Примере 2, и смесь перемешивают 4 часа при комнатной температуре. Полученный продукт выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок, выделенный методом центрифугирования, очищают посредством лиофильной сушки из бензола. Выход продукта 0,98 г (98%). Установлено, что молекулярный вес полимера, выделенного методом гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
В соответствии со спектром ядерного (углеродного) магнитного резонанса полученного полимера в дейтерохлороформе в нем полностью отсутствует гидроксильная группа в ω-концевой части и вместо нее появляется пик, обусловленный аллильной группой. Установлено, что продукт является гетеротелехелатным ПЭО/ПЛ олигомером, содержащим ацетальную группу в -концевой части и аллильную группу в ω-концевой части (фиг. 6).
Пример 7
Добавляют 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и 5 г паратолуолсульфонилхлорида к 20 мл тетрагидрофурана, в котором растворен 1 г блок-сополимера, полученного в Примере 4, и смесь перемешивают 4 часа при комнатной температуре. Полученный продукт выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок, выделенный методом центрифугирования, очищают посредством лиофильной сушки из бензола. Выход продукта 0,95 г (95%). Установлено, что молекулярный вес полимера, выделенного методом гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
Добавляют 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и 5 г паратолуолсульфонилхлорида к 20 мл тетрагидрофурана, в котором растворен 1 г блок-сополимера, полученного в Примере 4, и смесь перемешивают 4 часа при комнатной температуре. Полученный продукт выливают в охлажденный пропанол, осаждая образовавшийся полимер. Этот осадок, выделенный методом центрифугирования, очищают посредством лиофильной сушки из бензола. Выход продукта 0,95 г (95%). Установлено, что молекулярный вес полимера, выделенного методом гель-проникающей хроматографии, не изменился по сравнению с молекулярным весом до реакции.
В соответствии со спектром ядерного (углеродного) магнитного резонанса полученного полимера в дейтерохлороформе в нем полностью отсутствует гидроксильная группа в ω-концевой части и вместо нее появляется пик, обусловленный паратолуолсульфонильной группой. Установлено, что продукт является гетеротелехелатным ПЭО/ПЛ олигомером, содержащим ацетальную группу в α-концевой части и паратолуолсульфонильную группу в ω-концевой части (фиг. 7).
Пример 8
Растворяют 50 мг блок-сополимера, полученного в Примере 2, в воде или подходящем буферном растворе до достижения концентрации 0,01 - 0,1 вес. /объем.%. Когда образование мицеллы в этом растворе подтверждается распределением частиц по размерам, измеренным методом динамического светорассеяния, было установлено образование единственной полимерной мицеллы со средним диаметром зерна 30 нм (фиг. 8). Критическая концентрация мицелл для этой полимерной мицеллы составляет 10 мг/л.
Растворяют 50 мг блок-сополимера, полученного в Примере 2, в воде или подходящем буферном растворе до достижения концентрации 0,01 - 0,1 вес. /объем.%. Когда образование мицеллы в этом растворе подтверждается распределением частиц по размерам, измеренным методом динамического светорассеяния, было установлено образование единственной полимерной мицеллы со средним диаметром зерна 30 нм (фиг. 8). Критическая концентрация мицелл для этой полимерной мицеллы составляет 10 мг/л.
Пример 9
В реактор загружают 30 мл тетрагидрофурана, 0,13 г 3,3-диэтоксипропанола и 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и полученную смесь перемешивают 3 минуты в атмосфере аргона; таким образом получают 3,3-диэтоксипропаноксид калия.
В реактор загружают 30 мл тетрагидрофурана, 0,13 г 3,3-диэтоксипропанола и 2 мл 0,5-молярного раствора нафталинкалия в тетрагидрофуране и полученную смесь перемешивают 3 минуты в атмосфере аргона; таким образом получают 3,3-диэтоксипропаноксид калия.
В этот раствор добавляют 7,0 г этиленоксида, который затем перемешивают при комнатной температуре и атмосферном давлении. После взаимодействия в течение 2 суток добавляют в этот реакционный раствор 7,2 г лактида молочной кислоты и затем перемешивают эту смесь еще 1 час. Полученный таким образом раствор выливают в охлажденный пропанол, осаждая образовавшийся полимер. Осадок, выделенный методом центрифугирования, очищают посредством лиофильной сушки из бензола. Выход продукта 11,5 г (79%). Полимер, выделенный методом гель-проникающей хроматографии, является мономодальным, его среднечисловой молекулярный вес равен 11000.
Спектр протонного ядерного магнитного резонанса полученного полимера в дейтерохлороформе свидетельствует, что он является гетеротелехелатным олигомером, имеющим как полиэтиленоксидные, так и полилактидные блоки, и количественно содержит ацетальную группу в α-концевой части и гидроксильную группу в ω-концевой части. Что касается среднечислового молекулярного веса каждого сегмента блок-полимера, найденного по интегральному отношению в спектре, то он равен 5800 для полиэтиленоксида и 5100 для полилактида.
Растворяют 200 мг полученного блок-сополимера в 40 мл диметилацетамида и образовавшийся раствор подвергают диализу относительно воды с использованием мембраны для диализа, имеющей фракционный молекулярный вес 12000 - 14000, в течение 24 часов (воду меняли спустя 2,5 и 8 ч, каждый раз по 2 л). Измерения методом динамического светорассеяния показали, что в полученном растворе образовались высокомолекулярные мицеллы со средним размером частиц 40 нм. Критическая концентрация мицелл для этой полимерной мицеллы составляет 5 мг/л.
Пример 10
Добавляют по каплям 0,1-нормальную соляную кислоту к 10 мл мицеллярного раствора, полученного в Примере 9, так чтобы значение pH установилось равным 2, и затем раствор перемешивают в течение 2 ч при комнатной температуре. После этого раствор нейтрализуют 0,1-нормальным водным раствором гидроксида натрия и затем образовавшийся раствор подвергают диализу относительно воды с использованием мембраны для диализа, имеющей фракционный молекулярный вес 12000 - 14000, в течение 24 часов (воду меняли спустя 2,5 и 8 ч, каждый раз по 2 л). Измерения методом динамического светорассеяния показали, что в полученном растворе образовались высокомолекулярные мицеллы со средним размером частиц 40 нм. Критическая концентрация мицелл для этой полимерной мицеллы составляет 5 мг/л.
Добавляют по каплям 0,1-нормальную соляную кислоту к 10 мл мицеллярного раствора, полученного в Примере 9, так чтобы значение pH установилось равным 2, и затем раствор перемешивают в течение 2 ч при комнатной температуре. После этого раствор нейтрализуют 0,1-нормальным водным раствором гидроксида натрия и затем образовавшийся раствор подвергают диализу относительно воды с использованием мембраны для диализа, имеющей фракционный молекулярный вес 12000 - 14000, в течение 24 часов (воду меняли спустя 2,5 и 8 ч, каждый раз по 2 л). Измерения методом динамического светорассеяния показали, что в полученном растворе образовались высокомолекулярные мицеллы со средним размером частиц 40 нм. Критическая концентрация мицелл для этой полимерной мицеллы составляет 5 мг/л.
Этот мицеллярный раствор подвергли лиофильной сушке и затем остаток растворили в дейтеро-диметилсульфоксиде и исследовали методом ЯМР. Было установлено, что сигнал, обусловленный наличием ацетальной группы при 1,2 и 4,6 м. д., полностью исчез и что наблюдается сигнал, обусловленный наличием водорода метиленкарбонильной группы и водорода альдегидной группы при 2,7 (триплет) и 9,8 м.д. (синглет) соответственно. Из соотношения площадей этих сигналов было найдено, что 95% ацеталя гидролизовались в альдегид.
Пример 11
Растворяют 200 мг блок-сополимера ПЭО/ПЛ (среднечисловой молекулярный вес каждого сегмента равен 4500 для полиэтиленоксида и 13000 для полилактида), полученного таким же образом, как в Примере 1, в 40 мл диметилацетамида. Образовавшийся раствор подвергают диализу относительно воды с использованием мембраны для диализа, имеющей фракционный молекулярный вес 12000 - 14000, в течение 24 часов (воду меняли спустя 2,5 и 8 ч, каждый раз по 2 л). Измерения методом динамического светорассеяния показали, что в полученном растворе образовались высокомолекулярные мицеллы со средним размером частиц 30 нм. Критическая концентрация мицелл для этой полимерной мицеллы составляет 4 мг/л.
Растворяют 200 мг блок-сополимера ПЭО/ПЛ (среднечисловой молекулярный вес каждого сегмента равен 4500 для полиэтиленоксида и 13000 для полилактида), полученного таким же образом, как в Примере 1, в 40 мл диметилацетамида. Образовавшийся раствор подвергают диализу относительно воды с использованием мембраны для диализа, имеющей фракционный молекулярный вес 12000 - 14000, в течение 24 часов (воду меняли спустя 2,5 и 8 ч, каждый раз по 2 л). Измерения методом динамического светорассеяния показали, что в полученном растворе образовались высокомолекулярные мицеллы со средним размером частиц 30 нм. Критическая концентрация мицелл для этой полимерной мицеллы составляет 4 мг/л.
Промышленная применимость
Это изобретение обеспечивает гетеротелехелатный олигомер или полимер, который имеет различные функциональные группы на обоих концах молекулы и в то же время содержит в основной цепи гидрофильный сегмент и гидрофобный сегмент. Из составляющих компонентов можно ожидать, что этот олигомер или полимер будет обладать превосходной биологической пригодностью. Сверх того, этот олигомер или полимер способен образовывать высокомолекулярную мицеллу, которая вполне стабильна в водном растворителе. Поэтому весьма вероятно, что олигомер или полимер может использоваться для живых организмов или может применяться в такой области, где получается и/или используется носитель для подачи лекарств.
Это изобретение обеспечивает гетеротелехелатный олигомер или полимер, который имеет различные функциональные группы на обоих концах молекулы и в то же время содержит в основной цепи гидрофильный сегмент и гидрофобный сегмент. Из составляющих компонентов можно ожидать, что этот олигомер или полимер будет обладать превосходной биологической пригодностью. Сверх того, этот олигомер или полимер способен образовывать высокомолекулярную мицеллу, которая вполне стабильна в водном растворителе. Поэтому весьма вероятно, что олигомер или полимер может использоваться для живых организмов или может применяться в такой области, где получается и/или используется носитель для подачи лекарств.
Claims (12)
1. Гетеротелехелатный, блок-сополимер, который представлен следующей формулой:
в которой R1 и R2 независимо означают C1-10-алкокси или арил-С1-3-алкилокси, или R1 и R2, соединенные вместе, означают этилендиоксигруппу (-O-CH(R')-СН2-O, в которой R1 означает атом водорода или С1-6-алкил), которая может быть замещена С1-6-алкилом, или в сочетании друг с другом, означают оксогруппу (=0);
L означает группу
или
в которой R3 и R4 независимо означают атом водорода, C1-10-алкил, арил или арил-С1-3-алкил, и r означает целое число от 2 до 5;
m означает целое число от 2 до 10000;
n означает целое число от 2 до 10000;
p означает целое число от 1 до 5;
q означает целое число от 0 до 20,
Z означает, когда q равно нулю, атом водорода, щелочной металл, ацетил, акрилоил, метакрилоил, циннамоил, паратолуолсульфонил, 2-меркаптопропионил, или 2-аминопропионил, или аллил, или винилбензил, в то время как, когда q является целым числом от 1 до 20, Z означает С1-6-алкоксикарбонил, карбокси-, меркапто- или аминогруппу.
в которой R1 и R2 независимо означают C1-10-алкокси или арил-С1-3-алкилокси, или R1 и R2, соединенные вместе, означают этилендиоксигруппу (-O-CH(R')-СН2-O, в которой R1 означает атом водорода или С1-6-алкил), которая может быть замещена С1-6-алкилом, или в сочетании друг с другом, означают оксогруппу (=0);
L означает группу
или
в которой R3 и R4 независимо означают атом водорода, C1-10-алкил, арил или арил-С1-3-алкил, и r означает целое число от 2 до 5;
m означает целое число от 2 до 10000;
n означает целое число от 2 до 10000;
p означает целое число от 1 до 5;
q означает целое число от 0 до 20,
Z означает, когда q равно нулю, атом водорода, щелочной металл, ацетил, акрилоил, метакрилоил, циннамоил, паратолуолсульфонил, 2-меркаптопропионил, или 2-аминопропионил, или аллил, или винилбензил, в то время как, когда q является целым числом от 1 до 20, Z означает С1-6-алкоксикарбонил, карбокси-, меркапто- или аминогруппу.
2. Гетеротелехелатный блок-сополимер по п.1, отличающийся тем, что R1 и R2, соединенные вместе, означают оксогруппу.
3. Гетеротелехелатный блок-сополимер по п.1, отличающийся тем, что R1 и R2 независимо означают С1-6-алкокси- или бензилоксигруппу, или, когда соединены вместе, означают этилендиоксигруппу, которая может быть замещена С1-3-алкилом.
4. Гетеротелехелатный блок-cополимер по п.1, отличающийся тем, что R1 и R2, соединенные вместе, означают оксогруппу, а в группе L как R3, так и R4 представляют собой атом водорода или метил, или r означает целое число, равное 4; и q означает целое число от 0 до 3.
5. Гетеротелехелатный блок-cополимер по п.1, отличающийся тем, что R1 и R2 независимо означают С1-6-алкоксигруппу, а в группе L как R3, так и R4 представляют собой атом водорода или метил, или r означает целое число, равное 4; и q означает целое число от 0 до 3.
6. Гетеротелехелатный блок-сополимер по п.1, отличающийся тем, что m означает целое число от 10 до 200 и n означает целое число от 10 до 200.
7. Гетеротелехелатный блок-сополимер по п.1, отличающийся тем, что R1 и R2, соединенные вместе, означают оксогруппу, а в группе L как R3, так и R4 представляют собой атом водорода или метил, или r означает целое число, равное 4; q равно нулю и Z означает атом водорода, ацетил, акрилоил, метакрилоил, циннамоил, паратолуолсульфонил, аллил или винилбензил.
8. Гетеротелехелатный блок-сополимер по п.1, отличающийся тем, что R1 и R2 независимо означают С1-6-алкоксигруппу, а в группе L как R3, так и R4 представляют собой метил, или r означает целое число, равное 4; и q равно нулю; Z означает атом водорода, или натрий, калий, или цезий.
9. Гетеротелехелатный блок-сополимер по п.1, отличающийся тем, что R1 и R2, соединенные вместе, означают оксогруппу, а в группе L как R3, так и R4 представляют собой метил, или r означает целое число, равное 4; q является целым числом от 1 до, и Z означает С1-6-алкоксикарбонил, карбоксил-, меркапто- или аминогруппу.
10. Способ получения гетеротелехелатного блок-сополимера формулы I по п. 1, включающий следующие стадии:
Стадия 1)
взаимодействие инициатора полимеризации, представленного следующей формулой II:
в которой R1-1 и R2-1 независимо означают C1-10-алкокси- или, соединенные вместе, означают этилендиоксигруппу, которая может быть замещена С1-6-алкилом, p означает целое число от 1 до 5 и М означает щелочной металл,
c этиленоксидом таким образом, чтобы можно было получить соединение, представленное следующей формулой III:
в которой R1-1 и R2-1, p и M такие, как определено в формуле II;
m означает целое число от 2 до 10 000;
Стадия 2)
взаимодействие соединения формулы III с лактидом или лактоном, который представлен следующей формулой III-a или III-b:
или
в которой R3 и R4 независимо означают атом водорода, С1-10-алкил, арил или арил-С1-3-алкил и r означает целое число от 2 до 5,
таким образом, чтобы можно было получить блок-сополимер, представленный следующей формулой IV:
в которой L означает группу
или
R1-1, R2-1, p, m, n, М такие, как определено выше;
и, кроме того, в некоторых случаях
Стадия 3)
i) селективный гидролиз алкоксида щелочного металла формулы IV c получением блок-сополимера следующей формулы V:
в которой R1-1, R2-1, p, m, L и n такие, как определено выше; или
ii) полный гидролиз блок-сополимера формулы IV с получением блок-сополимера следующей формулы VI:
в которой p, m, L и n такие, как определено выше;
Стадия 4)
взаимодействие блок-сополимера формулы V с i) уксусной кислотой, акриловой кислотой, метакриловой кислотой, коричной кислотой или паратолуолсульфоновой кислотой, или их реакционноспособными производными, или с ii) аллилгалогенидом, или винилбензилгалогенидом, или с iii) галогенидом, представленным следующей формулой VII:
в которой X представляет собой атом хлора, брома или йода, q' является целым числом от 1 до 20, и Z' является С1-6,- алкоксикарбонилом или защищенной аминогруппой; и в некоторых случаях
Стадия 5)
трансэтерификацию полученной на стадии 4) -i) производной эфира паратолуолсульфоновой кислоты или гидролиз полученных на стадиях 4) - i), ii) или iii) производных.
Стадия 1)
взаимодействие инициатора полимеризации, представленного следующей формулой II:
в которой R1-1 и R2-1 независимо означают C1-10-алкокси- или, соединенные вместе, означают этилендиоксигруппу, которая может быть замещена С1-6-алкилом, p означает целое число от 1 до 5 и М означает щелочной металл,
c этиленоксидом таким образом, чтобы можно было получить соединение, представленное следующей формулой III:
в которой R1-1 и R2-1, p и M такие, как определено в формуле II;
m означает целое число от 2 до 10 000;
Стадия 2)
взаимодействие соединения формулы III с лактидом или лактоном, который представлен следующей формулой III-a или III-b:
или
в которой R3 и R4 независимо означают атом водорода, С1-10-алкил, арил или арил-С1-3-алкил и r означает целое число от 2 до 5,
таким образом, чтобы можно было получить блок-сополимер, представленный следующей формулой IV:
в которой L означает группу
или
R1-1, R2-1, p, m, n, М такие, как определено выше;
и, кроме того, в некоторых случаях
Стадия 3)
i) селективный гидролиз алкоксида щелочного металла формулы IV c получением блок-сополимера следующей формулы V:
в которой R1-1, R2-1, p, m, L и n такие, как определено выше; или
ii) полный гидролиз блок-сополимера формулы IV с получением блок-сополимера следующей формулы VI:
в которой p, m, L и n такие, как определено выше;
Стадия 4)
взаимодействие блок-сополимера формулы V с i) уксусной кислотой, акриловой кислотой, метакриловой кислотой, коричной кислотой или паратолуолсульфоновой кислотой, или их реакционноспособными производными, или с ii) аллилгалогенидом, или винилбензилгалогенидом, или с iii) галогенидом, представленным следующей формулой VII:
в которой X представляет собой атом хлора, брома или йода, q' является целым числом от 1 до 20, и Z' является С1-6,- алкоксикарбонилом или защищенной аминогруппой; и в некоторых случаях
Стадия 5)
трансэтерификацию полученной на стадии 4) -i) производной эфира паратолуолсульфоновой кислоты или гидролиз полученных на стадиях 4) - i), ii) или iii) производных.
11. Высокомолекулярная мицелла, включающая в качестве активного компонента гетеротелехелатный блок-сополимер формулы I по п.1, где Z означает группу, отличающуюся от щелочного металла, в воде, буферном растворе и/или органическом растворителе.
12. Высокомолекулярная мицелла по п.11, отличающаяся тем, что в гетеротелехелатном блок-cополимере формулы I по п.1 Z означает группу, отличающуюся от щелочного металла, в то время как R1 и R2, соединенные вместе, означают оксогруппу.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP93928/1995 | 1995-04-19 | ||
| JP9392895 | 1995-04-19 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU97119062A RU97119062A (ru) | 1999-08-10 |
| RU2169742C2 true RU2169742C2 (ru) | 2001-06-27 |
Family
ID=14096103
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU97119062/04A RU2169742C2 (ru) | 1995-04-19 | 1996-04-18 | Гетеротелехелатный блок-сополимер и способ его получения |
Country Status (16)
| Country | Link |
|---|---|
| US (1) | US5925720A (ru) |
| EP (1) | EP0822217B1 (ru) |
| JP (1) | JP3855279B2 (ru) |
| KR (1) | KR19990007861A (ru) |
| CN (1) | CN1085987C (ru) |
| AT (1) | ATE226603T1 (ru) |
| AU (1) | AU5346896A (ru) |
| BR (1) | BR9608330A (ru) |
| CA (1) | CA2218495A1 (ru) |
| DE (1) | DE69624475T2 (ru) |
| HU (1) | HUP9801633A3 (ru) |
| NO (1) | NO314762B1 (ru) |
| NZ (1) | NZ305471A (ru) |
| RU (1) | RU2169742C2 (ru) |
| SI (1) | SI9620067A (ru) |
| WO (1) | WO1996033233A1 (ru) |
Families Citing this family (173)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB9721367D0 (en) | 1997-10-09 | 1997-12-10 | Univ Liverpool | Delivery system |
| JP2001048978A (ja) | 1999-08-04 | 2001-02-20 | Nano Career Kk | オキサゾリン由来のポリマーセグメントを有するブロックコポリマー |
| US7807211B2 (en) | 1999-09-03 | 2010-10-05 | Advanced Cardiovascular Systems, Inc. | Thermal treatment of an implantable medical device |
| US20070032853A1 (en) | 2002-03-27 | 2007-02-08 | Hossainy Syed F | 40-O-(2-hydroxy)ethyl-rapamycin coated stent |
| US7682647B2 (en) * | 1999-09-03 | 2010-03-23 | Advanced Cardiovascular Systems, Inc. | Thermal treatment of a drug eluting implantable medical device |
| US6790228B2 (en) * | 1999-12-23 | 2004-09-14 | Advanced Cardiovascular Systems, Inc. | Coating for implantable devices and a method of forming the same |
| JP2001131092A (ja) * | 1999-11-04 | 2001-05-15 | Kazunori Kataoka | 薬物の通過を制御するための層状構造物 |
| CA2389917A1 (en) | 1999-11-04 | 2001-05-10 | Kazunori Kataoka | A polymer micelle as monolayer or layer-laminated surface |
| JP2001208754A (ja) * | 2000-01-26 | 2001-08-03 | Kazunori Kataoka | 生物学的な被検体を検出するための組成物 |
| AU5667901A (en) | 2000-05-11 | 2001-11-20 | Center For Advanced Science And Technology Incubation, Ltd. | Polymer composition for forming surface of biosensor |
| US7682648B1 (en) | 2000-05-31 | 2010-03-23 | Advanced Cardiovascular Systems, Inc. | Methods for forming polymeric coatings on stents |
| US6451373B1 (en) | 2000-08-04 | 2002-09-17 | Advanced Cardiovascular Systems, Inc. | Method of forming a therapeutic coating onto a surface of an implantable prosthesis |
| US6953560B1 (en) | 2000-09-28 | 2005-10-11 | Advanced Cardiovascular Systems, Inc. | Barriers for polymer-coated implantable medical devices and methods for making the same |
| US7807210B1 (en) | 2000-10-31 | 2010-10-05 | Advanced Cardiovascular Systems, Inc. | Hemocompatible polymers on hydrophobic porous polymers |
| US6824559B2 (en) * | 2000-12-22 | 2004-11-30 | Advanced Cardiovascular Systems, Inc. | Ethylene-carboxyl copolymers as drug delivery matrices |
| US6663662B2 (en) * | 2000-12-28 | 2003-12-16 | Advanced Cardiovascular Systems, Inc. | Diffusion barrier layer for implantable devices |
| US6780424B2 (en) * | 2001-03-30 | 2004-08-24 | Charles David Claude | Controlled morphologies in polymer drug for release of drugs from polymer films |
| US6712845B2 (en) * | 2001-04-24 | 2004-03-30 | Advanced Cardiovascular Systems, Inc. | Coating for a stent and a method of forming the same |
| US6656506B1 (en) * | 2001-05-09 | 2003-12-02 | Advanced Cardiovascular Systems, Inc. | Microparticle coated medical device |
| US6881484B2 (en) | 2001-05-30 | 2005-04-19 | Mitsubishi Kagaku Iatron, Inc. | Core-shell particle including signal-generating substance enclosed therein and process for producing the same |
| EP1405871A4 (en) * | 2001-05-30 | 2004-11-17 | Mitsubishi Kagaku Iatron Inc | METHOD FOR BINDING A SUBSTANCE TO BE INCORPORATED AT A POLYMER END |
| US6743462B1 (en) * | 2001-05-31 | 2004-06-01 | Advanced Cardiovascular Systems, Inc. | Apparatus and method for coating implantable devices |
| US7094810B2 (en) * | 2001-06-08 | 2006-08-22 | Labopharm, Inc. | pH-sensitive block copolymers for pharmaceutical compositions |
| US6939564B2 (en) * | 2001-06-08 | 2005-09-06 | Labopharm, Inc. | Water-soluble stabilized self-assembled polyelectrolytes |
| US8741378B1 (en) | 2001-06-27 | 2014-06-03 | Advanced Cardiovascular Systems, Inc. | Methods of coating an implantable device |
| US6695920B1 (en) | 2001-06-27 | 2004-02-24 | Advanced Cardiovascular Systems, Inc. | Mandrel for supporting a stent and a method of using the mandrel to coat a stent |
| CA2450949C (en) * | 2001-06-28 | 2009-04-28 | John Samuel | Methods and compositions for polyene antibiotics with reduced toxicity |
| JP4063510B2 (ja) * | 2001-07-13 | 2008-03-19 | ナノキャリア株式会社 | 薬物含有高分子ミセルの凍結乾燥用組成物およびその凍結乾燥製剤 |
| WO2003010302A1 (fr) | 2001-07-26 | 2003-02-06 | Kazunori Kataoka | Construction cellulaire cultivee contenant des spheroides de cellules animales cultivees et utilisation correspondante |
| US7682669B1 (en) | 2001-07-30 | 2010-03-23 | Advanced Cardiovascular Systems, Inc. | Methods for covalently immobilizing anti-thrombogenic material into a coating on a medical device |
| US8303651B1 (en) | 2001-09-07 | 2012-11-06 | Advanced Cardiovascular Systems, Inc. | Polymeric coating for reducing the rate of release of a therapeutic substance from a stent |
| US7285304B1 (en) | 2003-06-25 | 2007-10-23 | Advanced Cardiovascular Systems, Inc. | Fluid treatment of a polymeric coating on an implantable medical device |
| US7989018B2 (en) | 2001-09-17 | 2011-08-02 | Advanced Cardiovascular Systems, Inc. | Fluid treatment of a polymeric coating on an implantable medical device |
| US6753071B1 (en) | 2001-09-27 | 2004-06-22 | Advanced Cardiovascular Systems, Inc. | Rate-reducing membrane for release of an agent |
| US7223282B1 (en) | 2001-09-27 | 2007-05-29 | Advanced Cardiovascular Systems, Inc. | Remote activation of an implantable device |
| US6709514B1 (en) | 2001-12-28 | 2004-03-23 | Advanced Cardiovascular Systems, Inc. | Rotary coating apparatus for coating implantable medical devices |
| EP1489415A4 (en) * | 2002-03-11 | 2006-02-22 | Toudai Tlo Ltd | POLY (ETHYLENE OXIDE) SURFACE WITH BRUSH TYPE STRUCTURE HAVING HIGH DENSITY |
| US7919075B1 (en) | 2002-03-20 | 2011-04-05 | Advanced Cardiovascular Systems, Inc. | Coatings for implantable medical devices |
| WO2003082303A1 (en) * | 2002-03-29 | 2003-10-09 | Wisconsin Alumni Research Foundation | Polymeric micelle formulations of hydrophobic compounds and methods |
| US8506617B1 (en) | 2002-06-21 | 2013-08-13 | Advanced Cardiovascular Systems, Inc. | Micronized peptide coated stent |
| US7033602B1 (en) | 2002-06-21 | 2006-04-25 | Advanced Cardiovascular Systems, Inc. | Polycationic peptide coatings and methods of coating implantable medical devices |
| US7056523B1 (en) | 2002-06-21 | 2006-06-06 | Advanced Cardiovascular Systems, Inc. | Implantable medical devices incorporating chemically conjugated polymers and oligomers of L-arginine |
| US7217426B1 (en) | 2002-06-21 | 2007-05-15 | Advanced Cardiovascular Systems, Inc. | Coatings containing polycationic peptides for cardiovascular therapy |
| US7794743B2 (en) | 2002-06-21 | 2010-09-14 | Advanced Cardiovascular Systems, Inc. | Polycationic peptide coatings and methods of making the same |
| US7087263B2 (en) * | 2002-10-09 | 2006-08-08 | Advanced Cardiovascular Systems, Inc. | Rare limiting barriers for implantable medical devices |
| AU2003301409A1 (en) * | 2002-10-15 | 2004-05-04 | Wisconsin Alumni Research Foundation | Encapsulation and deaggregation of polyene antibiotics using poly(ethylene glycol)-phospholipid micelles |
| US6896965B1 (en) | 2002-11-12 | 2005-05-24 | Advanced Cardiovascular Systems, Inc. | Rate limiting barriers for implantable devices |
| US6982004B1 (en) | 2002-11-26 | 2006-01-03 | Advanced Cardiovascular Systems, Inc. | Electrostatic loading of drugs on implantable medical devices |
| US7776926B1 (en) | 2002-12-11 | 2010-08-17 | Advanced Cardiovascular Systems, Inc. | Biocompatible coating for implantable medical devices |
| US7758880B2 (en) | 2002-12-11 | 2010-07-20 | Advanced Cardiovascular Systems, Inc. | Biocompatible polyacrylate compositions for medical applications |
| US7074276B1 (en) | 2002-12-12 | 2006-07-11 | Advanced Cardiovascular Systems, Inc. | Clamp mandrel fixture and a method of using the same to minimize coating defects |
| US7758881B2 (en) | 2004-06-30 | 2010-07-20 | Advanced Cardiovascular Systems, Inc. | Anti-proliferative and anti-inflammatory agent combination for treatment of vascular disorders with an implantable medical device |
| US8435550B2 (en) | 2002-12-16 | 2013-05-07 | Abbot Cardiovascular Systems Inc. | Anti-proliferative and anti-inflammatory agent combination for treatment of vascular disorders with an implantable medical device |
| US20060002968A1 (en) | 2004-06-30 | 2006-01-05 | Gordon Stewart | Anti-proliferative and anti-inflammatory agent combination for treatment of vascular disorders |
| US7063884B2 (en) | 2003-02-26 | 2006-06-20 | Advanced Cardiovascular Systems, Inc. | Stent coating |
| US6926919B1 (en) * | 2003-02-26 | 2005-08-09 | Advanced Cardiovascular Systems, Inc. | Method for fabricating a coating for a medical device |
| US7563483B2 (en) * | 2003-02-26 | 2009-07-21 | Advanced Cardiovascular Systems Inc. | Methods for fabricating a coating for implantable medical devices |
| US7279174B2 (en) | 2003-05-08 | 2007-10-09 | Advanced Cardiovascular Systems, Inc. | Stent coatings comprising hydrophilic additives |
| US20050118344A1 (en) | 2003-12-01 | 2005-06-02 | Pacetti Stephen D. | Temperature controlled crimping |
| US7056591B1 (en) * | 2003-07-30 | 2006-06-06 | Advanced Cardiovascular Systems, Inc. | Hydrophobic biologically absorbable coatings for drug delivery devices and methods for fabricating the same |
| US7645474B1 (en) | 2003-07-31 | 2010-01-12 | Advanced Cardiovascular Systems, Inc. | Method and system of purifying polymers for use with implantable medical devices |
| US7431959B1 (en) * | 2003-07-31 | 2008-10-07 | Advanced Cardiovascular Systems Inc. | Method and system for irradiation of a drug eluting implantable medical device |
| US7785512B1 (en) | 2003-07-31 | 2010-08-31 | Advanced Cardiovascular Systems, Inc. | Method and system of controlled temperature mixing and molding of polymers with active agents for implantable medical devices |
| US7441513B1 (en) | 2003-09-26 | 2008-10-28 | Advanced Cardiovascular Systems, Inc. | Plasma-generated coating apparatus for medical devices and a method of coating deposition |
| US7198675B2 (en) | 2003-09-30 | 2007-04-03 | Advanced Cardiovascular Systems | Stent mandrel fixture and method for selectively coating surfaces of a stent |
| US7318932B2 (en) * | 2003-09-30 | 2008-01-15 | Advanced Cardiovascular Systems, Inc. | Coatings for drug delivery devices comprising hydrolitically stable adducts of poly(ethylene-co-vinyl alcohol) and methods for fabricating the same |
| US7704544B2 (en) * | 2003-10-07 | 2010-04-27 | Advanced Cardiovascular Systems, Inc. | System and method for coating a tubular implantable medical device |
| US7329413B1 (en) * | 2003-11-06 | 2008-02-12 | Advanced Cardiovascular Systems, Inc. | Coatings for drug delivery devices having gradient of hydration and methods for fabricating thereof |
| US9114198B2 (en) | 2003-11-19 | 2015-08-25 | Advanced Cardiovascular Systems, Inc. | Biologically beneficial coatings for implantable devices containing fluorinated polymers and methods for fabricating the same |
| US8192752B2 (en) | 2003-11-21 | 2012-06-05 | Advanced Cardiovascular Systems, Inc. | Coatings for implantable devices including biologically erodable polyesters and methods for fabricating the same |
| US7560492B1 (en) | 2003-11-25 | 2009-07-14 | Advanced Cardiovascular Systems, Inc. | Polysulfone block copolymers as drug-eluting coating material |
| US7807722B2 (en) * | 2003-11-26 | 2010-10-05 | Advanced Cardiovascular Systems, Inc. | Biobeneficial coating compositions and methods of making and using thereof |
| US7220816B2 (en) | 2003-12-16 | 2007-05-22 | Advanced Cardiovascular Systems, Inc. | Biologically absorbable coatings for implantable devices based on poly(ester amides) and methods for fabricating the same |
| US7435788B2 (en) | 2003-12-19 | 2008-10-14 | Advanced Cardiovascular Systems, Inc. | Biobeneficial polyamide/polyethylene glycol polymers for use with drug eluting stents |
| US8309112B2 (en) * | 2003-12-24 | 2012-11-13 | Advanced Cardiovascular Systems, Inc. | Coatings for implantable medical devices comprising hydrophilic substances and methods for fabricating the same |
| WO2005073370A1 (ja) * | 2004-01-31 | 2005-08-11 | Transparent Inc. | 酵素複合体 |
| US8685431B2 (en) | 2004-03-16 | 2014-04-01 | Advanced Cardiovascular Systems, Inc. | Biologically absorbable coatings for implantable devices based on copolymers having ester bonds and methods for fabricating the same |
| US8551512B2 (en) | 2004-03-22 | 2013-10-08 | Advanced Cardiovascular Systems, Inc. | Polyethylene glycol/poly(butylene terephthalate) copolymer coated devices including EVEROLIMUS |
| US8778014B1 (en) | 2004-03-31 | 2014-07-15 | Advanced Cardiovascular Systems, Inc. | Coatings for preventing balloon damage to polymer coated stents |
| US7820732B2 (en) | 2004-04-30 | 2010-10-26 | Advanced Cardiovascular Systems, Inc. | Methods for modulating thermal and mechanical properties of coatings on implantable devices |
| US8293890B2 (en) | 2004-04-30 | 2012-10-23 | Advanced Cardiovascular Systems, Inc. | Hyaluronic acid based copolymers |
| US9561309B2 (en) | 2004-05-27 | 2017-02-07 | Advanced Cardiovascular Systems, Inc. | Antifouling heparin coatings |
| US7563780B1 (en) | 2004-06-18 | 2009-07-21 | Advanced Cardiovascular Systems, Inc. | Heparin prodrugs and drug delivery stents formed therefrom |
| US20050287184A1 (en) | 2004-06-29 | 2005-12-29 | Hossainy Syed F A | Drug-delivery stent formulations for restenosis and vulnerable plaque |
| US7494665B1 (en) | 2004-07-30 | 2009-02-24 | Advanced Cardiovascular Systems, Inc. | Polymers containing siloxane monomers |
| US8357391B2 (en) | 2004-07-30 | 2013-01-22 | Advanced Cardiovascular Systems, Inc. | Coatings for implantable devices comprising poly (hydroxy-alkanoates) and diacid linkages |
| US7311980B1 (en) | 2004-08-02 | 2007-12-25 | Advanced Cardiovascular Systems, Inc. | Polyactive/polylactic acid coatings for an implantable device |
| US7648727B2 (en) | 2004-08-26 | 2010-01-19 | Advanced Cardiovascular Systems, Inc. | Methods for manufacturing a coated stent-balloon assembly |
| US7244443B2 (en) | 2004-08-31 | 2007-07-17 | Advanced Cardiovascular Systems, Inc. | Polymers of fluorinated monomers and hydrophilic monomers |
| US8110211B2 (en) | 2004-09-22 | 2012-02-07 | Advanced Cardiovascular Systems, Inc. | Medicated coatings for implantable medical devices including polyacrylates |
| US7166680B2 (en) | 2004-10-06 | 2007-01-23 | Advanced Cardiovascular Systems, Inc. | Blends of poly(ester amide) polymers |
| JP4920593B2 (ja) * | 2004-10-25 | 2012-04-18 | インテザイン テクノロジーズ, インコーポレイテッド | ヘテロ二官能性ポリ(エチレングリコール)およびそれらの使用 |
| US8603634B2 (en) | 2004-10-27 | 2013-12-10 | Abbott Cardiovascular Systems Inc. | End-capped poly(ester amide) copolymers |
| US7481835B1 (en) | 2004-10-29 | 2009-01-27 | Advanced Cardiovascular Systems, Inc. | Encapsulated covered stent |
| US7390497B2 (en) | 2004-10-29 | 2008-06-24 | Advanced Cardiovascular Systems, Inc. | Poly(ester amide) filler blends for modulation of coating properties |
| US7214759B2 (en) | 2004-11-24 | 2007-05-08 | Advanced Cardiovascular Systems, Inc. | Biologically absorbable coatings for implantable devices based on polyesters and methods for fabricating the same |
| US8609123B2 (en) | 2004-11-29 | 2013-12-17 | Advanced Cardiovascular Systems, Inc. | Derivatized poly(ester amide) as a biobeneficial coating |
| US7588642B1 (en) | 2004-11-29 | 2009-09-15 | Advanced Cardiovascular Systems, Inc. | Abluminal stent coating apparatus and method using a brush assembly |
| US7892592B1 (en) | 2004-11-30 | 2011-02-22 | Advanced Cardiovascular Systems, Inc. | Coating abluminal surfaces of stents and other implantable medical devices |
| US7604818B2 (en) | 2004-12-22 | 2009-10-20 | Advanced Cardiovascular Systems, Inc. | Polymers of fluorinated monomers and hydrocarbon monomers |
| US7419504B2 (en) | 2004-12-27 | 2008-09-02 | Advanced Cardiovascular Systems, Inc. | Poly(ester amide) block copolymers |
| US8007775B2 (en) | 2004-12-30 | 2011-08-30 | Advanced Cardiovascular Systems, Inc. | Polymers containing poly(hydroxyalkanoates) and agents for use with medical articles and methods of fabricating the same |
| US7202325B2 (en) | 2005-01-14 | 2007-04-10 | Advanced Cardiovascular Systems, Inc. | Poly(hydroxyalkanoate-co-ester amides) and agents for use with medical articles |
| AU2006221448B2 (en) * | 2005-03-09 | 2012-03-15 | Toray Industries, Inc. | Microparticle and pharmaceutical composition |
| US7795467B1 (en) | 2005-04-26 | 2010-09-14 | Advanced Cardiovascular Systems, Inc. | Bioabsorbable, biobeneficial polyurethanes for use in medical devices |
| US8778375B2 (en) | 2005-04-29 | 2014-07-15 | Advanced Cardiovascular Systems, Inc. | Amorphous poly(D,L-lactide) coating |
| EP2656840B1 (en) | 2005-06-09 | 2015-09-16 | NanoCarrier Co., Ltd. | Method for producing polymerized coordination compounds of platinum complex |
| US7823533B2 (en) | 2005-06-30 | 2010-11-02 | Advanced Cardiovascular Systems, Inc. | Stent fixture and method for reducing coating defects |
| US8021676B2 (en) | 2005-07-08 | 2011-09-20 | Advanced Cardiovascular Systems, Inc. | Functionalized chemically inert polymers for coatings |
| US7785647B2 (en) | 2005-07-25 | 2010-08-31 | Advanced Cardiovascular Systems, Inc. | Methods of providing antioxidants to a drug containing product |
| US7735449B1 (en) | 2005-07-28 | 2010-06-15 | Advanced Cardiovascular Systems, Inc. | Stent fixture having rounded support structures and method for use thereof |
| US7976891B1 (en) | 2005-12-16 | 2011-07-12 | Advanced Cardiovascular Systems, Inc. | Abluminal stent coating apparatus and method of using focused acoustic energy |
| US7591841B2 (en) | 2005-12-16 | 2009-09-22 | Advanced Cardiovascular Systems, Inc. | Implantable devices for accelerated healing |
| US7867547B2 (en) | 2005-12-19 | 2011-01-11 | Advanced Cardiovascular Systems, Inc. | Selectively coating luminal surfaces of stents |
| US7638156B1 (en) | 2005-12-19 | 2009-12-29 | Advanced Cardiovascular Systems, Inc. | Apparatus and method for selectively coating a medical article |
| US20070196428A1 (en) | 2006-02-17 | 2007-08-23 | Thierry Glauser | Nitric oxide generating medical devices |
| US7601383B2 (en) | 2006-02-28 | 2009-10-13 | Advanced Cardiovascular Systems, Inc. | Coating construct containing poly (vinyl alcohol) |
| JP5277439B2 (ja) | 2006-03-01 | 2013-08-28 | 国立大学法人 東京大学 | 核酸内包高分子ミセル複合体 |
| US7713637B2 (en) | 2006-03-03 | 2010-05-11 | Advanced Cardiovascular Systems, Inc. | Coating containing PEGylated hyaluronic acid and a PEGylated non-hyaluronic acid polymer |
| KR20080106219A (ko) * | 2006-03-06 | 2008-12-04 | 나노캬리아 가부시키가이샤 | 소수성 화합물의 안정화제 |
| EP2011516A4 (en) | 2006-04-24 | 2010-06-23 | Nanocarrier Co Ltd | PROCESS FOR THE PRODUCTION OF A POLYMERIC MICELLE THAT CONTAINS A CHEMICAL PRODUCT OF LOW MOLECULAR WEIGHT ENCAPSULATED IN IT |
| WO2007127440A2 (en) | 2006-04-27 | 2007-11-08 | Intezyne Technologies, Inc. | Heterofunctional poly(ethylene glycol) containing acid-labile amino protecting groups and uses thereof |
| US8304012B2 (en) | 2006-05-04 | 2012-11-06 | Advanced Cardiovascular Systems, Inc. | Method for drying a stent |
| US8003156B2 (en) | 2006-05-04 | 2011-08-23 | Advanced Cardiovascular Systems, Inc. | Rotatable support elements for stents |
| US7985441B1 (en) | 2006-05-04 | 2011-07-26 | Yiwen Tang | Purification of polymers for coating applications |
| US7775178B2 (en) | 2006-05-26 | 2010-08-17 | Advanced Cardiovascular Systems, Inc. | Stent coating apparatus and method |
| US8568764B2 (en) | 2006-05-31 | 2013-10-29 | Advanced Cardiovascular Systems, Inc. | Methods of forming coating layers for medical devices utilizing flash vaporization |
| US9561351B2 (en) | 2006-05-31 | 2017-02-07 | Advanced Cardiovascular Systems, Inc. | Drug delivery spiral coil construct |
| US8703167B2 (en) | 2006-06-05 | 2014-04-22 | Advanced Cardiovascular Systems, Inc. | Coatings for implantable medical devices for controlled release of a hydrophilic drug and a hydrophobic drug |
| US8778376B2 (en) | 2006-06-09 | 2014-07-15 | Advanced Cardiovascular Systems, Inc. | Copolymer comprising elastin pentapeptide block and hydrophilic block, and medical device and method of treating |
| US8603530B2 (en) | 2006-06-14 | 2013-12-10 | Abbott Cardiovascular Systems Inc. | Nanoshell therapy |
| US8114150B2 (en) | 2006-06-14 | 2012-02-14 | Advanced Cardiovascular Systems, Inc. | RGD peptide attached to bioabsorbable stents |
| US8048448B2 (en) | 2006-06-15 | 2011-11-01 | Abbott Cardiovascular Systems Inc. | Nanoshells for drug delivery |
| US8017237B2 (en) | 2006-06-23 | 2011-09-13 | Abbott Cardiovascular Systems, Inc. | Nanoshells on polymers |
| US9028859B2 (en) | 2006-07-07 | 2015-05-12 | Advanced Cardiovascular Systems, Inc. | Phase-separated block copolymer coatings for implantable medical devices |
| US8685430B1 (en) | 2006-07-14 | 2014-04-01 | Abbott Cardiovascular Systems Inc. | Tailored aliphatic polyesters for stent coatings |
| CN101489574A (zh) | 2006-07-18 | 2009-07-22 | 那野伽利阿株式会社 | 内包生理活性多肽或蛋白质的高分子聚合物胶束及其制造方法 |
| US8703169B1 (en) | 2006-08-15 | 2014-04-22 | Abbott Cardiovascular Systems Inc. | Implantable device having a coating comprising carrageenan and a biostable polymer |
| KR20090080046A (ko) * | 2006-09-22 | 2009-07-23 | 라보팜 인코포레이트 | pH 표적화된 약물 운반용 조성물 및 방법 |
| WO2008062909A1 (fr) | 2006-11-22 | 2008-05-29 | The University Of Tokyo | Support d'arnsi sensible à l'environnement utilisant une micelle polymérique à pont disulfure |
| US8597673B2 (en) | 2006-12-13 | 2013-12-03 | Advanced Cardiovascular Systems, Inc. | Coating of fast absorption or dissolution |
| US8147769B1 (en) | 2007-05-16 | 2012-04-03 | Abbott Cardiovascular Systems Inc. | Stent and delivery system with reduced chemical degradation |
| US9056155B1 (en) | 2007-05-29 | 2015-06-16 | Abbott Cardiovascular Systems Inc. | Coatings having an elastic primer layer |
| US20100178316A1 (en) * | 2007-05-30 | 2010-07-15 | Anuj Chauhan | Extended release of bioactive molecules from silicone hydrogels |
| US8048441B2 (en) | 2007-06-25 | 2011-11-01 | Abbott Cardiovascular Systems, Inc. | Nanobead releasing medical devices |
| US8109904B1 (en) | 2007-06-25 | 2012-02-07 | Abbott Cardiovascular Systems Inc. | Drug delivery medical devices |
| US8075909B2 (en) * | 2007-09-04 | 2011-12-13 | University Of Florida Research Foundation, Incorporated | Contact lens based bioactive agent delivery system |
| EP2284210B1 (en) | 2008-04-30 | 2017-12-06 | The University of Tokyo | Charge conversional ternary polyplex |
| WO2009133647A1 (ja) * | 2008-05-02 | 2009-11-05 | 国立大学法人筑波大学 | 高分子化環状二トロキシドラジカル化合物およびその使用 |
| US8895076B2 (en) * | 2008-06-24 | 2014-11-25 | Nanocarrier Co., Ltd. | Liquid composition of cisplatin coordination compound |
| WO2009157561A1 (ja) | 2008-06-26 | 2009-12-30 | 独立行政法人科学技術振興機構 | Mri造影能を有する重合体-金属錯体複合体、並びにそれを用いたmri造影用及び/又は抗腫瘍用組成物 |
| US20110081293A1 (en) | 2009-10-07 | 2011-04-07 | Sanford-Burnham Medical Research Institute | Methods and compositions related to clot-binding lipid compounds |
| JP4829351B2 (ja) | 2010-02-05 | 2011-12-07 | ナノキャリア株式会社 | 易崩壊型ポリマーミセル組成物 |
| US8685433B2 (en) | 2010-03-31 | 2014-04-01 | Abbott Cardiovascular Systems Inc. | Absorbable coating for implantable device |
| CA2795289A1 (en) | 2010-04-08 | 2011-10-13 | Sanford-Burnham Medical Research Institute | Methods and compositions for enhanced delivery of compounds |
| JP5843763B2 (ja) | 2010-05-21 | 2016-01-13 | 国立研究開発法人科学技術振興機構 | 物質内包ベシクル及びその製造方法 |
| WO2012005376A1 (ja) | 2010-07-09 | 2012-01-12 | 国立大学法人 東京大学 | 核酸送達用組成物及び担体組成物、それを用いた医薬組成物、並びに核酸送達方法 |
| CA2819635A1 (en) | 2010-12-01 | 2012-06-07 | Spinal Modulation, Inc. | Directed delivery of agents to neural anatomy |
| WO2012118778A1 (en) | 2011-02-28 | 2012-09-07 | Sanford-Burnham Medical Research Institute | Truncated car peptides and methods and compositions using truncated car peptides |
| JP5907418B2 (ja) * | 2011-03-25 | 2016-04-26 | 日油株式会社 | 水酸基含有アセタール化合物の製造方法 |
| US10179801B2 (en) | 2011-08-26 | 2019-01-15 | Sanford-Burnham Medical Research Institute | Truncated LYP-1 peptides and methods and compositions using truncated LYP-1 peptides |
| JP5982798B2 (ja) * | 2011-12-01 | 2016-08-31 | 三菱レイヨン株式会社 | ポリエステル(メタ)アクリレートの製造方法 |
| CN109663550B (zh) | 2013-03-01 | 2021-08-06 | 国立研究开发法人科学技术振兴机构 | 物质包封微囊及其制备方法 |
| JP5692887B1 (ja) | 2013-05-17 | 2015-04-01 | ナノキャリア株式会社 | ポリマーミセル医薬組成物 |
| JP2015046867A (ja) | 2013-07-31 | 2015-03-12 | 株式会社リコー | 撮像装置 |
| AU2014303571B2 (en) | 2013-08-06 | 2017-03-02 | Japan Science And Technology Agency | Nucleic acid-encapsulating polymer micelle complex and method for producing same |
| JP6145612B2 (ja) | 2013-08-23 | 2017-06-14 | 国立大学法人 東京大学 | 高分子ナノ粒子複合体、及びそれを含むmri造影用組成物 |
| JP5971264B2 (ja) | 2014-01-10 | 2016-08-17 | Jfeスチール株式会社 | 極厚肉油井管用ねじ継手 |
| WO2015163195A1 (ja) * | 2014-04-25 | 2015-10-29 | 日産化学工業株式会社 | レジスト下層膜形成組成物及びそれを用いたレジストパターンの形成方法 |
| WO2016210423A2 (en) | 2015-06-25 | 2016-12-29 | Sanford Burnham Prebys Medical Discovery Institute | Compositions for delivery to and treatment of atherosclerotic plaques |
| US11981752B2 (en) | 2017-05-02 | 2024-05-14 | Sanford Burnham Prebys Medical Discovery Institute | Tumor associated monocyte/macrophage binding peptide and methods of use thereof |
| WO2020161602A1 (en) | 2019-02-04 | 2020-08-13 | University Of Tartu | Bi-specific extracellular matrix binding peptides and methods of use thereof |
| JPWO2023068347A1 (ru) * | 2021-10-22 | 2023-04-27 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE4039193A1 (de) * | 1990-12-08 | 1992-06-11 | Bayer Ag | In wasser dispergierbare, elektrolytstabile polyetherester-modifizierte polyurethanionomere |
| US5410016A (en) * | 1990-10-15 | 1995-04-25 | Board Of Regents, The University Of Texas System | Photopolymerizable biodegradable hydrogels as tissue contacting materials and controlled-release carriers |
| FR2678168B1 (fr) * | 1991-06-28 | 1993-09-03 | Rhone Poulenc Rorer Sa | Nanoparticules ayant un temps de capture par le dysteme reticulo endothelial allonge. |
-
1996
- 1996-04-18 BR BR9608330-1A patent/BR9608330A/pt not_active IP Right Cessation
- 1996-04-18 EP EP96910195A patent/EP0822217B1/en not_active Expired - Lifetime
- 1996-04-18 DE DE69624475T patent/DE69624475T2/de not_active Expired - Lifetime
- 1996-04-18 US US08/930,898 patent/US5925720A/en not_active Expired - Lifetime
- 1996-04-18 SI SI9620067A patent/SI9620067A/sl not_active IP Right Cessation
- 1996-04-18 NZ NZ305471A patent/NZ305471A/en unknown
- 1996-04-18 RU RU97119062/04A patent/RU2169742C2/ru active
- 1996-04-18 AU AU53468/96A patent/AU5346896A/en not_active Abandoned
- 1996-04-18 CA CA002218495A patent/CA2218495A1/en not_active Abandoned
- 1996-04-18 CN CN96194818A patent/CN1085987C/zh not_active Expired - Lifetime
- 1996-04-18 AT AT96910195T patent/ATE226603T1/de not_active IP Right Cessation
- 1996-04-18 JP JP53161996A patent/JP3855279B2/ja not_active Expired - Lifetime
- 1996-04-18 WO PCT/JP1996/001057 patent/WO1996033233A1/ja active IP Right Grant
- 1996-04-18 KR KR1019970707384A patent/KR19990007861A/ko active IP Right Grant
- 1996-04-18 HU HU9801633A patent/HUP9801633A3/hu unknown
-
1997
- 1997-10-10 NO NO19974678A patent/NO314762B1/no not_active IP Right Cessation
Non-Patent Citations (1)
| Title |
|---|
| Энциклопедия полимеров. -М.: Советская энциклопедия, 1974, т.2, С.933-935. * |
Also Published As
| Publication number | Publication date |
|---|---|
| EP0822217B1 (en) | 2002-10-23 |
| NZ305471A (en) | 2000-02-28 |
| NO974678L (no) | 1997-12-02 |
| EP0822217A4 (en) | 2000-09-20 |
| AU5346896A (en) | 1996-11-07 |
| US5925720A (en) | 1999-07-20 |
| HUP9801633A3 (en) | 1999-03-01 |
| KR19990007861A (ko) | 1999-01-25 |
| CA2218495A1 (en) | 1996-10-24 |
| BR9608330A (pt) | 1999-11-30 |
| MX9708025A (es) | 1998-07-31 |
| NO974678D0 (no) | 1997-10-10 |
| WO1996033233A1 (fr) | 1996-10-24 |
| DE69624475D1 (de) | 2002-11-28 |
| SI9620067A (sl) | 1998-06-30 |
| HUP9801633A2 (hu) | 1998-11-30 |
| CN1085987C (zh) | 2002-06-05 |
| CN1187829A (zh) | 1998-07-15 |
| JP3855279B2 (ja) | 2006-12-06 |
| ATE226603T1 (de) | 2002-11-15 |
| NO314762B1 (no) | 2003-05-19 |
| EP0822217A1 (en) | 1998-02-04 |
| DE69624475T2 (de) | 2003-05-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2169742C2 (ru) | Гетеротелехелатный блок-сополимер и способ его получения | |
| RU2193574C2 (ru) | Полиоксиэтилен, имеющий сахар на одном конце и другую функциональную группу на другом конце, и способ его получения | |
| RU2174989C2 (ru) | Блок-полимер, имеющий функциональные группы на обоих концах | |
| US7960479B2 (en) | Brush copolymers | |
| US20040166089A1 (en) | Biodegradable polyacetals | |
| EP1345982A2 (en) | Synthesis of high molecular weight non-peptidic polymer derivatives | |
| AU2002246705A1 (en) | Synthesis of high molecular weight non-peptidic polymer derivatives | |
| JP2007504298A (ja) | 酸感受性ポリアセタールおよび製造方法 | |
| EP1076671B1 (fr) | Polyetherester sequence non-reticule, sa preparation, et ses utilisations | |
| JP4581248B2 (ja) | 片末端に保護されていてもよいアミノ基を有するポリオキシエチレン誘導体及びその製造方法 | |
| US10814004B2 (en) | Hydrophilic polyester and a block copolymer thereof | |
| EP1219661B1 (en) | Block copolymer having polymer segment derived from oxazoline | |
| AU744832B2 (en) | Heterotelechelic block copolymers and process for preparing same | |
| KR100288002B1 (ko) | 폴리엘락타이드와 폴리에틸렌옥사이드의 스타형 공중합체 | |
| CN109054010A (zh) | 一种咪唑环修饰的酸敏感聚碳酸酯材料及其制备和应用 | |
| CN113861403B (zh) | 一种纳米材料及其制备方法和应用 | |
| Bizzarri et al. | Synthesis and Characterization of Segmented Hydrosoluble Poly (Tartaraide) s | |
| JP3832633B2 (ja) | アミノ基含有ポリマーセグメントを有するブロックコポリマー | |
| Lee et al. | Temperature-sensitive biodegradable poly (ethylene glycol) | |
| US20230416462A1 (en) | Functionalised polyglycine-poly(alkylene imine)-copolymers, the preparation thereof and use thereof for preparing formulations of or for complexing anionic active ingredients and effect substances | |
| Chen et al. | AN APPROACH TO SYNTHESIZE POLY (ETHYLENE GLYCOL)-b-POLY (ε-CAPROLACTONE) WITH TERMINAL AMINO GROUP via SCHIFF'S BASE AS AN INITIATOR | |
| CN118576547A (zh) | 一种苯甲醛修饰的寡糖基自组装材料的制备方法 | |
| Cuong et al. | Preparation of nanoparticle of methoxy poly (ethylene glycol)/poly (ɛ-caprolactone)/methoxy poly (ethylene glycol) triblock copolymer for drug delivery applications | |
| NZ502021A (en) | Heterotelechelic block copolymer and a polymeric micelle comprising the heterotelechelic block copolymer in an aqueous solvent | |
| Han et al. | Construction of micelles based on biocompatible pseudo-graft polymers via b-cyclodextrin/cholesterol interaction for protein delivery |