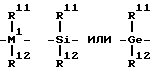RU2142466C1 - Металлоцены, содержащая их каталитическая система, способ полимеризации олефинов, полиолефин, формованное изделие - Google Patents
Металлоцены, содержащая их каталитическая система, способ полимеризации олефинов, полиолефин, формованное изделие Download PDFInfo
- Publication number
- RU2142466C1 RU2142466C1 RU94045142A RU94045142A RU2142466C1 RU 2142466 C1 RU2142466 C1 RU 2142466C1 RU 94045142 A RU94045142 A RU 94045142A RU 94045142 A RU94045142 A RU 94045142A RU 2142466 C1 RU2142466 C1 RU 2142466C1
- Authority
- RU
- Russia
- Prior art keywords
- indenyl
- methyl
- metallocene
- polymerization
- hydrogen atom
- Prior art date
Links
- 238000006116 polymerization reaction Methods 0.000 title claims abstract description 48
- 239000003054 catalyst Substances 0.000 title claims abstract description 27
- 238000000034 method Methods 0.000 title claims abstract description 22
- 150000001336 alkenes Chemical class 0.000 title claims abstract description 21
- 229920000098 polyolefin Polymers 0.000 title claims abstract description 18
- 239000003446 ligand Substances 0.000 claims abstract description 33
- 150000001875 compounds Chemical class 0.000 claims abstract description 27
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 claims abstract description 13
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 claims abstract description 9
- 125000001424 substituent group Chemical group 0.000 claims abstract description 7
- 150000003623 transition metal compounds Chemical class 0.000 claims abstract description 3
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 26
- 125000003118 aryl group Chemical group 0.000 claims description 19
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 claims description 12
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 claims description 10
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 10
- 125000004429 atom Chemical group 0.000 claims description 8
- 239000000460 chlorine Substances 0.000 claims description 6
- 125000004122 cyclic group Chemical group 0.000 claims description 6
- 125000005843 halogen group Chemical group 0.000 claims description 5
- 229910052751 metal Inorganic materials 0.000 claims description 5
- 239000002184 metal Substances 0.000 claims description 5
- QCWXUUIWCKQGHC-UHFFFAOYSA-N Zirconium Chemical compound [Zr] QCWXUUIWCKQGHC-UHFFFAOYSA-N 0.000 claims description 4
- 230000003197 catalytic effect Effects 0.000 claims description 4
- 229910052732 germanium Inorganic materials 0.000 claims description 4
- GNPVGFCGXDBREM-UHFFFAOYSA-N germanium atom Chemical compound [Ge] GNPVGFCGXDBREM-UHFFFAOYSA-N 0.000 claims description 4
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 claims description 4
- 230000000737 periodic effect Effects 0.000 claims description 4
- 229910052710 silicon Inorganic materials 0.000 claims description 4
- 239000010703 silicon Substances 0.000 claims description 4
- 229910052726 zirconium Inorganic materials 0.000 claims description 4
- 229910052801 chlorine Inorganic materials 0.000 claims description 3
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 claims description 2
- 238000007334 copolymerization reaction Methods 0.000 claims description 2
- 125000000923 (C1-C30) alkyl group Chemical group 0.000 claims 1
- 239000003426 co-catalyst Substances 0.000 claims 1
- 230000000694 effects Effects 0.000 abstract description 38
- 229920000642 polymer Polymers 0.000 abstract description 27
- 239000000126 substance Substances 0.000 abstract description 2
- -1 polypropylenes Polymers 0.000 description 155
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 87
- 229910007926 ZrCl Inorganic materials 0.000 description 74
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 50
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 39
- 238000002844 melting Methods 0.000 description 37
- 230000008018 melting Effects 0.000 description 37
- 150000003254 radicals Chemical class 0.000 description 31
- 239000004743 Polypropylene Substances 0.000 description 24
- 229920001155 polypropylene Polymers 0.000 description 24
- 239000000203 mixture Substances 0.000 description 20
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 20
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 20
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 16
- 239000007787 solid Substances 0.000 description 16
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 15
- 239000000725 suspension Substances 0.000 description 15
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 13
- 229910052782 aluminium Inorganic materials 0.000 description 13
- 239000001257 hydrogen Substances 0.000 description 13
- 229910052739 hydrogen Inorganic materials 0.000 description 13
- 238000005160 1H NMR spectroscopy Methods 0.000 description 12
- 239000005977 Ethylene Substances 0.000 description 12
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 12
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 11
- 238000006243 chemical reaction Methods 0.000 description 11
- 238000002425 crystallisation Methods 0.000 description 11
- 230000008025 crystallization Effects 0.000 description 11
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 11
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 10
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 10
- 229920001577 copolymer Polymers 0.000 description 10
- 239000000741 silica gel Substances 0.000 description 10
- 229910002027 silica gel Inorganic materials 0.000 description 10
- 239000002904 solvent Substances 0.000 description 10
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 9
- 238000001816 cooling Methods 0.000 description 9
- 238000004587 chromatography analysis Methods 0.000 description 8
- 239000000706 filtrate Substances 0.000 description 8
- 238000001914 filtration Methods 0.000 description 8
- 239000007789 gas Substances 0.000 description 8
- 239000000047 product Substances 0.000 description 8
- 238000003756 stirring Methods 0.000 description 8
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 8
- 125000000217 alkyl group Chemical group 0.000 description 7
- 238000004519 manufacturing process Methods 0.000 description 7
- 230000037048 polymerization activity Effects 0.000 description 7
- 238000005086 pumping Methods 0.000 description 7
- NMJQKZSYJLCZRP-UHFFFAOYSA-L [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=CC=CC=C12)C)C1C(=CC2=C(C=C(C=C12)C(C)C)C(C)C)C)C Chemical compound [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=CC=CC=C12)C)C1C(=CC2=C(C=C(C=C12)C(C)C)C(C)C)C)C NMJQKZSYJLCZRP-UHFFFAOYSA-L 0.000 description 6
- 229910052786 argon Inorganic materials 0.000 description 6
- 230000000052 comparative effect Effects 0.000 description 6
- DIOQZVSQGTUSAI-UHFFFAOYSA-N decane Chemical compound CCCCCCCCCC DIOQZVSQGTUSAI-UHFFFAOYSA-N 0.000 description 6
- 239000007788 liquid Substances 0.000 description 6
- LIKMAJRDDDTEIG-UHFFFAOYSA-N 1-hexene Chemical compound CCCCC=C LIKMAJRDDDTEIG-UHFFFAOYSA-N 0.000 description 5
- 239000004215 Carbon black (E152) Substances 0.000 description 5
- IJWJAVHBOCRHSP-UHFFFAOYSA-L [Cl-].[Cl-].C1=CC=C2C([Zr+2])C(C)=CC2=C1 Chemical compound [Cl-].[Cl-].C1=CC=C2C([Zr+2])C(C)=CC2=C1 IJWJAVHBOCRHSP-UHFFFAOYSA-L 0.000 description 5
- AJCKLOJBLGNWCG-UHFFFAOYSA-L [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=C(C=CC=C12)C1=CC=CC=C1)C)C1C(=CC2=C(C=C(C=C12)C)C)C)C Chemical compound [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=C(C=CC=C12)C1=CC=CC=C1)C)C1C(=CC2=C(C=C(C=C12)C)C)C)C AJCKLOJBLGNWCG-UHFFFAOYSA-L 0.000 description 5
- HPBOKPHNHXTBOO-UHFFFAOYSA-L [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=C(C=CC=C12)C1=CC=CC=C1)C)C1C(=CC2=CC=CC=C12)C)C Chemical compound [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=C(C=CC=C12)C1=CC=CC=C1)C)C1C(=CC2=CC=CC=C12)C)C HPBOKPHNHXTBOO-UHFFFAOYSA-L 0.000 description 5
- 230000005595 deprotonation Effects 0.000 description 5
- 238000010537 deprotonation reaction Methods 0.000 description 5
- LIKFHECYJZWXFJ-UHFFFAOYSA-N dimethyldichlorosilane Chemical compound C[Si](C)(Cl)Cl LIKFHECYJZWXFJ-UHFFFAOYSA-N 0.000 description 5
- 229930195733 hydrocarbon Natural products 0.000 description 5
- CPOFMOWDMVWCLF-UHFFFAOYSA-N methyl(oxo)alumane Chemical compound C[Al]=O CPOFMOWDMVWCLF-UHFFFAOYSA-N 0.000 description 5
- 229910052757 nitrogen Inorganic materials 0.000 description 5
- 239000000843 powder Substances 0.000 description 5
- DUNKXUFBGCUVQW-UHFFFAOYSA-J zirconium tetrachloride Chemical compound Cl[Zr](Cl)(Cl)Cl DUNKXUFBGCUVQW-UHFFFAOYSA-J 0.000 description 5
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 4
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 4
- YSAXEHWHSLANOM-UHFFFAOYSA-N 2-methyl-1h-indene Chemical compound C1=CC=C2CC(C)=CC2=C1 YSAXEHWHSLANOM-UHFFFAOYSA-N 0.000 description 4
- KAKZBPTYRLMSJV-UHFFFAOYSA-N Butadiene Chemical compound C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 description 4
- 0 CC**(N)N(C)NC(C)C1CC1 Chemical compound CC**(N)N(C)NC(C)C1CC1 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 230000004913 activation Effects 0.000 description 4
- 238000007792 addition Methods 0.000 description 4
- 238000009835 boiling Methods 0.000 description 4
- 125000004432 carbon atom Chemical group C* 0.000 description 4
- LMLNKUQAGCNMEI-UHFFFAOYSA-N diethylgermanium Chemical compound CC[Ge]CC LMLNKUQAGCNMEI-UHFFFAOYSA-N 0.000 description 4
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 4
- 150000002430 hydrocarbons Chemical class 0.000 description 4
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 4
- 239000012071 phase Substances 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- VPGLGRNSAYHXPY-UHFFFAOYSA-L zirconium(2+);dichloride Chemical compound Cl[Zr]Cl VPGLGRNSAYHXPY-UHFFFAOYSA-L 0.000 description 4
- VXNZUUAINFGPBY-UHFFFAOYSA-N 1-Butene Chemical compound CCC=C VXNZUUAINFGPBY-UHFFFAOYSA-N 0.000 description 3
- ASGNRCDZSRNHOP-UHFFFAOYSA-N 2-methyl-4-phenyl-1h-indene Chemical compound C1C(C)=CC2=C1C=CC=C2C1=CC=CC=C1 ASGNRCDZSRNHOP-UHFFFAOYSA-N 0.000 description 3
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 150000001768 cations Chemical class 0.000 description 3
- 125000001309 chloro group Chemical group Cl* 0.000 description 3
- 150000002431 hydrogen Chemical class 0.000 description 3
- 239000012442 inert solvent Substances 0.000 description 3
- 229910052740 iodine Inorganic materials 0.000 description 3
- 239000000178 monomer Substances 0.000 description 3
- OFBQJSOFQDEBGM-UHFFFAOYSA-N n-pentane Natural products CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 3
- 239000012074 organic phase Substances 0.000 description 3
- XOJVVFBFDXDTEG-UHFFFAOYSA-N pristane Chemical compound CC(C)CCCC(C)CCCC(C)CCCC(C)C XOJVVFBFDXDTEG-UHFFFAOYSA-N 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 125000006736 (C6-C20) aryl group Chemical group 0.000 description 2
- KWKAKUADMBZCLK-UHFFFAOYSA-N 1-octene Chemical compound CCCCCCC=C KWKAKUADMBZCLK-UHFFFAOYSA-N 0.000 description 2
- WSSSPWUEQFSQQG-UHFFFAOYSA-N 4-methyl-1-pentene Chemical compound CC(C)CC=C WSSSPWUEQFSQQG-UHFFFAOYSA-N 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 2
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 2
- HJAVWBIOWBZBJR-UHFFFAOYSA-L [Cl-].[Cl-].CC1=Cc2c(cccc2-c2ccccc2)C1[Zr++](C1C=Cc2ccccc12)=[Si](C)C Chemical compound [Cl-].[Cl-].CC1=Cc2c(cccc2-c2ccccc2)C1[Zr++](C1C=Cc2ccccc12)=[Si](C)C HJAVWBIOWBZBJR-UHFFFAOYSA-L 0.000 description 2
- CGELJBSWQTYCIY-UHFFFAOYSA-L [Cl-].[Cl-].CC1=Cc2ccccc2[C@H]1[Zr++]([C@@H]1C(C)=Cc2ccccc12)=[Si](C)C Chemical compound [Cl-].[Cl-].CC1=Cc2ccccc2[C@H]1[Zr++]([C@@H]1C(C)=Cc2ccccc12)=[Si](C)C CGELJBSWQTYCIY-UHFFFAOYSA-L 0.000 description 2
- HZGZUAGSEQAQHN-UHFFFAOYSA-L [Cl-].[Cl-].CC=1C(C2=CC=CC(=C2C=1)C1=CC=CC2=CC=CC=C12)[Zr+2]C1C=CC2=CC=CC=C12 Chemical compound [Cl-].[Cl-].CC=1C(C2=CC=CC(=C2C=1)C1=CC=CC2=CC=CC=C12)[Zr+2]C1C=CC2=CC=CC=C12 HZGZUAGSEQAQHN-UHFFFAOYSA-L 0.000 description 2
- TZOVODTYCURFAW-UHFFFAOYSA-L [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=C(C=CC=C12)C1=CC=CC=C1)C)C1C(=CC2=CC=C3C(=C12)C1=CC=CC2=CC=CC3=C12)C)C Chemical compound [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=C(C=CC=C12)C1=CC=CC=C1)C)C1C(=CC2=CC=C3C(=C12)C1=CC=CC2=CC=CC3=C12)C)C TZOVODTYCURFAW-UHFFFAOYSA-L 0.000 description 2
- 229920001400 block copolymer Polymers 0.000 description 2
- 150000001639 boron compounds Chemical class 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- 239000012876 carrier material Substances 0.000 description 2
- 239000012230 colorless oil Substances 0.000 description 2
- 229940125904 compound 1 Drugs 0.000 description 2
- 229940125782 compound 2 Drugs 0.000 description 2
- 229940126214 compound 3 Drugs 0.000 description 2
- BWUPRNSPZFPYEK-UHFFFAOYSA-N dichloro(diethyl)germane Chemical compound CC[Ge](Cl)(Cl)CC BWUPRNSPZFPYEK-UHFFFAOYSA-N 0.000 description 2
- 150000001993 dienes Chemical class 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- HQQADJVZYDDRJT-UHFFFAOYSA-N ethene;prop-1-ene Chemical group C=C.CC=C HQQADJVZYDDRJT-UHFFFAOYSA-N 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- 230000009477 glass transition Effects 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 238000001819 mass spectrum Methods 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- UAEPNZWRGJTJPN-UHFFFAOYSA-N methylcyclohexane Chemical compound CC1CCCCC1 UAEPNZWRGJTJPN-UHFFFAOYSA-N 0.000 description 2
- 230000007935 neutral effect Effects 0.000 description 2
- YWAKXRMUMFPDSH-UHFFFAOYSA-N pentene Chemical compound CCCC=C YWAKXRMUMFPDSH-UHFFFAOYSA-N 0.000 description 2
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 2
- 239000002685 polymerization catalyst Substances 0.000 description 2
- 229910052723 transition metal Inorganic materials 0.000 description 2
- 150000003624 transition metals Chemical class 0.000 description 2
- PRBHEGAFLDMLAL-GQCTYLIASA-N (4e)-hexa-1,4-diene Chemical compound C\C=C\CC=C PRBHEGAFLDMLAL-GQCTYLIASA-N 0.000 description 1
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 1
- 125000002733 (C1-C6) fluoroalkyl group Chemical group 0.000 description 1
- CAYKGPJSXROKPC-UHFFFAOYSA-N 1-(2-methyl-1h-inden-4-yl)naphthalene Chemical compound C1=CC=C2C(C3=CC=CC4=C3C=C(C4)C)=CC=CC2=C1 CAYKGPJSXROKPC-UHFFFAOYSA-N 0.000 description 1
- OSNBXQPGMJVNOI-UHFFFAOYSA-N 2,4,6-trimethyl-1h-indene Chemical compound C1=C(C)C=C(C)C2=C1CC(C)=C2 OSNBXQPGMJVNOI-UHFFFAOYSA-N 0.000 description 1
- LATXWLSATQMXRJ-UHFFFAOYSA-N 2-chloro-1-[2-(2-chloro-1h-inden-1-yl)ethyl]-1h-indene;hafnium Chemical compound [Hf].ClC1=CC2=CC=CC=C2C1CCC1C2=CC=CC=C2C=C1Cl LATXWLSATQMXRJ-UHFFFAOYSA-N 0.000 description 1
- BSHJHVHMLRKHBZ-UHFFFAOYSA-N 2-ethyl-1h-indene Chemical compound C1=CC=C2CC(CC)=CC2=C1 BSHJHVHMLRKHBZ-UHFFFAOYSA-N 0.000 description 1
- XFNIQDLAPZZUMH-UHFFFAOYSA-N 2-methyl-4,6-di(propan-2-yl)-1h-indene Chemical compound CC(C)C1=CC(C(C)C)=CC2=C1C=C(C)C2 XFNIQDLAPZZUMH-UHFFFAOYSA-N 0.000 description 1
- JQCCMEDYANGBOG-UHFFFAOYSA-N 2-methyl-7-phenyl-1h-indene Chemical compound C=12CC(C)=CC2=CC=CC=1C1=CC=CC=C1 JQCCMEDYANGBOG-UHFFFAOYSA-N 0.000 description 1
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 1
- GKMHIUUTNXOKMS-UHFFFAOYSA-N C1C=CC2=CC=CC=C12.CC1CC=2C=CC=C3C=CC=C1C23 Chemical compound C1C=CC2=CC=CC=C12.CC1CC=2C=CC=C3C=CC=C1C23 GKMHIUUTNXOKMS-UHFFFAOYSA-N 0.000 description 1
- 239000005046 Chlorosilane Substances 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- LCGLNKUTAGEVQW-UHFFFAOYSA-N Dimethyl ether Chemical group COC LCGLNKUTAGEVQW-UHFFFAOYSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- NHTMVDHEPJAVLT-UHFFFAOYSA-N Isooctane Chemical compound CC(C)CC(C)(C)C NHTMVDHEPJAVLT-UHFFFAOYSA-N 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 229910000528 Na alloy Inorganic materials 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- MCMNRKCIXSYSNV-UHFFFAOYSA-N ZrO2 Inorganic materials O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 description 1
- RHCKTFQGHZBIAW-UHFFFAOYSA-L [Cl-].[Cl-].C=C.C1=CC(CCCC2)=C2C1[Hf+2]C1C=CC2=C1CCCC2 Chemical compound [Cl-].[Cl-].C=C.C1=CC(CCCC2)=C2C1[Hf+2]C1C=CC2=C1CCCC2 RHCKTFQGHZBIAW-UHFFFAOYSA-L 0.000 description 1
- BLJCVRMHRMXLAA-UHFFFAOYSA-L [Cl-].[Cl-].CC=1C(C2=CC=CC(=C2C=1)C1=CC=CC=C1)[Zr+2]C1C(=CC2=CC=CC=C12)CC Chemical compound [Cl-].[Cl-].CC=1C(C2=CC=CC(=C2C=1)C1=CC=CC=C1)[Zr+2]C1C(=CC2=CC=CC=C12)CC BLJCVRMHRMXLAA-UHFFFAOYSA-L 0.000 description 1
- GVIVLTWZZBCGSN-UHFFFAOYSA-L [Cl-].[Cl-].CC=1C(C2=CC=CC=C2C=1)[Zr+2]C1C(=CC2=C(C=CC=C12)C1=CC=CC=C1)C Chemical compound [Cl-].[Cl-].CC=1C(C2=CC=CC=C2C=1)[Zr+2]C1C(=CC2=C(C=CC=C12)C1=CC=CC=C1)C GVIVLTWZZBCGSN-UHFFFAOYSA-L 0.000 description 1
- BTVTVYDJLNOHQA-UHFFFAOYSA-L [Cl-].[Cl-].CCC1=CC2=CC=CC=C2C1[Zr+2]([GeH](CC)CC)C1C(C)=CC2=C1C=CC=C2C1=CC=CC=C1 Chemical compound [Cl-].[Cl-].CCC1=CC2=CC=CC=C2C1[Zr+2]([GeH](CC)CC)C1C(C)=CC2=C1C=CC=C2C1=CC=CC=C1 BTVTVYDJLNOHQA-UHFFFAOYSA-L 0.000 description 1
- BDUOJPXPGBVEOF-UHFFFAOYSA-L [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=CC=CC=C12)C)C1C(=CC2=C(C=CC=C12)C1=CC=CC2=CC=CC=C12)C)C Chemical compound [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=CC=CC=C12)C)C1C(=CC2=C(C=CC=C12)C1=CC=CC2=CC=CC=C12)C)C BDUOJPXPGBVEOF-UHFFFAOYSA-L 0.000 description 1
- LCTFFCNOOPHXKY-UHFFFAOYSA-L [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=CC=CC=C12)C)C1C(=CC2=C(C=CC=C12)C1=CC=CC=C1)CC)C Chemical compound [Cl-].[Cl-].C[Si](=[Zr+2](C1C(=CC2=CC=CC=C12)C)C1C(=CC2=C(C=CC=C12)C1=CC=CC=C1)CC)C LCTFFCNOOPHXKY-UHFFFAOYSA-L 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 1
- 229920001585 atactic polymer Polymers 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 239000001273 butane Substances 0.000 description 1
- IAQRGUVFOMOMEM-UHFFFAOYSA-N butene Natural products CC=CC IAQRGUVFOMOMEM-UHFFFAOYSA-N 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- KOPOQZFJUQMUML-UHFFFAOYSA-N chlorosilane Chemical compound Cl[SiH3] KOPOQZFJUQMUML-UHFFFAOYSA-N 0.000 description 1
- 239000002826 coolant Substances 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- YQECBLVSMFAWIZ-UHFFFAOYSA-N dichloro(dimethyl)germane Chemical compound C[Ge](C)(Cl)Cl YQECBLVSMFAWIZ-UHFFFAOYSA-N 0.000 description 1
- 239000002283 diesel fuel Substances 0.000 description 1
- JVSWJIKNEAIKJW-UHFFFAOYSA-N dimethyl-hexane Natural products CCCCCC(C)C JVSWJIKNEAIKJW-UHFFFAOYSA-N 0.000 description 1
- QAIUTSJMFUOGED-UHFFFAOYSA-N dimethylgermanium Chemical compound C[Ge]C QAIUTSJMFUOGED-UHFFFAOYSA-N 0.000 description 1
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 238000005194 fractionation Methods 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229910052735 hafnium Inorganic materials 0.000 description 1
- VBJZVLUMGGDVMO-UHFFFAOYSA-N hafnium atom Chemical compound [Hf] VBJZVLUMGGDVMO-UHFFFAOYSA-N 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- JUJWWFXGMQILNM-UHFFFAOYSA-N lithium;2-methyl-1h-inden-1-ide Chemical compound [Li+].C1=CC=C2[CH-]C(C)=CC2=C1 JUJWWFXGMQILNM-UHFFFAOYSA-N 0.000 description 1
- DWWZPYPYUFXZTL-UHFFFAOYSA-N lithium;2h-inden-2-ide Chemical compound [Li+].C1=CC=C2[CH-]C=CC2=C1 DWWZPYPYUFXZTL-UHFFFAOYSA-N 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 239000000155 melt Substances 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 239000012968 metallocene catalyst Substances 0.000 description 1
- GYNNXHKOJHMOHS-UHFFFAOYSA-N methyl-cycloheptane Natural products CC1CCCCCC1 GYNNXHKOJHMOHS-UHFFFAOYSA-N 0.000 description 1
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- TVMXDCGIABBOFY-UHFFFAOYSA-N n-Octanol Natural products CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 1
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 description 1
- SJYNFBVQFBRSIB-UHFFFAOYSA-N norbornadiene Chemical compound C1=CC2C=CC1C2 SJYNFBVQFBRSIB-UHFFFAOYSA-N 0.000 description 1
- 238000006384 oligomerization reaction Methods 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- RVTZCBVAJQQJTK-UHFFFAOYSA-N oxygen(2-);zirconium(4+) Chemical compound [O-2].[O-2].[Zr+4] RVTZCBVAJQQJTK-UHFFFAOYSA-N 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000002574 poison Substances 0.000 description 1
- 231100000614 poison Toxicity 0.000 description 1
- 230000000379 polymerizing effect Effects 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 125000001339 silanediyl group Chemical group [H][Si]([H])(*)* 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 238000001256 steam distillation Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 238000010557 suspension polymerization reaction Methods 0.000 description 1
- 229920006027 ternary co-polymer Polymers 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- MCULRUJILOGHCJ-UHFFFAOYSA-N triisobutylaluminium Chemical compound CC(C)C[Al](CC(C)C)CC(C)C MCULRUJILOGHCJ-UHFFFAOYSA-N 0.000 description 1
- JLTRXTDYQLMHGR-UHFFFAOYSA-N trimethylaluminium Chemical compound C[Al](C)C JLTRXTDYQLMHGR-UHFFFAOYSA-N 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F210/00—Copolymers of unsaturated aliphatic hydrocarbons having only one carbon-to-carbon double bond
- C08F210/04—Monomers containing three or four carbon atoms
- C08F210/06—Propene
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F17/00—Metallocenes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/0805—Compounds with Si-C or Si-Si linkages comprising only Si, C or H atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/30—Germanium compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F10/00—Homopolymers and copolymers of unsaturated aliphatic hydrocarbons having only one carbon-to-carbon double bond
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/42—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors
- C08F4/44—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides
- C08F4/60—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides together with refractory metals, iron group metals, platinum group metals, manganese, rhenium technetium or compounds thereof
- C08F4/62—Refractory metals or compounds thereof
- C08F4/64—Titanium, zirconium, hafnium or compounds thereof
- C08F4/659—Component covered by group C08F4/64 containing a transition metal-carbon bond
- C08F4/65912—Component covered by group C08F4/64 containing a transition metal-carbon bond in combination with an organoaluminium compound
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/42—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors
- C08F4/44—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides
- C08F4/60—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides together with refractory metals, iron group metals, platinum group metals, manganese, rhenium technetium or compounds thereof
- C08F4/62—Refractory metals or compounds thereof
- C08F4/64—Titanium, zirconium, hafnium or compounds thereof
- C08F4/659—Component covered by group C08F4/64 containing a transition metal-carbon bond
- C08F4/6592—Component covered by group C08F4/64 containing a transition metal-carbon bond containing at least one cyclopentadienyl ring, condensed or not, e.g. an indenyl or a fluorenyl ring
- C08F4/65922—Component covered by group C08F4/64 containing a transition metal-carbon bond containing at least one cyclopentadienyl ring, condensed or not, e.g. an indenyl or a fluorenyl ring containing at least two cyclopentadienyl rings, fused or not
- C08F4/65927—Component covered by group C08F4/64 containing a transition metal-carbon bond containing at least one cyclopentadienyl ring, condensed or not, e.g. an indenyl or a fluorenyl ring containing at least two cyclopentadienyl rings, fused or not two cyclopentadienyl rings being mutually bridged
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F110/00—Homopolymers of unsaturated aliphatic hydrocarbons having only one carbon-to-carbon double bond
- C08F110/04—Monomers containing three or four carbon atoms
- C08F110/06—Propene
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F2420/00—Metallocene catalysts
- C08F2420/08—Heteroatom bridge, i.e. Cp or analog where the bridging atom linking the two Cps or analogs is a heteroatom different from Si
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/42—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors
- C08F4/44—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides
- C08F4/60—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides together with refractory metals, iron group metals, platinum group metals, manganese, rhenium technetium or compounds thereof
- C08F4/62—Refractory metals or compounds thereof
- C08F4/639—Component covered by group C08F4/62 containing a transition metal-carbon bond
- C08F4/63912—Component covered by group C08F4/62 containing a transition metal-carbon bond in combination with an organoaluminium compound
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/42—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors
- C08F4/44—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides
- C08F4/60—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides together with refractory metals, iron group metals, platinum group metals, manganese, rhenium technetium or compounds thereof
- C08F4/62—Refractory metals or compounds thereof
- C08F4/639—Component covered by group C08F4/62 containing a transition metal-carbon bond
- C08F4/63916—Component covered by group C08F4/62 containing a transition metal-carbon bond supported on a carrier, e.g. silica, MgCl2, polymer
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/42—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors
- C08F4/44—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides
- C08F4/60—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides together with refractory metals, iron group metals, platinum group metals, manganese, rhenium technetium or compounds thereof
- C08F4/62—Refractory metals or compounds thereof
- C08F4/639—Component covered by group C08F4/62 containing a transition metal-carbon bond
- C08F4/6392—Component covered by group C08F4/62 containing a transition metal-carbon bond containing at least one cyclopentadienyl ring, condensed or not, e.g. an indenyl or a fluorenyl ring
- C08F4/63922—Component covered by group C08F4/62 containing a transition metal-carbon bond containing at least one cyclopentadienyl ring, condensed or not, e.g. an indenyl or a fluorenyl ring containing at least two cyclopentadienyl rings, fused or not
- C08F4/63927—Component covered by group C08F4/62 containing a transition metal-carbon bond containing at least one cyclopentadienyl ring, condensed or not, e.g. an indenyl or a fluorenyl ring containing at least two cyclopentadienyl rings, fused or not two cyclopentadienyl rings being mutually bridged
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F4/00—Polymerisation catalysts
- C08F4/42—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors
- C08F4/44—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides
- C08F4/60—Metals; Metal hydrides; Metallo-organic compounds; Use thereof as catalyst precursors selected from light metals, zinc, cadmium, mercury, copper, silver, gold, boron, gallium, indium, thallium, rare earths or actinides together with refractory metals, iron group metals, platinum group metals, manganese, rhenium technetium or compounds thereof
- C08F4/62—Refractory metals or compounds thereof
- C08F4/64—Titanium, zirconium, hafnium or compounds thereof
- C08F4/659—Component covered by group C08F4/64 containing a transition metal-carbon bond
- C08F4/65916—Component covered by group C08F4/64 containing a transition metal-carbon bond supported on a carrier, e.g. silica, MgCl2, polymer
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S526/00—Synthetic resins or natural rubbers -- part of the class 520 series
- Y10S526/943—Polymerization with metallocene catalysts
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Crystallography & Structural Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Transition And Organic Metals Composition Catalysts For Addition Polymerization (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Catalysts (AREA)
Abstract
Предложены новые металлоценовые соединения общей формулы (I), в которой оба типа инденил-лигандов имеют отличные друг от друга заместители. Металлоценовые соединения могут использоваться в качестве компонента катализатора для полимеризации олефинов. Изобретение касается также способа получения олефинового полимера путем полимеризации в присутствии катализатора, который содержит по меньшей мере один из заявленных металлоценов в качестве соединения переходного металла и по меньшей мере один сокатализатор. 5 с. и 5 з. п. ф-лы, 2 табл.
Description
Изобретение относится к металлоценам, которые при технически приемлемых температурах может использоваться для получения полиолефинов с высокой изотактичностью и высокой молярной массой.
Из литературы известно получение полиолефинов с помощью растворимых металлоценовых соединений в комбинации с алюминоксанами или другими сокатализаторами, которые на основании их кислотности по Льюису могут переводить нейтральный металлоцен в катион и стабилизировать его.
Например, был предложен специальный метод предварительной активации металлоцена с помощью алюминоксана, который приводит к значительному повышению активности системы катализаторов и к явному улучшению морфологии зерен полимера (сравни Европейский патент N 0302424). Хотя предварительная активация повышает молярную массу, однако значительное повышение достигнуто быть не может.
Дальнейшее, но еще недостаточное повышение молекулярной массы могло быть реализовано благодаря использованию специально соединенных гетероатомными мостиками металлоценов при высокой их активности (Европейская выложенная заявка N 0336128).
Кроме того, известны катализаторы на основе этиленбисинденилдихлорида гафния, этилен-бис(4,5,6,7-тетрагидро-1-инденил)дихлорида гафния и метилалюминоксана, с помощью которых путем суспензионной полимеризации можно получать высокомолекулярные полипропилены (сравни: J. A. Ewen et al., J. Am. Chem. Soc. 109 (1987) 6544). Однако при технически важных условиях полимеризации морфология зерен полученных таким образом полимеров является неудовлетворительной и активность использованных катализаторов сравнительно невелика. Таким образом с помощью этих систем экономически выгодная полимеризация невозможна, что связано с высокой стоимостью катализаторов.
Явного повышения молекулярной массы можно было бы добиться благодаря применению металлоценов, у которых зафиксированные с помощью мостика ароматические π- лиганды имеют заместители в положении 2 (Европейский патент N 485822) и в положении 2 и 4, 6 (Европейский патент N 545303).
При необходимости крупнотехнического, требующего небольших затрат производства полимеризация должна осуществляться при возможно более высоких температурах реакции, так как при более высоких температурах полимеризация образующаяся теплота полимеризации может отводиться с помощью меньшего количества охлаждающей среды и поэтому может быть реализовано с помощью контура водяного охлаждения, имеющего явно меньшие размеры.
Вышеупомянутые металлоцены с заместителями в положении 2 или 4 или 6 для мостичной связи в этом отношении при температуре полимеризации 70oC уже очень эффективны, несмотря на то, что получаемые молярные массы при технически важных температурах полимеризации (например, 70oC) для некоторых технических областей применения, как, например, получение полимеров для труб и больших пустотелых корпусов, а также специальных волокон, все еще слишком малы.
Металлоцены с двумя замещенными циклопентадиенил -π- лигандами, как, например, диметил-силандиил(2-метил-4-трет-бутил-1-циклопентадиенил)2 ZrCl2, также были предложены в качестве катализаторов полимеризации (H.-H. Brintzinger et al., Angew. Chem. 102 (1990) 339), однако эти системы никоим образом не приемлемы с точки зрения достигаемой молекулярной массы полимера, стереоспецифичности или температуры плавления полимера, помимо этого их полимеризационная активность очень низка и очень сложно необходимое разделение получающихся при синтезе мезоформ и рацформ, только с помощью рацформы можно получить изотактический полиолефин. Кроме того, мезоформа получается в таком же количестве, что и рацформа, что означает, что половина исходных веществ используется нерентабельно и может быть использована только половина продукта.
В Европейском патенте N 544308 предлагаются катализаторы с двумя различными π- лигандами, как, например, изопропилиден(4-метил-1-циклопентадиенил) (3-трет-бутил-1-инденил) ZrCl2, которые по причине их асимметрии априори не имеют мезоформы и таким образом не возникает проблема разделения на рац- и мезоформу, однако дефициты относительно свойств полимера и активности катализатора не могли быть ликвидированы.
Из работ Эвена и других (J. Am. Chem. Soc. 110 (1988) 6255) известны такие катализаторы с двумя различными π- лигандами, как, например, изопропилиден (циклопентадиенил) (фторфенил) ZrCl2. Эти асимметричные соединения позволяют, однако, получать синдиотактические полиолефины, тем самым получение изотактических полиолефинов невозможно.
Таким образом задача заключалась в разработке системы катализаторов, которая предотвращает недостатки уровня техники и, в частности, при технически важных температурах полимеризации с высокой изотактической стереоселективностью и полимеризационной активностью позволяет получать полиолефины с высокой молекулярной массой.
Было обнаружено, что эта задача может быть решена с помощью металлоценового соединения с двумя отличными друг от друга инденил-лигандами, которые замещены определенным образом.
Вследствие их химической структуры металлоцены в соответствии с изобретением не имеют мезоформы, которую необходимо было отделять дорогостоящим образом, так как с мезоформами можно получить только атактический полиолефин.
Помимо этого на основании предложенной концепции металлоценовых катализаторов можно с помощью комбинации мало отличных друг от друга π- лигандов приготовить получаемую с меньшими затратами палитру катализаторов полимеризации, отвечающих различным требованиям, предъявляемым к продукту.
Настоящее изобретение касается металлоценов формулы I
в которой M2 - является металлом группы IVb Периодической системы;
радикалы R1 - обозначают атом галогена или метильную группу;
радикалы R2 - обозначают атом водорода;
радикалы R3 - одинаковы или различны и обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу, или два или больше радикалов R3 образуют вместе с соединяющими их атомами кольцевую систему;
радикалы R4 одинаковы или различны и обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу;
радикал R5 - обозначает атом галогена, C1-C10-алкильную группу;
радикал R6 - обозначает атом водорода, C1-C10-алкильную группу;
радикалом R7 является
причем радикалы R8, R9, R11, R12 одинаковы или различны и обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу;
M1 является кремнием или германием;
m=0 или 1;
при этом оба инденильных лиганда имеют отличные друг от друга заместители.
в которой M2 - является металлом группы IVb Периодической системы;
радикалы R1 - обозначают атом галогена или метильную группу;
радикалы R2 - обозначают атом водорода;
радикалы R3 - одинаковы или различны и обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу, или два или больше радикалов R3 образуют вместе с соединяющими их атомами кольцевую систему;
радикалы R4 одинаковы или различны и обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу;
радикал R5 - обозначает атом галогена, C1-C10-алкильную группу;
радикал R6 - обозначает атом водорода, C1-C10-алкильную группу;
радикалом R7 является
причем радикалы R8, R9, R11, R12 одинаковы или различны и обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу;
M1 является кремнием или германием;
m=0 или 1;
при этом оба инденильных лиганда имеют отличные друг от друга заместители.
Алкил представляет собой алкил с линейной или разветвленной цепью. Галоген обозначает фтор, хлор, бром или йод, предпочтительно фтор или хлор. Радикалы можно различать с помощью тех же самых индексов.
M2 является металлом группы IVb Периодической системы, например титаном, цирконием, гафнием, особенно предпочтителен цирконий.
Радикалы R3 являются соответственно одинаковыми и различными и обозначают атом водорода, C1-C20-, предпочтительно C1-C10-алкильную группу, C6-C30-, предпочтительно C6-C20-алкильную группу, или два или несколько радикалов R3 совместно с соединяющими их атомами образуют кольцевую систему, которая является одноядерной или многоядерной.
Радикалы R4 являются соответственно одинаковыми или различными и обозначают атом водорода, C1-C20-, предпочтительно C1-C10-алкильную группу, C6-C30-, предпочтительно C6-C20-арильную группу.
Радикал R5 обозначает атом галогена, предпочтительно атом фтора, хлора, брома, C1-C10-, предпочтительно C1-C4-алкильную группу.
Радикал R6 обозначает атом водорода, C1-C10-, предпочтительно C1-C4-алкильную группу.
Радикалом R7 является
причем R11, R12 одинаковы или различны и обозначают атом водорода, C1-C20-, предпочтительно C1-C10-алкильную группу, C6-C30-, предпочтительно C6-C20-арильную группу.
причем R11, R12 одинаковы или различны и обозначают атом водорода, C1-C20-, предпочтительно C1-C10-алкильную группу, C6-C30-, предпочтительно C6-C20-арильную группу.
M1 - это кремний или германий.
Радикал R7 - это предпочтительно =CR11R12, =SiR11R12, =GeR11R12.
Радикалы R8 и R9 одинаковы и обозначают атом водорода.
m = 0 или 1.
Эти инденил-лиганды имеют отличные друг от друга образцы заместителей, в частности в шестичленном цикле.
Предпочтительными являются металлоцены формулы (I), в которой M2 обозначает цирконий, радикалы R1 одинаковы и обозначают метил или хлор, радикал R2 является водородом, радикалы R3 обозначают атом водорода, C1-C20-алкильную группу или C6-C30-арильную группу, или два или большее количество радикалов R3 образуют совместно с соединяющими их атомами кольцевую систему, радикалы R4 обозначают атом водорода, C1-C20-алкильную группу или C6-C30-арильную группу, радикал R5 является C1-C10-, предпочтительно C1-C4-алкильной группой, радикал R6 является атомом водорода или C1-C10-, предпочтительно C1-C4-алкильной группой, радикал R7 обозначает группу
предпочтительно
в которой R11 и R12 одинаковы или различны и являются C1-C20-алкильной группой или C6-C30-арильной группой, R8 и R9 одинаковы и обозначают атом водорода, в частности, такие соединения формулы I, в которых по меньшей мере один из двух инденил-лигандов имеет в положении 2-, 2,4-, 2,5-, 2,6-, 2,4,6, 2,4,5-, 2,4,5,6- или 2,5,6-заместители, отличные от водорода.
предпочтительно
в которой R11 и R12 одинаковы или различны и являются C1-C20-алкильной группой или C6-C30-арильной группой, R8 и R9 одинаковы и обозначают атом водорода, в частности, такие соединения формулы I, в которых по меньшей мере один из двух инденил-лигандов имеет в положении 2-, 2,4-, 2,5-, 2,6-, 2,4,6, 2,4,5-, 2,4,5,6- или 2,5,6-заместители, отличные от водорода.
Особенно предпочтительные соединения формулы I состоят из следующих молекулярных фрагментов a, b, c и d:
a) -(CR8R9)m-R7 - аналогичен с диалкилсиландиилом, алкил(арил)силандиилом, 1,2-этандиилом, 1,2-бутандиилом, диарилсиландиилом, диалкилметиленом, диарилметиленом, алкил(арил)метиленом, алкил(винил)силандиилом, арил(винил)силандиилом или диалкилгермилом;
b) R4 3R2R5 -1-инденил аналогичен с 2-алкил-4-арил-1-инденилом, 2,4-диалкил-1-инденилом, 2,4,6-триалкил-1-инденилом, 2-алкил-4,5-бензо-1-инденилом, 2,5-диалкил-1-инденилом, 2,5,6-триалкил-1-инденилом, 2,4,5-триалкил-1-инденилом, 2-алкил-1-инденилом, 2-арил-1-инденилом, 2,6-алкил-4-арил-1-инденилом, 2-алкил-5-арил-1-инденилом, 2-алкил-5,6-диарил-инденилом, 2-алкил-4,5-диарил-1-инденилом или 2-алкил-4,6-диарил-инденилом;
c) R4 4R2R6 -1-инденил - аналогичен с 2-алкил-4-арил-1-инденилом, 2,4-диалкил-1-инденилом, 2,4,6-триалкил-1-инденилом, 2-алкил-4,5-бензо-1-инденилом, 2,5-диалкил-1-инденилом, 2,5,6-триалкил-1-инденилом, 2,4,5-триалкил-1-инденилом, 2-алкил-1-инденилом, 2-арил-1-инденилом, 2,6-алкил-4-арил-1-инденилом, 2-алкил-5-арил-1-инденилом, 2-алкил-5,6-диарил-1-инденилом, 2-алкил-5,6-диарил-1-инденилом, 2-алкил-4,5-диарил-1-инденилом;
d) M2R2 1 аналогичен с ZrCl2, Zr(Me)Cl или ZrMe2.
a) -(CR8R9)m-R7 - аналогичен с диалкилсиландиилом, алкил(арил)силандиилом, 1,2-этандиилом, 1,2-бутандиилом, диарилсиландиилом, диалкилметиленом, диарилметиленом, алкил(арил)метиленом, алкил(винил)силандиилом, арил(винил)силандиилом или диалкилгермилом;
b) R4 3R2R5 -1-инденил аналогичен с 2-алкил-4-арил-1-инденилом, 2,4-диалкил-1-инденилом, 2,4,6-триалкил-1-инденилом, 2-алкил-4,5-бензо-1-инденилом, 2,5-диалкил-1-инденилом, 2,5,6-триалкил-1-инденилом, 2,4,5-триалкил-1-инденилом, 2-алкил-1-инденилом, 2-арил-1-инденилом, 2,6-алкил-4-арил-1-инденилом, 2-алкил-5-арил-1-инденилом, 2-алкил-5,6-диарил-инденилом, 2-алкил-4,5-диарил-1-инденилом или 2-алкил-4,6-диарил-инденилом;
c) R4 4R2R6 -1-инденил - аналогичен с 2-алкил-4-арил-1-инденилом, 2,4-диалкил-1-инденилом, 2,4,6-триалкил-1-инденилом, 2-алкил-4,5-бензо-1-инденилом, 2,5-диалкил-1-инденилом, 2,5,6-триалкил-1-инденилом, 2,4,5-триалкил-1-инденилом, 2-алкил-1-инденилом, 2-арил-1-инденилом, 2,6-алкил-4-арил-1-инденилом, 2-алкил-5-арил-1-инденилом, 2-алкил-5,6-диарил-1-инденилом, 2-алкил-5,6-диарил-1-инденилом, 2-алкил-4,5-диарил-1-инденилом;
d) M2R2 1 аналогичен с ZrCl2, Zr(Me)Cl или ZrMe2.
Примерами соединений формулы I являются:
диметил-силандиил(2-метил-4,5-бензо-1-инденил)(2-этил-4- фенил-1-инденил) ZrCl2,
диметил-силандиил(2,5,6-триметил-1-инденил)(2-этил-4-фенил -1-инденил) ZrCl2,
диметил-силандиил(2-этил-1-инденил)(-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-1-инденил)(2-метил-4-фенил -1-инденил) ZrСl2,
диметил-силандиил(2-метил-4-изопропил-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил -α- аценафт-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,5-бензо-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-5-изобутил-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2,5,6-триметил-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(4-фенил-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изопропил-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандиил(2-метил -α- аценафт-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандии(4,5-бензо-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандиил(2,5,6-триметил-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандиил(4,6-диметил-1-инденил) (2,4,6-триметил-1-инденил) ZrCl2,
диметил-силандиил(2-метил -α- аценафт-1-инденил) (2,4,6-триметил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (2,4,6-триметил-1-инденил) ZrCl2,
диметил-силандиил(2,6,6-триметил-1-инденил) (2,4,6-триметил-1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-1-инденил) (2-метил-4,6-диизопропил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изопропил-1- инденил)(2-метил-4,6-диизопропил-1-инденил) ZrCl2,
диметил-силандиил(2-метил -α- аценафт-1-инденил) (2-метил-4,6-диизопропил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-фенил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-этил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-(1-нафтил)-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-2-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изопропил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил -α- аценафт-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,5-бензо-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-5-изобутил-1-инденил (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-(2,5,6-триметил-1-инденил) (2-метил-1-инденил) ZrCl2,
фенил(метил)силандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
1,2-этандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
1,2-бутандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметилгермил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
метил(винил)силандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
фенил(винил)силандиил(2-метил-4-фенил-1-инденил (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-фенил-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4(1-нафтил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2,5,6-триметил-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изопропил-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил( α -аценафт-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2 и
диметил-силандиил(2,5,6-триметил-1-инденил) 2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изопропил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изобутил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2,4-диметил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2,5,6-триметил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил- α -аценафт-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,5-бензо-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-5-изобутил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-этил-4-(1-нафтил)-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-фенил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-этил-4-фенил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-(1-нафтил)-1-инденил) (1-инденил) ZrCl2,
диэтилгермил(2-метил-4-(1-нафтил)-1-инденил) (1-инденил) ZrCl2.
диметил-силандиил(2-метил-4,5-бензо-1-инденил)(2-этил-4- фенил-1-инденил) ZrCl2,
диметил-силандиил(2,5,6-триметил-1-инденил)(2-этил-4-фенил -1-инденил) ZrCl2,
диметил-силандиил(2-этил-1-инденил)(-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-1-инденил)(2-метил-4-фенил -1-инденил) ZrСl2,
диметил-силандиил(2-метил-4-изопропил-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил -α- аценафт-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,5-бензо-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-5-изобутил-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2,5,6-триметил-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(4-фенил-1-инденил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изопропил-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандиил(2-метил -α- аценафт-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандии(4,5-бензо-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандиил(2,5,6-триметил-1-инденил) (2-метил-4,5-бензо-1-инденил) ZrCl2,
диметил-силандиил(4,6-диметил-1-инденил) (2,4,6-триметил-1-инденил) ZrCl2,
диметил-силандиил(2-метил -α- аценафт-1-инденил) (2,4,6-триметил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (2,4,6-триметил-1-инденил) ZrCl2,
диметил-силандиил(2,6,6-триметил-1-инденил) (2,4,6-триметил-1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-1-инденил) (2-метил-4,6-диизопропил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изопропил-1- инденил)(2-метил-4,6-диизопропил-1-инденил) ZrCl2,
диметил-силандиил(2-метил -α- аценафт-1-инденил) (2-метил-4,6-диизопропил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-фенил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-этил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-(1-нафтил)-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-2-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изопропил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил -α- аценафт-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,5-бензо-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-5-изобутил-1-инденил (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-(2,5,6-триметил-1-инденил) (2-метил-1-инденил) ZrCl2,
фенил(метил)силандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
1,2-этандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
1,2-бутандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
диметилгермил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
метил(винил)силандиил(2-метил-4-фенил-1-инденил) (2-метил-1-инденил) ZrCl2,
фенил(винил)силандиил(2-метил-4-фенил-1-инденил (2-метил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-фенил-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4(1-нафтил) (2-метил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2,5,6-триметил-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изопропил-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил( α -аценафт-1-инденил) (2-этил-4-фенил-1-инденил) ZrCl2 и
диметил-силандиил(2,5,6-триметил-1-инденил) 2-этил-4-фенил-1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,6-диизопропил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2,4,6-триметил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изопропил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-изобутил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2,4-диметил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2,5,6-триметил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил- α -аценафт-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4,5-бензо-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-5-изобутил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-этил-4-(1-нафтил)-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-фенил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-этил-4-фенил-1-инденил) (1-инденил) ZrCl2,
диметил-силандиил(2-метил-4-(1-нафтил)-1-инденил) (1-инденил) ZrCl2,
диэтилгермил(2-метил-4-(1-нафтил)-1-инденил) (1-инденил) ZrCl2.
Разделение стереоизомеров, в принципе, известно.
Металлоцены формулы I, в принципе, могут быть получены в соответствии с нижеследующей схемой реакции:
H2Rc + бутил Li ---> HRcLi
X = Cl, Br, I, O-тозил;
(сравни: Journal of Organomet. Chem. (1985), стр. 63 - 67 и Европейскую выложенную заявку N 320762).
H2Rc + бутил Li ---> HRcLi
X = Cl, Br, I, O-тозил;
(сравни: Journal of Organomet. Chem. (1985), стр. 63 - 67 и Европейскую выложенную заявку N 320762).
Настоящее изобретение касается также способа получения олефинового полимера путем полимеризации, по меньшей мере, одного полимера в присутствии катализатора, который содержит по меньшей мере один металлоцен в качестве соединения переходного металла и, по меньшей мере, один сокатализатор, отличающееся тем, что металлоценом является соединение формулы I.
Полимеризацию можно выполнять как гомополимеризацию или сополимеризацию. Предпочтительно осуществляется гомополимеризация или сополимеризация олефинов формулы Ra-CH=CH-Rb, причем радикалы Ra и Rb одинаковы или различны и обозначают атом водорода или углеводородный радикал с 1 - 20 атомами углерода, в частности с 1 - 10 атомами углерода или Ra и Rb совместно с соединяющими их атомами, образуют одно или несколько колец. Примерами таких олефинов являются 1-олефины, как, например, этилен, пропилен, 1-бутен, 1-пентен, 1-гексен, 4-метил-1-пентен или 1-октен, стирол, диены, как, например, 1,3-бутадиен или 1,4-гексадиен, и циклические олефины, как, например, норборны, тетрациклододеканы, норборнадиены и винилнорборны.
Предпочтительно при способе в соответствии с изобретением осуществляется гомополимеризация этилена или пропилена, или сополимеризация этилена с одним или несколькими 1-олефинами с 3 - 20 атомами углерода, как, например, пропилен, и/или с одним или несколькими диенами с 4 - 20 атомами углерода, как, например, 1,3-бутадиен. Примерами сополимеров являются этилен/пропилен-сополимеры, этилен/пропилен/1,4-гексадиен-сополимеры, этилен/пропилен/5-этилиден-2-норнборн-сополимеры или этилен-норборн-сополимеры.
Способ в соответствии с изобретением пригоден, в частности, для получения изотактических олефионовых полимеров.
Полимеризация проводится предпочтительно при температуре от 0 до 200oC, особенно предпочтительно от 50 до 80oC. Давление предпочтительно составляет от 0,5 до 100 бар, в частности от 5 до 64 бар.
Полимеризация может проводиться в растворе, суспензии или в газовой фазе непрерывно или периодически, в одну стадию или многоступенчато.
Предпочтительно используемый в способе в соответствии с изобретением катализатор содержит металлоцен и сокатализатор. Могут использоваться также смеси двух или нескольких металлоценов, в частности, для получения полиолефинов с широким или мультимодальным распределением молекулярной массы.
В принципе в качестве сокатализатора в способе в соответствии с изобретением пригодно любое соединение, которое на основании его кислотности по Льюису может переводить нейтральный металлоцен в катион и стабилизировать его ("лабильная координация"). Помимо этого сокатализатор или образованный из него анион не должен вступать в дальнейшую реакцию с образованным металлоценовым катионом (Европейский патент - N 427697). В качестве сокатализатора предпочтительно используются соединения алюминия и/или бора.
В качестве соединения алюминия в способе в соответствии с изобретением используется алюминоксан, в частности формулы II
для линейного типа и/или формулы III
для циклического типа, причем в формулах II и III радикалы R13 могут быть одинаковыми или различными и обозначают C1-C6-алкильную группу, C1-C6-фторалкильную группу, C6-C18-арильную группу, C1-C6-фторарильную группу или водород и n является целым числом от 0 до 50, или вместо алюминоксана используется элемент из смеси алюминоксана с соединением AlR3 14, в котором R14 имеет такое же значение, что и R13.
для линейного типа и/или формулы III
для циклического типа, причем в формулах II и III радикалы R13 могут быть одинаковыми или различными и обозначают C1-C6-алкильную группу, C1-C6-фторалкильную группу, C6-C18-арильную группу, C1-C6-фторарильную группу или водород и n является целым числом от 0 до 50, или вместо алюминоксана используется элемент из смеси алюминоксана с соединением AlR3 14, в котором R14 имеет такое же значение, что и R13.
Предпочтительно радикалы R13 одинаковы и обозначают метил, изобутил, фенил или бензил, особенно предпочтителен метил.
Если радикалы R13 различны, то они являются предпочтительно метилом и водородом или альтернативно метилом и изобутилом, причем доля водорода или изобутила предпочтительно от 0,01 до 40% (от общего количества радикалов R13). Вместо алюминоксана при полимеризации в качестве сокатализатора может использоваться смесь, состоящая из алюминоксана и AlR3 14, причем R14 имеет значение R13. Предпочтительно R14 является метилом, этилом, изобутилом, фенилом или бензилом.
Алюминоксан можно получать различными видами в соответствии с известными способами. Согласно одному из методов, например, алюмоуглеводородное соединение и/или гидридалюмоуглеводородное соединение взаимодействует с водой (в газообразной, твердой, жидкой или связанной форме, например, в виде кристаллизационной воды) в инертном растворителе (как, например, толуол). Для получения алюминоксана с различными алкильными группами R13 в соответствии с желаемым составом превращают два различных алюмотриалкила (AlR3 13 + AlR'3 14) с водой (сравни: S. Pasynkiewicz, Polyhedron 9 (1990) 429 и Европейскую выложенную заявку N 302424).
Точная пространственная структура алюминоксанов не известна (A.R. Barron et al. , J. Am. Chem. Soc. 115 (1993) 4971).Например, допустимо также, что цепи или кольца соединяются в большие двухмерные или трехмерные структуры.
Независимо от способа получения для всех алюминоксановых растворов общим является непостоянное содержание непревращенного исходного соединения алюминия, которое присутствует в свободной форме или в виде аддитивного соединения.
Можно металлоцены перед использованием в реакции полимеризации предварительно активировать с помощью сокатализатора, в частности алюминоксана. Благодаря этому существенно повышается активность полимеризации и улучшается морфология зерен.
Предварительная активации металлоценов осуществляется в растворе. При этом предпочтительно металлоцены в виде твердого вещества в растворе алюминоксана растворяются в инертном углеводороде. В качестве инертного углеводорода пригодным является алифатический или ароматический углеводород. Предпочтительно используется толуол или C6-C10-углеводород.
Концентрация алюминоксана в растворе предпочтительно находится в пределах примерно от 1 весового процента до предела насыщения, предпочтительно от 5 до 30 весовых процентов, соответственно относительно общего раствора. Металлоцены могут использоваться в такой же концентрации, однако предпочтительно они используются в количестве от 10-4 до 1 моля на моль алюминоксана. Время предварительной активации составляет от 1 минуты до 60 часов, предпочтительно от 2 до 60 минут. Работа ведется при температуре от -78 до 100oC, предпочтительно от 0 до 70oC.
Металлоцен (при необходимости вместе с сокатализатором) можно наносить на носитель и/или форполимеризировать. Для форполимеризации предпочтительно применяется используемый (или один из используемых) в полимеризации олефин (олефинов).
Пригодными носителями являются, например, силикагели, окиси алюминия, твердый алюминоксан, комбинации алюминоксана на носителе, как, например, силикагель, или другие неорганические материалы-носители. Пригодным материалом-носителем является также полиолефиновый порошок в высокодисперсной форме.
Другой возможный вариант выполнения способа в соответствии с изобретением заключается в том, что вместо или наряду с алюминоксаном используют солесодержащее соединение бора формулы RxNH4-xB(R')4 или формулы R3PHB(R')4 в качестве сокатализатора. При этом x = 1,2 или 3, R = алкил или арил одинаковы или различны, а R' = арил, который может быть также фторирован или частично фторирован. В этом случае катализатор состоит из продукта реакции металлоксидов с одним из упомянутых соединений (сравни: Европейская заявка на патент N 277004).
Для удаления содержащихся в олефине каталитических ядов предпочтительно является очистка с помощью алюминийалкила, например AlMe3 или AlEt3. Эта очистка может осуществляться или в самой системе полимеризации, или олефин перед добавлением в систему полимеризации приводится в контакт с соединением алюминия и затем вновь отделяется.
В качестве регулятора молярной массы, если необходимо, добавляется водород. Добавление водорода вызывает дополнительное сильное повышение активности полимеризации.
Общее давление в системе полимеризации составляет от 0,5 до 100 бар. Предпочтительной является полимеризация в технически особенно интересном диапазоне давлений от 5 до 64 бар.
Металлоцены используются предпочтительно в концентрации, отнесенной к переходному металлу, от 10-3 до 10-8, предпочтительно от 10-4 до 10-7 моля переходного металла на дм3 растворителя или на дм3 объема реактора. Сокатализатор, как, например, алюминоксан или смесь алюминоксана и Al(R14)3 используется предпочтительно в концентрации от 10-5 до 10-1 моля, предпочтительно от 10-4 до 10-2 моля на дм3 растворителя или на дм3 объема реактора. Однако, в принципе, возможны также более высокие концентрации.
Если полимеризация проводится в суспензии или растворе, используется употребительный для способа низкого давления по Циглеру инертный растворитель. Например, работу проводят в алифатическом или циклоалифатическом углеводороде, в качестве такового следовало бы назвать, например, пропан, бутан, пентан, гексан, гептан, декан, изооктан, циклогексан, метилциклогексан.
Кроме того, можно использовать бензиновую фракцию или гидрированную фракцию дизельного топлива. Можно использовать также толуол. Предпочтительно полимеризация осуществляется в жидких мономерах.
Если используются инертные растворители, дозами добавляют газообразные или жидкие мономеры.
Продолжительность полимеризации может быть любой, так как используемая в соответствии с изобретением катализаторная система позволяет лишь незначительное в зависимости от времени снижение полимеризационной активности.
Полученные способом в соответствии с изобретением изотактические полиолефины имеют, в частности, значение для изготовления формованных тел, как, например, пленки, плиты или крупногабаритные полые тела (например, трубы).
Металлоцены в соответствии с изобретением отличаются тем, что в технически интересном диапазоне температур от 50 до 100oC с очень высокой полимеризационной активностью получаются полимеры с высокой молекулярной массой и высокой температурой плавления.
Кроме того, при синтезе металлоцена не образуется мезоформа, так что излишним является дорогостоящее ее отделение. Благодаря комбинации различных лигандов металлоценовые соединения пригодны для получения полиолефинов с относительно ограниченными свойствами.
В частности, металлоцены на носителе приводят к полиолефинам с очень хорошей морфологией зерен.
Нижеследующие примеры должны более подробно пояснить изобретение. В примерах обозначают:
KB = коэффициент вязкости в см3/г,
Mw = средневесовая молекулярная масса в г/моль (определен с помощью ГПХ),
Mw/Mn = полидисперсность (определена с помощью ГПХ),
ИИ = изотактический индекс (мм + 1/2 мP) (определен с помощью 13C-ЯМР),
n1so = изотактическая длина блока (определена с помощью 13C-ЯМР),
nsyndio = синдиотактическая длина блока (определена с помощью 13C-ЯМР),
ИТР(230/2.16) - индекс плавления определен в соответствии с ДИН 53735 в дг/мин,
ИТР(230/5) - индекс плавления определен в соответствии с ДИН 53735 в дг/мин,
Tпл = температура плавления определена с помощью ДСК в oC (скорость нагревания и охлаждения 20oC/мин),
pr = "псевдорацемический": у псевдорацемических соединений инденил-лигандные структурные сетки находятся в мезорасположении, благодаря различному замещению инденил-лигандов у центрального атома M2 имеется хиральный центр, так что соединения являются рацемическими.
KB = коэффициент вязкости в см3/г,
Mw = средневесовая молекулярная масса в г/моль (определен с помощью ГПХ),
Mw/Mn = полидисперсность (определена с помощью ГПХ),
ИИ = изотактический индекс (мм + 1/2 мP) (определен с помощью 13C-ЯМР),
n1so = изотактическая длина блока (определена с помощью 13C-ЯМР),
nsyndio = синдиотактическая длина блока (определена с помощью 13C-ЯМР),
ИТР(230/2.16) - индекс плавления определен в соответствии с ДИН 53735 в дг/мин,
ИТР(230/5) - индекс плавления определен в соответствии с ДИН 53735 в дг/мин,
Tпл = температура плавления определена с помощью ДСК в oC (скорость нагревания и охлаждения 20oC/мин),
pr = "псевдорацемический": у псевдорацемических соединений инденил-лигандные структурные сетки находятся в мезорасположении, благодаря различному замещению инденил-лигандов у центрального атома M2 имеется хиральный центр, так что соединения являются рацемическими.
Все стеклянные приборы прогревались в вакууме и промывались аргоном. Все операции проводились при исключении влажности и кислорода в специальных сосудах. Использованный растворитель был очищен за исключением дихлорметана от сплава натрия с калием в присутствии аргона. Дихлорметан в присутствии аргона был отогнан от CaH2.
Пример A.
Диметилсиландиил(2-метил-1-инденил)(2-метил-4-фенил-1-инденил)циркондихлорид (1)
К раствору 15 г (73 миллимоля) 2-метил-7-фенил-индена (получение описано в патенте ФРГ N 4221244) в 150 мл толуола 7,5 мл Et2O при комнатной температуре в течение 30 минут каплями добавляли 29 мл 2,5 М раствора бутиллития в гексане и затем дополнительно перемешивали в течение 2 часов при температуре 40oC. Затем суспензию при комнатной температуре каплями добавляли к раствору 35,3 мл (290 миллимолей) диметилдихлорсилана в 100 мл толуола и дополнительно перемешивали в течение 3 часов при комнатной температуре. Растворитель удаляли в вакууме, остаток высушивали в вакууме (0,1 торр) и затем растворяли в 200 мл толуола. К этому раствору при комнатной температуре в течение 50 минут каплями добавляли суспензию из 2-метил-инденил-лития (полученного путем взаимодействия 9,5 г (73 миллимоля) 2-метил-индена в 60 мл толуола и 6 мл тетрагидрофурана с 29 мл 2,5 М раствора бутиллития в гексане при комнатной температуре и дополнительного перемешивания в течение 1 часа при температуре 40oC) и затем дополнительно перемешивали еще в течение 2 часов при комнатной температуре. Реакционную смесь смешивали со 100 мл воды, фазы разделяли и органическую фазу промывали с помощью 50 мл воды. Растворитель удаляли в вакууме и остаток очищали с помощью хроматографии на 400 г силикагеля (гексан/метиленхлорид 9:1). Наряду с 0,7 г продукта присоединения было получено 16,1 г (67%) лигандной системы соединения 1 в виде бесцветного масла.
К раствору 15 г (73 миллимоля) 2-метил-7-фенил-индена (получение описано в патенте ФРГ N 4221244) в 150 мл толуола 7,5 мл Et2O при комнатной температуре в течение 30 минут каплями добавляли 29 мл 2,5 М раствора бутиллития в гексане и затем дополнительно перемешивали в течение 2 часов при температуре 40oC. Затем суспензию при комнатной температуре каплями добавляли к раствору 35,3 мл (290 миллимолей) диметилдихлорсилана в 100 мл толуола и дополнительно перемешивали в течение 3 часов при комнатной температуре. Растворитель удаляли в вакууме, остаток высушивали в вакууме (0,1 торр) и затем растворяли в 200 мл толуола. К этому раствору при комнатной температуре в течение 50 минут каплями добавляли суспензию из 2-метил-инденил-лития (полученного путем взаимодействия 9,5 г (73 миллимоля) 2-метил-индена в 60 мл толуола и 6 мл тетрагидрофурана с 29 мл 2,5 М раствора бутиллития в гексане при комнатной температуре и дополнительного перемешивания в течение 1 часа при температуре 40oC) и затем дополнительно перемешивали еще в течение 2 часов при комнатной температуре. Реакционную смесь смешивали со 100 мл воды, фазы разделяли и органическую фазу промывали с помощью 50 мл воды. Растворитель удаляли в вакууме и остаток очищали с помощью хроматографии на 400 г силикагеля (гексан/метиленхлорид 9:1). Наряду с 0,7 г продукта присоединения было получено 16,1 г (67%) лигандной системы соединения 1 в виде бесцветного масла.
К раствору 8,0 г (20,4 миллимолей) лигандной системы соединения 1 в 20 мл толуола при температуре 50oC в течение 20 минут каплями добавляли 15,2 мл (40 миллимолей) 20-процентного раствора бутиллития в толуоле и затем дополнительно перемешивали еще в течение 2 часов при температуре 100oC. После окончания выделения газа смесь была охлаждена до температуры -40oC, было примешано 4,75 г (20,4 миллимолей) ZrCl4 и в течение 1 часа при комнатной температуре осуществлялось дополнительное перемешивание. Смесь вновь охлаждали до температуры -40oC, смешивали с 2 мл тетрагидрофурана и фильтровали через G3 -Шленк-фритту. Фильтрат был концентрирован до половины и кристаллизован при температуре -30oC. Излишний раствор был отобран пипеткой от выпавшего в осадок твердого вещества, осадок был трижды промыт соответственно с помощью 1 мл толуола и 5 мл гексана и затем высушен. Было получено 3,4 г (30%) рацемической формы соединения (I) в виде желтого твердого вещества.
1H-ЯМР (100 МГц, CDCl2): от 6,9 до 7,8 (м, 14H, аром. H и β- H), 2,1 (2c, 6H, CH3), 1,2 (2 с, 6H, CH3Si). Масс-спектр: 550M+, правильный образец распада.
После концентрирования фильтрата и кристаллизации при температуре -30oC было получено еще 2,8 г (25%) псевдорацемической формы соединения (I) в виде желтого твердого вещества.
1H-ЯМР (100 МГц, CDCl2): от 6,7 до 7,7 (м, 14H, аром. H и β- H-IndH), 2,4 (д, 6H, CH3), 1,4 и 1,2 (2с, 6H, CH3Si).
Пример B.
Диметилсиландиил (1-инденил) (2-метил-4-фенил-1-инденил)циркондихлорид (2).
К раствору 26,1 г (87 миллимолей) диметил (2-метил-4-фенилинден)хлоризилану в 200 мл толуола и 10 мл тетрагидрофурана при комнатной температуре в течение 50 минут каплями добавляли суспензию инденил-лития (полученного путем превращения раствора 10,1 г (87 миллимолей) индена (90-процентного) в 100 мл толуола и 5 мл тетрагидрофурана при комнатной температуре с помощью 35 мл 2,5 М раствора бутиллития в гексане и дополнительного перемешивания в течение 1 часа при температуре 40oC) и затем дополнительно перемешивали еще в течение 2 часов при комнатной температуре. Реакционная смесь была смешана со 100 мл H2O, были разделены фазы и органическая фаза была промыта с помощью 50 мл H2O. Растворитель был удален в вакууме и остаток очищен путем кристаллизации (гексан/дихлорметан). Было получено 18,8 г (56%) лигандной системы соединения 2 в виде бесцветного твердого вещества.
К раствору 10,0 г (26,4 миллимолей) лигандной системы соединения 2 в 80 мл толуола в присутствии аргона при температуре 50oC в течение 20 минут каплями добавляли 19,7 мл (52,8 миллимолей) 20-процентного раствора бутиллития в толуоле и затем дополнительно перемешивали еще в течение 2 часов при температуре 100oC. После окончания выделения газа смесь охлаждалась до температуры - 40oC, было примешано 6,15 г (25,4 миллимолей) ZrCl4 и в течение 1 часа при комнатной температуре осуществлялось дополнительное перемешивание. Смесь вновь охлаждали до температуры - 40oC, смешивали с 2 мл тетрагидрофурана и фильтровали через G3-Шленк-фритту. Из фильтрата было кристаллизовано при температуре -20oC 3,9 г (26%) рацемической формы соединения (2) в виде желтого твердого вещества.
1H-ЯМР (300 МГц, CDCl3): от 6,9 до 7,7 (м, 14H, аром. H и β- H), 6,2 (д, 1H, α- IndH), 2,3 (с, 3H, CH3), 1,3 (2с, 6H, CH3Si). Масс-спектр: 538 М+, правильный образец распада.
После концентрирования фильтрата и кристаллизации при температуре -30oC было получено еще 2,3 г (15%) псевдорацемической формы соединения (2) в виде желтого твердого вещества.
IH-ЯМР (300 МГц, CDCl3): от 6,9 до 7,7 (м, 14H, аром. H и β- H-IhdH), 2,35 (с, 3H, CH3); 1,5 и 1,1 (2с, 6H, CH3Si).
Пример C.
Диметилсиландиил (2-метил-4,5-бензо-1-инденил)(2-метил-1-инденил)циркондихлорид (3).
К раствору 50,1 г (278 миллимолей) 2-метил-4,5-бензоинденила (получение описано в Европейском патенте N 549900) в 500 мл толуола и 25 мл Et2O при комнатной температуре в течение 30 минут каплями добавляли 111 мл 2,5 М раствора бутиллития в гексане и затем дополнительно перемешивали в течение 2 часов при температуре 40oC. Затем суспензию при комнатной температуре каплями добавляли к раствору 135 мл (1112 миллимолей) диметилдихлорсилана в 200 мл толуола и дополнительно перемешивали в течение 3 часов при комнатной температуре. Растворитель был удален в вакууме, остаток высушен в вакууме (0,1 торр) и затем растворен в 200 мл толуола. Суспензия была отфильтрована от хлорида лития и растворитель фильтрата был удален в вакууме. Получили 43 г (57%) красного маслянистого продукта.
14,9 г (51,9 миллимолей) диметил(2-метил-4,5-бензоинденил) хлорсилана было помещено в 60 мл тетрагидрофурана и при комнатной температуре в течение 15 минут каплями добавляли суспензию 2-метилидениллития (полученную путем превращения 7,1 г (54,5 миллимолей) 2-метилиндена в 20 мл тетрагидрофурана с помощью 21,8 мл 2,5 М раствора бутиллития в гексане и дополнительного перемешивания в течение 1 часа при температуре 40oC) и затем дополнительно перемешивали смесь еще в течение 2 часов при комнатной температуре. Реакционную смесь смешали со 100 мл воды, разделили фазы и органическую фазу промыли с помощью 50 мл воды. Растворитель был удален в вакууме и остаток был очищен с помощью хроматографии на 400 г силикагеля (гексан/метиленхлорид 9:1). Было получено 8,18 г (43%) лигандной системы соединения 3 в виде бесцветного масла.
К раствору 4,18 г (11,4 миллимолей) лигандной системы соединения 3 в 50 мл толуола и 5 мл тетрагидрофурана при комнатной температуре в течение 20 минут каплями добавляли 9,6 мл (24 миллимоля) 20-процентного раствора бутиллития в толуоле и затем дополнительно перемешивали еще в течение 2 часов при температуре 50oC. После окончания выделения газа смесь охлаждали до температуры - 40oC, смешивали с 2,33 г (10 миллимолей) ZrCl4 и дополнительно перемешивали в течение 1 часа при комнатной температуре. Суспензию фильтровали через G3-фритту, дважды дополнительно промывали с помощью 20 мл толуола и фритованный остаток высушивали в вакууме. Было получено 3,36 г (56%) продуктовой смеси из рацемического и "псевдорацемического" соединения в соотношении 3: 2. Продуктовая смесь была экстрагирована с помощью 100 мл CH2Cl2, фильтрат был сконцентрирован до 1/5 его объема и помещен для кристаллизации при температуре - 30oC. Было получено 1,1 г "псевдорацемического" комплекса в виде желтого твердого вещества.
IH-ЯМР (100 МГц, CDCl3): δ = от 7,75 до 7,00 (м, 11H, аром. H и бензоинденил-H), 6,70 (м, 1H, Ind-H), 2,52/2,48 (кажд. с, кажд. 3H, CH3-Ind. и CH3-бензо.); 1,40/1,25 (кажд. с, кажд, 3H, (CH2)2Si).
Благодаря дальнейшей экстракции фритованного остатка с помощью 200 мл CH2Cl2 концентрирования фильтрата до 20 мл, охлаждения до -30oC и отфильтрования твердого вещества было получено 1,4 г рацемического соединения.
IH-ЯМР (100 МГц, CDCl3); δ = от 8,03 до 7,10 (м, 11H, аром. H и бензоинденил-H), 6,78 (м, 1H, Ind-H), 2,29/2,26 (кажд. с, кажд. 3H, CH3-Ind. и CH3-бензо.); 1,30 (с, 6H, (CH3)2Si).
Пример D.
Рацемический диэтилгерманийдиил (2-метил-4-фенил-инденил)(2-этилинденил)цирконхлорид (4)
В соответствии с примером А из 20 г (97 миллимолей) 2-метил-4-фенил-индена, 97 миллимолей бутиллития, 60,5 г (300 миллимолей) диэтилдихлоргермания, 13,9 г (97 миллимолей) 2-этил-индена, 97 миллимолей бутиллития после хроматографии с помощью силикагеля было получено 30,2% г (65%) лигандной системы диэтилгерманийдиил (2-метил-4-фенил-инденил) (2-этил-инденила).
В соответствии с примером А из 20 г (97 миллимолей) 2-метил-4-фенил-индена, 97 миллимолей бутиллития, 60,5 г (300 миллимолей) диэтилдихлоргермания, 13,9 г (97 миллимолей) 2-этил-индена, 97 миллимолей бутиллития после хроматографии с помощью силикагеля было получено 30,2% г (65%) лигандной системы диэтилгерманийдиил (2-метил-4-фенил-инденил) (2-этил-инденила).
Из 10 г (20,8 миллимолей) лигандной системы после депротонирования с помощью 42 миллимолей бутиллития и преобразования с помощью 4,7 г (20 миллимолей) тетрахлорида циркония после фильтрации и кристаллизации получают 3,6 г (28%) рацемического диэтилгерманийдиил (2-метил-4-фенил-инденил)(2-этил-инденил)циркондихлорида.
Пример E.
Рацемический диметил-силандиил (2,4,6-триметил-инденил)(2-метил-4-фенил-инденил)циркондихлорид (5)
В соответствии с примером А из 10 г (63 миллимоля) 2,4,6-триметил-индена, 63 миллимолей бутиллития, 32,3 г (250 миллимолей) диметилдихлорсилана, 13,0 г (63 миллимолей) 2-метил-4-фенил-индена, 63 миллимолей бутиллития после хроматографии с помощью силикагеля было получено 18,8 г (71%) лигандной системы диметил-силандиил (2,4,6-триметил-инденил)(2-метил-4-фенил-инденила).
В соответствии с примером А из 10 г (63 миллимоля) 2,4,6-триметил-индена, 63 миллимолей бутиллития, 32,3 г (250 миллимолей) диметилдихлорсилана, 13,0 г (63 миллимолей) 2-метил-4-фенил-индена, 63 миллимолей бутиллития после хроматографии с помощью силикагеля было получено 18,8 г (71%) лигандной системы диметил-силандиил (2,4,6-триметил-инденил)(2-метил-4-фенил-инденила).
Из 10 г (23,7 миллимолей) лигандной системы после депротонирования с помощью 47,4 миллимолей бутиллития и преобразования с помощью 5,5 г (23,7 миллимолей) цирконтетрахлорида после фильтрации и кристаллизации получают 4,3 г (31%) рацемического диметил-силандиил (2,4,6-триметил-инденил)(2-метил-4-фенил-инденил)циркондихлорида.
Пример F.
Рацемический диметил-силандиил (2-метил-4,6-диизопропилинденил) (2-метил-инденил)циркондихлорид (6)
В соответствии с примером А из 10 г (47 миллимолей) 2-метил-4,6-диизопропилиндена, 47 миллимолей бутиллития, 24,3 г (188 миллимолей) диметилдихлорсилана, 6,1 г (47 миллимолей) 2-метил-индена, 47 миллимолей бутиллития после хроматографии с помощью силикагеля было получено 12,2 (65%) лигандной системы диметил-силандиил (2-метил-4,6-диизопропил-инденил)(2-метил-инденила).
В соответствии с примером А из 10 г (47 миллимолей) 2-метил-4,6-диизопропилиндена, 47 миллимолей бутиллития, 24,3 г (188 миллимолей) диметилдихлорсилана, 6,1 г (47 миллимолей) 2-метил-индена, 47 миллимолей бутиллития после хроматографии с помощью силикагеля было получено 12,2 (65%) лигандной системы диметил-силандиил (2-метил-4,6-диизопропил-инденил)(2-метил-инденила).
Из 10 г (25 миллимолей) лигандной системы после депротонирования с помощью 50 миллимолей бутиллития и преобразования с помощью 5,8 г (25 миллимолей) тетрахлорида циркония после фильтрации и кристаллизации получают 3,5 г (25%) рацемического диметил-силандиил (2-метил-4,6-диизопропилинденил)(2-метил-инденил)циркондихлорида.
Пример G.
Рацемический диметилгерманийдиил(2-метил-4-фенил-инденил)(2-метил-инденил)циркондихлорид (7).
В соответствии с примером А из 5 г (24 миллимолей) 2-метил-4-фенол-индена, 24 миллимолей бутиллития, 16,7 г (96 миллимолей) диметилдихлоргермания, 3,1 г (24 миллимолей) 2-метил-индена, 24 миллимолей бутиллития после хроматографии с помощью силикагеля было получено 6,1 г (58%) лигандной системы диметилгерманийдиил (2-метил-4-фенил-инденил)(2-метил-инденила).
Из 5,0 г (11,4 миллимолей) лигандной системы после депротонирования с помощью 22,8 миллимолей бутиллития и преобразования с помощью 2,7 г (11,4 миллимолей) тетрахлорида циркония после фильтрации и кристаллизации получают 2,2 г (33%) рацемического диметилгерманийдиил (2-метил-4-фенил-инденил)(2-метил-инденил)цирконийдихлорида.
Пример H.
Рацемический диметил-силандиил (2-метил-аценафт-инденил)(2-метил-4-фенилинденил)циркондихлорид (8).
В соответствии с примером А из 10 г (48 миллимолей) 2-метилаценафт-индена, 48 миллимолей бутиллития, 24,5 г (190 миллимолей) диметилдихлорсилана, 10 г (48 миллимолей) 2-метил-4-фенил-индена, 48 миллимолей бутиллития после хроматографии с помощью силикагеля было получено 16 г (71%) лигандной системы диметил-силандиил (2-метил-аценафт-инденил)(2-метил-4-фенил-инденила).
Из 10 г (21,3 миллимолей) лигандной системы после депротонирования с помощью 42,6 миллимолей бутиллития и преобразования с помощью 4,9 г (21,3 миллимолей) тетрахлорид циркония после фильтрации и кристаллизации получают 3,9 г (29%) рацемического диметил-силандиил(2-метил-аценафт-инденил) (2-метил-4-фенил-инденил)циркондихлорида.
Пример J.
Рацемический диэтилгерманийдиил(2-метил-4-(1-нафтил)-инденил) (инденил)циркондихлорид (9)
В соответствии с примером A из 5 г (19,5 миллимолей) 2-метил-4-(1-нафтил)-индена, 20 миллимолей бутиллития, 15,7 г (78 миллимолей)диэтилдихлоргермания, 2,5 г (19,5 миллимолей)индена, 20 миллимолей бутиллития после хроматографии с помощью силикагеля было получено 6,2 г (62%) лигандной системы диэтилгерманийдиил(2-метил-4-(1-нафтил)-инденил)(инденила).
В соответствии с примером A из 5 г (19,5 миллимолей) 2-метил-4-(1-нафтил)-индена, 20 миллимолей бутиллития, 15,7 г (78 миллимолей)диэтилдихлоргермания, 2,5 г (19,5 миллимолей)индена, 20 миллимолей бутиллития после хроматографии с помощью силикагеля было получено 6,2 г (62%) лигандной системы диэтилгерманийдиил(2-метил-4-(1-нафтил)-инденил)(инденила).
Из 5,0 г (9,7 миллимолей) лигандной системы после депротенирования с помощью 19,5 миллимолей и преобразования с помощью 2,3 г (9,7 миллимолей)тетрахлорида циркония после фильтрации и кристаллизации получают 1,6 г (24%) рацемического диэтилгерманийдиил(2-метил-4-(1-нафтил)-инденил)(инденил)циркондихлорида.
Примеры полимеризации
Пример 1
Сухой реактор емкостью 24 дм3 был промыт пропиленом и заполнен 12 дм3 жидкого пропилена и 25 см3 толуольного раствора метилалюминооксана (соответственно 37 миллимолей алюминия, средняя степень олигомеризации составляла n=20). Содержимое в течение 5 минут перемешивалось при температуре 30oC с частотой вращения 250 об/мин. Параллельно с этим 0,9 мг рацемического диметил-силандиил(2-метил-4-фенил-1-инденил)(2-метил-1-инденил) циркондихлорида было растворено в 10 см3 толуольного раствора метилалюминооксана (17 миллимолей алюминия) и предварительно активировано с помощью пятиминутной выдержки. Раствор был подан в реактор и в течение 1 часа проводилась полимеризация при температуре 70oC. Было получено 0,73 кг полипропилена. Активность металлоцена составила 811 кг пропилена/г металлоцена • час. У полимеров были определены следующие свойства: KB = 379 см3/г; Mw = 537500 г/моль, Mw/Mn 2,2; ИТР (230/2) = 0,3 дг/мин, ИТР (230/5) = 1,5 дг/мин; температура плавления = 155oC, ИН = 98,3%, niso = 86.
Пример 1
Сухой реактор емкостью 24 дм3 был промыт пропиленом и заполнен 12 дм3 жидкого пропилена и 25 см3 толуольного раствора метилалюминооксана (соответственно 37 миллимолей алюминия, средняя степень олигомеризации составляла n=20). Содержимое в течение 5 минут перемешивалось при температуре 30oC с частотой вращения 250 об/мин. Параллельно с этим 0,9 мг рацемического диметил-силандиил(2-метил-4-фенил-1-инденил)(2-метил-1-инденил) циркондихлорида было растворено в 10 см3 толуольного раствора метилалюминооксана (17 миллимолей алюминия) и предварительно активировано с помощью пятиминутной выдержки. Раствор был подан в реактор и в течение 1 часа проводилась полимеризация при температуре 70oC. Было получено 0,73 кг полипропилена. Активность металлоцена составила 811 кг пропилена/г металлоцена • час. У полимеров были определены следующие свойства: KB = 379 см3/г; Mw = 537500 г/моль, Mw/Mn 2,2; ИТР (230/2) = 0,3 дг/мин, ИТР (230/5) = 1,5 дг/мин; температура плавления = 155oC, ИН = 98,3%, niso = 86.
Сравнительный опыт 1
Поступали так же, как и в случае с примером 1, однако был использован металлоцен рацемический диметил-силандиил БИС (2-метил-1-инденил)циркондихлорид. Активность металлоцена составила 350 кг пропилена/г металлоцена • час.
Поступали так же, как и в случае с примером 1, однако был использован металлоцен рацемический диметил-силандиил БИС (2-метил-1-инденил)циркондихлорид. Активность металлоцена составила 350 кг пропилена/г металлоцена • час.
KB = 180 см3/г; Mw = 187000 г/моль, Mw/Mn = 2,5; ИТР (230/2) = 13 дг/мин, ИТР (230/5) = 37 дг/мин; температура плавления = 145oC.
Пример 2
Поступали так же, как и в случае с примером 1, однако было использовано 2,5 мг металлоцена и температура полимеризации составила 50oC. Активность металлоцена составила 398 кг пропилена/г металлоцена • час и у полимера были определены следующие параметры:
KB = 553 см3/г; Mw = 811000 г/моль, Mw/Mn = 2,3; ИТР (230/2) = 0,1 дг/мин, ИТР (230/5) = 0,5 дг/мин; температура плавления = 158oC.
Поступали так же, как и в случае с примером 1, однако было использовано 2,5 мг металлоцена и температура полимеризации составила 50oC. Активность металлоцена составила 398 кг пропилена/г металлоцена • час и у полимера были определены следующие параметры:
KB = 553 см3/г; Mw = 811000 г/моль, Mw/Mn = 2,3; ИТР (230/2) = 0,1 дг/мин, ИТР (230/5) = 0,5 дг/мин; температура плавления = 158oC.
Сравнительный опыт 2
Пример 2 был повторен с применением металлоцена: рацемического диметил-силандиил-бис(2-метил-1-инденил)циркондихлорида.
Пример 2 был повторен с применением металлоцена: рацемического диметил-силандиил-бис(2-метил-1-инденил)циркондихлорида.
Активность металлоцена составила 125 кг пропилена/г металлоцена • час.
KB = 250 см3/г; Mw = 318000 г/моль, Mw/Mn = 2,1; ИТР (230/5) = 10 дг/мин; температура плавления = 148oC.
Пример 3
Поступали так же, как и в случае с примером 1, однако дополнительно было использовано еще 5 ндм3 водорода. Активность металлоцена составила 1187 кг пропилена/г металлоцена • час.
Поступали так же, как и в случае с примером 1, однако дополнительно было использовано еще 5 ндм3 водорода. Активность металлоцена составила 1187 кг пропилена/г металлоцена • час.
KB = 226 см3/г; Mw = 282500 г/моль, Mw/Mn = 1,9; ИТР (230/2) = 7 дг/мин, ИТР (230/5) = 20 дг/мин; температура плавления = 160oC, ИИ = 98,6, niso = 125. Пример подтверждает хорошую регулируемость моллекулярной массы с помощью водорода.
Пример 4
Поступали так же, как и в случае с примером 1, однако использовали металлоцен с рацемической/"псевдорацемической" смеси (1:1). Активность металлоцена составила 656 кг пропилена/г металлоцена • час.
Поступали так же, как и в случае с примером 1, однако использовали металлоцен с рацемической/"псевдорацемической" смеси (1:1). Активность металлоцена составила 656 кг пропилена/г металлоцена • час.
KB = 351 см3/г; Mw = 502500 г/моль, Mw/Mn = 2,3; ИТР (230/5) = 2,6 дг/мин; температура плавления = 155oC.
Пример 5
Поступали так же, как и в примере 4, однако было использовано соотношение 1: 5 рацемической фракции к псевдорацемической фракции. Активность металлоцена составила 510 кг пропилена/г металлоцена • час.
Поступали так же, как и в примере 4, однако было использовано соотношение 1: 5 рацемической фракции к псевдорацемической фракции. Активность металлоцена составила 510 кг пропилена/г металлоцена • час.
KB = 315 см3/г; Mw = 354500 г/моль, Mw/Mn = 2,3; ИТР (230/5) = 3,0 дг/мин; температура плавления = 153oC.
Пример 6
Пример 5 был повторен при температуре полимеризации 50oC. Активность металлоцена составила 215 кг пропилена/г металлоцена • час.
Пример 5 был повторен при температуре полимеризации 50oC. Активность металлоцена составила 215 кг пропилена/г металлоцена • час.
KB = 451 см3/г; Mw = 587500 г/моль, Mw/Mn = 2,6; ИТР (230/5 = 1,6 дг/мин; температура плавления = 150oC.
Сравнительный опыт 3
Пример 5 был повторен с металлоценом мезо-диметилсиландиилбис-(2-метил-1-инденил)циркондихлоридом. Порошок полимера не был получен. Полученная масса была мягкой и клейкой, у аморфной массы не было точки плавления, а коэффициент вязкости составил 42 см3/г. 13C-ЯМР-измерения подтвердили, что речь идет о чисто атактическом полимере (niso = 2, nsyndio = 2,11 = 52%). Точно так же невозможно было определить параметр плавления на основании жидкоплавкости полимера. Активность металлоцена в полимеризации составила 8,6 кг полипропилена/г металлоцена/час.
Пример 5 был повторен с металлоценом мезо-диметилсиландиилбис-(2-метил-1-инденил)циркондихлоридом. Порошок полимера не был получен. Полученная масса была мягкой и клейкой, у аморфной массы не было точки плавления, а коэффициент вязкости составил 42 см3/г. 13C-ЯМР-измерения подтвердили, что речь идет о чисто атактическом полимере (niso = 2, nsyndio = 2,11 = 52%). Точно так же невозможно было определить параметр плавления на основании жидкоплавкости полимера. Активность металлоцена в полимеризации составила 8,6 кг полипропилена/г металлоцена/час.
Сравнительный опыт 4
Пример 5 был повторен с металлоценом мезо-диметилсиландиилбис(2-метил-4-фенил)-1-инденил)циркондихлоридом. Полученный полимер по своим свойствам соответствовал полимеру из сравнительного опыта 3, речь идет об атактическом полипропилене, у которого KB = 110 см3/г; активность металлоцена = 52 кг полипропилена/г металлоцена • час.
Пример 5 был повторен с металлоценом мезо-диметилсиландиилбис(2-метил-4-фенил)-1-инденил)циркондихлоридом. Полученный полимер по своим свойствам соответствовал полимеру из сравнительного опыта 3, речь идет об атактическом полипропилене, у которого KB = 110 см3/г; активность металлоцена = 52 кг полипропилена/г металлоцена • час.
Пример 7
Поступали так же, как в примере 1, однако использовали металлоцен рацемический диметилсиландиил(2-метил-4,5-бензо-1-инденил) (2-метил-1-инденил)циркондихлорид. Активность металлоцена составила 496 кг полипропилена/г металлоцена • час.
Поступали так же, как в примере 1, однако использовали металлоцен рацемический диметилсиландиил(2-метил-4,5-бензо-1-инденил) (2-метил-1-инденил)циркондихлорид. Активность металлоцена составила 496 кг полипропилена/г металлоцена • час.
KB = 164 см3/г; Mw = 190000 г/моль, Mw/Mn = 2,2; ИТР (230/2) = 8 дг/мин, ИТР (230/5) = 25 дг/мин; температура плавления = 144oC.
Пример 8
Поступали так же, как в примере 2, однако использовали металлоцен из примера 7. Активность металлоцена составила 496 кг полипропилена/г металлоцена • час. KB = 164 см3/г; Mw = 349500 г/моль, Mw/Mn = 2,3; ИТР (230/2) = 2 дг/мин, ИТР (230/5) = 6 дг/мин; температура плавления = 148oC, ИИ = 97,5%, niso = 66.
Поступали так же, как в примере 2, однако использовали металлоцен из примера 7. Активность металлоцена составила 496 кг полипропилена/г металлоцена • час. KB = 164 см3/г; Mw = 349500 г/моль, Mw/Mn = 2,3; ИТР (230/2) = 2 дг/мин, ИТР (230/5) = 6 дг/мин; температура плавления = 148oC, ИИ = 97,5%, niso = 66.
Пример 9
Поступали так же, как в примере 2, однако использовали металлоцен диметилсиландиил(2-метил-4,5-бензо-1-инденил) (2-метил-1-инденил)циркондихлорид в рацемической/"псевдорацемической" смеси (1: 10). Активность металлоцена составила 214 кг полипропиолена/г металлоцена • час. KB = 269 см3/; Mw = 382000 г/моль, Mw/Mn = 2,2; ИТР (230/2) = 3,1 дг/мин; ИТР (230/5) = 9 дг/мин; температура плавления = 1436oC.
Поступали так же, как в примере 2, однако использовали металлоцен диметилсиландиил(2-метил-4,5-бензо-1-инденил) (2-метил-1-инденил)циркондихлорид в рацемической/"псевдорацемической" смеси (1: 10). Активность металлоцена составила 214 кг полипропиолена/г металлоцена • час. KB = 269 см3/; Mw = 382000 г/моль, Mw/Mn = 2,2; ИТР (230/2) = 3,1 дг/мин; ИТР (230/5) = 9 дг/мин; температура плавления = 1436oC.
Пример 10
Поступали так же, как в примере 2, однако использовали металлоцен диметилсиландиил(2-метил-4,5-бензо-1-инденил) (2-метил-1-инденил)циркондихлорид в соотношении рацемический:псевдорацемический 3:2, как это наблюдается при экссинтезе после фильтрации через G3-фритту в фильтрате. Активность металлоцена составила 249 кг полипропилена/г металлоцена • час.
Поступали так же, как в примере 2, однако использовали металлоцен диметилсиландиил(2-метил-4,5-бензо-1-инденил) (2-метил-1-инденил)циркондихлорид в соотношении рацемический:псевдорацемический 3:2, как это наблюдается при экссинтезе после фильтрации через G3-фритту в фильтрате. Активность металлоцена составила 249 кг полипропилена/г металлоцена • час.
KB = 282 см3/г; Mw = 384500 г/моль, Mw/Mn = 2,2; ИТР (230/2) = 2 дг/мин, ИТР (230/5) = 5,5 дг/мин; температура плавления =148oC, ИИ = 97,6%, niso = 59.
Пример 11
Поступали так же, как в примере 1, однако использовали металлоцен рацемической диметилсиландиил(2-метил-4-фенил-1-инденил) (1-инденил)циркондихлорид. Активность металлоцена составила 935 кг полипропилена/г металлоцена • час.
Поступали так же, как в примере 1, однако использовали металлоцен рацемической диметилсиландиил(2-метил-4-фенил-1-инденил) (1-инденил)циркондихлорид. Активность металлоцена составила 935 кг полипропилена/г металлоцена • час.
KB = 136 см3/г; Mw = 128500 г/моль, Mw/Mn = 2,0; ИТР (230/2); 35 дг/мин; температура плавления = 151oC.
Пример 12
Поступали так же, как в примере 2, однако использовали металлоцен из примера 11. Активность металлоцена составила 399 кг полипропилена/г металлоцена • час. KB = 190 см3/г; Mw = 204500 г/моль, Mw/Mn = 2,0; ИТР (230/2) = 9 дг/мин; температура плавления = 154oC.
Поступали так же, как в примере 2, однако использовали металлоцен из примера 11. Активность металлоцена составила 399 кг полипропилена/г металлоцена • час. KB = 190 см3/г; Mw = 204500 г/моль, Mw/Mn = 2,0; ИТР (230/2) = 9 дг/мин; температура плавления = 154oC.
Пример 13
Поступали так же, как в примере 2, однако использовали металлоцен диметилсиландиил(2-метил-4,5-бензо-1-инденил) (2-метил-1-инденил)циркондихлорид в смеси рацемический: "псевдорацемический" (1: 8). Активность металлоцена составила 228 полипропилена/г металлоцена • час. KB = 182 см3/г; Mw = 201500 г/моль, Mw/Mn = 2,2; ИТР (230/2) = 12,5 дг/мин; температура плавления = 154oC.
Поступали так же, как в примере 2, однако использовали металлоцен диметилсиландиил(2-метил-4,5-бензо-1-инденил) (2-метил-1-инденил)циркондихлорид в смеси рацемический: "псевдорацемический" (1: 8). Активность металлоцена составила 228 полипропилена/г металлоцена • час. KB = 182 см3/г; Mw = 201500 г/моль, Mw/Mn = 2,2; ИТР (230/2) = 12,5 дг/мин; температура плавления = 154oC.
Пример 14
Поступали так же, как в примере 1, однако использовали металлоцен диметилсиландиил(2-метил-4-фенил-1-инденил) (1-инденил)циркодихлорид в получающейся при экссинтезе изомерной смеси рацемический: "псевдорацемический" = 1:0,6. Активность металлоцена составила 382 кг полипропилена/г металлоцена • час. КВ = 184 см3/г; Mw = 216000 г/моль, Mw/Mn = 3,3; ИТР (230/2) = 8 дг/мин; температура плавления = 155oC; ИИ = 98,0, niso = 82.
Поступали так же, как в примере 1, однако использовали металлоцен диметилсиландиил(2-метил-4-фенил-1-инденил) (1-инденил)циркодихлорид в получающейся при экссинтезе изомерной смеси рацемический: "псевдорацемический" = 1:0,6. Активность металлоцена составила 382 кг полипропилена/г металлоцена • час. КВ = 184 см3/г; Mw = 216000 г/моль, Mw/Mn = 3,3; ИТР (230/2) = 8 дг/мин; температура плавления = 155oC; ИИ = 98,0, niso = 82.
Сравнительный опыт 5
Поступали так же, как в примере 11, однако использовали металлоцен рацемический диметилоксиландмилбис(1-инденил)циркоиндихлорид не в соответствии с изобретением. Активность металлоцена составила 559 кг полипропилена/г металлоцена • час. КВ = 43 см3/г; Mw = 34900 г/моль, Nw/Mn = 2,5; ИТР измерить нельзя, так как слишком велика жидкоплавкость; температура плавления = 137oC.
Поступали так же, как в примере 11, однако использовали металлоцен рацемический диметилоксиландмилбис(1-инденил)циркоиндихлорид не в соответствии с изобретением. Активность металлоцена составила 559 кг полипропилена/г металлоцена • час. КВ = 43 см3/г; Mw = 34900 г/моль, Nw/Mn = 2,5; ИТР измерить нельзя, так как слишком велика жидкоплавкость; температура плавления = 137oC.
Пример 15
Пример 1 был повторен с металлоценом диметилсиландиил(2-этил-4-фенил-1-инденил)(2-метил-1-инденил) циркондихлоридом, соотношение форм рацемической: "псевдорацемической" составило 4:1,5 (эксинтез). Активность металлоцена составила 671 кг полипропилена/г металлоцена • час. КВ = 357 см3/г; Mw = 494000 г/моль, Mw= Mn=2,4; ИТР (230/5) = 3 дг/мин; температура плавления = 159oC.
Пример 1 был повторен с металлоценом диметилсиландиил(2-этил-4-фенил-1-инденил)(2-метил-1-инденил) циркондихлоридом, соотношение форм рацемической: "псевдорацемической" составило 4:1,5 (эксинтез). Активность металлоцена составила 671 кг полипропилена/г металлоцена • час. КВ = 357 см3/г; Mw = 494000 г/моль, Mw= Mn=2,4; ИТР (230/5) = 3 дг/мин; температура плавления = 159oC.
Пример 16
Пример 15 был повторен при температуре полимеризации 50oC. Активность металлоцена составила 329 кг полипропилена/г металлоцена • час. КВ = 534 см3/г; Mw = 698000 г/моль, Mw/Mn = 2,0; ИТР (230/5) = 1 дг/мин; температура плавления = 163oC.
Пример 15 был повторен при температуре полимеризации 50oC. Активность металлоцена составила 329 кг полипропилена/г металлоцена • час. КВ = 534 см3/г; Mw = 698000 г/моль, Mw/Mn = 2,0; ИТР (230/5) = 1 дг/мин; температура плавления = 163oC.
Пример 17
Пример 1 был повторен с металлоценом диметилсиландиил(2-метил- 4-(1-нафтил)-1-инденил)(2-метил-1-инденил)циркондихлоридом, соотношение форм рацемической: "псевдорацемической" составило 3:1,4. Активность металлоцена составила 749 кг полипропилена/г металлоцена • час. KB = 449 см3/г; Mw = 647500 г/моль, Mw/Mn = 2,2; температура плавления = 156oC.
Пример 1 был повторен с металлоценом диметилсиландиил(2-метил- 4-(1-нафтил)-1-инденил)(2-метил-1-инденил)циркондихлоридом, соотношение форм рацемической: "псевдорацемической" составило 3:1,4. Активность металлоцена составила 749 кг полипропилена/г металлоцена • час. KB = 449 см3/г; Mw = 647500 г/моль, Mw/Mn = 2,2; температура плавления = 156oC.
Пример 18
Пример 1 был повторен с металлоценом 1,2-этандиил(2-этил-4-(1-нафтил)-1-инденил)(2-метил-1-инденил) циркондихлоридом, соотношение форм рацемической: "псевдорацемической" составило 2,5:1 (экссинтез). Активность металлоцена составила 519 кг полипропилена/г металлоцена • час. KB = 401 см3/г; Mw = 584500 г/моль, Mw/Mn = 2,0; температура плавления = 152oC.
Пример 1 был повторен с металлоценом 1,2-этандиил(2-этил-4-(1-нафтил)-1-инденил)(2-метил-1-инденил) циркондихлоридом, соотношение форм рацемической: "псевдорацемической" составило 2,5:1 (экссинтез). Активность металлоцена составила 519 кг полипропилена/г металлоцена • час. KB = 401 см3/г; Mw = 584500 г/моль, Mw/Mn = 2,0; температура плавления = 152oC.
Пример 19
Был повторен пример 1, однако перед добавлением пропилена в реактор было добавлено 2,5 ндм3 водорода и во время полимеризации в качестве сомономера дозами добавляли дополнительно 60 г этилена.
Был повторен пример 1, однако перед добавлением пропилена в реактор было добавлено 2,5 ндм3 водорода и во время полимеризации в качестве сомономера дозами добавляли дополнительно 60 г этилена.
Активность металлоцена составила 1386 кг сополимера/г металлоцена • час. У полимера были определены следующие свойства: содержание этилена 4,1 весовых процентов, KB = 179 см3/г, Mw = 217500 г/моль, Mw/Mn =2,0; температура плавления = 136oC, 0,75% полимера можно экстрагировать кипящим гексаном.
Пример 20
Пример 19 был повторен с 60 г 1-гексена в качестве сополимера. Активность металлоцена составила 998 кг сополимера/г металлоцена • час. У полимера были определены следующие свойства: содержание гексена 5,6 весовых процентов. KB = 208 см3/г, Mw=237000 г/моль, Mw/Mn = 1,9; температура плавления = 127oC.
Пример 19 был повторен с 60 г 1-гексена в качестве сополимера. Активность металлоцена составила 998 кг сополимера/г металлоцена • час. У полимера были определены следующие свойства: содержание гексена 5,6 весовых процентов. KB = 208 см3/г, Mw=237000 г/моль, Mw/Mn = 1,9; температура плавления = 127oC.
Пример 21
Пример 19 был повторен с 1-бутеном в качестве сополимера. Содержание бутена в полимере составило 5,1 весовых процентов. Температура плавления = около 130oC.
Пример 19 был повторен с 1-бутеном в качестве сополимера. Содержание бутена в полимере составило 5,1 весовых процентов. Температура плавления = около 130oC.
Пример 22
Сухой реактор емкостью 150 дм3 был промыт азотом и заполнен при температуре 20oC 100 дм3 деароматизированной бензиновой фракцией с пределами кипения от 100 до 120oC. Затем газовая камера была промыта путем пятикратного накачивания пропилена под давлением 2 бара и сброса давления без азота. После добавления 50 литров жидкого пропилена было добавлено 64 см3 толуольного раствора металлалюминоксана (соответственно 100 миллимолей алюминия) и содержимое реактора нагрето до температуры 50oC. Путем добавления дозами водорода его содержание в газовой камере было установлено на уровне 1,5% и затем путем дополнительного добавления дозами в течение всего времени полимеризации пропилена поддерживалось постоянным (газовая хроматография, комплексное измерение). 15 мг металлоцена рацемического диэтилгермил-(2-метил-4-фенил-1-инденил)(2-этил-1-инденил)- циркондихлорида было растворено в 16 см2 толуольного раствора метилалюминоксана (соответственно 25 миллимолей алюминия) и спустя 15 минут добавлено в реактор. С помощью охлаждения температура полимеризации в реакторе поддерживалась в течение 5 часов на уровне 55oC. После выпуска водорода и пропилена до давления пропилена в реакторе 1,5 бара полимеризация проводилась после добавления 2,5 кг этилена еще в течение 3 часов при температуре 50oC.
Сухой реактор емкостью 150 дм3 был промыт азотом и заполнен при температуре 20oC 100 дм3 деароматизированной бензиновой фракцией с пределами кипения от 100 до 120oC. Затем газовая камера была промыта путем пятикратного накачивания пропилена под давлением 2 бара и сброса давления без азота. После добавления 50 литров жидкого пропилена было добавлено 64 см3 толуольного раствора металлалюминоксана (соответственно 100 миллимолей алюминия) и содержимое реактора нагрето до температуры 50oC. Путем добавления дозами водорода его содержание в газовой камере было установлено на уровне 1,5% и затем путем дополнительного добавления дозами в течение всего времени полимеризации пропилена поддерживалось постоянным (газовая хроматография, комплексное измерение). 15 мг металлоцена рацемического диэтилгермил-(2-метил-4-фенил-1-инденил)(2-этил-1-инденил)- циркондихлорида было растворено в 16 см2 толуольного раствора метилалюминоксана (соответственно 25 миллимолей алюминия) и спустя 15 минут добавлено в реактор. С помощью охлаждения температура полимеризации в реакторе поддерживалась в течение 5 часов на уровне 55oC. После выпуска водорода и пропилена до давления пропилена в реакторе 1,5 бара полимеризация проводилась после добавления 2,5 кг этилена еще в течение 3 часов при температуре 50oC.
Содержимое реактора было выпущено на напорный нутч-фильтр, с помощью перегонки с водяным паром продукт был отделен от остаточного суспендирующего агента и высушен в течение 24 часов при температуре 80oC и давлении 200 мбар. Было получено 21,5 кг порошка блок-сополимера, соответственно активность металлоцена составила 179,2 кг сополимера/г металлоцена. Блок-сополимер содержал 10,8 весовых процентов этилена, фракционирование дало содержание 22,7 весовых процентов этиленпропилового каучука, температура стеклования каучука составила минус 54,5oC. ИТР (230/2) всего полимера составил 16 дг/мин.
Пример 23
Был повторен пример 19, однако в реактор наряду с 500 г этилена было загружено еще 150 мл 5-этилиден-2-корборна в течение времени полимеризации. Загрузка осуществлялась дозами. Температура полимеризации составила 50oC. Был получен тройной сополимер каучука с температурой стеклования -59,8oC. Содержание этилена в полимере составило 42 весовых процента и содержание этилиденорборна составило 4,8 весовых процента.
Был повторен пример 19, однако в реактор наряду с 500 г этилена было загружено еще 150 мл 5-этилиден-2-корборна в течение времени полимеризации. Загрузка осуществлялась дозами. Температура полимеризации составила 50oC. Был получен тройной сополимер каучука с температурой стеклования -59,8oC. Содержание этилена в полимере составило 42 весовых процента и содержание этилиденорборна составило 4,8 весовых процента.
Пример 24
Применение металлоцена на носителе в качестве катализатора.
Применение металлоцена на носителе в качестве катализатора.
а) Получение сокатализаторов на носителе.
Получение сокатализаторов на носителе осуществлялось так, как описано в Европейском патенте N 92107331,8, нижеописанным образом в реакторе из высококачественной стали во взрывобезопасном исполнении с системой перекачивания ступени давления 60 бар, с подачей инертного газа, с поддержанием необходимой температуры путем охлаждения оболочки и со вторым охлаждающим контуром с помощью теплообменника в системе перекачивания. Система перекачивании всасывала содержимое реактора через соединительный элемент в днище реактора с помощью насоса, нагнетала в смеситель и возвращала его с помощью нагнетательного трубопровода через теплообменник в реактор. Смеситель был включен таким образом, что в подводящей линии находилась труба с уменьшенным поперечным сечением, где создавалась повышенная скорость потока, и в зоне завихрения аксиально и вдоль направления потока направлен тонкий подводящий трубопровод, с помощью которого циклично можно было подавать соответственно определенное количество воды при давлении аргона 40 бар. Контроль реакции осуществлялся с помощью пробоотборника на контуре перекачивания.
В описанный выше реактор объемом 16 дм3 было загружено 5 дм3 декана при инертных условиях. При температуре 25oC было добавлено 0,3 дм3 ( = 3,1 моля) триметилалюминия. Затем через воронку для загрузки твердого вещества в реактор дозами было загружено 250 г силикагеля SD 3116-30 (Граце АГ), который предварительно был высушен при температуре 120oC в созданном аргоном псевдоожиженном слое, и с помощью мешалки и системы перекачивания гомогенно распределено. Общее количество воды 45,9 г порциями в 0,1 см3 добавлялось в реактор в течение 2 часов соответственно через каждые 15 секунд. Давление, создаваемое аргоном и образовавшимися газами, поддерживалось с помощью регулирующих клапанов постоянным на уровне 10 бар. После того, как была введена вся вода, система перекачивания была отключена и перемешивание продолжалось еще в течение 5 часов при температуре 25oC. С помощью нагнетательного нутч-фильтра был удален растворитель и твердое вещество сокатализатора было принято с помощью декана. Затем оно было высушено в вакууме. Изолированное твердое вещество содержало 18,4 весовых процентов алюминия. 15 г этого твердого вещества (102 миллимоля алюминия) было суспендировано в сосуде с мешалкой в 100 см3 толуола и суспензия охлаждена до температуры -30oC. Одновременно 200 мг в соответствии форм рацемическая: "псевдорацемическая" 7:1 Me2Si (2,4,6-триметил-1-индецил)(2-метил-4-фенил-1-инденил) ZrCl2 было растворено в 75 см3 толуола в течение 30 минут каплями добавлено в суспензию. Суспензия медленно при перемешивании была нагрета до комнатной температуры, причем суспензия приобрела красную окраску. Затем суспензия перемешивалась в течение часа при температуре 50oC, после охлаждения до комнатной температуры смесь была профильтрована и твердое вещество было промыто трижды соответственно с помощью 100 см3 толуола и один раз с помощью 100 см3 гексана. Остающийся, смоченный гексаном остаток на фильтре был высушен в вакууме. Получили 14,2 г свободного текучего, светло-красного катализатора на носителе. Анализ показал содержание 10,9 мг двуокиси циркония на грамм катализатора.
b) Полимеризация
1,2 г полученного в пункте а) катализатора было суспендировано в 25 см3 деароматизированной бензиновой фракции с пределами кипения от 100 до 120oC.
1,2 г полученного в пункте а) катализатора было суспендировано в 25 см3 деароматизированной бензиновой фракции с пределами кипения от 100 до 120oC.
Параллельно с этим сухой реактор объемом 24 дм3 вначале был промыт азотом и затем пропиленом и заполнен 12 дм3 пропилена и 1,5 дм3 водорода. Затем 3 см3 триизобутилалюминия (12 миллимолей) было разбавлено 30 мл гексана, добавлено в реактор и исходная смесь перемешивалась при температуре 30oC в течение 15 минут. Затем в реактор была загружена суспензия катализатора, нагрета до температуры полимеризации 80oC (со скоростью 10oC/мин) и полимеризационная система с помощью охлаждения выдерживалась при температуре 80oC в течение 1 часа. Полимеризация была прекращена путем добавления 20 мл изопропанола. Избыточный мономер был отведен, полимер высушен в вакууме. Получалось 2,78 кг порошка полипропилена. Таким образом, активность металлоцена составила 212,5 кг полипропилена/г металлоцена • час. У полимера были определены следующие свойства: KB = 298 см3/г; MW = 378500 г/моль, MW/Mn = 2,0; ИТР (230/5) = 3,9 дг/мин; ИТР (230/2) = 1,2 дг/мин; температура плавления = 150oC. Морфология порошка: нет зерен менее 200 мкм, средний размер зерен d50 = 735 мкм, нет излишнего рога более 1500 мкм, плотный гранулометрический состав s = ln(d50/D16) = 0,25; кажущаяся плотность 495 г/дм3.
Примеры 25 - 28
Был повторен пример 1, однако в качестве металлоценов были использованы приведенные в таблице соединения. Активности и данные полимеров представлены в таблице 1.
Был повторен пример 1, однако в качестве металлоценов были использованы приведенные в таблице соединения. Активности и данные полимеров представлены в таблице 1.
Примеры 29 - 34
Сухой реактор объемом 1,5 дм3 был промыт азотом и при температуре 20oC заполнен 0,75 дм3 деароматизированной бензиловой фракцией с пределами кипения от 100 до 120oC. Затем газовая камера реактора была промыта путем пятикратного накачивания этилена при давлении 2 бара и сброса давления без азота. Затем было добавлено 3,75 см3 толуольного раствора метилалюминоксана (5 миллимолей алюминия, n = 18). При перемешивании реактор был нагрет до температуры 30oC (в течение 15 минут) и при скорости перемешивания 500 об/мин путем добавления этилена было установлено общее давление 5 бар. Параллельно с этим было растворено 0,125 мг металлоцена (название соединения смотри в таблице 2) в 1,25 см3 толуольного раствора метилалюминоксана (1,67 миллимоля алюминия, n = 18) и в течение 15-минутной выдержки смесь была доведена для полной реакции. Затем раствор был добавлен в реактор, полимеризационная система была доведена до температуры 70oC при соответствующем охлаждении выдержана в течение 1 часа при этой температуре. Благодаря соответствующей подаче этилена давление в течение этого времени поддерживалось на уровне 5 бар. Затем путем добавления 2 мл изопропанола полимеризация была прекращена, полимер был отфильтрован и высушен в вакууме. Результаты полимеризации представлены в таблице 2.
Сухой реактор объемом 1,5 дм3 был промыт азотом и при температуре 20oC заполнен 0,75 дм3 деароматизированной бензиловой фракцией с пределами кипения от 100 до 120oC. Затем газовая камера реактора была промыта путем пятикратного накачивания этилена при давлении 2 бара и сброса давления без азота. Затем было добавлено 3,75 см3 толуольного раствора метилалюминоксана (5 миллимолей алюминия, n = 18). При перемешивании реактор был нагрет до температуры 30oC (в течение 15 минут) и при скорости перемешивания 500 об/мин путем добавления этилена было установлено общее давление 5 бар. Параллельно с этим было растворено 0,125 мг металлоцена (название соединения смотри в таблице 2) в 1,25 см3 толуольного раствора метилалюминоксана (1,67 миллимоля алюминия, n = 18) и в течение 15-минутной выдержки смесь была доведена для полной реакции. Затем раствор был добавлен в реактор, полимеризационная система была доведена до температуры 70oC при соответствующем охлаждении выдержана в течение 1 часа при этой температуре. Благодаря соответствующей подаче этилена давление в течение этого времени поддерживалось на уровне 5 бар. Затем путем добавления 2 мл изопропанола полимеризация была прекращена, полимер был отфильтрован и высушен в вакууме. Результаты полимеризации представлены в таблице 2.
Примеры 35 и 36
Пример 24 был повторен при температурах полимеризации 65oC (пример 35) и 80oC (пример 36). При температуре 88oC вследствие высокой полимеризационной активности полимеризация была закончена по истечении 30 минут. Для полимера были измерены температуры плавления, которые составили 148oC (пример 35) и 156oC (пример 36).
Пример 24 был повторен при температурах полимеризации 65oC (пример 35) и 80oC (пример 36). При температуре 88oC вследствие высокой полимеризационной активности полимеризация была закончена по истечении 30 минут. Для полимера были измерены температуры плавления, которые составили 148oC (пример 35) и 156oC (пример 36).
ЯМР-данные целевых продуктов примеров D-I
Пример D:
Рац-диэтилгерманийдиил(2-метил-4-фенил-инденил)2-этил-инденил) цирконийдихлорид (4)
1H-ЯМР (400 МГц, CDCl3): 7,6 - 6,9 (m, 14H, аром.-H), 2,65 (m, 1H, CH2-этил), 2,45 (m, 1H, CH2-этил), 2,34 (s, 3H, CH3), 2,05, 1,95 (каждый m, каждый 2H, CH2-этил-Ge), 1,15 (t, 6H, CH3-этил-Ge), 1,02 (t, 3H, CH3-этил) ppm.
Пример D:
Рац-диэтилгерманийдиил(2-метил-4-фенил-инденил)2-этил-инденил) цирконийдихлорид (4)
1H-ЯМР (400 МГц, CDCl3): 7,6 - 6,9 (m, 14H, аром.-H), 2,65 (m, 1H, CH2-этил), 2,45 (m, 1H, CH2-этил), 2,34 (s, 3H, CH3), 2,05, 1,95 (каждый m, каждый 2H, CH2-этил-Ge), 1,15 (t, 6H, CH3-этил-Ge), 1,02 (t, 3H, CH3-этил) ppm.
Пример E:
Рац-диметилсиландиил(2,4,6-триметил-инденил)(2-метил-4-фенил-инденил)цирконийдихлорид (5)
1H-ЯМР (400 МГц, CDCl3): 7,6 - 7,0 (m, 12H, аром.-H), 2,34 (s, 3H, CH3), 2,32, 2,27, 2,20 (каждый s, каждый 3H, CH3-инденил), 1,38 (s, 6H, CH3-Si) ppm.
Рац-диметилсиландиил(2,4,6-триметил-инденил)(2-метил-4-фенил-инденил)цирконийдихлорид (5)
1H-ЯМР (400 МГц, CDCl3): 7,6 - 7,0 (m, 12H, аром.-H), 2,34 (s, 3H, CH3), 2,32, 2,27, 2,20 (каждый s, каждый 3H, CH3-инденил), 1,38 (s, 6H, CH3-Si) ppm.
Пример F:
Рац-диметилсиландиил(2-метил-4,6-диизопропилинденил)(2-метил- инденил)цирконийдихлорид (6)
1H-ЯМР (400 МГц, CDCl3): 7,3 - 6,9 (m, 8H, аром.-H), 2,95, 2,61 (каждый m, каждый 1H, CH-изопропил), 2,32 (s, 3H, CH3), 2,21 (s, 3H, CH3), 1,34 (s, 6H, CH3-Si), 1,25 - 0,9 (m, 24H, CH3-изопропил) ppm.
Рац-диметилсиландиил(2-метил-4,6-диизопропилинденил)(2-метил- инденил)цирконийдихлорид (6)
1H-ЯМР (400 МГц, CDCl3): 7,3 - 6,9 (m, 8H, аром.-H), 2,95, 2,61 (каждый m, каждый 1H, CH-изопропил), 2,32 (s, 3H, CH3), 2,21 (s, 3H, CH3), 1,34 (s, 6H, CH3-Si), 1,25 - 0,9 (m, 24H, CH3-изопропил) ppm.
Пример G:
Рац-диметилгерманийдиил(2-метил-4-фенил-инденил)(2-метил- инденил)цирконийдихлорид (7)
1H-ЯМР (400 МГц, CDCl3): 7,6 - 7,0 (m, 14H, аром.-H), 2,35 (s, 3H, CH3), 2,18 s, 3H, CH3-инденил), 1,41 (s, 6H, CH3-Ge) ppm.
Рац-диметилгерманийдиил(2-метил-4-фенил-инденил)(2-метил- инденил)цирконийдихлорид (7)
1H-ЯМР (400 МГц, CDCl3): 7,6 - 7,0 (m, 14H, аром.-H), 2,35 (s, 3H, CH3), 2,18 s, 3H, CH3-инденил), 1,41 (s, 6H, CH3-Ge) ppm.
Пример H:
Рац-диметилсиландиил(2-метил-аценафти-инденил)(2-метил-4-фенил- инденил)цирконийдихлорид (8)
1H-ЯМР (400 МГц, CDCl3): 7,5 - 7,0 (m, 15H, аром.-H), 5,14 (s, 4H, CH2-аценафтил), 2,45 (s, 3H, CH3), 2,33 (s, 3H, CH3), 1,40 (s, 6H, CH3-Si) ppm.
Рац-диметилсиландиил(2-метил-аценафти-инденил)(2-метил-4-фенил- инденил)цирконийдихлорид (8)
1H-ЯМР (400 МГц, CDCl3): 7,5 - 7,0 (m, 15H, аром.-H), 5,14 (s, 4H, CH2-аценафтил), 2,45 (s, 3H, CH3), 2,33 (s, 3H, CH3), 1,40 (s, 6H, CH3-Si) ppm.
Пример I
Рац-диэтилгерманийдиил(2-метил-4-/1-нафтил/-инденил)(инденил) цирконийдихлорид (9)
1H-ЯМР (400 МГц, CDCl3): 7,2 - 6,8 (m, 15H, аром.-H), 6,21 (d, 1H, -H-инденил), 2,24 (s, 3H, CH3), 2,02, 1,98 (каждый m, каждый 2H, CH2-этил-Ge), 1,20 (t, 6H, CH3-этил-Ge) ppm.
Рац-диэтилгерманийдиил(2-метил-4-/1-нафтил/-инденил)(инденил) цирконийдихлорид (9)
1H-ЯМР (400 МГц, CDCl3): 7,2 - 6,8 (m, 15H, аром.-H), 6,21 (d, 1H, -H-инденил), 2,24 (s, 3H, CH3), 2,02, 1,98 (каждый m, каждый 2H, CH2-этил-Ge), 1,20 (t, 6H, CH3-этил-Ge) ppm.
Дополнительные примеры
Пример А
Повторяют пример 1, однако в качестве металлоцена используют рац-диметилсиландиил(2-метил-4-фенил-1-инденил)(2-метил-1-инденил) циркондиметил в таком же количестве. Активность металлоцена составила 785 кг полипропилена /г металлоцена в час, Mw = 527000 г/моль, Mw/Mn = 2,1, ИТР = 0,5 дг/мин, температура плавления 154oC, ИИ = 97,8%, niso = 79.
Пример А
Повторяют пример 1, однако в качестве металлоцена используют рац-диметилсиландиил(2-метил-4-фенил-1-инденил)(2-метил-1-инденил) циркондиметил в таком же количестве. Активность металлоцена составила 785 кг полипропилена /г металлоцена в час, Mw = 527000 г/моль, Mw/Mn = 2,1, ИТР = 0,5 дг/мин, температура плавления 154oC, ИИ = 97,8%, niso = 79.
Пример Б
Повторяют пример 1, однако в качестве металлоцена используют рац-диметилсиландиил(2,4-диметил-1-инденил)(2-метил-1-инденил) циркондихлорид в таком же количестве. Активность металлоцена составила 245 кг полипропилена /г металлоцена в час, Mw = 127000 г/моль, Mw/Mn = 2,3, температура плавления 143oC, ИИ = 94,5%.
Повторяют пример 1, однако в качестве металлоцена используют рац-диметилсиландиил(2,4-диметил-1-инденил)(2-метил-1-инденил) циркондихлорид в таком же количестве. Активность металлоцена составила 245 кг полипропилена /г металлоцена в час, Mw = 127000 г/моль, Mw/Mn = 2,3, температура плавления 143oC, ИИ = 94,5%.
Пример В
Повторяют пример 1, однако в качестве металлоцена используют рац-дифенилметилиден(2-метил-4-фенил-1-инденил)(2-метил-1-инденил) циркондиметил в таком же количестве. Активность металлоцена составила 385 кг полипропилена /г металлоцена в час, Mw = 158000 г/моль, Mw/Mn = 2,0.
Повторяют пример 1, однако в качестве металлоцена используют рац-дифенилметилиден(2-метил-4-фенил-1-инденил)(2-метил-1-инденил) циркондиметил в таком же количестве. Активность металлоцена составила 385 кг полипропилена /г металлоцена в час, Mw = 158000 г/моль, Mw/Mn = 2,0.
Пример Г
Повторяют пример 1, однако в качестве металлоцена используют рац-этандиил(2-этил-4-фенил-1-инденил)(2-метил-1-инденил) циркондихлорид в таком же количестве. Активность металлоцена составила 985 кг полипропилена /г металлоцена в час, Mw = 327000 г/моль, Mw/Mn = 2,0, температура плавления 141oC, ИИ = 95,3%.
Повторяют пример 1, однако в качестве металлоцена используют рац-этандиил(2-этил-4-фенил-1-инденил)(2-метил-1-инденил) циркондихлорид в таком же количестве. Активность металлоцена составила 985 кг полипропилена /г металлоцена в час, Mw = 327000 г/моль, Mw/Mn = 2,0, температура плавления 141oC, ИИ = 95,3%.
Пример Д
Повторяют пример 1, однако в качестве металлоцена используют 0,5 мг рац-диметилсиландиил(2-метил-4-фенил-1-инденил)(2-метил-1-инденил) циркондихлорида и рац-диметилсиландиил(2-этил-4-фенил-1-инденил) (2-этил-1-инденил)циркондиметил. Активность металлооцена составила 694 кг полипропилена /г металлоцена в час, Mw = 498000 г/моль, Mw/Mn = 2,6, ИТР = 0,7 дг/мин, температура плавления 157oC, ИИ = 98,4%, niso = 98.
Повторяют пример 1, однако в качестве металлоцена используют 0,5 мг рац-диметилсиландиил(2-метил-4-фенил-1-инденил)(2-метил-1-инденил) циркондихлорида и рац-диметилсиландиил(2-этил-4-фенил-1-инденил) (2-этил-1-инденил)циркондиметил. Активность металлооцена составила 694 кг полипропилена /г металлоцена в час, Mw = 498000 г/моль, Mw/Mn = 2,6, ИТР = 0,7 дг/мин, температура плавления 157oC, ИИ = 98,4%, niso = 98.
Claims (10)
1. Металлоцены формулы I
в которой M2 - металл группы IV b Периодической системы;
R1 - атом галогена или метильная группа;
R2 - атом водорода;
R3 - одинаковые или различные, обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу или два или более R3 образуют вместе с соединяющими их атомами кольцевую систему;
R4, одинаковые или различные, обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу,
R5 - атом водорода, C1-C10-алкильная группа;
R6 - атом водорода, C1-C10-алкильная группа;
R7 является
причем R8, R9, R11 и R12, одинаковые или различные, обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу;
M1 - кремний или германий;
m = 0 или 1,
при этом оба инденильных лиганда имеют отличные друг от друга заместители.
в которой M2 - металл группы IV b Периодической системы;
R1 - атом галогена или метильная группа;
R2 - атом водорода;
R3 - одинаковые или различные, обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу или два или более R3 образуют вместе с соединяющими их атомами кольцевую систему;
R4, одинаковые или различные, обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу,
R5 - атом водорода, C1-C10-алкильная группа;
R6 - атом водорода, C1-C10-алкильная группа;
R7 является
причем R8, R9, R11 и R12, одинаковые или различные, обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу;
M1 - кремний или германий;
m = 0 или 1,
при этом оба инденильных лиганда имеют отличные друг от друга заместители.
2. Металлоцены формулы I по п.1, в которой M2 - цирконий, R1 одинаковые и обозначают метильную группу или хлор; R5 - C1-C10-алкильная группа; R11 и R12, одинаковые или различные, обозначают C1-C20-алкильную группу или C6-C30-арильную группу.
3. Металлоцены формулы I по п.1, применяемые в катализаторах для полимеризации олефинов.
4. Каталитическая система, включающая компонент катализатора, содержащий металлоцен, и сокатализатор, отличающаяся тем, что в качестве металлоцена она содержит по меньшей мере одно соединение по п.1 или 2.
5. Каталитическая система по п.4, отличающаяся тем, что она включает компонент катализатора на носителе и/или предварительно полимеризированный компонент катализатора, содержащий по меньшей мере одно металлоценовое соединение в соответствии с п.1 или 2.
6. Способ полимеризации олефинов путем гомополимеризации или сополимеризации по меньшей мере одного олефина в присутствии катализатора, который содержит по меньшей мере один металлоцен в качестве соединения переходного металла и по меньшей мере один сокатализатор, отличающийся тем, что металлоцен является соединением формулы I
в которой M2 - металл группы IVb Периодической системы;
R1 - атом галогена или метильная группа;
R2 - атом водорода;
R3 - одинаковые или различные, обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу или два или более радикалов R3 образуют вместе с соединяющими их атомами кольцевую систему;
R4, одинаковые или различные, обозначают атом водорода, C1-C30-алкильную группу, C6-C30-арильную группу,
R5 - атом водорода, C1-C10-алкильная группа;
R6 - атом водорода, C1-C10-алкильная группа;
R7 является
причем R8, R9, R11 и R12, одинаковые или различные, обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу;
M1 - кремний или германий;
m = 0 или 1,
при этом оба инденильных лиганда имеют отличные друг от друга заместители.
в которой M2 - металл группы IVb Периодической системы;
R1 - атом галогена или метильная группа;
R2 - атом водорода;
R3 - одинаковые или различные, обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу или два или более радикалов R3 образуют вместе с соединяющими их атомами кольцевую систему;
R4, одинаковые или различные, обозначают атом водорода, C1-C30-алкильную группу, C6-C30-арильную группу,
R5 - атом водорода, C1-C10-алкильная группа;
R6 - атом водорода, C1-C10-алкильная группа;
R7 является
причем R8, R9, R11 и R12, одинаковые или различные, обозначают атом водорода, C1-C20-алкильную группу, C6-C30-арильную группу;
M1 - кремний или германий;
m = 0 или 1,
при этом оба инденильных лиганда имеют отличные друг от друга заместители.
7. Способ по п.6, отличающийся тем, что используют каталитическую систему, в которой металлоцен нанесен на носитель и/или форполимеризован.
8. Способ по п.6, отличающийся тем, что используют каталитическую систему, в которой сокатализатором является алюминоксан.
9. Полиолефин, который является продуктом способа по пп.6 - 8.
10. Формованное изделие, выполненное из полиолефина, отличающееся тем, что оно выполнено из полиолефина по п.9, полученного по пп.6 - 8.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE4344689A DE4344689A1 (de) | 1993-12-27 | 1993-12-27 | Metallocenverbindung |
| DEP4344689.2 | 1993-12-27 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU94045142A RU94045142A (ru) | 1996-11-20 |
| RU2142466C1 true RU2142466C1 (ru) | 1999-12-10 |
Family
ID=6506375
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU94045142A RU2142466C1 (ru) | 1993-12-27 | 1994-12-26 | Металлоцены, содержащая их каталитическая система, способ полимеризации олефинов, полиолефин, формованное изделие |
Country Status (10)
| Country | Link |
|---|---|
| US (3) | US5532396A (ru) |
| EP (2) | EP1188763B1 (ru) |
| JP (1) | JP3789502B2 (ru) |
| KR (1) | KR950018027A (ru) |
| CN (1) | CN1068332C (ru) |
| AT (2) | ATE290536T1 (ru) |
| BR (1) | BR9405252A (ru) |
| DE (3) | DE4344689A1 (ru) |
| ES (2) | ES2174860T3 (ru) |
| RU (1) | RU2142466C1 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2670752C2 (ru) * | 2014-09-05 | 2018-10-25 | ЭлДжи КЕМ, ЛТД. | Полимер на основе олефинов с исключительной способностью к переработке |
Families Citing this family (82)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TW309523B (ru) * | 1991-11-30 | 1997-07-01 | Hoechst Ag | |
| EP0582195B1 (de) * | 1992-08-03 | 2000-12-20 | TARGOR GmbH | Verfahren zur Herstellung eines Olefinpolymers unter Verwendung spezieller Metallocene |
| NL9201970A (nl) * | 1992-11-11 | 1994-06-01 | Dsm Nv | Indenylverbindingen en katalysatorcomponenten voor de polymerisatie van olefinen. |
| NL9400758A (nl) * | 1994-05-06 | 1995-12-01 | Dsm Nv | Werkwijze voor de bereiding van een hoogmoleculair polymeer uit etheen, alfa-olefine en eventueel dieen. |
| US5563284A (en) * | 1994-09-09 | 1996-10-08 | Phillips Petroleum Company | Cyclopentadienyl-type ligands, metallocenes, catalyst systems, preparation, and use |
| DE4436113A1 (de) * | 1994-10-10 | 1996-04-11 | Hoechst Ag | Metallocenverbindung |
| TW383313B (en) * | 1994-12-20 | 2000-03-01 | Mitsui Petrochemical Ind | Preparation of ethylene-alpha-olefin-nonconjugate polyene random copolymers, the copolymers obtaining which, and the use of the copolymers |
| IT1272923B (it) * | 1995-01-23 | 1997-07-01 | Spherilene Srl | Composti metallocenici,procedimento per la loro preparazione,e loro utilizzo in catalizzatori per la polimerizzazione delle olefine |
| DE19516803A1 (de) * | 1995-05-08 | 1996-11-14 | Hoechst Ag | Organometallverbindung |
| JPH08325327A (ja) * | 1995-06-02 | 1996-12-10 | Chisso Corp | 高立体規則性ポリプロピレン |
| DE19527047A1 (de) * | 1995-07-25 | 1997-01-30 | Danubia Petrochem Deutschland | Metallocene mit silylsubstituierten Brücken und deren Einsatz für die Olefinpolymerisation |
| WO1997015582A1 (en) * | 1995-10-27 | 1997-05-01 | The Dow Chemical Company | Supportable biscyclopentadienyl metal complexes |
| US6787618B1 (en) | 1995-12-01 | 2004-09-07 | Basell Polypropylen Gmbh | Metallocene compound and high molecular weight copolymers of propylene and olefins having two or four to thirty-two carbon atoms |
| US5679814A (en) * | 1995-12-11 | 1997-10-21 | Albemarle Corporation | Purification of metallocenes |
| DE19548288A1 (de) * | 1995-12-22 | 1997-06-26 | Hoechst Ag | Geträgertes Katalysatorsystem, Verfahren zu seiner Herstellung und seine Verwendung zur Polymerisation von Olefinen |
| WO1997040075A1 (fr) * | 1996-04-22 | 1997-10-30 | Japan Polyolefins Co., Ltd. | Procede de production de polyolefine et catalyseur approprie |
| US5710299A (en) * | 1996-06-27 | 1998-01-20 | Albemarle Corporation | Production of bridged metallocene complexes and intermediates therefor |
| US5760262A (en) * | 1996-09-17 | 1998-06-02 | Albemarle Corporation | Enhanced production of bridged hafnocenes |
| US5936108A (en) * | 1996-10-17 | 1999-08-10 | Albemarle Corporation | Metallocene synthesis |
| DE69719490T2 (de) * | 1996-11-22 | 2003-09-25 | Boulder Scient Co | Herstellung von chiralen titanocenen |
| US5889128A (en) * | 1997-04-11 | 1999-03-30 | Massachusetts Institute Of Technology | Living olefin polymerization processes |
| US6037428A (en) * | 1997-04-25 | 2000-03-14 | Shin-Etsu Chemical Co., Ltd. | Polymerization of vinyl chloride with peroxide mixtures |
| US5905162A (en) * | 1997-08-12 | 1999-05-18 | Albemarle Corporation | Enhanced production of bridged hafnocenes |
| AT405834B (de) | 1997-10-09 | 1999-11-25 | Borealis Ag | Metallocene mit ferrocenyl-substituierten brücken und deren einsatz für die olefinpolymerisation |
| KR100274973B1 (ko) * | 1997-11-24 | 2000-12-15 | 성재갑 | 올레핀계 단량체의 중합 촉매 |
| ES2195443T3 (es) * | 1997-12-23 | 2003-12-01 | Exxonmobil Chem Patents Inc | Procedimiento de polimerizacion de etileno en un medio de reaccion liquido. |
| AU2569699A (en) * | 1998-01-30 | 1999-08-16 | Boulder Scientific Company | Silylated and n-silylated compound synthesis |
| US6818585B2 (en) * | 1998-12-30 | 2004-11-16 | Univation Technologies, Llc | Catalyst compounds, catalyst systems thereof and their use in a polymerization process |
| US6034192A (en) * | 1998-12-30 | 2000-03-07 | Univation Technologies, Llc | Germanium bridged metallocenes producing polymers with increased melt strength |
| EP1074557A3 (de) | 1999-07-31 | 2003-02-26 | Basell Polyolefine GmbH | Übergangsmetallverbindung, Ligandensystem, Katalysatorsystem und seine Verwendung zur Polymerisation von Olefinen |
| US6399722B1 (en) * | 1999-12-01 | 2002-06-04 | Univation Technologies, Llc | Solution feed of multiple catalysts |
| WO2001032758A1 (en) | 1999-11-04 | 2001-05-10 | Exxon Chemical Patents Inc. | Propylene copolymer foams and their use |
| BR0016146A (pt) * | 1999-12-01 | 2002-08-13 | Univation Tech Llc | Compostos catalisadores, sistemas catalisadores dos mesmos e seus usos em um processo de polimerização |
| ATE269887T1 (de) * | 1999-12-13 | 2004-07-15 | Basf Ag | Pigmentkonzentrate und verfahren zu ihrer herstellung |
| BR0016618B1 (pt) * | 1999-12-22 | 2013-12-03 | Composição adesiva à base de polipropileno | |
| CN100575324C (zh) | 1999-12-23 | 2009-12-30 | 巴塞尔聚烯烃有限公司 | 过渡金属化合物,配体体系,催化剂体系及其在烯烃的聚合反应和共聚反应中的用途 |
| JP2003522194A (ja) * | 2000-02-08 | 2003-07-22 | エクソンモービル・ケミカル・パテンツ・インク | 第14族架橋ビスシクロペンタジエニル・リガンドの調製方法 |
| ATE444975T1 (de) * | 2001-06-12 | 2009-10-15 | Basell Polyolefine Gmbh | Verfahren zur polymerisation von buten-1 |
| WO2002100908A1 (en) * | 2001-06-12 | 2002-12-19 | Basell Polyolefine Gmbh | Process for the polymerization of 1-butene |
| US6916892B2 (en) | 2001-12-03 | 2005-07-12 | Fina Technology, Inc. | Method for transitioning between Ziegler-Natta and metallocene catalysts in a bulk loop reactor for the production of polypropylene |
| US20030236365A1 (en) * | 2002-06-24 | 2003-12-25 | Fina Technology, Inc. | Polyolefin production with a high performance support for a metallocene catalyst system |
| US6995279B2 (en) | 2002-08-02 | 2006-02-07 | Chisso Corporation | Metallocene compounds, processes for the production of olefin polymers using catalysts containing the compounds, and olefin polymers produced by the processes |
| US7541402B2 (en) * | 2002-10-15 | 2009-06-02 | Exxonmobil Chemical Patents Inc. | Blend functionalized polyolefin adhesive |
| US7223822B2 (en) | 2002-10-15 | 2007-05-29 | Exxonmobil Chemical Patents Inc. | Multiple catalyst and reactor system for olefin polymerization and polymers produced therefrom |
| US7700707B2 (en) | 2002-10-15 | 2010-04-20 | Exxonmobil Chemical Patents Inc. | Polyolefin adhesive compositions and articles made therefrom |
| US7550528B2 (en) * | 2002-10-15 | 2009-06-23 | Exxonmobil Chemical Patents Inc. | Functionalized olefin polymers |
| EP1620479B1 (en) | 2002-10-15 | 2013-07-24 | ExxonMobil Chemical Patents Inc. | Polyolefin adhesive compositions and articles made therefrom |
| US7589160B2 (en) * | 2002-12-04 | 2009-09-15 | Basell Polyolefine Gmbh | Process for preparing 1-butene polymers |
| DE60329523D1 (de) * | 2002-12-04 | 2009-11-12 | Basell Polyolefine Gmbh | 1-Buten-Copolymere und Herstellungsverfahren dafür |
| US7195806B2 (en) * | 2003-01-17 | 2007-03-27 | Fina Technology, Inc. | High gloss polyethylene articles |
| JP2005099712A (ja) * | 2003-08-28 | 2005-04-14 | Sharp Corp | 表示装置の駆動回路および表示装置 |
| JP2007514685A (ja) | 2003-12-19 | 2007-06-07 | バーゼル、ポリオレフィン、ゲゼルシャフト、ミット、ベシュレンクテル、ハフツング | モノシクロペンタジエニル錯体 |
| US20050234198A1 (en) * | 2004-04-20 | 2005-10-20 | Fina Technology, Inc. | Heterophasic copolymer and metallocene catalyst system and method of producing the heterophasic copolymer using the metallocene catalyst system |
| US7285608B2 (en) * | 2004-04-21 | 2007-10-23 | Novolen Technology Holdings C.V. | Metallocene ligands, metallocene compounds and metallocene catalysts, their synthesis and their use for the polymerization of olefins |
| US7169864B2 (en) * | 2004-12-01 | 2007-01-30 | Novolen Technology Holdings, C.V. | Metallocene catalysts, their synthesis and their use for the polymerization of olefins |
| CN101163738B (zh) * | 2005-04-21 | 2011-07-13 | 巴塞尔聚烯烃意大利有限责任公司 | 双轴取向丙烯聚合物膜 |
| US7232869B2 (en) * | 2005-05-17 | 2007-06-19 | Novolen Technology Holdings, C.V. | Catalyst composition for olefin polymerization |
| EP1847555A1 (en) * | 2006-04-18 | 2007-10-24 | Borealis Technology Oy | Multi-branched Polypropylene |
| EP2235071A2 (en) * | 2007-10-25 | 2010-10-06 | Novolen Technology Holdings, C.V. | Metallocene compounds, catalysts comprising them, process for producing an olefin polymer by use of the catalysts, and olefin homo and copolymers |
| WO2011061151A1 (en) * | 2009-11-17 | 2011-05-26 | Basell Polyolefine Gmbh | Ethylene copolymers |
| EP2573091A1 (en) | 2011-09-23 | 2013-03-27 | Lummus Novolen Technology Gmbh | Process for recycling of free ligand from their corresponding metallocene complexes |
| EP3301119B1 (en) | 2013-07-17 | 2021-03-17 | ExxonMobil Chemical Patents Inc. | Isotactic propylene polymers |
| US9938364B2 (en) | 2013-07-17 | 2018-04-10 | Exxonmobil Chemical Patents Inc. | Substituted metallocene catalysts |
| CN110845546A (zh) | 2013-07-17 | 2020-02-28 | 埃克森美孚化学专利公司 | 取代的茂金属催化剂 |
| SG11201508750SA (en) | 2013-07-17 | 2015-11-27 | Exxonmobil Chem Patents Inc | Cyclopropyl substituted metallocene catalysts |
| EP3022238B1 (en) | 2013-07-17 | 2017-09-20 | ExxonMobil Chemical Patents Inc. | Metallocenes and catalyst compositions derived therefrom |
| WO2015009472A1 (en) | 2013-07-17 | 2015-01-22 | Exxonmobil Chemcal Patents Inc. | Metallocenes and catalyst compositions derived therefrom |
| KR101675983B1 (ko) * | 2014-10-06 | 2016-11-14 | 한양대학교 에리카산학협력단 | 다이플루오로알킬기가 도입된 유기 화합물의 제조 방법 |
| US10759886B2 (en) | 2015-06-05 | 2020-09-01 | Exxonmobil Chemical Patents Inc. | Single reactor production of polymers in gas or slurry phase |
| US9809664B2 (en) | 2015-06-05 | 2017-11-07 | Exxonmobil Chemical Patents Inc. | Bimodal propylene polymers and sequential polymerization |
| US10280233B2 (en) | 2015-06-05 | 2019-05-07 | Exxonmobil Chemical Patents Inc. | Catalyst systems and methods of making and using the same |
| US10294316B2 (en) | 2015-06-05 | 2019-05-21 | Exxonmobil Chemical Patents Inc. | Silica supports with high aluminoxane loading capability |
| US10329360B2 (en) | 2015-06-05 | 2019-06-25 | Exxonmobil Chemical Patents Inc. | Catalyst system comprising supported alumoxane and unsupported alumoxane particles |
| EP3885373A1 (en) | 2015-06-05 | 2021-09-29 | ExxonMobil Chemical Patents Inc. | Production of heterophasic polymers in gas or slurry phase |
| WO2016196331A1 (en) | 2015-06-05 | 2016-12-08 | Exxonmobil Chemical Patents Inc. | Supported metallocene catalyst systems for polymerization |
| US10280235B2 (en) | 2015-06-05 | 2019-05-07 | Exxonmobil Chemical Patents Inc. | Catalyst system containing high surface area supports and sequential polymerization to produce heterophasic polymers |
| US11059918B2 (en) | 2016-05-27 | 2021-07-13 | Exxonmobil Chemical Patents Inc. | Metallocene catalyst compositions and polymerization process therewith |
| US10807998B2 (en) | 2017-01-13 | 2020-10-20 | Exxonmobil Chemical Patents Inc. | Bridged bis(indenyl) transitional metal complexes, production, and use thereof |
| WO2020056119A1 (en) | 2018-09-14 | 2020-03-19 | Fina Technology, Inc. | Polyethylene and controlled rheology polypropylene polymer blends and methods of use |
| US20200263000A1 (en) | 2019-02-20 | 2020-08-20 | Fina Technology, Inc. | Polymer Compositions with Low Warpage |
| US11472828B2 (en) | 2019-10-11 | 2022-10-18 | Exxonmobil Chemical Patents Inc. | Indacene based metallocene catalysts useful in the production of propylene polymers |
| CA3214562A1 (en) | 2021-04-26 | 2022-11-03 | Michael Mcleod | Thin single-site catalyzed polymer sheets |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE3726067A1 (de) * | 1987-08-06 | 1989-02-16 | Hoechst Ag | Verfahren zur herstellung von 1-olefinpolymeren |
| DE3808268A1 (de) * | 1988-03-12 | 1989-09-21 | Hoechst Ag | Verfahren zur herstellung eines 1-olefinpolymers |
| US5017714A (en) * | 1988-03-21 | 1991-05-21 | Exxon Chemical Patents Inc. | Silicon-bridged transition metal compounds |
| DE3840772A1 (de) * | 1988-12-03 | 1990-06-07 | Hoechst Ag | Verfahren zur herstellung einer heterogenen metallocenkatalysatorkomponente |
| DE69018376T3 (de) * | 1989-10-30 | 2002-05-16 | Fina Technology | Herstellung von Metallocenkatalysatoren für Olefinpolymerisation. |
| DE59107973D1 (de) * | 1990-11-12 | 1996-08-08 | Hoechst Ag | Verfahren zur Herstellung eines hochmolekularen Olefinpolymers |
| US5243001A (en) * | 1990-11-12 | 1993-09-07 | Hoechst Aktiengesellschaft | Process for the preparation of a high molecular weight olefin polymer |
| ES2071888T3 (es) * | 1990-11-12 | 1995-07-01 | Hoechst Ag | Bisindenilmetalocenos sustituidos en posicion 2, procedimiento para su preparacion y su utilizacion como catalizadores en la polimerizacion de olefinas. |
| JP3117231B2 (ja) * | 1991-03-11 | 2000-12-11 | 三井化学株式会社 | 幅広い分子量分布を有するシンジオタクチックポリ−α−オレフィンの製造方法 |
| US5436305A (en) * | 1991-05-09 | 1995-07-25 | Phillips Petroleum Company | Organometallic fluorenyl compounds, preparation, and use |
| US5391789A (en) * | 1991-08-08 | 1995-02-21 | Hoechst Aktiengesellschaft | Bridged, chiral metallocenes, processes for their preparation and their use as catalysts |
| TW300901B (ru) * | 1991-08-26 | 1997-03-21 | Hoechst Ag | |
| DE69224463T2 (de) * | 1991-11-28 | 1998-07-09 | Showa Denko Kk | Neues Metallocen und Verfahren zur Herstellung von Polyolefinen unter Verwendung desselben |
| TW318184B (ru) * | 1991-11-30 | 1997-10-21 | Hoechst Ag | |
| DK0574597T3 (da) * | 1992-06-13 | 1998-09-14 | Targor Gmbh | Fremgangsmåde til fremstilling af brosluttede chirale metallocenkatalysatorer af bisindenyltypen |
| DE4431643C2 (de) * | 1994-07-22 | 2002-08-08 | Borealis Polymere Holding Ag | Verfahren zur Herstellung von Silizium-verbrückten unsymmetrischen Cyclopentadienyl-, Indenyl- und Fluorenyl-Ligandsystemen |
-
1993
- 1993-12-27 DE DE4344689A patent/DE4344689A1/de not_active Withdrawn
-
1994
- 1994-12-19 DE DE59410090T patent/DE59410090D1/de not_active Expired - Lifetime
- 1994-12-19 ES ES94120070T patent/ES2174860T3/es not_active Expired - Lifetime
- 1994-12-19 AT AT01114147T patent/ATE290536T1/de not_active IP Right Cessation
- 1994-12-19 EP EP01114147A patent/EP1188763B1/de not_active Expired - Lifetime
- 1994-12-19 EP EP94120070A patent/EP0659757B1/de not_active Expired - Lifetime
- 1994-12-19 DE DE59410406T patent/DE59410406D1/de not_active Expired - Lifetime
- 1994-12-19 ES ES01114147T patent/ES2238364T3/es not_active Expired - Lifetime
- 1994-12-19 AT AT94120070T patent/ATE215091T1/de not_active IP Right Cessation
- 1994-12-22 US US08/361,762 patent/US5532396A/en not_active Expired - Lifetime
- 1994-12-26 RU RU94045142A patent/RU2142466C1/ru active
- 1994-12-26 BR BR9405252A patent/BR9405252A/pt not_active IP Right Cessation
- 1994-12-27 KR KR1019940037116A patent/KR950018027A/ko active IP Right Grant
- 1994-12-27 CN CN94107627A patent/CN1068332C/zh not_active Expired - Lifetime
- 1994-12-27 JP JP32496894A patent/JP3789502B2/ja not_active Expired - Lifetime
-
1995
- 1995-06-07 US US08/477,853 patent/US5612428A/en not_active Expired - Lifetime
- 1995-06-07 US US08/475,938 patent/US5576260A/en not_active Expired - Lifetime
Non-Patent Citations (1)
| Title |
|---|
| Eweh J.A. et al., J.Am Chem. Soc. - 1987, t.109, c.6544. Brihtzinger H.-H. et al. Angem. Chem. - 1990& t.102, с.399. J.Am. Chem Soc - 1988, t.110, с.6255. Фишер Э., Вернер Г. π-Комплексы металлов. - М.: Мир, 1968, с.43. * |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2670752C2 (ru) * | 2014-09-05 | 2018-10-25 | ЭлДжи КЕМ, ЛТД. | Полимер на основе олефинов с исключительной способностью к переработке |
| RU2670752C9 (ru) * | 2014-09-05 | 2018-12-20 | ЭлДжи КЕМ, ЛТД. | Полимер на основе олефинов с исключительной способностью к переработке |
| US10344102B2 (en) | 2014-09-05 | 2019-07-09 | Lg Chem, Ltd. | Olefin-based polymer with excellent processability |
Also Published As
| Publication number | Publication date |
|---|---|
| JP3789502B2 (ja) | 2006-06-28 |
| US5576260A (en) | 1996-11-19 |
| ATE290536T1 (de) | 2005-03-15 |
| ES2238364T3 (es) | 2005-09-01 |
| CN1107854A (zh) | 1995-09-06 |
| RU94045142A (ru) | 1996-11-20 |
| EP1188763B1 (de) | 2005-03-09 |
| BR9405252A (pt) | 1995-08-01 |
| US5612428A (en) | 1997-03-18 |
| DE4344689A1 (de) | 1995-06-29 |
| JPH0867689A (ja) | 1996-03-12 |
| ES2174860T3 (es) | 2002-11-16 |
| CN1068332C (zh) | 2001-07-11 |
| US5532396A (en) | 1996-07-02 |
| DE59410406D1 (de) | 2005-04-14 |
| KR950018027A (ko) | 1995-07-22 |
| EP1188763A3 (de) | 2004-01-02 |
| DE59410090D1 (de) | 2002-05-02 |
| EP1188763A2 (de) | 2002-03-20 |
| EP0659757A1 (de) | 1995-06-28 |
| EP0659757B1 (de) | 2002-03-27 |
| ATE215091T1 (de) | 2002-04-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2142466C1 (ru) | Металлоцены, содержащая их каталитическая система, способ полимеризации олефинов, полиолефин, формованное изделие | |
| RU2144539C1 (ru) | Металлоцены, содержащая их каталитическая система, способ получения полиолефинов, полиолефин | |
| US5776851A (en) | Metallocenes, process for their preparation and their use as catalysts | |
| RU2111211C1 (ru) | Способ получения полиолефинов | |
| JP4167254B2 (ja) | アリール置換インデニル誘導体をリガンドとして含んだメタロセンの合成のための中間体およびその使用方法 | |
| US5539066A (en) | Process for the preparation of syndiotactic polyolefins having a broad molecular weight distribution | |
| US5391789A (en) | Bridged, chiral metallocenes, processes for their preparation and their use as catalysts | |
| US5679812A (en) | Compound useful for the preparation of a 1-olefin polymer | |
| US6197902B1 (en) | Syndio-isoblock polymer and process for its preparation | |
| US5216095A (en) | Process for the preparation of a polyolefin | |
| JP4771500B2 (ja) | シンジオタクチック/アタクチックブロックポリオレフィン類、それを製造するための触媒および方法 | |
| JP4017202B2 (ja) | 有機金属化合物 | |
| JP3779759B2 (ja) | メタロセン化合物及び触媒成分としてのその使用 | |
| JPH09183788A (ja) | メタロセン化合物 | |
| US5880302A (en) | Organometallic compound | |
| US5945367A (en) | Metallocenes with silyl-substituted bridges and their use for olefin polymerization | |
| JP4153062B2 (ja) | 部分的に水素化されたπリガンドを含有するメタロセン | |
| JP2001525801A (ja) | 立体剛性メタロセン化合物 | |
| RU2140922C1 (ru) | Амфотерные соединения переходных металлов, способ их получения, способ полимеризации олефинов и компонент катализатора для этого способа | |
| RU2147587C1 (ru) | Металлоцены, способ их получения, каталитическая система, способ получения полиолефинов и полимерное формованное изделие |