KR920004318B1 - 무질서화된 활성재료로 제조된 전극 - Google Patents
무질서화된 활성재료로 제조된 전극 Download PDFInfo
- Publication number
- KR920004318B1 KR920004318B1 KR1019840006827A KR840006827A KR920004318B1 KR 920004318 B1 KR920004318 B1 KR 920004318B1 KR 1019840006827 A KR1019840006827 A KR 1019840006827A KR 840006827 A KR840006827 A KR 840006827A KR 920004318 B1 KR920004318 B1 KR 920004318B1
- Authority
- KR
- South Korea
- Prior art keywords
- hydrogen storage
- atomic percent
- electrode
- composition
- storage electrode
- Prior art date
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/24—Electrodes for alkaline accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/04—Construction or manufacture in general
- H01M10/0413—Large-sized flat cells or batteries for motive or stationary systems with plate-like electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/04—Construction or manufacture in general
- H01M10/045—Cells or batteries with folded plate-like electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/34—Gastight accumulators
- H01M10/345—Gastight metal hydride accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/24—Electrodes for alkaline accumulators
- H01M4/242—Hydrogen storage electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/24—Electrodes for alkaline accumulators
- H01M4/26—Processes of manufacture
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
- H01M4/383—Hydrogen absorbing alloys
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M6/00—Primary cells; Manufacture thereof
- H01M6/04—Cells with aqueous electrolyte
- H01M6/06—Dry cells, i.e. cells wherein the electrolyte is rendered non-fluid
- H01M6/10—Dry cells, i.e. cells wherein the electrolyte is rendered non-fluid with wound or folded electrodes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P70/00—Climate change mitigation technologies in the production process for final industrial or consumer products
- Y02P70/50—Manufacturing or production processes characterised by the final manufactured product
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S420/00—Alloys or metallic compositions
- Y10S420/90—Hydrogen storage
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Secondary Cells (AREA)
- Electrodes For Compound Or Non-Metal Manufacture (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Electrolytic Production Of Non-Metals, Compounds, Apparatuses Therefor (AREA)
Abstract
내용 없음.
Description
제 1a 도는 본 발명의 전극을 사용한 평탄형 셀의 실시예의 측면도.
제 1b 도는 제 1a 도에 도시된 본 발명의 다수의 셀들의 사용한 전지의 측면도.
제 1c 도는 본 발명의 전극을 사용한 젤리 롤형 셀(Jall roll cell)의 실시예의 측면도.
제 1d 도는 본 발명의 전극을 시용한 권취(wound)형 셀의 실시예의 평면도.
제 1f 도는 스풀형 셀의 구성요소들을 도시한 본 발명의 리본(ribbon)의 평면도.
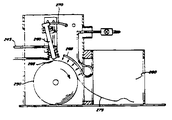
제 2 도는 급속응고처리에 사용되는 장치의 개략적인 측면도.
제 3 도는 본 발명의 전극상에 콜렉터를 데포지트시키는 장치의 블록도.
제 4 도는 티타늄-니켈-알루미늄-바나듐의 조성상태로 이루어진 본 발명의 리본전극의 지니는 셀에 관한 사이클 수명(cycle life) 대 셀 용랭의 그래프.
제 5 도는 본 발명의 리본전극을 지니는 다수의 셀들에 관한 방전율(discharge rate) 대 셀 용량의 그래프.
본 발명은 개선된 전지(battery)를 이용한 에너지의 축적 및 이용의 분양에 관한 것이며, 또한 그 전지에 사용되는 전극에 관한 것이다. 보다 상세히는, 본 발명은 급속히 응고됨으로써 형성될 수 있는 무질서 활성재료를 사용하며 기계적으로 자력지지(self-supporting)하는 리본(ribbon)형 전극을 갖는 전지에 관한 것이다. 본 발명의 전지의 전극은 전기화학적에너지를 저장한 후에 방출하여 전류를 발생시키는 반면에, 그와같은 사이클중에 구조적 결착성(結着性)을 유지한다.
수소형 2차 축전지들과 연루된 모종의 연구가 수행되어 왔지만, 그러한 전지들에 최적 특성을 부여하는, 방법을 실시하기 위한 기본적인 지식도 과학서 또는 특허문헌에 보고되어 있지 않다. 그와같은 연구결과의 예로서, 미합중국특허 제 3,699,745 호 및 제 3, 824,131 호가 있으며, 또한 표제가 "A New Type of Reversible Negative Electrode for Alkaline Storage Batteries Based on Metal Alloy Hydrides"로서 1974년 제 8 차 International Power Source Conference에 수록된 기술문헌이 있다. 이러한 연구결과는 이러한 전지기술의 상업적 이용의 보급을 만연(蔓延) 시키지 못했다. 결국, 지금까지의 연구는 니켈 카드뮴과 같은 전지시스템과 비교하여 상당히 개량된 점을 시사하고 있지 않다. 따라서, 수소형 축전지 시스템을 무시되었거나 또는 포기되어 있다.
수소가 탈착가능한 전극을 사용하는 2차 전지들의 동작은 납축전지, 니켈 카드뮴 또는 그 이외의 전지시스템과는 전혀 다르다. 수소형 축전지에는 수소를 전기화학적이고도 가역적으로 저장할 수 있는 양극(anode)과 수산화니켈이라는 재료를 구성된 음극(cathod)이 일반적으로 사용된다. 이러한 양극과 음극은 알카리성 전해질내에서 서로 이격 배치되어 있다. 전류가 양극에 흐르면, 양극재료(M)는 수소를 흡수함으로써 충전된다. 즉,
M+H2O+e- → M-H+OH-
방전시에는 저장된 수소가 방출되어 전류를 발생시킨다. 즉,
M-H+OH-→ M+H2O+e-
상기 반응들은 가역성이다. 또한, 음극에서 발생하는 반응도 가역성이다. 예를들면, 수소가 탈착가능한 2차 전지에서 종래의 수산화니켈의 음극을 사용하는 경우 음극에서 다음과 같은 반응이 생긴다. 즉,
충전방응시 : Ni(OH)2+OH-→ NiOOH +H2O+e-
방전반응시 : NiOOH+H2O+e- → Ni(OH)2+OH-
수소가 전기화학적으로 탈착가능한 양극을 사용하는 전지는 종래의 2차 전지들에 비교하여 중요한 잇점을 잠재적으로 갖고 있다. 수소가 탈착가능한 양극들은 납으로 구성된 양극 또는 카드뮴으로 구성된 양극보다도 높은 비충전용량(specific charge capacity)을 제공한다. 더우기, 납 축전지들 및 니켈-카드뮴 축전지들은 저장용량이 작고 싸이클 수명이 짧기때문에 비교적 효율이 양호하지 않다. 수소형 축전지는, 이들 종래의 전자시스템보다도 에너지밀도를 높일 수 있기 때문에 바테리 동작의 자동차 및 그 이외의 이동성이 있는 용도에 특히 적합하다. 그러나, 수소형 축전지는, 사용되는 재료의 기계적구조의 연구가 충분치 않기 때문에 잠재적으로 가능한 성능을 발휘하기에는 미흡하였다.
전지를 구성하며 수소가 탈착가능한 양극에 사용되는 재료의 선택은 극히 중요한데, 그 이유는 효율적인 충/방전(charge/discharge) 싸이클을 갖기 위하여 양극이 유용한 동작 파라메타들의 범위내에서 다수의 기능을 유호하게 이행하는 것이 요구되기 때문이다. 양극재료는 충전시에 수소를 효율적으로 저장할 수 있지만, 방전반응이 개시되기까지는 자체적인 방전을 하여서는 안된다. 충전/방전반응의 가역성이 필요하기 때문에, 수소가 양극의 저장부위에 매우 높은 안정성으로 결합됨은 바람직하지 않다. 그반면에, 수소원자들과 양극재료와의 결합이 매우 불안정한 경우에도 바람직하지 않다. 충전시에, 상기 결합이 매우 불안정하다면, 해리된 수소원자들이 양극에 의해 저장될 수 있는 것이 아니라, 재결합하여 물의 전기분해의 경우와 같이 수소가스를 형성할 것이다. 이로인해, 효율저하, 전해질의 손상 및 비효율적인 충전반응이 생길 수 있다.
수소가 탈착가능한 전극의 다른 중요한 특징은 그 구조에 있다. 선행기술에 따른 수소저장재료에는 결합재가 사용되며, 결합재는 수소저장재료를 결합상태로 유지하고, 또한 수소저장재료를 그리드 콜렉터(grid collector)와 전기적 접촉상태로 유지한다. 결합재 재료 자체는 수소저장용 활성재료가 아니기 때문에 결합재의 사용은 셀(cell)의 용량을 감소시킨다. 비활성재료의 중량의 증가는 또한, 전극을 사용하는 셀의 에너지밀도를 감소시킨다.
전극이 충전되고 방전됨에 따라, 수소저장재료는 팽창 및 수축한다. 이와같은 체적변화에 의해 전극의 구조적 결착성이 붕괴될 수 있다. 수소저장재료가 그리드 콜렙터와의 전기적 접촉을 잃어버리거나 또는 그리드 콜렉터로부터 떨어져나가면 고장나는 경향이 있다. 결합재를 더 많이 사용하면 이런 문제의 발생을 지연시키며 셀의 싸이클 수명을 연장시킬 수 있지만, 셀의 용량은 감소한다.
몇몇 종류의 수소가 탈착가능한 전극들에서 생기는 다른 문제는 충/방전율이 낮다는 점이다. 전극의 표면적을 증가시키는 경우 수소 확산 거리가 단축되면 충/방전율이 증가된다. 선행기술의 전극에서는 표면적으로 증가시키기 위해 다공율(多孔率)을 증기시키고 있다. 그러나, 다공율의 증가로 인해, 전해질이 전극 부식(腐食)과 전극의 구조적 결착성의 저하를 생기게 할 수 있다. 다시, 전극의 재료가 붕괴하고 그리드 콜렉터로부터 떨어져나가기 때문에 전극이 조기에 고장난다. 이러한 문제를 해결하기 위해 표면을 피박으로 보호하여 활성재료의 탈락(脫落)현상을 방지하는 제안도 시도되었지만, 어떠한 피막도 필요한 다공율을 감소시키기 때문에 유효한 해결방안이라고는 할 수 없다.
2차 전지들에 수소를 이용하려는 종래의 여러가지 제안은, 수소저장재료들을 사용한 경우 전극의 구조적 및 전기적 결착성이 양호하지 않기때문에 어느 제안도 성공하지 못한채로 종결되었다. 본 발명은, 높은 충/방전율, 고효율적인 가역성과 높은 전기적효율과, 본질적인 구조의 변화 또는 독물(毒物)발생을 수반하지 않고서의 다량의 수소저장고, 긴 싸이클 수명에 걸쳐서의 기계적 결착성의 유지와, 그리고 심원한 방전용량과를 허용하는 활성재료와 기계적구조를 갖는 전극의 사용하며, 새롭고 개량된 전지를 제공한다.
본 발명은 무질서화된 활성재료를 사용하는 전극을 포함한다. 본 발명에 의하면, 전술된 바와같은 선행기술의 전기화학적 셀들의 문제들이 해결되고, 또한 모든 셀의 전기화학적 성능이 개선된다.
무질서화된 재료는 티타늄 및 니켈을 포함하는 것이 바람직하며, 지로코늄, 알루미늄, 주석, 인듐, 납, 희토류금속(rare earth metals), 코발트, 크롬, 구리, 철, 바나듐, 니오븀, 마그네슘, 몰리브덴, 팔라듐, 실리콘, 붕소, 탄소 및 하프늄으로 이루어진 그룹으로부터 선정된 적어도 한 종류의 다른 원소를 포함하는 것이 바람직하다.
본 발명은 전해질을 포함하는 전기화학적 셀에 사용되는 전극을 제공하는데, 상기 전극은 실질적으로 비다공성, 또는 전해질의 불투과성인 활성재료를 포함한다.
본 발명은 또한, 적어도 하나의 에너지 저장용 전극수단을 포함하는 전기화학적 셀을 제공한다. 상기 전극수단은 무질서화된 활성재료로부터 형성된다. 이러한 셀은 또한, 상기 전극수단에 저장된 에너지를 방출하기 위한 적어도 하나의 대극(對極)수단을 포함한다. 상기 대극수단은 셀내에 배치되어 있고 전극수단과 작용적인 접촉할 수 있게 간격을 두고 있다. 또한, 상기 셀은, 전극수단과 대극수단과를 내장하는 케이싱(casing)을 포함한다.
또한, 자력지지(self-supporting)하는 전극을 사용하는 전기화학적 셀의 조립방법이 제공되는데, 상기 조립방법은 무질서화된 활성재료를 제조하는 단계와 상기 재료를 셀 케이싱내의 미리 결정된 위치에 정렬시키는 단계를 포함한다. 본 발명은 또한 전극의 제법을 제공하는데, 그러한 제법은 무질서화된 활성재료들을 급속응고(急速凝固) 시키는 단계를 포함한다.
따라서, 본 발명의 첫째 목적은 전기화학적 셀에서 사용되는 전극을 제공하는 것이다. 그 전극의 특징은 무질서화된 활성재료로 이루어진다는 점이다.
본 발명의 둘째 목적은 전해질을 포함하는 전기화학적 셀에서 사용되는 전극을 제공하는 것이다. 그 전극 특징은 활성재료가 실질적으로 전해질의 불투과성이 있다는 것이다.
본 발명의 세째 목적은 적어도 하나의 에너지 저장용 전극수단과, 이 전극수단에 저장된 에너지를 방출하기 위한 적어도 하나의 대극(對極)수단을 포함하는 전기화학적 셀을 제공하는 것이다. 상기 대극수단은 전극수단과 작용적인 접촉을 할 수 있게 간격을 두고 있다. 셀은 또한, 전극수단과 대극수단을 내장하는 케이싱을 포함한다. 그 전극수단의 특징은, 전극이 무질서화된 활성재료로 이루어진다는 점이다.
본 발명의 네째 목적은 자력지지하는 전극을 사용한 전기화학적 셀을 조립하는 방법을 제공하는 것이다. 그 방법 특징은 무질서화된 활성재료를 제조하는 단계와, 상기 전극을 셀 케이싱내의 미리 결정된 위치에 정렬시키는 단계를 포함하는 것이다.
본 발명의 다섯번째 목적은 전극의 제법을 제공하는 것이다. 그 방법의 특징은 무질서화된 활성재료를 급속응고시키는 단계를 포함하는 것이다.
일반적으로는, 본 발명은 급속응고시킴으로써 형성되는 것이 바람직한 무질서화된 활성재료를 포함하는 전극을 제공한다. 이와같이하여 형성된 재료는 전극으로서 사용된 다음에도 결합체를 필요로하지 않음으로써, 자력지지되는 것으로 생각된다. 이러한 재료는 또한 비다공성이며 전해질을 통과시키지 않는다. 상기 티타늄 및 니켈은 포함함과 아울러, 지르코늄, 니오븀, 하프늄 또는 바나듐과 같은 적어도 하나의 다른 원소를 포함한다. 이와같은 신규한 전극을 포함하는 전기화학적 셀에는 여러 부류의 대극계(對極系), 특히 전해질을 사용할 수 있다. 본 발명의 전극은 셀의 현저한 용량 저하를 수반하지 않고서 싸이클 수명을 대단히 향상되게 한다. 결합제와 같은 불활성 전극재료를 필요로하지 않기 때문에, 본 발명의 전극을 포함하는 셀의 에너지밀도는 상당히 증가된다.
특히, 본 발명의 전극은 무질서화된 재료를 제공한다. 본 명세서는 수소저장재료를 사용하는 신규한 전극에 대해 기술하고 있지만, 본 발명은 이것에만 한정하지 않고, 에너지의 발생 및 저장을 이행하는 다른 전지화학적시스템의 전극에서 사용되는 재료들도 포함한다. 따라서, 상기 무질서화된 재료는 수소를 저장한 다음에 적어도 일부를 방출하여 전자(電子)의 공급을 이행하는 수단을 포함할 수 있다. 그와같이 무질서화된 재료는 수소를 해리시키는 촉매 활성부위의 밀도와 수소저장부위의 밀도를 증가시킴으로써 전극의 전기화학적 성능을 향상시키기 위하여 설계된 적절한 국부적 화학환경을 지닌다.
무질서화된 재료는 단상 결정 격자의 대칭성 또는 화학양론(化學量論)에 의하여 제약을 받지 않기때문에 조작하기에 극히 적합하다. 조작을 구속하고 단상 결정 대칭성을 갖는 재료를 사용치 않게되면, 전기화학적 수소저장에 관련된 국부적인 구조 및 화학환경을 대폭적으로 변경시켜서 수소저장전극의 특성을 현저히 향상시킬 수 있다.
본 발명이 의도한 향상된 전기화학적 수소저장 특성을 얻기 위한 국부적 구조의 화학환경을 제공하는 무질서화된 구조체로서는 장거리 조성질서가 없는 다결정질 재료, 미소결정질(微小結晶質)재료, 비정질(非晶質)재료 또는 비정질상 및 결정상을 모두 포함하는 다상(多相)재료가 포함된다. 본 발명에 의한 무질서화된 구조체는 1. 장거리 조성질서가 없는 다결정성 재료, 2. 미세결정질 재료, 3. 다결정질상과 미세결정질상을 혼합한 것, 4. 다결정질상 또는 미세결정질상과 비정질상을 혼합하는 것, 5. 하나 또는 그 이상의 비정질상을 포함하는 비정질재료와 같이 분류된다.
이와같이 무질서화된 재료의 한 잇점은, 상기 조성상태로 인해, 구성성분의 원소의 함유 퍼센트를 사실상 연속적으로 변경시켜 그 재료, 결과적으로는 전극의 구조적 결착성을 향상시킬 수 있다는 점이다. 전극의 구조에 고도의 기계적 결착성을 제공하면, 전극의 싸이클 수명이 대폭적으로 연장된다. 더우기, 이와같은 무질서화된 재료를 사용하면, 전극의 구조적 결착성을 유지하면서 셀의 용량을 최대화할 수 있다.
본 발명의 전극을 사용한 셀의 용량의 싸이클 수명을 향상시킨 다음에는, 충전율 및 방전율의 특성도 또한 최적화될 수 있다. 상기 특성들은 전압과 시간의 관계를 충전율 및 방전율의 함수로서 설명한다. 본 발명의 전극의 폭과 두께는 표면적 대 체적의 비율을 제어하기 위하여 조정될 수 있으며, 따라서 이러한 조정에 의해 충전율-방전율의 특성이 변화한다. 본 발명의 재료는 이방성 크기를 지니며, 이것은 재료가 축을 따라 서로 다른 방향에서 측정된 경우에 상이한 길이를 나타내는 것을 의미한다. 따라서, 상기 재료는 대체로 상이한 길이, 폭 및 두께의 수치를 지니거나, 또는 최소한 길이 및 폭이 재료의 두께보다 훨씬 큰 수치를 지닌다. 적절한 이방성 재료의 예는 리본, 와이어(wire) 또는 시트(sheet)등이 있지만, 다른 형상(形狀)도 가능하다. 상기와 같은 크기와 형상을 갖는 전극 및 이러한 전극으로부터 만들어진 전지는, 용도에 따라 결정되며, 임의의 크기, 형상, 용량등의 전지일 수 있다. 상기 재료의 두께는 약 50미크론 미만인 것이 바람직하다. 상기 재료는 하나의 연속체로 제조한 후에 소망의 길이로 절단하여도 좋다.
선행기술의 분말전극은 충전율 및 방전율의 특성을 향상시키기 위하여 다공율 및 입자크기를 조정하여야 한다. 본 발명은 이와같은 구속이 없으며, 충전율-방전율의 특성을 증가시키기 위하여 재료의 다공성을 증가시키지 않는다. 부식과 구조의 붕괴에 대한 문제는, 다공성을 증가시키지 않으면 최소화된다. 본 발명의 전극으로서 사용되는 재료는 거의 비다공성이며 전해질이 통과하지 않도록 형성될 수 있으므로해서, 부식의 문제는 최소화된다. 따라서, 재료의 구조적 결착성이 유지되고, 그 결과 긴 싸이클이 보장된다.
본 발명에서는 다공성을 재료의 평균 기공 크기로서 고려할 수 있다. 본 발명의 경우 이러한 평균크기는 0.001미크론보다 작다. 변형적으로는, 임의의 종래방법, 예컨대 수은침입법(Mercury Intrusion Method)에 의해 측정된 재료의 총체적인 다공성으로서 나타내면, 이러한 것은 상기 재료의 체적당 약 5% 미만이다.
재료의 다공성과 본 발명 재료에 존재할 수 있는 공부(void space)와는 명확히 구별할 필요가 있다. 다공성(porosity)은 고체를 관통하는 미세통로, 즉 고체의 개방공간인 기공을 포함하는 성질을 나타낸다. 또한, 다공성은, 이와같은 기공이 점유하는 전체 체적을 의미한다. 공부(空部)는 고체내의 밀폐된 공간이며 고체를 관통하는 통로로서 존재하지 않는 경우에 사용된다. 공부는 재료밀도에 영향을 줄 수 있지만 다공성율에는 영향을 주지 못한다.
본 발명은 융기(ridge), 주름 및/또는 재료를 관통하는 구멍을 지니며, 따라서 이방 항장력 특성(anisotropic tecsile property)을 제공하는 불규칙한 표면을 형성한다. 이들 구멍이나 재료내의 다른 거대통로는 상기한 공부와는 구별되어야 한다.
본 발명의 전극을 만드는데 사용되는 재료의 밀도와 전극의 체적밀도(bulk density)는 성행기술의 재료 또는 이러한 재료로 제조된 전극의 밀도에 비해 상당히 크다. 재료 또는 전극의 밀도는 5g/cc이상, 8g/cc이하인 것이 바람직하고, 최적치로는 약 6-7.5g/cc의 범위이다. 본 발명재료는 혼합상의 다결정질 잉고트(ingot)형태의 재료의 밀도의 약 90%보다 더 큰 밀도를 지니는 것이 바람직하다. 전극의 체적 밀도는 활성재료의 밀도와 이 활성재료를 다중층으로 또는 권취한 것의 패킹밀도에 의해 결정된다. 패킹 밀도(packing clensity)란 결합제와 같은 다른 전극재료 또는 기공 및/또는 공부형태의 공간 대신에 활성재료로 체워진 전극공간의 백분율이다. 본 발명에서는 패킹밀도가 80% 이상일 수 있다.
본 발명은 수소를 흡수 및 저장함으로써 충전하고, 이후로 전자를 공급하도록 축전된 수소의 적어도 일부를 방출하는 무질서화된 재료의 조성을 포함한다. 적당한 조성물은 지르코늄, 알루미늄, 바나듐, 니오븀, 마그네슘, 몰리브덴, 팔라듐, 실리콘, 붕소, 탄소, 하프늄, 주석, 인듐, 납, 희토류금속, 코발트, 크롬으로 이루어진 그룹으로부터 선택된 적어도 한 원소와 티타늄과 니켈을 포함한다. 다른 적당한 이원조성물(二元祖成物)은 바나듐, 니오븀, 실리콘, 붕소 또는 탄수중 어느 하나와 니켈을 포함하며, 바람직하게는 상기 선택된 원소들의 적어도 하나와 함께 니켈을 포함한다.
유용한 삼원조성물은 티탄늄, 니켈, 및 알루미늄으로부터 이루어진다. 상기 삼원화합물에 부가되는 적어도 하나의 부가적인 원소는 니오븀, 지르코늄, 바나듐 및 하프늄으로 이루어진 그룹으로부터의 선택된 것이다.
재료에 내재하는 상기 원소들의 적당한 농도는, 원자백분율로 표시하면, 티타늄 40-70%, 니켈 15-55%, 알루미늄이 최소한 미량에서 15%를 넘지않는 량을 포함한다. 바람직하게는, 원자백분율로 나타낼때, 티타늄 44-60%, 니켈 35-40%, 및 알루미늄 3-5%와 같은 량을 포함한다.
삼원조성물은 바람직하게는 니오븀 또는 바나듐 또는 니오븀과 바나듐을 부가적인 원소로 포함할 수 있다. 다른 적당한 원소는 지르코늄, 크롬, 코발트, 구리, 그리고 철이다. 부가적인 원소의 량은 원자백분율로 나타낼때 약 11%을 초과하지 못하며, 또는 바람직하게는 약 3-5%이다.
4원조성물은 니켈, 티타늄, 니오븀 그리고 지르코늄으로 이루어진다. 이러한 원소들의 적당한 농도는 원자백분율로 나타낼 경우, 티타늄 5-55%, 니켈 30-60%, 니오븀 10-20%, 지르코늄 3-10%이다. 상기 4원조성물을 부가적으로 원자백분율로 나타낼때, 약 5%의 바나듐을 포함할 수 있다.
본 발명은 또한 에너지를 축적하는 적어도 하나의 전극장치를 포함하는 전기화학적 셀을 포함한다. 전극장치는 무질서화된 활성재료로부터 형성된다. 상기 무질서화된 재료는 전술된 조성물의 구조의 것이다. 상기 셀은 또한 전극장치에 축적된 에너지의 방출용으로 제공하는 최소한 하나의 대극(counter electrode)를 포함한다. 대극장치는 전극장치와 접촉하여 작용하도록 떨어져있다. 상기 셀은 또한 전극장치와 대극장치가 내부에 설치된 케이싱을 포함한다. 대극장치는 전극장치 및 대극장치와 접촉하여 작용하도록 담겨있는 전해질을 포함한다. 상기 셀들이 다수 모여 전지를 이룬다. 특히, 각각의 셀이 효율적인 가역성의 수소흡수 및 탈착용의 적어도 하나의 양극장치를 포함하여 수소축전지를 형성할 수 잇다. 적어도 하나의 음극장치가 가역성의 산화용으로 제공된다.
본 발명의 전극을 이용한 다양한 전기화학적 셀의 실시예들이 고려될 수 있다. 제 1a 도에 있어서, 도시된 평탄한 셀(10)은 앞에서 언급된 재료의 다수의 거의 평탄한 박판(15)들을 사용한다. 박판들(15)사이에 끼워져 있는 다수의 납작한 탭(tab)(20)은 박판(15)들의 모서리 너머로 연장되어서 버스(buss) 탭(25)들의 각각 전기적으로 접촉시키기 위하여 사용된다. 버스탭(25)은 박판(15)들과 탭(20)들과 탭(20)들을 함께 압착시키도록 성형되었다. 탭들(20)과 버스탭(25)은 니켈과 같은 적당한 전도체 재료로 만들어져 있다. 평탄형 셀(10)은 대체로 평탄하며 다수의 박판(15)들과 접촉하여 작용하게 배치되어 있는 대극장치(30)를 포함한다. 격리판(35)은 대극장치(30)와 박판들(15)사이에 배치되어 있다.
두번째의 다수의 대체로 평탄한 박판(40)들은 첫번째의 다수의 박판(15)들의 맞은편상에서 대극장치(30)와 접촉하여 작용되게 이격되어 있다. 다수의 두번째 평탄한 탭(45)들이 박판(40)들 사이에 비슷하게 삽입되어 있으며, 두번째의 버스탭(50)이 사용되었다. 두번째 격리판(55)이 탭들(45)의 각각과 대극장치(30)를 전기적으로 접촉시키기 위한 다수의 두번째 박판(40)사이에 배치되어 있다.
제 1a 도의 셀(10)은 플라스틱 덮개(60)와 같은 적당한 재료로 밀폐되어 있어서 상기 덮개(60)는 사용된 전해질과 접촉하여 변질되지 않으며 작용중에 셀(10)이 가스를 배출하도록 허용한다. 첫번째와 두번째 버스탭(25,50)들을 셀(10)의 플라스틱 덮개(55)밖으로 뻗어있는 제 1 세트의 리이드(lead)(65)에 전기적으로 연결되어 있다. 마찬가지로, 제 2 의 리이드(70)는 대극장치(30)에 전기적으로 연결되어 있으며 셀 플라스틱 덮개(60)밖으로 뻗어 있다.
제 1a 도의 셀(10)과 비슷한 다수의 셀들이 제 1b 도에 도시된 전지(75)로서 조립될 수 있다. 전지케이싱(80)은 개별적인 셀들을 포함하며 공동으로 부호(85)로 표시되어 있다. 케이싱(80)은 셀(85)들의 작용중에 과도한 가스를 배출하기 위한 배출장치(90)을 포함한다. 셀(85)들은 덮개(60)로 이미 밀폐되어 있기 때문에 케이싱(80)을 지닌 개별적인 셀벽들을 형성시킬 필요가 없어 케이싱(80)의 공간과 중량을 감소시킨다. 케이싱(80)은 강성재료 또는 에폭시(epoxy)와 같은 경화될 수 있는 재료로 만든다. 셀(85)들은 쉽게 중첩되어(도시되지않음) 모울드(mould)에 넣어지고 경화재료가 쌓여진 셀(85)들의 주변둘레로 도입된다. 첫번째와 두번째 리이드(65, 70)는 케이싱(80)을 통하여 연장되어 외부와의 연결용으로 쓰일 수 있다.
제 1c 도에 도시된 젤리형 셀(100)은 축(105)에 대해서 평탄형 셀을 나선형으로 감아서 만들어져 있다. 상기 셀(100)은 앞에서 설명된 다수의 박판(115)들과 삽입된 탭(100)을 접촉시키는 (도시되지않은) 전도성 접착제를 담고있는 캔(can)에 넣어질 수 있다. 격리판(120)은 박판(115)들과 대극장치(125) 사이에 끼워져 있다.
제 1d 도에 도시된 다른 셀 실시예는 평탄한 장방형 대극장치(155)를 포함하는 권취형 셀(150)을 보여준다. 격리판(160)은 대극장치(155)를 덮고 있다. 리본형태의 재료(165)는 대극장치(155) 둘레에 감겨져 있다. 감은 모습은 화살표(170)로 도시된 방향으로 이중으로 사선으로 감은 것이다. 이렇게 감은 것은 그 자체를 단단하게 조이는 대신에 감은 것을 풀지않고 셀(150)을 굽히는 것을 허용한다. 리본(165)이 대극장치(155)의 모서리(175)들에서 구부러지는 것을 막기 위하여 톱니형상(180)은 리본(165)이 모서리(175)에 바로 얹혀있도록 허용한다. 다른 적당한 실시예는 비-사선의 권취물상에서 평탄한 모서리를 사용한다.
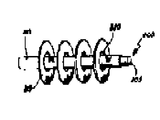
제 1e 도는 로드(rod)형 대극(205)을 포함하는 스풀형 셀(200)을 도시하고 있다. 격리판(210)이 대극(205)을 덮는다. 본 발명 재료는 각기 구멍(220)을 지니는 다수의 와셔(washer)형 몸체(215)로서 형성되어 있다. 대극(205)은 차례로 쌓여있는 각기 몸체(215)의 구멍(220)을 통하여 삽입된다. 와셔형 몸체(215)는 제 1f 도에 도시된 바와같이 리본(225)과 같이 형성된 재료에서 절단되어 형성될 수 있다. 몸체(215)는 지점(230)에서 연결되며 그다음 구멍(220)을 통하여 대극(205)을 삽입하기전에 차례로 접혀진다.
본 발명의 무질서화된 재료는 급히 응고시킴으로서 바람직하게 마련된다. 급속한 응고는 여러가지의 형태의 불평형 배치재료의 원자배열에서 원자위치를 고정시키기 위하여 충분히 큰 소입(quench) 속도로 액상(liquid state)으로부터 고상(solid state)으로재료를 급히 소입하는 방법 및 공정이다. 앞에서 설명된 바와 같이 그렇게 생산된 무질서화된 재료는 많은 형태의 구조들중 한가지 형태를 이룬다. 상기 구조는 특히 사실상 비정질이거나 또는 장거리 범위의 원자의 무질서가 없는 성격상 일반적으로 비정질의 복수상 재료이며, 또한 미세결정질 및 또는 다결정질 함유물과 같은 약간 국부적으로 원자가 질서를 가진 구조를 포함한다. 특히, 비정질은, 장거리 범위의 무질서를 갖는 합금 또는 재료이나, 그것은 짧은 또는 중간정도의 질서 또는 때로는 약간의 결정질 함유물을 지닐 수 있다.
재료는 완전한 결정화가 시작될 수 있기 전에 빠른 소입 환경, 예컨데, 응고용 냉각휠로 액체상태에서 분사된다. 일반적으로, 빠른 응고공정은 박막(thin film)을 형성시키기 위하여 기판에서 낮은 속도의 입자이동으로 처리되는 스퍼터링(sputtering) 또는 진공증착과 같은 박막 데포지션 공정과는 대조적이다. 용융방적(spinning), 제트 캐스팅(casting), 다수 제트 케스팅, 또는 평면 유동 캐스팅으로서 흔히 언급되는 빠른 응고 공정들이 사용된다. 본 발명은 공정 자체의 상세한 것 또는 사용된 특별한 장치들에는 상관하지 않고 이같은 빠른 응고 공정의 사용을 포함한다. 본 발명은 아래의 방법들로 만들어진 특별한 구조 또는 재료에 제한되지 않는다. 부가적으로, 이러한 방법들로 만들어진 어떤 전극은 처음에는 충전 또는 방전된 상태로 있다.
특히, 제 2 도는 본 발명에서 고려되는 빠른 응고 공정에 사용되는 장치를 나타내는 개략도이다. 여기서 휠로서 나타나있는 냉각표면(250)은 노즐오리피스(255)에 거의 밀접하여 화살표 방향으로 이동한다. 전술된 무질서화된 재료는 유도가열기(265)에 의해 도가니(260)에서 용융상태까지 가열된다. 도가니(260)에는 노즐 오리피스(255)를 통하여 배출시키기 위하여 용융된 무질서화된 재료를 가압하는 장치(270)가 설치되어 있다. 용융된 무질서화된 재료는 분산의 균일성을 유지하기 위하여 흔들어진다. 작용중에, 용융된 무질서화된 재료는 도가니(206)의 압력하에서 지속되며 노즐 오리피스(255)를 통하여 회전 냉각휠(250)의 표면에 분사되며 이방성의 크기를 지니는 재료, 다시 말해서 리본(275)으로서 언급되는 재료를 형성시키기 위하여 즉시 응고시킨다. 리본(275)은 수집장소(280)로 향하며 이때 냉각휠(250)로부터 제거될때 연속적인 박판으로서 또는 설정된 길이로 절단될 수 있다. 이 장치는 리본이 냉각휠을 떠날때 아르곤과 같은 불활성 가스를 리본에 분사하는 다수의 가스분사기(285)를 사용한다. 이것은 소입시간을 조절할 수 있게 한다. 용융재료의 응고를 위해 다른 장치들이 사용될 수 있다.
본 발명에 의해 바람직한 무질서화된 재료들을 얻기 위하여, 냉각휠(250)의 표면은 최소한 104℃의 영역에서 소입속도를 얻을 수 있어야 한다. 상당히 낮은 초당 소입속도는 결정질 리본을 초래한다. 무질서화된 재료를 만들기위한 상당히 높은 소입속도를 얻기 위하여 10인치 직경의 냉각휠은 보통 2000-3000rpm의 범위로 회전해야 한다. 냉각휠(250)은 그 내부를 통해 순환하는 냉각액과 같은 (도시되지 않은)냉각장치가 임의로 제공될 수 있다. 본 발명의 공정은 보통 조절된 분위기에서 수행된다.
급속 응고 공정을 통해 생산되는 리본의 폭과 두께는 체적유량, 노즐 오리피스(255)의 직경, 및 냉각휠의 표면속도사이의 상관관계를 변경시킴으로써 쉽게 조절될 수 있다. 일반적으로, 노즐오리피스는 약 0.0635-0.114cm의 직경을 지니며, 냉각휠(250)위에 대략 1-2nm 떨어져 있다. 도가니(220)를 통하는 축은 냉각휠(250)의 평면의 수직으로부터 88°기울어져 있다. 일반적으로 냉각휠 표면속도의 증가는 얇은 박판을 생산하게 되며, 반대로 속도가 감소하면 두꺼운 박판을 생산하게 된다.
본 발명은 무질서화된 재료를 급히 응고시키는 단계를 포함하는 전극을 생산하는 방법을 포함한다. 바람직한 재료의 구조와 조성은 이미 앞에서 설명되었다.
상기 방법은 또한 전극이 작용할때 생산되는 전자를 수집하도록 상기 재료와 전지적으로 접촉하는 콜렉터를 두는 것을 포함한다. 콜렉터는 제 3 도에 대체적으로 도시된 장치에서 재료에 계속적으로 데포지트된다. 상기 장치는 제 3 도에 개략적으로 도시되어 있다. 상기 공정은 일괄적으로 한묶음단위로 수행될 수 있지만 연속적인 공정이 바람직하다. 콜렉터는 챔버(300)에서 재료로 데포지트된다. 재료(305)는 릴(reel)(310)로부터 공급되어 챔버(300)를 통하는 동안 콜렉터가 데포지트된다. 콜렉터가 데포지트된 다음, 재료(305)는 릴(315)로 이동한다. 상기 공정은 관찰구멍(320) 또는 감시계 또는 제어기구를 통하여 관찰될 수 있다.
본 발명은 전해질과 작용적인 접촉을 할 수 있게 리본을 연마하는 부가적인 단계를 포함한다. 상기 연마작업은 재료와 전해질과의 접촉을 방해하는, 재료표면의 어떤 물질을 제거한다.
본 발명은 재료 표면을 화학적으로 에칭함으로써 재료표면의 이물질을 제거하는 다른 방법을 포함한다. 상기의 에칭 용액은 같은 량의 질산과 HF(하프늄)과, 물이 1 : 25의 비율로 혼합된 용액이 적당하다.
이물질이 제거되면 전극을 코팅할 수 있다. 그러한 코팅은 유해한 표면층의 재형성을 막으며, 그러나 전극의 기능을 방해하지는 않는다. 코팅은 또한 활성재료의 특성을 높일 수 있다. 예를들면, 본 발명 재료를 니켈 스퍼터(sputter) 코팅하는 것은 재료의 탈착 카이네틱스(desorption kinetics)을 향상시킨다. 적당한 피복물은 또한 티타늄/니켈 및 파라듐을 포함한다. 코팅은 그러한 코팅이 없는 재료에 비하여 재료의 표면과 잔류부분사이의 전자 교환속도를 증가시키는 수단을 포함한다.
본 발명은 자력지지되는 전극을 사용한 전기화학적 셀을 조립하는 다른 방법을 포함한다. 이 방법을 앞에서 설명한, 급히 응고시킴으로써 무질서화된 재료를 생산하는 단계들을 포함한다. 또한 상기 방법은 셀케이싱의 설정된 위치에 전극을 정렬시키는 것을 포함한다. 본 발명의 전극은 연장된 사용주기에서도 구조적인 결착성을 나타내므로, 제조직후 바로 정렬될 수 있다. 따라서 본 발명의 셀에서는 케이싱의 전극을 지지하기 위하여 특별한 기계적인 구조나 또는 결합재 재료를 부가할 필요가 없다. 그러한 자력으로 지지되는 전극은 쉽게 그리고 값싸게 제조 및 조립될 수 있다.
이러한 방법은 전극을 형성시키는 중에 결합제의 사용을 피할 수 있을 뿐만아니라 전극이 소결될 필요가 없다. 소결은 종종 소결함으로 야기되는 고유의 표면적 감소로 인한 충전/방전율의 감소를 초래하여 바람직하지 못하다.
본 방법은 앞에서 기술한 바와 같이 전해질과 접촉을 위해 표면의 오염물을 제거하도록 연마하거나 또는 부식하는 것을 포함할 수 있다. 전해질과 직접적인 유효한 접촉을 위해 재료를 노출시키도록 세척하는 것이 또한 고려된다.
부가적으로, 본 방법은 전극의 작용중에 생산되는 전자들을 수집하도록 재료와 전기적으로 접촉하도록 콜렉터를 배치하는 것을 포함하며, 또한, 전술된 문제들을 경감시키도록 전극을 코팅하는 것을 포함한다.
[실시예 1]
사용된 장치는 제 2 도의 장치와 비슷하다. 사용된 냉각휠은 직경 10인치이며, 폭이 1인치로서, 구리로 만들어져 있다. 상기 냉각휠은 약 2500rpm으로 회전된다. 직경 0.0889cm의 오리프스를 지나는 노즐이 냉각휠의 원주상 표면의 이동방향에 수직으로 설치되어 있다. 도가니를 통한 축은 냉각휠 축의 평면의 수평면으로부터 88도로 경사져 있다. 냉각휠의 표면과 노즐오리피스의 틈은 0.159㎝이다. Ti 58.8 CR 4.4 Ni 25.1 Al 11.7의 조성을 지니는 재료가 사용된다. 다수의 구멍을 지니는 다기관은 가스 압력이 냉각표면과 리본사이의 접촉을 증가시키는 방식으로 아르곤(argon)를 방출한다. 다기관은 냉각휠 표면에 평행하게 위치하며 상사점으로부터 상사점 다음의 지점(45)까지 뻗어있다. 아르곤 흐름은 보통 20psi의 압력에서 사용된다. 본 발명에서 사용되는 빠른 소입기술의 상세한 것은 여기에 참고로 적으면 1976년 11월 마그네틱스의 IEEE 회의록, Vol, MAG-12, 제 6 권의 리베르만씨등의 "비정질합금리본의 생산과 리본 크기에 대한 장치 매개변수의 영향"이라는 제목의 논문과, 1980년 43재료 과학 및 공학 203-210의 리베르만씨의 "냉각 블럭 용융-방적 공정 매개변수들에 대한 유리같은 합금 리본의 기하학적 형상의 의존"이라는 제목의 논문에 소개되어 있다.
0.15-0.35g의 몇개의 전극들이 리본에서 절단되었다. 내켈탭은 리본 전극들에 연결된 전자 콜렉터 누름쇠로서 사용되었다. 대극장치는 니켈 블랭트 전극이었다. 각기 전극은 4M KOH 전해질에서, 2시간동안 250mA/g의 충전율 및 -0.7VHg/H2O 기준 전극까지 50mA/g의 방전율로 순환되었다. 어느 한 전극에 의해서 공급된 처음 7주기동안의 가장 큰 용량은 172mAh/g이었다.
[실시예 2-6]
실시예 1의 진행은 티타늄, 니켈 및 알루미늄의 삼원조성에 기초를 둔 재료를 형성하기 위해 반복되었다. 같은 설비가 사용되었으며, 공정조건의 어떤 변화는 아래의 표 I에 나타나있다. 각각의 조성의 전극들이 실시예 1의 진행을 따라 전기화학적 성능을 시험받았다. 처음 7주기 동안 측정된 어느 전극의 최대 용량만이 표 1에 보고되었다. 급한 응고 공정의 매개변수의 수가 변화될 수 있기 때문에 같은 조성을 지니는 전극들은 구조에 있어서 다를 수 있다. 따라서 상이한 공정 매개 변수로 형성된 약간의 전극들은 시험중에 부서지거나 파괴되고 균열이 생겼다. 이런 경우에서는 본은 측정되지 않았으며 여기에 보고되지 않았다.
[표 1]
[실시예 7-11]
티타늄, 니켈, 알루미늄 및 바나듐 또는 지르코늄중 하나의 사원조성의 기초하에서 리본 전극을 형성하기위해 실시예 1의 진행의 반복되었다. 같은 설비가 사용되었으며 공정조건의 변화는 표 2에 적혀있다. 각 조성의 몇개의 전극은 실시예 1의 진행을 따라 전기화학적 성능을 시험받았다. 처음 7주기동안 측정된 어떤 전극의 최대 용량만이 표 2에 보고 되어 있다.
[표 2]
충전-방전 싸이클 시험은 전극의 싸이클 수명을 측정하기 위하여 실시예 9까지 연장되었다. 제 4 도는 315싸이클이 완전히 끝난 다음에도 용량이 현저하게 감소되지 않았다. 사실, 용량은 93-103주기와 305-315주기들을 비교하면 오직 약 13%만이 감소되었다. 각기 주기에 대하여 충전율은 2시간동안 250mA/g이며 방전율은 -0.7V까지 500mA/g이었다. 처음 93주기에 대하여 전극은 총용량의 56%까지 충전되었고, 그런다음 총용량에까지 충전되었다. 시험은 316주기에서 종결되었다.
실시예 9의 밀도는 공기중에서 리본의 중량을 측정하고 이어서 공지된 밀도의 유체에서 리본의 중량을 측정함으로써 계산되었다. 특히 이소 프로필알콜이 상기 유체로서 사용되었다. 리본의 밀도는 거의 5.9g/cc가 계산되었다.
[실시예 13-19]
실시예 1의 진행이 티타늄, 니켈, 니오븀의 3원조성물을 기초로 하여 리본 전극들을 형성하도록 반복되었다. 알루미늄, 지르코늄, 바나듐, 하프늄과 같은 다른 원소들이 또한 상기 3원 조성물에 따른 결합으로 부가되었다. 같은 설비가 사용되었으며 공정 조건의 어떤 변화도 아래의 표 3에 적혀있다. 각기 조성물이 여러 전극들이 실시예 1의 진행을 따라 전기화학적 성능을 시험받았다. 처음 7주기동안에 측정된 어떤 전극의 용량의 최대치가 표 3에 보고되어 있다.
[표 3]
실시예 17의 밀도는 리본의 중량을 공기중에서 측정하고 이어서 알려진 밀도의 유체에서 측정함으로써 계산되었다. 특히, 이소프로필 알콜이 상기 유체로서 사용되었다. 리본의 밀도는 거의 6.7g/cc로 계산되었다.
HF : H2O의 비율이 1 : 20인 용액이 준비되어 15분동안 실시예 17을 식각시키도록 사용되었다.
식각시키기 전과 후의 실시예 17의 3개의 전극들용 절반(half)셀용량이 2개의 방전율 51 및 257mA/g에서 표 4에 나타나있다. 식각된 전극들용 반셀 용량의 증가가 명백히 설명되어 있다.
[표 4]
실시예 15의 절반셀 용량은 제 5 도에 도시된 변하는 방전율에서 측정되었다. 첫번째의 방전율은 10주기동안 측정되며, 각기 후속적인 방전율은 7주기동안 측정되었다. 여기의 자료점들은 최종 5주기동안의 세전극들의 평균치이다.
[실시예 20과 21]
실시예 1의 진행이 티타늄 및 니켈과 여러 결합에 부가되는 주석, 지르코늄, 바나듐, 및 알루미늄과 같은 다른 원소를 지닌 2원 조성물을 기초로한 전극을 형성하도록 반복된다. 같은 설비가 사용되며, 공정조건에서 어떤 변화는 아래 표 5에 적혀있다. 각기 조성물의 전극들은 실시예 1의 진행을 따라 전기화학적 성능을 검사받는다. 처음 7주기 동안에 측정되는 전극의 초대용량들이 표 5에 보고되어 있다.
[표 5]
본 실시예들에 의해 도시된 바와 같이, 본 발명 전극을 사용함으로써 많은 이로운 점이 있다. 전극이 자력지지되기 때문에 전극에 구조적인 결착성을 주기 위하여 결합제 재료를 사용할 필요가 없다. 이것은 불활성 재료가 덜 사용되기 때문에 전극에 에너지 밀도가 빨리 얻어진다. 전극재료의 본래의 구조적 모습을 저하 및 손상시키지 않고 다공성의 증가없이도 셀용량이 증가될 수 있다. 전극의 전기화학 수행은 전지 용량의 증대한 감소없이 싸이클 수명이 연장되는 것을 나타낸다.
싸이클중에 본래의 구조적인 결착성을 유지하는 재료를 지니기 때문에 재료는 셀의 용량을 최대화시키는 유연성을 허용한다. 전극구조는 또한 수소의 흡수와 탈착증에 구조적인 저하없이 반복되는 체적확장과 수축을 허용한다. 전극은, 표면적대 체적의 비율이 전극의 두께와 폭을 변화시킴으로써 조절될 수 있기 때문에 충전율 및 방전율을 극대화를 허용한다.
일반적으로, 전극은 축전지 케이싱에 쉽게 정렬될 수 있도록 유연성이 있다. 전극을 정렬하기 위한 결합제 또는 특별한 구조적인 장치를 필요로하지 않기때문에 본 발명 전극을 전지에 조립하여 사용하는 것을 간단하며 비용은 많이들지 않는다.
본 발명의 많은 다양한 실시예가 있을 수 있으며, 따라서 본 발명은 첨부된 특허청구범위의 영역안에서 명세서에 기재된 것과 다르게 실시할 수 있는 것도 포함한다.
Claims (33)
- 자력 지지될 수 있으며 용융물이 빠르게 고화되었음으로해서 전체적으로 연속한 비정질 구조를 갖는 것으로 특징되는 비입자상의 이방성 형태를 가지는, 금속성이며 비정질인 최소한 하나의 전기화학적 고상활성체로 구성되며; 상기 활성체는 알루미늄, 붕소, 크롬, 코발트, 하프늄, 인듐, 납, 마그네슘, 몰리브레늄, 니오븀, 팔라듐, 주석, 지르코늄 및 희토류로 구성된 그룹으로부터 선택된 최소한 하나의 원소, 티타늄 및 니켈로 구성된 최소한 세가지 원소로 이루어진 조성을 지니며, 전극이 전기화학적 충전 및 방전 주기동안 구조적인 결착성을 유지하면서 에너지를 저장하기위해 전기화학적으로 수소를 흡수할 수 있으며 전기화학적으로 수소를 내보내므로써 에너지를 방출시킬 수 있도록, 이들 각각의 원소들이 유효량만큼 존재하는; 수소 저장 알칼리 전기화학전지용 수소 저장 전극.
- 제 1 항에 있어서, 상기 활성체의 조성물은 티타늄, 니켈 및 알루미늄을 포함하는 수소 저장 전극.
- 제 2 항에 있어서, 상기 활성체의 조성물은, 니오븀, 크로뮴, 바나듐, 코발트, 구리, 철, 지르코늄 및 하프늄으로 이루어진 그룹으로부터 선택된 최소한 하나의 원소를 포함하는 수소 저장 전극.
- 제 1 항에 있어서, 상기 활성체의 조성물은 약 40 내지 60원자 퍼센트의 티타늄, 약 15 내지 55 원자 퍼센트의 니켈, 및 미소량 내지 약 15원자 퍼센트의 알루미늄을 포함하는 수소 저장 전극.
- 제 1 항에 있어서, 상기 활성체의 전체적인 디공율은 체적의 약 5%미만인 수소 저장 전극.
- 제 1 항에 있어서, 상기 활성체의 조성물은 40 내지 약 75원자 퍼센트으 티타늄, 15 내지 55원자 퍼센트의 니켈, 및 미소량 내지 15원자 퍼센트의 알루미늄을 포함하는 수소 저장 전극.
- 제 6 항에 있어서, 상기 활성체의 조성물은, 니오븀, 크로뮴, 코발트, 구리, 철, 지르코늄, 바나듐 및 하프늄으로 이루어진 그룹으로부터 선택된 최소한 하나의 부가적인 원소를 포함하되, 최대 약 11원자 퍼센트로 존재하는 수소 저장 전극.
- 제 7 항에 있어서, 상기의 부가적인 원소는 약 3 내지 5원자 퍼센트의 양으로 존재하는 수소 저장 전극.
- 제 1 항에 있어서, 상기 활성체의 조성물은 44 내지 60원자 퍼센트의 티타늄, 35 내지 40원자 퍼센트의 니켈, 및 3 내지 5원자 퍼센트의 알루미늄을 포함하는 수소 저장 전극.
- 제 9 항에 있어서, 상기 활성체의 조성물은 5 내지 11원자 퍼센트의 니오븀을 포함하는 수소 저장 전극.
- 제 10 항에 있어서, 상기 활성체의 조성물은 약 5원자 퍼센트의 바나듐을 포함하는 수소 저장 전극.
- 제 1 항에 있어서, 상기 활성체의 조성물은 티타늄, 니켈, 니오븀 및 지르코늄을 포함하는 수소 저장 전극.
- 제 12 항에 있어서, 상기 활성체의 조성물은 바나듐을 포함하는 수소 저장 전극.
- 제 12 항에 있어서, 상기 활성체의 조성은 5 내지 약 55원자 퍼센트의 티타늄, 30 내지 60원자 퍼센트의 니켈, 10 내지 20원자 퍼센트의 니오븀, 및 3 내지 10원자 퍼센트의 지르코늄을 포함하는 수소 저장 전극.
- 제 14 항에 있어서, 상시 활성체의 조성물은 약 5중량 퍼센트의 바나듐을 포함하는 수소 저장 전극.
- 제 11 항에 있어서, 상기 활성체는 재충전이 가능한 수소 저장 전극.
- 제 1 항에 있어서, 상기 활성체는 주로 티타늄, 니켈, 니오븀, 및 지르코늄으로 이루어지는 수소 저장 전극.
- 제 1 항에 있어서, 상기 활성체는 필수적으로 티타늄, 니켈, 니오븀, 지르코늄, 및 바나듐으로 이루어지는 수소 저장 전극.
- 제 1 항에 있어서, 상기 최소한 하나의 부가적인 원소는 하프늄, 인듐, 납, 몰리브데늄, 및 주석으로 이루어진 그룹으로 선택된 수소 저장 전극.
- 자력 지지될 수 있으며 용융 상태로부터의 급속한 응고로 형성될 수 있으므로써연속적인 비정질 구조로 특징지워지는 비일자상의 이방성을 지닌 최소한 하나의 고상 비정질 활성체를 포함하고, 상기 활성체는 필수적으로 최소한 3가지의 원소로 이루어지고, 상기의 원소는 지르코늄, 알루미늄, 주석, 인듐, 납, 희토류 금속, 코발트, 크로뮴, 구리, 철, 바나듐, 니오븀, 마그네슘, 몰리브데늄, 팔라듐, 붕소 및 하프늄으부터 선택된 최소한 하나의 원소와 타타늄 및 니켈이고, 각각의 상기 원소들은 유효량으로 존재함으로써 상기 수소 저장 전극은 전기화학적 충전, 방전 주기동안 구조적인 결착성을 유지하면서 에너지를 저장하도록 수소로써 전기화학적으로 충전될 수 있고 수소를 배출시켜 에너지를 방출할 수 있는 수소 저장 알칼리 전기화학전지용 수소 저장 전극.
- 제 20 항에 있어서, 상기 활성체의 전체적인 다공성은 체적의 약 5% 미만인 수소 저장 전극.
- 제 20 항에 있어서, 상기 활성체의 조성물은 주로, 40 내지 75원자 퍼센트의 티타늄, 15 내지 55원자 퍼센트의 니켈 및 미소량 내지 약 15원자 퍼센트의 알루미늄으로 이루어진 수소 저장 전극.
- 제 20 항에 있어서, 상기 활성체의 조성물은 주로, 5 내지 55원자 퍼센트의 티타늄, 30 내지 60원자 퍼센트의 니켈, 10 내지 20원자 퍼센트의 니오븀 및 3 내지 10원자 퍼센트의 지르코늄으로 이루어지는 수소 저장 전극.
- 제 20 항에 있어서, 상기 활성체는 재충전될 수 있는 수소 저장 전극.
- (a) 용융 상태로부터의 급속한 응고로 형성됨으로써 연속적인 비정질 구조로 특징지워지는 비입자상의 이방성을 지닌 최소한 하나의 자력 지지되는 고상, 금속성, 비정질 전기화학적 활성체를 포함한 최소한 하나의 수소 저장 전기화학적 전지용 수소 저장 전극, (b)상기 수소 저장 전극내에 저장된 에너지를 방출 할 수 있는 최소한 하나의 대극수단, 및 (c) 내부에 위치한 상기 수소 저장 전극 및 상기 대극 수단을 지니는 케이싱 수단을 포함하고, 상기 활성체는 최소한 3개의 원소를 포함하는 조성물을 지니며, 상기 원소는 알루미늄, 붕소, 크로뮴, 코발트, 하프늄, 인듐, 납, 마그네슘, 몰리브데늄, 니오븀, 팔라듐, 주석, 지르코늄 및 희토류 금속으로 이루어진 그룹으로부터 선택된 최소한 하나의 원소 및 티타늄과 니켈이고, 상기 각각의 원소들은 유효량만큼 존재함으로써 상기 전극이 전기화학적으로 충전,방전하는 주기동안 구조적인 결착성을 유지하면서 에너지를 저장하도록 수소로써 전기화학적으로 충전될 수 있고, 전기화학적으로 수소를 배출시켜서 에너지를 방출할 수 있으며, 상기 대극 수단은 상기 전지내에서 상기 대극과의 작동관계로 이격되어 위치된 수소 저장 전기화학적 전지.
- 제 25 항에 있어서, 상기 활성체의 조성물은 티타늄, 니켈 및 알루미늄을 포함하는 수소 저장 전가화학적 전지.
- 제 26 항에 있어서, 상기 활성체의 조성물은 니오븀, 크로뮴, 코발트, 구리, 철, 지르코늄 및 하프늄으로 이루어진 그룹으로부터 선택된 최소한 하나의 요소를 포함하는 수소 저장 전기화학적 전지.
- 제 25 항에 있어서, 상기 활성체의 조성물은 5 내지 약 55원자 퍼센트의 티타늄, 30 내지 60원자 퍼센트의 니켈, 10 내지 20원자 퍼센트의 니오븀 및, 3 내지 10원자 퍼센트의 지르코늄을 포함하는 수소 저장 전기화학적 전지.
- 제 25 항에 있어서, 상기 수소 저장 전극 및 상기 대극 수단은 젤리-롤(jelly roll)형상으로 축에 관해 나선형으로 감겨있는, 수소 저장 전기화학적 전지.
- 제 25 항에 있어서, 상기 수소 저장 전극은 거의 평탄한 박판으로서 존재하는 상기 활성체를 포함하고, 상기 대극 수단은 최소한 하나의 거의 평탄한 박판을 포함하는 수소 저장 전기화학적 전지.
- 제 25 항에 있어서, 상기 활성체는 40 내지 75원자 퍼센트의 티타늄, 15 내지 55원자 퍼센트의 니켈, 및 미소량 내지 15원자 퍼센트의 알루미늄을 포함하는 조성물을 지닌, 수소 저장 전기화학적 전지.
- 제 25 항에 있어서, 상기 활성체는 44 내지 60원자 퍼센트의 티타늄, 35 내지 40원자 퍼센트의 니켈, 및 3 내지 5원자 퍼센트의 알루미늄을 포함하는 조성물은 지닌, 수소 저장 전기화학적 전지.
- 제 32 항에 있어서, 상기 활성체의 조성물은 5 내지 11원자 퍼센트의 니오븀을 포함하는 수소 저장 전기화학적 전지.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US54665183A | 1983-10-28 | 1983-10-28 | |
| US546,651 | 1983-10-28 | ||
| US546651 | 1983-10-28 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR850003072A KR850003072A (ko) | 1985-05-28 |
| KR920004318B1 true KR920004318B1 (ko) | 1992-06-01 |
Family
ID=24181394
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1019840006827A KR920004318B1 (ko) | 1983-10-28 | 1984-10-29 | 무질서화된 활성재료로 제조된 전극 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US4637967B1 (ko) |
| EP (1) | EP0140693B1 (ko) |
| JP (1) | JPS60115158A (ko) |
| KR (1) | KR920004318B1 (ko) |
| AT (1) | ATE48723T1 (ko) |
| AU (1) | AU566387B2 (ko) |
| BR (1) | BR8405505A (ko) |
| CA (1) | CA1240363A (ko) |
| DE (1) | DE3480755D1 (ko) |
| HK (1) | HK1791A (ko) |
| IN (1) | IN164471B (ko) |
| MX (1) | MX161854A (ko) |
| PH (1) | PH21889A (ko) |
| SG (1) | SG67290G (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008157532A3 (en) * | 2007-06-18 | 2009-03-05 | Federal Mogul Ignition Co | Electrode for an ignition device |
Families Citing this family (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4551400A (en) * | 1984-04-18 | 1985-11-05 | Energy Conversion Devices, Inc. | Hydrogen storage materials and methods of sizing and preparing the same for electrochemical applications |
| US4728580A (en) * | 1985-03-29 | 1988-03-01 | The Standard Oil Company | Amorphous metal alloy compositions for reversible hydrogen storage |
| US4814002A (en) * | 1985-03-29 | 1989-03-21 | The Standard Oil Company | Method of forming amorphous metal alloy compositions for reversible hydrogen storage |
| US4923770A (en) * | 1985-03-29 | 1990-05-08 | The Standard Oil Company | Amorphous metal alloy compositions for reversible hydrogen storage and electrodes made therefrom |
| CA1273828A (en) * | 1985-04-01 | 1990-09-11 | Michael A. Tenhover | Energy storage devices and amorphous alloy electrodes for use in acid environments |
| DE3681267D1 (de) * | 1985-08-16 | 1991-10-10 | Hughes Aircraft Co | Elektrolyt hoher lebensdauer fuer nickel-wasserstoff-zellen. |
| US4952465A (en) * | 1986-04-30 | 1990-08-28 | The Standard Oil Company | Additive for energy storage devices that evolve oxygen and hydrogen |
| US4728586A (en) * | 1986-12-29 | 1988-03-01 | Energy Conversion Devices, Inc. | Enhanced charge retention electrochemical hydrogen storage alloys and an enhanced charge retention electrochemical cell |
| JPH0693358B2 (ja) * | 1987-04-21 | 1994-11-16 | 松下電器産業株式会社 | 水素吸蔵電極の製造法 |
| JPS6481169A (en) * | 1987-09-21 | 1989-03-27 | Sanyo Electric Co | Manufacture of hydrogen storage alloy electrode |
| JP2980328B2 (ja) * | 1989-09-29 | 1999-11-22 | 株式会社東芝 | 電池用水素吸蔵合金、その製造方法及びニッケル水素二次電池 |
| JP2936604B2 (ja) * | 1989-12-13 | 1999-08-23 | 松下電器産業株式会社 | 水素貯蔵合金負極を用いる角形密閉アルカリ蓄電池 |
| US5149383A (en) * | 1990-04-03 | 1992-09-22 | Matsushita Electric Industrial Co., Ltd. | Hydrogen storage alloy electrode |
| DE69326374T2 (de) * | 1992-04-13 | 2000-04-06 | Matsushita Electric Ind Co Ltd | Wasserstoffspeicherlegierung Elektrode |
| US5492543A (en) * | 1993-10-08 | 1996-02-20 | Hughes Aircraft Company | Preparation of electrodes and Ni/MHx electrochemical storage cell |
| US5434022A (en) * | 1993-10-08 | 1995-07-18 | Hughes Aircraft Company | Electrodes and electrochemical storage cells utilizing tin-modified active materials |
| CA2126136C (en) * | 1994-06-17 | 2007-06-05 | Steven J. Thorpe | Amorphous metal/metallic glass electrodes for electrochemical processes |
| US5578393A (en) * | 1995-03-10 | 1996-11-26 | United States Advanced Battery Consortium | Thermal contact sheet for high temperature batteries |
| US5840440A (en) * | 1995-11-20 | 1998-11-24 | Ovonic Battery Company, Inc. | Hydrogen storage materials having a high density of non-conventional useable hydrogen storing sites |
| JP3027532B2 (ja) * | 1995-12-26 | 2000-04-04 | 昭和電工株式会社 | 水素吸蔵合金の製造方法 |
| DE60034870T2 (de) * | 1999-09-16 | 2008-01-17 | Matsushita Electric Industrial Co., Ltd., Kadoma | Abgedichtete zylindrische nickel-wasserstoffspeicherbatterie |
| US6627148B1 (en) * | 1999-11-06 | 2003-09-30 | Energy Conversion Devices, Inc. | Safe, ecomomical transport of hydrogen in pelletized form |
| US6500583B1 (en) * | 2000-07-17 | 2002-12-31 | Energy Conversion Devices, Inc. | Electrochemical hydrogen storage alloys for nickel metal hydride batteries, fuel cells and methods of manufacturing same |
| DE10224722C1 (de) * | 2002-05-30 | 2003-08-14 | Leibniz Inst Fuer Festkoerper | Hochfeste, plastisch verformbare Formkörper aus Titanlegierungen |
| US20040142203A1 (en) * | 2003-01-07 | 2004-07-22 | Woolley Christopher P. | Hydrogen storage medium |
| FR2876221B1 (fr) * | 2004-10-06 | 2006-12-22 | Batscap Sa | Module de batterie comprenant un element de stockage d'energie dont le contact est realise par serrage des couches entre elles |
| DE102007009295A1 (de) | 2007-02-16 | 2008-08-21 | Varta Microbattery Gmbh | Galvanisches Element mit hoher Kapazität |
| US20220293924A1 (en) * | 2021-03-15 | 2022-09-15 | Nanode Battery Technologies Ltd. | Tin Alloy Sheets as Negative Electrodes for Non-Aqueous Li and Na-ion Batteries |
Family Cites Families (23)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| NL69996C (ko) * | 1946-09-10 | |||
| DE1671976A1 (de) * | 1967-04-27 | 1971-10-21 | Varta Ag | Verfahren zur Herstellung von Vorkoerpern fuer hochporoese,positive Raney-Nickel-Elektroden fuer galvanische Akkumulatoren mit alkalischem Elektrolyten |
| CH495060A (de) * | 1967-05-02 | 1970-08-15 | Battelle Memorial Inst Interna | Akkumulator-Elektrode mit Speichervermögen für Wasserstoff und Verfahren zu deren Herstellung |
| DE2111372A1 (de) * | 1971-03-10 | 1972-09-28 | Siemens Ag | Verfahren zur Gewinnung von sproedem,mahlbarem Titannickelid |
| GB1446693A (en) * | 1973-02-17 | 1976-08-18 | Deutsche Automobilgesellsch | Hydrogen storage electrodes for galvanic cells |
| JPS5271633A (en) * | 1975-12-12 | 1977-06-15 | Hitachi Maxell | Method of making nonnaqueous electrolyte batteries |
| US4112199A (en) * | 1975-12-30 | 1978-09-05 | Communications Satellite Corporation | Lanthanum nickel hydride-hydrogen/metal oxide cell |
| NL7600029A (nl) * | 1976-01-05 | 1977-07-07 | Philips Nv | Elektrode, waarvan het elektrochemisch actieve deel uit een hydride vormende intermetallische verbinding bestaat en batterij en brandstofcel voorzien van een dergelijke elektrode. |
| JPS5945190B2 (ja) * | 1976-12-03 | 1984-11-05 | 松下電器産業株式会社 | 水素吸蔵電極 |
| GB1546613A (en) * | 1977-09-02 | 1979-05-23 | Atomic Energy Authority Uk | Electric cells |
| DE2919742A1 (de) * | 1979-05-16 | 1980-11-27 | Gerd Dipl Ing Kopmann | Gasspeicherung in festkoerpern |
| JPS592957B2 (ja) * | 1979-08-31 | 1984-01-21 | 松下電工株式会社 | 歩数計 |
| JPS5648561A (en) * | 1979-09-29 | 1981-05-01 | Toshiba Corp | Neutron detector |
| US4544473A (en) * | 1980-05-12 | 1985-10-01 | Energy Conversion Devices, Inc. | Catalytic electrolytic electrode |
| JPS5791736A (en) * | 1980-11-29 | 1982-06-08 | Daido Steel Co Ltd | Hydrogen occluding material |
| US4395322A (en) * | 1981-11-18 | 1983-07-26 | General Electric Company | Catalytic electrode |
| JPS58163157A (ja) * | 1982-03-23 | 1983-09-27 | Toshiba Corp | 金属酸化物・水素電池 |
| ZA832570B (en) * | 1982-04-28 | 1984-01-25 | Energy Conversion Devices Inc | Improved rechargeable battery and electrode used therein |
| US4431561A (en) * | 1982-04-28 | 1984-02-14 | Energy Conversion Devices, Inc. | Hydrogen storage materials and method of making same |
| US4545883A (en) * | 1982-07-19 | 1985-10-08 | Energy Conversion Devices, Inc. | Electrolytic cell cathode |
| US4430391A (en) * | 1982-07-19 | 1984-02-07 | Energy Conversion Devices, Inc. | Fuel cell cathode |
| US4487818A (en) * | 1982-07-19 | 1984-12-11 | Energy Conversion Devices, Inc. | Fuel cell anode based on a disordered catalytic material |
| JPS59186253A (ja) * | 1983-04-01 | 1984-10-23 | インタ−ナショナル ビジネス マシ−ンズ コ−ポレ−ション | 電池の電極 |
-
1984
- 1984-10-25 CA CA000466310A patent/CA1240363A/en not_active Expired
- 1984-10-26 DE DE8484307408T patent/DE3480755D1/de not_active Expired - Fee Related
- 1984-10-26 AT AT84307408T patent/ATE48723T1/de not_active IP Right Cessation
- 1984-10-26 EP EP84307408A patent/EP0140693B1/en not_active Expired
- 1984-10-26 AU AU34757/84A patent/AU566387B2/en not_active Ceased
- 1984-10-26 PH PH31370A patent/PH21889A/en unknown
- 1984-10-29 JP JP59227637A patent/JPS60115158A/ja active Pending
- 1984-10-29 KR KR1019840006827A patent/KR920004318B1/ko not_active IP Right Cessation
- 1984-10-29 MX MX203206A patent/MX161854A/es unknown
- 1984-10-29 BR BR8405505A patent/BR8405505A/pt not_active IP Right Cessation
- 1984-10-29 IN IN755/CAL/84A patent/IN164471B/en unknown
-
1985
- 1985-08-29 US US06770704 patent/US4637967B1/en not_active Expired - Lifetime
-
1990
- 1990-08-14 SG SG67290A patent/SG67290G/en unknown
-
1991
- 1991-01-03 HK HK17/91A patent/HK1791A/xx not_active IP Right Cessation
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008157532A3 (en) * | 2007-06-18 | 2009-03-05 | Federal Mogul Ignition Co | Electrode for an ignition device |
| US7707985B2 (en) | 2007-06-18 | 2010-05-04 | Federal-Mogul World Wide, Inc. | Electrode for an ignition device |
| US7866294B2 (en) | 2007-06-18 | 2011-01-11 | Federal-Mogul Worldwide, Inc. | Electrode for an ignition device |
Also Published As
| Publication number | Publication date |
|---|---|
| JPS60115158A (ja) | 1985-06-21 |
| EP0140693A2 (en) | 1985-05-08 |
| ATE48723T1 (de) | 1989-12-15 |
| MX161854A (es) | 1991-01-24 |
| EP0140693B1 (en) | 1989-12-13 |
| DE3480755D1 (de) | 1990-01-18 |
| SG67290G (en) | 1990-09-21 |
| US4637967B1 (en) | 1995-05-16 |
| BR8405505A (pt) | 1985-09-03 |
| CA1240363A (en) | 1988-08-09 |
| IN164471B (ko) | 1989-03-25 |
| KR850003072A (ko) | 1985-05-28 |
| AU566387B2 (en) | 1987-10-15 |
| EP0140693A3 (en) | 1986-10-01 |
| US4637967A (en) | 1987-01-20 |
| PH21889A (en) | 1988-03-25 |
| HK1791A (en) | 1991-01-11 |
| AU3475784A (en) | 1985-05-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR920004318B1 (ko) | 무질서화된 활성재료로 제조된 전극 | |
| CA2423608C (en) | Electrode for lithium secondary battery and lithium secondary battery | |
| KR100684392B1 (ko) | 용량, 레이트 케이퍼빌리티 및 촉매 활성이 증가된 개선된 전기화학 수소 저장 합금 | |
| WO2010084880A1 (ja) | 水素吸蔵合金およびニッケル水素蓄電池 | |
| JP3604156B2 (ja) | 電気化学的電池 | |
| JP5481803B2 (ja) | ニッケル水素蓄電池 | |
| JPH0969362A (ja) | 二次電池及び二次電池を用いた電源 | |
| JP2001291511A (ja) | 水素吸蔵合金電極、二次電池、ハイブリッドカー及び電気自動車 | |
| JP5532390B2 (ja) | ニッケル水素蓄電池 | |
| JPH10265875A (ja) | 水素吸蔵合金,その製造方法およびニッケル水素二次電池 | |
| JPH08120364A (ja) | 電池用水素吸蔵合金,その製造方法およびニッケル水素二次電池 | |
| JP3639494B2 (ja) | ニッケル−水素蓄電池 | |
| JPH10259436A (ja) | 水素吸蔵合金,その製造方法およびニッケル水素二次電池 | |
| JP4117918B2 (ja) | 水素吸蔵合金,その製造方法およびニッケル水素二次電池 | |
| JPH10259445A (ja) | 水素吸蔵合金,その製造方法およびニッケル水素二次電池 | |
| JPH10265888A (ja) | 水素吸蔵合金,その製造方法およびニッケル水素二次電池 | |
| JPH0945322A (ja) | 水素吸蔵合金およびそれを用いた水素吸蔵合金電極 | |
| JP3369148B2 (ja) | アルカリ蓄電池 | |
| JPH097591A (ja) | 水素吸蔵合金及びその製造方法並びにそれを用いた水素吸蔵合金電極 | |
| JP3136960B2 (ja) | 電池用水素吸蔵合金の処理方法 | |
| JP3498589B2 (ja) | 正極活物質および二次電池 | |
| JP3368772B2 (ja) | 水素吸蔵合金粉末の製造方法 | |
| JPH05258750A (ja) | 水素吸蔵合金電極の製造法 | |
| JPH10102170A (ja) | 水素吸蔵合金およびニッケル水素二次電池 | |
| JPH1060565A (ja) | 水素吸蔵合金およびニッケル水素二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| G160 | Decision to publish patent application | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 20030417 Year of fee payment: 12 |
|
| LAPS | Lapse due to unpaid annual fee |