KR20230040953A - 치환된 피페리딘 화합물 및 이의 적용례 - Google Patents
치환된 피페리딘 화합물 및 이의 적용례 Download PDFInfo
- Publication number
- KR20230040953A KR20230040953A KR1020227044679A KR20227044679A KR20230040953A KR 20230040953 A KR20230040953 A KR 20230040953A KR 1020227044679 A KR1020227044679 A KR 1020227044679A KR 20227044679 A KR20227044679 A KR 20227044679A KR 20230040953 A KR20230040953 A KR 20230040953A
- Authority
- KR
- South Korea
- Prior art keywords
- pharmaceutically acceptable
- acceptable salt
- mmol
- azabicyclo
- compound
- Prior art date
Links
- 150000003053 piperidines Chemical class 0.000 title description 2
- 150000001875 compounds Chemical class 0.000 claims abstract description 142
- 150000003839 salts Chemical class 0.000 claims abstract description 50
- 102000002512 Orexin Human genes 0.000 claims description 27
- 108060005714 orexin Proteins 0.000 claims description 27
- DLFVBJFMPXGRIB-UHFFFAOYSA-N thioacetamide Natural products CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 claims description 25
- 238000000034 method Methods 0.000 claims description 24
- 201000003631 narcolepsy Diseases 0.000 claims description 20
- 208000001573 Cataplexy Diseases 0.000 claims description 14
- 239000008194 pharmaceutical composition Substances 0.000 claims description 11
- 238000004519 manufacturing process Methods 0.000 claims description 9
- 239000003814 drug Substances 0.000 claims description 8
- 238000002360 preparation method Methods 0.000 claims description 7
- 229940124597 therapeutic agent Drugs 0.000 claims description 4
- 239000000018 receptor agonist Substances 0.000 claims description 3
- 229940044601 receptor agonist Drugs 0.000 claims description 3
- 230000000694 effects Effects 0.000 abstract description 15
- 108050000742 Orexin Receptor Proteins 0.000 abstract description 3
- 102000008834 Orexin receptor Human genes 0.000 abstract description 3
- 239000000556 agonist Substances 0.000 abstract description 2
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 141
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 114
- 239000000203 mixture Substances 0.000 description 54
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 37
- 239000000243 solution Substances 0.000 description 34
- 239000011541 reaction mixture Substances 0.000 description 30
- 230000015572 biosynthetic process Effects 0.000 description 27
- 238000003786 synthesis reaction Methods 0.000 description 27
- 239000012044 organic layer Substances 0.000 description 26
- 241000699670 Mus sp. Species 0.000 description 24
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 24
- 238000012360 testing method Methods 0.000 description 22
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 21
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 21
- 238000004808 supercritical fluid chromatography Methods 0.000 description 21
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 21
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 18
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 18
- 238000005160 1H NMR spectroscopy Methods 0.000 description 16
- 239000012071 phase Substances 0.000 description 16
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 15
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 15
- 230000014759 maintenance of location Effects 0.000 description 15
- 230000007958 sleep Effects 0.000 description 15
- 239000013078 crystal Substances 0.000 description 14
- JMMWKPVZQRWMSS-UHFFFAOYSA-N isopropanol acetate Natural products CC(C)OC(C)=O JMMWKPVZQRWMSS-UHFFFAOYSA-N 0.000 description 14
- 229940011051 isopropyl acetate Drugs 0.000 description 14
- GWYFCOCPABKNJV-UHFFFAOYSA-N isovaleric acid Chemical compound CC(C)CC(O)=O GWYFCOCPABKNJV-UHFFFAOYSA-N 0.000 description 14
- 239000002904 solvent Substances 0.000 description 13
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 12
- -1 piperidine compound Chemical class 0.000 description 12
- 239000000741 silica gel Substances 0.000 description 12
- 229910002027 silica gel Inorganic materials 0.000 description 12
- 239000007787 solid Substances 0.000 description 12
- 238000004458 analytical method Methods 0.000 description 11
- 239000000126 substance Substances 0.000 description 11
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 10
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 10
- 238000005406 washing Methods 0.000 description 10
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 9
- 208000007590 Disorders of Excessive Somnolence Diseases 0.000 description 9
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 9
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 9
- 238000001514 detection method Methods 0.000 description 9
- 230000033001 locomotion Effects 0.000 description 9
- 238000005259 measurement Methods 0.000 description 9
- 238000002441 X-ray diffraction Methods 0.000 description 8
- 206010020765 hypersomnia Diseases 0.000 description 8
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 7
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 7
- 229910021529 ammonia Inorganic materials 0.000 description 7
- 239000012131 assay buffer Substances 0.000 description 7
- 238000004440 column chromatography Methods 0.000 description 7
- 238000001816 cooling Methods 0.000 description 7
- 239000012043 crude product Substances 0.000 description 7
- 239000000706 filtrate Substances 0.000 description 7
- 210000002569 neuron Anatomy 0.000 description 7
- 230000003287 optical effect Effects 0.000 description 7
- 230000002269 spontaneous effect Effects 0.000 description 7
- 208000011580 syndromic disease Diseases 0.000 description 7
- NTOIKDYVJIWVSU-WOJBJXKFSA-N (2r,3r)-2,3-dihydroxy-2,3-bis(4-methylbenzoyl)butanedioic acid Chemical compound C1=CC(C)=CC=C1C(=O)[C@@](O)(C(O)=O)[C@](O)(C(O)=O)C(=O)C1=CC=C(C)C=C1 NTOIKDYVJIWVSU-WOJBJXKFSA-N 0.000 description 6
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- 101000969553 Homo sapiens Cell surface glycoprotein CD200 receptor 1 Proteins 0.000 description 6
- 241000699666 Mus <mouse, genus> Species 0.000 description 6
- 102100037588 Orexin receptor type 2 Human genes 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 6
- 239000007864 aqueous solution Substances 0.000 description 6
- 210000004027 cell Anatomy 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 6
- 239000003480 eluent Substances 0.000 description 6
- RHLMXWCISNJNDH-UHFFFAOYSA-N n-[2-[3-[[5-[3-(dimethylcarbamoyl)phenyl]-2-methoxyphenyl]sulfonylamino]anilino]ethyl]-3-methylbenzamide Chemical compound COC1=CC=C(C=2C=C(C=CC=2)C(=O)N(C)C)C=C1S(=O)(=O)NC(C=1)=CC=CC=1NCCNC(=O)C1=CC=CC(C)=C1 RHLMXWCISNJNDH-UHFFFAOYSA-N 0.000 description 6
- OFNHNCAUVYOTPM-IIIOAANCSA-N orexin-a Chemical compound C([C@@H](C(=O)N[C@@H](C)C(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(C)C)C(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)CNC(=O)[C@H](C)NC(=O)CNC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H]1NC(=O)[C@H](CO)NC(=O)[C@@H]2CSSC[C@@H](C(=O)N[C@H](C(N[C@@H](CCCN=C(N)N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(=O)N2)[C@@H](C)O)=O)CSSC1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC(C)C)NC(=O)[C@H]1N(CCC1)C(=O)[C@H]1NC(=O)CC1)C1=CNC=N1 OFNHNCAUVYOTPM-IIIOAANCSA-N 0.000 description 6
- 239000000047 product Substances 0.000 description 6
- 239000007790 solid phase Substances 0.000 description 6
- 208000024891 symptom Diseases 0.000 description 6
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 5
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 5
- 238000003556 assay Methods 0.000 description 5
- 238000004587 chromatography analysis Methods 0.000 description 5
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 5
- 238000001914 filtration Methods 0.000 description 5
- 229910052739 hydrogen Inorganic materials 0.000 description 5
- 239000001257 hydrogen Substances 0.000 description 5
- 239000010410 layer Substances 0.000 description 5
- UKVIEHSSVKSQBA-UHFFFAOYSA-N methane;palladium Chemical compound C.[Pd] UKVIEHSSVKSQBA-UHFFFAOYSA-N 0.000 description 5
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 5
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 5
- 229910000027 potassium carbonate Inorganic materials 0.000 description 5
- 239000000523 sample Substances 0.000 description 5
- DYHSDKLCOJIUFX-UHFFFAOYSA-N tert-butoxycarbonyl anhydride Chemical compound CC(C)(C)OC(=O)OC(=O)OC(C)(C)C DYHSDKLCOJIUFX-UHFFFAOYSA-N 0.000 description 5
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 5
- 238000011830 transgenic mouse model Methods 0.000 description 5
- 239000003643 water by type Substances 0.000 description 5
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 4
- 241000699660 Mus musculus Species 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- 239000002253 acid Substances 0.000 description 4
- 239000011324 bead Substances 0.000 description 4
- 231100000673 dose–response relationship Toxicity 0.000 description 4
- 229940079593 drug Drugs 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- 238000010992 reflux Methods 0.000 description 4
- NDVLTYZPCACLMA-UHFFFAOYSA-N silver oxide Chemical compound [O-2].[Ag+].[Ag+] NDVLTYZPCACLMA-UHFFFAOYSA-N 0.000 description 4
- AGYUQBNABXVWMS-UHFFFAOYSA-N 2-chloro-5-fluoropyrimidine Chemical compound FC1=CN=C(Cl)N=C1 AGYUQBNABXVWMS-UHFFFAOYSA-N 0.000 description 3
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 3
- AONHBESCCBXPAD-UHFFFAOYSA-N 3-nitro-4-pyrrolidin-1-ylbenzaldehyde Chemical compound [O-][N+](=O)C1=CC(C=O)=CC=C1N1CCCC1 AONHBESCCBXPAD-UHFFFAOYSA-N 0.000 description 3
- 102000007371 Ataxin-3 Human genes 0.000 description 3
- 108010032947 Ataxin-3 Proteins 0.000 description 3
- 101001098357 Homo sapiens Orexin receptor type 2 Proteins 0.000 description 3
- 101000986786 Homo sapiens Orexin/Hypocretin receptor type 1 Proteins 0.000 description 3
- 238000005481 NMR spectroscopy Methods 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- 230000036626 alertness Effects 0.000 description 3
- 239000012298 atmosphere Substances 0.000 description 3
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 3
- 229910000024 caesium carbonate Inorganic materials 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 239000012141 concentrate Substances 0.000 description 3
- 238000010586 diagram Methods 0.000 description 3
- 239000011521 glass Substances 0.000 description 3
- 102000044543 human HCRTR1 Human genes 0.000 description 3
- 102000044551 human HCRTR2 Human genes 0.000 description 3
- 238000002372 labelling Methods 0.000 description 3
- 238000006386 neutralization reaction Methods 0.000 description 3
- 229910052757 nitrogen Inorganic materials 0.000 description 3
- FBUKVWPVBMHYJY-UHFFFAOYSA-N nonanoic acid Chemical compound CCCCCCCCC(O)=O FBUKVWPVBMHYJY-UHFFFAOYSA-N 0.000 description 3
- TVMXDCGIABBOFY-UHFFFAOYSA-N octane Chemical compound CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 3
- 230000000144 pharmacologic effect Effects 0.000 description 3
- 229920001983 poloxamer Polymers 0.000 description 3
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Chemical compound [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 108090000623 proteins and genes Proteins 0.000 description 3
- 102000004169 proteins and genes Human genes 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 3
- 238000004809 thin layer chromatography Methods 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical group N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- RQLZQHFUAKKMNC-SCSAIBSYSA-N (2R)-2-bromo-3-methylbutanamide Chemical compound CC(C)[C@@H](Br)C(N)=O RQLZQHFUAKKMNC-SCSAIBSYSA-N 0.000 description 2
- UEBARDWJXBGYEJ-SCSAIBSYSA-N (2r)-2-bromo-3-methylbutanoic acid Chemical compound CC(C)[C@@H](Br)C(O)=O UEBARDWJXBGYEJ-SCSAIBSYSA-N 0.000 description 2
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 2
- XOTQYJVUQQSZDS-UHFFFAOYSA-N 2-bromo-2-cyclopropylacetamide Chemical compound NC(=O)C(Br)C1CC1 XOTQYJVUQQSZDS-UHFFFAOYSA-N 0.000 description 2
- KVVDRQDTODKIJD-UHFFFAOYSA-N 2-cyclopropylacetic acid Chemical compound OC(=O)CC1CC1 KVVDRQDTODKIJD-UHFFFAOYSA-N 0.000 description 2
- JLLJPPBGJVCFGG-UHFFFAOYSA-N 3-chloropyridine-4-carbonitrile Chemical compound ClC1=CN=CC=C1C#N JLLJPPBGJVCFGG-UHFFFAOYSA-N 0.000 description 2
- SUZIOAPLIWZQST-UHFFFAOYSA-N 3-methoxypyridine-4-carbonitrile Chemical compound COC1=CN=CC=C1C#N SUZIOAPLIWZQST-UHFFFAOYSA-N 0.000 description 2
- 229920000936 Agarose Polymers 0.000 description 2
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 2
- 206010002091 Anaesthesia Diseases 0.000 description 2
- 238000011740 C57BL/6 mouse Methods 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- BHPQYMZQTOCNFJ-UHFFFAOYSA-N Calcium cation Chemical compound [Ca+2] BHPQYMZQTOCNFJ-UHFFFAOYSA-N 0.000 description 2
- 241000282465 Canis Species 0.000 description 2
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 2
- 239000007995 HEPES buffer Substances 0.000 description 2
- 239000012981 Hank's balanced salt solution Substances 0.000 description 2
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 2
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 2
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 2
- 239000004677 Nylon Substances 0.000 description 2
- 102100028141 Orexin/Hypocretin receptor type 1 Human genes 0.000 description 2
- 208000018737 Parkinson disease Diseases 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 2
- 235000010724 Wisteria floribunda Nutrition 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 235000001014 amino acid Nutrition 0.000 description 2
- 230000037005 anaesthesia Effects 0.000 description 2
- 238000010171 animal model Methods 0.000 description 2
- 125000004429 atom Chemical group 0.000 description 2
- LPCWKMYWISGVSK-UHFFFAOYSA-N bicyclo[3.2.1]octane Chemical compound C1C2CCC1CCC2 LPCWKMYWISGVSK-UHFFFAOYSA-N 0.000 description 2
- IPWKHHSGDUIRAH-UHFFFAOYSA-N bis(pinacolato)diboron Chemical compound O1C(C)(C)C(C)(C)OB1B1OC(C)(C)C(C)(C)O1 IPWKHHSGDUIRAH-UHFFFAOYSA-N 0.000 description 2
- 210000004556 brain Anatomy 0.000 description 2
- 239000012267 brine Substances 0.000 description 2
- 239000000872 buffer Substances 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 229910001424 calcium ion Inorganic materials 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- OSQPUMRCKZAIOZ-UHFFFAOYSA-N carbon dioxide;ethanol Chemical compound CCO.O=C=O OSQPUMRCKZAIOZ-UHFFFAOYSA-N 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 230000002950 deficient Effects 0.000 description 2
- 239000000539 dimer Substances 0.000 description 2
- 238000010828 elution Methods 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 230000005284 excitation Effects 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 238000005194 fractionation Methods 0.000 description 2
- 238000004128 high performance liquid chromatography Methods 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 239000002198 insoluble material Substances 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 229960002725 isoflurane Drugs 0.000 description 2
- 238000011813 knockout mouse model Methods 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 238000004949 mass spectrometry Methods 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- 229920001778 nylon Polymers 0.000 description 2
- OHOWSYIKESXDMN-WMQZXSDYSA-N orexin-b Chemical compound C([C@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)CNC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@@H](N)CCSC)[C@@H](C)O)[C@@H](C)CC)C(=O)N[C@@H](CC(N)=O)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CCCN=C(N)N)C(N)=O)C1=CNC=N1 OHOWSYIKESXDMN-WMQZXSDYSA-N 0.000 description 2
- NRNCYVBFPDDJNE-UHFFFAOYSA-N pemoline Chemical compound O1C(N)=NC(=O)C1C1=CC=CC=C1 NRNCYVBFPDDJNE-UHFFFAOYSA-N 0.000 description 2
- 229920001992 poloxamer 407 Polymers 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- DBABZHXKTCFAPX-UHFFFAOYSA-N probenecid Chemical compound CCCN(CCC)S(=O)(=O)C1=CC=C(C(O)=O)C=C1 DBABZHXKTCFAPX-UHFFFAOYSA-N 0.000 description 2
- 229960003081 probenecid Drugs 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 230000002035 prolonged effect Effects 0.000 description 2
- 125000001501 propionyl group Chemical group O=C([*])C([H])([H])C([H])([H])[H] 0.000 description 2
- 235000018102 proteins Nutrition 0.000 description 2
- 239000008213 purified water Substances 0.000 description 2
- 230000036385 rapid eye movement (rem) sleep Effects 0.000 description 2
- 238000011160 research Methods 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 238000000926 separation method Methods 0.000 description 2
- 229910001923 silver oxide Inorganic materials 0.000 description 2
- 201000002859 sleep apnea Diseases 0.000 description 2
- 230000008667 sleep stage Effects 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 2
- 238000000935 solvent evaporation Methods 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- 230000004083 survival effect Effects 0.000 description 2
- MENILFUADYEXNU-UHFFFAOYSA-N tert-butyl 3-oxo-8-azabicyclo[3.2.1]octane-8-carboxylate Chemical compound C1C(=O)CC2CCC1N2C(=O)OC(C)(C)C MENILFUADYEXNU-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N tetrahydropyridine hydrochloride Natural products C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 238000004704 ultra performance liquid chromatography Methods 0.000 description 2
- OYSWCWFZUHBBBQ-GFCCVEGCSA-N (4S)-3-(2-cyclopropylacetyl)-4-phenyl-1,3-oxazolidin-2-one Chemical compound O=C(CC1CC1)N([C@H](CO1)C2=CC=CC=C2)C1=O OYSWCWFZUHBBBQ-GFCCVEGCSA-N 0.000 description 1
- QDMNNMIOWVJVLY-MRVPVSSYSA-N (4s)-4-phenyl-1,3-oxazolidin-2-one Chemical compound C1OC(=O)N[C@H]1C1=CC=CC=C1 QDMNNMIOWVJVLY-MRVPVSSYSA-N 0.000 description 1
- WSLDOOZREJYCGB-UHFFFAOYSA-N 1,2-Dichloroethane Chemical compound ClCCCl WSLDOOZREJYCGB-UHFFFAOYSA-N 0.000 description 1
- VHSVJTYBTJCDFL-UHFFFAOYSA-L 1,2-dimethoxyethane;nickel(2+);dibromide Chemical compound Br[Ni]Br.COCCOC VHSVJTYBTJCDFL-UHFFFAOYSA-L 0.000 description 1
- JVSFQJZRHXAUGT-UHFFFAOYSA-N 2,2-dimethylpropanoyl chloride Chemical compound CC(C)(C)C(Cl)=O JVSFQJZRHXAUGT-UHFFFAOYSA-N 0.000 description 1
- CEJAHXLRNZJPQH-UHFFFAOYSA-N 2,5-dichloropyrimidine Chemical compound ClC1=CN=C(Cl)N=C1 CEJAHXLRNZJPQH-UHFFFAOYSA-N 0.000 description 1
- VZSRBBMJRBPUNF-UHFFFAOYSA-N 2-(2,3-dihydro-1H-inden-2-ylamino)-N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]pyrimidine-5-carboxamide Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C(=O)NCCC(N1CC2=C(CC1)NN=N2)=O VZSRBBMJRBPUNF-UHFFFAOYSA-N 0.000 description 1
- VJXRKZJMGVSXPX-UHFFFAOYSA-N 4-ethylpyridine Chemical compound CCC1=CC=NC=C1 VJXRKZJMGVSXPX-UHFFFAOYSA-N 0.000 description 1
- CJIJXIFQYOPWTF-UHFFFAOYSA-N 7-hydroxycoumarin Natural products O1C(=O)C=CC2=CC(O)=CC=C21 CJIJXIFQYOPWTF-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- UXZAJSZFFARTEI-YRPNKDGESA-N CS(=O)(=O)N[C@@H]1[C@@H](N(CCC1)C(=O)OC)CO[C@@H]1CC[C@@H](CC1)C1=CC=CC=C1 Chemical compound CS(=O)(=O)N[C@@H]1[C@@H](N(CCC1)C(=O)OC)CO[C@@H]1CC[C@@H](CC1)C1=CC=CC=C1 UXZAJSZFFARTEI-YRPNKDGESA-N 0.000 description 1
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 206010010071 Coma Diseases 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 1
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 1
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 1
- 206010064571 Gene mutation Diseases 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 208000035895 Guillain-Barré syndrome Diseases 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- 208000016588 Idiopathic hypersomnia Diseases 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical class OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical compound [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 description 1
- 206010049567 Miller Fisher syndrome Diseases 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- AFCARXCZXQIEQB-UHFFFAOYSA-N N-[3-oxo-3-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)propyl]-2-[[3-(trifluoromethoxy)phenyl]methylamino]pyrimidine-5-carboxamide Chemical compound O=C(CCNC(=O)C=1C=NC(=NC=1)NCC1=CC(=CC=C1)OC(F)(F)F)N1CC2=C(CC1)NN=N2 AFCARXCZXQIEQB-UHFFFAOYSA-N 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- 108090000189 Neuropeptides Proteins 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- 108010038807 Oligopeptides Proteins 0.000 description 1
- 102000015636 Oligopeptides Human genes 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 206010062519 Poor quality sleep Diseases 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 1
- 206010041349 Somnolence Diseases 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- ZVQOOHYFBIDMTQ-UHFFFAOYSA-N [methyl(oxido){1-[6-(trifluoromethyl)pyridin-3-yl]ethyl}-lambda(6)-sulfanylidene]cyanamide Chemical compound N#CN=S(C)(=O)C(C)C1=CC=C(C(F)(F)F)N=C1 ZVQOOHYFBIDMTQ-UHFFFAOYSA-N 0.000 description 1
- 239000000370 acceptor Substances 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 238000001042 affinity chromatography Methods 0.000 description 1
- 125000004414 alkyl thio group Chemical group 0.000 description 1
- WQZGKKKJIJFFOK-PHYPRBDBSA-N alpha-D-galactose Chemical compound OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-PHYPRBDBSA-N 0.000 description 1
- VREFGVBLTWBCJP-UHFFFAOYSA-N alprazolam Chemical compound C12=CC(Cl)=CC=C2N2C(C)=NN=C2CN=C1C1=CC=CC=C1 VREFGVBLTWBCJP-UHFFFAOYSA-N 0.000 description 1
- 235000019270 ammonium chloride Nutrition 0.000 description 1
- 230000037007 arousal Effects 0.000 description 1
- 150000001510 aspartic acids Chemical class 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 238000010533 azeotropic distillation Methods 0.000 description 1
- 150000001540 azides Chemical class 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical class OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 150000001558 benzoic acid derivatives Chemical class 0.000 description 1
- RWCCWEUUXYIKHB-UHFFFAOYSA-N benzophenone Chemical compound C=1C=CC=CC=1C(=O)C1=CC=CC=C1 RWCCWEUUXYIKHB-UHFFFAOYSA-N 0.000 description 1
- 239000012965 benzophenone Substances 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- 230000036772 blood pressure Effects 0.000 description 1
- 230000036760 body temperature Effects 0.000 description 1
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- VQXINLNPICQTLR-UHFFFAOYSA-N carbonyl diazide Chemical compound [N-]=[N+]=NC(=O)N=[N+]=[N-] VQXINLNPICQTLR-UHFFFAOYSA-N 0.000 description 1
- 150000007942 carboxylates Chemical class 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 210000004720 cerebrum Anatomy 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 239000000460 chlorine Substances 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 229940125904 compound 1 Drugs 0.000 description 1
- 229940125773 compound 10 Drugs 0.000 description 1
- 229940126214 compound 3 Drugs 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000009402 cross-breeding Methods 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 229960001270 d- tartaric acid Drugs 0.000 description 1
- 125000001295 dansyl group Chemical group [H]C1=C([H])C(N(C([H])([H])[H])C([H])([H])[H])=C2C([H])=C([H])C([H])=C(C2=C1[H])S(*)(=O)=O 0.000 description 1
- DIXBSCZRIZDQGC-UHFFFAOYSA-N diaziridine Chemical compound C1NN1 DIXBSCZRIZDQGC-UHFFFAOYSA-N 0.000 description 1
- 125000000664 diazo group Chemical group [N-]=[N+]=[*] 0.000 description 1
- FAVAVMFXAKZTMV-UHFFFAOYSA-N dibutylboranyl trifluoromethanesulfonate Chemical compound CCCCB(CCCC)OS(=O)(=O)C(F)(F)F FAVAVMFXAKZTMV-UHFFFAOYSA-N 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- IJKVHSBPTUYDLN-UHFFFAOYSA-N dihydroxy(oxo)silane Chemical compound O[Si](O)=O IJKVHSBPTUYDLN-UHFFFAOYSA-N 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 229950004683 drostanolone propionate Drugs 0.000 description 1
- 238000009509 drug development Methods 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 230000002526 effect on cardiovascular system Effects 0.000 description 1
- 239000006274 endogenous ligand Substances 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 230000004634 feeding behavior Effects 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229930182830 galactose Natural products 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical group 0.000 description 1
- 229910001385 heavy metal Inorganic materials 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- 150000002431 hydrogen Chemical class 0.000 description 1
- 210000003016 hypothalamus Anatomy 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 229940042040 innovative drug Drugs 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 238000007914 intraventricular administration Methods 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- HVTICUPFWKNHNG-UHFFFAOYSA-N iodoethane Chemical compound CCI HVTICUPFWKNHNG-UHFFFAOYSA-N 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 125000000468 ketone group Chemical group 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 229910052747 lanthanoid Inorganic materials 0.000 description 1
- 150000002602 lanthanoids Chemical class 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- HWYHZTIRURJOHG-UHFFFAOYSA-N luminol Chemical compound O=C1NNC(=O)C2=C1C(N)=CC=C2 HWYHZTIRURJOHG-UHFFFAOYSA-N 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 229910052748 manganese Inorganic materials 0.000 description 1
- 239000011572 manganese Substances 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000001819 mass spectrum Methods 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- AFVFQIVMOAPDHO-UHFFFAOYSA-M methanesulfonate group Chemical class CS(=O)(=O)[O-] AFVFQIVMOAPDHO-UHFFFAOYSA-M 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 150000002772 monosaccharides Chemical class 0.000 description 1
- 239000012452 mother liquor Substances 0.000 description 1
- 238000002610 neuroimaging Methods 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 230000008452 non REM sleep Effects 0.000 description 1
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- 150000002924 oxiranes Chemical class 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 238000005222 photoaffinity labeling Methods 0.000 description 1
- 238000002600 positron emission tomography Methods 0.000 description 1
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 229910001426 radium ion Inorganic materials 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 230000029058 respiratory gaseous exchange Effects 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical compound [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- 239000012488 sample solution Substances 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 238000002603 single-photon emission computed tomography Methods 0.000 description 1
- 208000019116 sleep disease Diseases 0.000 description 1
- 230000004620 sleep latency Effects 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- QDRKDTQENPPHOJ-UHFFFAOYSA-N sodium ethoxide Chemical compound [Na+].CC[O-] QDRKDTQENPPHOJ-UHFFFAOYSA-N 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- 229910000104 sodium hydride Inorganic materials 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-N sulfuric acid Substances OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- HNSFEWHPNDVESC-AGUYFDCRSA-N tert-butyl (1R,5S)-3-(3-methoxypyridin-4-yl)-8-azabicyclo[3.2.1]octane-8-carboxylate Chemical compound CC(C)(C)OC(N([C@H](CC1)C2)[C@@H]1CC2C1=CC=NC=C1OC)=O HNSFEWHPNDVESC-AGUYFDCRSA-N 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- 238000002560 therapeutic procedure Methods 0.000 description 1
- 238000003354 tissue distribution assay Methods 0.000 description 1
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical class CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- ORHBXUUXSCNDEV-UHFFFAOYSA-N umbelliferone Chemical compound C1=CC(=O)OC2=CC(O)=CC=C21 ORHBXUUXSCNDEV-UHFFFAOYSA-N 0.000 description 1
- 238000002424 x-ray crystallography Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/08—Bridged systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Hydrogenated Pyridines (AREA)
- Plural Heterocyclic Compounds (AREA)
- Epidemiology (AREA)
- Pain & Pain Management (AREA)
Abstract
Description
본 발명은 오렉신 제2형 수용체(orexin type 2 receptor)-활성화 활성을 갖는 치환된 피페리딘 화합물, 및 이의 약학적으로 허용되는 염 및 의학 용도에 관한 것이다. 본 발명은 또한 활성 성분으로서 상기 화합물을 포함하는 약물에 관한 것이다.
뇌 시상하부의 바깥 부분에 국한된 특정 뉴런에 의해 특이적으로 생성되는 두 가지 유형의 뇌내 신경 펩티드인 오렉신-A(OX-A)와 오렉신-B(OX-B)는 오렉신 수용체의 내인성 리간드로 밝혀졌고(PTL 1 내지 4), 이는 주로 대뇌에 존재하는 G 단백질-결합 수용체이다(PTL 5 및 NPL 1 참조). 오렉신 수용체의 두 가지 아형, 즉 제1 아형 OX1 수용체(OX1R) 및 제2 아형 OX2 수용체(OX2R)가 공지되어 있다. 오렉신은 래트(rat)의 섭식 거동을 촉진하는 것으로 밝혀졌다(NPL 1).
OX2R 유전자 돌연변이는 개 기면증의 원인 중 하나로 보고되었고(NPL 2), 오렉신 녹아웃(knockout) 마우스는 인간 또는 개 기면증과 매우 유사한 기면증-유사 증상을 나타낸다(NPL 3). 오렉신 뉴런이 변형된 형질전환 마우스와 이들 마우스를 오렉신-과발현 형질전환 마우스와의 교잡육종에 의해 수득된 이중 형질전환 마우스를 사용한 연구는, 오렉신 뉴런의 변형에 의해 나타나는 기면증-유사 증상이 오렉신의 지속적인 발현에 의해 제거되는 것을 보여주었다(NPL 4). 유사하게, 오렉신 뉴런이 변형된 형질전환 마우스에 대한 OX-A의 뇌실내 투여가 탈력 발작(cataplexy)(정동적 탈력 발작)-유사 정지 작용을 억제하고, 예를 들어 각성도를 증가시킴으로써 기면증의 증상을 개선하는 것이 밝혀졌다(NPL 4). 또한, OX2R 녹아웃 마우스에 대한 연구는, OX2R이 각성도 유지에 중요하다는 것을 시사한다(NPL 5). 또한, 오렉신 신경의 소실이 파킨슨병 환자의 주간 졸음의 원인임을 시사하였다(NPL 6). 또한, 혈장 OX-A 농도 수준이 수면 무호흡 증후군 환자에서 낮음을 시사하였다(NPL 7). 이를 기반으로 OX2R 작용제가 기면증 치료제, 또는 수면과다증을 나타내는 다른 수면 장애에 대한 치료제로서 작용할 수 있음을 사사하였다(NPL 8).
따라서, OX2R-활성화 활성을 갖는 화합물은, 기면증, 특발성 수면과다증, 수면과다증, 수면 무호흡 증후군, 혼수 상태와 같은 의식 장애 상태, 기면증 유사 증상을 동반하는 기면 증후군, 및 주간 수면과다증을 동반하는 수면과다 증후군(예를 들어, 파킨슨병, 길랭-바레 증후군 및 클라인 레빈 증후군)에 대한 치료제로서 사용될 수 있는 것으로 여겨진다.
OX2R-활성화 활성을 갖는 화합물인 TAK-925는 건강한 사람과 기면증 환자를 대상으로 한 I상 시험(정맥내 주입)에 진입하였다.
Sakurai T. et al, Cell, 1998, 92, 573-585
Lin L. et al, Cell, 1999, 98, 365-376
Chemelli R.M. et al, Cell, 1999, 98, 437-451
Mieda M. et al, Proc. Natl. Acad. Sci. USA, 2004, 101, 4649-4654
Willie J.T. et al, Neuron, 2003, 38, 715-730
Thannickal T.C. et al, Brain. 2007, 130, 1586-1595
Busquets X. et al, Respiration, 2004, 71, 575-579
Mieda M. et al, CNS Drugs, 2013, 27, 83-90
본 발명의 목적은 오렉신 제2형 수용체-활성화 활성을 갖는 피페리딘 화합물 및 이의 약학적으로 허용되는 염, 및 이를 포함하는 약학 조성물을 제공하는 것이다.
구체적으로, 본 발명은 하기 <1> 내지 <21>에 관한 것이다.
<1> 하기 화학식 I로 표현되는 (2R)-2-사이클로프로필-2-{(1R,3S,5S)-3-[(3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일]-8-아자바이사이클로[3.2.1]옥탄-8-일}아세트아미드:
[화학식 I]
하기 화학식 II로 표현되는 (R)-2-((1R,3S,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)-3-메틸부탄아미드:
[화학식 II]
하기 화학식 III으로 표현되는 (R)-2-((1R,3S,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-에톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)-2-사이클로프로필 아세트아미드:
[화학식 III]
및 하기 화학식 IV로 표현되는 (R)-2-사이클로프로필-2-((1R,3S,5S)-3-((2S,4S)-1-(5-플루오로피리미딘-2-일)-2-메틸피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)아세트아미드:
[화학식 IV]
로 이루어진 군으로부터 선택되는 화합물; 또는 이의 약학적으로 허용되는 염.
<2> 하기 화학식 I로 표현되는 (2R)-2-사이클로프로필-2-{(1R,3S,5S)-3-[(3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일]-8-아자바이사이클로[3.2.1]옥탄-8-일}아세트아미드:
[화학식 I]
또는 이의 약학적으로 허용되는 염.
<3> 하기 화학식 II로 표현되는 (R)-2-((1R,3S,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)-3-메틸부탄아미드:
[화학식 II]
또는 이의 약학적으로 허용되는 염.
<4> 하기 화학식 III으로 표현되는 (R)-2-((1R,3S,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-에톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)-2-사이클로프로필 아세트아미드:
[화학식 III]
또는 이의 약학적으로 허용되는 염.
<5> 하기 화학식 IV로 표현되는 (R)-2-사이클로프로필-2-((1R,3S,5S)-3-((2S,4S)-1-(5-플루오로피리미딘-2-일)-2-메틸피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)아세트아미드:
[화학식 IV]
또는 이의 약학적으로 허용되는 염.
<6> 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염을 포함하는 약학 조성물.
<7> 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염을 포함하는 오렉신 제2형 수용체 작용제(orexin type 2 receptor agonist).
<8> 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염을 포함하는 기면증 치료제.
<9> 대상체에 약리학적 유효 용량의 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염을 투여하는 단계를 포함하는 기면증의 치료 방법.
<10> 대상체에 약리학적 유효 용량의 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염을 투여하는 단계를 포함하는 오렉신 제2형 수용체의 활성화 방법.
<11> 대상체에 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염을 투여하는 단계를 포함하는 기면증의 치료 방법.
<12> 기면증 치료용 약학 조성물의 제조를 위한 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염의 용도.
<13> 기면증 치료에서 사용하기 위한 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염.
<14> 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염을 포함하는 탈력 발작 치료제.
<15> 대상체에 약리학적 유효 용량의 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염을 투여하는 단계를 포함하는 탈력 발작의 치료 방법.
<16> 탈력 발작의 치료에서 사용하기 위한 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염.
<17> 탈력 발작 치료용 약학 조성물의 제조를 위한 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염의 용도.
<18> 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염을 포함하는 수면과다 증후군 치료제.
<19> 대상체에 약리학적 유효 용량의 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염을 투여하는 단계를 포함하는 수면과다 증후군의 치료 방법.
<20> 수면과다 증후군의 치료에서 사용하기 위한 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염.
<21> 수면과다 증후군 치료용 약학 조성물의 제조를 위한 상기 <1> 내지 <5> 중 어느 하나에 따른 화합물 또는 이의 약학적으로 허용되는 염의 용도.
본 발명에 따른 화학식 I, II, III 및 IV로 표현되는 치환된 피페리딘 화합물(이하, 화합물 I, II, III 및 IV로 지칭함) 또는 이의 약학적으로 허용되는 염은 아래에 기재되는 약리학적 시험 실시예에서 활성 데이터로 표현한 바와 같이 오렉신 제2형 수용체-활성화 활성을 갖는다. 본 발명의 화합물 I, II, III 및 IV는 오렉신 제2형 수용체-활성화 활성을 가지며 기면증 치료제로서 사용될 수 있다.
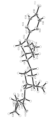
도 1은 실시예 1에서 수득한 화합물의 X-선 결정학 분석의 결과를 보여주는 ORTEP 다이어그램이다.
도 2는 실시예 3에서 수득한 화합물(2개의 부가된 아세토니트릴 분자를 포함하는 이량체)의 X-선 결정학 분석의 결과를 보여주는 ORTEP 다이어그램이다.
도 3은 실시예 4에서 수득한 화합물의 X-선 결정학 분석의 결과를 보여주는 ORTEP 다이어그램이다.
도 2는 실시예 3에서 수득한 화합물(2개의 부가된 아세토니트릴 분자를 포함하는 이량체)의 X-선 결정학 분석의 결과를 보여주는 ORTEP 다이어그램이다.
도 3은 실시예 4에서 수득한 화합물의 X-선 결정학 분석의 결과를 보여주는 ORTEP 다이어그램이다.
본 발명은 이제 상세히 설명될 것이다.
본 발명의 화합물의 다형 결정이 또한 존재할 수 있고, 임의의 결정 형태 또는 이들의 혼합물, 뿐만 아니라 비정질 형태가 임의의 제한 없이 사용될 수 있으면서, 본 발명의 화합물은 또한 무수 형태 및 용매화된(특히 수화된) 형태 둘 다를 포함한다.
화합물 I, II, III 및 IV의 동위원소-표지된 형태가 또한 본 발명에 포함된다. 하나 이상의 원자가 자연에서 일반적으로 관찰되는 원자량 또는 질량수와 상이한 원자량 또는 질량수를 갖는 원자로 대체된 것을 제외하고, 동위원소-표지된 화합물은 화합물 I, II, III 및 IV 중 임의의 것과 동일하다. 본 발명의 화합물에 혼입될 수 있는 동위원소의 예에는 수소의 동위원소, 탄소의 동위원소, 질소의 동위원소, 산소의 동위원소, 불소의 동위원소, 인의 동위원소, 황의 동위원소, 요오드의 동위원소 및 염소의 동위원소, 구체적으로 2H, 3H, 11C, 14C, 15N, 18O, 18F, 32P, 35S, 123I 및 125I가 포함된다.
동위원소-표지된 화합물, 예컨대 3H 및/또는 14C와 같은 방사성 동위원소를 포함하는 화합물은 약물 및/또는 기질의 조직 분포 분석에 유용하다. 동위원소 3H와 14C는 이의 제조 및 검출의 용이성으로 인해 유용한 것으로 간주된다. 동위원소 11C와 18F는 PET(양전자 방출 단층 촬영)에 유용한 것으로 간주되는 반면, 동위원소 125I는 SPECT(단일 광자 방출 컴퓨터 단층 촬영)에 유용한 것으로 간주되고, 따라서 이들 모두는 뇌 영상화에 유용하다. 더 무거운 동위원소에 의한 2H 등의 치환은 더 높은 대사 안정성으로 인해 특정 유형의 치료에 있어서 이점, 예컨대 더 긴 생체내 반감기 및 더 낮은 필요 용량을 제공하고, 따라서 일부 상황 하에 유용한 것으로 간주된다. 이러한 동위원소-표지된 화합물은 동위원소로 표지되지 않은 시약 대신에 용이하게 사용할 수 있는 동위원소-표지된 시약을 사용하여 아래 실시예에 개시된 절차에 의해 균일하게 제조될 수 있다.
"약학적으로 허용되는 염"은, 본원에 언급된 바와 같이, 본 발명의 화합물과 함께 형성되는 것이라면 특별히 한정되지 않으며, 구체적인 예로는 산 부가 염, 예컨대 무기산 염, 유기산 염 또는 산성 아미노산 염이 포함된다.
달리 명시되지 않는 한, 본원에서 사용된 용어 "약학적으로 허용되는 염"은, 적절한 비율로 형성된 염의 경우, 1 분자의 화합물에 대한 산 분자의 수가, 비제한적으로, 바람직하게는 1 분자의 화합물에 대해 약 0.5 내지 약 2 산 분자, 보다 바람직하게는 1 분자의 화합물에 대해 약 0.5, 약 1 또는 약 2 산 분자인 것을 지칭한다.
무기산 염의 바람직한 예에는 하이드로클로라이드, 하이드로브로마이드, 설페이트, 니트레이트 및 포스페이트가 포함되고, 유기산 염의 바람직한 예에는 아세테이트, 석시네이트, 퓨마레이트, 말레에이트, 타르트레이트, 시트레이트, 락테이트, 스테아레이트, 벤조에이트, 메탄설포네이트, p-톨루엔설포네이트 및 벤젠설포네이트가 포함된다.
산성 아미노산 염의 바람직한 예에는 아스파르트산 염 및 글루탐산 염이 포함된다.
본 발명의 화합물 I, II, III 및 IV 중 임의의 것이 유리 형태로 수득되는 경우, 이는 통상적인 방법으로 화합물 I, II, III 또는 IV의 허용되는 염 또는 수화물로 전환될 수 있다.
본 발명의 화합물 I, II, III 및 IV 중 어느 하나가 화합물 I, II, III 또는 IV의 염 또는 화합물 I, II, III 또는 IV의 수화물로서 수득되는 경우, 이는 통상적인 방법으로 화합물 I, II, III 또는 IV의 유리 형태로 전환될 수 있다.
본 발명의 화합물 I, II, III 및 IV에 대해 수득된 다양한 이성질체(예를 들어, 광학 이성질체, 회전 이성질체 및 입체 이성질체)는, 예를 들어 재결정화, 부분입체 이성질체 염 방법, 효소적 분해 또는 크로마토그래피 방법(예를 들어, 박층 크로마토그래피, 컬럼 크로마토그래피 또는 기체 크로마토그래피)과 같은 통상적인 분리 방법을 사용하여 정제되고 단리될 수 있다.
[제형화]
본 발명의 약학 조성물은, 약학적으로 허용되는 첨가제를 화합물 군 I, II, III 및 IV 중에서 선택되는 화합물 또는 이의 약학적으로 허용되는 염과 혼합함으로써 제조될 수 있다. 본 발명의 약학 조성물은 공지된 방법, 예컨대 문헌[General Rules for Preparations of the Japanese Pharmacopoeia, 17th Edition]에 기재된 방법에 의해 제조될 수 있다.
본 발명의 약학 조성물은 제형(dosage form)에 따라 적절하게 환자에게 투여될 수 있다.
본 발명에 따른 화합물 I, II, III 및 IV 중 임의의 것 또는 이의 약학적으로 허용되는 염의 투여량은 증상의 중증도, 환자의 연령, 성별 및 체중, 제형 또는 염의 유형, 및 질병의 특정 유형에 따라 달라질 수 있으나, 이는 일반적으로, 성인의 경우 1일 1회 또는 분할 용량으로, 경구 투여의 경우 약 30 μg 내지 10 g, 바람직하게는 100 μg 내지 5 g, 보다 더 바람직하게는 100 μg 내지 1 g일 것이고, 주사 투여의 경우 약 30 μg 내지 1 g, 바람직하게는 100 μg 내지 500 mg, 보다 더 바람직하게는 100 μg 내지 300 mg일 것이다.
본원에 사용된 바와 같이, "오렉신 제2형 수용체 작용제"는, 오렉신 제2형 수용체에 결합하고 오렉신 제2형 수용체 및 생체내 리간드를 활성화시키는 작용을 하는 제제를 지칭한다.
본 발명의 화합물은 또한 생리학적으로 활성인 저분자량 화합물의 표적 단백질을 포획하는 화학적 프로브로서 사용될 수 있다. 구체적으로, 본 발명의 화합물은, 예를 들어 문헌[J. Mass Spectrum. Soc. Jpn. Vol. 51, No. 5 2003, p492-498] 또는 WO2007/139149에 기재된 방법에 의해 이들의 활성 발현에 필수적인 구조적 부분 이외의 화합물의 부분에 표지기(labeling group) 또는 링커(linker)를 도입함으로써 친화성 크로마토그래피 또는 광친화성 프로브로 전환될 수 있다.
화학 프로브에 사용되는 표지기 또는 링커는, 예를 들어 하기 (1) 내지 (5) 중 어느 하나의 기일 수 있다.
(1) 광친화성 표지기(예를 들어, 벤조일, 벤조페논, 아지드, 카본일 아지드, 다이아지리딘, 엔온, 다이아조 및 니트로 기) 및 화학적 친화성 기(예를 들어, 알파 탄소 원자가 할로겐 원자로 치환된 케톤 기, 카바모일, 에스터 및 알킬티오 기, α,β-불포화 케톤, 마이클 수용체, 예컨대 에스터 및 옥시란)를 포함하는 단백질 표지기,
(2) 절단성 링커, 예컨대 -S-S-, -O-Si-O-, 모노사카라이드(예컨대, 글루코스 또는 갈락토스) 및 다이사카라이드(예컨대, 락토스), 및 효소 반응에 의해 절단가능한 올리고펩티드 링커,
(3) 피싱 태그(fishing tag) 기, 예컨대 비오틴, 3-(4,4-다이플루오로-5,7-다이메틸-4H-3a 및 4a-다이아자-4-보라-s-인다센-3-일)프로피온일,
(4) 방사성 표지기, 예컨대 125I, 32P, 3H 및 14C; 형광 표지기, 예컨대 플루오레세인, 로다민, 단실, 움벨리페론, 7-니트로푸라잔일, 3-(4,4-다이플루오로-5,7-다이메틸-4H-3a 및 4a-다이아자-4-보라-s-인다센-3-일)프로피온일 기; 화학발광 기, 예컨대 루미페린 및 루미놀; 및 중금속 이온, 예컨대 란탄족 금속 이온 및 라듐 이온을 포함하는 검출가능한 마커; 또는
(5) 고체상(solid phase) 담체, 예컨대 유리 비드(bead), 유리 베드(bed), 마이크로타이터 플레이트, 아가로스 비드, 아가로스 베드, 폴리스티렌 비드, 폴리스티렌 베드, 나일론 비드 및 나일론 베드와 결합하는 기.
상기 언급된 문헌에 기재된 방법에 의해 상기 (1) 내지 (5) 중에서 선택되는 표지기를 본 발명의 화합물에 도입함으로써 제조된 프로브는, 새로운 혁신적인 약물 개발 표적의 발견에 유용한 표지된 단백질의 식별을 위한 화학적 프로브로서 사용될 수 있다.
실시예
본 발명의 화합물 I, II, III 및 IV는 하기 실시예에 기재된 공정에 의해 제조될 수 있고, 화합물의 효과는 시험 실시예에 기재된 방법에 의해 확인될 수 있다. 그러나, 이들 특정 예는 단지 예시일 뿐이고 어떤 식으로든 본 발명을 제한하도록 의도되지 않으며, 예컨대 본 발명의 범위 내에서 다양한 변형이 또한 구현될 수 있다.
공개된 문헌과 관련하여 언급된 화합물은 해당 문헌에 기재된 방법으로 제조된다.
전반에 걸쳐 사용된 약어는 당업자에게 통상적으로 공지된 것이다. 특히 하기가 사용된다.
n-: 노멀(normal)
tert-: 3급
1H-NMR: 양성자 핵 자기 공명 분광법
MS: 질량 분석법
HPLC: 고성능 액체 크로마토그래피
실시예 및 제조 실시예 전반에 걸쳐 사용된 용어 "실온"은 일반적으로 약 10℃ 내지 35℃의 범위를 지칭한다. 백분율 값은 달리 명시되지 않는 한 중량%이다.
양성자 핵 자기 공명 스펙트럼의 화학적 이동은 테트라메틸실란에 대해 δ 단위(ppm)로 기록되고, 커플링 상수는 헤르츠(Hz)로 기록된다. 패턴은 하기와 같이 표현된다: s: 단일항, d: 이중항, t: 삼중항, q: 사중항, m: 다중항, br: 넓음, 및 brs: 넓은 단일항.
질량 분석을, Waters Co.의 Acquity UPLCTM 또는 Acquity UPC2TM을 사용하여 수행하였다.
크로마토그래피를 위해, Merck의 Silica Gel60(70 내지 230 메쉬 또는 230 내지 400 메쉬 ASTM) 또는 Fuji Silysia Chemical, Ltd.의 PSQ60B를 실리카겔로서 사용하거나, 사전에 패킹된 컬럼{컬럼: Yamazen의 Hi-FlashTM Column(실리카겔), 크기: S(16 × 60 mm), M(20 × 75 mm), L(26 × 100 mm), 2L(26 × 150 mm) 또는 3L(46 × 130 mm), 또는 Biotage Co.의 BiotageTM SNAP Ultra Silica Cartridge, 크기: 10 g, 25 g 또는 50 g}을 사용하였다. 초임계 유체 크로마토그래피(SFC)에 의한 분획을 Waters Co.의 Prep100q를 사용하여 수행하였다.
NH 실리카겔로서, Fuji Silysia Chemical, Ltd.의 CHROMATOREX NH-DM2035를 사용하거나, 사전 패킹된 컬럼{컬럼: Yamazen의 Hi-FlashTM Column(Amino), 크기: S(16 × 60 mm), M(20 × 75 mm), L(26 × 100 mm), 2L(26 × 150 mm) 또는 3L(46 × 130 mm), 또는 Wako Pure Chemical Industries, Ltd.의 PresepTM(Luer Lock) NH2(HC), 크기: 유형 M(14 g/25 mL), 유형 L(34 g/70 mL), 유형 2L(50 g/100 mL) 또는 유형 3L(110 g/200 mL)}을 사용하였다.
하기 화합물의 명명법은 통상적으로 사용되는 시약을 제외하고 "E-Notebook" 버전 12 또는 13(Perkin-Elmer)에 나타낸 것과 같다.
제조 실시예 1
2-브로모-2-사이클로프로필 아세트아미드의 합성
옥살릴 클로라이드(CAS 번호 79-37-8)(3.11 mL, 36.3 mmol) 및 N,N-다이메틸포름아미드(60.0 μL, 0.775 mmol)를 1,2-다이클로로에탄(60 mL) 중의 사이클로프로필아세트산(CAS 번호 5239-82-7)(3.30 g, 33.0 mmol)의 용액에 첨가하고, 혼합물을 40분 동안 실온에서 교반하였다. 브롬화 수소산(56.0 mg, 0.330 mmol) 및 N-브로모석신이미드(CAS 번호 128-08-5)(7.04 g, 39.6 mmol)를 반응 혼합물에 첨가한 후에, 이를 18시간 동안 가열하여 환류시켰다. 반응 혼합물을 0℃에서 암모니아(28% 수용액, 60 mL, 2.77 mol)에 첨가한 후에, 에틸 아세테이트 및 수산화 나트륨(2 N 수용액)을 분리를 위해 첨가하였다. 유기층을 무수 황산 마그네슘으로 건조시키고 여과하고 감압 하에 농축하였다. 생성된 고체를 에틸 아세테이트/n-헵탄을 사용하여 마쇄하고, 침전물을 여과하였다. 생성된 고체를 감압 하에 건조시켜 표제 화합물(1.20 g)을 수득하였다.
MS (ESI)m/z: 178[M+H]+
제조 실시예 2
3-메톡시이소니코티노니트릴의 합성
나트륨 에톡사이드(CAS 번호 124-41-4)(3.90 g, 72.2 mmol)를 실온에서 테트라하이드로퓨란(36.0 mL) 중의 3-클로로-4-시아노피리딘(CAS 번호 68325-15-5)(5.00 g, 36.1 mmol)의 용액에 첨가하고, 혼합물을 1시간 동안 가열하여 환류시켰다. 물 및 에틸 아세테이트를 반응 혼합물에 첨가하고, 유기층을 분리하였다. 유기층을 무수 황산 마그네슘으로 건조시키고 여과하고 감압 하에 농축하였다. 생성된 고체를 에틸 아세테이트/n-헵탄을 사용하여 마쇄하고, 침전물을 여과하였다. 생성된 고체를 감압 하에 건조시켜 표제 화합물(1.91 g)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 4.06 (s, 3H), 7.44 (d, J = 5.0 Hz, 1H), 8.37 (d, J = 4.5 Hz, 1H), 8.49 (s, 1H).
MS (ESI)m/z: 135[M+H]+
제조 실시예 3
(R)-2-브로모-3-메틸부탄아미드의 합성
옥살릴 클로라이드(9.28 mL, 108 mmol) 및 N,N-다이메틸포름아미드(30.0 μL, 0.387 mmol)를 0℃에서 메틸렌 클로라이드(100 mL) 중의 (R)-2-브로모-3-메틸부티르산(CAS 번호 76792-22-8)(9.80 g, 54.1 mmol)의 용액에 첨가하고, 혼합물을 6시간 동안 실온에서 교반하였다. 반응 혼합물을 0℃에서 암모니아(28% 수용액, 50.0 mL, 2.31 mol)에 첨가한 후에, 메틸렌 클로라이드로 추출하였다. 유기층을 무수 황산 마그네슘으로 건조시키고 여과하고 감압 하에 농축하였다. 생성된 고체를 에틸 아세테이트/n-헵탄을 사용하여 마쇄하고, 침전물을 여과하였다. 생성된 고체를 감압 하에 건조시켜 표제 화합물(8.20 g)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 1.01 (d, J = 6.3 Hz, 3H), 1.07 (d, J = 6.8 Hz, 3H), 2.34-2.39 (m, 1H), 4.28 (d, J = 4.5 Hz, 1H), 5.58 (brs, 1H), 6.41 (brs, 1H).
MS (ESI)m/z: 180[M+H]+
제조 실시예 4
(1R,3s,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄의 합성
(1)
tert
-부틸 (1R,3r,5S)-3-하이드록시-3-(3-메톡시피리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트의 합성
3-메톡시이소니코티노니트릴(1.19 g, 8.88 mmol) 및 비스(피나콜라토)다이보론(CAS 번호 73183-34-3)(2.25 g, 8.88 mmol)을 메틸 tert-부틸 에터(18.0 mL) 중의 N-(tert-부톡시카본일)-노르트로피논(CAS 번호 185099-67-6)(1.00 g, 4.44 mmol)의 용액에 첨가한 후에, 혼합물을 16시간 동안 가열하여 환류시켰다. 탄산 나트륨(2 mol/L 수용액, 20.0 mL)을 0℃에서 반응 혼합물에 첨가하고, 혼합물을 20분 동안 0℃에서 교반하였다. 에틸 아세테이트를 반응 혼합물에 첨가하고, 유기층을 분리하였다. 유기층을 무수 황산 마그네슘으로 건조시키고 여과하고 감압 하에 농축하였다. 잔사를 컬럼 크로마토그래피(실리카겔, 0 내지 20% 메탄올/에틸 아세테이트)로 정제하여 표제 화합물(1.12 g)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 1.48 (s, 9H), 1.77 (m, 2H), 1.94-1.99 (m, 2H), 2.21-2.32 (m, 2H), 2.37-2.48 (m, 1H), 2.63-2.74 (m, 1H), 2.78 (s, 1H), 3.96 (s, 3H), 4.22-4.29 (m, 1H), 4.31-4.42 (m, 1H), 7.28 (d, J = 5.4 Hz, 1H), 8.22-8.25 (m, 2H).
MS (ESI)m/z: 335[M+H]+
(2)
tert
-부틸 (1R,5S)-3-(3-메톡시피리딘-4-일)-8-아자바이사이클로[3.2.1]옥트-2-엔-8-카복실레이트의 합성
진한 황산(1.60 mL, 30.0 mmol)을 tert-부틸 (1R,3r,5S)-3-하이드록시-3-(3-메톡시피리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(610 mg, 1.82 mmol)에 첨가하고, 혼합물을 40분 동안 실온에서 교반하였다. 반응 혼합물을 0℃에서 물(10.0 mL) 중의 수산화 칼륨(5.00 g, 89.1 mmol)의 용액에 첨가하였다. 테트라하이드로퓨란(10.0 mL) 및 다이-tert-부틸 다이카보네이트(CAS 번호 24424-99-5)(478 mg, 2.19 mmol)를 반응 혼합물에 첨가한 후에, 이를 10분 동안 실온에서 교반하였다. 에틸 아세테이트를 반응 혼합물에 첨가하고, 유기층을 분리하였다. 유기층을 무수 황산 마그네슘으로 건조시키고 여과하고 감압 하에 농축하였다. 잔사를 컬럼 크로마토그래피(실리카겔, 5 내지 100% 에틸 아세테이트/n-헵탄)로 정제하여 표제 화합물(420 mg)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 1.46 (s, 9H), 1.72-1.81 (m, 1H), 1.97-2.03 (m, 2H), 2.05-2.36 (m, 2H), 2.94-3.26 (m, 1H), 3.87 (s, 3H), 4.21-4.61 (m, 2H), 6.30 (brs, 1H), 6.99 (d, J = 4.5 Hz, 1H), 8.17 (d, J = 5.0 Hz, 1H), 8.21 (s, 1H).
MS (ESI)m/z: 317[M+H]+
(3)
tert
-부틸 (1R,5S)-3-(3-메톡시피리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트의 합성
10% 팔라듐-탄소(AD, 52.7% 수성, 284 mg, 0.126 mmol, Kawaken Fine Chemicals Co., Ltd. 제품)를 메탄올(3.00 mL) 중의 tert-부틸 (1R,5S)-3-(3-메톡시피리딘-4-일)-8-아자바이사이클로[3.2.1]옥트-2-엔-8-카복실레이트(400 mg, 1.26 mmol)의 용액에 첨가한 후에, 혼합물을 1시간 동안 실온에서 수소 대기 하에 교반하였다. 반응 혼합물을 CeliteTM로 여과하고, 잔사를 에틸 아세테이트로 세정하였다. 수득한 여과액을 감압 하에 농축하여 엔도 형태 및 엑소 형태의 혼합물(엔도:엑소 = 1:2, 398 mg)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 1.49 (s, 6H), 1.50 (s, 3H), 1.61-2.13 (m, 22/3H), 2.40-2.45 (m, 2/3H), 2.96-3.01 (m, 1/3H), 3.47-3.59 (m, 2/3H), 3.88 (s, 1H), 3.90 (s, 2H), 4.16-4.28 (m, 1H), 4.34 (brs, 1H), 7.04 (d, J = 4.5 Hz, 2/3H), 7.06 (d, J = 5.0 Hz, 1/3H), 8.13-8.23 (m, 2H).
MS (ESI)m/z: 319[M+H]+
(4)
tert
-부틸 (1R,3s,5S)-3-(3-메톡시피리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트의 합성
칼륨 tert-부톡사이드(281 mg, 2.50 mmol)를 tert-부탄올(4.00 mL) 중의 tert-부틸 (1R,5S)-3-(3-메톡시피리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(398 mg, 1.25 mmol)의 용액에 첨가하고, 혼합물을 17시간 동안 가열하여 환류시켰다. 에틸 아세테이트 및 염수를 반응 혼합물에 첨가하고, 유기층을 분리하였다. 이어서, 유기층을 무수 황산 마그네슘으로 건조시키고 여과하고 감압 하에 농축하여 표제 화합물(385 mg)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 1.49 (s, 9H), 1.58-2.06 (m, 8H), 3.49-3.56 (m, 1H), 3.90 (s, 3H), 4.24 (brs, 1H), 4.34 (brs, 1H), 7.04 (d, J = 5.0 Hz, 1H), 8.17-8.19 (m, 2H).
MS (ESI)m/z: 319[M+H]+
(5)
tert
-부틸 (1R,3s,5S)-3-(1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트의 합성
10% 팔라듐-탄소(AD, 52.7% 수성, 7.91 g, 3.52 mmol, Kawaken Fine Chemicals Co., Ltd. 제품)를 아세트산(100 mL) 중의 tert-부틸 (1R,3s,5S)-3-(3-메톡시피리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(11.2 g, 35.2 mmol)의 용액에 첨가한 후에, 혼합물을 18시간 동안 70℃에서 수소 대기 하에 교반하였다. 반응 혼합물을 CeliteTM로 여과하고, 잔사를 에틸 아세테이트로 세정하였다. 여과액을 감압 하에 농축하였다. 에틸 아세테이트 및 수산화 나트륨(2 N)을 잔사에 첨가하고, 유기층을 분리하였다. 유기층을 ISOLUTETM HM-N으로 건조시키고 여과하고 감압 하에 농축하였다. N,N-다이메틸포름아미드(50.0 mL), 2-클로로-5-플루오로피리미딘(CAS 번호 62802-42-0)(5.21 mL, 42.2 mmol) 및 탄산 칼륨(7.29 g, 52.8 mmol)을 잔사에 첨가한 후에, 혼합물을 40분 동안 80℃에서 교반하였다. 에틸 아세테이트 및 염수를 반응 혼합물에 첨가하고, 유기층을 분리하였다. 유기층을 무수 황산 마그네슘으로 건조시키고 여과하고 감압 하에 농축하였다. 잔사를 컬럼 크로마토그래피(실리카겔, 10 내지 60% 에틸 아세테이트/n-헵탄)로 정제하여 표제 화합물(9.84 g)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 1.19-1.30 (m, 3H), 1.46 (s, 9H), 1.46-1.65 (m, 6H), 1.81-1.97 (m, 3H), 2.68 (d, J = 14.5 Hz, 1H), 2.71-2.81 (m, 1H), 3.30 (s, 3H), 3.35 (brs, 1H), 4.08-4.31 (m, 2H), 4.64-4.77 (m, 1H), 5.04-5.18 (m, 1H), 8.13 (s, 2H).
MS (ESI)m/z: 421[M+H]+
(6)
tert
-부틸 (1R,3s,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트의 합성
화합물 tert-부틸 (1R,3s,5S)-3-(1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(7.00 g, 16.6 mmol)를 Daicel의 CHIRALPAKR IC/SFC(3 cm × 25 cm)를 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(90:10), 120 bar, 40℃, 유량: 100 mL/분)에 의해 한 번에 100 mg을 분획화하여 후속 용리되는 표제 화합물(3.02 g)을 체류 시간 8.45분에 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 1.17-1.29 (m, 3H), 1.46 (s, 9H), 1.46-1.66 (m, 6H), 1.85-1.97 (m, 3H), 2.68 (d, J = 15.0 Hz, 1H), 2.75 (td, J = 12.9, 3.2 Hz, 1H), 3.30 (s, 3H), 3.35 (brs, 1H), 4.11-4.31 (m, 2H), 4.66-4.76 (m, 1H), 5.10 (dt, J = 14.4, 2.6 Hz, 1H), 8.13 (s, 2H).
MS (ESI)m/z: 443[M+Na]+
(분석 조건) Daicel의 CHIRALPAKTM IC-3(3.0 mm × 50 mm)을 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(85:15), 40℃, 유량: 1.2 mL/분, 검출: UV(254 nm)).
(분석 결과) 표제 화합물의 체류 시간은 1.34분이었고, 광학 순도는 >99% ee였다.
(7) (1R,3s,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄의 합성
트라이플루오로아세트산(5.00 mL, 64.9 mmol)을 tert-부틸 (1R,3s,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(1.00 g, 2.38 mmol)에 첨가하고, 혼합물을 20분 동안 실온에서 교반하였다. 반응 혼합물을 감압 하에 농축하였다. 2 N 수산화 나트륨 포화 수용액을 잔사에 첨가하고, 추출을 에틸 아세테이트를 사용하여 수행하였다(3회). 합한 유기층을 무수 황산 마그네슘으로 건조시키고 여과하고 감압 하에 농축하여 표제 화합물(620 mg)을 수득하였다.
MS (ESI)m/z: 321[M+H]+
제조 실시예 5
(S)-2-브로모-2-사이클로프로필 아세트아미드의 합성
(1) (S)-3-(2-사이클로프로필아세틸)-4-페닐옥사졸리딘-2-온의 합성
피발로일 클로라이드(302 mL, 2470 mmol)를 실온에서 테트라하이드로퓨란(7000 mL)에 첨가하였다. 사이클로프로필아세트산(238 mL, 2450 mmol)을 실온에서 첨가하고, 혼합물을 0℃까지 냉각시켰다. 트라이에틸아민(350 mL)을 10분의 기간에 걸쳐 적가한 후에, 트라이에틸아민(400 mL, 총량: 5340 mmol)을 첨가하고, 혼합물을 76분 동안 0℃에서 교반하였다. 이어서, (S)-4-페닐옥사졸리딘-2-온(350 g, 2140 mmol)을 반응 혼합물에 모두 한 번에 첨가한 후에, 염화 리튬(109 g, 2570 mmol)을 모두 한 번에 추가로 첨가하였다. 반응 혼합물을 18시간 동안 실온에서 교반한 후에, 에틸 아세테이트(7000 mL) 및 물(3500 mL)을 첨가하고, 혼합물을 40분 동안 실온에서 교반하였다. 유기층을 분리하고 5% 탄산수소 나트륨 수용액(3500 mL) 및 물(1750 mL)로 순서대로 세정하였다. 수득한 유기층을 1750 mL로 농축하였다. 에틸 아세테이트(2100 mL)를 첨가하고 1750 mL로 농축하는 공비 절차를 3회 반복한 후에, 에틸 아세테이트(1050 mL)를 첨가하고, 혼합물을 1750 mL로 농축하였다. 수득한 농축물을 교반하고, n-헵탄(1000 mL)을 적가하였다. 이렇게 제조한 현탁액을 10분 동안 교반하고, n-헵탄(2500 mL)을 추가로 적가하였다. 액체 혼합물을 밤새 실온에서 교반한 후에, 3.5시간 동안 0℃에서 추가로 교반하였다. 생성된 고체를 유리 필터를 사용하여 여과하고 에틸 아세테이트/n-헵탄(1:3 혼합물 550 mL)으로 세정하였다. 생성된 고체를 감압 하에 건조시켜 표제 화합물(407 g)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 0.09-0.24 (m, 2H)0.46-0.58 (m, 2H)1.00-1.13 (m, 1H), 2.74-2.83 (m, 1H), 2.88-2.98 (m, 1H), 4.25-4.32 (m, 1H), 4.70 (t, J = 8.83 Hz, 1H), 5.45 (dd, J = 8.83, 3.85 Hz, 1H), 7.28-7.43 (m, 5H).
(2) (S)-2-브로모-2-사이클로프로필 아세트아미드의 합성
얼음 상에서 냉각시키면서 다이부틸보론 트라이플레이트의 1 M 다이클로로메탄 용액(500 mL, 500 mmol)을 다이클로로메탄(1000 mL) 중의 (S)-3-(2-사이클로프로필아세틸)-4-페닐옥사졸리딘-2-온(100 g, 408 mmol)의 용액에 40분의 기간에 걸쳐 적가한 후에, 얼음 상에서 냉각시키면서 혼합물을 10분 동안 교반하였다. 얼음 상에서 냉각시키면서 N,N-다이이소프로필에틸아민(92 mL, 530 mmol)을 25분의 기간에 걸쳐 적가한 후에, 얼음 상에서 냉각시키면서 혼합물을 1시간 동안 교반하였다. 이어서, 반응 혼합물을 드라이아이스-에탄올 욕에서 -72℃의 내부 온도까지 냉각시켰다. 이어서, N-브로모석신이미드(80 g, 448 mmol)를 모두 한 번에 첨가하고, 혼합물을 드라이아이스-에탄올 욕에서 1시간 20분 동안 교반하였다. 28 내지 30% 암모니아수(800 mL, 6390 mmol) 및 테트라하이드로퓨란(1000 mL)을 첨가한 후에, 혼합물을 2시간 동안 수 욕에서 교반하였다. 유기층과 수층을 분리하고, 수층을 3회 에틸 아세테이트(500 mL)로 추출하였다. 수득한 유기층을 감압 하에 농축하고, 수득한 잔사를 실리카겔 컬럼 크로마토그래피(4 kg 실리카겔, 30 내지 40% 에틸 아세테이트/n-헵탄)로 정제하여 미가공 생성물(132 g)을 수득하였다. tert-부틸 메틸 에터(1440 mL)를 수득한 미가공 생성물에 첨가하고 1시간 동안 50℃에서 용해될 때까지 교반한 후에, 혼합물을 1일 동안 실온에서 추가로 교반하였다. 생성된 고체를 여과하고 tert-부틸 메틸 에터(200 mL)로 세정하였다. 여과액 및 세정 용액을 합하고, 에틸 아세테이트(700 mL) 및 활성탄(SEISEI SHIRASAGI, 26 g)을 첨가하고, 혼합물을 30분 동안 실온에서 교반하였다. 활성탄을 CeliteR 여과로 제거하고, 활성탄을 에틸 아세테이트(700 mL)로 세정하였다. 여과액 및 세정 용액을 합한 후에, 혼합물을 감압 하에 농축하여 표제 화합물(97.1 g, 65.9% 함량)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 0.40-0.52 (m, 1H), 0.63-0.73 (m, 1H), 0.77-0.86 (m, 1H), 0.86-0.97 (m, 1H), 1.41-1.50 (m, 1H), 3.59-3.83 (m, 1H), 5.34-5.71 (m, 1H), 5.94-6.30 (m, 1H).
MS (ESI)m/z: 180[M+H]+
(분석 조건) Daicel의 CHIRALPAKTM IA(0.46 cm × 25 cm × 2)를 사용하는 크로마토그래피(이동상: 에탄올:n-헥산(10:90), 40℃, 유량: 0.8 mL/분, 검출: UV(210 nm)).
(분석 결과) 표제 화합물의 체류 시간은 24.5분이었다.
실시예 1
(R)-2-사이클로프로필-2-((1R,3S,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)아세트아미드의 합성
2-브로모-2-사이클로프로필 아세트아미드(433 mg, 2.43 mmol), 탄산 세슘(793 mg, 2.43 mmol) 및 산화 은(564 mg, 2.43 mmol)을 아세토니트릴(4.00 mL) 중의 (1R,3S,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄(260 mg, 0.811 mmol)의 용액에 첨가한 후에, 혼합물을 40시간 동안 실온에서 교반하였다. 반응 혼합물을 직접 컬럼 크로마토그래피(실리카겔, 20% 메탄올/에틸 아세테이트)로 정제하였다. 수득한 생성물을 메탄올(10 mL)에 용해시키고 Waters Porapak RxnTM CX(2개의 2 g 카트리지)에 제공하였다. 각각의 고체상을 메탄올(20 mL)로 세정한 후에, 각각의 생성물을 암모니아(2 mol/L 메탄올 용액, 20 mL)로 용리시키고, 용리액을 합하고 감압 하에 농축하였다. 잔사를 메탄올에 용해시키고 실행마다 10 mg/500 μL(메탄올)에서 Daicel의 CHIRALPAKTM(OD-H/SFC(2 cm × 25 cm)를 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(85:15), 120 bar, 40℃, 유량: 70 mL/분)로 분획화하여 6.41분의 체류 시간을 갖는 화합물(120 mg)을 거울상 이성질체 혼합물로서 수득하였다. 수득한 화합물을 메탄올에 용해시키고 실행마다 13 mg/500 μL(메탄올)에서 Daicel의 CHIRALPAKTM (IG/SFC(2 cm × 25 cm)를 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(75:25), 120 bar, 40℃, 유량: 70 mL/분)로 분획화하여 9.11분의 체류 시간을 갖는, 후속 용리 성분으로 주로 구성된 화합물(75 mg)을 수득하였다. 수득한 화합물을 메탄올에 용해시키고 실행마다 4 mg/100 μL(메탄올)에서 Daicel의 CHIRALPAKTM (IG/SFC(2 cm × 25 cm)를 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(75:25), 120 bar, 40℃, 유량: 70 mL/분)로 분획화하여 7.52분의 체류 시간을 갖는, 후속 용리 성분으로 주로 구성된 화합물(52 mg)을 수득하였다. 수득한 화합물을 메탄올에 용해시키고 실행마다 7 mg/500 μL(메탄올)에서 Daicel의 CHIRALPAKTM (IG/SFC(2 cm × 25 cm)를 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(75:25), 120 bar, 40℃, 유량: 70 mL/분)로 분획화하여 7.18분의 체류 시간을 갖는, 후속 용리 성분으로 주로 구성된 표제 화합물(31.3 mg)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 0.28-0.37 (m, 1H), 0.45-0.52 (m, 1H), 0.53-0.58 (m, 1H), 0.60-0.68 (m, 1H), 0.78 (dd, J = 8.8, 4.3 Hz, 1H), 1.20-1.27 (m, 2H), 1.32-1.45 (m, 2H), 1.46-1.52 (m, 2H), 1.59-1.65 (m, 3H), 1.70-1.80 (m, 2H), 1.81-1.88 (m, 1H), 2.08 (d, J = 9.1 Hz, 1H), 2.68 (dd, J = 14.3, 1.1 Hz, 1H), 2.75 (td, J = 12.8, 2.9 Hz, 1H), 3.21-3.24 (m, 1H), 3.30 (s, 3H), 3.36 (brs, 1H), 3.86-3.91 (m, 1H), 4.65-4.76 (m, 1H), 5.10 (dt, J = 14.2, 2.4 Hz, 1H), 5.14-5.24 (m, 1H), 6.92-7.02 (m, 1H), 8.14 (s, 2H).
MS (ESI)m/z: 418[M+H]+
(분석 조건) Daicel의 CHIRALPAKTM IA(0.46 cm × 15 cm)를 사용하는 크로마토그래피(이동상: 에탄올:헥산(20:80), 40℃, 유량: 1 mL/분, 검출: UV(254 nm)).
(분석 결과) 표제 화합물의 체류 시간은 4.91분이었고, 광학 순도는 >99% ee였다.
(R)-2-사이클로프로필-2-((1R,3S,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)아세트아미드 단결정의 제조 및 X-선 결정학 분석
실시예 1에서 수득한 표제 화합물(2.97 mg)을 메탄올(1 mL)에 용해시켰다. 바이알에 상기 용액(500 μL)을 넣은 후에, 캡을 약하게 닫았다(용매 증발법). 1일 후에, 표제 화합물의 단결정을 바이알에서 수득하였다. 수득한 단결정을 하기 조건 하에서 X-선 결정학 분석을 행하였다. 표제 화합물의 X-선 결정 구조를 도 1에 나타내었다.
분석 기기: XtaLAB PRO P200 MM007HF(Rigaku, Japan)
소프트웨어: CrysAlisPro(Rigaku Oxford Diffraction)
X-선: 다층 거울 단색화된 Cu-Kα(40 kV/30 mA)
측정: ω 축 진동 방법
카메라 길이: 35 mm
측정 온도: -170℃
실시예 1에서 합성한 (R)-2-사이클로프로필-2-((1R,3S,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)아세트아미드의 IUPAC 명칭은 (2R)-2-사이클로프로필-2-{(1R,3S,5S)-3-[(3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일]-8-아자바이사이클로[3.2.1]옥탄-8-일}아세트아미드이다.
실시예 2
(R)-2-((1R,3S,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)-3-메틸부탄아미드의 합성
(R)-2-브로모-3-메틸 부탄아미드(326 mg, 1.81 mmol), 탄산 세슘(590 mg, 1.81 mmol) 및 산화 은(419 mg, 1.81 mmol)을 아세토니트릴(8.00 mL) 중의 (1R,3s,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄(290 mg, 0.905 mmol)의 용액에 첨가한 후에, 혼합물을 40시간 동안 실온에서 교반하였다. 반응 혼합물을 실리카겔로 여과하고, 잔사를 20% 메탄올/에틸 아세테이트로 세정하였다. 여과액을 감압 하에 농축하였다. 잔사를 메탄올(5 mL)에 용해시키고 Waters Porapak RxnTM CX(벌크, 4 g)에 제공하였다. 고체상을 메탄올(40 mL)로 세정한 후에, 생성물을 암모니아(2 N 메탄올 용액, 40 mL)로 용리시키고, 용리액을 감압 하에 농축하였다. 잔사를 실행마다 5 mg에서 Daicel의 CHIRALPAKTM (IG/SFC(2 cm × 25 cm)를 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(80:20), 120 bar, 40℃, 유량: 70 mL/분)로 분획화하여 4.41분의 체류 시간을 갖는 표제 화합물(154 mg)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 0.95 (d, J = 6.8 Hz, 3H), 1.02 (d, J = 6.8 Hz, 3H), 1.15-1.56 (m, 8H), 1.75 (td, J = 10.8, 6.1 Hz, 3H), 1.86-2.10 (m, 2H), 2.67 (d, J = 13.1 Hz, 1H), 2.75 (td, J = 12.9, 3.2 Hz, 1H), 2.95 (d, J = 4.1 Hz, 1H), 3.19-3.27 (m, 1H), 3.30 (s, 3H), 3.33-3.46 (m, 2H), 4.70 (dt, J = 13.3, 2.2 Hz, 1H), 5.06-5.16 (m, 1H), 5.30-5.36 (m, 1H), 6.79 (brd, J = 5.0 Hz, 1H), 8.14 (s, 2H).
MS (ESI)m/z: 421[M+H]+
실시예 3
(R)-2-((1R,3S,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-에톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)-2-사이클로프로필 아세트아미드의 합성
(1)
tert
-부틸 (1R,3s,5S)-3-((3S,4R)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트 헤미(2S, 3S)-2,3-비스((4-메틸벤조일)옥시)석시네이트의 합성
tert-부틸 (1R,3s,5S)-3-(3-메톡시피리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(20 g, 62.8 mmol) 및 10% 팔라듐-탄소(유형 AD, 약 50% 수성, 6 g, Kawaken Fine Chemicals Co., Ltd. 제품)의 아세트산(160 mL) 혼합물을 밤새 70℃에서 수소 대기 하에 교반하였다. 팔라듐-탄소를 여과로 제거하고 메탄올(10-배 부피)로 세정하였고, 여과액을 약 2-배 농축하였다. 이소프로필 아세테이트(15-배 부피) 및 n-헵탄(3-배 부피)을 수득한 농축물에 첨가한 후에, 혼합물을 48% 수산화 나트륨 수용액(54.7 mL)으로 세정하였다. 이어서, n-헵탄(100 mL)을 첨가하고 물(5-배 부피)로 세정한 후에, 이를 약 5-배 농축하였다. 이소프로필 아세테이트(5-배 부피)를 수득한 농축물에 첨가하고 약 5-배 농축하는 공비 절차를 2회 반복하여 tert-부틸 (1R,3s,5S)-3-(3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(15.1 g)를 이소프로필 아세테이트 용액으로서 수득하였다.
(-)-다이-파라-톨루오일-L-타르타르산(2.70 g, 6.98 mmol)을 이소프로필 아세테이트(151 mL), 아세토니트릴(30.2 mL) 및 메탄올(38 mL) 중의 수득한 tert-부틸 (1R,3s,5S)-3-(3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(7.55 g, 23.3 mmol) 및 (+)-다이피발로일-D-타르타르산(1.85 g, 5.82 mmol)의 용액에 첨가한 후에, 혼합물을 3일 동안 실온에서 교반하여 고체를 수득하였다.
수득한 고체를 여과한 후에, 이소프로필 아세테이트 및 아세토니트릴의 혼합된 용액(9/1)으로 세정하였다. 수득한 모액을 10-배 농축하고, 이소프로필 아세테이트(10-배 부피), 5 N 수산화 나트륨 수용액(4.65 ml, 23.269 mmol) 및 물(4-배 부피)을 첨가하였다. 수층을 제거한 후에, 이를 물(4-배 부피)로 세정하였다. 이어서, 약 5-배 농축하고, 이소프로필 아세테이트(10-배 부피)를 첨가하고, 공비 증류를 약 5-배까지 수행한 후에, (+)-다이-파라-톨루오일-D-타르타르산(3.15 g, 8.144 mmol)을 메탄올(38 mL), 아세토니트릴(30.2 mL) 및 이소프로필 아세테이트(151 mL) 중의 (+)-다이피발로일-D-타르타르산(1.852 g, 5.817 mmol)의 용액에 첨가하고, 혼합물을 밤새 실온에서 교반하였다. 이어서, 화합물 (+)-다이-파라-톨루오일-D-타르타르산(0.05 당량) 및 이소프로필 아세테이트(10-배 부피)를 첨가하였다. 총량을 농축, 수산화 나트륨 중화 및 정제수 세정으로 회복시킨 후에, (+)-다이-파라-톨루오일-D-타르타르산(3.15 g, 8.144 mmol)을 이소프로필 아세테이트(151 mL), 아세토니트릴(30.2 mL) 및 메탄올(38 mL) 중의 (+)-다이피발로일-D-타르타르산(0.2 당량)의 용액에 첨가하고, 혼합물을 밤새 실온에서 교반하였다. 화합물 (+)-다이-파라-톨루오일-D-타르타르산(0.05 당량)을 반응 혼합물에 첨가하고, 혼합물을 4시간 동안 실온에서 교반하였다. 화합물 (+)-다이-파라-톨루오일-D-타르타르산(0.025 당량) 및 이소프로필 아세테이트(10-배 부피)를 반응 혼합물에 첨가하고, 혼합물을 밤새 실온에서 교반하였다. 총량을 농축, 수산화 나트륨 중화 및 정제수 세정으로 회복시키고, (+)-다이-파라-톨루오일-D-타르타르산(3.15 g, 8.14 mmol)을 이소프로필 아세테이트(151 mL), 아세토니트릴(30.2 mL) 및 메탄올(38 mL) 중의 (+)-다이피발로일-D-타르타르산(0.2 당량)의 용액에 첨가하고, 혼합물을 밤새 실온에서 교반하였다. 이어서, 이소프로필 아세테이트(10-배 부피)를 첨가하였다. 7시간 후에, 이렇게 생성된 고체를 여과하고 이소프로필 아세테이트로 세정하여 표제 화합물(3.45 g)을 수득하였다.
(분석 조건) Daicel의 CHIRALPAKTM IA(0.46 cm × 25 cm)를 사용하는 크로마토그래피(이동상: 에탄올:n-헥산(20:80), 40℃, 유량: 1.0 mL/분, 검출: UV(254 nm)).
(분석 결과) 표제 화합물의 체류 시간은 8.52분이었고, 광학 순도는 99.2% ee였다.
(2)
tert
-부틸 (1R,3s,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트의 합성
2,5-다이클로로피리미딘(288 mg, 1.93 mmol), tert-부틸 (1R,3s,5S)-3-((3S,4R)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트 헤미(2S, 3S)-2,3-비스((4-메틸벤조일)옥시)석시네이트(500 mg, 0.966 mmol) 및 탄산 칼륨(267 mg, 1.93 mmol)을 함유하는 N,N-다이메틸포름아미드(10 mL)를 24시간 동안 80℃에서 교반하였다. 반응 혼합물을 실온까지 냉각시킨 후에, 물을 첨가하고, 추출을 3회 에틸 아세테이트로 수행하였다. 유기층을 수집하고 농축하였다. 수득한 잔사를 컬럼 크로마토그래피(실리카겔, 10 내지 100% 에틸 아세테이트/n-헵탄)로 정제하여 표제 화합물(368 mg)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 1.24-1.27 (m, 2H), 1.41-1.49 (m, 2H), 1.46 (s, 9H), 1.61 (brs, 4H), 1.82-1.98 (m, 4H), 2.68 (d, J = 14.04 Hz, 1H), 2.75 (td, J = 12.91, 3.17 Hz, 1H), 3.30 (s, 3H), 3.36 (brs, 1H), 4.11-4.32 (m, 2H), 4.68-4.80 (m, 1H), 5.12 (dt, J = 14.27, 2.61 Hz, 1H), 8.16 (s, 2H).
(3)
tert
-부틸 (1R,3s,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-하이드록시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트의 합성
tert-부틸 (1R,3s,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(300 mg, 0.687 mmol) 및 48% 브롬화 수소산(5 mL)의 혼합물을 20분 동안 실온에서 교반한 후에, 2.5시간 동안 100℃에서 가열하였다. 이어서, 이를 밤새 실온에서 교반하고, 수득한 반응 혼합물을 감압 하에 농축하였다. 테트라하이드로퓨란(10 mL) 및 탄산수소 나트륨 포화 수용액을 수득한 잔사에 첨가한 후에, 다이-tert-부틸 다이카보네이트(165 mg, 0.755 mmol)를 실온에서 첨가하였다. UPLC로 반응의 완료를 확인한 후에, 에틸 아세테이트와 물을 첨가하고, 유기층을 분리하였다. 수층을 다시 에틸 아세테이트로 추출하고 이전에 수득한 유기층과 합하고 무수 황산 나트륨으로 건조시킨 후에, 감압 하에 농축하였다. 수득한 잔사를 10% 에틸 아세테이트/n-헵탄 혼합된 용매로 세정하여 표제 화합물(226 mg)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 1.28-1.34 (m, 2H), 1.46 (s, 9H), 1.59-1.72 (m, 6H), 1.75-1.97 (m, 4H), 2.70-2.83 (m, 1H), 2.91 (dd, J = 14.04, 0.91 Hz, 1H), 3.97-4.03 (m, 1H), 4.09-4.34 (m, 2H), 4.68-4.79 (m, 1H), 4.81-4.91 (m, 1H), 8.18 (s, 2H).MS (ESI)m/z: 423[M+H]+
(4)
tert
-부틸 (1R,3s,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-에톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트의 합성
얼음 상에서 냉각시키면서 수소화 나트륨(60%, 액체 파라핀에 분산됨, 7.09 mg, 0.177 mmol)을 N,N-다이메틸포름아미드(1 mL) 중의 tert-부틸 (1R,3s,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-하이드록시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(50 mg, 0.118 mmol)의 용액에 첨가하였다. 30분 동안 교반한 후에, 에틸 요오다이드(0.019 mL, 0.236 mmol)를 첨가하고, 혼합물을 16시간 동안 실온에서 교반하였다. 물 및 에틸 아세테이트를 반응 혼합물에 첨가한 후에, 유기층을 분리하고 농축하였다. 수득한 잔사를 컬럼 크로마토그래피(실리카겔, 1 내지 20% 에틸 아세테이트/n-헵탄)로 정제하여 표제 화합물(42.5 mg)을 수득하였다.
MS (ESI)m/z: 451[M+H]+
(5) (R)-2-((1R,3S,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-에톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)-2-사이클로프로필 아세트아미드의 합성
tert-부틸 (1R,3s,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-에톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(42.5 mg, 0.094 mmol)를 트라이플루오로아세트산(1 mL)으로 30분 동안 처리한 후에, 혼합물을 농축하였다. 수득한 잔사를 메탄올에 용해시키고 Waters Porapak RxnTM CX(0.4 g)에 제공하였다. 고체상을 메탄올(6 mL)로 세정한 후에, 생성물을 암모니아(2 mol/L 메탄올 용액, 6 mL)로 용리시키고, 용리액을 감압 하에 농축하였다. 수득한 잔사, 제조 실시예 5와 동일한 절차에 의해 수득한 (S)-2-브로모-2-사이클로프로필 아세트아미드(51.6 mg, 0.188 mmol), 탄산 칼륨(26.0 mg, 0.188 mmol) 및 아세토니트릴(2 mL)의 혼합물을 17일 동안 실온에서 교반하였다. 반응 혼합물을 아세토니트릴(3 mL)을 사용하여 여과하고, 수득한 여과액을 실행마다 500 μL에서 Daicel의 CHIRALPAKR (IA/SFC(3 cm × 25 cm)를 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(75:25), 120 bar, 40℃, 유량: 100 mL/분)로 분획화하여 7.55분의 체류 시간을 갖는 표제 화합물(22.2 mg)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 0.26-0.38 (m, 1H), 0.40-0.58 (m, 2H), 0.59-0.68 (m, 1H), 0.71-0.83 (m, 1H), 0.98-1.92 (m, 12H), 1.04 (t, J = 7.02 Hz, 3H), 2.07 (brd, J = 9.06 Hz, 1H), 2.61-2.81 (m, 2H), 3.13-3.30 (m, 2H), 3.45 (brs, 1H), 3.61-3.75 (m, 1H), 3.84-3.92 (m, 1H), 4.66-4.76 (m, 1H), 4.93-5.11 (m, 1H), 5.17-5.32 (m, 1H), 6.90-7.03 (m, 1H), 8.16 (s, 2H).
MS (ESI)m/z: 448[M+H]+
(분석 조건) Daicel의 CHIRALPAKTM IA-3(0.46 cm × 25 cm)을 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(80:20), 40℃, 유량: 1.2 mL/분, 검출: UV(257 nm)).
(분석 결과) 표제 화합물의 체류 시간은 2.19분이었고, 광학 순도는 >99.9% ee였다.
(R)-2-((1R,3S,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-에톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)-2-사이클로프로필 아세트아미드 단결정의 제조 및 X-선 결정학 분석
실시예 3에서 수득한 표제 화합물(1.37 mg)을 아세토니트릴(600 μL)에 용해시켰다. 바이알에 상기 용액(200 μL)을 넣은 후에, 캡을 약하게 닫았다(용매 증발법). 1일 후에, 표제 화합물의 단결정(2개의 아세토니트릴 기가 부가된 이량체의 결정)을 바이알에서 수득하였다. 수득한 단결정을 하기 조건 하에서 X-선 결정학 분석을 행하였다. 표제 화합물의 X-선 결정 구조를 도 2에 나타내었다.
분석 기기: XtaLAB PRO P200 MM007HF(Rigaku, Japan)
소프트웨어: CrysAlisPro(Rigaku Oxford Diffraction)
X-선: 다층 거울 단색화된 Cu-Kα(40 kV/30 mA)
측정: ω 축 진동 방법
카메라 길이: 35 mm
측정 온도: -170℃
실시예 4
(R)-2-사이클로프로필-2-((1R,3S,5S)-3-((2S, 4S)-1-(5-플루오로피리미딘-2-일)-2-메틸피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)아세트아미드의 합성
(1) 에틸 (1R,3s,5S)-3-((S)-2-메틸-1,2,3,6-테트라하이드로피리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트의 합성
13 mm 스크류 캡 시험 튜브에 에틸(1R,3s,5S)-3-(토실옥시)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(CAS 번호 2236076-85-8)(200 mg, 0.566 mmol), 니켈(II) 브로마이드-에틸렌글리콜 다이메틸 에터 착체(17.5 mg, 0.057 mmol), 4,4-다이-tert-부틸-2,2-다이피리딜(15.2 mg, 0.057 mmol), 칼륨 요오다이드(94.0 mg, 0.566 mmol) 및 망간(62.2 mg, 1.13 mmol)을 첨가하였다. 이어서, N,N-다이메틸 아세트아미드(4.0 mL) 중의 tert-부틸 (S)-2-메틸-4-(((트라이플루오로메틸)설폰일)옥시)-3,6-다이하이드로피리딘-1(2H)-카복실레이트(CAS 번호 876922-74-6)(195 mg, 0.566 mmol)의 용액 및 4-에틸피리딘(0.064 mL, 0.566 mmol)을 질소 스트림 하에 첨가하였다. 수득한 혼합물을 12.5시간 동안 80℃에서 질소 대기 하에 교반하였다. 반응 혼합물을 실온까지 냉각시킨 후에, 에틸 아세테이트로 희석하였다. 불용성 물질을 코튼 플러그 여과로 제거하고, 용리액을 물 및 에틸 아세테이트를 사용하여 분포시켰다. 수층을 분리하고 에틸 아세테이트로 추출하였다. 유기층을 합하고 물로 3회 세정하고 감압 하에 농축하고, 커플링 반응 생성물을 미가공 생성물로서 수득하였다.
트라이플루오로아세트산(1.0 mL)을 다이클로로메탄(4.0 mL) 중의 수득한 미가공 생성물의 용액에 첨가하고, 혼합물을 1시간 동안 실온에서 교반하였다. 질소를 반응 혼합물에 취입시켜 용매를 증류 제거하고, 잔사를 메탄올로 희석하였다. 수득한 메탄올 용액을 Waters PoraPak RxnTM CX(20 cc (2 g) 카트리지)에 제공하였다. 고체상을 메탄올(20.0 mL)로 세정한 후에, 이를 암모니아(2 N 메탄올 용액, 20 mL)로 용리시켰다. 용리액을 감압 하에 농축하여 표제 화합물의 미가공 생성물(120 mg)을 수득하였다.
MS (ESI)m/z: 279[M+H]+
(2) 에틸 (1R,3s,5S)-3-((2S,4S)-1-(5-플루오로피리미딘-2-일)-2-메틸피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트의 합성
에틸 (1R,3s,5S)-3-((S)-2-메틸-1,2,3,6-테트라하이드로피리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(120 mg, 0.431 mmol), 10% 팔라듐-탄소(48.47% 수성 제품, 183 mg, 0.083 mmol, N.E. Chemcat Corp.의 제품) 및 메탄올(4.0 mL)의 혼합물을 6.5시간 동안 수소 대기 하에 교반하였다. 불용성 물질을 CeliteTM 여과로 제거하고 감압 하에 농축하여 환원된 형태(113 mg)를 시스/트랜스 혼합물로서 수득하였다.
MS (ESI)m/z: 281[M+H]+
수득한 환원된 형태(113 mg), 2-클로로-5-플루오로피리미딘(0.048 mL, 0.517 mmol), 탄산 세슘(281 mg, 0.862 mmol) 및 N,N-다이메틸 아세트아미드(2.0 mL)의 혼합물을 8시간 동안 100℃에서 교반하였다. 혼합물을 컬럼 크로마토그래피(실리카겔, 0% 내지 30% 에틸 아세테이트/n-헵탄)로 정제하여 표제 화합물(82.0 mg)을 시스/트랜스 혼합물로서 수득하였다.
MS (ESI)m/z: 377[M+H]+
(분석 조건) Daicel의 CHIRALPAKTM IF-3(3.0 mm × 50 mm)을 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(70:30), 40℃, 유량: 1.2 mL/분, 검출: UV(210 내지 400 nm)).
(분석 결과) 표제 화합물의 체류 시간은 1.02분이었고, 트랜스-형태의 체류 시간은 1.23분이었다. 시스:트랜스 비는 4:5(피크 면적비)였고, 광학 순도는 >99% ee였다.
수득한 시스/트랜스 혼합물을 실행마다 10 mg에서 Daicel의 CHIRALPAKR (IF/SFC(3 cm × 25 cm)를 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(70:30), 120 bar, 40℃, 유량: 100 mL/분)로 분획화하여 5.55분의 체류 시간을 갖는, 첫 번째로 용리되는 표제 화합물(34.0 mg)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 1.17 (d, J = 6.34 Hz, 3H), 1.23 (t, J = 7.25 Hz, 3H), 1.19-2.02 (m, 14H), 3.09 (ddd, J = 13.70, 10.99, 5.66 Hz, 1H), 4.10 (q, J = 7.10 Hz, 2H), 4.17-4.30 (m, 3H), 4.34 (dd, J = 13.59, 7.25 Hz, 1H), 8.13 (s, 2H).
MS (ESI)m/z: 377[M+H]+
(분석 조건) Daicel의 CHIRALPAKTM IF-3(3.0 mm × 50 mm)을 사용하는 초임계 유체 크로마토그래피(이동상: CO2:메탄올(70:30), 40℃, 유량: 1.2 mL/분, 검출: UV(245 nm)).
(분석 결과) 표제 화합물의 체류 시간은 1.02분이었고, 시스:트랜스 비는 >99:1이었고, 광학 순도는 >99% ee였다.
(3) (1R,3s,5S)-3-((2S,4S)-1-(5-플루오로피리미딘-2-일)-2-메틸피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄의 합성
에틸 (1R,3s,5S)-3-((2S,4S)-1-(5-플루오로피리미딘-2-일)-2-메틸피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-카복실레이트(34 mg, 0.09 mmol) 및 48% 브롬화 수소산(2.0 mL)의 혼합물을 1시간 동안 100℃에서 교반하였다. 5 N 수산화 나트륨 수용액을 중화를 위해 0℃에서 반응 혼합물에 첨가하였다. 혼합물을 다이클로로메탄으로 3회 추출하고, 유기층을 무수 황산 마그네슘으로 건조시키고 감압 하에 농축하여 표제 화합물(21.7 mg)을 수득하였다.
MS (ESI)m/z: 305[M+H]+
(4) (R)-2-사이클로프로필-2-((1R,3S,5S)-3-((2S,4S)-1-(5-플루오로피리미딘-2-일)-2-메틸피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)아세트아미드의 합성
(1R,3s,5S)-3-((2S,4S)-1-(5-플루오로피리미딘-2-일)-2-메틸피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄(5.00 mg, 0.016 mmol), 탄산 칼륨(4.54 mg, 0.033 mmol), (S)-2-브로모-2-사이클로프로필 아세트아미드(8.24 mg, 0.033 mmol) 및 아세토니트릴(1.0 mL)의 혼합물을 실온에서 7일 동안 교반하였다. 탄산 칼륨(4.54 mg, 0.033 mmol) 및 (S)-2-브로모-2-사이클로프로필 아세트아미드(8.24 mg, 0.033 mmol)를 반응 혼합물에 첨가하고, 이를 실온에서 3일 동안 추가로 교반하였다. 염화 암모늄 수용액을 반응 혼합물에 첨가하여 반응을 중단시켰다. 혼합물을 에틸 아세테이트로 추출하고, 유기층을 물로 세정하고 감압 하에 농축하여 미가공 생성물을 수득하였다.
수득한 미가공 생성물을 메탄올로 희석하고 Waters PoraPak RxnTM CX(6 cc (400 mg) 카트리지)에 제공하였다. 고체상을 메탄올(6.0 mL)로 세정한 후에, 이를 암모니아(2 N 메탄올 용액, 6 mL)로 용리시켰다. 용리액을 감압 하에 농축하고, 수득한 잔사를 박층 크로마토그래피(NH, 다이클로로메탄)로 정제하여 표제 화합물(3.74 mg)을 수득하였다.
1H-NMR (400 MHz, CDCl3)δ(ppm): 0.25-0.36 (m, 1H), 0.39-0.51 (m, 1H), 0.51-0.59 (m, 1H), 0.59-0.70 (m, 1H), 0.70-0.84 (m, 1H), 1.18 (d, J = 6.34 Hz, 3H), 1.21-1.55 (m, 9H), 1.61-1.95 (m, 5H), 2.04 (d, J = 9.06 Hz, 1H), 3.10 (ddd, J = 13.70,10.99, 5.21 Hz, 1H), 3.15-3.28 (m, 1H), 3.80-3.94 (m, 1H), 4.17-4.29 (m, 1H), 4.35 (dd, J = 13.59, 7.25 Hz, 1H), 5.18 (brs, 1H), 6.94 (brs, 1H), 8.14 (s, 2H).
MS (ESI)m/z: 402[M+H]+
(R)-2-사이클로프로필-2-((1R,3S,5S)-3-((2S,4S)-1-(5-플루오로피리미딘-2-일)-2-메틸피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)아세트아미드 단결정의 제조 및 X-선 결정학 분석
실시예 4에서 수득한 표제 화합물(0.81 mg)을 메탄올(600 μL)에 용해시켰다. 이의 분획(200 μL)을 함유하는 바이알을 tert-부틸 메틸 에터(2 mL)를 함유하는 약간 더 큰 바이알에 조심히 넣고, 캡을 닫았다(스팀 확산 방법). 12일 후에, 표제 화합물의 단결정을 바이알에서 수득하였다. 수득한 단결정을 하기 조건 하에서 X-선 결정학 분석을 행하였다. 표제 화합물의 X-선 결정 구조를 도 3에 나타내었다.
분석 기기: XtaLAB PRO P200 MM007HF(Rigaku, Japan)
소프트웨어: CrysAlisPro(Rigaku Oxford Diffraction)
X-선: 다층 거울 단색화된 Cu-Kα(40 kV/30 mA)
측정: ω 축 진동 방법
카메라 길이: 35 mm
측정 온도: -170℃
약리학적 시험 실시예
실시예 1 내지 4의 화합물을 사용하여 하기 약리학적 시험을 수행하였다.
시험 실시예 1-1: OX1R 및 OX2R에 대한 활성의 평가
인간 OX1R(hOX1R) 또는 인간 OX2R(hOX2R)이 강제적으로 발현된 HEK293(인간 배아 신장 293) 세포를 384-웰 마이크로플레이트(Greiner)에 웰당 10,000개로 시딩하고, 첨가된 10% FBS(Thermo Scientific) 및 1% 페니실린-스트렙토마이신(FujiFilm Corp.-Wako Pure Chemical Industries, Ltd.)을 함유하는 고-글루코스-DMEM(FujiFilm Corp.-Wako Pure Chemical Industries, Ltd.)에서 1일 동안 배양하였다. 배지를 제거한 후에, 칼슘 4 염료(Molecular Device Corporation) 및 2.5 mM 프로베네시드(Sigma-Aldrich Japan, KK.)를 함유하는 40 μL의 분석 완충제(20 mM HEPES(Sigma-Aldrich Japan, KK.), 행크 평형 염 용액(Gibco), 0.1% BSA(Sigma-Aldrich Japan, KK.), 0.1% Pluronic F-127(Invitrogen))를 첨가하고, 플레이트를 60분 동안 인큐베이팅하였다. 20 μL의 분석 완충제를 추가로 첨가한 후에, 시험 화합물을 함유하는 20 μL의 분석 완충제를 첨가하고, 반응을 개시하였다. 반응 동안 세포 내 칼슘 이온 농도의 변화를, FDSS7000(Hamamatsu Photonics, K.K.)을 사용하여 480 nm의 여기 파장 및 540 nm의 검출 파장을 사용하여 형광 값에 대한 형광 강도 비율을 기반으로 측정하였다. 시험 화합물을 DMSO에 10 mM로 용해시키고, 분석 완충제로 3 × 10-10 M 내지 1 × 10-7 M의 최종 농도로 희석하였다(DMSO 최종 농도: 0.1%). 반수 최대 효과 농도(EC50 값)를, 다양한 농도의 시험 화합물을 첨가한 형광 값으로부터 결정하되, 화합물이 없는 완충제를 첨가한 웰의 형광 값은 0%이고, 10 nM OX-A(Peptide Research Lab)를 사용한 웰의 형광 값은 100%이다. 각각의 화합물의 EC50 값을 표 1에 나타내었다.
[표 1]
시험 실시예 1-2: OX1R 및 OX2R에 대한 활성화 활성의 평가
hOX1R 또는 hOX2R이 강제적으로 발현된 인간 배아 신장 세포 293(HEK293) 세포를 384-웰 마이크로플레이트(Greiner)에 웰당 10,000개로 시딩하고, 첨가된 10% FBS(Thermo Scientific) 및 1% 페니실린-스트렙토마이신(FujiFilm Corp.-Wako Pure Chemical Industries, Ltd.)을 함유하는 고-글루코스-DMEM(FujiFilm Corp.-Wako Pure Chemical Industries, Ltd.)에서 1일 동안 배양하였다. 배지를 제거한 후에, 칼슘 4 염료(Molecular Device Corporation) 및 2.5 mM 프로베네시드(Sigma-Aldrich Japan, KK.)를 함유하는 30 μL의 분석 완충제(20 mM HEPES(Sigma-Aldrich Japan, KK.), 행크 평형 염 용액(Gibco), 0.1% BSA(Sigma-Aldrich Japan, KK.), 0.1% Pluronic F-127(Invitrogen))를 첨가하고, 혼합물을 60분 동안 인큐베이팅하였다. 시험 화합물을 함유하는 분석 완충제의 30 μL의 분획을 첨가하고, 반응을 개시하였다. 반응에 의한 세포 내 칼슘 이온 농도의 변화를, FDSS7000(Hamamatsu Photonics, K.K.)을 사용하여 480 nm 및 540 nm의 이중 여기 파장을 사용하여 형광 값에 대한 형광 강도 비율을 기반으로 측정하였다. 시험 화합물을 DMSO에 10 mM로 용해시키고, 분석 완충제로 3 × 10-11 M 내지 1 × 10-5 M의 최종 농도로 희석하였다(DMSO 최종 농도: 0.1%). EC50 값을, 다양한 농도의 시험 화합물을 첨가한 형광 값으로부터 결정하되, 화합물이 없는 완충제를 첨가한 웰의 형광 값은 0%이고, 30 nM OX-A(Peptide Research Lab)를 사용한 웰의 형광 값은 100%이다. 각각의 화합물의 EC50 값을 표 2에 나타내었다.
[표 2]
시험 실시예 2: 자발 운동의 증가
체온의 증가, 또는 심혈관 파라미터, 예컨대 혈압의 증가와 유사하게, 마우스의 증가된 운동은 각성의 지표 중 하나이다. 본 시험 실시예에서, 마우스의 자발 운동을 측정함으로써 각성 효과를 평가하였다. 수컷 C57BL/6NCrl 마우스(18 내지 19주령, Charles River Laboratories, Japan Inc., 각각의 군 내 4마리의 마우스)를 본 실험에 사용하였다. 운동 측정 장치(VersaMax Oven Field, AccuScan Instruments, Inc.)를 사용하고, 측정 케이지의 측면으로부터 적외선을 조사하고, 마우스가 조사를 통과한 횟수를 정량화함으로써 자발 운동을 측정하였다. 마우스를 측정 케이지에 두고 3시간 동안 적응시킨 후에, 화합물을 경구 투여하였다(10 mg/kg). 자발 운동을 투여 2시간 후에 측정하였다. 시험 화합물 투여군에는 5%(v/v) DMSO 및 5%(v/v) KolliphorTM EL을 함유하는 0.1 moL/L 염산에 용해된 시험 화합물 용액을 투여하였다. 대조군의 경우 시험 화합물이 없는 용매만을 마우스에 투여하였다.
결과를 표 3에 나타내었다. 자발 운동을 시험 화합물 투여군의 경우 백분율로서 표현하되, 대조군의 자발 운동은 100%이다.
[표 3]
표 3에 나타낸 바와 같이, 본 발명의 화합물은 마우스에서 자발 운동을 증가시켰다. 달리 말하면, 본 발명의 화합물은 각성 효과가 있는 것으로 나타났다.
시험 실시예 3: 야생형 마우스에 대한 본 발명의 화합물의 경구 투여에 의한 각성 촉진 효과
사용된 실험 동물은 C57BL/6 계통 야생형(WT) 수컷 마우스였다. 뇌파 및 근전도 측정 전극을 이소플루란 마취 하에 13주령 마우스에 수술로 삽입하였다. 소등 30 내지 15분 전에 용매(0 mg/kg) 또는 용매에 용해된 실시예 1의 화합물의 용액(1, 3 또는 10 mg/kg)을 경구 투여하였다. 사용된 용매는 5%(v/v) DMSO 및 5%(v/v) KolliphorTM EL을 함유하는 0.1 moL/L 염산 용액이었다. 소등 1시간 전부터 뇌파 및 근전도를 약 24시간 동안 기록하였다. 마우스를, 2일 이상의 휴약 기간을 가지면서 반복적으로 사용하였다. 각각의 마우스에 대해 수득한 뇌파 및 근전도 데이터를, 수면 분석 소프트웨어(SleepSign: Kissei Comtec Co., Ltd.)를 사용하여 에폭(epoch)(10초)마다 수면 단계를 평가하는 데 사용하였다. 소등 후 초기 수면이 나타날 때까지의 시간(수면 개시 잠복기(sleep onset latency))(비-REM 수면 후 시작되는 8개 이상의 에폭 동안 수면)을 각각의 마우스에 대해 측정하였다. 각각의 투여군에 16마리의 마우스를 사용하여, 용매 투여군(대조군) 및 실시예 1의 화합물 투여군의 수면 개시 잠복기를, 실험의 수 및 동일한 개체의 사용을 고려하여 생존 시간 분석 후에 Dunnet형 다중 비교 시험으로 비교하였고, 이때 유의도 수준은 양쪽 말단 각각에서 5%였다.
용매 및 실시예 1의 화합물 1, 3 및 10 mg/kg을 투여한 마우스의 수면 잠복기는 각각 0.23시간, 0.28시간, 0.44시간 및 2.07시간이었다. 3 또는 10 mg/kg 실시예 1의 화합물 투여군에서, 수면 개시 잠복기는 용매 투여군에 비해 상당히 증가하였다. 구체적으로, 실시예 1의 화합물을 경구 투여한 경우, 수면 개시 잠복기는 용량 의존적 방식으로 연장되는 것으로 밝혀졌다.
시험 실시예 4: 오렉신-결핍 마우스(오렉신/아탁신-3(ataxin-3) Tg/+ 마우스)에 대한 본 발명의 화합물의 경구 투여에 의한 각성 촉진 효과 및 무-탈력 발작 상태 연장
사용된 실험 동물은 C57BL/6 유전적 배경을 갖는 오렉신/아탁신-3 Tg/+ 마우스(이하 "Tg 마우스"라 함, Hara et al., Neuron, 30, 345-54, 2001)였다. 뇌파 및 근전도 측정 전극을 이소플루란 마취 하에 12주령 마우스(±2주)에 수술로 삽입하였다. 소등 30 내지 15분 전에 용매(0 mg/kg) 또는 샘플 용액(용매에 용해된 실시예 1의 화합물: 0.3, 1 또는 3 mg/kg)을 경구 투여하였다. 사용된 용매는 5%(v/v) DMSO 및 5%(v/v) KolliphorTM EL을 함유하는 0.1 moL/L 염산 용액이었다. 소등 1시간 전부터 뇌파 및 근전도를 약 24시간 동안 기록하였다. 마우스를, 2일 이상의 휴약 기간을 가지면서 반복적으로 사용하였다. 각각의 마우스에 대해 수득한 뇌파 및 근전도 데이터를 사용하여, 수면 분석 소프트웨어(SleepSign: Kissei Comtec Co., Ltd.)를 사용하여 최대 4시간(컷-오프(cut-off) 값)까지 에폭(10초)마다 수면 단계를 평가하였다. 본 실험의 목적을 위해, 4개 이상의 에폭의 연속 기간 동안 각성 직후에 나타나는 REM 수면(각성에서 REM 수면으로의 직접적 전이(DREM))으로서 탈력 발작-유사 증상을 정의하였다. 마우스에서 DREM은 탈력 발작과 유사하다(Exp Neurol. 2009; 217:46-54). 각각의 마우스에 대해 소등 후 초기 수면이 나타날 때까지의 시간(DREM을 제외한 연속한 8개 이상의 에폭 동안의 수면)(수면 개시 잠복기) 및 초기 DREM이 나타날 때까지의 시간(DREM 잠복기)을 측정하였다. 비히클군 및 실시예 1의 화합물 투여군에서 마우스의 수는 14마리였다. 비히클 대조군 및 화합물 투여군의 수면 개시 잠복기 및 DREM 잠복기를, 실험의 수 및 동일한 개체의 사용을 고려하여 생존 시간 분석 후에 Dunnet형 다중 비교 시험으로 비교하였고, 이때 양쪽 말단 각각에서 유의도 수준은 5%였다.
용매 및 실시예 1의 화합물 0.3, 1 및 3 mg/kg을 투여한 Tg 마우스에 대한 수면 개시 잠복기는 각각 0.21시간, 0.31시간, 0.64시간 및 2.42시간이었고, 이는 1 및 3 mg/kg 실시예 1의 화합물 투여군에서 수면 개시 잠복기의 상당한 증가를 나타낸다. 구체적으로, 실시예 1의 화합물을 경구 투여한 경우, 오렉신-결핍 마우스에서 수면 개시 잠복기가 1 mg/kg에서 용량 의존적 방식으로 연장되는 것으로 밝혀졌다.
Tg 마우스에서 용매의 투여 및 실시예 1의 화합물 0.3, 1 및 3 mg/kg 투여에 따른 DREM 잠복기는 각각 1.16시간, 1.50시간, 2.26시간 및 4.00시간이었고, 이는 용매 투여군과 비교하여 DREM 잠복기가 0.3, 1 및 3 mg/kg 실시예 1의 화합물 투여군에서 상당히 용량 의존적 방식으로 증가하였음을 확인시켜준다. 달리 말하면, 뮤린 탈력 발작-유사 거동이 없는 상태는 본 발명의 화합물의 투여에 의해 용량 의존적 방식으로 확장되었다.
Claims (15)
- 하기 화학식 I로 표현되는 (2R)-2-사이클로프로필-2-{(1R,3S,5S)-3-[(3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일]-8-아자바이사이클로[3.2.1]옥탄-8-일}아세트아미드;
[화학식 I]
하기 화학식 II로 표현되는 (R)-2-((1R,3S,5S)-3-((3S,4R)-1-(5-플루오로피리미딘-2-일)-3-메톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)-3-메틸부탄아미드;
[화학식 II]
하기 화학식 III으로 표현되는 (R)-2-((1R,3S,5S)-3-((3S,4R)-1-(5-클로로피리미딘-2-일)-3-에톡시피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)-2-사이클로프로필 아세트아미드; 및
[화학식 III]
하기 화학식 IV로 표현되는 (R)-2-사이클로프로필-2-((1R,3S,5S)-3-((2S,4S)-1-(5-플루오로피리미딘-2-일)-2-메틸피페리딘-4-일)-8-아자바이사이클로[3.2.1]옥탄-8-일)아세트아미드:
[화학식 IV]
로 이루어진 군으로부터 선택되는 화합물 또는 이의 약학적으로 허용되는 염. - 제1항 내지 제5항 중 어느 한 항에 따른 화합물 또는 이의 약학적으로 허용되는 염을 포함하는 약학 조성물.
- 제1항 내지 제5항 중 어느 한 항에 따른 화합물 또는 이의 약학적으로 허용되는 염을 포함하는 오렉신 제2형 수용체 작용제(orexin type 2 receptor agonist).
- 제1항 내지 제5항 중 어느 한 항에 따른 화합물 또는 이의 약학적으로 허용되는 염을 포함하는 기면증 치료제.
- 대상체에 약리학적 유효 용량의 제1항 내지 제5항 중 어느 한 항에 따른 화합물 또는 이의 약학적으로 허용되는 염을 투여하는 단계를 포함하는 기면증의 치료 방법.
- 기면증 치료에서 사용하기 위한 제1항 내지 제5항 중 어느 한 항에 따른 화합물 또는 이의 약학적으로 허용되는 염.
- 기면증 치료용 약학 조성물의 제조를 위한 제1항 내지 제5항 중 어느 한 항에 따른 화합물 또는 이의 약학적으로 허용되는 염의 용도.
- 제1항 내지 제5항 중 어느 한 항에 따른 화합물 또는 이의 약학적으로 허용되는 염을 포함하는 탈력 발작(cataplexy) 치료제.
- 대상체에 약리학적 유효 용량의 제1항 내지 제5항 중 어느 한 항에 따른 화합물 또는 이의 약학적으로 허용되는 염을 투여하는 단계를 포함하는 탈력 발작의 치료 방법.
- 탈력 발작의 치료에서 사용하기 위한 제1항 내지 제5항 중 어느 한 항에 따른 화합물 또는 이의 약학적으로 허용되는 염.
- 탈력 발작 치료용 약학 조성물의 제조를 위한 제1항 내지 제5항 중 어느 한 항에 따른 화합물 또는 이의 약학적으로 허용되는 염의 용도.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020122864 | 2020-07-17 | ||
| JPJP-P-2020-122864 | 2020-07-17 | ||
| PCT/JP2021/026649 WO2022014680A1 (ja) | 2020-07-17 | 2021-07-15 | 置換ピペリジン化合物及びその用途 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20230040953A true KR20230040953A (ko) | 2023-03-23 |
Family
ID=79291962
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227044679A KR20230040953A (ko) | 2020-07-17 | 2021-07-15 | 치환된 피페리딘 화합물 및 이의 적용례 |
Country Status (17)
| Country | Link |
|---|---|
| US (1) | US11479552B2 (ko) |
| EP (1) | EP4151277A1 (ko) |
| JP (1) | JP7190612B2 (ko) |
| KR (1) | KR20230040953A (ko) |
| CN (1) | CN115884971A (ko) |
| AR (1) | AR122973A1 (ko) |
| AU (1) | AU2021308053A1 (ko) |
| BR (1) | BR112022026161A2 (ko) |
| CA (1) | CA3187835A1 (ko) |
| CL (1) | CL2022003666A1 (ko) |
| CO (1) | CO2022018446A2 (ko) |
| IL (1) | IL299125A (ko) |
| MX (1) | MX2022016388A (ko) |
| PE (1) | PE20231103A1 (ko) |
| TW (1) | TW202216705A (ko) |
| WO (1) | WO2022014680A1 (ko) |
| ZA (1) | ZA202213562B (ko) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BR112022009938A2 (pt) | 2019-11-25 | 2022-09-13 | Alkermes Inc | Compostos macrocíclicos substituídos e métodos de tratamento relacionados |
| US11760747B2 (en) | 2020-12-21 | 2023-09-19 | Alkermes, Inc. | Substituted piperidino compounds and related methods of treatment |
| WO2023136279A1 (ja) * | 2022-01-14 | 2023-07-20 | エーザイ・アール・アンド・ディー・マネジメント株式会社 | 置換ピペリジン化合物の結晶並びに置換ピペリジン化合物の塩及びそれらの結晶 |
| WO2024075825A1 (ja) * | 2022-10-07 | 2024-04-11 | キッセイ薬品工業株式会社 | シクロペンタン化合物 |
| WO2024095158A1 (en) | 2022-10-31 | 2024-05-10 | Takeda Pharmaceutical Company Limited | Dosing of orexin type 2 receptor agonists |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996034877A1 (en) | 1995-05-05 | 1996-11-07 | Human Genome Sciences, Inc. | Human neuropeptide receptor |
| JPH11178588A (ja) | 1997-07-25 | 1999-07-06 | Smithkline Beecham Corp | 新規なヒト7−トランスメンブランレセプターをコードするcDNAクローンMY1 |
| KR100229887B1 (ko) | 1995-03-01 | 1999-11-15 | 구이 앤드류 바즈 | 폭발 및 파편화에 저항성을 갖는 안전화용의 폴리우레탄 신발창 |
| KR100327888B1 (ko) | 1999-07-14 | 2002-03-09 | 정숭렬 | 도로포장 파손촉진 시험장치의 무선제어 시스템 |
| KR100327889B1 (ko) | 1997-02-18 | 2002-08-21 | 다이니치 세이카 고교 가부시키가이샤 | 잉크젯용기록시트 |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6309854B1 (en) | 1996-12-17 | 2001-10-30 | Smithkline Beecham Corporation | Polynucleotides encoding ligands of the neuropeptide receptor HFGAN72 |
| US5935814A (en) | 1997-04-30 | 1999-08-10 | Smithkline Beecham Corporation | Polynucleotides encoding HFGAN72Y receptor |
| US6020157A (en) | 1997-04-30 | 2000-02-01 | Smithkline Beecham Corporation | Polynucleotides encoding HFGAN72X receptor |
| CA2551037A1 (en) * | 2003-09-22 | 2005-03-31 | Banyu Pharmaceutical Co., Ltd. | Novel piperidine derivative |
| NZ553622A (en) | 2004-10-20 | 2010-08-27 | Neurosearch As | Novel diazabicyclic aryl derivatives and their medical use |
| JP2009184924A (ja) | 2006-05-31 | 2009-08-20 | Eisai R & D Management Co Ltd | 生物学的試薬用化合物 |
| TW201444849A (zh) | 2013-03-13 | 2014-12-01 | Janssen Pharmaceutica Nv | 經取代的7-氮雜雙環類及其作為食慾激素受體調節劑之用途 |
-
2021
- 2021-07-15 KR KR1020227044679A patent/KR20230040953A/ko unknown
- 2021-07-15 PE PE2022003006A patent/PE20231103A1/es unknown
- 2021-07-15 IL IL299125A patent/IL299125A/en unknown
- 2021-07-15 MX MX2022016388A patent/MX2022016388A/es unknown
- 2021-07-15 TW TW110126031A patent/TW202216705A/zh unknown
- 2021-07-15 AU AU2021308053A patent/AU2021308053A1/en active Pending
- 2021-07-15 US US17/376,452 patent/US11479552B2/en active Active
- 2021-07-15 AR ARP210101982A patent/AR122973A1/es unknown
- 2021-07-15 JP JP2022536446A patent/JP7190612B2/ja active Active
- 2021-07-15 EP EP21842047.9A patent/EP4151277A1/en active Pending
- 2021-07-15 WO PCT/JP2021/026649 patent/WO2022014680A1/ja active Application Filing
- 2021-07-15 CA CA3187835A patent/CA3187835A1/en active Pending
- 2021-07-15 CN CN202180044081.3A patent/CN115884971A/zh active Pending
- 2021-07-15 BR BR112022026161A patent/BR112022026161A2/pt unknown
-
2022
- 2022-12-14 ZA ZA2022/13562A patent/ZA202213562B/en unknown
- 2022-12-20 CL CL2022003666A patent/CL2022003666A1/es unknown
- 2022-12-20 CO CONC2022/0018446A patent/CO2022018446A2/es unknown
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100229887B1 (ko) | 1995-03-01 | 1999-11-15 | 구이 앤드류 바즈 | 폭발 및 파편화에 저항성을 갖는 안전화용의 폴리우레탄 신발창 |
| WO1996034877A1 (en) | 1995-05-05 | 1996-11-07 | Human Genome Sciences, Inc. | Human neuropeptide receptor |
| KR100327889B1 (ko) | 1997-02-18 | 2002-08-21 | 다이니치 세이카 고교 가부시키가이샤 | 잉크젯용기록시트 |
| JPH11178588A (ja) | 1997-07-25 | 1999-07-06 | Smithkline Beecham Corp | 新規なヒト7−トランスメンブランレセプターをコードするcDNAクローンMY1 |
| KR100327888B1 (ko) | 1999-07-14 | 2002-03-09 | 정숭렬 | 도로포장 파손촉진 시험장치의 무선제어 시스템 |
Non-Patent Citations (8)
| Title |
|---|
| Busquets X. et al, Respiration, 2004, 71, 575-579 |
| Chemelli R.M. et al, Cell, 1999, 98, 437-451 |
| Lin L. et al, Cell, 1999, 98, 365-376 |
| Mieda M. et al, CNS Drugs, 2013, 27, 83-90 |
| Mieda M. et al, Proc. Natl. Acad. Sci. USA, 2004, 101, 4649-4654 |
| Sakurai T. et al, Cell, 1998, 92, 573-585 |
| Thannickal T.C. et al, Brain. 2007, 130, 1586-1595 |
| Willie J.T. et al, Neuron, 2003, 38, 715-730 |
Also Published As
| Publication number | Publication date |
|---|---|
| CL2022003666A1 (es) | 2023-05-26 |
| ZA202213562B (en) | 2023-10-25 |
| CA3187835A1 (en) | 2022-01-20 |
| JPWO2022014680A1 (ko) | 2022-01-20 |
| BR112022026161A2 (pt) | 2023-01-31 |
| US20220017517A1 (en) | 2022-01-20 |
| US11479552B2 (en) | 2022-10-25 |
| IL299125A (en) | 2023-02-01 |
| EP4151277A1 (en) | 2023-03-22 |
| AU2021308053A1 (en) | 2023-02-02 |
| AR122973A1 (es) | 2022-10-19 |
| JP7190612B2 (ja) | 2022-12-15 |
| TW202216705A (zh) | 2022-05-01 |
| PE20231103A1 (es) | 2023-07-19 |
| WO2022014680A1 (ja) | 2022-01-20 |
| MX2022016388A (es) | 2023-01-30 |
| CN115884971A (zh) | 2023-03-31 |
| CO2022018446A2 (es) | 2023-03-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20230040953A (ko) | 치환된 피페리딘 화합물 및 이의 적용례 | |
| CN106163516B (zh) | 异吲哚啉组合物和治疗神经变性疾病的方法 | |
| TWI627177B (zh) | 選擇性bace1抑制劑 | |
| CN106103452B (zh) | 皮质抑素类似物及其合成和用途 | |
| TWI378101B (en) | Pyridine derivatives and their use in the treatment of psychotic disorders | |
| TWI473803B (zh) | 作為阿伐7正向異位調節劑之嗎福啉基噻唑 | |
| EP3766882B1 (en) | Phthalazine isoxazole alkoxy derivatives, preparation method thereof, pharmaceutical composition and use thereof | |
| JP6533799B2 (ja) | 放射標識された化合物 | |
| CN108473503A (zh) | 用于治疗疼痛的11,13-修饰的石房蛤毒素类化合物 | |
| KR102531680B1 (ko) | 6,7―디히드로피라졸로[1,5―a]피라진―4(5H)―온 화합물 및 MGLUR2 수용체의 음성 알로스테릭 조절제로서의 그 용도 | |
| EA025322B1 (ru) | Производные дигидробензооксазина и дигидропиридооксазина | |
| TW201605838A (zh) | 晶形 | |
| KR101800140B1 (ko) | 벤조티아졸론 화합물 | |
| KR20220106778A (ko) | 간 x 수용체 작용제로서의 1,2,4-옥사디아졸 유도체 | |
| EP3022201A1 (en) | Autotaxin inhibitors | |
| JP2024517678A (ja) | ソルチリン活性の修飾物質 | |
| TW201118070A (en) | Prodrugs of a piperidinyl derivative as modulators of chemokine receptor activity | |
| JP2023103981A (ja) | 置換ピペリジン化合物を含有する医薬 | |
| EA045865B1 (ru) | Замещенные пиперидиновые соединения и их применение | |
| WO2023136279A1 (ja) | 置換ピペリジン化合物の結晶並びに置換ピペリジン化合物の塩及びそれらの結晶 | |
| JP2021183587A (ja) | 複素環化合物 | |
| EP3881840A1 (en) | Sortilin antagonists for use inthe treatment of diabetic retinopathy | |
| TW201136588A (en) | Tropinone benzylamines as beta-tryptase inhibitors | |
| TW202340145A (zh) | 氘化有機化合物及其用途 | |
| TW202333671A (zh) | 氘化有機化合物及其用途 |