KR20200097749A - 향상된 iPSC 유래된 효과기 세포를 사용하는 면역요법 - Google Patents
향상된 iPSC 유래된 효과기 세포를 사용하는 면역요법 Download PDFInfo
- Publication number
- KR20200097749A KR20200097749A KR1020207019364A KR20207019364A KR20200097749A KR 20200097749 A KR20200097749 A KR 20200097749A KR 1020207019364 A KR1020207019364 A KR 1020207019364A KR 20207019364 A KR20207019364 A KR 20207019364A KR 20200097749 A KR20200097749 A KR 20200097749A
- Authority
- KR
- South Korea
- Prior art keywords
- cells
- cell
- car
- derivative
- receptor
- Prior art date
Links
- 239000012636 effector Substances 0.000 title claims abstract description 75
- 230000001976 improved effect Effects 0.000 title claims abstract description 34
- 238000009169 immunotherapy Methods 0.000 title description 6
- 238000000034 method Methods 0.000 claims abstract description 78
- 230000004069 differentiation Effects 0.000 claims abstract description 54
- 229940076838 Immune checkpoint inhibitor Drugs 0.000 claims abstract description 47
- 239000012274 immune-checkpoint protein inhibitor Substances 0.000 claims abstract description 47
- 102000037984 Inhibitory immune checkpoint proteins Human genes 0.000 claims abstract description 42
- 108091008026 Inhibitory immune checkpoint proteins Proteins 0.000 claims abstract description 42
- 239000000203 mixture Substances 0.000 claims abstract description 41
- 230000001225 therapeutic effect Effects 0.000 claims abstract description 39
- 238000010362 genome editing Methods 0.000 claims abstract description 26
- 210000004027 cell Anatomy 0.000 claims description 590
- 108010019670 Chimeric Antigen Receptors Proteins 0.000 claims description 186
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 124
- 230000014509 gene expression Effects 0.000 claims description 110
- 108090000623 proteins and genes Proteins 0.000 claims description 108
- 210000000822 natural killer cell Anatomy 0.000 claims description 104
- 101000917839 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-B Proteins 0.000 claims description 103
- 101000917858 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 claims description 101
- 102000005962 receptors Human genes 0.000 claims description 101
- 108020003175 receptors Proteins 0.000 claims description 101
- 239000000427 antigen Substances 0.000 claims description 95
- 108091007433 antigens Proteins 0.000 claims description 95
- 102000036639 antigens Human genes 0.000 claims description 95
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 93
- 206010028980 Neoplasm Diseases 0.000 claims description 90
- -1 41BBL Proteins 0.000 claims description 82
- 102000003812 Interleukin-15 Human genes 0.000 claims description 81
- 108090000172 Interleukin-15 Proteins 0.000 claims description 78
- 102000004127 Cytokines Human genes 0.000 claims description 70
- 108090000695 Cytokines Proteins 0.000 claims description 70
- 230000011664 signaling Effects 0.000 claims description 70
- 102000004196 processed proteins & peptides Human genes 0.000 claims description 62
- 102000040430 polynucleotide Human genes 0.000 claims description 57
- 108091033319 polynucleotide Proteins 0.000 claims description 57
- 239000002157 polynucleotide Substances 0.000 claims description 55
- 108091008874 T cell receptors Proteins 0.000 claims description 51
- 102000016266 T-Cell Antigen Receptors Human genes 0.000 claims description 51
- 210000000130 stem cell Anatomy 0.000 claims description 47
- 230000027455 binding Effects 0.000 claims description 42
- 229920001184 polypeptide Polymers 0.000 claims description 42
- 210000003958 hematopoietic stem cell Anatomy 0.000 claims description 37
- 108010081355 beta 2-Microglobulin Proteins 0.000 claims description 36
- 238000003780 insertion Methods 0.000 claims description 34
- 230000037431 insertion Effects 0.000 claims description 34
- 239000012634 fragment Substances 0.000 claims description 33
- 230000010056 antibody-dependent cellular cytotoxicity Effects 0.000 claims description 28
- 230000036961 partial effect Effects 0.000 claims description 28
- 102100022680 NKG2-D type II integral membrane protein Human genes 0.000 claims description 27
- 230000001965 increasing effect Effects 0.000 claims description 27
- 101001109501 Homo sapiens NKG2-D type II integral membrane protein Proteins 0.000 claims description 26
- 102000017578 LAG3 Human genes 0.000 claims description 25
- 102100028967 HLA class I histocompatibility antigen, alpha chain G Human genes 0.000 claims description 24
- 108010024164 HLA-G Antigens Proteins 0.000 claims description 24
- 102100040678 Programmed cell death protein 1 Human genes 0.000 claims description 24
- 102100034922 T-cell surface glycoprotein CD8 alpha chain Human genes 0.000 claims description 23
- 108010087819 Fc receptors Proteins 0.000 claims description 22
- 102000009109 Fc receptors Human genes 0.000 claims description 22
- 102100026122 High affinity immunoglobulin gamma Fc receptor I Human genes 0.000 claims description 22
- 101100382122 Homo sapiens CIITA gene Proteins 0.000 claims description 22
- 101000913074 Homo sapiens High affinity immunoglobulin gamma Fc receptor I Proteins 0.000 claims description 22
- 101000946843 Homo sapiens T-cell surface glycoprotein CD8 alpha chain Proteins 0.000 claims description 22
- 102100029193 Low affinity immunoglobulin gamma Fc region receptor III-A Human genes 0.000 claims description 22
- 102100026371 MHC class II transactivator Human genes 0.000 claims description 22
- 108700002010 MHC class II transactivator Proteins 0.000 claims description 22
- 230000003394 haemopoietic effect Effects 0.000 claims description 22
- 230000002688 persistence Effects 0.000 claims description 22
- 230000001404 mediated effect Effects 0.000 claims description 21
- 230000004936 stimulating effect Effects 0.000 claims description 21
- 102100034458 Hepatitis A virus cellular receptor 2 Human genes 0.000 claims description 20
- 102000037982 Immune checkpoint proteins Human genes 0.000 claims description 20
- 108091008036 Immune checkpoint proteins Proteins 0.000 claims description 20
- 108010002586 Interleukin-7 Proteins 0.000 claims description 20
- 238000012217 deletion Methods 0.000 claims description 20
- 230000037430 deletion Effects 0.000 claims description 20
- 230000004083 survival effect Effects 0.000 claims description 20
- 101000716102 Homo sapiens T-cell surface glycoprotein CD4 Proteins 0.000 claims description 19
- 101710163270 Nuclease Proteins 0.000 claims description 19
- 102100036011 T-cell surface glycoprotein CD4 Human genes 0.000 claims description 19
- 101000851370 Homo sapiens Tumor necrosis factor receptor superfamily member 9 Proteins 0.000 claims description 18
- 102100036856 Tumor necrosis factor receptor superfamily member 9 Human genes 0.000 claims description 18
- 238000004519 manufacturing process Methods 0.000 claims description 18
- 230000002829 reductive effect Effects 0.000 claims description 18
- 108010065805 Interleukin-12 Proteins 0.000 claims description 17
- 102000013462 Interleukin-12 Human genes 0.000 claims description 17
- 102100024222 B-lymphocyte antigen CD19 Human genes 0.000 claims description 16
- 102100031940 Epithelial cell adhesion molecule Human genes 0.000 claims description 16
- 102100028970 HLA class I histocompatibility antigen, alpha chain E Human genes 0.000 claims description 16
- 101000980825 Homo sapiens B-lymphocyte antigen CD19 Proteins 0.000 claims description 16
- 101000986085 Homo sapiens HLA class I histocompatibility antigen, alpha chain E Proteins 0.000 claims description 16
- 101000868279 Homo sapiens Leukocyte surface antigen CD47 Proteins 0.000 claims description 16
- 108010002350 Interleukin-2 Proteins 0.000 claims description 16
- 102000000588 Interleukin-2 Human genes 0.000 claims description 16
- 101150030213 Lag3 gene Proteins 0.000 claims description 16
- 102100032913 Leukocyte surface antigen CD47 Human genes 0.000 claims description 16
- 210000003719 b-lymphocyte Anatomy 0.000 claims description 16
- 229960000106 biosimilars Drugs 0.000 claims description 16
- 210000000581 natural killer T-cell Anatomy 0.000 claims description 16
- 102100029822 B- and T-lymphocyte attenuator Human genes 0.000 claims description 15
- 101000864344 Homo sapiens B- and T-lymphocyte attenuator Proteins 0.000 claims description 15
- 101710089372 Programmed cell death protein 1 Proteins 0.000 claims description 15
- 210000002865 immune cell Anatomy 0.000 claims description 15
- 210000001519 tissue Anatomy 0.000 claims description 15
- 239000013598 vector Substances 0.000 claims description 15
- 102100039498 Cytotoxic T-lymphocyte protein 4 Human genes 0.000 claims description 14
- 102100030704 Interleukin-21 Human genes 0.000 claims description 14
- 230000003013 cytotoxicity Effects 0.000 claims description 14
- 231100000135 cytotoxicity Toxicity 0.000 claims description 14
- 108020001507 fusion proteins Proteins 0.000 claims description 14
- 102000037865 fusion proteins Human genes 0.000 claims description 14
- 108010074108 interleukin-21 Proteins 0.000 claims description 14
- 229910052618 mica group Inorganic materials 0.000 claims description 14
- 108010035532 Collagen Proteins 0.000 claims description 13
- 102000008186 Collagen Human genes 0.000 claims description 13
- 102100031573 Hematopoietic progenitor cell antigen CD34 Human genes 0.000 claims description 13
- 101000777663 Homo sapiens Hematopoietic progenitor cell antigen CD34 Proteins 0.000 claims description 13
- 101001117317 Homo sapiens Programmed cell death 1 ligand 1 Proteins 0.000 claims description 13
- 101000713322 Homo sapiens SAP30-binding protein Proteins 0.000 claims description 13
- 102100030301 MHC class I polypeptide-related sequence A Human genes 0.000 claims description 13
- 102100024216 Programmed cell death 1 ligand 1 Human genes 0.000 claims description 13
- 102100036909 SAP30-binding protein Human genes 0.000 claims description 13
- 229960003852 atezolizumab Drugs 0.000 claims description 13
- 229920001436 collagen Polymers 0.000 claims description 13
- 229940126546 immune checkpoint molecule Drugs 0.000 claims description 13
- 230000002401 inhibitory effect Effects 0.000 claims description 13
- 239000010445 mica Substances 0.000 claims description 13
- 229960003301 nivolumab Drugs 0.000 claims description 13
- QIVBCDIJIAJPQS-UHFFFAOYSA-N tryptophan Chemical compound C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 claims description 13
- 108010021064 CTLA-4 Antigen Proteins 0.000 claims description 12
- 229940045513 CTLA4 antagonist Drugs 0.000 claims description 12
- 241000701022 Cytomegalovirus Species 0.000 claims description 12
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 claims description 12
- 102000004388 Interleukin-4 Human genes 0.000 claims description 12
- 108090000978 Interleukin-4 Proteins 0.000 claims description 12
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 claims description 12
- 210000000349 chromosome Anatomy 0.000 claims description 12
- 230000001939 inductive effect Effects 0.000 claims description 12
- 229960002621 pembrolizumab Drugs 0.000 claims description 12
- RJBDSRWGVYNDHL-XNJNKMBASA-N (2S,4R,5S,6S)-2-[(2S,3R,4R,5S,6R)-5-[(2S,3R,4R,5R,6R)-3-acetamido-4,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-2-[(2R,3S,4R,5R,6R)-4,5-dihydroxy-2-(hydroxymethyl)-6-[(E,2R,3S)-3-hydroxy-2-(octadecanoylamino)octadec-4-enoxy]oxan-3-yl]oxy-3-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-5-amino-6-[(1S,2R)-2-[(2S,4R,5S,6S)-5-amino-2-carboxy-4-hydroxy-6-[(1R,2R)-1,2,3-trihydroxypropyl]oxan-2-yl]oxy-1,3-dihydroxypropyl]-4-hydroxyoxane-2-carboxylic acid Chemical compound CCCCCCCCCCCCCCCCCC(=O)N[C@H](CO[C@@H]1O[C@H](CO)[C@@H](O[C@@H]2O[C@H](CO)[C@H](O[C@@H]3O[C@H](CO)[C@H](O)[C@H](O)[C@H]3NC(C)=O)[C@H](O[C@@]3(C[C@@H](O)[C@H](N)[C@H](O3)[C@H](O)[C@@H](CO)O[C@@]3(C[C@@H](O)[C@H](N)[C@H](O3)[C@H](O)[C@H](O)CO)C(O)=O)C(O)=O)[C@H]2O)[C@H](O)[C@H]1O)[C@@H](O)\C=C\CCCCCCCCCCCCC RJBDSRWGVYNDHL-XNJNKMBASA-N 0.000 claims description 11
- 108091032973 (ribonucleotides)n+m Proteins 0.000 claims description 11
- 102100022005 B-lymphocyte antigen CD20 Human genes 0.000 claims description 11
- 108010043471 Core Binding Factor Alpha 2 Subunit Proteins 0.000 claims description 11
- 101710083479 Hepatitis A virus cellular receptor 2 homolog Proteins 0.000 claims description 11
- 101000897405 Homo sapiens B-lymphocyte antigen CD20 Proteins 0.000 claims description 11
- 101001075432 Homo sapiens DNA-binding protein RFX5 Proteins 0.000 claims description 11
- 101000611936 Homo sapiens Programmed cell death protein 1 Proteins 0.000 claims description 11
- 101001012157 Homo sapiens Receptor tyrosine-protein kinase erbB-2 Proteins 0.000 claims description 11
- 108090000174 Interleukin-10 Proteins 0.000 claims description 11
- 102000003814 Interleukin-10 Human genes 0.000 claims description 11
- 102000000585 Interleukin-9 Human genes 0.000 claims description 11
- 108010002335 Interleukin-9 Proteins 0.000 claims description 11
- 101150069255 KLRC1 gene Proteins 0.000 claims description 11
- 101100404845 Macaca mulatta NKG2A gene Proteins 0.000 claims description 11
- 102100022682 NKG2-A/NKG2-B type II integral membrane protein Human genes 0.000 claims description 11
- 102100022683 NKG2-C type II integral membrane protein Human genes 0.000 claims description 11
- 102100030086 Receptor tyrosine-protein kinase erbB-2 Human genes 0.000 claims description 11
- 102100025373 Runt-related transcription factor 1 Human genes 0.000 claims description 11
- 229940126547 T-cell immunoglobulin mucin-3 Drugs 0.000 claims description 11
- 238000010459 TALEN Methods 0.000 claims description 11
- 102100028082 Tapasin Human genes 0.000 claims description 11
- 201000011510 cancer Diseases 0.000 claims description 11
- 230000003834 intracellular effect Effects 0.000 claims description 11
- 239000012528 membrane Substances 0.000 claims description 11
- 210000005259 peripheral blood Anatomy 0.000 claims description 11
- 239000011886 peripheral blood Substances 0.000 claims description 11
- 108010059434 tapasin Proteins 0.000 claims description 11
- 102100022464 5'-nucleotidase Human genes 0.000 claims description 10
- 102100030346 Antigen peptide transporter 1 Human genes 0.000 claims description 10
- 102100030343 Antigen peptide transporter 2 Human genes 0.000 claims description 10
- 108091033409 CRISPR Proteins 0.000 claims description 10
- 102100020986 DNA-binding protein RFX5 Human genes 0.000 claims description 10
- 102100021044 DNA-binding protein RFXANK Human genes 0.000 claims description 10
- 102100041003 Glutamate carboxypeptidase 2 Human genes 0.000 claims description 10
- 102100031181 Glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 claims description 10
- 101000678236 Homo sapiens 5'-nucleotidase Proteins 0.000 claims description 10
- 101001075464 Homo sapiens DNA-binding protein RFXANK Proteins 0.000 claims description 10
- 101000892862 Homo sapiens Glutamate carboxypeptidase 2 Proteins 0.000 claims description 10
- 101001137987 Homo sapiens Lymphocyte activation gene 3 protein Proteins 0.000 claims description 10
- 101001109503 Homo sapiens NKG2-C type II integral membrane protein Proteins 0.000 claims description 10
- 101000581981 Homo sapiens Neural cell adhesion molecule 1 Proteins 0.000 claims description 10
- 101001075466 Homo sapiens Regulatory factor X-associated protein Proteins 0.000 claims description 10
- 108010023335 Member 2 Subfamily B ATP Binding Cassette Transporter Proteins 0.000 claims description 10
- 102100027347 Neural cell adhesion molecule 1 Human genes 0.000 claims description 10
- 102100021043 Regulatory factor X-associated protein Human genes 0.000 claims description 10
- 101800000849 Tachykinin-associated peptide 2 Proteins 0.000 claims description 10
- 108020004445 glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 claims description 10
- 101000834898 Homo sapiens Alpha-synuclein Proteins 0.000 claims description 9
- 101001068133 Homo sapiens Hepatitis A virus cellular receptor 2 Proteins 0.000 claims description 9
- 101001023712 Homo sapiens Nectin-3 Proteins 0.000 claims description 9
- 101000979565 Homo sapiens Protein NLRC5 Proteins 0.000 claims description 9
- 101000652359 Homo sapiens Spermatogenesis-associated protein 2 Proteins 0.000 claims description 9
- 102000026633 IL6 Human genes 0.000 claims description 9
- 108090000177 Interleukin-11 Proteins 0.000 claims description 9
- 102000003815 Interleukin-11 Human genes 0.000 claims description 9
- 102000003810 Interleukin-18 Human genes 0.000 claims description 9
- 108090000171 Interleukin-18 Proteins 0.000 claims description 9
- 108090001005 Interleukin-6 Proteins 0.000 claims description 9
- 102000003735 Mesothelin Human genes 0.000 claims description 9
- 108090000015 Mesothelin Proteins 0.000 claims description 9
- 108010004217 Natural Cytotoxicity Triggering Receptor 1 Proteins 0.000 claims description 9
- 108010004222 Natural Cytotoxicity Triggering Receptor 3 Proteins 0.000 claims description 9
- 102100035487 Nectin-3 Human genes 0.000 claims description 9
- 102100023432 Protein NLRC5 Human genes 0.000 claims description 9
- 238000011467 adoptive cell therapy Methods 0.000 claims description 9
- 239000005557 antagonist Substances 0.000 claims description 9
- 229950002916 avelumab Drugs 0.000 claims description 9
- 230000008878 coupling Effects 0.000 claims description 9
- 238000010168 coupling process Methods 0.000 claims description 9
- 238000005859 coupling reaction Methods 0.000 claims description 9
- 230000004048 modification Effects 0.000 claims description 9
- 238000012986 modification Methods 0.000 claims description 9
- 102100027207 CD27 antigen Human genes 0.000 claims description 8
- 108010009685 Cholinergic Receptors Proteins 0.000 claims description 8
- 102100039061 Cytokine receptor common subunit beta Human genes 0.000 claims description 8
- 108010066687 Epithelial Cell Adhesion Molecule Proteins 0.000 claims description 8
- 102100029360 Hematopoietic cell signal transducer Human genes 0.000 claims description 8
- 101000914511 Homo sapiens CD27 antigen Proteins 0.000 claims description 8
- 101001033280 Homo sapiens Cytokine receptor common subunit beta Proteins 0.000 claims description 8
- 101000920667 Homo sapiens Epithelial cell adhesion molecule Proteins 0.000 claims description 8
- 101000990188 Homo sapiens Hematopoietic cell signal transducer Proteins 0.000 claims description 8
- 101000998120 Homo sapiens Interleukin-3 receptor subunit alpha Proteins 0.000 claims description 8
- 101001005728 Homo sapiens Melanoma-associated antigen 1 Proteins 0.000 claims description 8
- 101000914484 Homo sapiens T-lymphocyte activation antigen CD80 Proteins 0.000 claims description 8
- 101000809875 Homo sapiens TYRO protein tyrosine kinase-binding protein Proteins 0.000 claims description 8
- 101000655352 Homo sapiens Telomerase reverse transcriptase Proteins 0.000 claims description 8
- 108010064593 Intercellular Adhesion Molecule-1 Proteins 0.000 claims description 8
- 102100020793 Interleukin-13 receptor subunit alpha-2 Human genes 0.000 claims description 8
- 101710112634 Interleukin-13 receptor subunit alpha-2 Proteins 0.000 claims description 8
- 102100033493 Interleukin-3 receptor subunit alpha Human genes 0.000 claims description 8
- 108010043610 KIR Receptors Proteins 0.000 claims description 8
- 102100033627 Killer cell immunoglobulin-like receptor 3DL1 Human genes 0.000 claims description 8
- 102100025050 Melanoma-associated antigen 1 Human genes 0.000 claims description 8
- 102100032870 Natural cytotoxicity triggering receptor 1 Human genes 0.000 claims description 8
- 102100032852 Natural cytotoxicity triggering receptor 3 Human genes 0.000 claims description 8
- 108060006580 PRAME Proteins 0.000 claims description 8
- 102000036673 PRAME Human genes 0.000 claims description 8
- 101710120463 Prostate stem cell antigen Proteins 0.000 claims description 8
- 102100036735 Prostate stem cell antigen Human genes 0.000 claims description 8
- 101001039269 Rattus norvegicus Glycine N-methyltransferase Proteins 0.000 claims description 8
- 102100027222 T-lymphocyte activation antigen CD80 Human genes 0.000 claims description 8
- 102100038717 TYRO protein tyrosine kinase-binding protein Human genes 0.000 claims description 8
- 102100022153 Tumor necrosis factor receptor superfamily member 4 Human genes 0.000 claims description 8
- 101710165473 Tumor necrosis factor receptor superfamily member 4 Proteins 0.000 claims description 8
- 102000034337 acetylcholine receptors Human genes 0.000 claims description 8
- BGFTWECWAICPDG-UHFFFAOYSA-N 2-[bis(4-chlorophenyl)methyl]-4-n-[3-[bis(4-chlorophenyl)methyl]-4-(dimethylamino)phenyl]-1-n,1-n-dimethylbenzene-1,4-diamine Chemical compound C1=C(C(C=2C=CC(Cl)=CC=2)C=2C=CC(Cl)=CC=2)C(N(C)C)=CC=C1NC(C=1)=CC=C(N(C)C)C=1C(C=1C=CC(Cl)=CC=1)C1=CC=C(Cl)C=C1 BGFTWECWAICPDG-UHFFFAOYSA-N 0.000 claims description 7
- 108010008014 B-Cell Maturation Antigen Proteins 0.000 claims description 7
- 102000006942 B-Cell Maturation Antigen Human genes 0.000 claims description 7
- 102100038080 B-cell receptor CD22 Human genes 0.000 claims description 7
- 101000840545 Bacillus thuringiensis L-isoleucine-4-hydroxylase Proteins 0.000 claims description 7
- 102100024263 CD160 antigen Human genes 0.000 claims description 7
- 108010062802 CD66 antigens Proteins 0.000 claims description 7
- 101100463133 Caenorhabditis elegans pdl-1 gene Proteins 0.000 claims description 7
- 102100024533 Carcinoembryonic antigen-related cell adhesion molecule 1 Human genes 0.000 claims description 7
- 102100021396 Cell surface glycoprotein CD200 receptor 1 Human genes 0.000 claims description 7
- 101710093674 Cyclic nucleotide-gated cation channel beta-1 Proteins 0.000 claims description 7
- 102100029722 Ectonucleoside triphosphate diphosphohydrolase 1 Human genes 0.000 claims description 7
- 101000884305 Homo sapiens B-cell receptor CD22 Proteins 0.000 claims description 7
- 101000761938 Homo sapiens CD160 antigen Proteins 0.000 claims description 7
- 101000969553 Homo sapiens Cell surface glycoprotein CD200 receptor 1 Proteins 0.000 claims description 7
- 101001012447 Homo sapiens Ectonucleoside triphosphate diphosphohydrolase 1 Proteins 0.000 claims description 7
- 101001037256 Homo sapiens Indoleamine 2,3-dioxygenase 1 Proteins 0.000 claims description 7
- 101000589305 Homo sapiens Natural cytotoxicity triggering receptor 2 Proteins 0.000 claims description 7
- 101000971513 Homo sapiens Natural killer cells antigen CD94 Proteins 0.000 claims description 7
- 101001109698 Homo sapiens Nuclear receptor subfamily 4 group A member 2 Proteins 0.000 claims description 7
- 101001098352 Homo sapiens OX-2 membrane glycoprotein Proteins 0.000 claims description 7
- 101000831007 Homo sapiens T-cell immunoreceptor with Ig and ITIM domains Proteins 0.000 claims description 7
- 101000596234 Homo sapiens T-cell surface protein tactile Proteins 0.000 claims description 7
- 101000831496 Homo sapiens Toll-like receptor 3 Proteins 0.000 claims description 7
- 101000979190 Homo sapiens Transcription factor MafB Proteins 0.000 claims description 7
- 101000851376 Homo sapiens Tumor necrosis factor receptor superfamily member 8 Proteins 0.000 claims description 7
- 101000666896 Homo sapiens V-type immunoglobulin domain-containing suppressor of T-cell activation Proteins 0.000 claims description 7
- 102100040061 Indoleamine 2,3-dioxygenase 1 Human genes 0.000 claims description 7
- 102100037877 Intercellular adhesion molecule 1 Human genes 0.000 claims description 7
- 102100028198 Macrophage colony-stimulating factor 1 receptor Human genes 0.000 claims description 7
- 101710150918 Macrophage colony-stimulating factor 1 receptor Proteins 0.000 claims description 7
- 108010061593 Member 14 Tumor Necrosis Factor Receptors Proteins 0.000 claims description 7
- 102100032851 Natural cytotoxicity triggering receptor 2 Human genes 0.000 claims description 7
- 102100021462 Natural killer cells antigen CD94 Human genes 0.000 claims description 7
- 108010012255 Neural Cell Adhesion Molecule L1 Proteins 0.000 claims description 7
- 102100024964 Neural cell adhesion molecule L1 Human genes 0.000 claims description 7
- 102100022676 Nuclear receptor subfamily 4 group A member 2 Human genes 0.000 claims description 7
- 102100037589 OX-2 membrane glycoprotein Human genes 0.000 claims description 7
- 102100035591 POU domain, class 2, transcription factor 2 Human genes 0.000 claims description 7
- 101710084411 POU domain, class 2, transcription factor 2 Proteins 0.000 claims description 7
- 102100023606 Retinoic acid receptor alpha Human genes 0.000 claims description 7
- 101001037255 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) Indoleamine 2,3-dioxygenase Proteins 0.000 claims description 7
- 102100024834 T-cell immunoreceptor with Ig and ITIM domains Human genes 0.000 claims description 7
- 102100035268 T-cell surface protein tactile Human genes 0.000 claims description 7
- 102100024324 Toll-like receptor 3 Human genes 0.000 claims description 7
- 102100023234 Transcription factor MafB Human genes 0.000 claims description 7
- 102100025946 Transforming growth factor beta activator LRRC32 Human genes 0.000 claims description 7
- 101710169732 Transforming growth factor beta activator LRRC32 Proteins 0.000 claims description 7
- 102100040653 Tryptophan 2,3-dioxygenase Human genes 0.000 claims description 7
- 102100028785 Tumor necrosis factor receptor superfamily member 14 Human genes 0.000 claims description 7
- 102100036857 Tumor necrosis factor receptor superfamily member 8 Human genes 0.000 claims description 7
- 102100038282 V-type immunoglobulin domain-containing suppressor of T-cell activation Human genes 0.000 claims description 7
- 102100022748 Wilms tumor protein Human genes 0.000 claims description 7
- 101710127857 Wilms tumor protein Proteins 0.000 claims description 7
- IJJVMEJXYNJXOJ-UHFFFAOYSA-N fluquinconazole Chemical compound C=1C=C(Cl)C=C(Cl)C=1N1C(=O)C2=CC(F)=CC=C2N=C1N1C=NC=N1 IJJVMEJXYNJXOJ-UHFFFAOYSA-N 0.000 claims description 7
- 238000003881 globally optimized alternating phase rectangular pulse Methods 0.000 claims description 7
- 229950001907 monalizumab Drugs 0.000 claims description 7
- 108091008726 retinoic acid receptors α Proteins 0.000 claims description 7
- 108010082808 4-1BB Ligand Proteins 0.000 claims description 6
- 102100031585 ADP-ribosyl cyclase/cyclic ADP-ribose hydrolase 1 Human genes 0.000 claims description 6
- 102100026094 C-type lectin domain family 12 member A Human genes 0.000 claims description 6
- 102100032912 CD44 antigen Human genes 0.000 claims description 6
- 101000777636 Homo sapiens ADP-ribosyl cyclase/cyclic ADP-ribose hydrolase 1 Proteins 0.000 claims description 6
- 101000912622 Homo sapiens C-type lectin domain family 12 member A Proteins 0.000 claims description 6
- 101000868273 Homo sapiens CD44 antigen Proteins 0.000 claims description 6
- 101000934338 Homo sapiens Myeloid cell surface antigen CD33 Proteins 0.000 claims description 6
- 101000874179 Homo sapiens Syndecan-1 Proteins 0.000 claims description 6
- 102100020943 Leukocyte-associated immunoglobulin-like receptor 1 Human genes 0.000 claims description 6
- 102100025243 Myeloid cell surface antigen CD33 Human genes 0.000 claims description 6
- 102000003729 Neprilysin Human genes 0.000 claims description 6
- 108090000028 Neprilysin Proteins 0.000 claims description 6
- 102100035721 Syndecan-1 Human genes 0.000 claims description 6
- 102100032101 Tumor necrosis factor ligand superfamily member 9 Human genes 0.000 claims description 6
- 210000000601 blood cell Anatomy 0.000 claims description 6
- 239000003814 drug Substances 0.000 claims description 6
- 108010087914 epidermal growth factor receptor VIII Proteins 0.000 claims description 6
- 210000004700 fetal blood Anatomy 0.000 claims description 6
- 229960005386 ipilimumab Drugs 0.000 claims description 6
- 108010025001 leukocyte-associated immunoglobulin-like receptor 1 Proteins 0.000 claims description 6
- 244000052769 pathogen Species 0.000 claims description 6
- 229940124597 therapeutic agent Drugs 0.000 claims description 6
- 230000001960 triggered effect Effects 0.000 claims description 6
- 102000003886 Glycoproteins Human genes 0.000 claims description 5
- 108090000288 Glycoproteins Proteins 0.000 claims description 5
- 101000610551 Homo sapiens Prominin-1 Proteins 0.000 claims description 5
- 101000934341 Homo sapiens T-cell surface glycoprotein CD5 Proteins 0.000 claims description 5
- 206010062016 Immunosuppression Diseases 0.000 claims description 5
- 102100040120 Prominin-1 Human genes 0.000 claims description 5
- 101150066717 Rara gene Proteins 0.000 claims description 5
- 102100025244 T-cell surface glycoprotein CD5 Human genes 0.000 claims description 5
- 230000000981 bystander Effects 0.000 claims description 5
- 229960002204 daratumumab Drugs 0.000 claims description 5
- 230000001605 fetal effect Effects 0.000 claims description 5
- 239000003102 growth factor Substances 0.000 claims description 5
- 230000001506 immunosuppresive effect Effects 0.000 claims description 5
- 102000006495 integrins Human genes 0.000 claims description 5
- 108010044426 integrins Proteins 0.000 claims description 5
- 239000003446 ligand Substances 0.000 claims description 5
- 231100000590 oncogenic Toxicity 0.000 claims description 5
- 230000002246 oncogenic effect Effects 0.000 claims description 5
- 230000001717 pathogenic effect Effects 0.000 claims description 5
- 102000040650 (ribonucleotides)n+m Human genes 0.000 claims description 4
- 102100026402 Adhesion G protein-coupled receptor E2 Human genes 0.000 claims description 4
- 101710149863 C-C chemokine receptor type 4 Proteins 0.000 claims description 4
- 108010008629 CA-125 Antigen Proteins 0.000 claims description 4
- 108700012439 CA9 Proteins 0.000 claims description 4
- 102100032976 CCR4-NOT transcription complex subunit 6 Human genes 0.000 claims description 4
- 102100024210 CD166 antigen Human genes 0.000 claims description 4
- 102100038077 CD226 antigen Human genes 0.000 claims description 4
- 101150013553 CD40 gene Proteins 0.000 claims description 4
- 102100025221 CD70 antigen Human genes 0.000 claims description 4
- 102000024905 CD99 Human genes 0.000 claims description 4
- 108060001253 CD99 Proteins 0.000 claims description 4
- 102100025570 Cancer/testis antigen 1 Human genes 0.000 claims description 4
- 102100024423 Carbonic anhydrase 9 Human genes 0.000 claims description 4
- 102000001301 EGF receptor Human genes 0.000 claims description 4
- 102100030595 HLA class II histocompatibility antigen gamma chain Human genes 0.000 claims description 4
- 101000718211 Homo sapiens Adhesion G protein-coupled receptor E2 Proteins 0.000 claims description 4
- 101000980840 Homo sapiens CD166 antigen Proteins 0.000 claims description 4
- 101000884298 Homo sapiens CD226 antigen Proteins 0.000 claims description 4
- 101000934356 Homo sapiens CD70 antigen Proteins 0.000 claims description 4
- 101000856237 Homo sapiens Cancer/testis antigen 1 Proteins 0.000 claims description 4
- 101000851181 Homo sapiens Epidermal growth factor receptor Proteins 0.000 claims description 4
- 101001082627 Homo sapiens HLA class II histocompatibility antigen gamma chain Proteins 0.000 claims description 4
- 101000994365 Homo sapiens Integrin alpha-6 Proteins 0.000 claims description 4
- 101001078143 Homo sapiens Integrin alpha-IIb Proteins 0.000 claims description 4
- 101000945331 Homo sapiens Killer cell immunoglobulin-like receptor 2DL4 Proteins 0.000 claims description 4
- 101000945340 Homo sapiens Killer cell immunoglobulin-like receptor 2DS1 Proteins 0.000 claims description 4
- 101000984189 Homo sapiens Leukocyte immunoglobulin-like receptor subfamily B member 2 Proteins 0.000 claims description 4
- 101000633778 Homo sapiens SLAM family member 5 Proteins 0.000 claims description 4
- 101000662902 Homo sapiens T cell receptor beta constant 2 Proteins 0.000 claims description 4
- 101000914496 Homo sapiens T-cell antigen CD7 Proteins 0.000 claims description 4
- 101000946863 Homo sapiens T-cell surface glycoprotein CD3 delta chain Proteins 0.000 claims description 4
- 101000946860 Homo sapiens T-cell surface glycoprotein CD3 epsilon chain Proteins 0.000 claims description 4
- 101000738413 Homo sapiens T-cell surface glycoprotein CD3 gamma chain Proteins 0.000 claims description 4
- 102100032816 Integrin alpha-6 Human genes 0.000 claims description 4
- 102100025306 Integrin alpha-IIb Human genes 0.000 claims description 4
- 102100033633 Killer cell immunoglobulin-like receptor 2DL4 Human genes 0.000 claims description 4
- 102100033631 Killer cell immunoglobulin-like receptor 2DS1 Human genes 0.000 claims description 4
- 102100025583 Leukocyte immunoglobulin-like receptor subfamily B member 2 Human genes 0.000 claims description 4
- 108010008707 Mucin-1 Proteins 0.000 claims description 4
- 102000007298 Mucin-1 Human genes 0.000 claims description 4
- 101100346932 Mus musculus Muc1 gene Proteins 0.000 claims description 4
- 108091000080 Phosphotransferase Proteins 0.000 claims description 4
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 claims description 4
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 claims description 4
- 102100029216 SLAM family member 5 Human genes 0.000 claims description 4
- 229940100514 Syk tyrosine kinase inhibitor Drugs 0.000 claims description 4
- 102100037298 T cell receptor beta constant 2 Human genes 0.000 claims description 4
- 102100027208 T-cell antigen CD7 Human genes 0.000 claims description 4
- 102100035891 T-cell surface glycoprotein CD3 delta chain Human genes 0.000 claims description 4
- 102100035794 T-cell surface glycoprotein CD3 epsilon chain Human genes 0.000 claims description 4
- 102100037911 T-cell surface glycoprotein CD3 gamma chain Human genes 0.000 claims description 4
- 101800000385 Transmembrane protein Proteins 0.000 claims description 4
- 102100040245 Tumor necrosis factor receptor superfamily member 5 Human genes 0.000 claims description 4
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 claims description 4
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 claims description 4
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 claims description 4
- SRHNADOZAAWYLV-XLMUYGLTSA-N alpha-L-Fucp-(1->2)-beta-D-Galp-(1->4)-[alpha-L-Fucp-(1->3)]-beta-D-GlcpNAc Chemical compound O[C@H]1[C@H](O)[C@H](O)[C@H](C)O[C@H]1O[C@H]1[C@H](O[C@H]2[C@@H]([C@@H](NC(C)=O)[C@H](O)O[C@@H]2CO)O[C@H]2[C@H]([C@H](O)[C@H](O)[C@H](C)O2)O)O[C@H](CO)[C@H](O)[C@@H]1O SRHNADOZAAWYLV-XLMUYGLTSA-N 0.000 claims description 4
- 229940014144 folate Drugs 0.000 claims description 4
- 235000019152 folic acid Nutrition 0.000 claims description 4
- 239000011724 folic acid Substances 0.000 claims description 4
- OVBPIULPVIDEAO-LBPRGKRZSA-N folic acid Chemical compound C=1N=C2NC(N)=NC(=O)C2=NC=1CNC1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 OVBPIULPVIDEAO-LBPRGKRZSA-N 0.000 claims description 4
- 150000002270 gangliosides Chemical class 0.000 claims description 4
- 102000020233 phosphotransferase Human genes 0.000 claims description 4
- 108091035539 telomere Proteins 0.000 claims description 4
- 210000003411 telomere Anatomy 0.000 claims description 4
- 102000055501 telomere Human genes 0.000 claims description 4
- 229960000548 alemtuzumab Drugs 0.000 claims description 3
- 230000004186 co-expression Effects 0.000 claims description 3
- 229960004497 dinutuximab Drugs 0.000 claims description 3
- 229960002450 ofatumumab Drugs 0.000 claims description 3
- 229960002087 pertuzumab Drugs 0.000 claims description 3
- 229960000575 trastuzumab Drugs 0.000 claims description 3
- 229950004593 ublituximab Drugs 0.000 claims description 3
- 208000023275 Autoimmune disease Diseases 0.000 claims description 2
- 108091032955 Bacterial small RNA Proteins 0.000 claims description 2
- 208000002250 Hematologic Neoplasms Diseases 0.000 claims description 2
- 208000036142 Viral infection Diseases 0.000 claims description 2
- 239000002246 antineoplastic agent Substances 0.000 claims description 2
- 210000003850 cellular structure Anatomy 0.000 claims description 2
- 229940127089 cytotoxic agent Drugs 0.000 claims description 2
- 229950009791 durvalumab Drugs 0.000 claims description 2
- 239000000710 homodimer Substances 0.000 claims description 2
- 229940124622 immune-modulator drug Drugs 0.000 claims description 2
- 229950007752 isatuximab Drugs 0.000 claims description 2
- 239000003226 mitogen Substances 0.000 claims description 2
- 229960003347 obinutuzumab Drugs 0.000 claims description 2
- 230000035515 penetration Effects 0.000 claims description 2
- 230000002285 radioactive effect Effects 0.000 claims description 2
- 230000009385 viral infection Effects 0.000 claims description 2
- 102100027314 Beta-2-microglobulin Human genes 0.000 claims 4
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 claims 3
- 108050005493 CD3 protein, epsilon/gamma/delta subunit Proteins 0.000 claims 3
- 238000010354 CRISPR gene editing Methods 0.000 claims 3
- 102000000704 Interleukin-7 Human genes 0.000 claims 3
- 102100026882 Alpha-synuclein Human genes 0.000 claims 2
- 102100035875 C-C chemokine receptor type 5 Human genes 0.000 claims 1
- 101710149870 C-C chemokine receptor type 5 Proteins 0.000 claims 1
- 102000007269 CA-125 Antigen Human genes 0.000 claims 1
- ODINCKMPIJJUCX-UHFFFAOYSA-N Calcium oxide Chemical compound [Ca]=O ODINCKMPIJJUCX-UHFFFAOYSA-N 0.000 claims 1
- 101001000998 Homo sapiens Protein phosphatase 1 regulatory subunit 12C Proteins 0.000 claims 1
- 102100035620 Protein phosphatase 1 regulatory subunit 12C Human genes 0.000 claims 1
- 108010043645 Transcription Activator-Like Effector Nucleases Proteins 0.000 claims 1
- 230000006798 recombination Effects 0.000 claims 1
- 238000005215 recombination Methods 0.000 claims 1
- 101150047061 tag-72 gene Proteins 0.000 claims 1
- 238000002648 combination therapy Methods 0.000 abstract description 15
- 210000004263 induced pluripotent stem cell Anatomy 0.000 description 154
- 102100029185 Low affinity immunoglobulin gamma Fc region receptor III-B Human genes 0.000 description 82
- 230000010354 integration Effects 0.000 description 59
- 102000004169 proteins and genes Human genes 0.000 description 51
- 235000018102 proteins Nutrition 0.000 description 43
- 102000015736 beta 2-Microglobulin Human genes 0.000 description 35
- 238000013461 design Methods 0.000 description 31
- 230000008685 targeting Effects 0.000 description 27
- 239000000976 ink Substances 0.000 description 24
- 238000011282 treatment Methods 0.000 description 19
- 210000001778 pluripotent stem cell Anatomy 0.000 description 18
- 102100021592 Interleukin-7 Human genes 0.000 description 17
- 230000004568 DNA-binding Effects 0.000 description 16
- 230000000694 effects Effects 0.000 description 16
- 201000010099 disease Diseases 0.000 description 15
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 15
- 230000008672 reprogramming Effects 0.000 description 15
- 239000002773 nucleotide Substances 0.000 description 14
- 125000003729 nucleotide group Chemical group 0.000 description 14
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 13
- 230000004913 activation Effects 0.000 description 13
- 230000010261 cell growth Effects 0.000 description 13
- 210000004881 tumor cell Anatomy 0.000 description 13
- 239000011701 zinc Substances 0.000 description 13
- 229910052725 zinc Inorganic materials 0.000 description 13
- 108010076504 Protein Sorting Signals Proteins 0.000 description 11
- 230000015572 biosynthetic process Effects 0.000 description 11
- 238000010586 diagram Methods 0.000 description 11
- 238000000684 flow cytometry Methods 0.000 description 11
- 238000000338 in vitro Methods 0.000 description 11
- 238000001727 in vivo Methods 0.000 description 11
- 150000007523 nucleic acids Chemical class 0.000 description 11
- 108020003285 Isocitrate lyase Proteins 0.000 description 10
- 108700018351 Major Histocompatibility Complex Proteins 0.000 description 10
- 108091028043 Nucleic acid sequence Proteins 0.000 description 10
- 108010017070 Zinc Finger Nucleases Proteins 0.000 description 10
- 125000003275 alpha amino acid group Chemical group 0.000 description 10
- 238000013459 approach Methods 0.000 description 10
- 230000006870 function Effects 0.000 description 10
- 210000004379 membrane Anatomy 0.000 description 10
- 230000020382 suppression by virus of host antigen processing and presentation of peptide antigen via MHC class I Effects 0.000 description 10
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 9
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 9
- 241000699666 Mus <mouse, genus> Species 0.000 description 9
- 108010073062 Transcription Activator-Like Effectors Proteins 0.000 description 9
- 230000009977 dual effect Effects 0.000 description 9
- 210000004698 lymphocyte Anatomy 0.000 description 9
- 210000002540 macrophage Anatomy 0.000 description 9
- 108020004414 DNA Proteins 0.000 description 8
- 230000001413 cellular effect Effects 0.000 description 8
- 239000003795 chemical substances by application Substances 0.000 description 8
- 230000002950 deficient Effects 0.000 description 8
- 230000028993 immune response Effects 0.000 description 8
- 239000002609 medium Substances 0.000 description 8
- 210000003716 mesoderm Anatomy 0.000 description 8
- 108020004999 messenger RNA Proteins 0.000 description 8
- 210000000440 neutrophil Anatomy 0.000 description 8
- 230000008569 process Effects 0.000 description 8
- 230000004044 response Effects 0.000 description 8
- 239000000126 substance Substances 0.000 description 8
- 230000032258 transport Effects 0.000 description 8
- 230000035899 viability Effects 0.000 description 8
- 108091026890 Coding region Proteins 0.000 description 7
- 230000000735 allogeneic effect Effects 0.000 description 7
- 230000033228 biological regulation Effects 0.000 description 7
- 238000004113 cell culture Methods 0.000 description 7
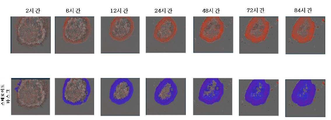
- 238000003384 imaging method Methods 0.000 description 7
- 239000003112 inhibitor Substances 0.000 description 7
- 230000037361 pathway Effects 0.000 description 7
- 239000000047 product Substances 0.000 description 7
- 230000001105 regulatory effect Effects 0.000 description 7
- 108010042407 Endonucleases Proteins 0.000 description 6
- 102000006601 Thymidine Kinase Human genes 0.000 description 6
- 108020004440 Thymidine kinase Proteins 0.000 description 6
- 230000024245 cell differentiation Effects 0.000 description 6
- 230000003915 cell function Effects 0.000 description 6
- 238000011161 development Methods 0.000 description 6
- 230000018109 developmental process Effects 0.000 description 6
- 210000003981 ectoderm Anatomy 0.000 description 6
- 210000001671 embryonic stem cell Anatomy 0.000 description 6
- 210000001900 endoderm Anatomy 0.000 description 6
- 230000005017 genetic modification Effects 0.000 description 6
- 239000001963 growth medium Substances 0.000 description 6
- 230000006801 homologous recombination Effects 0.000 description 6
- 238000002744 homologous recombination Methods 0.000 description 6
- 210000000265 leukocyte Anatomy 0.000 description 6
- 230000007246 mechanism Effects 0.000 description 6
- YOHYSYJDKVYCJI-UHFFFAOYSA-N n-[3-[[6-[3-(trifluoromethyl)anilino]pyrimidin-4-yl]amino]phenyl]cyclopropanecarboxamide Chemical class FC(F)(F)C1=CC=CC(NC=2N=CN=C(NC=3C=C(NC(=O)C4CC4)C=CC=3)C=2)=C1 YOHYSYJDKVYCJI-UHFFFAOYSA-N 0.000 description 6
- 102000039446 nucleic acids Human genes 0.000 description 6
- 108020004707 nucleic acids Proteins 0.000 description 6
- 229960004641 rituximab Drugs 0.000 description 6
- 150000003384 small molecules Chemical class 0.000 description 6
- 230000001052 transient effect Effects 0.000 description 6
- 102000000311 Cytosine Deaminase Human genes 0.000 description 5
- 108010080611 Cytosine Deaminase Proteins 0.000 description 5
- 241000699670 Mus sp. Species 0.000 description 5
- 108700026244 Open Reading Frames Proteins 0.000 description 5
- 102000018120 Recombinases Human genes 0.000 description 5
- 108010091086 Recombinases Proteins 0.000 description 5
- 102000040945 Transcription factor Human genes 0.000 description 5
- 108091023040 Transcription factor Proteins 0.000 description 5
- 230000003213 activating effect Effects 0.000 description 5
- 235000001014 amino acid Nutrition 0.000 description 5
- 230000030833 cell death Effects 0.000 description 5
- 230000004663 cell proliferation Effects 0.000 description 5
- 238000011284 combination treatment Methods 0.000 description 5
- 239000002299 complementary DNA Substances 0.000 description 5
- 210000002242 embryoid body Anatomy 0.000 description 5
- 210000002889 endothelial cell Anatomy 0.000 description 5
- 238000012239 gene modification Methods 0.000 description 5
- 230000030279 gene silencing Effects 0.000 description 5
- 235000013617 genetically modified food Nutrition 0.000 description 5
- 210000003071 memory t lymphocyte Anatomy 0.000 description 5
- 239000002679 microRNA Substances 0.000 description 5
- 238000013518 transcription Methods 0.000 description 5
- 230000035897 transcription Effects 0.000 description 5
- 102000004533 Endonucleases Human genes 0.000 description 4
- 108020005004 Guide RNA Proteins 0.000 description 4
- 108010073807 IgG Receptors Proteins 0.000 description 4
- 102000009490 IgG Receptors Human genes 0.000 description 4
- 108010017535 Interleukin-15 Receptors Proteins 0.000 description 4
- 102100029204 Low affinity immunoglobulin gamma Fc region receptor II-a Human genes 0.000 description 4
- 241001465754 Metazoa Species 0.000 description 4
- 101710136122 Tryptophan 2,3-dioxygenase Proteins 0.000 description 4
- 241000700605 Viruses Species 0.000 description 4
- 150000001413 amino acids Chemical class 0.000 description 4
- 208000006112 autosomal recessive hypercholesterolemia Diseases 0.000 description 4
- 230000008901 benefit Effects 0.000 description 4
- 102000003675 cytokine receptors Human genes 0.000 description 4
- 108010057085 cytokine receptors Proteins 0.000 description 4
- 238000002784 cytotoxicity assay Methods 0.000 description 4
- 231100000263 cytotoxicity test Toxicity 0.000 description 4
- 239000003596 drug target Substances 0.000 description 4
- 102000052116 epidermal growth factor receptor activity proteins Human genes 0.000 description 4
- 210000003743 erythrocyte Anatomy 0.000 description 4
- 238000011156 evaluation Methods 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 208000032655 familial 4 hypercholesterolemia Diseases 0.000 description 4
- 210000002950 fibroblast Anatomy 0.000 description 4
- 230000002068 genetic effect Effects 0.000 description 4
- 208000015181 infectious disease Diseases 0.000 description 4
- 208000032839 leukemia Diseases 0.000 description 4
- 238000012423 maintenance Methods 0.000 description 4
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 4
- 230000035755 proliferation Effects 0.000 description 4
- 230000019491 signal transduction Effects 0.000 description 4
- 210000001082 somatic cell Anatomy 0.000 description 4
- 230000000638 stimulation Effects 0.000 description 4
- RWQNBRDOKXIBIV-UHFFFAOYSA-N thymine Chemical compound CC1=CNC(=O)NC1=O RWQNBRDOKXIBIV-UHFFFAOYSA-N 0.000 description 4
- 238000010361 transduction Methods 0.000 description 4
- 230000026683 transduction Effects 0.000 description 4
- 210000001266 CD8-positive T-lymphocyte Anatomy 0.000 description 3
- 108090000397 Caspase 3 Proteins 0.000 description 3
- 108090000567 Caspase 7 Proteins 0.000 description 3
- 102100029855 Caspase-3 Human genes 0.000 description 3
- 102100038902 Caspase-7 Human genes 0.000 description 3
- 102100026550 Caspase-9 Human genes 0.000 description 3
- 108090000566 Caspase-9 Proteins 0.000 description 3
- 108010077544 Chromatin Proteins 0.000 description 3
- 102100026234 Cytokine receptor common subunit gamma Human genes 0.000 description 3
- 230000033616 DNA repair Effects 0.000 description 3
- 241000214054 Equine rhinitis A virus Species 0.000 description 3
- 108700024394 Exon Proteins 0.000 description 3
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 3
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 3
- 241000710198 Foot-and-mouth disease virus Species 0.000 description 3
- 102000001267 GSK3 Human genes 0.000 description 3
- 108060006662 GSK3 Proteins 0.000 description 3
- 101000917826 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor II-a Proteins 0.000 description 3
- 101000917824 Homo sapiens Low affinity immunoglobulin gamma Fc region receptor II-b Proteins 0.000 description 3
- 101000884271 Homo sapiens Signal transducer CD24 Proteins 0.000 description 3
- 101710099301 Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 3
- 229940124647 MEK inhibitor Drugs 0.000 description 3
- 102100023123 Mucin-16 Human genes 0.000 description 3
- 241001529936 Murinae Species 0.000 description 3
- 102000011755 Phosphoglycerate Kinase Human genes 0.000 description 3
- 108010029485 Protein Isoforms Proteins 0.000 description 3
- 102000001708 Protein Isoforms Human genes 0.000 description 3
- 102100038081 Signal transducer CD24 Human genes 0.000 description 3
- 101001099217 Thermotoga maritima (strain ATCC 43589 / DSM 3109 / JCM 10099 / NBRC 100826 / MSB8) Triosephosphate isomerase Proteins 0.000 description 3
- 241001648840 Thosea asigna virus Species 0.000 description 3
- 108700019146 Transgenes Proteins 0.000 description 3
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 3
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 3
- 230000002411 adverse Effects 0.000 description 3
- 230000000259 anti-tumor effect Effects 0.000 description 3
- 210000002459 blastocyst Anatomy 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 210000001185 bone marrow Anatomy 0.000 description 3
- 230000012292 cell migration Effects 0.000 description 3
- 238000002659 cell therapy Methods 0.000 description 3
- 210000003483 chromatin Anatomy 0.000 description 3
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 3
- 230000034994 death Effects 0.000 description 3
- 230000007812 deficiency Effects 0.000 description 3
- 210000004443 dendritic cell Anatomy 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 210000003038 endothelium Anatomy 0.000 description 3
- 108700015053 epidermal growth factor receptor activity proteins Proteins 0.000 description 3
- 230000005284 excitation Effects 0.000 description 3
- 210000002744 extracellular matrix Anatomy 0.000 description 3
- 230000004927 fusion Effects 0.000 description 3
- 210000001654 germ layer Anatomy 0.000 description 3
- 210000002443 helper t lymphocyte Anatomy 0.000 description 3
- 239000000833 heterodimer Substances 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 230000003993 interaction Effects 0.000 description 3
- 230000000670 limiting effect Effects 0.000 description 3
- 230000035800 maturation Effects 0.000 description 3
- 108091070501 miRNA Proteins 0.000 description 3
- 239000002829 mitogen activated protein kinase inhibitor Substances 0.000 description 3
- NFVJNJQRWPQVOA-UHFFFAOYSA-N n-[2-chloro-5-(trifluoromethyl)phenyl]-2-[3-(4-ethyl-5-ethylsulfanyl-1,2,4-triazol-3-yl)piperidin-1-yl]acetamide Chemical compound CCN1C(SCC)=NN=C1C1CN(CC(=O)NC=2C(=CC=C(C=2)C(F)(F)F)Cl)CCC1 NFVJNJQRWPQVOA-UHFFFAOYSA-N 0.000 description 3
- 235000015097 nutrients Nutrition 0.000 description 3
- 239000013612 plasmid Substances 0.000 description 3
- 230000006337 proteolytic cleavage Effects 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 239000011435 rock Substances 0.000 description 3
- 230000028327 secretion Effects 0.000 description 3
- 239000002356 single layer Substances 0.000 description 3
- 210000002536 stromal cell Anatomy 0.000 description 3
- 238000006467 substitution reaction Methods 0.000 description 3
- 230000002103 transcriptional effect Effects 0.000 description 3
- 230000014616 translation Effects 0.000 description 3
- 229950007217 tremelimumab Drugs 0.000 description 3
- 230000005909 tumor killing Effects 0.000 description 3
- 239000013603 viral vector Substances 0.000 description 3
- 230000003612 virological effect Effects 0.000 description 3
- 230000003442 weekly effect Effects 0.000 description 3
- FSPQCTGGIANIJZ-UHFFFAOYSA-N 2-[[(3,4-dimethoxyphenyl)-oxomethyl]amino]-4,5,6,7-tetrahydro-1-benzothiophene-3-carboxamide Chemical compound C1=C(OC)C(OC)=CC=C1C(=O)NC1=C(C(N)=O)C(CCCC2)=C2S1 FSPQCTGGIANIJZ-UHFFFAOYSA-N 0.000 description 2
- AHLWZBVXSWOPPL-RGYGYFBISA-N 20-deoxy-20-oxophorbol 12-myristate 13-acetate Chemical compound C([C@]1(O)C(=O)C(C)=C[C@H]1[C@@]1(O)[C@H](C)[C@H]2OC(=O)CCCCCCCCCCCCC)C(C=O)=C[C@H]1[C@H]1[C@]2(OC(C)=O)C1(C)C AHLWZBVXSWOPPL-RGYGYFBISA-N 0.000 description 2
- 102100037086 Bone marrow stromal antigen 2 Human genes 0.000 description 2
- 229940124292 CD20 monoclonal antibody Drugs 0.000 description 2
- 102100038078 CD276 antigen Human genes 0.000 description 2
- 102000000905 Cadherin Human genes 0.000 description 2
- 108050007957 Cadherin Proteins 0.000 description 2
- 101100366466 Caenorhabditis elegans spo-11 gene Proteins 0.000 description 2
- 241000282836 Camelus dromedarius Species 0.000 description 2
- 102000011727 Caspases Human genes 0.000 description 2
- 108010076667 Caspases Proteins 0.000 description 2
- 102000019034 Chemokines Human genes 0.000 description 2
- 108010012236 Chemokines Proteins 0.000 description 2
- 241000251730 Chondrichthyes Species 0.000 description 2
- 101710178046 Chorismate synthase 1 Proteins 0.000 description 2
- 108091033380 Coding strand Proteins 0.000 description 2
- 101710152695 Cysteine synthase 1 Proteins 0.000 description 2
- 102100036466 Delta-like protein 3 Human genes 0.000 description 2
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 2
- 102000012804 EPCAM Human genes 0.000 description 2
- 101150084967 EPCAM gene Proteins 0.000 description 2
- 102100031780 Endonuclease Human genes 0.000 description 2
- 108091029865 Exogenous DNA Proteins 0.000 description 2
- 102100035139 Folate receptor alpha Human genes 0.000 description 2
- 102100035143 Folate receptor gamma Human genes 0.000 description 2
- 102100021260 Galactosylgalactosylxylosylprotein 3-beta-glucuronosyltransferase 1 Human genes 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- 101000740785 Homo sapiens Bone marrow stromal antigen 2 Proteins 0.000 description 2
- 101000884279 Homo sapiens CD276 antigen Proteins 0.000 description 2
- 101000916489 Homo sapiens Chondroitin sulfate proteoglycan 4 Proteins 0.000 description 2
- 101001055227 Homo sapiens Cytokine receptor common subunit gamma Proteins 0.000 description 2
- 101000889276 Homo sapiens Cytotoxic T-lymphocyte protein 4 Proteins 0.000 description 2
- 101000928513 Homo sapiens Delta-like protein 3 Proteins 0.000 description 2
- 101001023230 Homo sapiens Folate receptor alpha Proteins 0.000 description 2
- 101001023202 Homo sapiens Folate receptor gamma Proteins 0.000 description 2
- 101000894906 Homo sapiens Galactosylgalactosylxylosylprotein 3-beta-glucuronosyltransferase 1 Proteins 0.000 description 2
- 101000878602 Homo sapiens Immunoglobulin alpha Fc receptor Proteins 0.000 description 2
- 101001103039 Homo sapiens Inactive tyrosine-protein kinase transmembrane receptor ROR1 Proteins 0.000 description 2
- 101001063456 Homo sapiens Leucine-rich repeat-containing G-protein coupled receptor 5 Proteins 0.000 description 2
- 101001103036 Homo sapiens Nuclear receptor ROR-alpha Proteins 0.000 description 2
- 101000829725 Homo sapiens Phospholipid hydroperoxide glutathione peroxidase Proteins 0.000 description 2
- 101001056234 Homo sapiens Sperm mitochondrial-associated cysteine-rich protein Proteins 0.000 description 2
- 101000801255 Homo sapiens Tumor necrosis factor receptor superfamily member 17 Proteins 0.000 description 2
- 206010061598 Immunodeficiency Diseases 0.000 description 2
- 108060003951 Immunoglobulin Proteins 0.000 description 2
- 102100038005 Immunoglobulin alpha Fc receptor Human genes 0.000 description 2
- 102100039615 Inactive tyrosine-protein kinase transmembrane receptor ROR1 Human genes 0.000 description 2
- 102100034343 Integrase Human genes 0.000 description 2
- 108010061833 Integrases Proteins 0.000 description 2
- 102100031036 Leucine-rich repeat-containing G-protein coupled receptor 5 Human genes 0.000 description 2
- 108060001084 Luciferase Proteins 0.000 description 2
- 239000005089 Luciferase Substances 0.000 description 2
- 201000007114 MHC class I deficiency Diseases 0.000 description 2
- 108700011259 MicroRNAs Proteins 0.000 description 2
- 241000711408 Murine respirovirus Species 0.000 description 2
- 206010061309 Neoplasm progression Diseases 0.000 description 2
- 102000015636 Oligopeptides Human genes 0.000 description 2
- 108010038807 Oligopeptides Proteins 0.000 description 2
- 241001602688 Pama Species 0.000 description 2
- 102100032831 Protein ITPRID2 Human genes 0.000 description 2
- 102100020718 Receptor-type tyrosine-protein kinase FLT3 Human genes 0.000 description 2
- 101710151245 Receptor-type tyrosine-protein kinase FLT3 Proteins 0.000 description 2
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 2
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 2
- 102100026503 Sperm mitochondrial-associated cysteine-rich protein Human genes 0.000 description 2
- 230000006044 T cell activation Effects 0.000 description 2
- 101150057140 TACSTD1 gene Proteins 0.000 description 2
- 108091005735 TGF-beta receptors Proteins 0.000 description 2
- 108020004566 Transfer RNA Proteins 0.000 description 2
- 102000016715 Transforming Growth Factor beta Receptors Human genes 0.000 description 2
- 102100033726 Tumor necrosis factor receptor superfamily member 17 Human genes 0.000 description 2
- ISAKRJDGNUQOIC-UHFFFAOYSA-N Uracil Chemical compound O=C1C=CNC(=O)N1 ISAKRJDGNUQOIC-UHFFFAOYSA-N 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 230000029918 bioluminescence Effects 0.000 description 2
- 238000005415 bioluminescence Methods 0.000 description 2
- 210000001772 blood platelet Anatomy 0.000 description 2
- 210000002798 bone marrow cell Anatomy 0.000 description 2
- 230000020411 cell activation Effects 0.000 description 2
- 230000011712 cell development Effects 0.000 description 2
- 230000004709 cell invasion Effects 0.000 description 2
- 230000011748 cell maturation Effects 0.000 description 2
- 229960005395 cetuximab Drugs 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 238000002512 chemotherapy Methods 0.000 description 2
- 108700010039 chimeric receptor Proteins 0.000 description 2
- 210000001228 classical NK T cell Anatomy 0.000 description 2
- 238000003776 cleavage reaction Methods 0.000 description 2
- 238000003501 co-culture Methods 0.000 description 2
- 230000000139 costimulatory effect Effects 0.000 description 2
- 238000012258 culturing Methods 0.000 description 2
- 230000009089 cytolysis Effects 0.000 description 2
- OPTASPLRGRRNAP-UHFFFAOYSA-N cytosine Chemical compound NC=1C=CNC(=O)N=1 OPTASPLRGRRNAP-UHFFFAOYSA-N 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 229940127276 delta-like ligand 3 Drugs 0.000 description 2
- 238000010494 dissociation reaction Methods 0.000 description 2
- 230000005593 dissociations Effects 0.000 description 2
- 230000034431 double-strand break repair via homologous recombination Effects 0.000 description 2
- 230000011559 double-strand break repair via nonhomologous end joining Effects 0.000 description 2
- 239000000975 dye Substances 0.000 description 2
- 230000013020 embryo development Effects 0.000 description 2
- 230000003511 endothelial effect Effects 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 230000007247 enzymatic mechanism Effects 0.000 description 2
- 238000005206 flow analysis Methods 0.000 description 2
- XRECTZIEBJDKEO-UHFFFAOYSA-N flucytosine Chemical compound NC1=NC(=O)NC=C1F XRECTZIEBJDKEO-UHFFFAOYSA-N 0.000 description 2
- 229960004413 flucytosine Drugs 0.000 description 2
- IRSCQMHQWWYFCW-UHFFFAOYSA-N ganciclovir Chemical compound O=C1NC(N)=NC2=C1N=CN2COC(CO)CO IRSCQMHQWWYFCW-UHFFFAOYSA-N 0.000 description 2
- 229960002963 ganciclovir Drugs 0.000 description 2
- 238000012226 gene silencing method Methods 0.000 description 2
- 230000005283 ground state Effects 0.000 description 2
- UYTPUPDQBNUYGX-UHFFFAOYSA-N guanine Chemical compound O=C1NC(N)=NC2=C1N=CN2 UYTPUPDQBNUYGX-UHFFFAOYSA-N 0.000 description 2
- 230000008102 immune modulation Effects 0.000 description 2
- 210000000987 immune system Anatomy 0.000 description 2
- 102000018358 immunoglobulin Human genes 0.000 description 2
- 230000002779 inactivation Effects 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 230000000977 initiatory effect Effects 0.000 description 2
- 238000011081 inoculation Methods 0.000 description 2
- 230000004068 intracellular signaling Effects 0.000 description 2
- 230000002147 killing effect Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 230000005012 migration Effects 0.000 description 2
- 238000013508 migration Methods 0.000 description 2
- 238000010232 migration assay Methods 0.000 description 2
- 230000003278 mimic effect Effects 0.000 description 2
- 210000001616 monocyte Anatomy 0.000 description 2
- 238000010172 mouse model Methods 0.000 description 2
- 230000035772 mutation Effects 0.000 description 2
- 210000004287 null lymphocyte Anatomy 0.000 description 2
- 210000004303 peritoneum Anatomy 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 229940002612 prodrug Drugs 0.000 description 2
- 239000000651 prodrug Substances 0.000 description 2
- 230000001737 promoting effect Effects 0.000 description 2
- 230000007115 recruitment Effects 0.000 description 2
- 230000022532 regulation of transcription, DNA-dependent Effects 0.000 description 2
- 210000003289 regulatory T cell Anatomy 0.000 description 2
- 230000007017 scission Effects 0.000 description 2
- 230000008093 supporting effect Effects 0.000 description 2
- 230000002123 temporal effect Effects 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 229940113082 thymine Drugs 0.000 description 2
- 230000001988 toxicity Effects 0.000 description 2
- 231100000419 toxicity Toxicity 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- 230000009261 transgenic effect Effects 0.000 description 2
- 230000010474 transient expression Effects 0.000 description 2
- 238000013519 translation Methods 0.000 description 2
- 102000035160 transmembrane proteins Human genes 0.000 description 2
- 108091005703 transmembrane proteins Proteins 0.000 description 2
- 230000005751 tumor progression Effects 0.000 description 2
- 210000003171 tumor-infiltrating lymphocyte Anatomy 0.000 description 2
- 241000701161 unidentified adenovirus Species 0.000 description 2
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 1
- 101150028074 2 gene Proteins 0.000 description 1
- 108010005465 AC133 Antigen Proteins 0.000 description 1
- 102000005908 AC133 Antigen Human genes 0.000 description 1
- 102100033793 ALK tyrosine kinase receptor Human genes 0.000 description 1
- 229930024421 Adenine Natural products 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N Adenine Chemical compound NC1=NC=NC2=C1N=CN2 GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 244000047478 Afzelia bijuga Species 0.000 description 1
- 229940122531 Anaplastic lymphoma kinase inhibitor Drugs 0.000 description 1
- 239000000592 Artificial Cell Substances 0.000 description 1
- 208000003950 B-cell lymphoma Diseases 0.000 description 1
- 101150076800 B2M gene Proteins 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- 102100024217 CAMPATH-1 antigen Human genes 0.000 description 1
- 238000011357 CAR T-cell therapy Methods 0.000 description 1
- 108010041397 CD4 Antigens Proteins 0.000 description 1
- 108010065524 CD52 Antigen Proteins 0.000 description 1
- 101100152304 Caenorhabditis elegans tap-1 gene Proteins 0.000 description 1
- 241000710190 Cardiovirus Species 0.000 description 1
- 102000014914 Carrier Proteins Human genes 0.000 description 1
- 108090000994 Catalytic RNA Proteins 0.000 description 1
- 102000053642 Catalytic RNA Human genes 0.000 description 1
- 101710189311 Cytokine receptor common subunit gamma Proteins 0.000 description 1
- 230000007067 DNA methylation Effects 0.000 description 1
- 230000008265 DNA repair mechanism Effects 0.000 description 1
- 230000004543 DNA replication Effects 0.000 description 1
- 102100025682 Dystroglycan 1 Human genes 0.000 description 1
- 102100025137 Early activation antigen CD69 Human genes 0.000 description 1
- 101150039808 Egfr gene Proteins 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 102100037241 Endoglin Human genes 0.000 description 1
- 229910052693 Europium Inorganic materials 0.000 description 1
- 108010021468 Fc gamma receptor IIA Proteins 0.000 description 1
- 108010021472 Fc gamma receptor IIB Proteins 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 1
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 1
- 101000834253 Gallus gallus Actin, cytoplasmic 1 Proteins 0.000 description 1
- 206010071602 Genetic polymorphism Diseases 0.000 description 1
- 102000001398 Granzyme Human genes 0.000 description 1
- 108060005986 Granzyme Proteins 0.000 description 1
- 108010043121 Green Fluorescent Proteins Proteins 0.000 description 1
- 102000025850 HLA-A2 Antigen Human genes 0.000 description 1
- 108010074032 HLA-A2 Antigen Proteins 0.000 description 1
- 101150046249 Havcr2 gene Proteins 0.000 description 1
- 101000934374 Homo sapiens Early activation antigen CD69 Proteins 0.000 description 1
- 101000881679 Homo sapiens Endoglin Proteins 0.000 description 1
- 101000935043 Homo sapiens Integrin beta-1 Proteins 0.000 description 1
- 101000599862 Homo sapiens Intercellular adhesion molecule 3 Proteins 0.000 description 1
- 101001055157 Homo sapiens Interleukin-15 Proteins 0.000 description 1
- 101001027081 Homo sapiens Killer cell immunoglobulin-like receptor 2DL1 Proteins 0.000 description 1
- 101000945333 Homo sapiens Killer cell immunoglobulin-like receptor 2DL3 Proteins 0.000 description 1
- 101001023379 Homo sapiens Lysosome-associated membrane glycoprotein 1 Proteins 0.000 description 1
- 101001126417 Homo sapiens Platelet-derived growth factor receptor alpha Proteins 0.000 description 1
- 101000800116 Homo sapiens Thy-1 membrane glycoprotein Proteins 0.000 description 1
- 101000687905 Homo sapiens Transcription factor SOX-2 Proteins 0.000 description 1
- 101100377226 Homo sapiens ZBTB16 gene Proteins 0.000 description 1
- 101150106931 IFNG gene Proteins 0.000 description 1
- 102000018071 Immunoglobulin Fc Fragments Human genes 0.000 description 1
- 108010091135 Immunoglobulin Fc Fragments Proteins 0.000 description 1
- 102100025304 Integrin beta-1 Human genes 0.000 description 1
- 102000015271 Intercellular Adhesion Molecule-1 Human genes 0.000 description 1
- 102100037871 Intercellular adhesion molecule 3 Human genes 0.000 description 1
- 102100037850 Interferon gamma Human genes 0.000 description 1
- 108010074328 Interferon-gamma Proteins 0.000 description 1
- 108091029795 Intergenic region Proteins 0.000 description 1
- 108010066719 Interleukin Receptor Common gamma Subunit Proteins 0.000 description 1
- 102000018682 Interleukin Receptor Common gamma Subunit Human genes 0.000 description 1
- 102000004556 Interleukin-15 Receptors Human genes 0.000 description 1
- 108010038453 Interleukin-2 Receptors Proteins 0.000 description 1
- 102000010789 Interleukin-2 Receptors Human genes 0.000 description 1
- 108010017411 Interleukin-21 Receptors Proteins 0.000 description 1
- 102000004527 Interleukin-21 Receptors Human genes 0.000 description 1
- 108010038486 Interleukin-4 Receptors Proteins 0.000 description 1
- 102000010787 Interleukin-4 Receptors Human genes 0.000 description 1
- 108010038498 Interleukin-7 Receptors Proteins 0.000 description 1
- 102000010782 Interleukin-7 Receptors Human genes 0.000 description 1
- 108010038414 Interleukin-9 Receptors Proteins 0.000 description 1
- 102000010682 Interleukin-9 Receptors Human genes 0.000 description 1
- 108091092195 Intron Proteins 0.000 description 1
- 102100037363 Killer cell immunoglobulin-like receptor 2DL1 Human genes 0.000 description 1
- 102100033634 Killer cell immunoglobulin-like receptor 2DL3 Human genes 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- 102100029205 Low affinity immunoglobulin gamma Fc region receptor II-b Human genes 0.000 description 1
- 102100035133 Lysosome-associated membrane glycoprotein 1 Human genes 0.000 description 1
- 102000043136 MAP kinase family Human genes 0.000 description 1
- 108091054455 MAP kinase family Proteins 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 108091034054 MiR-138 Proteins 0.000 description 1
- 108091033773 MiR-155 Proteins 0.000 description 1
- 108091027977 Mir-200 Proteins 0.000 description 1
- 108020005196 Mitochondrial DNA Proteins 0.000 description 1
- 229930192392 Mitomycin Natural products 0.000 description 1
- 102000007474 Multiprotein Complexes Human genes 0.000 description 1
- 108010085220 Multiprotein Complexes Proteins 0.000 description 1
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 1
- 108010001880 NK Cell Lectin-Like Receptor Subfamily C Proteins 0.000 description 1
- 108010001657 NK Cell Lectin-Like Receptor Subfamily K Proteins 0.000 description 1
- 230000006051 NK cell activation Effects 0.000 description 1
- 102000002755 Natural Cytotoxicity Triggering Receptor 1 Human genes 0.000 description 1
- 108010004220 Natural Cytotoxicity Triggering Receptor 2 Proteins 0.000 description 1
- 102000002751 Natural Cytotoxicity Triggering Receptor 2 Human genes 0.000 description 1
- 102000002752 Natural Cytotoxicity Triggering Receptor 3 Human genes 0.000 description 1
- 108010070047 Notch Receptors Proteins 0.000 description 1
- 102000005650 Notch Receptors Human genes 0.000 description 1
- 108020004711 Nucleic Acid Probes Proteins 0.000 description 1
- 101710160107 Outer membrane protein A Proteins 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 102100035423 POU domain, class 5, transcription factor 1 Human genes 0.000 description 1
- 101710126211 POU domain, class 5, transcription factor 1 Proteins 0.000 description 1
- 102000010292 Peptide Elongation Factor 1 Human genes 0.000 description 1
- 108010077524 Peptide Elongation Factor 1 Proteins 0.000 description 1
- 102000007079 Peptide Fragments Human genes 0.000 description 1
- 108010033276 Peptide Fragments Proteins 0.000 description 1
- 102100030485 Platelet-derived growth factor receptor alpha Human genes 0.000 description 1
- 241001672814 Porcine teschovirus 1 Species 0.000 description 1
- 108700003766 Promyelocytic Leukemia Zinc Finger Proteins 0.000 description 1
- 102000004278 Receptor Protein-Tyrosine Kinases Human genes 0.000 description 1
- 108090000873 Receptor Protein-Tyrosine Kinases Proteins 0.000 description 1
- 108700005075 Regulator Genes Proteins 0.000 description 1
- 108091028664 Ribonucleotide Proteins 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- 108010003723 Single-Domain Antibodies Proteins 0.000 description 1
- 108091027967 Small hairpin RNA Proteins 0.000 description 1
- 108700012920 TNF Proteins 0.000 description 1
- 206010043276 Teratoma Diseases 0.000 description 1
- 210000000447 Th1 cell Anatomy 0.000 description 1
- 210000004241 Th2 cell Anatomy 0.000 description 1
- 102100033523 Thy-1 membrane glycoprotein Human genes 0.000 description 1
- 108091028113 Trans-activating crRNA Proteins 0.000 description 1
- 102100024270 Transcription factor SOX-2 Human genes 0.000 description 1
- 206010064390 Tumour invasion Diseases 0.000 description 1
- 108090000848 Ubiquitin Proteins 0.000 description 1
- 102000044159 Ubiquitin Human genes 0.000 description 1
- 208000008383 Wilms tumor Diseases 0.000 description 1
- 230000004156 Wnt signaling pathway Effects 0.000 description 1
- 210000001766 X chromosome Anatomy 0.000 description 1
- 241000589634 Xanthomonas Species 0.000 description 1
- PTFCDOFLOPIGGS-UHFFFAOYSA-N Zinc dication Chemical compound [Zn+2] PTFCDOFLOPIGGS-UHFFFAOYSA-N 0.000 description 1
- 102100040314 Zinc finger and BTB domain-containing protein 16 Human genes 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 230000003044 adaptive effect Effects 0.000 description 1
- 230000004721 adaptive immunity Effects 0.000 description 1
- 229960000643 adenine Drugs 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 210000004504 adult stem cell Anatomy 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 238000011129 allogeneic cell therapy Methods 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 230000003321 amplification Effects 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 230000003042 antagnostic effect Effects 0.000 description 1
- 230000000692 anti-sense effect Effects 0.000 description 1
- 230000030741 antigen processing and presentation Effects 0.000 description 1
- 239000003080 antimitotic agent Substances 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 210000004507 artificial chromosome Anatomy 0.000 description 1
- 230000003305 autocrine Effects 0.000 description 1
- 230000002567 autonomic effect Effects 0.000 description 1
- 244000052616 bacterial pathogen Species 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 210000003651 basophil Anatomy 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 108091008324 binding proteins Proteins 0.000 description 1
- 230000031018 biological processes and functions Effects 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 238000001574 biopsy Methods 0.000 description 1
- 238000002619 cancer immunotherapy Methods 0.000 description 1
- 230000009400 cancer invasion Effects 0.000 description 1
- 230000000711 cancerogenic effect Effects 0.000 description 1
- 231100000315 carcinogenic Toxicity 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 230000005859 cell recognition Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000010307 cell transformation Effects 0.000 description 1
- 230000005889 cellular cytotoxicity Effects 0.000 description 1
- 230000008614 cellular interaction Effects 0.000 description 1
- 210000002230 centromere Anatomy 0.000 description 1
- 238000007385 chemical modification Methods 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 230000003399 chemotactic effect Effects 0.000 description 1
- 230000035605 chemotaxis Effects 0.000 description 1
- 239000013611 chromosomal DNA Substances 0.000 description 1
- 230000002759 chromosomal effect Effects 0.000 description 1
- 210000002808 connective tissue Anatomy 0.000 description 1
- 108091036078 conserved sequence Proteins 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 229940104302 cytosine Drugs 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 230000007402 cytotoxic response Effects 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 239000005547 deoxyribonucleotide Substances 0.000 description 1
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 210000004207 dermis Anatomy 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 238000006471 dimerization reaction Methods 0.000 description 1
- 231100000371 dose-limiting toxicity Toxicity 0.000 description 1
- 230000002222 downregulating effect Effects 0.000 description 1
- 230000002500 effect on skin Effects 0.000 description 1
- 229960004137 elotuzumab Drugs 0.000 description 1
- 210000002257 embryonic structure Anatomy 0.000 description 1
- 201000002491 encephalomyelitis Diseases 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 210000003979 eosinophil Anatomy 0.000 description 1
- 230000001973 epigenetic effect Effects 0.000 description 1
- 230000004049 epigenetic modification Effects 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- OGPBJKLSAFTDLK-UHFFFAOYSA-N europium atom Chemical compound [Eu] OGPBJKLSAFTDLK-UHFFFAOYSA-N 0.000 description 1
- 230000017188 evasion or tolerance of host immune response Effects 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 210000004475 gamma-delta t lymphocyte Anatomy 0.000 description 1
- 108091008053 gene clusters Proteins 0.000 description 1
- 238000003197 gene knockdown Methods 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 230000004034 genetic regulation Effects 0.000 description 1
- 210000004602 germ cell Anatomy 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 230000009036 growth inhibition Effects 0.000 description 1
- 108010072285 growth inhibitory proteins Proteins 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000002216 heart Anatomy 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 102000056003 human IL15 Human genes 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 230000005746 immune checkpoint blockade Effects 0.000 description 1
- 230000008629 immune suppression Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 239000000411 inducer Substances 0.000 description 1
- 230000008595 infiltration Effects 0.000 description 1
- 238000001764 infiltration Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 230000015788 innate immune response Effects 0.000 description 1
- 102000002467 interleukin receptors Human genes 0.000 description 1
- 108010093036 interleukin receptors Proteins 0.000 description 1
- 239000000543 intermediate Substances 0.000 description 1
- 230000009545 invasion Effects 0.000 description 1
- PGHMRUGBZOYCAA-UHFFFAOYSA-N ionomycin Natural products O1C(CC(O)C(C)C(O)C(C)C=CCC(C)CC(C)C(O)=CC(=O)C(C)CC(C)CC(CCC(O)=O)C)CCC1(C)C1OC(C)(C(C)O)CC1 PGHMRUGBZOYCAA-UHFFFAOYSA-N 0.000 description 1
- PGHMRUGBZOYCAA-ADZNBVRBSA-N ionomycin Chemical compound O1[C@H](C[C@H](O)[C@H](C)[C@H](O)[C@H](C)/C=C/C[C@@H](C)C[C@@H](C)C(/O)=C/C(=O)[C@@H](C)C[C@@H](C)C[C@@H](CCC(O)=O)C)CC[C@@]1(C)[C@@H]1O[C@](C)([C@@H](C)O)CC1 PGHMRUGBZOYCAA-ADZNBVRBSA-N 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 230000001788 irregular Effects 0.000 description 1
- 239000002085 irritant Substances 0.000 description 1
- 231100000021 irritant Toxicity 0.000 description 1
- 244000145841 kine Species 0.000 description 1
- 230000002045 lasting effect Effects 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 230000021633 leukocyte mediated immunity Effects 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000010297 mechanical methods and process Methods 0.000 description 1
- 239000012913 medium supplement Substances 0.000 description 1
- 210000003593 megakaryocyte Anatomy 0.000 description 1
- 230000001394 metastastic effect Effects 0.000 description 1
- 206010061289 metastatic neoplasm Diseases 0.000 description 1
- 108091028466 miR-130b stem-loop Proteins 0.000 description 1
- 108091030496 miR-138 stem-loop Proteins 0.000 description 1
- 108091057645 miR-15 stem-loop Proteins 0.000 description 1
- 108091091751 miR-17 stem-loop Proteins 0.000 description 1
- 108091044046 miR-17-1 stem-loop Proteins 0.000 description 1
- 108091065423 miR-17-3 stem-loop Proteins 0.000 description 1
- 108091088515 miR-197 stem-loop Proteins 0.000 description 1
- 108091074450 miR-200c stem-loop Proteins 0.000 description 1
- 108091039792 miR-20b stem-loop Proteins 0.000 description 1
- 108091055878 miR-20b-1 stem-loop Proteins 0.000 description 1
- 108091027746 miR-20b-2 stem-loop Proteins 0.000 description 1
- 108091062762 miR-21 stem-loop Proteins 0.000 description 1
- 108091041631 miR-21-1 stem-loop Proteins 0.000 description 1
- 108091044442 miR-21-2 stem-loop Proteins 0.000 description 1
- 108091039812 miR-28 stem-loop Proteins 0.000 description 1
- 108091047189 miR-29c stem-loop Proteins 0.000 description 1
- 108091054490 miR-29c-2 stem-loop Proteins 0.000 description 1
- 108091055145 miR-342 stem-loop Proteins 0.000 description 1
- 108091029119 miR-34a stem-loop Proteins 0.000 description 1
- 108091030938 miR-424 stem-loop Proteins 0.000 description 1
- 108091043720 miR-513 stem-loop Proteins 0.000 description 1
- 108091084017 miR-570 stem-loop Proteins 0.000 description 1
- 108091055140 miR-574 stem-loop Proteins 0.000 description 1
- 229960004857 mitomycin Drugs 0.000 description 1
- 238000007799 mixed lymphocyte reaction assay Methods 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 238000004264 monolayer culture Methods 0.000 description 1
- 230000000877 morphologic effect Effects 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 230000006654 negative regulation of apoptotic process Effects 0.000 description 1
- 210000001178 neural stem cell Anatomy 0.000 description 1
- 210000002569 neuron Anatomy 0.000 description 1
- 108091027963 non-coding RNA Proteins 0.000 description 1
- 102000042567 non-coding RNA Human genes 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 239000002853 nucleic acid probe Substances 0.000 description 1
- 210000004940 nucleus Anatomy 0.000 description 1
- 230000000771 oncological effect Effects 0.000 description 1
- 238000005457 optimization Methods 0.000 description 1
- 230000003076 paracrine Effects 0.000 description 1
- 244000045947 parasite Species 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000000149 penetrating effect Effects 0.000 description 1
- 210000005105 peripheral blood lymphocyte Anatomy 0.000 description 1
- 238000002823 phage display Methods 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 230000004526 pharmaceutical effect Effects 0.000 description 1
- 210000002826 placenta Anatomy 0.000 description 1
- 244000000003 plant pathogen Species 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 102000054765 polymorphisms of proteins Human genes 0.000 description 1
- 230000029279 positive regulation of transcription, DNA-dependent Effects 0.000 description 1
- 230000001124 posttranscriptional effect Effects 0.000 description 1
- 230000001323 posttranslational effect Effects 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 210000004986 primary T-cell Anatomy 0.000 description 1
- 210000004990 primary immune cell Anatomy 0.000 description 1
- 230000001686 pro-survival effect Effects 0.000 description 1
- 230000000770 proinflammatory effect Effects 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 230000009696 proliferative response Effects 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 238000001243 protein synthesis Methods 0.000 description 1
- 230000007420 reactivation Effects 0.000 description 1
- 238000007634 remodeling Methods 0.000 description 1
- 230000003252 repetitive effect Effects 0.000 description 1
- 108091008146 restriction endonucleases Proteins 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 230000001177 retroviral effect Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 239000002336 ribonucleotide Substances 0.000 description 1
- 125000002652 ribonucleotide group Chemical group 0.000 description 1
- 108020004418 ribosomal RNA Proteins 0.000 description 1
- 108091092562 ribozyme Proteins 0.000 description 1
- 235000002020 sage Nutrition 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 125000003607 serino group Chemical group [H]N([H])[C@]([H])(C(=O)[*])C(O[H])([H])[H] 0.000 description 1
- 238000009097 single-agent therapy Methods 0.000 description 1
- 210000001626 skin fibroblast Anatomy 0.000 description 1
- 239000004055 small Interfering RNA Substances 0.000 description 1
- 239000000243 solution Substances 0.000 description 1
- 230000000392 somatic effect Effects 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000004114 suspension culture Methods 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 238000010189 synthetic method Methods 0.000 description 1
- 230000009897 systematic effect Effects 0.000 description 1
- 101150080773 tap-1 gene Proteins 0.000 description 1
- 230000002992 thymic effect Effects 0.000 description 1
- 210000001541 thymus gland Anatomy 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 108091006106 transcriptional activators Proteins 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 230000004614 tumor growth Effects 0.000 description 1
- 210000000037 type II NK T lymphocyte Anatomy 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 241001430294 unidentified retrovirus Species 0.000 description 1
- 229940035893 uracil Drugs 0.000 description 1
- 238000010200 validation analysis Methods 0.000 description 1
- 229950000815 veltuzumab Drugs 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/17—Lymphocytes; B-cells; T-cells; Natural killer cells; Interferon-activated or cytokine-activated lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/48—Reproductive organs
- A61K35/54—Ovaries; Ova; Ovules; Embryos; Foetal cells; Germ cells
- A61K35/545—Embryonic stem cells; Pluripotent stem cells; Induced pluripotent stem cells; Uncharacterised stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/461—Cellular immunotherapy characterised by the cell type used
- A61K39/4611—T-cells, e.g. tumor infiltrating lymphocytes [TIL], lymphokine-activated killer cells [LAK] or regulatory T cells [Treg]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/461—Cellular immunotherapy characterised by the cell type used
- A61K39/4613—Natural-killer cells [NK or NK-T]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/463—Cellular immunotherapy characterised by recombinant expression
- A61K39/4631—Chimeric Antigen Receptors [CAR]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/464—Cellular immunotherapy characterised by the antigen targeted or presented
- A61K39/4643—Vertebrate antigens
- A61K39/4644—Cancer antigens
- A61K39/464402—Receptors, cell surface antigens or cell surface determinants
- A61K39/464429—Molecules with a "CD" designation not provided for elsewhere
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/46—Cellular immunotherapy
- A61K39/464—Cellular immunotherapy characterised by the antigen targeted or presented
- A61K39/4643—Vertebrate antigens
- A61K39/4644—Cancer antigens
- A61K39/464466—Adhesion molecules, e.g. NRCAM, EpCAM or cadherins
- A61K39/464468—Mesothelin [MSLN]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/54—Interleukins [IL]
- C07K14/5443—IL-15
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/70535—Fc-receptors, e.g. CD16, CD32, CD64 (CD2314/705F)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/715—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
- C12N5/0638—Cytotoxic T lymphocytes [CTL] or lymphokine activated killer cells [LAK]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0646—Natural killers cells [NK], NKT cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0696—Artificially induced pluripotent stem cells, e.g. iPS
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/31—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterized by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/38—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterised by the dose, timing or administration schedule
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K39/46
- A61K2239/46—Indexing codes associated with cellular immunotherapy of group A61K39/46 characterised by the cancer treated
- A61K2239/48—Blood cells, e.g. leukemia or lymphoma
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/705—Receptors; Cell surface antigens; Cell surface determinants
- C07K14/70503—Immunoglobulin superfamily
- C07K14/7051—T-cell receptor (TcR)-CD3 complex
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/03—Fusion polypeptide containing a localisation/targetting motif containing a transmembrane segment
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/50—Cell markers; Cell surface determinants
- C12N2501/515—CD3, T-cell receptor complex
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/50—Cell markers; Cell surface determinants
- C12N2501/599—Cell markers; Cell surface determinants with CD designations not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/45—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from artificially induced pluripotent stem cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2510/00—Genetically modified cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Immunology (AREA)
- Organic Chemistry (AREA)
- Cell Biology (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Microbiology (AREA)
- Medicinal Chemistry (AREA)
- Biochemistry (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- General Engineering & Computer Science (AREA)
- Hematology (AREA)
- Mycology (AREA)
- Developmental Biology & Embryology (AREA)
- Toxicology (AREA)
- Gastroenterology & Hepatology (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Reproductive Health (AREA)
- Oncology (AREA)
- Virology (AREA)
- Gynecology & Obstetrics (AREA)
- Transplantation (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
게놈 조작된 iPSC의 지시된 분화로부터 획득된 기능적으로 향상된 유도체 효과기 세포를 획득하기 위한 방법 및 조성물이 제공된다. 본 명세서에 제공된 유도체 세포는 개선된 또는 향상된 치료 효과를 전달하는 안정적이고 기능적인 게놈 편집을 갖는다. 또한 기능적으로 향상된 유도체 효과기 세포 단독 또는 병용 요법으로 유도체 효과기 세포와 항체 또는 면역관문 저해제를 포함하는 치료 조성물 및 이의 용도가 제공된다.
Description
관련 출원
본 출원은 미국 가출원 제62/596,659호(출원일: 2017년12월 8일) 및 미국 가출원 제62/657,626호(출원일: 2018년 4월 13일)에 대한 우선권을 주장하며, 이들의 개시내용은 이들의 전문이 참조에 의해 본 명세서에 포함된다.
전자적으로 제출된 서열 목록에 대한 언급
본 출원은 본 출원과 함께 제출된 ASCII 텍스트 형식의 서열 목록의 컴퓨터 판독 가능한 형태(Comupter Readable Form: CRF)를 참조에 의해 원용하며, 이의 파일명은 13601-195-228_SEQ_LISTING.txt이고, 이것은 2018년 11월 30일에 생성되었고, 크기가 36,336바이트이다.
기술분야
본 개시내용은 광범위하게는 오프 더 셀프(off-the-shelf) 면역세포 제품 분야에 관한 것이다. 보다 특별하게는, 본 개시내용은 생체내에서 치료 관련 특성을 전달할 수 있는 다기능성 효과기 세포(multifunctional effector cell)를 개발하기 위한 전략에 관한 것이다. 본 개시내용에 따라서 개발된 세포 생성물은 환자-기원의 세포 요법의 중요한 한계를 해결한다.
입양 세포 요법 분야는 환자-기원 세포 및 공여자-기원 세포의 사용에 초점을 맞추고 있으며, 이는 암 면역요법의 일관된 제조를 달성하고, 이로울 수 있는 모든 환자에게 요법을 전달하는 것을 특히 어렵게 한다. 유리한 환자 결과를 촉진시키기 위해서 입양에 의해서 전달되는 림프구의 효능 및 지속성을 개선할 필요가 있다. 림프구, 예컨대, T 세포 및 자연 살해(natural killer: NK) 세포는 선천 면역 및 적응 면역에서 중요한 역할을 하는 강력한 항-종양 효과기이다. 그러나, 입양 세포 요법을 위해서 이들 면역 세포를 사용하는 것은 여전히 어려운 과제이며, 개선을 위한 충족되지 못한 요구가 있다. 따라서, 입양 면역요법에서 T 세포 및 NK 세포 또는 다른 림프구의 완전한 잠재력을 이용하기 위한 상당한 기회가 남아있다.
반응 속도, 세포 고갈, 수혈된 세포의 손실(생존 및/또는 지속성), 표적 손실 또는 계통 전환을 통한 종양 탈출, 종양 표적화 정확도, 오프-타깃(off-target) 독성, 오프-종양 효과에서부터 고형 종양에 대한 효능, 즉, 종양 미세환경 및 관련 면역 억제, 모집, 수송(trafficking) 및 침윤까지의 범위의 문제를 해결하는 기능적으로 개선된 효과기 세포가 필요하다.
본 발명의 목적은 단일 세포 유래된 iPSC(유도 만능 줄기세포(induced pluripotent stem cell)) 클론주로부터 분화된 유도체 비-만능 세포를 생성시키기 위한 방법 및 조성물을 제공하는 것이며, iPSC주는 게놈 내에 하나 또는 몇몇 유전자 변형을 포함한다. 상기 하나 또는 몇몇 유전자 변형은 DNA 삽입, 결실 및 치환을 포함하고, 이러한 변형은 분화, 확장, 계대 및/또는 이식 후에 후속으로 유래되는 세포에서 유지되고, 기능을 유지한다.
본 출원의 iPSC 유래된 비-만능 세포는 CD34 세포, 조혈 내피 세포, HSC(조혈 줄기 및 전구 세포), 조혈 다능성 전구 세포(hematopoietic multipotent progenitor cell), T 세포 전구 세포, NK 세포 전구 세포, T 세포, NKT 세포, NK 세포 및 B 세포를 포함하지만 이들로 제한되지 않는다. 본 출원의 iPSC 유래 비-만능 세포는 동일한 유전자 변형을 포함하는 iPSC로부터의 분화를 통해서 게놈 내에 하나 또는 몇몇 유전자 변형을 포함한다. 유전자 조작된 유도체 세포를 획득하기 위한 조작된 클론성 iPSC 분화 전략은, 지시된 분화에서의 iPSC의 발달 가능성이 iPSC에서의 조작된 양상에 의해서 악영향을 받지 않고, 또한 조작된 양상이 유도체 세포에서 의도된 바와 같이 기능할 것을 요구한다. 추가로, 이러한 전략은 1차 림프구, 예컨대, 말초 혈액으로부터 획득된 T 세포 또는 NK 세포의 조작에서 현재 장벽을 극복하였는데, 그 이유는 이러한 세포가 조작하기 어렵고, 이러한 세포의 조작은 종종 재현성 및 균일성이 결여되어, 높은 세포사 및 낮은 세포 확장과 함께 불량한 세포 지속성을 나타내는 세포를 생성하기 때문이다. 또한, 이러한 전략은, 달리는 이질적인 1차 세포 공급원을 사용하여 획득되었을 이질 효과기 세포 집단의 생산을 회피한다.
본 발명의 일부 양상은, 각각 재프로그래밍 과정에 이어서, 그와 동시에 또는 그 이전에 게놈 조작의 전략을 반영하는, 하기 (I), (II) 또는 (III)을 포함하는 방법을 사용하여 획득된 게놈-조작된 iPSC를 제공한다:
(I): 임의의 순서의 하기 (i) 및 (ii) 중 하나 또는 둘 다에 의해서 iPSC를 유전자 조작하는 방법: (i) 선택된 부위(들)에서 표적화된 통합을 허용하도록 1종 이상의 작제물을 iPSC에 도입하는 단계; (ii) (a) 선택된 부위 인식이 가능한 1종 이상의 엔도뉴클레아제를 사용하여 선택된 부위(들)에서 하나 이상의 이중 가닥 브레이크(들)를 iPSC 내에 도입하는 단계; 및 (b) 내인성 DNA 수선을 허용하여 선택된 부위(들)에서 표적화된 in/del을 생성하도록 단계 (I)(ii)(a)의 iPSC를 배양함으로써; 부분적으로 또는 완전히 분화된 세포로 분화할 수 있는 게놈-조작된 iPSC를 수득하는 단계.
(II): 하기를 포함하는, 재프로그래밍 비-만능 세포를 유전자 조작하여 게놈-조작된 iPSC를 획득하는 방법: (i) 비-만능 세포를 1종 이상의 재프로그래밍 인자 및 선택적으로 TGFβ 수용체/ALK 저해제, MEK 저해제, GSK3 저해제 및/또는 ROCK 저해제를 포함하는 소분자 조성물과 접촉시켜 비-만능 세포의 재프로그래밍을 개시하는 단계; 및 (ii) 단계 (II)(i)의 재프로그래밍 비-만능 세포에 (a) 및 (b): (a) 선택된 부위에서 표적화된 통합을 허용하기 위한 1종 이상의 작제물(들); (b) 선택된 부위 인식이 가능한 적어도 하나의 엔도뉴클레아제를 사용하여 선택된 부위에서의 하나 이상의 이중 가닥 브레이크(들) 중 하나 또는 둘 다를 임의의 순서로 도입하고, 이어서 단계 (II)(ii)(b)의 세포를 내인성 DNA 수선을 허용하여 선택된 부위(들)에서 표적화된 in/del을 생성하도록 배양하고; 이에 의해서 획득된 게놈-조작된 iPSC는 적어도 하나의 기능성 표적화된 게놈 편집을 포함하고; 상기 게놈-조작된 iPSC는 부분적으로 또는 완전히 분화된 세포로 분화할 수 있는, 단계.
(III): 하기 (i) 및 (ii)를 포함하는, 재프로그래밍을 위해서 비-만능 세포를 유전자 조작하여 게놈-조작된 iPSC를 수득하는 방법: (i) (a) 및 (b): (a) 선택된 부위(들)에서 표적화된 통합을 허용하기 위한 1종 이상의 작제물(들); (b) 선택된 부위 인식이 가능한 적어도 하나의 엔도뉴클레아제를 사용하는 선택된 부위에서의 하나 이상의 이중 가닥 브레이크 중 하나 또는 둘 모두를 임의의 순서로 비-만능 세포에 도입하는 단계이되, 여기서 단계 (III)(i)(b)의 세포를 내인성 DNA 수선을 허용하여 선택된 부위에서 표적화된 in/del을 생성하도록 배양하는 단계; 및 (ii) 단계 (III)(i)의 세포를 1종 이상의 재프로그래밍 인자, 및 선택적으로 TGFβ 수용체/ALK 저해제, MEK 저해제, GSK3 저해제 및/또는 ROCK 저해제를 포함하는 소분자 조성물과 접촉시켜, 선택된 부위에서 표적화 편집을 포함하는 게놈-조작된 iPSC를 수득하고; 이에 의해서 적어도 하나의 기능성 표적화된 게놈 편집을 포함하는 게놈-조작된 iPSC를 수득하는 단계이되, 상기 게놈-조작된 iPSC는 부분적으로 분화된 세포 또는 완전히-분화된 세포로 분화될 수 있는, 단계.
상기 방법의 일 실시형태에서, 하나 이상의 선택된 부위에서의 적어도 하나의 표적화된 게놈 편집은 안전 스위치 단백질(safety switch protein), 표적화 양상, 수용체, 신호전달 분자, 전사 인자, 약제학적으로 활성인 단백질 및 펩타이드, 약물 표적 후보, 또는 게놈-조작된 iPSC 또는 이의 유도체 세포의 생착, 수송, 귀소(homing), 생존도, 자기-재생, 지속성 및/또는 생존을 촉진시키는 단백질을 암호화하는 1종 이상의 외인성 폴리뉴클레오타이드의 삽입을 포함한다. 일부 실시형태에서, 삽입을 위한 외인성 폴리뉴클레오타이드는 (1) CMV, EF1α, PGK, CAG, UBC, 또는 다른 구성적, 유도성, 일시적-, 조직- 또는 세포 유형-특이적 프로모터를 포함하는 1종 이상의 외인성 프로모터; 또는 (2) AAVS1, CCR5, ROSA26, 콜라겐, HTRP, H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1 또는 게놈 안전 하버(genome safe harbor)의 기준을 충족시키는 다른 유전자좌를 포함하는 선택된 부위 내에 포함된 1종 이상의 내인성 프로모터에 작동 가능하게 연결된다. 일부 실시형태에서, 상기 방법을 사용하여 생성된 게놈-조작된 iPSC는 카스파제, 티미딘 카이나제, 사이토신 데아미나제, 변형된 EGFR 또는 B-세포 CD20을 포함하는 단백질을 암호화하는 1종 이상의 상이한 외인성 폴리뉴클레오타이드를 포함하고, 여기서 게놈-조작된 iPSC가 2종 이상의 자살 유전자를 포함하는 경우, 자살 유전자는 AAVS1, CCR5, ROSA26, 콜라겐, HTRP, H11, H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1을 포함하는 상이한 안전 하버 유전자좌 내에 통합된다. 일 실시형태에서, 외인성 폴리뉴클레오타이드는 IL2, IL4, IL6, IL7, IL9, IL10, IL11, IL12, IL15, IL18, IL21 및/또는 이들의 각각의 수용체의 부분 또는 전체 펩타이드를 암호화한다. 일부 실시형태에서, 외인성 폴리뉴클레오타이드에 의해서 암호화된 IL2, IL4, IL6, IL7, IL9, IL10, IL11, IL12, IL15, IL18, IL21 및/또는 이들의 각각의 수용체의 부분 또는 전체 펩타이드는 융합 단백질의 형태이다.
일부 다른 실시형태에서, 본 명세서에 제공된 방법을 사용하여 생성된 게놈-조작된 iPSC는 표적화 양상, 수용체, 신호전달 분자, 전사 인자, 약물 표적 후보, 면역 반응 조절 및 조정, 또는 iPSC 또는 이의 유도체 세포의 생착, 수송, 귀소, 생존도, 자기-재생, 지속성 및/또는 생존을 억제하는 단백질과 연관된 1종 이상의 내인성 유전자에서 in/del을 포함한다. 일부 실시형태에서, 파괴를 위한 내인성 유전자는 B2M, TAP1, TAP2, 타파신(Tapasin), NLRC5, PD1, LAG3, TIM3, RFXANK, CIITA, RFX5, RFXAP 및 염색체 6p21 영역 내의 임의의 유전자 중 적어도 하나를 포함한다.
추가의 일부 다른 실시형태에서, 본 명세서에 제공된 방법을 사용하여 생성된 게놈-조작된 iPSC는 AAVS1 유전자좌에서 카스파제 암호화 외인성 폴리뉴클레오타이드, 및 H11 유전자좌에서 티미딘 카이나제 암호화 외인성 폴리뉴클레오타이드를 포함한다.
더 일부의 다른 실시형태에서, 접근법 (I), (II) 및/또는 (III)은 게놈-조작된 iPSC를 MEK 저해제, GSK3 저해제 및 ROCK 저해제를 포함하는 소분자 조성물과 접촉시켜, 게놈-조작된 iPSC의 만능성을 유지시키는 단계를 추가로 포함한다. 일 실시형태에서, 적어도 하나의 표적화된 게놈 편집을 포함하는 수득된 게놈 조작된 iPSC는 기능성이고, 분화 효력이 있고, 동일한 기능성의 게놈 편집을 포함하는 비-만능 세포로 분화할 수 있다.
본 발명은 또한 하기를 제공한다.
본 출원의 일 양상은 세포 또는 이의 집단을 제공하며, 여기서 세포는 유도 만능 세포(iPSC), 클론성 iPSC 또는 iPS 세포주 세포 또는 상기 iPSC 중 임의의 것의 분화로부터 획득된 유도체 세포이고; 여기서 상기 세포 중 임의의 것은 고 친화도 비-절단성 CD16(high affinity non-cleavable CD16: hnCD16) 또는 이의 변이체; 및 (2) 키메라 항원 수용체(CAR) 및 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드를 포함한다. iPSC 분화로부터 획득된 유도체 세포의 일부 실시형태에서, 유도체 세포는 CD34 세포, 조혈 내피 세포, HSC(조혈 줄기 및 전구 세포), 조혈 다능성 전구 세포, T 세포 전구 세포, NK 세포 전구 세포, T 세포, NKT 세포, NK 세포 및 B 세포를 포함하지만 이들로 제한되지 않는 조혈 세포이고; 조혈 세포(즉, 유도체 CD34 세포, 유도체 조혈 내피 세포 유도체 조혈 줄기 및 전구 세포, 유도체 조혈 다능성 전구 세포, 유도체 T 세포 전구 세포, 유도체 NK 세포 전구 세포, 유도체 T 세포, 유도체 NKT 세포, 유도체 NK 세포 또는 유도체 B 세포)는 말초 혈액, 제대혈 또는 임의의 다른 공여자 조직으로부터 획득된 네이티브 상대 세포에 비해서 더 긴 텔로미어(telomere)를 포함한다.
상기 iPSC, 및 hnCD16 또는 이의 변이체, CAR 및 선택적인 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드를 포함하는 유도체 세포를 포함하는 이의 유도체 세포의 일부 실시형태에서, 세포는 하기 게놈 편집 중 하나 이상을 추가로 포함한다: (i) B2M 널 또는 저; (ii) CIITA 널 또는 저; (iii) HLA-G 또는 비-절단성 HLA-G의 도입된 발현; (iv) 표 1에 열거된 유전자형 중 적어도 하나; (v) 염색체 6p21 영역 내의 TAP1, TAP2, 타파신, NLRC5, PD1, LAG3, TIM3, RFXANK, CIITA, RFX5, RFXAP 및 임의의 유전자 중 적어도 하나의 결실 또는 감소된 발현; 및 (vi) HLA-E, 41BBL, CD3, CD4, CD8, CD16, CD47, CD113, CD131, CD137, CD80, PDL1, A2AR, CAR, TCR, Fc 수용체, 관여자 및 이중- 또는 다중-특이적 또는 보편적 관여자(universal engager)와의 커플링을 위한 표면 촉발 수용체 중 적어도 하나의 도입된 또는 증가된 발현.
상기 및 본 출원 전체에 기재된 바와 같은 적어도 hnCD16 또는 이의 변이체 및 CAR 및 선택적인 추가 게놈 편집을 포함하는 상기 iPSC 및 이의 유도체 세포의 일부 실시형태에서, 세포는 (i) 하나의 안전 하버 유전자좌에 통합된 하나 이상의 외인성 폴리뉴클레오타이드; 또는 (ii) 상이한 안전 하버 유전자좌에 통합된 2개 초과의 외인성 폴리뉴클레오타이드를 포함할 수 있다. 일부 실시형태에서, 안전 하버 유전자좌는 AAVS1, CCR5, ROSA26, 콜라겐, HTRP, H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1 중 적어도 하나를 포함한다. 특정 일 실시형태에서, 안전 하버 유전자좌 TCR은 TCR 알파의 불변 영역이다.
세포 또는 이의 집단의 일부 실시형태에서, 고 친화도 비-절단성 CD16(hnCD16), CAR(세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드를 갖거나 갖지 않음) 및 선택적으로 상기 추가 게놈 편집 중 하나 이상을 포함하는 세포는 유도체 NK 또는 유도체 T 세포이고, 유도체 NK 또는 유도체 T 세포는, 말초 혈액, 제대혈 또는 임의의 다른 공여자 조직으로부터 획득된 네이티브 상대 NK 또는 T 세포와 비교할 때, (i) 개선된 지속성 및/또는 생존; (ii) 네이티브 면역 세포에 대한 증가된 내성; (iii) 증가된 세포독성; (iv) 개선된 종양 침투; (v) 향상된 또는 획득된 ADCC; (vi) 방관자 면역 세포(bystander immune cell)를 종양 부위로 이동시키고/시키거나 활성화 또는 모집하는 향상된 능력; (vii) 종양 면역억제를 감소시키는 향상된 능력; 및 (viii) 종양 항원 탈출을 구제하는 개선된 능력을 포함하지만 이들로 제한되지 않는 특징 중 적어도 하나를 갖는다.
세포 또는 이의 집단의 일 실시형태에서, hnCD16 또는 이의 변이체를 포함하는 세포는 (a) CD16의 엑토도메인 도메인 내의 F176V 및 S197P; (b) CD64로부터 기원된 전체 또는 부분 엑토도메인; (c) 비-네이티브(또는 비-CD16) 막관통 도메인; (d) 비-네이티브(또는 비-CD16) 세포내 도메인; (e) 비-네이티브(또는 비-CD16) 신호전달 도메인; (f) 비-네이티브 자극성 도메인; 및 (g) CD16로부터 기원되지 않고, 동일하거나 상이한 폴리펩타이드로부터 기원된 막관통 도메인, 신호전달 도메인 및 자극성 도메인 중 적어도 임의의 하나를 포함한다. 일부 실시형태에서, 비-네이티브 막관통 도메인은 CD3D, CD3E, CD3G, CD3ζ, CD4, CD8, CD8a, CD8b, CD27, CD28, CD40, CD84, CD166, 4-1BB, OX40, ICOS, ICAM-1, CTLA-4, PD-1, LAG-3, 2B4, BTLA, CD16, IL7, IL12, IL15, KIR2DL4, KIR2DS1, NKp30, NKp44, NKp46, NKG2C, NKG2D, 또는 T 세포 수용체(TCR) 폴리펩타이드로부터 유래된다. 일부 실시형태에서, 비-네이티브 자극성 도메인은 CD27, CD28, 4-1BB, OX40, ICOS, PD-1, LAG-3, 2B4, BTLA, DAP10, DAP12, CTLA-4 또는 NKG2D 폴리펩타이드로부터 유래된다. 일부 다른 실시형태에서, 비-네이티브 신호전달 도메인은 CD3ζ, 2B4, DAP10, DAP12, DNAM1, CD137 (41BB), IL21, IL7, IL12, IL15, NKp30, NKp44, NKp46, NKG2C 또는 NKG2D 폴리펩타이드로부터 유래된다. hnCD16 변이체의 일부 특정 실시형태에서, 비-네이티브 막관통 도메인은 NKG2D로부터 유래되고, 비-네이티브 자극성 도메인은 2B4로부터 유래되고, 비-네이티브 신호전달 도메인은 CD3ζ로부터 유래된다.
세포 또는 이의 집단의 일 실시형태에서, 세포는 hnCD16 또는 이의 변이체 및 CAR을 포함하고, 여기서 CAR은 하기 중 임의의 하나 이상일 수 있다: (i) T 세포 특이적 또는 NK 세포 특이적임; (ii) 이중특이적 항원 결합 CAR임; (iii) 전환 가능한 CAR임; (iv) 이량체화된 CAR임; (v) 스플리트 CAR임; (vi) 멀티-쇄 CAR임; (vii) 유도성 CAR임; (viii) 또 다른 CAR과 공동 발현됨; (ix) 선택적으로 개별 작제물 또는 바이-시스트론성(bi-cistronic) 작제물로 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드와 공동 발현됨; (xi) 면역관문 저해제, 선택적으로 개별 작제물 또는 바이-시스트론성 작제물로 면역관문 저해제와 공동 발현됨; (xii) CD19 또는 BCMA에 특이적임; 및/또는 (xiii) ADGRE2, 탄산 탈수효소 IX(CAlX), CCRI, CCR4, 암배아 항원(CEA), CD3, CD5, CD7, CD8, CD10, CD20, CD22, CD30, CD33, CD34, CD38, CD41, CD44, CD44V6, CD49f, CD56, CD70, CD74, CD99, CD123, CD133, CD138, CDS, CLEC12A, 사이토메갈로바이러스(CMV) 감염된 세포의 항원, 상피 당단백질2(EGP 2), 상피 당단백질-40(EGP-40), 상피 세포 접착 분자(EpCAM), EGFRvIII, 수용체 타이로신-단백질 카이나제 erb-B2,3,4, EGFIR, EGFR-VIII, ERBB 엽산염-결합 단백질(FBP), 태아 아세틸콜린 수용체(AChR), 엽산염 수용체-a, 강글리오사이드 G2(GD2), 강글리오사이드 G3(GD3), 인간 표피 성장 인자 수용체 2(HER-2), 인간 텔로머라제 역전사효소(human telomerase reverse transcriptase: hTERT), ICAM-1, 인테그린 B7, 인터류킨-13 수용체 소단위 알파-2(IL-13Rα2), κ-경쇄, 카이나제 삽입 도메인 수용체(KDR), Lewis A(CA19.9), Lewis Y(LeY), L1 세포 접착 분자(L1-CAM), LILRB2, 흑색종 항원 패밀리 A 1(MAGE-A1), MICA/B, 뮤신 1(Muc-1), 뮤신 16(Muc-16), 메소텔린(MSLN), NKCSI, NKG2D 리간드, c-Met, 암-고환 항원 NY-ESO-1, 종양태아성 항원(h5T4), PRAME, 전립선 줄기세포 항원(PSCA), PRAME 전립선-특이적 막 항원(PSMA), 종양-연관 당단백질 72(TAG-72), TIM-3, TRBCI, TRBC2, 혈관 내피 성장 인자 R2(VEGF-R2), 빌름스 종양 단백질(WT-1) 및 병원체 항원 중 임의의 하나에 특이적임.
면역관문 저해제가 CAR과 공동 발현되는 일부 실시형태에서, 면역관문 저해제는 PD-1, PDL-1, TIM-3, TIGIT, LAG-3, CTLA-4, 2B4, 4-1BB, 4-1BBL, A2aR, BATE, BTLA, CD39, CD47, CD73, CD94, CD96, CD160, CD200, CD200R, CD274, CEACAM1, CSF-1R, Foxpl, GARP, HVEM, IDO, EDO, TDO, LAIR-1, MICA/B, NR4A2, MAFB, OCT-2, Rara(레티노산 수용체 알파), TLR3, VISTA, NKG2A/HLA-E 또는 저해성 KIR을 포함하는 1종 이상의 면역관문에 대한 길항제이다. CAR과 공동 발현되는 면역관문 저해제는 상기 면역관문 분자 중 임의의 것에 특이적인 항체 또는 인간화된 또는 Fc 변형된 변이체 또는 이의 단편 및 기능성 등가물 및 바이오시밀러(biosimilar)일 수 있다. 일부 실시형태에서, (i) 내지 (ix) 중 임의의 하나의 CAR은 TRAC 유전자좌에서 삽입될 수 있다. 일부 실시형태에서, TRAC 유전자좌에서 삽입되는 (i) 내지 (ix) 중 임의의 하나의 CAR은 TCR의 내인성 프로모터에 의해서 지시될 수 있다. 일부 실시형태에서, TRAC 유전자좌에서 (i) 내지 (ix) 중 임의의 하나의 CAR의 삽입은 TCR 넉아웃으로 이어진다.
세포 또는 이의 집단의 일 실시형태에서, hnCD16 또는 이의 변이체 및 CAR을 포함하는 세포는 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드를 추가로 포함하고, 여기서 외인성 사이토카인 또는 이의 수용체는 IL2, IL4, IL6, IL7, IL9, IL10, IL11, IL12, IL15, IL18, IL21 및 이의 각각의 수용체 중 적어도 하나를 포함할 수 있거나; 또는 (i) 자가 절단 펩타이드를 사용한 IL15 및 IL15Rα의 공동-발현; (ii) IL15와 IL15Rα의 융합 단백질; (iii) 절두된 IL15Rα의 세포내 도메인을 갖는 IL15/IL15Rα 융합 단백질; (iv) IL15과 IL15Rα의 막 결합된 스시(Sushi) 도메인의 융합 단백질; (v) IL15과 IL15Rβ의 융합 단백질; (vi) IL15와 공통 수용체 γC의 융합 단백질(여기서 공통 수용체 γC는 네이티브이거나 또는 변형됨); 및 (vii) IL15Rβ의 동종이량체 중 적어도 하나를 포함할 수 있고; 여기서 (i) 내지 (vii) 중 임의의 하나는 별개의 작제물 또는 바이-시스트론성 작제물로 CAR과 공동 발현될 수 있다. 일부 실시형태에서, 세포 표면 외인성 사이토카인 또는 수용체의 부분 또는 전체 펩타이드는 본 명세서에 제공된 세포에서 일시적으로 발현된다.
세포 또는 이의 집단의 일 실시형태에서, hnCD16 또는 이의 변이체 및 CAR을 포함하는 세포는 유도체 NK 또는 유도체 T 세포이고, 여기서 유도체 NK 세포는 T 세포를 종양 부위로 모집 및/또는 이동시킬 수 있고, 여기서 유도체 NK 또는 유도체 T 세포는 1종 이상의 면역관문 저해제의 존재 하에서 종양 면역억제를 감소시킬 수 있다. 일부 실시형태에서, 면역관문 저해제는 PD-1, PDL-1, TIM-3, TIGIT, LAG-3, CTLA-4, 2B4, 4-1BB, 4-1BBL, A2aR, BATE, BTLA, CD39, CD47, CD73, CD94, CD96, CD160, CD200, CD200R, CD274, CEACAM1, CSF-1R, Foxpl, GARP, HVEM, IDO, EDO, TDO, LAIR-1, MICA/B, NR4A2, MAFB, OCT-2, Rara(레티노산 수용체 알파), TLR3, VISTA, NKG2A/HLA-E 또는 저해성 KIR을 포함하는 1종 이상의 면역관문 분자에 대한 길항제이다. 일부 다른 실시형태에서, 면역관문 저해제는 (a) 아테졸리주맙(atezolizumab), 아벨루맙(avelumab), 더발루맙(durvalumab), 이필리무맙(ipilimumab), IPH4102, IPH43, IPH33, 리릴루맙(lirimumab), 모날리주맙(monalizumab), 니볼루맙(nivolumab), 펨브롤리주맙(pembrolizumab) 및 이들의 유도체 또는 기능성 등가물 중 하나 이상; 또는 (b) 아테졸리주맙, 니볼루맙 및 펨브롤리주맙 중 적어도 1종을 포함한다.
본 출원의 또 다른 양상은 상기 및 본 출원 전체에 기재된 바와 같은 세포 또는 이의 집단 중 임의의 것을 포함하는 조성물을 제공한다. 일부 실시형태에서, iPSC 또는 iPSC 유래된 세포(유도체 세포)는 본 출원의 표 1에 열거된 유전자형 중 임의의 것을 포함할 수 있다. 일부 실시형태에서, iPSC 또는 이로부터의 유도체 세포는 hnCD16 및 CAR을 포함한다. 일부 실시형태에서, iPSC 또는 이로부터의 유도체 세포는 상기 및 본 출원 전체에 제공된 바와 같은 hnCD16, CAR 및 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드를 포함한다. hnCD16 및 CAR을 포함하는 세포의 일부 실시형태에서, CAR은 CD19에 특이적이다. hnCD16 및 CAR을 포함하는 세포의 일부 다른 실시형태에서, CAR은 CD269(BCMA)에 특이적이다. 추가의 일부 다른 실시형태에서, CAR은 ADGRE2, 탄산 탈수효소 IX(CAlX), CCRI, CCR4, 암배아 항원(CEA), CD3, CD5, CD7, CD8, CD10, CD20, CD22, CD30, CD33, CD34, CD38, CD41, CD44, CD44V6, CD49f, CD56, CD70, CD74, CD99, CD123, CD133, CD138, CDS, CLEC12A, 사이토메갈로바이러스(CMV) 감염된 세포의 항원(예를 들어, 세포 표면 항원), 상피 당단백질2(EGP 2), 상피 당단백질-40(EGP-40), 상피 세포 접착 분자(EpCAM), EGFRvIII, 수용체 타이로신-단백질 카이나제 erb-B2,3,4, EGFIR, EGFR-VIII, ERBB 엽산염-결합 단백질(FBP), 태아 아세틸콜린 수용체(AChR), 엽산염 수용체-a, 강글리오사이드 G2(GD2), 강글리오사이드 G3(GD3), 인간 표피 성장 인자 수용체 2(HER-2), 인간 텔로머라제 역전사효소(hTERT), ICAM-1, 인테그린 B7, 인터류킨-13 수용체 소단위 알파-2(IL-13Rα2), κ-경쇄, 카이나제 삽입 도메인 수용체(KDR), Lewis A(CA19.9), Lewis Y(LeY), L1 세포 접착 분자(L1-CAM), LILRB2, 흑색종 항원 패밀리 A 1(MAGE-A1), MICA/B, 뮤신 1(Muc-1), 뮤신 16(Muc-16), 메소텔린(MSLN), NKCSI, NKG2D 리간드, c-Met, 암-고환 항원 NY-ESO-1, 종양태아성 항원(h5T4), PRAME, 전립선 줄기세포 항원(PSCA), PRAME 전립선-특이적 막 항원(PSMA), 종양-연관 당단백질 72(TAG-72), TIM-3, TRBCI, TRBC2, 혈관 내피 성장 인자 R2(VEGF-R2), 빌름스 종양 단백질(WT-1) 및 당업계에 공지된 다양한 병원체 항원 중 임의의 하나에 특이적이다.
따라서, 본 출원의 추가 양상은 본 명세서에 제공된 바와 같은 유도체 세포 중 임의의 것에 더하여 1종 이상의 치료제를 포함하는 치료 용도를 위한 조성물을 제공한다. 치료 용도를 위한 조성물의 일부 실시형태에서, 치료제는 펩타이드, 사이토카인, 면역관문 저해제, 미토겐, 성장 인자, 작은 RNA, dsRNA(이중 가닥 RNA), 단핵 혈액 세포(mononuclear blood cell), 피더 세포(feeder cell), 피더 세포 성분 또는 이의 대체 인자, 관심대상의 하나 이상의 폴리핵산을 포함하는 벡터, 항체, 화학치료제 또는 방사성 모이어티 또는 면역조절 약물(immunomodulatory drug: IMiD)을 포함한다. 치료 용도를 위한 조성물의 일부 실시형태에서, 제공된 세포와 함께 사용되는 면역관문 저해제는 PD-1, PDL-1, TIM-3, TIGIT, LAG-3, CTLA-4, 2B4, 4-1BB, 4-1BBL, A2aR, BATE, BTLA, CD39, CD47, CD73, CD94, CD96, CD160, CD200, CD200R, CD274, CEACAM1, CSF-1R, Foxpl, GARP, HVEM, IDO, EDO, TDO, LAIR-1, MICA/B, NR4A2, MAFB, OCT-2, Rara(레티노산 수용체 알파), TLR3, VISTA, NKG2A/HLA-E 또는 저해성 KIR을 포함하는 1종 이상의 길항제 면역관문 분자를 포함한다. 치료 용도를 위한 조성물의 일부 실시형태에서, 제공된 세포와 함께 사용되는 면역관문 저해제는 아테졸리주맙, 아벨루맙, 더발루맙, 이필리무맙, IPH4102, IPH43, IPH33, 리릴루맙, 모날리주맙, 니볼루맙, 펨브롤리주맙 및 이들의 유도체 또는 기능성 등가물 중 1종 이상을 포함한다. 치료 용도를 위한 조성물의 일부 다른 실시형태에서, 제공된 세포와 함께 사용되는 면역관문 저해제는 아테졸리주맙, 니볼루맙 및 브롤리주맙 중 적어도 1종을 포함한다.
치료 용도를 위한 조성물의 일부 실시형태에서, 제공된 세포와 함께 사용되는 항체는 항-CD20, 항-HER2, 항-CD52, 항-EGFR, 항-CD123, 항-GD2, 항-PDL1, 및/또는 항-CD38 항체 중 임의의 하나를 포함한다. 치료 용도를 위한 조성물의 일부 실시형태에서, 제공된 세포와 함께 사용되는 항체는 레툭시맙, 벨투주맙, 오파투무맙, 유블리툭시맙, 오카라투주맙, 오비누투주맙, 트라스투주맙, 퍼투주맙, 알렘투주맙, 서툭시맙, 디누툭시맙, 아벨루맙, 다라투무맙, 이사툭시맙, MOR202, 7G3, CSL362, 엘로투주맙 및 이들의 인간화된 또는 Fc 변형된 변이체 또는 단편 및 이들의 기능성 등가물 및 바이오시밀러 중 1종 이상을 포함한다. 치료 용도를 위한 조성물의 더 일부의 다른 실시형태에서, 제공된 세포와 함께 사용되는 항체는 다라투무맙을 포함한다.
본 출원은 또한 입양 세포 요법에 적합한 대상체에게 조성물을 도입하는 본 명세서에 기재된 바와 같은 세포 또는 치료 조성물의 치료 용도를 제공한다. 일부 실시형태에서, 입양 세포 요법을 필요로 하거나 이에 적합한 대상체는 자가면역 장애; 혈액 악성종양; 고형 종양; 암 또는 바이러스 감염을 갖는다.
본 출원의 추가 양상은 본 명세서에 기재된 바와 같은 유도체 세포의 제조 방법을 제공하며, 이 방법은 hnCD16 및 CAR, 선택적으로 (i) B2M 널 또는 저; (ii) CIITA 널 또는 저; (iii) HLA-G 또는 비-절단성 HLA-G의 도입된 발현; (iv) 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드; (v) 표 1에 열거된 유전자형 중 적어도 하나; (vi) 염색체 6p21 영역 내의 TAP1, TAP2, 타파신, NLRC5, PD1, LAG3, TIM3, RFXANK, CIITA, RFX5, RFXAP 및 임의의 유전자 중 적어도 하나의 결실 또는 감소된 발현; 및 (vii) HLA-E, 41BBL, CD3, CD4, CD8, CD16, CD47, CD113, CD131, CD137, CD80, PDL1, A2AR, CAR, TCR, Fc 수용체, 관여자 및 이중- 또는 다중-특이적 또는 보편적 관여자와의 커플링을 위한 표면 촉발 수용체 중 하나 이상에서의 도입된 또는 증가된 발현 중 하나 이상을 포함하는 iPSC를 분화시키는 단계를 포함한다.
제조 방법의 일부 실시형태에서, 방법은 hnCD16 또는 이의 변이체, 또는 CAR을 삽입시키도록, 선택적으로는 B2M 및 CIITA를 넉 아웃시키도록, 또는 HLA-G 또는 비-절단성 HLA-G의 발현을 도입하도록 그리고/또는 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드를 도입하도록 클론성 iPSC를 게놈 조작하는 단계를 추가로 포함한다. 일부 실시형태에서, CAR 및 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드 둘 다를 포함하는 세포의 경우, 두 양상이 별개의 작제물로 또는 바이-시스트론성 작제물로 공동 발현된다. 제조 방법의 일부 실시형태에서, iPSC의 게놈 조작은 표적화 편집을 포함한다. 일부 실시형태에서, 표적화 편집은 결실, 삽입 또는 in/del을 포함한다. 일부 실시형태에서, 표적화 편집은 CRISPR, ZFN, TALEN, 귀소 뉴클레아제, 상동 재조합 또는 이들 방법의 임의의 다른 기능성 변경에 의해서 수행된다.
본 출원은 클론성 iPSC의 CRISPR 매개된 편집을 추가로 제공함으로써, hnCD16 또는 이의 변이체 및 CAR 또는 표 1에 열거된 유전자형 중 적어도 하나를 포함하는 편집된 클론성 iPSC를 생성시킨다. 표 1에 열거된 모든 유전자형은 hnCD16 및 CAR 삽입을 포함한다.
본 출원의 추가 양상은 종양 항원 탈출 및/또는 종양 재발을 예방 또는 감소시키는 방법을 제공하며, 이 방법은 대상체에게 치료 하에서 hnCD16 또는 이의 변이체, CAR, 및 선택적으로 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드를 포함하는 효과기 세포; 및 항원 특이적 단클론성 항체, 또는 이의 인간화된 또는 Fc 변형된 변이체 또는 단편, 기능성 등가물 및 바이오시밀러 중 임의의 것을 투여하는 단계를 포함하고, 여기서 항체에 의해서 표적화되는 항원은 CAR에 의해서 인식되는 종양 항원과 상이하다. 일부 실시형태에서, 효과기 세포는 표 1에 열거된 유전자형 중 적어도 하나를 포함한다.
본 명세서에 제공된 바와 같은 조성물 및 방법의 다양한 목적 및 이점은 첨부된 도면과 함께 제공된 하기 설명으로부터 명백할 것이며, 여기서 예시 및 예의 방식에 의해서 본 발명의 특정 실시형태가 언급되어 있다.
도 1은 iPSC 유래된 세포에서 세포 표면 발현된 사이토카인 또는 이의 수용체에 대한 몇몇 작제물 설계의 그래프 표현. IL15는 다른 목적하는 사이토카인과 대체될 수 있는 예시적인 예로서 사용된다.
도 2는 hnCD16 발현, B2M 넉아웃(HLA-A2 발현의 손실), HLA-G 발현 및 IL-15/IL-15ra(LNGFR) 작제물 발현의 단계적 조작을 나타내는 성숙 iPSC-유래된 NK 세포의 유세포 분석법의 그래프 표현.
도 3은 유세포 분석법에 의해서 결정된 텔로미어 길이의 그래프 표현(iPSC로부터의 성숙 유도체 NK 세포는 성인 말초 혈액 NK 세포에 비해서 더 긴 텔로미어를 유지함).
도 4는 B2M 넉아웃이 동종이계 CD8+ T 세포에 의해서 조작된 유도체 NK 세포의 시험관내 인식을 제거한 것을 나타낸 도면.
도 5는 HLA-G의 발현이 NK 세포에 의한 사멸로부터 B2M-/- iPSC를 구제한다는 것을 나타낸 도면. A: HLA-I의 손실은 동종이계 PBMC와 인큐베이션되는 경우 조작된 iPSC에 대한 증가된 세포독성을 야기한다. B: B2M-/- iPSC 상에서의 HLA-G의 발현에 의해서 조작된 iPSC의 동종이계 사멸이 부분적으로 역전되었다. Incucyte Zoom(상표명) 영상화 시스템을 사용하여 시간에 따라서 iPSC의 손실을 측정하였고, 효과기 세포가 없는 웰에서 iPSC의 수에 데이터를 정규화하고, 각각의 조건에 대해서 시간 = 0 내지 100%로 설정하였다.
도 6은 hnCD16/B2M-/-HLA-G iNK의 단일 용량이 난소암의 생체내 이종이식편 모델에서 종양 퇴행을 유도하였음을 나타낸 도면. A: 주사 후 32일의 기간에 걸친 각각의 마우스의 IVIS 영상. B: IVIS 영상화에 의한 종양 진행의 시간 경과.
도 7은 IL15/IL15Ra 작제물이 시험관내에서 가용성의 외인성 IL15의 첨가와 무관하게 iNK 세포 분화 및 생존을 촉진시킨다는 것을 나타낸 도면. A: 각각의 제시된 유전자형의 iNK 세포는 가용성 IL15의 첨가에 의해서 또는 첨가 없이 분화되었다. B: iNK 세포를 광범위하게 세척하고, 가용성 IL15-비의존적 세포 성장을 관찰하기 위해서 10ng/㎖ 내지 0ng/㎖ 범위의 농도의 가용성 IL15의 농도로 7일 동안 다시 배양액에 넣었다.
도 8은 IL15/IL15Ra 작제물의 발현이 가용성 IL15의 부재 하에서 생체내에서 iNK 지속성을 향상시킴을 나타낸 도면. iNK 세포를 A: 면역손상된 NOG 마우스; B: 인간 IL15에 대해해서 트랜스제닉인 NOG 마우스에게 입양에 의해서 전달하였다.
도 9는 표면 마커의 유세포 분석을 사용한 CAR-발현 iPSC 유래된 NK 세포의 표현형분석의 그래프 표현.
도 10은 다양한 효과기 대 표적(E:T)비에서 유로퓸-로딩된 메조-고 표적 세포와 공동 배양된 CAR4-발현 유도체 NK 세포의 항-종양 활성의 그래프 표현. A: K562 메조-고 표적 세포; B: A1847 메조-고 표적 세포.
도 11은 루시퍼라제-발현 A1847 메조 고 세포가 접종되고, A1847 접종 4일 후 상이한 유전자형의 1.5E7 NK 세포가 1회 투여된 이종이식편 NSG 마우스 모델에서 주 단위 생물발광 영상화에 의해서 결정된 종양 부하를 나타낸 도면.
도 12는 A: 생물발광을 사용하여 결정된 정량된 종양 부하; B: 루시퍼라제-발현 A1847 메조 고 세포가 접종되고, A1847 접종 4일 후 상이한 유전자형의 1.5E7 NK 세포가 1회 투여된 NSG 마우스군의 생존 백분율을 나타낸 카플란-마이어 곡선. 모든 군에 대해서 n=5.
도 13은 유세포 분석법에 의해서 평가된, (A) 말초 혈액, (B) 비장 및 (C) 복막으로부터 수집된 세포로부터의 유도체 CAR-NK 세포의 백분율 측정에 의한 생체내에서 CAR-iNK의 향상된 지속성을 나타낸 도면. 각각의 점은 하나의 수용자 마우스를 나타낸다. 중위값 ± SEM을 나타내고, P<0.05이다.
도 14는 hnCD16-iPSC의 클론성 집단으로부터의 CD16 발현 유도체 T 세포의 생성의 그래프 표현. A: hnCD16-iPSC 유동 분석; B: hnCD16-iT 유동 분석.
도 15는 hnCD16-iT 세포에 의한 ADCC 매개된 표적 세포 제거를 도시한 도면.
도 16은 CAR 및 hnCD16 둘 다의 발현이 효과기 세포, 예컨대, 유도체 T 세포 및 유도체 NK 세포에 대한 CAR-hnCD16-iPSC의 조혈 분화를 교란시키지 않는다는 것을 나타낸 도면. A: CAR-hnCD16 iPSC; B: CAR-hnCD16 iCD34 세포; C: CAR-hnCD16 유도체 T 세포의 유세포 분석법 분석.
도 17은 활성화된 hnCD16-iNK 세포가 CD69 양성 T 세포의 백분율에 의해서 측정된 T 세포 활성화를 향상시키는 가용성 인자를 생산한다는 것을 나타낸 도면.
도 18은 활성화된 hnCD16-iNK 세포가 트랜스-웰 검정에서 상부에서 하부 챔버로의 T 세포 이동 형태의 유세포 분석법에 의해서 정량된, T 세포 이동을 향상시키는 가용성 인자를 생산한다는 것을 나타낸 도면.
도 19는 유도체 NK 세포가 유세포 분석법에 의해서 정량된 바와 같이, 생체내에서 주사된 마우스 모델의 A: 혈액으로부터 B: 복막으로의 T 세포 이동을 향상시킨다는 것을 나타낸 도면. 각각의 데이터 지점은 개별 마우스를 나타낸다.
도 20은 적용된 알고리즘 마스크에 의해서 정의된 84시간에 걸친 종양 스페로이드 성장 및 형성의 IncuCyte(상표명) 실시간 영상화를 나타낸 도면.
도 21은 A: 시간에 따른 스페로이드 크기 및 총 적분 형광 강도의 변화를 연속적으로 모니터링하는 동안 SKOV3 스페로이드 형성의 유도체 NK 세포 침윤의 대표적인 IncuCyte(상표명) 영상화; B: T 세포 단독은 스페로이드의 중심을 관통하지 못했지만, 유도체 NK 세포의 첨가가 T 세포 침윤 및 후속 스페로이드 파괴를 촉진시켰다는 것을 나타낸 도면.
도 22는 IL-15/IL-15ra(IL-15RF로 표지됨)의 공동-발현이 가용성 IL-2의 부재 하에서 NK-CAR19 발현 유도체 NK 세포 시험관내 지속성을 향상시킨다는 것을 나타낸 도면.
도 23은, iPSC 유래된 NK 공배양물이 가장 큰 적색 대상 마스크 내의 총 적분 녹색 형광 강도를 측정함으로써 종양 스페로이드의 T 세포 침윤을 향상시킨다는 것을 나타낸 도면.
도 24는 iPSC 유래된 NK 세포가 SKOV-3 종양 스페로이드와의 공동 배양 동안 CD4+ 및 CD8+ T 세포 둘 다에 의해서 (A) TNFα 및 (B) IFNγ의 생산을 향상시키도록 T 세포와 상승작용한다는 것을 나타낸 도면.
도 25는 CD16의 고 친화도, 비-절단성 버전을 발현하는 조작된 CAR-iT 세포가 종양을 표적화하고, ADCC를 통한 종양 항원 탈출을 완화시키는 2차 접근법에 대한 기회를 나타낸다는 것을 도시한 도면. CAR 및 hnCD16 ADCC-매개된 세포독성이 CD19+/+ 및 CD19-/- Raji 세포 둘 다에 대해서 사용된다. 표적 세포의 생존은 항-CD20 단클론성 항체 리툭시맙의 존재 및 부재 하에서 36시간 후에 Incucyte Zoom에 의해서 정량되었다.
도 26은 35일 분화 과정 동안 TRAC-CAR-iT 세포의 세포 확장을 나타낸 도면(하나의 생산 실행에서 TRAC-CAR TiPSC를 시작한 후 세포 수율이 40,000배를 초과하게 증가함). 분화된 합성 세포를 대략 28일에 단층으로부터 현탁 배양물로 옮겼다.
도 27은 D35 TRAC-CAR-iT 세포를 4시간 동안 PMA/이오노마이신 자극에 반응한 (A) 전염증성(proinflammatory) 사이토카인 IFNg 및 TNFa; 및 (B) 생존촉진(pro-survival) 사이토카인 IL-2의 생성에 대해서 평가한 것을 도시한 도면.
도 28은 표적 세포로서의 넉아웃(CD19-/-) NALM-6 또는 야생형(CD19+/+)을 사용한 18시간 유세포 분석법 검정을 사용하여 (A) 1차 CAR-T 세포와 (B) 합성 T 세포 TRAC-CAR-iT 간의 시험관내 세포독성의 비교를 나타낸 도면. 3개의 개별 1차 CAR-T 세포에 대해서 3회의 독립적인 실험 및 3개의 개별 TRAC-CAR-iT 생산 배취에 대해서 3개의 독립적인 실험을 사용하였다.
도 29는 (A) D20 TRAC-CAR-iT 세포 및 (B) D28 TRAC-CAR-iT 세포를 사용한 트랜스-웰 이동 검정에서 제시된 흉선 유래 케모카인에 반응한 주화성에 대해서 평가한 것을 도시한 도면.
도 30은 hnCD16, 항-CD19 CAR 및 IL15/IL15Ra을 발현하는 iPSC-유래된 NK 세포에서의 향상된 NK 세포 성숙을 나타낸 도면: (A) 그랜자임 B의 증가된 생산; 및 (B) KIR2DL3 및 KIR2DL1의 증가된 발현.
도 31은 IL15/IL15Ra의 발현이 iNK 지속성 및 항원-유도된 확장을 촉진시킨다는 것을 나타낸 도면: (A) 1×107개 CAR iNK 또는 CAR-IL15/IL15Ra iNK 세포를 0, 7 및 14일에 면역손상된 NOD 마우스에 IV로 주사하였다. IL-2를 최초 3주 동안 주 2회 IP 주사하였고, iNK 세포를 지속성 평가를 위해서 9주 동안 주 단위로 혈액에서 측정하였다; (B) 5×105개 Nalm6 세포를 NSG 마우스에 IV로 이식하였다. 4 및 11일 후, 5×106 CAR iNK 또는 CAR-IL-15/IL-15ra iNK를 IV로 주사하였고, 혈액에서 iNK 세포 수치를 세포 확장 평가를 위해서 유세포 분석법에 의해서 주 단위로 결정하였다. IL-2를 주 2회 IP 투여하였다.
도 32는 (A) CAR-IL15/IL15Ra iNK 세포가 B 세포 림프종의 고도로 공격적인 산재성 모델에서 생존을 개선시키고(p = 0.018, CAR-IL-15/IL-15ra iNK 대 CAR iNK); (B) CAR-IL15/IL15Ra iNK 세포가 백혈병의 Nalm6 이종이식편 모델에서 생체내에서 종양 진행을 예방한다는 것을 나타낸 도면.
도 33는 (A) 증가하는 E:T 비에서 4시간 세포독성 검정에서 hnCD16-CAR-IL-15/IL-15ra iNK 세포를 사용하여 측정된 Nalm6 및 Nalm6 CD19-/-; (B) ARH-77 백혈병 세포 또는 (C) ARH-77 CD19-/- 세포에 대한 hnCD16-CAR-IL15/IL15Ra iNK 세포의 시험관내 세포독성을 사용하여 대조군으로서 비변형된 iNK 세포를 사용한 4시간 세포독성 검정에서 직접 세포독성 및 리툭시맙-유도된 ADCC를 측정한 것을 도시한 도면.
도 34는 hnCD16, CAR 및 IL-15/IL-15ra 양상이 혼합 배양 세포독성 검정에서 CD19+ 및 CD19- 표적을 근절시키도록 상승작용하는 것을 도시한 도면. 모체 ARH-77 세포(CD19+) 및 ARH-77 CD19- 세포에 각각 적색 및 녹색 형광 태그를 형질도입하였다. 이들 세포를 1:1로 혼합하고, 리툭시맙 항체의 존재 또는 부재 하에서 효과기 세포로서 다양한 iNK 세포 집단을 사용하는 장기간 세포독성 검정에서 표적 세포로서 사용하였다. Incucyte 영상화 시스템을 사용하여 검정 전체에서 녹색 CD19- 및 적색 CD19+ 표적의 빈도를 측정하여 단일 웰 내에서 표적 세포 둘 다에 대한 세포독성을 정량하였다. 데이터는 효과기 세포가 없는(종양 세포 단독) 대조군에 정규화된 두 표적 유형 모두에 대해서 남아있는 표적 세포의 빈도로서 플로팅된다.
도 35는, TRAC-CAR iT 세포가 표적 세포로서 HLA-미스매칭된 PBMC-유래된 T 세포에 대해서 TRAC-CAR iT 세포 및 일차 CAR-T 세포의 증식 반응을 비교하는 혼합 림프구 반응(Mixed Lymphocyte Reaction: MLR) 검정을 사용하여 HLA-미스매칭된 건강한 세포에 대해서 동종반응성(alloreactive)이 아니라는 것을 나타낸 도면. 반응자 세포(responder cell)를 세포 트레이스 염료로 표지하고, 유세포 분석법에 의해서 염료 희석을 위해서 4일 후에 평가하였다.
도 36은 hnCD16을 발현하는 TRAC-CAR iT 세포가 표적 종양에 대한 2차 접근법을 나타낸다는 것을 도시한 도면. CD19+/+ 및 CD19-/- Raji 세포에 대한 CAR 및 hnCD16 ADCC-매개된 세포독성을 비교하였다. 표적 세포의 생존을 항-CD20 단클론성 항체 리툭시맙의 존재 및 부재 하에서 72시간 후에 유세포 분석법에 의해서 정량하였다.
도 2는 hnCD16 발현, B2M 넉아웃(HLA-A2 발현의 손실), HLA-G 발현 및 IL-15/IL-15ra(LNGFR) 작제물 발현의 단계적 조작을 나타내는 성숙 iPSC-유래된 NK 세포의 유세포 분석법의 그래프 표현.
도 3은 유세포 분석법에 의해서 결정된 텔로미어 길이의 그래프 표현(iPSC로부터의 성숙 유도체 NK 세포는 성인 말초 혈액 NK 세포에 비해서 더 긴 텔로미어를 유지함).
도 4는 B2M 넉아웃이 동종이계 CD8+ T 세포에 의해서 조작된 유도체 NK 세포의 시험관내 인식을 제거한 것을 나타낸 도면.
도 5는 HLA-G의 발현이 NK 세포에 의한 사멸로부터 B2M-/- iPSC를 구제한다는 것을 나타낸 도면. A: HLA-I의 손실은 동종이계 PBMC와 인큐베이션되는 경우 조작된 iPSC에 대한 증가된 세포독성을 야기한다. B: B2M-/- iPSC 상에서의 HLA-G의 발현에 의해서 조작된 iPSC의 동종이계 사멸이 부분적으로 역전되었다. Incucyte Zoom(상표명) 영상화 시스템을 사용하여 시간에 따라서 iPSC의 손실을 측정하였고, 효과기 세포가 없는 웰에서 iPSC의 수에 데이터를 정규화하고, 각각의 조건에 대해서 시간 = 0 내지 100%로 설정하였다.
도 6은 hnCD16/B2M-/-HLA-G iNK의 단일 용량이 난소암의 생체내 이종이식편 모델에서 종양 퇴행을 유도하였음을 나타낸 도면. A: 주사 후 32일의 기간에 걸친 각각의 마우스의 IVIS 영상. B: IVIS 영상화에 의한 종양 진행의 시간 경과.
도 7은 IL15/IL15Ra 작제물이 시험관내에서 가용성의 외인성 IL15의 첨가와 무관하게 iNK 세포 분화 및 생존을 촉진시킨다는 것을 나타낸 도면. A: 각각의 제시된 유전자형의 iNK 세포는 가용성 IL15의 첨가에 의해서 또는 첨가 없이 분화되었다. B: iNK 세포를 광범위하게 세척하고, 가용성 IL15-비의존적 세포 성장을 관찰하기 위해서 10ng/㎖ 내지 0ng/㎖ 범위의 농도의 가용성 IL15의 농도로 7일 동안 다시 배양액에 넣었다.
도 8은 IL15/IL15Ra 작제물의 발현이 가용성 IL15의 부재 하에서 생체내에서 iNK 지속성을 향상시킴을 나타낸 도면. iNK 세포를 A: 면역손상된 NOG 마우스; B: 인간 IL15에 대해해서 트랜스제닉인 NOG 마우스에게 입양에 의해서 전달하였다.
도 9는 표면 마커의 유세포 분석을 사용한 CAR-발현 iPSC 유래된 NK 세포의 표현형분석의 그래프 표현.
도 10은 다양한 효과기 대 표적(E:T)비에서 유로퓸-로딩된 메조-고 표적 세포와 공동 배양된 CAR4-발현 유도체 NK 세포의 항-종양 활성의 그래프 표현. A: K562 메조-고 표적 세포; B: A1847 메조-고 표적 세포.
도 11은 루시퍼라제-발현 A1847 메조 고 세포가 접종되고, A1847 접종 4일 후 상이한 유전자형의 1.5E7 NK 세포가 1회 투여된 이종이식편 NSG 마우스 모델에서 주 단위 생물발광 영상화에 의해서 결정된 종양 부하를 나타낸 도면.
도 12는 A: 생물발광을 사용하여 결정된 정량된 종양 부하; B: 루시퍼라제-발현 A1847 메조 고 세포가 접종되고, A1847 접종 4일 후 상이한 유전자형의 1.5E7 NK 세포가 1회 투여된 NSG 마우스군의 생존 백분율을 나타낸 카플란-마이어 곡선. 모든 군에 대해서 n=5.
도 13은 유세포 분석법에 의해서 평가된, (A) 말초 혈액, (B) 비장 및 (C) 복막으로부터 수집된 세포로부터의 유도체 CAR-NK 세포의 백분율 측정에 의한 생체내에서 CAR-iNK의 향상된 지속성을 나타낸 도면. 각각의 점은 하나의 수용자 마우스를 나타낸다. 중위값 ± SEM을 나타내고, P<0.05이다.
도 14는 hnCD16-iPSC의 클론성 집단으로부터의 CD16 발현 유도체 T 세포의 생성의 그래프 표현. A: hnCD16-iPSC 유동 분석; B: hnCD16-iT 유동 분석.
도 15는 hnCD16-iT 세포에 의한 ADCC 매개된 표적 세포 제거를 도시한 도면.
도 16은 CAR 및 hnCD16 둘 다의 발현이 효과기 세포, 예컨대, 유도체 T 세포 및 유도체 NK 세포에 대한 CAR-hnCD16-iPSC의 조혈 분화를 교란시키지 않는다는 것을 나타낸 도면. A: CAR-hnCD16 iPSC; B: CAR-hnCD16 iCD34 세포; C: CAR-hnCD16 유도체 T 세포의 유세포 분석법 분석.
도 17은 활성화된 hnCD16-iNK 세포가 CD69 양성 T 세포의 백분율에 의해서 측정된 T 세포 활성화를 향상시키는 가용성 인자를 생산한다는 것을 나타낸 도면.
도 18은 활성화된 hnCD16-iNK 세포가 트랜스-웰 검정에서 상부에서 하부 챔버로의 T 세포 이동 형태의 유세포 분석법에 의해서 정량된, T 세포 이동을 향상시키는 가용성 인자를 생산한다는 것을 나타낸 도면.
도 19는 유도체 NK 세포가 유세포 분석법에 의해서 정량된 바와 같이, 생체내에서 주사된 마우스 모델의 A: 혈액으로부터 B: 복막으로의 T 세포 이동을 향상시킨다는 것을 나타낸 도면. 각각의 데이터 지점은 개별 마우스를 나타낸다.
도 20은 적용된 알고리즘 마스크에 의해서 정의된 84시간에 걸친 종양 스페로이드 성장 및 형성의 IncuCyte(상표명) 실시간 영상화를 나타낸 도면.
도 21은 A: 시간에 따른 스페로이드 크기 및 총 적분 형광 강도의 변화를 연속적으로 모니터링하는 동안 SKOV3 스페로이드 형성의 유도체 NK 세포 침윤의 대표적인 IncuCyte(상표명) 영상화; B: T 세포 단독은 스페로이드의 중심을 관통하지 못했지만, 유도체 NK 세포의 첨가가 T 세포 침윤 및 후속 스페로이드 파괴를 촉진시켰다는 것을 나타낸 도면.
도 22는 IL-15/IL-15ra(IL-15RF로 표지됨)의 공동-발현이 가용성 IL-2의 부재 하에서 NK-CAR19 발현 유도체 NK 세포 시험관내 지속성을 향상시킨다는 것을 나타낸 도면.
도 23은, iPSC 유래된 NK 공배양물이 가장 큰 적색 대상 마스크 내의 총 적분 녹색 형광 강도를 측정함으로써 종양 스페로이드의 T 세포 침윤을 향상시킨다는 것을 나타낸 도면.
도 24는 iPSC 유래된 NK 세포가 SKOV-3 종양 스페로이드와의 공동 배양 동안 CD4+ 및 CD8+ T 세포 둘 다에 의해서 (A) TNFα 및 (B) IFNγ의 생산을 향상시키도록 T 세포와 상승작용한다는 것을 나타낸 도면.
도 25는 CD16의 고 친화도, 비-절단성 버전을 발현하는 조작된 CAR-iT 세포가 종양을 표적화하고, ADCC를 통한 종양 항원 탈출을 완화시키는 2차 접근법에 대한 기회를 나타낸다는 것을 도시한 도면. CAR 및 hnCD16 ADCC-매개된 세포독성이 CD19+/+ 및 CD19-/- Raji 세포 둘 다에 대해서 사용된다. 표적 세포의 생존은 항-CD20 단클론성 항체 리툭시맙의 존재 및 부재 하에서 36시간 후에 Incucyte Zoom에 의해서 정량되었다.
도 26은 35일 분화 과정 동안 TRAC-CAR-iT 세포의 세포 확장을 나타낸 도면(하나의 생산 실행에서 TRAC-CAR TiPSC를 시작한 후 세포 수율이 40,000배를 초과하게 증가함). 분화된 합성 세포를 대략 28일에 단층으로부터 현탁 배양물로 옮겼다.
도 27은 D35 TRAC-CAR-iT 세포를 4시간 동안 PMA/이오노마이신 자극에 반응한 (A) 전염증성(proinflammatory) 사이토카인 IFNg 및 TNFa; 및 (B) 생존촉진(pro-survival) 사이토카인 IL-2의 생성에 대해서 평가한 것을 도시한 도면.
도 28은 표적 세포로서의 넉아웃(CD19-/-) NALM-6 또는 야생형(CD19+/+)을 사용한 18시간 유세포 분석법 검정을 사용하여 (A) 1차 CAR-T 세포와 (B) 합성 T 세포 TRAC-CAR-iT 간의 시험관내 세포독성의 비교를 나타낸 도면. 3개의 개별 1차 CAR-T 세포에 대해서 3회의 독립적인 실험 및 3개의 개별 TRAC-CAR-iT 생산 배취에 대해서 3개의 독립적인 실험을 사용하였다.
도 29는 (A) D20 TRAC-CAR-iT 세포 및 (B) D28 TRAC-CAR-iT 세포를 사용한 트랜스-웰 이동 검정에서 제시된 흉선 유래 케모카인에 반응한 주화성에 대해서 평가한 것을 도시한 도면.
도 30은 hnCD16, 항-CD19 CAR 및 IL15/IL15Ra을 발현하는 iPSC-유래된 NK 세포에서의 향상된 NK 세포 성숙을 나타낸 도면: (A) 그랜자임 B의 증가된 생산; 및 (B) KIR2DL3 및 KIR2DL1의 증가된 발현.
도 31은 IL15/IL15Ra의 발현이 iNK 지속성 및 항원-유도된 확장을 촉진시킨다는 것을 나타낸 도면: (A) 1×107개 CAR iNK 또는 CAR-IL15/IL15Ra iNK 세포를 0, 7 및 14일에 면역손상된 NOD 마우스에 IV로 주사하였다. IL-2를 최초 3주 동안 주 2회 IP 주사하였고, iNK 세포를 지속성 평가를 위해서 9주 동안 주 단위로 혈액에서 측정하였다; (B) 5×105개 Nalm6 세포를 NSG 마우스에 IV로 이식하였다. 4 및 11일 후, 5×106 CAR iNK 또는 CAR-IL-15/IL-15ra iNK를 IV로 주사하였고, 혈액에서 iNK 세포 수치를 세포 확장 평가를 위해서 유세포 분석법에 의해서 주 단위로 결정하였다. IL-2를 주 2회 IP 투여하였다.
도 32는 (A) CAR-IL15/IL15Ra iNK 세포가 B 세포 림프종의 고도로 공격적인 산재성 모델에서 생존을 개선시키고(p = 0.018, CAR-IL-15/IL-15ra iNK 대 CAR iNK); (B) CAR-IL15/IL15Ra iNK 세포가 백혈병의 Nalm6 이종이식편 모델에서 생체내에서 종양 진행을 예방한다는 것을 나타낸 도면.
도 33는 (A) 증가하는 E:T 비에서 4시간 세포독성 검정에서 hnCD16-CAR-IL-15/IL-15ra iNK 세포를 사용하여 측정된 Nalm6 및 Nalm6 CD19-/-; (B) ARH-77 백혈병 세포 또는 (C) ARH-77 CD19-/- 세포에 대한 hnCD16-CAR-IL15/IL15Ra iNK 세포의 시험관내 세포독성을 사용하여 대조군으로서 비변형된 iNK 세포를 사용한 4시간 세포독성 검정에서 직접 세포독성 및 리툭시맙-유도된 ADCC를 측정한 것을 도시한 도면.
도 34는 hnCD16, CAR 및 IL-15/IL-15ra 양상이 혼합 배양 세포독성 검정에서 CD19+ 및 CD19- 표적을 근절시키도록 상승작용하는 것을 도시한 도면. 모체 ARH-77 세포(CD19+) 및 ARH-77 CD19- 세포에 각각 적색 및 녹색 형광 태그를 형질도입하였다. 이들 세포를 1:1로 혼합하고, 리툭시맙 항체의 존재 또는 부재 하에서 효과기 세포로서 다양한 iNK 세포 집단을 사용하는 장기간 세포독성 검정에서 표적 세포로서 사용하였다. Incucyte 영상화 시스템을 사용하여 검정 전체에서 녹색 CD19- 및 적색 CD19+ 표적의 빈도를 측정하여 단일 웰 내에서 표적 세포 둘 다에 대한 세포독성을 정량하였다. 데이터는 효과기 세포가 없는(종양 세포 단독) 대조군에 정규화된 두 표적 유형 모두에 대해서 남아있는 표적 세포의 빈도로서 플로팅된다.
도 35는, TRAC-CAR iT 세포가 표적 세포로서 HLA-미스매칭된 PBMC-유래된 T 세포에 대해서 TRAC-CAR iT 세포 및 일차 CAR-T 세포의 증식 반응을 비교하는 혼합 림프구 반응(Mixed Lymphocyte Reaction: MLR) 검정을 사용하여 HLA-미스매칭된 건강한 세포에 대해서 동종반응성(alloreactive)이 아니라는 것을 나타낸 도면. 반응자 세포(responder cell)를 세포 트레이스 염료로 표지하고, 유세포 분석법에 의해서 염료 희석을 위해서 4일 후에 평가하였다.
도 36은 hnCD16을 발현하는 TRAC-CAR iT 세포가 표적 종양에 대한 2차 접근법을 나타낸다는 것을 도시한 도면. CD19+/+ 및 CD19-/- Raji 세포에 대한 CAR 및 hnCD16 ADCC-매개된 세포독성을 비교하였다. 표적 세포의 생존을 항-CD20 단클론성 항체 리툭시맙의 존재 및 부재 하에서 72시간 후에 유세포 분석법에 의해서 정량하였다.
iPSC(유도 만능 줄기세포)의 게놈 변형은 폴리뉴클레오타이드 삽입, 결실 및 치환을 포함한다. 게놈-조작된 iPSC에서의 외인성 유전자 발현은 종종 본래 게놈-조작된 iPSC의 연장된 클론성 확장 후, 세포 분화 후 및 게놈-조작된 iPSC로부터 유래된 세포로부터의 탈분화된 세포 유형에서 유전자 침묵 또는 유전자 발현 감소와 같은 문제를 경험한다. 다른 한편, 1차 면역 세포, 예컨대, T 또는 NK 세포의 직접 조작은 도전적이며, 입양 세포 요법을 위한 조작된 면역 세포의 제조 및 전달에 장애물을 제공한다. 본 발명은 자살 유전자 및 다른 기능성 양상을 비롯한 하나 이상의 외인성 유전자를 안정적으로 통합시키기 위한 효율적이고, 실현 가능하고, 표적화된 접근법을 제공하며, 이것은 직접 iPSC 분화로부터 획득된 iPSC 유도체 세포에 생착, 수송, 귀소, 이동, 세포독성, 생존력, 유지, 확장, 수명, 자가-재생, 지속성 및/또는 생존과 관련된 개선된 치료 특성을 제공하며, 유도체 세포는 HSC(조혈 줄기 및 전구 세포), T 세포 전구 세포, NK 세포 전구 세포, T 세포, NKT 세포, NK 세포를 포함하지만 이들로 제한되지 않는다.
정의
본 명세서에서 달리 정의되지 않는 한, 본 출원과 관련하여 사용된 과학 용어 및 기술 용어는 당업자에게 일반적으로 이해되는 의미를 가질 것이다. 또한, 문맥상 달리 요구되지 않는 한, 단수형은 복수를 포함하고 복수형은 단수를 포함할 것이다.
본 발명은 본 명세서에 기재된 특정 방법론, 프로토콜 및 시약 등에 제한되지 않으며, 다양할 수 있음을 이해해야 한다. 본 명세서에서 사용한 용어는 단지 특정 실시형태를 설명하기 위해 사용된 것으로, 본 발명의 범주를 한정하려는 의도가 아니며, 본 발명의 범주는 청구범위에 의해서만 정의된다.
본 명세서에서 사용된 바와 같이, 단수의 용어는 문법적 대상의 하나 또는 하나 초과(즉, 적어도 하나)를 지칭하기 위해 본 명세서에서 사용된다. 예로서, "요소"는 하나의 요소 또는 하나 초과의 요소를 의미한다.
대안의(예를 들어, "또는")의 사용은 대안 중 하나, 둘 다 또는 이들의 임의의 조합을 의미하는 것으로 이해되어야 한다.
용어 "및/또는"은 대안 중 하나, 또는 둘 다를 의미하는 것으로 이해되어야 한다.
본 명세서에 사용되는 바와 같은 용어 "약"또는 "대략"은 기준 양, 수준, 값, 숫자, 빈도, 백분율, 치수, 크기, 양, 중량 또는 길이에 비해 15%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% 또는 1%만큼 많이 변하는 빈도, 백분율, 치수, 크기, 양, 중량 또는 길이를 지칭한다. 일 실시형태에서, 용어 "약" 또는 "대략"은 양, 수준, 값, 숫자, 빈도, 백분율, 치수, 크기, 양, 중량 또는 길이에 관해 양, 수준, 값, 숫자, 빈도, 백분율, 치수, 크기, 양, 중량 또는 길이 ± 15%, ± 10%, ± 9%, ± 8%, ± 7%, ± 6%, ± 5%, ± 4%, ± 3%, ± 2% 또는 ± 1%의 범위를 지칭한다.
본 명세서에 사용되는 바와 같은 용어 "실질적으로" 또는 "본질적으로"는 기준 양, 수준, 값, 숫자, 빈도, 백분율, 치수, 크기, 양, 중량 또는 길이에 비해 약 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% 또는 99% 또는 더 높은 양, 수준, 값, 숫자, 빈도, 백분율, 치수, 크기, 양, 중량 또는 길이를 지칭한다. 일 실시형태에서, 용어 "본질적으로 동일한" 또는 "실질적으로 동일한"은 기준 양, 수준, 값, 숫자, 빈도, 백분율, 치수, 크기, 양, 중량 또는 길이와 거의 동일한 기준 양, 수준, 값, 숫자, 빈도, 백분율, 치수, 크기, 양, 중량 또는 길이의 범위를 지칭한다.
본 명세서에 사용되는 바와 같은 용어 "실질적으로 없는" 및 "본질적으로 없는"은 상호 호환적으로 사용되고, 조성물, 예컨대 세포 집단 또는 배양 배지를 기재하기 위해 사용될 때, 특정된 물질 또는 그의 공급원이 없는, 예컨대 구체화된 물질 또는 그의 공급원이 95% 없는, 96% 없는, 97% 없는, 98% 없는, 99% 없거나, 또는 통상적인 수단에 의해 측정하여 검출 불가능한 조성물을 지칭한다. 조성물 중의 특정 성분 또는 물질이 "없는" 또는 "본질적으로 없는"이라는 용어는 또한 이러한 성분 또는 물질이 (1) 임의의 농도로 조성물 중에 포함되지 않거나, 또는 (2) 기능적으로 비활성이지만, 저농도인 조성물 중에 포함되지 않는다는 것을 의미한다. 조성물의 특정 물질 또는 그의 공급원의 부재를 지칭할 때, 용어 "의 부재"에 유사한 의미가 적용될 수 있다.
본 명세서 전체적으로, 문맥에서 달리 요구되지 않는 한, 단어 "포함한다(포함한다)", "포함한다" 및 "포함하는"은 단계들 또는 요소들의 언급된 단계 또는 요소의 포함을 나타내지만, 단계들 또는 요소들의 임의의 다른 단계 또는 요소 또는 그룹의 제외를 나타내는 것으로 이해될 것이다. 특정 실시형태에서, 용어 "포함한다(include, comprise)", "갖는다(has)" 및 "함유한다(contain)"는 동의어로 사용된다.
"이루어진"은 어구 "이루어진"에 따르는 것은 무엇이든 포함하지만, 이것으로 제한되지 않는다는 것을 의미한다. 따라서, 어구 "이루어진"은 열거된 요소가 필요하거나 또는 필수적인 것, 다른 요소가 존재하지 않을 수도 있다는 것을 나타낸다.
"본질적으로 이루어진"은 어구 다음에 열거된 임의의 요소를 포함하고, 열거된 요소에 대해 개시내용에서 구체화된 활성 또는 작용을 방해하지 않거나 또는 기여하지 않는 다른 요소로 제한된다는 것을 의미한다. 따라서, 어구 "본질적으로 이루어진"은 열거된 요소가 필요하거나 또는 필수적인 것이지만, 다른 요소가 선택적이지는 않고, 그들이 열거된 요소의 활성 도는 작용에 영향을 미치는지의 여부에 따라 제공될 수도 있고 제공되지 않을 수도 있다는 것을 나타낸다.
본 명세서 전체적으로 "일 실시형태", "실시형태", "특정 실시형태", "관련된 실시형태", "특정 실시형태", "추가적인 실시형태" 또는 "추가 실시형태" 또는 이들의 조합에 대한 언급은 실시형태와 관련하여 기재된 특정 특성, 구조 또는 특징이 본 발명의 적어도 하나의 실시형태에 포함된다는 것을 의미한다. 따라서, 본 명세서 전체적으로 다양한 곳에서 앞서 언급한 어구의 출현은 반드시 동일한 실시형태를 모두 언급할 필요는 없다. 더 나아가, 특정 특성, 구조 또는 특징은 하나 이상의 실시형태에서 임의의 적합한 방식으로 조합될 수 있다.
용어 "생체외"는 일반적으로 유기체 외부, 예컨대 바람직하게는 자연 조건의 최소 변형을 갖는 유기체 외부의 인공 환경에서의 살아있는 조직 내 또는 살아있는 조직 상에서 행해지는 실험 또는 측정에서 일어나는 활성을 지칭한다. 특정 실시형태에서, "생체외" 절차는 유기체로부터 취해지고, 보통 멸균 조건 하에 실험 장치에서, 그리고 전형적으로 환경에 따라서 몇 시간 동안 또는 약 24시간까지(48시간 또는 72시간 또는 그 이상을 포함) 배양되는 살아있는 세포 또는 조직을 수반한다. 특정 실시형태에서, 이러한 조직 또는 세포는 수집되고, 냉동될 수 있고, 이후에 생체외 처리를 위해 해동될 수 있다. 살아있는 세포 또는 조직을 이용하여 며칠보다 더 길게 지속되는 조직 배양 실험 또는 절차는 전형적으로 "시험관내"가 (특정 실시형태에서, 이 용어가 생체외 상호 교환 가능하게 사용될 수는 있지만) 되는 것으로 고려된다.
용어 "생체내"는 일반적으로 유기체 내에서 일어나는 활동을 지칭한다.
본 명세서에 사용되는 바와 같은 용어 "재프로그래밍" 또는 "탈분화" 또는 세포 효력의 증가" 또는 "발생 효력의 증가"는 세포의 효력을 증가시키거나 또는 세포를 덜 분화된 상태로 분화시키는 방법을 지칭한다. 예를 들어, 증가된 세포 효력을 갖는 세포는 비-재프로그래밍 상태에서의 동일 세포에 비해 더 발생된 가소성을 가진다(즉, 더 많은 세포 유형으로 분화할 수 있음). 다시 말해서, 재프로그래밍된 세포는 비-재프로그래밍 상태에서의 동일 세포보다 덜 분화된 상태의 것이다.
본 명세서에 사용되는 바와 같은 용어 "분화"는 비전문화된("비전념된(uncommitted)") 또는 덜 전문화된 세포가 전문화된 세포, 예를 들어, 혈액 세포 또는 근육 세포의 특징을 획득하는 과정이다. 분화된 또는 분화-유도 세포는 세포 계통 내에서 더 전문화된("전념된(committed)") 위치 상에서 취해진 것이다. 용어 "전념된"은 분화 과정에 적용될 때, 정상 환경 하에서 그것이 특정 세포 유형 또는 세포 유형의 서브세트로 분화를 계속할 수 있는 지점으로 분화 경로에서 진행하고, 정상 환경 하에서 상이하나 세포 유형으로 분화하거나 또는 덜 분화된 세포 유형으로 되돌아가는 지점까지 분화 경로에서 진행되는 세포를 지칭한다. 본 명세서에 사용되는 바와 같은 용어 "만능"은 신체 또는 체세포의 모든 계통(즉, 배아 적합)을 형성하는 세포의 능력을 지칭한다. 예를 들어, 배아 줄기세포는 각각 3가지의 배층(외배엽, 중배엽 및 내배엽)으로부터의 세포를 형성할 수 있는 만능 줄기세포 유형이다. 만능성은 완전한 유기체를 더 원시적으로 발생되게 할 수 없는 불완전하게 또는 부분적으로 만능 세포(예를 들어, 원외배엽 줄기세포 또는 EpiSC), 완전한 유기체(예를 들어, 배아 줄기세포)가 생기게 할 수 있는 더 만능의 세포의 범위에 있는 발생 효력의 연속체이다.
본 명세서에 사용되는 바와 같은 용어 "유도 만능 줄기세포" 또는 iPSC는 줄기세포가 유도 또는 변화된, 즉, 모두 3가지의 배아 또는 진피층(중배엽, 내배엽 및 외배엽)으로 분화할 수 있는 세포로 재프로그래밍된 분화된 성인, 신생아 또는 태아 세포로부터 생성된다는 것을 의미한다. 생성된 iPSC는 그들이 자연에서 발견되기 때문에 세포를 지칭하지 않는다.
본 명세서에 사용되는 바와 같은 용어 "배아 줄기세포"는 배아 배반포의 내부 세포 덩어리의 자연 유래 만능 줄기세포를 지칭한다. 배아 줄기세포는 만능성이며, 3가지의 1차 배엽(외배엽, 내배엽 및 중배엽)의 모든 유도체로의 발생 동안 생기게 한다. 그들은 배아외막 또는 태반에 기여하지 않으며, 즉, 전능성(totipotent)이 아니다.
본 명세서에 사용되는 바와 같은 용어 "다능성 줄기세포"는 하나 이상의 배엽(외배엽, 중배엽 및 내배엽)(그러나 3가지 모두는 아님)의 세포로 분화하는 발생 가능성을 갖는 세포를 지칭한다. 따라서, 다능성 세포는 또한 "부분적으로 분화된 세포"로 지칭될 수 있다. 다능성 세포는 관련 기술 분야에 잘 공지되어 있고, 다능성 세포의 예는 성체 줄기세포, 예를 들어, 조혈 줄기세포 및 신경 줄기세포를 포함한다. "다능성"은 세포가 주어진 계통에서 다수 유형의 세포(그러나 다른 계통의 세포는 아님)를 형성할 수 있다는 것을 나타낸다. 예를 들어, 다능성 조혈 세포는 다수의 상이한 유형의 혈액 세포(적혈구, 백혈구, 혈소판 등)를 형성할 수 있지만, 뉴런을 형성할 수 없다. 따라서, 용어 "다능성"은 전능성 및 만능성보다 더 적은 발생 가능성 정도를 갖는 세포 상태를 지칭한다.
만능성은 부분적으로 세포의 만능성 특징을 평가함으로써 결정될 수 있다. 만능성 특징은 (i) 만능 줄기세포 형태; (ii) 비제한적 자기-재생을 위한 가능성; (iii) SSEA1(마우스 단독), SSEA3/4, SSEA5, TRA1-60/81, TRA1-85, TRA2-54, GCTM-2, TG343, TG30, CD9, CD29, CD133/프로미닌, CD140a, CD56, CD73, CD90, CD105, OCT4, NANOG, SOX2, CD30 및/또는 CD50을 포함하지만, 이들로 제한되지 않는 만능 줄기세포 마커의 발현; (iv) 모두 3가지의 체세포 계통(외배엽, 중배엽 및 내배엽)으로 분화하는 능력; (v) 3가지 체세포 계통으로 이루어진 기형종 형성; 및 (vi) 3가지 체세포 계통으로부터의 세포로 이루어진 배상체의 형성을 포함하지만, 이들로 제한되지 않는다.
2가지 유형의 만능성이 이전에 기재되었다: 후기 배반포의 원외배엽 줄기세포(EpiSC)와 유사한 만능성의 "프라이밍된" 또는 "전이성" 상태, 및 초기/이식전 배반포의 내부 세포 덩어리와 유사한 만능성의 "미경험" 또는 "바닥" 상태. 만능성 상태는 둘 다 상기 기재한 바와 같은 특징을 나타내지만, 미경험 또는 바닥 상태는 추가로 다음을 나타낸다: (i) 여성 세포에서 X-염색체의 사전-비활성화 또는 재활성화; (ii) 단일-세포 배양 동안 개선된 클론성 및 생존; (iii) DNA 메틸화에서의 전반적 감소; (iv) 발생 조절 유전자 프로모터에 대한 H3K27me3 억제 염색질 마크 침착의 감소; 및 (v) 만능 세포의 프라이밍된 상태에 비해 분화 마커의 감소된 발현. 외인성 만능성 유전자가 체세포에 도입되고, 발현되며, 이어서 얻어진 만능 세포로부터 침묵화되거나 제거된 세포 프로그래밍의 표준 방법은 일반적으로 만능성의 프라이밍-상태의 특징을 갖는 것으로 보인다. 표준 만능 세포 배양 조건 하에서, 외인성 이식유전자 발현이 유지되지 않는 한 이러한 세포는 프라이밍된 상태로 남아있되, 바닥 상태의 특징이 관찰된다.
본 명세서에 사용되는 바와 같은 용어 "만능 줄기세포 형태"는 배아 줄기세포의 고전적 형태 특징을 지칭한다. 정상 배아 줄기세포 형태는 높은 핵-대-세포질 비, 핵소체의 주목할 만한 존재 및 전형적인 세포내 간격과 함께 형상이 둥글고 작은 것을 특징으로 한다.
본 명세서에 사용되는 바와 같이, 용어 "대상체"는 임의의 동물, 바람직하게는, 인간 환자, 가축 또는 다른 집에서 기르는 동물을 지칭한다.
"만능 인자" 또는 "재프로그래밍 인자"는 단독으로 또는 다른 작용제와 조합하여, 세포의 발생 효력을 증가시킬 수 있는 작용제를 지칭한다. 만능 인자는 폴리뉴클레오타이드, 폴리펩타이드 및 소분자를 포함하지만, 이들로 제한되지 않는다. 예시적인 만능 인자는, 예를 들어, 전사 인자 및 소분자 재프로그래밍제를 포함한다.
"배양물" 또는 "세포 배양물"은 시험관내 환경에서 세포의 유지, 성장 및/또는 분화를 지칭한다. "세포 배양 배지", "배양 배지"(각각의 경우에 단수 "배지"), "보충물" 및 "배지 보충물"은 세포 배양물을 배양하는 영양 조성물을 지칭한다.
"배양하다" 또는 "유지하다"는, 예를 들어 멸균 플라스틱(또는 코팅된 플라스틱)세포 배양물 접시 또는 플라스크에서 조직 또는 신체 밖에서 세포를 지속하고/하거나, 증식(성장)시키고/시키거나 분화시키는 것을 지칭한다. "배양" 또는 "유지하는"은 세포를 증식시키고/시키거나 지속시키는 데 도움이 되는 영양소, 호르몬 및/또는 다른 인자의 공급원으로서 배양 배지를 이용할 수 있다.
본 명세서에 사용되는 바와 같은 용어 "중배엽"은 초기 배형성 동안 나타나고, 순환계, 근육, 심장, 진피, 골격 및 기타 지지 및 결합 조직의 혈액 세포를 포함하는 다양한 전문화된 세포 유형이 생기게 하는 3가지 배엽 중 하나를 지칭한다.
본 명세서에 사용되는 바와 같은 용어 "확정적 조혈 내피"(HE) 또는 "만능 줄기세포-유래 확정적 조혈 내피"(iHE)는 내피세포에서 조혈세포로의 이행(endothelial-to-hematopoietic transition)으로 불리는 과정에서 조혈 줄기 및 전구 세포를 생기게 하는 내피 세포의 서브세트를 지칭한다. 배아 내 조혈 세포의 발생은 혈액모세포에서 확정적 조혈 내피 및 조혈 전구 세포까지 측판 중배엽으로부터 순차적으로 진행된다.
용어 "조혈 줄기 및 전구 세포", "조혈 줄기세포", "조혈 전구 세포", 또는 "조혈 전구체 세포"는 조혈 계통에 전념되지만, 추가로 조혈 분화가 가능하고, 다능성 조혈 줄기세포(혈구모세포), 골수 전구 세포, 거핵세포 전구 세포, 적혈구 전구 세포 및 림프구 전구 세포를 포함하는 세포를 지칭한다. 조혈 줄기 및 전구 세포(HSC)는 골수(단핵구 및 대식세포, 호중구, 호염구, 호산구, 적혈구, 거핵세포/혈소판, 수지상 세포), 및 림프구 계통(T 세포, B 세포, NK 세포)을 비롯한, 혈액 세포 유형 모두를 생성시키는 다능성 줄기세포다. 용어 "확정적 조혈 줄기세포"는 본 명세서에 사용되는 바와 같이, 성숙 골수, 및 T 세포, NK 세포 및 B 세포를 비롯한 림프구 세포 유형 둘 모두를 생성할 수 있는 CD34+ 조혈 세포를 지칭한다. 조혈 세포는 또한 원시적 적혈구, 거핵세포 및 대식세포를 생성시키는 원시적 조혈 세포의 다양한 하위세트를 포함한다.
본 명세서에 사용되는 바와 같은 용어 "T 림프구" 및 "T 세포"는 상호 호환적으로 사용되고, 흉선에서 성숙을 완결하고, 신체에서 특이적 외부 항원의 식별 및 다른 면역 세포의 활성화 및 비활성화를 비롯한, 면역계에서 다양한 역할을 갖는 백혈구의 주요 유형을 지칭한다. T 세포는 임의의 T 세포, 예컨대 배양된 T 세포, 예를 들어, 1차 T 세포, 또는 배양된 T 세포주로부터의 T 세포, 예를 들어, Jurkat, SupT1 등, 또는 포유동물로부터 얻은 T 세포일 수 있다. T 세포는 CD3+ 세포일 수 있다. T 세포는 T 세포의 임의의 유형일 수 있고, CD4+/CD8+ 이중 양성 T 세포, CD4+ 헬퍼 T 세포(예를 들어, Th1 및 Th2 세포), CD8+ T 세포(예를 들어, 세포독성 T 세포), 말초 혈액 단핵 세포(PBMC), 말초 혈액 백혈구(PBL), 종양 침윤성 림프구(TIL), 기억 T 세포, 미경험 T 세포, 조절 T 세포, 감마 델타 T 세포(γδT 세포) 등을 포함하지만, 이들로 제한되지 않는 임의의 발생 단계를 가질 수 있다. 추가적인 유형의 헬퍼 T 세포는 Th3(Treg), Th17, Th9 또는 Tfh 세포와 같은 세포를 포함한다. 추가적인 유형의 기억 T 세포는 중앙 기억 T 세포(Tcm 세포), 효과기 기억 T 세포(Tem 세포 및 TEMRA 세포)와 같은 세포를 포함한다. T 세포는 또한 유전자 조작된 T 세포, 예컨대 T 세포 수용체(TCR) 또는 키메라 항원 수용체(CAR)를 발현시키도록 변형된 T 세포를 지칭할 수 있다. T 세포는 또한 줄기세포 또는 전구 세포로부터 분화될 수 있다.
"CD4+ T 세포"는 이의 표면 상에서 CD4를 발현하고, 세포-매개된 면역 반응과 연관된 T 세포의 하위세트를 지칭한다. 이것은 사이토카인, 예컨대 IFN-감마, TNF-알파, IL2, IL4 및 IL10의 분비를 포함할 수 있는, 자극 이후의 분비 프로파일을 특징으로 한다. "CD4"는 T-림프구 상의 분화 항원으로서 본래 정의되지만, 단핵구/대식세포를 비롯한 다른 세포 상에서도 발견되는 55-kD 당단백질이다. CD4 항원은 면역글로불린 초유전자 패밀리의 구성원이고, MHC(주요 조직적합 복합체(주요 조직적합 복합체)) 클래스 II-제한된 면역 반응에서 회합성 인식 요소로서 관련된다. T-림프구 상에서 이것은 헬퍼/유도자 하위세트를 정의한다.
"CD8+ T 세포"는 이의 표면 상에서 CD8을 발현하고, MHC 클래스 I-제한되고, 세포독성 T 세포로서 기능하는 T 세포의 하위세트를 지칭한다. "CD8" 분자는 흉선세포 상에서 그리고 세포독성 및 억제유전자(suppressor) T-림프구 상에서 발견되는 분화 항원이다. CD8 항원은 면역글로불린 초유전자 패밀리의 구성원이고, 주요 조직적합 복합체 클래스 I-제한된 상호작용에서 회합성 인식 요소이다.
본 명세서에 사용되는 바와 같은 용어 "NK 세포" 또는 "자연 살해 세포"는 CD56 또는 CD16의 발현 및 T 세포 수용체(CD3)의 부재에 의해 나타나는 말초 혈액 림프구의 서브세트를 지칭한다. 본 명세서에 사용되는 바와 같은 용어 "적응 NK 세포" 및 "기억 NK 세포"는 상호 교환 가능하며, NKG2C 및 CD57, 및 선택적으로, CD16 중 적어도 하나를 발현시키지만, 다음의 PLZF, SYK, FceR 및 EAT-2 중 하나 이상의 발현이 결여된 표현형으로 CD3- 및 CD56+인 NK 세포의 서브세트를 지칭한다. 일부 실시형태에서, CD56+ NK 세포의 단리된 하위집단은 CD16, NKG2C, CD57, NKG2D, NCR 리간드, NKp30, NKp40, NKp46, 활성화 및 저해 KIR, NKG2A 및/또는 DNAM-1의 발현을 포함한다. CD56+는 어두운 또는 밝은 발현일 수 있다.
본 명세서에 사용되는 바와 같은 용어 "NKT 세포" 또는 "자연 살해 T 세포"는 T 세포 수용체(TCR)를 발현시키는 CD1d-제한 T 세포를 지칭한다. 통상적인 주조직적합성(MHC) 분자에 의해 제시된 펩타이드 항원을 검출하는 통상적인 T 세포와 달리, NKT 세포는 CD1d, 비-고전적 MHC 분자에 의해 제시된 지질 항원을 인식한다. 2가지 유형의 NKT 세포가 인식된다. 비변이체 또는 I형 NKT 세포는 제한된 범위의 β 쇄(인간에서의 Vβ11)와 관련된 매우 제한된 TCR 레퍼토리 - 정규 α-쇄(인간에서의 Vα24-Jα18)를 발현시킨다. 비정규 또는 비변이체가 아닌 II형 NKT 세포로 불리는 NKT 세포의 제2 집단은 더 이종성의 TCR αβ 용법을 나타낸다. I형 NKT 세포는 면역요법에 적합한 것으로 고려된다. 적응 또는 비변이체(I형) NKT 세포는 다음의 마커, TCR Va24-Ja18, Vb11, CD1d, CD3, CD4, CD8, aGalCer, CD161 및 CD56 중 적어도 하나 이상의 발현에 의해 확인될 수 있다.
본 명세서에 사용되는 바와 같은 용어 "단리된" 등은 이의 본래 환경으로부터 분리된 세포 또는 세포의 집단을 지칭하고, 즉, 단리된 세포의 환경은 "비-단리된" 참조 세포가 존재하는 환경에서 발견되는 바와 같은 적어도 하나의 성분이 실질적으로 없다. 이 용어는 이것이 이의 자연 환경에서 발견되고, 예를 들어, 조직 또는 생검물 샘플에서 단리되는 바와 같은 일부 또는 모든 성분으로부터 제거된 세포를 포함한다. 이 용어는 또한 세포가 비-자연 발생 환경에서 발견되고, 예를 들어, 세포 배양물 또는 세포 현탁물로부터 단리되는 바와 같은 적어도 하나의, 일부의 또는 모든 성분으로부터 제거된 세포를 포함한다. 따라서, 단리된 세포는 이것이 자연에서 발견되는 바와 같은 또는 이것이 비-자연 발생 환경에서 성장, 저장 또는 존재하는 바와 같은, 다른 물질, 세포 또는 세포 집단을 비롯한 적어도 하나의 성분으로부터 부분적으로 또는 완전히 분리된다. 단리된 세포의 구체적인 예는 부분적으로 순수한 세포 조성물, 실질적으로 순수한 세포 조성물 및 비-자연 발생인 배지에서 배양된 세포를 포함한다. 단리된 세포는 목적하는 세포 또는 이의 집단을 환경에서의 다른 물질 또는 세포로부터 분리하거나, 또는 하나 이상의 다른 세포 집단 또는 하위집단을 환경으로부터 제거함으로써 수득될 수 있다.
본 명세서에 사용되는 바와 같은 용어 "순도" 등은 순도를 증가시키는 것을 지칭한다. 예를 들어 순도는 적어도 50%, 60%, 70%, 80%, 90%, 95%, 99%, 또는 100%로 증가될 수 있다.
본 명세서에 사용되는 바와 같은 용어 "암호화"는 뉴클레오타이드(즉, rRNA, tRNA 및 mRNA)의 정의된 서열 또는 아미노산의 정의된 서열 중 어느 하나 및 그로부터 생성된 생물학적 특성을 갖는 생물학적 과정에서 다른 중합체 및 거대분자의 합성을 위한 주형으로서 기능하는 폴리뉴클레오타이드, 예컨대 유전자, cDNA, 또는 mRNA에서의 뉴클레오타이드의 특이적 서열의 고유 특성을 지칭한다. 따라서, 유전자는, 그 유전자에 상응하는 mRNA의 전사 및 번역이 세포 또는 다른 생물계에서 단백질을 생산하는 경우 단백질을 암호화한다. 유전자 또는 cDNA의 전사를 위한 템플레이트로서 사용되는, 뉴클레오타이드 서열이 mRNA 서열과 동일하고, 통상적으로 서열 목록으로 제공되는 암호 가닥, 및 비-암호 가닥 둘 모두는 그 유전자 또는 cDNA의 단백질 또는 다른 산물을 암호화한다고 지칭될 수 있다.
"작제물"은 시험관내 또는 생체내에서 숙주 세포에 전달될 폴리뉴클레오타이드를 포함하는 거대분자 또는 분자의 복합체를 지칭한다. "벡터"는 본 명세서에 사용되는 바와 같이 외부 유전 물질의 표적 세포로의 전달 또는 이송을 안내할 수 있는 임의의 핵산 작제물을 지칭하고, 여기서 그것은 복제 및/또는 발현될 수 있다. 용어 "벡터"는 본 명세서에 사용되는 바와 같이 전달될 작제물을 포함한다. 벡터는 선형 또는 원형 분자일 수 있다. 벡터는 통합 또는 비통합될 수 있다. 벡터의 주요 유형은 플라스미드, 에피솜 벡터, 바이러스 벡터, 코스미드 및 인공 염색체를 포함하지만 이들로 제한되지 않는다. 바이러스 벡터는 아데노바이러스 벡터, 아데노-연관 바이러스 벡터, 레트로바이러스 벡터, 렌티바이러스 벡터, 센다이 바이러스 벡터 등을 포함하지만 이들로 제한되지 않는다.
"통합"이라는 것은, 작제물의 하나 이상의 뉴클레오타이드가 세포 게놈 내로 안정하게 삽입되는 것, 즉 세포의 염색체 DNA 내의 핵산 서열에 공유 연결되는 것을 의미한다. "표적화된 통합"이라는 것은, 작제물의 뉴클레오타이드(들)이 미리-선택된 부위 또는 "통합 부위"에서 세포의 염색체 또는 미토콘드리아 DNA에 삽입되는 것을 의미한다. 용어 "통합"은 본 명세서에 사용되는 바와 같이 통합 부위에서 내인성 서열 또는 뉴클레오타이드의 결실이 있거나 또는 결실이 없는, 작제물의 1종 이상의 외인성 서열 또는 뉴클레오타이드의 삽입에 관련된 과정을 추가로 지칭한다. 이 경우, 삽입 부위 내에 결실이 존재하는 경우, "통합"은 하나 이상의 삽입된 뉴클레오타이드가 결실된 내인성 서열 또는 뉴클레오타이드의 대체를 추가로 포함할 수 있다.
본 명세서에 사용되는 바와 같은 용어 "외인성"은 언급된 분자 또는 언급된 활성이 숙주 세포에 도입되거나 숙주 세포에 대해서 비-네이티브인 것을 의미하도록 의도된다. 분자는 예를 들어, 암호화 핵산을 숙주 유전 물질에 도입함으로써, 예컨대 숙주 염색체에 또는 비-염색체 유전 물질, 예컨대 플라스미드로서 통합시킴으로써 도입될 수 있다. 따라서, 암호화 핵산의 발현과 관련하여 사용되는 바와 같이 이 용어는 발현성 형태의 암호화 핵산의 세포로의 도입을 지칭한다. 용어 "내인성"은 숙수 세포에 존재하는 언급된 분자 또는 활성을 지칭한다. 유사하게, 암호화 핵산의 발현과 관련하여 사용되는 경우 이 용어는 외인성으로 도입된 것이 아닌 세포 내에 함유된 암호화 핵산의 발현을 지칭한다.
본 명세서에 사용되는 바와 같이, "관심 유전자" 또는 "관심 폴리뉴클레오타이드 서열"은 RNA로 전사되고, 일부예에서는 적절한 조절 서열의 제어 하에서 일어나는 경우 생체내에서 폴리펩타이드로 번역되는 DNA 서열이다. 관심대상 유전자 또는 폴리뉴클레오타이드는 원핵생물 서열, 진핵생물 mRNA로부터의 cDNA, 진핵생물(예를 들어 포유동물) DNA로부터의 게놈 DNA 서열 및 합성 DNA 서열을 포함할 수 있지만, 이들로 제한되지 않는다. 예를 들어, 관심 유전자는 miRNA, shRNA, 네이티브 폴리펩타이드(즉, 자연에서 발견되는 폴리펩타이드) 또는 이의 단편; 변이체 폴리펩타이드(즉, 네이티브 폴리펩타이드와 100% 미만의 서열 동일성을 갖는 네이티브 폴리펩타이드의 돌연변이) 또는 이의 단편; 조작된 폴리펩타이드 또는 펩타이드 단편, 치료 펩타이드 또는 폴리펩타이드, 영상화 마커, 선택성 마커 등을 암호화할 수 있다.
본 명세서에 사용되는 바와 같은 용어 "폴리뉴클레오타이드"는 데옥시리보뉴클레오타이드 또는 리보뉴클레오타이드 또는 이들의 유사체인, 임의의 길이의 뉴클레오타이드의 중합체 형태를 지칭한다. 폴리뉴클레오타이드의 서열은 4개의 뉴클레오타이드 염기: 아데닌(A); 사이토신(C); 구아닌(G); 티민(T); 및 폴리뉴클레오타이드가 RNA인 경우 티민에 대해서 우라실(U)으로 구성된다. 폴리뉴클레오타이드는 유전자 또는 유전자 단편(예를 들어, 프로브, 프라이머, EST 또는 SAGE 태그), 엑손, 인트론, 메신저 RNA(mRNA), 트랜스퍼 RNA, 리보솜 RNA, 리보자임, cDNA, 재조합 폴리뉴클레오타이드, 분지형 폴리뉴클레오타이드, 플라스미드, 벡터, 임의의 서열의 단리된 DNA, 임의의 서열의 단리된 RNA, 핵산 프로브 및 프라이머를 포함할 수 있다. 폴리뉴클레오타이드는 또한 이중-가닥 분자 및 단일-가닥 분자 둘 모두를 지칭한다.
본 명세서에 사용되는 바와 같은 용어 "펩타이드", "폴리펩타이드", 및 "단백질"은 상호 호환적으로 사용되고, 펩타이드 결합에 의해서 공유 연결된 아미노산 잔기를 갖는 분자를 지칭한다. 폴리펩타이드는 적어도 2개의 아미노산을 함유해야 하고, 폴리펩타이드의 아미노산의 최대 수에는 제한이 없다. 본 명세서에 사용되는 바와 같은 용어는 또한 일반적으로 관련 기술 분야에서 예를 들어, 펩타이드, 올리고펩타이드 및 올리고머라 지칭되는 단쇄, 및 일반적으로 관련 기술 분야에서 폴리펩타이드 또는 단백질이라 지칭되는 장쇄 둘 모두를 지칭한다. "폴리펩타이드"는 예를 들어, 특히 생물학적 활성 단편, 실질적으로 상동성인 폴리펩타이드, 올리고펩타이드, 동종이량체, 이종이량체, 폴리펩타이드의 변이체, 변형된 폴리펩타이드, 유도체, 유사체, 융합 단백질을 포함한다. 폴리펩타이드는 자연 폴리펩타이드, 재조합 폴리펩타이드, 합성 폴리펩타이드 또는 이들의 조합물을 포함한다.
"작동 가능하게-연결된"은 하나의 기능이 서로에 의해서 영향을 받도록 하는 단일 핵산 단편 상에서의 핵산 서열의 회합을 지칭한다. 예를 들어, 프로모터는 그것이 그 암호 서열 또는 기능성 RNA의 발현에 영향을 줄 수 있는 경우(즉, 암호 서열 또는 기능성 RNA가 프로모터의 전사 제어 하에 있는 경우) 암호 서열 또는 기능성 RNA와 작동 가능하게-연결된다. 암호 서열은 센스 또는 안티센스 방향으로 조절 서열에 작동 가능하게-연결될 수 있다.
본 명세서에 사용되는 바와 같은 용어 "유전자 각인"은 공급원 세포 또는 iPSC에서 우선적 치료적 속성에 기여하는 유전적 또는 후성적 정보를 지칭하고, 공급원 세포 유래 iPSC 및/또는 iPSC-유래 조혈 계통 세포에서 유지 가능하다. 본 명세서에 사용되는 바와 같은, "공급원 세포"는 재프로그래밍을 통해 iPSC를 생성하기 위해 사용될 수 있는 비만능 세포이고, 공급원 세포 유래 iPSC는 임의의 조혈 계통 세포를 포함하는 특정 세포 유형으로 추가로 분화될 수 있다. 공급원 세포 유래 iPSC, 및 그것으로부터의 분화 세포는 때때로 맥락에 따라서 "유래" 또는 "유도체" 세포로 총괄적으로 불린다. 예를 들어, 유도체 효과기 세포 또는 유도체 NK 세포 또는 유도체 T 세포는 본 출원 전체에서 사용된 바와 같이, 자연/네이티브 공급원, 예컨대, 말초 혈액, 제대혈 또는 다른 공여자 조직으로부터 획득된 이의 1차 상대물과 비교할 때 iPSC로부터 분화된 세포이다. 우선적 치료 속성을 부여하는 본 명세서에 사용되는 바와 같은 유전자 각인(들)은 공여자-, 질환- 또는 치료 반응-특이적인 선택된 공급원 세포의 재프로그래밍을 통해 또는 게놈 편집을 이용하여 유전자 변형된 양상을 iPSC에 도입하는 것을 통해 iPSC 내에 혼입된다. 구체적으로 선택된 공여자, 질환 또는 치료 내용으로부터 얻은 공급원 세포의 양상에서, 우선적 치료적 속성에 기여하는 유전자 각인은 동정되든 아니든 근본적인 분자 사건과 상관없이 선택된 공급원 세포의 유도 세포 상에서 통과된 유지 가능한 표현형, 즉, 우선적 치료 속성을 나타내는 임의의 내용 특이적인 유전적 또는 후성적 변형을 포함할 수 있다. 공여자-, 질환- 또는 치료 반응- 특이적 공급원 세포는 iPSC에서 유지 가능한 유전자 각인 및 유래된 조혈 계통 세포를 포함할 수 있으며, 이 유전자 각인은, 예를 들어, 바이러스 특이적 T 세포 또는 비변이체 자연 살해 T(iNKT) 세포로부터의 사전 배열된 단일 특이적 TCR; 추적할 수 있는 그리고 바람직한 유전적 다형성, 예를 들어, 선택된 공여자에서 고친화도 CD16 수용체를 암호화하는 점 돌연변이에 대한 동형접합성; 및 사전 결정된 HLA 필요, 즉, 증가된 집단을 갖는 단상형을 나타내는 선택된 HLA-매칭된 공여자 세포를 포함하지만, 이들로 제한되지 않는다. 본 명세서에 사용되는 바와 같이, 우선적 치료적 속성은 유래된 세포의 개선된 생착, 수송, 귀소, 생존도, 자기-재생, 지속성, 면역 반응 조절 및 조정, 생존 및 세포독성을 포함한다. 우선적 치료 속성은 또한 항원 표적화 수용체 발현; HLA 제시 또는 이의 결여; 종양 미세환경에 대한 내성; 방관자 면역 세포 및 면역 조정의 유도; 종양을 벗어난 효과가 감소된 개선된 표적에 대한 특이성; 화학요법과 같은 치료에 대한 내성에 관한 것일 수 있다.
본 명세서에 사용되는 바와 같은 용어 "향상된 치료적 특성"은 동일한 일반적 세포 유형의 전형적 면역 세포에 비해 향상된 세포의 치료적 특성을 지칭한다. 예를 들어, "치료적 특성"을 갖는 NK 세포는 전형적, 비변형 및/또는 자연 유래 NK 세포에 비해 향상된, 개선된 그리고/또는 증가된 치료적 특성을 가질 것이다. T면역 세포의 치료적 특성은 세포 생착, 수송, 귀소, 생존도, 자기-재생, 지속성, 면역 반응 조절 및 조정, 생존 및 세포독성을 포함할 수 있지만, 이들로 제한되지 않는다. 면역 세포의 치료적 특성은 또한 항원 표적화 수용체 발현; HLA 제시 또는 이의 결여; 종양 미세환경에 대한 내성; 방관자 면역 세포 및 면역 조정의 유도; 종양을 벗어난 효과가 감소된 개선된 표적에 대한 특이성; 화학요법과 같은 치료에 대한 내성에 의해 나타낸다.
본 명세서에 사용되는 바와 같은 용어 "관여자"는 면역 세포, 예를 들어, T 세포, NK 세포, NKT 세포, B 세포, 대식세포, 호중구 및 종양 세포 사이에 연결을 형성할 수 있고; 면역 세포를 활성화시킬 수 있는 분자, 예를 들어 융합 폴리펩타이드를 지칭한다. 관여자의 예는 이중 특이적 T 세포 관여자(BiTE), 이중 특이적 살해 세포 관여자(BiKE), 삼중 특이적 살해 세포 관여자 또는 다중 특이적 살해 세포 관여자 또는 다중 면역 세포 유형과 상용성인 보편적 관여자를 포함하지만, 이들로 제한되지 않는다.
본 명세서에 사용되는 바와 같은 용어 "표면 촉발 수용체"는 면역 반응, 예를 들어, 세포독성 반응을 촉발시키거나 또는 개시할 수 있는 수용체를 지칭한다. 표면 촉발 수용체는 조작될 수 있고, 효과기 세포, 예를 들어, T 세포, NK 세포, NKT 세포, B 세포, 대식세포, 호중구 상에서 발현될 수 있다. 일부 실시형태에서, 표면 촉발 수용체는 효과기 세포의 자연적 수용체 및 세포 유형과 독립적인 효과기 세포와 특정 표적 세포 예를 들어, 종양 세포 사이의 이중- 또는 다중-특이적 항체 맞물림을 용이하게 한다. 이 접근을 사용하여, 보편적 표면 촉발 수용체를 포함하는 iPSC를 생성할 수 있고, 이어서, 이러한 iPSC를 보편적 표면 촉발 수용체를 발현시키는 다양한 효과기 세포 유형의 집단으로 분화시킬 수 있다. "보편적"은 표면 촉발 수용체가 세포 유형과 상관 없이 임의의 효과기 세포에서 발현되고, 활성화시킬 수 있으며, 보편적 수용체를 발현시키는 모든 효과기 세포는 관여자의 종양 결합 특이성과 상관없이 표면 촉발 수용체에 의해 인식될 수 있는 동일한 에피토프를 갖는 관여자에 결합되거나 또는 연결될 수 있다는 것을 의미한다. 일부 실시형태에서, 동일한 종양 표적화 특이성을 갖는 관여자는 보편적 표면 촉발 수용체와 결합하기 위해 사용된다. 일부 실시형태에서, 상이한 종양 표적화 특이성을 갖는 관여자는 보편적 표면 촉발 수용체와 결합하기 위해 사용된다. 이렇게 해서, 하나 또는 다중 효과기 세포 유형은 일부 경우에 종양 세포의 하나의 특정 유형을 사멸시키기 위해 그리고 일부 다른 경우에 2 이상의 유형의 종양을 사멸시키기 위해 관여될 수 있다. 표면 촉발 수용체는 일반적으로 효과기 세포 활성화를 위한 공자극 도메인 및 관여자의 에피토프에 특이적인 항-에피토프를 포함한다. 이중 특이성 관여자는 한 말단 상에서 표면 촉발 수용체의 항-에피토프에 특이적이고, 다른 말단 상에서 종양 항원에 특이적이다.
본 명세서에 사용되는 바와 같은 용어 "안전 스위치 단백질"은 세포 요법의 잠재적인 독성 또는 다른 유해 효과를 방지하도록 설계된 조작 단백질을 지칭한다. 일부 상황에서, 안전 스위치 단백질 발현은 안전 스위치 단백질을 그의 게놈으로 암호화하는 유전자 내에 영구적으로 혼입된 이식 조작 세포에 대한 안전 문제를 처리하기 위해 조건적으로 제어된다. 이 조건적 조절은 가변적일 수 있고, 소분자-매개 번역 후 활성화 및 조직-특이적 및/또는 일시적 전사 조절을 통한 제어를 포함할 수 있다. 안전 스위치는 세포자멸사의 저해, 단백질 합성의 저해, DNA 복제, 성장 저지, 전사 및 전사 후 유전적 조절 및/또는 항체-매개 고갈을 매개할 수 있었다. 일부 예에서, 안전 스위치 단백질은 활성화될 때 치료 세포의 세포자멸사 및/또는 세포사를 촉발시키는 외인성 분자, 예를 들어, 전구약물에 의해 활성화된다. 안전 스위치 단백질의 예는 자살 유전자, 예컨대, 카스파제 9(또는 카스파제 3 또는 7), 티미딘 카이나제, 사이토신 데아미나제, B-세포 CD20, 변형된 EGFR 및 이들의 임의의 조합물을 포함하지만 이들로 제한되지 않는다. 이 전략에서, 유해 사건이 있는 경우에 투여되는 전구약물은 자살-유전자 산물에 의해 활성화되고, 형질도입 세포를 사멸시킨다.
본 명세서에 사용되는 바와 같은 용어 "약제학적으로 활성인 단백질 또는 펩타이드"는 유기체에 대한 생물학적 및/또는 약제학적 효과를 달성할 수 있는 단백질 또는 펩타이드를 지칭한다. 약제학적으로 활성인 단백질은 질환에 대한 치유하는 근치적 또는 고식적 특성을 가지며, 질환의 중증도를 개선시키거나, 경감시키거나, 완화시키거나, 반전시키거나 또는 줄이기 위해 투여될 수 있다. 약제학적으로 활성인 단백질은 또한 예방적 특성을 가지며, 질환의 개시를 방지하기 위해 또는 그것이 생길 때 이러한 질환 또는 병리적 병태의 중증도를 줄이기 위해 사용된다. 약제학적으로 활성인 단백질은 전체 단백질 또는 펩타이드 또는 이의 약제학적으로 활성인 단편을 포함한다. 또한 단백질 또는 펩타이드의 약제학적으로 활성인 유사체 또는 단백질 또는 펩타이드의 단편의 유사체를 포함한다. 용어 약제학적으로 활성인 단백질은 또한 치료적 이점을 제공하기 위해 협력적으로 또는 상승적으로 작용하는 복수의 단백질 또는 펩타이드를 지칭한다. 약제학적으로 활성인 단백질 또는 펩타이드의 예는 수용체, 결합 단백질, 전사 및 번역 인자, 종양 성장 억제 단백질, 항체 또는 이의 단편, 성장 인자 및/또는 사이토카인을 포함하지만, 이들로 제한되지 않는다.
본 명세서에 사용되는 바와 같은 용어 "신호전달 분자"는 세포 신호 형질도입을 조절하거나, 이에 참여하거나, 저해하거나, 활성화시키거나, 감소시키거나 또는 증가시키는 임의의 분자를 지칭한다. 신호 형질도입은 세포에서 생화학적 사건을 궁극적으로 촉발시키는 경로를 따라서 단백질 복합체의 동원에 의한 화학적 변형의 형태로 분자 신호의 전달을 지칭한다. 신호 형질도입 경로는 관련 기술 분야에 잘 공지되어 있고, G 단백질 결합 수용체 신호전달, 타이로신 카이나제 수용체 신호전달, 인테그린 신호전달, 톨 게이트 신호전달, 리간드-개폐 이온 통로 신호전달, ERK/MAPK 신호전달 경로, Wnt 신호전달 경로, cAMP-의존적인 경로, 및 IP3/DAG 신호전달 경로를 포함하지만, 이들로 제한되지 않는다.
본 명세서에 사용되는 바와 같은 용어 "표적화 양상"은 i) 독특한 키메라 항원 수용체(CAR) 또는 T 세포 수용체(TCR)와 관련된 항원 특이성, ii) 단클론성 항체 또는 이중특이성 관여자와 관련된 관여자 특이성, iii) 형질전환 세포의 표적화, iv) 암 줄기세포의 표적화, 및 v) 특정 항원 또는 표면 분자의 부재 하에서의 다른 표적화 전략을 포함하지만, 이들로 제한되지 않는 항원 및/또는 에피토프 특이성을 촉진시키기 위해 세포 내에 유전적으로 혼입된 분자, 예를 들어, 폴리펩타이드를 지칭한다.
본 명세서에 사용되는 바와 같은 용어 "특이적" 또는 "특이성"은 비특이적 또는 비선택적 결합과 대조적으로 표적 분자에 선택적으로 결합하는 분자, 예를 들어 수용체 또는 관여자의 능력을 지칭하기 위해 사용될 수 있다.
본 명세서에 사용되는 바와 같은 용어 "입양 세포 요법"은 본 명세서에 사용되는 바와 같이, 상기 형질도입 전에 생체외에서 확장된 유전자 변형된 또는 변형되지 않은 T 또는 B 세포로서 동정된 자가 또는 동종이계 림프구의 형질도입에 관한 세포 기반 면역요법을 지칭한다.
본 명세서에 사용되는 바와 같은 "치료적으로 충분한 양"은 그의 의미 내에서 비독성이지만 충분하고 그리고/또는 유효한 양의 특정 치료적 및/또는 약제학적 조성물을 포함하며, 목적으로 하는 치료 효과를 제공하는 것을 언급한다. 필요한 정확한 양은 환자의 일반적 건강상태, 환자의 연령 및 병기 및 병태의 중증도와 같은 인자에 따라서 대상체에 따라 달라질 것이다. 특정 실시형태에서, 치료적으로 충분한 양은 치료 중인 대상체의 질환 또는 병태와 관련된 적어도 하나의 증상을 개선시키고/시키거나, 감소시키고/시키거나 좋아지게 하는데 충분하고/하거나 효과적이다.
만능 줄기세포의 분화는 배양 시스템의 변화, 예컨대 배양 배지 또는 tHE 세포의 물리적 상태에서 자극제의 변화를 필요로 한다. 가장 통상적인 전략은 계통-특이적 분화를 개시하기 위해 통상적이고 중요한 중간체로서 배상체(EB)의 형성을 이용한다. "배상체"는 그들의 3차원 면적 내에서 수많은 계통을 생기게 하기 때문에 배아 발생을 모방하는 것으로 나타난 3차원 클러스터이다. 분화 과정, 전형적으로 몇 시간 내지 며칠을 통해, 단순한 EB(예를 들어, 응집된 만능 줄기세포는 분화하도록 유발됨)는 성숙을 계속하고, 그들이 추가로 분화를 계속하도록 진행되는 시간, 전형적으로 며칠 내지 몇주에 낭포성 EB로 발생된다. 세포의 3차원 다층 클러스터에서 만능 줄기세포가 서로 근접하게 함으로써 EB 형성이 개시되며, 전형적으로 이는 만능 세포가 액적 중의 침전을 허용하는 단계, 세포를 "U"형 바닥 웰-플레이트 내로 또는 기계적 교반에 의해 침전시키는 단계를 포함하는 몇몇 방법 중 하나에 의해 달성된다. EB 발생을 촉진시키기 위해, 만능 줄기세포 응집물은 추가적인 분화 신호가 필요한데, 만능성 배양물 유지 배지 내에 유지된 응집물이 적절한 EB를 형성하지 않기 때문이다. 이렇게 해서, 만능 줄기세포 응집물은 선택 계통에 대한 유발 신호를 제공하는 분화 배지로 전달될 필요가 있다. 만능 줄기세포의 EB-기반 배양물은 전형적으로 EB 세포 클러스터 내에서 보통의 증식을 갖는 분화된 세포 집단(외배엽, 중배엽 및 내배엽의 배엽)의 생성을 초래한다. 세포 분화를 용이하게 하는 것으로 증명되었지만, 그러나 EB는 3차원 구조에서 tHE 세포의 환경으로부터의 분화 신호에 대한관 일치되지 않는 노출 때문에 가변성 분화 상태로 이종성 세포가 생기게 한다. 추가로, EB는 생성 및 유지하는 데 힘이 든다. 게다가, EB를 통한 세포 분화는 보통 세포 확장을 수반하는데, 이는 또한 낮은 분화 효율에 기여한다.
비교하면, "EB 형성"과 별개인 "응집물 형성"은 만능 줄기세포 유래 세포의 집단을 확장시키는 데 사용될 수 있다. 예를 들어, 응집물-기반 만능 줄기세포 확장 동안, 배양 배지는 증식 및 만능성을 유지하도록 선택된다. 세포 증식은 일반적으로 응집물의 크기를 증가시켜 더 큰 응집물을 형성하고, 이들 응집물은 배양물 내의 세포 증식을 유지시키기 위해 그리고 세포 수를 증가시키기 위해 더 작은 응집물로 일상적으로 기계적으로 또는 효소적으로 해리될 수 있다. EB 배양물과 별개로, 유지 배양물 중의 응집물 내에서 배양된 세포는 만능성 마커를 유지한다. 만능 줄기세포 응집물은 분화를 유도하기 위한 추가적인 분화 신호를 필요로 한다.
본 명세서에 사용되는 바와 같이, "단일층 분화"는 세포의 3차원 다층 클러스터, 즉, "형성"을 통한 분화와 별개인 분화 방법을 지칭하는 용어이다. 단일층 분화, 본 명세서에 개시된 이점 중에서, 분화 개시를 위한 EB 형성에 대한 필요를 회피한다. 단일층 배양은 배아 발생, 예컨대 EB 형성을 모방하지 않기 때문에, 특정 계통에 대한 분화는 EB에서의 모두 3가지 배엽 분화에 비해 최소인 것으로 여겨진다.
본 명세서에 사용되는 바와 같은, "해리된" 세포는 다른 세포로부터 또는 표면(예를 들어, 배양 플레이트 표면)으로부터 실질적으로 분리되거나 또는 정제된 세포를 지칭한다. 예를 들어, 세포는 기계적 또는 효소적 방법에 의해 동물 또는 조직으로부터 해리될 수 있다. 대안적으로, 시험관내에서 응집하는 세포는 서로로부터, 예컨대 클러스터, 단일 세포 또는 단일 세포와 클러스터의 혼합물의 현탁액으로 해리에 의해 효소적으로 또는 기계적으로 해리될 수 있다. 또 다른 대안의 실시형태에서, 부착 세포는 배양 플레이트 또는 다른 표면으로부터 해리된다. 따라서 해리는 세포외 기질(ECM) 및 기질(예를 들어, 배양 표면)과의 세포 상호작용을 파괴하는 것 또는 세포 사이의 ECM을 파괴하는 것을 수반할 수 있다.
본 명세서에 사용되는 바와 같이, "피더 세포" 또는 "피더"는 피더 세포가 제2 세포 유형의 지지체에 대한 자극, 성장 인자 및 영양소를 제공하기 때문에 제2 유형의 세포가 성장, 확장 분화할 수 있는 환경을 제공하는 제2 유형의 세포와 함께 공동배양되는 한 가지 유형의 세포를 기재하는 용어이다. 피더 세포는 그들의 지지하는 세포와 상이한 종으로부터 선택적으로 유래된다. 예를 들어, 줄기세포를 포함하는 특정 유형의 인간 세포는 마우스 배아 섬유아세포, 또는 불멸 마우스 배아 섬유아세포의 1차 배양물에 의해 지지될 수 있다. 또 다른 예에서, 말초 혈액 유래된 세포 또는 형질전환된 백혈병 세포는 자연 살해 세포의 확장 및 성숙을 지지한다. 피더 세포는 그들이 지지하는 세포보다 더 커지는 것을 방지하기 위해 방사선 조사 또는 항-유사분열제, 예컨대 미토마이신에 의한 처리에 의해 다른 세포와 함께 공동배양시킬 때 전형적으로 비활성화될 수 있다. 피더 세포는 내피 세포, 기질 세포(예를 들어, 상피 세포 또는 섬유아세포) 및 백혈병 세포를 포함할 수 있다. 앞서 언급한 것으로 제한하는 일 없이, 한 가지의 특정 피더 세포 유형은 인간 피더, 예컨대 인간 피부 섬유아세포일 수 있다. 다른 피더 세포 유형은 마우스 배아 섬유아세포(MEF)일 수 있다. 일반적으로, 다양한 피더 세포는 만능성을 유지시키고, 특정 계통에 대한 분화를 지시하고, 증식 능력을 향상시키고, 전문화된 세포 유형, 예컨대, 효과기 세포로의 성숙을 촉진시키기 위해서 부분적으로 사용될 수 있다.
본 명세서에 사용되는 바와 같은, "피더-무함유"(feeder-free: FF) 환경은 피더 또는 기질 세포가 본질적으로 없고, 그리고/또는 피더 세포의 배양에 의해 사전 조건화되지 않은 배양 조건, 세포 배양물 또는 배양 배지와 같은 환경을 지칭한다. "사전 조건화된" 배지는 피더 세포가 시간 기간 동안, 예컨대 적어도 1일 동안 배지 내에서 배양된 후에 채취된 배지를 지칭한다. 사전 조건화된 배지는 배지에서 배양된 피더 세포에 의해 분화된 성장 인자 및 사이토카인을 포함하는 다수의 매개체 물질을 함유한다. 일부 실시형태에서, 피더-무함유 환경은 피더 또는 기질 세포 둘 다가 없고, 또한 피더 세포의 배양에 의해서 사전 조건화되지 않는다.
"기능성"은, iPSC 및 그로부터 분화된 유래된 비-만능 세포의 게놈 편집 또는 변형, 또는 비-만능 세포 및 그로부터 재프로그래밍된 유래된 iPSC의 게놈 편집 또는 변형의 맥락에서 사용되는 바와 같이, (1) 유전자 수준에서는--성공적인 넉-인, 넉-아웃, 넉-다운 유전자 발현, 유전자 이식된 또는 제어된 유전자 발현, 예컨대 목적하는 세포 발생 단계에서 유도성 또는 일시적 발현(이것은 직접적인 게놈 편집 또는 변형을 통해서 또는 초기에 게놈 조작된 출발 세포로부터의 분화 또는 출발 세포의 재프로그래밍을 통한 "패싱-온(passing-on)"을 통해서 달성됨)을 지칭하거나; 또는 (2) 세포 수준에서는 -(i) 직접적인 게놈 편집을 통해서 상기 세포에서 수득된 유전자 발현 변형, (ii) 초기에 게놈 조작된 출발 세포로부터의 분화 또는 출발 세포의 재프로그래밍을 통한 "패싱-온"을 통해서 상기 세포에서 유지된 유전자 발현 별형; (iii) 상기 세포의 초기 발달 단계에서만 보이거나, 또는 분화 또는 재프로그래밍을 통해서 상기 세포를 생성시키는 출발 세포에서만 보이는 유전자 발현 변형의 결과로서의 상기 세포에서의 하류 유전자 조절; 또는 (iv) iPSC, 전구체 또는 탈분화된 세포 기원에서 수행된 게놈 편집 또는 변형으로부터 초기에 유래된, 성숙 세포 산물 내에 나타난 향상되거나 또는 새로 성취된 세포 기능 또는 속성을 통해서 세포 기능/특징을 성공적으로 제거, 부가 또는 변경한 것을 지칭한다.
HLA-클래스 I 결핍, 또는 HLA-클래스 II 결핍, 또는 둘 모두를 비롯한, "HLA 결핍"은 HLA 클래스 I 단백질 이종이량체 및/또는 HLA 클래스 II 이종이량체를 포함하는 완전한 MHC 복합체의 표면 발현이 결여되거나 또는 더이상 유지되지 않거나 또는 감소되어, 줄어들거나 또는 감소된 수준이 다른 세포에 의해서 또는 합성 방법에 의해서 자연적으로 검출 가능한 수준보다 낮은, 세포를 지칭한다.
"변형된 HLA 결핍 iPSC"는 본 명세서에 사용되는 바와 같이, 개선된 분화 가능성, 항원 표적화, 항원 제시, 항체 인식, 지속성, 면역 회피, 억제에 대한 내성, 증식, 공자극, 사이토카인 자극, 사이토카인 생산(오토크린 또는 파라크린), 주화성, 및 세포 세포독성, 예컨대 비-고전적 HLA 클래스 I 단백질(예를 들어, HLA-E 및 HLA-G), 키메라 항원 수용체(CAR), T 세포 수용체(TCR), CD16 Fc 수용체, BCL11b, NOTCH, RUNX1, IL15, 41BB, DAP10, DAP12, CD24, CD3z, 41BBL, CD47, CD113 및 PDL1로 제한되지 않는 관련된 단백질을 발현하는 유전자를 도입함으로써 추가로 변형된 HLA 결핍 iPSC를 지칭한다. "변형된 HLA 결핍"된 세포는 iPSC가 아닌 세포를 또한 포함한다.
FcR로 약칭되는 "Fc 수용체"는 그것이 인식한 항체의 유형을 기반으로 분류된다. 예를 들어, 항체의 가장 일반적인 클래스, IgG에 결합하는 것은 Fc-감마 수용체(FcγR)라 지칭되며, IgA에 결합하는 것은 Fc-알파 수용체(FcαR)라 지칭되고, IgE에 결합하는 것은 Fc-엡실론 수용체(FcεR)라 지칭된다. FcR의 클래스는 또한 이를 발현하는 세포(대식세포, 과립구, 자연 살해 세포, T 및 B 세포) 및 각각의 수용체의 신호전달 특성에 의해서 구별된다. Fc-감마 수용체(FcγR)는 몇몇 구성원, FcγRI(CD64), FcγRIIA(CD32), FcγRIIB(CD32), FcγRIIIA(CD16a), FcγRIIIB(CD16b)을 포함하는데, 이것은 이의 상이한 분자 구조로 인해서 이의 항체 친화도가 상이하다.
CFcR로 약칭되는 "키메라 Fc 수용체"는 변형된 네이티브 막관통 및/또는 세포내 신호전달 도메인을 갖거나, 비-네이티브 막관통 및/또는 세포내 신호전달 도메인으로 대체된 조작된 Fc 도메인을 기재하기 위해서 사용되는 용어이다. 키메라 Fc 수용체의 일부 실시형태에서, 비-네이티브인 막관통 도메인 및 신호전달 도메인 중 하나 또는 둘 다를 갖는 것에 더하여, 세포 활성화, 수용체의 촉발 시 확장 및 기능을 향상시키기 위해서 하나 이상의 자극성 도메인이 조작된 Fc 수용체의 세포내 부분에 도입될 수 있다. 표적 항원에 대한 항원 결합 도메인을 함유하는 키메라 항원 수용체(CAR)와 달리, 키메라 Fc 수용체는 표적화된 세포를 근접하게 가까이 두거나 가까이 두지 않으면서 Fc 단편 또는 항체의 Fc 영역 또는 관여자 또는 결합 분자에 포함되고 세포 기능을 활성화시키는 Fc 영역에 결합한다. 예를 들어, Fcγ 수용체는 세포외 도메인에서 IgG의 결합에 반응하는 세포내 영역에 선택된 막관통 도메인, 자극성 도메인 및/또는 신호전달 도메인을 포함하여 CFcR을 생성시키도록 조작될 수 있다. 일례에서, CFcR은 CD16, Fcγ 수용체를 조작함으로써, 이의 막관통 도메인 및/또는 세포내 도메인을 대체함으로써 생산된다. CD16 기반 CFcR의 결합 친화도를 추가로 개선시키기 위해서, CD64 또는 CD16의 고친화도 변이체의 세포외 도메인(예를 들어, F176V)이 혼입될 수 있다. 고 친화도 CD16 세포외 도메인이 관여되는 CFcR의 일부 실시형태에서, 197번 위치에 세린을 포함하는 단백질분해 절단 부위는 제거되거나 또는 수용체의 세포외 도메인이 비-절단성이도록, 즉 쉐딩(shedding)되어 않아서 hnCD16 기반 CFcR을 얻도록 대체된다.
CD16, FcγR 수용체는 두 아이소폼, Fc 수용체 FcγRIIIa(CD16a) 및 FcγRIIIb(CD16b)를 갖는 것으로 식별되었다. CD16a는 표적 세포에 부착된 단량체 IgG에 결합하여 NK 세포를 활성화시켜 항체-의존적인 세포-매개된 세포독성(ADCC)을 가능하게 하는, NK 세포에 의해서 발현된 막관통 단백질이다. "고 친화도 CD16", "비-절단성 CD16", 또는 "고 친화도 비-절단성 CD16(hnCD16)"은, 본 명세서에서 사용되는 바와 같이, CD16의 자연 또는 비자연 변이체를 지칭한다. 야생형 CD16은 낮은 친화도를 갖고, NK 세포 활성화 시 백혈구 상의 다양한 세포 표면 분자의 세포 표면 밀도를 조절하는 단백질분해 절단 과정인, 엑토도메인 쉐딩에 적용된다. F176V 및 F158V는 높은 친화도를 갖는 예시적인 CD16 다형성 변이체이다. 변경된 또는 제거된 막-근위 영역(189 내지 212번 위치)에서 절단 부위(195 내지 198번 위치)를 갖는 CD16 변이체는 쉐딩에 적용되지 않는다. 절단 부위 및 막-근위 영역은 국제 특허 공개 제WO2015148926호에 상세하게 기재되어 있고, 이의 완전한 개시내용은 본 명세서에 참조에 의해서 포함된다. CD16 S197P 변이체는 조작된 CD16의 비-절단성 버전이다. F158V 및 S197P 둘 다를 포함하는 CD16 변이체는 높은 친화도를 갖고, 비-절단성이다. 또 다른 예시적인 고 친화도 및 비-절단성 CD16(hnCD16) 변이체는 CD64 엑토도메인의 3개의 엑손 중 하나 이상으로부터 유래된 엑토도메인을 포함하는 조작된 CD16이다.
I. 향상된 특성을 갖는 입양 세포 요법에 유용한 세포 및 조성물
본 명세서에는 유도체 세포의 치료 특성을 향상시키면서, iPSC의 분화 효력 및 iPSC 및 이의 유도체 세포의 세포 발달 생물학에 영향을 미치지 않고 클론성 iPSC의 조절 회로를 체계적으로 조작하기 위한 전략이 제공된다. 유도체 세포는 기능적으로 개선되고, 게놈 조작을 통해서 iPSC의 수준에서 세포에 도입될 선택적 양상의 조합 후 입양 세포 요법에 적합하다. 본 발명 이전에는, 하나 이상의 제고된 유전자 편집을 포함하는 변경된 iPSC가 조절된 활성을 유지하면서 세포 발달 및/또는 성숙에 들어가고/가거나 기능적으로 분화된 세포를 생성시키는 능력을 여전히 갖는지가 불명확하였다. iPSC로부터의 유도된 세포 분화 동안 예상치 못한 실패는, 발달 단계 특이적 유전자 발현 또는 이의 결핍, HLA 복합체 제시에 대한 요건, 도입된 표면 발현 양상의 단백질 쉐딩 및 세포에서 표현형 및/또는 기능성 변화를 가능하게 하는 분화 프로토콜의 재구성에 대한 필요성을 포함하지만 이들로 제한되지 않는 양상에 기여되었다. 본 출원은 본 명세서에 제공된 바와 같은 하나 이상의 선택된 게놈 변형이 iPSC 분화 효력에 부정적으로 영향을 미치지 않고, 조작된 iPSC로부터 유래된 기능성 효과기 세포가 iPSC 분화 이후에 효과기 세포에서 보유된 개별 또는 조합된 게놈 변형에 기인한 향상된 및/또는 획득된 치료 특성을 가짐을 나타내었다.
1. hnCD16 넉-인(knock-in)
CD16은 두 아이소폼, Fc 수용체 FcγRIIIa(CD16a; NM_000569.6) 및 FcγRIIIb(CD16b; NM_000570.4)로서 식별되어 있다. CD16a는 표적 세포에 부착된 단량체 IgG에 결합하여 NK 세포를 활성화시켜 항체-의존적인 세포-매개된 세포독성(ADCC)을 가능하게 하는, NK 세포에 의해서 발현된 막관통 단백질이다. CD16b는 인간 호중구에 의해서 독점적으로 발현된다. "고 친화도 CD16", "비-절단성 CD16", 또는 "고 친화도 비-절단성 CD16"은 본 명세서에서 사용된 바와 같이 다양한 CD16 변이체를 지칭한다. 야생형 CD16은 낮은 친화도를 갖고, NK 세포 활성화 시 백혈구 상의 다양한 세포 표면 분자의 세포 표면 밀도를 조절하는 단백질분해 절단 과정인, 엑토도메인 쉐딩에 적용된다. F176V(일부 간행물에서 F158V라고도 불림)는 높은 친화도를 갖는 예시적인 CD16 다형성 변이체이지만; S197P 변이체는 CD16의 유전자 조작된 비-절단성 버전의 예이다. F176V 및 S197P 둘 다를 포함하는 조작된 CD16 변이체는 높은 친화도를 갖고, 비-절단성인데, 이것은 전체 개시내용이 본 명세서에 참조에 의해 포함된 국제 특허 공개 제WO2015/148926호에 더 상세하게 기재되었다. 또한, CD64 엑토도메인의 적어도 일부로 본질적으로 대체된 CD16의 엑토도메인을 갖는 키메라 CD16 수용체는 또한 ADCC를 수행할 수 있는 CD16 수용체의 목적하는 높은 친화도 및 비-절단성 특징을 달성할 수 있다. 일부 실시형태에서, 키메라 CD16의 교체 엑토도메인은 CD64(UniPRotKB_P12314 또는 이의 아이소폼 또는 다형성 변이체)의 EC1, EC2 및 EC3 엑손 중 하나 이상을 포함한다.
이와 같이, 고-친화도 비-절단성 CD16 수용체(hnCD16)는 일부 실시형태에서 F176V 및 S197P 둘 다를 포함하고; 일부 실시형태에서, F176V를 포함하고, 절단 영역이 제거되어 있다. 일부 다른 실시형태에서, hnCD16은 예시적인 서열, 서열번호 1 내지 3(각각은 CD64 엑토도메인의 적어도 일부를 포함함) 중 임의의 것과 비교할 때 적어도 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 99%, 100% 또는 그 사이의 임의의 백분율의 동일성을 갖는 서열을 포함한다. 서열번호 1 내지 3은 각각 서열번호 4 내지 6을 예시함으로써 암호화된다. 본 명세서 및 본 출원 전체에서 사용되는 바와 같이, 두 서열 간의 동일성 백분율은 두 서열의 최적의 정렬을 위해 도입될 필요가 있는 갭의 수 및 각각의 갭의 길이를 고려하여, 서열에 의해서 공유된 동일한 위치의 수의 함수이다(즉, 동일성 % = 동일한 위치의 수/위치의 총 수 ×100). 두 서열 간의 서열의 비교 및 동일성 백분율의 결정은 당업계에 인식된 수학적 알고리즘을 사용하여 달성될 수 있다.
따라서, 본 명세서에는 다른 편집 중에서 본 명세서에서 고려되고 기술된 바와 같이 고-친화도 비-절단성 CD16 수용체(hnCD16)를 포함하도록 유전자 조작된 클론성 iPSC가 제공되며, 여기서 유전자 조작된 iPSC는 iPSC에 도입된 hnCD16을 포함하는 효과기 세포로 분화될 수 있다. 일부 실시형태에서, hnCD16을 포함하는 유래된 효과기 세포는 NK 세포이다. 일부 실시형태에서, hnCD16을 포함하는 유래된 효과기 세포는 T 세포이다. iPSC 또는 이의 유도체 세포에서 발현되는 외인성 hnCD16은 ADCC 항체 또는 이의 단편, 뿐만 아니라 상기 hnCD16의 CD16 또는 CD64 세포외 결합 도메인을 인식하는 이중, 삼중 또는 다중 특이적 관여자 또는 결합기에 대한 결합 시에 높은 친화도를 갖는다. 이중, 삼중 또는 다중 특이적 관여자 또는 결합기는 본 출원에서 하기에 추가로 기재되어 있다(섹션 I.6 참조). 이와 같이, 본 출원은 유도체 효과기 세포 상에서 발현되는 hnCD16의 세포외 도메인과의 고-친화도 결합을 통해서 하나 이상의 미리 선택된 ADCC 항체가 미리 로딩된 유도체 효과기 세포 또는 이의 세포 집단을, 하기 섹션 V.에 추가로 상세하게 기재된 바와 같이 병태, 질환 또는 감염의 치료에서 치료 용도에 충분한 양으로 제공하며, 여기서 상기 hnCD16은 F176V 및 S197P를 갖는 CD64 또는 CD16의 세포외 결합 도메인을 포함한다.
일부 다른 실시형태에서, hnCD16의 네이티브 CD16 막관통- 및/또는 세포내- 도메인은, 키메라 Fc 수용체(CFcR)가 비-네이티브 막관통 도메인, 비-네이티브 자극성 도메인 및/또는 비-네이티브 신호전달 도메인을 포함하기 위해서 생산되도록 추가로 변형 또는 대체된다. 본 명세서에 사용된 용어 "비-네이티브"는 막관통, 자극성 또는 신호전달 도메인이 세포외 도메인을 제공하는 수용체 이외의 상이한 수용체로부터 유래됨을 의미한다. 본 명세서의 예시에서, CD16 또는 이의 변이체를 기반으로 하는 CFcR은 CD16으로부터 유래된 막관통, 자극성 또는 신호전달 도메인을 갖지 않는다. 일부 실시형태에서, 외인성 hnCD16 기반 CFcR은 CD3D, CD3E, CD3G, CD3ζ, CD4, CD8, CD8a, CD8b, CD27, CD28, CD40, CD84, CD166, 4-1BB, OX40, ICOS, ICAM-1, CTLA-4, PD-1, LAG-3, 2B4, BTLA, CD16, IL7, IL12, IL15, KIR2DL4, KIR2DS1, NKp30, NKp44, NKp46, NKG2C, NKG2D, T 세포 수용체 폴리펩타이드로부터 유래된다. 일부 실시형태에서, 외인성 hnCD16 기반 CFcR은 CD27, CD28, 4-1BB, OX40, ICOS, PD-1, LAG-3, 2B4, BTLA, DAP10, DAP12, CTLA-4 또는 NKG2D 폴리펩타이드로부터 유래된 비-네이티브 자극성/저해성 도메인을 포함한다. 일부 실시형태에서, 외인성 hnCD16 기반 CFcR은 CD3ζ, 2B4, DAP10, DAP12, DNAM1, CD137(41BB), IL21, IL7, IL12, IL15, NKp30, NKp44, NKp46, NKG2C, 또는 NKG2D 폴리펩타이드로부터 유래된 비-네이티브 신호전달 도메인을 포함한다. hnCD16의 일 실시형태에서, 제공된 키메라 수용체는 막관통 도메인 및 신호전달 도메인을 포함하는데, 둘 다는 IL7, IL12, IL15, NKp30, NKp44, NKp46, NKG2C 및 NKG2D 폴리펩타이드 중 하나로부터 유래된다. hnCD16 기반 키메라 Fc 수용체의 특정 일 실시형태는 NKG2D의 막관통 도메인, 2B4의 자극성 도메인 및 CD3ζ의 신호전달 도메인을 포함하며; 여기서 hnCD16의 세포외 도메인은 CD64 또는 CD16의 세포외 도메인의 전체 길이 또는 부분 서열로부터 유래되고, 여기서 CD16의 세포외 도메인은 F176V 및 S197P를 포함한다. hnCD16 기반 키메라 Fc 수용체의 또 다른 실시형태는 CD3ζ의 막관통 도메인 및 신호전달 도메인을 포함하며; 여기서 hnCD16의 세포외 도메인은 CD64 또는 CD16의 세포외 도메인의 전체 길이 또는 부분 서열로부터 유래되고, 여기서 CD16의 세포외 도메인은 F176V 및 S197P를 포함한다.
상기에 기재된 바와 같은 hnCD16 기반 키메라 Fc 수용체의 다양한 실시형태는 높은 친화도로 항체의 Fc 영역 또는 이의 단편; 또는 이중, 삼중 또는 다중 특이적 관여자 또는 결합기의 Fc 영역에 결합할 수 있다. 결합 시, 키메라 수용체의 자극성 및/또는 신호전달 도메인은 효과기 세포의 활성화 및 사이토카인 분비 및 항체 또는 종양 항원 결합 성분 및 Fc 영역을 갖는 상기 이중, 삼중 또는 다중 특이적 관여자 또는 결합기에 의해서 표적화된 종양 세포의 사멸을 가능하게 한다. 이론에 얽매이고자 함은 아니지만, 비-네이티브 막관통, 자극성 및/또는 신호전달 도메인을 통해서, 또는 hnCD16 기반 키메라 Fc 수용체의 엑토도메인에 대한 관여자 결합을 통해서, CFcR은 효과기 세포의 증식 및/또는 확장 가능성을 증가시키면서, 효과기 세포의 사멸 능력에 기여할 수 있다. 항체 및 관여자는 항원을 발현하는 종양 세포 및 CFcR을 발현하는 효과기 세포를 근접하게 할 수 있는데, 이것은 또한 종양 세포의 향상된 사멸에 기여한다. 이중, 삼중, 다중 특이적 관여자 또는 결합기에 대한 예시적인 종양 항원은 B7H3, BCMA, CD10, CD19, CD20, CD22, CD24, CD30, CD33, CD34, CD38, CD44, CD79a, CD79b, CD123, CD138, CD179b, CEA, CLEC12A, CS-1, DLL3, EGFR, EGFRvIII, EPCAM, FLT-3, FOLR1, FOLR3, GD2, gpA33, HER2, HM1.24, LGR5, MSLN, MCSP, MICA/B, PSMA, PAMA, P-카드헤린 및 ROR1을 포함하지만 이들로 제한되지 않는다. 종양 세포 공격에서 hnCD16 기반 CFcR을 발현하는 효과기 세포를 결속시키기에 적합한 일부 비제한적인 예시적인 이중, 삼중, 다중 특이적 관여자 또는 결합기는 CD16(또는 CD64)-CD30, CD16(또는 CD64)-BCMA, CD16(또는 CD64)-IL15-EPCAM 및 CD16(또는 CD64)-IL15-CD33을 포함한다.
NK 세포 활성화 후 세포 표면으로부터 절단되는 1차 NK 세포에 의해서 발현되는 내인성 CD16 수용체와 달리, 유도체 NK에서 CD16의 비-절단성 버전은 CD16 쉐딩을 회피하고, 일정한 발현을 유지한다. 유도체 NK 세포에서, 비-절단성 CD16은 개선된 세포 기능성을 나타내는 TNFα 및 CD107a의 발현을 증가시킨다. 비-절단성 CD16은 또한 항체-의존적 세포-매개된 세포독성(ADCC) 및 이중, 삼중 또는 다중 특이적 관여자의 관여를 향상시킨다. ADCC는 항체-코팅된 표적 세포에 대한 CD16의 결합을 통한 NK 세포 매개된 용해의 기전이다. 유래된 NK 세포에서 도입된 hnCD16의 추가적인 고 친화도 특징은 또한 세포 요법을 필요로 하는 대상체에게 세포를 투여하기 전에 hnCD16을 통해서 NK 세포에 ADCC 항체를 시험관내에서 로딩하는 것을 가능하게 한다. 제공된 바와 같이, hnCD16은 일부 실시형태에서 F176V 및 S197P를 포함할 수 있거나 또는 서열번호 1, 2 또는 3으로 예시된 바와 같은 CD64로부터 유래된 전체 또는 부분 엑토도메인을 포함할 수 있거나 또는 비-네이티브 막관통 도메인, 자극성 도메인 및 신호전달 도메인 중 적어도 하나를 추가로 포함할 수 있다. 개시된 바와 같이, 본 출원은 또한 하나 이상의 미리 선택된 ADCC 항체가 하기 V.에 추가로 상세하게 기재된 바와 같이 병태, 질환 또는 감염의 치료에서의 치료 용도에 충분한 양으로 로딩된 유도체 NK 세포 또는 이의 세포 집단을 제공한다.
1차 NK 세포와 달리, 1차 공급원(즉, 자연/네이티브 공급원, 예컨대, 말초 혈액, 제대혈 또는 다른 공여자 조직)으로부터의 성숙 T 세포는 CD16을 발현하지 않는다. 발현된 외인성 비-절단성 CD16을 포함하는 iPSC가 T 세포 발달 생물학을 손상시키지 않고, 외인성 CD16을 발현할 뿐만 아니라, 획득된 ADCC 기전을 통해서 기능을 수행할 수 있는 기능성 유도체 T 세포로 분화할 수 있다는 것은 예상치 못한 것이었다. 유도체 T 세포에서의 이러한 획득된 ADCC는 이중 표적화 및/또는 CAR-T 세포 요법으로 종종 발생하는 항원 탈출을 구제하기 위한 접근법으로서 추가로 사용될 수 있고, 여기서 종양은 감소된 또는 손실된 CAR-T 표적화 항원 발현 또는 CAR(키메라 항원 수용체)에 의한 인식을 회피하기 위한 돌연변이된 항원의 발현으로 재발한다. 상기 유도체 T 세포가 외인성 CD16 발현을 통해서 획득된 ADCC를 포함하는 경우, 항체가 CAR에 의해서 표적화된 것과 상이한 종양 항원을 표적화하는 경우, 항체는 CAR-T 항원 탈출을 구제하기 위해서 그리고 CAR-T 치료에서 종종 관찰되는 표적화된 종양의 재발 또는 재발생을 감소시키거나 예방하기 위해서 사용될 수 있다. 이중 표적화를 달성하면서 항원 탈출을 감소시키고/시키거나 예방하기 위한 이러한 전략은 하나 이상의 CAR을 발현하는 NK 세포에 동등하게 적용 가능하다. 이러한 항원 탈출 감소 및 예방에 사용될 수 있는 다양한 CAR이 하기에 추가로 기술된다.
이와 같이, 본 발명은 외인성 CD16을 포함하는 유도체 T 세포를 제공한다. 일부 실시형태에서, 유도체 T 세포에 포함된 hnCD16은 F176V 및 S197P를 포함한다. 일부 다른 실시형태에서, 유도체 T 세포에 포함된 hnCD16은 서열번호 1, 2 또는 3으로 예시된 바와 같은 CD64로부터 기원된 전체 또는 부분 엑토도메인을 포함하거나, 비-네이티브 막관통 도메인, 자극성 도메인 및 신호전달 도메인 중 적어도 하나를 추가로 포함할 수 있다. 설명된 바와 같이, 이러한 유도체 T 세포는 항체의 치료 효과를 향상시키기 위해서 ADCC에 의해서 매개된 단클론성 항체로 종양을 표적화하기 위한 획득된 기전을 갖는다. 개시된 바와 같이, 본 출원은 또한 하나 이상의 미리 선택된 ADCC 항체가 하기 V.에 추가로 상세하게 기재된 바와 같이 병태, 질환 또는 감염의 치료에서의 치료 용도에 충분한 양으로 로딩된 유도체 T 세포 또는 이의 세포 집단을 제공한다.
2. CAR 발현
유전자 조작된 iPSC 및 이의 유도체 효과기 세포에 적용 가능한 것은 당업계에 공지된 임의의 CAR 설계일 수 있다. CAR, 키메라 항원 수용체는 일반적으로 항원 인식 영역을 포함하는 엑토도메인, 막관통 도메인, 및 엔도-도메인을 포함하는 융합 단백질이다. 일부 실시형태에서, 엑토도메인은 단일 펩타이드 또는 리더(leader) 서열 및/또는 스페이서를 추가로 포함할 수 있다. 일부 실시형태에서, 엔도-도메인은 CAR을 발현하는 효과기 세포를 활성화시키는 신호전달 펩타이드를 추가로 포함할 수 있다. 일부 실시형태에서, 항원 인식 도메인은 항원에 특이적으로 결합할 수 있다. 일부 실시형태에서, 항원 인식 도메인은 질환 또는 병원체와 연관된 항원에 특이적으로 결합할 수 있다. 일부 실시형태에서, 질환-연관된 항원은 종양 항원이며, 여기서 종양은 액체 또는 고형 종양일 수 있다. 일부 실시형태에서, CAR은 상기 CAR을 발현하는 T 또는 NK 세포를 활성화시키기에 적합하다. 일부 실시형태에서, CAR은 NK-특이적 신호전달 성분을 포함하는 것에 대해서 NK 세포 특이적이다. 특정 실시형태에서, 상기 T 세포는 CAR 발현 iPSC로부터 유래되고, 유도체 T 세포는 T 헬퍼 세포, 세포독성 T 세포, 기억 T 세포, 조절 T 세포, 자연 살해 T 세포, αβ T 세포, γδ T 세포 또는 이들의 조합물을 포함할 수 있다. 특정 실시형태에서, 상기 NK 세포는 CAR 발현 iPSC로부터 유래된다.
특정 실시형태에서, 상기 항원 인식 영역은 뮤린 항체, 인간 항체, 인간화된 항체, 낙타 Ig, 상어 중쇄-단독 항체(VNAR), Ig NAR, 키메라 항체, 재조합 항체 또는 이의 항체 단편을 포함한다. 항체 단편의 비제한적인 예는 Fab, Fab', F(ab)'2, F(ab)'3, Fv, 단일 쇄 항원 결합 단편(scFv), (scFv)2, 다이설파이드 안정화된 Fv(dsFv), 미니바디, 다이아바디, 트라이아바디, 테트라바디, 단일-도메인 항원 결합 단편(sdAb, 나노바디), 재조합 중쇄-단독 항체(VHH) 및 전체 항체의 결합 특이성을 유지하는 다른 항체 단편을 포함한다. CAR에 의해서 표적화될 수 있는 항원의 비제한적인 예는 ADGRE2, 탄산 탈수효소 IX(CAlX), CCRI, CCR4, 암배아 항원(CEA), CD3, CD5, CD7, CD8, CD10, CD19, CD20, CD22, CD30, CD33, CD34, CD38, CD41, CD44, CD44V6, CD49f, CD56, CD70, CD74, CD99, CD123, CD133, CD138, CD269(BCMA), CDS, CLEC12A, 사이토메갈로바이러스(CMV) 감염된 세포의 항원(예를 들어, 세포 표면 항원), 상피 당단백질2(EGP 2), 상피 당단백질-40(EGP-40), 상피 세포 접착 분자(EpCAM), EGFRvIII, 수용체 타이로신-단백질 카이나제 erb-B2,3,4, EGFIR, EGFR-VIII, ERBB 엽산염-결합 단백질(FBP), 태아 아세틸콜린 수용체(AChR), 엽산염 수용체-a, 강글리오사이드 G2(GD2), 강글리오사이드 G3(GD3), 인간 표피 성장 인자 수용체 2(HER-2), 인간 텔로머라제 역전사효소(hTERT), ICAM-1, 인테그린 B7, 인터류킨-13 수용체 소단위 알파-2(IL-13Rα2), κ-경쇄, 카이나제 삽입 도메인 수용체(KDR), Lewis A(CA19.9), Lewis Y(LeY), L1 세포 접착 분자(L1-CAM), LILRB2, 흑색종 항원 패밀리 A 1(MAGE-A1), MICA/B, 뮤신 1(Muc-1), 뮤신 16(Muc-16), 메소텔린(MSLN), NKCSI, NKG2D 리간드, c-Met, 암-고환 항원 NY-ESO-1, 종양태아성 항원(h5T4), PRAME, 전립선 줄기세포 항원(PSCA), PRAME 전립선-특이적 막 항원(PSMA), 종양-연관 당단백질 72(TAG-72), TIM-3, TRBCI, TRBC2, 혈관 내피 성장 인자 R2(VEGF-R2), 빌름스 종양 단백질(WT-1) 및 당업계에 공지된 다양한 병원체 항원을 포함한다. 병원체의 비제한적인 예는 질환을 유발할 수 있는 바이러스, 박테리아, 진균, 기생충 및 원생동물을 포함한다.
일부 실시형태에서, CAR의 막관통 도메인은 CD3D, CD3E, CD3G, CD3ζ, CD4, CD8, CD8a, CD8b, CD27, CD28, CD40, CD84, CD166, 4-1BB, OX40, ICOS, ICAM-1, CTLA-4, PD-1, LAG-3, 2B4, BTLA, CD16, IL7, IL12, IL15, KIR2DL4, KIR2DS1, NKp30, NKp44, NKp46, NKG2C, NKG2D, T 세포 수용체 폴리펩타이드의 네이티브 또는 변형된 막관통 영역의 전체 길이 또는 적어도 일부를 포함한다.
일부 실시형태에서, 엔도-도메인(또는 세포내 도메인)의 신호전달 펩타이드는 CD3ζ, 2B4, DAP10, DAP12, DNAM1, CD137 (41BB), IL21, IL7, IL12, IL15, NKp30, NKp44, NKp46, NKG2C 또는 NKG2D의 폴리펩타이드의 전체 길이 또는 적어도 일부를 포함한다. 일 실시형태에서, CAR의 신호전달 펩타이드는 CD3ζ의 적어도 하나의 ITAM(면역수용체 타이로신-기반 활성화 모티프)과 적어도 약 85%, 약 90%, 약 95%, 약 96%, 약 97%, 약 98% 또는 약 99% 동일한 아미노산 서열을 포함한다.
특정 실시형태에서, 상기 엔도-도메인은 적어도 하나의 공자극성 신호전달 영역을 추가로 포함한다. 상기 공자극성 신호전달 영역은 CD27, CD28, 4-1BB, OX40, ICOS, PD-1, LAG-3, 2B4, BTLA, DAP10, DAP12, CTLA-4 또는 NKG2D 또는 이들의 임의의 조합물의 폴리펩타이드의 전체 길이 또는 적어도 일부를 포함할 수 있다. 일 실시형태에서, 본 출원에 제공된 세포에 적용 가능한 CAR은 CD28로부터 유래된 공자극성 도메인 및 서열번호 7과 적어도 약 85%, 약 90%, 약 95%, 약 96%, 약 97%, 약 98% 또는 약 99% 동일한 아미노산 서열로 표현되는, CD3ζ의 네이티브 또는 변형된 ITAM1을 포함하는 신호전달 도메인을 포함한다. 추가 실시형태에서, CD28로부터 유래된 공자극성 도메인, 및 CD3ζ의 네이티브 또는 변형된 ITAM1을 포함하는 CAR은 또한 CD28로부터 유래된 힌지 도메인 및 막관통 도메인을 포함하고, 여기서 scFv는 힌지를 통해서 막관통 도메인에 연결될 수 있고, CAR은 서열번호 8의 적어도 약 85%, 약 90%, 약 95%, 약 96%, 약 97%, 약 98% 또는 약 99% 동일한 아미노산 서열을 포함한다.
또 다른 실시형태에서, 본 출원에 제공된 세포에 적용 가능한 CAR은 NKG2D로부터 유래된 막관통 도메인, 2B4로부터 유래된 공자극성 도메인 및 서열번호 9와 적어도 약 85%, 약 90%, 약 95%, 약 96%, 약 97%, 약 98% 또는 약 99% 동일한 아미노산 서열로 표현되는, 네이티브 또는 변형된 CD3ζ를 포함하는 신호전달 도메인을 포함한다. NKG2D로부터 유래된 막관통 도메인, 2B4로부터 유래된 공자극성 도메인 및 네이티브 또는 변형된 CD3ζ를 포함하는 신호전달 도메인을 포함하는 상기 CAR은 CD8 힌지를 추가로 포함할 수 있고, 여기서 이러한 구조의 아미노산 서열은 서열번호 10과 적어도 약 85%, 약 90%, 약 95%, 약 96%, 약 97%, 약 98% 또는 약 99% 동일성을 갖는다.
비제한적인 CAR 전략은 한 쌍의 세포내 도메인의 이량체화를 통한 이종이량체, 조건화 활성화된 CAR(예를 들어, 미국 특허 제9587020호 참고); 스플리트 CAR을 추가로 포함하고, 여기서 CAR을 생성시키기 위한 항원 결합, 힌지 및 엔도-도메인의 상동 재조합(예를 들어, 미국 특허 공개 제20170183407호 참고); 각각 항원 결합 도메인 및 신호전달 도메인에 연결된 두 막관통 도메인 간의 비공유 연결을 허용하는 멀티-쇄 CAR(예를 들어, 미국 특허 공개 제20140134142호 참고); 이중특이적 항원 결합 도메인을 갖는 CAR(예를 들어, 미국 특허 제9447194호 참고), 또는 동일하거나 또는 상이한 항원 또는 에피토프를 인식하는 한 쌍의 항원 결합 도메인을 갖는 CAR(예를 들어, 미국 특허 제8409577호) 또는 탠덤 CAR(예를 들어, 문헌[Hegde et al., J Clin Invest. 2016;126(8):3036-3052]); 유도성 CAR(예를 들어, 미국 특허 공개 제20160046700호, 제20160058857호, 제20170166877호); 전환 가능한 CAR(예를 들어, 미국 특허 공개 제20140219975호); 및 당업계에 공개된 임의의 다른 설계를 추가로 포함한다.
따라서 본 명세서는 게놈 조작된 iPSC의 분화로부터 획득된 유도체 세포를 포함하고, 여기서 iPSC 및 유도체 세포 둘 다는 외인성 hnCD16의 발현을 포함하지만 이들로 제한되지 않는 추가적인 변형된 양상과 함께 하나 이상의 CAR을 포함한다. 특정 일 실시형태에서, iPSC 및 이의 유도체 세포는 hnCD16, 및 선택된 종양 또는 바이러스 항원을 표적으로 하는 CAR을 포함하고, 여기서 유도체 세포는 NK 또는 T 세포이고, 여기서 유도체 세포는 동일한 종양의 이중 표적화를 달성하면서, hnCD16 결합을 통해서, 종양 항원 탈출을 회피하거나 감소시키기 위해서 CAR에 의해서 표적화된 것과 상이한 종양 항원을 표적으로 하는 하나 이상의 ADCC 항체 또는 이중, 삼중 또는 다중 특이적 관여자와 함께 사용될 수 있다. 추가 실시형태에서, CAR을 포함하는 iPSC 및 이의 유도체 T 세포는 TCR 불변 영역에 삽입된 CAR을 갖고, TCR 넉 아웃으로 이어지고, 내인성 TCR 프로모터의 제어 하에서 CAR 발현을 배치한다. 일부 실시형태에서, 조작된 iPSC로부터 유래된 유도체 TCR 널 CAR-T 세포는 CD16에 네이티브인 엑토도메인(F176V 및/또는 S197P)을 갖거나 또는 CD64로부터 유래된 hnCD16, 및 네이티브 또는 비-네이티브 막관통, 자극성 및 신호전달 도메인을 추가로 포함한다. 또 다른 실시형태에서, CAR을 포함하는 iPSC 및 이의 유도체 NK 세포는 NKG2A 유전자좌 또는 NKG2D 유전자좌에 삽입된 CAR을 갖고, NKG2A 또는 NKG2D 넉 아웃으로 이어지고, 내인성 NKG2A 또는 NKG2D 프로모터의 제어 하에서 CAR 발현을 배치한다.
3. 외인성으로 도입된 사이토카인 및/또는 사이토카인 신호전달
임상적으로 관련된 사이토카인의 체계적인 고용량 투여를 회피함으로써, 사이토카인 매개된 세포 자율성이 확립되면서, 이러한 실시로 인한 용량-제한적인 독성의 위험이 감소된다. 가용성 사이토카인을 추가로 투여할 필요성 없이, 림프구 자율성을 달성하기 위해서, IL2, IL4, IL6, IL7, IL9, IL10, IL11, IL12, IL15, IL18, IL21 및/또는 이들 각각의 수용체 중 하나 이상의 부분 또는 전체 펩타이드가 사이토카인 자체의 발현과 함께 또는 발현 없이 사이토카인 신호전달을 가능하게 하기 위해서 세포에 도입되고, 이에 의해서 사이토카인 독성의 위험 감소와 함께 세포 성장, 증식, 확장 및/또는 효과기 기능을 유지시키거나 개선시킨다. 일부 실시형태에서, 사이토카인 신호전달을 위한 도입된 사이토카인 및/또는 이의 각각의 네이티브 또는 변형된 수용체가 세포 표면 상에서 발현된다. 일부 실시형태에서, 사이토카인 신호전달은 구성적으로 활성화된다. 일부 실시형태에서, 사이토카인 신호전달의 활성화는 유도성이다. 일부 실시형태에서, 사이토카인 신호전달의 활성화는 일시적이고/이거나 순간적이다.
도 1은 예시적인 예로서 IL15를 사용하는 몇몇 작제물 설계를 제공한다. 도 1에서 설계 중 임의의 것의 막관통(TM) 도메인은 IL15 수용체에 대해서 네이티브일 수 있거나, 또는 임의의 다른 막 결합된 단백질의 막관통 도메인으로 변형 또는 대체될 수 있다.
설계 1: IL15 및 IL15Rα는 IL15의 시스-제시를 제거하지 않으면서, 자가-절단 펩타이드를 사용하고, IL15의 트랜스-제시를 모방함으로써 공동 발현된다.
설계 2: IL15Rα는 IL15 막-결합되는 것을 보장할 뿐만 아니라 IL15의 시스-제시를 제거하지 않으면서, 링커를 통해서 C-말단에서 IL15에 융합되고, 트랜스-제시를 모방한다. 재조합 단백질은 서열번호 11과 적어도 약 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% 또는 99% 동일한 아미노산 서열을 포함하고, 재조합 단백질은 신호 펩타이드의 하류에서 IL15 pro-펩타이드를 포함한다. 서열번호 12는 서열번호 11의 아미노산 서열을 암호화하는 예시적인 DNA 서열을 기재한다.
설계 3: 절두된 세포내 도메인을 갖는 IL15Rα는 링커를 통해서 C-말단에서 IL15에 융합되고, IL15의 트랜스-제시를 모방하고, IL15 막-결합되는 것을 유지하고, 추가로 잠재적인 시스-제시를 추가로 제거한다. 이러한 작제물은 서열번호 13에 적어도 75%, 80%, 85%, 90%, 95% 또는 99% 동일성의 아미노산 서열을 포함하고, 이것은 서열번호 14로 표현되는 예시적인 핵산 서열에 의해서 암호화될 수 있다.
당업자는 상기 신호 펩타이드 및 링커 서열이 예시적이고, 어떠한 방식으로도 신호 펩타이드 또는 링커로서 사용하기에 적합한 그들의 변이를 제한하지 않음을 이해할 것이다. 당업계에 공지되고 이용 가능한 다수의 적합한 신호 펩타이드 또는 링커 서열이 존재한다. 당업자는 신호 펩타이드 및/또는 링커 서열이 신호 펩타이드에 의해서 유도되거나 링커에 의해서 연결된 기능성 펩타이드의 활성을 변경시키지 않으면서 또 다른 서열 대신 치환될 수 있다는 것을 이해한다.
설계 4: 설계 3 작제물이 효과기 세포 생존 및 확장의 촉진에서 기능성인 것으로 나타났는데, 이는 IL15Rα의 세포질 도메인이 이러한 설계에서 IL15가 구비된 효과기 세포의 자율 특징부에 부정적으로 영향을 미치지 않으면서 누락될 수 있다는 것을 입증하기 때문에, 설계 4는 설계 3의 또 다른 작업 대안을 제공하는 작제물인데, 이로부터 본질적으로 전체 IL15Rα는 스시 도메인을 제외하고는 제거되고, 선택적으로 스시 도메인과 막관통 도메인 사이에 링커를 사용하여 한 단부에서 IL15와 그리고 다른 단부(mb-스시)에서 막관통 도메인과 융합된다. 융합된 IL5/mb-스시는 임의의 막 결합된 단백질의 막관통 도메인을 통해서 세포 표면에서 발현된다. 작제물, 예컨대, 설계 4를 사용하여, 시스-제시를 비롯한 IL15Rα를 통한 불필요한 신호전달은 단지 IL15의 목적하는 트랜스-제시가 유지될 때만 제거된다. 일부 실시형태에서, 스시 도메인과 융합된 IL15를 포함하는 성분은 서열번호 15와 적어도 75%, 80%, 85%, 90%, 95% 또는 99% 동일한 아미노산 서열을 포함하는데, 이것은 서열번호 16으로 표현되는 예시적인 핵산 서열에 의해서 암호화될 수 있다.
당업자는 상기 신호 펩타이드 및 링커 서열이 예시적이고, 어떠한 방식으로도 신호 펩타이드 또는 링커로서 사용하기에 적합한 그들의 변이를 제한하지 않음을 이해할 것이다. 당업계에 공지되고 이용 가능한 다수의 적합한 신호 펩타이드 또는 링커 서열이 존재한다. 당업자는 신호 펩타이드 및/또는 링커 서열이 신호 펩타이드에 의해서 유도되거나 링커에 의해서 연결된 기능성 펩타이드의 활성을 변경시키지 않으면서 또 다른 서열 대신 치환될 수 있다는 것을 이해한다.
설계 5: 네이티브 또는 변형된 IL15Rβ가 링커를 통해서 C-말단에서 IL15에 융합되어, 구성적 신호전달이 가능해지고, IL15 막 결합 및 트랜스-제시를 유지한다.
설계 6: 네이티브 또는 변형된 공통 수용체 γC는 사이토카인의 구성적 신호전달 및 막 결합된 트랜스-제시를 위해서 링커를 통해서 C-말단에서 IL15에 융합된다. 공통 수용체 γC는 또한 공통 감마 쇄 또는 CD132(IL2 수용체 소단위 감마 또는 IL2RG로도 공지됨)라고도 불린다. γC는 IL2, IL4, IL7, IL9, IL15 및 IL21 수용체를 포함하지만 이들로 제한되지 않는 다수의 인터류킨 수용체를 위한 수용체 복합체에 공통적인 사이토카인 수용체 소단위이다.
설계 7: IL15의 부재 하에서 동종이량체를 형성하는 조작된 IL15Rβ는 사이토카인의 구성적 신호전달을 생성시키기에 유용하다.
일부 실시형태에서, 사이토카인 IL2, IL4, IL6, IL7, IL9, IL10, IL11, IL12, IL15, IL18 및 IL21 및/또는 이의 수용체 중 하나 이상은 도 1의 설계 중 하나 이상을 사용하여 iPSC에 도입될 수 있고, iPSC 분화 시에 이의 유도체 세포에 도입될 수 있다. 일부 실시형태에서, IL2 또는 IL15 세포 표면 발현 및 신호전달은 설계 1 내지 7 중 임의의 하나에 예시된 작제물을 통한 것이다. 일부 실시형태에서, IL4, IL7, IL9 또는 IL21 세포 표면 발현 및 신호전달은 공통 수용체 또는 사이토카인 특이적 수용체를 사용함으로써 설계 5, 6 또는 7에 도시된 작제물을 통한 것이다. 도 1에서 설계 중 임의의 것의 막관통(TM) 도메인은 각각의 사이토카인 수용체에 대해서 네이티브일 수 있거나, 또는 임의의 다른 막 결합된 단백질의 막관통 도메인으로 변형 또는 대체될 수 있다.
CAR 및 외인성 사이토카인 및/또는 사이토카인 수용체 신호전달을 포함하는 iPSC 및 그로부터의 유도체 세포에서, CAR 및 IL은 별개의 작제물에서 발현될 수 있거나, CAR 및 IL 둘 다를 포함하는 바이-시스트론성 작제물로 공동발현될 수 있다. 일부 추가 실시형태에서, 도 1의 작제물 설계 중 임의의 것으로 표현되는 형태의 IL15는 예를 들어, CAR-2A-IL15 또는 IL15-2A-CAR로서 예시된 자가-절단 2A 암호 서열을 통해서 CAR 발현 작제물의 5' 또는 3' 단부에 연결될 수 있다. 이와 같이, IL15 및 CAR은 단일 오픈 리딩 프레임(single open reading frame)(ORF)에 존재한다. 일 실시형태에서, CAR-2A-IL15 또는 IL15-2A-CAR 작제물은 도 1의 설계 3의 IL15를 포함한다. 또 다른 실시형태에서, CAR-2A-IL15 또는 IL15-2A-CAR 작제물은 도 1의 설계 3의 IL15를 포함한다. 또 다른 추가 실시형태에서, CAR-2A-IL15 또는 IL15-2A-CAR 작제물은 도 1의 설계 7의 IL15를 포함한다. CAR-2A-IL15 또는 IL15-2A-CAR이 발현되는 경우, 자가-절단 2A 펩타이드는 발현된 CAR 및 IL15이 해리되게 하고, 이어서 해리된 IL15는 세포 표면에 제시될 수 있다. CAR-2A-IL15 또는 IL15-2A-CAR 바이-시스트론성 설계는 시기 및 양 둘 다에서 그리고 예를 들어, 단일 ORF의 발현을 위한 유도성 프로모터를 혼입하도록 선택될 수 있는 동일한 제어 기전 하에서 공동 작용성 CAR 및 IL15 발현을 허용한다. 자가-절단 펩타이드는 아프토바이러스, 예컨대, 구제역 바이러스(FMDV), 말 비염 A 바이러스(ERAV), 토세아 아시그나 바이러스(Thosea asigna virus: TaV) 및 돼지 테스코 바이러스- 1(porcine tescho virus-1: PTV-I)(Donnelly, ML, et al, J. Gen. Virol, 82, 1027-101 (2001); Ryan, MD, et al., J. Gen. Virol., 72, 2727-2732 (2001)) 및 카디오바이러스, 예컨대, 테일로바이러스(예를 들어, 뮤린 뇌척수염(Theiler's murine encephalomyelitis)) 및 뇌심근염 바이러스를 비롯한, 피코나비리대 바이러스 패밀리의 구성원에서 발견된다. FMDV, ERAV, PTV-I 및 TaV로부터 유래된 2 A 펩타이드는 때로는 각각 "F2A", "E2A", "P2A", 및 "T2A"로서도 지칭된다.
IL15에 대해서 본 명세서에 개시된 바와 같은 바이-시스트론성 CAR-2A-IL15 또는 IL15-2A-CAR 실시형태는 또한 본 명세서에 제공된 임의의 다른 사이토카인, 예를 들어, IL2, IL4, IL6, IL7, IL9, IL10, IL11, IL12, IL18 및 IL21의 발현을 위해서 고려된다. 일부 실시형태에서, IL2 세포 표면 발현 및 신호전달은 설계 1 내지 7 중 임의의 것에 예시된 작제물을 통해서이다. 일부 다른 실시형태에서, IL4, IL7, IL9 또는 IL21 세포 표면 발현 및 신호전달은 공통 수용체 및/또는 사이토카인 특이적 수용체를 사용함으로써 설계 5, 6 또는 7에 도시된 작제물을 통한 것이다.
4. HLA-I- 및 HLA-II-결핍
다수의 HLA 클래스 I 및 클래스 II 단백질은 동종이계 거부 문제를 회피하기 위해서 동종이계 수용자에서 조직적합성을 위해서 일치되어야 한다. 본 명세서에는 HLA 클래스 I 및 HLA 클래스 II 단백질 둘 다의 발현이 제거되거나 실질적으로 감소된 iPSC 세포주가 제공된다. HLA 클래스 I 결핍은 HLA 클래스 I 유전자좌(염색체 6p21)의 임의의 영역의 기능성 결실, 또는 베타-2 마이크로글로불린(B2M) 유전자, TAP 1 유전자, TAP 2 유전자 및 타파신을 포함하지만 이들로 제한되지 않는 HLA 클래스-I 연관된 유전자의 발현 수준을 결실 또는 감소시킴으로써 달성된다. 예를 들어, B2M 유전자는 모든 HLA 클래스 I 이종이량체의 세포 표면 발현에 필수적인 공통 소단위를 암호화한다. B2M 널 세포는 HLA-I 결핍성이다. HLA 클래스 II 결핍은 RFXANK, CIITA, RFX5 및 RFXAP를 포함하지만 이들로 제한되지 않는 HLA-II 연관된 유전자의 기능성 결실 또는 감소에 의해서 달성될 수 있다. CIITA는 클래스 II 단백질 발현에 필요한 전사 인자 RFX5의 활성화를 통해서 기능하는 전사 공활성화제이다. CIITA 널 세포는 HLA-II 결핍성이다. 본 명세서에는 B2M 및 CIITA 둘 다가 넉 아웃된 iPSC 주 및 이의 유도체 세포가 제공되며, 여기서 획득된 유도체 효과기 세포는 MHC(주요 조직적합 복합체) 매칭의 필요성을 제거함으로써 동종이계 세포 요법을 가능하게 하고, 숙주(동종이계) T 세포에 의한 인식 및 사멸을 회피한다.
일부 세포 유형의 경우, 클래스 I 발현의 부족은 NK 세포에 의한 용해로 이어진다. 이러한 "자기 미싱(missing self)" 반응을 극복하기 위해서, HLA-G는 NK 세포 인식 및 조작된 iPSC로부터 유래된 HLA-I 및 HLA-II 결핍 효과기 세포의 사멸을 회피하기 위해서 선택적으로 넉 인될 수 있다. 일 실시형태에서, HLA-I 및 HLA-II 결핍 iPSC 및 이의 유도체 세포는 유도체 T 및 NK 세포를 비롯한 유래된 효과기 세포의 기능 및 iPSC의 분화 가능성에 부정적인 영향을 미치지 않으면서 hnCD16, 선택적으로 CAR 및 IL 중 하나 또는 둘 다를 추가로 포함한다.
5. 본 명세서에 제공된 유전자 조작된 iPSC 주 및 유도체 세포
상기에 비추어, 본 출원은 hnCD16 및 CAR 발현 둘 다를 포함하는 iPSC, iPS 세포주 세포 또는 이로부터의 유도체 세포를 제공하며, 여기서 유도체 세포는 hnCD16 및 CAR을 포함하는 iPSC의 분화로부터 획득된 기능성 효과기 세포이다. 일부 실시형태에서, 유도체 세포는 조혈 세포이고, 이것은 확정적 조혈 내피(HE) 가능성을 갖는 중배엽 세포, 확정적 HE, CD34 조혈 세포, 조혈 줄기 및 전구 세포, 조혈 다능성 전구 세포(MPP), T 세포 전구 세포, NK 세포 전구 세포, 골수 세포, 호중구 전구 세포, T 세포, NKT 세포, NK 세포, B 세포, 호중구, 수지상 세포 및 대식세포를 포함하지만 이들로 제한되지 않는다. 일부 실시형태에서, 기능성 유도체 조혈 세포는 효과기 세포, 예컨대, T, NK 및 조절 세포를 포함한다.
일부 실시형태에서, 유도체 세포는 NK 또는 T 세포를 포함한다. hnCD16 및 CAR 둘 다를 포함하는 iPSC 유래된 NK 또는 T 세포는 항체와 CAR 표적화된 치료를 조합함으로써 CAR-T 단독 요법에서 관찰되는 종양 항원 탈출과 연관된 종양 재발을 극복하거나 감소시키기에 유용하되, 단, 항체 및 CAR은 종양의 상이한 항원에 대해서 특이성을 갖는다. hnCD16을 발현하는 유도체 CAR-T 세포는 획득된 ADCC를 가져서, CAR 표적화에 더하여 종양 사멸을 위한 추가 기전을 제공한다. 일부 실시형태에서, 유도체 세포는 NK 세포를 포함한다. hnCD16 및 CAR을 포함하는 iPSC 유래된 NK 세포는 향상된 세포독성을 갖고, 종양 세포를 침윤 및 사멸시키기 위해서 T 세포를 비롯한 방관자 세포를 모집하는데 효과적이다.
추가로 iPSC, iPS 세포주 세포, 또는 이로부터의 유도체 세포가 제공되는데, 이것은 hnCD16을 암호화하는 폴리뉴클레오타이드 및 CAR을 암호화하는 폴리뉴클레오타이드 및 세포 생존, 지속성 및/또는 확장에 기여하는 사이토카인 신호전달을 가능하게 하기 위해서 적어도 하나의 외인성 사이토카인 및/또는 이의 수용체(IL)를 암호화하는 폴리뉴클레오타이드를 포함하며, 여기서 iPSC 주는 개선된 생존, 지속성, 확장 및 효과기 세포 기능을 갖는 기능성 유도체 조혈 세포를 생성하도록 분화를 지시할 수 있다. 외인성으로 도입된 사이토카인 신호전달(들)은 IL2, IL4, IL6, IL7, IL9, IL10, IL11, IL12, IL15, IL18 및 IL21 중 임의의 하나 또는 2개 또는 그 초과의 신호전달을 포함한다. 일부 실시형태에서, 사이토카인 신호전달을 위한 사이토카인 및/또는 이의 각각의 수용체의 도입된 부분 또는 전체 펩타이드는 세포 표면 상에서 발현된다. 일부 실시형태에서, 사이토카인 신호전달은 구성적으로 활성화된다. 일부 실시형태에서, 사이토카인 신호전달의 활성화는 유도성이다. 일부 실시형태에서, 사이토카인 신호전달의 활성화는 일시적이고/이거나 시간적이다. 일부 실시형태에서, 세포 표면 사이토카인/사이토카인 수용체의 일시적/시간적 발현은 레트로바이러스, 센다이 바이러스, 아데노바이러스, 에피솜, 미니-서클 또는 mRNA를 비롯한 RNA를 통해서이다. 일부 실시형태에서, hnCD16/CAR iPSC 또는 이의 유도체 세포에 포함된 외인성 세포 표면 사이토카인 및/또는 수용체는 IL7 신호전달을 가능하게 한다. 일부 실시형태에서, hnCD16/CAR iPSC 또는 이의 유도체 세포에 포함된 외인성 세포 표면 사이토카인 및/또는 수용체는 IL10 신호전달을 가능하게 한다. 일부 실시형태에서, hnCD16/CAR iPSC 또는 이의 유도체 세포에 포함된 외인성 세포 표면 사이토카인 및/또는 수용체는 IL15 신호전달을 가능하게 한다. 상기 hnCD16/CAR/IL iPSC의 일부 실시형태에서, IL15 발현은 도 1의 작제물 3을 통한 것이다. 상기 hnCD16/CAR/IL iPSC의 일부 실시형태에서, IL15 발현은 도 1의 작제물 4를 통한 것이다. 상기 실시형태의 상기 hnCD16/CAR/IL iPSC 및 이의 유도체 세포는 시험관내 또는 생체내에서 추가로 공급된 가용성 사이토카인을 접촉하지 않으면서 세포 성장, 증식, 확장, 및/또는 효과기 기능을 유지 또는 개선시킬 수 있다. 일부 실시형태에서, hnCD16/CAR/IL iPSC 및 이의 유도체 효과기 세포는 종양 항원 탈출 및 후속 종양 재발을 감소 또는 제거시킴으로써 CAR 표적화된 종양 사멸과 상승작용하도록 ADCC를 유도하기 위해서 항체와 함께 사용될 수 있다.
또한 hnCD16; CAR; IL; B2M 넉아웃 및/또는 CIITA 넉아웃; 및 선택적으로 HLA-G를 암호화하는 폴리뉴클레오타이드를 포함하는 iPSC, iPS 세포주 세포 또는 이로부터의 유도체 세포가 제공되며, 여기서 iPSC는 기능성 유도체 조혈 세포를 생성하도록 분화를 지시할 수 있다. iPSC 및 이의 유도체 NK 또는 T 세포의 일 실시형태에서, 세포는 hnCD16/CAR/IL/B2M-/- CIITA-/-를 포함하고, HLA-I 및 HLA-II 결핍성 둘 다이고, CAR 표적화된 종양 세포 사멸과 함께 ADCC를 유도하도록 항체와 함께 사용될 수 있고, 여기서 iPSC 및 이의 효과기 세포는 개선된 지속성 및/또는 생존을 갖는다. 일부 실시형태에서, 효과기 세포는 생체내에서 증가된 지속성 및/또는 생존을 갖는다.
이와 같이, 본 명세서는 hnCD16 및 CAR, 및 선택적으로 외인성 사이토카인/수용체, B2M 넉아웃 및 CIITA 넉아웃 중 하나, 2개 또는 3개 모두를 포함하는 이로부터의 iPSC를 포함하며; 여기서 B2M이 넉 아웃된 경우, HLA-G를 암호화하는 폴리뉴클레오타이드가 선택적으로 도입되고, 여기서 iPSC는 기능성 유도체 조혈 세포를 생성하도록 분화를 지시할 수 있다. 또한 본 출원에는 hnCD16 및 CAR, 및 선택적으로 외인성 사이토카인/수용체, B2M 넉아웃 및 CIITA 넉아웃 중 하나, 2개 또는 3개 모두를 포함하는 기능성 iPSC 유도체 조혈 세포가 포함되고; 여기서 B2M이 넉 아웃된 경우, HLA-G를 암호화하는 폴리뉴클레오타이드가 선택적으로 도입되고, 여기서 유도체 조혈 세포는 확정적 조혈 내피(HE) 가능성을 갖는 중배엽 세포, 확정적 HE, CD34 조혈 세포, 조혈 줄기 및 전구 세포, 조혈 다능성 전구 세포(MPP), T 세포 전구 세포, NK 세포 전구 세포, 골수 세포, 호중구 전구 세포, T 세포, NKT 세포, NK 세포, B 세포, 호중구, 수지상 세포 및 대식세포를 포함하지만 이들로 제한되지 않는다.
이와 같이, 본 출원은 iPSC 및 이의 기능성 유도체 조혈 세포를 제공하며, 이것은 표 1의 하기 유전자형 중 임의의 하나를 포함한다. 제공된 바와 같이, "IL"은 어느 특이적 사이토카인/수용체 발현이 선택되는지에 따라서 IL2, IL4, IL6, IL7, IL9, IL10, IL11, IL12, IL15, IL18 및 IL21 중 하나를 나타낸다. iPSC 및 이의 기능성 유도체 조혈 세포가 CAR 및 IL 둘 다를 포함하는 유전자형을 갖는 경우, CAR 및 IL은 2A 서열을 포함하는 바이-시스트론성 발현 카세트에 포함된다. 비교로서, 일부 다른 실시형태에서, CAR 및 IL은 iPSC 및 이의 기능성 유도체 조혈 세포에 포함된 별개의 발현 카세트에 존재한다. 특정 일 실시형태에서, CAR 및 IL 둘 다를 발현하는 iPSC 및 이의 기능성 유도체 효과기 세포에는 도 1의 작제물 3 또는 4에서의 IL15가 포함되며, 여기서 IL15 작제물은 CAR을 갖는 발현 카세트 내에 또는 CAR과 별개로 포함된다.
6. 추가적인 변형
일부 실시형태에서, 표 1의 유전자형 중 임의의 하나를 포함하는 iPSC 및 이의 유도체 효과기 세포는 TAP1, TAP2, 타파신, NLRC5, PD1, LAG3, TIM3, RFXANK, RFX5, RFXAP 및 염색체 6p21 영역 내의 임의의 유전자 중 적어도 하나에서의 결실 또는 감소된 발현; 또는 HLA-E, 41BBL, CD3, CD4, CD8, CD47, CD113, CD131, CD137, CD80, PDL1, A2AR, TCR, Fc 수용체, 관여자, 및 이중- 또는 다중-특이적 또는 보편적 관여자와의 커플링을 위한 표면 촉발 수용체 중 적어도 하나의 도입된 또는 증가된 발현을 추가로 포함할 수 있다.
이중- 또는 다중-특이적 관여자는 상이한 항체의 2개 이상의 단일-쇄 가변 단편(scFv)으로 이루어진 융합 단백질이고, 적어도 하나의 scFv는 효과기 세포 표면 분자에 결합하고, 적어도 또 다른 것은 종양 특이적 표면 분자를 통해서 종양 세포에 결합한다. 이중 또는 다중특이적 관여자 인식 또는 커플링을 위해서 사용될 수 있는 예시적인 효과기 세포 표면 분자 또는 표면 촉발 수용체는 본 명세서에 개시된 바와 같은 CD3, CD28, CD5, CD16, NKG2D, CD64, CD32, CD89, NKG2C 및 키메라 Fc 수용체를 포함하지만 이들로 제한되지 않는다. 일부 실시형태에서, 관여자 인식을 위해서 효과기 세포의 표면 상에서 발현되는 CD16은 섹션 I.2에 기재된 바와 같은 CD16(F176V 및 선택적으로 S197P 함유) 또는 CD64 세포외 도메인 및 네이티브 또는 비-네이티브 막관통, 자극성 및/또는 신호전달 도메인을 포함하는 hnCD16이다. 일부 실시형태에서, 관여자 인식을 위해서 효과기 세포의 표면 상에서 발현되는 CD16은 hnCD16 기반 키메라 Fc 수용체(CFcR)이다. 일부 실시형태에서, hnCD16 기반 CfcR은 NKG2D의 막관통 도메인, 2B4의 자극성 도메인 및 CD3ζ의 신호전달 도메인을 포함하며; 여기서 hnCD16의 세포외 도메인은 CD64 또는 CD16의 세포외 도메인의 전체 길이 또는 부분 서열로부터 유래되고, 여기서 CD16의 세포외 도메인은 F176V 및 선택적으로 S197P를 포함한다. 이중- 또는 다중-특이적 관여자 인식을 위한 예시적인 종양 세포 표면 분자는 B7H3, BCMA, CD10, CD19, CD20, CD22, CD24, CD30, CD33, CD34, CD38, CD44, CD79a, CD79b, CD123, CD138, CD179b, CEA, CLEC12A, CS-1, DLL3, EGFR, EGFRvIII, EPCAM, FLT-3, FOLR1, FOLR3, GD2, gpA33, HER2, HM1.24, LGR5, MSLN, MCSP, MICA/B, PSMA, PAMA, P-카드헤린, ROR1을 포함하지만 이들로 제한되지 않는다. 일 실시형태에서, 이중특이적 항체는 CD3-CD19이다. 또 다른 실시형태에서, 이중특이적 항체는 CD16-CD30 또는 CD64-CD30이다. 또 다른 실시형태에서, 이중특이적 항체는 CD16-BCMA 또는 CD64-BCMA이다. 또 다른 추가 실시형태에서, 이중특이적 항체는 CD3-CD33이다. 또 다른 추가 실시형태에서, 이중특이적 항체는 효과기 세포와 종양 세포 항원 결합 도메인 사이에 링커를 포함하며, 예를 들어, 효과기 세포 확장을 가능하게 하기 위한 효과기 NK 세포를 위한 링커로서의 변형된 IL15(일부 간행물에서 TriKE, 또는 삼중특이적 사멸 관여자라고 부름)를 추가로 포함한다. 일 실시형태에서, TriKE는 CD16-IL15-EPCAM 또는 CD64-IL15-EPCAM이다. 또 다른 실시형태에서, TriKE는 CD16-IL15-CD33 또는 CD64-IL15-CD33이다. 또 다른 추가 실시형태에서, TriKE는 NKG2C-IL15-CD33이다.
일부 실시형태에서, 이중- 또는 다중-특이적 관여자를 위한 표면 촉발 수용체는 때때로 세포 유형에 따라서 효과기 세포에 내인성일 수 있다. 일부 다른 실시형태에서, 하나 이상의 외인성 표면 촉발 수용체는 본 명세서에 제공된 방법 및 조성물을 사용하여, 즉, 표 1에 열거된 유전자형을 포함하는 iPSC의 추가적인 조작, 그 다음 iPSC가 공급원 iPSC와 동일한 유전자형 및 표면 촉발 수용체를 포함하는 T, NK 또는 임의의 다른 효과기 세포로 분화하는 것을 지시함으로써 효과기 세포에 도입될 수 있다.
7. 면역요법을 위한 항체
일부 실시형태에서, 본 명세서에 제공된 바와 같은 게놈 조작된 효과기 세포에 더하여, 병태, 질환 또는 적응증과 연관된 항원을 표적으로 하는 항체 또는 항체 단편을 포함하는 추가 치료제가 병용 요법에서 이들 효과기 세포와 함께 사용될 수 있다. 일부 실시형태에서, 항체는 단클론성 항체이다. 일부 실시형태에서, 항체는 인간화된 항체, 인간화된 단클론성 항체 또는 키메라 항체이다. 일부 실시형태에서, 항체 또는 항체 단편은 바이러스 항원에 특이적으로 결합한다. 다른 실시형태에서, 항체 또는 항체 단편은 종양 항원에 특이적으로 결합한다. 일부 실시형태에서, 종양 또는 바이러스 특이적 항원은 투여된 iPSC 유래된 효과기 세포를 활성화시켜 사멸 능력을 향상시킨다. 일부 실시형태에서, 투여된 iPSC 유래된 효과기 세포에 대한 추가 치료제로서의 병용 치료에 적합한 항체는 항-CD20(리툭시맙, 벨투주맙, 오파투무맙, 유블리툭시맙, 오카라투주맙, 오비누투주맙), 항-HER2(트라스투주맙, 퍼투주맙), 항-CD52(알렘투주맙), 항-EGFR(서툭시맙), 항-GD2(디누툭시맙), 항-PDL1(아벨루맙), 항-CD38(다라투무맙, 이사툭시맙, MOR202), 항-CD123(7G3, CSL362), 항-SLAMF7(엘로투주맙); 및 이의 인간화된 또는 Fc 변형된 변이체 또는 단편 또는 이의 기능성 등가물 및 바이오시밀러를 포함하지만 이들로 제한되지 않는다. 일부 실시형태에서, iPSC 유래된 효과기 세포는 표 1에 열거된 유전자형을 포함하는 조혈 계통 세포를 포함한다. 일부 실시형태에서, iPSC 유래된 효과기 세포는 표 1에 열거된 유전자형을 포함하는 NK 세포를 포함한다. 일부 실시형태에서, iPSC 유래된 효과기 세포는 표 1에 열거된 유전자형을 포함하는 T 세포를 포함한다. 액체 또는 고형 종양을 치료하는데 유용한 조성물의 일부 실시형태에서, 조성물은 hnCD16 및 CAR을 포함하는 iPSC 유래된 NK 또는 T 세포, 및 CAR과 상이한 항원 특이성을 갖는 항체를 포함한다. 일부 추가 실시형태에서, hnCD16 발현 유도체 NK 또는 T 세포에 포함된 CAR은 CD19, BCMA, CD20, CD22, CD123, HER2, CD52, EGFR, GD2 및 PDL1 중 임의의 하나를 표적으로 하고; 세포는 CAR 표적화로부터 종양 항원 탈출을 감소 또는 예방하기 위해서 CAR에 의해서 인식된 것과 상이한 항원을 표적으로 하는 임의의 항체와 함께 사용될 수 있다. 예를 들어, 일 실시형태에서 hnCD16을 또한 발현하는 유래된 NK 또는 T 세포의 CAR이 CD123을 표적으로 하는 경우, 세포와 조합하여 사용될 항체는 항-CD123 항체가 아니다. 일부 다른 실시형태에서, 병용 치료에서 사용되는 iPSC 유래된 NK 또는 T 세포는 hnCD16, IL15 및 CAR을 포함하고; 여기서 IL15는 CAR과 함께 또는 별도로 발현되고; IL15는 도 1의 작제물 1 내지 7에 제시된 형태 중 임의의 하나로 존재하고; 여기서 병용 치료는 CAR과 비교할 때 상이한 항원을 표적으로 하는 항체를 포함한다. 일부 특별한 실시형태에서, IL15는 CAR과 함께 또는 별도로 발현되는 경우 작제물 3, 4 또는 7의 형태로 존재한다.
8. 면역관문 저해제
면역관문은 저해되지 않을 때 면역 반응을 억제 또는 하향조절할 수 있는 세포 분자, 종종 세포 표면 분자이다. 현재 종양은 특히 종양 항원에 특이적인 T 세포에 대한 면역 내성의 주요 기전으로서 면역-면역관문 경로를 선택한다는 것이 명백하다. 면역관문 저해제(CI)는 면역관문 유전자 발현 또는 유전자 생성물을 감소시키거나 면역관문 분자의 활성을 낮춤으로써, 저해성 면역관문을 차단하고, 면역계 기능을 회복시킬 수 있는 길항제이다. PD1/PDL1 또는 CTLA4를 표적으로 하는 면역관문 저해제의 개발은 종양학 환경을 변화시켰으며, 이들 작용제는 다중 적응증에서 장기간 완화를 제공한다. 그러나, 다수의 종양 아형은 면역관문 차단 요법에 내성이 있고, 재발은 중요한 관심사이다. 본 출원의 일 양상은, CI와의 병용 요법에서 제공된 바와 같은 게놈 조작된 기능성 유도체 세포를 포함시킴으로써 CI 내성을 극복하기 위한 치료적 접근법을 제공한다. 병용 요법의 일 실시형태에서, 유도체 세포는 NK 세포이다. 병용 요법의 또 다른 실시형태에서, 유도체 세포는 T 세포이다. 직접적인 항종양 능력을 나타내는 것에 더하여, 본 명세서에 제공된 유도체 NK 세포는 PDL1-PD1 매개된 저해에 저항하고, T 세포 이동을 향상시키고, T 세포를 종양 환경에 모집하고, 종양 부위에서 T 세포 활성화를 증강시키는 능력을 갖는 것으로 나타났다. 따라서, 기능적으로 강력한 게놈 조작된 유도체 NK 세포에 의해서 촉진된 T 세포의 종양 침윤은, 상기 NK 세포가 면역관문 저해제를 비롯한 T 세포 표적화 면역요법과 함께 상승작용하여 국소 면역억제를 완화시키고 종양 부하를 감소시킬 수 있음을 나타낸다.
일 실시형태에서, 면역관문 저해제 병용 요법을 위한 유래된 NK 세포는 hnCD16 및 CAR 및 선택적으로 B2M 넉아웃, CIITA 넉아웃 및 외인성 세포 표면 사이토카인 및/또는 수용체 발현 중 하나, 2개 또는 3개 모두를 포함하고; 여기서 B2M이 넉 아웃되는 경우, HLA-G가 선택적으로 포함된다. 일부 실시형태에서, 유도체 NK 세포는 표 1에 열거된 유전자형 중 임의의 하나를 포함한다. 일부 실시형태에서, 상기 유도체 NK 세포는 TAP1, TAP2, 타파신, NLRC5, PD1, LAG3, TIM3, RFXANK, RFX5, RFXAP 및 염색체 6p21 영역 내의 임의의 유전자 중 적어도 하나에서의 결실 또는 감소된 발현; 또는 HLA-E, 41BBL, CD3, CD4, CD8, CD47, CD113, CD131, CD137, CD80, PDL1, A2AR, CAR, TCR, Fc 수용체, 관여자, 및 이중- 또는 다중-특이적 또는 보편적 관여자와의 커플링을 위한 표면 촉발 수용체 중 적어도 하나의 도입된 또는 증가된 발현을 추가로 포함할 수 있다.
또 다른 실시형태에서, 면역관문 저해제 병용 요법을 위한 유래된 T 세포는 hnCD16 및 CAR 및 선택적으로 B2M 넉아웃, CIITA 넉아웃 및 외인성 세포 표면 사이토카인 및/또는 수용체 발현 중 하나, 2개 또는 3개 모두를 포함하고; 여기서 B2M이 넉 아웃되는 경우, HLA-G가 선택적으로 포함된다. 일부 실시형태에서, 유도체 T 세포는 표 1에 열거된 유전자형 중 임의의 하나를 포함한다. 일부 실시형태에서, 상기 유도체 T 세포는 TAP1, TAP2, 타파신, NLRC5, PD1, LAG3, TIM3, RFXANK, RFX5, RFXAP 및 염색체 6p21 영역 내의 임의의 유전자 중 적어도 하나에서의 결실 또는 감소된 발현; 또는 HLA-E, 41BBL, CD3, CD4, CD8, CD47, CD113, CD131, CD137, CD80, PDL1, A2AR, CAR, TCR, Fc 수용체, 관여자, 및 이중- 또는 다중-특이적 또는 보편적 관여자와의 커플링을 위한 표면 촉발 수용체 중 적어도 하나의 도입된 또는 증가된 발현을 추가로 포함할 수 있다.
상기한 상기 유도체 NK 또는 T 세포는 hnCD16 및 CAR 및 선택적으로 B2M 넉아웃, CIITA 넉아웃 및 외인성 세포 표면 사이토카인 및/또는 수용체 발현 중 하나, 2개 또는 3개 모두를 포함하는 iPSC 클론주를 분화시킴으로써 획득되고; 여기서 B2M이 넉 아웃되는 경우, HLA-G가 선택적으로 도입된다. 일부 실시형태에서, 상기한 상기 iPSC 클론주는 TAP1, TAP2, 타파신, NLRC5, PD1, LAG3, TIM3, RFXANK, RFX5, RFXAP 및 염색체 6p21 영역 내의 임의의 유전자 중 적어도 하나에서의 결실 또는 감소된 발현; 또는 HLA-E, 41BBL, CD3, CD4, CD8, CD47, CD113, CD131, CD137, CD80, PDL1, A2AR, CAR, TCR, Fc 수용체, 관여자, 및 이중- 또는 다중-특이적 또는 보편적 관여자와의 커플링을 위한 표면 촉발 수용체 중 적어도 하나의 도입된 또는 증가된 발현을 추가로 포함한다.
본 명세서에 제공된 바와 같은 유도체 NK 또는 T 세포와의 병용 요법에 적합한 면역관문 저해제는 PD-1(Pdcdl, CD279), PDL-1(CD274), TIM-3(Havcr2), TIGIT(WUCAM 및 Vstm3), LAG-3(Lag3, CD223), CTLA-4(Ctla4, CD152), 2B4(CD244), 4-1BB(CD137), 4-1BBL(CD137L), A2aR, BATE, BTLA, CD39(Entpdl), CD47, CD73(NT5E), CD94, CD96, CD160, CD200, CD200R, CD274, CEACAM1, CSF-1R, Foxpl, GARP, HVEM, IDO, EDO, TDO, LAIR-1, MICA/B, NR4A2, MAFB, OCT-2(Pou2f2), 레티노산 수용체 알파(Rara), TLR3, VISTA, NKG2A/HLA-E 및 저해성 KIR(예를 들어, 2DL1, 2DL2, 2DL3, 3DL1 및 3DL2)의 길항제를 포함하지만 이들로 제한되지 않는다.
일부 실시형태에서, 상기 면역관문 분자 중 임의의 것을 저해하는 길항제는 항체이다. 일부 실시형태에서, 면역관문 저해성 항체는 뮤린 항체, 인간 항체, 인간화된 항체, 낙타 Ig, 상어 중쇄-단독 항체(VNAR), Ig NAR, 키메라 항체, 재조합 항체 또는 이의 항체 단편일 수 있다. 항체 단편의 비제한적인 예는 Fab, Fab', F(ab)'2, F(ab)'3, Fv, 단일 쇄 항원 결합 단편(scFv), (scFv)2, 다이설파이드 안정화된 Fv(dsFv), 미니바디, 다이아바디, 트라이아바디, 테트라바디, 단일-도메인 항원 결합 단편(sdAb, 나노바디), 재조합 중쇄-단독 항체(VHH) 및 전체 항체의 결합 특이성을 보유하는 다른 항체 단편(이것은 제조하기에 더 비용 효과적일 수 있거나, 보다 용이하게 사용될 수 있거나, 전체 항체보다 더 민감할 수 있음)을 포함한다. 일부 실시형태에서, 1개, 2개 또는 3개 또는 그 초과의 면역관문 저해제는 아테졸리주맙(항-PDL1 mAb), 아벨루맙(항-PDL1 mAb), 더발루맙(항-PDL1 mAb), 트레멜리무맙(항-CTLA4 mAb), 이필리무맙(항-CTLA4 mAb), IPH4102(항-KIR), IPH43(항-MICA), IPH33(항-TLR3), 리릴루맙(항-KIR), 모날리주맙(항-NKG2A), 니볼루맙(항-PD1 mAb), 펨브롤리주맙(항-PD1 mAb) 및 이들의 임의의 유도체, 기능성 등가물 또는 바이오시밀러 중 적어도 하나를 포함한다.
일부 실시형태에서, 상기 면역관문 분자 중 임의의 것을 저해하는 길항제는, 다수의 miRNA가 면역관문의 발현을 제어하는 조절제로서 발견되는 바와 같은 마이크로RNA-기반이다(Dragomir et al., Cancer Biol Med. 2018, 15(2):103-115). 일부 실시형태에서, 면역관문 길항성 miRNA는 miR-28, miR-15/16, miR-138, miR-342, miR-20b, miR-21, miR-130b, miR-34a, miR-197, miR-200c, miR-200, miR-17-5p, miR-570, miR-424, miR-155, miR-574-3p, miR-513 및 miR-29c를 포함하지만 이들로 제한되지 않는다.
제공된 유도체 NK 또는 T 세포와의 병용 요법의 일부 실시형태는 적어도 1종의 면역관문 분자를 표적으로 하기 위해서 적어도 1종의 면역관문 저해제를 포함하며; 여기서 유도체 세포는 표 1에 열거된 유전자형을 갖는다. 제공된 유도체 NK 또는 T 세포와의 병용 요법의 일부 다른 실시형태는 2개, 3개 또는 그 초과의 면역관문 분자가 표적화되도록 2개, 3개 또는 그 초과의 면역관문 저해제를 포함한다. 적어도 1종의 면역관문 저해제 및 표 1에 열거된 유전자형을 갖는 유도체 세포를 포함하는 병용 요법의 일부 실시형태에서, 상기 면역관문 저해제는 항체, 또는 인간화된 또는 Fc 변형된 변이체 또는 단편, 또는 이들의 기능성 등가물 또는 바이오시밀러이고, 상기 면역관문 저해제는 상기 항체, 또는 이의 단편 또는 변이체를 암호화하는 외인성 폴리뉴클레오타이드 서열을 발현시킴으로써 유도체 세포에 의해서 생산된다. 일부 실시형태에서, 면역관문을 저해하는 항체 또는 단편 또는 이의 변이체를 암호화하는 외인성 폴리뉴클레오타이드 서열은 CAR 및 항체 또는 이의 단편을 암호화하는 서열 둘 다를 포함하는 바이-시스트론성 작제물로 또는 별개의 작제물로 CAR과 공동 발현된다. 일부 추가 실시형태에서, 항체 또는 이의 단편을 암호화하는 서열은 예를 들어, CAR-2A-CI 또는 CI-2A-CAR에 예시된 자가-절단 2A 암호 서열을 통해서 CAR 발현 작제물의 5' 또는 3' 단부에 연결될 수 있다. 이와 같이, 면역관문 저해제 및 CAR의 암호 서열은 단일 오픈 리딩 프레임(ORF)에 존재한다. 면역관문 저해제가 종양 미세환경(tumor microenvironment: TME)을 침윤할 수 있는 유도체 효과기 세포에 의해서 페이로드로서 전달, 발현 및 분비되는 경우, 그것은 TME와의 결속 시에 저해성 면역관문 분자에 대응하여, 양상, 예컨대, CAR을 활성화시키거나 수용체를 활성화시킴으로써 효과기 세포의 활성화를 가능하게 한다. 일부 실시형태에서, CAR과 공동 발현되는 면역관문 저해제는 면역관문 분자: PD-1, PDL-1, TIM-3, TIGIT, LAG-3, CTLA-4, 2B4, 4-1BB, 4-1BBL, A2aR, BATE, BTLA, CD39(Entpdl), CD47, CD73(NT5E), CD94, CD96, CD160, CD200, CD200R, CD274, CEACAM1, CSF-1R, Foxpl, GARP, HVEM, IDO, EDO, TDO, LAIR-1, MICA/B, NR4A2, MAFB, OCT-2(Pou2f2), 레티노산 수용체 알파(Rara), TLR3, VISTA, NKG2A/HLA-E 및 저해성 KIR 중 적어도 1종을 저해한다. 일부 실시형태에서, 표 1에 열거된 유전자형을 갖는 유도체 세포에서 CAR과 함께 공동 발현되는 면역관문 저해제는 아테졸리주맙, 아벨루맙, 더발루맙, 트레멜리무맙, 이필리무맙, IPH4102, IPH43, IPH33, 리릴루맙, 모날리주맙, 니볼루맙, 펨브롤리주맙, 및 이들의 인간화된 또는 Fc 변형된 변이체, 단편 및 이들의 기능성 등가물 또는 바이오시밀러를 포함하는 군으로부터 선택된다. 일부 실시형태에서, CAR과 함께 공동 발현되는 면역관문 저해제는 아테졸리주맙 또는 이의 인간화된 또는 Fc 변형된 변이체, 단편 또는 이의 기능성 등가물 또는 바이오시밀러이다. 일부 다른 실시형태에서, CAR과 함께 공동 발현되는 면역관문 저해제는 니볼루맙 또는 이의 인간화된 또는 Fc 변형된 변이체, 단편 또는 이의 기능성 등가물 또는 바이오시밀러이다. 일부 다른 실시형태에서, CAR과 함께 공동 발현되는 면역관문 저해제는 펨브롤리주맙 또는 이의 인간화된 또는 Fc 변형된 변이체, 단편 또는 이의 기능성 등가물 또는 바이오시밀러이다.
본 명세서에 제공된 유도체 세포 및 면역관문 분자를 저해하는 적어도 1종의 항체를 포함하는 병용 요법의 일부 다른 실시형태에서, 상기 항체는 유도체 세포에 의해서 또는 유도체 세포에서 생산되지 않고, 표 1에 열거된 유전자형을 갖는 유도체 세포의 투여 이전에, 투여와 함께 또는 투여 후에 추가로 투여된다. 일부 실시형태에서, 제공된 유도체 NK 또는 T 세포와의 병용 요법에서 1종, 2종 또는 3종 또는 그 초과의 면역관문 저해제의 투여는 동시 또는 순차적이다. 표 1에 열거된 유전자형을 갖는 유래된 NK 세포 또는 T 세포를 포함하는 병용 치료의 일 실시형태에서, 치료에 포함되는 면역관문 저해제는 아테졸리주맙, 아벨루맙, 더발루맙, 트레멜리무맙, 이필리무맙, IPH4102, IPH43, IPH33, 리릴루맙, 모날리주맙, 니볼루맙, 펨브롤리주맙 및 이들의 인간화된 또는 Fc 변형된 변이체, 단편 및 이들의 기능성 등가물 또는 바이오시밀러 중 1종 이상이다. 표 1에 열거된 유전자형을 갖는 유래된 NK 세포 또는 T 세포를 포함하는 병용 치료의 일부 실시형태에서, 치료에 포함되는 면역관문 저해제는 아테졸리주맙 또는 이의 인간화된 또는 Fc 변형된 변이체, 단편 및 이의 기능성 등가물 또는 바이오시밀러이다. 표 1에 열거된 유전자형을 갖는 유래된 NK 세포 또는 T 세포를 포함하는 병용 치료의 일부 실시형태에서, 치료에 포함되는 면역관문 저해제는 니볼루맙 또는 이의 인간화된 또는 Fc 변형된 변이체, 단편 또는 이의 기능성 등가물 또는 바이오시밀러이다. 표 1에 열거된 유전자형을 갖는 유래된 NK 세포 또는 T 세포를 포함하는 병용 치료의 일부 실시형태에서, 치료에 포함되는 면역관문 저해제는 펨브롤리주맙 또는 이의 인간화된 또는 Fc 변형된 변이체, 단편 또는 이의 기능성 등가물 또는 바이오시밀러이다.
II. iPSC 내의 선택된 유전자좌에서 표적화된 게놈 편집을 위한 방법
게놈 편집 또는 유전자 편집은 본 명세서에서 사용되는 바와 같이 DNA가 표적화된 세포의 게놈에서 삽입, 결실 및/또는 대체되는 유전자 조작의 유형이다. 표적화된 게놈 편집("표적화된 게놈 편집" 또는 "표적화된 유전자 편집"과 상호 호환적임)은 게놈 내의 미리-선택된 부위에서 삽입, 결실 및/또는 치환을 가능하게 한다. 내인성 서열이 표적화 편집 동안 삽입 부위 내에서 결실되는 경우, 영향을 받은 서열을 포함하는 내인성 유전자는 서열 결실로 인해서 넉-아웃 또는 넉-다운될 수 있다. 따라서, 표적화 편집은 또한 내인성 유전자 발현을 정확하게 파괴하기 위해서 사용될 수 있다. 삽입 부위에서 내인성 서열의 결실이 있거나 없는 1종 이상의 외인성 서열의 삽입을 포함하는 과정을 지칭하는 "표적화된 통합"이 유사하게 본 명세서에서 사용된다. 비교하면, 무작위로 통합된 유전자는 위치 효과 및 침묵화되어, 이의 발현이 신뢰할 수 없거나 예측할 수 없게 만드는 경향이 있다. 예를 들어, 동원체 및 하위-말단소체 영역은 특히 이식유전자 침묵화되는 경향이 있다. 상반되게, 새로 통합된 유전자는 주변 내인성 유전자 및 염색질에 영향을 주어, 가능하게는 세포 거동을 변경하거나 또는 세포 형질전환을 선호하는 경향이 있다. 따라서, 외인성 DNA를 미리-선택된 유전자좌, 예컨대 안전 하버 유전자좌 또는 게놈 안전 하버(GSH)에 삽입하는 것은 안전성, 효율성, 카피수 대조군 및 신뢰할 수 있는 유전자 반응 대조군을 위해서 중요하다.
표적화 편집은 뉴클레아제-독립적인 접근법을 통해서 또는 뉴클레아제-의존적인 접근법을 통해서 달성될 수 있다. 뉴클레아제-독립적인 표적화 편집 접근법에서, 상동 재조합은 숙주 세포의 효소적 기구를 통해서, 삽입될 외인성 폴리뉴클레오타이드에 측접하는 상동성 서열에 의해서 안내된다.
대안적으로, 표적화 편집은 특이적인 희귀한-절단 엔도뉴클레아제에 의해서 이중 가닥 브레이크(DSB)의 특이적 도입을 통해서 더 높은 빈도로 달성될 수 있다. 이러한 뉴클레아제-의존적인 표적화 편집은 비-상동 단부 결합(NHEJ)을 비롯한 DNA 수선 기전을 사용하는데, 이것은 DSB에 반응하여 일어난다. 외인성 유전 물질을 함유하는 공여자 벡터가 없는 경우, NHEJ는 종종 적은 수의 내인성 뉴클레오타이드의 무작위 삽입 또는 결실(in/del)로 이어진다. 비교하면, 상동성 아암의 쌍에 의해서 플랭킹된 외인성 유전 물질을 함유하는 공여자 벡터가 존재하는 경우, 외인성 유전 물질은 상동 재조합에 의해서 상동성 지향된 수선(HDR)으로 안내되어, "표적화된 통합"을 유발할 수 있다.
특이적이고, 표적화된 DSB를 도입할 수 있는 사용 가능한 엔도뉴클레아제는 아연-핑거 뉴클레아제(ZFN), 전사 활성자-유사 효과기 뉴클레아제(TALEN), RNA-안내 CRISPR(Clustered Regular Interspaced Short Palindromic Repeats) 시스템을 포함하지만 이들로 제한되지 않는다. 추가로, phiC31 및 Bxb1 인테그라제를 사용하는 DICE(이중 인테그라제 카세트 교환(dual integrase cassette exchange)) 시스템이 또한 표적화된 통합을 위한 유망한 툴이다.
ZFN은 아연 핑거 DNA 결합 도메인에 융합된 뉴클레아제를 포함하는 표적화된 뉴클레아제이다. "아연 핑거 DNA 결합 도메인" 또는 "ZFBD"라는 것은, 하나 이상의 아연 핑거를 통해서 서열-특이적인 방식으로 DNA에 결합하는 폴리펩타이드 도메인을 의미한다. 아연 핑거는 구조가 아연 이온의 배위를 통해서 안정화된 아연 핑거 결합 도메인 내의 약 30개 아미노산의 도메인이다. 아연 핑거의 예는 C2H2 아연 핑거, C3H 아연 핑거 및 C4 아연 핑거를 포함하지만 이들에 제한되지 않는다. "설계된" 아연 핑거 도메인은 그의 설계/조성이 합리적 기준, 예를 들어, 기존의 ZFP 설계 및 결합 데이터의 정보를 분류하는 데이터베이스에서의 치환 규칙 및 처리 정보를 위한 컴퓨터 계산된 알고리즘의 응용으로부터 원칙적으로 유래되는 자연에서 발생하지 않는 도메인이다(예를 들어, 미국 특허 제6,140,081호; 제6,453,242호; 및 제6,534,261호 참고; 또한 국제 특허 제WO 98/53058호; 제WO 98/53059호; 제WO 98/53060호; 제WO 02/016536호 및 제WO 03/016496호 참고). "선택된" 아연 핑거 도메인은 그의 생산이 경험적 공정, 예컨대 파지 디스플레이, 상호작용 트랩 또는 혼성 선택으로부터 주로 유발되는 자연에서 발견되지 않는 도메인이다. ZFN은 전체 개시내용이 참조에 의해 본 명세서에 포함된 미국 특허 제7,888,121호 및 미국 특허 제7,972,854호에 보다 상세하게 기술된다. 관련 기술 분야에서 ZFN의 가장 인식되는 예는 FokI 뉴클레아제와 아연 핑거 DNA 결합 도메인의 융합이다.
TALEN은 TAL 효과기 DNA 결합 도메인에 융합된 뉴클레아제를 포함하는 표적화된 뉴클레아제이다. "전사 활성자-유사 효과기 DNA 결합 도메인", "TAL 효과기 DNA 결합 도메인", 또는 "TALE DNA 결합 도메인"이라는 것은 DNA에 대한 TAL 효과기 단백질의 결합에 대한 책임이 있는 TAL 효과기 단백질의 폴리펩타이드 도메인을 의미한다. TAL 효과기 단백질은 감염 동안 산토모나스(Xanthomonas) 속의 식물 병원체에 의해서 분해된다. 이들 단백질은 식물 세포의 핵에 들어가서, 이의 DNA 결합 도메인을 통해서 효과기-특이적 DNA 서열에 결합하여, 이의 전사활성화 도메인을 통해서 이러한 서열에서 유전자 전사를 활성화시킨다. TAL 효과기 DNA 결합 도메인 특이성은 반복 가변-이중잔기(repeat variable-diresidues: RVD)라 지칭되는 선택된 반복 위치에서 다형성을 포함하는 불완전한 34개의 아미노산 반복부의 효과기-가변 수에 좌우된다. TALEN은 참조에 의해 본 명세서에 포함된 미국 특허 출원 제2011/0145940호에 보다 상세하게 기술되어 있다. 관련 기술 분야에서 TALEN의 가장 인식되는 예는 TAL 효과기 DNA 결합 도메인에 대한 FokI 뉴클레아제의 융합 폴리펩타이드이다.
본 방법에서의 용도를 발견한 표적화된 뉴클레아제의 또 다른 예는 DNA 결합 도메인, 예를 들어 관심 DNA 서열에 대해서 특이성을 갖는 아연 핑거 DNA 결합 도메인, TAL 효과기 DNA 결합 도메인 등에 융합된 뉴클레아제 활성을 갖는 Spo11 폴리펩타이드를 포함하는 폴리펩타이드인, 표적화된 Spo11 뉴클레아제이다(예를 들어, 개시내용이 참조에 의해 본 명세서에 포함된 미국 출원 제61/555,857호 참고).
본 발명에 적합한 표적화된 뉴클레아제의 추가 예는 개별적으로 사용되든지 조합으로 사용되든지에 관계 없이 Bxb1, phiC31, R4, PhiBT1, 및 Wβ/SPBc/TP901-1을 포함하지만 이들로 제한되지 않는다.
표적화된 뉴클레아제의 다른 비제한적인 예는 자연 발생 및 재조합 뉴클레아제; cas, cpf, cse, csy, csn, csd, cst, csh, csa, csm 및 cmr을 비롯한 패밀리로부터의 CRISPR 관련 뉴클레아제; 제한 엔도뉴클레아제; 메가뉴클레아제; 귀소 엔도뉴클레아제 등을 포함한다.
예시적인 예로서, CRISPR/Cas9는 2개의 주요 성분이 필요하다: (1) Cas9 엔도뉴클레아제 및 (2) crRNA-tracrRNA 복합체. 공동-발현되는 경우, 두 성분은 PAM 및 PAM 근처의 시딩 영역을 포함하는 표적 DNA 서열에 모집된 복합체를 형성한다. crRNA 및 tracrRNA는 Cas9가 선택된 서열을 표적화하는 것을 안내하기 위해서 키메라 가이드 RNA(gRNA)를 형성하도록 조합될 수 있다. 이어서 이러한 두 성분은 형질주입 또는 형질도입을 통해서 포유동물 세포에 전달될 수 있다.
DICE 매개된 삽입은 재조합효소, phiC31 및 Bxb1의 쌍을 사용하여, 각각의 효소 사진의 작은 attB 및 attP 인식 부위에 엄격하게 제한된 외인성 DNA의 단방향성 통합을 제공한다. 이러한 표적 att 부위는 포유동물 게놈에는 자연적으로 존재하지 않기 때문에, 이것은 목적하는 통합 부위에서 게놈에 먼저 도입되어야 한다(예를 들어, 개시내용이 본 명세서에 참조에 의해 포함된 미국 츨원 공개 제2015/0140665호 참고).
본 발명의 일 양상은 표적화된 게놈 통합을 위해서 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 작제물을 제공한다. 일 실시형태에서, 작제물은 목적하는 통합 부위에 특이적인 상동 아암의 쌍을 추가로 포함하고, 표적화된 통합의 방법은 세포 숙주 효소 기구에 의한 부위 특이적 상동 재조합이 가능하도록 작제물을 세포에 도입하는 단계를 포함한다. 또 다른 실시형태에서, 세포에서의 표적화된 통합 방법은 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 작제물을 세포에 도입하는 단계, 및 ZFN-매개된 삽입이 가능하도록 목적하는 통합 부위에 특이적인 DNA-결합 도메인을 포함하는 ZFN 발현 카세트를 세포에 도입하는 단계를 포함한다. 추가로 또 다른 실시형태에서, 세포에서의 표적화된 통합 방법은 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 작제물을 세포에 도입하는 단계, 및 TALEN-매개된 삽입이 가능하도록 목적하는 통합 부위에 특이적인 DNA-결합 도메인을 포함하는 TALEN 발현 카세트를 세포에 도입하는 단계를 포함한다. 또 다른 실시형태에서, 세포에서의 표적화된 통합 방법은 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 작제물 세포에 도입하는 단계, Cas9-매개된 삽입이 가능하도록 Cas9 발현 카세트, 및 목적하는 통합 부위에 특이적인 가이드 서열을 포함하는 gRNA를 세포에 도입하는 단계를 포함한다. 추가의 또 다른 실시형태에서, 세포에서의 표적화된 통합 방법은 DICE 재조합효소의 쌍의 하나 이상의 att 부위를 포함하는 작제물을 세포 내의 목적하는 통합 부위에 도입하는 단계, 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 작제물을 세포에 도입하는 단계, 및 DICE-매개된 표적화된 통합이 가능하도록, DICE 재조합효소를 위한 발현 카세트를 도입하는 단계를 포함한다.
표적화된 통합을 위한 유망한 부위는 안전 하버 유전자좌, 또는 게놈 안전 하버(GSH)를 포함하지만 이들로 제한되지 않으며, 이것은 숙주 세포 또는 유기체에 악영향을 미치지 않으면서 새로 통합된 DNA의 예측 가능한 발현을 이론적으로 수용할 수 있는 인간 게놈의 유전자내 또는 유전자외 영역이다. 유용한 안전 하버는 벡터-암호화된 단백질 또는 비-암호 RNA의 목적하는 수준을 산출하기에 충분한 이식유전자 발현을 허용해야 한다. 안전 하버는 또한 세포를 악성 형질전환하게 만들지도 않고 세포 기능을 변경시키지도 않아야 한다. 잠재적인 안전 하버 유전자좌일 통합 부위의 경우, 서열 주석에 의해서 판단되는 바와 같은, 조절 요소 또는 유전자의 파괴의 부재를 포함하지만 이에 제한되지 않는 기준을 충족하는 것이 이상적으로 필요하며; 이것은 반대 방향으로 전사되는 2개의 유전자 사이의 수렴부(convergence)에서의 유전자 밀집 면적 또는 위치 내의 유전자간 영역이고; 벡터-암호화된 전사 활성자와 인접한 유전자, 특히 암-관련된 유전자 및 마이크로RNA 유전자의 프로모터 간의 긴-범위 상호작용의 가능성을 최소화하는 거리를 유지하고; 넓은 공간 및 일시적 발현 서열 태그(EST) 발현 패턴에 의해서 반영되는 바와 같은, 흔한 전사 활성을 나타내는, 명백하게 흔한 전사 활성을 갖는다. 후자 특징은, 분화 동안 염색질 리모델링이 전형적으로 일부 유전자좌의 침묵 및 다른 것의 잠재적인 활성화로 이어지는 경우, 줄기세포에서 특히 중요하다. 외인성 삽입에 적합한 영역 내에서, 삽입을 위해서 선택된 정확한 유전자좌는 반복적인 요소 및 보존 서열이 없고, 상동성 아암의 증폭을 위한 프라이머가 쉽게 설계될 수 있다.
인간 게놈 편집 또는 구체적으로 표적화된 통합에 적합한 부위는 아데노-연관된 바이러스 부위 1(AAVS1), 케모카인(CC 모티프) 수용체 5(CCR5) 유전자 유전자좌 및 마우스 ROSA26 유전자좌의 인간 오쏘로그(orthologue)를 포함하지만 이에 제한되지 않는다. 추가로, 마우스 H11 유전자좌의 인간 오쏘로그는 또한 본 명세서에 개시된 표적화된 통합의 조성물 및 방법을 사용한 삽입에 적합한 부위일 수 있다. 추가로, 콜라겐 및 HTRP 유전자 유전자좌는 또한 표적화된 통합을 위한 안전 하버로서 사용될 수 있다. 그러나, 각각의 선택된 부위의 검증은 특이적 통합 사건 및 프로모터 선출, 외인성 유전자 서열 및 배열을 비롯한 삽입 전략의 최적화를 위해서 특히 줄기세포에서 필수적인 것으로 밝혀져 있고, 작제물 설계가 종종 필요하다.
표적화된 in/del을 위해서, 편집 부위는 종종 발현 및/또는 기능이 방해되도록 의도되는 내인성 유전자 내에 포함된다. 일 실시형태에서, 표적화된 in/del을 포함하는 내인성 유전자는 면역 반응 조절 및 조정과 연관된다. 일부 다른 실시형태에서, 표적화된 in/del을 포함하는 내인성 유전자는 표적화 양상, 수용체, 신호전달 분자, 전사 인자, 약물 표적 후보, 면역 반응 조절 및 조정, 또는 줄기세포 및/또는 전구 세포 및 그로부터 유래된 세포의 생착, 수송, 귀소, 생존도, 자기-재생, 지속성 및/또는 생존을 억제하는 단백질과 연관된다.
이와 같이, 본 발명의 일 양상은 계속적 또는 일시적 유전자 발현에 대해서 안전하고, 널리 조절되는 것으로 공지되거나 증명된 게놈 안전 하버 또는 미리 선택된 유전자좌를 비롯한 선택된 유전자좌, 예컨대 본 명세서에 제공된 바와 같은 B2M, TAP1, TAP2 또는 타파신 유전자좌에서의 표적화된 통합 방법을 제공한다. 일 실시형태에서, 표적화된 통합 방법을 위한 게놈 안전 하버는 AAVS1, CCR5, ROSA26, 콜라겐, HTRP, H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1 또는 게놈 안전 하버의 기준을 충족시키는 다른 유전자좌를 포함하는 하나 이상의 목적하는 통합 부위를 포함한다. 일 실시형태에서, 세포에서의 표적화된 통합 방법은 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 작제물을 세포에 도입하는 단계, 및 세포 숙주 효소 기구에 의한 부위 특이적 상동 재조합이 가능하도록, 목적하는 통합 부위 및 1종 이상의 외인성 서열에 특이적인 상동 아암의 쌍을 포함하는 작제물을 도입하는 단계를 포함하고, 여기서 목적하는 통합 부위는 AAVS1, CCR5, ROSA26, 콜라겐, HTRP, H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1 또는 게놈 안전 하버의 기준을 충족시키는 다른 유전자좌를 포함한다.
다른 실시형태에서, 세포에서의 표적화된 통합 방법은 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 작제물을 세포에 도입하는 단계, 및 ZFN-매개된 삽입이 가능하도록 목적하는 통합 부위에 특이적인 DNA-결합 도메인을 포함하는 ZFN 발현 카세트를 세포에 도입하는 단계를 포함하며, 여기서 목적하는 통합 부위는 AAVS1, CCR5, ROSA26, 콜라겐, HTRP, H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1 또는 게놈 안전 하버의 기준을 충족시키는 다른 유전자좌를 포함한다. 추가로 또 다른 실시형태에서, 세포에서의 표적화된 통합 방법은 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 작제물을 세포에 도입하는 단계, 및 TALEN-매개된 삽입이 가능하도록 목적하는 통합 부위에 특이적인 DNA-결합 도메인을 포함하는 TALEN 발현 카세트를 세포에 도입하는 단계를 포함하며, 여기서 목적하는 통합 부위는 AAVS1, CCR5, ROSA26, 콜라겐, HTRP, H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1 또는 게놈 안전 하버의 기준을 충족시키는 다른 유전자좌를 포함한다. 또 다른 실시형태에서, 세포에서의 표적화된 통합 방법은 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 작제물을 세포에 도입하는 단계, Cas9-매개된 삽입이 가능하도록 Cas9 발현 카세트, 및 목적하는 통합 부위에 특이적인 가이드 서열을 포함하는 gRNA를 세포에 도입하는 단계를 포함하며, 여기서 목적하는 통합 부위는 AAVS1, CCR5, ROSA26, 콜라겐, HTRP, H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1 또는 게놈 안전 하버의 기준을 충족시키는 다른 유전자좌를 포함한다. 추가의 또 다른 실시형태에서, 세포에서의 표적화된 통합 방법은 DICE 재조합효소의 쌍의 하나 이상의 att 부위를 포함하는 작제물을 세포 내의 목적하는 통합부위에 도입하는 단계, 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 작제물을 세포에 도입하는 단계, 및 DICE-매개된 표적화된 통합이 가능하도록 DICE 재조합효소를 위한 발현 카세트를 도입하는 단계를 포함하며, 여기서 목적하는 통합 부위는 AAVS1, CCR5, ROSA26, 콜라겐, HTRP, H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1 또는 게놈 안전 하버의 기준을 충족시키는 다른 유전자좌를 포함한다.
추가로, 본 명세서에 제공된 바와 같이, 상기 안전 하버에서의 표적화된 통합 방법을 사용하여 임의의 관심 폴리뉴클레오타이드, 예를 들어 안전 스위치 단백질, 표적화 양상, 수용체, 신호전달 분자, 전사 인자, 약제학적으로 활성인 단백질 및 펩타이드, 약물 표적 후보, 및 줄기세포 및/또는 전구 세포의 생착, 수송, 귀소, 생존도, 자기-재생, 지속성 및/또는 생존을 촉진하는 단백질을 암호화하는 폴리 뉴클레오타이드를 삽입한다. 일부 다른 실시형태에서, 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 작제물은 하나 이상의 마커 유전자를 추가로 포함한다. 일 실시형태에서, 본 발명의 작제물에서 외인성 폴리뉴클레오타이드는 안전 스위치 단백질을 암호화하는 자살 유전자이다. 유도된 세포사에 적합한 자살 유전자 시스템은 카스파제 9(또는 카스파제 3 또는 7) 및 AP1903; 티미딘 카이나제(TK) 및 간시클로버(GCV); 사이토신 데아미나제(CD) 및 5-플루오로사이토신(5-FC)을 포함하지만 이들로 제한되지 않는다. 추가로, 일부 자살 유전자 시스템은 세포 유형 특이적이고, 예를 들어, T 림프구의 B-세포 분자 CD20로의 유전자 변형은 mAb 리툭시맙의 투여 시에 이의 제거를 허용한다. 추가로, 세툭시맙에 의해서 인식되는 에피토프를 함유하는 변형된 EGFR을 사용하여 세포가 세툭시맙에 노출되는 경우 유전자 조작된 세포를 고갈시킬 수 있다. 이와 같이, 본 발명의 일 양상은 카스파제 9(카스파제 3 또는 7), 티미딘 카이나제, 사이토신 데아미나제, 변형된 EGFR 및 B-세포 CD20으로부터 선택된 안전 스위치 단백질을 암호화하는 하나 이상의 자살 유전자의 표적화된 통합 방법을 제공한다.
일부 실시형태에서, 본 명세서의 방법에 의해서 통합된 1종 이상의 외인성 폴리뉴클레오타이드는 표적화된 통합을 위해서 작제물 내에 포함된 작동 가능하게 연결된 외인성 프로모터에 의해서 유도된다. 프로모터는 유도성 또는 작제성일 수 있고, 일시적-, 조직- 또는 세포 유형-특이적일 수 있다. 본 발명의 방법에 적합한 작제성 프로모터는, 거대세포바이러스(CMV), 연장 인자 1α(EF1α), 포스포글리세레이트 카이나제(PGK), 혼성 CMV 증강자/닭 β-액틴(CAG) 및 유비퀴틴 C(UBC) 프로모터를 포함하지만 이들로 제한되지 않는다. 일 실시형태에서, 외인성 프로모터는 CAG이다.
본 발명에서 방법에 의해서 통합된 외인성 폴리뉴클레오타이드는 통합 부위에서, 숙주 게놈 내의 내인성 프로모터에 의해서 유도될 수 있다. 일 실시형태에서, 본 발명의 방법은 세포의 게놈 내의 AAVS1 유전자좌에서 1종 이상의 외인성 폴리뉴클레오타이드의 표적화된 통합을 위해서 사용된다. 일 실시형태에서, 적어도 하나의 통합된 폴리뉴클레오타이드는 내인성 AAVS1 프로모터에 의해서 유도된다. 다른 실시형태에서, 본 발명의 방법은 세포의 게놈 내의 ROSA26 유전자좌에서 표적화된 통합을 위해서 사용된다. 일 실시형태에서, 적어도 하나의 통합된 폴리뉴클레오타이드는 내인성 ROSA26 프로모터에 의해서 유도된다. 추가의 또 다른 실시형태에서, 본 발명의 방법은 세포의 게놈 내의 H11 유전자좌에서 표적화된 통합을 위해서 사용된다. 일 실시형태에서, 적어도 하나의 통합된 폴리뉴클레오타이드는 내인성 H11 프로모터에 의해서 유도된다. 다른 실시형태에서, 본 발명의 방법은 세포의 게놈 내의 콜라겐 유전자좌에서 표적화된 통합을 위해서 사용된다. 일 실시형태에서, 적어도 하나의 통합된 폴리뉴클레오타이드는 내인성 콜라겐 프로모터에 의해서 유도된다. 추가의 또 다른 실시형태에서, 본 발명의 방법은 세포의 게놈 내의 HTRP 유전자좌에서 표적화된 통합을 위해서 사용된다. 일 실시형태에서, 적어도 하나의 통합된 폴리뉴클레오타이드는 내인성 HTRP 프로모터에 의해서 유도된다. 이론적으로, 목적하는 장소에서의 올바른 삽입 만이 내인성 프로모터에 의해서 유도된 외인성 유전자의 유전자 발현을 가능하게 할 것이다.
일부 실시형태에서, 표적화된 통합 방법을 위한 작제물 내에 포함된 1종 이상의 외인성 폴리뉴클레오타이드는 하나의 프로모터에 의해서 유도된다. 일부 실시형태에서, 작제물은 동일한 프로모터에 의해서 유도된 2개의 인접한 폴리뉴클레오타이드 사이에 하나 이상의 링커 서열을 포함하여 모이어티들 사이에서 더 큰 물리적 분리를 제공하고, 효소 기구에 대한 접근성을 최대화한다. 링커 서열의 링커 펩타이드는 모이어티들(외인성 폴리뉴클레오타이드 및/또는 그로부터 암호화된 단백질 또는 펩타이드) 간의 물리적 분리를 관련 기능에 따라서 더 가요성이거나 더 강하게 만들도록 선택된 아미노산으로 이루어질 수 있다. 링커 서열은 프로테아제에 의해서 절단 가능하거나 또는 화학적으로 절단 가능하여 별개의 모이어티를 산출할 수 있다. 링커 내의 효소 절단 부위의 예는 단백질분해 효소, 예컨대 엔테로카이나제, 인자 Xa, 트립신, 콜라게나제 및 트롬빈에 의한 전달을 위한 부위를 포함한다. 일부 실시형태에서, 프로테아제는 숙주에 의해서 자연적으로 생성된 것이거나 또는 그것은 외인성으로 도입된다. 대안적으로, 링커 내의 절단 부위는 선택된 화학물질, 예를 들어, 시아노겐 브로마이드, 하이드록실아민, 또는 저 pH에 노출될 때 절단될 수 있는 부위일 수 있다. 선택적인 링커 서열은 절단 부위의 제공이 아닌 목적을 제공할 수 있다. 링커 서열은 모이어티를 위해서 또 다른 인접한 모이어티에 대한 모이어티의 효과적인 위치결정이 적절하게 기능하는 것을 허용해야 한다. 링커는 또한 모이어티들 간의 임의의 입체 장애를 예방하기에 충분한 길이의 단순한 아미노산 서열일 수 있다. 또한, 링커 서열은 예를 들어, 인산화 부위, 바이오티닐화 부위, 설페이션 부위, γ-카복실화 부위 등을 포함하지만 이들로 제한되지 않는 번역-후 변형을 제공할 수 있다. 일부 실시형태에서, 링커 서열은 생물학적 활성 펩타이드를 단일의 바람직하지 않은 컨포메이션으로 유지하지 않도록 가요성이다. 링커는 가요성을 제공하기 위해서, 작은 측쇄를 갖는 아미노산, 예컨대 글리신, 알라닌, 및 세린으로 주로 구성될 수 있다. 일부 실시형태에서 링커 서열 중 약 80 또는 90% 이상은 글리신, 알라닌, 또는 세린 잔기, 특히 글리신 및 세린 잔기를 포함한다. 몇몇 실시형태에서, G4S 링커 펩타이드는 융합 단백질의 단부-가공 도메인과 엔도뉴클레아제 도메인을 분리한다. 다른 실시형태에서, 2A 링커 서열은 2개의 별개의 단백질이 단일 번역으로부터 생성되는 것을 허용한다. 적합한 링커 서열은 경험적으로 쉽게 식별될 수 있다. 추가로, 링커 서열의 적합한 크기 및 서열은 또한 종래의 컴퓨터 모델링 기술에 의해서 결정될 수 있다. 일 실시형태에서, 링커 서열은 자가-절단 펩타이드를 암호화한다. 일 실시형태에서, 자가-절단 펩타이드는 2A이다. 일부 다른 실시형태에서, 링커 서열은 내부 리보솜 도입 서열(Internal Ribosome Entry Sequence: IRES)을 제공한다. 일부 실시형태에서, 임의의 2개의 연속적인 링커 서열은 상이하다.
표적화된 통합을 위해서 외인성 폴리뉴클레오타이를 포함하는 작제물을 세포에 도입하는 방법은 그 자체로 공지된 세포에 대한 유전자 도입 방법을 사용함으로써 달성될 수 있다. 일 실시형태에서, 작제물은 바이러스 벡터, 예컨대 아데노바이러스 벡터, 아데노-연관된 바이러스 벡터, 레트로바이러스 벡터, 렌티바이러스 벡터, 센다이 바이러스 벡터의 골격을 포함한다. 일부 실시형태에서, 외인성 폴리뉴클레오타이드의 표적 세포(예를 들어, pAl- 11, pXTl, pRc/CMV, pRc/RSV, pcDNAI/Neo)으로의 전달 및/또는 발현 등을 위해서 플라스미드 벡터가 사용된다. 일부 다른 실시형태에서, 외인성 폴리뉴클레오타이드를 표적 세포로 전달하기 위해서 에피솜 벡터가 사용된다. 상동 재조합을 통해서 삽입, 결실 또는 치환을 도입하도록 유전자 조작하기 위해서 재조합 아데노-연관된 바이러스(rAAV)가 사용될 수 있다. 렌티바이러스와 달리, rAAV는 숙주 게놈에 통합되지 않는다. 또한, 에피솜 rAAV 벡터는 종래의 표적화 플라스미드의 형질주입과 비교할 때 훨씬 떠 높은 비율로 상동성-지향된 유전자 표적화를 매개한다. 일부 실시형태에서, iPSC의 게놈 내의 표적 부위에서 삽입, 결실 또는 치환을 도입하기 위해서 AAV6 또는 AAV2 벡터가 사용된다. 일부 실시형태에서, 본 명세서의 방법 및 조성물을 사용하여 획득된 게놈 변형된 iPSC 및 이의 유도체 세포는 표 1에 열거된 적어도 하나의 유전자형을 포함한다.
III.
게놈-조작된 iPSC의 획득 및 유지 방법
본 발명은 하나 이상의 목적하는 부위에서 하나 이상의 표적화 편집을 포함하는 게놈-조작된 iPSC를 수득 및 유지하는 방법을 제공하고, 여기서 표적화 편집은 각각의 선택된 편집 부위에서 확장된 게놈-조작된 iPSC 또는 iPSC 유래된 비-만능 세포에서 무손상이고 기능성을 유지한다. 표적화 편집은 게놈 iPSC 및 그로부터의 유도체 세포 내에 삽입, 결실, 및/또는 치환, 즉, 선택된 부위에서 표적화된 통합 및/또는 in/del을 도입한다. 직접 조작된 환자-기원의 말초 혈액 기원의 1차 효과기 세포와 비교하면, 본 명세서에 제공된 바와 같은 iPSC의 편집 및 분화를 통해서 게놈 조작된 유도체 세포를 획득하는 것의 다수의 이점은 포함하지만 이들로 제한되지 않는다: 조작된 효과기 세포에 대한 무한한 공급원; 특히 다중 조작된 양상이 관여될 때 효과기 세포의 반복되는 조작에 대한 불필요; 획득된 효과기 세포가 연장된 텔로미어를 갖고, 소모를 덜 겪어서 활기를 회복함; 효과기 세포 집단이 대부분 본 명세서에 제공된 바와 같은 조작된 iPSC의 가능한 클론성 선택으로 인해서 편집 부위, 카피 수, 대립유전자 변이, 무작위 돌연변이 및 발현 변이의 결핍과 관련하여 균질함.
특정 실시형태에서, 하나 이상의 선택된 부위에서 하나 이상의 표적화 편집을 포함하는 게놈-조작된 iPSC은 운명 유지 배지(Fate Maintenance Medium: FMM)로서 표 2에 나타낸 세포 배양 배지 중에서 연장된 기간 동안 단일 세포로서 유지, 계대배양 및 확장되고, 여기서 iPSC는 선택된 부위(들)에서 표적화 편집 및 기능성 변형을 보유한다. 배지의 성분은 표 2에 나타낸 최적의 범위 내의 양으로 배지 중에 존재할 수 있다. FMM 중에서 배양된 iPSC는 이의 미분화되고, 기저이거나 또는 미경험, 프로파일; 배양물 세정 또는 선택이 필요 없는 게놈 안정성을 계속 유지시키는 것으로 나타났고; 배상체 또는 단일층(배상체의 형성 없음)을 통한 3개의 모든 체세포 계통, 시험관내 분화; 및 테라토마에 형성에 의한 생체내 분화를 쉽게 생성한다(예를 들어, 개시내용이 본 명세서에 참조에 의해 포함된 미국 출원 제61/947,979호 참고).
일부 실시형태에서, 하나 이상의 표적화된 통합 및/또는 in/del을 포함하는 게놈-조작된 iPSC는 MEKi, GSKi 및 ROCKi를 포함하고, TGFβ 수용체/ALK5 저해제가 없거나 본질적으로 없는 배지 중에서 유지, 계대배양 및 확장되고, 여기서 iPSC는 선택된 부위에서 무손상이고 기능성 표적화 편집을 보유한다.
본 발명의 다른 양상은 iPSC의 표적화 편집을 통해서; 또는 먼저 표적화 편집에 의해서 게놈-조작된 비-만능 세포를 생성하고, 이어서 선택된/단리된 게놈-조작된 비-만능 세포를 재프로그래밍하여 비-만능 세포와 동일한 표적화 편집을 포함하는 iPSC를 수득함으로써 게놈-조작된 iPSC를 생성시키는 방법을 제공한다. 본 발명의 추가 양상은 표적화된 통합 및/또는 표적화된 in/del을 세포에 도입함으로써 재프로그래밍을 병행하여 겪는 게놈-조작된 비-만능 세포를 제공하며, 여기서 접촉된 비-만능 세포는 재프로그래밍을 위해서 충분한 조건 하에 있고, 여기서 재프로그래밍을 위한 조건은 비-만능 세포를 1종 이상의 재프로그래밍 인자 및 선택적으로 소분자와 접촉시키는 것을 포함한다. 동시 게놈-조작 및 재프로그래밍을 위한 방법의 다양한 실시형태에서, 표적화된 통합 및/또는 표적화된 in/del은 비-만능 세포를 1종 이상의 재프로그래밍 인자 및 선택적으로 소분자와 접촉시킴으로써 재프로그래밍 개시 이전에, 또는 이것에 본질적으로 부수적으로 비-만능 세포에 도입될 수 있다.
일부 실시형태에서, 병행하여 게놈-조작하고, 비-만능 세포를 재프로그래밍하기 위해서, 표적화된 통합 및/또는 in/del은 또한 비-만능 세포를 1종 이상의 재프로그래밍 인자 및 소분자와 접촉시킴으로써 재프로그래밍의 수 일 공정이 개시된 후에 비-만능 세포에 도입될 수 있고, 여기서 작제물 보유 벡터는 재프로그래밍 세포가 SSEA4, Tra181 및 CD30을 포함하지만 이들로 제한되지 않는 1종 이상의 내인성 만능 유전자의 안정한 발현을 제시하기 전에 도입된다.
일부 실시형태에서, 재프로그래밍은 비-만능 세포를 적어도 하나의 재프로그래밍 인자 및 선택적으로 TGFβ 수용체/ALK 저해제, MEK 저해제, GSK3 저해제 및 ROCK 저해제의 조합물(FRM; 표 2)과 접촉시킴으로써 개시된다. 일부 실시형태에서, 상기 임의의 방법을 통과한 게놈-조작된 iPSC는 MEK 저해제, GSK3 저해제 및 ROCK 저해제의 조합물(FMM; 표 2)을 포함하는 혼합물을 사용하여 추가로 유지 및 확장된다.
게놈-조작된 iPSC를 생성시키는 상기 방법의 일부 실시형태에서, 방법은 하나 이상의 표적화된 통합 및/또는 in/del을 PSC에 도입하여 표 1에 열거된 적어도 하나의 유전자형을 갖는 게놈-조작된 iPSC를 수득함으로써 iPSC를 게놈 조작하는 단계를 포함한다. 대안적으로, 게놈-조작된 iPSC를 생성시키는 방법은 (a) 하나 이상의 표적화 편집을 비-만능 세포에 도입하여 선택된 부위에서 표적화된 통합 및/또는 in/del을 포함하는 게놈-조작된 비-만능 세포를 수득하는 단계, 및 (b) 게놈-조작된 비-만능 세포를 1종 이상의 재프로그래밍 인자, 및 선택적으로 TGFβ 수용체/ALK 저해제, MEK 저해제, GSK3 저해제 및/또는 ROCK 저해제를 포함하는 소분자 조성물과 접촉시켜 선택된 부위에서 표적화된 통합 및/또는 in/del을 포함하는 게놈-조작된 iPSC를 수득하는 단계를 포함한다. 대안적으로, 게놈-조작된 iPSC를 생성시키는 방법은 (a) 비-만능 세포를 1종 이상의 재프로그래밍 인자, 및 선택적으로 TGFβ 수용체/ALK 저해제, MEK 저해제, GSK3 저해제 및/또는 ROCK 저해제를 포함하는 소분자 조성물과 접촉시켜 비-만능 세포의 재프로그래밍을 개시하는 단계; (b) 하나 이상의 표적화된 통합 및/또는 in/del을 게놈-조작을 위해서 재프로그래밍 비-만능 세포에 도입하는 단계; 및 (C) 선택된 부위에서 표적화된 통합 및/또는 in/del을 포함하는 클론성 게놈-조작된 iPSC를 수득하는 단계를 포함한다.
재프로그래밍 인자는 개시내용이 본 명세서에 참조에 의해 포함된 국제 출원 제PCT/US2015/018801호 및 제PCT/US16/57136호에 개시된 바와 같이 OCT4, SOX2, NANOG, KLF4, LIN28, C-MYC, ECAT1, UTF1, ESRRB, SV40LT, HESRG, CDH1, TDGF1, DPPA4, DNMT3B, ZIC3, L1TD1 및 이들의 조합물로 이루어진 군으로부터 선택된다. 1종 이상의 재프로그래밍 인자는 폴리펩타이드의 형태일 수 있다. 재프로그래밍 인자는 또한 폴리뉴클레오타이드의 형태일 수 있고, 따라서 벡터, 예컨대 레트로바이러스, 센다이 바이러스, 아데노바이러스, 에피솜, 플라스미드 및 미니-서클에 의해서 비-만능 세포에 도입된다. 특정 실시형태에서, 적어도 하나의 재프로그래밍 인자를 암호화하는 하나 이상의 폴리뉴클레오타이드가 렌티바이러스 벡터에 의해서 도입된다. 일부 실시형태에서, 하나 이상의 폴리뉴클레오타이드 에피솜 벡터에 의해서 도입된다. 다양한 다른 실시형태에서, 하나 이상의 폴리뉴클레오타이드는 센다이 바이러스 벡터에 의해서 도입된다. 일부 실시형태에서, 하나 이상의 폴리뉴클레오타이드는 플라스미드의 조합물에 의해서 도입된다(예를 들어, 개시내용이 참조에 의해 본 명세서에 포함된 미국 출원 제62/571,105호).
일부 실시형태에서, 비-만능 세포는 동일하거나 또는 상이한 선택된 부위에서 표적화된 통합을 위해서 다수의 벡터에 의해서 상이한 외인성 폴리뉴클레오타이드를 포함하는 다수의 작제물 및/또는 상이한 프로모터와 함께 이송된다. 이러한 외인성 폴리뉴클레오타이드는 자살 유전자, 또는 표적화 양상을 암호화하는 유전자, 수용체, 신호전달 분자, 전사 인자, 약제학적으로 활성인 단백질 및 펩타이드, 약물 표적 후보, 또는 iPSC 또는 이의 유도 세포의 생착, 수송, 귀소, 생존도, 자기-재생, 지속성 및/또는 생존을 촉진하는 단백질을 암호화하는 유전자를 포함할 수 있다. 일부 실시형태에서, 외인성 폴리뉴클레오타이드는 siRNA, shRNA, miRNA 및 안티센스 핵산을 포함하지만 이들로 제한되지 않는 RNA를 암호화한다. 이들 외인성 폴리뉴클레오타이드는 구성적 프로모터, 유도성 프로모터, 일시적-특이적 프로모터, 및 조직 또는 세포 유형 특이적 프로모터로 이루어진 군으로부터 선택된 하나 이상의 프로모터에 의해서 유도될 수 있다. 따라서, 폴리뉴클레오타이드는 프로모터를 활성화시키는 조건 하에 있는 경우, 예를 들어 유도제의 존재 하에서 또는 특정 분화된 세포 유형 내에서 발현성이다. 일부 실시형태에서, 폴리뉴클레오타이드는 iPSC에서 그리고/또는 iPSC로부터 분화된 세포에서 발현된다. 일 실시형태에서, 하나 이상의 자살 유전자는 구성적 프로모터, 예를 들어 CAG에 의해서 유도된 카스파제-9에 의해서 유도된다. 이들 상이한 외인성 폴리뉴클레오타이드를 포함하는 작제물 및/또는 상이한 프로모터는 비-만능 세포로 동시에 또는 연속적으로 이송될 수 있다. 다수의 작제물의 표적화된 통합에 적용된 비-만능 세포는 1종 이상의 재프로그래밍 인자를 동시에 접촉하여 게놈 조작과 병행하여 재프로그래밍을 개시하여, 세포의 동일한 풀 중에서 다수의 표적화된 통합을 포함할 수 있는 게놈-조작된 iPSC를 수득할 수 있다. 이와 같이, 이러한 견고한 방법은 동시 재프로그래밍 및 조작 전략을 가능하게 하여 하나 이상의 선택된 표적 부위 내에 통합된 다수의 양상을 갖는 클론성 게놈 조작된 hiPSC를 유도한다. 일부 실시형태에서, 본 명세서의 방법 및 조성물을 사용하여 획득된 게놈 변형된 iPSC 및 이의 유도체 세포는 표 1에 열거된 적어도 하나의 유전자형을 포함한다.
IV. 게놈-조작된 iPSC를 분화시킴으로써 유전자 조작된 비-만능 세포를 획득하는 방법
본 발명의 추가 양상은 테라토마 형성에 의한 게놈-조작된 iPSC의 생체내 분화 방법을 제공하며, 여기서 게놈-조작된 iPSC로부터 생체내에서 유래된 분화된 세포는 목적하는 부위(들)에서 표적화된 통합 및/또는 in/del을 비롯한 무손상 및 기능성 표적화 편집을 보유한다. 일부 실시형태에서, 테라토마를 통해서 게놈-조작된 iPSC로부터 생체내에서 유래된 분화된 세포는 AAVS1, CCR5, ROSA26, 콜라겐, HTRP H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1 또는 게놈 안전 하버의 기준을 충족시키는 다른 유전자좌를 포함하는 하나 이상의 목적하는 부위에서 통합된 하나 이상의 유도성 자살 유전자를 포함한다. 일부 다른 실시형태에서, 테라토마를 통해서 게놈-조작된 iPSC로부터 생체내에서 유래된 분화된 세포는 표적화 양상을 암호화하거나, 또는 줄기세포 및/또는 전구 세포의 수송, 귀소, 생존도, 자기-재생, 지속성 및/또는 생존을 촉진하는 단백질을 암호화하는 폴리뉴클레오타이드를 포함한다. 일부 실시형태에서, 하나 이상의 유도성 자살 유전자를 포함하는 테라토마를 통해서 게놈-조작된 iPSC로부터 생체내에서 유래된 분화된 세포는 면역 반응 조절 및 매개와 연관된 내인성 유전자 내에 하나 이상의 in/del을 추가로 포함한다. 일부 실시형태에서, in/del은 1종 이상의 내인성 면역관문 유전자 내에 포함된다. 일부 실시형태에서, in/del은 1종 이상의 내인성 T 세포 수용체 유전자 내에 포함된다. 일부 실시형태에서, in/del은 1종 이상의 내인성 MHC 클래스 I 억제유전자 유전자 내에 포함된다. 일부 실시형태에서, in/del은 주요 조직적합 복합체와 연관된 1종 이상의 내인성 유전자 내에 포함된다. 일부 실시형태에서, in/del은 B2M, PD1, TAP1, TAP2, 타파신, TCR 유전자를 포함하지만 이들로 제한되지 않는 1종 이상의 내인성 유전자 내에 포함된다. 일 실시형태에서, 선택된 부위(들)에서 1종 이상의 외인성 폴리뉴클레오타이드를 포함하는 게놈-조작된 iPSC는 B2M(베타-2-마이크로글로불린) 암호화 유전자에서 표적화 편집을 추가로 포함한다.
특정 실시형태에서, 본 명세서에 제공된 바와 같은 하나 이상의 유전자 변형을 포함하는 게놈-조작된 iPSC는 시험관내에서 조혈 세포 계통 또는 임의의 다른 특이적 세포 유형을 유래시키는 데 사용되며, 여기서, 유래된 비-만능 세포는 선택된 부위(들)에서 표적화 편집을 포함하는 기능성 유전자 변형을 보유한다. 일 실시형태에서, 게놈-조작된 iPSC-유래 세포는 확정적 조혈 내피세포(HE) 퍼텐셜(definitive hemogenic endothelium potential)을 갖는 중배엽 세포, 확정적 HE, CD34 조혈 세포, 조혈 줄기 및 전구 세포, 조혈 다능성 전구체(MPP), T 세포 전구체, NK 세포 전구체, 골수성 세포, 호중구 전구세포, T 세포, NKT 세포, NK 세포, B 세포, 호중구, 수지상 세포 및 대식세포를 포함하지만 이들로 제한되지 않으며, 여기서 게놈-조작된 iPSC로부터 유래된 이들 세포는 목적하는 부위(들)에서 표적화 편집을 포함하는 기능성 유전자 변형을 보유한다.
iPSC-유래 조혈 세포 계통을 수득하는 적용 가능한 분화 방법 및 조성물을 예를 들어, 개시내용이 본 명세서에 참조에 의해 포함된 국제 출원 제PCT/US2016/044122호에 설명된 것을 포함한다. 제공된 바와 같이, 조혈 세포 계통을 생성시키는 방법 및 조성물은 EB 형성이 필요 없는 무-혈청, 피더-무함유 및/또는 기질-무함유 조건 하에서 그리고 플랫폼을 배양하는 확장 가능한 단일층에서의 hiPSC를 비롯한, 만능 줄기세포로부터 유래된 확정적 조혈 내피세포(HE)를 통한 것이다. 제공된 방법에 따라서 분화될 수 있는 세포는 만능 줄기세포로부터 특히 말단 분화된 세포 및 교차분화된 세포, 만능 중간체를 통하지 않는 조혈 운명으로 직접 전이되는 다양한 계통의 세포에 전념된 전구 세포까지의 범위이다. 유사하게, 줄기세포의 분화에 의해서 생산된 세포는 다능성 줄기 또는 전구 세포로부터 말단 분화된 세포, 및 모든 그 사이의 조혈 세포 계통까지의 범위이다.
단일층 배양물 중의 만능 줄기세포로부터 조혈 계통의 세포를 분화 및 확장시키는 방법은 만능 줄기세포를 BMP 경로 활성자, 및 선택적으로, bFGF와 접촉시키는 단계를 포함한다. 제공된 바와 같이, 만능 줄기세포-유래 중배엽 세포는 만능 줄기세포로부터 배상체를 형성하지 않고 수득 및 확장된다. 이어서 중배엽 세포를 BMP 경로 활성자, bFGF 및 WNT 경로 활성자와의 접촉에 적용하여 만능 줄기세포로부터 배상체를 형성하지 않고 확정적 조혈 내피세포(HE) 퍼텐셜을 갖는 확장된 중배엽 세포를 수득한다. bFGF, 및 선택적으로, ROCK 저해제 및/또는 WNT 경로 활성자와의 후속 접촉에 의해서, 확정적 HE 퍼텐셜을 갖는 중배엽 세포는 확정적 HE 세포로 분화되고, 이것은 분화 동안 확장된다.
조혈 계통의 세포를 수득하기 위한 본 명세서에 제공된 방법은 EB-매개된 만능 줄기세포 분화보다 우수한데, 그 이유는 EB 형성은 보통 최소 세포 확장으로 이어지고, 집단에서 세포의 균질한 확장 및 균질한 분화가 요구되는 다수의 응용에 중요한 단일층 배양물을 허용하지 않고, 힘들고, 낮은 효율이기 때문이다.
제공된 단일층 분화 플랫폼은 조혈 줄기세포 및 분화된 자손, 예컨대 T, B, NKT 및 NK 세포를 유도하는 확정적 조혈 내피세포로의 분화를 가능하게 한다. 단일층 분화 전략은 향상된 분화 효율과 다양한 치료적 응용을 위한 만능 줄기세포-유래 조혈 세포의 치료적으로 관련된 수의 전달을 가능하게 하는 대규모 확장을 조합한다. 추가로, 본 명세서에 제공된 방법을 사용하는 단일층 배양은 전체 범위의 시험관내 분화, 생체외 조정, 및 생체내 장기간 조혈 자기-재생, 재구성 및 생착을 가능하게 하는 기능성 조혈 계통 세포로 이어진다. 제공된 바와 같이, iPSC 유래 조혈 계통 세포은 확정적 조혈 내피세포, 조혈 다능성 전구 세포, 조혈 줄기 및 전구 세포, T 세포 전구체, NK 세포 전구체, T 세포, NK 세포, NKT 세포, B 세포, 대식세포 및 호중구를 포함하지만 이들로 제한되지 않는다.
만능 줄기세포의 확정적 조혈 계통의 세포로의 분화를 유도하는 방법은, 하기를 포함한다: (i) 만능 줄기세포를 BMP 활성자, 및 선택적으로 bFGF와 접촉시켜, 만능 줄기세포로부터 중배엽 세포의 분화 및 확장을 개시하는 단계; (ii) 중배엽 세포를 BMP 활성자, bFGF 및 GSK3 저해제를 포함하는 조성물과 접촉시켜(여기서 조성물은 선택적으로 TGFβ 수용체/ALK 저해제가 없음), 중배엽 세포로부터 확정적 HE 퍼텐셜을 갖는 중배엽 세포의 분화 확장을 개시하는 단계; (iii) 확정적 HE 퍼텐셜을 갖는 중배엽 세포를 ROCK 저해제; bFGF, VEGF, SCF, IGF, EPO, IL6 및 IL11로 이루어진 군으로부터 선택된 1종 이상의 성장 인자 및 사이토카인; 및 선택적으로, Wnt 경로 활성자를 포함하는 조성물과 접촉시켜(여기서 조성물은 선택적으로 TGFβ 수용체/ALK 저해제가 없음), 확정적 조혈 내피세포 퍼텐셜을 갖는 만능 줄기세포-유래 중배엽 세포로부터의 확정적 조혈 내피세포의 분화 및 확장을 개시하는 단계.
일부 실시형태에서, 방법은 만능 줄기세포를 MEK 저해제, GSK3 저해제 및 ROCK 저해제를 포함하는 조성물과 접촉시켜(여기서 조성물은 TGFβ 수용체/ALK 저해제가 없음), 만능 줄기세포를 시딩 및 확장시키는 단계를 추가로 포함한다. 일부 실시형태에서, 만능 줄기세포는 iPSC, 또는 미경험 iPSC, 또는 하나 이상의 유전자 각인을 포함하는 iPSC; 및 iPSC 내에 포함된 하나 이상의 유전자 각인은 그로부터 분화된 조혈 세포에서 보유된다. 만능 줄기세포의 조혈 계통의 세포로의 유도를 위한 상기 방법의 일부 실시형태에서, 만능 줄기세포의 조혈 계통의 세포로의 분화는 배상체의 생성이 없고, 단일층 배양 형태이다.
상기 방법의 일부 실시형태에서, 얻어진 만능 줄기세포-유래 확정적 조혈 내피 세포는 CD34+이다. 일부 실시형태에서, 얻어진 확정적 조혈 내피 세포는 CD34+CD43-이다. 일부 실시형태에서, 확정적 조혈 내피 세포는 CD34+CD43-CXCR4-CD73-이다. 일부 실시형태에서, 확정적 조혈 내피 세포는 CD34+ CXCR4-CD73-이다. 일부 실시형태에서, 확정적 조혈 내피 세포는 CD34+CD43-CD93-이다. 일부 실시형태에서, 확정적 조혈 내피 세포는 CD34+ CD93-이다.
상기 방법의 일부 실시형태에서, 방법은 하기 단계를 추가로 포함한다: (i) 만능 줄기세포-유래 확정적 조혈 내피세포를 ROCK 저해제; VEGF, bFGF, SCF, Flt3L, TPO 및 IL7로 이루어진 군으로부터 선택된 1종 이상의 성장 인자 및 사이토카인; 및 선택적으로 BMP 활성자를 포함하는 조성물과 접촉시켜; 확정적 조혈 내피세포의 프레-T(pre-T) 세포 전구체로의 분화를 개시하는 단계; 및 선택적으로, (ii) 프레-T 세포 전구체를 SCF, Flt3L 및 IL7로 이루어진 군으로부터 선택된 1종 이상의 성장 인자 및 사이토카인을 포함하지만, VEGF, bFGF, TPO, BMP 활성자 및 ROCK 저해제 중 하나 이상이 없는 조성물과 접촉시켜, 프레-T 세포 전구체의 T 세포 전구체 또는 T 세포로의 분화를 개시하는 단계. 상기 방법의 일부 실시형태에서, 만능 줄기세포-유래 T 세포 전구체는 CD34+CD45+CD7+이다. 상기 방법의 일부 실시형태에서, 만능 줄기세포-유래 T 세포 전구체는 CD45+CD7+이다.
만능 줄기세포의 조혈 계통의 세포로의 유도를 위한 상기 방법의 추가의 일부 실시형태에서, 방법은 하기 단계를 추가로 포함한다: (i) 만능 줄기세포-유래 확정적 조혈 내피세포를 ROCK 저해제; VEGF, bFGF, SCF, Flt3L, TPO, IL3, IL7 및 IL15로 이루어진 군으로부터 선택된 1종 이상의 성장 인자 및 사이토카인; 및 선택적으로, BMP 활성자를 포함하는 조성물과 접촉시켜, 확정적 조혈 내피세포의 프레-NK 세포 전구체로의 분화를 개시하는 단계, (ii) 만능 줄기세포-유래 프레-NK 세포 전구체를 SCF, Flt3L, IL3, IL7 및 IL15로 이루어진 군으로부터 선택된 1종 이상의 성장 인자 및 사이토카인을 포함하는 조성물과 접촉시켜(여기서 배지는 VEGF, bFGF, TPO, BMP 활성자 및 ROCK 저해제 중 하나 이상이 없음), 프레-NK 세포 전구체의 NK 세포 전구체 또는 NK 세포로의 분화를 개시하는 단계. 일부 실시형태에서, 만능 줄기세포-유래 NK 전구세포는 CD3-CD45+CD56+CD7+이다. 일부 실시형태에서, 만능 줄기세포-유래 NK 세포는 CD3-CD45+CD56+이고, 및 선택적으로 NKp46+, CD57+ 및 CD16+에 의해서 추가로 정의된다.
따라서, 상기 분화 방법을 사용하면, iPSC 유래 조혈 세포의 하나 이상의 집단 (i) iMPP-A, iTC-A2, iTC-B2, iNK-A2, 및 iNK-B2로부터 선택된 하나 이상의 배양 배지를 사용하면, CD34+ HE 세포(iCD34); (ii) iMPP-A, iTC-A2, iTC-B2, iNK-A2 및 iNK-B2로부터 선택된 하나 이상의 배양 배지를 사용하면, 확정적 조혈 내피세포(iHE); (iii) iMPP-A, iTC-A2, iTC-B2, iNK-A2 및 iNK-B2로부터 선택된 하나 이상의 배양 배지를 사용하면, 확정적 HSC; (iv) iMPP-A를 사용하면, 다능성 전구 세포(iMPP); (v) iTC-A2, 및 iTC-B2로부터 선택된 하나 이상의 배양 배지를 사용하면, T 세포 전구체(ipro-T); (vi) iTC-B2를 사용하면 T 세포(iTC); (vii) iNK-A2, 및 iNK-B2로부터 선택된 하나 이상의 배양 배지를 사용하면, NK 세포 전구체(ipro-NK); 및/또는 (viii) NK 세포(iNK), 및 iNK-B2을 수득할 수 있다. 일부 실시형태에서, 배지는 다음과 같다:
a. iCD34-C는 ROCK 저해제, bFGF, VEGF, SCF, IL6, IL11, IGF, 및 EPO로 이루어진 군으로부터 선택된 1종 이상의 성장 인자 및 사이토카인, 및 선택적으로, Wnt 경로 활성자를 포함하고; TGFβ 수용체/ALK 저해제가 없고;
b. iMPP-A는 BMP 활성자, ROCK 저해제, 및 TPO, IL3, GMCSF, EPO, bFGF, VEGF, SCF, IL6, Flt3L 및 IL11로 이루어진 군으로부터 선택된 1종 이상의 성장 인자 및 사이토카인을 포함하고;
c. iTC-A2는ROCK 저해제; SCF, Flt3L, TPO, 및 IL7로 이루어진 군으로부터 선택된 1종 이상의 성장 인자 및 사이토카인; 및 선택적으로, BMP 활성자를 포함하고;
d. iTC-B2는 SCF, Flt3L 및 IL7로 이루어진 군으로부터 선택된 1종 이상의 성장 인자 및 사이토카인을 포함하고;
e. iNK-A2는 ROCK 저해제, 및 SCF, Flt3L, TPO, IL3, IL7 및 IL15로 이루어진 군으로부터 선택된 1종 이상의 성장 인자 및 사이토카인; 및 선택적으로, BMP 활성자를 포함하고;
f. iNK-B2는 SCF, Flt3L, IL7 및 IL15로 이루어진 군으로부터 선택된 1종 이상의 성장 인자 및 사이토카인을 포함한다.
일부 실시형태에서, 상기 방법으로부터 수득된 게놈-조작된 iPSC-유래 세포는 AAVS1, CCR5, ROSA26, 콜라겐, HTRP, H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1 또는 게놈 안전 하버의 기준을 충족시키는 다른 유전자좌를 포함하는 하나 이상의 목적하는 통합 부위 내에 통합된 하나 이상의 유도성 자살 유전자를 포함한다. 일부 다른 실시형태에서, 게놈-조작된 iPSC-유래 세포는 안전 스위치 단백질, 표적화 양상, 수용체, 신호전달 분자, 전사 인자, 약제학적으로 활성인 단백질 및 펩타이드, 약물 표적 후보, 또는 줄기세포 및/또는 전구 세포의 수송, 귀소, 생존도, 자기-재생, 지속성 및/또는 생존을 촉진하는 단백질을 암호화하는 폴리뉴클레오타이드를 포함한다. 일부 실시형태에서, 하나 이상의 자살 유전자를 포함하는 게놈-조작된 iPSC-유래 세포는 면역관문 유전자, 내인성 T 세포 수용체 유전자, 및 MHC 클래스 I 억제유전자 유전자를 포함하지만 이들로 제한되지 않는, 면역 반응 조절 및 매개와 연관된 1종 이상의 내인성 유전자 내에 포함된 하나 이상의 in/del을 추가로 포함한다. 일 실시형태에서, 하나 이상의 자살 유전자를 포함하는 게놈-조작된 iPSC-유래 세포는 B2M 유전자 내에 in/del을 추가로 포함하고, 여기서 B2M이 넉 아웃된다.
추가로, 제1 운명의 게놈-조작된 조혈 세포를 제2 운명의 게놈-조작된 조혈 세포로 얻기 위한 적용 가능한 탈분화 방법 및 조성물은 예를 들어, 개시내용이 본 명세서에 참조에 의해 포함된 국제 공개 제WO2011/159726호에 설명된 것을 포함한다. 그것에 제공된 방법 및 조성물은 재프로그래밍 동안 내인성 Nanog 유전자의 발현을 제한하고; 비-만능 중간체 세포를 중간체 세포의 목적하는 세포 유형으로의 분화를 위한 조건에 적용함으로써 출발 비-만능 세포를 비-만능 중간체 세포로 부분적으로 재프로그래밍하는 것을 허용한다. 일부 실시형태에서, 본 명세서의 방법 및 조성물을 사용하여 획득된 게놈 변형된 iPSC 및 이의 유도체 세포는 표 1에 열거된 적어도 하나의 유전자형을 포함한다.
V. 유전자 조작된 iPSC로부터 분화된 기능성 양상을 갖는 유도체 면역 세포의 치료적 용도
본 발명은 일부 실시형태에서 개시된 바와 같은 방법 및 조성물을 사용하여 게놈 조작된 iPSC로부터 분화된 기능적으로 향상된 유도체 면역 세포의 단리된 집단 또는 하위집단을 포함하는 조성물을 제공한다. 일부 실시형태에서, iPSC는 iPSC-유래 면역 세포에 보유될 수 있는 하나 이상의 표적화된 유전자 편집을 포함하며, 여기서 유전자 조작된 iPSC 및 이의 유도체 세포는 세포 기반 입양 요법에 적합하다. 일 실시형태에서, 유전자 조작된 면역 세포의 단리된 집단 또는 하위집단은 iPSC 유래 CD34 세포를 포함한다. 일 실시형태에서, 유전자 조작된 면역 세포의 단리된 집단 또는 하위집단은 iPSC 유래 HSC 세포를 포함한다. 일 실시형태에서, 유전자 조작된 면역 세포의 단리된 집단 또는 하위집단은 iPSC 유래 proT 또는 T 세포 세포를 포함한다. 일 실시형태에서, 유전자 조작된 면역 세포의 단리된 집단 또는 하위집단은 iPSC 유래 proNK 또는 NK 세포를 포함한다. 일 실시형태에서, 유전자 조작된 면역 세포의 단리된 집단 또는 하위집단은 iPSC 유래 면역 조절 세포 또는 골수 유래 억제 세포(MDSC)를 포함한다. 일부 실시형태에서, iPSC 유래 유전자 조작된 면역 세포는 개선된 치료 가능성을 위해서 생체외에서 추가로 조절된다. 일 실시형태에서, iPSC로부터 유래된 유전자 조작된 면역 세포의 단리된 집단 또는 하위집단은 미경험 T 세포, 줄기세포 기억 T 세포 및/또는 중앙 기억 T 세포의 증가된 수 또는 비를 포함한다. 일 실시형태에서, iPSC로부터 유래된 유전자 조작된 면역 세포의 단리된 집단 또는 하위집단은 타입 I NKT 세포의 증가된 수 또는 비를 포함한다. 또 다른 실시형태에서, iPSC로부터 유래된 유전자 조작된 면역 세포의 단리된 집단 또는 하위집단은 적응성 NK 세포의 증가된 수 또는 비를 포함한다. 일부 실시형태에서, iPSC로부터 유래된 유전자 조작된 CD34 세포, HSC 세포, T 세포, NK 세포, 또는 골수 유래된 억제 세포의 단리된 집단 또는 하위집단은 동종이계이다. 일부 다른 실시형태에서, iPSC로부터 유래된 유전자 조작된 CD34 세포, HSC 세포, T 세포, NK 세포 또는 MDSC의 단리된 집단 또는 하위집단은 자연 발생적이다.
일부 실시형태에서, 분화를 위한 iPSC는 효과기 세포에서 목적하는 치료 속성을 전달하도록 선택된 유전자 각인을 포함하되, 분화 동안 세포 발달 생물학이 파괴되지 않고, 유전자 각인이 상기 iPSC로부터 유래된 분화된 조혈 세포에서 보유되고 기능성이어야 한다.
일부 실시형태에서, 만능 줄기세포의 유전자 각인은 (i) 비-만능 세포를 iPSC로 재프로그래밍한 동안에 또는 후에 만능 세포 게놈에서 게놈 삽입, 결실 또는 치환을 통해 얻은 하나 이상의 유전자 변형된 양상; 또는 (ii) 공여자-, 질환- 또는 치료 반응-특이적인 공급원 특이적 면역 세포의 하나 이상의 유지 가능한 치료적 속성을 포함하되, 상기 만능 세포는 공급원 특이적 면역 세포로부터 재프로그래밍되고, iPSC는 공급원 치료적 속성을 보유하는데, 이는 또한 iPSC 유래 조혈 계통 세포 내에 포함된다.
일부 실시형태에서, 유전자 변형된 양상은 안전한 스위치 단백질, 표적화 양상, 수용체, 신호전달 분자, 전사 인자, 약제학적으로 활성인 단백질 및 펩타이드, 약물 표적 후보; 또는 iPSC 또는 이의 유도 세포의 생착, 수송, 귀소, 생존도, 자기-재생, 지속성, 면역 반응 조절 및 조정, 및/또는 생존을 촉진시키는 단백질 중 하나 이상을 포함한다. 일부 실시형태에서, 유전자 변형된 iPSC 및 이의 유도체 세포는 표 1에 열거된 유전자형을 포함한다. 일부 다른 실시형태에서, 표 1에 열거된 유전자형을 포함하는 유전자 변형된 iPSC 및 이의 유도체 세포는 (1) TAP1, TAP2, 타파신, NLRC5, PD1, LAG3, TIM3, RFXANK, CIITA, RFX5 또는 RFXAP, 및 염색체 6p21 영역 내의 임의의 유전자의 결실 또는 감소된 발현 중 하나 이상; 및 (2) 이중- 또는 다중-특이적 또는 보편적 관여자와의 결합을 위한 HLA-E, 41BBL, CD3, CD4, CD8, CD47, CD113, CD131, CD137, CD80, PDL1, A2AR, CAR, TCR, Fc 수용체 또는 표면 촉발 수용체의 도입된 또는 증가된 발현을 포함하는 추가적인 유전자 변형된 양상을 추가로 포함한다.
더 일부의 다른 실시형태에서, 조혈 계통 세포는 (i) 하나 이상의 항원 표적화 수용체 발현; (ii) 변형된 HLA; (iii) 종양 미세환경에 대한 내성; (iv) 방관자 면역 세포의 모집 및 면역 조절; (iv) 종양을 벗어난 효과가 감소된 표적에 대한 특이성의 개선 및 (v) 개선된 귀소, 지속성, 세포독성 또는 항원 탈출 구제 중 적어도 2개의 조합물에 관련된 공급원 특이적 면역 세포의 치료적 속성을 포함한다.
일부 실시형태에서, 표 1에 열거된 유전자형을 포함하는 iPSC 유도체 조혈 세포 및 상기 세포는 IL2, IL4, IL6, IL7, IL9, IL10, IL11, IL12, IL15, IL18 또는 IL21 또는 이들의 임의의 변형된 단백질을 포함하는 적어도 하나의 사이토카인 및/또는 이의 수용체를 발현하고, 적어도 CAR 및 hnCD16을 발현한다. 일부 실시형태에서, 사이토카인(들) 및 CAR(들)의 조작된 발현은 NK 세포 특이적이다. 일부 다른 실시형태에서, 사이토카인(들) 및 CAR(들)의 조작된 발현은 T 세포 특이적이다. 일 실시형태에서, 유도체 조혈 세포의 CAR은 CD19, BCMA, CD20, CD22, CD123, HER2, CD52, EGFR, GD2 및 PDL1 항원 중 임의의 하나를 인식하는 결합 도메인을 포함한다. 일부 실시형태에서, 항원 특이적 유도체 효과기 세포는 액체 종양을 표적으로 한다. 일부 실시형태에서, 항원 특이적 유도체 효과기 세포는 고형 종양을 표적으로 한다. 일부 실시형태에서, 항원 특이적 iPSC 유도체 효과기 세포는 종양 항원 탈출을 구제할 수 있다.
입양 세포 요법에 적합한 대상체에게 본 발명의 면역 세포를 도입함으로써 다양한 질환이 개선될 수 있다. 일부 실시형태에서, 제공된 바와 같은 iPSC 유도체 조혈 세포는 동종이계 입양 세포 요법을 위한 것이다. 추가로, 본 발명은 일부 실시형태에서 입양 세포 요법에 적합한 대상체에게 조성물을 도입함으로써 상기 치료 조성물의 치료적 용도를 제공하며, 여기서 대상체는 자가면역 장애; 혈액 악성종양; 고형 종양; 또는 HIV, RSV, EBV, CMV, 아데노바이러스 또는 BK 폴리오마 바이러스와 관련된 감염을 갖는다.
혈액 악성종양의 예는 급성 및 만성 백혈병(급성 골수성 백혈병(AML), 급성 림프모구성 백혈병(ALL), 만성 골수성 백혈병(CML), 림프종, 비호지킨 림프종(NHL), 호지킨병, 다발성 골수종 및 골수이형성 증후군을 포함하지만 이들로 제한되지 않는다. 고형 암의 예는 뇌, 전립선, 유방, 폐, 결장, 자궁, 피부, 간, 뼈, 췌장, 난소, 고환, 방광, 신장, 머리, 목, 위, 자궁경부, 직장, 후두 및 식도의 암을 포함하지만 이들로 제한되지 않는다. 다양한 자가면역 장애의 예는 질환의 예는 원형 탈모증, 자가면역성 용혈성 빈혈, 자가면역성 간염, 피부근육염, 당뇨병(1형), 일부 형태의 소아 특발성 관절염, 사구체신염, 그레이브스병, 길랑-바레 증후군, 특발성 혈소판 감소성 자반증, 중증 근무력증, 일부 형태의 심근염, 다발성 경화증, 천포창/유사천포창, 악성빈혈, 결절성 다발동맥염, 다발근육염, 원발성 담즙성 간병변, 건선, 류마티스 관절염, 피부경화증/전신 경화증, 쇼그렌 증후군, 전신성 홍반성 낭창, 일부 형태의 갑상선염, 일부 형태의 포도막염, 백반증, 다발혈관염 육아종증(베게너 육아종증)을 포함하지만, 이들로 제한되지 않다. 바이러스 감염의 예는 HIV-(인간 면역결핍 바이러스), HSV-(단순 포진 바이러스), KSHV-(카포시 육종-연관 허피스바이러스), RSV-(호흡기 세포융합 바이러스), EBV-(엡스타인-바르 바이러스), CMV-(사이토메갈로바이러스), VZV(수두 대상 포진 바이러스), 아데노바이러스-, 렌티바이러스-, BK 폴리오마바이러스-연관 장애를 포함하지만 이들로 제한되지 않는다.
본 명세서에 개시된 실시형태의 유래된 조혈 계통 세포를 사용한 치료는 증상에 따라서 또는 재발 예방을 위해서 수행될 수 있다. 용어 "치료하는", "치료" 등은 일반적으로 목적으로 하는 약학적 및/또는 생리적 효과를 얻는 것을 의미하기 위해 본 명세서에서 사용된다. 효과는 질환을 완전히 또는 부분적으로 방지한다는 면에서 예방적일 수 있고/있거나 질환 및/또는 질환에 기여하는 유해 효과에 대한 부분적 또는 완전한 치유의 면에서 치료적일 수 있다. 본 명세서에 사용되는 바와 같은 "치료"는 대상체에서 질환의 임의의 개입을 포괄하며, 질환의 성향이 있을 수 있지만, 아직 그것이 있는 것으로 진단되지 않은 대상체에서 질환이 생기는 것을 방지하는 것; 질환을 저해하는 것, 즉, 그의 발생을 저지하는 것; 또는 질환을 없애는 것, 즉, 질환의 퇴보를 야기하는 것을 포함한다. 치료제 또는 조성물은 질환 또는 손상의 개시 전에, 동안에 또는 후에 투여될 수 있다. 치료가 환자의 바람직하지 않은 임상 증상을 안정화시키거나 또는 감소시키는 경우 진행 중인 질환의 치료는 또한 특정 관심 대상을 가진다. 특정 실시형태에서, 치료를 필요로 하는 대상체는 세포 요법에 의해서 적어도 하나의 연관된 증상이 포함, 개선 및/또는 향상될 수 있는 질환, 병태 및/또는 손상을 갖는다. 특정 실시형태는 세포 요법이 필요한 대상체가 골수 또는 줄기세포 이식을 위한 후보, 화학요법 또는 방사선 조사 요법을 받은 대상체, 과증식성 장애 또는 암, 예를 들어, 조혈계의 과증식성 장애 또는 암을 갖거나 또는 가질 위험에 있는 대상체, 종양, 예를 들어, 고형 종양이 있거나 또는 발생할 위험에 있는 대상체, 바이러스 감염 또는 바이러스 감염과 관련된 질환을 갖거나 또는 가질 위험에 있는 대상체를 포함하지만, 이들로 제한되지 않는다는 것을 고려한다.
본 명세서에 개시된 실시형태의 유래된 조혈 계통 세포를 포함하는 치료에 대한 반응을 평가하는 경우, 반응은 하기 중 적어도 하나를 포함하는 기준에 의해서 측정될 수 있다: 임상 유익비, 사망까지의 생존, 병리학적 완전 반응, 병리학적 반응의 반-정량적 측정, 임상적 완전 관해, 임상적 부분적 관해, 임상적으로 안정적인 질환, 재발이 없는 생존, 무전이 생존, 무질환 생존, 순환 종양 세포 감소, 순환 마커 반응 및 RECIST (Response Evaluation Criteria In Solid Tumors) 기준.
개시된 바와 같은 유래된 조혈 계통 세포를 포함하는 치료 조성물은 치료 전, 동안, 및/또는 후에 대상체에 투여될 수 있다. 이와 같이, 병용 치료법의 방법은 추가의 치료제의 사용 전, 동안, 및/또는 후에 iPSC 유래 면역 세포의 투여 또는 제조를 포함할 수 있다. 상기에 제공된 바와 같이, 하나 이상의 추가의 치료제는 펩타이드, 사이토카인, 면역관문 저해제, 미토겐, 성장 인자, 작은 RNA, dsRNA(이중 가닥 RNA), 단핵 혈액 세포, 피더 세포, 피더 세포 성분 또는 이의 대체 인자, 고려되는 하나 이상의 폴리핵산을 포함하는 벡터, 항체, 화학치료제, 또는 방사성 모이어티, 또는 면역조절 약물(IMiD)을 포함한다. iPSC 유래 면역 세포의 투여는 추가적인 치료 투여로부터 수 시간, 수 일 또는 심지어 수 주 시간적으로 분리될 수 있다. 추가적으로 또는 대안적으로, 투여는 항신생물제, 비-약물 치료법, 예를 들어, 수술과 같은, 그러나 비제한적으로, 다른 생물학적 활성자 또는 양상과 병용될 수 있다.
병용 세포 요법의 일부 실시형태에서, 치료 조합물은 본 명세서에 제공된 iPSC 유래 조혈 계통 세포 및 항체 또는 항체 단편인 추가적인 치료제를 포함한다. 일부 실시형태에서, 항체는 단클론성 항체이다. 일부 실시형태에서, 항체는 인간화된 항체, 인간화된 단클론성 항체 또는 키메라 항체일 수 있다. 일부 실시형태에서, 항체 또는 항체 단편은 바이러스 항원에 특이적으로 결합한다. 다른 실시형태에서, 항체 또는 항체 단편은 종양 항원에 특이적으로 결합한다. 일부 실시형태에서, 종양 또는 바이러스 특이적 항원은 이의 사멸 능력을 향상시키기 위해 투여된 iPSC 유래 조혈 계통 세포를 활성화시킨다. 일부 실시형태에서, 투여된 iPSC 유래 조혈 계통 세포에 추가의 치료제로서 병용 치료에 적합한 항체는 항-CD20(예를 들어, 리툭시맙, 벨투주맙, 오파투무맙, 유블리툭시맙, 오카라투주맙, 오비누투주맙), 항-HER2(예를 들어, 트라스투주맙, 퍼투주맙), 항-CD52(예를 들어, 알렘투주맙), 항-EGFR(예를 들어, 서툭시맙), 항-GD2(예를 들어, 디누툭시맙), 항-PDL1(예를 들어, 아벨루맙), 항-CD38(예를 들어, 다라투무맙, 이사툭시맙, MOR202), 항-CD123(예를 들어, 7G3, CSL362), 항-SLAMF7(엘로투주맙) 및 이들의 인간화된 또는 Fc 변형된 변이체 또는 단편 또는 이들의 기능성 등가물 또는 바이오시밀러를 포함하지만 이들로 제한되지 않는다.
일부 실시형태에서, 추가 치료제는 1종 이상의 면역관문 저해제를 포함한다. 면역관문은, 저해되지 않는 경우 면역 반응을 억제 또는 하향조절할 수 있는 세포 분자, 종종 세포 표면 분자를 지칭한다. 면역관문 저해제는 면역관문 유전자 발현 또는 유전자 생성물을 감소시킬 수 있거나 면역관문 분자의 활성을 감소시킬 수 있는 길항제이다. 본 명세서에 제공된 바와 같은 NK 또는 T 세포를 포함하는 유도체 효과기 세포와의 병용 요법에 적합한 면역관문 저해제는 PD-1(Pdcdl, CD279), PDL-1(CD274), TIM-3(Havcr2), TIGIT(WUCAM 및 Vstm3), LAG-3(Lag3, CD223), CTLA-4(Ctla4, CD152), 2B4(CD244), 4-1BB(CD137), 4-1BBL(CD137L), A2aR, BATE, BTLA, CD39(Entpdl), CD47, CD73(NT5E), CD94, CD96, CD160, CD200, CD200R, CD274, CEACAM1, CSF-1R, Foxpl, GARP, HVEM, IDO, EDO, TDO, LAIR-1, MICA/B, NR4A2, MAFB, OCT-2(Pou2f2), 레티노산 수용체 알파(Rara), TLR3, VISTA, NKG2A/HLA-E, 및 저해성 KIR(예를 들어, 2DL1, 2DL2, 2DL3, 3DL1 및 3DL2)의 길항제를 포함하지만 이들로 제한되지 않는다.
제공된 유도체 효과기 세포를 포함하는 병용 요법의 일부 실시형태는 면역관문 분자를 표적으로 하는 적어도 1종의 저해제를 추가로 포함한다. 제공된 유도체 효과기 세포와의 병용 요법의 일부 다른 실시형태는 2종, 3종 또는 그 초과의 면역관문 분자가 표적화되도록 2종, 3종 또는 그 초과의 저해제를 포함한다. 일부 실시형태에서, 본 명세서에 기재된 바와 같은 병용 요법을 위한 효과기 세포는 제공된 바와 같은 유도체 NK 세포이다. 일부 실시형태에서, 본 명세서에 기재된 바와 같은 병용 요법을 위한 효과기 세포는 유도체 NK 세포이다. 일부 실시형태에서, 병용 요법을 위한 유도체 NK 또는 T 세포는 본 명세서에 제공된 바와 같이 기능적으로 향상된다. 일부 실시형태에서, 2종, 3종 또는 그 초과의 면역관문 저해제는 유도체 효과기 세포와 함께, 이것의 투여 이전에 또는 투여 후에 병용 요법으로 투여될 수 있다. 일부 실시형태에서, 2종 이상의 면역관문 저해제가 동시에 또는 한번에 하나씩(순차적으로) 투여된다.
일부 실시형태에서, 상기 면역관문 분자 중 임의의 것을 저해하는 길항제는 항체이다. 일부 실시형태에서, 면역관문 저해성 항체는 뮤린 항체, 인간 항체, 인간화된 항체, 낙타 Ig, 상어 중쇄-단독 항체(VNAR), Ig NAR, 키메라 항체, 재조합 항체 또는 이의 항체 단편일 수 있다. 항체 단편의 비제한적인 예는 Fab, Fab', F(ab)'2, F(ab)'3, Fv, 단일 쇄 항원 결합 단편(scFv), (scFv)2, 다이설파이드 안정화된 Fv(dsFv), 미니바디, 다이아바디, 트라이아바디, 테트라바디, 단일-도메인 항원 결합 단편(sdAb, 나노바디), 재조합 중쇄-단독 항체(VHH) 및 전체 항체의 결합 특이성을 보유하는 다른 항체 단편(이것은 제조하기에 더 비용 효과적일 수 있거나, 보다 용이하게 사용될 수 있거나, 전체 항체보다 더 민감할 수 있음)을 포함한다. 일부 실시형태에서, 1종 또는 2종 또는 3종 또는 그 초과의 면역관문 저해제는 아테졸리주맙, 아벨루맙, 더발루맙, 이필리무맙, IPH4102, IPH43, IPH33, 리릴루맙, 모날리주맙, 니볼루맙, 펨브롤리주맙 및 이들의 유도체 또는 기능성 등가물 중 적어도 1종을 포함한다.
유도체 효과기 세포 및 하나 이상의 관문 저해제를 포함하는 병용 요법은 피부 T-세포 림프종, 비호지킨 림프종(NHL), 균상 식육종, 파제트병모양망상증(파제트병모양망상증), 시자리 증후군(Sezary syndrome), 육아종 이완 피부(Granulomatous slack skin), 림프종양구진증(Lymphomatoid papulosis), 만성 태선양 비강진(Pityriasis lichenoides chronica), 급성 태선상두진상비강진(Pityriasis lichenoides et varioliformis acuta), CD30+ 피부 T-세포 림프종, 이차 피부 CD30+ 거대 세포 림프종, 비-균상 식육종 CD30 피부 거대 T-세포 림프종, 다형성 T-세포 림프종, 레너트 림프종, 피하 T-세포 림프종, 혈관중심성 림프종(angiocentric lymphoma), 아구성 NK-세포 림프종, B-세포 림프종, 호지킨 림프종(HL), 두경부 종양; 편평 세포 암종, 횡문근육종, 루이스 폐암종(Lewis lung carcinoma: LLC), 비소세포 폐암, 식도 편평 세포 암종, 식도 선암종, 신장 세포 암종(RCC), 결장직장 암(CRC), 급성 골수 백혈병(AML), 유방암, 위암, 전립선 소세포 신경내분비 암종(prostatic small cell neuroendocrine carcinoma: SCNC), 간암, 교모세포종, 간암, 구강 편평 세포 암종, 췌장암, 유두갑상선암, 간내 담도세포 암종, 간세포 암종, 골암, 전이 및 비인두 암종을 포함하지만 이들로 제한되지 않는 액체암 및 고형암의 치료에 적용 가능하다.
일부 실시형태에서, 본 명세서에 제공된 바와 같은 유도체 효과기 세포 이외에, 치료적 용도를 위한 조합물은 화학치료제 또는 방사성 모이어티를 포함하는 1종 이상의 추가 치료제를 포함한다. 화학치료제는 세포독성 항신생물제, 즉, 우선적으로 신생 세포를 사멸시키거나 빠르게 증식하는 세포의 세포 주기를 파괴하거나 줄기 암 세포를 퇴치하고, 신생 세포의 성장을 예방하거나 감소시키기 위해 치료학적으로 사용되는 화학제를 지칭한다. 화학치료제는 또한, 때때로 항신생 또는 세포독성 약물 또는 작용제로서 지칭되고, 당업계에 널리 공지되어 있다.
일부 실시형태에서, 화학치료제는 안트라사이클린, 알킬화제, 알킬 설포네이트, 아지리딘, 에틸렌이민, 메틸렌아민, 질소 머스터드, 나이트로소유레아, 항생제, 항대사물질, 엽산 유사체, 퓨린 유사체, 피리미딘 유사체, 효소, 포도필로톡신, 백금-함유제, 인터페론 및 인터류킨을 포함한다. 예시적인 화학치료제는 알킬화제(사이클로포스포아마이드, 메클로르에타민, 메팔린, 클로람부실, 헤아메틸멜라민, 티오테파, 부설판, 카무스틴, 로무스틴, 세무스틴), 항대사물질(메토트렉세이트, 플루오로유라실, 플록수리딘, 사이타라빈, 6-머캅토퓨린, 티오구아닌, 펜토스타틴), 빈카 알칼로이드(빈크리스틴, 빈블라스틴, 빈데신), 에피도필로톡신(에토포사이드, 에토포사이드 오쏘퀴논, 및 테니포사이드), 항생제(다우노루비신, 독소루비신, 미톡산트론, 비산트렌, 악티노마이신 D, 플리카마이신, 퓨로마이신 및 그라미시딘 D), 파클리탁셀, 콜히친, 사이토칼라신 B, 에메틴, 메이탄신 및 암사크린을 포함하지만, 이들로 제한되지 않는다. 추가적인 작용제는 아민글루테티미드, 시스플라틴, 카보플라틴, 미토마이신, 알트레타민, 사이클로포스포아마이드, 로무스틴(CCNU), 카무스틴(BCNU), 이리노테칸(CPT-11), 알렘투자맙, 알트레타민, 아나스트로졸, L-아스파라기나제, 아자시티딘, 베바시주맙, 벡사로텐, 블레오마이신, 보르테조밉, 부설판, 칼루스테론, 카페시타빈, 셀레콕십, 세툭시맙, 클라드리빈, 클로푸라빈, 사이타라빈, 다카르바진, 데니류킨 디프티톡스, 다이에틀스틸베스트롤, 도세탁셀, 드로모스타놀론, 에피루비신, 에를로티닙, 에스트라무스틴, 에토포사이드, 에티닐 에스트라다이올, 엑셈스탄, 플록수리딘, 5-플루오로유라실, 플루다라빈, 플루타마이드, 풀베스트란트, 게피티닙, 겜시타빈, 고세렐린, 하이드록시유레아, 이브리투모맙, 이다루비신, 이포스파마이드, 이마티닙, 인터페론 알파(2a, 2b), 이리노테칸, 레트로졸, 류코보린, 류플로라이드, 레바미졸, 메클로르에타민, 메게스트롤, 멜팔린, 머캅토퓨린, 메토트렉세이트, 메톡스살렌, 미토마이신 C, 미토탄, 미톡산트론, 난드롤론, 노페투모맙, 옥살리플라틴, 파클리탁셀, 파미드로네이트, 페메트렉세드, 페가데마제, 페가스파라가제, 펜토스타틴, 피포브로만, 플리카마이신, 폴리페프로산, 포르피머, 프로카바진, 퀴나크린, 리툭시맙, 사르그라모스팀, 스트렙토조신, 타목시펜, 테모졸로마이드, 테니포사이드, 테스톨락톤, 티오구아닌, 티오테파, 토페테칸, 토레미펜, 토시투모맙, 트라스투주맙, 트레티노인, 유라실 머스터드, 발루비신, 비노렐빈, 및 졸레드로네이트를 포함한다. 다른 적합한 작용제는 화학치료제 또는 방사선치료제로서 인간 용도로 승인된 것(승인될 것을 포함) 및 당업계에 공지된 것이다. 이러한 작용제는 다수의 표준 의사 및 종양학자 문헌을 통해(예를 들어 문헌[Goodman & Gilman's The Pharmacological Basis of Therapeutics, Ninth Edition, McGraw-Hill, N.Y., 1995]) 또는 국립 암 연구소 웹사이트(fda.gov/cder/cancer/druglistfrarne.htm)를 통해(둘 다 시간에 따라 업데이트됨) 언급될 수 있다.
면역조절 약물(IMiD), 예를 들어, 탈리도마이드, 레날리도마이드 및 포말리도마이드는 NK 세포와 T 세포를 둘 다 자극한다. 본 명세서에 제공된 바와 같이, IMiD는 암 치료를 위해서 iPSC 유래 치료 면역 세포와 함께 사용될 수 있다.
치료 조성물에 포함된 iPSC 유래 조혈 계통 세포의 단리된 집단 이외에, 환자에 투여하기에 적합한 조성물은 하나 이상의 약제학적으로 허용 가능한 담체(첨가제) 및/또는 희석제(예를 들어, 약제학적으로 허용 가능한 배지, 예를 들어, 세포 배양 배지) 또는 다른 약제학적으로 허용 가능한 성분을 추가로 포함할 수 있다. 약제학적으로 허용 가능한 담체 및/또는 희석제는 투여될 특정 조성물뿐만 아니라 치료 조성물을 투여하는데 사용되는 특정 방법에 의해서 부분적으로 결정된다. 따라서, 본 발명의 치료 조성물의 광범위한 적합한 제형이 존재한다(개시내용이 참조에 의해서 본 명세서에 포함된 문헌[Remington's Pharmaceutical Sciences, 17th ed. 1985] 참고).
일 실시형태에서, 치료 조성물은 본 명세서에 개시된 방법 및 조성물에 의해서 제조된 만능 세포 유래 T 세포를 포함한다. 일 실시형태에서, 치료 조성물은 본 명세서에 개시된 방법 및 조성물에 의해서 제조된 만능 세포 유래 NK 세포를 포함한다. 일 실시형태에서, 치료 조성물은 본 명세서에 개시된 방법 및 조성물에 의해서 제조된 만능 세포 유래 CD34 + HE 세포를 포함한다. 일 실시형태에서, 치료 조성물은 본 명세서에 개시된 방법 및 조성물에 의해서 제조된 만능 세포 유래 HSC를 포함한다. 일 실시형태에서, 치료 조성물은 본 명세서에 개시된 방법 및 조성물에 의해서 제조된 만능 세포 유래 MDSC를 포함한다. 본 명세서에 개시된 바와 같은 iPSC 유래 조혈 계통 세포의 집단을 포함하는 치료 조성물은 정맥내, 복막내 또는 장내 또는 기관 투여 방법에 의해서 또는 목적하는 치료 목적에 영향을 주기 위해서 다른 적합한 화합물과 조합하여 별개로 투여될 수 있다.
이들 약제학적으로 허용 가능한 담체 및/또는 희석제는 약 3 내지 약 10의 치료 조성물의 pH를 유지시키기에 충분한 양으로 존재할 수 있다. 이와 같이, 완충제는 총 조성물을 기준으로 중량에 따라 약 5%만큼일 수 있다. 전해질, 예를 들어, 그러나 비제한적으로, 염화나트륨 및 염화칼륨이 또한 치료 조성물 중에 포함될 수 있다. 일 양상에서, 치료 조성물의 pH는 약 4 내지 약 10의 범위이다. 대안적으로, 치료 조성물의 pH는 약 5 내지 약 9, 약 6 내지 약 9 또는 약 6.5 내지 약 8의 범위이다. 또 다른 실시형태에서, 치료 조성물은 상기 pH 범위 중 하나의 pH를 갖는 완충제를 포함한다. 또 다른 실시형태에서, 치료 조성물은 약 7의 pH를 갖는다. 대안적으로, 치료 조성물은 약 6.8 내지 약 7.4 범위의 pH를 갖는다. 또 다른 추가 실시형태에서, 치료 조성물은 약 7.4의 pH를 갖는다.
본 발명은 또한, 부분적으로, 본 발명의 특정 조성물 및/또는 배양물에서의 약제학적으로 허용되는 세포 배양 배지의 용도를 제공한다. 이러한 조성물은 인간 대상체에 투여하기에 적합하다. 일반적으로 말하면, 본 발명의 실시형태에 따른 iPSC 유래 면역 세포의 유지, 성장, 및/또는 건강을 지지하는 임의의 배지는 약제학적 세포 배양 배지로서 사용하기에 적합하다. 특정 실시형태에서, 약제학적으로 허용되는 세포 배양 배지는 혈청-무함유 및/또는 피더-무함유 배지이다. 다양한 실시형태에서, 혈청-무함유 배지는 동물성이 아니고(animal-free), 선택적으로, 단백질-무함유일 수 있다. 선택적으로, 배지는 생약제학적으로 허용되는 재조합 단백질을 함유할 수 있다. 동물성이 아닌 배지는 성분이 비-동물 공급원로부터 유래된 배지를 지칭한다. 재조합 단백질은 동물성이 아닌 배지에서 천연 동물 단백질을 대체하며, 영양소는 합성, 식물 또는 미생물 공급원으로부터 얻어진다. 대조적으로, 단백질 무함유 배지는 단백질이 실질적으로 존재하지 않는 것으로서 규정된다. 당업자는, 상기 배지의 예가 예시적이고 어떠한 방식으로도 본 발명에서 사용하기에 적합한 배지의 제형을 제한하지 않는다는 것을 인식할 것이다.
단리된 만능 줄기세포 유래 조혈 계통 세포는 적어도 50%, 60%, 70%, 80%, 90%, 95%, 98%, 또는 99%의 T 세포, NK 세포, NKT 세포, proT 세포, proNK 세포, CD34+ HE 세포, HSC, B 세포, 골수-유래 억제 세포(MDSC), 조절 대식세포, 조절 수지상 세포 또는 간엽 기질 세포를 가질 수 있다. 일부 실시형태에서, 단리된 만능 줄기세포 유래 조혈 계통 세포는 약 95% 내지 약 100%의 T 세포, NK 세포, proT 세포, proNK 세포, CD34+ HE 세포 또는 골수-유래 억제 세포(MDSC)를 갖는다. 일부 실시형태에서, 본 발명은 세포 요법을 필요로 하는 대상체를 치료하기 위한 정제된 T 세포 또는 NK 세포를 갖는 치료 조성물, 예컨대, 약 95%의 T 세포, NK 세포, proT 세포, proNK 세포, CD34+ HE 세포 또는 골수-유래 억제 세포(MDSC)의 단리된 집단을 갖는 조성물을 제공한다.
일 실시형태에서, 병용 세포 요법은 치료 항체 또는 이의 단편 및 표 1에 열거된 유전자형을 포함하는 게놈 조작된 iPSC로부터 유래된 NK 세포의 집단을 포함하며, 여기서 유래된 NK 세포는 hnCD16 및 CAR을 포함한다. 또 다른 실시형태에서, 병용 세포 요법은 치료 항체 또는 이의 단편 및 표 1에 열거된 유전자형을 포함하는 게놈 조작된 iPSC로부터 유래된 T 세포의 집단을 포함하며, 여기서 유래된 T 세포는 hnCD16 및 CAR을 포함한다. 일부 실시형태에서, 병용 세포 요법은 리툭시맙, 벨투주맙, 오파투무맙, 유블리툭시맙, 오카라투주맙, 오비누투주맙, 트라스투주맙, 퍼투주맙, 알렘투주맙, 서툭시맙, 디누툭시맙, 아벨루맙, 다라투무맙, 이사툭시맙, MOR202, 7G3, CSL362 및 엘로투주맙 중 적어도 1종; 및 표 1에 열거된 유전자형을 포함하는 게놈 조작된 iPSC로부터 유래된 NK 또는 T 세포의 집단을 포함하며, 여기서 유래된 NK 또는 T 세포는 hnCD16 및 CAR을 포함한다. 추가의 일부 다른 실시형태에서, 병용 세포 요법은 엘로투주맙, 및 표 1에 열거된 유전자형을 포함하는 게놈 조작된 iPSC로부터 유래된 NK 또는 T 세포의 집단을 포함하며, 여기서 유래된 NK 또는 T 세포는 hnCD16 및 CD19, BCMA, CD38, CD20, CD22 또는 CD123을 표적으로 하는 CAR을 포함한다. 추가의 일부 추가적인 실시형태에서, 병용 세포 요법은 리툭시맙, 및 표 1에 열거된 유전자형을 포함하는 게놈 조작된 iPSC로부터 유래된 NK 또는 T 세포의 집단을 포함하며, 여기서 유래된 NK 또는 T 세포는 hnCD16 및 CAR 및 하나 이상의 외인성 사이토카인을 포함한다.
당업자는, 본 명세서의 방법 및 조성물을 기초로 하여 iPSC로부터 유래된 자가 및 동종이계 조혈 계통 세포 둘 모두가 전술한 바와 같은 세포 치료법에서 사용될 수 있다는 것을 이해할 것이다. 자가 이식에 대하여, 유래된 조혈 계통 세포의 단리된 집단은 환자와 완전 또는 부분 HLA-매칭된다. 또 다른 실시형태에서, 유래된 조혈 계통 세포는 대상체에 HLA-매칭되지 않고, 여기서 유래된 조혈 계통 세포는 HLA I 및 HLA II 널을 갖는 NK 세포 또는 T 세포이다.
일부 실시형태에서, 치료 조성물 중의 유래된 조혈 계통 세포의 수는 용량당 적어도 0.1×105개 세포, 적어도 1×105개 세포, 적어도 5×105개 세포, 적어도 1×106개 세포, 적어도 5×106개 세포, 적어도 1×107개 세포, 적어도 5×107개 세포, 적어도 1×108개 세포, 적어도 5×108개 세포, 적어도 1×109개 세포 또는 적어도 5×109개 세포이다. 일부 실시형태에서, 치료 조성물 중의 유래된 조혈 계통 세포의 수는 용량당 약 0.1×105개 세포 내지 약 1×106개 세포; 용량당 약 0.5×106개 세포 내지 약 1×107개 세포; 용량당 약 0.5×107개 세포 내지 약 1×108개 세포; 용량당 약 0.5×108개 세포 내지 약 1×109개 세포; 용량당 약 1×109개 세포 내지 약 5×109개 세포; 용량당 약 0.5×109개 세포 내지 약 8×109개 세포; 용량당 약 3×109개 세포 내지 약 3×1010개 세포 또는 이들 사이의 임의의 범위이다. 일반적으로, 1×108개 세포/용량은 60kg 환자에 대해서 1.67×106개 세포/㎏으로 변환된다.
일 실시형태에서, 치료 조성물 중의 유래된 조혈 계통 세포의 수는 부분 또는 단일 제대혈 중의 면역 세포의 수이거나 또는 적어도 0.1×105개 세포/㎏ 체중, 적어도 0.5×105개 세포/㎏ 체중, 적어도 1×105개 세포/㎏ 체중, 적어도 5×105개 세포/㎏ 체중, 적어도 10×105개 세포/㎏ 체중, 적어도 0.75×106개 세포/㎏ 체중, 적어도 1.25×106개 세포/㎏ 체중, 적어도 1.5×106개 세포/㎏ 체중, 적어도 1.75×106개 세포/㎏ 체중, 적어도 2×106개 세포/㎏ 체중, 적어도 2.5×106개 세포/㎏ 체중, 적어도 3×106개 세포/㎏ 체중, 적어도 4×106개 세포/㎏ 체중, 적어도 5×106개 세포/㎏ 체중, 적어도 10×106개 세포/㎏ 체중, 적어도 15×106개 세포/㎏ 체중, 적어도 20×106개 세포/㎏ 체중, 적어도 25×106개 세포/㎏ 체중, 적어도 30×106개 세포/㎏ 체중, 1×108개 세포/㎏ 체중, 5×108개 세포/㎏ 체중 또는 1×109개 세포/㎏ 체중이다.
일 실시형태에서, 유래된 조혈 계통 세포의 용량이 대상체에게 전달된다. 예시적인 일 실시형태에서, 대상체에게 제공되는 세포의 유효량은 적어도 2×106개 세포/㎏, 적어도 3×106개 세포/㎏, 적어도 4×106세포/㎏, 적어도 5×106개 세포/㎏, 적어도 6×106개 세포/㎏, 적어도 7×106개 세포/㎏, 적어도 8×106개 세포/㎏, 적어도 9×106개 세포/㎏, 또는 적어도 10×106개 세포/㎏ 또는 그 초과 개수의 세포/㎏이고, 모든 사이의 용량의 세포를 포함한다.
또 다른 예시적인 실시형태에서, 대상체에게 제공되는 세포의 유효량은 약 2×106개 세포/㎏, 약 3×106개 세포/㎏, 약 4×106세포/㎏, 약 5×106개 세포/㎏, 약 6×106개 세포/㎏, 약 7×106개 세포/㎏, 약 8×106개 세포/㎏, 약 9×106 세포/㎏ 또는 약 10×106개 세포/㎏ 또는 그 초과 개수의 세포/㎏이고, 모든 사이의 용량의 세포를 포함한다.
또 다른 예시적인 실시형태에서, 대상체에게 제공되는 세포의 유효량은 약 2×106 세포/㎏ 내지 약 10×106개 세포/㎏, 약 3×106 세포/㎏ 내지 약 10×106개 세포/㎏, 약 4×106 세포/㎏ 내지 약 10×106개 세포/㎏, 약 5×106 세포/㎏ 내지 약 10×106개 세포/㎏, 2×106 세포/㎏ 내지 약 6×106개 세포/㎏, 2×106 세포/㎏ 내지 약 7×106개 세포/㎏, 2×106 세포/㎏ 내지 약 8×106개 세포/㎏, 3×106 세포/㎏ 내지 약 6×106개 세포/㎏, 3×106 세포/㎏ 내지 약 7×106개 세포/㎏, 3×106 세포/㎏ 내지 약 8×106개 세포/㎏, 4×106 세포/㎏ 내지 약 6×106개 세포/㎏, 4×106 세포/㎏ 내지 약 7×106개 세포/㎏, 4×106 세포/㎏ 내지 약 8×106개 세포/㎏, 5×106 세포/㎏ 내지 약 6×106개 세포/㎏, 5×106 세포/㎏ 내지 약 7×106개 세포/㎏, 5×106 세포/㎏ 내지 약 8×106개 세포/㎏, 또는 6×106세포/㎏ 내지 약 8×106개 세포/㎏이고, 모든 사이의 용량의 세포를 포함한다.
일부 실시형태에서, 유래된 조혈 계통 세포의 치료적 용도는 단일-용량 치료이다. 일부 실시형태에서, 유래된 조혈 계통 세포의 치료적 용도는 다중-용량 치료이다. 일부 실시형태에서, 다중-용량 치료는 매일, 3일마다, 7일마다, 10일마다, 15일마다, 20일마다, 25일마다, 30일마다, 35일마다, 40일마다, 45일마다, 또는 50일마다, 또는 이들 사이의 임의의 일수마다 1회 용량이다.
본 발명의 유래된 조혈 계통 세포의 집단을 포함하는 조성물은 멸균성일 수 있고, 인간 환자에게 투여하기에 적합하고 준비될 수 있다(즉, 임의의 추가 가공 없이 투여될 수 있다). 투여를 위해 준비된 세포 기반 조성물은, 조성물이 대상체에 이식 또는 투여 전에 임의의 추가 가공 또는 조작을 필요로 하지 않음을 의미한다. 다른 실시형태에서, 본 발명은 하나 이상의 작용제와 함께 투여하기 전에 확장되고/되거나 조절되는 유래된 조혈 계통 세포의 단리된 집단을 제공한다. 재조합 TCR 또는 CAR을 발현시키기 위해 유전적으로 조작된 유래된 조혈 계통 세포에 대하여, 세포는 예를 들어, 미국 특허 제6,352,694호에 기술된 바와 같은 방법을 이용하여 활성화되고 확장될 수 있다.
특정 실시형태에서, 유래된 유전자 조작된 조혈 계통 세포에 대한 1차 자극 신호 및 공자극 신호는 상이한 프로토콜에 의해 제공될 수 있다. 예를 들어, 각각의 신호를 제공하는 작용제는 용액 중에 있을 수 있거나 또는 표면에 커플링될 수 있다. 표면에 커플링될 때, 작용제는 동일한 표면(즉, "시스" 형성)에 또는 별개의 표면(즉, "트랜스" 형성)에 커플링될 수 있다. 대안적으로, 하나의 작용제는 표면에 결합될 수 있고, 다른 작용제는 용액 중에 존재할 수 있다. 일 실시형태에서, 공자극 신호를 제공하는 신호는 세포 표면에 결합될 수 있고, 1차 활성화 신호를 제공하는 작용제는 용액 중에 있거나 또는 표면에 결합된다. 특정 실시형태에서, 작용제는 둘 다 용액 중에 있을 수 있다. 다른 실시형태에서, 작용제는 가용성 형태일 수 있고, 이어서, 세포 발현 Fc 수용체 또는 본 발명에서 T 림프구를 활성화 및 확장시키는데 있어서 사용하기 위해 고려되는 인공 항원 제시 세포(aAPC)에 대해 미국 특허 출원 공개 제20040101519호 및 제20060034810호에 개시된 것과 같은 작용제에 결합하는 다른 결합제와 같이 표면에 가교된다.
투여량, 빈도 및 프로토콜에서의 약간의 변경은 치료될 대상체의 상태에 따라서 본질적으로 일어날 것이다. 임의의 사례에서 투여 책임자는 개별 대상체에 대한 적절한 용량, 빈도 및 프로토콜을 결정할 것이다.
실시예
다음의 실시예는 예시의 방법에 의해, 그리고 제한의 방법에 의하지 않고 제공한다.
실시예 1 - 물질 및 방법
상이한 안전 하버 유전자좌 통합 전략과 조합하여 다양한 프로모터의 제어 하에서 자살 시스템을 효과적으로 선택 및 시험하기 위해서, 본 출원인의 소유의 hiPSC 플랫폼을 사용하였는데, 이는 단일 세포 계대배양 및 고-처리량, 96-웰 플레이트-기반 유세포 분석법 분류를 가능하게 하여, 단일 또는 다수의 유전자 조정을 갖는 클론성 hiPSC의 유도를 허용한다.
소분자 배양물 중에서의 hiPSC 유지 : 배양물의 컨플루언시가 75% 내지 90%에 도달된 후 hiPSC를 단일 세포로서 일상적으로 계대배양하였다. 단일-세포 해리를 위해서, hiPSC를 PBS(미디어테크사(Mediatech))로 1회 세척하고, 애큐타제(Accutase)(밀리포어사(Millipore))로 3 내지 5분 동안 37℃에서 처리한 후, 피펫팅하여 단일-세포 해리를 보장하였다. 이어서, 단일-세포 현탁물을 종래의 배지와 동일 부피로 혼합하고, 225×g에서 4분 동안 원심분리하고, FMM 중에 재현탁하고, 마트리겔-코팅된 표면 상에 플레이팅 하였다. 계대배양은 전형적으로 1:6 내지 1:8이었고, 마트리겔로 2 내지 4시간 동안 37℃에서 미리 코팅된 조직 배양 플레이트로 옮기고, FMM을 2 내지 3일 마다 공급하였다. 세포 배양물을 37℃및 5% CO2로 설정된 가습 인큐베이터에서 유지시켰다.
관심대상 양상의 표적화 편집을 위해서 ZFN, CRISPR을 사용한 인간 iPSC 조작 : ZFN 매개된 게놈 편집을 위해서, 예로서, ROSA26 표적화된 삽입을 사용하여, AAVS1 표적화된 삽입을 위해서 2백만개의 iPSC에 2.5ug ZFN-L(FTV893), 2.5ug ZFN-R(FTV894) 및 5ug 공여자 작제물의 혼합물을 형질주입하였다. CRISPR 매개된 게놈 편집을 위해서, 2백만개의 iPSC에 ROSA26 표적화된 삽입을 위해서 5ug ROSA26-gRNA/Cas9(FTV922) 및 5ug 공여자 작제물의 혼합물을 형질주입하였다. 형질주입은 파라미터 1500V, 10ms, 3펄스를 사용하여 네온 형질주입 시스템(Neon transfection system)(라이프 테크놀로지스사)을 사용하여 수행하였다. 형질주입 후 2 또는 3일에, 플라스미드가 인공 프로모터-드라이버 GFP 및/또는 RFP 발현 카세트를 함유하는 경우 유세포 분석법을 사용하여 형질주입 효율을 측정하였다. 형질주입 후 4일에, 퓨로마이신을 0.1ug/㎖의 농도로 처음 7일 동안 그리고 7일 후에는 0.2ug/㎖의 농도로 배지에 첨가하여 표적화된 세포를 선택하였다. 퓨로마이신 선택 동안, 세포를 10일에 새로운 마트리겔-코팅된 웰 상에서 계대배양하였다. 16일 또는 퓨로마이신 선택 이후에, 살아남은 세포를 GFP+ iPS 세포 백분율에 대해서 유세포 분석법에 의해서 분석하였다.
게놈-편집된 iPSC의 벌크 분류 및 클론 분류 : ZFN 또는 CRISPR-Cas9를 사용한 게놈 표적화 편집을 사용하여 iPSC를 벌크 분류하고, 퓨로마이신 선택 20일 후에 GFP+SSEA4+TRA181+ iPSC를 클론 분류하였다. 단일 세포 해리된 표적화된 iPSC 풀을 행크스 평형 염 용액(Hanks' Balanced Salt Solution)(미디어테크사(MediaTech)), 4% 우태아 혈청(인비트로젠사), 1×페니실린/스트렙토마이신(미디어테크사) 및 10mM 헤페스(Hepes)(미디어테크사)를 함유하고; 최적 성능을 위해서 새로 제조된 급냉 염색 완충제 중에 재현탁시켰다. SSEA4-PE, TRA181-알렉사 플루오르-647(비디 바이오사이언시스사(BD Biosciences))를 포함하는 접합된 1차 항체를 세포 용액에 첨가하고, 얼음 상에서 15분 동안 인큐베이션시켰다. 모든 항체를 백만개의 세포당 100㎕의 염색 완충제 중에서 7㎕로 사용하였다. 용액을 염색 완충제 중에서 1회 세척하고, 225g에서 4분 동안 스핀 다운하고, 10μM 티아조비빈을 함유하는 염색 완충제 중에 재현탁하고, 유세포 분석법 분류를 위해서 얼음 상에서 유지시켰다. 유세포 분석법 분류를 FACS 아리아 II(비디 바이오사이언시스사) 상에서 수행하였다. 벌크 분류를 위해서, GFP+SSEA4+TRA181+ 세포를 7㎖ FMM으로 충전된 15㎖ 캐노니컬 튜브(canonical tube) 내에서 게이팅 및 분류하였다. 클론 분류를 위해서, 분류된 세포를 100μM 노즐을 사용하여, 웰당 3개 사건의 농도로 직접 96-웰 플레이트에 배출하였다. 각각의 웰은 5㎍/㎖ 피브로넥틴 및 1x 페니실린/스트렙토마이신(미디어테크사)이 보충된 200㎕ FMM을 미리 충전되어 있었고, 이미 5x 마트리겔로 밤새 코팅되어 있었다. 5× 마트리겔 예비코팅은 EM/F12 5㎖에 마트리겔의 하나의 분취물을 첨가하고, 이어서 적절한 재현탁을 허용하도록 4℃에서 밤새 인큐베이션시키고, 마지막으로 96-웰 플레이트에 웰당 50㎕로 첨가한 후 밤새 37℃에서 인큐베이션시키는 것을 포함한다. 각각의 웰에 배지를 첨가하기 직전에 5x 마트리겔을 흡인시켰다. 분류가 완결된 후, 96-웰 플레이트를 인큐베이션 전에 225g에서 1 내지 2분 동안 원심분리하였다. 플레이트를 7일 동안 방해하지 않고 정치시켰다. 제7일에, 150㎕의 배지를 각각의 웰로부터 제거하고, 100㎕의 FMM으로 대체하였다. 분류 후 웰에 10일에 추가 100㎕의 FMM을 재공급하였다. 집락 형성을 초기 2일에 검출하고, 대부분의 집락을 분류 후 7일 내지 10일에 확장시켰다. 제1 계대배양에서, 웰을 PBS로 세척하고, 37℃에서 대략 10분 동안 30㎕의 애큐타제로 해리시켰다. 확장된 애큐타제 처리에 대한 요구는 연장된 기간 동안 배양물에서 한가롭게 있는 집락의 압축성을 반영한다. 세포가 해리된 것으로 보인 후, 200㎕의 FMM을 각각의 웰에 첨가하고, 수회 피펫팅하여 집락을 파괴하였다. 해리된 집락을 5x 마트리겔에 의해 미리 코팅된 96-웰 플레이트의 또 다른 웰로 옮기고, 이어서 인큐베이션 전에 225g에서 2분 동안 원심분리하였다. 확장 전에 초기 집락을 분산시키도록 이러한 1:1 계대배양을 수행하였다. 후속 계대배양을 3분 내지 5분 동안 애큐타제 처리 및 75 내지 90%의 컨플루언시 시 FMM에서 1×마트리겔로 미리 코팅된 더 큰 웰로 1:4 내지 1:8의 확장에 의해 일상적으로 수행하였다. 각각의 클론성 세포주를 GFP 형광 수준 및 TRA1-81 발현 수준에 대해서 분석하였다. 대략 100%의 GFP+ 및 TRA1-81+를 갖는 클론주를 추가 PCR 스크리닝 및 분석을 위해서 선택하였다. 유세포 분석법 분석을 구아바 이지사이트 8 HT(밀리포어사) 상에서 수행하고, 플로우조(Flowjo)(플로우조사(Flowjo, LLC))를 사용하여 분석하였다.
실시예 2 -자율적 유도체 세포에 대한 세포 표면 발현된 사이토카인의 작제물 및 설계
본 출원에서, 외인성 가용성 재조합 사이토카인을 대체하는 것은 iPSC로부터의 조혈 세포의 시험관내 유도를 지원할 뿐만 아니라 유도체 효과기 세포 생체내 지속성 및 생존을 지원한다는 것을 나타냈다. 임상적으로 관련된 사이토카인의 체계적인 고용량 투여를 회피함으로써, 사이토카인 매개된 세포 자율성이 확립되면서, 이러한 실시로 인한 용량-제한적인 독성의 위험이 감소된다. 도 1은 예시적인 예로서 IL15를 사용하는 몇몇 작제물 설계를 제공한다. 특히, 설계 3은 절두된 세포내 도메인을 갖는 IL15Rα는 링커를 통해서 C-말단에서 IL15에 융합되어, IL15의 트랜스-제시를 모방하고, IL15 막-결합되는 것을 유지하고, 추가로 잠재적인 시스-제시를 추가로 제거한다는 것을 입증한다. 설계 3의 대안으로서, 설계 4는 이로부터 본질적으로 전체 IL15Rα는 스시 도메인을 제외하고는 제거되고, 선택적으로 스시 도메인과 막관통 도메인 사이에 링커를 사용하여 한 단부에서 IL15와 그리고 다른 단부(mb-스시)에서 막관통 도메인과 융합된다. 융합된 IL5/mb-스시는 임의의 막 결합된 단백질의 막관통 도메인을 통해서 세포 표면에서 발현된다. 작제물, 예컨대, 설계 4를 사용하여, 시스-제시를 비롯한 IL15Rα를 통한 불필요한 신호전달은 단지 IL15의 목적하는 트랜스-제시가 유지될 때만 제거된다.
실시예 3 -- iPSC의 단계식 조작 및 변형된 유도체 NK 세포의 검증
유도 만능 줄기세포(iPSC)를 연속적으로 조작하여 고 친화도 비-절단성 CD16(hnCD16) 발현, B2M 유전자의 넉 아웃에 의한 HLA-I의 손실, CIITA의 넉 아웃에 의한 HLA-II의 손실, 비-고전적 HLA 분자 HLA-G의 과발현 및 연결된 IL15/IL15Rα 작제물의 발현을 획득하였다. 각각의 조작 단계 후에, 다음 조작 단계 이전에 iPSC를 목적하는 표현형을 위해서 분류하였다. 이어서, 조작된 iPSC를 시험관내에서 유지시키거나 대략 44일 기간의 분화 및 확장에 걸쳐서 NK 세포로 분화시켜 단일 iPSC 입력으로부터 대략 1E6 성숙 NK 세포를 수득할 수 있다. 이어서, 이들 유도체 NK 세포를 냉동 보존시키고, 필요 시에 환자에게 전달할 수 있다.
이러한 예시적인 예시에서, hnCD16 발현을 함유하도록 유전자 조작된 iPSC 유전자는 향상된 세포독성을 갖는다. 조작 없이 iPSC로부터 유래된 iNK는 매우 낮은 CD16 수준을 가진 반면, 말초 혈액으로부터의 NK 세포에 의해서 발현된 내인성 CD16 수용체는 NK 세포 활성화 후 세포 표면으로부터 절단된다. 이에 비해서, hnCD16를 함유하도록 조작된 iPSC로부터 유래된 iNK에서의 CD16의 비-절단성 버전은 변형된 CD16을 발현하며, CD16 쉐딩을 회피함으로써 일정한 발현 수준을 유지한다. 유도체 NK 세포에서, 비-절단성 CD16은 개선된 세포 기능성을 나타내는 TNFα 및 CD107a의 발현을 증가시킨다. 비-절단성 CD16은 또한 항체-의존적 세포-매개된 세포독성(ADCC)을 향상시킨다. ADCC는 항체-코팅된 표적 세포에 대한 CD16의 결합을 통한 NK 세포 매개된 용해의 기전이다.
NK 세포와 달리, 1차 공급원(즉, 자연/네이티브 공급원, 예컨대, 말초 혈액, 제대혈 또는 다른 공여자 조직)으로부터의 성숙 T 세포는 CD16을 발현하지 않는다. 본 발명에서, 발현된 외인성 비-절단성 CD16을 포함하는 iPSC가 T 세포 발달 생물학을 손상시키지 않고, 외인성 CD16을 발현할 뿐만 아니라, 획득된 ADCC 기전을 통해서 기능을 수행할 수 있는 기능성 유도체 T 세포로 분화할 수 있다는 것은 예상치 못한 것이다.
HLA 복합체 변형을 달성하기 위해서, hnCD16 iPSC 주에 Cas9 니카제(nickase)를 발현하는 플라스미드 내의 B2M-표적화 gRNA 쌍을 형질주입시켰는데, 이것은 야생형 Cas9에 비해서 더 약한 오프-타깃 효과를 제공하도록 조작된 것이다. 표적화 편집을 사용한 B2M-/- 및 HLA I-결핍 클론을 클론성 게놈 DNA 서열결정에 의해서 추가로 분석하였고, B2M 넉아웃 표현형을 초래하는 작은 결실 또는 삽입을 갖는 것으로 확인되었다. B2M 넉아웃은 HLA I-결핍 세포를 생성한다.
이어서, hnCD16 발현 및 HLA 클래스 I 결핍 iPSC를 예를 들어, 렌티바이러스를 사용하여 유전자 조작하여 HLA-G/B2M 융합 단백질을 도입하였다. HLA-G의 변형된 버전은 절단이 회피되어, HLA 클래스 I 변형된 iPSC의 지속성을 추가로 향상시킨다. 이어서, 획득된 iPSC 주를 IL15/IL15Rα 융합 단백질을 함유하도록 유전자 조작하였다. 변형된 iPSC는 이의 조혈 분화 능력을 유지하였는데, 그 이유는 다양하게 변형된 iPSC 주(hnCD16; hnCD16/B2M-/-, hnCD16/B2M-/-CIITA-/-; hnCD16/B2M-/-HLA-G; hnCD16/B2M-/-CIITA-/-HLA-G; hnCD16/B2M-/-HLA-G/IL15-IL15Rα; hnCD16/B2M-/- CIITA-/-HLA-G/IL15-IL15Rα)가 각각 확정적 HE 퍼텐셜을 갖는 CD34+ 세포를 통해서 NK 또는 T 세포로 분화되었기 때문이었다.
도 2에서 획득된 성숙 iPSC-유래된 NK 세포의 유세포 분석은, hnCD16 발현, B2M 넉아웃, HLA-G 발현 및 IL15/IL15Rα 발현의 단계식 조작을 나타내었는데, 이는 iPSC 게놈 조작을 통한 치료 관련 단백질의 발현 변경이 세포가 목적하는 세포 운명으로 시험관내에서 지시되어 발달하는 것을 교란시키지 않으면서 조혈 분화 동안 유지된다는 것을 입증한다.
실시예 4 -- 향상된 기능 및 지속성을 갖는 iPSC 유래 자연 살해(NK) 세포
텔로미어 단축은 세포 노화에 따라서 발생하며, 줄기세포 기능장애 및 세포 노화와 관련된다. 여기서, iPSC의 지시된 분화를 통해서 획득된 성숙 iNK 세포는 성인 말초 혈액 NK 세포에 비해서 더 긴 텔로미어를 함유하는 것을 나타낸다. 텔로미어 길이는 G0/1 세포의 DNA 지수에 대한 보정과 함께 대조군(100%)으로서 iPSC, 성인 말초 혈액 NK 세포 및 iPSC-유래된 NK 세포의 경우에는 1301 T 세포 백혈병 주를 사용하여 유세포 분석법에 의해서 결정하였다. 도 3에 도시된 바와 같이, iPSC-유래된 NK 세포는 성인 말초 혈액 NK 세포와 비교할 때 상당히 더 긴 텔로미어 길이를 유지하는데(p=.105, ANOVA), 이는 iPSC 유래 NK 세포에서의 더 큰 증식, 생존 및 지속 가능성을 나타낸다.
성숙하고 상이하게 조작된 iPSC-유래된 NK 세포주 세포를 각각 동일한 iNK 공여자에 대해서 프라이밍된 동종이계 CD8+ T 세포와 다양한 E:T(효과기:표적)비에서 인큐베이션시켰다. 결과는 2개의 공여자의 평균이며, 이를 각각의 표적 iNK 세포 유전자형에 대해만 표적 세포의 %로 정규화한다. 48시간 후, 남아있는 iNK 표적 세포를 유세포 분석법에 의해서 계수하였다. 도 4에 도시된 바와 같이, B2M-/-/HLA-I 결핍의 부재는 T 세포 인식 및 세포독성으로 인해서 iNK 세포 손실을 초래하였지만; B2M의 넉아웃은 동종이계 CD8+ T 세포에 의해서 조작된 iNK 세포의 시험관내 인식을 제거한다.
B2M-/-iPSC는 T 세포 매개된 사멸을 회피하는 능력으로 인해서 지속성이 개선되었다. 그러나, 이들 세포는 말초 NK 유도된 인식 및 사멸에 여전히 적용되었다. 상이하게 조작된 iPSC 주를 동종이계 PBMC와 함께 인큐베이션시킨 경우, iPSC의 각각의 손실을 Incucyte Zoom 영상화 시스템을 사용하여 시간에 따라서 측정하였다. 도 5A에 도시된 바와 같이, iPSC에서 HLA-I(B2M-/-)의 손실은 hnCD16 iPSC와 비교하여 증가된 세포독성 및 iPSC의 손실을 초래한다. 그러나, HLA-I 결핍 세포의 손실은 도 5B에 도시된 바와 같이 B2M-/- iPSC 상에서 HLA-G의 발현에 의해서 적어도 부분적으로 역전될 수 있다. 따라서, HLA-G의 발현은 동종이계 NK 세포에 의해서 사멸로부터 B2M-/- iPSC를 구제한다.
생체내에서 세포 기능성을 시험하기 위해서, 항-HER2 항체의 단일 투여로의 처리 전 4일째에 단독으로 또는 1E7 hnCD16/B2M-/-/HLA-G iNK 세포와 조합하여 NSG 마우스에 복막내 주사(IP)를 통해서 SKOV-3-루시퍼라제 난소 종양 세포를 이식하였다. 종양 진행을 모니터링하기 위해 IVIS(생체내 영상화 시스템) 영상화에 의해 종양 진행을 측정하였다. 각각의 마우스 IVIS 영상인 도 6A 또는 IVIS 영상화에 의한 종양 진행의 시간 경과인 도 6B에 도시된 바와 같이, hnCD16/B2M-/-HLA-G iNK의 단일 용량은 난소암의 생체내 이종이식편 모델에서 종양 퇴행을 유도하였다.
추가로, iPSC 및 iNK에서의 외인성 IL15/IL15Rα의 발현은 가용성, 외인성 IL15의 첨가와 무관하게 시험관내에서 유도체 NK 세포로의 iPSC 지시된 분화 및 유래된 iNK 세포의 생존을 촉진시키는 것으로 나타났다. 도 7A에 도시된 바와 같이, hnCD16 iPSC, hnCD16/B2M-/-HLA-G iPSC는 배지에서 가용성 IL15의 첨가로 더 양호하게 분화된 반면; hnCD16/B2M-/-HLA-G iPSC를 발현하는 IL15/IL15Rα는 가용성 IL15의 첨가로 또는 이를 첨가하지 않고 동일하게 잘 분화되었다. 유래된 iNK 세포에서의 외인성 IL15/IL15Rα 발현의 효과는 도 1에서 가용성 IL15 적정 시험을 설명하는 도 7B에서 입증되었다. 도 7B에 도시된 바와 같이, iNK 세포를 광범위하게 세척하고, 7일 동안 0ng/㎖ 내지 10ng/㎖의 범위의 가용성 IL15의 농도로 배양액에 다시 넣었고, IL15/IL15Rα를 발현하는 iNK 세포의 성장 및 확장은 배양액에서 가용성 IL15와 무관한 것으로 밝혀졌다.
IL15/IL15Rα 작제물의 발현은 가용성 IL15의 부재 하에서 생체내에서 iNK 지속성을 향상시킨다. 8백만 개의 hnCD16/B2M-/-/HLA-G 또는 hnCD16/B2M-/-/HLA-G/IL15 iNK 세포를 면역손상된 NOG 마우스(도 8A) 또는 인간 IL15를 발현하는 NOG 트랜스제닉 마우스(도 8B)에 입양적으로 전달하였다. 도 8A에 도시된 바와 같이, IL15/IL15Rα 작제물을 발현하는 세포만 생체내에서 가용성 IL15의 부재 하에서, 혈청 IL15의 존재에서의 iNK 유전자형 둘 다와 유사한 방식으로 유지되었다(도 8B). 이와 같이, IL15 수용체 알파 쇄(IL15-IL15Rα)와 연결된 IL15의 발현은 NK 세포 지시된 게놈 조작된 iPSC 분화를 향상시킬 뿐만 아니라, 시험관내 및 생체내에서 외인성 성장 인자의 부재 하에서 조작된 유도체 NK 세포 생존을 지원한다.
이어서 IL15/IL15Rα 작제물과 CAR의 공동-발현을, 매우 효과적이고, 지속적이며, 표적화된 NK 세포 요법을 생성하는데 있어서 두 양식 사이의 잠재적인 상승작용에 대해 조사하였다. NK-CAR은 NK 세포 신호전달에서 강한 증가를 매개하도록 NK 세포에 대해서 최적화된 키메라 항원 수용체이며, 이것은 NK 세포에서 발현된 분자로부터 유래된 분자로부터 유래된 적어도 하나의 도메인(막관통 도메인, 공-자극성 도메인 또는 세포질 신호전달 도메인), 예컨대, 예를 들어, CD16, NKp44, NKp46, NKG2D, 2B4(CD244), CD137(41BB), IL21, DAP10, DAP12, 및/또는 CD3ζ을 포함한다. 본 명세서에서 설명을 위해서 사용된 NK 세포 최적화된 CAR(NK-CAR)는 하나 이상의 ITAM을 포함하는 NKG2D 막관통 도메인, 2B4 공-자극성 도메인 및 CD3ζ 신호전달 도메인을 함유하는 골격을 갖는다. 도 22에 도시된 바와 같이, IL15/IL15Rα 작제물(도 22에서의 IL-15RF)의 공동-발현과 함께 또는 공동-발현 없이 NK-CAR19를 발현하는 유도체 NK 세포를 약 250U/㎖의 외인성 인간 IL-2의 존재 및 부재 하에서 9일 동안 배양하였다. 이와 같이, IL15/IL15Rα의 발현은 NK-CAR19 iNK 세포의 가용성 사이토카인 의존성을 제거하였다. 시험관내 지속성뿐만 아니라, IL15/IL15Ra의 발현은 또한 생체내에서 iNK 지속성을 촉진시키고(도 31 A), 마찬가지로 생체내 항원-유도된 확장을 향상시킨다(도 31B). 대안적인 IL15 작제물을 또한 사용하여 바이-시스트론성 벡터에서 CAR 및 IL 공동-발현을 포함하는, 유도체 세포 생존, 지속성 및 확장을 지원하는 능력을 시험하였다.
다음으로, Nalm6 및 Raji 이종이식편 모델에서, CAR-IL15/IL15Ra iNK 세포로 처리된 마우스는 대조군에 비해서 생존 연장을 나타내었다. 총 2.5×105개의 Raji-루시퍼라제(Raji-luc) 세포를 면역손상된 NSG 마우스에 IV로 주사하였다. 다음날, 마우스를 5×106 비변형된 iNK 세포, CAR iNK 세포 또는 CAR-IL15/IL15Ra iNK 세포로 처리하였다. 종양 진행을 주 단위 생물발광 영상화(BLI)에 의해서 모니터링하였고(도시하지 않음), 전체 생존을 모니터링하고, 도 32A에 나타내었다. 도시된 바와 같이, CAR-IL15/IL15Ra iNK는 B 세포 림프종의 매우 공격적인 전파 모델에서 생존 연장에서 CAR iNK보다 통계학적으로 우수하였다(p = 0.018, CAR-IL15/IL15Ra iNK 대 CAR iNK). 더욱이, 백혈병 모델에서, Nalm6 세포를 NSG 마우스에게 복강내 이식하였다. 마우스를 4일 후에 IL15/IL15Ra와 함께 또는 이것 없이 종래의 1928z CAR 작제물 또는 NK-중심 CAR을 발현하는 1×107개의 iNK 세포로 처리하였다. 개별 마우스에서의 종양 진행을 생물발광 영상화에 의해서 측정하였고(도시하지 않음), 각각의 처리군에 대한 전체 생존을 나타내고, 도 32B와 비교하였는데, CAR-IL15/IL15Ra iNK는 종양 진행을 예방하고, 동물의 생존을 유지할 수 있는 세포이다.
따라서, hnCD16 및/또는 IL15를 발현하는 변형된 HLA 클래스 I 및/또는 II를 갖는 이들 유도체 NK 세포는 면역 검출에 대해서 증가된 내성 및/또는 연장된 생체내 지속성을 가지며, 따라서 혈액암뿐만 아니라 고형암을 위한 보편적인 오프 더 셀프 치료 요법의 기원을 제공한다. 또한, iPSC-NK 세포는 또한 실시예 7 및 8에 추가로 상세하게 설명된 T 세포 모집 검정에 의해서 입증되는 바와 같이 생체내에서 순환으로부터의 T 세포 이동을 유도한다.
실시예 5 - CAR 및 hnCD16을 발현하는 유도체 NK 세포는 표적 세포를 제거하는데 있어서 항체와 상승작용한다
CAR-발현 iPSC로부터의 유도체 NK 세포를 본 명세서에 기재된 지시 분화 플랫폼에 따라서 획득하였다. 도 9는 CD56 및 CD3의 표면 마커의 유세포 분석법 분석을 사용한, CAR-발현 iPSC 유래 NK 세포의 표현형, 전사 마커 GFP의 발현, 및 CD56+ NK 세포 집단의 게이트에서 NK 세포 표면 수용체 NKp44, CD16, FasL: PBNK(말초 혈액 NK) 세포, iPSC-NK 세포, T CAR-iPSC-NK 세포(T 세포를 위해서 설계된 CAR을 발현하는 유도체 NK 세포), 및 CAR4(메조)-iPSC-NK 세포(NK 세포에 대해서 특이적으로 셜계된 CAR을 발현하는 유도체 NK 세포)를 기재한다. 본 실시예에서, 예시적인 T CAR은 SS1-CD28-41BBζ의 구조를 갖는 반면, NK CAR은 SS1-NKG2D-2B4ζ(CAR4)의 구조를 가지며, 이들 둘 다는 메소텔린 발현 종양 세포를 표적으로 한다. T-CAR 및 NK-CAR 발현 유도체 NK 세포는 PBNK 세포와 비교하여 KIR(CD158a, h, b1/b2, e1/e2 및 I; 도시하지 않음)의 발현을 잃어버리는 것을 발견하였다.
CAR4 발현 유도체 NK 세포의 항-종양 활성은, 각각의 세포가 다양한 효과기 대 표적 비(E:T)에서 K562메조 세포(도 10A) 및 A1847 세포(도 10B)와 같은 유로퓸 로딩된 메조-고 표적 세포와 공동 배양될 때 입증되었다. 특이적 종양 세포 용해 %의 평균 ± SD의 평균이 제시되고, 데이터는 3개의 유로퓸 방출 분석의 표현이다. 도 10에 도시된 바와 같이, iPSC-NK 세포, T-CAR(메조)-iPSC-NK 세포 및 CAR4(-)-iPSC-NK 세포(scFV가 없는 CAR4)는 NK-CAR4(메조)-iPSC-NK 세포에 비해서 메조고 표적 둘 다를 더 적게 사멸시킬 수 있었다. 클론-율래된 CAR4(메조)-iPSC-NK 세포(#1 및 #4)는 메조고 표적에 대해서 풀링된(비-클론성) CAR4(메조)-iPSC-NK로서 강력한 세포용해 활성을 요약한다.
생체내에서 CAR4-iPSC-NK 세포의 활성을 평가하기 위해서, A1847 난소암 세포의 사멸을 마우스 이종이식편 모델에서 시험하였다. 도 11에서, PBNK 세포, iPSC-NK 세포, T CAR(메조)-iPSC-NK 세포 및 CAR4(메조)-iPSC-NK 세포를 비교하였다. NSG 마우스에 루시퍼라제-발현 A1847 세포를 복강내 접종하고, 4일 후에 복강내로 1.5E7 각각의 NK 세포의 단일 주사를 제공하였다. 본 검정에서, IL15를 투여하여 생체내에서 NK 생존 및 확장을 촉진시켰지만, 실시예 6에 나타낸 바와 같이, 이 절차는 생략되거나 예시적인 IL15/IL15Rα 작제물을 발현시켜 생체내에서 유도체 NK 세포 자율성을 부여함으로써 대체될 수 있다. 마우스를 모니터링하고, 49일까지 생물발광 영상화(BLI)에 의해 종양 부하를 정량하였다. 도 11에 나타낸 바와 같이, 미처리 종양을 보유하는 마우스에 비해서, NK 세포로의 처리는 7일 후 종양 부하의 상당한 감소를 나타내었고(P<0.0001), 28일에 그리고 그 후에 CAR4-iPSC-NK 세포에서 최대 항-종양 활성이 관찰되었다(iPSC-NK 세포와 비교하여 P=0.0044; T CAR-iPSC-NK 세포와 비교하여 P<0.0001). PB-NK 세포, iPSC-NK 세포 및 T-CAR-iPSC-NK 세포에 비해서 CAR4-iPSC-NK 세포의 이러한 상당히 개선된 항-종양 활성은 모든 시간 지점에서 지속되었고(도 12A), iPSC-NK 세포(P=0.0017, HR=0.2236, 95%CI: 0.009016-0.2229) 및 T-CAR-iPSC-NK 세포(P=0.0018, HR=0.2153, 95%CI: 0.009771-0.2511)뿐만 아니라 PB-NK 세포(P=0.0018, 도 12B)와 비교할 때 상당히 개선된 생존으로 이어졌다. 주사 후 NK 세포의 생체내 지속을 평가하기 위해서, 혈액, 비장 및 복막액을 치료 과정 동안 NK 세포의 존재에 대해서 시험하였다. 10일째에, CAR4-iPSC-NK 세포는 PB-NK 세포, iPSC-NK 세포에 비해서 순환계(도 13A, 평균 4.28%, P=0.0143), 비장(도 13B, 평균 7.22%, P=0.0066), 및 복막액(도 13C, 평균 9.80%, P=0.0410)에서 상당히 증가되었다. 21일 후, CAR4-iPSC-NK 세포의 수는 PB-NK 세포, iPSC-NK 세포와 유사한 수준으로 복귀하였다. 28일까지, 이들 조직에서 소수의 NK 세포가 관찰되었다. 종합하면, 이들 연구는, NK-CAR-발현 iPSC-유래 NK 세포가 비-CAR 발현 PB-NK 세포 또는 iPSC-NK 세포에 비해서 개선된 항-종양 활성을 매개할 뿐만 아니라 T-CAR-발현 iPSC-NK 세포에 비해서 개선된 활성을 매개한다는 것을 입증한다.
추가로 상기 실시예 4의 관점에서, 본 명세서에 제시된 집단 데이터는 B2M-/-, HLA-G 및 IL15/IL15Rα 이외에 NK CAR 및 hnCD16 둘 다를 발현함으로써 향상된 유도체 NK 세포 생성물을 지지한다. 도 30은, NK 사멸 능력과 관련된 그랜자임 B의 생산 증가 및 KIR2DL3 및 KIR2DL1의 증가된 발현에 의해 입증된 바와 같이, hnCD16-CAR-IL-15/IL-15Ra iNK 세포에서 NK 세포 성숙이 향상되었음을 나타내며, 이는 NK 세포가 효과기 기능을 획득한 라이센싱된 상태를 부여한다. Nalm6 및 ARH-77 표적 세포주에 대한 hnCD16-CAR-IL15/IL15Ra iNK 세포의 시험관내 세포독성을 조사하였다. 도 33A는, Nalm6/CD19+ 및 Nalm6/CD19- 세포에 대한 4시간 세포독성 검정에서 증가하는 E:T 비에서 hnCD16-CAR-IL15/IL15Ra iNK 세포의 세포독성을 비교하는데, 이는 상기 iNK 세포에 의한 CD19 특이적 사멸을 나타낸다. 추가로 ARH-77/CD19+ 백혈병 세포(도 33 B) 또는 ARH-77/CD19- 세포(도 33 C)를 사용하여, 대조군으로서 비변형된 iNK 세포를 사용한 4시간 세포독성 검정을 사용하여 리툭시맙의 존재 또는 부재 하에서 hnCD16-CAR-IL15/IL15Ra iNK 세포의 직접 세포독성 및 리툭시맙-유도된 ADCC를 측정하였다. 결과는, hnC16-CAR-IL15/IL15Ra iNK 세포가 시험관내에서 B 세포 악성종양에 대해 CAR-지시 및 ADCC 둘 다를 매개한다는 것을 보여주었다. 추가 기능성 분석에서, 모체 ARH-77 세포(CD19+) 및 ARH-77 CD19- 세포에 각각 적색 및 녹색 형광 태그를 형질도입하였다. 이어서, 이들 세포를 1:1로 혼합하고, 리툭시맙 항체의 존재 또는 부재 하에서 효과기 세포로서 다양한 iNK 세포 집단을 사용하는 장기간 세포독성 검정에서 표적 세포로서 사용하였다. Incucyte(상표명) 영상화 시스템을 사용하여 검정 전체에서 녹색 CD19- 및 적색 CD19+ 표적의 빈도를 측정하여 단일 웰 내에서 표적 세포 둘 다에 대한 세포독성을 정량하였다. 도 34에 나타낸 혼합-배양물 세포독성 검정에서, 데이터를 효과기 세포가 없는(종양 세포 단독) 대조군에 정규화된 두 표적 유형 모두(CD19+ 또는 CD19-)에 대해서 남아있는 표적 세포의 빈도로서 플로팅하고, 효과기 세포의 hnCD16, CAR 및 IL15/IL15Ra 양상은 혼합-배양물 세포독성 검정에서 시험관내에서 CD19+ 및 CD19- 표적 둘다를 제거하는데 있어서 상승작용함을 나타낸다.
본 명세서에 제공된 유도체 NK 세포는 예를 들어, 치료 항체를 혼입함으로써 ADCC를 사용하여, 또는 실시예 7에 추가로 나타낸 면역관문 저해제를 혼입함으로써 T 세포 표적화된 면역요법을 사용하여, 병용 요법으로 사용될 때 생체내에서 지속되고, 개선된 사멸률을 갖고, 상승작용을 전달하는 일관되고 보편적인 치료용 동종이계 세포 생성물을 전달한다.
실시예 6 - CAR 항원 탈출을 구제하기 위한 병용 요법을 위한 향상된 유도체 T 세포
클론성 hiPSC에 고 친화도, 비-절단성 CD16 Fc 수용체(hnCD16)를 형질도입하고, 본 명세서에 제공된 바와 같은 지시 분화 프로토콜에 따라서 유도체 T 세포로 분화시켰다. 도 14A는 유세포 분석에 의해 인지되는 바와 같이 hiPSC의 세포 표면에서 hnCD16의 발현을 입증한다. 도 14B는 hiPSC-유래 CD8ab + T 세포의 세포 표면에서 hnCD16의 발현을 도시한다.
hnCD16-발현 유도체 T 세포를 증가하는 효과기 대 표적비에서 항체의 존재 및 부재 하에서 종양 표적 세포와 공동 배양하고, 표적 세포의 형광 생세포 영상화에 의해서 세포 세포독성을 평가하였다. 도 15는 hnCD16을 발현하는 iPSC 유래된 T 세포가 항체 표지된 표적 세포에 대한 ADCC의 능력을 획득했음을 입증한다.
다음으로, 도 16에 도시된 바와 같이, 클론 hiPSC를 키메라 항원 수용체(CAR) 및 hnCD16 Fc 수용체를 함유하는 렌티 바이러스로 형질 도입하여 hiPSC의 표면에서 CAR 및 hnCD16을 모두 발현시켰다. CAR 및 hnCD16의 발현이 조혈 분화를 교란시키지 않음을 입증하기 위해, CAR+hnCD16+ hiPSC를 제공된 바와 같은 iCD34 분화 플랫폼을 사용하여 분화시켰다. 분화 10일 후 CD34+ 집단에서 CAR 및 hnCD16 둘 다의 발현을 유세포 분석법에 의해서 나타낸다. 이어서 CAR+hnCD16+ iCD34 세포를 NK 또는 T 세포로 분화시키고, 각각의 유도체 효과기 세포에서 CAR 및 hnCD16의 발현을 유세포 분석법에 의해 모니터링하였다. CAR 및 hnCD16의 발현은 hiPSC-유래된 NK 및 T 세포 둘 다의 세포 표면에서 유지된다.
CAR-hnCD16 iT 세포가 CAR-매개된 세포독성 이외에 hnCD16-매개된 ADCC를 수행하여 이중 세포독성 표적화를 수행하고, CD19-CAR-T 세포에 의해 표적화되는 종양 세포의 CAR 항원 탈출을 완화시킬 수 있는지의 여부를 조사하기 위해서, CD19 및 CD20 발현 종양 세포(CD19+/+ 또는 CD19+) 및 CD20만을 발현하는 종양 세포(CD19-/-; 또는 CD19-) 분석에 사용하였다. 항-CD20 리툭시맙의 존재 하에서, 단클론성 항체의 Fc 부분에 의한 CD16의 관여는 hnCD16 발현 T 세포의 ADCC를 활성화시키고, 결과적으로 CAR-hnCD16 iT 세포는 CD19+/+ 및 CD19-/- Raji 세포 둘 다에 대해서 세포독성을 갖는다(도 25A). 표적 세포의 생존을 항-CD20 단클론성 항체 리툭시맙의 존재 및 부재 하에서 36시간 후에 IncucyteZoom(상표명)에 의해서 정량하였다. 도 25에 도시된 바와 같이, CAR-hnCD16 iT 세포는 CD19+/+ 표적의 실질적인 CAR-매개된 사멸 및 CD19-/- CD20+ 표적의 hnCD16 ADCC-매개된사멸을 매개하였다.
추가 입증에서, 내인성 조절 요소의 전사 제어 하에서 CD19 CAR의 T 세포 수용체(TRAC) 유전좌 내의 표적화된 삽입을 갖는 말초 혈액 유래된 T 세포를 단일 세포-유래된 클론성 TRAC-표적화 CAR 발현 마스터 hiPSC 주(TRAC-CAR TiPSC)를 생성시키도록 재프로그래밍하였다. 클론은 만능(> 95 % SSEA4/TRA181)인 것을 특징으로 하고 TRAC 유전자좌의 이중 대립 유전자 파괴로 구성되었다. 단계-특이적 분화 동안, TCR 발현의 손실에도 불구하고, TRAC-CAR hiPSC 주는 CD34 양성 세포로 발달할 수 있고, 이어서 균일한 CAR 발현(95 ± 5 %)을 갖는 CD8 양성 세포로 분화되었다. T 세포 분화 28일째에, 유래된 세포는 TCR 발현의 부재 하에서 현탁액에서 더 성장하고 확장할 수 있었다(도 26). 이러한 합성 T 세포(TRAC-CAR iT)는, 시험관내에서 효과기 사이토카인(IFNγ, TNFα, IL2)의 생산, 탈과립화(CD107a/b, 퍼포린, 그랜자임 B), 증식(>85% 세포 주기 진입) 및 활성화 마커 CD69 및 CD25의 상향조절과 함께 CD 19 항원에 대한 효율적인 세포독성 T 림프구 반응을 도출하는 기능성 능력을 입증하였다. 성숙 TRAC-CAR iT 세포에 의한 IFNγ 및 TNFα의 생산은 CAR을 발현하는 1차 T 세포보다 현저히 더 높다(도 27). TRAC-CAR iT는 또한 항원 특이적 방식으로, 그리고 CAR을 발현하는 1차 T 세포에서 보이는 항원 특이적 세포독성의 변동 없이 종양을 표적으로 한다(도 28). 이어서 D20 및 D28 TRAC-CAR-iT 세포를 트랜스-웰 이동 검정으로 도 29에서 제시된 흉선-유래 케모카인에 반응한 주화성에 대해서 평가하였다. 발달 중인 T 세포는 성숙 동안 흉선-유래 케모카인에 대한 이동 능력을 상실하여, 본 명세서의 실시예에서 입증된 T 세포 이동, 침윤 및 활성화를 향상시키는 유래된 NK 세포의 능력의 중요한 의미를 강조한다.
이어서, TRAC-CAR TiPSC를 hnCD16 수용체를 발현하도록 추가로 조작하고, 생성된 iPSC 주를 T 세포 서명 TCR 발현이 결여되고, 내인성 TCR 프로모터에 의해서 유래된 CAR을 발현하고, 또한 고 친화도 비-절단성 CD16을 발현하는 합성 T 세포(TRAC-CAR-hnCD16 iT)로 분화시킨다. 도 35에서, HLA-미스매칭된 PBMC-유래된 T 세포에 대한 TRAC-CAR iT 세포 및 1차 CAR-T 세포의 증식 반응을 혼합된 림프구 반응 검정을 사용하여 비교하였다. 반응자 세포, 즉, TRAC-CAR iT 세포 및 1차 CAR-T 세포를 각각 세포 트레이스 염색으로 표지하고, HLA-미스매칭된 PBMC-유래된 T 세포에 대한 동종재활성화(alloreactivation)로부터 유래한 세포 확장을 반영하는 염료 희석에 대해서 4일 후에 유세포 분석법에 의해서 평가하였다. 도 35는, 동종반응 촉발 또는 연관된 세포 확장 후 염료 희석을 나타내는 1차 CAR T 세포TRAC-CAR iT 세포와 대조적으로, TRAC-CAR iT 세포는 HLA-미스매칭된 건강한 세포에 대해서 동종반응성임을 나타낸다. CAR에 의해서 표적화된 종양 세포의 항원 탈출을 완화하는 능력 및 이중 세포독성 표적화에 대한 TRAC-CAR-hnCD16 iT의 분석 및 특징규명을 추가로 수행하고, 도 36에 도시된 바와 같이, 조작된 TRAC-CAR-hnCD16 iT 세포는 T 세포에 네이티브가 아닌 ADCC를 가능하게 하는 hnCD16을 발현함으로써 종양을 표적으로 하는 2차 접근법을 제공한다.
CAR 및 hnCD16을 발현하는 유도체 T 세포는 CAR에 의해서 인식되는 악성종양을 표적으로 할 뿐만 아니라, 이러한 유도체 T 세포는 네이티브 성숙 효과기 T 세포(말초 혈액, 제대혈 또는 조직으로부터의 1차 T 세포)에서 일반적으로 관찰되지 않는 ADCC 기전을 추가로 획득하였다. 또한, iPSC 유래 T 세포는 1차 공급원으로부터 단리된 네이티브 성숙 효과기 T 세포에 비해서 더 긴 텔로미어 길이를 갖고, 덜 소진된다. 이와 같이, CAR 및 hnCD16 둘 다를 발현하는 iPSC 분화로부터 획득된 유도체 T 세포는 치료 항체와 상승작용하여, 획득된 ADCC 기전을 통한 CAR-T 세포 항원 탈출을 해결함으로써 CAR-T 지시된 종양 제거를 향상시킬 수 있다. hnCD16 매개된 ADCC와 함께 사용될 액체 종양 또는 고형 종양을 표적으로 하는 예시적인 치료용 항체는 항-CD20(리툭시맙, 벨투주맙, 오파투무맙, 유블리툭시맙, 오카라투주맙, 오비누투주맙), 항-Her2(트라스투주맙), 항-CD52(알렘투주맙), 항-EGFR(서툭시맙), 항-CD38(다라투무맙), 항-SLAMF7(엘로투주맙) 및 이들의 인간화된 및 Fc 변형된 변이체 및 기능성 등가물을 포함하지만 이들로 제한되지 않는다. 추가로, NK 세포 상의 CD16을 인식하는 또 다른 Fab 영역과 조합하여, 종양 세포 항원을 표적으로 하는 항체, 예컨대, 항- CD19, CD20 및 CD33 항원의 Fab 영역에 융합된 이중 및 삼중특이적 항체의 설계는 NK 세포의 자극, 그 다음 종양 세포 사멸로 이어진다.
실시예 7 - 면역관문 저해제 길항제와의 병용 요법을 위한 유도체 NK 세포
면역관문은 저해되지 않을 때 면역 반응을 억제 또는 하향조절할 수 있는 세포 분자, 종종 세포 표면 분자이다. 면역관문 저해제는 면역관문 유전자 발현 또는 유전자 생성물을 감소시킬 수 있거나 면역관문 분자의 활성을 감소시킬 수 있는 길항제이다. PD1/PDL1 또는 CTLA4를 표적으로 하는 면역관문 저해제(CI)의 개발은 종양학 환경을 변화시켰으며, 이들 작용제는 다중 적응증에서 장기간 완화를 제공한다. 그러나, 다수의 종양 아형은 면역관문 차단 요법에 내성이 있고, 재발은 중요한 관심사이다. 따라서, CI 내성을 극복할 수있는 능력을 갖는 새로운 치료법이 필요하다.
본 개시내용에서, 본 명세서에 제공된 유도체 NK 세포는 종양 미세환경에 T 세포를 모집하고, 종양 부위에서 T 세포 활성화를 증강시키는 능력을 갖는 것으로 나타났다. 도 17에 나타낸 바와 같이, 활성화된 iNK 세포는 T 세포 활성화를 향상시키는 가용성 인자를 생산한다. 본 검정에서, hnCD16 iNK 세포를, ADCC-유도 항-PDL1 항체의 존재 하에서 높은 수준의 PDL1을 발현하는 K562 또는 K562와 조합하였다. 밤새 인큐베이션 후, 상청액을 수집하고, T 세포 활성화 마커, CD69의 공여자 T 세포의 발현에 대한 유세포 분석 염색 전에 동종 공여자 T 세포에서 4 또는 24시간 동안 인큐베이션시켰다. 유도 만능 줄기세포로부터의 시험관내 유도된 분화를 통해서 생성된 유도체 NK 세포는 세포 표면 PD-1에 대해서 음성이다. 이와 같이, 유도체 NK 세포에 대한 PDL1의 발현은 NK 세포 세포독성에 대해서 식별 가능한 효과를 갖지 않았다. 추가로, 항-PDL1 항체의 첨가는 유도체 NK 세포의 세포독성 또는 탈과립화에 영향을 미치지 않았는데, 이는 이들 세포가 PDL1-PD1 매개된 저해에 내성임을 시사한다. 추가로, 유도체 NK 세포의 활성화는 말초 혈액(PB) 또는 제대혈(UCB) NK 세포를 비롯한 1차 NK 세포와 비교할 때 CD69의 증가된 상향조절을 포함하여 가용성 인자의 분비를 유도하였는데, 이는 T 세포를 활성화하는 향상된 능력을 입증한다.
종래의 트랜스웰 이동 검정을 사용하여, 활성화된 T 세포의 지시된 이동은 본 발명의 활성화된 유도체 NK 세포에 의한 CCL3, CCL4, CXCL10 및 다른 가용성 인자의 분비 시에 촉진되었다. 본 검정에서, hnCD16 iNK 세포를, ADCC-유도 항-PDL1 항체의 존재 하에서 높은 수준의 PDL1을 발현하는 SKOV-3 또는 SKOV-3-PDL1와 조합하였다. 밤새 인큐베이션시킨 후, 상청액을 수집하고, 표준 트랜스웰 주화성 챔버의 하부 챔버에서 24시간 동안 인큐베이션시키고, 상부 챔버에서 동종 공여자 T 세포를 인큐베이션시켰다. 인큐베이션 후, 하부 챔버로의 T 세포 이동을 유세포 분석법에 의해서 정량하였다. 따라서, 도 18에 도시된 바와 같이, 활성화된 iNK 세포(중간 칼럼)는 T 세포 이동을 향상시킨다.
또한, 활성화 시, 본 명세서의 유도체 NK 세포는 인터페론 감마(IFNγ), CCL3, CCL4, CXCL10 및 CCL22를 포함하여, 풍부한 염증성 사이토카인 및 케모카인의 세포 생산에 의해 입증되는 직접적인 항종양 능력을 나타낸다. IFNγ는 항-종양 T 세포 활성을 조절하는데 결정적인 역할을 한다. 이러한 생체내 검정에서, NSG 마우스에게 1E7 iNK 세포를 I.P.(복강내)로 또는 5E6 활성화된 T 세포를 R.O.(안구뒤) 또는 둘 다로 주사하였다. 4일 후, 말초 혈액 및 복강을 유세포 분석법에 의해 T 세포의 존재에 대해 평가하였다. T 세포를 제공받지만 유도체 NK 세포를 제공받지 않은 마우스에 비해서, iPSC 유래 NK 세포 I.P.를 제공받은 마우스는 말초 혈액에서 T 세포 빈도가 감소하였고(도 19A), 복강에서 T 세포가 증가하였다(도 19B). 도 19A 및 19B에서, 각각의 데이터 지점은 개별 마우스를 나타낸다. 이러한 생체내 모집 모델에 나타난 바와 같이, 유도체 NK 세포는, 활성화된 T 세포를 순환계로부터 복막 내로 동원함으로써 T 세포 이동을 향상시키는 것으로 관찰되었다.
더욱이, 시험관내 3차원 종양 스페로이드 모델(이하 실시예에서 추가로 설명됨)을 이용하여, 제공된 유도체 NK 세포의 존재 하에서 T 세포의 종양 스페로이드 내로의 침투가 향상되는 것이 관찰되었다. 30,000개의 녹색 형광 표지된 T 세포를 SKOV-3 미소구체와 단독으로 배양하거나(적색 핵; 도 20의 하부 패널), 15,000개의 iNK 세포와 조합하여(도 20의 상부 패널) 배양하고, 15시간에 걸쳐 영상화하였다. 도 20에 도시된 바와 같이, T 세포만으로는 스페로이드의 중심을 침투하지 못했지만, iNK 세포의 첨가는 종양 스페로이드로의 T 세포 침윤 및 종양 스페로이드 파괴를 촉진시켰다.
유래된 NK 세포와 공동 배양될 때 종양 스페로이드의 강화된 T 세포 침윤 및 강화된 세포독성을, 가장 큰 적색 물체 마스크 내에서 총 적분된 녹색 형광 강도를 측정함으로써 도 23에 추가로 정량적으로 도시한다. SKOV-3 스페로이드 내로의 T 세포의 침윤을 유래된 NK 세포(1:1 비), CD3+ T 세포(2:1 비) 또는 iNK(1:1 비) + T 세포(2:1 비)와의 24시간 공동 배양에 대해 측정하였고, 도 23A에 도시된 바와 같이, 유래된 NK 세포는 종양 스페로이드의 T 세포 침윤을 향상시킨다.
3D 종양 스페로이드 모델에서 T 세포 및 iPSC 유래 NK 세포의 공동 배양은 또한 종양 세포 사멸 및 IFNγ 및 TNFα의 생산 증가를 초래하였다. SKOV-3 스페로이드(유래된 NK 세포(1:1 비), CD3+ T 세포(2:1 비) 또는 iNK(1:1 비) + T 세포(2:1 비))와의 효과기 세포 인큐베이션 7일 후에, 상청액을 수집하고, TNFα 및 IFNγ 생산에 대해서 평가하였다(도 24 A 및 도 24B). T 세포와 iPSC-NK의 공동 배양은 CD4+ 및 CD8+ T 세포 둘 다에 대해서 사이토카인 생산을 증가시켰는데, 이는 iPSC 유도체 NK 세포가 스페로이드 모델에서 고형 종양 사멸을 위해서 IFNγ 및 TNFα의 생산을 향상시키는데 있어서 T 세포와 상승작용한다는 것을 입증한다.
이와 같이, 종양 부위에 대한 T 세포의 모집을 촉진시킴으로써 그리고 T 세포 활성화 및 침윤을 향상시킴으로써, 이러한 기능적으로 강력한 유도체 NK 세포는 면역관문 저해제를 비롯한 T 세포 표적화 면역요법과 함께 상승작용하여 국소 면역억제를 완화시키고 종양 부하를 감소시킬 수 있다고 입증된다. 종합하면, 이들 데이터는 본 명세서에 제공된 유도체 NK 세포를 포함하는 동종이계 병용 요법을 뒷받침하고; 시험관내에서 유도체 NK 세포의 제조를 위한 재생 가능한 공급원으로서 마스터 만능 세포주를 뒷받침하는 증거를 제공한다. 본 명세서에 입증된 바와 같이, 마스터 만능 세포주는 하나 이상의 T 세포 표적화된 치료제를 포함하는 다양한 동종이계 병용 요법의 목적을 위해서 기능적으로 향상된 유도체 세포 생성물을 획득하기 위해서 목적하는 게놈 편집을 갖는 것일 수 있다.
본 명세서에 제공된 바와 같은 유도체 NK 세포와의 병용 요법에 적합한 면역관문 저해제는 PD-1(Pdcdl, CD279), PDL-1(CD274), TIM-3(Havcr2), TIGIT(WUCAM 및 Vstm3), LAG-3(Lag3, CD223), CTLA-4(Ctla4, CD152), 2B4(CD244), 4-1BB(CD137), 4-1BBL(CD137L), A2aR, BATE, BTLA, CD39(Entpdl), CD47, CD73(NT5E), CD94, CD96, CD160, CD200, CD200R, CD274, CEACAM1, CSF-1R, Foxpl, GARP, HVEM, IDO, EDO, TDO, LAIR-1, MICA/B, NR4A2, MAFB, OCT-2(Pou2f2), 레티노산 수용체 알파(Rara), TLR3, VISTA, NKG2A/HLA-E 및 저해성 KIR(예를 들어, 2DL1, 2DL2, 2DL3, 3DL1 및 3DL2)의 길항제를 포함하지만 이들로 제한되지 않는다. 제공된 유도체 NK 세포와의 병용 요법의 일부 실시형태는 1종의 면역관문 분자를 표적으로 하는 저해제를 포함한다. 제공된 유도체 NK 세포와의 병용 요법의 일부 다른 실시형태는 2종, 3종 또는 그 초과의 면역관문 분자가 표적화되도록 2종, 3종 또는 그 초과의 저해제를 포함한다. 일부 실시형태에서, 제공된 유도체 NK 세포와의 병용 요법에서 2종 또는 3종 또는 그 초과의 면역관문 저해제의 투여는 동시 또는 순차적이다. 일부 실시형태에서, 상기 면역관문 분자 중 임의의 것을 저해하는 길항제는 항체이다. 일부 실시형태에서, 면역관문 저해성 항체는 뮤린 항체, 인간 항체, 인간화된 항체, 낙타 Ig, 상어 중쇄-단독 항체(VNAR), Ig NAR, 키메라 항체, 재조합 항체 또는 이의 항체 단편일 수 있다. 항체 단편의 비제한적인 예는 Fab, Fab', F(ab)'2, F(ab)'3, Fv, 단일 쇄 항원 결합 단편(scFv), (scFv)2, 다이설파이드 안정화된 Fv(dsFv), 미니바디, 다이아바디, 트라이아바디, 테트라바디, 단일-도메인 항원 결합 단편(sdAb, 나노바디), 재조합 중쇄-단독 항체(VHH) 및 전체 항체의 결합 특이성을 보유하는 다른 항체 단편(이것은 제조하기에 더 비용 효과적일 수 있거나, 보다 용이하게 사용될 수 있거나, 전체 항체보다 더 민감할 수 있음)을 포함한다. 일부 실시형태에서, 1종 또는 2종 또는 3종 또는 그 초과의 면역관문 저해제는 아테졸리주맙, 아벨루맙, 더발루맙, 이필리무맙, IPH4102, IPH43, IPH33, 리릴루맙, 모날리주맙, 니볼루맙, 펨브롤리주맙 및 이들의 유도체 또는 기능성 등가물 중 적어도 1종을 포함한다.
유도체 NK 세포 및 하나 이상의 관문 저해제를 포함하는 병용 요법은 피부 T-세포 림프종, 비호지킨 림프종, 균상 식육종, 파제트병모양망상증(파제트병모양망상증), 시자리 증후군, 육아종 이완 피부, 림프종양구진증, 만성 태선양 비강진, 급성 태선상두진상비강진, CD30+ 피부 T-세포 림프종, 이차 피부 CD30+ 거대 세포 림프종, 비-균상 식육종 CD30 피부 거대 T-세포 림프종, 다형성 T-세포 림프종, 레너트 림프종, 피하 T-세포 림프종, 혈관중심성 림프종, 아구성 NK-세포 림프종, B-세포 림프종, 호지킨 림프종(HL), 두경부 종양; 편평 세포 암종, 횡문근육종, 루이스 폐암종(LLC), 비소세포 폐암, 식도 편평 세포 암종, 식도 선암종, 신장 세포 암종(RCC), 결장직장 암(CRC), 급성 골수 백혈병(AML), 유방암, 위암, 전립선 소세포 신경내분비 암종(SCNC), 간암, 교모세포종, 간암, 구강 편평 세포 암종, 췌장암, 유두갑상선암, 간내 담도세포 암종, 간세포 암종, 골암, 전이 및 비인두 암종을 포함하지만 이들로 제한되지 않는 액체암 및 고형암의 치료에 적용 가능하다.
증명된 유도체 NK 세포 및 항-면역 면역관문 저해제(들)를 포함하는 병용 요법에 대한 반응을 평가하는 경우, 반응은 하기 중 적어도 하나를 포함하는 기준에 의해서 측정될 수 있다: 임상 유익비, 사망까지의 생존, 병리학적 완전 반응, 병리학적 반응의 반-정량적 측정, 임상적 완전 관해, 임상적 부분적 관해, 임상적으로 안정적인 질환, 재발이 없는 생존, 무전이 생존, 무질환 생존, 순환 종양 세포 감소, 순환 마커 반응 및 RECIST(Response Evaluation Criteria In Solid Tumors) 기준.
실시예 8 -
생체내 세포 침윤 및 관련 기능을 평가하기 위한 고형 종양을 모방한 3차원 종양 스페로이드 모델
자동화된 색상 태그가 있는 3차원 종양 스페로이드 모델(생체내 종양원성 모델으로도 불림)을 인-하우스에서 개발하였고, 이를 IncuCyte(상표명) S3에 의해서 사용하여 본 명세서에 제공된 유도체 효과기 세포에 의해서 유도된 암 성장 및 형태학적 변화를 모니터링 및 정량할 수 있다. 이러한 3D 종양 스페로이드 모델은 효과기 세포 생체내 기능, 종양 세포와의 상호작용 및 종양 세포 반응을 평가하기 위해서 생리학적으로 관련된 다수의 시험관내 고형암 시스템을 유도할 수 있는데, 이는 현재 암 면역학 연구에 사용되는 2D 대안에 의해서 달성될 수 없는 것이다.
여기서, 다수의 고형 종양 세포주를 먼저 3D 종양 스페로이드를 형성하는 능력에 대해서 시험하였다. 종양에 대한 생체내 종양형성 모델이 확립되면, 면역관문 저해제(들)와의 병용 요법에서 기능성 향상을 갖거나 갖지 않는 유도체 NK 및/또는 T 세포의 효과를 분석 및 비교하고, 종양 세포 표적화 사멸, T 세포(또는 임의의 다른 방관자 효과기 세포) 모집, 종양 침윤에서의 세포의 생체내 능력을 평가하였다.
종양 스페로이드는 핵 국지화 형광 단백질 NucLight(상표명) Red(NLR)이 사전에 형질도입된 부착성 세포주를 사용하여 마트리겔의 존재 하에서 둥근 바닥 96웰 조직 배양 플레이트에서 개시된다. 종양 스페로이드를 확립하는데 사용되는 세포주는 SKOV-3(난소암), A549(폐암), MCF7(유방암), PANC1(췌장암) 및 다수의 기타(예를 들어, 문헌[Arya et. al., J. Chem. Pharm. Res., 2011, 3(6):514-520] 참고)를 포함한다. 종양 스페로이드 형성은 약 3 내지 4일에 걸쳐 진행되며. Incucyte Zoom(상표명) 영상화 시스템에서 적색 형광 영상 분석에 의해 정량된다. 예시로서, 도 20은 SKOV3-NLR 형질도입된 세포가 2.5% MTG의 존재 하에서 84시간 과정에 걸쳐서 구체를 형성하고, 지시된 시점에 각각의 프레임이 라이브 동역학 영상화에 의해서 캡처되고(상부 패널), 적용된 알고리즘 마스크에 의해서 정의된다(하단 패널)는 것을 나타낸다.
종양 세포독성 실험을 위해서, 효과기 세포, 예컨대, 제공된 유도체 NK 또는 T 세포를 정의된 수로 스페로이드에 첨가하였다. 효과기 세포의 첨가 후, 종양 스페로이드 구조의 파괴를 Incucyte(상표명) 영상화에 의해서 시각적으로 모니터링하였고, 적색 형광 면적, 강도 또는 적분 강도를 측정하여 정량하였다. 효과기 세포 종양 침윤은 각각의 시점으로부터의 영상의 엑스포트 후 상업적으로 입수 가능한 영상 분석 소프트웨어에서 정량할 수 있다.
도 21A는 48시간에 걸친 SKOV3-NLR 스페로이드 내로의 유도체 NK 세포 침윤을 도시한다. 유도체 NK 세포를 RapidCytoLight(상표명) Green 시약으로 사전 표지하였고, 마스크(마젠타)는 스페로이드 중심을 정의한다. 스페로이드 크기 및 총 적분 형광 강도의 변화를 시간에 따라서 연속적으로 모니터링하였다(도 21A).
스페로이드 내로의 T 세포 침윤의 관찰은 녹색 형광 염료로 형광 표지된 T 세포를 사용하여 달성되었다. T 세포에 의한 종양 침윤을 도 21B에 도시한다. 총 30,000개의 녹색 형광 표지된 T 세포를 SKOV-3 미소구체와 단독으로 배양하거나(적색 핵), 15,000개의 iNK 세포와 조합하여 배양하고(표지되지 않음), 15시간에 걸쳐 영상화하였다. T 세포 침윤은 적색 종양 스페로이드 내의 녹색 T 세포의 축적을 가시화함으로써 결정되었다. 도 21B에 도시된 바와 같이, T 세포만으로는 종양 스페로이드의 중심을 침투하지 못했지만, iNK 세포의 첨가는 T 세포 침윤 및 종양 스페로이드 파괴를 촉진시켰는데, 이는 생체내에서 고형암을 표적으로 하는 본 출원의 유도체 NK 세포와 면역관문 저해제를 사용한 병용 요법에 대한 지지를 제공한다.
당업자는 본 명세서에 기술된 방법, 조성물 및 생성물이 예시적인 실시형태를 대표하고, 본 발명의 범주를 제한하는 것으로 의도되지 않는다는 것을 쉽게 인식할 것이다. 다양한 치환 및 변형은 본 발명의 범주 및 사상으로부터 벗어나지 않으면서 본 명세서에 개시된 본 개시내용에 행해질 수 있음은 당업자에게 쉽게 자명할 것이다.
본 명세서에 언급된 모든 특허 및 간행물은 당업자의 수준을 나타낸다. 모든 특허 및 간행물은 각각의 개별 간행물이 구체적으로 그리고 개별적으로 참조에 의해 포함된 것과 동일한 정도로 본 명세서에 참조에 의해 포함된다.
본 명세서에 예시적으로 기술된 본 개시내용은 본 명세서에 구체적으로 개시되지 않은 임의의 요소 또는 요소들, 제한 또는 제한들의 부재 하에서 적합하게 실시될 수 있다. 따라서, 예를 들어, 각각의 예에서 본 명세서에서 용어 "포함하는", "본질적으로 이루어진" 및 "이루어진" 중 임의의 것은 다른 2개의 용어 중 어느 하나에 의해 대체될 수 있다. 사용된 용어 및 표현은 제한이 아니라 설명의 관점에서 사용되고, 도시되고 기술된 특징의 임의의 등가물 또는 이의 부분을 배제하는 이러한 용어 및 표현의 사용에서 의도가 없지만, 다양한 변형이 청구된 개시내용의 범주 내에서 가능하다는 것이 인식된다. 따라서, 본 개시내용이 바람직한 실시형태 및 선택적인 특징에 의해 구체적으로 개시되어 있지만, 본 명세서에 개시된 개념의 변형 및 변경은 관련 기술 분야의 통사의 기술자에 의해서 분류될 수 있고, 이러한 변형 및 변경은 첨부된 청구범위에 의해서 정의되는 바와 같은 본 발명의 범주에 포함되는 것으로 간주되는 것으로 이해되어야 한다.
SEQUENCE LISTING
<110> Fate Therapeutics, Inc.
<120> IMMUNOTHERAPIES USING ENHANCED iPSC DERIVED EFFECTOR CELLS
<130> 13601-195-228
<140> TBA
<141> 2018-11-30
<150> US 62/596,659
<151> 2017-12-08
<150> US 62/657,626
<151> 2018-04-13
<160> 16
<170> PatentIn version 3.5
<210> 1
<211> 340
<212> PRT
<213> Artificial Sequence
<220>
<223> CD64 domain-based construction
<400> 1
Met Trp Phe Leu Thr Thr Leu Leu Leu Trp Val Pro Val Asp Gly Gln
1 5 10 15
Val Asp Thr Thr Lys Ala Val Ile Thr Leu Gln Pro Pro Trp Val Ser
20 25 30
Val Phe Gln Glu Glu Thr Val Thr Leu His Cys Glu Val Leu His Leu
35 40 45
Pro Gly Ser Ser Ser Thr Gln Trp Phe Leu Asn Gly Thr Ala Thr Gln
50 55 60
Thr Ser Thr Pro Ser Tyr Arg Ile Thr Ser Ala Ser Val Asn Asp Ser
65 70 75 80
Gly Glu Tyr Arg Cys Gln Arg Gly Leu Ser Gly Arg Ser Asp Pro Ile
85 90 95
Gln Leu Glu Ile His Arg Gly Trp Leu Leu Leu Gln Val Ser Ser Arg
100 105 110
Val Phe Thr Glu Gly Glu Pro Leu Ala Leu Arg Cys His Ala Trp Lys
115 120 125
Asp Lys Leu Val Tyr Asn Val Leu Tyr Tyr Arg Asn Gly Lys Ala Phe
130 135 140
Lys Phe Phe His Trp Asn Ser Asn Leu Thr Ile Leu Lys Thr Asn Ile
145 150 155 160
Ser His Asn Gly Thr Tyr His Cys Ser Gly Met Gly Lys His Arg Tyr
165 170 175
Thr Ser Ala Gly Ile Ser Val Thr Val Lys Glu Leu Phe Pro Ala Pro
180 185 190
Val Leu Asn Ala Ser Val Thr Ser Pro Leu Leu Glu Gly Asn Leu Val
195 200 205
Thr Leu Ser Cys Glu Thr Lys Leu Leu Leu Gln Arg Pro Gly Leu Gln
210 215 220
Leu Tyr Phe Ser Phe Tyr Met Gly Ser Lys Thr Leu Arg Gly Arg Asn
225 230 235 240
Thr Ser Ser Glu Tyr Gln Ile Leu Thr Ala Arg Arg Glu Asp Ser Gly
245 250 255
Leu Tyr Trp Cys Glu Ala Ala Thr Glu Asp Gly Asn Val Leu Lys Arg
260 265 270
Ser Pro Glu Leu Glu Leu Gln Val Leu Gly Leu Gln Leu Pro Thr Pro
275 280 285
Val Trp Phe His Tyr Gln Val Ser Phe Cys Leu Val Met Val Leu Leu
290 295 300
Phe Ala Val Asp Thr Gly Leu Tyr Phe Ser Val Lys Thr Asn Ile Arg
305 310 315 320
Ser Ser Thr Arg Asp Trp Lys Asp His Lys Phe Lys Trp Arg Lys Asp
325 330 335
Pro Gln Asp Lys
340
<210> 2
<211> 336
<212> PRT
<213> Artificial Sequence
<220>
<223> CD64 exon-based construction
<400> 2
Met Trp Phe Leu Thr Thr Leu Leu Leu Trp Val Pro Val Asp Gly Gln
1 5 10 15
Val Asp Thr Thr Lys Ala Val Ile Thr Leu Gln Pro Pro Trp Val Ser
20 25 30
Val Phe Gln Glu Glu Thr Val Thr Leu His Cys Glu Val Leu His Leu
35 40 45
Pro Gly Ser Ser Ser Thr Gln Trp Phe Leu Asn Gly Thr Ala Thr Gln
50 55 60
Thr Ser Thr Pro Ser Tyr Arg Ile Thr Ser Ala Ser Val Asn Asp Ser
65 70 75 80
Gly Glu Tyr Arg Cys Gln Arg Gly Leu Ser Gly Arg Ser Asp Pro Ile
85 90 95
Gln Leu Glu Ile His Arg Gly Trp Leu Leu Leu Gln Val Ser Ser Arg
100 105 110
Val Phe Thr Glu Gly Glu Pro Leu Ala Leu Arg Cys His Ala Trp Lys
115 120 125
Asp Lys Leu Val Tyr Asn Val Leu Tyr Tyr Arg Asn Gly Lys Ala Phe
130 135 140
Lys Phe Phe His Trp Asn Ser Asn Leu Thr Ile Leu Lys Thr Asn Ile
145 150 155 160
Ser His Asn Gly Thr Tyr His Cys Ser Gly Met Gly Lys His Arg Tyr
165 170 175
Thr Ser Ala Gly Ile Ser Val Thr Val Lys Glu Leu Phe Pro Ala Pro
180 185 190
Val Leu Asn Ala Ser Val Thr Ser Pro Leu Leu Glu Gly Asn Leu Val
195 200 205
Thr Leu Ser Cys Glu Thr Lys Leu Leu Leu Gln Arg Pro Gly Leu Gln
210 215 220
Leu Tyr Phe Ser Phe Tyr Met Gly Ser Lys Thr Leu Arg Gly Arg Asn
225 230 235 240
Thr Ser Ser Glu Tyr Gln Ile Leu Thr Ala Arg Arg Glu Asp Ser Gly
245 250 255
Leu Tyr Trp Cys Glu Ala Ala Thr Glu Asp Gly Asn Val Leu Lys Arg
260 265 270
Ser Pro Glu Leu Glu Leu Gln Val Leu Gly Leu Phe Phe Pro Pro Gly
275 280 285
Tyr Gln Val Ser Phe Cys Leu Val Met Val Leu Leu Phe Ala Val Asp
290 295 300
Thr Gly Leu Tyr Phe Ser Val Lys Thr Asn Ile Arg Ser Ser Thr Arg
305 310 315 320
Asp Trp Lys Asp His Lys Phe Lys Trp Arg Lys Asp Pro Gln Asp Lys
325 330 335
<210> 3
<211> 335
<212> PRT
<213> Artificial Sequence
<220>
<223> CD64 exon-based construction
<400> 3
Met Trp Phe Leu Thr Thr Leu Leu Leu Trp Val Pro Val Asp Gly Gln
1 5 10 15
Val Asp Thr Thr Lys Ala Val Ile Thr Leu Gln Pro Pro Trp Val Ser
20 25 30
Val Phe Gln Glu Glu Thr Val Thr Leu His Cys Glu Val Leu His Leu
35 40 45
Pro Gly Ser Ser Ser Thr Gln Trp Phe Leu Asn Gly Thr Ala Thr Gln
50 55 60
Thr Ser Thr Pro Ser Tyr Arg Ile Thr Ser Ala Ser Val Asn Asp Ser
65 70 75 80
Gly Glu Tyr Arg Cys Gln Arg Gly Leu Ser Gly Arg Ser Asp Pro Ile
85 90 95
Gln Leu Glu Ile His Arg Gly Trp Leu Leu Leu Gln Val Ser Ser Arg
100 105 110
Val Phe Thr Glu Gly Glu Pro Leu Ala Leu Arg Cys His Ala Trp Lys
115 120 125
Asp Lys Leu Val Tyr Asn Val Leu Tyr Tyr Arg Asn Gly Lys Ala Phe
130 135 140
Lys Phe Phe His Trp Asn Ser Asn Leu Thr Ile Leu Lys Thr Asn Ile
145 150 155 160
Ser His Asn Gly Thr Tyr His Cys Ser Gly Met Gly Lys His Arg Tyr
165 170 175
Thr Ser Ala Gly Ile Ser Val Thr Val Lys Glu Leu Phe Pro Ala Pro
180 185 190
Val Leu Asn Ala Ser Val Thr Ser Pro Leu Leu Glu Gly Asn Leu Val
195 200 205
Thr Leu Ser Cys Glu Thr Lys Leu Leu Leu Gln Arg Pro Gly Leu Gln
210 215 220
Leu Tyr Phe Ser Phe Tyr Met Gly Ser Lys Thr Leu Arg Gly Arg Asn
225 230 235 240
Thr Ser Ser Glu Tyr Gln Ile Leu Thr Ala Arg Arg Glu Asp Ser Gly
245 250 255
Leu Tyr Trp Cys Glu Ala Ala Thr Glu Asp Gly Asn Val Leu Lys Arg
260 265 270
Ser Pro Glu Leu Glu Leu Gln Val Leu Gly Phe Phe Pro Pro Gly Tyr
275 280 285
Gln Val Ser Phe Cys Leu Val Met Val Leu Leu Phe Ala Val Asp Thr
290 295 300
Gly Leu Tyr Phe Ser Val Lys Thr Asn Ile Arg Ser Ser Thr Arg Asp
305 310 315 320
Trp Lys Asp His Lys Phe Lys Trp Arg Lys Asp Pro Gln Asp Lys
325 330 335
<210> 4
<211> 1032
<212> DNA
<213> Artificial Sequence
<220>
<223> CD64 domain-based construction (encoding SEQ ID NO. 1)
<400> 4
cttggagaca acatgtggtt cttgacaact ctgctccttt gggttccagt tgatgggcaa 60
gtggacacca caaaggcagt gatcactttg cagcctccat gggtcagcgt gttccaagag 120
gaaaccgtaa ccttgcattg tgaggtgctc catctgcctg ggagcagctc tacacagtgg 180
tttctcaatg gcacagccac tcagacctcg acccccagct acagaatcac ctctgccagt 240
gtcaatgaca gtggtgaata caggtgccag agaggtctct cagggcgaag tgaccccata 300
cagctggaaa tccacagagg ctggctacta ctgcaggtct ccagcagagt cttcacggaa 360
ggagaacctc tggccttgag gtgtcatgcg tggaaggata agctggtgta caatgtgctt 420
tactatcgaa atggcaaagc ctttaagttt ttccactgga attctaacct caccattctg 480
aaaaccaaca taagtcacaa tggcacctac cattgctcag gcatgggaaa gcatcgctac 540
acatcagcag gaatatctgt cactgtgaaa gagctatttc cagctccagt gctgaatgca 600
tctgtgacat ccccactcct ggaggggaat ctggtcaccc tgagctgtga aacaaagttg 660
ctcttgcaga ggcctggttt gcagctttac ttctccttct acatgggcag caagaccctg 720
cgaggcagga acacatcctc tgaataccaa atactaactg ctagaagaga agactctggg 780
ttatactggt gcgaggctgc cacagaggat ggaaatgtcc ttaagcgcag ccctgagttg 840
gagcttcaag tgcttggcct ccagttacca actcctgtct ggtttcatta ccaagtctct 900
ttctgcttgg tgatggtact cctttttgca gtggacacag gactatattt ctctgtgaag 960
acaaacattc gaagctcaac aagagactgg aaggaccata aatttaaatg gagaaaggac 1020
cctcaagaca aa 1032
<210> 5
<211> 1020
<212> DNA
<213> Artificial Sequence
<220>
<223> CD64 exon-based construction (encoding SEQ ID NO. 2)
<400> 5
cttggagaca acatgtggtt cttgacaact ctgctccttt gggttccagt tgatgggcaa 60
gtggacacca caaaggcagt gatcactttg cagcctccat gggtcagcgt gttccaagag 120
gaaaccgtaa ccttgcattg tgaggtgctc catctgcctg ggagcagctc tacacagtgg 180
tttctcaatg gcacagccac tcagacctcg acccccagct acagaatcac ctctgccagt 240
gtcaatgaca gtggtgaata caggtgccag agaggtctct cagggcgaag tgaccccata 300
cagctggaaa tccacagagg ctggctacta ctgcaggtct ccagcagagt cttcacggaa 360
ggagaacctc tggccttgag gtgtcatgcg tggaaggata agctggtgta caatgtgctt 420
tactatcgaa atggcaaagc ctttaagttt ttccactgga attctaacct caccattctg 480
aaaaccaaca taagtcacaa tggcacctac cattgctcag gcatgggaaa gcatcgctac 540
acatcagcag gaatatctgt cactgtgaaa gagctatttc cagctccagt gctgaatgca 600
tctgtgacat ccccactcct ggaggggaat ctggtcaccc tgagctgtga aacaaagttg 660
ctcttgcaga ggcctggttt gcagctttac ttctccttct acatgggcag caagaccctg 720
cgaggcagga acacatcctc tgaataccaa atactaactg ctagaagaga agactctggg 780
ttatactggt gcgaggctgc cacagaggat ggaaatgtcc ttaagcgcag ccctgagttg 840
gagcttcaag tgcttggttt gttctttcca cctgggtacc aagtctcttt ctgcttggtg 900
atggtactcc tttttgcagt ggacacagga ctatatttct ctgtgaagac aaacattcga 960
agctcaacaa gagactggaa ggaccataaa tttaaatgga gaaaggaccc tcaagacaaa 1020
<210> 6
<211> 1005
<212> DNA
<213> Artificial Sequence
<220>
<223> CD64 exon-based construction (encoding SEQ ID NO. 3)
<400> 6
atgtggttct tgacaactct gctcctttgg gttccagttg atgggcaagt ggacaccaca 60
aaggcagtga tcactttgca gcctccatgg gtcagcgtgt tccaagagga aaccgtaacc 120
ttgcactgtg aggtgctcca tctgcctggg agcagctcta cacagtggtt tctcaatggc 180
acagccactc agacctcgac ccccagctac agaatcacct ctgccagtgt caatgacagt 240
ggtgaataca ggtgccagag aggtctctca gggcgaagtg accccataca gctggaaatc 300
cacagaggct ggctactact gcaggtctcc agcagagtct tcacggaagg agaacctctg 360
gccttgaggt gtcatgcgtg gaaggataag ctggtgtaca atgtgcttta ctatcgaaat 420
ggcaaagcct ttaagttttt ccactggaac tctaacctca ccattctgaa aaccaacata 480
agtcacaatg gcacctacca ttgctcaggc atgggaaagc atcgctacac atcagcagga 540
atatctgtca ctgtgaaaga gctatttcca gctccagtgc tgaatgcatc tgtgacatcc 600
ccactcctgg aggggaatct ggtcaccctg agctgtgaaa caaagttgct cttgcagagg 660
cctggtttgc agctttactt ctccttctac atgggcagca agaccctgcg aggcaggaac 720
acatcctctg aataccaaat actaactgct agaagagaag actctgggtt atactggtgc 780
gaggctgcca cagaggatgg aaatgtcctt aagcgcagcc ctgagttgga gcttcaagtg 840
cttggcttct ttccacctgg gtaccaagtc tctttctgct tggtgatggt actccttttt 900
gcagtggaca caggactata tttctctgtg aagacaaaca ttcgaagctc aacaagagac 960
tggaaggacc ataaatttaa atggagaaag gaccctcaag acaaa 1005
<210> 7
<211> 153
<212> PRT
<213> Artificial Sequence
<220>
<223> CD28 co-stim + CD3-zeta-ITAM construct
<400> 7
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe Ser Arg Ser
35 40 45
Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr Asn Glu
50 55 60
Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg
65 70 75 80
Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln
85 90 95
Glu Gly Leu Phe Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Phe
100 105 110
Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp
115 120 125
Gly Leu Phe Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Phe Asp Ala
130 135 140
Leu His Met Gln Ala Leu Pro Pro Arg
145 150
<210> 8
<211> 219
<212> PRT
<213> Artificial Sequence
<220>
<223> CD28 hinge + CD28 TM + CD28 co-stim + CD3-zeta-ITAM construct
<400> 8
Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser Asn
1 5 10 15
Gly Thr Ile Ile His Val Lys Gly Lys His Leu Cys Pro Ser Pro Leu
20 25 30
Phe Pro Gly Pro Ser Lys Pro Phe Trp Val Leu Val Val Val Gly Gly
35 40 45
Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe
50 55 60
Trp Val Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn
65 70 75 80
Met Thr Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr
85 90 95
Ala Pro Pro Arg Asp Phe Ala Ala Tyr Arg Ser Arg Val Lys Phe Ser
100 105 110
Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln Leu Tyr
115 120 125
Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys
130 135 140
Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn
145 150 155 160
Pro Gln Glu Gly Leu Phe Asn Glu Leu Gln Lys Asp Lys Met Ala Glu
165 170 175
Ala Phe Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly
180 185 190
His Asp Gly Leu Phe Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Phe
195 200 205
Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
210 215
<210> 9
<211> 263
<212> PRT
<213> Artificial Sequence
<220>
<223> NKG2D TM + 2B4 + CD3-zeta construct
<400> 9
Ser Asn Leu Phe Val Ala Ser Trp Ile Ala Val Met Ile Ile Phe Arg
1 5 10 15
Ile Gly Met Ala Val Ala Ile Phe Cys Cys Phe Phe Phe Pro Ser Trp
20 25 30
Arg Arg Lys Arg Lys Glu Lys Gln Ser Glu Thr Ser Pro Lys Glu Phe
35 40 45
Leu Thr Ile Tyr Glu Asp Val Lys Asp Leu Lys Thr Arg Arg Asn His
50 55 60
Glu Gln Glu Gln Thr Phe Pro Gly Gly Gly Ser Thr Ile Tyr Ser Met
65 70 75 80
Ile Gln Ser Gln Ser Ser Ala Pro Thr Ser Gln Glu Pro Ala Tyr Thr
85 90 95
Leu Tyr Ser Leu Ile Gln Pro Ser Arg Lys Ser Gly Ser Arg Lys Arg
100 105 110
Asn His Ser Pro Ser Phe Asn Ser Thr Ile Tyr Glu Val Ile Gly Lys
115 120 125
Ser Gln Pro Lys Ala Gln Asn Pro Ala Arg Leu Ser Arg Lys Glu Leu
130 135 140
Glu Asn Phe Asp Val Tyr Ser Arg Val Lys Phe Ser Arg Ser Ala Asp
145 150 155 160
Ala Pro Ala Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn
165 170 175
Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg
180 185 190
Asp Pro Glu Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly
195 200 205
Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu
210 215 220
Ile Gly Met Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu
225 230 235 240
Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His
245 250 255
Met Gln Ala Leu Pro Pro Arg
260
<210> 10
<211> 308
<212> PRT
<213> Artificial Sequence
<220>
<223> CD8 hinge + NKG2D TM + 2B4 + CD3-zeta construct
<400> 10
Thr Thr Thr Pro Ala Pro Arg Pro Pro Thr Pro Ala Pro Thr Ile Ala
1 5 10 15
Ser Gln Pro Leu Ser Leu Arg Pro Glu Ala Cys Arg Pro Ala Ala Gly
20 25 30
Gly Ala Val His Thr Arg Gly Leu Asp Phe Ala Cys Asp Ser Asn Leu
35 40 45
Phe Val Ala Ser Trp Ile Ala Val Met Ile Ile Phe Arg Ile Gly Met
50 55 60
Ala Val Ala Ile Phe Cys Cys Phe Phe Phe Pro Ser Trp Arg Arg Lys
65 70 75 80
Arg Lys Glu Lys Gln Ser Glu Thr Ser Pro Lys Glu Phe Leu Thr Ile
85 90 95
Tyr Glu Asp Val Lys Asp Leu Lys Thr Arg Arg Asn His Glu Gln Glu
100 105 110
Gln Thr Phe Pro Gly Gly Gly Ser Thr Ile Tyr Ser Met Ile Gln Ser
115 120 125
Gln Ser Ser Ala Pro Thr Ser Gln Glu Pro Ala Tyr Thr Leu Tyr Ser
130 135 140
Leu Ile Gln Pro Ser Arg Lys Ser Gly Ser Arg Lys Arg Asn His Ser
145 150 155 160
Pro Ser Phe Asn Ser Thr Ile Tyr Glu Val Ile Gly Lys Ser Gln Pro
165 170 175
Lys Ala Gln Asn Pro Ala Arg Leu Ser Arg Lys Glu Leu Glu Asn Phe
180 185 190
Asp Val Tyr Ser Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala
195 200 205
Tyr Lys Gln Gly Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg
210 215 220
Arg Glu Glu Tyr Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu
225 230 235 240
Met Gly Gly Lys Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn
245 250 255
Glu Leu Gln Lys Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met
260 265 270
Lys Gly Glu Arg Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly
275 280 285
Leu Ser Thr Ala Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala
290 295 300
Leu Pro Pro Arg
305
<210> 11
<211> 414
<212> PRT
<213> Artificial Sequence
<220>
<223> a construct mimicking trans-presentation of IL15 (Design 2)
<400> 11
Met Asp Trp Thr Trp Ile Leu Phe Leu Val Ala Ala Ala Thr Arg Val
1 5 10 15
His Ser Gly Ile His Val Phe Ile Leu Gly Cys Phe Ser Ala Gly Leu
20 25 30
Pro Lys Thr Glu Ala Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys
35 40 45
Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr
50 55 60
Glu Ser Asp Val His Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe
65 70 75 80
Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile
85 90 95
His Asp Thr Val Glu Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser
100 105 110
Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu
115 120 125
Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser Phe Val His Ile Val
130 135 140
Gln Met Phe Ile Asn Thr Ser Ser Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Ser Leu
165 170 175
Gln Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp
180 185 190
Val Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser
195 200 205
Gly Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu
210 215 220
Asn Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys
225 230 235 240
Ile Arg Asp Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Ser Thr
245 250 255
Val Thr Thr Ala Gly Val Thr Pro Gln Pro Glu Ser Leu Ser Pro Ser
260 265 270
Gly Lys Glu Pro Ala Ala Ser Ser Pro Ser Ser Asn Asn Thr Ala Ala
275 280 285
Thr Thr Ala Ala Ile Val Pro Gly Ser Gln Leu Met Pro Ser Lys Ser
290 295 300
Pro Ser Thr Gly Thr Thr Glu Ile Ser Ser His Glu Ser Ser His Gly
305 310 315 320
Thr Pro Ser Gln Thr Thr Ala Lys Asn Trp Glu Leu Thr Ala Ser Ala
325 330 335
Ser His Gln Pro Pro Gly Val Tyr Pro Gln Gly His Ser Asp Thr Thr
340 345 350
Val Ala Ile Ser Thr Ser Thr Val Leu Leu Cys Gly Leu Ser Ala Val
355 360 365
Ser Leu Leu Ala Cys Tyr Leu Lys Ser Arg Gln Thr Pro Pro Leu Ala
370 375 380
Ser Val Glu Met Glu Ala Met Glu Ala Leu Pro Val Thr Trp Gly Thr
385 390 395 400
Ser Ser Arg Asp Glu Asp Leu Glu Asn Cys Ser His His Leu
405 410
<210> 12
<211> 1242
<212> DNA
<213> Artificial Sequence
<220>
<223> exemplary DNA sequence encoding the amino acid sequence of
SEQ ID NO: 11
<400> 12
atggactgga cctggattct gttcctggtc gcggctgcaa cgcgagtcca tagcggtatc 60
catgttttta ttcttgggtg tttttctgct gggctgccta agaccgaggc caactgggta 120
aatgtcatca gtgacctcaa gaaaatagaa gaccttatac aaagcatgca cattgatgct 180
actctctaca ctgagtcaga tgtacatccc tcatgcaaag tgacggccat gaaatgtttc 240
ctcctcgaac ttcaagtcat atctctggaa agtggcgacg cgtccatcca cgacacggtc 300
gaaaacctga taatactcgc taataatagt ctctcttcaa atggtaacgt aaccgagtca 360
ggttgcaaag agtgcgaaga gttggaagaa aaaaacataa aggagttcct gcaaagtttc 420
gtgcacattg tgcagatgtt cattaatacc tctagcggcg gaggatcagg tggcggtgga 480
agcggaggtg gaggctccgg tggaggaggt agtggcggag gttctcttca aataacttgt 540
cctccaccga tgtccgtaga acatgcggat atttgggtaa aatcctatag cttgtacagc 600
cgagagcggt atatctgcaa cagcggcttc aagcggaagg ccggcacaag cagcctgacc 660
gagtgcgtgc tgaacaaggc caccaacgtg gcccactgga ccacccctag cctgaagtgc 720
atcagagatc ccgccctggt gcatcagcgg cctgcccctc caagcacagt gacaacagct 780
ggcgtgaccc cccagcctga gagcctgagc ccttctggaa aagagcctgc cgccagcagc 840
cccagcagca acaatactgc cgccaccaca gccgccatcg tgcctggatc tcagctgatg 900
cccagcaaga gccctagcac cggcaccacc gagatcagca gccacgagtc tagccacggc 960
accccatctc agaccaccgc caagaactgg gagctgacag ccagcgcctc tcaccagcct 1020
ccaggcgtgt accctcaggg ccacagcgat accacagtgg ccatcagcac ctccaccgtg 1080
ctgctgtgtg gactgagcgc cgtgtcactg ctggcctgct acctgaagtc cagacagacc 1140
cctccactgg ccagcgtgga aatggaagcc atggaagcac tgcccgtgac ctggggcacc 1200
agctccagag atgaggatct ggaaaactgc tcccaccacc tg 1242
<210> 13
<211> 379
<212> PRT
<213> Artificial Sequence
<220>
<223> a construct mimicking trans-presentation of IL15 (Design 3)
<400> 13
Met Asp Trp Thr Trp Ile Leu Phe Leu Val Ala Ala Ala Thr Arg Val
1 5 10 15
His Ser Gly Ile His Val Phe Ile Leu Gly Cys Phe Ser Ala Gly Leu
20 25 30
Pro Lys Thr Glu Ala Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys
35 40 45
Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr
50 55 60
Glu Ser Asp Val His Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe
65 70 75 80
Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile
85 90 95
His Asp Thr Val Glu Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser
100 105 110
Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu
115 120 125
Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser Phe Val His Ile Val
130 135 140
Gln Met Phe Ile Asn Thr Ser Ser Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Ser Leu
165 170 175
Gln Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp
180 185 190
Val Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser
195 200 205
Gly Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu
210 215 220
Asn Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys
225 230 235 240
Ile Arg Asp Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Ser Thr
245 250 255
Val Thr Thr Ala Gly Val Thr Pro Gln Pro Glu Ser Leu Ser Pro Ser
260 265 270
Gly Lys Glu Pro Ala Ala Ser Ser Pro Ser Ser Asn Asn Thr Ala Ala
275 280 285
Thr Thr Ala Ala Ile Val Pro Gly Ser Gln Leu Met Pro Ser Lys Ser
290 295 300
Pro Ser Thr Gly Thr Thr Glu Ile Ser Ser His Glu Ser Ser His Gly
305 310 315 320
Thr Pro Ser Gln Thr Thr Ala Lys Asn Trp Glu Leu Thr Ala Ser Ala
325 330 335
Ser His Gln Pro Pro Gly Val Tyr Pro Gln Gly His Ser Asp Thr Thr
340 345 350
Val Ala Ile Ser Thr Ser Thr Val Leu Leu Cys Gly Leu Ser Ala Val
355 360 365
Ser Leu Leu Ala Cys Tyr Leu Lys Ser Arg Gln
370 375
<210> 14
<211> 1140
<212> DNA
<213> Artificial Sequence
<220>
<223> exemplary nucleic acid sequence encoding the amino acid sequence of
SEQ ID NO: 13
<400> 14
atggactgga cctggattct gttcctggtc gcggctgcaa cgcgagtcca tagcggtatc 60
catgttttta ttcttgggtg tttttctgct gggctgccta agaccgaggc caactgggta 120
aatgtcatca gtgacctcaa gaaaatagaa gaccttatac aaagcatgca cattgatgct 180
actctctaca ctgagtcaga tgtacatccc tcatgcaaag tgacggccat gaaatgtttc 240
ctcctcgaac ttcaagtcat atctctggaa agtggcgacg cgtccatcca cgacacggtc 300
gaaaacctga taatactcgc taataatagt ctctcttcaa atggtaacgt aaccgagtca 360
ggttgcaaag agtgcgaaga gttggaagaa aaaaacataa aggagttcct gcaaagtttc 420
gtgcacattg tgcagatgtt cattaatacc tctagcggcg gaggatcagg tggcggtgga 480
agcggaggtg gaggctccgg tggaggaggt agtggcggag gttctcttca aataacttgt 540
cctccaccga tgtccgtaga acatgcggat atttgggtaa aatcctatag cttgtacagc 600
cgagagcggt atatctgcaa cagcggcttc aagcggaagg ccggcacaag cagcctgacc 660
gagtgcgtgc tgaacaaggc caccaacgtg gcccactgga ccacccctag cctgaagtgc 720
atcagagatc ccgccctggt gcatcagcgg cctgcccctc caagcacagt gacaacagct 780
ggcgtgaccc cccagcctga gagcctgagc ccttctggaa aagagcctgc cgccagcagc 840
cccagcagca acaatactgc cgccaccaca gccgccatcg tgcctggatc tcagctgatg 900
cccagcaaga gccctagcac cggcaccacc gagatcagca gccacgagtc tagccacggc 960
accccatctc agaccaccgc caagaactgg gagctgacag ccagcgcctc tcaccagcct 1020
ccaggcgtgt accctcaggg ccacagcgat accacagtgg ccatcagcac ctccaccgtg 1080
ctgctgtgtg gactgagcgc cgtgtcactg ctggcctgct acctgaagtc cagacagtga 1140
<210> 15
<211> 242
<212> PRT
<213> Artificial Sequence
<220>
<223> a construct mimicking trans-presentation of IL15 (Design 4)
<400> 15
Met Asp Trp Thr Trp Ile Leu Phe Leu Val Ala Ala Ala Thr Arg Val
1 5 10 15
His Ser Gly Ile His Val Phe Ile Leu Gly Cys Phe Ser Ala Gly Leu
20 25 30
Pro Lys Thr Glu Ala Asn Trp Val Asn Val Ile Ser Asp Leu Lys Lys
35 40 45
Ile Glu Asp Leu Ile Gln Ser Met His Ile Asp Ala Thr Leu Tyr Thr
50 55 60
Glu Ser Asp Val His Pro Ser Cys Lys Val Thr Ala Met Lys Cys Phe
65 70 75 80
Leu Leu Glu Leu Gln Val Ile Ser Leu Glu Ser Gly Asp Ala Ser Ile
85 90 95
His Asp Thr Val Glu Asn Leu Ile Ile Leu Ala Asn Asn Ser Leu Ser
100 105 110
Ser Asn Gly Asn Val Thr Glu Ser Gly Cys Lys Glu Cys Glu Glu Leu
115 120 125
Glu Glu Lys Asn Ile Lys Glu Phe Leu Gln Ser Phe Val His Ile Val
130 135 140
Gln Met Phe Ile Asn Thr Ser Ser Gly Gly Gly Ser Gly Gly Gly Gly
145 150 155 160
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Ser Leu
165 170 175
Gln Ile Thr Cys Pro Pro Pro Met Ser Val Glu His Ala Asp Ile Trp
180 185 190
Val Lys Ser Tyr Ser Leu Tyr Ser Arg Glu Arg Tyr Ile Cys Asn Ser
195 200 205
Gly Phe Lys Arg Lys Ala Gly Thr Ser Ser Leu Thr Glu Cys Val Leu
210 215 220
Asn Lys Ala Thr Asn Val Ala His Trp Thr Thr Pro Ser Leu Lys Cys
225 230 235 240
Ile Arg
<210> 16
<211> 726
<212> DNA
<213> Artificial Sequence
<220>
<223> exemplary nucleic acid sequence encoding the amino acid sequence of
SEQ ID NO: 15
<400> 16
atggactgga cctggattct gttcctggtc gcggctgcaa cgcgagtcca tagcggtatc 60
catgttttta ttcttgggtg tttttctgct gggctgccta agaccgaggc caactgggta 120
aatgtcatca gtgacctcaa gaaaatagaa gaccttatac aaagcatgca cattgatgct 180
actctctaca ctgagtcaga tgtacatccc tcatgcaaag tgacggccat gaaatgtttc 240
ctcctcgaac ttcaagtcat atctctggaa agtggcgacg cgtccatcca cgacacggtc 300
gaaaacctga taatactcgc taataatagt ctctcttcaa atggtaacgt aaccgagtca 360
ggttgcaaag agtgcgaaga gttggaagaa aaaaacataa aggagttcct gcaaagtttc 420
gtgcacattg tgcagatgtt cattaatacc tctagcggcg gaggatcagg tggcggtgga 480
agcggaggtg gaggctccgg tggaggaggt agtggcggag gttctcttca aataacttgt 540
cctccaccga tgtccgtaga acatgcggat atttgggtaa aatcctatag cttgtacagc 600
cgagagcggt atatctgcaa cagcggcttc aagcggaagg ccggcacaag cagcctgacc 660
gagtgcgtgc tgaacaaggc caccaacgtg gcccactgga ccacccctag cctgaagtgc 720
atcaga 726
Claims (27)
- 세포 또는 이의 집단으로서,
(i) 상기 세포는 (a) 유도 만능 세포(induced pluripotent cell: iPSC), 클론성 iPSC, 또는 iPS 세포주 세포; 또는 (b) 상기 (a)의 세포의 분화로부터 획득된 유도체 세포(derivative cell)이고; 그리고
(ii) 상기 세포는,
(1) 고 친화도 비-절단성 CD16(high affinity non-cleavable CD16: hnCD16) 또는 이의 변이체; 및
(2) 키메라 항원 수용체(chimeric antigen receptor: CAR), 및 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드 중 하나 또는 둘 다
를 포함하는, 세포 또는 이의 집단. - 제1항에 있어서, 상기 (i)(b)의 유도체 세포는 조혈 세포이고, 말초 혈액, 제대혈 또는 임의의 다른 공여자 조직으로부터 획득된 네이티브 상대 세포에 비해서 더 긴 텔로미어(telomere)를 포함하는, 세포 또는 이의 집단.
- 제1항에 있어서, 상기 세포는,
(i) B2M 널(null) 또는 저(low);
(ii) CIITA 널 또는 저;
(iii) HLA-G 또는 비-절단성 HLA-G의 도입된 발현;
(iv) 표 1에 열거된 유전자형 중 적어도 하나;
(v) TAP1, TAP2, 타파신(Tapasin), NLRC5, PD1, LAG3, TIM3, RFXANK, CIITA, RFX5, RFXAP, 및 염색체 6p21 영역 내의 임의의 유전자 중 적어도 하나의 결실 또는 감소된 발현; 및
(vi) HLA-E, 41BBL, CD3, CD4, CD8, CD16, CD47, CD113, CD131, CD137, CD80, PDL1, A2AR, CAR, TCR, Fc 수용체, 관여자, 및 이중- 또는 다중-특이적 또는 보편적 관여자와의 커플링을 위한 표면 촉발 수용체 중 적어도 하나의 도입된 또는 증가된 발현
중 하나 이상을 더 포함하는, 세포 또는 이의 집단. - 제1항 또는 제3항에 있어서, 상기 세포는 유도체 NK 또는 유도체 T 세포이고, 그리고
말초 혈액, 제대혈 또는 임의의 다른 공여자 조직으로부터 획득된 네이티브 상대 NK 또는 T 세포와 비교할 때,
(i) 개선된 지속성 및/또는 생존;
(ii) 네이티브 면역 세포에 대한 증가된 내성;
(iii) 증가된 세포독성;
(iv) 개선된 종양 침투;
(v) 향상된 또는 획득된 ADCC;
(vi) 방관자 면역 세포(bystander immune cell)를 종양 부위로 이동시키고/시키거나 활성화 또는 모집하는 향상된 능력;
(vii) 종양 면역억제를 감소시키는 향상된 능력; 및
(viii) 종양 항원 탈출을 구제하는 개선된 능력
을 포함하는 특징 중 적어도 하나를 갖는, 세포 또는 이의 집단. - 제1항에 있어서, 상기 고 친화도 비-절단성 CD16(hnCD16) 또는 이의 변이체는,
(a) CD16의 엑토도메인 도메인 내의 F176V 및 S197P;
(b) CD64로부터 기원된 전체 또는 부분 엑토도메인;
(c) 비-네이티브(또는 비-CD16) 막관통 도메인;
(d) 비-네이티브(또는 비-CD16) 세포내 도메인;
(e) 비-네이티브(또는 비-CD16) 신호전달 도메인;
(f) 비-네이티브 자극성 도메인; 및
(g) CD16로부터 기원되지 않고, 동일하거나 상이한 폴리펩타이드로부터 기원된 막관통 도메인, 신호전달 도메인 및 자극성 도메인
중 적어도 하나를 포함하는, 세포 또는 이의 집단. - 제5항에 있어서,
(a) 상기 비-네이티브 막관통 도메인은 CD3D, CD3E, CD3G, CD3ζ, CD4, CD8, CD8a, CD8b, CD27, CD28, CD40, CD84, CD166, 4-1BB, OX40, ICOS, ICAM-1, CTLA-4, PD-1, LAG-3, 2B4, BTLA, CD16, IL7, IL12, IL15, KIR2DL4, KIR2DS1, NKp30, NKp44, NKp46, NKG2C, NKG2D 또는 T 세포 수용체(TCR) 폴리펩타이드로부터 유래되거나;
(b) 상기 비-네이티브 자극성 도메인은 CD27, CD28, 4-1BB, OX40, ICOS, PD-1, LAG-3, 2B4, BTLA, DAP10, DAP12, CTLA-4 또는 NKG2D 폴리펩타이드로부터 유래되거나;
(c) 상기 비-네이티브 신호전달 도메인은 CD3ζ, 2B4, DAP10, DAP12, DNAM1, CD137 (41BB), IL21, IL7, IL12, IL15, NKp30, NKp44, NKp46, NKG2C 또는 NKG2D 폴리펩타이드로부터 유래되거나;
(d) 상기 비-네이티브 막관통 도메인은 NKG2D로부터 유래되고, 상기 비-네이티브 자극성 도메인은 2B4로부터 유래되고, 상기 비-네이티브 신호전달 도메인은 CD3ζ로부터 유래되는, 세포 또는 이의 집단. - 제1항에 있어서, 상기 CAR은,
(i) T 세포 특이적 또는 NK 세포 특이적이고/이거나;
(ii) 이중특이적 항원 결합 CAR이고/이거나;
(iii) 전환 가능한 CAR이고/이거나;
(iv) 이량체화된 CAR이고/이거나;
(v) 스플리트 CAR이고/이거나;
(vi) 멀티-쇄 CAR이고/이거나;
(vii) 유도성 CAR이고/이거나;
(viii) 또 다른 CAR과 공동 발현되고/되거나;
(ix) 선택적으로 별개의 작제물로 또는 바이-시스트론성 작제물(bi-cistronic construct)로 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드와 공동 발현되고/되거나;
(xi) 선택적으로 별개의 작제물로 바이-시스트론성 작제물로 면역관문 저해제와 공동 발현되고/되거나;
(xii) CD19 또는 BCMA에 특이적이고/이거나;
(xiii) ADGRE2, 탄산 탈수효소 IX(CAlX), CCRI, CCR4, 암배아 항원(CEA), CD3, CD5, CD7, CD8, CD10, CD20, CD22, CD30, CD33, CD34, CD38, CD41, CD44, CD44V6, CD49f, CD56, CD70, CD74, CD99, CD123, CD133, CD138, CDS, CLEC12A, 사이토메갈로바이러스(CMV) 감염된 세포의 항원, 상피 당단백질2(EGP 2), 상피 당단백질-40(EGP-40), 상피 세포 접착 분자(EpCAM), EGFRvIII, 수용체 타이로신-단백질 카이나제 erb-B2,3,4, EGFIR, EGFR-VIII, ERBB 엽산염-결합 단백질(FBP), 태아 아세틸콜린 수용체(AChR), 엽산염 수용체-a, 강글리오사이드 G2(GD2), 강글리오사이드 G3(GD3), 인간 표피 성장 인자 수용체 2(HER-2), 인간 텔로머라제 역전사효소(human telomerase reverse transcriptase: hTERT), ICAM-1, 인테그린 B7, 인터류킨-13 수용체 소단위 알파-2(IL-13Rα2), κ-경쇄, 카이나제 삽입 도메인 수용체(KDR), Lewis A(CA19.9), Lewis Y(LeY), L1 세포 접착 분자(L1-CAM), LILRB2, 흑색종 항원 패밀리 A 1(MAGE-A1), MICA/B, 뮤신 1(Muc-1), 뮤신 16(Muc-16), 메소텔린(MSLN), NKCSI, NKG2D 리간드, c-Met, 암-고환 항원 NY-ESO-1, 종양태아성 항원(h5T4), PRAME, 전립선 줄기세포 항원(PSCA), PRAME 전립선-특이적 막 항원(PSMA), 종양-연관 당단백질 72(TAG-72), TIM-3, TRBCI, TRBC2, 혈관 내피 성장 인자 R2(VEGF-R2), 빌름스 종양 단백질(WT-1) 및 병원체 항원 중 임의의 하나에 특이적이되,
상기 (i) 내지 (xiii) 중 임의의 하나의 CAR은 선택적으로 TRAC 유전자좌에 선택적으로 삽입되고/되거나 TCR의 내인성 프로모터에 의해서 유도되고/되거나 상기 TCR은 상기 CAR 삽입에 의해서 넉 아웃되는, 세포 또는 이의 집단. - 제1항에 있어서, 상기 세포는 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드를 더 포함하되, 상기 외인성 사이토카인 또는 이의 수용체는,
(a) IL2, IL4, IL6, IL7, IL9, IL10, IL11, IL12, IL15, IL18, IL21 및 이의 각각의 수용체 중 적어도 하나를 포함하거나;
(b) (i) 자가 절단 펩타이드를 사용한 IL15 및 IL15Rα의 공동-발현;
(ii) IL15와 IL15Rα의 융합 단백질;
(iii) 절두된 IL15Rα의 세포내 도메인을 갖는 IL15/IL15Rα 융합 단백질;
(iv) IL15와 IL15Rα의 막 결합된 스시 도메인의 융합 단백질;
(v) IL15과 IL15Rβ의 융합 단백질;
(vi) IL15와 공통 수용체 γC의 융합 단백질(상기 공통 수용체 γC는 네이티브이거나 또는 변형됨); 및
(vii) IL15Rβ의 동종이량체
중 적어도 하나를 포함하되;
(i) 내지 (vii) 중 임의의 하나는 별개의 작제물 또는 바이-시스트론성 작제물로 CAR과 공동 발현될 수 있고;
선택적으로,
(c) 일시적으로 발현되는, 세포 또는 이의 집단. - 제3항에 있어서, 상기 세포는 유도체 NK 또는 유도체 T 세포이되,
(i) 상기 유도체 NK 세포는 T 세포를 종양 부위로 모집 및/또는 이동시킬 수 있고,
(ii) 상기 유도체 NK 또는 상기 유도체 T 세포는 1종 이상의 면역관문 저해제의 존재 하에서 종양 면역억제를 감소시킬 수 있는, 세포 또는 이의 집단. - 제7항 또는 제9항에 있어서, 상기 면역관문 저해제는 PD-1, PDL-1, TIM-3, TIGIT, LAG-3, CTLA-4, 2B4, 4-1BB, 4-1BBL, A2aR, BATE, BTLA, CD39, CD47, CD73, CD94, CD96, CD160, CD200, CD200R, CD274, CEACAM1, CSF-1R, Foxpl, GARP, HVEM, IDO, EDO, TDO, LAIR-1, MICA/B, NR4A2, MAFB, OCT-2, Rara(레티노산 수용체 알파), TLR3, VISTA, NKG2A/HLA-E 또는 저해성 KIR을 포함하는 1종 이상의 면역관문 분자에 대한 길항제인, 세포 또는 이의 집단.
- 제9항에 있어서, 상기 면역관문 저해제는,
(a) 아테졸리주맙(atezolizumab), 아벨루맙(avelumab), 더발루맙(durvalumab), 이필리무맙(ipilimumab), IPH4102, IPH43, IPH33, 리릴루맙(lirimumab), 모날리주맙(monalizumab), 니볼루맙(nivolumab), 펨브롤리주맙(pembrolizumab) 및 이들의 유도체 또는 기능성 등가물 중 1종 이상; 또는
(b) 아테졸리주맙, 니볼루맙 및 펨브롤리주맙 중 적어도 1종
을 포함하는, 세포 또는 이의 집단. - 제2항에 있어서, 상기 유도체 세포는 유도체 CD34 세포, 유도체 조혈 줄기 및 전구 세포, 유도체 조혈 다능성 전구 세포(derivative hematopoietic multipotent progenitor cell), 유도체 T 세포 전구 세포, 유도체 NK 세포 전구 세포, 유도체 T 세포, 유도체 NKT 세포, 유도체 NK 세포 또는 유도체 B 세포를 포함하는, 세포 또는 이의 집단.
- 제1항에 있어서, 상기 세포는,
(i) 하나의 안전 하버 유전자좌(safe harbor locus)에 통합된 하나 이상의 외인성 폴리뉴클레오타이드; 또는
(ii) 상이한 안전 하버 유전자좌에 통합된 2개 초과의 외인성 폴리뉴클레오타이드
를 포함하는, 세포 또는 이의 집단. - 제13항에 있어서, 상기 안전 하버 유전자좌는 AAVS1, CCR5, ROSA26, 콜라겐, HTRP, H11, 베타-2 마이크로글로불린, GAPDH, TCR 또는 RUNX1 중 적어도 하나를 포함하는, 세포 또는 이의 집단.
- 제15항에 있어서, 상기 안전 하버 유전자좌 TCR은 TCR 알파의 불변 영역인, 세포 또는 이의 집단.
- 제1항 내지 제15항 중 어느 한 항의 세포 또는 이의 집단을 포함하는, 조성물.
- 제1항 내지 제15항 중 어느 한 항의 유도체 세포 및 1종 이상의 치료제를 포함하는, 치료 용도를 위한 조성물.
- 제17항에 있어서, 상기 치료제는 펩타이드, 사이토카인, 면역관문 저해제, 미토겐, 성장 인자, 작은 RNA, dsRNA(이중 가닥 RNA), 단핵 혈액 세포(mononuclear blood cell), 피더 세포(feeder cell), 피더 세포 성분 또는 이의 대체 인자, 관심대상의 하나 이상의 폴리핵산을 포함하는 벡터, 항체, 화학치료제 또는 방사성 모이어티 또는 면역조절 약물(immunomodulatory drug: IMiD)을 포함하는, 조성물.
- 제18항에 있어서, 상기 면역관문 저해제는,
(a) PD-1, PDL-1, TIM-3, TIGIT, LAG-3, CTLA-4, 2B4, 4-1BB, 4-1BBL, A2aR, BATE, BTLA, CD39, CD47, CD73, CD94, CD96, CD160, CD200, CD200R, CD274, CEACAM1, CSF-1R, Foxpl, GARP, HVEM, IDO, EDO, TDO, LAIR-1, MICA/B, NR4A2, MAFB, OCT-2, Rara(레티노산 수용체 알파), TLR3, VISTA, NKG2A/HLA-E 또는 저해성 KIR을 포함하는 1종 이상의 길항제 면역관문 분자;
(b) 아테졸리주맙, 아벨루맙, 더발루맙, 이필리무맙, IPH4102, IPH43, IPH33, 리릴루맙, 모날리주맙, 니볼루맙, 펨브롤리주맙 및 이들의 유도체 또는 기능성 등가물 중 1종 이상;
(c) 아테졸리주맙, 니볼루맙 및 펨브롤리주맙 중 적어도 1종
을 포함하는, 조성물. - 제18항에 있어서, 상기 항체는,
(a) 항-CD20, 항-HER2, 항-CD52, 항-EGFR, 항-CD123, 항-GD2, 항-PDL1 및/또는 항-CD38 항체;
(b) 레툭시맙, 벨투주맙, 오파투무맙, 유블리툭시맙, 오카라투주맙, 오비누투주맙, 트라스투주맙, 퍼투주맙, 알렘투주맙, 서툭시맙, 디누툭시맙, 아벨루맙, 다라투무맙, 이사툭시맙, MOR202, 7G3, CSL362, 엘로투주맙 및 이들의 인간화된 또는 Fc 변형된 변이체 또는 단편 및 이들의 기능성 등가물 및 바이오시밀러(biosimilar) 중 1종 이상; 또는
(c) 다라투무맙
을 포함하는, 조성물. - 제16항 내지 제20항 중 어느 한 항의 치료 조성물의 치료 용도로서, 입양 세포 요법에 적합한 대상체에게 조성물을 도입하되, 상기 대상체는 자가면역 장애; 혈액 악성종양; 고형 종양; 암 또는 바이러스 감염을 가지는, 치료 용도.
- 제1항 내지 제15항 중 어느 한 항의 유도체 세포의 제조 방법으로서, iPSC를 분화시키는 단계를 포함하되, 상기 iPSC는,
(i) 고 친화도 비-절단성 CD16(hnCD16) 또는 이의 변이체; 및
(ii) 키메라 항원 수용체(CAR), 및 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드 중 하나 또는 둘 다; 및 선택적으로
(1) B2M 널 또는 저;
(2) CIITA 널 또는 저;
(3) HLA-G 또는 비-절단성 HLA-G의 도입된 발현;
(4) 표 1에 열거된 유전자형 중 적어도 하나;
(5) TAP1, TAP2, 타파신, NLRC5, PD1, LAG3, TIM3, RFXANK, CIITA, RFX5, RFXAP, 및 염색체 6p21 영역 내의 임의의 유전자 중 적어도 하나의 결실 또는 감소된 발현; 및
(6) HLA-E, 41BBL, CD3, CD4, CD8, CD16, CD47, CD113, CD131, CD137, CD80, PDL1, A2AR, CAR, TCR, Fc 수용체, 관여자, 및 이중- 또는 다중-특이적 또는 보편적 관여자와의 커플링을 위한 표면 촉발 수용체 중 적어도 하나의 도입된 또는 증가된 발현 중 하나 이상
을 포함하는, 유도체 세포의 제조 방법. - 제22항에 있어서,
(i) 고 친화도 비-절단성 CD16(hnCD16) 또는 이의 변이체; 및
(ii) 키메라 항원 수용체(CAR), 및 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드 중 하나 또는 둘 다
의 발현을 도입하도록; 그리고 선택적으로
(1) B2M 널을 넉 아웃시키거나;
(2) CIITA를 넉 아웃시키거나;
(3) HLA-G 또는 비-절단성 HLA-G의 발현을 도입하도록
클론성 iPSC를 게놈 조작하는 단계를 더 포함하되;
상기 CAR 및 상기 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드는 별개의 작제물로 또는 바이-시스트론성 작제물로 공동 발현되는, 유도체 세포의 제조 방법. - 제22항에 있어서, 상기 게놈 조작은 표적화 편집(targeted editing)을 포함하는, 유도체 세포의 제조 방법.
- 제24항에 있어서, 상기 표적화 편집은 결실, 삽입 또는 in/del을 포함하되, 상기 표적화 편집은 CRISPR, ZFN, TALEN, 귀소 뉴클레아제(homing nuclease), 상동 재조합(homology recombination) 또는 이들 방법의 임의의 다른 기능성 변경에 의해서 수행되는, 유도체 세포의 제조 방법.
- 클론성 iPSC의 CRISPR 매개된 편집으로서, 상기 편집된 클론성 iPSC는,
(a) (i) 고 친화도 비-절단성 CD16(hnCD16) 또는 이의 변이체; 및
(ii) 키메라 항원 수용체(CAR) 및 선택적으로 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드; 또는
(b) 표 1에 열거된 유전자형 중 적어도 하나
를 포함하되;
상기 CAR은 선택적으로 TRAC 유전자좌에 선택적으로 삽입되고/되거나 TCR의 내인성 프로모터에 의해서 유도되고/되거나 상기 TCR은 상기 CAR 삽입에 의해서 넉 아웃되는, 클론성 iPSC의 CRISPR 매개된 편집. - 종양 항원 탈출 및/또는 종양 재발을 예방 또는 감소시키는 방법으로서, 대상체에게 치료 하에서
(a) (i) 고 친화도 비-절단성 CD16(hnCD16) 또는 이의 변이체; 및
(ii) 키메라 항원 수용체(CAR) 및 선택적으로 세포 표면 발현된 외인성 사이토카인 또는 이의 수용체의 부분 또는 전체 펩타이드; 또는
(b) 표 1에 열거된 유전자형 중 적어도 하나
를 포함하는 효과기 세포; 및
항원 특이적 단클론성 항체, 또는 이의 인간화된 또는 Fc 변형된 변이체 또는 단편, 기능성 등가물 및 바이오시밀러 중 임의의 것을 투여하는 단계를 포함하되, 상기 항체에 의해서 표적화되는 상기 항원은 상기 CAR에 의해서 인식되는 종양 항원과 상이한, 종양 항원 탈출 및/또는 종양 재발을 예방 또는 감소시키는 방법.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762596659P | 2017-12-08 | 2017-12-08 | |
| US62/596,659 | 2017-12-08 | ||
| US201862657626P | 2018-04-13 | 2018-04-13 | |
| US62/657,626 | 2018-04-13 | ||
| PCT/US2018/063362 WO2019112899A2 (en) | 2017-12-08 | 2018-11-30 | IMMUNOTHERAPIES USING ENHANCED iPSC DERIVED EFFECTOR CELLS |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200097749A true KR20200097749A (ko) | 2020-08-19 |
Family
ID=66749947
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207019364A KR20200097749A (ko) | 2017-12-08 | 2018-11-30 | 향상된 iPSC 유래된 효과기 세포를 사용하는 면역요법 |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US20210015859A1 (ko) |
| EP (1) | EP3720946A4 (ko) |
| JP (2) | JP2021505131A (ko) |
| KR (1) | KR20200097749A (ko) |
| CN (1) | CN111556892A (ko) |
| AU (1) | AU2018381191A1 (ko) |
| BR (1) | BR112020010597A2 (ko) |
| CA (1) | CA3083109A1 (ko) |
| IL (1) | IL275180A (ko) |
| MX (1) | MX2020005477A (ko) |
| SG (1) | SG11202004833SA (ko) |
| WO (1) | WO2019112899A2 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023182861A1 (ko) * | 2022-03-25 | 2023-09-28 | 에이치케이이노엔 주식회사 | 항-hla-g 키메라 항원 수용체 및 이의 용도 |
Families Citing this family (54)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL309585A (en) | 2017-12-22 | 2024-02-01 | Fate Therapeutics Inc | Enhanced effector training cells and their use |
| CA3128888A1 (en) * | 2019-02-15 | 2020-08-20 | Editas Medicine, Inc. | Modified natural killer (nk) cells for immunotherapy |
| EP3953453A4 (en) * | 2019-04-11 | 2022-12-28 | Fate Therapeutics, Inc. | CD3 RECONSTITUTION IN MANIPULATED IPSC AND IMMUNE EFFECTOR CELLS |
| MX2022000553A (es) * | 2019-07-17 | 2022-04-25 | Fate Therapeutics Inc | Modificación de células efectoras inmunitarias y uso de las mismas. |
| JP2022541016A (ja) * | 2019-07-17 | 2022-09-21 | ナショナル ユニヴァーシティー オブ シンガポール | 免疫細胞によって合成され、分泌される機能的バインダー |
| KR20220085779A (ko) * | 2019-09-25 | 2022-06-22 | 페이트 세러퓨틱스, 인코포레이티드 | 다중-표적화 효과기 세포 및 이의 용도 |
| BR112022006440A2 (pt) * | 2019-10-07 | 2022-07-05 | Fate Therapeutics Inc | Receptor de antígeno quimérico intensificado para manipulação de célula efetora imune e uso do mesmo |
| US20240131156A1 (en) * | 2019-10-17 | 2024-04-25 | Fate Therapeutics, Inc. | Enhanced chimeric antigen receptor for immune effector cell engineering and use thereof |
| EP4069827A4 (en) * | 2019-12-06 | 2024-05-29 | Fate Therapeutics Inc | ENHANCEMENT OF AN IPSC-DERIVED IMMUNE EFFECTOR CELL USING SMALL COMPOUNDS |
| CN111269326A (zh) * | 2020-02-28 | 2020-06-12 | 南京北恒生物科技有限公司 | 新型嵌合抗原受体及其用途 |
| WO2021258016A1 (en) * | 2020-06-19 | 2021-12-23 | Fate Therapeutics, Inc. | Combining ipsc-derived effector cell types for immunotherapy use |
| CN113528452B (zh) * | 2020-07-06 | 2023-06-06 | 上海鑫湾生物科技有限公司 | 共表达IL-21和hrCD16嵌合受体的免疫细胞及其应用 |
| EP4185616A1 (en) * | 2020-07-24 | 2023-05-31 | Cellectis S.A. | T-cells expressing immune cell engagers in allogenic settings |
| CN114276996A (zh) * | 2020-09-28 | 2022-04-05 | 未来智人再生医学研究院(广州)有限公司 | 一种表达pd-1/pd-l1阻断物的多能干细胞衍生物及应用 |
| EP4237004A1 (en) * | 2020-10-28 | 2023-09-06 | SRI International | Genetically engineered antigen-specific natural killer cells for in situ synthesis of proteins |
| CN114426953A (zh) * | 2020-10-29 | 2022-05-03 | 未来智人再生医学研究院(广州)有限公司 | 一种表达il-12的多能干细胞衍生物及应用 |
| CN114457022A (zh) * | 2020-10-30 | 2022-05-10 | 未来智人再生医学研究院(广州)有限公司 | 一种表达ox40激活型抗体的多能干细胞及其衍生物与应用 |
| CN114457028A (zh) * | 2020-10-30 | 2022-05-10 | 未来智人再生医学研究院(广州)有限公司 | 一种表达cd38抗体的多能干细胞及其衍生物与应用 |
| CN114457031A (zh) * | 2020-10-30 | 2022-05-10 | 未来智人再生医学研究院(广州)有限公司 | 一种表达b7-h5阻断物的多能干细胞或其衍生物及应用 |
| CN114457025A (zh) * | 2020-10-30 | 2022-05-10 | 未来智人再生医学研究院(广州)有限公司 | 一种表达btla阻断物的多能干细胞或其衍生物及应用 |
| CN114525258A (zh) * | 2020-10-30 | 2022-05-24 | 未来智人再生医学研究院(广州)有限公司 | 一种表达pcsk9阻断物的多能干细胞或其衍生物及应用 |
| CN114525259A (zh) * | 2020-11-03 | 2022-05-24 | 南京北恒生物科技有限公司 | 靶向cd7的嵌合抗原受体及其用途 |
| TW202233831A (zh) * | 2020-11-03 | 2022-09-01 | 中國大陸商杭州啟函生物科技有限公司 | 增強免疫療法的系統和方法 |
| US20230390337A1 (en) * | 2020-11-04 | 2023-12-07 | Fate Therapeutics, Inc. | Engineered ipsc and persistent immune effector cells |
| IL302476A (en) * | 2020-11-04 | 2023-06-01 | Fate Therapeutics Inc | Induced pluripotent stem cells and immune effector cells for heterogeneous tumor control |
| EP4251741A1 (en) * | 2020-11-30 | 2023-10-04 | CRISPR Therapeutics AG | Gene-edited natural killer cells |
| US11661459B2 (en) | 2020-12-03 | 2023-05-30 | Century Therapeutics, Inc. | Artificial cell death polypeptide for chimeric antigen receptor and uses thereof |
| EP4263600A1 (en) | 2020-12-18 | 2023-10-25 | Century Therapeutics, Inc. | Chimeric antigen receptor systems with adaptable receptor specificity |
| CN114645018A (zh) * | 2020-12-18 | 2022-06-21 | 未来智人再生医学研究院(广州)有限公司 | 一种表达cd38靶向抑制因子的多能干细胞及其衍生物与应用 |
| CN114645020A (zh) * | 2020-12-21 | 2022-06-21 | 未来智人再生医学研究院(广州)有限公司 | 一种表达靶向nr4a1抑制因子的多能干细胞及其衍生物与应用 |
| CN114657135A (zh) * | 2020-12-22 | 2022-06-24 | 未来智人再生医学研究院(广州)有限公司 | 一种表达Tim-3靶向抑制因子的多能干细胞及其衍生物与应用 |
| WO2022137181A1 (en) * | 2020-12-23 | 2022-06-30 | Crispr Therapeutics Ag | Co-use of lenalidomide with car-t cells |
| US11473060B2 (en) | 2020-12-30 | 2022-10-18 | Crispr Therapeutics Ag | Compositions and methods for differentiating stem cells into NK cells |
| AU2021414617A1 (en) | 2020-12-31 | 2023-08-10 | Crispr Therapeutics Ag | Universal donor cells |
| KR20230142470A (ko) * | 2021-01-29 | 2023-10-11 | 알로젠 테라퓨틱스 인코포레이티드 | 동종이계 세포 산물의 T 세포 인식을 완화하기 위한TAP2, NLRC5, β2m, TRAC, RFX5, RFXAP, 및 RFXANK 중 하나 이상의 녹다운 또는 녹아웃 |
| KR20230170703A (ko) * | 2021-04-07 | 2023-12-19 | 센츄리 쎄라퓨틱스 인코포레이티드 | 유도 만능 줄기세포로부터 감마-델타 t 세포의 생성을 위한 조성물 및 방법 |
| WO2022251367A1 (en) * | 2021-05-27 | 2022-12-01 | Sana Biotechnology, Inc. | Hypoimmunogenic cells comprising engineered hla-e or hla-g |
| US20230014010A1 (en) * | 2021-06-23 | 2023-01-19 | Crispr Therapeutics Ag | Engineered cells with improved protection from natural killer cell killing |
| WO2023019185A1 (en) * | 2021-08-10 | 2023-02-16 | Gentibio, Inc. | Compositions and methods for engineering stable tregs |
| CN114107378A (zh) * | 2021-09-13 | 2022-03-01 | 钦元再生医学(珠海)有限公司 | 一种通用型car-t细胞的制备方法 |
| AU2022382406A1 (en) * | 2021-11-08 | 2024-05-23 | Fate Therapeutics, Inc. | Engineered effector cells for trafficking of allogeneic cell therapies in solid tumors |
| CN116103239A (zh) * | 2021-11-11 | 2023-05-12 | 南京北恒生物科技有限公司 | 工程化免疫细胞及其用途 |
| CN114414541A (zh) * | 2021-12-17 | 2022-04-29 | 上海药明生物医药有限公司 | 一种应用3d细胞成像分析系统检测t细胞杀伤效力的方法 |
| WO2023116929A1 (en) * | 2021-12-24 | 2023-06-29 | Hemacell Therapeutics Inc. | Method for producing human induced pluripotent stem cells through homologous recombination and integrase-mediated recombination |
| CN114317607A (zh) * | 2021-12-31 | 2022-04-12 | 西安桑尼赛尔生物医药有限公司 | 融合一代靶向cd7 car和二代靶向bcma的双靶点通用car-t细胞及制备方法 |
| JP2024515920A (ja) * | 2022-04-08 | 2024-04-11 | フェイト セラピューティクス,インコーポレイティド | 固形腫瘍標的化骨格を有する細胞及びその使用 |
| CN114478806B (zh) * | 2022-04-14 | 2022-07-01 | 呈诺再生医学科技(北京)有限公司 | 一种提升免疫细胞杀伤活性的嵌合受体及其应用 |
| WO2023240248A2 (en) | 2022-06-09 | 2023-12-14 | Umoja Biopharma, Inc. | Compositions and methods for nk cell differentiation |
| EP4299734A1 (en) * | 2022-07-01 | 2024-01-03 | ETH Zurich | Cell line for discovering tcr antigens and uses thereof |
| WO2024026391A1 (en) | 2022-07-27 | 2024-02-01 | Umoja Biopharma, Inc. | Differentiation of stem cells in suspension culture |
| CN116042527B (zh) * | 2022-09-07 | 2023-08-22 | 广州瑞臻再生医学科技有限公司 | 一种促进NK细胞分化的iPS细胞系及其构建方法与应用 |
| WO2024102954A1 (en) | 2022-11-10 | 2024-05-16 | Massachusetts Institute Of Technology | Activation induced clipping system (aics) |
| CN116445414A (zh) * | 2023-03-03 | 2023-07-18 | 广州瑞臻再生医学科技有限公司 | 基因修饰多潜能干细胞衍生的增强型nk细胞的方法及其应用 |
| CN116410336B (zh) * | 2023-06-02 | 2023-09-22 | 云南赛元生物技术有限公司 | 一种嵌合抗原受体的编码核苷酸、car-nk细胞及其构建方法和应用 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2537933A1 (en) * | 2011-06-24 | 2012-12-26 | Institut National de la Santé et de la Recherche Médicale (INSERM) | An IL-15 and IL-15Ralpha sushi domain based immunocytokines |
| CA3185368A1 (en) * | 2013-04-03 | 2014-10-09 | Memorial Sloan-Kettering Cancer Center | Effective generation of tumor-targeted t cells derived from pluripotent stem cells |
| EP3307282A4 (en) * | 2015-06-12 | 2019-05-01 | Immunomedics, Inc. | TREATMENT OF DISEASES WITH CHIMERIC ANTIGEN RECEPTOR (CAR) AND T-CELL (T-CAR) OR NK (CAR-NK) CELL EXPRESSION CONSTRUCTIONS CAR CONSTRUCTIONS |
| CA2999294A1 (en) * | 2015-09-25 | 2017-03-30 | Altor Bioscience Corporation | Interleukin-15 superagonist significantly enhances graft-versus-tumor activity |
| WO2017079673A1 (en) * | 2015-11-04 | 2017-05-11 | Fate Therapeutics, Inc. | Genomic engineering of pluripotent cells |
| US11413309B2 (en) * | 2016-01-20 | 2022-08-16 | Fate Therapeutics, Inc. | Compositions and methods for immune cell modulation in adoptive immunotherapies |
-
2018
- 2018-11-30 SG SG11202004833SA patent/SG11202004833SA/en unknown
- 2018-11-30 MX MX2020005477A patent/MX2020005477A/es unknown
- 2018-11-30 BR BR112020010597-0A patent/BR112020010597A2/pt unknown
- 2018-11-30 KR KR1020207019364A patent/KR20200097749A/ko unknown
- 2018-11-30 JP JP2020529376A patent/JP2021505131A/ja active Pending
- 2018-11-30 WO PCT/US2018/063362 patent/WO2019112899A2/en unknown
- 2018-11-30 CN CN201880085614.0A patent/CN111556892A/zh active Pending
- 2018-11-30 US US16/765,369 patent/US20210015859A1/en active Pending
- 2018-11-30 CA CA3083109A patent/CA3083109A1/en active Pending
- 2018-11-30 AU AU2018381191A patent/AU2018381191A1/en active Pending
- 2018-11-30 EP EP18886079.5A patent/EP3720946A4/en active Pending
-
2020
- 2020-06-07 IL IL275180A patent/IL275180A/en unknown
-
2023
- 2023-11-13 JP JP2023192955A patent/JP2024020364A/ja active Pending
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023182861A1 (ko) * | 2022-03-25 | 2023-09-28 | 에이치케이이노엔 주식회사 | 항-hla-g 키메라 항원 수용체 및 이의 용도 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3720946A2 (en) | 2020-10-14 |
| CN111556892A (zh) | 2020-08-18 |
| WO2019112899A3 (en) | 2019-07-18 |
| SG11202004833SA (en) | 2020-06-29 |
| AU2018381191A1 (en) | 2020-06-04 |
| EP3720946A4 (en) | 2021-08-18 |
| JP2024020364A (ja) | 2024-02-14 |
| CA3083109A1 (en) | 2019-06-13 |
| US20210015859A1 (en) | 2021-01-21 |
| WO2019112899A2 (en) | 2019-06-13 |
| JP2021505131A (ja) | 2021-02-18 |
| WO2019112899A8 (en) | 2019-08-22 |
| IL275180A (en) | 2020-07-30 |
| MX2020005477A (es) | 2020-11-06 |
| BR112020010597A2 (pt) | 2020-10-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7467339B2 (ja) | 強化された免疫エフェクター細胞およびその使用 | |
| KR20200097749A (ko) | 향상된 iPSC 유래된 효과기 세포를 사용하는 면역요법 | |
| US20210163622A1 (en) | Immune effector cell engineering and use thereof | |
| US20220378831A1 (en) | Multi-targeting effector cells and use thereof | |
| KR20200127250A (ko) | 조작된 면역 효과기 세포 및 이의 용도 | |
| KR20210099601A (ko) | 향상된 iPSC 유래 효과기 세포를 사용한 면역요법 | |
| KR20210139472A (ko) | 조작된 iPSC 및 면역 효과기 세포에서의 CD3 재구성 | |
| KR20230040337A (ko) | 면역요법 사용을 위한 iPSC-유래 이펙터 세포 유형들의 조합 | |
| US20230381235A1 (en) | Multiplexed engineered ipscs and immune effector cells targeting solid tumors | |
| US20230390337A1 (en) | Engineered ipsc and persistent immune effector cells | |
| KR20230084533A (ko) | 조작된 iPSC 및 보강된 면역 효과기 세포 | |
| US20230405121A1 (en) | Engineered ipsc and immune effector cells for heterogenous tumor control | |
| KR20240031361A (ko) | 동종이계 입양 세포 치료를 위한 보호된 이펙터 세포 및 이의 용도 |