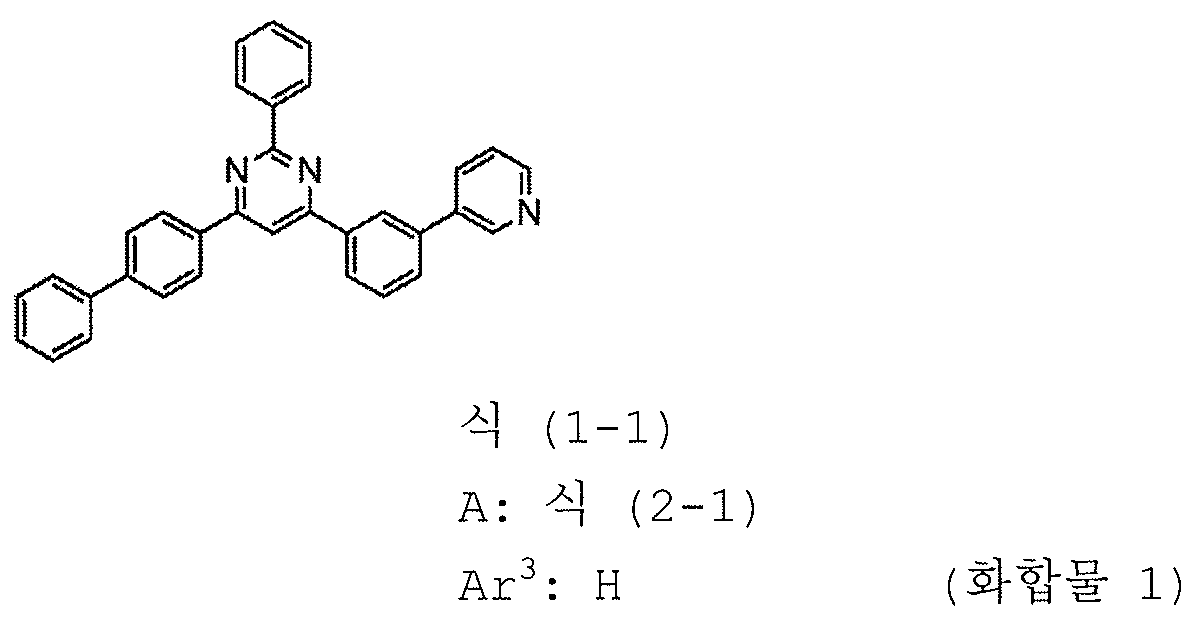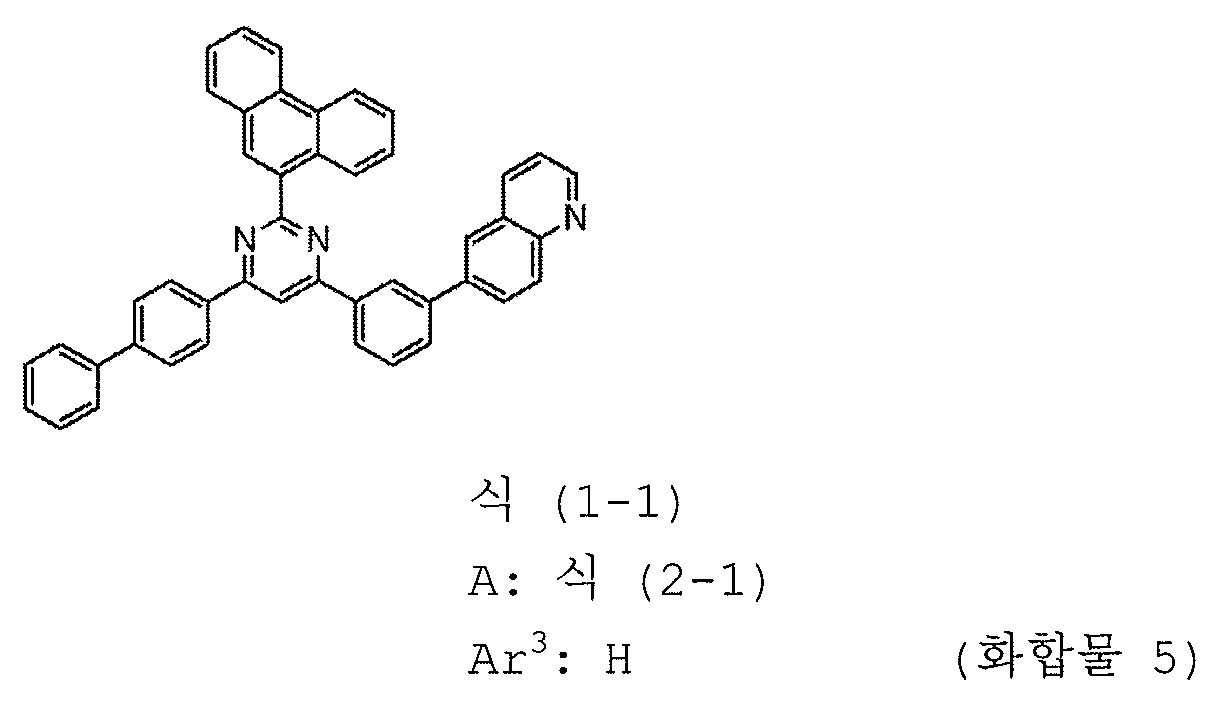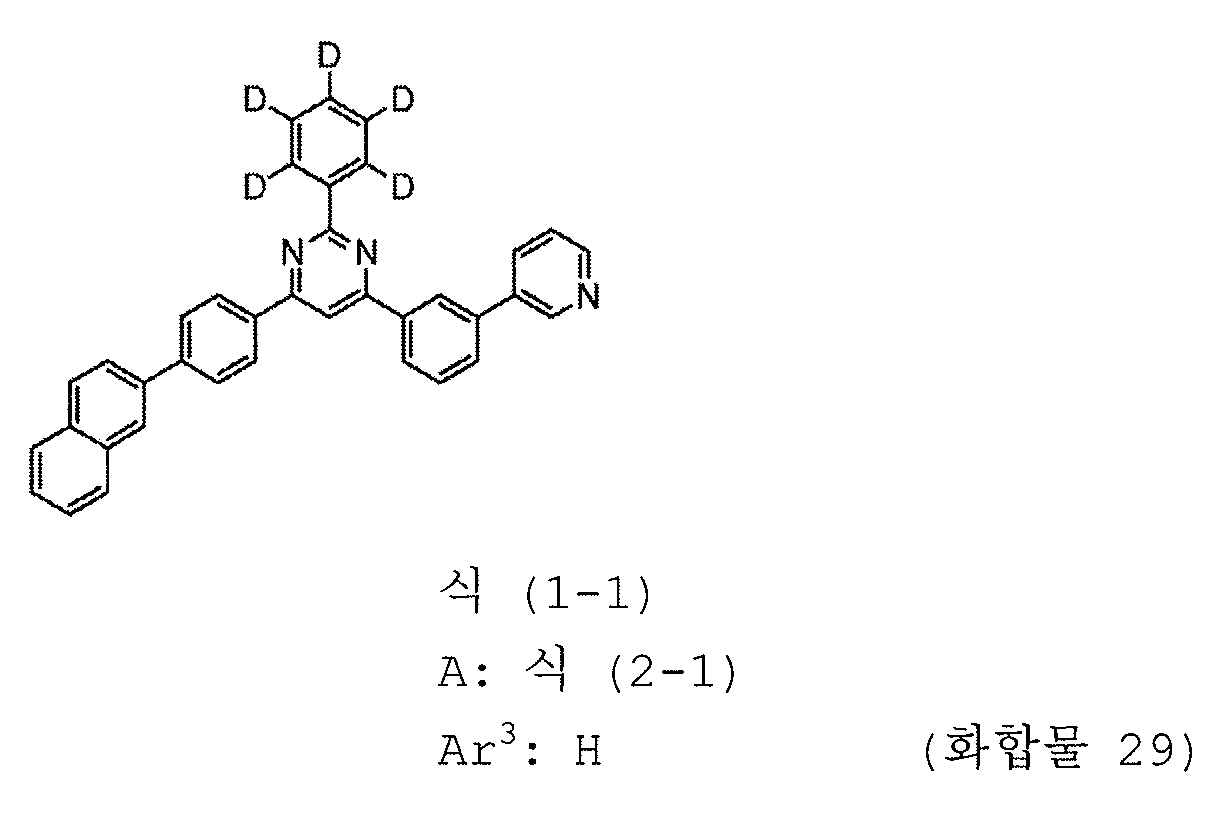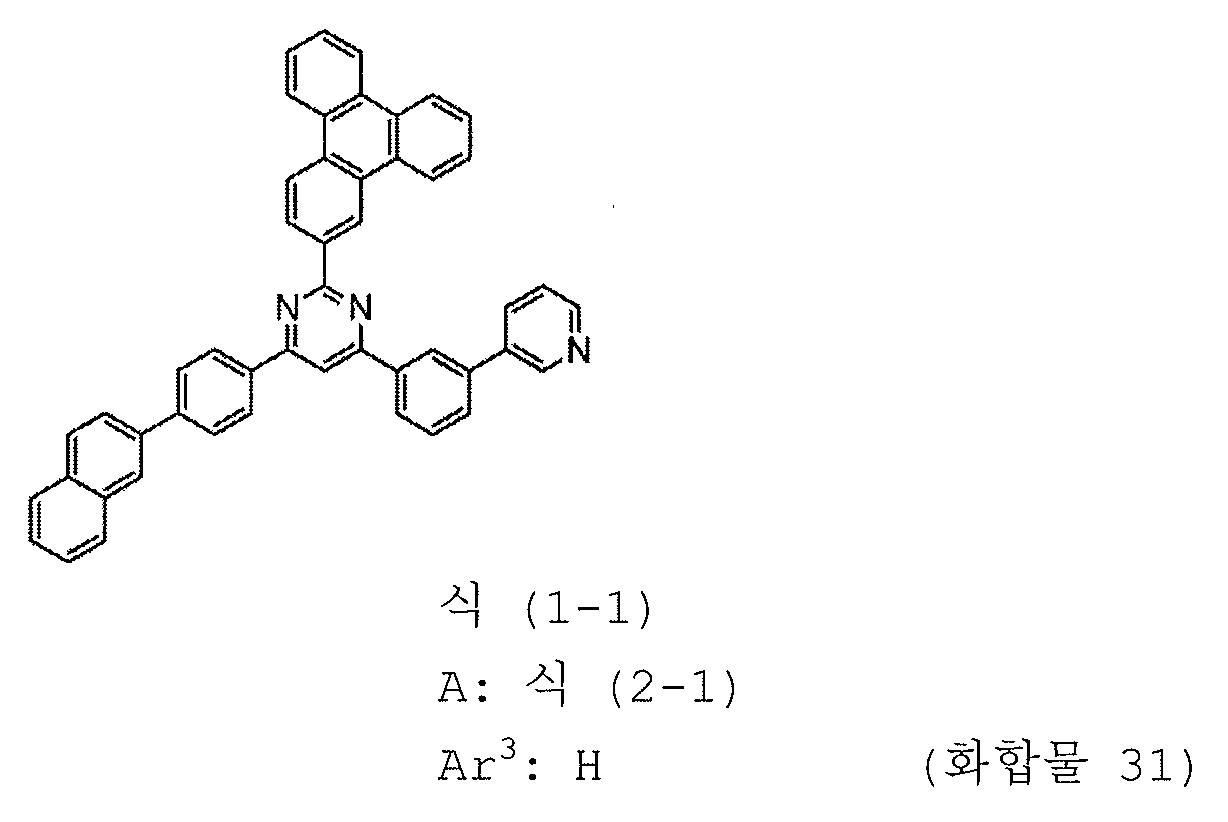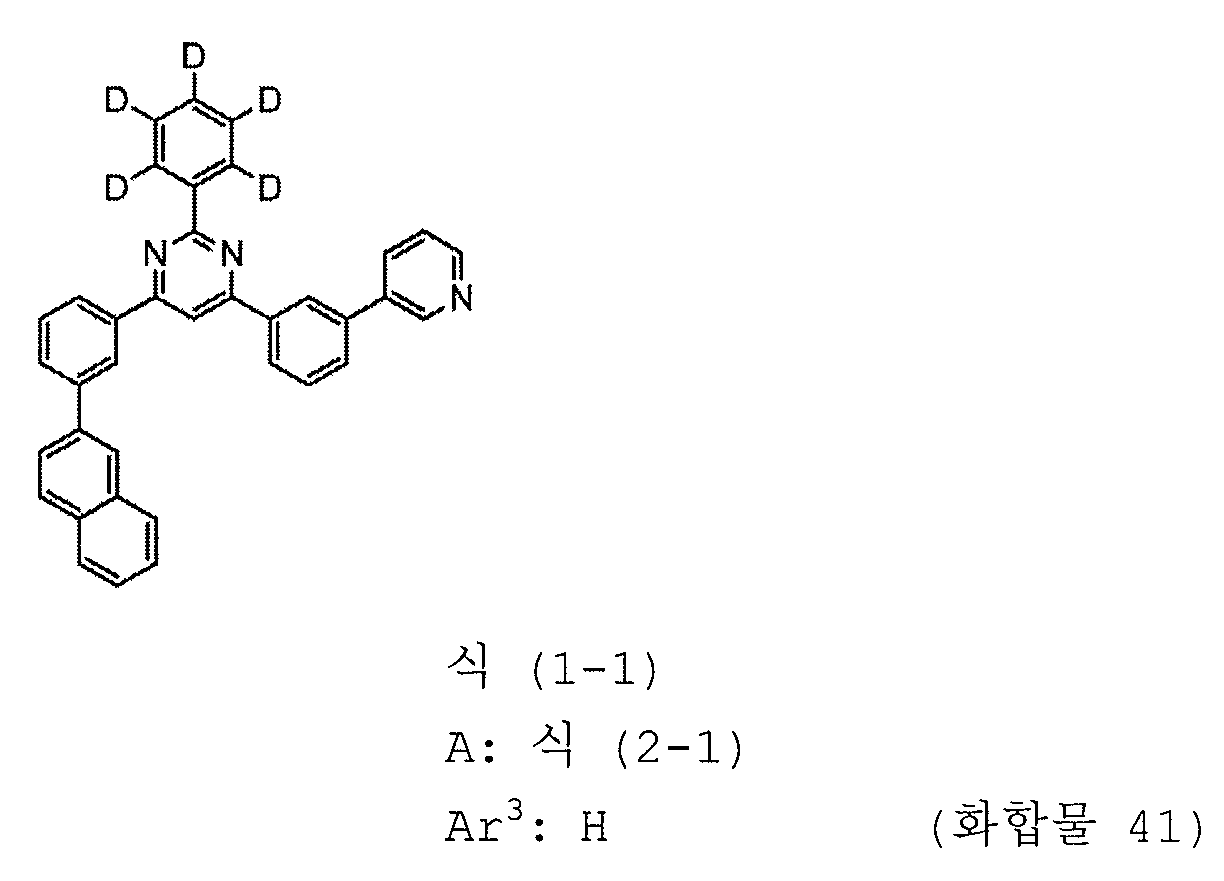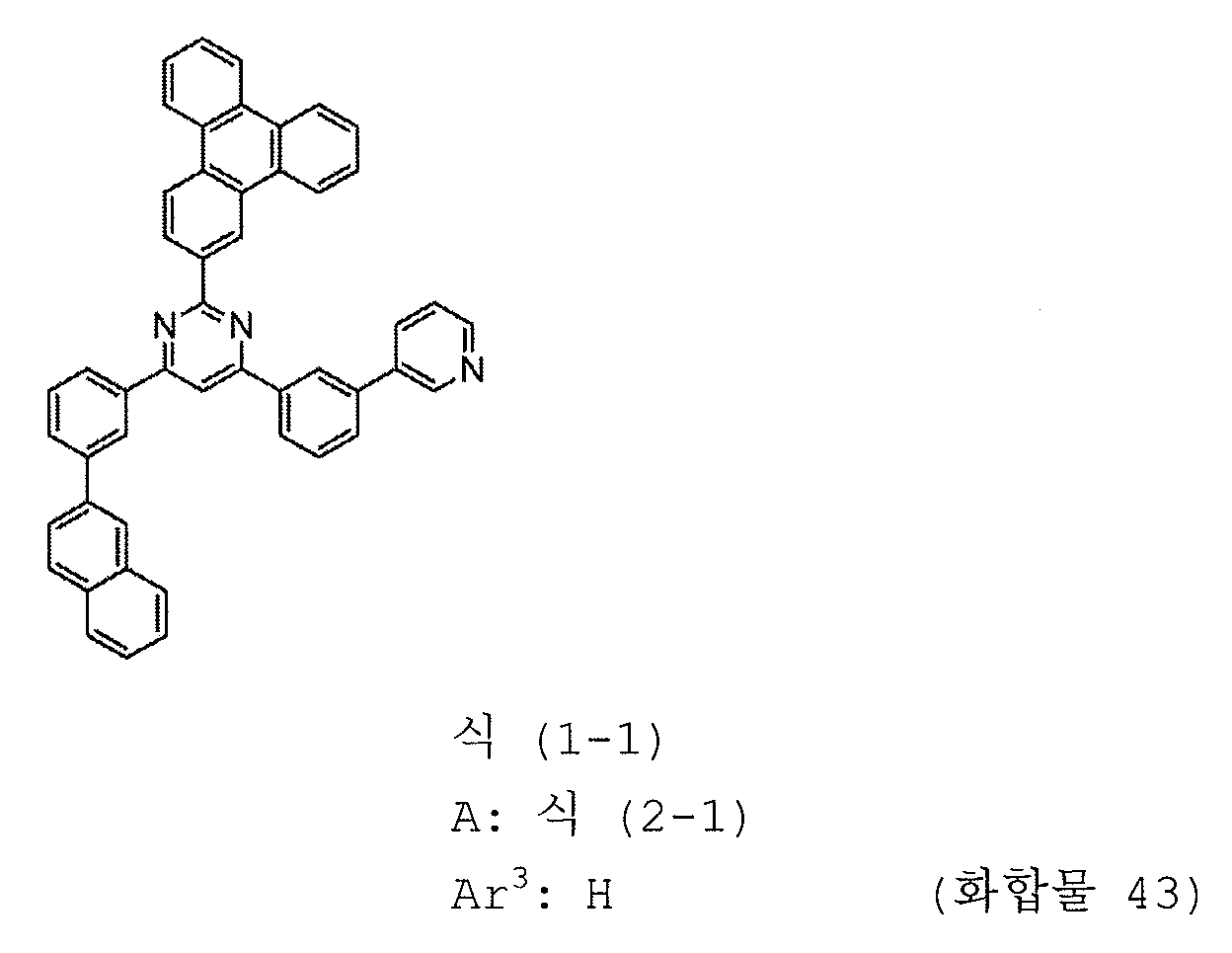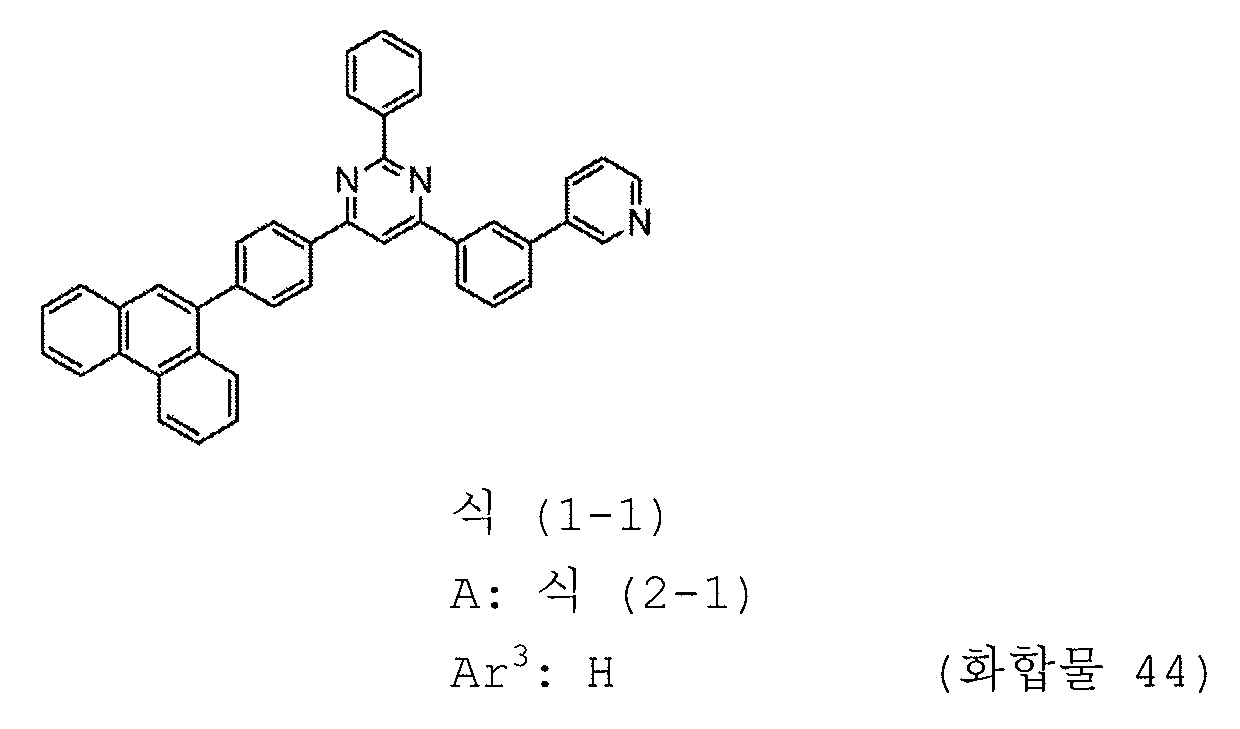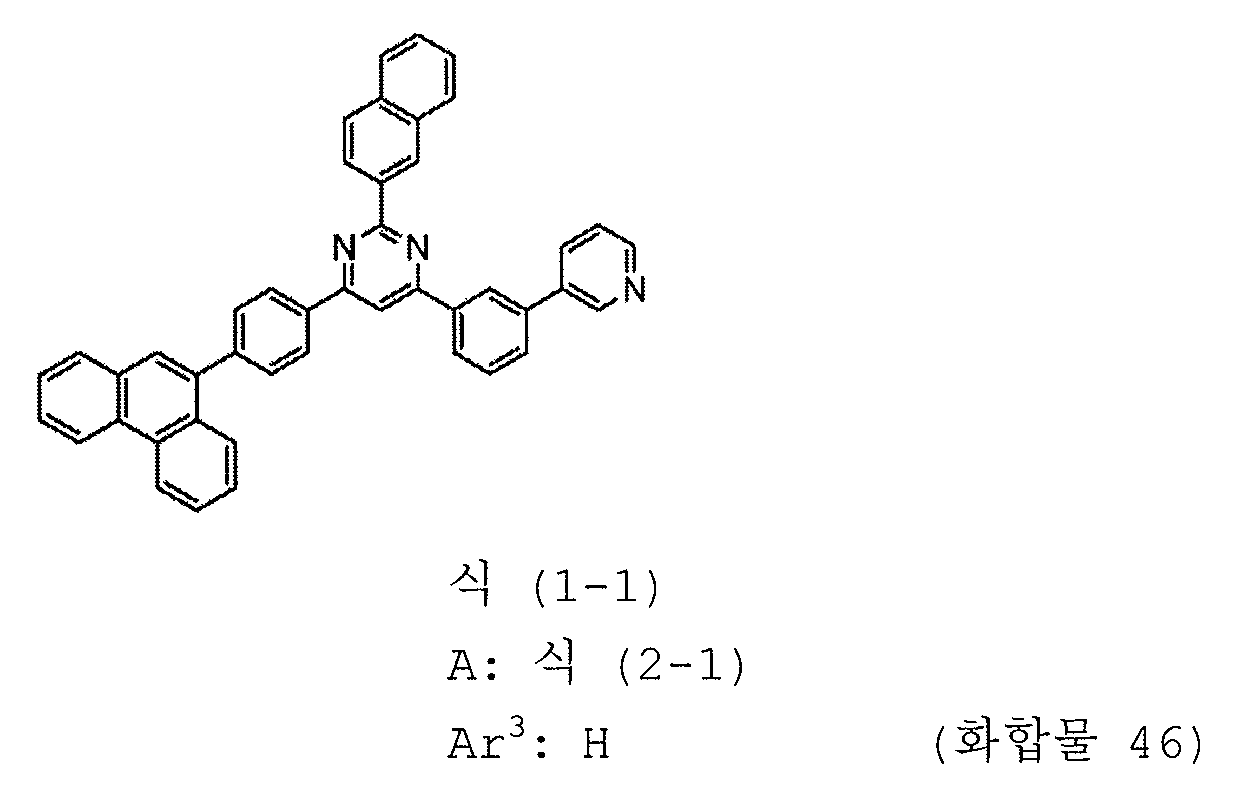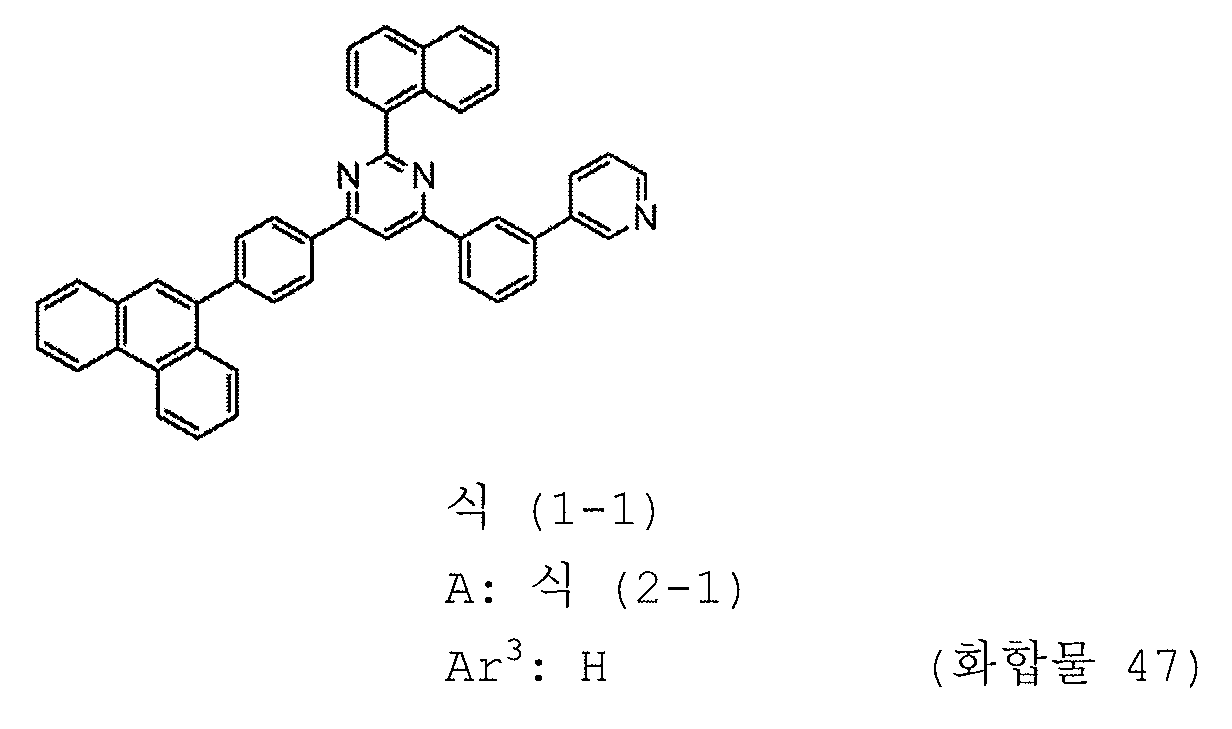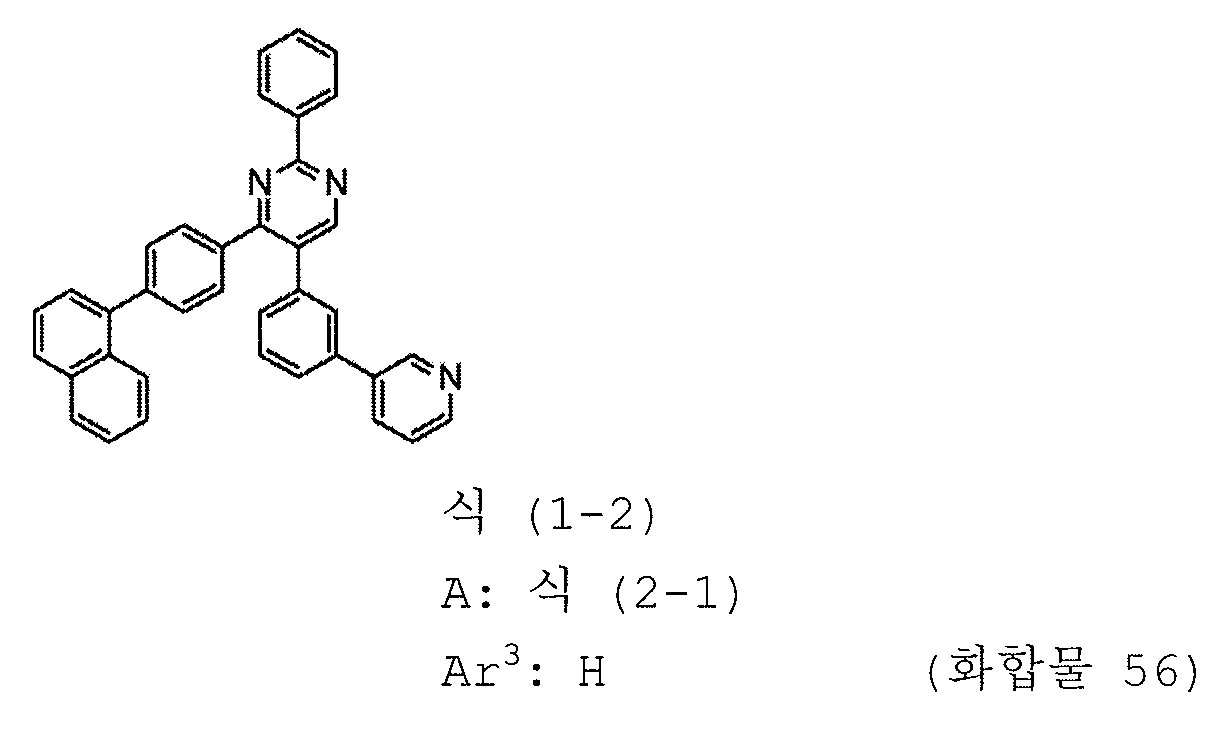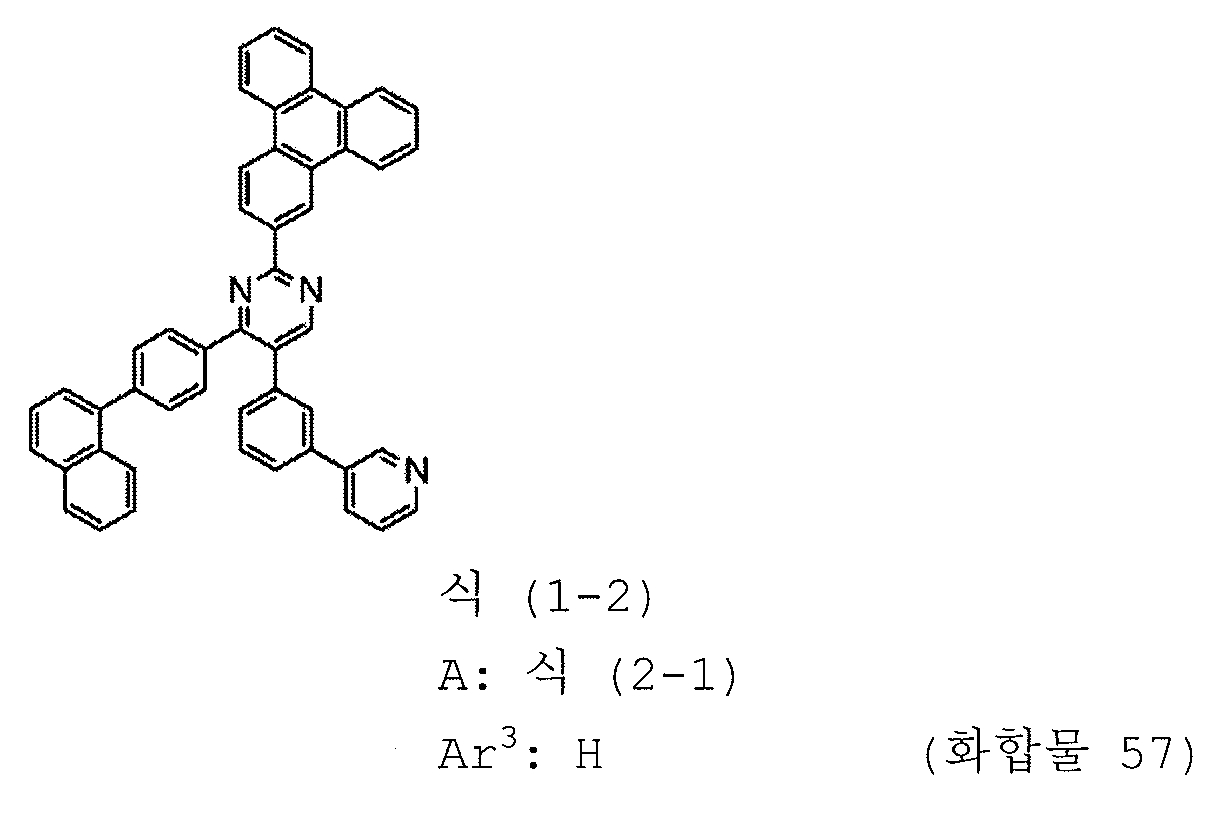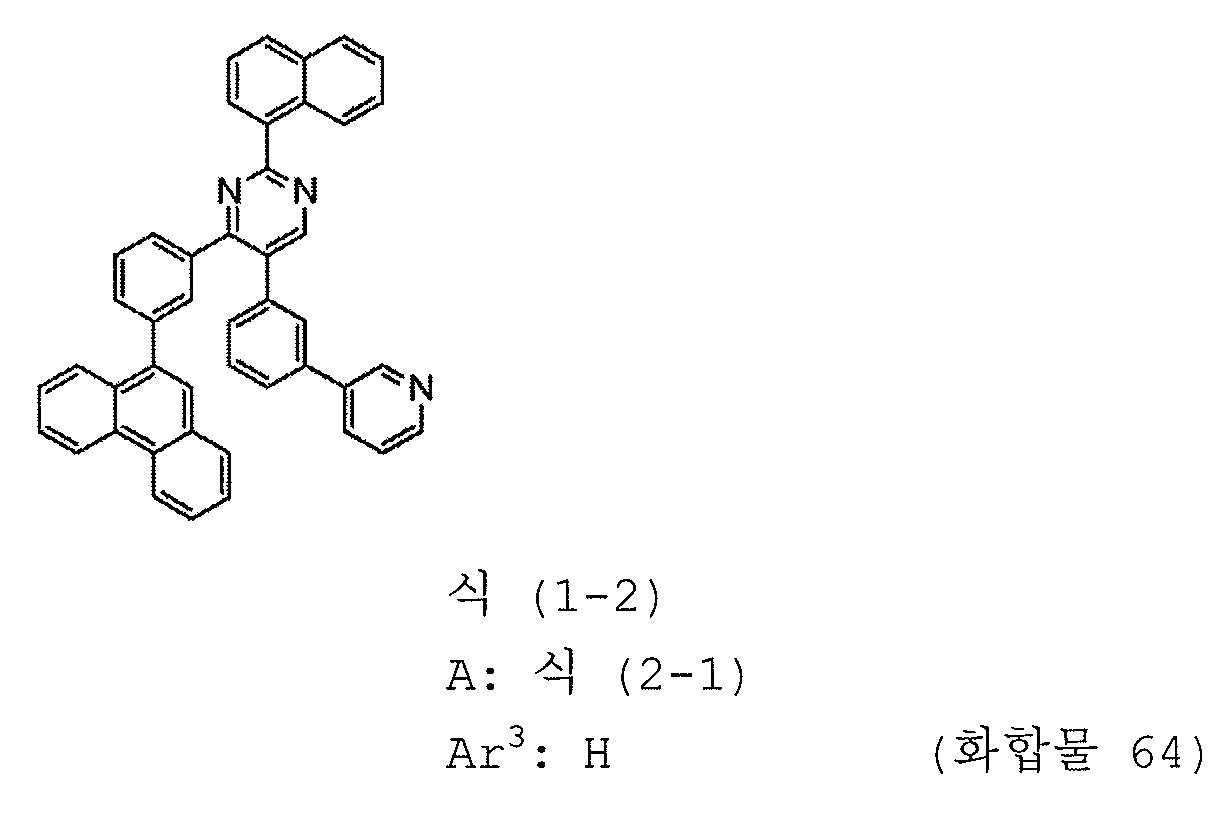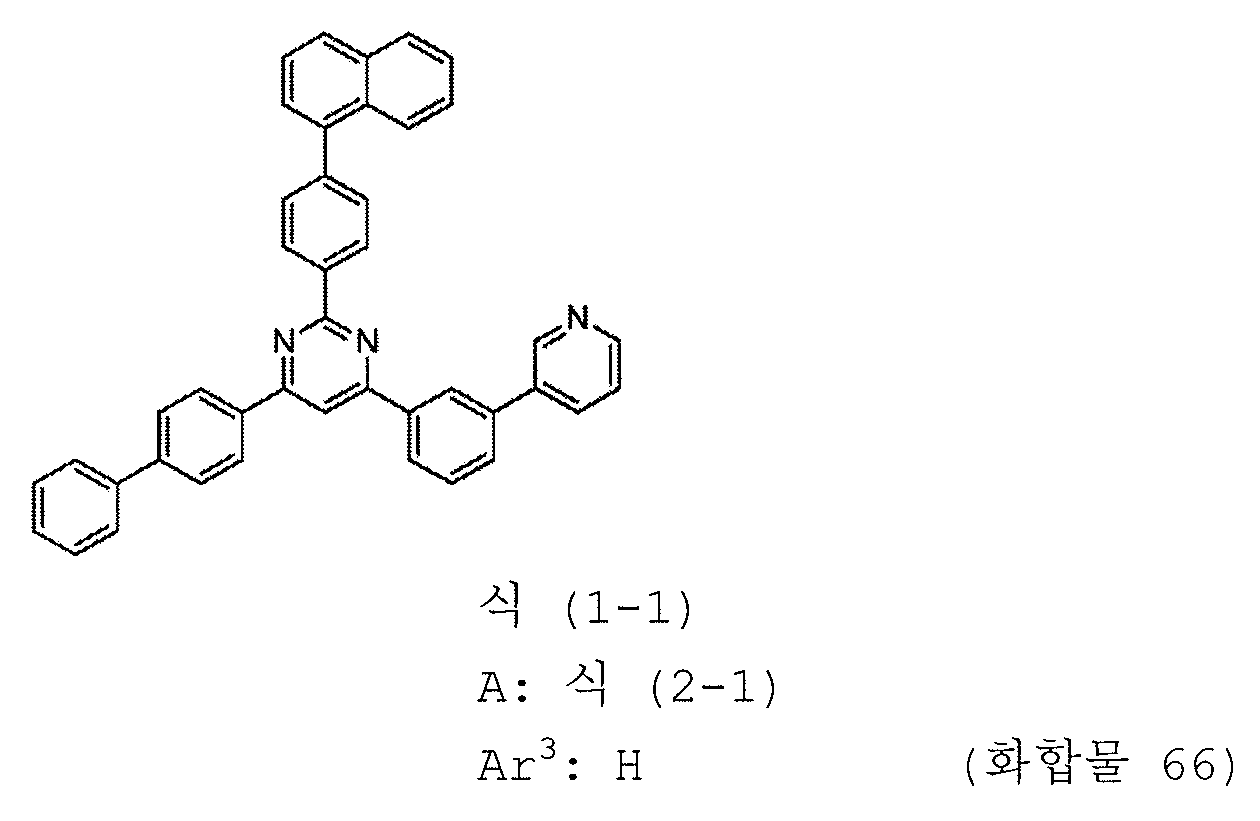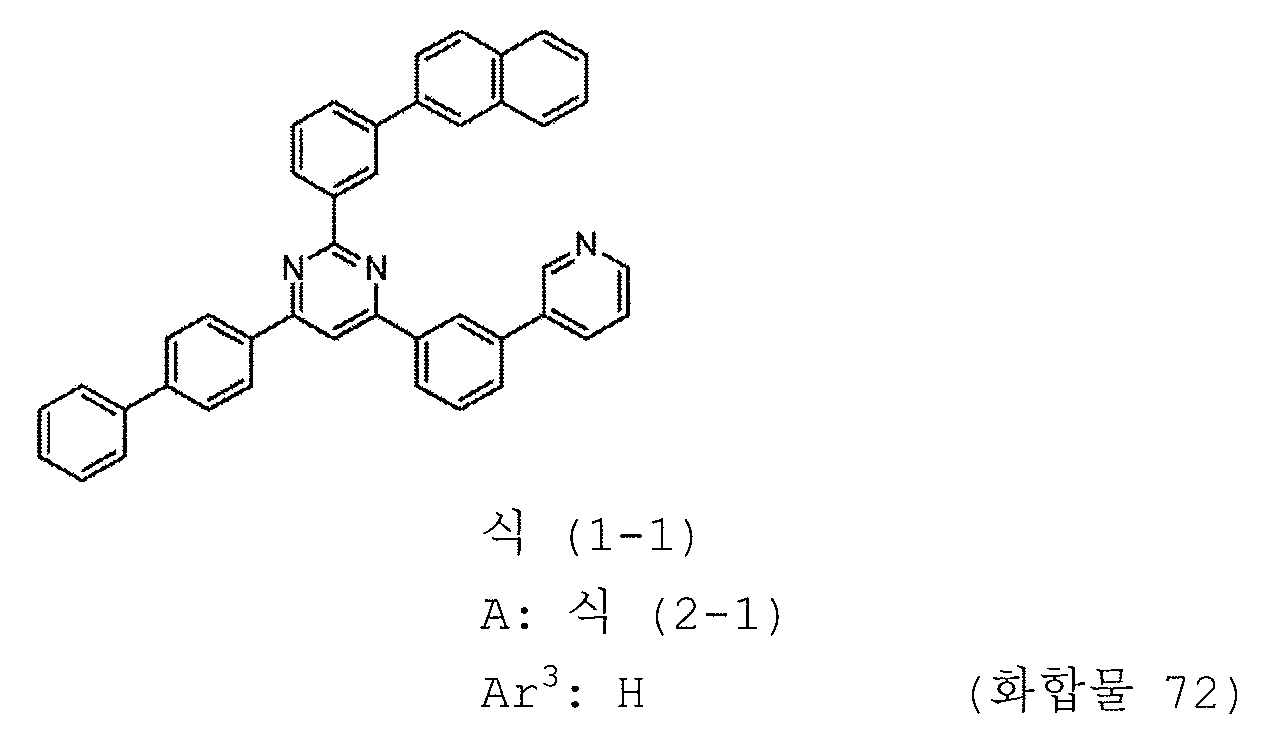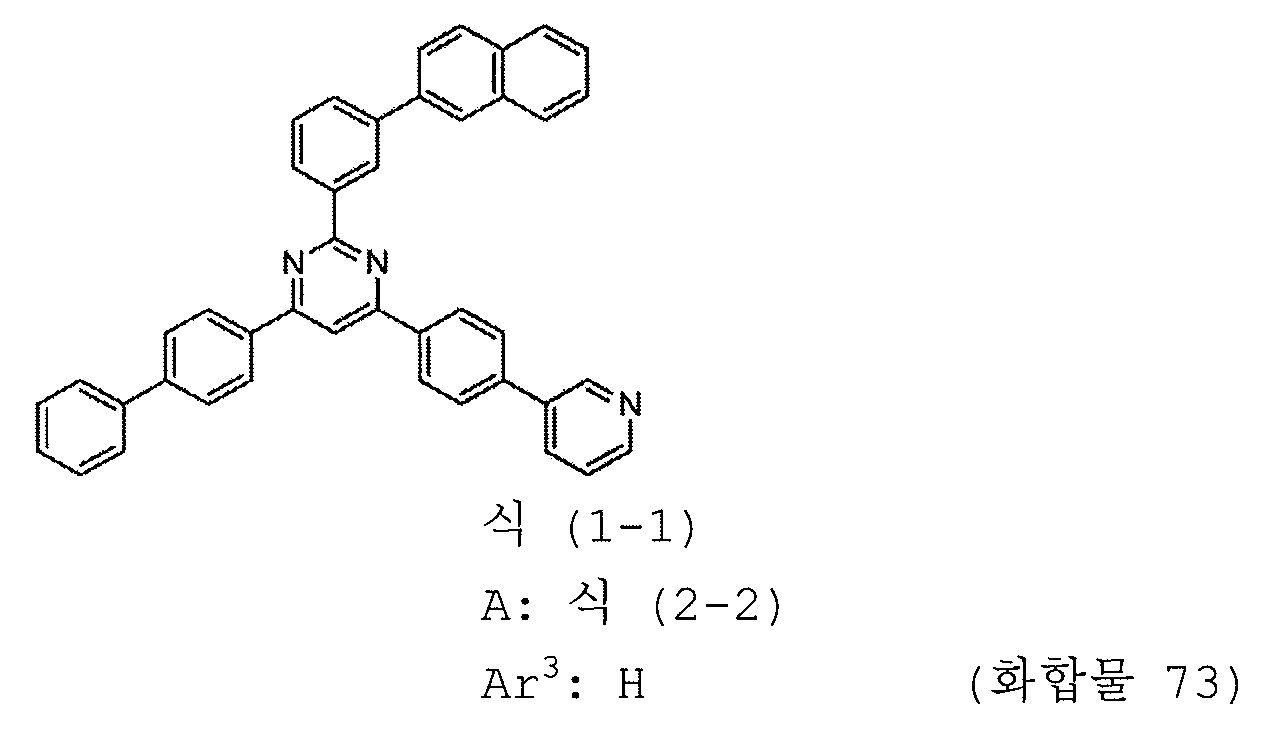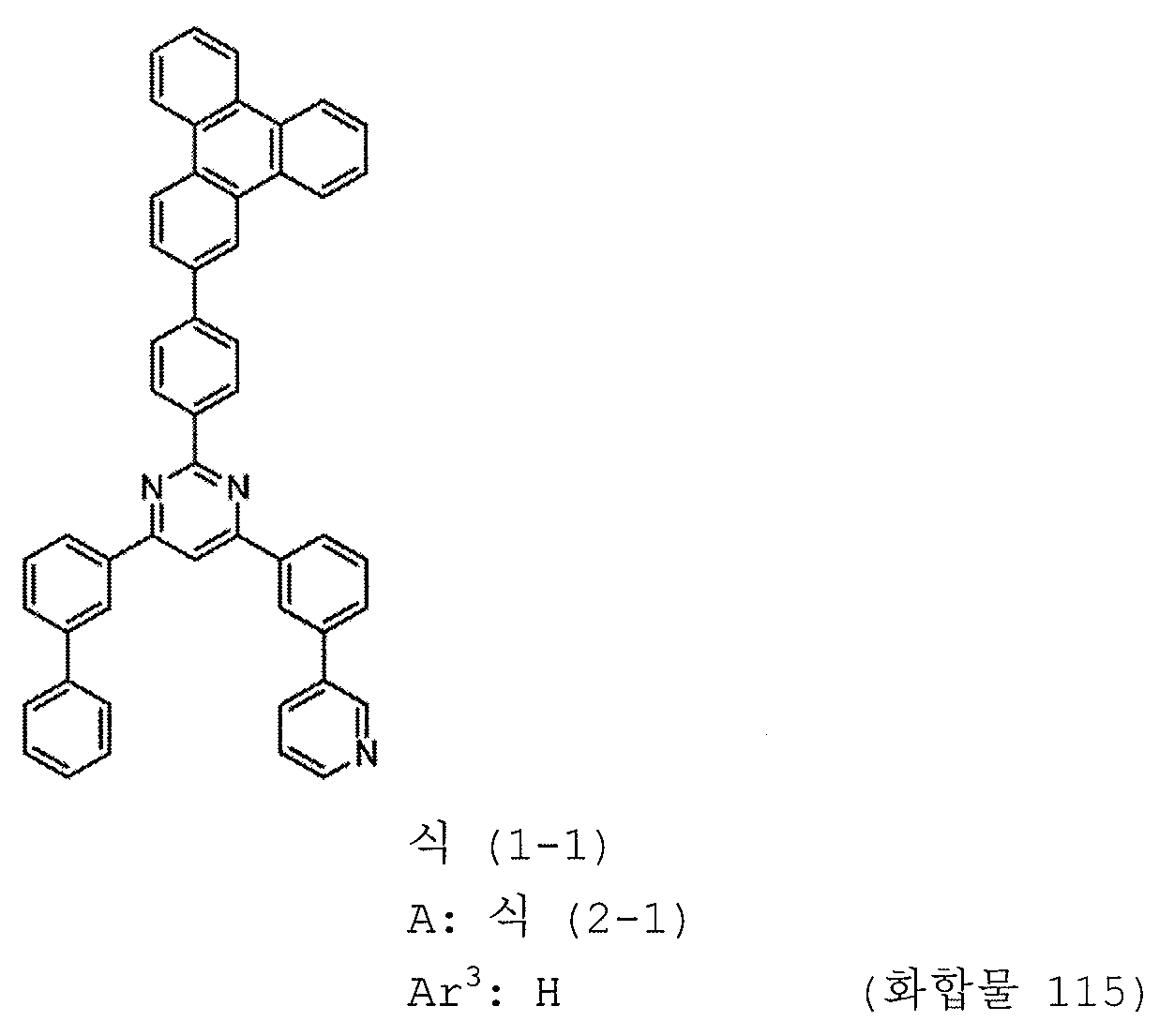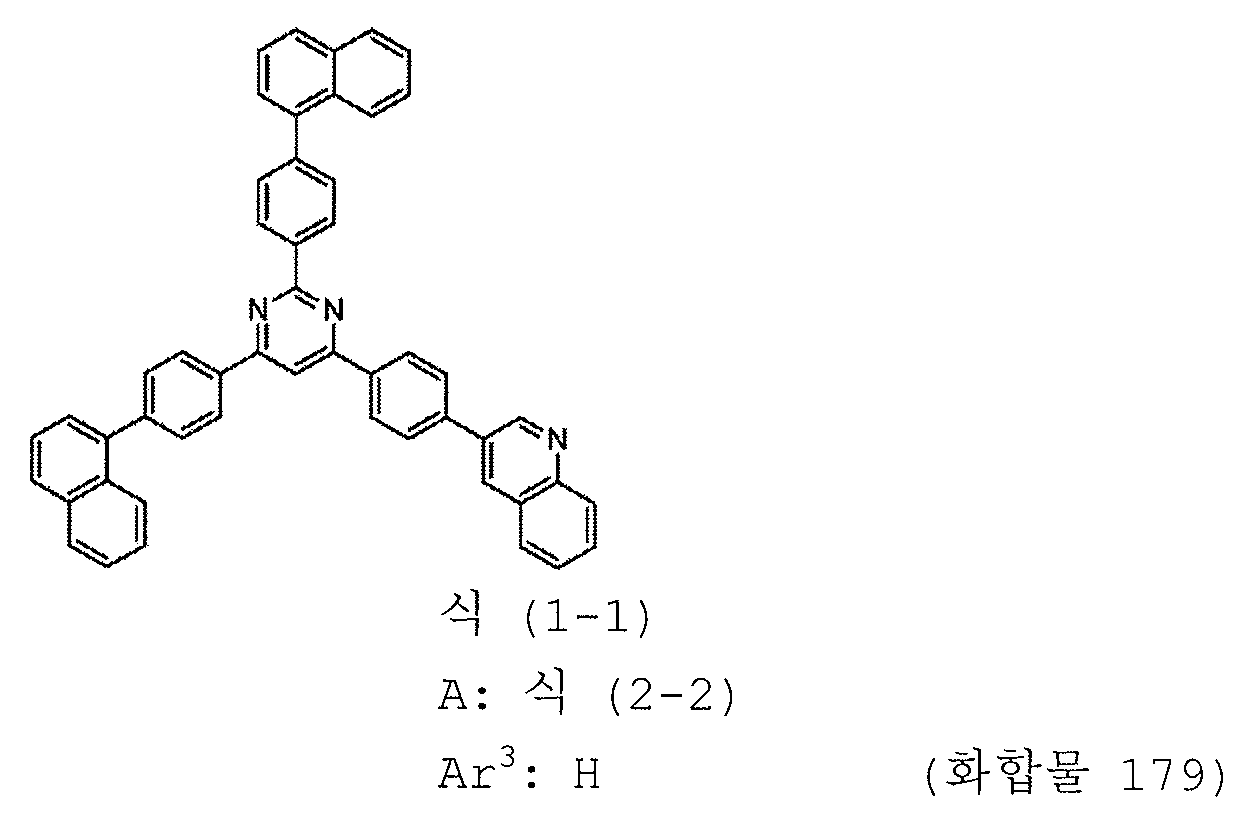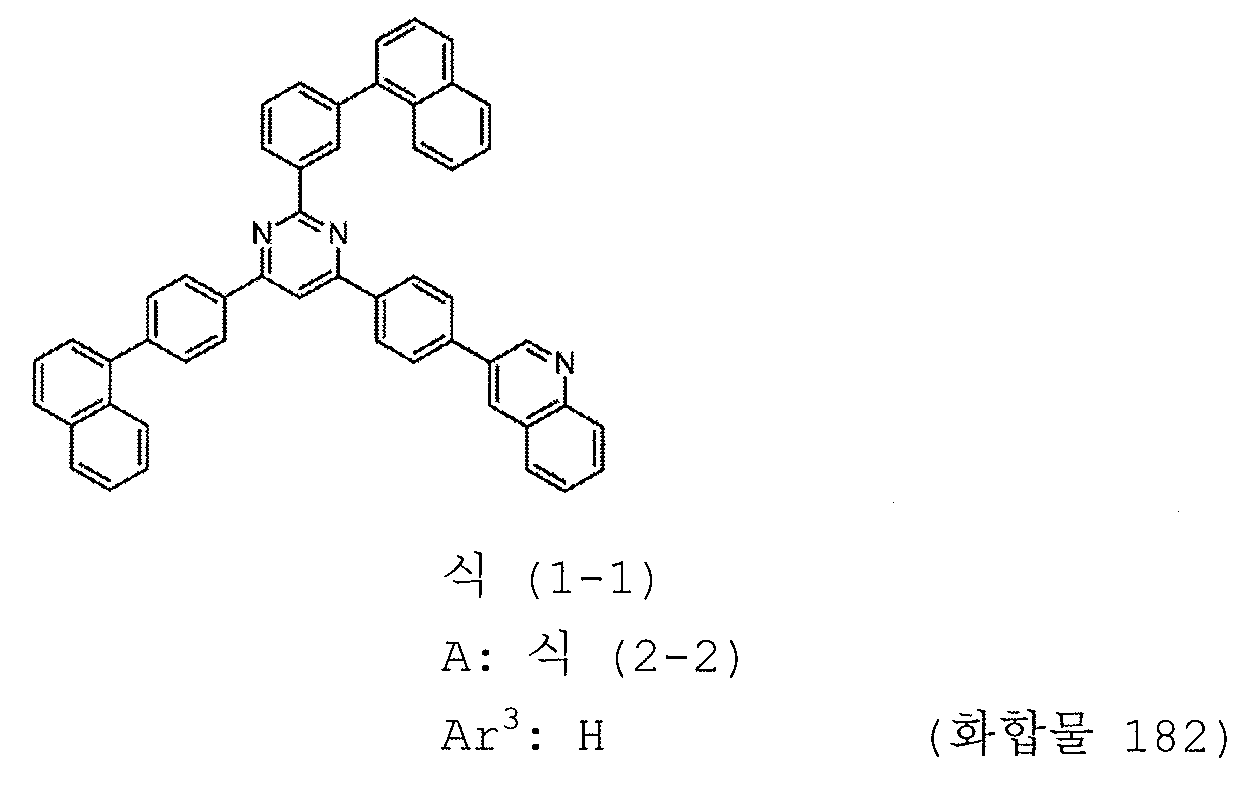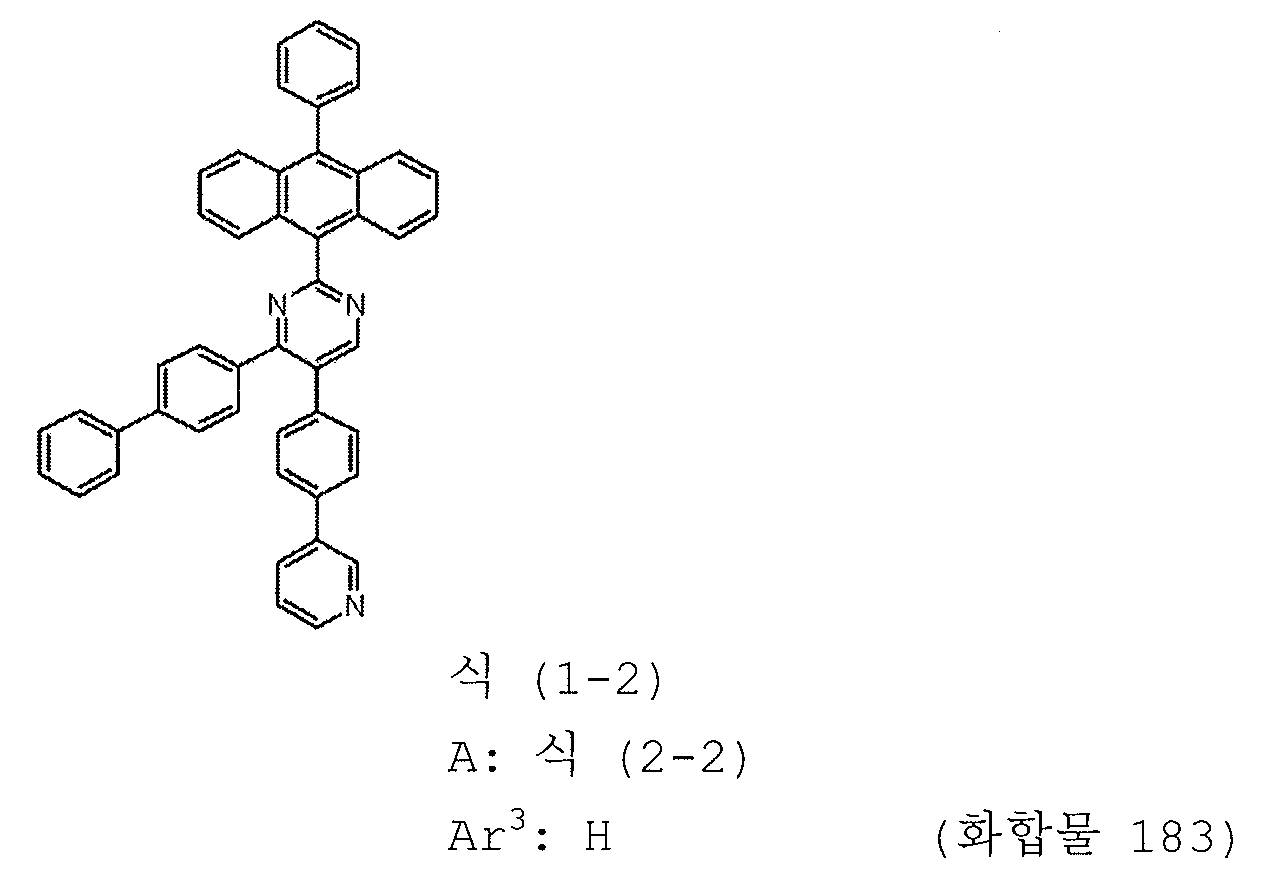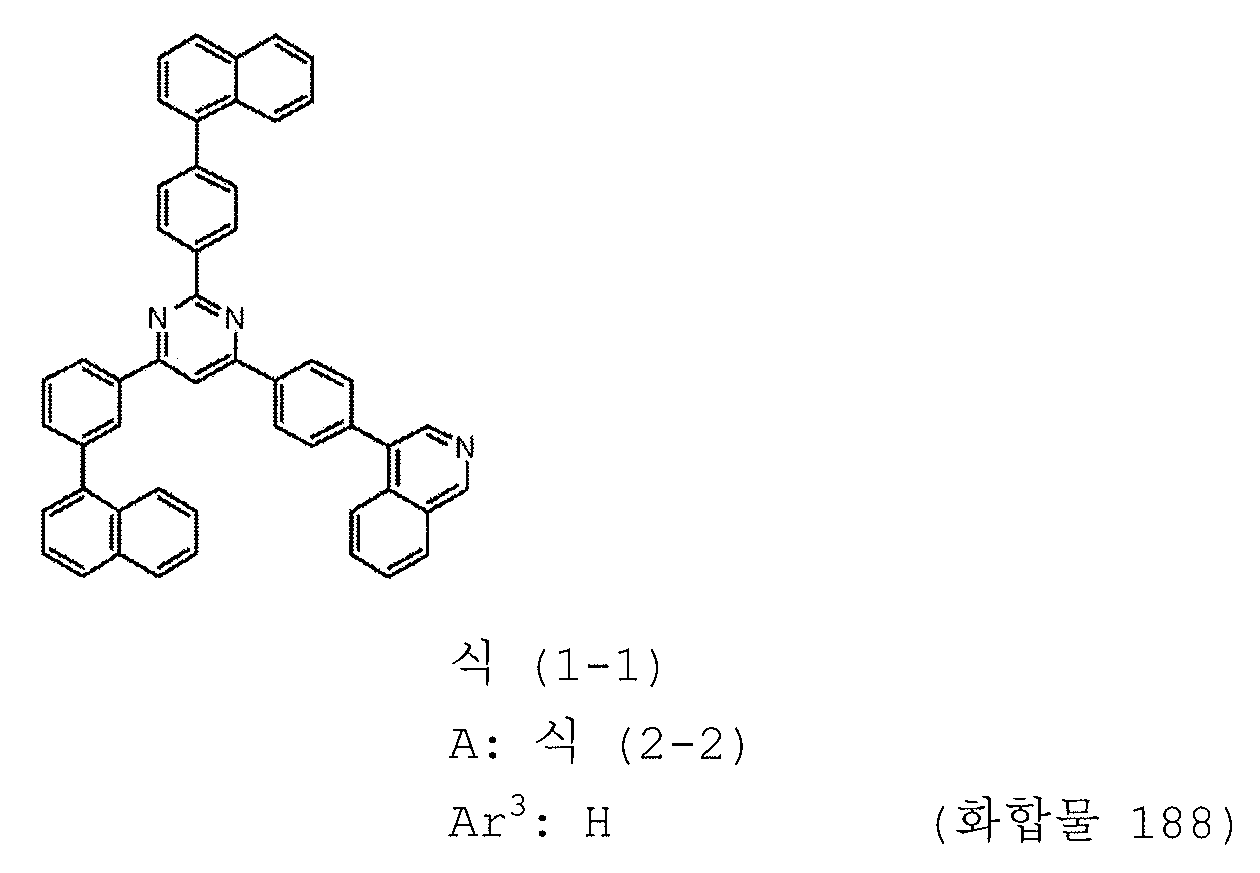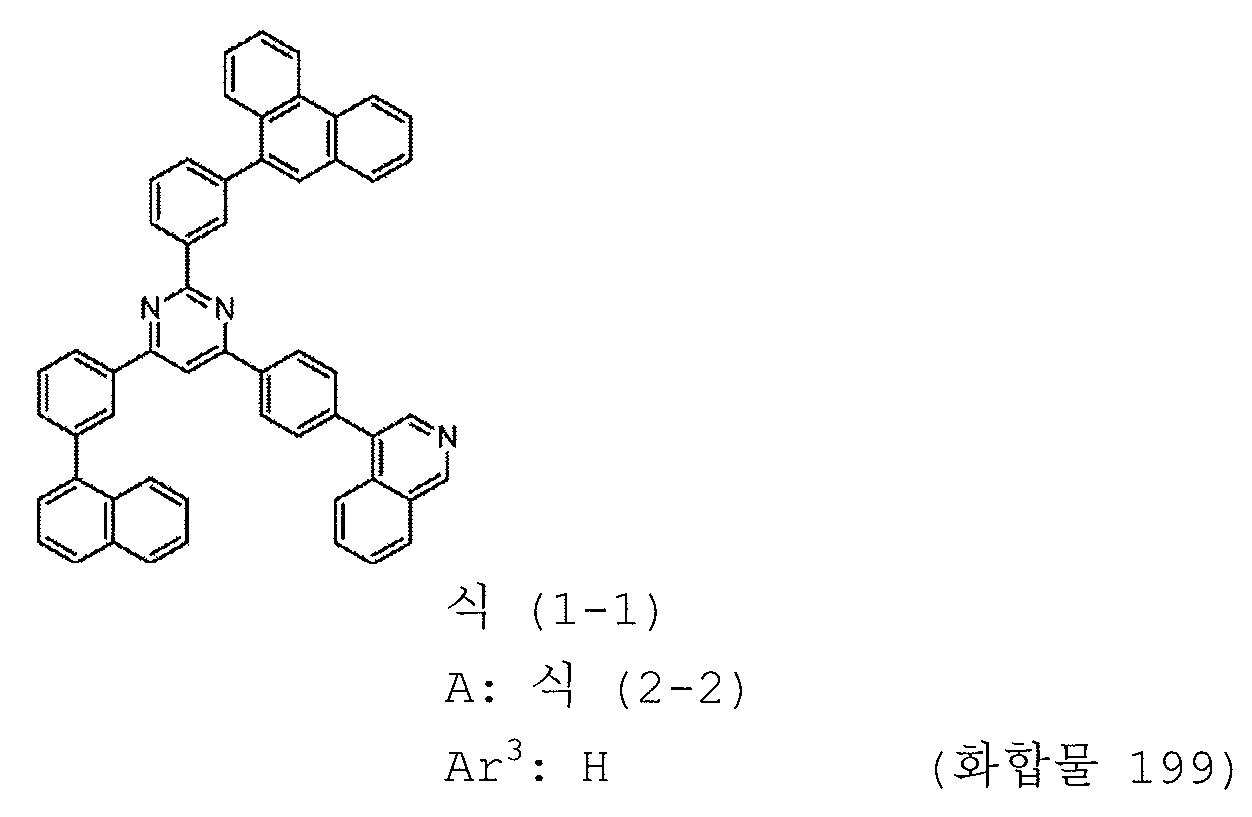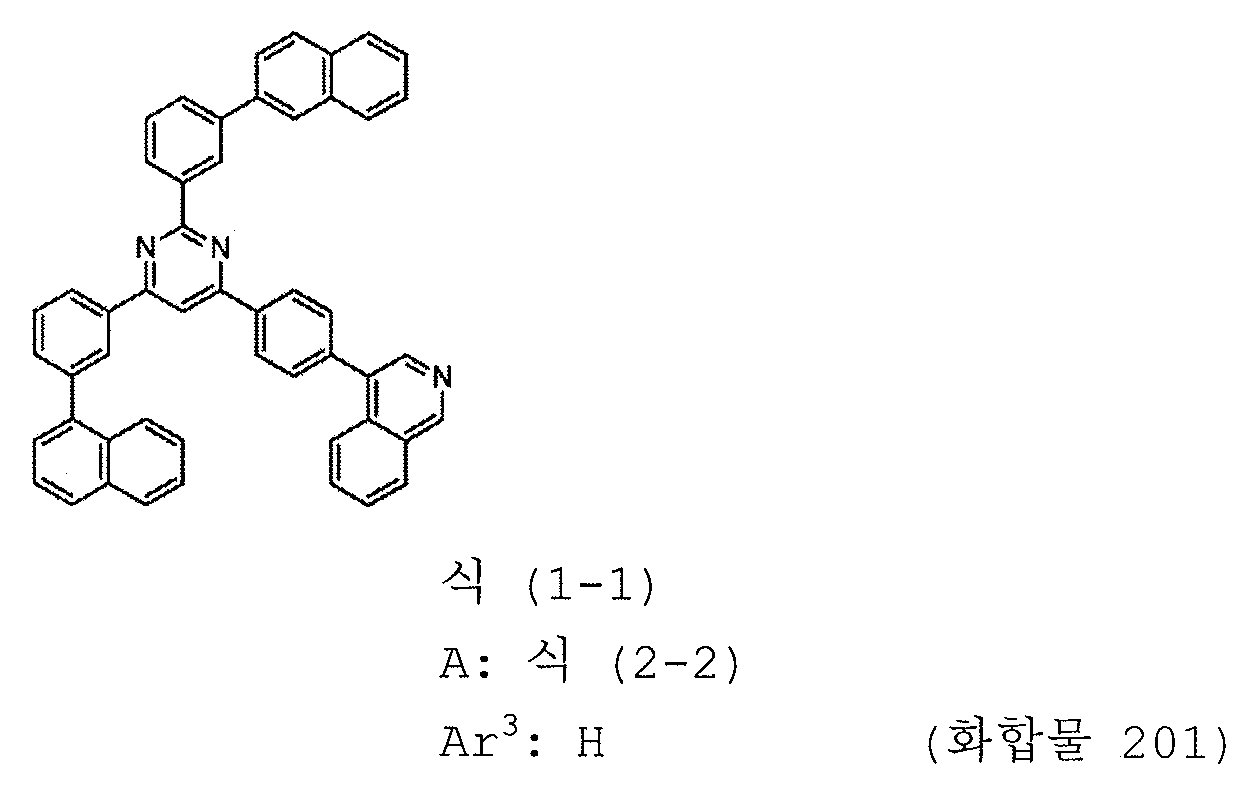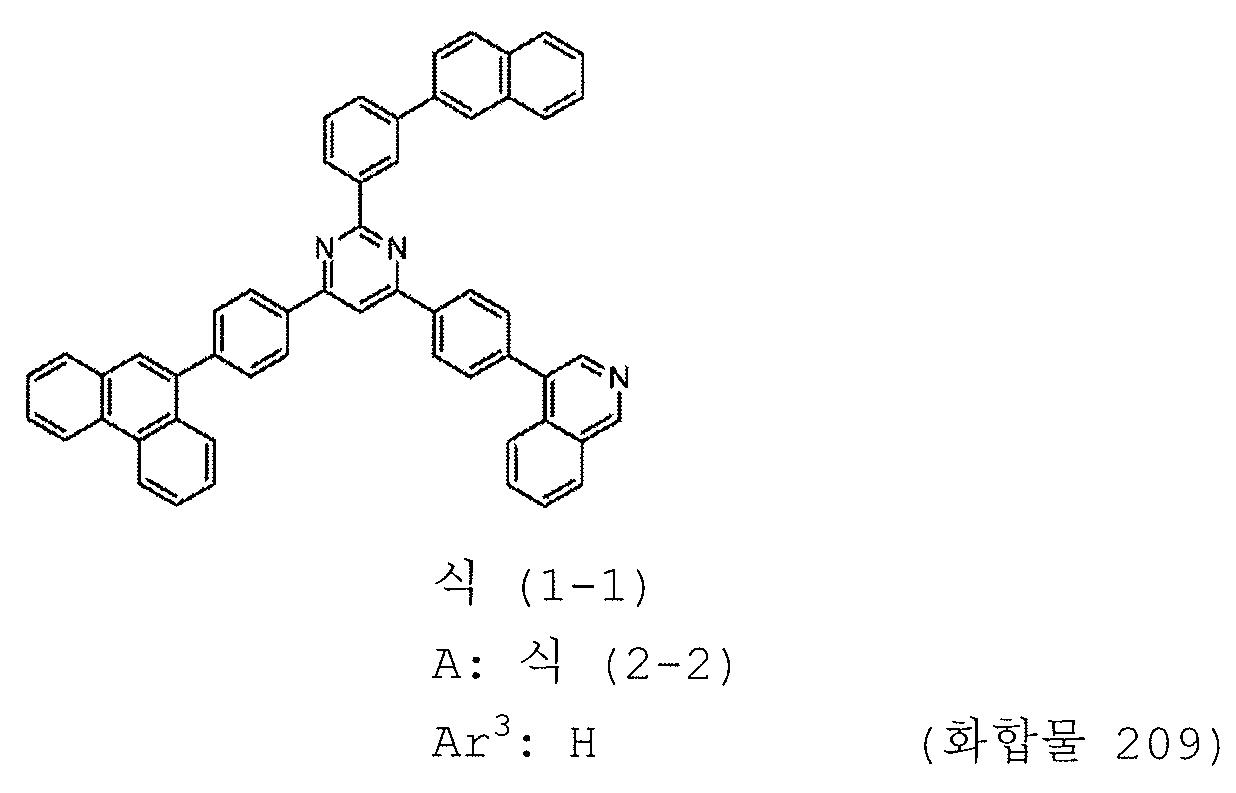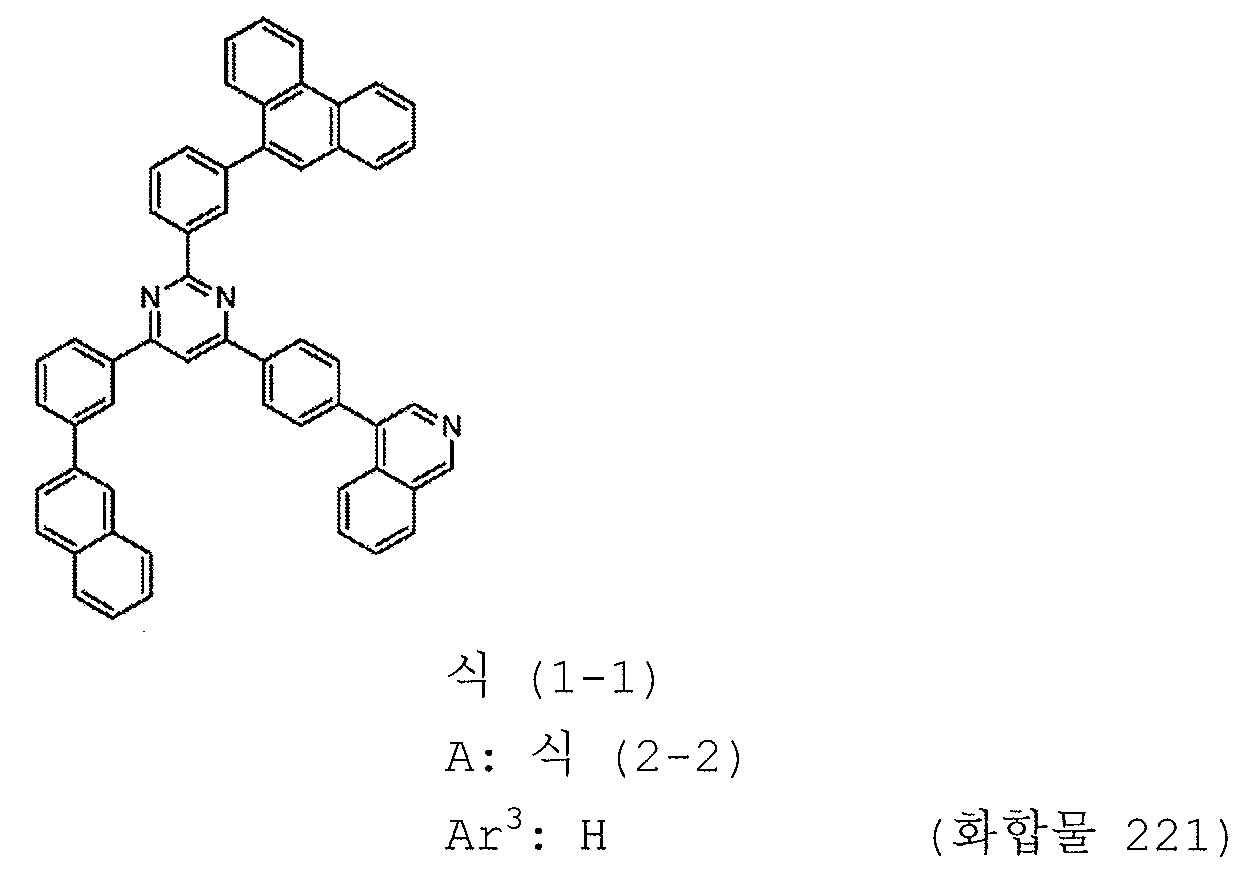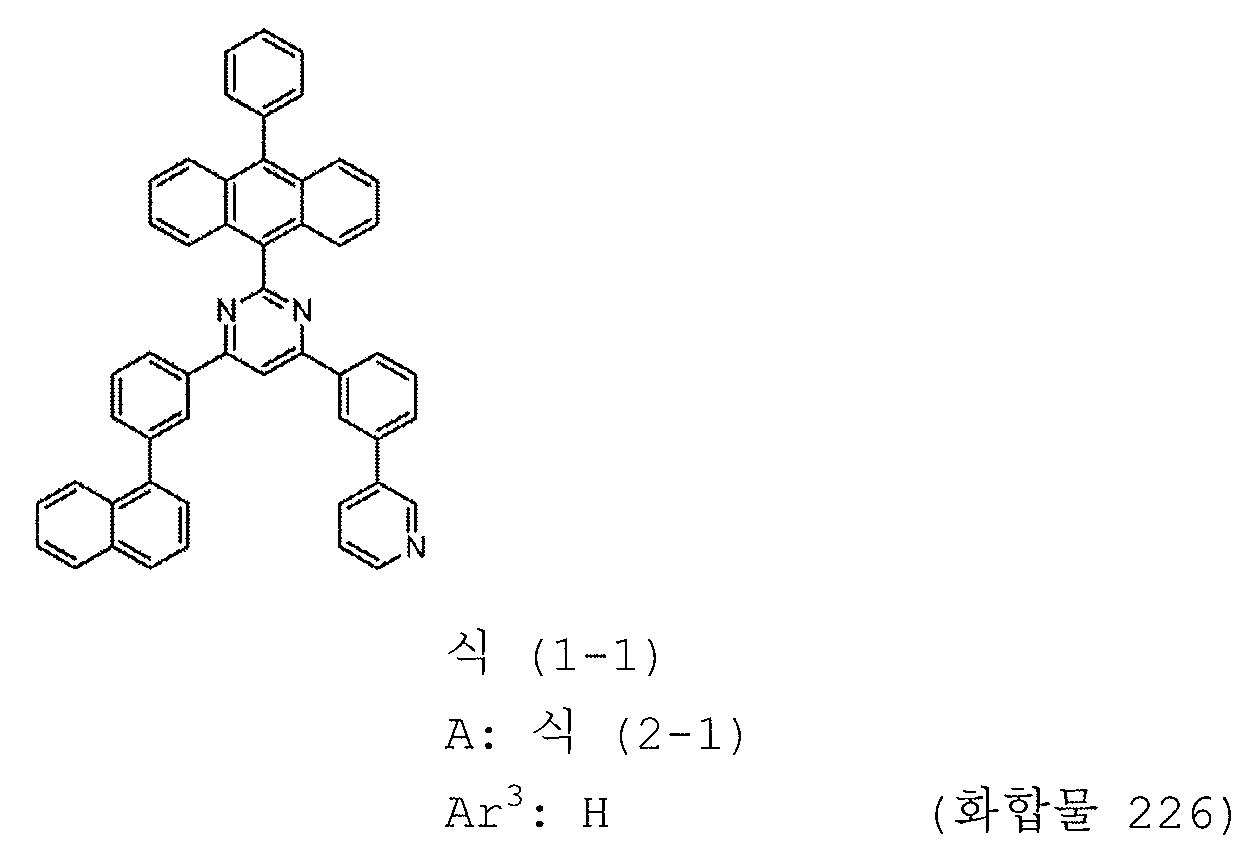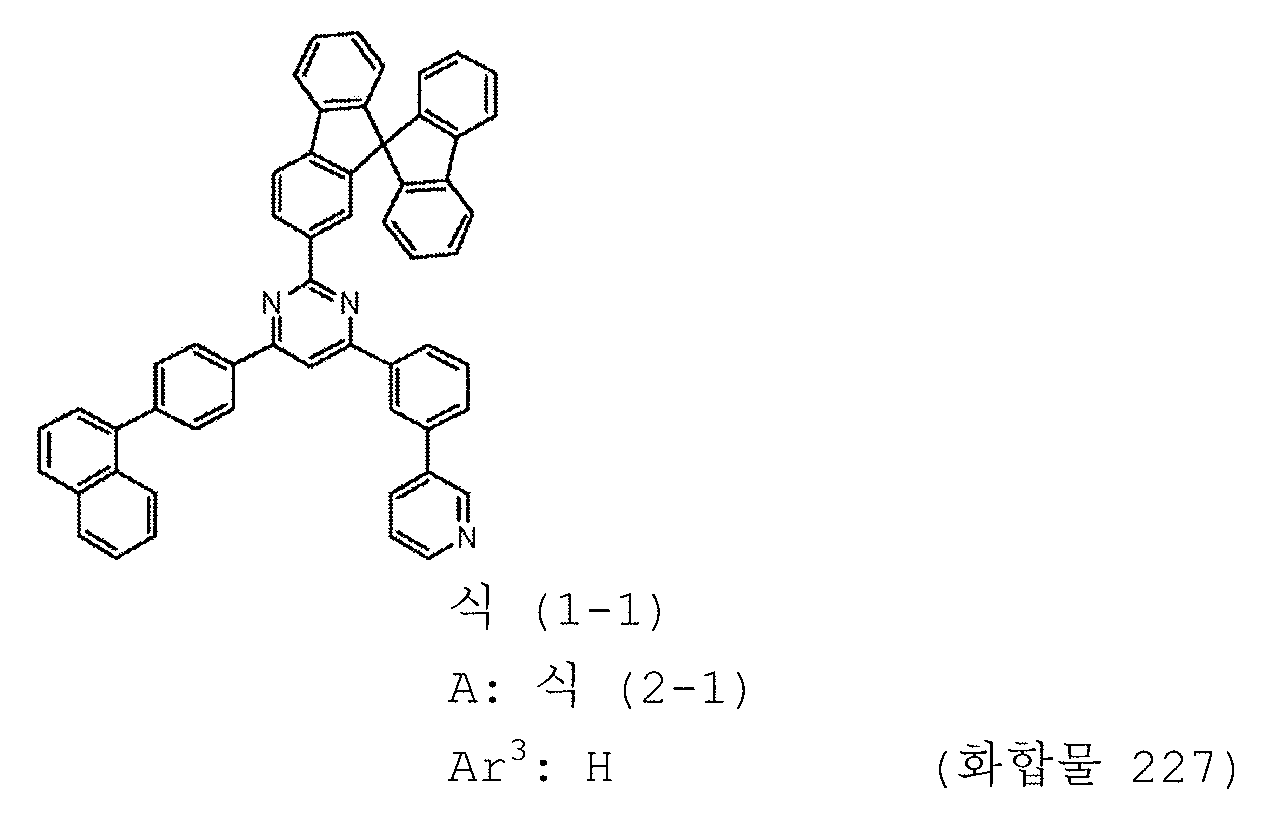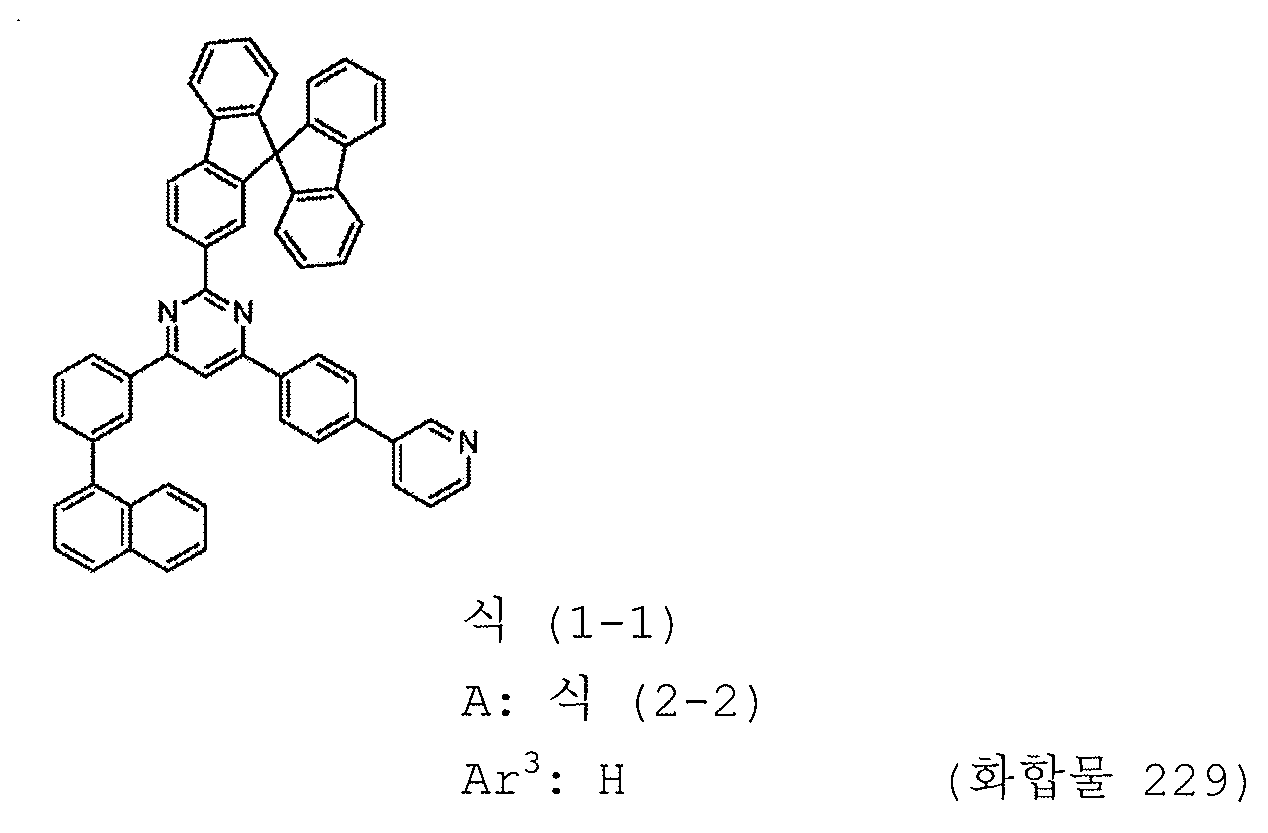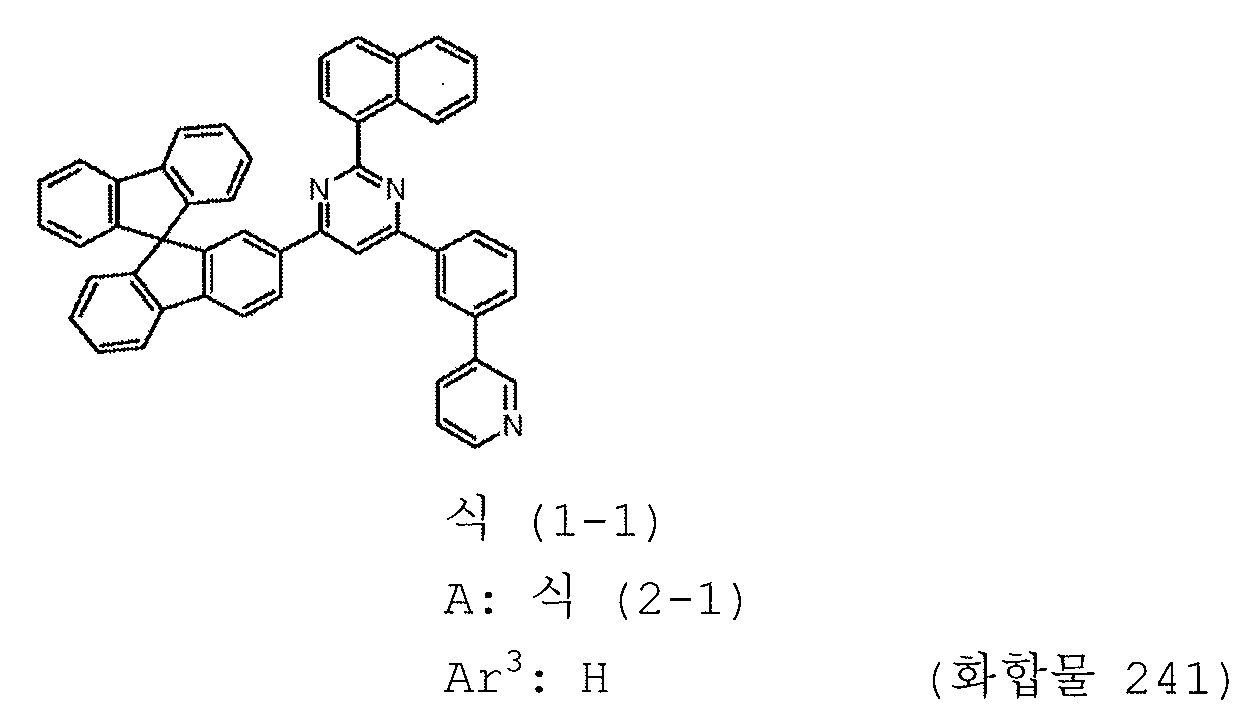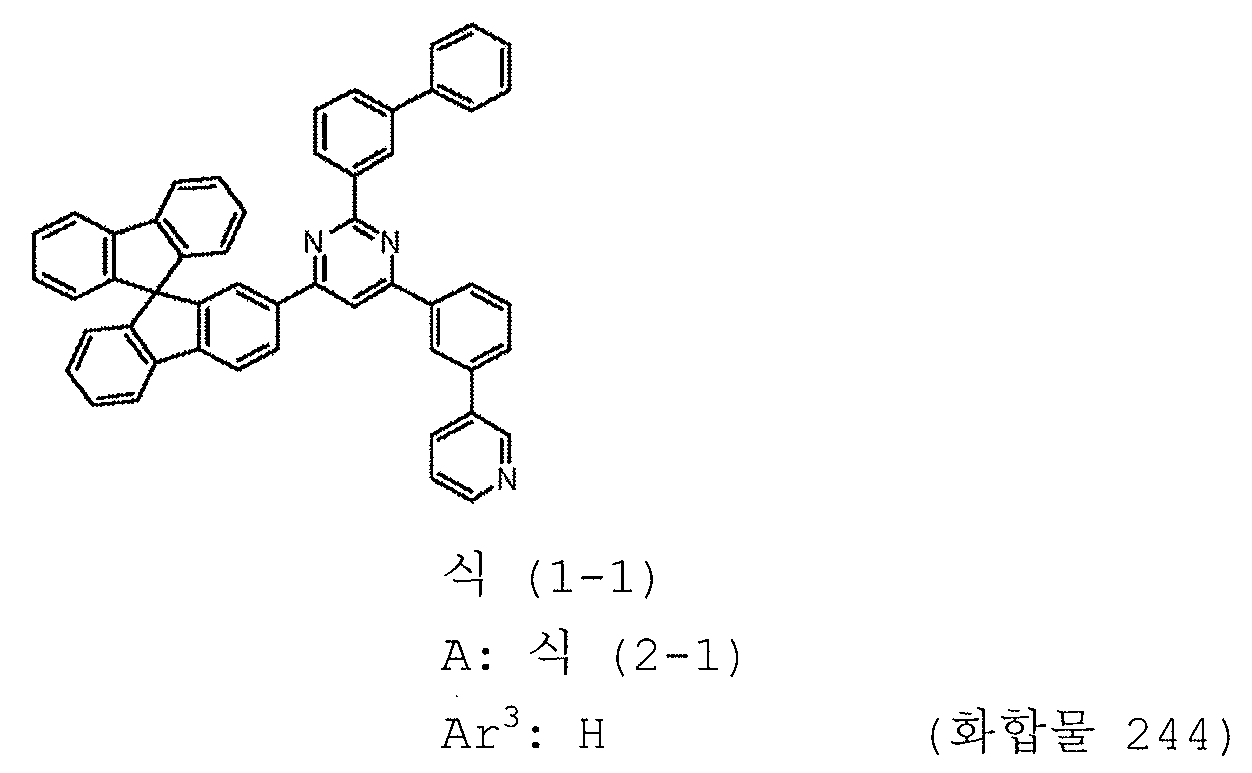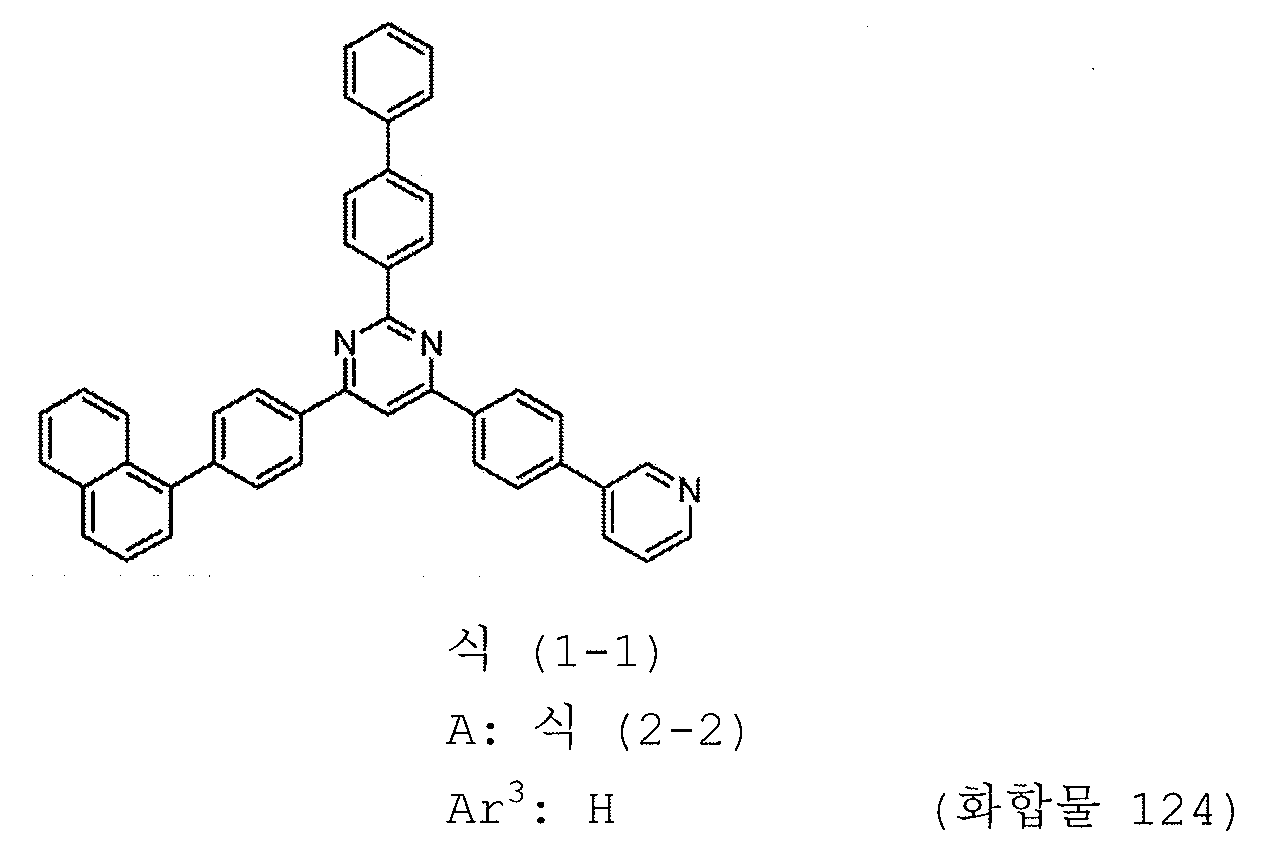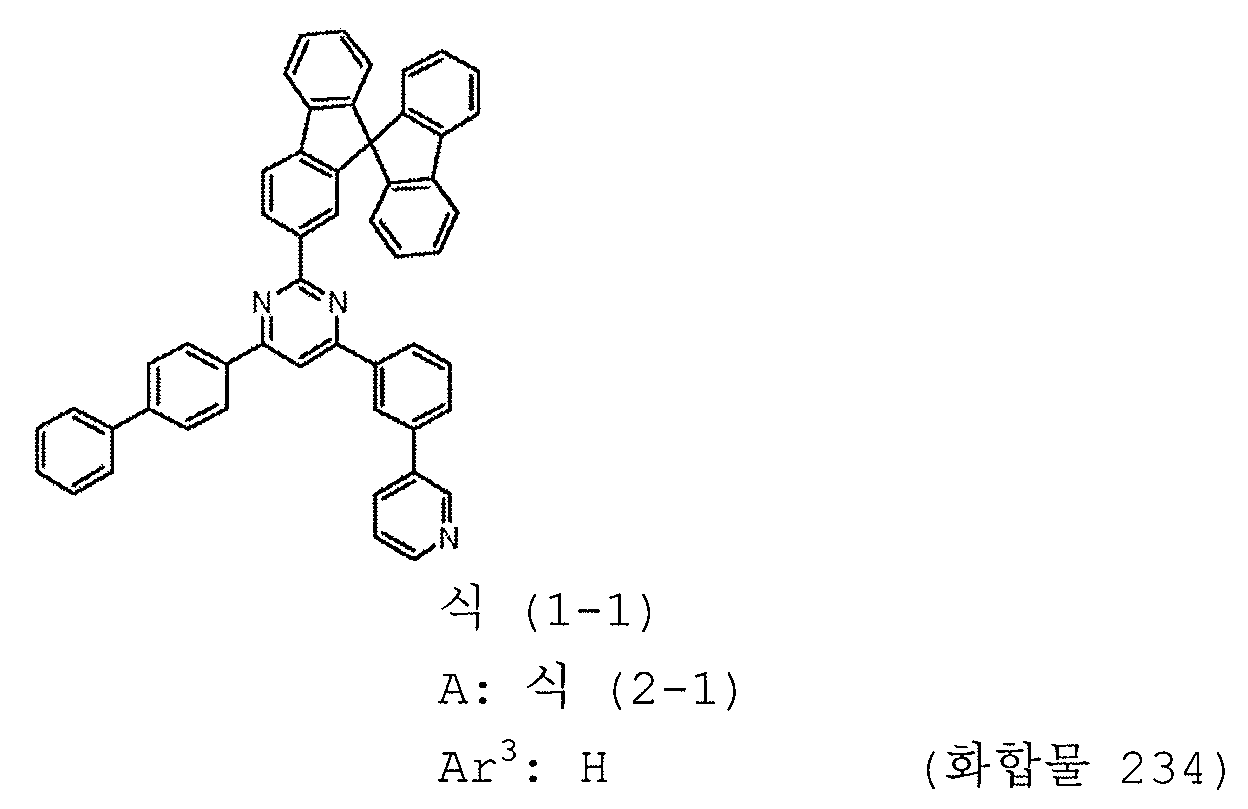KR20170016936A - 피리미딘 유도체 및 유기 전계발광 소자 - Google Patents
피리미딘 유도체 및 유기 전계발광 소자 Download PDFInfo
- Publication number
- KR20170016936A KR20170016936A KR1020177000298A KR20177000298A KR20170016936A KR 20170016936 A KR20170016936 A KR 20170016936A KR 1020177000298 A KR1020177000298 A KR 1020177000298A KR 20177000298 A KR20177000298 A KR 20177000298A KR 20170016936 A KR20170016936 A KR 20170016936A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- phenyl
- compound
- pyrimidine derivative
- pyrimidine
- Prior art date
Links
- 150000003230 pyrimidines Chemical class 0.000 title claims abstract description 62
- 239000000463 material Substances 0.000 claims abstract description 85
- 230000000903 blocking effect Effects 0.000 claims abstract description 40
- 239000012044 organic layer Substances 0.000 claims abstract description 15
- 239000000470 constituent Substances 0.000 claims abstract description 4
- 150000001875 compounds Chemical class 0.000 claims description 191
- 239000010410 layer Substances 0.000 claims description 133
- -1 diazafluorenyl group Chemical group 0.000 claims description 128
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 85
- 125000001424 substituent group Chemical group 0.000 claims description 69
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 47
- 125000002029 aromatic hydrocarbon group Chemical group 0.000 claims description 38
- 125000006615 aromatic heterocyclic group Chemical group 0.000 claims description 36
- 229910052717 sulfur Inorganic materials 0.000 claims description 19
- 125000004432 carbon atom Chemical group C* 0.000 claims description 18
- 125000000714 pyrimidinyl group Chemical group 0.000 claims description 18
- 125000000217 alkyl group Chemical group 0.000 claims description 14
- 125000004076 pyridyl group Chemical group 0.000 claims description 10
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 claims description 10
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 9
- 125000005956 isoquinolyl group Chemical group 0.000 claims description 9
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 9
- 125000005493 quinolyl group Chemical group 0.000 claims description 9
- 125000004434 sulfur atom Chemical group 0.000 claims description 9
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 8
- 125000001041 indolyl group Chemical group 0.000 claims description 8
- 229910052801 chlorine Inorganic materials 0.000 claims description 7
- 229910052805 deuterium Inorganic materials 0.000 claims description 7
- 229910052731 fluorine Inorganic materials 0.000 claims description 7
- 125000001153 fluoro group Chemical group F* 0.000 claims description 7
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 claims description 5
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 claims description 5
- 125000004193 piperazinyl group Chemical group 0.000 claims 9
- 125000004431 deuterium atom Chemical group 0.000 claims 1
- 238000002347 injection Methods 0.000 abstract description 21
- 239000007924 injection Substances 0.000 abstract description 21
- 238000005160 1H NMR spectroscopy Methods 0.000 description 69
- 239000000843 powder Substances 0.000 description 47
- 230000015572 biosynthetic process Effects 0.000 description 30
- 238000005259 measurement Methods 0.000 description 25
- 238000003786 synthesis reaction Methods 0.000 description 25
- 238000005481 NMR spectroscopy Methods 0.000 description 24
- 238000006243 chemical reaction Methods 0.000 description 23
- 229910052739 hydrogen Inorganic materials 0.000 description 23
- 239000001257 hydrogen Substances 0.000 description 23
- HFXYUCJLQZCNPD-UHFFFAOYSA-N (3-naphthalen-1-ylphenyl)boronic acid Chemical compound OB(O)C1=CC=CC(C=2C3=CC=CC=C3C=CC=2)=C1 HFXYUCJLQZCNPD-UHFFFAOYSA-N 0.000 description 21
- 239000010408 film Substances 0.000 description 19
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 14
- 238000002156 mixing Methods 0.000 description 13
- 239000010409 thin film Substances 0.000 description 13
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 12
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 12
- 125000003914 fluoranthenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC=C4C1=C23)* 0.000 description 11
- 125000002541 furyl group Chemical group 0.000 description 11
- 125000001624 naphthyl group Chemical group 0.000 description 11
- 125000001792 phenanthrenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C=CC12)* 0.000 description 11
- 125000003960 triphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C3=CC=CC=C3C12)* 0.000 description 11
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 10
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 10
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 10
- 125000004988 dibenzothienyl group Chemical group C1(=CC=CC=2SC3=C(C21)C=CC=C3)* 0.000 description 10
- 239000011593 sulfur Substances 0.000 description 10
- 125000001544 thienyl group Chemical group 0.000 description 10
- 230000005525 hole transport Effects 0.000 description 9
- 125000001725 pyrenyl group Chemical group 0.000 description 9
- 239000000758 substrate Substances 0.000 description 9
- 125000000335 thiazolyl group Chemical group 0.000 description 9
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 8
- 230000000052 comparative effect Effects 0.000 description 8
- 230000009477 glass transition Effects 0.000 description 8
- 229910052751 metal Inorganic materials 0.000 description 8
- 239000002184 metal Substances 0.000 description 8
- 229910052760 oxygen Inorganic materials 0.000 description 8
- 239000001301 oxygen Substances 0.000 description 8
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 description 8
- BQHVXFQXTOIMQM-UHFFFAOYSA-N (4-naphthalen-1-ylphenyl)boronic acid Chemical compound C1=CC(B(O)O)=CC=C1C1=CC=CC2=CC=CC=C12 BQHVXFQXTOIMQM-UHFFFAOYSA-N 0.000 description 7
- STPKWKPURVSAJF-LJEWAXOPSA-N (4r,5r)-5-[4-[[4-(1-aza-4-azoniabicyclo[2.2.2]octan-4-ylmethyl)phenyl]methoxy]phenyl]-3,3-dibutyl-7-(dimethylamino)-1,1-dioxo-4,5-dihydro-2h-1$l^{6}-benzothiepin-4-ol Chemical compound O[C@H]1C(CCCC)(CCCC)CS(=O)(=O)C2=CC=C(N(C)C)C=C2[C@H]1C(C=C1)=CC=C1OCC(C=C1)=CC=C1C[N+]1(CC2)CCN2CC1 STPKWKPURVSAJF-LJEWAXOPSA-N 0.000 description 7
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 7
- 125000006267 biphenyl group Chemical group 0.000 description 7
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 7
- 238000000034 method Methods 0.000 description 7
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 6
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- 125000000641 acridinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3C=C12)* 0.000 description 6
- 125000003545 alkoxy group Chemical group 0.000 description 6
- 150000001975 deuterium Chemical group 0.000 description 6
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 6
- VONFKUBDOCWFAS-UHFFFAOYSA-N 2-chloro-4-(4-naphthalen-1-ylphenyl)-6-(4-pyridin-3-ylphenyl)pyrimidine Chemical compound ClC1=NC(=CC(=N1)C1=CC=C(C=C1)C1=CC=CC2=CC=CC=C12)C1=CC=C(C=C1)C=1C=NC=CC=1 VONFKUBDOCWFAS-UHFFFAOYSA-N 0.000 description 5
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 5
- GSDQYSSLIKJJOG-UHFFFAOYSA-N 4-chloro-2-(3-chloroanilino)benzoic acid Chemical compound OC(=O)C1=CC=C(Cl)C=C1NC1=CC=CC(Cl)=C1 GSDQYSSLIKJJOG-UHFFFAOYSA-N 0.000 description 5
- 0 Cc1c(*)c(*)c(*)c(*)c1* Chemical compound Cc1c(*)c(*)c(*)c(*)c1* 0.000 description 5
- AVYVHIKSFXVDBG-UHFFFAOYSA-N N-benzyl-N-hydroxy-2,2-dimethylbutanamide Chemical compound C(C1=CC=CC=C1)N(C(C(CC)(C)C)=O)O AVYVHIKSFXVDBG-UHFFFAOYSA-N 0.000 description 5
- 125000004062 acenaphthenyl group Chemical group C1(CC2=CC=CC3=CC=CC1=C23)* 0.000 description 5
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 5
- 125000000319 biphenyl-4-yl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 5
- GWNFQAKCJYEJEW-UHFFFAOYSA-N ethyl 3-[8-[[4-methyl-5-[(3-methyl-4-oxophthalazin-1-yl)methyl]-1,2,4-triazol-3-yl]sulfanyl]octanoylamino]benzoate Chemical compound CCOC(=O)C1=CC(NC(=O)CCCCCCCSC2=NN=C(CC3=NN(C)C(=O)C4=CC=CC=C34)N2C)=CC=C1 GWNFQAKCJYEJEW-UHFFFAOYSA-N 0.000 description 5
- 239000011521 glass Substances 0.000 description 5
- 125000005843 halogen group Chemical group 0.000 description 5
- YGBMCLDVRUGXOV-UHFFFAOYSA-N n-[6-[6-chloro-5-[(4-fluorophenyl)sulfonylamino]pyridin-3-yl]-1,3-benzothiazol-2-yl]acetamide Chemical compound C1=C2SC(NC(=O)C)=NC2=CC=C1C(C=1)=CN=C(Cl)C=1NS(=O)(=O)C1=CC=C(F)C=C1 YGBMCLDVRUGXOV-UHFFFAOYSA-N 0.000 description 5
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 5
- 125000004625 phenanthrolinyl group Chemical group N1=C(C=CC2=CC=C3C=CC=NC3=C12)* 0.000 description 5
- 125000003226 pyrazolyl group Chemical group 0.000 description 5
- 229940083082 pyrimidine derivative acting on arteriolar smooth muscle Drugs 0.000 description 5
- 125000000168 pyrrolyl group Chemical group 0.000 description 5
- 125000004306 triazinyl group Chemical group 0.000 description 5
- DFRAKBCRUYUFNT-UHFFFAOYSA-N 3,8-dicyclohexyl-2,4,7,9-tetrahydro-[1,3]oxazino[5,6-h][1,3]benzoxazine Chemical compound C1CCCCC1N1CC(C=CC2=C3OCN(C2)C2CCCCC2)=C3OC1 DFRAKBCRUYUFNT-UHFFFAOYSA-N 0.000 description 4
- YKKFZNIPMRGSKO-UHFFFAOYSA-N 4-(4-naphthalen-1-ylphenyl)-6-(4-pyridin-3-ylphenyl)pyrimidine Chemical compound C1(=CC=CC2=CC=CC=C12)C1=CC=C(C=C1)C1=NC=NC(=C1)C1=CC=C(C=C1)C=1C=NC=CC=1 YKKFZNIPMRGSKO-UHFFFAOYSA-N 0.000 description 4
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 4
- 238000006069 Suzuki reaction reaction Methods 0.000 description 4
- 229910052782 aluminium Inorganic materials 0.000 description 4
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 4
- 125000002102 aryl alkyloxo group Chemical group 0.000 description 4
- 125000004104 aryloxy group Chemical group 0.000 description 4
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 4
- 239000007772 electrode material Substances 0.000 description 4
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 4
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 150000004322 quinolinols Chemical class 0.000 description 4
- UFHFLCQGNIYNRP-VVKOMZTBSA-N Dideuterium Chemical group [2H][2H] UFHFLCQGNIYNRP-VVKOMZTBSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 125000002252 acyl group Chemical group 0.000 description 3
- 125000003609 aryl vinyl group Chemical group 0.000 description 3
- HFACYLZERDEVSX-UHFFFAOYSA-N benzidine Chemical class C1=CC(N)=CC=C1C1=CC=C(N)C=C1 HFACYLZERDEVSX-UHFFFAOYSA-N 0.000 description 3
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 3
- 125000006268 biphenyl-3-yl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C1=C([H])C(*)=C([H])C([H])=C1[H] 0.000 description 3
- UFVXQDWNSAGPHN-UHFFFAOYSA-K bis[(2-methylquinolin-8-yl)oxy]-(4-phenylphenoxy)alumane Chemical compound [Al+3].C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC=C([O-])C2=NC(C)=CC=C21.C1=CC([O-])=CC=C1C1=CC=CC=C1 UFVXQDWNSAGPHN-UHFFFAOYSA-K 0.000 description 3
- 239000011248 coating agent Substances 0.000 description 3
- 230000003111 delayed effect Effects 0.000 description 3
- 238000000151 deposition Methods 0.000 description 3
- 230000008021 deposition Effects 0.000 description 3
- 239000002019 doping agent Substances 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- 238000003475 lamination Methods 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 239000011368 organic material Substances 0.000 description 3
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 3
- 238000005215 recombination Methods 0.000 description 3
- 230000006798 recombination Effects 0.000 description 3
- 125000005504 styryl group Chemical group 0.000 description 3
- 229940042055 systemic antimycotics triazole derivative Drugs 0.000 description 3
- WLKQDOGZCIYEOM-UHFFFAOYSA-N (3-naphthalen-2-ylphenyl)boronic acid Chemical compound OB(O)C1=CC=CC(C=2C=C3C=CC=CC3=CC=2)=C1 WLKQDOGZCIYEOM-UHFFFAOYSA-N 0.000 description 2
- NGZGJCQVEUFTHA-UHFFFAOYSA-N (3-phenanthren-9-ylphenyl)boronic acid Chemical compound OB(O)C1=CC=CC(C=2C3=CC=CC=C3C3=CC=CC=C3C=2)=C1 NGZGJCQVEUFTHA-UHFFFAOYSA-N 0.000 description 2
- BRMXCUCHGKWTIO-UHFFFAOYSA-N (4-phenanthren-9-ylphenyl)boronic acid Chemical compound C1=CC(B(O)O)=CC=C1C1=CC2=CC=CC=C2C2=CC=CC=C12 BRMXCUCHGKWTIO-UHFFFAOYSA-N 0.000 description 2
- XPEIJWZLPWNNOK-UHFFFAOYSA-N (4-phenylphenyl)boronic acid Chemical compound C1=CC(B(O)O)=CC=C1C1=CC=CC=C1 XPEIJWZLPWNNOK-UHFFFAOYSA-N 0.000 description 2
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 2
- DPVIABCMTHHTGB-UHFFFAOYSA-N 2,4,6-trichloropyrimidine Chemical compound ClC1=CC(Cl)=NC(Cl)=N1 DPVIABCMTHHTGB-UHFFFAOYSA-N 0.000 description 2
- CHQBCAQLLVYFRU-UHFFFAOYSA-N 2-chloro-4-(3-naphthalen-1-ylphenyl)-6-(4-pyridin-3-ylphenyl)pyrimidine Chemical compound ClC1=NC(=CC(=N1)C1=CC(=CC=C1)C1=CC=CC2=CC=CC=C12)C1=CC=C(C=C1)C=1C=NC=CC=1 CHQBCAQLLVYFRU-UHFFFAOYSA-N 0.000 description 2
- SEKMGWFPINXSMX-UHFFFAOYSA-N 2-chloro-4-(3-naphthalen-2-ylphenyl)-6-(4-pyridin-3-ylphenyl)pyrimidine Chemical compound ClC1=NC(=CC(=N1)C1=CC(=CC=C1)C1=CC2=CC=CC=C2C=C1)C1=CC=C(C=C1)C=1C=NC=CC=1 SEKMGWFPINXSMX-UHFFFAOYSA-N 0.000 description 2
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 2
- UIBZWBDRPOXLIU-UHFFFAOYSA-N 4-(4-phenylphenyl)-6-(3-pyridin-3-ylphenyl)pyrimidine Chemical compound C1(=CC=C(C=C1)C1=NC=NC(=C1)C1=CC(=CC=C1)C=1C=NC=CC=1)C1=CC=CC=C1 UIBZWBDRPOXLIU-UHFFFAOYSA-N 0.000 description 2
- AWXGSYPUMWKTBR-UHFFFAOYSA-N 4-carbazol-9-yl-n,n-bis(4-carbazol-9-ylphenyl)aniline Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(N(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 AWXGSYPUMWKTBR-UHFFFAOYSA-N 0.000 description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- VFUDMQLBKNMONU-UHFFFAOYSA-N 9-[4-(4-carbazol-9-ylphenyl)phenyl]carbazole Chemical group C12=CC=CC=C2C2=CC=CC=C2N1C1=CC=C(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C=C1 VFUDMQLBKNMONU-UHFFFAOYSA-N 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- 101000837344 Homo sapiens T-cell leukemia translocation-altered gene protein Proteins 0.000 description 2
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 2
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 2
- 229920001609 Poly(3,4-ethylenedioxythiophene) Polymers 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- 102100028692 T-cell leukemia translocation-altered gene protein Human genes 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- 150000001454 anthracenes Chemical class 0.000 description 2
- 150000001543 aryl boronic acids Chemical class 0.000 description 2
- 150000001556 benzimidazoles Chemical class 0.000 description 2
- 125000000051 benzyloxy group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])O* 0.000 description 2
- XJHCXCQVJFPJIK-UHFFFAOYSA-M caesium fluoride Chemical compound [F-].[Cs+] XJHCXCQVJFPJIK-UHFFFAOYSA-M 0.000 description 2
- 150000001716 carbazoles Chemical class 0.000 description 2
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 238000004440 column chromatography Methods 0.000 description 2
- 239000012043 crude product Substances 0.000 description 2
- 238000002425 crystallisation Methods 0.000 description 2
- 230000008025 crystallization Effects 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 125000001072 heteroaryl group Chemical group 0.000 description 2
- 229910052740 iodine Inorganic materials 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 2
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 150000002894 organic compounds Chemical class 0.000 description 2
- 150000007978 oxazole derivatives Chemical class 0.000 description 2
- 150000005041 phenanthrolines Chemical class 0.000 description 2
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 2
- 229920001467 poly(styrenesulfonates) Polymers 0.000 description 2
- 239000002861 polymer material Substances 0.000 description 2
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 2
- 125000002572 propoxy group Chemical group [*]OC([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 2
- 238000001953 recrystallisation Methods 0.000 description 2
- 239000000741 silica gel Substances 0.000 description 2
- 229910002027 silica gel Inorganic materials 0.000 description 2
- 238000004528 spin coating Methods 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 150000003918 triazines Chemical class 0.000 description 2
- 239000013638 trimer Substances 0.000 description 2
- DETFWTCLAIIJRZ-UHFFFAOYSA-N triphenyl-(4-triphenylsilylphenyl)silane Chemical compound C1=CC=CC=C1[Si](C=1C=CC(=CC=1)[Si](C=1C=CC=CC=1)(C=1C=CC=CC=1)C=1C=CC=CC=1)(C=1C=CC=CC=1)C1=CC=CC=C1 DETFWTCLAIIJRZ-UHFFFAOYSA-N 0.000 description 2
- ODHXBMXNKOYIBV-UHFFFAOYSA-N triphenylamine Chemical compound C1=CC=CC=C1N(C=1C=CC=CC=1)C1=CC=CC=C1 ODHXBMXNKOYIBV-UHFFFAOYSA-N 0.000 description 2
- 238000001771 vacuum deposition Methods 0.000 description 2
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 2
- GOXICVKOZJFRMB-UHFFFAOYSA-N (3-phenylphenyl)boronic acid Chemical compound OB(O)C1=CC=CC(C=2C=CC=CC=2)=C1 GOXICVKOZJFRMB-UHFFFAOYSA-N 0.000 description 1
- ICQAKBYFBIWELX-UHFFFAOYSA-N (4-naphthalen-2-ylphenyl)boronic acid Chemical compound C1=CC(B(O)O)=CC=C1C1=CC=C(C=CC=C2)C2=C1 ICQAKBYFBIWELX-UHFFFAOYSA-N 0.000 description 1
- PXLYGWXKAVCTPX-UHFFFAOYSA-N 1,2,3,4,5,6-hexamethylidenecyclohexane Chemical class C=C1C(=C)C(=C)C(=C)C(=C)C1=C PXLYGWXKAVCTPX-UHFFFAOYSA-N 0.000 description 1
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 1
- KTADSLDAUJLZGL-UHFFFAOYSA-N 1-bromo-2-phenylbenzene Chemical group BrC1=CC=CC=C1C1=CC=CC=C1 KTADSLDAUJLZGL-UHFFFAOYSA-N 0.000 description 1
- XNCMQRWVMWLODV-UHFFFAOYSA-N 1-phenylbenzimidazole Chemical compound C1=NC2=CC=CC=C2N1C1=CC=CC=C1 XNCMQRWVMWLODV-UHFFFAOYSA-N 0.000 description 1
- ZABORCXHTNWZRV-UHFFFAOYSA-N 10-[4-(4,6-diphenyl-1,3,5-triazin-2-yl)phenyl]phenoxazine Chemical compound O1C2=CC=CC=C2N(C2=CC=C(C=C2)C2=NC(=NC(=N2)C2=CC=CC=C2)C2=CC=CC=C2)C2=C1C=CC=C2 ZABORCXHTNWZRV-UHFFFAOYSA-N 0.000 description 1
- IVCGJOSPVGENCT-UHFFFAOYSA-N 1h-pyrrolo[2,3-f]quinoline Chemical class N1=CC=CC2=C(NC=C3)C3=CC=C21 IVCGJOSPVGENCT-UHFFFAOYSA-N 0.000 description 1
- PRWATGACIORDEL-UHFFFAOYSA-N 2,4,5,6-tetra(carbazol-9-yl)benzene-1,3-dicarbonitrile Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=C(C#N)C(N2C3=CC=CC=C3C3=CC=CC=C32)=C(N2C3=CC=CC=C3C3=CC=CC=C32)C(N2C3=CC=CC=C3C3=CC=CC=C32)=C1C#N PRWATGACIORDEL-UHFFFAOYSA-N 0.000 description 1
- GIKMWFAAEIACRF-UHFFFAOYSA-N 2,4,5-trichloropyrimidine Chemical compound ClC1=NC=C(Cl)C(Cl)=N1 GIKMWFAAEIACRF-UHFFFAOYSA-N 0.000 description 1
- RIKNNBBGYSDYAX-UHFFFAOYSA-N 2-[1-[2-(4-methyl-n-(4-methylphenyl)anilino)phenyl]cyclohexyl]-n,n-bis(4-methylphenyl)aniline Chemical compound C1=CC(C)=CC=C1N(C=1C(=CC=CC=1)C1(CCCCC1)C=1C(=CC=CC=1)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)C1=CC=C(C)C=C1 RIKNNBBGYSDYAX-UHFFFAOYSA-N 0.000 description 1
- GEQBRULPNIVQPP-UHFFFAOYSA-N 2-[3,5-bis(1-phenylbenzimidazol-2-yl)phenyl]-1-phenylbenzimidazole Chemical compound C1=CC=CC=C1N1C2=CC=CC=C2N=C1C1=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=CC(C=2N(C3=CC=CC=C3N=2)C=2C=CC=CC=2)=C1 GEQBRULPNIVQPP-UHFFFAOYSA-N 0.000 description 1
- RKVIAZWOECXCCM-UHFFFAOYSA-N 2-carbazol-9-yl-n,n-diphenylaniline Chemical compound C1=CC=CC=C1N(C=1C(=CC=CC=1)N1C2=CC=CC=C2C2=CC=CC=C21)C1=CC=CC=C1 RKVIAZWOECXCCM-UHFFFAOYSA-N 0.000 description 1
- OFJOMJSMALNLCY-UHFFFAOYSA-N 2-chloro-4-(4-naphthalen-1-ylphenyl)-6-(3-pyridin-3-ylphenyl)pyrimidine Chemical compound ClC1=NC(=CC(=N1)C1=CC=C(C=C1)C1=CC=CC2=CC=CC=C12)C1=CC(=CC=C1)C=1C=NC=CC=1 OFJOMJSMALNLCY-UHFFFAOYSA-N 0.000 description 1
- OXTJLWGEPAQECS-UHFFFAOYSA-N 2-chloro-4-(4-naphthalen-2-ylphenyl)-6-(3-pyridin-3-ylphenyl)pyrimidine Chemical compound ClC1=NC(=CC(=N1)C1=CC=C(C=C1)C1=CC2=CC=CC=C2C=C1)C1=CC(=CC=C1)C=1C=NC=CC=1 OXTJLWGEPAQECS-UHFFFAOYSA-N 0.000 description 1
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 1
- VQGHOUODWALEFC-UHFFFAOYSA-N 2-phenylpyridine Chemical compound C1=CC=CC=C1C1=CC=CC=N1 VQGHOUODWALEFC-UHFFFAOYSA-N 0.000 description 1
- GOLORTLGFDVFDW-UHFFFAOYSA-N 3-(1h-benzimidazol-2-yl)-7-(diethylamino)chromen-2-one Chemical compound C1=CC=C2NC(C3=CC4=CC=C(C=C4OC3=O)N(CC)CC)=NC2=C1 GOLORTLGFDVFDW-UHFFFAOYSA-N 0.000 description 1
- YAADHARYAJYGGE-UHFFFAOYSA-N 3-[4-[2-chloro-6-(4-naphthalen-1-ylphenyl)pyrimidin-4-yl]phenyl]quinoline Chemical compound ClC1=NC(=CC(=N1)C1=CC=C(C=C1)C1=CC=CC2=CC=CC=C12)C1=CC=C(C=C1)C=1C=NC2=CC=CC=C2C=1 YAADHARYAJYGGE-UHFFFAOYSA-N 0.000 description 1
- OGGKVJMNFFSDEV-UHFFFAOYSA-N 3-methyl-n-[4-[4-(n-(3-methylphenyl)anilino)phenyl]phenyl]-n-phenylaniline Chemical compound CC1=CC=CC(N(C=2C=CC=CC=2)C=2C=CC(=CC=2)C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C=C(C)C=CC=2)=C1 OGGKVJMNFFSDEV-UHFFFAOYSA-N 0.000 description 1
- ZOKIJILZFXPFTO-UHFFFAOYSA-N 4-methyl-n-[4-[1-[4-(4-methyl-n-(4-methylphenyl)anilino)phenyl]cyclohexyl]phenyl]-n-(4-methylphenyl)aniline Chemical compound C1=CC(C)=CC=C1N(C=1C=CC(=CC=1)C1(CCCCC1)C=1C=CC(=CC=1)N(C=1C=CC(C)=CC=1)C=1C=CC(C)=CC=1)C1=CC=C(C)C=C1 ZOKIJILZFXPFTO-UHFFFAOYSA-N 0.000 description 1
- MZYDBGLUVPLRKR-UHFFFAOYSA-N 9-(3-carbazol-9-ylphenyl)carbazole Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C1=CC(N2C3=CC=CC=C3C3=CC=CC=C32)=CC=C1 MZYDBGLUVPLRKR-UHFFFAOYSA-N 0.000 description 1
- FOUNKDBOYUMWNP-UHFFFAOYSA-N 9-[4-[2-(4-carbazol-9-ylphenyl)-2-adamantyl]phenyl]carbazole Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C(C=C1)=CC=C1C1(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C(C2)CC3CC1CC2C3 FOUNKDBOYUMWNP-UHFFFAOYSA-N 0.000 description 1
- GFEWJHOBOWFNRV-UHFFFAOYSA-N 9-[4-[9-(4-carbazol-9-ylphenyl)fluoren-9-yl]phenyl]carbazole Chemical compound C12=CC=CC=C2C2=CC=CC=C2N1C(C=C1)=CC=C1C1(C=2C=CC(=CC=2)N2C3=CC=CC=C3C3=CC=CC=C32)C2=CC=CC=C2C2=CC=CC=C12 GFEWJHOBOWFNRV-UHFFFAOYSA-N 0.000 description 1
- 229910001316 Ag alloy Inorganic materials 0.000 description 1
- LSIOUZPMMPIAOL-UHFFFAOYSA-N C(C1)C=Cc2c1c1ccccc1c(cc1)c2cc1-c1cc(-c2nc(-c(cc3)ccc3C3=CC=CNC3)cc(C(CC3)=CC=C3c3ccccc3)n2)ccc1 Chemical compound C(C1)C=Cc2c1c1ccccc1c(cc1)c2cc1-c1cc(-c2nc(-c(cc3)ccc3C3=CC=CNC3)cc(C(CC3)=CC=C3c3ccccc3)n2)ccc1 LSIOUZPMMPIAOL-UHFFFAOYSA-N 0.000 description 1
- CJWOBMPFLPUEFE-UHFFFAOYSA-N C1C=CC(c2ccccc2)=CC1c1nc(-c2cc3c(cccc4)c4c(cccc4)c4c3cc2)nc(-c2cc(-c3cccnc3)ccc2)c1 Chemical compound C1C=CC(c2ccccc2)=CC1c1nc(-c2cc3c(cccc4)c4c(cccc4)c4c3cc2)nc(-c2cc(-c3cccnc3)ccc2)c1 CJWOBMPFLPUEFE-UHFFFAOYSA-N 0.000 description 1
- NDBZMJJJGWLRJF-WCKQMBFRSA-N C=C(c(cc1)ccc1-c1cccc2c1cccc2)/N=C(\C=C(\c(cc1)ccc1-c1cncc2c1cccc2)/N)/c(cc1)ccc1-c1c(cccc2)c2c(cccc2)c2c1 Chemical compound C=C(c(cc1)ccc1-c1cccc2c1cccc2)/N=C(\C=C(\c(cc1)ccc1-c1cncc2c1cccc2)/N)/c(cc1)ccc1-c1c(cccc2)c2c(cccc2)c2c1 NDBZMJJJGWLRJF-WCKQMBFRSA-N 0.000 description 1
- IYLNGUSHZUMGRE-UHFFFAOYSA-N CC(C1c2cc(-c3nc(-c(cc4)ccc4-c4cc5c(cccc6)c6c(cccc6)c6c5cc4)nc(-c(cc4)ccc4-c4cnccc4)c3)ccc2)C=Cc2c1cccc2 Chemical compound CC(C1c2cc(-c3nc(-c(cc4)ccc4-c4cc5c(cccc6)c6c(cccc6)c6c5cc4)nc(-c(cc4)ccc4-c4cnccc4)c3)ccc2)C=Cc2c1cccc2 IYLNGUSHZUMGRE-UHFFFAOYSA-N 0.000 description 1
- DULTWHHLLXVSFF-UHFFFAOYSA-N CC1(C=CC(c2cc(C(CC3)=CC=C3c3ccccc3)nc(-c(cc3)ccc3-c3cc4ccccc4cc3)n2)=CC1)c1cncc2c1cccc2 Chemical compound CC1(C=CC(c2cc(C(CC3)=CC=C3c3ccccc3)nc(-c(cc3)ccc3-c3cc4ccccc4cc3)n2)=CC1)c1cncc2c1cccc2 DULTWHHLLXVSFF-UHFFFAOYSA-N 0.000 description 1
- QXDGBAOHTLLEFO-XPXRSFDGSA-N CC1(C=CC=CC1C12c3ccccc3C(C)=C1/C=C(\C)/c1nc(-c3cccc4c3cccc4)nc(-c3cccc(-c4cnccc4)c3)c1)c1c2cccc1 Chemical compound CC1(C=CC=CC1C12c3ccccc3C(C)=C1/C=C(\C)/c1nc(-c3cccc4c3cccc4)nc(-c3cccc(-c4cnccc4)c3)c1)c1c2cccc1 QXDGBAOHTLLEFO-XPXRSFDGSA-N 0.000 description 1
- KTBVTHHUATWANI-UHFFFAOYSA-N CC1c2ccccc2N=CC1c(cc1)ccc1-c1cc(-c(cc2)ccc2-c2c(cccc3)c3ccc2)nc(-c(cc2)ccc2-c2cc(cccc3)c3c3c2cccc3)n1 Chemical compound CC1c2ccccc2N=CC1c(cc1)ccc1-c1cc(-c(cc2)ccc2-c2c(cccc3)c3ccc2)nc(-c(cc2)ccc2-c2cc(cccc3)c3c3c2cccc3)n1 KTBVTHHUATWANI-UHFFFAOYSA-N 0.000 description 1
- 101100042788 Caenorhabditis elegans him-1 gene Proteins 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical class [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 241000284156 Clerodendrum quadriloculare Species 0.000 description 1
- 229910000846 In alloy Inorganic materials 0.000 description 1
- 229910000861 Mg alloy Inorganic materials 0.000 description 1
- CBENFWSGALASAD-UHFFFAOYSA-N Ozone Chemical compound [O-][O+]=O CBENFWSGALASAD-UHFFFAOYSA-N 0.000 description 1
- NRCMAYZCPIVABH-UHFFFAOYSA-N Quinacridone Chemical compound N1C2=CC=CC=C2C(=O)C2=C1C=C1C(=O)C3=CC=CC=C3NC1=C2 NRCMAYZCPIVABH-UHFFFAOYSA-N 0.000 description 1
- FUHDUDFIRJUPIV-UHFFFAOYSA-N [4-[9-(4-carbazol-9-ylphenyl)fluoren-9-yl]phenyl]-triphenylsilane Chemical compound C1=CC=CC=C1[Si](C=1C=CC(=CC=1)C1(C2=CC=CC=C2C2=CC=CC=C21)C=1C=CC(=CC=1)N1C2=CC=CC=C2C2=CC=CC=C21)(C=1C=CC=CC=1)C1=CC=CC=C1 FUHDUDFIRJUPIV-UHFFFAOYSA-N 0.000 description 1
- JZXXUZWBECTQIC-UHFFFAOYSA-N [Li].C1=CC=CC2=NC(O)=CC=C21 Chemical compound [Li].C1=CC=CC2=NC(O)=CC=C21 JZXXUZWBECTQIC-UHFFFAOYSA-N 0.000 description 1
- JHYLKGDXMUDNEO-UHFFFAOYSA-N [Mg].[In] Chemical compound [Mg].[In] JHYLKGDXMUDNEO-UHFFFAOYSA-N 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- CUJRVFIICFDLGR-UHFFFAOYSA-N acetylacetonate Chemical compound CC(=O)[CH-]C(C)=O CUJRVFIICFDLGR-UHFFFAOYSA-N 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 229910045601 alloy Inorganic materials 0.000 description 1
- 239000000956 alloy Substances 0.000 description 1
- REDXJYDRNCIFBQ-UHFFFAOYSA-N aluminium(3+) Chemical compound [Al+3] REDXJYDRNCIFBQ-UHFFFAOYSA-N 0.000 description 1
- SNAAJJQQZSMGQD-UHFFFAOYSA-N aluminum magnesium Chemical compound [Mg].[Al] SNAAJJQQZSMGQD-UHFFFAOYSA-N 0.000 description 1
- 229940058303 antinematodal benzimidazole derivative Drugs 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 150000001562 benzopyrans Chemical class 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- XZDLZXKMEXNSGQ-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)ccc1-c(nc(-c1cccc2c1cccc2)nc1)c1-c1cc(-c2cccnc2)ccc1 Chemical compound c(cc1)ccc1-c(cc1)ccc1-c(nc(-c1cccc2c1cccc2)nc1)c1-c1cc(-c2cccnc2)ccc1 XZDLZXKMEXNSGQ-UHFFFAOYSA-N 0.000 description 1
- JXZYZGLPNBIISK-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)ccc1-c1nc(-c(cc2)ccc2-c2cc3ccccc3c3ccccc23)nc(-c(cc2)ccc2-c2cnccc2)c1 Chemical compound c(cc1)ccc1-c(cc1)ccc1-c1nc(-c(cc2)ccc2-c2cc3ccccc3c3ccccc23)nc(-c(cc2)ccc2-c2cnccc2)c1 JXZYZGLPNBIISK-UHFFFAOYSA-N 0.000 description 1
- GSMOSRONCBXFAI-UHFFFAOYSA-N c(cc1)ccc1-c(nc1)nc(-c(cc2)ccc2-c2cccc3c2cccc3)c1-c1cc(-c2cccnc2)ccc1 Chemical compound c(cc1)ccc1-c(nc1)nc(-c(cc2)ccc2-c2cccc3c2cccc3)c1-c1cc(-c2cccnc2)ccc1 GSMOSRONCBXFAI-UHFFFAOYSA-N 0.000 description 1
- FQSLURBJBKBAQY-UHFFFAOYSA-N c(cc1)ccc1-c1cccc(-c2nc(-c(cc3)ccc3-c3cc4c(cccc5)c5c(cccc5)c5c4cc3)nc(-c(cc3)ccc3-c3cnccc3)c2)c1 Chemical compound c(cc1)ccc1-c1cccc(-c2nc(-c(cc3)ccc3-c3cc4c(cccc5)c5c(cccc5)c5c4cc3)nc(-c(cc3)ccc3-c3cnccc3)c2)c1 FQSLURBJBKBAQY-UHFFFAOYSA-N 0.000 description 1
- VDARUUOFQBGJHA-UHFFFAOYSA-N c(cc1)ccc1-c1cccc(-c2nc(-c3cccc(-c4cc(cccc5)c5c5ccccc45)c3)nc(-c(cc3)ccc3-c3cncc4c3cccc4)c2)c1 Chemical compound c(cc1)ccc1-c1cccc(-c2nc(-c3cccc(-c4cc(cccc5)c5c5ccccc45)c3)nc(-c(cc3)ccc3-c3cncc4c3cccc4)c2)c1 VDARUUOFQBGJHA-UHFFFAOYSA-N 0.000 description 1
- BLCGORMAQVKVAR-UHFFFAOYSA-N c1cc2c(cccc3)c3c(cc(cc3)-c(nc4)nc(-c5cccc(-c6ccccc6)c5)c4-c4cc(-c5cnccc5)ccc4)c3c2cc1 Chemical compound c1cc2c(cccc3)c3c(cc(cc3)-c(nc4)nc(-c5cccc(-c6ccccc6)c5)c4-c4cc(-c5cnccc5)ccc4)c3c2cc1 BLCGORMAQVKVAR-UHFFFAOYSA-N 0.000 description 1
- ZKMIBUOGAVHJBO-UHFFFAOYSA-N c1ccc(cc(cc2)-c3nc(-c4cc(-c5cccnc5)ccc4)cc(-c(cc4)ccc4-c4cccc5c4cccc5)n3)c2c1 Chemical compound c1ccc(cc(cc2)-c3nc(-c4cc(-c5cccnc5)ccc4)cc(-c(cc4)ccc4-c4cccc5c4cccc5)n3)c2c1 ZKMIBUOGAVHJBO-UHFFFAOYSA-N 0.000 description 1
- UHOVQNZJYSORNB-UHFFFAOYSA-N c1ccccc1 Chemical compound c1ccccc1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 1
- 229910052792 caesium Inorganic materials 0.000 description 1
- TVFDJXOCXUVLDH-UHFFFAOYSA-N caesium atom Chemical compound [Cs] TVFDJXOCXUVLDH-UHFFFAOYSA-N 0.000 description 1
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 1
- 150000001718 carbodiimides Chemical class 0.000 description 1
- 239000004927 clay Substances 0.000 description 1
- 150000004696 coordination complex Chemical class 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 239000003480 eluent Substances 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- RBTKNAXYKSUFRK-UHFFFAOYSA-N heliogen blue Chemical compound [Cu].[N-]1C2=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=NC([N-]1)=C(C=CC=C3)C3=C1N=C([N-]1)C3=CC=CC=C3C1=N2 RBTKNAXYKSUFRK-UHFFFAOYSA-N 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- 150000002391 heterocyclic compounds Chemical class 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 229910052741 iridium Inorganic materials 0.000 description 1
- GKOZUEZYRPOHIO-UHFFFAOYSA-N iridium atom Chemical compound [Ir] GKOZUEZYRPOHIO-UHFFFAOYSA-N 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000004491 isohexyl group Chemical group C(CCC(C)C)* 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000010030 laminating Methods 0.000 description 1
- 239000003446 ligand Substances 0.000 description 1
- 238000012538 light obscuration Methods 0.000 description 1
- 239000004973 liquid crystal related substance Substances 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- ORUIBWPALBXDOA-UHFFFAOYSA-L magnesium fluoride Chemical compound [F-].[F-].[Mg+2] ORUIBWPALBXDOA-UHFFFAOYSA-L 0.000 description 1
- 229910001635 magnesium fluoride Inorganic materials 0.000 description 1
- SJCKRGFTWFGHGZ-UHFFFAOYSA-N magnesium silver Chemical compound [Mg].[Ag] SJCKRGFTWFGHGZ-UHFFFAOYSA-N 0.000 description 1
- 229910044991 metal oxide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- IBHBKWKFFTZAHE-UHFFFAOYSA-N n-[4-[4-(n-naphthalen-1-ylanilino)phenyl]phenyl]-n-phenylnaphthalen-1-amine Chemical compound C1=CC=CC=C1N(C=1C2=CC=CC=C2C=CC=1)C1=CC=C(C=2C=CC(=CC=2)N(C=2C=CC=CC=2)C=2C3=CC=CC=C3C=CC=2)C=C1 IBHBKWKFFTZAHE-UHFFFAOYSA-N 0.000 description 1
- VMFMUJZRXZXYAH-UHFFFAOYSA-N n-[5-[[5-chloro-4-[2-[2-(dimethylamino)-2-oxoacetyl]anilino]pyrimidin-2-yl]amino]-4-methoxy-2-(4-methylpiperazin-1-yl)phenyl]prop-2-enamide Chemical compound C=CC(=O)NC=1C=C(NC=2N=C(NC=3C(=CC=CC=3)C(=O)C(=O)N(C)C)C(Cl)=CN=2)C(OC)=CC=1N1CCN(C)CC1 VMFMUJZRXZXYAH-UHFFFAOYSA-N 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000004433 nitrogen atom Chemical group N* 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- 150000004866 oxadiazoles Chemical class 0.000 description 1
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical compound O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- CSHWQDPOILHKBI-UHFFFAOYSA-N peryrene Natural products C1=CC(C2=CC=CC=3C2=C2C=CC=3)=C3C2=CC=CC3=C1 CSHWQDPOILHKBI-UHFFFAOYSA-N 0.000 description 1
- YNPNZTXNASCQKK-UHFFFAOYSA-N phenanthrene Chemical compound C1=CC=C2C3=CC=CC=C3C=CC2=C1 YNPNZTXNASCQKK-UHFFFAOYSA-N 0.000 description 1
- XEXYATIPBLUGSF-UHFFFAOYSA-N phenanthro[9,10-b]pyridine-2,3,4,5,6,7-hexacarbonitrile Chemical group N1=C(C#N)C(C#N)=C(C#N)C2=C(C(C#N)=C(C(C#N)=C3)C#N)C3=C(C=CC=C3)C3=C21 XEXYATIPBLUGSF-UHFFFAOYSA-N 0.000 description 1
- 125000001791 phenazinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3N=C12)* 0.000 description 1
- 125000001484 phenothiazinyl group Chemical group C1(=CC=CC=2SC3=CC=CC=C3NC12)* 0.000 description 1
- 125000001644 phenoxazinyl group Chemical group C1(=CC=CC=2OC3=CC=CC=C3NC12)* 0.000 description 1
- 229910052697 platinum Inorganic materials 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229910000027 potassium carbonate Inorganic materials 0.000 description 1
- 150000003220 pyrenes Chemical class 0.000 description 1
- 150000003222 pyridines Chemical class 0.000 description 1
- 238000000197 pyrolysis Methods 0.000 description 1
- 125000004548 quinolin-3-yl group Chemical group N1=CC(=CC2=CC=CC=C12)* 0.000 description 1
- 229910052761 rare earth metal Inorganic materials 0.000 description 1
- 150000002910 rare earth metals Chemical class 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- PYWVYCXTNDRMGF-UHFFFAOYSA-N rhodamine B Chemical class [Cl-].C=12C=CC(=[N+](CC)CC)C=C2OC2=CC(N(CC)CC)=CC=C2C=1C1=CC=CC=C1C(O)=O PYWVYCXTNDRMGF-UHFFFAOYSA-N 0.000 description 1
- YYMBJDOZVAITBP-UHFFFAOYSA-N rubrene Chemical compound C1=CC=CC=C1C(C1=C(C=2C=CC=CC=2)C2=CC=CC=C2C(C=2C=CC=CC=2)=C11)=C(C=CC=C2)C2=C1C1=CC=CC=C1 YYMBJDOZVAITBP-UHFFFAOYSA-N 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 150000003967 siloles Chemical class 0.000 description 1
- 239000002356 single layer Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 238000000859 sublimation Methods 0.000 description 1
- 230000008022 sublimation Effects 0.000 description 1
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000004867 thiadiazoles Chemical class 0.000 description 1
- 150000007979 thiazole derivatives Chemical class 0.000 description 1
- TVIVIEFSHFOWTE-UHFFFAOYSA-K tri(quinolin-8-yloxy)alumane Chemical compound [Al+3].C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1.C1=CN=C2C([O-])=CC=CC2=C1 TVIVIEFSHFOWTE-UHFFFAOYSA-K 0.000 description 1
- 125000005259 triarylamine group Chemical group 0.000 description 1
- 150000001651 triphenylamine derivatives Chemical class 0.000 description 1
- 125000006617 triphenylamine group Chemical group 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H01L51/0067—
-
- H01L51/5012—
-
- H01L51/5072—
-
- H01L51/5092—
-
- H01L51/5096—
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/16—Electron transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
- H10K50/171—Electron injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/624—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing six or more rings
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/626—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing more than one polycyclic condensed aromatic rings, e.g. bis-anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/18—Carrier blocking layers
Abstract
본 발명에 의하면, 아래 나타낸 일반식 (1) 로 표시되는 피리미딘 유도체, 및 한 쌍의 전극, 및 한 쌍의 전극 사이에 끼워진 적어도 하나의 유기 층을 포함하는 유기 전계발광 소자로서, 피리미딘 유도체가 적어도 하나의 유기 층의 구성 재료로서 사용되는 유기 전계발광 소자가 제공된다. 본 발명의 피리미딘 유도체는 고효율, 고내구성 유기 전계발광 소자용 재료로서, 전자 주입/수송 성능이 우수하고 정공 저지 능력이 우수한 특성을 갖는다.
Description
본 발명은 유기 전계발광 소자에 적합한 화합물, 및 소자에 관한 것이다. 더욱 구체적으로, 본 발명은 피리미딘 유도체, 및 상기 유도체를 이용한 유기 전계발광 소자 (이하 유기 EL 소자로 약칭) 에 관한 것이다.
유기 EL 소자는 자기 발광 소자이므로, 액정 소자보다 밝고, 시인성이 뛰어나고, 선명한 표시가 가능하다. 따라서, 유기 EL 소자에 대한 활발한 연구가 이루어져 왔다.
1987 년에, 이스트만 코닥 사의 C. W. Tang 들은 다양한 역할을 상이한 재료에 분담한 적층 구조 소자를 개발함으로써, 유기 재료를 이용한 유기 EL 소자에 실용성을 부여했다. 그들은 전자를 수송할 수 있는 형광체의 층과, 정공을 수송할 수 있는 유기물의 층을 적층했다. 전자 및 정공의 전하를 형광체 층에 주입하여 발광시킴으로써, 소자가 10V 이하의 전압에서 1,000 cd/m2 이상의 고휘도를 얻을 수 있었다 (특허 문헌 1 및 특허 문헌 2 참조).
유기 EL 소자의 실용화를 위해 많은 개선이 이루어져 왔다. 예를 들어, 다양한 역할을 더 많은 유형의 재료에 분담하고, 기판 상에 순차적으로 제공된 양극, 정공 주입층, 정공 수송층, 발광층, 전자 수송층, 전자 주입층, 및 음극을 갖는 전계 발광 소자에 의해 고효율 및 내구성이 달성되고 있다.
발광 효율의 추가의 향상을 목적으로, 삼중항 여기자의 이용이 시도되었고, 인광성 발광 화합물의 이용이 검토되었다. 더욱이, 열 활성화 지연 형광 (TADF) 에 의한 발광을 이용하는 소자도 개발되었다. 열 활성화 지연 형광 재료를 이용한 소자에 의해 5.3 % 의 외부 양자 효율이 실현되었다.
발광층은 일반적으로 호스트 재료로 불리는 전하 수송성 화합물에 형광 화합물, 인광성 발광 화합물, 또는 지연 형광을 방출하는 재료를 도핑하여 제작할 수 있다. 유기 EL 소자의 유기 재료의 선택은 소자의 효율 및 내구성 등의 특성에 큰 영향을 미친다.
유기 EL 소자는 양쪽 전극에서 주입된 전하가 발광층에서 재결합하여 발광을 얻을 수 있지만, 정공 및 전자의 전하를 얼마나 효율적으로 발광층에 전달할 수 있는가가 중요하다. 전자 주입성을 높이고, 전자 이동성을 크게 하여 정공과 전자가 재결합하는 확률을 향상시킨다. 나아가서는, 발광층에서 생성된 여기자를 가둔다. 그렇게 함으로써, 높은 발광 효율을 얻을 수 있다. 따라서, 전자 수송 재료의 역할은 중요하며, 전자 주입성이 높고, 전자 이동성이 크고, 정공 저지성이 높고, 정공에 대한 내구성이 높은 전자 수송 재료가 요구되고 있다.
소자 수명의 관점에서, 재료의 내열성이나 비정질성도 중요하다. 내열성이 낮은 재료로는 소자 구동시 발생하는 열에 의해 저온에서도 열분해가 일어나, 재료가 열화한다. 비정질성이 낮은 재료로는, 단시간이라도 박막의 결정화가 일어나, 소자가 열화한다. 따라서, 사용하는 재료는 내열성이 높고, 비정질성이 양호할 것이 요구된다.
대표적인 발광 재료인, 트리스(8-히드록시퀴놀린)알루미늄 (이하 Alq 로 약칭) 은 전자 수송 재료로서도 일반적으로 사용된다. 그러나, 정공 저지 성능은 불충분하다.
정공의 일부가 발광층을 통과하지 못하게 하고 발광층에서의 전하 재결합 확률을 향상시키는 방안으로는 정공 저지층을 삽입하는 방법이 있다. 정공 저지 재료로는, 예를 들어, 트리아졸 유도체 (특허 문헌 3 참조), 바소쿠프로인 (이하 BCP 로 약칭), 및 알루미늄 혼합 리간드 착물 [알루미늄 (III) 비스(2-메틸-8-퀴놀리나토)-4-페닐페놀레이트 (이하 BAlq 로 약칭) 등이 제안되었다.
또한 정공 저지성이 뛰어난 전자 수송 재료로서, 3-(4-비페닐일)-4-페닐-5-(4-t-부틸페닐)-1,2,4-트리아졸 (이하 TAZ 로 약칭) 이 제안되었다 (특허 문헌 4 참조).
TAZ 는 일 함수가 6.6eV 로 크고 정공 저지 능력이 높다. 따라서, TAZ 는 진공증착, 도포 등에 의해 제작된 형광 발광층 또는 인광성 발광층의 음극 측에 적층되어, 전자 수송성을 갖는 정공 저지층으로 사용된다. 따라서 TAZ 는 유기 EL 소자의 고효율화에 기여한다.
그러나, TAZ 는 전자 수송성이 낮다. 그러므로, TAZ 를 보다 전자 수송성이 높은 전자 수송 재료와 결합하여 유기 EL 소자를 제작하는 것이 필요했다.
또한 BCP 도 일 함수가 6.7 eV 로 크고 정공 저지 능력이 높다. 그러나, BCP 의 유리 전이점 (Tg) 이 83 ℃ 로 낮기 때문에 박막의 안정성이 부족하다.
즉, 위에서 언급한 재료들은 소자 수명이 부족하거나 또는 정공을 저지하는 기능이 부족하다. 따라서, 유기 EL 소자의 소자 특성을 개선하기 위해, 전자 주입/수송 성능과 정공 저지 능력이 뛰어난 소자 수명이 긴 유기 화합물이 요구되고 있다.
본 발명의 목적은 고효율, 고내구성의 유기 EL 소자용 재료로서, 전자 주입/수송 성능이 우수하고 정공 저지 능력이 우수한 특성을 가지는 유기 화합물을 제공하는 것이다.
본 발명의 다른 목적은 이 화합물을 이용하여 고효율, 고내구성, 및 장수명의 유기 EL 소자를 제공하는 것이다.
상기 목적을 달성하기 위해, 본 발명자들은 전자 친화력을 갖는 피리미딘 고리의 질소 원자가 금속에 배위할 능력을 가지고 있으며, 또한 내열성이 뛰어나다는 점에 주목했다. 이들 사실에 기초하여, 본 발명자들은 피리미딘 고리 구조를 갖는 화합물을 설계하고 화학적으로 합성했다. 또한, 상기 화합물을 이용하여 다양한 유기 EL 소자를 실험적으로 생산하여 소자의 특성 평가를 광범위하게 하였다. 그 결과, 본 발명자들은 본 발명을 완성하기에 이르렀다.
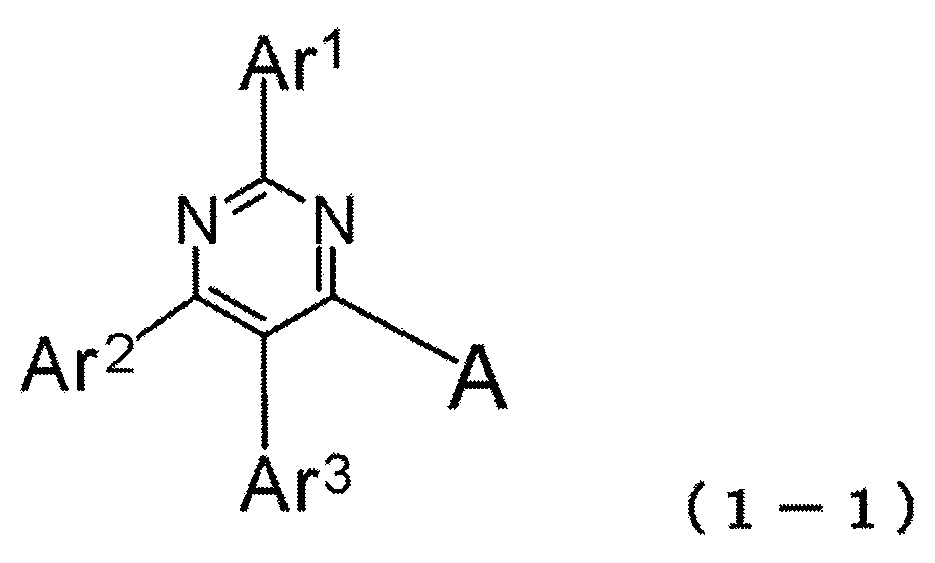
본 발명에 의하면, 하기 일반식 (1) 로 표시되는 피리미딘 유도체가 제공된다
식에서,
Ar1 은 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기를 나타내고,
Ar2 및 Ar3 은 동일 또는 상이할 수 있고, 각각 수소 원자, 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기를 나타내고,
Ar2 및 Ar3 이 동시에 수소 원자는 아니고,
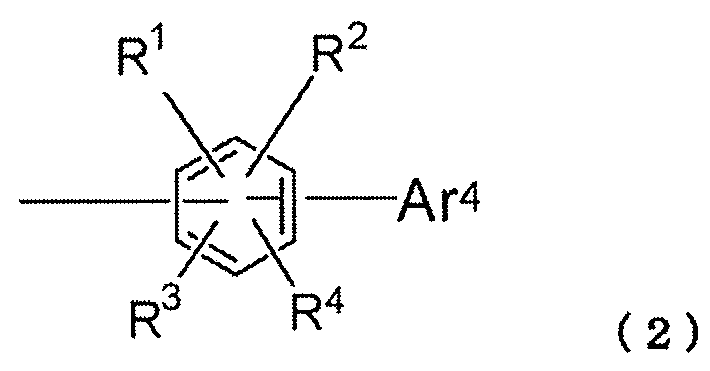
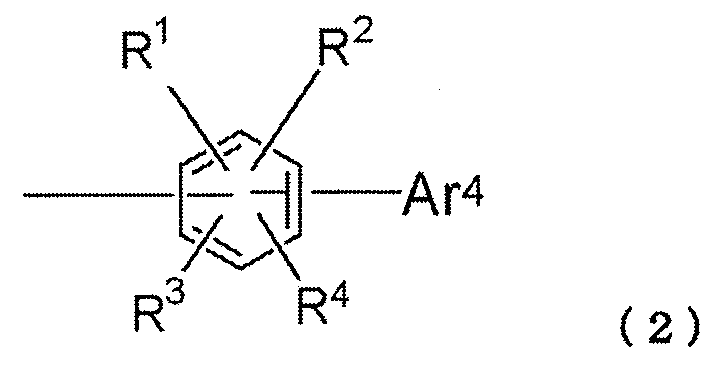
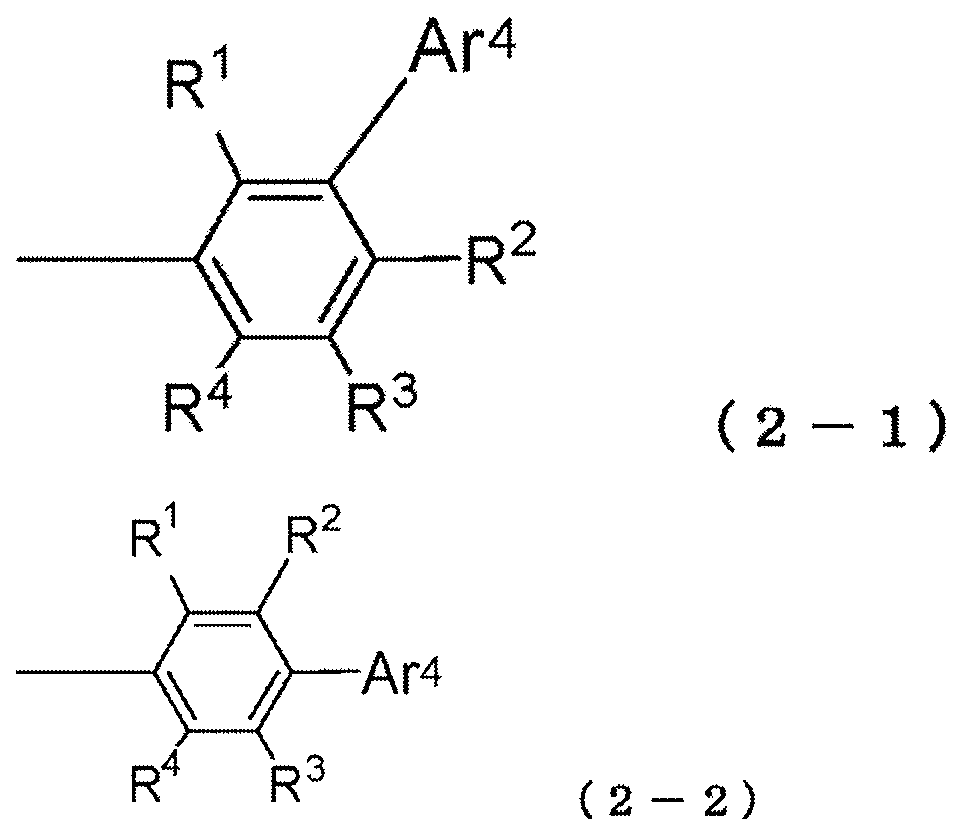
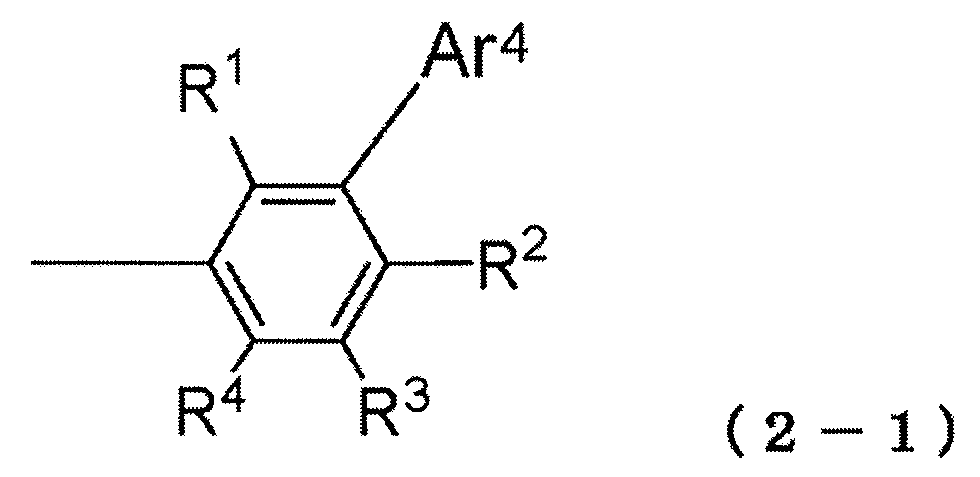
A 는 하기 구조식 (2) 로 표시되는 1 가 기를 나타내고,
식에서,
Ar4 는 방향족 헤테로고리 기를 나타내고,
R1 내지 R4 는 동일 또는 상이할 수 있고, 각각 수소 원자, 중수소 원자, 불소 원자, 염소 원자, 시아노 기, 트리플루오로메틸 기, 1 내지 6 개의 탄소 원자를 갖는 알킬 기, 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기를 나타내고,
R1 내지 R4 및 Ar4 는 단일 결합, 메틸렌 기, 산소 원자, 또는 황 원자를 통해 서로 결합하여 고리를 형성할 수 있다.
본 발명의 피리미딘 유도체에 있어서는, 하기가 바람직하다:
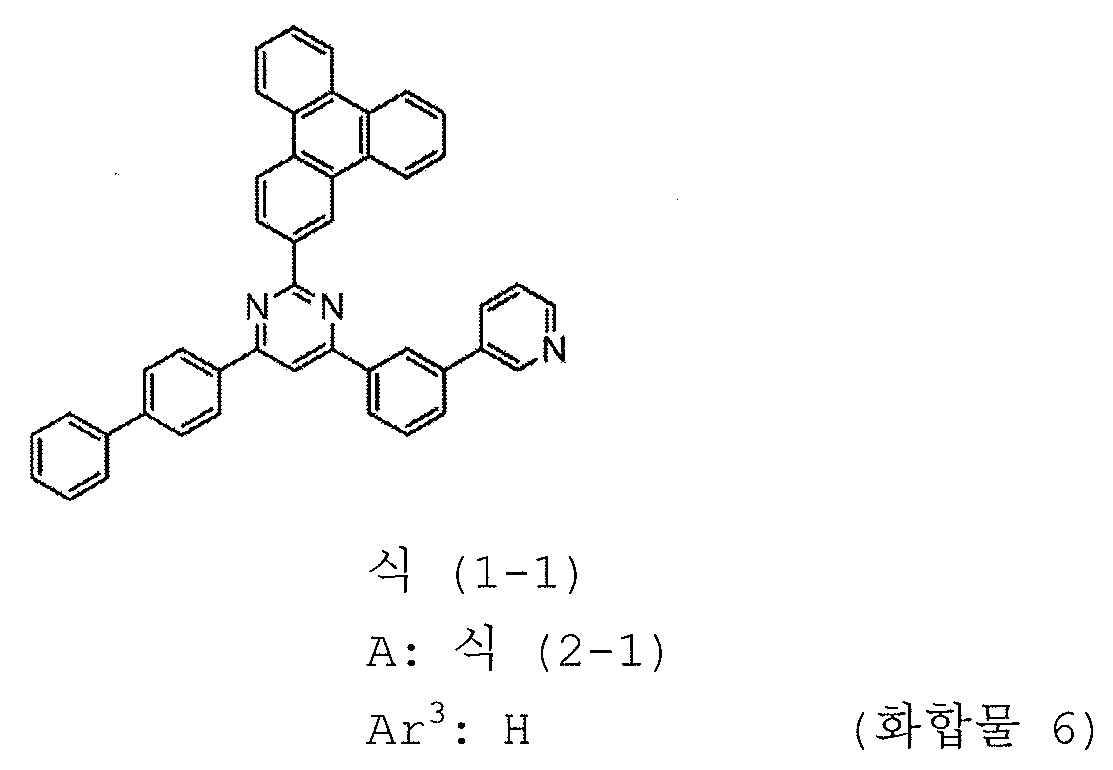
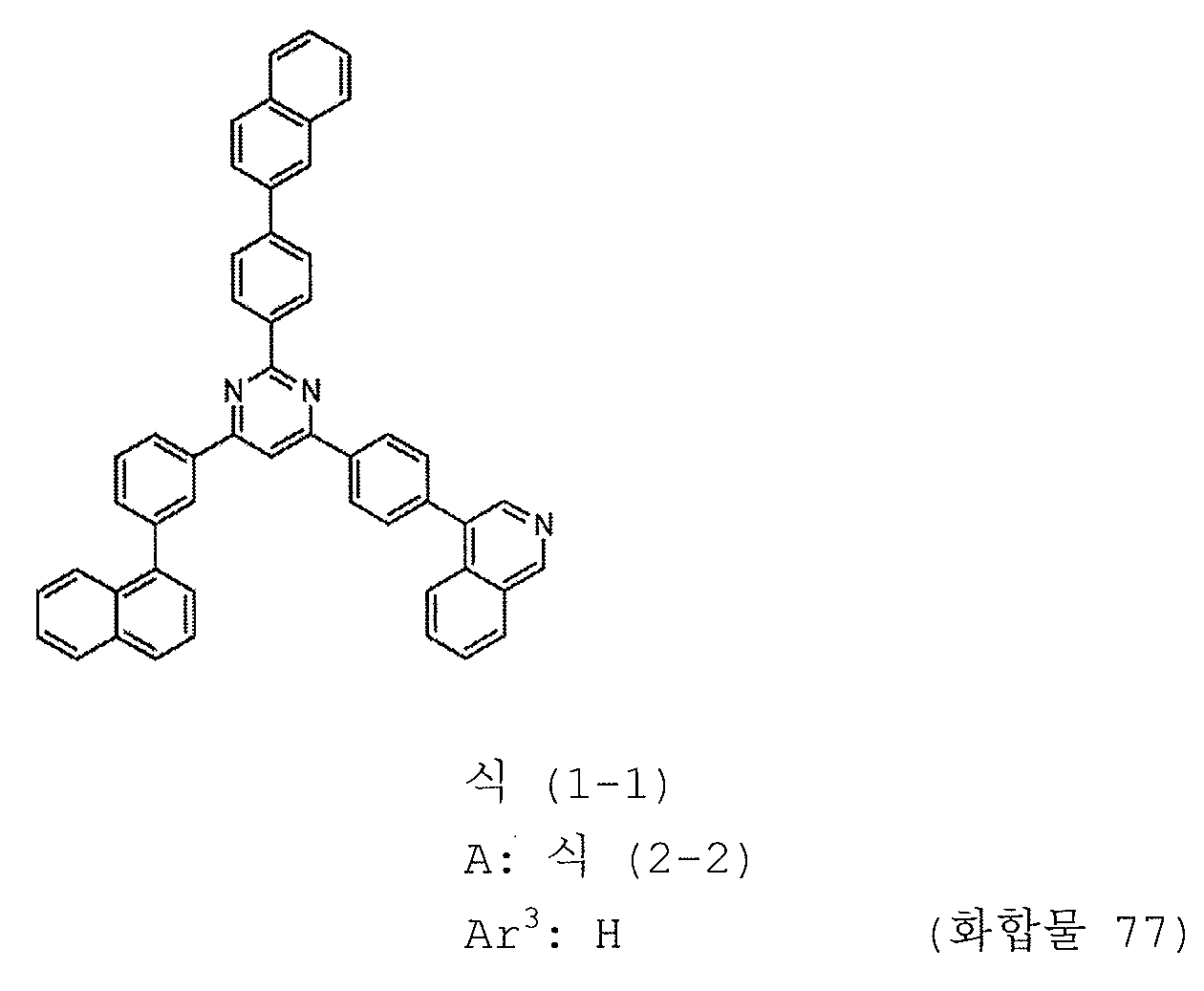
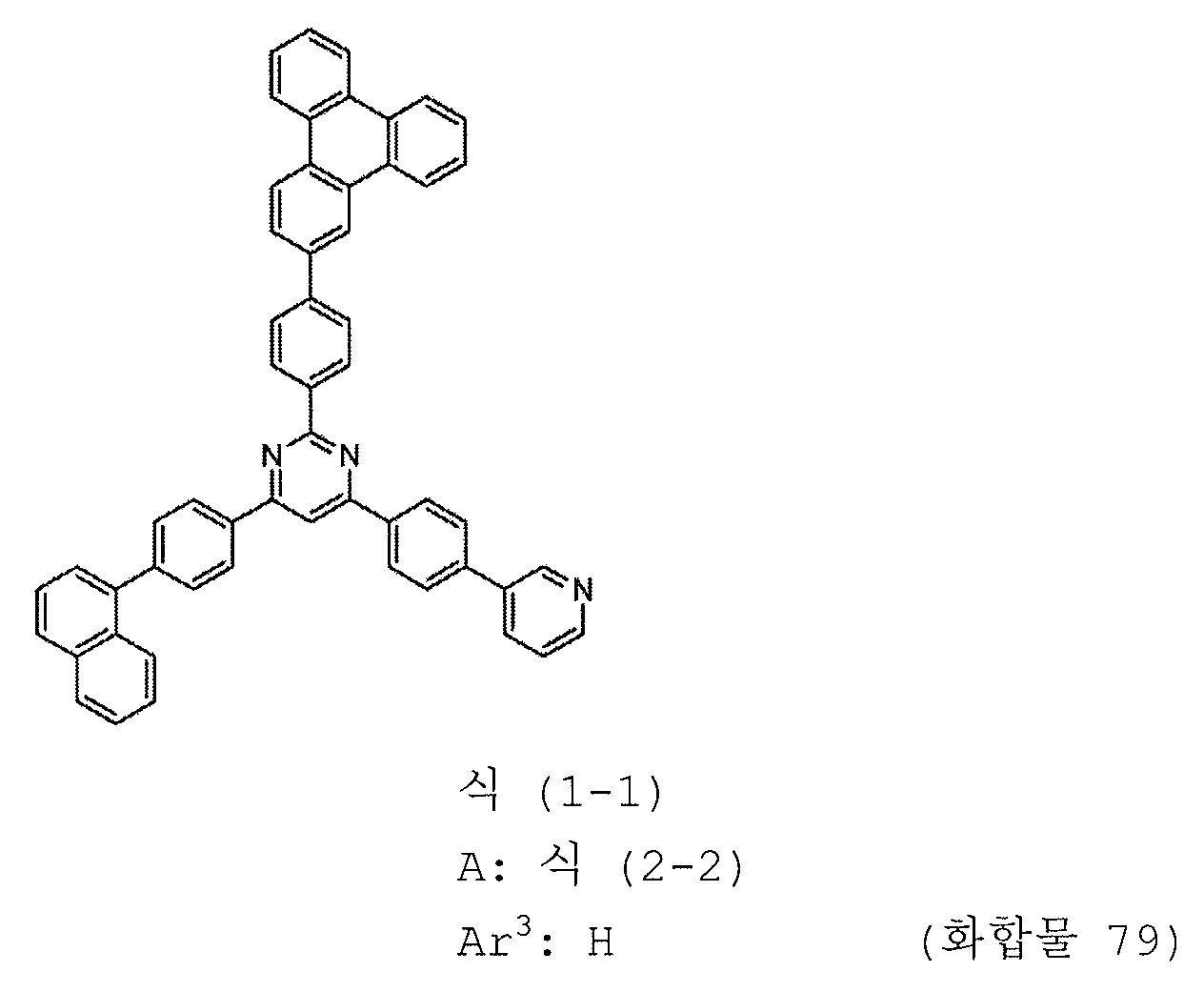
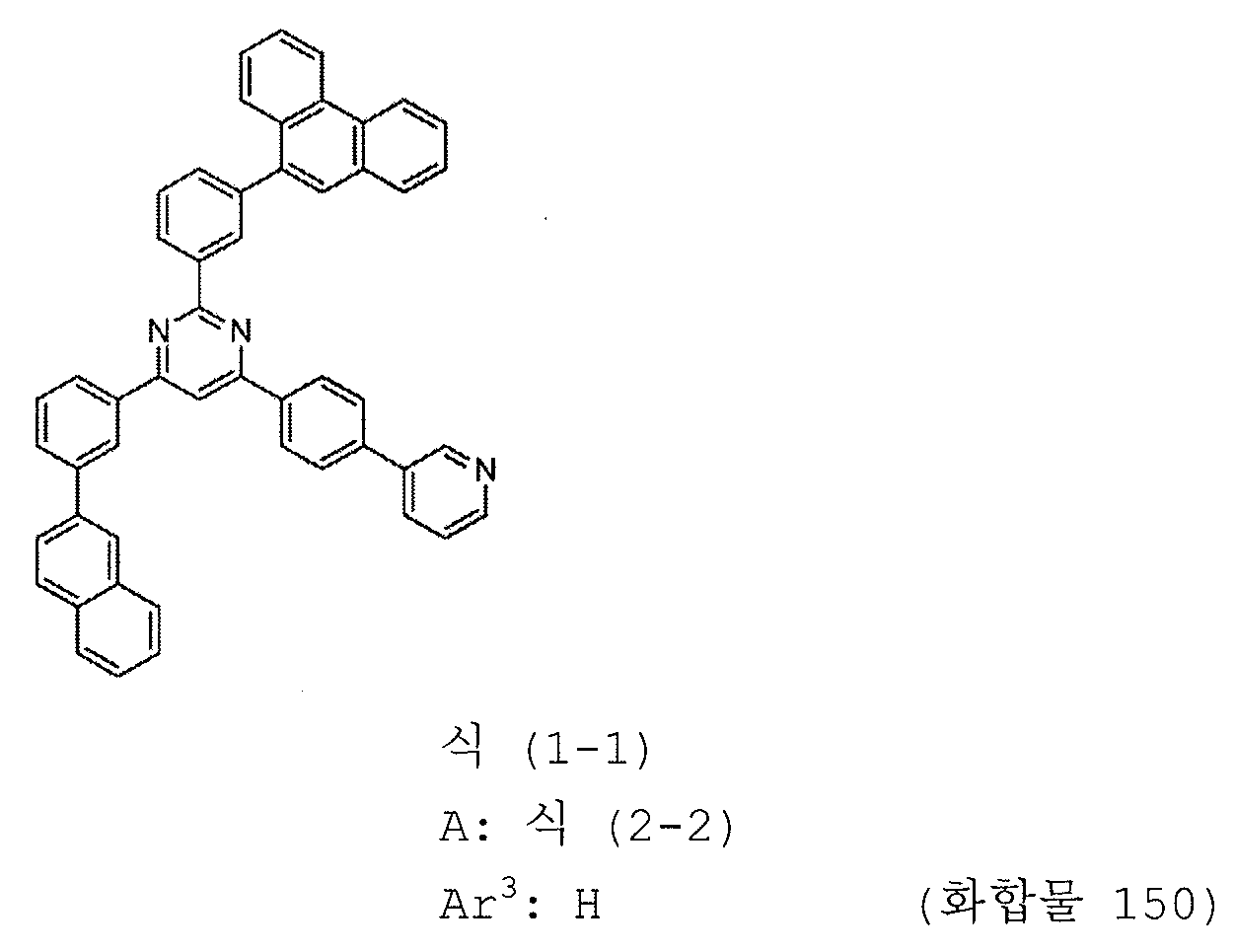
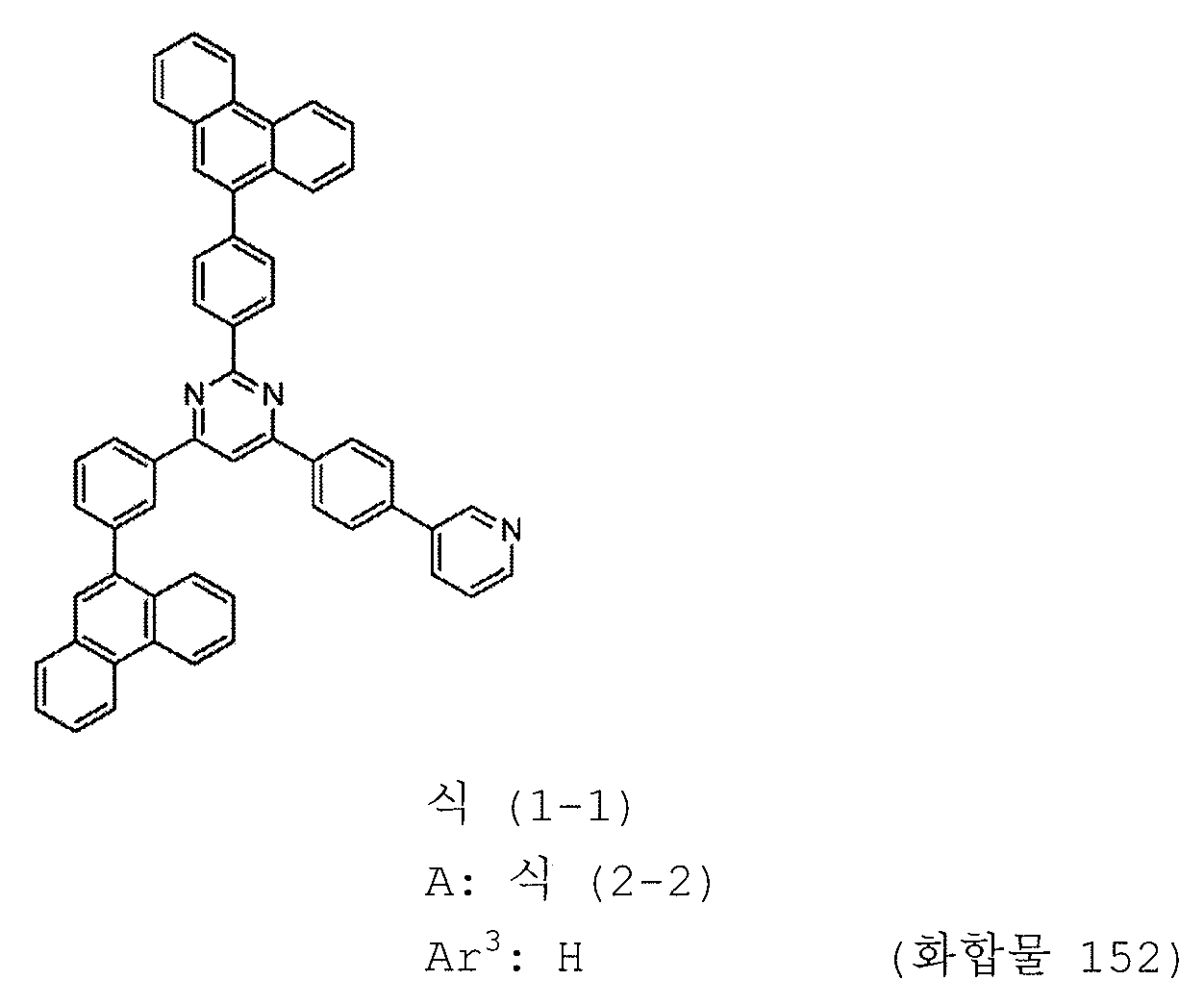
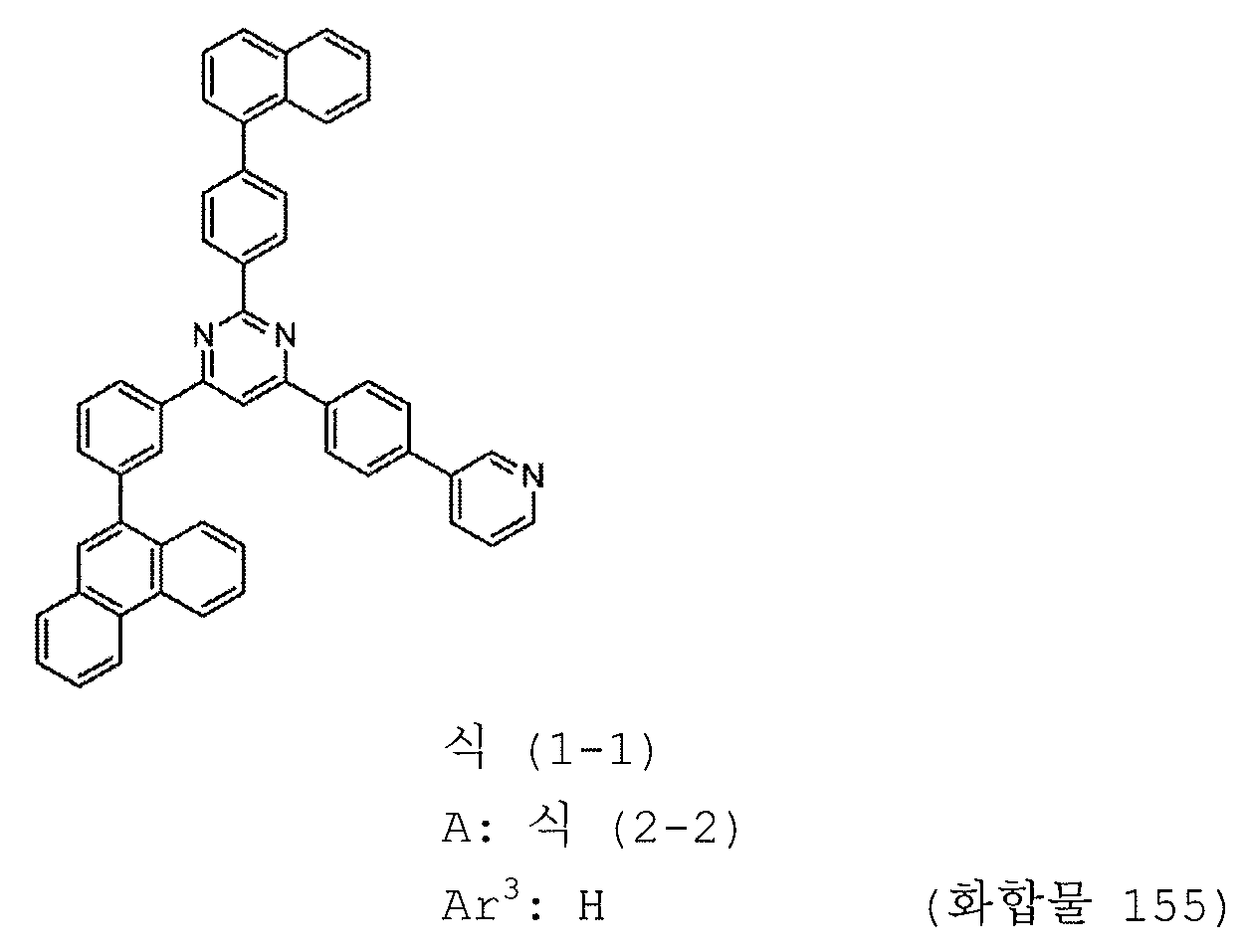
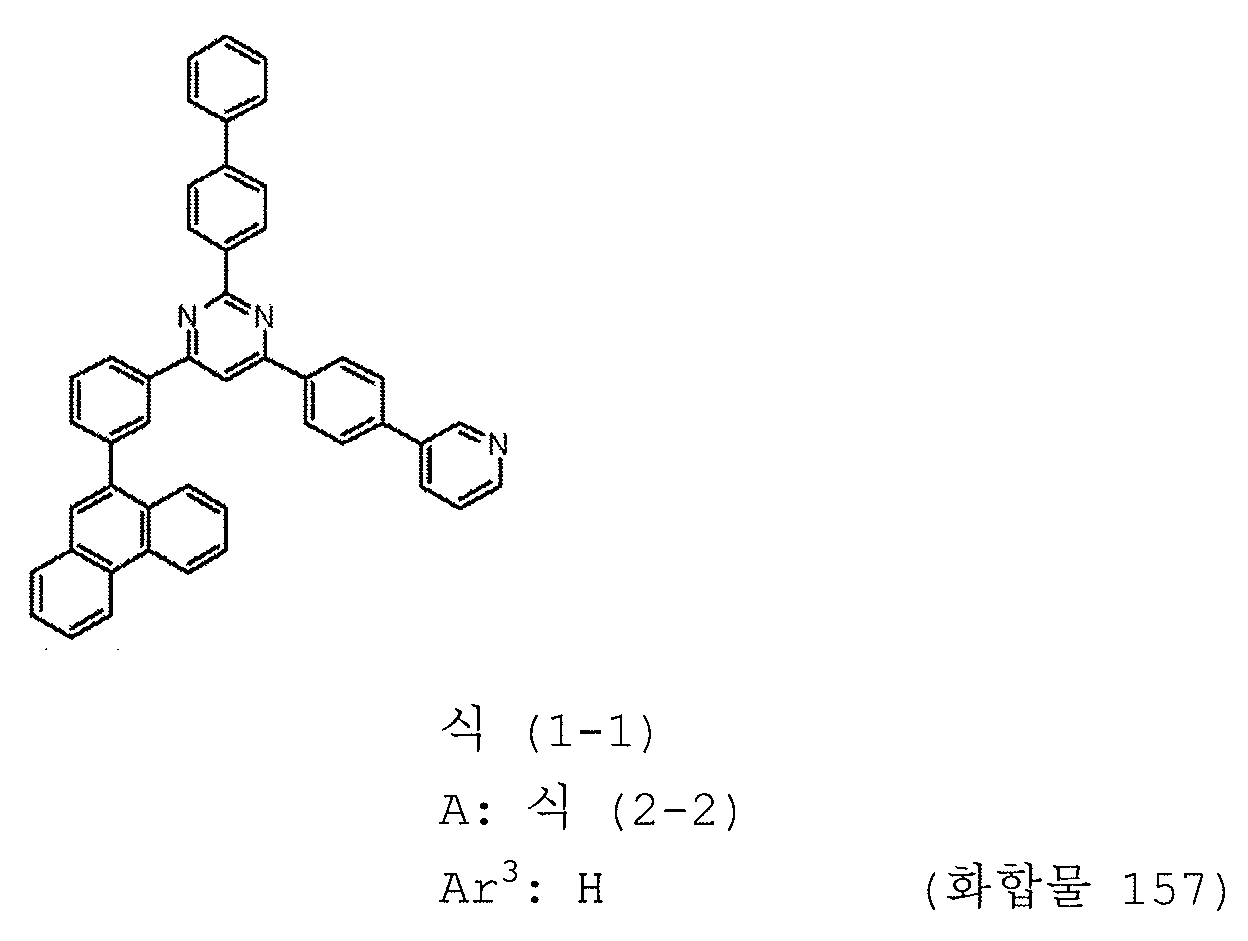
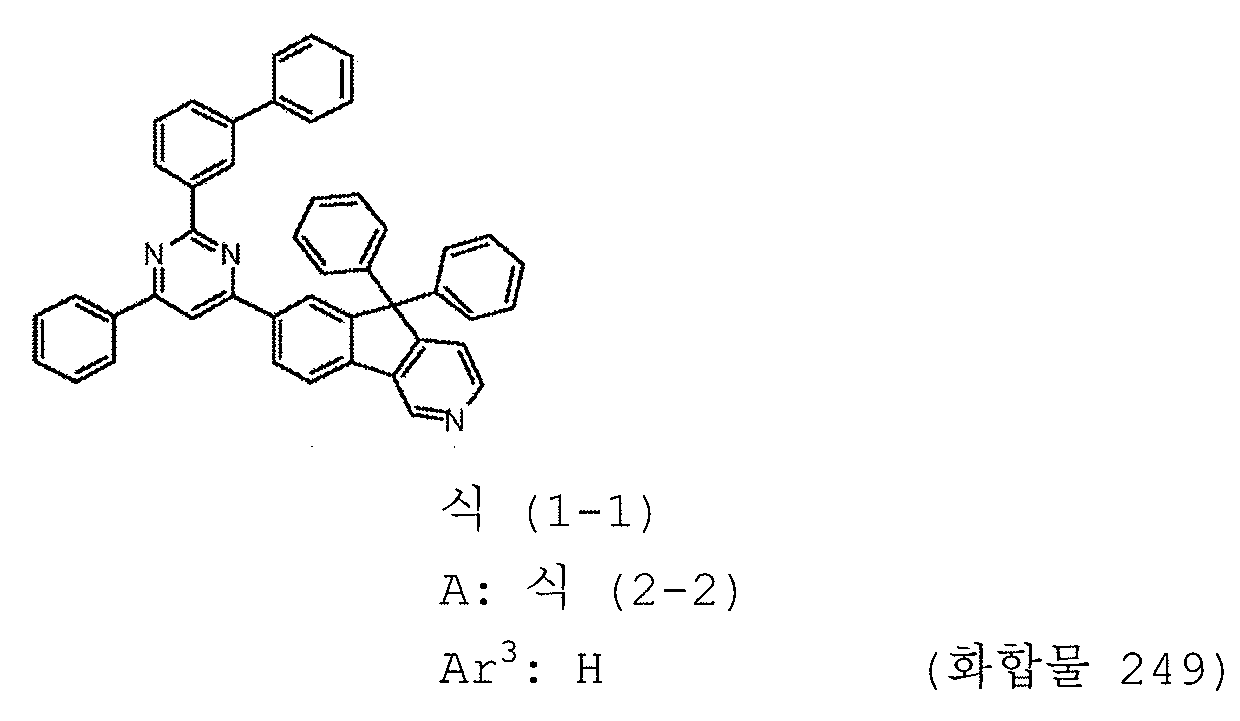
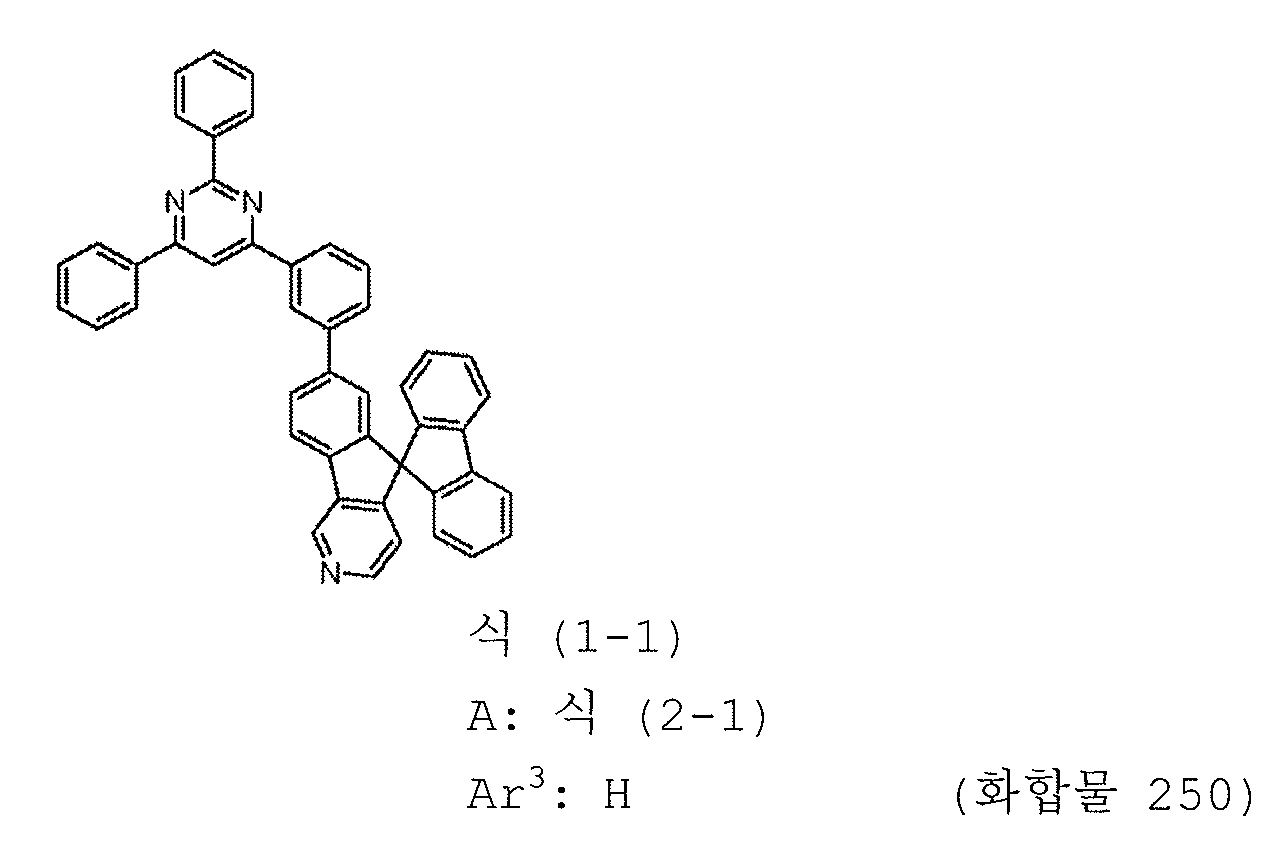
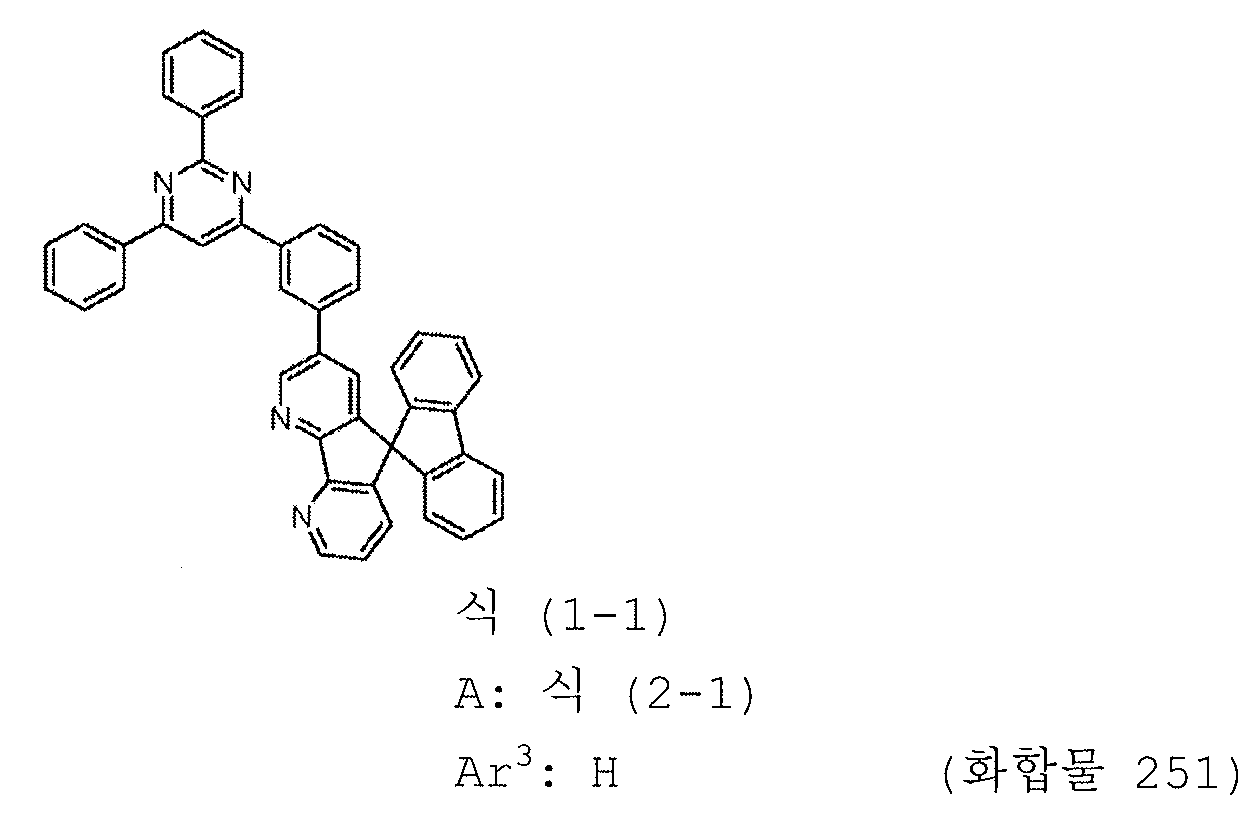
1) 피리미딘 유도체는 하기 일반식 (1-1) 로 표시되는 피리미딘 유도체이다:
식에서,
Ar1 내지 Ar3 및 A 는 상기 일반식 (1) 에 관해 정의된 의미를 갖는다.
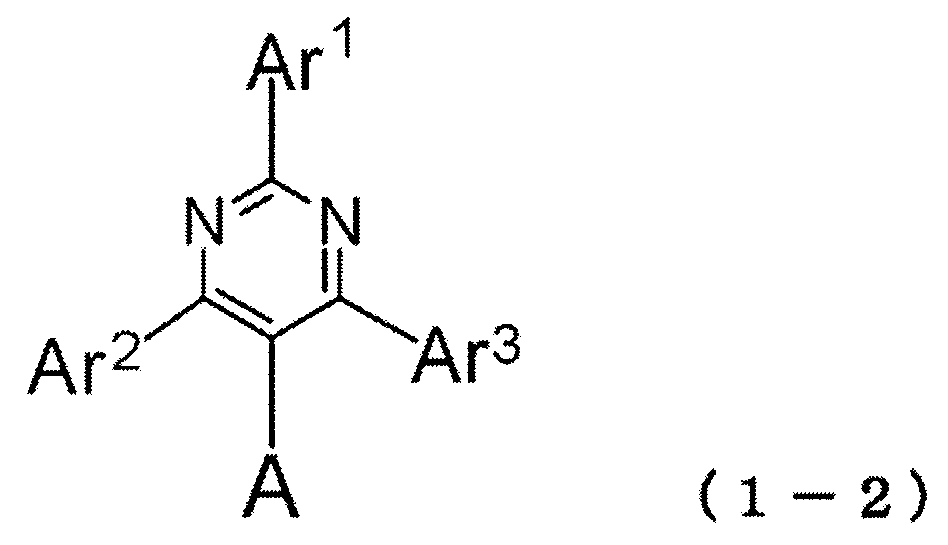
2) 피리미딘 유도체는 하기 일반식 (1-2) 로 표시되는 피리미딘 유도체이다:
식에서,
Ar1 내지 Ar3 및 A 는 상기 일반식 (1) 에 관해 정의된 의미를 갖는다.
3) A 는 하기 구조식 (2-1) 로 표시되는 1 가 기이다:
식에서,
Ar4 및 R1 내지 R4 는 상기 구조식 (2) 에 관해 정의된 의미를 갖는다.
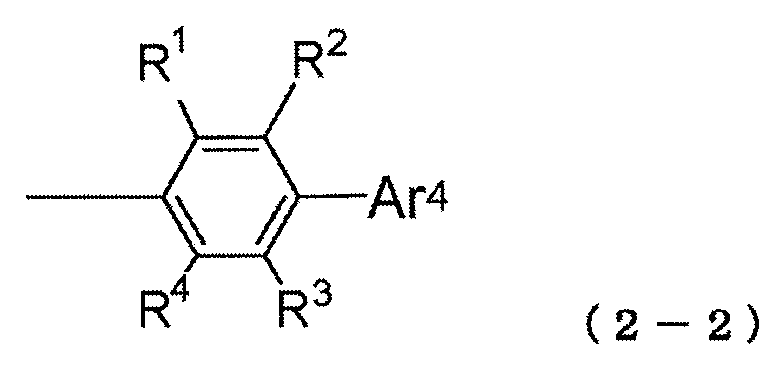
4) A 는 하기 구조식 (2-2) 로 표시되는 1 가 기이다:
식에서,
Ar4 및 R1 내지 R4 는 상기 구조식 (2) 에 관해 정의된 의미를 갖는다.
5) Ar1 은 방향족 탄화수소 기 또는 축합 다환 방향족 기를 나타내고, Ar2 및 Ar3 은 동일 또는 상이할 수 있고, 각각 수소 원자, 방향족 탄화수소 기, 또는 축합 다환 방향족 기를 나타낸다.
6) Ar4 는 피리딜 기, 피리미디닐 기, 퀴놀릴 기, 이소퀴놀릴 기, 인돌릴 기, 아자플루오레닐 기, 디아자플루오레닐 기, 퀴녹살리닐 기, 벤지미다졸릴 기, 나프티리디닐 기, 페난트롤리닐 기, 아크리디닐 기, 아자스피로비플루오레닐 기, 또는 디아자스피로비플루오레닐 기이다.
7) Ar2 는 치환기를 갖는 페닐 기이다.
8) Ar2 는 치환기를 갖는 페닐 기이고, 치환기는 방향족 탄화수소 기 또는 축합 다환 방향족 기이다.
9) Ar2 는 치환기를 갖는 페닐 기이고, 치환기는 방향족 탄화수소 기이다.
10) Ar2 는 치환기를 갖는 페닐 기이고, 치환기는 축합 다환 방향족 기이다.
11) Ar3 은 수소 원자이다.
12) Ar1 은 치환기를 갖는 페닐 기이다.
13) Ar1 은 치환기를 갖는 페닐 기이고, 치환기는 축합 다환 방향족 기이다.
14) Ar1 은 축합 다환 방향족 기이다.
15) Ar1 은 무치환 페닐 기이다.
또한, 본 발명에 의하면, 한 쌍의 전극 및 그 한 쌍의 전극 사이에 끼워진 적어도 하나의 유기 층을 포함하는 유기 EL 소자에 있어서, 상기 피리미딘 유도체가 적어도 하나의 유기 층의 구성 재료로서 사용되는 유기 EL 소자가 제공된다.
본 발명의 유기 EL 소자에 있어서는, 피리미딘 유도체가 사용되는 유기 층이 전자 수송층, 정공 저지층, 발광층, 또는 전자 주입층인 것이 바람직하다.
본 발명의 피리미딘 유도체는 신규 화합물이며, 하기 특성을 갖는다:
(1) 전자 주입성이 좋다.
(2) 전자 이동성이 크다.
(3) 정공 저지 능력이 우수하다.
(4) 박막 상태가 안정적이다.
(5) 내열성이 우수하다.
또한, 본 발명의 유기 EL 소자는 하기 특성을 갖는다:
(6) 발광 효율이 높다.
(7) 발광 개시 전압이 낮다.
(8) 실용 구동 전압이 낮다.
(9) 수명이 길다.
본 발명의 피리미딘 유도체는 전자 주입 및 이동 속도가 빠르다. 따라서, 본 발명의 피리미딘 유도체를 이용하여 제작된 전자 주입층 및/또는 전자 수송층을 갖는 유기 EL 소자에서, 전자 수송층에서 발광층으로의 전자 수송 효율이 향상되어 발광 효율이 향상된다. 또한, 구동 전압이 낮아져서, 유기 EL 소자의 내구성이 향상된다.
발명의 피리미딘 유도체는 우수한 정공 저지 능력을 갖고, 전자 수송성이 우수하며, 박막 상태가 안정적이다. 따라서, 본 발명의 피리미딘 유도체를 이용하여 제작된 정공 저지층을 갖는 유기 EL 소자는 높은 발광 효율을 갖고, 구동 전압이 낮고, 전류 내성이 개선되어, 유기 EL 소자의 최대 발광 휘도가 향상된다.
본 발명의 피리미딘 유도체는 전자 수송성이 우수하며 밴드 갭이 넓다. 따라서, 본 발명의 피리미딘 유도체를 호스트 재료로 사용하여 도판트로 불리는 형광 발광 물질, 인광 발광 물질 또는 지연 형광 발광 물질을 담지시켜 발광층을 형성한다. 이에 따라 구동 전압이 낮고, 발광 효율이 개선된 유기 EL 소자를 실현할 수 있다.
이상에서 본 발명의 피리미딘 유도체는 유기 EL 소자의 전자 주입층, 전자 수송층, 정공 저지층 또는 발광층의 구성 재료로서 유용하다. 본 발명의 유기 EL 소자는 발광층에서 생성된 여기자를 가둘 수 있으며, 또한 정공과 전자가 재결합하는 확률을 향상시켜 높은 발광 효율을 얻을 수 있다. 또한, 구동 전압이 낮아서 높은 내구성을 실현할 수 있다.
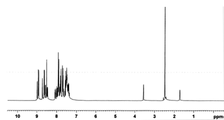
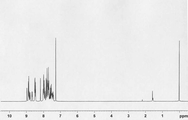
[도 1] 실시예 1 의 화합물 (화합물 74) 의 1H-NMR 차트다.
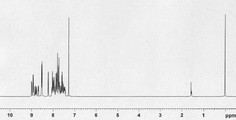
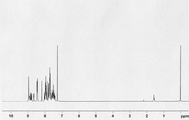
[도 2] 실시예 2 의 화합물 (화합물 84) 의 1H-NMR 차트다.
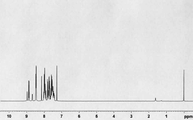
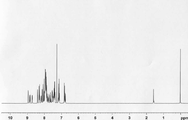
[도 3] 실시예 3 의 화합물 (화합물 89) 의 1H-NMR 차트다.
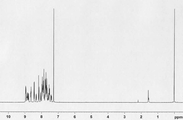
[도 4] 실시예 4 의 화합물 (화합물 130) 의 1H-NMR 차트다.
[도 5] 실시예 5 의 화합물 (화합물 131) 의 1H-NMR 차트다.
[도 6] 실시예 6 의 화합물 (화합물 92) 의 1H-NMR 차트다.
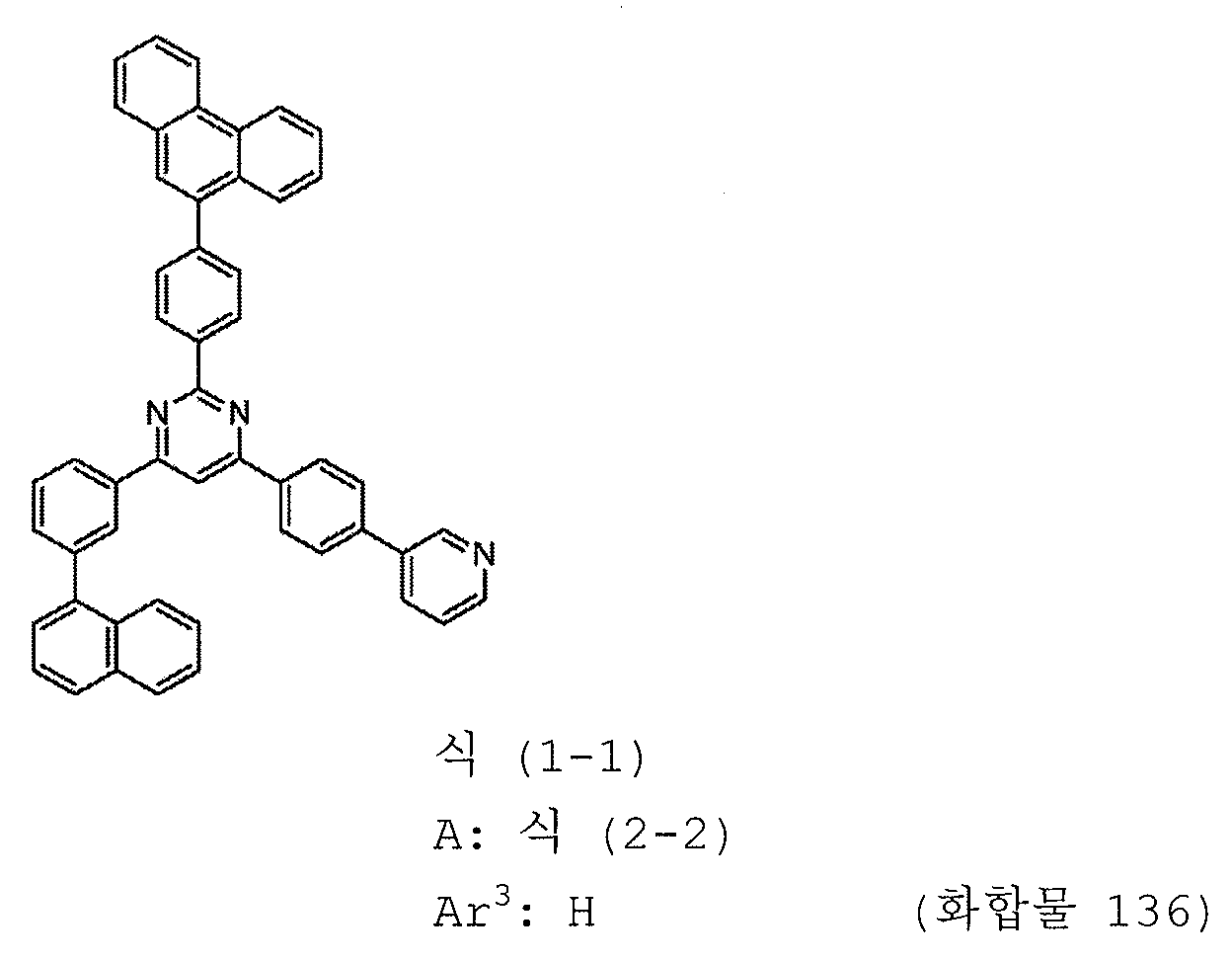
[도 7] 실시예 7 의 화합물 (화합물 136) 의 1H-NMR 차트다.
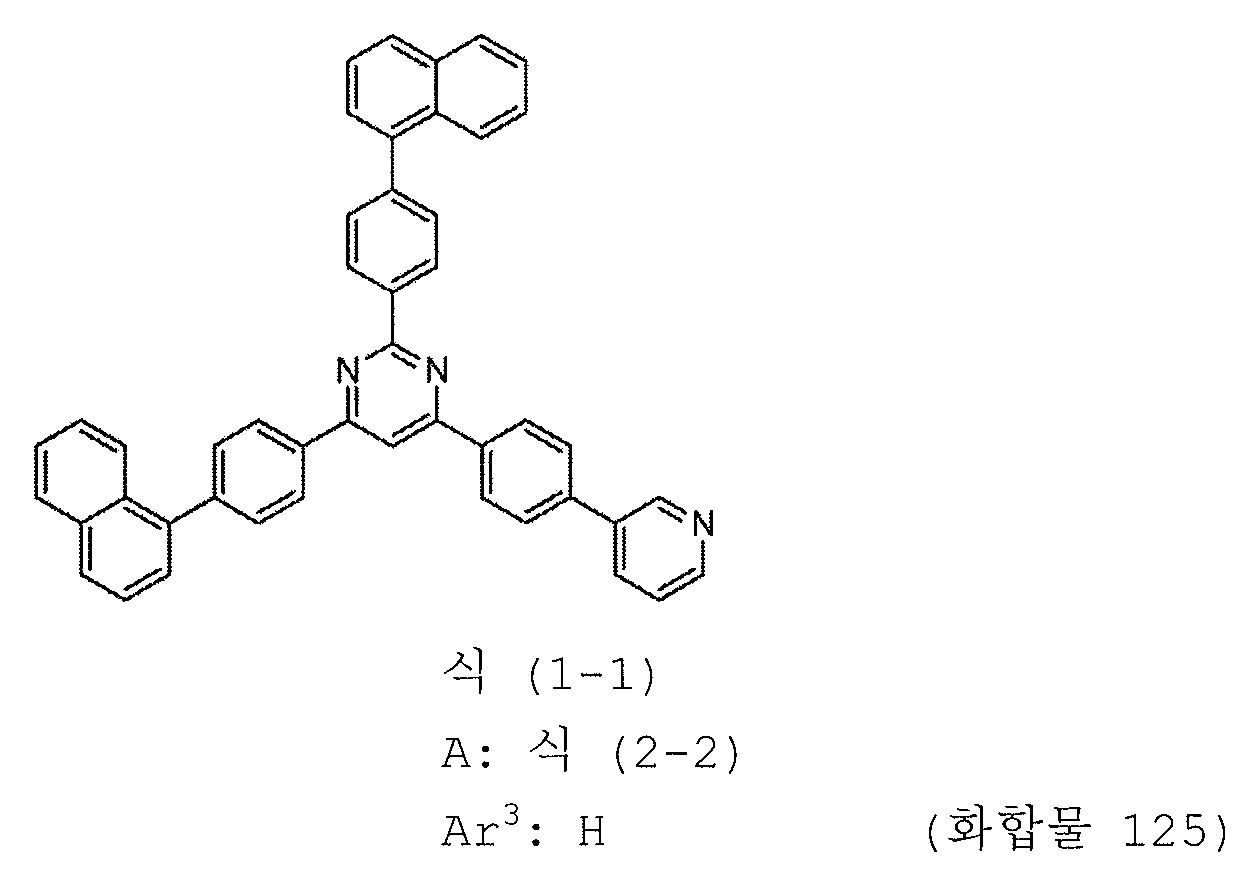
[도 8] 실시예 8 의 화합물 (화합물 125) 의 1H-NMR 차트다.
[도 9] 실시예 9 의 화합물 (화합물 138) 의 1H-NMR 차트다.
[도 10] 실시예 10 의 화합물 (화합물 78) 의 1H-NMR 차트다.
[도 11] 실시예 11 의 화합물 (화합물 76) 의 1H-NMR 차트다.
[도 12] 실시예 12 의 화합물 (화합물 126) 의 1H-NMR 차트다.
[도 13] 실시예 13 의 화합물 (화합물 124) 의 1H-NMR 차트다.
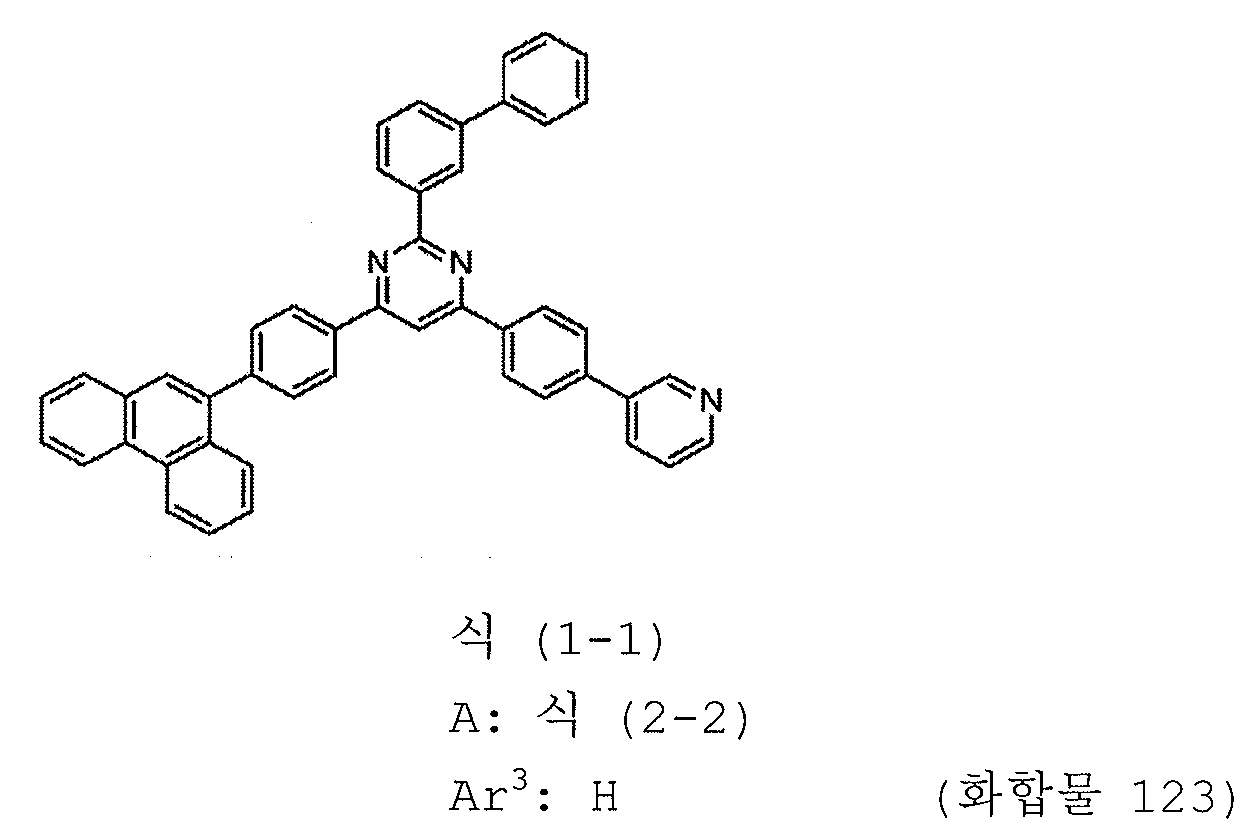
[도 14] 실시예 14 의 화합물 (화합물 123) 의 1H-NMR 차트다.
[도 15] 실시예 15 의 화합물 (화합물 146) 의 1H-NMR 차트다.
[도 16] 실시예 16 의 화합물 (화합물 98) 의 1H-NMR 차트다.
[도 17] 실시예 17 의 화합물 (화합물 153) 의 1H-NMR 차트다.
[도 18] 실시예 18 의 화합물 (화합물 155) 의 1H-NMR 차트다.
[도 19] 실시예 19 의 화합물 (화합물 82) 의 1H-NMR 차트다.
[도 20] 실시예 20 의 화합물 (화합물 182) 의 1H-NMR 차트다.
[도 21] 실시예 21 의 화합물 (화합물 227) 의 1H-NMR 차트다.
[도 22] 실시예 22 의 화합물 (화합물 234) 의 1H-NMR 차트다.
[도 23] 실시예 23 의 화합물 (화합물 235) 의 1H-NMR 차트다.
[도 24] 유기 EL 소자 실시예 1 내지 20 및 유기 EL 소자 비교예 1 의 EL 소자 구성을 나타내는 도면이다.
[도 2] 실시예 2 의 화합물 (화합물 84) 의 1H-NMR 차트다.
[도 3] 실시예 3 의 화합물 (화합물 89) 의 1H-NMR 차트다.
[도 4] 실시예 4 의 화합물 (화합물 130) 의 1H-NMR 차트다.
[도 5] 실시예 5 의 화합물 (화합물 131) 의 1H-NMR 차트다.
[도 6] 실시예 6 의 화합물 (화합물 92) 의 1H-NMR 차트다.
[도 7] 실시예 7 의 화합물 (화합물 136) 의 1H-NMR 차트다.
[도 8] 실시예 8 의 화합물 (화합물 125) 의 1H-NMR 차트다.
[도 9] 실시예 9 의 화합물 (화합물 138) 의 1H-NMR 차트다.
[도 10] 실시예 10 의 화합물 (화합물 78) 의 1H-NMR 차트다.
[도 11] 실시예 11 의 화합물 (화합물 76) 의 1H-NMR 차트다.
[도 12] 실시예 12 의 화합물 (화합물 126) 의 1H-NMR 차트다.
[도 13] 실시예 13 의 화합물 (화합물 124) 의 1H-NMR 차트다.
[도 14] 실시예 14 의 화합물 (화합물 123) 의 1H-NMR 차트다.
[도 15] 실시예 15 의 화합물 (화합물 146) 의 1H-NMR 차트다.
[도 16] 실시예 16 의 화합물 (화합물 98) 의 1H-NMR 차트다.
[도 17] 실시예 17 의 화합물 (화합물 153) 의 1H-NMR 차트다.
[도 18] 실시예 18 의 화합물 (화합물 155) 의 1H-NMR 차트다.
[도 19] 실시예 19 의 화합물 (화합물 82) 의 1H-NMR 차트다.
[도 20] 실시예 20 의 화합물 (화합물 182) 의 1H-NMR 차트다.
[도 21] 실시예 21 의 화합물 (화합물 227) 의 1H-NMR 차트다.
[도 22] 실시예 22 의 화합물 (화합물 234) 의 1H-NMR 차트다.
[도 23] 실시예 23 의 화합물 (화합물 235) 의 1H-NMR 차트다.
[도 24] 유기 EL 소자 실시예 1 내지 20 및 유기 EL 소자 비교예 1 의 EL 소자 구성을 나타내는 도면이다.
발명을 실시하기 위한 형태
본 발명의 피리미딘 유도체는 피리미딘 고리 구조를 갖는 신규 화합물이며, 하기 일반식 (1) 로 표시된다.
본 발명의 피리미딘 유도체는, 구체적으로는, 하기 일반식 (1-1) 또는 (1-2) 의 구조를 갖는다:
상기 일반식 (1), (1-1) 및 (1-2) 에서,
Ar1 은 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기를 나타내고,
Ar2 및 Ar3 은 동일 또는 상이할 수 있고, 각각 수소 원자, 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기를 나타낸다.
Ar2 및 Ar3 이 동시에 수소 원자는 아니다.
A 는 아래 기재된 구조식 (2) 로 표시되는 1 가 기를 나타낸다.
<Ar1 내지 Ar3>
Ar1 내지 Ar3 로 표시되는, 방향족 탄화수소 기 또는 축합 다환 방향족 기로서는 예를 들어 페닐 기, 비페닐일 기, 테르페닐일 기, 테트라키스페닐 기, 스티릴 기, 나프틸 기, 안트라세닐 기, 아세나프테닐 기, 페난트레닐 기, 플루오레닐 기, 인데닐 기, 피레닐 기, 페릴레닐 기, 플루오란테닐 기, 트리페닐레닐 기, 스피로비플루오레닐 기 등을 들 수 있다.
Ar1 내지 Ar3 로 표시되는, 방향족 헤테로고리 기로서는 예를 들어 산소-함유 방향족 탄화수소 기 예컨대 푸릴 기, 벤조푸라닐 기, 또는 디벤조푸라닐 기; 황-함유 방향족 헤테로고리 기 예컨대 티에닐 기, 벤조티에닐 기, 또는 디벤조티에닐 기; 등을 들 수 있다.
Ar1 내지 Ar3 로 표시되는, 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기는 무치환이어도 좋지만 치환기를 가질 수 있다. 치환기로서는 예를 들어 하기를 들 수 있다:
중수소 원자;
시아노 기;
니트로 기;
할로겐 원자, 예를 들어, 불소 원자, 염소 원자, 브롬 원자, 또는 요오드 원자;
1 내지 6 개의 탄소 원자를 갖는 알킬 기, 예를 들어, 메틸 기, 에틸 기, n-프로필 기, 이소프로필 기, n-부틸 기, 이소부틸 기, tert-부틸 기, n-펜틸 기, 이소펜틸 기, 네오펜틸 기, 또는 n-헥실 기;
1 내지 6 개의 탄소 원자를 갖는 알킬옥시 기, 예를 들어, 메틸옥시 기, 에틸옥시 기, 또는 프로필옥시 기;
알케닐 기, 예를 들어, 비닐 기 또는 알릴 기;
아릴옥시 기, 예를 들어, 페닐옥시 기 또는 톨릴옥시 기;
아릴알킬옥시 기, 예를 들어, 벤질옥시 기 또는 페네틸옥시 기;
방향족 탄화수소 기 또는 축합 다환 방향족 기, 예를 들어, 페닐 기, 비페닐일 기, 테르페닐일 기, 나프틸 기, 안트라세닐 기, 페난트레닐 기, 플루오레닐 기, 인데닐 기, 피레닐 기, 페릴레닐 기, 플루오란테닐 기, 트리페닐레닐 기, 또는 스피로비플루오레닐 기;
방향족 헤테로고리 기, 예를 들어, 피리딜 기, 티에닐 기, 푸릴 기, 피롤릴 기, 퀴놀릴 기, 이소퀴놀릴 기, 벤조푸라닐 기, 벤조티에닐 기, 인돌릴 기, 카르바졸릴 기, 벤족사졸릴 기, 벤조티아졸릴 기, 퀴녹살리닐 기, 벤지미다졸릴 기, 피라졸릴 기, 디벤조푸라닐 기, 디벤조티에닐 기, 아자플루오레닐 기, 디아자플루오레닐 기, 카르볼리닐 기, 아자스피로비플루오레닐 기, 또는 디아자스피로비플루오레닐 기;
아릴비닐 기, 예를 들어, 스티릴 기, 또는 나프틸비닐 기; 및
아실 기, 예를 들어, 아세틸 기, 또는 벤조일 기.
1 내지 6 개의 탄소 원자를 갖는 알킬 기, 및 1 내지 6 개의 탄소 원자를 갖는 알킬옥시 기는 직쇄형 또는 분지형일 수 있다. 상기 치환기는 또한 상기 예시한 치환기로 치환되어 있어도 좋다. 상기 치환기는 각각 독립적으로 존재할 수 있으나, 단일 결합, 치환 또는 무치환 메틸렌 기, 산소 원자, 또는 황 원자를 통해 서로 결합하여 고리를 형성할 수 있다. 또한, 치환기 및 당해 치환기가 결합된 Ar1, Ar2 또는 Ar3 은 산소 원자 또는 황 원자를 통해 서로 결합하여 고리를 형성할 수 있으나, 각각 독립적으로 존재하여 고리를 형성하고 있지 않을 수 있다.
<A>
A 는 하기 구조식 (2) 로 표시되는 1 가 기를 나타낸다:
식에서,
Ar4 는 방향족 헤테로고리 기를 나타내고,
R1 내지 R4 는 동일 또는 상이할 수 있고, 각각 수소 원자, 중수소 원자, 불소 원자, 염소 원자, 시아노 기, 트리플루오로메틸 기, 1 내지 6 개의 탄소 원자를 갖는 알킬 기, 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기를 나타낸다.
R1 내지 R4 및 Ar4 는 각각 독립적으로 존재할 수 있으나, 단일 결합, 치환 또는 무치환 메틸렌 기, 산소 원자, 또는 황 원자를 통해 서로 결합하여 고리를 형성할 수 있다.
(Ar4)
Ar4 로 표시되는, 방향족 헤테로고리 기로서는 예를 들어 트리아지닐 기, 피리딜 기, 피리미디닐 기, 푸릴 기, 피롤릴 기, 티에닐 기, 퀴놀릴 기, 이소퀴놀릴 기, 벤조푸라닐 기, 벤조티에닐 기, 인돌릴 기, 카르바졸릴 기, 벤족사졸릴 기, 벤조티아졸릴 기, 퀴녹살리닐 기, 벤지미다졸릴 기, 피라졸릴 기, 디벤조푸라닐 기, 디벤조티에닐 기, 아자플루오레닐 기, 디아자플루오레닐 기, 나프티리디닐 기, 페난트롤리닐 기, 아크리디닐 기, 카르볼리닐 기, 아자스피로비플루오레닐 기, 디아자스피로비플루오레닐 기 등을 들 수 있다.
Ar4 로 표시되는, 방향족 헤테로고리 기는 무치환이어도 좋지만 치환기를 가질 수 있다. 치환기로서는 예를 들어 Ar1 내지 Ar3 로 표시되는, 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기가 임의로 가질 수 있는 치환기로 나타낸 것과 같은 것을 들 수 있다. 치환기가 가질 수 있는 형태도 예시한 치환기에 관한 것과 동일하다.
(R1 내지 R4)
R1 내지 R4 로 표시되는, 1 내지 6 개의 탄소 원자를 갖는 알킬 기로서는 예를 들어 메틸 기, 에틸 기, n-프로필 기, i-프로필 기, n-부틸 기, 2-메틸프로필 기, t-부틸 기, n-펜틸 기, 3-메틸부틸 기, tert-펜틸 기, n-헥실 기, 이소-헥실 기, 및 tert-헥실 기를 들 수 있다. 1 내지 6 개의 탄소 원자를 갖는 알킬 기는 직쇄형 또는 분지형일 수 있다.
R1 내지 R4 로 표시되는, 1 내지 6 개의 탄소 원자를 갖는 알킬 기는 무치환이어도 좋지만 치환기를 가질 수 있다. 치환기로서는 예를 들어 하기를 들 수 있다:
중수소 원자;
시아노 기;
니트로 기;
할로겐 원자, 예를 들어, 불소 원자, 염소 원자, 브롬 원자, 또는 요오드 원자;
1 내지 6 개의 탄소 원자를 갖는 알킬옥시 기, 예를 들어, 메틸옥시 기, 에틸옥시 기, 또는 프로필옥시 기;
알케닐 기, 예를 들어, 비닐 기 또는 알릴 기;
아릴옥시 기, 예를 들어, 페닐옥시 기 또는 톨릴옥시 기;
아릴알킬옥시 기, 예를 들어, 벤질옥시 기 또는 페네틸옥시 기;
방향족 탄화수소 기 또는 축합 다환 방향족 기, 예를 들어, 페닐 기, 비페닐일 기, 테르페닐일 기, 나프틸 기, 안트라세닐 기, 페난트레닐 기, 플루오레닐 기, 인데닐 기, 피레닐 기, 페릴레닐 기, 플루오란테닐 기, 또는 트리페닐레닐 기; 및
방향족 헤테로고리 기, 예를 들어, 피리딜 기, 피리미디닐 기, 트리아지닐 기, 티에닐 기, 푸릴 기, 피롤릴 기, 퀴놀릴 기, 이소퀴놀릴 기, 벤조푸라닐 기, 벤조티에닐 기, 인돌릴 기, 카르바졸릴 기, 벤족사졸릴 기, 벤조티아졸릴 기, 퀴녹살리닐 기, 벤지미다졸릴 기, 피라졸릴 기, 디벤조푸라닐 기, 디벤조티에닐 기, 페녹사지닐 기, 페노티아지닐 기, 카르볼리닐 기, 아크리디닐 기, 또는 페나지닐 기.
1 내지 6 개의 탄소 원자를 갖는 알킬옥시 기는 직쇄형 또는 분지형일 수 있다. 상기 치환기는 또한 상기 예시한 치환기로 치환되어 있어도 좋다. 상기 치환기는 각각 독립적으로 존재할 수 있으나, 단일 결합, 치환 또는 무치환 메틸렌 기, 산소 원자, 또는 황 원자를 통해 서로 결합하여 고리를 형성할 수 있다.
R1 내지 R4 로 표시되는, 방향족 탄화수소 기 또는 축합 다환 방향족 기로서는 예를 들어 페닐 기, 비페닐일 기, 테르페닐일 기, 테트라키스페닐 기, 스티릴 기, 나프틸 기, 안트라세닐 기, 아세나프테닐 기, 페난트레닐 기, 플루오레닐 기, 인데닐 기, 피레닐 기, 페릴레닐 기, 플루오란테닐 기, 트리페닐레닐 기, 및 스피로비플루오레닐 기를 들 수 있다.
R1 내지 R4 로 표시되는, 방향족 헤테로고리 기로서는 예를 들어 트리아지닐 기, 피리딜 기, 피리미디닐 기, 푸릴 기, 피롤릴 기, 티에닐 기, 퀴놀릴 기, 이소퀴놀릴 기, 벤조푸라닐 기, 벤조티에닐 기, 인돌릴 기, 카르바졸릴 기, 벤족사졸릴 기, 벤조티아졸릴 기, 퀴녹살리닐 기, 벤지미다졸릴 기, 피라졸릴 기, 디벤조푸라닐 기, 디벤조티에닐 기, 아자플루오레닐 기, 디아자플루오레닐 기, 나프티리디닐 기, 페난트롤리닐 기, 아크리디닐 기, 카르볼리닐 기, 아자스피로비플루오레닐 기, 디아자스피로비플루오레닐 기 등을 들 수 있다.
R1 내지 R4 로 표시되는, 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기는 무치환이어도 좋지만 치환기를 가질 수 있다. 치환기로서는 예를 들어 Ar1 내지 Ar3 로 표시되는, 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기가 임의로 가질 수 있는 치환기로 나타낸 것과 같은 것을 들 수 있다. 치환기가 가질 수 있는 형태도 예시한 치환기에 관한 것과 동일하다.
<바람직한 구현예>
본 발명에서, 합성의 용이성의 관점에서, 하기 일반식 (1-1) 로 표시되는 바와 같이, 기 A 가 피리미딘 고리의 6-위치에 결합되어 있는 화합물이 바람직하다.
(바람직한 Ar1)
바람직한 Ar1 로서는, 방향족 탄화수소 기 또는 축합 다환 방향족 기를 들 수 있다. 방향족 탄화수소 기 또는 축합 다환 방향족 기는 무치환이어도 좋고, 치환기를 가지고 있어도 좋다.
대안적으로, 페닐 기, 축합 다환 방향족 기, 또는 산소-함유 또는 황-함유 방향족 헤테로고리 기를 바람직한 Ar1 로서 들 수 있다. 바람직한 예는 페닐 기, 나프틸 기, 안트라세닐 기, 아세나프테닐 기, 페난트레닐 기, 플루오레닐 기, 인데닐 기, 피레닐 기, 페릴레닐 기, 플루오란테닐 기, 트리페닐레닐 기, 스피로비플루오레닐 기, 푸릴 기, 벤조푸라닐 기, 디벤조푸라닐 기, 티에닐 기, 벤조티에닐 기, 및 디벤조티에닐 기이다.
특히 바람직한 Ar1 로서는, 페닐 기, 나프틸 기, 페난트레닐 기, 플루오레닐 기, 피레닐 기, 플루오란테닐 기, 트리페닐레닐 기, 스피로비플루오레닐 기, 디벤조푸라닐 기, 및 디벤조티에닐 기를 들 수 있다.
바람직한 또는 특히 바람직한 Ar1 인, 축합 다환 방향족 기, 및 산소-함유 또는 황-함유 방향족 헤테로고리 기는 무치환이어도 좋고, 치환기를 가지고 있어도 좋다.
바람직한 또는 특히 바람직한 Ar1 인, 페닐 기는 무치환이어도 좋으나, 바람직하게는 치환기를 갖는다.
페닐 기가 갖는 치환기로서는, 페닐 기, 비페닐 기, 또는 축합 다환 방향족 기가 바람직하다.
특히, 페닐 기가 갖는 치환기로서 페닐 기, 비페닐 기, 나프틸 기, 페난트레닐 기, 피레닐 기, 플루오란테닐 기, 트리페닐레닐 기, 또는 스피로비플루오레닐 기가 바람직하다.
페닐 기가 갖는 치환기인, 축합 다환 방향족 기는 추가로 치환기를 가질 수 있으나, 무치환이어도 좋다. 페닐 기 및 치환기는 산소 원자 또는 황 원자를 통해 서로 결합하여 고리를 형성할 수 있으나, 각각 독립적으로 존재하여 고리를 형성하고 있지 않을 수 있다.
(바람직한 Ar2)
바람직한 Ar2 로서는, 수소 원자, 방향족 탄화수소 기, 또는 축합 다환 방향족 기를 들 수 있다. 방향족 탄화수소 기 또는 축합 다환 방향족 기는 무치환이어도 좋고, 치환기를 가지고 있어도 좋다.
대안적으로, 페닐 기; 스피로비플루오레닐 기; 산소-함유 방향족 헤테로고리 기, 예를 들어, 푸릴 기, 벤조푸라닐 기, 또는 디벤조푸라닐 기; 및 황-함유 방향족 헤테로고리 기, 예를 들어, 티에닐 기, 벤조티에닐 기, 또는 디벤조티에닐 기;를 Ar2 의 바람직한 예로서 들 수 있다.
스피로비플루오레닐 기, 및 산소-함유 또는 황-함유 방향족 헤테로고리 기는 치환기를 가져도 좋고, 무치환이어도 좋다.
페닐 기는 바람직하게는 치환기를 갖는다. 페닐 기가 갖는 치환기로서 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 산소- 또는 황-함유 방향족 헤테로고리 기가 바람직하다. 바람직한 예는 방향족 탄화수소 기, 예컨대 페닐 기, 비페닐일 기, 또는 테르페닐 기; 축합 다환 방향족 기, 예컨대 나프틸 기, 아세나프테닐 기, 페난트레닐 기, 플루오레닐 기, 인데닐 기, 피레닐 기, 페릴레닐 기, 플루오란테닐 기, 트리페닐레닐 기, 또는 스피로비플루오레닐 기; 산소-함유 방향족 헤테로고리 기, 예컨대 푸릴 기, 벤조푸라닐 기, 또는 디벤조푸라닐 기; 및 황-함유 방향족 헤테로고리 기, 예컨대 티에닐 기, 벤조티에닐 기, 또는 디벤조티에닐 기이다. 더욱 바람직한 예는 페닐 기, 나프틸 기, 페난트레닐 기, 플루오레닐 기, 피레닐 기, 플루오란테닐 기, 트리페닐레닐 기, 스피로비플루오레닐 기, 디벤조푸라닐 기, 및 디벤조티에닐 기이다. 상기 페닐 기가 갖는 바람직한 치환기는 추가로 치환기를 가질 수 있으나, 무치환이어도 좋다. 페닐 기 및 치환기 는 산소 원자 또는 황 원자를 통해 서로 결합하여 고리를 형성할 수 있으나, 각각 독립적으로 존재하여 고리를 형성하고 있지 않을 수 있다.
Ar2 가 임의로 갖는 치환기로서 방향족 헤테로고리 기 이외의 기, 즉, 중수소 원자, 시아노 기, 니트로 기, 할로겐 원자, 1 내지 6 개의 탄소 원자를 갖는 알킬 기, 1 내지 6 개의 탄소 원자를 갖는 알킬옥시 기, 알케닐 기, 아릴옥시 기, 아릴알킬옥시 기, 방향족 탄화수소 기, 축합 다환 방향족 기, 아릴비닐 기, 또는 아실 기가 바람직하다.
(바람직한 Ar3)
바람직한 Ar3 로서는, 수소 원자, 방향족 탄화수소 기, 또는 축합 다환 방향족 기를 들 수 있다. 방향족 탄화수소 기 또는 축합 다환 방향족 기는 무치환이어도 좋고, 치환기를 가지고 있어도 좋다.
대안적으로, 수소 원자, 페닐 기, 스피로비플루오레닐 기, 또는 산소-함유 또는 황-함유 방향족 헤테로고리 기를 Ar3 의 바람직한 예로서 들 수 있다.
Ar3 의 더욱 바람직한 예는 수소 원자, 페닐 기, 스피로비플루오레닐 기, 푸릴 기, 벤조푸라닐 기, 디벤조푸라닐 기, 티에닐 기, 벤조티에닐 기, 및 디벤조티에닐 기이다.
바람직한 또는 더욱 바람직한 Ar3 인, 스피로비플루오레닐 기, 또는 산소-함유 또는 황-함유 방향족 헤테로고리 기는 치환기를 가져도 좋고 무치환이어도 좋다.
바람직한 또는 더욱 바람직한 Ar3 인, 페닐 기는 바람직하게는 치환기를 갖는다. 페닐 기가 갖는 치환기로서 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 산소- 또는 황-함유 방향족 헤테로고리 기가 바람직하다. 바람직한 예는 페닐 기, 비페닐 기, 테르페닐 기, 나프틸 기, 아세나프테닐 기, 페난트레닐 기, 플루오레닐 기, 인데닐 기, 피레닐 기, 페릴레닐 기, 플루오란테닐 기, 트리페닐레닐 기, 스피로비플루오레닐 기, 푸릴 기, 벤조푸라닐 기, 디벤조푸라닐 기, 티에닐 기, 벤조티에닐 기, 및 디벤조티에닐 기이다.
페닐 기가 갖는 치환기로서 페닐 기, 나프틸 기, 페난트레닐 기, 플루오레닐 기, 피레닐 기, 플루오란테닐 기, 트리페닐레닐 기, 스피로비플루오레닐 기, 디벤조푸라닐 기, 또는 디벤조티에닐 기가 특히 바람직하다.
페닐 기가 치환기를 갖는 경우, 치환기 및 페닐 기는 산소 원자 또는 황 원자를 통해 서로 결합하여 고리를 형성할 수 있으나, 각각 독립적으로 존재하여 고리를 형성하고 있지 않을 수 있다.
특히 바람직한 Ar3 로서는, 수소 원자를 들 수 있다.
Ar3 가 임의로 갖는 치환기로서 방향족 헤테로고리 기 이외의 기, 즉, 중수소 원자, 시아노 기, 니트로 기, 할로겐 원자, 1 내지 6 개의 탄소 원자를 갖는 알킬 기, 1 내지 6 개의 탄소 원자를 갖는 알킬옥시 기, 알케닐 기, 아릴옥시 기, 아릴알킬옥시 기, 방향족 탄화수소 기, 축합 다환 방향족 기, 아릴비닐 기, 또는 아실 기가 바람직하다.
Ar1 및 Ar2 는 동일할 수 있으나, 박막 안정성의 관점에서, 바람직하게는 상이하다. Ar1 및 Ar2 가 동일한 기를 나타내는 경우에, Ar1 및 Ar2 는 상이한 치환기를 가져도 좋고, 동일한 치환기를 상이한 치환 위치에 가져도 좋다.
Ar2 및 Ar3 은 동일한 기일 수 있으나, 분자 전체의 대칭성이 증가하면 결정화하기 쉽다. 따라서, 박막 상태의 안정성의 관점에서, Ar2 및 Ar3 이 상이한 기인 것이 바람직하다.
Ar2 및 Ar3 중 하나는 바람직하게는 수소 원자이고, Ar3 은 특히 바람직하게는 수소 원자이다. 이미 언급한 바와 같이, 본 발명에서, Ar2 및 Ar3 이 동시에 수소 원자는 아니다.
(바람직한 A)
기 A 는 박막 안정성의 관점에서 바람직하게는 하기 구조식 (2-1) 로 표시된다. 즉, 기 Ar4 는 바람직하게는, 벤젠 고리에서, 일반식 (1) 로 표시되는 피리미딘 고리에 대해 메타 위치에서 결합되어 있다.
대안적으로, 기 A 는 합성의 관점에서 바람직하게는 구조식 (2-2) 로 표시된다. 즉, 기 Ar4 는 바람직하게는, 벤젠 고리에서, 일반식 (1) 로 표시되는 피리미딘 고리에 대해 메타 위치에서 결합되어 있다.
바람직한 Ar4 로서는 예를 들어 질소-함유 헤테로고리 기, 예를 들어, 트리아지닐 기, 피리딜 기, 피리미디닐 기, 피롤릴 기, 퀴놀릴 기, 이소퀴놀릴 기, 인돌릴 기, 카르바졸릴 기, 벤족사졸릴 기, 벤조티아졸릴 기, 퀴녹살리닐 기, 벤지미다졸릴 기, 피라졸릴 기, 아자플루오레닐 기, 디아자플루오레닐 기, 나프티리디닐 기, 페난트롤리닐 기, 아크리디닐 기, 카르볼리닐 기, 아자스피로비플루오레닐 기, 및 디아자스피로비플루오레닐 기를 들 수 있다.
더욱 바람직한 Ar4 로서는, 트리아지닐 기, 피리딜 기, 피리미디닐 기, 퀴놀릴 기, 이소퀴놀릴 기, 인돌릴 기, 퀴녹살리닐 기, 아자플루오레닐 기, 디아자플루오레닐 기, 벤지미다졸릴 기, 나프티리디닐 기, 페난트롤리닐 기, 아크리디닐 기, 아자스피로비플루오레닐 기 및 디아자스피로비플루오레닐 기를 들 수 있다.
가장 바람직한 Ar4 로서는, 피리딜 기, 피리미디닐 기, 퀴놀릴 기, 이소퀴놀릴 기, 인돌릴 기, 아자플루오레닐 기, 디아자플루오레닐 기, 퀴녹살리닐 기, 벤지미다졸릴 기, 나프티리디닐 기, 페난트롤리닐 기, 아크리디닐 기, 아자스피로비플루오레닐 기 및 디아자스피로비플루오레닐 기를 들 수 있다.
피리딜 기로서는, 피리딘-3-일 기가 바람직하다.
바람직한 R1 내지 R4 로서는, 수소 원자, 중수소 원자, 불소 원자, 염소 원자, 시아노 기, 트리플루오로메틸 기, 1 내지 6 개의 탄소 원자를 갖는 알킬 기, 방향족 탄화수소 기 또는 축합 다환 방향족 기를 들 수 있다. 더욱 바람직한 R1 내지 R4 로서는, 수소 원자, 중수소 원자, 불소 원자, 염소 원자, 시아노 기, 트리플루오로메틸 기 또는 1 내지 6 개의 탄소 원자를 갖는 알킬 기를 들 수 있다. 특히 바람직한 R1 내지 R4 로서는, 수소 원자 또는 중수소 원자를 들 수 있다.
<제조 방법>
본 발명의 피리미딘 유도체는, 예를 들어, 하기 방법에 의해 생산될 수 있다: 2,4,6-트리클로로피리미딘과 4-위치에 상당하는 기를 갖는 아릴보론산 또는 아릴보론산 에스테르 사이의 스즈키 커플링 반응을 실시한다. 이어서, 상당하는 헤테로아릴 기를 치환기로 갖는 페닐보론산 또는 페닐보론산 에스테르를 첨가하고, 스즈키 커플링 반응을 실시한다. 두 단계의 스즈키 커플링 반응을 실시함으로써, 상당하는 기를 피리미딘 고리의 4-위치에 도입하고, 상당하는 헤테로아릴 기를 치환기로 갖는 페닐 기를 6-위치에 도입한다. 더욱이, 2-위치에 상당하는 기를 갖는 아릴보론산 또는 아릴보론산 에스테르를 사용하여 스즈키 커플링 반응을 실시하여, 상당하는 기를 피리미딘 고리의 2-위치에 도입한다. 이러한 방식으로, 본 발명의 피리미딘 유도체가 생산될 수 있다.
상기 제조 방법에 있어서, 피리미딘 고리의 2-위치, 4-위치 및 6-위치에 각각의 기를 도입하는 순서는 적절히 변경할 수 있다.
또한, 상기 제조 방법에 있어서, 할로겐 원자 예컨대 클로로 기로 상이한 위치에서 치환된 피리미딘, 예를 들어, 2,4,5-트리클로로피리미딘이 2,4,6-트리클로로피리미딘 대신 사용될 수 있다. 이 경우에, 치환 위치가 상이한 피리미딘 유도체가 생산될 수 있다.
얻어진 화합물의 정제는 컬럼 크로마토그래피에 의한 정제, 실리카겔, 활성탄, 활성 백토 등에 의한 흡착 정제, 용매에 의한 재결정화 또는 결정화, 승화 정제 등에 의해 수행할 수 있다. 화합물의 동정은 NMR 분석하여 수행할 수 있다. 물성치로서, 일 함수와 글라스 전이점 (Tg) 을 측정할 수 있다.
일 함수는 정공 저지 특성의 지표가 되는 것이다. 일 함수는 ITO 기판 위에 100 nm 의 박막을 제작하여 이온화 포텐셜 측정 장치 (스미토모 중기계공업 제, PYS-202 형) 를 이용하여 측정 할 수 있다.
글라스 전이점 (Tg) 은 박막 상태의 안정성의 지표가 된다. 글라스 전이점 (Tg) 은, 예를 들면, 분말을 이용하여 고감도 시차 주사 열량계 (Bruker AXS K.K. 제, DSC3100S) 에 의해 측정할 수 있다.
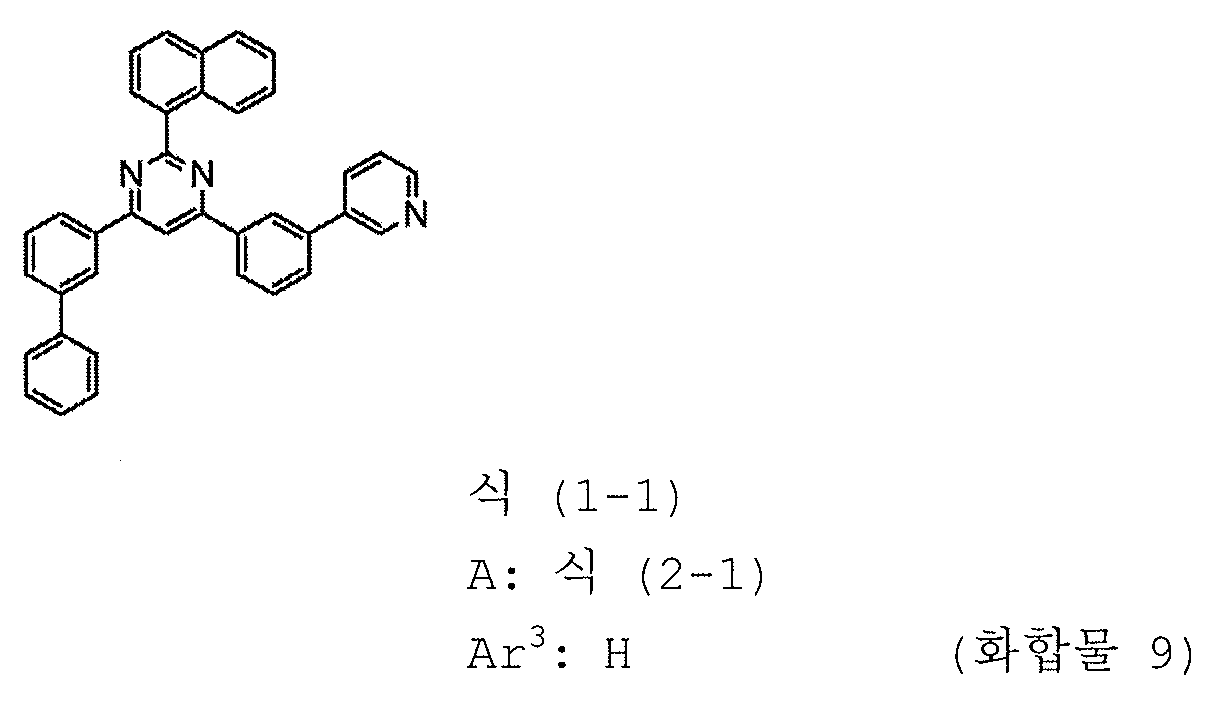
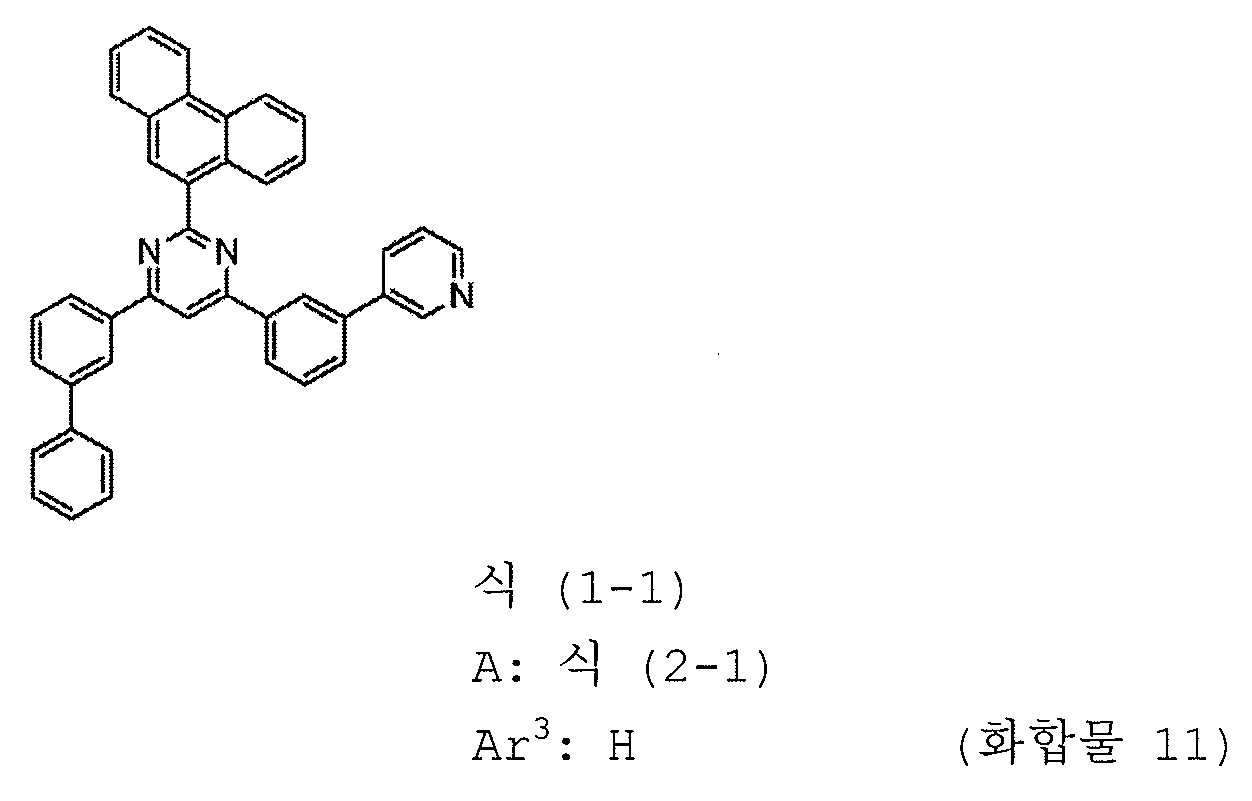
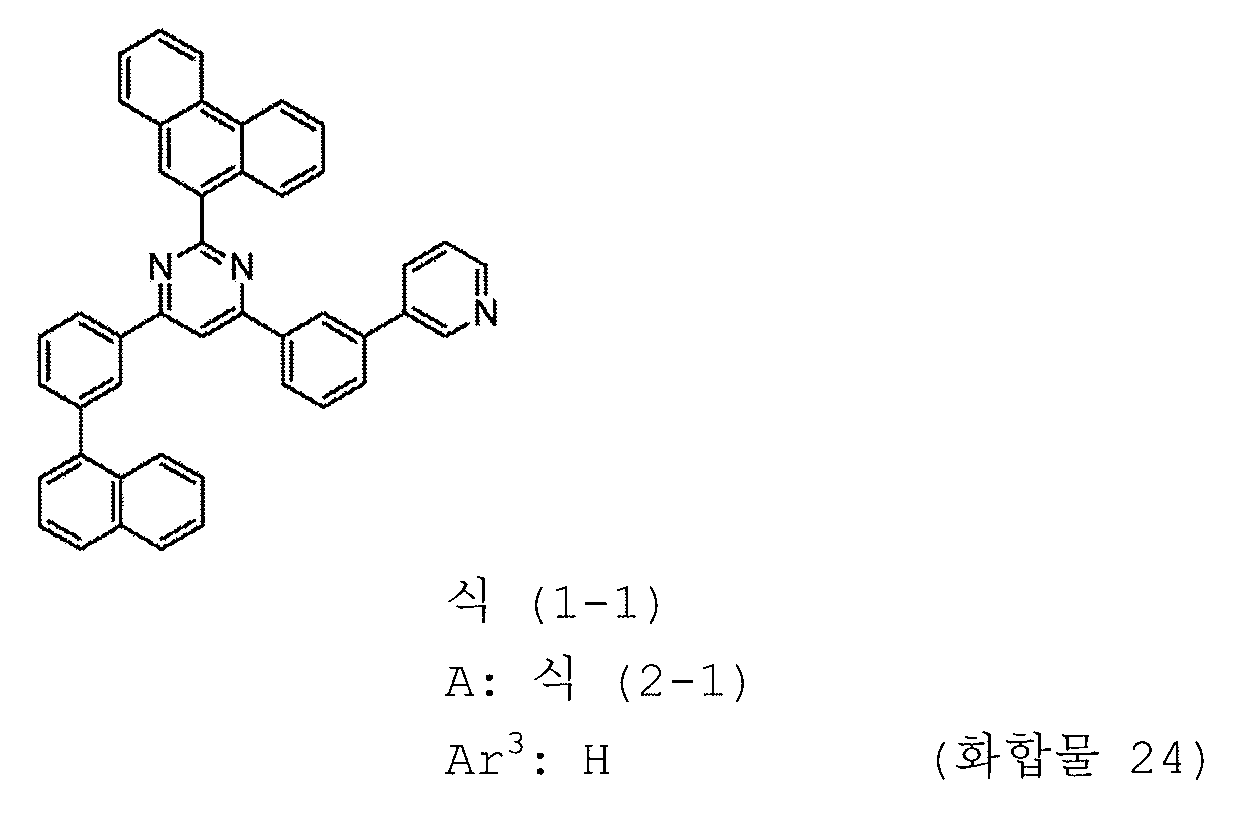
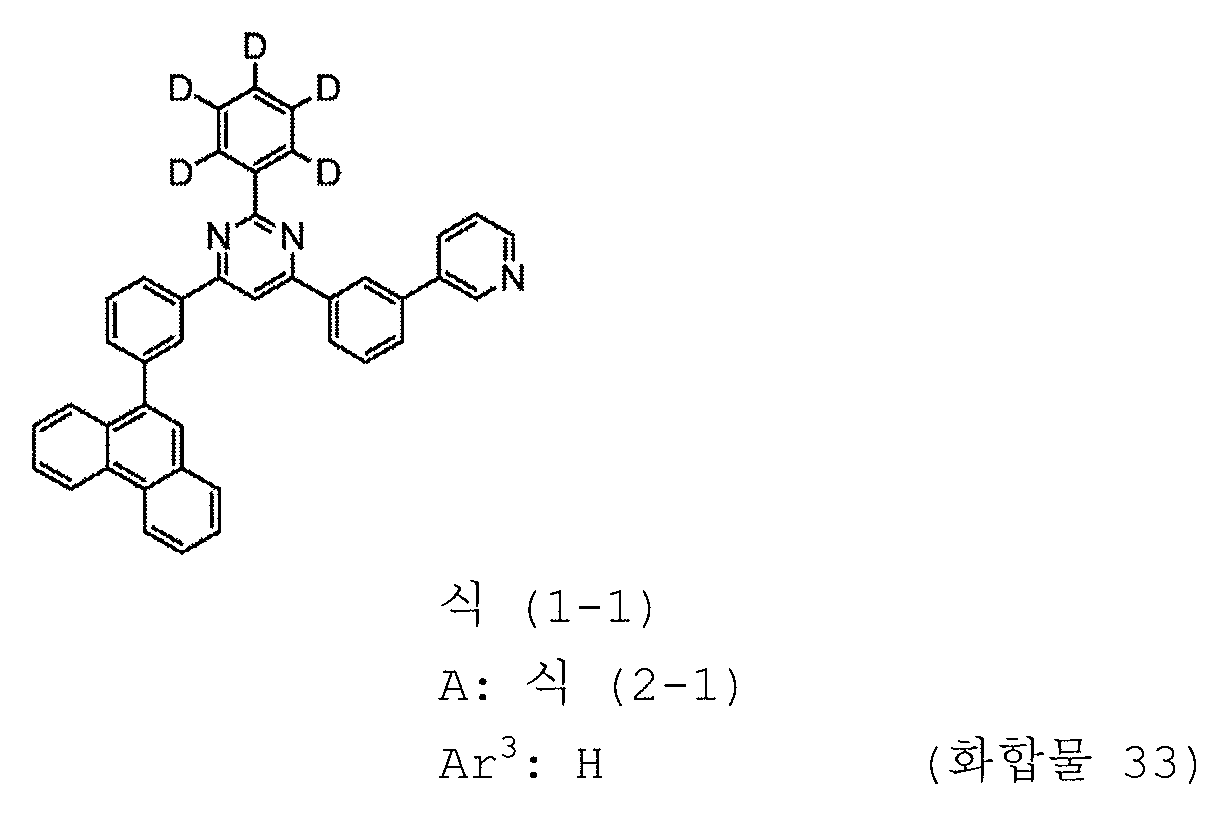
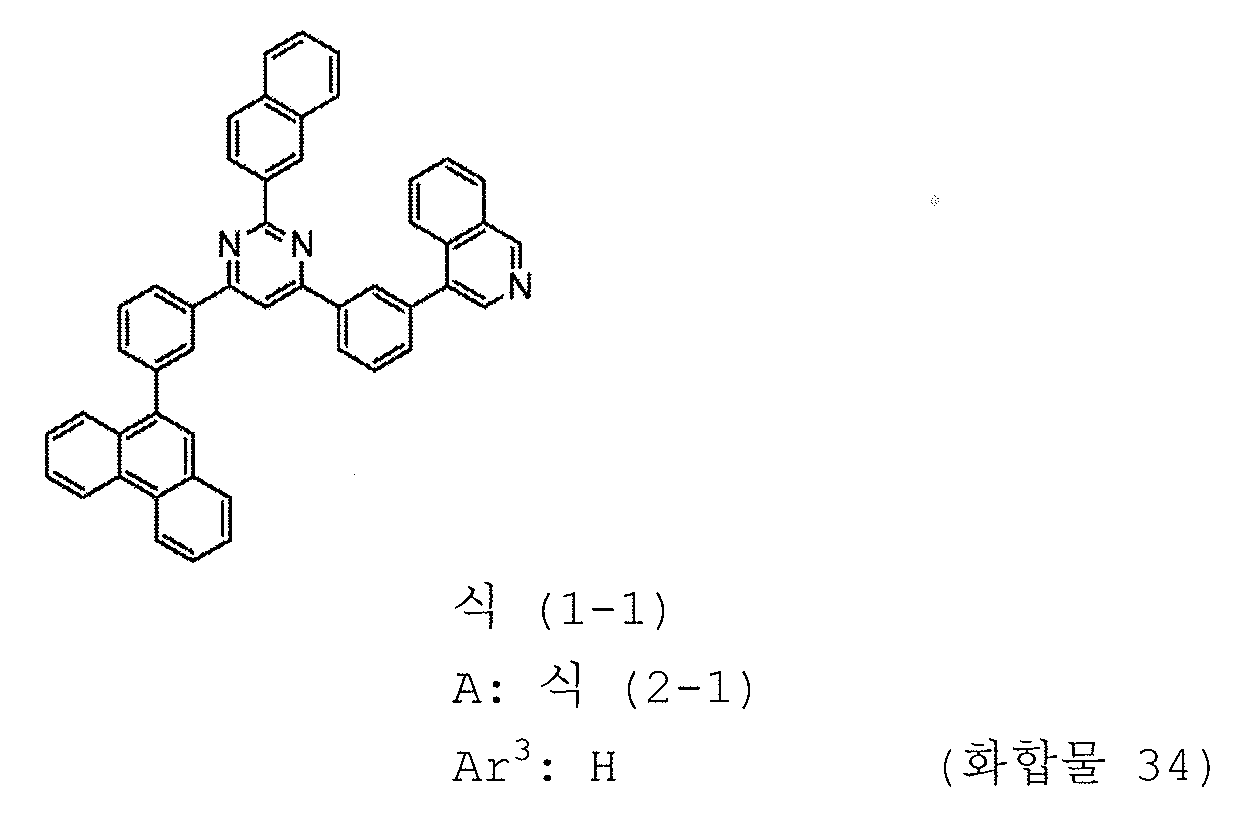
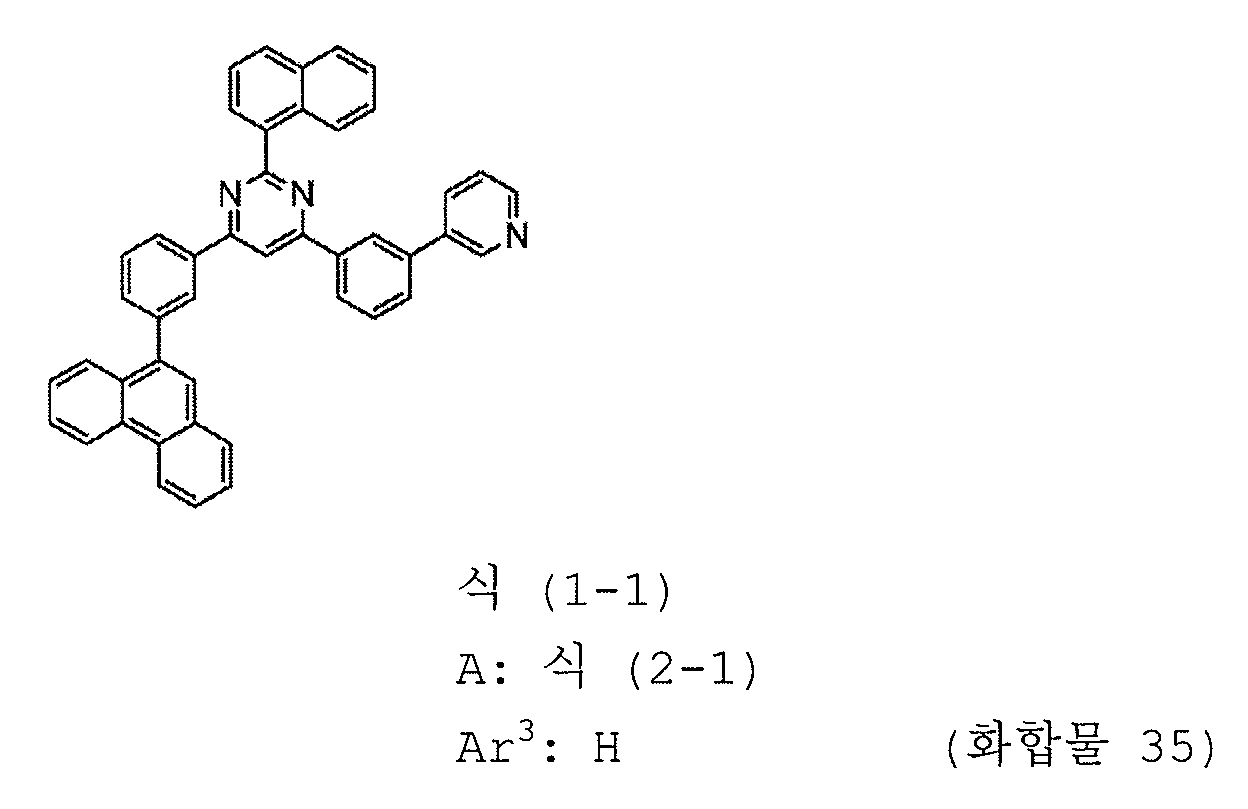
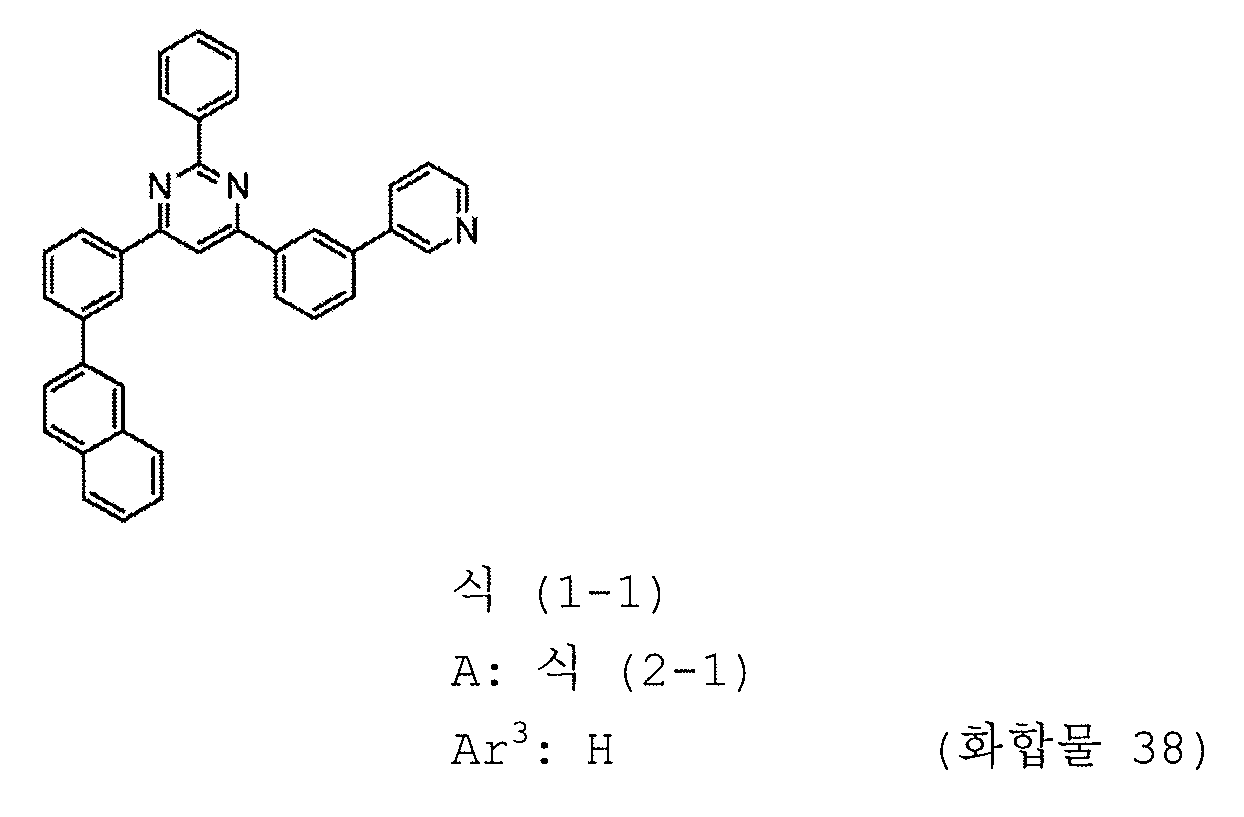
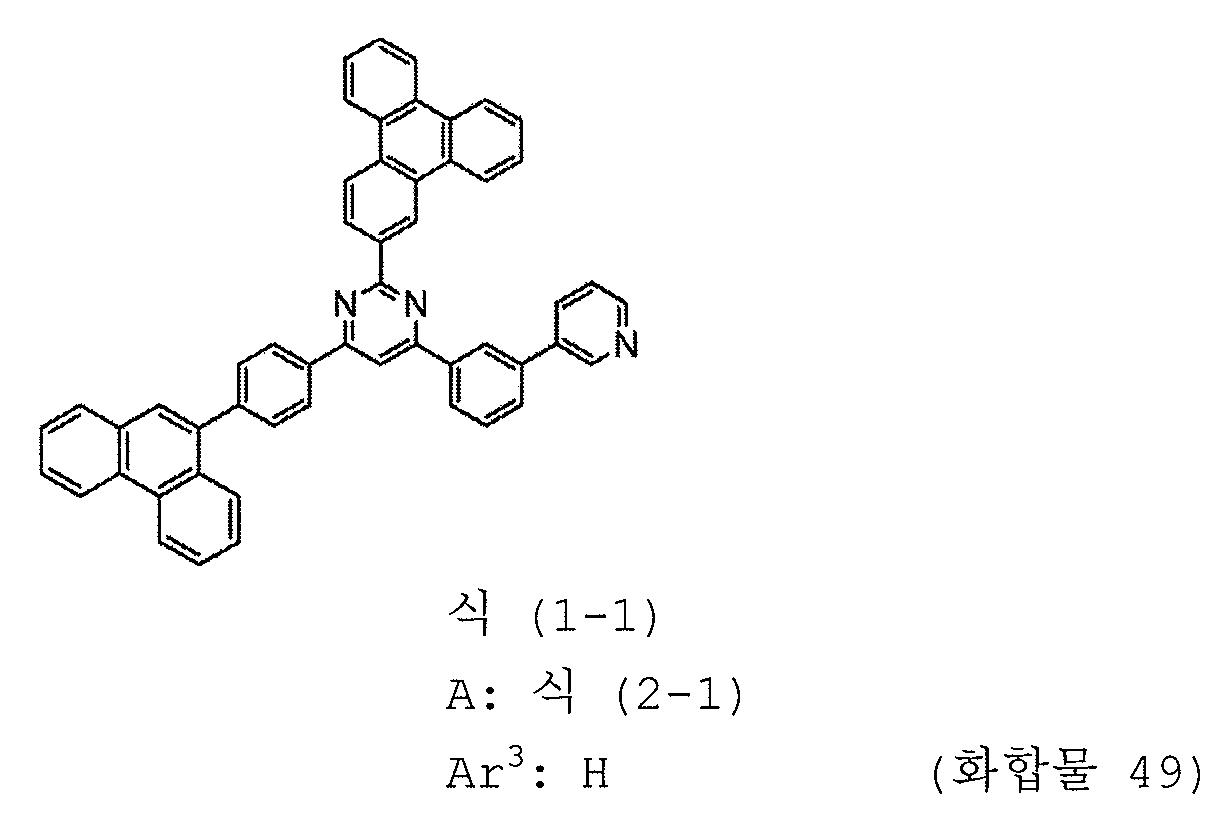
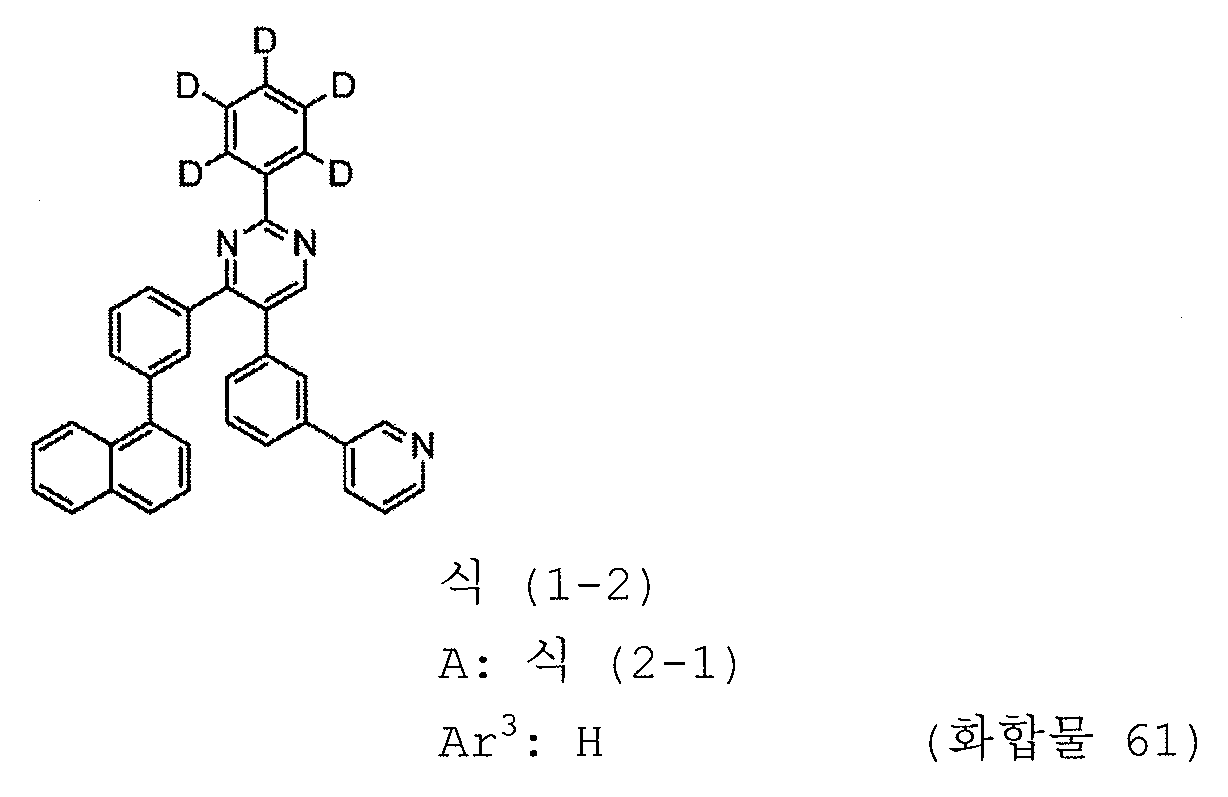
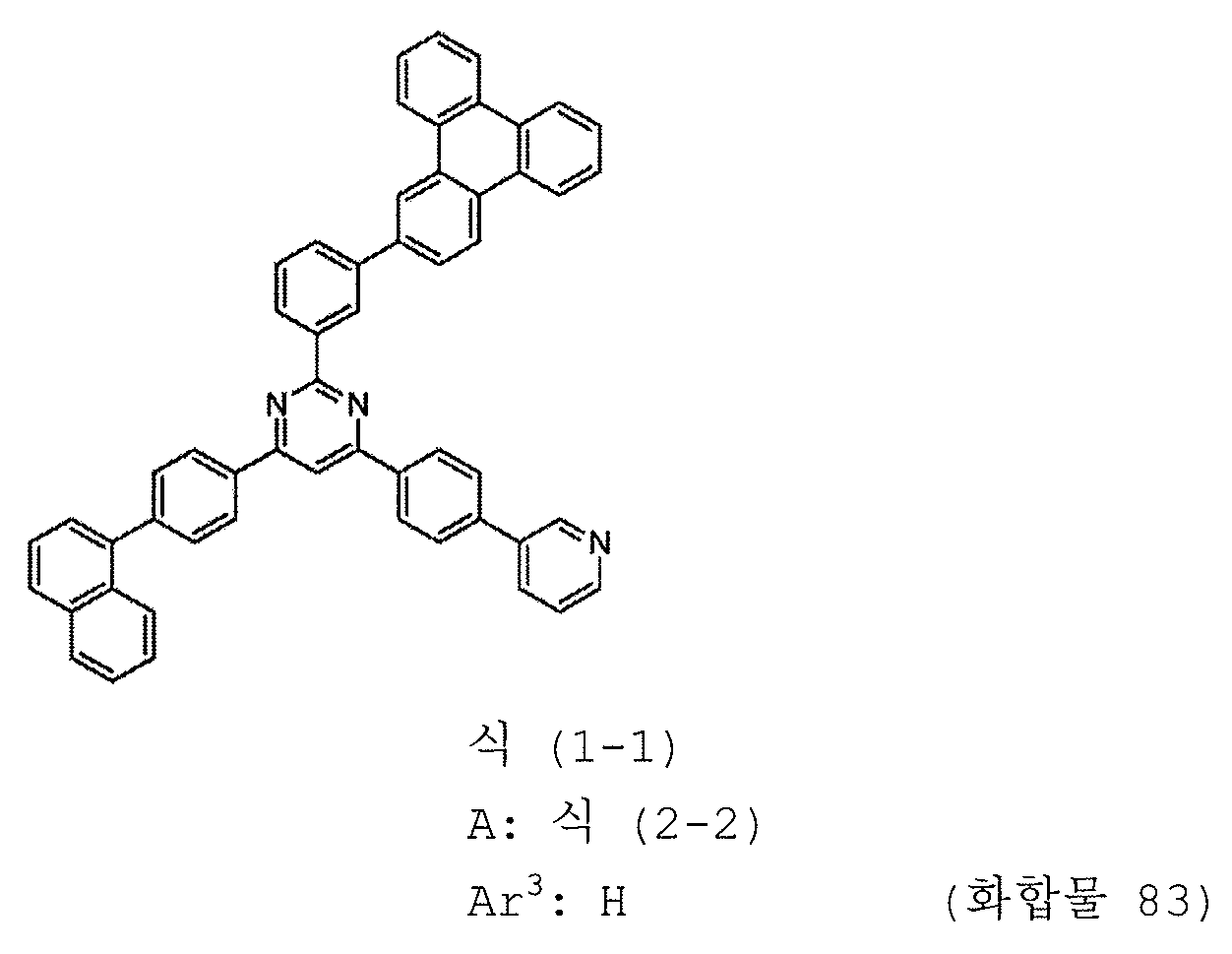
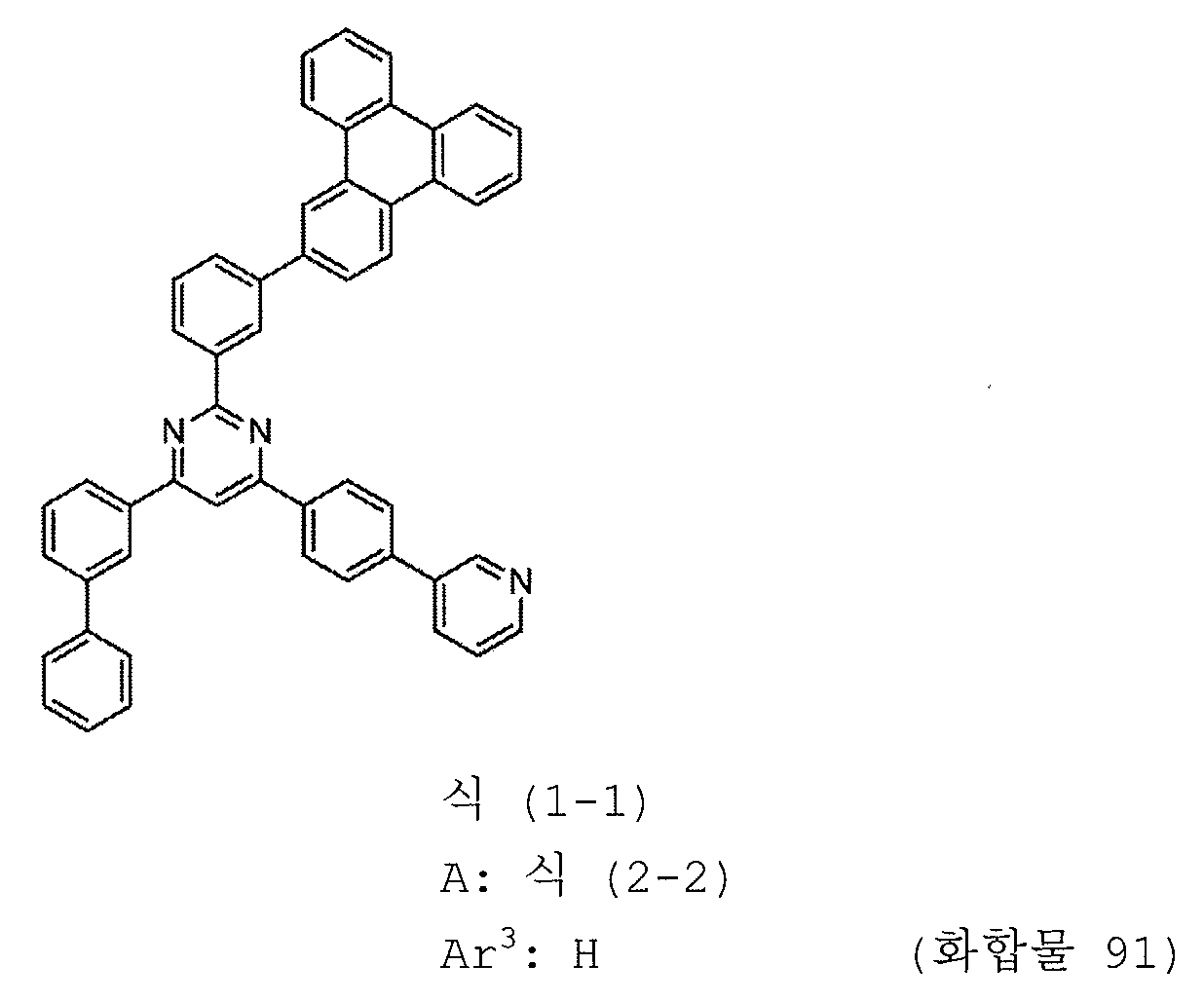
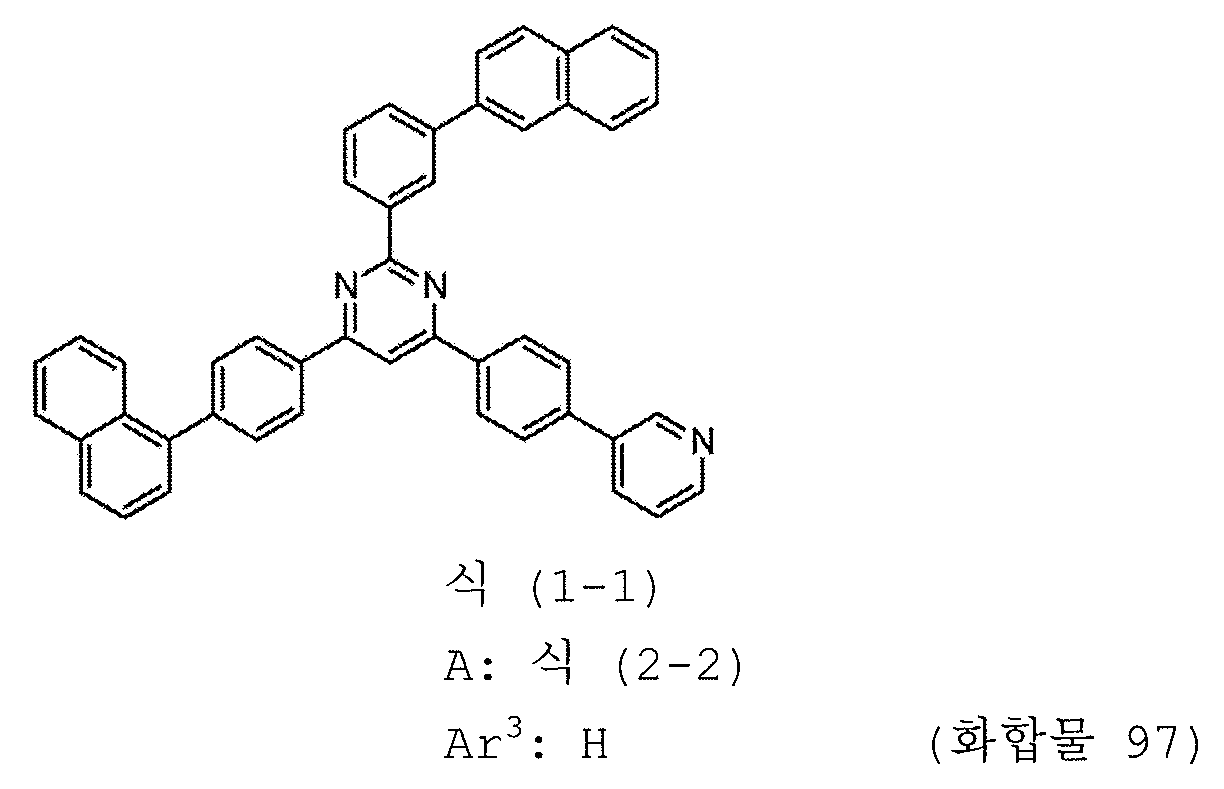
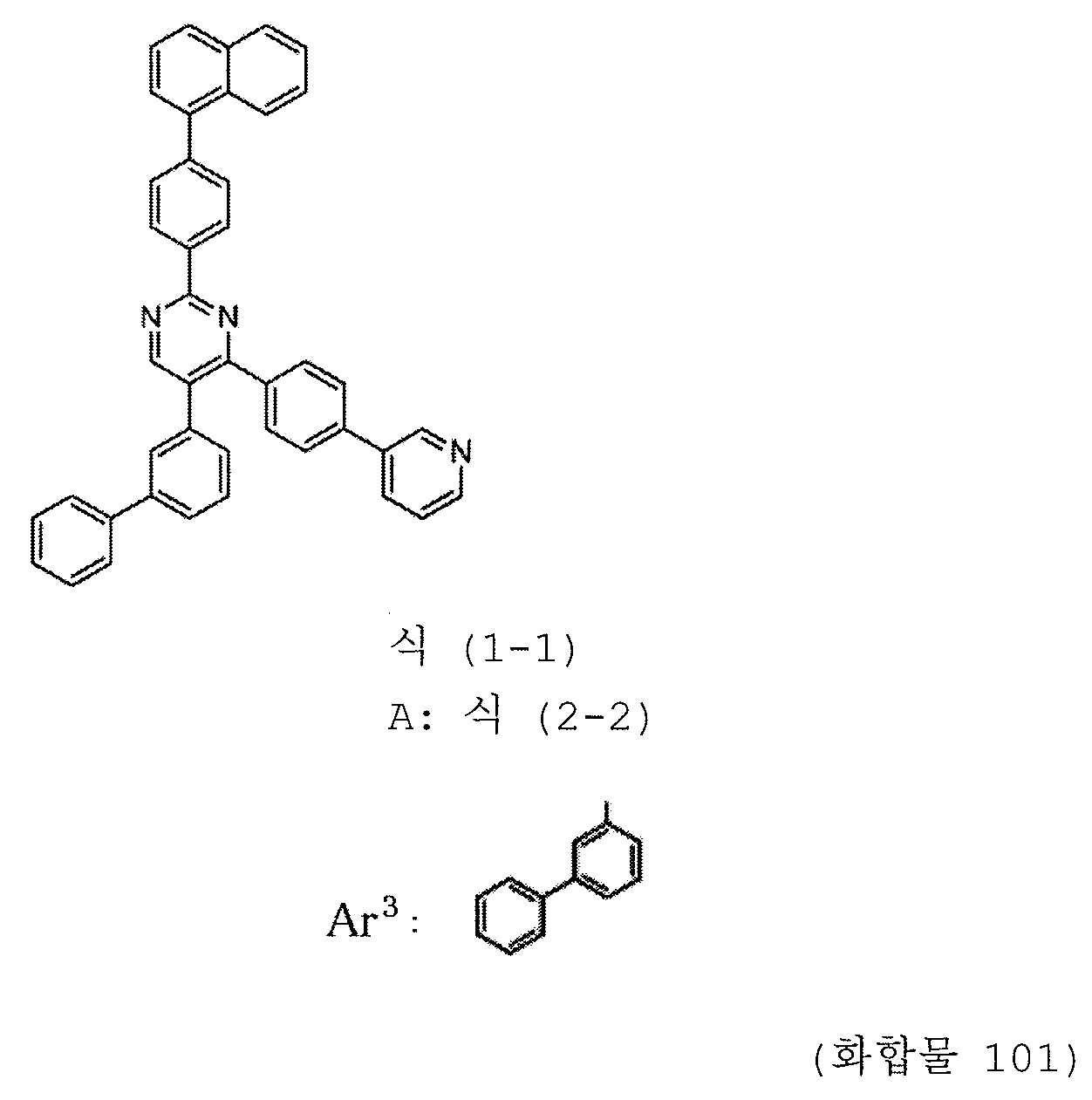
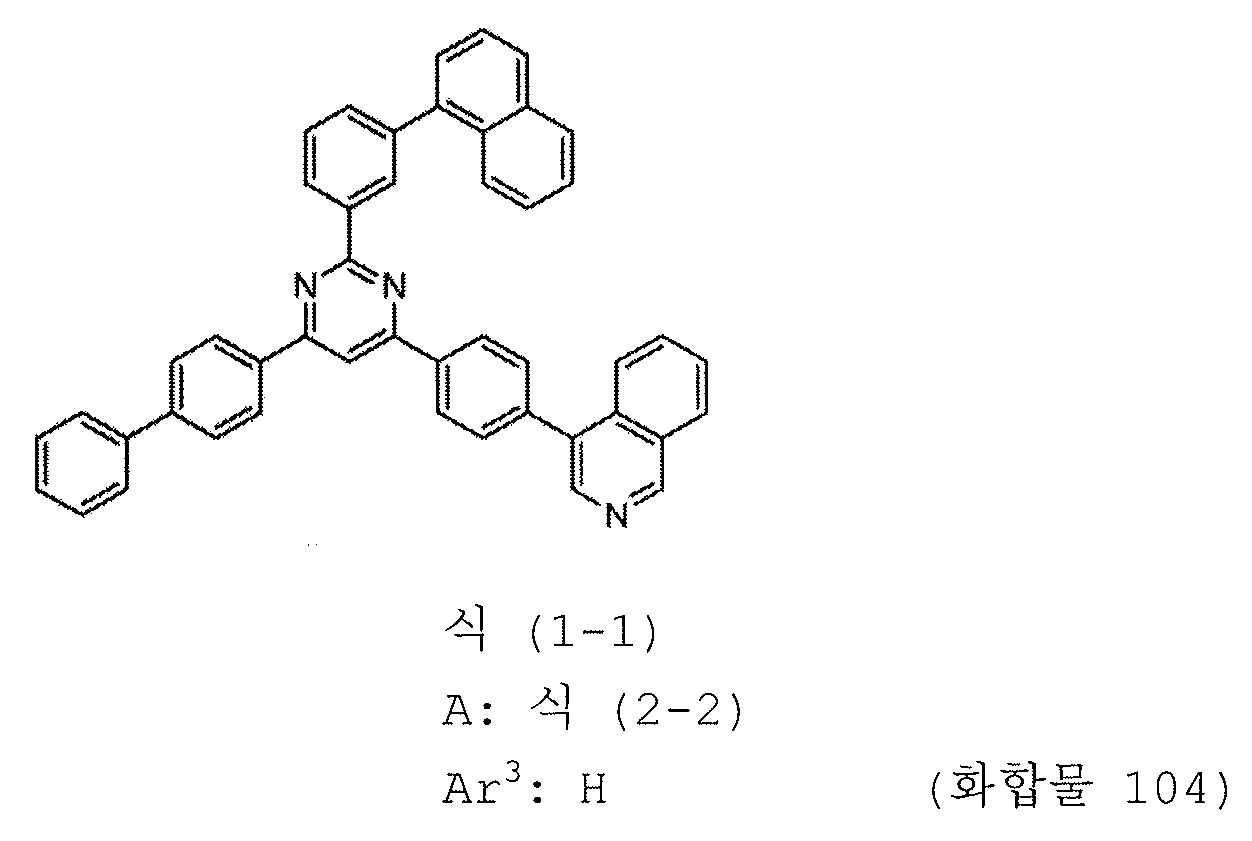
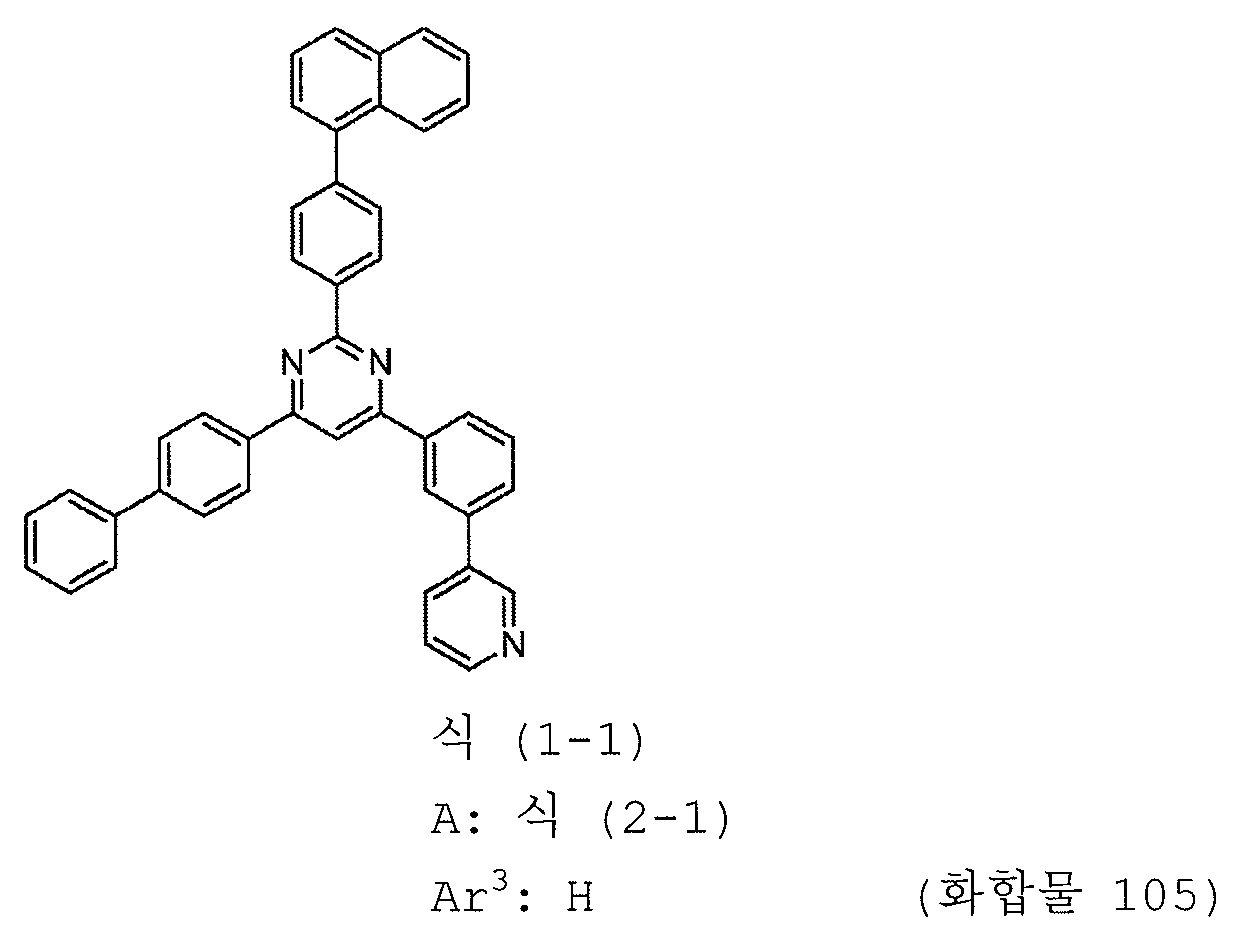
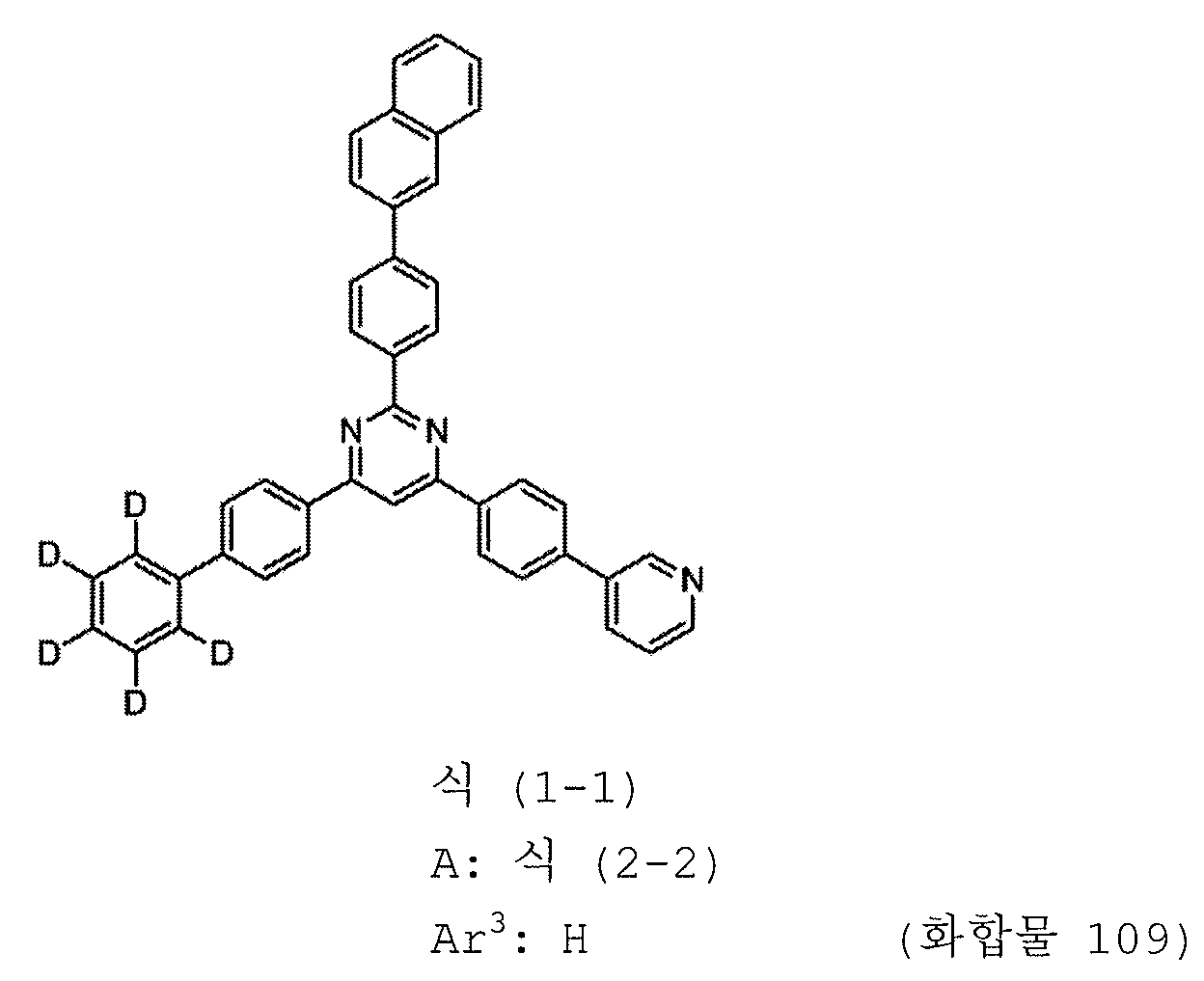
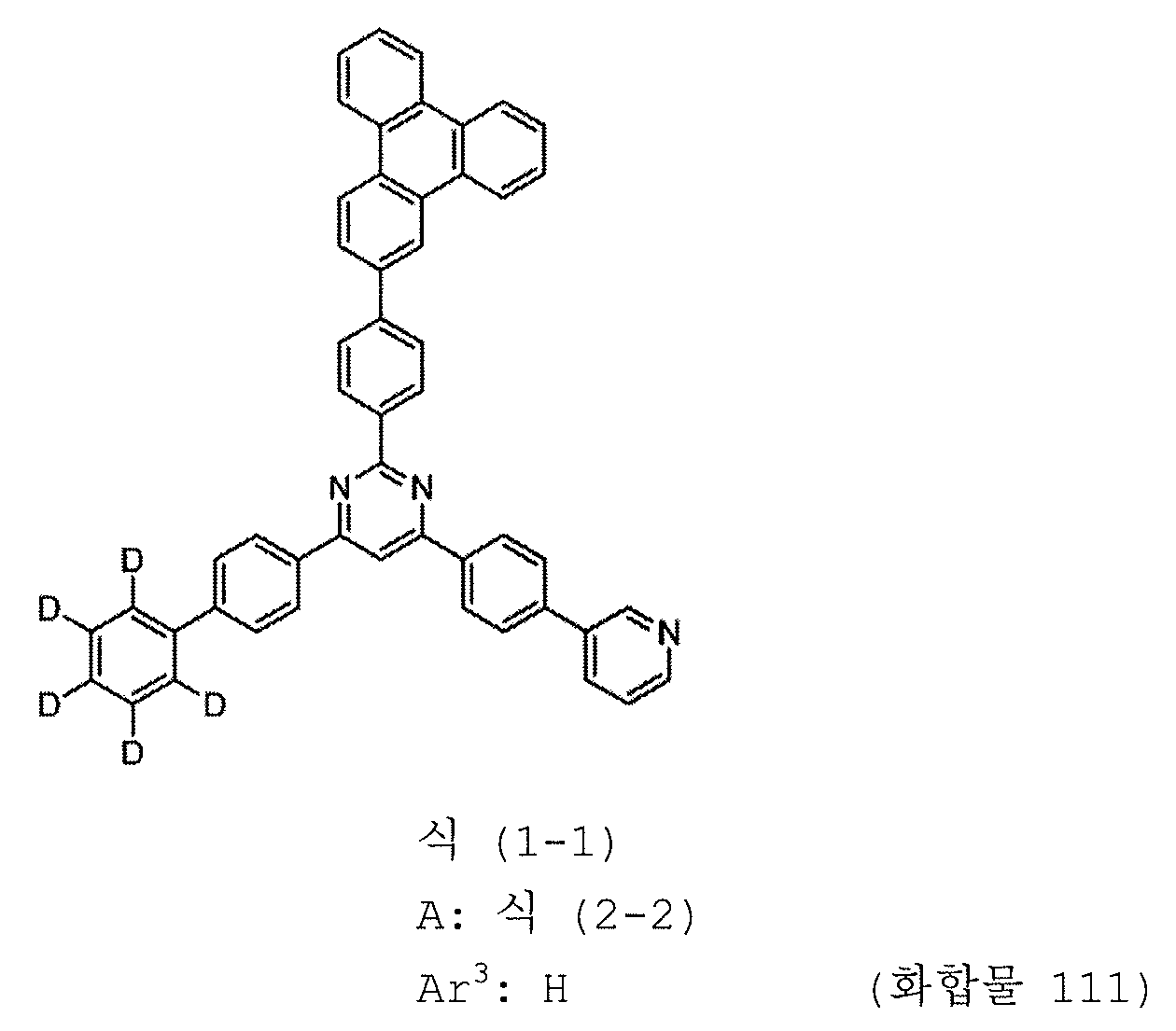
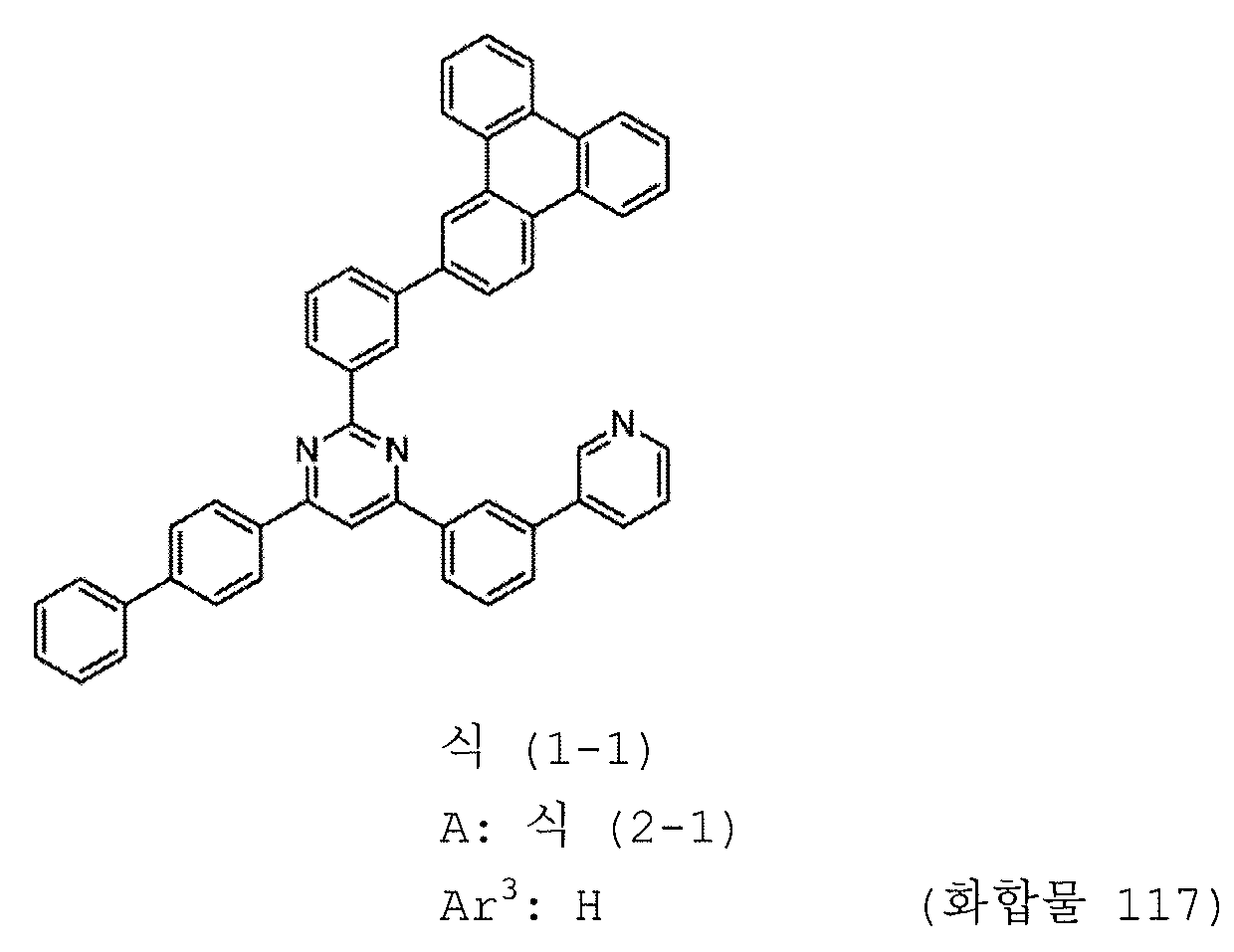
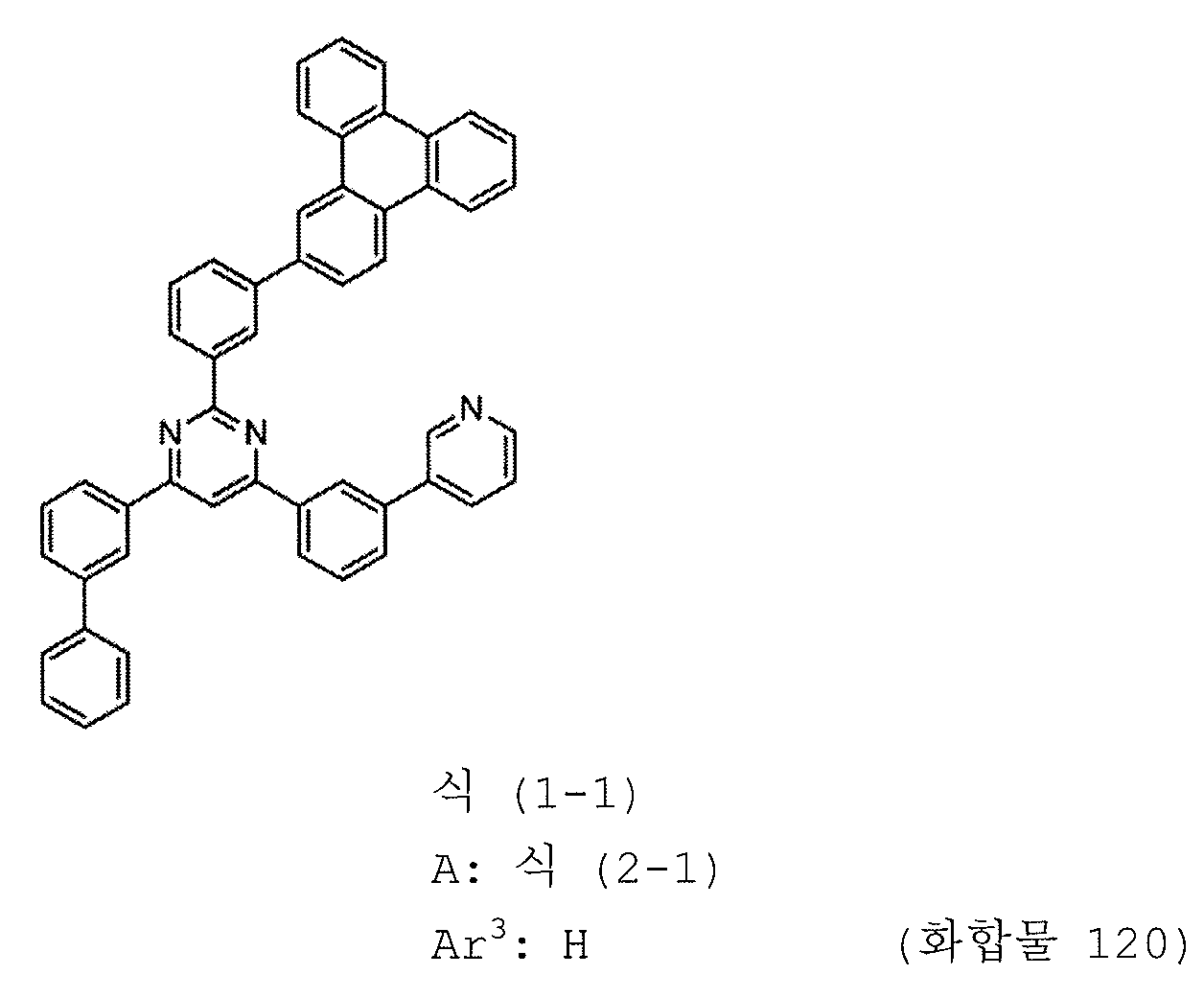
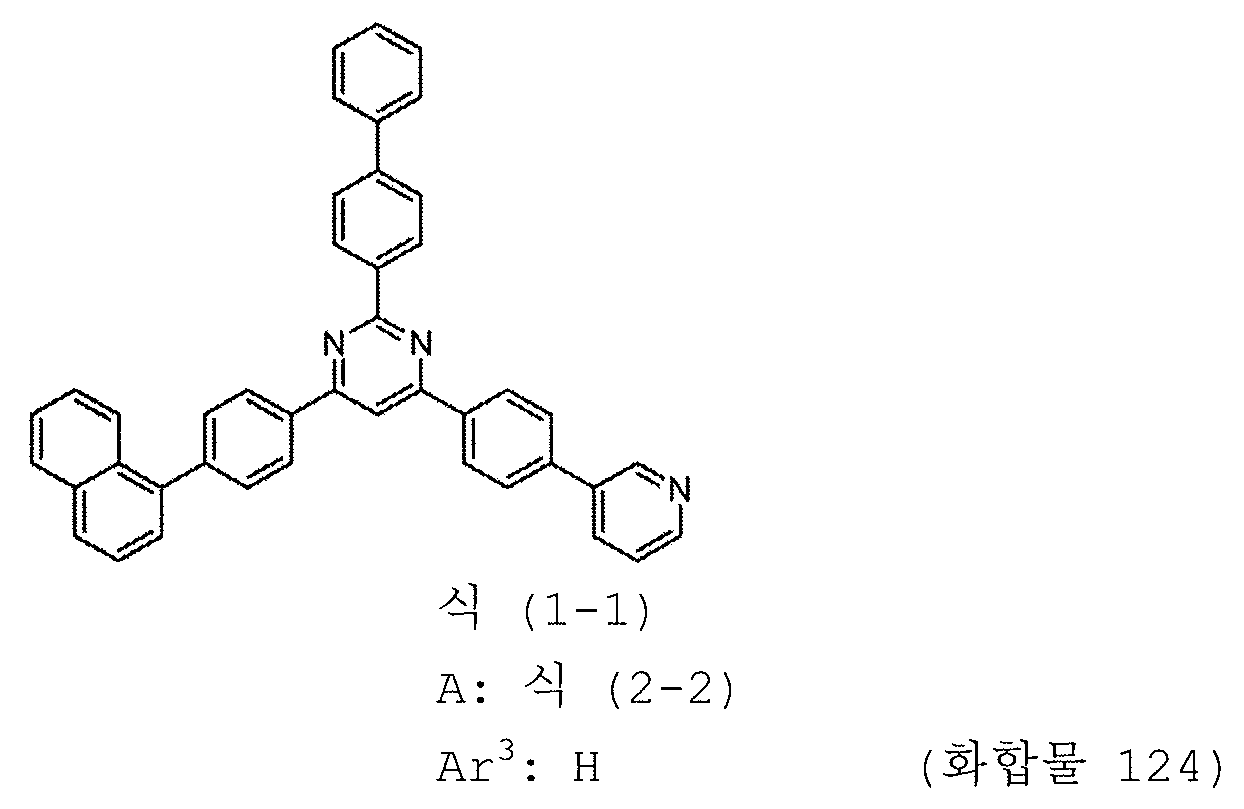
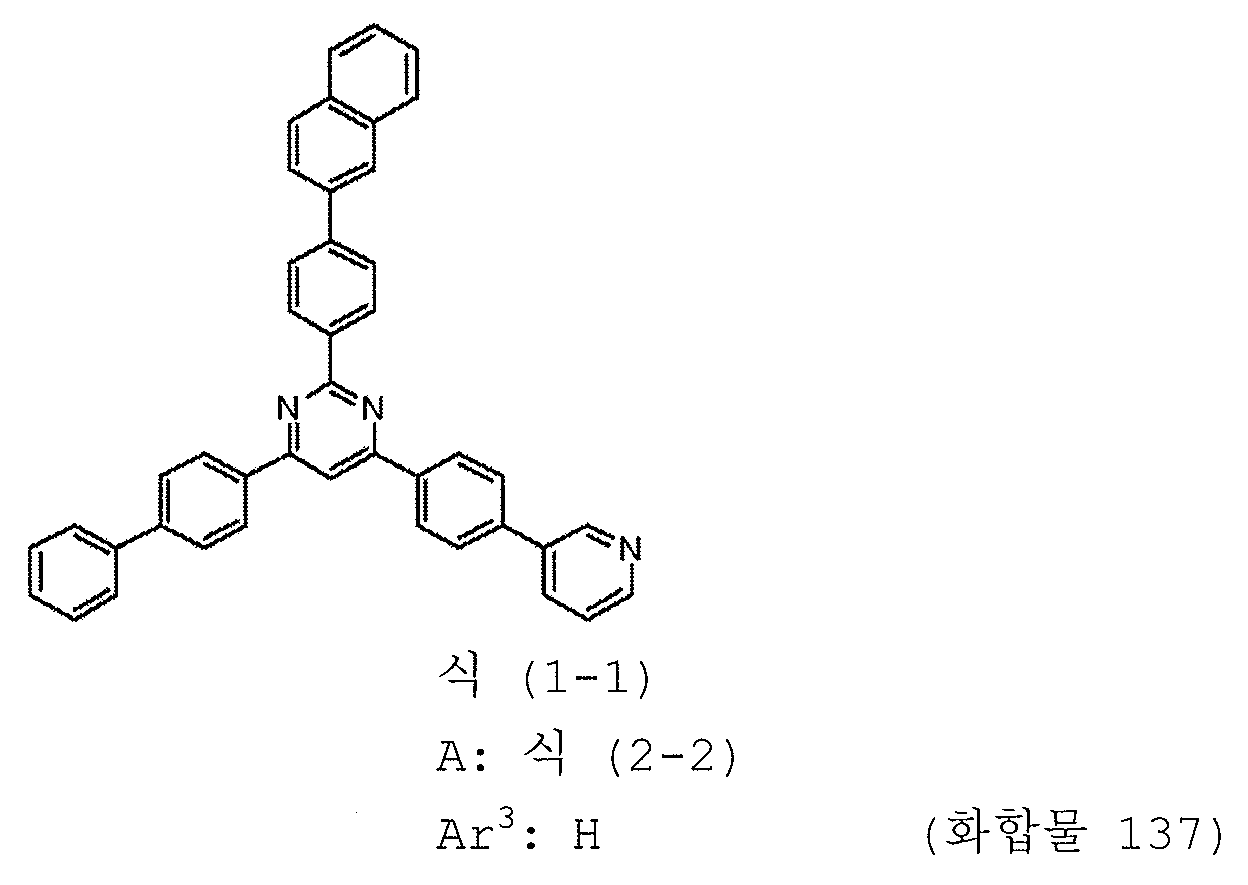
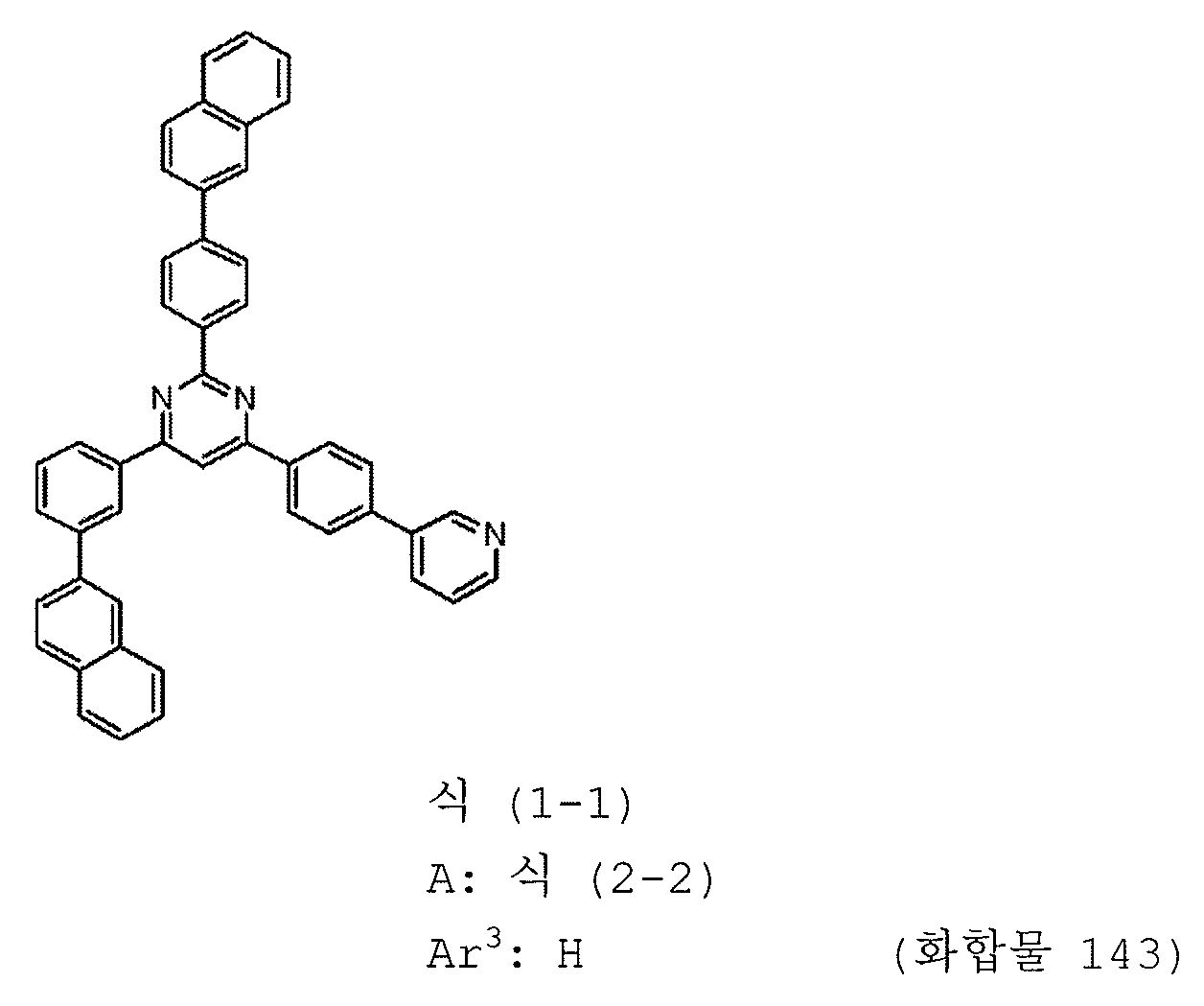
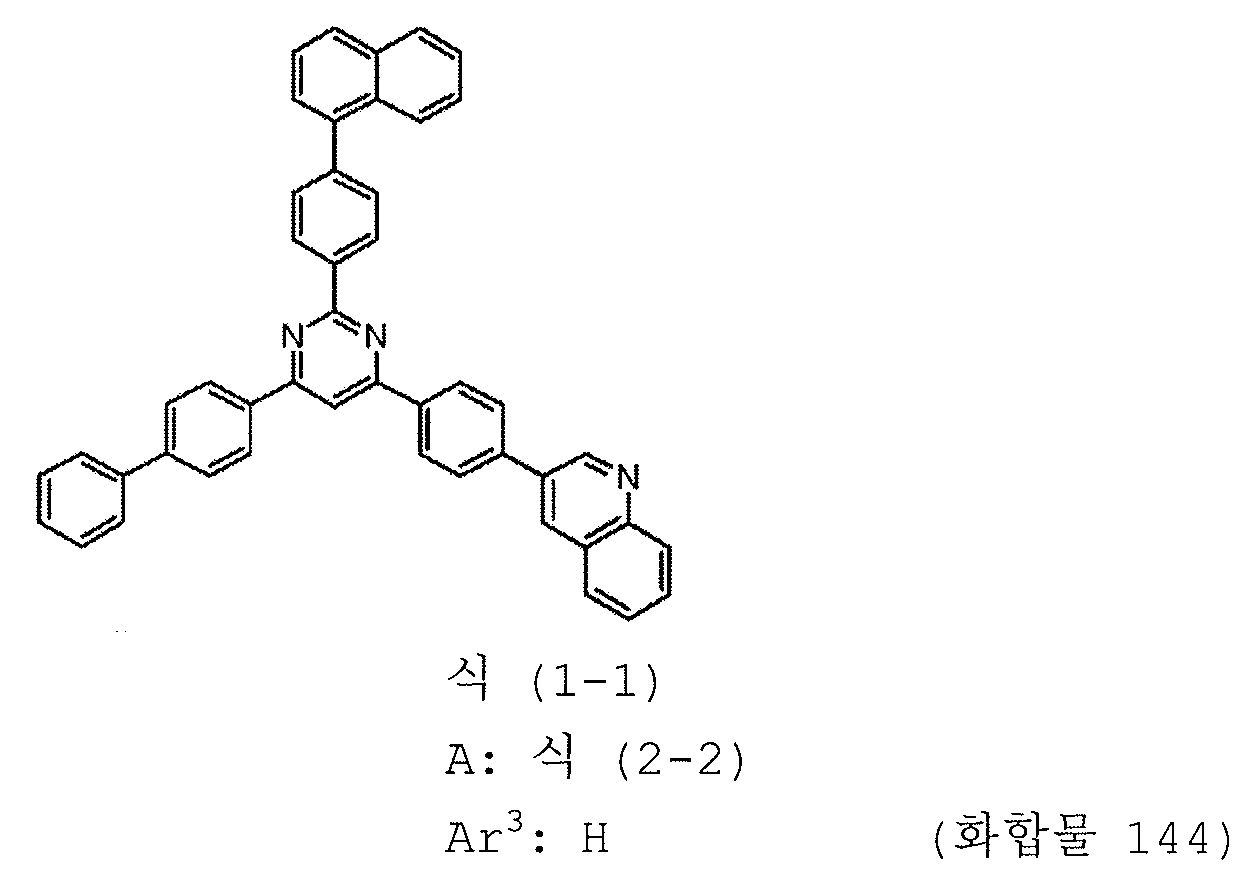
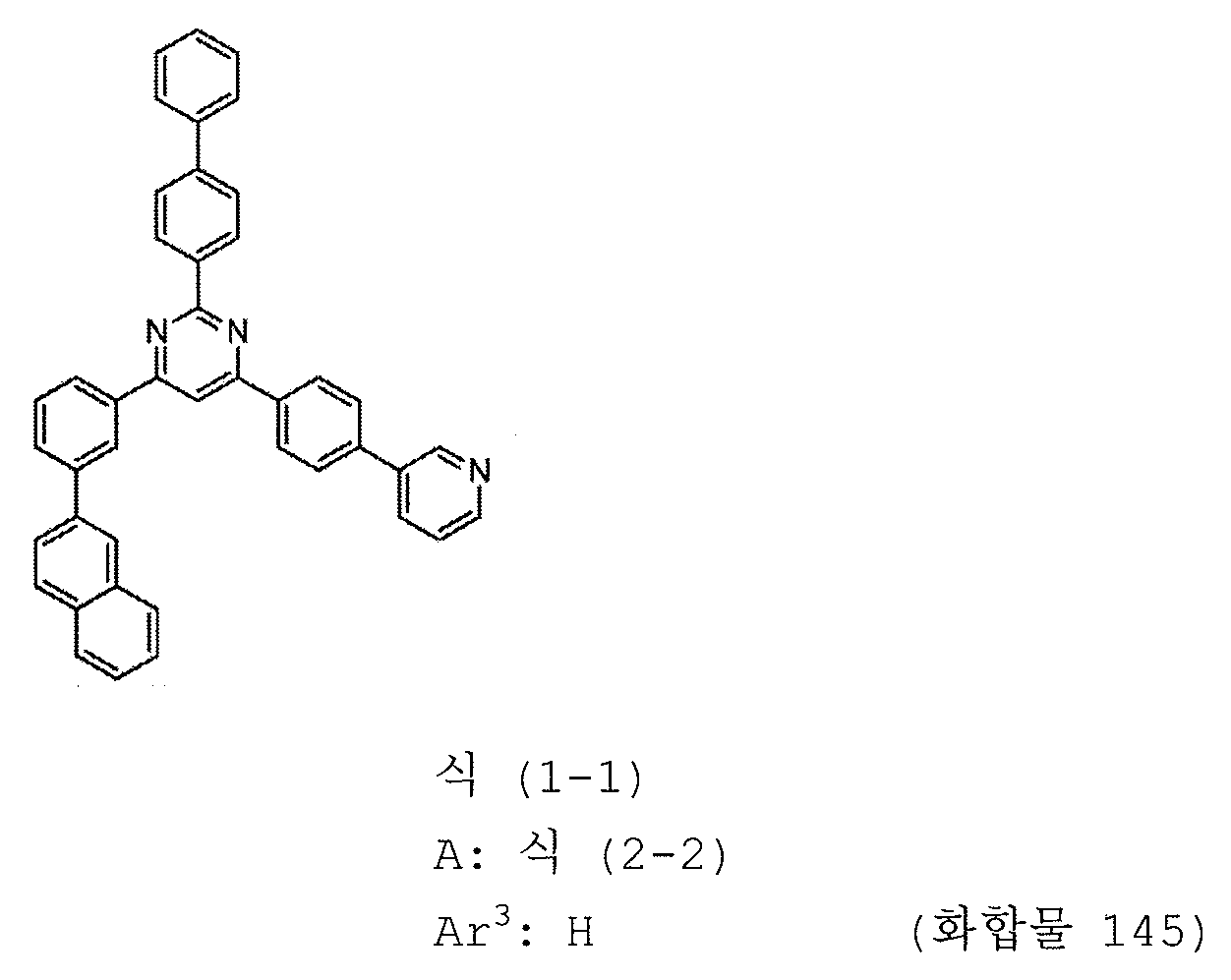
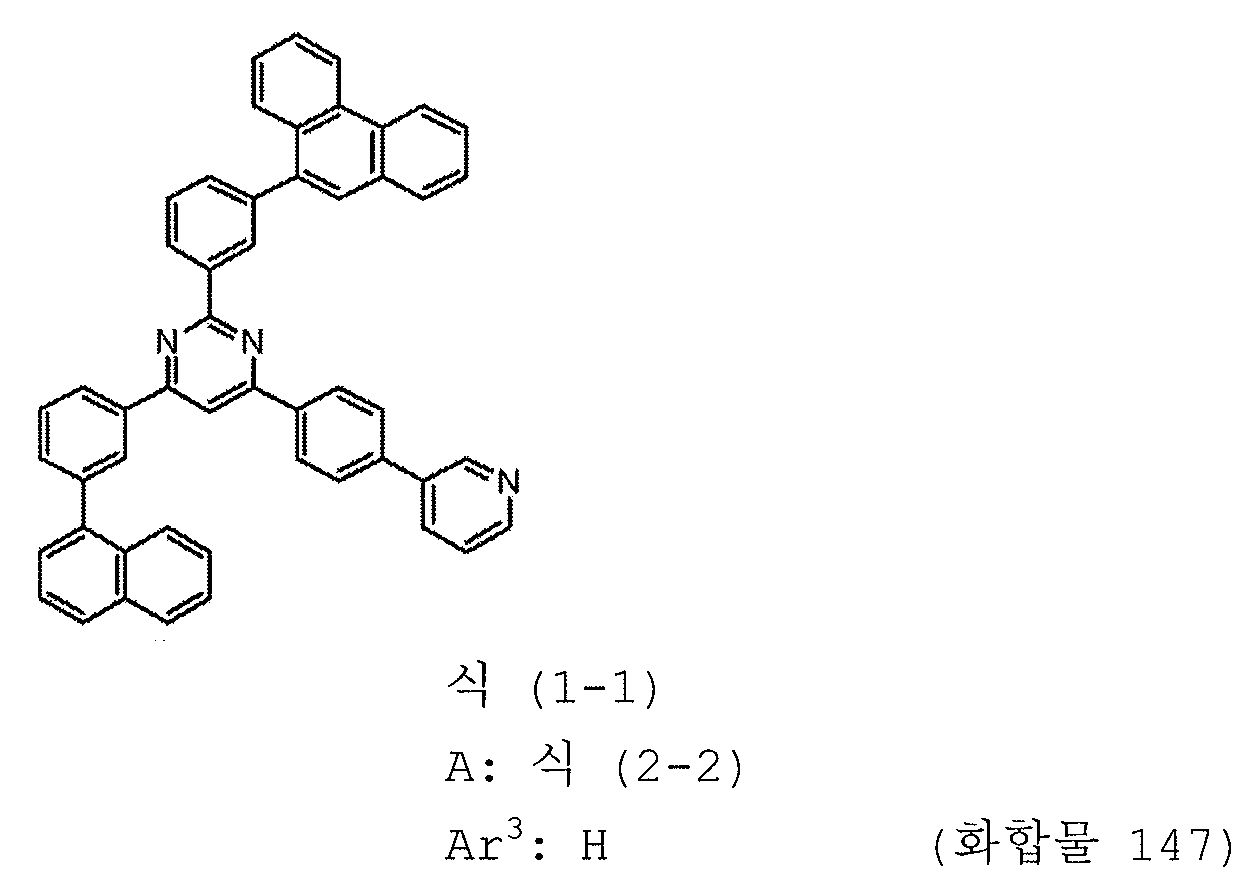
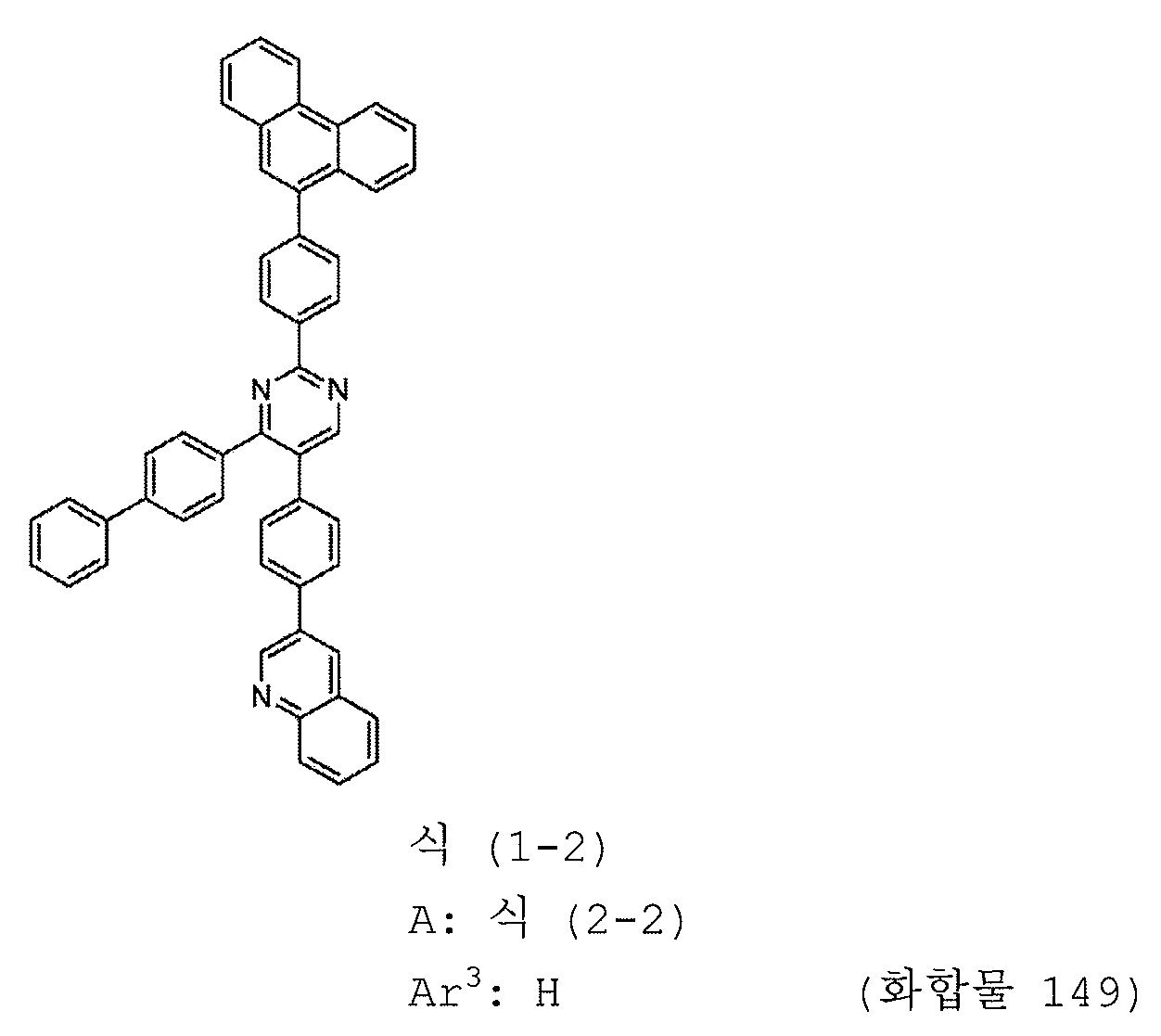
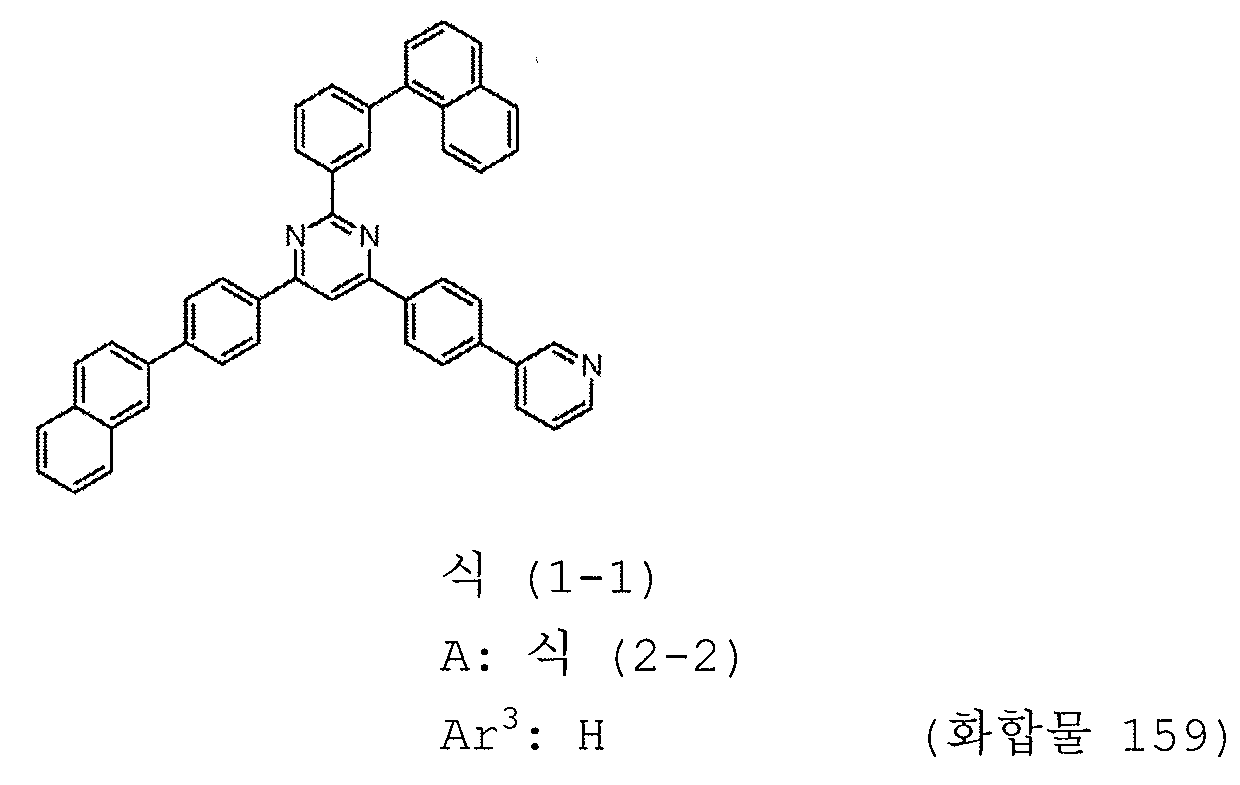
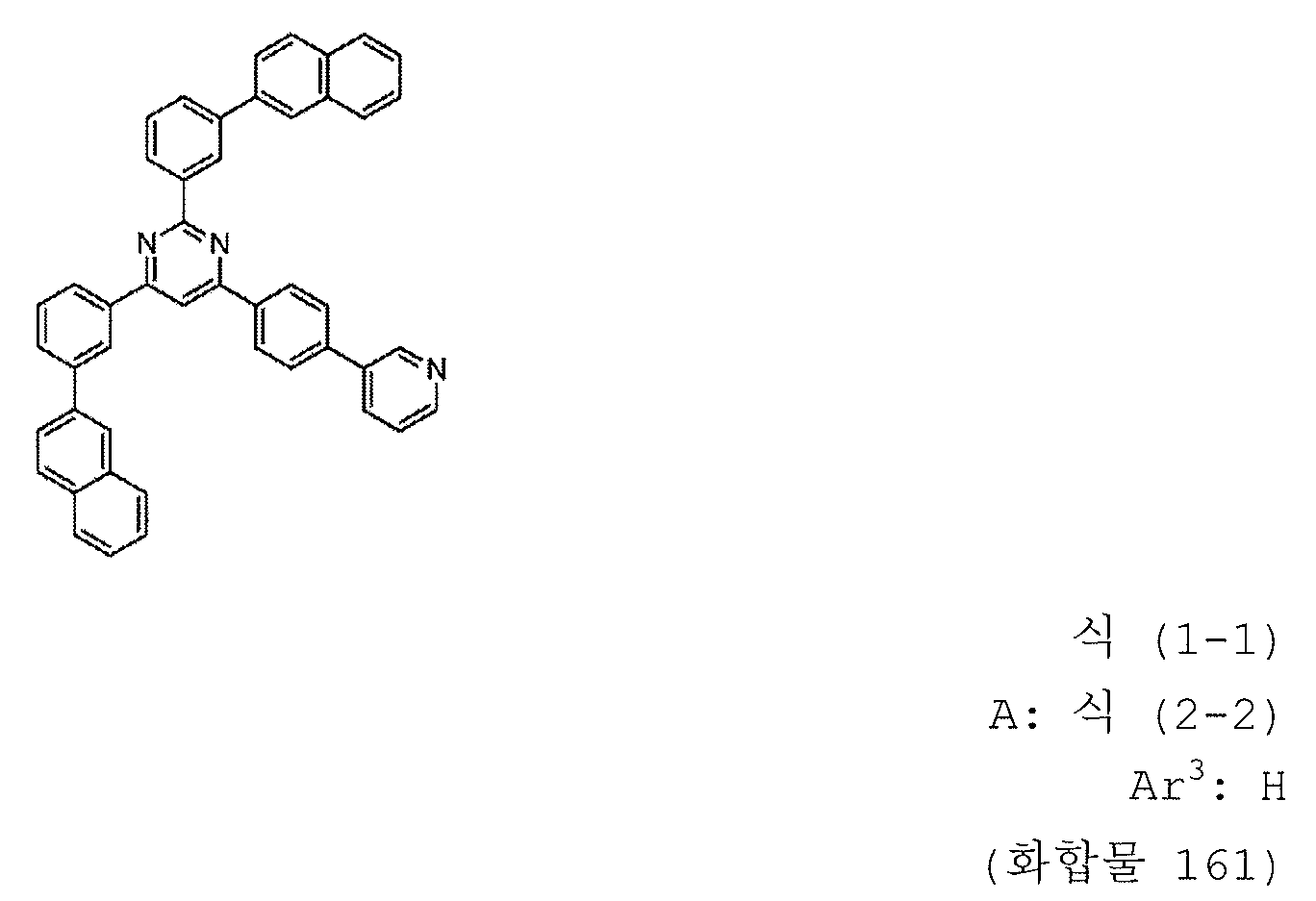
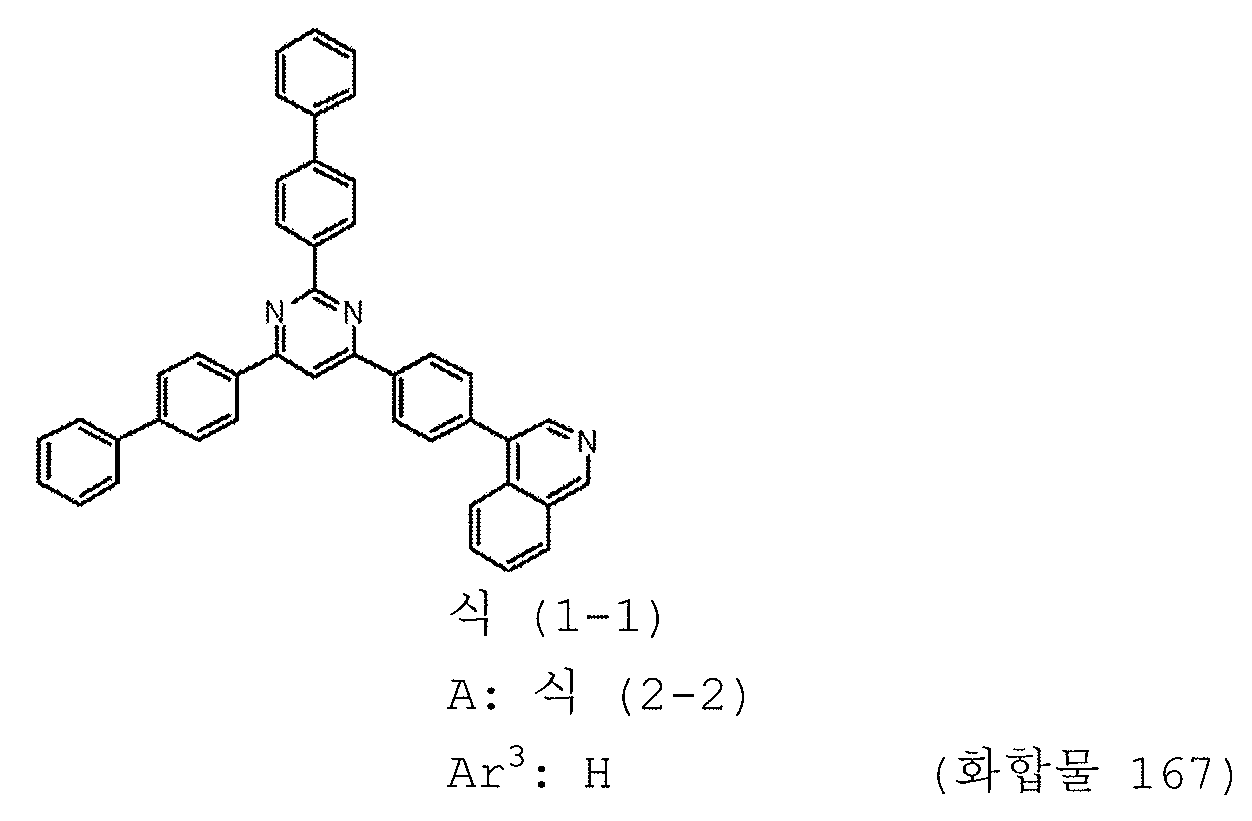
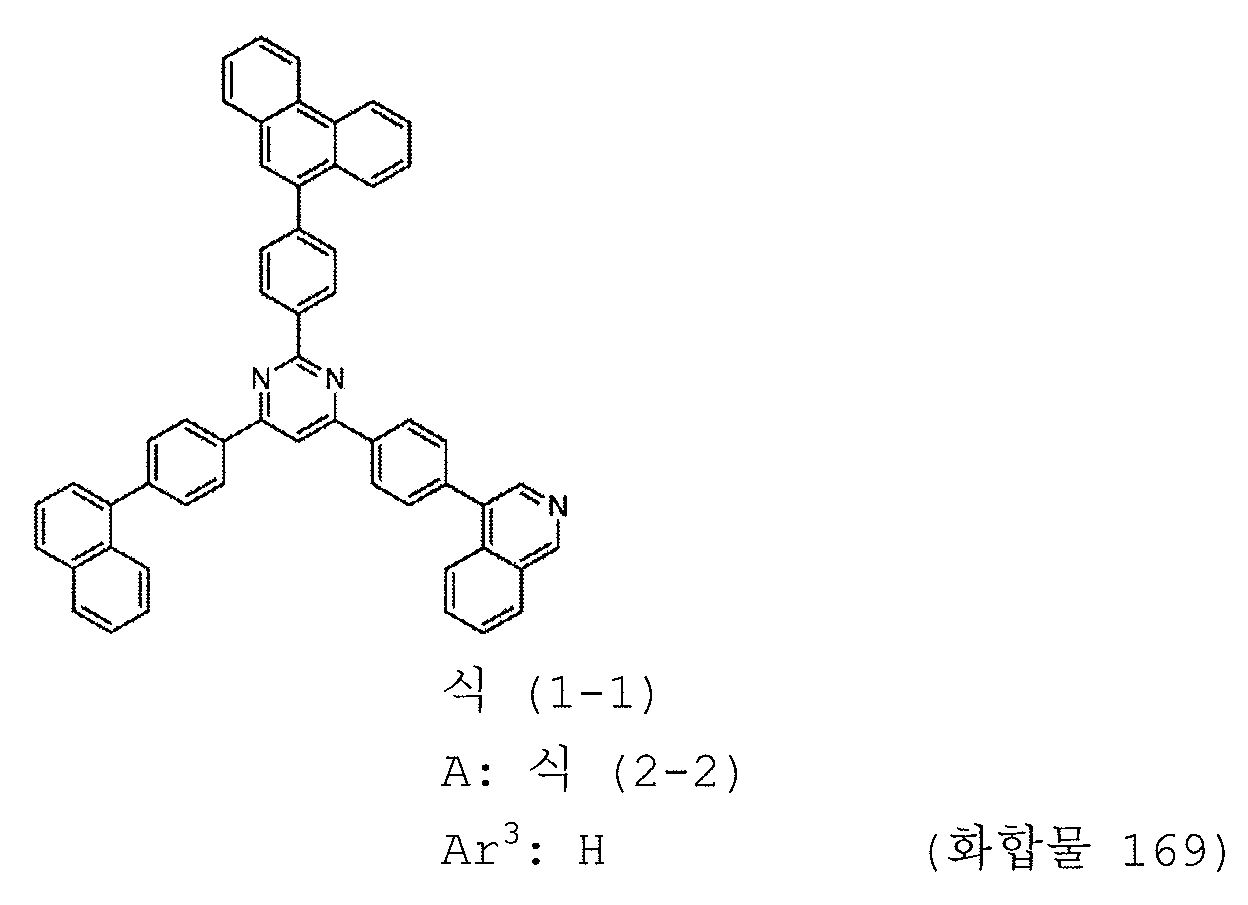
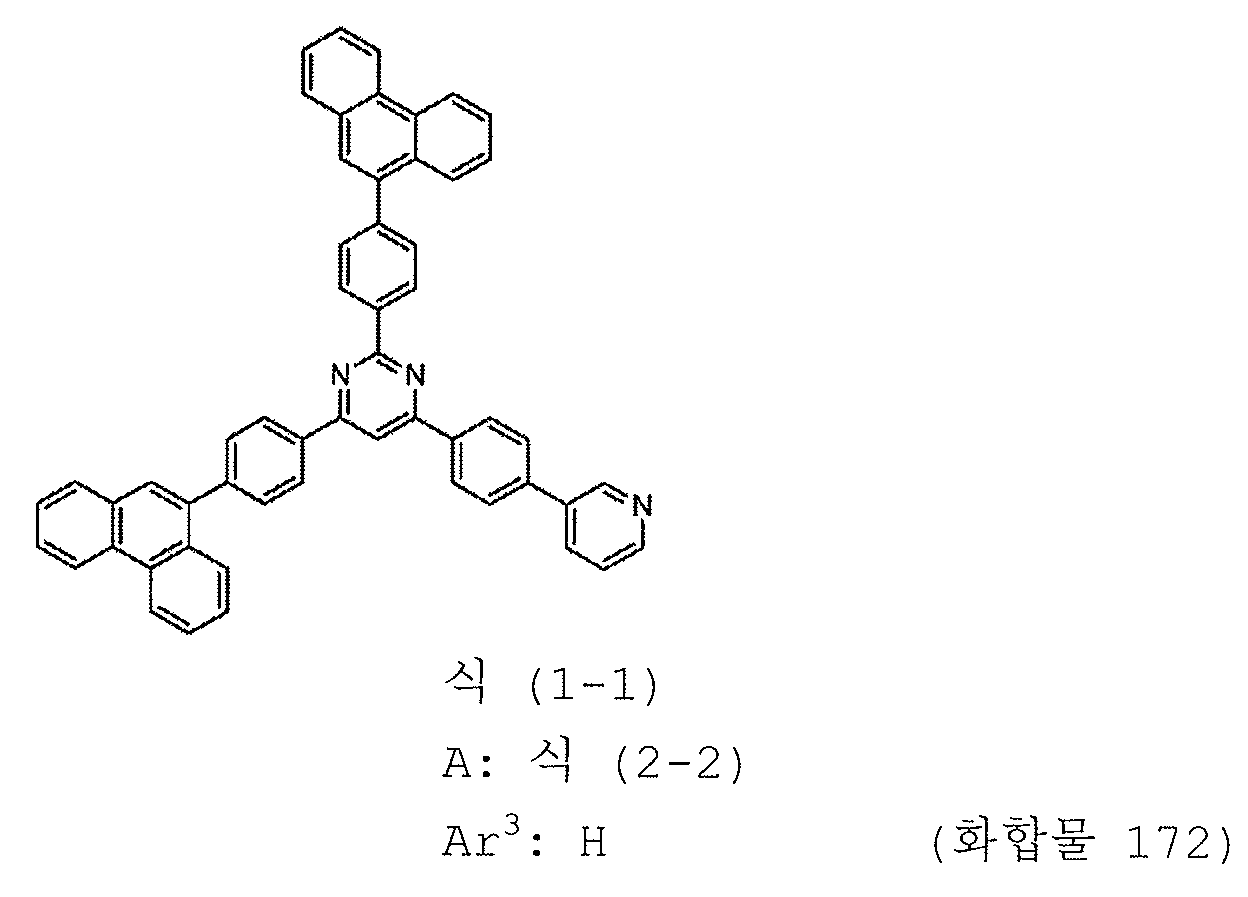
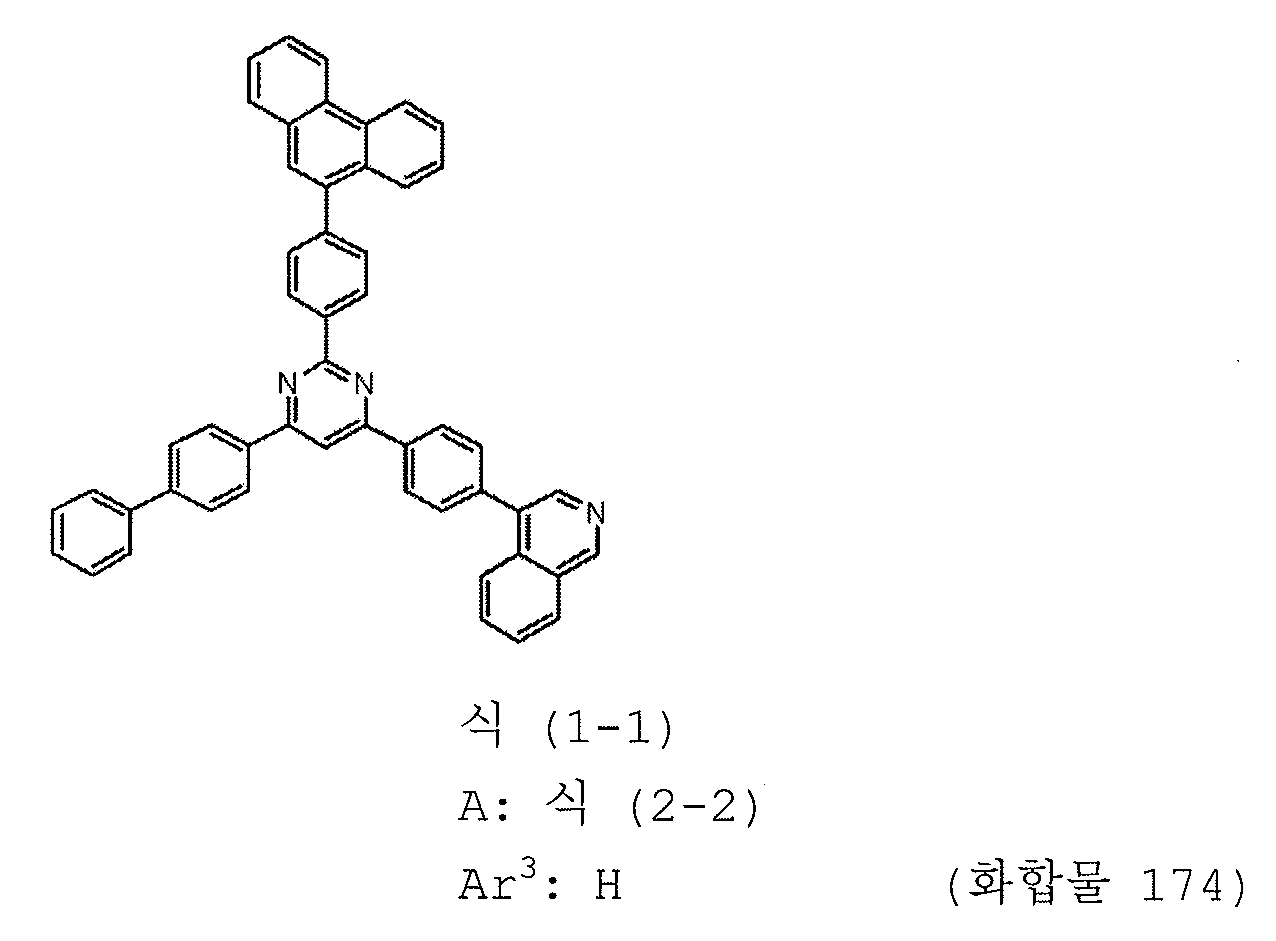
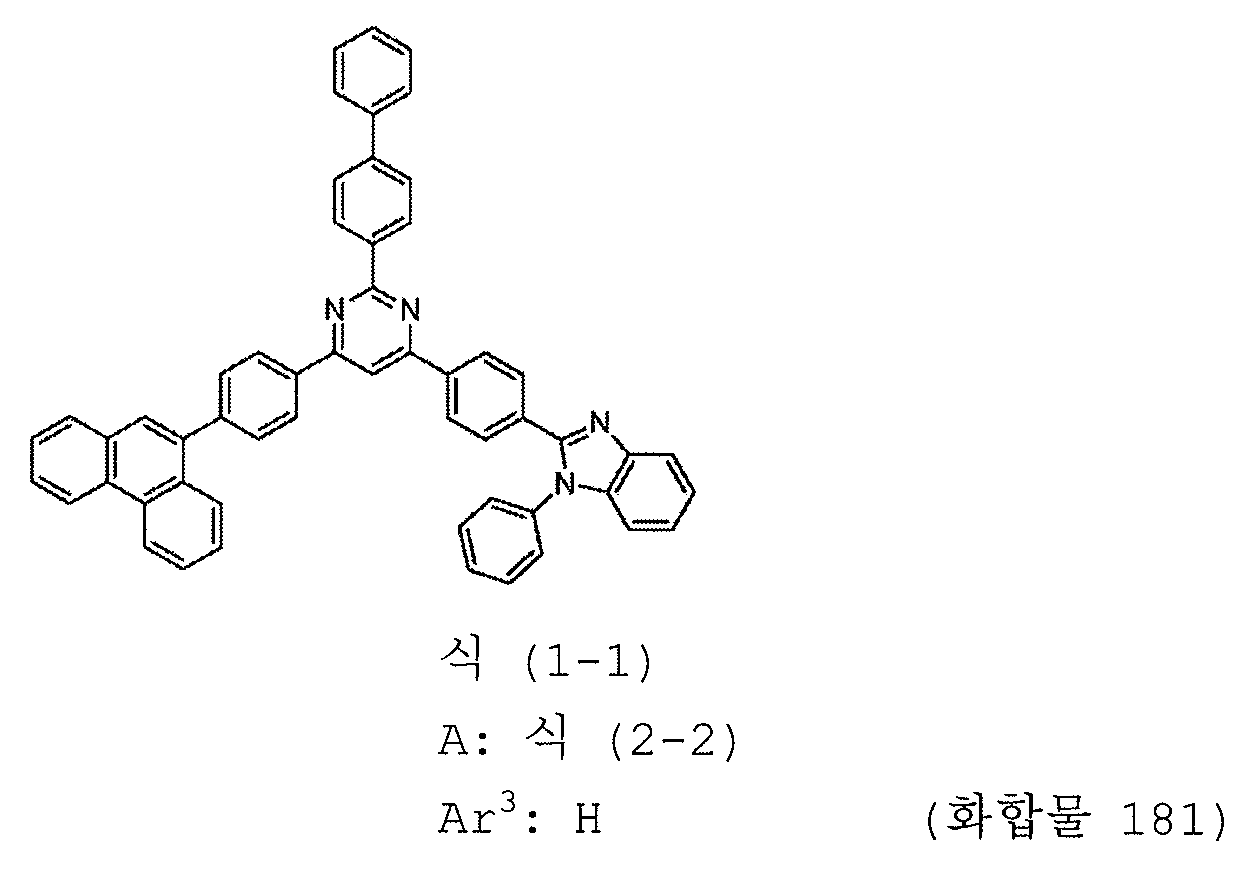
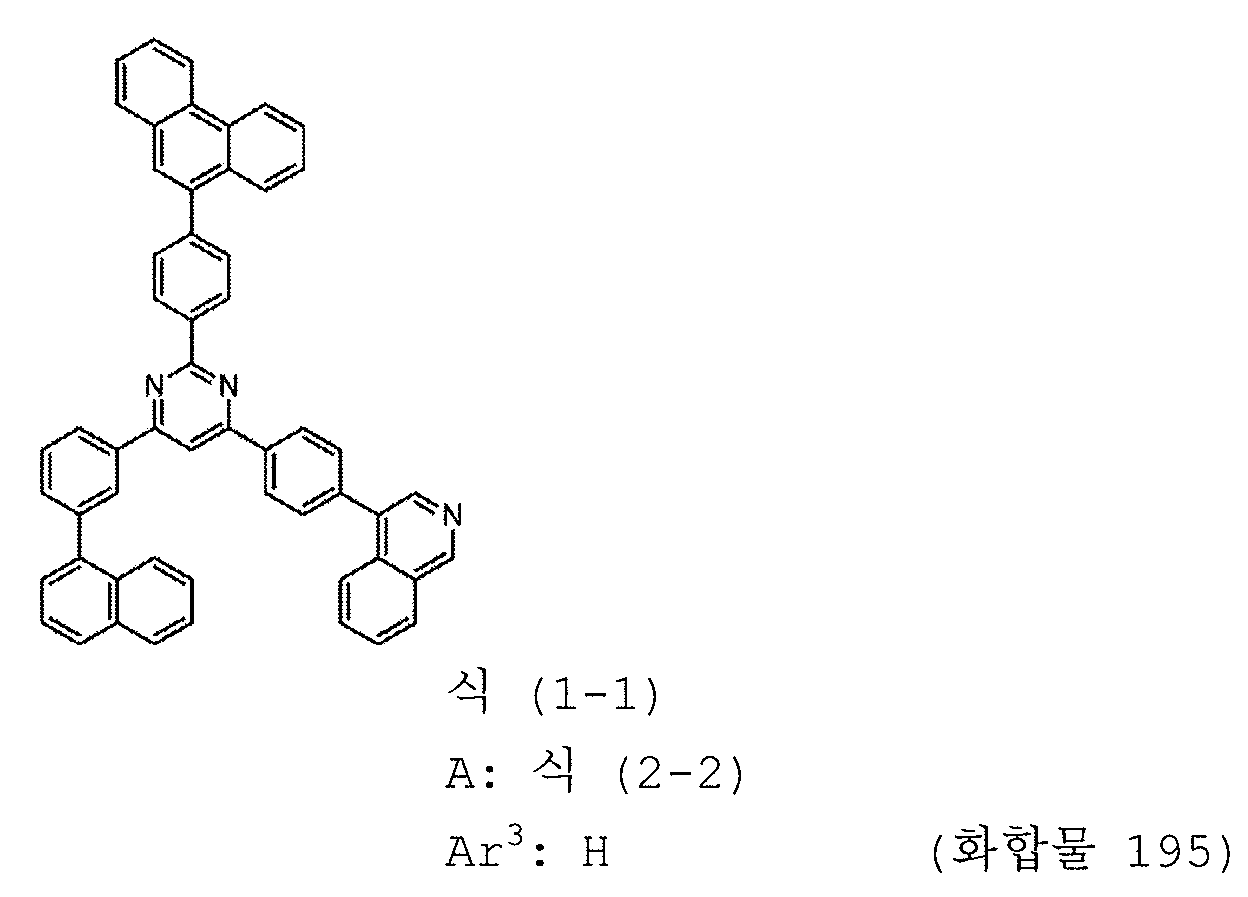
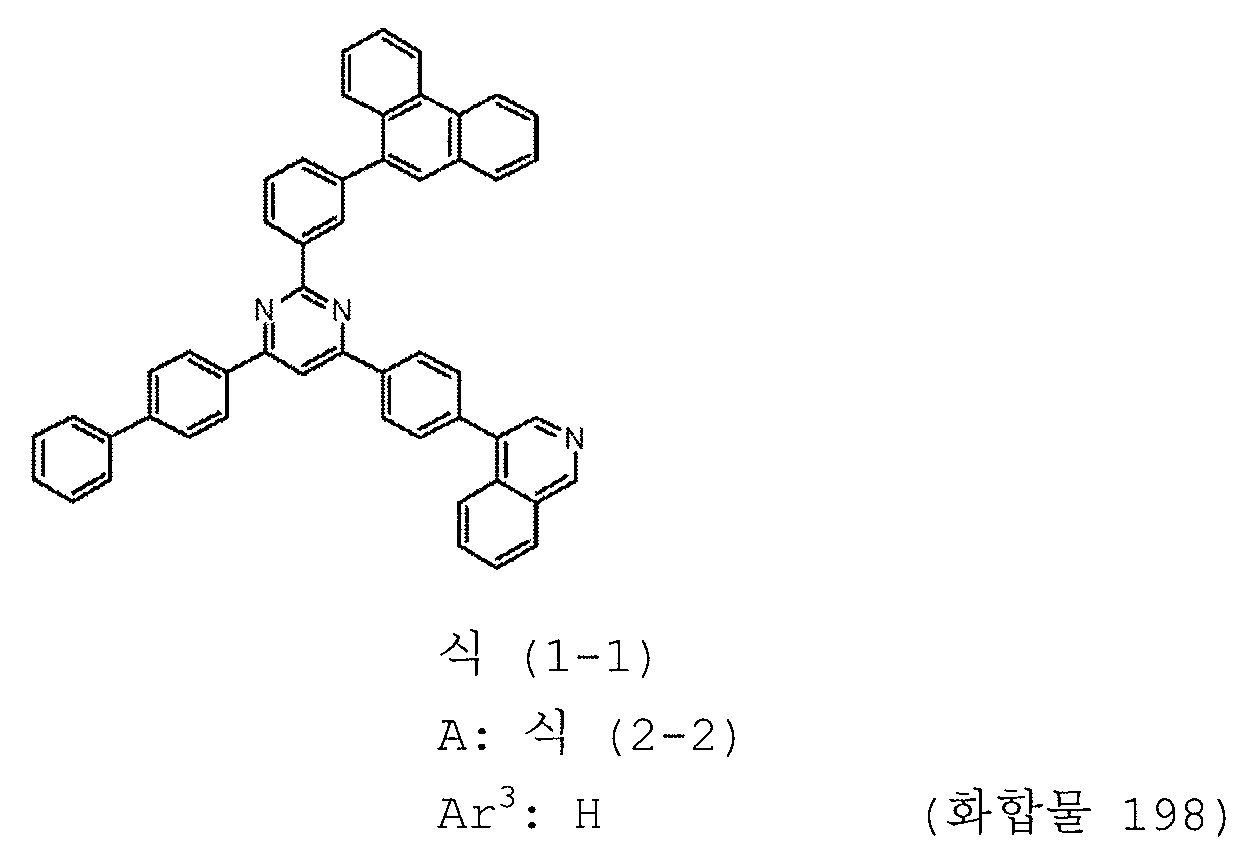
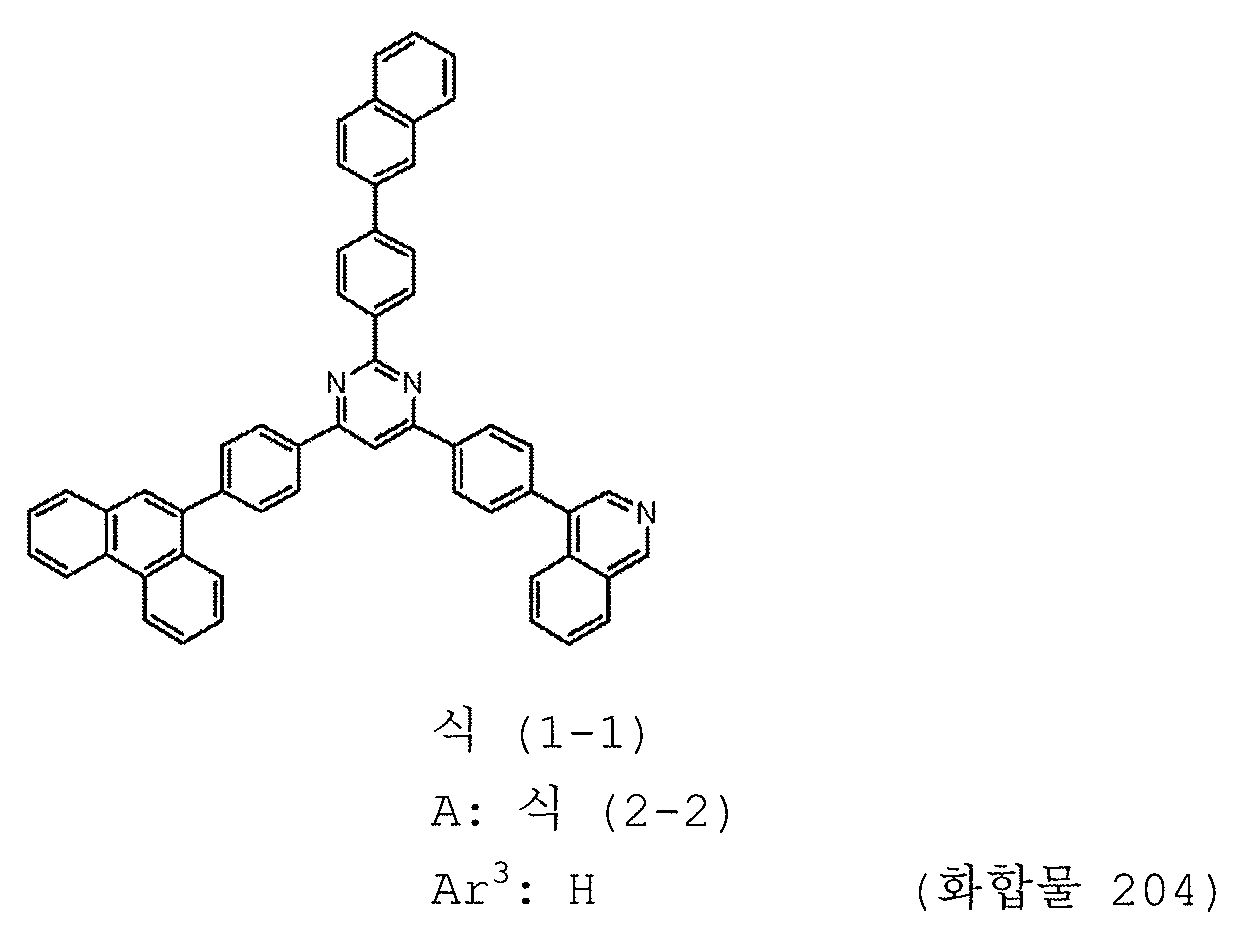
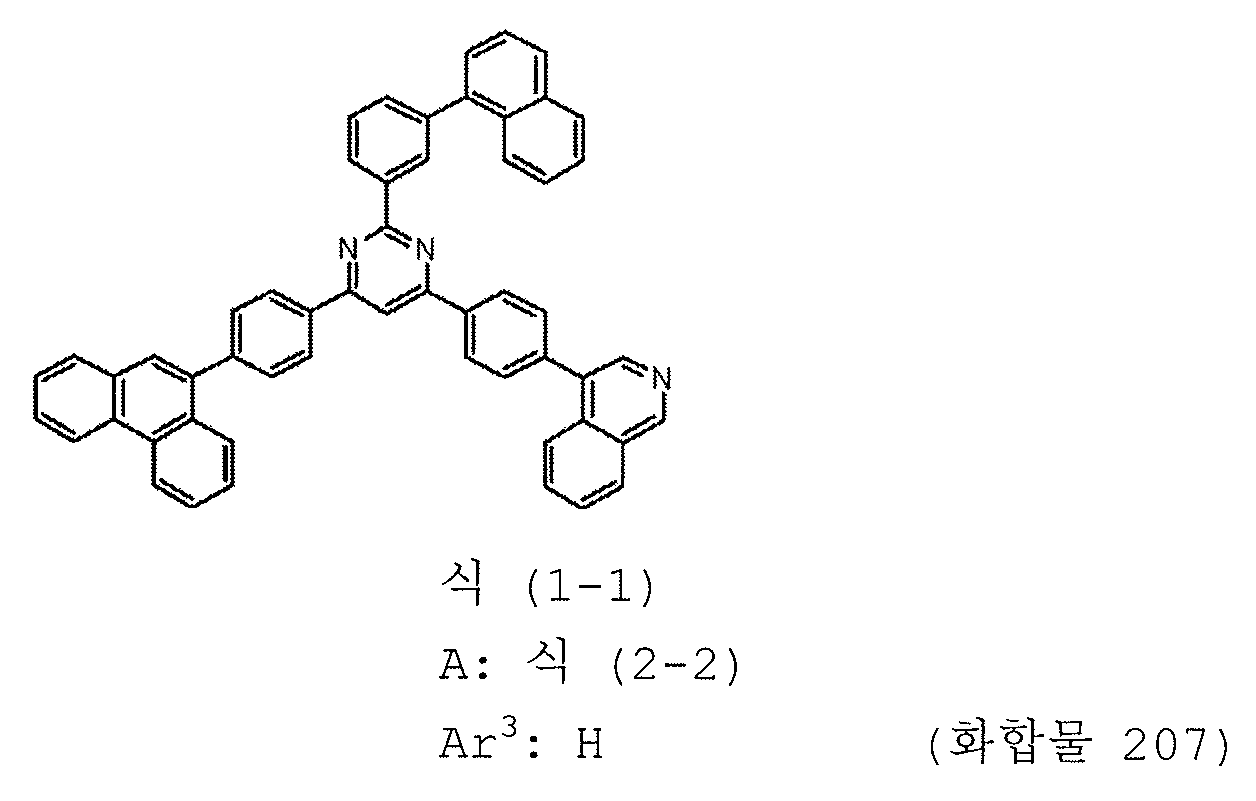
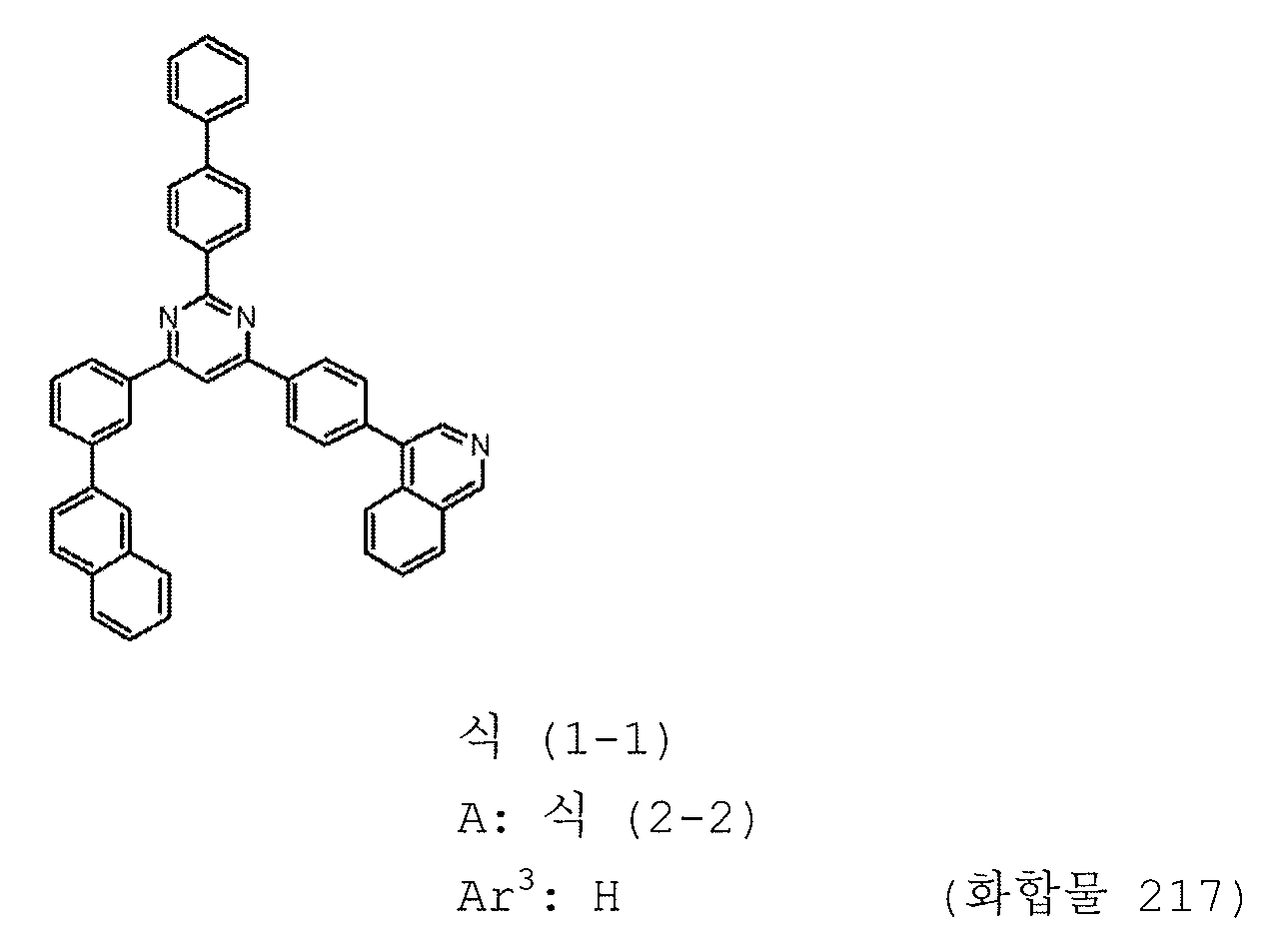
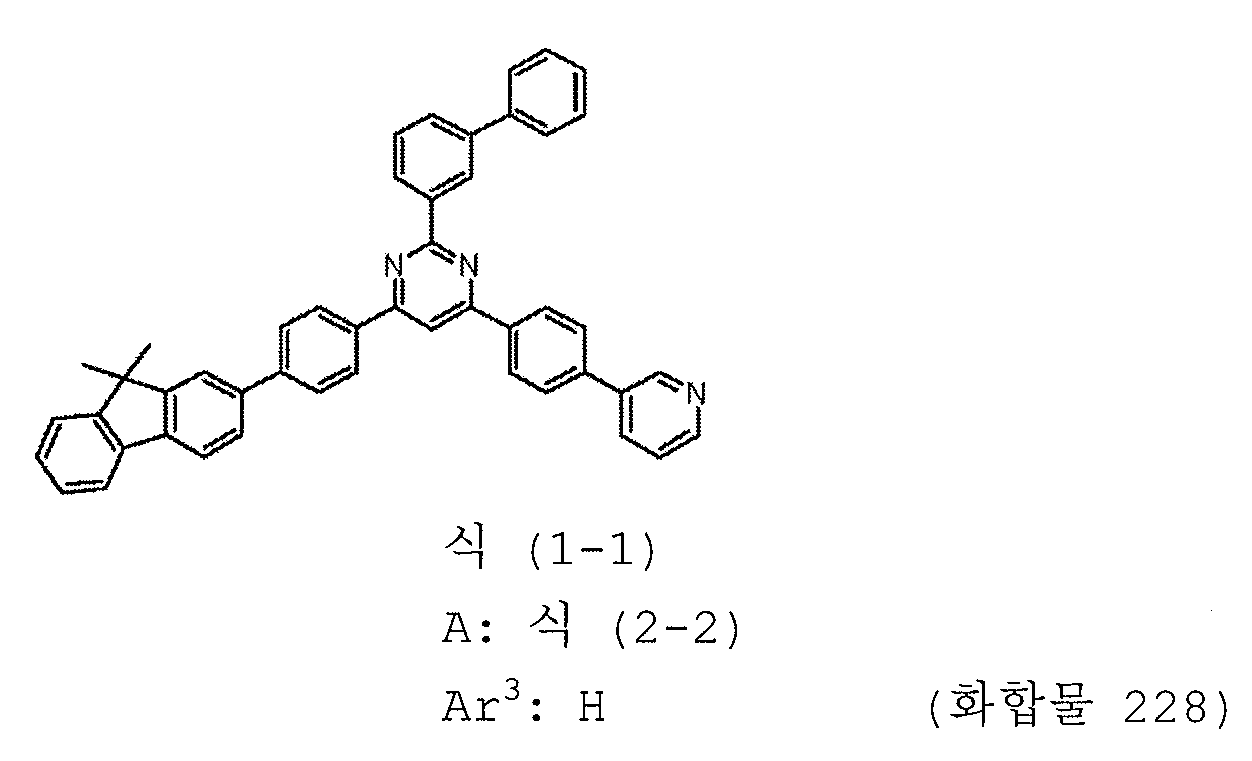
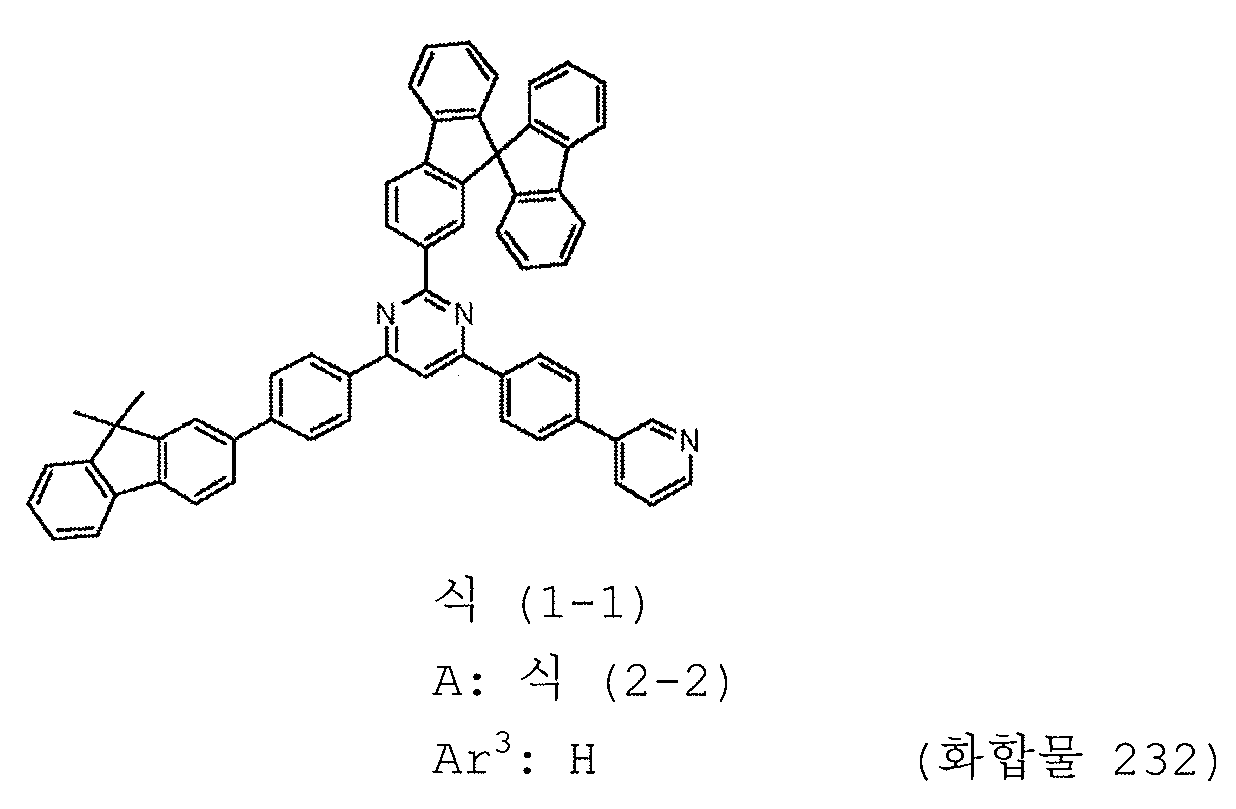
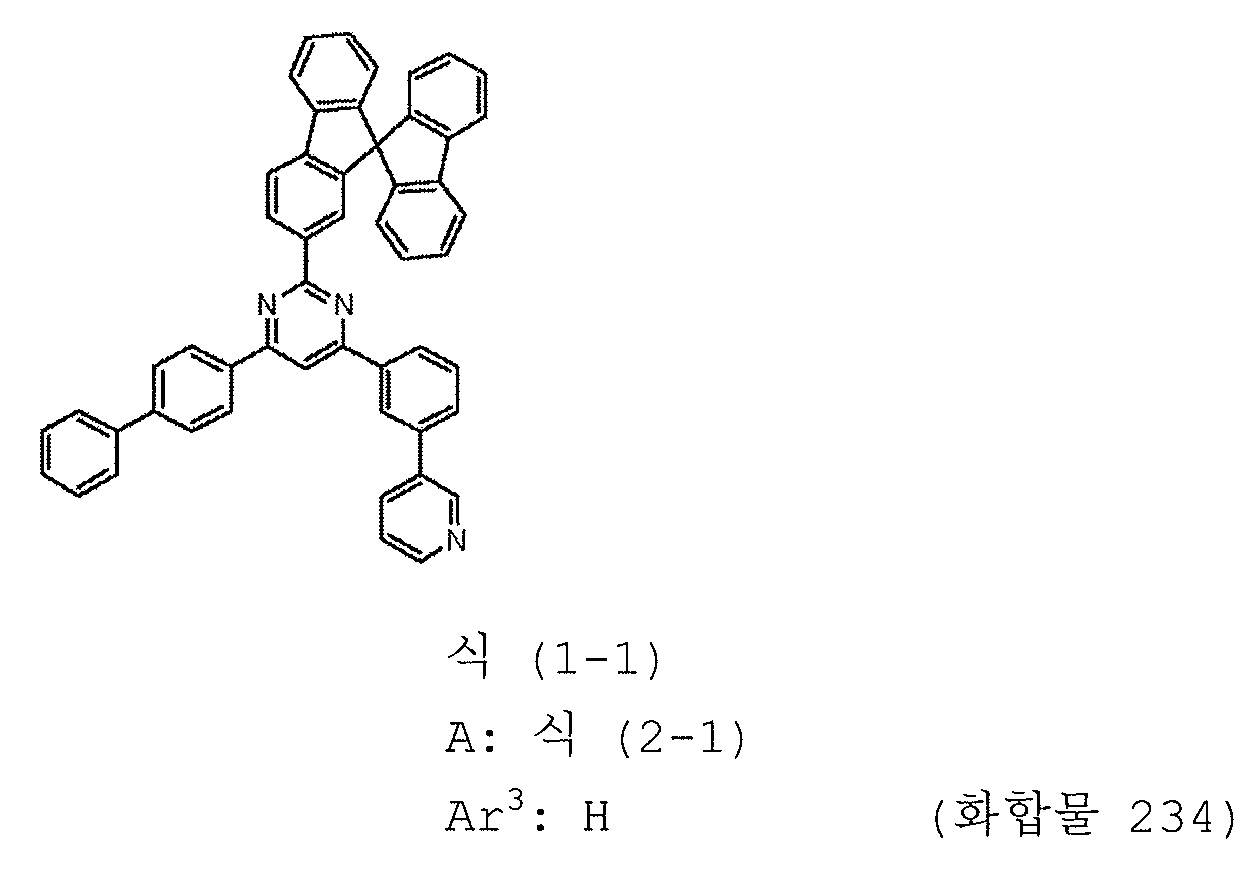
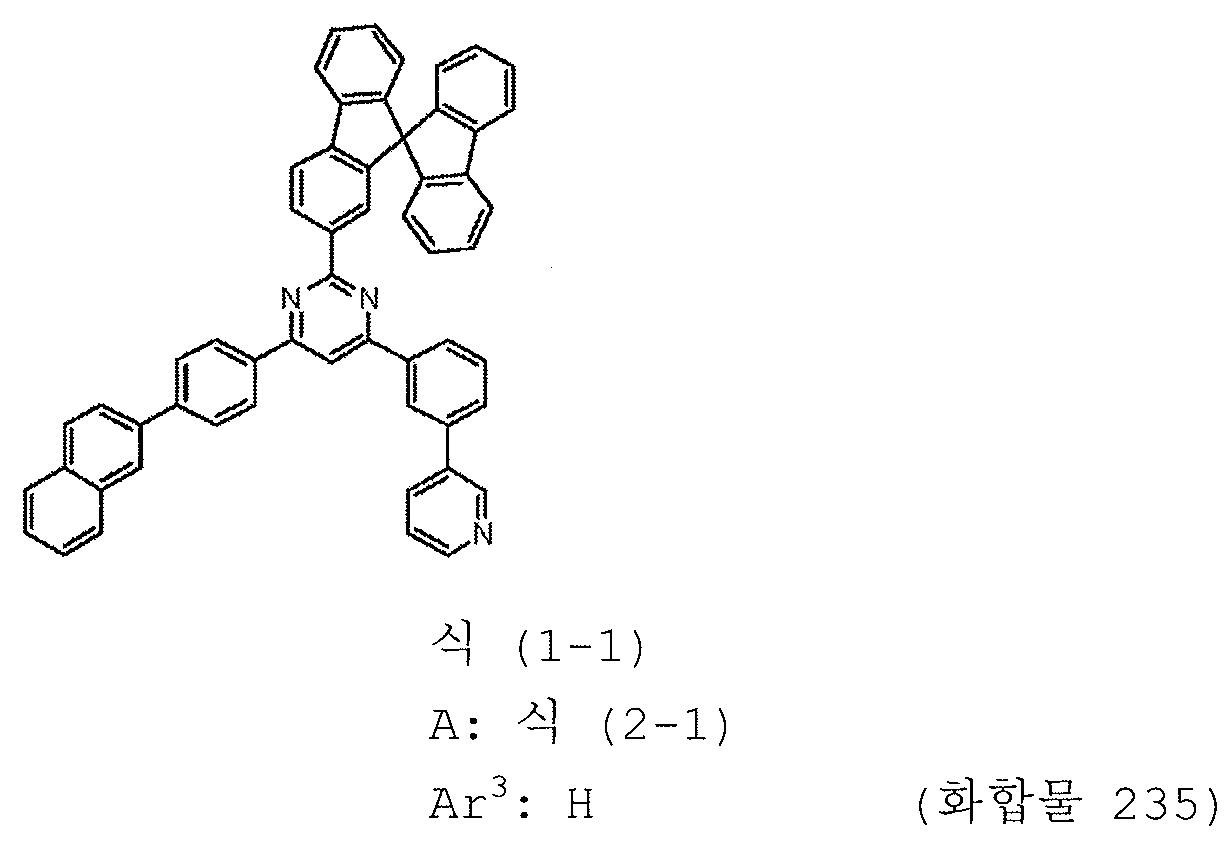
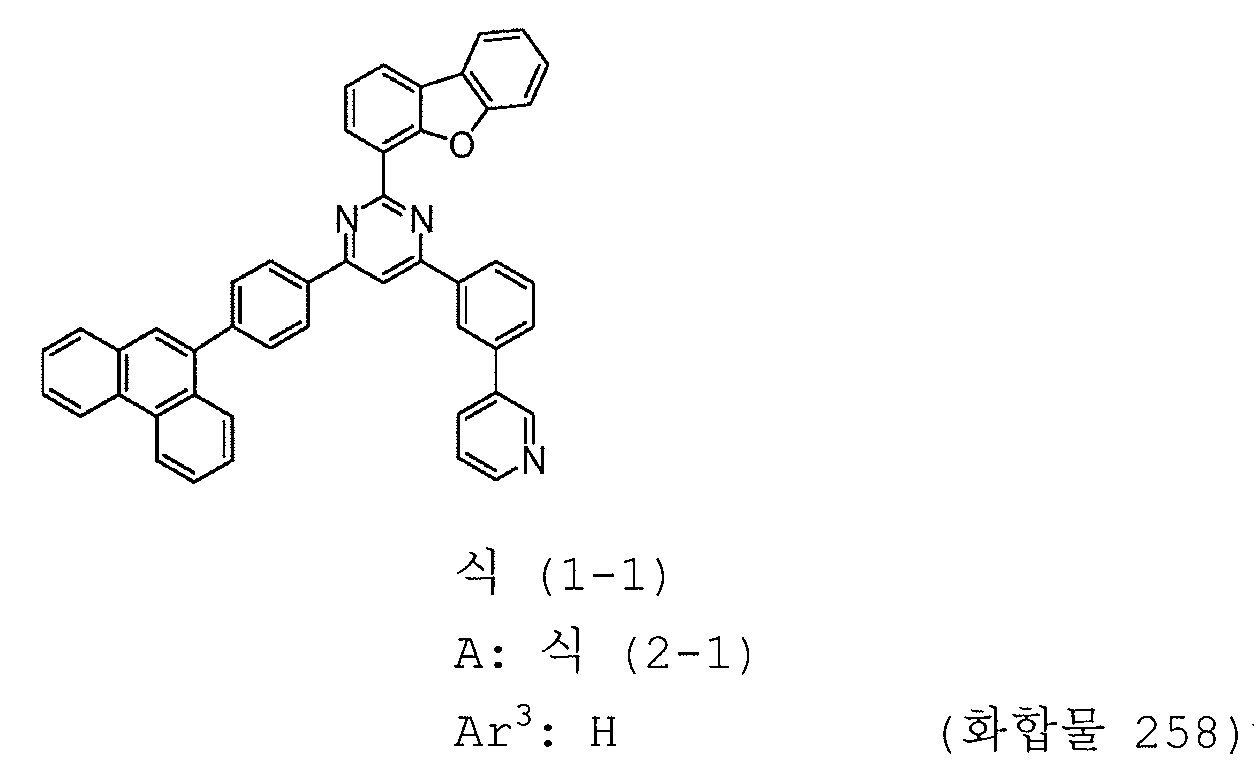
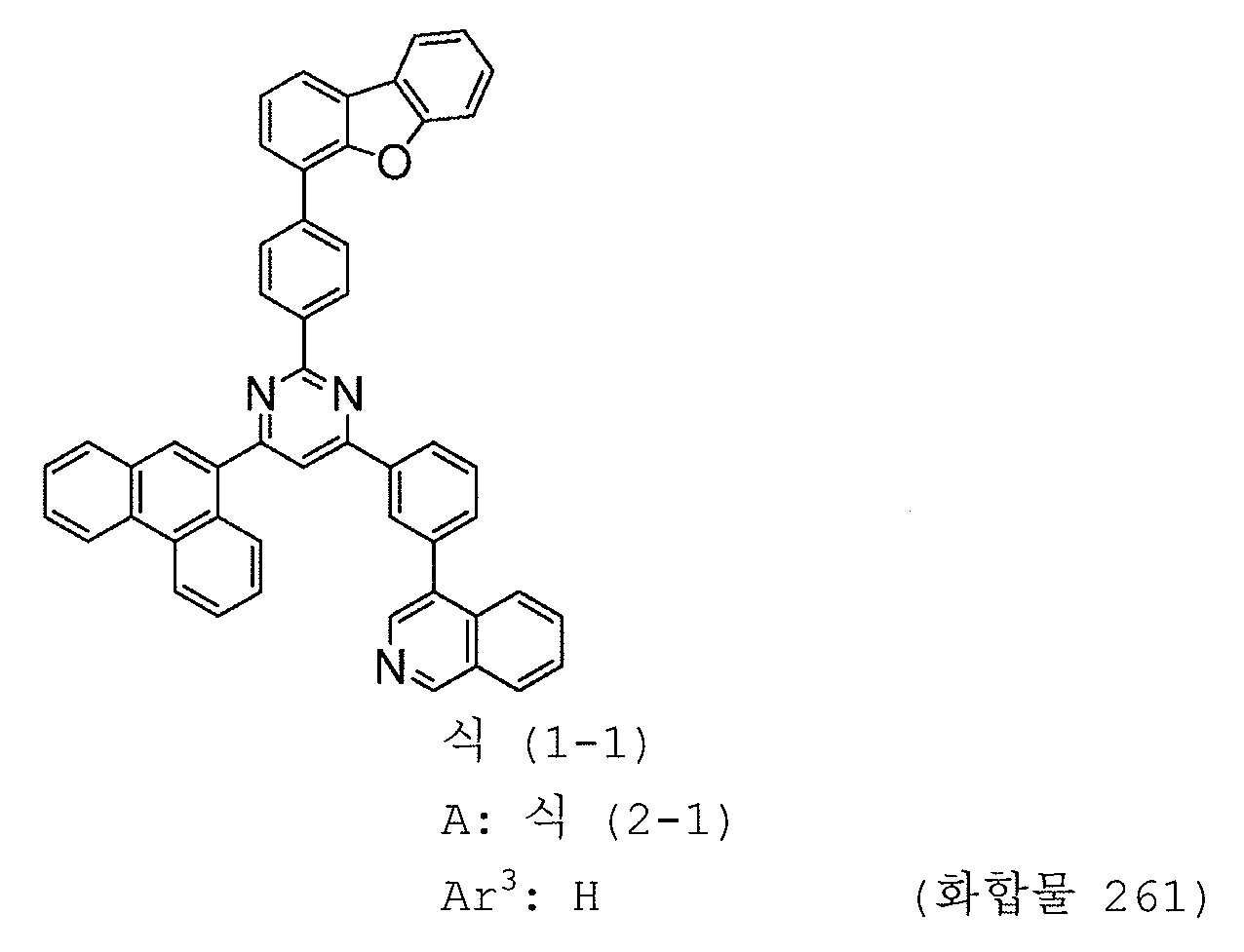
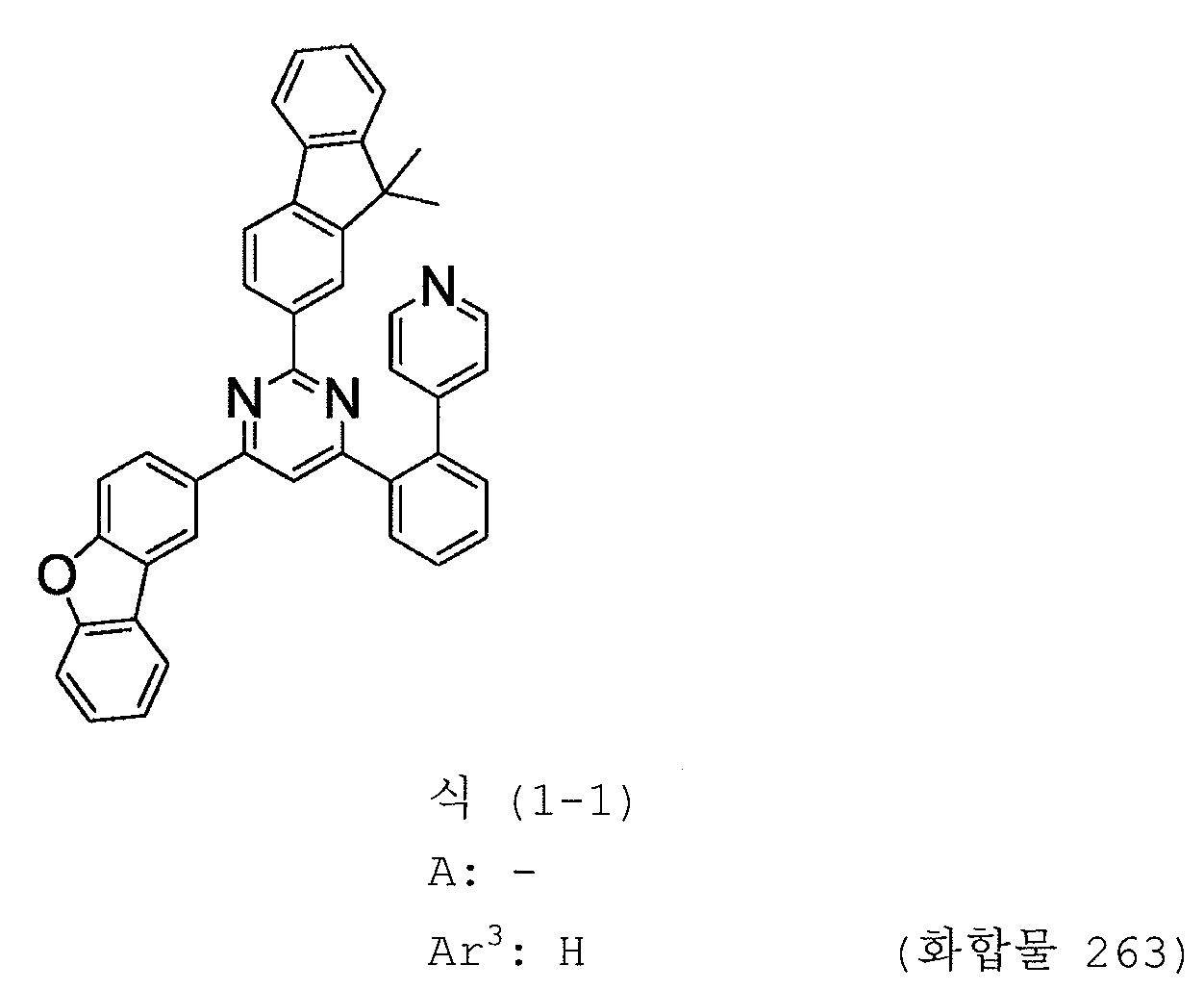
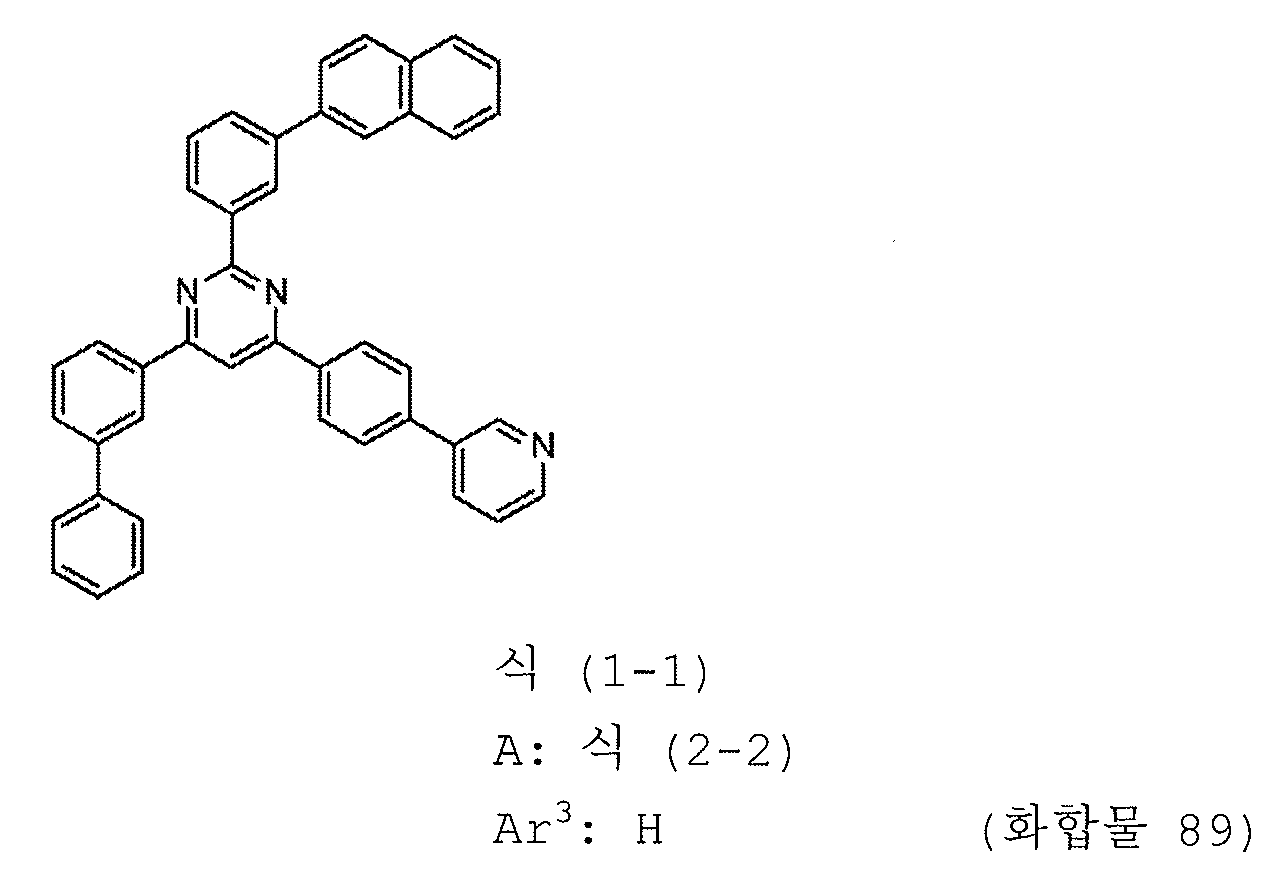
본 발명의 피리미딘 유도체 중 바람직한 화합물의 구체적인 예는 다음과 같으나, 본 발명은 이들 화합물에 한정되는 것은 아니다.
<유기 EL 소자>
한 쌍의 전극 사이에, 상술한 본 발명의 피리미딘 유도체를 사용하여 형성되는 유기 층을 적어도 1 층 구비한 유기 EL 소자 (이하 본 발명의 유기 EL 소자로 언급할 수 있다) 는, 예를 들어, 도 24 에 나타내는 계층 구조를 갖는다. 즉, 본 발명의 유기 EL 소자에 있어서는, 예를 들어, 기판 상에 순차적으로 양극 (2), 정공 주입층 (3), 정공 수송층 (4), 발광층 (5), 정공 저지층 (6), 전자 수송층 (7), 전자 주입층 (8), 및 음극 (9) 이 설치되어 있다.
본 발명의 유기 EL 소자는 이러한 구조에 한정되는 것이 아니라, 예를 들어, 정공 수송층 (4) 과 발광층 (5) 사이에 전자 저지층 (도시되지 않음) 을 가질 수 있다. 이러한 다층 구조에서는 유기 층을 여러 층 생략해도 좋다. 예를 들어, 양극 (2) 과 정공 수송층 (4) 사이에 정공 주입층 (3), 발광층 (5) 과 전자 수송층 (7) 사이에 정공 저지층 (6), 및 전자 수송층 (7) 과 음극 (9) 사이에 전자 주입층 (8) 을 생략하고, 기판 (1) 상에 순차적으로 양극 (2), 정공 수송층 (4), 발광층 (5), 전자 수송층 (7), 및 음극 (9) 을 갖는 구성을 할 수도 있다.
양극 (2) 은 자체 공지의 전극 재료로 구성되어도 좋고, 예를 들어, ITO 또는 금과 같은 일 함수가 큰 전극 재료가 사용된다.
정공 주입층 (3) 은 정공 주입 특성을 갖는 그 자체 공지의 재료로 구성되어도 좋고, 예를 들어, 하기 재료를 사용하여 형성 할 수 있다:
구리 프탈로시아닌으로 대표되는 포르피린 화합물;
스타버스트 형의 트리페닐아민 유도체;
트리페닐아민 3 량체 및 4 량체, 예를 들어, 분자 중에 트리페닐아민 구조를 3 개 이상 단일 결합 또는 헤테로 원자를 포함하지 않는 2 가 기로 연결한 구조를 갖는 아릴아민 화합물;
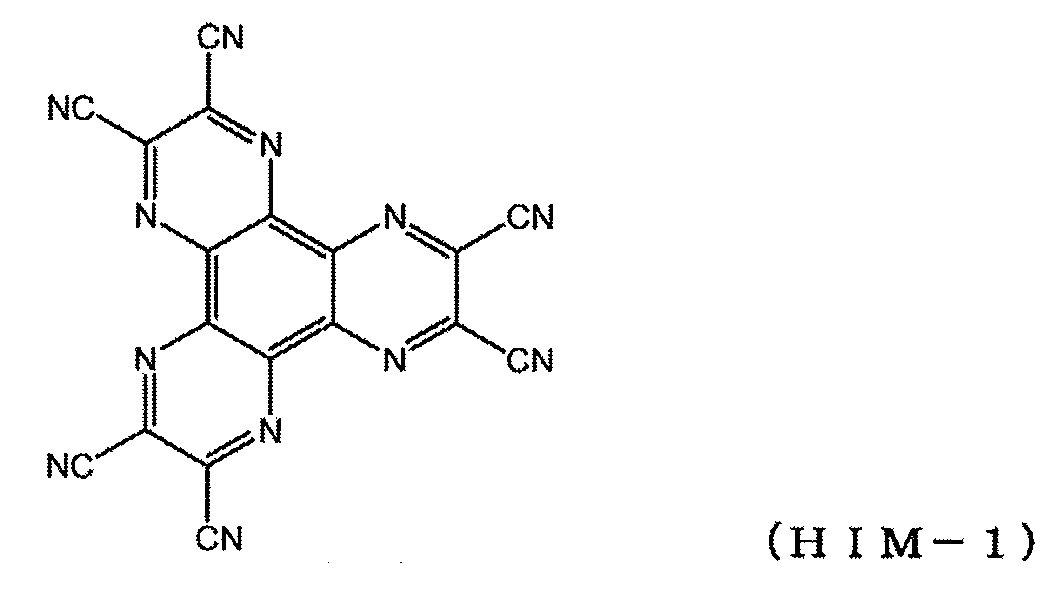
수용체 형의 헤테로고리 화합물, 예를 들어, 헥사시아노아자트리페닐렌; 및
도포 형의 고분자 재료.
정공 주입층 3 (박막) 은 증착법 또는 다른 스핀 코트 법 또는 잉크젯 법 등의 공지의 방법에 의해 형성될 수 있다. 아래에서 설명하는 다양한 계층 역시 증착, 스핀 코트, 또는 잉크젯 등의 공지의 방법에 의해 성막할 수 있다.
정공 수송층 (4) 은 정공 수송성을 갖는 그 자체 공지의 재료로 구성되어도 좋고, 예를 들어, 하기 재료를 사용하여 형성할 수 있다:
벤지딘 유도체, 예를 들어,
N,N'-디페닐-N,N'-디(m-톨릴)벤지딘
(이하 TPD 로 약칭),
N,N'-디페닐-N,N'-디(α-나프틸)벤지딘
(이하 NPD 로 약칭), 및
N,N,N',N'-테트라비페닐일벤지딘;
1,1-비스[(디-4-톨릴아미노)페닐]시클로헥산
(이하 TAPC 로 약칭); 및
다양한 트리페닐아민 3 량체 및 4 량체.
상기 정공 수송 재료는 단독으로 성막에 사용해도 좋지만, 다른 재료와 혼합하여 성막할 수 있다. 정공 수송층을 상기 재료 단독으로 층을 형성한 적층 구조, 상기 재료를 혼합하여 층을 형성한 적층 구조, 또는 상기 재료 단독으로 형성한 층과 상기 재료를 혼합하여 형성한 층을 적층한 적층 구조로 해도 좋다.
또한, 본 발명에서는, 정공 주입층 (3) 및 정공 수송층 (4) 을 겸한 층을 형성할 수도 있다. 이러한 정공 주입/수송층은 도포 형의 고분자 재료 예컨대 폴리(3,4-에틸렌디옥시티오펜) (이하 PEDOT 로 약칭)/폴리(스티렌술포네이트) (이하 PSS 로 약칭) 를 사용하여 형성할 수 있다.
정공 주입층 (3) 또는 정공 수송층 (4) 을 형성할 때, 이러한 층에 일반적으로 사용되는 재료에 추가로 트리스브로모페닐라미늄 헥사클로로안티모네이트 또는 라디알렌 유도체 (특허 문헌 5 참조) 를 P 도핑하여 층에 사용할 수 있고, 또는 TPD 등의 벤지딘 유도체의 구조를 그 부분 구조에 갖는 고분자 화합물도 일반적 재료에 더하여 층에 사용할 수 있다.
전자 저지층 (도시되지 않음) 은 전자 저지 작용을 하는 공지의 화합물을 사용하여 형성할 수 있다. 공지의 전자 저지 화합물로서는 예를 들어 하기를 들 수 있다:
카르바졸 유도체, 예를 들어,
4,4',4"-트리(N-카르바졸릴)트리페닐아민
(이하 TCTA 로 약칭),
9,9-비스[4-(카르바졸-9-일)페닐]플루오렌,
1,3-비스(카르바졸-9-일)벤젠 (이하 mCP 로 약칭), 및
2,2-비스(4-카르바졸-9-일페닐)아다만탄
(이하 Ad-Cz 로 약칭); 및
트리페닐실릴 기를 갖는 화합물 및
트리아릴아민 구조, 예를 들어,
9-[4-(카르바졸-9-일)페닐]-9-[4-(트리페닐실릴)페닐]-9H-플루오렌.
상기 전자 저지층 재료는 단독으로 성막에 사용해도 좋지만, 다른 재료와 혼합하여 성막할 수 있다. 또한 전자 저지층을 상기 재료 단독으로 층을 형성한 적층 구조, 상기 재료를 혼합하여 층을 형성한 적층 구조, 또는 상기 재료 단독으로 형성한 층과 상기 재료를 혼합하여 형성한 층을 적층한 적층 구조로 해도 좋다.
발광층 (5) 은 본 발명의 피리미딘 유도체 외에 공지의 재료를 사용하여 형성할 수 있다. 공지의 재료로서는 예를 들어 하기를 들 수 있다:
Alq3 를 비롯한 퀴놀리놀 유도체의 금속 착물;
다양한 금속 착물;
안트라센 유도체;
비스스티릴벤젠 유도체;
피렌 유도체;
옥사졸 유도체; 및
폴리파라페닐렌비닐렌 유도체.
발광층 (5) 은 호스트 재료 및 도판트 재료로 구성될 수 있다. 호스트 재료로서, 본 발명의 피리미딘 유도체 및 상기 발광 재료 외에 티아졸 유도체, 벤지미다졸 유도체, 및 폴리디알킬플루오렌 유도체 등을 사용할 수 있다.
도판트 재료로는, 예를 들어, 퀴나크리돈, 쿠마린, 루브렌, 페릴렌 및 그 유도체; 벤조피란 유도체; 로다민 유도체; 및 아미노스티릴 유도체를 사용할 수 있다.
상기 발광층 재료는 단독으로 성막에 사용해도 좋지만, 다른 재료와 혼합하여 성막할 수 있다. 또한 발광층을 상기 재료 단독으로 층을 형성한 적층 구조, 상기 재료를 혼합하여 층을 형성한 적층 구조, 또는 상기 재료 단독으로 형성한 층과 상기 재료를 혼합하여 형성한 층을 적층한 적층 구조로 해도 좋다.
더욱이, 발광 재료로서 인광성 발광체를 사용할 수 있다. 인광성 발광체로서, 이리듐, 백금 등을 함유하는 금속 착물 형태의 인광성 발광체를 사용할 수 있다. 구체적으로는,
녹색 인광성 발광체 예컨대 Ir(ppy)3;
청색 인광성 발광체 예컨대 FIrpic 또는 FIr6;
적색 인광성 발광체 예컨대 Btp2Ir(acac); 등
을 사용할 수 있다. 이 경우에 사용되는 호스트 재료의 정공 주입성/수송성 호스트 재료로서, 본 발명의 피리미딘 유도체 외에
카르바졸 유도체, 예를 들어,
4,4'-디(N-카르바졸릴)비페닐 (이하 CBP 로 약칭),
TCTA, 및
mCP
을 사용할 수 있다. 전자 수송성 호스트 재료의 예는 다음과 같다:
p-비스(트리페닐실릴)벤젠 (이하 UGH2 로 약칭); 및
2,2',2"-(1,3,5-페닐렌)-트리스(1-페닐-1H-벤지미다졸) (이하 TPBI 로 약칭).
이러한 재료를 사용하여, 고성능 유기 EL 소자를 제작할 수 있다.
인광성 발광 재료에 의한 호스트 재료의 도핑은 발광층 농도 소광을 피하기 위해 발광층 전체에 대하여 1 내지 30 중량% 범위로 공증착하여 도핑하는 것이 바람직하다.
또한 발광 재료로서 지연 형광을 방출하는 재료, 예컨대 CDCB 유도체, 예를 들어, PIC-TRZ, CC2TA, PXZ-TRZ, 4CzIPN 등을 사용하는 것도 가능하다.
정공 저지층 (6) 은 본 발명의 피리미딘 유도체 외에도 정공 저지 특성을 갖는 공지의 화합물을 사용하여 형성할 수 있다. 정공 저지 특성을 갖는 공지의 화합물로서는 예를 들어 하기를 들 수 있다:
페난트롤린 유도체, 예를 들어, 바소쿠프로인 (이하 BCP 로 약칭);
퀴놀리놀 유도체의 금속 착물, 예를 들어, BAlq;
다양한 희토류 착물;
옥사졸 유도체;
트리아졸 유도체; 및
트리아진 유도체.
정공 저지 재료는 단독으로 성막에 사용해도 좋지만, 다른 재료와 혼합하여 성막할 수 있다. 또한 정공 저지층을 상기 재료 단독으로 층을 형성한 적층 구조, 상기 재료를 혼합하여 층을 형성한 적층 구조, 또는 상기 재료 단독으로 형성한 층과 상기 재료를 혼합하여 형성한 층을 적층한 적층 구조로 해도 좋다.
상기 정공 저지 특성을 갖는 공지의 재료는 또한 아래 기재된 전자 수송층 (7) 의 형성에도 사용할 수 있다. 즉, 상기 정공 저지 특성을 갖는 공지의 재료를 사용하여 정공 저지층 (6) 및 전자 수송층 (7) 을 겸한 층을 형성할 수도 있다.
전자 수송층 (7) 은 본 발명의 피리미딘 유도체 외에도 전자 수송성을 갖는 공지의 화합물을 사용하여 형성한다. 전자 수송성을 갖는 공지의 화합물로서는 예를 들어 하기를 들 수 있다:
Alq3 및 BAlq 를 비롯한 퀴놀리놀 유도체의 금속 착물;
다양한 금속 착물;
트리아졸 유도체;
트리아진 유도체;
옥사디아졸 유도체;
피리딘 유도체;
벤지미다졸 유도체;
티아디아졸 유도체;
안트라센 유도체;
카르보디이미드 유도체;
퀴녹살린 유도체;
피리도인돌 유도체;
페난트롤린 유도체; 및
실롤 유도체.
전자 수송 재료는 단독으로 성막에 사용해도 좋지만, 다른 재료와 혼합하여 성막할 수 있다. 또한 전자 수송층을 상기 재료 단독으로 층을 형성한 적층 구조, 상기 재료를 혼합하여 층을 형성한 적층 구조, 또는 상기 재료 단독으로 형성한 층과 상기 재료를 혼합하여 형성한 층을 적층한 적층 구조로 해도 좋다.
전자 주입층 (8) 은 본 발명의 피리미딘 유도체 외에도 그 자체 공지의 재료를 사용하여 형성할 수 있다. 그러한 재료의 예는 다음과 같다:
알칼리 금속 염 예컨대 불화 리튬 및 불화 세슘;
알칼리토 금속 염 예컨대 불화 마그네슘;
퀴놀리놀 유도체의 금속 착물 예컨대 리튬 퀴놀리놀; 및
금속 산화물 예컨대 산화 알루미늄.
전자 수송층 및 음극의 바람직한 선택에서, 전자 주입층 (8) 은 생략할 수 있다.
또한, 전자 주입층 (7) 또는 전자 수송층 (8) 에서는, 이러한 층에 일반적으로 사용되는 재료에 추가로 금속 예컨대 세슘을 N 도핑하고, 일반적 재료에 더하여 층에 사용할 수 있다.
음극 (9) 과 관련하여, 알루미늄과 같은 일 함수가 낮은 전극 재료, 또는 마그네슘-은 합금, 마그네슘-인듐 합금, 또는 알루미늄-마그네슘 합금과 같은 보다 일 함수가 낮은 합금을 전극 재료로서 사용한다.
실시예
이하, 본 발명의 실시예에 대하여 실시예에 의해 구체적으로 설명하지만, 본 발명은 그 요지를 넘지 않는 한, 하기 실시예에 한정되는 것은 아니다.
<실시예 1: 화합물 74 의 합성>
4-(비페닐-4-일)-2-{3-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘의 합성:
질소-퍼징된 반응 용기에
3-(나프탈렌-1-일)페닐보론산
5.0 g,
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘
7.0 g,
테트라키스트리페닐포스핀
0.96 g,
칼륨 카르보네이트
6.9 g,
톨루엔
35 ml,
1,4-디옥산
70 ml 및
물
35 ml
를 채웠다.
혼합물을 가열하고, 12 시간 동안 85℃ 에서 교반했다. 혼합물을 실온까지 냉각하고, 유기 층을 분액 조작에 의해 채취했다. 그 후, 유기 층을 감압 농축하여 조(粗)생성물을 얻었다. 조생성물을 칼럼 크로마토그래피 (담체: 실리카 겔, 용리액: 헵탄/디클로로메탄/THF) 에 의해 정제한 후, 클로로벤젠/디클로로메탄 혼합 용매를 이용한 재결정화에 의한 정제를 실시하여 4-(비페닐-4-일)-2-{3-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 74) 의 백색 분말 3.1 g (수율 32%) 을 얻었다.
얻어진 백색 분말에 대해 NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 1 에 나타내었다. 1H-NMR (THF-d8) 에서, 다음의 29 개의 수소 신호를 감지했다.
δ (ppm) =
8.97-8.84 (3H)
8.60-8.45 (6H)
8.08-7.32 (20H)
<실시예 2: 화합물 84 의 합성>
4-(비페닐-3-일)-2-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
4-(나프탈렌-1-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-(비페닐-3-일)-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 3.8 g (수율 39%) 의 4-(비페닐-3-일)-2-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 84) 을 백색 분말로서 얻었다.
얻어진 백색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 2 에 나타내었다. 1H-NMR (THF-d8) 에서, 다음의 29 개의 수소 신호를 감지했다.
δ (ppm) =
8.99 (1H)
8.93 (2H)
8.72 (1H)
8.65 (2H)
8.59 (1H)
8.52 (1H)
8.49 (1H)
8.09 (1H)
8.04-7.34 (19H)
<실시예 3: 화합물 89 의 합성>
4-(비페닐-3-일)-2-{3-(나프탈렌-2-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
3-(나프탈렌-2-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-(비페닐-3-일)-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 5.8 g (수율 59%) 의 4-(비페닐-3-일)-2-{3-(나프탈렌-2-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 89) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 3 에 나타내었다. 1H-NMR (THF-d8) 에서, 다음의 29 개의 수소 신호를 감지했다.
δ (ppm) =
9.21 (1H)
8.98 (1H)
8.80 (1H)
8.74 (1H)
8.64 (2H)
8.59 (1H)
8.53 (1H)
8.46 (1H)
8.29 (1H)
8.08 (1H)
8.00-7.76 (10H)
7.72-7.62 (2H)
7.55-6.34 (6H)
<실시예 4: 화합물 130 의 합성>
2-{3-(나프탈렌-1-일)페닐}-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
2-클로로-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 9.3 g (수율 35%) 의 2-{3-(나프탈렌-1-일)페닐}-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 130) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 4 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 33 개의 수소 신호를 감지했다.
δ (ppm) =
8.98-8.84 (3H)
8.84 (1H)
8.78 (1H)
8.68 (1H)
8.47-8.44 (4H)
8.19 (1H)
8.06-7.93 (6H)
7.81-7.41 (16H)
<실시예 5: 화합물 131 의 합성>
2-{4-(나프탈렌-1-일)페닐}-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
4-(나프탈렌-1-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 22.6 g (수율 85%) 의 2-{4-(나프탈렌-1-일)페닐}-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 131) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 5 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 33 개의 수소 신호를 감지했다.
δ (ppm) =
9.00 (1H)
8.94 (2H)
8.85 (1H)
8.78 (1H)
8.69 (1H)
8.55-8.51 (4H)
8.23 (1H)
8.23-7.44 (22H)
<실시예 6: 화합물 92 의 합성>
2-{4-(나프탈렌-1-일)페닐}-4-{3-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
4-(나프탈렌-1-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{3-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 6 g (수율 74%) 의 2-{4-(나프탈렌-1-일)페닐}-4-{3-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 92) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 6 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 31 개의 수소 신호를 감지했다.
δ (ppm) =
8.98 (1H)
8.87 (2H)
8.67 (1H)
8.48-8.46 (4H)
8.16 (1H)
8.04-7.82 (7H)
7.80 (2H)
7.76-7.42 (13H)
<실시예 7: 화합물 136 의 합성>
2-{4-(페난트렌-9-일)페닐}-4-{3-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
4-(페난트렌-9-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{3-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 2 g (수율 26%) 의 2-{4-(페난트렌-9-일)페닐}-4-{3-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 136) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 7 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 33 개의 수소 신호를 감지했다.
δ (ppm) =
8.98 (1H)
8.90 (2H)
8.83 (1H)
8.78 (1H)
8.68 (1H)
8.50-8.45 (4H)
8.17 (1H)
8.04-7.94 (6H)
7.83-7.41 (16H)
<실시예 8: 화합물 125 의 합성>
2-{4-(나프탈렌-1-일)페닐}-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
4-(나프탈렌-1-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 21.6 g (수율 80%) 의 2-{4-(나프탈렌-1-일)페닐}-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 125) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 8 에 나타내었다. 1H-NMR (THF-d8) 에서, 다음의 31 개의 수소 신호를 감지했다.
δ (ppm) =
9.00 (1H)
8.95 (2H)
8.68 (1H)
8.54-8.48 (4H)
8.22 (1H)
8.21-7.91 (7H)
7.82 (2H)
7.79-7.72 (4H)
7.64-7.42 (9H)
<실시예 9: 화합물 138 의 합성>
2-{4-(나프탈렌-2-일)페닐}-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
4-(나프탈렌-2-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 3.5 g (수율 43%) 의 2-{4-(나프탈렌-2-일)페닐}-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 138) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 9 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 31 개의 수소 신호를 감지했다.
δ (ppm) =
9.00 (1H)
8.92 (2H)
8.68 (1H)
8.53-8.48 (4H)
8.20 (2H)
8.03-7.81 (12H)
7.77 (2H)
7.63-7.42 (7H)
<실시예 10: 화합물 78 의 합성>
2-{4-(페난트렌-9-일)페닐}-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
4-(페난트렌-9-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 16.2 g (수율 56%) 의 2-{4-(페난트렌-9-일)페닐}-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 78) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 10 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 33 개의 수소 신호를 감지했다.
δ (ppm) =
9.00 (1H)
8.95 (2H)
8.83 (1H)
8.76 (1H)
8.69 (1H)
8.52-8.48 (4H)
8.22 (1H)
8.08-7.91 (6H)
7.86-7.42 (16H)
<실시예 11: 화합물 76 의 합성>
2-{4-(나프탈렌-1-일)페닐}-4-{3-(나프탈렌-2-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
4-(나프탈렌-1-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{3-(나프탈렌-2-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 24.0 g (수율 52%) 의 2-{4-(나프탈렌-1-일)페닐}-4-{3-(나프탈렌-2-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 76) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 11 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 31 개의 수소 신호를 감지했다.
δ (ppm) =
9.00 (1H)
8.90 (2H)
8.68 (2H)
8.53 (2H)
8.37 (1H)
8.21 (2H)
8.08-7.81 (11H)
7.78-7.71 (3H)
7.64-7.42 (7H)
<실시예 12: 화합물 126 의 합성>
2-(비페닐-4-일)-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
4-비페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 6.5 g (수율 85%) 의 2-(비페닐-4-일)-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 126) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 12 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 31 개의 수소 신호를 감지했다.
δ (ppm) =
9.00 (1H)
8.92-8.76 (4H)
8.68 (1H)
8.54-8.46 (4H)
8.18 (1H)
8.05-7.94 (3H)
7.88-7.38 (17H)
<실시예 13: 화합물 124 의 합성>
2-(비페닐-4-일)-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
4-비페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 17.6 g (수율 64%) 의 2-(비페닐-4-일)-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 124) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 13 에 나타내었다. 1H-NMR (THF-d8) 에서, 다음의 29 개의 수소 신호를 감지했다.
δ (ppm) =
9.00 (1H)
8.89 (2H)
8.67 (1H)
8.51-8.48 (4H)
8.17 (1H)
8.03-7.93 (4H)
7.86-7.81 (4H)
7.78-7.72 (4H)
7.63-7.38 (8H)
<실시예 14: 화합물 123 의 합성>
2-(비페닐-3-일)-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
3-비페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 3.0 g (수율 38%) 의 2-(비페닐-3-일)-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 123) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 14 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 31 개의 수소 신호를 감지했다.
δ (ppm) =
9.02 (2H)
8.86-8.76 (3H)
8.69 (1H)
8.52-8.48 (4H)
8.21 (1H)
8.05-7.93 (3H)
7.89-7.40 (17H)
<실시예 15: 화합물 146 의 합성>
2-{4-(나프탈렌-1-일)페닐}-4-(비페닐-4-일)-6-{4-(퀴놀린-3-일)페닐}피리미딘:
실시예 1 에서,
4-(나프탈렌-1-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-(비페닐-4-일)-6-{4-(퀴놀린-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 1.2 g (수율 15%) 의 2-{4-(나프탈렌-1-일)페닐}-4-(비페닐-4-일)-6-{4-(퀴놀린-3-일)페닐}피리미딘 (화합물 146) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 15 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 31 개의 수소 신호를 감지했다.
δ (ppm) =
9.34 (1H)
8.91 (2H)
8.62-8.52 (4H)
8.37 (1H)
8.22 (1H)
8.14-7.90 (5H)
7.86-7.40 (17H)
<실시예 16: 화합물 98 의 합성>
2-{3-(페난트렌-9-일)페닐}-4-{3-(나프탈렌-2-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
3-(페난트렌-9-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{3-(나프탈렌-2-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 5.0 g (수율 57%) 의 2-{3-(페난트렌-9-일)페닐}-4-{3-(나프탈렌-2-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 98) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 16 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 33 개의 수소 신호를 감지했다.
δ (ppm) =
8.98-8.78 (5H)
8.68-8.62 (2H)
8.45 (2H)
8.32 (1H)
8.17 (2H)
8.03 (1H)
8.00-7.39 (20H)
<실시예 17: 화합물 153 의 합성>
2-{3-(나프탈렌-2-일)페닐}-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
3-(나프탈렌-2-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 15.4 g (수율 73%) 의 2-{3-(나프탈렌-2-일)페닐}-4-{4-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 153) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 17 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 33 개의 수소 신호를 감지했다.
δ (ppm) =
9.15 (1H)
9.00 (1H)
8.83 (2H)
8.78 (1H)
8.68 (1H)
8.53-8.47 (4H)
8.22 (2H)
8.04-7.42 (21H)
<실시예 18: 화합물 155 의 합성>
2-{4-(나프탈렌-1-일)페닐}-4-{3-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
4-(나프탈렌-1-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{3-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 2.5 g (수율 42%) 의 2-{4-(나프탈렌-1-일)페닐}-4-{3-(페난트렌-9-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 155) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 18 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 33 개의 수소 신호를 감지했다.
δ (ppm) =
8.97 (1H)
8.97-8.76 (4H)
8.67 (1H)
8.52-8.46 (4H)
8.17 (1H)
8.01-7.43 (22H)
<실시예 19: 화합물 82 의 합성>
2-{3-(페난트렌-9-일)페닐}-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
3-(페난트렌-9-일)페닐보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 6.3 g (수율 72%) 의 2-{3-(페난트렌-9-일)페닐}-4-{4-(나프탈렌-1-일)페닐}-6-{4-(피리딘-3-일)페닐}피리미딘 (화합물 82) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 19 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 33 개의 수소 신호를 감지했다.
δ (ppm) =
8.97-8.88 (3H)
8.87-8.76 (2H)
8.66 (1H)
8.49-8.42 (4H)
8.20 (1H)
8.08-7.84 (7H)
7.83-7.40 (15H)
<실시예 20: 화합물 182 의 합성>
2-{3-(나프탈렌-1-일)페닐}-4-{4-(나프탈렌-1-일)페닐}-6-{4-(퀴놀린-3-일)페닐}피리미딘:
실시예 1 에서,
2-클로로-4-{4-(나프탈렌-1-일)페닐}-6-{4-(퀴놀린-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 1.5 g (수율 23%) 의 2-{3-(나프탈렌-1-일)페닐}-4-{4-(나프탈렌-1-일)페닐}-6-{4-(퀴놀린-3-일)페닐}피리미딘 (화합물 182) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 20 에 나타내었다. 1H-NMR (THF-d8) 에서, 다음의 33 개의 수소 신호를 감지했다.
δ (ppm) =
9.33 (1H)
8.94 (2H)
8.59-8.42 (5H)
8.23-8.17 (2H)
8.04-7.90 (9H)
7.82-7.72 (5H)
7.64-7.45 (9H)
<실시예 21: 화합물 227 의 합성>
2-(9,9'-스피로비[9H-플루오렌]-2-일)-4-{4-(나프탈렌-1-일)페닐}-6-{3-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
9,9'-스피로비[9H-플루오렌]-2-보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{4-(나프탈렌-1-일)페닐}-6-{3-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 1.3 g (수율 20%) 의 2-(9,9'-스피로비[9H-플루오렌]-2-일)-4-{4-(나프탈렌-1-일)페닐}-6-{3-(피리딘-3-일)페닐}피리미딘 (화합물 227) 을 황색 분말로서 얻었다.
얻어진 황색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 21 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 35 개의 수소 신호를 감지했다.
δ (ppm) =
8.95 (1H)
8.86 (1H)
8.70 (1H)
8.42 (1H)
8.30 (2H)
8.22 (1H)
8.12-8.03 (3H)
8.01-7.89 (7H)
7.74 (1H)
7.67-7.37 (11H)
7.20-7.10 (3H)
6.83 (2H)
6.78 (1H)
<실시예 22: 화합물 234 의 합성>
2-(9,9'-스피로비[9H-플루오렌]-2-일)-4-(비페닐-4-일)-6-{3-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
9,9'-스피로비[9H-플루오렌]-2-보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-(비페닐-4-일)-6-{3-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 1.5 g (수율 25%) 의 2-(9,9'-스피로비[9H-플루오렌]-2-일)-4-(비페닐-4-일)-6-{3-(피리딘-3-일)페닐}피리미딘 (화합물 234) 을 백색 분말로서 얻었다.
얻어진 백색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 22 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 33 개의 수소 신호를 감지했다.
δ (ppm) =
8.96 (1H)
8.86 (1H)
8.72 (1H)
8.39 (1H)
8.26 (2H)
8.17 (1H)
8.12-7.89 (7H)
7.78-7.60 (6H)
7.53-7.25 (7H)
7.21-7.10 (3H)
6.83-6.75 (3H)
<실시예 23: 화합물 235 의 합성>
2-(9,9'-스피로비[9H-플루오렌]-2-일)-4-{4-(나프탈렌-2-일)페닐}-6-{3-(피리딘-3-일)페닐}피리미딘:
실시예 1 에서,
9,9'-스피로비[9H-플루오렌]-2-보론산을
3-(나프탈렌-1-일)페닐보론산 대신에 사용하고,
2-클로로-4-{4-(나프탈렌-2-일)페닐}-6-{3-(피리딘-3-일)페닐}피리미딘을
2-클로로-4-(비페닐-4-일)-6-{4-(피리딘-3-일)페닐}피리미딘 대신에 사용하여,
동일한 조건에서 반응을 수행하였다. 그 결과, 2.0 g (수율 32%) 의 2-(9,9'-스피로비[9H-플루오렌]-2-일)-4-{4-(나프탈렌-2-일)페닐}-6-{3-(피리딘-3-일)페닐}피리미딘 (화합물 235) 을 백색 분말로서 얻었다.
얻어진 백색 분말에 대해, NMR 을 사용하여 구조를 동정했다. 1H-NMR 측정 결과를 도 23 에 나타내었다. 1H-NMR (CDCl3) 에서, 다음의 35 개의 수소 신호를 감지했다.
δ (ppm) =
8.96 (1H)
8.85 (1H)
8.71 (1H)
8.41 (1H)
8.30 (2H)
8.19 (1H)
8.12 (1H)
8.79-7.39 (21H)
7.20-7.11 (3H)
6.83 (2H)
6.78 (1H)
<일 함수의 측정>
본 발명의 화합물을 이용하여 ITO 기판 위에 두께 100 nm 의 증착막을 제작하고, 이온화 포텐셜 측정 장치 (스미토모 중기계공업 주식회사제, PYS-202 형) 를 이용하여 일 함수를 측정했다.
일 함수
실시예 1 의 화합물 (화합물 74) 6.63 eV
실시예 2 의 화합물 (화합물 84) 6.60 eV
실시예 3 의 화합물 (화합물 89) 6.39 eV
실시예 4 의 화합물 (화합물 130) 6.50 eV
실시예 5 의 화합물 (화합물 131) 6.50 eV
실시예 6 의 화합물 (화합물 92) 6.51 eV
실시예 7 의 화합물 (화합물 136) 6.47 eV
실시예 8 의 화합물 (화합물 125) 6.50 eV
실시예 9 의 화합물 (화합물 138) 6.47 eV
실시예 10 의 화합물 (화합물 78) 6.48 eV
실시예 11 의 화합물 (화합물 76) 6.55 eV
실시예 12 의 화합물 (화합물 126) 6.56 eV
실시예 13 의 화합물 (화합물 124) 6.50 eV
실시예 14 의 화합물 (화합물 123) 6.53 eV
실시예 15 의 화합물 (화합물 146) 6.53 eV
실시예 16 의 화합물 (화합물 98) 6.48 eV
실시예 17 의 화합물 (화합물 153) 6.46 eV
실시예 18 의 화합물 (화합물 155) 6.51 eV
실시예 19 의 화합물 (화합물 82) 6.46 eV
실시예 20 의 화합물 (화합물 182) 6.54 eV
실시예 21 의 화합물 (화합물 227) 6.55 eV
실시예 22 의 화합물 (화합물 234) 6.55 eV
실시예 23 의 화합물 (화합물 235) 6.54 eV
상기와 같이, 본 발명의 화합물은 NPD 또는 TPD 등의 일반적인 정공 수송 재료가 갖는 일 함수 5.5 eV 보다 큰 값을 가지고 있어, 큰 정공 저지 능력을 갖고 있다.
<글라스 전이점의 측정>
실시예 4 내지 23 에서 얻은 화합물을 고감도 시차 주사 열량계 (Bruker AXS K.K. 제, DSC3100S) 를 이용하여 글라스 전이점을 측정했다.
글라스 전이점
실시예 4 의 화합물 (화합물 130) 129℃
실시예 5 의 화합물 (화합물 131) 138℃
실시예 6 의 화합물 (화합물 92) 108℃
실시예 7 의 화합물 (화합물 136) 128℃
실시예 8 의 화합물 (화합물 125) 117℃
실시예 9 의 화합물 (화합물 138) 111℃
실시예 10 의 화합물 (화합물 78) 138℃
실시예 11 의 화합물 (화합물 76) 103℃
실시예 12 의 화합물 (화합물 126) 129℃
실시예 13 의 화합물 (화합물 124) 107℃
실시예 14 의 화합물 (화합물 123) 116℃
실시예 15 의 화합물 (화합물 146) 114℃
실시예 16 의 화합물 (화합물 98) 116℃
실시예 17 의 화합물 (화합물 153) 116℃
실시예 18 의 화합물 (화합물 155) 132℃
실시예 19 의 화합물 (화합물 82) 131℃
실시예 20 의 화합물 (화합물 182) 114℃
실시예 21 의 화합물 (화합물 227) 150℃
실시예 22 의 화합물 (화합물 234) 143℃
실시예 23 의 화합물 (화합물 235) 146℃
본 발명의 화합물은 100 ℃ 이상, 특히 140 ℃ 이상의 글라스 전이점을 가지고 있으며, 이는 본 발명의 화합물이 박막 상태에서 안정하다는 것을 나타낸다.
<유기 EL 소자 실시예 1>
도 24 에 나타낸 바와 같이, 글라스 기판 (1) 위에 투명 양극 (2) 으로 미리 형성한 ITO 전극 위에 정공 주입층 (3), 정공 수송층 (4), 발광층 (5), 정공 저지층 (6), 전자 수송층 (7), 전자 주입층 (8), 및 음극 (알루미늄 전극) (9) 을 이 순서로 증착하여 유기 EL 소자를 제작하였다.
구체적으로는, 두께 150 nm 의 ITO 막을 증착한 글라스 기판 (1) 을 이소프로필 알코올 중에서 초음파 세척을 20 분간 실시한 후, 200℃ 로 가열한 열판에서 10 분간 건조를 실시했다. 그 후, ITO 막을 갖는 글라스 기판에 UV/오존 처리를 15 분간 실시했다. 그 후, ITO 막을 갖는 글라스 기판을 진공증착기 내에 설치하고 0.001 Pa 이하까지 감압했다. 그 후, 투명 양극 (2) 을 덮도록, 정공 주입층 (3) 으로서 아래 나타낸 구조식으로 표시되는 화합물 HIM-1 의 막을 막 두께 5 nm 가 되도록 형성했다. 정공 주입층 (3) 위에, 정공 수송층 (4) 으로서 아래 나타낸 구조식으로 표시되는 화합물 HTM-1 의 막을 막 두께 65 nm 가 되도록 형성했다. 정공 수송층 (4) 위에, 아래 나타낸 구조식으로 표시되는 화합물 EMD-1, 및 아래 나타낸 구조식으로 표시되는 화합물 EMH-1 을 증착 속도 비가 EMD-1:EMH-1=5:95 이 되는 증착 속도로 이원화 증착하여, 발광층 (5) 을 막 두께 20 nm 가 되도록 형성했다. 이 발광층 (5) 위에, 실시예 1 의 화합물 (화합물 74) 및 아래 나타낸 구조식으로 표시되는 화합물 ETM-1 을 증착 속도 비가 실시예 1 의 화합물 (화합물 74):ETM-1=50:50 이 되는 증착 속도로 이원화 증착하여, 정공 저지층 (6) 및 전자 수송층 (7) 을 겸하는 막을 막 두께 30 nm 가 되도록 형성했다. 정공 저지층 (6)/전자 수송층 (7) 위에, 전자 주입층 (8) 으로서 불화 리튬의 막을 막 두께 1 nm 가 되도록 형성했다. 마지막으로, 알루미늄을 막 두께 100 nm 가 되도록 증착하여 음극 (9) 을 형성했다.
<유기 EL 소자 실시예 2 내지 20>
표 1 에 나타낸 바와 같이, 정공 저지층 (6)/전자 수송층 (7) 의 재료로서, 실시예 1 의 화합물 (화합물 74) 대신에 실시예 2 내지 20 각각의 화합물을 사용한 점 외에는, 유기 EL 소자 실시예 1 과 동일한 조건에서 유기 EL 소자를 제작하였다.
<유기 EL 소자 비교예 1>
비교를 위해, 정공 저지층 (6)/전자 수송층 (7) 의 재료로서, 실시예 1 의 화합물 (화합물 74) 대신에 아래 나타낸 구조식으로 표시되는 화합물 ETM-2 (특허 문헌 4 참조) 을 사용한 점 외에는, 유기 EL 소자 실시예 1 과 동일한 조건에서 유기 EL 소자를 제작하였다.
유기 EL 소자 실시예 1 내지 20, 및 유기 EL 소자 비교예 1 에서 제작한 유기 EL 소자에 대해 대기 중 상온에서 직류 전압을 인가했을 때의 발광 특성을 측정했다. 결과를 표 1 에 나타내었다.
유기 EL 소자 실시예 1 내지 20, 및 유기 EL 소자 비교예 1 에서 제작한 유기 EL 소자에 대해 소자 수명을 측정했다. 구체적으로는, 소자 수명을 발광 개시시의 발광 휘도 (초기 휘도) 를 2000 cd/m2 로 설정하여 정전류 구동을 수행했을 때, 발광 휘도가 1900 cd/m2 (초기 휘도를 100 % 로 했을 때의 95 % 에 해당: 95 % 감쇠) 으로 감소할 때까지의 시간으로 측정했다. 결과를 표 1 에 나타내었다.
[표 1]
표 1 에 나타낸 바와 같이, 전류 밀도 10 mA/cm2 의 전류가 흐를 때의 발광 효율은 유기 EL 소자 비교예 1 이 6.35 cd/A 의 값을 보이는데 반해, 유기 EL 소자 실시예 1 내지 20 에서는 6.86 내지 8.23 cd/A 로 크게 향상된 값을 보였다.
전력 효율에 대해서도 유기 EL 소자 비교예 1 이 5.20 lm/W 인 반면, 유기 EL 소자 실시예 1 내지 20 에서는 5.76 내지 6.98 lm/W 로 큰 향상을 보였다.
특히, 소자 수명 (95% 감쇠) 에서는, 유기 EL 소자 비교예 1 이 55 시간인 반면, 유기 EL 소자 실시예 1 내지 20 에서는 128 내지 276 시간으로 장수명화를 보였다. 이처럼 장수명화를 실현할 수 있었던 것은, 본 발명의 피리미딘 유도체가 종래의 유기 EL 소자용 재료에 비해 박막 상태가 안정하고, 내열성이 우수하기 때문인 것으로 생각된다. 또한, 이러한 효과는 본 발명의 피리미딘 유도체의 담체 밸런스가 뛰어나기 때문인 것으로 추측된다.
더욱이, 구동 전압에 대해 유기 EL 소자 실시예 1 내지 20 의 값은 유기 EL 소자 비교예 1 와 동일한 정도로 낮거나 그 이상으로 낮았다.
상기와 같이 본 발명의 유기 EL 소자는 일반적인 전자 수송 재료인 화합물 ETM-2 를 이용한 소자에 비해 발광 효율 및 전력 효율이 뛰어나 긴 수명의 유기 EL 소자를 실현할 수 있는 것으로 나타났다.
본 발명의 피리미딘 유도체는 전자 주입성이 좋고, 정공 저지 능력이 뛰어나고, 박막 상태가 안정적이기 때문에, 유기 EL 소자용 화합물로서 뛰어나다. 상기 화합물을 이용하여 유기 EL 소자를 제작함으로써 높은 효율을 얻을 수 있는 동시에, 구동 전압을 저하시킬 수 있으며, 내구성을 향상시킬 수 있다. 따라서, 본 발명의 유기 EL 소자를 가전 제품 및 조명 용도로 사용할 수 있다.
1 글라스 기판
2 투명 양극
3 정공 주입층
4 정공 수송층
5 발광층
6 정공 저지층
7 전자 수송층
8 전자 주입층
9 음극
2 투명 양극
3 정공 주입층
4 정공 수송층
5 발광층
6 정공 저지층
7 전자 수송층
8 전자 주입층
9 음극
Claims (21)
- 하기 일반식 (1) 로 표시되는 피리미딘 유도체:
식에서,
Ar1 은 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기를 나타내고,
Ar2 및 Ar3 은 동일 또는 상이할 수 있고, 각각 수소 원자, 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기를 나타내고,
Ar2 및 Ar3 이 동시에 수소 원자는 아니고,
A 는 하기 구조식 (2) 로 표시되는 1 가 기를 나타내고:
식에서,
Ar4 는 방향족 헤테로고리 기를 나타내고,
R1 내지 R4 은 동일 또는 상이할 수 있고, 각각 수소 원자, 중수소 원자, 불소 원자, 염소 원자, 시아노 기, 트리플루오로메틸 기, 1 내지 6 개의 탄소 원자를 갖는 알킬 기, 방향족 탄화수소 기, 축합 다환 방향족 기, 또는 방향족 헤테로고리 기를 나타내고,
R1 내지 R4 및 Ar4 는 단일 결합, 메틸렌 기, 산소 원자, 또는 황 원자를 통해 서로 결합하여 고리를 형성할 수 있음. - 제 1 항에 있어서, Ar1 은 방향족 탄화수소 기 또는 축합 다환 방향족 기를 나타내고, Ar2 및 Ar3 은 동일 또는 상이할 수 있고, 각각 수소 원자, 방향족 탄화수소 기, 또는 축합 다환 방향족 기를 나타내는 피리미딘 유도체.
- 제 1 항에 있어서, Ar4 는 피리딜 기, 피리미디닐 기, 퀴놀릴 기, 이소퀴놀릴 기, 인돌릴 기, 아자플루오레닐 기, 디아자플루오레닐 기, 퀴녹살리닐 기, 벤지미다졸릴 기, 나프티리디닐 기, 페난트롤리닐 기, 아크리디닐 기, 아자스피로비플루오레닐 기, 또는 디아자스피로비플루오레닐 기인 피리미딘 유도체.
- 제 1 항에 있어서, Ar2 는 치환기를 갖는 페닐 기인 피리미딘 유도체.
- 제 8 항에 있어서, Ar2 는 치환기를 갖는 페닐 기이고, 치환기는 방향족 탄화수소 기 또는 축합 다환 방향족 기인 피리미딘 유도체.
- 제 9 항에 있어서, Ar2 는 치환기를 갖는 페닐 기이고, 치환기는 방향족 탄화수소 기인 피리미딘 유도체.
- 제 9 항에 있어서, Ar2 는 치환기를 갖는 페닐 기이고, 치환기는 축합 다환 방향족 기인 피리미딘 유도체.
- 제 1 항에 있어서, Ar3 은 수소 원자인 피리미딘 유도체.
- 제 1 항에 있어서, Ar1 은 치환기를 갖는 페닐 기인 피리미딘 유도체.
- 제 13 항에 있어서, Ar1 은 치환기를 갖는 페닐 기이고, 치환기는 축합 다환 방향족 기인 피리미딘 유도체.
- 제 1 항에 있어서, Ar1 은 축합 다환 방향족 기인 피리미딘 유도체.
- 제 1 항에 있어서, Ar1 은 무치환 페닐 기인 피리미딘 유도체.
- 하기를 포함하는 유기 전계발광 소자:
한 쌍의 전극, 및
한 쌍의 전극 사이에 끼워진 적어도 하나의 유기 층,
여기에서 제 1 항에 따른 피리미딘 유도체가 적어도 하나의 유기 층의 구성 재료로서 사용됨. - 제 17 항에 있어서, 피리미딘 유도체가 사용되는 유기 층이 전자 수송층인 유기 전계발광 소자.
- 제 17 항에 있어서, 피리미딘 유도체가 사용되는 유기 층이 정공 저지층인 유기 전계발광 소자.
- 제 17 항에 있어서, 피리미딘 유도체가 사용되는 유기 층이 발광층인 유기 전계발광 소자.
- 제 17 항에 있어서, 피리미딘 유도체가 사용되는 유기 층이 전자 주입층인 유기 전계발광 소자.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014120362 | 2014-06-11 | ||
| JPJP-P-2014-120362 | 2014-06-11 | ||
| PCT/JP2015/066251 WO2015190400A1 (ja) | 2014-06-11 | 2015-06-04 | ピリミジン誘導体および有機エレクトロルミネッセンス素子 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170016936A true KR20170016936A (ko) | 2017-02-14 |
Family
ID=54833493
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177000298A KR20170016936A (ko) | 2014-06-11 | 2015-06-04 | 피리미딘 유도체 및 유기 전계발광 소자 |
Country Status (7)
| Country | Link |
|---|---|
| US (2) | US20170186967A1 (ko) |
| EP (2) | EP3663289A1 (ko) |
| JP (1) | JP6501771B2 (ko) |
| KR (1) | KR20170016936A (ko) |
| CN (2) | CN111205270B (ko) |
| TW (2) | TWI676623B (ko) |
| WO (1) | WO2015190400A1 (ko) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2021086142A1 (ko) * | 2019-10-31 | 2021-05-06 | 솔브레인 주식회사 | 유기 화합물, 이를 포함하는 유기 발광 다이오드 및 상기 유기 발광 다이오드를 포함하는 표시장치 |
| CN114835686A (zh) * | 2021-02-02 | 2022-08-02 | 江苏三月科技股份有限公司 | 一种含有菲与三嗪结构的化合物及其应用 |
| KR20220127220A (ko) * | 2017-07-20 | 2022-09-19 | 솔루스첨단소재 주식회사 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
Families Citing this family (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN107112427B (zh) * | 2014-11-14 | 2019-09-24 | 保土谷化学工业株式会社 | 有机电致发光器件 |
| JP6634028B2 (ja) * | 2014-12-24 | 2020-01-22 | 保土谷化学工業株式会社 | 有機エレクトロルミネッセンス素子 |
| TWI682920B (zh) * | 2015-01-08 | 2020-01-21 | 日商保土谷化學工業股份有限公司 | 有機電致發光元件 |
| KR102002031B1 (ko) * | 2015-06-12 | 2019-07-23 | 에스에프씨주식회사 | 고효율을 갖는 유기 발광 소자 |
| WO2016204150A1 (ja) * | 2015-06-16 | 2016-12-22 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子及び電子機器 |
| CN105355798A (zh) * | 2015-11-25 | 2016-02-24 | 京东方科技集团股份有限公司 | 有机电致发光器件及其制作方法、显示装置 |
| TWI745361B (zh) * | 2016-03-17 | 2021-11-11 | 德商麥克專利有限公司 | 具有螺聯茀結構之化合物 |
| EP3432688B1 (en) | 2016-04-22 | 2023-12-20 | Hodogaya Chemical Co., Ltd. | Organic electroluminescence element |
| US11672169B2 (en) | 2017-03-15 | 2023-06-06 | Hodogaya Chemical Co., Ltd. | Organic electroluminescent element |
| KR102232510B1 (ko) * | 2017-05-26 | 2021-03-26 | 삼성에스디아이 주식회사 | 인광 호스트용 조성물, 유기 광전자 소자 및 표시 장치 |
| CN110998889B (zh) * | 2017-08-04 | 2022-07-26 | 保土谷化学工业株式会社 | 含有具有苯并唑环结构的化合物的有机电致发光元件 |
| US20200277272A1 (en) | 2017-09-11 | 2020-09-03 | Hodogaya Chemical Co., Ltd. | Compound having pyrimidine ring structure and organic electroluminescence device |
| US20200328355A1 (en) * | 2017-11-06 | 2020-10-15 | Hodogaya Chemical Co., Ltd. | Compound having indenocarbazole ring structure, and organic electroluminescence device |
| EP3712975A4 (en) | 2017-11-16 | 2021-08-25 | Hodogaya Chemical Co., Ltd. | ORGANIC ELECTROLUMINESCENT ELEMENT |
| CN111433930B (zh) | 2017-12-05 | 2023-06-06 | 保土谷化学工业株式会社 | 芳基胺化合物及有机电致发光元件 |
| KR20190070586A (ko) | 2017-12-13 | 2019-06-21 | 엘지디스플레이 주식회사 | 전자수송 재료용 화합물 및 이를 포함하는 유기 발광 다이오드 |
| TWI630260B (zh) * | 2017-12-21 | 2018-07-21 | 昱鐳光電科技股份有限公司 | 經喹啉取代之二苯基嘧啶化合物及其有機電激發光元件 |
| CN109988159A (zh) * | 2017-12-29 | 2019-07-09 | 昱镭光电科技股份有限公司 | 经吡啶取代的二苯基嘧啶化合物及其有机电致发光元件 |
| EP3754739A4 (en) * | 2018-02-15 | 2021-11-17 | Hodogaya Chemical Co., Ltd. | ORGANIC ELECTROLUMINESCENT ELEMENT |
| US20220052268A1 (en) | 2018-10-17 | 2022-02-17 | Hodogaya Chemical Co., Ltd. | Compound having pyrimidine ring structure and organic electroluminescent element |
| CN114599646A (zh) * | 2019-10-31 | 2022-06-07 | 秀博瑞殷株式公社 | 有机化合物、包含其的有机发光二极管以及包括所述有机发光二极管的显示装置 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0848656A (ja) | 1994-02-08 | 1996-02-20 | Tdk Corp | 有機el素子用化合物および有機el素子 |
| JP2734341B2 (ja) | 1993-03-26 | 1998-03-30 | 住友電気工業株式会社 | 有機エレクトロルミネッセンス素子 |
| JP3194657B2 (ja) | 1993-11-01 | 2001-07-30 | 松下電器産業株式会社 | 電界発光素子 |
| WO2003060956A2 (en) | 2002-01-18 | 2003-07-24 | Lg Chem, Ltd. | New material for transporting electrons and organic electroluminescent display using the same |
| WO2014009310A1 (en) | 2012-07-09 | 2014-01-16 | Novaled Ag | Doped organic semiconductive matrix material |
Family Cites Families (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR101389735B1 (ko) * | 2004-12-10 | 2014-04-29 | 미쓰비시 가가꾸 가부시키가이샤 | 유기 화합물, 전하 수송 재료 및 유기 전계 발광 소자 |
| EP1829871B1 (en) * | 2004-12-24 | 2015-08-12 | Pioneer Corporation | Organic compound, charge-transporting material, and organic electroluminescent element |
| JP5201956B2 (ja) * | 2007-11-20 | 2013-06-05 | ケミプロ化成株式会社 | 新規なジ(ピリジルフェニル)誘導体、それよりなる電子輸送材料およびそれを含む有機エレクトロルミネッセンス素子 |
| JP5357150B2 (ja) * | 2008-06-05 | 2013-12-04 | 出光興産株式会社 | ハロゲン化合物、多環系化合物及びそれを用いた有機エレクトロルミネッセンス素子 |
| KR100958641B1 (ko) * | 2008-08-18 | 2010-05-20 | 삼성모바일디스플레이주식회사 | 광효율 개선층을 구비한 유기 발광 소자 |
| KR101174090B1 (ko) * | 2008-08-25 | 2012-08-14 | 제일모직주식회사 | 유기광전소자용 재료 및 이를 포함하는 유기광전소자 |
| KR101233377B1 (ko) * | 2008-12-30 | 2013-02-18 | 제일모직주식회사 | 신규한 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| WO2011005060A2 (ko) * | 2009-07-10 | 2011-01-13 | 제일모직 주식회사 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| JP4474493B1 (ja) * | 2009-07-31 | 2010-06-02 | 富士フイルム株式会社 | 有機電界発光素子 |
| KR101761431B1 (ko) * | 2009-08-21 | 2017-07-25 | 토소가부시키가이샤 | 환상 아진 유도체와 그들의 제조방법 및 그들을 구성 성분으로 하는 유기 전계발광소자 |
| KR101288566B1 (ko) * | 2009-12-16 | 2013-07-22 | 제일모직주식회사 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| KR20110079197A (ko) * | 2009-12-31 | 2011-07-07 | 제일모직주식회사 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| KR101297158B1 (ko) * | 2010-02-22 | 2013-08-21 | 제일모직주식회사 | 유기광전소자용 화합물 및 이를 포함하는 유기광전소자 |
| KR101181280B1 (ko) * | 2010-03-05 | 2012-09-10 | 덕산하이메탈(주) | 2개 이상의 오원자 헤테로고리를 포함하는 화합물이 2개 이상 포함하는 화합물 및 이를 이용한 유기전기소자, 그 단말 |
| JP5664128B2 (ja) * | 2010-10-29 | 2015-02-04 | 三菱化学株式会社 | ピリミジン化合物、有機電界発光素子用材料、有機電界発光素子用組成物、有機電界発光素子、照明装置及び表示装置 |
| DE102010054316A1 (de) * | 2010-12-13 | 2012-06-14 | Merck Patent Gmbh | Substituierte Tetraarylbenzole |
| CN103261172B (zh) * | 2010-12-21 | 2016-05-04 | E.I.内穆尔杜邦公司 | 包括嘧啶化合物的电子装置 |
| CN103765623B (zh) * | 2011-08-22 | 2016-06-01 | 默克专利有限公司 | 有机电致发光器件 |
| CN107586290B (zh) * | 2011-11-22 | 2021-05-11 | 出光兴产株式会社 | 芳香族杂环衍生物、有机电致发光元件用材料以及有机电致发光元件 |
| JP6088979B2 (ja) * | 2011-11-22 | 2017-03-01 | 出光興産株式会社 | 芳香族複素環誘導体、有機エレクトロルミネッセンス素子用材料および有機エレクトロルミネッセンス素子 |
| KR102013399B1 (ko) * | 2011-11-29 | 2019-08-22 | 에스에프씨 주식회사 | 안트라센 유도체 및 이를 포함하는 유기전계발광소자 |
| KR101497134B1 (ko) * | 2011-12-29 | 2015-03-02 | 제일모직 주식회사 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| KR101497137B1 (ko) * | 2011-12-30 | 2015-03-03 | 제일모직 주식회사 | 유기광전자소자용 화합물, 이를 포함하는 유기발광소자 및 상기 유기발광소자를 포함하는 표시장치 |
| KR102154055B1 (ko) * | 2012-03-27 | 2020-09-09 | 에스에프씨 주식회사 | 카바졸 유도체 및 이를 이용한 유기전계발광소자 |
| KR102169444B1 (ko) * | 2012-06-22 | 2020-10-26 | 에스에프씨 주식회사 | 방향족 화합물 및 이를 포함하는 유기전계발광소자 |
| KR101540053B1 (ko) * | 2012-07-05 | 2015-07-29 | 주식회사 엠비케이 | 신규한 유기발광화합물 및 이를 포함하는 유기전기발광소자 |
| KR102265997B1 (ko) * | 2012-08-10 | 2021-06-16 | 메르크 파텐트 게엠베하 | 유기 전계발광 소자용 물질 |
| JP2014075556A (ja) * | 2012-10-05 | 2014-04-24 | Idemitsu Kosan Co Ltd | 有機エレクトロルミネッセンス素子用材料、及びそれを用いた有機エレクトロルミネッセンス素子 |
| CN107963972B (zh) * | 2013-02-22 | 2021-09-03 | 保土谷化学工业株式会社 | 有机电致发光器件 |
| CN103396404B (zh) * | 2013-07-31 | 2015-04-22 | 华南理工大学 | 一种以三苯基嘧啶为核的化合物及其制备方法和应用 |
| WO2016175211A1 (ja) * | 2015-04-27 | 2016-11-03 | 保土谷化学工業株式会社 | 有機エレクトロルミネッセンス素子 |
-
2015
- 2015-06-04 EP EP20153606.7A patent/EP3663289A1/en not_active Withdrawn
- 2015-06-04 KR KR1020177000298A patent/KR20170016936A/ko not_active IP Right Cessation
- 2015-06-04 WO PCT/JP2015/066251 patent/WO2015190400A1/ja active Application Filing
- 2015-06-04 EP EP15807524.2A patent/EP3156402B1/en active Active
- 2015-06-04 CN CN202010108854.7A patent/CN111205270B/zh active Active
- 2015-06-04 JP JP2016527776A patent/JP6501771B2/ja active Active
- 2015-06-04 CN CN201580039162.9A patent/CN106573911A/zh active Pending
- 2015-06-04 US US15/317,320 patent/US20170186967A1/en not_active Abandoned
- 2015-06-10 TW TW104118700A patent/TWI676623B/zh active
- 2015-06-10 TW TW108106685A patent/TWI721379B/zh active
-
2020
- 2020-04-06 US US16/840,797 patent/US20200303658A1/en not_active Abandoned
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2734341B2 (ja) | 1993-03-26 | 1998-03-30 | 住友電気工業株式会社 | 有機エレクトロルミネッセンス素子 |
| JP3194657B2 (ja) | 1993-11-01 | 2001-07-30 | 松下電器産業株式会社 | 電界発光素子 |
| JPH0848656A (ja) | 1994-02-08 | 1996-02-20 | Tdk Corp | 有機el素子用化合物および有機el素子 |
| WO2003060956A2 (en) | 2002-01-18 | 2003-07-24 | Lg Chem, Ltd. | New material for transporting electrons and organic electroluminescent display using the same |
| WO2014009310A1 (en) | 2012-07-09 | 2014-01-16 | Novaled Ag | Doped organic semiconductive matrix material |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20220127220A (ko) * | 2017-07-20 | 2022-09-19 | 솔루스첨단소재 주식회사 | 유기 발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| WO2021086142A1 (ko) * | 2019-10-31 | 2021-05-06 | 솔브레인 주식회사 | 유기 화합물, 이를 포함하는 유기 발광 다이오드 및 상기 유기 발광 다이오드를 포함하는 표시장치 |
| CN114835686A (zh) * | 2021-02-02 | 2022-08-02 | 江苏三月科技股份有限公司 | 一种含有菲与三嗪结构的化合物及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN106573911A (zh) | 2017-04-19 |
| EP3156402A1 (en) | 2017-04-19 |
| TWI721379B (zh) | 2021-03-11 |
| TW201602097A (zh) | 2016-01-16 |
| WO2015190400A1 (ja) | 2015-12-17 |
| EP3156402B1 (en) | 2021-11-10 |
| EP3663289A1 (en) | 2020-06-10 |
| JP6501771B2 (ja) | 2019-04-17 |
| EP3156402A4 (en) | 2017-12-06 |
| CN111205270A (zh) | 2020-05-29 |
| TW201920148A (zh) | 2019-06-01 |
| JPWO2015190400A1 (ja) | 2017-04-20 |
| US20170186967A1 (en) | 2017-06-29 |
| US20200303658A1 (en) | 2020-09-24 |
| CN111205270B (zh) | 2023-04-28 |
| TWI676623B (zh) | 2019-11-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20200303658A1 (en) | Pyrimidine derivative and an organic electroluminescent device | |
| JP6731355B2 (ja) | ピリミジン誘導体および有機エレクトロルミネッセンス素子 | |
| JP7245777B2 (ja) | ベンゾアゾール環構造を有する化合物を含有する有機エレクトロルミネッセンス素子 | |
| KR20180017130A (ko) | 아릴아민 화합물 및 유기 전계발광 소자 | |
| TWI790280B (zh) | 有機電致發光元件 | |
| JP7394050B2 (ja) | ベンゾイミダゾール環構造を有する化合物および有機エレクトロルミネッセンス素子 | |
| JP7369714B2 (ja) | アザベンゾオキサゾール環構造を有する化合物および有機エレクトロルミネッセンス素子 | |
| WO2020246484A1 (ja) | ベンゾトリアゾール環構造を有する化合物および有機エレクトロルミネッセンス素子 | |
| JP7406500B2 (ja) | ピリミジン環構造を有する化合物および有機エレクトロルミネッセンス素子 | |
| KR102603365B1 (ko) | 피리미딘 고리 구조를 갖는 화합물 및 유기 일렉트로 루미네선스 소자 | |
| CN113557233A (zh) | 分子末端具有含氮杂环的三取代苯化合物及有机电致发光元件 | |
| JP6479770B2 (ja) | キノリノトリアゾール誘導体および有機エレクトロルミネッセンス素子 | |
| JP7179734B2 (ja) | インデノベンゾアゾール環構造を有する化合物および有機エレクトロルミネッセンス素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal | ||
| AMND | Amendment | ||
| E601 | Decision to refuse application | ||
| AMND | Amendment | ||
| X601 | Decision of rejection after re-examination |