KR20150110562A - Lna 올리고뉴클레오타이드 탄수화물 컨쥬게이트 - Google Patents
Lna 올리고뉴클레오타이드 탄수화물 컨쥬게이트 Download PDFInfo
- Publication number
- KR20150110562A KR20150110562A KR1020157020832A KR20157020832A KR20150110562A KR 20150110562 A KR20150110562 A KR 20150110562A KR 1020157020832 A KR1020157020832 A KR 1020157020832A KR 20157020832 A KR20157020832 A KR 20157020832A KR 20150110562 A KR20150110562 A KR 20150110562A
- Authority
- KR
- South Korea
- Prior art keywords
- lna
- region
- oligomer
- conjugate
- antisense oligomer
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/712—Nucleic acids or oligonucleotides having modified sugars, i.e. other than ribose or 2'-deoxyribose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/713—Double-stranded nucleic acids or oligonucleotides
-
- A61K47/481—
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/55—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound the modifying agent being also a pharmacologically or therapeutically active agent, i.e. the entire conjugate being a codrug, i.e. a dimer, oligomer or polymer of pharmacologically or therapeutically active compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1131—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against viruses
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1137—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
- C12N2310/113—Antisense targeting other non-coding nucleic acids, e.g. antagomirs
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/31—Chemical structure of the backbone
- C12N2310/315—Phosphorothioates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/323—Chemical structure of the sugar modified ring structure
- C12N2310/3231—Chemical structure of the sugar modified ring structure having an additional ring, e.g. LNA, ENA
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/34—Spatial arrangement of the modifications
- C12N2310/341—Gapmers, i.e. of the type ===---===
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
- C12N2310/3513—Protein; Peptide
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2330/00—Production
- C12N2330/30—Production chemically synthesised
Abstract
본 발명은 상당히 향상된 효능, 확장된 치료 지수 및 감소된 독성을 가지는 LNA 치료제 올리고뉴클레오타이드 탄수화물 컨쥬게이트를 제공한다.
Description
본 발명은 LNA 치료적 단일 가닥의 안티센스 올리고뉴클레오타이드 컨쥬게이트의 분야에 관한 것이다. 본 발명은 상당히 향상된 효능, 확장된 치료 지수 및 감소된 독성을 가지는 LNA 치료제 올리고뉴클레오타이드 탄수화물 컨쥬게이트를 제공한다.
올리고뉴클레오타이드 컨쥬게이트는 siRNA 에서 사용하기 위해 광범위하게 평가되었으며, 여기서, 이들은 충분한 생체내 효능을 수득하기 위해 필수적인 것으로 고려된다. 예를 들면, WO 2004/044141 을 참조하면 RNA 간섭 경로를 통해 유전자 발현을 조절하는 변형된 올리고머성 화합물을 언급하고 있다. 올리고머성 화합물은 부착된 올리고머성 화합물의 약동학적 및 약력학적 특성을 변형하거나 개선할 수 있는 하나 이상의 컨쥬게이트 모이어티 (moiety) 를 포함한다.
WO2012/083046 은 siRNA 에 대한 모이어티를 표적화하는 갈락토오스 클러스터-약동학 조절제에 대해 보고하고 있다.
이와 대조적으로, 단일 가닥의 안티센스 올리고뉴클레오타이드는 전형적으로 컨쥬게이션 또는 제형화 없이 치료학적으로 투여된다. 안티센스 올리고뉴클레오타이드에 대한 주요 표적 조직은 간 및 신장이지만, 림프절, 비장, 골수를 비롯한 광범위한 다른 조직도 또한 안티센스 양상에 의해 접근가능하다.
문헌 [van Poelgeest et al., American Journal of Kidney Disease, In Press] 에 따르면, 인간 임상 시험에서의 LNA 안티센스 올리고뉴클레오타이드의 투여는 급성 신장 손상을 초래할 수 있다. 문헌 [Swayze et al., NAR, Dec. 2006, advanced online publication] 에 따르면, 잠금 핵산을 함유하는 안티센스 올리고뉴클레오타이드는 동물에서 효능을 향상시키지만 현저한 간독성을 초래한다.
WO 2004/087931 은 산 절단가능한 친수성 폴리머 (PEG) 컨쥬게이트를 포함하는 올리고뉴클레오타이드를 언급하고 있다.
WO 2005/086775 는 치료적 화학 모이어티, 절단가능한 링커 및 라벨링 도메인을 사용하여 특정 장기에 대한 치료제의 표적화 전달을 언급하고 있다. 절단가능한 링커는, 예를 들면, 디설파이드기, 펩타이드 또는 제한 효소 절단가능한 올리고뉴클레오타이드 도메인일 수 있다.
WO 2011/126937 은 소형 분자 리간드와의 컨쥬게이션을 통한 올리고뉴클레오타이드의 표적화 세포내 전달을 언급하고 있다.
WO2009/025669 는 피리딜 디설파이드 모이어티를 함유하는 폴리머성 (폴리에틸렌 글리콜) 링커를 언급하고 있다. 또한 문헌 [Zhao et al., Bioconjugate Chem. 2005 16 758-766.Zhao et al., Bioconjugate Chem. 2005 16 758-766] 을 참조한다.
문헌 [Chaltin et al ., Bioconjugate Chem. 2005 16 827-836] 은 안티센스 올리고뉴클레오타이드를 양이온성 리포좀 내로 도입하여 덴드리머성 (dendrimeric) 전달 시스템을 생성하는데 사용되는 콜레스테롤 변형된 모노머성, 이량체성 및 사량체성 올리고뉴클레오타이드를 보고하고 있다. 콜레스테롤은 라이신 링커를 통해 올리고뉴클레오타이드에 컨쥬게이트되어 있다.
기타 비-절단가능한 콜레스테롤 컨쥬게이트는 간에 대해 siRNA 및 안타고미르를 표적화하는데 사용되었다 - 예를 들면, 문헌 [Soutscheck et al., Nature 2004 vol. 432 173-178; 및 Krutzfeldt et al., Nature 2005 vol 438, 685-689] 을 참조한다. 부분적으로 포스포로티올화 siRNA 및 안타고미르의 경우, 간 표적화 실체 (entity) 로서의 콜레스테롤의 사용은 생체내 활성에 필수적인 것으로 밝혀졌다.
문헌 [Bhat et al., AASLD November 7-11th 2013 (poster)] 은 전임상 연구에서 HCV 의 감소를 위한 miR-122 를 표적화하는 GalNac 컨쥬게이트된 anti-miR, RG-101 의 사용으로부터의 데이터를 개시하고 있다. RG-101 의 정체는 개시되지 않았다.
본 발명은 단일 가닥의 LNA 안티센스 올리고뉴클레오타이드의 효능, 생체 분포 및 치료 지수가 탄수화물 컨쥬게이트, 예를 들면, GalNAc 컨쥬게이트에 대한 LNA 올리고뉴클레오타이드의 컨쥬게이션에 의해 상당히 개선될 수 있다는 발견에 근거한다.
관련 출원
본 출원은 EP13153296.2 (2013-01-30 출원), EP13157237.2 (2013-02-28 출원), EP13174092.0 (2013-06-27 출원), EP13192938.2 (2013-11-14 출원), EP13192931.7 (2013-11-14 출원), EP13192930.9 (2013-11-14 출원), PCT/EP2013/073859 (2013-11-14 출원) 및 PCT/EP2013/073859 (2013-11-14 출원) 으로부터의 우선권을 주장한다: 이들 출원의 이들 내용은 참조에 의해 본원에 도입된다.
발명의 개요
본 발명은 안티센스 올리고머 및 추가의 영역 (영역 C 로서 언급함) 의 일부를 형성할 수 있는 아시알로당단백질 수용체 표적화 컨쥬게이트 모이어티, 예를 들면, GalNAc 모이어티를 포함하는 LNA 안티센스 올리고머 (본원에서 영역 A 로서 언급할 수 있음) 를 제공한다.
본 발명은 안티센스 올리고머 및 추가의 영역 (영역 C 로서 언급함) 의 일부를 형성할 수 있는 GalNAc 모이어티, 예를 들면, 3가 GalNAc 모이어티를 포함하는 LNA 안티센스 올리고머 (본원에서 영역 A 로서 언급할 수 있음) 를 제공한다.
본 발명은 LNA 안티센스 갭머 올리고머 및 추가의 영역 (영역 C 로서 언급함) 의 일부를 형성할 수 있는 아시알로당단백질 수용체 표적화 컨쥬게이트 모이어티, 예를 들면, GalNAc 모이어티를 포함하는 LNA 안티센스 올리고머 갭머 (본원에서 영역 A 로서 언급할 수 있음) 를 제공한다. LNA 안티센스 올리고머 갭머는, 예를 들면, mRNA 또는 바이러스 RNA 표적을 표적화할 수 있다.
본 발명은 LNA 안티센스 믹스머 올리고머 및 추가의 영역 (영역 C 로서 언급함) 의 일부를 형성할 수 있는 아시알로당단백질 수용체 표적화 컨쥬게이트 모이어티, 예를 들면, GalNAc 모이어티를 포함하는 LNA 안티센스 올리고머 믹스머 (본원에서 영역 A 로서 언급할 수 있음) 를 제공한다. LNA 안티센스 올리고머 믹스머는, 예를 들면, mRNA, 예를 들면, mRNA 스플라이스 부위 또는 microRNA 표적을 표적화할 수 있다.
본 발명은 LNA 안티센스 토탈머 올리고머 및 추가의 영역 (영역 C 로서 언급함) 의 일부를 형성할 수 있는 아시알로당단백질 수용체 표적화 컨쥬게이트 모이어티, 예를 들면, GalNAc 모이어티를 포함하는 LNA 안티센스 올리고머 토탈머 (본원에서 영역 A 로서 언급할 수 있음) 를 제공한다. LNA 안티센스 올리고머 믹스머는, 예를 들면, microRNA 표적을 표적화할 수 있다.
LNA 안티센스 올리고머는 7-30 개, 예를 들면, 8-26 개, 또는 일부 실시형태에서는 8-18 개 길이의 뉴클레오사이드일 수 있으며, 이것은 하나 이상의 LNA 단위 (뉴클레오사이드) 를 포함한다. 따라서, 본 발명은 안티센스 올리고머 및 추가의 영역 (영역 C 로서 언급함) 의 일부를 형성할 수 있는 아시알로당단백질 수용체 표적화 컨쥬게이트 모이어티, 예를 들면, GalNAc 모이어티를 포함하는 LNA 안티센스 올리고머 (본원에서 영역 A 로서 언급할 수 있음) 를 제공한다.
본 발명은 (비-뉴클레오사이드) 탄수화물 모이어티, 예를 들면, 탄수화물 컨쥬게이트 모이어티에 공유 합류된 (예를 들면, 연결된) LNA 안티센스 올리고머를 제공한다. 일부 실시형태에서, 탄수화물 모이어티는 선형 탄수화물 폴리머가 아니다. 그러나, 탄수화물 모이어티는 다가, 예를 들면, 예를 들면, 2가, 3가, 4가일 수 있거나, 4가의 동일 또는 비동일한 탄수화물 모이어티는, 임의로 링커 또는 링커들을 통해, 올리고머에 공유적으로 합류될 수 있다.
본 발명은 안티센스 올리고머 및 탄수화물을 포함하는 컨쥬게이트 모이어티, 예를 들면, 탄수화물 컨쥬게이트 모이어티를 포함하는 LNA 안티센스 올리고머 (컨쥬게이트) 를 제공한다.
본 발명은 본 발명의 LNA 올리고머성 화합물 및 약학적으로 허용가능한 희석제, 담체, 염 또는 보조제를 포함하는 약제학적 조성물을 제공한다.
본 발명은 세포에서 핵산 표적의 억제에 사용하기 위한 본 발명에 따른 올리고머성 화합물을 제공한다. 일부 실시형태에서, 용도는 시험관내이다. 일부 실시형태에서, 용도는 생체내이다.
본 발명은 의약품에서 사용하기 위한, 예를 들면, 약제로서 사용하기 위한 본 발명의 올리고머성 화합물을 제공한다.
본 발명은 의학적 질환 또는 장애의 치료에 사용하기 위한 본 발명의 올리고머성 화합물을 제공한다.
본 발명은 질환 또는 장애, 예를 들면, 대사성 질환 또는 장애의 치료를 위한 약제를 제조하기 위한 본 발명의 올리고머성 화합물의 용도를 제공한다.
본 발명은 8-24 개의 포스포로티오에이트 연결된 뉴클레오사이드의 인접 영역을 포함하고 LNA 올리고머와 인접한 1 개와 6 개 사이의 DNA 뉴클레오사이드를 추가로 포함하는 LNA 올리고머를 또한 제공하는 것으로서, 여기서, DNA 사이 및/또는 DNA 뉴클레오사이드(들) 에 인접한 인터뉴클레오사이드 연결은 포스포디에스테르 결합이므로 생리학적으로 불안정하다. 이러한 LNA 올리고머는 본원에서 기재되는 컨쥬게이트의 형태일 수 있다. 컨쥬게이트되는 경우, 컨쥬게이트는, 예를 들면, 탄수화물, 예를 들면, GalNac 컨쥬게이트, 예를 들면, GalNac 클러스터, 예를 들면, 트리GalNac, 또는 본원에서 기재된 다른 컨쥬게이트일 수 있다.
도 1: LNA 올리고뉴클레오타이드 GalNAc 컨쥬게이션 단계
도 2: FVII 단백질 수준
도 3: FVII mRNA 수준
도 4a-4d: 실시예 3 - 혈청 중의 FVII 수준
도 5a-5d: 실시예 3 - 간 중의 FVII mRNA 수준
도 6: 실시예 3 - 간 및 신장에서의 올리고뉴클레오타이드 함량
도 7a 및 도 7b: 상이한 monoGalNAc 컨쥬게이트에 의한 IApoB mRNA 의 생체내 침묵화 (silencing). 생체-절단가능한 (bio-cleavable) 링커 없이, 디티오-링커 (SS) 또는 DNA/PO-링커 (PO) (A) 를 가지는 상이한 ApoB monoGalNAc 컨쥬게이트로 마우스를 처리하고, DNA/PO-링커를 가지는 MonoGalNAc 를 GalNAc 클러스터 (B) 와 비교하였다. RNA 를 간 샘플 (A) 및 신장 샘플 (B) 로부터 단리하고, ApoB mRNA 녹 다운에 대해 분석하였다. 데이터는 식염수 (=1) 와 비교하여 나타낸다.
도 8: 실시예 5 - ApoB mRNA 발현
도 9: 실시예 5 - 혈청 중의 총 콜레스테롤
도 10: 실시예 5 - 간 및 신장에서의 올리고뉴클레오타이드 함량
도 11: 실시예 6 - 혈청 중의 FVII 수준
도 12: 실시예 6 - 간 중의 FVII mRNA 수준
도 13: 실시예에서 사용된 화합물 및 컨쥬게이트 모이어티의 예
도 14: 사용될 수 있는 트리-GalNac 컨쥬게이트의 예. 컨쥬게이트 1-4 는 4 개의 적합한 GalNac 컨쥬게이트 모이어티를 도시한 것이고, 컨쥬게이트 1a-4a 는 컨쥬게이트를 올리고머 (영역 A 또는 생체-절단가능한 링커, 예를 들면, 영역 B) 에 연결시키는데 사용되는 추가의 링커 모이어티 (Y) 를 가지는 동일한 컨쥬게이트를 의미한다. 물결선은 올리고머에 대한 공유 연결을 나타낸다.
도 15: 래트 안정성 연구로부터의 Kim-1 발현 (실시예 10 참조).
도 16: 1 mg/kg 또는 2.5 mg/kg 의 서열 번호 32 또는 서열 번호 17 의 단일 투여량으로 처리된 마우스에서의 혈청 ApoB 및 LDL-C 수준.
도 17: 씨드 (seed) -표적화 타이니 (tiny) LNA 에 의한 마우스 간에서의 miR-122 의 침묵화. (a) 20 mg/kg 타이니 antimiR-122, 15-mer antimiR-122 또는 LNA 스크램블 (scramble) 대조군의 3 개의 정맥내 투여량으로 또는 식염수로 처리한 후. 마우스로부터의 간 RNA 의 RNA 블롯 분석
도 18: 투여 전, 4 일째 및 7 일째에서의 총 콜레스테롤 분석. 콜레스테롤은 감소된 miR122 로 인해 상향조절된다.
도 19: Aldo A 및 Bckdk 의 발현을 표준 TaqMan Q-PCR 분석법으로 측정하였다. 이들 유전자의 mRNA 수준은 감소된 miR122 로 인해 상향조절된다.
도 20: ALT 를 최종 혈청 (7 일째) 으로부터 측정하여, 화합물의 내약성 (tolerability) 을 평가한다.
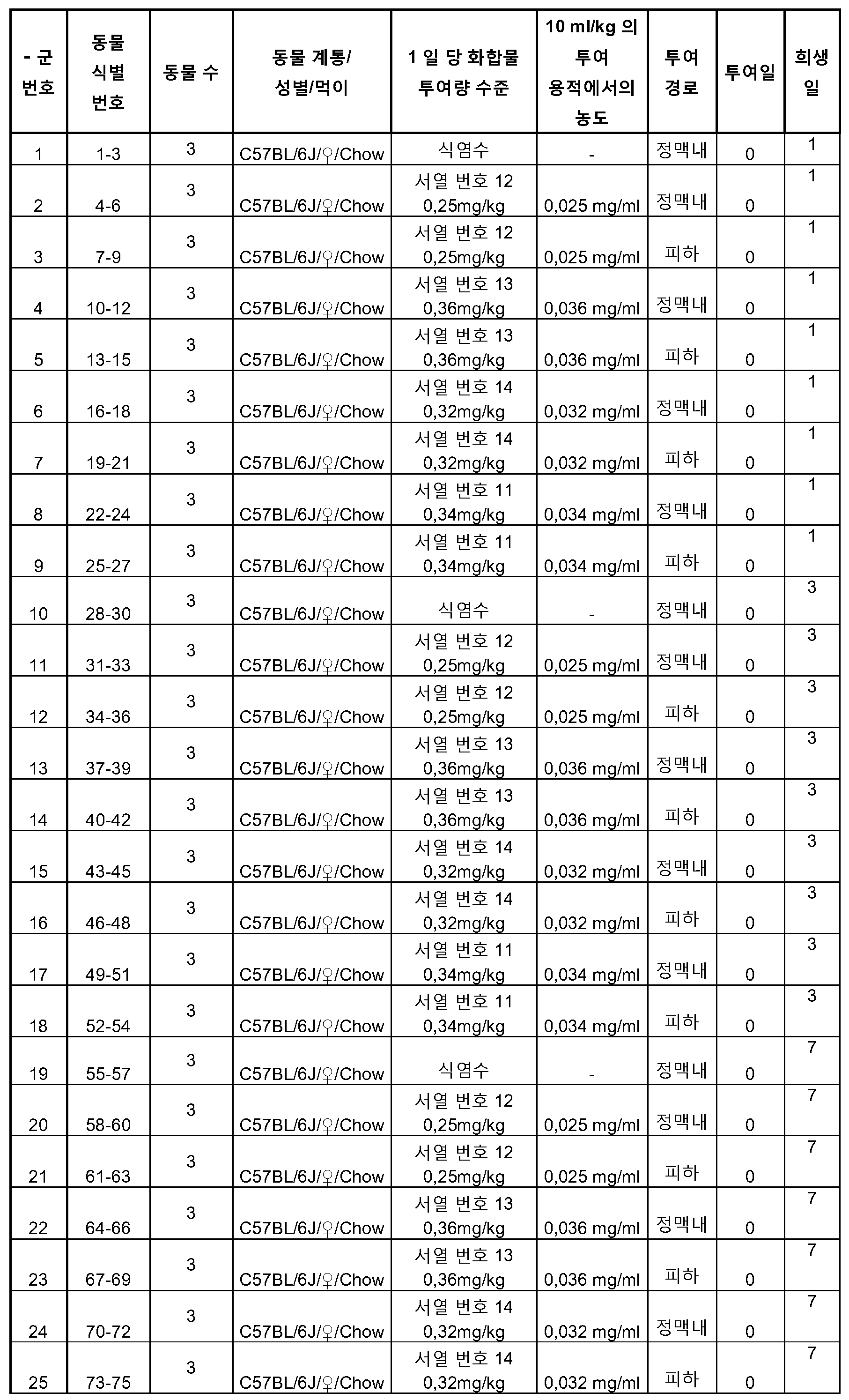
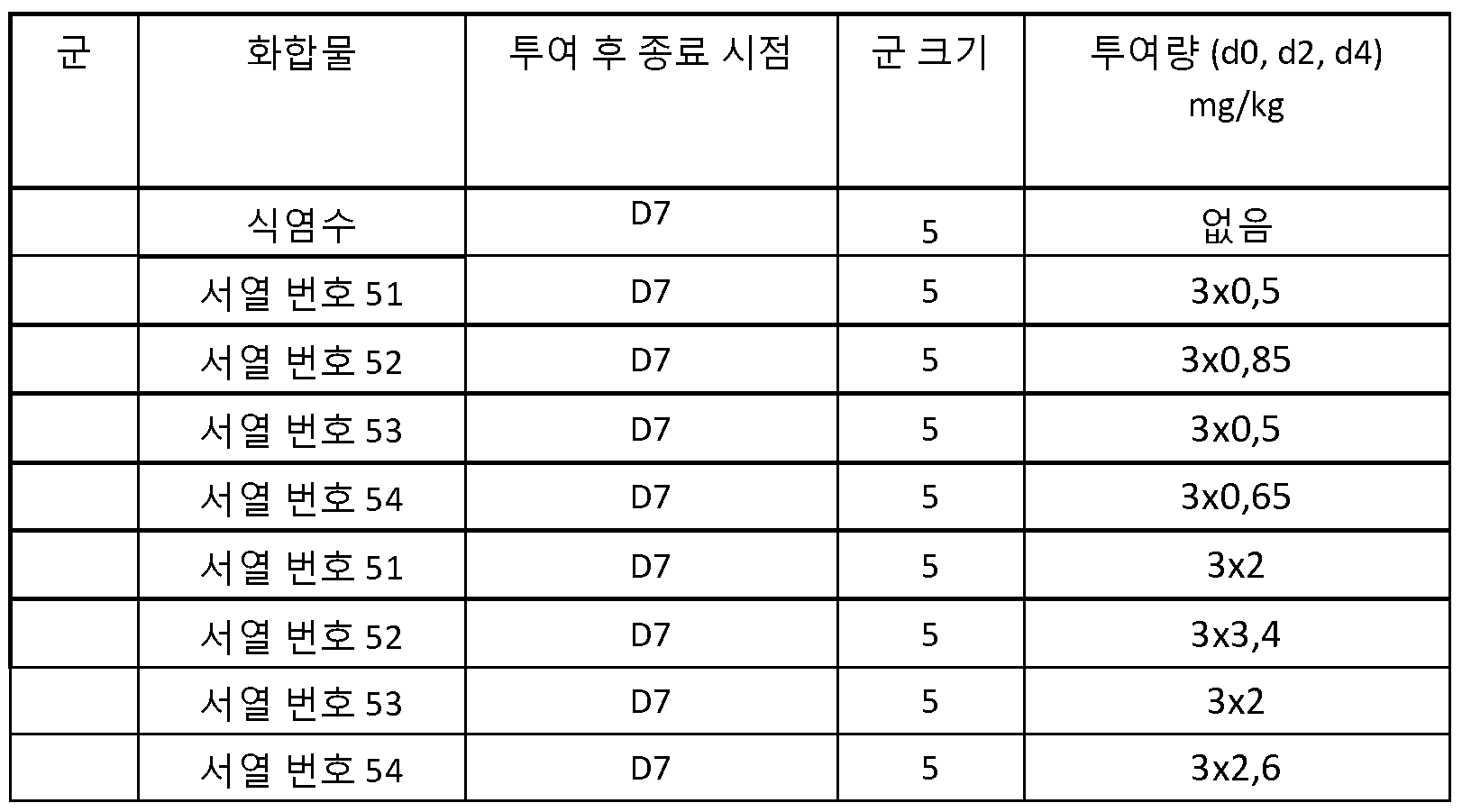
도 21: pAAV2/HBV 의 유체역학적 꼬리 정맥 주입 후 7 일째에 Balb/C 마우스의 간에서의 바이러스 복제를 측정하여, LNA 화합물 서열 번호 55 및 서열 번호 56 의 항바이러스 효과를 측정하였다. 유체역학적 주입 24 시간 전에 화합물을 표시된 투여량 수준의 단일 투여량으로 정맥내 제공하고, 유체역학적 주입 24 시간 후부터 매일 경구적으로 제공된 엔테카비르와 비교하였다. HBV DNA 를 qPCR 로 정량화하고, 100ng 간 DNA 당 게놈 당량 (genome equivalent) 으로 보고하였다.
도 2: FVII 단백질 수준
도 3: FVII mRNA 수준
도 4a-4d: 실시예 3 - 혈청 중의 FVII 수준
도 5a-5d: 실시예 3 - 간 중의 FVII mRNA 수준
도 6: 실시예 3 - 간 및 신장에서의 올리고뉴클레오타이드 함량
도 7a 및 도 7b: 상이한 monoGalNAc 컨쥬게이트에 의한 IApoB mRNA 의 생체내 침묵화 (silencing). 생체-절단가능한 (bio-cleavable) 링커 없이, 디티오-링커 (SS) 또는 DNA/PO-링커 (PO) (A) 를 가지는 상이한 ApoB monoGalNAc 컨쥬게이트로 마우스를 처리하고, DNA/PO-링커를 가지는 MonoGalNAc 를 GalNAc 클러스터 (B) 와 비교하였다. RNA 를 간 샘플 (A) 및 신장 샘플 (B) 로부터 단리하고, ApoB mRNA 녹 다운에 대해 분석하였다. 데이터는 식염수 (=1) 와 비교하여 나타낸다.
도 8: 실시예 5 - ApoB mRNA 발현
도 9: 실시예 5 - 혈청 중의 총 콜레스테롤
도 10: 실시예 5 - 간 및 신장에서의 올리고뉴클레오타이드 함량
도 11: 실시예 6 - 혈청 중의 FVII 수준
도 12: 실시예 6 - 간 중의 FVII mRNA 수준
도 13: 실시예에서 사용된 화합물 및 컨쥬게이트 모이어티의 예
도 14: 사용될 수 있는 트리-GalNac 컨쥬게이트의 예. 컨쥬게이트 1-4 는 4 개의 적합한 GalNac 컨쥬게이트 모이어티를 도시한 것이고, 컨쥬게이트 1a-4a 는 컨쥬게이트를 올리고머 (영역 A 또는 생체-절단가능한 링커, 예를 들면, 영역 B) 에 연결시키는데 사용되는 추가의 링커 모이어티 (Y) 를 가지는 동일한 컨쥬게이트를 의미한다. 물결선은 올리고머에 대한 공유 연결을 나타낸다.
도 15: 래트 안정성 연구로부터의 Kim-1 발현 (실시예 10 참조).
도 16: 1 mg/kg 또는 2.5 mg/kg 의 서열 번호 32 또는 서열 번호 17 의 단일 투여량으로 처리된 마우스에서의 혈청 ApoB 및 LDL-C 수준.
도 17: 씨드 (seed) -표적화 타이니 (tiny) LNA 에 의한 마우스 간에서의 miR-122 의 침묵화. (a) 20 mg/kg 타이니 antimiR-122, 15-mer antimiR-122 또는 LNA 스크램블 (scramble) 대조군의 3 개의 정맥내 투여량으로 또는 식염수로 처리한 후. 마우스로부터의 간 RNA 의 RNA 블롯 분석
도 18: 투여 전, 4 일째 및 7 일째에서의 총 콜레스테롤 분석. 콜레스테롤은 감소된 miR122 로 인해 상향조절된다.
도 19: Aldo A 및 Bckdk 의 발현을 표준 TaqMan Q-PCR 분석법으로 측정하였다. 이들 유전자의 mRNA 수준은 감소된 miR122 로 인해 상향조절된다.
도 20: ALT 를 최종 혈청 (7 일째) 으로부터 측정하여, 화합물의 내약성 (tolerability) 을 평가한다.
도 21: pAAV2/HBV 의 유체역학적 꼬리 정맥 주입 후 7 일째에 Balb/C 마우스의 간에서의 바이러스 복제를 측정하여, LNA 화합물 서열 번호 55 및 서열 번호 56 의 항바이러스 효과를 측정하였다. 유체역학적 주입 24 시간 전에 화합물을 표시된 투여량 수준의 단일 투여량으로 정맥내 제공하고, 유체역학적 주입 24 시간 후부터 매일 경구적으로 제공된 엔테카비르와 비교하였다. HBV DNA 를 qPCR 로 정량화하고, 100ng 간 DNA 당 게놈 당량 (genome equivalent) 으로 보고하였다.
본 발명은 비-뉴클레오타이드 탄수화물 컨쥬게이트 기에 공유 연결되어 있는 LNA 올리고머성 화합물, 예를 들면, LNA 안티센스 올리고뉴클레오타이드에 관한 것이다.
올리고머
본 발명은 LNA 안티센스 올리고머 및 상기 LNA 안티센스 올리고머에 공유 결합된 탄수화물을 포함하는 컨쥬게이트 모이어티, 예를 들면, 탄수화물 컨쥬게이트 모이어티를 포함하는 LNA 안티센스 올리고머 컨쥬게이트를 제공한다.
본 발명은 세포에서 표적 핵산을 조절하는데, 예를 들면, 억제하는데 사용하기 위한 LNA 올리고머성 화합물 (본원에서 LNA 올리고머 또는 LNA 올리고뉴클레오타이드로도 또한 언급함) 을 이용한다. LNA 올리고머는 하나 이상의 "잠금 핵산" (Locked Nucleic Acid: LNA) 뉴클레오사이드, 예를 들면, 2' 번 위치와 4' 번 위치 사이에서의 공유 브릿지 (라디칼로도 또한 언급함) (2'-4' 브릿지) 를 포함하는 뉴클레오사이드를 포함한다. LNA 뉴클레오사이드는 또한 "바이사이클릭 뉴클레오사이드" 로도 또한 언급된다. LNA 올리고머는 전형적으로 단일 가닥의 안티센스 올리고뉴클레오타이드이다.
일부 실시형태에서, LNA 올리고머는 갭머를 포함하거나 갭머이다. 일부 실시형태에서, LNA 올리고머는 믹스머를 포함하거나 믹스머이다. 일부 실시형태에서, LNA 올리고머는 토탈머를 포함하거나 토탈머이다.
일부 실시형태에서, 상기 올리고머에 존재하는 뉴클레오사이드 유사체는 모두 LNA 이고, 상기 올리고머는 RNA 또는 DNA, 예를 들면, DNA 뉴클레오사이드 (예를 들면. 갭머 또는 믹스머에서) 를 임의로 추가로 포함할 수 있다.
각종 실시형태에서, 본 발명의 화합물은 RNA (단위) 를 포함하지 않는다. 일부 실시형태에서, 상기 올리고머는 선형 분자이거나 선형 분자로서 합성되는 단일 인접 서열을 가진다. 따라서, 상기 올리고머는 단일 가닥의 분자일 수 있다. 일부 실시형태에서, 상기 올리고머는 동일한 올리고머 내의 동등한 영역 (즉, 이중체) 에 상보적인, 예를 들면, 적어도 3 개, 4 개 또는 5 개의 근접 뉴클레오타이드의 짧은 영역을 포함하지 않는다. 상기 올리고머는, 일부 실시형태에서, (본질적으로) 이중 가닥이 아닐 수 있다. 상기 올리고머는 본질적으로 이중 가닥이 아니고, 예를 들면, siRNA 가 아니다. 일부 실시형태에서, 상기 올리고머성 화합물은 (실질적으로) 상보적인 올리고뉴클레오타이드를 가지는 이중체의 형태가 아니다 - 예를 들면, siRNA 가 아니다.
길이
본 발명의 문맥에서의 용어 "올리고머" 란, 2 개 이상의 뉴클레오타이드 (즉, 올리고뉴클레오타이드) 의 공유 결합에 의해 형성된 분자를 의미한다. 본원에서, 단일 뉴클레오타이드 (단위) 는 모노머 또는 단위로도 또한 언급될 수 있다. 일부 실시형태에서, 용어 "뉴클레오사이드", "뉴클레오타이드", "단위" 및 "모노머" 는 상호교환적으로 사용된다. 뉴클레오타이드 또는 모노머의 서열을 언급할 때, 언급하는 것은 염기, 예를 들면, A, T, G, C 또는 U 의 서열인 것으로 인식될 것이다.
상기 올리고머는 7-30 개, 예를 들면, 7-26 개 또는 8-25 개, 예를 들면, 9 개, 10 개, 11 개, 12 개, 13 개, 14 개, 15 개, 16 개, 17 개, 18 개, 19 개, 20 개, 21 개, 22 개, 23 개, 24 개, 25 개 길이의 뉴클레오타이드, 예를 들면, 10-20 개 길이의 뉴클레오사이드의 인접 뉴클레오타이드 서열로 이루어지거나 구성될 수 있다. 일부 실시형태에서, LNA 올리고머의 길이는 10-16 개의 뉴클레오사이드, 예를 들면, 12 개, 13 개 또는 14 개의 뉴클레오사이드이다. 일부 실시형태에서, LNA 올리고머는 7 개, 8 개, 9 개 길이의 뉴클레오사이드, 예를 들면, "타이니" LNA 이다.
일부 실시형태에서, 상기 올리고머는 총 10-22 개, 예를 들면, 12-18 개, 예를 들면, 13-17 개 또는 12-16 개, 예를 들면, 13 개, 14 개, 15 개, 16 개 길이의 인접 뉴클레오사이드의 인접 뉴클레오타이드 서열로 이루어지거나 구성될 수 있다.
일부 실시형태에서, 상기 올리고머는 총 10 개, 11 개, 12 개, 13 개, 또는 14 개 길이의 인접 뉴클레오사이드의 인접 뉴클레오타이드 서열로 이루어지거나 구성될 수 있다.
일부 실시형태에서, 본 발명에 따른 올리고머는 22 개 이하의 뉴클레오사이드, 예를 들면, 20 개 이하의 뉴클레오사이드, 예를 들면, 18 개 이하의 뉴클레오사이드, 예를 들면, 15 개, 16 개 또는 17 개의 뉴클레오사이드로 이루어진다. 일부 실시형태에서, 본 발명의 올리고머는 20 개 미만의 뉴클레오사이드를 포함한다. 올리고머 또는 인접 뉴클레오타이드 서열 길이에 대한 범위가 제시될 때, 이것은 그 범위 내에 제공된 하한 및 상한 길이를 포함하고, 예를 들면, 10-30 (또는 사이) 은 10 과 30 둘 다를 포함하는 것으로 이해되어야 한다.
일부 실시형태에서, 본 발명에 따른 탄수화물 컨쥬게이트의 사용은 짧은 갭머, 믹스머 또는 토탈머 (타이니), 예를 들면, 20 개 미만, 예를 들면, 18 개 미만, 예를 들면, 16nts 이하 또는 15nts 이하 또는 14nts 이하의 LNA 올리고머를 비롯한 짧은 LNA 올리고머에 특히 적합한 것으로 밝혀졌다.
인터뉴클레오사이드
연결
일부 실시형태에서, LNA 올리고머의 인터뉴클레오사이드 연결은 포스포디에스테르 이외의 하나 이상의 인터뉴클레오사이드 연결을 포함하고, 예를 들면, 영역 A 중 인터뉴클레오사이드 연결의 하나 이상, 예를 들면, 50% 이상, 예를 들면, 75% 이상, 예를 들면, 90% 이상, 예를 들면, 100% 는 포스포디에스테르 이외이다. 일부 실시형태에서, 포스포디에스테르 이외의 인터뉴클레오사이드 연결은 인터뉴클레오사이드 연결을 함유하는 황, 예를 들면, 포스포로티오에이트, 포스포로디티오에이트, 예를 들면, 포스포로티오에이트이다.
LNA 올리고머는 하나 이상의 포스포로티오에이트 인터뉴클레오사이드 연결, 예를 들면, 적어도 2 개, 3 개 또는 4 개의 포스포로티오에이트 결합을 포함할 수 있고, 일부 실시형태에서, 인터뉴클레오사이드 연결의 50% 이상은 포스포로티오에이트일 수 있고, 예를 들면, (절단가능한 링커에 임의로 존재하는 것들 이외의) 인터뉴클레오사이드 연결의 75% 이상, 90% 이상 또는 모두는 포스포로티오에이트일 수 있다. 일부 실시형태에서, 5' 말단, 3' 말단, 또는 5' 말단과 3' 말단 둘 다에서의 2 개의 말단 뉴클레오사이드 사이의 (존재하는 경우, 영역 B 이외에서의) 인터뉴클레오사이드 연결은, 인터뉴클레오사이드 연결을 함유하는 황, 예를 들면, 포스포로티오에이트이다. 일부 실시형태에서, 상기 올리고머는 연속 DNA 뉴클레오사이드의 하나 이상의 영역, 예를 들면, 2 개, 3 개, 4 개, 5 개, 6 개, 7 개, 8 개, 9 개, 10 개, 11 개, 12 개의 연속 DNA 뉴클레오사이드의 영역을 포함하고, 여기서, DNA 뉴클레오사이드 사이의 인터뉴클레오사이드 연결은 인터뉴클레오사이드 연결을 함유하는 황, 예를 들면, 포스포로티오에이트이다. 일부 실시형태에서, 연속 DNA 뉴클레오사이드의 영역을 전형적으로 포함하는 갭머 (Y) 의 중심 영역은, 뉴클레오사이드 사이, 예를 들면, 연속 DNA 뉴클레오사이드 사이 및/또는 DNA 뉴클레오사이드와 핵산 유사체 뉴클레오사이드, 예를 들면, 본원에서, 예를 들면, LNA 로 언급되는 당 변형된 뉴클레오사이드 사이의 인터뉴클레오사이드 연결을 함유하는 황, 예를 들면, 포스포로티오에이트를 가진다.
상기 올리고머에 사용될 수 있는 인터뉴클레오사이드 연결의 다른 예는 메틸포스포네이트 (CH3P=O) 및 메틸티오노포스페이트 (CH3P=S) 및 보라노포스페이트를 포함한다.
잠금 핵산
뉴클레오사이드
(
LNA
)
바이사이클릭 뉴클레오사이드 유사체 (LNA 뉴클레오사이드) 는 리보오스 고리의 2 번 및 4 번 탄소를 연결하는 브릿지 (또는 바이라디칼) (C4*-C2* 브릿지 또는 바이라디칼) 를 전형적으로 포함하는 뉴클레오사이드 유사체를 포함한다. 2 번 및 4 번 탄소 사이의 바이라디칼의 존재는 리보오스를 3' 엔도-(북쪽) 확인 (confirmation) 내로 잠그고, C2*-C4* 바이라디칼을 가지는 이러한 바이사이클릭 뉴클레오사이드 유사체는 종종 잠금 핵산 (LNA) 또는 바이사이클릭 핵산 (bicyclic nucleic acid: BNA) 으로 언급된다. 용어 LNA 및 BNA 는 본원에서 상호교환적으로 사용된다.
일부 실시형태에서, LNA 올리고머의 뉴클레오사이드의 일부 또는 모두는 본원에서 뉴클레오사이드 유사체로도 또한 언급되는 변형된 뉴클레오사이드, 예를 들면, 당 변형된 뉴클레오사이드 유사체, 예를 들면, 바이사이클릭 뉴클레오사이드 유사체 (예를 들면, LNA) 및/또는 2' 치환된 뉴클레오사이드 유사체일 수 있다. 일부 실시형태에서, 상기 올리고머에 존재하는 뉴클레오사이드 유사체는 모두 동일한 당 변형을 포함하고, 예를 들면, 모든 바이사이클릭 뉴클레오사이드 유사체이고, 예를 들면, 이들은 베타-D-X-LNA 또는 알파-L-X-LNA (여기서, X 는 옥시, 아미노 또는 티오이다) 로 이루어진 군으로부터 (임의로 독립적으로) 선택될 수 있거나, (R/S) cET, cMOE 또는 5'-Me-LNA 를 포함하지만 이들에 한정되지 않는 본원에서 기재된 기타 LNA 이다.
일부 실시형태에서, 상기 올리고머는 하나 이상의 바이사이클릭 뉴클레오사이드 (LNA) 및 하나 이상의 추가의 뉴클레오사이드 유사체, 예를 들면, 하나 이상의 2' 치환된 뉴클레오사이드를 포함할 수 있다. 일부 실시형태에서, 상기 올리고머의 뉴클레오사이드의 일부 또는 모두는 본원에서 뉴클레오사이드 유사체로도 또한 언급되는 변형된 뉴클레오사이드일 수 있다.
일부 실시형태에서, 제 1 영역은 하나 이상, 예를 들면, 2 개 이상, 3 개 이상, 4 개 이상, 5 개 이상, 6 개 이상, 7 개 이상, 8 개 이상, 9 개 이상, 10 개 이상, 11 개 이상, 12 개 이상, 13 개 이상, 14 개 이상, 15 개 이상, 16 개 이상, 17 개 이상, 18 개 이상, 19 개 이상, 20 개 이상, 21 개 이상, 22 개 이상, 23 개 이상, 24 개 이상 또는 25 개의 뉴클레오사이드 유사체를 포함한다. 일부 실시형태에서, 뉴클레오사이드 유사체는 바이사이클릭 뉴클레오사이드 유사체 (예를 들면, LNA) 및/또는 2' 치환된 뉴클레오사이드 유사체로 이루어진 군으로부터 (임의로 독립적으로) 선택되고, 예를 들면, 2'-O-알킬-RNA 단위, 2'-OMe-RNA 단위, 2'-아미노-DNA 단위, 2'-AP, 2'-FANA, 2'-(3-하이드록시)프로필 및 2'-플루오로-DNA 단위, 및/또는 기타 (임의로) 당 변형된 뉴클레오사이드 유사체, 예를 들면, 모르폴리노, 펩타이드 핵산 (peptide nucleic acid: PNA), CeNA, 비연결된 핵산 (unlinked nucleic acid: UNA), 헥시톨 핵산 (hexitol nucleoic acid: HNA). 바이사이클로-HNA 로 이루어진 군으로부터 (임의로 독립적으로) 선택된다 (예를 들면, WO 2009/100320 참조). 일부 실시형태에서, 추가의 뉴클레오사이드 유사체는 이의 표적 핵산 (또는 상보적 DNA 또는 RNA 서열) 에 대한 제 1 영역의 친화성를 증가시킨다. 각종 뉴클레오사이드 유사체는 참조로서 도입되는 문헌 [Freier & Altmann; Nucl . Acid Res ., 1997, 25, 4429-4443; 및 Uhlmann; Curr . Opinion in Drug Development, 2000, 3(2), 293-213] 에 개시되어 있다.
일부 실시형태에서, LNA 올리고머는 2 개 이상, 3 개 이상, 4 개 이상, 5 개 이상, 6 개 이상, 7 개 이상, 8 개 이상, 9 개 이상, 10 개 이상, 11 개 이상, 12 개 이상, 13 개 이상, 14 개 이상, 15 개 이상, 16 개 이상의, 예를 들면, 모든 뉴클레오사이드 유사체 (또는 토탈머에서의 모든 뉴클레오사이드), 바이사이클릭 뉴클레오사이드 유사체, 예를 들면, LNA, 예를 들면, 베타-D-X-LNA 또는 알파-L-X-LNA (여기서, X 는 옥시, 아미노 또는 티오이다), 또는 (R/S) cET, cMOE 또는 5'-Me-LNA 를 포함하지만 이들에 한정되지 않는 본원에서 기재된 기타 LNA 를 포함한다. 일부 실시형태에서, LNA 올리고머는 DNA 및 당 변형된 뉴클레오사이드 유사체, 예를 들면, 바이사이클릭 뉴클레오사이드 유사체 및/또는 2' 치환된 뉴클레오사이드 유사체를 포함한다. 일부 실시형태에서, 상기 올리고머는 DNA 및 LNA 뉴클레오사이드 단위를 포함한다.
WO 05/013901, WO 07/027775, WO 07027894 는 완전히 2' 치환된 올리고머, 예를 들면, 완전히 2'-O-MOE 를 언급하고 있다. 일부 실시형태에서, 상기 올리고머의 제 1 영역은 2' 치환된 뉴클레오사이드로 구성될 수 있다. WO 07/027775 는 또한 microRNA 를 표적화하는데 사용하기 위한 MOE, LNA, DNA 믹스머를 언급하고 있다.
표적
본 발명의 LNA 올리고머 컨쥬게이트는 전형적으로 본원에서 표적으로 언급되는 핵산 표적을 표적화하는데 사용하기 위한 것이다. 일부 실시형태에서, 비제한적인 예의 경우, 본 발명의 올리고머는 mRNA, microRNA, lncRNA (long non-coding RNA: 긴 비암호화 RNA), snRNA, snoRNA, 및 바이러스 RNA 로 이루어진 군으로부터 선택된 핵산 (즉, 표적) 을 조절하는데 사용하기 위한 것이다.
일부 실시형태에서, 상기 올리고머는 간-발현 RNA, 예를 들면, 간-발현 mRNA 또는 microRNA 를 표적화한다. 일부 실시형태에서, LNA 안티센스 올리고머는 인자 VII, PCSK9, ApoB, GCGR, CRP, DGAT2, GCCR, PTEN, PTP1B, SGLT2 및 SOD1 로 이루어진 군으로부터 선택된 mRNA 를 표적화한다 (예를 들면, 참조로서 본원에 도입된 WO 2007/146511 참조). 본 발명자들은 구체적으로는 WO 2007/146511 의 42-43 페이지의 표 1 을 도입한다. 일부 실시형태에서, 표적은 다음으로 이루어진 군으로부터 선택될 수 있다: ApoB Human NM 000384.1, ApoB Mouse XM 137955.5, SGLT2 Human NM 003041.1 , PCSK9 Human NM 174936.2, SODI Human X02317, CRP Human NM 000567.1, GCCR Mouse BC031885.1, GCGR Human NM 000160.1, DGAT2 Human NM 032564.2, PTPIB Human NM 002827.2, PTEN Mouse U92437.1, PTEN Human NM 000314.4 (GENBANK 수탁 번호 참조), 보체 인자 VII, 보체 인자 C6, 및 TTR. 인자 VII 을 암호화하는 뉴클레오타이드 서열은 다음을 포함하지만, 이들에 한정되는 것은 아니다: GENBANK 수탁 번호 NM 000131.3, GENBANK 수탁 번호 NM 019616.2, GENBANK 수탁 번호 NT 027140.6 의 뉴클레오사이드 1255000 내지 5 1273000, GENBANK 수탁 번호 NM 010172.3, 및 GENBANK 수탁 번호 NT 039455.6 의 뉴클레오사이드 10024000 내지 10037000. 보체 인자 C6 뉴클레오타이드 서열은 BC035723.1, J05024.1 GI:187824, 및 J05064.1 GI:179703 을 포함한다. 보체 인자 C6 을 표적화하는 LNA 올리고를 언급하는 EP 2320925 A2 도 또한 참조한다. TTR (트랜스타이레틴) 뉴클레오타이드 서열은 BC020791.1 GI:18089144, 및 BC005310.1 GI:13529049 를 포함한다.
PCSK9 를 표적화하는 LNA 올리고머의 예는 WO 2008/043753 및 WO 2001/009697 에서 제공되며, 이들은 본원에 참조로 도입된다.
ApoB 를 표적화하는 LNA 올리고머의 예는 WO 2010014280 및 WO 2008/113830 에서 제공되며, 이들은 본원에 참조로 도입된다.
표적은, 일부 실시형태에서, Bcl2 mRNA 일 수 있다- Bcl2 를 표적화하는 LNA 올리고머 (예를 들면, M13994.1 GI:179366) 를 개시하는 WO 2005/061710 을 참조한다.
표적은 간에서 발현되는 RNA 일 수 있다. 표적은 의학적 장애 또는 질환 병태와 관련되는 간 표적일 수 있다. 수많은 대사성 질환은 간과 관련되어 있으며, 일부 실시형태에서는 본 발명의 화합물을 사용하여 치료될 수 있다. 간 관련 대사성 질환 또는 장애 표적은, 예를 들면, Apo-B (고 LDL 콜레스테롤, ACS), ApoCIII (고 혈청 트리글리세라이드), ApoA (심혈관 질환), FGFR4 (비만증), GCCR (T2 당뇨병), GCGR (T2 당뇨병), PTP1B (T2 당뇨병), DGAT2 (NASH), PCSK9 (고지혈증 및 관련 장애), MtGPAT, miR-122 (고 콜레스테롤) 및 miR-33 (대사성 증후군, 죽상동맥경화증) 을 포함한다.
표적은 바이러스 핵산, 예를 들면, 바이러스 RNA 일 수 있다. 그 예는 간염 바이러스, 예를 들면, B 형 간염 및 C 형 간염 (HCV) 을 포함한다. 바이러스 간염은 A 형 간염, B 형 간염, C 형 간염, D 형 간염 및 E 형 간염을 포함한다. HCV LNA 안티센스 올리고머는, 예를 들면, 문헌 [Laxton et al., Antimicrobial Agents and Chemotherapy 2011 Vol 55 3105-3114] 에 개시되어 있다.
따라서, 상기 올리고머는 간 관련 (또는 연관) 대사성 질환 - 일반적으로 대사성 간 질환으로 언급됨 - 의 치료에서 사용하기 위한 것일 수 있다. 간 관련 대사성 질환은, 예를 들면, 대사성 증후군, 비만증, 고지혈증 , 죽상동맥경화증, HDL/LDL 콜레스테롤 불균형, 이상지질혈증, 예를 들면, 가족성 결합 고지혈증 (familial combined hyperlipidaemia: FCHL), 후천성 고지혈증, 스타틴-내성 고콜레스테롤혈증, 심혈관 질환, 관상 동맥 질환 (coronary artery disease: CAD) 및 관상동맥 심장 질환 (coronary heart disease: CHD), 죽상동맥경화증, 심장 질환, 단뇨병 (I 및/또는 II), NASH, 급성 관상동맥 증후군 (acute coronary syndrome: ACS) 을 포함한다. 일부 실시형태에서, 간 관련 또는 연관 장애 또는 질환은 간 핵산 표적의 발현, 예를 들면, 과발현과 연관되어 있다.
일부 실시형태에서, 예를 들면, 표적이 microRNA-122 인 경우, 질환은 바이러스 질환, 예를 들면, B 형 간염 및 C 형 간염을 비롯한 간염, 또는 상승된 콜레스테롤과 관련된 대사성 질환, 예를 들면, 죽상동맥경화증 및 고지혈증 및 관련 질환일 수 있다. miR-122 를 암호화하는 올리고머는 또한 간 기능의 개선을 위해 (예를 들면, PCT/EP2012/071934 참조), 괴사염증의 치료를 위해, 간 기능의 혈청 바이오마커의 개선을 위해, HCV 로 감염될 수 있거나 될 수 없고 간 기능이 악화될 위험이 있는 인간 피험자에서 간 기능의 소실의 예방 (또는 소실 속도의 감소) 을 위해, HCV 로 감염되거나 되지 않고 간 기능이 개선될 필요가 있는 인간 피험자에서 간 기능의 개선을 위해 사용될 수 있다. 간 질환은 비알코올성 지방간 질환 및 비알코올성 지방간염으로 이루어진 군으로부터; 또는 사이토메갈로바이러스 감염, 주혈흡충증 감염 및 렙토스피라증 감염으로 이루어진 군으로부터 선택된 질환 또는 장애일 수 있다.
일부 실시형태에서, 본 발명의 올리고머는 간 발현 microRNA, 예를 들면, miR-122 를 표적화한다. miR-122 를 표적화하는 올리고머는 WO 2007/112754, WO 2007/112753, WO 2009/043353 에 개시되어 있으며, 믹스머, 예를 들면, 미라비르센 (miravirsen) 으로도 또한 언급되는 SPC3649 (이것은 서열 5'-CcAttGTcaCaCtCC-3' (서열 번호 57) 을 가지고, 여기서, 대문자는 베타-D-옥시 LNA 이고, 소분자는 DNA 이고, 완전 포스포로티오에이트 및 LNA C 는 5-메틸 시토신이다), 또는 타이니 LNA, 예를 들면, WO 2009/043353 에 개시된 것들 (예를 들면, 5'-ACACTCC-3', 5'-CACACTCC-3', 5'-TCACACTCC-3', 서열 번호 58, 59 및 33 으로서, 여기서, 대문자는 (임의로 베타-D-옥시) LNA 이고, 완전 포스포로티오에이트 및 LNA C 는 임의로 5-메틸 시토신이다) 일 수 있다. 일부 실시형태에서, miR-122 표적화 올리고머는 8 개, 9 개, 10 개, 11 개, 12 개, 13 개, 14 개, 15 개, 16 개, 17 개 또는 18 개 길이의 뉴클레오타이드를 가진다. 일부 실시형태에서, miR-122 표적화 올리고머는 올리고머의 길이에 걸쳐 측정시 miR-122 에 완전히 상보적인 서열, 바람직하게는 서열 5'-CACACTCC-3' 을 포함한다. miRBase 에 따르면, 성숙 microRNA-122 서열은 5' uggagugugacaaugguguuugu 3' (서열 번호 34) 이다. 일부 실시형태에서, microRNA, 예를 들면, miR-122 를 표적화하는 올리고머는 올리고머의 길이에 걸쳐 microRNA 의 상응하는 영역에 상보적이고, 일부 실시형태에서, 올리고머의 3' 뉴클레오사이드는 miR-122 와 같은 microRNA 의 첫번째, 두번째, 세번째 또는 네번째 5' 뉴클레오타이드, 예를 들면, miR-122 와 같은 microRNA 의 두번째 5' 뉴클레오타이드에 상보적이다 (즉, 정렬한다).
일부 실시형태에서, 본 발명의 올리고머는 대사성 장애, 예를 들면, 죽상동맥경화증을 치료하는데 사용될 수 있는 간 발현 microRNA, 예를 들면, miR-33 (miR-33a 및/또는 miR-33b) 를 표적화한다 (예를 들면, WO2010/120508 참조). miR-33a/b 를 표적화하는 올리고머는 5'-TACAATGCA-3', 5'-ACAATGCAC-3', 5'-ACAATGCA-3' 및 5'-CAATGCA-3' (서열 번호 35-38) 으로 이루어진 군으로부터 선택된 핵염기 서열을 포함할 수 있고, miR-33a/b 를 표적화하는 특정 올리고머는 5'-TACAATGCA-3', 5'-ACAATGCA-3' 및 5'-CAATGCA-3' 일 수 있으며, 여기서, 대문자는 (임의로 베타-D-옥시) LNA 이고, 완전 포스포로티오에이트 및 LNA C 는 임의로, 5-메틸 시토신이다. miRBase 에 따르면, 성숙 microRNA-33a 서열은 5'-GUGCAUUGUAGUUGCAUUGCA-3' (서열 번호 39) 이고, miR-33b 는 5'-GUGCAUUGCUGUUGCAUUGC-3' (서열 번호 40) 이다.
일부 실시형태에서, 본 발명의 올리고머는 간 섬유증 또는 간세포 암종과 같은 질환을 치료하는데 사용될 수 있는 간 발현 microRNA, 예를 들면, miR-21 을 표적화한다. miR-21 을 표적화하는 올리고머는 5'-TGATAAGCT-3', 5'-GATAAGCT-3', 5'-ATAAGCT-3' (서열 번호 41-43) 으로 이루어진 군으로부터 선택된 핵염기 서열을 포함할 수 있고, miR-21 을 표적화하는 특정 올리고머는 5'-TGATAAGCT-3', 5'-GATAAGCT-3', 5'-ATAAGCT-3' 또는 5'-TcAGtCTGaTaAgCT-3' (서열 번호 44) 일 수 있으며, 여기서, 대문자는 (임의로 베타-D-옥시) LNA 이고, 소문자는 DNA 이고, 완전 포스포로티오에이트 및 LNA C 는 임의로 5-메틸 시토신이다. 서열 5'-GATAAGCT-3' (LNA C 는 5-메틸 시토신이다) 을 가지는 완전 LNA 올리고머 포스포로티오에이트 (예를 들면, 베타-D-옥시-LNA) 는 miR-21 (서열 번호 51) 을 억제하기 위해 생체내에서 광범위하게 사용되었다. miRBase 에 따르면, 성숙 microRNA-21 서열은 5'-UAGCUUAUCAGACUGAUGUUGA -3' (서열 번호 45) 이다.
일부 실시형태에서, 본 발명의 올리고머는, 예를 들면, 간세포 암종을 치료하는데 사용될 수 있는 간 발현 microRNA, 예를 들면, miR-221 을 표적화한다. miR-221 을 표적화하는 올리고머는 5'-CAATGTAGC-3', 5'-AATGTAGC-3' 및 5'-ATGTAGC-3' (서열 번호 46-48) 으로 이루어진 군으로부터 선택된 핵염기 서열을 포함할 수 있고, miR-221 을 표적화하는 특정 올리고머는 5'-CAATGTAGC-3', 5'-AATGTAGC-3' 및 5'-ATGTAGC-3' 을 포함하며, 여기서, 대문자는 (임의로 베타-D-옥시) LNA 이고, 완전 포스포로티오에이트 및 LNA C 는 임의로 5-메틸 시토신이다. miRBase 에 따르면, 성숙 microRNA-221 서열은 5'-AGCUACAUUGUCUGCUGGGUUUC-3' (서열 번호 49) 이다.
본 발명의 올리고머 또는 이의 인접 뉴클레오타이드 서열 또는 이의 일부로서 사용될 수 있는 이들을 표적화하는 기타 microRNA 표적 및 화합물은 WO 2007/112754 에 개시되어 있고, 예를 들면, WO 2007/112754 의 표 2 및 실시예 29 에 개시된 것들이며, 이것은 구체적으로 본원에 참조로 도입된다. 본 발명의 올리고머 또는 이의 인접 뉴클레오타이드 서열 또는 이의 일부로서 사용될 수 있는 이들을 표적화하는 기타 microRNA 표적 및 화합물은 WO 2007/043353 에 개시되어 있고, 예를 들면, WO 2007/043353 의 표 1 에 개시된 화합물 및 표적이며, 이것은 구체적으로 본원에 참조로 도입된다.
일부 실시형태에서, 본 발명의 올리고머는 표적 (예를 들면, 표적 핵산) 의 발현을 하향 조절 (예를 들면, 감소 또는 제거) 할 수 있다. 이와 관련하여, 본 발명의 올리고머는 표적의 억제에 영향을 미칠 수 있다. 일부 실시형태에서, 본 발명의 올리고머는 표적 핵산에 결합하고, 정상 발현 수준과 비교하여 10% 이상 또는 20% 이상의 발현 억제, 보다 바람직하게는 정상 발현 수준 (예를 들면, 올리고머(들) 또는 컨쥬게이트(들) 의 부재 하의 발현 수준) 과 비교하여 30% 이상, 40% 이상, 50% 이상, 60% 이상, 70% 이상, 80% 이상, 90% 이상 또는 95% 이상의 발현 억제에 영향을 미친다. 일부 실시형태에서, 이러한 조절은 0.04 nM 내지 25 nM, 예를 들면, 0.8 nM 내지 20 nM 농도의 본 발명의 화합물을 사용할 때 관찰된다. 동일하거나 상이한 실시형태에서, 발현의 억제는 100% 미만, 예를 들면, 98% 억제 미만, 95% 억제 미만, 90% 억제 미만, 80% 억제 미만, 예를 들면, 70% 억제 미만이다. 발현 수준의 조절은 단백질 수준을 측정함으로써, 예를 들면, SDS-PAGE 와 같은 방법에 이은, 표적 단백질에 대하여 발생되는 적합한 항체를 사용하는 웨스턴 블롯팅에 의해 결정될 수 있다. 다르게는, 발현 수준의 조절은 mRNA 의 수준을 측정함으로써, 예를 들면, 노던 블롯팅 또는 정량적 RT-PCR 에 의해 결정될 수 있다. mRNA 수준을 통한 측정시, 적절한 투약량, 예를 들면, 0.04 nM 내지 25 nM, 예를 들면, 0.8 nM 내지 20 nM 농도를 사용할 때의 하향 조절의 수준은, 일부 실시형태에서, 전형적으로 본 발명의 화합물, 컨쥬게이트 또는 조성물의 부재 하의 정상 수준의 10-20% 수준이다.
그러므로, 본 발명은 표적을 발현하고 있는 세포에서 표적의 발현을 하향 조절 또는 억제하는 방법을 제공하는 것으로서, 상기 방법은 상기 세포에게 본 발명에 따른 올리고머 또는 컨쥬게이트를 투여하여 상기 세포에서 표적의 발현을 하향 조절 또는 억제하는 단계를 포함한다. 적합하게는, 세포는 포유동물 세포, 예를 들면, 인간 세포이다. 투여는, 일부 실시형태에서, 시험관 내에서 일어날 수 있다. 투여는, 일부 실시형태에서, 생체 내에서 일어날 수 있다.
본 발명의 화합물, 예를 들면, 이의 올리고머 및 컨쥬게이트는 간에서 발현되는 상이한 표적, 예를 들면, mRNA 또는 microRNA 또는 기타 핵산 표적에 표적화될 수 있다 (NCBI Genbank / Gene ID 에 대한 참조를 본 발명의 화합물에 의해 표적화될 수 있는 서열의 예로서 제시한다 - Genbank / NCBI 서열은 본원에 참조로 도입된다).
ApoB
일부 실시형태에서, 제 1 영역 (또는 제 1 및 제 2 영역) 은 ApoB mRNA 표적 (즉, 표적들) ApoB-100 (본원에 참조로 도입되는 NCBI Genbank ID NM_000384.2 GI:105990531) 의 상응하는 영역에 상보적인 단일 인접 핵염기 서열을 형성한다.
ApoB 를 표적화하는 본 발명의 화합물은 급성 관상동맥 증후군의 치료에 사용될 수 있다 (WO 20100076248 참조). 그러므로, 본 발명은 급성 관상동맥 증후군의 치료에 사용하기 위해 ApoB100 을 표적화하는 본 발명에 따른 올리고머를 제공한다. 그러므로, 본 발명은 급성 관상동맥 증후군의 치료 방법을 추가로 제공하는 것으로서, 상기 방법은 상기 치료를 필요로 하는 피험자에 대한 본 발명의 올리고머의 투여를 포함한다.
ApoB 를 표적화하는 본 발명의 화합물은 죽상동맥경화증의 치료에 사용될 수 있다. 그러므로, 본 발명은 죽상동맥경화증의 치료에 사용하기 위해 ApoB100 을 표적화하는 본 발명에 따른 올리고머를 제공한다. 본 발명은 죽상동맥경화증의 치료 방법을 추가로 제공하는 것으로서, 상기 방법은 상기 치료를 필요로 하는 피험자에 대한 본 발명의 올리고머의 투여를 포함한다.
ApoB 를 표적화하는 본 발명의 화합물은 고콜레스테롤혈증 또는 고지혈증의 치료에 사용될 수 있다. 그러므로, 본 발명은 고콜레스테롤혈증 또는 고지혈증의 치료에 사용하기 위해 ApoB100 을 표적화하는 본 발명에 따른 올리고머를 제공한다. 본 발명은 고콜레스테롤혈증 또는 고지혈증의 치료 방법을 추가로 제공하는 것으로서, 상기 방법은 상기 치료를 필요로 하는 피험자에 대한 본 발명의 올리고머의 투여를 포함한다.
본 발명은 ApoB 를 발현하고 있는 세포에서 ApoB 의 억제를 위한 생체내 또는 시험관내 방법을 제공하는 것으로서, 상기 방법은 본 발명에 따른 올리고머 또는 컨쥬게이트 또는 약제학적 조성물을 상기 세포에 투여하여 상기 세포에서 ApoB 를 억제하는 단계를 포함한다.
본 발명의 올리고머/컨쥬게이트에서 제 1 영역으로서 사용될 수 있는 LNA 올리고머의 예는, 예를 들면, 본원에 참조로 도입되는 WO 2007/031081, WO 2008/113830, WO 2007131238 및 WO2010142805 에 기재된 것들을 포함한다. 구체적인 바람직한 화합물은 하기를 포함한다:
5'-Gs mCsaststsgsgstsastsTs mCsA-3' (서열 번호 12)
5'-GsTstsgsascsascstsgsTs mC-3' (서열 번호 50)
여기서, 대문자는 베타-D-옥시 LNA 단위 (뉴클레오사이드) 이고, 소문자는 DNA 단위이고, 아래첨자 s 는 포스포로티오에이트 결합이고, 대문자 C 앞의 위첨자 m 은 모든 LNA 시토신이 5-메틸 시토신인 것을 나타낸다. ApoB 를 표적화하는 본 발명의 화합물은 본원에 개시된 바와 같이, 간에 대해 올리고머를 표적화하는 컨쥬게이트, 예를 들면, 탄수화물 또는 친유성 컨쥬게이트, 예를 들면, GalNac 컨쥬게이트 또는 스테롤 컨쥬게이트 (예를 들면, 콜레스테롤 또는 토코페롤) 에 컨쥬게이션될 수 있다. 컨쥬게이트는, 예를 들면, 올리고머 화합물의 5' 말단 또는 3' 말단 (일부 실시형태에서, 영역 B 를 통해) 에 존재할 수 있다.
ApoB 를 표적화하는 기타 올리고머는 WO 03/011887, WO 04/044181, WO 2006/020676, WO 2007/131238, WO 2007/031081 및 WO 2010142805 에 개시되어 있다.
PCSK9
일부 실시형태에서, 제 1 영역 (또는 제 1 및 제 2 영역) 은 PCSK9 mRNA 표적 (즉, 표적들), 예를 들면, 인간 PCSK9 mRNA: 본원에 참조로 도입되는 NCBI Genbank ID NM_174936.3 GI:299523249 의 상응하는 영역에 상보적인 단일 인접 핵염기 서열을 형성한다.
본 발명은, 예를 들면, 고콜레스테롤혈증 또는 관련 장애, 예를 들면, 죽상동맥경화증, 고지혈증, 고콜레스테롤혈증, 가족성 고콜레스테롤혈증, 예를 들면, PCSK9 에서의 기능 돌연변이의 획득, HDL/LDL 콜레스테롤 불균형, 이상지질혈증, 예를 들면, 가족성 고지혈증 (FCHL), 후천성 고지혈증, 스타틴 내성 고콜레스테롤혈증, 관상 동맥 질환 (CAD) 및 관상 심장 질환 (CHD) 으로 이루어진 군으로부터 선택된 장애의 치료를 위한 약제로서 사용하기 위한, PCSK9 를 표적화하는 본 발명에 따른 올리고머를 제공한다.
본 발명은 고콜레스테롤혈증 또는 관련 장애, 예를 들면, 죽상동맥경화증, 고지혈증, 고콜레스테롤혈증, 가족성 고콜레스테롤혈증, 예를 들면, PCSK9 에서의 기능 돌연변이의 획득, HDL/LDL 콜레스테롤 불균형, 이상지질혈증, 예를 들면, 가족성 고지혈증 (FCHL), 후천성 고지혈증, 스타틴 내성 고콜레스테롤혈증, 관상 동맥 질환 (CAD) 및 관상 심장 질환 (CHD) 으로 이루어진 군으로부터 선택된 장애의 치료를 위한 약제를 제조하기 위한, PCSK9 를 표적화하는 본 발명의 올리고머의 용도를 제공한다.
본 발명은 고콜레스테롤혈증 또는 관련 장애, 예를 들면, 죽상동맥경화증, 고지혈증, 고콜레스테롤혈증, 가족성 고콜레스테롤혈증, 예를 들면, PCSK9 에서의 기능 돌연변이의 획득, HDL/LDL 콜레스테롤 불균형, 이상지질혈증, 예를 들면, 가족성 고지혈증 (FCHL), 후천성 고지혈증, 스타틴 내성 고콜레스테롤혈증, 관상 동맥 질환 (CAD) 및 관상 심장 질환 (CHD) 으로 이루어진 군으로부터 선택된 장애를 치료하는 방법을 제공하는 것으로서, 상기 방법은 고콜레스테롤혈증 또는 관련 장애를 앓고 있거나 이를 앓기 쉬운 환자에게, PCSK9 를 표적화하는 본 발명에 따른 올리고머를 유효량으로 투여하는 단계를 포함한다
본 발명은 PCSK9 를 발현하고 있는 세포에서 PCSK9 의 억제를 위한 생체내 또는 시험관내 방법을 제공하는 것으로서, 상기 방법은 PCSK9 를 표적화하는 본 발명에 따른 올리고머를 상기 세포에 투여하여 상기 세포에서 PCSK9 를 억제하는 단계를 포함한다.
하기는 인간 PCSK9 mRNA 를 표적화하는 올리고머이며, 본 발명의 화합물에서 영역 A 로서 사용될 수 있다.
5'-T s G s m C s t s a s c s a s a s a s a s c s m C s m C s A-3' (서열 번호 22)
여기서, 대문자는 베타-D-옥시 LNA 단위 (뉴클레오사이드) 이고, 소문자는 DNA 단위이고, 아래첨자 s 는 포스포로티오에이트 결합이고, 대문자 C 앞의 위첨자 m 은 모든 LNA 시토신이 5-메틸 시토신인 것을 나타낸다. PCSK9 를 표적화하는 본 발명의 화합물은 본원에 개시된 바와 같이, 간에 대해 올리고머를 표적화하는 컨쥬게이트, 예를 들면, 탄수화물 또는 친유성 컨쥬게이트, 예를 들면, GalNac 컨쥬게이트 또는 스테롤 컨쥬게이트 (예를 들면, 콜레스테롤 또는 토코페롤) 에 컨쥬게이션될 수 있다. 컨쥬게이트는, 예를 들면, 올리고머 화합물의 5' 말단 또는 3' 말단 (일부 실시형태에서, 영역 B 를 통해) 에 존재할 수 있다.
PCSK9 를 표적화하는 기타 올리고머는 실시예 뿐만 아니라, 본원에 참조로 도입되는 WO2008/043753, WO2011/009697, WO08/066776, WO07/090071, WO07/146511, WO07/143315, WO09/148605, WO11/123621 및 WO11133871 에 개시되어 있다. 본 발명의 화합물에 사용될 수 있는, PCSK9 를 표적화하는 기타 화합물은 실시예에 나타낸다.
miR
-122
일부 실시형태에서, 제 1 영역 (또는 제 1 및 제 2 영역) 은 microRNA-122, 예를 들면, miR-122a (즉, 표적들), 예를 들면, 하기와 같은 has-miR-122 서열 (miRBase release 20: MI0000442) 의 상응하는 영역에 상보적인 단일 인접 핵염기 서열을 형성한다:
>hsa-mir-122 MI0000442
CCUUAGCAGAGCUGUGGAGUGUGACAAUGGUGUUUGUGUCUAAACUAUCAAACGCCAUUAUCACACUAAAUAGCUACUGCUAGGC
>hsa-miR-122-5p MIMAT0000421
UGGAGUGUGACAAUGGUGUUUG
miR-122 는 HCV 감염에서 나타나며, 여기서, 이것은 감염의 유지에 필요한 필수 숙주 인자이다. 그러므로, miR-122 의 억제제는 C 형 간염 감염의 치료에 사용될 수 있다.
miR-122 를 표적화하는 본 발명의 화합물은 HCV 감염의 치료에 사용될 수 있다. 그러므로, 본 발명은 HCV 감염의 치료에 사용하기 위해 miR-122 를 표적화하는 본 발명에 따른 올리고머를 제공한다. 본 발명은 HCV 감염의 치료 방법을 추가로 제공하는 것으로서, 상기 방법은 상기 치료를 필요로 하는 피험자에 대한 본 발명의 올리고머의 투여를 포함한다.
본 발명은 HCV 감염의 치료를 위한 약제를 제조하기 위한, miR-122 를 표적화하는 본 발명의 올리고머의 용도를 제공한다.
본 발명은 HCV 감염의 치료 방법을 제공하는 것으로서, 상기 방법은 HCV 감염을 앓고 있는 환자에게, miR-122 를 표적화하는 본 발명에 따른 올리고머를 유효량으로 투여하는 단계를 포함한다.
본 발명은 miR-122 를 발현하고 있는 세포, 예를 들면, HCV 감염 세포 또는 HCV 복제단위 발현 세포에서 miR-122 의 억제를 위한 생체내 또는 시험관내 방법을 제공하는 것으로서, 상기 방법은 본 발명에 따른 올리고머 또는 컨쥬게이트 또는 약제학적 조성물을 상기 세포에 투여하여 상기 세포에서 miR-122 를 억제하는 단계를 포함한다.
miR-122 는 또한 콜레스테롤 대사에서 나타나고, 이것은 miR-122 의 억제가 혈장 콜레스테롤 수준을 감소시키기 위한 치료에 사용될 수 있는 것으로 제시되었다 [Esau, Cell Metab. 2006 Feb;3(2):87-98].
그러므로, miR-122 의 억제제는 혈장 콜레스테롤 수준을 감소시키기 위한 치료에, 또는 증가된 수준의 콜레스테롤과 연관된 대사성 질환 (관련 장애), 예를 들면, 간 지방증, 죽상동맥경화증, 고지혈증, 고콜레스테롤혈증, 가족성 고콜레스테롤혈증, 이상지질혈증, 관상 동맥 질환 (CAD) 및 관상 심장 질환 (CHD) 으로 이루어진 군으로부터 선택된 징후의 치료에 사용될 수 있다.
miR-122 를 표적화하는 본 발명의 화합물은 상승된 콜레스테롤 수준 또는 관련 장애의 치료에 사용될 수 있다. 그러므로, 본 발명은 상승된 콜레스테롤 수준 또는 관련 장애의 치료에 사용하기 위해 miR-122 를 표적화하는 본 발명에 따른 올리고머를 제공한다. 본 발명은 상승된 콜레스테롤 수준 또는 관련 장애의 치료 방법을 추가로 제공하는 것으로서, 상기 방법은 상기 치료를 필요로 하는 피험자에 대한 본 발명의 올리고머의 투여를 포함한다.
본 발명은 상승된 콜레스테롤 수준 또는 관련 장애의 치료를 위한 약제를 제조하기 위한, miR-122 를 표적화하는 본 발명의 올리고머의 용도를 제공한다.
본 발명은 상승된 콜레스테롤 수준 또는 관련 장애의 치료 방법을 제공하는 것으로서, 상기 방법은 상기 장애를 앓고 있는 환자에게, miR-122 를 표적화하는 본 발명에 따른 올리고머를 유효량으로 투여하는 단계를 포함한다.
본 발명은 miR-122 를 발현하고 있는 세포, 예를 들면, HCV 감염 세포 또는 HCV 복제단위 발현 세포에서 miR-122 의 억제를 위한 생체내 또는 시험관내 방법을 제공하는 것으로서, 상기 방법은 본 발명에 따른 올리고머 또는 컨쥬게이트 또는 약제학적 조성물을 상기 세포에 투여하여 상기 세포에서 miR-122 를 억제하는 단계를 포함한다.
miR-122 를 표적화하는 올리고머는 WO 2007/112754, WO 2007/112753, WO 2009/043353 에 개시되어 있으며, 믹스머, 예를 들면, 미라비르센으로도 또한 언급되는 SPC3649, 또는 타이니 LNA, 예를 들면, WO 2009/043353 에 개시된 것들 (예를 들면, 5'-ACACTCC-3', 5'-CACACTCC-3', 5'-TCACACTCC-3' (서열 번호 58, 서열 번호 64 및 서열 번호 33) 으로서, 여기서, 대문자는 베타-D-옥시 LNA 이고, 완전 포스포로티오에이트 및 LNA C 는 5-메틸 시토신이다) 일 수 있다. 일부 실시형태에서, miR-122 표적화 올리고머는 8 개, 9 개, 10 개, 11 개, 12 개, 13 개, 14 개, 15 개, 16 개, 17 개 또는 18 개 (또는 19 개, 20 개, 21 개, 22 개 또는 23 개) 길이의 뉴클레오타이드를 가진다. 일부 실시형태에서, miR-122 표적화 올리고머는 올리고머의 길이에 걸쳐 측정시 miR-122 에 완전히 상보적인 서열, 바람직하게는 서열 5'-CACACTCC-3' 을 포함한다. 일부 실시형태에서, microRNA, 예를 들면, miR-122 를 표적화하는 올리고머는 올리고머의 길이에 걸쳐 microRNA 의 상응하는 영역에 상보적이고, 일부 실시형태에서, 올리고머의 3' 뉴클레오사이드는 miR-122 와 같은 microRNA 의 첫번째, 두번째, 세번째 또는 네번째 5' 뉴클레오타이드, 예를 들면, miR-122 와 같은 microRNA 의 두번째 5' 뉴클레오타이드에 상보적이다 (즉, 정렬한다).
하기는 has-miR-122 (인간 miR-122) 를 표적화하는 올리고머이며, 본 발명의 화합물에서 영역 A 로서 사용될 수 있다.
미라비르센 (Miravirsen): 5'- m C s c s A s t s t s G s T s c s a s m C s a s m C s t s m C s m C-3' (서열 번호 57)
본 발명의 문맥에서 사용될 수 있는 기타 miR-122 표적화 화합물 (영역 A) 은 WO 2007/027894, WO 2007/027775 에 개시되어 있다.
MtGPAT : (NCBI 유전자 ID 57678 - 염색체: 10; NC_000010.10 (113907971..113975153, 보체) 미토콘드리아 글리세롤-3-포스페이트 아실트랜스페라아제 1 (EC 2.3.1.15, 또한 GPAT1, mtGPAT1, GPAM, mtGPAM 으로도 공지됨) 은 간 트리글리세라이드 형성에 중요한 역할을 하고, 여기서, 고수준의 mtGPAT1 활성은 지방간 (간지방증) 을 야기하는 반면, mtGPAT1 의 부재는 낮은 수준의 간 트리글리세라이드 및 자극된 지방산 산화 (mtGPAT 를 표적화하는 올리고머를 개시하고 있는 WO 2010/000656 참조) 를 야기한다. MtGPAT 를 표적화하는 본 발명의 화합물은 과체중, 비만증, 지방간, 간지방증, 비알코올성 지방간 질환 (non alcoholic fatty liver disease: NAFLD), 비알코올성 지방간염 (non alcoholic steatohepatitis: NASH), 인슐린 저항성, 당뇨병, 예를 들면, 비인슐린 의존성 진성 당뇨병 (non insulin dependent diabetes mellitus: NIDDM) 과 같은 병태를 치료하기 위해 사용될 수 있다.
하기 올리고머 (서열 번호 60) 은 인간 mTGPAt 를 표적화하고, 본 발명의 화합물에서 올리고머 영역 (제 1 영역) 으로서 사용될 수 있으며, 대문자는 LNA, 예를 들면, 베타-D-옥시-LNA 이고, 소문자는 DNA 이고, 아래첨자 s 는 포스포로티오에이트 결합이다. LNA 시토신은 5-메틸 시토신일 수 있다.
AsTsTscscscstsgscscstsGsTsG-3'
인자 VII (NCBI Gene ID 2155, NCBI J02933.1 GI:180333, 또는 EU557239.1 GI:182257998). 본 발명의 올리고머 또는 컨쥬게이트는 인자 VII 을 표적화할 수 있어, 조직 인자 응고 경로의 핵심 성분인 인자 VII 의 생성을 억제한다. 인자 VII 을 표적화하는 본 발명의 화합물은 혈전증 질환 (전형적으로 출혈을 야기하지 않음) 및 심장 마비, 뇌졸중 및 혈액 응고 또는 염증성 병태의 치료 또는 예방에 사용될 수 있다. 본원에 참조로 도입되는 WO 2013/119979 및 WO 2012/174154 는 본 발명의 컨쥬게이트 내에 도입될 수 있는 FVII 을 표적화하는 올리고뉴클레오타이드 화합물을 개시하고 있다.
인자 XI (NCBI Genbank BC122863.1 GI:114108211) - 인자 XI, 간에서 생성되는 응고 인자. 높은 수준의 인자 XI 은 심장 마비, 뇌졸중 및 혈액 응고와 연관되어 있다. 본원에 참조로 도입되는 WO 2013/070771 은 본 발명의 컨쥬게이트 내에 도입될 수 있는 XI 을 표적화하는 올리고뉴클레오타이드 화합물을 개시하고 있다. 인자 XI 을 표적화하는 본 발명의 화합물은 혈전증 질환 및 심장 마비, 뇌졸중 및 혈액 응고 또는 염증성 병태, 예를 들면, 관절염 및 대장염의 치료 또는 예방에 사용될 수 있다.
ApoCIII (NCBI Genbank BC027977.1 GI:20379764) 혈액에서 트리글리세라이드 대사를 조절하는 단백질. 고수준의 apoC-III 은 염증, 고 트리글리세라이드, 죽상동맥경화증 및 대사성 증후군과 연관되어 있다. ApoCIII 을 표적화하는 본 발명의 화합물은 단일 제제로서 또는 기타 트리글리세라이드 저하제와의 조합으로, 혈청 트리글리세라이드 수준을 감소시키기 위해 사용되거나, 예를 들면, 가족성 킬로미크론혈증 증후군 및 중증 고 트리글리세라이드의 치료에 사용될 수 있다. 본원에 참조로 도입되는 WO 11085271 은 본 발명의 컨쥬게이트 내에 도입될 수 있는 ApoCIII 을 표적화하는 올리고뉴클레오타이드 화합물을 개시하고 있다.
Apo (a) (NCBI Genbank NM_005577.2 GI:116292749) 는 간에서 apo(a) 의 생성을 억제하고, 심혈관 질환에 대한 독립적인 위험 인자인 Lp(a) 의 감소에 대한 직접적인 접근법을 제공하도록 디자인된다. 고수준의 Lp(a) 는 죽상동맥경화증, 관상 심장 질환, 심장 마비 및 뇌졸중의 위험 증가와 연관되어 있다. Lp(a) 는 동맥에서 조기 플라크 축적 또는 죽상동맥경화증을 촉진한다. Apo(a) 를 표적화하는 본 발명의 화합물은, 예를 들면, 죽상동맥경화증 또는 관상 심장 질환의 치료에 사용될 수 있다. 본원에 참조로 도입되는 WO 05000201 및 WO 03014307 은 본 발명의 컨쥬게이트 내에 도입될 수 있는 아포지질단백질 (a) 을 표적화하는 올리고뉴클레오타이드 화합물을 개시하고 있다.
B 형 간염 ( HBV ) (예를 들면, NCBID23683.1 D23684.1 GI:560092; D23683.1 GI: 560087; D23682.1 GI: 560082; D23681.1 GI: 560077; D23680.1 GI: 560072; D23679.1 GI: 560067; D23678.1 GI: 560062; D23677.1 GI: 560057 참조; 이들 모두는 본원에 참조로 도입된다).
HBV 를 표적화하는 올리고머는 당업계에 잘 공지되어 있으며, 예를 들면, WO 96/03152, WO 97/03211, WO 2011/052911, WO 2012/145674, WO 2012/145697, WO 2013/003520 및 WO 2013/159109 를 참조한다.
HBV 를 표적화하는 본 발명의 화합물은 HBV 감염의 치료에 사용될 수 있다. 그러므로, 본 발명은 HBV 의 치료에 사용하기 위해 HBV 를 표적화하는 본 발명에 따른 올리고머를 제공한다. 본 발명은 HBV 감염의 치료 방법을 추가로 제공하는 것으로서, 상기 방법은 상기 치료를 필요로 하는 피험자에 대한 본 발명의 올리고머의 투여를 포함한다.
본 발명은, 예를 들면, B 형 간염 감염 또는 관련 장애의 치료를 위한, 약제로서 사용하기 위한, B 형 간염 (HBV) 를 표적화하는 본 발명의 올리고머 또는 컨쥬게이트를 제공한다.
본 발명은 B 형 간염 감염 또는 관련 장애의 치료를 위한 약제를 제조하기 위한, B 형 간염 (HBV) 를 표적화하는 본 발명의 올리고머 또는 컨쥬게이트 또는 약제학적 조성물의 용도를 제공한다.
본 발명은 B 형 간염 감염 또는 관련 장애의 치료 방법을 제공하는 것으로서, 상기 방법은 B 형 간염 바이러스로 감염된 환자에게, HBV 를 표적화하는 본 발명에 따른 올리고머 또는 컨쥬게이트를 유효량으로 투여하는 단계를 포함한다.
본 발명은 HBV 로 감염된 세포에서 HBV 복제의 억제를 위한 생체내 또는 시험관내 방법을 제공하는 것으로서, 상기 방법은 HBV 를 표적화하는 본 발명의 올리고머 또는 컨쥬게이트를 상기 세포에 투여하여 상기 세포에서 HBV 복제를 억제하는 단계를 포함한다. HBV 를 표적화하는 LNA 올리고머의 예는 (WO 2011/47312 에 개시된 바와 같이) 본 발명의 올리고머 (영역 A) 로서 사용될 수 있는 5'-G s A s G s G s c s a s t s a s g s c s a s g s m C s A s G s G-3' 이다. 추가의 화합물은 본원에 참조로 도입되는 WO 2011/47312 의 표 1, 및 WO 2011/052911, WO 2012/145674, WO 2012/145697, WO 2013/003520 및 WO 2013/159109 에 개시되어 있다.
RG-101 은 miR-122 를 표적화하고 Galnac 컨쥬게이트를 포함하는 화합물이며, Regulus Therapeutics 사에 의해 HCV 의 치료를 위해 개발되고 있다.
ANGPTL3, (예를 들면, NCBI BC007059.1 GI: 14712025 또는 BC058287.1 GI: 34849466) ANGIOPOIETIN-LIKE 3 - 지질, 글루코오스 및 에너지 대사를 조절하는 단백질. 상승된 수준의 ANGPTL3 을 가진 인간은 조기 심장 마비의 위험 증가, 동맥 벽 두께 증가 뿐 아니라 다중성 대사 이상, 예를 들면, 인슐린 저항성과 연관된 고지혈증을 가진다. 이와 대조적으로, 낮은 수준의 ANGPTL3 을 가진 인간은 LDL-C 및 트리글리세라이드 수준의 저하 및 심혈관 질환의 위험 저하를 가진다. ANGPTL3 을 표적화하는 본 발명의 화합물은, 예를 들면, 고지혈증 및 관련 장애, 대사성 장애, 죽상동맥경화증, 관상 심장 질환 또는 인슐린 저항의 치료에 사용될 수 있다. 본원에 참조로 도입되는 WO 11085271 은 본 발명의 컨쥬게이트 내에 도입될 수 있는 ANGPTL3 을 표적화하는 올리고뉴클레오타이드 화합물을 개시하고 있다.
글루카곤 수용체 또는 GCGR (BC112041.1 GI: 85567507; L20316.1 GI: 405189): 글루카곤은 인슐린의 작용과 반대되고 특히 제 2 형 당뇨병에서, 글루코오스를 생성하도록 간을 자극하는 호르몬이다. 진행 당뇨병 환자에서, 비조절된 글루카곤 작용은 혈당 수준의 현저한 증가를 야기한다. 그러므로, 글루카곤 작용의 약화는 중증 당뇨병 환자에서 현저한 글루코오스 저하 효과를 가질 수 있다. 추가로, GCGR 의 감소는 보다 활성의 글루카곤-유사 펩타이드, 또는 췌장 기능을 보존하고 인슐린 분비를 향상시키는 호르몬인 GLP-1 을 생성한다. GCGR 를 표적화하는 본 발명의 화합물은, 예를 들면, 인슐린 저항성, 고혈당증, 당뇨병, 예를 들면, 제 1 형 당뇨병 또는 제 2 형 당뇨병의 치료, 췌장 기능의 보존 및 혈당 수준의 조절에 사용될 수 있다. WO 2007/134014 는 본 발명의 컨쥬게이트 내에 도입될 수 있는 GCGR 을 표적화하는 올리고뉴클레오타이드 화합물을 개시하고 있다.
섬유아세포 성장 인자 수용체 4 또는 FGFR4 (NCBI Gene 2264 - NC_000005.9 (176513906..176525143). FGFR4 는 간 및 지방 조직에서 발현되고, 신체의 지방 축적 능력을 감소시키면서 지방 연소 및 에너지 소비를 증가시키는 것으로 나타난다. 많은 항-비만증 약물은 뇌에 작용하여 식욕을 억제하고, 통상적으로 CNS 부작용을 야기한다. FGFR4 를 표적화하는 본 발명의 화합물은, 예를 들면, 인슐린 저항성, 고혈당증, 당뇨병, 예를 들면, 제 1 형 당뇨병 또는 제 2 형 당뇨병의 치료, 비만증의 보존 (예를 들면, 식욕 억제 약물과 병용하여 사용될 때), 체중의 감소, 및 인슐린 감수성, 당뇨병, 예를 들면, 제 1 형 또는 제 2 형 당뇨병의 개선 및 혈당 수준의 조절에 사용될 수 있다. 본원에 참조로 도입되는 WO 09046141 및 WO 12174476 은 본 발명의 컨쥬게이트 내에 도입될 수 있는 FGFR4 를 표적화하는 올리고뉴클레오타이드 화합물을 개시하고 있다.
디아실글리세롤 아실트랜스페라아제 -2 또는 DGAT -2 (NCBI GENE ID 84649): 트리글리세라이드의 합성에서의 핵심 성분. DGAT 의 억제는 비알코올성 지방간염 (NASH) 환자에서 간 지방을 감소시킬 수 있고, 또한 제 2 형 당뇨병 및 인슐린 저항상을 치료하기 위해 사용될 수 있다. DGAT-2 를 표적화하는 본 발명의 화합물은 NASH 의 치료, 간 지방의 감소, 당뇨병, 예를 들면, 제 2 형 당뇨병의 치료, 및 인슐린 저항성의 치료에 사용될 수 있다. 본원에 참조로 도입되는 WO 05019418 및 WO 2007136989 는 본 발명의 컨쥬게이트 내에 도입될 수 있는 DGAT-2 를 표적화하는 올리고뉴클레오타이드 화합물을 개시하고 있다.
글루코코르티코이드 수용체 또는 GCC (BC150257.1 GI: 152013043): 글루코코르티코이드 호르몬은 신체 전반에 걸쳐 다양한 과정에 영향을 미치며, 과도한 수준의 글루코코르티코이드 호르몬은 체내에서 다수의 조직 및 기관에 악영향을 미칠 수 있다. 쿠싱 증후군은 고수준의 글루코코르티코이드에 장기간 노출되어 야기된 고아 질환 (orphan disease) 이다. 치료하지 않으면, 쿠싱 증후군 환자는 고혈압, 당뇨병 및 면역 기능 손상을 발달시킬 수 있고, 조기 사망의 위험이 증가한다. 쿠싱 증후군에 대한 승인된 치료제가 있지만, 현행 의약품은 상당한 부작용, 예를 들면, 고혈압 및 당뇨병과 연관되어 있고, 이들 환자에 대한 신규한 치료에 대한 높은 충족되지 않은 의학적 필요성이 여전히 존재한다. GCCR-2 를 표적화하는 본 발명의 화합물은 쿠싱 증후군 및 연관 증상 (예를 들면, 상기에서 열거된 것들) 을 치료하는데 사용될 수 있다. 본원에 참조로 도입되는 WO 07035759 및 WO 2007136988 은 본 발명의 컨쥬게이트 내에 도입될 수 있는GCCR 을 표적화하는 올리고뉴클레오타이드 화합물을 개시하고 있다.
보체 성분 C5 (M57729.1 GI: 179982): 보체계는 숙주 방어를 위한 보호 메커니즘으로서 면역에서 중추적인 역할을 하지만, 이의 조절이상은 그 중에서도 발작성 야간 헤모글로빈뇨증 (paroxysmal nocturnal hemoglobinuria: PNH), 이례적인 용혈성 요독 증후군 (atypical hemolytic-uremic syndrome: aHUS), 중증 근무력증, 시각신경척수염을 비롯한 광범위한 인간 질환에서 심각한 생명-위협 합병증을 야기한다. 보체 성분 C5 를 표적화하는 본 발명의 화합물은 이들 질환 중 하나 이상을 치료하는데 사용될 수 있다. C5 는 유전적으로 및 임상적으로 입증된 표적으로서; 기능 소실 인간 돌연변이는 특정 감염에 대해 약화된 면역 방어와 연관되어 있고, 정맥 투여된 항-C5 단일클론 항체 요법은 다수의 보체-매개된 질환에서 임상적 활성 및 내약성을 입증하였다. 베타-지중해빈혈증 및 철 과부하 장애의 치료를 위한 막통과 프로테아제, 세린 6 (Tmprss6).
알파-1 항트립신 ( AAT ): (M11465.1 GI: 177826) 연관된 간 질환 - 본원에 참조로 도입되는 WO 13142514 는 본 발명의 올리고머 또는 컨쥬게이트 내에 도입될 수 있는 AAT 를 표적화하는 올리고뉴클레오타이드 화합물을 개시하고 있다. AAT 를 표적화하는 본 발명의 화합물은 AIAT mRNA 및 단백질 발현을 감소시키고, 이를 필요로 하는 개체에서 섬유증, 예를 들면, AIATD 연관된 간 질환, 및 폐 질환, 예를 들면, AIATD 연관된 폐 질환을 치료하거나 개선하거나 예방하거나 이의 진행을 둔화시키거나 이의 진행을 중단시키기 위한 방법에서 사용될 수 있다.
트랜스타이레틴 - TTR (BC005310.1 GI: 13529049): TTR 을 표적화하는 본 발명의 올리고머는 조직에서 누진적으로 축적되는 잘못 접힌 형태의 TTR 을 생성하는 돌연변이 유전자를 환자가 물려받은 중증 및 희귀 유전 질환인 트랜스타이레틴 아밀로이드증, 또는 TTR 아밀로이드증을 치료하는데 사용될 수 있다. TTR 아밀로이드증 환자에서, TTR 의 돌연변이체와 정상 형태 둘 다는 심장, 말초 신경 및 위장관을 비롯한 조직에서 원섬유로서 축적될 수 있다. TTR 원섬유의 존재는 이들 조직의 정상 기능을 방해하고, TTR 단백질 원섬유가 더 확대될수록 조직 손상이 일어나고 질환이 악화된다. TTR 은 혈액에서 갑상선 호르몬 및 레티놀을 수송하는 운반체 단백질이다. ITTR 아밀로이드증 환자에서, TTR 의 돌연변이체와 정상 형태 둘 다는 조직에서 원섬유로서 축적될 수 있다. 본 발명의 화합물은 TTR 아밀로이드증을 치료하는데 사용될 수 있다. 문헌 [Benson et al., Amyloid. 2010 Jun; 17(2): 43-9; 및 Ackermann et al., Amyloid. 2012 Jun; 19 Suppl 1: 43-4] 을 참조한다. 본 발명의 올리고머 또는 컨쥬게이트에서 사용될 수 있는 TTR 을 표적화하는 안티센스 화합물은 본원에 참조로 도입되는 US 8101743, WO 11139917 및 WO 10017509 에 개시되어 있다.
아미노레불리네이트 신타아제 -1 ( ALAS -1) (BC011798.2 GI: 33877783; AK312566.1 GI: 164690365; NM_199166.2 GI: 362999012; NM_000688.5 GI: 362999011). ALAS1 은 포르피린증의 치료, 예를 들면, 급성 간헐성 포르피린증 (acute intermittent porphyria: AIP) 을 비롯한 간 포르피린증의 치료를 위한 입증된 표적이다. ALAS-1 을 표적화하는 본 발명의 화합물은 이들 장애의 치료에 사용될 수 있다.
혈관 내피 성장 인자 또는 VEGF (GENE ID 7422, 인간 서열: 염색체: 6; NC_000006.11 (43737946..43754224)). VEGF 는 암에서 나타난다. VEGF 를 표적화하는 본 발명의 화합물은 과증식성 질환, 예를 들면, 암, 예를 들면, 간암의 치료에 사용될 수 있다.
표 3 은 본 발명의 화합물에 의해 표적화될 수 있는 간 표적의 군 뿐 아니라, 이러한 화합물을 사용하여 치료할 수 있는 의학적 징후/장애 (예를 들면, 연관 장애를 앓고 있는 사람) 을 제공한다 (문헌 [Sehgal et al., Liver as a target for oligonucleotide therapeutics, J. of Hepatology 2013, In Press] 참조).
서열
일부 실시형태에서, 올리고머 또는 이의 제 1 영역은 표적 핵산 (즉, 올리고머가 표적화하는 서열) 에 존재하는 뉴클레오타이드 서열의 역상보에 상응하는 인접 뉴클레오타이드 서열을 포함한다. 표 3 은 관련 징후에 대해 올리고뉴클레오타이드 화합물을 사용하는 전임상적 또는 임상적 개발 중에 있고, 따라서, 본 발명의 화합물로 표적화하는데 적합한 mRNA 및 miRNA 표적의 군을 제공한다.
일부 실시형태에서, 표적은 다음으로 이루어진 군으로부터 선택된다: miR-122, ApoB-100, ApoCIII, PCSK9, CRP, KSP, VEGF, PLK1 ,miR-34, FGFR4, 인자 IXa, 인자 XI, TTR, GCCR, PTP-1B, GCGR, AAT, ALDH2, HAMP 경로, miR-33, Apo(a), miR-7, miR-378, miR-21, Myc, miR-122, HCV 게놈, 예를 들면, HCV 5'UTR 또는 HCV NS5B RNA 또는 NS3 RNA, TMPRSS6, 항트롬빈 III, ApoCIII, ANGPLT3, MTP, DGAT2, ALAS1, 항트롬빈 III, 혈청 아민로이드 A 및 인자 VII.
일부 실시형태에서, 인접 뉴클레오타이드 서열은 표적 서열에 혼성화될 때 불과 단일 불일치 (mismatch) 만을 포함한다. 그러나, 영역 B 는 비상보적일 수 있고, 따라서 상보성 정도를 결정할 때 무시될 수 있다.
본 발명의 올리고머 (또는 이의 영역) 과 핵산의 표적 영역, 예를 들면, 본원에 기재된 것들 사이의 "상보성" 정도를 결정할 때, "상보성" (또한, "상동성" 또는 "동일성") 정도는 올리고머 (또는 이의 영역) 의 서열과 이와 최상으로 정렬하는 표적 영역 (또는 표적 영역의 역상보) 의 서열 사이의 % 동일성 (또는 % 상동성) 으로서 표현된다. 백분율은 2 개의 서열 사이에 동일한 정렬 염기의 수를 세고, 올리고머에서의 인접 모노머의 총 수로 나누고, 100 을 곱함으로써 산출된다. 이러한 비교에서, 갭이 존재하는 경우, 이러한 갭은 갭 내의 모노머의 수가 본 발명의 올리고머와 표적 영역 사이에 상이한 영역 보다는 오히려 단지 불일치인 것이 바람직하다.
본원에 사용되는 용어 "상동" 및 "상동성" 은 용어 "동일성" 및 "동일" 과 상호교환가능하다.
용어 "...에 상응하는" 및 "...에 상응한다" 란, 올리고머의 뉴클레오타이드 서열 (즉, 핵염기 또는 염기 서열) 또는 인접 뉴클레오타이드 서열 (제 1 영역) 과 i) 핵산 표적의 역상보의 하위 서열로부터 선택된 추가의 서열의 동등한 인접 뉴클레오타이드 서열 사이의 비교를 의미한다. 뉴클레오타이드 유사체는 이들의 동등하거나 상응하는 뉴클레오타이드와 직접 비교된다. i) 또는 ii) 하의 추가의 서열에 상응하는 제 1 서열은 전형적으로 제 1 서열 (예를 들면, 인접 뉴클레오타이드 서열) 의 길이에 대해 서열과 동일하거나, 본원에서 기재된 바와 같이, 일부 실시형태에서, 상응하는 서열과 80% 이상 상동, 예를 들면, 85% 상동, 90% 상동, 91% 상동, 92% 상동, 93% 상동, 94% 상동, 95% 상동, 96% 상동 상동, 예를 들면, 100% 상동 (동일) 한다.
용어 상응하는 뉴클레오타이드 유사체" 및 "상응하는 뉴클레오타이드" 란, 뉴클레오타이드 유사체 내의 뉴클레오타이드 및 천연 뉴클레오타이드가 동일한 것을 의미하는 것으로 의도된다. 예를 들면, 뉴클레오타이드의 2-데옥시리보오스 단위는 아데닌에 연결되어 있으며, "상응하는 뉴클레오타이드 유사체" 는 아데닌에 연결된 펜토오스 단위 (2-데옥시리보오스와 상이함) 를 함유한다.
본원에서 사용되는 용어 "역상보", "역상보적" 및 "역상보성" 은 용어 "상보", "상보적" 및 "상보성" 과 상호교환가능하다.
그러므로, 상기 올리고머의 인접 핵염기 서열은 표적, 예를 들면, 본원에서 언급된 것들에 상보적일 수 있다.
뉴클레오사이드
및
뉴클레오사이드
유사체
본원에 사용되는 용어 "뉴클레오타이드" 란, 당 모이어티 (또는 이의 유사체), 염기 모이어티 및 공유 연결기 (연결기), 예를 들면, 포스페이트 또는 포스포로티오에이트 인터뉴클레오타이드 연결기를 포함하는 글리코사이드를 의미하며, 천연 뉴클레오타이드, 예를 들면, DNA 또는 RNA 와, 본원에서 "뉴클레오타이드 유사체" 로서 또한 언급되는, 변형된 당 및/또는 염기 모이어티를 포함하는 비-천연 뉴클레오타이드 둘 다를 포괄한다. 본원에서, 단일 뉴클레오타이드 (단위) 는 또한 모노머 또는 핵산 단위로서 언급될 수 있다.
본 발명의 문맥에서, 용어 뉴클레오사이드 및 뉴클레오타이드란, 천연 뉴클레오타이드/뉴클레오사이드, 예를 들면, DNA 및 RNA 뿐 아니라, 뉴클레오타이드/뉴클레오사이드 유사체 둘 다를 의미하는 것으로 사용된다는 것을 인식할 것이다.
생화학 분야에서, 용어 "뉴클레오사이드" 란, 통상적으로 당 모이어티 및 염기 모이어티를 포함하는 글리코사이드를 의미하는 것으로 사용되고, 따라서, 올리고머의 뉴클레오타이드 사이의 인터뉴클레오사이드 연결에 의해 공유 연결된 뉴클레오타이드 단위를 언급할 때 사용될 수 있다. 생명공학 분야에서, 용어 "뉴클레오타이드" 란, 종종 핵산 모노머 또는 단위를 의미하는 것으로 사용되고, 올리고뉴클레오타이드의 문맥에서와 같이, 염기 - 예를 들면, "뉴클레오타이드 서열" 을 의미할 수 있으며, 전형적으로는 핵염기 서열을 의미한다 (즉, 당 백본 및 인터뉴클레오사이드 연결의 존재를 내포한다). 마찬가지로, 특히 인터뉴클레오사이드 연결기 중 하나 이상이 변형되는 올리고뉴클레오타이드의 경우, 용어 "뉴클레오타이드" 란, "뉴클레오사이드" 를 의미할 수 있으며, 예를 들면, 용어 "뉴클레오타이드" 는 심지어 뉴클레오사이드 사이의 연결의 존재 또는 성질을 구체화할 때 사용될 수 있다.
당업자가 인지하는 바와 같이, 비록 5' 말단 기를 포함할 수 있거나 포함하지 않을 수 있지만, 올리고뉴클레오타이드의 5' 말단 뉴클레오타이드는 5' 인터뉴클레오사이드 연결기를 포함하지 않는다. 비-천연 뉴클레오타이드는 변형된 당 모이어티, 예를 들면, 바이사이클릭 뉴클레오타이드 또는 2' 변형된 뉴클레오타이드, 예를 들면, 2' 치환된 뉴클레오타이드를 가진 뉴클레오타이드를 포함한다.
"뉴클레오타이드 유사체" 는 당 및/또는 염기 모이어티 중의 변형에 의한, 천연 뉴클레오타이드, 예를 들면, DNA 또는 RNA 뉴클레오타이드의 변이체이다. 유사체는 원칙적으로 올리고뉴클레오타이드의 문맥에서 천연 뉴클레오타이드에 대해 단지 "침묵" 또는 이와 "동등한" 것일 수 있으며, 즉, 올리고뉴클레오타이드가 표적 유전자 발현을 억제하도록 작동하는 방식에 기능적인 영향을 미치지 않는다. 그럼에도 불구하고, 이러한 "동등한" 유사체는, 예를 들면, 이들이 제조하기가 보다 용이하거나 보다 저렴한 경우, 또는 저장 또는 제조 조건에서 보다 안정한 경우, 또는 태그 또는 라벨을 나타내는 경우, 유용할 수 있다. 그러나, 바람직하게는, 유사체는, 예를 들면, 표적에 대한 결합 친화성 증가 및/또는 세포내 뉴클레아제에 대한 내성 증가 및/또는 세포내로의 수송의 용이성 증가를 초래함으로써, 올리고머가 발현을 억제하도록 작동하는 방식에 기능적인 영향을 미칠 것이다. 뉴클레오사이드 유사체의 특이적인 예는 예를 들면, 문헌 [Freier & Altmann; Nucl . Acid Res ., 1997, 25, 4429-4443; 및 Uhlmann; Curr . Opinion in Drug Development, 2000, 3(2), 293-213] 및 하기 도식 1 에 의해 기재된다:
도식 1
따라서, 상기 올리고머는 천연 뉴클레오타이드 - 바람직하게는 2'-데옥시뉴클레오타이드 (본원에서 일반적으로 "DNA" 로서 언급됨) 뿐만 아니라, 가능하게는 리보뉴클레오타이드 (본원에서 일반적으로 "RNA" 로서 언급됨), 또는 이러한 천연 뉴클레오타이드 및 하나 이상의 비-천연 뉴클레오타이드, 즉, 뉴클레오타이드 유사체의 조합의 단순 서열을 포함하거나 이들로 이루어질 수 있다. 이러한 뉴클레오타이드 유사체는 적합하게는 표적 서열에 대한 올리고머의 친화성을 향상시킬 수 있다.
적합하고 바람직한 뉴클레오타이드 유사체의 예는 WO 2007/031091 에 의해 제공되거나 그 안에 참조되어 있다. 본 발명의 올리고머에서 사용될 수 있는 기타 뉴클레오타이드 유사체는 트리사이클릭 핵산을 포함하고, 예를 들면, 본원에 참조로 도입되는 WO 2013154798 및 WO 2013154798 을 참조한다.
올리고머성 화합물, 예를 들면, 안티센스 올리고뉴클레오타이드, 예를 들면, 영역 A, 및 일부 선택적 실시형태에서는 영역 B 를 비롯한 본원에 언급된 화합물은, 당 기가 변형된 하나 이상의 뉴클레오사이드를 함유할 수 있다. 이러한 당 변형된 뉴클레오사이드 (뉴클레오사이드 유사체) 는 뉴클레아제 안정성 향상, 결합 친화성 증가 또는 일부 기타 유리한 생물학적 특성을 안티센스 화합물에 부여할 수 있다. 일부 실시형태에서, 뉴클레오사이드는 화학적으로 변형된 리보피라노오스 고리 모이어티를 포함한다.
일부 실시형태에서, 올리고머 또는 이의 제 1 영역은 하나 이상, 예를 들면, 2 개 이상, 3 개 이상, 4 개 이상, 5 개 이상, 6 개 이상, 7 개 이상, 8 개 이상, 9 개 이상, 10 개 이상, 11 개 이상, 12 개 이상, 13 개 이상, 14 개 이상, 15 개 이상, 16 개 이상, 17 개 이상, 18 개 이상, 19 개 이상, 20 개 이상, 21 개 이상, 22 개 이상, 23 개 이상, 24 개 이상 또는 25 개의 뉴클레오사이드 유사체, 예를 들면, 당 변형된 뉴클레오사이드 유사체를 포함한다.
일부 실시형태에서, 뉴클레오사이드 유사체는 바이사이클릭 뉴클레오사이드 유사체 (예를 들면, LNA) 및/또는 2' 치환된 뉴클레오사이드 유사체로 이루어진 군으로부터 (임의로 독립적으로) 선택되고, 예를 들면, 2'-O-알킬-RNA 단위, 2'-OMe-RNA 단위, 2'-아미노-DNA 단위, 2'-AP, 2'-FANA, 2'-(3-하이드록시)프로필 및 2'-플루오로-DNA 단위, 및/또는 기타 (임의로) 당 변형된 뉴클레오사이드 유사체, 예를 들면, 모르폴리노, 펩타이드 핵산 PNA), CeNA, 비연결된 핵산 (UNA), 헥시톨 핵산 (HNA). 바이사이클로-HNA 로 이루어진 군으로부터 (임의로 독립적으로) 선택된다 (예를 들면, WO 2009/100320 참조). 일부 실시형태에서, 뉴클레오사이드 유사체는 이의 표적 핵산 (또는 상보적 DNA 또는 RNA 서열) 에 대한 제 1 영역의 친화성를 증가시킨다.
일부 실시형태에서, 상기 올리고머는 하나 이상의 바이사이클릭 뉴클레오타이드 유사체, 예를 들면, LNA 를 포함한다. 일부 실시형태에서, 제 1 영역은 하나 이상의 바이사이클릭 뉴클레오사이드 유사체 (예를 들면, LNA) 및/또는 2' 치환된 뉴클레오사이드 유사체를 포함한다. 일부 실시형태에서, 상기 올리고머에 존재하는 뉴클레오사이드 유사체는 모두 동일한 당 변형을 포함한다. 일부 실시형태에서, 제 1 영역에 존재하는 하나 이상의 뉴클레오사이드 유사체는 바이사이클릭 뉴클레오사이드 유사체이고, 예를 들면, 2 개 이상, 3 개 이상, 4 개 이상, 5 개 이상, 6 개 이상, 7 개 이상, 8 개 이상, 9 개 이상, 10 개 이상, 11 개 이상, 12 개 이상, 13 개 이상, 14 개 이상, 15 개 이상, 16 개 이상의, 예를 들면, 모든 뉴클레오사이드 유사체 (영역 B 의 DNA 및 또는 RNA 뉴클레오사이드 제외) 는 당 변형된 뉴클레오사이드 유사체, 예를 들면, 바이사이클릭 뉴클레오사이드 유사체, 예를 들면, LNA, 예를 들면, 베타-D-X-LNA 또는 알파-L-X-LNA (여기서, X 는 옥시, 아미노 또는 티오이다), 또는 (R/S) cET, cMOE 또는 5'-Me-LNA 를 포함하나 이들에 한정되지 않는 본원에 기재된 기타 LNA 이다.
화학적으로 변형된 리보피라노오스 고리의 예는, 치환기 군 (5' 및 2' 치환기 군을 포함함) 의 첨가; 바이사이클릭 핵산 (BNA) 을 형성하기 위한 비-같은자리 (non-geminal) 고리 원자의 브릿지 형성; S, N(R) 또는 C(R1)(R2) (R = H, C1-C2 알킬 또는 보호기이다) 에 의한 리보실 고리 산소 원자의 대체; 및 이들의 조합을 포함하지만, 이들에 한정되는 것은 아니다. 화학적으로 변형된 당의 예는, 2'-F-5'-메틸 치환된 뉴클레오사이드 (기타 기재된 5',2'-비스 치환된 뉴클레오사이드에 대해 8/21/08 자로 공개된 PCT 국제 출원 공개 WO 2008/101157 참조), 2'-위치에서의 추가 치환을 가지는 S 에 의한 리보실 고리 산소 원자의 대체 (2005 년 6 월 16 일자로 공개된 미국 특허 출원 US 2005/0130923 참조) 또는 다르게는 BNA 의 5'-치환 (LNA 가, 예를 들면, 5'-메틸기 또는 5'-비닐기로 치환된 11/22/07 자에 공개된 PCT 국제 출원 WO 2007/134181 참조) 을 포함한다.
변형된 당 모이어티를 가진 뉴클레오사이드의 예는 5'-비닐, 5'-메틸 (R 또는 S), 4'-S, 2'-F, 2'-OCH3, 및 2'-O(CH2)2OCH3 치환기 군을 포함하는 뉴클레오사이드를 포함하지만, 이들에 한정되는 것은 아니다. 2' 위치에서의 치환기는 또한 알릴, 아미노, 아지도, 티오, O-알릴, O-C1-C10 알킬, OCF3, O(CH2)2SCH3, O(CH2)2-O-N(Rm)(Rn) 및 O-CH2-C(=O)-N(Rm)(Rn) (여기서, 각각의 Rm 및 Rn 은 독립적으로 H 또는 치환 또는 비치환된 C1-C10 알킬이다) 으로부터 선택될 수 있다.
본원에서 사용되는 "바이사이클릭 뉴클레오사이드" 란, 바이사이클릭 당 모이어티를 포함하는 변형된 뉴클레오사이드를 의미한다. 바이사이클릭 뉴클레오사이드의 예는 4' 리보실 고리 원자와 2' 리보실 고리 원자 사이에 브릿지를 포함하는 뉴클레오사이드를 포함하지만, 이들에 한정되는 것은 아니다. 일부 실시형태에서, 본원에서 제공된 화합물은, 브릿지가 4' 내지 2' 바이사이클릭 뉴클레오사이드를 포함하는 하나 이상의 바이사이클릭 뉴클레오사이드를 포함한다. 이러한 4' 내지 2' 바이사이클릭 뉴클레오사이드의 예는 다음 식 중 하나 이상을 포함하지만, 이들에 한정되는 것은 아니다: 4'-(CH2)-O-2' (LNA); 4'-(CH2)-S-2'; 4'-(CH2)2-O-2' (ENA); 4'-CH(CH3)-O-2' 및 4'-CH(CH2OCH3)-O-2*, 및 이들의 유사체 (2008 년 7 월 15 일자로 발행된 U.S. 특허 7,399,845 참조); 4'-C(CH3)(CH3)-O-2' 및 이의 유사체 (2009 년 1 월 8 일자로 공개된 PCT 국제 출원 공개 WO 2009/006478 참조); 4'-CH2-N(OCH3)-2' 및 이의 유사체 (2008 년 12 월 11 일자로 공개된 PCT 국제 출원 공개 WO 2008/150729 참조); 4'-CH2-O-N(CH3)-2' (2004 년 9 월 2 일자로 공개된 U.S. 특허 출원 공개 US 2004/0171570 참조); 4'-CH2-N(R)-O-2' (여기서, R 은 H, C1-C10 알킬 또는 보호기이다) (2008 년 9 월 23 일자로 발행된 U.S. 국제 7,427,672 참조); 4'-CH2-C(H)(CH3)-2' (문헌 [Chattopadhyaya, et al., J. Org. Chem.,2009, 74, 118-134] 참조); 및 4'-CH2-C(=CH2)-2' 및 이의 유사체 (2008 년 12 월 8 일자로 공개된 PCT 국제 출원 공개 WO 2008/154401 참조). 또한, 예를 들면, 문헌 [Singh et al., Chem. Commun., 1998, 4, 455-456; Koshkin et al., Tetrahedron, 1998, 54, 3607-3630; Wahlestedt et al., Proc. Natl. Acad. Sci. U. S. A., 2000, 97, 5633-5638; Kumar et al., Bioorg. Med. Chem. Lett., 1998, 8, 2219-2222; Singh et al., J. Org. Chem., 1998, 63, 10035-10039; Srivastava et al., J. Am. Chem. Soc, 129(26) 8362-8379 (Jul. 4, 2007); Elayadi et al., Curr. Opinion Invens. Drugs, 2001, 2, 558-561; Braasch et al., Chem. Biol, 2001, 8, 1-7; Oram et al., Curr. Opinion Mol. Ther., 2001, 3, 239-243]; U.S. 특허 번호 U.S. 6,670,461, 7,053,207, 6,268,490, 6,770,748, 6,794,499, 7,034,133, 6,525,191, 7,399,845; PCT 국제 출원 공개 WO 2004/106356, WO 94/14226, WO 2005/021570, 및 WO 2007/134181; U.S. 특허 공개 번호 US 2004/0171570, US 2007/0287831 및 US 2008/0039618; 및 U.S. 특허 연속 출원 번호 12/129,154, 60/989,574, 61/026,995, 61/026,998, 61/056,564, 61/086,231, 61/097,787 및 61/099,844; 및 PCT 국제 출원 번호 PCT/US2008/064591, PCT/US2008/066154, 및 PCT/US2008/068922 를 참조한다. 상기 바이사이클릭 뉴클레오사이드의 각각은, 예를 들면, a-L-리보푸라노오스 및 베타-D-리보푸라노오스를 비롯한 하나 이상의 입체화학적 당 배치를 가지도록 제조될 수 있다 (WO 99/14226 으로서 1999 년 3 월 25 일자로 공개된 PCT 국제 출원 PCT DK98/00393).
일부 실시형태에서, BNA 뉴클레오사이드의 바이사이클릭 당 모이어티는 펜토푸라노실 당 모이어티의 4' 위치와 2' 위치 사이에 하나 이상의 브릿지를 가진 화합물을 포함하지만 이에 한정되는 것은 아니고, 여기서, 이러한 브릿지는 독립적으로 -[CiRaXRb)]-, -C(Ra)=C(Rb)-, -C(Ra)=N-, -C(=NRa)-, -C(=O)-, -C(=S)-, -O-, -Si(Ra)2-, -S(=O)x- 및 -N(Ra)- 로부터 독립적으로 선택된 1 개, 또는 2 개 내지 4 개의 연결기를 포함하고, 여기서, x 는 0, 1 또는 2 이고; n 은 1, 2, 3 또는 4 이고; 각각의 Ra 및 Rb 는 독립적으로 H, 보호기, 하이드록실, C1-C12 알킬, 치환된 C1-C12 알킬, C2-C12 알케닐, 치환된 C2-C12 알케닐, C2-C12 알키닐, 치환된 C2-C12 알키닐, C5-C20 아릴, 치환된 C5-C20 아릴, 헤테로사이클 라디칼, 치환된 헤테로사이클 라디칼, 헤테로아릴, 치환된 헤테로아릴, C5-C7 지환족 라디칼, 치환된 C5-C7 지환족 라디칼, 할로겐, OJ1, NJ1J2, SJ1, N3, COOJ1, 아실 (C(=O)-H), 치환된 아실, CN, 설포닐 (S(=O)2-J1), 또는 설폭실 (S(=O)-J1) 이고; 각각의 J1 및 J2 는독립적으로 H, C1-C6 알킬, 치환된 C1-C12 알킬, C2-C12 알케닐, 치환된 C2-C12 알케닐, C2-C12 알키닐, 치환된 C2-C12 알키닐, C5-C20 아릴, 치환된 C5-C20 아릴, 아실 (C(=O)-H), 치환된 아실, 헤테로사이클 라디칼, 치환된 헤테로사이클 라디칼, C1-C12 아미노알킬, 치환된 C1-C12 아미노알킬 또는 보호기이다.
일부 실시형태에서, 바이사이클릭 당 모이어티의 브릿지는 -[C(Ra)(Rb)]n-, -[C(Ra)(Rb)]n-O-, -C(RaRb)-N(R)-O- 또는 -C(RaRb)-O-N(R)- 이다. 일부 실시형태에서, 상기 브릿지는 4'-CH2-2', 4'-(CH2)2-2', 4'-(CH2)3-2', 4'-CH2-O-2', 4*-(CH2)2-O-2', 4'-CH2-O-N(R)-2' 및 4'-CH2-N(R)-O-2'- 이고, 여기서, 각각의 R 은 독립적으로 H, 보호기, 또는 C1-C12 알킬이다.
일부 실시형태에서, 바이사이클릭 뉴클레오사이드는 이성질체 배치에 의해 추가로 정의된다. 예를 들면, 4'-2' 메틸렌-옥시 브릿지를 포함하는 뉴클레오사이드는 a-L 배치 또는 베타-D 배치로 존재할 수 있다. 이전에, a-L-메틸렌옥시 (4'-CH2-O-2') BNA 는 안티센스 활성을 나타내는 안티센스 올리고뉴클레오타이드 내로 도입되었다 [Frieden et al., Nucleic Acids Research, 2003, 21, 6365-6372].
일부 실시형태에서, 바이사이클릭 뉴클레오사이드는 하기에 도시된 바와 같은 (A) a-L-메틸렌옥시 (4'-CH2-O-2') BNA, (B) 베타-D-메틸렌옥시 (4'-CH2-O-2') BNA, (C) 에틸렌옥시 (4'-(CH2)2-O-2') BNA, (D) 아미노옥시 (4'-CH2-O-N(R)-2') BNA, (E) 옥시아미노 (4'-CH2-N(R)-O-2') BNA, (F) 메틸(메틸렌옥시) (4'-CH(CH3)-O-2') BNA, (G) 메틸렌-thio (4'-CH2-S-2') BNA, (H) 메틸렌-아미노 (4'-CH2-N(R)-2') BNA, (I) 메틸 카보사이클릭 (4'-CH2-CH(CH3)-2') BNA 및 (J) 프로필렌 카보사이클릭 (4'-(CH2)3-2') BNA 를 포함하지만, 이들에 한정되는 것은 아니다.
여기서, Bx 는 모이어티이고, R 은 독립적으로 H, 보호기 또는 C1-C2 알킬이다. 일부 실시형태에서, 바이사이클릭 뉴클레오사이드는 하기 식 I 을 가진다:
여기서,
Bx 는 헤테로사이클릭 염기 모이어티이고;
-Qa-Qb-Qc- 는 -CH2-N(Rc)-CH2-, -C(=O)-N(Rc)-CH2-, -CH2-O-N(Rc)-, -CH2-N(Rc)-O- 또는 -N(Rc)-O-CH2 이고;
Rc 는 C1-C12 알킬 또는 아미노 보호기이고;
Ta 및 Tb 는 각각 독립적으로 H, 하이드록실 보호기, 컨쥬게이트 기, 반응성 인 기, 인 모이어티 또는 지지 매질에 대한 공유 부착점이다.
일부 실시형태에서, 바이사이클릭 뉴클레오사이드는 하기 식 II 를 가진다:
여기서,
Bx 는 헤테로사이클릭 염기 모이어티이고;
Ta 및 Tb 는 각각 독립적으로 H, 하이드록실 보호기, 컨쥬게이트 기, 반응성 인 기, 인 모이어티 또는 지지 매질에 대한 공유 부착점이고 Za 는 C1-C6 알킬, C2-C6 알케닐, C2-C6 알키닐, 치환된 C1-C6 알킬, 치환된 C2-C6 알케닐, 치환된 C2-C6 알키닐, 아실, 치환된 아실, 치환된 아미드, 티올 또는 치환된 티오이다.
일부 실시형태에서, 치환된 기의 각각은 독립적으로 할로겐, 옥소, 하이드록실, OJc, NJd, SJC, N3, OC(=X)Jc, 및 NJeC(=X)NJcJd 로 일치환 또는 다치환되고, 여기서, 각각의 Jc, Jd, 및 Je 는 독립적으로 H, C1-C6 알킬 또는 치환된 C1-C6 알킬이고, X 는 O 또는 NJC 이다.
일부 실시형태에서, 바이사이클릭 뉴클레오사이드는 하기 식 III 을 가진다:
여기서,
Bx 는 헤테로사이클릭 염기 모이어티이고;
Ta 및 Tb 는 각각 독립적으로 H, 하이드록실 보호기, 컨쥬게이트 기, 반응성 인 기, 인 모이어티 또는 지지 매질에 대한 공유 부착점이고;
Rd 는 C1-C6 알킬, C2-C6 알케닐, C2-C6 알키닐, 치환된 C1-C6 알킬, 치환된 C2-C6 알케닐, 치환된 C2-C6 알키닐 또는 치환된 아실 (C(=O)-) 이다.
일부 실시형태에서, 바이사이클릭 뉴클레오사이드는 하기 식 IV 를 가진다:
여기서,
Bx 는 헤테로사이클릭 염기 모이어티이고;
Ta 및 Tb 는 각각 독립적으로 H, 하이드록실 보호기, 컨쥬게이트 기, 반응성 인 기, 인 모이어티 또는 지지 매질에 대한 공유 부착점이고;
Rd 는 C1-C6 알킬, 치환된 C1-C6 알킬, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐, 치환된 C2-C6 알키닐이고; 각각의 qb, qc 및 qd 는 독립적으로 H, 할로겐, C1-C6 알킬, 치환된 C1-C6 알킬, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐 또는 치환된 C2-C6 알키닐, C1-C6 알콕실, 치환된 Q-C6 알콕실, 아실, 치환된 아실, C1-C6 아미노알킬 또는 치환된 C1-C6 아미노알킬이다.
일부 실시형태에서, 바이사이클릭 뉴클레오사이드 하기 식 V 를 가진다:
여기서,
Bx 는 헤테로사이클릭 염기 모이어티이고;
Ta 및 Tb 는 각각 독립적으로 H, 하이드록실 보호기, 컨쥬게이트 기, 반응성 인 기, 인 모이어티, 또는 지지 매질에 대한 공유 부착점이고; qa, qb, qc 및 qf 는 각각 독립적으로 수소, 할로겐, C1-C12 알킬, 치환된 C1-C12 알킬, C2-C12 알케닐, 치환된 C2-C12 알케닐, C2-C12 알키닐, 치환된 C2-C12 알키닐, C1-C12 알콕시, 치환된 C1-C12 알콕시, OJj, SJj, SOJj, SO2Jj, NJjJk, N3, CN, C(=O)OJj, C(=O)NJjJk, C(=O)Jj, O-C(=O)NJjJk, N(H)C(=NH)NJjJk, N(H)C(=O)NJjJk 또는 N(H)C(=S)NJjJk 이거나; qe 및 qf 는 함께 =C(qg)(qh) 이고; qg 및 qh 는 각각 독립적으로 H, 할로겐, C1-C12 알킬 또는 치환된 C1-C12 알킬이다.
메틸렌옥시 (4'-CH2-O-2') BNA 모노머 아데닌, 시토신, 구아닌, 5-메틸-시토신, 티민 및 우라실의 합성 및 제조, 및 이들의 올리고머화와 함께, 및 핵산 인지 특성은 기재되어 있다 (예를 들면, 문헌 [Koshkin et al., Tetrahedron, 1998, 54, 3607-3630] 참조) BNA 및 이의 제조는 또한 WO 98/39352 및 WO 99/14226 에 기재되어 있다.
메틸렌옥시 (4'-CH2-O-2') BNA, 메틸렌옥시 (4'-CH2-O-2') BNA 및 2'-티오-BNA 의 유사체도 또한 제조되었다 (예를 들면, 문헌 [Kumar et al., Bioorg. Med. Chem. Lett., 1998, 8, 2219-2222] 참조) 핵산 폴리머라아제에 대한 기질로서 올리고데옥시리보뉴클레오타이드 이중체를 포함하는 잠금 뉴클레오사이드 유사체의 제조도 또한 기재되어 있다 (예를 들면, Wengel et al., WO 99/14226 참조). 또한, 신규한 형태적으로 제약된 고친화성 올리고뉴클레오타이드 유사체인 2'-아미노-BNA 의 합성도 당업계에 기재되어 있다 (예를 들면, 문헌 [Singh et al., J. Org. Chem., 1998, 63, 10035-10039] 참조). 또한, 2'-아미노-BNA 및 2'-메틸아미노-BNA 가 제조되었고, 상보적 RNA 및 DNA 가닥을 가진 이들의 이중체의 열 안정성은 이전에 보고되었다.
일부 실시형태에서, 바이사이클릭 뉴클레오사이드는 하기 식 VI 을 가진다:
여기서,
Bx 는 헤테로사이클릭 염기 모이어티이고;
Ta 및 Tb 는 각각 독립적으로 H, 하이드록실 보호기, 컨쥬게이트 기, 반응성 인 기, 인 모이어티, 또는 지지 매질에 대한 공유 부착점이고; 각각의 qi, qj, qk 및 ql 은 독립적으로 H, 할로겐, C1-C12 알킬, 치환된 C1-C12 알킬, C2-C12 알케닐, 치환된 C2-C12 알케닐, C2-C12 알키닐, 치환된 C2-C12 알키닐, C1-C12 알콕실, 치환된 C2-C12 알콕실, OJj, SJj, SOJj, SO2Jj, NJjJk, N3, CN, C(=O)OJj, C(=O)NJjJk, C(=O)Jj, O-C(=O)NJjJk, N(H)C(=NH)NJjJk, N(H)C(=O)NJjJk, 또는 (H)C(=S)NJjJk 이고; qi 와 qj, 또는 ql 과 qk 는 함께 =C(qg)(qh) 이고, 여기서, qg 및 qh 는 각각 독립적으로 H, 할로겐, C1-C12 알킬 또는 치환된 C1-C6 알킬이다.
4'-(CH2)3-2' 브릿지 및 알케닐 유사체, 브릿지 4'-CH=CH-CH2-2' 를 가지는 하나의 카보사이클릭 바이사이클릭 뉴클레오사이드가 기재되어 있다 (예를 들면, 문헌 [Freier et al., Nucleic Acids Research, 1997, 25(22), 4429- 4443; 및 Albaek et al., J. Org. Chem., 2006, 71, 7731-7740] 참조). 카르보사이클릭 바이사이클릭 뉴클레오사이드의 합성 및 제조, 및 이들의 올리고머화와 함께 및 생화학적 연구도 또한 기재되었다 (예를 들면, [Srivastava et al., J. Am. Chem. Soc. 2007, 129(26), 8362-8379] 참조).
본원에서 사용되는 "4'-2' 바이사이클릭 뉴클레오사이드" 또는 "4' 내지 2' 바이사이클릭 뉴클레오사이드" 란, 2' 탄소 원자 및 4' 탄소 원자를 연결하는 브릿지를 포함하는 푸라노스 고리를 포함하는 바이사이클릭 뉴클레오사이드를 의미한다.
본원에서 사용되는 "모노사이클릭 뉴클레오사이드" 란, 바이사이클릭 당 모이어티가 아닌 변형된 당 모이어티를 포함하는 뉴클레오사이드를 의미한다. 일부 실시형태에서, 뉴클레오사이드의 당 모이어티 또는 당 모이어티 유사체는 임의의 위치에서 변형되거나 치환될 수 있다.
본원에서 사용되는 "2'-변형된 당" 이란, 2' 위치에서 변형된 푸라노실 당을 의미한다. 일부 실시형태에서, 이러한 변형은 치환 및 비치환된 알콕시, 치환 및 비치환된 티오알킬, 치환 및 비치환된 아미노 알킬, 치환 및 비치환된 알킬, 치환 및 비치환된 알릴, 및 치환 및 비치환된 알키닐을 포함하지만 이들에 한정되지 않는 할라이드로부터 선택된 치환기를 포함한다. 일부 실시형태에서, 2' 변형은 O[(CH2)nO]mCH3, O(CH2)mNH2, O(CH2)mCH3, O(CH2)mONH2, OCH2C(=O)N(H)CH3 및 O(CH2)nON[(CH2)nCH3]2 를 포함하지만 이들에 한정되지 않는 치환기로부터 선택되고, 여기서, n 및 m 은 1 내지 약 10 이다. 기타 2'-치환기 군은 또한 C1-C12 알킬; 치환된 알킬; 알케닐; 알키닐; 알크아릴; 아르알킬; O-알크아릴 또는 O-아르알킬; SH; SCH3; OCN; CI; Br; CN; CF3; OCF3; SOCH3; SO2CH3; ONO2; NO2; N3; NH2; 헤테로사이클로알킬; 헤테로사이클로알크아릴; 아미노알킬아미노; 폴리알킬아미노; 치환된 실릴; R; 절단 기; 리포터 기; 삽입제 (intercalator); 약동학 특성을 개선하기 위한 기; 및 안티센스 화합물의 약력학 특성을 개선하기 위한 기, 및 유사한 특성을 가진 기타 치환기로부터 선택될 수 있다. 일부 실시형태에서, 변형된 뉴클레오사이드는 2'-MOE 측쇄를 포함한다 (예를 들면, 문헌 [Baker et al., J. Biol. Chem., 1997, 272, 1 1944-12000] 참조). 이러한 2'-MOE 치환은 비변형된 뉴클레오사이드 및 기타 변형된 뉴클레오사이드, 예를 들면, 2'-O-메틸, O-프로필 및 O-아미노프로필과 비교하여 개선된 결합 친화성을 가진 것으로 기재되어 있다. 2-MOE 치환기를 가진 올리고뉴클레오타이드는 또한 생체내 용도를 위한 유망한 특성을 가진 유전자 발현의 안티센스 억제제인 것으로 나타났다 (예를 들면, 문헌 [Martin, P., He/v. Chim. Acta, 1995, 78, 486-504; Altmann et al., Chimia, 1996, 50, 168-176; Altmann et al., Biochem. Soc. Trans., 1996, 24, 630-637; 및 Altmann et al., Nucleosides Nucleotides, 1997, 16, 917-926] 참조).
본원에서 사용되는 "변형된 테트라히드로피란 뉴클레오사이드" 또는 "변형된 THP 뉴클레오사이드" 란, 정상 뉴클레오사이드에서 펜토푸라노실 잔기에 대해 치환된 6 원 테트라히드로피란 "당" (당 대용물) 을 가진 뉴클레오사이드를 의미한다. 변형된 THP 뉴클레오사이드는 헥시톨 핵산 (HNA), 아니톨 핵산 (anitol nucleic acid: ANA), 만니톨 핵산 (manitol nucleic acid: MNA) (문헌 [Leumann, CJ. Bioorg. and Med. Chem. (2002) 10: 841-854] 참조), 플루오로 HNA (F-HNA), 또는 하기 식 X 를 가진 화합물로서 당업계에서 언급되는 것들을 포함하지만, 이들에 한정되는 것은 아니다:
식 X
여기서, 식 X 의 상기 하나 이상의 테트라하이드로피란 뉴클레오사이드 유사체의 각각에 대해,
Bx 는 헤테로사이클릭 염기 모이어티이고;
T3 및 T4 는 각각 독립적으로 테트라하이드로피란 뉴클레오사이드 유사체를 안티센스 화합물에 연결시키는 인터뉴클레오사이드 연결기이거나, T3 및 T4 중 하나는 테트라하이드로피란 뉴클레오사이드 유사체를 안티센스 화합물에 연결시키는 인터뉴클레오사이드 연결기이고, T3 및 T4 중 나머지는 H, 하이드록실 보호기, 연결된 컨쥬게이트 기, 또는 5' 또는 3'-말단기이고; q1 q2 q3 q4 q5, q6 및 q7 은 각각 독립적으로 H, C1-C6 알킬, 치환된 C1-C6 알킬, C2-C6 알케닐, 치환된 C2-C6 알케닐, C2-C6 알키닐 또는 치환된 C2-C6 알키닐이고; R1 및 R2 중 하나는 수소이고, 나머지는 할로겐, 치환 또는 비치환된 알콕시, NJ, J2, SJ, N3, OC(=X)J1, OC(=X)NJ1J2, NJ3C(=X)NJ1J2 및 CN 으로부터 선택되고, X 는 O, S 또는 NJ1 이고, 각각의 J1, J2 및 J3 은 독립적으로 H 또는 C1-C6 알킬이다.
일부 실시형태에서, qm, qn, qp, qr, qs, qt , 및 qu 가 각각 H 인 식 X 의 변형된 THP 뉴클레오사이드가 제공된다. 일부 실시형태에서, qm, qn, qp, qr, qs, qt 및 qu 중 하나 이상은 H 이외의 것이다. 일부 실시형태에서, qm, qn, qp, qr, qs, qt 및 qu 중 하나 이상은 메틸이다. 일부 실시형태에서, R1 및 R2 중 하나가 F 인 식 X 의 THP 뉴클레오사이드가 제공된다. 일부 실시형태에서, R1 은 플루오로이고 R2 는 H 이고, R1 은 메톡시이고 R2 는 H 이고, R1 은 메톡시에톡시이고 R2 는 H 이다.
본원에서 사용되는 "2'-변형된" 또는 "2'-치환된" 이란, H 또는 OH 이외의 2' 위치에서 치환기를 포함하는 당을 포함하는 뉴클레오사이드를 의미한다. 2'-변형된 뉴클레오사이드는 브릿지 비형성 2' 치환기를 가진 뉴클레오사이드, 예를 들면, 알릴, 아미노, 아지도, 티오, O-알릴, O-C1-C10 알킬, -OCF3, O-(CH2)2-O-CH3, 2'-O(CH2)2SCH3, O-(CH2)2-O-N(Rm)(Rn) 또는 O-CH2-C(=O)-N(Rm)(Rn) 을 포함하지만 이들에 한정되는 것은 아니고, 여기서, 각각의 Rm 및 Rn 은 독립적으로 H, 또는 치환 또는 비치환된 C1-C10 알킬이다. 2'-변형된 뉴클레오사이드는, 예를 들면, 당의 다른 위치에서 및/또는 핵염기에서 기타 변형을 추가로 포함할 수 있다.
본원에서 사용되는 "2'-F" 란, 2' 위치에서 플루오로 기를 포함하는 당을 의미한다.
본원에서 사용되는 "2'-OMe" 또는 "2'-OCH3" 또는 "2'-O-메틸" 이란, 각각 당 고리의 2' 위치에서 -OCH3 기를 포함하는 당을 포함하는 뉴클레오사이드를 의미한다.
본원에서 사용되는 "올리고뉴클레오타이드" 란, 복수의 연결된 뉴클레오사이드를 포함하는 화합물을 의미한다.
일부 실시형태에서, 복수의 뉴클레오사이드 중 하나 이상은 변형된다. 일부 실시형태에서, 올리고뉴클레오타이드는 하나 이상의 리보뉴클레오사이드 (RNA) 및/또는 데옥시리보뉴클레오사이드 (DNA) 를 포함한다.
안티센스 화합물 내로 도입하기 위해 뉴클레오사이드를 변형하는데 사용될 수 있는 다수의 기타 바이사이클로 및 트리사이클로 당 대용물 고리 시스템은 또한 당업자에게 공지되어 있다 (예를 들면, 검토 논문: 문헌 [Leumann, J. C, Bioorganic and Medicinal Chemistry, 2002, 10, 841-854] 참조). 이러한 고리 시스템은 활성을 향상시키기 위해 다양한 추가의 치환을 수행할 수 있다. 변형된 당의 제조 방법은 당업자에게 잘 공지되어 있다. 변형된 당 모이어티를 가진 뉴클레오타이드에서, 핵염기 모이어티 (천연, 변형, 또는 이의 조합) 은 적절한 핵산 표적과의 혼성화를 위해 유지된다.
일부 실시형태에서, 안티센스 화합물은 변형된 당 모이어티를 가진 하나 이상의 뉴클레오타이드를 포함한다. 일부 실시형태에서, 변형된 당 모이어티는 2'-MOE 이다. 일부 실시형태에서, 2'-MOE 변형된 뉴클레오타이드는 갭머 모티프로 정렬되어 있다. 일부 실시형태에서, 변형된 당 모이어티는 cEt 이다. 일부 실시형태에서, cEt 변형된 뉴클레오타이드는 갭머 모티프의 날개를 통해 정렬되어 있다.
일부 실시형태에서, BNA (LNA) 에서, R4 * 및 R2 * 는 함께 바이라디칼 -O-CH(CH2OCH3)-(2' O-메톡시에틸 바이사이클릭 핵산 - [Seth at al., 2010, J. Org. Chem]) - 을 R-배치 또는 S-배치로 지정한다.
일부 실시형태에서, BNA (LNA) 에서, R4 * 및 R2 * 는 함께 바이라디칼 -O-CH(CH2CH3)-(2' O-에틸 바이사이클릭 핵산 - [Seth at al., 2010, J. Org. Chem]) - 을 R-배치 또는 S-배치로 지정한다.
일부 실시형태에서, BNA (LNA) 에서, R4 * 및 R2 * 는 함께 바이라디칼 -O-CH(CH3)- - 을 R-배치 또는 S-배치로 지정한다. 일부 실시형태에서, R4 * 및 R2 * 는 함께 바이라디칼 -O-CH2-O-CH2- 를 지정한다 - [Seth at al., 2010, J. Org. Chem].
일부 실시형태에서, BNA (LNA) 에서, R4 * 및 R2 * 는 함께 바이라디칼 -O-NR-CH3- 을 지정한다 - [Seth at al., 2010, J. Org. Chem] .
일부 실시형태에서, LNA 단위는 하기 기로부터 선택된 구조를 가진다:
본 발명자들은 cET 화합물의 신장독성을 평가하고 (서열 (WO 2009/12495 의 화합물 ID 6/411847 및 비교용 베타-D-옥시 LNA 화합물 (WO 2009/12495 의 6/392063) 을 가지는 (S)-cET 를 사용함), cET 화합물이 놀랍게도 베타-D-옥시 LNA 대조군과 비교하여 높은 신장독성을 유발하는 것을 밝혀냈다. 상기 연구는 3 일 후 희생시킨 단일 투여량 연구였다 (비록 본 발명자들은 NMRI 마우스를 사용하였지만, EP 1984381 의 방법론에 대한 실시예 41 을 참조한다). 신장독성은 조직학 분석으로 확인되었다. 특히, 잘 알려져 있는 형혈 ALT 의 것들 이하의 cET 화합물의 투약량에서 본 발명자들이 관찰한 신경독성 징후는 cET 화합물에 대해 신경독성이 특정한 문제일 수 있는 것을 나타낸다. 그러므로, 본 발명의 컨쥬게이트, 예를 들면, 3가 GalNAc 컨쥬게이트의 사용은 LNA 화합물, 예를 들면, cET 화합물의 신경독성을 감소시키는데 상당히 유용하다.
따라서, 상기 올리고머는 천연 뉴클레오타이드 - 바람직하게는 2'-데옥시뉴클레오타이드 (본원에서 일반적으로 "DNA" 로서 언급됨) 뿐만 아니라, 가능하게는 리보뉴클레오타이드 (본원에서 일반적으로 "RNA" 로서 언급됨), 또는 이러한 천연 뉴클레오타이드 및 하나 이상의 비-천연 뉴클레오타이드, 즉, 뉴클레오타이드 유사체의 조합의 단순 서열을 포함하거나 이들로 이루어질 수 있다. 이러한 뉴클레오타이드 유사체는 적합하게는 표적 서열에 대한 올리고머의 친화성을 향상시킬 수 있다.
올리고머 내에 친화성-향상 뉴클레오타이드 유사체, 예를 들면, LNA 또는 2'-치환된 당의 도입은 특이적 결합 올리고머의 크기를 감소시킬 수 있고, 또한 비특이적 또는 일탈 결합이 일어나기 전에 올리고머의 크기에 대한 상한을 감소시킬 수 있다.
일부 실시형태에서, 상기 올리고머는 1 개 이상의 뉴클레오사이드 유사체를 포함한다. 일부 실시형태에서, 상기 올리고머는 2 개 이상의 뉴클레오타이드 유사체를 포함한다. 일부 실시형태에서, 상기 올리고머는 3-8 개의 뉴클레오타이드 유사체, 예를 들면, 6 개 또는 7 개의 뉴클레오타이드 유사체를 포함한다. 훨씬 가장 바람직한 실시형태에서, 상기 뉴클레오타이드 유사체의 하나 이상은 BNA, 예를 들면, 잠금 핵산 (LNA) 이고; 예를 들면, 상기 뉴클레오타이드 유사체의 3 개 이상 또는 4 개 이상 또는 5 개 이상 또는 6 개 이상 또는 7 개 이상 또는 8 개 이상은 BNA, 예를 들면, LNA 일 수 있다. 일부 실시형태에서, 모든 뉴클레오사이드 유사체는 BNA, 예를 들면, LNA 일 수 있다.
오로지 뉴클레오타이드만으로 이루어지는 바람직한 뉴클레오타이드 서열 모티프 또는 뉴클레오타이드 서열을 언급할 때, 서열에 의해 정의된 본 발명의 올리고머는 상기 서열에 존재하는 뉴클레오타이드 중 하나 이상 대신에 상응하는 뉴클레오타이드 유사체, 예를 들면, 올리고머/표적 이중체 (즉, 친화성 향상 뉴클레오타이드 유사체) 의 이중체 안정성/Tm 을 상승시키는 BNA 단위 또는 기타 뉴클레오타이드 유사체를 포함할 수 있는 것으로 인지할 것이다.
바람직한 뉴클레오타이드 유사체는 LNA, 예를 들면, 옥시-LNA (예를 들면, 베타-D-옥시-LNA 및 알파-L-옥시-LNA) 및/또는 아미노-LNA (예를 들면, 베타-D-아미노-LNA 및 알파-L-아미노-LNA) 및/또는 티오-LNA (예를 들면, 베타-D-티오-LNA 및 알파-L-티오-LNA) 및/또는 ENA (예를 들면, 베타-D-ENA 및 알파-L-ENA) 이다
일부 실시형태에서, 본 발명의 올리고머 내에 존재하는 추가의 클레오타이드 유사체는, 예를 들면, 2'-O-알킬-RNA 단위, 2'-아미노-DNA 단위, 2'-플루오로-DNA 단위, BNA 단위, 예를 들면, LNA 단위, 아라비노 핵산 (ANA) 단위, 2'-플루오로-ANA 단위, HNA 단위, INA (삽입형 핵산 - 참조로 본원에 도입되는 문헌 [Christensen, 2002. Nucl. Acids. Res. 2002 30: 4918-4925] 참조) 단위 및 2' MOE 단위로부터 독립적으로 선택된다. 일부 실시형태에서, 본 발명의 올리고머에 존재하는 상기 유형의 뉴클레오타이드 유사체 중 오직 하나, 예를 들면, 제 1 영역 또는 이의 인접 뉴클레오타이드 서열이 존재한다.
일부 실시형태에서, 추가의 뉴클레오타이드 유사체는 2'-O-메톡시에틸-RNA (2' MOE), 2'-플루오로-DNA 모노머 또는 LNA 뉴클레오타이드 유사체이고, 이와 같이 본 발명의 올리고뉴클레오타이드는 이들 3 개 유형의 유사체로부터 독립적으로 선택된 뉴클레오타이드 유사체를 포함할 수 있거나, 3 개 유형으로부터 선택된 유사체 중 오직 하나의 유형을 포함할 수 있다. 일부 실시형태에서, 상기 뉴클레오타이드 유사체 중 하나 이상은 2'-MOE-RNA, 예를 들면, 2 개, 3 개, 4 개, 5 개, 6 개, 7 개, 8 개, 9 개 또는 10 개의 2'-MOE-RNA 뉴클레오타이드 단위이다. 일부 실시형태에서, 상기 뉴클레오타이드 유사체 중 하나 이상은 2'-플루오로 DNA, 예를 들면, 2 개, 3 개, 4 개, 5 개, 6 개, 7 개, 8 개, 9 개 또는 10 개의 2'-플루오로 DNA 뉴클레오타이드 단위이다.
본 발명에 따른 올리고머는 하나 이상의 BNA, 예를 들면, 잠금 핵산 (LNA) 단위, 예를 들면, 1 개, 2 개, 3 개, 4 개, 5 개, 6 개, 7 개 또는 8 개의 BNA/LNA 단위, 예를 들면, 3-7 개 또는 4 내지 8 개의 BNA/LNA 단위, 또는 3 개, 4 개, 5 개, 6 개 또는 7 개의 BNA/LNA 단위를 포함한다. 일부 실시형태에서, 모든 뉴클레오타이드 유사체는 BNA, 예를 들면, LNA 이다. 일부 실시형태에서, 상기 올리고머는 베타-D-옥시-LNA 와, 티오-LNA, 아미노-LNA, 옥시-LNA 및/또는 ENA 와 같은 LNA 단위 중 하나 이상 둘 다를 베타-D 배치 또는 알파-L 배치 또는 이들의 조합으로 포함할 수 있다. 일부 실시형태에서, 모든 BNA, 예를 들면, LNA, 시토신 단위는 5'-메틸-시토신이다. 본 발명의 일부 실시형태에서, 상기 올리고머 (예를 들면, 제 1 영역 및 임의로 제 2 영역) 는 BNA 및 LNA 및 DNA 단위 둘 다를 포함할 수 있다. 일부 실시형태에서, LNA 및 DNA 단위의 조합된 총 수는 10-25 개, 예를 들면, 10-24 개, 바람직하게는 10-20 개, 예를 들면, 10-18 개, 예를 들면, 12-16 개이다. 본 발명의 일부 실시형태에서, 상기 올리고머 또는 이의 제 1 영역의 뉴클레오타이드 서열, 예를 들면, 인접 뉴클레오타이드 서열은 하나 이상의 BNA, 예를 들면, LNA 로 이루어지고, 나머지 뉴클레오타이드 단위는 DNA 단위이다. 일부 실시형태에서, 상기 올리고머 또는 이의 제 1 영역은 변형된 인터뉴클레오타이드 연결, 예를 들면, 포스포로티오에이트를 가지는, 오로지 BNA, 예를 들면, LNA, 뉴클레오타이드 유사체 및 천연 뉴클레오타이드 (예를 들면, RNA 또는 DNA, 가장 바람직하게는 DNA 뉴클레오타이드) 를 포함한다.
용어 "핵염기" 란, 뉴클레오타이드의 염기 모이어티를 의미하고 천연 뿐만 아니라 비-천연 변이체 둘 다를 포괄한다. 따라서, "핵염기" 란, 공지된 퓨린 및 피리미딘 헤테로사이클 뿐만 아니라 또한 이의 헤테로사이클릭 유사체 및 토토머도 포괄한다. 영역 B 의 DNA 또는 RNA 뉴클레오사이드는 천연 및/또는 비-천연 핵염기(들), 예를 들면, A, C, T 및 G 의 군, 또는 C, T 및 G 의 군으로부터 독립적으로 선택된 DNA 핵염기를 가질 수 있다는 것을 인식할 것이다.
핵염기의 예는 아데닌, 구아닌, 시토신, 티미딘, 우라실, 잔틴, 하이포잔틴, 5-메틸시토신, 이소시토신, 슈도이소시토신, 5-브로모우라실, 5-프로피닐우라실, 6-아미노퓨린, 2-아미노퓨린, 이노신, 디아미노퓨린 및 2-클로로-6-아미노퓨린을 포함하지만, 이들에 한정되는 것은 아니다. 일부 실시형태에서, 핵염기는 아데닌, 구아닌, 시토신, 티미딘, 우라실, 5-메틸시토신으로 이루어진 군으로부터 독립적으로 선택될 수 있다. 일부 실시형태에서, 핵염기는 아데닌, 구아닌, 시토신, 티미딘 및 5-메틸시토신으로 이루어진 군으로부터 독립적으로 선택될 수 있다.
일부 실시형태에서, 올리고머에 존재하는 핵염기 중 하나 이상은 5-메틸시토신, 이소시토신, 슈도이소시토신, 5-브로모우라실, 5-프로피닐우라실, 6-아미노퓨린, 2-아미노퓨린, 이노신, 디아미노퓨린 및 2-클로로-6-아미노퓨린으로 이루어진 군으로부터 선택되는 변형된 핵염기이다.
LNA
용어 "LNA" 란, C2*-C4* 바이라디칼 (브릿지) 을 포함하는 바이사이클릭 뉴클레오사이드 유사체를 의미하며, "잠금 핵산" 으로 공지되어 있다. 이것은 LNA 모노머를 의미할 수 있거나, "LNA 올리고뉴클레오타이드" 의 문맥에서 사용될 때, LNA 는 하나 이상의 이러한 바이사이클릭 뉴클레오타이드 유사체를 함유하는 올리고뉴클레오타이드를 의미한다. 일부 측면에서, 바이사이클릭 뉴클레오사이드 유사체는 LNA 뉴클레오타이드이고, 따라서, 이들 용어는 상호교환적으로 사용될 수 있으며, 이러한 실시형태에서, 둘 다는 리보오스 당 고리의 C2' 과 C4' 사이에 링커 기 (예를 들면, 브릿지) 의 존재를 특징으로 한다.
일부 실시형태에서, 본 발명의 올리고뉴클레오타이드 화합물에 사용되는 LNA 는 바람직하게는 하기 일반식 II 의 구조를 가진다:
여기서, Y 는 -O-, -CH2O-, -S-, -NH-, N(Re) 및/또는 -CH2- 로 이루어진 군으로부터 선택되고; Z 및 Z* 는 인터뉴클레오타이드 연결, RH, 말단기 또는 보호기 중에서 독립적으로 선택되고; B 는 천연 또는 비-천연 뉴클레오타이드 염기 모이어티 (핵염기) 를 구성하고, RH 는 수소 및 C1 -4-알킬로 이루어진 군으로부터 선택되고; Ra, Rb Rc, Rd 및 Re 는 임의로 독립적으로 수소, 임의로 치환된 C1 -12-알킬, 임의로 치환된 C2 -12-알케닐, 임의로 치환된 C2 -12-알키닐, 하이드록시, C1 -12-알콕시, C2 -12-알콕시알킬, C2 -12-알케닐옥시, 카복시, C112-알콕시카보닐, C1 -12-알킬카보닐, 포르밀, 아릴, 아릴옥시-카보닐, 아릴옥시, 아릴카보닐, 헤테로아릴, 헤테로아릴옥시-카보닐, 헤테로아릴옥시, 헤테로아릴카보닐, 아미노, 모노(C16-알킬)아미노 및 디(C16-알킬)아미노, 카바모일, 모노(C1 -6-알킬)-아미노-카보닐 및 디(C1 -6-알킬)-아미노-카보닐, 아미노-C1 -6-알킬-아미노카보닐, 모노(C1-6-알킬)아미노-C1 -6-알킬-아미노카보닐 및 디(C1-6-알킬)아미노-C1 -6-알킬-아미노카보닐, C16-알킬-카보닐아미노, 카바미도, C1 -6-알카노일옥시, 설포노, C1 -6-알킬설포닐옥시, 니트로, 아지도, 설파닐, C1 -6-알킬티오, 할로겐, DNA 삽입제, 광화학적 활성 기, 열화학적 활성 기, 킬레이트기, 리포터 기 및 리간드로 이루어진 군으로부터 선택되고, 여기서, 아릴 및 헤테로아릴은 임의로 치환될 수 있고, 2 개의 같은자리 치환기 Ra 및 Rb 는 함께 임의로 치환된 메틸렌 (=CH2) 을 나타낼 수 있고; RH 는 수소 및 C1 -4-알킬로 이루어진 군으로부터 선택된다. 일부 실시형태에서, Ra, Rb Rc, Rd 및 Re 는 임의로 독립적으로 수소 및 C1 -6 알킬, 예를 들면, 메틸로 이루어진 군으로부터 선택된다. 모든 키랄 중심에 대해, 비대칭 기는 R 또는 S 배향으로 발견될 수 있는데, 예를 들면, 2 개의 예시적 입체화학 이성질체는 베타-D 이소형 및 알파-L 이소형을 포함하며, 이것은 하기와 같이 도시될 수 있다:
특정한 예시적인 LNA 단위 하기와 같이 나타낸다:
용어 "티오-LNA" 는 상기 일반식 중의 Y 가 S 또는 -CH2-S- 로부터 선택된 잠금 뉴클레오타이드를 포함한다. 티오-LNA 는 베타-D 배치와 알파-L-배치 둘 다일 수 있다.
용어 "아미노-LNA" 는 상기 일반식 중의 Y 가 -N(H)-, N(R)-, CH2-N(H)- 및 -CH2-N(R)- 로부터 선택되는 잠금 뉴클레오타이드를 포함하고, 여기서, R 는 수소 및 C1-4-알킬로부터 선택된다 아미노-LNA 는 베타-D 배치와 알파-L-배치 둘 다일 수 있다.
용어 "옥시-LNA" 는 상기 일반식 중의 Y 가 -O- 를 나타내는 잠금 뉴클레오타이드를 포함한다. 옥시-LNA 는 베타-D 배치와 알파-L-배치 둘 다일 수 있다.
용어 "ENA" 는 상기 일반식 중의 Y 가 -CH2-O- (여기서, -CH2-O- 의 산소 원자는 염기 B 에 대해 2'-위치에 부착되어 있다) 인 잠금 뉴클레오타이드를 포함한다. Re 는 수소 또는 메틸이다.
일부 예시적인 실시형태에서, LNA 는 베타-D-옥시-LNA, 알파-L-옥시-LNA, 베타-D-아미노-LNA 및 베타-D-티오-LNA, 특히 베타-D-옥시-LNA 로부터 선택된다.
RNAse
동원
올리고머성 화합물은 표적 mRNA 의 비-RNase 매개된 분해를 통해, 예를 들면, 번역의 입체 장애 또는 다른 방법에 의해 작용할 수 있는 것을 인지한다. 일부 실시형태에서, 본 발명의 올리고머는 엔도리보뉴클레아제 (RNase), 예를 들면, RNase H 를 동원할 수 있다.
이러한 올리고머, 예를 들면, 영역 A 또는 인접 뉴클레오타이드 서열은, 상보적 표적 RNA 와 이중체로 형성될 때, RNase 를 동원할 수 있는, 7 개, 8 개, 9 개, 10 개, 11 개, 12 개, 13 개, 14 개, 15 개 또는 16 개의 연속 뉴클레오타이드를 비롯한, 6 개 이상, 예를 들면, 7 개 이상의 연속 뉴클레오타이드 단위, 예를 들면, 8 개 이상 또는 9 개 이상의 연속 뉴클레오타이드 단위 (잔기) 의 영역을 포함하는 것이 바람직하다. RNAse 를 동원할 수 있는 인접 서열은 본원에서 기재된 바와 같은 갭머의 문맥에서 언급되는 바와 같은 영역 Y' 일 수 있다. 일부 실시형태에서, RNAse 를 동원할 수 있는 인접 서열, 예를 들면, 영역 Y' 의 크기는 더 높을 수 있고, 예를 들면, 10 개, 11 개, 12 개, 13 개, 14 개, 15 개, 16 개, 17 개, 18 개, 19 개 또는 20 개의 뉴클레오타이드 단위일 수 있다.
EP 1 222 309 는 RNase H 를 동원하는 능력을 측정하는데 사용될 수 있는, RNase H 활성의 측정을 위한 시험관내 방법을 제공한다. 올리고머는, 상보적 RNA 표적과 함께 제공될 때, pmol/l/분으로 측정된 초기 속도를, EP 1 222 309 의 실시예 91-95 에 의해 제공되는 방법론을 사용하여, 올리고뉴클레오타이드에서 모든 모노머 사이의 포스포로티오에이트 연결 기를 가지고 2' 치환이 없는 동일한 염기 서열을 가지지만 DNA 모노머만을 함유하는 DNA 유일한 올리고뉴클레오타이드를 사용하여 측정된 상기 초기 속도의 1% 이상, 예를 들면, 5% 이상, 예를 들면, 10% 이상 또는 20% 초과로 가지는 경우. RNase H 를 동원할 수 있는 것으로 간주된다.
일부 실시형태에서, 올리고머는, 상보적 RNA 표적과 함께 제공될 때, pmol/l/분으로 측정된 R Nase H 의 초기 속도가, EP 1 222 309 의 실시예 91-95 에 의해 제공되는 방법론을 사용하여, 올리고뉴클레오타이드에서 모든 뉴클레오타이드 사이의 포스포로티오에이트 연결 기를 가지고 2' 치환이 없는 동등한 DNA 유일한 올리고뉴클레오타이드를 사용하여 측정된 상기 초기 속도의 1% 미만, 예를 들면, 5% 미만, 예를 들면, 10% 미만 또는 20% 미만인 경우, RNase H 를 본질적으로 동원할 수 없는 것으로 간주된다.
일부 실시형태에서, 올리고머는, 상보적 RNA 표적과 함께 제공될 때, pmol/l/분으로 측정된 R Nase H 의 초기 속도가, EP 1 222 309 의 실시예 91-95 에 의해 제공되는 방법론을 사용하여, 올리고뉴클레오타이드에서 모든 뉴클레오타이드 사이의 포스포로티오에이트 연결 기를 가지고 2' 치환이 없는 동등한 DNA 유일한 올리고뉴클레오타이드를 사용하여 측정된 상기 초기 속도의 20% 이상, 예를 들면, 40% 이상, 예를 들면, 60% 이상, 예를 들면, 80% 이상인 경우, RNase H 를 동원할 수 있는 것으로 간주된다.
전형적으로, 상보적 표적 RNA 와 이중체로 형성될 때, RNase 를 동원할 수 있는 연속 뉴클레오타이드 단위를 형성하는 올리고머의 영역은 RNA 표적과 함께 DNA/RNA 유사 이중체를 형성하는 뉴클레오타이드 단위로 이루어진다. 본 발명의 올리고머, 예를 들면, 제 1 영역은 뉴클레오타이드와 뉴클레오타이드 유사체 둘 다를 포함하는 뉴클레오타이드 서열을 포함할 수 있고, 예를 들면, 갭머, 헤드머 또는 믹스머의 형태일 수 있다.
"헤드머" 란, 영역 X' 의 3'-최대 모노머에 연결된 영역 Y' 의 5'-최대 모노머와 함께, 그곳에 인접한 영역 X' 및 영역 Y' 를 포함하는 올리고머로 정의한다. 영역 X' 는 비-RNase 동원 뉴클레오사이드 유사체의 인접 신장부 (stretch) 를 포함하고, 영역 Y' 는 RNase 에 의해 인식가능하고 절단가능한 DNA 모노머 또는 뉴클레오사이드 유사체 모노머의 인접 신장부 (예를 들면, 7 개 이상의 인접 모노머) 를 포함한다.
"테일머 (tailmer)" 란, 영역 X' 의 3'-최대 모노머에 연결된 영역 Y' 의 5'-최대 모노머와 함께, 그곳에 인접한 영역 X' 및 영역 Y' 를 포함하는 올리고머로 정의한다. 영역 X' 는 RNase 에 의해 인식가능하고 절단가능한 DNA 모노머 또는 뉴클레오사이드 유사체 모노머의 인접 신장부 (예를 들면, 7 개 이상의 인접 모노머) 를 포함하고, 영역 X' 는 비-RNase 동원 뉴클레오사이드 유사체의 인접 신장부를 포함한다.
"믹스머" 로 호칭되는 기타 "키메라" 올리고머는 (i) RNase 에 의해 인식가능하고 절단가능한 DNA 모노머 또는 뉴클레오사이드 유사체 모노머, 및 (ii) 비-RNase 동원 뉴클레오사이드 유사체 모노머의 교호 조성물로 이루어진다.
일부 실시형태에서, 표적 영역에 대한 올리고머의 친화성을 향상시키는 것에 추가하여, 일부 뉴클레오사이드 유사체는 또한 RNase (예를 들면, RNase H) 결합 및 절단을 매개한다. α-L-LNA (BNA) 모노머가 RNase H 활성을 특정 범위까지 동원하기 때문에, 일부 실시형태에서, α-L-LNA 모노머를 함유하는 올리고머의 갭 영역 (예를 들면, 본원에서 언급되는 영역 Y') 은 RNase H 에 의해 인식가능하고 절단가능한 더 적은 모노머로 이루어지고, 믹스머 작제물 내에 더 많은 유연성이 도입된다.
갭머
디자인
일부 실시형태에서, 본 발명의 올리고머, 예를 들면, 제 1 영역은 갭머를 포함하거나 갭머이다. 갭머 올리고머는 RNAse, 예를 들면, RNAseH 를 동원할 수 있는 뉴클레오타이드의 인접 신장부, 예를 들면, 본원에서 영역 Y' (Y') 로 언급되는 6 개 이상 또는 7 개 이상의 DNA 뉴클레오타이드의 영역을 포함하는 올리고머이고, 여기서, 영역 Y' 는 친화성 향상 뉴클레오타이드 유사체의 영역에 의해, 예를 들면, 1-6 개의 뉴클레오타이드 유사체 5' 및 3' 로부터 RNAse 를 동원할 수 있는 뉴클레오타이드의 인접 신장부까지, 5' 과 3' 둘 다의 측면에 배치되어 있다 - 이들 영역은 각각 영역 X' (X') 및 영역 Z' (Z') 로서 언급된다. 갭머의 예는 WO 2004/046160, WO 2008/113832 및 WO 2007/146511 에 기재되어 있다.
일부 실시형태에서, RNAse 를 동원할 수 있는 모노머는 DNA 모노머, 알파-L-LNA 모노머, C4' 알킬화 DNA 모노머 (본원에 참조로 도입되는, PCT/EP2009/050349 및 문헌 [Vester et al., Bioorg. Med. Chem. Lett. 18 (2008) 2296-2300] 참조) 및 UNA (비연결된 핵산) 뉴클레오타이드 (원에 참조로 도입되는 문헌 [Fluiter et al., Mol. Biosyst., 2009, 10, 1039] 참조) 로 이루어진 군으로부터 선택된다. UNA 는, 전형적으로 리보오스의 C2-C3 C-C 결합이 제거되어, 미잠금 "당" 잔기를 형성하는 미잠금 핵산이다. 바람직하게는 갭머는 식 (5' 내지 3'), X'-Y'-Z' 의 (폴리)뉴클레오타이드 서열을 포함하고, 여기서, 영역 X' (X') (5' 영역) 은 하나 이상의 뉴클레오타이드 유사체, 예를 들면, 하나 이상의 BNA (예를 들면, LNA) 단위, 예를 들면, 1-6 개의 뉴클레오타이드 유사체, 예를 들면, BNA (예를 들면, LNA) 단위로 이루어지거나, 이를 포함하고; 영역 Y' (Y') 는 RNAse 를 동원할 수 있는 5 개 이상의 연속 뉴클레오타이드 (상보적 RNA 분자, 예를 들면, mRNA 표적과 이중체로 형성될 때), 예를 들면, DNA 뉴클레오타이드로 이루어지거나, 이를 포함하고; 영역 Z' (Z') (3' 영역) 은 하나 이상의 뉴클레오타이드 유사체, 예를 들면, 하나 이상의 BNA (예를 들면, LNA 단위), 예를 들면, 1-6 개의 뉴클레오타이드 유사체, 예를 들면, BNA (예를 들면, LNA) 단위로 이루어지거나, 이를 포함한다.
일부 실시형태에서, 영역 X' 는 1 개, 2 개, 3 개, 4 개, 5 개 또는 6 개의 뉴클레오타이드 유사체, 예를 들면, BNA (예를 들면, LNA) 단위, 예를 들면, 2-5 개의 뉴클레오타이드 유사체, 예를 들면, 2-5 개의 LNA 단위, 예를 들면, 3 개 또는 4 개의 뉴클레오타이드 유사체, 예를 들면, 3 개 또는 4 개의 LNA 단위로 이루어지고/지거나; 영역 Z' 는 1 개, 2 개, 3 개, 4 개, 5 개 또는 6 개의 뉴클레오타이드 유사체, 예를 들면, BNA (예를 들면, LNA) 단위, 예를 들면, 2-5 개의 뉴클레오타이드 유사체, 예를 들면, 2-5 개의 BNA (예를 들면, LNA 단위), 예를 들면, 3 개 또는 4 개의 뉴클레오타이드 유사체, 예를 들면, 3 개 또는 4 개의 BNA (예를 들면, LNA) 단위로 이루어진다.
일부 실시형태에서, Y' 는 RNAse 를 동원할 수 있는 5 개, 6 개, 7 개, 8 개, 9 개, 10 개, 11 개 또는 12 개의 연속 뉴클레오사이드, 또는 RNAse 를 동원할 수 있는 6-10 개 또는 7-9 개, 예를 들면, 8 개의 연속 뉴클레오사이드로 이루어지거나, 이들을 포함한다. 일부 실시형태에서, 영역 Y' 는 하나 이상의 DNA 뉴클레오타이드 단위, 예를 들면, 1-12 개의 DNA 단위, 바람직하게는 4-12 개의 DNA 단위, 보다 바람직하게는 6-10 개의 DNA 단위, 예를 들면, 7-10 개의 DNA 단위, 가장 바람직하게는 8 개, 9 개 또는 10 개의 DNA 단위로 이루어지거나, 이들을 포함한다.
일부 실시형태에서, 영역 X' 는 3 개 또는 4 개의 뉴클레오타이드 유사체, 예를 들면, BNA (예를 들면, LNA) 로 이루어지고, 영역 X' 는 7 개, 8 개, 9 개 또는 10 개의 DNA 단위로 이루어지고, 영역 Z' 는 3 개 또는 4 개의 뉴클레오타이드 유사체, 예를 들면, BNA (예를 들면, LNA) 로 이루어진다. 이러한 디자인은 (X'-Y'-Z') 3-10-3, 3-10-4, 4-10-3, 3-9-3, 3-9-4, 4-9-3, 3-8-3, 3-8-4, 4-8-3, 3-7-3, 3-7-4, 4-7-3 을 포함한다.
추가의 갭머 디자인은 본원에 참조로 도입되는 WO 2004/046160 에 기재되어 있다. 본원에 참조로 도입되는 US 가출원 60/977,409 로부터 우선권을 주장하는 WO 2008/113832 는 '숏트머' 갭머 올리고머를 언급하고 있다. 일부 실시형태에서, 본원에 제시된 올리고머는 이러한 숏트머 갭머일 수 있다.
일부 실시형태에서, 올리고머, 예를 들면, 영역 X' 는 총 10 개, 11 개, 12 개, 13 개 또는 14 개의 뉴클레오타이드 단위의 인접 뉴클레오타이드 서열로 이루어지고, 여기서, 인접 뉴클레오타이드 서열은 식 (5'-3'), X'-Y'-Z' 이거나 이를 포함하고, 여기서, X' 는 1 개, 2 개 또는 3 개의 뉴클레오타이드 유사체 단위, 예를 들면, BNA (예를 들면, LNA) 단위로 이루어지고; Y' 는 상보적 RNA 분자 (예를 들면, mRNA 표적) 와 이중체로 형성될 때 RNAse 를 동원할 수 있는 7 개, 8 개 또는 9 개의 인접 뉴클레오타이드 단위로 이루어지고; Z' 는 1 개, 2 개 또는 3 개의 뉴클레오타이드 유사체 단위, 예를 들면, BNA (예를 들면, LNA) 단위로 이루어진다.
일부 실시형태에서, X' 는 1 개의 BNA (예를 들면, LNA) 단위로 이루어진다. 일부 실시형태에서, X' 는 2 개의 BNA (예를 들면, LNA) 단위로 이루어진다. 일부 실시형태에서, X' 는 3 개의 BNA (예를 들면, LNA) 단위로 이루어진다. 일부 실시형태에서, Z' 는 1 개의 BNA (예를 들면, LNA) 단위로 이루어진다. 일부 실시형태에서, Z' 는 2 개의 BNA (예를 들면, LNA) 단위로 이루어진다. 일부 실시형태에서, Z' 는 3 개의 BNA (예를 들면, LNA) 단위로 이루어진다. 일부 실시형태에서, Y' 는 7 개의 뉴클레오타이드 단위로 이루어진다. 일부 실시형태에서, Y' 는 8 개의 뉴클레오타이드 단위로 이루어진다. 일부 실시형태에서, Y' 는 9 개의 뉴클레오타이드 단위로 이루어진다. 특정 실시형태에서, 영역 Y' 는 10 개의 뉴클레오사이드 모노머로 이루어진다. 특정 실시형태에서, 영역 Y' 는 1-10 개의 DNA 모노머로 이루어지거나, 이를 포함한다. 일부 실시형태에서, Y' 는 1-9 개의 DNA 단위, 예를 들면, 2 개, 3 개, 4 개, 5 개, 6 개, 7 개, 8 개 또는 9 개의 DNA 단위를 포함한다. 일부 실시형태에서, Y' 는 DNA 단위로 이루어진다. 일부 실시형태에서, Y' 는 알파-L-배치로 존재하는 하나 이상의 BNA 단위, 예를 들면, 알파-L-배치에서 2 개, 3 개, 4 개, 5 개, 6 개, 7 개, 8 개 또는 9 개의 LNA 단위를 포함한다. 일부 실시형태에서, Y' 는 하나 이상의 알파-L-옥시 BNA/LNA 단위를 포함하거나, 알파-L-배치의 모든 LNA 단위는 알파-L-옥시 LNA 단위이다. 일부 실시형태에서, X'-Y'-Z' 에 존재하는 뉴클레오사이드의 수는 다음 (뉴클레오타이드 유사체 단위 - 영역 Y' - 뉴클레오타이드 유사체 단위) 으로 이루어진 군으로부터 선택된다: 1-8-1, 1-8-2, 2-8-1, 2-8-2, 3-8-3, 2-8-3, 3-8-2, 4-8-1, 4-8-2, 1-8-4, 2-8-4; 또는 1-9-1, 1-9-2, 2-9-1, 2-9-2, 2-9-3, 3-9-2, 1-9-3, 3-9-1, 4-9-1, 1-9-4; 또는 1-10-1, 1-10-2, 2-10-1, 2-10-2, 1-10-3, 3-10-1. 일부 실시형태에서, X'-Y'-Z' 중 뉴클레오사이드의 수는 다음으로 이루어진 군으로부터 선택된다: 2-7-1, 1-7-2, 2-7-2, 3-7-3, 2-7-3, 3-7-2, 3-7-4 및 4-7-3. 특정 실시형태에서, 영역 X' 및 영역 Y' 의 각각은 3 개의 BNA (예를 들면, LNA) 모노머로 이루어지고, 영역 Y' 는 8 개 또는 9 개 또는 10 개의 뉴클레오사이드 모노머, 바람직하게는 DNA 모노머로 이루어진다. 일부 실시형태에서, 영역 X' 와 영역 Z' 둘 다는 2 개의 BNA (예를 들면, LNA) 단위 각각으로 이루어지고, Y' 는 8 개 또는 9 개의 뉴클레오타이드 단위, 바람직하게는 DNA 단위로 이루어진다. 각종 실시형태에서, 기타 갭머 디자인은 영역 X' 및/또는 영역 Z' 가 3 개, 4 개, 5 개 또는 6 개의 뉴클레오사이드 유사체, 예를 들면, 2'-O-메톡시에틸-리보오스 당 (2'-MOE) 을 함유하는 모노머 또는 2'-플루오로-데옥시리보오스 당을 함유하는 모노머로 이루어지고 영역 Y' 가 8 개, 9 개, 10 개, 11 개 또는 12 개의 뉴클레오사이드, 예를 들면, DNA 모노머로 이루어진 것들을 포함하고, 여기서, 영역 X'-Y'-Z' 는 3-9-3, 3-10-3, 5-10-5 또는 4-12-4 모노머를 가진다. 추가의 갭머 디자인은 본원에 참조로 도입되는 WO 2007/146511A2 에 기재되어 있다.
BNA 및 LNA 갭머: 용어 BNA 및 LNA 는 상호교환적으로 사용된다. BNA 갭머는 하나 이상의 BNA 뉴클레오타이드를 포함하는 갭머 올리고머 (영역 A) 이다. LNA 갭머는 하나 이상의 LNA 뉴클레오타이드를 포함하는 갭머 올리고머 (영역 A) 이다.
스플라이스
스위칭
올리고머
(
Splice
switching
oligomers
)
일부 실시형태에서, 안티센스 올리고뉴클레오타이드는 스플라이스 스위칭 올리고머 - 즉, pre-mRNA 의 대체 스플라이싱을 야기하는 pre-mRNA 를 표적화하는 올리고머이다.
스플라이스 스위칭 올리고머에 대한 표적은 TNF 수용체를 포함할 수 있고, 예를 들면, SSO 는 본원에 참조로 도입되는 WO 2007/058894, WO 08051306 A1 및 PCT/EP2007/061211 에 기재된 TNFR SSO 중 하나 이상일 수 있다.
스플라이스 스위칭 올리고머는 RNase H 를 전형적으로 (본질적으로) 동원할 수 없고, 이와 같이 갭머, 테일머 또는 헤드머 디자인은 일반적으로 바람직하지 않다. 그러나, 믹스머 및 토탈머 디자인은 SSO 에 적합한 디자인이다.
스플라이스 스위칭 올리고머는 또한 뒤시엔느 근위축증에서 디스트로핀 결핍을 표적화하는데 사용되었다.
믹스머
대부분의 안티센스 올리고뉴클레오타이드는 의도된 표적을 분해하기 위한 RNase 효소 (예를 들면, RNase H) 를 동원하기 위해 디자인된 화합물이다. 이러한 화합물은 DNA 포스포로티오에이트 올리고뉴클레오타이드 및 갭머, 헤드머 및 테일머를 포함한다. 전형적으로, 이들 화합물은 5 개 또는 6 개의 DNA 뉴클레오타이드의 영역을 포함하고, 갭머의 경우, 친화성 향상 뉴클레오타이드 유사체에 의해 어느 한 쪽의 측면 상에 위치한다.
본 발명의 올리고머는 RNase (예를 들면, RNase H) 비의존성 메카니즘을 통해 작동할 수 있다. 비-RNase H (또는 비-RNase) 메카니즘을 통해 작동하는 올리고머의 예는 믹스머 및 토탈머이다.
용어 '믹스머' 란, 갭머, 테일머 및 헤드머와 반대로, 5 개 초과의 인접 서열이 없고, 일부 실시형태에서, 4 개 이하의 연속 천연 뉴클레오타이드, 예를 들면, 3 개 이하의 연속 천연 뉴클레오타이드, 예를 들면, DNA 단위인 천연 뉴클레오타이드와 비-천연 뉴클레오타이드 둘 다를 포함하는 올리고머를 의미한다. 일부 실시형태에서, 믹스머는 5 개 초과의 연속 뉴클레오사이드 유사체, 예를 들면, BNA (LNA) 를 포함하지 않으며, 일부 실시형태에서, 4 개 이하의 연속 뉴클레오사이드 유사체, 예를 들면, 3 개 이하의 연속 뉴클레오사이드 유사체, 예를 들면, BNA (LNA) 를 포함한다. 이러한 믹스머에서, 나머지 뉴클레오사이드는, 예를 들면, DNA 뉴클레오사이드 및/또는 비-바이사이클릭 뉴클레오사이드 유사체, 예를 들면, 본원에 언급된 것들, 예를 들면, 2' 치환된 뉴클레오사이드 유사체, 예를 들면, 2'-O-MOE 및/또는 2'-플루오로일 수 있다.
본 발명에 따른 올리고머는 믹스머일 수 있다 - 실제로 각종 믹스머 디자인은, 특히 mRNA (Blockmir) 상의 microRNA 결합 부위 또는 스플라이스 스위칭 올리고머 (SSO) 로서, microRNA (antimiR) 를 표적화할 때, 올리고머 또는 이의 제 1 영역으로서 상당히 효과적이다. 예를 들면, WO 2007/112754 (LNA-AntimiRsTM), WO 2008/131807 (LNA 스플라이스 스위칭 올리고머) 를 참조한다.
일부 실시형태에서, 상기 올리고머 또는 믹스머는, DNA 뉴클레오사이드를 임의로 가지는, BNA 및 2' 치환된 뉴클레오사이드 유사체로 구성될 수 있다 - 예를 들면, 본원에 참조로 도입되는 WO 07027894 및 WO 2007/112754 를 참조한다. 특정 예는 LNA, 2'-O-MOE 및 DNA, LNA, 2'-플루오로 및 2'-O-MOE, 2'-O-MOE 및 2'-플루오로, 2'-O-MOE 및 2'-플루오로 및 LNA, 또는 LNA 및 2'-O-MOE 및 LNA 및 DNA 를 포함하는 올리고머 또는 제 1 영역을 포함한다.
일부 실시형태에서, 올리고머 또는 믹스머는 뉴클레오타이드 유사체 및 천연 뉴클레오타이드, 또는 뉴클레오타이드 유사체의 하나의 유형 및 뉴클레오타이드 유사체의 두번째 유형의 반복 패턴의 인접 뉴클레오타이드 서열을 포함하거나, 이들로 이루어진다. 반복 패턴은, 예를 들면, 예를 들면, 매 두번째 또는 매 세번째 뉴클레오타이드 또는 뉴클레오타이드 유사체, 예를 들면, BNA (LNA) 이고, 나머지 뉴클레오타이드는 천연 뉴클레오타이드, 예를 들면, DNA 이거나, 2'-치환된 뉴클레오타이드 유사체, 예를 들면, 본원에서 언급된 2'-플루오로 유사체의 2' MOE 이거나, 일부 실시형태에서, 본원에서 언급된 뉴클레오타이드 유사체의 군으로부터 선택된다. 뉴클레오타이드 유사체, 예를 들면, LNA 단위의 반복 패턴은 고정 위치에서 - 예를 들면, 5' 또는 3' 말단에서 - 뉴클레오타이드 유사체와 조합될 수 있는 것으로 인식된다.
일부 실시형태에서, 3' 말단으로부터 계산되는 올리고머 또는 믹스머의 첫번째 뉴클레오타이드는, 뉴클레오타이드 유사체, 예를 들면, LNA 뉴클레오타이드이다.
동일하거나 상이할 수 있는 일부 실시형태에서, 3' 말단으로부터 계산되는 올리고머 또는 믹스머의 두번째 뉴클레오타이드는 뉴클레오타이드 유사체, 예를 들면, LNA 뉴클레오타이드이다.
동일하거나 상이할 수 있는 일부 실시형태에서, 3' 말단으로부터 계산되는 상기 올리고머 또는 믹스머의 일곱번째 및/또는 여덟번째 뉴클레오타이드, 동일하거나 상이할 수 있는 일부 실시형태에서, 3' 말단으로부터 계산되는 상기 올리고머 또는 믹스머의 아홉번째 및/또는 열번째 뉴클레오사이드는, 뉴클레오타이드 유사체, 예를 들면, LNA 뉴클레오사이드이다.
동일하거나 상이할 수 있는 일부 실시형태에서, 올리고머 또는 믹스머의 5' 말단은 뉴클레오타이드 유사체, 예를 들면, LNA 뉴클레오타이드이다.
상기 디자인 특징은, 일부 실시형태에서, 믹스머 디자인, 예를 들면, antimiR 믹스머 내로 도입될 수 있다
일부 실시형태에서, 올리고머 또는 믹스머는 4 개 초과의 연속 DNA 뉴클레오타이드 단위 또는 3 개의 연속 DNA 뉴클레오타이드 단위의 영역을 포함하지 않는다. 일부 실시형태에서, 믹스머는 2 개 초과의 연속 DNA 뉴클레오타이드 단위의 영역을 포함하지 않는다.
일부 실시형태에서, 올리고머 또는 믹스머는 2 개 이상의 연속 뉴클레오타이드 유사체 단위, 예를 들면, 2 개 이상의 연속 LNA 단위로 이루어진 영역을 적어도 포함한다.
일부 실시형태에서, 올리고머 또는 믹스머는 3 개 이상의 연속 뉴클레오타이드 유사체 단위, 예를 들면, 3 개 이상의 연속 LNA 단위로 이루어진 영역을 적어도 포함한다.
일부 실시형태에서, 본 발명의 올리고머 또는 믹스머는 7 개 초과의 연속 뉴클레오타이드 유사체 단위, 예를 들면, LNA 단위의 영역을 포함하지 않는다. 일부 실시형태에서, 본 발명의 올리고머 또는 믹스머는 6 개 초과의 연속 뉴클레오타이드 유사체 단위, 예를 들면, LNA 단위의 영역을 포함하지 않는다. 일부 실시형태에서, 본 발명의 올리고머 또는 믹스머는 5 개 초과의 연속 뉴클레오타이드 유사체 단위, 예를 들면, LNA 단위의 영역을 포함하지 않는다. 일부 실시형태에서, 본 발명의 올리고머 또는 믹스머는 4 개 초과의 연속 뉴클레오타이드 유사체 단위, 예를 들면, LNA 단위의 영역을 포함하지 않는다. 일부 실시형태에서, 본 발명의 올리고머 또는 믹스머는 3 개 초과의 연속 뉴클레오타이드 유사체 단위, 예를 들면, LNA 단위의 영역을 포함하지 않는다. 일부 실시형태에서, 본 발명의 올리고머 또는 믹스머는 2 개 초과의 연속 뉴클레오타이드 유사체 단위, 예를 들면, LNA 단위의 영역을 포함하지 않는다.
하기 실시형태는 믹스머 또는 토탈머 올리고머 (예를 들면, 영역 A) 에 적용될 수 있다:
본 발명의 올리고머 (예를 들면, 영역 A) 는, 일부 실시형태에서, LNA 및 비-LNA 뉴클레오타이드 (예를 들면, DNA 또는 2' 치환된 뉴클레오타이드 유사체) 의 2 개 이상의 교호 영역을 포함할 수 있다.
본 발명의 올리고머는, 일부 실시형태에서, 식 5' ([LNA 뉴클레오사이드]1-5 및 [비-LNA 뉴클레오사이드]1-4)2-12. 3' 의 인접 서열을 포함한다.
일부 실시형태에서, 인접 뉴클레오타이드 서열 (또는 올리고머) 의 5' 뉴클레오타이드는 LNA 뉴클레오타이드를 가진다.
일부 실시형태에서, 인접 뉴클레오타이드 서열의 3' 뉴클레오타이드는 뉴클레오타이드 유사체, 예를 들면, LNA 이거나, 2 개, 3 개, 4 개, 5 개의 3' 뉴클레오사이드는 뉴클레오타이드 유사체, 예를 들면, LNA 뉴클레오사이드, 또는 올리고머에 향상된 혈청 안정성을 부여하는 기타 뉴클레오타이드 유사체이다.
일부 실시형태에서, 올리고머의 인접 뉴클레오타이드 서열은 식 5' ([LNA 뉴클레오사이드]1-5 - [비-LNA 뉴클레오사이드]1-4)2-11 - [LNA 뉴클레오사이드]1-5 3' 을 가진다.
일부 실시형태에서, 올리고머의 인접 뉴클레오타이드 서열은 LNA 및 비-LNA 뉴클레오사이드의 2 개, 3 개 또는 4 개의 인접 영역을 가진다 - 예를 들면, 추가의 3' LNA 영역 [LNA 뉴클레오사이드]1-5 를 임의로 가지는, 식 5' ([LNA 뉴클레오사이드]1-5 및 [비-LNA 뉴클레오사이드]1-4)2- 3 를 포함한다.
일부 실시형태에서, 올리고머의 인접 뉴클레오타이드 서열은 추가의 3' LNA 영역 [LNA 뉴클레오사이드]1-3 를 임의로 가지는, 5' ([LNA 뉴클레오사이드]1-3 및 [비-LNA 뉴클레오사이드]1-3)2- 5 를 포함한다.
일부 실시형태에서, 올리고머의 인접 뉴클레오타이드 서열은 추가의 3' LNA 영역 [LNA 뉴클레오사이드]1-3 를 임의로 가지는, 5' ([LNA 뉴클레오타이드]1-3 및 [비-LNA 뉴클레오사이드]1-3)3 를 포함한다.
일부 실시형태에서, 비-LNA 뉴클레오사이드는 모두 DNA 뉴클레오사이드이다.
일부 실시형태에서, 비-LNA 뉴클레오사이드는 DNA 단위, RNA 단위, 2'-O-알킬-RNA 단위, 2'-OMe-RNA 단위, 2'-아미노-DNA 단위 및 2'-플루오로-DNA 단위로 이루어진 군으로부터 독립적으로 또는 의존적으로 선택된다.
일부 실시형태에서, 비-LNA 뉴클레오타이드는 2' 치환된 뉴클레오사이드 유사체로 이루어진 군으로부터 (임의로 독립적으로) 선택되고, 예를 들면, 2'-O-알킬-RNA 단위, 2'-OMe-RNA 단위, 2'-아미노-DNA 단위, 2'-AP, 2'-FANA, 2'-(3-하이드록시)프로필 및 2'-플루오로-DNA 단위, 및/또는 기타 (임의로) 당 변형된 뉴클레오사이드 유사체, 예를 들면, 모르폴리노, 펩타이드 핵산 (PNA), CeNA, 비연결된 핵산 (UNA), 헥시톨 핵산 (HNA). 바이사이클로-HNA 로 이루어진 군으로부터 (임의로 독립적으로) 선택된다 (예를 들면, WO 2009/100320 참조). 일부 실시형태에서, 뉴클레오사이드 유사체는 이의 표적 핵산 (또는 상보적 DNA 또는 RNA 서열) 에 대한 제 1 영역의 친화성을 증가시킨다. 각종 뉴클레오사이드 유사체는 본원에 참조로 도입되는 문헌 [Freier & Altmann; Nucl . Acid Res ., 1997, 25, 4429-4443; 및 Uhlmann; Curr . Opinion in Drug Development, 2000, 3(2), 293-213] 에 개시되어 있다.
일부 실시형태에서, 비-LNA 뉴클레오타이드는 모두 DNA 뉴클레오타이드이다. 일부 실시형태에서, 상기 올리고머 또는 인접 뉴클레오타이드 서열은 친화성 향상 뉴클레오타이드 유사체 및/또는 혈청 안정성을 향상시키는 뉴클레오타이드 유사체일 수 있는 LNA 뉴클레오사이드 및 임의로 기타 뉴클레오타이드 유사체 (예를 들면, 비-LNA 뉴클레오사이드 하에 열거된 뉴클레오타이드 유사체) 를 포함한다.
일부 실시형태에서, 상기 올리고머 또는 이의 인접 뉴클레오타이드 서열은 상기 뉴클레오타이드 유사체의 인접 뉴클레오타이드 서열로 이루어진다.
일부 실시형태에서, 상기 올리고머 또는 이의 인접 뉴클레오타이드 서열은 LNA 뉴클레오타이드의 인접 뉴클레오타이드 서열로 이루어진다.
일부 실시형태에서, 상기 올리고머 또는 인접 뉴클레오타이드 서열은 8-12 nts, 예를 들면, 8-10 nts, 또는 10-20 nts, 예를 들면, 12-18 nts 또는 14-16 nts 의 길이이다.
일부 실시형태에서, 상기 올리고머 또는 인접 뉴클레오타이드 서열은 상보적 단일 가닥의 RNA 핵산 분자와 포스포디에스테르 인터뉴클레오사이드 연결과 함께 이중체를 형성할 수 있고, 여기서, 이중체는 약 60℃ 이상, 예를 들면, 65℃ 이상의 Tm 을 가진다.
Tm 어세이의 예: 올리고뉴클레오타이드: 올리고뉴클레오타이드 및 RNA 표적 (PO) 이중체를 500 ml 의 RNase-무함유 물로 3 mM 까지 희석하고, 500 ml 2x Tm-버퍼 (200mM NaCl, 0.2mM EDTA, 20mM Na 포스페이트, pH 7.0) 과 혼합한다. 용액을 95℃ 로 3 분 동안 가열한 후, 실온에서 30 분 동안 어닐링 (anneal) 한다. 이중체 용융 온도 (Tm) 는 PE Templab 소프트웨어를 사용하는 Peltier 온도 프로그래머 PTP6 이 구비된 Lambda 40 UV/VIS Spectrophotometer (Perkin Elmer) 상에서 측정한다. 온도를 20℃ 에서 95℃ 로 상승시킨 후, 25℃ 로 하강시키고, 260 nm 에서의 흡광도를 기록한다. 첫번째 유도체, 및 용융과 어닐링 둘 다의 극대값을 사용하여 이중체 Tm 을 평가한다.
토탈머
토탈머는 비-천연 뉴클레오사이드, 예를 들면, 당-변형된 뉴클레오사이드 유사체 만을 포함하는 단일 가닥의 올리고머이다.
본 발명에 따른 제 1 영역은 토탈머일 수 있다 - 실제로 각종 토탈머 디자인은, 예를 들면, 특히 스플라이스 스위칭 올리고머 (SSO) 로서 microRNA (antimiR) 를 표적화할 때, 올리고머 또는 이의 제 1 영역으로서 상당히 효과적이다. 일부 실시형태에서, 토탈머는 하나 이상의 XYX 또는 YXY 서열 모티프, 예를 들면, 반복 서열 XYX 또는 YXY 를 포함하거나 이들로 이루어지고, 여기서, X 는 LNA 이고, Y 는 대체 (즉, 비-LNA) 뉴클레오타이드 유사체, 예를 들면, 2'-O-MOE RNA 단위 및 2'-플루오로 DNA 단위이다. 상기 서열 모티프는, 일부 실시형태에서, 예를 들면, XXY, XYX, YXY 또는 YYX 일 수 있다.
일부 실시형태에서, 상기 토탈머는 7 개와 16 개 사이의 뉴클레오사이드, 예를 들면, 9 개, 10 개, 11 개, 12 개, 13 개, 14 개 또는 15 개의 뉴클레오사이드, 예를 들면, 7 개와 12 개 사이의 뉴클레오사이드의 인접 뉴클레오타이드 서열을 포함하거나 이들로 이루어질 수 있다.
일부 실시형태에서, 토탈머의 인접 뉴클레오타이드 서열은 30% 이상, 예를 들면, 40% 이상, 예를 들면, 50% 이상, 예를 들면, 60% 이상, 예를 들면, 70% 이상, 예를 들면, 80% 이상, 예를 들면, 90% 이상, 예를 들면, 95% 이상,예를 들면, 100% 의 BNA (LNA) 단위를 포함한다. 나머지 단위는 2'-O-알킬-RNA 단위, 2'-OMe-RNA 단위, 2'-아미노-DNA 단위, 2'-플루오로-DNA 단위, LNA 단위, PNA 단위, HNA 단위, INA 단위 및 2' MOE RNA 단위로 이루어진 군, 또는 2'-OMe RNA 단위 및 2'-플루오로 DNA 단위로 이루어진 군으로부터 선택된 것들과 같은 본원에서 언급되는 비-LNA 뉴클레오타이드 유사체로부터 선택될 수 있다.
일부 실시형태에서, 토탈머는 LNA 단위만으로 이루어진 인접 뉴클레오타이드 서열을 포함하거나 이들로 이루어진다. 일부 실시형태에서, 토탈머, 예를 들면, LNA 토탈머는 7-12 개 사이의 뉴클레오사이드 단위의 길이이다. 일부 실시형태에서, 토탈머 (올리고머 또는 이의 제 1 영역) 는 본원에 참조로 도입되는 WO 2009/043353 에 언급되는 바와 같이 microRNA (즉, antimiR) 에 대해 표적화될 수 있다.
일부 실시형태에서, 상기 올리고머 또는 인접 뉴클레오타이드 서열은 친화성 향상 뉴클레오타이드 유사체 및/또는 혈청 안정성을 향상시키는 뉴클레오타이드 유사체일 수 있는 LNA 뉴클레오타이드 및 임의로 기타 뉴클레오타이드 유사체를 포함한다.
일부 실시형태에서, 상기 올리고머 또는 이의 인접 뉴클레오타이드 서열은 상기 뉴클레오타이드 유사체의 인접 뉴클레오타이드 서열로 이루어진다.
일부 실시형태에서, 상기 올리고머 또는 이의 인접 뉴클레오타이드 서열은 LNA 뉴클레오타이드의 인접 뉴클레오타이드 서열로 이루어진다.
본 발명의
올리고머를
통한
microRNA
조절
일부 실시형태에서, 상기 올리고머 또는 이의 제 1 영역은 microRNA 서열, 예를 들면, 성숙 microRNA 또는 이의 일부에 상응하거나 완전히 상보적인 인접 뉴클레오타이드 서열을 포함하거나 이들로 이루어지는 올리고머, 예를 들면, LNA-antimiR® (LNA 믹스머 또는 토탈머) 이다. microRNA 의 생체내 활성을 조절하는데 있어서의 본 발명의 용도는 microRNA 가 전형적으로 피험자에서의 수많은 mRNA 를 조절한다는 사실로 인해 일차적으로 중요한 것으로 간주된다. 그러므로, 치료적 antimiR 를 불활성화시키는 능력은 매우 바람직하다.
수많은 microRNA 는 다수의 질환과 관련되어 있다 - 예를 들면, WO 2009/043353 참조. 상기 올리고머는, 일부 실시형태에서, microRNA (이의 상응하는 영역) 에 완전히 상보적인 인접 뉴클레오타이드 서열을 표적화한다 (즉, 이들을 포함하거나 이들로 이루어진다). microRNA 는 간 발현 microRNA, 예를 들면, microRNA-21, microRNA-221, miR-122 또는 miR-33 (miR33a & miR-33b) 일 수 있다.
그러므로, 본 발명의 일부 측면은 microRNA 의 발현과 연관되는 질환의 치료에 관한 것이다. 일부 실시형태에서, 본 발명에 따른 올리고머 또는 이의 제 1 영역은 microRNA 서열, 예를 들면, 성숙 microRNA, 예를 들면, miRBase 에 공개된 인간 microRNA 에 상응하거나 완전히 상보적인 인접 뉴클레오타이드 서열을 포함하거나 이들로 이루어진다 (http://microrna.sanger.ac.uk/cgi-bin/sequences/mirna_summary.pl?org=hsa). 일부 실시형태에서, microRNA 는 바이러스 microRNA 이다. 본 명세서의 작성 시점에서, miRbase 19 에는, 각각의 인간 microRNA 의 성숙 microRNA 서열을 비롯한, 모두 본원에 참조로 도입되는 miRBase 에서 1600 개의 전구체 및 2042 개의 성숙 인간 miRNA 서열이 존재한다. 일부 실시형태에서, 본 발명에 따른 올리고머는, hsa-miR122 (NR_029667.1 GI:262205241), 예를 들면, 성숙 has-miR-122 에 상응하거나 이에 완전히 상보적인 인접 뉴클레오타이드 서열로 이루어지거나 이를 포함한다. 일부 실시형태에서, 본 발명에 따른 올리고머는, hsa-miR122 (NR_029667.1 GI:262205241), 예를 들면, 올리고머의 길이를 통해 성숙 has-miR-122 에 상응하거나 이에 완전히 상보적인 인접 뉴클레오타이드 서열로 이루어지거나 이를 포함한다.
일부 실시형태에서, 올리고머 또는 이의 제 1 영역이 miR-122 를 표적화할 때, 올리고머는 C 형 간염 감염의 치료에 사용되기 위한 것이다.
일부 실시형태에서, 상기 올리고머는, 예를 들면,대사성 질환, 예를 들면, 대사성 증후군, 죽상동맥경화증, 고콜레스테롤혈증 및 관련 장애의 치료에서 사용하기 위해 has-miR-33, 예를 들면, has-miR-33a (GUGCAUUGUAGUUGCAUUGCA ) 또는 has-miR-33b (GUGCAUUGCUGUUGCAUUGC) 를 표적화한다. 문헌 [Najafi-Shoushtar et al., Science 328 1566-1569; Rayner et al., Science 328 (1570-1573); Horie et al., J Am Heart Assoc. 2012, Dec 1(6)] 을 참조한다. 대사성 질환에서 나타나는 기타 간 발현 microRNA 는 콜레스테롤 유출을 직접 조절하는 것으로 공지되어 있는, miR-758, miR-10b, miR-26 및 miR-106b 를 포함한다 (문헌 [Davalos & Fernandez-Hernando, Pharmacol Res. 2013 Feb] 참조) 그러므로, 표적은 miR-122 (MIMAT0004590), miR-33 (MIMAT0000091, MIMAT0003301), miR-758 (MIMAT0003879), miR-10b (MIPF0000033), miR-26a (MIMAT0000082) 및 miR-106b (MIMAT0004672) 로 이루어진 군으로부터 선택된 microRNA 일 수 있다. microRNA 기준은 miRBase release 19 이다.
AntimiR
올리고머
바람직한 올리고머 또는 이의 제 1 영역 'antimiR' 디자인 및 올리고머는 모두 본원에 참조로 도입되는 WO 2007/112754, WO 2007/112753, PCT/DK2008/000344 및 US 가출원 60/979217 및 61/028062 에 개시되어 있다. 일부 실시형태에서, 올리고머 또는 이의 제 1 영역은 믹스머 또는 토탈머인 antimiR 이다. 그러므로, 용어 AntimiR 는 용어 올리고머로 대체될 수 있다.
AntimiR 올리고머는 microRNA 서열 또는 이의 상응하는 서브-서열에 완전히 상보적이거나, 본질적으로 상보적인 (즉, 1 개 또는 2 개의 불일치를 포함할 수 있는) 인접 뉴클레오타이드 서열로 이루어지거나 이를 포함하는 올리고머이다. 이와 관련하여, antimiR 은 전체 성숙 microRNA 에 상보적이거나 본질적으로 상보적인 인접 뉴클레오타이드 서열을 포함할 수 있거나, antimiR 은 성숙 microRNA 또는 전-microRNA 의 하위 서열에 상보적이거나 본질적으로 상보적인 인접 뉴클레오타이드 서열을 포함할 수 있다 - 이러한 하위 서열 (따라서, 상응하는 인접 뉴클레오타이드 서열) 은 전형적으로 8 개 이상의 길이의 뉴클레오타이드, 예를 들면, 8 개와 25 개 사이의 뉴클레오타이드, 예를 들면, 9 개, 10 개, 11 개, 12 개, 13 개, 14 개, 15 개, 16 개, 17 개, 18 개, 19 개, 20 개, 21 개, 22 개, 23 개, 24 개 길이의 뉴클레오타이드, 예를 들면, 10-17 개 사이 또는 10-16 개 사이의 뉴클레오타이드, 예를 들면, 12-15 개 사이의 뉴클레오타이드인 것으로 고려된다.
수많은 디자인의 AntimiR 가 제안되었고, 전형적으로 치료적 용도를 위한 antimiR, 예를 들면, 이의 인접 뉴클레오타이드 서열은 하나 이상의 뉴클레오타이드 유사체 단위를 포함한다.
일부 실시형태에서, antimiR 은 본원에서 기재된 바와 같은 갭머 구조를 가질 수 있다. 그러나, WO 2007/112754 및 WO 2007/112753 에서 설명되는 바와 같이, 기타 디자인, 예를 들면, 믹스머 또는 토탈머가 바람직할 수 있다.
둘 다 참조로 본원에 도입되는 WO 2007/112754 및 WO 2007/112753 은, 올리고머가 성숙 microRNA 에 상보적인 antimiR 올리고머 및 antimiR 올리고머 디자인을 제공한다.
일부 실시형태에서, antimiR 의 하위 서열은 miRNA 시드 영역 (seed region) 에 상응한다. 일부 실시형태에서, 올리고머의 첫번째 또는 두번째 3' 핵염기는 microRNA 서열의 두번째 5' 뉴클레오타이드에 상응한다.
일부 antimiR 실시형태에서, 올리고머의 영역 3' 말단으로부터 측정된 올리고머의 핵염기 단위 1 내지 6 (포함) 은 microRNA 시드 영역 서열에 상보적이다.
일부 antimiR 실시형태에서, 올리고머의 영역 3' 말단으로부터 측정된 올리고머의 핵염기 단위 1 내지 7 (포함) 은 microRNA 시드 영역 서열에 상보적이다.
일부 antimiR 실시형태에서, 올리고머의 영역 3' 말단으로부터 측정된 올리고머의 핵염기 단위 2 내지 7 (포함) 은 microRNA 시드 영역 서열에 상보적이다.
일부 실시형태에서, antimiR 올리고머는, miRNA 시드 영역에 상보적인 영역 내에 있는 위치에서, 하나 이상의 뉴클레오타이드 유사체 단위, 예를 들면, 하나 이상의 LNA 단위를 포함한다. antimiR 올리고머는, 일부 실시형태에서, miRNA 시드 영역에 상보적인 영역 내에 있는 위치에서, 1 개와 6 개 사이 또는 1 개와 7 개 사이의 뉴클레오타이드 유사체 단위, 예를 들면, 1 개와 6 개 사이 및 1 개와 7 개 사이의 LNA 단위를 포함할 수 있다.
일부 실시형태에서, 본 발명의 antimiR 은 7 개, 8 개 또는 9 개 길이의 뉴클레오타이드이고, 인간 또는 바이러스 microRNA 의 시드 영역에 상보적인 인접 뉴클레오타이드 서열을 포함하고, 여기서, 뉴클레오타이드의 80% 이상, 예를 들면, 85% 이상, 예를 들면, 90% 이상, 예를 들면, 95% 이상, 예를 들면, 100% 는 LNA 이다.
일부 실시형태에서, 본 발명의 antimiR 은 7 개, 8 개 또는 9 개 길이의 뉴클레오타이드이고, 인간 또는 바이러스 microRNA 의 시드 영역에 상보적인 인접 뉴클레오타이드 서열을 포함하고, 여기서, 뉴클레오타이드의 80% 이상은 LNA 이고, 인터뉴클레오타이드 결합의 80% 이상, 예를 들면, 85% 이상, 예를 들면, 90% 이상, 예를 들면, 95% 이상, 예를 들면, 100% 는 포스포로티오에이트 결합이다.
일부 실시형태에서, antimiR 은 3' 말단으로부터 계산하여, 3 위치 내지 8 위치에서 1 개 또는 2 개의 LNA 단위를 포함한다. 이것은 올리고뉴클레오타이드:microRNA 이중체, RNA:RNA 이중체를 닮은 구조의 이중체에 의해 형성된 A-나선의 안정성에 대해 유리한 것으로 고려된다.
WO 2007/112754 의 48 페이지 15 줄 내지 51 페이지 9 줄에 있는 표는 항 microRNA 올리고머 (즉, 올리고머 또는 이의 제 1 영역일 수 있는 antimiR) 의 예를 제공하며, 본원에 참조로 구체적으로 도입된다.
microRNA
모방체
일부 실시형태에서, 올리고머 또는 이의 제 1 영역은 하나 이상의 mRNA 표적(들) 의 발현을 억제하도록 세포 내에 도입될 수 있는 miRNA 모방체의 형태이다. miRNA 모방체는 전형적으로 전장 miRNA 서열에 완전히 상보적이다. miRNA 모방체는 본원에 제공되거나 참조된 miRNA 서열 중 하나 이상의 상응하는 영역에 상동인 인접 뉴클레오타이드 서열을 포함하는 화합물이다. miRNA 모방체 또는 antimiR 의 용도는 mRNA 표적을 (임의로) 추가 억제시키거나, miRNA 를 침묵 (하향 조절) 시킴으로써, 내생 miRNA 의 기능을 억제하고, mRNA 표적의 탈억제를 유발하고 발현을 증가시키기 위해 사용될 수 있다.
앱타머
(
Aptamer
)
일부 실시형태에서, 올리고머 또는 이의 제 1 영역은 치료적 앱타머인 스피에겔머 (spiegelmer) 일 수 있다. 앱타머는 또한 리간드, 예를 들면, 수용체 리간드일 수 있고, 따라서 표적화 모이어티 (즉, 영역 3) 으로서 사용될 수 있다는 것을 유의한다. 뉴클레오타이드의 서열보다는 이들의 형태적 구조에 근거하여 선택된 20 개와 50 개 사이의 길이의 뉴클레오타이드의 핵산으로서의 본 발명의 문맥에서의 앱타머 (또한 스피에겔머) - 이들은 생체 내에서 직접 표적 단백질과의 결합에 의해 이들의 치료 효과를 유발하고, 따라서, 이들은 이들의 표적의 역상보를 포함하지 않는다 - 실제로 이들의 표적은 핵산이 아니라 단백질이다. 올리고머 또는 이의 제 1 영역일 수 있는 특정 앱타머는 Macugen (OSI Pharmaceuticals) 또는 ARC1779 (Archemix, Cambridge, MA) 를 포함한다. 일부 실시형태에서, 올리고머 또는 이의 제 1 영역은 앱타머가 아니다. 일부 실시형태에서, 올리고머 또는 이의 제 1 영역은 앱타머 또는 스피에겔머가 아니다.
인터뉴클레오타이드
연결
본원에서 기재된 올리고머 (예를 들면, 제 1 영역 및 제 2 영역) 의 뉴클레오사이드 모노머는 [인터뉴클레오사이드] 연결기를 통해 함께 커플링된다. 적합하게, 각각의 모노머는 연결기를 통해 3' 인접 모노머에 연결된다.
본 발명의 문맥에서, 올리고머의 말단에서의 5' 모노머는, 비록 5' 말단기를 포함할 수 있거나 포함할 수 없더라도, 5' 연결기를 포함하지 않는다는 것을 당업자는 이해할 것이다.
용어 "연결기" 또는 "인터뉴클레오타이드 연결" 이란, 2 개의 뉴클레오타이드를 함께 공유 커플링할 수 있는 기를 의미하는 것으로 의도된다. 특이적이고 바람직한 예는 포스페이트 기 및 포스포로티오에이트 기를 포함한다.
본 발명의 올리고머의 뉴클레오타이드 또는 이의 인접 뉴클레오타이드 서열은 연결기를 통해 함께 커플링된다. 적합하게, 각각의 뉴클레오타이드는 연결기를 통해 3' 인접 뉴클레오타이드에 연결된다.
적합한 인터뉴클레오타이드 연결은 WO 2007/031091 에서 열거된 것들, 예를 들면, WO 2007/031091 (본원에 참조로 도입됨) 의 34 페이지의 첫번째 단락에 열거된 인터뉴클레오타이드 연결을 포함한다.
일부 실시형태에서, 포스포디에스테르 연결(들) 또는 영역 B 이외에, 이의 정상 포스포디에스테르로부터 뉴클레아제 공격에 대해 더욱 저항성인 것, 예를 들면, 포스포로티오에이트 또는 보라노포스페이트로 인터뉴클레오타이드 연결을 변형하는 것이 바람직하다 - RNase H 에 의해 절단가능한 이들 2 개는 또한 안티센스 억제의 경로가 표적 유전자의 발현을 감소시키도록 한다.
본원에서 제공되는 적합한 황 (S) 함유 인터뉴클레오타이드 연결, 예를 들면, 포스포로티오에이트 또는 포스포디티오에이트가 바람직할 수 있다. 포스포로티오에이트 인터뉴클레오타이드 연결은 또한, 예를 들면, 갭머, 믹스머, 안티미르 스플라이스 스위칭 올리고머 및 토탈머에서 특히 제 1 영역에 대해 바람직하다.
갭머의 경우, 올리고머에서의 인터뉴클레오타이드 연결은, 예를 들면, 포스포로티오에이트 또는 보라노포스페이트일 수 있어서, 표적화 RNA 의 RNase H 절단을 가능하게 한다. 개선된 뉴클레아제 저항성 및 다른 이유, 예를 들면, 제조의 용이성을 위해서, 포스포로티오에이트가 바람직하다.
하나의 측면에서, 제 1 영역과 제 2 영역 사이, 및 임의로 영역 B 내의 포스포디에스테르 연결, 본 발명의 올리고머의 나머지 인터뉴클레오사이드 연결을 제외하고, 뉴클레오타이드 및/또는 뉴클레오타이드 유사체는 포스포로티오에이트 기에 의해 서로 연결된다. 일부 실시형태에서, 제 1 영역에서의 뉴클레오사이드 사이의 인터뉴클레오사이드 연결의 50% 이상, 예를 들면, 70% 이상, 예를 들면, 80% 이상, 예를 들면, 90% 이상, 예를 들면, 모두는 포스포디에스테르 (포스페이트) 이외의 것이고, 예를 들면, 포스포로티오에이트, 포스포로디티오에이트 또는 보라노포스페이트로 이루어진 군으로부터 선택된다. 일부 실시형태에서, 제 1 영역에서의 뉴클레오사이드 사이의 인터뉴클레오사이드 연결의 50% 이상, 예를 들면, 70% 이상, 예를 들면, 80% 이상, 예를 들면, 90% 이상, 예를 들면, 모두는 포스포로티오에이트이다.
WO 09124238 은 중성 인터뉴클레오사이드 연결에 의해 3' 말단 또는 5' 말단에 부착된 하나 이상의 바이사이클릭 뉴클레오사이드를 가진 올리고머성 화합물을 언급하고 있다. 그러므로, 본 발명의 올리고머는 중성 인터뉴클레오사이드 연결, 예를 들면, 하나 이상의 포스포트리에스테르, 메틸포스포네이트, MMI, 아미드-3, 포름아세탈 또는 티오포름아세탈에 의해 3' 말단 또는 5' 말단에 부착된 하나 이상의 바이사이클릭 뉴클레오사이드를 가질 수 있다. 나머지 연결은 포스포로티오에이트일 수 있다.
컨쥬게이트
,
표적화
모이어티
및 차단기
용어 "컨쥬게이트" 란, 본원에서 기재된 올리고머의 공유 부착 ("컨쥬게이션") 에 의해 형성된 이종 분자가 하나 이상의 비-뉴클레오타이드 또는 이들에 컨쥬게이트된 비-폴리뉴클레오타이드 모이어티를 가지는 것을 의미하는 것으로 의도된다.
탄수화물
컨쥬게이트
일부 실시형태에서, 컨쥬게이트 기는 탄수화물 모이어티이다.
일부 실시형태에서, 컨쥬게이트는 탄수화물이거나 탄수화물을 포함할 수 있거나 탄수화물 기를 포함한다. 일부 실시형태에서, 탄수화물은 갈락토오스, 락토오스, n-아세틸갈락토사민, 만노오스 및 만노오스-6-포스페이트로 이루어진 군으로부터 선택된다. 일부 실시형태에서, 컨쥬게이트 기는 만노오스 또는 만노오스-6-포스페이트이거나 이를 포함할 수 있다. 탄수화물 컨쥬게이트는 조직의 범위, 예를 들면, 간 및/또는 근육에서 전달 또는 활성을 향상시키는데 사용될 수 있다. 예를 들면, EP 1495769, WO 99/65925, 문헌 [Yang et al., Bioconjug Chem (2009) 20(2): 213-21; Zatsepin & Oretskaya Chem Biodivers. (2004) 1(10): 1401-17] 을 참조한다.
추가로, 올리고머는 하나 이상의 추가의 컨쥬게이트 모이어티를 추가로 포함할 수 있고, 이의 친유성 또는 소수성 모이어티가 특히 관심이 있다. 이들은, 예를 들면, 약동학 조절제로서 작용할 수 있고, 탄수화물 컨쥬게이트, 탄수화물 컨쥬게이트를 올리고머에 연결시키는 링커 또는 다중 탄수화물 컨쥬게이트 (다가) 를 컨쥬게이트에 연결시키는 링커, 또는 올리고머에, 임의로 생체-절단가능한 링커와 같은 링커를 통해 공유 연결될 수 있다.
약동학 조절제
본 발명의 화합물은 하나 이상의 추가의 컨쥬게이트 모이어티를 추가로 포함할 수 있고, 컨쥬게이트 기가 탄수화물 모이어티일 때와 같이 이의 친유성 또는 소수성 모이어티는 특히 관심이 있다. 이러한 친유성 또는 소수성 모이어티는 약동학 조절제로서 작용할 수 있고, 탄수화물 컨쥬게이트, 탄수화물 컨쥬게이트를 올리고머에 연결시키는 링커 또는 다중 탄수화물 컨쥬게이트 (다가) 를 컨쥬게이트에 연결시키는 링커, 또는 올리고머에, 임의로 링커, 예를 들면, 생체-절단가능한 링커를 통해 공유 연결될 수 있다.
그러므로, 올리고머 또는 컨쥬게이트 모이어티는 약동학 조절제, 예를 들면, 친유성 또는 소수성 모이어티를 포함할 수 있다. 이러한 모이어티는 WO 2012/082046 에서 siRNA 컨쥬게이트의 문맥 내에 기재되어 있다. 소수성 모이어티는 포화 또는 불포화될 수 있는 C8-C36 지방산을 포함할 수 있다. 일부 실시형태에서, C10, C12, C14, C16, C18, C20, C22, C24, C26, C28, C30, C32 및 C34 지방산이 사용될 수 있다. 소수성 기는 16 개 이상의 탄소 원자를 가질 수 있다. 예시적인 적합한 소수성 기는 스테롤, 콜레스테롤, 팔미토일, 헥사데크-8-에노일, 올레일, (9E,12E)-옥타데카-9,12-디에노일, 디옥타노일 및 C16-C20 아실을 포함하는 군으로부터 선택될 수 있다. WO'346 에 따르면, 16 개 미만의 탄소 원자를 가진 소수성 기는 폴리뉴클레오타이드 표적화를 향상시키는데는 덜 효과적이지만, 이들은 효능을 향상시키기 위해 다중 카피 (예를 들면, 2x, 예를 들면, 2x C8 또는 C10, C12 또는 C14) 로 사용될 수 있다. 폴리뉴클레오타이드 표적화 모이어티로서 유용한 약동학 조절제는 콜레스테롤, 알킬기, 알케닐기, 알키닐기, 아릴기, 아르알킬기, 아르알케닐기 및 아르알키닐기로 이루어진 군으로부터 선택될 수 있으며, 이들 각각은 선형, 분지형 또는 사이클릭일 수 있다. 약동학 조절제는 바람직하게는 오직 탄소 및 수소 원자만을 함유하는 탄화수소이다. 그러나, 소수성을 유지하는 치환 또는 헤테로원자, 예를 들면, 불소가 허용될 수 있다.
놀랍게도, 본 발명자들은 LNA 올리고머와 함께 사용하기 위한 GalNac 컨쥬게이트가 약동학 조절제를 필요로 하지 않으며, 또한, 일부 실시형태에서, GalNac 컨쥬게이트가 친유성 또는 소수성 모이어티, 예를 들면, 본원에 기재된 것들에 공유 결합되지 않는데, 예를 들면, C8-C36 지방산 또는 스테롤을 포함하지 않는다는 것을 밝혀냈다. 그러므로, 본 발명은 또한 친유성 또는 소수성 약동학 조절제 또는 컨쥬게이트 모이어티/기를 포함하지 않는 LNA 올리고머 GalNac 컨쥬게이트를 제공한다.
GalNAc
컨쥬게이트
본 발명은 또한 아시알로당단백질 수용체 표적화 모이어티에 컨쥬게이트된 LNA 안티센스 올리고뉴클레오타이드를 제공한다. 일부 실시형태에서, 컨쥬게이트 모이어티 (예를 들면, 제 3 영역 또는 영역 C) 은 아시알로당단백질 수용체 표적화 모이어티, 예를 들면, 갈락토오스, 갈락토사민, N-포르밀-갈락토사민, N-아세틸갈락토사민, N-프로피오닐-갈락토사민, N-n-부타노일-갈락토사민, 및 N-이소부타노일갈락토사민을 포함한다. 일부 실시형태에서, 컨쥬게이트는 갈락토오스 클러스터, 예를 들면, N-아세틸갈락토사민 삼량체를 포함한다. 일부 실시형태에서, 컨쥬게이트 모이어티는 GalNAc (N-아세틸갈락토사민), 예를 들면, 1가, 2가, 3가 또는 4가 GalNAc 를 포함한다. 3가 GalNAc 컨쥬게이트는 화합물을 사용하여 간를 표적화할 수 있다. GalNAc 컨쥬게이트는 메틸포스포네이트 및 PNA 안티센스 올리고뉴클레오타이드와 함께 사용되었다 (예를 들면, US 5,994517 문헌 [Hangeland et al., Bioconjug Chem. 1995 Nov-Dec; 6(6): 695-701]) 및 siRNA (예를 들면, WO 2009/126933, WO 2012/089352 및 WO 2012/083046). GalNAc 참조 및 여기서 사용된 특정 컨쥬게이트는 본원에 참조로 도입된다. 기타 GalNAc 컨쥬게이트 모이어티는, 예를 들면, 올리고당 및 탄수화물 클러스터, 예를 들면, Tyr-Glu-Glu-(아미노헥실 GalNAc)3 (YEE(ahGalNAc)3; 간세포 상의 Gal/GalNAc 수용체에 결합하는 글리코트리펩타이드 (예를 들면, 문헌 [Duff, et al., Methods Enzymol, 2000, 313, 297] 참조); 라이신계 갈락토오스 클러스터 (예를 들면, L3G4; 문헌 [Biessen, et al., Cardovasc. Med., 1999, 214] 참조); 및 콜란계 갈락토오스 클러스터 (예를 들면, 아시알로당단백질 수용체에 대한 탄수화물 인지 모티프) 를 포함할 수 있다. 추가의 적합한 컨쥬게이트는 아시알로당단백질-수용체 (ASGP-R) 상에서 발견되는 탄수화물 인지 도메인 (carbohydrate recognition domain: CRD) 에 결합할 수 있는 올리고당을 포함할 수 있다. 올리고당 및/또는 탄수화물 복합체를 함유하는 컨쥬게이트 모이어티의 예는 그 전문이 참조로 본원에 인용되는 U.S. 특허 번호 6,525,031 에 제공된다.
WO 2012/083046 은 본 발명에서 사용하기에 적합한 절단가능한 약동학 조절제를 포함하는 GalNAc 컨쥬게이트 모이어티를 가진 siRNA 를 기재하고 있으며, 바람직한 약동학 조절제는 C16 소수성 기, 예를 들면, 팔미토일, 헥사데크-8-에노일, 올레일, (9E,12E)-옥타데카-9,12-디에노일, 디옥타노일 및 C16-C20 아실이다. WO 2012/083046 의 절단가능한 약동학 조절제는 또한 콜레스테롤일 수 있다.
표적화 모이어티 (컨쥬게이트 모이어티) 는 갈락토오스, 갈락토사민, N-포르밀-갈락토사민, N-아세틸갈락토사민, N-프로피오닐-갈락토사민, N-n-부타노일-갈락토사민, N-이소-부타노일갈락토사민, 갈락토오스 클러스터 및 N-아세틸갈락토사민 삼량체로 이루어진 군으로부터 선택될 수 있으며, 16 개 이상의 탄소 원자를 가진 소수성 기, 16-20 개의 탄소 원자를 가진 소수성 기, 팔미토일, 헥사데크-8-에노일, 올레일, (9E,12E)-옥타데카-9,12-디에노일, 디옥타노일, C16-C20 아실 및 콜레스테롤로 이루어진 군으로부터 선택된 약동학 조절제를 가질 수 있다. WO 2012/083046 에 기재된 특정 GalNac 클러스터는 (E)-헥사데크-8-에노일 (C16), 올레일 (C18), (9E,12E)-옥타데카-9,12-디에노일 (C18), 옥타노일 (C8), 도데세카노일 (C12), C-20 아실, C24 아실, 디옥타노일 (2xC8) 을 포함한다. 표적화 모이어티-약동학 조절제 표적화 모이어티는 생리학적으로 불안정한 결합 또는, 예를 들면, 디설파이드 결합 또는 PEG 링커를 통해 폴리뉴클레오타이드에 연결될 수 있다. 본 발명은 또한 올리고머와 컨쥬게이트 기 사이의 포스포디에스테르 링커, 예를 들면, DNA 포스포디에스테르 링커 (이들은 본원에서 영역 B 로서 언급되고, 적합하게는 LNA 올리고머와 탄수화물 컨쥬게이트 기 사이에 위치한다) 의 용도에 관한 것이다.
간에서 간세포를 표적화하기 위해서, 바람직한 표적화 리간드는 갈락토오스 클러스터이다. 갈락토오스 클러스터는 2 개 내지 4 개의 말단 갈락토오스 유도체를 가진 분자, 예를 들면, 이를 포함하는 분자를 포함한다. 본원에서 사용되는 용어 갈락토오스 유도체는 갈락토오스의 친화성과 동등하거나 이보다 높은 아시알로당단백질 수용체에 대한 친화성을 가진 갈락토오스의 갈락토오스와 유도체 둘 다를 포함한다. 말단 갈락토오스 유도체는 이의 C-I 탄소를 통해 분자에 부착된다. 아시알로당단백질 수용체 (ASGPr) 는 간세포에 대해 독특하고, 분지형 갈락토오스-말단 당단백질에 결합한다. 바람직한 갈락토오스 클러스터는 각각 아시알로당단백질 수용체에 대한 친화성을 가진 3 개의 말단 갈락토사민 또는 갈락토사민 유도체를 가진다. 더욱 바람직한 갈락토오스 클러스터는 3 개의 말단 N-아세틸-갈락토사민을 가진다. 당업계에 공통적인 다른 용어는 3-안테나형 (tri-antennary) 갈락토오스, 3가 갈락토오스 및 갈락토오스 삼량체를 포함한다. 3-안테나형 갈락토오스 유도체 클러스터는 2-안테나형 또는 1-안테나형 갈락토오스 유도체 구조보다 큰 친화성으로 ASGPr 에 결합된다는 것으로 공지되어 있다 [Baenziger and Fiete, 1980, Cell, 22, 611-620; Connolly et al., 1982,1. Biol. Chern., 257, 939-945]. 다가는 nM 친화성을 달성하는데 필요하다. WO 2012/083046 에 따르면, 아시알로당단백질 수용체에 대한 친화성을 가진 단일 갈락토오스 유도체의 부착은, 전달 폴리머와 함께 공동 투여될 때, 생체 내에서 간세포에 대한 RNAi 폴리뉴클레오타이드의 기능적인 전달을 할 수 없게 한다.
갈락토오스 클러스터는 중심 분지점에 각각 연결된 2 개의 또는 바람직하게는 3 개의 갈락토오스 유도체를 포함할 수 있다. 갈락토오스 유도체는 당류의 C-l 탄소를 통해 중앙 분지점에 부착된다. 갈락토오스 유도체는 바람직하게는 링커 또는 스페이서를 통해 분지점에 연결된다. 바람직한 스페이서는 유연한 친수성 스페이서이다 (U.S. Patent 5885968; Biessen et al. J. Med. Chern. 1995 Vol. 39 p. 1538-1546). 바람직한 유연한 친수성 스페이서는 PEG 스페이서이다. 바람직한 PEG 스페이서는 PEG3 스페이서이다. 분지점은 3 개의 갈락토오스 유도체의 부착을 허용하고, 올리고머에 대한 분지점의 부착을 추가로 허용하는 임의의 소형 분자일 수 있다. 예시적인 분지점 그룹은 디-라이신이다. 디-라이신 분자는 3 개의 갈락토오스 유도체를 부착하게 할 수 있는 3 개의 아민기와, 디-라이신을 올리고머에 부착하게 할 수 있는 카복실 반응성 기를 함유한다. 올리고머에 대한 분지점의 부착은 링커 또는 스페이서를 통해 일어날 수 있다. 바람직한 스페이서는 유연한 친수성 스페이서이다. 바람직한 유연한 친수성 스페이서는 PEG 스페이서이다. 바람직한 PEG 스페이서는 PEG3 스페이서 (3 개의 에틸렌 단위) 이다. 갈락토오스 클러스터는 당업계에 공지된 방법을 사용하여 올리고머의 3' 말단 또는 5' 말단에 부착될 수 있다.
바람직한 갈락토오스 유도체는 N-아세틸-갈락토사민 (GalNAc) 이다. 아시알로당단백질 수용체에 대한 친화성을 가진 기타 당류는 갈락토사민, N-n-부타노일갈락토사민 및 N-이소-부타노일갈락토사민을 포함하는 목록으로부터 선택될 수 있다. 아시알로당단백질 수용체에 대한 수많은 갈락토오스 유도체의 친화성은 연구되었거나 (예를 들면, [Jobst, S.T. and Drickamer, K. JB.C. 1996, 271, 6686] 참조), 당업계에 전형적인 방법을 사용하여 쉽게 결정된다.
갈락토오스 클러스터의 하나의 실시형태
분지점과 핵산 사이에 PEG 를 가진 갈락토오스 클러스터
GalNac 컨쥬게이트는 도 1 에 예시되어 있다. 본 발명의 컨쥬게이트의 추가의 예는 하기에 예시된다:
그러므로, 탄수화물 컨쥬게이트 (예를 들면, GalNAc) 는 링커, 예를 들면, (폴리)에틸렌 글리콜 링커 (PEG), 예를 들면, 디, 트리, 테트라, 펩타, 헥사-에틸렌 글리콜 링커를 통해 올리고머에 연결될 수 있다.
그러므로, 본원에 기재되는 탄수화물 컨쥬게이트 (예를 들면, GalNAc) 는 생체-절단가능한 링커, 예를 들면, 본원에서 정의된 바와 같은 영역 B, 및 임의로 상기 도표에 디-라이신으로서 예시된 영역 Y 를 통해 올리고머에 연결될 수 있다.
상기 GalNac 클러스터 컨쥬게이트 내에 소수성 또는 친유성 (또는 추가의 컨쥬게이트) 모이어티 (즉, 약동학 조절제) 가 있는 장소는, BNA 또는 LNA 올리고머, 예를 들면, LNA 안티센스 올리고뉴클레오타이드를 사용할 때, 임의적이다.
본 연구에서 사용되는 특정 GalNac 클러스터에 대한 도면의 Conj 1, 2, 3, 4 및 Conj1a, 2a, 3a 및 4a (이것은 GalNac 클러스터를 올리고머에 연결하는 임의의 C6 링커와 함께 나타나 있다) 을 참조한다.
그러므로, GalNAc 클러스터의 각각의 탄수화물 모이어티 (예를 들면, GalNAc) 는 스페이서, 예를 들면, (폴리)에틸렌 글리콜 링커 (PEG), 예를 들면, 디, 트리, 테트라, 펜타, 헥사-에틸렌 글리콜 링커를 통해 올리고머에 연결될 수 있다. 상기 나타내는 바와 같이, PEG 모이어티는 갈락토오스 당 모이어티와 펩타이드 (트리-라이신이 제시된다) 링커 사이에서 스페이서를 형성한다.
탄수화물 컨쥬게이트 (예를 들면, GalNAc) 또는 탄수화물-링커 모이어티 (예를 들면, 탄수화물-PEG 모이어티) 는, 예를 들면, 라이신, 디-라이신 또는 트리-라이신 또는 테트라-라이신과 같은 적합하게는 2 개 이상 (예를 들면, 3 개, 4 개 또는 5 개) 의 아미노기를 포함하는 분지점 기, 예를 들면, 아미노산 또는 펩타이드를 통해 올리고머에 공유 합류 (연결) 될 수 있다. 트리-라이신 분자는 3 개의 탄수화물 컨쥬게이트 기, 예를 들면, 갈락토오스 및 유도체 (예를 들면, GalNAc) 및 추가의 컨쥬게이트, 예를 들면, 소수성 또는 친유성 모이어티/기를 부착하게 할 수 있는 4 개의 아민기와, 트리-라이신을 올리고머에 부착하게 할 수 있는 카복실 반응성 기를 함유한다. 추가의 컨쥬게이트, 예를 들면, 친유성/소수성 모이어티는 올리고머에 부착된 라이신 잔기에 부착될 수 있다.
일부 실시형태에서, GalNac 클러스터는 펩타이드 링커, 예를 들면, Tyr-Asp(Asp) 트리펩타이드 또는 Asp(Asp) 디펩타이드를 포함하고, 이것은 바이라디칼 링커를 통해 올리고머에 (또는 영역 Y 또는 영역 B 에) 부착되며, 예를 들면, GalNac 클러스터는 하기 바이라디칼 링커를 포함할 수 있다:
R1 은 바람직하게는 -C2H4-, -C3H6-, -C4H8-, -C5H10-, -C6H12-, 1,4-사이클로헥실 (-C6H10-), 1,4-페닐 (-C6H4-), -C2H4OC2H4-, -C2H4(OC2H4)2- 또는 -C2H4(OC2H4)3-, C(O)CH2-, -C(O)C2H4-, -C(O)C3H6-, -C(O)C4H8-, -C(O)C5H10-, -C(O)C6H12-, 1,4-사이클로헥실 (-C(O)C6H10-), 1,4-페닐 (-C(O)C6H4-), -C(O)C2H4OC2H4-, -C(O)C2H4(OC2H4)2- 또는 -C(O)C2H4(OC2H4)3- 으로부터 선택된 바이라디칼이다. 일부 실시형태에서, R1 은 바람직하게는 -C2H4-, -C3H6-, -C4H8-, -C5H10-, -C6H12-, 1,4-사이클로헥실 (-C6H10-), 1,4-페닐 (-C6H4-), -C2H4OC2H4-, -C2H4(OC2H4)2- 또는 -C2H4(OC2H4)3- 으로부터 선택된 바이라디칼이다.
아미노
알킬
중간체
본 발명은 (예를 들면, 말단 5' 또는 말단 3') 아미노 알킬, 예를 들면, C2-C36 아미노 알킬기, 예를 들면, C6 및 C12 아미노 알킬기를 포함하는 안티센스 LNA 올리고머를 포함하는 LNA 올리고머 중간체를 추가로 제공한다 아미노 알킬기는, 예를 들면, (예를 들면, 보호된) 아미노 알킬 포스포라미디트를 사용하여, 표준 올리고뉴클레오타이드 합성의 일부로서 LNA 올리고머에 첨가될 수 있다. 아미노 알킬과 LNA 올리고머 사이의 연결기는, 예를 들면, 포스포로티오에이트 또는 포스포디에스테르, 또는, 예를 들면, 본원에서 언급된 기타 뉴클레오사이드 연결기 중의 하나일 수 있다. 아미노 알킬기는, 예를 들면, 뉴클레오사이드 연결기, 예를 들면, 포스포로티오에이트 또는 포스포디에스테르 연결기에 의해., 예를 들면, LNA 올리고머의 5' 또는 3' 에 공유 연결될 수 있다.
본 발명은 아미노 알킬기를 상기 올리고머에, 예를 들면, 올리고뉴클레오타이드 합성의 제 1 또는 마지막 라운드 과정에서 첨가하는 단계를 포함하는, LNA 올리고머의 순차적 합성, 예를 들면, 고상 올리고뉴클레오타이드 합성을 포함하는 LNA 올리고머의 합성 방법을 또한 제공한다. 상기 합성 방법은 탄수화물 컨쥬게이트를 아미노 알킬-LNA 올리고머에 반응시키는 단계 (컨쥬게이션 단계) 를 추가로 포함한다. 탄수화물 컨쥬게이트는 적합한 링커 및/또는 분지점 기, 및 임의로 추가의 컨쥬게이트 기, 예를 들면, 본원에 기재된 소수성 기 또는 친유성 기를 포함할 수 있다. 컨쥬게이션 단계는, 상기 올리고머가 고체 지지체에 결합되는 동안 (예를 들면, 올리고뉴클레오타이드 합성 후이지만 상기 고체 지지체로부터 올리고머의 용출 전에), 또는 후속적으로 (즉, 용출 후에) 수행될 수 있다. 본 발명은 본 발명의 올리고머의 합성에서의 아미노 알킬 링커의 용도를 제공한다.
본 발명은 올리고머성 화합물 화합물, 예를 들면, 본 발명의 올리고머성 화합물의 합성 (또는 제조) 방법을 제공하는 것으로서, 상기 방법은 제 1 영역 (A) 및 (임의로, 존재하는 경우) 제 2 영역 (B) 의 [순차적] 올리고뉴클레오타이드의 합성 단계를 포함하고, 여기서, 상기 합성 단계는 본원에서 기재된 탄수화물 컨쥬게이트 기, 예를 들면, GalNAc 컨쥬게이트, 예를 들면, 3가 GalNAc (예를 들면, Conj1, Conj2, Conj3, Conj 4, Conj1a, Conj2a, Conj3a, 및 Conj 4a 로 이루어진 군으로부터 선택된 컨쥬게이트) 또는 기타 3가 GalNAc 컨쥬게이트 모이어티, 예를 들면, 본원에서 기재된 것들을 포함하는 제 3 영역 [포스포라미디트] (X 또는 링커 X-Y) 의 첨가 단계로 이어지고, [고체] 지지체로부터의 상기 올리고머성 화합물의 절단 단계로 이어진다.
그러나, 컨쥬게이트 영역 (예를 들면, X 또는 X-Y) 은 고체 지지체로부터의 절단 후에 첨가될 수 있다는 것으로 인지된다. 다르게는, 합성 방법은 제 1 영역 (A), 및 임의로 제 2 영역 (B) 의 합성 단계 이후, 지지체로부터의 올리고머의 절단 단계를, 제 3 영역, 예를 들면, X 또는 X-Y 기의 올리고머에 대한 후속적 첨가 단계와 함께 포함할 수 있다. 제 3 영역의 첨가는, 예를 들면, 지지체로부터의 절단 후, 임의로 X 또는 Y (존재하는 경우) 기 상의 활성화 기를 통해, X 또는 X-Y 기에 합류되는데 사용될 수 있는, 올리고머 합성 (지지체 상에서) 의 최종 단계에서 아미노 포스포라미디트 단위를 첨가함으로써, 달성될 수 있다. 절단가능한 링커가 뉴클레오타이드 영역이 아닌 실시형태에서, 영역 B 는 영역 X (또한 영역 C 로서 언급됨) 의 일부를 형성하거나 영역 Y (또는 이의 일부) 일 수 있는 비-뉴클레오타이드 절단가능한 링커, 예를 들면, 펩타이드 링커일 수 있다.
방법의 일부 실시형태에서, 영역 X (예를 들면, C) 또는 (X-Y), 예를 들면, 컨쥬게이트 (예를 들면, GalNAc 컨쥬게이트) 는 활성화 기, (활성화된 작용기) 를 포함하고, 합성 방법에서, 활성화된 컨쥬게이트 (또는 영역 x 또는 X-Y) 는 제 1 영역 및 제 2 영역, 예를 들면, 아미노 연결된 올리고머에 첨가된다. 아미노기는, 예를 들면, 올리고머 합성의 최종 단계 (이것은 전형적으로 올리고머의 5' 말단에서 아미노기를 초래할 것이다) 로서, 표준 포스포라미디트 화학에 의해 올리고머에 첨가될 수 있다. 예를 들면, 올리고뉴클레오타이드 합성의 최종 단계 동안, 보호된 아미노-알킬 포스포라미디트, 예를 들면, TFA-아미노C6 포스포라미디트 (6-(트리플루오로아세틸아미노)-헥실-(2-시아노에틸)-(N,N-디이소프로필)-포스포라미디트) 를 사용한다. 아미노기는, 예를 들면, 올리고머 합성의 제 1 단계 (이것은 전형적으로 올리고머의 3' 말단에서 아미노기를 초래할 것이다) 로서, 올리고머에 첨가될 수 있다. 예를 들면, 이는 N-(6-(O-(4,4'-디메톡시트리틸))-헥실)-(2-카복스아미드)-프탈이미딜을 가지는 고체 지지체 사용에 의한 것이다.
영역 X (또는 본원에서 언급되는 바와 같은 영역 C), 예를 들면, 컨쥬게이트 (예를 들면, GalNac 컨쥬게이트) 는 NHS 에스테르 방법을 통해 활성화될 수 있고, 이후 아미노연결된 올리고머가 첨가된다. 예를 들면, N-하이드록시석신이미드 (NHS) 는 영역 X (또는 영역 C), 예를 들면, 컨쥬게이트, 예를 들면, GalNac 컨쥬게이트 모이어티에 대한 활성화 기로서 사용될 수 있다.
친유성
컨쥬게이트
올리고머는 또 다른 컨쥬게이트, 예를 들면, 친유성 컨쥬게이트 (예를 들면, 약동학 조절제로서) 를 추가로 포함할 수 있다. 대표적인 컨쥬게이트 모이어티는 스테로이드 분자를 포함하는 친유성 분자 (방향족 및 비방향족); 단백질 (예를 들면, 항체, 효소, 혈청 단백질); 펩타이드; 비타민 (수용성 또는 지용성); 폴리머 (수용성 또는 지용성); 약물, 독소, 리포터 분, 및 수용체 리간드를 비롯한 소형 분자; 탄수화물 복합체; 핵산 절단 복합체; 금속 킬레이트제 (예를 들면, 포르피린, 텍사피린, 크라운 에테르 등); 혼성 광뉴클레아제/삽입제를 포함하는 삽입제; 가교결합제 (예를 들면, 광활성, 산화환원 활성); 및 이들의 조합 및 유도체를 포함할 수 있다. 수많은 적합한 컨쥬게이트 모이어티, 이의 제조, 및 올리고머성 화합물에 대한 연결은, 예를 들면, 각각 그 전체가 본원에 참조로 도입되는 WO 93/07883 및 U.S. 특허 번호 6,395,492 에 제공된다. 올리고뉴클레오타이드 컨쥬게이트 및 이의 합성은 또한 각각 그 전체가 본원에 참조로 도입되는 문헌 [Manoharan in Antisense Drug Technology, Principles, Strategies, and Applications, S.T. Crooke, ed., Ch. 16, Marcel Dekker, Inc., 2001; 및 Manoharan, Antisense and Nucleic Acid Drug Development, 2002, 12, 103] 에 포괄적인 검토에서 보고되어 있다. 친유성 컨쥬게이트 모이어티는, 예를 들면, 올리고머성 화합물의 친수성 특성에 대응하고 세포 침투를 향상시키기 위해 사용될 수 있다. 친유성 모이어티는, 예를 들면, 스테로이드 및 관련 화합물, 예를 들면, 콜레스테롤 (U.S. 특허 번호 4,958,013 및 문헌 [Letsinger et al., Proc. Natl. Acad. Sci. USA, 1989, 86, 6553]), 티오콜레스테롤 [Oberhauser et al, Nucl Acids Res., 1992, 20, 533], 라노스테롤, 코프로스타놀, 스티그마스테롤, 에르고스테롤, 칼시페롤, 콜산, 데옥시콜산, 에스트론, 에스트라디올, 에스트라트리올, 프로게스테론, 스틸베스트롤, 테스토스테론, 안드로스테론, 데옥시코르티코스테론, 코르티손, 17-하이드록시코르티코스테론, 이들의 유도체 등을 포함한다.
기타 친유성 컨쥬게이트 모이어티는 지방족 기, 예를 들면, 예를 들면, 직쇄, 분지형 및 사이클릭 알킬, 알케닐 및 알키닐을 포함한다. 지방족 기는, 예를 들면, 5 개 내지 약 50 개, 6 개 내지 약 50 개, 8 개 내지 약 50 개 또는 10 개 내지 약 50 개의 탄소 원자를 가질 수 있다. 지방족 기의 예는 운데실, 도데실, 헥사데실, 헵타데실, 옥타데실, 노나데실, 테르펜, 보르닐, 아다만틸, 이들의 유도체 등을 포함한다. 일부 실시형태에서, 지방족 기 중 하나 이상의 탄소 원자는 헤테로원자, 예를 들면, O, S 또는 N 에 의해 대체될 수 있다 (예를 들면, 게라닐옥시헥실). 추가의 적합한 친유성 컨쥬게이트 모이어티는 글리세롤의 지방족 유도체, 예를 들면, 알킬글리세롤, 비스(알킬)글리세롤, 트리스(알킬)글리세롤, 모노글리세라이드, 디글리세라이드 및 트리글리세라이드를 포함한다. 일부 실시형태에서, 친유성 컨쥬게이트는 디-헥실데실-rac-글리세롤 또는 1,2-디-O-헥실데실-rac-글리세롤 [Manoharan et al., Tetrahedron Lett., 1995, 36, 3651; Shea, et al., Nuc. Acids Res., 1990, 18, 3777] 또는 이들의 포스포네이트이다. Acids Res., 1990, 18, 3777) 또는 포스포네이트 thereof. 포화 및 불포화 지방 작용기, 예를 들면, 지방산, 지방 알코올, 지방 에스테르 및 지방 아민은 또한 친유성 컨쥬게이트 모이어티로서의 역할을 할 수 있다. 일부 실시형태에서, 지방 작용기는 약 6 개 내지 약 30 개 또는 약 8 개 내지 약 22 개의 탄소 원자를 함유할 수 있다. 지방산의 예는 카프르산, 카프릴산, 라우르산, 팔미트산, 미리스트산, 스테아르산, 올레산, 리놀레산, 리놀렌산, 아라키돈산, 에이코센산 등을 포함한다.
추가의 실시형태에서, 친유성 컨쥬게이트 기는 6 개 내지 약 50 개, 10 개 내지 약 50 개 또는 14 개 내지 약 40 개의 탄소 원자를 가진 폴리사이클릭 방향족 기일 수 있다. 폴리사이클릭 방향족 기의 예는 피렌, 퓨린, 아크리딘, 잔텐, 플루오렌, 페난트렌, 안트라센, 퀴놀린, 이소퀴놀린, 나프탈렌, 이들의 유도체 등을 포함한다. 기타 적합한 친유성 컨쥬게이트 모이어티는 멘톨, 트리틸 (예를 들면, 디메톡시트리틸 (DMT)), 페녹사진, 리포산, 인지질, 에테르, 티오에테르 (예를 들면, 헥실-S-트리틸티올), 이들의 유도체 등을 포함한다. 올리고머성 화합물의 친유성 컨쥬게이트의 제조는 당업계에 잘 기술되어 있다 (예를 들면, [Saison-Behmoaras et al., EMBO J., 1991, 10, 1111; Kabanov et al., FEBSLett., 1990, 259, 327; Svinarchuk et al., Biochimie, 1993, 75, 49; Mishra et al., Biochim. Biophys. Acta, 1995, 1264, 229; 및 Manoharan et al., Tetrahedron Lett., 1995, 36, 3651]).
저밀도 지단백질 (low density lipoprotein: LDL) 에 대한 친화성을 가진 컨쥬게이트 모이어티를 함유하는 올리고머성 화합물은 효과적인 표적화 전달 시스템을 제공하는 것을 도울 수 있다. 종양 세포 상의 LDL 에 대한 수용체의 높은 발현 수준은 LDL 을 이들 세포에 대한 약물의 선택적 전달을 위한 매력적인 담체로 만든다 [Rump, et al., Bioconjugate Chem., 1998, 9, 341; Firestone, Bioconjugate Chem., 1994, 5, 105; Mishra, et al., Biochim. Biophys. Acta, 1995, 1264, 229]. LDL 에 대한 친화성을 가진 모이어티는 다수의 친유성 기, 예를 들면, 스테로이드 (예를 들면, 콜레스테롤), 지방산, 이들의 유도체 및 이들의 조합을 포함한다. 일부 실시형태에서, LDL 친화성을 가진 컨쥬게이트 모이어티는 콜산의 디올레일 에스테르, 예를 들면, 케노데옥시콜산 및 리소콜산일 수 있다.
일부 실시형태에서, 컨쥬게이트 기는 친유성 모이어티, 예를 들면, 스테롤 (예를 들면, 콜레스테롤, 콜레스테릴, 콜레스타놀, 스티그마스테롤, 콜란산 및 에르고스테롤) 이거나 이들을 포함할 수 있다. 일부 실시형태에서, 컨쥬게이트는 콜레스테롤이거나 이를 포함할 수 있다. 예를 들면, 문헌 [Soutschek et al., Nature (2004) 432, 173; Krutzfeldt Nature 2005, NAR 2007] 을 참조한다.
일부 실시형태에서, 컨쥬게이트는 지질, 인지질 또는 친유성 알코올, 예를 들면, 양이온성 지질, 중성 지질, 스핑고지질, 및 지방산, 예를 들면, 스테아르산, 올레산, 엘라이드산, 리놀레산, 리놀레아이드산, 리놀렌산 및 미리스트산이거나 이들을 포함할 수 있다. 일부 실시형태에서, 지방산은 C4-C30 포화 또는 불포화 알킬 쇄를 포함한다. 알킬 쇄는 선형 또는 분지형일 수 있다.
일부 실시형태에서, 친유성 컨쥬게이트는 비오틴일 수 있거나 이를 포함할 수 있다. 일부 실시형태에서, 친유성 컨쥬게이트는 글리세라이드 또는 글리세라이드 에스테르일 수 있거나 이들을 포함할 수 있다.
친유성 컨쥬게이트, 예를 들면, 콜레스테롤 또는 본원에 기재된 것들은, 예를 들면, 간 (전형적으로는 간세포) 에 대한 올리고뉴클레오타이드의 전달을 향상시키는데 사용될 수 있다.
다음 문헌은 친유성 컨쥬게이트의 용도를 언급하고 있다: [Kobylanska et al., Acta Biochim Pol. (1999) 46(3): 679-91; Felber et al.,. Biomaterials (2012) 33(25): 599-65); Grijalvo et al., J Org Chem (2010) 75(20): 6806-13; Koufaki et al., Curr Med Chem (2009) 16(35): 4728-42; Godeau et al., J. Med. Chem. (2008) 51(15): 4374-6].
일부 실시형태에서, 컨쥬게이트 모이어티 친수성이다. 일부 실시형태에서, 컨쥬게이트 기는 친유성 치환기 군, 예를 들면, 지방산 치환기 군, 예를 들면, C8-C26, 예를 들면, 팔미토일 치환기 군을 포함하지 않거나, 스테롤, 예를 들면, 콜레스테롤 치환기 군을 포함하지 않는다. 이와 관련하여, 본 발명의 일부는 LNA 올리고머 GalNAC 컨쥬게이트가 심지어 약동학 조절제, 예를 들면, 지방산 치환기 군 (예를 들면, > C8 또는 > C16 의 지방산 군) 의 사용 없이도 현저한 약동학 특성가진다는 놀라운 발견에 기초한다.
링커
연결 또는 링커는 하나 이상의 공유 결합을 통해 관심 대상의 하나의 화학기 또는 분절을 관심 대상의 또 다른 화학기 또는 분절에 연결하는 2 개의 원자 사이의 연결이다. 컨쥬게이트 모이어티 (또는 표적화 또는 차단 모이어티) 는 직접 또는 연결 모이어티 (링커 또는 테더 (thther)) - 링커를 통해 올리고머성 화합물에 부착될 수 있다. 링커는 제 3 영역, 예를 들면, 컨쥬게이트 모이어티를 올리고머성 화합물 (예를 들면, 영역 B) 에 공유 연결하는 역할을 하는 이작용성 모이어티이다. 일부 실시형태에서, 링커는 에틸렌 글리콜 또는 아미노산 단위와 같은 반복 단위의 쇄 구조 또는 올리고머를 포함한다. 링커는 2 개 이상의 작용기를 가질 수 있는데, 하나는 올리고머성 화합물에 부착하기 위한 것이고, 나머지는 컨쥬게이트 모이어티에 부착하기 위한 것이다. 링커 작용기의 예는 올리고머 또는 컨쥬게이트 모이어티 상의 친핵성 기와 반응하기 위해 친전자성이거나, 친전자성 기와 반응하기 위해 친핵성일 수 있다. 일부 실시형태에서, 링커 작용기는 아미노, 하이드록실, 카복실산, 티올, 포스포라미데이트, 포스페이트, 포스파이트, 불포화 (예를 들면, 이중 또는 삼중 결합) 등을 포함한다. 링커의 일부 예는 8-아미노-3,6-디옥사옥탄산 (ADO), 석신이미딜 4-(N-말레이미도메틸)사이클로헥산-1-카복실레이트 (SMCC), 6-아미노헥산산 (AHEX 또는 AHA), 6-아미노헥실옥시, 4-아미노부티르산, 4-아미노사이클로헥실카복실산, 석신이미딜 4-(N-말레이미도메틸)사이클로헥산-1-카복시-(6-아미도-카프로에이트) (LCSMCC), 석신이미딜 m-말레이미도-벤조일레이트 (MBS), 석신이미딜 N-e-말레이미도-카프로일레이트 (EMCS), 석신이미딜 6-(베타-말레이미도-프로피온아미도) 헥사노에이트 (SMPH), 석신이미딜 N-(a-말레이미도 아세테이트) (AMAS), 석신이미딜 4-(p-말레이미도페닐)부티레이트 (SMPB), 베타-알라닌 (베타-ALA), 페닐글리신 (PHG), 4-아미노사이클로헥산산 (ACHC), 베타-(사이클로프로필) 알라닌 (베타-CYPR), 아미노 도데칸산 (ADC), 알릴렌 디올, 폴리에틸렌 글리콜, 아미노산 등을 포함한다.
올리고머성 화합물에 대한 컨쥬게이트 모이어티의 부착에 유용할 수 있는 광범위한 추가의 링커 기는 당업계에 공지되어 있다. 다수의 유용한 링커 기의 검토는, 예를 들면, 문헌 [Antisense Research and Applications, S. T. Crooke and B. Lebleu, Eds., CRC Press, Boca Raton, Fla., 1993, p. 303-350] 에서 찾을 수 있다. 디설파이드 연결은 올리고뉴클레오타이드의 3' 말단을 펩타이드에 연결하는데 사용되었다 [Corey, et al., Science 1987, 238, 1401; Zuckermann, et al., J Am. Chem. Soc. 1988, 110, 1614; 및 Corey, et al., J Am. Chem. Soc. 1989, 111, 8524]. 문헌 [Nelson, et al., Nuc. Acids Res. 1989, 17, 7187] 은 올리고뉴클레오타이드의 3'-말단에 비오틴을 부착하기 위한 연결 시약을 기술하고 있다. 이러한 시약인 N-Fmoc-O-DMT-3-아미노-1,2-프로판디올은 Clontech Laboratories 사 (Palo Alto, Calif.) 에서 3'-아민 명칭으로 시판된다. 이것은 또한 3'-Amino-Modifier 시약 명칭으로 Glen Research Corporation 사 (Sterling, Va.) 에서 시판된다. 이러한 시약은 또한 문헌 [Judy, et al., Tetrahedron Letters 1991, 32, 879] 에서 보고된 바와 같이 펩타이드를 올리고뉴클레오타이드에 연결하기 위해 사용되었다. 올리고뉴클레오타이드의 5'-말단에 연결하기 위한 유사한 시판 시약은 5'-Amino-Modifier C6 이다. 이러한 시약은 Glen Research Corporation 사 (Sterling, Va.) 에서 시판된다. 이들 화합물 또는 유사 화합물은 문헌 [Krieg, et al., 안티센스 Research 및 Development 1991, 1, 161] 에 의해 올리고뉴클레오타이드의 5'-말단에 플루오레세인을 연결시키기 위해 사용되었다. 아크리딘과 같은 기타 화합물은 폴리메틸렌 연결을 통해 올리고뉴클레오타이드의 3'-말단 포스페이트기에 부착되었다 [Asseline, et al., Proc. Natl. Acad. Sci. USA 1984, 81, 3297]. 상기 기 중 임의는 단일 링커로서 또는 하나 이상의 추가의 링커와 조합으로 사용될 수 있다.
링커, 및 올리고머성 화합물의 컨쥬게이트의 제조에서의 이의 용도는 WO 96/11205 및 WO 98/52614 및 U.S. 특허 번호 4,948,882; 5,525,465; 5,541,313; 5,545,730; 5,552,538; 5,580,731; 5,486,603; 5,608,046; 4,587,044; 4,667,025; 5,254,469; 5,245,022; 5,112,963; 5,391,723; 5,510475; 5,512,667; 5,574,142; 5,684,142; 5,770,716; 6,096,875; 6,335,432; 및 6,335,437; WO 2012/083046 에서와 같이 당업계 전반에 걸쳐 제공되며, 이들 각각은 그 전체가 본원에 참조로 도입된다.
본원에 사용되는, 생리학적으로 불안정한 결합은 포유동물 체내에서 정상적으로 마주하거나 마주하는 것과 유사한 조건 하에서 절단가능한 불안정한 결합 (또한 절단가능한 링커로서 언급됨) 이다. 생리학적으로 불안정한 연결 기는 특정한 생리학적 조건으로 존재하는 경우에 화학적 변형 (예를 들면, 절단) 을 겪도록 선택된다. 포유동물 세포내 조건은 포유동물 세포에서 발견되거나 마주하는 것과 유사한 화학적 조건, 예를 들면, pH, 온도, 산화 또는 환원 조건 또는 제제 및 염 농도를 포함한다. 포유동물 세포내 조건은 또한 단백질분해 또는 가수분해 효소와 같은 포유동물 세포에 정상적으로 존재하는 효소적 활성의 존재를 포함한다. 일부 실시형태에서, 절단가능한 링커는, 예를 들면, 표적 세포에서 발현될 수 있는 뉴클레아제(들) 에 감수성이 있고 - 또한, 본원에 상세히 설명한 바와 같이, 링커는 짧은 영역 (예를 들면, 1-10) 포스포디에스테르 연결된 뉴클레오사이드, 예를 들면, DNA 뉴클레오사이드일 수 있다.
화학적 변형 (불안정한 결합의 절단) 은 세포에 대한 약학적으로 허용가능한 제제의 첨가에 의해 개시될 수 있거나, 불안정한 결합을 함유하는 분자가 적합한 세포내 및/또는 세포외 환경에 도달할 때 자발적으로 일어날 수 있다. 예를 들면, pH 불안정한 결합은 분자가 산성화된 엔도솜에 유입될 때 절단될 수 있다. 따라서, pH 불안정한 결합은 엔도솜 절단가능한 결합인 것으로 간주될 수 있다. 효소 절단가능한 결합은 엔도솜 또는 라이소좀에 또는 세포질에 존재하는 것과 같은 효소에 노출될 때 절단될 수 있다. 디설파이드 결합은 분자가 세포질의 좀더 환원성 환경으로 유입될 때 절단될 수 있다. 따라서, 디설파이드는 세포질성 절단가능한 결합인 것으로 간조될 수 있다. 본원에 사용되는, pH-불안정한 결합은 산성 조건 (pH < 7) 하에서 선택적으로 파괴되는 불안정한 결합이다. 이러한 결합은 또한 엔도솜성 불안정한 결합으로서 불릴 수 있는데, 이는 세포 엔도솜 및 라이소좀이 7 미만의 pH 를 가지기 때문이다.
링커 (예를 들면, 영역 Y)
연결 또는 링커는 하나 이상의 공유 결합을 통해 관심 대상의 하나의 화학기 또는 분절을 관심 대상의 또 다른 화학기 또는 분절에 연결하는 2 개의 원자 사이의 연결이다. 컨쥬게이트 모이어티 (또는 표적화 또는 차단 모이어티) 는 직접 또는 연결 모이어티 (링커 또는 테더 (thther)) - 링커를 통해 올리고머성 화합물에 부착될 수 있다. 링커는 제 3 영역, 예를 들면, 컨쥬게이트 모이어티를 올리고머성 화합물 (예를 들면, 영역 B) 에 공유 연결하는 역할을 하는 이작용성 모이어티이다. 일부 실시형태에서, 링커는 에틸렌 글리콜 또는 아미노산 단위와 같은 반복 단위의 쇄 구조 또는 올리고머를 포함한다. 링커는 2 개 이상의 작용기를 가질 수 있는데, 하나는 올리고머성 화합물에 부착하기 위한 것이고, 나머지는 컨쥬게이트 모이어티에 부착하기 위한 것이다. 링커 작용기의 예는 올리고머 또는 컨쥬게이트 모이어티 상의 친핵성 기와 반응하기 위해 친전자성이거나, 친전자성 기와 반응하기 위해 친핵성일 수 있다. 일부 실시형태에서, 링커 작용기는 아미노, 하이드록실, 카복실산, 티올, 포스포라미데이트, 포스포로티오에이트, 포스페이트, 포스파이트, 불포화 (예를 들면, 이중 또는 삼중 결합) 등을 포함한다. 링커의 일부 예는 8-아미노-3,6-디옥사옥탄산 (ADO), 석신이미딜 4-(N-말레이미도메틸)사이클로헥산-1-카복실레이트 (SMCC), 6-아미노헥산산 (AHEX 또는 AHA), 6-아미노헥실옥시, 4-아미노부티르산, 4-아미노사이클로헥실카복실산, 석신이미딜 4-(N-말레이미도메틸)사이클로헥산-1-카복시-(6-아미도-카프로에이트) (LCSMCC), 석신이미딜 m-말레이미도-벤조일레이트 (MBS), 석신이미딜 N-e-말레이미도-카프로일레이트 (EMCS), 석신이미딜 6-(베타-말레이미도-프로피온아미도) 헥사노에이트 (SMPH), 석신이미딜 N-(a-말레이미도 아세테이트) (AMAS), 석신이미딜 4-(p-말레이미도페닐)부티레이트 (SMPB), 베타-알라닌 (베타-ALA), 페닐글리신 (PHG), 4-아미노사이클로헥산산 (ACHC), 베타-(사이클로프로필) 알라닌 (베타-CYPR), 아미노 도데칸산 (ADC), 알릴렌 디올, 폴리에틸렌 글리콜, 아미노산 등을 포함한다.
올리고머성 화합물에 대한 컨쥬게이트 모이어티의 부착에 유용할 수 있는 광범위한 추가의 링커 기는 당업계에 공지되어 있다. 다수의 유용한 링커 기의 검토는, 예를 들면, 문헌 [Antisense Research and Applications, S. T. Crooke and B. Lebleu, Eds., CRC Press, Boca Raton, Fla., 1993, p. 303-350] 에서 찾을 수 있다. 디설파이드 연결은 올리고뉴클레오타이드의 3' 말단을 펩타이드에 연결하는데 사용되었다 [Corey, et al., Science 1987, 238, 1401; Zuckermann, et al., J Am. Chem. Soc. 1988, 110, 1614; 및 Corey, et al., J Am. Chem. Soc. 1989, 111, 8524]. 문헌 [Nelson, et al., Nuc. Acids Res. 1989, 17, 7187] 은 올리고뉴클레오타이드의 3'-말단에 비오틴을 부착하기 위한 연결 시약을 기술하고 있다. 이러한 시약인 N-Fmoc-O-DMT-3-아미노-1,2-프로판디올은 Clontech Laboratories 사 (Palo Alto, Calif.) 에서 3'-아민 명칭으로 시판된다. 이것은 또한 3'-Amino-Modifier 시약 명칭으로 Glen Research Corporation 사 (Sterling, Va.) 에서 시판된다. 이러한 시약은 또한 문헌 [Judy, et al., Tetrahedron Letters 1991, 32, 879] 에서 보고된 바와 같이 펩타이드를 올리고뉴클레오타이드에 연결하기 위해 사용되었다. 올리고뉴클레오타이드의 5'-말단에 연결하기 위한 유사한 시판 시약은 5'-Amino-Modifier C6 이다. 이러한 시약은 Glen Research Corporation 사 (Sterling, Va.) 에서 시판된다. 이들 화합물 또는 유사 화합물은 문헌 [Krieg, et al., 안티센스 Research 및 Development 1991, 1, 161] 에 의해 올리고뉴클레오타이드의 5'-말단에 플루오레세인을 연결시키기 위해 사용되었다. 아크리딘과 같은 기타 화합물은 폴리메틸렌 연결을 통해 올리고뉴클레오타이드의 3'-말단 포스페이트기에 부착되었다 [Asseline, et al., Proc. Natl. Acad. Sci. USA 1984, 81, 3297]. 상기 기 중 임의는 단일 링커로서 또는 하나 이상의 추가의 링커와 조합으로 사용될 수 있다.
링커, 및 올리고머성 화합물의 컨쥬게이트의 제조에서의 이의 용도는 WO 96/11205 및 WO 98/52614 및 U.S. 특허 번호 4,948,882; 5,525,465; 5,541,313; 5,545,730; 5,552,538; 5,580,731; 5,486,603; 5,608,046; 4,587,044; 4,667,025; 5,254,469; 5,245,022; 5,112,963; 5,391,723; 5,510475; 5,512,667; 5,574,142; 5,684,142; 5,770,716; 6,096,875; 6,335,432; 및 6,335,437; WO 2012/083046 에서와 같이 당업계 전반에 걸쳐 제공되며, 이들 각각은 그 전체가 본원에 참조로 도입된다.
본원에 사용되는, 생리학적으로 불안정한 결합은 포유동물 체내에서 정상적으로 마주하거나 마주하는 것과 유사한 조건 하에서 절단가능한 불안정한 결합 (또한 절단가능한 링커로서 언급됨) 이다. 생리학적으로 불안정한 연결 기는 특정한 생리학적 조건으로 존재하는 경우에 화학적 변형 (예를 들면, 절단) 을 겪도록 선택된다. 포유동물 세포내 조건은 포유동물 세포에서 발견되거나 마주하는 것과 유사한 화학적 조건, 예를 들면, pH, 온도, 산화 또는 환원 조건 또는 제제 및 염 농도를 포함한다. 포유동물 세포내 조건은 또한 단백질분해 또는 가수분해 효소와 같은 포유동물 세포에 정상적으로 존재하는 효소적 활성의 존재를 포함한다. 일부 실시형태에서, 절단가능한 링커는, 예를 들면, 표적 세포에서 발현될 수 있는 뉴클레아제(들) 에 감수성이 있고 - 또한, 본원에 상세히 설명한 바와 같이, 링커는 짧은 영역 (예를 들면, 1-10) 포스포디에스테르 연결된 뉴클레오사이드, 예를 들면, DNA 뉴클레오사이드일 수 있다.
화학적 변형 (불안정한 결합의 절단) 은 세포에 대한 약학적으로 허용가능한 제제의 첨가에 의해 개시될 수 있거나, 불안정한 결합을 함유하는 분자가 적합한 세포내 및/또는 세포외 환경에 도달할 때 자발적으로 일어날 수 있다. 예를 들면, pH 불안정한 결합은 분자가 산성화된 엔도솜에 유입될 때 절단될 수 있다. 따라서, pH 불안정한 결합은 엔도솜 절단가능한 결합인 것으로 간주될 수 있다. 효소 절단가능한 결합은 엔도솜 또는 라이소좀에 또는 세포질에 존재하는 것과 같은 효소에 노출될 때 절단될 수 있다. 디설파이드 결합은 분자가 세포질의 좀더 환원성 환경으로 유입될 때 절단될 수 있다. 따라서, 디설파이드는 세포질성 절단가능한 결합인 것으로 간조될 수 있다. 본원에 사용되는, pH-불안정한 결합은 산성 조건 (pH < 7) 하에서 선택적으로 파괴되는 불안정한 결합이다. 이러한 결합은 또한 엔도솜성 불안정한 결합으로서 불릴 수 있는데, 이는 세포 엔도솜 및 라이소좀이 7 미만의 pH 를 가지기 때문이다.
올리고머
연결된 생체-절단가능한
컨쥬게이트
올리고머성 화합물은 올리고머 (영역 A 로서 언급됨) 와 컨쥬게이트 (영역 C 로서 언급됨) 사이에 위치한 제 2 영역 (영역 B) 을 임의로 포함할 수 있다. 영역 B 는 절단가능한 링커 (또한 생리학적으로 불안정한 연결로서 언급됨) 와 같은 링커일 수 있다.
실시예 9 에 나타낸 어세이에서의 절단에 대한 감수성은 링커가 생체-절단가능하거나 생리학적으로 불안정한지를 결정하는데 사용될 수 있다.
본 발명에 따른 생체-절단가능한 링커는 표적 조직 (즉, 생리학적으로 불안정한 조직), 예를 들면, 간 및/또는 신장에서 절단하기 쉬운 링커를 의미한다. 표적 조직에서 관찰된 절단 속도는 혈청에서 발견된 것보다 큰 것이 바람직하다. 조직 (예를 들면, 간 또는 신장) 및 혈청에서의 절단 수준 (%) 을 결정하는데 적합한 방법은 실시예 9 에서 발견된다. 일부 실시형태에서, 생체-절단가능한 링커 (또한 생리학적으로 불안정한 링커 또는 뉴클레아제 감수성 링커로서 언급됨), 예를 들면, 본 발명의 화합물에서의 영역 B 는 실시예 9 의 간 또는 신장 균질물 어세이에서, 약 20% 이상 절단되고, 예를 들면, 약 30% 이상 절단되고, 예를 들면, 약 40% 이상 절단되고, 예를 들면, 약 50% 이상 절단되고, 예를 들면, 약 60% 이상 절단되고, 예를 들면, 약 70% 이상 절단되고, 예를 들면, 약 75% 이상 절단된다. 일부 실시형태에서, 실시예 9 의 어세이에서 사용되는 혈청 중의 절단 (%) 은 약 30% 미만이고, 약 20% 미만, 예를 들면, 약 10% 미만, 예를 들면, 5% 미만, 예를 들면, 약 1% 미만이다.
동일하거나 상이할 수 있는 일부 실시형태에서, 생체-절단가능한 링커 (또한 생리학적으로 불안정한 링커 또는 뉴클레아제 감수성 링커로서 언급됨), 예를 들면, 본 발명의 화합물에서의 영역 B 는 S1 뉴클레아제 절단에 감수성이 있다. S1 절단에 대한 감수성은 실시예 9 에 나타낸 S1 뉴클레아제 어세이를 사용하여 평가될 수 있다. 일부 실시형태에서, 생체-절단가능한 링커 (또한 생리학적으로 불안정한 링커 또는 뉴클레아제 감수성 링커로서 언급됨), 예를 들면, 본 발명의 화합물에서의 영역 B 는 실시예 9 에서 사용되는 어세이에 따라 S1 뉴클레아제와의 120 분 항온처리 후, 약 30% 이상 절단되고, 예를 들면, 약 40% 이상 절단되고, 예를 들면, 약 50% 이상 절단되고, 예를 들면, 약 60% 이상 절단되고, 예를 들면, 약 70% 이상 절단되고, 예를 들면, 약 80% 이상 절단되고, 예를 들면, 약 90% 이상 절단되고, 예를 들면, 약 95% 이상 절단된다.
뉴클레아제 감수성 생리학적 불안정 연결
올리고머성 화합물은 LNA 올리고머 (영역 A 로서 언급됨) 와 탄수화물 컨쥬게이트 (영역 C 로서 언급됨) 사이에 위치한 제 2 영역 (영역 B) 을 임의로 포함할 수 있다. 영역 B 는 절단가능한 링커 (또한 생리학적으로 불안정한 연결로서 언급됨) 와 같은 링커일 수 있다.
일부 실시형태에서, 영역 B 는, 예를 들면, 인터뉴클레오사이드 연결기, 예를 들면, 포스포디에스테르 연결을 통해 제 1 영역의 5' 또는 3' 뉴클레오타이드에 공유 연결된 1- 10 개 사이의 뉴클레오타이드를 포함고, 여기서,
a. 제 1 영역과 제 2 영역 사이의 인터뉴클레오사이드 연결은 포스포디에스테르 연결이고, 제 1 영역에 인접한 [예를 들면, 바로 옆에] 제 2 영역의 뉴클레오사이드는 DNA 또는 RNA 이고/이거나;
b. 제 2 영역의 1 개 이상의 뉴클레오사이드는 포스포디에스테르 연결된 DNA 또는 RNA 뉴클레오사이드이다.
일부 실시형태에서, 영역 A 및 영역 B 는 8-35 개 길이의 뉴클레오타이드의 단일 인접 뉴클레오타이드 서열을 형성한다. 일부 측면에서, 제 1 영역과 제 2 영역 사이의 인터뉴클레오사이드 연결은 제 2 영역의 고려된 부분일 수 있다.
일부 실시형태에서, 제 2 영역과 제 3 영역 사이에 인 함유 연결 기가 존재한다. 인 연결 기는, 예를 들면, 포스페이트 (포스포디에스테르), 포스포로티오에이트, 포스포로디티오에이트 또는 보라노포스페이트 기일 수 있다. 일부 실시형태에서, 이러한 인 함유 연결기는 제 3 영역에 부착된 링커 영역과 제 2 영역 사이에 위치한다. 일부 실시형태에서, 포스페이트 기는 포스포디에스테르이다.
그러므로, 일부 측면에서, 올리고머성 화합물은 2 개 이상의 포스포디에스테르 기를 포함하고, 여기서, 하나 이상은 본 발명의 상기 언급에 따른 바와 같고, 나머지는 제 2 영역과 제 3 영역 사이에, 임의로 링커 기와 제 2 영역 사이에 위치한다.
일부 실시형태에서, 제 3 영역은 활성화 기, 예를 들면, 컨쥬게이션에서 사용하기 위한 활성화 기이다. 이와 관련하여, 본 발명은 또한 영역 A, 영역 B 및 활성화 기, 예를 들면, 제 3 영역에 대한 후속적 연결에 적합한 중간체, 예를 들면, 컨쥬게이션에 적합한 중간체를 포함하는 활성화된 올리고머를 제공한다.
일부 실시형태에서, 제 3 영역은 반응성 기, 예를 들면, 컨쥬게이션에서 사용하기 위한 반응성 기이다. 이와 관련하여, 본 발명은 또한 영역 A, 영역 B 및 반응성 기, 예를 들면, 제 3 영역에 대한 후속적 연결에 적합한 중간체, 예를 들면, 컨쥬게이션에 적합한 중간체를 포함하는 활성화된 올리고머를 제공한다. 반응성 기는, 일부 실시형태에서, 알코올 기의 아민, 예를 들면, 아민기를 포함할 수 있다.
일부 실시형태에서, 영역 A 는 하나 이상, 예를 들면, 2 개, 3 개, 4 개, 5 개, 6 개, 7 개, 8 개, 9 개, 10 개, 11 개, 12 개, 13 개, 14 개, 15 개, 16 개, 17 개, 18 개, 19 개, 20 개, 21 개, 22 개, 23 개 또는 24 개의 포스포디에스테르 이외의 인터뉴클레오사이드 연결, 예를 들면, 포스포로티오에이트, 포스포로디티오에이트, 보라노포스페이트 및 메틸포스포네이트로 이루어진 군으로부터 [임의로 독립적으로] 선택된 인터뉴클레오사이드 연결, 예를 들면, 포스포로티오에이트를 포함한다. 일부 실시형태에서, 영역 A 는 하나 이상의 포스포로티오에이트 연결을 포함한다. 일부 실시형태에서, 영역 A 내의 인터뉴클레오사이드 연결의 50% 이상, 예를 들면, 75% 이상, 예를 들면, 90% 이상, 예를 들면, 모든 인터뉴클레오사이드 연결은 포스포디에스테르 이외의 것이고, 예를 들면, 포스포로티오에이트 연결이다. 일부 실시형태에서, 영역 A 중 모든 인터뉴클레오사이드 연결은 포스포디에스테르 이외의 것이다.
일부 실시형태에서, 올리고머성 화합물은 안티센스 올리고뉴클레오타이드, 예를 들면, 안티센스 올리고뉴클레오타이드 컨쥬게이트를 포함한다. 안티센스 올리고뉴클레오타이드는 제 1 영역 및 임의로 제 2 영역일 수 있거나, 이들을 포함할 수 있다. 이와 관련하여, 일부 실시형태에서, 영역 B 는 (핵산) 표적에 상보적인 인접 핵염기 서열의 일부를 형성할 수 있다. 다른 실시형태에서, 영역 B 는 표적에 대한 상보성이 결여될 수 있다.
다르게 명시되면, 일부 실시형태에서, 본 발명은, 포스포디에스테르 연결을 통해 올리고뉴클레오타이드의 인접 뉴클레오사이드에 연결된 하나 이상의 말단 (5' 및/또는 3') DNA 또는 RNA 뉴클레오사이드를 가진, 비-포스포디에스테르 연결된 올리고뉴클레오타이드, 예를 들면, 포스포로티오에이트 연결된 올리고뉴클레오타이드 (예를 들면, 안티센스 올리고뉴클레오타이드) 를 제공하는 것으로, 여기서, 말단 DNA 또는 RNA 뉴클레오사이드는 임의로 링커 모이어티를 통해, 컨쥬게이트 모이어티, 표적화 모이어티 또는 차단 모이어티에 추가로 공유 연결된다.
제 1 영역은, 예를 들면, 5' 말단 또는 3' 말단 인터뉴클레오사이드 연결, 예를 들면, 포스포디에스테르 연결을 통해 제 2 영역에 공유 연결된다. 그러므로, 포스포디에스테르 연결은 영역 A 의 5' 최대 뉴클레오사이드와 영역 B 의 3' 최대 뉴클레오사이드 사이에, 및/또는 영역 A 의 3' 최대 뉴클레오사이드와 영역 B 의 5' 최대 뉴클레오사이드 사이에 위치할 수 있다. 이와 관련하여, 일부 실시형태에서, 영역 A 에 공유 합류된 2 개의 영역 B 이 존재하는데, 하나는 영역 A 의 5' 말단에 존재하고, 하나는 영역 A 의 3' 말단에 존재한다. 2 개의 영역 B 는 동일하거나 상이할 수 있으며, 이들은 임의로 및 독립적으로 링커 (Y) 를 통해 동일하거나 상이한 제 3 영역에 공유 연결될 수 있다.
올리고머는 8-35 개 길이의 인접 뉴클레오타이드를 가질 수 있고, 예를 들면, 7- 5 개의 인접 뉴클레오타이드의 제 1 영역, 및 1-10 개의 인접 뉴클레오타이드의 제 2 영역을 포함하고, 여기서, 예를 들면, 제 1 영역과 제 2 영역 사이의 인터뉴클레오사이드 연결은 제 2 영역의 첫번째 (또는 유일한) DNA 또는 RNA 뉴클레오사이드에 연결된 포스포디에스테르이거나, 영역 B 는 하나 이상의 포스포디에스테르 연결된 DNA 또는 RNA 뉴클레오사이드를 포함한다.
제 2 영역은, 일부 실시형태에서, 포스포디에스테르 연결될 수 있는 추가의 DNA 또는 RNA 뉴클레오사이드를 포함할 수 있다. 제 2 영역은, 예를 들면, 컨쥬게이트 잔기일 수 있거나 이를 포함할 수 있는 제 3 영역에 추가로 공유 연결된다.
제 2 영역은 포스포디에스테르 연결을 통해 제 1 영역에 연결된 하나 이상의 DNA 또는 RNA 뉴클레오사이드를 포함하거나 이들로 이루어질 수 있다. 일부 측면에서, 제 1 영역과 제 2 영역 사이의 인터뉴클레오사이드 연결은 영역 B 의 일부로서 간주된다.
일부 실시형태에서, 제 2 영역은 적어도 1 개와 10 개 사이의 연결된 뉴클레오사이드, 예를 들면, 1 개, 2 개, 3 개, 4 개, 5 개, 6 개, 7 개, 8 개, 9 개 또는 10 개의 연결된 DNA 또는 RNA 뉴클레오타이드를 포함하거나 이들로 이루어진다. DNA/RNA 포스포디에스테르의 영역이 절단가능한 링커의 제공에 중요한 것으로 간주되면서, 영역 B 는 또한 당-변형된 뉴클레오사이드 유사체, 예를 들면, 상기 제 1 영역 하에 언급된 것들을 포함하는 것이 가능하다. 그러나, 일부 실시형태에서, 영역 B 의 뉴클레오사이드는 DNA 및 RNA 로 이루어진 군으로부터 (임의로 독립적으로) 선택된다. 영역 B 의 뉴클레오사이드는 천연 또는 비-천연 핵염기를 포함할 수 있는 것으로 인식될 것이다. 영역 B 는 하나 이상의 포스포디에스테르 연결된 DNA 또는 RNA 뉴클레오사이드 (이것은 일부 실시형태에서, 영역 A 에 인접한 첫번째 뉴클레오사이드일 수 있다) 를 포함한다. 영역 B 가 다른 뉴클레오사이드를 포함하는 경우, 영역 B 는 또한 포스포디에스테르 이외의 다른 뉴클레오사이드 연결, 예를 들면, 포스포로티오에이트, 포스포디티오에이트, 보라노포스페이트 또는 메틸 포스포네이트를 (임의로 독립적으로) 포함할 수 있다. 그러나, 다른 실시형태에서, 영역 B 중 모든 인터뉴클레오사이드 연결은 포스포로티오에이트이다. 일부 실시형태에서, 영역 B 의 모든 뉴클레오사이드는 2'-OH 리보오스 당 (RNA) 또는 2'-H 당 - 즉, RNA 또는 DNA 를 (임의로 독립적으로) 포함한다.
일부 실시형태에서, 제 2 영역은 적어도 1 개와 10 개 사이의 (예를 들면, 포스포디에스테르) 연결된 DNA 또는 RNA 뉴클레오사이드, 예를 들면, 1 개, 2 개, 3 개, 4 개, 5 개, 6 개, 7 개, 8 개, 9 개 또는 10 개의 (예를 들면, 포스포디에스테르) 연결된 DNA 또는 RNA 뉴클레오타이드를 포함하거나 이들로 이루어진다.
일부 실시형태에서, 영역 B 는 3 개 이하 또는 4 개 이하의 연속 DNA 또는 RNA 뉴클레오사이드 (예를 들면, DNA 뉴클레오사이드) 를 포함한다. 또한, 영역 B 가 표적에 상보적인 단일 인접 핵염기 서열의 일부를 형성하지 않을 때 중요할 수 있는 측면에서, 영역 B 는 RNase H 를 동원하지 못하기 때문에 너무 짧다. 예를 들면, 1-4 nts 길이의 짧은 영역 B 는 또한 일부 실시형태에서 바람직할 수 있는데, 이는 이들이 서열 특이적 제한 효소의 표적이 아닌 것 같기 때문이다. 또한, 엔도뉴클레아제 절단에 대한 영역 B 의 감수성을 변화시키고, 따라서 생체 내에서 또는 심지어 세포 내에서 활성 올리고머의 활성화 속도를 미세하게 조정하는 것이 가능하다. 적합하게, 매우 빠른 활성화가 요구되는 경우, 더욱 긴 영역 B 및/또는 제한 효소의 인지 부위 (예를 들면, 세포 또는 조직 특이적 또는 차별적으로 발현됨) 를 포함하는 영역 B 를 사용할 수 있다.
실시예에서 예시되는 바와 같이, 영역 B 는, 예를 들면, 포스포디에스테르 연결 및/또는 임의로 적합한 링커 기, 예를 들면, 본원에 제공된 것들을 포함할 수 있는 링커 기를 통해, 작용기 (X), 예를 들면, 컨쥬게이트, 표적화 반응성 기, 활성화 기 또는 차단기에 컨쥬게이션될 수 있다. 예를 들면, 포스페이트 뉴클레오사이드 연결 (예를 들면, 포스포디에스테르, 포스포로티오에이트, 포스포디티오에이트, 보라노포스페이트 또는 메틸포스포네이트) 또는 트리아졸 기. 일부 측면에서, 연결기는 영역 A 와 영역 B 사이의 연결기와 동일하고, 포스포디에스테르 연결일 수 있다. 일부 측면에서, 연결기는 포스포로티오에이트 연결이다.
일부 실시형태에서, 제 2 영역의 DNA 또는 RNA 뉴클레오타이드는 DNA 및 RNA 뉴클레오타이드로부터 독립적으로 선택된다. 일부 실시형태에서, 제 2 영역의 DNA 또는 RNA 뉴클레오타이드는 DNA 뉴클레오타이드이다. 일부 실시형태에서, 제 2 영역의 DNA 또는 RNA 뉴클레오타이드는 RNA 뉴클레오타이드이다.
제 2 영역의 문맥에서, 용어 DNA 및 RNA 뉴클레오사이드는 천연 또는 비-천연 염기 (또한 염기 유사체 또는 변형된 염기로서 언급됨) 를 포함할 수 있다.
일부 실시형태에서, 제 2 영역은 기타 뉴클레오타이드 또는 뉴클레오타이드 유사체를 추가로 포함할 수 있는 것으로 인식될 것이다. 일부 실시형태에서, 제 2 영역은 오직 DNA 또는 RNA 뉴클레오사이드만을 포함한다. 일부 실시형태에서, 제 2 영역이 1 개 초과의 뉴클레오사이드를 포함할 때, 제 2 영역 중 인터뉴클레오사이드 연결은 포스포디에스테르 연결을 포함한다. 일부 실시형태에서, 제 2 영역이 1 개 초과의 뉴클레오사이드를 포함할 때, 제 2 영역 중 모든 인터뉴클레오사이드 연결은 포스포디에스테르 연결을 포함한다.
일부 실시형태에서, 제 2 영역의 2 개 이상의 연속 뉴클레오사이드는 DNA 뉴클레오사이드 (예를 들면, 3 개 이상 또는 4 개 이상 또는 5 개 이상의 연속 DNA 뉴클레오타이드) 이다. 일부 실시형태에서, 제 2 영역의 2 개 이상의 연속 뉴클레오사이드는 RNA 뉴클레오사이드 (예를 들면, 3 개 이상 또는 4 개 이상 또는 5 개 이상의 연속 RNA 뉴클레오타이드) 이다. 일부 실시형태에서, 제 2 영역의 2 개 이상의 연속 뉴클레오사이드는 하나 이상의 DNA 및 하나 이상의 RNA 뉴클레오사이드이다. 영역 A 와 영역 B 사이의 인터뉴클레오사이드 연결은 포스포디에스테르 연결이다. 일부 실시형태에서, 영역 B 가 1 개 초과의 뉴클레오사이드를 포함할 때, 하나 이상의 추가의 인터뉴클레오사이드 연결은 포스포디에스테르 - 예를 들면, 영역 A 에 인접한 2 개 (또는 3 개 또는 4 개 또는 5 개) 의 뉴클레오사이드들 사이의 연결기(들) - 이다.
제 2 영역은 하나의 측면 (5' 또는 3') 및 다른 측면 (3' 또는 5') 상에 각각, 컨쥬게이트 모이어티 또는 유사한 기 (예를 들면, 차단 모이어티/기, 표적화 모이어티/기 또는 치료적 소형 분자 모이어티) 를 통해, 임의로 링커 기 (즉, 제 2 영역과 컨쥬게이트/차단기 등 모이어티 사이) 를 통해, 제 1 영역, 예를 들면, 안티센스 올리고뉴클레오타이드 옆에 위치한다.
이러한 실시형태에서, 본 발명의 올리고뉴클레오타이드는 하기 식에 따라 설명될 수 있다:
5'-A-PO-B [Y)X-3' 또는 3'-A-PO-B [Y)X-5'
여기서, A 는 영역 A 이고, PO 는 포스포디에스테르 연결이고, B 는 영역 B 이고, Y 는 임의의 연결기이고, X 는 컨쥬게이트 기, 표적화 기, 차단기, 반응성 기 또는 활성화 기이다.
일부 실시형태에서, 영역 B 는 3'-5' 또는 5'-3': i) 영역 A 의 5' 또는 3' 뉴클레오사이드에 대한 포스포디에스테르 연결, ii) DNA 또는 RNA 뉴클레오사이드, 예를 들면, DNA 뉴클레오사이드, 및 iii) 추가의 포스포디에스테르 연결을 포함한다:
5'-A-PO-B - PO-3' 또는 3'-A-PO-B - PO- 5'
추가의 포스포디에스테르 연결은 영역 B 뉴클레오사이드를 하나 이상의 추가의 뉴클레오사이드, 예를 들면, 하나 이상의 DNA 또는 RNA 뉴클레오사이드와 연결시키거나, 임의로 연결기 (Y) 를 통해 X (이것은 컨쥬게이트 기, 표적화 기 또는 차단기 또는 반응성 기 또는 활성화 기이다) 에 연결할 수 있다.
일부 실시형태에서, 영역 B 는 3'-5' 또는 5'-3': i) 영역 A 의 5' 또는 3' 뉴클레오사이드에 대한 포스포디에스테르 연결, ii) 2-10 개의 DNA 또는 RNA 포스포디에스테르 연결된 뉴클레오사이드, 예를 들면, DNA 뉴클레오사이드, 및 iii) 추가의 포스포디에스테르 연결을 포함한다:
5'-A-[PO-B]n - [Y]-X 3' 또는 3'-A-[PO-B]n -[Y]-X 5'
5'-A-[PO-B]n - PO-[Y]-X 3' 또는 3'-A-[PO-B]n - PO-[Y]-X 5'
여기서, A 는 영역 A 을 나타내고, [PO-B]n 은 영역 B 를 나타내고, n 은 1-10, 예를 들면, 1, 2, 3, 4, 5, 6, 7, 8, 9 또는 10 이고, PO 는 영역 B 와 X (또는 존재하는 경우, Y)) 사이의 임의의 포스포디에스테르 연결기이다.
일부 실시형태에서, 본 발명은 하기 식 중 하나에 따른 (또는 이를 포함하는) 화합물을 제공한다:
5' [영역 A] - PO - [영역 B] 3' -Y - X
5' [영역 A] - PO - [영역 B] -PO 3' -Y - X
5' [영역 A] - PO - [영역 B] 3' - X
5' [영역 A] - PO - [영역 B] -PO 3' - X
3' [영역 A] - PO - [영역 B] 5' -Y - X
3' [영역 A] - PO - [영역 B] -PO 5' -Y - X
3' [영역 A] - PO - [영역 B] 5' - X
3' [영역 A] - PO - [영역 B] -PO 5' - X
영역 B 는, 예를 들면, 하기를 포함하거나 하기로 이루어진다:
5' DNA3'
3' DNA 5'
5' DNA-PO-DNA-3'
3' DNA-PO-DNA-5'
5' DNA-PO-DNA-PO-DNA 3'
3' DNA-PO-DNA-PO-DNA 5'
5' DNA-PO-DNA-PO-DNA-PO-DNA 3'
3' DNA-PO-DNA-PO-DNA-PO-DNA 5'
5' DNA-PO-DNA-PO-DNA-PO-DNA-PO-DNA 3'
3' DNA-PO-DNA-PO-DNA-PO-DNA-PO-DNA 5'
제 2 영역에서의 서열 선택:
일부 실시형태에서, 영역 B 는 올리고뉴클레오타이드 영역 A 및 영역 B 가 상보적 표적 서열에 대해 정렬될 때 상보적 서열을 형성하지 않는다.
일부 실시형태에서, 영역 B 는 올리고뉴클레오타이드 영역 A 및 영역 B 가 상보적 표적 서열에 대해 정렬될 때 상보적 서열을 형성한다. 이와 관련하여, 영역 A 및 영역 B 는 함께 표적 서열에 대해 상보적인 단일 인접 서열을 형성할 수 있다.
일부 실시형태에서, 영역 B 중 염기 서열은, 표적 조직 또는 세포 또는 세포 하위 구획 내에 존재하는 두드러진 엔도뉴클레아제 절단 효소에 기초하여, 최적의 엔도뉴클레아제 절단 부위를 제공하도록 선택된다. 이와 관련하여, 표적 조직 및 비-표적 조직으로부터의 세포 추출물을 단리함으로써, 영역 B 에서 사용하기 위한 엔도뉴클레아제 절단 서열은, 비-표적 세포 (예를 들면, 신장) 와 비교하여, 목적하는 표적 세포 (예를 들면, 간/간세포) 에서의 우선적인 절단 활성에 기초하여 선택될 수 있다. 이와 관련하여, 표적 하향 조절을 위한 화합물의 효능은 목적하는 조직/세포에 대해 최적화될 수 있다.
일부 실시형태에서, 영역 B 는 서열 AA, AT, AC, AG, TA, TT, TC, TG, CA, CT, CC, CG, GA, GT, GC 또는 GG 의 디뉴클레오타이드를 포함하고, 여기서, C 는 5-메틸시토신일 수 있고/있거나, T 는 U 로 대체될 수 있다. 일부 실시형태에서, 영역 B 는 서열 AAA, AAT, AAC, AAG, ATA, ATT, ATC, ATG, ACA, ACT, ACC, ACG, AGA, AGT, AGC, AGG, TAA, TAT, TAC, TAG, TTA, TTT, TTC, TAG, TCA, TCT, TCC, TCG, TGA, TGT, TGC, TGG, CAA, CAT, CAC, CAG, CTA, CTG, CTC, CTT, CCA, CCT, CCC, CCG, CGA, CGT, CGC, CGG, GAA, GAT, GAC, CAG, GTA, GTT, GTC, GTG, GCA, GCT, GCC, GCG, GGA, GGT, GGC 및 GGG 의 트리뉴클레오타이드를 포함하고, 여기서, C 는 5-메틸시토신일 수 있고/있거나, T 는 U 로 대체될 수 있다. 일부 실시형태에서, 영역 B 는 서열 AAAX, AATX, AACX, AAGX, ATAX, ATTX, ATCX, ATGX, ACAX, ACTX, ACCX, ACGX, AGAX, AGTX, AGCX, AGGX, TAAX, TATX, TACX, TAGX, TTAX, TTTX, TTCX, TAGX, TCAX, TCTX, TCCX, TCGX, TGAX, TGTX, TGCX, TGGX, CAAX, CATX, CACX, CAGX, CTAX, CTGX, CTCX, CTTX, CCAX, CCTX, CCCX, CCGX, CGAX, CGTX, CGCX, CGGX, GAAX, GATX, GACX, CAGX, GTAX, GTTX, GTCX, GTGX, GCAX, GCTX, GCCX, GCGX, GGAX, GGTX, GGCX 및 GGGX 의 트리뉴클레오타이드를 포함하고, 여기서, X 는 A, T, U, G, C 및 이들의 유사체로 이루어진 군으로부터 선택될 수 있고, C 는 5-메틸시토신일 수 있고/있거나, T 는 U 로 대체될 수 있다. (천연) 핵염기 A, T, U, G, C 를 언급할 때, 이들은 동등한 천연 핵염기 (예를 들면, 상보적 뉴클레오사이드를 가진 염기 쌍) 로서 작용하는 핵염기 유사체로 치환될 수 있는 것으로 인식될 것이다.
일부 실시형태에서, 본 발명의 화합물은 1 개 초과의 컨쥬게이트 기 (또는 1 개 초과의 작용기 X - 예를 들면, 컨쥬게이트 기, 표적화 기, 차단기 또는 활성화된 기 또는 반응성 기 또는 활성화 기), 예를 들면, 2 개 또는 3 개의 이러한 기를 포함할 수 있다. 일부 실시형태에서, 영역 B 는 임의로 [예를 들면, 비-뉴클레오타이드] 링커 기) 를 통해, 하나 이상의 작용기, 예를 들면, 2 개 또는 3 개의 작용기에 공유 연결된다. 일부 실시형태에서, 제 1 영역은 (예를 들면, 인터뉴클레오사이드 연결, 예를 들면, 포스포디에스테르 연결을 통해), 2 개의 영역 B , 예를 들면, 제 1 영역에 대한 하나의 5' 및 하나의 3' 에 공유 연결될 수 있고, 여기서, 각각의 영역 B 는 본원에서 기재된 영역 B 로부터 (임의로 독립적으로) 선택될 수 있다. 이와 관련하여, 하나의 영역 B 는 하나 이상의 작용기를 가질 수 있고, 제 2 영역 B 는 하나 이상의 작용기를 가질 수 있고, 여기서, 각각의 영역 B 의 작용기는 컨쥬게이트 기, 표적화 기, 차단기 또는 반응성/활성화 기로부터 독립적으로 선택될 수 있다.
상기에서 설명된 바와 같이 상기 올리고머와 컨쥬게이트 모이어티 (X 또는 X-Y) 사이에서의 영역 B, 예를 들면, "PO DNA 링커" 의 사용이 특히 유리한데, 이는 일단 올리고머가 표적 세포 (예를 들면, 간세포) 로 전달되면, 이것은 올리고머 서열로부터 컨쥬게이트 모이어티의 균일한 절단을 보장하기 때문이다. 균일한 절단은 모 화합물의 최대 세포내 효능을 유지할 뿐만 아니라, 올리고머 컨쥬게이트의 안성성 프로파일을 향상시키는데 유용할 수 있다.
폴리
올리고머성
화합물
본 발명은 제 1 영역 (영역 A), (임의로 제 2 영역 (영역 B)) 및 제 3 영역 (영역 C) 을 포함할 수 있는 폴리 올리고머성 화합물을 제공하는 것으로, 여기서, 상기 제 1 영역은 하나 이상의 추가의 올리고머성 화합물 (영역 A') 에 공유 연결되고, 상기 제 1 영역 (영역 A) 및 영역 A' 는, 예를 들면, 본원에 기재된 바와 같은 제 2 영역, 예를 들면, 하나 이상의 포스포디에스테르 연결된 DNA 또는 RNA (예를 들면, DNA), 예를 들면, 2 개, 3 개, 4 개 또는 5 개의 포스포디에스테르 연결된 DNA 또는 RNA 뉴클레오사이드 (예를 들면, DNA 뉴클레오사이드) 의 영역에 따른 것일 수 있는 생체-절단가능한 링커 (영역 B') 를 통해 공유 연결된다. 영역 B 를 포함하는 실시형태에서, 영역 B 및 영역 B' 는, 일부 실시형태에서, 동일한 구조, 예를 들면, 동일한 수의 DNA/RNA 뉴클레오사이드 및 포스포디에스테르 연결 및/또는 동일한 핵염기 서열을 가질 수 있다. 다른 실시형태에서, 영역 B 및 영역 B' 는 상이할 수 있다. 예를 들면, 이러한 폴리 올리고머성 화합물은 다음과 같은 구조를 가질 수 있다: (5'-3' 또는 3'-5') 컨쥬게이트-PO-ON-PO'-ON', 여기서, 컨쥬게이트는 영역 C 이고, PO 는 영역 B 이고, PO' 는 영역 B' 이고, ON 은 영역 A 이고, ON' 는 영역 A' 이다.
올리고머 영역 A' 는, 일부 실시형태에서, 생체-절단가능한 링커, 예를 들면, 컨쥬게이트-PO-ON-PO-ON'-PO"-ON" 또는 컨쥬게이트-PO-ON-[PO-ON']n (여기서, n 은, 예를 들면, 1, 2 또는 3 일 수 있고, 각각의 ON' 는 동일하거나 상이할 수 있고, 상이한 경우, 동일하거나 상이한 표적을 가질 수 있다) 를 통해 연속으로 (또는 병행하여) 연결된 복수의 추가의 올리고머성 화합물 (예를 들면, 추가의 2 개 또는 3 개의 올리고머성 화합물) 을 포함할 수 있는 것으로 이해되어야 한다.
본 발명은 식 [LNAs]7-18-[DNA]1-5-[LNAs]7- 18 의 인접 뉴클레오타이드 서열, 및 비-핵염기 컨쥬게이트, 예를 들면, GalNAc 컨쥬게이트 모이어티, 예를 들면, 3가 GalNAc 컨쥬게이트 컨쥬게이트, 예를 들면, Conj1, 2, 3, 4, 1a, 2a, 3a, 4a 중 어느 하나로 이루어진 군으로부터 선택된 컨쥬게이트 모이어티, 또는 기타 3가 GalNAc 컨쥬게이트, 예를 들면, 본원에서 기재된 것들을 포함하는 올리고머성 화합물을 제공한다 아래첨자 s 는 포스포로티오에이트 연결을 의미한다. -[DNA]1-5- 영역 내의 또는 이에 인접한 하나 이상의 인터뉴클레오사이드 연결은 포스포디에스테르 결합이다. 일부 실시형태에서, -[DNA]1-5- 영역 내의 또는 이에 인접한 모든 인터뉴클레오사이드 연결은 포스포디에스테르 결합다. 일부 실시형태에서, -[DNA]1-5- 영역은 포스포디에스테르 결합에 의해 합류되는 2 개, 3 개, 4 개 또는 5 개의 인접 DNA 뉴클레오사이드를 가진다. 이러한 실시형태에서, -[DNA]2-5 - 사이의 인터뉴클레오사이드 연결은 포스포디에스테르 결합이고, 임의로 영역 -[DNA]1-5 와 LNA 영역 [LNAs]7-18 사이의 인터뉴클레오사이드 연결은 독립적으로 포스포로티오에이트 또는 포스포디에스테르 결합, 예를 들면, 둘 다 포스포디에스테르 또는 둘 다 포스포로티오에이트, 또는 하나의 포스포디에스테르 및 하나의 포스포로티오에이트이다. 실시형태에서, DNA 영역이 단일 DNA 뉴클레오사이드일 때, DNA 영역에 인접한 인터뉴클레오사이드 연결의 하나 이상 또는 둘 다는 포스포디에스테르이고, 오직 단일 포스포디에스테르인 경우, 나머지는 포스포로티오에이트일 수 있다. 영역 -[DNA]1-5 는 본원에서 영역 B 로 설명된 바와 같이 정의될 수 있다 - 즉, 생리학적으로 절단가능한 뉴클레오사이드 링커 영역일 수 있다. 각각의 [LNAs]7-18 은 LNA 포스포로티오에이트 올리고머이고, 예를 들면, LNA 갭머, LNA 믹스머 또는 LNA 토탈머로 이루어진 군으로부터 독립적으로 선택될 수 있다. GalNAc 컨쥬게이트는, 예를 들면, 인접 뉴클레오타이드 서열에 대한 5' 또는 3' 에 위치할 수 있다. 바람직한 실시형태에서, LNA 올리고머의 하나 이상, 또는 폴리 올리고머 컨쥬게이트의 둘 다는 7-12 개, 예를 들면, 8 개, 9 개 또는 10 개 길이의 뉴클레오사이드의 LNA 토탈머이다. 일부 실시형태에서, LNA 토탈머는 포스포로티오에이트 결합에 의해 연결된 오직 LNA 뉴클레오사이드, 예를 들면, 베타-D-옥시 LNA 뉴클레오사이드만을 포함할 수 있다. 예를 들면, 폴리 올리고머 컨쥬게이트는 인접 뉴클레오사이드 서열 [LNAs]7-10-[DNA]1-5-[LNAs]7-10,예를 들면, [LNAs]7-10-[DNA]2-[LNAs]7-10 또는 [LNAs]7-10-[DNA]3-[LNAs]7-10 또는 [LNAs]7-10-[DNA]4-[LNAs]7-10.을 포함할 수 있다. 하나의 실시형태에서, 인접 뉴클레오타이드 서열은 [LNAs]8-[DNA]1-5-[LNAs]8, 예를 들면, [LNAs]8-[DNA]2-[LNAs]8, [LNAs]8-[DNA]3-[LNAs]8, 또는 [LNAs]8-[DNA]4-[LNAs]8.을 포함한다. 이러한 폴리 올리고머성 복합체는 microRNA, 예를 들면, 성숙 microRNA 를 표적화하는데 특히 유용하다. 제 1 표적 (예를 들면, mRNA, microRNA 또는 바이러스 서열) 을 표적화하는 제 1 LNA 올리고머 영역 및 제 2 표적 (예를 들면, mRNA, microRNA 또는 바이러스 서열) 을 표적화하는 제 2 LNA 올리고머 영역을 이용함으로써, 2 개의 뚜렷한 표적을 표적화하는 단일 화합물을 제조할 수 있고, 예를 들면, 제 1 올리고머 영역은 ApoB 를 표적화할 수 있고, 제 2 올리고머 영역은 또 다른 mRNA, 예를 들면, mtGPAT mRNA, 예를 들면,
영역 C-5' [서열 번호 50]-[영역 B]-[서열 번호 59] 3'. (예를 들면, 서열 번호 61:
(3가 GalNAc)- GsTstsgsascsascstsgsTsCcaAsTsTscscscstsgscscstsGsTsG - 3')
를 표적화할 수 있다.
영역 C 는 3가 GalNAc 컨쥬게이트, 예를 들면, Conj2a, 또는 본원에서 기재된 기타 GalNAc 컨쥬게이트일 수 있다. 영역 B 는 DNA 디뉴클레오타이드 "ca" 일 수 있는데, 여기서, DNA 디뉴클레오타이드 사이의 인터뉴클레오타이드 결합 및 디뉴클레오타이드에 인접한 인터뉴클레오타이드 결합은 포스포디에스테르이다.
하나의 microRNA 를 표적화하는 제 1 LNA 올리고머 영역 (예를 들면, [LNAs]7-10) 및 제 2 microRNA 를 표적화하는 제 2 LNA 올리고머 영역을 이용함으로써, 2 개의 상이한 microRNA, 예를 들면, miR-21 및 miR-221 을 표적화하는 단일 화합물을 제조할 수 있고, 이들 둘 다는 간세포 암종에서 나타나 있다. 다르게는, 제 1 및 제 2 올리고머 영역은 2 개의 올리고머가 단일 컨쥬게이트 모이어티를 위해 표적 세포에 전달되도록 허용하는 동일한 microRNA, 예를 들면, miR-122, miR-21, miR-155, miR-33, miR-221 을 표적화할 수 있다.
이것은, 예를 들면, 아시알로당단백질 수용체 컨쥬게이트에 의한 수용체 매개 컨쥬게이트 표적화에 특히 중요하고, 여기서, 예를 들면, GalNAc 컨쥬게이트된 올리고머의 수용체 매개된 흡수는 표적 세포의 표면 상의 유리 수용체의 이용에 의해 제한되고, 폴리-올리고머 컨쥬게이트의 사용은 표적 세포에 대한 전달을 향상시킬 수 있다. 중요한 생물학적 기능을 수행하고 있는 세포 표면 수용체의 완전한 포화를 방지하는 것이 또한 중요하고, 따라서, 폴리-올리고머 전략의 사용은 충분한 화합물의 효과적인 전달을 가능하게 하여 관련 약리학을 보장하면서 컨쥬게이트 모이어티에 의한 수용체 포화/경쟁에 기인하는 부작용의 위험을 감소시킨다. 그러므로, 폴리-올리고머 컨쥬게이트의 사용은 치료 지수를 향상시키는데 효과적인 용액을 제공한다 - 원치 않은 부작용의 감소와 함께 올리고머 전달 및 활성 증가.
조성물
본 발명의 올리고머는 약제학적 제형 및 조성물에 사용될 수 있다. 적합하게는, 이러한 조성물은 약제학적으로 허용가능한 희석제, 담체, 염 또는 보조제를 포함한다. 참조로 본원에 도입되는 WO 2007/031091 은 적합하고 바람직한 약제학적으로 허용가능한 희석제, 담체 및 보조제를 제공한다. 적합한 투여량, 제형, 투여 경로, 조성물, 투여 형태, 다른 치료제와의 병용, 전구약물 제형도 또한 참조로 본원에 도입되는 WO 2007/031091 에서 제공된다.
안티센스 올리고뉴클레오타이드는 약제학적 조성물 또는 제형의 제조를 위해 약제학적으로 허용가능한 활성 또는 불활성 성분과 혼합될 수 있다. 조성물 및 약제학적 조성물의 제형화 방법은 투여 경로, 질환 정도, 또는 투여하고자 하는 투여량을 포함하지만 이들에 한정되지 않는 다수의 기준에 따라 달라진다.
안티센스 화합물은 안티센스 화합물을 적합한 약제학적으로 허용가능한 희석제 또는 담체와 조합함으로써 약제학적 조성물로 이용될 수 있다. 약제학적으로 허용가능한 희석제는 포스페이트-완충 식염수 (PBS) 를 포함한다. PBS 는 비경구로 전달하고자 하는 조성물에서 사용하기에 적합한 희석제이다.
안티센스 화합물을 포함하는 약제학적 조성물은, 인간을 비롯한 동물에 대한 투여시, (직접적으로 또는 간접적으로) 생물학적 활성 대사물질 또는 이의 잔기를 제공할 수 있는, 임의의 약제학적으로 허용가능한 염, 에스테르, 또는 이러한 에스테르의 염, 또는 임의의 기타 올리고뉴클레오타이드를 포괄한다. 따라서, 예를 들면, 본 개시내용은 또한 안티센스 화합물의 약제학적으로 허용가능한 염, 전구약물, 이러한 전구약물의 약제학적으로 허용가능한 염, 및 기타 생물학적 등가물에 관한 것이다. 적합한 약제학적으로 허용가능한 염은 나트륨 및 칼륨 염을 포함하지만, 이들에 한정되는 것은 아니다. 일부 실시형태에서, 본 발명의 올리고머는 전구약물이다.
적용
본 발명의 올리고머는, 예를 들면, 진단, 치료 및 예방을 위한 연구 시약으로서 유용할 수 있다.
연구에서, 일부 실시형태에서, 이러한 올리고머는 세포 및 실험 동물에서 단백질의 합성 (전형적으로는 mRNA 를 분해 또는 억제하고, 따라서 단백질 형성을 방지함) 을 특이적으로 억제하는데 사용되고, 이에 의해 표적의 작용적 분석 또는 치료적 개입을 위한 표적으로서의 이의 유용성의 평가를 용이하게 할 수 있다.
치료를 위해, 표적의 발현을 조절함으로써 치료될 수 있는 질환 또는 장애를 가진 것으로 의심되는 동물 또는 인간은 본 발명에 따른 올리고머성 화합물을 투여함으로써 치료된다. 본 발명의 하나 이상의 올리고머 또는 조성물을 치료적적 또는 예방적 유효량으로 투여함으로써 표적의 발현과 연관된 질환 또는 병태를 가진 것으로 의심되거나 이를 갖기 쉬운 포유동물을 치료하는 방법, 예를 들면, 인간을 치료하는 방법이 추가로 제공된다. 본 발명에 따른 올리고머, 컨쥬게이트 또는 약제학적 조성물은 전형적으로 유효량으로 투여된다.
본 발명은 또한 본원에서 기재된 바와 같은 장애의 치료를 위한 약제를 제조하기 위한 기재된 바와 같은 본 발명의 화합물 또는 컨쥬게이트의 용도, 또는 본원에서 기재된 바와 같은 장애의 치료 방법을 제공한다. 일부 실시형태에서, 질환 또는 장애는 간 관련 또는 간 연관 질환 또는 장애, 예를 들면, 본 발명에 기재된 바와 같은 것들로 이루어진 군으로부터 선택된 질환 또는 장애이다.
본 발명은 또한 본원에서 기재된 바와 같은 본 발명에 따른 화합물, 및/또는 본 발명에 따른 컨쥬게이트, 및/또는 본 발명에 따른 약제학적 조성물을 이를 필요로 하는 환자에게 투여하는 단계를 포함하는, 본원에 언급된 바와 같은 장애의 치료 방법을 제공한다.
의학적 징후
본 발명은 의약품에서 사용하기 위한 LNA 안티센스 올리고머 컨쥬게이트를 제공한다.
본 발명은 간-발현 RNA 를 하향 조절하는데 사용하기 위한 LNA 안티센스 올리고머 컨쥬게이트를 제공한다. 본 발명은 대사성 질환 또는 장애, 예를 들면, 간 질환 또는 장애의 치료에서 사용하기 위한 LNA 안티센스 올리고머 컨쥬게이트를 제공한다. 본 발명은 간염, 예를 들면, B 형 간염 또는 C 형 간염의 치료에서 사용하기 위한 LNA 안티센스 올리고머 컨쥬게이트를 제공한다.
일부 실시형태에서, 질환은 간 질환 또는 장애이다. 일부 실시형태에서, 질환 또는 장애는 간 섬유증이거나, 이를 유발하거나, 이와 연관된다. 일부 실시형태에서, 질환 또는 장애는 혈액 응고 장애, 예를 들면, 혈전색전성 합병증, 예를 들면, 혈전증, 색전증 및 혈전색전증, 심부 정맥 색전증, 폐 색전증, 심근 경색증 및 뇌졸중이다. 인자 VII 표적화 올리고머, 예를 들면, 인자 VII 안티센스 올리고뉴클레오사이드는 피험자에서 혈액 응고 장애의 치료를 위해 또는 혈액 응고를 조절하기 위해 사용될 수 있다 - US 2010/0298417 및 WO 2012/174154 참조.
인자 VII 표적화 올리고머는 또한 염증성 질환/장애, 암, 류마티스 관절염 및 섬유증의 치료를 위해 사용될 수 있다 (US 2010/0298417 및 WO 2012/174154 참조). 따라서, 일부 실시형태에서, 상기 질환 및 장애는 또한 본 발명의 화합물에 의해 치료될 수 있다. 따라서, 일부 실시형태에서, 본 발명은 염증성 질환/장애, 암, 류마티스 관절염 및 섬유증; 또는 혈액 응고 장애, 예를 들면, 혈전색전성 합병증, 예를 들면, 혈전증, 색전증 및 혈전색전증, 심부 정맥 색전증, 폐 색전증, 심근 경색증 및 뇌졸중으로 이루어진 군으로부터 선택된 질환 또는 장애의 치료에 사용하기 위한 올리고머를 제공한다.
일부 실시형태에서, 질환 또는 장애는 간 질환 또는 장애이다.
일부 실시형태에서, 질환 또는 장애는, 예를 들면, 간 질환 또는 장애 및/또는 일부 측면에서, 심혈관 질환 또는 장애일 수 있는 대사성 장애이다.
심혈관/대사성 질환은, 예를 들면, 대사성 증후군, 비만증, 고지혈증, HDL/LDL 콜레스테롤 불균형, 이상지질혈증, 예를 들면, 가족성 결합 고지혈증 (FCHL), 후천성 고지혈증, 스타틴-저항성, 고콜레스테롤혈증, 관상 동맥 질환 (CAD), 및 관상동맥 심장 질환 (CHD), 죽상동맥경화증, 심장 질환, 당뇨병 (I 및/또는 II), NASH, 급성 관상동맥 증후군 (ACS), NASH, 만성 심부전, 심혈관 질환, 심장 대사성 질환, 고지혈증 및 관련 질환, 대사성 증후군, 죽상동맥경화증, 만성 심부전, 혈관 질환, 말초 동맥 질환, 심장 질환, 허혈증, 제 2 형 당뇨병 및/또는 제 1 형 당뇨병을 포함한다.
일부 실시형태에서, 질환 또는 장애는 대사성 증후군, 비만증, 고지혈증 , 죽상동맥경화증, HDL/LDL 콜레스테롤 불균형, 이상지질혈증, 예를 들면, 가족성 결합 고지혈증 (FCHL), 후천성 고지혈증, 스타틴-저항성, 고콜레스테롤혈증, 관상 동맥 질환 (CAD) 및 관상동맥 심장 질환 (CHD) 으로 이루어진 군으로부터 선택된다.
일부 실시형태에서, 질환 또는 장애는 만성 심부전, 심혈관 질환, 심장 대사성 질환, 만성 심부전, 혈관 질환, 말초 동맥 질환, 심장 질환, 허혈증, 급성 관상동맥 증후군 (ACS) 으로 이루어진 군으로부터 선택된다.
일부 실시형태에서, 질환 또는 장애는 제 2 형 당뇨병 및/또는 제 1 형 당뇨병이다.
일부 실시형태에서, 질환 또는 장애는 바이러스 질환, 예를 들면, 바이러스 간염, 예를 들면, C 형 간염, B 형 간염이다. 일부 실시형태에서, 간 질환은 비알코올성 지방간 질환 및 비알코올성 지방간염으로 이루어진 군으로부터 선택된 질환 또는 장애일 수 있다.
본 발명은 질환, 장애 또는 병태, 예를 들면, 본원에서 언급된 것들의 치료를 위한 약제의 제조에서의 본 발명의 화합물의 용도를 추가로 제공한다.
일반적으로 명시된다면, 본 발명의 일부 측면은 포유동물에게 하나 이상의 LNA 단위를 포함하는 표적에 표적화된 올리고머를 치료학적 유효량으로 투여하는 단계를 포함하는, 비정상 수준의 표적과 연관된 병태를 겪고 있거나 겪기 쉬운 포유동물의 치료 방법에 관한 것이다. 본 발명에 따른 올리고머, 컨쥬게이트 또는 약제학적 조성물은 전형적으로 유효량으로 투여된다.
본 발명의 흥미로운 측면은 본원에서 언급된 질환, 장애 또는 병태의 치료를 위한 약제를 제조하기 위한 본원에서 정의된 바와 같은 화합물의 용도에 관한 것이다.
더욱이, 본 발명은 질환 또는 병태, 예를 들면, 본원에서 언급되는 것들을 겪고 있는 피험자, 예를 들면, 포유동물, 예를 들면, 인간의 치료 방법에 관한 것이다.
치료를 필요로 하는 환자는 질환 또는 장애를 겪고 있거나 겪을 것 같은 환자이다.
일부 실시형태에서, 본원에 사용되는 용어 '치료' 란, 기존 질환 (예를 들면, 본원에서 언급되는 질환 또는 장애) 의 치료 또는 질환의 방지, 즉, 예방 모두를 의미한다. 그러므로, 본원에서 언급되는 치료는, 일부 실시형태에서, 예방적일 수 있는 것으로 인지될 것이다.
실시예
마우스 실험: 달리 명시되지 않는다면, 마우스 실험은 하기와 같이 수행될 수 있다:
투여량 투여 및 샘플채취:
7-10 주령의 C57Bl6-N 마우스를 사용하였고, 동물을 연령 및 성별에 일치시켰다 (연구 1, 2 및 4 에 대해서는 암컷, 연구 3 에서는 수컷). 화합물을 꼬리 정맥 내로 i.v. 주사하였다. 중간 혈청 샘플채취를 위해서, 2-3 방울의 혈액을 안면정맥 (vena facialis) 의 천공에 의해 수집하였고, 마지막 출혈을 하대정맥으로부터 채취하였다. 혈청을 겔-함유 혈청-분리 튜브 (Greiner) 에 수집하고, 분석까지 동결 유지시켰다.
C57BL6 마우스에 제시된 정보에 따라 식염수로 제형화된 1 mg/kg ASO (또는 제시된 양) 또는 식염수 단독의 단일 투여량으로 i.v. 투여하였다. 동물에게 투여한 후, 예를 들면, 4 일째 또는 7 일째 (또는 제시된 시간) 에 희생시키고, 간 및 신장을 샘플채취하였다.
RNA 단리 및 mRNA 분석: 조직으로부터의 mRNA 분석을 제조사 프로토콜에 따라, Qantigene mRNA 정량화 키트 ("bDNA-assay", Panomics/Affimetrix) 를 사용하여 수행하였다. 조직 용해물의 경우, 50-80 mg 의 조직을 Proteinase K 를 함유하는 용해-버퍼 1 ml 에서 초음파에 의해 용해시켰다. 용해물을 RNA 추출 없이 bDNA-어세이에 직접 사용하였다. 표적 및 GAPDH 를 위한 프로브세트를 Panomics 사로부터 맞춤 디자인하여 수득하였다. 분석을 위해, 표적 유전자에 대해 수득된 발광 단위를 하우스키퍼 (housekeeper) GAPDH 에 대해 표준화시켰다.
ALT, AST 및 콜레스테롤에 대한 혈청 분석을 10μl 의 혈청을 사용하여 "Cobas INTEGRA 400 plus" 임상 화학 플랫폼 (Roche Diagnostics) 상에서 수행하였다.
인자 VII 혈청 수준의 정량화를 위해서, BIOPHEN FVII 효소 활성 키트 (#221304, Hyphen BioMed) 를 제조사의 프로토콜에 따라 사용하였다.
올리고뉴클레오타이드의 정량화를 위해서, 형광-라벨링된 PNA 프로브를 조직 용해물 중의 관심 대상의 올리고에 혼성화시킨다. 정확하게 칭량된 양의 조직을 가지는 동일한 용해물을 bDNA-어세이에 사용한다. 헤테로-이중체는 AEX-HPLC 및 형광 검출을 사용하여 정량한다.
실시예
1:
올리고뉴클레오타이드
합성
하기 LNA 갭머 올리고뉴클레오타이드를 동일한 13mer 마우스 인자 VII 서열에 기초하여 제조하였다.
기호 설명: 대문자 L: 베타-D-옥시 LNA; s: 포스포로티오에이트; 대문자 D: DNA; (NH2C6): 아미노링커; (Chol1): 콜레스테롤; (C6SSC6): 생분해성 디설파이드 링커
시판되는 포스포라미디트를 사용하여 GalNac 컨쥬게이트 이외의 화합물을 고상 합성을 통해 합성하고, IEX HPLC 를 통해 정제하였다. 3가 GalNAc 클러스터를 본원에 참조로 도입되는 US 2012/0157509 에 따라 제조하였다 (도 1 참조).
실시예
2:
GalNac
및 콜레스테롤
컨쥬게이트를
비교하는
FVII 의
생체
내 억제
생체내 마우스 연구는 총 9 개의 군의 마우스 (n=3) 를 사용하여 GalNac 및 콜레스테롤 컨쥬게이트 테스트를 나란히 준비하였다. 각각의 마우스에게 단일 i.v. 투여량의 LNA 화합물을 1 mg/kg 또는 4 mg/kg 으로 투여하였다. 식염수 대조군을 포함하였다. 마우스를 투여 전 1 일째에 미리 출혈시키고, 6 시간, 24 시간, 48 시간에서 후속 출혈시키고, 3 일 후에 마우스를 희생시키고, 간, 신장 및 혈액 샘플을 채취하였다.
인자 VII 혈청 수준 및 mRNA 수준을 표준 어세이 기술을 사용하여 측정하였다 (도 2 및 도 3 참조). FVII GalNac 와 콜레스테롤 (포스포로티오에이트 화합물) 둘 다는 혈청에서 FVII 녹 다운을 향상시켰고, FVII GalNac 는 콜레스테롤 보다 더 효과적이었다 (도 2 의 1mg/kg 참조).
실시예
3:
FVII
GalNac
및 콜레스테롤
컨쥬게이트
투여량 상승 연구의 생체내 억제
화합물
대문자 L 은 LNA 뉴클레오사이드 (예를 들면, 베타-D-옥시 LNA) 이고, 소문자 d 는 DNA 뉴클레오사이드이다. 아래첨자 s 는 포스포로티오에이트 인터뉴클레오사이드 연결 (영역 A) 을 나타낸다. 2PO 링커 (영역 B) 는 서열 영역 A 에 대해 5' 이고, 포스포디에스테르 연결에 의해 연결된 2 개의 DNA 뉴클레오사이드를 포함하고, 영역 A 의 3' DNA뉴클레오사이드와 영역 A 의 5' LNA 뉴클레오사이드 사이의 인터뉴클레오사이드 연결은 또한 포스포디에스테르이다. 연결기 (Y) 를 사용하여 컨쥬게이트 기를, 존재하는 경우, 영역 B 또는 영역 A (예를 들면, 서열 번호 3) 에 연결하였다.
생체내 마우스 연구는 총 16 개의 군의 마우스 (n=3) 를 사용하여 준비하였다. 각각의 마우스에게 단일 i.v. 투여량의 LNA 화합물을, 1 mg/kg, 0.5 mg/kg, 0.25 mg/kg, 0.1 mg/kg 또는 0.05 mg/kg 으로 투여하였다. 식염수 대조군을 포함하였다. 마우스를 투여 전 1 일째에 미리 출혈시키고, 연구 동안 다양한 시점에서 후속 출혈시켰다. 4 일째, 14 일째 또는 24 일째에 마우스를 희생시키고, 간, 신장 및 혈액 샘플을 채취하였다. 연구 설정을 위해 하기 표를 참조한다. 인자 VII 혈청 수준 (도 4), mRNA 수준 (도 5) 및 올리고뉴클레오타이드 조직 함량 (도 6) 을 표준 어세이 기술을 사용하여 측정하였다.
결론: FVII 표적화 LNA 올리고뉴클레오타이드 (서열 번호 3 및 서열 번호 6) 에 컨쥬게이트된 GalNAc 는 비컨쥬게이트된 LNA 올리고뉴클레오타이드 (서열 번호 1) 와 비교하여 혈청 중의 FVII 단백질 (도 4) 및 간 중의 mRNA (도 5) 에 대해 매우 양호한 활성을 나타낸다. 심지어 매우 낮은 투여량에서도, 활성은 나타났다. 더욱이, GalNAc 클러스터는 콜레스테롤 컨쥬게이트 (서열 번호 4 및 서열 번호 7) 와 비교하여 FVII 단백질 및 mRNA 에 대해 보다 더 활성인 것으로 나타났다 (도 4d 및 도 5d). 간 및 신장 중의 조직 함량은 도 6 에 도시되어 있고, 여기서, GalNAc 클러스터 (서열 번호 3 및 6) 는 비컨쥬게이트된 LNA FVII 표적화 올리고뉴클레오타이드 (서열 번호 1) 와 비교하여 간에서 흡수를 향상시키고, 신장에서 낮은 흡수를 제공하는 것으로 나타났다. GalNAc 컨쥬게이트된 LNA 올리고뉴클레오타이드 (서열 번호 3 및 서열 번호 6) 를 콜레스테롤 컨쥬게이트된 LNA 올리고뉴클레오타이드 (서열 번호 4 및 서열 번호 7) 와 비교할 때, 간에서 도달된 수준은 유사한 것으로 나타났지만, GalNAc 컨쥬게이트된 LNA 올리고뉴클레오타이드가 보다 양호한 활성을 나타냈기 때문에, 이들은 콜레스테롤 컨쥬게이트된 LNA 올리고뉴클레오타이드 보다 양호한 특이적 활성을 제공하는 것으로 보인다. PO 링커는 조직 흡수를 향상시킬 수 있고 (도 6), 더 높은 효능을 야기할 수 있는 것으로 보인다 (도 4).
재료 및 방법:
실험 디자인:
암컷 마우스를 i.v. 투여하고, 상기 도식에 따라 모두 희생시키고 간, 신장 및 혈액을 샘플채취하였다.
실시예
4: 상이한
monoGalNAc
컨쥬게이트에
의한
ApoB
mRNA 의
시험관
내
침묵화
화합물.
Expedite 8900/MOSS 합성기 (Multiple Oligonucleotide Synthesis System) 상에서 4 μmol 규모로, 포스포라미디트 접근법을 사용하여 우리딘 범용 지지체 상에서 올리고뉴클레오타이드를 합성하였다. 합성 종료시에, 올리고뉴클레오타이드를 1-2 시간 동안 실온에서 수성 암모니아를 사용하여 고체 지지체로부터 절단하였고, 16 시간 동안 65℃ 에서 추가로 탈보호하였다. 올리고뉴클레오타이드를 역상 HPLC (RP-HPLC) 로 정제하고, UPLC 로 특성화하고, 분자 질량을 ESI-MS 에 의해 추가로 확인하였다. 더욱 상세내용은 하기를 참조한다.
올리고뉴클레오타이드의
신장
β-시아노에틸-포스포라미디트 (DNA-A(Bz), DNA-G(ibu), DNA-C(Bz), DNA-T, LNA-5-메틸-C(Bz), LNA-A(Bz), LNA-G(dmf), LNA-T 또는 C6-S-S 링커) 의 커플링은 아세토니트릴 중의 0.1 M 의 5'-O-DMT-보호된 아미다이트 및 활성화제로서의 아세토니트릴 (0.25 M) 중의 DCI (4,5-디시아노이미다졸) 의 용액을 사용하여 수행된다. 최종 사이클을 위해서, 시판되는 C6-연결된 콜레스테롤 포스포라미디트를 DCM 중의 0.1M 로 사용하였다. 포스포르티오에이트 연결의 도입을 위한 티올화는 수소화 잔탄 (아세토니트릴/피리딘 9:1 중의 0.01 M) 을 사용하여 수행된다. 포스포르디에스테르 연결은 THF/피리딘/물 7:2:1 중의 0.02 M 요오드를 사용하여 도입된다. 시약의 나머지는 올리고뉴클레오타이드 합성에 전형적으로 사용되는 것들이다. 고상 합성 후 배치 동안, 시판되는 C6 아미노링커 포스포라미디트를 고상 합성의 마지막 사이클에서 사용하고, 탈보호 및 고체 지지체로부터의 절단 후, 아미노 연결된 탈보호 올리고뉴클레오타이드를 단리하였다. 표준 합성 방법을 사용하여 컨쥬게이트를 작용기의 활성화를 통해 도입하였다.
대문자는 LNA 뉴클레오사이드 (예를 들면, 베타-D-옥시 LNA) 이고, 소문자는 DNA 뉴클레오사이드이다. 아래첨자 s 는 포스포로티오에이트 인터뉴클레오사이드 연결 (영역 A) 을 나타낸다. LNA 시토신은 임의로 5-메틸 시토신이다. 2PO 링커 (영역 B) 는 서열 영역 A 에 대해 5' 이고, 포스포디에스테르 연결에 의해 연결된 2 개의 DNA 뉴클레오사이드를 포함하고, 영역 A 의 3' DNA뉴클레오사이드와 영역 A 의 5' LNA 뉴클레오사이드 사이의 인터뉴클레오사이드 연결은 또한 포스포디에스테르이다. 연결기 (Y) 를 사용하여 컨쥬게이트 기를, 존재하는 경우, 영역 B 또는 영역 A (예를 들면, 서열 번호 8 및 서열 번호 11) 에 연결할 수 있다.
상이한 링커를 가지는 monoGalNAc 컨쥬게이트와 GalNAc 클러스터를 비교하기 위해서, C57BL6 마우스를, 식염수 대조군으로, 또는 생체-절단가능한 링커의 부재 또는 디티오-링커 (SS) 의 존재 또는 DNA/PO-링커 (PO) 의 존재 하의 Mono-GalNAc 에 컨쥬게이트된 ASO 의 1 mg/kg 의 단일 투여량으로 (도 7a), 또는 Mono-GalNAc 또는 GalNAc 클러스터 에 컨쥬게이트된 ASO 의 0.25mg/kg 으로 (도 7b) i.v. 처리하였다. 7 일 후, 동물을 희생시키고, RNA 를 간 및 신장 샘플로부터 단리하고, ApoB mRNA 발현에 대해 분석하였다.
결론: 비컨쥬게이트된 화합물 (#12) 과 비교하여, 생체-절단가능한 링커 (#8) 의 부재 또는 DNA/PO-링커 (#10) 의 존재 하의 mono-GalNAc 의 배치는 간에서 명확히 향상된 활성을 나타낸다 (도 7a). 다양한 GalNAc 컨쥬게이트, 예를 들면, mono GalNAcPO (#10) 및 GalNAc 클러스터 (#11) 의 배치는 또한 간 또는 신장에 대해 집중적인 화합물 활성의 미세 조정을 허용한다 (도 7b).
재료 및 방법:
실험 디자인:
투여량 투여 및 샘플채취 : C57BL6 마우스에 상기 표에 따라 식염수로 제형화된 1 mg/kg 또는 0.25 mg/kg 의 ASO 또는 식염수 단독의 단일 투여량으로 i.v. 투여하였다. 투여한 후, 7 일째에 동물을 희생시키고, 간 및 신장을 샘플채취하였다.
RNA 단리 및 mRNA 분석. 총 RNA 를 간 및 신장 샘플로부터 추출하고, 분기형 DNA 어세이를 사용하여 ApoB mRNA 수준을 분석하였다.
실시예
5: 생체 내에서
GalNAc
-
컨쥬게이트에
의한
ApoB
mRNA
, 조직 함량 및 총 콜레스테롤의
녹 다운
화합물
대문자는 LNA 뉴클레오사이드 (예를 들면, 베타-D-옥시 LNA) 이고, 소문자는 DNA 뉴클레오사이드이다. 아래첨자 s 는 포스포로티오에이트 인터뉴클레오사이드 연결 (영역 A) 을 나타낸다. LNA 시토신은 임의로 5-메틸 시토신이다. 2PO 링커 (영역 B) 는 서열 영역 A 에 대해 5' 이고, 포스포디에스테르 연결에 의해 연결된 2 개의 DNA 뉴클레오사이드를 포함하고, 영역 A 의 3' DNA뉴클레오사이드와 영역 A 의 5' LNA 뉴클레오사이드 사이의 인터뉴클레오사이드 연결은 또한 포스포디에스테르이다. 연결기 (Y) 를 사용하여 컨쥬게이트 기를, 존재하는 경우, 영역 B 또는 영역 A (예를 들면, 서열 번호 13 및 서열 번호 11) 에 연결할 수 있다.
C57BL6/J 마우스에게, 단일 투여량 식염수 또는 0.25 mg/kg 의 비컨쥬게이트된 LNA-안티센스 올리고뉴클레오타이드 (서열 번호 12) 또는 등몰량의 GalNAc1, GalNAc2 또는 콜레스테롤 (2PO) 에 컨쥬게이트된 LNA 안티센스 올리고뉴클레오타이드로 i.v. 또는 s.c. 주사하고, 하기 표 (실험 디자인) 에 따라 1-7 일째에 희생시켰다.
RNA 를 간 및 신장으로부터 단리하고, qPCR 을 ApoB 특이적 프라이머 및 프로브로 수행하여 ApoB mRNA 녹 다운을 분석하였다. ELISA 방법을 사용하여 올리고뉴클레오타이드 함량을 측정하고, 혈청 중의 총 콜레스테롤을 측정하였다.
결론: ApoB LNA 안티센스 올리고뉴클레오타이드 (서열 번호 11 및 서열 번호 13) 에 컨쥬게이트된 GalNAc1 및 GalNAc2 는 비컨쥬게이트된 ApoB LNA 보다 양호한 ApoB mRNA 의 녹 다운을 나타냈다 (도 8). GalNAc 1 컨쥬게이트 (서열 번호 13) 는 i.v. 투여가 s.c. 투여 보다 양호한 것으로 보이는데, 이것은 그 반대가 또 다른 GalNAc 클러스터에 대해 보고되었기 때문에 놀라운 것이다 [Alnylam, 9th Annual Meeting of the Oligonucleotide Therapeutics Society]. 총 콜레스테롤 데이터는 GalNAc 클러스터 컨쥬게이트 (서열 번호 11 및 서열 번호 13) 가 i.v. 와 s.c. 둘 다 투여시 비컨쥬게이트된 화합물 및 콜레스테롤 컨쥬게이트된 화합물 (서열 번호 12 및 서열 번호 14) 에 얼마나 양호한 효과를 제공하는지를 나타낸다 (도 9a 및 도 9b). 올리고뉴클레오사이드의 조직 함량 (도 10a-10f) 은 컨쥬게이트가 모 화합물과 비교하여 신장에서 흡수를 덜 제공하면서 간에서 흡수를 얼마나 향상시키는지를 나타낸다. 이것은 i.v. 와 s.c. 투여 둘 다에 대해 유지한다. i.v. 투여시, GalNAc 1 (서열 번호 13) 은 GalNAc 2 (서열 번호 11) 와 비교할 때 간에서 매우 많은 흡수를 제공하지만, 활성은 두 화합물에 대해 양호하기 때문에, GalNAc 2 컨쥬게이트는 GalNAc 1 컨쥬게이트 보다 높은 특이적 활성을 유도하는 것으로 보이는데, 이것은 약동학 조절제 무함유 GalNAc 컨쥬게이트가 LNA 안티센스 올리고뉴클레오타이드에 특히 유용할 수 있는 것을 나타낸다.
재료 및 방법:
실험 디자인:
투여량 투여. 도착시 대략 20 g 인 C57BL/6JBom 암컷 동물에게, 식염수로 제형화된 화합물 또는 식염수 단독의 10 ml/kg BW (0 일 체중에 따름) 를 상기 표에 따라 i.v. 또는 s.c. 투여하였다.
간 및 신장 조직의 샘플채취 . 동물을 70% CO2-30% O2 로 마취시키고, 상기 표에 따라 경부 탈구에 의해 희생시켰다. 큰 간엽의 하나의 절반 및 하나의 신장을 다지고, RNAlater 에 수몰시켰다. 간의 나머지 절반 및 나머지 신장을 동결시키고, 조직 분석을 위해 사용하였다.
총 RNA 단리 및 첫번째 가닥 합성. Qiagen RNeasy 키트 (Qiagen cat. no. 74106) 를 사용하여 제조사의 설명서에 따라 총 RNA 를 RLT-Lysis 버퍼의 존재 하에 비드-분쇄 (bead-milling) 에 의해 균질화된 조직 최대 30 mg 으로부터 추출하였다. Ambion 으로부터의 Reverse Transcriptase 시약을 사용하여 제조사의 설명서에 따라 첫번째 가닥 합성을 수행하였다.
각각의 샘플에 대해, 0.5 μg 의 총 RNA 를 RNase 무함유 H2O 로 (10.8 μl) 로 조정하고, 2 μl 의 랜덤 십량체 (50 μM) 및 4 μl 의 dNTP 믹스 (2.5 mM 각각 dNTP) 와 혼합하고, 70℃ 로 3 분 동안 가열한 후, 샘플을 얼음 상에서 신속히 냉각시켰다. 2 μl 10x Buffer RT, 1 μl 의 MMLV Reverse Transcriptase (100 U/μl) 및 0.25 μl 의 RNase 억제제 (10 U/μl) 를 각각의 샘플에 첨가한 후, 42℃ 에서 60 분 동안 항온처리하고, 95℃ 에서 10 분 동안 효소의 열 불활성화 후 및 샘플을 4℃ 로 냉각시켰다. cDNA 샘플을 1: 5 로 희석하고, 제조사의 프로토콜에 따라 Taqman Fast Universal PCR Master Mix 2x (Applied Biosystems Cat #4364103) 및 Taqman 유전자 발현 어세이 (mApoB, Mn01545150_m1 및 mGAPDH #4352339E) 를 사용하여 RT-QPCR 를 수행하고, Applied Biosystems RT-qPCR 기기 (7500/7900 또는 ViiA7) 에서 신속 모드로 처리하였다. 샌드위치 ELISA 방법을 사용하여 간 및 신장 중의 올리고뉴클레오타이드 함량을 측정하였다.
혈청 콜레스테롤 분석: 희생시키기 직전에, 혈청 제조를 위한 S-monovette Serum-Gel 바이알 (Sarstedt, Numbrecht, Germany) 을 사용하여 안구 뒤 부비강 혈액 (retro-orbital sinus blood) 을 수집하였다. ABX Pentra Cholesterol CP (Triolab, Brondby, Denmark) 를 사용하여 제조사의 설명서에 따라 혈청을 총 콜레스테롤에 대해 분석하였다.
실시예
6:
FVII 의
시험관내
억제 (낮은 투여량,
24 일
)
사용 화합물 - 실시예 1 참조
생체내 마우스 연구는 총 7 개의 군의 마우스 (n=3) 를 사용하여 준비하였다. 각각의 마우스에게 단일 i.v. 투여량의 LNA 화합물을 0.25mg/kg 또는 0.1mg/kg 으로 투여하였다. 식염수 대조군을 포함하였다. 마우스를 투여 전 1 일째에 미리 출혈시키고, 연구 동안 4 일, 7 일, 11 일, 14 일, 18 일 및 24 일에서 후속 출혈시켰다. 24 일째에 마우스를 희생시키고, 간, 신장 및 혈액 샘플을 채취하였다. 연구 설정을 위해 하기 표 (실험 디자인) 를 참조한다. 인자 VII 혈청 수준 및 mRNA 수준을 표준 어세이 기술을 사용하여 측정하였다.
결론: FVII 표적화 LNA 올리고뉴클레오타이드 (서열 번호 3 및 서열 번호 6) 에 컨쥬게이트된 GalNAc 는 0.1 mg/kg 만의 단일 투여량 투여 후 24 일 동안 혈청 중의 FVII 단백질 (도 11) 및 간 중의 24 일째의 mRNA (도 12) 에 대해 매우 양호한 활성을 나타낸다. GalNAc 클러스터 (서열 번호 3 및 서열 번호 6) 는 콜레스테롤 컨쥬게이트 (서열 번호 4 및 서열 번호 7) 와 비교하여 FVII 단백질 및 mRNA 에 대해 보다 더 활성인 것으로 나타났다.
재료 및 방법: 수컷 마우스를 i.v. 투여하고, 하기 도식에 따라 모두 희생시키고 간, 신장 및 혈액을 샘플채취하였다.
실험 디자인:
실시예
7: 비-인간 영장류 연구 -
GalNac
컨쥬게이트
연구 -
PCSK9
및
ApoB
화합물:
대문자는 LNA 뉴클레오사이드 (예를 들면, 베타-D-옥시 LNA) 이고, 소문자는 DNA 뉴클레오사이드이다. 아래첨자 s 는 포스포로티오에이트 인터뉴클레오사이드 연결을 나타낸다. LNA 시토신은 임의로 5-메틸 시토신이다.
본 연구를 위한 일차적 목적은 시아노몰구스 (cynomolgus) 원숭이에 대한 GalNac 클러스터에 컨쥬게이트된 항-PCSK9 및 항-ApoB LNA (Conj2a) 의 느린 일시 주입 후 7 주에 걸쳐 선택된 지질 마커를 조사하고 원숭이에서의 화합물의 잠재적 독성을 평가하기 위한 것이다. 상기 화합물은 멸균 식염수 (0.9%) 중에서 0.625 mg/ml 및 2.5 mg/ml 의 초기 농도로 제조하였다.
24 월령 이상의 수컷 원숭이 (PCSK9) 또는 암컷 원숭이 (ApoB) 원숭이를 사용하고, 수돗물에 자유롭게 접근하게 하고, 180g 의 MWM(E) SQC SHORT 확장 규정식 (Dietex France, SDS, Saint Gratien, France) 을 동물마다 매일 분배할 것이다. 각각의 케이지에 분배된 음식물의 총량은 그 날 케이지에서의 동물의 수에 따라 계산될 것이다. 또한, 과일 또는 채소를 각각의 동물에게 매일 제공할 것이다. 처리 기간의 시작 전에 동물을 14 일 이상의 기간 동안 연구 조건에 적응시킬 것이다. 이러한 기간 동안, 전-처리 연구가 수행될 것이다. 예를 들면, 0.25 mg/kg 또는 1 mg/kg 의 투여량으로 동물에게 i.v. 투여한다. 투여 용적은 0.4 mL/kg 일 것이다. 군 당 2 마리의 동물을 사용한다. 3 주 후, 데이터를 분석할 것이고, 높거나 낮은 투여 섭생을 사용하는 동물의 두번째 군을 개시할 수 있다 - 예비 투여량 설정은 0.5 mg/kg 및 1 mg/kg 이거나, 첫번째 데이터 세트에 기반한 것보다 적다.
투여 제형은 1 일 1 회 투여될 것이다. 처리 후 7 주의 기간 동안 동물을 관찰할 것이며, 51 일째에 연구로부터 방출시킬 것이다. 1 일은 처리 기간의 첫번째 날짜에 상응한다. 임상적 관찰 및 체중 및 음식물 섭취 (군 당) 를 연구 전 및 연구 동안 기록할 것이다.
하기 시점에 혈액을 샘플채취하고, 분석한다:
혈액 생화학
하기 파라미터를 하기에 표시된 경우에 모든 생존 동물에 대해 결정할 것이다:
● 전체 생화학 패널 (하기 완전한 목록) - -8 일째, 15 일째 및 50 일째,
● 간 안정성 (오직 ASAT, ALP, ALAT, TBIL 및 GGT 만) - 4 일째, 8 일째, 22 일째 및 36 일째,
● 지질 프로파일 (총 콜레스테롤, HDL-C, LDL-C 및 트리글리세라이드) 및 Apo-B 만 - -1 일째, 4 일째, 8 일째, 22 일째, 29 일째, 36 일째 및 43 일째.
혈액 (대략 1.0 mL) 을 리튬 헤파린 튜브 내에 충전한다 (ADVIA 1650 혈액 생화학 분석기를 사용함): Apo-B, 나트륨, 칼륨, 클로라이드, 칼슘, 무기 인, 글루코오스, HDL-C, LDL-C, 우레아, 크레아티닌, 총 빌리루빈 (TBIL), 총 콜레스테롤, 트리글리세라이드, 알칼리성 포스파타아제 (ALP), 알라닌 아미노트랜스페라아제 (ALAT), 아스파르테이트 아미노트랜스페라아제 (ASAT), 크레아틴 키나아제, 감마-글루타밀 트랜스페라아제 (GGT), 락테이트 탈수소효소, 총 단백질, 알부민, 알부민/글로불린 비.
혈액 분석: 혈액 샘플을 16 개 군의 동물로부터 오직 -8 일째, -1 일째, 4 일째, 8 일째, 15 일째, 22 일째, 29 일째, 36 일째, 43 일째 및 50 일째에 수집할 것이다.
정맥 혈액 (대략 2 mL) 을 Serum Separating Tube (SST) 내로 각각의 동물의 적절한 정맥으로부터 수집할 것이고, 실온에서 적어도 60±30 분 동안 혈액이 응고되도록 한다. 혈액을 1000 g 에서 10 분 동안 냉장 조건 (+4℃ 로 유지하도록 설정함) 하에서 원심분리할 것이다. 혈청을 3 개의 개별적인 튜브 내로 이동시킬 것이고, ELISA 방법을 사용하여 CitoxLAB France 에서 분석할 때까지 80℃ 에서 저장할 것이다 (Circulex Human PCSK9 ELISA 키트, CY-8079, 사이노몰구스 원숭이로부터의 샘플에 대해 입증됨).
기타 분석: WO 2011009697 및 WO 2010142805 는 다음과 같은 분석을 위한 방법을 제공한다: qPCR, PCSK9 / ApoB mRNA 분석. 기타 분석은 PCSK9 / ApoB 단백질 ELISA, ELISA 에 의한 혈청 Lp(a) 분석 (Mercodia No. 10-1106-01), 조직 및 혈장 올리고뉴클레오타이드 분석 (약물 함량), 샘플, 표준 - 및 QC-샘플의 추출, ELISA 에 의한 올리고뉴클레오타이드 함량 측정을 포함한다. ApoB 컨쥬게이트에 대한 데이터는 도 16 에 도시되어 있다. 동일한 올리고뉴클레오타이드 서열을 보유하는 화합물 11 및 화합물 14 는 사용 투여량에서 현저한 약리학을 나타내지 않은 반면, 동일한 올리고뉴클레오사이드 서열을 공유하는 화합물 서열 번호 17 및 서열 번호 32 는 유효하였고, GalNac 컨쥬게이트된 화합물 (서열 번호 17) 은 콜레스테롤 컨쥬게이트된 화합물 보다 상당히 더 강력하다. ApoB 표적화 화합물에 대한 간독성 또는 신장독성의 징후는 없었다.
PCSK9 표적화 화합물에 대한 데이터는 하기 표에 나타나 있다:
PCSK9 표적화 화합물에 대한 간독성 또는 신장독성의 징후는 없었다. 특히, PCSK9-GalNac 화합물은 광범위한 기간 (연구의 전체 길이) 에 걸쳐 유지된 PCSK9 의 신속하고 높은 효과적인 하향 조절을 제공하였고, GalNac 컨쥬게이트된 화합물은 신속한 초기 녹 다운과 장기 지속 둘 다의 면에서 보다 효과적인 것을 나타내고, 이들은 비컨쥬게이트된 모 화합물과, 대체 컨쥬게이션 기술, 예를 들면, 콜레스테롤 컨쥬게이션을 사용하는 화합물 둘 다와 비교하여 비교적 드물게 낮은 투여량으로 투여될 수 있다. 유사한 결과가 ApoB 표적화 화합물 (도 16 참조) 중의 하나에 대해 나타났는데, 여기서, GalNac 화합물은 또한 콜레스테롤 컨쥬게이트된 화합물 보다 현저하게 더 강력한 것으로 밝혀졌으며, 작용의 보다 긴 지속을 제공하였다. 서열 번호 28 은 연구 기간에 걸쳐 PCSK9 및 LDL-C 의 신속하고 일관된 하향 조절을 제공하였다 (2.5mg/kg 투여량으로 34 일째에 나타났고, 현저한 PCSK9 하향 조절은 2.5mg/kg 단일 투여량의 투여 후 48 일째에 나타났다).
실시예
8:
래트에서의
간 및 신장 독성 평가
본 발명의 화합물을 설치류, 예를 들면, 마우스 또는 래트에서 이의 독성 프로파일에 대해 평가할 수 있다. 예를 들면, 다음과 같은 프로토콜을 사용할 수 있다: Wistar Han Crl:WI(Han) 를 대략 8 주령의 연령에서 사용한다. 이 연령에서, 수컷은 대략 250 g 의 체중이어야 한다. 모든 동물은 SSNIFF R/M-H 펠렛형 유지 규정식 (SSNIFF Spezialdiaten GmbH, Soest, Germany) 및 병에 담긴 수돗물 (0.22 μm 필터로 여과됨) 에 자유롭게 접근한다. 10 mg/kg/투여량 및 40 mg/kg/투여량의 투여 수준을 (피하 투여) 사용하고, 1 일째 및 8 일째에 투여한다. 동물을 15 일째에 안락사시킨다. 소변 및 혈액 샘플을 7 일째 및 14 일째에 수집한다. 임상 병리학 평가를 14 일째에 수행한다. 체중을 연구 전, 투여 첫째 날, 및 부검 1 주일 전에 측정한다. 군 당 음식물 소비를 매일 평가할 것이다. 혈액 샘플을 금식 6 시간 후 꼬리 정맥을 통해 채취한다. 다음과 같은 혈청 분석을 수행한다: 백혈구 계수, 평균 세포 용적, 팩킹된 세포 용적, 헤모글로빈, 평균 세포 헤모글로빈 농도, 평균 세포 헤모글로빈, 혈소판 계수, 백혈구 계수, 세포 형태학을 가진 감별 백혈구 계수, 망상적혈구 계수, 나트륨, 칼륨, 클로라이드, 칼슘, 무기 인, 글루코오스, 우레아, 크레아티닌, 총 빌리루빈, 총 콜레스테롤, 트리글리세라이드, 알칼리성 포스파타아제, 알라닌 아미노트랜스페라아제, 아스파르테이트 아미노트랜스페라아제, 총 단백질, 알부민, 알부민/글로불린 비. α-GST, β-2 마이크로글로불린, 칼빈딘, 클루스테린, 시스타틴 C, KIM-1, 오스테오폰틴, TIMP-1, VEGF 및 NGAL 에 대해 소변분석을 수행한다. 7 가지 분석물 (칼빈딘, 클루스테린, GST-α, KIM-1, 오스테오폰틴, TIMP-1, VEGF) 을 패널 1 (MILLIPLEX® MAP Rat Kidney Toxicity Magnetic Bead Panel 1, RKTX1MAG-37K) 하에 정량할 것이다. 3 가지 분석물 (β-2 마이크로글로불린, 시스타틴 C, 리포칼린-2/NGAL) 을 패널 2 (MILLIPLEX® MAP Rat Kidney Toxicity Magnetic Bead Panel 2, RKTX2MAG-37K) 하에 정량할 것이다. 래트 소변에서의 이들 바이오마커의 농도의 측정을 위한 어세이는 Luminex xMAP® 기술에 근거한다. 항-α-GST / β-2 마이크로글로불린 / 칼빈딘 / 클루스테린 / 시스타신 C / KIM-1 / 오스테오폰틴 / TIMP-1 / VEGF / NGAL 항체로 코팅된 마이크로스피어를 2 가지 상이한 형광 염료로 색상-암호화한다. 다음과 같은 파라미터를 측정한다 (ADVIA 1650 를 사용하는 소변): 소변 단백질, 소변 크레아티닌. 정량적 파라미터: 용적, pH (10-Multistix SG 테스트 스트립/Clinitek 500 소변 분석기를 사용함), 비중 (굴절계를 사용함). 반-정량적 파라미터 (10-Multistix SG 테스트 스트립/Clinitek 500 소변 분석기를 사용함): 단백질, 글루코오스, 케톤, 빌리루빈, 니트라이트, 혈액, 유로빌리노겐, 침전물의 세포학 (현미경 검사에 의함). 정성적 파라미터: 외양, 색상. 희생시킨 후, 체중 및 신장, 간 및 비장 중량을 측정하고 기관 대 체중 비를 계산한다. 신장 및 간 샘플을 채취하고, 동결시키거나 포르말린에 저장할 것이다. 현미경 분석을 실시한다.
실시예
9:
FAM
라벨
컨쥬게이트를
가지는
ApoB
표적화
화합물
대문자는 LNA 뉴클레오사이드 (예를 들면, 베타-D-옥시 LNA) 이고, 소문자는 DNA 뉴클레오사이드이다. 아래첨자 s 는 포스포로티오에이트 인터뉴클레오사이드 연결을 나타낸다. LNA 시토신은 임의로 5-메틸 시토신이다.
상이한 DNA/PO-링커를 가진 FAM-라벨링된 ASO 에 S1 뉴클레아제 추출물 - 하기 표 참조 - 에서 시험관내 절단을 실시하였다. 간 또는 신장 균질물 또는 혈청 (하기 표 참조).
상이한 DNA/PO-링커를 가진 FAM-라벨링된 ASO 100 μM 에, 20 분 및 120 분 동안 뉴클레아제 버퍼 (60 U pr. 100 μL) 중에서 S1 뉴클레아제에 의한 시험관내 절단을 실시하였다 (A). EDTA 를 버퍼에 첨가함으로써 효소적 활성을 정지시켰다. 이어서, Dionex DNApac p-100 컬럼 및 10mM-1M 나트륨 퍼클로레이트 (pH 7.5) 의 범위의 구배를 사용하는 Dionex Ultimate 3000 상에서 AIE HPLC 분석을 상기 용액에 실시하였다. 절단 및 비-절단된 올리고뉴클레오타이드의 함량을 615 nm 에서의 형광 검출기와 260 nm 에서의 UV 검출기 둘 다를 사용하여 표준에 대해 측정하였다.
결론: PO 링커 (또는 본원에 언급된 영역 B) 는 컨쥬게이트 (또는 C 기) 가 절단 제거 (cleaved off) 되도록 야기하고, 링커의 길이 및/또는 서열 조성 둘 다는 영역 B 의 핵분해 절단에 대한 감수성을 조절하는데 사용될 수 있다. DNA/PO-링커의 서열은 뉴클레아제 S1 추출물 (상기 표 참조) 에서 20 분 후에 나타나는 바와 같이 절단 속도를 조절할 수 있다. 그러므로, 영역 B 에 대한 (예를 들면, DNA/PO-링커에 대한) 서열 선택은 또한 표적 조직의 세포내 및 혈청내 절단 수준을 조절하는데 사용될 수 있다.
간, 신장 및 혈청 (하기 표 참조) 은 올리고뉴클레오타이드 서열 번호 21 을 이용하여 200 μg/g 조직의 농도까지 급등하였다. NMRI 마우스로부터 수집된 간 및 신장 샘플을 균질화 버퍼 (0.5% Igepal CA-630, 25 mM Tris pH 8.0, 100 mM NaCl, pH 8.0 (1N NaOH 로 조정됨) 에서 균질화하였다. 균질물을 24 시간 동안 37℃ 에서 항온처리하고, 이후 균질물을 페놀-클로로포름으로 추출하였다. 간 및 신장으로부터와 혈청으로부터의 추출물 중 절단 및 비 절단된 올리고뉴클레오타이드의 함량을 상기 HPLC 방법을 사용하여 표준에 대해 측정하였다.
결론: PO 링커 (또는 본원에 언급된 영역 B) 는 간 또는 신장 균질물 중에서는 올리고뉴클레오타이드로부터 컨쥬게이트 (또는 C 기) 의 절단을 야기하지만, 혈청에서는 아니다. 참고: 상기 어세이에서의 절단은 절단가능한 링커의 절단을 의미하고, 올리고머 또는 영역 A 는 기능적으로 온전하게 유지되어야 한다.
상기 어세이에서의 절단에 대한 감수성은 링커가 생체-절단가능하거나 생리학적으로 불안정한지를 결정하는데 사용될 수 있다.
실시예
10:
GalNac
컨쥬게이트
:
래트
독성 연구
방법론: 실시예 8 참조
래트 안전성 연구는 CiToxLabs (France) 에서 수행하였다. 수컷 Wistar 래트 (n=4/군) 를 본 연구를 위해 선택하였는데, 이는 사용된 연구 설정 (투여량 범위 및 시간 경과) 에서의 Wistar Han 래트가 인간에서 신장 (및 어느 정도까지의 간) 독성을 예측하는 것으로 입증되었기 때문이다. 컨쥬게이트된 LNA 화합물 (10 mg/kg) 또는 상응하는 비컨쥬게이트된 "모 화합물" 40 mg/kg) 을 1 일째 및 8 일째에 동물에게 s.c. 주사하였다. 7 일째 및 14 일째에 소변을 수집하고, 분석 때까지 얼음 상에서 유지하였다. 소변 샘플을 원심분리하고 (대략 380 g, 5 분, +4℃ 에서), Luminex xMAP® 기술에 기반하는 다중 어세이로 소변 손상 마커의 패널을 분석하였다.
최근에 소변 신장 손상 마커의 메타-분석에서 KIM-1에 대해 기술된 바와 같이, 소변 신장 손상 마커의 패널 중에서 연구 KIM-1 (신장 손상 마커 1) 에서 가장 큰 동적 범위와 가장 명확한 신호를 나타냈다 [Vlasakova et al, Evaluation of the Relative Performance of Twelve Urinary Biomarkers for Renal Safety across Twenty Two Rat Sensitivity and Specificity Studies Toxicol . Sci . December 21, 2013].
사용 화합물: 서열 번호 11 및 서열 번호 17 (표적 ApoB) 및 하기 PCSK9 표적화 화합물 서열 번호:
그 결과는 Galnac 컨쥬게이트의 사용이 모 LNA 화합물의 신장독성 프로파일을 크게 향상시킬 수 있는 것을 설명하는 도 15 에 나타나 있다. 그러므로, GalNac 컨쥬게이트된 LNA 화합물은 이의 모 화합물 보다 상당히 더 강력할 뿐만 아니라, 신장독성의 위험에서의 현저한 감소와 연관되어 있다.
실시예
11:
LNA
antimiR
GalNac
컨쥬게이트
화합물
대문자는 LNA, 예를 들면, 베타-D-옥시 LNA 이다. 소문자는 DNA 이다. 아래첨자 s 는 포스포로티오에이트 연결이다. 기타 인터뉴클레오사이드 연결은 포스포디에스테르 (포스페이트) 연결이다. C 앞의 위첨자 m 은 LNA 5-메틸 시토신 (임의적) 을 나타낸다. 일부 실시형태에서, 화합물은 또한 LNA 시토신으로 제조될 수 있다. 일부 실시형태에서, Conj1a 군은 또 다른 GalNAc 컨쥬게이트 기, 예를 들면, 본원에서 기재된 것들, 예를 들면, Conj2a 일 수 있다.
miR-122 (타이니) 5'- mCsAs mCsAs mCsTs mCs mC -3' (서열 번호 51)
GalNAc-타이니 5'-Conj1a mCsAs mCsAs mCsTs mCs mC -3' (서열 번호 52)
타이니-링커-타이니 5'- mCsAs mCsAs mCsTs mCs mCcamCsAs mCsAs mCsTs mCs mC -3' (서열 번호 53)
GalNac-타이니-링커-타이니 5'-Conj1a mCsAs mCsAs mCsTs mCs mCcamCsAs mCsAs mCsTs mCs mC -3' (서열 번호 54)
생체내 마우스 연구는 총 9 개의 군의 마우스 (n=5) 를 사용하여 수행하였다. 0 일째, 2 일째 및 4 일째에 각각의 마우스에게 모 LNA 화합물과 비교되는 GalNAc 컨쥬게이트된 LNA 를 0.5 mg/kg 또는 2 mg/kg 또는 등몰 투여량으로 i.v. 투여하였다. 식염수 대조군을 포함하였다 (표 1 에서 설정된 연구 참조). 혈청 샘플을 투여 4 일전, 중간일 4 일째 및 종료일 7 일째에 채취하였다. 간 및 신장 샘플을 후에 RNA 에 저정하였다. miR122 의 miR122 녹 다운의 검증을 문헌 [Obad Nat Genet. 2011 Mar 20; 43(4): 371-8] 에서 기재된 바와 같이 수행하였다 (도 17). 혈청 중 콜레스테롤 수준을 문헌 [Elmen J, et al. LNA-mediated microRNA silencing in non-human primates. Nature. 2008; 452: 896-899] 에 기재된 바와 같이 분석하하고 (도 18), 2 개의 miR122 하향 조절 유전자 (Aldo A 및 Bckdk) 의 mRNA 수준을 표준 QPCR 어세이 기술을 사용하여 분석하였다 (도 19). ALT 를 측정하여 화합물의 내약성을 평가하였다 (도 20).
연구 설정
결론: anti-miR122 에 대한 GalNAc 의 컨쥬게이션 (서열 번호 52 및 서열 번호 54) 은, 낮은 투여량 군에서 이미 감소된 총 콜레스테롤 수준 (도 2) 및 Aldo A 및 Bckdk mRNA 의 하향 조절 (도 3, 3x 0,5 mg/kg) 로 표시되는, 간에서 miR122 녹 다운의 현저한 향상을 나타냈다. anti- miR122 올리고뉴클레오타이드의 효과는 신장에서 나타나지 않았다. 하나의 GalNAc (서열 번호 54) 에 대한 2 개의 올리고뉴클레오타이드의 컨쥬게이션에 의해 향상하는 경향을 나타낸 서열 번호 52 에 대해서 ALT 에서의 감소를 측정하였다.
실시예
12:
HBV
표적화
올리고뉴클레오타이드에
대한
GalNac
컨쥬게이트
Expedite 8900/MOSS 합성기 (Multiple Oligonucleotide Synthesis System) 상에서 4 μmol 규모로, 포스포라미디트 접근법을 사용하여 우리딘 범용 지지체 상에서 올리고뉴클레오타이드를 합성하였다. 합성 종료시에, 올리고뉴클레오타이드를 1-2 시간 동안 실온에서 수성 암모니아를 사용하여 고체 지지체로부터 절단하였고, 16 시간 동안 65℃ 에서 추가로 탈보호하였다. 올리고뉴클레오타이드를 역상 HPLC (RP-HPLC) 로 정제하고, UPLC 로 특성화하고, 분자 질량을 ESI-MS 에 의해 추가로 확인하였다. 더욱 상세내용은 하기를 참조한다.
올리고뉴클레오타이드의
신장
β-시아노에틸-포스포라미디트 (DNA-A(Bz), DNA-G(ibu), DNA-C(Bz), DNA-T, LNA-5-메틸-C(Bz), LNA-A(Bz), LNA-G(dmf), LNA-T 또는 C6-S-S 링커) 의 커플링은 아세토니트릴 중의 0.1 M 의 5'-O-DMT-보호된 아미다이트 및 활성화제로서의 아세토니트릴 (0.25 M) 중의 DCI (4,5-디시아노이미다졸) 의 용액을 사용하여 수행하였다. 최종 사이클을 위해서, 시판되는 C6-연결된 콜레스테롤 포스포라미디트를 DCM 중의 0.1M 로 사용하였다. 포스포르티오에이트 연결의 도입을 위한 티올화는 수소화 잔탄 (아세토니트릴/피리딘 9:1 중의 0.01 M) 을 사용하여 수행된다. 포스포르디에스테르 연결은 THF/피리딘/물 7:2:1 중의 0.02 M 요오드를 사용하여 도입된다. 시약의 나머지는 올리고뉴클레오타이드 합성에 전형적으로 사용되는 것들이다. 고상 합성 후 배치 동안, 시판되는 C6 아미노링커 포스포라미디트를 고상 합성의 마지막 사이클에서 사용하고, 탈보호 및 고체 지지체로부터의 절단 후, 아미노 연결된 탈보호 올리고뉴클레오타이드를 단리하였다. 표준 합성 방법을 사용하여 컨쥬게이트를 작용기의 활성화를 통해 도입하였다.
RP - HPLC 에 의한 정제:
조 화합물을 Phenomenex Jupiter C18 10μ 150x10 mm 컬럼 상의 분취용 RP-HPLC 에 의해 정제하였다. 0.1 M 암모늄 아세테이트 pH 8 및 아세토니트릴을 5 mL/분의 유속으로 버퍼로서 사용하였다. 수집된 분획을 동결건조시켜, 백색 고체로서 전형적으로 정제된 화합물을 수득하였다.
약어:
DCI:
4,5-디시아노이미다졸
DCM:
디클로로메탄
DMF:
디메틸포름아미드
DMT:
4,4'-디메톡시트리틸
THF:
테트라하이드로푸란
Bz:
벤조일
Ibu:
이소부티릴
RP-HPLC: 역상 고성능 액체 크로마토그래피
LNA 갭머는 하기와 같았다:
5'-G s A s G s G s c s a s t s a s g s c s a s g s m C s A s G s G - 3' (서열 번호 55)
5' GalNac (Conj1a) 를 가지는 5'-G s A s G s G s c s a s t s a s g s c s a s g s m C s A s G s G - 3' (서열 번호 56).
상기 갭머 화합물 (비컨쥬게이트 버젼) 은 HBV 에 대해 특히 효과적인 것으로 당업계에서 이미 강조되었다 (WO 2011/47312).
대문자는 LNA 뉴클레오사이드, 예를 들면, 베타-D-옥시 LNA 이고, 소문자는 DNA 뉴클레오사이드이고, 아래첨자 s 는 포스포로티오에이트 연결이다. LNA 시토신은 5-메틸 시토신일 수 있다.
LNA 올리고머를 마우스 계통, 예를 들면, BALB/c 또는 C57B/6 에서 생체내 항바이러스 효과에 대해 평가할 수 있는데, 여기서, HBV 복제는 플라스미드, 예를 들면, 부분 반복 HBV 전유전체 RNA 를 발현하는 pAAV/HBV1.3 [J Virol. 1995 Oct;69(10):6158-69] 또는 또는 pAAV2/HBV1.3, 이의 유도체 (WuxiAppTech, Wuxi, China) 의 유체역학적 꼬리 정맥 주입에 의해 확립될 수 있다. 마우스의 체질량의 8-12% 인 높은 용적의 식염수 중의 플라스미드의 주입은 간에서 바이러스 전유전체 RNA 의 축적 및 발현을 초래하고, 후속적으로 급성 HBV 감염의 확립을 유도할 것이다. LNA 올리고머에 의한 동물의 처리는 플라스미드 주입 1 일 이상 전에 또는 플라스미드 주입 1 일후에 개시될 수 있다. 식염수 중의 LNA 올리고머의 전달을 정맥내 또는 피하 주사로 수행할 수 있다.
연구 설정
생체내 실험을 서열 번호 55 및 서열 번호 56 에 대해 수행하였고, 후자는 전자의 GalNAC 컨쥬게이트이다 (conj1a). Balb/C 마우스 계통을 사용하는 마우스 유체역학적 꼬리 정맥 주입 모델에서 HBV 에 대한 효능에 대해 LNA 화합물을 테스트하였다. LNA 화합물을 등몰 투여량; 2 mg/kg 및 10 mg/kg, 단일 주입 (서열 번호 55) 및 2.7 mg/kg 및 13.5 mg/kg, 단일 주입 (서열 번호 56) 으로 테스트하였다. LNA 항-HBV 화합물을 식염수 및 HBV 역전사 효소의 억제제 엔테카비르와 비교하였다. 엔테카비르를 0.1 mg/kg.으로 매일 p.o. 투여하였다. 적용가능한 경우, 동물을 유체역학적 주입 24 시간 전에 LNA 화합물로 처리하였다. 유체역학적 주입 24 시간 후부터, 기술된 바와 같이 엔테카비르를 일일 투여량으로 제공하였다.
생체 내에서 HBV 복제를 개시하기 위해서, 모든 동물에게 꼬리 정맥을 통해 식염수 중의 pAAV2/ HBV 플라스미드 DNA 20 μg 을 주입하였다. 마우스 체중의 8% 와 동등한 식염수 용액으로 주입을 수행하고, 총 투여량을 5 초 이내에 제공하였다. 동물을 2 시간 이상 동안 관찰하여 유체역학적 쇼크로부터의 회복을 보장하였다.
모든 동물을 생체내 연구 기간 동안 체중 변화 및 임상적 징후에 대해 매일 모니터링하였다. 유체역학적 주입 후 1 일째, 3 일째, 5 일째 및 7 일째에, 엔테카비르의 투여 4 시간 후 턱밑샘 출혈에 의해 혈액 샘플을 모든 동물로부터 수집하였다. 7 일째에, 엔테카비르의 마지막 투여 4 시간 후 안락사시에 모든 동물로부터 심장 천공을 통해 혈액을 채취하였다. 이들의 간을 수확하고, 샘플을 즉시 동결시켰다. 모든 혈액 샘플을 헤파린 나트륨을 함유하는 튜브 내에 수집하였다.
각 간의 좌측 간엽의 일부를 사용하여 qPCR 에 의한 HBV DNA 복제의 수준을 간의 단위 중량 당 카피로서 측정하였는데, 여기서, 총 HBV DNA 수준의 양은 pAAV2/HBV DNA 수준의 양에 의해 감산된다. 7 일째에 수집된 혈장 샘플을 ALT 수준에 대해 샌드위치 ELISA 어세이 (Cusabio; Cat. NO. CSB-E16539m) 를 사용하여 테스트하였다. LNA 컨쥬게이트 올리고머에 대한 내약성은 양호하였으며, ALT 의 현저한 상승은 관찰되지 않았다.
결론: HBV 에 대해 특히 효과적인 것으로 당업계에서 이미 강조된 서열 번호 55 (WO2011/47312) 는, 본 연구에서 사용된 투여량 수준으로 간에서 HBV 의 복제에 대해 거의 영향을 미치지 않은 것으로 밝혀졌다. 이와 대조적으로, 동일한 올리고뉴클레오타이드로 이루어지고 부착된 GalNAC 컨쥬게이트만을 가지는 서열 번호 56 은, 단일 투여량 전달 후 8 일째 및 감염 개시 후 7 일째에 간에서 바이러스 역가 (virus titer) 의 90% 감소와 함께, 간에서 HBV DNA 수준에 대해 탁월한 투여량-의존적 항바이러스 효과 (도 22) 를 가지는 것으로 나타났다. 화합물에 대한 내약성은 양호하였으며, 임의의 화합물의 ALT 수준에서의 투여량-의존적 증가의 증거는 없었다. LNA 안티센스 올리고뉴클레오타이드는 컨쥬게이션의 부재 하에 간에 대해 효율적으로 표적화되는 것으로 알려져 있다 - 모 화합물의 비교적인 무효성과 컨쥬게이트된 화합물의 매우 강력한 효과는 주목할만한 것이다.
SEQUENCE LISTING
<110> Santaris Pharma A/S
<120> LNA OLIGONUCLEOTIDE CARBOHYDRATE CONJUGATES
<130> 1139WO
<150> EP13153296.2
<151> 2013-01-30
<150> EP13157237.2
<151> 2013-02-28
<150> EP13174092.0
<151> 2013-06-27
<150> EP13192938.2
<151> 2013-11-14
<150> EP13192931.7
<151> 2013-11-14
<150> EP13192930.9
<151> 2013-11-14
<150> PCT/EP2013/073859
<151> 2013-11-14
<160> 62
<170> PatentIn version 3.5
<210> 1
<211> 13
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(13)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(13)
<223> n is a, c, g, or t
<220>
<221> misc_feature
<222> (11)..(13)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 1
nnnnnnnnnn nnn 13
<210> 2
<211> 13
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(13)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(13)
<223> n is a, c, g, or t
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 C6 amino linkage group
<220>
<221> misc_feature
<222> (11)..(13)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 2
nnnnnnnnnn nnn 13
<210> 3
<211> 13
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(13)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(13)
<223> n is a, c, g, or t
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 GalNac cluster
<220>
<221> misc_feature
<222> (11)..(13)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 3
nnnnnnnnnn nnn 13
<210> 4
<211> 13
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(13)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(13)
<223> n is a, c, g, or t
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 disulphide linked cholesterol conjugate
<220>
<221> misc_feature
<222> (11)..(13)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 4
nnnnnnnnnn nnn 13
<210> 5
<211> 13
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(10)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(13)
<223> n is a, c, g, or t
<220>
<221> misc_feature
<222> (1)..(1)
<223> disulphide liked cholesterol conjugate
<220>
<221> misc_feature
<222> (11)..(13)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 5
nnnnnnnnnn nnn 13
<210> 6
<211> 15
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(15)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 3xGalNac cluster Conj1a
<220>
<221> misc_feature
<222> (3)..(5)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (3)..(15)
<223> n is a, c, g, or t
<220>
<221> misc_feature
<222> (13)..(15)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 6
cannnnnnnn nnnnn 15
<210> 7
<211> 15
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(15)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(1)
<223> cholesterol conjugate
<220>
<221> misc_feature
<222> (3)..(5)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (3)..(15)
<223> n is a, c, g, or t
<220>
<221> misc_feature
<222> (13)..(15)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 7
cannnnnnnn nnnnn 15
<210> 8
<211> 13
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(13)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 monoGalNAc
<220>
<221> misc_feature
<222> (11)..(13)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 8
gcattggtat tca 13
<210> 9
<211> 13
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(13)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 disulphide linked monoGalNAc
<220>
<221> misc_feature
<222> (11)..(13)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 9
gcattggtat tca 13
<210> 10
<211> 15
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(3)
<223> phosphodiester lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 GalNAc conjugate
<220>
<221> misc_feature
<222> (3)..(15)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (3)..(4)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (13)..(15)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 10
cagcattggt attca 15
<210> 11
<211> 13
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(13)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 3xGalNAc cluster Conj2a
<220>
<221> misc_feature
<222> (11)..(13)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 11
gcattggtat tca 13
<210> 12
<211> 13
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(13)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (11)..(13)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 12
gcattggtat tca 13
<210> 13
<211> 13
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(13)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 3xGalNAc cluster Conj1a
<220>
<221> misc_feature
<222> (11)..(13)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 13
gcattggtat tca 13
<210> 14
<211> 15
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(3)
<223> phosphodiester lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 cholesterol conjugate
<220>
<221> misc_feature
<222> (3)..(15)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (3)..(4)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (13)..(15)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 14
cagcattggt attca 15
<210> 15
<211> 16
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(16)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(3)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 3xGalNAc cluster Conj2a
<220>
<221> misc_feature
<222> (14)..(16)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 15
aatgctacaa aaccca 16
<210> 16
<211> 16
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(16)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 3xGalNAc cluster Conj2a
<220>
<221> misc_feature
<222> (14)..(16)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 16
tgctgtgtga gcttgg 16
<210> 17
<211> 12
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(12)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 3xGalNAc cluster Conj2a
<220>
<221> misc_feature
<222> (11)..(12)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 17
gttgacactg tc 12
<210> 18
<211> 14
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(2)
<223> phosphodiester lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 FAM conjugate
<220>
<221> misc_feature
<222> (2)..(14)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (2)..(3)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (12)..(14)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 18
agcattggta ttca 14
<210> 19
<211> 16
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(4)
<223> phosphodiester lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 FAM conjugate
<220>
<221> misc_feature
<222> (4)..(16)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (4)..(5)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (14)..(16)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 19
gacgcattgg tattca 16
<210> 20
<211> 13
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(13)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 FAM conjugate
<220>
<221> misc_feature
<222> (11)..(13)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 20
gcattggtat tca 13
<210> 21
<211> 16
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(4)
<223> phosphodiester lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 FAM conjugate
<220>
<221> misc_feature
<222> (4)..(16)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (4)..(5)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (14)..(16)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 21
tcagcattgg tattca 16
<210> 22
<211> 14
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(14)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(3)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (12)..(14)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 22
tgctacaaaa ccca 14
<210> 23
<211> 16
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(16)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(3)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (13)..(16)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 23
aatgctacaa aaccca 16
<210> 24
<211> 16
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(16)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(3)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (14)..(16)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 24
aatgctacaa aaccca 16
<210> 25
<211> 15
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(15)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (14)..(15)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 25
gctgtgtgag cttgg 15
<210> 26
<211> 16
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(16)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (14)..(16)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 26
tgctgtgtga gcttgg 16
<210> 27
<211> 14
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(14)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(3)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 3xGalNAc cluster Conj2a
<220>
<221> misc_feature
<222> (12)..(14)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 27
tgctacaaaa ccca 14
<210> 28
<211> 16
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(16)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(3)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 3xGalNAc cluster Conj2a
<220>
<221> misc_feature
<222> (13)..(16)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 28
aatgctacaa aaccca 16
<210> 29
<211> 15
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(15)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 3xGalNAc cluster Conj2a
<220>
<221> misc_feature
<222> (14)..(15)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 29
gctgtgtgag cttgg 15
<210> 30
<211> 18
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 cholesterol conjugate
<220>
<221> misc_feature
<222> (3)..(18)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (3)..(5)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (15)..(18)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 30
caaatgctac aaaaccca 18
<210> 31
<211> 18
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 cholesterol conjugate
<220>
<221> misc_feature
<222> (3)..(18)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (3)..(4)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (16)..(18)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 31
catgctgtgt gagcttgg 18
<210> 32
<211> 14
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 cholesterol conjugate
<220>
<221> misc_feature
<222> (3)..(14)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (3)..(4)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (13)..(14)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 32
cagttgacac tgtc 14
<210> 33
<211> 9
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(9)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(9)
<223> LNA nucleosides, LNA C optionally 5-methyl C
<400> 33
tcacactcc 9
<210> 34
<211> 23
<212> RNA
<213> H.sapiens
<220>
<221> misc_feature
<223> Mature microRNA-122
<400> 34
uggaguguga caaugguguu ugu 23
<210> 35
<211> 9
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(9)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(9)
<223> LNA nucleosides, LNA C optionally 5-methyl C
<400> 35
tacaatgca 9
<210> 36
<211> 9
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(9)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(9)
<223> LNA nucleosides, LNA C optionally 5-methyl C
<400> 36
acaatgcac 9
<210> 37
<211> 8
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(8)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(8)
<223> LNA nucleosides, LNA C optionally 5-methyl C
<400> 37
acaatgca 8
<210> 38
<211> 7
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(7)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(7)
<223> LNA nucleosides, LNA C optionally 5-methyl C
<400> 38
caatgca 7
<210> 39
<211> 21
<212> RNA
<213> H.sapiens
<220>
<221> misc_feature
<223> Mature microRNA-33a
<400> 39
gugcauugua guugcauugc a 21
<210> 40
<211> 20
<212> RNA
<213> H.sapiens
<220>
<221> misc_feature
<223> Mature microRNA-33a
<400> 40
gugcauugcu guugcauugc 20
<210> 41
<211> 9
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(9)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(9)
<223> LNA nucleosides, LNA C optionally 5-methyl C
<400> 41
tgataagct 9
<210> 42
<211> 8
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(8)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(8)
<223> LNA nucleosides, LNA C optionally 5-methyl C
<400> 42
gataagct 8
<210> 43
<211> 7
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(7)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(7)
<223> LNA nucleosides, LNA C optionally 5-methyl C
<400> 43
ataagct 7
<210> 44
<211> 15
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(15)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(15)
<223> LNA nucleosides at positions 1, 3, 4, 6, 7, 8, 10, 12, 14, 15 &
LNA C optionally 5-methyl C
<400> 44
tcagtctgat aagct 15
<210> 45
<211> 22
<212> RNA
<213> H.sapiens
<220>
<221> misc_feature
<223> Mature microRNA-21
<400> 45
uagcuuauca gacugauguu ga 22
<210> 46
<211> 9
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(9)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(9)
<223> LNA nucleosides, LNA C optionally 5-methyl C
<400> 46
caatgtagc 9
<210> 47
<211> 8
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(8)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(8)
<223> LNA nucleosides, LNA C optionally 5-methyl C
<400> 47
aatgtagc 8
<210> 48
<211> 7
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(7)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(7)
<223> LNA nucleosides, LNA C optionally 5-methyl C
<400> 48
atgtagc 7
<210> 49
<211> 23
<212> RNA
<213> H.sapiens
<220>
<221> misc_feature
<223> Mature microRNA-221
<400> 49
agcuacauug ucugcugggu uuc 23
<210> 50
<211> 12
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide
<220>
<221> misc_feature
<222> (1)..(12)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (11)..(12)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 50
gttgacactg tc 12
<210> 51
<211> 8
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(9)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(9)
<223> LNA beta-D-oxy-nucleosides, LNA C are 5-methyl C
<400> 51
cacactcc 8
<210> 52
<211> 8
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(9)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(9)
<223> LNA beta-D-oxy-nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 3xGalNAc conjugate, e.g Conj1a or conj2a.
<400> 52
cacactcc 8
<210> 53
<211> 18
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(8)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(9)
<223> LNA beta-D-oxy-nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (11)..(18)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (11)..(18)
<223> LNA beta-D-oxy-nucleosides, LNA C are 5-methyl C
<400> 53
cacactccca cacactcc 18
<210> 54
<211> 18
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(8)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(9)
<223> LNA beta-D-oxy-nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 3xGalNAc conjugate, e.g Conj1a or conj2a.
<220>
<221> misc_feature
<222> (11)..(18)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (11)..(18)
<223> LNA beta-D-oxy-nucleosides, LNA C are 5-methyl C
<400> 54
cacactccca cacactcc 18
<210> 55
<211> 16
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(16)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(4)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (13)..(16)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 55
gaggcatagc agcagg 16
<210> 56
<211> 16
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(16)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(4)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5GalNAc conjugate, e.g. conj1a or Conj2a
<220>
<221> misc_feature
<222> (13)..(16)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 56
gaggcatagc agcagg 16
<210> 57
<211> 15
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(15)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(15)
<223> LNA nucleosides at position 1, 3, 6, 7, 10, 12, 14 & 15, LNA C
are 5-methyl C
<400> 57
ccattgtcac actcc 15
<210> 58
<211> 7
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(7)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(7)
<223> LNA nucleosides, LNA C are optionally 5-methyl C
<400> 58
acactcc 7
<210> 59
<211> 8
<212> DNA
<213> artificial
<220>
<223> LNA antisense oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(7)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(7)
<223> LNA nucleosides, LNA C are optionally 5-methyl C
<400> 59
cacactcc 8
<210> 60
<211> 14
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(14)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(3)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> optional 5 conjugate e.g 5 3xGalNAc conjugate, e.g. conj1a or
Conj2a
<220>
<221> misc_feature
<222> (12)..(14)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 60
attccctgcc tgtg 14
<210> 61
<211> 28
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer poly-oligonucleotide
<220>
<221> misc_feature
<222> (1)..(12)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(2)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 conjugate e.g 5 3xGalNAc conjugate, e.g. conj1a or Conj2a
<220>
<221> misc_feature
<222> (11)..(12)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (15)..(28)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (15)..(17)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (26)..(28)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 61
gttgacactg tccaattccc tgcctgtg 28
<210> 62
<211> 15
<212> DNA
<213> artificial
<220>
<223> LNA antisense gapmer oligonucleotide conjugate
<220>
<221> misc_feature
<222> (1)..(3)
<223> phosphodiester lnternucleoside linkages
<220>
<221> misc_feature
<222> (1)..(1)
<223> 5 FAM conjugate
<220>
<221> misc_feature
<222> (3)..(15)
<223> phosphorothioate lnternucleoside linkages
<220>
<221> misc_feature
<222> (3)..(4)
<223> LNA nucleosides, LNA C are 5-methyl C
<220>
<221> misc_feature
<222> (13)..(15)
<223> LNA nucleosides, LNA C are 5-methyl C
<400> 62
cagcattggt attca 15
Claims (29)
- LNA 안티센스 올리고머 및 상기 LNA 안티센스 올리고머에 공유 결합된, 탄수화물을 포함하는 컨쥬게이트 모이어티 (moiety), 예를 들면, 탄수화물 컨쥬게이트 모이어티를 포함하는 LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항에 있어서, 상기 탄수화물 컨쥬게이트 모이어티는 갈락토오스, 갈락토사민, N-포르밀-갈락토사민, N-아세틸갈락토사민, N-프로피오닐-갈락토사민, N-n-부타노일-갈락토사민 및 N-이소부타노일갈락토사민으로 이루어진 군으로부터 선택되는, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 또는 제 2 항에 있어서, 상기 탄수화물 컨쥬게이트 모이어티는 아시알로당단백질 수용체 표적화 모이어티인, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 3 항 중 어느 한 항에 있어서, 상기 컨쥬게이트 모이어티는 약동학 조절제, 예를 들면, 소수성 기, 예를 들면, C16-20 소수성 기, 스테롤, 콜레스테롤을 추가로 포함하는, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 4 항 중 어느 한 항에 있어서, 상기 탄수화물 컨쥬게이트 모이어티는 갈락토오스, 예를 들면, 갈락토오스 클러스터를 포함하는, LNA 안티센스 올리고머 컨쥬게이트.
- 제 5 항에 있어서, 상기 갈락토오스 클러스터는 N-아세틸갈락토사민 삼량체로 이루어지는, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 6 항 중 어느 한 항에 있어서, 상기 탄수화물 컨쥬게이트 모이어티는 생리학적으로 절단가능한 링커를 통해 상기 올리고머에 공유 연결되어 있는, LNA 안티센스 올리고머 컨쥬게이트.
- 제 7 항에 있어서, 상기 생리학적으로 절단가능한 링커는 산 불안정성 링커, 디설파이드 링커, 포스포디에스테르 링커 뉴클레오사이드의 영역 (영역 B) 으로 이루어진 군으로부터 선택되는, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 8 항 중 어느 한 항에 있어서, 상기 컨쥬게이트 모이어티는 링커, 예를 들면, 생리학적으로 절단가능한 링커를 통해 상기 탄수화물 컨쥬게이트 모이어티에 부착되어 있는 약동학 조절제를 추가로 포함하는, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 9 항 중 어느 한 항에 있어서, 올리고뉴클레오타이드는 7-26 개, 예를 들면, 7-18 개, 7-10 개, 10-16 개, 12-14 개의 인접 뉴클레오사이드를 가지는, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 10 항 중 어느 한 항에 있어서, 상기 LNA 안티센스 올리고머는 LNA 갭머, 및 LNA 믹스머, LNA 토탈머 또는 LNA 타이니 (tiny) 올리고머인, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 10 항 중 어느 한 항에 있어서, 상기 LNA 안티센스 올리고머는 포스포로티오에이트 링커 올리고머인, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 12 항 중 어느 한 항에 있어서, 상기 올리고머는 간-발현 핵산, 예를 들면, RNA, 예를 들면, 간-발현 mRNA 또는 microRNA 또는 바이러스 핵산을 표적화하는, LNA 안티센스 올리고머 컨쥬게이트.
- 제 13 항에 있어서, 상기 간-발현 RNA 는 (보체) 인자 VII, 보체 인자 C6, Bcl2, TTR, PCSK9, ApoB, GCGR, CRP, DGAT2, GCCR, PTEN, PTP1B, SGLT2 및 SOD1, 또는 바이러스 RNA, 예를 들면, C 형 간염 또는 B 형 간염으로 이루어진 군으로부터 선택된 mRNA 인, LNA 안티센스 올리고머 컨쥬게이트.
- 제 13 항 또는 제 14 항에 있어서, 상기 올리고머는 갭머 또는 숏트머 올리고머인, LNA 안티센스 올리고머 컨쥬게이트.
- 제 13 항에 있어서, 상기 올리고머는 간-발현 microRNA, 예를 들면, miR-122 를 표적화하는, LNA 안티센스 올리고머 컨쥬게이트.
- 제 13 항 또는 제 16 항에 있어서, 상기 올리고머는 8-18 개 사이의 길이의 뉴클레오타이드인, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 17 항 중 어느 한 항에 있어서, B 형 간염 핵산, 예를 들면, HBV DNA 및/또는 RNA 서열을 표적화하는, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 18 항 중 어느 한 항에 있어서, 의약품에서 사용하기 위한, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 18 항 중 어느 한 항에 있어서, 간-발현 RNA 를 하향 조절하는데 사용하기 위한, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 18 항 중 어느 한 항에 있어서, 대사성 질환 또는 장애, 예를 들면, 간 질환 또는 장애의 치료에 사용하기 위한, LNA 안티센스 올리고머 컨쥬게이트.
- 제 16 항 내지 제 18 항 중 어느 한 항에 있어서, 간염, 예를 들면, B 형 간염 또는 C 형 간염의 치료에 사용하기 위한, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 18 항 중 어느 한 항에 있어서, 질환 또는 장애, 예를 들면, 제 1 항 내지 제 22 항 중 어느 한 항에서 정의된 것들의 치료를 위한 약제의 제조에서 사용하기 위한, LNA 안티센스 올리고머 컨쥬게이트.
- 제 1 항 내지 제 23 항 중 어느 한 항에 따른 LNA 안티센스 올리고머 컨쥬게이트, 및 약제학적으로 허용가능한 희석제, 담체, 염 또는 보조제를 포함하는 약제학적 조성물.
- 제 24 항에 있어서, 상기 조성물은 완충된 식염수 용액 및 LNA 안티센스 올리고머 컨쥬게이트를 포함하는 약제학적 조성물.
- 세포에서 표적 유전자의 발현을 억제하는 생체내 또는 시험관내 방법으로서, 상기 방법은 제 1 항 내지 제 25 항 중 어느 한 항에 따른 LNA 안티센스 올리고머 컨쥬게이트를 상기 표적 유전자를 발현하고 있는 세포에, 적합하게는 상기 세포에서 표적 유전자의 발현을 감소시키는데 유효한 양으로 투여하는 단계를 포함하는 방법.
- 피험자의 간에서 RNA 의 발현을 억제하는 방법으로서, 상기 방법은 제 1 항 내지 제 26 항 중 어느 한 항에 따른 LNA 안티센스 올리고머 컨쥬게이트를 피험자에게, 적합하게는 상기 피험자의 간에서 표적 유전자의 발현을 감소시키는데 유효한 양으로 투여하는 단계를 포함하는 방법.
- 치료를 필요로 하는 피험자에서 질환 또는 장애를 치료하는 방법으로서, 상기 방법은 본 발명의 올리고머성 화합물을 포함하는 약제학적 조성물을 상기 피험자에게 치료학적 유효량으로 투여하는 단계를 포함하는 방법.
- 5' 또는 3' 말단 아미노 알킬기를 포함하는 LNA 올리고머.
Applications Claiming Priority (15)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP13153296 | 2013-01-30 | ||
| EP13153296.2 | 2013-01-30 | ||
| EP13157237.2 | 2013-02-28 | ||
| EP13157237 | 2013-02-28 | ||
| EP13174092.0 | 2013-06-27 | ||
| EP13174092 | 2013-06-27 | ||
| EPPCT/EP2013/073859 | 2013-11-14 | ||
| PCT/EP2013/073859 WO2014076196A1 (en) | 2012-11-15 | 2013-11-14 | Anti apob antisense conjugate compounds |
| EP13192938 | 2013-11-14 | ||
| EP13192930 | 2013-11-14 | ||
| PCT/EP2013/073858 WO2014076195A1 (en) | 2012-11-15 | 2013-11-14 | Oligonucleotide conjugates |
| EP13192938.2 | 2013-11-14 | ||
| EP13192930.9 | 2013-11-14 | ||
| EPPCT/EP2013/073858 | 2013-11-14 | ||
| PCT/EP2014/051781 WO2014118267A1 (en) | 2013-01-30 | 2014-01-30 | Lna oligonucleotide carbohydrate conjugates |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20150110562A true KR20150110562A (ko) | 2015-10-02 |
Family
ID=51261485
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020157020832A KR20150110562A (ko) | 2013-01-30 | 2014-01-30 | Lna 올리고뉴클레오타이드 탄수화물 컨쥬게이트 |
Country Status (16)
| Country | Link |
|---|---|
| US (1) | US20150368642A1 (ko) |
| EP (1) | EP2951305B1 (ko) |
| JP (1) | JP6580993B2 (ko) |
| KR (1) | KR20150110562A (ko) |
| CN (1) | CN104955952A (ko) |
| AU (1) | AU2014211406B2 (ko) |
| BR (1) | BR112015018161A2 (ko) |
| CA (1) | CA2893801A1 (ko) |
| DK (1) | DK2951305T3 (ko) |
| HK (1) | HK1215718A1 (ko) |
| IL (1) | IL238924A0 (ko) |
| MX (1) | MX2015009056A (ko) |
| MY (1) | MY177989A (ko) |
| RU (2) | RU2649367C2 (ko) |
| SG (1) | SG11201505387PA (ko) |
| WO (1) | WO2014118267A1 (ko) |
Families Citing this family (69)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DK2752488T3 (da) | 2002-11-18 | 2020-04-20 | Roche Innovation Ct Copenhagen As | Antisense-design |
| KR101881596B1 (ko) | 2008-12-02 | 2018-07-24 | 웨이브 라이프 사이언시스 재팬 인코포레이티드 | 인 원자 변형된 핵산의 합성 방법 |
| IN2012DN00720A (ko) | 2009-07-06 | 2015-06-19 | Ontorii Inc | |
| US10428019B2 (en) | 2010-09-24 | 2019-10-01 | Wave Life Sciences Ltd. | Chiral auxiliaries |
| BR112014001244A2 (pt) | 2011-07-19 | 2017-02-21 | Wave Life Sciences Pte Ltd | métodos para a síntese de ácidos nucléicos funcionalizados |
| BR112015000784A8 (pt) | 2012-07-13 | 2018-04-03 | Wave Life Sciences Japan | Grupo auxiliar assimétrico |
| EP2872147B1 (en) | 2012-07-13 | 2022-12-21 | Wave Life Sciences Ltd. | Method for making chiral oligonucleotides |
| WO2014076195A1 (en) | 2012-11-15 | 2014-05-22 | Santaris Pharma A/S | Oligonucleotide conjugates |
| EA031393B1 (ru) | 2013-05-01 | 2018-12-28 | Ионис Фармасьютикалз, Инк. | Композиции и способы модулирования экспрессии hbv и ttr |
| WO2014179445A1 (en) | 2013-05-01 | 2014-11-06 | Regulus Therapeutics Inc. | Compounds and methods for enhanced cellular uptake |
| MX371093B (es) | 2013-05-01 | 2020-01-16 | Regulus Therapeutics Inc | Compuestos de microarn y metodos para modular al mir-122. |
| EA201592215A1 (ru) | 2013-06-27 | 2016-05-31 | Рош Инновейшен Сентер Копенгаген А/С | Антисмысловые олигомеры и их конъюгаты, направленные на пропротеин конвертазу субтилизин/кексин типа 9 (pcsk9) |
| US9994846B2 (en) | 2013-10-25 | 2018-06-12 | Regulus Therapeutics Inc. | MicroRNA compounds and methods for modulating miR-21 activity |
| CA2928349A1 (en) * | 2013-11-14 | 2015-05-21 | Roche Innovation Center Copenhagen A/S | Apob antisense conjugate compounds |
| JPWO2015108048A1 (ja) | 2014-01-15 | 2017-03-23 | 株式会社新日本科学 | 抗腫瘍作用を有するキラル核酸アジュバンド及び抗腫瘍剤 |
| WO2015108047A1 (ja) | 2014-01-15 | 2015-07-23 | 株式会社新日本科学 | 免疫誘導活性を有するキラル核酸アジュバンド及び免疫誘導活性剤 |
| KR20230152178A (ko) | 2014-01-16 | 2023-11-02 | 웨이브 라이프 사이언시스 리미티드 | 키랄 디자인 |
| CA2946003A1 (en) | 2014-05-01 | 2015-11-05 | Ionis Pharmaceuticals, Inc. | Compositions and methods for modulating angiopoietin-like 3 expression |
| BR112016022593B1 (pt) | 2014-05-01 | 2022-04-26 | Ionis Pharmaceuticals, Inc | Compostos oligoméricos, composições que os compreendem, e usos dos mesmos |
| GB201408623D0 (en) | 2014-05-15 | 2014-07-02 | Santaris Pharma As | Oligomers and oligomer conjugates |
| JP6819907B2 (ja) * | 2014-07-31 | 2021-01-27 | エイジェンシー・フォー・サイエンス,テクノロジー・アンド・リサーチ | 修飾抗mir−138オリゴヌクレオチド |
| MA40463A (fr) | 2014-08-07 | 2017-06-14 | Regulus Therapeutics Inc | Ciblage de micro-arn pour traiter des troubles métaboliques |
| WO2016030863A1 (en) * | 2014-08-29 | 2016-03-03 | Glaxosmithkline Intellectual Property Development Limited | Compounds and methods for treating viral infections |
| SG11201702877TA (en) | 2014-10-10 | 2017-05-30 | Hoffmann La Roche | Galnac phosphoramidites, nucleic acid conjugates thereof and their use |
| US20180016575A1 (en) * | 2014-11-19 | 2018-01-18 | Roche Innovation Center Copenhagen A/S | LNA Gapmer Oligonucleotides Comprising Chiral Phosphorothioate Linkages |
| US10815481B2 (en) | 2014-12-16 | 2020-10-27 | Roche Innovation Center Copenhagen A/S | Chiral library screen |
| WO2016128583A2 (en) * | 2015-02-15 | 2016-08-18 | Ribo Task Aps | Acyl-amino-lna and/or hydrocarbyl-amino-lna oligonucleotides |
| WO2016179342A2 (en) | 2015-05-06 | 2016-11-10 | Alnylam Pharmaceuticals, Inc. | Factor xii (hageman factor) (f12), kallikrein b, plasma (fletcher factor) 1 (klkb1), and kininogen 1 (kng1) irna compositions and methods of use thereof |
| MA43072A (fr) | 2015-07-22 | 2018-05-30 | Wave Life Sciences Ltd | Compositions d'oligonucléotides et procédés associés |
| KR20180043819A (ko) | 2015-08-24 | 2018-04-30 | 로슈 이노베이션 센터 코펜하겐 에이/에스 | Lna-g 방법 |
| US10577388B2 (en) | 2015-10-02 | 2020-03-03 | Roche Innovation Center Copenhagen A/S | Oligonucleotide conjugation process |
| WO2017067970A1 (en) | 2015-10-22 | 2017-04-27 | Roche Innovation Center Copenhagen A/S | In vitro toxicity screening assay |
| AU2016343775B2 (en) * | 2015-10-28 | 2021-07-29 | Tufts Medical Center | Novel polypeptides with improved proteolytic stability, and methods of preparing and using same |
| WO2017079739A1 (en) | 2015-11-06 | 2017-05-11 | Ionis Pharmaceuticals, Inc. | MODULATING APOLIPOPROTEIN (a) EXPRESSION |
| US10883107B2 (en) * | 2016-01-08 | 2021-01-05 | Alnylam Pharmaceuticals, Inc. | Polynucleotide agents targeting factor XII (hageman factor) (F12) and methods of use thereof |
| JP6983797B2 (ja) | 2016-03-07 | 2021-12-17 | アローヘッド ファーマシューティカルズ インコーポレイテッド | 治療化合物用の標的化リガンド |
| HUE053172T2 (hu) | 2016-03-14 | 2021-06-28 | Hoffmann La Roche | Oligonukleotidok a PD-L1 expresszió csökkentésére |
| KR102468177B1 (ko) | 2016-04-14 | 2022-11-16 | 에프. 호프만-라 로슈 아게 | 트리틸-모노-GalNAc 화합물 및 이의 용도 |
| SG11201809002RA (en) | 2016-04-29 | 2018-11-29 | Univ Nanyang Tech | G-quadruplex-containing antisense oligonucleotides |
| WO2017216325A1 (en) | 2016-06-17 | 2017-12-21 | F. Hoffmann-La Roche Ag | In vitro nephrotoxicity screening assay |
| US11105794B2 (en) | 2016-06-17 | 2021-08-31 | Hoffmann-La Roche Inc. | In vitro nephrotoxicity screening assay |
| EP3500673B1 (en) | 2016-08-16 | 2021-10-06 | BioNTech Delivery Technologies GmbH | Carboxylated 2'-amino-lna nucleotides and oligonucleotides comprising the same |
| CN116942841A (zh) | 2016-09-02 | 2023-10-27 | 箭头药业股份有限公司 | 靶向配体 |
| JP7043078B2 (ja) | 2016-09-23 | 2022-03-29 | 国立大学法人 東京医科歯科大学 | 血液脳関門通過型ヘテロ2本鎖核酸 |
| KR20190065341A (ko) | 2016-10-06 | 2019-06-11 | 아이오니스 파마수티컬즈, 인코포레이티드 | 올리고머 화합물들의 접합 방법 |
| EP3594346A4 (en) | 2017-03-10 | 2020-12-16 | National Center For Child Health And Development | ANTISENSE OLIGONUCLEOTIDE AND COMPOSITION FOR THE PREVENTION OR TREATMENT OF GLYCOGEN STORAGE DISEASE TYPE IA |
| WO2018215049A1 (en) * | 2017-05-23 | 2018-11-29 | F. Hoffmann-La Roche Ag | Process for galnac oligonucleotide conjugates |
| EP3633036A4 (en) * | 2017-05-26 | 2021-03-17 | National Cerebral and Cardiovascular Center | ANTISENSE NUCLEIC ACID AGAINST PCSK9 |
| EP3599844A4 (en) * | 2017-06-07 | 2021-01-13 | University of Massachusetts | ANTI-ADAM33 OLIGONUCLEOTIDES AND RELATED PROCESSES |
| SG11202003461TA (en) * | 2017-10-16 | 2020-05-28 | Hoffmann La Roche | NUCLEIC ACID MOLECULE FOR REDUCTION OF PAPD5 AND PAPD7 mRNA FOR TREATING HEPATITIS B INFECTION |
| WO2019105419A1 (zh) | 2017-12-01 | 2019-06-06 | 苏州瑞博生物技术有限公司 | 一种核酸、含有该核酸的组合物与缀合物及制备方法和用途 |
| AU2018374219C1 (en) | 2017-12-01 | 2023-05-11 | Suzhou Ribo Life Science Co., Ltd. | Double-stranded oligonucleotide, composition and conjugate comprising double-stranded oligonucleotide, preparation method therefor and use thereof |
| EP3677679A4 (en) * | 2017-12-26 | 2020-12-02 | Guangzhou Ribobio Co., Ltd. | ARNSI MOLECULE INHIBITING PCSK9 GENE EXPRESSION AND ITS APPLICATION |
| AU2018394875B2 (en) | 2017-12-29 | 2023-08-03 | Suzhou Ribo Life Science Co., Ltd. | Conjugates and preparation and use thereof |
| JP2021511029A (ja) * | 2018-01-18 | 2021-05-06 | ロシュ イノベーション センター コペンハーゲン エーエス | Srebp1を標的とするアンチセンスオリゴヌクレオチド |
| CN115976028A (zh) | 2018-03-09 | 2023-04-18 | 第一三共株式会社 | 糖原病Ia型治疗药 |
| JP7333079B2 (ja) | 2018-03-19 | 2023-08-24 | 国立大学法人 東京医科歯科大学 | 毒性が軽減した核酸 |
| EP3790989A1 (en) | 2018-05-07 | 2021-03-17 | Roche Innovation Center Copenhagen A/S | Massively parallel discovery methods for oligonucleotide therapeutics |
| WO2020007826A1 (en) | 2018-07-05 | 2020-01-09 | Roche Innovation Center Copenhagen A/S | Antisense oligonucleotides targeting mbtps1 |
| WO2020011745A2 (en) | 2018-07-11 | 2020-01-16 | Roche Innovation Center Copenhagen A/S | Antisense oligonucleotides targeting cers6 |
| WO2020011744A2 (en) | 2018-07-11 | 2020-01-16 | Roche Innovation Center Copenhagen A/S | Antisense oligonucleotides targeting cers5 |
| WO2020038377A1 (zh) | 2018-08-21 | 2020-02-27 | 苏州瑞博生物技术有限公司 | 一种核酸、含有该核酸的药物组合物和缀合物及其用途 |
| CN109136224B (zh) * | 2018-08-21 | 2022-03-18 | 上海交通大学医学院附属瑞金医院 | miR-221/222及其抑制剂用于制备调控肝脂肪沉积、肝纤维化和肝细胞癌的药物 |
| EP3862024A4 (en) | 2018-09-30 | 2022-08-17 | Suzhou Ribo Life Science Co., Ltd. | SHORT INTERFERENT RNA CONJUGATE, METHOD FOR PREPARATION AND USE THEREOF |
| JP2022522430A (ja) | 2019-02-26 | 2022-04-19 | ロシュ イノベーション センター コペンハーゲン エーエス | オリゴヌクレオチドの製剤化方法 |
| TW202113079A (zh) | 2019-05-31 | 2021-04-01 | 美商艾利格斯醫療公司 | 經修飾之間隙子寡核苷酸及其使用方法 |
| CA3144467A1 (en) * | 2019-07-30 | 2021-02-04 | Jonathan Miles Brown | Subcutaneous delivery of multimeric oligonucleotides with enhanced bioactivity |
| WO2021249484A1 (zh) * | 2020-06-10 | 2021-12-16 | 南京明德新药研发有限公司 | 缀合基团及其缀合物 |
| WO2022172083A2 (en) * | 2021-01-21 | 2022-08-18 | Sirnaomics, Inc. | Targeted nucleic acid therapy for hepatitis b |
Family Cites Families (128)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2699808A (en) | 1944-10-06 | 1955-01-18 | Mark W Lowe | Apparatus for peeling tomatoes |
| JPS5927900A (ja) | 1982-08-09 | 1984-02-14 | Wakunaga Seiyaku Kk | 固定化オリゴヌクレオチド |
| US4948882A (en) | 1983-02-22 | 1990-08-14 | Syngene, Inc. | Single-stranded labelled oligonucleotides, reactive monomers and methods of synthesis |
| US4587044A (en) | 1983-09-01 | 1986-05-06 | The Johns Hopkins University | Linkage of proteins to nucleic acids |
| US5430136A (en) | 1984-10-16 | 1995-07-04 | Chiron Corporation | Oligonucleotides having selectably cleavable and/or abasic sites |
| US5525465A (en) | 1987-10-28 | 1996-06-11 | Howard Florey Institute Of Experimental Physiology And Medicine | Oligonucleotide-polyamide conjugates and methods of production and applications of the same |
| DE3738460A1 (de) | 1987-11-12 | 1989-05-24 | Max Planck Gesellschaft | Modifizierte oligonukleotide |
| US5391723A (en) | 1989-05-31 | 1995-02-21 | Neorx Corporation | Oligonucleotide conjugates |
| US4958013A (en) | 1989-06-06 | 1990-09-18 | Northwestern University | Cholesteryl modified oligonucleotides |
| US5254469A (en) | 1989-09-12 | 1993-10-19 | Eastman Kodak Company | Oligonucleotide-enzyme conjugate that can be used as a probe in hybridization assays and polymerase chain reaction procedures |
| US5486603A (en) | 1990-01-08 | 1996-01-23 | Gilead Sciences, Inc. | Oligonucleotide having enhanced binding affinity |
| US6395492B1 (en) | 1990-01-11 | 2002-05-28 | Isis Pharmaceuticals, Inc. | Derivatized oligonucleotides having improved uptake and other properties |
| US5608046A (en) | 1990-07-27 | 1997-03-04 | Isis Pharmaceuticals, Inc. | Conjugated 4'-desmethyl nucleoside analog compounds |
| US5245022A (en) | 1990-08-03 | 1993-09-14 | Sterling Drug, Inc. | Exonuclease resistant terminally substituted oligonucleotides |
| US5512667A (en) | 1990-08-28 | 1996-04-30 | Reed; Michael W. | Trifunctional intermediates for preparing 3'-tailed oligonucleotides |
| KR930702373A (ko) | 1990-11-08 | 1993-09-08 | 안토니 제이. 페이네 | 합성 올리고누클레오티드에 대한 다중 리포터(Reporter)그룹의 첨합 |
| ATE239484T1 (de) | 1991-10-24 | 2003-05-15 | Isis Pharmaceuticals Inc | Derivatisierte oligonukleotide mit verbessertem aufnahmevermögen |
| WO2002081494A1 (en) * | 2001-03-26 | 2002-10-17 | Sirna Therapeutics, Inc. | Oligonucleotide mediated inhibition of hepatitis b virus and hepatitis c virus replication |
| NL9201440A (nl) | 1992-08-11 | 1994-03-01 | Univ Leiden | Triantennaire clusterglycosiden, hun bereiding en toepassing. |
| JPH08504559A (ja) | 1992-12-14 | 1996-05-14 | ハネウエル・インコーポレーテッド | 個別に制御される冗長巻線を有するモータシステム |
| US5574142A (en) | 1992-12-15 | 1996-11-12 | Microprobe Corporation | Peptide linkers for improved oligonucleotide delivery |
| US5646262A (en) | 1994-07-28 | 1997-07-08 | Georgetown University | Antisense oligonucleotides against hepatitis B viral replication |
| US5580731A (en) | 1994-08-25 | 1996-12-03 | Chiron Corporation | N-4 modified pyrimidine deoxynucleotides and oligonucleotide probes synthesized therewith |
| EP0804456B1 (en) | 1994-10-06 | 2002-08-21 | Isis Pharmaceuticals, Inc. | Peptide nucleic acid conjugates |
| US5684142A (en) | 1995-06-07 | 1997-11-04 | Oncor, Inc. | Modified nucleotides for nucleic acid labeling |
| US5985662A (en) | 1995-07-13 | 1999-11-16 | Isis Pharmaceuticals Inc. | Antisense inhibition of hepatitis B virus replication |
| US5994517A (en) | 1995-11-22 | 1999-11-30 | Paul O. P. Ts'o | Ligands to enhance cellular uptake of biomolecules |
| US20030014318A1 (en) | 1996-11-08 | 2003-01-16 | Matthew Byrne | International trading system and method |
| JP3756313B2 (ja) | 1997-03-07 | 2006-03-15 | 武 今西 | 新規ビシクロヌクレオシド及びオリゴヌクレオチド類縁体 |
| US6770748B2 (en) | 1997-03-07 | 2004-08-03 | Takeshi Imanishi | Bicyclonucleoside and oligonucleotide analogue |
| US5770716A (en) | 1997-04-10 | 1998-06-23 | The Perkin-Elmer Corporation | Substituted propargylethoxyamido nucleosides, oligonucleotides and methods for using same |
| CN1263473A (zh) | 1997-05-21 | 2000-08-16 | 利兰·斯坦福青年大学托管委员会 | 增加跨生物膜转运的组合物和方法 |
| US6794499B2 (en) | 1997-09-12 | 2004-09-21 | Exiqon A/S | Oligonucleotide analogues |
| CA2303299C (en) | 1997-09-12 | 2016-02-23 | Exiqon A/S | Oligonucleotide analogues |
| US6096875A (en) | 1998-05-29 | 2000-08-01 | The Perlein-Elmer Corporation | Nucleotide compounds including a rigid linker |
| US6300319B1 (en) | 1998-06-16 | 2001-10-09 | Isis Pharmaceuticals, Inc. | Targeted oligonucleotide conjugates |
| US6335432B1 (en) | 1998-08-07 | 2002-01-01 | Bio-Red Laboratories, Inc. | Structural analogs of amine bases and nucleosides |
| US6335437B1 (en) | 1998-09-07 | 2002-01-01 | Isis Pharmaceuticals, Inc. | Methods for the preparation of conjugated oligomers |
| ATE356824T1 (de) | 1999-05-04 | 2007-04-15 | Santaris Pharma As | L-ribo-lna analoge |
| US6525191B1 (en) | 1999-05-11 | 2003-02-25 | Kanda S. Ramasamy | Conformationally constrained L-nucleosides |
| US20040146516A1 (en) | 1999-06-17 | 2004-07-29 | Utah Ventures Ii L.P. | Lumen-exposed molecules and methods for targeted delivery |
| US6617442B1 (en) | 1999-09-30 | 2003-09-09 | Isis Pharmaceuticals, Inc. | Human Rnase H1 and oligonucleotide compositions thereof |
| JP2003511016A (ja) * | 1999-10-04 | 2003-03-25 | エクシコン エ/エス | オリゴヌクレオチドを補充する高親和性rnアーゼhの設計 |
| US7407943B2 (en) | 2001-08-01 | 2008-08-05 | Isis Pharmaceuticals, Inc. | Antisense modulation of apolipoprotein B expression |
| US7227014B2 (en) | 2001-08-07 | 2007-06-05 | Isis Pharmaceuticals, Inc. | Antisense modulation of apolipoprotein (a) expression |
| US7259150B2 (en) | 2001-08-07 | 2007-08-21 | Isis Pharmaceuticals, Inc. | Modulation of apolipoprotein (a) expression |
| EP1578765A4 (en) | 2002-11-05 | 2008-04-23 | Isis Pharmaceuticals Inc | OLIGOMERIC COMPOUNDS CONTAINING SUGAR SUBSTITUTE AND COMPOSITIONS FOR USE IN GENE MODULATION |
| CA2505090A1 (en) | 2002-11-05 | 2004-05-27 | Isis Pharmaceuticals, Inc. | Conjugated oligomeric compounds and their use in gene modulation |
| AU2003291753B2 (en) | 2002-11-05 | 2010-07-08 | Isis Pharmaceuticals, Inc. | Polycyclic sugar surrogate-containing oligomeric compounds and compositions for use in gene modulation |
| EP1569695B1 (en) | 2002-11-13 | 2013-05-15 | Genzyme Corporation | Antisense modulation of apolipoprotein b expression |
| DK2752488T3 (da) | 2002-11-18 | 2020-04-20 | Roche Innovation Ct Copenhagen As | Antisense-design |
| AU2003219576A1 (en) | 2003-04-03 | 2004-10-25 | Korea Advanced Institute Of Science And Technology | Conjugate for gene transfer comprising oligonucleotide and hydrophilic polymer, polyelectrolyte complex micelles formed from the conjugate, and methods for preparation thereof |
| WO2004106356A1 (en) | 2003-05-27 | 2004-12-09 | Syddansk Universitet | Functionalized nucleotide derivatives |
| EP1495769B1 (en) | 2003-07-11 | 2008-02-27 | LBR Medbiotech B.V. | Mannose-6-phosphate receptor mediated gene transfer into muscle cells |
| CA2533701A1 (en) | 2003-07-31 | 2005-02-17 | Isis Pharmaceuticals, Inc. | Oligomeric compounds and compositions for use in modulation of small non-coding rnas |
| US7825235B2 (en) | 2003-08-18 | 2010-11-02 | Isis Pharmaceuticals, Inc. | Modulation of diacylglycerol acyltransferase 2 expression |
| US7427672B2 (en) | 2003-08-28 | 2008-09-23 | Takeshi Imanishi | Artificial nucleic acids of n-o bond crosslinkage type |
| AU2004274021B2 (en) | 2003-09-18 | 2009-08-13 | Isis Pharmaceuticals, Inc. | 4'-thionucleosides and oligomeric compounds |
| US7622453B2 (en) | 2003-12-23 | 2009-11-24 | Santaris Pharma A/S | Oligomeric compounds for the modulation of Bcl-2 |
| US20050244869A1 (en) | 2004-04-05 | 2005-11-03 | Brown-Driver Vickie L | Modulation of transthyretin expression |
| DK2997980T3 (en) | 2004-08-10 | 2018-03-26 | Kastle Therapeutics Llc | PROCEDURES FOR MODULATING LIPROPROTEIN AND CHOLESTEROL LEVELS |
| US20120122801A1 (en) * | 2005-01-05 | 2012-05-17 | Prosensa B.V. | Mannose-6-phosphate receptor mediated gene transfer into muscle cells |
| WO2006078217A1 (en) * | 2005-01-24 | 2006-07-27 | Avaris Ab | COMPLEX CONTAINING SiRNA, ShRNA OR ANTISENSE MOLECULE AND FUNCTIONAL ENTITY, FOR IMPROVED SPECIFICITY AND DELIVERY |
| US20090203893A1 (en) | 2005-08-29 | 2009-08-13 | Regulus Therapeutics, Llc | Antisense compounds having enhanced anti-microrna activity |
| AU2006284855B2 (en) * | 2005-08-29 | 2011-10-13 | Regulus Therapeutics Inc. | Methods for use in modulating miR-122a |
| WO2007031091A2 (en) | 2005-09-15 | 2007-03-22 | Santaris Pharma A/S | Rna antagonist compounds for the modulation of p21 ras expression |
| WO2007031081A2 (en) | 2005-09-15 | 2007-03-22 | Santaris Pharma A/S | RNA ANTAGONIST COMPOUNDS FOR THE INHIBITION OF APO-Bl00 EXPRESSION |
| US20070066557A1 (en) | 2005-09-19 | 2007-03-22 | Monia Brett P | Modulation of glucocorticoid receptor expression |
| WO2007058894A2 (en) | 2005-11-10 | 2007-05-24 | The University Of North Carolina At Chapel Hill | Splice switching oligomers for tnf superfamily receptors and their use in treatment of disease |
| EP2314594B1 (en) | 2006-01-27 | 2014-07-23 | Isis Pharmaceuticals, Inc. | 6-modified bicyclic nucleic acid analogs |
| WO2008051306A1 (en) | 2006-10-20 | 2008-05-02 | Ercole Biotech, Inc. | Soluble tnf receptors and their use in treatment of disease |
| CA3024953A1 (en) | 2006-04-03 | 2007-10-11 | Roche Innovation Center Copenhagen A/S | Pharmaceutical composition comprising anti-mirna antisense oligonucleotides |
| US20090326041A1 (en) | 2006-05-05 | 2009-12-31 | Isis Pharmaceuticals, Inc. | Compounds and methods for modulating expression of sglt2 |
| DK2066684T3 (da) | 2006-05-11 | 2012-10-22 | Isis Pharmaceuticals Inc | 5´-Modificerede bicycliske nukleinsyreanaloge |
| US20100216864A1 (en) | 2006-10-09 | 2010-08-26 | Ellen Marie Straarup | RNA Antagonist Compounds for the Modulation of PCSK9 |
| CA2670563A1 (en) | 2006-11-27 | 2008-06-05 | Isis Pharmaceuticals, Inc. | Methods for treating hypercholesterolemia |
| US20100190837A1 (en) | 2007-02-15 | 2010-07-29 | Isis Pharmaceuticals, Inc. | 5'-Substituted-2-F' Modified Nucleosides and Oligomeric Compounds Prepared Therefrom |
| EP2126079A1 (en) | 2007-03-22 | 2009-12-02 | Santaris Pharma A/S | Rna antagonist compounds for the inhibition of apo-b100 expression |
| DK2149605T3 (da) | 2007-03-22 | 2013-09-30 | Santaris Pharma As | Korte RNA antagonist forbindelser til modulering af det ønskede mRNA |
| CA3165250A1 (en) | 2007-05-01 | 2008-11-06 | Santaris Pharma A/S | Splice switching oligomers for tnf superfamily receptors and their use in treatment of disease |
| EA018986B1 (ru) * | 2007-05-01 | 2013-12-30 | Сантарис Фарма А/С | Соединения-антагонисты рнк для модуляции активности бета-катенина |
| AU2008260277C1 (en) | 2007-05-30 | 2014-04-17 | Isis Pharmaceuticals, Inc. | N-substituted-aminomethylene bridged bicyclic nucleic acid analogs |
| DK2173760T4 (en) | 2007-06-08 | 2016-02-08 | Isis Pharmaceuticals Inc | Carbocyclic bicyclic nukleinsyreanaloge |
| ES2376507T5 (es) | 2007-07-05 | 2015-08-31 | Isis Pharmaceuticals, Inc. | Análogos de ácidos nucleicos bicíclicos 6-disustituidos |
| CN101816010A (zh) | 2007-07-19 | 2010-08-25 | 数据匙电子有限公司 | Rf令牌和接纳器系统与方法 |
| AU2007357885A1 (en) | 2007-08-20 | 2009-02-26 | Enzon Pharmaceuticals, Inc. | Polymeric linkers containing pyridyl disulfide moieties |
| BRPI0817527A2 (pt) | 2007-10-01 | 2017-05-02 | Isis Pharmaceuticals Inc | modulação antissenso da expressão do receptor de fator de crescimento de fibroblasto humano 4 |
| AU2008306327B2 (en) * | 2007-10-04 | 2014-05-15 | Roche Innovation Center Copenhagen A/S | Micromirs |
| RU2010119775A (ru) | 2007-11-09 | 2011-12-27 | Айсис Фармасьютикалс,Инк. (Us) | Модулирование экспрессии фактора 7 |
| CN101932709B (zh) * | 2007-11-26 | 2014-09-10 | 桑塔里斯制药公司 | 靶向雄激素受体的lna拮抗剂 |
| CA2910760C (en) * | 2007-12-04 | 2019-07-09 | Muthiah Manoharan | Targeting lipids |
| WO2009100320A2 (en) | 2008-02-07 | 2009-08-13 | Isis Pharmaceuticals, Inc. | Bicyclic cyclohexitol nucleic acid analogs |
| DK2285819T3 (da) | 2008-04-04 | 2013-12-02 | Isis Pharmaceuticals Inc | Oligomere forbindelser omfattende neutralt bundne, terminale bicykliske nukleosider |
| CA2721183C (en) | 2008-04-11 | 2019-07-16 | Alnylam Pharmaceuticals, Inc. | Site-specific delivery of nucleic acids by combining targeting ligands with endosomolytic components |
| WO2009148605A2 (en) | 2008-06-04 | 2009-12-10 | Isis Pharmaceuticals, Inc. | Methods for treating hypercholesterolemia |
| BRPI0915837A2 (pt) * | 2008-07-03 | 2015-11-03 | Santaris Pharma As | compostos antagonistas de rna para a inibição da expressão de glicerol-3-fosfato aciltransferase mitocondrial 1 (mtgpat1) |
| US8703730B2 (en) | 2008-07-10 | 2014-04-22 | Regenesance B.V. | Complement antagonists and uses thereof |
| US9033197B2 (en) | 2008-07-17 | 2015-05-19 | Nir Bar | Spool holder |
| US7932256B2 (en) | 2008-07-31 | 2011-04-26 | Bristol-Myers Squibb Company | (S)-4-(1-cyclopropyl-2-methoxyethyl)-6-(6-(difluoromethoxy)-2,5-dimethylpyridin-3-ylamino)-5-oxo-4,5-dihydropyrazine-2-carbonitrile: a pyrazinone modulator of corticotropin-releasing factor receptor activity |
| WO2010017509A1 (en) | 2008-08-07 | 2010-02-11 | Isis Pharmaceuticals, Inc. | Modulation of transthyretin expression for the treatment of cns related disorders |
| EP2384197B1 (en) * | 2008-12-31 | 2016-04-06 | Roche Innovation Center Copenhagen A/S | Use of lna apob antisense oligomers for the treatment of acute coronary syndromes |
| EP2414521B1 (en) | 2009-03-31 | 2016-10-26 | The General Hospital Corporation | Regulation of mir-33 micrornas in the treatment of cholesterol-related disorders |
| WO2010122538A1 (en) * | 2009-04-24 | 2010-10-28 | Santaris Pharma A/S | Pharmaceutical compositions for treatment of hcv patients that are non-responders to interferon |
| CA2764822A1 (en) | 2009-06-12 | 2010-12-16 | Santaris Pharma A/S | New potent anti apob antisense compounds |
| US8563528B2 (en) | 2009-07-21 | 2013-10-22 | Santaris Pharma A/S | Antisense oligomers targeting PCSK9 |
| US8598334B2 (en) | 2009-10-16 | 2013-12-03 | Glaxo Group Limited | HBV antisense inhibitors |
| KR101663617B1 (ko) | 2009-10-29 | 2016-10-07 | 엘지전자 주식회사 | 하향링크 기준신호 송수신 방법 및, 이를 이용한 기지국 및 사용자기기 |
| US8653047B2 (en) | 2010-01-08 | 2014-02-18 | Isis Pharmaceuticals, Inc. | Modulation of angiopoietin-like 3 expression |
| WO2011123621A2 (en) | 2010-04-01 | 2011-10-06 | Alnylam Pharmaceuticals Inc. | 2' and 5' modified monomers and oligonucleotides |
| WO2011126937A1 (en) | 2010-04-06 | 2011-10-13 | The University Of North Carolina At Chapel Hill | Targeted intracellular delivery of oligonucleotides via conjugation with small molecule ligands |
| US9725479B2 (en) | 2010-04-22 | 2017-08-08 | Ionis Pharmaceuticals, Inc. | 5′-end derivatives |
| ES2625689T3 (es) | 2010-04-29 | 2017-07-20 | Ionis Pharmaceuticals, Inc. | Modulación de la expresión de transtiretina |
| PL2652897T3 (pl) | 2010-12-13 | 2017-10-31 | Ericsson Telefon Ab L M | Wymiana parametrów dotyczących okresów pomiaru |
| SG189474A1 (en) * | 2010-12-17 | 2013-05-31 | Arrowhead Res Corp | Galactose cluster-pharmacokinetic modulator targeting moiety for sirna |
| WO2012089352A1 (en) | 2010-12-29 | 2012-07-05 | F. Hoffmann-La Roche Ag | Small molecule conjugates for intracellular delivery of nucleic acids |
| EP2699583A4 (en) | 2011-04-21 | 2015-04-15 | Isis Pharmaceuticals Inc | MODULATION OF EXPRESSION OF HEPATITIS B VIRUS (HBV) |
| US20120295961A1 (en) | 2011-04-21 | 2012-11-22 | Swayze Eric E | Modulation of hepatitis b virus (hbv) expression |
| WO2012174154A1 (en) | 2011-06-13 | 2012-12-20 | Isis Pharmaceuticals, Inc. | Modulation of inflammatory responses by factor vii |
| CA2839437A1 (en) | 2011-06-16 | 2012-12-20 | Isis Pharmaceuticals, Inc. | Antisense modulation of fibroblast growth factor receptor 4 expression |
| TW202244278A (zh) | 2011-06-30 | 2022-11-16 | 美商艾羅海德製藥公司 | 用於抑制b型肝炎病毒基因表現之組合物及方法 |
| AU2012327227A1 (en) | 2011-11-07 | 2013-05-23 | Isis Pharmaceuticals, Inc. | Administration of Factor XI antisense oligonucleotides |
| AU2013216852A1 (en) | 2012-02-08 | 2014-08-21 | Isis Pharmaceuticals, Inc. | Methods and compositions for modulating Factor VII expression |
| US9340784B2 (en) | 2012-03-19 | 2016-05-17 | Ionis Pharmaceuticals, Inc. | Methods and compositions for modulating alpha-1-antitrypsin expression |
| EP2850092B1 (en) | 2012-04-09 | 2017-03-01 | Ionis Pharmaceuticals, Inc. | Tricyclic nucleic acid analogs |
| WO2013159109A1 (en) | 2012-04-20 | 2013-10-24 | Isis Pharmaceuticals, Inc. | Modulation of hepatitis b virus (hbv) expression |
| US9984408B1 (en) | 2012-05-30 | 2018-05-29 | Amazon Technologies, Inc. | Method, medium, and system for live video cooperative shopping |
| WO2014076195A1 (en) * | 2012-11-15 | 2014-05-22 | Santaris Pharma A/S | Oligonucleotide conjugates |
| EA031393B1 (ru) * | 2013-05-01 | 2018-12-28 | Ионис Фармасьютикалз, Инк. | Композиции и способы модулирования экспрессии hbv и ttr |
-
2014
- 2014-01-30 RU RU2015133167A patent/RU2649367C2/ru not_active IP Right Cessation
- 2014-01-30 JP JP2015555701A patent/JP6580993B2/ja not_active Expired - Fee Related
- 2014-01-30 EP EP14704307.9A patent/EP2951305B1/en not_active Not-in-force
- 2014-01-30 CA CA2893801A patent/CA2893801A1/en not_active Abandoned
- 2014-01-30 RU RU2018108405A patent/RU2018108405A/ru not_active Application Discontinuation
- 2014-01-30 MY MYPI2015702453A patent/MY177989A/en unknown
- 2014-01-30 WO PCT/EP2014/051781 patent/WO2014118267A1/en active Application Filing
- 2014-01-30 SG SG11201505387PA patent/SG11201505387PA/en unknown
- 2014-01-30 CN CN201480006635.0A patent/CN104955952A/zh active Pending
- 2014-01-30 US US14/764,658 patent/US20150368642A1/en not_active Abandoned
- 2014-01-30 DK DK14704307.9T patent/DK2951305T3/en active
- 2014-01-30 MX MX2015009056A patent/MX2015009056A/es unknown
- 2014-01-30 BR BR112015018161A patent/BR112015018161A2/pt not_active Application Discontinuation
- 2014-01-30 KR KR1020157020832A patent/KR20150110562A/ko not_active Application Discontinuation
- 2014-01-30 AU AU2014211406A patent/AU2014211406B2/en not_active Ceased
-
2015
- 2015-05-20 IL IL238924A patent/IL238924A0/en unknown
-
2016
- 2016-03-29 HK HK16103586.6A patent/HK1215718A1/zh unknown
Also Published As
| Publication number | Publication date |
|---|---|
| CN104955952A (zh) | 2015-09-30 |
| HK1215718A1 (zh) | 2016-09-09 |
| MX2015009056A (es) | 2015-10-05 |
| AU2014211406B2 (en) | 2019-07-18 |
| US20150368642A1 (en) | 2015-12-24 |
| RU2649367C2 (ru) | 2018-04-02 |
| EP2951305B1 (en) | 2018-08-15 |
| JP6580993B2 (ja) | 2019-09-25 |
| IL238924A0 (en) | 2015-07-30 |
| RU2015133167A (ru) | 2017-03-06 |
| AU2014211406A1 (en) | 2015-06-04 |
| EP2951305A1 (en) | 2015-12-09 |
| RU2018108405A (ru) | 2019-02-26 |
| CA2893801A1 (en) | 2014-08-07 |
| MY177989A (en) | 2020-09-28 |
| JP2016508367A (ja) | 2016-03-22 |
| WO2014118267A1 (en) | 2014-08-07 |
| BR112015018161A2 (pt) | 2017-08-22 |
| DK2951305T3 (en) | 2018-10-29 |
| SG11201505387PA (en) | 2015-08-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2014211406B2 (en) | LNA oligonucleotide carbohydrate conjugates | |
| JP6452614B2 (ja) | オリゴヌクレオチドコンジュゲート | |
| KR102287532B1 (ko) | 생분해성 컨쥬게이트를 갖는 폴리 올리고머 화합물 | |
| KR102226110B1 (ko) | Pcsk9 를 표적화하는 안티센스 올리고머 및 접합체 | |
| WO2016055601A1 (en) | Galnac phosphoramidites, nucleic acid conjugates thereof and their use |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application |