발명의 개요
본 발명은 하기 화학식 I에 따른 화합물 또는 그의 염, 특히 제약상 허용되는 염에 관한 것이고, 또한 화학식 I의 화합물 또는 그의 염을 포함하는 제약 조성물, HDAC를 화학식 I의 화합물 또는 그의 염과 접촉시킴으로써 HDAC를 억제하는 방법, 및 HDAC의 억제에 의해 매개되는 질환 또는 장애를 갖는 대상체에게 화학식 I의 화합물 또는 그의 염, 또는 화학식 I의 화합물 또는 그의 염을 포함하는 제약 조성물을 투여하는 것을 포함하는, 상기 대상체의 치료 방법에 관한 것이다.
<화학식 I>
상기 식에서:
R1은 할로(C1-C4)알킬이고, 여기서 상기 할로(C1-C4)알킬은 2개 이상의 할로 기를 함유하고;
Y는 결합이고, X1은 O, N 또는 NH이고, X2는 N 또는 CH이고, X3은 N 또는 NH이거나,
또는 Y는 -C(O)-이고, X1 및 X2는 CH 또는 N이고, X3은 O 또는 S이거나,
또는 Y는 -C(O)-이고, X1은 O이고, X2는 CH 또는 N이고, X3은 CH 또는 N이고;
A는 임의로 치환된 (C3-C6)시클로알킬, 페닐, 나프틸, 4 내지 7원 헤테로시클로알킬, 5 내지 6원 헤테로아릴 또는 9 내지 10원 헤테로아릴이고,
여기서 임의의 임의로 치환된 시클로알킬, 페닐, 나프틸, 헤테로시클로알킬 또는 헤테로아릴은 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, 할로(C1-C4)알콕시, -NRARA 및 -((C1-C4)알킬)NRARA로부터 독립적으로 선택된 1 내지 3개의 기에 의해 임의로 치환되고;
Z는 -C(=O)NRX-, -NRXC(=O)NRX, -NRXC(=O)-, -SO2-, -SO2NRX-, -NRXSO2-, -NHCH(CF3)-, -CH(CF3)NH-, -CH(CF3)-, -(C1-C4)알킬-, -NRX- 또는 -(C1-C3)알킬-NRX-이고;
n은 0 내지 4이고;
n이 0인 경우에, R2 및 R3은 독립적으로 H 및 임의로 치환된 (C1-C4)알킬, 아릴(C1-C4)알킬- 및 (C3-C7)시클로알킬(C1-C4)알킬-로부터 선택되고,
n이 1 내지 4인 경우에, R2 및 R3은 독립적으로 H, 플루오로 및 임의로 치환된 (C1-C4)알킬, 아릴(C1-C4)알킬- 및 (C3-C7)시클로알킬(C1-C4)알킬-로부터 선택되고, 여기서 n이 1이고, R2가 F이고, R3이 H인 경우에, Z는 -C(=O)NRX-, -NRXC(=O)NRX, -SO2NRX-, -NHCH(CF3)-, -CH(CF3)NH-, -CH(CF3)-, -(C1-C4)알킬-, -NRX- 또는 -(C1-C3)알킬-NRX-이고,
n이 1 내지 4인 경우에, R2는 -NRARB, -(C1-C4)알킬-NRARB, -CONRARB, -(C1-C4)알킬-CONRARB, -CO2H, -(C1-C4)알킬-CO2H, 히드록실, 히드록시(C1-C4)알킬-, (C1-C3)알콕시 및 (C1-C3)알콕시(C1-C4)알킬-로부터 선택되고, R3은 H 및 임의로 치환된 (C1-C4)알킬, 아릴(C1-C4)알킬- 및 (C3-C7)시클로알킬(C1-C4)알킬-로부터 선택되고,
여기서 임의의 R2 및 R3 중 상기 임의로 치환된 (C1-C4)알킬, 아릴(C1-C4)알킬- 및 (C3-C7)시클로알킬(C1-C4)알킬-의 아릴, 시클로알킬 및 각각의 (C1-C4)알킬 모이어티는 할로겐, 시아노, (C1-C4)알킬, 할로(C1-C4)알킬, (C1-C4)알콕시, 할로(C1-C4)알콕시, -NRARA, -((C1-C4)알킬)NRARA 및 히드록실로부터 독립적으로 선택된 1, 2 또는 3개의 기에 의해 임의로 치환되거나;
또는 R2 및 R3은 이들이 연결되어 있는 원자와 함께, 임의로 치환된 4, 5, 6 또는 7원 시클로알킬 또는 헤테로시클로알킬 기를 형성하고, 여기서 상기 헤테로시클로알킬 기는 N, O 및 S로부터 독립적으로 선택된 1 또는 2개의 헤테로원자를 함유하고, 상기 임의로 치환된 시클로알킬 또는 헤테로시클로알킬 기는 (C1-C4)알킬, 할로(C1-C4)알킬, 할로겐, 시아노, 아릴(C1-C4)알킬-, (C3-C7)시클로알킬(C1-C4)알킬-, -ORY, -NRYRY, -C(=O)ORY, -C(=O)NRYRY, -NRYC(=O)RY, -SO2NRYRY, -NRYSO2RY, -OC(=O)NRYRY, -NRYC(=O)ORY 및 -NRYC(=O)NRYRY로부터 독립적으로 선택된 1, 2 또는 3개의 치환기에 의해 임의로 치환되고;
L은 5 내지 6원 헤테로아릴 또는 페닐이고, 이는 R4에 의해 치환되고 임의로 추가 치환되고,
여기서 L이 추가 치환되는 경우에, L은 할로겐, 시아노 및 (C1-C4)알킬로부터 독립적으로 선택된 1 또는 2개의 치환기에 의해 치환되고;
R4는 H, (C1-C4)알킬, 할로, 할로(C1-C4)알킬, (C1-C4)알콕시, ((C1-C4)알킬)((C1-C4)알킬)N(C1-C4)알콕시, ((C1-C4)알킬)((C1-C4)알킬)N(C1-C4)알킬-, (C1-C4)할로알콕시-, (C1-C4)알킬아미노, 임의로 치환된 (C3-C6)시클로알킬, 임의로 치환된 페닐, 임의로 치환된 5 내지 6원 헤테로시클로알킬 또는 임의로 치환된 5 내지 6원 헤테로아릴이고,
여기서 상기 임의로 치환된 시클로알킬, 페닐, 헤테로시클로알킬 또는 헤테로아릴은 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, (C1-C4)알킬티오-, 할로(C1-C4)알콕시, 히드록실, -NRARC 및 -((C1-C4)알킬)NRARC로부터 독립적으로 선택된 1, 2 또는 3개의 기에 의해 임의로 치환되거나;
또는 L-R4는 함께, 1,3-벤조디옥솔릴, 2,3-디히드로-1,4-벤조디옥시닐, 벤조푸라닐, 테트라히드로이소퀴놀릴 또는 이소인돌리닐 기를 형성하고, 여기서 상기 벤조푸라닐, 테트라히드로이소퀴놀릴 또는 이소인돌리닐 기는 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, (C1-C4)알킬티오-, 할로(C1-C4)알콕시, 히드록실, -NRARC 및 -((C1-C4)알킬)NRARC로부터 독립적으로 선택된 1, 2 또는 3개의 기에 의해 임의로 치환되고;
여기서 각각의 RA는 독립적으로 H 및 (C1-C4)알킬로부터 선택되고;
RB는 H, (C1-C4)알킬, 할로(C1-C4)알킬, -C(=O)(C1-C4)알킬, -C(=O)O(C1-C4)알킬, -C(=O)NH2, -C(=O)NH(C1-C4)알킬, -C(=O)N((C1-C4)알킬)((C1-C4)알킬), -SO2(C1-C4)알킬이거나, 또는 RA 및 RB는 이들이 부착되어 있는 원자와 함께 N, O 및 S로부터 선택된 1개의 추가의 헤테로원자를 임의로 함유하고 (C1-C4)알킬에 의해 임의로 치환된 4 내지 6원 헤테로시클릭 고리를 형성하고;
RC는 H, (C1-C4)알킬, 페닐, 5 내지 6원 헤테로시클로알킬 또는 5 내지 6원 헤테로아릴이거나, 또는 RA 및 RC는 이들이 부착되어 있는 원자와 함께 N, O 및 S로부터 선택된 1개의 추가의 헤테로원자를 임의로 함유하고 (C1-C4)알킬에 의해 임의로 치환된 4 내지 8원 헤테로시클릭 고리를 형성하고;
각각의 RX는 독립적으로 H, (C1-C6)알킬 및 임의로 치환된 (C2-C6)알킬이고, 여기서 상기 임의로 치환된 (C2-C6)알킬은 히드록실, 시아노, 아미노, (C1-C4)알콕시, (C1-C4)알킬)NH- 또는 ((C1-C4)알킬)((C1-C4)알킬)N-에 의해 임의로 치환되고;
각각의 RY는 독립적으로 H, (C1-C4)알킬, 페닐 및 -(C1-C4)알킬페닐로부터 선택된다.
한 실시양태에서, 화학식 I의 화합물 또는 그의 염은 하기 화합물을 제외한다:
N-[(4-플루오로페닐)메틸]-4-[5-(2,2,2-트리플루오로아세틸)-2-티에닐]-벤즈아미드,
N-[(4-플루오로페닐)메틸]-3-[5-(2,2,2-트리플루오로아세틸)-2-티에닐]-벤즈아미드,
4-메톡시-N-[2-[3-(트리플루오로메틸)-1H-1,2,4-트리아졸-5-일]-3-티에닐]-벤젠아세트아미드,
N-[(4-메톡시페닐)메틸]-4-[5-(트리클로로메틸)-1,2,4-옥사디아졸-3-일]-1,2,5-옥사디아졸-3-아민,
4-(트리플루오로메틸)-N-[3-(트리플루오로메틸)-4-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]페닐]-벤젠프로판아미드,
3-[4-(트리플루오로메틸)페닐]-N-{3-(트리플루오로메틸)-4-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]페닐}프로판아미드,
3-{7-메틸-2-[4-(3-메틸-5-이속사졸릴)부틸]-1-벤조푸란-5-일}-5-(트리플루오로메틸)-1,2,4-옥사디아졸,
1-[3-(3-메틸-5-이속사졸릴)프로필]-5-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]-1H-인돌,
7-메틸-1-[4-(3-메틸-5-이속사졸릴)부틸]-5-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]-1H-인돌,
7-메틸-1-[5-(3-메틸-5-이속사졸릴)펜틸]-5-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]-1H-인돌,
7-메틸-1-[3-(3-메틸-5-이속사졸릴)프로필]-5-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]-2,3-디히드로-1H-인돌 또는
N-(페닐메틸)-4-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]-1,2,5-옥사디아졸-3-아민.
본 발명은 또한 본 발명의 화합물을 포함하는 제약 조성물에 관한 것이다. 본 발명은 또한 본 발명의 화합물, 또는 본 발명의 화합물을 포함하는 제약 조성물을 사용하여, HDAC 효소를 억제하고 상기 효소와 연관된 상태를 치료하는 방법에 관한 것이다.
발명의 상세한 설명
명세서 전반에 걸쳐 제공된 화학식 I의 다양한 기 및 치환기에 대한 대안적 정의는 특히, 본원에 개시된 각각의 화합물 종을 개별적으로, 뿐만 아니라 하나 이상의 화합물 종의 군을 기재하기 위한 의도이다. 본 발명의 범주는 이들 기 및 치환기 정의의 임의의 조합을 포함한다.
본 발명의 한 실시양태에서, R1은 2개 이상의 플루오로 기 (원자)를 함유하는 플루오로-알킬 기이다. 또 다른 실시양태에서, R1은 2개 이상의 플루오로 기를 함유하는 (C1-C2)알킬 기이다. 구체적 실시양태에서, R1은 CHF2 또는 CF3이고; 보다 구체적으로, R1은 CF3 이다.
선택된 실시양태에서, Y가 결합인 경우에, X1, X2 및 X3은 이들이 부착되어 있는 원자와 함께 옥사디아졸릴 (X1은 O이고, X2 및 X3은 N임), 옥사졸릴 (X1은 O이고, X2는 CH이고, X3은 N임), 이미다졸릴 (X1은 N 또는 NH이고, X2는 CH이고, X3은 N 또는 NH임); 또는 트리아졸릴 (X1은 N 또는 NH이고, X2는 N이고, X3은 N 또는 NH임) 고리 모이어티를 형성한다. 구체적 실시양태에서, Y가 결합인 경우에, X1, X2 및 X3은 이들이 부착되어 있는 원자와 함께 옥사디아졸릴 고리 모이어티를 형성한다.
선택된 실시양태에서, Y가 -C(O)-인 경우에, X1, X2 및 X3은 이들이 부착되어 있는 원자와 함께 티아졸릴 (X3은 S이고, X1은 CH이고, X2는 N이거나, 또는 X3은 S이고, X1은 N이고, X2는 CH임), 옥사졸릴 (X3은 O이고, X1은 CH이고, X2는 N이거나, 또는 X3은 O이고, X1은 N이고, X2는 CH임), 티에닐 (X1 및 X2는 CH이고, X3은 S임) 또는 푸라닐 (X1 및 X2는 CH이고, X3은 O임) 고리 모이어티를 형성한다. 구체적 실시양태, Y가 -C(O)-인 경우에, X1, X2 및 X3은 이들이 부착되어 있는 원자와 함께 티에닐, 티아졸릴 또는 옥사졸릴 고리 모이어티, 보다 구체적으로 티에닐 모이어티를 형성한다.
선택된 실시양태에서, Y가 -C(O)-인 경우에, X1, X2 및 X3은 이들이 부착되어 있는 원자와 함께 푸라닐 또는 푸릴 (X1은 O이고, X2 및 X3은 CH임), 옥사졸릴 (X1은 O이고, X2는 CH이고, X3은 N임), 이속사졸릴 (X1은 O이고, X2는 N이고, X3은 CH임) 또는 옥사디아졸릴 (X1은 O이고, X2 및 X3은 N임) 고리 모이어티를 형성한다. 구체적 실시양태에서, Y가 -C(O)-인 경우에, X1, X2 및 X3은 이들이 부착되어 있는 원자와 함께 푸라닐 (푸릴) 고리 모이어티를 형성한다.
본 발명은 또한 하기 화학식 (I-a)의 화합물에 관한 것이다.
상기 식에서, R1, R2, R3, R4, A, Z, n 및 L은 본원에 정의된 바와 같다.
본 발명은 또한 하기 화학식 (I-b)의 화합물에 관한 것이다.
상기 식에서, R1, R2, R3, R4, A, Z, n 및 L은 본원에 정의된 바와 같다.
본 발명은 또한 하기 화학식 (I-c), (I-d) 또는 (I-e)의 화합물에 관한 것이다.
상기 식에서, R1, R2, R3, R4, A, Z, n 및 L은 본원에 정의된 바와 같다.
본 발명은 또한 하기 화학식 (I-f), (I-g), (I-h), (I-i) 또는 (I-j)의 화합물에 관한 것이다.
상기 식에서, R1, R2, R3, R4, A, Z, n 및 L은 본원에 정의된 바와 같다.
본 발명은 또한 하기 화학식 (I-k), (I-l), (I-m) 또는 (I-n)의 화합물에 관한 것이다.
상기 식에서, R1, R2, R3, R4, A, n 및 L은 본원에 정의된 바와 같다.
또 다른 실시양태에서, A는 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, 할로(C1-C4)알콕시, -NRARA 및 -((C1-C4)알킬)NRARA로부터 독립적으로 선택된 1 내지 2개의 기에 의해 임의로 치환된 페닐 기이다. 추가 실시양태에서, A는 메틸, 에틸, 플루오로, 클로로, 트리플루오로메틸, 메톡시, 에톡시, 트리플루오로메톡시, 시아노, -NRARA 및 -((C1-C4)알킬)NRARA로부터 선택된 1개의 기에 의해 임의로 치환된 페닐 기이고, 여기서 각각의 RA는 독립적으로 H 또는 메틸이다. 구체적 실시양태에서, A는 비치환된 페닐 기, 또는 에틸, 플루오로, 시아노 또는 메톡시 기에 의해 치환된 페닐 기이다.
또 다른 실시양태에서, A는 (C1-C4)알킬, (C1-C4)알콕시, -NRARA 및 -((C1-C4)알킬)NRARA로부터 독립적으로 선택된 1 내지 2개의 기에 의해 임의로 치환된 시클로프로필, 시클로펜틸 또는 시클로헥실 기이다. 추가 실시양태에서, A는 메틸, 에틸, tert-부틸, 메톡시, 에톡시, -NRARA 및 -((C1-C4)알킬)NRARA로부터 독립적으로 선택된 1 내지 2개의 기에 의해 임의로 치환된 시클로프로필, 시클로펜틸 또는 시클로헥실 기이고, 여기서 각각의 RA는 독립적으로 H 또는 메틸이다. 본 발명의 선택된 실시양태에서, A는 시클로프로필, 시클로펜틸 또는 시클로헥실 기이다.
본 발명의 또 다른 실시양태에서, A는 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, 할로(C1-C4)알콕시, -NRARA 및 -((C1-C4)알킬)NRARA로부터 독립적으로 선택된 1 내지 2개의 기에 의해 임의로 치환된 나프틸이다.
본 발명의 또 다른 실시양태에서, A는 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, 할로(C1-C4)알콕시, 옥소, -NRARA 및 -((C1-C4)알킬)NRARA로부터 독립적으로 선택된 1 내지 3개의 기에 의해 임의로 치환된 4 내지 7원 헤테로시클로알킬 기이다.
본 발명의 또 다른 실시양태에서, A는 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, 할로(C1-C4)알콕시, 옥소, -NRARA 및 -((C1-C4)알킬)NRARA로부터 독립적으로 선택된 1 내지 2개의 기에 의해 임의로 치환된 9 내지 10원 헤테로아릴이다. 선택된 실시양태에서, A는 이소퀴놀릴, 인다졸릴, 테트라히드로이소퀴놀리노닐, 이소인돌리노닐 및 인돌리닐이다.
추가 실시양태에서, A는 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, 할로(C1-C4)알콕시, -NRARA 및 -((C1-C4)알킬)NRARA로부터 독립적으로 선택된 1 내지 2개의 기에 의해 임의로 치환된 5 내지 6원 헤테로아릴이다. 추가 실시양태에서, A는 메틸, 에틸, 플루오로, 트리플루오로메틸, -NRARA 및 -((C1-C4)알킬)NRARA로부터 선택된 1개의 기에 의해 임의로 치환된 5 내지 6원 헤테로아릴이고, 여기서 각각의 RA는 독립적으로 H 또는 메틸이고 5 내지 6원 헤테로아릴은 N, O 및 S로부터 선택된 1개의 고리 헤테로원자를 함유하고 1개의 추가의 고리 질소 원자를 임의로 함유한다. 선택된 실시양태에서, A는 메틸 기에 의해 임의로 치환된 옥사졸릴, 피라졸릴 또는 티에닐이다. 다른 선택된 실시양태에서, A는 메틸 기에 의해 임의로 치환된 피라졸릴 또는 티에닐이다. 구체적 실시양태에서, A는 티에닐이다. 다른 구체적 실시양태에서, A는 옥사졸릴이다.
또 다른 실시양태에서, A는 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, 할로(C1-C4)알콕시, -NRARA 및 -((C1-C4)알킬)NRARA로부터 독립적으로 선택된 1 내지 2개의 기에 의해 임의로 치환된 피리딜 또는 피리딜-N-옥시드 기이다. 추가 실시양태에서, A는 메틸, 에틸, 플루오로, 클로로, 트리플루오로메틸, 메톡시, 에톡시, 트리플루오로메톡시, 시아노, -NRARA 및 -((C1-C4)알킬)NRARA로부터 선택된 1개의 기에 의해 임의로 치환된 피리딜 또는 피리딜-N-옥시드 기이고, 여기서 각각의 RA는 독립적으로 H 또는 메틸이다. 선택된 실시양태에서, A는 피리딜 또는 피리딜-N-옥시드이다. 구체적 실시양태에서, A는 피리딜이다.
본 발명의 또 다른 실시양태에서, Z는 -C(=O)NRX-, -NRXC(=O)NRX 또는 -NRXC(=O)-; 특히 -C(=O)NRX- 또는 -NRXC(=O)-이다. 본 발명의 또 다른 실시양태에서, Z는 -SO2NRX- 또는 -NRXSO2-이다. 본 발명의 또 다른 실시양태에서, Z는 -NHCH(CF3)- 또는 -CH(CF3)NH-이다. 본 발명의 또 다른 실시양태에서, Z는 -CH(CF3)- 또는 -(C1-C4)알킬-이다. 본 발명의 또 다른 실시양태에서, Z는 -NRX- 또는 -(C1-C3)알킬-NRX-이다.
Z의 각각의 상기 실시양태에 있어서, RX, 또는 -NRXC(=O)NRX에 대해 각각의 RX는 독립적으로 H, (C1-C4)알킬 및 임의로 치환된 (C2-C4)알킬로부터 선택될 수 있고, 여기서 상기 임의로 치환된 (C2-C4)알킬은 히드록실, 시아노, 아미노, (C1-C4)알콕시, (C1-C4)알킬)NH- 또는 ((C1-C4)알킬)((C1-C4)알킬)N-에 의해 임의로 치환된다. Z의 각각의 상기 실시양태에 있어서, RX, 또는 -NRXC(=O)NRX에 대해 각각의 RX는 독립적으로 H, 메틸, 에틸, tert-부틸, 히드록시에틸-, 메톡시메틸-, 시아노에틸-, N-메틸아미노에틸- 및 디메틸아미노에틸-로부터 선택될 수 있다. 구체적 실시양태에서, 각각의 RX는 독립적으로 H, 메틸 또는 시아노에틸이고, 보다 구체적으로, RX는 H 또는 메틸이다.
특정한 실시양태에서, Z는 -C(=O)NRX-, -SO2-, -SO2NRX-, -CH(CF3)NH-, 메틸 (메틸레닐), 에틸 (에틸레닐), -NRX- 또는 -(C1-C3)알킬-NRX-이고, 여기서 각각의 RX는 독립적으로 H, 메틸 또는 에틸이다. 구체적 실시양태에서, 각각의 RX는 H이다. 선택된 실시양태에서, Z는 -C(=O)NH-, -SO2NH-, -CH(CF3)NH-, 에틸 (에틸레닐), -CH2NH-, -CH2N(CH2CH3)-, -CH(CH3)N(CH2CH3)- 또는 -CH(CH3)NH-이다. 구체적 실시양태에서, Z는 -C(=O)NH- 또는 -CH2NH-이다.
본 발명의 또 다른 실시양태에서, n은 0 내지 4; 특히 0 내지 3이다. 구체적 실시양태에서, n은 1이거나 n은 0이다.
또 다른 실시양태에서, R2 및 R3 중 하나는 수소 이외의 것이다. 또 다른 실시양태에서, R2 및 R3은 둘 다 C1 - 4알킬 (예를 들어, 메틸)이다. 추가 실시양태에서, R2 및 R3 중 하나는 H이고, R2 및 R3 중 다른 하나는 C1 - 4알킬 (예를 들어, 메틸)이다. 추가 실시양태에서, R2 및 R3은 이들이 연결되어 있는 원자와 함께, 임의로 치환된 4, 5 또는 6원 시클로알킬 또는 헤테로시클로알킬 기를 형성하고, 여기서 상기 헤테로시클로알킬 기는 N, O 및 S로부터 선택된 1개의 헤테로원자를 함유하고, 상기 임의로 치환된 시클로알킬 또는 헤테로시클로알킬 기는 (C1-C4)알킬, 할로(C1-C4)알킬, 할로겐, 시아노, 아릴(C1-C2)알킬-, (C3-C6)시클로알킬(C1-C2)알킬-, -ORYa, -NRYaRYb, -C(=O)ORYa, -C(=O)NRYaRYb, -NRYbC(=O)RYa, -SO2NRYaRYb 및 -NRYbSO2RYa로부터 선택된 치환기에 의해 임의로 치환되고, 여기서 RYa는 H, (C1-C4)알킬, 페닐(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택되고, 각각의 RYb는 독립적으로 H 및 (C1-C4)알킬, 구체적으로 H 및 메틸로부터 선택된다.
본 발명의 또 다른 실시양태에서, n이 0인 경우에, R2 및 R3은 독립적으로 H 및 임의로 치환된 (C1-C4)알킬, 페닐(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택된다.
또 다른 실시양태에서, n이 1인 경우에, R2 및 R3은 독립적으로 H 및 임의로 치환된 (C1-C4)알킬, 페닐(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택된다.
또 다른 실시양태에서, n이 1이고, R2가 F이고, R3이 H인 경우에, Z는 -C(=O)NH-, -NHC(=O)NH, -SO2NH-, -NHCH(CF3)-, -CH(CF3)NH-, -CH(CF3)-, -(C1-C4)알킬-, -NH- 또는 -CH2NH-이고; 보다 구체적으로, Z는 -C(=O)NH- 또는 -CH2NH-이다.
또 다른 실시양태에서, n이 2 내지 4인 경우에, R2 및 R3은 독립적으로 H, 플루오로 및 임의로 치환된 (C1-C4)알킬, 페닐(C1-C4)알킬- 및 (C3-C6)시클로알킬(C1-C4)알킬-로부터 선택된다.
본 발명의 또 다른 실시양태에서, n이 1 내지 4 인 경우에, R2는 아미노, (C1-C4)알킬아미노, ((C1-C3)알킬)((C1-C3)알킬)아미노, 아미노(C1-C4)알킬, (C1-C3)알킬아미노(C1-C4)알킬, ((C1-C3)알킬)((C1-C3)알킬)아미노(C1-C4)알킬, (치환된(C1-C3)알킬)((C1-C3)알킬)아미노(C1-C4)알킬 (여기서, 상기 (치환된(C1-C3)알킬 모이어티는 -C(=O)OH, -C(=O)O(C1-C4)알킬 또는 1 내지 8개의 플루오로 기에 의해 치환됨), 아미노카르보닐(C1-C4)알킬, (C1-C3)알킬아미노카르보닐(C1-C4)알킬, ((C1-C3)알킬)((C1-C3)알킬)아미노카르보닐(C1-C4)알킬, 히드록실, 히드록시(C1-C4)알킬-, (C1-C4)알콕시 및 (C1-C4)알콕시(C1-C4)알킬-로부터 선택되고, R3은 H 및 임의로 치환된 (C1-C4)알킬, 아릴(C1-C4)알킬- 및 (C3-C7)시클로알킬(C1-C4)알킬-로부터 선택된다.
본 발명의 또 다른 실시양태에서, n이 1 내지 4인 경우에, R2는 아미노, 히드록실 및 (C1-C4)알콕시로부터 선택되고, R3은 H 및 임의로 치환된 (C1-C4)알킬, 페닐(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택된다. 또 다른 실시양태에서, n은 1 내지 3이고, R2는 히드록실이고, R3은 H 또는 메틸이고; 보다 구체적으로, n은 1이고, R2는 히드록실이고, R3은 H 또는 메틸이다. 본 발명의 또 다른 실시양태에서, (n의 임의의 값에 대해) R2 및 R3은 독립적으로 H 및 임의로 치환된 (C1-C4)알킬, 페닐(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택된다.
본 발명의 또 다른 실시양태에서, (n의 임의의 값에 대해) R2는 H 및 임의로 치환된 (C1-C4)알킬, 페닐(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택되고, R3은 H 및 메틸로부터 선택된다.
본 발명의 구체적 실시양태에서, (n의 임의의 값에 대해) R2 및 R3은 독립적으로 H 및 메틸로부터 선택된다. 보다 구체적인 실시양태에서, R2 및 R3은 둘 다 H이거나, 또는 R2 및 R3은 둘 다 메틸이다.
본 발명의 또 다른 실시양태에서, 임의의 R2 및 R3 중 상기 임의로 치환된 (C1-C4)알킬, 아릴(C1-C4)알킬-, 페닐 (C1-C4)알킬-, (C3-C7)시클로알킬(C1-C4)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-의 아릴, 페닐, 시클로알킬 및 각각의 (C1-C4)알킬 또는 (C1-C2)알킬 모이어티는 1, 2 또는 3개의 할로겐 (구체적으로 플루오린) 기 및/또는 시아노, (C1-C4)알킬, 할로(C1-C4)알킬, (C1-C4)알콕시, 할로(C1-C4)알콕시, NRARA, -((C1-C4)알킬)NRARA 및 히드록실로부터 독립적으로 선택된 1 또는 2개의 기에 의해 임의로 치환된다.
본 발명의 또 다른 실시양태에서, R2 및 R3은 이들이 연결되어 있는 원자와 함께, 임의로 치환된 4, 5 또는 6원 시클로알킬 또는 헤테로시클로알킬 기를 형성하고, 여기서 상기 헤테로시클로알킬 기는 N, O 및 S로부터 선택된 1개의 헤테로원자를 함유하고, 상기 임의로 치환된 시클로알킬 또는 헤테로시클로알킬 기는 (C1-C4)알킬, 할로(C1-C4)알킬, 할로겐, 시아노, 아릴(C1-C2)알킬-, (C3-C6)시클로알킬(C1-C2)알킬-, -ORYa, -NRYaRYb, -C(=O)ORYa, -C(=O)NRYaRYb, -NRYbC(=O)RYa, -SO2NRYaRYb 및 -NRYbSO2RYa로부터 선택된 치환기에 의해 임의로 치환되고, 여기서 RYa는 H, (C1-C4)알킬 페닐(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택되고, 각각의 RYb는 독립적으로 H 및 (C1-C4)알킬, 구체적으로 H 및 메틸로부터 선택된다.
본 발명의 구체적 실시양태에서, R2 및 R3은 이들이 연결되어 있는 원자와 함께, 임의로 치환된 4, 5 또는 6원 시클로알킬 또는 헤테로시클로알킬 기를 형성하고, 여기서 상기 헤테로시클로알킬 기는 N 및 O로부터 선택된 1개의 헤테로원자를 함유하고, 상기 임의로 치환된 시클로알킬 또는 헤테로시클로알킬 기는 (C1-C4)알킬, 아릴(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택된 치환기에 의해 임의로 치환된다.
본 발명의 선택된 실시양태에서, R2 및 R3은 이들이 연결되어 있는 원자와 함께, 테트라히드로피라닐, 2,2-디메틸-테트라히드로피라닐, 시클로펜틸, 1-메틸-피페리디닐, 시클로프로필, 시클로헥실, 1-에틸-피페리디닐, 테트라히드로푸라닐, 피페리디닐, 1-메틸-피롤리디닐, 1-벤질-피롤리디닐, 1-시클로프로필메틸-피롤리디닐, 옥세타닐, 아제티디닐, 1-메틸-아제티디닐, 1-벤질-아제티디닐 또는 1-시클로프로필메틸-아제티디닐 기를 형성한다.
본 발명의 구체적 실시양태에서, R2 및 R3은 이들이 연결되어 있는 원자와 함께, 테트라히드로피라닐, 2,2-디메틸-테트라히드로피라닐, 시클로펜틸, 1-메틸-피페리디닐 기를 형성한다.
본 발명의 또 다른 실시양태에서, L은 5 내지 6원 헤테로아릴 또는 페닐이고, 이는 R4에 의해 치환되고 임의로 추가 치환되고, 여기서 L이 추가 치환되는 경우에, L은 할로겐, 시아노 및 메틸로부터 독립적으로 선택된 1 또는 2개의 치환기에 의해 치환된다.
본 발명의 또 다른 실시양태에서, L은 5-원 헤테로아릴, 피리딜 또는 페닐이고, 이는 R4에 의해 치환되고 임의로 추가 치환되고, 여기서 L이 추가 치환되는 경우에, L은 클로로, 플루오로, 시아노 및 메틸로부터 선택된 1개의 치환기에 의해 치환된다.
선택된 실시양태에서, L은 피라졸릴, 옥사디아졸릴, 1-메틸-이미다졸릴, 티아졸릴, 티에닐, 트리아졸릴, 피리딜, 페닐, 옥사졸릴 또는 이속사졸릴이고, 이 중 임의의 것은 메틸 기에 의해 치환된다.
구체적 실시양태에서, L은 티아졸릴, 티에닐, 트리아졸릴, 피리딜, 페닐 또는 옥사졸릴이고, 이 중 임의의 것은 메틸 기에 의해 치환된다.
본 발명의 또 다른 실시양태에서, R4는 H, 할로겐, (C1-C4)알킬, 할로(C1-C2)알킬, (C1-C2)알콕시, ((C1-C2)알킬)((C1-C2)알킬)N(C1-C3)알콕시-, ((C1-C2)알킬)((C1-C2)알킬)N(C1-C3)알킬-, (C1-C2)할로알킬, (C1-C3)알킬아미노, 임의로 치환된 (C3-C6)시클로알킬, 임의로 치환된 페닐, 임의로 치환된 5 내지 6원 헤테로시클로알킬 또는 임의로 치환된 5 내지 6원 헤테로아릴이고, 여기서 상기 임의로 치환된 시클로알킬, 페닐, 헤테로시클로알킬 또는 헤테로아릴은 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C2)알킬, (C1-C2)알콕시, 할로(C1-C2)알콕시, 히드록실, -NRARC 및 -((C1-C4)알킬)NRARC로부터 독립적으로 선택된 1 또는 2개의 기에 의해 임의로 치환된다.
선택된 실시양태에서, R4는 H, 메틸, 브로모, 트리플루오로메틸, 디메틸아미노에톡시-, 디메틸아미노프로필- 및 임의로 치환된 피리딜, 시클로헥실, 피페리디닐, 피페라지닐, 이미다졸릴, 티에닐 또는 페닐이고, 여기서 피리딜, 시클로헥실, 피페리디닐, 피페리지닐, 이미다졸릴, 티에닐 또는 페닐은 메틸, 클로로, 브로모, 플루오로, 트리플루오로메틸, 메톡시 및 시아노로부터 독립적으로 선택된 1 내지 2개의 치환기에 의해 임의로 치환된다.
선택된 실시양태에서, R4는 H, 메틸, 브로모, 트리플루오로메틸, 디메틸아미노에톡시-, 페닐, 4-클로로페닐, 2-브로모페닐, 4-플루오로페닐, 4-시아노페닐, 3-트리플루오로메틸페닐, 4-메톡시페닐, 시클로헥실, 이미다졸릴, 티에닐, 피리드-2-일, 피리드-3-일 또는 피리드-4-일이다.
본 발명의 다른 실시양태에서, L-R4는 함께 메틸, 트리플루오로메틸, 클로로, 플루오로, 시아노, 메톡시, 페닐 및 모르폴리닐프로필-로부터 독립적으로 선택된 1 또는 2개의 기로 임의로 치환된 1,3-벤조디옥솔릴, 티에노피리미디닐, 벤조-이소티아졸릴, 2,3-디히드로-1,4-벤조디옥시닐, 벤조푸라닐, 벤즈이미다졸릴, 벤즈이미다졸로닐, 테트라히드로이소퀴놀릴, 인돌리닐 또는 이소인돌리닐 기를 형성한다.
본 발명의 선택된 실시양태에서, L-R4는 함께, 1,3-벤조디옥솔릴, 테트라히드로이소퀴놀릴 또는 이소인돌리닐 기를 형성한다.
본 발명의 또 다른 실시양태에서, 각각의 RA 및 RC는 독립적으로 H 및 (C1-C4)알킬로부터 선택되고; 구체적으로 각각의 RA 및 RC는 독립적으로 H, 메틸 및 에틸로부터 선택된다.
본 발명의 또 다른 실시양태에서, 각각의 RY는 독립적으로 H, (C1-C4)알킬, 페닐 및 -(C1-C4)알킬페닐로부터 선택되고; 구체적으로 각각의 RY 는 독립적으로 H, 메틸, 에틸, 페닐, 벤질 및 -에틸페닐로부터 선택된다.
본원에 사용된 바와 같이, 용어 "알킬"은 포화, 직쇄형 또는 분지형 탄화수소 모이어티를 나타내며, 이는 비치환되거나 본원에 정의된 1개 이상의 치환기에 의해 치환된다. 예시적 알킬은 메틸 (Me), 에틸 (Et), n-프로필, 이소프로필, n-부틸, 이소부틸, sec-부틸, t-부틸, n-펜틸, 이소-펜틸 (3-메틸-부틸), 네오-펜틸 (2,2-디메틸프로필) 등을 포함하나, 이에 제한되는 것은 아니다. 용어 "C1-C4"는 1 내지 4개의 탄소 원자를 포함하는 알킬을 지칭한다.
용어 "알킬"이 다른 치환기와 함께 사용되는 경우, 예컨대 "할로알킬" 또는 "시클로알킬-알킬" 또는 "아릴알킬"에서, 용어 "알킬"은 2가 직쇄형 또는 분지쇄 탄화수소 라디칼을 포함하도록 의도된다. 예를 들어, "아릴알킬"은, 그의 알킬 모이어티가 2가 직쇄형 또는 분지쇄 탄소 라디칼이고, 아릴 모이어티가 본원에 정의된 바와 같은, 벤질 기에 존재하는 결합 배열에 의해 나타내어지는 라디칼 -알킬아릴 (-CH2-페닐)을 의미하는 것을 의도한다.
또한, 용어 "알킬"은 2가 치환기, 예컨대 2개의 다른 기에 결합된 기를 정의하는데 사용될 수 있다. 이 경우에, 용어 "알킬"은 2가 직쇄형 또는 분지쇄 탄화수소 라디칼을 포함하도록 의도된다. 예를 들어, "펜틸"은 펜틸렌 디라디칼을 나타내는 것을 의도하며 - 여기서 펜틸 모이어티는 2가 직쇄형 (-CH2CH2CH2CH2CH2-) 또는 분지형 (-CH2CH(CH3)CH2CH2-, -CH2CH2CH(CH2CH3)-, -CH2CH2C(CH3)2-) 쇄 5-탄소 라디칼 중 임의의 하나이다.
본원에 사용된 바와 같이, 용어 "시클로알킬"은 비-방향족 포화, 시클릭 탄화수소 고리를 지칭한다. 용어 "(C3-C8)시클로알킬"은 3 내지 8개의 고리 탄소 원자를 갖는 비-방향족 시클릭 탄화수소 고리를 지칭한다. 본 발명에 유용한 예시적 "(C3-C8)시클로알킬" 기는 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실, 시클로헵틸 및 시클로옥틸을 포함한다.
"알콕시"는 산소 연결 원자를 통해 부착된 알킬 라디칼을 함유하는 기를 지칭한다. 용어 "(C1-C4)알콕시"는 산소 연결 원자를 통해 부착된, 1개 이상 4개 이하의 탄소 원자를 갖는 직쇄 또는 분지쇄 탄화수소 라디칼을 지칭한다. 본 발명에 유용한 예시적 "(C1-C4)알콕시" 기는 메톡시, 에톡시, n-프로폭시, 이소프로폭시, n-부톡시, s-부톡시 및 t-부톡시를 포함하나, 이에 제한되는 것은 아니다.
"아릴"은 6 내지 10개의 탄소 고리 원자를 함유하는 방향족, 1가 모노시클릭 또는 비시클릭 탄화수소 라디칼을 포함하는 기 또는 모이어티를 나타내고, 이는 비치환되거나 본원에 정의된 치환기 중 1개 이상에 의해 치환될 수 있고, 여기에 1개 이상의 시클로알킬 고리가 융합될 수 있고, 이는 비치환되거나 본원에 정의된 1개 이상의 치환기에 의해 치환되거나 될 수 있다.
일반적으로, 본 발명의 화합물에서, 아릴은 페닐이다.
헤테로시클릭 기는 헤테로아릴 또는 헤테로시클로알킬 기일 수 있다. "헤테로시클로알킬"은, 3 내지 10개의 고리 원자를 함유하며 질소, 산소 및 황으로부터 선택된 1 내지 4개의 헤테로원자를 포함하고, 본원에 정의된 치환기 중 1개 이상에 의해 또는 치환되거나 비치환될 수 있는, 포화 또는 부분 불포화의, 안정한 비-방향족, 1가 모노시클릭 또는 비시클릭 라디칼을 포함하는 기 또는 모이어티를 나타낸다. 헤테로시클로알킬은 안정한 구조의 형성을 초래하는 모노시클릭 또는 비시클릭 라디칼의 임의의 원자에 의해 부착될 수 있다. 이 용어는 2,5-디아자비시클로[2.2.1]헵틸, 2-아자비시클로[2.2.1]헵틸, 2-옥사-5-아자비시클로[2.2.1]헵틸, 7-옥사-2-아자비시클로[2.2.1]헵틸, 2-티아-5-아자비시클로[2.2.1]헵틸, 7-아자비시클로[2.2.1]헵틸, 2,6-디아자트리시클로[3.3.1.13,7]데실, 2-아자트리시클로[3.3.1.13,7]데실, 2,4,9-트리아자트리시클로[3.3.1.13,7]데실, 8-아자비시클로[3.2.1]옥틸, 2,5-디아자비시클로[2.2.2]옥틸, 2-아자비시클로[2.2.2]옥틸, 3-아자비시클로[3.2.1]옥틸, 8-아자비시클로[3.2.1]옥틸, 옥타히드로-1H-피롤로[3,2-b]피리딜 기로 결합 배열에 의해 예시된 바와 같이, 고리가 고리당 2개의 원자에서 연결된 비시클릭 헤테로시클로알킬 모이어티를 포함한다. 이 용어는 구체적으로, 1-옥사-2-아자스피로[4.5]데스-2-엔-3-일 기로 결합 배열에 의해 예시된 바와 같이, 고리가 고리당 단일 원자에서 연결된 (스피로), 비시클릭 헤테로시클로알킬 모이어티를 제외한다. 헤테로시클로알킬의 예시적 예는 아제티디닐, 피롤리딜 (또는 피롤리디닐), 피페리디닐, 피페라지닐, 모르폴리닐, 테트라히드로-2H-1,4-티아지닐, 테트라히드로푸릴 (또는 테트라히드로푸라닐), 디히드로푸릴, 옥사졸리닐, 티아졸리닐, 피라졸리닐, 테트라히드로피라닐, 디히드로피라닐, 1,3-디옥솔라닐, 1,3-디옥사닐, 1,4-디옥사닐, 1,3-옥사티올라닐, 1,3-옥사티아닐, 1,3-디티아닐 아자비시클로[3.2.1]옥틸, 아자비시클로[3.3.1]노닐, 아자비시클로[4.3.0]노닐, 옥사비시클로[2.2.1]헵틸 및 1,5,9-트리아자시클로도데실을 포함하나, 이에 제한되는 것은 아니다.
일반적으로, 본 발명의 화합물에서, 헤테로시클로알킬 기는 5-원 및/또는 6-원 헤테로시클로알킬 기, 예컨대 피롤리딜 (또는 피롤리디닐), 테트라히드로푸릴 (또는 테트라히드로푸라닐), 테트라히드로티에닐, 디히드로푸릴, 옥사졸리닐, 티아졸리닐 또는 피라졸리닐, 피페리딜 (또는 피페리디닐), 피페라지닐, 모르폴리닐, 테트라히드로피라닐, 디히드로피라닐, 1,3-디옥사닐, 테트라히드로-2H-1,4-티아지닐, 1,4-디옥사닐, 1,3-옥사티아닐 및 1,3-디티아닐이다.
"헤테로아릴"은, 5 내지 10개의 고리 원자를 함유하며 질소, 산소 및 황으로부터 선택된 1 내지 4개의 헤테로원자를 포함하고, 본원에 정의된 1개 이상의 치환기에 의해 치환되거나 비치환될 수 있는, 방향족 1가 모노시클릭 또는 비시클릭 라디칼을 포함하는 기 또는 모이어티를 나타낸다. 이 용어는 또한 5 내지 10개의 고리 원자를 함유하며 질소, 산소 및 황으로부터 선택된 1 내지 4개의 헤테로원자를 포함하고, 본원에 정의된 1개 이상의 치환기에 의해 치환되거나 비치환될 수 있는, 헤테로시클로알킬 고리 모이어티에 융합된 아릴 고리 모이어티를 함유하는 비시클릭 헤테로시클릭-아릴 화합물을 포함한다. 이 용어는 또한 질소 및/또는 황을 함유하며 여기서 질소 또는 황 헤테로원자가 임의로 산화된 헤테로시클릭 기를 포함하는 것을 의도한다. 헤테로아릴의 예시적 예는 티에닐, 피롤릴, 이미다졸릴, 피라졸릴, 푸릴 (또는 푸라닐), 이소티아졸릴, 푸라자닐, 이속사졸릴, 옥사졸릴, 옥사디아졸릴, 티아졸릴, 피리딜 (또는 피리디닐), 피리딜-N-옥시드, 피라지닐, 피리미디닐, 피리다지닐, 트리아지닐, 테트라지닐, 트리아졸릴, 테트라졸릴, 벤조[b]티에닐, 이소벤조푸릴, 2,3-디히드로벤조푸릴, 크로메닐, 크로마닐, 인돌리지닐, 이소인돌릴, 인돌릴, 인다졸릴, 퓨리닐, 이소퀴놀릴, 퀴놀릴, 프탈라지닐, 나프티리디닐, 퀴나졸리닐, 벤조티아졸릴, 벤즈이미다졸릴, 테트라히드로퀴놀리닐, 테트라히드로이소퀴놀리닐, 이소인돌리닐, 인돌리닐, 신놀리닐, 프테리디닐, 이소티아졸릴을 포함하나, 이에 제한되는 것은 아니다.
본 발명의 화합물에 존재하는 헤테로아릴 기 중 일부는 5 내지 6원 모노시클릭 헤테로아릴 기이다. 선택된 5-원 헤테로아릴 기는 1개의 질소, 산소 또는 황 고리 헤테로원자를 함유하고, 1, 2 또는 3개의 추가의 질소 고리 원자를 임의로 함유한다. 선택된 6-원 헤테로아릴 기는 1, 2, 3 또는 4개의 질소 고리 헤테로원자를 함유한다. 선택된 5- 또는 6-원 헤테로아릴 기는 티에닐, 피롤릴, 이미다졸릴, 피라졸릴, 푸릴, 이소티아졸릴, 푸라자닐, 이속사졸릴, 옥사졸릴, 옥사디아졸릴, 티아졸릴, 트리아졸릴 및 테트라졸릴 또는 피리딜, 피라지닐, 피리미디닐, 피리다지닐, 트리아지닐 및 티아디아졸릴을 포함한다.
본 발명의 화합물에 존재하는 헤테로아릴 기 중 일부는 9 내지 10원 비시클릭 헤테로아릴 기이다. 선택된 9-원 헤테로아릴 기는 1개의 질소, 산소 또는 황 고리 헤테로원자를 함유하고, 1, 2 또는 3개의 추가의 질소 고리 원자를 임의로 함유한다. 선택된 10-원 헤테로아릴 기는 1개의 질소, 산소 또는 황 고리 헤테로원자를 함유하고, 1, 2, 3 또는 4개의 추가의 질소 고리 원자를 임의로 함유한다. 선택된 9 내지 10원 헤테로아릴 기는 벤조[b]티에닐, 이소벤조푸릴, 2,3-디히드로벤조푸릴, 크로메닐, 크로마닐, 인돌리지닐, 이소인돌릴, 인돌릴, 인다졸릴, 퓨리닐, 이소퀴놀릴, 퀴놀릴, 프탈라지닐, 나프티리디닐, 퀴나졸리닐, 벤조티아졸릴, 벤즈이미다졸릴, 테트라히드로퀴놀리닐, 신놀리닐, 프테리디닐을 포함한다.
용어 "할로겐" 및 "할로"는 클로로, 플루오로, 브로모 또는 아이오도 치환기를 나타낸다. "히드록시" 또는 "히드록실"은 라디칼 -OH을 의미하도록 의도된다. 용어 "옥소"는 피롤리딘-2-온 고리 상에 존재하는 바와 같은 케토 디라디칼 (=O)을 의미하도록 의도된다.
본 발명의 화합물은 오직 당업자에 의해 인지되는 바와 같이 "화학적으로 안정한" 것으로 고려되는 것이다.
구체적으로, 본 발명은 하기 화학식 (I-a)에 따른 화합물 또는 그의 염, 특히 제약상 허용되는 염에 관한 것이다.
상기 식에서:
R1은 -CF3이고;
A는 임의로 치환된 (C3-C6)시클로알킬, 페닐, 나프틸, 4 내지 7원 헤테로시클로알킬, 5 내지 6원 헤테로아릴 또는 9 내지 10원 헤테로아릴이고,
여기서 임의의 임의로 치환된 시클로알킬, 페닐, 나프틸, 헤테로시클로알킬 또는 헤테로아릴은 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, 할로(C1-C4)알콕시, -NRARA 및 -((C1-C4)알킬)NRARA로부터 독립적으로 선택된 1 내지 3개의 기에 의해 임의로 치환되고;
Z는 -C(=O)NRX-, -NRXC(=O)NRX, -NRXC(=O)-, -SO2-, -SO2NRX-, -NRXSO2-, -NHCH(CF3)-, -CH(CF3)NH-, -CH(CF3)-, -(C1-C4)알킬-, -NRX- 또는 -(C1-C3)알킬-NRX-이고;
n은 0 내지 4이고;
n이 0인 경우에, R2 및 R3은 독립적으로 H 및 임의로 치환된 (C1-C4)알킬, 아릴(C1-C4)알킬- 및 (C3-C7)시클로알킬(C1-C4)알킬-로부터 선택되고,
n이 1 내지 4인 경우에, R2 및 R3은 독립적으로 H, 플루오로 및 임의로 치환된 (C1-C4)알킬, 아릴(C1-C4)알킬- 및 (C3-C7)시클로알킬(C1-C4)알킬-로부터 선택되고, 여기서 n이 1이고, R2가 F이고, R3이 H인 경우에, Z는 -C(=O)NRX-, -NRXC(=O)NRX, -SO2NRX-, -NHCH(CF3)-, -CH(CF3)NH-, -CH(CF3)-, -(C1-C4)알킬-, -NRX- 또는 -(C1-C3)알킬-NRX-이고,
n이 1 내지 4인 경우에, R2는 아미노, 히드록실 및 (C1-C4)알콕시로부터 선택되고, R3은 H 및 임의로 치환된 (C1-C4)알킬, 아릴(C1-C4)알킬- 및 (C3-C7)시클로알킬(C1-C4)알킬-로부터 선택되고,
여기서 임의의 R2 및 R3 중 상기 임의로 치환된 (C1-C4)알킬, 아릴(C1-C4)알킬- 및 (C3-C7)시클로알킬(C1-C4)알킬-의 아릴, 시클로알킬 및 각각의 (C1-C4)알킬 모이어티는 할로겐, 시아노, (C1-C4)알킬, 할로(C1-C4)알킬, (C1-C4)알콕시, 할로(C1-C4)알콕시, 할로겐, -NRARA, -((C1-C4)알킬)NRARA, (C1-C4)알콕시, 히드록실, 시아노, 할로(C1-C4)알킬 및 할로(C1-C4)알콕시로부터 독립적으로 선택된 1, 2 또는 3개의 기에 의해 임의로 치환되거나;
또는 R2 및 R3은 이들이 연결되어 있는 원자와 함께, 임의로 치환된 4, 5, 6 또는 7원 시클로알킬 또는 헤테로시클로알킬 기를 형성하고, 여기서 상기 헤테로시클로알킬 기는 N, O 및 S로부터 독립적으로 선택된 1 또는 2개의 헤테로원자를 함유하고, 상기 임의로 치환된 시클로알킬 또는 헤테로시클로알킬 기는 (C1-C4)알킬, 할로(C1-C4)알킬, 할로겐, 시아노, 아릴(C1-C4)알킬-, (C3-C7)시클로알킬(C1-C4)알킬-, -ORY, -NRYRY, -C(=O)ORY, -C(=O)NRYRY, -NRYC(=O)RY, -SO2NRYRY, -NRYSO2RY, -OC(=O)NRYRY, -NRYC(=O)ORY 및 -NRYC(=O)NRYRY로부터 독립적으로 선택된 1, 2 또는 3개의 치환기에 의해 임의로 치환되고;
L은 5 내지 6원 헤테로아릴 또는 페닐이고, 이는 R4에 의해 치환되고 임의로 추가 치환되고,
여기서 L이 추가 치환되는 경우에, L은 할로겐, 시아노 및 (C1-C4)알킬로부터 독립적으로 선택된 1 또는 2개의 치환기에 의해 치환되고;
R4는 H, (C1-C4)알킬, 할로, 할로(C1-C4)알킬, (C1-C4)알콕시, ((C1-C4)알킬)((C1-C4)알킬)N(C1-C4)알콕시, ((C1-C4)알킬)((C1-C4)알킬)N(C1-C4)알킬-, (C1-C4)할로알콕시-, (C1-C4)알킬아미노, 임의로 치환된 (C3-C6)시클로알킬, 임의로 치환된 페닐, 임의로 치환된 5 내지 6원 헤테로시클로알킬 또는 임의로 치환된 5 내지 6원 헤테로아릴이고,
여기서 상기 임의로 치환된 시클로알킬, 페닐, 헤테로시클로알킬 또는 헤테로아릴은 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, (C1-C4)알킬티오-, 할로(C1-C4)알콕시, 히드록실, -NRARC 및 -((C1-C4)알킬)NRARC로부터 독립적으로 선택된 1, 2 또는 3개의 기에 의해 임의로 치환되거나;
또는 L-R4는 함께, 1,3-벤조디옥솔릴, 2,3-디히드로-1,4-벤조디옥시닐, 벤조푸라닐, 테트라히드로이소퀴놀릴 또는 이소인돌리닐 기를 형성하고, 여기서 상기 벤조푸라닐, 테트라히드로이소퀴놀릴 또는 이소인돌리닐 기는 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C4)알킬, (C1-C4)알콕시, (C1-C4)알킬티오-, 할로(C1-C4)알콕시, 히드록실, -NRARC 및 -((C1-C4)알킬)NRARC로부터 독립적으로 선택된 1, 2 또는 3개의 기에 의해 임의로 치환되고;
여기서 각각의 RA는 독립적으로 H 및 (C1-C4)알킬로부터 선택되고;
RC는 H, (C1-C4)알킬, 페닐, 5 내지 6원 헤테로시클로알킬 또는 5 내지 6원 헤테로아릴이거나, 또는 RA 및 RC는 이들이 부착되어 있는 원자와 함께, N, O 및 S로부터 선택된 1개의 추가의 헤테로원자를 임의로 함유하는 임의로 치환된 4 내지 8원 헤테로시클릭 고리를 형성하고;
각각의 RX는 독립적으로 H, (C1-C6)알킬 및 임의로 치환된 (C2-C6)알킬로부터 선택되고, 여기서 상기 임의로 치환된 (C2-C6)알킬은 히드록실, 시아노, 아미노, (C1-C4)알콕시, (C1-C4)알킬)NH- 또는 ((C1-C4)알킬)((C1-C4)알킬)N-에 의해 임의로 치환되고;
각각의 RY는 독립적으로 H, (C1-C4)알킬, 페닐 및 -(C1-C4)알킬페닐로부터 선택되고;
단, 화합물은
3-[4-(트리플루오로메틸)페닐]-N-{3-(트리플루오로메틸)-4-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]페닐}프로판아미도,
3-{7-메틸-2-[4-(3-메틸-5-이속사졸릴)부틸]-1-벤조푸란-5-일}-5-(트리플루오로메틸)-1,2,4-옥사디아졸,
1-[3-(3-메틸-5-이속사졸릴)프로필]-5-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]-1H-인돌,
7-메틸-1-[4-(3-메틸-5-이속사졸릴)부틸]-5-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]-1H-인돌,
7-메틸-1-[5-(3-메틸-5-이속사졸릴)펜틸]-5-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]-1H-인돌,
7-메틸-1-[3-(3-메틸-5-이속사졸릴)프로필]-5-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]-2,3-디히드로-1H-인돌 또는
N-(페닐메틸)-4-[5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일]-1,2,5-옥사디아졸-3-아민이 아니다.
따라서, 본 발명은
R1이 CHF2 또는 CF3이고;
Y가 결합이고, X1이 O이고, X2 및 X3이 N이거나, 또는
Y가 -C(O)-이고, X1 및 X2가 CH이고, X3이 S이거나, 또는
Y가 -C(O)-이고, X1이 O이고, X2 및 X3이 CH이고;
A가 메틸, 에틸, 플루오로, 클로로, 트리플루오로메틸, 메톡시, 에톡시, 트리플루오로메톡시, 시아노, -NRARA 및 -((C1-C4)알킬)NRARA로부터 선택된 1개의 기에 의해 임의로 치환된 페닐 기이거나, 또는
A가 메틸, 에틸, tert-부틸, 메톡시, 에톡시, -NRARA 및 -((C1-C4)알킬)NRARA 로부터 독립적으로 선택된 1 내지 2개의 기에 의해 임의로 치환된 시클로프로필, 시클로펜틸 또는 시클로헥실 기이거나, 또는
A가 메틸, 에틸, 플루오로, 트리플루오로메틸, -NRARA 및 -((C1-C4)알킬)NRARA로부터 선택된 1개의 기에 의해 임의로 치환된 5 내지 6원 헤테로아릴 또는 9 내지 10원 헤테로아릴이고, 여기서 5 내지 6원 헤테로아릴 또는 9 내지 10원 헤테로아릴이 N, O 및 S로부터 선택된 1개의 고리 헤테로원자를 함유하고 1개의 추가의 고리 질소 원자를 임의로 함유하고,
여기서 각각의 RA가 독립적으로 H 또는 메틸이고;
Z가 -C(=O)NRX-, -NRXC(=O)NRX, -NRXC(=O)-, -NHCH(CF3)-, -CH(CF3)NH-, -CH(CF3)-, -(C1-C4)알킬- 또는 -(C1-C4)알킬NRX-이고, 여기서 RX가 H, (C1-C4)알킬 또는 임의로 치환된 (C2-C4)알킬이고, 여기서 상기 임의로 치환된 (C2-C4)알킬이 히드록실, 시아노, 아미노, (C1-C4)알콕시, (C1-C4)알킬)NH- 또는 ((C1-C4)알킬)((C1-C4)알킬)N-에 의해 임의로 치환되고;
n이 0 내지 3이고, R2 및 R3이 독립적으로 H, 임의로 치환된 (C1-C4)알킬, 페닐(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택되거나, 또는
n이 1 내지 3이고, R2가 히드록실이고, R3이 H 또는 메틸이거나, 또는
n이 0 내지 3이고, R2 및 R3이 이들이 연결되어 있는 원자와 함께, 임의로 치환된 4, 5 또는 6원 시클로알킬 또는 헤테로시클로알킬 기를 형성하고, 여기서 상기 헤테로시클로알킬 기가 N, O 및 S로부터 선택된 1개의 헤테로원자를 함유하고, 상기 임의로 치환된 시클로알킬 또는 헤테로시클로알킬 기가 (C1-C4)알킬, 할로(C1-C4)알킬, 할로겐, 시아노, 아릴(C1-C2)알킬-, (C3-C6)시클로알킬(C1-C2)알킬-, -ORYa, -NRYaRYb, -C(=O)ORYa, -C(=O)NRYaRYb, -NRYbC(=O)RYa, -SO2NRYaRYb 및 -NRYbSO2RYa로부터 선택된 치환기에 의해 임의로 치환되고, 여기서 RYa가 H, (C1-C4)알킬 페닐(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택되고, 각각의 RYb가 독립적으로 H 및 (C1-C4)알킬로부터 선택되고;
L이 5 내지 6원 헤테로아릴 또는 페닐이고, 이것이 R4에 의해 치환되고 임의로 추가 치환되고, 여기서 L이 추가 치환되는 경우에, L이 할로겐, 시아노 및 메틸로부터 독립적으로 선택된 1 또는 2개의 치환기에 의해 치환되고;
R4가 H, 할로겐, (C1-C4)알킬, 할로(C1-C2)알킬, (C1-C2)알콕시, ((C1-C2)알킬)((C1-C2)알킬)N(C1-C3)알콕시-, ((C1-C2)알킬)((C1-C2)알킬)N(C1-C3)알킬-, (C1-C2)할로알킬, (C1-C3)알킬아미노, 임의로 치환된 (C3-C6)시클로알킬, 임의로 치환된 페닐, 임의로 치환된 5 내지 6원 헤테로시클로알킬 또는 임의로 치환된 5 내지 6원 헤테로아릴이고, 여기서 상기 임의로 치환된 시클로알킬, 페닐, 헤테로시클로알킬 또는 헤테로아릴이 (C1-C4)알킬, 할로겐, 시아노, 할로(C1-C2)알킬, (C1-C2)알콕시, 할로(C1-C2)알콕시, 히드록실, -NRARC 및 -((C1-C4)알킬)NRARC로부터 독립적으로 선택된 1 또는 2개의 기에 의해 임의로 치환된 것인
화학식 I에 따른 화합물 또는 그의 염, 특히 제약상 허용되는 염에 관한 것이다.
본 발명은 또한
n이 0 내지 3이고, R2 및 R3이 독립적으로 H 및 임의로 치환된 (C1-C4)알킬, 페닐(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택되거나, 또는
n이 1 내지 3이고, R2가 히드록실이고, R3이 H 또는 메틸이거나, 또는
n이 0 내지 3이고, R2 및 R3이 이들이 연결되어 있는 원자와 함께, 임의로 치환된 4, 5 또는 6원 시클로알킬 또는 헤테로시클로알킬 기를 형성하고, 여기서 상기 헤테로시클로알킬 기가 N 및 O로부터 선택된 1개의 헤테로원자를 함유하고, 상기 임의로 치환된 시클로알킬 또는 헤테로시클로알킬 기가 (C1-C4)알킬, 아릴(C1-C2)알킬- 및 (C3-C6)시클로알킬(C1-C2)알킬-로부터 선택된 치환기에 의해 임의로 치환되고;
RX가 H, 메틸 또는 시아노에틸이고;
L이 5-원 헤테로아릴, 피리딜 또는 페닐이고, 이것이 R4에 의해 치환되고 임의로 추가 치환되고, 여기서 L이 추가 치환되는 경우에, L이 클로로, 플루오로, 시아노 및 메틸로부터 선택된 1개의 치환기에 의해 치환되고;
R4가 H, 메틸, 브로모, 트리플루오로메틸, 디메틸아미노에톡시-, 디메틸아미노프로필- 및 임의로 치환된 피리딜, 시클로헥실, 피페리디닐, 피페라지닐, 이미다졸릴, 티에닐 또는 페닐이고, 여기서 피리딜, 시클로헥실, 피페리디닐, 피페리지닐, 이미다졸릴, 티에닐 또는 페닐이 메틸, 클로로, 브로모, 플루오로, 트리플루오로메틸, 메톡시 및 시아노로부터 독립적으로 선택된 1 내지 2개의 치환기에 의해 임의로 치환된 것인
본원에 정의된 바와 같은 화합물 또는 그의 염, 특히 제약상 허용되는 염에 관한 것이다.
본 발명은 구체적으로
R1이 CHF2 또는 CF3이고;
Y가 결합이고, X1이 O이고, X2 및 X3이 N이거나, 또는
Y가 -C(O)-이고, X1 및 X2가 CH이고, X3이 S이거나, 또는
Y가 -C(O)-이고, X1이 O이고, X2 및 X3이 CH이고;
A가 비치환된 페닐 기, 또는 에틸, 플루오로, 시아노 또는 메톡시 기에 의해 치환된 페닐 기, 또는 티에닐, 피리딜, 시클로프로필, 시클로펜틸 또는 시클로헥실 기이고;
Z가 -C(=O)NH- 또는 -CH2NH-이고;
n이 0 또는 1이고, R2 및 R3이 둘 다 H이거나, 또는 R2 및 R3이 둘 다 메틸이거나, 또는
n이 1이고, R2이 히드록실이고, R3이 H 또는 메틸이거나, 또는
n이 0 또는 1이고, R2 및 R3이 이들이 연결되어 있는 원자와 함께, 테트라히드로피라닐, 2,2-디메틸-테트라히드로피라닐, 시클로펜틸, 1-메틸-피페리디닐 기를 형성하고;
L이 티아졸릴, 티에닐, 트리아졸릴, 피리딜, 페닐 또는 옥사졸릴이고, 이 중 임의의 것이 메틸 기에 의해 임의로 치환되고;
R4가 H, 메틸, 브로모, 트리플루오로메틸, 디메틸아미노에톡시-, 페닐, 4-클로로페닐, 2-브로모페닐, 4-플루오로페닐, 4-시아노페닐, 3-트리플루오로메틸페닐, 4-메톡시페닐, 시클로헥실, 이미다졸릴, 티에닐, 피리드-2-일, 피리드-3-일 또는 피리드-4-일이거나; 또는
L-R4가 함께, 1,3-벤조디옥솔릴, 테트라히드로이소퀴놀릴 또는 이소인돌리닐 기를 형성하는 것인
화학식 I에 따른 화합물 또는 그의 염, 특히 제약상 허용되는 염에 관한 것이다.
본 발명은 보다 구체적으로
R1이 CHF2 또는 CF3이고;
Y가 결합이고, X1이 O이고, X2 및 X3이 N이고;
A가 비치환된 페닐 또는 피리딜 기이고;
Z가 -C(=O)NH- 또는 -CH2NH-이고;
n이 1이고;
R2 및 R3이 둘 다 메틸이거나, 또는
R2가 히드록실이고, R3이 메틸이거나, 또는
R2 및 R3이 둘 다 수소이거나, 또는
R2가 메틸이고, R3이 수소이거나, 또는
R2가 히드록실이고, R3이 수소이거나, 또는
R2가 디메틸아미노이고, R3이 H이거나, 또는
R2가 N,N-디메틸아미노에틸이고, R3이 H이거나, 또는
R2 및 R3이 이들이 연결되어 있는 원자와 함께, 테트라히드로피라닐, 2,2-디메틸-테트라히드로피라닐 또는 1-메틸-피페리디닐 기를 형성하고;
L이 티아졸릴, 티에닐, 트리아졸릴, 피리딜, 페닐 또는 옥사졸릴이고, 이 중 임의의 것이 메틸 기에 의해 임의로 치환되고;
R4가 할로 (클로로 또는 플루오로), 시아노, 할로(C1-C2)알킬 또는 (C1-C2)알콕시에 의해 임의로 치환된 페닐인
화학식 I에 따른 화합물 또는 그의 염, 특히 제약상 허용되는 염에 관한 것이다.
본원에 사용된 바와 같이, 용어 "본 발명의 화합물(들)"은 임의의 형태, 즉 그의 임의의 염 또는 비-염 형태 (예를 들어, 유리 산 또는 염기 형태로서, 또는 그의 제약상 허용되는 염으로서) 및 임의의 물리적 형태 (예를 들어, 비-고체 형태 (예를 들어, 액체 또는 반-고체 형태) 및 고체 형태 (예를 들어, 무정형 또는 결정질 형태, 특정 다형체 형태, 용매화물, 예컨대 수화물 (예를 들어, 1수화물, 2수화물 및 반수화물) 포함) 및 다양한 형태의 혼합물인 화학식 I의 화합물 (상기 정의된 바와 같음)을 의미한다.
본원에 사용된 바와 같이, 용어 "임의로 치환된"은 비치환된 기 또는 고리 (예를 들어, 시클로알킬, 헤테로사이클 및 헤테로아릴 고리) 및 1개 이상의 명시된 치환기로 치환된 기 또는 고리를 의미한다.
화학식 I에 따른 화합물은 하나 이상의 비대칭 중심 (키랄 중심으로 또한 지칭됨)을 함유할 수 있고, 이에 따라 개별 거울상이성질체, 부분입체이성질체 또는 다른 입체이성질체 형태, 또는 그의 혼합물로 존재할 수 있다. 키랄 중심, 예컨대 키랄 탄소 원자는 또한 알킬 기와 같은 치환기에 존재할 수 있다. 화학식 I, 또는 본원에 예시한 임의의 화학 구조에 존재하는 키랄 중심의 입체화학이 명시되지 않는 경우, 구조는 모든 개별 입체이성질체 및 그의 모든 혼합물을 포함하는 것으로 의도된다. 따라서, 하나 이상의 키랄 중심을 함유하는 화학식 I에 따른 화합물은 라세미체 혼합물, 비라세미 혼합물로서, 또는 부분입체이성질체적으로 또는 거울상이성질체적으로 순수한 물질로서 사용될 수 있다.
하나 이상의 비대칭 중심을 함유하는 화학식 I에 따른 화합물의 개별 입체이성질체는 당업자에게 공지된 방법에 의해 분할할 수 있다. 예를 들어, 이러한 분할은 (1) 부분입체이성질체 염, 착물 또는 다른 유도체의 형성; (2) 입체이성질체-특이적 시약과의 선택적인 반응, 예를 들어 효소적 산화 또는 환원; 또는 (3) 키랄 환경, 예를 들어 키랄 지지체, 예컨대 결합 키랄 리간드를 갖는 실리카 상에서 또는 키랄 용매의 존재 하에 기체-액체 또는 액체 크로마토그래피에 의해 수행될 수 있다. 당업자는 원하는 입체이성질체가 상기 기재된 분리 절차 중 하나에 의해 또 다른 화학 물질로 전환되고, 원하는 형태를 유리시키기 위해 추가의 단계가 필요함을 인지할 것이다. 대안적으로, 특정한 입체이성질체는 광학 활성 시약, 기질, 촉매 또는 용매를 사용하는 비대칭 합성에 의해, 또는 하나의 거울상이성질체를 비대칭 변환에 의해 다른 것으로 전환시킴으로써 합성할 수 있다.
개시된 화합물 또는 그의 염이 구조에 의해 명명되거나 도시되는 경우, 화합물 또는 염 (용매화물 (특히, 수화물) 포함)이 결정질 형태, 비-결정질 형태 또는 그의 혼합물로 존재할 수 있음을 이해해야 한다. 화합물 또는 염 또는 그의 용매화물 (특히, 수화물)은 또한 다형성 (즉, 다양한 결정질 형태로 존재하는 능력)을 나타낼 수 있다. 이러한 다양한 결정질 형태는 전형적으로 "다형체"로 공지되어 있다. 구조에 의해 명명되거나 도시되는 경우, 개시된 화합물 또는 그의 용매화물 (특히, 수화물)은 또한 그의 모든 다형체를 포함한다는 것을 이해해야 한다. 다형체는 동일한 화학적 조성을 갖지만, 패킹, 기하학적 배열 및 결정질 고체 상태의 다른 설명적 특성이 상이하다. 따라서, 다형체는 상이한 물리적 특성, 예컨대 형상, 밀도, 경도, 변형가능성, 안정성 및 용해 특성을 가질 수 있다. 다형체는 전형적으로, 식별에 사용될 수 있는 상이한 융점, IR 스펙트럼 및 X-선 분말 회절 패턴을 나타낸다. 당업자는, 예를 들어 화합물을 결정화/재결정화하는데 사용되는 조건을 변화시키거나 조정함으로써 다양한 다형체를 제조할 수 있음을 인식할 것이다.
의약에서의 그의 잠재적인 용도로 인해, 화학식 I의 화합물의 염은 바람직하게는 제약상 허용되는 염이다. 적합한 제약상 허용되는 염은 문헌 [Berge, Bighley and Monkhouse, J.Pharm.Sci (1977) 66, pp 1-19]에 의해 기재된 것을 포함한다. 용어 "제약상 허용되는 염" 내에 포함되는 염은 본 발명의 화합물의 비독성 염을 지칭한다.
전형적으로, 염은 적절한 경우에 바람직한 산 또는 염기를 사용하여 용이하게 제조할 수 있다. 염은 용액으로부터 침전시켜 여과에 의해 수집할 수 있거나, 또는 용매의 증발에 의해 회수할 수 있다.
본 발명의 화합물이 염기인 (염기성 모이어티를 함유하는) 경우에, 바람직한 염 형태는 당업계에 공지된 임의의 적합한 방법에 의해, 예컨대 유리 염기를 무기 산, 예컨대 염산, 브로민화수소산, 황산, 질산, 인산, 등으로, 또는 유기 산, 예컨대 아세트산, 트리플루오로아세트산, 말레산, 숙신산, 만델산, 푸마르산, 말론산, 피루브산, 옥살산, 글리콜산, 살리실산, 등으로, 또는 피라노시딜산, 예컨대 글루쿠론산 또는 갈락투론산으로, 또는 알파-히드록시 산, 예컨대 시트르산 또는 타르타르산으로, 또는 아미노산, 예컨대 아스파르트산 또는 글루탐산으로, 또는 방향족 산, 예컨대 벤조산 또는 신남산으로, 또는 술폰산, 예컨대 p-톨루엔술폰산, 메탄술폰산, 에탄술폰산 등으로 처리함으로써 제조할 수 있다.
적합한 부가염은 비-독성 염을 형성하는 산으로부터 형성되며, 예는 아세테이트, p-아미노벤조에이트, 아스코르베이트, 아스파르테이트, 벤젠술포네이트, 벤조에이트, 비카르보네이트, 비스메틸렌살리실레이트, 비술페이트, 비타르트레이트, 보레이트, 칼슘 에데테이트, 캄실레이트, 카르보네이트, 클라불라네이트, 시트레이트, 시클로헥실술파메이트, 에데테이트, 에디실레이트, 에스톨레이트, 에실레이트, 에탄디술포네이트, 에탄술포네이트, 포르메이트, 푸마레이트, 글루셉테이트, 글루코네이트, 글루타메이트, 글리콜레이트, 글리콜릴아르사닐레이트, 헥실레소르시네이트, 히드라바민, 히드로브로마이드, 히드로클로라이드, 디히드로클로라이드, 히드로푸마레이트, 히드로겐 포스페이트, 히드로아이오다이드, 히드로말레에이트, 히드로숙시네이트, 히드록시나프토에이트, 이세티오네이트, 이타코네이트, 락테이트, 락토비오네이트, 라우레이트, 말레이트, 말레에이트, 만델레이트, 메실레이트, 메틸브로마이드, 메틸니트레이트, 메틸술페이트, 모노포타슘 말레에이트, 뮤케이트, 납실레이트, 니트레이트, N-메틸글루카민, 옥살레이트, 옥살로아세테이트, 파모에이트 (엠보네이트), 팔메이트, 팔미테이트, 판토테네이트, 포스페이트/디포스페이트, 피루베이트, 폴리갈락투로네이트, 프로피오네이트, 사카레이트, 살리실레이트, 스테아레이트, 서브아세테이트, 숙시네이트, 술페이트, 탄네이트, 타르트레이트, 테오클레이트, 토실레이트, 트리에티오다이드, 트리플루오로아세테이트 및 발레레이트를 포함한다.
다른 예시적 산 부가염은 피로술페이트, 술파이트, 비술파이트, 데카노에이트, 카프릴레이트, 아크릴레이트, 이소부티레이트, 카프로에이트, 헵타노에이트, 프로피올레이트, 옥살레이트, 말로네이트, 수베레이트, 세바케이트, 부틴-1,4-디오에이트, 헥신-1,6-디오에이트, 클로로벤조에이트, 메틸벤조에이트, 디니트로벤조에이트, 히드록시벤조에이트, 메톡시벤조에이트, 프탈레이트, 페닐아세테이트, 페닐프로피오네이트, 페닐부트레이트, 락테이트, γ-히드록시부티레이트, 만델레이트 및 술포네이트, 예컨대 크실렌술포네이트, 프로판술포네이트, 나프탈렌-1-술포네이트 및 나프탈렌-2-술포네이트를 포함한다.
본 발명의 염기성 화합물이 염으로서 단리되는 경우, 상기 화합물의 상응하는 유리 염기 형태는 당업계에 공지된 임의의 적합한 방법, 예컨대 염을 무기 또는 유기 염기, 적합하게는 화합물의 유리 염기 형태보다 높은 pKa를 갖는 무기 또는 유기 염기로 처리함으로써 제조할 수 있다.
본 발명의 화합물이 산인 (산성 모이어티를 함유하는) 경우, 바람직한 염은 당업계에 공지된 임의의 적합한 방법에 의해, 예컨대 유리 산을 무기 또는 유기 염기, 예컨대 아민 (1급, 2급 또는 3급), 알칼리 금속 또는 알칼리 토금속 수산화물 등으로 처리함으로써 제조할 수 있다. 적합한 염의 예시적 예는 아미노산, 예컨대 글리신 및 아르기닌, 암모니아, 1급, 2급, 3급 아민 및 시클릭 아민, 예컨대 N-메틸-D-글루카민, 디에틸아민, 이소프로필아민, 트리메틸아민, 에틸렌 디아민, 디시클로헥실아민, 에탄올아민, 피페리딘, 모르폴린 및 피페라진으로부터 유도된 유기 염, 뿐만 아니라 나트륨, 칼슘, 칼륨, 마그네슘, 망가니즈, 철, 구리, 아연, 알루미늄 및 리튬으로부터 유도된 무기 염을 포함한다.
본 발명의 특정 화합물은 1당량 이상의 산 (화합물이 염기성 모이어티를 함유하는 경우) 또는 염기 (화합물이 산성 모이어티를 함유하는 경우)와의 염을 형성할 수 있다. 본 발명은 그의 범주 내에 모든 가능한 화학량론적 및 비-화학량론적 염 형태를 포함한다.
염기성 및 산성 모이어티 둘 다를 갖는 본 발명의 화합물은 쯔비터이온, 염기성 모이어티의 산 부가염 또는 산성 모이어티의 염기 염의 형태일 수 있다.
본 발명은 또한 본 발명의 화합물의 하나의 제약상 허용되는 염, 예를 들어 히드로클로라이드 염의, 본 발명의 화합물의 또 다른 제약상 허용되는 염, 예를 들어 나트륨 염으로의 전환을 제공한다.
결정질 형태의 화학식 I의 화합물 또는 그의 염의 용매화물에 있어서, 당업자는 용매 분자가 결정화 동안 결정질 격자에 혼입되어 제약상 허용되는 용매화물이 형성될 수 있음을 인지할 것이다. 용매화물은 비-수성 용매, 예컨대 에탄올, 이소프로판올, DMSO, 아세트산, 에탄올아민 및 에틸 아세테이트를 포함할 수 있거나, 또는 이들은 결정질 격자에 혼입된 용매로서 물을 포함할 수 있다. 결정질 격자에 혼입되는 용매가 물인 용매화물은 전형적으로 "수화물"로 지칭된다. 수화물은 가변량의 물을 함유하는 화학량론적 수화물 뿐만 아니라 조성물을 포함한다. 본 발명은 이러한 모든 용매화물을 포함한다.
본 발명은 또한 1개 이상의 원자가 자연에서 가장 흔하게 발견되는 원자 질량 또는 질량수와 상이한 원자 질량 또는 질량수를 갖는 원자로 대체된다는 점을 제외하고는 화학식 I에서 언급한 것과 동일한, 동위원소-표지 화합물을 포함한다. 본 발명의 화합물에 혼입될 수 있는 동위원소의 예는 수소, 탄소, 질소, 산소, 플루오린, 아이오딘 및 염소의 동위원소, 예컨대 3H, 11C, 14C, 18F, 123I 또는 125I를 포함한다.
상기 언급된 동위원소 및/또는 다른 원자의 동위원소를 함유하는 본 발명의 화합물 및 상기 화합물의 제약상 허용되는 염은 본 발명의 범주 내에 있다. 본 발명의 동위원소 표지 화합물, 예를 들어 방사성 동위원소, 예컨대 3H 또는 14C가 혼입된 화합물은 약물 및/또는 기질 조직 분포 검정에 유용하다. 삼중수소, 즉 3H, 및 탄소-14, 즉 14C 동위원소가 그의 제조 용이성 및 검출감도로 인해 특히 바람직하다. 11C 및 18F 동위원소가 PET (양전자 방출 단층촬영)에 특히 유용하다.
화학식 I의 화합물이 제약 조성물로 사용하기 위한 의도를 갖기 때문에, 이들 각각이 실질적으로 순수한 형태, 예를 들어 60% 이상 순수한 형태, 보다 적합하게는 75% 이상 순수한 형태, 바람직하게는 85% 이상 순수한 형태, 특히 98% 이상 순수한 형태로 제공되는 것이 바람직하다는 것을 쉽게 이해할 것이다 (%는 중량 대 중량 기준임). 화합물의 불순한 제조물이 제약 조성물에 사용되는 보다 순수한 형태를 제조하기 위해 사용될 수 있다.
화학식 I의 화합물은 하기 반응식에 예시된 합성 절차를 사용함으로써 또는 유기 화학 당업자의 지식에서 도출함으로써 수득할 수 있다. 이들 반응식에 제공된 합성은, 필요한 경우 적합하게 보호된 적절한 전구체를 사용하여 본원에 개략화된 반응과의 상용성을 달성하여 다양한 R1 및 R2 기를 갖는 본 발명의 화합물의 제조에 적용할 수 있다. 필요한 경우 후속적 탈보호는 일반적으로 개시된 특성의 화합물을 제공한다. 반응식이 단지 화학식 I의 화합물을 나타내지만, 이들은 본 발명의 화합물을 제조하는데 사용될 수 있는 방법을 예시한다.
중간체 (본 발명의 화합물의 제조에 사용된 화합물)는 또한 염으로서 존재할 수 있다. 따라서, 중간체에 관련하여, 어구 "화학식 (번호)의 화합물(들)"은 그 구조 화학식을 갖는 화합물 또는 그의 제약상 허용되는 염을 의미한다.
본 발명의 구체적인 화합물은 실시예 1 내지 141의 화합물을 포함한다.
대표적인 본 발명의 화합물은 다음을 포함한다:
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(4-(2-(디메틸아미노)에톡시)벤질)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(디메틸아미노)에톡시)벤질)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(4-(1H-이미다졸-1-일)벤질)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-시아노에틸)-N-(피리딘-3-일메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)-N-((4-(4-(트리플루오로메틸)페닐)테트라히드로-2H-피란-4-일)메틸)벤즈아미드,
1-(4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤질)메탄아민,
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-((4-(4-페닐티오펜-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((1-(4-페닐티아졸-2-일)시클로펜틸)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(3-페닐-1H-1,2,4-트리아졸-5-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(2-페닐티아졸-4-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-(4-메톡시페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-(4-클로로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-메틸-2-(4-페닐티아졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((1-메틸-4-(4-페닐티아졸-2-일)피페리딘-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-(4-플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(5-메틸-4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-시클로헥실티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-(피리딘-2-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-(피리딘-4-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)티오펜-2-카르복스아미드,
N-((4-(4-(티오펜-2-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
3-플루오로-N-(2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
3-시아노-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
3-메톡시-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(4-(4-플루오로페닐)티아졸-2-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-(4-시아노페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-(4-플루오로페닐)티아졸-2-일)-2,2-디메틸테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤젠술폰아미드,
3-에틸-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(3-브로모페닐)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)-N-((4-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤즈아미드,
N-(2-메틸-2-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)시클로프로판카르복스아미드,
N-((1-메틸-4-(2-페닐티아졸-4-일)피페리딘-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(2-(4-클로로페닐)티아졸-4-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-((4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(2-(4-클로로페닐)티아졸-4-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-클로로페닐)티아졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)이소니코틴아미드,
N-(2-(2-(4-플루오로페닐)티아졸-4-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)티아졸-4-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-6-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)피콜린아미드,
N-(2-(디메틸아미노)-2-(4-페닐티아졸-2-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(3-페닐-1H-1,2,4-트리아졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((1-(4-페닐티아졸-2-일)시클로프로필)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
3-(4-(4-플루오로페닐)티아졸-2-일)-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)페닐)프로판아미드,
N-(2-(2-(4-클로로페닐)티아졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-페닐티아졸-2-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(4-(4-플루오로페닐)티아졸-2-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(4-(4-클로로페닐)티아졸-2-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(4-(4-클로로페닐)티아졸-2-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-((4-(3,4-디히드로이소퀴놀린-2(1H)-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-메틸-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)티아졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(2-(4-플루오로페닐)티아졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
2,2,2-트리플루오로-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-1-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)페닐)에탄아민,
N-(2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-메틸-2-(3-페닐-1H-1,2,4-트리아졸-5-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-메틸-2-(3-페닐-1H-1,2,4-트리아졸-5-일)프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-6-메틸-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(3-(4-페닐티아졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(5-페닐티아졸-2-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(3-플루오로페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-2-메틸-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-메틸-2-(5-페닐티아졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-([1,1'-비페닐]-3-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-([1,1'-비페닐]-3-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-((2-(4-플루오로페닐)옥사졸-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(2-(4-플루오로페닐)옥사졸-4-일)-1-메틸피페리딘-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-메틸-2-(2-페닐옥사졸-4-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤질)프로판-1-아민,
3-(3-(4-(4-페닐티아졸-2-일)부틸)페닐)-5-(트리플루오로메틸)-1,2,4-옥사디아졸,
N-(2-메틸-2-(5-페닐옥사졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-페닐티아졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-메틸-2-(2-페닐티아졸-5-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-5-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)니코틴아미드,
N-((4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-일)메틸)-3-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤즈아미드,
2-플루오로-N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)옥사졸-4-카르복스아미드,
N-(2-(1-메틸-2-페닐-1H-이미다졸-5-일)프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
5-(5-(디플루오로메틸)-1,2,4-옥사디아졸-3-일)-N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)니코틴아미드,
N-(2-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드 히드로클로라이드,
N-(2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로필)-5-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)니코틴아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-2-메톡시-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-5-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(4-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)부틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(4-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)부틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-((4-(2-(4-클로로페닐)옥사졸-4-일)-1-메틸피페리딘-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤질)프로판-1-아민,
N-(2-(2-(4-플루오로페닐)옥사졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-([1,1'-비페닐]-3-일)-1-메틸피페리딘-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-메톡시페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
2-클로로-N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(3-(2-(4-플루오로페닐)옥사졸-4-일)-3-히드록시프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-시아노페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(2-(2-플루오로페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
3-(5-(2,2-디플루오로아세틸)티오펜-2-일)-N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(2,2,2-트리플루오로아세틸)티아졸-2-일)벤즈아미드,
N-(2-(1-메틸-2-페닐-1H-이미다졸-4-일)프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(2,2,2-트리플루오로아세틸)푸란-2-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메톡시에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(4-(4-플루오로페닐)티아졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-([1,1'-비페닐]-3-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(4'-플루오로-[1,1'-비페닐]-3-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-((4-(4-(3,5-디플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(4-(3,5-디플루오로페닐)티아졸-2-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-페닐옥사졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-페닐옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(2-(4-클로로페닐)옥사졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-클로로페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-메틸-2-(2-페닐옥사졸-4-일)프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(3-페닐-1,2,4-옥사디아졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-메틸-2-(3-페닐-1H-피라졸-5-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-((4-([1,1'-비페닐]-3-일)-1-메틸피페리딘-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(4-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(2,2,2-트리플루오로아세틸)푸란-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(2,2,2-트리플루오로아세틸)티오펜-3-일)벤즈아미드,
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(2,2,2-트리플루오로아세틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
및 그의 염, 특히 제약상 허용되는 염.
본 발명의 특정한 화합물은 다음을 포함한다:
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-메틸-2-(2-페닐옥사졸-4-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로필)-5-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)니코틴아미드,
N-(4-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)부틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(2,2,2-트리플루오로아세틸)티아졸-2-일)벤즈아미드,
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드,
(3-(5-(4-플루오로페닐)옥사졸-2-일)피페리딘-1-일)(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)페닐)메타논,
및 그의 염, 특히 제약상 허용되는 염.
화합물 명칭은 캠브리지소프트 코포레이션(CambridgeSoft Corporation., 미국 02140 매사추세츠주 캠브리지 캠브리지파크 드라이브 100 (http://www.cambridgesoft.com))으로부터 입수가능한 프로그램 켐드로우(ChemDraw) 11.0이라는 소프트웨어를 사용하여 생성하였다.
화학식 I의 화합물은 아래 개략화된 방법에 따라 제조할 수 있다.
본 발명은 또한 화학식 I의 화합물의 다양한 중수소화 형태를 포함한다. 탄소 원자에 부착된 각각의 이용가능한 수소 원자는 독립적으로 중수소 원자로 대체될 수 있다. 당업자는 화학식 I의 화합물의 중수소화 형태를 합성하는 방법을 알 것이다. 예를 들어, 중수소화 알킬 기 (예를 들어, N-(듀테로-메틸)아민)를 통상의 기술에 의해 제조할 수 있다 (예를 들어, 알드리치 케미칼 캄파니(Aldrich Chemical Co., 위스콘신주 밀워키)로부터 입수가능한 메틸-d3-아민, 카탈로그 번호 489,689-2 참조). 이러한 화합물을 사용함으로써, N-메틸 기의 다양한 수소 원자가 중수소 원자로 대체된 화학식 I의 화합물을 제조할 수 있을 것이다.
본 발명은 아세틸라제를 화학식 I의 화합물 또는 그의 염, 특히 그의 제약상 허용되는 염과 접촉시키는 것을 포함하는 HDAC의 억제 방법에 관한 것이다. 본 발명은 또한 HDAC-매개 질환 또는 장애의 치료가 필요한 환자, 구체적으로 인간에게 치료 유효량의 화학식 I의 화합물 또는 그의 염, 특히 그의 제약상 허용되는 염을 투여하는 것을 포함하는, HDAC-매개 질환 또는 장애의 치료 방법에 관한 것이다. 본원에 사용된 바와 같이, "환자"는 포유동물, 구체적으로 인간을 지칭한다. 치료 "유효량"은 상기 치료가 필요한 환자에게 투여시, 본원에 정의된 바와 같은 치료를 달성하기에 충분한 화합물의 양을 의미하는 것으로 의도된다. 따라서, 예를 들어, 치료 유효량의 화학식 I의 화합물 또는 그의 제약상 허용되는 염은 이들이 필요한 인간에게 투여시, HDAC의 활성에 의해 매개되는 질환 상태가 감소, 완화 또는 예방되도록 HDAC의 활성을 억제하기에 충분한 본 발명의 작용제의 양이다. 이러한 양에 상응하는 주어진 화합물의 양은 특정한 화합물 (예를 들어, 특정한 화합물의 효력 (pXC50), 효능 (EC50) 및 생물학적 반감기), 질환 상태 및 그의 중증도, 치료를 필요로 하는 환자의 정체 (예를 들어, 연령, 사이즈 및 체중)와 같은 요인에 따라 달라질 것이나, 그럼에도 불구하고 당업자에 의해 통상적으로 결정될 수 있다. 마찬가지로, 치료의 지속시간 및 화합물의 투여 기간 (투여 사이의 기간 및 투여 시기, 예를 들어 식전/식간/식후)은 치료가 필요한 포유동물의 정체 (예를 들어, 체중), 특정한 화합물 및 그의 특성 (예를 들어, 제약적 특성), 질환 또는 상태 및 그의 중증도 및 특정한 조성물 및 사용 방법에 따라 달라질 것이나, 그럼에도 불구하고 당업자에 의해 결정될 수 있다.
"치료하는" 또는 "치료"는 환자에서 HDAC에 의해 유발되거나 매개되는 질환 상태를 적어도 완화시키는 것을 의미하도록 의도된다. 질환 상태의 완화를 위한 치료 방법은 본 발명의 화합물을 임의의 통상적으로 허용되는 방식으로, 예를 들어 질환의 예방, 지연, 방지, 치료 또는 치유를 위해 사용하는 것을 포함한다.
한 실시양태에서, 본 발명은, 환자에게 본 발명의 화합물을, 환자에서 Treg 세포의 수준 및/또는 활성 또는 Treg 세포의 수를 증가시켜, 그로 인해 환자에서 자가면역 장애, 염증성 장애, 이식/이식편 거부, 림프구감소증 또는 이식편-대-숙주 질환 (GvHD)을 치료, 개선 또는 예방하기에 충분한 양으로 투여하는 것을 포함하는, 환자, 특히 인간에서 자가면역 장애, 면역 질환, 염증성 장애, 이식/이식편 거부 (예를 들어, 동종이식편), 림프구감소증 또는 이식편-대-숙주 질환 (GvHD)을 치료, 개선 또는 예방하는 방법에 관한 것이다.
본 발명의 화합물로 치료할 수 있는 질환 및 상태의 추가의 예는 제II형 당뇨병, 관상 동맥 질환, 알레르기 및 알레르기 반응 및 패혈증/독성 쇼크를 포함하나, 이에 제한되는 것은 아니다.
예시적 자가면역 장애는 다발성 경화증, 소아 특발성 관절염, 건선성 관절염, C형 간염 바이러스-연관 혼합형 한랭글로불린혈증, 다발근염, 피부근염, 제II형 다선성 증후군, 자가면역 간 질환, 가와사키병, 중증 근무력증, 면역조절이상 다발성내분비병증 장병증 X-연관 증후군 (IPEX (증후군)), 제I형 당뇨병, 건선, 갑상선기능저하증, 용혈성 빈혈, 자가면역 다발성내분비병증-칸디다증-외배엽 이영양증 (APECED), 혈소판감소증, 척추관절염, 쇼그렌 증후군, 류마티스 관절염, 염증성 장 질환 (IBD), 크론병, 궤양성 결장염, 습진, 위염 또는 갑상선염을 포함하나, 이에 제한되는 것은 아니다. 비제한적 목록의 일부로, 염증성 장애는 접촉성 과민증, 아토피성 피부염 또는 스틸병일 수 있다.
자가면역 질환의 추가의 예는 골관절염, 전신 경화증, 사르코이드증, 인슐린 의존성 당뇨병 (IDDM, 제I형 당뇨병), 반응성 관절염, 경피증, 혈관염, 베게너 육아종증, 하시모토병, 경피증, 난소염, 루푸스 (SLE), 그레이브스병, 천식, 한랭글로불린혈증, 원발성 담즙성 경화증, 심상성 천포창, 용혈성 빈혈 및 악성 빈혈을 포함한 자가면역 질환을 포함하나, 이에 제한되는 것은 아니다.
이식/이식편 거부 (예를 들어, 동종이식편), 림프구감소증 또는 이식편-대-숙주 질환 (GvHD)의 예는 세포, 조직 및 기관 이식 절차, 예컨대 치료 세포 이식, 예컨대 줄기 세포, 근육 세포, 예컨대 심장 세포, 도세포, 간 세포, 골수 이식, 피부 이식편, 골 이식, 폐 이식, 신장 이식, 간 이식 및 심장 이식으로부터 발생하는 것이다.
본 발명의 화합물로 치료될 수 있는 질환 및 상태의 다른 예는 낭성 섬유증, 골다공증, 비만, 간질, 우울증, 지중해빈혈, 겸상 적혈구성 빈혈, 근위축성 측삭 경화증 (ALS) 및 통각과민, 심장 질환 (예를 들어, 졸중, 고혈압, 아테롬성혈전성 질환, 아테롬성동맥경화증, 또는 급성 관상동맥 증후군에서의 경색 크기의 제한), 근육 위축, 겐타미신-유발 청력 상실, 약물 내성 (예를 들어, 골육종 및 결장암 세포에서의 약물 내성), 감염성 질환 및 면역 결핍/면역손상 환자와 관련된 질환 또는 장애를 포함하나, 이에 제한되는 것은 아니다. 감염성 질환의 예는 다양한 병원체 감염, 예컨대 바이러스, 진균, 박테리아, 미코플라즘, 및 단세포 및 다세포 진핵 유기체에 의한 감염과 관련된다. 통상적인 인간 병원체는 HIV, HSV, HPV, 간염 A, B 및 C 바이러스, 인플루엔자, 뎅기, 조스트렐라, 풍진, RSV, 로타바이러스, 그람 양성, 그람 음성, 스트렙토코쿠스, 파상풍, 스타필코쿠스, 결핵, 리스테리아 및 말라리아를 포함하나, 이에 제한되는 것은 아니다.
또 다른 실시양태에서, 본 발명은 HDAC의 억제제, 및 신생물성 세포, 예를 들어, 암 세포 및 종양 세포의 성장을 중지시키거나 감소시키기 위한 그의 용도에 관한 것이다.
하기 암 유형에서 발견되는 암 세포 및/또는 종양 세포의 성장은 본 발명의 화합물을 사용한 치료에 의해 감소될 수 있다: 암종 (예를 들어, 선암종), 간세포 암종, 육종, 골수종 (예를 들어, 다발성 골수종), 다발성 골수종, 백혈병, 소아 급성 림프모구성 백혈병 및 림프종 (예를 들어, 피부 세포 림프종)에서의 골 질환의 치료, 및 혼합된 유형의 암, 예컨대 선편평세포 암종, 혼합형 중배엽 종양, 암육종 및 기형암종.
본 발명의 한 측면에서, 유방 또는 전립선암 또는 종양은 본 발명의 HDAC 억제제를 사용하여 치료된다.
본 발명의 화합물을 사용하여 치리될 수 있는 다른 암은 방광암, 유방암, 전립선암, 위암, 폐암, 결장암, 직장암, 결장직장암, 간암, 자궁내막암, 췌장암, 자궁경부암, 난소암; 두경부암 및 흑색종을 포함하나, 이에 제한되는 것은 아니다.
본 발명의 억제제는 단독으로 또는 신생물성 세포, 예를 들어, 종양 및 암을 위한 표준 항암 요법, 치료와 함께 사용될 수 있다.
본 발명의 화합물은 전신 투여 및 국소 투여 둘 다를 포함한 임의의 적합한 투여 경로에 의해 투여될 수 있다. 전신 투여는 경구 투여, 비경구 투여, 경피 투여, 직장 투여 및 흡입 투여를 포함한다. 비경구 투여는 경장, 경피 또는 흡입 이외의 투여 경로를 지칭하며, 전형적으로 주사 또는 주입에 의한 투여이다. 비경구 투여는 정맥내, 근육내 및 피하 주사 또는 주입을 포함한다. 흡입은 구강을 통해 흡입되는지 비도를 통해 흡입되는지 여부에 관계없이 환자의 폐로 투여하는 것을 지칭한다. 국소 투여는 피부에 대한 도포를 포함한다.
본 발명의 화합물은 1회 투여될 수 있거나 또는 주어진 기간 동안 다수의 용량이 다양한 시간 간격으로 투여되는 투여 요법에 따라 투여될 수 있다. 예를 들어, 용량은 1일 1, 2, 3 또는 4회 투여될 수 있다. 용량은 원하는 치료 효과가 달성되거나 또는 원하는 치료 효과가 무기한 유지될 때까지 투여될 수 있다. 본 발명의 화합물에 적합한 투여 요법은 상기 화합물의 약동학적 특성, 예컨대 흡수, 분포 및 반감기에 따라 달라지며, 이는 당업자에 의해 결정될 수 있다. 또한, 본 발명의 화합물에 대한 적합한 투여 요법 (상기 요법이 투여되는 기간을 포함)은 치료되는 상태, 치료되는 상태의 중증도, 치료되는 환자의 연령 및 신체 상태, 치료되는 환자의 병력, 병용 요법의 특성, 원하는 치료 효과 및 당업자의 지식 및 숙련도 내의 유사 인자에 따라 달라진다. 또한, 당업자는 적합한 투여 요법이 투여 요법에 대한 개별 환자의 반응이 주어지도록 조정되거나 또는 시간이 지나 개별 환자 요구가 변화함에 따라 조정을 필요로 할 수 있음을 이해할 것이다.
HDAC-매개 질환 상태의 치료는 본 발명의 화합물을 단독요법으로서, 또는 이중 또는 다중 조합 요법으로, 예컨대 기타 작용제와 함께, 예를 들어 하기 작용제: DNA 메틸트랜스퍼라제 억제제, 아세틸 트랜스퍼라제 인핸서, 프로테아솜 또는 HSP90 억제제 및 T 억제자 세포를 활성화시키지 않는 하나 이상의 면역억제제, 예컨대 비제한적으로 코르티코스테로이드, 라파마이신, 아자티오프린, 미코페놀레이트, 시클로스포린, 메르캅토퓨린 (6-MP), 바실릭시맙, 다클리주맙, 시롤리무스, 타크롤리무스, 무로모납-CD3, 시클로포스파미드 및 메토트렉세이트 중 하나 이상과 함께 사용하여 달성될 수 있으며, 이는 종래 기술에 공지된 바와 같은 유효량으로 투여된다.
본 발명의 화합물은 보통 환자에게 투여하기 전에 제약 조성물로 제제화되지만, 반드시 그런 것은 아니다. 따라서, 또 다른 측면에서, 본 발명은 본 발명의 화합물 및 제약상 허용되는 부형제를 포함하는 제약 조성물에 관한 것이다.
본 발명의 제약 조성물은, 유효량의 본 발명의 화합물을 추출한 다음, 예컨대 분말, 시럽 및 주사용 용액으로 환자에게 제공할 수 있는 벌크 형태로 제조 및 포장될 수 있다. 대안적으로, 본 발명의 제약 조성물은 단위 투여 형태로 제조되고 포장될 수 있다. 경구 적용을 위해, 예를 들어 하나 이상의 정제 또는 캡슐을 투여할 수 있다. 제약 조성물의 용량은 적어도 치료 유효량의 본 발명의 화합물 (즉, 화학식 I의 화합물 또는 그의 염, 특히 제약상 허용되는 염)을 함유한다. 단위 투여 형태로 제조하는 경우, 제약 조성물은 본 발명의 화합물 1 mg 내지 1000 mg을 함유할 수 있다.
본 발명의 제약 조성물은 전형적으로 본 발명의 하나의 화합물을 함유한다. 그러나, 특정 실시양태에서, 본 발명의 제약 조성물은 하나 초과의 본 발명의 화합물을 함유한다. 또한, 본 발명의 제약 조성물은 임의로 하나 이상의 추가의 제약 활성 화합물을 추가로 포함할 수 있다.
본원에 사용된 바와 같이, "제약상 허용되는 부형제"는 제공 형태에 포함되거나 또는 조성물에 적합한 물질, 조성물 또는 비히클을 의미한다. 각각의 부형제는, 환자에게 투여하였을 때 본 발명의 화합물의 효능을 실질적으로 감소시키는 상호작용 및 제약상 허용되지 않는 제약 조성물을 초래하는 상호작용이 일어나지 않도록, 혼합되었을 때 제약 조성물의 다른 성분과 상용성이어야 한다. 또한, 각각의 부형제는 물론 이를 제약상 허용되도록 하기에 충분히 높은 순도의 것이어야 한다.
본 발명의 화합물 및 제약상 허용되는 부형제 또는 부형제들은 전형적으로 환자에게 바람직한 투여 경로로 투여하기에 적합한 투여 형태로 제제화될 것이다. 종래 투여 형태는 (1) 경구 투여를 위해 적합화된 형태, 예컨대 정제, 캡슐, 캐플릿, 환제, 트로키, 분말, 시럽, 엘릭시르, 현탁액, 용액, 에멀젼, 사쉐 및 카쉐; (2) 비경구 투여를 위해 적합화된 형태, 예컨대 멸균 용액, 현탁액 및 재구성용 분말; (3) 경피 투여를 위해 적합화된 형태, 예컨대 경피 패치; (4) 직장 투여를 위해 적합화된 형태, 예컨대 좌제; (5) 흡입을 위해 적합화된 형태, 예컨대 에어로졸 및 용액 및 (6) 국소 투여를 위해 적합화된 형태, 예컨대 크림, 연고, 로션, 용액, 페이스트, 스프레이, 폼 및 겔이 포함된다.
적합한 제약상 허용되는 부형제는 선택된 특정 투여 형태에 따라 달라질 것이다. 또한, 적합한 제약상 허용되는 부형제는 이들이 조성물에 제공할 수 있는 특정 기능에 대해 선택될 수 있다. 예를 들어, 특정 제약상 허용되는 부형제는 균질한 투여 형태의 생성을 용이하게 하는 그의 능력에 대해 선택될 수 있다. 특정 제약상 허용되는 부형제는 안정한 투여 형태의 생성을 용이하게 하는 그의 능력에 대해 선택될 수 있다. 특정 제약상 허용되는 부형제는 환자에게 투여되었을 때 본 발명의 화합물 또는 화합물을 한 기관 또는 신체 일부에서 다른 기관 또는 신체 일부로 운반 또는 수송하는 것을 용이하게 하는 그의 능력에 대해 선택될 수 있다. 특정 제약상 허용되는 부형제는 환자 순응성을 향상시키는 그의 능력에 대해 선택될 수 있다.
적합한 제약상 허용되는 부형제는 하기 유형의 부형제를 포함한다: 희석제, 충전제, 결합제, 붕해제, 윤활제, 활택제, 과립화제, 코팅제, 습윤제, 용매, 공용매, 현탁화제, 유화제, 감미제, 향미제, 향미 차폐제, 착색제, 케이킹방지제, 보습제, 킬레이트화제, 가소제, 점도 증가제, 항산화제, 보존제, 안정화제, 계면활성제 및 완충제. 당업자는 특정 제약상 허용되는 부형제가 한 가지 초과의 기능을 제공할 수 있으며, 제제에 얼마나 많은 부형제가 존재하는지 및 제제에 어떠한 다른 성분이 존재하는지에 따라 다른 기능을 제공할 수 있음을 인지할 것이다.
당업자는 본 발명에서의 용도에 대해 적절한 양으로 적합한 제약상 허용되는 부형제를 선택할 수 있는 당업계의 지식 및 기술을 보유하고 있다. 또한, 제약상 허용되는 부형제가 기재되어 있고, 적합한 제약상 허용되는 부형제를 선택하는데 유용할 수 있는, 당업자에게 이용가능한 다수의 자료가 존재한다. 그 예는 문헌 [Remington's Pharmaceutical Sciences (Mack Publishing Company)], [The Handbook of Pharmaceutical Additives (Gower Publishing Limited)] 및 [The Handbook of Pharmaceutical Excipients (the American Pharmaceutical Association 및 the Pharmaceutical Press)]을 포함한다.
본 발명의 제약 조성물은 당업자에게 공지된 기술 및 방법을 이용하여 제조된다. 당업계에서 통상적으로 사용되는 방법 중 일부가 문헌 [Remington's Pharmaceutical Sciences (Mack Publishing Company)]에 기재되어 있다.
한 측면에서, 본 발명은 유효량의 본 발명의 화합물 및 희석제 또는 충전제를 포함하는, 고체 경구 투여 형태, 예컨대 정제 또는 캡슐에 관한 것이다. 적합한 희석제 및 충전제는 락토스, 수크로스, 덱스트로스, 만니톨, 소르비톨, 전분 (예를 들어, 옥수수 전분, 감자 전분 및 예비젤라틴화 전분), 셀룰로스 및 그의 유도체 (예를 들어, 미세결정질 셀룰로스), 황산칼슘 및 이염기성 황산칼슘을 포함한다. 경구 고체 투여 형태는 결합제를 추가로 포함할 수 있다. 적합한 결합제는 전분 (예를 들어, 옥수수 전분, 감자 전분 및 예비젤라틴화 전분), 젤라틴, 아카시아, 알긴산나트륨, 알긴산, 트라가칸트, 구아 검, 포비돈 및 셀룰로스 및 그의 유도체 (예를 들어, 미세결정질 셀룰로스)를 포함한다. 경구 고체 투여 형태는 붕해제를 추가로 포함할 수 있다. 적합한 붕해제는 크로스포비돈, 나트륨 전분 글리콜레이트, 크로스카르멜로스, 알긴산 및 나트륨 카르복시메틸 셀룰로스를 포함한다. 경구 고체 투여 형태는 윤활제를 추가로 포함할 수 있다. 적합한 윤활제는 스테아르산, 스테아르산마그네슘, 스테아르산칼슘 및 활석을 포함한다.
실시예
하기 실시예는 본 발명을 예시한다. 이들 실시예는 본 발명의 범주를 제한하는 것으로 의도되지 않으며, 오히려 당업자에게 본 발명의 화합물, 조성물 및 방법의 제조 및 사용에 대한 지침을 제공한다. 본 발명의 특정한 실시양태를 기재하였지만, 당업자는 본 발명의 취지 및 범주를 벗어나지 않으면서 다양한 변화 및 변형이 이루어질 수 있음을 인지할 것이다.
하기 실험 설명에서, 하기 약어가 사용될 수 있다:
실시예 1
단계 1: 2-(4-페닐티아졸-2-일)아세토니트릴
EtOH (25 mL) 중 2-브로모아세토페논 (2 g, 10 mmol) 및 2-시아노티오아세트아미드 (1 g, 10 mmol)의 혼합물을 80℃로 4시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 수성 암모니아 용액에 부었다 (최종 pH는 >7이었음). 이어서, 혼합물을 EtOAc로 추출하고, 유기 층을 H2O 및 염수로 세척하였다. 용매를 감압 하에 제거하고, 조 생성물을 플래쉬 칼럼 크로마토그래피 (실리카 겔 230-400 메쉬, 용리액 석유 에테르 중 8% EtOAc)에 의해 정제하여 2-(4-페닐티아졸-2-일)아세토니트릴 (1.5 g, 수율 75%)을 황색 고체로서 수득하였다:
단계 2: 4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
THF (25 mL) 중 2-(4-페닐티아졸-2-일)아세토니트릴 (0.84 g, 4.19 mmol)의 용액을 0℃로 냉각시켰다. NaH (0.5 g, 오일 중 60% 분산액)를 10분에 걸쳐 조금씩 첨가하였다. 생성된 혼합물을 실온으로 가온되도록 하고, 20분 동안 교반하였다. 2-브로모에틸 에테르 (1.58 mL, 12.5 mmol)를 적가하였다. 반응 혼합물을 실온에서 1시간 동안 추가로 교반한 다음, 포화 NH4Cl 용액으로 켄칭하였다. 반응 혼합물을 EtOAc로 희석하고, 유기 층을 H2O 및 염수로 세척하였다. 유기 층을 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 4-8% EtOAc)에 의해 정제하여 4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴 (0.97 g, 수율 85%)을 황색 고체로서 수득하였다:
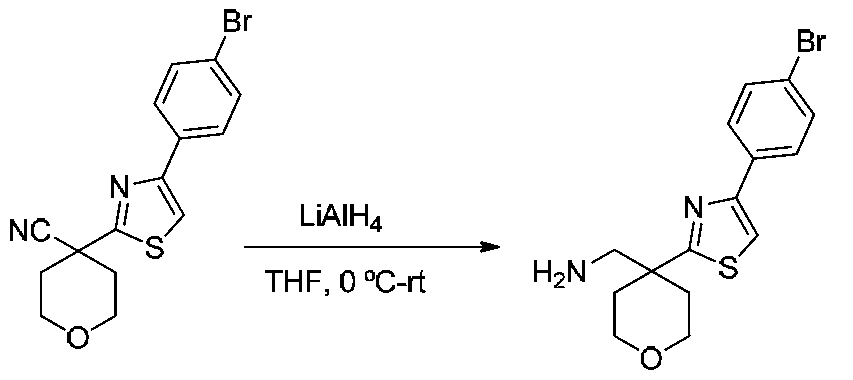
단계 3: (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
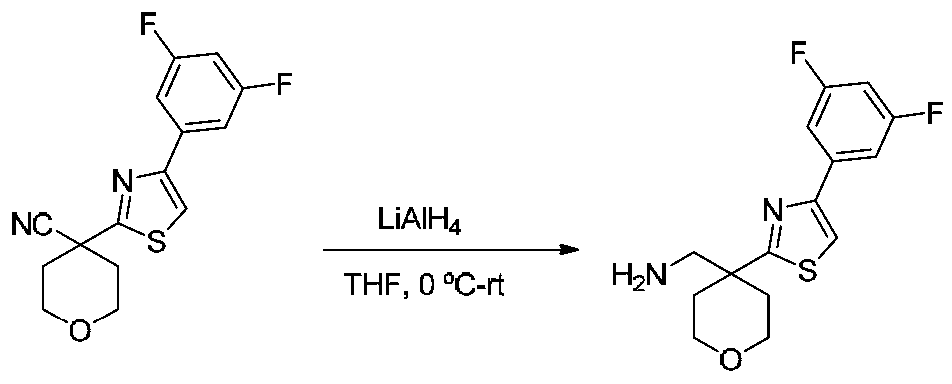
건조 THF (10 mL) 중 LiAlH4 (220 mg, 5.9 mmol)의 현탁액에 0℃에서 건조 THF (10 mL) 중 4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴 (400 mg, 1.47 mmol)의 용액을 첨가하였다. 반응 혼합물을 실온에서 1시간 동안 교반한 다음, 물로 조심스럽게 켄칭하고, EtOAc로 희석하였다. 유기 층을 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 칼럼 크로마토그래피 (중성 알루미나, 용리액 CHCl3 중 5% MeOH)에 의해 정제하여 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 (150 mg, 수율 37%)을 수득하였다:
단계 4: 3-(N'-히드록시카르밤이미도일)벤조산
8-히드록시퀴놀린 (5 mg, 0.03 mmol)을 50 mL 에탄올 중 3-시아노벤조산 (1 g, 6.8 mmol)의 용액에 첨가하였다. 이 반응 혼합물에 먼저 물 (8 mL) 중 히드록실아민 염산 (950 mg, 13.6 mmol)을 첨가하고, 이어서 물 (12 mL) 중 탄산나트륨 (1.2 g, 10.9 mmol)을 첨가하였다. 혼합물을 환류 하에 4시간 동안 가열하였다. 감압 하에 에탄올을 제거한 후, 잔류물을 물로 희석하고, 수용액을 10% HCl을 사용하여 pH ~3으로 산성화시켰다. 백색 침전물을 여과하고, 물 및 아세톤으로 세척한 다음, 감압 하에 건조시켜 화합물 3-(N'-히드록시카르밤이미도일)벤조산 (1 g, 수율 82%)을 수득하였다:
단계 5: 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산
무수 피리딘 (15 mL) 중 화합물 3-(N'-히드록시카르밤이미도일)벤조산 (1 g, 5.6 mmol)의 용액을 0℃로 냉각시키고, 트리플루오로아세트산 무수물 (2.3 mL, 16.7 mmol)을 적가하였다. 반응 혼합물을 실온으로 천천히 가온하고, 추가로 50℃로 3시간 동안 가열하였다. 반응 혼합물을 빙수에 붓고, 1.5N HCl을 첨가하여 pH ~4로 조정하였다. 생성물을 EtOAc로 추출하고, 용매를 감압 하에 제거하였다. 조 생성물을 칼럼 크로마토그래피 [실리카 겔 60-120 메쉬, 용리액: 석유 에테르 중 10% EtOAc]에 의해 정제하여 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산 (400 mg, 수율 28%)을 수득하였다:
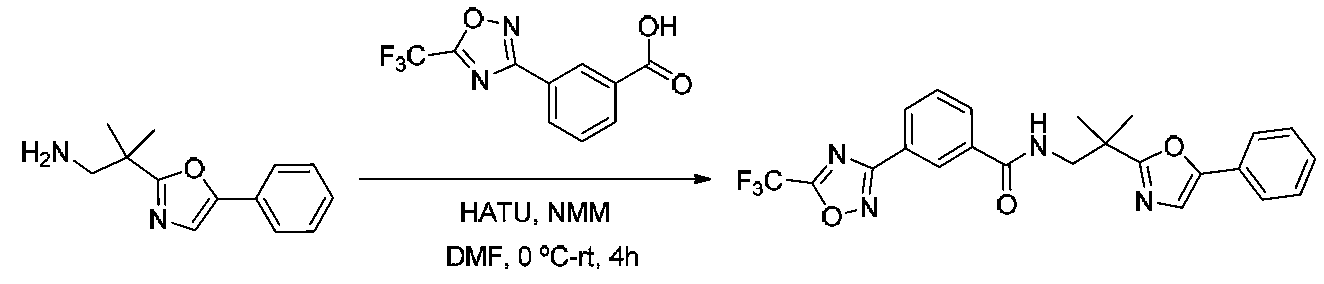
단계 6: N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
CH2Cl2 (2 ml) 중 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산 (52 mg, 0.202 mmol), (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 (50 mg, 0.184 mmol), 및 EDCI (38.5 mg, 0.202 mmol)의 혼합물을 실온에서 8시간 동안 교반하였다. 이어서, 반응 혼합물을 메틸렌 클로라이드 (10 ml)로 희석하고, 물 (5 ml)로 세척하고, MgSO4 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 ISCO (실리카 겔, 용리액: CH2Cl2 중 2% 메탄올)에 의해 정제하여 N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드를 백색 고체 생성물 (59 mg, 62% 수율)로서 수득하였다:
실시예 2-6을 스크리닝 수집의 일부로서 유사한 방식으로 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산 및 용이하게 입수가능한 아민으로부터 합성하고, LCMS 및 1H NMR로 특성화하였다.
실시예 7
(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)페닐)메탄올
보란 디메틸 술피드 착체 (0.3 mL, 2.9 mmol)를 건조 THF (10 mL) 중 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산 (0.5 g, 1.9 mmol)의 교반 용액에 0℃에서 첨가하였다. 반응 혼합물을 실온으로 천천히 가온하고, 추가로 50℃로 4시간 동안 가열하였다. 이어서, 반응 혼합물을 건조 MeOH로 조심스럽게 켄칭하고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 10-15% EtOAc)에 의해 정제하여 순수한 알콜 화합물 (3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)페닐)메탄올 (190 mg, 수율 41%)을 수득하였다:
3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈알데히드
건조 CH2Cl2 (10 mL) 중 화합물 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)페닐)메탄올 (150 mg, 0.6 mmol)의 용액을 아르곤으로 10분 동안 퍼징하고, 데스-마르틴 퍼아이오디난 (0.39g, 0.9 mmol)을 용액에 0℃에서 첨가하였다. 반응 혼합물을 실온이 되도록 하고, 5시간 동안 교반하였다. 이어서, 반응 혼합물을 포화 티오황산나트륨 용액으로 켄칭하고, CH2Cl2로 추출하였다. 유기 층을 염수로 세척하고, 무수 황산나트륨 상에서 건조시켰다. 용매를 감압 하에 농축시켜 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈알데히드 (140 mg, 조물질)를 수득하였으며, 이를 추가 정제 없이 달성하였다.
1-(4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤질)메탄아민
나트륨 트리아세톡시 보로히드라이드 (200 mg, 0.9 mmol)를 건조 디클로로에탄 (20 mL) 중 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈알데히드 (140 mg, 0.6 mmol) 및 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 (170 mg, 0.6 mmol)의 용액에 0℃에서 질소 분위기 하에 첨가하고, 실온에서 8시간 동안 교반하였다. 반응 혼합물을 10% NaHCO3 용액으로 조심스럽게 켄칭하고, EtOAc로 추출하였다. 유기 층을 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 20-25% EtOAc)에 의해 정제하여 1-(4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤질)메탄아민 (65 mg, 수율 22%)을 수득하였다:
실시예 8
메틸-5-브로모니코티네이트
MeOH (200 mL) 중 5-브로모니코틴산 (10 g, 49.5 mmol)의 용액을 0℃로 냉각시키고, 진한 H2SO4 (5 mL)를 적가하였다. 반응 혼합물을 환류 하에 12시간 동안 가열하였다. 완결된 후, 반응 혼합물을 감압 하에 농축시키고, 물로 희석하고, 수성 층을 EtOAc로 세척하였다. 생성된 혼합물을 수성 포화 NaHCO3 용액에 부어 pH 7-8로 조정한 다음, 이것을 EtOAc로 추출하고, 유기 층을 무수 Na2SO4 상에서 건조시켰다. 용매를 감압 하에 증발시켜 고체 생성물 메틸 5-브로모니코티네이트를 회백색 고체 (7 g, 수율 66%)로서 수득하였다:
메틸 5-시아노니코티네이트
CuCN (5.22 g, 58.3 mmol)을 건조 DMF (150 mL) 중 메틸 5-브로모니코티네이트 (6 g, 27.8 mmol)의 용액에 첨가하였다. 용액을 아르곤으로 퍼징하고, 아르곤 분위기 하에 160℃로 12시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시킨 다음, 포화 NH4Cl 용액으로 켄칭하였다. 추가로 EtOAc를 첨가하고, 반응 혼합물을 10분 동안 교반하였다. 반응 혼합물을 셀라이트 플러그를 통해 여과하고, 유기 층을 분리하고, 물 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시켰다. 용매를 감압 하에 증발시켜 메틸-5-시아노-니코티네이트를 녹색빛-백색 고체 (2.7g, 수율 60%)로서 수득하였다:
3-시아노니코틴산
LiOH (150 mg, 6.2 mmol)를 THF-H2O (7:3 v/v, 50 mL) 중 메틸 5-시아노니코티네이트 (1 g, 6.17 mmol)의 용액에 0℃에서 첨가하였다. 반응 혼합물을 실온에서 1시간 동안 교반하였다. 이어서, THF를 감압 하에 제거하고, 반응 혼합물을 물로 희석하고, EtOAc로 세척하였다. 생성된 반응 혼합물을 1.5N HCl을 사용하여 pH 3-4로 산성화시켰다. 혼합물을 EtOAc로 추출하고, 유기 층을 무수 Na2SO4 상에서 건조시켰다. 용매를 감압 하에 증발시켜 3-시아노니코틴산을 회백색 고체 (0.7 g, 수율 78%)로서 수득하였다:
5-(N'-히드록시카르밤이미도일)니코틴산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 5-시아노니코틴산으로부터 합성하였다 (330 mg, 수율 54%):
5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 5-(N'-히드록시카르밤이미도일)니코틴산으로부터 합성하였다 (260 mg, 수율 63%).
단계 6: N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
건조 DMF (5 mL) 중 화합물 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산 (100 mg, 0.4 mmol)의 교반 용액에 0℃에서 HATU (180 mg, 0.46 mmol)에 이어서 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민의 히드로클로라이드 염 (120 mg, 0.4 mmol) 및 NMM (0.12 mL, 1.1 mmol)을 첨가하였다. 반응 혼합물을 실온으로 천천히 가온하고, 추가로 10시간 동안 교반하였다. 반응 혼합물을 EtOAc로 희석하였다. 유기 층을 물 및 염수 용액으로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 50-60% EtOAc)에 의해 정제하여 순수한 생성물 N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드 (70 mg, 수율 37%)를 수득하였다:
실시예 9
5-((4-페닐티오펜-2-일)메틸렌)-2-티옥소티아졸리딘-4-온
빙초산 10 mL 중 4-페닐 티오펜-2-카르복스알데히드 (1 g, 5.3 mmol) 및 로다닌 (700 mg, 5.3 mmol)의 용액을 무수 아세트산나트륨 (1.22 g, 14.8 mmol)을 사용하여 2시간 동안 가열하였다. 이어서, 반응 혼합물을 냉수에 부었다. 침전물을 여과하고, 물로 세척하고, 감압 하에 건조시켜 5-((4-페닐티오펜-2-일)메틸렌)-2-티옥소티아졸리딘-4-온 (1.4 g, 수율 87%)을 수득하였다.
조 생성물을 추가의 정제 없이 달성하였다.
3-(4-페닐티오펜-2-일)-2-티옥소프로판산
10% 수성 NaOH 12 mL 중 생성물 5-((4-페닐티오펜-2-일)메틸렌)-2-티옥소티아졸리딘-4-온 (1.4 g, 4.6 mmol)의 현탁액을 95℃로 1시간 동안 가열하였다. 용액을 실온으로 냉각시키고, 물로 희석하였다. 수성 상을 EtOAc로 세척하고, 10% HCl로 산성화시켰다. 형성된 침전물을 여과하고, 물로 세척하고, 감압 하에 건조시켜 생성물 3-(4-페닐티오펜-2-일)-2-티옥소프로판산 (0.9 g, 수율 74%)을 수득하였다.
조 생성물을 추가의 정제 없이 달성하였다.
2-(히드록시이미노)-3-(4-페닐티오펜-2-일)프로판산
3-(4-페닐티오펜-2-일)-2-티옥소프로판산 (0.9 g, 3.4 mmol), 히드록실아민 히드로클로라이드 (740 mg, 10.6 mmol), 및 에탄올성 용액 나트륨 에톡시드 [나트륨 0.4 g 및 무수 에탄올 30 mL로부터 제조됨]를 1.5시간 동안 환류하였다. 용매를 감압 하에 제거하고, 잔류물을 물로 희석하고, 1.5N HCl로 산성화시켜 용액의 pH를 ~3으로 조정하였다. 고체 생성물을 EtOAc로 추출하였다. 유기 층을 무수 Na2SO4 상에서 건조시킨 다음, 용매를 감압 하에 제거하여 2-(히드록시이미노)-3-(4-페닐티오펜-2-일)프로판산 (0.8 g, 수율 89%)을 회백색 고체로서 수득하였다.
2-(4-페닐티오펜-2-일)아세토니트릴
2-(히드록시이미노)-3-(4-페닐티오펜-2-일)프로판산 (0.8 g, 3.1 mmol)을 아세트산 무수물 (5 mL)에서 1.5시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 물로 처리하였다. 생성물을 EtOAc로 추출하고, 유기 층을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 10 -15% EtOAc)에 의해 정제하여 2-(4-페닐티오펜-2-일)아세토니트릴 (0.45 g, 수율 73%)을 연황색 고체로서 수득하였다.
4-(4-페닐티오펜-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-페닐티오펜-2-일)아세토니트릴로부터 황색 고체로서 합성하였다 (0.32 g, 수율 68%).
(4-(4-페닐티오펜-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-페닐티오펜-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였다 (210 mg, 수율 65%).
N-((4-(4-페닐티오펜-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-페닐티오펜-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (80 mg, 수율 20%).
실시예 10
1-(4-페닐티아졸-2-일)시클로펜탄카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-페닐티아졸-2-일)아세토니트릴로부터 1,4-디브로모부탄을 사용하여 합성하였다 (580 mg, 수율 91%).
(1-(4-페닐티아졸-2-일)시클로펜틸)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 1-(4-페닐티아졸-2-일)시클로펜탄카르보니트릴로부터 합성하였다 (250 mg, 수율 42%).
N-((1-(4-페닐티아졸-2-일)시클로펜틸)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (1-(4-페닐티아졸-2-일)시클로펜틸)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (65 mg, 수율 34%).
실시예 11
4-(3-페닐-1H-1,2,4-트리아졸-5-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 (5-페닐-2H-[1,2,4]트리아졸-3-일)-아세토니트릴로부터 합성하였다 (0.22 g, 수율 16%).
(4-(3-페닐-1H-1,2,4-트리아졸-5-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(3-페닐-1H-1,2,4-트리아졸-5-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였다 (170 mg, 조물질).
N-((4-(3-페닐-1H-1,2,4-트리아졸-5-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(3-페닐-1H-1,2,4-트리아졸-5-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (80 mg, 수율 24%).
실시예 12
4-(2-페닐티아졸-4-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 (2-페닐-티아졸-4-일)-아세토니트릴로부터 황색 고체로서 합성하였다 (0.53 g, 수율 79%).
(4-(2-페닐티아졸-4-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(2-페닐티아졸-4-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였다 (380 mg, 수율 72%).
N-((4-(2-페닐티아졸-4-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(2-페닐티아졸-4-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (85 mg, 수율 45%).
실시예 13
2-(4-(4-메톡시페닐)티아졸-2-일)아세토니트릴
이 화합물을 실시예 1 단계 1에 기재된 바와 같이 2-브로모-1-(4-메톡시페닐)에타논 및 2-시아노티오아세트아미드로부터 합성하였다 (1.5 g, 수율 75%).
4-(4-(4-메톡시페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(4-메톡시페닐)티아졸-2-일)아세토니트릴로부터 합성하였다 (1.6 g, 수율 82%).
(4-(4-(4-메톡시페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-(4-메톡시페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였다 (200 mg, 수율 40%).
N-((4-(4-(4-메톡시페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-(4-메톡시페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (80 mg, 수율 38%).
실시예 14
2-(4-(4-클로로페닐)티아졸-2-일)아세토니트릴
이 화합물을 실시예 1 단계 1에 기재된 바와 같이 2-브로모-1-(4-클로로페닐)에타논 및 2-시아노티오아세트아미드로부터 합성하였다 (1.51 g, 수율 75%).
4-(4-(4-클로로페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(4-클로로페닐)티아졸-2-일)아세토니트릴로부터 합성하였다 (1.15 g, 수율 86%).
(4-(4-(4-클로로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-(4-클로로페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였다 (250 mg, 수율 50%).
N-((4-(4-(4-클로로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-(4-클로로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (75 mg, 수율 42%).
실시예 15
2-메틸-2-(4-페닐티아졸-2-일)프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-페닐티아졸-2-일)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였다 (250 mg, 조물질).
2-메틸-2-(4-페닐티아졸-2-일)프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-메틸-2-(4-페닐티아졸-2-일)프로판니트릴로부터 합성하였다 (100 mg, 수율 45%).
N-(2-메틸-2-(4-페닐티아졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-메틸-2-(4-페닐티아졸-2-일)프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (75 mg, 수율 38%).
실시예 16
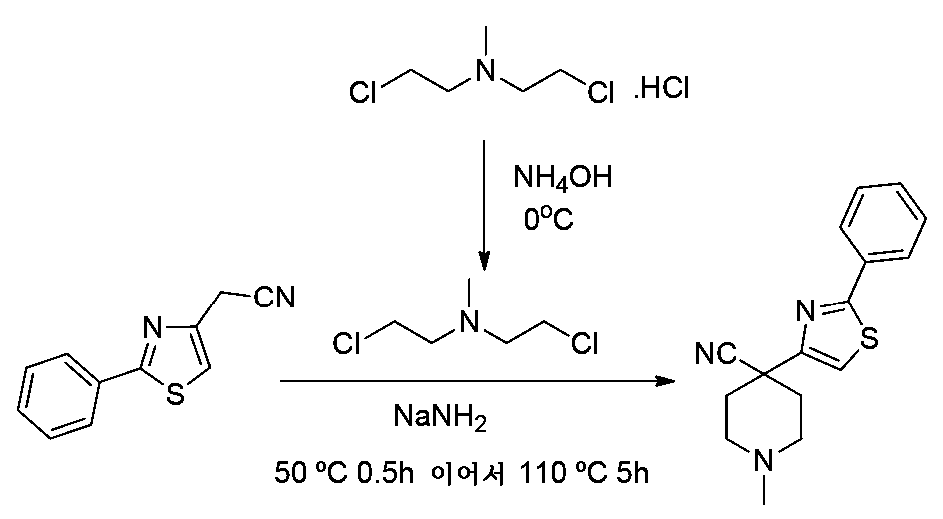
1-메틸-4-(4-페닐티아졸-2-일)피페리딘-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-페닐티아졸-2-일)아세토니트릴로부터 2-클로로-N-(2-클로로에틸)-N-메틸에탄아민 히드로클로라이드를 사용하고 반응 혼합물을 60℃에서 밤새 가열하여 합성하였다 (200 mg, 40% 수율).
단계 1b: 1-메틸-4-(4-페닐티아졸-2-일)피페리딘-4-카르보니트릴의 대안적 합성
나트륨 아미드 (878 mg, 22.4 mmol)를 톨루엔 (15 mL) 중에 현탁시키고, 0℃로 냉각시켰다. 이 현탁액에 톨루엔 (10 mL) 중 (4-페닐-티아졸-2-일)-아세토니트릴 (1.5 g, 7.4 mmol)의 용액을 0℃에서 온도를 유지하면서 적가하였다. 반응 혼합물을 20분 동안 교반하였다. 별도로 비스-(2-클로로에틸)메틸아민 히드로클로라이드 (1.45 g, 7.4 mmol)를 물 (8 mL)에 녹이고, 0℃로 냉각시키고, 수성 암모니아 용액을 사용하여 염기성화시켰다 (용액의 pH를 ~8로 조정함). 유성 층을 수성 층으로부터 분리하고, 유기 생성물을 톨루엔으로 추출하였다. 톨루엔 층을 수산화나트륨 펠릿 상에서 건조시켰다. 비스-(2-클로로에틸)메틸아민의 건조 톨루엔 용액을 반응 혼합물에 0℃에서 첨가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 추가로 110℃로 3시간 동안 가열하였다. 이어서, 반응 혼합물을 실온으로 냉각시키고, EtOAc로 희석하고, EtOAc로 추출하였다. 합한 추출물을 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 CH2Cl2 중 5% MeOH)에 의해 정제하여 1-메틸-4-(4-페닐티아졸-2-일)피페리딘-4-카르보니트릴 (350 mg, 수율 17%)을 수득하였다.
(1-메틸-4-(4-페닐티아졸-2-일)피페리딘-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 1-메틸-4-(4-페닐티아졸-2-일)피페리딘-4-카르보니트릴로부터 합성하였다 (200 mg, 조물질).
N-((1-메틸-4-(4-페닐티아졸-2-일)피페리딘-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (1-메틸-4-(4-페닐티아졸-2-일)피페리딘-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (9 mg, 23% 수율):
실시예 17
2-(4-(4-플루오로페닐)티아졸-2-일)아세토니트릴
이 화합물을 실시예 1 단계 1에 기재된 바와 같이 2-브로모-1-(4-플루오로페닐)에타논 및 2-시아노티오아세트아미드로부터 합성하였다 (3.2 g, 수율 72%).
4-(4-(4-플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(4-플루오로페닐)티아졸-2-일)아세토니트릴로부터 합성하였다 (3.0 g, 수율 66%).
(4-(4-(4-플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-(4-플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였고 (600 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-((4-(4-(4-플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-(4-플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (11 mg, 27% 수율):
실시예 18
2-(5-메틸-4-페닐티아졸-2-일)아세토니트릴
이 화합물을 실시예 1 단계 1에 기재된 바와 같이 2-브로모-1-페닐프로판-1-온 및 2-시아노티오아세트아미드로부터 합성하였다 (1.7 g, 56% 수율%).
4-(5-메틸-4-페닐티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(5-메틸-4-페닐티아졸-2-일)아세토니트릴로부터 합성하였다 (3.0 g, 수율 66%).
(4-(5-메틸-4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(5-메틸-4-페닐티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였고 (600 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-((4-(5-메틸-4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(5-메틸-4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (55 mg, 89% 수율):
실시예 19
2-(4-시클로헥실티아졸-2-일)아세토니트릴
이 화합물을 실시예 1 단계 1에 기재된 바와 같이 2-브로모-1-시클로헥실에타논 및 2-시아노티오아세트아미드로부터 합성하였다 (0.4 g, 수율 80%).
4-(4-시클로헥실티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-시클로헥실티아졸-2-일)아세토니트릴로부터 황색 고체로서 합성하였다 (0.3 g, 수율 60%).
(4-(4-시클로헥실티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-시클로헥실티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였다 (120 mg, 수율 40%).
N-((4-(4-시클로헥실티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-시클로헥실티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (70 mg, 수율 32%).
실시예 20
2-(4-(피리딘-2-일)티아졸-2-일)아세토니트릴
이 화합물을 실시예 1 단계 1에 기재된 바와 같이 2-브로모-1-(피리딘-2-일)에타논 및 2-시아노티오아세트아미드로부터 합성하였다 (0.37 g, 수율 73%):
4-(4-(피리딘-2-일)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(피리딘-2-일)티아졸-2-일)아세토니트릴로부터 합성하였다 (0.37 g, 수율 74%):
(4-(4-(피리딘-2-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-(피리딘-2-일)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였고 (150 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-((4-(4-(피리딘-2-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-(피리딘-2-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (35 mg, 수율 13%).
실시예 21
2-(4-(피리딘-4-일)티아졸-2-일)아세토니트릴
이 화합물을 실시예 1 단계 1에 기재된 바와 같이 2-브로모-1-(피리딘-4-일)에타논 및 2-시아노티오아세트아미드로부터 합성하였다 (0.23 g, 수율 46%):
4-(4-(피리딘-4-일)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(피리딘-4-일)티아졸-2-일)아세토니트릴로부터 합성하였다 (0.18 g, 수율 58%):
(4-(4-(피리딘-4-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-(피리딘-4-일)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였고 (90 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-((4-(4-(피리딘-4-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-(피리딘-4-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (60 mg, 수율 38%):
실시예 22
메틸 5-((히드록시이미노)메틸)티오펜-2-카르복실레이트
히드록실아민 히드로클로라이드 (420 mg, 6.1 mmol) 및 피리딘 (0.5 mL)을 EtOH (25 mL) 중 메틸 5-포르밀티오펜-2-카르복실레이트 (690 mg, 4.1 mmol)의 용액에 첨가하였다. 반응 혼합물을 3시간 동안 환류하고, 실온으로 냉각시키고, 감압 하에 농축시켰다. 잔류물을 디에틸 에테르 중에 용해시키고, 유기 층을 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시켰다. 용매를 감압 하에 제거하여 생성물 메틸 5-((히드록시이미노)메틸)티오펜-2-카르복실레이트 (440 mg, 수율 60%)를 수득하였으며, 이를 추가 정제 없이 달성하였다.
메틸 5-시아노티오펜-2-카르복실레이트
아세트산 무수물 (10 mL) 중 메틸 5-((히드록시이미노)메틸)티오펜-2-카르복실레이트 (440 mg, 2.4 mmol)의 용액을 16시간 동안 환류하였다. 완결된 후, 반응 혼합물을 실온으로 냉각시키고, 감압 하에 농축시키고, 잔류물을 디에틸 에테르 중에 용해시켰다. 유기 층을 10% 수성 NaOH 용액, 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시켰다. 용매를 감압 하에 제거하여 메틸 5-시아노티오펜-2-카르복실레이트 (5-시아노-티오펜-2-카르복실산 메틸 에스테르) (400 mg, 수율 90%)를 수득하였으며, 이를 추가 정제 없이 달성하였다.
메틸 및 에틸 5-(N'-히드록시카르밤이미도일)티오펜-2-카르복실레이트
이 화합물의 혼합물을 실시예 1 단계 4에 기재된 바와 같이 메틸 5-시아노티오펜-2-카르복실레이트로부터 합성하였고, 이것을 메틸 및 에틸 에스테르의 혼합물 (2:3 비율)로서 단리시켰고, 이를 추가 정제 없이 달성하였다.
메틸 및 에틸 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)티오펜-2-카르복실레이트
이 화합물의 혼합물을 실시예 1 단계 5에 기재된 바와 같이 메틸 및 에틸 5-(N'-히드록시카르밤이미도일)티오펜-2-카르복실레이트의 혼합물로부터 합성하였고, 이것을 메틸 및 에틸 에스테르의 혼합물 (2:3 비율)로서 단리시켰고, 이를 추가 정제 없이 달성하였다.
5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)티오펜-2-카르복실산
LiOH (37 mg)를 THF: H2O (10 mL, 7:3 v/v) 중 화합물 메틸 및 에틸 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)티오펜-2-카르복실레이트 (300 mg)의 혼합물의 용액에 첨가하고, 혼합물을 실온에서 2일 동안 교반하였다. 이어서, 반응 혼합물을 물로 희석하고, 수성 층을 EtOAc로 세척하였다. 수성 층을 pH ~4로 산성화시키고, EtOAc로 추출하였다. 합한 추출물을 감압 하에 농축시켜 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)티오펜-2-카르복실산 (60 mg)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)티오펜-2-카르복스아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)티오펜-2-카르복실산으로부터 합성하였다 (25 mg, 수율 22%):
실시예 23
2-(4-(티오펜-2-일)티아졸-2-일)아세토니트릴
이 화합물을 실시예 1 단계 1에 기재된 바와 같이 2-브로모-1-(티오펜-2-일)에타논 및 2-시아노티오아세트아미드로부터 합성하였다 (0.25 g, 수율 49%):
4-(4-(티오펜-2-일)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(티오펜-2-일)티아졸-2-일)아세토니트릴로부터 합성하였다 (0.2 g, 수율 60%):
(4-(4-(티오펜-2-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-(티오펜-2-일)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였다 (80 mg, 수율 40%):
N-((4-(4-(티오펜-2-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-(티오펜-2-일)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (70 mg, 수율 46%):
실시예 24
2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(4-플루오로페닐)티아졸-2-일)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였고, 이것을 어떠한 정제도 없이 후속 단계에 직접 사용하였다.
2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로판니트릴로부터 합성하였다 (29 mg, 6% 수율).
단계 6: N-(2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
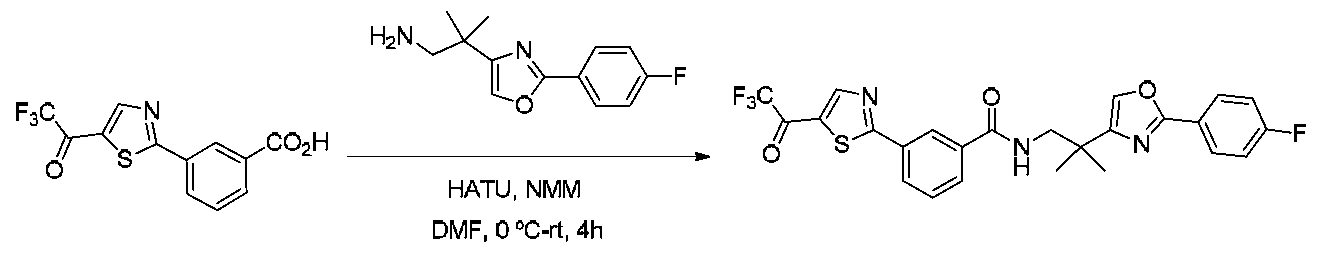
2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로판-1-아민 (140 mg, 0.56 mmol), 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산 (144.37 mg, 0.56 mmol), N-(3-디메틸아미노프로필)-N'-에틸카르보디이미드 히드로클로라이드 (EDCI) (214.42 mg, 1.12 mmol), 및 1-히드록시벤조트리아졸 (HOBt) (120.91 mg, 0.89 mmol)을 실온에서 디클로로메탄 (3 mL) 중에 용해시켰다. 이어서, 디이소프로필에틸아민 (DIEA) (0.39 mL, 2.24 mmol)을 실온에서 도입하고, 반응 혼합물을 실온에서 2시간 동안 교반하였다. 반응 혼합물을 디클로로메탄 (60 mL)으로 희석하고, 물 (1 X 20 mL) 및 염수 (1 X 20 mL)로 세척하였다. 이어서, 유기 층을 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 조 생성물을 수득하였다. 이어서, 조 생성물을 콤비플래쉬 ISCO (0-30% 에틸 아세테이트:헥산)에 의해 정제하여 목적 생성물 (164 mg, 60% 수율)을 수득하였다.
실시예 25
2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(4-클로로페닐)티아졸-2-일)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였다 (470 mg, 수율 94%):
2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로판니트릴로부터 합성하였다 (120 mg, 수율 47%):
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (80 mg, 수율 35%):
실시예 26
3-플루오로-5-(N'-히드록시카르밤이미도일)벤조산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 3-시아노-5-플루오로벤조산으로부터 합성하였고 (442 mg, 수율 37%), 이를 추가 정제 없이 달성하였다.
3-플루오로-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 3-플루오로-5-(N'-히드록시카르밤이미도일)벤조산으로부터 합성하였고 (351 mg, 수율 51%), 이를 추가 정제 없이 달성하였다.
3-플루오로-N-(2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로판-1-아민 및 3-플루오로-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (23 mg, 수율 32%):
실시예 27
메틸 3,5-디시아노벤조에이트
3,5-디브로모메틸벤조에이트 (1 g, 3.4 mmol)를 건조 DMF (35 mL) 중에 용해시키고, 시안화구리 (1.2 g, 13.6 mmol)를 첨가하였다. 반응 혼합물을 아르곤 분위기 하에 160℃로 26시간 동안 가열하고, 실온으로 냉각되도록 한 다음, 포화 염화암모늄 용액으로 켄칭하였다. 반응 혼합물을 EtOAc로 희석하고, 셀라이트 플러그를 통해 여과하였다. 여과물을 EtOAc로 희석하고, 유기 층을 물 및 염수로 세척하였다. 용매를 감압 하에 증발시켜 조 메틸 3,5-디시아노벤조에이트 (400 mg, 조물질, GC-MS에 의해 확인함)를 수득하였으며, 이를 추가 정제 없이 달성하였다.
3,5-디시아노벤조산
메틸 3,5-디시아노벤조에이트 (400 mg, 2.1 mmol)를 THF-H2O (7:3 v/v, 30 mL) 중에 용해시키고, 용액을 0℃로 냉각시키고, LiOH (51 mg, 2.1 mmol)를 첨가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 1시간 동안 교반하였다. THF를 감압 하에 제거하고, 수성 층을 EtOAc로 세척하고, 1.5N HCl을 사용하여 pH ~2-3으로 산성화시키고, EtOAc로 추출하였다. 유기 층을 무수 황산나트륨 상에서 건조시키고, 용매를 감압 하에 제거하였다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 CHCl3 중 20% MeOH)에 의해 정제하여 순수한 생성물 3,5-디시아노벤조산 (100 mg, 수율 28%)을 수득하였다:
3-시아노-5-(N'-히드록시카르밤이미도일)벤조산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 3,5-디시아노벤조산으로부터 합성하였고 (120 g, 조물질), 이를 추가 정제 없이 달성하였다.
3-시아노-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 3-시아노-5-(N'-히드록시카르밤이미도일)벤조산으로부터 합성하였다 (45 mg, 수율 27%):
3-시아노-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-시아노-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (25 mg, 수율 30%):
실시예 28
3-(N'-히드록시카르밤이미도일)-5-메톡시벤조산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 3-시아노-5-메톡시벤조산으로부터 합성하였다 (500 mg, 수율 84%):
3-메톡시-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 3-(N'-히드록시카르밤이미도일)-5-메톡시벤조산으로부터 합성하였고 (170 mg, 수율 40%), 이를 추가 정제 없이 달성하였다.
3-메톡시-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-메톡시-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (70 mg, 수율 46%):
실시예 29
2-(4-(4-플루오로페닐)티아졸-2-일)에탄아민
2-(4-(4-플루오로페닐)티아졸-2-일)아세토니트릴 (400 mg, 1.83 mmol)을 실온에서 테트라히드로푸란 (10 mL) 중에 용해시켰다. 보란 테트라히드로푸란 착체 용액 (테트라히드로푸란 중 1M, 9.16 mL, 9.16 mmol)을 첨가하고, 반응 혼합물을 실온에서 1시간 동안 교반하였다. 반응 혼합물을 0℃로 냉각시키고, 메탄올 (5 eq., 0.4 mL)로 켄칭하였다. 반응물을 실온으로 가온되도록 하고, 2N HCl을 pH 시험지에 의해 반응 혼합물이 산성인 것을 확인할 때까지 첨가하였다. 이어서, 반응 혼합물을 65℃에서 30분 동안 환류하였다. 이어서, 반응 혼합물을 실온으로 냉각되도록 하고, 감압 하에 농축시켰다. 수득한 고체를 에테르 (2 X 20 mL) 및 디클로로메탄 (2 X 20 mL)으로 연화처리하였다. 나머지 고체를 물 (50 mL) 중에 용해시키고, NaOH 펠릿을 사용하여 pH ~11로 염기성화시켰다. 이어서, 수성 혼합물을 에테르 (2 X 100 mL)로 추출하였다. 유기 층을 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 조 생성물을 수득하였으며, 이를 직접 후속 단계에 어떠한 정제도 없이 사용하였다 (100 mg, 25% 수율).
N-(2-(4-(4-플루오로페닐)티아졸-2-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 26 단계 6에 기재된 바와 같이 2-(4-(4-플루오로페닐)티아졸-2-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (180 mg, 86% 수율).
실시예 30
2-(4-(4-브로모페닐)티아졸-2-일)아세토니트릴
이 화합물을 실시예 1 단계 1에 기재된 바와 같이 2-브로모-1-(4-브로모페닐)에타논 및 2-시아노티오아세트아미드로부터 합성하였고 (2.4 g, 48% 수율), 이를 추가 정제 없이 달성하였다.
4-(4-(4-브로모페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(4-브로모페닐)티아졸-2-일)아세토니트릴로부터 합성하였다 (1.9 g, 수율 80%).
(4-(4-(4-브로모페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-(4-브로모페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였고 (1.7 g), 이를 추가 정제 없이 달성하였다.
4-(2-(4-(아미노메틸)테트라히드로-2H-피란-4-일)티아졸-4-일)벤조니트릴
(4-(4-(4-브로모페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 (200 mg, 0.56 mmol), 시안화아연 (53 mg, 0.45 mmol), 및 DMF (2 mL)를 마이크로웨이브 튜브에 넣고, 탈기하였다. 1,1'-비스(디페닐포스피노)페로센-팔라듐(II)디클로라이드 (41 mg, 0.05 mmol)를 첨가하였다. 반응물을 완결될 때까지 200℃에서 10분 동안 마이크로웨이브로 처리하였다. 반응물을 수산화암모늄/물 (1:4)로 켄칭하고, 에틸 아세테이트로 세척하였다. 유기 층을 황산나트륨 상에서 건조시켰다. 조물질을 에틸 아세테이트 세척에 이어서 1% 트리에틸아민을 포함하는 디클로로메탄 중 10%메탄올을 이용하는 실리카 크로마토그래피로 정제하여 4-(2-(4-(아미노메틸)테트라히드로-2H-피란-4-일)티아졸-4-일)벤조니트릴 (20 mg, 10% 수율)을 수득하였다.
N-((4-(4-(4-시아노페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 4-(2-(4-(아미노메틸)테트라히드로-2H-피란-4-일)티아졸-4-일)벤조니트릴 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (3 mg, 7% 수율).
실시예 31
4-(4-(4-플루오로페닐)티아졸-2-일)-2,2-디메틸테트라히드로-2H-피란-4-카르보니트릴
DMF (5 mL) 중 2-(4-(4-플루오로페닐)티아졸-2-일)아세토니트릴 (325 mg, 1.5 mmol), 탄산칼륨 (617 mg, 4.47 mmol), 및 1-클로로-2-(2-클로로에톡시)-2-메틸프로판 (254 mg, 1.5 mmol)을 160℃에서 5분에 이어서 20분 동안 마이크로웨이브로 처리하였다. 탄산칼륨 및 1-클로로-2-(2-클로로에톡시)-2-메틸프로판을 한번 더 첨가하고, 이어서 반응물을 다시 30분 동안 2회 마이크로웨이브로 처리하였다. 반응물을 에틸 아세테이트로 희석하고, 물로 세척하였다. 유기 층을 황산나트륨 상에서 건조시키고, 0-30% 에틸 아세테이트/헥산의 구배를 이용하는 실리카에 의해 정제하여 4-(4-(4-플루오로페닐)티아졸-2-일)-2,2-디메틸테트라히드로-2H-피란-4-카르보니트릴 (228 mg, 48% 수율)을 수득하였다.
(4-(4-(4-플루오로페닐)티아졸-2-일)-2,2-디메틸테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-(4-플루오로페닐)티아졸-2-일)-2,2-디메틸테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였고 (100 mg), 이를 추가 정제 없이 달성하였다.
N-((4-(4-(4-플루오로페닐)티아졸-2-일)-2,2-디메틸테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-(4-플루오로페닐)티아졸-2-일)-2,2-디메틸테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (7 mg, 수율 17%):
실시예 32
3-시아노벤젠-1-술포닐 클로라이드
3-아미노벤조니트릴 (2.5 g, 21 mmol)을 진한 HCl (20 mL) 및 물 (20 mL) 중에 용해시키고, 0℃로 냉각시키고, 물 (5 mL) 중 아질산나트륨 (1.5 g, 22 mmol)의 용액을 적가하였다. 반응 혼합물을 10분 동안 교반하여 디아조늄 염 형성을 완결시켰다. 별도의 플라스크에 AcOH 중 이산화황의 포화 용액 (25 mL) 상에 염화구리(I) (0.2 g)를 첨가하고, 0℃에서 10분 동안 교반하였다. 생성된 용액을 디아조늄 염에 적가하고, 0℃에서 1시간 동안 교반하였다. 반응 혼합물을 빙수에 붓고, 생성물을 tert-부틸메틸에테르로 추출하였다. 합한 유기 층을 물 및 염수로 세척하였다. 조 생성물을 칼럼 크로마토그래피 (석유 에테르 중 5% EtOAc를 이용하는 실리카 겔 60-120 메쉬)에 의해 정제하여 순수한 3-시아노벤젠-1-술포닐 클로라이드 (1.9 g, 수율 45%)를 회백색 고체로서 수득하였다.
3-시아노-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤젠술폰아미드
Et3N (0.15 mL, 1.43 mmol)을 건조 CH2Cl2 (3 mL) 중 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 (130 mg, 0.48 mmol)의 빙냉 용액에 적가하였다. 생성된 반응 혼합물을 0℃에서 5분 동안 교반한 다음, 건조 CH2Cl2 (2 mL) 중 3-시아노벤젠-1-술포닐 클로라이드 (105 mg, 0.52 mmol)의 용액을 적가하였다. 반응 혼합물을 실온에서 1시간 동안 추가로 교반하였다. 반응 혼합물을 CH2Cl2로 희석하고, 유기 층을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 35% EtOAc)에 의해 정제하여 화합물 3-시아노-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤젠술폰아미드 (0.13 g, 수율 61%)를 회백색 고체로서 수득하였다.
N'-히드록시-3-(N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)술파모일)벤즈이미드아미드
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 3-시아노-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤젠술폰아미드로부터 합성하였고 (125 mg, 수율 89%), 이를 추가 정제 없이 달성하였다.
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤젠술폰아미드
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 N'-히드록시-3-(N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)술파모일)벤즈이미드아미드로부터 합성하였다 (80 mg, 수율 57%).
실시예 33
3-브로모-5-(메톡시카르보닐)벤조산
디메틸-5-브로모이소프탈레이트 (3 g, 11.0 mmol)를 아세톤-H2O (2:1 v/v, 60 mL) 중에 용해시키고, NaOH (0.40 g, 11.0 mmol)를 첨가하였다. 반응 혼합물을 4시간 동안 교반되도록 하였다. 아세톤을 감압 하에 제거하고, 수성 층을 EtOAc로 세척하고, 1.5N HCl을 사용하여 pH ~ 2-3으로 산성화시키고, EtOAc로 추출하였다. 유기 층을 무수 황산나트륨 상에서 건조시키고, 용매를 감압 하에 제거하여 3-브로모-5-(메톡시카르보닐)벤조산 (2.55 g, 수율 89%)을 수득하였다:
메틸 3-브로모-5-(메톡시(메틸)카르바모일)벤조에이트
N,O-디메틸히드록실아민 히드로클로라이드 (1.15 g, 11.8 mmol)를 CH2Cl2 (50 mL) 중에 용해시키고, Et3N (4.8 mL, 34.4 mmol)을 첨가하였다. 용액을 30분 동안 교반하였다. 생성된 용액을 0℃로 냉각시키고, 화합물 3-브로모-5-(메톡시카르보닐)벤조산 (2.55 g, 9.84 mmol)을 첨가하고, 이어서 EDC.HCl (3.77 g, 19.6 mmol) 및 HOBt (0.26 g, 1.96 mmol)를 첨가하였다. 반응 혼합물을 실온이 되도록 하고, 추가로 4시간 동안 교반하였다. 완결된 후, 반응 혼합물을 CH2Cl2로 희석하였다. 유기 층을 물 및 염수 용액으로 세척하고, 무수 황산나트륨 상에서 건조시켰다. 용매를 감압 하에 제거하고, 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 20% EtOAc)에 의해 정제하여 메틸 3-브로모-5-(메톡시(메틸)카르바모일)벤조에이트 (2.3 g, 수율 77%)를 무색 액체로서 수득하였다.
메틸 3-아세틸-5-브로모벤조에이트
화합물 메틸 3-브로모-5-(메톡시(메틸)카르바모일)벤조에이트 (2.3 g, 7.6 mmol)를 건조 THF (50 mL) 중에 용해시키고, 용액을 0℃로 냉각시키고, 메틸마그네슘 클로라이드 (THF 중 3M, 2.5 mL, 7.6 mmol)을 적가하였다. 반응 혼합물을 천천히 실온이 되도록 하고, 추가로 6시간 동안 교반하였다. 반응 혼합물을 0℃로 냉각시키고, 포화 NH4Cl 용액으로 켄칭하였다. 생성물을 EtOAc로 추출하였다. 유기 층을 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시켰다. 용매를 감압 하에 제거하였다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 5% EtOAc)에 의해 정제하여 메틸 3-아세틸-5-브로모벤조에이트 (0.95 g, 수율 49%)를 백색 고체로서 수득하였다.
3-브로모-5-에틸벤조산
화합물 메틸 3-아세틸-5-브로모벤조에이트 (1.2 g, 4.8 mmol)를 에틸렌 글리콜 (10 mL) 중에 용해시키고, KOH (0.41 g, 7.3 mmol)에 이어서 히드라진 수화물 (0.44 mL, 7.3 mmol)을 첨가하였다. 반응 혼합물을 200℃로 1시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 물로 희석하였다. 수성 층의 pH를 1.5N HCl을 사용하여 2-3으로 조정하였다. 생성물을 EtOAc로 추출하였다. 유기 층을 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시켰다. 용매를 감압 하에 제거하였다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 50% EtOAc)에 의해 정제하여 3-브로모-5-에틸벤조산 (0.95 g, 수율 89%)을 황색 고체로서 수득하였다.
메틸 3-브로모-5-에틸벤조에이트
화합물 3-브로모-5-에틸벤조산 (0.95 g, 4.14 mmol)을 MeOH (50 mL) 중에 용해시키고, 반응 혼합물을 0℃로 냉각시키고, SOCl2 (0.5 mL)를 첨가하였다. 반응 혼합물을 실온에서 10시간 동안 교반되도록 하였다. 반응 혼합물을 감압 하에 농축시키고, CH2Cl2로 희석하였다. 유기 층을 10% NaHCO3 용액, 물 및 염수로 세척하였다. 유기 상을 무수 황산나트륨 상에서 건조시키고, 용매를 감압 하에 제거하였다. 메틸 3-브로모-5-에틸벤조에이트 (0.92 g, 수율 92%)를 무색 액체로서 단리시켰으며, 추가 정제 없이 달성하였다.
메틸 3-시아노-5-에틸벤조에이트
생성물 메틸 3-브로모-5-에틸벤조에이트 (0.9 g, 3.7 mmol)를 건조 DMF (50 mL) 중에 용해시키고, 시안화구리 (0.84 g, 9.43 mmol)를 첨가하였다. 반응 혼합물을 아르곤 분위기 하에 150℃로 12시간 동안 가열하였다 (TLC에 의해 모니터링함; 석유 에테르/EtOAc 9:1). 반응 혼합물을 실온이 되도록 한 다음, 포화 염화암모늄 용액으로 켄칭하였다. 반응 혼합물을 EtOAc로 희석하고, 셀라이트 층을 통해 여과하였다. 여과물을 EtOAc로 희석하고, 유기 층을 물 및 염수로 세척하였다. 용매를 감압 하에 증발시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 5% EtOAc)에 의해 정제하여 메틸 3-시아노-5-에틸벤조에이트 (0.27 g, 수율 39%)를 무색 액체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
3-시아노-5-에틸벤조산
화합물 메틸 3-시아노-5-에틸벤조에이트 (270 mg, 1.42 mmol)를 THF-H2O (7:3 v/v, 10 mL) 중에 용해시키고, 용액을 0℃로 냉각시키고, LiOH (59 mg, 1.42 mmol)를 첨가하였다. 반응 혼합물을 실온이 되도록 하고, 3시간 동안 교반하였다 (TLC에 의해 모니터링함; 석유 에테르/EtOAc 1:1). 용매 THF를 감압 하에 제거하고, 수성 층을 EtOAc로 세척하여 비-극성 불순물을 제거하였다. 수성 층의 pH를 1.5N HCl을 사용하여 2-3으로 조정하였다. 생성물을 EtOAc로 추출하였다. 유기 층을 무수 황산나트륨 상에서 건조시키고, 용매를 감압 하에 제거하여 3-시아노-5-에틸벤조산 (200 mg, 수율 80%)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
3-에틸-5-(N'-히드록시카르밤이미도일)벤조산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 3-시아노-5-에틸벤조산으로부터 합성하였고 (200 mg, 조물질), 이를 추가 정제 없이 달성하였다.
3-에틸-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 3-에틸-5-(N'-히드록시카르밤이미도일)벤조산으로부터 합성하였다 (130 mg, 수율 52%).
3-에틸-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-에틸-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (85 mg, 수율 45%).
실시예 34
4-(3-브로모페닐)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(3-브로모페닐)아세토니트릴로부터 합성하였다 (1.3 g, 65% 수율).
(4-(3-브로모페닐)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(3-브로모페닐)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였고 (1.3 g, 조물질), 이를 추가 정제 없이 달성하였다.
N-((4-(3-브로모페닐)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(3-브로모페닐)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (40 mg, 34% 수율).
실시예 35
2-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)아세토니트릴
이 화합물을 실시예 1 단계 1에 기재된 바와 같이 2-브로모-1-(4-(트리플루오로메틸)페닐)에타논 및 2-시아노티오아세트아미드로부터 합성하였고 (2.4 g, 48% 수율), 이를 추가 정제 없이 달성하였다.
4-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)아세토니트릴로부터 합성하였고 (690 mg, 수율 98%), 이를 추가 정제 없이 달성하였다.
(4-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였다. 물질을 추가 정제 없이 달성하였다.
3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)-N-((4-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (9 mg, 19% 수율).
실시예 36
2-메틸-2-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였고 (620 mg, 수율 73%), 이를 추가 정제 없이 달성하였다.
2-메틸-2-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-메틸-2-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)프로판니트릴로부터 합성하였다. 물질을 추가 정제 없이 달성하였다.
N-(2-메틸-2-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-메틸-2-(4-(4-(트리플루오로메틸)페닐)티아졸-2-일)프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (10 mg, 24% 수율).
실시예 37
1-(2-에톡시-2-옥소에틸)테트라히드로-1H-티오페늄 브로마이드
테트라히드로티오펜 (10 g, 113 mmol) 및 에틸 브로모아세테이트 (13 mL, 113 mmol)를 아세톤 (50 mL)에 녹이고, 실온에서 3일 동안 교반하였다. 침전물을 여과하고, 아세톤으로 세척하고, 공기 건조시켜 1-(2-에톡시-2-옥소에틸)테트라히드로-1H-티오페늄 브로마이드 (23 g, 수율 82%)를 수득하였으며, 이를 추가 정제 없이 달성하였다.
에틸 2-시아노시클로프로판카르복실레이트
50% KOH 용액 (16 mL) 및 포화 K2CO3 용액 (60 mL)을 CHCl3 (70 mL) 중 수득된 화합물 1-(2-에톡시-2-옥소에틸)테트라히드로-1H-티오페늄 브로마이드 (23 g, 90 mmol)의 냉각된 용액에 첨가하였다. 혼합물을 0℃에서 1시간 동안 교반하였다. 유기 층을 분리하고, 수성 층을 추가로 CHCl3으로 추출하였다. 합한 유기 추출물을 무수 황산나트륨 상에서 건조시키고, 용매를 감압 하에 제거하여 쯔비터이온성 중간체 (11 g, 수율 76%)를 수득하였다. 이 조 중간체를 CHCl3 (100 mL) 중에 용해시키고, 0℃로 냉각시켰다. 아크릴로니트릴 (4 mL, 68.3 mmol)을 반응 혼합물에 첨가하고, 혼합물을 실온에서 48시간 동안 추가로 교반하였다. 용매를 감압 하에 증발시키고, 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 30% EtOAc)에 의해 정제하여 에틸 2-시아노시클로프로판카르복실레이트 (5 g, 수율 53%)를 수득하였다.
2-시아노시클로프로판카르복실산
에틸 2-시아노시클로프로판카르복실레이트 (5 g, 35.9 mmol)를 MeOH (20 mL) 중에 용해시키고, 1N NaOH (35 mL)를 첨가하였다. 반응 혼합물을 실온에서 2시간 동안 교반하였다. 반응의 완결 후, MeOH를 감압 하에 증발시켰다. 수성 층의 pH를 1.5N HCl을 사용하여 2-3으로 조정하였다. 백색 침전물을 여과에 의해 수집하고, 감압 하에 건조시켜 2-시아노시클로프로판카르복실산 (3.3 g, 수율 85%)을 수득하였다:
2-시아노-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)시클로프로판카르복스아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 2-시아노시클로프로판카르복실산으로부터 합성하였다 (90 mg, 수율 29%):
2-(N'-히드록시카르밤이미도일)-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)시클로프로판카르복스아미드
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 2-시아노-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)시클로프로판카르복스아미드로부터 합성하였고 (90 mg, 조물질), 이를 추가 정제 없이 사용하였다.
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)시클로프로판카르복스아미드
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 2-(N'-히드록시카르밤이미도일)-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)시클로프로판카르복스아미드로부터 합성하였다 (45 mg, 수율 45%):
실시예 38
2-클로로-N-(2-클로로에틸)-N-메틸에탄아민 히드로클로라이드
1,5-디클로로아자펜탄 히드로클로라이드 (1.0 g, 5.6 mmol)를 포름산 (0.43 mL, 11.2 mmol)에 녹였다. 포름알데히드 용액 (1.2 mL, 물 중 37%)을 첨가하고, 반응 혼합물을 100℃로 4시간 동안 가열한 다음, 120℃로 0.5시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 용매를 감압 하에 제거하였다. 조 혼합물을 헥산으로 세척하여 2-클로로-N-(2-클로로에틸)-N-메틸에탄아민 히드로클로라이드 (1.0 g, 수율 92%)를 백색 고체로서 수득하였다.
1-메틸-4-(2-페닐티아졸-4-일)피페리딘-4-카르보니트릴
이 화합물을 실시예 16 단계 1b에 기재된 바와 같이 (2-페닐-티아졸-4-일)-아세토니트릴 및 2-클로로-N-(2-클로로에틸)-N-메틸에탄아민 히드로클로라이드로부터 합성하였다 (135 mg, 수율 25%).
(1-메틸-4-(2-페닐티아졸-4-일)피페리딘-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 1-메틸-4-(2-페닐티아졸-4-일)피페리딘-4-카르보니트릴로부터 합성하였고 (110 mg), 이를 추가 정제 없이 달성하였다.
N-((1-메틸-4-(2-페닐티아졸-4-일)피페리딘-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (1-메틸-4-(2-페닐티아졸-4-일)피페리딘-4-일)메탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (15 mg, 수율 8%).
실시예 39
4-(클로로메틸)-2-(4-클로로페닐)티아졸
EtOH-THF (20 mL-10 mL) 중 4-클로로티오벤즈아미드 (0.5 g, 2.9 mmol) 및 1,3-디클로로아세톤 (0.4 g, 3.18 mmol)의 혼합물을 85℃로 10시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 10% NaHCO3 용액으로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 유기 층을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시켰다. 용매를 감압 하에 제거하고, 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 3-5% EtOAc)에 의해 정제하여 4-(클로로메틸)-2-(4-클로로페닐)티아졸 (0.55 g, 수율 77%)을 백색 고체로서 수득하였다.
2-(2-(4-클로로페닐)티아졸-4-일)아세토니트릴
촉매량의 18-크라운-6-에테르 (20 mg)를 아세토니트릴 (20 mL) 중 4-(클로로메틸)-2-(4-클로로페닐)티아졸 (0.55 g, 2.25 mmol)의 용액에 첨가하고, 이어서 시안화칼륨 (0.22 g, 3.37 mmol)을 첨가하고, 반응 혼합물을 10시간 동안 환류하였다. 이어서, 반응 혼합물을 물로 켄칭하고, 유기 생성물을 EtOAc로 추출하였다. 합한 추출물을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 15% EtOAc)에 의해 정제하여 2-(2-(4-클로로페닐)티아졸-4-일)아세토니트릴 (0.43 g, 수율 82%)을 회백색 고체로서 수득하였다.
2-(2-(4-클로로페닐)티아졸-4-일)-2-메틸프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(2-(4-클로로페닐)티아졸-4-일)아세토니트릴로부터 아이오도메탄을 사용하여 연황색 고체로서 합성하였다 (0.15 g, 수율 70%).
2-(2-(4-클로로페닐)티아졸-4-일)-2-메틸프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(2-(4-클로로페닐)티아졸-4-일)-2-메틸프로판니트릴로부터 합성하였다 (60 mg, 수율 40%).
N-(2-(2-(4-클로로페닐)티아졸-4-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-클로로페닐)티아졸-4-일)-2-메틸프로판-1-아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (50 mg, 수율 51%).
실시예 40
4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-카르보니트릴
이 화합물을 실시예 16 단계 1b에 기재된 바와 같이 2-(2-(4-클로로페닐)티아졸-4-일)아세토니트릴 및 2-클로로-N-(2-클로로에틸)-N-메틸에탄아민 히드로클로라이드로부터 합성하였다 (350 mg, 수율 32%).
(4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-카르보니트릴로부터 합성하였고 (130 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-((4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-일)메탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (17 mg, 수율 11%).
실시예 41
N-(2-(2-(4-클로로페닐)티아졸-4-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-클로로페닐)티아졸-4-일)-2-메틸프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (75 mg, 수율 25%).
실시예 42
2-(2-(4-클로로페닐)티아졸-4-일)에탄아민
보란 디메틸 술피드 착체 (0.24 mL, 2.5 mmol)를 건조 THF (15 mL) 중 2-(2-(4-클로로페닐)티아졸-4-일)아세토니트릴 (150 mg, 0.63 mmol)의 용액에 실온에서 첨가하였다. 반응 혼합물을 0.5시간 동안 환류한 다음, 메탄올로 조심스럽게 켄칭하였다. 반응 혼합물을 감압 하에 농축시키고, EtOAc로 희석하였다. 유기 층을 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 2-(2-(4-클로로페닐)티아졸-4-일)에탄아민 (150 mg, 조물질)을 수득하였으며, 이를 후속 단계에 그대로 사용하였다.
N-(2-(2-(4-클로로페닐)티아졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-클로로페닐)티아졸-4-일)에탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (13 mg, 수율 23%).
실시예 43
메틸 2-시아노이소니코티네이트
트리메틸실릴 시아나이드 (3.8 g, 0.0386 mol) 및 디메틸카르바밀 클로라이드 (5.0 g, 0.0483 mol)를 건조 CH2Cl2 (50 mL) 중 메틸이소니코티네이트 N-옥시드 (5.0 g, 0.0322 mol)의 용액에 실온에서 첨가하였다. 반응 혼합물을 실온에서 12시간 동안 교반한 다음, 10% K2CO3 용액으로 켄칭하였다. 유기 생성물을 CH2Cl2로 추출하고, 유기 층을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 플래쉬 칼럼 크로마토그래피 (실리카 230-400 메쉬, 용리액 CH2Cl2 중 1-2% MeOH)에 의해 정제하여 메틸 2-시아노이소니코티네이트 (1.75 g, 수율 33%)를 회백색 고체로서 수득하였다.
2-시아노이소니코틴산
수산화리튬 (96 mg, 4.0 mmol)을 THF-H2O (20 mL, 7:3 v/v) 중 메틸 2-시아노이소니코티네이트 (0.6 g, 3.7 mmol)의 용액에 0℃에서 첨가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 1시간 동안 추가로 교반하였다. 반응 혼합물을 감압 하에 농축시킨 다음, 물로 희석하였다. 수성 층을 EtOAc로 세척하였다. 수성 층의 pH를 1.5N HCl을 사용하여 ~3으로 조정하고, 유기 생성물을 EtOAc로 추출하였다. 유기 층을 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 2-시아노이소니코틴산 (490 mg, 수율 89%)을 백색 고체로서 수득하였다.
2-(N'-히드록시카르밤이미도일)이소니코틴산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 2-시아노이소니코틴산으로부터 합성하였고 (500 mg, 조물질), 이를 추가 정제 없이 달성하였다.
2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)이소니코틴산
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 2-(N'-히드록시카르밤이미도일)이소니코틴산으로부터 백색 고체로서 합성하였다 (200 mg, 수율 23%).
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)이소니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로판-1-아민 및 2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)이소니코틴산으로부터 합성하였다 (65 mg, 수율 33%).
실시예 44
4-(클로로메틸)-2-(4-플루오로페닐)티아졸
이 화합물을 실시예 39 단계 1에 기재된 바와 같이 4-플루오로티오벤즈아미드 및 1,3-디클로로아세톤으로부터 백색 고체로서 합성하였다 (0.65 g, 수율 89%).
2-(2-(4-플루오로페닐)티아졸-4-일)아세토니트릴
이 화합물을 실시예 39 단계 2에 기재된 바와 같이 4-(클로로메틸)-2-(4-플루오로페닐)티아졸로부터 회백색 고체로서 합성하였다 (0.27 g, 수율 80%).
2-(2-(4-플루오로페닐)티아졸-4-일)-2-메틸프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(2-(4-플루오로페닐)티아졸-4-일)아세토니트릴 및 메틸 아이오다이드로부터 합성하였다 (250 mg, 수율 75%).
2-(2-(4-플루오로페닐)티아졸-4-일)-2-메틸프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(2-(4-플루오로페닐)티아졸-4-일)-2-메틸프로판니트릴로부터 합성하였고 (200 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-플루오로페닐)티아졸-4-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)티아졸-4-일)-2-메틸프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (55 mg, 수율 30%).
실시예 45
N-(2-(2-(4-플루오로페닐)티아졸-4-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)티아졸-4-일)-2-메틸프로판-1-아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (50 mg, 수율 26%).
실시예 46
6-((벤질옥시)카르보닐)피콜린산
2,6-피리딘디카르복실산 (10 g, 0.06 mol) 및 벤질 알콜 (68 mL, 0.66 mol)의 혼합물을 물 (25 mL)에 녹이고, 진한 H2SO4 (3.5 mL)를 첨가하였다. 반응 혼합물을 10시간 동안 환류하고, 추가로 실온에서 24시간 동안 교반되도록 하였다. 반응 혼합물을 감압 하에 농축시키고, 유기 생성물을 CHCl3으로 추출하였다. 용매를 감압 하에 제거하고, 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 CH2Cl2 중 5% MeOH)에 의해 정제하여 6-((벤질옥시)카르보닐)피콜린산 (4.6 g, 수율 30%)을 백색 고체로서 수득하였다.
6-카르바모일피콜린산
포화 NH4OH (100 mL) 중 6-((벤질옥시)카르보닐)피콜린산 (3.0 g, 11.7 mmol)의 용액을 밀봉된 튜브에서 90℃에서 6시간 동안 가열하고, TLC (CHCl3/MeOH 8:2 v/v)에 의해 모니터링하였다. 반응 혼합물을 증발 건조시켜 6-카르바모일피콜린산 (1.8 g, 수율 94%)을 백색 고체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
6-시아노피콜린산
6-카르바모일피콜린산 (1.0 g, 6.0 mmol)을 옥시염화인 (20 mL)에 녹이고, 환류 하에 4시간 동안 가열하였다. 과량의 POCl3을 감압 하에 제거하고, 잔류물을 빙수로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 용매를 감압 하에 제거하여 6-시아노피콜린산 (500 mg, 수율 56%)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
6-(N'-히드록시카르밤이미도일)피콜린산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 6-시아노피콜린산으로부터 합성하였고 (500 mg, 조물질), 이를 추가 정제 없이 달성하였다.
6-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)피콜린산
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 6-(N'-히드록시카르밤이미도일)피콜린산으로부터 회백색 고체로서 합성하였다 (110 mg, 수율 20%).
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-6-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)피콜린아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 6-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)피콜린산 및 2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로판-1-아민으로부터 합성하였다 (55 mg, 수율 56%).
실시예 47
(4-페닐티아졸-2-일)메탄올
수산화칼륨 (1.06 g, 18.84 mmol)을 EtOH (40 mL) 중 벤조산 (4-페닐티아졸-2-일)메틸 벤조에이트 (3.71 g, 12.56 mmol)의 빙냉 용액에 첨가하였다. 반응 혼합물을 실온으로 천천히 가온하고, 1시간 동안 교반되도록 하였다. 반응 혼합물을 감압 하에 농축시킨 다음, 물로 희석하였다. 유기 생성물을 EtOAc로 추출하고, 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 10% EtOAc)에 의해 정제하여 순수한 (4-페닐티아졸-2-일)메탄올 (2.1 g, 수율 87%)을 수득하였다.
4-페닐티아졸-2-카르브알데히드
건조 CH2Cl2 (50 mL) 중 (4-페닐티아졸-2-일)메탄올 (2.1 g, 10.98 mmol)의 용액을 아르곤으로 10분 동안 퍼징하고, 데스-마르틴 퍼아이오디난 (7.0 g, 16.5 mmol)을 용액에 0℃에서 첨가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 추가로 3시간 동안 교반하였다 (TLC에 의해 모니터링함, 석유 에테르/EtOAc 8:2 v/v). 이어서, 반응 혼합물을 포화 티오황산나트륨 용액으로 켄칭하였다. 유기 생성물을 CH2Cl2로 추출하고, 유기 층을 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 알데히드 4-페닐티아졸-2-카르브알데히드 (1.95 g, 수율 94%)를 수득하였으며, 이를 추가 정제 없이 달성하였다.
2-(디메틸아미노)-2-(4-페닐티아졸-2-일)아세토니트릴
시안화나트륨 (124 mg, 2.53 mmol)을 물 (10 mL) 중 디메틸아민 히드로클로라이드 (280 mg, 3.43 mmol)의 용액에 첨가하고, 이어서 메탄올 (20 mL) 중 4-페닐티아졸-2-카르브알데히드 (400 mg, 2.11 mmol)의 용액을 ~25℃에서 온도를 유지하면서 첨가하였다. 반응 혼합물을 동일한 온도에서 추가로 4시간 동안 교반하고, 이어서 이를 물로 희석하고, 유기 생성물을 EtOAc로 추출하였다. 유기 층을 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 조 생성물을 수득하였으며, 이를 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 15% EtOAc)에 의해 정제하여 2-(디메틸아미노)-2-(4-페닐티아졸-2-일)아세토니트릴 (160 mg, 수율 31%)을 수득하였다.
N,N-디메틸-1-(4-페닐티아졸-2-일)에탄-1,2-디아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(디메틸아미노)-2-(4-페닐티아졸-2-일)아세토니트릴로부터 합성하였고 (130 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(디메틸아미노)-2-(4-페닐티아졸-2-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 N,N-디메틸-1-(4-페닐티아졸-2-일)에탄-1,2-디아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (16 mg, 수율 17%).
실시예 48
2-(3-페닐-1H-1,2,4-트리아졸-5-일)에탄아민
보란 디메틸 술피드 착체 (0.2 mL, 2.16 mmol)를 건조 THF (5 mL) 중 화합물 2-(3-페닐-1H-1,2,4-트리아졸-5-일)아세토니트릴 (100 mg, 0.54 mmol)의 용액에 실온에서 첨가하였다. 반응 혼합물을 1시간 동안 환류하고, 이어서 메탄올로 조심스럽게 켄칭하고, 다시 환류 하에 0.5시간 동안 가열하였다. 반응 혼합물을 감압 하에 농축시킨 다음, EtOAc로 희석하였다. 유기 층을 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 2-(3-페닐-1H-1,2,4-트리아졸-5-일)에탄아민 (130 mg, 조물질)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
N-(2-(3-페닐-1H-1,2,4-트리아졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(3-페닐-1H-1,2,4-트리아졸-5-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (17 mg, 수율 21%).
실시예 49
1-(4-페닐티아졸-2-일)시클로프로판카르보니트릴
벤질트리에틸 암모늄 클로라이드 (34 mg, 0.15 mmol) 및 50% 수성 NaOH 용액 (물 1 mL 중에 용해된 0.59 g)을 CH2Cl2 (10 mL) 중 2-(4-페닐티아졸-2-일)아세토니트릴 (0.3 g, 1.5 mmol)의 용액에 첨가하였다. 반응 혼합물을 0℃에서 냉각시키고, 1,2-디브로모에탄 (0.15 mL, 1.79 mmol)을 적가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 10시간 동안 교반하였다. 반응 혼합물을 CH2Cl2로 희석하고, 유기 층을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 5% EtOAc)에 의해 정제하여 1-(4-페닐티아졸-2-일)시클로프로판카르보니트릴 (0.14 g, 수율 41%)을 회백색 고체로서 수득하였다.
(1-(4-페닐티아졸-2-일)시클로프로필)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 1-(4-페닐티아졸-2-일)시클로프로판카르보니트릴로부터 연황색 액체로서 합성하였다 (59 mg, 수율 42%).
N-((1-(4-페닐티아졸-2-일)시클로프로필)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (1-(4-페닐티아졸-2-일)시클로프로필)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (47 mg, 수율 49%).
실시예 50
N'-히드록시-3-니트로벤즈이미드아미드
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 3-니트로벤조니트릴로부터 합성하였고 (5.5 g, 조물질), 이를 추가 정제 없이 달성하였다.
3-(3-니트로페닐)-5-(트리플루오로메틸)-1,2,4-옥사디아졸
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 N'-히드록시-3-니트로벤즈이미드아미드로부터 합성하였고 (1.6 g, 수율 56%), 이를 추가 정제 없이 달성하였다.
3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)아닐린
이아티온산나트륨 (1.61 g, 9.2 mmol) 및 촉매량의 테트라-n-부틸암모늄 브로마이드 (20 mg)를 THF-H2O (30 mL, 1:1 v/v) 중 3-(3-니트로페닐)-5-(트리플루오로메틸)-1,2,4-옥사디아졸 (1.6 g, 6.1 mmol)의 용액에 첨가하고, 반응 혼합물을 실온에서 2시간 동안 교반하고, TLC (석유 에테르/EtOAc 1:1)에 의해 모니터링하였다. 용매를 감압 하에 제거하고, 생성물을 EtOAc로 추출하였다. 유기 층을 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 30-35% EtOAc)에 의해 정제하여 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)아닐린 (0.8 g, 수율 57%)을 수득하였다.
메틸 4-아미노-4-티옥소부타노에이트
메틸 숙신아메이트 (2 g, 15.2 mmol)를 건조 THF (50 mL) 중에 용해시키고, P2S5 (3.4 g, 15.2 mmol)를 첨가하고, 반응 혼합물을 실온에서 6시간 동안 교반하였다. 반응 혼합물을 소결 깔때기를 통해 여과하고, 투명한 여과물을 감압 하에 농축시켜 조 생성물을 수득하였으며, 이를 추가로 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 50% EtOAc)에 의해 정제하여 메틸 4-아미노-4-티옥소부타노에이트 (1.25 g, 수율 53%)를 백색 고체로서 수득하였다.
에틸 3-(4-(4-플루오로페닐)티아졸-2-일)프로파노에이트
EtOH (10 mL) 중 메틸 4-아미노-4-티옥소부타노에이트 (0.3 g, 2.03 mmol) 및 2-브로모-4-플루오로아세토페논 (0.440 g, 2.03 mmol)의 혼합물을 3시간 동안 환류하였다. 반응 혼합물을 실온으로 냉각시키고, 용매를 감압 하에 제거하였다. 유기 생성물을 EtOAc로 추출하고, 유기 층을 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 8-10% EtOAc)에 의해 정제하여 에틸 3-(4-(4-플루오로페닐)티아졸-2-일)프로파노에이트 (0.45 g, 7%의 메틸 에스테르 생성물을 함유하는 조물질)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
3-(4-(4-플루오로페닐)티아졸-2-일)프로판산
1N NaOH (5 mL)를 MeOH (5 mL) 중 조 에틸 3-(4-(4-플루오로페닐)티아졸-2-일)프로파노에이트 (450 mg, 1.61 mmol)의 빙냉된 용액에 첨가하고, 용액을 실온에서 1시간 동안 교반되도록 하였다. 용매를 증발시키고, 반응 혼합물을 물로 희석하였다. 수성 층을 EtOAc로 세척하고, 수용액의 pH를 1N HCl을 사용하여 ~2로 조정하였다. 유기 생성물을 EtOAc로 추출하고, 유기 층을 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 3-(4-(4-플루오로페닐)티아졸-2-일)프로판산 (320 mg, 수율 79%)을 백색 고체로서 수득하였다.
3-(4-(4-플루오로페닐)티아졸-2-일)-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)페닐)프로판아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)아닐린 및 3-(4-(4-플루오로페닐)티아졸-2-일)프로판산으로부터 합성하였다 (80 mg, 수율 43%).
실시예 51
N-(2-(2-(4-클로로페닐)티아졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-클로로페닐)티아졸-4-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (40 mg, 수율 22%).
실시예 52
N-((4-페닐티아졸-2-일)메틸)벤즈아미드
EtOH (10 mL) 중 N-(2-아미노-2-티옥소에틸)벤즈아미드 (300 mg, 1.54 mmol) 및 2-브로모아세토페논 (305 mg, 1.54 mmol)의 혼합물을 80℃로 2시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 용매를 감압 하에 증발시켰다. 농축된 반응 혼합물을 EtOAc로 희석하고, 유기 층을 H2O 및 염수로 세척하고, 감압 하에 농축시켜 N-((4-페닐티아졸-2-일)메틸)벤즈아미드 (0.4 g, 수율 88%)를 백색 고체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
(4-페닐티아졸-2-일)메탄아민
6N HCl (4.5 mL)을 디옥산 (10 mL) 중 N-((4-페닐티아졸-2-일)메틸)벤즈아미드 (150 mg, 0.51 mmol)의 용액에 첨가하고, 반응 혼합물을 100℃에서 24시간 동안 교반하였다 (반응을 TLC에 의해 모니터링함, 용리액 CHCl3/MeOH). 반응 혼합물을 감압 하에 농축시키고, 잔류물을 물 중에 용해시켰다. 수성 층을 EtOAc로 2회 세척하였다. 이어서, 수성 층의 pH를 10% NaHCO3을 사용하여 pH ~9로 조정하고, 유기 생성물을 EtOAc로 추출하였다. 유기 층을 염수로 세척하고, 감압 하에 농축시켜 (4-페닐티아졸-2-일)메탄아민 (75 mg, 수율 77%)을 오렌지색 액체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
N-((4-페닐티아졸-2-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-페닐티아졸-2-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 백색 고체로서 합성하였다 (60 mg, 수율 38%).
실시예 53
N-(2-(4-(4-플루오로페닐)티아졸-2-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(4-(4-플루오로페닐)티아졸-2-일)에탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (50 mg, 수율 29%).
실시예 54
2-(4-(4-클로로페닐)티아졸-2-일)에탄아민
이 화합물을 실시예 42 단계 1에 기재된 바와 같이 2-(4-(4-클로로페닐)티아졸-2-일)아세토니트릴로부터 합성하였고 (400 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(4-(4-클로로페닐)티아졸-2-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(4-(4-클로로페닐)티아졸-2-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (30 mg, 수율 16%).
실시예 55
N-(2-(4-(4-클로로페닐)티아졸-2-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(4-(4-클로로페닐)티아졸-2-일)에탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (65 mg, 수율 35%).
실시예 56
4-(3,4-디히드로이소퀴놀린-2(1H)-일)테트라히드로-2H-피란-4-카르보니트릴
3,4,5,6-테트라히드로-4H-피란-4-온 (0.37 g, 3.75 mmol)을 진한 HCl (0.4 mL) 중 1,2,3,4-테트라히드로이소퀴놀린 (0.47 mL, 3.75 mmol)의 용액에 첨가하고, 빙수 (1.5 mL)로 희석하고, 이어서 물 (2 mL) 중에 용해된 KCN (0.24 g, 3.75 mmol)의 용액을 첨가하고, 반응 혼합물을 실온에서 2시간 동안 교반하였다. 이어서, 반응 혼합물을 물로 희석하고, 유기 생성물을 EtOAc로 추출하였다. 유기 층을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 6% EtOAc)에 의해 정제하여 4-(3,4-디히드로이소퀴놀린-2(1H)-일)테트라히드로-2H-피란-4-카르보니트릴 (300 mg, 수율 33%)을 수득하였다.
(4-(3,4-디히드로이소퀴놀린-2(1H)-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(3,4-디히드로이소퀴놀린-2(1H)-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였다 (80 mg, 수율 26%).
N-((4-(3,4-디히드로이소퀴놀린-2(1H)-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(3,4-디히드로이소퀴놀린-2(1H)-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (40 mg, 수율 30%).
실시예 57
N-메틸-1-(4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
(4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 (300 mg, 1.1 mmol)을 1,2-디클로로에탄 (30 mL) 중에 용해시키고, 0℃로 냉각시켰다. 포르말린 용액 (~0.1 mL, 35%)을 상기 용액에 첨가하고, 이어서 나트륨트리아세톡시 보로히드라이드 (0.16 g, 0.76 mmol)를 첨가하였다. 반응 혼합물을 추가로 동일한 온도를 유지하면서 45분 동안 교반하였다. 이어서, 반응 혼합물을 10% NaHCO3 용액으로 켄칭하고, CH2Cl2로 희석하였다. 유기 층을 분리하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 잔류물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 CHCl3 중 10-20% MeOH)에 의해 정제하여 N-메틸-1-(4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 (120 mg, 수율 38%)을 수득하였다.
N-메틸-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 N-메틸-1-(4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (30 mg, 수율 14%).
실시예 58
2-(2-(4-플루오로페닐)티아졸-4-일)에탄아민
이 화합물을 실시예 42 단계 1에 기재된 바와 같이 2-(2-(4-플루오로페닐)티아졸-4-일)아세토니트릴로부터 합성하였고 (150 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-플루오로페닐)티아졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)티아졸-4-일)에탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (30 mg, 수율 17%).
실시예 59
N-(2-(2-(4-플루오로페닐)티아졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)티아졸-4-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (60 mg, 수율 45%).
실시예 60
N-(2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(4-(4-플루오로페닐)티아졸-2-일)-2-메틸프로판-1-아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (55 mg, 수율 42%).
실시예 61
3-(2,2,2-트리플루오로-1-(((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)이미노)에틸)벤조니트릴
트리에틸아민 (1.0 mL, 2.7 mmol)을 건조 CH2Cl2 (25 mL) 중 3-시아노-2,2,2-트리플루오로아세토페논 (0.48 g, 2.4 mmol) 및 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 (0.66 g, 2.4 mmol)의 용액에 첨가하고, 이어서 0℃에서 CH2Cl2 중 사염화티타늄의 용액 (1.2 mL, 1.2 mmol, CH2Cl2 중 1M 용액)을 첨가하고, 반응 혼합물을 실온으로 가온하고, 8시간 동안 추가로 교반하였다. 반응물을 감압 하에 농축시키고, 유기 생성물을 EtOAc로 추출하였다. 유기 층을 물 및 염수 용액으로 세척하고, 무수 황산나트륨 상에서 건조시키고, 용매를 감압 하에 제거하여 3-(2,2,2-트리플루오로-1-(((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)이미노)에틸)벤조니트릴 (0.6 g, 조물질)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
3-(2,2,2-트리플루오로-1-(((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)아미노)에틸)벤조니트릴
3-(2,2,2-트리플루오로-1-(((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)이미노)에틸)벤조니트릴 (600 mg, 1.3 mmol)을 MeOH-H2O (20 mL, 8:2 v/v) 중에 용해시키고, 0℃로 냉각시켰다. 수소화붕소나트륨 (250 mg, 6.6 mmol)을 이 용액에 조금씩 첨가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 2시간 동안 교반한 다음, 물로 켄칭하고, 감압 하에 농축시켜 MeOH를 제거하였다. 수성 혼합물을 EtOAc로 희석하고, 유기 층을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 15-20% EtOAc)에 의해 정제하여 3-(2,2,2-트리플루오로-1-(((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)아미노)에틸)벤조니트릴 (300 mg, 수율 50%)을 수득하였다.
N'-히드록시-3-(2,2,2-트리플루오로-1-(((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)아미노)에틸)벤즈이미드아미드
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 3-(2,2,2-트리플루오로-1-(((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)아미노)에틸)벤조니트릴 산으로부터 합성하였고 (300 mg, 조물질), 이를 추가 정제 없이 달성하였다.
2,2,2-트리플루오로-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-1-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)페닐)에탄아민
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 N'-히드록시-3-(2,2,2-트리플루오로-1-(((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)아미노)에틸)벤즈이미드아미드 산으로부터 합성하였다 (70 mg, 수율 20%).
실시예 62
메틸 4-플루오로벤즈이미데이트 히드로클로라이드
건조 HCl (g)을 건조 MeOH-CH2Cl2 (20 mL, 1:1 v/v) 중 4-플루오로벤조니트릴 (5.0 g, 0.041 mol)의 용액을 통해 포화될 때까지 버블링하였다. 투명한 용액을 0℃에서 2일 동안 정치시켜 히드로클로라이드 염으로서 메틸 4-플루오로벤즈이미데이트를 결정화시키고, 이를 여과에 의해 단리시켰다 (2.8 g, 수율 36%).
2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)아세토니트릴
2-시아노아세토히드라지드 (172 mg, 1.74 mmol) 및 NaOH (66 mg, 1.66 mmol)를 건조 MeOH (5 mL) 중 메틸 4-플루오로벤즈이미데이트 히드로클로라이드 (300 mg, 1.58 mmol)의 용액에 첨가하고, 혼합물을 환류 하에 1시간 동안 가열하였다. 반응 혼합물을 감압 하에 농축시키고, 수득한 잔류물을 EtOAc로 희석하였다. 유기 층을 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 20-25% EtOAc)에 의해 정제하여 2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)아세토니트릴 (150 mg, 수율 47%)을 수득하였다.
2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)에탄아민
이 화합물을 실시예 42 단계 1에 기재된 바와 같이 2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)아세토니트릴로부터 합성하였고 (40 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (11 mg, 수율 13%).
실시예 63
메틸 4-클로로벤즈이미데이트 히드로클로라이드
이 화합물을 실시예 62 단계 1에 기재된 바와 같이 4-클로로벤조니트릴로부터 합성하였다 (3.5 g, 47%).
2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)아세토니트릴
이 화합물을 실시예 62 단계 2에 기재된 바와 같이 메틸 4-클로로벤즈이미데이트 히드로클로라이드로부터 합성하였다 (200 mg, 수율 38%).
2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)에탄아민
이 화합물을 실시예 42 단계 1에 기재된 바와 같이 2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)아세토니트릴로부터 합성하였고 (90 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (15 mg, 수율 13%).
실시예 64
메틸 2-시아노-2-메틸프로파노에이트
NaH (15.5 g, 오일 중 60% 분산액)를 건조 DMF (300 mL) 중 에틸 시아노아세테이트 (20 g, 0.177 mol)의 용액에 0℃에서 10분에 걸쳐 조금씩 첨가하였다. 생성된 반응 혼합물을 실온에서 30분 동안 교반하고, 0℃로 다시 냉각시켰다. THF (50 mL) 중 메틸 아이오다이드 (28 mL, 0.44 mol)를 적가하고, 반응 혼합물을 실온에서 12시간 동안 교반한 다음, 포화 NH4Cl 용액으로 켄칭하였다. 이어서, 혼합물을 EtOAc로 희석하고; 유기 층을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 조 생성물을 수득하였으며, 이를 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 5% EtOAc)에 의해 정제하여 메틸 2-시아노-2-메틸프로파노에이트 (12 g, 수율 48%)를 연황색 고체로서 수득하였다.
2-시아노-2-메틸프로판히드라지드
히드라진 수화물 (1.8 mL, 35 mmol)을 EtOH (5 mL) 중 메틸 2-시아노-2-메틸프로파노에이트 (5.0 g, 35.0 mmol)의 용액에 첨가하고, 반응 혼합물을 실온에서 1시간 동안 교반하였다 (TLC에 의해 모니터링함, 용리액 석유 에테르:EtOAc 7:3 v/v). 반응 혼합물을 디에틸 에테르로 희석하고, 형성된 침전물을 여과하였다. 투명한 여과물을 감압 하에 농축시켜 2-시아노-2-메틸프로판히드라지드 (1.75 g, 수율 38%)를 수득하였으며, 이를 추가 정제 없이 달성하였다.
2-메틸-2-(3-페닐-1H-1,2,4-트리아졸-5-일)프로판니트릴
2-시아노-2-메틸프로판히드라지드 (100 mg, 0.78 mmol) 및 Et3N (0.1 mL, 0.86 mmol)을 건조 MeOH (10 mL) 중 메틸 벤즈이미데이트 히드로클로라이드 (100 mg, 0.58 mmol)의 용액에 첨가하고, 혼합물을 환류 하에 1시간 동안 가열하였다. 이어서, 반응 혼합물을 감압 하에 농축시키고, 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 15% EtOAc)에 의해 정제하여 2-메틸-2-(3-페닐-1H-1,2,4-트리아졸-5-일)프로판니트릴 (80 mg, 수율 51%)을 수득하였다.
2-메틸-2-(3-페닐-1H-1,2,4-트리아졸-5-일)프로판-1-아민
DIBAL-H (0.75 mL, 0.75 mmol, THF 중 1M)를 건조 THF (5 mL) 중 2-메틸-2-(3-페닐-1H-1,2,4-트리아졸-5-일)프로판니트릴 (80 mg, 0.37 mmol)의 용액에 0℃에서 첨가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 2시간 동안 추가로 교반하였다. 이어서, 반응 혼합물을 물로 조심스럽게 켄칭하고, EtOAc로 희석하였다. 유기 층을 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 2-메틸-2-(3-페닐-1H-1,2,4-트리아졸-5-일)프로판-1-아민 (70 mg, 조물질)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
N-(2-메틸-2-(3-페닐-1H-1,2,4-트리아졸-5-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-메틸-2-(3-페닐-1H-1,2,4-트리아졸-5-일)프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (35 mg, 수율 25%).
실시예 65
N-(2-메틸-2-(3-페닐-1H-1,2,4-트리아졸-5-일)프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-메틸-2-(3-페닐-1H-1,2,4-트리아졸-5-일)프로판-1-아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (20 mg, 수율 23%).
실시예 66
2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로판니트릴
이 화합물을 실시예 64 단계 3에 기재된 바와 같이 2-시아노-2-메틸프로판히드라지드 및 메틸 4-플루오로벤즈이미데이트 히드로클로라이드로부터 합성하였다 (300 mg, 수율 70%).
2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로판-1-아민
이 화합물을 실시예 64 단계 4에 기재된 바와 같이 2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로판니트릴로부터 합성하였고 (200 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (12 mg, 수율 7%).
실시예 67
N-(2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로판-1-아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (20 mg, 수율 11%).
실시예 68
2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로판니트릴
이 화합물을 실시예 64 단계 3에 기재된 바와 같이 2-시아노-2-메틸프로판히드라지드 및 메틸 4-클로로벤즈이미데이트 히드로클로라이드로부터 합성하였다 (220 mg, 수율 55%).
2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로판-1-아민
이 화합물을 실시예 64 단계 4에 기재된 바와 같이 2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로판니트릴로부터 합성하였고 (140 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(3-(4-클로로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (15 mg, 수율 8%).
실시예 69
에틸 5-시아노-6-메틸니코티네이트
염화암모늄 (3.58 g, 10 mL 물 중 66.7 mmol)을 디옥산-THF-DMF (50 mL, 3:1:1) 중 에틸 2-클로로-5-시아노-6-메틸니코티네이트 (1.0 g, 4.4 mmol)의 용액에 첨가하고, 이어서 실온에서 조금씩 아연 분말 (2.3 g, 35.6 mmol)을 첨가하였다. 반응 혼합물을 실온에서 3시간 동안 교반되도록 하고, EtOAc로 희석하고, 셀라이트의 패드를 통해 여과하였다. 유기 층의 투명한 여과물을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 10-15% EtOAc)에 의해 정제하여 에틸 5-시아노-6-메틸니코티네이트 (230 mg, 수율 27%)를 백색 고체로서 수득하였다.
5-시아노-6-메틸니코틴산
이 화합물을 실시예 43 단계 2에 기재된 바와 같이 에틸 5-시아노-6-메틸니코티네이트로부터 백색 고체로서 합성하였다 (150 mg, 수율 76%).
5-(N'-히드록시카르밤이미도일)-6-메틸니코틴산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 5-시아노-6-메틸니코틴산으로부터 합성하였고 (130 mg, 조물질), 이를 추가 정제 없이 달성하였다.
6-메틸-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 5-(N'-히드록시카르밤이미도일)-6-메틸니코틴산으로부터 백색 고체로서 합성하였다 (25 mg, 수율 15%).
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-6-메틸-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로판-1-아민 및 6-메틸-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (28 mg, 수율 59%).
실시예 70
메틸 4-아미노-4-티옥소부타노에이트
THF (60 mL) 중 메틸 숙신아메이트 (2.5 g, 0.019 mol)의 용액을 0℃로 냉각시키고, P2S5 (4.2 g, 0.019 mol)를 첨가하였다. 반응 혼합물을 실온으로 가온하고, 6시간 동안 교반하였다. 용매를 감압 하에 제거하고, 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 35-40% EtOAc)에 의해 정제하여 메틸 4-아미노-4-티옥소부타노에이트 (1.6 g, 수율 57%)를 수득하였다.
에틸 3-(4-페닐티아졸-2-일)프로파노에이트
EtOH (15 mL) 중 2-브로모 아세토페논 (2.1 g, 10.55 mmol) 및 메틸 4-아미노-4-티옥소부타노에이트 (1.6 g, 10.86 mmol)의 혼합물을 80℃로 3시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 용매를 감압 하에 증발시켰다. 생성물을 EtOAc로 추출하고, 유기 층을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 에틸 3-(4-페닐티아졸-2-일)프로파노에이트 (1.1 g, 수율 40%)를 백색 고체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
3-(4-페닐티아졸-2-일)프로판-1-올
MeOH-H2O (10 mL, 9:1 v/v) 중 에틸 3-(4-페닐티아졸-2-일)프로파노에이트 (0.5 g, 1.91 mmol)의 용액을 0℃로 냉각시키고, 수소화붕소나트륨 (0.29 g, 7.65 mmol)을 첨가하였다. 반응 혼합물을 실온으로 가온하고, 8시간 동안 추가로 교반하였다. 혼합물을 빙수로 켄칭하고, 유기 생성물을 EtOAc로 추출하였다. 합한 추출물을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 3-(4-페닐티아졸-2-일)프로판-1-올 (0.4 g, 수율 95%)을 무색 액체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
3-(4-페닐티아졸-2-일)프로필 메탄술포네이트
건조 피리딘 (8 mL) 중 3-(4-페닐티아졸-2-일)프로판-1-올 (0.4 g, 1.82 mmol)의 용액을 0℃로 냉각시키고, 메탄술포닐 클로라이드 (0.43 mL, 5.47 mmol)를 적가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 1시간 동안 교반하고, 빙수로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 유기 층을 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 3-(4-페닐티아졸-2-일)프로필 메탄술포네이트 (0.4 g, 수율 74%)를 연황색 액체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
2-(3-아지도프로필)-4-페닐티아졸
나트륨 아지드 (263 mg, 4.05 mmol)를 건조 DMF (8 mL) 중 3-(4-페닐티아졸-2-일)프로필 메탄술포네이트 (0.4 g, 1.35 mmol)의 용액에 첨가하고, 반응 혼합물을 100℃로 2시간 동안 가열하였다. 혼합물을 실온으로 냉각되도록 하고, EtOAc로 희석하였다. 유기 생성물을 EtOAc로 추출하고, 유기 층을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 2-(3-아지도프로필)-4-페닐티아졸 (0.3 g, 수율 91%)을 연한 오렌지색 액체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
3-(4-페닐티아졸-2-일)프로판-1-아민
트리페닐포스핀 (485 mg, 1.85 mmol)을 THF-H2O (10 mL, 8:2 v/v) 중 2-(3-아지도프로필)-4-페닐티아졸 (0.3 g, 1.23 mmol)의 용액에 0℃에서 첨가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 8시간 동안 교반한 다음, 감압 하에 농축시켰다. 잔류물을 1.5N HCl로 희석하고, 수성 층을 CH2Cl2로 세척하였다. 수성 층의 pH를 10% NaOH 용액을 사용하여 ~8-9로 조정하고, 유기 생성물을 CH2Cl2로 추출하였다. 합한 추출물을 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 3-(4-페닐티아졸-2-일)프로판-1-아민 (240 mg, 수율 89%)을 연황색 액체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
N-(3-(4-페닐티아졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 3-(4-페닐티아졸-2-일)프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (100 mg, 수율 70%).
실시예 71
4-(클로로메틸)-2-(4-플루오로페닐)옥사졸
EtOH-THF (20 mL-10 mL) 중 4-플루오로벤즈아미드 (2.5 g, 17.9 mmol) 및 1,3-디클로로아세톤 (2.7 g, 21.6 mmol)의 혼합물을 85℃로 24시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 10% NaHCO3 용액으로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 유기 층을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 6-10% EtOAc)에 의해 정제하여 4-(클로로메틸)-2-(4-플루오로페닐)옥사졸 (1.2 g, 수율 32%)을 백색 고체로서 수득하였다.
2-(2-(4-플루오로페닐)옥사졸-4-일)아세토니트릴
KI (3.14 g, 18.9 mmol)를 건조 DMF (20 mL) 중 4-(클로로메틸)-2-(4-플루오로페닐)옥사졸 (1.0 g, 4.7 mmol)의 용액에 실온에서 첨가하였다. 반응 혼합물을 30분 동안 교반하고, EtOAc로 희석하고, 물 및 염수로 세척하였다. 유기 층을 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 조 2-(4-플루오로페닐)-4-(아이오도메틸)옥사졸을 수득하였다. 조 생성물을 DMF (20 mL) 중에 용해시키고, 시안화나트륨 (0.46 g, 9.4 mmol)을 용액에 첨가하였다. 반응 혼합물을 실온에서 6시간 동안 교반하고, 물로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 유기 층을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 10-15% EtOAc)에 의해 정제하여 2-(2-(4-플루오로페닐)옥사졸-4-일)아세토니트릴 (0.75 g, 수율 78%)을 회백색 고체로서 수득하였다.
2-(2-(4-플루오로페닐)옥사졸-4-일)에탄아민
이 화합물을 실시예 64 단계 4에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)아세토니트릴로부터 합성하였고 (120 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)에탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (55 mg, 수율 46%).
실시예 72
에틸 2-옥소-2-((2-옥소-2-페닐에틸)아미노)아세테이트
트리에틸아민 (36 mL, 262.1 mmol)을 건조 CH2Cl2 (300 mL) 중 2-아미노아세토페논 히드로클로라이드 (15.0 g, 87.39 mmol)의 용액에 첨가하고, 이어서 에틸 클로로옥소아세테이트 (10 mL, 87.39 mmol)를 0℃에서 첨가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 16시간 동안 교반하였다. 이어서, 혼합물을 물로 희석하고, EtOAc로 추출하였다. 합한 추출물을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 20-30% EtOAc)에 의해 정제하여 에틸 2-옥소-2-((2-옥소-2-페닐에틸)아미노)아세테이트 (13.5 g, 수율 66%)를 수득하였다.
에틸 5-페닐티아졸-2-카르복실레이트
P2S5 (25.5 g, 114.7 mmol)를 건조 CHCl3 (150 mL) 중 에틸 2-옥소-2-((2-옥소-2-페닐에틸)아미노)아세테이트 (13.5 g, 57.39 mmol)의 용액에 첨가하고, 생성된 반응 혼합물을 환류 하에 5시간 동안 가열하였다. 반응 혼합물을 물로 켄칭하고, 유기 생성물을 CHCl3으로 추출하였다. 합한 추출물을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 10-15% EtOAc)에 의해 정제하여 에틸 5-페닐티아졸-2-카르복실레이트 (10 g, 수율 75%)를 백색 고체로서 수득하였다.
(5-페닐티아졸-2-일)메탄올
이 화합물을 실시예 64 단계 4에 기재된 바와 같이 에틸 5-페닐티아졸-2-카르복실레이트로부터 합성하였고 (3.5 g, 수율 71%), 이를 추가 정제 없이 달성하였다.
2-(브로모메틸)-5-페닐티아졸
CBr4 (8.65 g, 26.1 mmol) 및 Ph3P (5.1 g, 19.6 mmol)를 건조 CH2Cl2 (30 mL) 중 (5-페닐티아졸-2-일)메탄올 (2.5 g, 13.07 mmol)의 용액에 0℃에서 첨가하였다. 생성된 반응 혼합물을 실온에서 1시간 동안 교반한 다음, 감압 하에 농축시켰다. 잔류물을 디에틸 에테르로 희석하고, 여과하였다. 투명한 여과물을 감압 하에 제거하고, 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 5-10% EtOAc)에 의해 정제하여 2-(브로모메틸)-5-페닐티아졸 (2 g, 수율 60%)을 수득하였다.
2-(5-페닐티아졸-2-일)아세토니트릴
NaCN (0.46 g, 9.4 mmol)을 건조 EtOH (10 mL) 중 2-(브로모메틸)-5-페닐티아졸 (2.0 g, 7.87 mmol)의 용액에 첨가하였다. 생성된 반응 혼합물을 70℃에서 2시간 동안 교반한 다음, 감압 하에 농축시키고, 에틸 아세테이트로 희석하였다. 유기 층을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 10% EtOAc)에 의해 정제하여 2-(5-페닐티아졸-2-일)아세토니트릴 (350 mg, 수율 22%)을 백색 고체로서 수득하였다.
2-(5-페닐티아졸-2-일)에탄아민
이 화합물을 실시예 42 단계 1에 기재된 바와 같이 2-(5-페닐티아졸-2-일)아세토니트릴로부터 합성하였고 (100 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(5-페닐티아졸-2-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(5-페닐티아졸-2-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (7 mg, 수율 5%).
실시예 73
2-(2-(4-플루오로페닐)옥사졸-4-일)프로판니트릴
NaH (360 mg, 오일 중 60% 분산액)를 건조 THF (60 mL) 중 2-(2-(4-플루오로페닐)옥사졸-4-일)아세토니트릴 (1.5 g, 7.42 mmol)의 용액에 0℃에서 5분에 걸쳐 조금씩 첨가하였다. 생성된 반응 혼합물을 천천히 실온으로 가온되도록 하고, 1시간 동안 교반하였다. 반응 혼합물을 다시 0℃로 냉각시키고, 건조 THF (10 mL) 중 메틸 아이오다이드 (0.5 mL, 7.4 mmol)의 용액을 0℃에서 30분에 걸쳐 적가하였다. 반응 혼합물을 0℃에서 1시간 동안 교반한 다음, 실온에서 추가로 1시간 동안 교반하였다. 반응 혼합물을 포화 NH4Cl 용액으로 켄칭하고, EtOAc로 희석하고, 추가로 EtOAc로 추출하였다. 합한 추출물을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 10% EtOAc)에 의해 정제하여 2-(2-(4-플루오로페닐)옥사졸-4-일)프로판니트릴 (360 mg, 수율 23%)을 수득하였다.
2-(2-(4-플루오로페닐)옥사졸-4-일)프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)프로판니트릴로부터 합성하였고 (320 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 황색 고체로서 합성하였다 (95 mg, 수율 36%).
실시예 74
4-(클로로메틸)-2-(3-플루오로페닐)옥사졸
1,3-디클로로아세톤 (3.65 g, 28.75 mmol)을 건조 톨루엔 (20 mL) 중 3-플루오로벤즈아미드 (2 g, 14.37 mmol)의 용액에 첨가하였다. 생성된 반응 혼합물을 100℃에서 5시간 동안 교반하였다. 반응 혼합물을 감압 하에 농축시키고, 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 10% EtOAc)에 의해 정제하여 4-(클로로메틸)-2-(3-플루오로페닐)옥사졸 (1.2 g, 수율 39%)을 황색 액체로서 수득하였다.
2-(2-(3-플루오로페닐)옥사졸-4-일)아세토니트릴
이 화합물을 실시예 71 단계 2에 기재된 바와 같이 4-(클로로메틸)-2-(3-플루오로페닐)옥사졸로부터 합성하였다 (0.15 g, 수율 35%).
2-(2-(3-플루오로페닐)옥사졸-4-일)에탄아민
이 화합물을 실시예 42 단계 1에 기재된 바와 같이 2-(2-(3-플루오로페닐)옥사졸-4-일)아세토니트릴로부터 합성하였고 (120 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(3-플루오로페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(3-플루오로페닐)옥사졸-4-일)에탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (15 mg, 수율 9%).
실시예 75
메틸 6-클로로-5-시아노-2-메틸니코티네이트
메틸-5-시아노-6-히드록시-2-메틸니코티네이트 (2.0 g, 10.41 mmol), POCl3 (40 mL) 및 PCl5 (1.08 g, 5.2 mmol)의 혼합물을 110℃로 24시간 동안 가열하였다. 반응 혼합물을 감압 하에 농축시키고, 빙수로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 유기 층을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 10-15% EtOAc)에 의해 정제하여 메틸 6-클로로-5-시아노-2-메틸니코티네이트 (1.5 g, 수율 68%)를 수득하였다.
메틸 5-시아노-2-메틸니코티네이트
이 화합물을 실시예 69 단계 1에 기재된 바와 같이 메틸 6-클로로-5-시아노-2-메틸니코티네이트로부터 합성하였다 (230 mg, 수율 23%).
5-시아노-2-메틸니코틴산
이 화합물을 실시예 69 단계 2에 기재된 바와 같이 메틸 5-시아노-2-메틸니코티네이트로부터 백색 고체로서 합성하였다 (175 mg, 수율 83%).
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-5-시아노-2-메틸니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로판-1-아민 및 5-시아노-2-메틸니코틴산으로부터 합성하였다 (200 mg, 수율 46%).
5-((2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)카르바모일)-6-메틸니코티노히드라조산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 메틸 5-시아노-2-메틸니코티네이트로부터 합성하였고 (200 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-2-메틸-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 5-((2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)카르바모일)-6-메틸니코티노히드라조산으로부터 합성하였다 (20 mg, 수율 9%).
실시예 76
2-메틸-2-(5-페닐티아졸-2-일)프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(5-페닐티아졸-2-일)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였다 (200 mg, 수율 58%).
2-메틸-2-(5-페닐티아졸-2-일)프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-메틸-2-(5-페닐티아졸-2-일)프로판니트릴로부터 합성하였고 (70 mg, 수율 34%), 이를 추가 정제 없이 달성하였다.
N-(2-메틸-2-(5-페닐티아졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-메틸-2-(5-페닐티아졸-2-일)프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (20 mg, 수율 17%).
실시예 77
2-([1,1'-비페닐]-3-일)아세토니트릴
NaCN (1.1 g, 22.26 mmol)을 건조 DMF (100 mL) 중 3-페닐벤질 브로마이드 (5.0 g, 20.23 mmol)의 용액에 첨가하였다. 생성된 반응 혼합물을 실온에서 3시간 동안 교반한 다음, 물로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 합한 추출물을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 5% EtOAc)에 의해 정제하여 2-([1,1'-비페닐]-3-일)아세토니트릴 (3.8 g, 수율 97%)을 수득하였다.
4-([1,1'-비페닐]-3-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 2-브로모에틸 에테르를 사용하여 실시예 1 단계 2에 기재된 바와 같이 2-([1,1'-비페닐]-3-일)아세토니트릴로부터 합성하였다 (0.5 g, 73%).
(4-([1,1'-비페닐]-3-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-([1,1'-비페닐]-3-일)테트라히드로-2H-피란-4-카르보니트릴로부터 연황색 오일로서 합성하였다 (230 mg, 수율 46%).
N-((4-([1,1'-비페닐]-3-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-([1,1'-비페닐]-3-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 백색 고체로서 합성하였다 (110 mg, 수율 56%).
실시예 78
N-((4-([1,1'-비페닐]-3-일)테트라히드로-2H-피란-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-([1,1'-비페닐]-3-일)테트라히드로-2H-피란-4-일)메탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 백색 고체로서 합성하였다 (95 mg, 수율 48%).
실시예 79
2-(4-플루오로페닐)-4-(아이오도메틸)옥사졸
KI (3.14 g, 18.9 mmol)를 건조 DMF (10 mL) 중 4-클로로메틸-2-(4-플루오로페닐)-옥사졸 (1 g, 4.7 mmol)의 용액에 실온에서 첨가하였다. 생성된 반응 혼합물을 30분 동안 교반한 다음, EtOAc로 희석하였다. 혼합물을 EtOAc로 추출하고, 합한 추출물을 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 2-(4-플루오로페닐)-4-(아이오도메틸)옥사졸 (1.2 g, 조물질)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
4-(아지도메틸)-2-(4-플루오로페닐)옥사졸
건조 DMF (10 mL) 중 2-(4-플루오로페닐)-4-(아이오도메틸)옥사졸 (1.2 g, 3.96 mmol)의 용액에 나트륨 아지드 (515 mg, 7.9 mmol)를 첨가하고, 반응 혼합물을 70℃로 8시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각되도록 하고, EtOAc로 희석하였다. 혼합물을 EtOAc로 추출하고, 합한 추출물을 물 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 4-(아지도메틸)-2-(4-플루오로페닐)옥사졸 (0.73 g, 수율 85%)을 연한 오렌지색 액체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
(2-(4-플루오로페닐)옥사졸-4-일)메탄아민
THF-H2O (15 mL, 8:2 v/v) 중 4-(아지도메틸)-2-(4-플루오로페닐)옥사졸 (0.5 g, 2.3 mmol)의 용액을 0℃로 냉각시키고, 트리페닐포스핀 (892 mg, 3.4 mmol)을 첨가하였다. 반응 혼합물을 실온으로 가온되도록 한 다음, 4시간 동안 교반하였다. 반응 혼합물을 감압 하에 농축시키고, 잔류물을 1.5N HCl로 희석하였다. 수성 층을 CH2Cl2로 세척한 다음, 수성 층의 pH를 10% NaOH 용액을 사용하여 ~ 8-9로 조정하였다. 유기 생성물을 CH2Cl2로 추출하고, 유기 층을 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 (2-(4-플루오로페닐)옥사졸-4-일)메탄아민 (330 mg, 수율 75%)을 연황색 액체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
N-((2-(4-플루오로페닐)옥사졸-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (2-(4-플루오로페닐)옥사졸-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 백색 고체로서 합성하였다 (65 mg, 수율 26%).
실시예 80
4-(2-(4-플루오로페닐)옥사졸-4-일)-1-메틸피페리딘-4-카르보니트릴
이 화합물을 실시예 16 단계 1b에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)아세토니트릴 및 2-클로로-N-(2-클로로에틸)-N-메틸에탄아민 히드로클로라이드로부터 합성하였다 (430 mg, 수율 30%).
(4-(2-(4-플루오로페닐)옥사졸-4-일)-1-메틸피페리딘-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(2-(4-플루오로페닐)옥사졸-4-일)-1-메틸피페리딘-4-카르보니트릴로부터 합성하였고 (170 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-((4-(2-(4-플루오로페닐)옥사졸-4-일)-1-메틸피페리딘-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(2-(4-플루오로페닐)옥사졸-4-일)-1-메틸피페리딘-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (50 mg, 수율 24%).
실시예 81
4-(클로로메틸)-2-페닐옥사졸
이 화합물을 실시예 71 단계 1에 기재된 바와 같이 1,3-디클로로아세톤 및 벤즈아미드로부터 백색 고체로서 합성하였다 (65 g, 수율 68%).
2-(2-페닐옥사졸-4-일)아세토니트릴
이 화합물을 실시예 71 단계 2에 기재된 바와 같이 4-(클로로메틸)-2-페닐옥사졸로부터 백색 고체로서 합성하였다 (24 g, 수율 50%).
2-메틸-2-(2-페닐옥사졸-4-일)프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(2-페닐옥사졸-4-일)아세토니트릴로부터 아이오도메탄을 사용하여 황색 고체로서 합성하였다 (18 g, 수율 65%).
2-메틸-2-(2-페닐옥사졸-4-일)프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-메틸-2-(2-페닐옥사졸-4-일)프로판니트릴로부터 합성하였고 (16.2 g, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-메틸-2-(2-페닐옥사졸-4-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-메틸-2-(2-페닐옥사졸-4-일)프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 백색 고체로서 합성하였다 (15 g, 수율 44%).
실시예 82
2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)아세토니트릴로부터 아이오도메탄을 사용하여 백색 고체로서 합성하였다 (15 g, 수율 66%).
2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판니트릴로부터 합성하였고 (14 g, 조물질), 이를 추가 정제 없이 달성하였다.
2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤질)프로판-1-아민
나트륨트리아세톡시 보로히드라이드 (197 mg, 0.9 mmol)를 건조 DCE (2 mL) 중 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈알데히드 (150 mg, 0.62 mmol) 및 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 (150 mg, 0.64 mmol)의 용액에 0℃에서 질소 분위기 하에 첨가하고, 8시간 동안 실온에서 교반하였다 (TLC에 의해 모니터링함, 석유 에테르/EtOAc 6:4). 반응 혼합물을 10% NaHCO3 용액으로 조심스럽게 켄칭하고, 유기 생성물을 EtOAc로 추출하였다. 합한 추출물을 염수로 세척하고, 무수 Na2SO 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 10-15% EtOAc)에 의해 정제하여 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤질)프로판-1-아민 (50 mg, 수율 18%)을 수득하였다.
실시예 83
4-페닐티아졸-2(3H)-온
건조 DMF (25 mL) 중 2-브로모아세토페논 (5 g, 0.0251 mol), 칼륨 티오시아네이트 (8.6 g, 0.088 mol) 및 아이오딘화칼륨 (0.25 g, 0.0015 mol)의 현탁액을 80℃로 2시간 동안 가열하였다. 반응 혼합물을 감압 하에 농축 건조시키고, 잔류물을 빙초산 (25 mL) 중에 용해시키고, 50% 수성 H2SO4를 여기에 첨가하였다. 반응 혼합물을 100℃로 10분 동안 가열하였다. 반응 혼합물을 빙수에 붓고, 형성된 침전물을 여과하고, 감압 하에 건조시켜 4-페닐티아졸-2(3H)-온 (3.3 g, 수율 75%)을 갈색 고체로서 수득하였으며, 이를 추가 정제 없이 달성하였다.
2-브로모-4-페닐티아졸
4-페닐티아졸-2(3H)-온 (300 mg, 1.7 mmol) 및 POBr3 (4.85 g, 17.0 mmol)의 혼합물을 밀봉된 튜브에서 100℃로 10시간 동안 가열하였다. 반응 혼합물을 빙수에 붓고, 유기 생성물을 EtOAc로 추출하였다. 합한 추출물을 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 1% EtOAc)에 의해 정제하여 2-브로모-4-페닐티아졸 (300 mg, 수율 73%)을 밝은 갈색 액체로서 수득하였다.
3-(4,4-디브로모부트-3-엔-1-일)벤조니트릴
테트라부틸 암모늄 클로라이드 (6.0 g, 21.83 mmol) 및 중탄산나트륨 (4.5 g, 54.5 mmol)을 건조 DMF (15 mL)에 녹이고, 0℃로 냉각시키고, 3-아이오도벤조니트릴 (5.0 g, 21.83 mmol)을 첨가하였다. 알릴 알콜 (2.2 mL, 32.7 mmol)을 반응 혼합물에 첨가하고, 이어서 촉매량의 Pd(OAc)2 (146 mg, 0.65 mmol)를 첨가하고, 혼합물을 0℃에서 30분 동안 교반하였다. 반응 혼합물을 실온으로 천천히 가온하고, 2시간 동안 추가로 교반하였다. 반응 혼합물을 물로 희석하고, 유기 생성물을 에테르로 추출하였다. 합한 추출물을 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 조 생성물 알데히드를 수득하였다. 조 알데히드 (5.0 g, 31.4 mmol)를 CH2Cl2 (100 mL) 중 사브로민화탄소 (20.8 g, 62.8 mmol) 및 트리페닐 포스핀 (32.8 g, 125 mmol)의 차가운 용액에 0℃에서 첨가하였다. 반응 혼합물을 추가로 동일한 온도를 유지하면서 2시간 동안 교반하였다. 이어서, 혼합물을 헥산으로 희석하고, 형성된 침전물을 여과하였다. 투명한 여과물을 농축시켜 조 생성물을 수득하였으며, 이를 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 10-15% EtOAc)에 의해 정제하여 3-(4,4-디브로모부트-3-엔-1-일)벤조니트릴 (2.25 g, 총 수율 33%)을 갈색 오일로서 수득하였다.
3-(부트-3-인-1-일)벤조니트릴
나트륨 비스(트리메틸실릴)아미드 (10.7 mL, 10.7 mmol, THF 중 1M)를 건조 THF (45 mL) 중 3-(4,4-디브로모부트-3-엔-1-일)벤조니트릴 (2.25 g, 7.14 mmol)의 용액에 -60℃에서 적가하였다. 반응 혼합물을 동일한 온도를 유지하면서 추가로 0.5시간 동안 교반하였다. 이어서, 혼합물을 -70℃로 냉각시키고, n-BuLi (8.9 mL, 14.3 mmol, 헥산 중 1.6 M)를 적가하였다. 반응 혼합물을 0.5시간 동안 교반하고, 포화 NH4Cl 용액으로 켄칭하고, EtOAc로 추출하였다. 합한 추출물을 감압 하에 농축시켜 3-(부트-3-인-1-일)벤조니트릴 (600 mg, 수율 54%)을 수득하였다.
3-(4-(4-페닐티아졸-2-일)부트-3-인-1-일)벤조니트릴
3-(부트-3-인-1-일)벤조니트릴 (462 mg, 2.98 mmol) 및 2-브로모-4-페닐티아졸 (650 mg, 2.71 mmol)을 건조 DMF (20 mL)에 녹이고, 질소 기체로 15분 동안 퍼징하였다. Et3N (1.9 mL, 13.5 mmol)을 반응 혼합물에 첨가하고, 이어서 촉매량의 아이오딘화구리 (51 mg, 0.27 mmol) 및 Pd(PPh3)4 (115 mg, 0.1 mmol)를 첨가하였다. 반응 혼합물을 실온에서 12시간 동안 교반한 다음, 물로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 합한 추출물을 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 15-20% EtOAc)에 의해 정제하여 3-(4-(4-페닐티아졸-2-일)부트-3-인-1-일)벤조니트릴 (430mg, 수율 50%)을 연황색 고체로서 수득하였다.
3-(4-(4-페닐티아졸-2-일)부틸)벤조니트릴
목탄 상 10% 팔라듐 (215 mg)을 에탄올 (15 mL) 중 3-(4-(4-페닐티아졸-2-일)부트-3-인-1-일)벤조니트릴 (430 mg, 1.37 mmol)의 용액에 첨가하고, 반응 혼합물을 ~2kg H2-압력 하에 48시간 동안 두었다. 반응 혼합물을 셀라이트 층을 통해 여과하고, EtOAc로 완전히 세척하였다. 용매를 감압 하에 농축시켜 3-(4-(4-페닐티아졸-2-일)부틸)벤조니트릴 (330 mg, 76%)을 무색 점성 액체로서 수득하였다.
N'-히드록시-3-(4-(4-페닐티아졸-2-일)부틸)벤즈이미드아미드
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 3-(4-(4-페닐티아졸-2-일)부틸)벤조니트릴로부터 합성하였고 (290 mg, 조물질), 이를 추가 정제 없이 달성하였다.
3-(3-(4-(4-페닐티아졸-2-일)부틸)페닐)-5-(트리플루오로메틸)-1,2,4-옥사디아졸
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 N'-히드록시-3-(4-(4-페닐티아졸-2-일)부틸)벤즈이미드아미드로부터 황색 액체로서 합성하였다 (70 mg, 수율 20%).
실시예 84
2-디아조-1-페닐에타논
DBU (7.5 mL, 50.2 mmol)를 건조 THF (30 mL) 중 2-브로모-1-페닐에타논 (2.0 g, 10.05 mmol) 및 N,N'-비스(p-톨루엔술포닐) 히드라진 (6.8 g, 20.1 mmol)의 용액에 0℃에서 적가하였다. 반응 혼합물을 0℃에서 30분 동안 교반하고, 수성 포화 NaHCO3 용액으로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 합한 추출물을 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 10-15% EtOAc)에 의해 정제하여 2-디아조-1-페닐에타논 (1.2 g, 수율 82%)을 황색 고체로서 수득하였다.
2-(5-페닐옥사졸-2-일)아세토니트릴
BF3.Et2O (1.1 mL, 8.5 mmol)를 건조 CH2Cl2 (20 mL) 중 말로노니트릴 (2.26 g, 34.2 mmol)의 용액에 0℃에서 적가하고, 이어서 DCM (5 mL) 중 2-디아조-1-페닐에타논 (0.5 g, 3.4 mmol)을 첨가하였다. 반응 혼합물을 실온에서 1시간 동안 교반한 다음, 수성 10% NaOH 용액으로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 합한 추출물을 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 5-10% EtOAc)에 의해 정제하여 2-(5-페닐옥사졸-2-일)아세토니트릴 (200 mg, 수율 32%)을 갈색 고체로서 수득하였다.
2-메틸-2-(5-페닐옥사졸-2-일)프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(5-페닐옥사졸-2-일)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였다 (150 mg, 수율 65%).
2-메틸-2-(5-페닐옥사졸-2-일)프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-메틸-2-(5-페닐옥사졸-2-일)프로판니트릴로부터 합성하였고 (100 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-메틸-2-(5-페닐옥사졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-메틸-2-(5-페닐옥사졸-2-일)프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 황색 점성 액체로서 합성하였다 (18 mg, 수율 10%).
실시예 85
에틸 2-페닐티아졸-5-카르복실레이트
에틸-3-에톡시아크릴레이트 (4.0 g, 27.7 mmol)를 디옥산-H2O (30 ml, 1:1 v/v) 중에 용해시키고, -10℃로 냉각시켰다. N-브로모숙신이미드 (5.43 g, 30.5 mmol)를 이 용액에 첨가하고, 반응 혼합물을 실온으로 가온되도록 하고, 1시간 동안 추가로 교반하였다. 이어서, 티오벤즈아미드 (3.8 g, 27.7 mmol)를 첨가하고, 반응 혼합물을 추가로 80℃로 1시간 동안 가열하였다. 이어서, 반응 혼합물을 실온으로 냉각시키고, 수성 암모니아 용액으로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 합한 추출물을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 5-10% EtOAc)에 의해 정제하여 에틸 2-페닐티아졸-5-카르복실레이트 (1.1 g, 수율 17%)를 황색 고체로서 수득하였다.
(2-페닐티아졸-5-일)메탄올
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 에틸 2-페닐티아졸-5-카르복실레이트로부터 황색 고체로서 합성하였다 (390 mg, 수율 95%).
5-(브로모메틸)-2-페닐티아졸
(2-페닐티아졸-5-일)메탄올 (390 mg, 2.03 mmol)을 건조 CH2Cl2 (10 mL) 중에 용해시키고, 0℃로 냉각시켰다. 이어서, 트리페닐 포스핀 (800 mg, 3.05 mmol)을 첨가하고, 이어서 사브로민화탄소 (1.35 g, 4.07 mmol)를 첨가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 1시간 동안 교반하였다. 이어서, 반응 혼합물을 감압 하에 농축시키고, 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 5% EtOAc)에 의해 정제하여 5-(브로모메틸)-2-페닐티아졸 (250 mg, 수율 48%)을 담황색 고체로서 수득하였다.
2-(2-페닐티아졸-5-일)아세토니트릴
KCN (154 mg, 2.36 mmol)을 건조 DMF (10 mL) 중 5-(브로모메틸)-2-페닐티아졸 (400 mg, 1.57 mmol)의 용액에 첨가하였다. 생성된 반응 혼합물을 실온에서 10시간 동안 교반하였다. 이어서, 혼합물을 물로 켄칭하고, 유기 생성물을 EtOAc로 추출하였다. 합한 추출물을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 20% EtOAc)에 의해 정제하여 2-(2-페닐티아졸-5-일)아세토니트릴 (230 mg, 수율 73%)을 백색 고체로서 수득하였다.
2-(2-페닐티아졸-5-일)에탄아민
이 화합물을 실시예 42 단계 1에 기재된 바와 같이 2-(2-페닐티아졸-5-일)아세토니트릴로부터 합성하였고 (150 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-페닐티아졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-페닐티아졸-5-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 회백색 고체로서 합성하였다 (35 mg, 수율 27%).
실시예 86
2-메틸-2-(2-페닐티아졸-5-일)프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(2-페닐티아졸-5-일)아세토니트릴로부터 아이오도메탄을 사용하여 황색 액체로서 합성하였다 (210 mg, 수율 80%).
2-메틸-2-(2-페닐티아졸-5-일)프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-메틸-2-(2-페닐티아졸-5-일)프로판니트릴로부터 합성하였고 (100 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-메틸-2-(2-페닐티아졸-5-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-메틸-2-(2-페닐티아졸-5-일)프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (70 mg, 수율 51%).
실시예 87
N-((4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (50 mg, 수율 23%).
실시예 88
1-(5-브로모티오펜-2-일)-2,2,2-트리플루오로에탄올
CsF (400 mg, 2.6 mmol)를 건조 1,2-디메톡시에탄 (20 mL) 중 5-브로모티오펜-2-카르브알데히드 (5.0 g, 26.17 mmol)의 용액에 첨가하고, 이어서 트리플루오로메틸 트리메틸실란 (4.6 mL, 31.4 mmol)을 0℃에서 적가하였다. 반응 혼합물을 실온에서 3시간 동안 교반하고, 1.5N HCl로 켄칭하고, 추가로 30분 동안 교반하였다. 조 생성물을 CH2Cl2로 추출하였다. 합한 추출물을 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 5-10% EtOAc)에 의해 정제하여 1-(5-브로모티오펜-2-일)-2,2,2-트리플루오로에탄올 (4 g, 수율 59%)을 수득하였다.
1-(5-브로모티오펜-2-일)-2,2,2-트리플루오로에타논
이 화합물을 실시예 47 단계 2에 기재된 바와 같이 1-(5-브로모티오펜-2-일)-2,2,2-트리플루오로에탄올로부터 합성하였다 (0.8g, 수율 42%).
3-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤조산
1-(5-브로모티오펜-2-일)-2,2,2-트리플루오로에타논 (0.8 g, 3.09 mmol) 및 3-카르복시페닐보론산 (0.5 g, 3.01 mmol)을 DMF (10 mL) 중에 용해시키고, 용액을 아르곤으로 10분 동안 퍼징하였다. Na2CO3 (0.65 g, 6.17 mmol) 및 촉매 Pd(PPh3)4 (178 mg, 0.15 mmol)의 2M 수용액을 반응 혼합물에 첨가하고, 90℃로 10시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 물로 희석하고, 1.5 N HCl을 사용하여 pH ~6으로 산성화시켰다. 조 생성물을 EtOAc로 추출하였다. 합한 추출물을 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 디에틸 에테르로 연화처리하여 3-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤조산 (700 mg, 수율 79%)을 수득하였다.
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 3-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤조산으로부터 합성하였다 (8 mg, 수율 5%).
실시예 89
5-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)니코틴산
이 화합물을 실시예 88 단계 3에 기재된 바와 같이 1-(5-브로모티오펜-2-일)-2,2,2-트리플루오로에타논 및 5-보로노니코틴산으로부터 합성하였다 (470 mg, 수율 82%).
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-5-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 5-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)니코틴산으로부터 합성하였다 (45 mg, 수율 26%).
실시예 90
N-((4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-일)메틸)-3-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(2-(4-클로로페닐)티아졸-4-일)-1-메틸피페리딘-4-일)메탄아민 및 3-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤조산으로부터 합성하였다 (8.5 mg, 수율 4%).
실시예 91
5-시아노-2-플루오로벤조산
물 (3.5 mL) 중 NaH2PO4 (87 mg, 0.724 mmol)를 아세토니트릴 (7 mL) 중 5-시아노-2-플루오로벤즈알데히드 (500 mg, 3.35 mmol)의 용액에 첨가하고, 이어서 30% H2O2 (0.31 mL)를 첨가하였다. 물 (3.5 mL) 중 아염소산나트륨 (434 mg, 4.8 mmol)을 이 반응 혼합물에 0℃에서 적가하였다. 혼합물을 실온에서 1시간 동안 교반하고, 수성 아황산나트륨 용액으로 0℃에서 켄칭한 다음, 1.5N HCl 용액으로 산성화시켰다. 수용액을 EtOAc로 추출하고, 합한 추출물을 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 5-시아노-2-플루오로벤조산 (500 mg, 수율 90%)을 수득하였다.
2-플루오로-5-(N'-히드록시카르밤이미도일)벤조산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 5-시아노-2-플루오로벤조산으로부터 합성하였고 (400 mg, 조물질), 이를 추가 정제 없이 달성하였다.
2-플루오로-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 2-플루오로-5-(N'-히드록시카르밤이미도일)벤조산으로부터 합성하였다 (130 mg, 수율 23%).
2-플루오로-N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 2-플루오로-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 황색 점성 액체로서 합성하였다 (75 mg, 수율 32%).
실시예 92
(E)-에틸 2-스티릴옥사졸-4-카르복실레이트
에틸 브로모피루베이트 (10 mL, 81.55 mmol)를 무수 THF (120 mL) 중 3-페닐아크릴아미드 (5 g, 33.97 mmol) 및 NaHCO3 (11.42 g, 135.89 mmol)의 용액에 0℃에서 적가하였다. 반응 혼합물을 환류 하에 23시간 동안 가열하였다. 이어서, 혼합물을 셀라이트를 통해 여과하고, 용매를 감압 하에 제거하였다. 조 생성물을 무수 THF (80 mL) 중에 용해시키고, 트리플루오로아세트산 무수물 (37 mL)을 0℃에서 적가하였다. 반응 혼합물을 실온에서 10시간 동안 교반하고, 0℃에서 포화 NaHCO3 용액으로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 합한 추출물을 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 10% EtOAc)에 의해 정제하여 (E)-에틸 2-스티릴옥사졸-4-카르복실레이트 (4.22 g, 수율 51%)를 회백색 고체로서 수득하였다.
에틸 2-포르밀옥사졸-4-카르복실레이트
OsO4 [10 mL, 0.41 mmol, H2O 중 4%]을 아세톤-H2O (88 mL; 10:1 v/v) 중 (E)-에틸 2-스티릴옥사졸-4-카르복실레이트 (4 g, 16.44 mmol) 및 트리메틸아민 N-옥시드 (1.84 g, 24.5 mmol)의 용액에 적가하였다. 반응 혼합물을 실온에서 3시간 동안 교반한 다음, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 50% EtOAc)에 의해 정제하여 중간체 (1.5 g, 5.41 mmol)를 수득하였으며, 이를 무수 벤젠 (30 mL) 중에 용해시켰다. K2CO3 (0.85 g, 6.17 mmol)을 반응 혼합물에 첨가하고, 이어서 Pb(OAc)4 (2.73 g, 6.17 mmol)를 첨가하였다. 반응 혼합물을 실온에서 20분 동안 교반한 다음, 포화 NaHCO3 용액으로 켄칭하였다. 유기 생성물을 EtOAc로 추출하였다. 용매를 감압 하에 제거하고, 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 30% EtOAc)에 의해 정제하여 에틸 2-포르밀옥사졸-4-카르복실레이트 (0.65g, 총 수율 24%)를 회백색 고체로서 수득하였다.
에틸 2-시아노옥사졸-4-카르복실레이트
메탄올 (25 mL) 중 에틸 2-포르밀옥사졸-4-카르복실레이트 (650 mg, 3.84 mmol)의 용액을 0℃로 냉각시키고, 50% 수성 히드록실아민 (0.22 mL, 7.68 mmol)을 적가하였다. 반응 혼합물을 실온에서 3시간 동안 교반하였다. 용매를 감압 하에 제거하고, 수득한 조 생성물 (0.52 g)을 DMF (20 mL) 중에 용해시켰다. T3P (3.4 mL, 5.65 mmol; EtOAc 중 50%)를 반응 혼합물에 첨가하고, 100℃로 2시간 동안 가열하였다. 반응 혼합물을 포화 NaHCO3 용액으로 켄칭하고, 유기 생성물을 EtOAc로 추출하였다. 용매를 감압 하에 제거하고, 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 10% EtOAc)에 의해 정제하여 에틸 2-시아노옥사졸-4-카르복실레이트 (0.34 g, 수율 53%)를 회백색 고체로서 수득하였다.
에틸 2-(N'-히드록시카르밤이미도일)옥사졸-4-카르복실레이트
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 에틸 2-시아노옥사졸-4-카르복실레이트로부터 합성하였고 (500 mg, 조물질), 이를 추가 정제 없이 달성하였다.
에틸 2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)옥사졸-4-카르복실레이트
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 에틸 2-(N'-히드록시카르밤이미도일)옥사졸-4-카르복실레이트로부터 합성하였다 (50 mg, 수율 7%).
2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)옥사졸-4-카르복실산
이 화합물을 실시예 43 단계 2에 기재된 바와 같이 에틸 2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)옥사졸-4-카르복실레이트로부터 회백색 고체로서 합성하였다 (25 mg, 56%).
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)옥사졸-4-카르복스아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 2-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)옥사졸-4-카르복실산으로부터 합성하였다 (6 mg, 수율 13%).
실시예 93
메틸 1-메틸-2-페닐-1H-이미다졸-5-카르복실레이트
메틸-2-브로모-1-메틸-1H-이미다졸-5-카르복실레이트 (1 g, 4.56 mmol) 및 페닐보론산 (0.67 g, 5.48 mmol)을 톨루엔-EtOH (80 mL, 5:3 v/v) 중에 용해시키고, 용액을 아르곤으로 10분 동안 퍼징하였다. K2CO3 (10 mL, 2M 용액) 및 촉매 PdCl2(dppf) (82 mg, 0.12 mmol)를 첨가하고, 반응 혼합물을 100℃로 1시간 동안 가열하였다. 이어서, 반응 혼합물을 실온으로 냉각시키고, 감압 하에 농축시켰다. 잔류물을 물로 희석하고, EtOAc로 세척하였다. 수성 층을 1.5N HCl을 사용하여 pH ~6으로 산성화시키고, 조 생성물을 EtOAc로 추출하였다. 합한 추출물을 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 35-45% EtOAc)에 의해 정제하여 메틸 1-메틸-2-페닐-1H-이미다졸-5-카르복실레이트 (800 mg, 수율 81%)를 연황색 고체로서 수득하였다.
(1-메틸-2-페닐-1H-이미다졸-5-일)메탄올
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 1-메틸-2-페닐-1H-이미다졸-5-카르복실레이트로부터 백색 고체로서 합성하였다 (600 mg, 수율 86%).
5-(클로로메틸)-1-메틸-2-페닐-1H-이미다졸 히드로클로라이드
건조 SOCl2 (11 mL) 중 (1-메틸-2-페닐-1H-이미다졸-5-일)메탄올 (0.600 g, 3.19 mmol)의 용액을 80℃에서 1시간 동안 환류하였다. 반응 혼합물을 감압 하에 농축시키고, 잔류물을 CH2Cl2와 공증발시킨 다음, 디에틸 에테르로 연화처리하고, 여과하고, 흡인 하에 건조시켜 5-(클로로메틸)-1-메틸-2-페닐-1H-이미다졸 히드로클로라이드 (0.67 g, 수율 86%)를 백색 고체로서 수득하였다.
2-(1-메틸-2-페닐-1H-이미다졸-5-일)아세토니트릴
이 화합물을 실시예 77 단계 1에 기재된 바와 같이 5-(클로로메틸)-1-메틸-2-페닐-1H-이미다졸 히드로클로라이드로부터 합성하였다 (400 mg, 수율 90%).
2-(1-메틸-2-페닐-1H-이미다졸-5-일)프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(1-메틸-2-페닐-1H-이미다졸-5-일)아세토니트릴로부터 무색 오일로서 합성하였다 (170 mg, 수율 53%).
2-(1-메틸-2-페닐-1H-이미다졸-5-일)프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(1-메틸-2-페닐-1H-이미다졸-5-일)프로판니트릴로부터 합성하였고 (155 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(1-메틸-2-페닐-1H-이미다졸-5-일)프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(1-메틸-2-페닐-1H-이미다졸-5-일)프로판-1-아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (35 mg, 수율 28%).
실시예 94
메틸 2-(4-플루오로페닐)-4,5-디히드로옥사졸-4-카르복실레이트
N,N-디이소프로필에틸아민 (11 mL, 63.3 mmol)을 건조 CH2Cl2 (200 mL) 중 메틸 4-플루오로벤즈이미데이트 히드로클로라이드 (10 g, 52.74 mmol) 및 DL-세린 메틸 에스테르 HCl 염 (9.9 g, 63.63 mmol)의 용액에 0℃에서 적가하였다. 반응 혼합물을 실온에서 24시간 동안 교반한 다음, 감압 하에 농축시켰다. 반응 혼합물을 CH2Cl2로 희석하고, 유기 층을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 메틸 2-(4-플루오로페닐)-4,5-디히드로옥사졸-4-카르복실레이트 (9.5 g, 수율 81%)를 오렌지색 액체로서 수득하였다.
메틸 2-(4-플루오로페닐)옥사졸-4-카르복실레이트
벤조일 퍼옥시드 (0.49 g, 2.0 mmol)를 건조 벤젠 (180 mL) 중 메틸 2-(4-플루오로페닐)-4,5-디히드로옥사졸-4-카르복실레이트 (9.0 g, 40.3 mmol)의 용액에 첨가하고, 혼합물을 15분 동안 환류하였다. 이어서, N-브로모숙신이미드 (8.6 g, 48.3 mmol)를 첨가하고, 반응 혼합물을 2시간 동안 환류하였다. 반응 혼합물을 빙냉수로 켄칭하고, 조 생성물을 EtOAc로 추출하였다. 합한 추출물을 10% 수성 NaHCO3 용액, H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 10-15% EtOAc)에 의해 정제하여 메틸 2-(4-플루오로페닐)옥사졸-4-카르복실레이트 (6 g, 수율 67%)를 백색 고체로서 수득하였다.
(2-(4-플루오로페닐)옥사졸-4-일)메탄올
이 화합물을 실시예 64 단계 4에 기재된 바와 같이 메틸 2-(4-플루오로페닐)옥사졸-4-카르복실레이트로부터 황색 고체로서 합성하였다 (4.5 g, 수율 86%).
2-(4-플루오로페닐)옥사졸-4-카르브알데히드
이 화합물을 실시예 47 단계 2에 기재된 바와 같이 (2-(4-플루오로페닐)옥사졸-4-일)메탄올로부터 백색 고체로서 합성하였다 (2.8g, 수율 63%).
2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시아세토니트릴
KH2PO4 (712 mg, 5.23 mmol) 및 NaCN (251 mg, 5.12 mmol)을 DMF-H2O (10 mL, 4:6, v/v) 중 2-(4-플루오로페닐)옥사졸-4-카르브알데히드 (500 mg, 2.62 mmol)의 용액에 첨가하였다. 생성된 반응 혼합물을 실온에서 1시간 동안 교반한 다음, 물로 희석하고, EtOAc로 추출하였다. 합한 추출물을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시아세토니트릴 (500 mg, 수율 87%)을 수득하였다.
2-아미노-1-(2-(4-플루오로페닐)옥사졸-4-일)에탄올
트리플루오로아세트산 (0.35 mL, 4.60 mmol)을 건조 THF (10 mL) 중 NaBH4 (0 174 g, 4.60 mmol)의 현탁액에 0℃에서 적가하고, 이어서 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시아세토니트릴 (0 20 g, 0.92 mmol)을 또한 조금씩 첨가하였다. 반응 혼합물을 실온에서 8시간 동안 교반한 다음, 감압 하에 농축시키고, 빙수로 희석하였다. 혼합물을 0℃에서 1.5N HCl를 사용하여 pH ~2로 산성화시킨 다음, 50℃로 20분 동안 가열하였다. 용액을 수성 NH4OH 용액으로 염기성화시키고, 유기 생성물을 CHCl3으로 추출하였다. 합한 추출물을 염수로 세척하고, 감압 하에 농축시켜 2-아미노-1-(2-(4-플루오로페닐)옥사졸-4-일)에탄올 (120 mg, 조물질)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-아미노-1-(2-(4-플루오로페닐)옥사졸-4-일)에탄올 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (70 mg, 수율 39%).
실시예 95
5-(5-(디플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 에틸 디플루오로아세테이트를 사용하여 5-(N'-히드록시카르밤이미도일)니코틴산으로부터 합성하였다 (100 mg, 수율 30%).
5-(5-(디플루오로메틸)-1,2,4-옥사디아졸-3-일)-N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 5-(5-(디플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (45 mg, 수율 24%).
실시예 96
2-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)아세토니트릴
2-(4-플루오로페닐)옥사졸-4-카르브알데히드 (1.0 g, 5.23 mmol)를 THF-MeOH (20 mL, 1:1 v/v) 중에 용해시켰다. 이 용액을 물 중 디메틸아민 히드로클로라이드 (470 mg, 5.7 mmol) 및 NaCN (640 mg, 13.0 mmol)의 용액에 첨가하였다. 생성된 반응 혼합물을 실온에서 2시간 동안 교반한 다음, 물로 희석하고, EtOAc로 추출하였다. 합한 추출물을 H2O 및 염수로 세척하고, 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 2-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)아세토니트릴 (1.0 g, 조물질)을 갈색 오일로서 수득하였으며, 이를 추가 정제 없이 사용하였다.
1-(2-(4-플루오로페닐)옥사졸-4-일)-N1,N1-디메틸에탄-1,2-디아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)아세토니트릴로부터 합성하였고 (0.6 g), 이를 추가 정제 없이 달성하였다.
N-(2-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드 히드로클로라이드
N-(2-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드를 실시예 8 단계 6에 기재된 바와 같이 1-(2-(4-플루오로페닐)옥사졸-4-일)-N1,N1-디메틸에탄-1,2-디아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다. 이어서, 유리 염기를 디옥산 용액 중 HCl (4 mL)과 함께 0.5시간 동안 0℃ 내지 실온에서 교반하였다. 반응 혼합물을 농축시키고, 디에틸 에테르로 연화처리하여 N-(2-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드 히드로클로라이드 (130 mg, 수율 16%)를 밝은 갈색 고체로서 수득하였다.
실시예 97
N-(2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로필)-5-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(3-(4-플루오로페닐)-1H-1,2,4-트리아졸-5-일)-2-메틸프로판-1-아민 및 5-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)니코틴산으로부터 황색 점성 액체로서 합성하였다 (28 mg, 수율 20%).
실시예 98
메틸 5-시아노-2-메톡시벤조에이트
건조 아세톤 (50 mL) 중 산 메틸 5-시아노-2-히드록시벤조에이트 (2 g, 11.2 mmol)의 용액을 0℃로 냉각시키고, K2CO3 (2.34 g, 16.9 mmol)에 이어서 MeI (1.1 mL, 16.9 mmol)를 적가하였다. 반응 혼합물을 65℃에서 10시간 동안 교반되도록 한 다음, EtOAc로 희석하였다. 유기 층을 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 메틸 5-시아노-2-메톡시벤조에이트 (600 mg, 조물질)를 수득하였으며, 이를 추가 정제 없이 달성하였다.
5-시아노-2-메톡시벤조산
이 화합물을 실시예 43 단계 2에 기재된 바와 같이 5-시아노-2-메톡시벤조산으로부터 백색 고체로서 합성하였다 (300 mg, 수율 72%).
5-(N'-히드록시카르밤이미도일)-2-메톡시벤조산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 5-시아노-2-메톡시벤조산으로부터 합성하였고 (300 mg), 이를 추가 정제 없이 달성하였다.
2-메톡시-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 5-(N'-히드록시카르밤이미도일)-2-메톡시벤조산으로부터 합성하였다 (40 mg, 수율 35%).
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-2-메톡시-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 2-메톡시-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (40 mg, 수율 36%).
실시예 99
2-(2-(4-플루오로페닐)옥사졸-5-일)-2-메틸프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-5-일)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였다 (170 mg, 수율 60%).
2-(2-(4-플루오로페닐)옥사졸-5-일)-2-메틸프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-5-일)-2-메틸프로판니트릴로부터 합성하였고 (100 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-플루오로페닐)옥사졸-5-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-5-일)-2-메틸프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (30 mg, 수율 15%).
실시예 100
4-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)부탄니트릴
이 화합물을 실시예 16 단계 1b에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)아세토니트릴 및 2-클로로-N,N-디메틸에탄아민 히드로클로라이드로부터 합성하였다 (400 mg, 수율 48%).
3-(2-(4-플루오로페닐)옥사졸-4-일)-N1,N1-디메틸부탄-1,4-디아민
염화코발트(II) (380 mg, 2.9 mmol)를 건조 메탄올 (10 mL) 중 4-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)부탄니트릴 (400 mg, 1.46 mmol)의 용액에 0℃에서 첨가하고, 이어서 수소화붕소나트륨 (550 mg, 14.6 mmol)을 조금씩 첨가하였다. 생성된 혼합물을 실온에서 1시간 동안 교반한 다음, 빙수로 조심스럽게 켄칭하고, 셀라이트 층을 통해 여과하였다. 여과물을 감압 하에 농축시켜 조 3-(2-(4-플루오로페닐)옥사졸-4-일)-N1,N1-디메틸부탄-1,4-디아민 (180 mg, 조물질)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
N-(4-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)부틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 3-(2-(4-플루오로페닐)옥사졸-4-일)-N1,N1-디메틸부탄-1,4-디아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (17 mg, 수율 10%).
실시예 101
N-(4-(디메틸아미노)-2-(2-(4-플루오로페닐)옥사졸-4-일)부틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 3-(2-(4-플루오로페닐)옥사졸-4-일)-N1,N1-디메틸부탄-1,4-디아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (16 mg, 수율 10%).
실시예 102
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-아미노-1-(2-(4-플루오로페닐)옥사졸-4-일)에탄올 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (120 mg, 수율 45%).
실시예 103
4-(클로로메틸)-2-(4-클로로페닐)옥사졸
이 화합물을 실시예 74 단계 1에 기재된 바와 같이 4-클로로벤즈아미드 및 1,3-디클로로아세톤으로부터 합성하였다 (3.4 g, 수율 46%).
2-(2-(4-클로로페닐)옥사졸-4-일)아세토니트릴
이 화합물을 실시예 71 단계 2에 기재된 바와 같이 4-(클로로메틸)-2-(4-클로로페닐)옥사졸로부터 합성하였다 (1.7 g, 수율 53%).
4-(2-(4-클로로페닐)옥사졸-4-일)-1-메틸피페리딘-4-카르보니트릴
이 화합물을 실시예 16 단계 1b에 기재된 바와 같이 2-(2-(4-클로로페닐)옥사졸-4-일)아세토니트릴로부터 합성하였다 (140 mg, 수율 20%).
(4-(2-(4-클로로페닐)옥사졸-4-일)-1-메틸피페리딘-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(2-(4-클로로페닐)옥사졸-4-일)-1-메틸피페리딘-4-카르보니트릴로부터 합성하였고 (100 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-((4-(2-(4-클로로페닐)옥사졸-4-일)-1-메틸피페리딘-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드 히드로클로라이드
이 화합물을 실시예 96 단계 3에 기재된 바와 같이 (4-(2-(4-클로로페닐)옥사졸-4-일)-1-메틸피페리딘-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (12 mg, 수율 5%).
실시예 104
2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(2-(4-클로로페닐)옥사졸-4-일)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였다 (300 mg, 수율 53%).
2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸프로판니트릴로부터 합성하였고 (155 mg, 수율 59%), 이를 추가 정제 없이 사용하였다.
2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤질)프로판-1-아민 히드로클로라이드
2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤질)프로판-1-아민을 실시예 7 단계 3에 기재된 바와 같이 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈알데히드 및 2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸프로판-1-아민으로부터 합성하였다. 이어서, 유리 아민을 0℃에서 디옥산 중 HCl (2M)로 처리하고, 실온에서 30분 동안 교반하였다. 반응 혼합물을 감압 하에 농축시켰다. 조물질을 세척에 의해 건조 헥산을 사용하여 정제하여 2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸-N-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤질)프로판-1-아민 히드로클로라이드 (20 mg, 수율 6%)를 수득하였다.
실시예 105
2-(2-(4-플루오로페닐)옥사졸-5-일)에탄아민
이 화합물을 실시예 42 단계 1에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-5-일)아세토니트릴로부터 합성하였고 (70 mg), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-플루오로페닐)옥사졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-5-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (28 mg, 수율 20%).
실시예 106
4-([1,1'-비페닐]-3-일)-1-메틸피페리딘-4-카르보니트릴
이 화합물을 실시예 16 단계 1b에 기재된 바와 같이 2-([1,1'-비페닐]-3-일)아세토니트릴로부터 합성하였다 (500 mg, 수율 35%).
(4-([1,1'-비페닐]-3-일)-1-메틸피페리딘-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-([1,1'-비페닐]-3-일)-1-메틸피페리딘-4-카르보니트릴로부터 합성하였다 (250 mg, 수율 50%).
N-((4-([1,1'-비페닐]-3-일)-1-메틸피페리딘-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-([1,1'-비페닐]-3-일)-1-메틸피페리딘-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 회백색 고체로서 합성하였다 (60 mg, 수율 31%).
실시예 107
4-(클로로메틸)-2-(4-메톡시페닐)옥사졸
이 화합물을 실시예 74 단계 1에 기재된 바와 같이 4-메톡시벤즈아미드 및 1,3-디클로로아세톤으로부터 황색 고체로서 합성하였다 (2.3 g, 수율 78%).
2-(2-(4-메톡시페닐)옥사졸-4-일)아세토니트릴
이 화합물을 실시예 71 단계 2에 기재된 바와 같이 4-(클로로메틸)-2-(4-메톡시페닐)옥사졸로부터 회백색 고체로서 합성하였다 (0.65 g, 수율 57%).
2-(2-(4-메톡시페닐)옥사졸-4-일)에탄아민
이 화합물을 실시예 42 단계 1에 기재된 바와 같이 2-(2-(4-메톡시페닐)옥사졸-4-일)아세토니트릴로부터 합성하였고 (130 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-메톡시페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-메톡시페닐)옥사졸-4-일)에탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 백색 고체로서 합성하였다 (35 mg, 수율 19%).
실시예 108
2-클로로-5-시아노벤조산
물 (10 mL) 중 NaNO2 (2.21 g, 32 mmol)의 용액을 물 (40 mL) 중 5-아미노-2-클로로벤조산 (5.0 g, 29.14 mmol)의 용액에 0℃에서 첨가하고, 이어서 진한 HCl (10 mL)을 -5℃에서 첨가하였다. 반응 혼합물을 -5℃에서 추가로 1시간 동안 교반한 다음, 디아조늄 용액을 칼륨 쿠프로테트라시아나이드의 용액 [70℃에서 물 (18 mL) 중 KCN (10 g, 15.38 mmol)의 용액을 물 (12 mL) 중 CuSO4 (7 g, 43.8 mmol)의 용액에 적가함으로써 제조됨]에 50℃에서 1시간 동안 적가하였다. 반응 혼합물을 1.5 N HCl 용액을 사용하여 산성화시키고, 생성물을 EtOAc로 추출하였다. 합한 추출물을 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 CHCl3 중 1-2% MeOH)에 의해 정제하여 2-클로로-5-시아노벤조산 (1.8 g, 수율 34%)을 수득하였다.
2-클로로-5-시아노-N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 2-클로로-5-시아노벤조산으로부터 합성하였다 (300 mg, 수율 44%).
4-클로로-3-((2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)카르바모일) 벤조히드라조산
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 2-클로로-5-시아노-N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)벤즈아미드로부터 합성하였고 (230 mg, 조물질), 이를 추가 정제 없이 달성하였다.
2-클로로-N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 1 단계 5에 기재된 바와 같이 4-클로로-3-((2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)카르바모일)벤조히드라조산으로부터 합성하였다 (100 mg, 수율 37%).
실시예 109
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (18 mg, 수율 12%).
실시예 110
1-(2-(4-플루오로페닐)옥사졸-4-일)에타논
건조 클로로포름 (5 mL) 중 2-(4-플루오로페닐)옥사졸-4-카르브알데히드 (400 mg, 2.09 mmol)의 용액을 0℃로 냉각시키고, 에테르 (20 mL) 중 디아조메탄의 새로이 제조한 용액을 첨가하였다. 반응 혼합물을 1시간 동안 교반하고, 10% 수성 NaHCO3 용액으로 켄칭하였다. 조 생성물을 CH2Cl2로 추출하고, 합한 추출물을 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 5-8% EtOAc)에 의해 정제하여 1-(2-(4-플루오로페닐)옥사졸-4-일)에타논 (250 mg, 수율 58%)을 백색 고체로서 수득하였다.
3-(2-(4-플루오로페닐)옥사졸-4-일)-3-히드록시프로판니트릴
DMF-H2O (7 mL; 2:5 v/v) 중 1-(2-(4-플루오로페닐)옥사졸-4-일)에타논 (250 mg, 1.22 mmol)의 용액을 0℃로 냉각시키고, KH2PO4 (327 mg, 2.4 mmol)를 첨가하고, 이어서 KCN (116 mg, 1.8 mmol)을 첨가하였다. 반응 혼합물을 80℃에서 10시간 교반하고, 이어서 물로 희석하였다. 유기 생성물을 EtOAc로 추출하고, 합한 추출물을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 8-12% EtOAc)에 의해 정제하여 3-(2-(4-플루오로페닐)옥사졸-4-일)-3-히드록시프로판니트릴 (60 mg, 수율 21%)을 담황색 고체로서 수득하였다.
3-아미노-1-(2-(4-플루오로페닐)옥사졸-4-일)프로판-1-올
이 화합물을 실시예 94 단계 6에 기재된 바와 같이 3-(2-(4-플루오로페닐)옥사졸-4-일)-3-히드록시프로판니트릴로부터 합성하였고 (110 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(3-(2-(4-플루오로페닐)옥사졸-4-일)-3-히드록시프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 3-아미노-1-(2-(4-플루오로페닐)옥사졸-4-일)프로판-1-올 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 백색 고체로서 합성하였다 (35 mg, 수율 19%).
실시예 111
2-(4-브로모페닐)-4-(클로로메틸)옥사졸
이 화합물을 실시예 74 단계 1에 기재된 바와 같이 4-브로모벤즈아미드 및 1,3-디클로로아세톤으로부터 백색 고체로서 합성하였다 (1.5 g, 수율 14%).
2-(2-(4-브로모페닐)옥사졸-4-일)아세토니트릴
이 화합물을 실시예 71 단계 2에 기재된 바와 같이 2-(4-브로모페닐)-4-(클로로메틸)옥사졸로부터 회백색 고체로서 합성하였다 (1.4 g, 수율 76%).
2-(2-(4-브로모페닐)옥사졸-4-일)에탄아민
이 화합물을 실시예 42 단계 1에 기재된 바와 같이 2-(2-(4-브로모페닐)옥사졸-4-일)아세토니트릴로부터 황색 액체로서 합성하였다 (0.4 g, 수율 56%).
N-(2-(2-(4-브로모페닐)옥사졸-4-일)에틸)-2,2,2-트리플루오로아세트아미드
트리에틸아민 (0.31 mL, 2.24 mmol)을 건조 메탄올 (20 mL) 중 2-(2-(4-브로모페닐)옥사졸-4-일)에탄아민 (0.4 g, 1.49 mmol)의 용액에 첨가하고, 이어서 에틸 트리플루오로 아세테이트 (0.27 mL, 2.25 mmol)를 0℃에서 적가하였다. 반응 혼합물을 실온으로 천천히 가온하고, 2시간 동안 추가로 교반하였다. 이어서, 반응 혼합물을 감압 하에 농축시켰다. 반응 혼합물을 EtOAc로 희석하고, 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 CHCl3 중 1% MeOH)에 의해 정제하여 N-(2-(2-(4-브로모페닐)옥사졸-4-일)에틸)-2,2,2-트리플루오로아세트아미드 (0.26 g, 수율 48%)를 회백색 고체로서 수득하였다.
N-(2-(2-(4-시아노페닐)옥사졸-4-일)에틸)-2,2,2-트리플루오로아세트아미드
N-(2-(2-(4-브로모페닐)옥사졸-4-일)에틸)-2,2,2-트리플루오로아세트아미드 (200 mg, 0.55 mmol)를 건조 DMF (10 mL) 중에 용해시키고, 용액을 아르곤으로 10분 동안 퍼징하였다. Zn(CN)2 (97 mg, 0.83 mmol) 및 PdCl2(dppf) (302 mg, 0.04 mmol)을 반응 혼합물에 첨가하고, 150℃로 48시간 동안 가열하였다. 반응 혼합물을 셀라이트를 통해 여과하고, 여과물을 감압 하에 농축시켰다. 잔류물을 물로 희석하고, 생성물을 EtOAc로 추출하였다. 합한 추출물을 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 N-(2-(2-(4-시아노페닐)옥사졸-4-일)에틸)-2,2,2-트리플루오로아세트아미드 (150 mg)를 수득하였으며, 이를 후속 단계에 추가 정제 없이 사용하였다.
4-(4-(2-아미노에틸)옥사졸-2-일)벤조니트릴
K2CO3 (0.20 g, 1.45 mmol)을 건조 메탄올:물 (10 mL, 7:3 v/v) 중 N-(2-(2-(4-시아노페닐)옥사졸-4-일)에틸)-2,2,2-트리플루오로아세트아미드 (0.15 g, 0.49 mmol)의 용액에 조금씩 첨가하였다. 반응 혼합물을 실온에서 3시간 동안 교반한 다음, 물로 희석하였다. 조 생성물을 클로로포름으로 추출하였다. 유기 층을 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 4-(4-(2-아미노에틸)옥사졸-2-일)벤조니트릴 (80 mg)을 수득하였으며, 이를 후속 단계에 추가 정제 없이 사용하였다.
N-(2-(2-(4-시아노페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 4-(4-(2-아미노에틸)옥사졸-2-일)벤조니트릴 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 회백색 고체로서 합성하였다 (30 mg, 수율 23%).
실시예 112
4-(클로로메틸)-2-(2-플루오로페닐)옥사졸
2-플루오로벤즈아미드 (500 mg, 3.59 mmol) 및 1,3-디클로로아세톤 (1.82 g, 14.36 mmol)의 혼합물을 밀봉된 튜브에서 130℃로 2시간 동안 가열하였다. 반응 혼합물을 EtOAc로 희석하고, 물 및 염수로 세척하였다. 용매를 감압 하에 제거하고, 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 2-3% EtOAc)에 의해 정제하여 4-(클로로메틸)-2-(2-플루오로페닐)옥사졸 (500 mg, 수율 66%)을 백색 고체로서 수득하였다.
2-(2-(2-플루오로페닐)옥사졸-4-일)아세토니트릴
이 화합물을 실시예 71 단계 2에 기재된 바와 같이 4-(클로로메틸)-2-(2-플루오로페닐)옥사졸로부터 백색 고체로서 합성하였다 (0.2 g, 수율 29%).
2-(2-(2-플루오로페닐)옥사졸-4-일)에탄아민
이 화합물을 실시예 42 단계 1에 기재된 바와 같이 2-(2-(2-플루오로페닐)옥사졸-4-일)아세토니트릴로부터 합성하였고 (100 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(2-플루오로페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(2-플루오로페닐)옥사졸-4-일)에탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 백색 고체로서 합성하였다 (10 mg, 수율 6%).
실시예 113
1-(5-브로모티오펜-2-일)-2,2-디플루오로에타논
건조 THF (5 mL) 중 2-브로모티오펜 (0.5 g, 3.00 mmol)의 용액을 -78℃로 냉각시키고, 새로이 제조한 리튬 디이소프로필아미드 (디이소프로필 아민 (0.5 mL, 3.60 mmol) 및 nBuLi (2.3 mL, 3.60 mmol, THF 중 1.6M)로부터 제조됨)를 적가하였다. 반응 혼합물을 -78℃에서 1시간 동안 교반하였다. 에틸 디플루오로 아세테이트 (409 mg, 3.30 mmol)를 -78℃에서 적가하고, 반응 혼합물을 1시간 동안 교반한 다음, 실온으로 천천히 가온하고, 포화 NH4Cl 용액으로 켄칭하였다. 유기 생성물을 EtOAc로 추출하고, 무수 황산나트륨 상에서 건조시켰다. 용매를 감압 하에 농축시켜 1-(5-브로모티오펜-2-일)-2,2-디플루오로에타논 (500 mg, 수율 69%)을 수득하였다.
3-(5-(2,2-디플루오로아세틸)티오펜-2-일)벤조산
이 화합물을 실시예 88 단계 3에 기재된 바와 같이 1-(5-브로모티오펜-2-일)-2,2-디플루오로에타논으로부터 갈색 고체로서 합성하였다 (300 mg, 수율 51%).
3-(5-(2,2-디플루오로아세틸)티오펜-2-일)-N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 3-(5-(2,2-디플루오로아세틸)티오펜-2-일)벤조산으로부터 합성하였다 (60 mg, 수율 34%).
실시예 114
1-(2-브로모티아졸-5-일)-2,2,2-트리플루오로에탄올
이 화합물을 실시예 88 단계 1에 기재된 바와 같이 2-브로모티아졸-5-카르브알데히드로부터 합성하였다 (0.6 g, 수율 44%).
1-(2-브로모티아졸-5-일)-2,2,2-트리플루오로에타논
이 화합물을 실시예 47 단계 2에 기재된 바와 같이 1-(2-브로모티아졸-5-일)-2,2,2-트리플루오로에탄올로부터 합성하였다 (0.35 g, 수율 59%).
3-(5-(2,2,2-트리플루오로아세틸)티아졸-2-일)벤조산
이 화합물을 실시예 88 단계 3에 기재된 바와 같이 1-(2-브로모티아졸-5-일)-2,2,2-트리플루오로에타논으로부터 합성하였고 (120 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(2,2,2-트리플루오로아세틸)티아졸-2-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 3-(5-(2,2,2-트리플루오로아세틸)티아졸-2-일)벤조산으로부터 합성하였다 (7 mg, 수율 3%).
실시예 115
4-(((tert-부틸디페닐실릴)옥시)메틸)-2-페닐-1H-이미다졸
tBuPh2SiCl (5.5 g, 19.9 mmol)을 건조 CH2Cl2 (60 mL) 중 2-페닐-1H-이미다졸-4-메탄올 (2.9 g, 16.65 mmol) 및 이미다졸 (1.7 g, 24.97 mmol)의 현탁액에 0℃에서 적가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 8시간 동안 교반하였다. 반응 혼합물을 CH2Cl2로 희석하고, 유기 층을 10% NaHCO3 용액, 물 및 염수로 세척하였다. 유기 층을 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켜 4-(((tert-부틸디페닐실릴)옥시)메틸)-2-페닐-1H-이미다졸 (5.7 g, 수율 83%)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
4-(((tert-부틸디페닐실릴)옥시)메틸)-1-메틸-2-페닐-1H-이미다졸
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 4-(((tert-부틸디페닐실릴)옥시)메틸)-2-페닐-1H-이미다졸로부터 황색 점성 액체로서 합성하였다 (1.25 g, 수율 21%).
(1-메틸-2-페닐-1H-이미다졸-4-일)메탄올
건조 THF (25 mL) 중 4-(((tert-부틸디페닐실릴)옥시)메틸)-1-메틸-2-페닐-1H-이미다졸 (1.25 g, 2.93 mmol)의 용액을 0℃로 냉각시키고, 테트라부틸암모늄 플루오라이드 (5.9 mL, 5.86 mmol, THF 중 1M)를 적가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 3시간 동안 추가로 교반하였다. 반응 혼합물을 염수로 켄칭하고, EtOAc로 추출하였다. 유기 층을 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 CH2Cl2 중 2-4% MeOH)에 의해 정제하여 (1-메틸-2-페닐-1H-이미다졸-4-일)메탄올 (0.26 mg, 수율 47%)을 백색 고체로서 수득하였다.
4-(클로로메틸)-1-메틸-2-페닐-1H-이미다졸
이 화합물을 실시예 93 단계 3에 기재된 바와 같이 (1-메틸-2-페닐-1H-이미다졸-4-일)메탄올로부터 히드로클로라이드 염으로서 갈색 고체로서 합성하였다 (0.28 g, 조물질).
2-(1-메틸-2-페닐-1H-이미다졸-4-일)아세토니트릴
이 화합물을 실시예 77 단계 1에 기재된 바와 같이 4-(클로로메틸)-1-메틸-2-페닐-1H-이미다졸로부터 갈색 액체로서 합성하였다 (120 mg, 수율 44%).
2-(1-메틸-2-페닐-1H-이미다졸-4-일)프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(1-메틸-2-페닐-1H-이미다졸-4-일)아세토니트릴로부터 담황색 오일로서 합성하였다 (60 mg, 수율 47%).
2-(1-메틸-2-페닐-1H-이미다졸-4-일)프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(1-메틸-2-페닐-1H-이미다졸-4-일)프로판니트릴로부터 합성하였고 (60 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(1-메틸-2-페닐-1H-이미다졸-4-일)프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(1-메틸-2-페닐-1H-이미다졸-4-일)프로판-1-아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (10 mg, 수율 16%).
실시예 116
1-(5-브로모푸란-2-일)-2,2,2-트리플루오로에탄올
이 화합물을 실시예 88 단계 1에 기재된 바와 같이 5-브로모푸란-2-카르브알데히드로부터 합성하였다 (2.6 g, 수율 62%).
1-(5-브로모푸란-2-일)-2,2,2-트리플루오로에타논
이 화합물을 실시예 47 단계 2에 기재된 바와 같이 1-(5-브로모푸란-2-일)-2,2,2-트리플루오로에탄올로부터 합성하였다 (1.2 g, 수율 47%).
3-(5-(2,2,2-트리플루오로아세틸)푸란-2-일)벤조산
이 화합물을 실시예 88 단계 3에 기재된 바와 같이 1-(5-브로모푸란-2-일)-2,2,2-트리플루오로에타논으로부터 합성하였다 (500 mg, 조물질).
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(2,2,2-트리플루오로아세틸)푸란-2-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 3-(5-(2,2,2-트리플루오로아세틸)푸란-2-일)벤조산으로부터 합성하였다 (20 mg, 수율 6%).
실시예 117
4-(디메톡시메틸)-2-(4-플루오로페닐)옥사졸
메톡시트리메틸실란 (545 mg, 5.23 mmol) 및 트리메틸실릴 트리플루오로메탄술포네이트 (30 mg, 0.13 mmol)를 건조 CH2Cl2 (2 mL) 중 2-(4-플루오로페닐)옥사졸-4-카르브알데히드 (500 mg, 2.62 mmol)의 용액에 -78℃에서 첨가하였다. 반응 혼합물을 실온으로 가온되도록 하고, 24시간 동안 교반하고, 포화 수성 NaHCO3 용액으로 켄칭하고, 조 생성물을 EtOAc로 추출하였다. 유기 층을 10% NaHCO3 용액, 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시켰다. 용매를 감압 하에 제거하여 4-(디메톡시메틸)-2-(4-플루오로페닐)옥사졸 (400 mg, 조물질)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메톡시아세토니트릴
트리메틸실릴 시아나이드 (4.13 g, 41.76 mmol)를 4-(디메톡시메틸)-2-(4-플루오로페닐)옥사졸의 용액 (400 mg, 1.69 mmol)에 실온에서 첨가하고, 이어서 삼플루오린화붕소 디에틸 에테레이트 (37 mg, 0.26 mmol)를 첨가하였다. 반응 혼합물을 20분 동안 교반하고, 포화 수성 NaHCO3 용액으로 켄칭하고, EtOAc로 추출하였다. 합한 추출물을 H2O 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 8-10% EtOAc)에 의해 정제하여 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메톡시아세토니트릴 (100 mg, 수율 16%)을 담황색 액체로서 수득하였다.
2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메톡시에탄아민
이 화합물을 실시예 94 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메톡시아세토니트릴로부터 합성하였고 (100 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메톡시에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메톡시에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 회백색 고체로서 합성하였다 (44 mg, 수율 22%).
실시예 118
2-(4-(4-플루오로페닐)티아졸-2-일)프로판니트릴
-78℃에서 THF (10 mL) 중 2-(4-(4-플루오로페닐)티아졸-2-일)아세토니트릴 (500 mg, 2.29 mmol)의 교반 용액에 LiHMDS (THF 중 1M; 2.06 mL, 2.06 mmol)를 첨가하고, 반응 혼합물을 -78℃에서 10분 동안 교반하였다. 이어서, THF (2 mL) 중 아이오도메탄 (0.12 mL, 2.06 mmol)을 적가하고, 반응 혼합물을 -78℃에서 30분 동안 교반하였다. 반응 혼합물을 EtOAc로 희석하고, 포화 수성 NH4Cl 용액, 물, 염수로 세척하고, 무수 황산나트륨 상에서 건조시켰다. 유기 층을 감압 하에 농축시켜 조 생성물을 수득하였으며, 이를 텔레다인(Teledyne) ISCO 자동화 칼럼 크로마토그래피 시스템 (0 - 30% EtOAc / 헥산)에 의해 정제하여 2-(4-(4-플루오로페닐)티아졸-2-일)프로판니트릴 (180 mg, 수율 34%)을 수득하였다.
2-(4-(4-플루오로페닐)티아졸-2-일)프로판-1-아민
실온에서 THF (3 mL) 중 2-(4-(4-플루오로페닐)티아졸-2-일)프로판니트릴 (140 mg, 0.6 mmol)의 교반 용액에 보란 (THF 중 1M; 3.01 mL, 3.01 mmol)을 첨가하고, 반응 혼합물을 실온에서 1시간 동안 교반한 다음, 40℃에서 1시간 동안 가열하였다. 이어서, 반응 혼합물을 0℃로 냉각시키고, MeOH (~5eq, ~0.2 mL)로 켄칭하고, 실온으로 가온되도록 하고, 여기에 2N HCl 용액을 pH ~ 2까지 첨가하였다. 반응 혼합물을 65℃에서 15분 동안 환류한 다음, 실온으로 냉각시키고, 감압 하에 농축시켰다. 수득한 고체를 에테르로 2회 및 디클로로메탄으로 추가로 2회 연화처리하였다. 나머지 고체를 물 (~50 mL) 중에 용해시키고, NaOH 펠릿을 사용하여 pH ~ 11로 염기성화시켰다. 이어서, 수성 혼합물을 에테르로 추출하고, 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 2-(4-(4-플루오로페닐)티아졸-2-일)프로판-1-아민 (75 mg, 수율 52%)을 수득하였으며, 이를 추가 정제 없이 달성하였다;
N-(2-(4-(4-플루오로페닐)티아졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
2-(4-(4-플루오로페닐)티아졸-2-일)프로판-1-아민 (50 mg, 0.21 mmol), 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산 (54.62 mg, 0.21 mmol), N-(3-디메틸아미노프로필)-N'-에틸카르보디이미드 히드로클로라이드 (EDC) (81.12 mg, 0.42 mmol), 및 1-히드록시벤조트리아졸 (HOBt) (45.74 mg, 0.39 mmol)을 실온에서 디클로로메탄 (3 mL) 중에 용해시켰다. 이어서, 디이소프로필에틸아민 (DIEA) (0.147 mL, 0.85 mmol)을 실온에서 도입하고, 반응 혼합물을 실온에서 밤새 교반하였다. 반응 혼합물을 디클로로메탄 (100 mL)으로 희석하고, 물 (1 X 20 mL) 및 염수 (1 X 20 mL)로 세척하였다. 이어서, 유기 층을 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 조 생성물을 수득하였으며, 이를 텔레다인 ISCO 자동화 칼럼 크로마토그래피 시스템 (0 - 30% EtOAc / 헥산)에 의해 정제하여 N-(2-(4-(4-플루오로페닐)티아졸-2-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드 (36 mg, 36% 수율)를 수득하였다.
실시예 119
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤즈아미드
이 화합물을 실시예 118 단계 3에 기재된 바와 같이 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤조산으로부터 합성하였다 (0.022 g, 수율 15%).
실시예 120
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (45 mg, 수율 27%).
실시예 121
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 5-(5-트리플루오로메틸-[1,2,4]옥사디아졸-3-일)-니코틴산으로부터 합성하였다 (19 mg, 수율 13%).
실시예 122
2-(3-브로모페닐)-2-메틸프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(3-브로모페닐)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였고 (1.2 g, 사용된 조물질), 이를 추가 정제 없이 달성하였다.
2-(3-브로모페닐)-2-메틸프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(3-브로모페닐)-2-메틸프로판니트릴로부터 합성하였고 (1.3 g, 사용된 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(3-브로모페닐)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(3-브로모페닐)-2-메틸프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (90 mg, 수율 83%).
N-(2-([1,1'-비페닐]-3-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
THF (1.2 mL) 중 N-(2-(3-브로모페닐)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드 (30 mg, 0.064 mmol) 및 페닐 보론산 (39 mg, 0.32 mmol)의 용액을 질소로 탈기하였다. 디클로로 [1,1' 비스(디-tert-부틸포스피노)]페로센 팔라듐(II) (5 mg, 0.006 mmol) 및 1M 탄산칼륨 (1.2 mL)을 첨가하였다. 반응물을 60℃에서 밤새 가열하였다. 반응물을 에틸 아세테이트로 추출하고, 황산나트륨 상에서 건조시켰다. 조물질을 30% EA/헥산을 사용하는 정제용 TLC에 의해 정제하여 N-(2-([1,1'-비페닐]-3-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드 (6 mg, 수율 18%)를 수득하였다.
실시예 123
N-(2-(4'-플루오로-[1,1'-비페닐]-3-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 122 단계 4에 기재된 바와 같이 N-(2-(3-브로모페닐)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드 및 4-플루오로보론산으로부터 합성하였다 (8 mg, 25% 수율).
실시예 124
2-(4-(3,5-디플루오로페닐)티아졸-2-일)아세토니트릴
이 화합물을 실시예 1 단계 1에 기재된 바와 같이 2-브로모-1-(3,5-디플루오로페닐)에타논으로부터 합성하였다 (3 g, 수율 94%).
4-(4-(3,5-디플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-브로모에틸 에테르를 사용하여 2-(4-(3,5-디플루오로페닐)티아졸-2-일)아세토니트릴로부터 합성하였다 (1.0 g, 수율 59%).
(4-(4-(3,5-디플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 4-(4-(3,5-디플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-카르보니트릴로부터 합성하였고 (1 g, 조물질), 이를 추가 정제 없이 달성하였다.
N-((4-(4-(3,5-디플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-(3,5-디플루오로페닐)티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (20 mg, 10% 수율).
실시예 125
2-(4-(3,5-디플루오로페닐)티아졸-2-일)-2-메틸프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(4-(3,5-디플루오로페닐)티아졸-2-일)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였다 (1.0 g, 수율 60%).
2-(4-(3,5-디플루오로페닐)티아졸-2-일)-2-메틸프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(4-(3,5-디플루오로페닐)티아졸-2-일)-2-메틸프로판니트릴로부터 합성하였고 (1 g, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(4-(3,5-디플루오로페닐)티아졸-2-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(4-(3,5-디플루오로페닐)티아졸-2-일)-2-메틸프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (85 mg, 수율 24%).
실시예 126
2-(2-페닐옥사졸-4-일)에탄아민
이 화합물을 실시예 64 단계 4에 기재된 바와 같이 2-(2-페닐옥사졸-4-일)아세토니트릴로부터 합성하였고 (400 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-페닐옥사졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-페닐옥사졸-4-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (40 mg, 수율 25%).
실시예 127
N-(2-(2-페닐옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-페닐옥사졸-4-일)에탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (42 mg, 수율 32%).
실시예 128
2-(2-(4-클로로페닐)옥사졸-4-일)에탄아민
이 화합물을 실시예 64 단계 4에 기재된 바와 같이 2-(2-(4-클로로페닐)옥사졸-4-일)아세토니트릴로부터 합성하였고 (466 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-클로로페닐)옥사졸-4-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-클로로페닐)옥사졸-4-일)에탄아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (4 mg, 2% 수율).
실시예 129
N-(2-(2-(4-클로로페닐)옥사졸-4-일)에틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-클로로페닐)옥사졸-4-일)에탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (14 mg, 10% 수율).
실시예 130
N-(2-메틸-2-(2-페닐옥사졸-4-일)프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-메틸-2-(2-페닐옥사졸-4-일)프로판-1-아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (19 mg, 13% 수율).
실시예 131
2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(2-(4-클로로페닐)옥사졸-4-일)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였고 (100 mg, 조물질), 이를 추가 정제 없이 달성하였다.
2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸프로판-1-아민
이 화합물을 실시예 1 단계 3에 기재된 바와 같이 2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸프로판니트릴로부터 합성하였고 (100 mg, 조물질), 이를 추가 정제 없이 달성하였다.
N-(2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-클로로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (8 mg, 수율 14%).
실시예 132
메틸 3-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미도)프로파노에이트
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 메틸 3-아미노프로파노에이트 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (120 mg, 수율 75%).
3-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미도)프로판산
수산화나트륨 용액 (0.2 mL, 5 M)을 THF/MeOH/물 (4:1:1, 15 mL) 중 메틸 3-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미도)프로파노에이트의 용액에 첨가하였다. 반응물을 30분 동안 교반하고, 2M HCl로 산성화시켰다. 반응물을 에틸 아세테이트로 여러 번 추출하고, 황산나트륨 상에서 건조시키고, 그대로 사용하였다.
N-(2-(3-페닐-1,2,4-옥사디아졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
HOBt (47 mg, 0.35 mmol), EDCI (67 mg, 0.35 mmol) 및 디이소프로필에틸아민 (0.7 mL, 1.0 mmol)을 디클로로메탄 (3.5 mL) 중 3-(3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미도)프로판산 (115 mg, 0.35 mmol) 및 N'-히드록시벤즈이미드아미드 (47 mg, 0.35 mmol)의 용액에 몇 방울의 DMF와 함께 첨가하였다. 반응물을 1시간 동안 교반한 다음, 톨루엔을 첨가하고, 반응물을 90℃로 1시간 동안 가열하였다. 반응물을 에틸 아세테이트로 희석하고, 유기 층을 포화 중탄산나트륨으로 세척하고, 황산나트륨 상에서 건조시켰다. 생성물을 역상에 의해 물/아세토니트릴을 사용하여 정제하여 N-(2-(3-페닐-1,2,4-옥사디아졸-5-일)에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드 (10 mg, 수율 7%)를 수득하였다.
실시예 133
에틸 1-벤질-5-페닐-1H-피라졸-3-카르복실레이트
벤질 브로마이드 (696 mg, 4.01 mmol)를 DMF (8 mL) 중 에틸 5-페닐-1H-피라졸-3-카르복실레이트 (880 mg, 4.1 mmol) 및 탄산칼륨 (562 mg, 4.01)에 첨가하였다. 반응물을 몇 시간 동안 교반한 다음, 물로 희석하였다. 혼합물을 에틸 아세테이트로 여러 번 세척하고, 합한 추출물을 황산나트륨 상에서 건조시켰다. 용매를 감압 하에 제거하고, 잔류물을 ISCO에 의해 0-100% 에틸 아세테이트/헥산 구배를 사용하여 정제하여 에틸 1-벤질-5-페닐-1H-피라졸-3-카르복실레이트 (1.3g, 정량적)를 수득하였다.
(1-벤질-5-페닐-1H-피라졸-3-일)메탄올
0℃에서, LAH (1.8 mL, 3.7 mmol, THF 중 2M)를 THF (18 mL) 중 에틸 1-벤질-5-페닐-1H-피라졸-3-카르복실레이트 (560 mg, 1.8 mmol)에 첨가하였다. 반응물을 10분 동안 교반한 다음, 실온으로 1시간 동안 가온하였다. 최소량의 물을 반응에 천천히 첨가하고, 이어서 5M 수산화나트륨 1 mL를 첨가하였다. 반응물을 30분 동안 교반하고, 황산나트륨을 첨가하고, 고체를 여과에 의해 제거하였다. 여과물을 감압 하에 농축시켜 조 (1-벤질-5-페닐-1H-피라졸-3-일)메탄올을 수득하였으며, 이를 추가 정제 없이 달성하였다.
1-벤질-3-(브로모메틸)-5-페닐-1H-피라졸
사브로민화탄소 (2.5 g, 7.6 mmol)에 이어서 트리페닐포스핀 (2.0 g, 7.6 mmol)을 디클로로메탄 (38 mL) 중 (1-벤질-5-페닐-1H-피라졸-3-일)메탄올 (1.0 g, 3.8 mmol)에 0℃에서 첨가하였다. LCMS에 의해 모니터링하여 반응이 완결된 후, 반응물을 메틸렌 클로라이드로 세척하는 실리카를 통해 여과한 다음, 0-30% 에틸 아세테이트/헥산을 이용하는 ISCO에 의해 정제하여 1-벤질-3-(브로모메틸)-5-페닐-1H-피라졸 (0.5 g, 수율 43%)을 수득하였다.
2-(1-벤질-5-페닐-1H-피라졸-3-일)아세토니트릴
1-벤질-3-(브로모메틸)-5-페닐-1H-피라졸 (200 mg, 0.6 mmol) 및 시안화나트륨 (30 mg, 0.6 mmol)을 DMF (6 mL) 중에서 교반하였다. 수시간 후, 추가량의 시안화나트륨 (60 mg, 1.2 mmol)을 반응물에 첨가하였다. 물 중 25% 수산화암모늄 용액을 반응에 첨가하고, 반응 혼합물을 에틸 아세테이트로 추출하였다. 합한 추출물을 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 2-(1-벤질-5-페닐-1H-피라졸-3-일)아세토니트릴 (130 mg, 수율 80%)을 수득하였다.
2-(1-벤질-5-페닐-1H-피라졸-3-일)-2-메틸프로판니트릴
이 화합물을 실시예 1 단계 2에 기재된 바와 같이 2-(1-벤질-5-페닐-1H-피라졸-3-일)아세토니트릴로부터 아이오도메탄을 사용하여 합성하였다 (500 mg, 수율 91%).
2-(1-벤질-5-페닐-1H-피라졸-3-일)-2-메틸프로판-1-아민
2-(1-벤질-5-페닐-1H-피라졸-3-일)-2-메틸프로판니트릴 (50 mg, 0.16 mmol)을 THF (1.6 mL) 중에 용해시켰다. 보란-테트라히드로푸란 (0.8 mL, 1M 용액)을 첨가하고, 반응물을 60℃로 3시간 동안 가열하였다. 최소량의 물을 첨가하여 반응물을 켄칭하였다. 에틸 아세테이트를 첨가하고, 이어서 황산나트륨을 첨가하고, 고체를 여과에 의해 제거하였다. 여과물을 감압 하에 농축시켜 2-(1-벤질-5-페닐-1H-피라졸-3-일)-2-메틸프로판-1-아민 (50 mg, 조물질)을 수득하였으며, 이를 추가 정제 없이 달성하였다.
2-메틸-2-(5-페닐-1H-피라졸-3-일)프로판-1-아민
2-(1-벤질-5-페닐-1H-피라졸-3-일)-2-메틸프로판-1-아민 (50 mg, 0.2 mmol)을 메탄올/진한 황산 (5:1, 5 mL) 중에서 탄소 상 5% 팔라듐 (350 mg)과 함께 수소 분위기 하에 교반하였다. 수시간 후, 추가량의 탄소 상 팔라듐 (350 mg)을 첨가하였다. 3일 후 출발 물질이 남아 있는 채로 반응을 중지시켰다. 용액을 탈기하고, 셀라이트를 통해 여과하였다. 메탄올을 진공 하에 제거하고, 1M 탄산칼륨을 반응물이 염기성일 때까지 첨가하였다. 슬러리를 30% 이소프로판올/클로로포름으로 여러 번 추출하였다. 합한 유기 층을 황산나트륨 상에서 건조시키고, 감압 하에 농축시켜 2-메틸-2-(5-페닐-1H-피라졸-3-일)프로판-1-아민을 수득하였으며, 이를 추가 정제 없이 달성하였다.
N-(2-메틸-2-(3-페닐-1H-피라졸-5-일)프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-메틸-2-(5-페닐-1H-피라졸-3-일)프로판-1-아민 및 3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤조산으로부터 합성하였다 (10 mg, 수율 11%).
실시예 134
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)프로판-1-아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 황색 고체로서 합성하였다 (75 mg, 수율 28%).
실시예 135
N-(2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로필)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(4-(4-클로로페닐)티아졸-2-일)-2-메틸프로판-1-아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 합성하였다 (18 mg, 수율 16%).
실시예 136
N-((4-([1,1'-비페닐]-3-일)-1-메틸피페리딘-4-일)메틸)-5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-([1,1'-비페닐]-3-일)-1-메틸피페리딘-4-일)메탄아민 및 5-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)니코틴산으로부터 회백색 고체로서 합성하였다 (60 mg, 수율 30%).
실시예 137
5-브로모티오펜-3-카르브알데히드
무수 염화알루미늄 (5.9 g, 44.5 mmol)을 CH2Cl2 (100 mL) 중 티오펜-3-카르브알데히드 (2.0 g, 17.8 mmol)의 용액에 온도를 0℃에서 유지하면서 2시간에 걸쳐 조금씩 첨가하였다. 이어서, CH2Cl2 (50 mL) 중 브로민 (2.56 g, 16.0 mmol)을 반응 혼합물에 0℃에서 적가하였다. 반응 혼합물을 40℃에서 1시간 동안 환류하고, 물로 켄칭하고, CH2Cl2로 추출하였다. 합한 추출물을 무수 Na2SO4 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 60-120 메쉬, 용리액 석유 에테르 중 10% EtOAc)에 의해 정제하여 5-브로모티오펜-3-카르브알데히드 (3.0 g, 수율 88%)를 수득하였다.
1-(5-브로모티오펜-3-일)-2,2,2-트리플루오로에탄올
이 화합물을 실시예 88 단계 1에 기재된 바와 같이 5-브로모티오펜-3-카르브알데히드로부터 황색 액체로서 합성하였다 (3.0 g, 수율 73%).
1-(5-브로모티오펜-3-일)-2,2,2-트리플루오로에타논
이 화합물을 실시예 47 단계 2에 기재된 바와 같이 1-(5-브로모티오펜-3-일)-2,2,2-트리플루오로에탄올로부터 합성하였다 (1.85 g, 수율 62%).
3-(4-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤조산
이 화합물을 실시예 88 단계 3에 기재된 바와 같이 1-(5-브로모티오펜-3-일)-2,2,2-트리플루오로에타논 및 3-카르복시페닐보론산으로부터 황색 고체로서 합성하였다 (150 mg, 수율 16%).
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(4-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 3-(4-(2,2,2-트리플루오로아세틸)티오펜-2-일)벤조산으로부터 합성하였다 (75 mg, 수율 30%).
실시예 138
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-옥소에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 47 단계 2에 기재된 바와 같이 N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드로부터 회백색 고체로서 합성하였다 (150 mg, 수율 43%).
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-옥소에틸)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드 (150 mg, 0.33 mmol)를 건조 THF (10 mL) 중에 용해시키고, 반응 혼합물을 -50℃로 냉각시켰다. 이어서, 메틸마그네슘 클로라이드 (0.32 mL, 0.98 mmol, THF 중 3M)을 첨가하고, 반응 혼합물을 -50℃에서 3시간 동안 교반하였다. 반응 혼합물을 수성 포화 NH4Cl 용액으로 켄칭하고, EtOAc로 추출하였다. 합한 추출물을 물 및 염수로 세척하고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 25-30% EtOAc)에 이어서 정제용 TLC (석유 에테르 중 용리액 30% EtOAc)에 의해 정제하여 N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-히드록시프로필)-3-(5-(트리플루오로메틸)-1,2,4-옥사디아졸-3-일)벤즈아미드 (15 mg, 수율 10%)를 백색 고체로서 수득하였다.
실시예 139
1-(4-브로모푸란-2-일)-2,2,2-트리플루오로에탄올
이 화합물을 실시예 88 단계 1에 기재된 바와 같이 4-브로모푸란-2-카르브알데히드로부터 연황색 액체로서 합성하였다 (1.0 g, 수율 72%).
1-(4-브로모푸란-2-일)-2,2,2-트리플루오로에타논
이 화합물을 실시예 47 단계 2에 기재된 바와 같이 1-(4-브로모푸란-2-일)-2,2,2-트리플루오로에탄올로부터 합성하였고 (0.8 g, 수율 81%), 이를 후속 단계에 추가 정제 없이 사용하였다.
3-(5-(2,2,2-트리플루오로아세틸)푸란-3-일)벤조산
이 화합물을 실시예 88 단계 3에 기재된 바와 같이 1-(4-브로모푸란-2-일)-2,2,2-트리플루오로에타논 및 3-카르복시페닐보론산으로부터 연황색 고체로서 합성하였다 (150 mg, 수율 26%).
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(2,2,2-트리플루오로아세틸)푸란-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 3-(5-(2,2,2-트리플루오로아세틸)푸란-3-일)벤조산으로부터 합성하였다 (30 mg, 수율 14%).
실시예 140
1-(4-브로모티오펜-2-일)-2,2,2-트리플루오로에탄올
이 화합물을 실시예 88 단계 1에 기재된 바와 같이 4-브로모티오펜-2-카르브알데히드로부터 연황색 액체로서 합성하였다 (2.0 g, 수율 74%).
1-(4-브로모티오펜-2-일)-2,2,2-트리플루오로에타논
이 화합물을 실시예 47 단계 2에 기재된 바와 같이 1-(4-브로모티오펜-2-일)-2,2,2-트리플루오로에탄올로부터 암갈색 액체로서 합성하였다 (1.5 g, 수율 75%).
3-(5-(2,2,2-트리플루오로아세틸)티오펜-3-일)벤조산
이 화합물을 실시예 88 단계 3에 기재된 바와 같이 1-(4-브로모티오펜-2-일)-2,2,2-트리플루오로에타논 및 3-카르복시페닐보론산으로부터 연황색 고체로서 합성하였다 (400 mg, 수율 46%).
N-(2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로필)-3-(5-(2,2,2-트리플루오로아세틸)티오펜-3-일)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 2-(2-(4-플루오로페닐)옥사졸-4-일)-2-메틸프로판-1-아민 및 3-(5-(2,2,2-트리플루오로아세틸)티오펜-3-일)벤조산으로부터 합성하였다 (30 mg, 수율 17%).
실시예 141
3-시아노-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤즈아미드
이 화합물을 실시예 8 단계 6에 기재된 바와 같이 (4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메탄아민 및 3-시아노벤조산으로부터 백색 고체로서 합성하였다 (6.6 g, 수율 89%).
(N'-히드록시카르밤이미도일)-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤즈아미드
이 화합물을 실시예 1 단계 4에 기재된 바와 같이 3-시아노-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤즈아미드로부터 합성하였고 (6.8 g, 조물질), 이를 추가 정제 없이 사용하였다.
에틸 3-(3-(((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)카르바모일) 페닐)-1,2,4-옥사디아졸-5-카르복실레이트
3-(N'-히드록시카르밤이미도일)-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤즈아미드 (6.8 g, 15.57 mmol)를 무수 피리딘 (68 mL) 중에 용해시키고, 반응 혼합물을 0℃로 냉각시켰다. 에틸 클로로옥소아세테이트 (5.2 mL, 46.73 mmol)를 적가하고, 반응 혼합물을 60℃에서 1시간 동안 가열하고, 1.5N HCl 용액으로 켄칭하고, EtOAc로 희석하였다. 유기 층을 물 및 염수로 세척하고, 무수 황산나트륨 상에서 건조시키고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액 석유 에테르 중 25-30% EtOAc)에 의해 정제하여 에틸 3-(3-(((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)카르바모일)페닐)-1,2,4-옥사디아졸-5-카르복실레이트 (6.8 g, 수율 87%)를 수득하였다.
3-(5-(히드록시메틸)-1,2,4-옥사디아졸-3-일)-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤즈아미드
에틸 3-(3-(((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)카르바모일)페닐)-1,2,4-옥사디아졸-5-카르복실레이트 (1.0 g, 1.93 mmol)를 무수 THF (20 mL) 중에 용해시키고, 반응 혼합물을 0℃로 냉각시켰다. 수소화붕소리튬 (1.15 mL, 2.3 mmol, THF 중 2M)을 첨가하고, 반응 혼합물을 30분 동안 교반하고, 얼음으로 켄칭하고, EtOAc로 희석하였다. 유기 층을 물 및 염수로 세척하고, 감압 하에 농축시켰다. 조 생성물을 칼럼 크로마토그래피 (실리카 겔 60-120 메쉬, 용리액: 석유 에테르 중 70-80% EtOAc)에 의해 정제하여 3-(5-(히드록시메틸)-1,2,4-옥사디아졸-3-일)-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤즈아미드 (300 mg, 수율 32%)를 수득하였다.
3-(5-포르밀-1,2,4-옥사디아졸-3-일)-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤즈아미드
이 화합물을 실시예 47 단계 2에 기재된 바와 같이 3-(5-(히드록시메틸)-1,2,4-옥사디아졸-3-일)-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤즈아미드로부터 합성하였다 (340 mg, 수율 57%).
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(2,2,2-트리플루오로-1-히드록시에틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 88 단계 1에 기재된 바와 같이 3-(5-포르밀-1,2,4-옥사디아졸-3-일)-N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)벤즈아미드로부터 합성하였다 (30 mg, 수율 17%).
N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(2,2,2-트리플루오로아세틸)-1,2,4-옥사디아졸-3-일)벤즈아미드
이 화합물을 실시예 47 단계 2에 기재된 바와 같이 N-((4-(4-페닐티아졸-2-일)테트라히드로-2H-피란-4-일)메틸)-3-(5-(2,2,2-트리플루오로-1-히드록시에틸)-1,2,4-옥사디아졸-3-일)벤즈아미드로부터 합성하였다 (5 mg, 수율 17%).
제약 조성물
실시예 A
정제를 통상적인 방법을 사용하여 제조하고, 하기와 같이 제제화하였다:
실시예 B
캡슐을 통상적인 방법을 사용하여 제조하고, 다음과 같이 제제화하였다:
히스톤 데아세틸라제 9 (HDAC9) 억제 검정:
신규 히스톤 데아세틸라제 9 (HDAC9) 억제제를 시험관내 생화학적 기능적 검정에서 특성화하였다. 검정은 HDAC9에 의한 형광 기질의 탈아세틸화로 인한 증가된 형광 신호를 측정하였다. 상업적으로 입수가능한 기질은 클래스 IIa HDAC-특이적이고, 아세틸화 리신 잔기를 함유하고, 탈아세틸화 후 트립신 절단시 형광 신호를 방출하였다.
구체적으로, 100% DMSO에 다양한 농도로 희석된 시험 화합물을 우선 384-웰 검정 플레이트로 분배하였다. 이어서, 완전 검정 완충제 (50 mM 트리스(Tris)-HCl, pH 8.0, 137 mM NaCl, 2.7 mM KCl, 1 mM MgCl2, 0.05% BSA & 0.005% 트윈(Tween) 20) 중 재조합 HDAC9 이소형 4 (BPS 바이오사이언스(BPS Bioscience)로부터 구입)를 멀티드롭 콤비(Multidrop Combi (써모 사이언티픽(Thermo Scientific))를 사용하여 각 웰에 첨가한 후 (5 uL/웰), 5 uL/웰 기질 (BPS 사이언티픽으로부터 구입, 4.5 uM 최종)을 첨가하였다. 실온에서 45분 인큐베이션 후, 10 uL 2x 현상제 용액 (40 uM 트립신 및 20 uM 트리코스타틴 A를 갖는 검정 완충제)을 첨가하였다. 이어서, 플레이트를 실온에서 1시간 인큐베이션한 후, 엔비전(Envision) (퍼킨 엘머 (Perkin Elmer)) 플레이트 판독기에서 450 nm의 형광 세기 모드에서 판독하였다. 각 시험 웰 중 화합물에 의한 HDAC9 활성의 퍼센트 억제를, DMSO만을 함유하는 대조군 웰에서의 형광 신호로 정규화함으로써 계산하였다. 시험 화합물의 pIC50 값을 100 uM 최종 화합물 농도에서 시작하는 11 포인트 3x 희석 시리즈로부터, 액티비티베이스5(ActivityBase5) 데이터 분석 도구 (IDBS)를 사용하여 비-선형 곡선 피팅으로부터 계산하였다.
용량 반응 실험을 위해, 정규화된 데이터를 방정식 y = a + (b-a)/(1+(10^x/10^c)^d) (식에서, a는 최소 % 활성이고, b는 최대 % 활성이고, c는 pIC50이고, d는 힐(Hill) 기울기임)을 사용하는 ABASE/XC50에 의해 피팅하였다.
pIC50을 최소 2회 실험에 대해 평균하여 평균 값을 측정하였다. 상기 방법을 사용하여 측정하였을 때, 실시예 1 내지 141의 화합물은 4.8 초과의 pIC50을 나타내었다. 예를 들어, 실시예 21, 32, 78, 110 및 132의 화합물이 상기 방법에서 평균 pIC50 > 6으로 HDAC9를 억제하였다.
참고문헌: