KR100633270B1 - 5-아자퀴녹살린계 화합물, 이의 합성 방법, 이를 사용한 세린/트레오닌 단백질키나제 작용의 조절 방법 및 이를 포함하는 약제학적 조성물 - Google Patents
5-아자퀴녹살린계 화합물, 이의 합성 방법, 이를 사용한 세린/트레오닌 단백질키나제 작용의 조절 방법 및 이를 포함하는 약제학적 조성물 Download PDFInfo
- Publication number
- KR100633270B1 KR100633270B1 KR1020007003656A KR20007003656A KR100633270B1 KR 100633270 B1 KR100633270 B1 KR 100633270B1 KR 1020007003656 A KR1020007003656 A KR 1020007003656A KR 20007003656 A KR20007003656 A KR 20007003656A KR 100633270 B1 KR100633270 B1 KR 100633270B1
- Authority
- KR
- South Korea
- Prior art keywords
- compound
- azaquinoxaline
- cells
- serine
- protein kinase
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4985—Pyrazines or piperazines ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Abstract
본 발명은 부분적으로는 5-아자퀴녹살린계 화합물을 사용하여 세린/트레오닌 단백질 키나제의 작용을 조절하는 방법에 관한 것이다. 상기 방법은 RAF 같은 세린/트레오닌 단백질 키나제를 발현하는 세포를 포함한다. 부가적으로, 본 발명은 본 발명에 의해 확인된 화합물을 사용하여 유기체내에서 세린/트레오닌 단백질 키나제 관련된 비정상적인 상태를 예방하고 치료하는 방법을 기술한다. 또한, 본 발명은 5-아자퀴녹살린 화합물 및 이러한 화합물을 포함하는 약제학적 조성물에 관한 것이다.
세린/트레오닌 단백질 키나제, 5-아자퀴녹살린, RAF, MEK, MAPK, 표현형, 세포 증식, 촉매 활성, 상호 작용, 항체, 포스페이트, SAQAR 화합물, 신호 전달 경로, 환원제, 라니 니켈
Description
본 발명의 배경 기술에 대한 하기 기술은 본 발명을 이해하는 것을 보조하기 위해서 제공되며 본 발명에 대한 선행 기술로 인정하고자 하는 것은 아니다.
세포성 신호 전달 과정은 다양한 세포성 과정을 조절하는 외부 자극이 세포 내부로 중계되는 근본적인 메카니즘이다. 신호 전달 과정의 주요한 생화학적 메카니즘의 하나는 단백질의 가역적인 인산화와 관련되며, 이는 이들의 구조 및 작용을 변화시킴으로써 성숙한 단백질의 활성을 조절하는 것을 가능하게 한다.
진핵생물에서 가장 특성화된 단백질 키나제들은 세린, 트레오닌, 및 티로신 잔기의 알콜 부분에서 단백질을 인산화시킨다. 이러한 키나제는 주로 2개의 그룹, 세린 및 트레오닌을 인산화시키는데 특이적인 것들, 및 티로신을 인산화시키는데 특이적인 것들로 분류된다. "이중 특이성" 키나제로서 인용되는 일부 키나제들은 세린/트레오닌 잔기 뿐만 아니라 티로신을 인산화시킬 수 있다.
단백질 키나제는 또한 세포내 이들의 위치에 의해서도 특성화될 수 있다. 일부 키나제들은 세포막 외부에서 리간드와 결합할 수 있는 트랜스막 수용체 단백 질이다. 리간드와의 결합은 수용체 단백질 키나제의 촉매 활성을 변화시킨다. 일부는 트랜스막 도메인이 결핍된 비-수용체 단백질이다. 비-수용체 단백질 키나제는 세포막 내부면 내지 핵에 걸친 다양한 세포성 구획에서 발견할 수 있다.
많은 키나제들이 조절성 케스케이드(cascade)에 관계하며, 이의 기질들은 인산화 상태에서 이의 활성이 조절되는 기타 키나제들을 포함할 수 있다. 궁극적으로 하류 효능인자(effector)의 활성은 상기 경로의 활성화로부터 기인하는 인산화에 의해 조절된다.
세린/트레오닌 키나제 계열은 세포 성장, 이동, 분화, 유전자 발현, 근육 수축, 글루코스 대사, 세포성 단백질 합성, 및 세포 주기 조절을 조정하는 케스케이드(cascade)를 포함하는 신호 전달 케스케이드의 많은 단계들을 조절하는 구성원들을 포함한다.
세린 및 트레오닌 잔기에 대해 단백질 표적을 인산화시키는 비-수용체 단백질 키나제의 예는 RAF이다. RAF는 유사분열물질 활성화된 단백질 키나제(MAPK)를 인산화시켜 활성화시키는 단백질 키나제 같은 기타 단백질 키나제의 촉매 활성을 조절한다. RAF 그 자체는 막 결합된 단백질 RAS에 의해 활성화되며, RAS는 차례로 표피 성장 인자 수용체(EGFR) 및 혈소판-유도된 성장 인자 수용체(PDGFR) 같은 리간드 활성화된 티로신 수용체 단백질 키나제에 반응하여 활성화된다. 세포성 사건을 조절하는데 있어서 RAF의 생물학적 중요성은 RAF의 변형된 형태가 유기체내에서 암을 유발시킬 수 있다는 발견에 의해 강조된다. 악성 종양에서 RAF의 중요성에 대한 증거는 문헌[Monia et al., 1996, Nature Medicine 2: 668]에 의해 제공되며, 도면 및 표를 포함하는 이의 전문은 참조로 본원에 인용된다.
암 및 기타 질환의 신규한 치료 방법을 찾고자 하는 노력으로, 생의학 연구자 및 화학자들은 단백질 키나제의 작용을 억제하는 분자를 디자인하고, 합성하고 시험해 왔다. 일부 작은 유기 분자들은 단백질 키나제 작용을 조절하는 화합물의 한 부류를 형성한다. 단백질 키나제의 작용을 억제하는 것으로 공지된 분자들의 예는 비스 모노사이클릭, 비사이클릭 또는 헤테로사이클릭 아릴 화합물[PCT WO 제92/20642호], 비닐렌-아자인돌 유도체[PCT WO 제94/14808호], 1-사이클로프로필-4-피리딜-퀴놀론[미국 특허 제5,330,992호], 스티릴 화합물[Levitzki, et al., 미국 특허 제5,217,999호, 및 표제 "Styryl Compounds which Inhibit EGF Receptor Protein Tyrosine Kinase, Lyon & Lyon Docket No. 208/050], 스티릴-치환된 피리딜 화합물[미국 특허 제5,302,606호], 특정 퀴나졸린 유도체[유럽 특허원 제0 566 266 A1호], 셀레오인돌 및 셀레나이드[PCT WO 제94/03427호], 트리사이클릭 폴리하이드록실 화합물[PCT WO 제92/21660호], 및 벤질포스폰산 화합물[PCT WO 제91/15495호]이다.
세포막을 횡단할 수 있고 산 가수분해에 내성이 있는 화합물은, 환자에게 경구 투여된 후 높은 생체 유용성이 있을 수 있기 때문에, 잠재적으로 유리한 치료제이다. 그러나, 이러한 단백질 키나제 억제제의 다수는 단백질 키나제의 작용을 매우 약하게 억제할 뿐이다. 부가적으로, 다수는 다양한 단백질 키나제를 억제하며 따라서 질병에 대한 치료제로서 복합적인 부작용을 유발하게 된다.
암을 치료하기 위한 화합물의 개발에서 현저한 진전이 있었음에도 불구하고, 당해 분야에서는 특정 단백질 키나제의 작용을 조절할 수 있는 화합물을 형성시키는 특정 구조 및 치환 패턴을 확인할 필요가 있다.
발명의 요약
본 발명은 부분적으로, 5-아자퀴녹살린 기초한 화합물을 사용하여 세린/트레오닌 단백질 키나제의 작용을 조절하는 방법에 관한 것이다. 상기 방법은 RAF 같은 세린/트레오닌 단백질 키나제를 발현시키는 세포를 포함한다. 부가적으로, 본 발명은 본원에서 기술된 방법에 의해 확인된 화합물을 사용하여 유기체내에서 세린/트레오닌 단백질 키나제-관련된 비정상적인 상태를 예방하고 치료하는 방법을 기술한다. 추가로, 본 발명은 본 발명의 방법에 의해 확인된 화합물을 포함하는 약제학적 조성물에 관한 것이다.
I. 세린/트레오닌 단백질 키나제 작용을 조절하는 화합물을 스크리닝하는 방법
본 발명의 방법은 수용체성 및 세포질성 세린/트레오닌 단백질 키나제 모두의 작용을 조절하는 방법을 제공한다. 이러한 방법은 시험관내 및 생체내 모두에서 상기 효소를 조절하는 방법을 제공한다. 시험관내 적용에 있어서, 본 발명의 방법은 부분적으로 세린/트레오닌 단백질 키나제의 작용을 조절하는 화합물을 동정하는 방법에 관한 것이다.
따라서, 제1 양태에서, 본 발명은 아자벤즈이미다졸-기초한 화합물을 사용하여 세린/트레오닌 단백질 키나제의 작용을 조절하는 방법을 특징으로 한다. 아자 벤즈이미다졸 화합물은 임의로 유기 그룹에 의해 치환된다. 상기 방법은 세린/트레오닌 단백질 키나제를 발현하는 세포를 상기 화합물과 접촉시킴을 포함한다.
용어 "작용"은 세린/트레오닌 단백질 키나제의 세포성 역할을 의미한다. 세린/트레오닌 단백질 키나제 계열은 세포 성장, 이동, 분화, 유전자 발현, 근육 수축, 글루코스 대사, 세포성 단백질 합성, 및 세포 주기 조절을 조정하는 케스케이드를 포함하는, 신호 전달 케스케이드에서 수 많은 단계들을 조절하는 구성원을 포함한다.
본 발명의 내용에서 용어 "촉매 활성"은 단백질 키나제가 기질을 인산화시키는 속도를 정의한다. 촉매 활성은 예를 들면, 시간 함수로서 생성물로 전환된 기질의 양을 결정함으로써 측정할 수 있다. 기질의 인산화는 단백질 키나제의 활성 부위에서 일어난다. 활성 부위는 일반적으로 공동(cavity)으로, 여기에서 기질이 단백질 키나제에 결합하여 인산화된다.
본원에서 사용되는 바와 같이, 용어 "기질"은 세린/트레오닌 단백질 키나제에 의해서 인산화되는 분자를 의미한다. 기질은 바람직하게는 펩타이드이며 보다 바람직하게는 단백질이다. 단백질 키나제 RAF와 관련하여, 바람직한 기질은 MEK 및 MEK 기질 MAPK이다.
용어 "활성화시키다"는 단백질 키나제의 세포성 작용을 증가시킴을 의미한다. 상기 단백질 키나제 작용은 바람직하게는 천연 결합 상대와의 상호 작용이며 가장 바람직하게는 촉매 활성이다.
용어 "억제하다"는 단백질 키나제의 세포성 작용을 감소시킴을 의미한다. 상기 단백질 키나제 작용은 바람직하게는 천연 결합 상대와의 상호 작용이며 가장 바람직하게는 촉매 활성이다.
용어 "조절하다"는 단백질 키나제와 천연 결합 상대간의 복합체가 형성되는 가능성을 증가시키거나 감소시킴으로써 단백질 키나제의 작용을 변화시키는 것을 의미한다. 조절 인자는 바람직하게는 단백질 키나제와 천연 결합 상대간의 복합체 형성 가능성을 증가시키고, 보다 바람직하게는 단백질 키나제에 노출되는 화합물의 농도에 따라서 단백질 키나제와 천연 결합 상대간의 복합체 형성 가능성을 증가시키거나 감소시키며, 가장 바람직하게는 단백질 키나제와 천연 결합 상대간의 복합체 형성 가능성을 감소시킨다. 조절 인자는 바람직하게는 단백질 키나제의 촉매 활성을 활성화시키고, 보다 바람직하게는 단백질 키나제에 노출되는 화합물의 농도에 따라서 단백질 키나제의 촉매 활성을 증가시키거나 감소시키며, 가장 바람직하게는 단백질 키나제의 촉매 활성을 억제시킨다.
용어 "복합체"는 2개 이상의 분자가 서로 결합하는 어셈블리를 의미한다. 신호 전달 복합체는 종종 서로 결합된 2개 이상의 단백질 분자를 함유한다. 예를 들면, 단백질 티로신 수용체 단백질 키나제, GRB2, SOS, RAF, 및 RAS는 유사분열물질성 리간드에 반응하여 결합하여 신호 전달 복합체를 형성한다.
용어 "천연 결합 상대"는 세포내에서 단백질 키나제에 결합하는 폴리펩타이드를 의미한다. 천연 결합 상대는 단백질 키나제 신호 전달 과정에서 신호를 전달하는 역할을 수행할 수 있다. 단백질 키나제와 천연 결합 상대간의 상호 작용에서의 변화는 그 자체가 상호 작용이 형성되는 증가된 또는 감소된 가능성으로서, 또는 단백질 키나제/천연 결합 상대 복합체의 증가된 또는 감소된 농도로서 나타날 수 있다.
단백질 키나제 천연 결합 상대는 높은 친화도로 단백질 키나제의 세포내 영역에 결합할 수 있다. 높은 친화도는 10-6M 이하에서 평형 결합 상수를 나타낸다. 부가적으로, 천연 결합 상대는 또한 단백질 키나제 세포내 영역과 일시적으로 상호 작용하여 이를 화학적으로 변형시킬 수 있다. 단백질 키나제 천연 결합 상대는 SRC 동족체 2(SH2) 또는 3(SH3) 도메인, 기타 포스포릴 티로신 결합(PTB) 도메인, 구아닌 뉴클레오타이드 교환 인자, 단백질 포스파타제, 및 기타 단백질 키나제를 포함하지만, 이에 제한되지는 않는 그룹으로부터 선택된다. 단백질 키나제와 천연 결합 상대간의 상호 작용에서 변화를 측정하는 방법은 당해 분야에서 용이하게 이용할 수 있다.
용어 "세린/트레오닌 단백질 키나제"는 세린 및 트레오닌 잔기상에서 단백질을 인산화시키는 기타 효소와 10% 이상의 아미노산 동일성을 갖는 아미노산 서열을 갖는 효소를 의미한다. 세린/트레오닌 단백질 키나제는 세린 및 트레오닌 잔기상에서 단백질에 포스페이트의 부가를 촉매한다. 세린/트레오닌 단백질 키나제는 막 결합 단백질 또는 세포성 단백질로서 존재할 수 있다.
본원에서 사용되는 바와 같이 용어 "접촉시키는"이란 본 발명의 5-아자퀴녹살린 화합물을 포함하는 용액을 상기 방법의 세포를 둘러싼 액체 배지와 함께 혼합함을 의미한다. 상기 화합물을 포함하는 용액은 또한 또 다른 성분, 즉 디메틸설 폭사이드(DMSO)를 포함할 수 있으며, 이는 5-아자퀴녹살린 화합물 또는 화합물들이 상기 방법의 세포내로 흡수되는 것을 촉진시킨다. 5-아자퀴녹살린 화합물을 포함하는 용액은 피펫-기초 장치 또는 주사기-기초 장치 같은 전달 장치를 사용하여 세포를 둘러싼 배지에 부가할 수 있다.
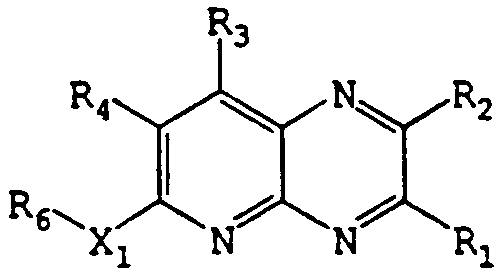
용어 "5-아자퀴녹살린계 화합물"은 화학적 치환체로 치환된 5-아자퀴녹살린 유기 화합물을 의미한다. 5-아자퀴녹살린 화합물은 하기의 일반적인 구조를 갖는다:
본 발명에 인용되는 용어 "치환된"이란 임의 수의 화학적 치환체로 유도체화된 5-아자퀴녹살린 화합물을 의미한다.
바람직한 양태에서, 본 발명은 단백질 키나제가 RAF인 세린/트레오닌 단백질 키나제의 작용을 조절하는 방법에 관한 것이다.
RAF 단백질 키나제는 세린 또는 트레오닌 잔기상에서 단백질 표적을 인산화시킨다. 이러한 한 가지 단백질 표적은 유사분열물질 활성화된 단백질 키나제(MAPK)를 인산화시켜 결과적으로 활성화시키는 단백질 키나제(MEK)이다. RAF 그 자체는 표피 성장 인자 수용체(EGFR) 및 혈소판-유도된 성장 인자 수용체(PDGFR) 같은 유사분열물질-자극된 수용체 단백질 키나제에 반응하여 막-결합된 구아닌 트리포스페이트 가수분해 효소 RAS에 의해 활성화된다.
본 발명의 방법은 세포에서 RAF 단백질 키나제의 작용을 조절하는 화합물을 검출할 수 있다. RAF는 단백질 키나제 (MEK)를 인산화시키고 이는 차례로 유사분열물질-활성화된 단백질 키나제 (MAPK)를 활성화시킨다. RAF에 의한 MEK의 인산화 만을 모니터하는 분석법은 MEK의 인산화 수준이 현저하지 않기 때문에 민감성이 떨어진다. 이러한 민감성 문제를 해결하기 위해서, 본 발명의 분석법에서는 MEK 및 MAPK 모두의 인산화를 수행한다. MAPK 인산화 신호는 MEK 인산화 신호를 증폭시키며 RAF-의존적인 인산화가 효소-결합된 면역흡착 분석법 같은 분석법에서 수행되는 것을 가능하게 한다. 부가적으로, 본 발명의 분석법은 많은 화합물이 신속하게 짧은 시간내에 모니터링될 수 있게 매우 효율적인 방식으로 수행된다.
또 다른 양태에서, 본 발명은 세린/트레오닌 단백질 키나제를 발현하는 세포를 상기 화합물과 접촉시키고 세포에 대한 효과를 모니터링하는 단계를 포함하는, 세린/트레오닌 단백질 키나제의 작용을 조절하는 화합물을 동정하는 방법을 기술한다.
용어 "모니터링하는"이란 상기 방법의 세포에 대한 상기 화합물의 부가 효과를 관찰하는 것을 의미한다. 상기 효과는 세포 표현형, 세포 증식, 단백질 키나제 촉매 활성, 또는 단백질 키나제와 천연 결합 상대간의 상호 작용에서의 변화로 나타날 수 있다.
용어 "효과"는 세포 표현형 또는 세포 증식에서의 변화 또는 불변을 기술한다. "효과"는 또한 단백질 키나제의 촉매 활성에서의 변화 또는 불변을 기술할 수 있다. "효과"는 또한 단백질 키나제와 천연 결합 상대간의 상호 작용에서의 변화 또는 불변을 나타낼 수 있다.
본 발명의 바람직한 양태는 상기 효과가 세포 표현형의 변화 또는 불변인, 세린/트레오닌 단백질 키나제의 작용을 조절하는 화합물을 동정하는 방법에 관한 것이다.
용어 "세포 표현형"은 세포 또는 조직의 외관, 또는 세포 또는 조직의 작용을 의미한다. 세포 표현형의 예는 세포 크기(감소 또는 증가), 세포 증식(세포의 증가 또는 감소된 수), 세포 분화(세포 형태의 변화 또는 불변), 세포 생존, 어팝토시스(세포 사멸), 또는 대사 영양분의 이용(예를 들면, 글루코스 흡수)이다. 세포 표현형의 변화 또는 불변은 당해 분야에 공지된 기술에 의해 용이하게 측정된다.
또 다른 바람직한 양태에서, 본 발명은 효과가 세포 증식에서의 변화 또는 불변인, 세린/트레오닌 단백질 키나제의 작용을 조절하는 화합물을 동정하는 방법에 관한 것이다.
용어 "세포 증식"은 일군의 세포가 분열하는 속도를 의미한다. 용기내에서 성장하는 세포의 수는 통상적인 광학 현미경을 사용하여 한정된 부피내의 세포 수를 시각적으로 계수함으로써 당해 분야의 숙련자에 의해 정량화할 수 있다. 대안적으로, 세포 증식율은 적합한 배지내에서 세포의 밀도를 광학적으로 또는 전도적으로 계수하는 실험실 장치로 정량화할 수 있다.
또 다른 바람직한 양태에서, 본 발명은 효과가 세린/트레오닌 단백질 키나제와 천연 결합 상대의 상호 작용에서의 변화 또는 불변인, 세린/트레오닌 단백질 키나제의 작용을 조절하는 화합물을 동정하는 방법에 관한 것이다.
본 발명의 내용에서 용어 "상호 작용"은 단백질 키나제의 세포내 영역 및 천연 결합 상대 또는 화합물 사이에 형성되는 복합체를 기술한다. 용어 "상호 작용"은 또한 본 발명의 화합물과 연구중인 단백질 키나제의 세포내 영역 및 세포외 영역 사이에서 형성되는 복합체로 확장시킬 수 있다. 세포질성 단백질 키나제는 어떠한 세포외 영역을 갖지 않지만, 수용체 단백질 키나제는 세포외 및 세포내 영역 모두를 갖는다.
본원에서 사용되는 바와 같이 용어 "세포내 영역"은 세포 내부에 존재하는 단백질 키나제의 부분을 의미한다. 본원에서 사용되는 바와 같이 용어 "세포외 영역"은 세포 외부에 존재하는 단백질 키나제의 부분을 의미한다.
바람직한 양태에서, 본 발명은 (a) 세포를 용해시켜 세린/트레오닌 단백질 키나제를 포함하는 용해물을 제조하고; (b) 세린/트레오닌 단백질 키나제를 항체에 흡착시키고; (c) 흡착된 세린/트레오닌 단백질 키나제를 기질 또는 기질들과 항온 처리하며; (d) 기질 또는 기질들을 고체 지지체 또는 항체에 흡착시키는 단계들을 추가로 포함하는, 세린/트레오닌 단백질 키나제의 작용을 조절하는 화합물을 동정하는 방법에 관한 것이다. 세포 상에서 효과를 모니터링하는 단계는 기질 또는 기질들의 포스페이트 농도를 측정하는 것을 포함한다.
본원에서 사용되는 바와 같이 용어 "용해시키는"이란 세포 내부 내용물이 개방되도록 세포의 온전한 상태를 파괴하는 방법을 의미한다. 세포 용해는 당해 분야의 숙련자에게 공지된 많은 기술들에 의해 달성된다. 상기 방법은 바람직하게는 초음파 또는 세포 전단 기술에 의해 달성되며, 보다 바람직하게는 세제 기술에 의해 달성된다.
본원에서 사용되는 바와 같이 용어 "항체"는 단백질 키나제에 특이적으로 결합하는 단백질 분자를 의미한다. 항체는 바람직하게는 한가지 부류의 단백질 키나제에 결합하며 보다 바람직하게는 RAF 단백질 키나제에 특이적으로 결합한다.
본원에서 사용되는 바와 같이 용어 "특이적으로 결합한다"는 또 다른 단백질 키나제 또는 세포성 단백질 보다 높은 친화도로 단백질 키나제에 결합하는 항체를 의미한다. 단백질 키나제에 특이적으로 결합하는 항체는 임의의 다른 단백질 키나제 또는 세포성 단백질 보다 더 높은 농도의 특정 단백질 키나제와 결합할 것이다.
본원에서 사용되는 바와 같이 용어 "흡착시키는"이란 항체 또는 고체 지지체의 표면에 분자를 결합시키는 것을 의미한다. 고체 지지체의 예는 포스포셀룰로스 같은 화학적으로 변형된 셀룰로스 및 나일론이다. 항체는 당해 분야의 통상의 숙련자에게 숙지된 기술을 사용하여 고체 지지체에 결합시킬 수 있다. 문헌 참조[예를 들면, Harlo & Lane, Antibodies, A Laboratory Manual, 1989, Cold Spring Harbor Laboratories].
본원에서 사용되는 바와 같이 용어 "포스페이트 농도를 측정하는"이란 당해 분야의 통상의 숙련자에게 일반적으로 공지된 기술을 의미한다. 이러한 기술들은 기질내의 포스페이트 농도를 정량화하거나 기질내의 포스페이트의 상대적인 양을 결정하는 것과 관련된다. 이러한 기술들은 기질을 막에 흡착시키고 방사성 측정법으로 기질내의 포스페이트의 양을 검출하는 것을 포함할 수 있다.
또 다른 바람직한 양태에서, 본 발명은 (a) 세포를 용해시켜 RAF를 포함하는 용해물을 제조하고; (b) RAF를 항체에 흡착시키고; (c) 흡착된 RAF를 MEK 및 MAPK와 함께 항온 처리하며; (d) MEK 및 MAPK를 고체 지지체, 또는 항체 또는 항체들에 흡착시키는 단계를 추가로 포함하는 세린/트레오닌 단백질 키나제의 작용을 조절하는 화합물을 동정하는 방법에 관한 것이다. 세포상에서 효과를 측정하는 단계는 상기 MEK 및 MAPK의 포스페이트 농도를 모니터링하는 것을 포함한다.
바람직한 양태에서, 본 발명은, 5-아자퀴녹살린계 화합물이 본원에서 정의한 바와 같은 화학식 I에서 제시하거나 본원에서 정의한 이의 서브 그룹 중 하나에서 제시한 구조를 갖는, 세린/트레오닌 단백질 키나제의 작용을 조절하는 화합물을 동정하는 방법에 관한 것이다.
용어 "화합물"은 상기 화합물 또는 이의 약제학적으로 허용되는 염, 에스테르, 아미드, 프로드럭, 이성체, 또는 대사산물을 의미한다.
용어 "약제학적으로 허용되는 염"이란 상기 화합물의 생물학적 활성 및 특성을 손상시키지 않는 화합물의 제형을 의미한다. 약제학적 염은 본 발명의 화합물을 염산, 브롬화수소산, 황산, 질산, 인산, 메탄설폰산, 에탄설폰산, p-톨루엔설폰산, 살리실산 등과 같은 무기 또는 유기산과 반응시켜 수득할 수 있다.
용어 "프로드럭"은 생체내에서 모 드럭으로 전환되는 제제를 의미한다. 프로드럭은 특정 상황하에서 모 드럭 보다 투여하기가 보다 용이할 수 있다. 예를 들면, 프로드럭은 경구 투여하기에 생체 적합성인데 모 드럭은 그렇지 않을 수 있거나, 프로드럭이 용해도를 개선시켜 정맥내 투여를 가능하게 할 수도 있다.
또 다른 바람직한 양태에서, 본 발명은 5-아자퀴녹살린계 화합물이 화학식 I에서 제시된 구조를 가지며, SAQAR 화합물로 이루어지는 그룹으로부터 선택되는, 세린/트레오닌 단백질 키나제의 작용을 조절하는 화합물을 동정하는 방법에 관한 것이다.
용어 "SAQAR 화합물"은 화학식 I에서 제시되며 하기 표에서 A-1 내지 A-90에 걸쳐 열거된 구조를 갖는 5-아자퀴녹살린계 화합물의 그룹을 의미한다:
II. 비정상 상태의 예방 및 치료 방법
또 다른 양태에서, 본 발명은 유기체내에서 비정상 상태의 예방 및 치료 방법에 관한 것이다. 상기 방법은 (a) 본원에서 제공하는 임의의 제한으로 화학식 I로 본원에서 명시한 바와 같은 본 발명의 화합물을 유기체에 투여하며; (b) 비정상 상호 작용을 촉진하거나 파괴하는 단계를 포함한다.
용어 "유기체"는 하나 이상의 세포를 포함하는 모든 살아있는 실체를 의미한다. 유기체는 하나의 진핵 세포와 같이 단순하거나 포유동물처럼 복합체일 수 있 다. 바람직한 양태에서, 유기체는 사람 또는 포유동물이다.
용어 "예방하는"이란 유기체가 비정상 상태에 놓이거나 비정상 상태로 발전할 가능성을 감소시키거나 제거하는 본 발명의 방법을 의미한다.
용어 "치료하는"이란 유기체내에서 치료학적 효과를 가지며 비정상 상태를 최소한 부분적으로 경감시키거나 파괴시키는 본 발명의 방법을 의미한다.
용어 "치료학적 효과"란 비정상 상태(예를 들면, 암)를 야기하거나 비정상 상태에 기여하는 세포 성장을 억제하는 것을 의미한다. 용어 "치료학적 효과"는 또한 비정상 상태를 야기하거나 비정상 상태에 기여하는 성장 인자를 억제하는 것을 의미한다. 치료학적 효과는 비정상 상태의 증상 하나 이상을 어느 정도까지 경감시킨다. 암의 치료와 관련하여, 치료학적 효과는 (a) 종양 크기 감소; (b) 종양 전이 억제(즉, 완화 또는 정지); (c) 종양 성장 억제; (d) 비정상 상태와 관련된 증상 하나 이상을 어느 정도까지 경감시키는 것 중 하나 이상을 의미한다. 백혈병에 대한 효능을 나타내는 화합물은 본원에 기술된 바와 같이 확인할 수 있지만, 단 전이를 억제하기 보다는, 대신 상기 화합물은 세포 증식 또는 세포 성장을 완화시키거나 감소시킬 수 있다.
용어 "비정상 상태"란 유기체내에서 이의 정상 작용으로부터 벗어난 유기체의 세포 또는 조직에서의 작용을 의미한다. 비정상 상태는 세포 증식, 세포 분화 또는 세포 생존과 관련될 수 있다.
비정상적인 세포 증식 상태는 섬유성 및 맥관막성 질환, 비정상적인 혈관형성 및 맥관형성 같은 암, 부상 치유, 건선, 당뇨병 및 염증을 포함한다.
비정상적인 분화 상태는 신경퇴행성 질환, 느린 부상 치유율, 및 조직 이식 기술을 포함하지만, 이에 제한되지는 않는다.
비정상적인 세포 생존 상태는 프로그램된 세포 사멸(어팝토시스) 경로가 활성화되거나 파괴되는 상태를 의미한다. 수 많은 단백질 키나제가 어팝토시스 경로에 관여한다. 단백질 키나제 중 하나의 작용에서 비정상화는 세포 불멸 또는 미성숙 세포 사멸을 초래할 수 있다.
세포 증식, 분화 및 생존은 당해 분야의 방법으로 쉽게 측정되는 현상이다. 이러한 방법은 시간(예를 들면, 일수)에 따라 현미경하에서 세포 수 또는 세포 외관을 관찰하는 것과 관련될 수 있다.
용어 "투여하는"이란 대략적으로 유기체의 세포 또는 조직내로 화합물을 공급하는 것, 보다 구체적으로는 혼입하는 방법에 관한 것이다. 비정상적인 상태는 유기체의 세포 또는 조직이 유기체 내부 또는 유기체 외부에 존재하는 경우 예방 또는 치료될 수 있다. 유기체 외부에 존재하는 세포는 세포 배양 디쉬내에서 유지되거나 성장시킬 수 있다. 유기체내에서 수득한 세포에 있어서, 당해 분야에서 경구, 비경구, 표피, 주사 및 에어로졸 적용을 포함하지만, 이에 제한되지는 않는 화합물을 투여하는 많은 기술들이 존재한다. 유기체 외부의 세포에 있어서, 당해 분야에서 세포 미세주사 기술, 형질전환 기술, 및 운반체 기술을 포함하지만, 이에 제한되지는 않는 화합물을 투여하는 많은 기술들이 존재한다.
바람직한 양태에서, 본 발명은 5-아자퀴녹살린계 화합물은 본원에서 정의한 바와 같이 화학식 I에서 제시된 구조 또는 본원에서 제시된 이의 서브 그룹 중 하나를 갖는, 유기체에서 비정상적인 상태를 예방하거나 치료하는 방법에 관한 것이다.
다른 바람직한 양태에서, 본 발명은 화학식 I에서 제시된 구조를 갖는 5-아자퀴녹살린계 화합물이 SAQAR 화합물로 이루어지는 그룹으로부터 선택되는, 유기체내에서 비정상적인 상태를 예방하거나 치료하는 방법에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 유기체가 포유동물인, 유기체내에서 비정상적인 상태를 예방하거나 치료하는 방법에 관한 것이다.
용어 "포유동물"은 마우스, 랫트, 래빗, 기니아 피그, 및 염소, 보다 바람직하게는 원숭이 및 꼬리없는 원숭이, 및 가장 바람직하게는 사람 같은 유기체를 의미한다.
또한 바람직한 양태에서, 본 발명은 유기체에서 암 또는 섬유성 질환인 비정상적인 상태를 예방하거나 치료하는 방법에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 암이 폐암, 난소암, 유방암, 뇌암, 축내성 뇌암, 결장암, 전립선암, 육종, 카포시 육종, 흑색종, 및 신경교종으로 이루어지는 그룹으로부터 선택되는, 유기체에서 비정상적인 상태를 예방하거나 치료하는 방법에 관한 것이다.
또한 또 다른 바람직한 양태에서, 본 발명은 세린/트레오닌 단백질 키나제와 천연 결합 상대간의 상호 작용으로 특성화되는 신호 전달 과정의 이상과 관련된 비정상적인 상태에 적용되는, 유기체에서 비정상적인 상태를 예방하거나 치료하는 방법에 관한 것이다.
용어 "신호 전달 경로"는 신호의 전달을 의미한다. 일반적으로, 세포외 신호는 세포막을 통해 전달되어 세포내 신호가 된다. 이후, 이러한 신호는 세포성 반응을 자극할 수 있다. 상기 용어는 또한 세포내에서 전적으로 전달되는 신호를 포함한다. 신호 전달 과정에 관여하는 폴리펩타이드 분자는 전형적으로 수용체 및 비-수용체성 단백질 키나제, 수용체 및 비-수용체 단백질 포스파타제, 뉴클레오타이드 교환 인자, 및 전사 인자들이다.
신호 전달 과정과 관련하여, 용어 "비정상"이란 유기체내에서 초과- 또는 감소-발현되거나, 야생형 단백질 키나제 활성 보다 이의 촉매 활성이 저하 또는 상승되도록 돌연변이되거나, 더 이상 천연 결합 상대와 상호 작용하지 않도록 돌연변이되거나, 또 다른 단백질 키나제 또는 단백질 포스파타제에 의해 변형되지 않거나 천연 결합 상대와 더 이상 상호 작용하지 않게 된 단백질 키나제를 의미한다.
용어 "비정상적인 상호 작용을 촉진하거나 파괴하는"이란 본 발명의 화합물을 유기체내의 세포 또는 조직으로 투여함으로써 달성할 수 있는 방법을 의미한다. 화합물은 복합체 접촉면에서 다수의 원자들과 적합한 상호 작용을 형성함으로써 단백질 키나제와 천연 결합 상대간의 상호 작용을 촉진시킬 수 있다. 대안으로, 화합물은 복합체 접촉면에서 원자들 사이에 형성된 적합한 상호 작용을 손상시킴으로써 단백질 키나제와 천연 결합 상대간의 상호 작용을 억제시킬 수 있다. 또 다른 바람직한 양태에서, 본 발명은 세린/트레오닌 단백질 키나제가 RAF인, 유기체내에서 비정상적인 상태를 예방하거나 치료하는 방법에 관한 것이다.
III. 본 발명의 화합물 및 약제학적 조성물
또 다른 양태에서, 본 발명은 화학식 I에서 제시된 구조를 갖는 5-아자퀴녹살린 화합물에 관한 것이다.
화학식 I
상기식에서,
(a) R1, R2 및 R6은 독립적으로,
(i) 수소;
(ii) 포화되거나 불포화된 알킬;
(iii) 화학식 NX2X3의 아민(여기서, X2 및 X3은 독립적으로 수소, 포화되거나 불포화된 알킬, 및 5- 또는 6-원 아릴 또는 헤테로아릴 환 잔기로 이루어지는 그룹으로부터 선택된다);
(iv) 할로겐 또는 트리할로메틸;
(v) 화학식 -CO-X4의 케톤(여기서, X4는 수소, 알킬, 및 5- 또는 6-원 아릴 또는 헤테로아릴 잔기로 이루어지는 그룹으로부터 선택된다);
(vi) 화학식 -(X5)n-COOH의 카복실산 또는 화학식 -(X6)n-COO-X
7의 에스테르(여기서, X5, X6 및 X7은 독립적으로 알킬 및 5- 또는 6-원 아릴 또는 헤테로아릴 잔 기로 이루어지는 그룹으로부터 선택되며, n은 0 또는 1이다);
(vii) 화학식 (X8)n-OH의 알콜 또는 화학식 -(X8)n-O-X9
의 알콕시 잔기[여기서, X8 및 X9는 독립적으로 수소, 포화되거나 불포화된 알킬, 및 5- 또는 6-원 아릴 또는 헤테로아릴 환 잔기(이때, 환은 독립적으로 알킬, 할로겐, 트리할로메틸, 카복실레이트, 니트로, 및 에스테르로 이루어지는 그룹으로부터 선택되는 치환체 하나 이상에 의해 임의로 치환된다)로 이루어지는 그룹으로부터 선택되며, n은 0 또는 1이다];
(viii) 화학식 -NHCOX10의 아미드[여기서, X10은 알킬, 하이드록실, 및 5- 또는 6-원 아릴 또는 헤테로아릴 환 잔기(이때, 환은 독립적으로 알킬, 할로겐, 트리할로메틸, 카복실레이트, 니트로, 또는 에스테르로 이루어지는 그룹으로부터 선택되는 치환체 하나 이상에 의해 임의로 치환된다)로 이루어지는 그룹으로부터 선택된다];
(ix) -SO2NX11X12(여기서, X11 및 X12는 독립적으로 수소, 알킬 및 5- 또는 6-원 아릴 또는 헤테로아릴 환 잔기로 이루어지는 그룹으로부터 선택된다);
(x) 알킬, 할로겐, 트리할로메틸, 카복실레이트, 니트로, 및 에스테르 잔기로 이루어지는 그룹으로부터 독립적으로 선택된 1개 내지 3개의 치환체로 임의로 치환된 5- 또는 6-원 아릴 또는 헤테로아릴 환 잔기;
(xi) 화학식 -CO-H의 알데하이드; 및
(xii) 화학식 -SO2-X13의 설폰(여기서, X13은 포화되거나 불포화된 알킬 및 5- 또는 6-원 아릴 또는 헤테로아릴 잔기로 이루어지는 그룹으로부터 선택된다)으로 이루어지는 그룹으로부터 선택되며;
(b) X1은 질소, 황 및 산소로 이루어지는 그룹으로부터 선택된다.
용어 "포화된 알킬"이란 어떠한 알켄 또는 알킨 잔기를 함유하지 않는 알킬 잔기를 의미한다. 알킬 잔기는 측쇄 또는 비-측쇄일 수 있다.
용어 "불포화된 알킬"이란 알켄 또는 알킨 잔기 하나 이상을 함유하는 알킬 잔기를 의미한다. 알킬 잔기는 측쇄 또는 비-측쇄일 수 있다.
용어 "아민"은 화학식 NR1R2[여기서, R1 및 R2는 독립적으로 수소, 포화되거나 불포화된 알킬, 및 5- 또는 6-원 아릴 또는 헤테로아릴 환 잔기(이때, 환은 독립적으로 알킬, 할로겐, 트리할로메틸, 카복실레이트, 니트로 및 에스테르 잔기로 이루어지는 그룹으로부터 선택된 치환체 하나 이상으로 임의로 치환된다)로 이루어지는 그룹으로부터 선택된다]의 화학적 잔기를 의미한다.
용어 "아릴"은 접합된 pi 전자계를 갖는 환 하나 이상을 가지며 카보사이클릭 아릴(예를 들면, 페닐) 및 헤테로사이클릭 아릴 그룹(예를 들면, 피리딘) 모두를 포함하는 방향족 그룹을 의미한다. 용어 "카보사이클릭"은, 공유 결합적으로 폐환된 환 구조 하나 이상을 함유하며 환의 골격을 형성하는 원자들이 모두 탄소 원자인 화합물을 의미한다. 따라서 상기 용어는 카보사이클릭을 환 골격이 탄소 이외의 원자 하나 이상을 함유하는 헤테로사이클릭 환으로부터 구별되게 한다. 용어 "헤테로아릴"은 하나 이상의 헤테로사이클릭 환을 함유하는 아릴 그룹을 의미한다.
용어 "할로겐"은 불소, 염소, 브롬 및 요오드로 이루어지는 그룹으로부터 선택되는 원자를 의미한다.
용어 "케톤"은 화학식 -(R)n-CO-R'를 갖는 화학적 잔기(여기서, R 및 R'은 포화되거나 불포화된 알킬 및 5- 또는 6-원 아릴 또는 헤테로아릴 잔기로 이루어지는 그룹으로부터 선택되며, n은 0 또는 1이다)를 의미한다.
용어 "카복실산"은 화학식 -(R)n-COOH를 갖는 화학적 잔기(여기서, R은 포화되거나 불포화된 알킬 및 5- 또는 6-원 아릴 또는 헤테로아릴 잔기로 이루어지는 그룹으루부터 선택되며, n은 0 또는 1이다)를 의미한다.
용어 "에스테르"는 화학식 -(R)n-COOR'를 갖는 화학적 잔기(여기서, R 및 R'는 독립적으로 포화되거나 불포화된 알킬 및 5- 또는 6-원 아릴 또는 헤테로아릴 잔기로 이루어지는 그룹으로부터 선택되며, n은 0 또는 1이다)를 의미한다.
용어 "알콜"은 화학식 -ROH[여기서, R은 수소, 포화되거나 불포화된 알킬 및 5- 또는 6-원 아릴 또는 헤테로아릴 환 잔기(이때, 환은 독립적으로 알킬, 할로겐, 트리할로메틸, 카복실레이트, 니트로 및 에스테르 잔기로 이루어지는 그룹으로부터 선택되는 치환체 하나 이상으로 임의로 치환된다)로 이루어지는 그룹으로부터 선택된다]의 화학적 치환체를 의미한다.
용어 "아미드"는 화학식 -NHCOR[여기서, R은 수소, 알킬, 하이드록실, 및 5- 또는 6-원 아릴 또는 헤테로아릴 환 잔기(이때, 환은 독립적으로 알킬, 할로겐, 트리할로메틸, 카복실레이트, 니트로 또는 에스테르로 이루어지는 그룹으로부터 선택되는 치환체 하나 이상으로 임의로 치환된다)로 이루어지는 그룹으로부터 선택된다]의 화학적 치환체를 의미한다.
용어 "알콕시 잔기"는 화학식 -OR(여기서, R은 수소 또는 포화되거나 불포화된 알킬 잔기이다)의 화학적 치환체를 의미한다.
용어 "알데하이드"는 화학식 -(R)n-CHO(여기서, R은 포화되거나 불포화된 알킬 및 5- 또는 6-원 아릴 또는 헤테로아릴 잔기이며, n은 0 또는 1이다)를 갖는 화학적 잔기를 의미한다.
용어 "설폰"은 화학식 -SO2-R(여기서, R은 포화되거나 불포화된 알킬 및 5- 또는 6-원 아릴 또는 헤테로아릴 잔기로 이루어지는 그룹으로부터 선택된다)을 갖는 화학적 잔기를 의미한다.
또 다른 바람직한 양태에서, 본 발명은 R3 및 R4가 독립적으로 수소 및 포화되거나 불포화된 알킬로 이루어진 그룹으로부터 선택되는, 화학식 I에서 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 R3 및 R4가 수소인, 화학식 I에서 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
다른 바람직한 양태에서, 본 발명은 R1 및 R2가 알킬, 수소, 포화되거나 불포화된 알킬, 및 할로겐, 트리할로메틸, 하이드록시, 알콕시, 카복실레이트, 니트로 및 에스테르 잔기로 이루어지는 그룹으로부터 독립적으로 선택되는 1개 내지 3개의 치환체로 임의로 치환되는 5- 또는 6-원 아릴 또는 헤테로아릴 환 잔기로 이루어지는 그룹으로부터 선택되는, 화학식 I에서 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 R1이 알킬, 할로겐, 하이드록시 및 알콕시 잔기로 이루어지는 그룹으로부터 독립적으로 선택되는 1개 내지 3개의 치환체로 임의로 치환되는 페닐인, 화학식 I에서 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 R1이 페닐인 화학식 I에서 제시된 구조를 갖는 5-아자퀴녹살린계 화합물이다.
또 다른 바람직한 양태에서, 본 발명은 R1이 4-하이드록시페닐인 화학식 I에서 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
다른 바람직한 양태에서, 본 발명은 R2가 수소, 포화되거나 불포화된 알킬, 및 알킬, 할로겐, 하이드록시 및 알콕시 잔기로 이루어진 그룹으로부터 독립적으로 선택된 1개 내지 3개의 치환체로 임의로 치환된 페닐로 이루어진 그룹으로부터 선택되는, 화학식 I에서 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 R2가 수소인 화학식 I에 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 R2가 메틸인 화학식 I에 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 R2가 페닐인 화학식 I에 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 X1이 질소 또는 산소인 화학식 I에 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 X1이 산소인 화학식 I에 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 X1이 질소인 화학식 I에 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
다른 바람직한 양태에서, 본 발명은 R6이 수소; 알킬, 할로겐, 트리할로메틸, 하이드록시, 알콕시, 카복실레이트, 니트로 및 에스테르 잔기로 이루어진 그룹으로부터 독립적으로 선택되는 1개 내지 3개의 치환체로 임의로 치환된 5- 또는 6원 아릴 또는 헤테로아릴 환에 의해 임의로 치환된 포화되거나 불포화된 알킬; 및 알킬, 할로겐, 트리할로메틸, 하이드록시, 알콕시, 카복실레이트, 니트로 및 에스테르 잔기로 이루어진 그룹으로부터 독립적으로 선택되는 1개 내지 3개의 치환체로 임의로 치환된 5- 또는 6-원 아릴 또는 헤테로아릴 환 잔기로 이루어지는 그룹으로부터 선택되는, 화학식 I에 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 R6 및 X1 잔기가 함께 SAQAR 치환체로 이루어지는 그룹으로부터 선택되는 화합물을 형성하는, 화학식 I에서 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
용어 "SAQAR 치환체"는 메톡시, 벤질아미노, 4-플루오로벤질아미노, 2-카복시벤질아미노, 3-카복시벤질아미노, 4-카복시벤질아미노, 2-니트로벤질아미노, 3-니트로벤질아미노, 4-니트로벤질아미노, 2-메틸벤질아미노, 3-메틸벤질아미노, 4-메틸벤질아미노, 2-클로로벤질아미노, 3-클로로벤질아미노, 4-클로로벤질아미노, 2-플루오로벤질아미노, 3-플루오로벤질아미노, 4-플루오로벤질아미노, 2-(트리플루오로메틸)벤질아미노, 3-(트리플루오로메틸)벤질아미노, 4-(트리플루오로메틸)벤질아미노, 펜에틸-1-아미노, 페닐아미노, 2-카복시페닐아미노, 3-카복시페닐아미노, 4-카복시페닐아미노, 2-니트로페닐아미노, 3-니트로페닐아미노, 4-니트로페닐아미노, 2-메틸페닐아미노, 3-메틸페닐아미노, 4-메틸페닐아미노, 2-클로로페닐아미노, 3-클로로페닐아미노, 4-클로로페닐아미노, 2-플루오로페닐아미노, 3-플루오로페닐아미노, 4-플루오로페닐아미노, 2-(트리플루오로메틸)페닐아미노, 3-(트리플루오로메틸)페닐아미노, 4-(트리플루오로메틸)페닐아미노, 피리드-2-아미노, 피리드-3-아 미노, 피리드-4-아미노, 및 피리드-2-메틸아미노로 이루어지는 치환체 그룹을 의미한다.
용어 "피리드-2-아미노"는 2번 위치에서 NH 그룹으로 치환된 피리딘 환을 의미한다. 유사하게, 용어 "피리드-3-아미노" 및 "피리드-4-아미노"는 각각, 3번 및 4번 위치에서 NH 그룹으로 치환된 피리딘 환을 의미한다.
또 다른 바람직한 양태에서, 본 발명은 SAQAR 화합물로 이루어진 그룹으로부터 선택되는, 화학식 I에서 제시된 구조를 갖는 5-아자퀴녹살린계 화합물에 관한 것이다.
IV. 본 발명의 합성 방법
또 다른 양태에서, 본 발명은 본원에서 정의되는 화학식 I의 구조 또는 본원에서 제시된 이의 서브 그룹 중 하나를 갖는 화합물, 또는 이의 염 및 생리학적으로 허용되는 담체 또는 희석제를 포함하는 약제학적 조성물에 관한 것이다.
바람직한 양태에서, 본 발명은 5-아자퀴녹살린계 화합물이 SAQAR 화합물로 이루어지는 그룹으로부터 선택되는, 약제학적 조성물에 관한 것이다.
용어 "약제학적 조성물"은 본 발명의 5-아자퀴녹살린 화합물과 희석제 또는담체 같은 기타 화학적 성분의 혼합물을 의미한다. 약제학적 조성물은 상기 화합물의 유기체로의 투여를 촉진시킨다. 경구, 주사, 에어로졸, 비경구 및 국소 투여를 포함하지만 이에 제한되지는 않는 다수의 화합물 투여 기술이 당해 분야에 존재한다. 약제학적 조성물은 또한 화합물을 염산, 브롬화수소산, 황산, 질산, 인산, 메탄설폰산, 에탄설폰산, p-톨루엔설폰산, 살리실산 등과 같은 무기산과 반응시켜 수득할 수 있다.
용어 "생리학적으로 허용되는"이란 상기 화합물의 생물학적 활성 및 특성을 손상시키기 않는 담체 또는 희석제를 의미한다.
용어 "담체"는 화합물의 세포 또는 조직내로의 혼입을 촉진하는 화학적 화합물을 의미한다. 예를 들면, 디메틸 설폭사이드(DMSO)는 수 많은 유기 화합물의 유기체의 세포 또는 조직내로의 흡수를 촉진하기 때문에 흔히 사용되는 담체이다.
용어 "희석제"는 화합물의 생물학적 활성 형태를 안정화시킬 뿐만 아니라 당해 화합물을 용해시키는 수 희석된 화학적 화합물을 의미한다. 완충액에 용해된 염이 당해 분야에서 희석제로 사용된다. 흔히 사용되는 완충액 중 하나는 인산염 완충된 염수이며, 이는 사람 혈액의 염 농도와 유사하기 때문이다. 완충염은 낮은 농도로 용액의 pH를 조절할 수 있으며, 완충된 희석액은 화합물의 생물학적 활성을 거의 변화시키지 않는다.
또 다른 양태에서, 본 발명은 (a) 2-아미노-6-클로로-3-니트로피리딘을 용매 중에서 염기의 존재하에 제2 반응물(제2 반응물은 알콜 및 아민으로 이루어진 그룹으로부터 선택된다)과 반응시켜 제1 중간체를 수득하고; (b) 제1 중간체를 촉매 및 환원제의 존재하에 1,2-디온과 반응시키며; (c) 최종 생성물을 정제하는 단계를 포함하는, 본 발명의 화합물을 합성하는 방법에 관한 것이다.
용어 "1,2-디온"은 화학식 R1-C(O)C(O)-R2(여기서, R1 및 R2는 독립적으로, 수소; 알킬, 할로겐, 트리할로메틸, 하이드록시, 알콕시, 카복실레이트, 니트로 및 에스테르 잔기로 이루어지는 그룹으로부터 독립적으로 선택되는 1개 내지 3개의 치환체로 임의로 치환된 5- 내지 6-원 아릴 또는 헤테로아릴 환 잔기로 임의로 치환되는 포화되거나 불포화된 알킬; 및 알킬, 할로겐, 트리할로메틸, 하이드록시, 알콕시, 카복실레이트, 니트로 및 에스테르 잔기로 이루어지는 그룹으로부터 독립적으로 선택되는 1개 내지 3개의 치환체로 임의로 치환되는 5- 내지 6-원 아릴 또는 헤테로아릴 환 잔기로 이루어지는 그룹으로부터 선택된다)의 화학적 잔기를 의미한다.
바람직한 양태에서, 본 발명은 용매가 n-부탄올인 본 발명의 화합물을 합성하는 방법에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 염기가 분말 탄산칼륨인 본 발명의 화합물을 합성하는 방법에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 제2 반응물이 SAQAR 반응물로 이루어지는 그룹으로부터 선택되는, 본 발명의 화합물을 합성하는 방법에 관한 것이다.
용어 "SAQAR 반응물"이란 메탄올, 벤질아민, 4-플루오로벤질아민, 2-카복시벤질아민, 3-카복시벤질아민, 4-카복시벤질아민, 2-니트로벤질아민, 3-니트로벤질아민, 4-니트로벤질아민, 2-메틸벤질아민, 3-메틸벤질아민, 4-메틸벤질아민, 2-클로로벤질아민, 3-클로로벤질아민, 4-클로로벤질아민, 2-플루오로벤질아민, 3-플루오로벤질아민, 4-플루오로벤질아민, 2-(트리플루오로메틸)벤질아민, 3-(트리플루오로메틸)벤질아민, 4-(트리플루오로메틸)벤질아민, 펜에틸-1-아민, 아닐린, 2-카복시아닐린, 3-카복시아닐린, 4-카복시아닐린, 2-니트로아닐린, 3-니트로아닐린, 4-니트로아닐린, 2-톨루이딘, 3-톨루이딘, 4-톨루이딘, 2-클로로아닐린, 3-클로로아닐린, 4-클로로아닐린, 2-플루오로아닐린, 3-플루오로아닐린, 4-플루오로아닐린, 2-(트리플루오로메틸)아닐린, 3-(트리플루오로메틸)아닐린, 4-(트리플루오로메틸)아닐린, 2-아미노피리딘, 3-아미노피리딘, 4-아미노피리딘 및 2-메틸아미노피리딘으로 이루어지는 반응물 그룹을 의미한다.
또 다른 바람직한 양태에서, 본 발명은 제3 반응물이 4-하이드록시페닐글리옥살, 1-페닐-1,2-프로판디온, 및 벤질로 이루어지는 그룹으로부터 선택되는, 본 발명의 화합물을 합성하는 방법에 관한 것이다.
본원에서 사용되는 바와 같이 용어 "촉매"는 반응물 그룹에 부가하는 경우, 시약이 반응하여 생성물을 형성하는 속도를 증가시킬 수 있는 화학적 분자를 의미한다. 수 많은 유형의 촉매가 당해 분야의 통상의 숙련자에게 숙지되어 있다.
바람직한 양태에서, 본 발명은 환원제가 수소인 본 발명의 화합물을 합성하는 방법에 관한 것이다.
또 다른 바람직한 양태에서, 본 발명은 촉매가 라니 니켈인 본 발명의 화합물을 합성하는 방법에 관한 것이다.
상기에서 기술된 본 발명의 요약은 비제한적이며 본 발명의 기타 특징 및 장점은 하기 바람직한 양태의 기술 및 특허청구범위로부터 명백할 것이다.
바람직한 양태의 기술
본 발명은 부분적으로 5-아자퀴녹살린계 화합물을 사용하여 세린/트레오닌 단백질 키나제의 작용을 조절하는 방법에 관한 것이다. 부가적으로, 본 발명은 부분적으로 세린/트레오닌 단백질 키나제의 작용을 조절하는 화합물을 동정하는 방법에 관한 것이다. 상기 방법은 RAF 같은 세린/트레오닌 단백질 키나제를 발현하는 세포를 포함한다.
RAF는 구아닌 트리포스페이트 가수분해 효소인, 활성화된 RAS에 결합하는 경우, 세포막에 보충되는 비-수용체성 단백질 키나제이다. RAS는 EGFR 또는 PDGFR 같은 활성화된 수용체 단백질 티로신 키나제가 어댑터 단백질, GRB2 및 구아닌 뉴클레오타이드 교환 인자, SOS에 결합하는 경우에 활성화된다. SOS는 RAS로부터 구아닌 디포스페이트를 제거하고, 이를 구아닌 트리포스페이트로 교체하여 결과적으 로 RAS를 활성화시킨다. 이후, RAS는 RAF에 결합하여 결과적으로 RAF를 활성화시킨다. 이후, RAF는 유사분열물질-활성화된 단백질 키나제(MAPK)를 인산화시켜 결과적으로 활성화시키는 키나제(MEK) 같은 기타 단백질 표적을 세린 및 트레오닌 잔기상에서 인산화시킬 수 있다. 따라서, RAF는 유사분열물질-활성화된 신호 전달에서 중간 조절 인자로서 작용한다.
세포내에서 RAF의 중요한 조절 역할로 인해, RAF의 아미노산 서열의 변형은 이의 작용을 변화시킬 수 있고 결과적으로 세포성 행동을 변화시킬 수 있다. 세포 증식에서 RAF의 역할은 RAF의 아미노산 서열에 대한 돌연변이는 종양 및 암과 관련된다는 관찰로부터 강조된다. 세포내에서 암을 유발하는 RAF에 대한 돌연변이는 조절되지 않는 촉매 활성을 나타내는 RAF 분자를 초래하기 때문에, RAF의 억제제는 이러한 세포내에서 암을 유발하는 세포 증식을 경감시키거나 중지시킬 수 있다.
본 발명의 방법은 세포내에서 단백질 키나제 RAF의 작용을 조절하는 화합물을 검출할 수 있다. RAF는 단백질 키나제(MEK)를 인산화시키고, 이는 차례로 유사분열물질-활성화된 단백질 키나제(MAPK)을 인산화시킨다. RAF에 의한 MEK의 인산화만을 모니터링하는 분석법은 MEK의 인산화가 현저하지 않기 때문에 민감성이 떨어진다. 이러한 민감성 문제를 해결하기 위해서, 본 발명의 분석법에서는 MEK 및 MAPK 모두의 인산화를 수행한다. MAPK 인산화 신호는 MEK 인산화 신호를 증폭시키며 이는 효소-결합된 면역흡착 분석법에서 RAF-의존성 인산화가 수행되는 것을 가능하게 한다. 부가적으로, 본 발명의 분석법은 바람직하게는 수 많은 화합물이 신속하게 짧은 시간에 모니터링될 수 있는 매우 효율적인 방식으로 수행된다.
본 발명의 방법은 RAF 단백질 키나제의 작용을 억제하는 화합물을 확인시켜 준다. 이러한 화합물은 5-아자퀴녹살린계 유도체이다. 5-아자퀴녹살린계 유도체가 세균에서 뉴클레오타이드 합성과 관련된 효소를 억제하는 능력에 대해서는 이미 시험된 적이 있지만, 이러한 화합물의 대다수는 아직 단백질 키나제 억제와 관련해서는 현저하게 연구되지 못했다.
RAF는 기타 세린/트레오닌 단백질 키나제에 상당한 아미노산 상동성을 나타내기 때문에, 본 발명의 5-아자퀴녹살린계 화합물은 RAF 이외에 세린/트레오닌 단백질 키나제를 마찬가지로 억제할 수 있다. 따라서, 본 발명의 방법은 또한 수용체 및 비-수용체 세린/트레오닌 단백질 키나제를 포함하는, RAF 이외의 세린/트레오닌 단백질 키나제에 관한 것이다.
본 발명은, 또한 상기 방법의 높은 처리 효율로 인해 짧은 시간내에 광범위한 분자를 시험하는 것이 가능하기 때문에, 세포내에서 RAF 작용을 조절하는 기타 화합물에 관한 것이다. 따라서, 본 발명의 방법은 RAF 작용을 조절하는 본 발명에 기술되지 않은 현존하는 분자를 확인할 수 있다.
I. 5-아자퀴녹살린계 화합물의 생물학적 활성
본 발명의 5-아자퀴녹살린계 화합물을 RAF 단백질 키나제 작용을 억제하는 능력에 대해 시험한다. 생물학적 분석법 및 이러한 억제 연구 결과를 본원에서 보고한다. 단백질 키나제 작용에 대한 5-아자퀴녹살린계 화합물의 조절을 측정하는데 사용되는 방법은 본 방법의 높은 처리 효율 측면에서 문헌[미국 특허원 제08/702,232호, by Tang et al., and 표제 "Indolinone Conbinatorial Libraries and Related Products and Methods for the Treatment of Disease," (Lyon & Lyon Docket No. 221/187), filed August 23, 1996]에 기술된 방법들과 유사하다. 상기 특허원 제08/702,232호는 임의의 도면을 포함하여 이의 전문을 본원에 참조로 인용한다.
II. 1,4,5-트리아자나프탈렌-기초 화합물에 의해 치료되는 표적 질환들
본원에 기술된 방법, 화합물 및 약제학적 조성물은 RAF 단백질 키나제의 작용을 조절함으로써 세포 증식 질환을 억제하기 위해서 디자인하였다. 증식 질환은 다세포 유기체내의 세포의 서브 세트 하나 이상의 바람직하지 않은 세포 증식을 초래하여 유기체에 유해하다. 본원에 기술된 방법, 화합물 및 약제학적 조성물은 또한 미성숙 세포 사멸(즉, 신경학적 질환) 또는 염증과 관련된 질환 같은 유기체내 기타 질환을 치료하고 예방하는데 유용할 수 있다. 이러한 질환은 부적절하게 작용하는 RAF 분자 또는 부적절하게 작용하는 RAF-관련 단백질 키나제 분자의 결과물일 수 있다.
RAF 단백질 키나제 또는 RAF 관련 단백질 키나제의 작용에서의 변화는 특정 질환에서 명백한 강화된 또는 감소된 세포 증식 상태를 초래할 수 있다. 비정상적인 세포 증식 상태는 암, 섬유성 질환, 맥관막성 질환, 비정상적인 혈관형성 및 맥관형성, 부상 치유, 건선, 재발협착증, 및 염증을 포함한다.
섬유성 질환은 세포성 세포외 간질의 비정상적인 형성과 관련된다. 섬유성 질환의 예는 간경변이다. 간경변은 간 엽흔의 형성을 초래하는 세포외 간질 성분의 증가된 농도로 특성화된다. 간경변은 간의 경변증 같은 질환을 야기할 수 있다.
맥관막성 세포 증식 질환은 맥관막 세포의 비정상적인 증식에 의해 발생한다. 맥관막 증식 질환은 사구체신염, 당뇨성 신장 장애, 악성 신장 경화증, 혈전성 세관이상증, 이식물 거부, 및 사구체 질환 같은 다양한 사람 신장 질환을 포함한다.
본 발명의 방법 및 화합물로 치료할 수 있는 바람직한 암의 유형은 폐암, 난소암, 유방암, 뇌암, 축내성 뇌암, 결장암, 전립선암, 카포시 육종, 흑색종 및 신경교종이다. 본 발명의 화합물 및 방법이 효과적으로 암 세포의 증식을 저지하고 역전시키는데 사용될 수 있다는 증거가 참조로 본원에 제공된다.
혈관 및 맥관형성 질환은 혈관의 과도한 증식에서 기인한다. 혈관 증식은 배 발생, 황체 형성, 부상 치유 및 기관 재생 같은 다양한 정상적인 생리학적 과정에서 필요하다. 그러나, 혈관 증식은 또한 암 종양 발생에서도 필수적이다. 혈관 증식성 질환의 기타 예는 신생 모세혈관이 관점을 공격하여 연골을 파괴하는 관절염을 포함한다. 부가적으로, 혈관 증식 질환은 망막내 신생 모세혈관이 유리체를 공격하고 출혈시키고 시각 상실을 야기하는 당뇨성 망막 질환 같은 안 질환을 포함한다. 반대로, 재발협착증 같은 혈관의 감소, 수축 또는 폐쇄와 관련된 질환이 또한 단백질 키나제의 역 조절과 관련이 있다.
또한, 맥관 및 혈관형성은 악성 고상 종양의 성장 및 전이와 관련이 있다. 활발하게 성장하는 암은 지속적인 성장을 위해서 영양분 및 산소가 풍부한 혈액 공급을 필요로 한다. 결과적으로, 비정상적으로 대량의 모세혈관이 종종 종양과 함께 성장하며 종양에 대한 공급로로서 작용한다. 종양에 영양분을 공급하는데 부가하여, 종양에 연결된 신생 혈관은 종양 세포가 순환계로 나아가 유기체내의 원격 부위까지 전이되기 위한 출구를 제공한다. 문헌 참조[Folkman, 1990, J. Natl. Cancer Inst. 82:4-6].
부적절한 RAF 활성은 세포 증식성 질환을 자극할 수 있다. RAF 단백질 키나제의 작용을 조절하기 위해서 특이적으로 디자인된 분자들은 세포 증식을 억제하는 것으로 나타난다. 특히, 안티센스 핵산 분자(이는 RAF 단백질 키나제를 암호화하는 mRNA에 결합하여 메세지의 해독을 차단하도록 디자인되었다)는 시험관내에서 A549 세포의 형질전환을 효과적으로 무효화시킨다. 문헌 참조[Monia et al., 1996, Nature Medicine 2: 688, 모든 도면 및 표를 포함한 이의 전문이 참조로 본원에 인용됨]. A549 세포는 사람 악성 종양 세포이다.
이러한 RAF-표적화된 안티센스 연구는 RAF 단백질 키나제의 작용을 조절하는 본 발명의 5-아자퀴녹살린 분자가 유기체내에서 악성 세포의 증식을 저지하고 마찬가지로 무효화시킬 수 있다는 증거를 제공한다. 이러한 5-아자퀴녹살린 화합물은 본원 실시예로 제공되는 시험관내 방법으로 시험할 수 있다. 추가로, 5-아자퀴녹살린 화합물은 또한 본원 실시예로 제공되는 이종이식 방법에 의해 생체내에서 종양 세포에 대한 이의 효과를 시험할 수 있다.
부적절한 RAF 활성이 특정 유형의 세포의 바람직하지 않은 세포 증식을 자극할 수 있는 2개 이상의 방법이 존재한다: (1) 직접적으로 특정 세포의 성장을 자극하거나, (2) 종양 조직 같은 특정 영역의 혈관 신생을 증가시켜 이로인해 조직의 성장을 촉진시킨다.
본 발명의 사용은 우선 세포 증식성 질환이 RAF 구동되는지를 확인함으로써 촉진된다. 일단 상기 질환들이 확인되면, 상기 질환으로부터 고통받는 환자들은 당해 분야에서 통상의 기술을 가진 의사 또는 수의사에게 숙지된 방법을 사용하여 이의 증상을 분석함으로써 확인할 수 있다. 이후, 상기 환자들은 본원에 기술된 바와 같이 치료할 수 있다.
세포 증식성 질환이 RAF 구동되는지를 결정하는 것은 우선 세포내 또는 환자의 신체내 특정 위치에서 발생하는 RAF 활성의 수준을 결정함으로써 달성할 수 있다. 예를 들면, 암 세포의 경우, 하나 이상의 RAF 활성의 수준을 비-RAF 구동된 암과 RAF 구동된 암에 대해 비교할 수 있다. 암 세포가 RAF 구동된 암 보다 더 높은 RAF 활성 수준을 갖는 경우, 바람직하게는 RAF 구동된 암과 동일하거나 더 높은 경우, 이들은 본 발명의 기술된 RAF-조절 방법 및 화합물을 사용하여 치료할 대상이 된다.
비-암 세포의 바람직하지 않은 증식에 기인하여 야기된 세포 증식성 질환인 경우, RAF 활성 수준을 일반적인 집단에서 발생되는 수준(예를 들면, 세포 증식성 질환으로 고통받는 사람 또는 동물을 제외한 사람 또는 동물의 일반 집단에서 발생하는 평균 수준)과 비교한다. 바람직하지 않은 세포 증식성 질환이 일반 집단에서 발생하는 것보다 더 높은 RAF 수준으로 특성화되는 경우, 상기 질환은 본 발명의 기술된 RAF 조절 방법 및 화합물을 사용하여 치료할 대상이 된다.
III. 5-아자퀴녹살린계 화합물의 약제학적 조성물 및 투여
상기 화합물의 약제학적 제형을 제조하는 방법, 환자에게 투여해야할 화합물의 양을 결정하는 방법, 및 유기체에 화합물을 투여하는 방식은 문헌[미국 특허원 제08/702,232호, by Tang et al., and entitled "Indolinone Combinatorial Libraries and Related Products and Methods for the Treatment of Disease," (Lyon & Lyon Docket No. 221/187), filed August 23, 1996, 및 국제 특허원 제WO 96/22976호, by Buzzetti et al., and entitled "Hydrosoluble 3-Arylidene-2-Oxindole Derivatives as Tyrosine kinase Inhibitors," published August 1, 1996]에 기술되어 있으며, 이들 모두는 임의의 도면을 포함하여 이의 전문을 참조로 본원에 인용한다. 당해 분야의 숙련자는 상기 기술들을 본 발명에 적용할 수 있고 이에 용이하게 변형시킬 수 있다는 것을 인식할 것이다.
하기 실시예는 비제한적이며 단지 본 발명의 다양한 양태 및 특징을 예시하는 것이다. 본 실시예는 본 발명의 화합물의 합성 방법 및 RAF 단백질 키나제의 작용에 대한 화합물의 효과를 측정하는 방법을 기술한다.
상기 방법에 사용되는 세포는 시판중이다. 세포에 의해 제공되는 핵산 벡터도 또한 시판중이며 다양한 단백질 키나제의 유전자 서열은 서열 데이터 뱅크에서 용이하게 접근할 수 있다. 따라서, 당해 분야의 통상의 숙련자는 당해 분야에서 통상의 숙련자가 용이하게 이용할 수 있는 기술을 사용하여 시판중인 세포, 시판중인 핵산 벡터, 및 단백질 키나제 유전자를 혼합함으로써 적시에 세포주를 용이하게 재창조할 수 있다.
실시예 1: 본 발명의 5-아자퀴녹살린계 화합물을 합성하는 방법
본 발명은 이제 하기 비-제한적인 실시예로 예시되며, 특별한 언급이 없는 한 다음과 같다:
(i) 증발은 진공하에서 회전 증발기에서 수행하고;
(ii) 작업은 질소 같은 불활성 가스의 대기하에서 수행하고;
(iii) 고성능 액체 크로마토그래피(HPLC)는 제조원(E. Merck, Darmstadt, Germany)으로부터 수득된 Merck LiChrosorb RP-18 역상 실리카상에서 수행하고;
(iv) 수율은 단지 예시를 위한 것이며 반드시 수득할 수 있는 최대값은 아니고;
(v) 융점은 보정되지 않았으며 HWS Mainz SG 2000 디지탈 융점 장치를 사용하여 측정하고;
(vi) 본 발명의 화학식 (I)의 모든 화합물의 구조는 Bruker AMX500-NMR 분광 측광기상에서 양성자 자기 공명 분광학, 원소 미세분석, 및 특정한 경우, 질량 분광학으로 확인하고;
(vii) 구조의 순도는 실리카 겔(Merck Silica Gel 60 F254)을 사용하는 박층 크로마토그래피(TLC)로 또는 HPLC로 수행하며;
(viii) 중간체는 일반적으로 완전히 특성화되지 않으며 순도는 박층 크로마토그래피(TLC) 또는 HPLC로 결정한다.
합성 방법
화합물 A-2: 6-벤질아미노-3-(4-하이드록시페닐)-5-아자퀴녹살린
4-하이드록시페닐글리옥살은 공지된 방법[J. Amer. Chem. Soc., 71, 1045 (1949)]에 따라서 4-하이드록시아세토페논(Lancaster, Acros)으로부터 제조한다.
2-아미노-6-벤질아미노-3-니트로피리딘은 다음과 같이 2-아미노-6-클로로-3-니트로피리딘으로부터 제조한다: n-부탄올(100㎖) 중 2-아미노-6-클로로-3-니트로피리딘(17.35g, 0.10mol), 벤질아민(Fluka)(10.72g, 0.10mol) 및 분말 탄산칼륨(10.4g, 0.035mol)을 환류하에서 2시간 동안 가열한다. 상기 현탁액을 여과하고 실온으로 냉각시킨 후, 고체를 여과하여 회수하고, 부탄올로 세척한 후 진공에서 50℃에서 건조시켜 2-아미노-6-벤질아미노-3-니트로피리딘(22.2g, 91%, 융점: 145 내지 146℃)을 수득한다.
6-벤질아미노-3-(4-하이드록시페닐)-5-아자퀴녹살린은 다음과 같이 2-아미노 -6-벤질아미노-3-니트로피리딘으로부터 제조한다: 2-아미노-6-벤질아미노-3-니트로피리딘(25g, 0.10mol)을 60℃에서 디옥산 400㎖ 중 라니-니켈 10g의 존재하에 H2 5.5bar하에서 수소화시킨다. 2시간 후, 반응 혼합물을 실온으로 냉각시키고, 여과하고 4-하이드록시 페닐글리옥살을 부가하여 아르곤 대기하에서 2시간 동안 교반시킨다. 이후 상기 현탁액을 물로 희석하고, 고체를 여과하여 수거하고, 물로 세척하고, 2-프로판올로부터 재결정화한 후 진공하에서 50℃에서 건조시켜 6-벤질아미노-3-(4-하이드록시페닐)-5-아자퀴녹살린(8g, 24.4%, 융점: 271 내지 273℃)을 수득한다.
화합물 A-1: 6-페닐아미노-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-2의 방법에서 벤질아민을 페닐아민으로 치환함으로써, 동일한 방법으로 6-페닐아미노-3-(4-하이드록시페닐)-5-아자퀴녹살린을 수득한다.
화합물 A-3: 6-메톡시-2-메틸-3-페닐-5-아자퀴녹살린
화합물 A-2의 방법에서 4-하이드록시페닐글리옥살을 1-페닐-1,2-프로판디온으로 및 벤질아민을 메탄올로 치환시킴으로써, 동일한 방법으로 6-메톡시-2-메틸-3-페닐-5-아자퀴녹살린을 수득한다.
화합물 A-4: 6-메톡시-2,3-디페닐-5-아자퀴녹살린
화합물 A-2의 방법에서 4-하이드록시페닐글리옥살을 벤질로 및 벤질아민을 메탄올로 치환시킴으로써, 동일한 방법으로 6-메톡시-2,3-디페닐-5-아자퀴녹살린을 수득한다.
화합물 A-5: 6-(4-플루오로벤질아미노)-2-메틸-3-페닐-5-아자퀴녹살린
화합물 A-2의 방법에서 4-하이드록시페닐글리옥살을 1-페닐-1,2-프로판디온 으로 및 벤질아민을 4-플루오로벤질아민으로 치환시킴으로써, 동일한 방법으로 6-(4-플루오로벤질아미노)-2-메틸-3-페닐-5-아자퀴녹살린을 수득한다.
화합물 A-6: 2,3-디페닐-6-(4-플루오로벤질아미노)-5-아자퀴녹살린
화합물 A-2의 방법에서 4-하이드록시페닐글리옥살을 벤질로 및 벤질아민을 4-플루오로벤질아민으로 치환시킴으로써, 동일한 방법으로 2,3-디페닐-6-(4-플루오로벤질아미노)-5-아자퀴녹살린을 수득한다.
화합물 A-7: 3-페닐-6-페닐아미노-5-아자퀴녹살린
화합물 A-2의 방법에서 4-하이드록시페닐글리옥살을 페닐글리옥살로 및 벤질아민을 아닐린으로 치환시킴으로써, 동일한 방법으로 3-페닐-6-페닐아미노-5-아자퀴녹살린을 수득한다.
화합물 A-8 내지 A-26
화합물 A-2의 방법에서 벤질아민을 적절히 치환된 벤질아민으로 치환시킴으로써, 동일한 방법으로 하기 화합물들을 수득한다:
화합물 A-8: 6-(2-카복시벤질아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-9: 6-(3-카복시벤질아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-10: 6-(4-카복시벤질아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-11: 3-(4-하이드록시페닐)-6-(2-니트로벤질아미노)-5-아자퀴녹살린
화합물 A-12: 3-(4-하이드록시페닐)-6-(3-니트로벤질아미노)-5-아자퀴녹살린
화합물 A-13: 3-(4-하이드록시페닐)-6-(4-니트로벤질아미노)-5-아자퀴녹살린
화합물 A-14: 3-(4-하이드록시페닐)-6-(2-메틸벤질아미노)-5-아자퀴녹살린
화합물 A-15: 3-(4-하이드록시페닐)-6-(3-메틸벤질아미노)-5-아자퀴녹살린
화합물 A-16: 3-(4-하이드록시페닐)-6-(4-메틸벤질아미노)-5-아자퀴녹살린
화합물 A-17: 6-(2-클로로벤질아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-18: 6-(3-클로로벤질아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-19: 6-(4-클로로벤질아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-20: 6-(2-플루오로벤질아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-21: 6-(3-플루오로벤질아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-22: 6-(4-플루오로벤질아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-23: 3-(4-하이드록시페닐)-6-[2-(트리플루오로메틸)벤질아미노]-5-아자퀴녹살린
화합물 A-24: 3-(4-하이드록시페닐)-6-[3-(트리플루오로메틸)벤질아미노]-5-아자퀴녹살린
화합물 A-25: 3-(4-하이드록시페닐)-6-[4-(트리플루오로메틸)벤질아미노]-5-아자퀴녹살린
화합물 A-26: 3-(4-하이드록시페닐)-6-(펜에틸-1-아미노)-5-아자퀴녹살린
화합물 A-27 내지 A-48
화합물 A-2의 방법에서 벤질아민을 적절히 치환된 아닐린으로 치환시킴으로써, 동일한 방법을 하기 화합물들을 수득한다:
화합물 A-27: 6-(2-카복시페닐아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-28: 6-(3-카복시페닐아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-29: 6-(4-카복시페닐아미노)-3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-30: 3-(4-하이드록시페닐)-6-(2-니트로페닐아미노)-5-아자퀴녹살린
화합물 A-31: 3-(4-하이드록시페닐)-6-(3-니트로페닐아미노)-5-아자퀴녹살린
화합물 A-32: 3-(4-하이드록시페닐)-6-(4-니트로페닐아미노)-5-아자퀴녹살린
화합물 A-33: 3-(4-하이드록시페닐)-6-(2-메틸페닐아미노)-5-아자퀴녹살린
화합물 A-34: 3-(4-하이드록시페닐)-6-(3-메틸페닐아미노)-5-아자퀴녹살린
화합물 A-35: 3-(4-하이드록시페닐)-6-(4-메틸페닐아미노)-5-아자퀴녹살린
화합물 A-36: 6-(2-클로로페닐아미노)3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-37: 6-(3-클로로페닐아미노)3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-38: 6-(4-클로로페닐아미노)3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-39: 6-(2-플루오로페닐아미노)3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-40: 6-(3-플루오로페닐아미노)3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-41: 6-(4-플루오로페닐아미노)3-(4-하이드록시페닐)-5-아자퀴녹살린
화합물 A-42: 3-(4-하이드록시페닐)-6-[(2-트리플루오로메틸)페닐아미노]-5-아자퀴 녹살린
화합물 A-43: 3-(4-하이드록시페닐)-6-[(3-트리플루오로메틸)페닐아미노]-5-아자퀴녹살린
화합물 A-44: 3-(4-하이드록시페닐)-6-[(4-트리플루오로메틸)페닐아미노]-5-아자퀴녹살린
화합물 A-45: 3-(4-하이드록시페닐)-6-(피리드-2-아미노)-5-아자퀴녹살린
화합물 A-46: 3-(4-하이드록시페닐)-6-(피리드-3-아미노)-5-아자퀴녹살린
화합물 A-47: 3-(4-하이드록시페닐)-6-(피리드-4-아미노)-5-아자퀴녹살린
화합물 A-48: 3-(4-하이드록시페닐)-6-(피리드-2-메틸아미노)-5-아자퀴녹살린
화합물 A-49 내지 A-67
화합물 A-2의 방법에서 벤질아민을 적절히 치환된 벤질아민으로 및 4-하이드록시페닐글리옥살을 페닐글리옥살로 치환시킴으로써, 동일한 방법으로 하기 화합물을 수득한다:
화합물 A-49: 6-(2-카복시벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-50: 6-(3-카복시벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-51: 6-(4-카복시벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-52: 6-(2-니트로벤질아미노-3-페닐)-5-아자퀴녹살린
화합물 A-53: 6-(3-니트로벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-54: 6-(4-니트로벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-55: 6-(2-메틸벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-56: 6-(3-메틸벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-57: 6-(4-메틸벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-58: 6-(2-클로로벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-59: 6-(3-클로로벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-60: 6-(4-클로로벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-61: 6-(2-플루오로벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-62: 6-(3-플루오로벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-63: 6-(4-플루오로벤질아미노)-3-페닐-5-아자퀴녹살린
화합물 A-64: 3-페닐-6-[2-(트리플루오로메틸)벤질아미노]-5-아자퀴녹살린
화합물 A-65: 3-페닐-6-[3-(트리플루오로메틸)벤질아미노]-5-아자퀴녹살린
화합물 A-66: 3-페닐-6-[4-(트리플루오로메틸)벤질아미노]-5-아자퀴녹살린
화합물 A-67: 3-페닐-6-(펜에틸-1-아미노)-5-아자퀴녹살린
화합물 A-68 내지 A-89
화합물 A-2의 방법에서 벤질아민을 적절히 치환된 아닐린으로 및 4-하이드록시페닐글리옥살을 페닐글리옥살로 치환시킴으로써, 동일한 방법으로 하기 화합물들을 수득한다:
화합물 A-68: 6-(2-카복시페닐아미노)-3-페닐-5-아자퀴녹살린
화합물 A-69: 6-(3-카복시페닐아미노)-3-페닐-5-아자퀴녹살린
화합물 A-70: 6-(4-카복시페닐아미노)-3-페닐-5-아자퀴녹살린
화합물 A-71: 6-(2-니트로페닐아미노)-3-페닐-5-아자퀴녹살린
화합물 A-72: 6-(3-니트로페닐아미노)-3-페닐-5-아자퀴녹살린
화합물 A-73: 6-(4-니트로페닐아미노)-3-페닐-5-아자퀴녹살린
화합물 A-74: 6-(2-메틸페닐아미노)-3-페닐-5-아자퀴녹살린
화합물 A-75: 6-(3-메틸페닐아미노)-3-페닐-5-아자퀴녹살린
화합물 A-76: 6-(4-메틸페닐아미노)-3-페닐-5-아자퀴녹살린
화합물 A-77: 6-(2-클로로페닐아미노)-3-페닐-5-아자퀴녹살린
화합물 A-78: 6-(3-클로로페닐아미노)3-페닐-5-아자퀴녹살린
화합물 A-79: 6-(4-클로로페닐아미노)-3-페닐-5-아자퀴녹살린
화합물 A-80: 6-(2-플루오로페닐아미노)3-페닐-5-아자퀴녹살린
화합물 A-81: 6-(3-플루오로페닐아미노)3-페닐-5-아자퀴녹살린
화합물 A-82: 6-(4-플루오로페닐아미노)3-페닐-5-아자퀴녹살린
화합물 A-83: 3-페닐-6-[(2-트리플루오로메틸)페닐아미노]-5-아자퀴녹살린
화합물 A-84: 3-페닐-6-[(3-트리플루오로메틸)페닐아미노]-5-아자퀴녹살린
화합물 A-85: 3-페닐-6-[(4-트리플루오로메틸)페닐아미노]-5-아자퀴녹살린
화합물 A-86: 3-페닐-6-(피리드-2-아미노)-5-아자퀴녹살린
화합물 A-87: 3-페닐-6-(피리드-3-아미노)-5-아자퀴녹살린
화합물 A-88: 3-페닐-6-(피리드-4-아미노)-5-아자퀴녹살린
화합물 A-89: 3-페닐-6-(피리드-2-메틸아미노)-5-아자퀴녹살린
화합물 A-90: 6-페닐아미노-3-(4-메톡시페닐)-5-아자퀴녹살린
화합물 A-1의 방법에서 4-하이드록시페닐을 4-메톡시페닐로 치환시킴으로써, 동일한 방법으로 6-페닐아미노-3-(4-메톡시페닐)-5-아자퀴녹살린을 수득한다.
실시예 2: RAF의 인산화 작용을 측정하는 분석법
하기 분석법은 MEK의 표적 MAPK 뿐만 아니라 표적 단백질 MEK의 RAF-촉매된 인산화량을 보여준다. RAF 유전자 서열은 문헌[Bonner et al., 1985, Molec. Cell. Biol. 5: 1400-1407]에 기술되어 있으며, 다수의 유전자 서열 데이터 뱅크에서 용이하게 입수가능하다. 본 발명의 이부분에서 사용되는 핵산 벡터 작제물 및 세포주는 문헌[Morrison et al., 1988, Proc. Natl. Acad. Sci. USA 85: 8855-8859]에 완전하게 기술되어 있다.
재료 및 시약
1. Sf9(Spodoptera frugiperda) 세포(제조원: GIBCO-BRL, Gaithersburg, MD).
2. RIPA 완충액: 20mM 트리스/HCl pH 7.4, 137mM NaCl, 10% 글리세롤, 1mM PMSF, 5㎎/ℓ 아프로테닌, 0.5% 트리톤 X-100.
3. 티오레독신-MEK 융합 단백질(T-MEK): 친화성 크로마토그래피에 의한 T-MEK 발현 및 정제는 제조원의 방법에 따라 수행한다(Catalog # K 350-01 및 R 350-40, Invitrogen Corp., San Diego, CA).
4. His-MAPK(ERK 2): His-태그된 MAPK는 His-MAPK를 암호화하는 pUC18 벡터로 형질전환시킨 XL1 Blue 세포에서 발현시킨다. His-MAPK는 본원에서 기술된 바와 같이, Ni-친화성 크로마토그래피에 의해 정제한다(Catalog # 27-4949-01, Pharmacia, Alameda, CA,).
5. 양 항마우스 IgG(제조원: Jackson laboratories, West Grove, PA. Catalog # 515-006-008, Lot # 28563).
6. RAF-1 단백질 키나제 특이적인 항체: UBI로부터의 URP2653.
7. 코팅 완충액: PBS, 인산염 완충된 염수(제조원: GIBCO-BRL, Gaithersburg, MD).
8. 세척 완충액: TBST - 50mM 트리스/HCl pH 7.2, 150mM NaCl, 0.1% 트리톤 X-100.
9. 차단 완충액: TBST, 0.1% 에탄올아민 pH 7.4.
10. DMSO(제조원: Sigma, St. Louis, MO).
11. 키나제 완충액(KB): 20mM Hepes/HCl pH 7.2, 150mM NaCl, 0.1% 트리톤 X-100, 1mM PMSF, 5㎎/ℓ 아프로테닌, 75μM 나트륨 오르토 바나데이트, 0.5mM DTT 및 10mM MgCl2.
12. ATP 혼합물: 100mM MgCl2, 300μM ATP, 10μCi λ-33P ATP(제조원: Dupont-NEN)/㎖.
13. 종결 용액: 1% 인산(제조원: Fisher, Pittsburgh, PA).
14. 왈락 셀룰로스 포스페이트 필터 매트(Wallac Cellulose Phosphate Filter mats)(제조원: Wallac, Turku, Finnland).
15. 필터 세척액: 1% 인산(제조원: Fisher, Pittsburgh, PA).
16. 톰텍 플레이트 수확기(제조원: Wallac, Turku, Finnland).
17. 왈락 베타 플레이트 판독기 # 1205(제조원: Wallac, Turku, Finnland).
18. 화합물용 NUNC 96-웰 V 바닥 폴리프로필렌 플레이트(제조원: Applied Scientific Catalog # AS-72092).
방법
하기 모든 단계들은 특별한 언급이 없는 한, 실온에서 수행한다.
1. ELISA 플레이트 코팅: ELISA 웰을 4℃에서 밤새 양 항마우스 친화성 정제된 항혈청 100㎕(1㎍/코팅 완충액 100㎕)으로 코팅한다. ELISA 플레이트를 4℃에서 보관하는 경우 2주일 동안 사용할 수 있다.
2. 상기 플레이트를 뒤집어 액체를 제거한다. 차단 용액 100㎕를 부가하고 30분 동안 항온 처리한다.
3. 차단 용액을 제거하고 세척 완충액으로 4회 세척한다. 종이 타월상에서 상기 플레이트를 가볍게 두드려 과량의 액체를 제거한다.
4. 각각의 웰에 RAF-1에 특이적인 항체 1㎍을 부가하고 1시간 동안 항온 처리한다. 단계 3에서 기술된 바와 같이 세척한다.
5. RAS/RAF 감염된 Sf9 세포로부터의 용해액을 해동시켜 10㎍/100㎕가 되도록 TBST로 희석한다. 희석시킨 용해액 10㎍을 웰에 부가하고 1시간 동안 항온 처리한다. 항온 처리 동안 플레이트를 진탕시킨다. 네가티브 대조군은 어떠한 용해액도 포함하지 않는다. 각각의 바이러스에 대해 MOI가 5에서 재조합 배큘로바이러스를 사용하여 세포를 감염시킨 후 48시간 후에 회수하여 RAS/RAF 감염된 Sf9 곤충 세포로부터의 용해액을 제조한다. 세포를 PBS로 1회 세척하고 RIPA 완충액에서 용해시킨다. 불용성 물질을 원심분리(10000 x g에서 5분)시켜 제거한다. 용해액의 분취액을 드라이 아이스/에탄올 중에서 동결시켜 사용시까지 -80℃에서 보관한다.
6. 결합되지 않은 물질을 제거하고 상기(단계 3)에서 기술된 바와 같이 세척한다.
7. 웰 당 T-MEK 2㎍ 및 His-MAPK 2㎍을 부가하고 키나제 완충액을 사용하여 용적을 40㎕로 조절한다. 세포 추출액으로부터 T-MEK 및 MAPK를 정제하는 방법은 본원 실시예에서 제공한다.
8. 1% DMSO를 함유하는 TBST 중에서 화합물(스톡 용액 10㎎/㎖ DMSO) 또는 추출액을 20배로 예비희석시킨다. 예비희석된 화합물/추출액 5㎕를 단계 6에서 기술된 웰에 부가한다. 20분 동안 항온 처리한다. 대조군은 어떠한 약제도 함유하지 않는다.
9. ATP 혼합물 5㎕를 부가하여 키나제 반응을 개시한다. 항온 처리 동안 ELISA 플레이트 진탕기에서 플레이트를 진탕시킨다.
10. 60분 후에 각 웰에 종결 용액 30㎕를 부가하여 키나제 반응을 종결시킨다.
11. 포스포셀룰로스 매트 및 ELISA 플레이트를 톰텍 플레이트 수확기내에 위치시킨다. 제조원의 권장에 따라 필터 세척액을 사용하여 필터를 수거하고 세척한다. 필터 매트를 건조시킨다. 필터 매트를 밀봉하고 홀더내에 위치시킨다. 상기 홀더를 방사능 검출 장치내로 삽입하고 필터 매트 상의 방사성 인을 정량화한다.
대안으로, 상기 분석 플레이트의 각 웰로부터 분취액 40㎕를 포스포셀룰로스 필터 매트상의 상응하는 위치로 전이시킬 수 있다. 필터를 공기 건조시킨 후, 필터를 트레이에 위치시킨다. 15분 간격으로 1시간 동안 세척액을 교체하면서 조금스럽게 트레이를 진탕시킨다. 필터 매트를 공기 건조시킨다. 필터 매트를 밀봉하고 샘플 중 방사성 인을 측정하기에 적합한 홀더내로 위치시킨다. 홀더를 검출 장치내로 삽입하고 필터 매트상의 방사성 인을 정량화시킨다.
IC50 값을 RAF-1 ELISA 분석법에서 하기 5-아자퀴녹살린계 화합물을 위한 프로토콜에 따라서 측정한다.
IC50 값은 인산화된 표적 단백질 또는 세포 성장의 최대량을 50%까지 감소시키는데 필요한 5-아자퀴녹살린계 억제제의 농도이다. RAF-1 인산화 분석법에서 측정된 IC50 값은 표 1에 나타낸다.
| 화합물 | IC50(μM) |
| A-1 | 11.5 |
| A-2 | 7.8 |
| A-7 | 33 |
| A-36 | 45.6 |
| A-77 | 20.3 |
| A-90 | 98.0 |
실시예 3: MAPK 및 MEK의 정제
MAPK 및 MEK 단백질은 폴리-히스티딘 태그과 함께 단백질을 발현하는 시판중인 벡터내로 상기 단백질을 암호화하는 유전자를 서브클로닝함으로써 세포에서 용이하게 발현시킨다. 상기 단백질들을 암호화하는 유전자는 일반적으로 상기 단백질을 사용하는 연구실로부터 또는 cDNA 라이브러리를 함유하는 세포로부터 이러한 유전자를 클로닝함으로써 용이하게 입수할 수 있다. 상기 라이브러리는 시판중이며 당해 분야의 숙련자는 Genbank 같은 다수의 유전자 데이터 베이스에서 입수가능한 MEK 및 MAPK의 핵산 서열로부터 MEK 또는 MAPK를 암호화하는 cDNA에 상동성인 핵산 탐침을 용이하게 디자인할 수 있다. 유전자의 클로닝은 당해 분야의 숙련자에게 최근 유용한 기술들을 사용하여 짧은 시간내에 달성할 수 있다.
세포 추출물로부터의 MEK 및 MAPK 단백질의 정제는 문헌[Robbins et al., 1993, J. Biol. Chem. 268: 5097-5106]으로부터 변형된 하기 프로토콜에 따라서 달성할 수 있다:
1. 당해 분야의 숙련자가 용이하게 입수가능한 초음파, 삼투압, 또는 프렌치 프레스 기술(French Press technique)로 세포를 용출시킨다. 적합한 초음파 완충액은 하기에 제공된다.
2. 니켈 또는 코발트가 접합된 고체 지지체를 하기에 기술되는 평형 완충액으로 평형시킨다. 폴리-히스티딘 태그를 고체 지지체상의 니켈 및 코발트 원자에 특이적으로 결합시킨다. 고체 지지체의 용적에 10배의 평형 완충액 용적을 사용하여 상기 수지를 3회 세척함으로써 평형이 달성될 수 있다. 고체 지지체는 당해 분야의 통상의 숙련자가 용이하게 입수할 수 있다.
3. 세포 용해액을 고체 지지체에 부가하고 시간 주기동안 용기내를 평형시킨다. 대안으로, 고체 지지체를 단백질 크로마토그래피 컬럼내에 팩킹시킬 수 있으며 용해액을 고체 지지체를 통해 유입시킬 수 있다.
4. 고체 지지체를 하기 기술된 세척 완충액으로 세척한다.
5. 고체 지지체로부터 일정량의 용출 완충액(하기 제공됨, 이는 고체 지지체로부터 상당 부분의 상기 단백질을 제거시킨다)을 사용하여 MEK 또는 MAPK 단백질을 용출시킨다.
초음파 완충액
50mM 인산나트륨 pH 8.0
0.3M 염화나트륨
10mM β-머캅토에탄올
1% NP40
10mM NaF
0.5mM Pefablock
평형 완충액
50mM 인산나트륨 pH 8.0
0.3M 염화나트륨
10mM β-머캅토에탄올
1% NP40
10mM NaF
1mM 이미다졸
세척 완충액
50mM 인산나트륨 pH 8.0
0.3M 염화나트륨
10mM β-머캅토에탄올
1% NP40
10mM NaF
10mM 이미다졸
용출 완충액
50mM 인산나트륨 pH 8.0
0.3M 염화나트륨
10mM β-머캅토에탄올
1% NP40
10mM NaF
10 내지 500mM 이미다졸
실시예 4: EGF 수용체의 인산화 작용을 측정하는 분석법
전체 세포에서 EGF 수용체 키나제 활성(EGFR-NIH3T3 분석법)은 문헌[PCT 공보 제WO 9640116호, filed June 5, 1996, by Tang et al., and entitled "Indolinone Compounds for the Treatment of Disease,"; 임의의 도면을 포함하는 이의 전문이 본원에 참조로 인용된다]에 기술된 바와 같이 측정한다.
EGF 수용체 인산화 분석에서 측정된 IC50 값은 표 2에 나타낸다:
| 화합물 | IC50(μM) |
| A-2 | > 50 |
| A-3 | > 100 |
| A-4 | > 100 |
| A-5 | > 100 |
| A-6 | > 100 |
| A-7 | > 50 |
실시예 5: RAS를 발현하는 세포의 성장에 대한 5-아자퀴녹살린계 화합물의 효과를 측정하는 분석법
하기 분석법은 RAS를 발현하는 NIH-3T3 세포에 대한 성장율을 측정한다. 본 분석의 목적은 H-RAS를 과발현하는 NIH-3T3 세포의 성장에 대한 화합물의 효과를 결정하는 것이다.
재료
96-웰 평저 멸균 플레이트
96-웰 환저 멸균 플레이트
멸균된 25㎖ 또는 100㎖ 저장 용기
피펫, 다관 피펫맨
멸균 피펫 팁
멸균된 15㎖ 및 50㎖ 튜브
시약
1% 아세트산 중 0.4% SRB
10mM 트리스 염기
10% TCA
1% 아세트산
멸균된 DMSO(제조원: Sigma)
DMSO 중 화합물(100mM 이하의 스톡 용액)
트립신-EDTA(제조원: GIBCO-BRL)
세포주
3T3/H-Ras(발암유전자 H-Ras의 게놈성 단편을 발현하는 NIH 3T3 클론 7 세포들)
세포를 하기 프로토콜을 사용하여 작제할 수 있다:
1. RAS를 암호화하는 유전자 단편을 NIH-3T3 세포를 안정하게 형질감염하는 시판중인 벡터내로 서브클로닝시킨다. 상기 단편은 cHa-ras의 게놈성 형질전환 대 립형질로부터 유도된 것이다.
2. NIH-3T3 세포를 칼슘 포스페이트 방법으로 서브클로닝된 벡터를 사용하여 형질감염시킨다. 2% 혈청을 함유하는 DMEM중에서 Ras 작제물을 발현하는 세포를 선택한다. 가시적인 병소가 2주 후 관찰된다. 형질전환된 세포를 모아 안정하게 형질전환된 세포주를 생성시킨다.
성장 배지
2% 소 혈청/DMEM + 2mM 글루타민, 페니실린/스트렙토마이신
프로토콜
0 일: 세포 플레이팅 :
분석의 본 과정은 박판 유동 후드에서 수행한다.
1. 세포를 트립신 처리한다. 이소톤(isotone) 10㎖에 세포 현탁액 200㎕를 전달한다. Coulter 계수기로 세포를 계수한다.
2. 성장 배지 중에 세포를 60,000 세포/㎖로 희석시킨다. 세포 100㎕를 96-웰 평저 플레이트 중 각각의 웰에 전달하여 6000 세포/웰을 수득한다.
3. 각각 화합물에 대해 플레이트의 반(4개 열) 및 각각 화합물 농도에 대한 4배수의 웰 및 한 세트의 배지 대조군에 대한 4개의 웰을 사용한다.
4. 약하게 플레이트를 진탕시켜 세포 균일하게 부착되도록 한다.
5. 10% CO2 인큐베이터에서 37℃에서 플레이트를 배양한다.
1일: 화합물의 첨가
분석의 본 과정은 박판 유동 후드에서 수행한다.
1. 96-웰 환저 플레이트에, 화합물의 최고 스크리닝 농도에서 발견되는 2X 최종 % DMSO를 함유하는 성장 배지 120㎕를 컬럼 1 내지 11에 부가한다. 예를 들면, 최고의 스크리닝 농도가 100μM이고, 이것이 100mM 스톡에서 제조되는 경우, 1X DMSO는 0.1%이고, 따라서 2X DMSO는 0.2%이다. 상기 플레이트를 화합물 당 4개 열에서 화합물을 적정하는데 사용한다.
2. 멸균된 15㎖ 튜브에서, 성장 배지 + 2X DMSO 중 최고 스크리닝 농도의 화합물 2X 용액을 제조한다. 세포주 당 1㎖가 필요하다. 화합물의 출발 농도는 일반적으로 100μM이지만, 이 농도는 화합물의 용해도에 따라 다양할 수 있다.
3. 2X 출발 화합물 용액 240㎕를 96-웰 환저 플레이트의 컬럼 12내 4배수의 웰에 전달한다. 컬럼 12에서 컬럼 11로, 컬럼 11에서 컬럼 10으로 등의 방식으로 컬럼 2까지 12㎕를 전달함으로써 오른쪽에서 왼쪽으로 플레이트를 가로질러 일련의 1:2 희석을 수행한다. 화합물 희석액 100㎕ 및 컬럼 1내의 배지 100㎕를 96-웰 평저 플레이트의 상응하는 웰내 세포상의 배지 100㎕ 상에 전달한다. 전체 용적은 웰당 200㎕가 되어야만 한다.
4. 플레이트를 인큐베이터내로 되돌려 놓고 3일간 항온 처리한다.
4 일: 분석의 진행
분석의 본 과정은 벤치에서 수행한다.
1. 배지를 흡인 제거하거나 쏟아낸다. 차가운 10% TCA 200㎕를 각 웰에 부가하여 세포를 고정시킨다. 플레이트를 4℃에서 60분 이상 항온 처리한다.
2. TCA를 제거하고 웰을 수돗물로 5회 세정한다. 플레이트를 종이 타월에 엎어 건조시킨다.
3. 세포를 웰 당 0.4% SRB 100㎕를 사용하여 10분 동안 염색시킨다.
4. SRB를 쏟아내고 웰을 1% 아세트산으로 5회 세정한다. 플레이트를 종이 타월에 엎어 완전히 건조시킨다.
5. 진탕기상에서 5 내지 10분 동안 웰 당 10mM 트리스 염기 100㎕를 사용하여 염료를 용해시킨다.
6. Dynatech ELISA 플레이트 판독기상에서 570nm에서 플레이트를 판독하고 참조용으로는 630nm에서 판독한다.
표 3에서 예시되는 바와 같이, RAS 과발현 세포의 성장 속도를 억제하는 화합물을 선별한다.
3. 각각 화합물에 대해 플레이트의 반(4개 열) 및 각각 화합물 농도에 대한 4배수의 웰 및 한 세트의 배지 대조군에 대한 4개의 웰을 사용한다.
4. 약하게 플레이트를 진탕시켜 세포 균일하게 부착되도록 한다.
5. 10% CO2 인큐베이터에서 37℃에서 플레이트를 배양한다.
1일: 화합물의 첨가
분석의 본 과정은 박판 유동 후드에서 수행한다.
1. 96-웰 환저 플레이트에, 화합물의 최고 스크리닝 농도에서 발견되는 2X 최종 % DMSO를 함유하는 성장 배지 120㎕를 컬럼 1 내지 11에 부가한다. 예를 들면, 최고의 스크리닝 농도가 100μM이고, 이것이 100mM 스톡에서 제조되는 경우, 1X DMSO는 0.1%이고, 따라서 2X DMSO는 0.2%이다. 상기 플레이트를 화합물 당 4개 열에서 화합물을 적정하는데 사용한다.
2. 멸균된 15㎖ 튜브에서, 성장 배지 + 2X DMSO 중 최고 스크리닝 농도의 화합물 2X 용액을 제조한다. 세포주 당 1㎖가 필요하다. 화합물의 출발 농도는 일반적으로 100μM이지만, 이 농도는 화합물의 용해도에 따라 다양할 수 있다.
3. 2X 출발 화합물 용액 240㎕를 96-웰 환저 플레이트의 컬럼 12내 4배수의 웰에 전달한다. 컬럼 12에서 컬럼 11로, 컬럼 11에서 컬럼 10으로 등의 방식으로 컬럼 2까지 12㎕를 전달함으로써 오른쪽에서 왼쪽으로 플레이트를 가로질러 일련의 1:2 희석을 수행한다. 화합물 희석액 100㎕ 및 컬럼 1내의 배지 100㎕를 96-웰 평저 플레이트의 상응하는 웰내 세포상의 배지 100㎕ 상에 전달한다. 전체 용적은 웰당 200㎕가 되어야만 한다.
4. 플레이트를 인큐베이터내로 되돌려 놓고 3일간 항온 처리한다.
4 일: 분석의 진행
분석의 본 과정은 벤치에서 수행한다.
1. 배지를 흡인 제거하거나 쏟아낸다. 차가운 10% TCA 200㎕를 각 웰에 부가하여 세포를 고정시킨다. 플레이트를 4℃에서 60분 이상 항온 처리한다.
2. TCA를 제거하고 웰을 수돗물로 5회 세정한다. 플레이트를 종이 타월에 엎어 건조시킨다.
3. 세포를 웰 당 0.4% SRB 100㎕를 사용하여 10분 동안 염색시킨다.
4. SRB를 쏟아내고 웰을 1% 아세트산으로 5회 세정한다. 플레이트를 종이 타월에 엎어 완전히 건조시킨다.
5. 진탕기상에서 5 내지 10분 동안 웰 당 10mM 트리스 염기 100㎕를 사용하여 염료를 용해시킨다.
6. Dynatech ELISA 플레이트 판독기상에서 570nm에서 플레이트를 판독하고 참조용으로는 630nm에서 판독한다.
표 3에서 예시되는 바와 같이, RAS 과발현 세포의 성장 속도를 억제하는 화합물을 선별한다.
| 화합물 | IC50 (μM) RAS/NIH3T3 |
| A-1 | 1.04 |
| A-2 | 7.6 |
| A-6 | 13.5 |
| A-36 | 0.18 |
| A-77 | 0.7 |
실시예 6: A549 세포의 성장에 대한 5-아자퀴녹살린계 화합물의 효과를 측정하는 분석법
하기 분석법은 A549 세포의 성장률을 측정한다. 본 분석법의 목적은 A549 사람 폐암 세포의 성장에 대한 화합물의 효과를 측정하는 것이다. A549 세포는 ATCC(CCL185) 같은 상업적인 공급원으로부터 용이하게 수득할 수 있다.
재료:
96-웰 평저 멸균 플레이트
96-웰 환저 멸균 플레이트
멸균된 25㎖ 또는 100㎖ 저장 용기
피펫, 다관 피펫맨
멸균된 피펫 팁
멸균된 15㎖ 및 50㎖ 튜브
시약:
1% 아세트산 중 0.4% SRB
10mM 트리스 염기
10% TCA
1% 아세트산
멸균된 DMSO(제조원: Sigma)
DMSO 중 화합물(100mM 이하 스톡 용액)
트립신-EDTA(제조원: GIBCO BRL)
세포주 및 성장 배지:
A549 사람 폐암 세포(ATCC CCL185)
햄의 F12-K 중 10% 송아지 태 혈청
프로토콜:
0 일: 세포 플레이팅:
분석의 본 과정은 박판 유동 후드에서 수행한다.
1. 세포를 트립신 처리한다. 세포 현탁액 200㎕를 이소톤 10㎖중에 전달한다. Coulter 계수기로 세포를 계수한다.
2. 세포를 20,000 세포/㎖로 성장 배지내에서 희석시킨다. 96-웰 환저 플레이트 중 각각의 웰에 세포 100㎕를 전달하여 2000 세포/웰을 수득한다.
3. 각 화합물에 대해 플레이트의 반(4개 열) 및 각각의 화합물의 농도에 대해 4배수의 웰을 사용하며, 배지 대조군에 대해 4개 웰의 한 세트를 사용한다.
4. 조심스럽게 플레이트를 진탕시켜 세포의 균일한 부착을 가능하게 한다.
5. 10% CO2 인큐베이터내에서 37℃에서 플레이트를 항온 처리한다.
1 일: 화합물의 부가
분석의 본 과정은 박판 유동 후드에서 수행한다.
1. 96-웰 환저 플레이트에, 화합물의 최고 스크리닝 농도에서 발견되는 2X 최종 % DMSO를 함유하는 성장 배지 120㎕를 컬럼 1 내지 11에 부가한다. 예를 들면, 최고의 스크리닝 농도가 100μM이고, 이는 100mM 스톡에서 제조되는 경우, 1X DMSO는 0.1%이고, 따라서 2X DMSO는 0.2%이다. 상기 플레이트를 화합물 당 4개 열에서 화합물을 적정하는데 사용한다.
2. 멸균된 15㎖ 튜브에서, 성장 배지 + 2X DMSO 중 최고 스크리닝 농도의 화합물 2X 용액을 제조한다. 세포주 당 1㎖가 필요하다. 화합물의 출발 농도는 일반적으로 100μM이지만, 이 농도는 화합물의 용해도에 따라 다양할 수 있다.
3. 2X 출발 화합물 용액 240㎕를 96-웰 환저 플레이트의 컬럼 12내 4배수의 웰에 전달한다. 컬럼 12에서 컬럼 11로, 컬럼 11에서 컬럼 10으로 등의 방식으로 컬럼 2까지 120㎕를 전달함으로써 오른쪽에서 왼쪽으로 플레이트를 가로질러 일련의 1:2 희석을 수행한다. 화합물 희석액 100㎕ 및 컬럼 1내의 배지 100㎕를 96-웰 평저 플레이트의 상응하는 웰내 세포상의 배지 100㎕ 상에 전달한다. 전체 용적은 웰당 200㎕가 된다.
4. 플레이트를 인큐베이터내로 되돌려 놓고 3일간 항온 처리한다.
5 일: 분석의 진행
분석의 본 과정은 벤치에서 수행한다.
1. 배지를 흡인 제거하거나 쏟아낸다. 차가운 10% TCA 200㎕를 각 웰에 부가하여 세포를 고정시킨다. 플레이트를 4℃에서 60분 이상 항온 처리한다.
2. TCA를 제거하고 웰을 수돗물로 5회 세정한다. 플레이트를 종이 타월에 엎어 건조시킨다.
3. 세포를 웰 당 0.4% SRB 100㎕를 사용하여 10분 동안 염색시킨다.
4. SRB를 쏟아내고 웰을 1% 아세트산으로 5회 세정한다. 플레이트를 종이 타월에 엎어 완전히 건조시킨다.
5. 진탕기상에서 5 내지 10분 동안 웰 당 10mM 트리스 염기 100㎕를 사용하여 염료를 용해시킨다.
6. Dynatech ELISA 플레이트 판독기상에서 570nm에서 플레이트를 판독하고 참조용으로는 630nm에서 판독한다.
표 4에서 예시되는 바와 같이, A549 세포의 성장률을 억제하는 화합물을 선별한다.
| 화합물 | IC50(μM) A549 |
| A-2 | 25.1 > 10 (2% FBS) |
| A-6 | 23.8 > 10 (2% FBS) |
실시예 7: 생체내에서 RAF 조절 인자의 생물학적 활성을 결정하는 방법
이종이식 연구는 난소, 흑색종, 전립선, 폐 및 유방암 세포의 억제에 대한 본 발명의 화합물의 효과를 모니터링하기 위해서 사용할 수 있다. 분석을 위한 프로토콜은 문헌[PCT 공보 제WO 9640116호, filed June 5, 1996, by Tang et al., and entitled "Indolinone Compounds for the Treatment of Disease,"; 임의의 도면을 포함하는 이의 전문이 참조로 본원에 인용됨]에서 상세히 기술된다.
본원에서 예시적으로 기술된 본 발명은 본원에서 특별히 기술되지 않은 임의의 성분 또는 성분들, 제한 또는 제한들의 부재하에서도 수행될 수 있다. 사용된 용어 및 표현들은 기술을 위한 용어로서 사용되며 제한을 위한 용어가 아니며, 상기 용어 및 표현들의 사용이 나타내고 기술한 특성의 임의의 상응물 또는 이의 일부를 배제하고자 의도하는 것은 아니며, 다양한 변형들이 청구된 본 발명의 범위내에서 가능하다는 것을 인식해야 한다. 따라서, 본 발명이 바람직한 양태 및 임의 특성에 의해 구체적으로 기술되었다 하더라도, 본원에 기술된 개념의 변화 및 변형이 당해 분야의 숙련자에 의해 재분류될 수 있는 것으로 이해되어야 하며, 그러한 변화 및 변형은 첨부된 특허청구범위에 의해 정의된 바와 같이 본 발명의 범위내에 존재하는 것으로 이해되어야 한다.
특허 및 비-특허 참조 문헌을 모두 포함하여, 참조 문헌으로서 본원에서 이전에 인용하지 않은 참조 문헌들이 모든 목적을 위해서 본원에 참조로 인용된다. 기타 양태들은 하기 특허청구의 범위내에 존재한다.
Claims (40)
- 삭제
- 삭제
- (a) 세린/트레오닌 단백질 키나제를 발현하는 Sf9 세포, NIH-3T3 세포 또는 A549 세포를 5-아자퀴녹살린계 화합물과 접촉시키는 단계 및(b) 세포에 대한 효과를 모니터링하는 단계를 포함하는, 세린/트레오닌 단백질 키나제의 작용을 억제하는 화합물을 동정하는 시험관내 방법.
- 제3항에 있어서, 세포에 대한 효과가 세포 표현형의 변화 또는 불변인 시험관내 방법.
- 제3항에 있어서, 세포에 대한 효과가 세포 증식의 변화 또는 불변인 시험관내 방법.
- 제3항에 있어서, 세포에 대한 효과가 세린/트레오닌 단백질 키나제의 촉매 활성의 변화 또는 불변인 시험관내 방법.
- 제3항에 있어서, 세포에 대한 효과가 본원에 기술된 바와 같이 세린/트레오닌 단백질 키나제와 천연 결합 상대간의 상호 작용에서의 변화 또는 불변인 시험관내 방법.
- 제3항에 있어서,(a) 세포를 용해시켜 세린/트레오닌 단백질 키나제를 포함하는 용해액을 수득하는 단계;(b) 단계(a)의 세린/트레오닌 단백질 키나제를 항체에 흡착시키는 단계;(c) 단계(b)의 흡착된 세린/트레오닌 단백질 키나제를 기질 또는 기질들과 함께 항온 처리하는 단계 및(d) 단계(c)의 기질 또는 기질들을 고체 지지체 또는 항체에 흡착시키는 단계를 포함하며, 이때 세포 상에서 세포에 대한 효과를 모니터링하는 단계가 기질 또는 기질들의 포스페이트 농도를 측정하는 것을 포함하는 시험관내 방법.
- 제3항에 있어서, 세린/트레오닌 단백질 키나제가 RAF이고,(a) 세포를 용해시켜 RAF를 포함하는 용해액을 수득하는 단계;(b) 단계(a)의 RAF를 항체에 흡착시키는 단계;(c) 단계(b)의 흡착된 RAF를 MEK 및 MAPK와 함께 항온 처리하는 단계 및(d) 단계(c)의 MEK 및 MAPK를 고체 지지체 또는 항체 또는 항체들에 흡착시키는 단계를 포함하며, 이때 세포 상에서 세포에 대한 효과를 측정하는 단계가 MEK 및 MAPK의 포스페이트 농도를 모니터링하는 것을 포함하는 시험관내 방법.
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 제16항에 있어서, R1 및 R2가 독립적으로 (i) 메틸 또는 (ii) 치환되지 않거나 하이드록시 또는 C1-6 알콕시로 치환된 페닐로 이루어진 그룹으로부터 선택되는 약제학적 조성물.
- 삭제
- 삭제
- 삭제
- 삭제
- 삭제
- 제16항에 있어서, 암이 폐암, 난소암, 유방암, 뇌암, 축내성 뇌암, 결장암, 전립선암, 육종, 카포시 육종, 흑색종 및 신경교종으로 이루어지는 그룹으로부터 선택되는 약제학적 조성물.
- 삭제
- 삭제
- 삭제
- 제27항에 있어서, R3 및 R4가 수소인 화합물.
- 제29항에 있어서, R1 및 R2가 독립적으로 (i) 페닐로 치환된 메틸 또는 (ii) 하이드록시로 치환된 페닐로 이루어지는 그룹으로부터 선택되는 화합물.
- 제29항에 있어서, R1 및 R2가 4-하이드록시페닐인 화합물.
- 삭제
- 삭제
- 삭제
- 삭제
- (a) n-부탄올중에서 분말 탄산칼륨의 존재하에 2-아미노-6-클로로-3-니트로피리딘인 제1 반응물을 벤질아미노인 제2 반응물과 반응시켜 제1 중간체를 수득하는 단계;(b) 라니 니켈 및 수소의 존재하에 제1 중간체를 4-하이드록시페닐글리옥살 또는 벤질인 제3 반응물과 반응시키는 단계 및(c) 제27항에 따른 5-아자퀴녹살린계 화합물을 정제하는 단계를 포함하는, 제27항에 따른 화학식 I의 5-아자퀴녹살린계 화합물을 합성하는 방법.
- 삭제
- 삭제
- 삭제
- 삭제
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US6112397P | 1997-10-06 | 1997-10-06 | |
| US60/061,123 | 1997-10-06 | ||
| PCT/US1998/020910 WO1999017759A2 (en) | 1997-10-06 | 1998-10-05 | Methods of modulating serine/threonine protein kinase function with 5-azaquinoxaline-based compounds |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20010030934A KR20010030934A (ko) | 2001-04-16 |
| KR100633270B1 true KR100633270B1 (ko) | 2006-10-16 |
Family
ID=22033733
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020007003656A KR100633270B1 (ko) | 1997-10-06 | 1998-10-05 | 5-아자퀴녹살린계 화합물, 이의 합성 방법, 이를 사용한 세린/트레오닌 단백질키나제 작용의 조절 방법 및 이를 포함하는 약제학적 조성물 |
Country Status (31)
| Country | Link |
|---|---|
| US (2) | US6180631B1 (ko) |
| EP (1) | EP1028729B1 (ko) |
| JP (1) | JP2001518496A (ko) |
| KR (1) | KR100633270B1 (ko) |
| CN (1) | CN1169527C (ko) |
| AR (1) | AR013542A1 (ko) |
| AT (1) | ATE336250T1 (ko) |
| AU (1) | AU757585B2 (ko) |
| BG (1) | BG64969B1 (ko) |
| BR (1) | BR9814814A (ko) |
| CA (1) | CA2306257C (ko) |
| CY (1) | CY1106223T1 (ko) |
| CZ (1) | CZ298775B6 (ko) |
| DE (1) | DE69835612T2 (ko) |
| DK (1) | DK1028729T3 (ko) |
| ES (1) | ES2268791T3 (ko) |
| HK (1) | HK1031836A1 (ko) |
| HU (1) | HUP0100302A3 (ko) |
| IL (2) | IL135103A0 (ko) |
| MX (1) | MXPA03011007A (ko) |
| NO (1) | NO316598B1 (ko) |
| NZ (1) | NZ503431A (ko) |
| PL (1) | PL192039B1 (ko) |
| PT (1) | PT1028729E (ko) |
| RU (1) | RU2223753C2 (ko) |
| SK (1) | SK4722000A3 (ko) |
| TR (2) | TR200000906T2 (ko) |
| TW (1) | TWI245765B (ko) |
| UA (1) | UA71555C2 (ko) |
| WO (1) | WO1999017759A2 (ko) |
| ZA (1) | ZA988961B (ko) |
Families Citing this family (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| UA71555C2 (en) | 1997-10-06 | 2004-12-15 | Zentaris Gmbh | Methods for modulating function of serine/threonine protein kinases by 5-azaquinoline derivatives |
| US8124630B2 (en) * | 1999-01-13 | 2012-02-28 | Bayer Healthcare Llc | ω-carboxyaryl substituted diphenyl ureas as raf kinase inhibitors |
| EP2298311B1 (en) * | 1999-01-13 | 2012-05-09 | Bayer HealthCare LLC | w-Carboxy aryl substituted diphenyl ureas as p38 kinase inhibitors |
| AU1053501A (en) * | 1999-11-02 | 2001-05-14 | Ajinomoto Co., Inc. | Polyazanaphthalene compound and medicinal use thereof |
| US7371763B2 (en) * | 2001-04-20 | 2008-05-13 | Bayer Pharmaceuticals Corporation | Inhibition of raf kinase using quinolyl, isoquinolyl or pyridyl ureas |
| US20080108672A1 (en) * | 2002-01-11 | 2008-05-08 | Bernd Riedl | Omega-Carboxyaryl Substituted Diphenyl Ureas As Raf Kinase Inhibitors |
| MXPA04007832A (es) * | 2002-02-11 | 2005-09-08 | Bayer Pharmaceuticals Corp | Aril-ureas con actividad inhibitoria de angiogenesis. |
| AU2003270727A1 (en) * | 2002-09-17 | 2004-04-08 | Luna Innovations, Inc. | Remote temperature sensing of small volume and related apparatus thereof |
| US7557129B2 (en) | 2003-02-28 | 2009-07-07 | Bayer Healthcare Llc | Cyanopyridine derivatives useful in the treatment of cancer and other disorders |
| CA2526617C (en) * | 2003-05-20 | 2015-04-28 | Bayer Pharmaceuticals Corporation | Diaryl ureas with kinase inhibiting activity |
| DE102004022383A1 (de) * | 2004-05-06 | 2005-12-01 | Zentaris Gmbh | Neue Pyridopyrazine und deren Verwendung als Modulatoren von Kinasen |
| MXPA05012645A (es) * | 2003-05-23 | 2006-02-08 | Zentaris Gmbh | Piridopirazinas novedosas y su uso como moduladores de cinasa. |
| DE10323345A1 (de) * | 2003-05-23 | 2004-12-16 | Zentaris Gmbh | Neue Pyridopyrazine und deren Verwendung als Kinase-Inhibitoren |
| EP1635835B1 (en) * | 2003-06-13 | 2010-01-06 | Novartis AG | 2-aminopyrimidine derivatives as raf kinase inhibitors |
| UA84156C2 (ru) | 2003-07-23 | 2008-09-25 | Байер Фармасьютикалс Корпорейшн | Фторозамещённая омега-карбоксиарилдифенилмочевина для лечения и профилактики болезней и состояний |
| US8217042B2 (en) | 2005-11-11 | 2012-07-10 | Zentaris Gmbh | Pyridopyrazines and their use as modulators of kinases |
| AU2006313701B2 (en) | 2005-11-11 | 2012-05-31 | Aeterna Zentaris Gmbh | Novel pyridopyrazines and their use as modulators of kinases |
| EP1790342A1 (de) | 2005-11-11 | 2007-05-30 | Zentaris GmbH | Pyridopyrazin-Derivate und deren Verwendung als Modulatoren der Signaltransduktionswege |
| WO2010003308A1 (zh) * | 2008-07-10 | 2010-01-14 | 卞化石 | 一氧化氮及其信息传递系统在制备恶性肿瘤靶向治疗药物中的应用 |
| GB0812969D0 (en) | 2008-07-15 | 2008-08-20 | Sentinel Oncology Ltd | Pharmaceutical compounds |
| GB201007286D0 (en) | 2010-04-30 | 2010-06-16 | Astex Therapeutics Ltd | New compounds |
| GB201020179D0 (en) | 2010-11-29 | 2011-01-12 | Astex Therapeutics Ltd | New compounds |
| EP2508184A1 (en) | 2011-04-06 | 2012-10-10 | Æterna Zentaris GmbH | Pyridopyrazine derivatives and their use |
| GB201118656D0 (en) | 2011-10-28 | 2011-12-07 | Astex Therapeutics Ltd | New compounds |
| GB201118654D0 (en) | 2011-10-28 | 2011-12-07 | Astex Therapeutics Ltd | New compounds |
| GB201118652D0 (en) | 2011-10-28 | 2011-12-07 | Astex Therapeutics Ltd | New compounds |
| GB201118675D0 (en) | 2011-10-28 | 2011-12-14 | Astex Therapeutics Ltd | New compounds |
| GB201209613D0 (en) | 2012-05-30 | 2012-07-11 | Astex Therapeutics Ltd | New compounds |
| GB201209609D0 (en) | 2012-05-30 | 2012-07-11 | Astex Therapeutics Ltd | New compounds |
| WO2014109414A1 (ja) * | 2013-01-11 | 2014-07-17 | 富士フイルム株式会社 | 含窒素複素環化合物またはその塩 |
| GB201307577D0 (en) | 2013-04-26 | 2013-06-12 | Astex Therapeutics Ltd | New compounds |
| DE102013008118A1 (de) * | 2013-05-11 | 2014-11-13 | Merck Patent Gmbh | Arylchinazoline |
| HUE053654T2 (hu) | 2014-03-26 | 2021-07-28 | Astex Therapeutics Ltd | FGFR- és CMET-inhibitorok kombinációi a rák kezelésére |
| RU2715893C2 (ru) | 2014-03-26 | 2020-03-04 | Астекс Терапьютикс Лтд | Комбинации ингибитора fgfr и ингибитора igf1r |
| JO3512B1 (ar) | 2014-03-26 | 2020-07-05 | Astex Therapeutics Ltd | مشتقات كينوكسالين مفيدة كمعدلات لإنزيم fgfr كيناز |
| DK3174868T3 (da) | 2014-08-01 | 2021-11-08 | Nuevolution As | Forbindelser, der er aktive mod bromodomæner |
| JOP20200201A1 (ar) | 2015-02-10 | 2017-06-16 | Astex Therapeutics Ltd | تركيبات صيدلانية تشتمل على n-(3.5- ثنائي ميثوكسي فينيل)-n'-(1-ميثيل إيثيل)-n-[3-(ميثيل-1h-بيرازول-4-يل) كينوكسالين-6-يل]إيثان-1.2-ثنائي الأمين |
| US10478494B2 (en) | 2015-04-03 | 2019-11-19 | Astex Therapeutics Ltd | FGFR/PD-1 combination therapy for the treatment of cancer |
| SI3353177T1 (sl) | 2015-09-23 | 2020-08-31 | Janssen Pharmaceutica Nv | Triciklični heterocikli za zdravljenje raka |
| EP3353164B1 (en) | 2015-09-23 | 2021-11-03 | Janssen Pharmaceutica, N.V. | Bi-heteroaryl substituted 1,4-benzodiazepines and uses thereof for the treatment of cancer |
| US20190256492A1 (en) * | 2018-02-19 | 2019-08-22 | Washington University | Alpha-synuclein ligands |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4001017A (en) * | 1972-12-05 | 1977-01-04 | Ciba-Geigy Ag | Process for the photopolymerization of ethylenically unsaturated compounds |
| US4043819A (en) * | 1974-06-11 | 1977-08-23 | Ciba-Geigy Ag | Photo-polymerizable material for the preparation of stable polymeric images and process for making them by photopolymerization in a matrix |
| US5217999A (en) | 1987-12-24 | 1993-06-08 | Yissum Research Development Company Of The Hebrew University Of Jerusalem | Styryl compounds which inhibit EGF receptor protein tyrosine kinase |
| DE3804990A1 (de) * | 1988-02-18 | 1989-08-31 | Basf Ag | Herbizid wirksame, heterocyclisch substituierte sulfonamide |
| FR2656606B1 (fr) * | 1989-12-28 | 1993-06-25 | Roussel Uclaf | Utilisation de derives du 9,10-dihydrophenanthrene pour la preparation d'un medicament anti-tumoral, application a titre de medicaments de derives du 9,10-dihydrophenanthrene et produits derives de cette structure. |
| DE69105495T2 (de) | 1990-04-02 | 1995-04-06 | Pfizer | Benzylphosphonsäure-tyrosinkinaseinhibitoren. |
| US5302606A (en) | 1990-04-16 | 1994-04-12 | Rhone-Poulenc Rorer Pharmaceuticals Inc. | Styryl-substituted pyridyl compounds which inhibit EGF receptor tyrosine kinase |
| SG64322A1 (en) | 1991-05-10 | 1999-04-27 | Rhone Poulenc Rorer Int | Bis mono and bicyclic aryl and heteroaryl compounds which inhibit egf and/or pdgf receptor tyrosine kinase |
| JPH06503095A (ja) | 1991-05-29 | 1994-04-07 | ファイザー・インコーポレーテッド | 三環式ポリヒドロキシ系のチロシンキナーゼ阻害薬 |
| AU661533B2 (en) | 1992-01-20 | 1995-07-27 | Astrazeneca Ab | Quinazoline derivatives |
| HUT71553A (en) | 1992-08-06 | 1995-12-28 | Warner Lambert Co | 2-thioindoles (selenoindoles) and related disulfides (selenides) which inhibit protein tyrosine kinases and which have antitumor properties |
| US5330992A (en) | 1992-10-23 | 1994-07-19 | Sterling Winthrop Inc. | 1-cyclopropyl-4-pyridyl-quinolinones |
| GB9226855D0 (en) | 1992-12-23 | 1993-02-17 | Erba Carlo Spa | Vinylene-azaindole derivatives and process for their preparation |
| US5700823A (en) * | 1994-01-07 | 1997-12-23 | Sugen, Inc. | Treatment of platelet derived growth factor related disorders such as cancers |
| GB9501567D0 (en) | 1995-01-26 | 1995-03-15 | Pharmacia Spa | Hydrosoluble 3-arylidene-2-oxindole derivatives as tyrosine kinase inhibitors |
| US5593997A (en) * | 1995-05-23 | 1997-01-14 | Pfizer Inc. | 4-aminopyrazolo(3-,4-D)pyrimidine and 4-aminopyrazolo-(3,4-D)pyridine tyrosine kinase inhibitors |
| US5880141A (en) | 1995-06-07 | 1999-03-09 | Sugen, Inc. | Benzylidene-Z-indoline compounds for the treatment of disease |
| US5723462A (en) * | 1996-04-26 | 1998-03-03 | Neurogen Corporation | Certain fused pyrrolecarboxamides a new class of GABA brain receptor ligands |
| UA71555C2 (en) | 1997-10-06 | 2004-12-15 | Zentaris Gmbh | Methods for modulating function of serine/threonine protein kinases by 5-azaquinoline derivatives |
| GB9726851D0 (en) * | 1997-12-19 | 1998-02-18 | Zeneca Ltd | Human signal transduction serine/threonine kinase |
-
1998
- 1998-05-10 UA UA2000052578A patent/UA71555C2/uk unknown
- 1998-10-01 ZA ZA9808961A patent/ZA988961B/xx unknown
- 1998-10-05 US US09/166,723 patent/US6180631B1/en not_active Expired - Fee Related
- 1998-10-05 AU AU95141/98A patent/AU757585B2/en not_active Ceased
- 1998-10-05 HU HU0100302A patent/HUP0100302A3/hu not_active Application Discontinuation
- 1998-10-05 RU RU2000111434/15A patent/RU2223753C2/ru not_active IP Right Cessation
- 1998-10-05 DE DE69835612T patent/DE69835612T2/de not_active Expired - Fee Related
- 1998-10-05 PL PL339860A patent/PL192039B1/pl not_active IP Right Cessation
- 1998-10-05 MX MXPA03011007A patent/MXPA03011007A/es not_active IP Right Cessation
- 1998-10-05 EP EP98948606A patent/EP1028729B1/en not_active Expired - Lifetime
- 1998-10-05 CZ CZ20001129A patent/CZ298775B6/cs not_active IP Right Cessation
- 1998-10-05 NZ NZ503431A patent/NZ503431A/en unknown
- 1998-10-05 BR BR9814814-1A patent/BR9814814A/pt not_active Application Discontinuation
- 1998-10-05 WO PCT/US1998/020910 patent/WO1999017759A2/en active IP Right Grant
- 1998-10-05 DK DK98948606T patent/DK1028729T3/da active
- 1998-10-05 SK SK472-2000A patent/SK4722000A3/sk unknown
- 1998-10-05 ES ES98948606T patent/ES2268791T3/es not_active Expired - Lifetime
- 1998-10-05 TR TR2000/00906T patent/TR200000906T2/xx unknown
- 1998-10-05 JP JP2000514630A patent/JP2001518496A/ja not_active Withdrawn
- 1998-10-05 IL IL13510398A patent/IL135103A0/xx not_active IP Right Cessation
- 1998-10-05 PT PT98948606T patent/PT1028729E/pt unknown
- 1998-10-05 TR TR2001/00385T patent/TR200100385T2/xx unknown
- 1998-10-05 AT AT98948606T patent/ATE336250T1/de not_active IP Right Cessation
- 1998-10-05 CA CA002306257A patent/CA2306257C/en not_active Expired - Fee Related
- 1998-10-05 CN CNB988099403A patent/CN1169527C/zh not_active Expired - Fee Related
- 1998-10-05 KR KR1020007003656A patent/KR100633270B1/ko not_active IP Right Cessation
- 1998-10-06 TW TW087116559A patent/TWI245765B/zh not_active IP Right Cessation
- 1998-10-06 AR ARP980104970A patent/AR013542A1/es unknown
-
2000
- 2000-03-15 IL IL135103A patent/IL135103A/en unknown
- 2000-04-05 NO NO20001748A patent/NO316598B1/no unknown
- 2000-04-28 BG BG104392A patent/BG64969B1/bg unknown
- 2000-10-16 US US09/688,199 patent/US6727252B1/en not_active Expired - Fee Related
-
2001
- 2001-04-10 HK HK01102529A patent/HK1031836A1/xx not_active IP Right Cessation
-
2006
- 2006-10-30 CY CY20061101554T patent/CY1106223T1/el unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR100633270B1 (ko) | 5-아자퀴녹살린계 화합물, 이의 합성 방법, 이를 사용한 세린/트레오닌 단백질키나제 작용의 조절 방법 및 이를 포함하는 약제학적 조성물 | |
| KR100547929B1 (ko) | 세린/트레오닌 단백질 키나제 기능을 조절하기 위한 아자벤즈이미다졸계 화합물, 이의 제조방법 및 이를 포함하는 약제학적 조성물 | |
| US6204267B1 (en) | Methods of modulating serine/thereonine protein kinase function with quinazoline-based compounds | |
| MXPA00003255A (en) | Methods of modulating serine/threonine protein kinase function with 5-azaquinoxaline-based compounds | |
| MXPA00002910A (en) | Azabenzimidazole-based compounds for modulating serine/threonine protein kinase function | |
| CZ2000990A3 (cs) | Způsob in vitro modulace funkce serin/threonin protein kinázy, způsob in vitro identifikace sloučenin pro tuto modulaci, sloučeniny na bázi azabenzimidazolu,jejich použití, způsob jejich výroby a farmaceutické kompozice |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| N231 | Notification of change of applicant | ||
| A201 | Request for examination | ||
| N231 | Notification of change of applicant | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| LAPS | Lapse due to unpaid annual fee |