JP7458317B2 - 崩壊が改善された経口用固形製剤組成物及びその製造方法 - Google Patents
崩壊が改善された経口用固形製剤組成物及びその製造方法 Download PDFInfo
- Publication number
- JP7458317B2 JP7458317B2 JP2020523987A JP2020523987A JP7458317B2 JP 7458317 B2 JP7458317 B2 JP 7458317B2 JP 2020523987 A JP2020523987 A JP 2020523987A JP 2020523987 A JP2020523987 A JP 2020523987A JP 7458317 B2 JP7458317 B2 JP 7458317B2
- Authority
- JP
- Japan
- Prior art keywords
- weight
- soluble
- water
- gastric
- soluble polymer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/436—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a six-membered ring having oxygen as a ring hetero atom, e.g. rapamycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/21—Esters, e.g. nitroglycerine, selenocyanates
- A61K31/215—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids
- A61K31/216—Esters, e.g. nitroglycerine, selenocyanates of carboxylic acids of acids having aromatic rings, e.g. benactizyne, clofibrate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/365—Lactones
- A61K31/366—Lactones having six-membered rings, e.g. delta-lactones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/4025—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil not condensed and containing further heterocyclic rings, e.g. cromakalim
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4178—1,3-Diazoles not condensed 1,3-diazoles and containing further heterocyclic rings, e.g. pilocarpine, nitrofurantoin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4184—1,3-Diazoles condensed with carbocyclic rings, e.g. benzimidazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4412—Non condensed pyridines; Hydrogenated derivatives thereof having oxo groups directly attached to the heterocyclic ring
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/50—Pyridazines; Hydrogenated pyridazines
- A61K31/501—Pyridazines; Hydrogenated pyridazines not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/50—Pyridazines; Hydrogenated pyridazines
- A61K31/502—Pyridazines; Hydrogenated pyridazines ortho- or peri-condensed with carbocyclic ring systems, e.g. cinnoline, phthalazine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/50—Pyridazines; Hydrogenated pyridazines
- A61K31/5025—Pyridazines; Hydrogenated pyridazines ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/517—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with carbocyclic ring systems, e.g. quinazoline, perimidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/32—Macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. carbomers, poly(meth)acrylates, or polyvinyl pyrrolidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2009—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2013—Organic compounds, e.g. phospholipids, fats
- A61K9/2018—Sugars, or sugar alcohols, e.g. lactose, mannitol; Derivatives thereof, e.g. polysorbates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/2027—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2059—Starch, including chemically or physically modified derivatives; Amylose; Amylopectin; Dextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1635—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/16—Agglomerates; Granulates; Microbeadlets ; Microspheres; Pellets; Solid products obtained by spray drying, spray freeze drying, spray congealing,(multiple) emulsion solvent evaporation or extraction
- A61K9/1605—Excipients; Inactive ingredients
- A61K9/1629—Organic macromolecular compounds
- A61K9/1652—Polysaccharides, e.g. alginate, cellulose derivatives; Cyclodextrin
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Inorganic Chemistry (AREA)
- Physiology (AREA)
- Nutrition Science (AREA)
- Emergency Medicine (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
特に明記しない限り、本明細書全体で使用されるいくつかの用語は、次のように定義される。
解決手段の発見
本発明は、生理学的有効成分と高分子物質を含む、崩壊、分散又は溶出を改善させることができる経口用固形製剤組成物及びその製造方法を提供する。
前記有効成分は、薬物、薬物の薬学的に許容される塩、及び薬物の異性体からなる群から選ばれる1種以上を含んでいてもよい。
健康機能性食品。
本発明における高分子は、可溶化担体として用いられる水溶性又は胃溶性高分子を示す。
経口用組成物の製造において、最終製品は様々な方法で製剤化することができる。
崩壊特性、分散特性、溶出特性、水溶液内での溶解維持特性などが最終製品においても維持する必要がある。しかし、高分子は、粘性が大きく、強い結合力を有するので、最終製品の崩壊、分散、溶出を遅らせる役割を果たす可能性がある。特に、ヒプロメロース(=ヒドロキシプロピルメチルセルロース)やポビドン(=ポリビニルピロリドン)は、水をよく吸収する性質を有する親水性高分子である。親水性高分子、有効成分及びその他の賦形剤からなる錠剤が水と接触すると、高分子が水和して膨潤面を形成すると同時に、乾燥したコア状態であった錠剤にガラスのような層を形成する。その後、時間が経過すると、ゲル層となって拡散層が形成され、この拡散層を介して有効成分分子が徐々に外部媒体に放出される。しばらくすると、錠剤は浸食表面を形成し、腸の蠕動運動などの外部刺激によって錠剤の表面に侵食が生じる。このような過程により、有効成分の放出の遅延が発生する。これは2280、2910などの高分子には、より高い遅延効果がある。
NaHCO3(s)+HCl(aq)→NaCl(aq)+H2O(l)+CO2(g)
ヒドロキシプロピルメチルセルロース(HPMC)0.5gとタクロリムス0.5gをエタノール35gに溶解又は分散した後、混合物を情報させ、対流式オーブンで乾燥させた。その後、ミキサーを使用して約300μm以下に粉砕して、固体分散体を製造した。
2.5gのHPMC2910及び34.375gの水を定量的に混合し、泡立ちを防ぐために撹拌しながら完全に溶解した。0.5gのタクロリムス及び51.5625gのエタノールを定量した後、完全に溶解するまで混合及び撹拌した。前記タクロリムス溶液と前記HPMC水溶液を均一に混合し、0.825gのタルクを定量して混合物に加えた。その後、撹拌を続けて沈殿を防ぎ、コーティング液を製造した。
ポリエチレングリコール6000(Macrogol6000、三洋化成工業社、日本)20gとポロキサーマ188(Lutrol F68、BASF社、ドイツ)40gをビーカーに入れ、約90℃に加熱し、溶解し、撹拌して混合した。完全に溶融した後、ヒドロキシプロピルメチルセルロース2910(Pharmacoat606、信越化学工業社、日本)20gを前の溶融液に加え、撹拌して均一にした。ここにフェノフィブラート20gを加え、撹拌して溶解した。完全に溶解混合した後、混合物を別の容器に4時間広げて室温で冷却した。
HPMC(2910シリーズ、信越化学工業社、以下同じ)10gを水90gと混合し、撹拌して完全に溶解した10%w/w溶液を製造した。フェノフィブラート2gをエタノール200gと混合し、撹拌して完全に溶解させた。2つの溶液を混合及び撹拌して、沈殿のない溶液を製造した。フェノフィブラートとHPMCの割合は、重量で1:5(フェノフィブラート重量:HPMC重量)であった。
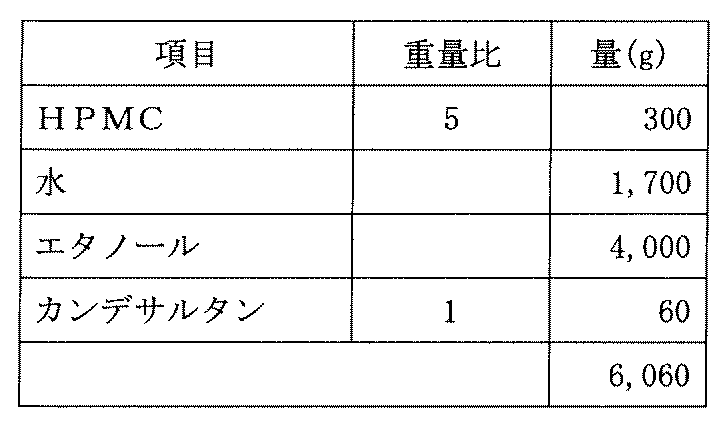
HPMC450gを水2550gと混合し、撹拌して完全に溶解させた15%w/w溶液を製造した。フェノフィブラート90gをエタノール5500gと混合し、撹拌して完全に溶解させた。2つの溶液を混合及び撹拌し、沈殿のない溶液を製造した。フェノフィブラートとHPMCの割合は、重量で1:5であった。
HPMC6gを水60gと混合し、撹拌して完全に溶解させた10%w/w溶液を製造した。セレコキシブ2gとポロキサーマ1882gをエタノール200gに入れ、40~50℃に加熱しながら撹拌して完全に溶解させた。2つの溶液を混合及び撹拌して、沈殿のない溶液を製造した。セレコキシブ:HPMC:ポロキサーマ188の割合は1:3:1であった。
PVPK302g、ポロキサーマ4072gをエタノール60mLが入ったビーカーに加え、40~50℃に加熱しながら撹拌して、完全に溶解した。その後、セレコキシブ2gをさらに加えて透明に溶解することを確認した。セレコキシブ:PVPK30:ポロキサーマ407の割合は1:1:1であった。
HPC-SSL2g、ポロキサーマ4072gをエタノール60mLが入ったビーカーに加え、40~50℃に加熱しながら撹拌して、完全に溶解させた。その後、セレコキシブ2gをさらに加えて透明に溶解することを確認した。セレコキシブ:HPC-SSL:ポロキサーマ407の割合は1:1:1であった。
HPC-SL240g、PVPK30240g、ポロキサーマ407480gをエタノール14.4Lが入板容器に加え、40~50℃に加熱しながら撹拌し、完全に溶解させた。その後、セレコキシブ480gをさらに加えて透明に溶解することを確認した。セレコキシブ:HPC-SL:PVPK30:ポロキサーマ407の割合は1:0.5:0.5:1であった。
クエン酸0.30gを精製水50mLに完全に溶解した後、イマチニブ遊離塩基2gを加えて溶解した。ポリビニルピロリドンK25(Kollidon(登録商標)25、BASF社、ドイツ)0.25gをエタノール50mLに完全に溶解させ、前記溶液に加え、撹拌して透明な液体を得た。
ソラフェニブトシラート(結晶形III型)2.67gとEudragit(登録商標)E1005.34gを150mLのEtOHに溶解した後(37℃、ロータリーエバポレーター)を使用して減圧下で蒸留し、真空ポンプを使用して溶媒を完全に除去した。壁面に形成されたソラフェニブトシラートとEudragit(登録商標)Eの固体分散体を得た。収率は65%であった。
ソラフェニブトシラートIII型7.2g、ヒプロメロース1.8g、ポビドン0.7g、ポロキサーマ0.2gを混合して製造した。次に、固体分散体にEudragit E2.9gを混合し、ふるいいにかけてソラフェニブ固体分散体混合物を製造した。
スニチニブ遊離塩基4g、ヒプロメロース8gをエタノールと水(エタノール:水=8:2)混合溶媒に溶解した後、混合物をロータリーエバポレーターを使用して減圧下で蒸留し、真空ポンプを使用して溶媒を完全に除去した。壁面に形成された固体分散体を得た。
ダサチニブ無水物6.2g、ヒプロメロース12.4g、ツイーン80(Tween 80)0.62gをエタノールと水(エタノール:水=7:3)混合溶媒に溶解した後、混合物をロータリーエバポレーターを使用して減圧下で蒸留し、真空ポンプを使用して溶媒を完全に除去した。壁面に形成された固体分散体を得た。
パゾパニブ塩酸塩10g、ヒプロメロース10g、ツイーン80(Tween 80)1gをエタノールと水(エタノール:水=7:3)混合溶媒に溶解し後、混合物をロータリーエバポレーターを使用して減圧下で蒸留し、真空ポンプを使用して溶媒を完全に除去した。壁面に形成された固体分散体を得た。
ラパチニブジトシレート10g、ヒプロメロース10g、ツイーン80(Tween 80)1gをエタノールと水(エタノール:水=7:3)混合溶媒に溶解した後、混合物をロータリーエバポレーターを使用して減圧下で蒸留し、真空ポンプを使用して溶媒を完全に除去した。壁面に形成された固体分散体を得た。
アキシチニブ3g、ヒプロメロース4gをエタノールと水(エタノール:水=7:3)混合溶媒に溶解した後、混合物をロータリーエバポレーターを使用して減圧下で蒸留し、真空ポンプを使用して溶媒を完全に除去した。壁面に形成された固体分散体を得た。
カボザンチニブリンゴ酸塩3g、ヒプロメロース3g、ツイーン80(Tween 80)1gをエタノールと水(エタノール:水=7:3)混合溶媒に溶解した後、混合物をロータリーエバポレーターを使用して減圧下で蒸留し、真空ポンプを使用して溶媒を完全に除去した。壁面に形成された固体分散体を得た。
ポナチニブ3g、ヒプロメロース6gをエタノールと水(エタノール:水=7:3)混合溶媒に溶解した後、混合物をロータリーエバポレーターを使用して減圧下で蒸留し、真空ポンプを使用して溶媒を完全に除去した。壁面に形成された固体分散体を得た。収率は62%であった。
バンデタニブ3.5g、ヒプロメロース3.5gをエタノールと水(エタノール:水=8:2)混合溶媒に溶解した後、混合物をロータリーエバポレーターを使用して減圧下で蒸留し、真空ポンプを使用して溶媒を完全に除去した。壁面に形成された固体分散体を得た。
ニロチニブ塩酸塩3g、ヒプロメロース6g、ツイーン80(Tween 80)0.5gをエタノールと水(エタノール:水=7:3)混合溶媒に溶解した後、混合物をロータリーエバポレーターを使用して減圧下で蒸留し、真空ポンプを使用して溶媒を完全に除去した。壁面に形成された固体分散体を得た。
エベロリムス3g、ヒプロメロース9gをエタノールと水(エタノール:水=8:2)混合溶媒に溶解した後、混合物をロータリーエバポレーターを使用して減圧下で蒸留し、真空ポンプを使用して溶媒を完全に除去した。壁面に形成された固体分散体を得た。
製造例15で得られた固体分散体混合物12.8g、マンニトール3.4g、デンプングリコール酸ナトリウム0.8g、炭酸水素ナトリウム1.3gをふるいにかけ、混合した後、そこにステアリン酸マグネシウム0.1gを篩過し、添加して最終混合した。この混合物を1錠当たり350.0mg重量に対して、11mmの円状パンチで打錠した。
製造例15で得られた固体分散体混合物12.9g、マンニトール2.0g、デンプングリコール酸ナトリウム0.8g、炭酸水素ナトリウム2.6gをふるいにかけ、混合した後、そこにステアリン酸マグネシウム0.1gを篩過し、添加して最終混合した。この混合物を1錠当たり350.0mg重量に対して、11mmの円状パンチで打錠した。
製造例15で得られた固体分散体混合物12.9g、マンニトール1.5g、デンプングリコール酸ナトリウム0.8g、炭酸水素ナトリウム3.2gをふるいにかけ、混合した後、そこにステアリン酸マグネシウム0.1gを篩過し、添加して最終混合した。この混合物を1錠当たり350.0mg重量に対して、11mmの円状パンチで打錠した。
製造例15で得られた固体分散体混合物12.9g、マンニトール1.0g、デンプングリコール酸ナトリウム0.8g、炭酸水素ナトリウム3.7gを篩過して、混合した後、そこにステアリン酸マグネシウム0.1gを篩過し、添加して最終混合した。この混合物を1錠当たり350.0mg重量に対して、11mmの円状パンチで打錠した。
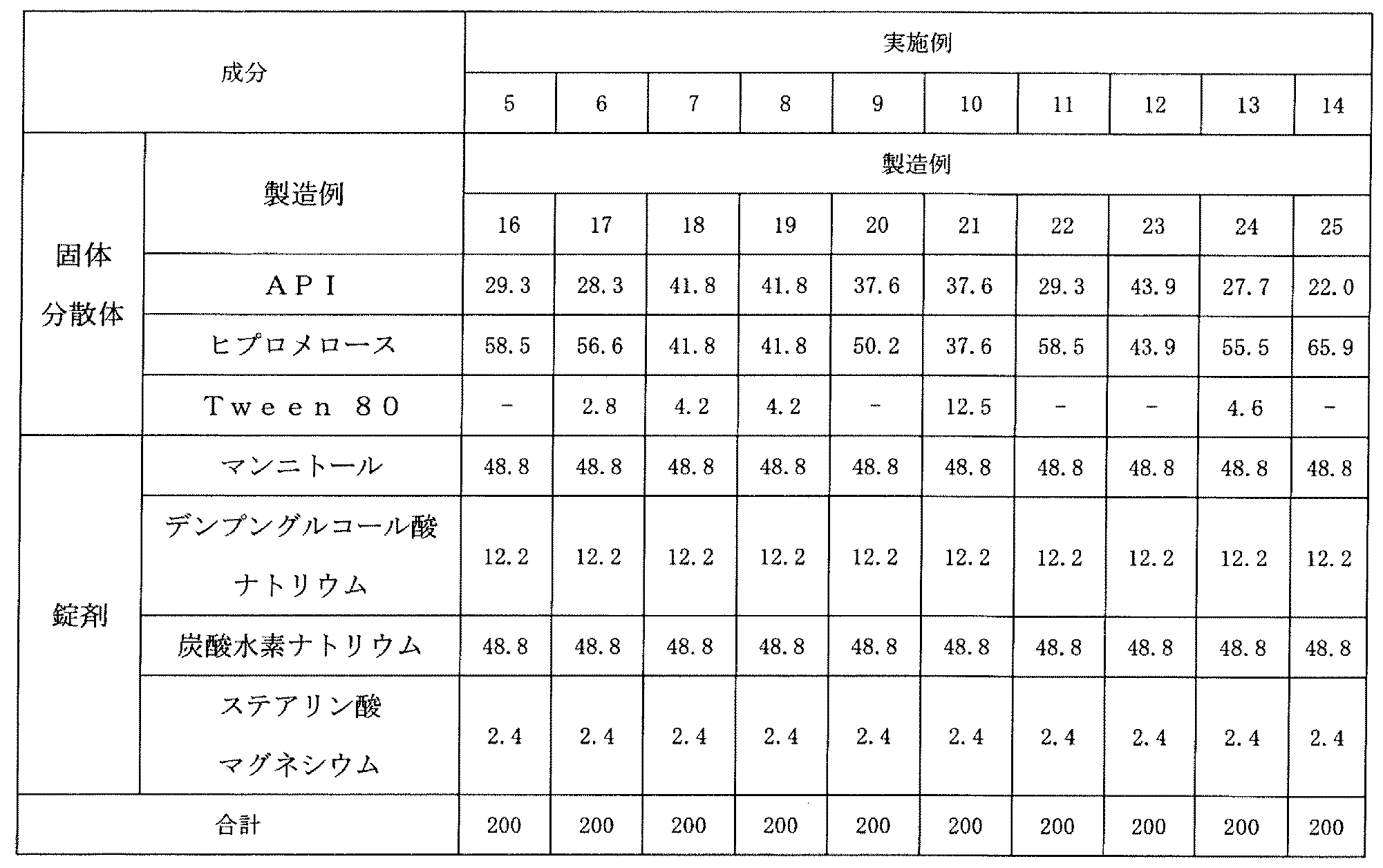
製造例16~25で得られた固体分散体1.8g、マンニトール1g、デンプングリコール酸ナトリウム0.3g、炭酸水素ナトリウム1gを篩過して混合した後、そこにステアリン酸マグネシウム0.05gを篩過し、添加してそれぞれを最終混合した。この混合物を1錠当たり200.0mg重量に対して、8.5mmの円状パンチで手動打錠した。
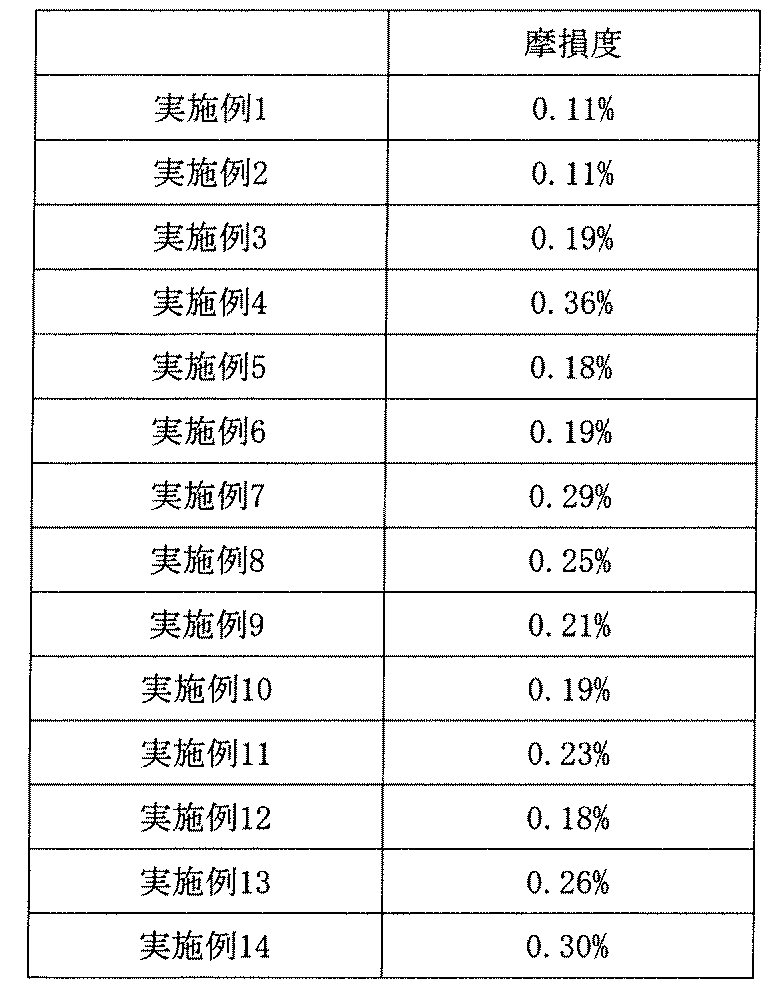
[摩損度測定]
摩損度は、米国薬局方1216錠剤摩損度カテゴリに記載されている方法であり、10個の錠剤でレッパイン摩損率試験機使用して測定した。その結果を下記表6に示した(測定時間=4分)。
Claims (3)
- 有効成分及び可溶化担体である水溶性又は胃溶性高分子を含む混合物、並びに崩壊促進剤として、発泡成分を含み、
発泡成分が発泡剤を含み、酸性化剤を含まず、
水溶性又は胃溶性高分子がヒドロキシプロピルメチルセルロースおよびポリメタクリレート共重合体の混合物であり、
有効成分が組成物全重量に対して、30~50重量%で含まれ、
有効成分がイマチニブ、エルロチニブ、スニチニブ、ソラフェニブ、ラパチニブ、ゲフィチニブ、ダサチニブ、レナリドミド、ニロチニブ、クリゾチニブ、パゾパニブ、バンデタニブ、アキシチニブ、レゴラフェニブ、アパチニブ、ベムラフェニブ、ルキソリチニブ、テモゾロミド、ラドチニブ、エベロリムス、ポマリドミド、オラパリブ、エンザルタミド、パルボシクリブ、オシメルチニブ、イブルチニブ、レンバチニブ、セリチニブ、ボスチニブ、カボザンチニブ、ダブラフェニブ、ポナチニブ、およびそれらの薬学的に許容される塩からなる群から選択され、
水溶性又は胃溶性高分子が組成物全重量に対して、20~30重量%で含まれ、
発泡剤が水溶性又は胃溶性高分子100重量部に対して50~80重量部で含まれ、
および
ポリメタクリレート共重合体は、ジメチルアミノエチルメタクリレートが共重合されたカチオン性高分子であり、および20000~80000g/モルの重量平均分子量を有する、経口用固形製剤組成物。 - 有効成分及び可溶化担体である水溶性又は胃溶性高分子高分子を含む混合物が、固体分散体形態である請求項1に記載の経口用固形製剤組成物。
- (1)有効成分及び可溶化担体である水溶性又は胃溶性高分子を含む混合物を製造する工程;及び
(2)前記混合物に崩壊促進剤として、発泡成分を添加する工程;
を含み、
発泡成分が発泡剤を含み、酸性化剤を含まず、
水溶性又は胃溶性高分子がヒドロキシプロピルメチルセルロースおよびポリメタクリレート共重合体の混合物であり、
有効成分が組成物全重量に対して、30~50重量%で含まれ、
有効成分がイマチニブ、エルロチニブ、スニチニブ、ソラフェニブ、ラパチニブ、ゲフィチニブ、ダサチニブ、レナリドミド、ニロチニブ、クリゾチニブ、パゾパニブ、バンデタニブ、アキシチニブ、レゴラフェニブ、アパチニブ、ベムラフェニブ、ルキソリチニブ、テモゾロミド、ラドチニブ、エベロリムス、ポマリドミド、オラパリブ、エンザルタミド、パルボシクリブ、オシメルチニブ、イブルチニブ、レンバチニブ、セリチニブ、ボスチニブ、カボザンチニブ、ダブラフェニブ、ポナチニブ、およびそれらの薬学的に許容される塩からなる群から選択され、
水溶性又は胃溶性高分子が組成物全重量に対して、20~30重量%で含まれ、
発泡剤が水溶性又は胃溶性高分子100重量部に対して50~80重量部で含まれ、および
ポリメタクリレート共重合体は、ジメチルアミノエチルメタクリレートが共重合されたカチオン性高分子であり、および20000~80000g/モルの重量平均分子量を有する、経口用固形製剤組成物の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2022124986A JP2022153652A (ja) | 2017-10-31 | 2022-08-04 | 崩壊が改善された経口用固形製剤組成物及びその製造方法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20170144139 | 2017-10-31 | ||
| KR10-2017-0144139 | 2017-10-31 | ||
| PCT/KR2018/013034 WO2019088669A1 (ko) | 2017-10-31 | 2018-10-30 | 붕해가 개선된 경구용 고형 제제 조성물 및 이의 제조 방법 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022124986A Division JP2022153652A (ja) | 2017-10-31 | 2022-08-04 | 崩壊が改善された経口用固形製剤組成物及びその製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021501166A JP2021501166A (ja) | 2021-01-14 |
| JP7458317B2 true JP7458317B2 (ja) | 2024-03-29 |
Family
ID=66332189
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020523987A Active JP7458317B2 (ja) | 2017-10-31 | 2018-10-30 | 崩壊が改善された経口用固形製剤組成物及びその製造方法 |
| JP2022124986A Pending JP2022153652A (ja) | 2017-10-31 | 2022-08-04 | 崩壊が改善された経口用固形製剤組成物及びその製造方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022124986A Pending JP2022153652A (ja) | 2017-10-31 | 2022-08-04 | 崩壊が改善された経口用固形製剤組成物及びその製造方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US11980610B2 (ja) |
| EP (1) | EP3705118B1 (ja) |
| JP (2) | JP7458317B2 (ja) |
| KR (3) | KR102333609B1 (ja) |
| WO (1) | WO2019088669A1 (ja) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7458317B2 (ja) * | 2017-10-31 | 2024-03-29 | サムヤン、ホールディングス、コーポレーション | 崩壊が改善された経口用固形製剤組成物及びその製造方法 |
| CA3168680A1 (en) | 2020-01-31 | 2021-08-05 | Nanocopoeia, Llc | Amorphous nilotinib microparticles and uses thereof |
| WO2021222739A1 (en) * | 2020-04-30 | 2021-11-04 | Nanocopoeia, Llc | Orally disintegrating tablet comprising amorphous solid dispersion of nilotinib |
| IT202000027678A1 (it) * | 2020-11-18 | 2022-05-18 | Indena Spa | Dispersioni solide amorfe di cabozantinib-(s)-malato e processi per la loro preparazione |
| WO2022115464A1 (en) * | 2020-11-25 | 2022-06-02 | Nanocopoeia, Llc | Amorphous cabozantinib particles and uses thereof |
| CN116887866A (zh) | 2020-12-03 | 2023-10-13 | 巴特尔纪念研究院 | 聚合物纳米颗粒和dna纳米结构组合物及用于非病毒递送的方法 |
| US20230310393A1 (en) * | 2020-12-07 | 2023-10-05 | Tianjin Creatron Biotechnology Co., Ltd. | Sorafenib pharmaceutical composition with high bioavailability and use thereof |
| US11590122B2 (en) * | 2021-02-19 | 2023-02-28 | Slayback Pharma Llc | Pharmaceutical compositions of cabozantinib |
| WO2022216977A1 (en) | 2021-04-07 | 2022-10-13 | Batelle Memorial Institute | Rapid design, build, test, and learn technologies for identifying and using non-viral carriers |
| CN113069418A (zh) * | 2021-04-21 | 2021-07-06 | 海南通用三洋药业有限公司 | 一种阿莫西林颗粒的制备方法 |
| WO2023021411A1 (en) * | 2021-08-19 | 2023-02-23 | Neuheit Pharma Technologies Pvt. Ltd | Levothyroxine compositions and it's process |
| CN114306271B (zh) * | 2021-11-24 | 2023-04-07 | 石药集团中奇制药技术(石家庄)有限公司 | 一种仑伐替尼组合物 |
| WO2025072751A1 (en) | 2023-09-29 | 2025-04-03 | Battelle Memorial Institute | Polymer nanoparticle compositions for in vivo expression of polypeptides |
| US12441996B2 (en) | 2023-12-08 | 2025-10-14 | Battelle Memorial Institute | Use of DNA origami nanostructures for molecular information based data storage systems |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998029137A1 (en) | 1996-12-25 | 1998-07-09 | Yamanouchi Pharmaceutical Co., Ltd. | Immediately disintegrable medicinal compositions |
| WO2002069932A1 (en) | 2001-03-05 | 2002-09-12 | Nippon Shinyaku Co., Ltd. | Foaming compositions |
| JP2009514884A (ja) | 2005-11-04 | 2009-04-09 | イーストマン ケミカル カンパニー | 難溶性医薬活性剤の投与のためのカルボキシアルキルセルロースエステル |
| JP2012510987A (ja) | 2008-12-04 | 2012-05-17 | インテック ファーマ リミテッド | ザレプロン胃内滞留性薬剤送達システム |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100522239B1 (ko) | 2002-07-16 | 2005-10-18 | 주식회사 서울제약 | 아세트아미노펜을 함유하는 제어방출성의 경구용 제제 |
| KR101381999B1 (ko) | 2007-07-06 | 2014-04-14 | 동아에스티 주식회사 | 위염 치료제의 효력을 극대화시키기 위한 가용화 위체류시스템 매트릭스 제제 |
| CA2718255C (en) | 2008-03-11 | 2016-08-23 | Aska Pharmaceutical Co., Ltd. | Solid dispersion and pharmaceutical composition of the same, and production processes thereof |
| KR101071502B1 (ko) * | 2008-06-18 | 2011-10-10 | 한국콜마 주식회사 | 매스틱을 포함하는 발포성 속붕해정 |
| US20110071169A1 (en) * | 2009-08-26 | 2011-03-24 | Mai De Ltd | Preparation of polymorphic form of lapatinib ditosylate |
| KR101257919B1 (ko) | 2011-07-14 | 2013-04-30 | 주식회사 바이오파마티스 | 콜린 알포세레이트 또는 이의 약학적으로 허용되는 염을 포함하는 경구용 고형 제제 및 이의 제조방법 |
| CN102319251A (zh) * | 2011-07-19 | 2012-01-18 | 淄博职业学院 | 阿司匹林双嘧达莫胃内漂浮胶囊及其制备方法 |
| KR20130068291A (ko) * | 2011-12-15 | 2013-06-26 | 주식회사 삼양바이오팜 | 이매티닙 유리염기를 포함하는 고체분산체 및 그의 제조방법 |
| JP7458317B2 (ja) * | 2017-10-31 | 2024-03-29 | サムヤン、ホールディングス、コーポレーション | 崩壊が改善された経口用固形製剤組成物及びその製造方法 |
-
2018
- 2018-10-30 JP JP2020523987A patent/JP7458317B2/ja active Active
- 2018-10-30 US US16/760,302 patent/US11980610B2/en active Active
- 2018-10-30 WO PCT/KR2018/013034 patent/WO2019088669A1/ko not_active Ceased
- 2018-10-30 KR KR1020180130400A patent/KR102333609B1/ko not_active Expired - Fee Related
- 2018-10-30 EP EP18872612.9A patent/EP3705118B1/en active Active
-
2021
- 2021-11-26 KR KR1020210165553A patent/KR102546742B1/ko active Active
-
2022
- 2022-08-04 JP JP2022124986A patent/JP2022153652A/ja active Pending
-
2023
- 2023-06-19 KR KR1020230078247A patent/KR102788075B1/ko active Active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998029137A1 (en) | 1996-12-25 | 1998-07-09 | Yamanouchi Pharmaceutical Co., Ltd. | Immediately disintegrable medicinal compositions |
| US20020031547A1 (en) | 1996-12-25 | 2002-03-14 | Yamanouchi Pharmaceutical Co., Ltd. | Immediately disintegrable medicinal composition |
| WO2002069932A1 (en) | 2001-03-05 | 2002-09-12 | Nippon Shinyaku Co., Ltd. | Foaming compositions |
| JP2009514884A (ja) | 2005-11-04 | 2009-04-09 | イーストマン ケミカル カンパニー | 難溶性医薬活性剤の投与のためのカルボキシアルキルセルロースエステル |
| JP2012510987A (ja) | 2008-12-04 | 2012-05-17 | インテック ファーマ リミテッド | ザレプロン胃内滞留性薬剤送達システム |
Non-Patent Citations (1)
| Title |
|---|
| Future Journal of Pharmaceutical Sciences,Volume 3,Issue 1,June 2017,p.33-45(https://doi.org/10.1016/j.fjps.2017.02.001) |
Also Published As
| Publication number | Publication date |
|---|---|
| KR102333609B1 (ko) | 2021-12-01 |
| KR102788075B1 (ko) | 2025-03-31 |
| JP2021501166A (ja) | 2021-01-14 |
| WO2019088669A1 (ko) | 2019-05-09 |
| KR20190049543A (ko) | 2019-05-09 |
| KR102546742B1 (ko) | 2023-06-23 |
| KR20230093401A (ko) | 2023-06-27 |
| KR20210149002A (ko) | 2021-12-08 |
| US20200261426A1 (en) | 2020-08-20 |
| EP3705118A1 (en) | 2020-09-09 |
| EP3705118B1 (en) | 2024-02-14 |
| EP3705118A4 (en) | 2021-08-18 |
| US11980610B2 (en) | 2024-05-14 |
| JP2022153652A (ja) | 2022-10-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7458317B2 (ja) | 崩壊が改善された経口用固形製剤組成物及びその製造方法 | |
| TWI682789B (zh) | 控釋藥物組合物及其製備方法 | |
| JP6545839B2 (ja) | 口腔内崩壊錠及びその製造方法 | |
| US11839684B2 (en) | Mucoadhesive pharmaceutical composition and preparation method therefor | |
| JP5777170B2 (ja) | 速溶性固体剤形 | |
| US9526789B2 (en) | Highly robust fast-disintegrating tablet and process for manufacturing the same | |
| ES2673182T3 (es) | Composición farmacéutica que contiene un derivado de diamina | |
| JP7096164B2 (ja) | ジアミン誘導体を含む口腔内崩壊錠 | |
| KR101317592B1 (ko) | 프레가발린, 폴리에틸렌옥사이드 및 폴리비닐알코올-폴리에틸렌글리콜 그라프트 공중합체를 함유하는 위체류형 서방성 제제 | |
| CA2501345A1 (en) | Gastro-retentive levodopa delivery form | |
| BRPI0714514B1 (pt) | Grânulo compreendendo núcleo revestido por oxicodona, bem como comprimido para desintegração oral e seu processo de fabricação | |
| CN102143738A (zh) | 药物固体制剂 | |
| CN110603035A (zh) | 具有改善的水溶解度及生物利用率的组合物 | |
| CN105025882B (zh) | 熔融挤出而成的控释药物组合物及包含其的口服制剂 | |
| KR20180096530A (ko) | 이토프리드 염산염을 포함하는 속효성과 지속성을 갖는 약학적 제제 | |
| EP2277511B1 (en) | Extended release pharmaceutical compositions of levetiracetam | |
| JPWO2003075919A1 (ja) | 塩酸ピルジカイニド含有錠剤(乾式) | |
| WO2003075918A1 (fr) | Comprime contenant du chlorhydrate de pilsicainide (voie humide) | |
| JP6150564B2 (ja) | 口腔内速崩壊性錠剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200625 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210525 |
|
| A711 | Notification of change in applicant |
Free format text: JAPANESE INTERMEDIATE CODE: A712 Effective date: 20210719 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210824 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211022 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20220405 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220804 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20220804 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20220815 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20220816 |
|
| A912 | Re-examination (zenchi) completed and case transferred to appeal board |
Free format text: JAPANESE INTERMEDIATE CODE: A912 Effective date: 20220902 |
|
| C211 | Notice of termination of reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C211 Effective date: 20220906 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231204 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240318 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7458317 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |