JP7340139B2 - 低濃度アトロピン眼科用製剤の安定性を改善するための方法 - Google Patents
低濃度アトロピン眼科用製剤の安定性を改善するための方法 Download PDFInfo
- Publication number
- JP7340139B2 JP7340139B2 JP2021540354A JP2021540354A JP7340139B2 JP 7340139 B2 JP7340139 B2 JP 7340139B2 JP 2021540354 A JP2021540354 A JP 2021540354A JP 2021540354 A JP2021540354 A JP 2021540354A JP 7340139 B2 JP7340139 B2 JP 7340139B2
- Authority
- JP
- Japan
- Prior art keywords
- atropine sulfate
- slurry
- solvent
- slurry washing
- water
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/46—8-Azabicyclo [3.2.1] octane; Derivatives thereof, e.g. atropine, cocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/16—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing nitrogen, e.g. nitro-, nitroso-, azo-compounds, nitriles, cyanates
- A61K47/18—Amines; Amides; Ureas; Quaternary ammonium compounds; Amino acids; Oligopeptides having up to five amino acids
- A61K47/183—Amino acids, e.g. glycine, EDTA or aspartame
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/16—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing nitrogen, e.g. nitro-, nitroso-, azo-compounds, nitriles, cyanates
- A61K47/18—Amines; Amides; Ureas; Quaternary ammonium compounds; Amino acids; Oligopeptides having up to five amino acids
- A61K47/186—Quaternary ammonium compounds, e.g. benzalkonium chloride or cetrimide
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/547—Chelates, e.g. Gd-DOTA or Zinc-amino acid chelates; Chelate-forming compounds, e.g. DOTA or ethylenediamine being covalently linked or complexed to the pharmacologically- or therapeutically-active agent
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/10—Ophthalmic agents for accommodation disorders, e.g. myopia
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D451/00—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof
- C07D451/02—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof containing not further condensed 8-azabicyclo [3.2.1] octane or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane; Cyclic acetals thereof
- C07D451/04—Heterocyclic compounds containing 8-azabicyclo [3.2.1] octane, 9-azabicyclo [3.3.1] nonane, or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane or granatane alkaloids, scopolamine; Cyclic acetals thereof containing not further condensed 8-azabicyclo [3.2.1] octane or 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring systems, e.g. tropane; Cyclic acetals thereof with hetero atoms directly attached in position 3 of the 8-azabicyclo [3.2.1] octane or in position 7 of the 3-oxa-9-azatricyclo [3.3.1.0<2,4>] nonane ring system
- C07D451/06—Oxygen atoms
- C07D451/10—Oxygen atoms acylated by aliphatic or araliphatic carboxylic acids, e.g. atropine, scopolamine
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Ophthalmology & Optometry (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Emergency Medicine (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Description
有効医薬成分であるアトロピン硫酸塩を、スラリー洗浄用溶媒a、スラリー洗浄用溶媒b及びスラリー洗浄用溶媒cをそれぞれ用いてスラリー洗浄するステップを含み、
スラリー洗浄用溶媒aは、低極性溶媒であり、
スラリー洗浄用溶媒bは、アセトン-水混合溶媒(水の体積は2%~10%を占め、例えば、5%を占める)であり、
スラリー洗浄用溶媒cは、低極性溶媒である、
方法を提供する。
アトロピン硫酸塩 0.001%~0.1%(好ましくは、0.005%~0.05%)
増粘剤 0.1%~10%
錯化剤 0.001%~0.05%
pH調整剤 医薬組成物のpHを3.5~6.5に調整する量
及び、水 残部
のとおりであり、
任意選択で、医薬組成物は、0.001%~0.05%の静菌剤をさらに含み、
任意選択で、医薬組成物は、0.1%~2%の浸透圧調節剤をさらに含む。
処方1:
アトロピン硫酸塩 0.005%~0.02%
ヒドロキシプロピルメチルセルロース 1%
エデト酸二ナトリウム 0.01%
塩化ベンザルコニウム 0.01%
リン酸二水素ナトリウム一水和物 0.25%
リン酸水素二ナトリウム 0.0025%
及び、水 残部
アトロピン硫酸塩 0.005%~0.02%
ヒドロキシプロピルメチルセルロース 1%
ヒアルロン酸ナトリウム 2%
エデト酸二ナトリウム 0.01%
塩化ベンザルコニウム 0.01%
リン酸二水素ナトリウム一水和物 0.25%
リン酸水素二ナトリウム 0.0025%
及び、水 残部
アトロピン硫酸塩 0.005%~0.01%
ヒドロキシプロピルメチルセルロース 1%
プロピレングリコール 0.3%
エデト酸二ナトリウム 0.01%
塩化ベンザルコニウム 0.01%
ホウ酸 1.8%
及び、水 残部
アトロピン硫酸塩 0.005%~0.01%
ヒドロキシプロピルメチルセルロース 1%
エデト酸二ナトリウム 0.01%
ホウ酸 1.8%
及び、水 残部
増粘剤を、60℃~90℃(例えば、70℃~90℃、80℃~90℃)の水中で拡散及び膨潤させ、20℃~30℃(例えば、20℃~25℃)の水を補充して溶解させて、液体aを得るステップと、
pH調整剤、錯化剤、静菌剤、及び任意選択の浸透圧調節剤を60℃~80℃(例えば、65℃~80℃、65℃~75℃)の水に個別に溶解させ、30℃未満(例えば、室温)に冷却し、アトロピン硫酸塩を加えて、溶解後に液体bを得るステップと、
液体a及び液体bを混合し、残部の水を加えて、医薬組成物を得るステップとを含み、
任意選択で、得られた医薬組成物をろ過する、好ましくは得られた医薬組成物を0.22μmのろ過膜でろ過するステップをさらに含む、方法を提供する。
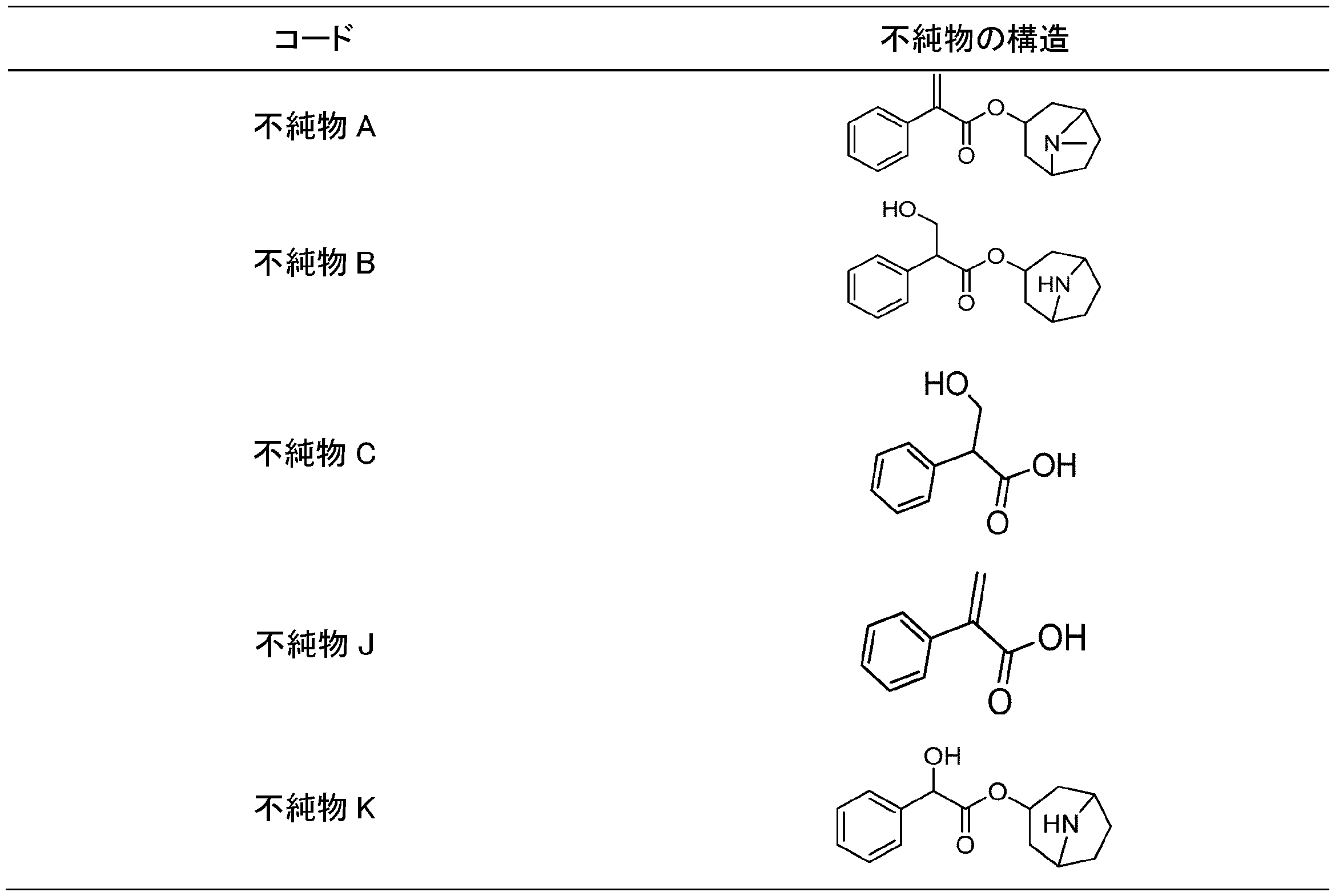
純度99%超の市販の有効医薬成分であるアトロピン硫酸塩A又はBを、60-メッシュ微粉砕機に入れ、徐々に微粉砕してふるいにかけ、ふるいの下の原材料を後で使用するために回収した。50gの微粉砕した有効医薬成分を取って、3000mLの三つ口フラスコに入れ、20倍量の無水アセトンを加え、3時間の間40℃で撹拌してスラリー洗浄を実施し、次いで吸引ろ過にかけて湿った生成物1を得た。この湿った生成物1を取って、3000mLの三つ口フラスコに入れ、15倍量の、水の体積が5%を占めるアセトン-水混合溶媒を加え、4時間の間40℃で撹拌してスラリー洗浄を実施し、次いで吸引ろ過にかけて湿った生成物2を得た。この湿った生成物2を取って、1000mLの三つ口フラスコに入れ、10倍量のアセトンを加え、1.5時間の間5℃で撹拌してスラリー洗浄を実施し、次いで吸引ろ過にかけ、6時間の間減圧下で乾燥して、収率82%で41gのアトロピン硫酸塩を得た。不純物のHPLC分析を実施し、結果を図1~2及び表1~2に示した。
表3の処方/配合に従って、アトロピン眼科用製剤を下記の調製方法によって調製した。
(1)10gの80℃~90℃の注入水を取り、規定量のヒドロキシプロピルメチルセルロース又はヒアルロン酸ナトリウムを注入水に加え、充分に拡散及び膨潤させ、30℃未満の温度の注入水を補充して20gにし、撹拌して溶解させ、後で使用するための透明な溶液を得た。
(2)50gの65℃~75℃の温度の注入水を取り、規定量のリン酸二水素ナトリウム一水和物、リン酸水素二ナトリウム、エデト酸二ナトリウム及び塩化ベンザルコニウムを、順次加えて溶解し、静置して30℃未満に冷却し、実施例1の方法に従って精製した規定量のアトロピン硫酸塩を加えて、撹拌して溶解した。
(3)(1)で得たヒドロキシプロピルメチルセルロース溶液及び(2)で得た溶液を均一に混合した。
(4)(3)で得た混合溶液に、水を補充して合計量を100gにし、均一に撹拌し、0.22μmろ過膜のろ過によって無菌化して、瓶詰めした。
対応する表4の処方/配合に従って、アトロピン眼科用製剤を下記の調製方法によって調製した。
(1)10gの80℃~90℃の注入水を取り、規定量のヒドロキシプロピルメチルセルロースを注入水に加えて十分に拡散及び膨潤させ、30℃未満の温度の注入水を補充して20gにし、撹拌して溶解させ、後で使用するための透明な溶液を得た。
(2)50gの65℃~75℃の温度の注入水を取り、規定量のホウ酸、エデト酸二ナトリウム、及び塩化ベンザルコニウムを順次加えて溶解し、静置して30℃未満に冷却して、実施例1の方法に従って精製した規定量のアトロピン硫酸塩を加えて、撹拌して溶解した。
(3)(1)で得たヒドロキシプロピルメチルセルロース溶液、及び(2)で得た溶液を均一に混合した。
(4)(3)で得た混合溶液に、水を補充して合計量を100gにし、均一に撹拌し、0.22μmろ過膜のろ過によって無菌化して、瓶詰めした。
対応する表3の処方/配合に従って、アトロピン眼科用製剤を、下記の調製方法によって調製した。
(1)10gの80℃~90℃の注入水を取り、規定量のヒドロキシプロピルメチルセルロース又はヒアルロン酸ナトリウムを注入水に加え、十分に拡散及び膨潤させ、30℃未満の温度の注入水を補充して20gにし、撹拌して溶解させ、後で使用するための透明な溶液を得た。
(2)50gの65℃~75℃の温度の注入水を取り、規定量のリン酸二水素ナトリウム一水和物、リン酸水素二ナトリウム、エデト酸二ナトリウム及び塩化ベンザルコニウムを順次加えて溶解し、静置して30℃未満に冷却し、規定量の有効医薬成分であるアトロピン硫酸塩B160903を加え、撹拌して溶解させた。
(3)(1)で得たヒドロキシプロピルメチルセルロース溶液、及び(2)で得た溶液を、均一に混合した。
(4)水を補充して合計量を100gにし、均一に撹拌し、0.22μmろ過膜のろ過によって無菌化して、瓶詰めした。
対応する表4の処方/配合に従って、アトロピン眼科用製剤を、下記の調製方法によって調製した。
(1)10gの80℃~90℃の注入水を取り、規定量のヒドロキシプロピルメチルセルロースを注入水に加え、十分に拡散及び膨潤させ、30℃未満の温度の注入水を補充して20gにし、撹拌して溶解させ、後で使用するための透明な溶液を得た。
(2)50gの65℃~75℃の温度の注入水を取り、規定量のホウ酸、エデト酸二ナトリウム、及び塩化ベンザルコニウムを順次加えて溶解し、静置して30℃未満に冷却し、規定量の有効医薬成分であるアトロピン硫酸塩B160903を加え、撹拌して溶解させた。
(3)(1)で得たヒドロキシプロピルメチルセルロース溶液、及び(2)で得た溶液を、均一に混合した。
(4)(3)で得た混合溶液に、水を補充して合計量を100gにし、均一に撹拌し、0.22μmろ過膜のろ過によって無菌化して、瓶詰めした。
実施例1で精製した有効医薬成分であるアトロピン硫酸塩(バッチ番号:160903-P01)を取り、包装して(医薬品用の低密度ポリエチレン袋を内層として、アルミニウム製筒を外層として用い、樹脂で封止した)、40℃±2℃、相対湿度75%±5%の条件下で貯蔵し、製品の変化を0か月、1か月、2か月、3か月、及び6か月目でそれぞれ観察した。結果を表5に示した。
実施例2~9及び比較例1~8で得られたアトロピン眼科用製剤を取り、40℃±2℃、相対湿度25%±5%の条件下で貯蔵し、有効成分の含有量及び主要分解物の不純物Cの含有量を、0か月、1か月、2か月、3か月、及び6か月目でそれぞれ試験した。結果を表6に示した。
Claims (11)
- アトロピン硫酸塩製剤の安定性を改善するための方法であって、有効医薬成分であるアトロピン硫酸塩の総不純物の含有量を≦0.25%、及び/又は単一不純物の含有量を≦0.05%に制御することを特徴とし、
前記制御が、有効医薬成分であるアトロピン硫酸塩に、スラリー洗浄用溶媒a、スラリー洗浄用溶媒b及びスラリー洗浄用溶媒cをこの順番にて用い、スラリー洗浄を実施することによって行われ、
スラリー洗浄用溶媒aが無水アセトンであり、
スラリー洗浄用溶媒bが、水の体積が5%を占めるアセトン-水混合溶媒であり、
スラリー洗浄用溶媒cがアセトンである、方法。 - スラリー洗浄用溶媒aが、アトロピン硫酸塩1グラムあたり3~30mlのスラリー洗浄用溶媒aが加えられる量で使用され、スラリー洗浄用溶媒aを用いるスラリー洗浄が、0℃~50℃で0.5~6時間の間実施され、
スラリー洗浄用溶媒bが、アトロピン硫酸塩1グラムあたり5~20mlのスラリー洗浄用溶媒bが加えられる量で使用され、スラリー洗浄用溶媒bを用いるスラリー洗浄が、0℃~50℃で0.5~6時間の間実施され、
スラリー洗浄用溶媒cが、アトロピン硫酸塩1グラムあたり3~30mlのスラリー洗浄用溶媒cが加えられる量で使用され、スラリー洗浄用溶媒cを用いるスラリー洗浄が、0.5~6時間の間実施される、請求項1に記載の方法。 - アトロピン硫酸塩を精製するための方法であって、
有効医薬成分であるアトロピン硫酸塩に、スラリー洗浄用溶媒a、スラリー洗浄用溶媒b及びスラリー洗浄用溶媒cをこの順番にて用い、スラリー洗浄を実施するステップを含み、
スラリー洗浄用溶媒aが無水アセトンであり、
スラリー洗浄用溶媒bが、水の体積が5%を占めるアセトン-水混合溶媒であり、
スラリー洗浄用溶媒cがアセトンである、方法。 - スラリー洗浄の前に、有効医薬成分であるアトロピン硫酸塩を微粉砕するステップをさらに含む、請求項3に記載の方法。
- スラリー洗浄用溶媒aが、アトロピン硫酸塩1グラムあたり3~30mlのスラリー洗浄用溶媒aが加えられる量で使用され、スラリー洗浄用溶媒aを用いるスラリー洗浄が、0℃~50℃で0.5~6時間の間実施され、
スラリー洗浄用溶媒bが、アトロピン硫酸塩1グラムあたり5~20mlのスラリー洗浄用溶媒bが加えられる量で使用され、スラリー洗浄用溶媒bを用いるスラリー洗浄が、0℃~50℃で0.5~6時間の間実施され、
スラリー洗浄用溶媒cが、アトロピン硫酸塩1グラムあたり3~30mlのスラリー洗浄用溶媒cが加えられる量で使用され、スラリー洗浄用溶媒cを用いるスラリー洗浄が、0.5~6時間の間実施される、請求項3に記載の方法。 - 請求項3~5のいずれか一項に記載の方法によって調製されるアトロピン硫酸塩を含むアトロピン硫酸塩製剤であって、
アトロピン硫酸塩製剤の重量組成が、以下:
アトロピン硫酸塩 0.001%~0.1%
増粘剤 0.1%~10%
錯化剤 0.001%~0.05%
pH調整剤 アトロピン硫酸塩製剤のpHを3.5~6.5に調整する量
及び、水 残部
のとおりであり、
任意選択で、アトロピン硫酸塩製剤が、0.001%~0.05%の静菌剤をさらに含み、
任意選択で、アトロピン硫酸塩製剤が、0.1%~2%の浸透圧調節剤をさらに含む、アトロピン硫酸塩製剤。 - 増粘剤が、セルロース誘導体、架橋ポリビニルアルコールピロリドン、ヒアルロン酸ナトリウム、ポリビニルピロリドン、ポリビニルアルコール、ポリエチレングリコール、及びそれらのいずれかの組合せからなる群から選択され、
錯化剤が、エデト酸、エデト酸二ナトリウム及びエデト酸カルシウムナトリウムからなる群から選択され、
pH調整剤が、炭酸緩衝系、ホスフェート緩衝系、クエン酸緩衝系、酢酸緩衝系、バルビツール酸緩衝系、トリス(ヒドロキシメチル)アミノメタン緩衝系、ホウ酸、ホウ砂、水酸化ナトリウム、塩酸、クエン酸及びそれらの塩からなる群から選択される1つ又は複数である、請求項6に記載のアトロピン硫酸塩製剤。 - 処方1~4:
処方1:
アトロピン硫酸塩 0.005%~0.02%
ヒドロキシプロピルメチルセルロース 1%
エデト酸二ナトリウム 0.01%
塩化ベンザルコニウム 0.01%
リン酸二水素ナトリウム一水和物 0.25%
リン酸水素二ナトリウム 0.0025%
及び、水 残部
処方2:
アトロピン硫酸塩 0.005%~0.02%
ヒドロキシプロピルメチルセルロース 1%
ヒアルロン酸ナトリウム 2%
エデト酸二ナトリウム 0.01%
塩化ベンザルコニウム 0.01%
リン酸二水素ナトリウム一水和物 0.25%
リン酸水素二ナトリウム 0.0025%
及び、水 残部
処方3:
アトロピン硫酸塩 0.005%~0.01%
ヒドロキシプロピルメチルセルロース 1%
プロピレングリコール 0.3%
エデト酸二ナトリウム 0.01%
塩化ベンザルコニウム 0.01%
ホウ酸 1.8%
及び、水 残部
処方4:
アトロピン硫酸塩 0.005%~0.01%
ヒドロキシプロピルメチルセルロース 1%
エデト酸二ナトリウム 0.01%
ホウ酸 1.8%
及び、水 残部
から選択される、請求項6に記載のアトロピン硫酸塩製剤。 - 請求項6~8のいずれか一項に記載のアトロピン硫酸塩製剤を調製するための方法であって、
増粘剤を、60℃~90℃の水中で拡散及び膨潤させ、20℃~30℃の水を補充して溶解させて、液体aを得るステップと、
pH調整剤、錯化剤、任意選択の静菌剤、及び任意選択の浸透圧調節剤を60℃~80℃の水に個別に溶解させ、30℃未満に冷却し、アトロピン硫酸塩を加えて、溶解後に液体bを得るステップと、
液体a及び液体bを混合し、残部の水を加えて、アトロピン硫酸塩製剤を得るステップとを含み、
任意選択で、得られたアトロピン硫酸塩製剤をろ過するステップをさらに含む、方法。 - 子供又は青年の近視を含む視力欠陥の予防及び/又は治療のための医薬の製造における、請求項6~8のいずれか一項に記載のアトロピン硫酸塩製剤の使用。
- 子供又は青年の近視を含む視力欠陥の予防及び/又は治療における使用のための、請求項6~8のいずれか一項に記載のアトロピン硫酸塩製剤。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023061268A JP2023085454A (ja) | 2018-09-25 | 2023-04-05 | 低濃度アトロピン眼科用製剤の安定性を改善するための方法 |
| JP2023061269A JP2023085455A (ja) | 2018-09-25 | 2023-04-05 | 低濃度アトロピン眼科用製剤の安定性を改善するための方法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201811112830.8 | 2018-09-25 | ||
| CN201811112830.8A CN110934816B (zh) | 2018-09-25 | 2018-09-25 | 一种提高低浓度阿托品眼用制剂稳定性的方法 |
| PCT/CN2019/105010 WO2020063320A1 (zh) | 2018-09-25 | 2019-09-10 | 一种提高低浓度阿托品眼用制剂稳定性的方法 |
Related Child Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023061269A Division JP2023085455A (ja) | 2018-09-25 | 2023-04-05 | 低濃度アトロピン眼科用製剤の安定性を改善するための方法 |
| JP2023061268A Division JP2023085454A (ja) | 2018-09-25 | 2023-04-05 | 低濃度アトロピン眼科用製剤の安定性を改善するための方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022501437A JP2022501437A (ja) | 2022-01-06 |
| JP7340139B2 true JP7340139B2 (ja) | 2023-09-07 |
Family
ID=69905278
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021540354A Active JP7340139B2 (ja) | 2018-09-25 | 2019-09-10 | 低濃度アトロピン眼科用製剤の安定性を改善するための方法 |
| JP2023061269A Pending JP2023085455A (ja) | 2018-09-25 | 2023-04-05 | 低濃度アトロピン眼科用製剤の安定性を改善するための方法 |
| JP2023061268A Pending JP2023085454A (ja) | 2018-09-25 | 2023-04-05 | 低濃度アトロピン眼科用製剤の安定性を改善するための方法 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023061269A Pending JP2023085455A (ja) | 2018-09-25 | 2023-04-05 | 低濃度アトロピン眼科用製剤の安定性を改善するための方法 |
| JP2023061268A Pending JP2023085454A (ja) | 2018-09-25 | 2023-04-05 | 低濃度アトロピン眼科用製剤の安定性を改善するための方法 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US20210393609A1 (ja) |
| JP (3) | JP7340139B2 (ja) |
| CN (3) | CN114533652A (ja) |
| WO (1) | WO2020063320A1 (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN111821259A (zh) * | 2020-07-14 | 2020-10-27 | 艾尔健康眼药(辽宁)有限公司 | 一种眼用药物组合物 |
| CN112321729A (zh) * | 2020-12-03 | 2021-02-05 | 安徽森淼实业有限公司 | 一种羟丙基甲基纤维素的制备方法 |
| CN114668762B (zh) * | 2020-12-24 | 2024-04-16 | 江苏恒瑞医药股份有限公司 | 一种药物组合物 |
| CN117295491A (zh) * | 2021-09-13 | 2023-12-26 | 安徽欧普视方医药科技有限公司 | 阿托品滴眼液及其制备方法 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017522292A (ja) | 2014-06-24 | 2017-08-10 | シドネキシス,インク. | 眼科用組成物 |
| JP2018021007A (ja) | 2016-05-25 | 2018-02-08 | シンガポール ヘルス サービシーズ ピーティーイー リミテッド | アトロピン含有水性組成物 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SU417422A1 (ja) * | 1971-07-23 | 1974-02-28 | ||
| CN102813651B (zh) * | 2011-06-07 | 2015-02-11 | 成都国为医药科技有限公司 | 一种含埃索美拉唑钠的药物组合物及其制备方法 |
| WO2014102829A1 (en) * | 2012-12-31 | 2014-07-03 | Mylan Laboratories Ltd. | Crystalline atropine sulfate |
| CN103816126B (zh) * | 2014-03-24 | 2015-09-30 | 海南双成药业股份有限公司 | 一种含有丁溴东莨菪碱的药物组合物 |
| CN104069064A (zh) * | 2014-06-23 | 2014-10-01 | 天津金耀集团有限公司 | 盐酸消旋山莨菪碱注射液组合物 |
| WO2016172712A2 (en) * | 2015-04-23 | 2016-10-27 | Sydnexis, Inc. | Ophthalmic composition |
| WO2016016692A1 (en) * | 2014-08-01 | 2016-02-04 | Rouver Investment S.À.R.L | Process for preparation of atropine |
| JP7120018B2 (ja) * | 2016-10-07 | 2022-08-17 | ライオン株式会社 | 眼科用製品及び粘度低下抑制方法 |
| CN106855535A (zh) * | 2016-12-29 | 2017-06-16 | 北京中医药大学 | 一种山莨菪碱及其对映体的分离方法 |
| CN107456440A (zh) * | 2017-08-07 | 2017-12-12 | 杭州赫尔斯科技有限公司 | 一种低浓度阿托品类药物滴眼液及其制备方法 |
| CN107982212A (zh) * | 2017-11-28 | 2018-05-04 | 杭州赫尔斯科技有限公司 | 一种阿托品类药物缓释滴眼液及其制备方法 |
-
2018
- 2018-09-25 CN CN202210227935.8A patent/CN114533652A/zh active Pending
- 2018-09-25 CN CN201811112830.8A patent/CN110934816B/zh active Active
- 2018-09-25 CN CN202210229677.7A patent/CN114557955A/zh active Pending
-
2019
- 2019-09-10 JP JP2021540354A patent/JP7340139B2/ja active Active
- 2019-09-10 WO PCT/CN2019/105010 patent/WO2020063320A1/zh active Application Filing
- 2019-09-10 US US17/279,554 patent/US20210393609A1/en active Pending
-
2023
- 2023-04-05 JP JP2023061269A patent/JP2023085455A/ja active Pending
- 2023-04-05 JP JP2023061268A patent/JP2023085454A/ja active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2017522292A (ja) | 2014-06-24 | 2017-08-10 | シドネキシス,インク. | 眼科用組成物 |
| JP2018021007A (ja) | 2016-05-25 | 2018-02-08 | シンガポール ヘルス サービシーズ ピーティーイー リミテッド | アトロピン含有水性組成物 |
Non-Patent Citations (1)
| Title |
|---|
| IN 201611015904 A,2016年 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN114557955A (zh) | 2022-05-31 |
| JP2023085455A (ja) | 2023-06-20 |
| CN110934816A (zh) | 2020-03-31 |
| US20210393609A1 (en) | 2021-12-23 |
| CN114533652A (zh) | 2022-05-27 |
| CN110934816B (zh) | 2022-04-08 |
| JP2022501437A (ja) | 2022-01-06 |
| WO2020063320A1 (zh) | 2020-04-02 |
| JP2023085454A (ja) | 2023-06-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7340139B2 (ja) | 低濃度アトロピン眼科用製剤の安定性を改善するための方法 | |
| AU2007338210B2 (en) | Gel useful for the delivery of ophthalmic drugs | |
| US20070110812A1 (en) | Ophthalmic composition for dry eye therapy | |
| CN117205209A (zh) | 含有阿托品的水性组合物 | |
| JP7141420B2 (ja) | 眼疾患を処置するためのオキシメタゾリン組成物および方法 | |
| EP2612671B1 (en) | A clinical preparation of scutellarin and the preparation method thereof | |
| CN103553996B (zh) | 抗胆碱药物组合物 | |
| CN102784382A (zh) | 一种阿加曲班药物组合物及其制备方法和应用 | |
| CN106963730A (zh) | 高度稳定的奈帕芬胺眼用药物组合物 | |
| CN110693861A (zh) | 一种硫酸特布他林雾化吸入用溶液制剂及其制备方法 | |
| TW202233170A (zh) | 藥物中的降解化合物 | |
| CN102716074A (zh) | 一种贝美前列素滴眼剂及其制备方法 | |
| CN114668762B (zh) | 一种药物组合物 | |
| CN112156067A (zh) | 一种含有米力农的药物组合物及其制备方法 | |
| KR100894385B1 (ko) | 녹내장을 치료하기 위한 망막보호제로서의 비여성화에스트로겐의 용도 | |
| CN117205150A (zh) | 硫酸阿托品注射液及其作为m胆碱受体阻滞剂的用途 | |
| WO2023185852A1 (zh) | 一种环状内酰胺类化合物的注射用药物组合物及其制备方法 | |
| CN113230206A (zh) | 一种甲硫酸新斯的明组合物及其制备方法 | |
| CN116687842A (zh) | 一种拉坦前列素滴眼液及其制备方法 | |
| CN117957002A (zh) | 一种药物组合物及其制备方法和应用 | |
| CN115531307A (zh) | 氟维司群混悬液及其制备方法和应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210517 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220531 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220824 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20221206 |
|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20230322 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230405 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20230405 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20230413 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20230418 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230725 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230802 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7340139 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |