JP7305548B2 - ペルオキシソーム増殖剤応答性受容体活性化剤 - Google Patents
ペルオキシソーム増殖剤応答性受容体活性化剤 Download PDFInfo
- Publication number
- JP7305548B2 JP7305548B2 JP2019554256A JP2019554256A JP7305548B2 JP 7305548 B2 JP7305548 B2 JP 7305548B2 JP 2019554256 A JP2019554256 A JP 2019554256A JP 2019554256 A JP2019554256 A JP 2019554256A JP 7305548 B2 JP7305548 B2 JP 7305548B2
- Authority
- JP
- Japan
- Prior art keywords
- thio
- cyanophenyl
- benzo
- group
- acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/428—Thiazoles condensed with carbocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/275—Nitriles; Isonitriles
- A61K31/277—Nitriles; Isonitriles having a ring, e.g. verapamil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/02—Drugs for disorders of the urinary system of urine or of the urinary tract, e.g. urine acidifiers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/04—Drugs for disorders of the urinary system for urolithiasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/10—Anti-acne agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/14—Drugs for dermatological disorders for baldness or alopecia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/38—Drugs for disorders of the endocrine system of the suprarenal hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/48—Drugs for disorders of the endocrine system of the pancreatic hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/02—Antithrombotic agents; Anticoagulants; Platelet aggregation inhibitors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
Description
本願は、2017年11月15日に日本に出願された、特願2017-220362号及び2018年7月12日に日本に出願された、特願2018-132701に基づき優先権主張し、その内容をここに援用する。
イッセマン(Isseman)らによりこのペルオキシソーム増殖剤によって活性化される核内受容体が同定され、ペルオキシソーム増殖剤応答性受容体(peroxisome proliferator activated receptor:以下、PPAR)と命名された(非特許文献1)。
PPARはこれまでPPARα、PPARγ及びPPARδの3種のサブ・タイプの存在が確認されている(非特許文献2)。このうちPPARαは、腎臓、肝臓、心臓及び骨格筋など脂肪酸を多量に消費する臓器に高度に発現していることが報告されている(非特許文献3)。
上述したフィブラート系薬剤は、このPPARαに対しリガンド効果を有し、強い血清TG(トリグリセリド)の低下作用を有するため、高脂血症治療薬として用いられている。
フィブラート系薬剤としては、例えば次式、
次式、
次式、
またPPARαには、高脂血症以外にも例えば動脈硬化や肥満、糖尿病、メタボリック・シンドローム、心不全、慢性腎臓病等に関連することが報告されており(非特許文献4)、これらの疾患治療/予防薬として期待される。また、これらの疾患には酸性尿を伴う場合が多く、尿路結石、特に尿酸結石のリスクを上昇させることが知られているが(非特許文献5、非特許文献6)、フィブラート系薬剤には酸性尿の改善効果があることも報告されている(非特許文献7)。
ところで本発明者らは、次式で示される誘導体が尿酸トランスポーターURAT1を介する尿酸の再吸収を阻害し、痛風又は高尿酸血症の予防及び治療剤として有用であることを見出し、特許出願している(特許文献4)。
QはCR8、NR9又はNを表し、
QがCR8の場合、R3とR8とが結合し、点線からなる環と一緒になって、ナフタレン環、若しくはキノリン環を形成するか、
又は、R1とR2、R2とR8及びR3とR8から選択される何れか1つの組み合わせで結合し、これらが結合している2個の炭素原子と一緒になって、窒素原子、酸素原子及び硫黄原子から選択される1~3個のヘテロ原子を環構成元素として含有する5員環のヘテロアリール環を形成し、さらに該ヘテロアリール環は点線からなる環とで縮合環を形成し、
ここで、点線からなる環は、環内の2重結合の数が最大となる環であり、
QがNの場合、R1とR2が結合し、点線からなる環と一緒になってキノリン環を形成し、
QがNR9の場合、R3とR9又はR2とR9が結合し、点線からなる環と一緒になって、イミダゾ[1,2-a]ピリジン環を形成し、
R1、R2,R3及びR8は、環を構成しない場合は、同一又は異なっていても良く、水素原子、ハロゲン原子、炭素数1~8のアルキル基、3~7員環のシクロアルキル基、炭素数1~8のアルコキシ基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、1~3個のハロゲン原子で置換された炭素数1~8のアルコキシ基、炭素数2~8のアルケニル基、炭素数2~8のアルキニル基、炭素数1~8のアルキルアミノ基、炭素数2~12のジアルキルアミノ基、アルキル基の炭素数が1~8であるアルキルオキシカルボニル基、ヒドロキシ基、アミノ基、カルボキシル基、ニトロ基、シアノ基、CONR’R’’、SR’、又はSO2NR’R’’を表し、
ここで、R’及びR’’は、同一又は異なっていても良く、水素原子又は炭素数1~8のアルキル基であり、
R1、R2,R3及びR8が環を構成する場合は、該環は1~4個の同一又は異なっても良い、前記の環を構成しない場合のR1と同じ置換基を有していても良く、
Aは1~5個の同一又は異なっていても良い前記の環を構成しない場合のR1と同じ置換基を有していても良いフェニル基、ナフチル基、ピリジル基、ピリミジル基、ピラジル基、ピリダジル基、キノリル基又はイソキノリル基を表し、
ここで、Aは環を構成する炭素原子を介して点線からなる環と結合し、
Xは、NR11、酸素原子又は硫黄原子を表し、
ここで、R11は、水素原子、炭素数1~8のアルキル基又は1~3個のハロゲン原子で置換された炭素数1~8のアルキル基を表し、
Yは、炭素数1~8のアルキレン鎖を表し、
ここで、該アルキレン鎖は、1~4個の同一又は異なる炭素数1~8のアルキル基、炭素数1~8のアルコキシ基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、1~3個のハロゲン原子で置換された炭素数1~8のアルコキシ基、3~7員環のシクロアルキル基又は環構成元素として酸素原子、硫黄原子及び窒素原子から選択される1~2個のヘテロ原子を含む4~7員環の飽和ヘテロ環で置換されていても良く、また該アルキレン鎖は、直鎖アルキレン鎖であっても分枝鎖アルキレン鎖であってもよく、分枝鎖アルキレン鎖は、同一又は異なる炭素原子に結合する側鎖が、これらが結合している炭素原子と一緒になって3~7員環を形成しても良く、さらに該アルキレン鎖が炭素数2~8のアルキレン鎖の場合、途中で2重結合を有していても良く、
Zは、CO2H,CON(R12)(R13),CO2(R14),SO2N(R15)(R16)又はテトラゾリル基を表す。
ここで、R12、R14、及びR15は水素原子、炭素数1~8のアルキル基又は1~3個のハロゲン原子で置換された炭素数1~8のアルキル基を表し、
R13及びR16は水素原子、炭素数1~8のアルキル基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、置換基を有していても良いフェニル基、置換基を有していても良いピリジル基、ピリダジル基、ピリミジル基、若しくはピラジル基又は置換基を有していても良い窒素原子、酸素原子及び硫黄原子から選択される1~3個のヘテロ原子を環構成元素として含有する5員環のヘテロアリール環を表す。
但し、R3とR8とが結合し、点線からなる環と一緒になってナフタレン環を形成し、Xが酸素原子で、Aがナフタレンで、Aの1位で点線からなる環と結合する場合、Aの2位は、炭素数1~8のアルコキシ基又はヒドロキシ基でなく、更にまた3-[[1-(2-フルオロフェニル)ナフタレン-2-イル]チオ]プロパン酸エチルでない。)
しかしながら、前記特許文献には、明確にこれらの化合物がペルオキシソーム増殖剤応答性受容体の活性作用を有する旨の記載はない。また、URAT1阻害等を機序とする尿酸排泄促進薬は尿中への尿酸の排泄を促進するため尿酸結石のリスクを有するが、酸性尿ではリスクがさらに高まることが懸念される。
(1)次の一般式、
R1、R2、R3及びR8が環を構成する場合は、R1とR2、R2とR8及びR3とR8から選択される何れか1つの組み合わせで結合し、これらが結合している2個の炭素原子と一緒になって、ベンゼン環、ピリジン環又は窒素原子、酸素原子及び硫黄原子から選択される1~3個のヘテロ原子を環構成元素として含有する5員環のヘテロアリール環を形成し、
ここで、かかるベンゼン環、ピリジン環及びヘテロアリール環は、無置換又は1~4個の同一又は異なるハロゲン原子、炭素数1~8のアルキル基、炭素数1~8のアルコキシ基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、1~3個のハロゲン原子で置換された炭素数1~8のアルコキシ基、ヒドロキシ基、アミノ基、カルボキシル基、メルカプト基、炭素数1~8のアルキルスルファニル基、ニトロ基又はシアノ基から選択される置換基を有していても良く、
R4及びR5は、R4及びR5が結合している2個の炭素原子と一緒になってベンゼン環を形成するか、又は前述したR1と同じものを表し、
ここで、かかるベンゼン環は、無置換又は1~4個の同一又は異なるハロゲン原子、炭素数1~8のアルキル基、炭素数1~8のアルコキシ基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、1~3個のハロゲン原子で置換された炭素数1~8のアルコキシ基、ヒドロキシ基、アミノ基、カルボキシル基、メルカプト基、炭素数1~8のアルキルスルファニル基、ニトロ基又はシアノ基から選択される置換基を有していても良く、
Wは、CR9又はNを表し、
ここで、R9は前述したR1と同じものを表し、
Xは、NR10、酸素原子又は硫黄原子を表し、
ここで、R10は、水素原子、炭素数1~8のアルキル基又は1~3個のハロゲン原子で置換された炭素数1~8のアルキル基を表し、
Yは、炭素数1~8のアルキレン鎖又は炭素数2~6のアルケニレン鎖を表し、
ここで、該アルキレン鎖及びアルケニレン鎖は、無置換又は1~4個の炭素数1~8のアルキル基、炭素数1~8のアルコキシ基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、1~3個のハロゲン原子で置換された炭素数1~8のアルコキシ基で置換されていても良く、また該アルキレン鎖は、直鎖アルキレン鎖であっても分枝鎖アルキレン鎖であってもよく、分枝鎖アルキレン鎖は、同一又は異なる炭素原子に結合する側鎖が、これらが結合している炭素原子と一緒になって3~7員環を形成しても良く、さらに該アルキレン鎖が炭素数2~8のアルキレン鎖の場合、途中で2重結合を有していても良く、
Zは、CO2H、CO2R11、テトラゾリル基又はSO2NR12R13を表し
ここで、R11は炭素数1~8のアルキル基を表し、R12及びR13は同一又は異なっていても良く水素原子、炭素数1~8のアルキル基又は1~3個のハロゲン原子で置換された炭素数1~8のアルキル基を表す。
但し、R3及びR8が、R3及びR8が結合している2個の炭素原子と一緒になってベンゼン環を形成し、Xが酸素原子で、R4及びR5が、R4及びR5が結合している2個の炭素原子と一緒になってベンゼン環を形成する場合、R7は炭素数1~8のアルコキシ基又はヒドロキシ基でない。)で表される化合物、該化合物の互変異性体、立体異性体、若しくはその薬学的に許容される塩又はそれらの溶媒和物を含有するペルオキシソーム増殖剤活性化受容体αの活性化剤。
(2)R3及びR8が、R3及びR8が結合している2個の炭素原子と一緒になって、ベンゼン環又はピリジン環を形成する前記化合物、該化合物の互変異性体、立体異性体、若しくはその薬学的に許容される塩又はそれらの溶媒和物を含有する前記(1)記載のペルオキシソーム増殖剤活性化受容体αの活性化剤。
(3)R3及びR8が、R3及びR8が結合している2個の炭素原子と一緒になって、窒素原子、酸素原子及び硫黄原子から選択される2個のヘテロ原子を環構成元素として含有する5員環のヘテロアリール環を形成する前記化合物、該化合物の互変異性体、立体異性体、若しくはその薬学的に許容される塩又はそれらの溶媒和物を含有する前記(1)記載のペルオキシソーム増殖剤活性化受容体αの活性化剤。
(4)R3及びR8が、R3及びR8が結合している2個の炭素原子と一緒になって、チアゾール又はイソチアゾールを形成する前記化合物、該化合物の互変異性体、立体異性体、若しくはその薬学的に許容される塩又はそれらの溶媒和物を含有する前記(1)又は(3)記載のペルオキシソーム増殖剤活性化受容体αの活性化剤。
(5)R1、R2、R6、及びR7が、同一又は異なっていても良く、水素原子、ハロゲン原子、炭素数1~8のアルキル基、炭素数1~8のアルコキシ基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、1~3個のハロゲン原子で置換された炭素数1~8のアルコキシ基又はシアノ基である前記化合物、該化合物の互変異性体、立体異性体、若しくはその薬学的に許容される塩又はそれらの溶媒和物を含有する前記(1)~(4)記載のペルオキシソーム増殖剤活性化受容体αの活性化剤。
(6)R6がハロゲン原子、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、シアノ基である前記化合物、該化合物の互変異性体、立体異性体、若しくはその薬学的に許容される塩又はそれらの溶媒和物を含有する前記(1)~(5)記載のペルオキシソーム増殖剤活性化受容体αの活性化剤。
(7)Wが、CHである前記化合物、該化合物の互変異性体、立体異性体、若しくはその薬学的に許容される塩又はそれらの溶媒和物含有する前記(1)~(6)記載のペルオキシソーム増殖剤活性化受容体αの活性化剤。
(8)Xが、酸素原子又は硫黄原子である前記化合物、該化合物の互変異性体、立体異性体、若しくはその薬学的に許容される塩又はそれらの溶媒和物を含有する前記(1)~(7)記載のペルオキシソーム増殖剤活性化受容体αの活性化剤。
(9)Yが、次の一般式(II)、
で表される前記化合物、該化合物の互変異性体、立体異性体、若しくはその薬学的に許容される塩又はそれらの溶媒和物を含有する前記(1)~(8)記載のペルオキシソーム増殖剤活性化受容体αの活性化剤。
(10)ZがCO2Hである前記化合物、該化合物の互変異性体、立体異性体、若しくはその薬学的に許容される塩又はそれらの溶媒和物を含有する前記(1)~(9)記載のペルオキシソーム増殖剤活性化受容体αの活性化剤。
(11)前記(1)~(10)の何れか記載の化合物又はその塩を必要とする患者に治療学的な有効量を投与することを特徴とするペルオキシソーム増殖剤活性化受容体αに媒介される疾患の治療および/または予防方法。
(12)ペルオキシソーム増殖剤活性化受容体αに媒介される疾患が、高脂血症、脂質異常症、高コレステロール血症、高TG血症、低HDL血症、高LDL血症、non-HDL血症、高VLDL血症、リポタンパク異常症、低アポリポタンパクA-I血症、アテローム動脈硬化症、動脈硬化性疾患、冠動脈性疾患、脳血管障害、末梢血管障害、メタボリック・シンドローム、シンドロームX、内臓脂肪型肥満を含む肥満、糖尿病、高血糖、インスリン抵抗性、耐糖能異常、高インスリン血症、糖尿病性合併症、心不全、心筋梗塞、心筋症、高血圧、慢性腎臓病、脂肪肝、非アルコール性脂肪肝炎、血栓、アルツハイマー病、神経変性疾患、脱髄性疾患、多発性硬化症、副腎白質ジストロフィー、皮膚炎、乾癬、にきび、皮膚老化、発毛異常、炎症、関節炎、喘息、過敏性腸症候群、潰瘍性大腸炎、クローン病、膵炎並びに結腸癌、大腸癌、皮膚癌、乳癌、前立腺癌、卵巣癌及び肺がんを含む癌であることを特徴とする前記(11)記載の治療および/または予防方法。
(13)ペルオキシソーム増殖剤活性化受容体αに媒介される疾患が種々の脂質異常症、メタボリック・シンドローム、内臓脂肪型肥満を含む肥満、アテローム動脈硬化症およびその関連疾患又は糖尿病であることを特徴とする前記(11)又は(12)に記載の治療および/または予防方法。
(14)ペルオキシソーム増殖剤活性化受容体αに媒介される疾患の治療および/または予防のための前記(1)~(10)の何れか記載の化合物又はその塩の使用。
(15)ペルオキシソーム増殖剤活性化受容体αに媒介される疾患が高脂血症、脂質異常症、高コレステロール血症、高TG血症、低HDL血症、高LDL血症、non-HDL血症、高VLDL血症、リポタンパク異常症、低アポリポタンパクA-I血症、アテローム動脈硬化症、動脈硬化性疾患、冠動脈性疾患、脳血管障害、末梢血管障害、メタボリック・シンドローム、シンドロームX、内臓脂肪型肥満を含む肥満、糖尿病、高血糖、インスリン抵抗性、耐糖能異常、高インスリン血症、糖尿病性合併症、心不全、心筋梗塞、心筋症、高血圧、慢性腎臓病、脂肪肝、非アルコール性脂肪肝炎、血栓、アルツハイマー病、神経変性疾患、脱髄性疾患、多発性硬化症、副腎白質ジストロフィー、皮膚炎、乾癬、にきび、皮膚老化、発毛異常、炎症、関節炎、喘息、過敏性腸症候群、潰瘍性大腸炎、クローン病、膵炎並びに結腸癌、大腸癌、皮膚癌、乳癌、前立腺癌、卵巣癌及び肺がんを含む癌である前記(14)記載の使用。
(16)PPARに媒介される疾患が種々の脂質異常症、メタボリック・シンドローム、内臓脂肪型肥満を含む肥満、アテローム動脈硬化症およびその関連疾患又は糖尿病である前記(14)又は(15)記載の使用。
(17)ペルオキシソーム増殖剤活性化受容体αに媒介される疾患に伴う酸性尿を改善するために前記(1)~(10)記載の化合物又はその塩の有効量を投与することを特徴とする酸性尿の改善方法。
(18)ペルオキシソーム増殖剤活性化受容体αに媒介される疾患に伴う酸性尿を改善するための前記(1)~(10)記載の化合物又はその塩の使用。
(19)尿路結石、尿酸結石を治療および/または予防するための前記(17)記載の方法。
(20)尿路結石、尿酸結石を治療および/または予防するための前記(18)記載の使用。
(21)尿路結石、尿酸結石による腎障害を治療および/または予防するための前記(17)または(19)記載の方法。
(22)尿路結石、尿酸結石による腎障害を治療および/または予防するための前記(18)または(20)記載の使用。
本明細書において、R1~R13、Ra及びRbで表される炭素数1~8のアルキル基としては、メチル基、エチル基、プロピル基、iso-プロピル基、ブチル基、iso-ブチル基、tert-ブチル基、ペンチル基又はヘキシル基等が挙げられ、好ましくは炭素数1~3のメチル基、エチル基、プロピル基等が挙げられる。
R1及びR13で表される1~3個のハロゲン原子で置換された炭素数1~8のアルキル基としては、1~3個のフッ素原子、塩素原子若しくは臭素原子等のハロゲン原子により置換された前記アルキル基が挙げられ、好ましくはトリフルオロメチル基、クロロメチル基、2-クロロエチル基、2-ブロモエチル基又は2-フルオロエチル基等が挙げられ、より好ましくはトリフルオロメチル基が挙げられる。
R1~R9で表される炭素数1~8のアルコキシ基としては、メトキシ基、エトキシ基、プロポキシ基、イソプロポキシ基、ブトキシ基、iso-ブトキシ基、tert-ブトキシ基、ペンチルオキシ基又はヘキシルオキシ基等が挙げられ、好ましくはメトキシ基、エトキシ基、プロポキシ基、ブトキシ基等が挙げられる。
R1~R9で表される1~3個のハロゲン原子で置換された炭素数1~8のアルコキシ基としては、1~3個のフッ素原子、塩素原子若しくは臭素原子等のハロゲン原子により置換されたメトキシ基、エトキシ基、プロポキシ基、iso-プロポキシ基、ブトキシ基又はtert-ブトキシ基等が挙げられ、好ましくはトリフルオロメトキシ基、クロロメトキシ基、2-クロロエトキシ基、2-ブロモエトキシ基又は2-フルオロエトキシ基等が挙げられる。
R1~R9で表されるアルキルスルファニル基としては、炭素数1~8の直鎖又は分岐鎖のものが挙げられ、例えばメチルスルファニル基、エチルスルファニル基、プロピルスルファニル基、ブチルスルファニル基、iso-ブチルスルファニル基、tert-ブチルスルファニル基等が挙げられ、好ましくはメチルスルファニル基、エチルスルファニル基が挙げられる。
R1~R9で表されるハロゲン原子としては、フッ素原子、塩素原子、臭素原子又はヨウ素原子が挙げられ、好ましくはフッ素原子、塩素原子である。
R1、R2,R3及びR8が環を構成する場合において、R3とR8の組み合わせで結合することが好ましい。かかる場合、R3及びR8が結合している2個の炭素原子と一緒になって窒素原子、酸素原子及び硫黄原子から選択される1~3個のヘテロ原子を環構成元素として含有する5員環のヘテロアリール環を形成する場合のヘテロアリール環としては、チアゾール、イソチアゾール、オキサゾール、イソオキサゾール、2,1,3-チアジアゾール等が挙げられ、好ましくはチアゾール、イソチアゾールが挙げられる。
R1、R2,R3及びR8が環を構成する場合において、前記ベンゼン環、ピリジン環及びヘテロアリール環の環上の置換基としては、1~4個の同一又は異なるハロゲン原子、炭素数1~8のアルキル基、炭素数1~8のアルコキシ基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、1~3個のハロゲン原子で置換された炭素数1~8のアルコキシ基、ヒドロキシ基、アミノ基、カルボキシル基、メルカプト基、炭素数1~8のアルキルスルファニル基、ニトロ基又はシアノ基が挙げられ、好ましくはハロゲン原子、炭素数1~8のアルキル基、炭素数1~8のアルコキシ基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、ヒドロキシ基、アミノ基、カルボキシル基、メルカプト基、ニトロ基又はシアノ基が挙げられ、より好ましくは炭素数1~8のアルキル基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基等が挙げられる。
R4及びR5が結合している2個の炭素原子と一緒になって形成してもよいベンゼン環の環上の置換基としては、1~4個の同一又は異なるハロゲン原子、炭素数1~8のアルキル基、炭素数1~8のアルコキシ基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、1~3個のハロゲン原子で置換された炭素数1~8のアルコキシ基、ヒドロキシ基、アミノ基、カルボキシル基、メルカプト基、炭素数1~8のアルキルスルファニル基、ニトロ基又はシアノ基が挙げられ、好ましくはハロゲン原子、炭素数1~8のアルキル基、炭素数1~8のアルコキシ基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、ヒドロキシ基、アミノ基、カルボキシル基、メルカプト基、ニトロ基又はシアノ基が挙げられ、より好ましくはハロゲン原子、炭素数1~8のアルキル基、ヒドロキシ基が挙げられる。
Ra及びRbが結合し、これらが結合している炭素原子と一緒になって表される3~7員環のシクロアルカンとしては、シクロプロパン環、シクロブタン環、シクロペンタン環、シクロヘキサン環等が挙げられ、好ましくはシクロブタン環、シクロペンタン環が挙げられる。
Yで表されるアルキレン鎖としては、メチレン、エチレン、プロピレン、ブチレン、iso-ブチレン等の炭素数1~8の直鎖又は分岐鎖のものが挙げられ、好ましくはメチレン、エチレン、プロピレンが挙げられる。
Yで表されるアルケニレン鎖としては、1~3個の二重結合を有する炭素原子数2~6の直鎖又は分岐鎖のものを意味し、例えば、ビニレン、アリレン、1-プロペニレン、イソプロペニレン、1-、2-または3-ブテニレン、1,3-ブタジエニレン等が挙げられ、好ましくはビニレン、アリレンが挙げられる。
Yで表されるアルキレン鎖及びアルケニレン鎖上の置換基としては、1~4個の炭素数1~8のアルキル基、炭素数1~8のアルコキシ基、1~3個のハロゲン原子で置換された炭素数1~8のアルキル基、1~3個のハロゲン原子で置換された炭素数1~8のアルコキシ基が挙げられ、好ましくは炭素数1~8のアルキル基が挙げられる。
また、置換基の数としては2が好ましい。
Yで表される分枝鎖アルキレン鎖において、同一又は異なる炭素原子に結合する側鎖が、これらが結合している炭素原子と一緒になって形成しても良い3~7員環としては、シクロプロパン、シクロブタン、シクロペンタン等が挙げられる。
また化合物(I)には、シス・トランス異性体や光学活性体、ラセミ体等の立体異性体が存在する場合もあるが、何れも本発明に用いることができる。
また、化合物(I)としては、互変異性体、水和物、アルコール等の有機溶媒との溶媒和物、重水素などの安定同位体で置換された誘導体さらにはプロドラッグであっても良い。
(1) PPARαに対するアゴニスト活性の測定
PPARαに対するアゴニスト活性の測定にはEnBio RCAS for PPARα kit (PPARA-CBP、 藤倉化成株式会社) を用い、キットプロトコルに従い吸光度測定を行った。試料はジメチルスルホキシドに溶解し、評価濃度が10 μMとなるように96ウェルプレートに添加した。最大反応ウェルにはGW7647を0.5 μMとなるように添加した。バックグラウンドウェルにはジメチルスルホキシドを添加した。各試料添加ウェルの吸光度からバックグラウンドウェルの吸光度を差引いた後、最大反応ウェルに対する各試料添加ウェルの比を算出してPPARαに対するアゴニスト活性 (Binding ratio, %)を評価した。なお、各試料添加ウェル及びバックグラウンドウェルはduplicate、最大反応ウェルはquadruplicateとした。陽性対照として既知のPPARαアゴニストであるFenofibric acid (東京化成工業株式会社) 10 μMを用いた。
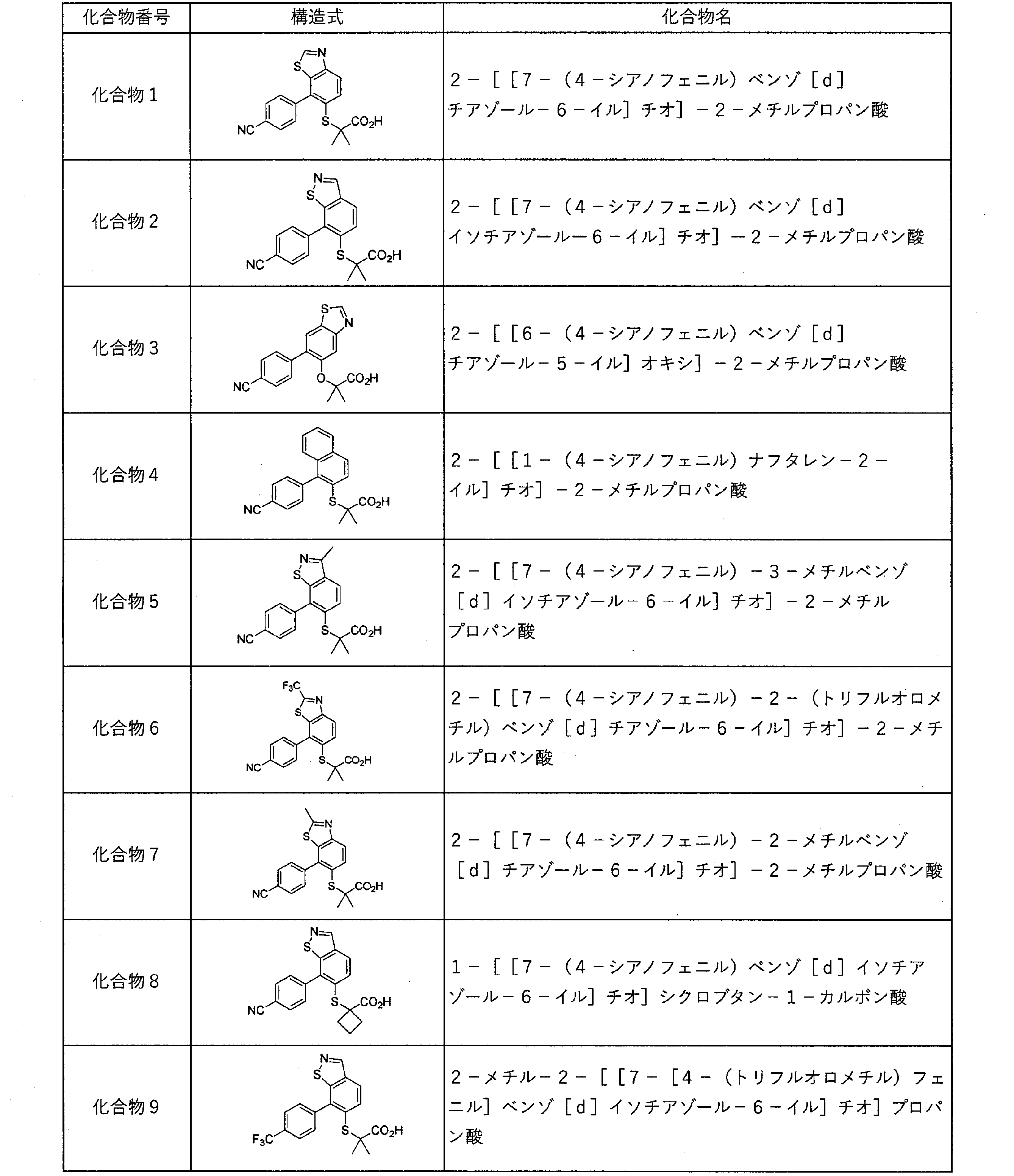
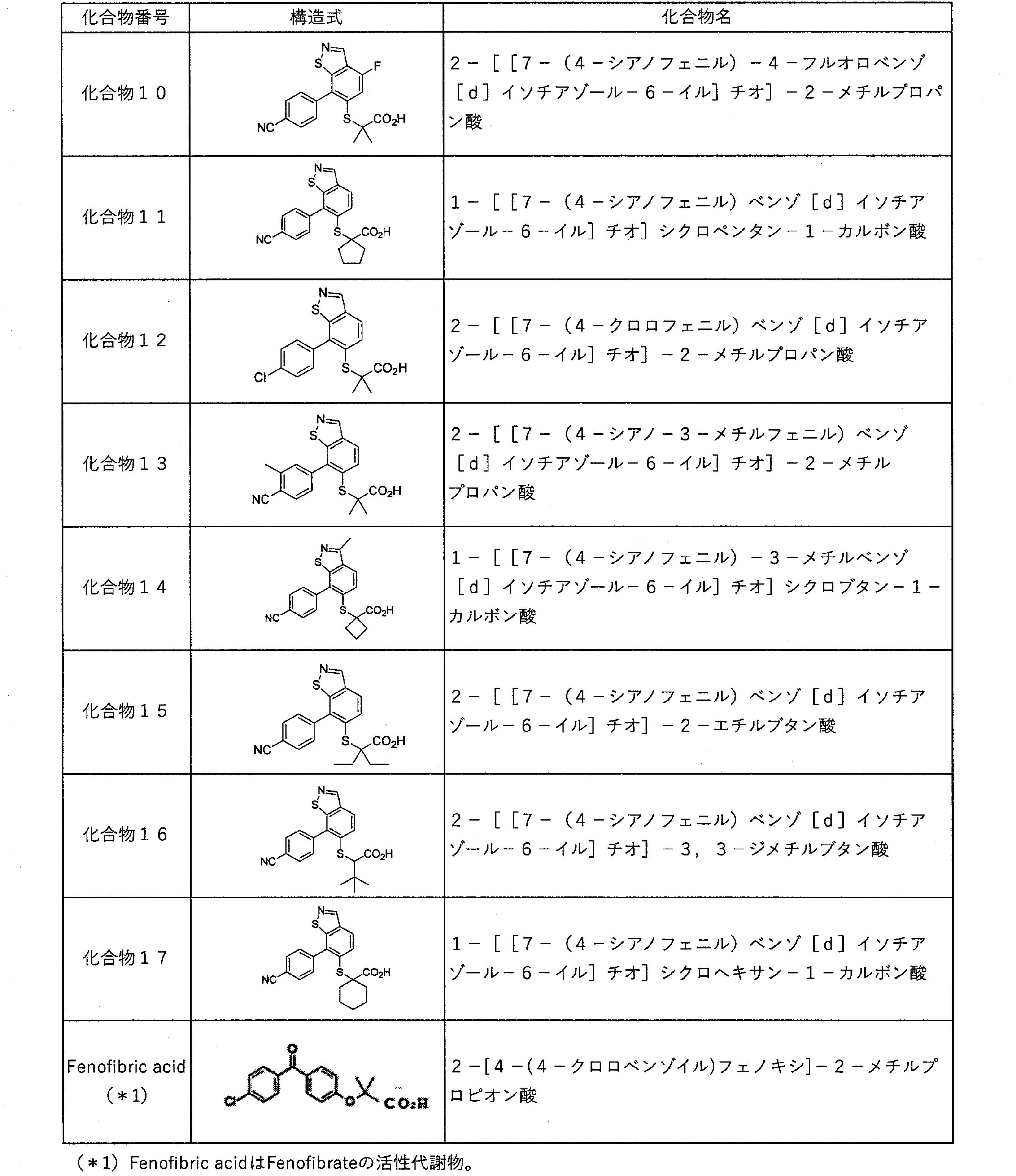
上記試験に基づき[表1-1]及び[表1-2]中の(化合物1)~(化合物17)についてPPARαに対するアゴニスト活性を評価した。
試験結果を表2に示す。
(1)メチオニン・コリン欠乏飼料誘発による非アルコール性脂肪性肝疾患(NAFLD)モデルラットを用いた評価
NAFLDモデルとして、メチオニン・コリン欠乏(MCD)飼料摂餌ラットを用い実験を行った。MCD飼料摂餌モデルはNAFLD/NASHのモデルとして汎用されている。
Wistarラット(雄性、8週齢、日本チャールス・リバー株式会社)に、MCD飼料(A02082002B, Research Diets, Inc.)を5週間摂餌させた。上記の飼料を1週間摂餌させた時点から、群間で体重に差が無いようにVehicle群、化合物2(50 mg/kg)群、及びFenofibrate(100 mg/kg)群に群分けした(各群4例)。Normal群にはMCD飼料のコントロール飼料であるMCS飼料を同期間摂餌させた(A02082003B, Research Diets, Inc.)。投与容量は10 mL/kgとし、Vehicle群及びNormal群には1% メチルセルロース溶液を、化合物2群及びFenofibrate群にはそれぞれの薬液を1日1回4週間反復経口投与した。
最終投与終了後翌日、非絶食、イソフルラン吸入麻酔下で後大静脈より採血し、血漿を分取した。さらに肝臓を採取し、一部を凍結保存した。血漿中ALTはJSCC標準化対応法で測定した。肝臓中トリグリセリド(TG)量は肝臓からクロロホルム:メタノール混液(2:1, v/v)で抽出し、蒸発乾固後2-プロパノールで溶解してトリグリセライドEテストワコーを用いて測定した。結果はそれぞれ平均値 ± 標準偏差で表した。有意差検定は、Normal群とVehicle群間ではWelchのt検定法(Unpaired)にて行い(#: p < 0.05及び ###: p < 0.001)、Vehicle群と被験物質投与群間ではDunnett法にて行った(*: p < 0.05, **: p < 0.01及び***: p < 0.001)。
試験結果を図1A及び図1Bに示す。肝障害の指標である血漿中ALTは、MCS飼料を摂餌させたNormal群と比べMCD飼料を摂餌させたVehicle群で有意に増加した。一方でVehicle群と比べ化合物2群及びFenofibrate群では有意に低値を示した(図1A)。さらに、脂肪肝の指標である肝臓中TG量もNormal群と比べVehicle群で有意に増加したが、Vehicle群と比べ化合物2群及びFenofibrate群では有意に低値を示した(図1B)。
これらの結果より本発明化合物は、MCD飼料摂餌ラットに反復経口投与することで血漿中ALT減少及び肝臓中TG量減少が認められ、NAFLD病態改善作用を有することが明らかになった。
(1)糖尿病モデルZucker diabetic fatty(ZDF)ラットを用いた評価
本実施例では、低pH尿を呈する糖尿病モデル動物ZDFラットを用いて化合物2の低pH尿改善作用の評価を行った。比較対照化合物として既知のURAT1阻害剤であるVerinuradの評価も併せて行った(VerinuradのPPARα活性化作用は試験例1記載の方法により評価した結果、評価濃度10 μMにおけるBinding ratioが3.80%であり、効果は確認されなかった)。
ZDF(Leprfa/Leprfa)ラット(雄性、投与開始時7週齢、日本チャールス・リバー株式会社)を、群間で体重に差が無いようにVehicle群、化合物2(25 mg/kg)群、化合物2(50 mg/kg)群、及びVerinurad(50 mg/kg)群に群分けした(各群5例)。Lean群としてZDF(Leprfa/Leprfa)ラットのコントロール動物であるZDF(Lean)ラットを用いた(5例)。投与容量は10 mL/kgとし、Vehicle群及びLean群には1%メチルセルロース溶液を、化合物2群及びVerinurad群にはそれぞれの薬液を1日1回15日間反復経口投与した。
投与期間中、蓄尿により得た尿試料のpHを、コンパクトpHメータ(B-712,株式会社堀場製作所)を用いて測定した。畜尿は投与開始6日前(pre)、投与初日、7日目及び14日目に行い、代謝ケージ内で24時間蓄尿した。結果はそれぞれ平均値±標準偏差で表した。有意差検定は、各時点においてLean群とVehicle群間ではStudentのt検定法(Unpaired)にて行い(###: p < 0.001)、Vehicle群と被験物質投与群間では一元配置分散分析後、Dunnett法にて行った(*: p < 0.05,**: p < 0.01及び***: p < 0.001)。
試験結果を図2に示す。Vehicle群では投与開始前から試験期間を通してLean群と比べて有意に低く、低pH尿を呈した。化合物2群ではVehicle群と比べ25 mg/kgでは投与7日目から、50 mg/kgでは投与初日から尿pHの有意な上昇がみられ、用量依存的な低pH尿改善作用を示した。一方で、Verinurad群では投与期間を通して低pH尿改善作用はみられなかった。
これらの結果より本発明化合物は、低pH尿を呈するZDFラットに経口投与することで低pH尿改善作用を有することが明らかとなった。
Claims (4)
- 2-[[7-(4-シアノフェニル)ベンゾ[d]チアゾール-6-イル]チオ]-2-メチルプロパン酸、2-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾールー6-イル]チオ]ー2-メチルプロパン酸、2-[[6-(4-シアノフェニル)ベンゾ[d]チアゾール-5-イル]オキシ]-2-メチルプロパン酸、2-[[1-(4-シアノフェニル)ナフタレン-2-イル]チオ]-2-メチルプロパン酸、2-[[7-(4-シアノフェニル)-3-メチルベンゾ[d]イソチアゾール-6-イル]チオ]-2-メチルプロパン酸、2-[[7-(4-シアノフェニル)-2-(トリフルオロメチル)ベンゾ[d]チアゾール-6-イル]チオ]-2-メチルプロパン酸、2-[[7-(4-シアノフェニル)-2-メチルベンゾ[d]チアゾール-6-イル]チオ]-2-メチルプロパン酸、1-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]シクロブタン-1-カルボン酸、2-メチル-2-[[7-[4-(トリフルオロメチル)フェニル]ベンゾ[d]イソチアゾール-6-イル]チオ]プロパン酸、2-[[7-(4-シアノフェニル)-4-フルオロベンゾ[d]イソチアゾール-6-イル]チオ]-2-メチルプロパン酸、1-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]シクロペンタン-1-カルボン酸、2-[[7-(4-クロロフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]-2-メチルプロパン酸、2-[[7-(4-シアノ-3-メチルフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]-2-メチルプロパン酸、1-[[7-(4-シアノフェニル)-3-メチルベンゾ[d]イソチアゾール-6-イル]チオ]シクロブタン-1-カルボン酸、2-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]-2-エチルブタン酸、2-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]-3,3-ジメチルブタン酸、若しくは1-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]シクロヘキサン-1-カルボン酸から選択される化合物又はその塩を有効成分として含有する、種々の脂質異常症、メタボリック・シンドローム、内臓脂肪型肥満を含む肥満、アテローム動脈硬化症およびその関連疾患又は糖尿病から選ばれるペルオキシソーム増殖剤活性化受容体αに媒介される疾患の治療剤および/または予防剤。
- 2-[[7-(4-シアノフェニル)ベンゾ[d]チアゾール-6-イル]チオ]-2-メチルプロパン酸、2-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾールー6-イル]チオ]ー2-メチルプロパン酸、2-[[6-(4-シアノフェニル)ベンゾ[d]チアゾール-5-イル]オキシ]-2-メチルプロパン酸、2-[[1-(4-シアノフェニル)ナフタレン-2-イル]チオ]-2-メチルプロパン酸、2-[[7-(4-シアノフェニル)-3-メチルベンゾ[d]イソチアゾール-6-イル]チオ]-2-メチルプロパン酸、2-[[7-(4-シアノフェニル)-2-(トリフルオロメチル)ベンゾ[d]チアゾール-6-イル]チオ]-2-メチルプロパン酸、2-[[7-(4-シアノフェニル)-2-メチルベンゾ[d]チアゾール-6-イル]チオ]-2-メチルプロパン酸、1-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]シクロブタン-1-カルボン酸、2-メチル-2-[[7-[4-(トリフルオロメチル)フェニル]ベンゾ[d]イソチアゾール-6-イル]チオ]プロパン酸、2-[[7-(4-シアノフェニル)-4-フルオロベンゾ[d]イソチアゾール-6-イル]チオ]-2-メチルプロパン酸、1-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]シクロペンタン-1-カルボン酸、2-[[7-(4-クロロフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]-2-メチルプロパン酸、2-[[7-(4-シアノ-3-メチルフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]-2-メチルプロパン酸、1-[[7-(4-シアノフェニル)-3-メチルベンゾ[d]イソチアゾール-6-イル]チオ]シクロブタン-1-カルボン酸、2-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]-2-エチルブタン酸、2-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]-3,3-ジメチルブタン酸、若しくは1-[[7-(4-シアノフェニル)ベンゾ[d]イソチアゾール-6-イル]チオ]シクロヘキサン-1-カルボン酸から選択される化合物又はその塩を有効成分として含有する、ペルオキシソーム増殖剤活性化受容体αに媒介される疾患に伴う酸性尿の改善剤。
- 尿路結石、尿酸結石を治療および/または予防するための請求項2記載の改善剤。
- 尿路結石、尿酸結石による腎障害を治療および/または予防するための請求項2または3記載の改善剤。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023105254A JP2023123704A (ja) | 2017-11-15 | 2023-06-27 | ペルオキシソーム増殖剤応答性受容体活性化剤 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017220362 | 2017-11-15 | ||
| JP2017220362 | 2017-11-15 | ||
| JP2018132701 | 2018-07-12 | ||
| JP2018132701 | 2018-07-12 | ||
| PCT/JP2018/042133 WO2019098238A1 (ja) | 2017-11-15 | 2018-11-14 | ペルオキシソーム増殖剤応答性受容体活性化剤 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023105254A Division JP2023123704A (ja) | 2017-11-15 | 2023-06-27 | ペルオキシソーム増殖剤応答性受容体活性化剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2019098238A1 JPWO2019098238A1 (ja) | 2020-11-19 |
| JP7305548B2 true JP7305548B2 (ja) | 2023-07-10 |
Family
ID=66540254
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019554256A Active JP7305548B2 (ja) | 2017-11-15 | 2018-11-14 | ペルオキシソーム増殖剤応答性受容体活性化剤 |
| JP2023105254A Pending JP2023123704A (ja) | 2017-11-15 | 2023-06-27 | ペルオキシソーム増殖剤応答性受容体活性化剤 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023105254A Pending JP2023123704A (ja) | 2017-11-15 | 2023-06-27 | ペルオキシソーム増殖剤応答性受容体活性化剤 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US11278528B2 (ja) |
| EP (1) | EP3705120A4 (ja) |
| JP (2) | JP7305548B2 (ja) |
| KR (1) | KR20200092971A (ja) |
| CN (1) | CN111343976A (ja) |
| WO (1) | WO2019098238A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115894379A (zh) * | 2022-01-20 | 2023-04-04 | 中国药科大学 | 海因类化合物及其医药用途 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013530186A (ja) | 2010-06-16 | 2013-07-25 | アルデア バイオサイエンシーズ インク. | フェニルチオ酢酸化合物、組成物、および、その使用方法 |
| WO2016108282A1 (ja) | 2014-12-29 | 2016-07-07 | 日本ケミファ株式会社 | Urat1阻害剤 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2230383C3 (de) | 1971-10-01 | 1981-12-03 | Boehringer Mannheim Gmbh, 6800 Mannheim | Phenoxyalkylcarbonsäurederivate und Verfahren zur Herstellung derselben |
| JPS5515457B2 (ja) | 1971-11-13 | 1980-04-23 | ||
| JPS5112618A (en) | 1974-07-21 | 1976-01-31 | Sanwa Kogyosho Kk | 3 sojudodendokino seidohoshiki |
| FR2408577A1 (fr) | 1977-11-14 | 1979-06-08 | Devinter Sa | Nouveau procede de synthese d'esters para chlorobenzoyl phenoxy isobutyriques |
| FR2869611B1 (fr) * | 2004-05-03 | 2006-07-28 | Merck Sante Soc Par Actions Si | Derives de l'acide hexenoique, procedes pour leur preparation, compositions pharmaceutiques les contenant et applications en therapeutique |
| CN102643248A (zh) * | 2006-04-18 | 2012-08-22 | 日本化学医药株式会社 | 过氧化物酶体增殖剂激活受体δ的激活剂 |
| JP6737639B2 (ja) | 2016-06-08 | 2020-08-12 | トヨタ自動車株式会社 | 燃料電池用セパレータの製造方法 |
| JP2018132701A (ja) | 2017-02-16 | 2018-08-23 | 株式会社オプトエレクトロニクス | 情報読取装置 |
-
2018
- 2018-11-14 CN CN201880073457.1A patent/CN111343976A/zh active Pending
- 2018-11-14 KR KR1020207015288A patent/KR20200092971A/ko not_active Application Discontinuation
- 2018-11-14 JP JP2019554256A patent/JP7305548B2/ja active Active
- 2018-11-14 WO PCT/JP2018/042133 patent/WO2019098238A1/ja unknown
- 2018-11-14 EP EP18879461.4A patent/EP3705120A4/en active Pending
- 2018-11-14 US US16/762,981 patent/US11278528B2/en active Active
-
2023
- 2023-06-27 JP JP2023105254A patent/JP2023123704A/ja active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013530186A (ja) | 2010-06-16 | 2013-07-25 | アルデア バイオサイエンシーズ インク. | フェニルチオ酢酸化合物、組成物、および、その使用方法 |
| WO2016108282A1 (ja) | 2014-12-29 | 2016-07-07 | 日本ケミファ株式会社 | Urat1阻害剤 |
Also Published As
| Publication number | Publication date |
|---|---|
| US11278528B2 (en) | 2022-03-22 |
| TW201922691A (zh) | 2019-06-16 |
| JPWO2019098238A1 (ja) | 2020-11-19 |
| US20200268719A1 (en) | 2020-08-27 |
| JP2023123704A (ja) | 2023-09-05 |
| WO2019098238A1 (ja) | 2019-05-23 |
| KR20200092971A (ko) | 2020-08-04 |
| EP3705120A1 (en) | 2020-09-09 |
| EP3705120A4 (en) | 2021-08-11 |
| CN111343976A (zh) | 2020-06-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10550149B2 (en) | PPAR agonists and methods of use thereof | |
| Agrawal et al. | Balaglitazone: a second generation peroxisome proliferator-activated receptor (PPAR) gamma (γ) agonist | |
| US11578052B2 (en) | PPAR agonists, compounds, pharmaceutical compositions, and methods of use thereof | |
| BR112019018162A2 (pt) | Composições farmacêuticas para terapia de combinação | |
| AU2018212614B2 (en) | Pharmaceutical compositions for combination therapy | |
| JP2003525217A (ja) | 肥満治療用薬剤 | |
| JP2023123704A (ja) | ペルオキシソーム増殖剤応答性受容体活性化剤 | |
| US20110092517A1 (en) | Use of PPAR Delta Ligands for the Treatment or Prevention of Inflammation or Energy Metabolism/Production Related Diseases | |
| KR20080086523A (ko) | 물질대사 장애의 치료용 화합물 | |
| US8288438B2 (en) | Methods for avoiding edema in the treatment or prevention of PPARγ-responsive diseases, including cancer | |
| JPWO2021160127A5 (ja) | ||
| TWI308564B (en) | Use of alpha-phenylthiocarboxylic and alpha-phenyloxycarboxylic acids with serum-glucose-lowering and serum-lipid-lowering activity | |
| CN102947269A (zh) | 噻唑烷二酮化合物的新的合成方法 | |
| TWI833718B (zh) | 過氧化體增殖物活化受體之活化劑 | |
| WO2001014350A1 (fr) | Derives de benzylthiazolidine-2,4-dione substitues | |
| JP2013535504A (ja) | チアゾリジンジオン化合物のための新規合成 | |
| JP2023528274A (ja) | 置換ピラゾリル化合物及びその使用方法 | |
| FR3103701A1 (fr) | Composés de typen2-arylméthyl-4-haloalkyl-pyridazin-3-one et leur utilisation | |
| McClure | Best of Both Worlds: Linking Nitric Oxide Donors and Rosiglitazone | |
| KR20080097418A (ko) | 물질대사 장애의 치료용 화합물 | |
| JP2000309573A (ja) | 2−メルカプトカルボン酸誘導体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211105 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20211105 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20221206 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20230124 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230403 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A821 Effective date: 20230403 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230530 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230628 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7305548 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |