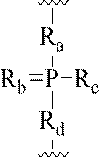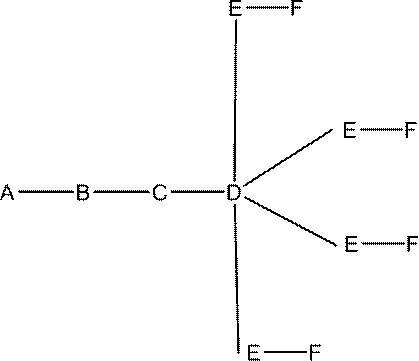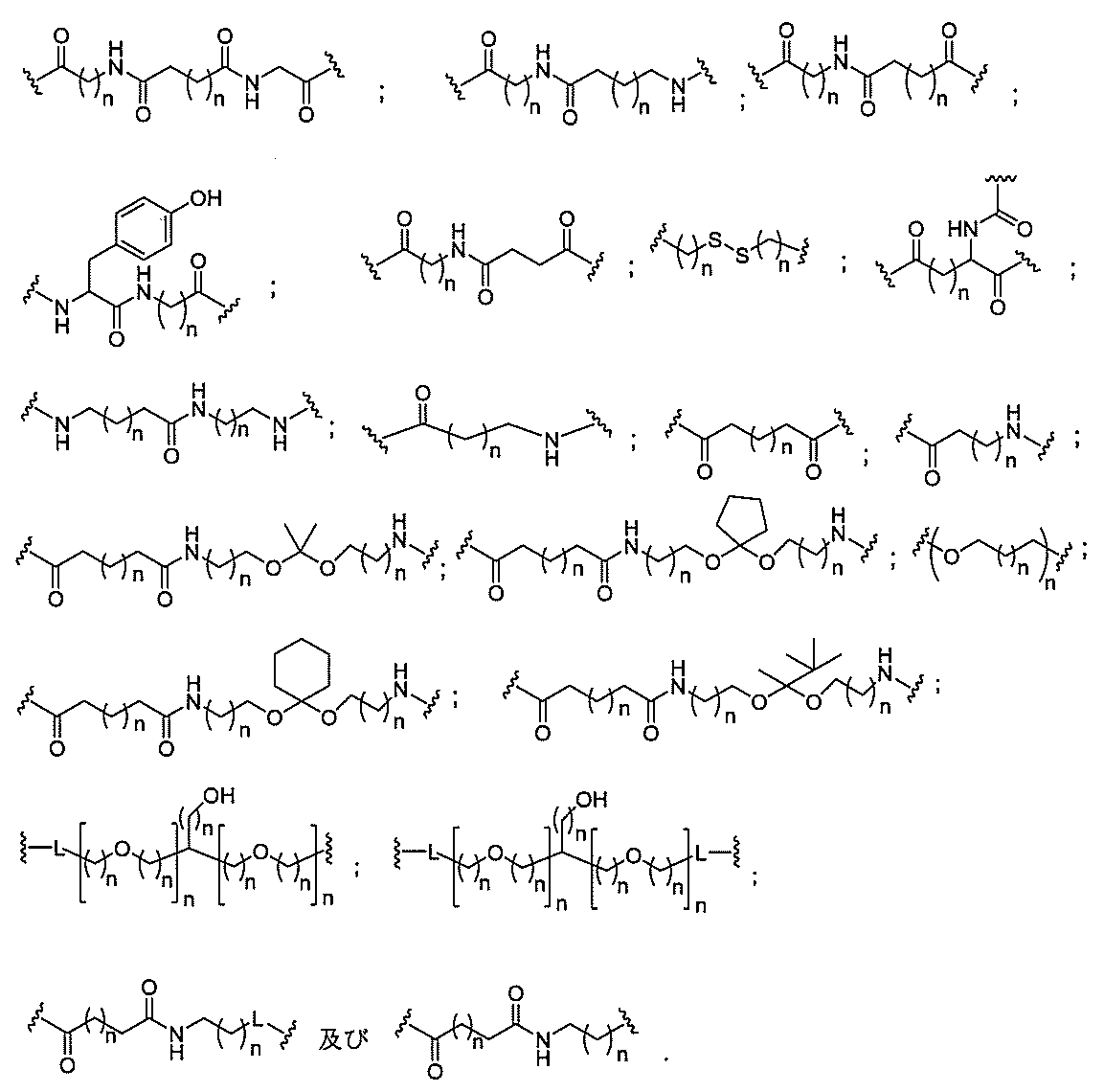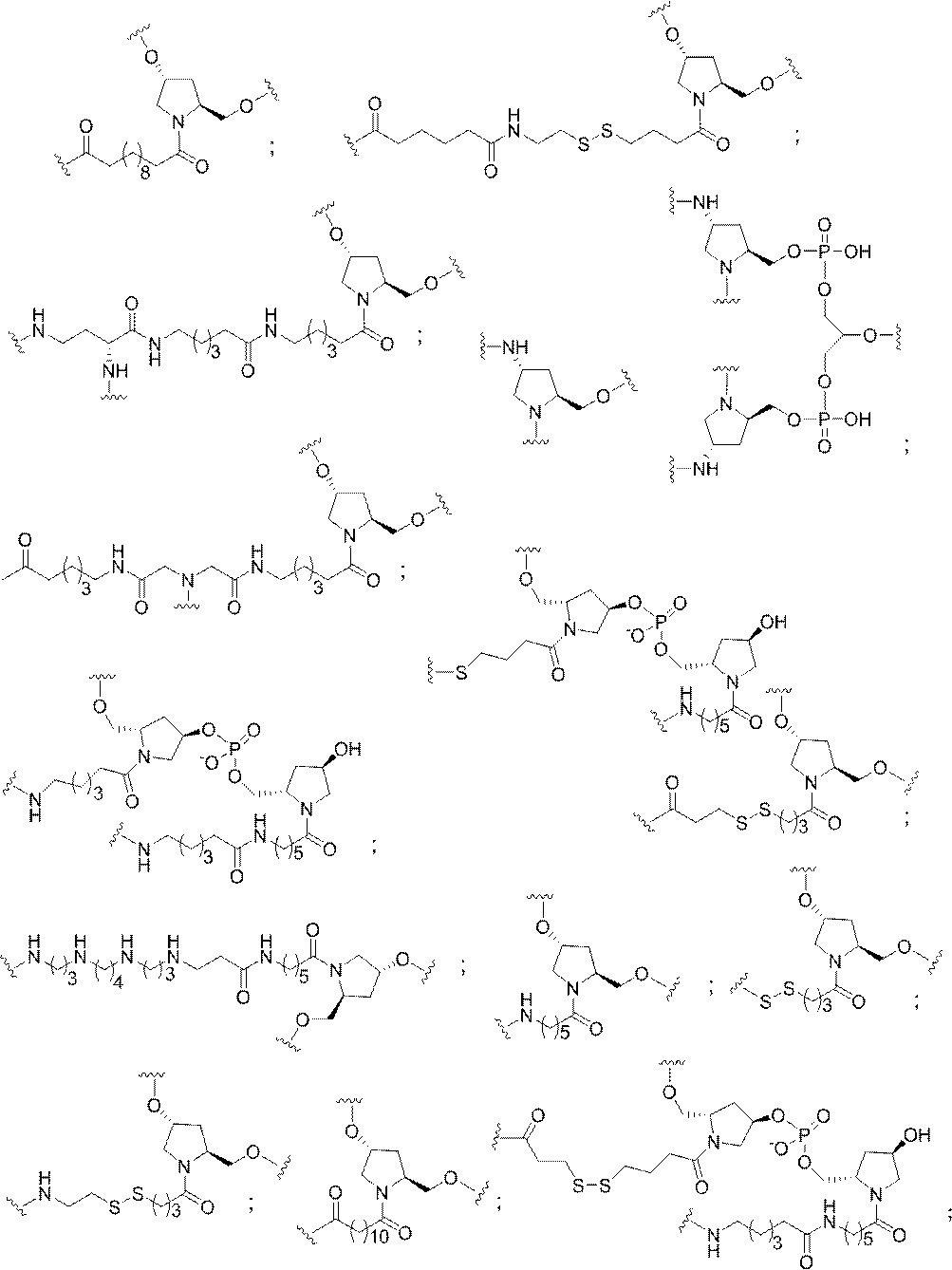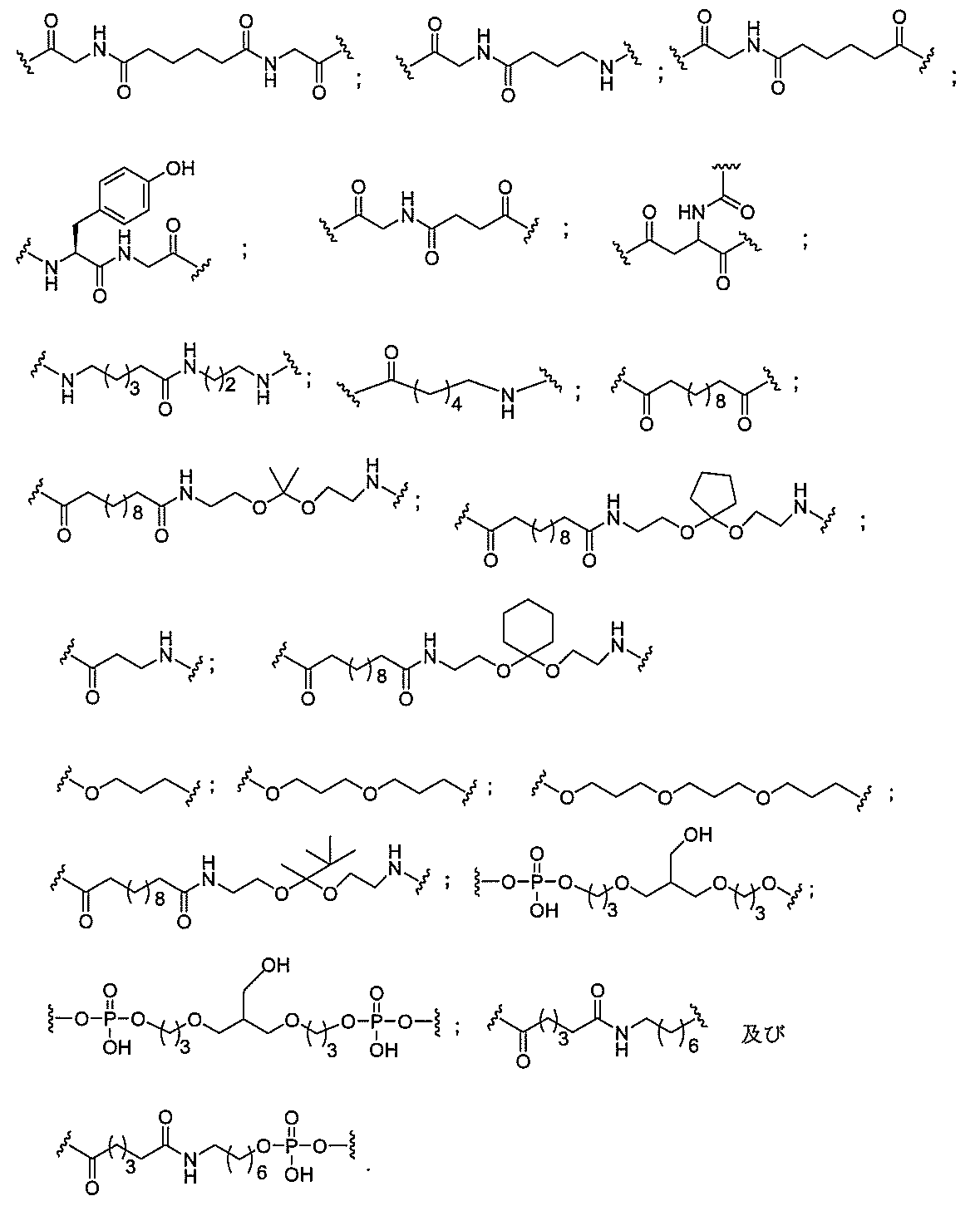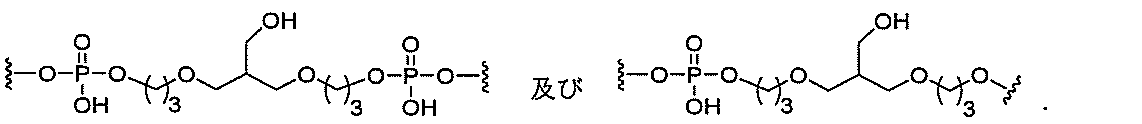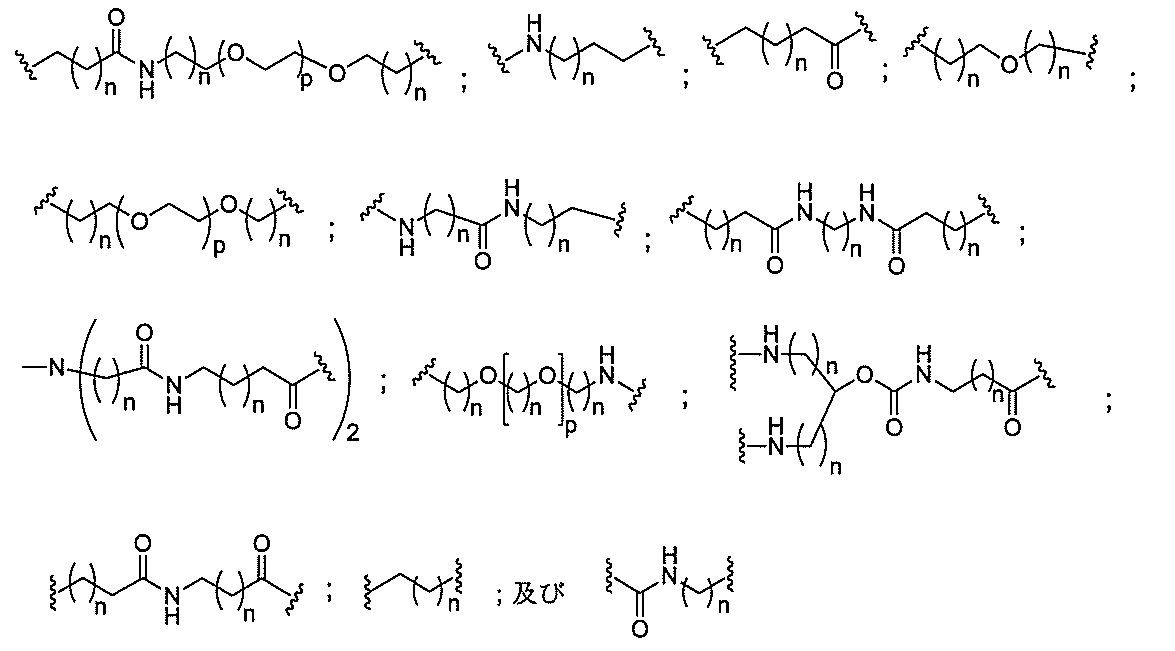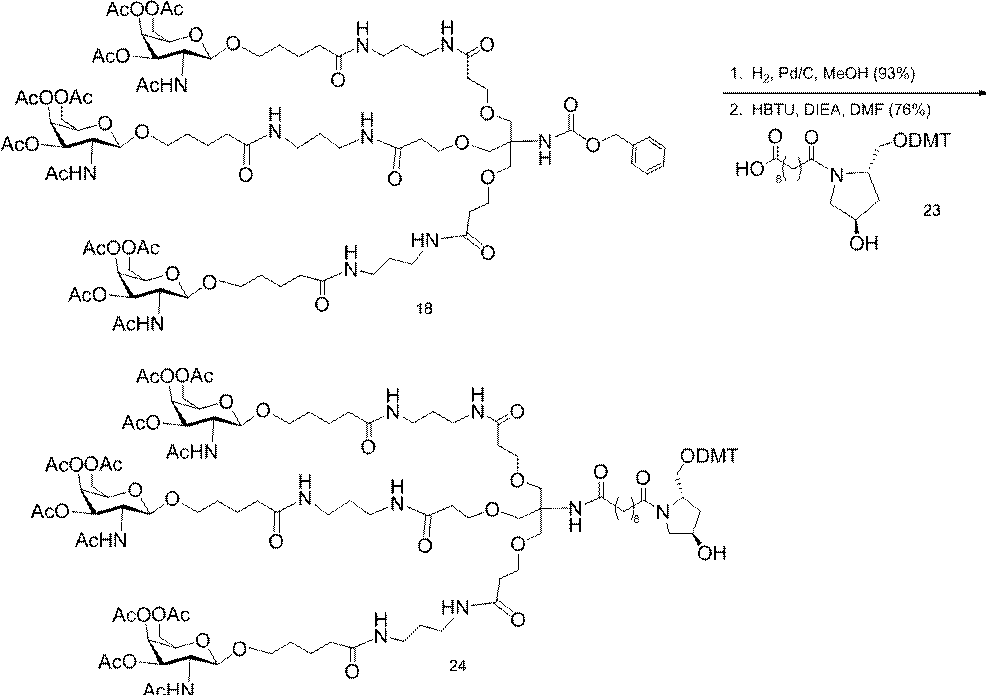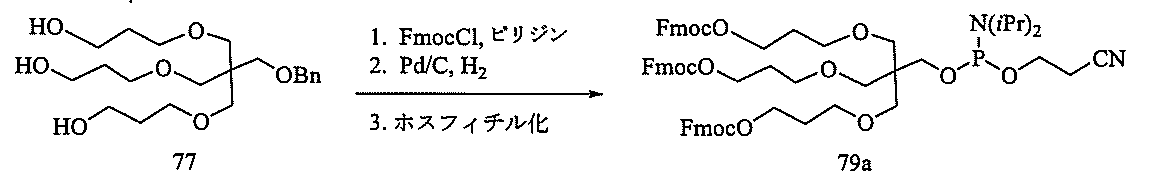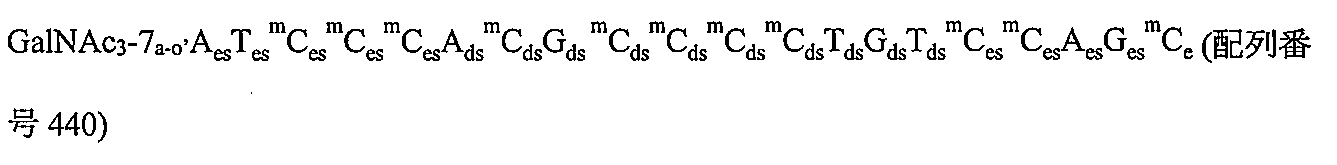JP7001663B2 - 補体b因子発現を調節するための組成物及び方法 - Google Patents
補体b因子発現を調節するための組成物及び方法 Download PDFInfo
- Publication number
- JP7001663B2 JP7001663B2 JP2019228789A JP2019228789A JP7001663B2 JP 7001663 B2 JP7001663 B2 JP 7001663B2 JP 2019228789 A JP2019228789 A JP 2019228789A JP 2019228789 A JP2019228789 A JP 2019228789A JP 7001663 B2 JP7001663 B2 JP 7001663B2
- Authority
- JP
- Japan
- Prior art keywords
- certain embodiments
- compound
- nucleoside
- antisense
- nucleic acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CCCCCC(C)CC(C(C1C(C)CCC1)C(CCC)=CCCC)*12C(C)CC1C2C Chemical compound CCCCCC(C)CC(C(C1C(C)CCC1)C(CCC)=CCCC)*12C(C)CC1C2C 0.000 description 94
- MGNZXYYWBUKAII-UHFFFAOYSA-N C1C=CC=CC1 Chemical compound C1C=CC=CC1 MGNZXYYWBUKAII-UHFFFAOYSA-N 0.000 description 1
- NSELYKZLLNWRED-UHFFFAOYSA-N C=C1CCOCC1 Chemical compound C=C1CCOCC1 NSELYKZLLNWRED-UHFFFAOYSA-N 0.000 description 1
- KERZFPLDNXTKRC-UHFFFAOYSA-N C=[O]CCCOCC(COCCCO)(COCCCO)COCc1ccccc1 Chemical compound C=[O]CCCOCC(COCCCO)(COCCCO)COCc1ccccc1 KERZFPLDNXTKRC-UHFFFAOYSA-N 0.000 description 1
- JZLMSSPUFNCMQK-PJYQUQDBSA-N CC(C(C([C@H](O)OCO)NC(C)=O)O)O Chemical compound CC(C(C([C@H](O)OCO)NC(C)=O)O)O JZLMSSPUFNCMQK-PJYQUQDBSA-N 0.000 description 1
- GBMSZXWHMSSBGP-LURJTMIESA-N CC(C)[C@@H](C)CN Chemical compound CC(C)[C@@H](C)CN GBMSZXWHMSSBGP-LURJTMIESA-N 0.000 description 1
- CKAXGFSUVDSQBA-GHMZBOCLSA-N CC(C)[C@H]([C@@](NC(C)=O)(OC)[IH]OC(C)C)O Chemical compound CC(C)[C@H]([C@@](NC(C)=O)(OC)[IH]OC(C)C)O CKAXGFSUVDSQBA-GHMZBOCLSA-N 0.000 description 1
- CRNNUIMHSLATJF-UHFFFAOYSA-N CC(CC(C)(C)C(C(C)OP(O)(OC(C)(C)C(C)=C)=O)NN=C)C(C)=C Chemical compound CC(CC(C)(C)C(C(C)OP(O)(OC(C)(C)C(C)=C)=O)NN=C)C(C)=C CRNNUIMHSLATJF-UHFFFAOYSA-N 0.000 description 1
- AFOLJKPXMANEEC-NCYGAZKESA-N CC(CO)OC(C(C(O)O)NC(C)=O)OCCOCCOCCNC(CCC(CCC(NCCOCCOCCOC(C(C1O)NC(C)=O)OC(CO)C1O)=O)(CCC(NCCOCCOCCOC(C(C1O)NC(C)=O)OC(CO)C1O)=O)NC(CCCC(NOC1CC(CC2C[C@@H](C)CCC2)CC1)=O)=O)=O Chemical compound CC(CO)OC(C(C(O)O)NC(C)=O)OCCOCCOCCNC(CCC(CCC(NCCOCCOCCOC(C(C1O)NC(C)=O)OC(CO)C1O)=O)(CCC(NCCOCCOCCOC(C(C1O)NC(C)=O)OC(CO)C1O)=O)NC(CCCC(NOC1CC(CC2C[C@@H](C)CCC2)CC1)=O)=O)=O AFOLJKPXMANEEC-NCYGAZKESA-N 0.000 description 1
- ZEVOCXOZYFLVKN-UHFFFAOYSA-N CC(NC(C1O)C(OC)OC(CO)C1O)=O Chemical compound CC(NC(C1O)C(OC)OC(CO)C1O)=O ZEVOCXOZYFLVKN-UHFFFAOYSA-N 0.000 description 1
- PXTJVZJEAPXWCR-ZVOIOQAGSA-O CC(NC(C1OC(C)=O)[C@H](OCCCCCC[OH2+])O[C@@H](COC(C)=O)C1OC(C)=O)=O Chemical compound CC(NC(C1OC(C)=O)[C@H](OCCCCCC[OH2+])O[C@@H](COC(C)=O)C1OC(C)=O)=O PXTJVZJEAPXWCR-ZVOIOQAGSA-O 0.000 description 1
- CEUAFAGIMNJHIB-WTIBDHCWSA-N CC(O[C@@](C1N)(C1(O)OC1)C1=C)=O Chemical compound CC(O[C@@](C1N)(C1(O)OC1)C1=C)=O CEUAFAGIMNJHIB-WTIBDHCWSA-N 0.000 description 1
- OONDBEOXHAAVPK-FSVFDIHESA-N CC([C@H](C)NC(C)=O)C(CC(CO)O)O Chemical compound CC([C@H](C)NC(C)=O)C(CC(CO)O)O OONDBEOXHAAVPK-FSVFDIHESA-N 0.000 description 1
- ADNHKZRYBOUYGM-UHFFFAOYSA-N CC1C(CC2)CC2C1C Chemical compound CC1C(CC2)CC2C1C ADNHKZRYBOUYGM-UHFFFAOYSA-N 0.000 description 1
- KZPNTGPYTJTSOU-UHFFFAOYSA-N CCC(C(N)=O)NC(C(CC)NC(C1(CC1)NC)=O)=O Chemical compound CCC(C(N)=O)NC(C(CC)NC(C1(CC1)NC)=O)=O KZPNTGPYTJTSOU-UHFFFAOYSA-N 0.000 description 1
- DURSJWNUIWKMKG-UHFFFAOYSA-O CCC(CNCCC[NH2+]C)C[U]CCC[Cl](C)[U] Chemical compound CCC(CNCCC[NH2+]C)C[U]CCC[Cl](C)[U] DURSJWNUIWKMKG-UHFFFAOYSA-O 0.000 description 1
- SNDPXSYFESPGGJ-UHFFFAOYSA-N CCCC(C(O)=O)N Chemical compound CCCC(C(O)=O)N SNDPXSYFESPGGJ-UHFFFAOYSA-N 0.000 description 1
- OLLZXQIFCRIRMH-UHFFFAOYSA-N CCCC(NC)=O Chemical compound CCCC(NC)=O OLLZXQIFCRIRMH-UHFFFAOYSA-N 0.000 description 1
- CXLZFJAVKDMLPX-UHFFFAOYSA-N CCCCNCC(CNCCCNP(Cl)=N)(COC)CO[U] Chemical compound CCCCNCC(CNCCCNP(Cl)=N)(COC)CO[U] CXLZFJAVKDMLPX-UHFFFAOYSA-N 0.000 description 1
- KRABAWXNIPSDEF-PQLWYXDDSA-N CCO[C@@H](C(C1O)NC(C)=O)OC(CO)C1O Chemical compound CCO[C@@H](C(C1O)NC(C)=O)OC(CO)C1O KRABAWXNIPSDEF-PQLWYXDDSA-N 0.000 description 1
- SOMVZFCIPTUWJL-UHFFFAOYSA-N CC[IH](CC[U])(N)[U]C Chemical compound CC[IH](CC[U])(N)[U]C SOMVZFCIPTUWJL-UHFFFAOYSA-N 0.000 description 1
- BXELQCNPFFKPGY-UHFFFAOYSA-N CNC(CCCC(N)=O)=O Chemical compound CNC(CCCC(N)=O)=O BXELQCNPFFKPGY-UHFFFAOYSA-N 0.000 description 1
- KUJWACOIDUPULI-SNVBAGLBSA-N C[C@H](CCCCNC(OC(C)(C)C)=O)C=O Chemical compound C[C@H](CCCCNC(OC(C)(C)C)=O)C=O KUJWACOIDUPULI-SNVBAGLBSA-N 0.000 description 1
- RUQQPEBSTNFNEA-UHFFFAOYSA-N N#CCCOCC(CO)(COCCC#N)COCCC#N Chemical compound N#CCCOCC(CO)(COCCC#N)COCCC#N RUQQPEBSTNFNEA-UHFFFAOYSA-N 0.000 description 1
- WJBCMPGEMGBKCH-RXMQYKEDSA-N OC[C@@H]1[IH]CCN1C=O Chemical compound OC[C@@H]1[IH]CCN1C=O WJBCMPGEMGBKCH-RXMQYKEDSA-N 0.000 description 1
- VYSAWXOKFKHRBJ-YFKPBYRVSA-N OP(O)(O)OC[C@H]1NCCC1 Chemical compound OP(O)(O)OC[C@H]1NCCC1 VYSAWXOKFKHRBJ-YFKPBYRVSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/555—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound pre-targeting systems involving an organic compound, other than a peptide, protein or antibody, for targeting specific cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1137—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against enzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y304/00—Hydrolases acting on peptide bonds, i.e. peptidases (3.4)
- C12Y304/21—Serine endopeptidases (3.4.21)
- C12Y304/21047—Alternative-complement-pathway C3/C5 convertase (3.4.21.47), i.e. properdin factor B
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/31—Chemical structure of the backbone
- C12N2310/315—Phosphorothioates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/32—Chemical structure of the sugar
- C12N2310/321—2'-O-R Modification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/33—Chemical structure of the base
- C12N2310/334—Modified C
- C12N2310/3341—5-Methylcytosine
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/34—Spatial arrangement of the modifications
- C12N2310/341—Gapmers, i.e. of the type ===---===
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/34—Spatial arrangement of the modifications
- C12N2310/346—Spatial arrangement of the modifications having a combination of backbone and sugar modifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/352—Nature of the modification linked to the nucleic acid via a carbon atom
- C12N2310/3525—MOE, methoxyethoxy
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- General Engineering & Computer Science (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Microbiology (AREA)
- Biophysics (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Immunology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Epidemiology (AREA)
- Virology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Urology & Nephrology (AREA)
- Ophthalmology & Optometry (AREA)
- Cell Biology (AREA)
- Analytical Chemistry (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Medicinal Preparation (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
本願は、電子形式の配列表とともに出願されている。この配列表は、2015年4月28日に作成されたサイズ204kbのBIOL0251WOSEQ_ST25.txtという名称のファイルとして提供される。この配列表の電子形式の情報は、参照によりその全体が本明細書に組み込まれる。
補体系は自然免疫を媒介し、傷害に対する正常な炎症応答に重要な役割を果たすが、その調節異常は重度の傷害を引き起こしうる。代替補体経路がその構成的「アイドリング」レベルを超えて活性化すると、無制限な機能亢進が起こり、補体調節異常の疾患として顕在化しうる。
前記一般的な説明及び以下の詳細な説明はどちらも例示的かつ説明的であるにすぎず、本願に係る発明を限定するものではないと理解すべきである。本明細書において、単数形の使用は、別段の明示がある場合を除き、複数形を含む。本明細書において「または(or)」の使用は、別段の言明がある場合を除き、「及び/または(and/or)」を意味する。さらに、「~を含む(including)」という用語、ならびに「~を含む(includes)」及び「含まれる(included)」などの他の形態の使用は、限定的ではない。また、「要素」または「成分」などの用語は、別段の明示がある場合を除き、1つのユニットを含む要素及び成分と2つ以上のサブユニットを含む要素及び成分をどちらも包含する。
Society,ワシントンD.C.,1994、「Remington’s Pharmaceutical Sciences」Mack Publishing Co.,ペンシルベニア州イーストン,第21版,2005、及び「Antisense Drug Technology,Principles,Strategies,and Applications」Stanley T.Crooke編,CRC Press,フロリダ州ボカラトン、ならびにSambrook et al.,「Molecular Cloning,A laboratory Manual」第2版,Cold Spring Harbor Laboratory Press,1989に見いだすことができ、これらは、あらゆる目的のために参照により本明細書に組み込まれる。許容される場合、本開示の全体を通して言及する特許、出願、公開された出願、及び他の出版物、ならびに他のデータはすべて、参照によりそれらの全体が本明細書に組み込まれる。
別段の表示がある場合を除き、以下の用語は、以下の意味を有する。
、場合によっては、さらなる置換基を含みうる。
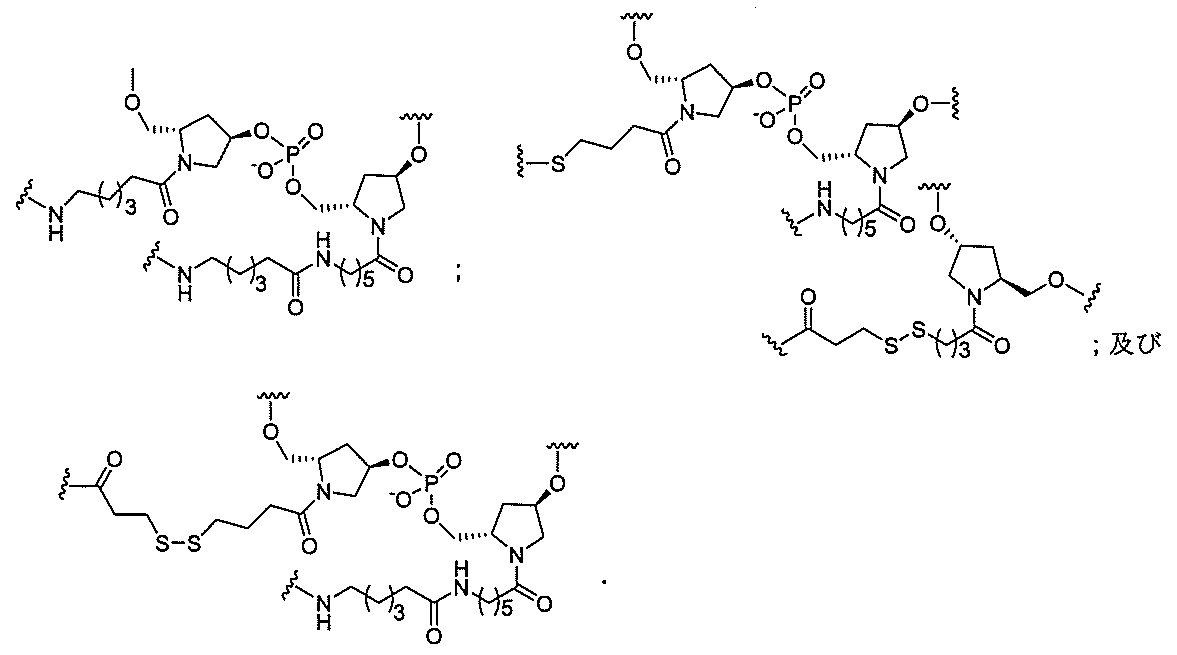
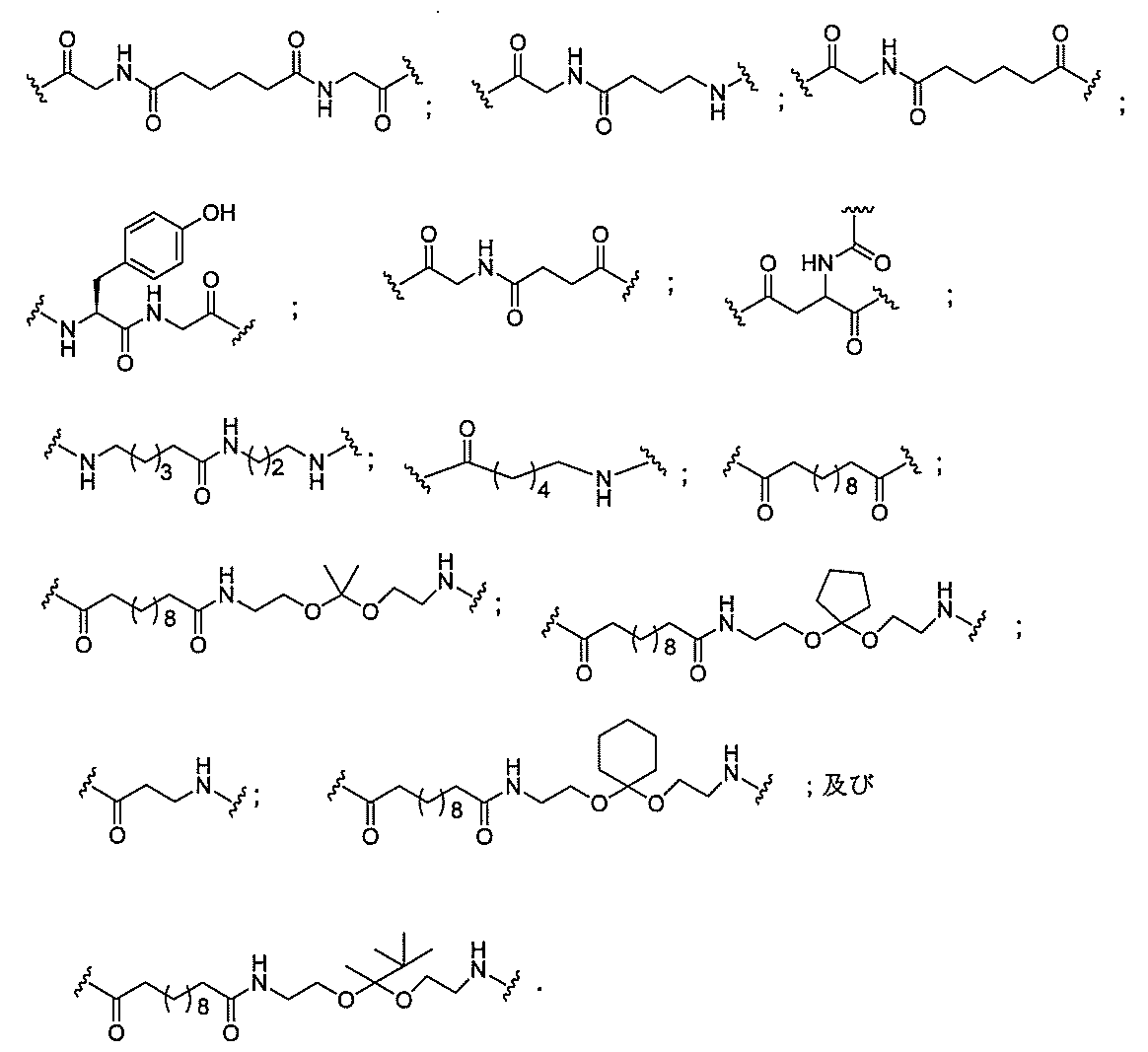
S)-、-O-、-Si(R1)2-、-S(=O)x-及び-N(R1)-[ここで、xは0、1、または2であり、nは1、2、3、または4であり、各R1及びR2は、独立して、H、保護基、ヒドロキシル、C1-C12アルキル、置換C1-C12アルキル、C2-C12アルケニル、置換C2-C12アルケニル、C2-C12アルキニル、置換C2-C12アルキニル、C5-C20アリール、置換C5-C20アリール、複素環ラジカル、置換複素環ラジカル、ヘテロアリール、置換ヘテロアリール、C5-C7脂環式ラジカル、置換C5-C7脂環式ラジカル、ハロゲン、OJ1、NJ1J2、SJ1、N3、COOJ1、アシル(C(=O)-H)、置換アシル、CN、スルホニル(S(=O)2-J1)、またはスルホキシル(S(=O)-J1)であり、各J1及び J2は、独立して、H、C1-C12アルキル、置換C1-C12アルキル、C2-C12アルケニル、置換C2-C12アルケニル、C2-C12アルキニル、置換C2-C12アルキニル、C5-C20アリール、置換C5-C20アリール、アシル(C(=O)-H)、置換アシル、複素環ラジカル、置換複素環ラジカル、C1-C12アミノアルキル、置換C1-C12アミノアルキルまたは保護基である]から独立して選択される1つまたは2~4つの連結基を、独立して含むものが含まれるが、これらに限定されない。
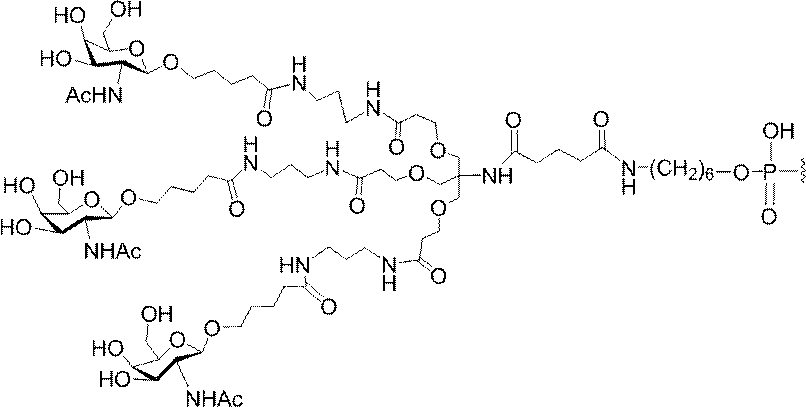
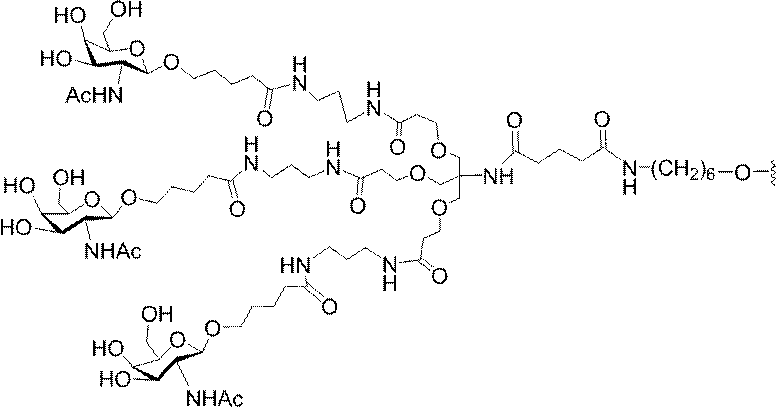
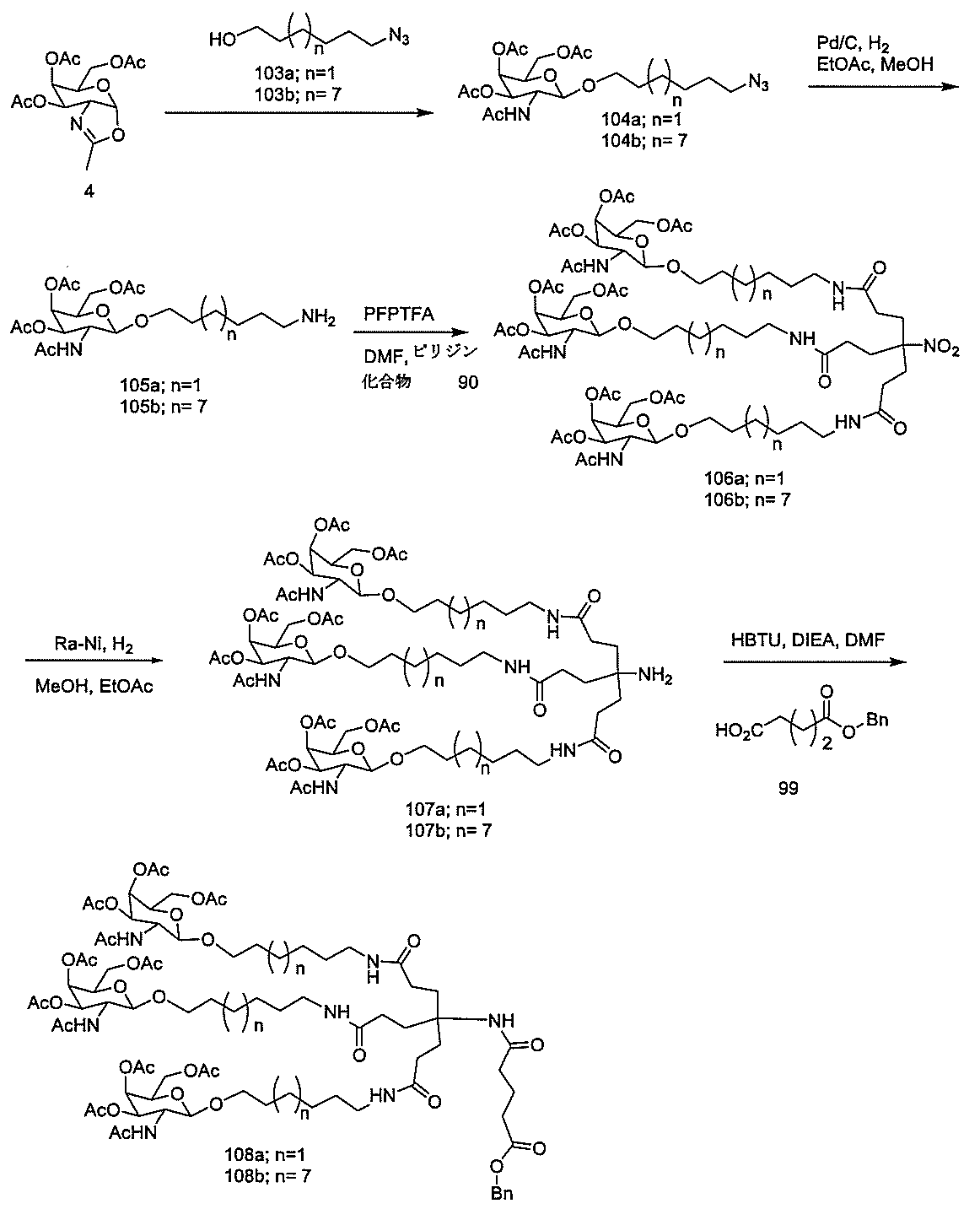
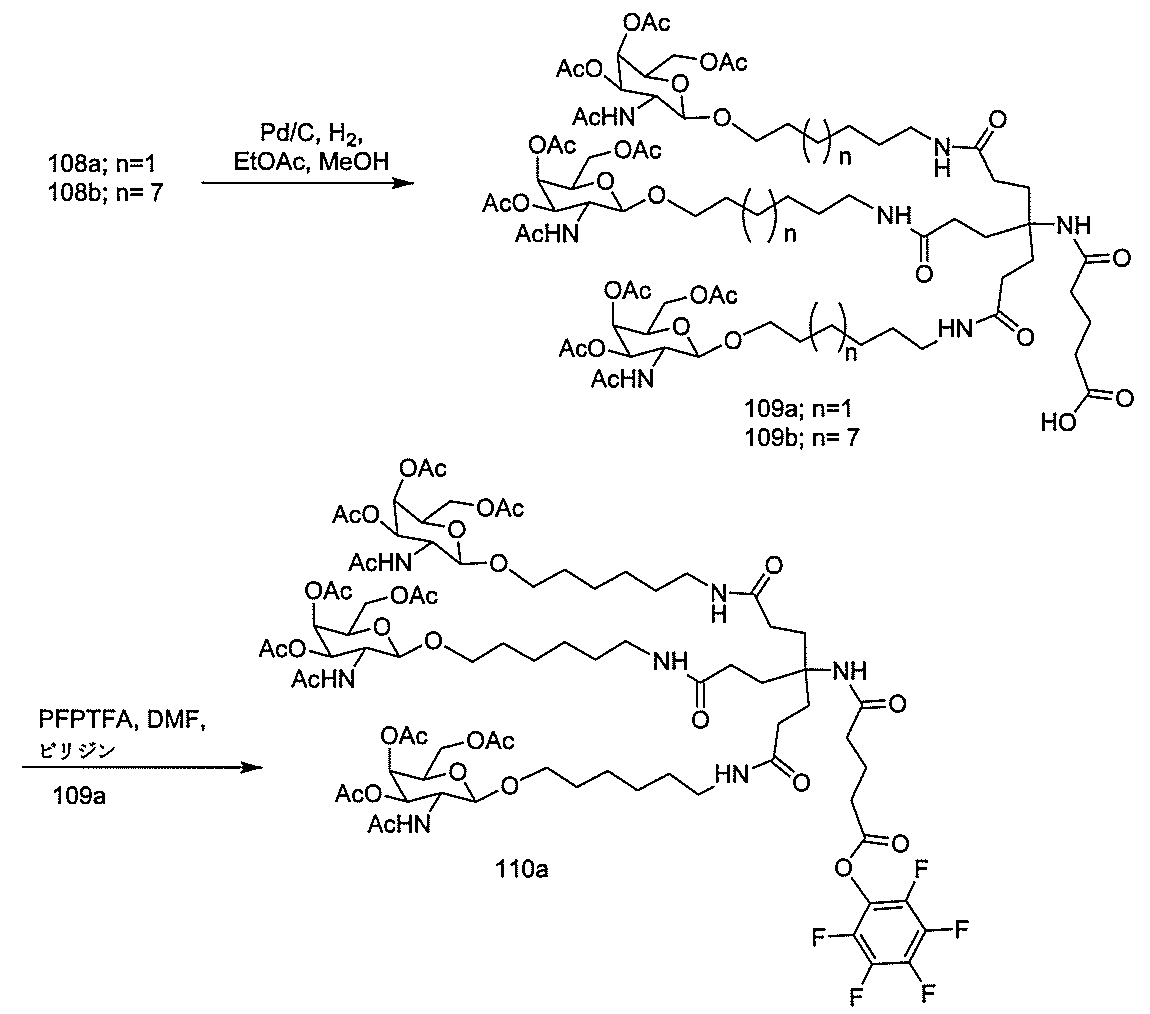
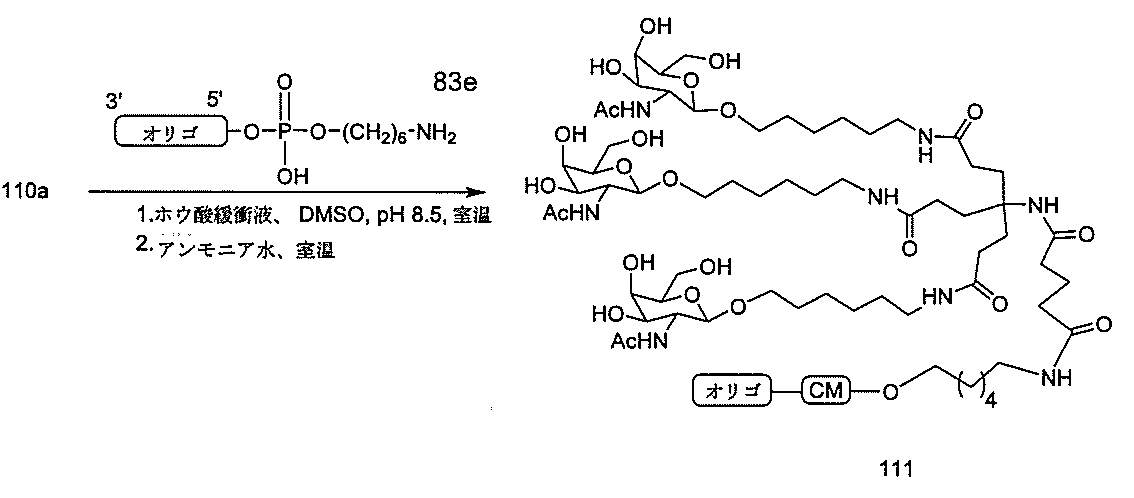
Targeting of Lipoproteins to the Hepatic Asiaglycoprotein Receptor」J.Med.Chem.2004,(47):5798-5808を参照のこと)。
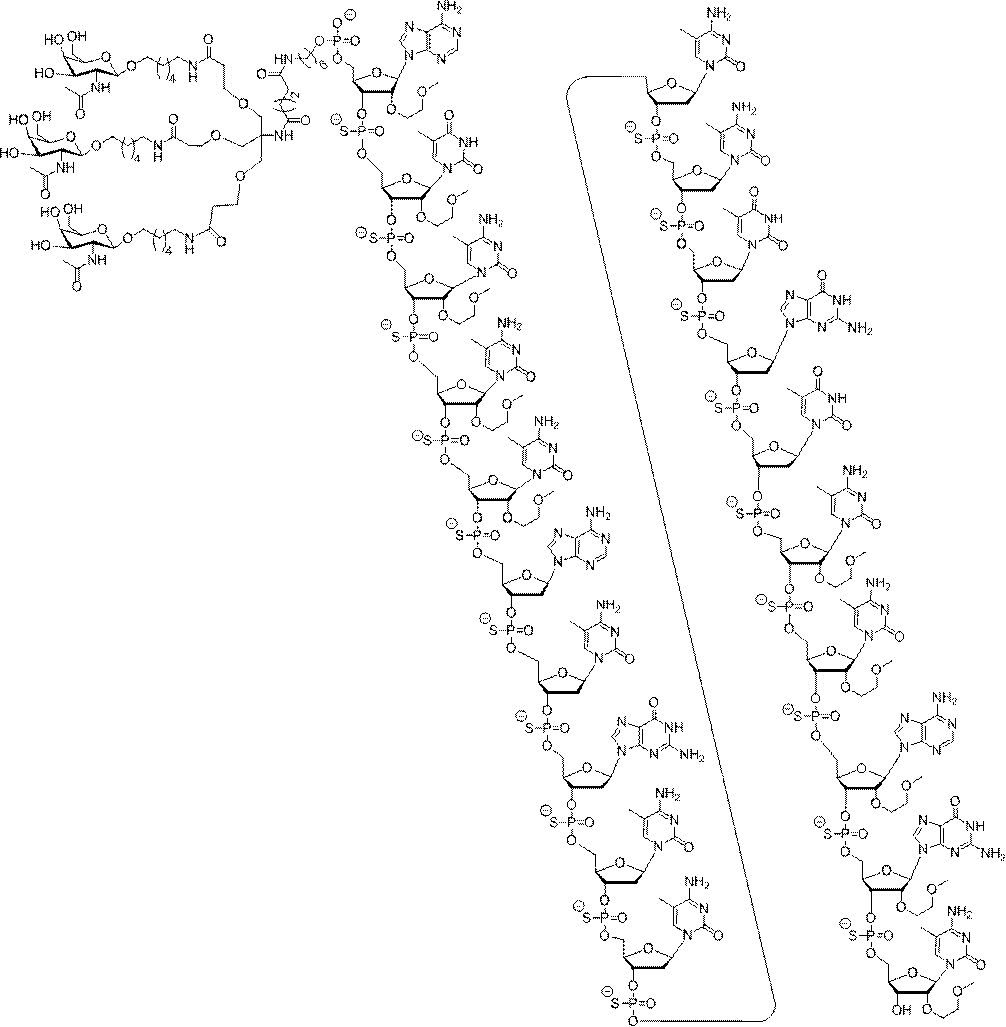
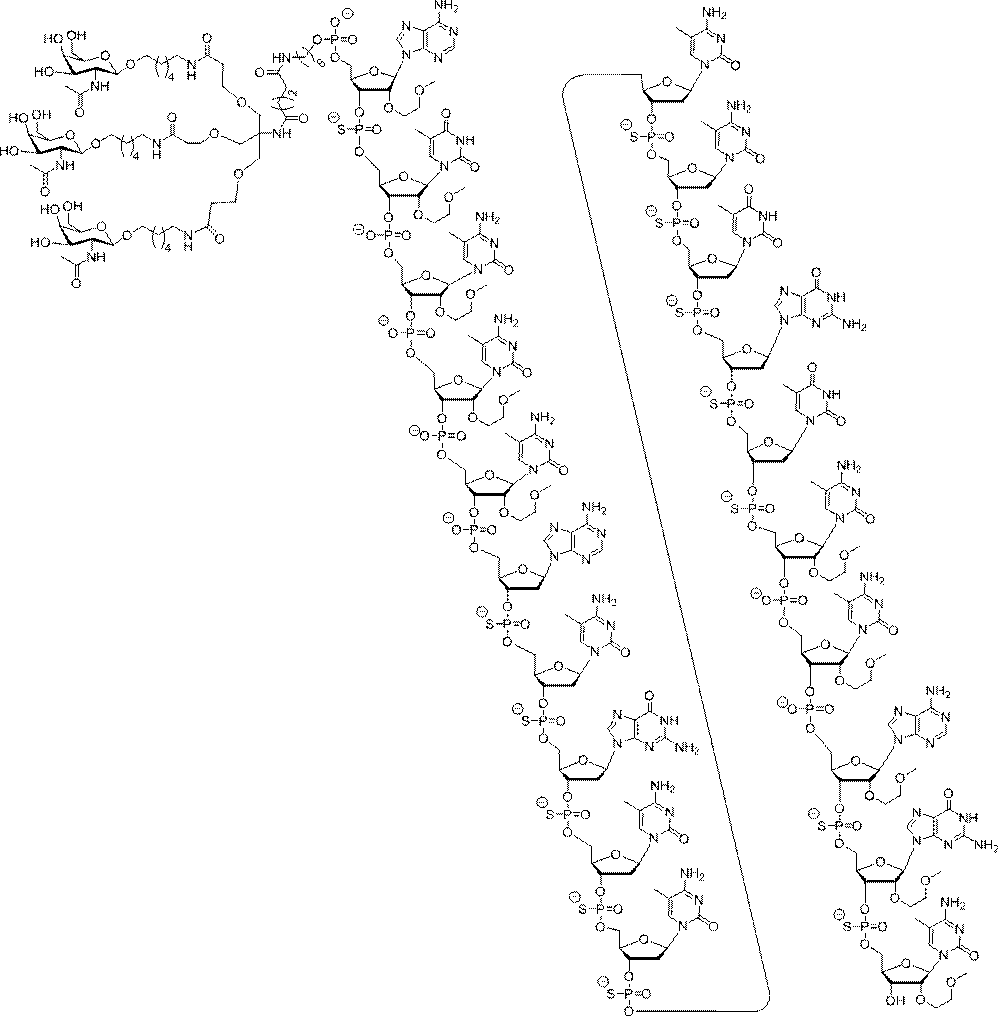
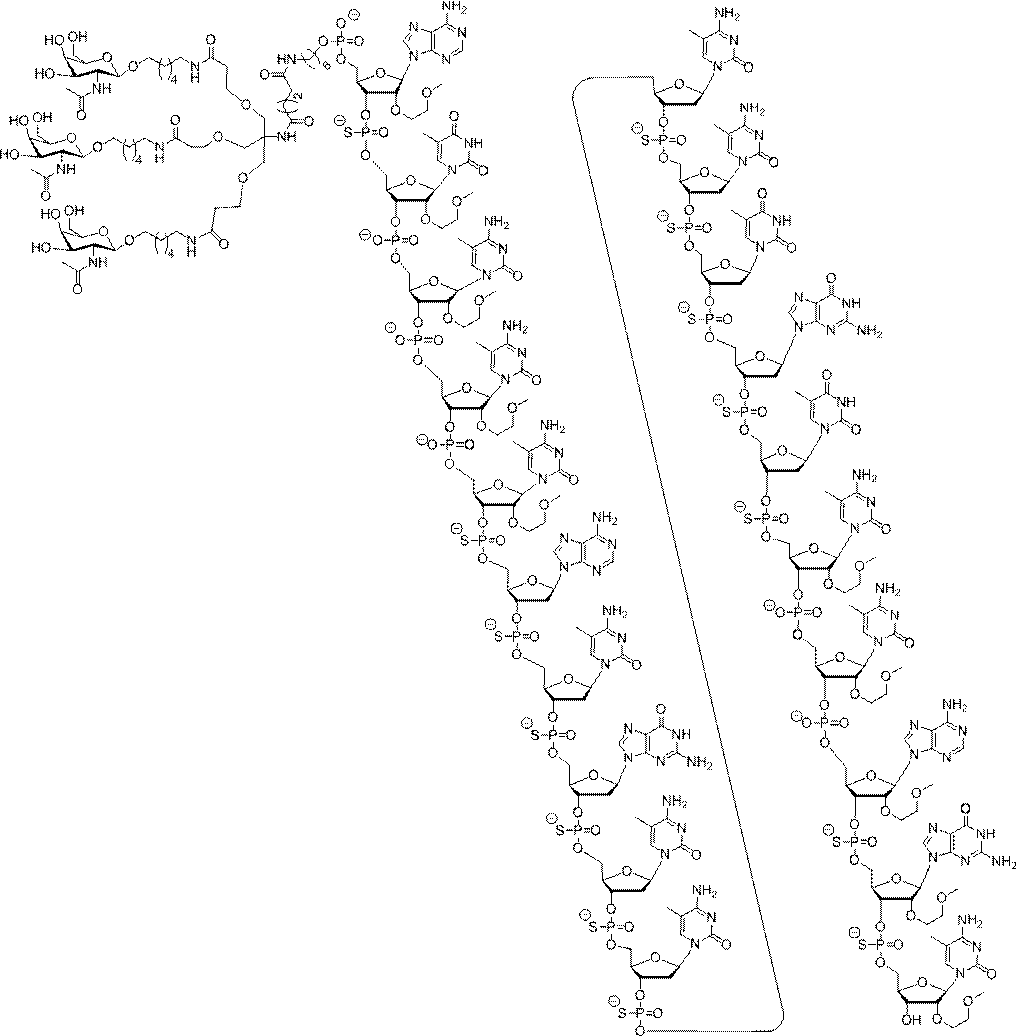
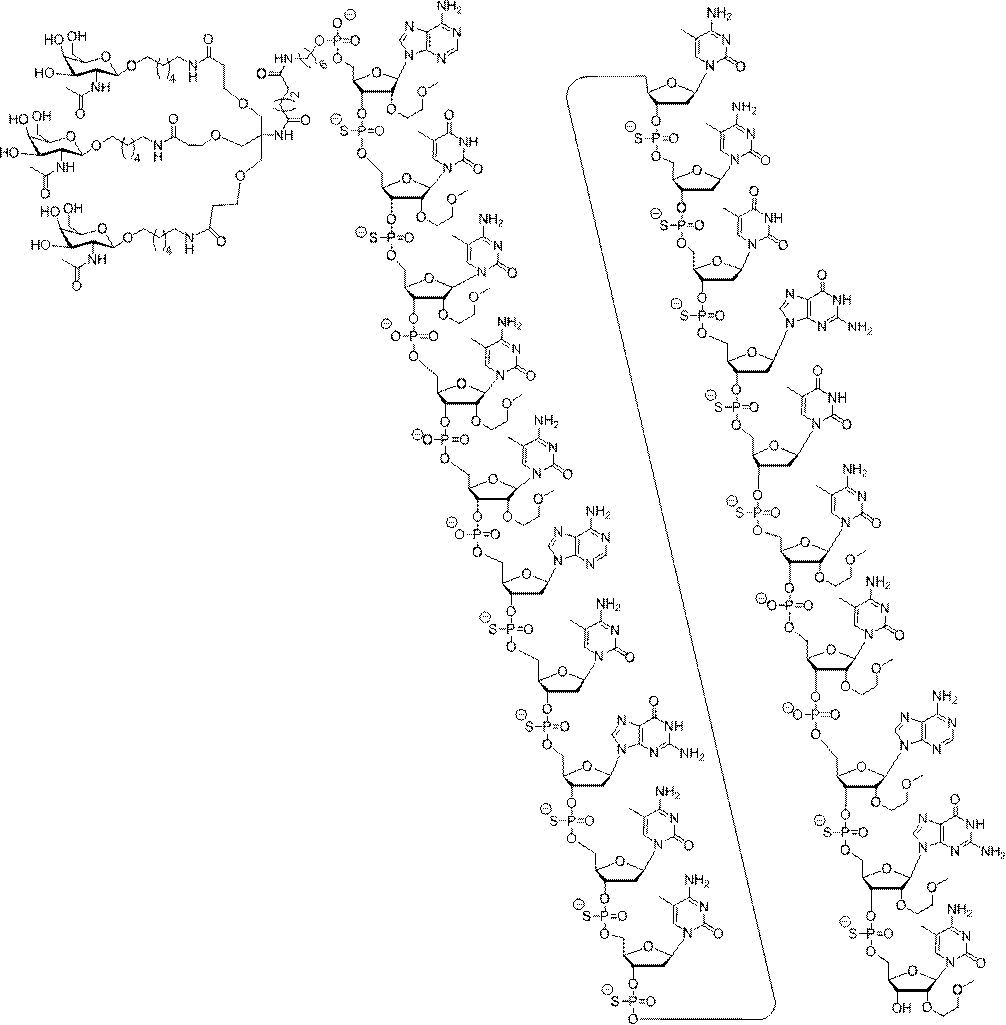
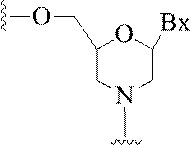
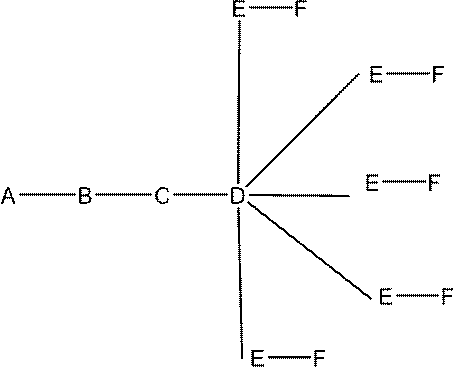
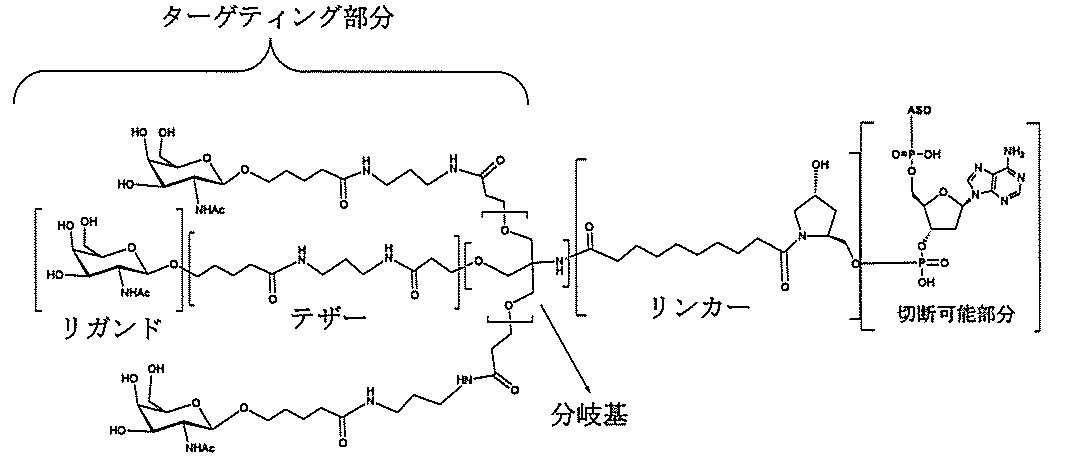
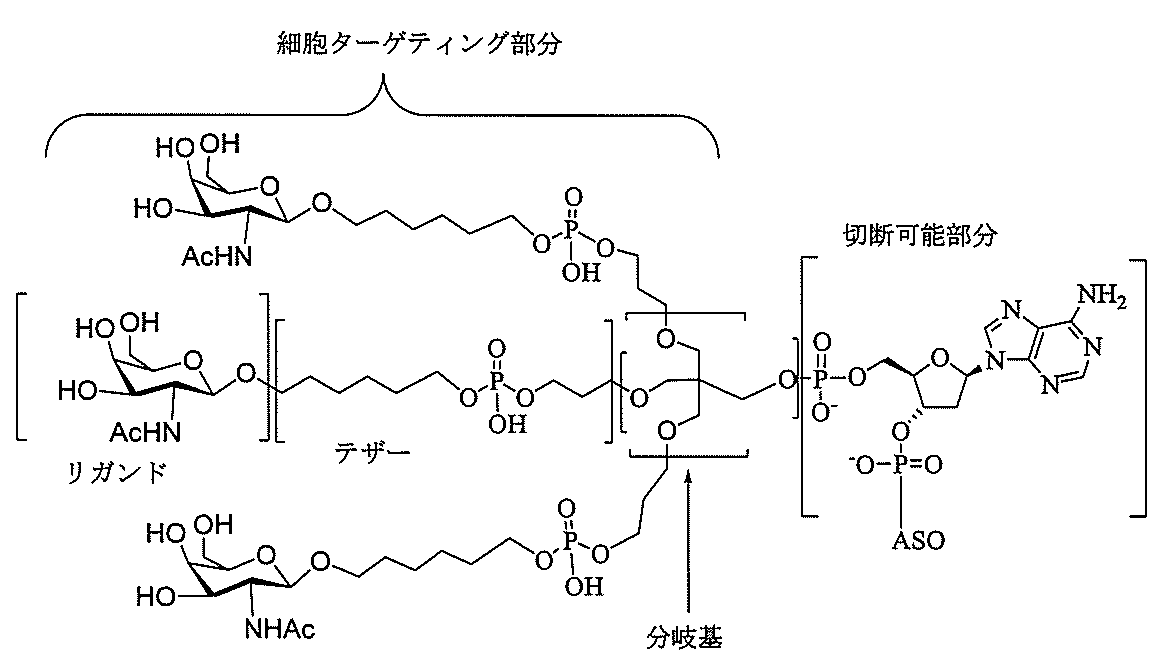
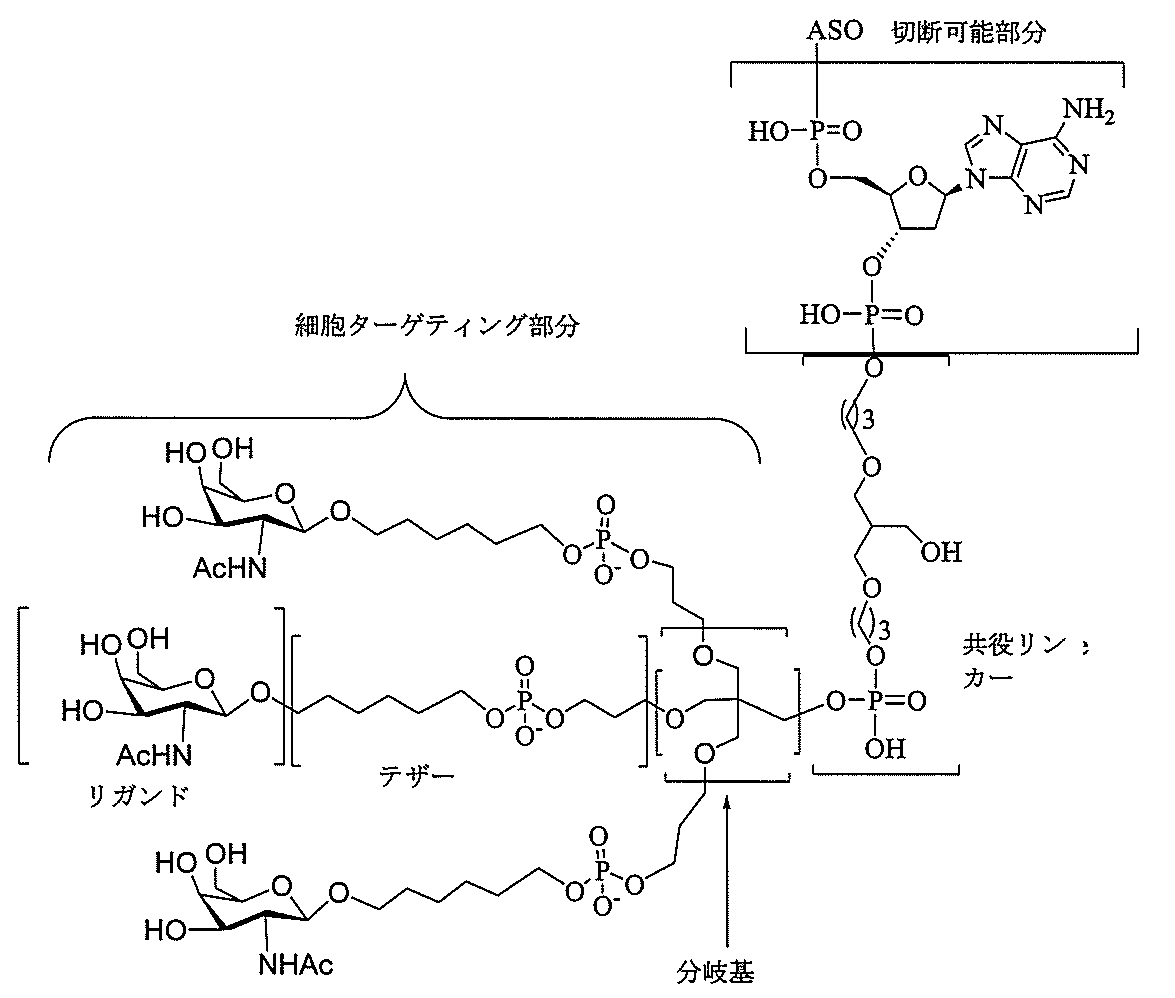
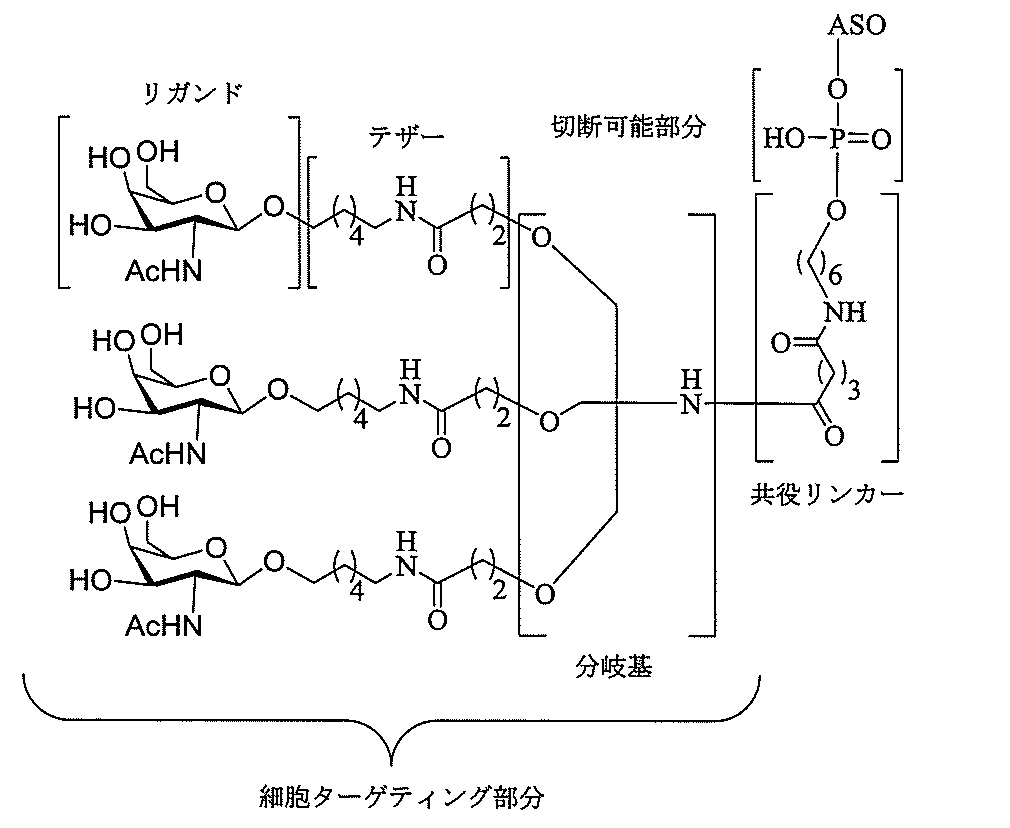
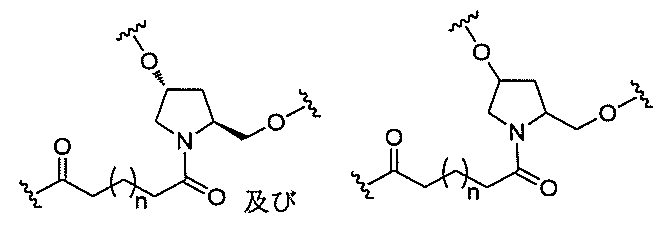
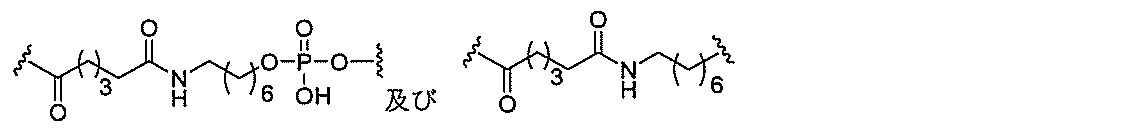
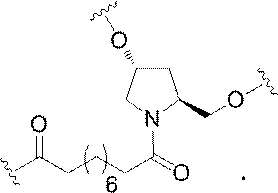
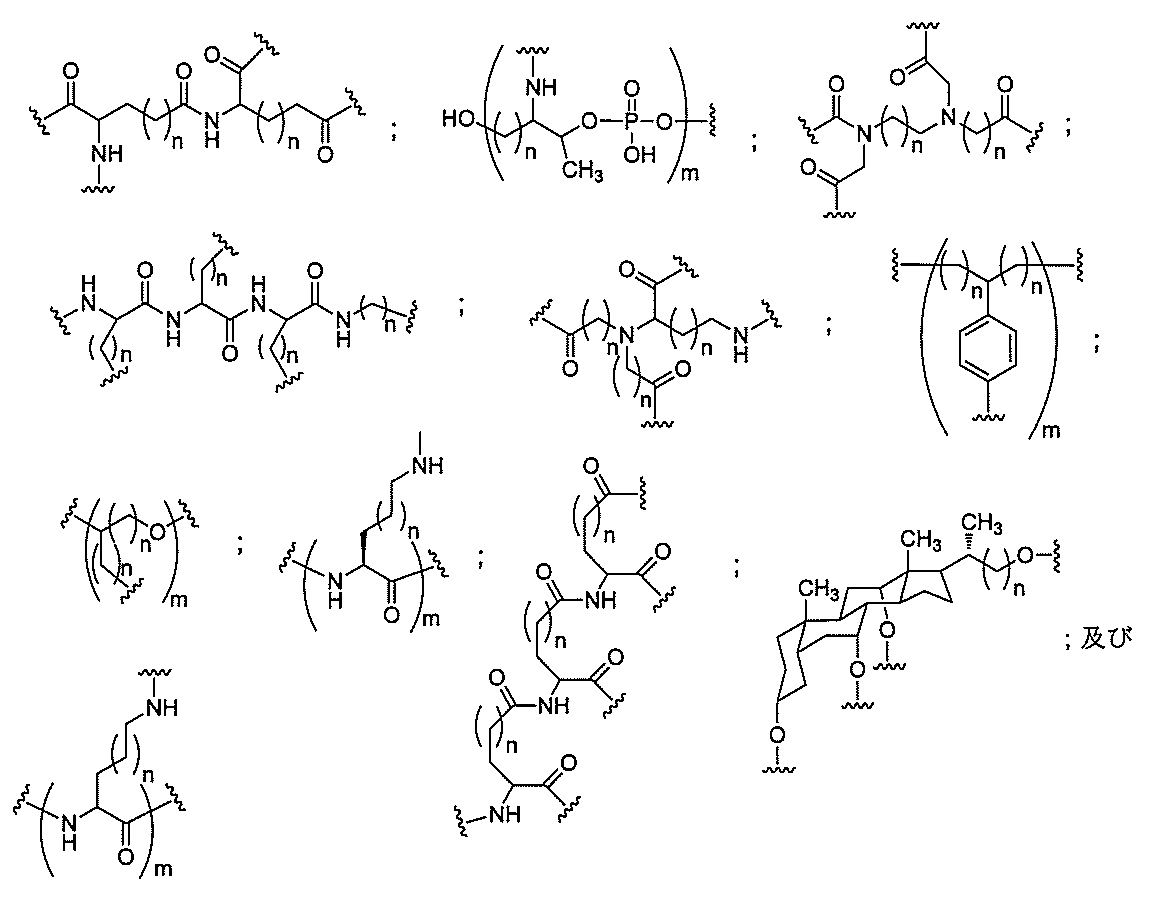
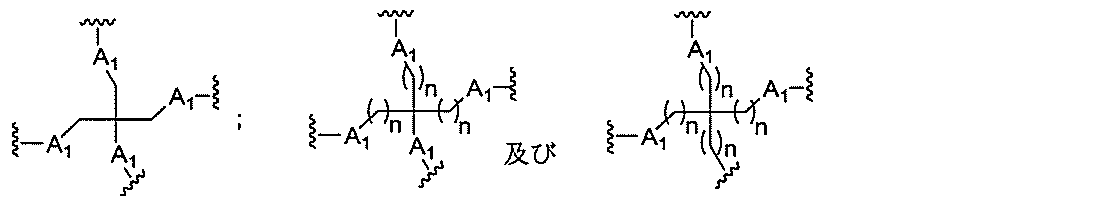
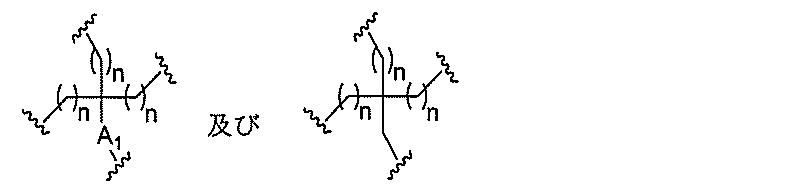
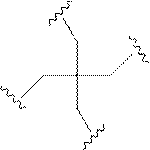
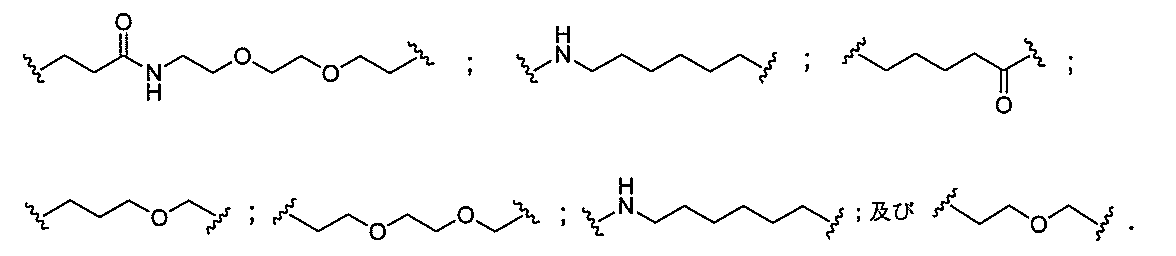
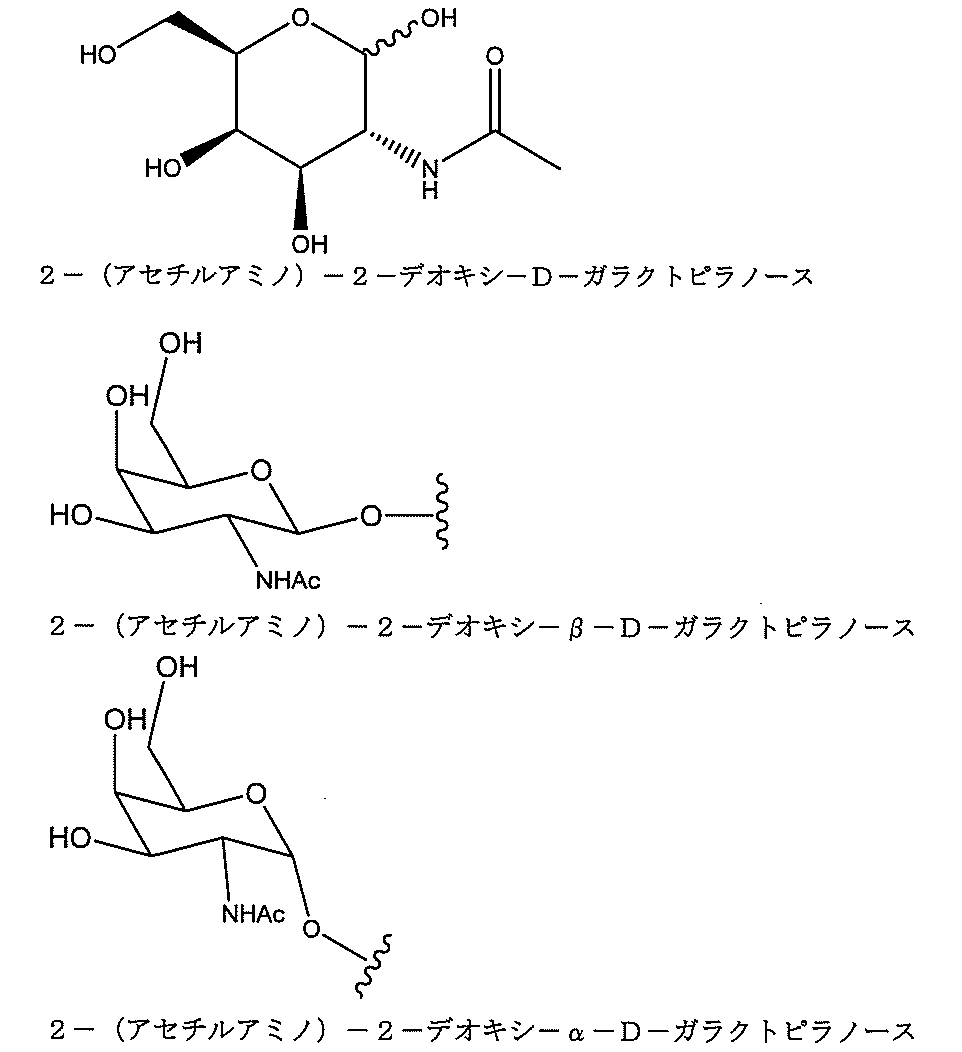
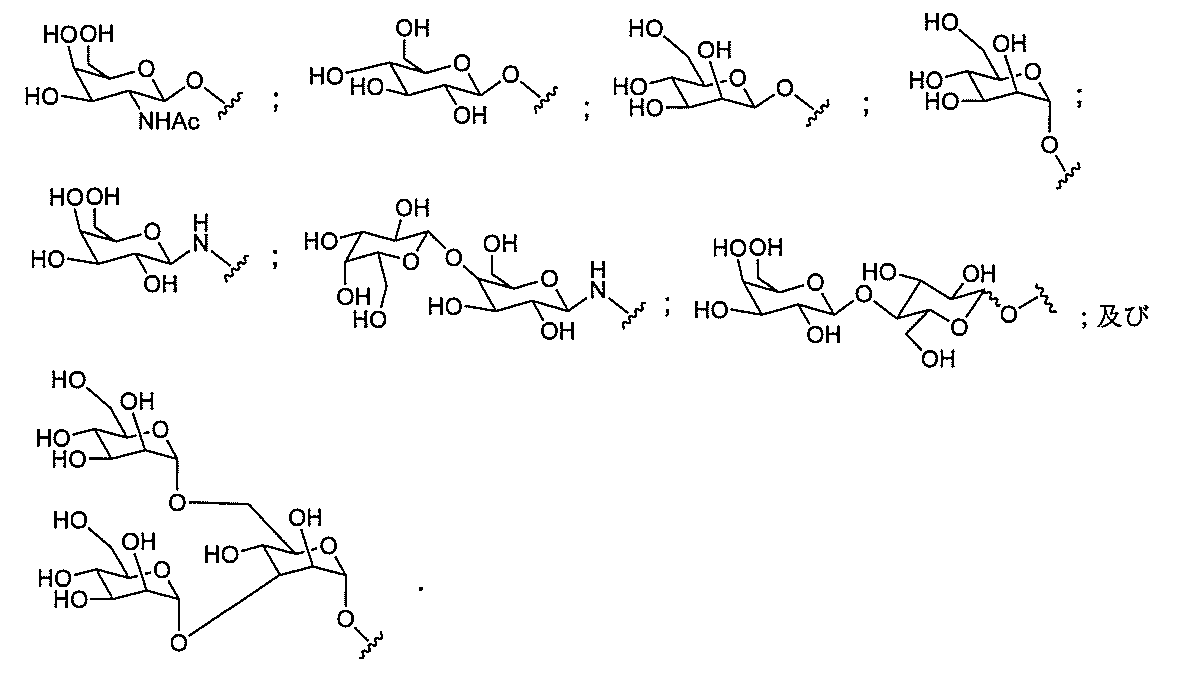
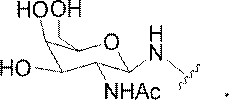
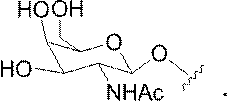
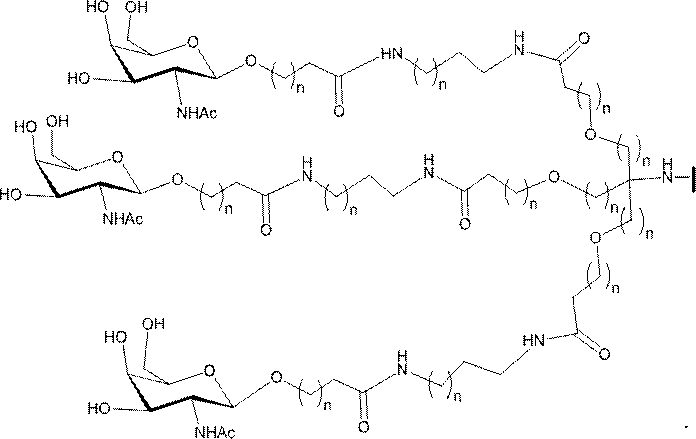
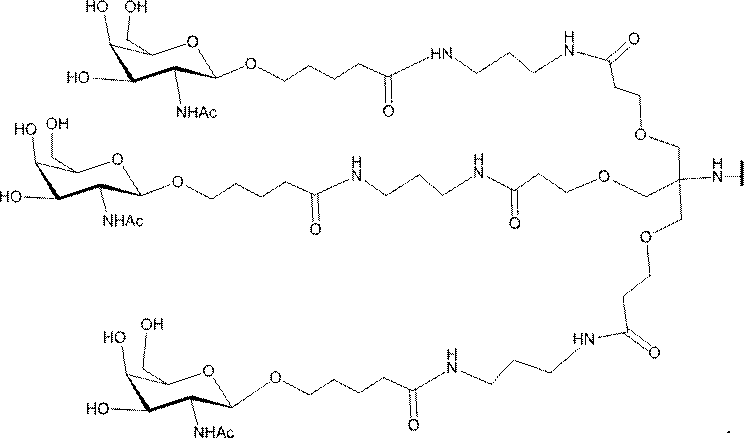
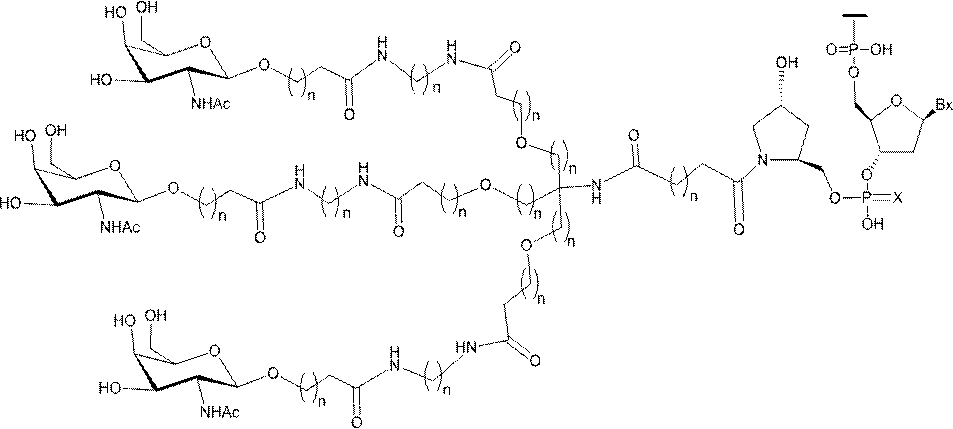
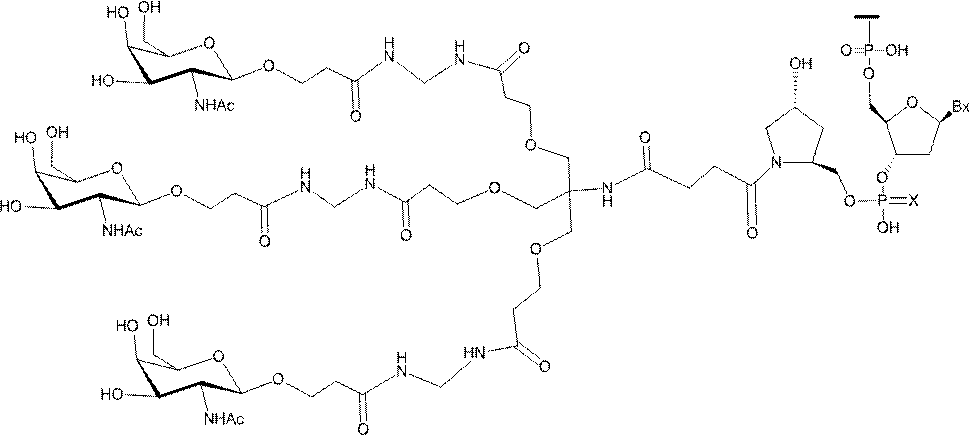
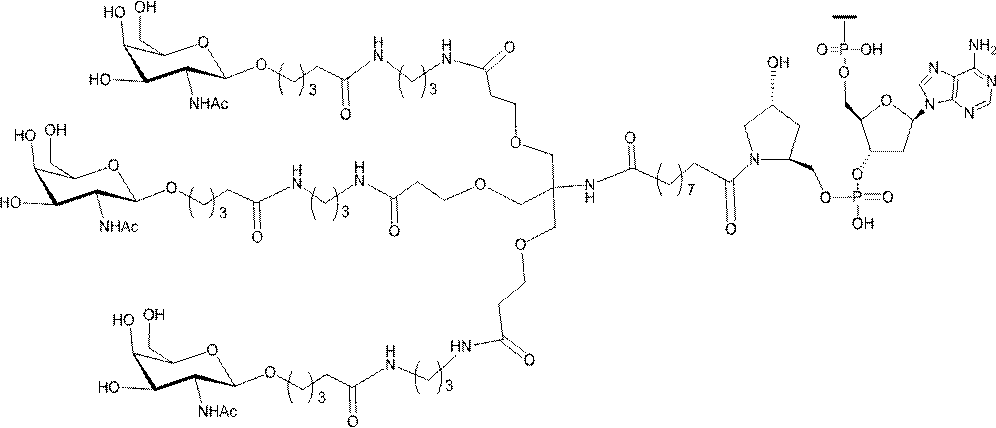
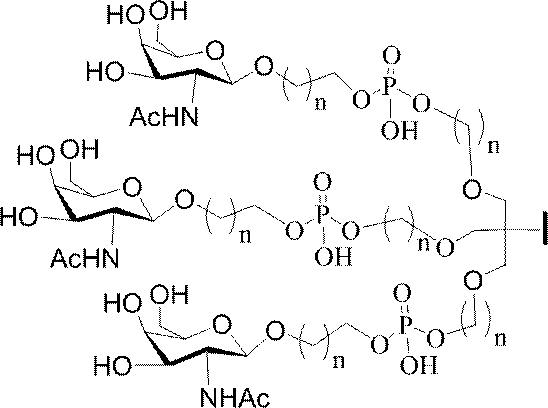
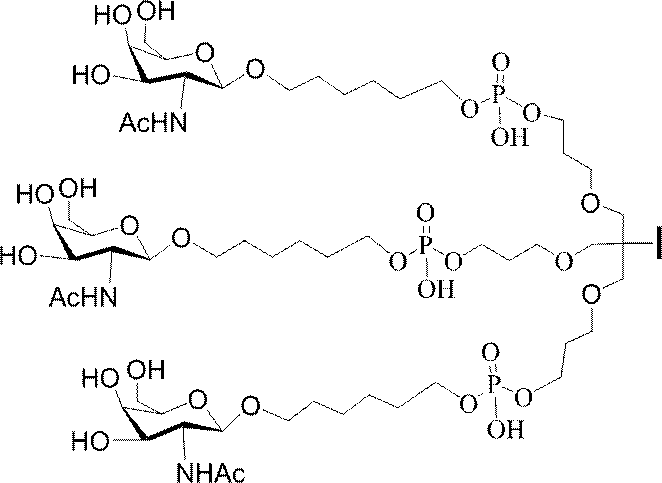
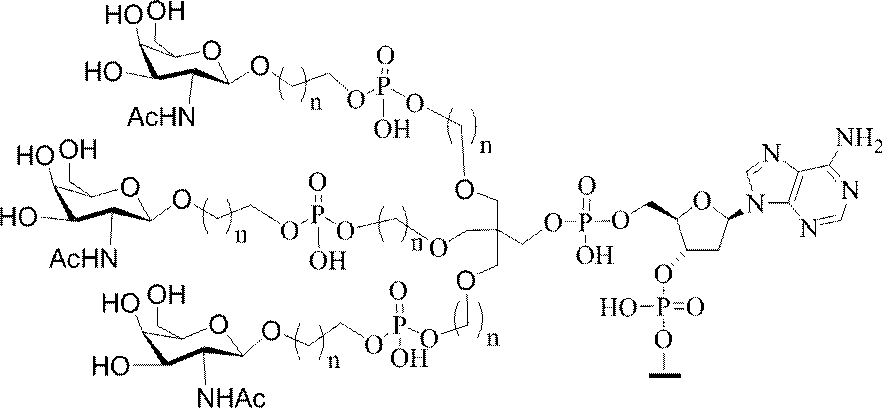
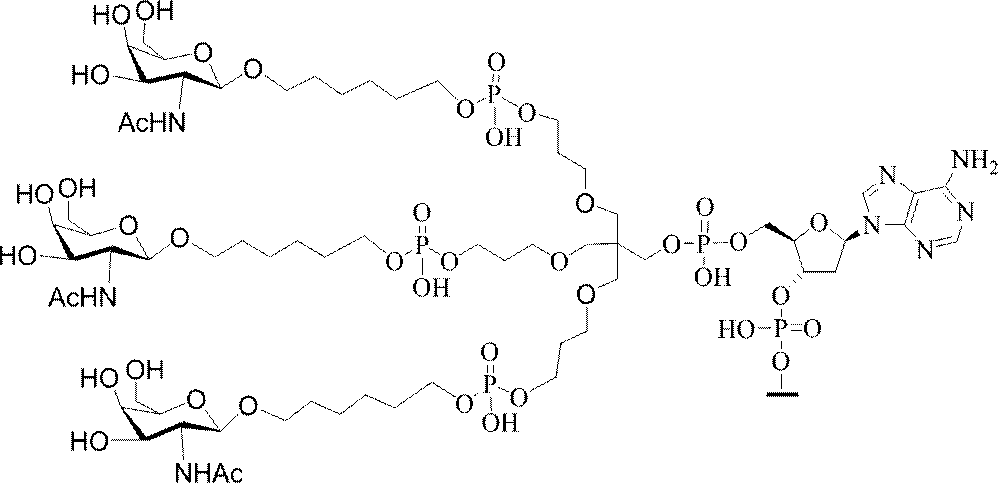
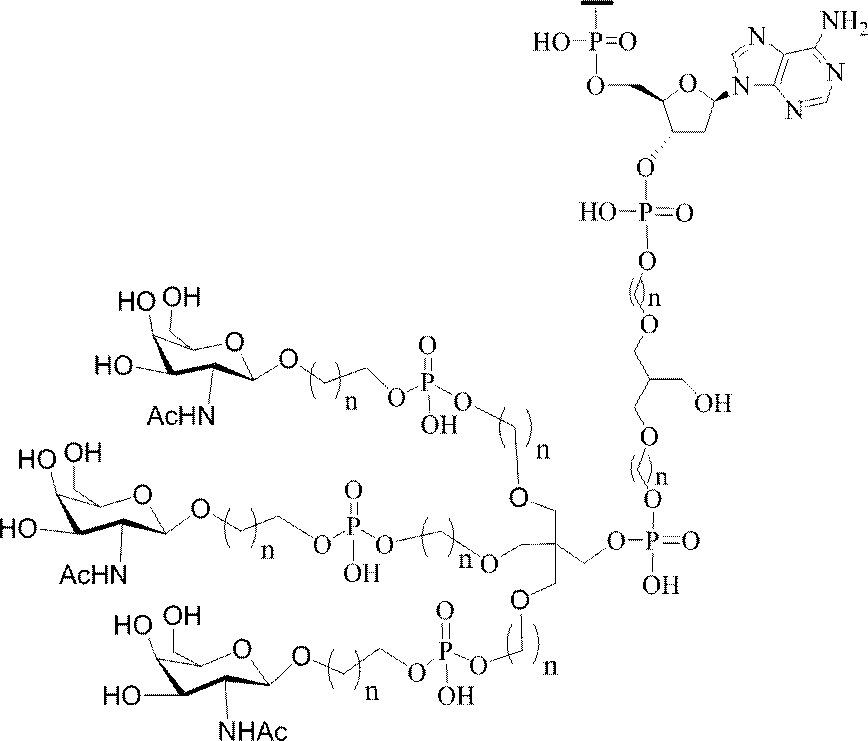
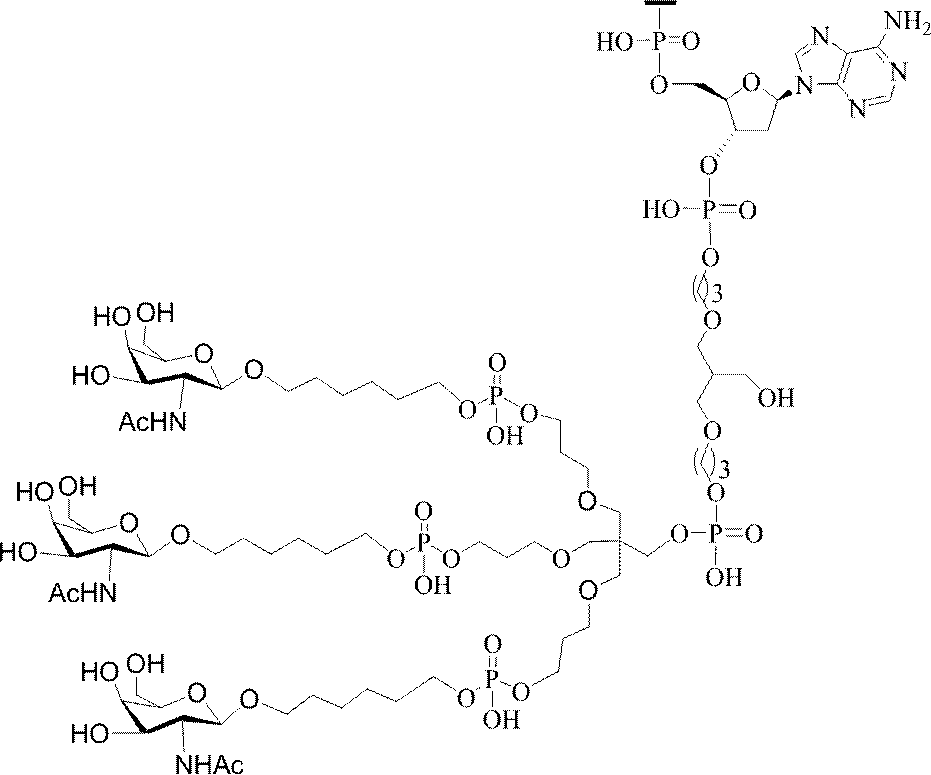
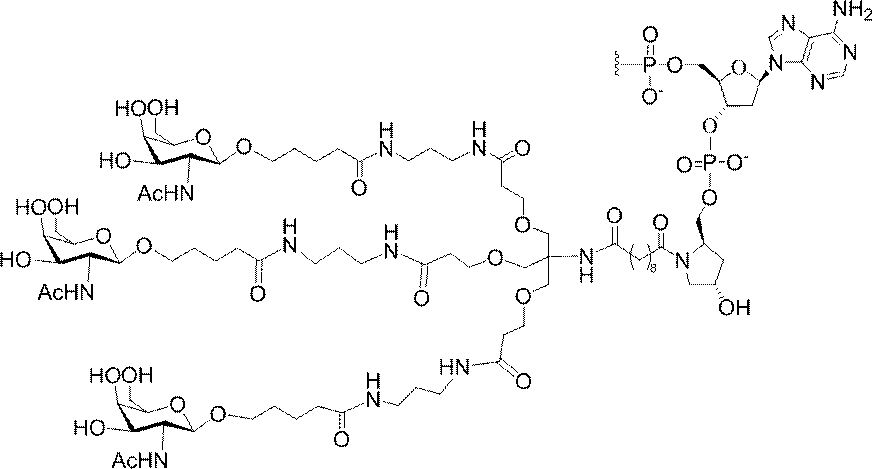
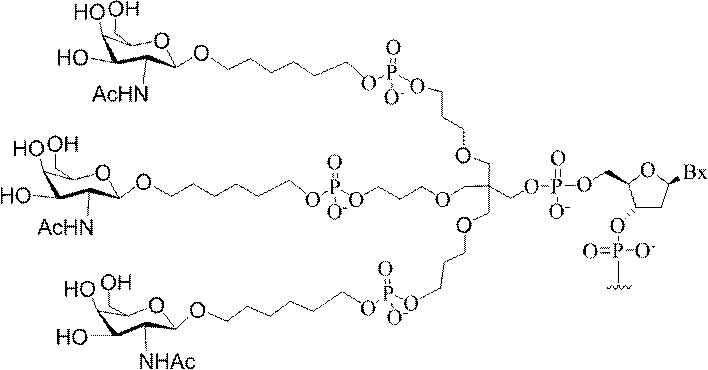
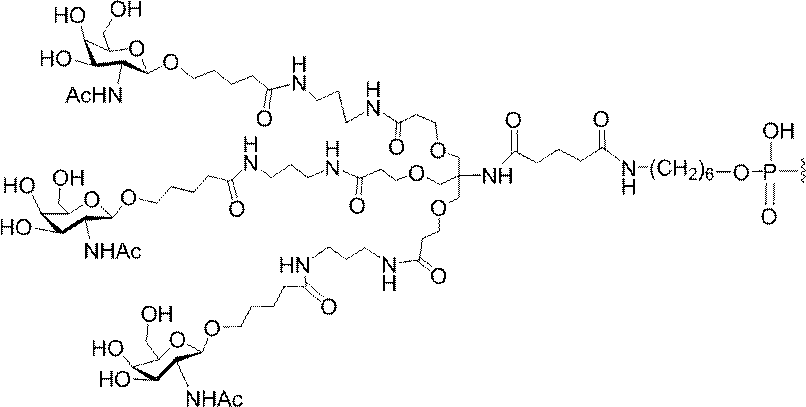
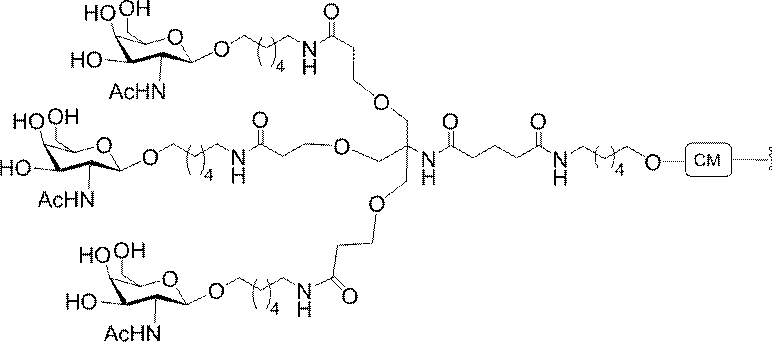
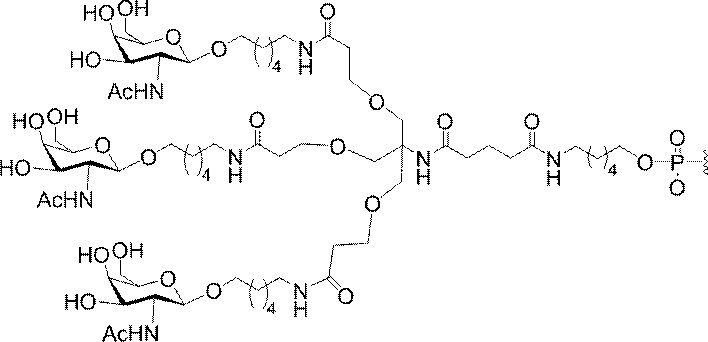
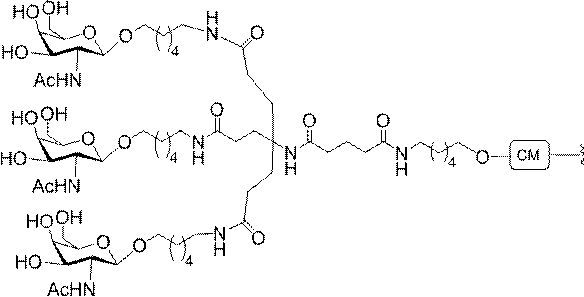
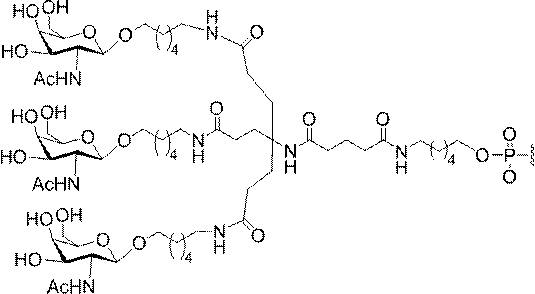
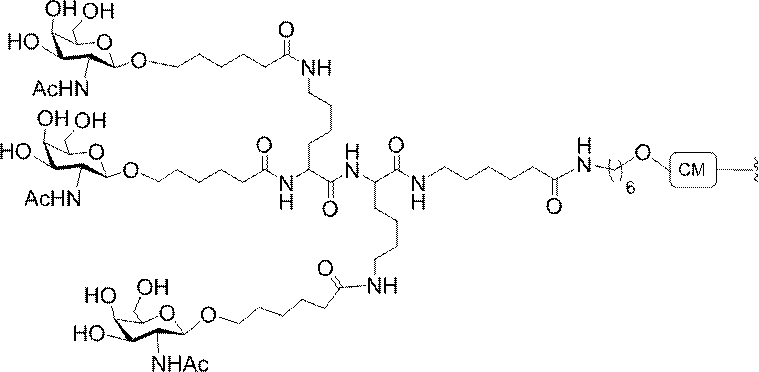
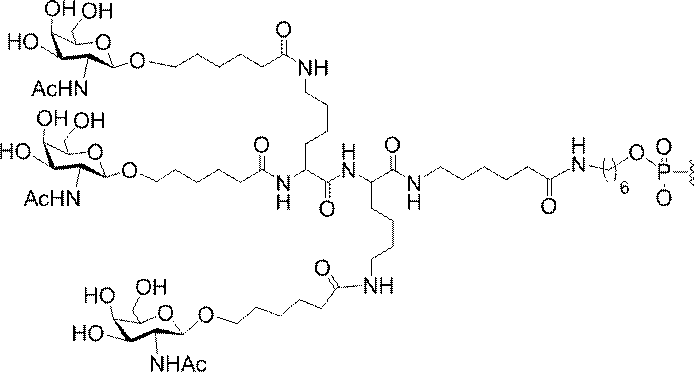
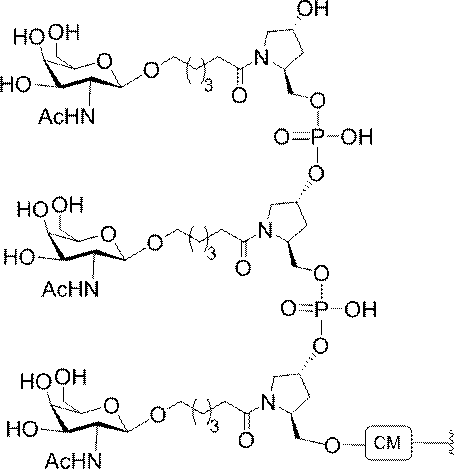
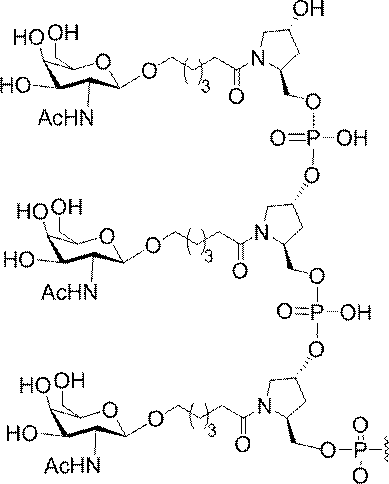
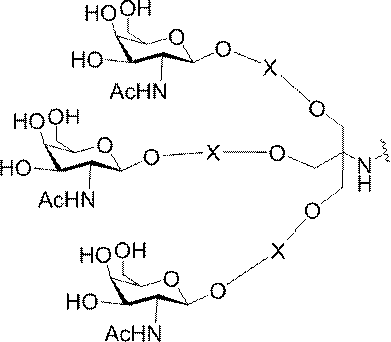
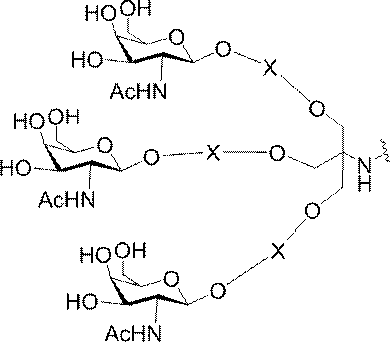
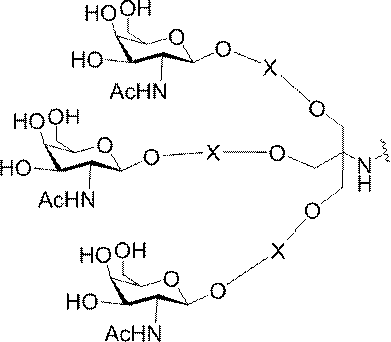
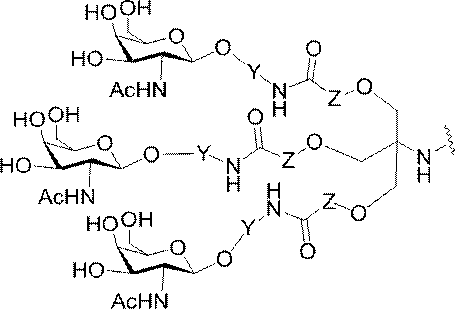
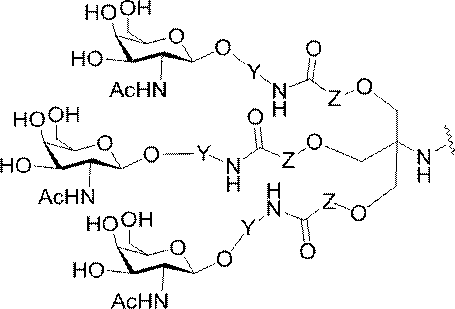
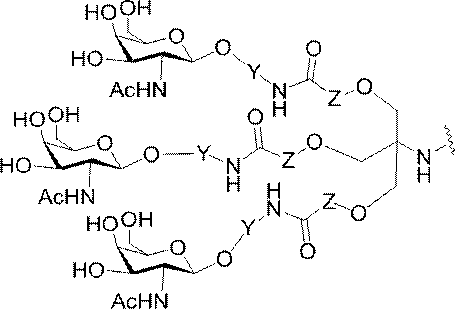
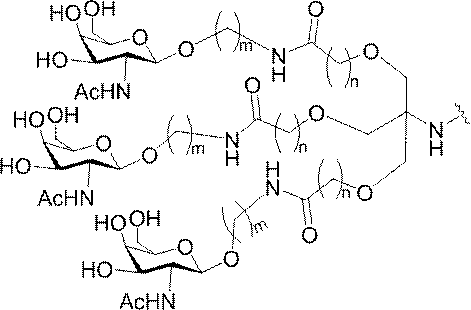
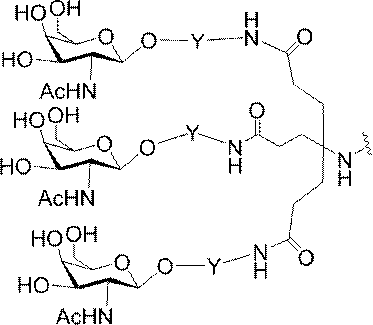
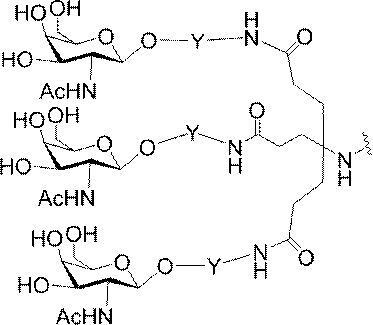
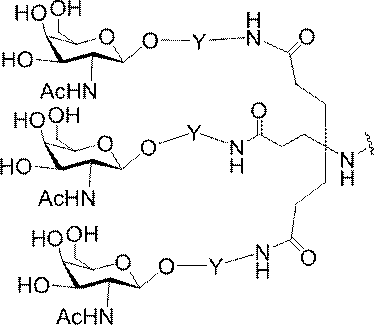
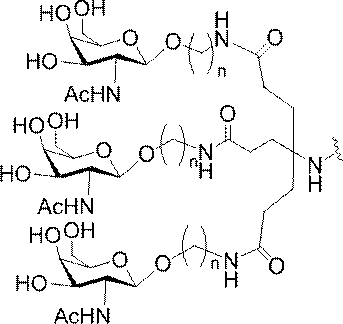
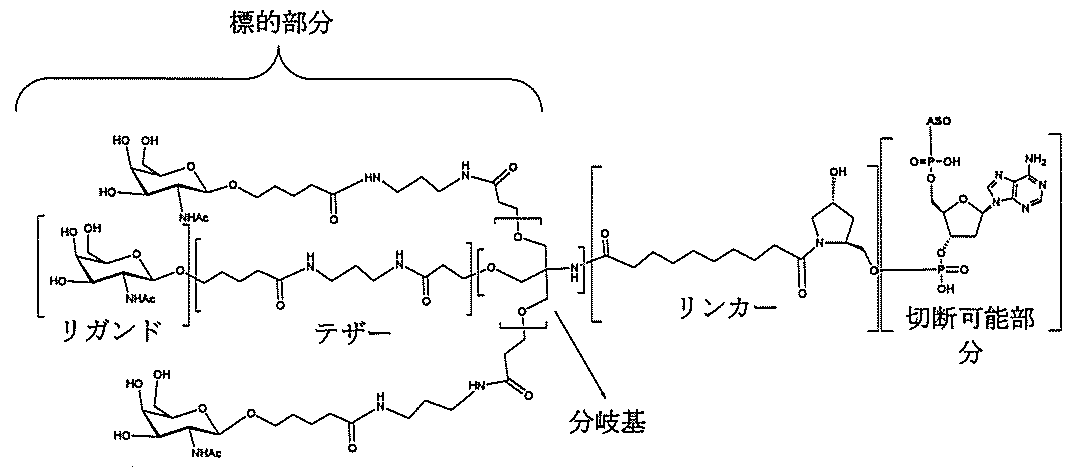
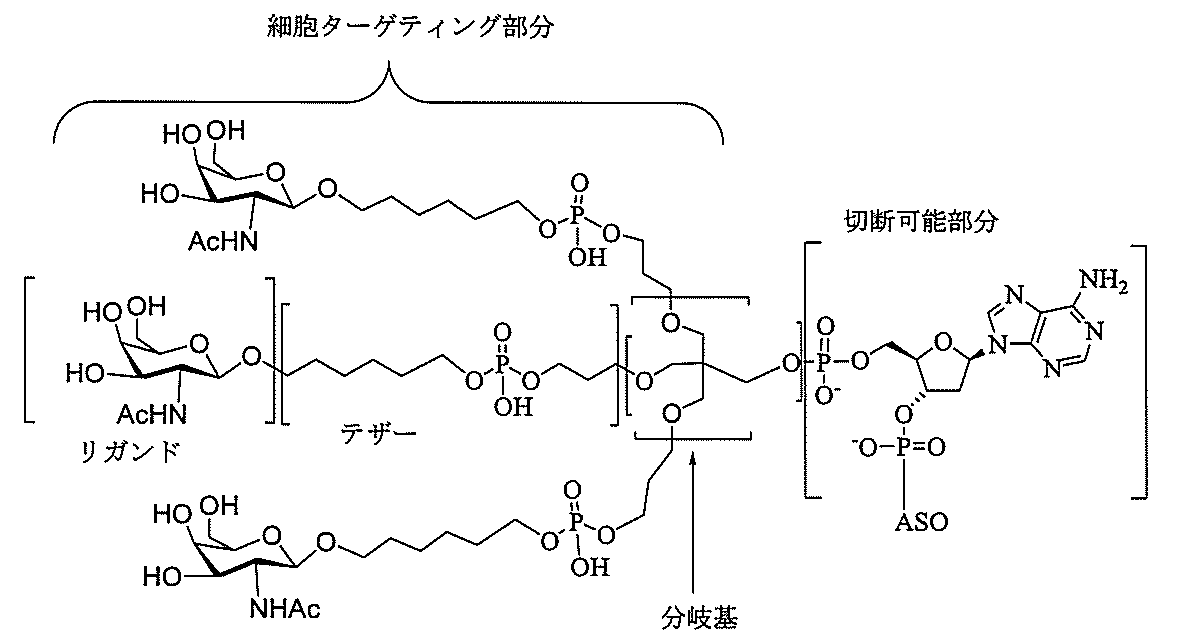
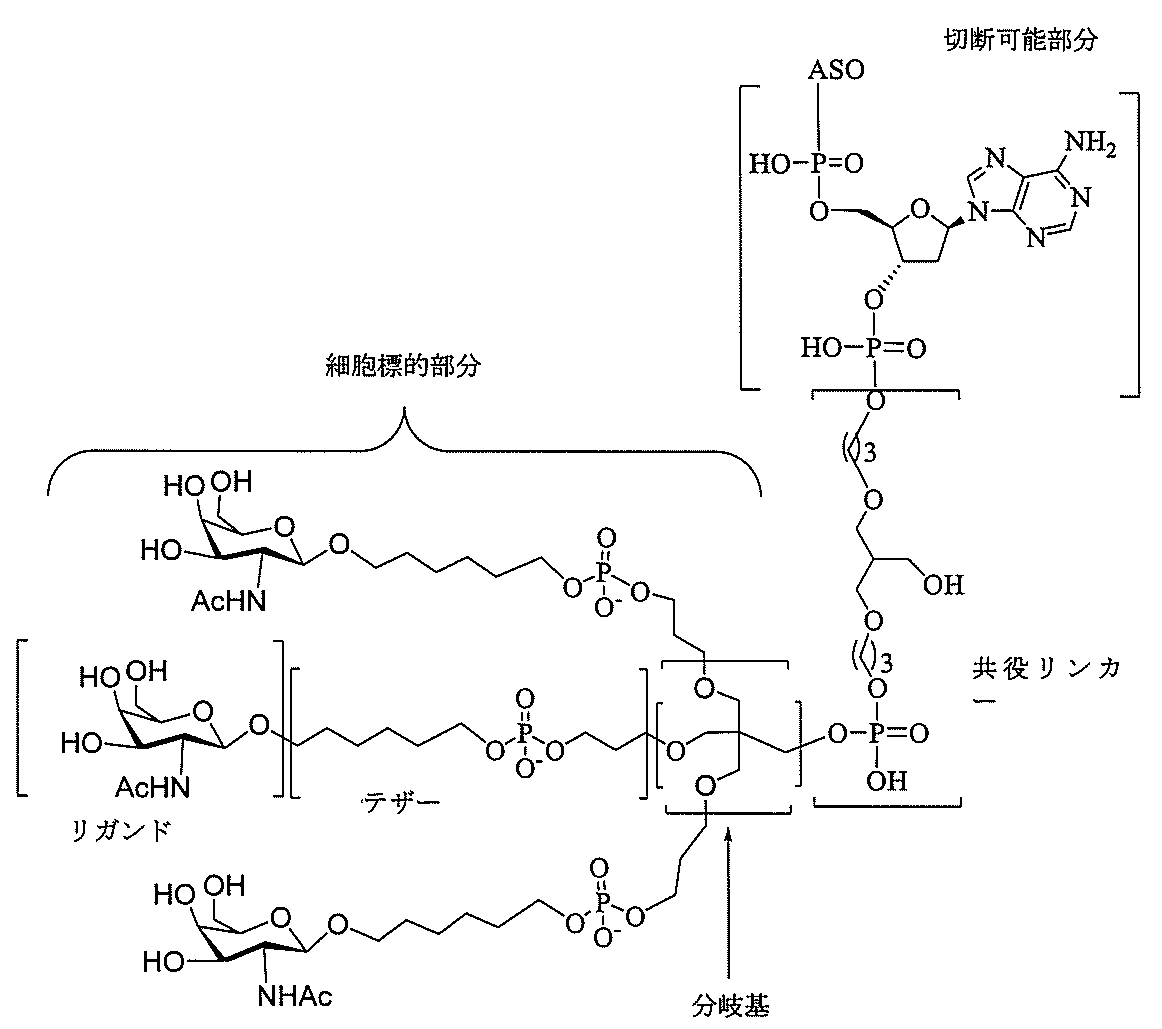
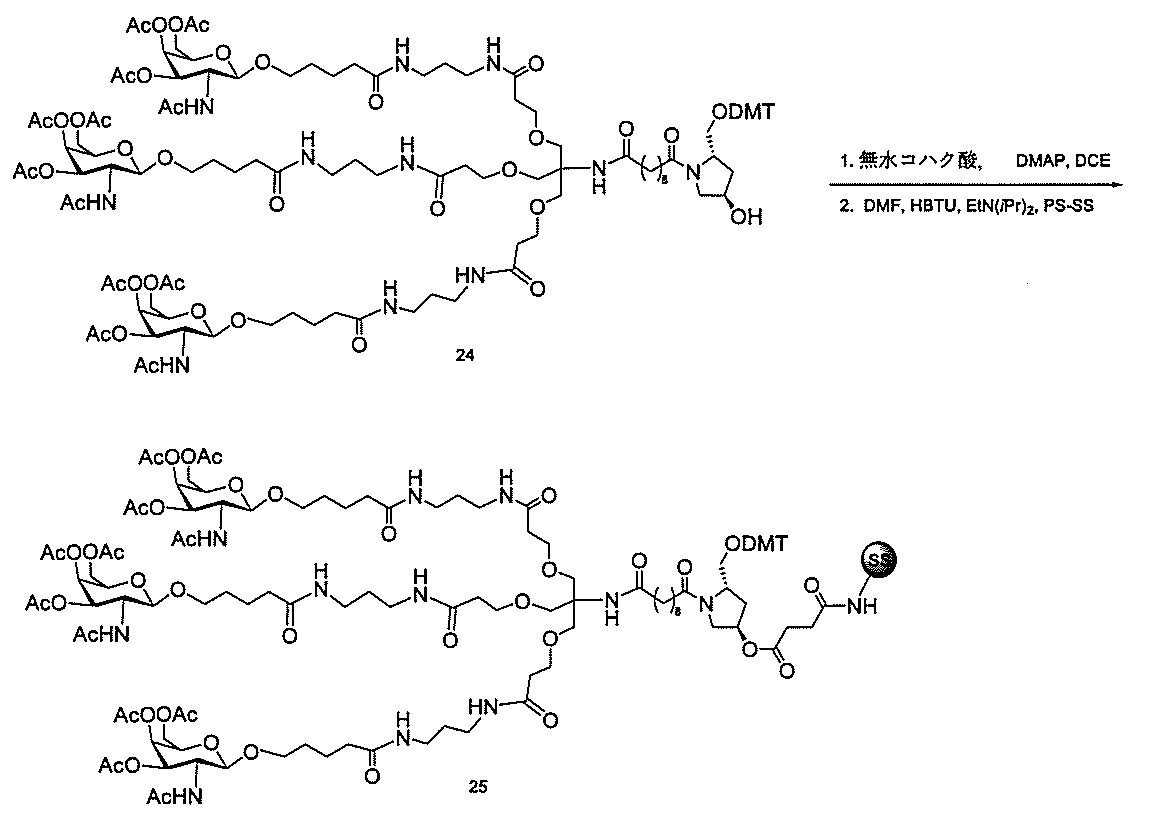
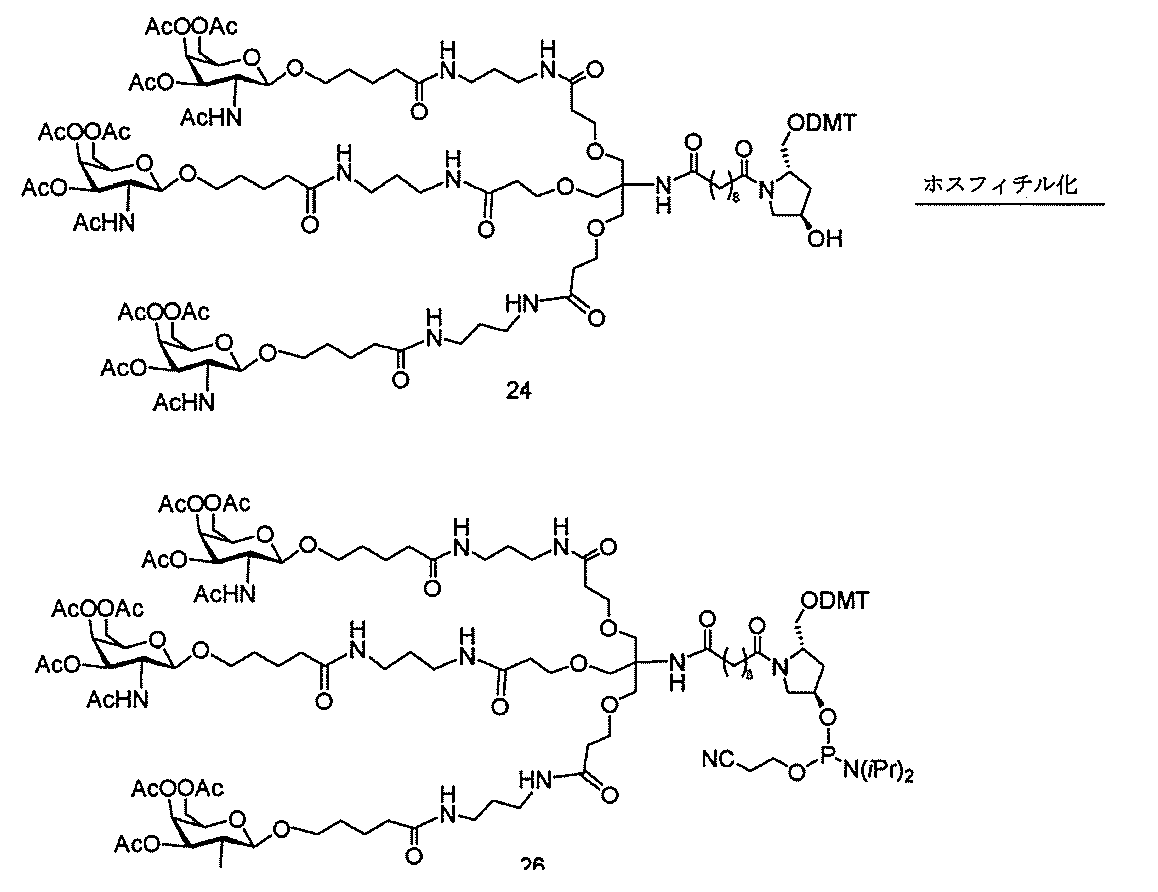
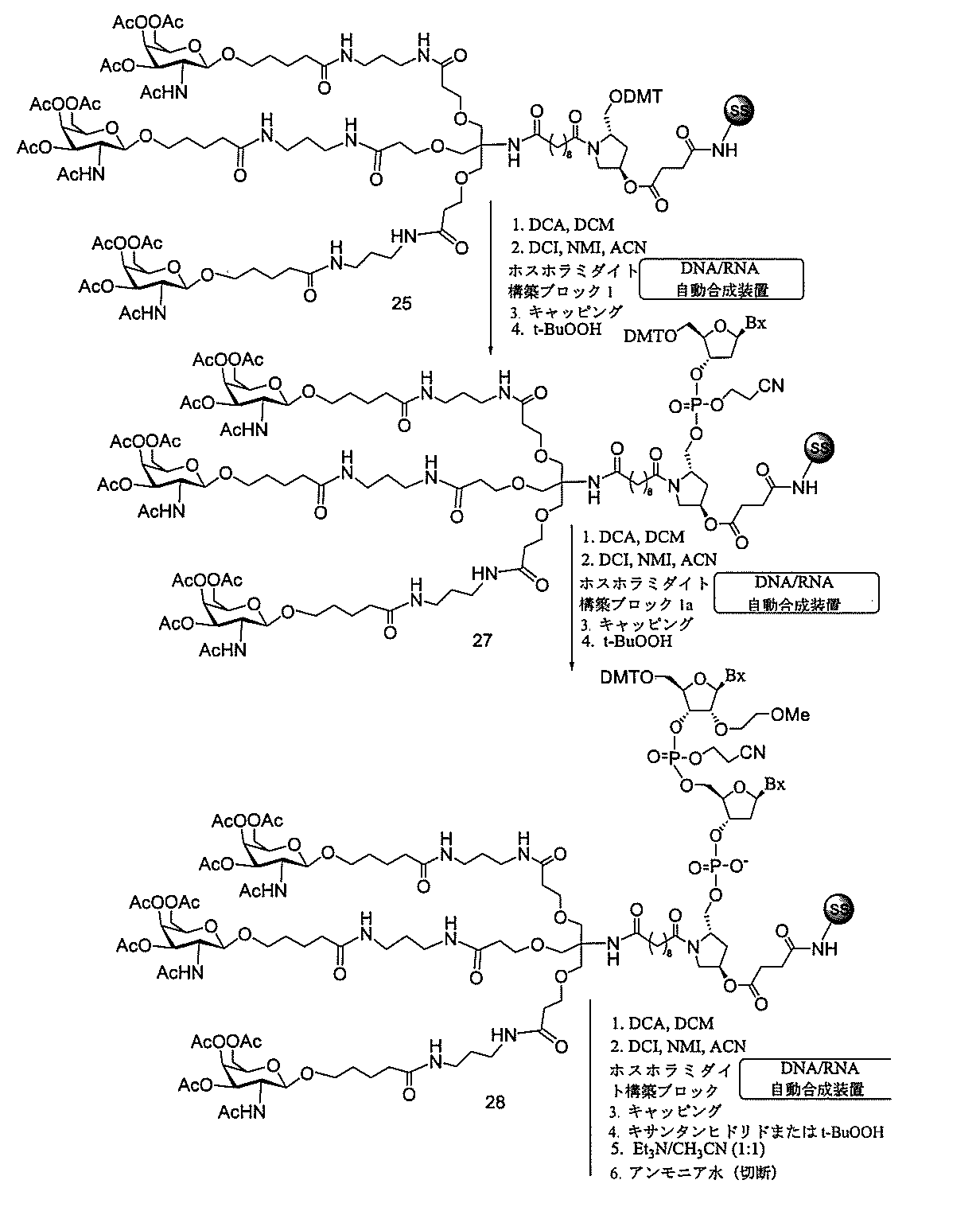
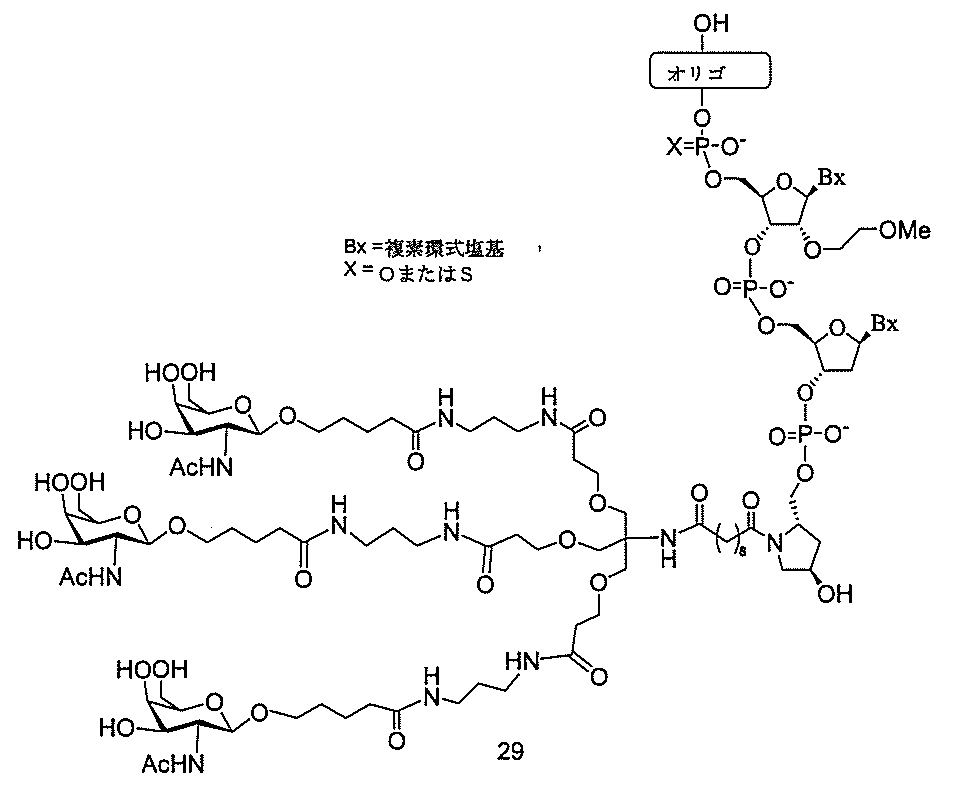
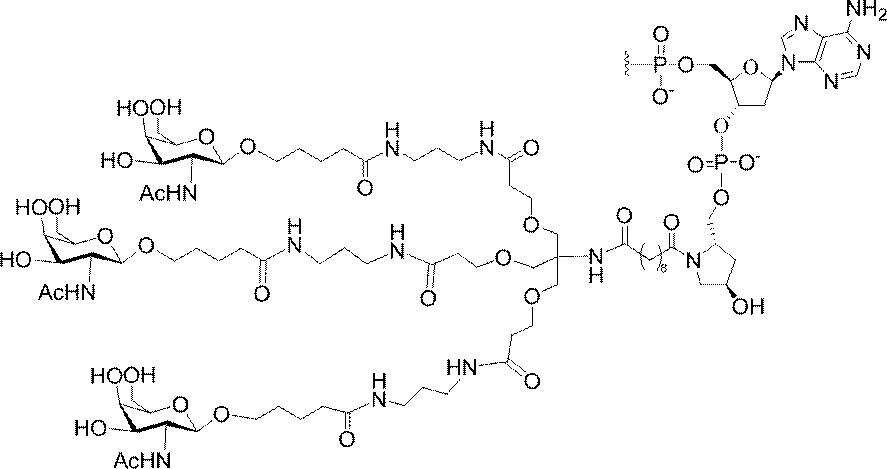
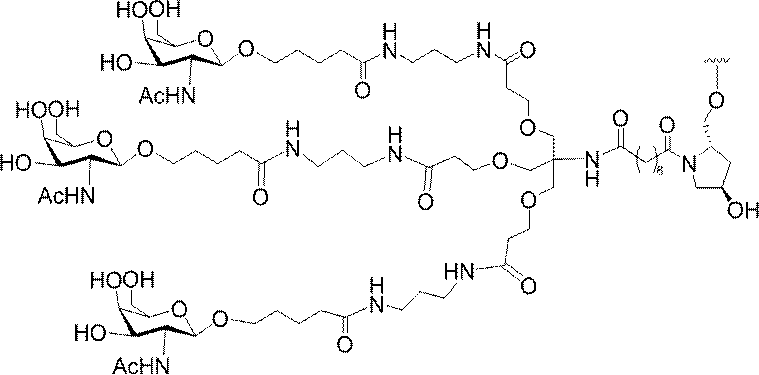
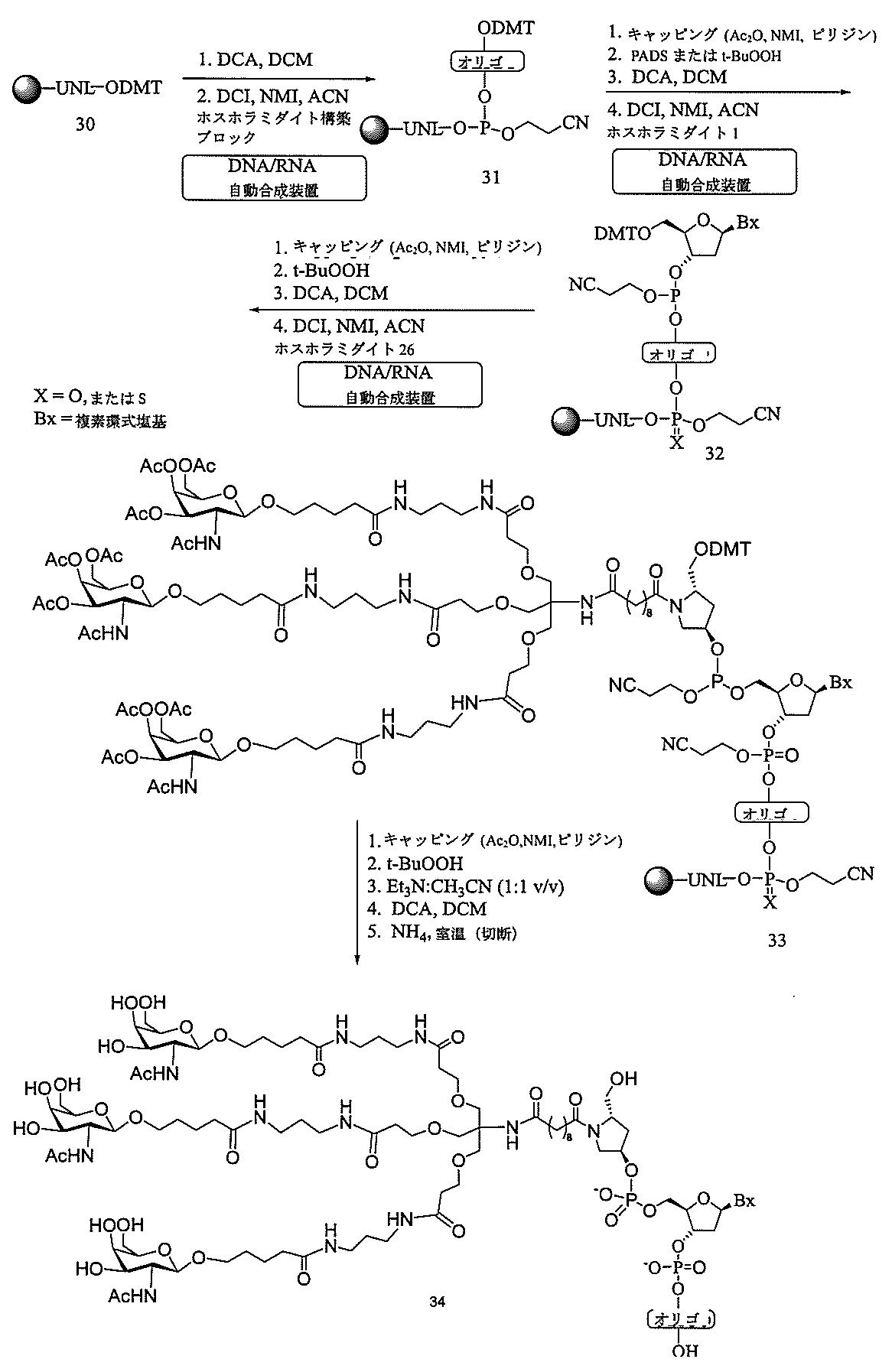
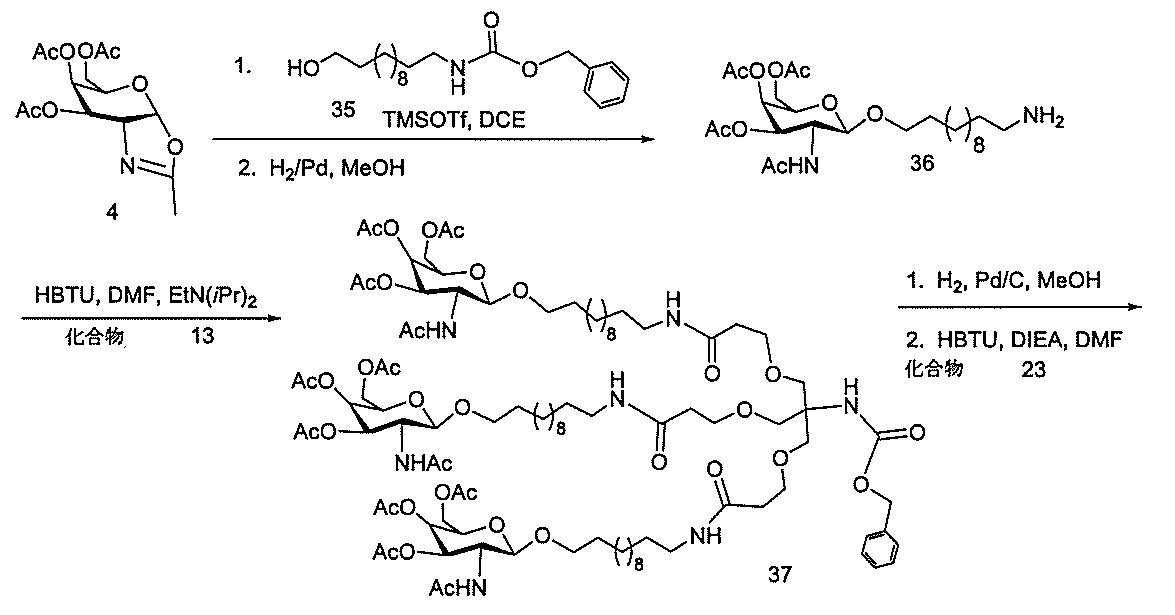
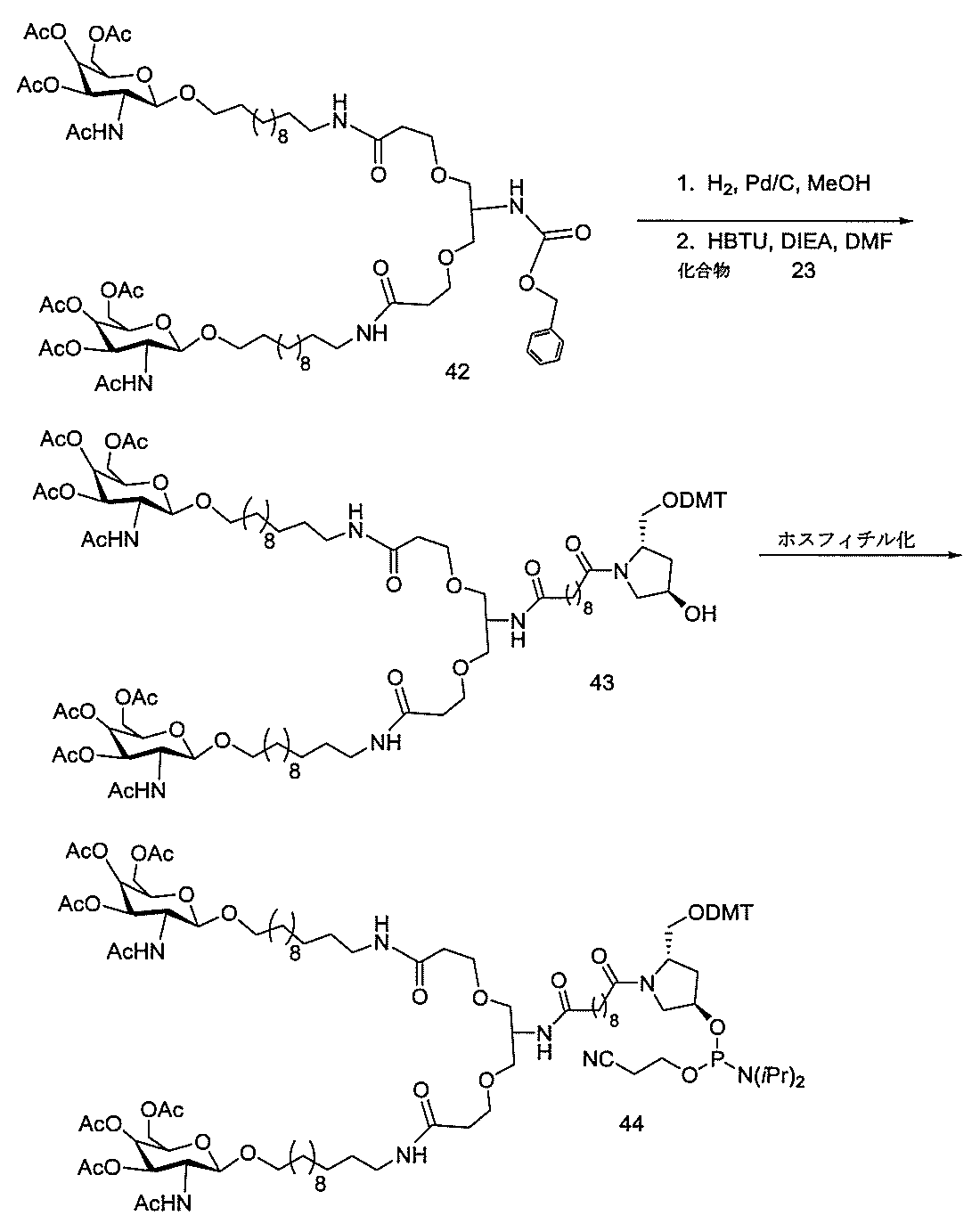
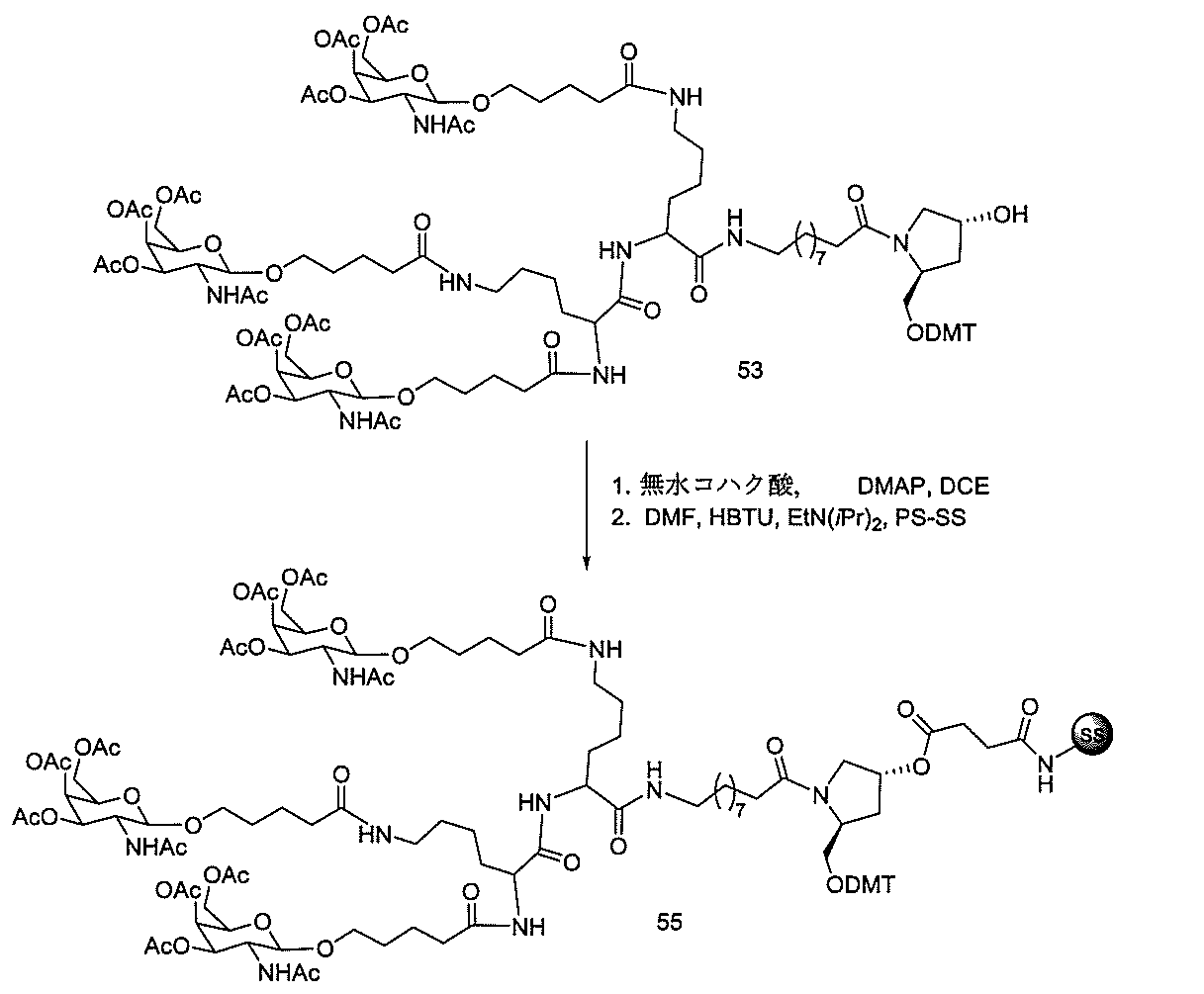
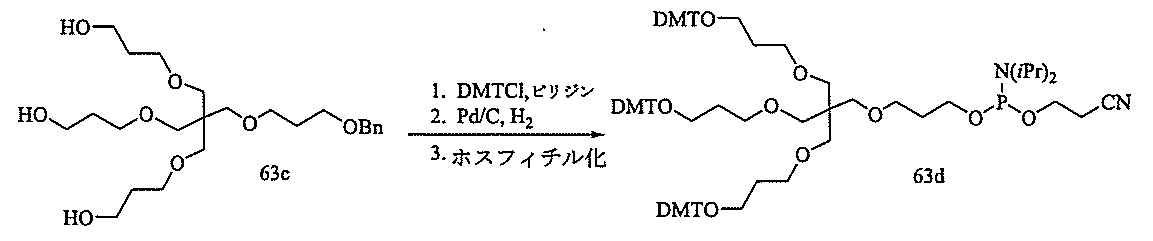
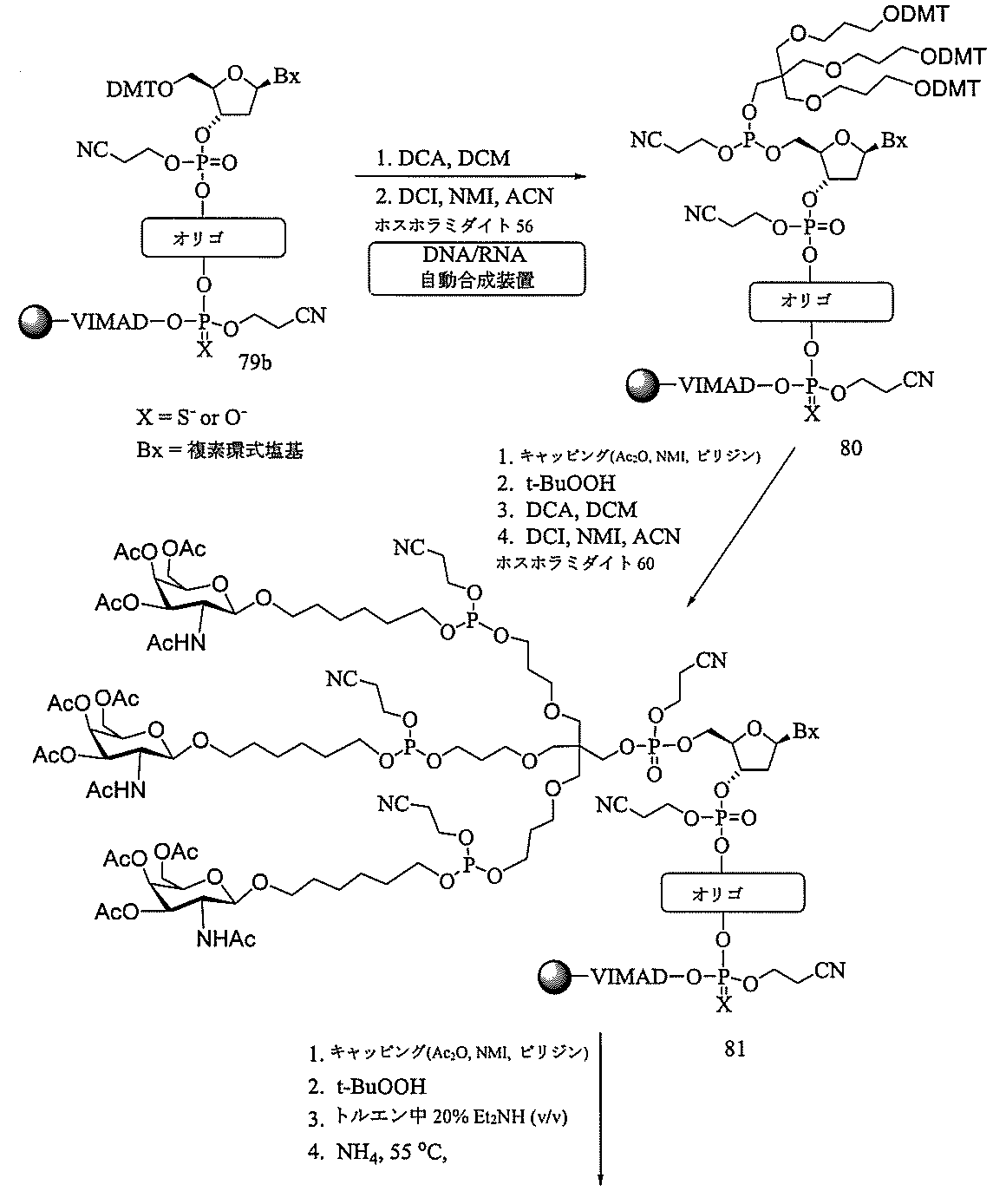
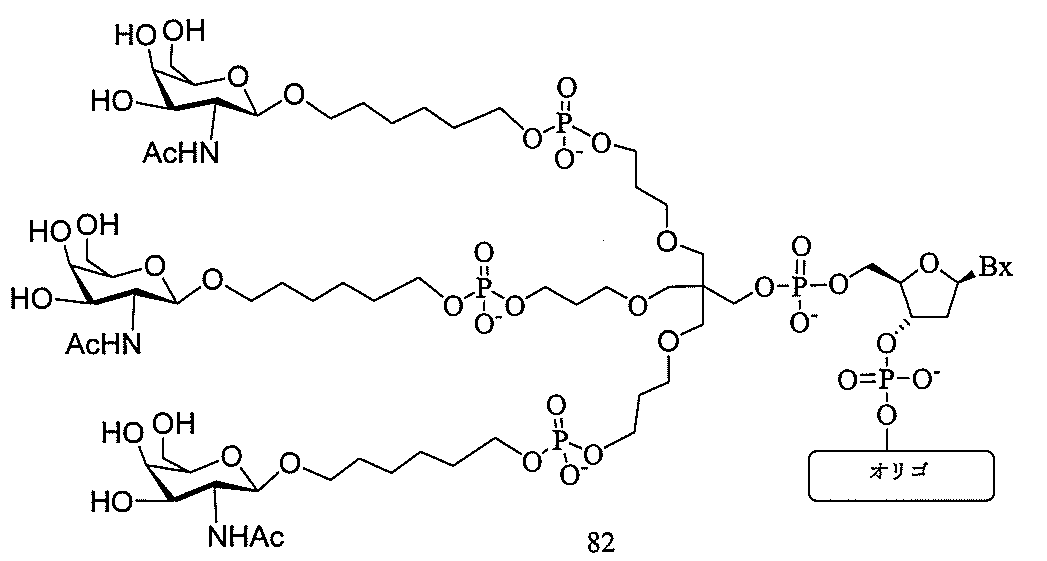
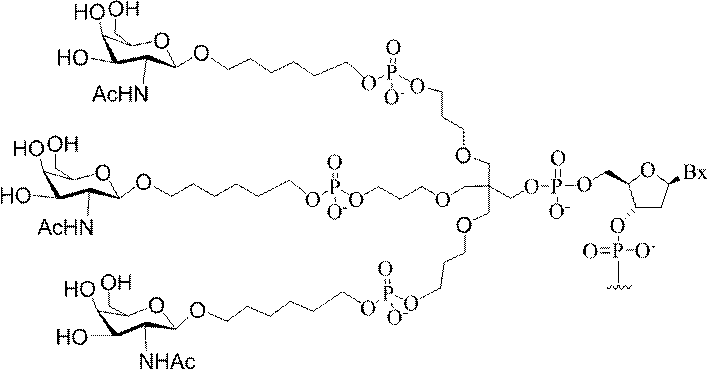
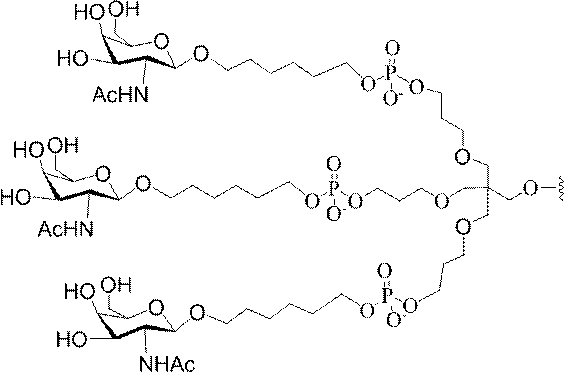
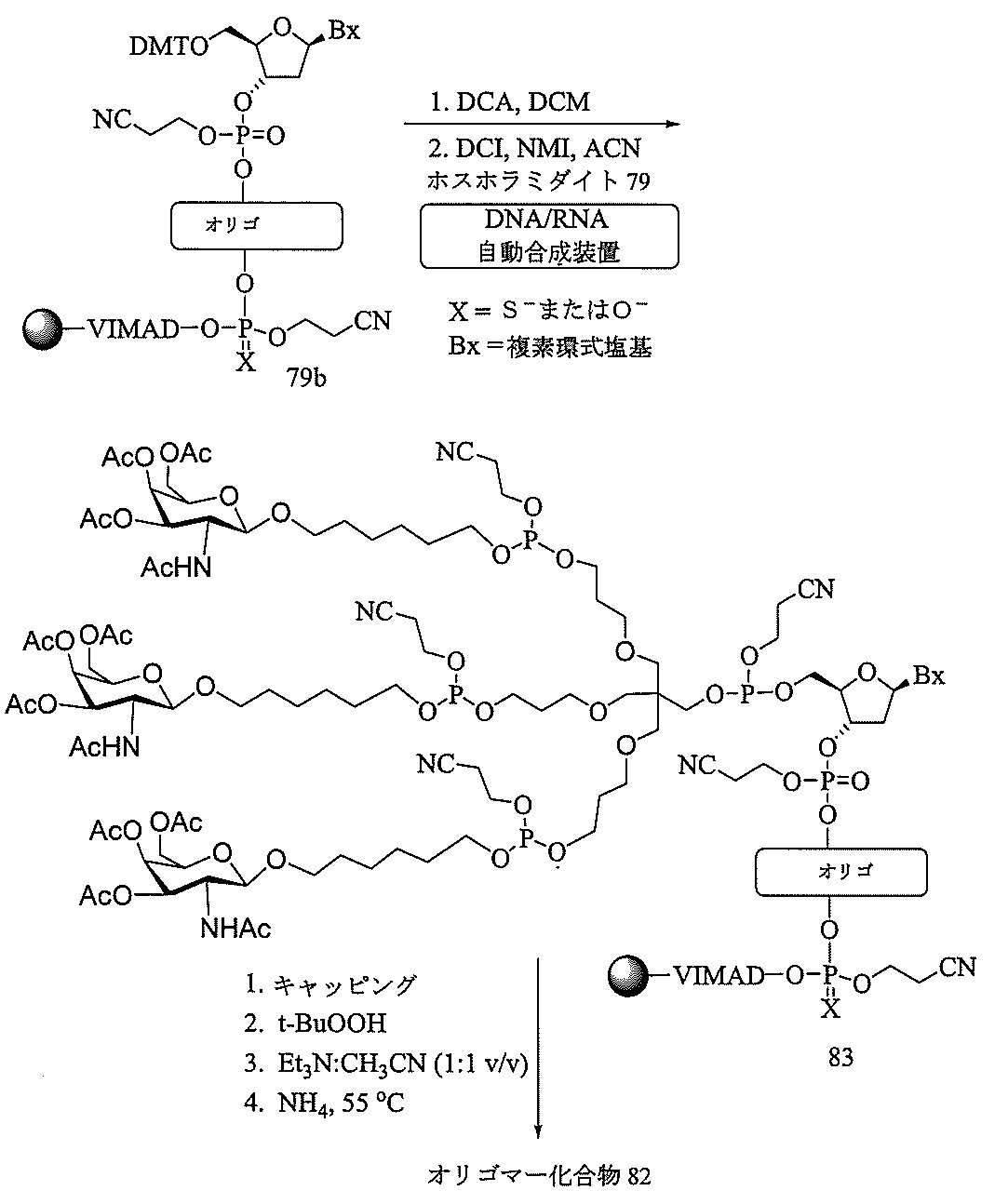
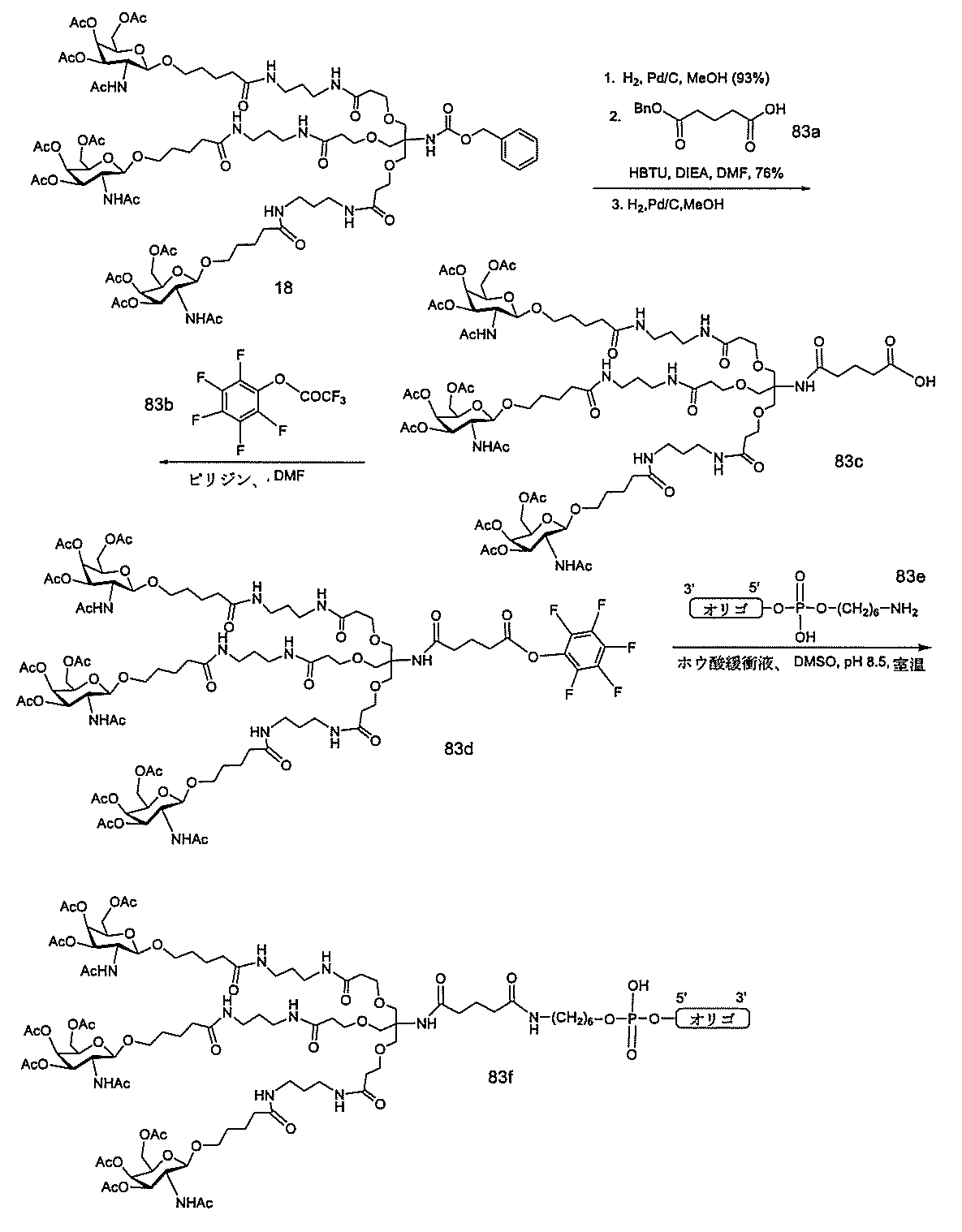
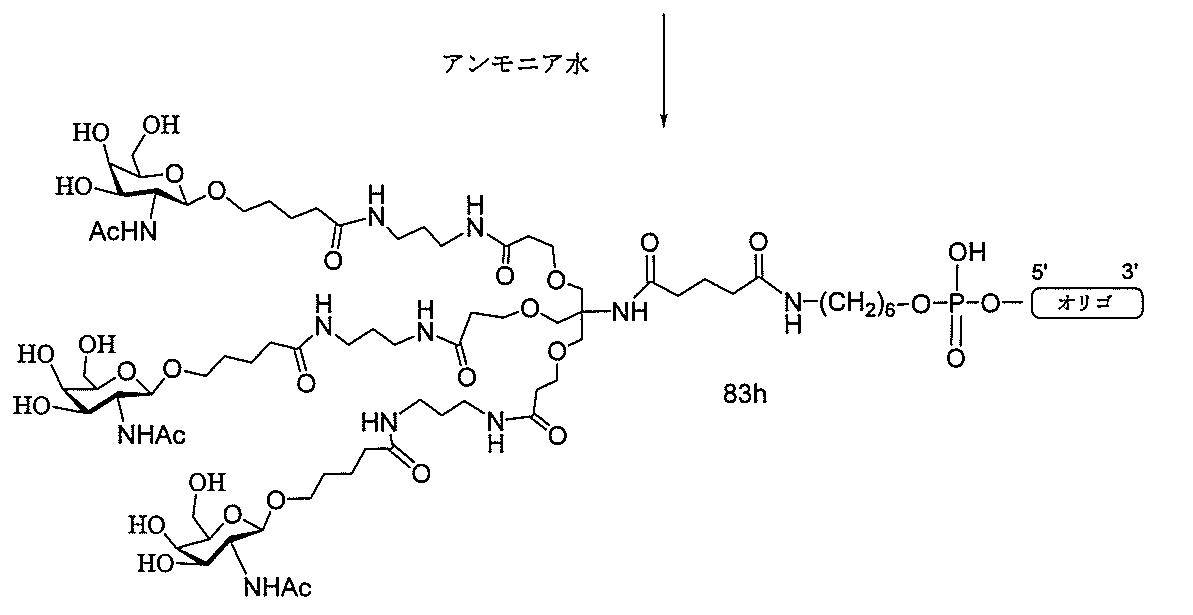
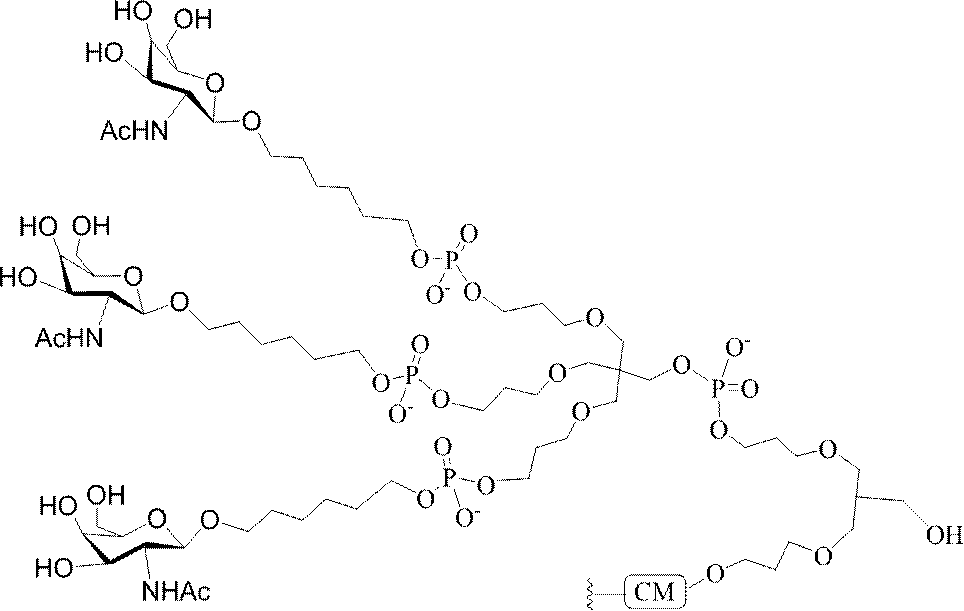
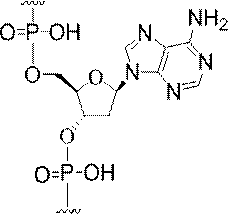
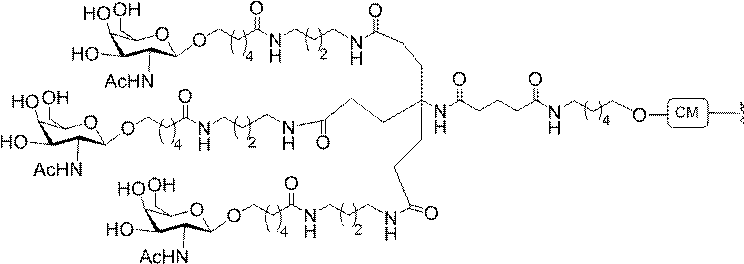
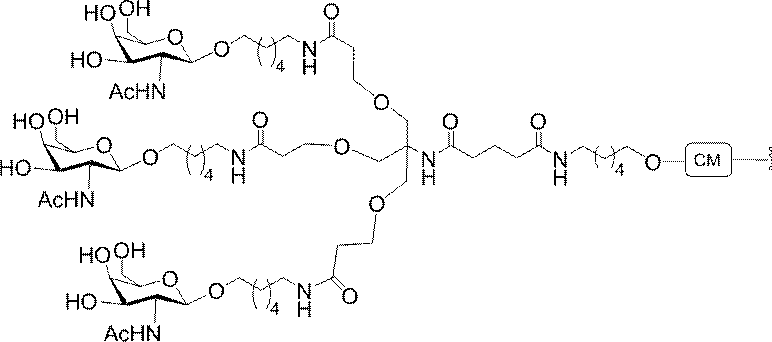
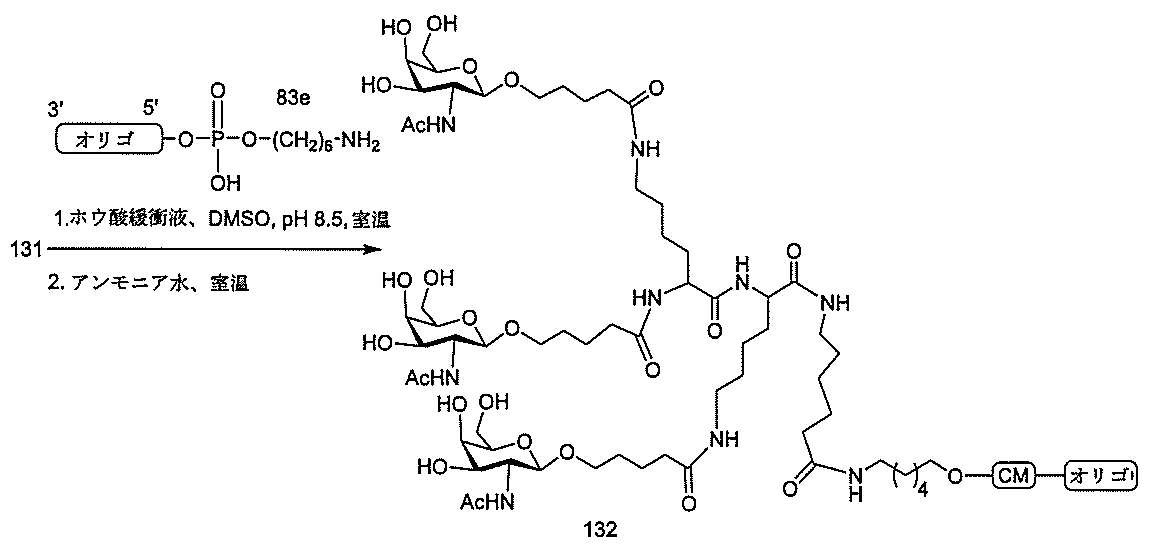
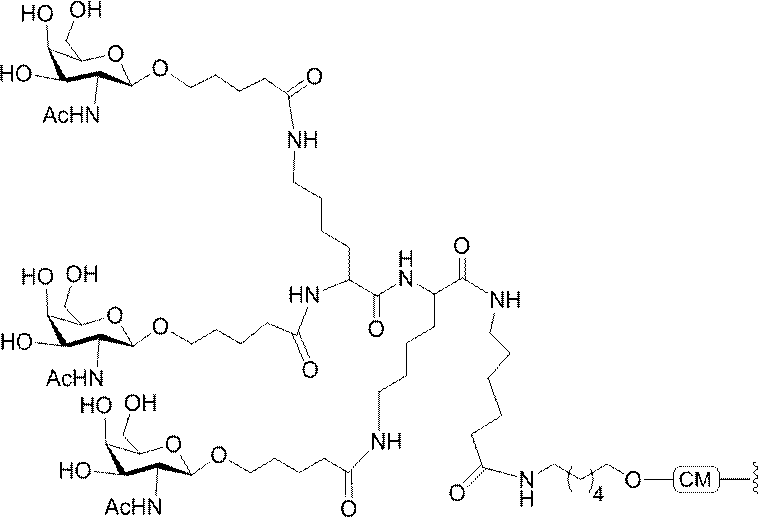
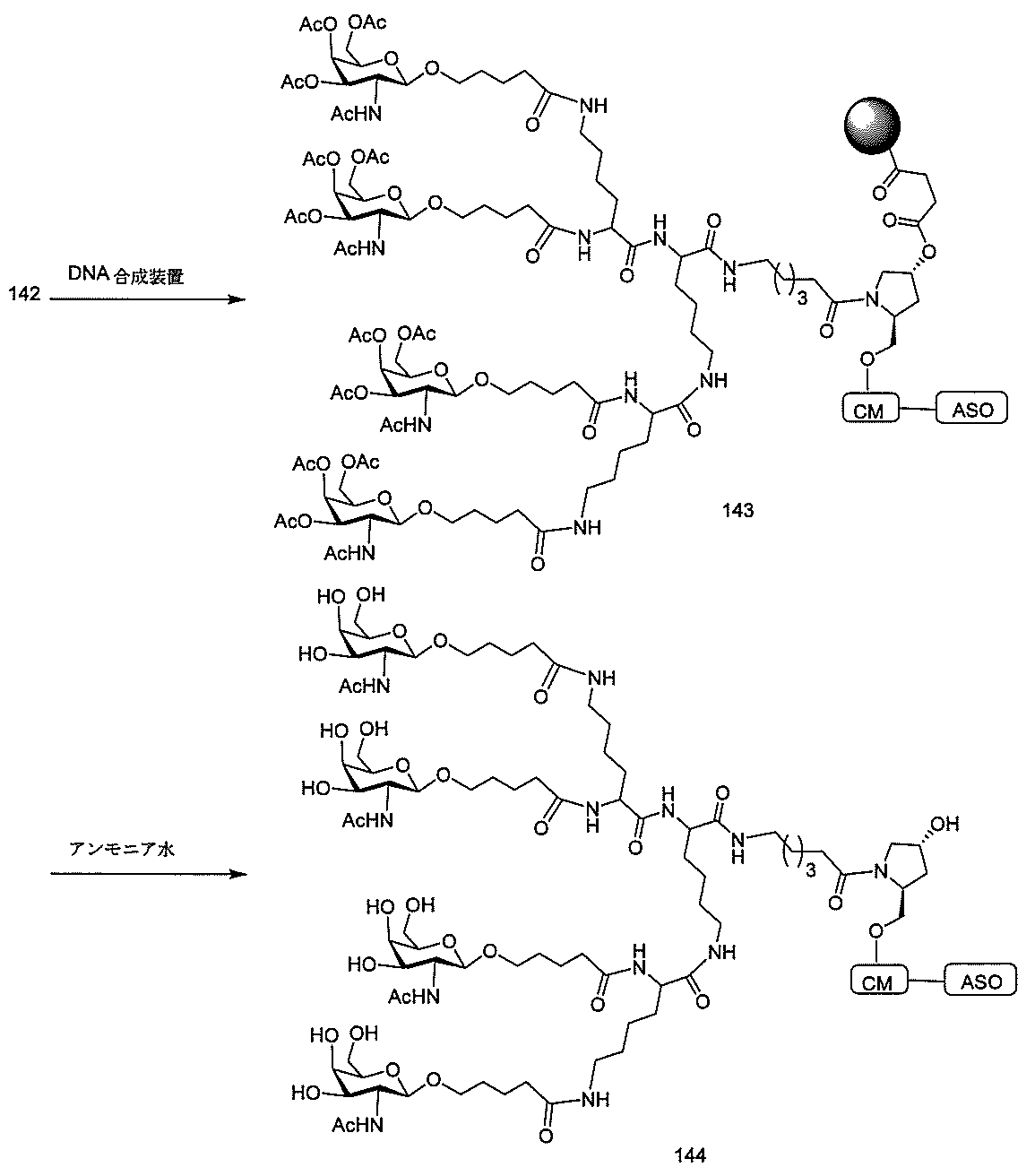
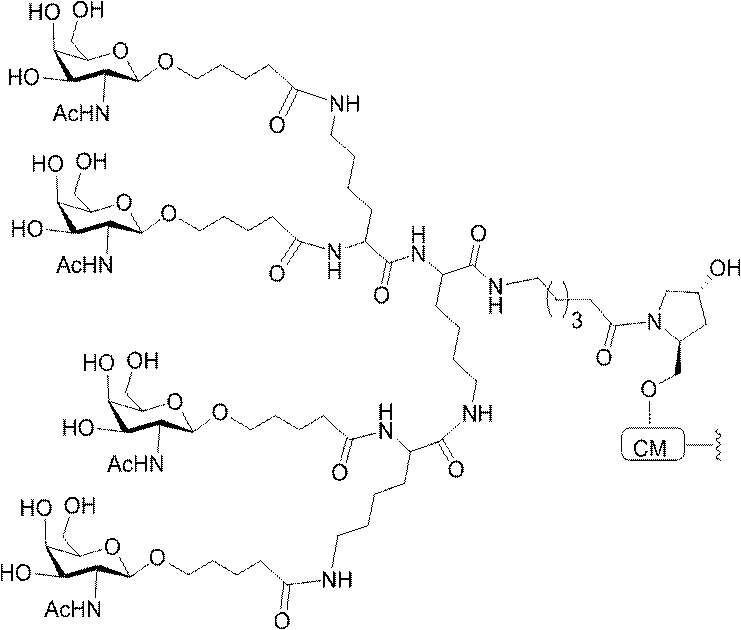
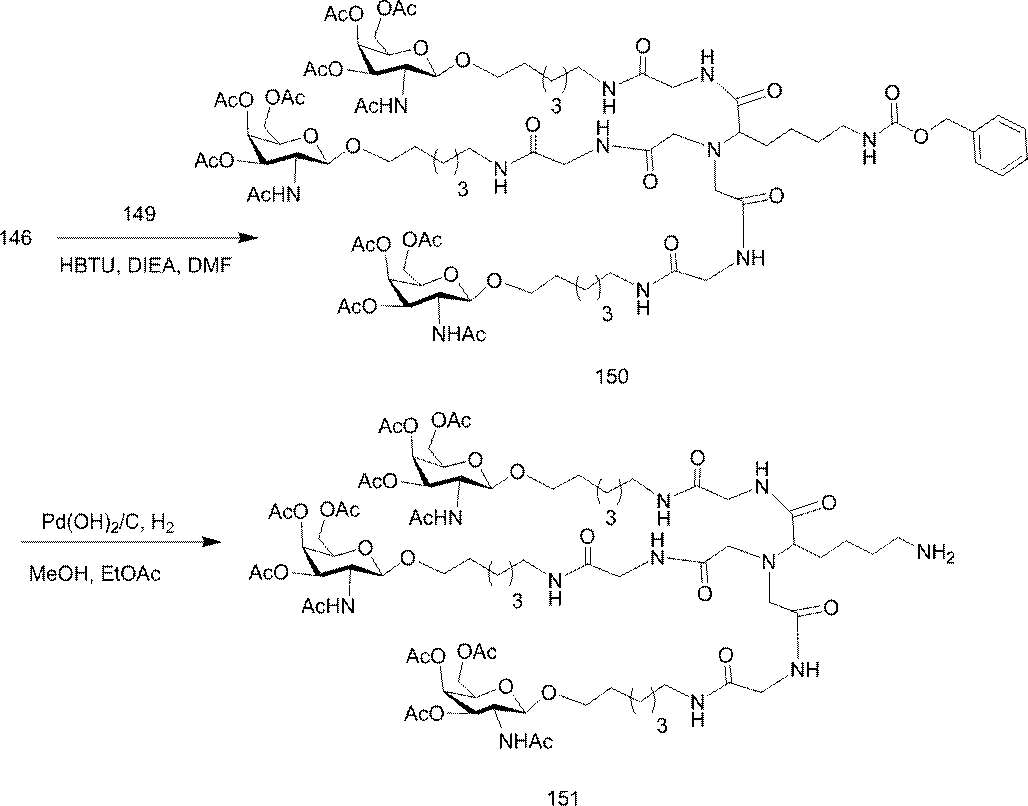
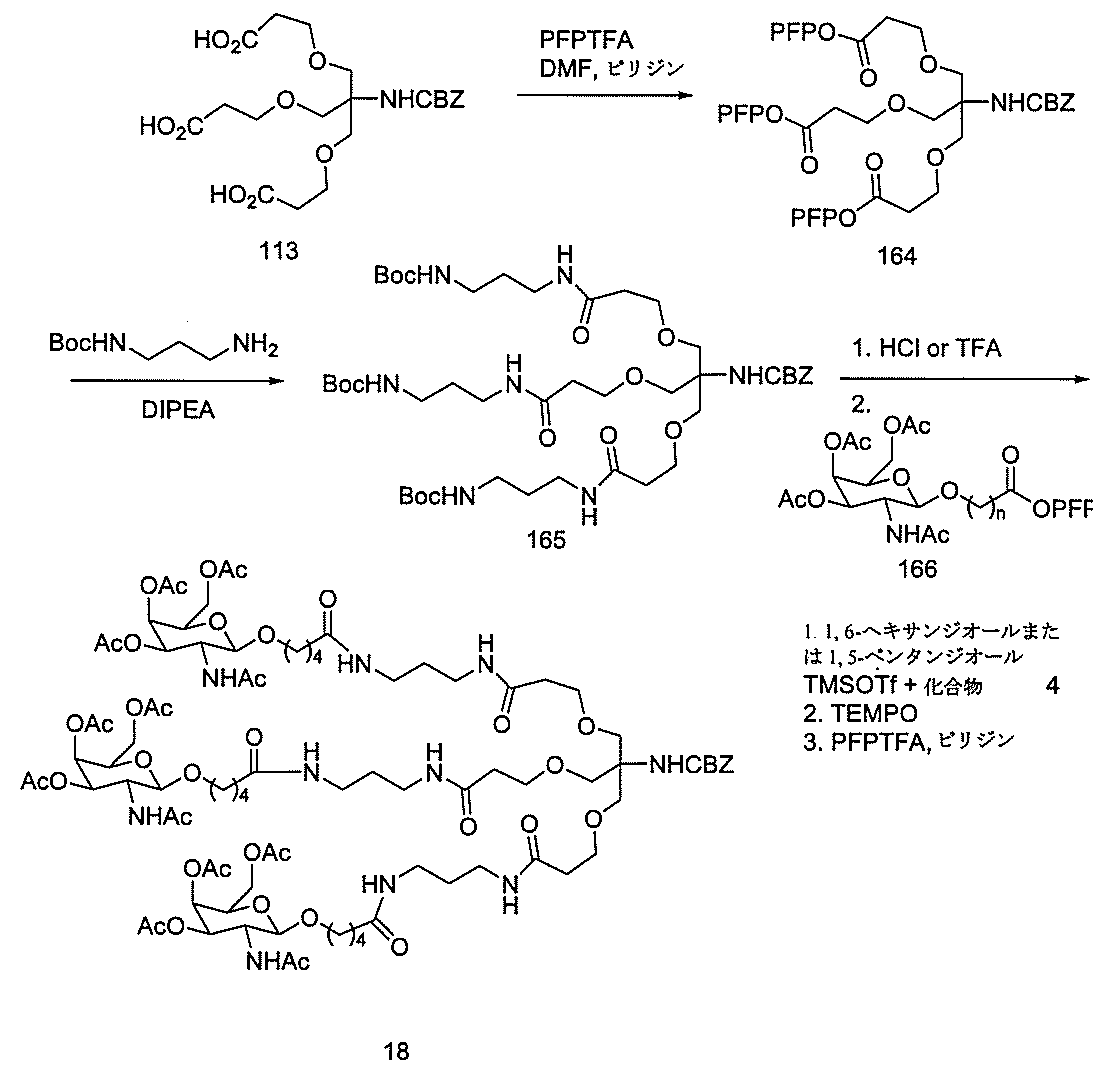
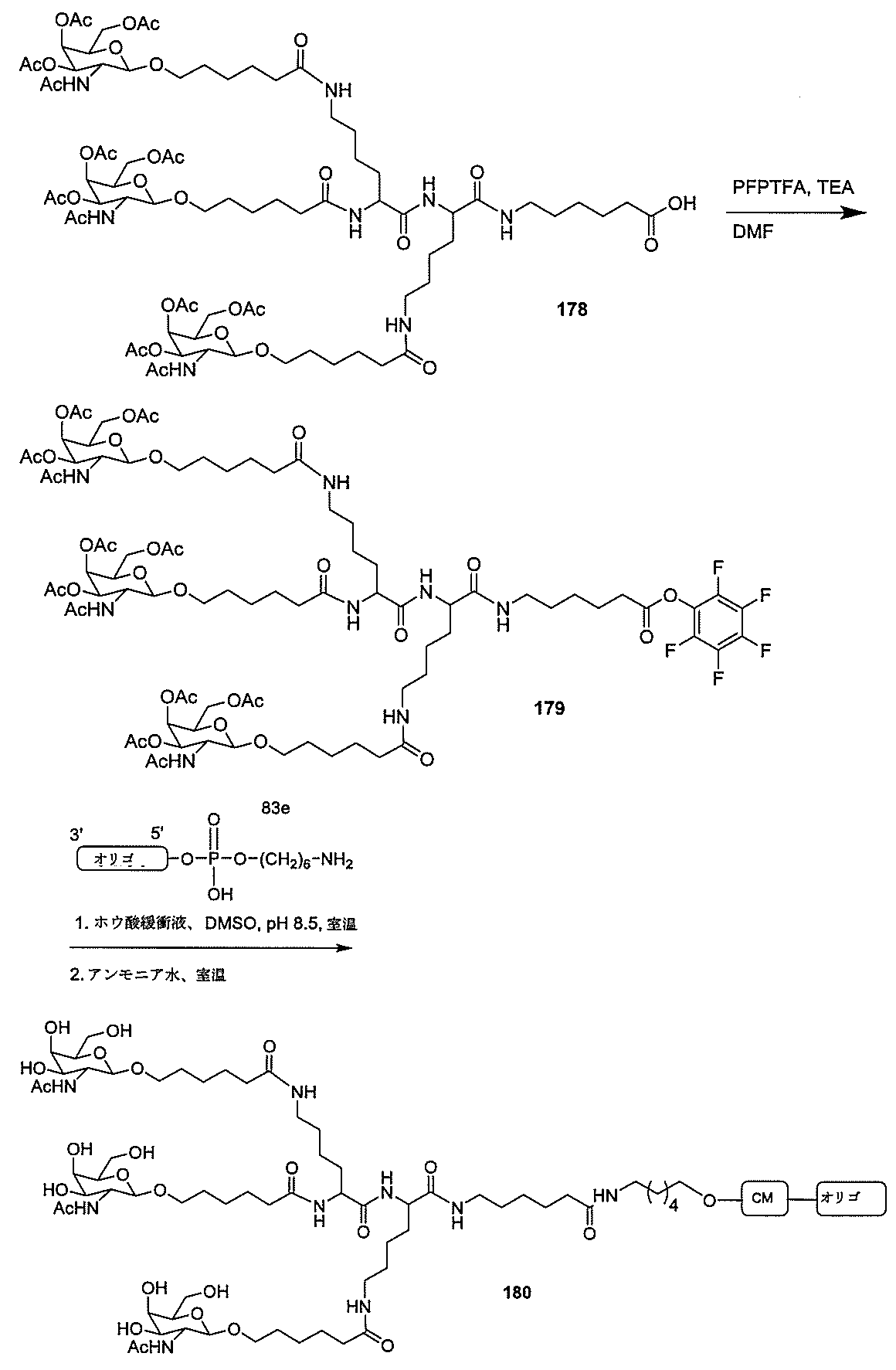
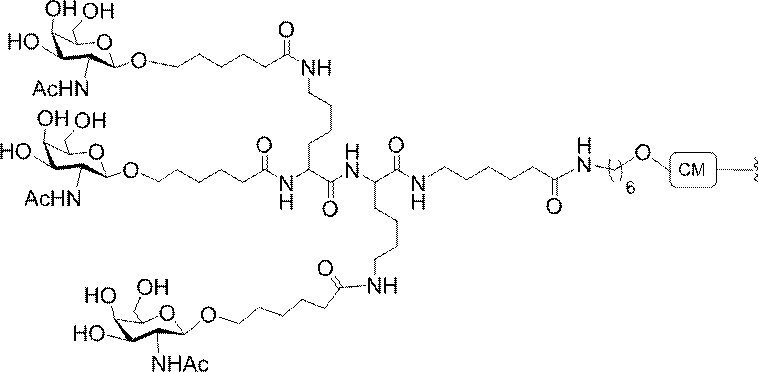
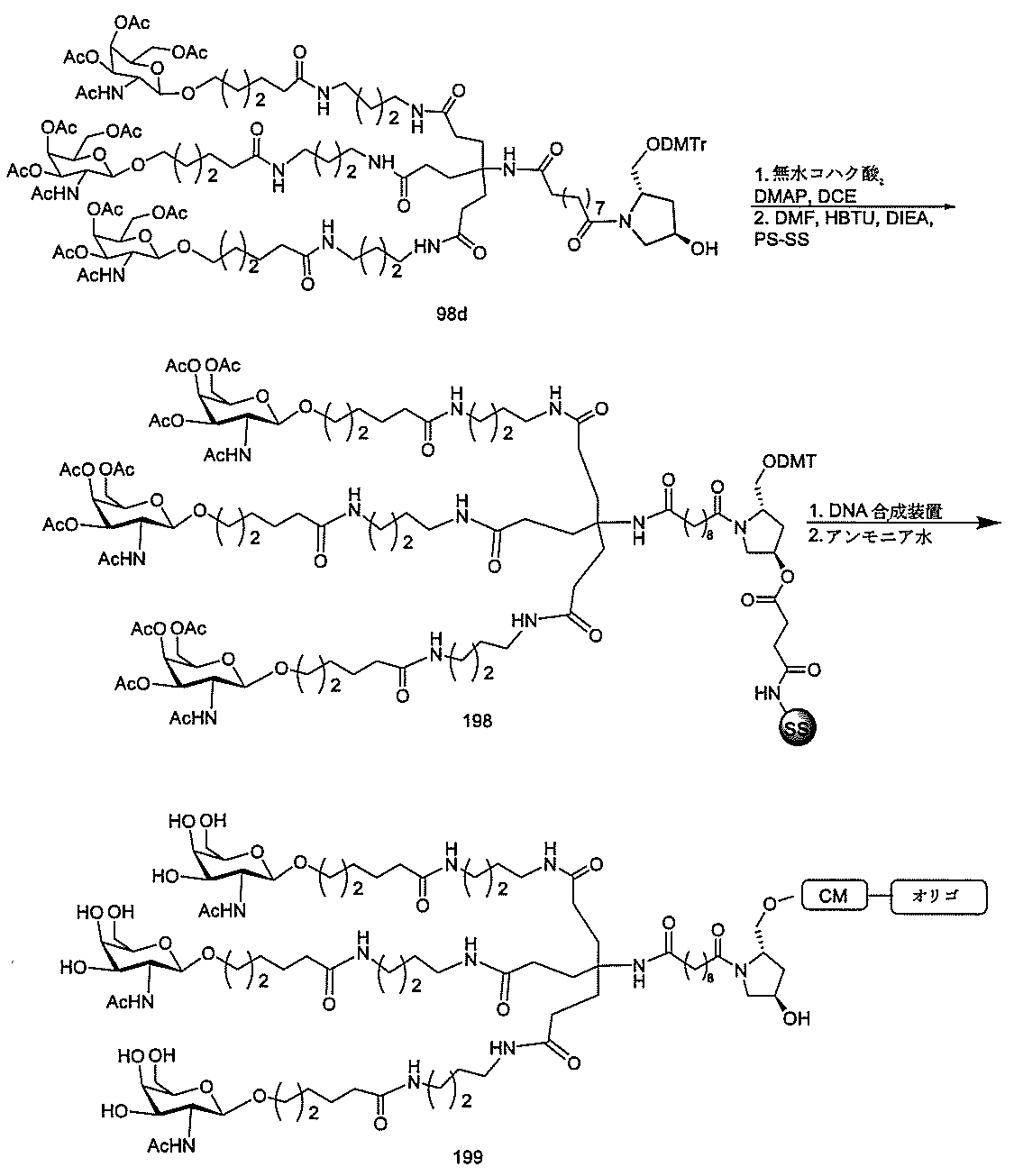
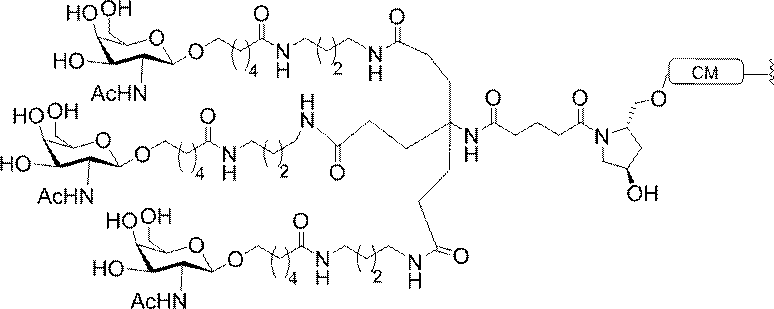
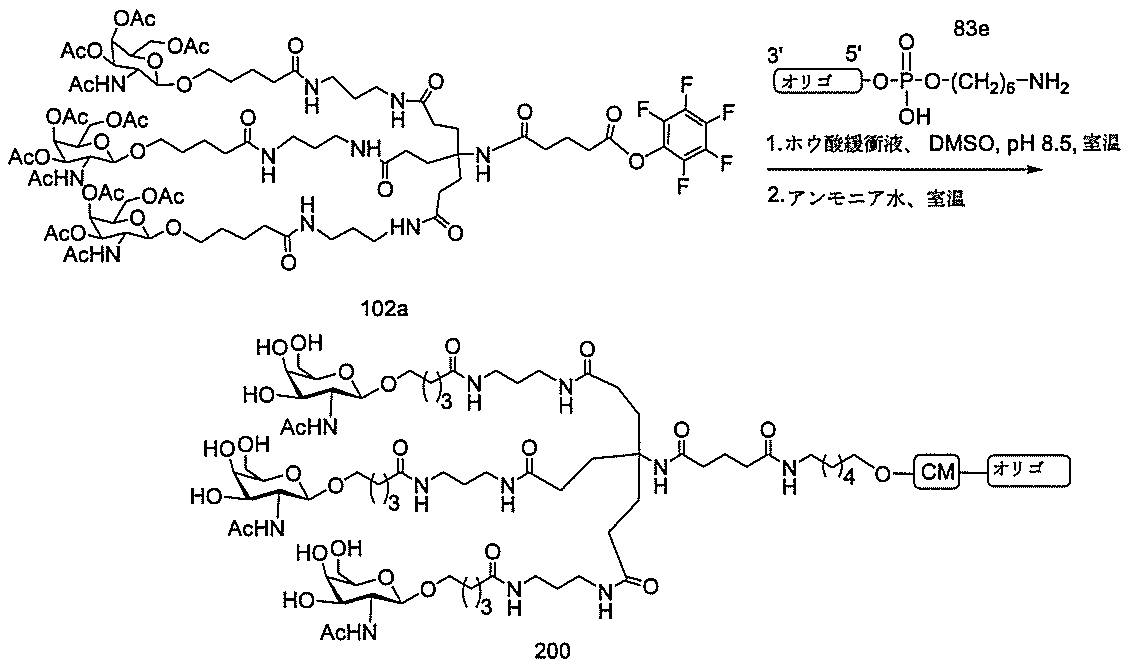
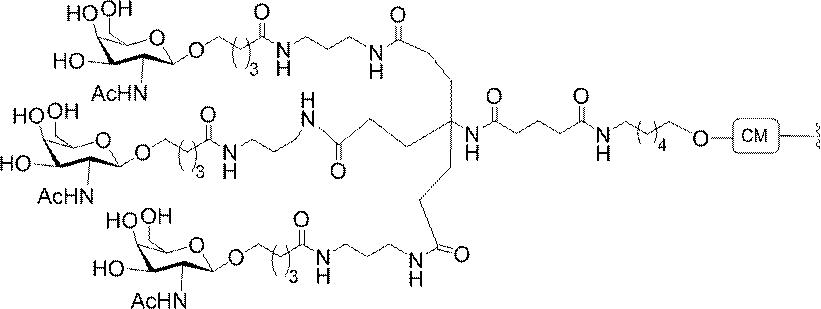
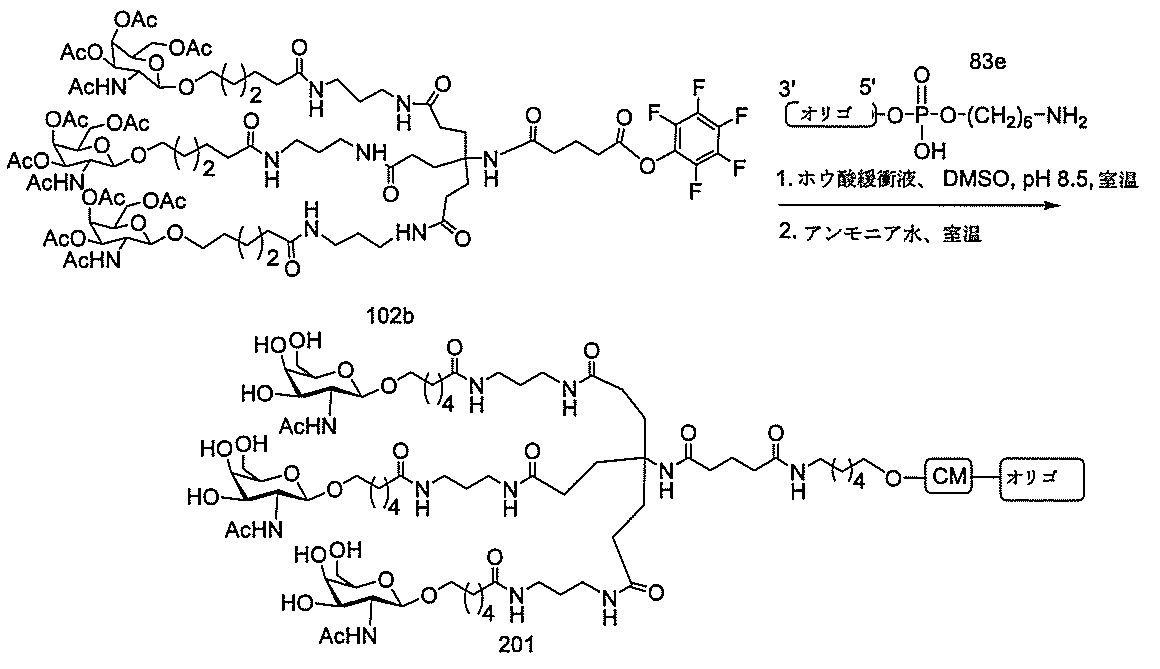
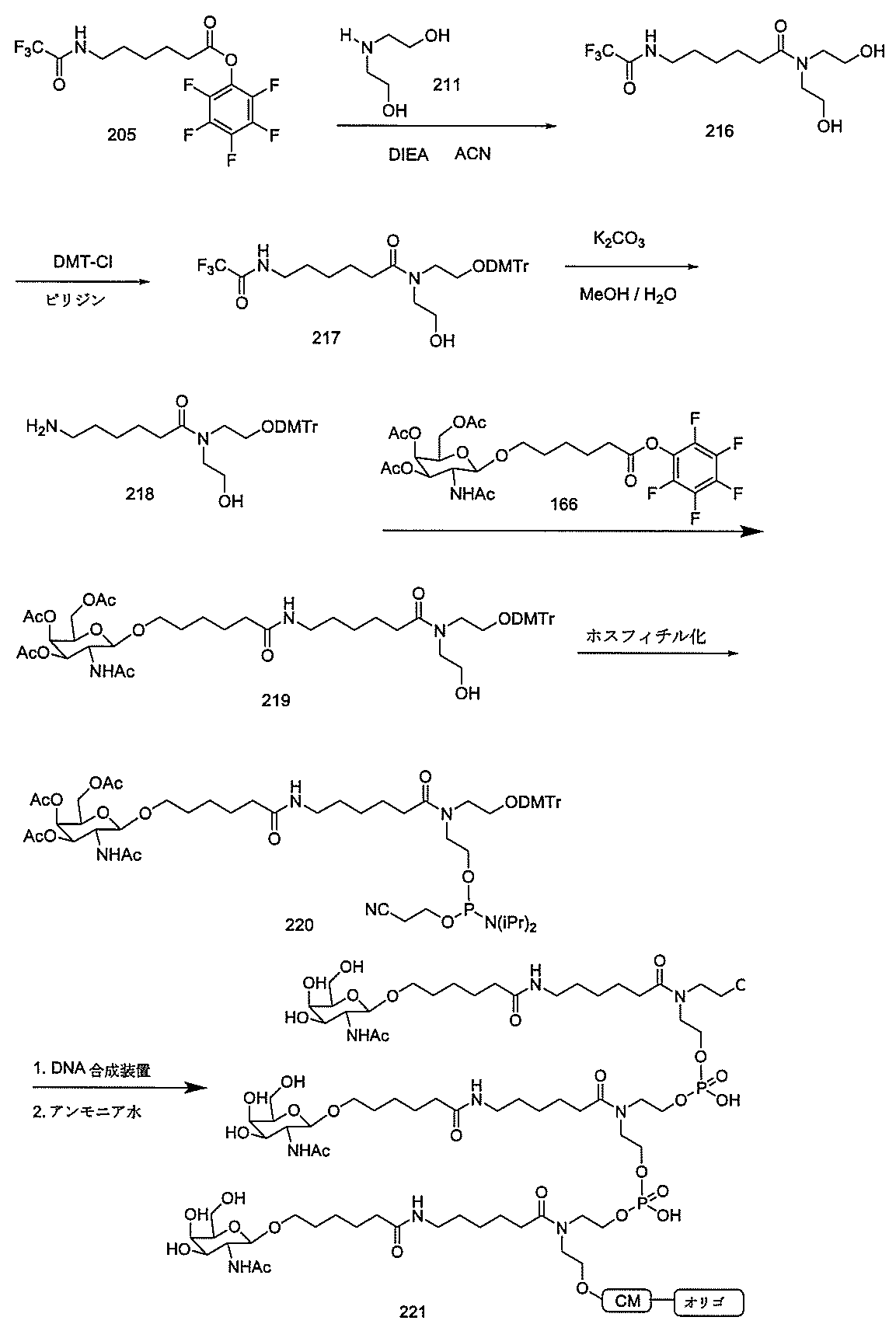
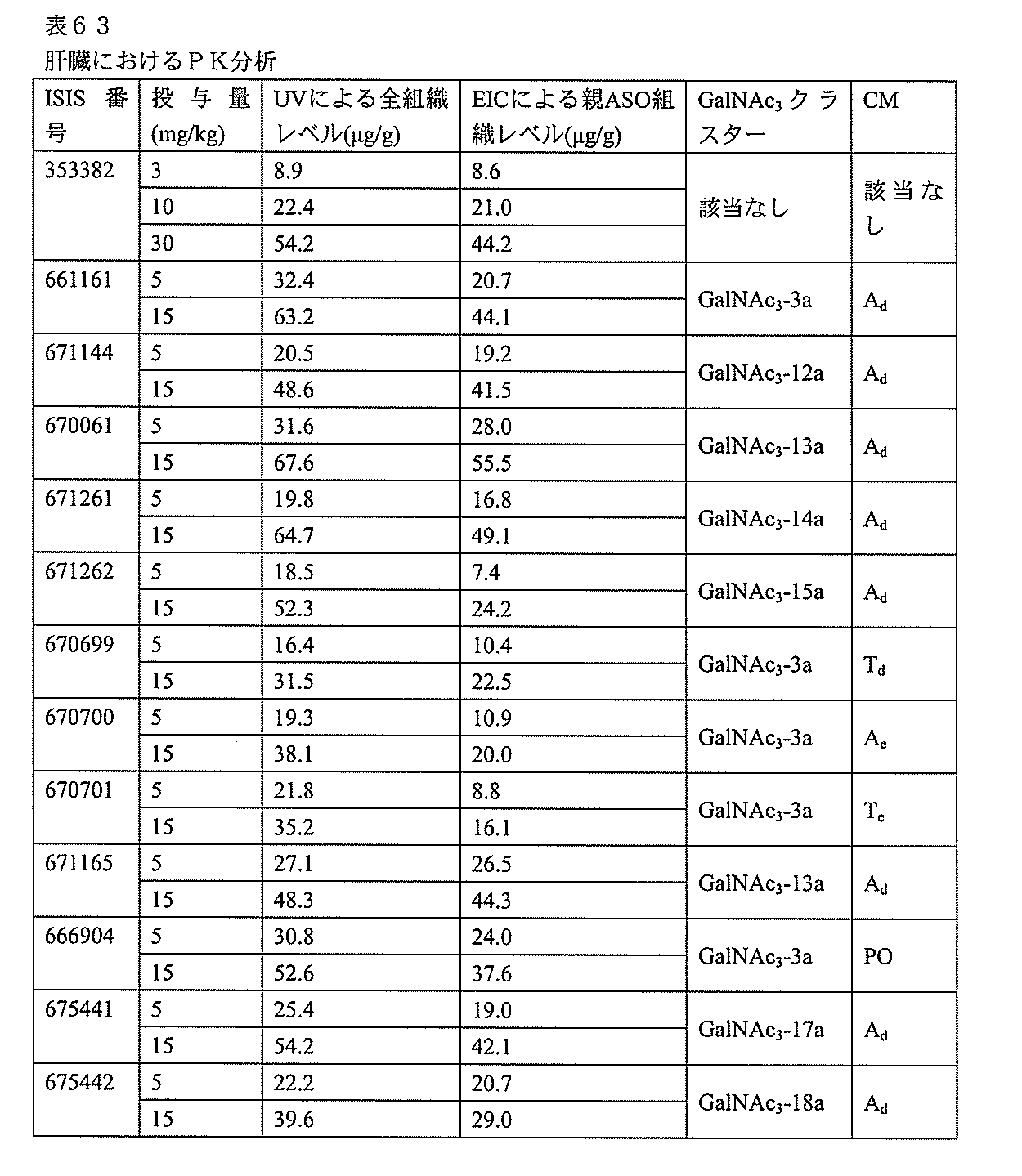
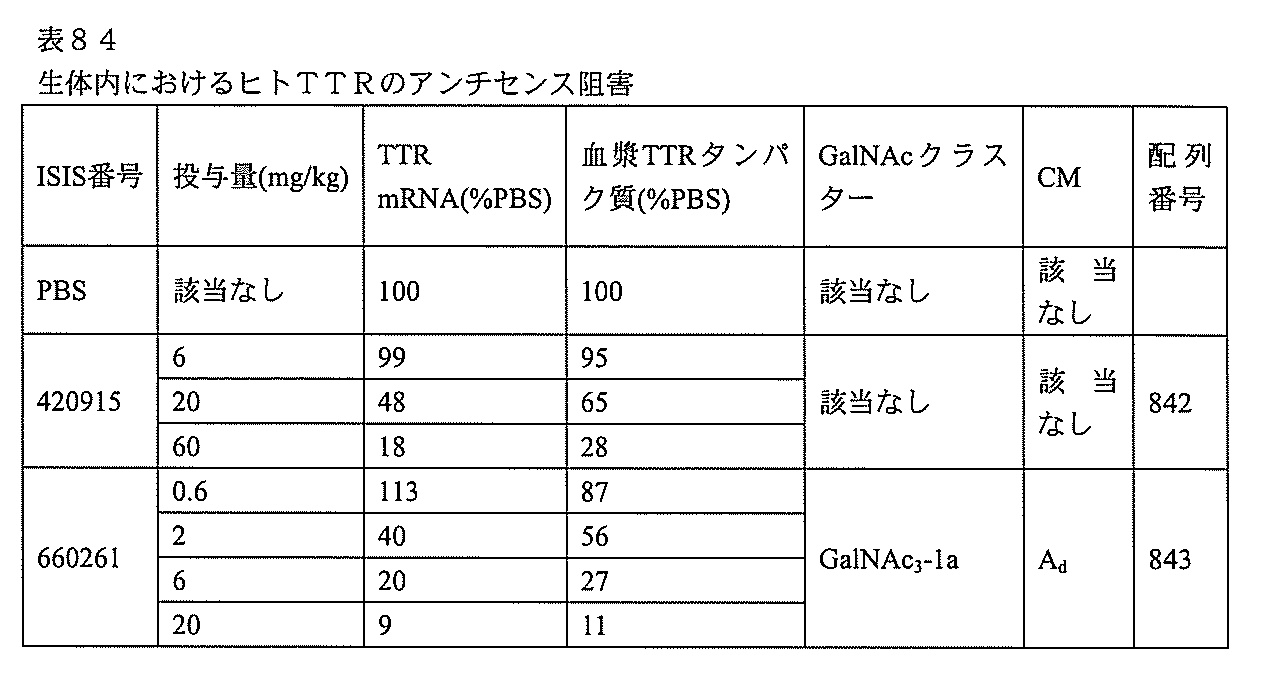
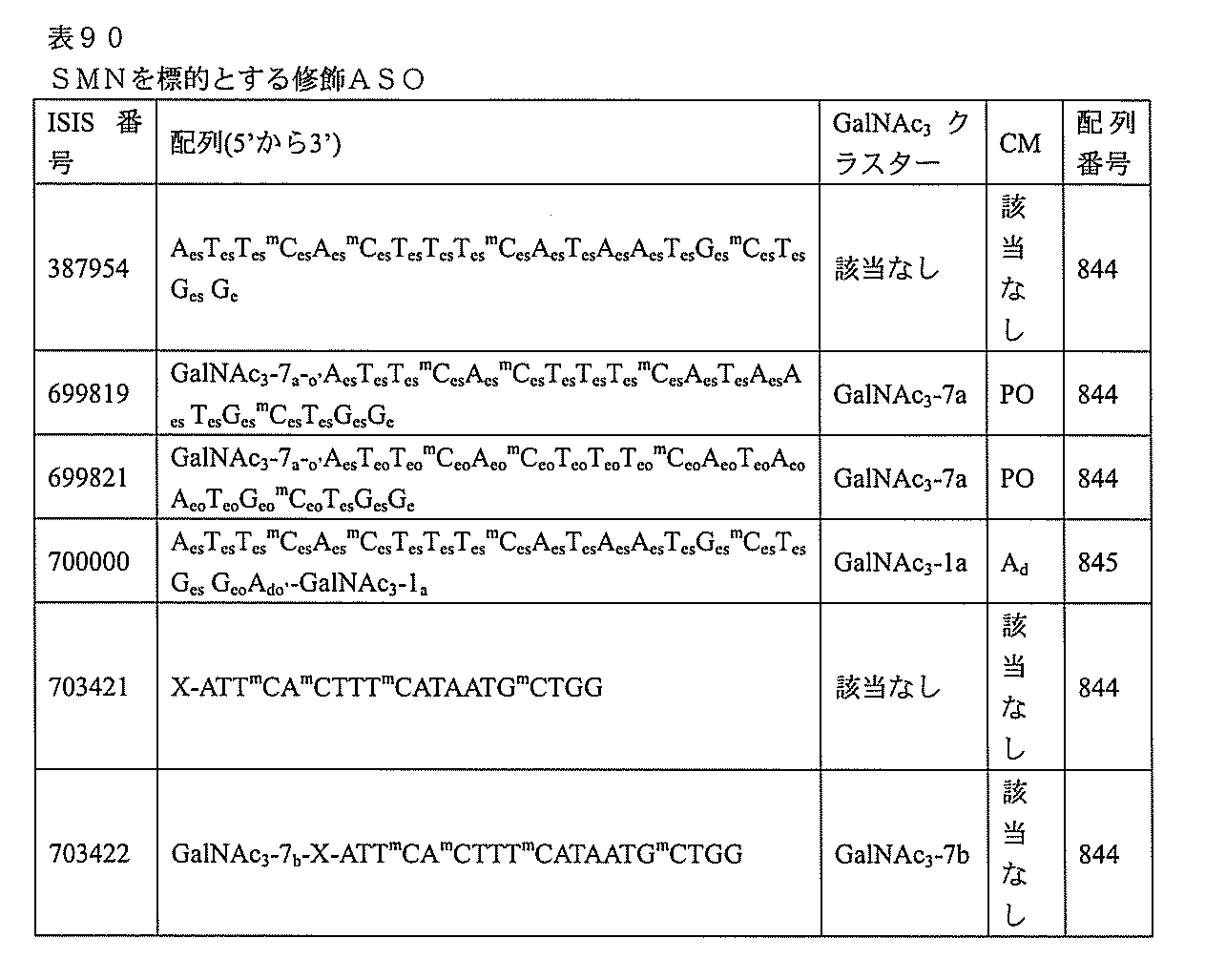
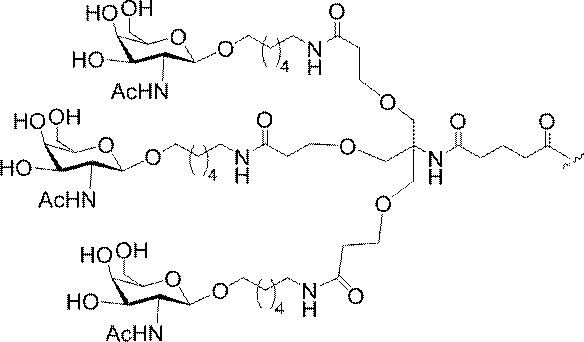
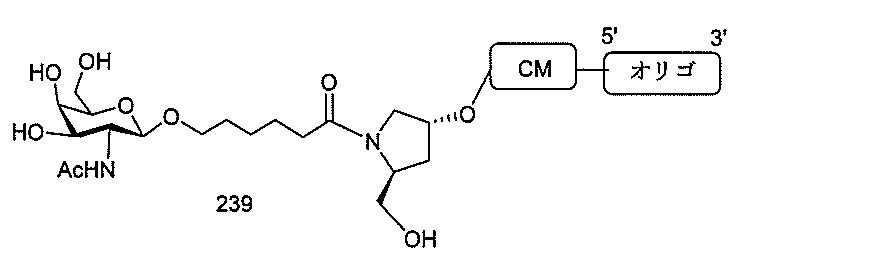
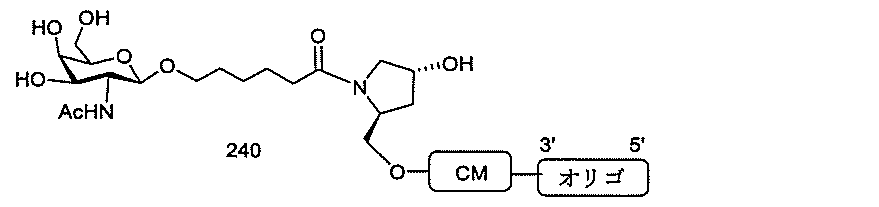
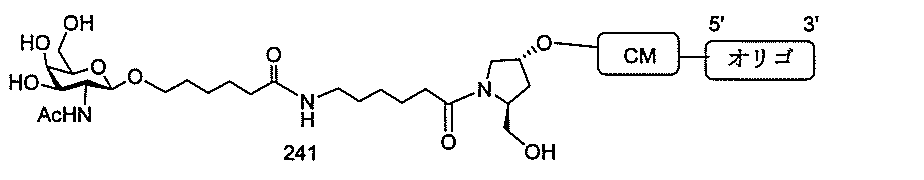
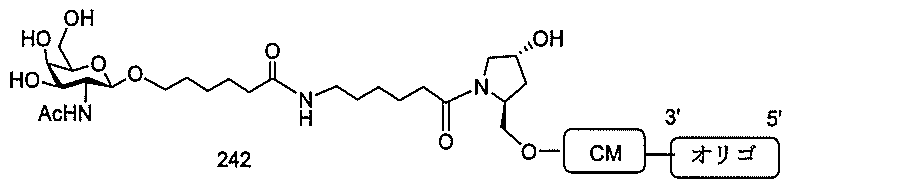
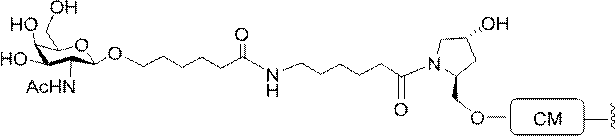
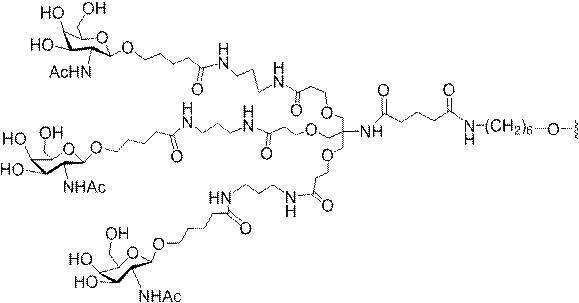
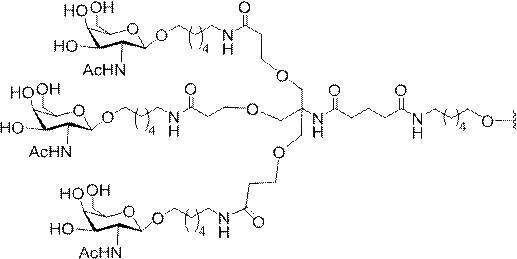
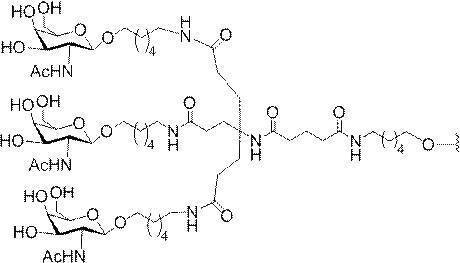
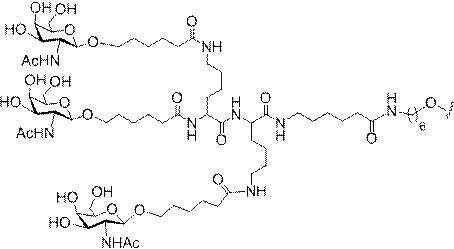
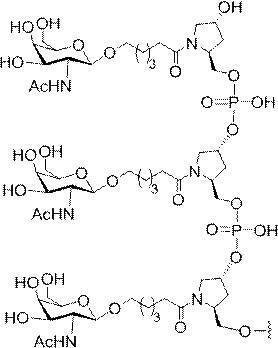
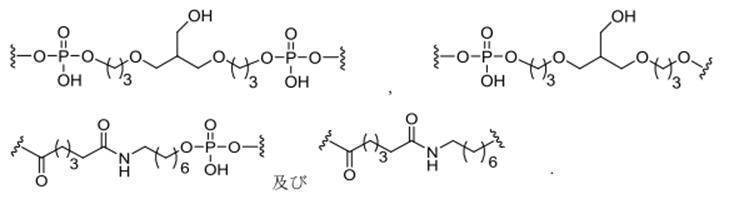
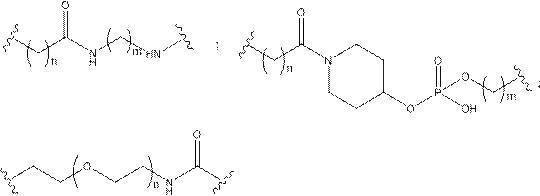
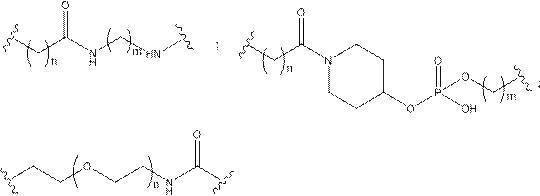
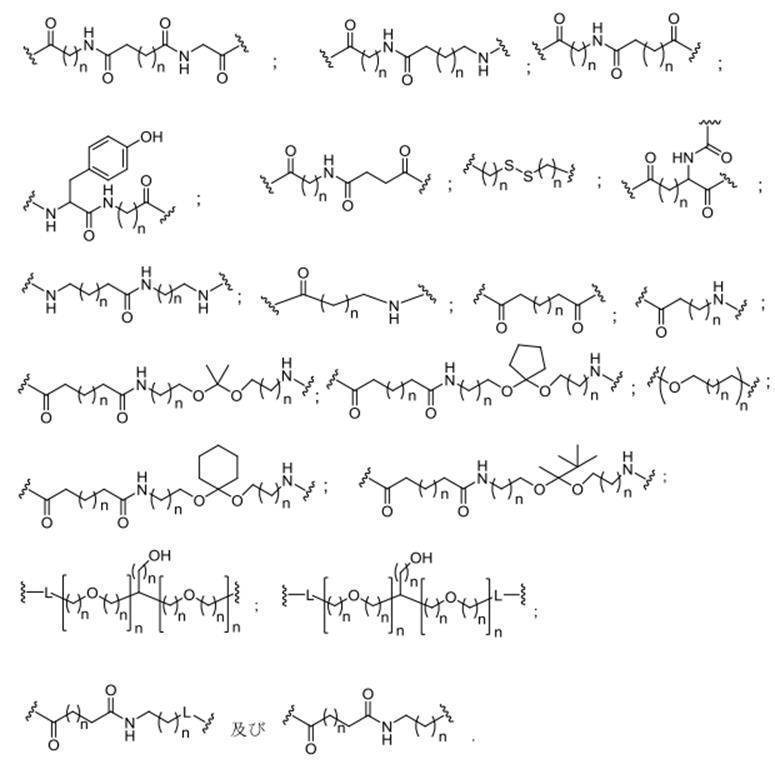
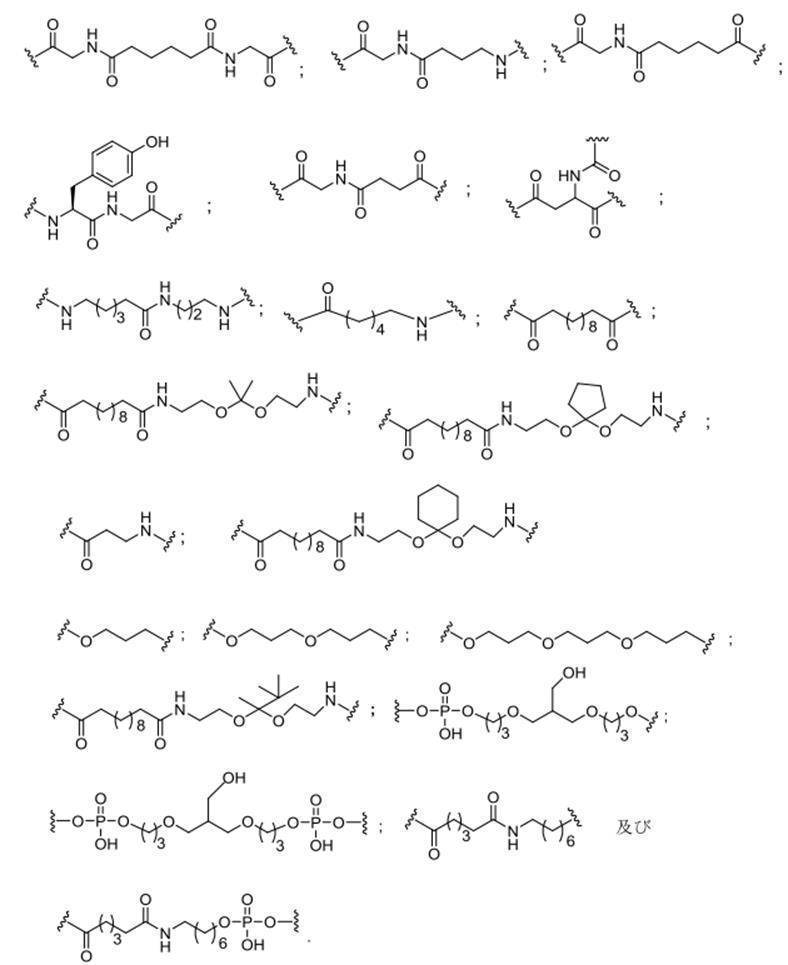
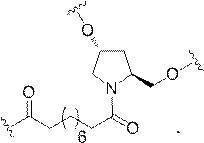
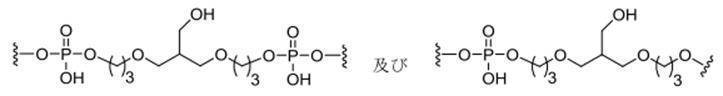
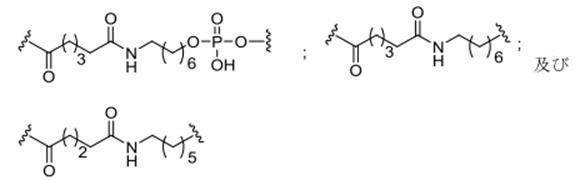
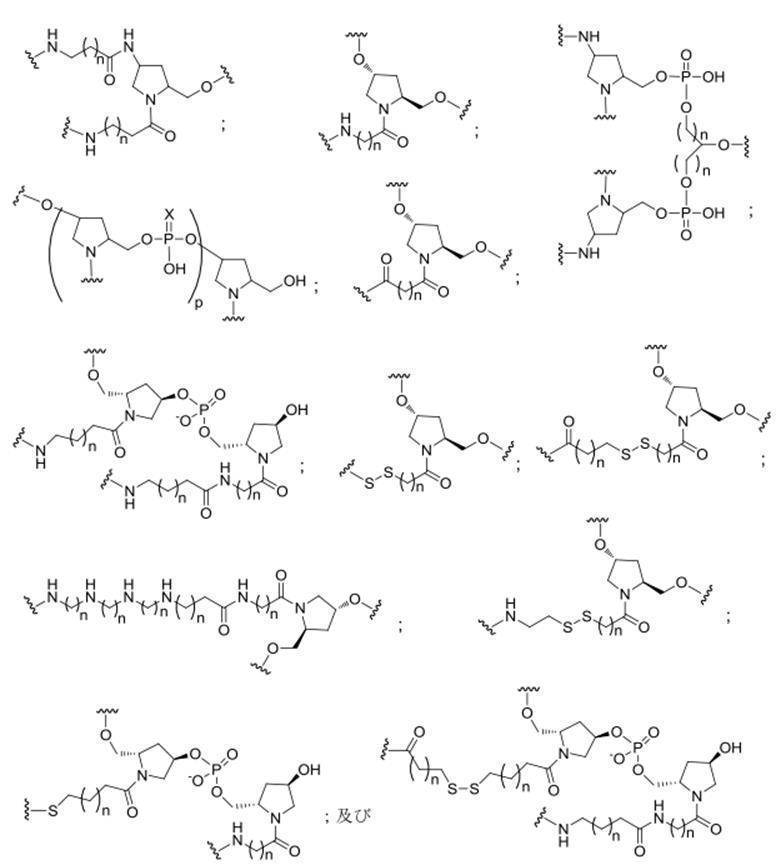
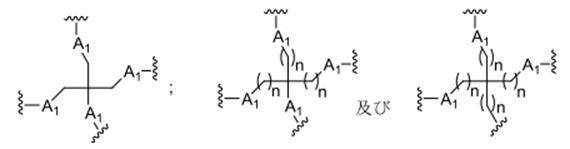
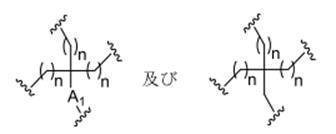
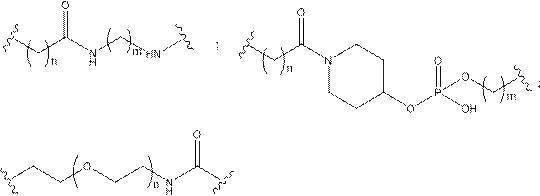
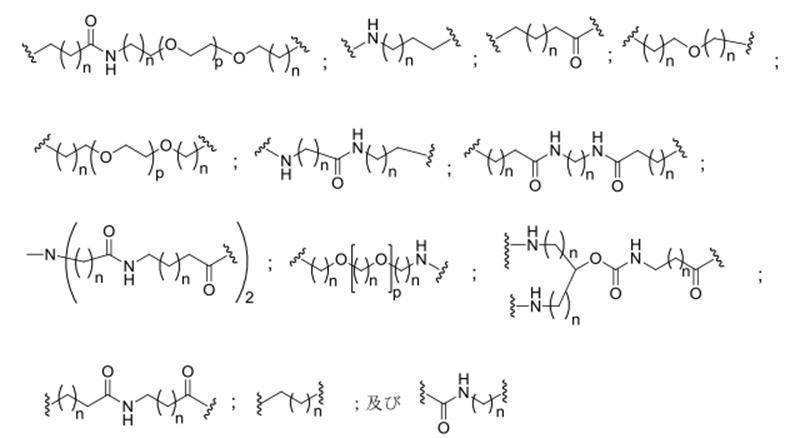
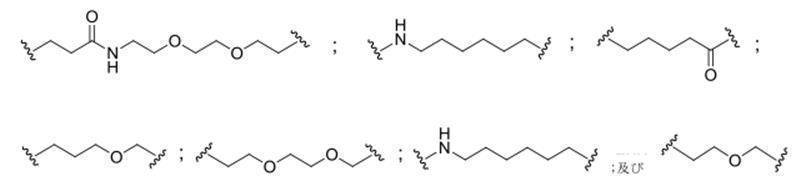
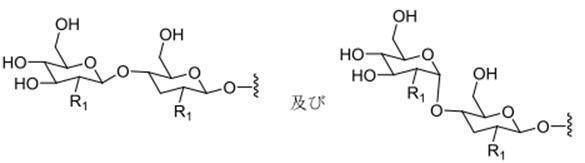
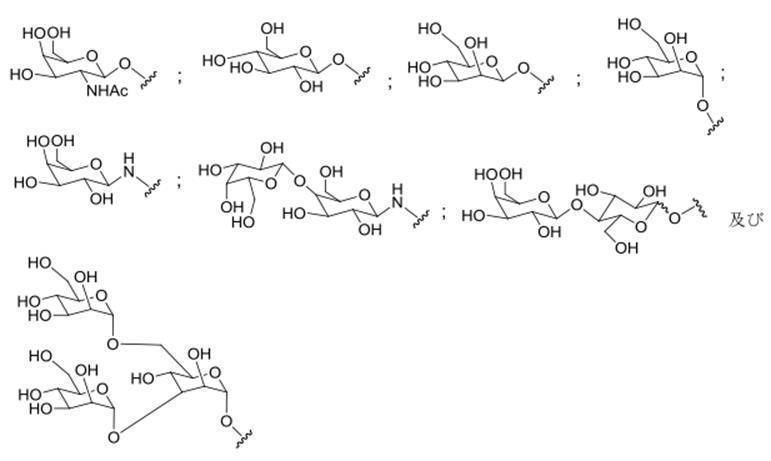
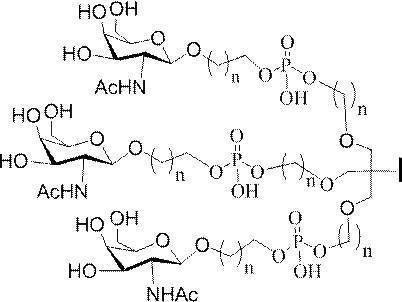
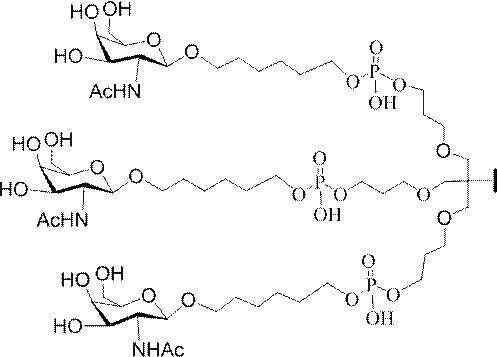
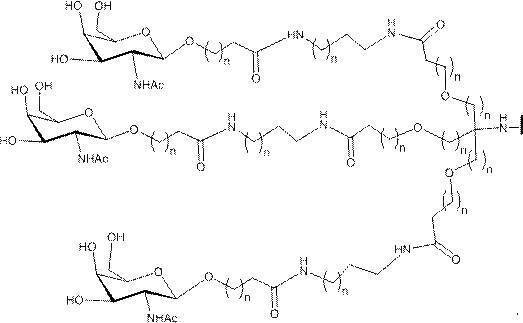
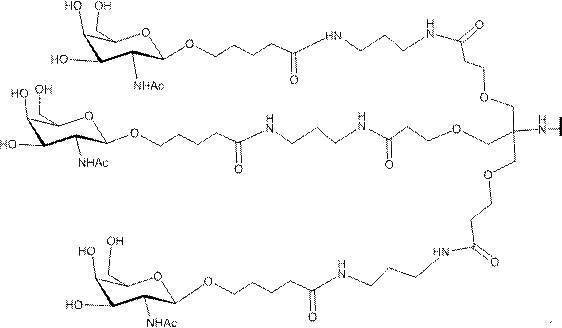
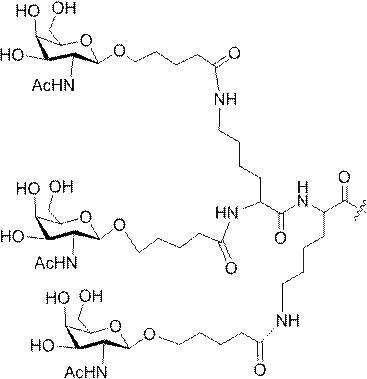
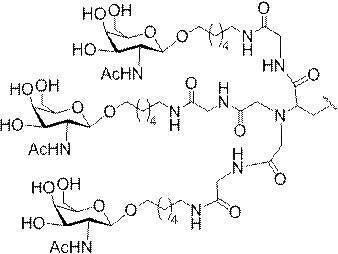
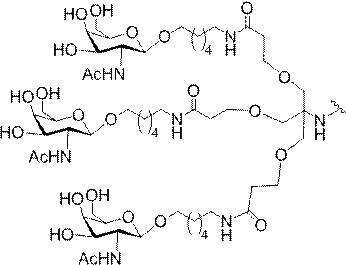
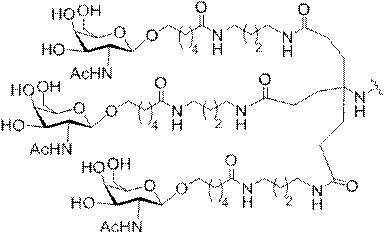
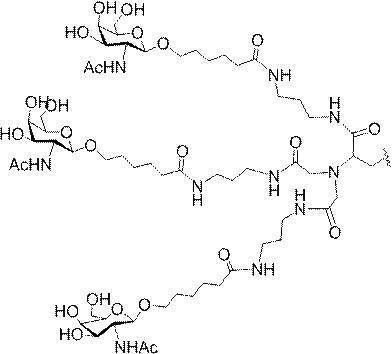
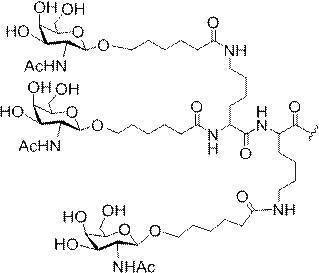
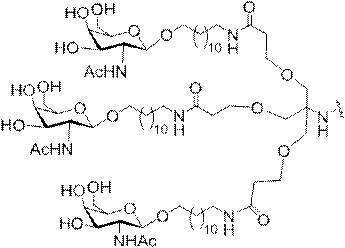
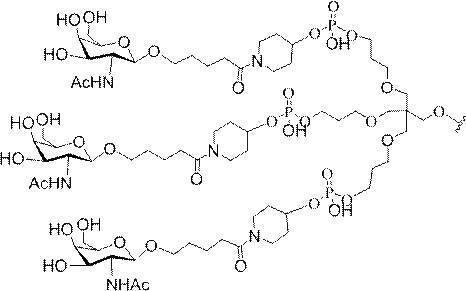
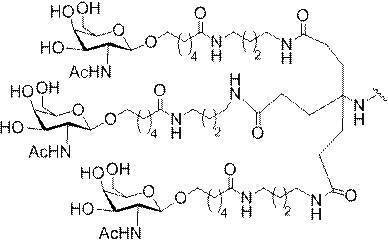
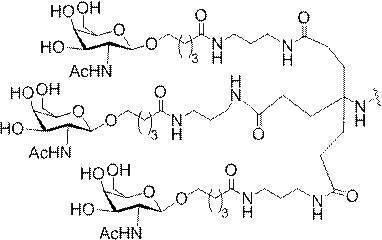
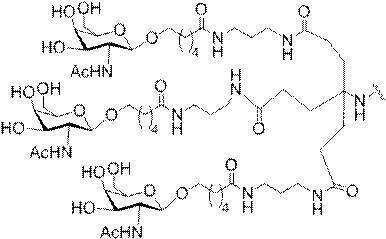
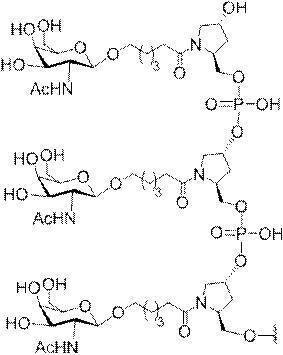
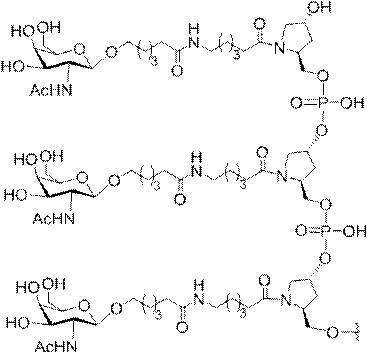
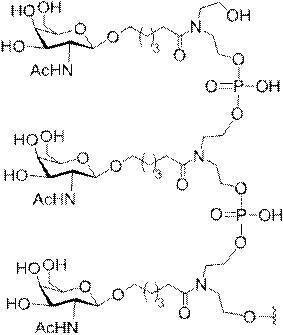
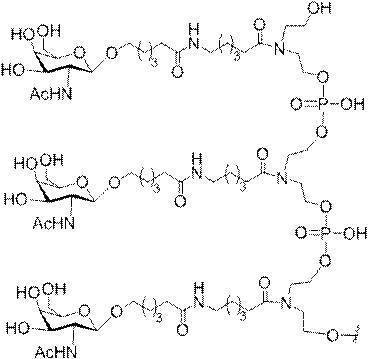
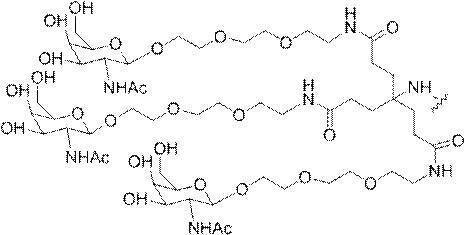
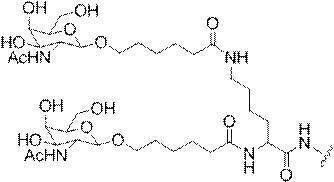
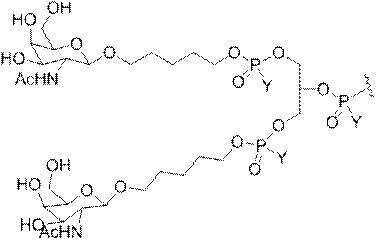
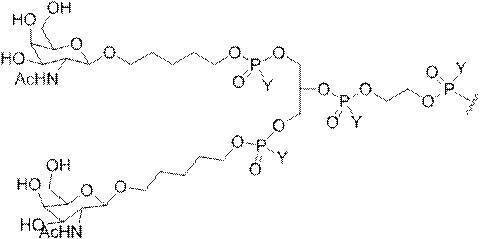
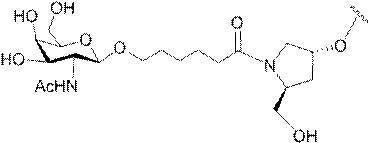
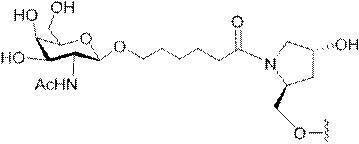
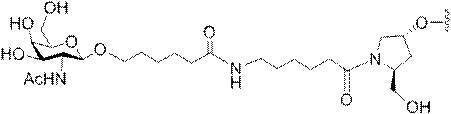
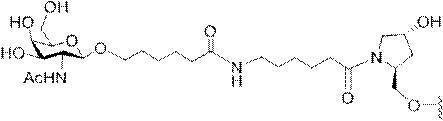
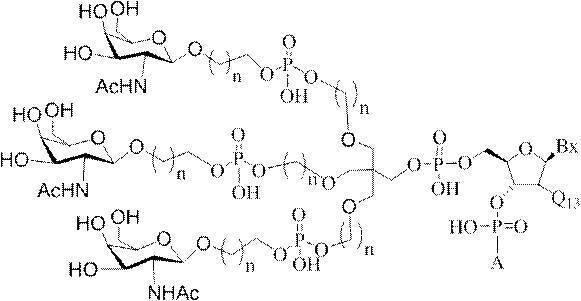
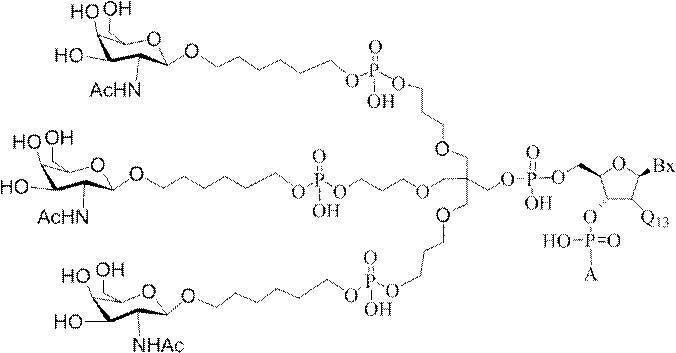
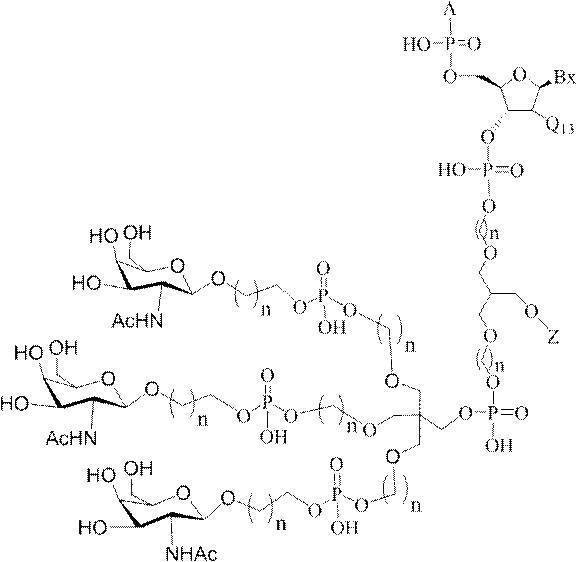
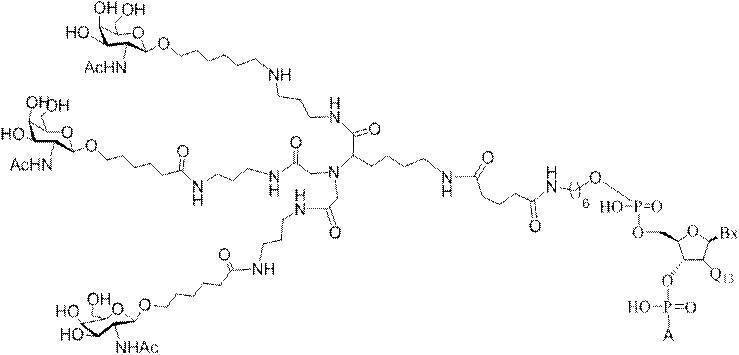
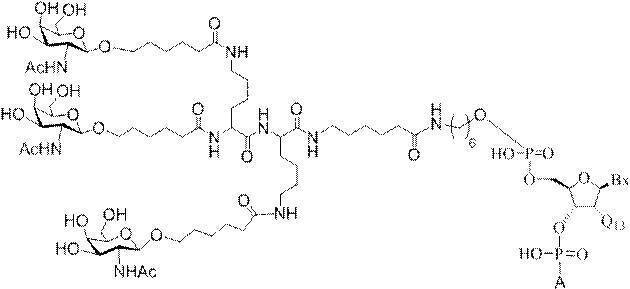
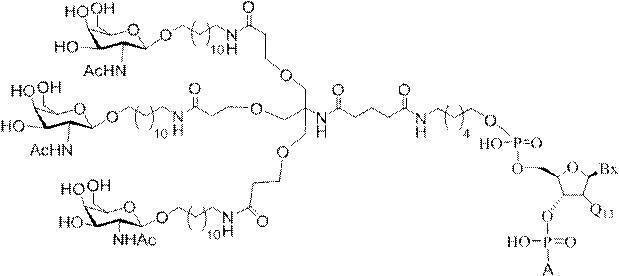
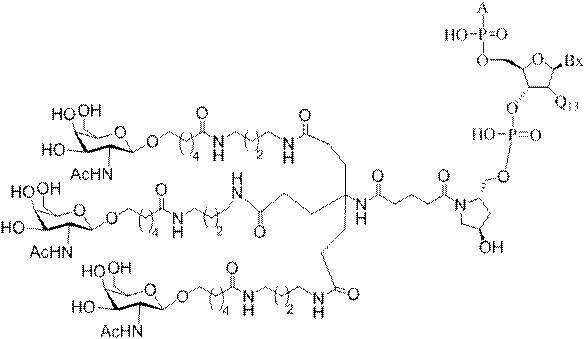
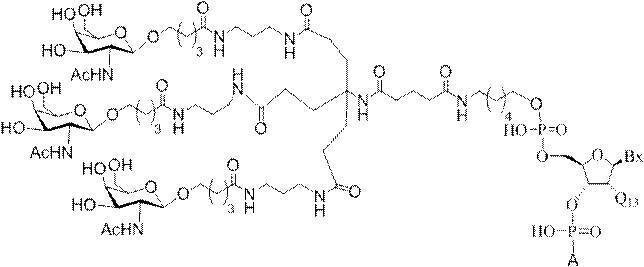
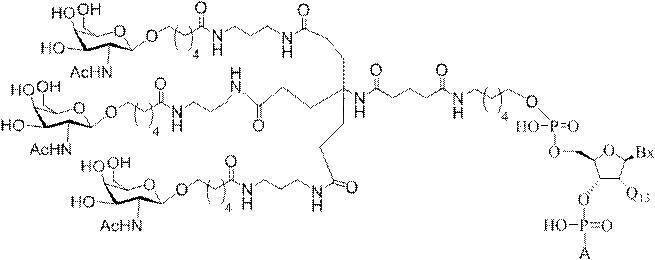
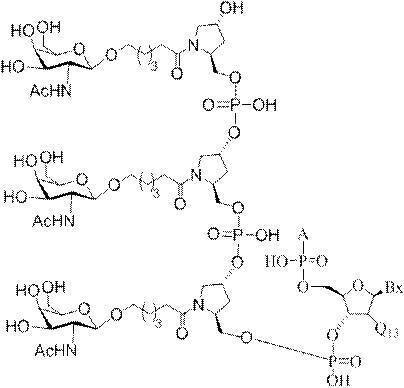
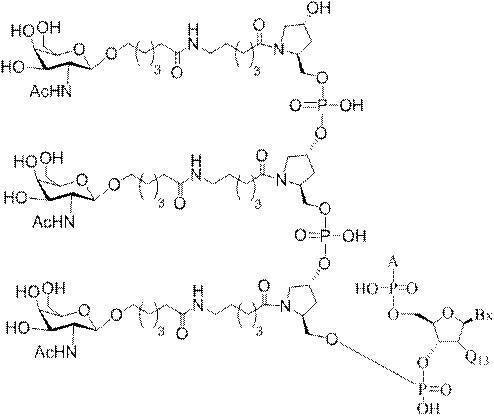
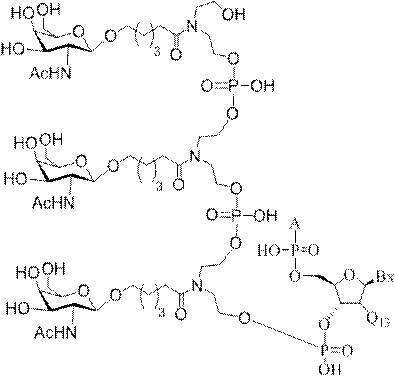
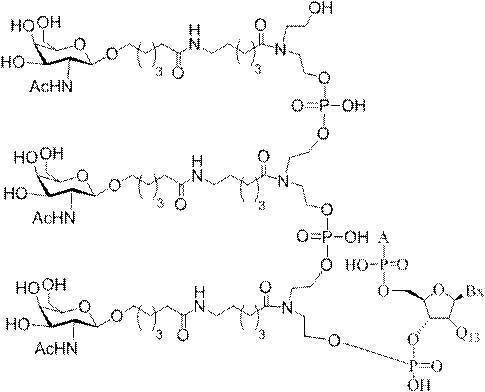
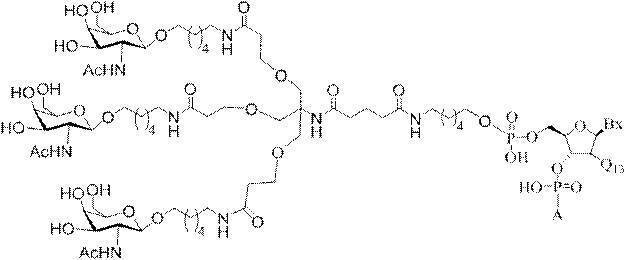
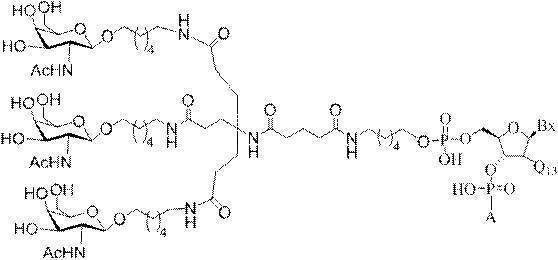
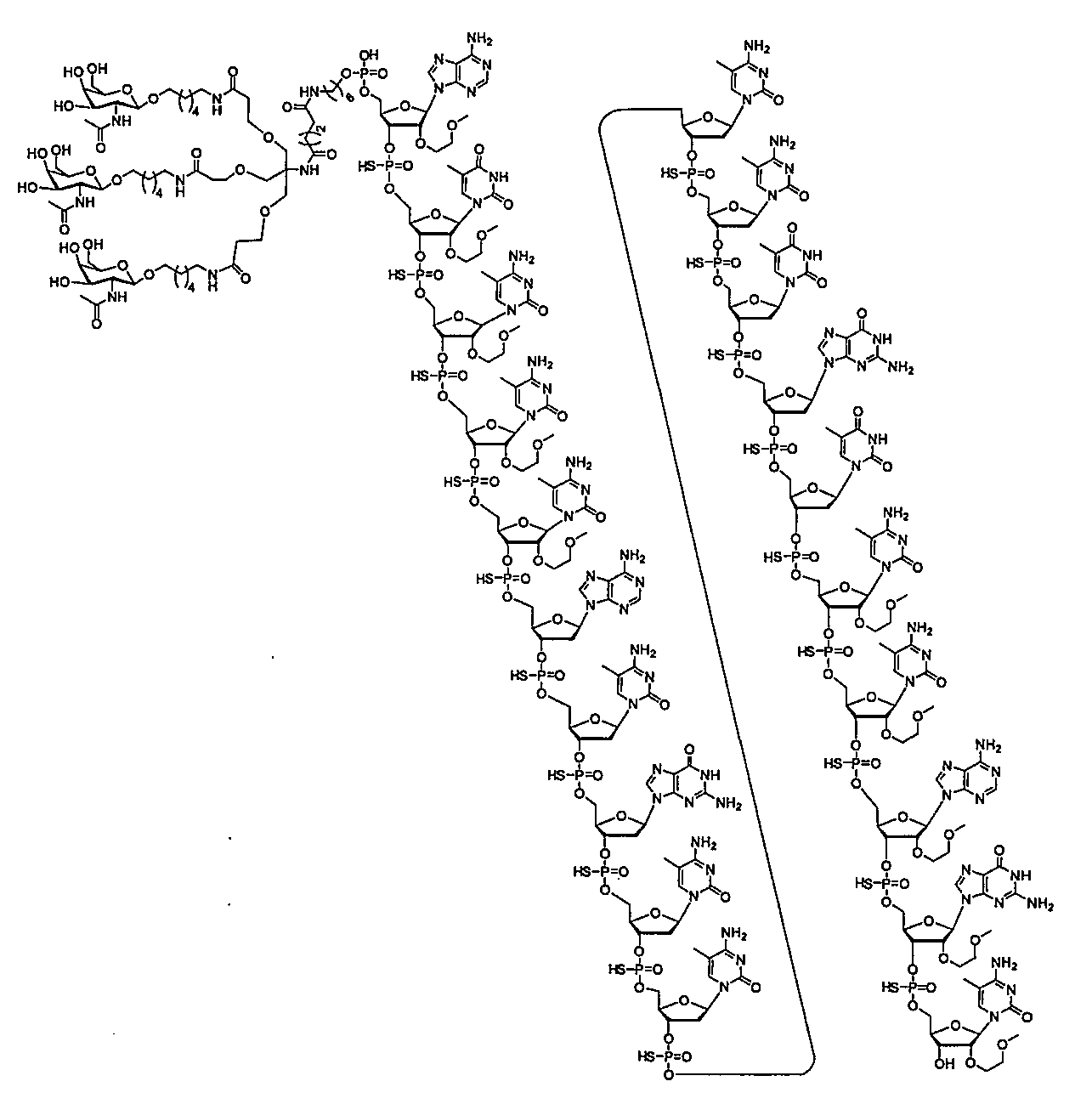
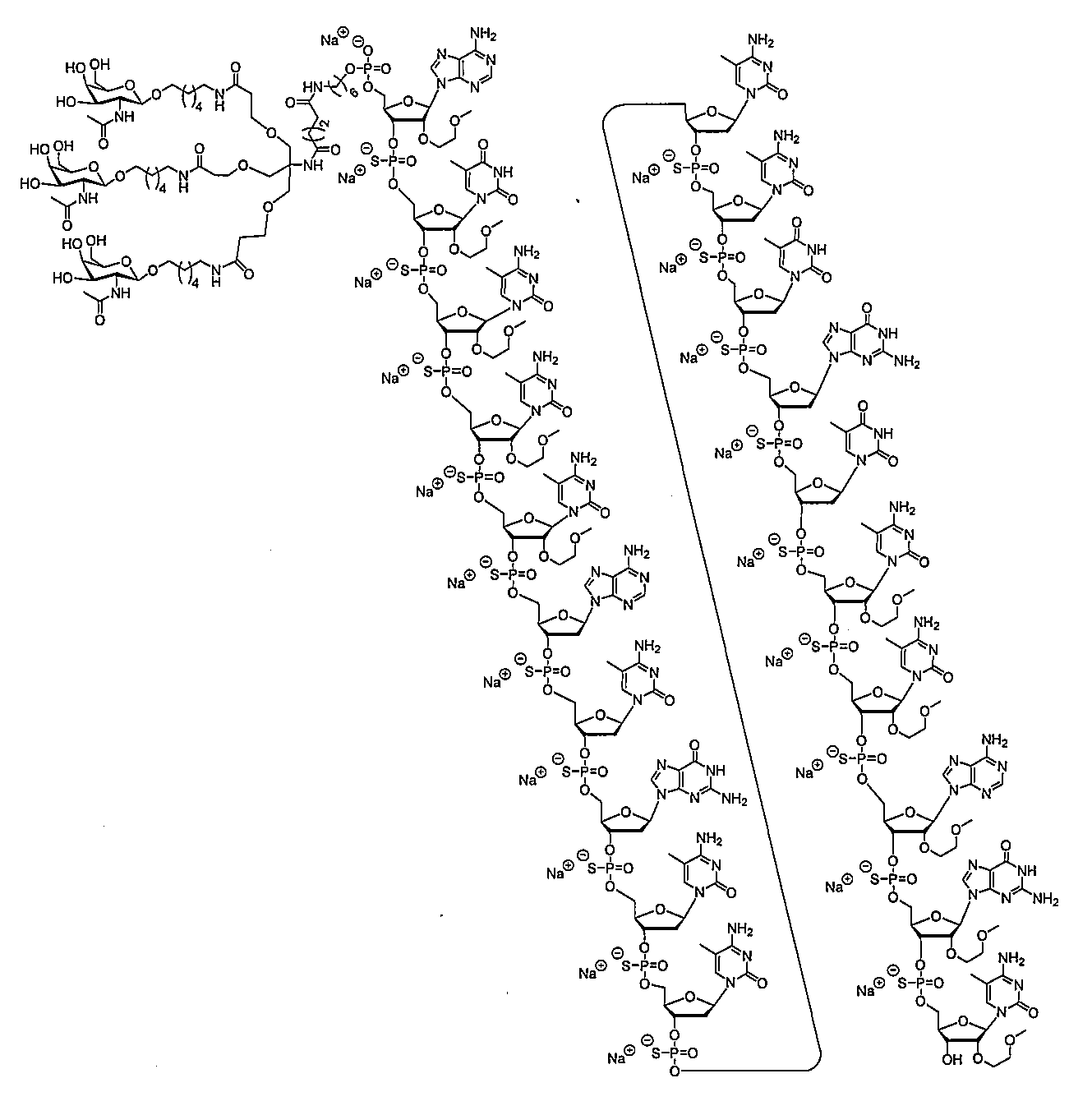
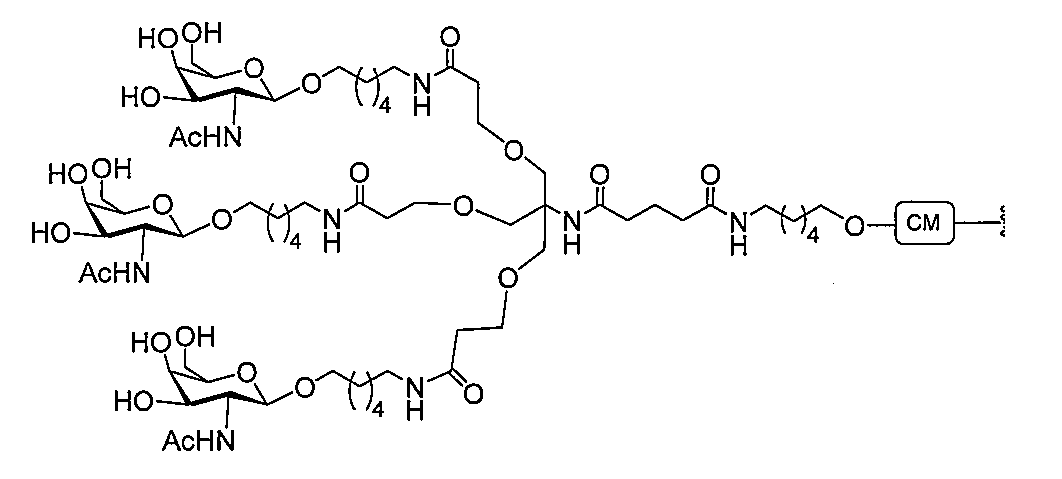
の実体によって特定される。例えば、ある特定の実施形態では、炭水化物クラスター部分が3個のGalNAc基を含み、「GalNAc3」と表記される。ある特定の実施形態では、炭水化物クラスター部分が4個のGalNAc基を含み、「GalNAc4」と表記される。具体的な炭水化物クラスター部分(具体的なテザー基、分岐基、及び共役リンカー基を有するもの)を、本明細書では、ローマ数字と、それに続く下付き文字「a」で説明し、表記する。したがって、「GalNac3-1a」とは、3個のGalNac基、ならびに具体的に特定されたテザー基、分岐基、及び連結基を有する共役基の具体的炭水化物クラスター部分を指す。そのような炭水化物クラスター断片は、切断可能な結合または切断可能なヌクレオシドなどの切断可能部分を介してオリゴマー化合物に取り付けられる。
たは複数のヌクレオシドと化学的に異なっているものを意味する。前記内側領域を「ギャップ」と呼び、前記外側領域を「ウイング」と呼ぶことができる。
た多環式のラジカル環系から選択されるすべての環系を包含するものとし、脂肪族、脂環式、アリール、ヘテロアリール、アラルキル、アリールアルキル、複素環式、ヘテロアリール、ヘテロ芳香族、及びヘテロアリールアルキルから個別に選択される単一の環系及び混成環系を包含するものとする。そのような単環式及び多環式の構造は、それぞれが同一のレベルの飽和を有する環を含有するか、またはそれぞれが独立して、完全飽和、部分飽和、もしくは完全不飽和を含むさまざまな飽和度を有する環を含有することができる。各環は、複素環式環が生じるように、そしてまた、例えば一方の環が炭素環原子のみを有しかつ縮合している環が2つの窒素原子を有するベンズイミダゾールなどの混合モチーフに存在しうるC環原子のみを含む環が生じるように、C、N、O、及びSから選択される環原子を含むことができる。単環式または多環式の環系は、例えば一方の環に2つの=O基が取り付けられているフタルイミドのように、さらに置換基で置換することができる。単環式または多環式の環系は、環原子を介した直接結合、複数の環原子を介した縮合、置換基を介した結合、または二機能性連結部分を介した結合などといったさまざまな戦略を用いて、親分子に取り付けることができる。
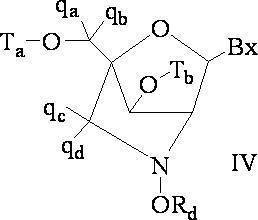
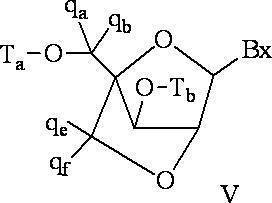
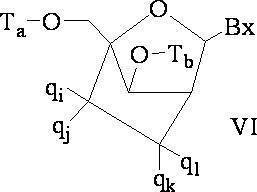
式中、
Ra及びRdはそれぞれ、独立して、O、S、CH2、NH、またはNJ1であり、J1は、C1~C6アルキルまたは置換C1~C6アルキルであり、
Rbは、OまたはSであり、
Rcは、OH、SH、C1~C6アルキル、置換C1~C6アルキル、C1~C6アルコキシ、置換C1~C6アルコキシ、アミノ、または置換アミノであり、
J1は、Rbは、OまたはSである。
リン連結基には、ホスホジエステル、ホスホロチオエート、ホスホロジチオエート、ホスホネート、ホスホラミデート、ホスホロチオアミデート、チオノアルキルホスホネート、ホスホトリエステル、チオノアルキルホスホトリエステル、及びボラノホスフェートが含まれるが、これらに限定されない。
& Sons,Inc,ニューヨークに見いだすことができる。
分には、2’位、3’位、5’位及び/または4’位に置換基を含むフラノシルなどがあるが、これらに限定されない。特定の置換糖部分は二環式糖部分である。
医薬組成物を前記動物に投与することができる。
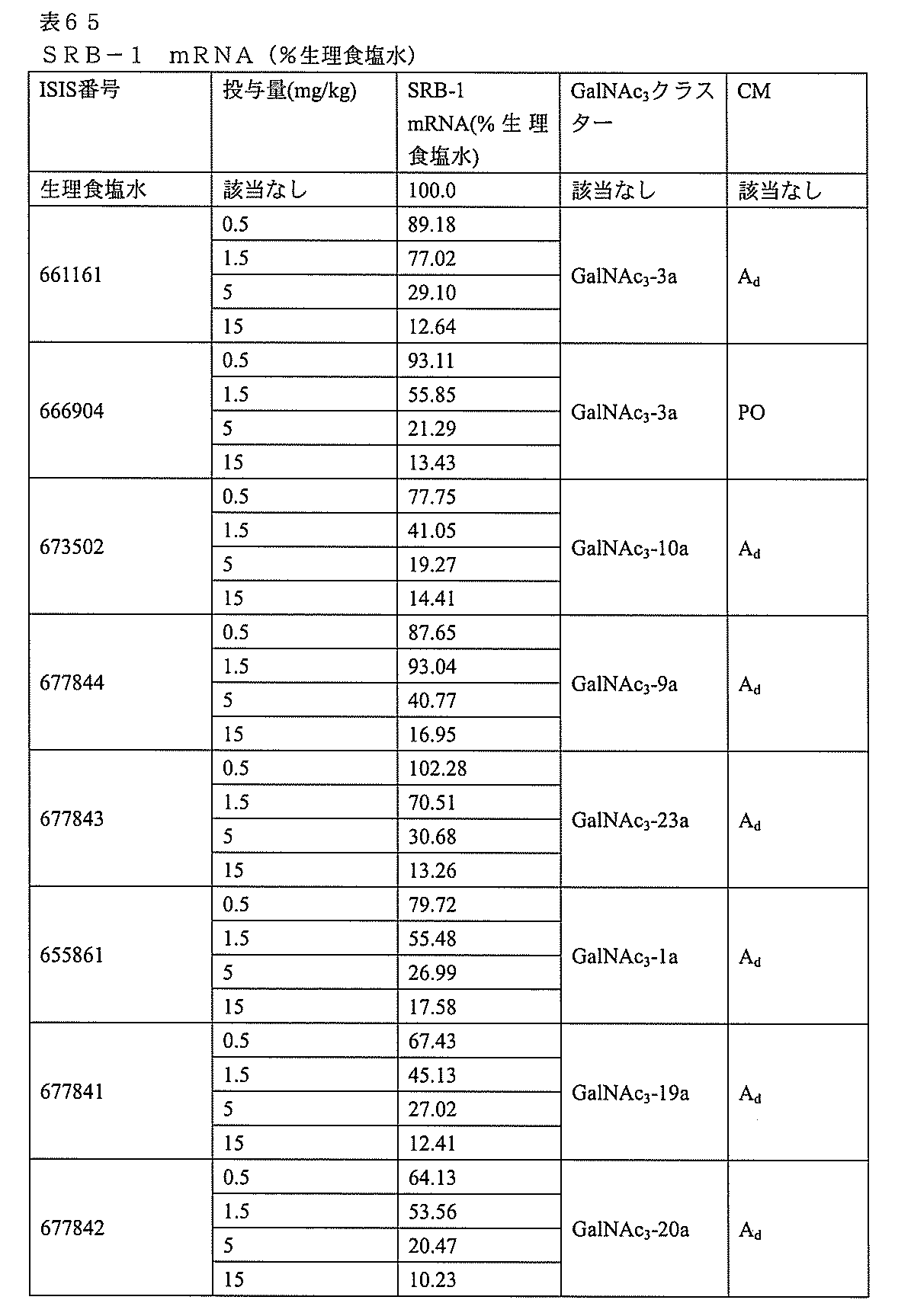
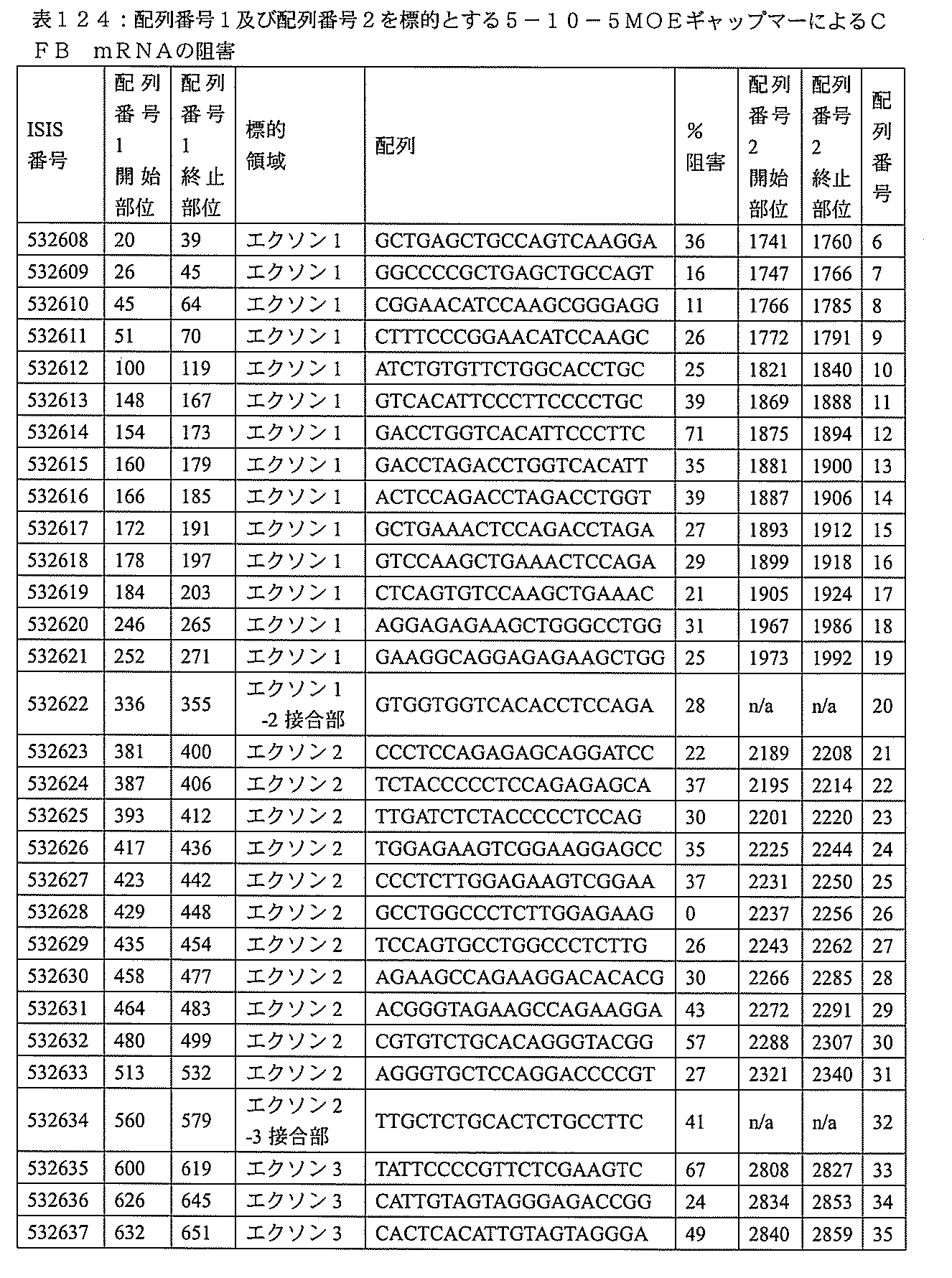
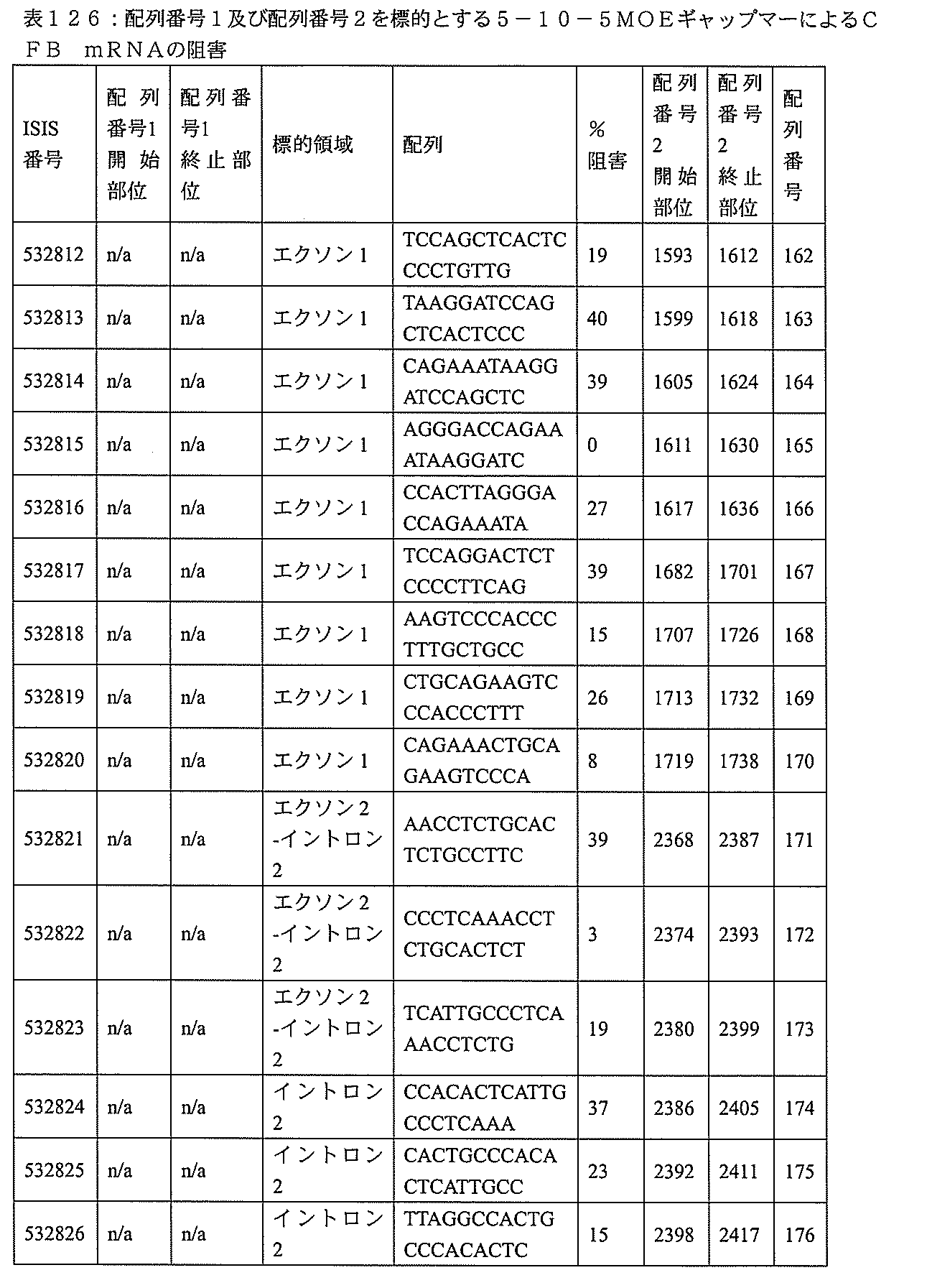
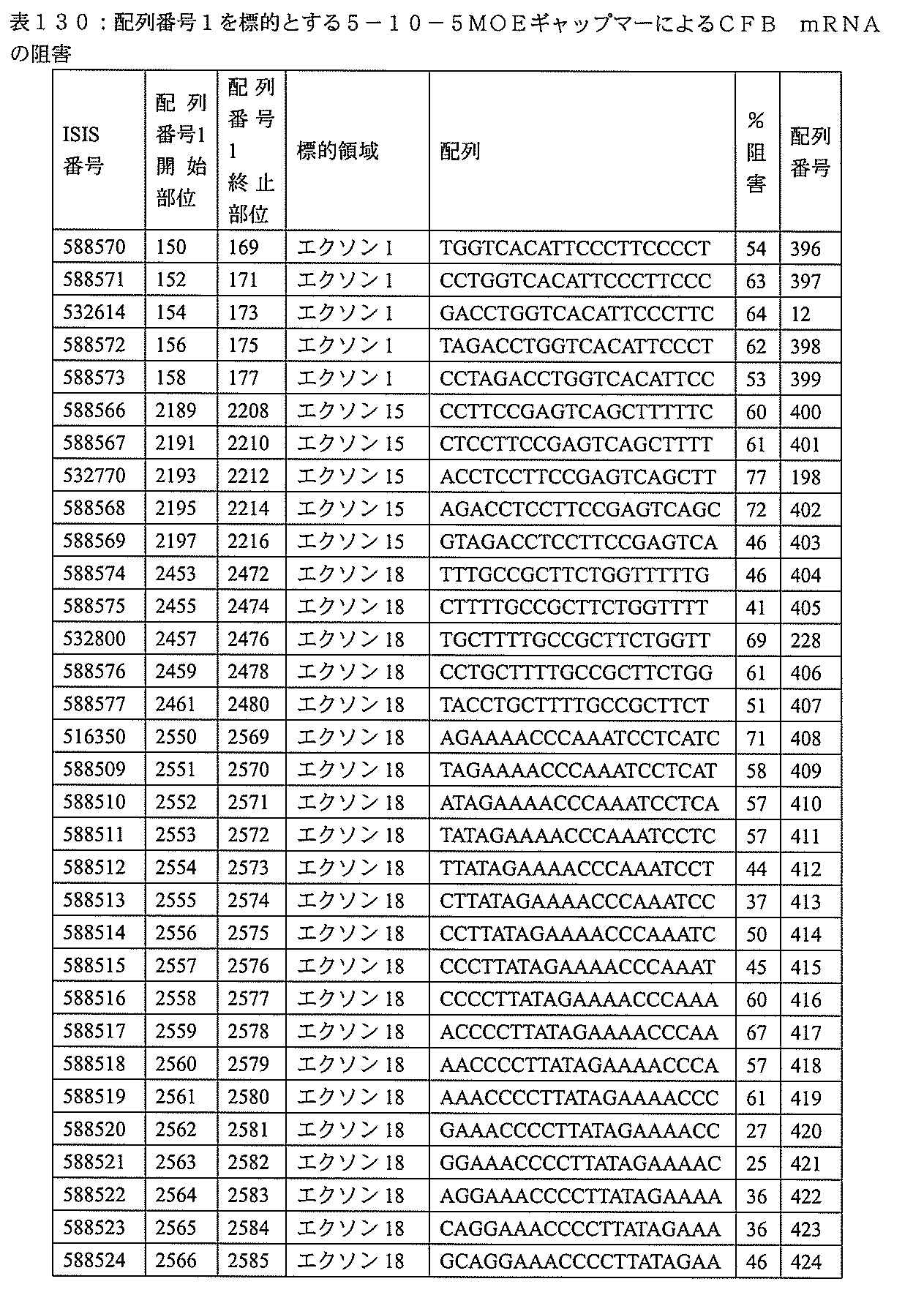
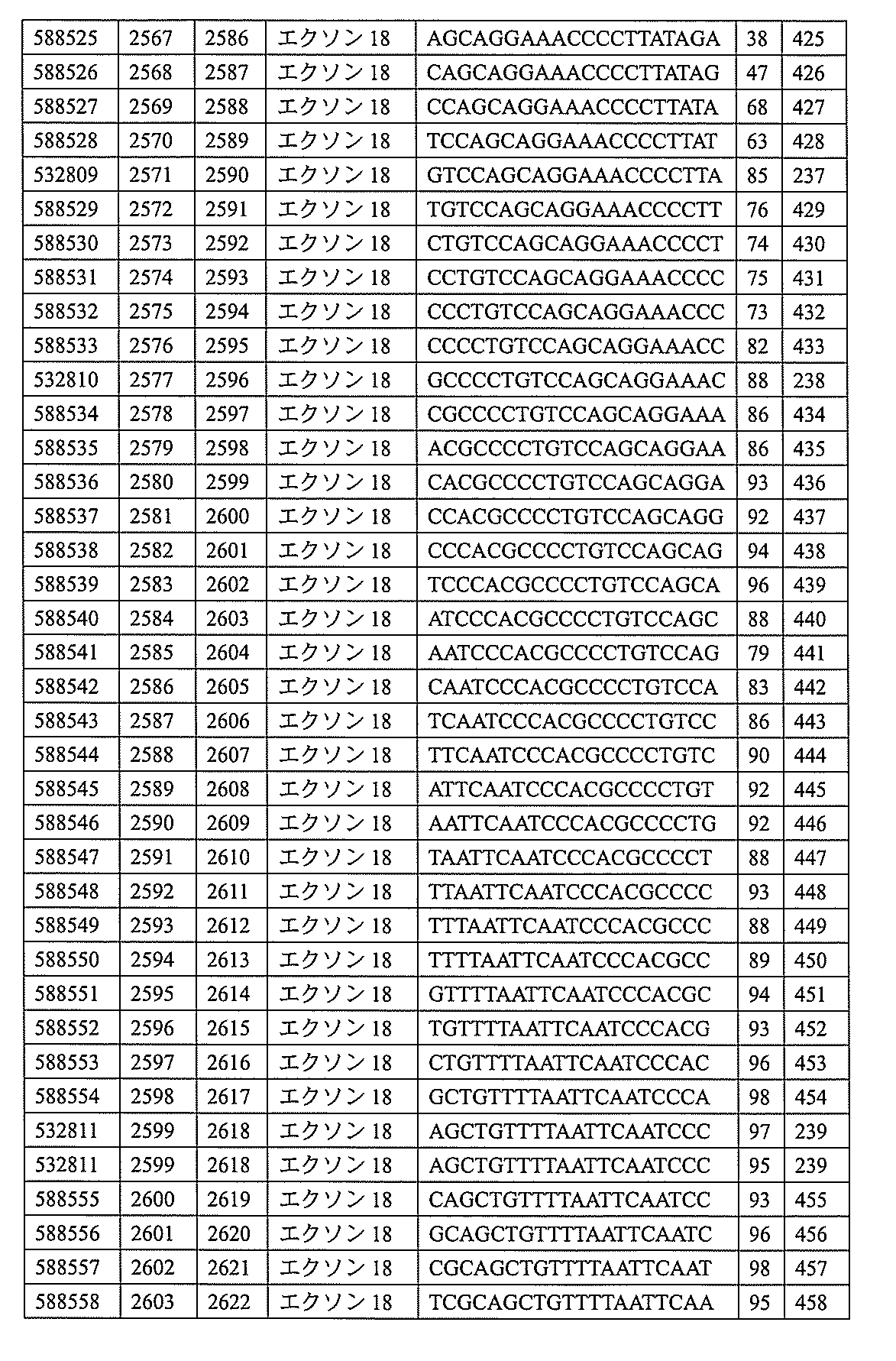
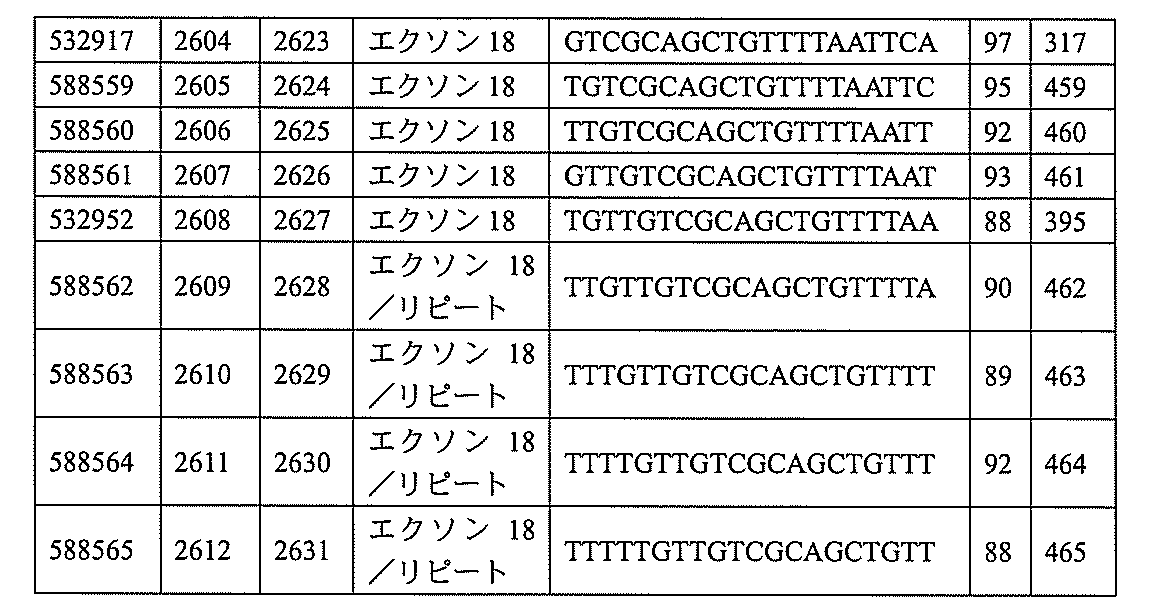
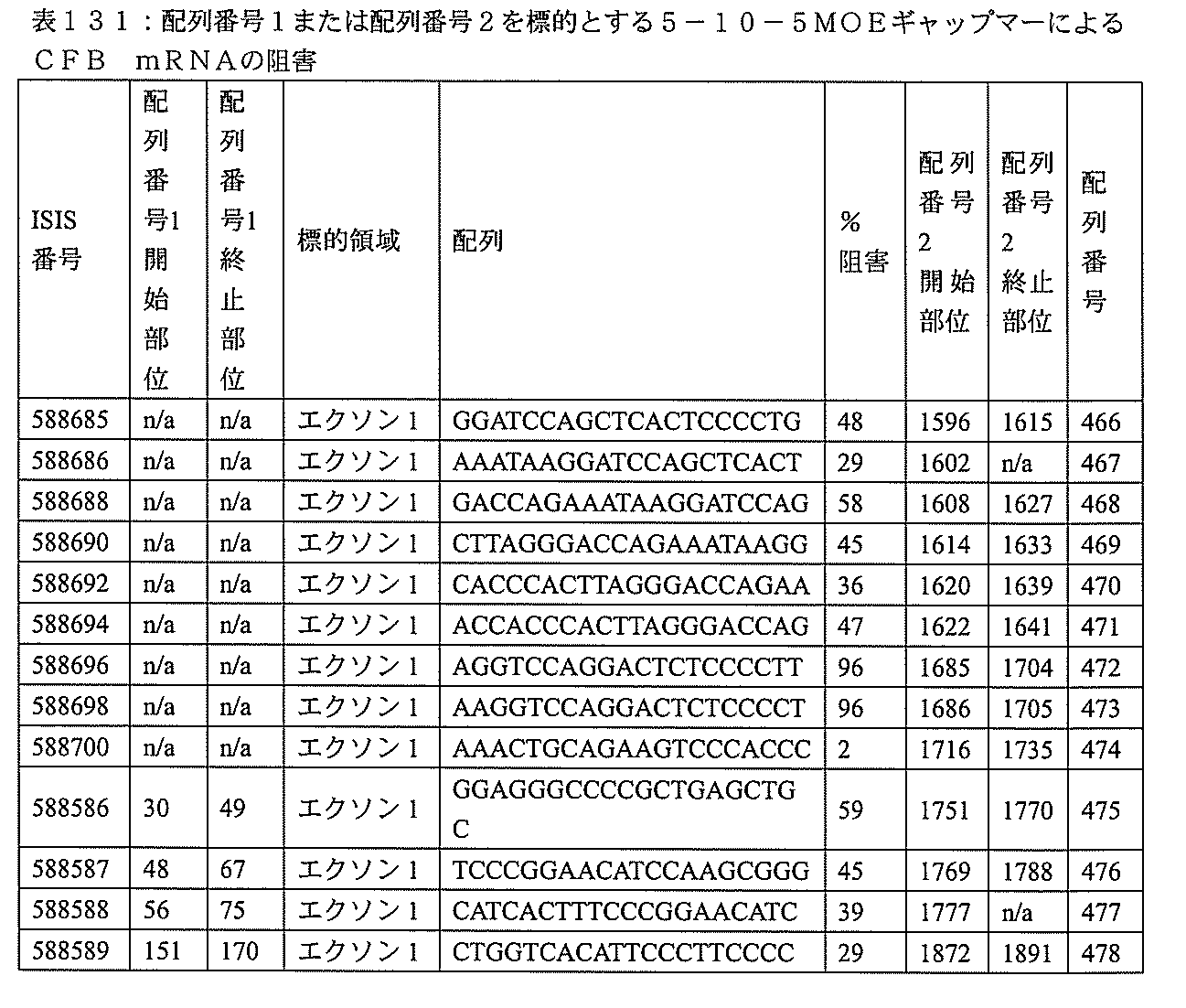
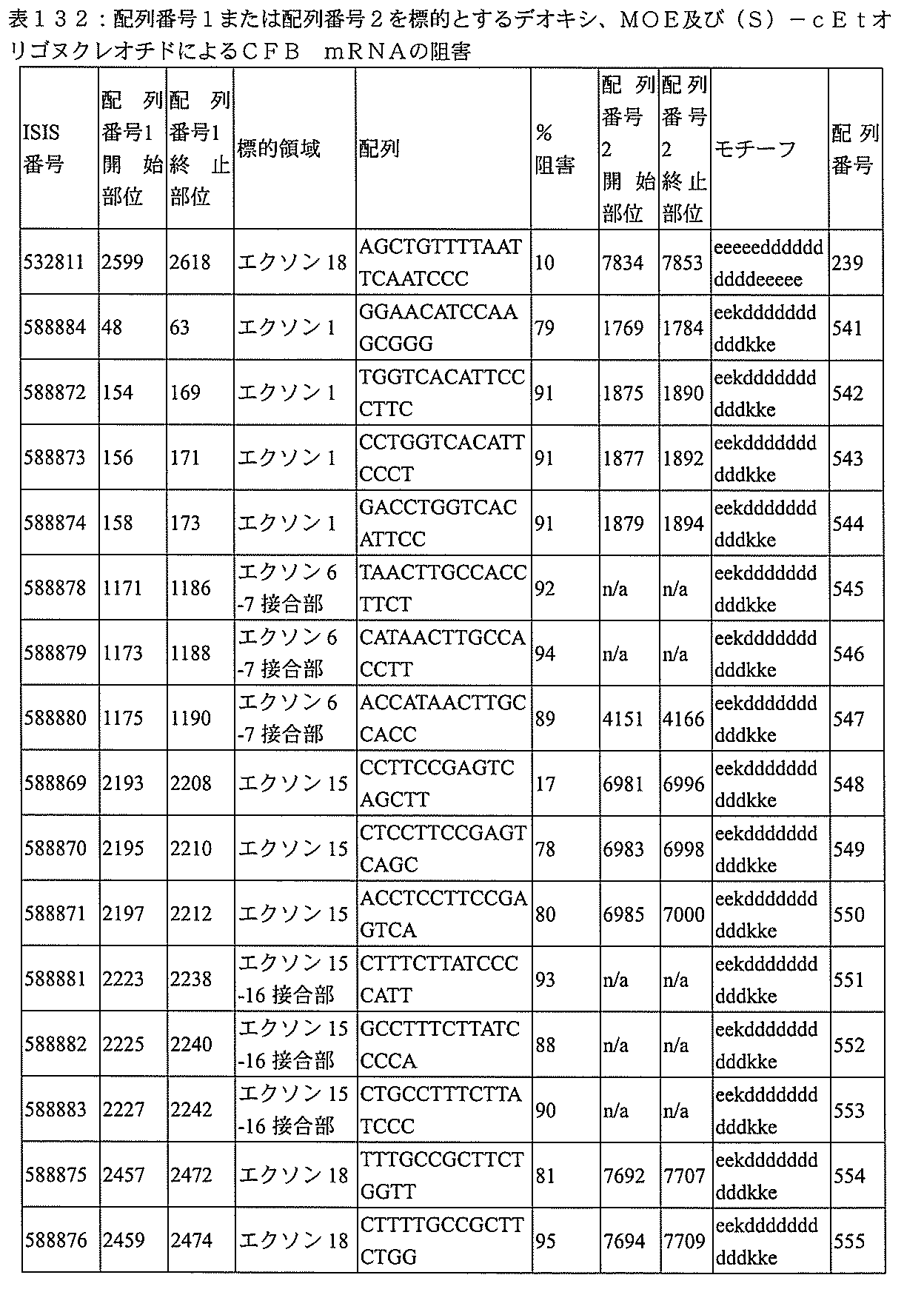
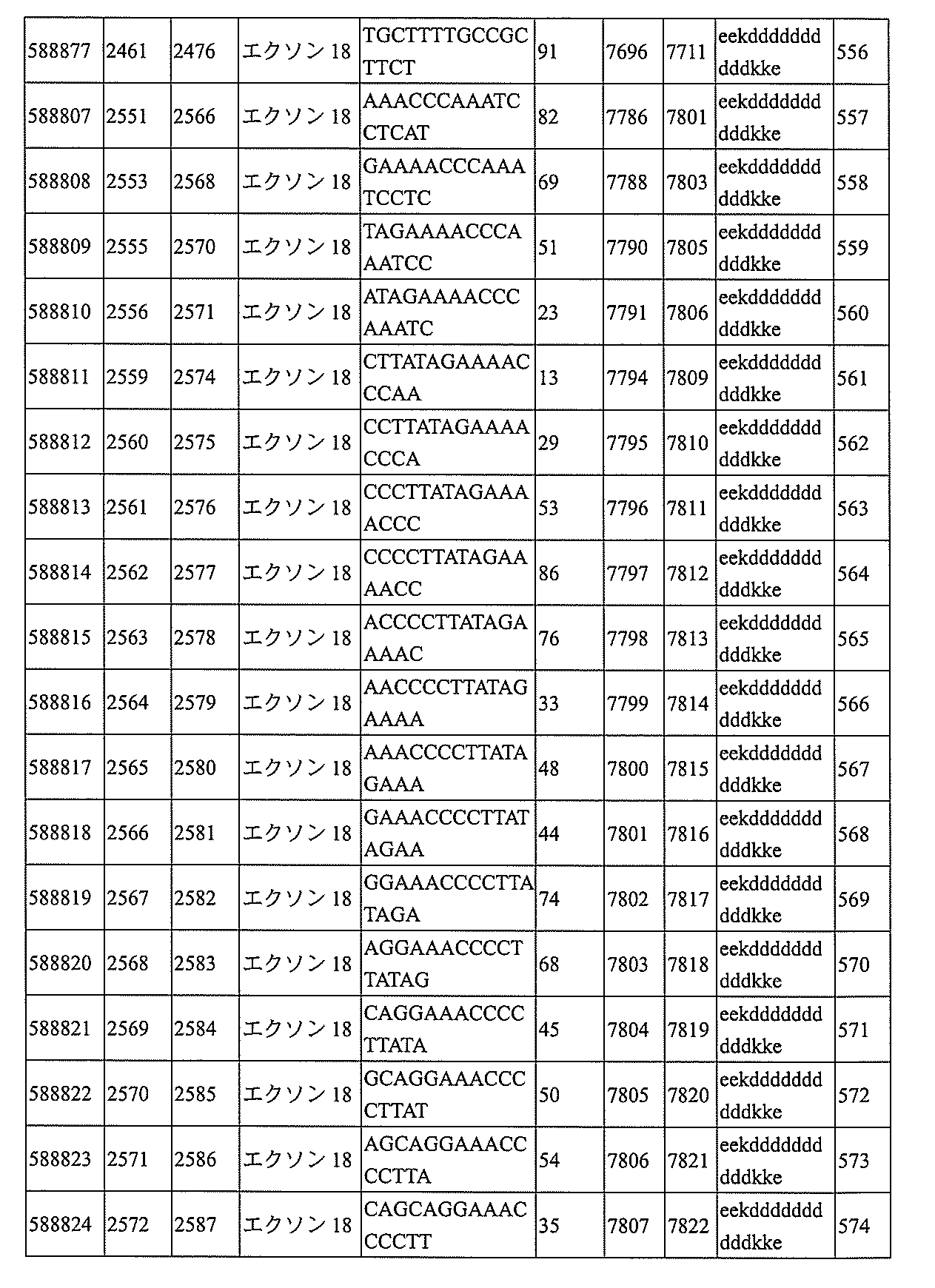
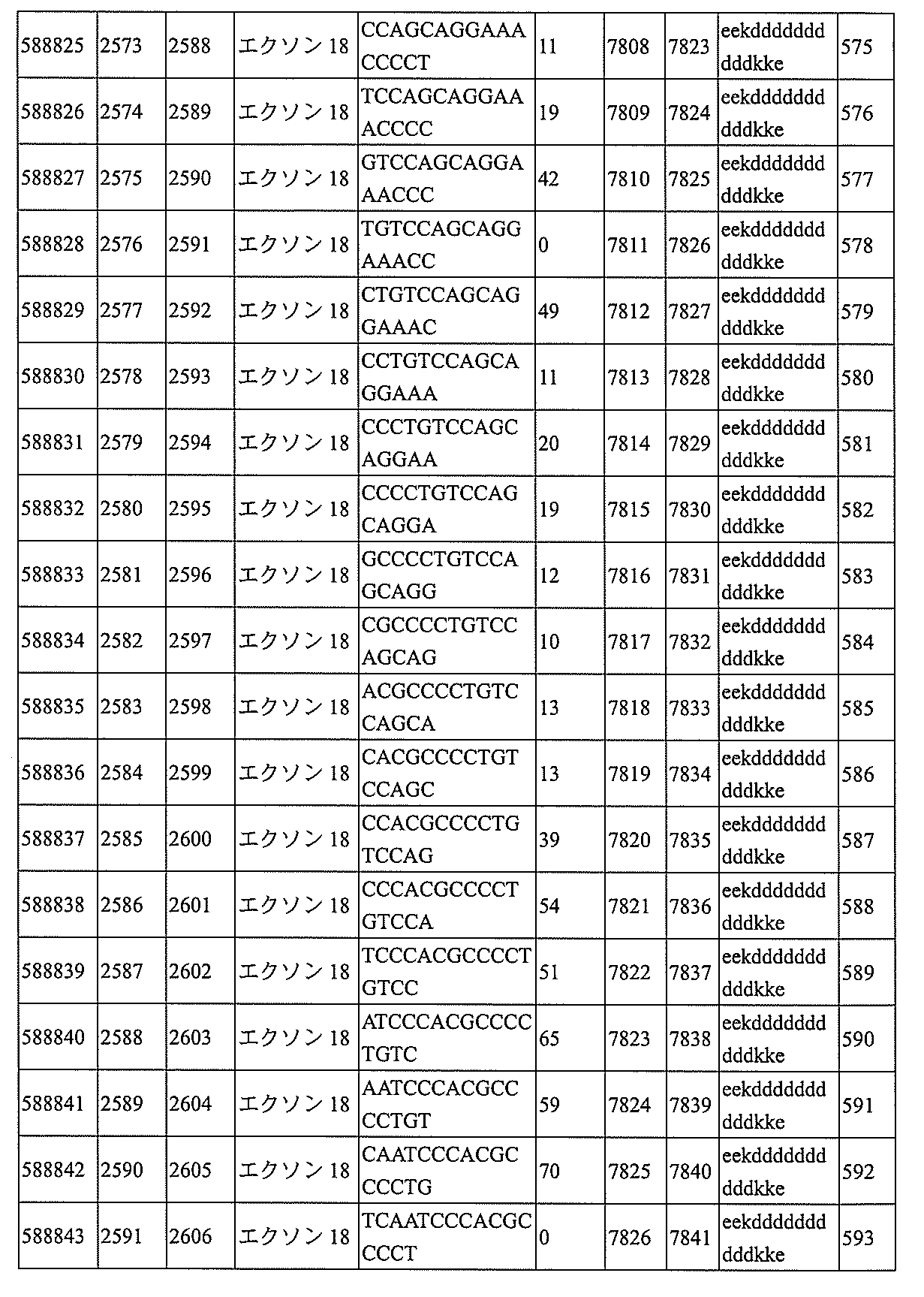
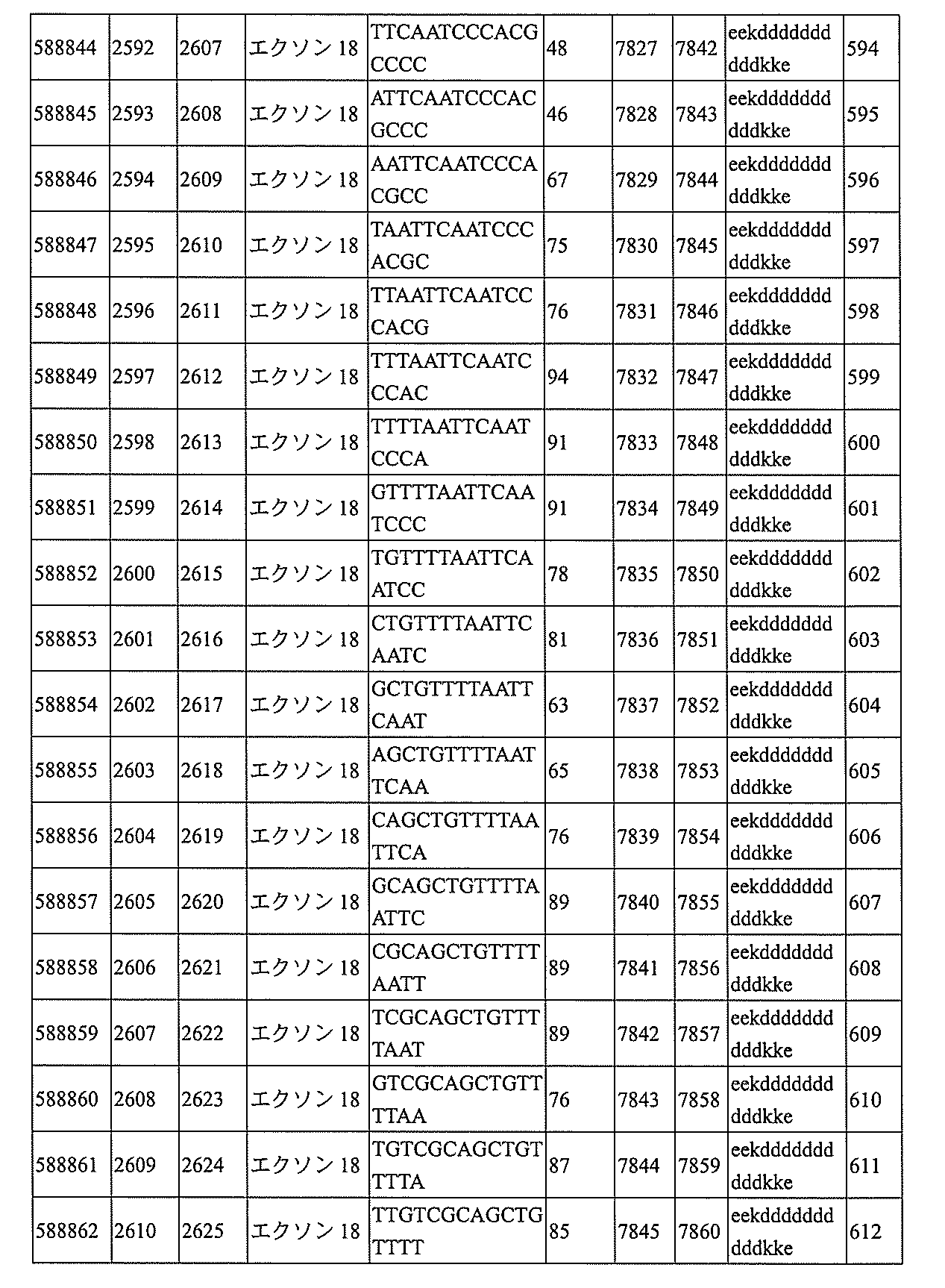
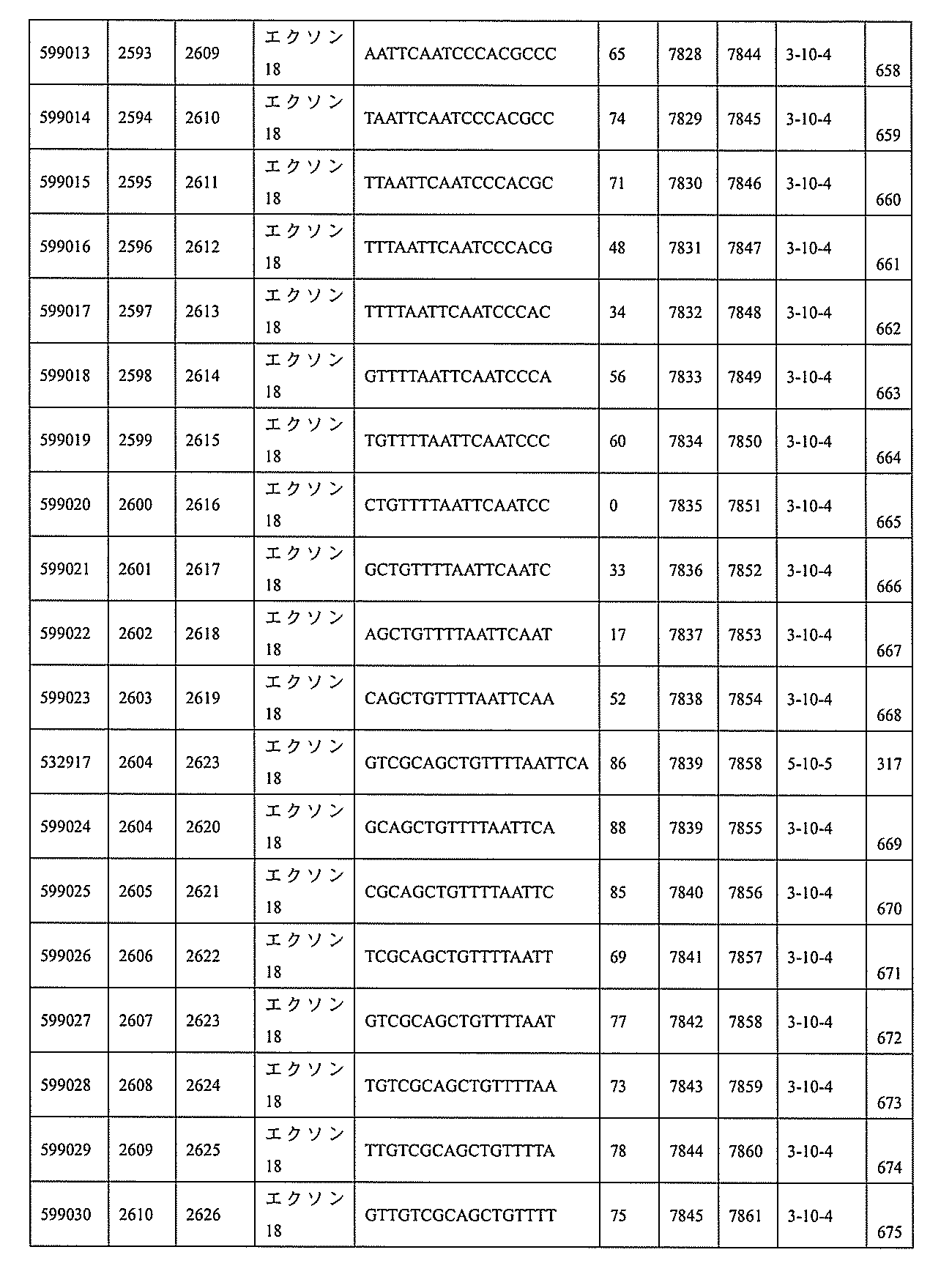
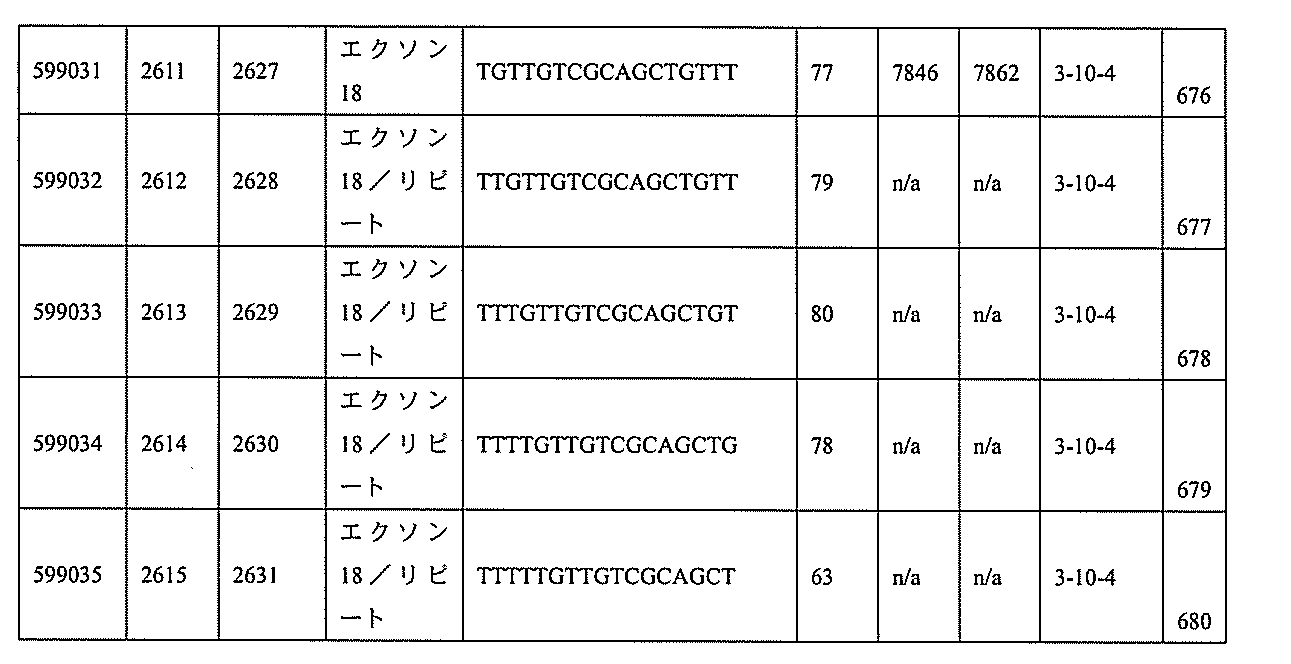
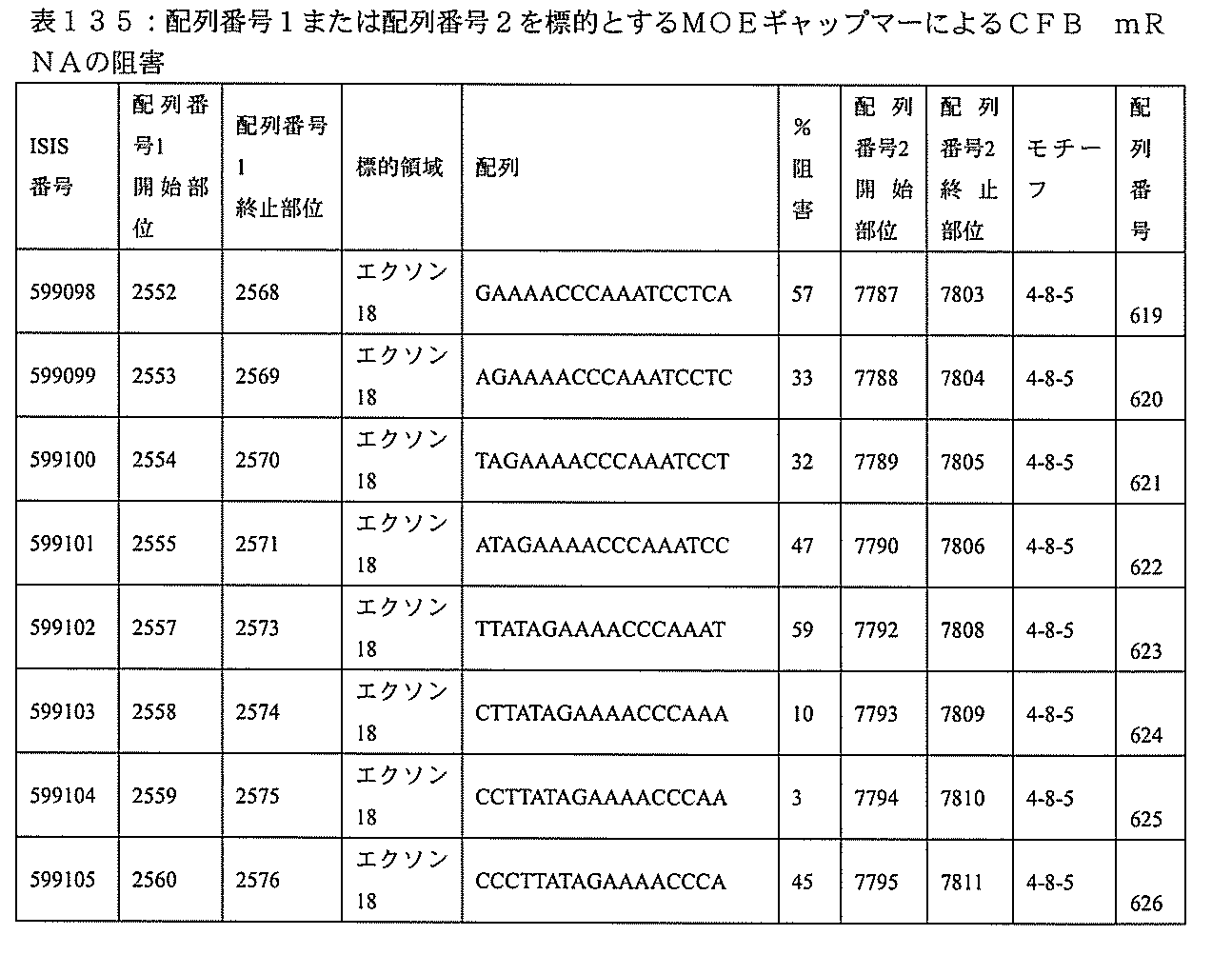
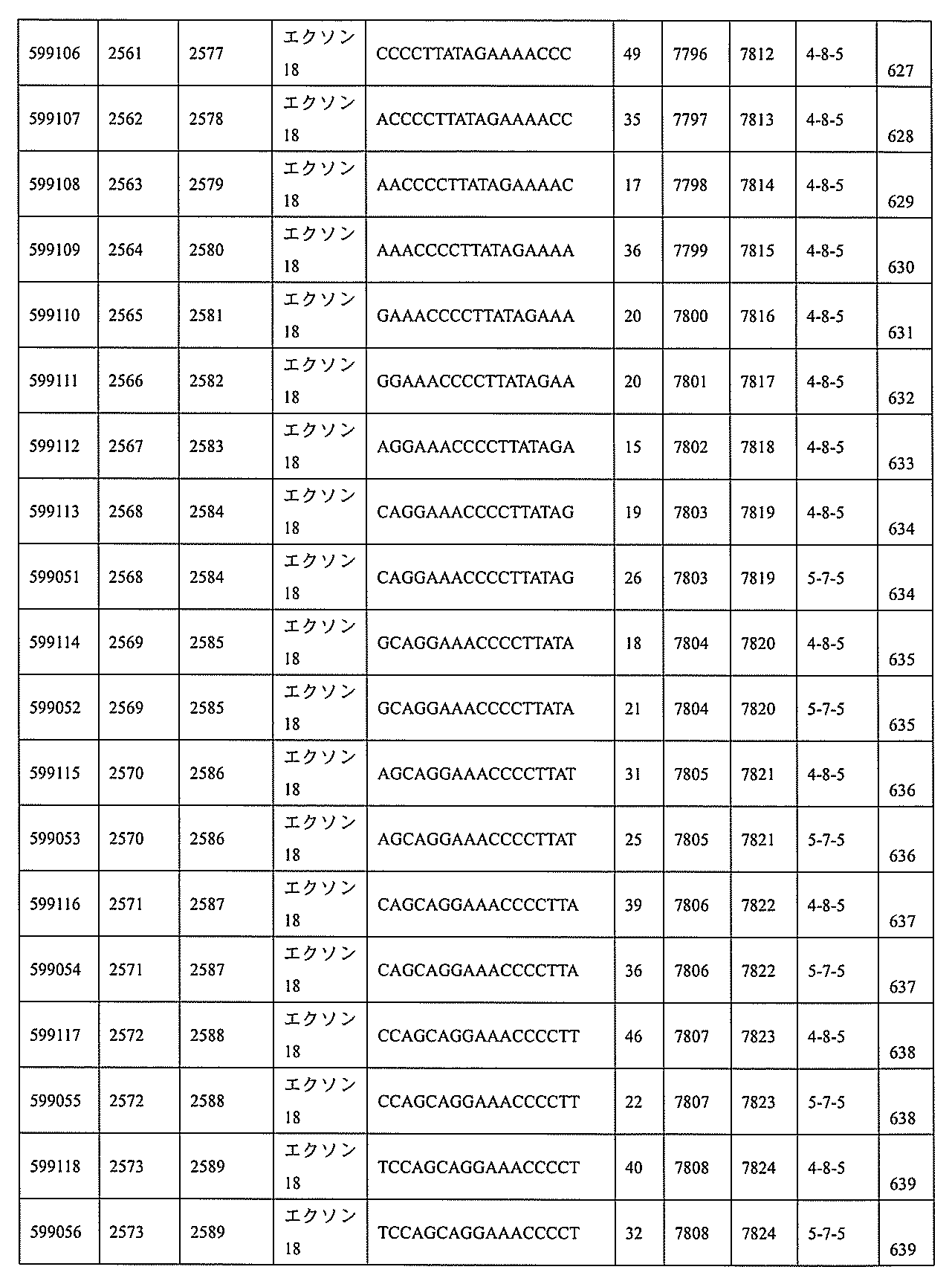
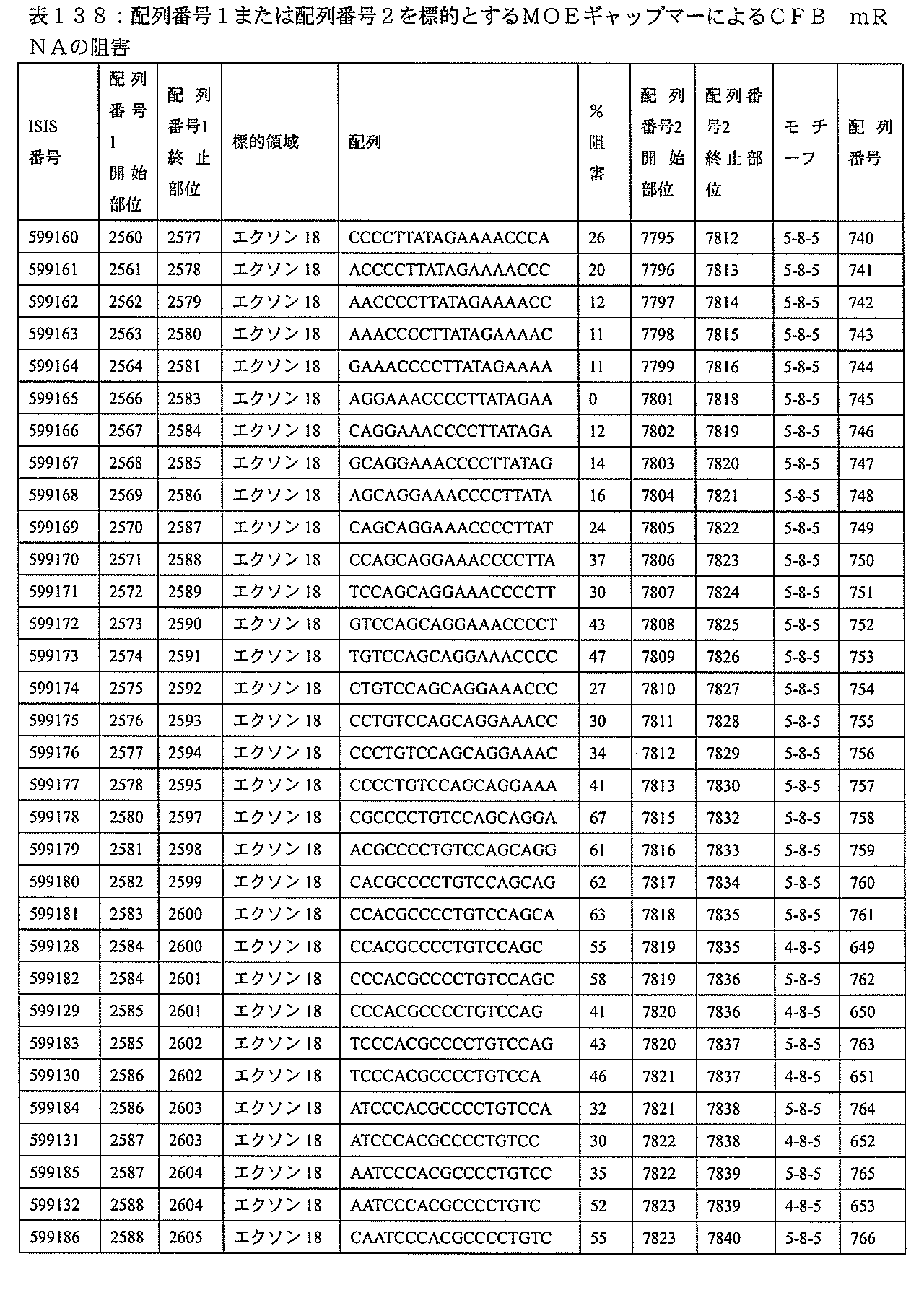
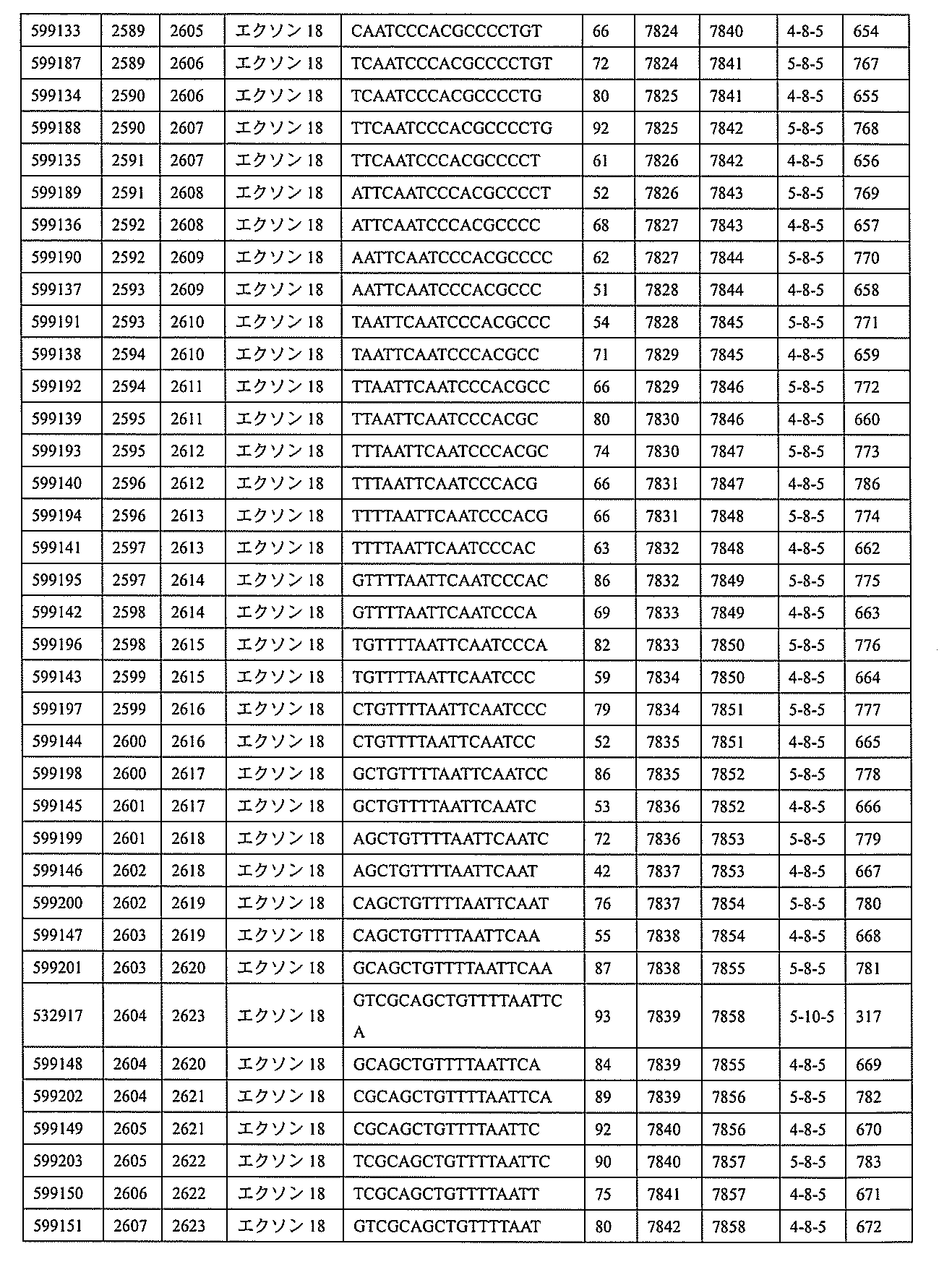
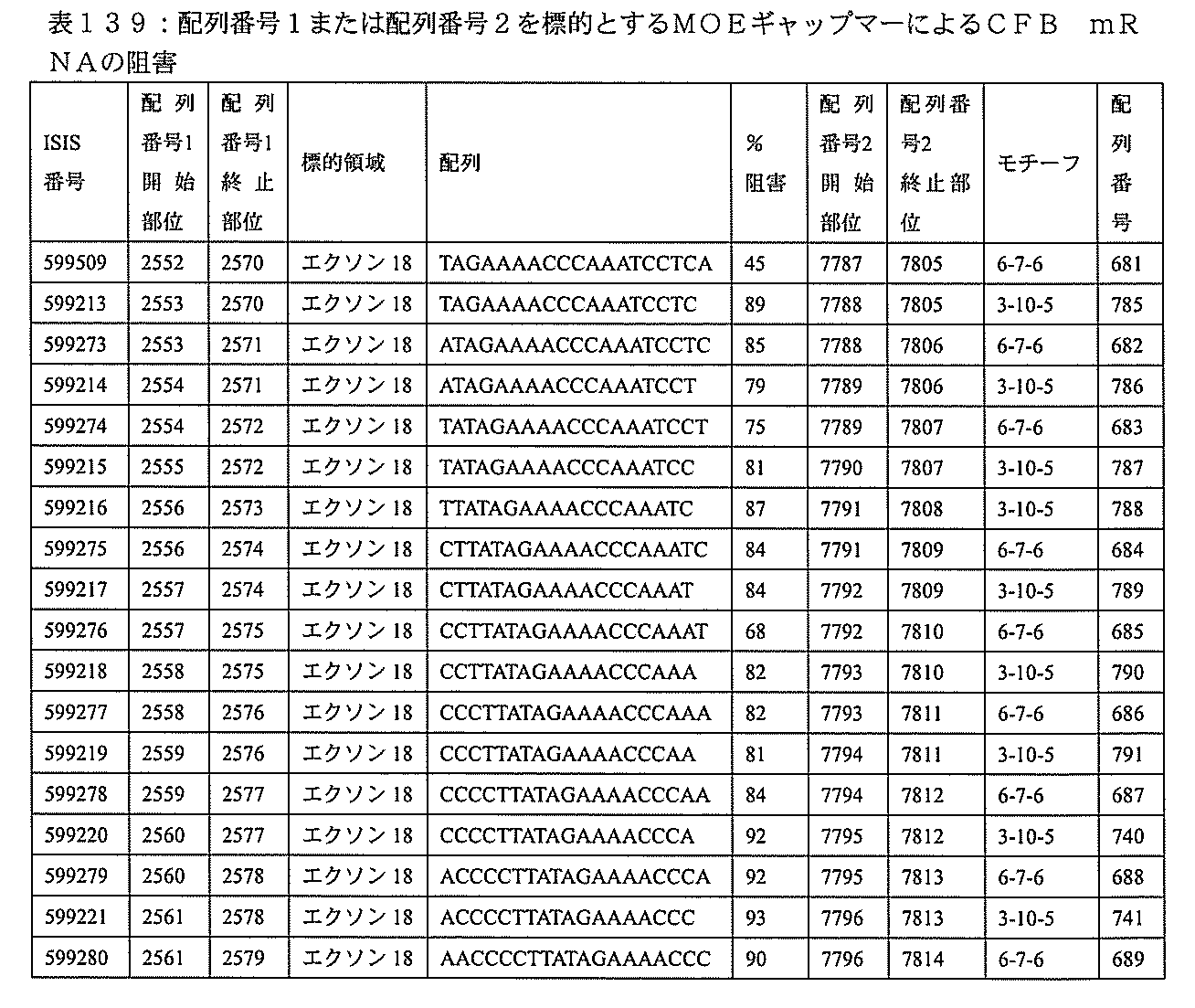
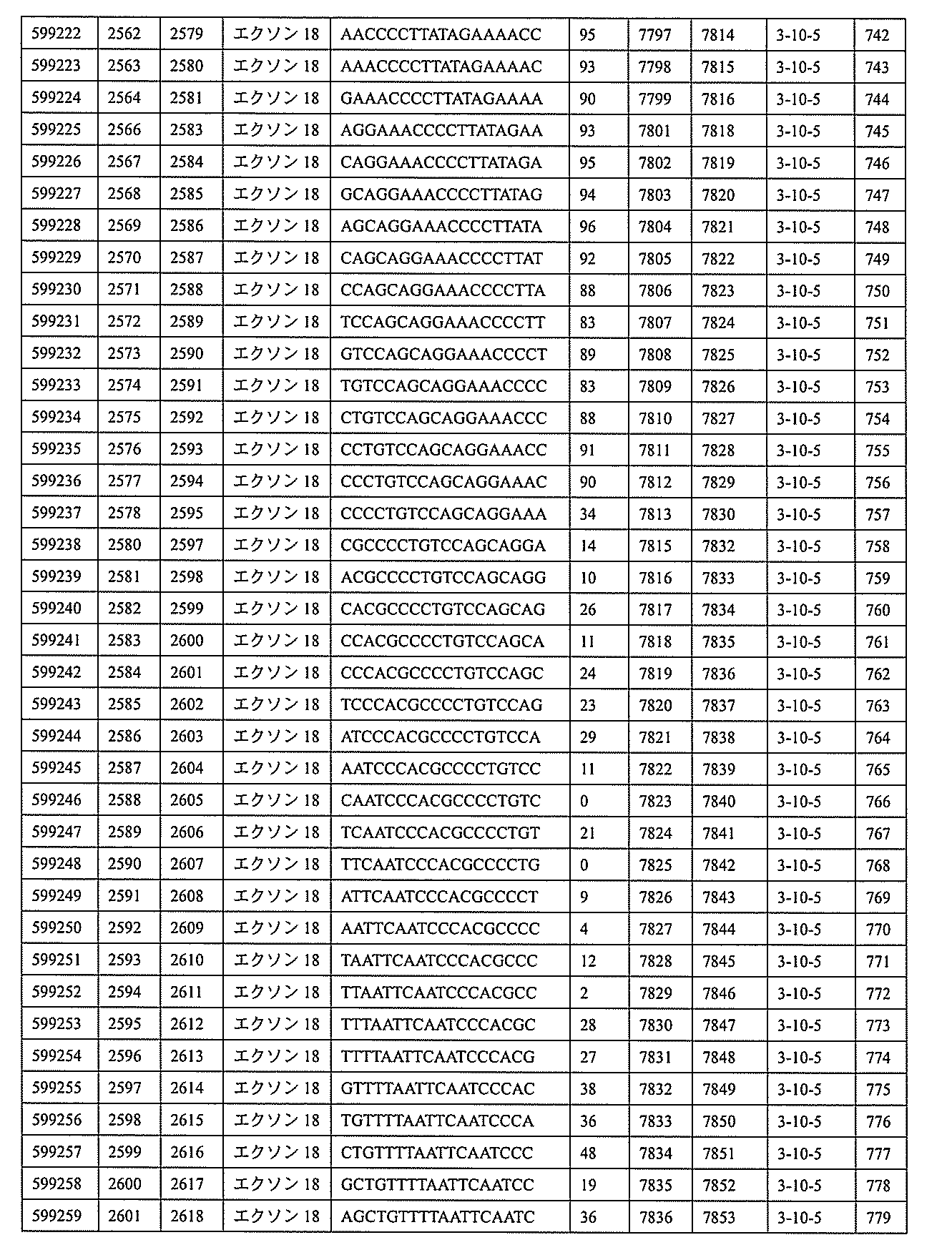
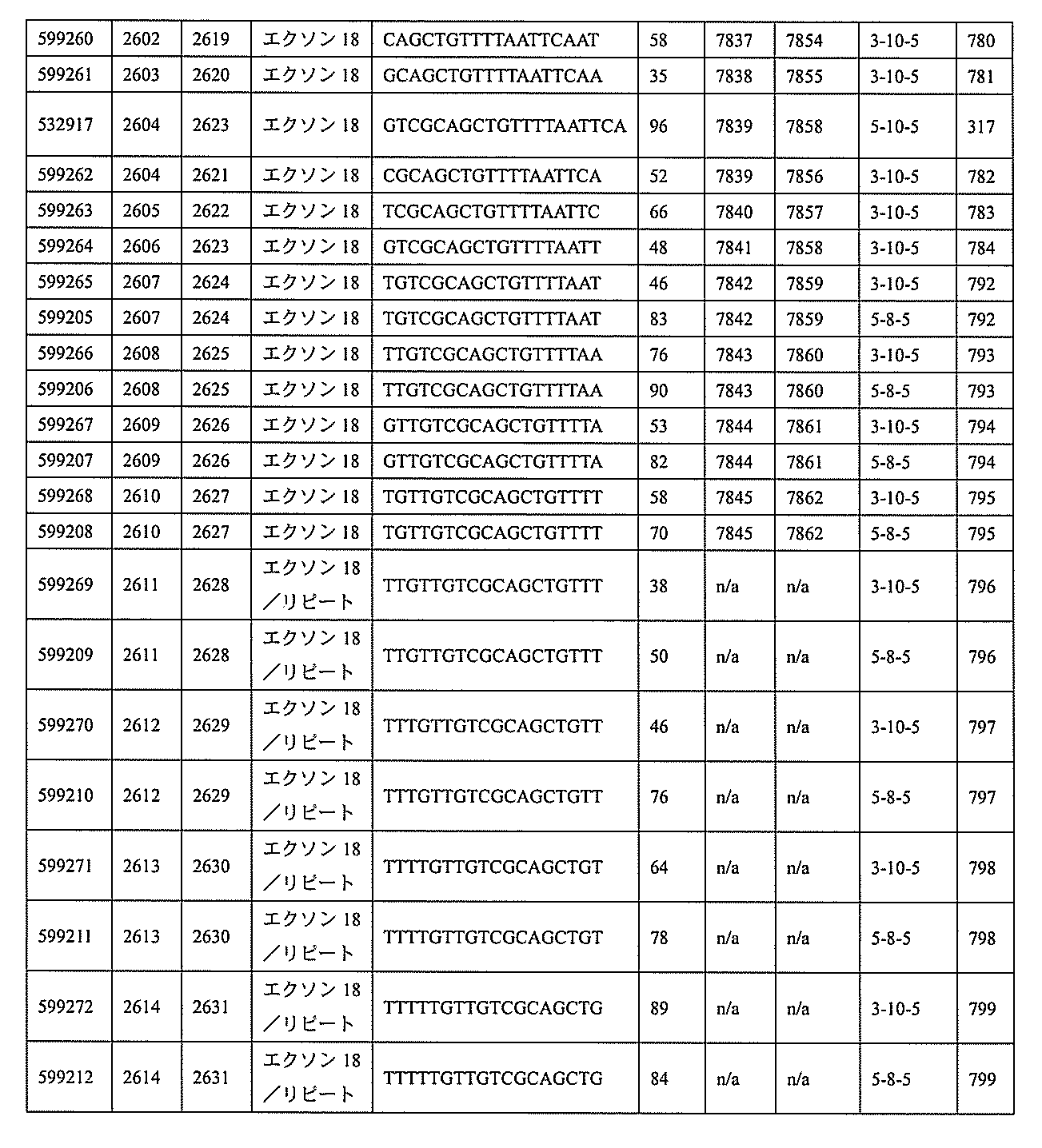
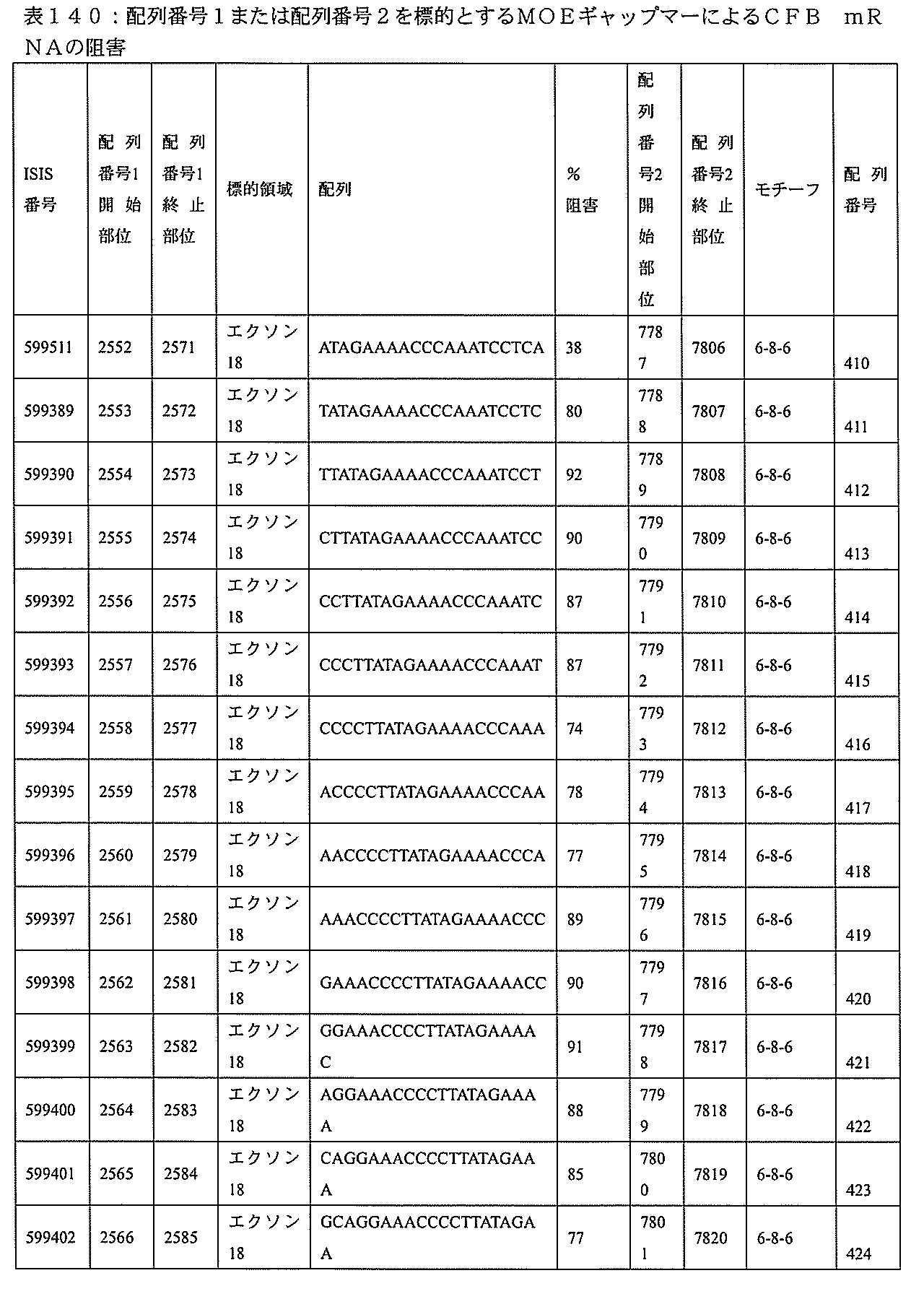
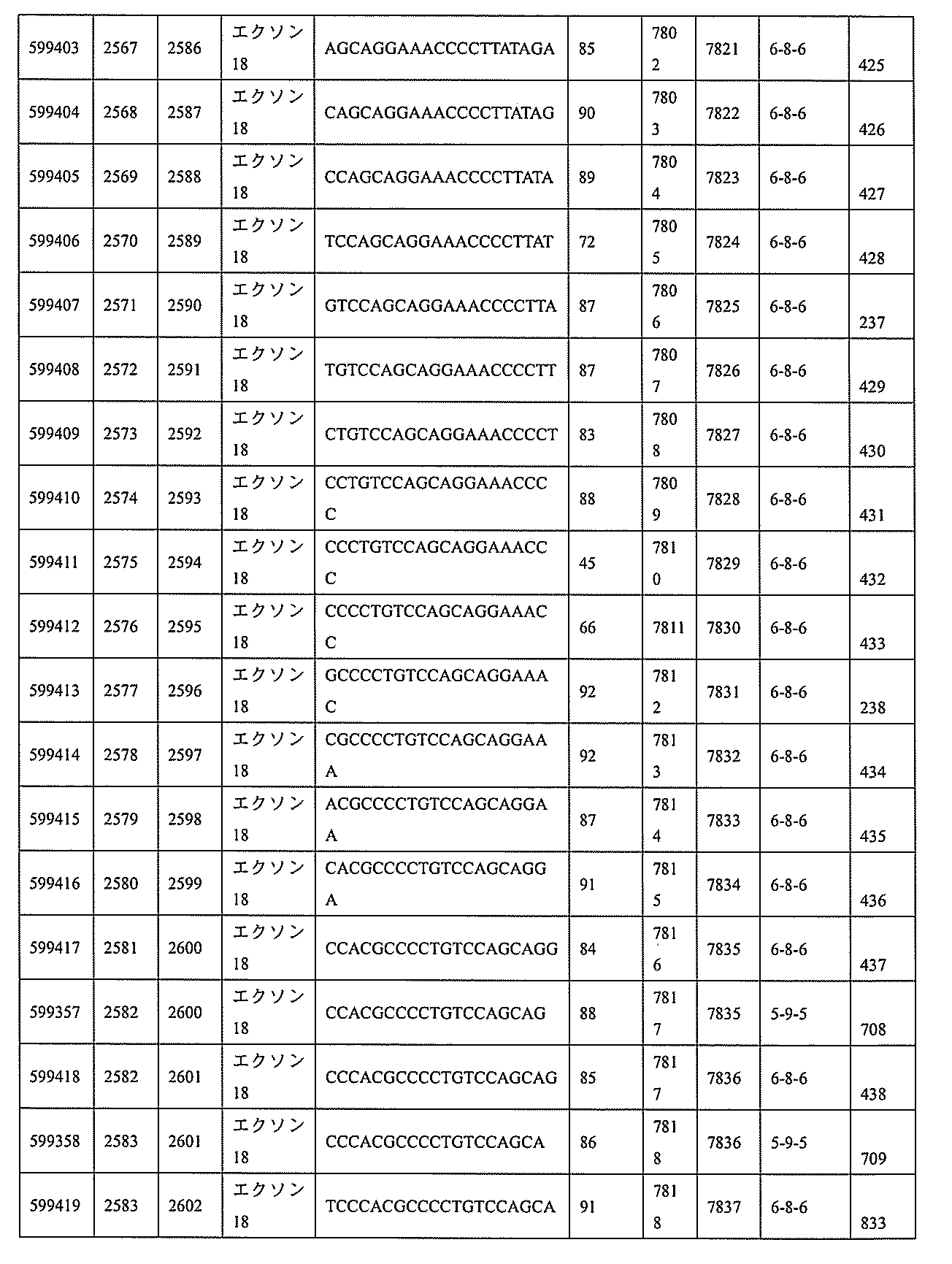
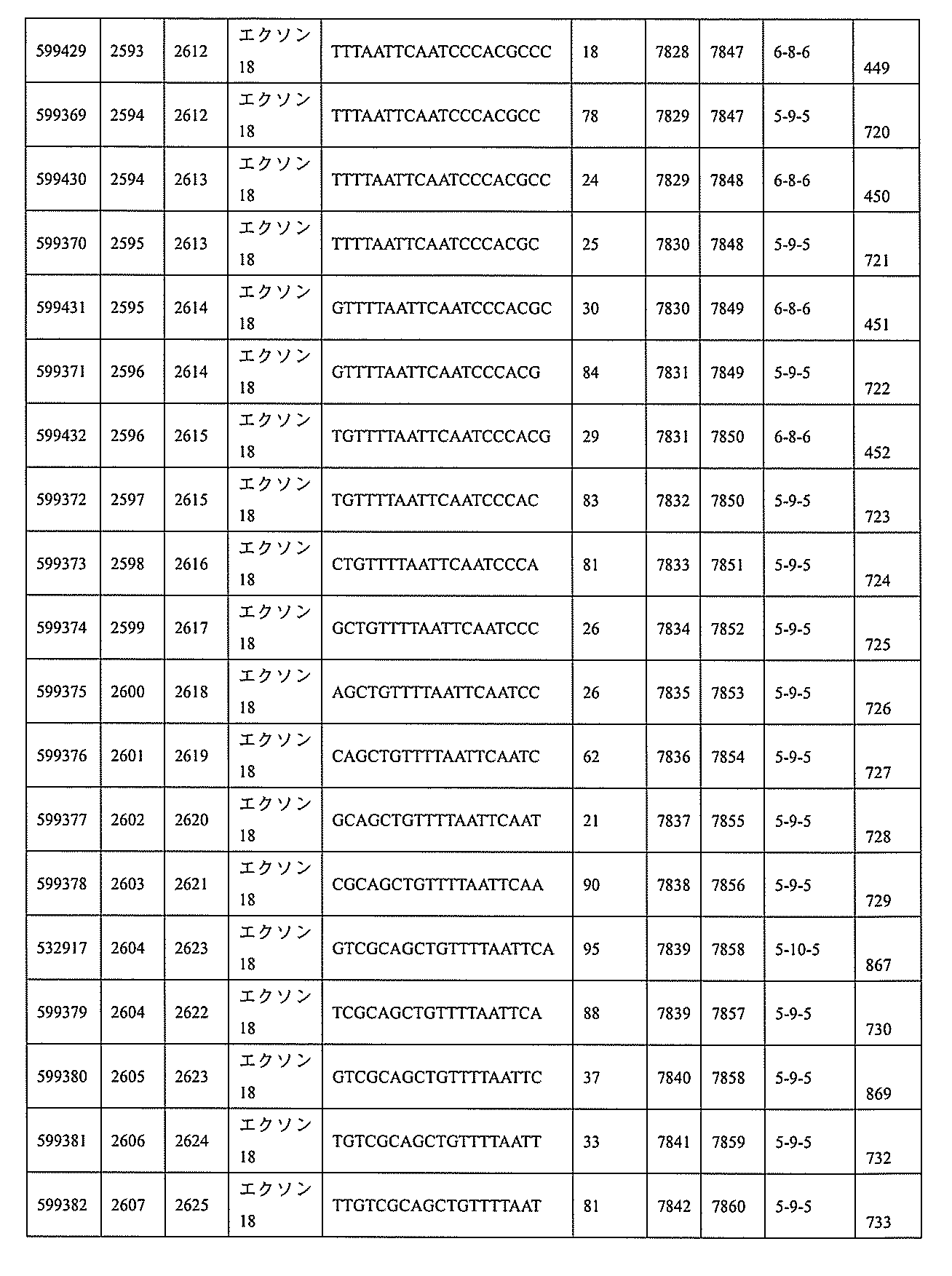
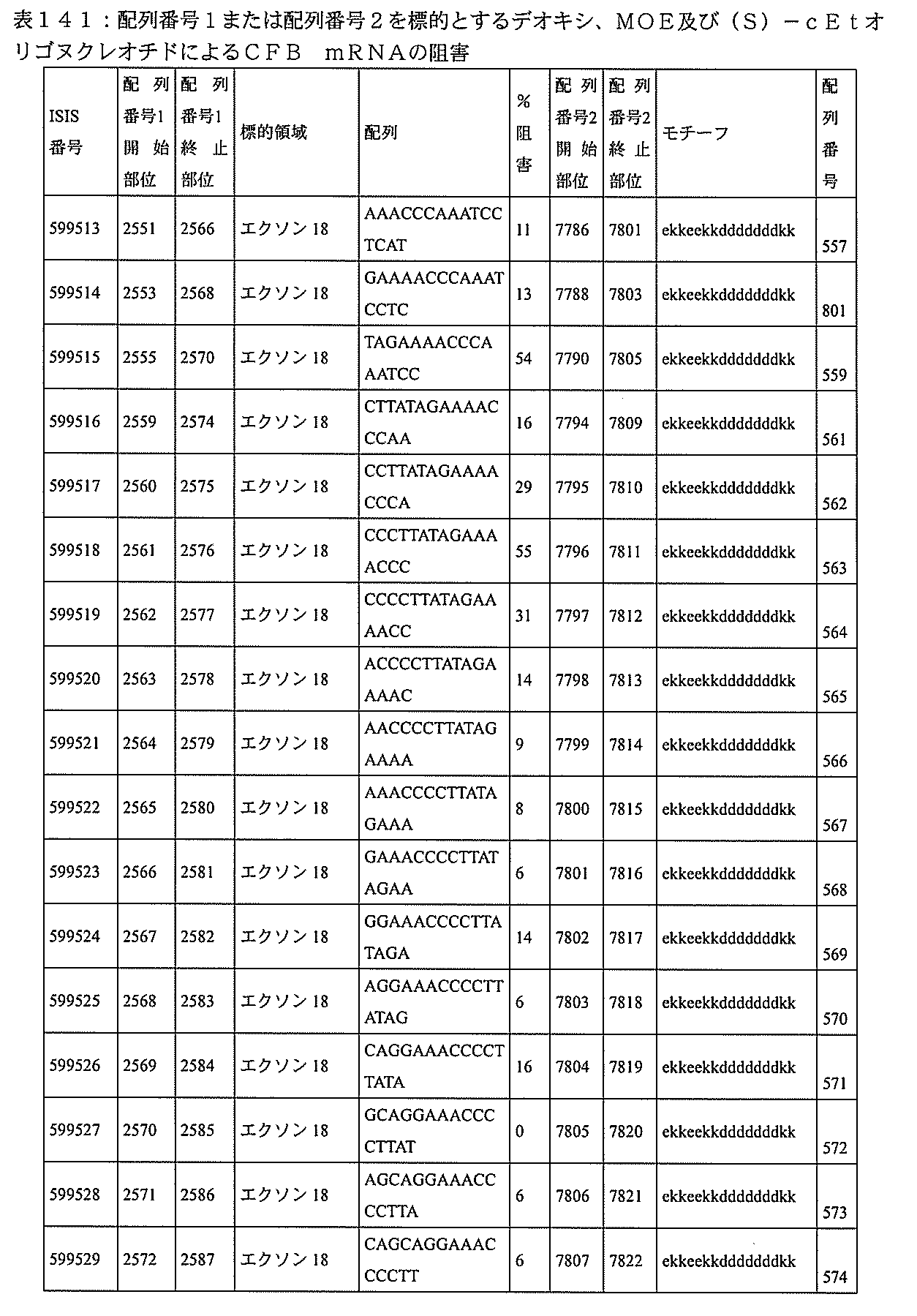
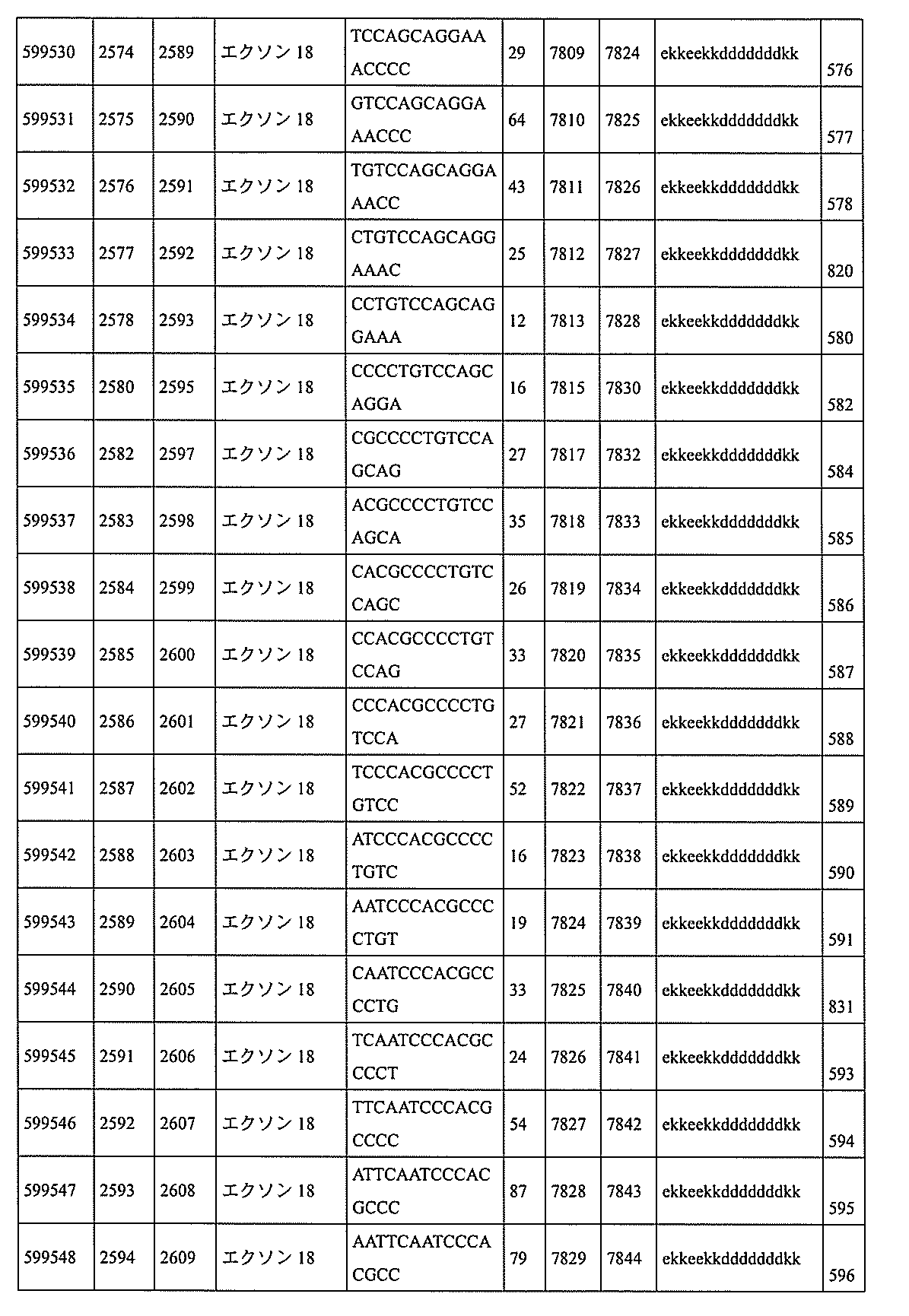
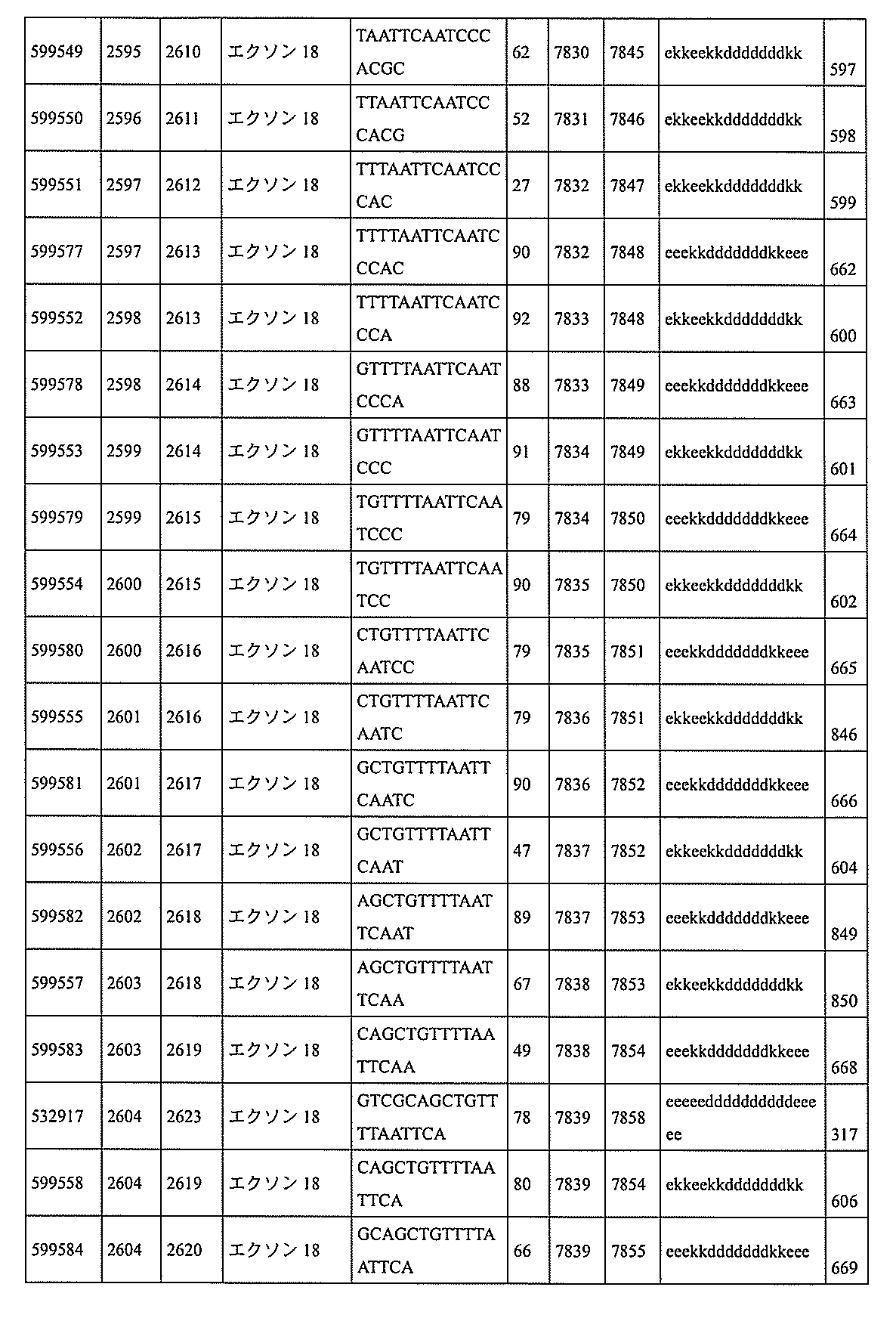
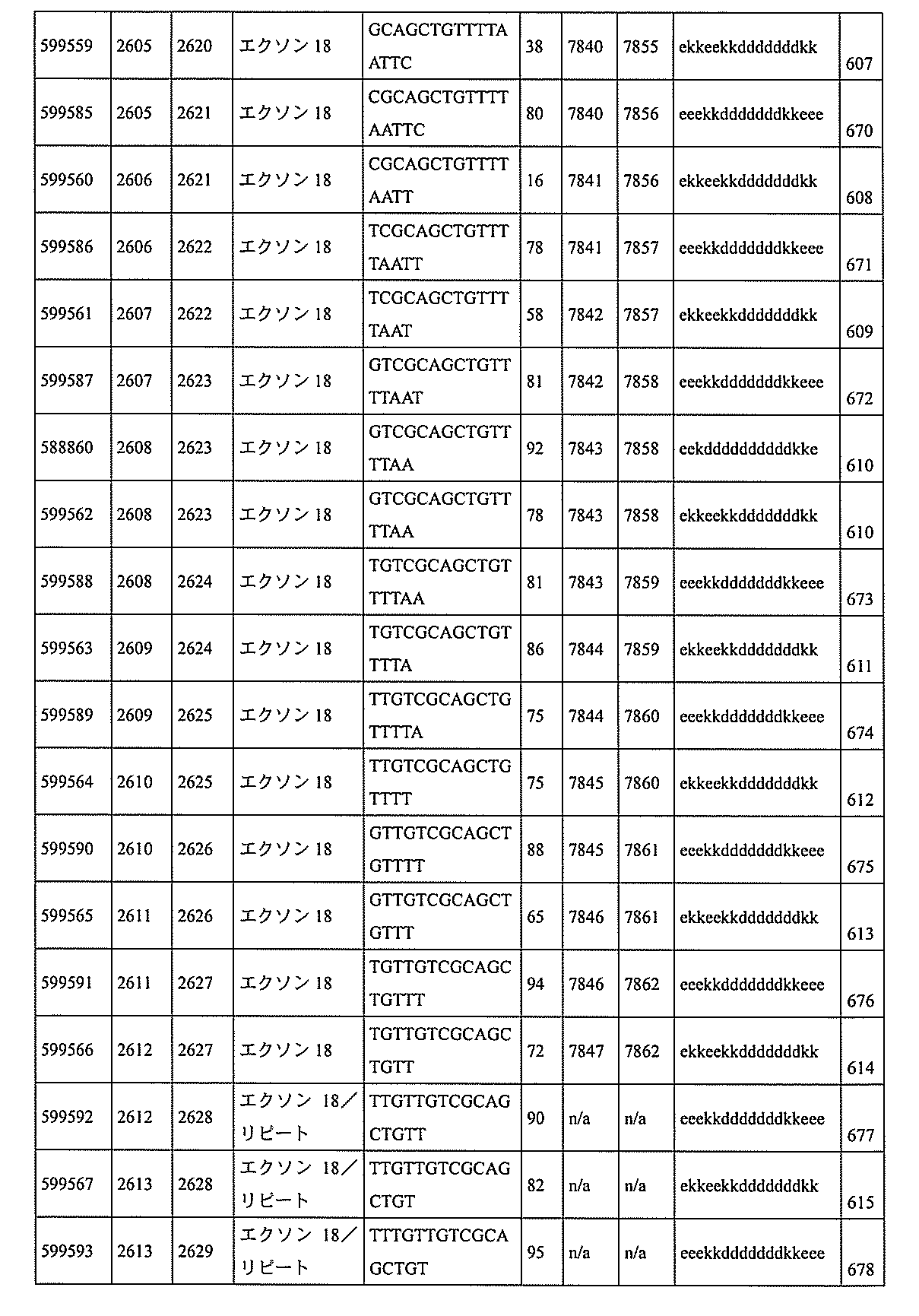
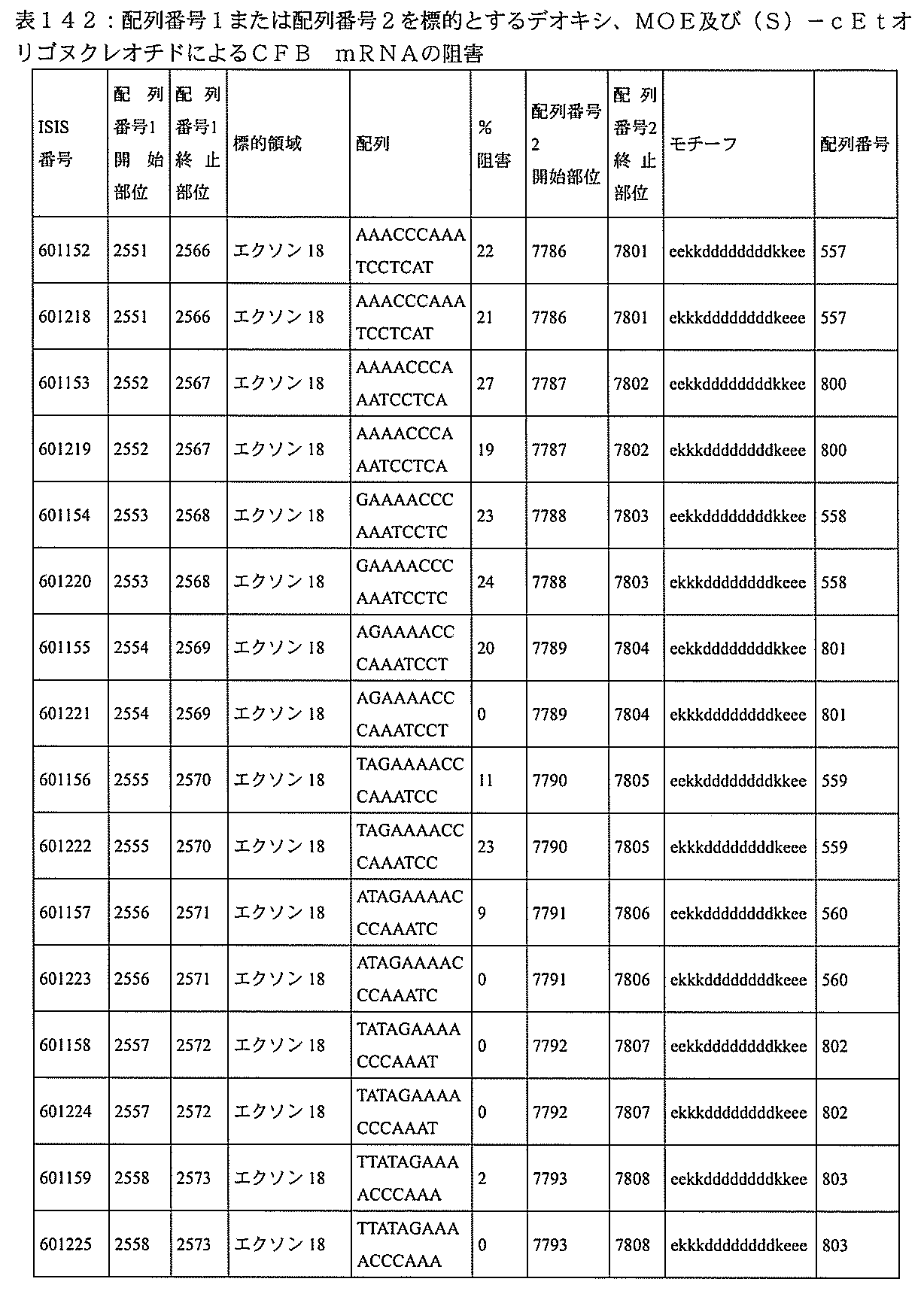
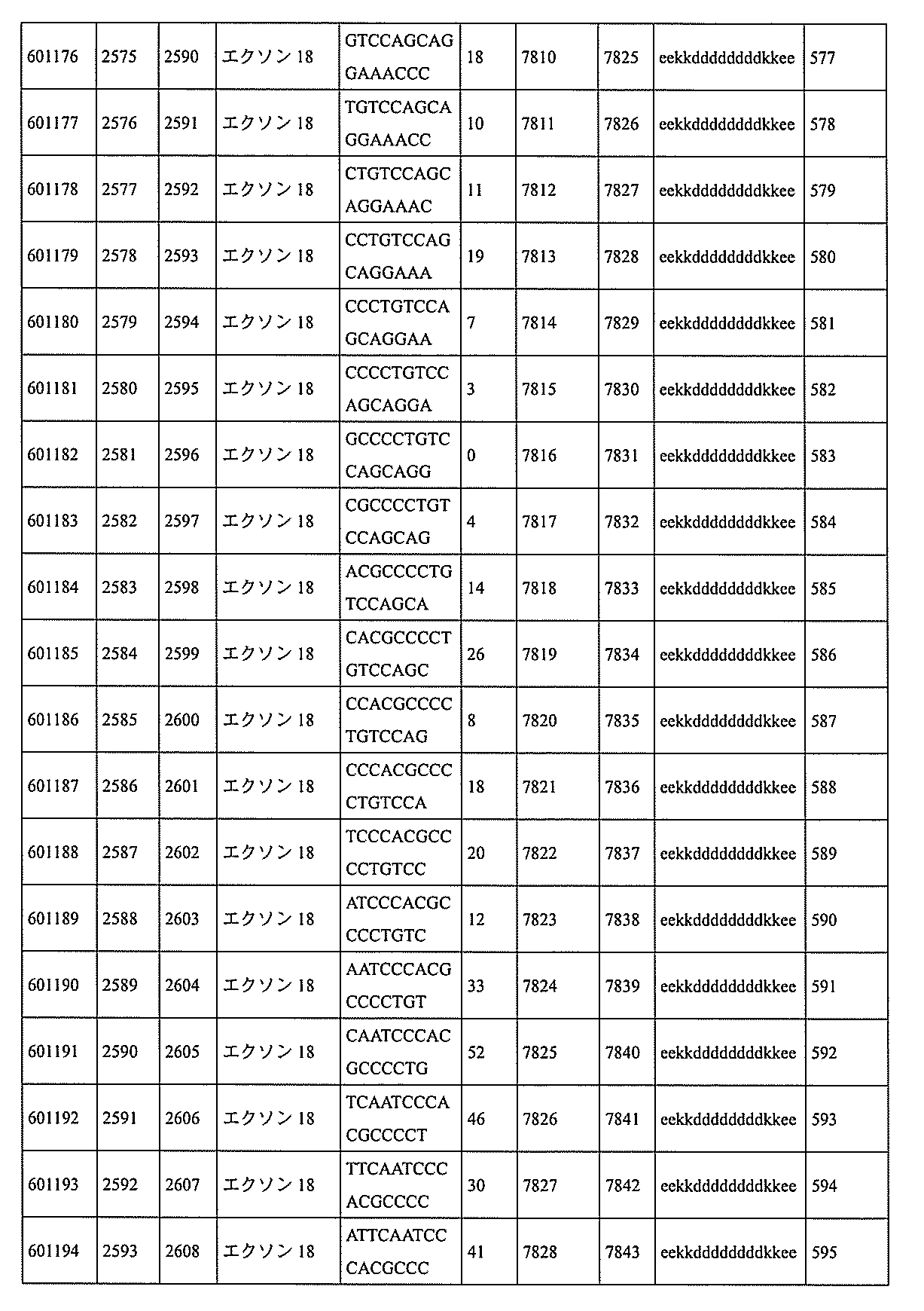
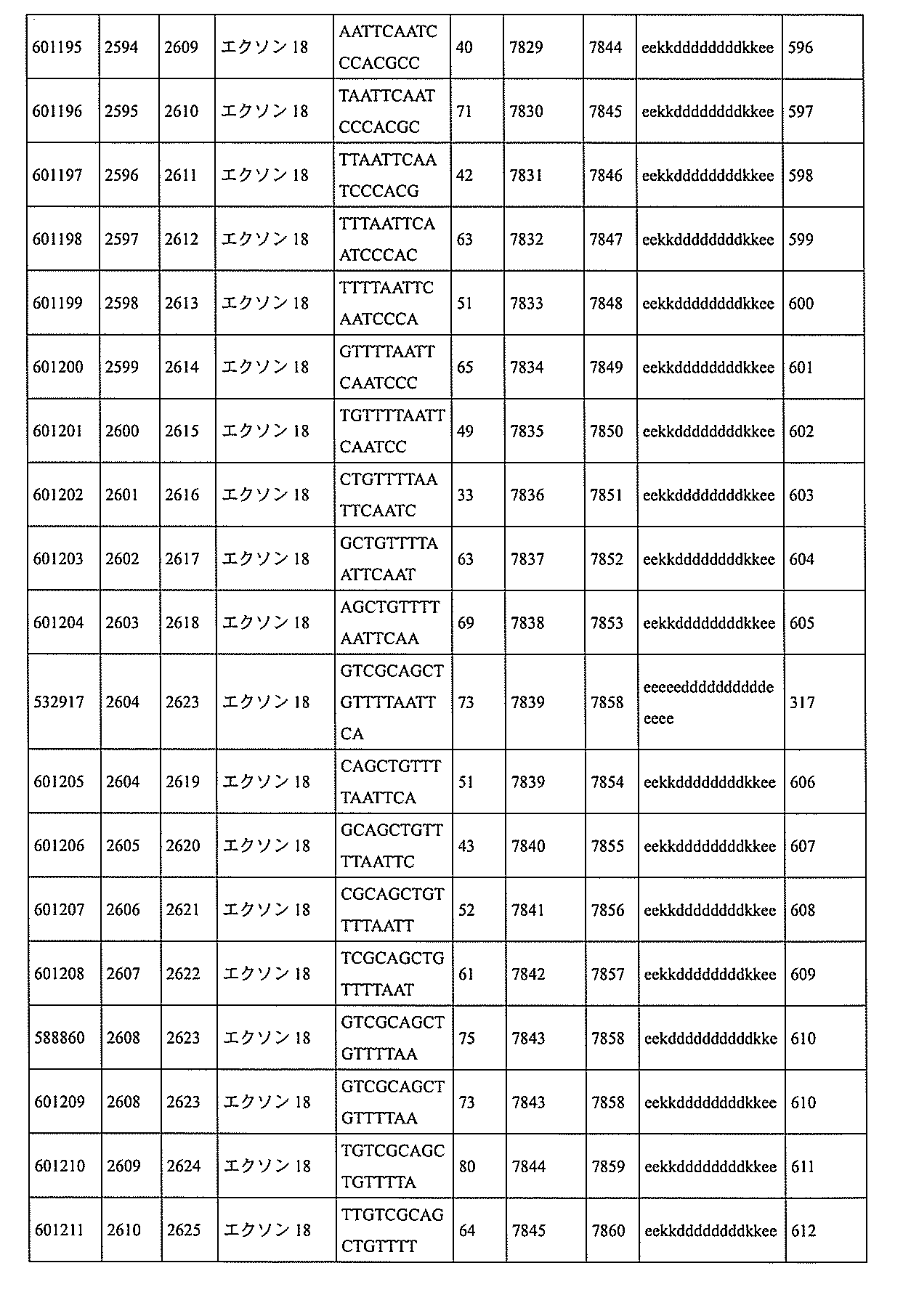
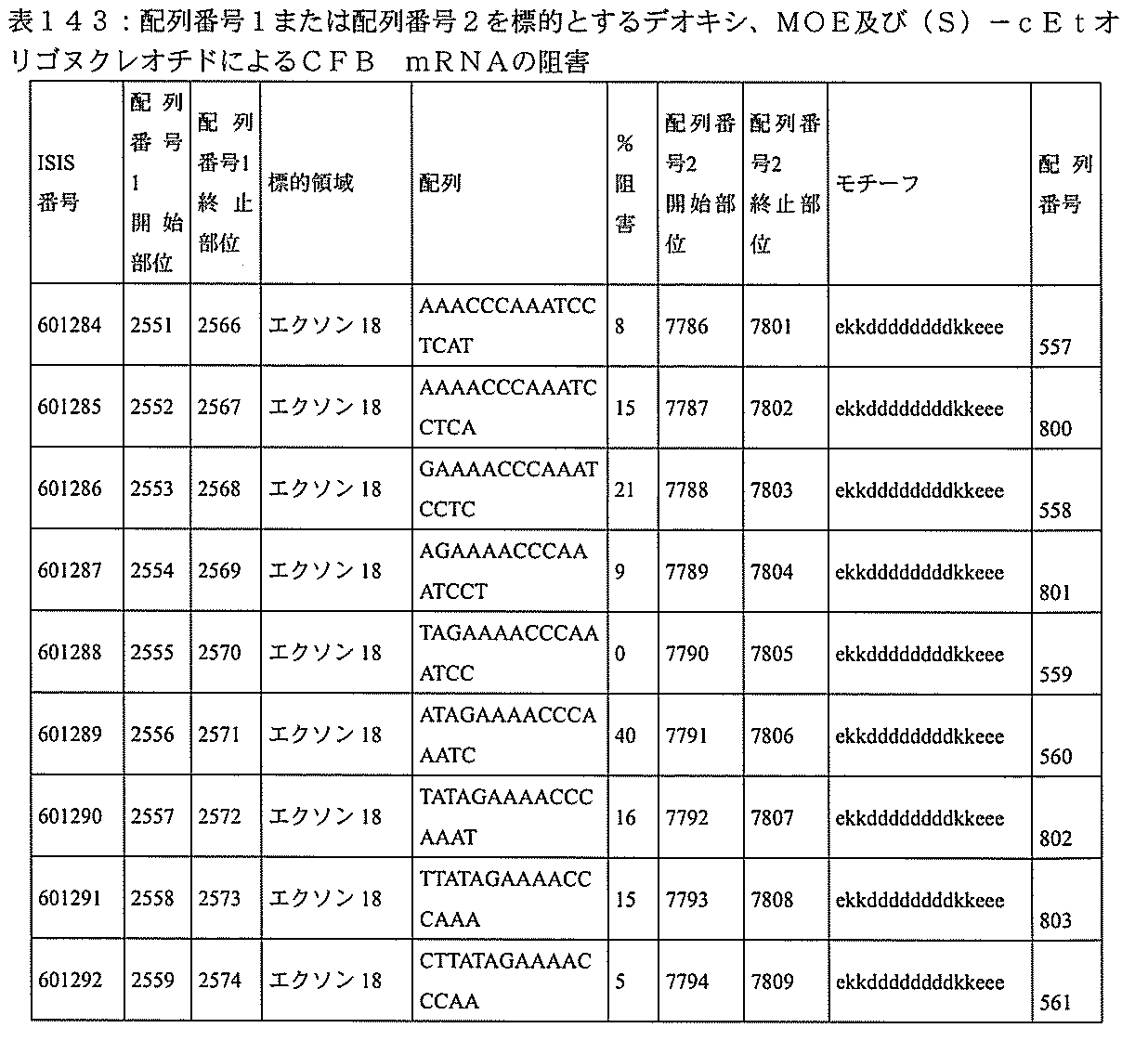
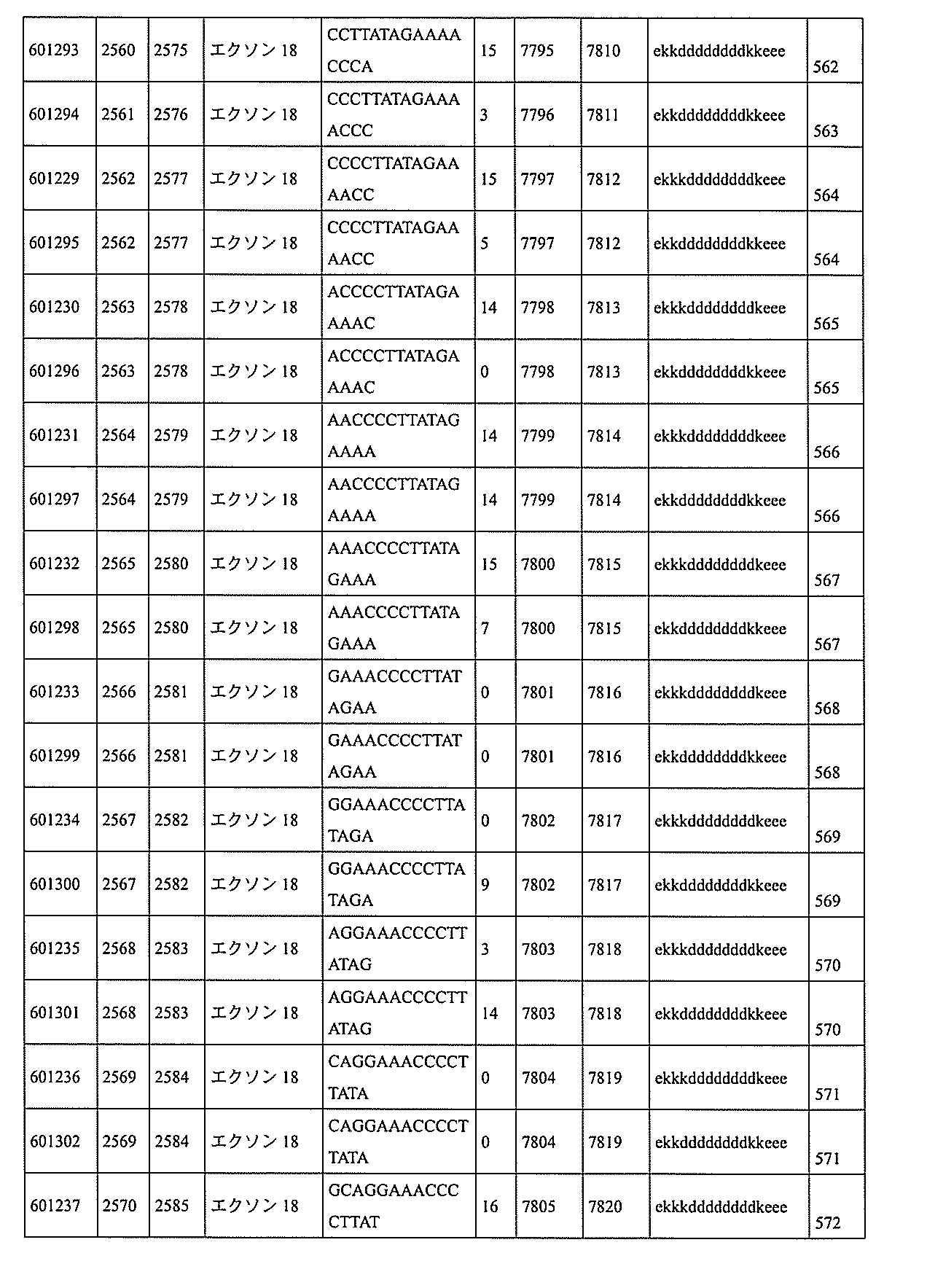
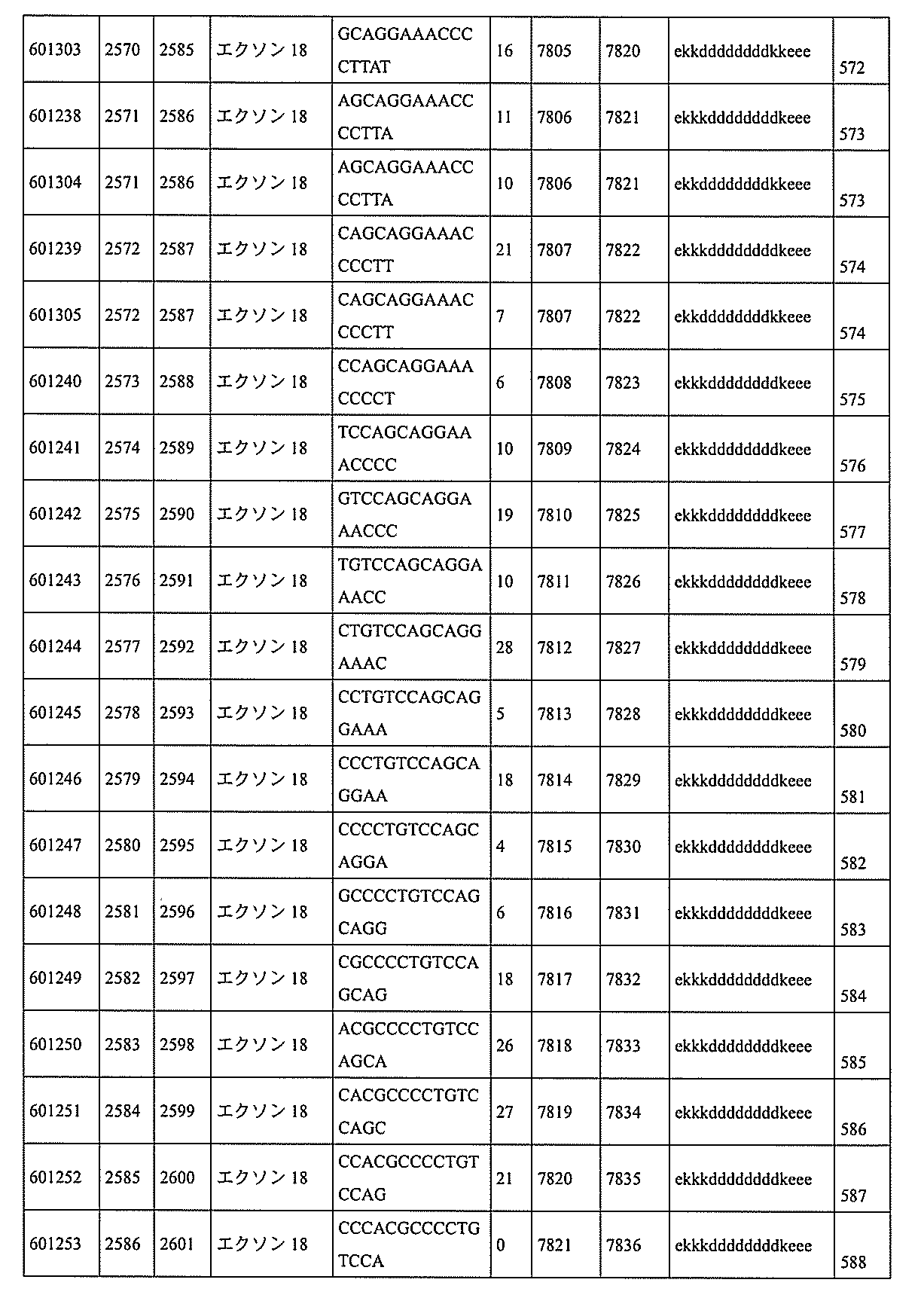
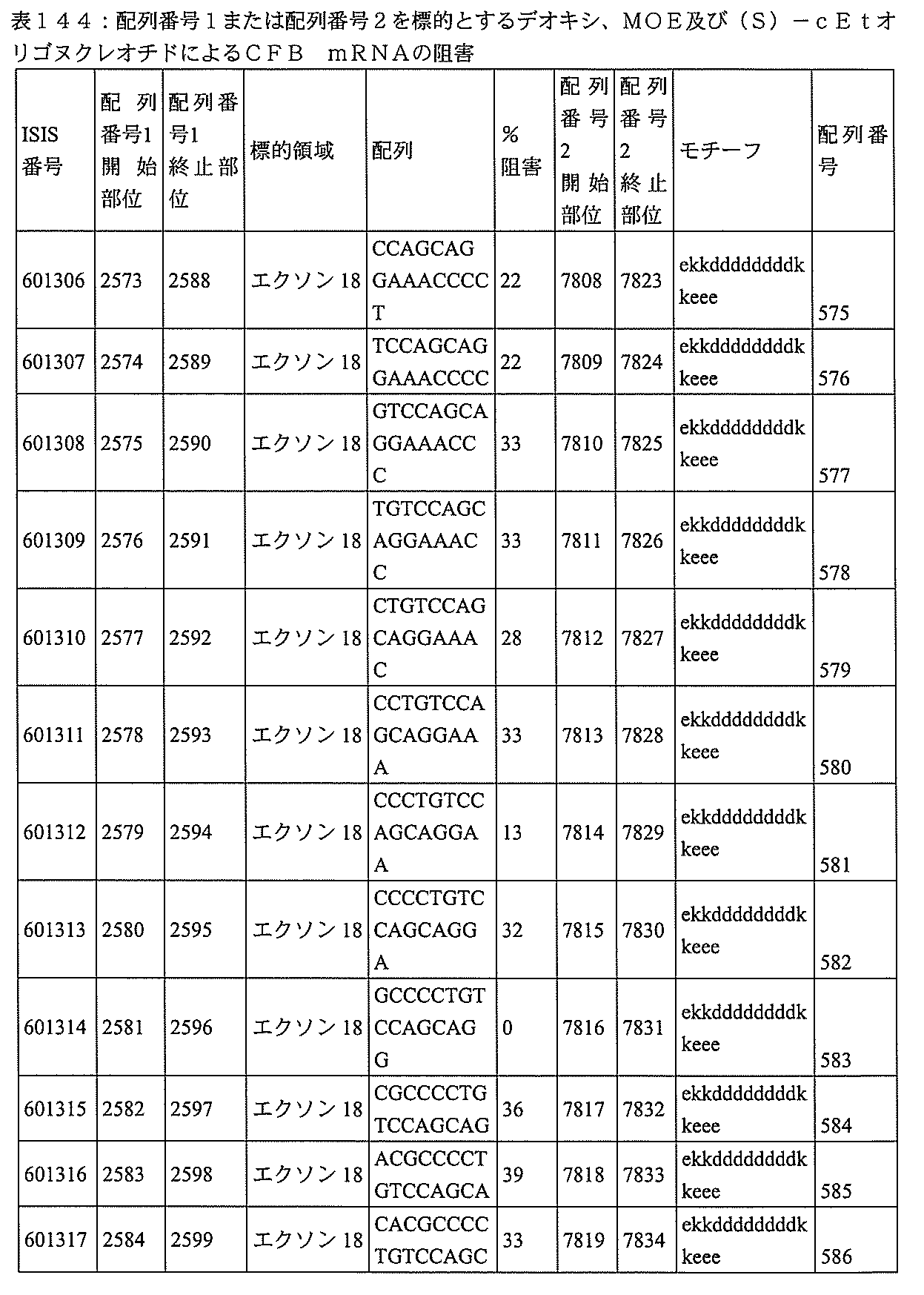
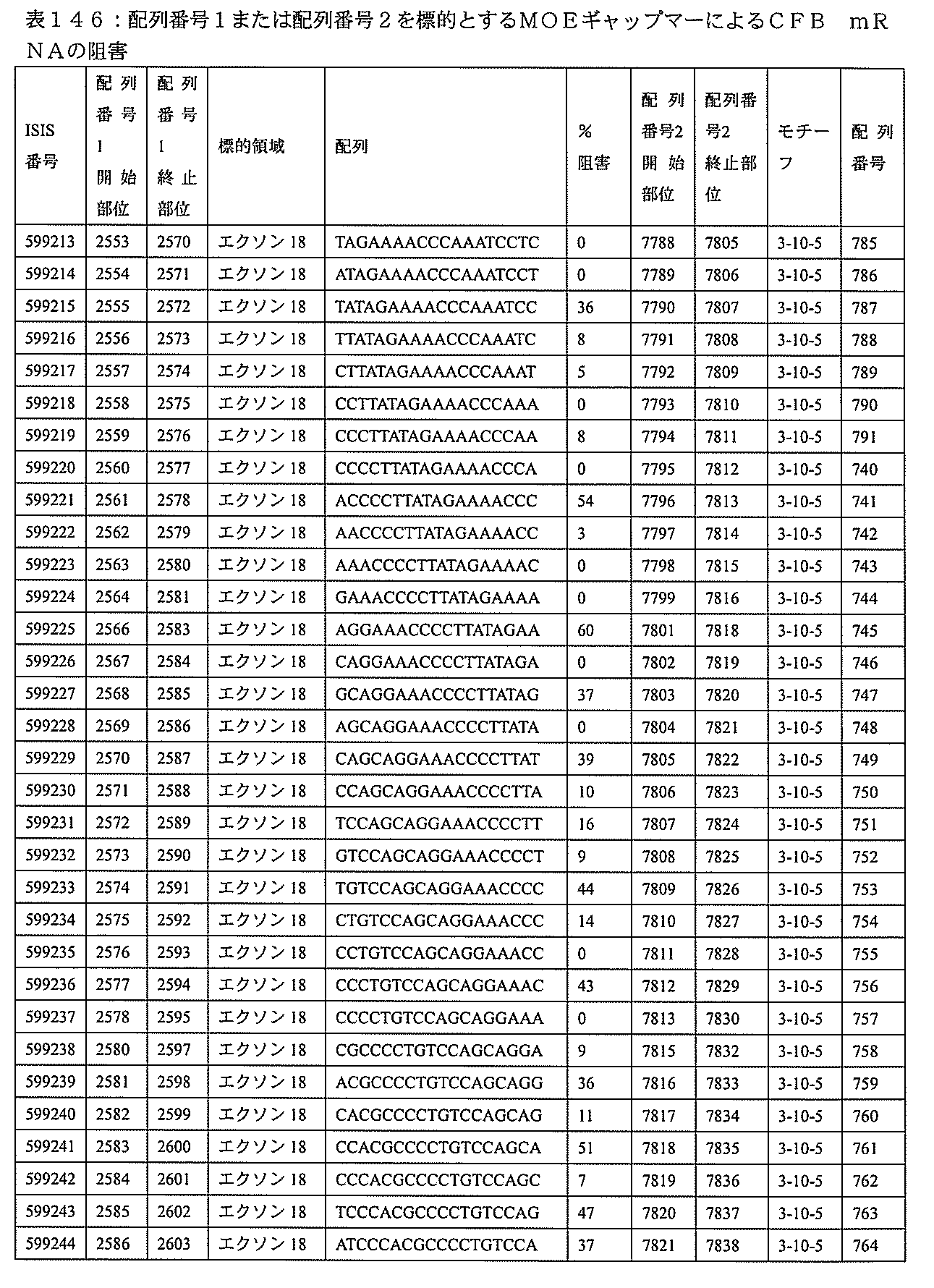
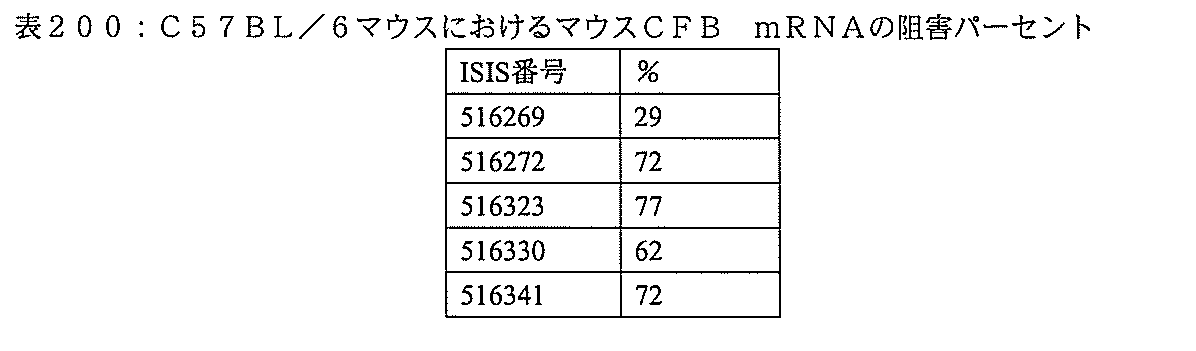
特定の実施形態は、補体B因子(CFB)発現を阻害するための方法、化合物及び組成物を提供する。
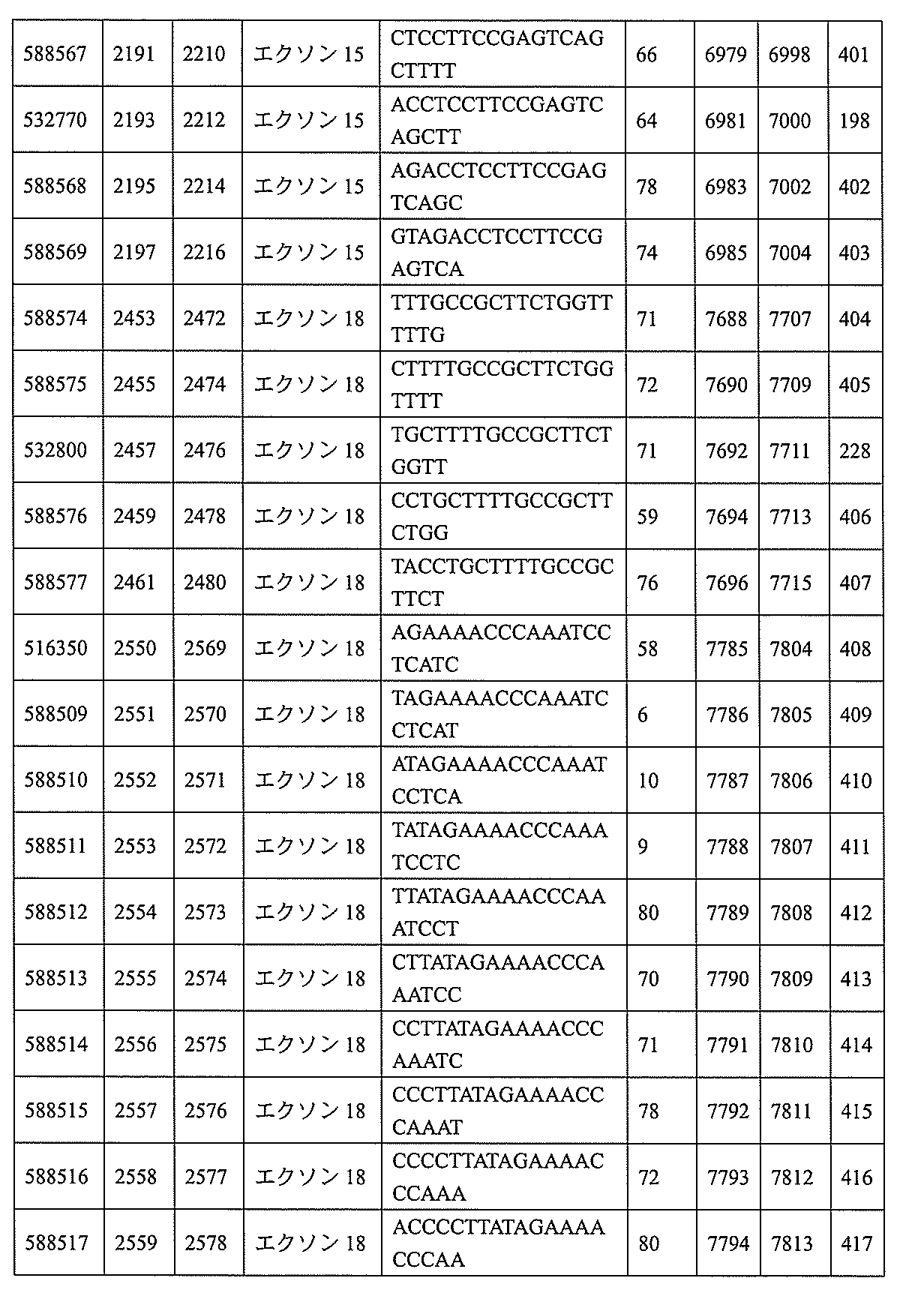
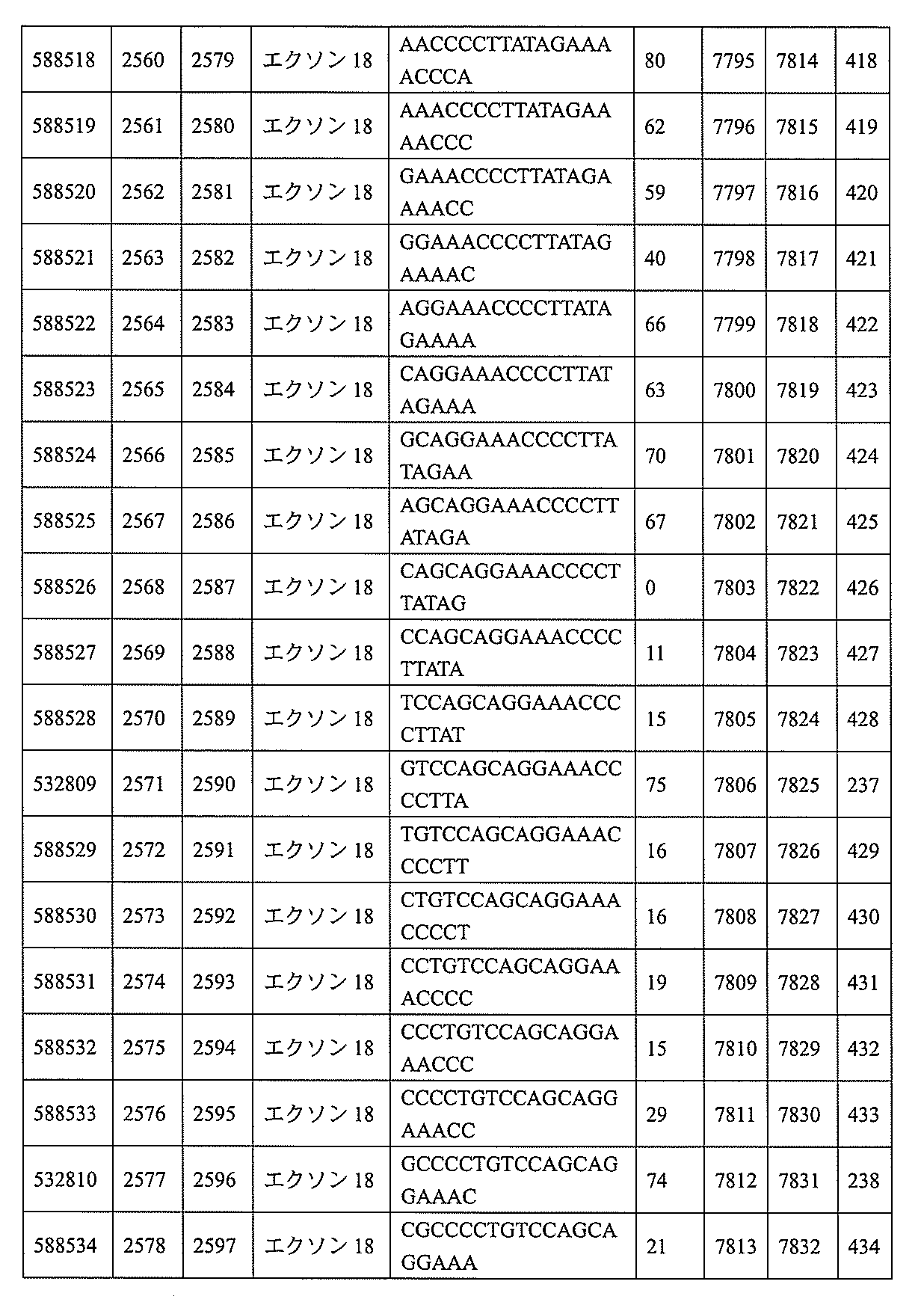
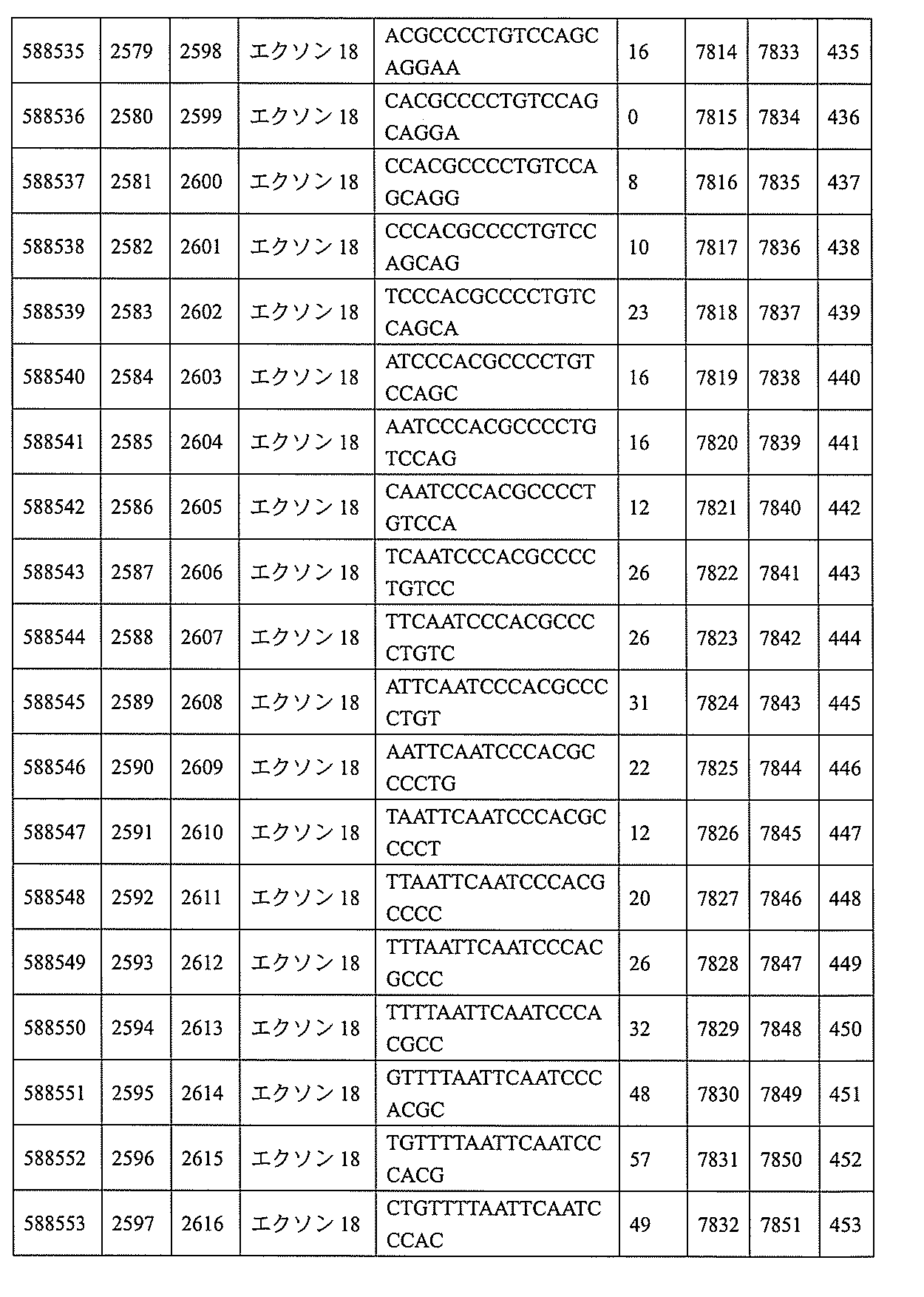
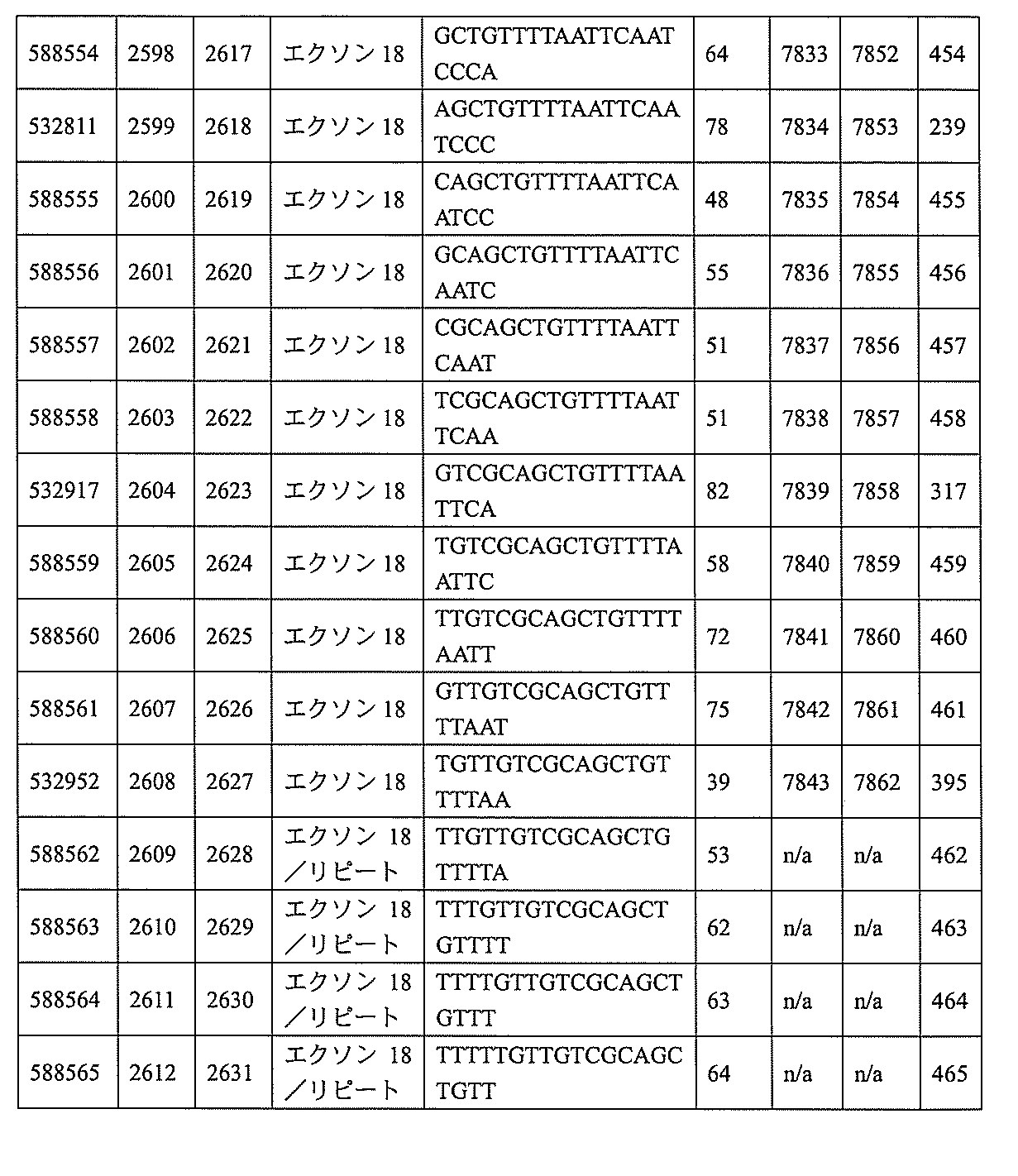
593、2575~2590、2575~2591、2575~2592、2575~2594、2576~2593、2576~2595、2577~2594、2577~2595、2577~2596、2578~2594、2578~2596、2578~2597、2579~2598、2580~2596、2580~2597、2580~2598、2580~2599、2581~2597、2581~2598、2581~2599、2581~2600、2582~2598、2582~2599、2582~2600、2582~2601、2583~2599、2583~2600、2583~2601、2583~2602、2584~2600、2584~2601、2584~2602、2584~2603、2585~2601、2585~2603、2585~2604、2586~2601、2586~2602、2586~2604、2586~2605、2587~2602、2587~2603、2587~2605、2587~2606、2588~2603、2588~2604、2588~2605、2588~2606、2588~2607、2589~2604、2589~2605、2589~2606、2589~2607、2589~2608、2590~2605、2590~2606、2590~2607、2590~2608、2590~2609、2590~2609、2591~2607、2591~2608、2591~2609、2591~2610、2592~2607、2592~2608、2592~2609、2592~2610、2592~2611、2593~2608、2593~2609、2593~2610、2593~2612、2594~2609、2594~2610、2594~2611、2594~2612、2594~2613、2595~2610、2595~2611、2595~2612、2595~2613、2595~2614、2596~2611、2596~2612、2596~2613、2596~2614、2596~2615、2597~2612、2597~2612、2597~2613、2597~2614、2597~2615、2597~2616、2598~2613、2598~2614、2598~2615、2598~2616、2598~2617、2599~2614、2599~2615、2599~2616、2599~2617、2599~2618、2600~2615、2600~2616、2600~2617、2600~2618、2600~2619、2601~2616、2601~2617、2601~2618、2601~2619、2601~2620、2602~2617、2602~2618、2602~2619、2602~2620、2602~2621、2603~2618、2603~2619、2603~2620、2603~2621、2603~2622、2604~2619、2604~2620、2604~2621、2604~2622、2604~2623、2605~2620、2605~2621、2605~2622、2605~2623、2605~2624、2606~2621、2606~2622、2606~2623、2606~2624、2606~2625、2607~2622、2607~2623、2607~2624、2607~2625、2607~2626、2608~2623、2608~2624、2608~2625、2608~2626、2608~2627、2609~2624、2609~2625、2609~2626、2609~2627、2609~2628、2610~2625、2610~2626、2610~2627、2610~2628、2610~2629、2611~2626、2611~2627、2611~2628、2611~2629、2611~2630、2612~2627、2612~2628、2612~2629、2612~2630、2612~2631、2613~2628、2613~2629、2613~2630、2613~2631、2614~2629、2614~2630、2614~2631、2615~2630、2615~2631、または2616~2631内で相補的な10~30個の連結されたヌクレオシドからなり、かつ該修飾オリゴヌクレオチドが、配列番号1に対して少なくとも85%、少なくとも90%、少なくとも95%、または100%相補的であるものを提供する。
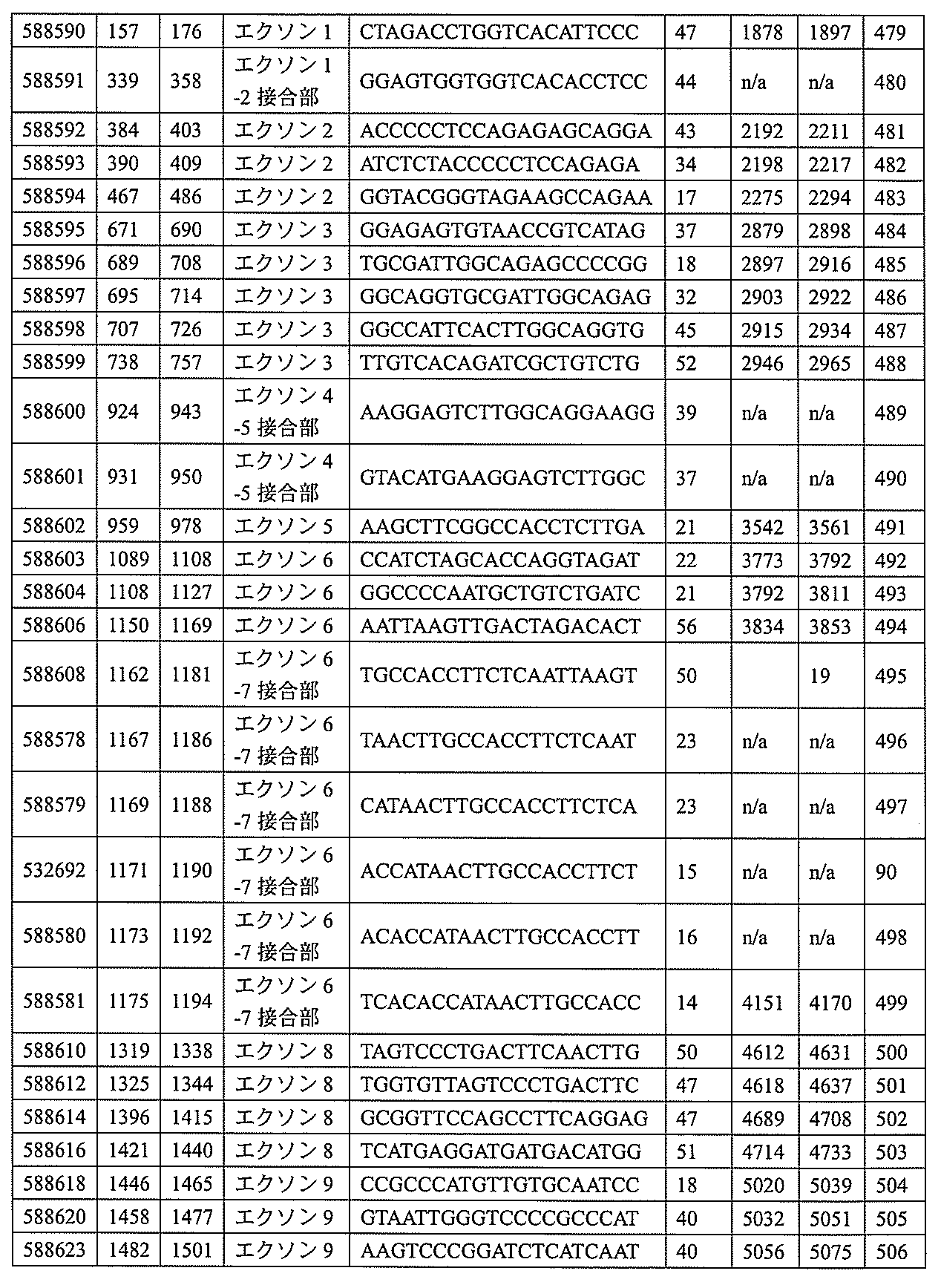
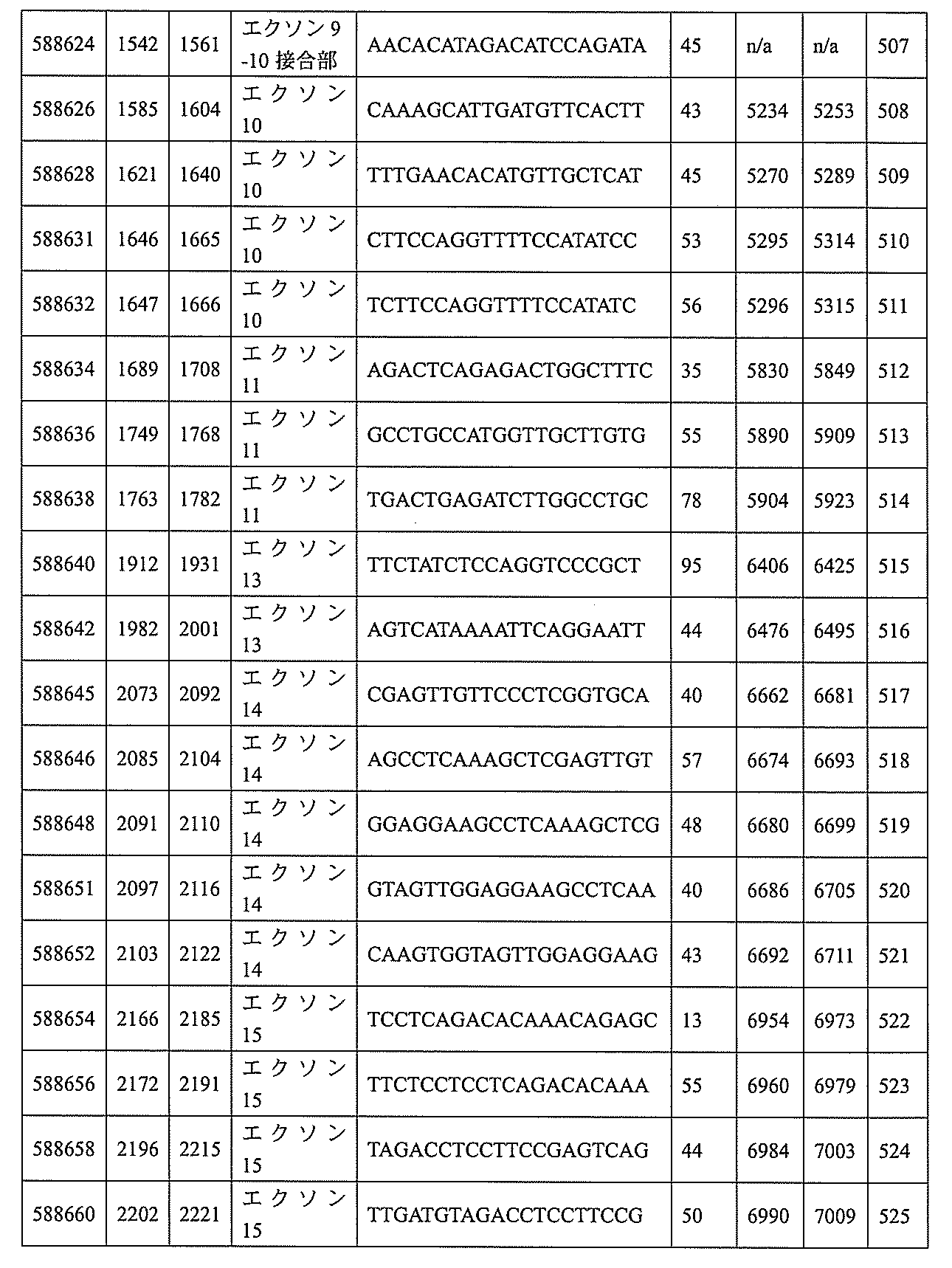
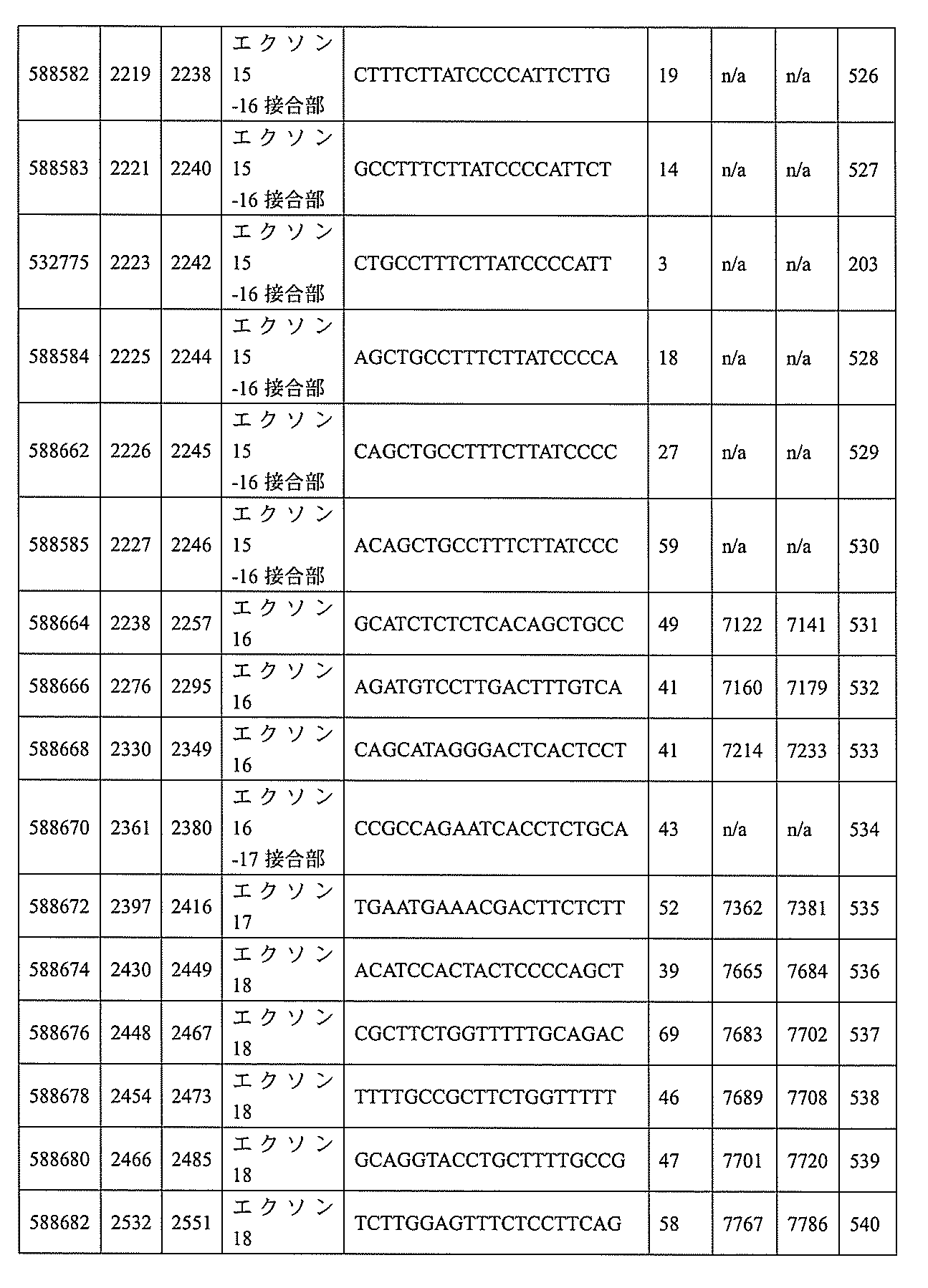
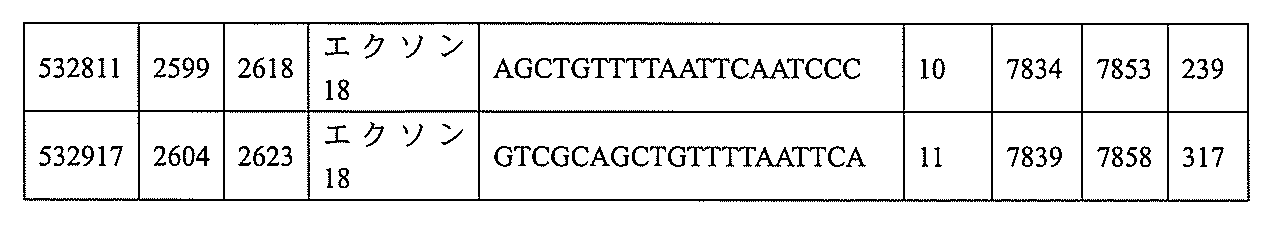
飾オリゴヌクレオチドが、配列番号1の核酸塩基30~49、48~63、150~169、151~170、152~171、154~169、154~173、156~171、156~175、157~176、158~173、158~177、480~499、600~619、638~657、644~663、738~757、1089~1108、1135~1154、1141~1160、1147~1166、1150~1169、1153~1172、1159~1178、1162~1181、1165~1184、1171~1186、1171~1190、1173~1188、1173~1192、1175~1190、1175~1194、1177~1196、1183~1202、1208~1227、1235~1254、1298~1317、1304~1323、1310~1329、1316~1335、1319~1338、1322~1341、1328~1347、1349~1368、1355~1374、1393~1412、1396~1415、1399~1418、1405~1424、1421~1440、1621~1640、1646~1665、1646~1665、1647~1666、1689~1708、1749~1768、1763~1782、1912~1931、2073~2092、2085~2104、2166~2185、2172~2191、2189~2208、2191~2210、2193~2212、2195~2210、2195~2214、2196~2215、2197~2212、2197~2216、2202~2221、2223~2238、2223~2242、2225~2240、2226~2245、2227~2242、2227~2246、2238~2257、2241~2260、2267~2286、2361~2380、2388~2407、2397~2416、2448~2467、2453~2472、2455~2474、2457~2472、2457~2476、2459~2474、2459~2478、2461~2476、2461~2480、2532~2551、2550~2569、2551~2566、2551~2570、2552~2568、2552~2570、2552~2571、2553~2568、2553~2570、2553~2571、2553~2572、2554~2571、2554~2572、2554~2573、2555~2570、2555~2572、2555~2574、2556~2573、2556~2574、2556~2575、2557~2573、2557~2574、2557~2575、2557~2576、2558~2575、2558~2576、2558~2577、2559~2576、2559~2577、2559~2578、2560~2577、2560~2578、2560~2579、2561~2576、2561~2578、2561~2579、2561~2580、2562~2577、2562~2579、2562~2581、2563~2578、2563~2580、2563~2582、2564~2581、2564~2583、2565~2584、2566~2583、2566~2585、2567~2582、2567~2584、2567~2586、2568~2583、2568~2585、2568~2587、2569~2586、2569~2588、2570~2585、2570~2587、2570~2589、2571~2586、2571~2588、2571~2590、2572~2589、2572~2590、2572~2591、2573~2590、2573~2592、2574~2590、2574~2591、2574~2593、2575~2590、2575~2591、2575~2592、2575~2594、2576~2593、2576~2595、2577~2594、2577~2595、2577~2596、2578~2594、2578~2596、2578~2597、2579~2598、2580~2596、2580~2597、2580~2598、2580~2599、2581~2597、2581~2598、2581~2599、2581~2600、2582~2598、2582~2599、2582~2600、2582~2601、2583~2599、2583~2600、2583~2601、2583~2602、2584~2600、2584~2601、2584~2602、2584~2603、2585~2601、2585~2603、2585~2604、2586~2601、2586~2602、2586~2604、2586~2
605、2587~2602、2587~2603、2587~2605、2587~2606、2588~2603、2588~2604、2588~2605、2588~2606、2588~2607、2589~2604、2589~2605、2589~2606、2589~2607、2589~2608、2590~2605、2590~2606、2590~2607、2590~2608、2590~2609、2590~2609、2591~2607、2591~2608、2591~2609、2591~2610、2592~2607、2592~2608、2592~2609、2592~2610、2592~2611、2593~2608、2593~2609、2593~2610、2593~2612、2594~2609、2594~2610、2594~2611、2594~2612、2594~2613、2595~2610、2595~2611、2595~2612、2595~2613、2595~2614、2596~2611、2596~2612、2596~2613、2596~2614、2596~2615、2597~2612、2597~2612、2597~2613、2597~2614、2597~2615、2597~2616、2598~2613、2598~2614、2598~2615、2598~2616、2598~2617、2599~2614、2599~2615、2599~2616、2599~2617、2599~2618、2600~2615、2600~2616、2600~2617、2600~2618、2600~2619、2601~2616、2601~2617、2601~2618、2601~2619、2601~2620、2602~2617、2602~2618、2602~2619、2602~2620、2602~2621、2603~2618、2603~2619、2603~2620、2603~2621、2603~2622、2604~2619、2604~2620、2604~2621、2604~2622、2604~2623、2605~2620、2605~2621、2605~2622、2605~2623、2605~2624、2606~2621、2606~2622、2606~2623、2606~2624、2606~2625、2607~2622、2607~2623、2607~2624、2607~2625、2607~2626、2608~2623、2608~2624、2608~2625、2608~2626、2608~2627、2609~2624、2609~2625、2609~2626、2609~2627、2609~2628、2610~2625、2610~2626、2610~2627、2610~2628、2610~2629、2611~2626、2611~2627、2611~2628、2611~2629、2611~2630、2612~2627、2612~2628、2612~2629、2612~2630、2612~2631、2613~2628、2613~2629、2613~2630、2613~2631、2614~2629、2614~2630、2614~2631、2615~2630、2615~2631、または2616~2631のうちの長さが等しい部分に相補的な少なくとも8個の連続する核酸塩基部分を含む核酸塩基配列を有する10~30個の連結されたヌクレオシドからなり、かつ前記修飾オリゴヌクレオチドの核酸塩基配列が、配列番号1に対して少なくとも85%、少なくとも90%、少なくとも95%、または100%相補的であるものを提供する。
8、4612~4631、4615~4634、4621~4640、4642~4661、4648~4667、4686~4705、4689~4708、4692~4711、4698~4717、4714~4733、5270~5289、5295~5314、5296~5315、5830~5849、5890~5909、5904~5923、6406~6425、6662~6681、6674~6693、6954~6973、6960~6979、6977~6996、6979~6998、6981~7000、6983~6998、6983~7002、6984~7003、6985~7000、6985~7004、6990~7009、7122~7141、7125~7144、7151~7170、7353~7372、7362~7381、7683~7702、7688~7707、7690~7709、7692~7707、7692~7711、7694~7709、7694~7713、7696~7711、7696~7715、7767~7786、7785~7804、7786~7801、7787~7803、7787~7805、7787~7806、7788~7803、7788~7805、7788~7806、7788~7807、7789~7806、7789~7807、7789~7808、7790~7805、7790~7807、7790~7809、7791~7808、7791~7809、7791~7810、7792~7808、7792~7809、7792~7810、7792~7811、7793~7810、7793~7811、7793~7812、7794~7811、7794~7812、7794~7813、7795~7812、7795~7813、7795~7814、7796~7811、7796~7813、7796~7814、7796~7815、7797~7812、7797~7814、7797~7816、7798~7813、7798~7815、7798~7817、7799~7816、7799~7818、7800~7819、7801~7818、7801~7820、7802~7817、7802~7819、7802~7821、7803~7818、7803~7820、7803~7822、7804~7821、7804~7823、7805~7820、7805~7822、7805~7824、7806~7821、7806~7823、7806~7825、7807~7824、7807~7825、7807~7826、7808~7825、7808~7827、7809~7825、7809~7826、7809~7828、7810~7825、7810~7826、7810~7827、7810~7829、7811~7828、7811~7830、7812~7829、7812~7830、7812~7831、7813~7829、7813~7831、7813~7832、7814~7833、7815~7831、7815~7832、7815~7833、7815~7834、7816~7832、7816~7833、7816~7834、7816~7835、7817~7833、7817~7834、7817~7835、7817~7836、7818~7834、7818~7835、7818~7836、7818~7837、7819~7835、7819~7836、7819~7837、7819~7838、7820~7836、7820~7838、7820~7839、7821~7836、7821~7837、7821~7839、7821~7840、7822~7837、7822~7838、7822~7840、7822~7841、7823~7838、7823~7839、7823~7839、7823~7840、7823~7841、7823~7842、7824~7839、7824~7840、7824~7840、7824~7841、7824~7842、7824~7843、7825~7840、7825~7841、7825~7842、7825~7843、7825~7844、7826~7842、7826~7843、7826~7844、7826~7845、7827~7842、7827~7843、7827~7844、7827~7845、7827~7846、7828~7843、7828~7844、7828~7845、7828~7847、7829~7844、7829~7845、7829~7846、7829~7847、7829~7848、7830~7845、7830~7846、7830~7847、7830~7848、7830~7849、7831~7846、7831~7847、7831~784
8、7831~7849、7831~7850、7832~7847、7832~7848、7832~7849、7832~7850、7832~7851、7833~7848、7833~7849、7833~7850、7833~7851、7833~7852、7834~7849、7834~7850、7834~7851、7834~7852、7834~7853、7835~7850、7835~7851、7835~7852、7835~7853、7835~7854、7836~7851、7836~7852、7836~7853、7836~7854、7836~7855、7837~7852、7837~7853、7837~7854、7837~7855、7837~7856、7838~7853、7838~7854、7838~7855、7838~7856、7838~7857、7839~7854、7839~7855、7839~7856、7839~7857、7839~7858、7840~7855、7840~7856、7840~7857、7840~7858、7840~7859、7841~7856、7841~7857、7841~7858、7841~7859、7841~7860、7842~7857、7842~7858、7842~7859、7842~7860、7842~7861、7843~7858、7843~7859、7843~7860、7843~7861、7843~7862、7844~7859、7844~7860、7844~7861、7844~7862、7845~7860、7845~7861、7845~7862、7846~7861、または7846~7862内で相補的な10~30個の連結されたヌクレオシドからなり、該修飾オリゴヌクレオチドが、配列番号2に対して少なくとも85%、少なくとも90%、少なくとも95%、または100%相補的であるものを提供する。
2、7794~7813、7795~7812、7795~7813、7795~7814、7796~7811、7796~7813、7796~7814、7796~7815、7797~7812、7797~7814、7797~7816、7798~7813、7798~7815、7798~7817、7799~7816、7799~7818、7800~7819、7801~7818、7801~7820、7802~7817、7802~7819、7802~7821、7803~7818、7803~7820、7803~7822、7804~7821、7804~7823、7805~7820、7805~7822、7805~7824、7806~7821、7806~7823、7806~7825、7807~7824、7807~7825、7807~7826、7808~7825、7808~7827、7809~7825、7809~7826、7809~7828、7810~7825、7810~7826、7810~7827、7810~7829、7811~7828、7811~7830、7812~7829、7812~7830、7812~7831、7813~7829、7813~7831、7813~7832、7814~7833、7815~7831、7815~7832、7815~7833、7815~7834、7816~7832、7816~7833、7816~7834、7816~7835、7817~7833、7817~7834、7817~7835、7817~7836、7818~7834、7818~7835、7818~7836、7818~7837、7819~7835、7819~7836、7819~7837、7819~7838、7820~7836、7820~7838、7820~7839、7821~7836、7821~7837、7821~7839、7821~7840、7822~7837、7822~7838、7822~7840、7822~7841、7823~7838、7823~7839、7823~7839、7823~7840、7823~7841、7823~7842、7824~7839、7824~7840、7824~7840、7824~7841、7824~7842、7824~7843、7825~7840、7825~7841、7825~7842、7825~7843、7825~7844、7826~7842、7826~7843、7826~7844、7826~7845、7827~7842、7827~7843、7827~7844、7827~7845、7827~7846、7828~7843、7828~7844、7828~7845、7828~7847、7829~7844、7829~7845、7829~7846、7829~7847、7829~7848、7830~7845、7830~7846、7830~7847、7830~7848、7830~7849、7831~7846、7831~7847、7831~7848、7831~7849、7831~7850、7832~7847、7832~7848、7832~7849、7832~7850、7832~7851、7833~7848、7833~7849、7833~7850、7833~7851、7833~7852、7834~7849、7834~7850、7834~7851、7834~7852、7834~7853、7835~7850、7835~7851、7835~7852、7835~7853、7835~7854、7836~7851、7836~7852、7836~7853、7836~7854、7836~7855、7837~7852、7837~7853、7837~7854、7837~7855、7837~7856、7838~7853、7838~7854、7838~7855、7838~7856、7838~7857、7839~7854、7839~7855、7839~7856、7839~7857、7839~7858、7840~7855、7840~7856、7840~7857、7840~7858、7840~7859、7841~7856、7841~7857、7841~7858、7841~7859、7841~7860、7842~7857、7842~7858、7842~7859、7842~7860、7842~7861、7843~7858、7843~7859、7843~7860、7843~7861、7843~7862、7844~7859、7844~7860、7844~7861、7844~7862、7845~7860、7845~7861、7845~7862、7846~7861、及び7846~7862のうちの長さが
等しい部分に相補的な少なくとも8個の連続する核酸塩基部分を含む核酸塩基配列を有する10~30個の連結されたヌクレオシドからなり、かつ前記修飾オリゴヌクレオチドの核酸塩基配列が、配列番号2に対して少なくとも85%、少なくとも90%、少なくとも95%、または100%相補的であるものを提供する。
590、2572~2589、2572~2590、2572~2591、2573~2590、2573~2592、2574~2590、2574~2591、2574~2593、2575~2590、2575~2591、2575~2592、2575~2594、2576~2593、2576~2595、2577~2594、2577~2595、2577~2596、2578~2594、2578~2596、2578~2597、2579~2598、2580~2596、2580~2597、2580~2598、2580~2599、2581~2597、2581~2598、2581~2599、2581~2600、2582~2598、2582~2599、2582~2600、2582~2601、2583~2599、2583~2600、2583~2601、2583~2602、2584~2600、2584~2601、2584~2602、2584~2603、2585~2601、2585~2603、2585~2604、2586~2601、2586~2602、2586~2604、2586~2605、2587~2602、2587~2603、2587~2605、2587~2606、2588~2603、2588~2604、2588~2605、2588~2606、2588~2607、2589~2604、2589~2605、2589~2606、2589~2607、2589~2608、2590~2605、2590~2606、2590~2607、2590~2608、2590~2609、2590~2609、2591~2607、2591~2608、2591~2609、2591~2610、2592~2607、2592~2608、2592~2609、2592~2610、2592~2611、2593~2608、2593~2609、2593~2610、2593~2612、2594~2609、2594~2610、2594~2611、2594~2612、2594~2613、2595~2610、2595~2611、2595~2612、2595~2613、2595~2614、2596~2611、2596~2612、2596~2613、2596~2614、2596~2615、2597~2612、2597~2612、2597~2613、2597~2614、2597~2615、2597~2616、2598~2613、2598~2614、2598~2615、2598~2616、2598~2617、2599~2614、2599~2615、2599~2616、2599~2617、2599~2618、2600~2615、2600~2616、2600~2617、2600~2618、2600~2619、2601~2616、2601~2617、2601~2618、2601~2619、2601~2620、2602~2617、2602~2618、2602~2619、2602~2620、2602~2621、2603~2618、2603~2619、2603~2620、2603~2621、2603~2622、2604~2619、2604~2620、2604~2621、2604~2622、2604~2623、2605~2620、2605~2621、2605~2622、2605~2623、2605~2624、2606~2621、2606~2622、2606~2623、2606~2624、2606~2625、2607~2622、2607~2623、2607~2624、2607~2625、2607~2626、2608~2623、2608~2624、2608~2625、2608~2626、2608~2627、2609~2624、2609~2625、2609~2626、2609~2627、2609~2628、2610~2625、2610~2626、2610~2627、2610~2628、2610~2629、2611~2626、2611~2627、2611~2628、2611~2629、2611~2630、2612~2627、2612~2628、2612~2629、2612~2630、2612~2631、2613~2628、2613~2629、2613~2630、2613~2631、2614~2629、2614~2630、2614~2631、2615~2630、2615~2631、及び2616~2631。
そのような化合物またはオリゴヌクレオチドが、前記領域のうちの長さが等しい核酸塩基部分に相補的な連続する核酸塩基部分を有する。例えば前記部分は、本明細書に示す領域のうちの長さが等しい部分に相補的な、少なくとも8、9、10、11、12、13、14、15、または16個の連続する核酸塩基部分であることができる。特定の実施形態では、化合物が、共役体と配列番号2の以下のヌクレオチド領域を標的とする修飾オリゴヌクレオチドとを含むか、またはそれらからなる:1608~1627、1685~1704、1686~1705、1751~1770、1769~1784、1871~1890、1872~1891、1873~1892、1875~1890、1875~1894、1877~1892、1877~1896、1878~1897、1879~1894、1879~1898、2288~2307、2808~2827、2846~2865、2852~2871、2946~2965、3773~3792、3819~3838、3825~3844、3831~3850、3834~3853、3837~3856、3843~3862、4151~4166、4151~4170、4153~4172、4159~4178、4184~4203、4211~4230、4609~4628、4612~4631、4615~4634、4621~4640、4642~4661、4648~4667、4686~4705、4689~4708、4692~4711、4698~4717、4714~4733、5270~5289、5295~5314、5296~5315、5830~5849、5890~5909、5904~5923、6406~6425、6662~6681、6674~6693、6954~6973、6960~6979、6977~6996、6979~6998、6981~7000、6983~6998、6983~7002、6984~7003、6985~7000、6985~7004、6990~7009、7122~7141、7125~7144、7151~7170、7353~7372、7362~7381、7683~7702、7688~7707、7690~7709、7692~7707、7692~7711、7694~7709、7694~7713、7696~7711、7696~7715、7767~7786、7785~7804、7786~7801、7787~7803、7787~7805、7787~7806、7788~7803、7788~7805、7788~7806、7788~7807、7789~7806、7789~7807、7789~7808、7790~7805、7790~7807、7790~7809、7791~7808、7791~7809、7791~7810、7792~7808、7792~7809、7792~7810、7792~7811、7793~7810、7793~7811、7793~7812、7794~7811、7794~7812、7794~7813、7795~7812、7795~7813、7795~7814、7796~7811、7796~7813、7796~7814、7796~7815、7797~7812、7797~7814、7797~7816、7798~7813、7798~7815、7798~7817、7799~7816、7799~7818、7800~7819、7801~7818、7801~7820、7802~7817、7802~7819、7802~7821、7803~7818、7803~7820、7803~7822、7804~7821、7804~7823、7805~7820、7805~7822、7805~7824、7806~7821、7806~7823、7806~7825、7807~7824、7807~7825、7807~7826、7808~7825、7808~7827、7809~7825、7809~7826、7809~7828、7810~7825、7810~7826、7810~7827、7810~7829、7811~7828、7811~7830、7812~7829、7812~7830、7812~7831、7813~7829、7813~7831、7813~7832、7814~7833、7815~7831、7815~7832、7815~7833、7815~7834、7816~7832、7816~7833、7816~7834、7816~7835、7817~7833、7817~7834、7817~7835、7817~7836、7818~7834、7818~7835、7818~7836、7818~7837、7819~7835、7819~783
6、7819~7837、7819~7838、7820~7836、7820~7838、7820~7839、7821~7836、7821~7837、7821~7839、7821~7840、7822~7837、7822~7838、7822~7840、7822~7841、7823~7838、7823~7839、7823~7839、7823~7840、7823~7841、7823~7842、7824~7839、7824~7840、7824~7840、7824~7841、7824~7842、7824~7843、7825~7840、7825~7841、7825~7842、7825~7843、7825~7844、7826~7842、7826~7843、7826~7844、7826~7845、7827~7842、7827~7843、7827~7844、7827~7845、7827~7846、7828~7843、7828~7844、7828~7845、7828~7847、7829~7844、7829~7845、7829~7846、7829~7847、7829~7848、7830~7845、7830~7846、7830~7847、7830~7848、7830~7849、7831~7846、7831~7847、7831~7848、7831~7849、7831~7850、7832~7847、7832~7848、7832~7849、7832~7850、7832~7851、7833~7848、7833~7849、7833~7850、7833~7851、7833~7852、7834~7849、7834~7850、7834~7851、7834~7852、7834~7853、7835~7850、7835~7851、7835~7852、7835~7853、7835~7854、7836~7851、7836~7852、7836~7853、7836~7854、7836~7855、7837~7852、7837~7853、7837~7854、7837~7855、7837~7856、7838~7853、7838~7854、7838~7855、7838~7856、7838~7857、7839~7854、7839~7855、7839~7856、7839~7857、7839~7858、7840~7855、7840~7856、7840~7857、7840~7858、7840~7859、7841~7856、7841~7857、7841~7858、7841~7859、7841~7860、7842~7857、7842~7858、7842~7859、7842~7860、7842~7861、7843~7858、7843~7859、7843~7860、7843~7861、7843~7862、7844~7859、7844~7860、7844~7861、7844~7862、7845~7860、7845~7861、7845~7862、7846~7861、及び7846~7862。
457~2596、2457~2597、2457~2598、2457~2599、2457~2600、2457~2601、2457~2602、2457~2603、2457~2604、2457~2605、2457~2606、2457~2607、2457~2608、2457~2609、2457~2610、2457~2611、2457~2612、2457~2613、2457~2614、2457~2615、2457~2616、2457~2617、2457~2618、2457~2619、2457~2620、2457~2621、2457~2622、2457~2623、2457~2624、2457~2625、2457~2626、2457~2627、2457~2628、2457~2629、2457~2630、2457~2631、2459~2474、2459~2476、2459~2566、2459~2570、2459~2571、2459~2572、2459~2573、2459~2574、2459~2575、2459~2576、2459~2577、2459~2578、2459~2579、2459~2580、2459~2581、2459~2582、2459~2583、2459~2584、2459~2585、2459~2586、2459~2587、2459~2588、2459~2589、2459~2590、2459~2591、2459~2592、2459~2593、2459~2594、2459~2595、2459~2596、2459~2597、2459~2598、2459~2599、2459~2600、2459~2601、2459~2602、2459~2603、2459~2604、2459~2605、2459~2606、2459~2607、2459~2608、2459~2609、2459~2610、2459~2611、2459~2612、2459~2613、2459~2614、2459~2615、2459~2616、2459~2617、2459~2618、2459~2619、2459~2620、2459~2621、2459~2622、2459~2623、2459~2624、2459~2625、2459~2626、2459~2627、2459~2628、2459~2629、2459~2630、2459~2631、2461~2476、2461~2566、2461~2570、2461~2571、2461~2572、2461~2573、2461~2574、2461~2575、2461~2576、2461~2577、2461~2578、2461~2579、2461~2580、2461~2581、2461~2582、2461~2583、2461~2584、2461~2585、2461~2586、2461~2587、2461~2588、2461~2589、2461~2590、2461~2591、2461~2592、2461~2593、2461~2594、2461~2595、2461~2596、2461~2597、2461~2598、2461~2599、2461~2600、2461~2601、2461~2602、2461~2603、2461~2604、2461~2605、2461~2606、2461~2607、2461~2608、2461~2609、2461~2610、2461~2611、2461~2612、2461~2613、2461~2614、2461~2615、2461~2616、2461~2617、2461~2618、2461~2619、2461~2620、2461~2621、2461~2622、2461~2623、2461~2624、2461~2625、2461~2626、2461~2627、2461~2628、2461~2629、2461~2630、2461~2631、2551~2566、2551~2570、2551~2571、2551~2572、2551~2573、2551~2574、2551~2575、2551~2576、2551~2577、2551~2578、2551~2579、2551~2580、2551~2581、2551~2582、2551~2583、2551~2584、2551~2585、2551~2586、2551~2587、2551~2588、2551~2589、2551~2590、2551~2591、2551~2592、2551~2593、2551~2594、2551~2595、2551~2596、2551~2597、2551~2598、2551~2599、2551~2600、2551~2601、2551~2602、2551~2603、2
551~2604、2551~2605、2551~2606、2551~2607、2551~2608、2551~2609、2551~2610、2551~2611、2551~2612、2551~2613、2551~2614、2551~2615、2551~2616、2551~2617、2551~2618、2551~2619、2551~2620、2551~2621、2551~2622、2551~2623、2551~2624、2551~2625、2551~2626、2551~2627、2551~2628、2551~2629、2551~2630、2551~2631、2553~2570、2553~2571、2553~2572、2553~2573、2553~2574、2553~2575、2553~2576、2553~2577、2553~2578、2553~2579、2553~2580、2553~2581、2553~2582、2553~2583、2553~2584、2553~2585、2553~2586、2553~2587、2553~2588、2553~2589、2553~2590、2553~2591、2553~2592、2553~2593、2553~2594、2553~2595、2553~2596、2553~2597、2553~2598、2553~2599、2553~2600、2553~2601、2553~2602、2553~2603、2553~2604、2553~2605、2553~2606、2553~2607、2553~2608、2553~2609、2553~2610、2553~2611、2553~2612、2553~2613、2553~2614、2553~2615、2553~2616、2553~2617、2553~2618、2553~2619、2553~2620、2553~2621、2553~2622、2553~2623、2553~2624、2553~2625、2553~2626、2553~2627、2553~2628、2553~2629、2553~2630、2553~2631、2554~2573、2554~2574、2554~2575、2554~2576、2554~2577、2554~2578、2554~2579、2554~2580、2554~2581、2554~2582、2554~2583、2554~2584、2554~2585、2554~2586、2554~2587、2554~2588、2554~2589、2554~2590、2554~2591、2554~2592、2554~2593、2554~2594、2554~2595、2554~2596、2554~2597、2554~2598、2554~2599、2554~2600、2554~2601、2554~2602、2554~2603、2554~2604、2554~2605、2554~2606、2554~2607、2554~2608、2554~2609、2554~2610、2554~2611、2554~2612、2554~2613、2554~2614、2554~2615、2554~2616、2554~2617、2554~2618、2554~2619、2554~2620、2554~2621、2554~2622、2554~2623、2554~2624、2554~2625、2554~2626、2554~2627、2554~2628、2554~2629、2554~2630、2554~2631、2555~2572、2555~2573、2555~2574、2555~2575、2555~2576、2555~2577、2555~2578、2555~2579、2555~2580、2555~2581、2555~2582、2555~2583、2555~2584、2555~2585、2555~2586、2555~2587、2555~2588、2555~2589、2555~2590、2555~2591、2555~2592、2555~2593、2555~2594、2555~2595、2555~2596、2555~2597、2555~2598、2555~2599、2555~2600、2555~2601、2555~2602、2555~2603、2555~2604、2555~2605、2555~2606、2555~2607、2555~2608、2555~2609、2555~2610、2555~2611、2555~2612、2555~2613、2555~2614、2555~2615、2555~2616、2555~2617、2555~2618、2555~2619、2555~2620、2555~2621、2555~2622、2
555~2623、2555~2624、2555~2625、2555~2626、2555~2627、2555~2628、2555~2629、2555~2630、2555~2631、2556~2573、2556~2574、2556~2575、2556~2576、2556~2577、2556~2578、2556~2579、2556~2580、2556~2581、2556~2582、2556~2583、2556~2584、2556~2585、2556~2586、2556~2587、2556~2588、2556~2589、2556~2590、2556~2591、2556~2592、2556~2593、2556~2594、2556~2595、2556~2596、2556~2597、2556~2598、2556~2599、2556~2600、2556~2601、2556~2602、2556~2603、2556~2604、2556~2605、2556~2606、2556~2607、2556~2608、2556~2609、2556~2610、2556~2611、2556~2612、2556~2613、2556~2614、2556~2615、2556~2616、2556~2617、2556~2618、2556~2619、2556~2620、2556~2621、2556~2622、2556~2623、2556~2624、2556~2625、2556~2626、2556~2627、2556~2628、2556~2629、2556~2630、2556~2631、2557~2574、2557~2575、2557~2576、2557~2577、2557~2578、2557~2579、2557~2580、2557~2581、25
57~2582、2557~2583、2557~2584、2557~2585、2557~2586、2557~2587、2557~2588、2557~2589、2557~2590、2557~2591、2557~2592、2557~2593、2557~2594、2557~2595、2557~2596、2557~2597、2557~2598、2557~2599、2557~2600、2557~2601、2557~2602、2557~2603、2557~2604、2557~2605、2557~2606、2557~2607、2557~2608、2557~2609、2557~2610、2557~2611、2557~2612、2557~2613、2557~2614、2557~2615、2557~2616、2557~2617、2557~2618、2557~2619、2557~2620、2557~2621、2557~2622、2557~2623、2557~2624、2557~2625、2557~2626、2557~2627、2557~2628、2557~2629、2557~2630、2557~2631、2558~2575、2558~2576、2558~2577、2558~2578、2558~2579、2558~2580、2558~2581、2558~2582、2558~2583、2558~2584、2558~2585、2558~2586、2558~2587、2558~2588、2558~2589、2558~2590、2558~2591、2558~2592、2558~2593、2558~2594、2558~2595、2558~2596、2558~2597、2558~2598、2558~2599、2558~2600、2558~2601、2558~2602、2558~2603、2558~2604、2558~2605、2558~2606、2558~2607、2558~2608、2558~2609、2558~2610、2558~2611、2558~2612、2558~2613、2558~2614、2558~2615、2558~2616、2558~2617、2558~2618、2558~2619、2558~2620、2558~2621、2558~2622、2558~2623、2558~2624、2558~2625、2558~2626、2558~2627、2558~2628、2558~2629、2558~2630、2558~2631、2559~2576、2559~2577、2559~2578、2559~2579、2559~2580、25
59~2581、2559~2582、2559~2583、2559~2584、2559~2585、2559~2586、2559~2587、2559~2588、2559~2589、2559~2590、2559~2591、2559~2592、2559~2593、2559~2594、2559~2595、2559~2596、2559~2597、2559~2598、2559~2599、2559~2600、2559~2601、2559~2602、2559~2603、2559~2604、2559~2605、2559~2606、2559~2607、2559~2608、2559~2609、2559~2610、2559~2611、2559~2612、2559~2613、2559~2614、2559~2615、2559~2616、2559~2617、2559~2618、2559~2619、2559~2620、2559~2621、2559~2622、2559~2623、2559~2624、2559~2625、2559~2626、2559~2627、2559~2628、2559~2629、2559~2630、2559~2631、2560~2577、2560~2578、2560~2579、2560~2580、2560~2581、2560~2582、2560~2583、2560~2584、2560~2585、2560~2586、2560~2587、2560~2588、2560~2589、2560~2590、2560~2591、2560~2592、2560~2593、2560~2594、2560~2595、2560~2596、2560~2597、2560~2598、2560~2599、2560~2600、2560~2601、2560~2602、2560~2603、2560~2604、2560~2605、2560~2606、2560~2607、2560~2608、2560~2609、2560~2610、2560~2611、2560~2612、2560~2613、2560~2614、2560~2615、2560~2616、2560~2617、2560~2618、2560~2619、2560~2620、2560~2621、2560~2622、2560~2623、2560~2624、2560~2625、2560~2626、2560~2627、2560~2628、2560~2629、2560~2630、2560~2631、2561~2578、2561~2579、2561~2580、2561~2581、2561~2582、2561~2583、2561~2584、2561~2585、2561~2586、2561~2587、2561~2588、2561~2589、2561~2590、2561~2591、2561~2592、2561~2593、2561~2594、2561~2595、2561~2596、2561~2597、2561~2598、2561~2599、2561~2600、2561~2601、2561~2602、2561~2603、2561~2604、2561~2605、2561~2606、2561~2607、2561~2608、2561~2609、2561~2610、2561~2611、2561~2612、2561~2613、2561~2614、2561~2615、2561~2616、2561~2617、2561~2618、2561~2619、2561~2620、2561~2621、2561~2622、2561~2623、2561~2624、2561~2625、2561~2626、2561~2627、2561~2628、2561~2629、2561~2630、2561~2631、2562~2577、2562~2578、2562~2579、2562~2580、2562~2581、2562~2582、2562~2583、2562~2584、2562~2585、2562~2586、2562~2587、2562~2588、2562~2589、2562~2590、2562~2591、2562~2592、2562~2593、2562~2594、2562~2595、2562~2596、2562~2597、2562~2598、2562~2599、2562~2600、2562~2601、2562~2602、2562~2603、2562~2604、2562~2605、2562~2606、2562~2607、2562~2608、2562~2609、2562~2610、2562~2611、2562~2612、2562~2613、2562~2614、2562~2615、2562~2616、25
62~2617、2562~2618、2562~2619、2562~2620、2562~2621、2562~2622、2562~2623、2562~2624、2562~2625、2562~2626、2562~2627、2562~2628、2562~2629、2562~2630、2562~2631、2563~2580、2563~2581、2563~2582、2563~2583、2563~2584、2563~2585、2563~2586、2563~2587、2563~2588、2563~2589、2563~2590、2563~2591、2563~2592、2563~2593、2563~2594、2563~2595、2563~2596、2563~2597、2563~2598、2563~2599、2563~2600、2563~2601、2563~2602、2563~2603、2563~2604、2563~2605、2563~2606、2563~2607、2563~2608、2563~2609、2563~2610、2563~2611、2563~2612、2563~2613、2563~2614、2563~2615、2563~2616、2563~2617、2563~2618、2563~2619、2563~2620、2563~2621、2563~2622、2563~2623、2563~2624、2563~2625、2563~2626、2563~2627、2563~2628、2563~2629、2563~2630、2563~2631、2564~2581、2564~2582、2564~2583、2564~2584、2564~2585、2564~2586、2564~2587、2564~2588、2564~2589、2564~2590、2564~2591、2564~2592、2564~2593、2564~2594、2564~2595、2564~2596、2564~2597、2564~2598、2564~2599、2564~2600、2564~2601、2564~2602、2564~2603、2564~2604、2564~2605、2564~2606、2564~2607、2564~2608、2564~2609、2564~2610、2564~2611、2564~2612、2564~2613、2564~2614、2564~2615、2564~2616、2564~2617、2564~2618、2564~2619、2564~2620、2564~2621、2564~2622、2564~2623、2564~2624、2564~2625、2564~2626、2564~2627、2564~2628、2564~2629、2564~2630、2564~2631、2565~2584、2565~2585、2565~2586、2565~2587、2565~2588、2565~2589、2565~2590、2565~2591、2565~2592、2565~2593、2565~2594、2565~2595、2565~2596、2565~2597、2565~2598、2565~2599、2565~2600、2565~2601、2565~2602、2565~2603、2565~2604、2565~2605、2565~2606、2565~2607、2565~2608、2565~2609、2565~2610、2565~2611、2565~2612、2565~2613、2565~2614、2565~2615、2565~2616、2565~2617、2565~2618、2565~2619、2565~2620、2565~2621、2565~2622、2565~2623、2565~2624、2565~2625、2565~2626、2565~2627、2565~2628、2565~2629、2565~2630、2565~2631、2566~2583、2566~2584、2566~2585、2566~2586、2566~2587、2566~2588、2566~2589、2566~2590、2566~2591、2566~2592、2566~2593、2566~2594、2566~2595、2566~2596、2566~2597、2566~2598、2566~2599、2566~2600、2566~2601、2566~2602、2566~2603、2566~2604、2566~2605、2566~2606、2566~2607、2566~2608、2566~2609、2566~2610、2566~2611、2566~2612、2566~2613、2566~2614、2566~2615、2566~2616、25
6
6~2617、2566~2618、2566~2619、2566~2620、2566~2621、2566~2622、2566~2623、2566~2624、2566~2625、2566~2626、2566~2627、2566~2628、2566~2629、2566~2630、2566~2631、2567~2584、2567~2585、2567~2586、2567~2587、2567~2588、2567~2589、2567~2590、2567~2591、2567~2592、2567~2593、2567~2594、2567~2595、2567~2596、2567~2597、2567~2598、2567~2599、2567~2600、2567~2601、2567~2602、2567~2603、2567~2604、2567~2605、2567~2606、2567~2607、2567~2608、2567~2609、2567~2610、2567~2611、2567~2612、2567~2613、2567~2614、2567~2615、2567~2616、2567~2617、2567~2618、2567~2619、2567~2620、2567~2621、2567~2622、2567~2623、2567~2624、2567~2625、2567~2626、2567~2627、2567~2628、2567~2629、2567~2630、2567~2631、2568~2585、2568~2586、2568~2587、2568~2588、2568~2589、2568~2590、2568~2591、2568~2592、2568~2593、2568~2594、2568~2595、2568~2596、2568~2597、2568~2598、2568~2599、2568~2600、2568~2601、2568~2602、2568~2603、2568~2604、2568~2605、2568~2606、2568~2607、2568~2608、2568~2609、2568~2610、2568~2611、2568~2612、2568~2613、2568~2614、2568~2615、2568~2616、2568~2617、2568~2618、2568~2619、2568~2620、2568~2621、2568~2622、2568~2623、2568~2624、2568~2625、2568~2626、2568~2627、2568~2628、2568~2629、2568~2630、2568~2631、2569~2586、2569~2587、2569~2588、2569~2589、2569~2590、2569~2591、2569~2592、2569~2593、2569~2594、2569~2595、2569~2596、2569~2597、2569~2598、2569~2599、2569~2600、2569~2601、2569~2602、2569~2603、2569~2604、2569~2605、2569~2606、2569~2607、2569~2608、2569~2609、2569~2610、2569~2611、2569~2612、2569~2613、2569~2614、2569~2615、2569~2616、2569~2617、2569~2618、2569~2619、2569~2620、2569~2621、2569~2622、2569~2623、2569~2624、2569~2625、2569~2626、2569~2627、2569~2628、2569~2629、2569~2630、2569~2631、2569~2586、2569~2587、2569~2588、2569~2589、2569~2590、2569~2591、2569~2592、2569~2593、2569~2594、2569~2595、2569~2596、2569~2597、2569~2598、2569~2599、2569~2600、2569~2601、2569~2602、2569~2603、2569~2604、2569~2605、2569~2606、2569~2607、2569~2608、2569~2609、2569~2610、2569~2611、2569~2612、2569~2613、2569~2614、2569~2615、2569~2616、2569~2617、256
9~2618、2569~2619、2569~2620、2569~2621、2569~2622、2569~2623、2569~2624、2569~2625、2569~2626、2569~2627、2569~2628、2569~2629、2569~2630、2569~2631、2571~2588、2571~2589、2571~2590、2571~2591、2571~2592、2571~2593、2571~2594、2571~2595、2571~2596、2571~2597、2571~2598、2571~2599、2571~2600、2571~2601、2571~2602、2571~2603、2571~2604、2571~2605、2571~2606、2571~2607、2571~2608、2571~2609、2571~2610、2571~2611、2571~2612、2571~2613、2571~2614、2571~2615、2571~2616、2571~2617、2571~2618、2571~2619、2571~2620、2571~2621、2571~2622、2571~2623、2571~2624、2571~2625、2571~2626、2571~2627、2571~2628、2571~2629、2571~2630、2571~2631、2572~2589、2572~2590、2572~2591、2572~2592、2572~2593、2572~2594、2572~2595、2572~2596、2572~2597、2572~2598、2572~2599、2572~2600、2572~2601、2572~2602、2572~2603、2572~2604、2572~2605、2572~2606、2572~2607、2572~2608、2572~2609、2572~2610、2572~2611、2572~2612、2572~2613、2572~2614、2572~2615、2572~2616、2572~2617、2572~2618、2572~2619、2572~2620、2572~2621、2572~2622、2572~2623、2572~2624、2572~2625、2572~2626、2572~2627、2572~2628、2572~2629、2572~2630、2572~2631、2573~2590、2573~2591、2573~2592、2573~2593、2573~2594、2573~2595、2573~2596、2573~2597、2573~2598、2573~2599、2573~2600、2573~2601、2573~2602、2573~2603、2573~2604、2573~2605、2573~2606、2573~2607、2573~2608、2573~2609、2573~2610、2573~2611、2573~2612、2573~2613、2573~2614、2573~2615、2573~2616、2573~2617、2573~2618、2573~2619、2573~2620、2573~2621、2573~2622、2573~2623、2573~2624、2573~2625、2573~2626、2573~2627、2573~2628、2573~2629、2573~2630、2573~2631、2574~2591、2574~2592、2574~2593、2574~2594、2574~2595、2574~2596、2574~2597、2574~2598、2574~2599、2574~2600、2574~2601、2574~2602、2574~2603、2574~2604、2574~2605、2574~2606、2574~2607、2574~2608、2574~2609、2574~2610、2574~2611、2574~2612、2574~2613、2574~2614、2574~2615、2574~2616、2574~2617、2574~2618、2574~2619、2574~2620、2574~2621、2574~2622、2574~2623、2574~2624、2574~2625、2574~2626、2574~2627、2574~2628、2574~2629、2574~2630、2574~2631、2575~2592、2575~2593、2575~2594、2575~2595、2575~2596、2575~2597、2575~2598、2575~2599、2575~2600、2575~2601、2575~2602、2575~2603、2575~2604、2575~2605、2575~2606、2575~2607、257
5~2608、2575~2609、2575~2610、2575~2611、2575~2612、2575~2613、2575~2614、2575~2615、2575~2616、2575~2617、2575~2618、2575~2619、2575~2620、2575~2621、2575~2622、2575~2623、2575~2624、2575~2625、2575~2626、2575~2627、2575~2628、2575~2629、2575~2630、2575~2631、2576~2593、2576~2594、2576~2595、2576~2596、2576~2597、2576~2598、2576~2599、2576~2600、2576~2601、2576~2602、2576~2603、2576~2604、2576~2605、2576~2606、2576~2607、2576~2608、2576~2609、2576~2610、2576~2611、2576~2612、2576~2613、2576~2614、2576~2615、2576~2616、2576~2617、2576~2618、2576~2619、2576~2620、2576~2621、2576~2622、2576~2623、2576~2624、2576~2625、2576~2626、2576~2627、2576~2628、2576~2629、2576~2630、2576~2631、2577~2594、2577~2595、2577~2596、2577~2597、2577~2598、2577~2599、2577~2600、2577~2601、2577~2602、2577~2603、2577~2604、2577~2605、2577~2606、2577~2607、2577~2608、2577~2609、2577~2610、2577~2611、2577~2612、2577~2613、2577~2614、2577~2615、2577~2616、2577~2617、2577~2618、2577~2619、2577~2620、2577~2621、2577~2622、2577~2623、2577~2624、2577~2625、2577~2626、2577~2627、2577~2628、2577~2629、2577~2630、2577~2631、2578~2597、2578~2598、2578~2599、2578~2600、2578~2601、2578~2602、2578~2603、2578~2604、2578~2605、2578~2606、2578~2607、2578~2608、2578~2609、2578~2610、2578~2611、2578~2612、2578~2613、2578~2614、2578~2615、2578~2616、2578~2617、2578~2618、2578~2619、2578
~2620、2578~2621、2578~2622、2578~2623、2578~2624、2578~2625、2578~2626、2578~2627、2578~2628、2578~2629、2578~2630、2578~2631、2579~2598、2579~2599、2579~2600、2579~2601、2579~2602、2579~2603、2579~2604、2579~2605、2579~2606、2579~2607、2579~2608、2579~2609、2579~2610、2579~2611、2579~2612、2579~2613、2579~2614、2579~2615、2579~2616、2579~2617、2579~2618、2579~2619、2579~2620、2579~2621、2579~2622、2579~2623、2579~2624、2579~2625、2579~2626、2579~2627、2579~2628、2579~2629、2579~2630、2579~2631、2580~2598、2580~2599、2580~2600、2580~2601、2580~2602、2580~2603、2580~2604、2580~2605、2580~2606、2580~2607、2580~2608、2580~2609、2580~2610、2580~2611、2580~2612、2580~2613、2580~2614、2580~2615、2580
~2616、2580~2617、2580~2618、2580~2619、2580~2620、2580~2621、2580~2622、2580~2623、2580~2624、2580~2625、2580~2626、2580~2627、2580~2628、2580~2629、2580~2630、2580~2631、2581~2597、2581~2598、2581~2599、2581~2600、2581~2601、2581~2602、2581~2603、2581~2604、2581~2605、2581~2606、2581~2607、2581~2608、2581~2609、2581~2610、2581~2611、2581~2612、2581~2613、2581~2614、2581~2615、2581~2616、2581~2617、2581~2618、2581~2619、2581~2620、2581~2621、2581~2622、2581~2623、2581~2624、2581~2625、2581~2626、2581~2627、2581~2628、2581~2629、2581~2630、2581~2631、2582~2600、2582~2601、2582~2602、2582~2603、2582~2604、2582~2605、2582~2606、2582~2607、2582~2608、2582~2609、2582~2610、2582~2611、2582~2612、2582~2613、2582~2614、2582~2615、2582~2616、2582~2617、2582~2618、2582~2619、2582~2620、2582~2621、2582~2622、2582~2623、2582~2624、2582~2625、2582~2626、2582~2627、2582~2628、2582~2629、2582~2630、2582~2631、2583~2601、2583~2602、2583~2603、2583~2604、2583~2605、2583~2606、2583~2607、2583~2608、2583~2609、2583~2610、2583~2611、2583~2612、2583~2613、2583~2614、2583~2615、2583~2616、2583~2617、2583~2618、2583~2619、2583~2620、2583~2621、2583~2622、2583~2623、2583~2624、2583~2625、2583~2626、2583~2627、2583~2628、2583~2629、2583~2630、2583~2631、2585~2603、2585~2604、2585~2605、2585~2606、2585~2607、2585~2608、2585~2609、2585~2610、2585~2611、2585~2612、2585~2613、2585~2614、2585~2615、2585~2616、2585~2617、2585~2618、2585~2619、2585~2620、2585~2621、2585~2622、2585~2623、2585~2624、2585~2625、2585~2626、2585~2627、2585~2628、2585~2629、2585~2630、2585~2631、2586~2604、2586~2605、2586~2606、2586~2607、2586~2608、2586~2609、2586~2610、2586~2611、2586~2612、2586~2613、2586~2614、2586~2615、2586~2616、2586~2617、2586~2618、2586~2619、2586~2620、2586~2621、2586~2622、2586~2623、2586~2624、2586~2625、2586~2626、2586~2627、2586~2628、2586~2629、2586~2630、2586~2631、2587~2605、2587~2606、2587~2607、2587~2608、2587~2609、2587~2610、2587~2611、2587~2612、2587~2613、2587~2614、2587~2615、2587~2616、2587~2617、2587~2618、2587~2619、2587~2620、2587~2621、2587~2622、2587~2623、2587~2624、2587~2625、2587~2626、2587~2627、2587~2628、2587~2629、2587~2630、2587~2631、2588~2606、2588~2607、2588
~2608、2588~2609、2588~2610、2588~2611、2588~2612、2588~2613、2588~2614、2588~2615、2588~2616、2588~2617、2588~2618、2588~2619、2588~2620、2588~2621、2588~2622、2588~2623、2588~2624、2588~2625、2588~2626、2588~2627、2588~2628、2588~2629、2588~2630、2588~2631、2589~2607、2589~2608、2589~2609、2589~2610、2589~2611、2589~2612、2589~2613、2589~2614、2589~2615、2589~2616、2589~2617、2589~2618、2589~2619、2589~2620、2589~2621、2589~2622、2589~2623、2589~2624、2589~2625、2589~2626、2589~2627、2589~2628、2589~2629、2589~2630、2589~2631、2590~2606、2590~2607、2590~2608、2590~2609、2590~2610、2590~2611、2590~2612、2590~2613、2590~2614、2590~2615、2590~2616、2590~2617、2590~2618、2590~2619、2590~2620、2590~2621、2590~2622、2590~2623、2590~2624、2590~2625、2590~2626、2590~2627、2590~2628、2590~2629、2590~2630、2590~2631、2591~2610、2591~2611、2591~2612、2591~2613、2591~2614、2591~2615、2591~2616、2591~2617、2591~2618、2591~2619、2591~2620、2591~2621、2591~2622、2591~2623、2591~2624、2591~2625、2591~2626、2591~2627、2591~2628、2591~2629、2591~2630、2591~2631、2592~2611、2592~2612、2592~2613、2592~2614、2592~2615、2592~2616、2592~2617、2592~2618、2592~2619、2592~2620、2592~2621、2592~2622、2592~2623、2592~2624、2592~2625、2592~2626、2592~2627、2592~2628、2592~2629、2592~2630、2592~2631、2593~2608、2593~2612、2593~2613、2593~2614、2593~2615、2593~2616、2593~2617、2593~2618、2593~2619、2593~2620、2593~2621、2593~2622、2593~2623、2593~2624、2593~2625、2593~2626、2593~2627、2593~2628、2593~2629、2593~2630、2593~2631、2594~2612、2594~2613、2594~2614、2594~2615、2594~2616、2594~2617、2594~2618、2594~2619、2594~2620、2594~2621、2594~2622、2594~2623、2594~2624、2594~2625、2594~2626、2594~2627、2594~2628、2594~2629、2594~2630、2594~2631、2595~2611、2595~2612、2595~2613、2595~2614、2595~2615、2595~2616、2595~2617、2595~2618、2595~2619、2595~2620、2595~2621、2595~2622、2595~2623、2595~2624、2595~2625、2595~2626、2595~2627、2595~2628、2595~2629、2595~2630、2595~2631、2596~2614、2596~2615、2596~2616、2596~2617、2596~2618、2596~2619、2596~2620、2596~2621、2596~2622、2596~2623、2596~2624、2596~2625、2596~2626、2596~2627、2596~2628、2596~2629、2596~2630、2596~2631、2597~2612、2597~2613、2597
~2614、2597~2615、2597~2616、2597~2617、2597~2618、2597~2619、2597~2620、2597~2621、2597~2622、2597~2623、2597~2624、2597~2625、2597~2626、2597~2627、2597~2628、2597~2629、2597~2630、2597~2631、2598~2613、2598~2614、2598~2615、2598~2616、2598~2617、2598~2618、2598~2619、2598~2620、2598~2621、2598~2622、2598~2623、2598~2624、2598~2625、2598~2626、2598~2627、2598~2628、2598~2629、2598~2630、2598~2631、2599~2614、2599~2615、2599~2616、2599~2617、2599~2618、2599~2619、2599~2620、2599~2621、2599~2622、2599~2623、2599~2624、2599~
2625、2599~2626、2599~2627、2599~2628、2599~2629、2599~2630、2599~2631、2600~2615、2600~2616、2600~2617、2600~2618、2600~2619、2600~2620、2600~2621、2600~2622、2600~2623、2600~2624、2600~2625、2600~2626、2600~2627、2600~2628、2600~2629、2600~2630、2600~2631、2601~2616、2601~2617、2601~2618、2601~2619、2601~2620、2601~2621、2601~2622、2601~2623、2601~2624、2601~2625、2601~2626、2601~2627、2601~2628、2601~2629、2601~2630、2601~2631、2602~2618、2602~2619、2602~2620、2602~2621、2602~2622、2602~2623、2602~2624、2602~2625、2602~2626、2602~2627、2602~2628、2602~2629、2602~2630、2602~2631、2603~2620、2603~2621、2603~2622、2603~2623、2603~2624、2603~2625、2603~2626、2603~2627、2603~2628、2603~2629、2603~2630、2603~2631、2604~2619、2604~2620、2604~2621、2604~2622、2604~2623、2604~2624、2604~2625、2604~2626、2604~2627、2604~2628、2604~2629、2604~2630、2604~2631、2605~2620、2605~2621、2605~2622、2605~2623、2605~2624、2605~2625、2605~2626、2605~2627、2605~2628、2605~2629、2605~2630、2605~2631、2606~2621、2606~2622、2606~2623、2606~2624、2606~2625、2606~2626、2606~2627、2606~2628、2606~2629、2606~2630、2606~2631、2607~2622、2607~2623、2607~2624、2607~2625、2607~2626、2607~2627、2607~2628、2607~2629、2607~2630、2607~2631、2608~2623、2608~2624、2608~2625、2608~2626、2608~2627、2608~2628、2608~2629、2608~2630、2608~2631、2609~2624、2609~2625、2609~2626、2609~2627、2609~2628、2609~2629、2609~2630、2609~2631、2610~2625、2610~2626、2610~2627、2610~2628、2610~2629、2610~2630、2610~2631、2611~2626、2611~2627、2611~2628、2611~2629、2611~
2630、2611~2631、2612~2627、2612~2628、2612~2629、2612~2630、2612~2631、2613~2628、2613~2629、2613~2630、2613~2631、2614~2629、2614~2630、2614~2631、2615~2630、2615~2631、または2616~2631内の一領域を標的とする修飾オリゴヌクレオチドとを含むか、またはそれらからなる。特定の態様では、アンチセンス化合物またはアンチセンスオリゴヌクレオチドが、前述の核酸塩基領域内の少なくとも8、9、10、11、12、13、14、15、または16個の連続する核酸塩基を標的とする。
590、2574~2591、2574~2593、2575~2590、2575~2591、2575~2592、2575~2594、2576~2593、2576~2595、2577~2594、2577~2595、2577~2596、2578~2594、2578~2596、2578~2597、2579~2598、2580~2596、2580~2597、2580~2598、2580~2599、2581~2597、2581~2598、2581~2599、2581~2600、2582~2598、2582~2599、2582~2600、2582~2601、2583~2599、2583~2600、2583~2601、2583~2602、2584~2600、2584~2601、2584~2602、2584~2603、2585~2601、2585~2603、2585~2604、2586~2601、2586~2602、2586~2604、2586~2605、2587~2602、2587~2603、2587~2605、2587~2606、2588~2603、2588~2604、2588~2605、2588~2606、2588~2607、2589~2604、2589~2605、2589~2606、2589~2607、2589~2608、2590~2605、2590~2606、2590~2607、2590~2608、2590~2609、2590~2609、2591~2607、2591~2608、2591~2609、2591~2610、2592~2607、2592~2608、2592~2609、2592~2610、2592~2611、2593~2608、2593~2609、2593~2610、2593~2612、2594~2609、2594~2610、2594~2611、2594~2612、2594~2613、2595~2610、2595~2611、2595~2612、2595~2613、2595~2614、2596~2611、2596~2612、2596~2613、2596~2614、2596~2615、2597~2612、2597~2612、2597~2613、2597~2614、2597~2615、2597~2616、2598~2613、2598~2614、2598~2615、2598~2616、2598~2617、2599~2614、2599~2615、2599~2616、2599~2617、2599~2618、2600~2615、2600~2616、2600~2617、2600~2618、2600~2619、2601~2616、2601~2617、2601~2618、2601~2619、2601~2620、2602~2617、2602~2618、2602~2619、2602~2620、2602~2621、2603~2618、2603~2619、2603~2620、2603~2621、2603~2622、2604~2619、2604~2620、2604~2621、2604~2622、2604~2623、2605~2620、2605~2621、2605~2622、2605~2623、2605~2624、2606~2621、2606~2622、2606~2623、2606~2624、2606~2625、2607~2622、2607~2623、2607~2624、2607~2625、2607~2626、2608~2623、2608~2624、2608~2625、2608~2626、2608~2627、2609~2624、2609~2625、2609~2626、2609~2627、2609~2628、2610~2625、2610~2626、2610~2627、2610~2628、2610~2629、2611~2626、2611~2627、2611~2628、2611~2629、2611~2630、2612~2627、2612~2628、2612~2629、2612~2630、2612~2631、2613~2628、2613~2629、2613~2630、2613~2631、2614~2629、2614~2630、2614~2631、2615~2630、2615~2631、及び2616~2631。
0、1769~1784、1871~1890、1872~1891、1873~1892、1875~1890、1875~1894、1877~1892、1877~1896、1878~1897、1879~1894、1879~1898、2288~2307、2808~2827、2846~2865、2852~2871、2946~2965、3773~3792、3819~3838、3825~3844、3831~3850、3834~3853、3837~3856、3843~3862、4151~4166、4151~4170、4153~4172、4159~4178、4184~4203、4211~4230、4609~4628、4612~4631、4615~4634、4621~4640、4642~4661、4648~4667、4686~4705、4689~4708、4692~4711、4698~4717、4714~4733、5270~5289、5295~5314、5296~5315、5830~5849、5890~5909、5904~5923、6406~6425、6662~6681、6674~6693、6954~6973、6960~6979、6977~6996、6979~6998、6981~7000、6983~6998、6983~7002、6984~7003、6985~7000、6985~7004、6990~7009、7122~7141、7125~7144、7151~7170、7353~7372、7362~7381、7683~7702、7688~7707、7690~7709、7692~7707、7692~7711、7694~7709、7694~7713、7696~7711、7696~7715、7767~7786、7785~7804、7786~7801、7787~7803、7787~7805、7787~7806、7788~7803、7788~7805、7788~7806、7788~7807、7789~7806、7789~7807、7789~7808、7790~7805、7790~7807、7790~7809、7791~7808、7791~7809、7791~7810、7792~7808、7792~7809、7792~7810、7792~7811、7793~7810、7793~7811、7793~7812、7794~7811、7794~7812、7794~7813、7795~7812、7795~7813、7795~7814、7796~7811、7796~7813、7796~7814、7796~7815、7797~7812、7797~7814、7797~7816、7798~7813、7798~7815、7798~7817、7799~7816、7799~7818、7800~7819、7801~7818、7801~7820、7802~7817、7802~7819、7802~7821、7803~7818、7803~7820、7803~7822、7804~7821、7804~7823、7805~7820、7805~7822、7805~7824、7806~7821、7806~7823、7806~7825、7807~7824、7807~7825、7807~7826、7808~7825、7808~7827、7809~7825、7809~7826、7809~7828、7810~7825、7810~7826、7810~7827、7810~7829、7811~7828、7811~7830、7812~7829、7812~7830、7812~7831、7813~7829、7813~7831、7813~7832、7814~7833、7815~7831、7815~7832、7815~7833、7815~7834、7816~7832、7816~7833、7816~7834、7816~7835、7817~7833、7817~7834、7817~7835、7817~7836、7818~7834、7818~7835、7818~7836、7818~7837、7819~7835、7819~7836、7819~7837、7819~7838、7820~7836、7820~7838、7820~7839、7821~7836、7821~7837、7821~7839、7821~7840、7822~7837、7822~7838、7822~7840、7822~7841、7823~7838、7823~7839、7823~7839、7823~7840、7823~7841、7823~7842、7824~7839、7824~7840、7824~7840、7824~7841、7824~7842、7824~7843、7825~784
0、7825~7841、7825~7842、7825~7843、7825~7844、7826~7842、7826~7843、7826~7844、7826~7845、7827~7842、7827~7843、7827~7844、7827~7845、7827~7846、7828~7843、7828~7844、7828~7845、7828~7847、7829~7844、7829~7845、7829~7846、7829~7847、7829~7848、7830~7845、7830~7846、7830~7847、7830~7848、7830~7849、7831~7846、7831~7847、7831~7848、7831~7849、7831~7850、7832~7847、7832~7848、7832~7849、7832~7850、7832~7851、7833~7848、7833~7849、7833~7850、7833~7851、7833~7852、7834~7849、7834~7850、7834~7851、7834~7852、7834~7853、7835~7850、7835~7851、7835~7852、7835~7853、7835~7854、7836~7851、7836~7852、7836~7853、7836~7854、7836~7855、7837~7852、7837~7853、7837~7854、7837~7855、7837~7856、7838~7853、7838~7854、7838~7855、7838~7856、7838~7857、7839~7854、7839~7855、7839~7856、7839~7857、7839~7858、7840~7855、7840~7856、7840~7857、7840~7858、7840~7859、7841~7856、7841~7857、7841~7858、7841~7859、7841~7860、7842~7857、7842~7858、7842~7859、7842~7860、7842~7861、7843~7858、7843~7859、7843~7860、7843~7861、7843~7862、7844~7859、7844~7860、7844~7861、7844~7862、7845~7860、7845~7861、7845~7862、7846~7861、及び7846~7862。
2568~2585、2568~2587、2569~2586、2569~2588、2570~2587、2570~2589、2571~2588、2572~2590、2572~2591、2573~2590、2573~2592、2574~2591、2574~2593、2575~2590、2575~2592、2575~2594、2576~2593、2576~2595、2577~2594、2577~2595、2577~2596、2578~2594、2578~2597、2579~2598、2580~2596、2580~2597、2580~2598、2580~2599、2581~2597、2581~2598、2581~2599、2581~2600、2582~2598、2582~2599、2582~2600、2582~2601、2583~2599、2583~2600、2583~2601、2583~2602、2584~2600、2584~2602、2584~2603、2585~2601、2585~2603、2585~2604、2586~2602、2586~2604、2586~2605、2587~2603、2587~2605、2587~2606、2588~2603、2588~2604、2588~2606、2588~2607、2589~2605、2589~2606、2589~2607、2589~2608、2590~2605、2590~2606、2590~2607、2590~2608、2590~2609、2591~2607、2591~2609、2591~2610、2592~2608、2592~2609、2592~2611、2593~2608、2593~2609、2593~2612、2594~2609、2594~2610、2594~2611、2594~2612、2594~2613、2595~2610、2595~2611、2595~2612、2595~2613、2595~2614、2596~2611、2596~2612、2596~2613、2596~2614、2596~2615、2597~2612、2597~2613、2597~2614、2597~2615、2597~2616、2598~2613、2598~2614、2598~2615、2598~2616、2598~2617、2599~2614、2599~2615、2599~2616、2599~2617、2599~2618、2600~2615、2600~2616、2600~2617、2600~2618、2600~2619、2601~2616、2601~2617、2601~2618、2601~2619、2601~2620、2602~2617、2602~2618、2602~2619、2602~2620、2602~2621、2603~2618、2603~2619、2603~2620、2603~2621、2603~2622、2604~2619、2604~2620、2604~2621、2604~2622、2604~2623、2605~2620、2605~2621、2605~2622、2605~2623、2605~2624、2606~2621、2606~2622、2606~2623、2606~2624、2606~2625、2607~2622、2607~2623、2607~2624、2607~2625、2607~2626、2608~2623、2608~2624、2608~2625、2608~2625、2608~2626、2608~2627、2609~2624、2609~2625、2609~2626、2609~2627、2609~2628、2610~2625、2610~2626、2610~2627、2610~2628、2610~2629、2611~2626、2611~2626、2611~2627、2611~2628、2611~2629、2611~2630、2612~2627、2612~2628、2612~2629、2612~2630、2612~2631、2613~2628、2613~2629、2613~2630、2613~2631、2614~2629、2614~2630、2614~2631、2615~2630、2615~2630、2615~2631、2615~2631、及び2616~2631。
0、1873~1892、1875~1890、1875~1894、1877~1892、1877~1896、1879~1894、1879~1898、2808~2827、3819~3838、3825~3844、3831~3850、3837~3856、4151~4166、5890~5909、5904~5923、5904~5923、6406~6425、6977~6996、6979~6998、6981~7000、6983~6998、6983~7002、6985~7000、6985~7004、7122~7141、7683~7702、7688~7707、7690~7709、7692~7707、7692~7711、7694~7709、7696~7711、7696~7715、7786~7801、7787~7806、7788~7803、7788~7805、7788~7806、7788~7807、7789~7806、7789~7807、7789~7808、7790~7807、7790~7809、7791~7808、7791~7809、7791~7810、7792~7809、7792~7810、7792~7811、7793~7810、7793~7811、7793~7812、7794~7811、7794~7812、7794~7813、7795~7812、7795~7813、7795~7814、7796~7813、7796~7814、7796~7815、7797~7812、7797~7814、7797~7816、7798~7813、7798~7815、7798~7817、7799~7816、7799~7818、7800~7819、7801~7818、7801~7820、7802~7817、7802~7819、7802~7821、7803~7818、7803~7820、7803~7822、7804~7821、7804~7823、7805~7822、7805~7824、7806~7823、7806~7825、7807~7824、7807~7825、7807~7826、7808~7825、7808~7827、7809~7826、7809~7828、7810~7825、7810~7827、7810~7829、7811~7828、7811~7830、7812~7829、7812~7830、7812~7831、7813~7829、7813~7832、7814~7833、7815~7831、7815~7832、7815~7833、7815~7834、7816~7832、7816~7833、7816~7834、7816~7835、7817~7833、7817~7834、7817~7835、7817~7836、7818~7834、7818~7835、7818~7836、7818~7837、7819~7835、7819~7837、7819~7838、7820~7836、7820~7838、7820~7839、7821~7837、7821~7839、7821~7840、7822~7838、7822~7840、7822~7841、7823~7838、7823~7839、7823~7841、7823~7842、7824~7840、7824~7841、7824~7842、7824~7843、7825~7840、7825~7841、7825~7842、7825~7843、7825~7844、7826~7842、7826~7844、7826~7845、7827~7843、7827~7844、7827~7846、7828~7843、7828~7844、7828~7847、7829~7844、7829~7845、7829~7846、7829~7847、7829~7848、7830~7845、7830~7846、7830~7847、7830~7848、7830~7849、7831~7846、7831~7847、7831~7848、7831~7849、7831~7850、7832~7847、7832~7848、7832~7849、7832~7850、7832~7851、7833~7848、7833~7849、7833~7850、7833~7851、7833~7852、7834~7849、7834~7850、7834~7851、7834~7852、7834~7853、7835~7850、7835~7851、7835~7852、7835~7853、7835~7854、7836~7851、7836~7852、7836~7853、7836~7854、7836~7855、7837~7852、7837~7853、7837~7854、7837~7855、7837~7856、7838~7853、7838~785
4、7838~7855、7838~7856、7838~7857、7839~7854、7839~7855、7839~7856、7839~7857、7839~7858、7840~7855、7840~7856、7840~7857、7840~7858、7840~7859、7841~7856、7841~7857、7841~7858、7841~7859、7841~7860、7842~7857、7842~7858、7842~7859、7842~7860、7842~7861、7843~7858、7843~7859、7843~7860、7843~7861、7843~7862、7844~7859、7844~7860、7844~7861、7844~7862、7845~7860、7845~7861、7845~7862、7846~7861、7846~7862、及び7847~7862。
5、2597~2616、2598~2613、2598~2614、2598~2615、2598~2616、2598~2617、2599~2614、2599~2615、2599~2616、2599~2617、2599~2618、2600~2615、2600~2616、2600~2617、2600~2618、2600~2619、2601~2616、2601~2617、2601~2618、2601~2619、2601~2620、2602~2617、2602~2618、2602~2619、2602~2620、2602~2621、2603~2619、2603~2620、2603~2621、2603~2622、2604~2619、2604~2620、2604~2621、2604~2622、2604~2623、2605~2620、2605~2621、2605~2622、2605~2623、2605~2624、2606~2621、2606~2622、2606~2623、2606~2624、2606~2625、2607~2622、2607~2623、2607~2624、2607~2625、2607~2626、2608~2623、2608~2624、2608~2625、2608~2626、2608~2627、2609~2624、2609~2625、2609~2626、2609~2627、2609~2628、2610~2625、2610~2626、2610~2627、2610~2628、2610~2629、2611~2626、2611~2627、2611~2629、2611~2630、2612~2627、2612~2628、2612~2629、2612~2630、2612~2631、2613~2628、2613~2629、2613~2630、2613~2631、2614~2629、2614~2630、2614~2631、2615~2630、2615~2630、2615~2631、及び2616~2631。
6、7818~7834、7818~7836、7818~7837、7819~7835、7819~7837、7819~7838、7820~7836、7820~7838、7820~7839、7821~7840、7822~7841、7823~7839、7823~7841、7823~7842、7824~7840、7824~7841、7824~7842、7824~7843、7825~7840、7825~7841、7825~7842、7825~7844、7826~7842、7826~7845、7827~7846、7828~7843、7828~7847、7829~7844、7829~7845、7829~7847、7829~7848、7830~7845、7830~7846、7830~7847、7830~7848、7830~7849、7831~7846、7831~7849、7831~7850、7832~7847、7832~7848、7832~7849、7832~7850、7832~7851、7833~7848、7833~7849、7833~7850、7833~7851、7833~7852、7834~7849、7834~7850、7834~7851、7834~7852、7834~7853、7835~7850、7835~7851、7835~7852、7835~7853、7835~7854、7836~7851、7836~7852、7836~7853、7836~7854、7836~7855、7837~7852、7837~7853、7837~7854、7837~7855、7837~7856、7838~7854、7838~7855、7838~7856、7838~7857、7839~7854、7839~7855、7839~7856、7839~7857、7839~7858、7840~7855、7840~7856、7840~7857、7840~7858、7840~7859、7841~7856、7841~7857、7841~7858、7841~7859、7841~7860、7842~7857、7842~7858、7842~7859、7842~7860、7842~7861、7843~7858、7843~7859、7843~7860、7843~7861、7843~7862、7844~7859、7844~7860、7844~7861、7844~7862、7845~7860、7845~7861、7845~7862、7846~7861、7846~7862、及び7847~7862。
604、2586~2605、2587~2606、2588~2607、2589~2608、2590~2606、2590~2607、2590~2609、2591~2610、2592~2611、2593~2608、2593~2612、2594~2613、2595~2611、2595~2614、2596~2615、2597~2612、2597~2613、2597~2614、2597~2615、2597~2616、2598~2613、2598~2613、2598~2614、2598~2615、2598~2616、2598~2617、2599~2614、2599~2617、2599~2618、2600~2615、2600~2617、2600~2618、2600~2619、2601~2616、2601~2617、2601~2619、2601~2620、2602~2618、2602~2621、2603~2620、2603~2621、2603~2622、2604~2619、2604~2620、2604~2621、2604~2622、2604~2623、2605~2620、2605~2621、2605~2622、2605~2623、2605~2624、2606~2621、2606~2622、2606~2623、2606~2624、2606~2625、2607~2622、2607~2623、2607~2624、2607~2625、2607~2626、2608~2623、2608~2624、2608~2625、2608~2627、2609~2624、2609~2626、2609~2627、2609~2628、2610~2625、2610~2626、2610~2628、2610~2629、2611~2626、2611~2627、2611~2629、2611~2630、2612~2627、2612~2628、2612~2630、2612~2631、2613~2628、2613~2629、2613~2631、2614~2629、2614~2630、2614~2631、2615~2630、及び2616~2631。
0、7833~7851、7833~7852、7834~7849、7834~7852、7834~7853、7835~7850、7835~7852、7835~7853、7835~7854、7836~7851、7836~7852、7836~7854、7836~7855、7837~7853、7837~7856、7838~7855、7838~7856、7838~7857、7839~7854、7839~7855、7839~7856、7839~7857、7839~7858、7840~7855、7840~7856、7840~7857、7840~7858、7840~7859、7841~7856、7841~7857、7841~7858、7841~7859、7841~7860、7842~7857、7842~7858、7842~7859、7842~7860、7842~7861、7843~7858、7843~7859、7843~7860、7843~7862、7844~7859、7844~7861、7844~7862、7845~7860、7845~7861、7846~7862、及び7847~7862。
9、7834~7853、7835~7850、7836~7852、7836~7855、7837~7856、7838~7856、7839~7857、7839~7858、7840~7856、7840~7857、7840~7859、7843~7858、7843~7860、及び7846~7862。
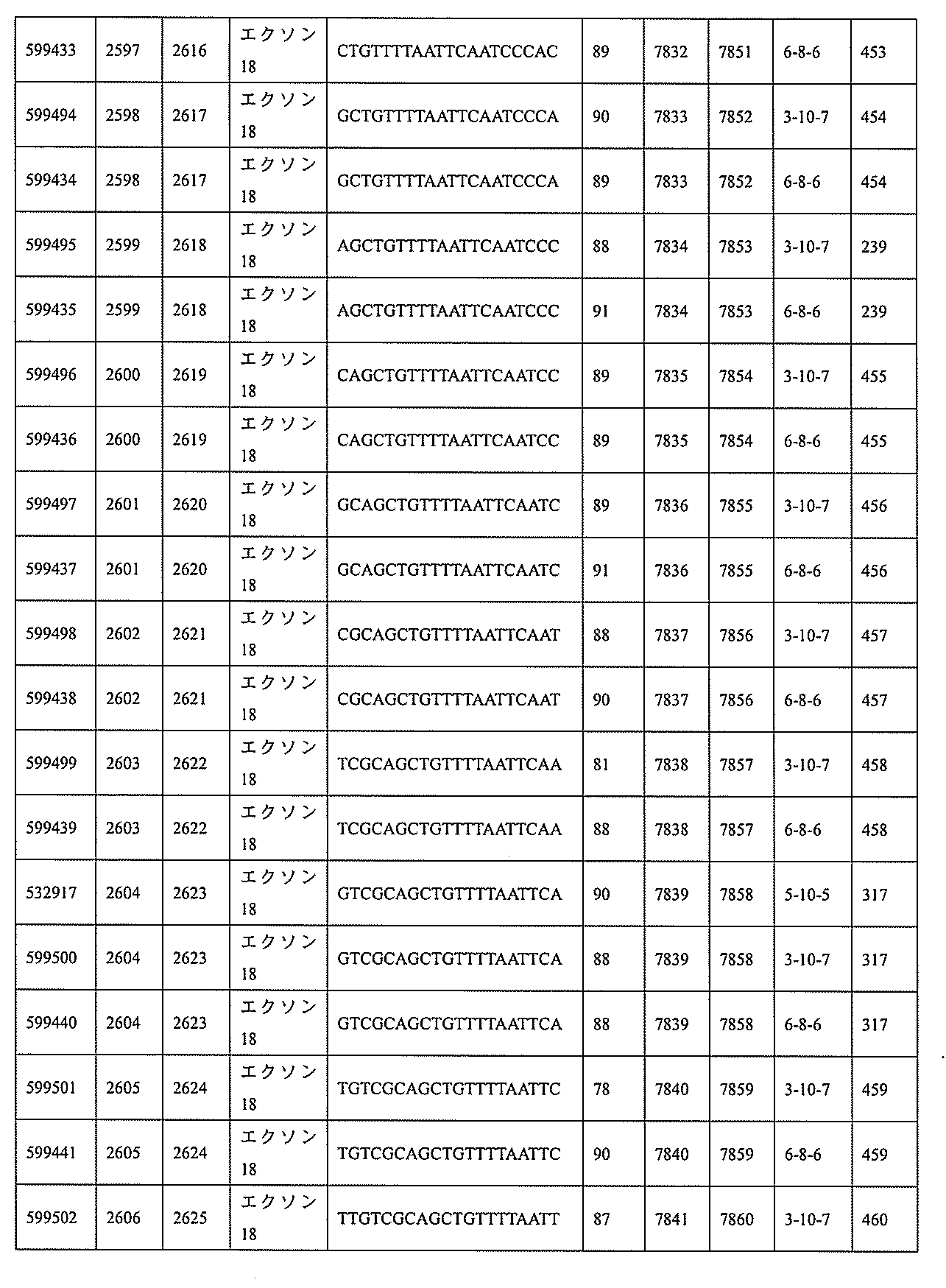
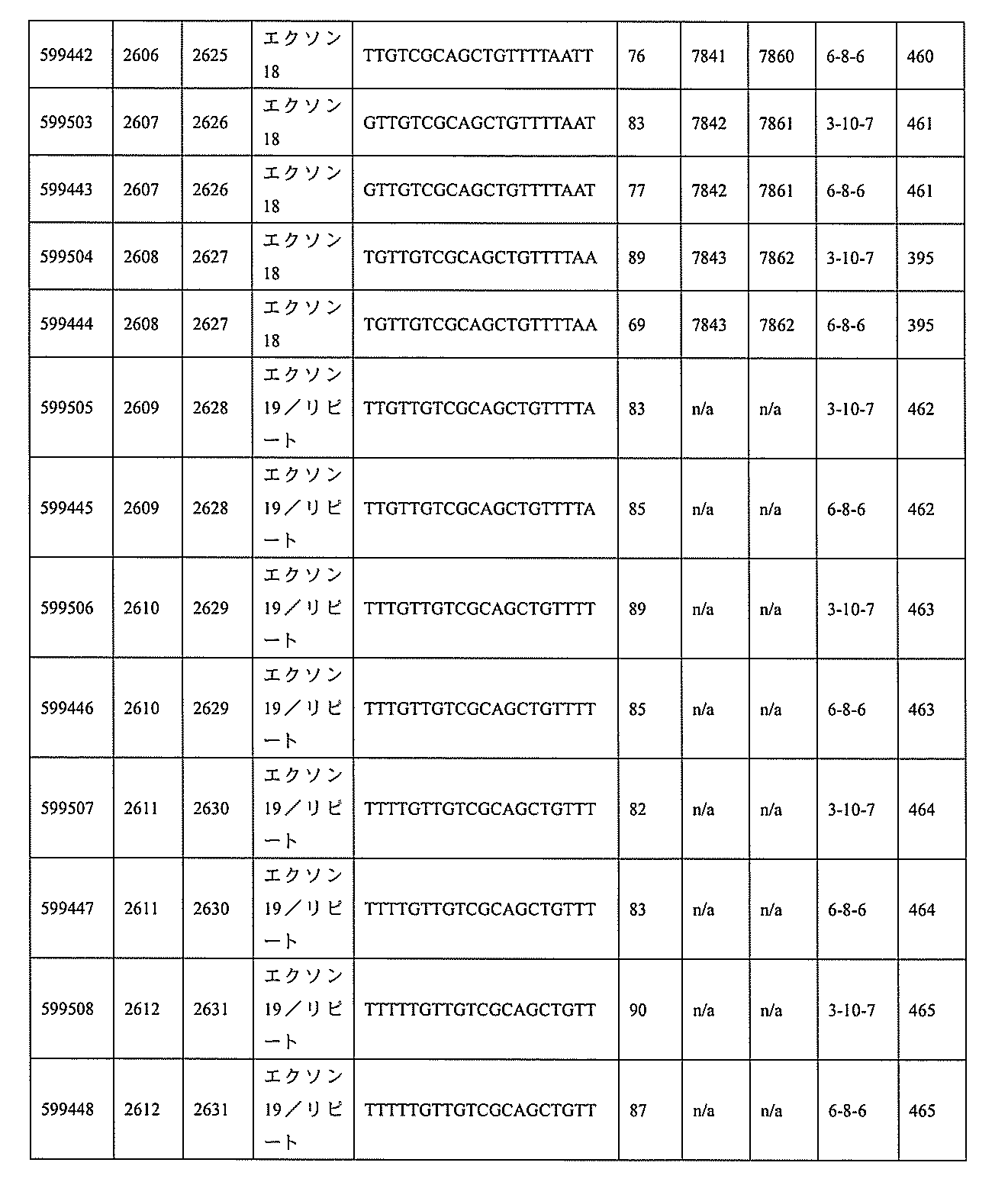
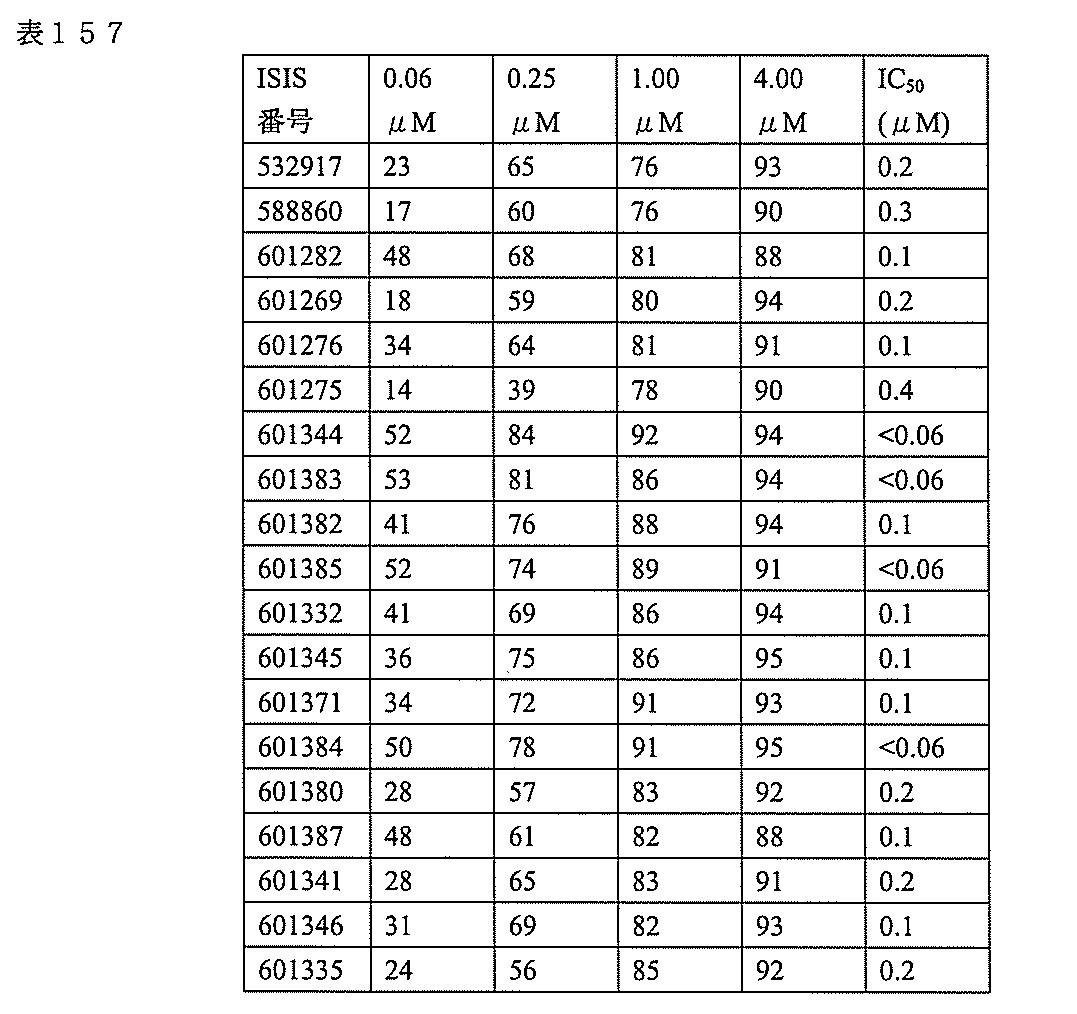
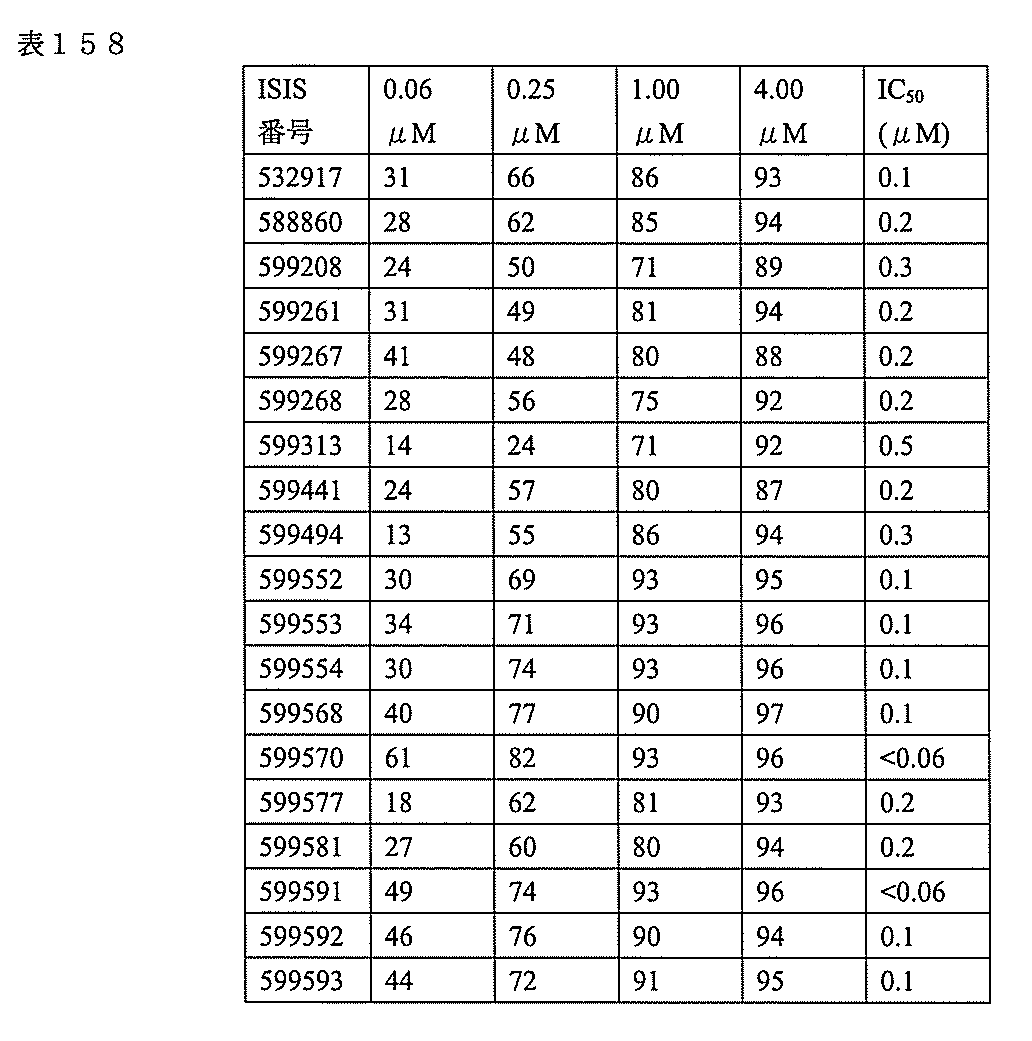
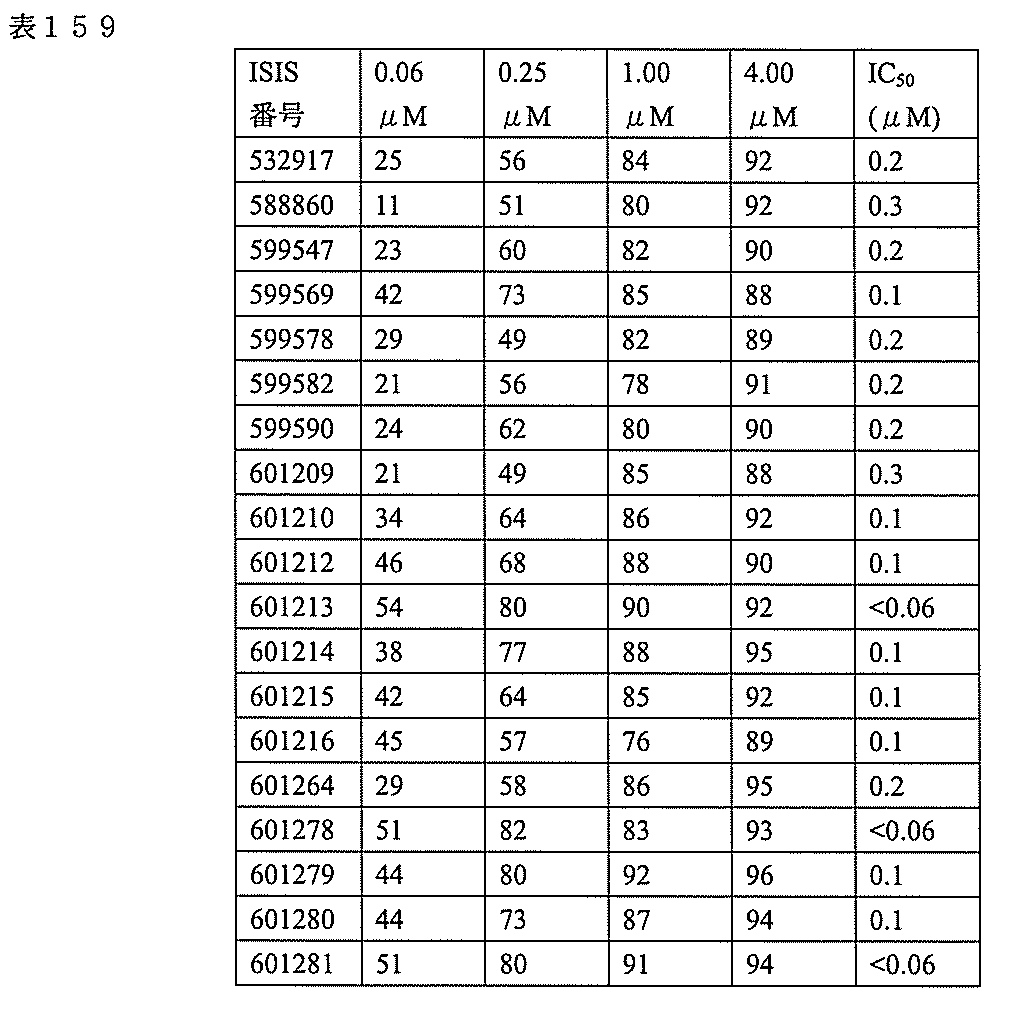
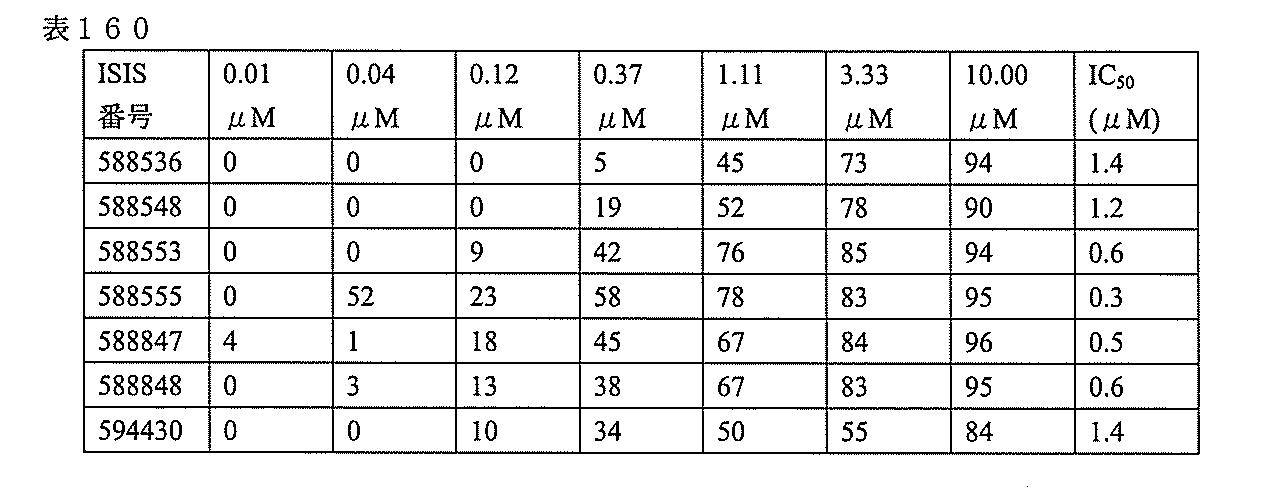
3、599084、599085、599086、599087、599088、599089、599090、599091、599092、599093、599094、599095、599096、599097、599098、599102、599119、599123、599124、599125、599126、599127、599128、599132、599133、599134、599135、599136、599137、599138、599139、599140、599141、599142、599143、599144、599145、599147、599148、599149、599150、599151、599152、599153、599154、599155、599156、599157、599158、599159、599178、599179、599180、599181、599182、599186、599187、599188、599189、599190、599191、599192、599193、599194、599195、599196、599197、599198、599199、599200、599201、599202、599203、599204、599205、599206、599207、599208、599209、599210、599211、599212、599213、599214、599215、599216、599217、599218、599219、599220、599221、599221、599222、599223、599224、599225、599226、599227、599228、599229、599230、599231、599232、599233、599234、599235、599236、599241、599247、599248、599249、599255、599256、599257、599258、599260、599261、599262、599263、599264、599265、599266、599267、599268、599269、599270、599271、599272、599273、599274、599275、599276、599277、599278、599279、599280、599297、599299、599306、599307、599308、599309、599311、599312、599313、599314、599315、599316、599317、599318、599319、599320、599321、599322、599323、599324、599325、599326、599327、599328、599329、599330、599338、599349、599353、599354、599355、599356、599357、599358、599359、599360、599361、599362、599363、599364、599369、599371、599372、599373、599376、599378、599379、599382、599383、599384、599385、599386、599387、599388、599389、599390、599391、599392、599393、599394、599395、599396、599397、599398、599399、599400、599401、599402、599403、599404、599405、599406、599407、599408、599409、599410、599412、599413、599414、599415、599416、599417、599418、599419、599420、599421、599422、599423、599424、599425、599426、599433、599434、599435、599436、599437、599438、599439、599440、599441、599442、599443、599444、599445、599446、599447、599448、599450、599454、599455、599456、599467、599468、599469、599471、599472、599473、599474、599475、599476、599477、599478、599479、599480、599481、599482、599483、599484、599485、599486、599487、599488、599489、599490、599491、599492、599493、599494、599495、599496、599497、599498、599499、599500、599501、599502、599503、599504、599505、599
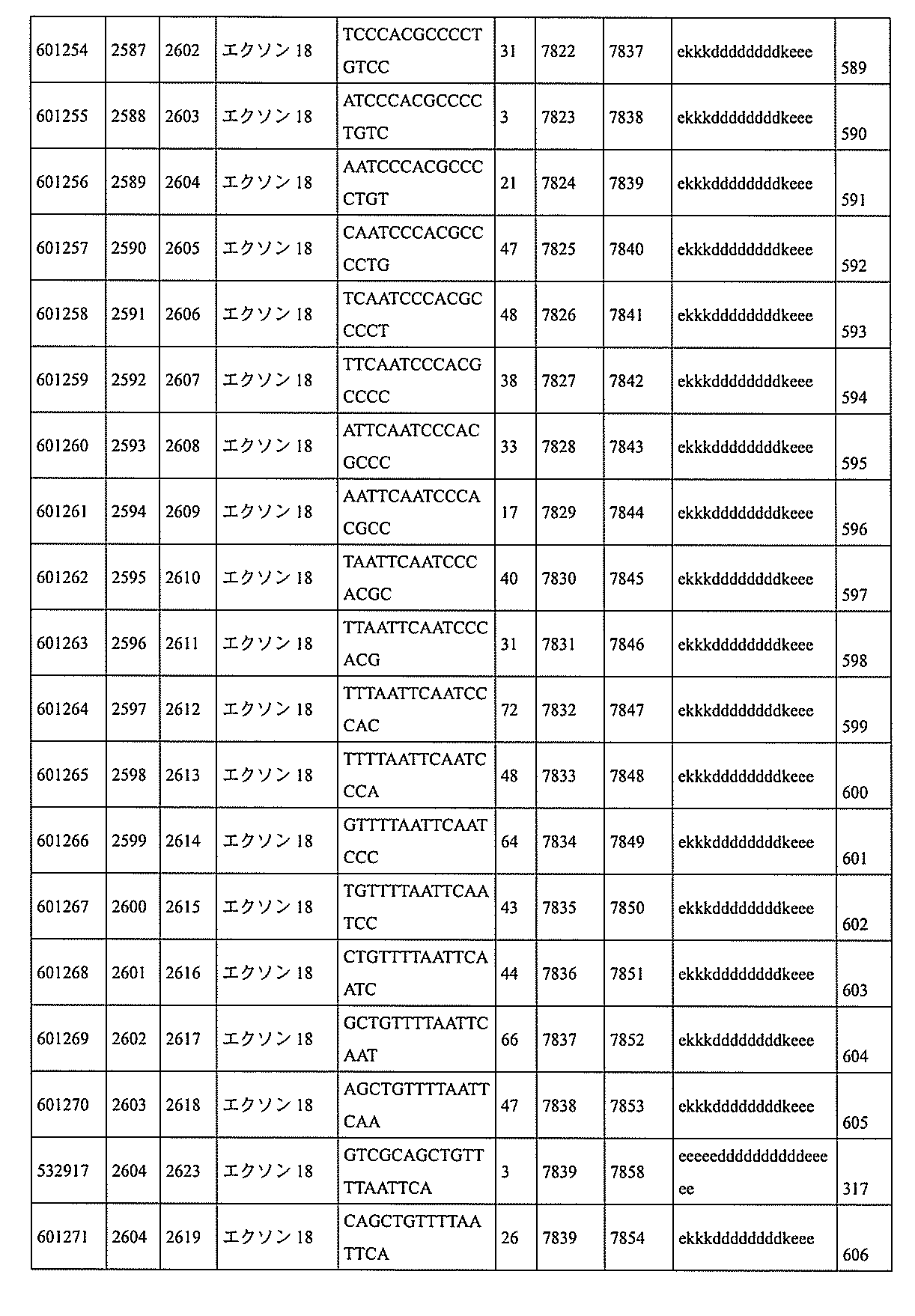
506、599507、599508、599509、599512、599515、599518、599531、599541、599541、599546、599547、599548、599549、599550、599552、599553、599554、599555、599557、599558、599561、599562、599563、599564、599565、599566、599567、599568、599569、599570、599577、599578、599579、599580、599581、599581、599582、599584、599585、599586、599587、599588、599589、599590、599591、599592、599593、599594、599595、601321、601322、601323、601325、601327、601328、601329、601330、601332、601333、601334、601335、601336、601337、601338、601339、601341、601342、601343、601344、601345、601346、601347、601348、601349、601362、601367、601368、601369、601371、601372、601373、601374、601375、601377、601378、601380、601381、601382、601383、601384、601385、601386、601387、及び601388。
、758、759、760、761、762、766、767、768、769、770、771、772、773、774、775、776、777、778、779、780、781、782、783、784、785、786、787、788、789、790、791、792、793、794、795、796、797、798、799、813、833、834、841、846、849、850、867、及び873
599219、599220、599221、599222、599223、599224、599225、599226、599227、599228、599229、599230、599231、599232、599233、599234、599235、599236、599247、599255、599256、599257、599263、599264、599265、599266、599270、599271、599272、599273、599274、599275、599276、599277、599278、599279、599280、599306、599307、599308、599311、599312、599313、599314、599315、599316、599317、599318、599319、599320、599321、599322、599323、599324、599325、599327、599328、599329、599330、599349、599353、599355、599356、599357、599358、599359、599360、599361、599362、599363、599364、599369、599371、599372、599373、599376、599378、599379、599382、599384、599386、599387、599388、599389、599390、599391、599392、599393、599394、599395、599396、599397、599398、599399、599400、599401、599402、599403、599404、599405、599406、599407、599408、599409、599410、599412、599413、599414、599415、599416、599417、599418、599419、599420、599421、599422、599423、599424、599425、599433、599434、599435、599436、599437、599438、599439、599440、599441、599442、599443、599444、599445、599446、599447、599448、599456、599467、599468、599471、599472、599473、599474、599475、599476、599477、599478、599479、599480、599481、599482、599483、599484、599485、599486、599487、599488、599489、599490、599491、599492、599493、599494、599495、599496、599497、599498、599499、599500、599501、599502、599503、599504、599505、599506、599507、599508、599512、599531、599547、599548、599549、599552、599553、599554、599555、599557、599558、599562、599563、599564、599565、599566、599567、599568、599569、599570、599577、599578、599579、599580、599581、599582、599584、599585、599586、599587、599588、599589、599590、599591、599592、599593、599594、599595、601323、601327、601329、601332、601333、601333、601334、601335、601336、601338、601339、601341、601342、601343、601344、601345、601346、601347、601348、601349、601368、601369、601371、601372、601374、601375、601377、601378、601380、601381、601382、601383、601384、601385、601386、601387、及び601388。
、414、415、416、417、418、419、420、421、422、423、424、425、426、427、428、429、430、431、432、433、434、435、436、437、438、439、440、441、442、443、444、445、446、447、448、449、450、451、452、453、454、455、456、457、458、459、460、461、462、463、464、465、472、473、513、514、515、531、537、541、542、543、544、545、546、547、549、550、551、552、553、554、555、556、557、558、564、565、569、570、577、590、592、595、596、597、598、599、600、601、602、603、604、605、606、607、608、609、610、611、612、613、614、615、616、617、618、644、645、646、647、648、649、650、651、652、653、654、655、656、657、658、659、660、661、662、663、664、665、666、667、668、669、670、671、672、673、674、675、676、677、678、679、680、682、683、684、685、686、687、688、689、700、704、706、707、708、709、711、712、713、714、715、716、717、720、721、722、723、724、725、726、727、727、728、729、730、731、732、733、734、736、737、738、739、740、741、742、743、744、745、745、746、747、748、749、750、751、752、753、754、755、756、758、759、760、761、767、768、770、772、773、774、775、775、776、776、777、777、778、779、780、781、782、783、783、784、784、785、786、787、788、789、790、791、792、793、794、795、796、797、798、799、813、833、834、841、846、849、及び850。
599024、599025、599027、599028、599029、599030、599031、599032、599033、599034、599072、599077、599080、599085、599086、599087、599088、599089、599090、599091、599093、599094、599095、599096、599097、599125、599126、599134、599138、599139、599148、599149、599150、599151、599152、599154、599155、599156、599157、599158、599187、599188、599193、599195、599196、599197、599198、599199、599200、599201、599202、599203、599204、599205、599206、599207、599208、599210、599211、599212、599213、599214、599215、599216、599217、599218、599219、599220、599221、599222、599223、599224、599225、599226、599227、599228、599229、599230、599231、599232、599233、599234、599235、599236、599266、599272、599272、599273、599274、599275、599277、599278、599279、599280、599280、599306、599311、599312、599313、599314、599315、599316、599317、599318、599319、599320、599321、599322、599323、599325、599327、599328、599329、599330、599355、599357、599358、599359、599360、599361、599362、599363、599364、599369、599371、599372、599373、599378、599379、599382、599384、599386、599387、599388、599389、599390、599391、599392、599393、599394、599395、599396、599397、599398、599399、599400、599401、599402、599403、599404、599405、599406、599407、599408、599409、599410、599413、599414、599415、599416、599417、599418、599419、599420、599421、599422、599423、599424、599433、599434、599435、599436、599437、599438、599439、599440、599441、599442、599443、599445、599446、599447、599448、599472、599473、599474、599475、599476、599477、599478、599479、599480、599481、599482、599483、599484、599485、599486、599487、599488、599489、599490、599491、599492、599493、599494、599495、599496、599497、599498、599499、599500、599501、599502、599503、599504、599505、599506、599507、599508、599512、599547、599548、599552、599553、599554、599555、599558、599562、599563、599564、599566、599567、599568、599569、599570、599577、599578、599579、599580、599581、599582、599585、599586、599587、599588、599589、599590、599591、599592、599593、599594、599595、601332、601335、601341、601343、601344、601345、601346、601347、601348、601349、601371、601372、601380、601382、601383、601384、601385、601386、及び601387。
ドがCFB核酸の一領域を標的とし、少なくとも70%のCFB mRNA阻害を達成する;配列番号:12、84、85、86、198、228、237、238、239、317、395、396、397、398、399、402、403、404、405、407、408、410、411、412、412、413、414、415、416、417、418、419、420、421、422、423、424、425、426、427、428、429、430、431、432、433、433、434、435、436、437、438、439、440、441、442、443、444、445、446、447、448、449、450、451、452、453、454、455、456、457、458、459、460、461、462、463、464、464、465、472、473、513、514、515、541、542、543、544、545、546、547、549、550、551、552、553、554、555、556、557、564、565、569、592、595、596、597、598、599、600、601、602、603、604、606、607、608、609、610、611、612、613、614、615、616、617、618、645、646、647、648、649、650、653、654、655、656、659、660、662、663、664、665、666、668、669、670、671、672、673、674、675、676、677、677、678、679、680、682、683、684、686、687、688、689、706、708、709、711、712、713、714、715、720、721、722、723、724、725、726、727、728、729、730、731、732、733、734、736、737、738、739、740、741、742、743、744、745、746、747、748、749、750、751、752、753、754、755、756、767、768、773、775、776、777、778、779、780、781、782、783、784、785、786、787、788、789、790、791、792、793、793、794、795、797、798、799、813、833、834、841、846、849、867、及び873。
599226、599227、599228、599229、599230、599231、599232、599233、599234、599235、599236、599272、599273、599275、599277、599278、599279、599280、599311、599313、599314、599316、599317、599318、599320、599321、599322、599323、599327、599328、599329、599330、599355、599357、599358、599359、599360、599361、599362、599363、599364、599371、599372、599373、599378、599379、599382、599384、599386、599387、599388、599389、599390、599391、599392、599393、599397、599398、599399、599400、599401、599403、599404、599405、599407、599408、599409、599410、599413、599414、599415、599416、599417、599418、599419、599420、599421、599422、599423、599424、599433、599434、599435、599436、599437、599438、599439、599440、599441、599445、599446、599447、599448、599474、599476、599477、599479、599481、599482、599483、599485、599486、599487、599488、599489、599490、599491、599492、599494、599495、599496、599497、599498、599499、599500、599502、599503、599504、599505、599506、599507、599508、599547、599552、599553、599554、599558、599563、599567、599568、599569、599570、599577、599578、599581、599582、599585、599587、599588、599590、599591、599592、599593、599594、601332、601344、601345、601382、601383、及び601385。
。
連結されたデオキシヌクレオシドからなるギャップセグメント、
連結されたヌクレオシドからなる5’ウイングセグメント、及び
連結されたヌクレオシドからなる3’ウイングセグメント
を含む修飾オリゴヌクレオチドとを含み、前記ギャップセグメントは前記5’ウイングセグメントと前記3’ウイングセグメントの間に配置されており、各ウイングセグメントの各ヌクレオシドは修飾糖を含む。特定の実施形態では、前記オリゴヌクレオチドが、配列番号198、228、237、440、444、448、450、453、455、549、または598に示す配列を含む核酸塩基配列を有する10~30個の連結されたヌクレオシドからなる。
10個の連結されたデオキシヌクレオシドからなるギャップセグメント、
5個の連結されたヌクレオシドからなる5’ウイングセグメント、及び
5個の連結されたヌクレオシドからなる3’ウイングセグメント
を含み、前記ギャップセグメントは前記5’ウイングセグメントと前記3’ウイングセグメントの間に配置されており、各ウイングセグメントの各ヌクレオシドは2’-O-メトキシエチル糖を含み、各ヌクレオシド間連結部はホスホロチオエート連結部であり、かつ各シトシンは5-メチルシトシンである。
10個の連結されたデオキシヌクレオシドからなるギャップセグメント、
5個の連結されたヌクレオシドからなる5’ウイングセグメント、及び
5個の連結されたヌクレオシドからなる3’ウイングセグメント
を含み、前記ギャップセグメントは前記5’ウイングセグメントと前記3’ウイングセグメントの間に配置されており、各ウイングセグメントの各ヌクレオシドは2’-O-メトキシエチル糖を含み;各ヌクレオシド間連結部はホスホロチオエート連結部であり、各シトシンは5-メチルシトシンである。
10個の連結されたデオキシヌクレオシドからなるギャップセグメント、
3個の連結されたヌクレオシドからなる5’ウイングセグメント、及び
3個の連結されたヌクレオシドからなる3’ウイングセグメント
を含み、前記ギャップセグメントは前記5’ウイングセグメントと前記3’ウイングセ
グメントの間に配置されており、各ウイングセグメントの各ヌクレオシドはcEt糖を含み、各ヌクレオシド間連結部はホスホロチオエート連結部であり、かつ各シトシンは5-メチルシトシンである。
10個の連結されたデオキシヌクレオシドからなるギャップセグメント、
3個の連結されたヌクレオシドからなる5’ウイングセグメント、及び
3個の連結されたヌクレオシドからなる3’ウイングセグメント
を含み、前記ギャップセグメントは前記5’ウイングセグメントと前記3’ウイングセグメントの間に配置されており、前記5’ウイングセグメントは5’→3’方向に2’-O-メトキシエチル糖、2’-O-メトキシエチル糖、及びcEt糖を含み、前記3’ウイングセグメントは5’→3’方向にcEt糖、cEt糖、及び2’-O-メトキシエチル糖を含み、各ヌクレオシド間連結部はホスホロチオエート連結部であり、かつ各シトシンは5-メチルシトシンである。
[式中、R1は-OCH2CH2OCH3(MOE)であり、かつR2がHであるか、またはR1とR2とが全体として橋を形成し、その場合、R1は-O-であり、R2は-CH2-、-CH(CH3)-、または-CH2CH2-であって、R1とR2は、結果として生じる橋が-O-CH2-、-O-CH(CH3)-、及び-O-CH2CH2-から選択されることになるように直接つながれている。
また、同じ環上のR3とR4の各ペアについては、環ごとに独立して、R3がH及び-OCH2CH2OCH3から選択され、かつR4がHであるか、またはR3とR4とが全体として橋を形成し、その場合、R3は-O-、かつR4は-CH2-、-CH(CH3)-、または-CH2CH2-であって、R3とR4は、結果として生じる橋が-O-CH2-、-O-CH(CH3)-、及び-O-CH2CH2-から選択されることになるように直接つながれている;
また、R5はH及び-CH3から選択され、
また、ZはS-及びO-から選択される]。
組成物が、約40センチポアズ(cP)未満、約30センチポアズ(cP)未満、約20センチポアズ(cP)未満、約15センチポアズ(cP)未満、または約10センチポアズ(cP)未満の粘度を有する。特定の態様では、上述した粘度のいずれかを有する前記組成物が、ここに提供する化合物を、約100mg/mL、約125mg/mL、約150mg/mL、約175mg/mL、約200mg/mL、約225mg/mL、約250mg/mL、約275mg/mL、または約300mg/mLの濃度で含む。特定の態様では、上述した粘度及び/または化合物濃度のいずれかを有する前記組成物が、室温または約20℃、約21℃、約22℃、約23℃、約24℃、約25℃、約26℃、約27℃、約28℃、約29℃、もしくは約30℃の温度を有する。
の連結されたヌクレオシドからなる。特定の実施形態では、補体代替経路の調節異常に関連する疾患を有するかまたは前記疾患を有するリスクがある対象における補体B因子(CFB)の発現を阻害する方法が、ISIS696844、ISIS696845、ISIS698969、もしくはISIS698970を含むかまたはそれからなる化合物を前記対象に投与することを含む。特定の態様では、前記化合物または組成物を投与することにより、眼におけるCFBの発現が阻害される。特定の態様において、前記対象は、加齢黄斑変性(AMD)、例えば滲出型AMD及び乾性AMDを有するか、またはそれらを有するリスクがある。特定の態様では、乾性AMDが地図状萎縮でありうる。地図状萎縮は、網膜の変性を伴う進行した形態の乾性AMDとみなされる。特定の態様では、前記化合物または組成物を投与することにより、腎臓、例えば糸球体におけるCFBの発現が阻害される。特定の態様において、前記対象は、ループス腎炎、全身性エリテマトーデス(SLE)、デンスデポジット病(DDD)、C3糸球体腎炎(C3GN)、CFHR5ネフロパシー、もしくは非典型溶血性尿毒症症候群(aHUS)、またはそれらの任意の組み合わせを有するか、またはそれらを有するリスクがある。
しまたはC3沈着の蓄積を阻害する方法が、修飾オリゴヌクレオチドと共役基とを含むかまたはそれらからなる化合物を前記対象に投与することを含み、前記修飾オリゴヌクレオチドは、配列番号198、228、237、440、444、448、450、453、455、549、及び598のいずれか一つを含む核酸塩基配列を有する10~30個の連結されたヌクレオシドからなる。特定の実施形態では、補体代替経路の調節異常に関連する疾患を有するかまたは前記疾患を有するリスクがある対象の腎臓におけるC3沈着を低減しまたはC3沈着の蓄積を阻害する方法が、ISIS696844、ISIS696845、ISIS698969、もしくはISIS698970を含むかまたはそれからなる化合物を前記対象に投与することを含む。特定の態様では、前記対象が、ループス腎炎、全身性エリテマトーデス(SLE)、デンスデポジット病(DDD)、C3糸球体腎炎(C3GN)、CFHR5ネフロパシー、もしくは非典型溶血性尿毒症症候群(aHUS)、またはそれらの任意の組み合わせを有するか、またはそれらを有するリスクがある。特定の態様において、前記化合物または組成物が前記対象に非経口投与される。
オリゴマー化合物には、オリゴヌクレオチド、オリゴヌクレオシド、オリゴヌクレオチド類似体、オリゴヌクレオチド模倣物、アンチセンス化合物、アンチセンスオリゴヌクレオチド、及びsiRNAが含まれるが、これらに限定されない。オリゴマー化合物は、標的核酸に対して「アンチセンス」である(つまり、水素結合によって標的核酸にハイブリダイゼーションを起こす能力を有する)ことができる。
列を有する。
特定の実施形態では、アンチセンス化合物が、強化された阻害活性、標的核酸に対する増加した結合アフィニティ、またはインビボヌクレアーゼによる分解に対する耐性などといった性質が前記アンチセンス化合物に付与されるようなパターンまたはモチーフで配置された化学修飾サブユニットを有する。
のハイブリダイゼーションが関与し、そのハイブリダイゼーションが最終的に生物学的活性をもたらす機序であれば、どの機序に起因するものであってもよい。特定の実施形態では、標的核酸の量及び/または活性が調節される。特定の実施形態では、標的核酸の量及び/または活性が低減する。特定の実施形態では、標的核酸へのアンチセンス化合物のハイブリダイゼーションが、最終的に、標的核酸分解をもたらす。特定の実施形態では、標的核酸へのアンチセンス化合物のハイブリダイゼーションが、標的核酸分解をもたらさない。特定のそのような実施形態では、標的核酸とハイブリダイズしたアンチセンス化合物の存在(占有)が、アンチセンス活性の調節をもたらす。特定の実施形態では、ある特定の化学モチーフまたは化学修飾のパターンを有するアンチセンス化合物が、1つ以上の機序を活用するのに、特に適している。特定の実施形態では、2つ以上の機序によって、かつ/またはまだ解明されていない機序によって、アンチセンス化合物が機能する。したがって、本明細書に記載するアンチセンス化合物は、ある特定の機序に限定されるものではない。
特定の実施形態では、アンチセンス活性が、少なくとも部分的には、RNase Hによる標的RNAの分解に起因する。RNase Hは、RNA:DNA二重鎖のRNA鎖を切断する細胞エンドヌクレアーゼである。「DNA様」の一本鎖アンチセンス化合物は哺乳動物細胞においてRNase H活性を引き出すことが、当技術分野では知られている。したがって、DNAヌクレオシドまたはDNA様ヌクレオシドの少なくとも一部分を含むアンチセンス化合物は、RNase Hを活性化して、標的核酸の切断をもたらしうる。特定の実施形態では、RNase Hを利用するアンチセンス化合物が、1つ以上の修飾ヌクレオシドを含む。特定の実施形態では、そのようなアンチセンス化合物が、1~8個の修飾ヌクレオシドのブロックを少なくとも1つは含む。特定のそのような実施形態では、前記修飾ヌクレオシドがRNase H活性を支持しない。特定の実施形態では、そのようなアンチセンス化合物が、本明細書に記載するギャップマーである。特定のそのような実施形態では、前記ギャップマーのギャップがDNAヌクレオシドを含む。特定のそのような実施形態では、前記ギャップマーのギャップがDNA様ヌクレオシドを含む。特定のそのような実施形態では、前記ギャップマーのギャップがDNAヌクレオシドとDNA様ヌクレオシドを含む。
2’-MOEや、拘束エチルまたはLNAなどの二環式糖部分を含む。特定の実施形態では、ウイングがいくつかの修飾糖部分と無修飾糖部分を含む。特定の実施形態では、ウイングが、2’-MOEヌクレオシド、拘束エチルヌクレオシドやLNAヌクレオシドなどの二環式糖部分、及び2’-デオキシヌクレオシドのさまざまな組み合わせを含みうる。
式中、
各Aは独立して2’置換ヌクレオシドであり、
各Bは独立して二環式ヌクレオシドであり、
各Jは独立して2’-置換ヌクレオシドまたは2’-デオキシヌクレオシドであり、
各Dは2’-デオキシヌクレオシドであり、
mは0~4であり、nは0~2であり、pは0~2であり、rは0~2であり、tは0~2であり、vは0~2であり、wは0~4であり、xは0~2であり、yは0~2であり、zは0~4であり、gは6~14である;
ただし、
m、n、及びrのうちの少なくとも1つは0ではなく、
w及びyのうちの少なくとも1つは0ではなく、
m、n、p、r、及びtの和は2~5であり、かつ
v、w、x、y、及びzの和は2~5であるものとする。
特定の実施形態では、アンチセンス化合物が干渉RNA化合物(RNAi)であり、これには、二本鎖RNA化合物(短鎖干渉RNAまたはsiRNAともいう)と一本鎖RNAi化合物(すなわちssRNA)が含まれる。そのような化合物は、少なくとも部分的には、RISC経路によって作動して、標的核酸を分解しかつ/または隔離する(したがってマイクロRNA/マイクロRNA模倣化合物を含む)。特定の実施形態では、アンチセンス化合物が、それらをそのような機序に特に適したものにする修飾を含む。
特定の実施形態において、アンチセンス化合物(一本鎖RNAi化合物(ssRNA)としての使用に特に適したものを含む)は、修飾5’末端を含む。特定のそのような実施形態では、前記5’末端が修飾ホスフェート部分を含む。特定の実施形態では、そのような修飾ホスフェートが安定化されている(例えば無修飾5’-ホスフェートと比較して分解/切断に対して耐性である)。特定の実施形態では、そのような5’末端ヌクレオシドが5’-リン部分を安定化する。当技術分野では、いくつかの修飾5’末端ヌクレオシドを、例えばWO/2011/139702などに見いだすことができる。
Q1及びQ2は、それぞれ独立して、H、ハロゲン、C1-C6アルキル、置換C1-C6アルキル、C1-C6アルコキシ、置換C1-C6アルコキシ、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニル、置換C2-C6アルキニルまたはN(R3)(R4)であり、
Q3は、O、S、N(R5)またはC(R6)(R7)であり、
各R3、R4、R5、R6及びR7は、独立して、H、C1-C6アルキル、置換C1-C6アルキルまたはC1-C6アルコキシであり、
M3は、O、S、NR14、C(R15)(R16)、C(R15)(R16)C(R17)(R18)、C(R15)=C(R17)、OC(R15)(R16)またはOC(R15)(Bx2)であり、
R14は、H、C1-C6アルキル、置換C1-C6アルキル、C1-C6アルコキシ、置換C1-C6アルコキシ、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニルまたは置換C2-C6アルキニルであり、
R15、R16、R17及びR18は、それぞれ独立して、H、ハロゲン、C1-C6アルキル、置換C1-C6アルキル、C1-C6アルコキシ、置換C1-C6アルコキシ、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニルまたは置換C2-C6アルキニルであり、
Bx1は複素環式塩基部分であるか;または
Bx2が存在する場合には、Bx2が複素環式塩基部分であり、かつBx1がH、ハロゲン、C1-C6アルキル、置換C1-C6アルキル、C1-C6アルコキシ、置換C1
-C6アルコキシ、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニルまたは置換C2-C6アルキニルであり、
J4、J5、J6及びJ7は、それぞれ独立して、H、ハロゲン、C1-C6アルキル、置換C1-C6アルキル、C1-C6アルコキシ、置換C1-C6アルコキシ、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニルまたは置換C2-C6アルキニルであるか;または
J4が、J5またはJ7の一方と共に、O、S、NR19、C(R20)(R21)、C(R20)=C(R21)、C[=C(R20)(R21)]及びC(=O)から選択される1~3個の連結されたビラジカル基を含む橋を形成し、かつJ5、J6及びJ7の残り2つが、それぞれ独立して、H、ハロゲン、C1-C6アルキル、置換C1-C6アルキル、C1-C6アルコキシ、置換C1-C6アルコキシ、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニルまたは置換C2-C6アルキニルであり、
各R19、R20及びR21は、独立して、H、C1-C6アルキル、置換C1-C6アルキル、C1-C6アルコキシ、置換C1-C6アルコキシ、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニルまたは置換C2-C6アルキニルであり、
Gは、H、OH、ハロゲンまたはO-[C(R8)(R9)]n-[(C=O)m-X1]j-Zであり、
各R8及びR9は、独立して、H、ハロゲン、C1-C6アルキルまたは置換C1-C6アルキルであり、
X1は、O、SまたはN(E1)であり、
Zは、H、ハロゲン、C1-C6アルキル、置換C1-C6アルキル、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニル、置換C2-C6アルキニルまたはN(E2)(E3)であり、
E1、E2及びE3は、それぞれ独立して、H、C1-C6アルキルまたは置換C1-C6アルキルであり、
nは、1~約6であり、
mは、0または1であり、
jは、0または1であり、
各置換基は、ハロゲン、OJ1、N(J1)(J2)、=NJ1、SJ1、N3、CN、OC(=X2)J1、OC(=X2)N(J1)(J2)及びC(=X2)N(J1)(J2)から独立して選択される1つ以上の置換されていてもよい置換基を含み、
X2は、O、SまたはNJ3であり、
各J1、J2及びJ3は、独立して、HまたはC1-C6アルキルであり、
jが1である場合、ZはハロゲンでもN(E2)(E3)でもなく、かつ
前記オリゴマー化合物は8~40個のモノマー型サブユニットを含み、標的核酸の少なくとも一部分にハイブリダイズ可能である。
式中、
Q1及びQ2は、それぞれ独立して、H、ハロゲン、C1-C6アルキル、置換C1-C6アルキル、C1-C6アルコキシまたは置換C1-C6アルコキシである。特定の実施形態では、Q1及びQ2が、それぞれHである。特定の実施形態では、Q1及びQ2が、それぞれ独立して、Hまたはハロゲンである。特定の実施形態では、Q1及びQ2がHであり、Q1及びQ2の他方がF、CH3またはOCH3である。
を有し、
式中、
Ra及びRcは、それぞれ独立して、保護ヒドロキシル、保護チオール、C1-C6アルキル、置換C1-C6アルキル、C1-C6アルコキシ、置換C1-C6アルコキシ、保護アミノまたは置換アミノであり、かつ
Rbは、OまたはSである。特定の実施形態では、RbがOであり、Ra及びRcが、それぞれ独立して、OCH3、OCH2CH3またはCH(CH3)2である。
AABBAA、
ABBABB、
AABAAB、
ABBABAABB、
ABABAA、
AABABAB、
ABABAA、
ABBAABBABABAA、
BABBAABBABABAA、または
ABABBAABBABABAA
[式中、Aは第1タイプのヌクレオシドであり、Bは第2タイプのヌクレオシドである]。特定の実施形態では、A及びBは、それぞれ2’-F、2’-OMe、BNA、及びMOEから選択される。
-(A)2-(B)x-(A)2-(C)y-(A)3-
式中、Aは第1タイプの修飾ヌクレオシドであり、
B及びCは、Aとは異なる修飾がなされたヌクレオシドであるが、BとCとは互いに同じ修飾を有しても異なる修飾を有してもよく、
x及びyは1~15である。
5’-(Q)-(AB)xAy-(D)z
式中、
Qは、安定化されたホスフェート部分を含むヌクレオシドであり(特定の実施形態では、Qが、式IIcまたは式IIeを有するヌクレオシドである)、
Aは、第1タイプの修飾ヌクレオシドであり、
Bは、第2タイプの修飾ヌクレオシドであり、
Dは、Dと隣り合うヌクレオシドとは異なる修飾を含む修飾ヌクレオシドであり(したがって、もしyが0であれば、Dには、Bとは異なる修飾がなされていなければならず、yが1であれば、Dには、Aとは異なる修飾がなされていなくてはならない。特定の実施形態では、Dが、AともBとも異なる)、
Xは5~15であり、
Yは0または1であり、
Zは0~4である。
5’-(Q)-(A)x-(D)z
式中、
Qは、安定化されたホスフェート部分を含むヌクレオシドであり(特定の実施形態では、Qが式IIcまたは式IIeを有するヌクレオシドである)、
Aは、第1タイプの修飾ヌクレオシドであり、
Dは、Aとは異なる修飾を含む修飾ヌクレオシドであり、
Xは11~30であり、
Zは0~4である。
ヌクレオシドを表す。特定の実施形態では、そのような末端ヌクレオシドが、標的核酸にハイブリダイズするようには設計されていない(ただし偶然ハイブリダイズするものは多少あるかもしれない)。特定の実施形態では、各Dヌクレオシドの核酸塩基が、標的核酸の対応する位置にある核酸塩基の実体には関わりなく、アデニンである。特定の実施形態では、各Dヌクレオシドの核酸塩基がチミンである。
特定の実施形態では、アンチセンス化合物が二本鎖RNAi化合物(siRNA)である。そのような実施形態では、一方の鎖または両方の鎖が、ssRNAについて上述した任意の修飾モチーフを含みうる。特定の実施形態において、ssRNA化合物は無修飾RNAでありうる。特定の実施形態において、siRNA化合物は無修飾RNAヌクレオシドと修飾ヌクレオシド間連結部とを含みうる。
ヌクレオチド配列を含む(例えば、二本鎖オリゴヌクレオチド分子のうちの約15~約25ヌクレオチドまたはそれ以上が、標的核酸またはその一部分に相補的である)。あるいは、前記二本鎖オリゴヌクレオチドは単一のオリゴヌクレオチドから組み立てられ、この場合、siRNAの自己相補的なセンス領域及びアンチセンス領域は、核酸系リンカーまたは非核酸系リンカーを利用して連結されている。
よる遺伝子発現のエピジェネティックな調整は、遺伝子発現を改変するためのクロマチン構造またはメチル化パターンのsiRNA媒介修飾に起因しうる(例えばVerdel et al.,2004,Science,303,672-676;Pal-Bhadra et al.,2004,Science,303,669-672;Allshire,2002,Science,297,1818-1819;Volpe et al.,2002,Science,297,1833-1837;Jenuwein,2002,Science,297,2215-2218;及びHall et al.,2002,Science,297,2232-2237を参照されたい)。
を含有する単一の環状核酸であるか、またはdsRNAが、環状核酸と第二の環状核酸または線状核酸とを含む(例えば2000年4月19日に出願されたWO00/63364または1999年4月21日に出願された米国出願第60/130,377号を参照されたい)。例示的環状核酸として、ヌクレオチドの遊離5’ホスホリル基がもう一つのヌクレオチドの2’ヒドロキシル基に輪を描いて元に戻るように連結された状態になる、投げ縄(lariat)構造が挙げられる。
特定の実施形態では、アンチセンス化合物が、RNase Hによる標的核酸の切断をもたらすとも、RISC経路による切断または隔離をもたらすとも予想されない。特定のそのような実施形態では、アンチセンス活性が占有に起因しうる。この場合は、ハイブリダイズしたアンチセンス化合物の存在が、標的核酸の活性を妨害する。特定のそのような実施形態では、アンチセンス化合物が、一様に修飾されていてもよいし、修飾物が混在し、かつ/または修飾ヌクレオシドと無修飾ヌクレオシドとが混在していてもよい。
補体B因子(CFB)をコードするヌクレオチド配列には、次に挙げるものがあるが、これらに限定されない:GENBANKアクセッション番号NM_001710.5(本明細書には配列番号1として組み込まれる)、ヌクレオチド31852000~31861000が切り出されたGENBANKアクセッション番号NT_007592.15(本明細書には配列番号2として組み込まれる)、ヌクレオチド536000~545000が切り出されたGENBANKアクセッション番号NW_001116486.1(本明細書には配列番号3として組み込まれる)、GENBANKアクセッション番号XM_001113553.2(本明細書には配列番号4として組み込まれる)、またはGENBANKアクセッション番号NM_008198.2(本明細書には配列番号5として組み込まれる)。
いくつかの実施形態では、本明細書に開示するアンチセンス化合物とCFB核酸との間
でハイブリダイゼーションが起こる。最もよくあるハイブリダイゼーションの機序は、核酸分子の相補的核酸塩基間での水素結合形成(例えばワトソン-クリック型、フーグスティーン型または逆フーグスティーン型水素結合形成)を必要とする。
アンチセンス化合物の十分な数の核酸塩基が、所望の効果(例えばCFB核酸などの標的核酸のアンチセンス阻害)が生じるような形で、標的核酸の対応する核酸塩基と水素結合することができるのであれば、そのアンチセンス化合物と標的核酸とは互いに相補的である。
410;Zhang and Madden,Genome Res.,1997,7,649 656)を使って、ルーチンに決定することができる。相同性パーセント、配列同一性パーセントまたは配列相補性パーセントは、例えばSmithとWatermanのアルゴリズム(Adv.Appl.Math.,1981,2,482 489)を使用するGapプログラム(Wisconsin Sequence Analysis
Package,Version 8 for Unix,Genetics Com
puter Group,ウィスコンシン州マディソン、ユニバーシティ・リサーチ・パーク)により、デフォルト設定を使って決定することができる。
実施形態では、アンチセンス化合物が、ある標的セグメントの少なくとも13核酸塩基部分に相補的である。特定の実施形態では、アンチセンス化合物が、ある標的セグメントの少なくとも14核酸塩基部分に相補的である。特定の実施形態では、アンチセンス化合物が、ある標的セグメントの少なくとも15核酸塩基部分に相補的である。ある標的セグメントの少なくとも9、10、11、12、13、14、15、16、17、18、19、20核酸塩基部分もしくはそれ以上の核酸塩基部分、またはこれらの値のうちの任意の2つによって画定される範囲に相補的な、アンチセンス化合物も考えられる。
ここに提供するアンチセンス化合物は、ある特定ヌクレオチド配列、配列番号、もしくは具体的Isis番号によって表される化合物、またはその一部分に対して、所定の同一性パーセントも有しうる。本明細書にいうアンチセンス化合物は、それが同じ核酸塩基対合能を有するのであれば、本明細書に開示する配列と同一である。例えば、ウラシルとチミジンはどちらもアデニンと対合するので、開示したDNA配列中のチミジンの代わりにウラシルを含有するRNAは、前記DNA配列と同一であるとみなされるであろう。本明細書に記載するアンチセンス化合物の短縮型及び延長型、ならびにここに提供するアンチセンス化合物と比較して非同一塩基を有する化合物も考えられる。非同一塩基は互いに隣り合っていてもよいし、アンチセンス化合物全体に散在していてもよい。アンチセンス化合物のパーセント同一性は、比較対象である配列との比較で同一塩基対合を有する塩基の数に従って計算される。
ヌクレオシドは塩基-糖の組み合わせである。ヌクレオシドの核酸塩基(塩基ともいう)部分は、通常、複素環式塩基部分である。ヌクレオチドは、ヌクレオシドの糖部分に共有結合で連結されたリン酸基をさらに含むヌクレオシドである。ペントフラノシル糖を含むヌクレオシドの場合は、リン酸基を、糖の2’、3’または5’ヒドロキシル部分に連結することができる。オリゴヌクレオチドは、互いに隣り合うヌクレオシドを共有結合で連結して、線状ポリマー状のオリゴヌクレオチドを形成させることによって形成される。オリゴヌクレオチド構造内では、リン酸基は、オリゴヌクレオチドのヌクレオシド間連結部を形成していると、一般に言われる。
多い。
RNA及びDNAの天然に存在するヌクレオシド間連結部は、3’→5’ホスホジエステル連結部である。1つ以上の修飾(すなわち天然に存在しない)ヌクレオシド間連結部を有するアンチセンス化合物は、例えば強化された細胞取り込み、核酸標的に対する強化されたアフィニティ、及びヌクレアーゼの存在下での増加した安定性などといった望ましい性質ゆえに、天然に存在するヌクレオシド間連結部を有するアンチセンス化合物よりも選択されることが多い。
クレオシド間連結部を含む。特定の実施形態では、オリゴヌクレオチドが少なくとも8つのホスホロチオエートヌクレオシド間連結部を含む。特定の実施形態では、オリゴヌクレオチドが少なくとも10個のホスホロチオエートヌクレオシド間連結部を含む。特定の実施形態では、オリゴヌクレオチドが少なくとも6つの連続するホスホロチオエートヌクレオシド間連結部のブロックを少なくとも1つは含む。特定の実施形態では、オリゴヌクレオチドが少なくとも8つの連続するホスホロチオエートヌクレオシド間連結部のブロックを少なくとも1つは含む。特定の実施形態では、オリゴヌクレオチドが少なくとも10個の連続するホスホロチオエートヌクレオシド間連結部のブロックを少なくとも1つは含む。特定の実施形態では、オリゴヌクレオチドが少なくとも12個の連続するホスホロチオエートヌクレオシド間連結部のブロックを少なくとも1つは含む。特定のそのような実施形態では、少なくとも1つの上述のブロックが、オリゴヌクレオチドの3’端に位置する。特定のそのような実施形態では、少なくとも1つの上述のブロックがオリゴヌクレオチドの3’端から3ヌクレオシド以内に位置する。
アンチセンス化合物は、場合によっては、糖基が修飾されているヌクレオシドを1つ以上含有しうる。そのような糖修飾ヌクレオシドは、強化されたヌクレアーゼ安定性、増加した結合アフィニティ、または他の何らかの有益な生物学的性質を、アンチセンス化合物に付与しうる。特定の実施形態では、ヌクレオシドが化学修飾リボフラノース環部分を含む。化学修飾リボフラノース環の例には、置換基の付加(5’置換基、2’置換基、非ジェミナル環原子の架橋による二環式核酸(BNA)の形成、S、N(R)、またはC(R1)(R2)(R、R1及びR2は、それぞれ独立して、H、C1-C12アルキルまたは保護基である)によるリボシル環酸素原子の置き換え、及びそれらの組み合わせなどがあるが、これらに限定されない。化学修飾糖の例としては、2’-F-5’-メチル置換ヌクレオシド(開示されている他の5’,2’-ビス置換ヌクレオシドについては、PCT国際出願WO2008/101157(公開日2008年8月21日)を参照されたい)、またはSによるリボシル環酸素原子の置き換えと2’位におけるさらなる置換(米国特許出願公開US2005-0130923(公開日2005年6月16日)参照)、あるいはBNAの5’-置換(PCT国際出願WO2007/134181(公開日2007年11月22日)参照、この場合はLNAが例えば5’-メチル基または5’-ビニル
基で置換されている)などがある。
WO2009/067647;同WO2011/017521;同WO2010/036698;同WO1999/014226;同WO2004/106356;同WO2005/021570;同WO2007/134181;同WO2008/150729;同WO2008/154401;及び同WO2009/006478参照。前述の二環式ヌクレオシドのそれぞれは、例えばα-L-リボフラノースとβ-D-リボフラノースなど、1つ以上の立体化学的糖配置を有するものを調製することができる(1999年3月25日にWO99/14226として公開されたPCT国際出願PCT/DK98/00393を参照されたい)。
式中、
xは、0、1、または2であり、
nは、1、2、3、または4であり、
各Ra及びRbは、独立して、H、保護基、ヒドロキシル、C1-C12アルキル、置換C1-C12アルキル、C2-C12アルケニル、置換C2-C12アルケニル、C2-C12アルキニル、置換C2-C12アルキニル、C5-C20アリール、置換C5-C20アリール、複素環ラジカル、置換複素環ラジカル、ヘテロアリール、置換ヘテロアリール、C5-C7脂環式ラジカル、置換C5-C7脂環式ラジカル、ハロゲン、OJ1、NJ1J2、SJ1、N3、COOJ1、アシル(C(=O)-H)、置換アシル、CN、スルホニル(S(=O)2-J1)、またはスルホキシル(S(=O)-J1)であり、かつ
各J1及びJ2は、独立して、H、C1-C12アルキル、置換C1-C12アルキル、C2-C12アルケニル、置換C2-C12アルケニル、C2-C12アルキニル、置換C2-C12アルキニル、C5-C20アリール、置換C5-C20アリール、アシル(C(=O)-H)、置換アシル、複素環ラジカル、置換複素環ラジカル、C1-C12アミノアルキル、置換C1-C12アミノアルキルまたは保護基である。
NA、(D)アミノオキシ(4’-CH2-O-N(R)-2’)BNA、(E)オキシアミノ(4’-CH2-N(R)-O-2’)BNA、及び(F)メチル(メチレンオキシ)(4’-CH(CH3)-O-2’)BNA、(G)メチレン-チオ(4’-CH2-S-2’)BNA、(H)メチレン-アミノ(4’-CH2-N(R)-2’)BNA、(I)メチル炭素環式(4’-CH2-CH(CH3)-2’)BNA、(J)プロピレン炭素環式(4’-(CH2)3-2’)BNA、及び(K)ビニルBNAが挙げられるが、これらに限定されない:
[式中、
Bxは、複素環式塩基部分であり、
-Qa-Qb-Qc-は、-CH2-N(Rc)-CH2-、-C(=O)-N(Rc)-CH2-、-CH2-O-N(Rc)-、-CH2-N(Rc)-O-または-N(Rc)-O-CH2であり、
Rcは、C1-C12アルキルまたはアミノ保護基であり、かつ
Ta及びTbは、それぞれ独立して、H、ヒドロキシル保護基、共役基、反応性リン基、リン部分または支持媒体への共有結合による取り付けである]
を有する二環式ヌクレオシドが提供される。
[式中、
Bxは、複素環式塩基部分であり、
Ta及びTbは、それぞれ独立して、H、ヒドロキシル保護基、共役基、反応性リン基、リン部分または支持媒体への共有結合による取り付けであり、
Zaは、C1-C6アルキル、C2-C6アルケニル、C2-C6アルキニル、置換C1-C6アルキル、置換C2-C6アルケニル、置換C2-C6アルキニル、アシル、置換アシル、置換アミド、チオールまたは置換チオである]
を有する二環式ヌクレオシドが提供される。
[式中、
Bxは、複素環式塩基部分であり、
Ta及びTbは、それぞれ独立して、H、ヒドロキシル保護基、共役基、反応性リン基、リン部分または支持媒体への共有結合による取り付けであり、
Zbは、C1-C6アルキル、C2-C6アルケニル、C2-C6アルキニル、置換C1-C6アルキル、置換C2-C6アルケニル、置換C2-C6アルキニルまたは置換アシル(C(=O)-)である]
を有する二環式ヌクレオシドが提供される。
[式中、
Bxは、複素環式塩基部分であり、
Ta及びTbは、それぞれ独立して、H、ヒドロキシル保護基、共役基、反応性リン基、リン部分または支持媒体への共有結合による取り付けであり、
Rdは、C1-C6アルキル、置換C1-C6アルキル、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニルまたは置換C2-C6アルキニルであり、
各qa、qb、qc及びqdは、独立して、H、ハロゲン、C1-C6アルキル、置換C1-C6アルキル、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニルまたは置換C2-C6アルキニル、C1-C6アルコキシル、置換C1-C6アルコキシル、アシル、置換アシル、C1-C6アミノアルキルまたは置換C1-C6アミノアルキルである]
を有する二環式ヌクレオシドが提供される。
[式中、
Bxは、複素環式塩基部分であり、
Ta及びTbは、それぞれ独立して、H、ヒドロキシル保護基、共役基、反応性リン基、リン部分または支持媒体への共有結合による取り付けであり、
qa、qb、qe及びqfは、それぞれ独立して、水素、ハロゲン、C1-C12アルキル、置換C1-C12アルキル、C2-C12アルケニル、置換C2-C12アルケニル、C2-C12アルキニル、置換C2-C12アルキニル、C1-C12アルコキシ、置換C1-C12アルコキシ、OJj、SJj、SOJj、SO2Jj、NJjJk、N3、CN、C(=O)OJj、C(=O)NJjJk、C(=O)Jj、O-C(=O)-NJjJk、N(H)C(=NH)NJjJk、N(H)C(=O)-NJjJkまたはN(H)C(=S)NJjJkであるか、または
qe及びqfが全体として=C(qg)(qh)であり、
qg及びqhは、それぞれ独立して、H、ハロゲン、C1-C12アルキルまたは置換C1-C12アルキルである]
を有する二環式ヌクレオシドが提供される。
’-アミノ-BNAの合成も、当技術分野では既に記述されている(Singh et al.,J.Org.Chem.,1998,63,10035-10039)。加えて、2’-アミノ-及び2’-メチルアミノ-BNAも調製されており、相補的なRNA鎖及び相補的DNA鎖とのそれらの二重鎖の熱安定性が、以前に報告されている。
[式中、
Bxは、複素環式塩基部分であり、
Ta及びTbは、それぞれ独立して、H、ヒドロキシル保護基、共役基、反応性リン基、リン部分または支持媒体への共有結合による取り付けであり、
各qi、qj、qk及びqlは、独立して、H、ハロゲン、C1-C12アルキル、置換C1-C12アルキル、C2-C12アルケニル、置換C2-C12アルケニル、C2-C12アルキニル、置換C2-C12アルキニル、C1-C12アルコキシル、置換C1-C12アルコキシル、OJj、SJj、SOJj、SO2Jj、NJjJk、N3、CN、C(=O)OJj、C(=O)NJjJk、C(=O)Jj、O-C(=O)-NJjJk、N(H)C(=NH)NJjJk、N(H)C(=O)-NJjJkまたはN(H)C(=S)NJjJkであり、かつ
qiとqjまたはqlとqkは、全体として、=C(qg)(qh)であり、式中、qg及びqhは、それぞれ独立して、H、ハロゲン、C1-C12アルキルまたは置換C1-C12アルキルである]
を有する二環式ヌクレオシドが提供される。
、置換及び無置換アルキル、置換及び無置換アリル、及び置換及び無置換アルキニルから選択される置換基を含む。特定の実施形態では、2’修飾が、限定するわけではないが、O[(CH2)nO]mCH3、O(CH2)nNH2、O(CH2)nCH3、O(CH2)nF、O(CH2)nONH2、OCH2C(=O)N(H)CH3、及びO(CH2)nON[(CH2)nCH3]2などといった置換基(式中、n及びmは1~約10である)から選択される。他の2’-置換基は、C1-C12アルキル、置換アルキル、アルケニル、アルキニル、アルカリール、アラルキル、O-アルカリールまたはO-アラルキル、SH、SCH3、OCN、Cl、Br、CN、F、CF3、OCF3、SOCH3、SO2CH3、ONO2、NO2、N3、NH2、ヘテロシクロアルキル、ヘテロシクロアルカリール、アミノアルキルアミノ、ポリ-アルキルアミノ、置換シリル、RNA切断基、レポーター基、インターカレーター、アンチセンス化合物の薬物動態特性を改良するための基または薬力学的性質を改良するための基、及び類似する性質を有する他の置換基から選択することもできる。特定の実施形態では、修飾ヌクレオシドが2’-MOE側鎖を含む(Baker et al.,J.Biol.Chem.,1997,272,11944-12000)。そのような2’-MOE置換は、無修飾ヌクレオシド及び他の修飾ヌクレオシド、例えば2’-O-メチル、O-プロピル、及びO-アミノプロピルと比較して、改良された結合アフィニティを有すると記述されている。2’-MOE置換基を有するオリゴヌクレオチドは、インビボ用途に有望な特徴を持つ遺伝子発現のアンチセンス阻害剤であることも示されている(Martin,Helv.Chim.Acta,1995,78,486-504;Altmann et al.,Chimia,1996,50,168-176;Altmann et al.,Biochem.Soc.Trans.,1996,24,630-637;及びAltmann et al.,Nucleosides Nucleotides,1997,16,917-926)。
式中、前記少なくとも1つの式VIIのテトラヒドロピランヌクレオシド類似体のそれぞれについて、独立して、
Bxは、複素環式塩基部分であり、
Ta及びTbは、それぞれ独立して、テトラヒドロピランヌクレオシド類似体をアンチセンス化合物に連結するヌクレオシド間連結基であるか、またはTa及びTbのうちの一方がテトラヒドロピランヌクレオシド類似体をアンチセンス化合物に連結するヌクレオシド間連結基であり、Ta及びTbのうちの他方がH、ヒドロキシル保護基、連結された共役基または5’もしくは3’末端基であり、
q1、q2、q3、q4、q5、q6及びq7は、それぞれ独立して、H、C1-C6アルキル、置換C1-C6アルキル、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニルまたは置換C2-C6アルキニルであり、かつR1及びR2のそれぞれは、水素、ヒドロキシル、ハロゲン、置換または無置換アルコキシ、NJ1J2、SJ1、N3、OC(=X)J1、OC(=X)NJ1J2、NJ3C(=X)NJ1J2及びCNであり、XはO、SまたはNJ1であり、かつ各J1、J2及びJ3は、独立して、HまたはC1-C6アルキルである。
。特定の実施形態では、例えば上記モルホリノ構造にさまざまな置換基を付加するか、上記モルホリノ構造のさまざまな置換基を改変することによって、モルホリノが修飾されていてもよい。そのような糖代用物を本明細書では「修飾モルホリノ」という。
メチル基または5’-ビニル基でさらに置換されている)なども提供される。炭素環式二環式ヌクレオシドの合成及び調製も、それらのオリゴマー化及び生化学的試験と共に記載されている(例えば、Srivastava et al.,J.Am.Chem.Soc.2007,129(26),8362-8379を参照のこと)。
式中、前記少なくとも1つの式Xのシクロヘキセニルヌクレオシド類似体のそれぞれについて、独立して、
Bxは、複素環式塩基部分であり、
T3及びT4は、それぞれ独立して、シクロヘキセニルヌクレオシド類似体をアンチセンス化合物に連結するヌクレオシド間連結基であるか、またはT3及びT4のうちの一方がテトラヒドロピランヌクレオシド類似体をアンチセンス化合物に連結するヌクレオシド間連結基であり、かつT3及びT4のうちの他方がH、ヒドロキシル保護基、連結された共役基、または5’末端基もしくは3’末端基であり、かつ
q1、q2、q3、q4、q5、q6、q7、q8及びq9は、それぞれ独立して、H
、C1-C6アルキル、置換C1-C6アルキル、C2-C6アルケニル、置換C2-C6アルケニル、C2-C6アルキニル、置換C2-C6アルキニルまたは他の糖置換基である。
などがあり、これらはそれぞれ参照により本明細書にそのまま組み込まれる。
組み合わせ)は、適当な核酸標的とのハイブリダイゼーションのために維持される。
核酸塩基(または塩基)の修飾または置換は、天然に存在する無修飾核酸塩基または合成無修飾核酸塩基とは構造上識別できるが、機能的には天然に存在する無修飾核酸塩基または合成無修飾核酸塩基と交換可能である。天然核酸塩基と修飾核酸塩基はどちらも水素結合に参加する能力を有する。そのような核酸塩基修飾は、ヌクレアーゼ安定性、結合アフィニティまたは他の何らかの有益な生物学的性質をアンチセンス化合物に付与することができる。修飾核酸塩基には、例えば5-メチルシトシン(5-me-C)などの合成及び天然核酸塩基が含まれる。5-メチルシトシン置換などの特定の核酸塩基置換は、標的核酸に対するアンチセンス化合物の結合アフィニティを増加させるのに特に有用である。例えば5-メチルシトシン置換は、核酸二重鎖安定性を0.6~1.2℃増加させることが示されている(Sanghvi,Y.S.、Crooke,S.T.及びLebleu,B.編「Antisense Research and Applications」CRC Press,ボカラトン,1993,pp.276-278)。
キニル誘導体、6-アゾウラシル、シトシン及びチミン、5-ウラシル(シュードウラシル)、4-チオウラシル、8-ハロ、8-アミノ、8-チオール、8-チオアルキル、8-ヒドロキシルならびに他の8-置換アデニン及びグアニン、5-ハロ、特に5-ブロモ、5-トリフルオロメチルならびに他の5-置換ウラシル及びシトシン、7-メチルグアニン及び7-メチルアデニン、2-F-アデニン、2-アミノ-アデニン、8-アザグアニン及び8-アザアデニン、7-デアザグアニン及び7-デアザアデニンならびに3-デアザグアニン及び3-デアザアデニンが挙げられる。
特定の実施形態において、本開示は、共役アンチセンス化合物を提供する。特定の実施形態において、本開示は、核酸転写産物に相補的なアンチセンスオリゴヌクレオチドを含む共役アンチセンス化合物を提供する。特定の実施形態において、本開示は、細胞を、核酸転写産物に相補的なアンチセンスオリゴヌクレオチドを含む共役アンチセンス化合物と接触させることを含む方法を提供する。特定の実施形態において、本開示は、細胞を、アンチセンスオリゴヌクレオチドを含む共役アンチセンス化合物と接触させること、及び細胞内の核酸転写産物の量または活性を低減させることを含む方法を提供する。
クレオシドが、ホスホジエステル連結部によってアンチセンスオリゴヌクレオチド(アンチセンス化合物)に取り付けられる。特定の実施形態では、共役基が、2つまたは3つの切断可能なヌクレオシドを含みうる。そのような実施形態では、上述の切断可能なヌクレオシドが、切断可能な結合(ホスホジエステル連結部のもの)によって、互いに、アンチセンス化合物に、かつ/またはクラスターに連結される。本明細書における特定の共役体は、切断可能なヌクレオシドを含まず、代わりに切断可能な結合を含む。オリゴヌクレオチドからの共役体の十分な切離は、細胞内で切断を受けやすい少なくとも1つの結合(切断可能な結合)によってもたらされることを示す。
クレオチドや二本鎖オリゴヌクレオチド(例えばsiRNA)のどちらかの鎖などといった任意のアンチセンス化合物に取り付けることができる。
[式中、
Aは、アンチセンスオリゴヌクレオチドであり、
Bは、切断可能部分であり、
Cは、共役リンカーであり、
Dは、分岐基であり、
各Eは、テザーであり、
各Fは、リガンドであり、かつ
qは、1~5の整数である]
によって表される共役アンチセンス化合物を提供する。
特定の実施形態において、切断可能部分は、切断可能な結合である。特定の実施形態において、切断可能部分は、切断可能な結合を含む。特定の実施形態において、共役基は、切断可能部分を含む。特定のそのような実施形態において、切断可能部分は、アンチセンスオリゴヌクレオチドに結合する。特定のそのような実施形態において、切断可能部分は、細胞ターゲティング部分に直接結合する。特定のそのような実施形態において、切断可能部分は、共役リンカーに結合する。特定の実施形態において、切断可能部分は、ホスフェートまたはホスホジエステルを含む。特定の実施形態において、切断可能部分は、切断可能なヌクレオシドまたはヌクレオシド類似体である。特定の実施形態において、ヌクレオシドまたはヌクレオシド類似体は、プリン、置換プリン、ピリミジン、または置換ピリミジンから選択される場合によっては保護された複素環式塩基を含む。特定の実施形態において、切断可能部分は、ウラシル、チミン、シトシン、4-N-ベンゾイルシトシン、5-メチルシトシン、4-N-ベンゾイル-5-メチルシトシン、アデニン、6-N-ベンゾイルアデニン、グアニン、及び2-N-イソブチリルグアニンから選択される、場合
によっては保護された複素環式塩基を含むヌクレオシドである。特定の実施形態では、切断可能部分が、ホスホジエステル連結部によってアンチセンスオリゴヌクレオチドの3’位に取り付けられ、かつホスホジエステルまたはホスホロチオエート連結部によってリンカーに取り付けられた2’-デオキシヌクレオシドである。特定の実施形態では、切断可能部分が、ホスホジエステル連結部によってアンチセンスオリゴヌクレオチドの3’位に取り付けられ、かつホスホジエステルまたはホスホロチオエート連結部によってリンカーに取り付けられた2’-デオキシアデノシンである。特定の実施形態では、切断可能部分が、ホスホジエステル連結部によってアンチセンスオリゴヌクレオチドの3’位に取り付けられ、かつホスホジエステル連結部によってリンカーに取り付けられた2’-デオキシアデノシンである。
特定の実施形態において、共役基は、リンカーを含む。特定のそのような実施形態において、リンカーは、切断可能部分に共有結合される。特定のそのような実施形態において、リンカーは、アンチセンスオリゴヌクレオチドに共有結合される。特定の実施形態において、リンカーは、細胞ターゲティング部分に共有結合される。特定の実施形態において、リンカーは、固体支持体への共有結合をさらに含む。特定の実施形態において、リンカーは、タンパク質結合部分への共有結合をさらに含む。特定の実施形態において、リンカーは、固体支持体への共有結合をさらに含み、タンパク質結合部分への共有結合もさらに含む。特定の実施形態において、リンカーは、係留される(tethered)リガンドを取り付けるための位置を複数含んでいる。特定の実施形態において、リンカーは、係留されるリガンドを取り付けるための位置を複数含み、分岐基には取り付けられない。特定の実施形態において、リンカーは、1つ以上の切断可能な結合をさらに含む。特定の実施形態において、共役基は、リンカーを含まない。
実施形態では、線状基が足場基に共有結合され、足場基は、切断可能部分、リンカー、タンパク質結合部分、及び固体支持体に共有結合される。特定の実施形態において、前記足場基は1つ以上の切断可能な結合を含む。
特定の実施形態において、共役基は、細胞ターゲティング部分を含む。特定のそのような細胞ターゲティング部分は、アンチセンス化合物の細胞取り込みを増加させる。特定の実施形態において、細胞ターゲティング部分は、分岐基、1つ以上のテザー、及び1つ以上のリガンドを含む。特定の実施形態において、細胞ターゲティング部分は、分岐基、1つ以上のテザー、1つ以上のリガンド、及び1つ以上の切断可能な結合を含む。
1.特定の分岐基
Z1は、C(=O)O-R2であり、
Z2は、H、C1~C6アルキル、または置換C1~C6アルキルであり、
R2は、H、C1~C6アルキルまたは置換C1~C6アルキルであり、
各m1は、独立して、0~20であり、各テザーにつき少なくとも1つのm1は0より大きい。
3.特定のリガンド
式中、Y及びZは、C1~C12置換もしくは無置換アルキル、アルケニル、もしくはアルキニル基、またはエーテル、ケトン、アミド、エステル、カルバメート、アミン、ピペリジン、ホスフェート、ホスホジエステル、ホスホロチオエート、トリアゾール、ピロリジン、ジスルフィド、もしくはチオエーテルを含む基から独立して選択される。
式中、Y及びZは、C1~C12置換もしくは無置換アルキル基、または厳密に1個のエーテルもしくは厳密に2個のエーテル、アミド、アミン、ピペリジン、ホスフェート、ホスホジエステル、またはホスホロチオエートを含む基から独立して選択される。
式中、Yは、C1~C12置換もしくは無置換アルキル、アルケニル、もしくはアルキニル基、またはエーテル、ケトン、アミド、エステル、カルバメート、アミン、ピペリジン、ホスフェート、ホスホジエステル、ホスホロチオエート、トリアゾール、ピロリジン、ジスルフィド、もしくはチオエーテルを含む基から選択される。
a 特定の共役アンチセンス化合物
式中、
Aは、アンチセンスオリゴヌクレオチドであり、
Bは、切断可能部分であり、
Cは、共役リンカーであり、
Dは、分岐基であり、
各Eは、テザーであり、
各Fは、リガンドであり、
qは、1~5の整数である。
a Triantennary Galactoside with High Affinity for the Hepatic Asialoglycoprotein Receptor:a Potent Cholesterol Lowering
Agent」J.Med.Chem.(1995)38:1846-1852、BIESSEN et al.「Synthesis of Cluster Galactoside with High Affinity for the Hepatic Asialoglycoprotein Receptor」J.Med.Chem.(1995)38:1538-1546、LEE et al.「New and more efficient multivalent glyco-ligands for asialoglycoprotein receptor of mammalian hepatocytes」Bioorganic & Medicinal Ch
emistry(2011)19:2494-2500、RENSEN et al.「Determination of the Upper Size Limit for Uptake and Processing of Ligands by the Asialoglycoprotein Receptor on Hepatocytes in Vitro and in Vivo」J.Biol.Chem.(2001)276(40):37577-37584、RENSEN et al.「Design and Synthesis of Novel N-Acetylgalactosamine-Terminated Glycolipids for Targeting of Lipoproteins to the Hepatic Asialoglycoprotein Receptor」J.Med.Chem.(2004)47:5798-5808、SLIEDREGT et al.「Design and Synthesis of Novel Amphiphilic Dendritic Galactosides for Selective Targeting of Liposomes to the Hepatic Asialoglycoprotein Receptor」J.Med.Chem.(1999)42:609-618、及びValentijn et al.「Solid-phase synthesis of lysine-based Cluster galactosides with high affinity for the Asialoglycoprotein Receptor」Tetrahedron,1997,53(2),759-770が含まれるが、これらに限定されず、これらの文献のそれぞれは、参照によりその全体が本明細書に組み込まれる。
、Sliedregt et al.,J Med Chem,1999,42,609-618、Rensen et al.,J Med Chem,2004,47,5798-5808、Rensen et al.,Arterioscler Thromb Vasc Biol,2006,26,169-175、van Rossenberg et al.,Gene Ther,2004,11,457-464、Sato
et al.,J Am Chem Soc,2004,126,14013-14022、Lee et al.,J Org Chem,2012,77,7564-7571、Biessen et al.,FASEB J,2000,14,1784-1792、Rajur et al.,Bioconjug Chem,1997,8,935-940、Duff et al.,Methods Enzymol,2000,313,297-321、Maier et al.,Bioconjug Chem,2003,14,18-29、Jayaprakash et al.,Org Lett,2010,12,5410-5413、Manoharan,Antisense Nucleic Acid Drug Dev,2002,12,103-128、Merwin et al.,Bioconjug Chem,1994,5,612-620、Tomiya et al.,Bioorg Med Chem,2013,21,5275-5281、国際出願WO1998/013381;WO2011/038356;WO1997/046098;WO2008/098788;WO2004/101619;WO2012/037254;WO2011/120053;WO2011/100131;WO2011/163121;WO2012/177947;WO2013/033230;WO2013/075035;WO2012/083185;WO2012/083046;WO2009/082607;WO2009/134487;WO2010/144740;WO2010/148013;WO1997/020563;WO2010/088537;WO2002/043771;WO2010/129709;WO2012/068187;WO2009/126933;WO2004/024757;WO2010/054406;WO2012/089352;WO2012/089602;WO2013/166121;WO2013/165816;米国特許4,751,219;8,552,163;6,908,903;7,262,177;5,994,517;6,300,319;8,106,022;7,491,805;7,491,805;7,582,744;8,137,695;6,383,812;6,525,031;6,660,720;7,723,509;8,541,548;8,344,125;8,313,772;8,349,308;8,450,467;8,501,930;8,158,601;7,262,177;6,906,182;6,620,916;8,435,491;8,404,862;7,851,615;米国特許出願公開US2011/0097264;US2011/0097265;US2013/0004427;US2005/0164235;US2006/0148740;US2008/0281044;US2010/0240730;US2003/0119724;US2006/0183886;US2008/0206869;US2011/0269814;US2009/0286973;US2011/0207799;US2012/0136042;US2012/0165393;US2008/0281041;US2009/0203135;US2012/0035115;US2012/0095075;US2012/0101148;US2012/0128760;US2012/0157509;US2012/0230938;US2013/0109817;US2013/0121954;US2013/0178512;US2013/0236968;US2011/0123520;US2003/0077829;US2008/0108801;及びUS2009/0203132のうちのいずれかにおいて見いだされる任意の共役基を含み、これらの文献のそれぞれは参照によりその全体が組み込まれる。
本明細書には、細胞をアンチセンスオリゴヌクレオチドで処置するための方法を記載する。この方法には、他のアンチセンス化合物による処置のために、適宜変更を加えることができる。
エレクトロポレーションによるトランスフェクションの場合は、それより高い625nMから20,000nMまでの範囲の濃度で、アンチセンスオリゴヌクレオチドが使用される。
RNA分析は、全細胞RNAまたはポリ(A)+mRNAに関して行うことができる。RNA単離の方法は当技術分野ではよく知られている。RNAは当技術分野において周知の方法を使って、例えばTRIZOL試薬(Invitrogen,カリフォルニア州カールズバッド)を製造者が推奨するプロトコルに従って使用することによって、調製される。
ここに提供する特定の実施形態は、対象における補体代替経路の調節異常に関連する疾患を、CFBを標的とするアンチセンス化合物などのCFB特異的阻害剤の投与によって処置し、防止し、または改善する方法に関する。
vige et al.,J Am Soc Nephrol.(2011)22(8):1403-15。腎臓疾患と眼疾患に補体経路が関与することの証拠がある。例えば、遺伝性補体調節タンパク質欠損は、非典型溶血性尿毒症症候群及びAMDに対する素因の原因になる。Richards A et al.,Adv Immunol.(2007)96:141-77。加えて、慢性腎臓疾患はAMDに関連付けられている。Nitsch,D.et al.,Ophthalmic Epidemiol.(2009)16(3):181-6;Choi,J.et al,Ophthalmic Epidemiol.(2011)18(6):259-63。補体代替経路の調節異常に関連する腎臓疾患であるデンスデポジット病(DDD)は、急性腎炎症候群と眼ドルーゼを特徴とする。Cruz and Smith, GeneReviews(2007)Jul
20。さらに、補体代替経路の構成要素の遺伝子欠失を保因するマウスでは、腎疾患表現型と眼疾患表現型が共存する。CFHホモ接合ヌルマウスはDDDを発症し、網膜異常及び視覚機能障害を呈すると報告されている。Pickering et al.,Nat Genet.(2002)31(4):424-8。補体代替経路の調節異常に関連する腎疾患のマウスモデルは、AMDのモデルとしても受け入れられている。Pennesi ME et al.,Mol Aspects Med(2012)33:487-509。例えばCFHヌルマウスはDDDなどの腎疾患とAMDのモデルとして受け入れられている。さらにまた、AMDが補体因子の全身性供給源に関連することも報告されており、これらの補体因子が眼に局所的に蓄積することで代替経路補体活性化を駆動する。Loyet et al.,Invest Ophthalmol Vis Sci.(2012)53(10):6628-37。
化合物3(2-アセトアミド-1,3,4,6-テトラ-O-アセチル-2-デオキシ-β-Dガラクトピラノースまたはガラクトサミンペンタアセテート)は、市販のものである。化合物5を公開された手順(Weber et al.,J.Med.Chem.,1991,34,2692)に従って調製した。
実施例3:化合物11の調製
実施例4:化合物18の調製
実施例5:化合物23の調製
実施例6:化合物24の調製
実施例7:化合物25の調製
実施例8:化合物26の調製
実施例9:3’末端にGalNAc3-1を含む共役ASO(化合物29)の一般的調製
実施例10:5’末端にGalNAc3-1を含む共役ASO(化合物34)の一般的調製
ック(化合物1及び1a)を実施例1に例証される手順どおりに調製した。他のホスホラミダイト構築ブロックを用いて既定の配列及び組成を有するオリゴマー化合物を調製することができるため、例証されるホスホラミダイトは、代表的なものであり、限定する意図はない。固体支持体に添加されるホスホラミダイトの順序及び量を調整して、本明細書に記載するギャップトオリゴマー化合物を調製することができる。そのようなギャップトオリゴマー化合物は、任意の所与の標的によって決まる既定の組成及び塩基配列を有しうる。
実施例11:化合物39の調製
実施例12:化合物40の調製
実施例13:化合物44の調製
実施例14:化合物45の調製
実施例15:化合物47の調製
実施例16:化合物53の調製
実施例17:化合物54の調製
実施例18:化合物55の調製
実施例19:固相技法による3’位にGalNAc3-1を含む共役ASOの調製のための一般的方法(ISIS647535、647536、及び651900の調製)
ボヌクレオシド及び2’-MOEに用いた。
で、ホスホジエステルヌクレオシド間連結部を得た。
実施例20:huApoC IIIトランスジェニックマウスにおけるヒトApoC IIIの用量依存的アンチセンス阻害
IIIトランスジェニックマウスにおけるヒトApoC IIIを阻害するそれらの能力について評価した。
処理
た。注入のためにASOを0.9%PBS中に溶解した。
ApoC III mRNA分析
処理
ホスホロチオエートバージョン(ISIS 647535)を有する。
実施例22:生体内におけるSRB-1を標的とするGalNAc3-1共役修飾ASOの影響
処理
って添加した(合計100μL/ウェル)。プレートを振盪器に設置し、約1分間混合させた。37℃、5%CO2で24時間インキュベートした後、プレートを400×gで10分間遠心分離し、その後、MSDサイトカインアッセイ(すなわち、ヒトIL-6、IL-10、IL-8、及びMCP-1)のために上澄みを除去した。
実施例24:hPBMCアッセイにおけるGalNAc3-1共役ASOの炎症誘発作用の評価
ドで処理した。約16時間の処理期間後、RNAを細胞から単離し、mRNAレベルを定量的リアルタイムPCRで測定し、hApoC III mRNAレベルをRIBOGREENで測定された全RNA含有量に従って調整した。
実施例26:ApoC III ASO活性へのPO/PS連結部の影響
実施例28:化合物60の調製
実施例29:化合物63の調製
実施例30:化合物63bの調製
実施例31:化合物63dの調製
実施例32:化合物67の調製
al.の公開されたPCT国際出願第WO2009003009号によって報告された手順と同様の手順を用いて調製する。他の保護基、例えば限定するわけではないが、本明細書に提示されるものを用いることができるため、化合物65に用いた保護基は、代表的なものであり、限定する意図はない。
実施例33:化合物70の調製
実施例34:化合物75aの調製
実施例35:化合物79の調製
実施例36:化合物79aの調製
実施例37:固体支持体による5’末端にホスホジエステル連結GalNAc3-2共役体を含む共役オリゴマー化合物82の調製のための一般的方法(方法I)
示されるものを用いて、5’末端にホスホジエステル連結共役基を有するオリゴマー化合物を調製することができるため、例証されるホスホラミダイトは、代表的なものであり、限定する意図はない。固体支持体に添加されるホスホラミダイトの順序及び量を調整して、任意の既定の配列及び組成を有する本明細書に記載するオリゴマー化合物を調製することができる。
実施例38:5’末端にホスホジエステル連結GalNAc3-2共役体を含むオリゴマー化合物82の調製のための代替方法(方法II)
スホラミダイトは、代表的なものであり、限定する意図はない。固体支持体に添加されるホスホラミダイトの順序及び量を調整して、任意の既定の配列及び組成を有する本明細書に記載するオリゴマー化合物を調製することができる。
実施例39:固体支持体による5’末端にGalNAc3-3共役体(5’末端結合のためにGalNAc3-1修飾されたもの)を含むオリゴマー化合物83hの調製のための一般的方法
実施例41:固相技法による5’位にホスホジエステル連結GalNAc3-2(Bxがアデニンである実施例37を参照のこと)共役体を含むASOの調製のための一般的方法(ISIS 661134の調製)
を商業的供給源から購入する。標準のホスホラミダイト構築ブロック及び固体支持体を、例えば、T、A、G、及びmC残基を含む、ヌクレオシド残基の組み込みのために用いる。ホスホラミダイト化合物56及び60を用いて、5’末端のホスホジエステル連結GalNAc3-2共役体を合成した。無水アセトニトリル中のホスホラミダイトの0.1M溶液をb-D-2’-デオキシリボヌクレオシド及び2’-MOEに用いた。
al.,2003)でのホスホラミダイトカップリング法により、ASO合成を、ABI 394合成装置(1~2μmolの規模)またはGE Healthcare Bioscience AeKTAオリゴパイロット合成装置(40~200μmolの規模)で実行した。このカップリングステップについて、固体支持体の初期負荷量に対して4倍過剰のホスホラミダイトを送達し、ホスホラミダイトカップリングを10分間行った。すべての他のステップは、製造業者から提供された標準のプロトコルに従った。トルエン中の6%ジクロロ酢酸溶液を用いて、ヌクレオチドの5’-ヒドロキシル基からジメトキシトリチル(DMT)基を除去した。カップリングステップ中、無水CH3CN中の4,5-ジシアノイミダゾール(0.7M)を活性化剤として用いた。ホスホロチオエート連結部を、3分間の接触時間で、1:1のピリジン/CH3CN中のキサンタンヒドリドの0.1M溶液による硫化によって導入した。6%の水を含有するCH3CN中の20%のtert-ブチルヒドロペルオキシドの溶液を酸化剤として用いて、12分間の接触時間で、ホスホジエステルヌクレオシド間連結部を提供した。
」は、-O-P(=O)(OH)-を示す。上付き文字「m」は、5-メチルシトシンを示す。GalNAc3-2aの構造が実施例37に示される。
実施例42:固相技法による5’位にGalNAc3-3共役体を含むASOの調製のための一般的方法(ISIS 661166の調製)
実施例43:生体内におけるSRB-1を標的とする5’末端でのホスホジエステル連結GalNAc3-2の用量依存的試験(Bxがアデニンである実施例37及び41を参照のこと)
処理
下の結果は、PBS処理対照に対して標準化された各処理群のSRB-1 mRNAレベルの平均パーセントとして提示され、「%PBS」で表示される。前記方法と同様の方法を用いてED50を測定し、以下に提示する。
薬物動態分析(PK)
を示した(データ示されず)。検出可能なレベルでさらなる代謝物は観察されなかった。その対応物とは異なり、先の表23aに報告された代謝物と同様のさらなる代謝物が、3’末端にGalNAc3-1共役体を有するASO(ISIS 651900)で観察された。これらの結果は、ホスホジエステル連結GalNAc3-1またはGalNAc3-2共役体を有することで、それらの力価を損なうことなくASOのPKプロファイルを改善しうることを示唆する。
実施例44:SRB-1を標的とする3’末端にGalNAc3-1共役体(実施例9を参照のこと)を含むASOのアンチセンス阻害へのPO/PS連結部の影響
処理
処理対照に対して標準化する前に(Ribogreenを用いて)SRB-1 mRNAレベルを全RNAとの比較で相対的に決定した。以下の結果は、PBS処理対照に対して標準化された各処理群のSRB-1 mRNAレベルの平均パーセントとして提示され、「%PBS」で表示される。前記方法と同様の方法を用いてED50を測定し、以下に報告する。
MRは、その構造と一致した。
実施例46:PFPエステル(オリゴヌクレオチド111)との共役のための一般的手順;ISIS 666881(GalNAc3-10)の調製
実施例47:GalNAc3-8を含むオリゴヌクレオチド102の調製
ロピルエチルアミン(12.35mL、72mmole)中に溶解した。トリフルオロ酢酸ペンタフルオロフェニル(8.9mL、52mmole)をアルゴン下で滴加し、反応物を室温で30分間撹拌させた。Boc-ジアミン91aまたは91b(68.87mmol)をN,N-ジイソプロピルエチルアミン(12.35mL、72mmole)とともに添加し、反応物を室温で16時間撹拌させた。この時点で、DMFを減圧下で75%超、減量し、その後、混合物をジクロロメタン中に溶解した。有機層を重炭酸ナトリウム、水、及びブラインで洗浄した。その後、有機層を分離し、硫酸ナトリウム上で乾燥させ、濾過し、減圧下で減量して、油状物とした。結果として生じた油状物をシリカゲルクロマトグラフィー(2%→10%メタノール/ジクロロメタン)によって精製して、約80%の収率で化合物92a及び92bを得た。LCMS及びプロトンNMRは、その構造と一致した。
燥させ、濾過し、減圧下で減量して、油状物とした。結果として生じた油状物をシリカゲルクロマトグラフィー(5%→20%メタノール/ジクロロメタン)によって精製して、40~60%の収率で化合物100a~dを得た。LCMS及びプロトンNMRは、その構造と一致した。
mol)、及びDIEA(0.26mL、1.5mmol)を無水DMF(5mL)中に溶解し、反応混合物を室温で5分間撹拌した。これに、無水DMF中の化合物115(1.22g、0.75mmol)の溶液を添加し、反応物を室温で6時間撹拌した。溶媒を減圧下で除去し、残渣をCH2Cl2中に溶解した。有機層を飽和NaHCO3水溶液及びブラインで洗浄し、無水Na2SO4上で乾燥させ、濾過した。有機層を濃縮乾固させ、得られた残渣をシリカゲルカラムクロマトグラフィーによって精製し、ジクロロメタン中の3~15%MeOHで溶出して、化合物116(0.84g、61%)を得た。この構造を、LC MS及び1H NMR分析によって確認した。
及び1H NMRは、その構造と一致した。質量(m/z)478.2[M+H]+。
.57g)を得た。LCMSは、所望の生成物と一致した。この生成物を4mLの乾燥DMF中に溶解し、次のステップで即座に使用した。
nフィルター、0.45μm)。濾液を回転蒸発によって濃縮し、高真空下で短時間乾燥させて、化合物153(0.33g、定量的)を得た。LCMSは、所望の生成物と一致した。
燥させた化合物を無水DMF(50mL)中に溶解した。これに、1H-テトラゾール(0.43g、6.09mmol)及びN-メチルイミダゾール(0.3mL、3.81mmol)及び2-シアノエチル-N,N,N’,N’-テトライソプロピルホスホロジアミダイト(3.65mL、11.50mmol)を添加した。反応混合物をアルゴン雰囲気下で4時間撹拌した。反応混合物を酢酸エチル(200mL)で希釈した。反応混合物を飽和NaHCO3及びブラインで洗浄した。有機相を分離し、乾燥させ(Na2SO4)、濾過し、蒸発させた。残渣をシリカゲルカラムクロマトグラフィーによって精製し、ヘキサン中の50~90%酢酸エチルで溶出して、化合物159(7.82g、80.5%)を得た。この構造を、LCMS及び31P NMR分析によって確認した。
実施例54:化合物18(GalNAc3-1a及びGalNAc3-3a)の調製のための代替手順
実施例55:生体内におけるSRB-1を標的とする3’-共役基または5’-共役基のいずれかを含むオリゴヌクレオチド(GalNAc3-1、3、8、及び9の比較)の用量依存的試験
処理
3-9共役体を含むISIS 664078は、3’末端にGalNAc3-1共役体を含むISIS 655861と比較して、本質的に等効力であった。それぞれ、GalNAc3-3またはGalNAc3-9を含む5’共役アンチセンスオリゴヌクレオチドISIS 661161及びISIS 665001は、3’共役アンチセンスオリゴヌクレオチド(ISIS 655861及びISIS 664078)と比較して、力価を増加させた。
処理
様式でSRB-1 mRNAレベルを低下させた。実際には、共役アンチセンスオリゴヌクレオチドは、非共役アンチセンスオリゴヌクレオチド(ISIS 353382)と比較して、力価の大幅な改善を示した。5’共役アンチセンスオリゴヌクレオチドは、3’共役アンチセンスオリゴヌクレオチドと比較して、力価のわずかな増加を示した。
ロトコルを用いて、生理食塩水を注入したマウスとの比較で相対的に測定した。総ビリルビン及びBUNも評価した。体重の変化を評価したが、生理食塩水群との有意な変化は見られなかった。ALT、AST、総ビリルビン、及びBUN値が、以下の表44に示される。
(血漿TG)レベルを42日間にわたって監視した。各群におけるヒトAPOC-IIIを発現する3匹のトランスジェニックマウスを用いて、この試験を実行した。
実施例58:生体内におけるSRB-1を標的とする3’-共役基を含むオリゴヌクレオチドの用量依存的試験(GalNAc3-1及びGalNAc4-11の比較)
B-1のアンチセンス阻害について試験した。非共役ISIS 440762を非共役標準物として含めた。共役基のそれぞれは、ホスホジエステル連結2’-デオキシアデノシンヌクレオシド(切断可能部分)によってそれぞれのオリゴヌクレオチドの3’末端に取り付けられた。
処理
H3二環式ヌクレオシドを示し、「d」は、β-D-2’-デオキシリボヌクレオシドを示し、「s」は、ホスホロチオエートヌクレオシド間連結部(PS)を示し、「o」は、ホスホジエステルヌクレオシド間連結部(PO)を示し、「o’」は、-O-P(=O)(OH)-を示す。共役基は、太字で表示されている。
処理
ノシンヌクレオシドの切断可能部分によってそれぞれのオリゴヌクレオチドの3’末端または5’末端に取り付けられた。
処理
実施例61:GalNAc3-12を含むオリゴマー化合物175の調製
IEAをDMF中の5-(ベンジルオキシ)-5-オキソペンタン酸に添加することによって、ベンジル(ペルフルオロフェニル)グルタレートを調製した。実施例46に例証される一般的手順を用いて、GalNAc3-12共役基を含むオリゴマー化合物175を化合物174から調製した。共役基GalNAc3-12(GalNAc3-12a)のGalNAc3クラスター部分を任意の切断可能部分と組み合わせて、さまざまな共役基を提供することができる。特定の実施形態において、切断可能部分は、-P(=O)(OH)-Ad-P(=O)(OH)-である。GalNAc3-12(GalNAc3-12a-CM-)の構造は、以下に示される:
OH)-Ad-P(=O)(OH)-である。GalNAc3-13(GalNAc3-13a-CM-)の構造は、以下に示される:
アデノシンヌクレオシド(切断可能部分)によってそれぞれのオリゴヌクレオチドの5’末端に取り付けられた。
処理
殺して、リアルタイムPCR及びRIBOGREEN(登録商標)RNA定量化試薬(Molecular Probes,Inc.Eugene,OR)を用いて、肝臓におけるSRB-1 mRNAレベルを標準プロトコルに従って決定した。以下の結果は、生理食塩水(対照)に対して標準化された各処理群のSRB-1 mRNAレベルの平均パーセントとして提示される。
処理
される:
22(GalNAc3-22a-CM-)の構造は、以下に示される:
処理
Harbor,ME)に、表60に列記されるオリゴヌクレオチドまたは生理食塩水を、以下に示される投与量で1回、皮下注入した。各処理群は、4匹の動物からなった。最終投与の72時間後にマウスを屠殺して、リアルタイムPCR及びRIBOGREEN(登録商標)RNA定量化試薬(Molecular Probes,Inc.Eugene,OR)を用いて、肝臓におけるSRB-1 mRNAレベルを決定した。以下の結果は、生理食塩水(対照)に対して標準化された各処理群のSRB-1 mRNAレベルの平均パーセントとして提示される。
実施例76:GalNAc3-23を含むオリゴマー化合物230の調製
、室温で2時間撹拌した。その後、反応物を蒸発乾固し、カラムクロマトグラフィーによって精製し、ジクロロメタン中の2~10%メタノールの勾配で溶出して、化合物228を得た。LCMS及びNMRは、その構造と一致した。化合物228(1.7g、1.02mmol)をエタノール(100mL)中のラネーニッケル(約2g、湿性)で、水素雰囲気下で処理した。12時間後、触媒を濾去し、有機層を蒸発させて固体にし、これを次のステップで直接使用した。LCMS及びNMRは、その構造と一致した。この固体(0.87g、0.53mmol)をDMF(5mL)中のベンジルグルタル酸(0.18g、0.8mmol)、HBTU(0.3g、0.8mmol)、及びDIEA(273.7μL、1.6mmol)で処理した。16時間後、DMFを減圧下で65℃で除去して油状物とし、この油状物をジクロロメタン中に溶解した。有機層を飽和NaHCO3、ブラインで洗浄し、Na2SO4上で乾燥させた。有機層を蒸発させた後、化合物をカラムクロマトグラフィーによって精製し、ジクロロメタン中の2~20%メタノールの勾配で溶出して、カップリング生成物を得た。LCMS及びNMRは、その構造と一致した。ベンジルエステルをパールマン触媒で、水素雰囲気下で1時間脱保護した。その後、この触媒を濾去し、溶媒を除去乾固して、酸を得た。LCMS及びNMRは、その構造と一致した。酸(486mg、0.27mmol)を乾燥DMF(3mL)中に溶解した。ピリジン(53.61μL、0.66mmol)を添加し、反応物をアルゴンでパージした。ペンタフルオロトリフルオロアセテート(46.39μL、0.4mmol)を反応混合物に緩徐に添加した。反応物の色が淡黄色からワイン色に変化し、少しの煙を発し、この煙をアルゴン流で吹き飛ばした。反応物を室温で1時間撹拌させた(反応の完了をLCMSによって確認した)。この溶媒を減圧下(回転蒸発)で70℃で除去した。残渣をDCMで希釈し、1N NaHSO4、ブライン、飽和重炭酸ナトリウム、及び再度ブラインで洗浄した。有機物をNa2SO4上で乾燥させ、濾過し、濃縮乾固させて、黄色の脆い泡状物として225mgの化合物229を得た。LCMS及びNMRは、その構造と一致した。
処理
Harbor,ME)のそれぞれに、表64に列記されるオリゴヌクレオチドまたは生理食塩水を、以下に示される投与量で1回、皮下注入した。各処理群は、4匹の動物からなった。最終投与の72時間後にマウスを屠殺して、リアルタイムPCR及びRIBOGREEN(登録商標)RNA定量化試薬(Molecular Probes,Inc.
Eugene,OR)を用いて、肝臓におけるSRB-1 mRNAレベルを決定した。以下の結果は、生理食塩水(対照)に対して標準化された各処理群のSRB-1 mRNAレベルの平均パーセントとして提示される。
阻害について試験した。
処理
処理
処理
mRNA及び血漿タンパク質レベルの平均パーセントとして提示される。
処理
66)よりも強力であり、かつより長い作用持続時間を有したことを示す。さらに、5’-GalNAc共役体を含むオリゴヌクレオチド(ISIS 678381、678382、678383、及び678384)は、概して、3’-GalNAc共役体を含むオリゴヌクレオチド(ISIS 656326)よりもさらに強力であり、さらに長い作用持続時間を有した。
。オリゴヌクレオチド添加の16時間後に細胞を溶解し、RNease 3000 BioRobot(Qiagen)を用いて全RNAを精製した。リアルタイムPCR及びRIBOGREEN(登録商標)RNA定量化試薬(Molecular Probes,Inc.Eugene,OR)を用いて、SRB-1 mRNAレベルを標準のプロトコルに従って決定した。Prism 4ソフトウェア(GraphPad)を用いて、IC50値を決定した。結果は、さまざまな異なるGalNAc共役基及びさまざまな異なる切断可能部分を含むオリゴヌクレオチドが、生体外自由取り込み実験において、GalNAc共役基を欠く親オリゴヌクレオチド(ISIS 353382及び666841)よりも著しく強力であることを示す。
実施例83:GalNAc3クラスターを含む、第XI因子を標的とするオリゴヌクレオチドによる生体内におけるアンチセンス阻害
処理
処理
、678347、678348、及び678349)は、3’-GalNAc共役体を含むオリゴヌクレオチド(ISIS 656173)よりもさらに強力であり、さらに長い作用持続時間を有した。
処理
量依存的様式でSRB-1 mRNAレベルを低下させた。
処理
,CA)を用いて、TTRタンパク質レベルを測定した。標準のプロトコルに従ってリアルタイムPCR及びRIBOGREEN(登録商標)RNA定量化試薬(Molecular Probes,Inc.Eugene,OR)を用いて、肝臓におけるヒトTTR
mRNAレベルを決定した。表84~87に提示される結果は、各処理群の平均値である。mRNAレベルは、PBS群の平均と比較した平均値である。血漿タンパク質レベルは、ベースラインでのPBS群の平均値と比較した平均値である。体重は、個々の処理群それぞれを屠殺するまでのベースラインからの平均体重変化率である。示される臓器重量は、動物の体重に対して標準化されており、各処理群の平均標準化臓器重量は、PBS群の平均標準化臓器重量との比較で提示される。
処理
実施例88:GalNAc3共役体を含むSMNを標的とするオリゴヌクレオチドによる生体内におけるスプライシング調節
処理
雌からなった。投与の3日後にマウスを屠殺して、標準のプロトコルに従ってリアルタイムPCRを用いて、エキソン7を有する場合とエキソン7を有しない場合の肝臓におけるヒトSMN mRNAレベルを決定した。Ribogreen試薬を用いて総RNAを測定した。SMN mRNAレベルを総mRNAに対して標準化し、さらに生理食塩水処理群の平均に対して標準化した。結果として生じたエキソン7を含むSMN mRNAとエキソン7を欠くSMN mRNAとの平均比が、表91に示される。結果は、スプライシングを調節し、かつGalNAc共役体を含む完全修飾オリゴヌクレオチドが、GlaNAc共役体を欠く親オリゴヌクレオチドよりも肝臓におけるスプライシングの改変に著しく強力であることを示す。さらに、この傾向は、2’-MOE及びモルホリノ修飾オリゴヌクレオチドを含む複数の修飾化学でも維持される。
処理
処理
群の平均値と比較した平均値である。「BL」は、第1の投与の直前に測定したベースラインを示す。表96に例証されるように、アンチセンスオリゴヌクレオチドでの処理は、用量依存的様式でTTR発現レベルを低下させた。GalNAc共役体を含むオリゴヌクレオチドは、GalNAc共役体を欠く親(ISIS 420915)よりも強力であり、ホスホジエステルまたはデオキシアデノシンの切断可能部分を含むオリゴヌクレオチドは、共役体を欠く親と比較して、力価の著しい改善を示した(ISIS番号682883及び666943対420915、ならびに実施例86及び87を参照のこと)。
処理
実施例93:混成ウイング及び5’-GalNAc3共役体を含むSRB-1を標的とするオリゴヌクレオチドによる生体内におけるアンチセンス阻害
処理
Harbor,ME)に、表100に列記されるオリゴヌクレオチドまたは生理食塩水を、以下に示される投与量で1回、皮下注入した。各処理群は、4匹の動物からなった。最終投与の72時間後にマウスを屠殺した。リアルタイムPCRを用いて、肝臓におけるSRB-1 mRNAレベルを測定した。標準のプロトコルに従って、SRB-1 mRNAレベルをシクロフィリンmRNAレベルに対して標準化した。結果は、生理食塩水対照群と比較した各処理群のSRB-1 mRNAレベルの平均パーセントとして提示される。表101に例証されるように、アンチセンスオリゴヌクレオチドでの処理は、用量依存的様式でSRB-1 mRNAレベルを低下させ、GalNAc共役体を含み、かつ完全cEtまたは混成糖修飾のいずれかのウイングを有するギャップマーオリゴヌクレオチドは、共役体を欠き、かつ完全cEt修飾ウイングを含む親オリゴヌクレオチドよりも著しく強力であった。
処理
処理
ク質結合に大きな影響を与えないことを示す。さらに、完全PSヌクレオシド間連結部を有するオリゴヌクレオチドも混成PO/PS連結部を有するオリゴヌクレオチドも血漿タンパク質に結合し、完全PS連結部を有するオリゴヌクレオチドは、混合PO/PS連結部を有するオリゴヌクレオチドよりも若干高い程度に血漿タンパク質に結合する。
実施例98:hPMBCアッセイにおけるGalNAc共役体を含むオリゴヌクレオチドの炎症誘発作用の評価
レオチドよりも1.5~16倍高い親和性を有することを示す。
処理
実施例102:GalNAc共役体を含むアンチセンスオリゴヌクレオチドの肝臓における分布
処理
びAPOC-IIIレベルの平均パーセントとして提示される。実施例79の表71における結果と以下の表115における結果の比較は、ホスホジエステルヌクレオシド間連結部及びホスホロチオエートヌクレオシド間連結部の両方を含むオリゴヌクレオチドが、ホスホロチオエートヌクレオシド間連結部のみを含む等価オリゴヌクレオチドよりも増加した作用持続時間を示したことを示す。
し、濃縮して、カルボン酸を得た。カルボン酸(1.32g、1.15mmol、クラスター遊離酸)をDMF(3.2mL)中に溶解した。これに、N,N-ジイソプロピルエチルアミン(0.3mL、1.73mmol)及びPFPTFA(0.30mL、1.73mmol)を添加した。室温で30分間撹拌した後、反応混合物を水(40mL)に注ぎ、EtOAc(2×50mL)で抽出した。上述のように標準の後処理を完了して、化合物234を得た。LCMS及びNMRは、その構造と一致した。実施例46に記載される一般的手順を用いて、オリゴヌクレオチド235を調製した。共役基GalNAc2-24のGalNAc2クラスター部分(GalNAc2-24a)をオリゴヌクレオチド上に存在する任意の切断可能部分と組み合わせて、さまざまな共役基を提供することができる。GalNAc2-24(GalNAc2-24a-CM)の構造は、以下に示される:
処理
に記載される手順を用いて、オリゴヌクレオチドの5’末端に付加する。共役基GalNAc1-26のGalNAc1クラスター部分(GalNAc1-26a)をオリゴヌクレオチド上に存在する任意の切断可能部分と組み合わせて、さまざまな共役基を得ることができる。GalNAc1-26(GalNAc1-26a-CM)の構造は、以下に示される:
処理
表121に列挙するオリゴヌクレオチドを、マウスにおけるヒト補体B因子(CFB)のアンチセンス阻害について、用量依存的試験で調べた。
ヒトCFBを発現するトランスジェニックマウス(Jackson Laboratory,メイン州バーハーバー)に、表122に列挙するオリゴヌクレオチドまたは生理食塩水を週に1回、3週にわたって皮下注射した(合計4回)。ISIS番号588540を投与した4つの処置群には、1回あたり6、12、25、または50mg/kgを与えた。ISIS番号687301を投与した4つの処置群には、1回あたり0.25、0.5、2、または6mg/kgを与えた。各処置群は4匹からなった。最後の投与の2日後にマウスを屠殺し、肝臓及び腎臓のヒトCFB及びシクロフィリンmRNAレベルを、リアルタイムPCRを用いて標準的プロトコルに従って決定した。CFB mRNAレベルをシクロフィリンレベルに対して標準化し、各処置群の平均を使って、ヒトCFB転写産物発現の50%阻害を達成する用量(ED50)を決定した。結果は、2つの異なるプライマープローブセットを使って実施した4回の実験の平均であり、これを表122に示す。
表123に列挙するオリゴヌクレオチドを、マウスにおけるヒトCFBのアンチセンス阻害について、用量依存的試験で調べた。
ヒトCFBを発現するトランスジェニックマウス(Jackson Laboratory,メイン州バーハーバー)に、0.6、1、6、または18mg/kgの表123に列挙したオリゴヌクレオチドまたは生理食塩水を1回皮下注射した。各処置群は4匹または5匹からなった。この投薬の72時間後にマウスを屠殺し、肝臓のヒトCFB及びシクロフィリンmRNAレベルを、リアルタイムPCRを用いて標準的プロトコルに従って決定した。CFB mRNAレベルをシクロフィリンレベルに対して標準化し、各処置群の平均を使って、ヒトCFB転写産物発現の50%阻害を達成する用量(ED50)を決定した。結果を表123に示す。
ヒト補体B因子(CFB)核酸を標的とするアンチセンスオリゴヌクレオチドを設計し、CFB mRNAに対するそれらの効果をインビトロで試験した。アンチセンスオリゴヌクレオチドは、培養条件が類似する一連の実験で試験した。各実験に関する結果を以下に示す別々の表に掲載する。1ウェルあたり20,000細胞の密度の培養HepG2細胞を、エレクトロポレーションにより、4,500nMアンチセンスオリゴヌクレオチドでトランスフェクトした。約24時間の処理期間後に、細胞からRNAを単離し、定量リアルタイムPCRによってCFB mRNAレベルを測定した。ヒトプライマープローブセットRTS3459(フォワード配列AGTCTCTGTGGCATGGTTTGG,本明細書では配列番号810と呼ぶ;リバース配列GGGCGAATGACTGAGAT
CTTG,本明細書では配列番号811と呼ぶ;プローブ配列TACCGATTACCACAAGCAACCATGGCA,本明細書では配列番号812と呼ぶ)を使ってmRNAレベルを測定した。RIBOGREEN(登録商標)によって測定される全RNA含有量に従ってCFB mRNAレベルを調整した。結果を、無処理対照細胞との比較で、CFBの阻害パーセントとして表す。
ヒト補体B因子(CFB)核酸を標的とする新たなアンチセンスオリゴヌクレオチドを設計し、CFB mRNAに対するそれらの効果をインビトロで試験した。1ウェルあたり20,000細胞の密度の培養HepG2細胞を、エレクトロポレーションにより、4,500nMアンチセンスオリゴヌクレオチドでトランスフェクトした。約24時間の処理期間後に、RNAを細胞から単離し、CFB mRNAレベルを定量リアルタイムPCRで測定した。ヒトプライマープローブセットRTS3460_MGB(フォワード配列
CGAAGCAGCTCAATGAAATCAA,本明細書では配列番号813と呼ぶ;リバース配列TGCCTGGAGGGCCTTCTT,本明細書では配列番号814と呼ぶ;プローブ配列AGACCACAAGTTGAAGTC,本明細書では配列番号815と呼ぶ)を使って、mRNAレベルを測定した。RIBOGREEN(登録商標)によって測定される全RNA含有量に従ってCFB mRNAレベルを調整した。結果を、無処理対照細胞との比較で、CFBの阻害パーセントとして表す。
ヒト補体B因子(CFB)核酸を標的とする新たなアンチセンスオリゴヌクレオチドを設計し、CFB mRNAに対するそれらの効果をインビトロで試験した。これらのアンチセンスオリゴヌクレオチドを、培養条件が類似する一連の実験で試験した。各実験に関する結果を以下に示す別々の表に掲載する。1ウェルあたり20,000細胞の密度の培養HepG2細胞を、エレクトロポレーションにより、5,000nMアンチセンスオリゴヌクレオチドでトランスフェクトした。約24時間の処理期間後に、細胞からRNAを単離し、定量リアルタイムPCRによってCFB mRNAレベルを測定した。ヒトプライマープローブセットRTS3459を使ってmRNAレベルを測定した。RIBOGREEN(登録商標)によって測定される全RNA含有量に従ってCFB mRNAレベルを調整した。結果を、無処理対照細胞との比較で、CFBの阻害パーセントとして表す。
ヒト補体B因子(CFB)核酸を標的とするアンチセンスオリゴヌクレオチドを設計し、CFB mRNAに対するそれらの効果をインビトロで試験した。これらのアンチセンスオリゴヌクレオチドを、培養条件が類似する一連の実験で試験した。各実験に関する結果を以下に示す別々の表に掲載する。1ウェルあたり20,000細胞の密度の培養HepG2細胞を、エレクトロポレーションにより、3,000nMアンチセンスオリゴヌクレオチドでトランスフェクトした。約24時間の処理期間後に、細胞からRNAを単離し、定量リアルタイムPCRによってCFB mRNAレベルを測定した。ヒトプライマープローブセットRTS3459を使ってmRNAレベルを測定した。RIBOGREEN(登録商標)によって測定される全RNA含有量に従ってCFB mRNAレベルを調整した。結果を、無処理対照細胞との比較で、CFBの阻害パーセントとして表す。
ヒト補体B因子(CFB)核酸を標的とする新たなアンチセンスオリゴヌクレオチドを設計し、CFB mRNAに対するそれらの効果をインビトロで試験した。これらのアンチセンスオリゴヌクレオチドを、培養条件が類似する一連の実験で試験した。各実験に関する結果を以下に示す別々の表に掲載する。1ウェルあたり20,000細胞の密度の培養HepG2細胞を、エレクトロポレーションにより、2,000nMアンチセンスオリゴヌクレオチドでトランスフェクトした。約24時間の処理期間後に、細胞からRNAを単離し、定量リアルタイムPCRによってCFB mRNAレベルを測定した。ヒトプラ
イマープローブセットRTS3459を使ってmRNAレベルを測定した。RIBOGREEN(登録商標)によって測定される全RNA含有量に従ってCFB mRNAレベルを調整した。結果を、無処理対照細胞との比較で、CFBの阻害パーセントとして表す。
て配列番号1と呼ぶヒトCFB mRNA(GENBANKアクセッション番号NM_001710.5)もしくは本明細書において配列番号2と呼ぶヒトCFBゲノム配列(ヌクレオチド31852000から31861000までを切り出したGENBANKアクセッション番号NT_007592.15)、またはその両方を標的とする。「n/a」は、そのアンチセンスオリゴヌクレオチドが当該特定遺伝子配列を100%の相補性では標的としないことを示す。
ヒト補体B因子(CFB)核酸を標的とする新たなアンチセンスオリゴヌクレオチドを設計し、CFB mRNAに対するそれらの効果をインビトロで試験した。1ウェルあたり20,000細胞の密度の培養HepG2細胞を、エレクトロポレーションにより、1,000nMアンチセンスオリゴヌクレオチドでトランスフェクトした。約24時間の処理期間後に、細胞からRNAを単離し、定量リアルタイムPCRによってCFB mRNAレベルを測定した。ヒトプライマープローブセットRTS3459を使ってmRNAレベルを測定した。RIBOGREEN(登録商標)によって測定される全RNA含有量に従ってCFB mRNAレベルを調整した。結果を、無処理対照細胞との比較で、CFBの阻害パーセントとして表す。
ヒト補体B因子(CFB)核酸を標的とする新たなアンチセンスオリゴヌクレオチドを設計し、CFB mRNAに対するそれらの効果をインビトロで試験した。これらのアンチセンスオリゴヌクレオチドを、培養条件が類似する一連の実験で試験した。各実験に関する結果を以下に示す別々の表に掲載する。1ウェルあたり20,000細胞の密度の培養HepG2細胞を、エレクトロポレーションにより、500nMアンチセンスオリゴヌクレオチドでトランスフェクトした。約24時間の処理期間後に、細胞からRNAを単離し、定量リアルタイムPCRによってCFB mRNAレベルを測定した。ヒトプライマープローブセットRTS3459を使ってmRNAレベルを測定した。RIBOGREEN(登録商標)によって測定される全RNA含有量に従ってCFB mRNAレベルを調整した。結果を、無処理対照細胞との比較で、CFBの阻害パーセントとして表す。
19ヌクレオシド長であり、中央のギャップセグメントは7個の2’-デオキシヌクレオシドで構成され、5’側と3’側にそれぞれ6個のヌクレオシドを含むウイングセグメントが隣接している。6-8-6MOEギャップマーは20ヌクレオシド長であり、中央のギャップセグメントは8個の2’-デオキシヌクレオシドで構成され、5’側と3’側にそれぞれ6個のヌクレオシドを含むウイングセグメントが隣接している。5’ウイングセグメント中の各ヌクレオシド及び3’ウイングセグメント中の各ヌクレオシドは2’-MOE修飾を有する。ヌクレオシド間連結部は、各ギャップマーの全体を通して、ホスホロチオエート(P=S)連結部である。シトシン残基は、各ギャップマーの全体を通してすべて、5-メチルシトシンである。
上記の試験から、CFB mRNAのインビトロ阻害を呈するギャップマーを選択し、HepG2細胞において、さまざまな用量で試験した。細胞を1ウェルあたり20,000細胞の密度でプレーティングし、エレクトロポレーションにより、以下の表に指定するとおり、0.313μM、0.625μM、1.25μM、2.50μM、5.00μM、または10.00μM濃度のアンチセンスオリゴヌクレオチドでトランスフェクトした。約16時間の処理期間後に、RNAを細胞から単離し、CFB mRNAレベルを定量リアルタイムPCRによって測定した。ヒトプライマープローブセットRTS3459を使ってmRNAレベルを測定した。RIBOGREEN(登録商標)によって測定される全RNA含有量に従ってCFB mRNAレベルを調整した。結果を、無処理対照細胞との比較で、CFBの阻害パーセントとして表す。
上記の試験から、CFB mRNAのインビトロ阻害を呈するギャップマーを選択し、HepG2細胞において、さまざまな用量で試験した。類似する培養条件を使用するいくつかの実験でアンチセンスオリゴヌクレオチドを試験した。各実験に関する結果を以下に示す別々の表に掲載する。細胞を1ウェルあたり20,000細胞の密度でプレーティングし、エレクトロポレーションにより、以下の表に指定するとおり、0.08μM、0.25μM、0.74μM、2.22μM、6.67μM、及び20.00μM濃度のアンチセンスオリゴヌクレオチドでトランスフェクトした。約16時間の処理期間後に、RNAを細胞から単離し、CFB mRNAレベルを定量リアルタイムPCRによって測定した。ヒトプライマープローブセットRTS3459を使ってmRNAレベルを測定した。RIBOGREEN(登録商標)によって測定される全RNA含有量に従ってCFB mRNAレベルを調整した。結果を、無処理対照細胞との比較で、CFBの阻害パーセントとして表す。
上記の試験から、CFB mRNAのインビトロ阻害を呈するギャップマーを選択し、HepG2細胞において、さまざまな用量で試験した。類似する培養条件を使用するいくつかの実験でアンチセンスオリゴヌクレオチドを試験した。各実験に関する結果を以下に示す別々の表に掲載する。細胞を1ウェルあたり20,000細胞の密度でプレーティングし、エレクトロポレーションにより、以下の表に指定するとおり、0.06μM、0.25μM、1.00μM、及び4.00μM濃度のアンチセンスオリゴヌクレオチドでトランスフェクトした。約16時間の処理期間後に、RNAを細胞から単離し、CFB mRNAレベルを定量リアルタイムPCRによって測定した。ヒトプライマープローブセットRTS3459を使ってmRNAレベルを測定した。RIBOGREEN(登録商標)によって測定される全RNA含有量に従ってCFB mRNAレベルを調整した。結果を、無処理対照細胞との比較で、CFBの阻害パーセントとして表す。
上記の試験から、CFB mRNAのインビトロ阻害を呈するギャップマーを選択し、HepG2細胞において、さまざまな用量で試験した。加えて、もう一つのデオキシ、MOE及び(S)-cEtオリゴヌクレオチドISIS588870と同じ配列(CTCCTTCCGAGTCAGC、配列番号549)及び標的領域(標的開始部位は配列番号1の2195と配列番号2の6983)を持つデオキシ、MOE及び(S)-cEtオリゴヌクレオチドの一つ、ISIS594430を設計した。ISIS594430は3-10-3(S)-cEtギャップマーである。
CD1(登録商標)マウス(Charles River,マサチューセッツ州)は多目的マウスモデルであり、安全性及び効力の試験にはよく利用されている。このマウスを上述の試験から選択したISISアンチセンスオリゴヌクレオチドで処置し、さまざまな血漿中化学マーカーのレベルの変化について評価した。
7週齢雄CD1マウスの群に、週に1回、6週にわたって100mg/kgのISISオリゴヌクレオチドを皮下注射した。1つの雄CD1マウス群には、週1回、6週にわたってPBSを皮下注射した。1つのマウス群には、週1回、6週にわたって、100mg/kgの対照オリゴヌクレオチドISIS141923(CCTTCCCTGAAGGTTCCTCC,本明細書では配列番号809と呼ぶ、既知のマウス標的がない5-10-5MOEギャップマー)を皮下注射した。最後の投薬の48時間後にマウスを安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝臓機能及び腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、トランスアミナーゼ及びBUNの血漿中レベルを測定した。結果を以下の表に掲載する。肝臓機能マーカーまたは腎臓機能マーカーのいずれかのレベルを、アンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
40日目にマウスの屠殺に先だってマウスの体重を測定した。肝臓、腎臓、及び膵臓の臓器重量もマウスの屠殺後に測定した。結果を以下の表に掲載する。アンチセンスオリゴヌクレオチドに予想される範囲外にまで重量を変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
6~8週齢の雄CD1マウスの群に、週1回、6週にわたって100mg/kgのISISオリゴヌクレオチドを皮下注射した。2つの雄CD1マウス群には、週1回、6週にわたって、PBSを皮下注射した。1つのマウス群には、週1回、6週にわたって、100mg/kgの対照オリゴヌクレオチドISIS141923を皮下注射した。マウスを最後の投薬の48時間後に安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝臓機能及び腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、トランスアミナーゼ、アルブミン、及びBUNの血漿中レベルを測定した。結果を以下の表に掲載する。肝臓機能マーカーまたは腎臓機能マーカーのいずれかのレベルを、アンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
42日目にマウスの体重を測定した。45日目にマウスを屠殺した後、肝臓、腎臓、及び膵臓の臓器重量も測定した。結果を以下の表に掲載する。アンチセンスオリゴヌクレオチドに予想される範囲外にまで重量を変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
6~8週齢の雄CD1マウスの群に、週1回、6週にわたって、100mg/kgのISISオリゴヌクレオチドを皮下注射した。2つの雄CD1マウス群には、週1回、6週にわたって、PBSを皮下注射した。マウスを最後の投薬の48時間後に安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝臓機能及び腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、トランスアミナーゼ、アルブミン、及びBUNの血漿中レベルを測定した。結果を以下の表に掲載する。肝臓機能マーカーまたは腎臓機能マーカーのいずれかのレベルを、アンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
42日目にマウスの体重を測定した。42日目にマウスを屠殺した後、肝臓、腎臓、及び膵臓の臓器重量も測定した。結果を以下の表に掲載する。アンチセンスオリゴヌクレオチドに予想される範囲外にまで重量を変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
10週齢の雄CD1マウスの群に、50mg/kgの、上述の試験で得たISISオリゴヌクレオチドを、週1回、6週にわたって、皮下注射した。加えて、2つのオリゴヌクレオチドISIS594431及びISIS594432を3-10-3(S)-cEtギャップマーとして設計し、それらもこの試験で調べた。ISIS594431(ACCTCCTTCCGAGTCA、配列番号550)は、デオキシ、MOE及び(S)-cEtギャップマーであるISIS588871と同じ領域(標的開始部位は配列番号1の2197及び配列番号2の6985)を標的とする。ISIS594432(TGGTCACATTCCCTTC、配列番号542)は、デオキシ、MOE及び(S)-cEtギャップマーであるISIS588872と同じ領域(標的開始部位は配列番号1の154及び配列番号2の1875)を標的とする。
肝臓機能及び腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、トランスアミナーゼ、アルブミン、クレアチニン、及びBUNの血漿中レベルを測定した。結果を以下の表に掲載する。肝臓機能マーカーまたは腎臓機能マーカーのいずれかのレベルを、アンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
39日目にマウスの体重を測定した。42日目にマウスを屠殺した後、肝臓、腎臓、及び膵臓の臓器重量も測定した。結果を以下の表に掲載する。アンチセンスオリゴヌクレオチドに予想される範囲外にまで重量を変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
8~9週齢の雄CD1マウスの群に、週1回、6週にわたって、50mg/kgのISISオリゴヌクレオチドを皮下注射した。2つの雄CD1マウス群には、週1回、6週にわたって、PBSを皮下注射した。マウスを最後の投薬の48時間後に安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝臓機能及び腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、トランスアミナーゼ、アルブミン、クレアチニン、及びBUNの血漿中レベルを測定した。結果を以下の表に掲載する。肝臓機能マーカーまたは腎臓機能マーカーのいずれかのレベルを、アンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
40日目にマウスの体重を測定した。42日目にマウスを屠殺した後、肝臓、腎臓、及び膵臓の臓器重量も測定した。結果を以下の表に掲載する。アンチセンスオリゴヌクレオチドに予想される範囲外にまで重量を変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
8~9週齢の雄CD1マウスの群に、週1回、6週にわたって、50mg/kgのデオキシ、MOE、及び(S)-cEtオリゴヌクレオチドを皮下注射した。2つの雄CD1マウス群には、週1回、6週にわたって、PBSを皮下注射した。マウスを最後の投薬の48時間後に安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝臓機能及び腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、トランスアミナーゼ、アルブミン、クレアチニン、ビリルビン、及びBUNの血漿中レベルを測定した。結果を以下の表に掲載する。肝臓機能マーカーまたは腎臓機能マーカーのいずれかのレベルを、アンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
40日目にマウスの体重を測定した。45日目にマウスを屠殺した後、肝臓、腎臓、及び膵臓の臓器重量も測定した。結果を以下の表に掲載する。アンチセンスオリゴヌクレオチドに予想される範囲外にまで重量を変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
8~9週齢の雄CD1マウスの群に、週1回、6週にわたって、100mg/kgのISISオリゴヌクレオチドを皮下注射した。1つの雄CD1マウス群に、週1回、6週にわたって、PBSを皮下注射した。マウスを最後の投薬の48時間後に安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝臓機能及び腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、トランスアミナーゼ、アルブミン、クレアチニン、及びBUNの血漿中レベルを測定した。結果を以下の表に掲載する。肝臓機能マーカーまたは腎臓機能マーカーのいずれかのレベルを、アンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
44日目にマウスの体重を測定した。49日目にマウスを屠殺した後、肝臓、腎臓、及び膵臓の臓器重量も測定した。結果を以下の表に掲載する。アンチセンスオリゴヌクレオチドに予想される範囲外にまで重量を変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
8~9週齢の雄CD1マウスの群に、週1回、6週にわたって、100mg/kgのMOEギャップマー、または50mg/kgのデオキシ、MOE及び(S)-cEtオリゴヌクレオチドもしくは(S)-cEtギャップマーを皮下注射した。1つの雄CD1マウス群には、週1回、6週にわたって、PBSを皮下注射した。マウスを最後の投薬の48時間後に安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝臓機能及び腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、トランスアミナーゼ、アルブミン、クレアチニン、及びBUNの血漿中レベルを測定した。結果を以下の表に掲載する。
36日目にマウスの体重を測定した。43日目にマウスを屠殺した後、肝臓、腎臓、及び膵臓の臓器重量も測定した。臓器重量に関する結果を体重に対する比として表し、PBS対照比に対して標準化した。
すべてのマウス群から得た血液を、IL-6、MDC、MIP1β、IP-10、MCP1、MIP-1α、及びRANTESなどといったさまざまなサイトカインの測定のために、Antech Diagnosticsに送った。結果を表54に掲載する。
すべてのマウス群から得た血液を、ヘマトクリット(HCT)の測定、ならびにWBC、RBC、及び血小板などのさまざまな血球及び総ヘモグロビン(Hb)含有量の測定のために、Antech Diagnosticsに送った。結果を表55に掲載する。
スプレーグ・ドーリーラットは、安全性や効力の評価に使用される多目的モデルである。これらのラットを、上記実施例で述べた試験によって得たISISアンチセンスオリゴヌクレオチドで処置し、さまざまな血漿中化学マーカーのレベルの変化を評価した。
7~8週齢の雄スプレーグ・ドーリーラットを12時間明/暗周期で飼育し、Purina通常ラット用飼料ダイエット5001を不断給餌した。スプレーグ・ドーリーラット各4匹の群に、週1回、6週にわたって、100mg/kgの5-10-5MOEギャップマーを皮下注射した。ラット6匹の対照群1つには、週1回、6週にわたって、PBSを皮下注射した。最後の投薬の48時間後に、ラットを安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、トランスアミナーゼの血漿中レベルを測定した。ALT(アラニントランスアミナーゼ)とAST(アスパラギン酸トランスアミナーゼ)の血漿中レベルを測定し、結果をIU/Lの単位で表して、以下の表に掲載する。肝臓機能のいずれかのマーカーのレベルをアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、血中尿素窒素(BUN)及びクレアチニンの血漿中レベルを測定した。結果をmg/dLの単位で表して、以下の表に掲載する。腎臓機能マーカーのいずれかのレベルをアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
体重測定は39日目に行った。42日目の試験終了時に肝臓、心臓、脾臓及び腎臓の重量を測定した。それらを以下の表に掲載する。臓器重量をアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
9~10週齢の雄スプレーグ・ドーリーラットを12時間明/暗周期で飼育し、Purina通常ラット飼料ダイエット5001を不断給餌した。スプレーグ・ドーリーラット各4匹の群に、週1回、6週にわたって、100mg/kgのデオキシ、MOE、及び(S)-cEtオリゴヌクレオチドを皮下注射した。ラット各3匹の対照群2つには、週1回、6週にわたって、PBSを皮下注射した。最後の投薬の48時間後に、ラットを安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、42日目に、トランスアミナーゼの血漿中レベルを測定した。ALT(アラニントランスアミナーゼ)とAST(アスパラギン酸トランスアミナーゼ)及びアルブミンの血漿中レベルを測定し、それらの結果を以下の表に掲載する。肝臓機能のいずれかのマーカーのレベルをアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、血中尿素窒素(BUN)及びクレアチニンの血漿中レベルを測定した。結果をmg/dLの単位で表して、以下の表に掲載する。腎臓機能マーカーのいずれかのレベルをアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
体重測定は39日目に行った。42日目の試験終了時に肝臓、心臓、脾臓及び腎臓の重量を測定した。それらを以下の表に掲載する。臓器重量をアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
9~10週齢の雄スプレーグ・ドーリーラットを12時間明/暗周期で飼育し、Pur
ina通常ラット飼料ダイエット5001を不断給餌した。スプレーグ・ドーリーラット各4匹の群に、週1回、6週にわたって、100mg/kgのMOEギャップマーを皮下注射した。ラット6匹の対照群1つには、週1回、6週にわたって、PBSを皮下注射した。最後の投薬の48時間後に、ラットを安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、43日目に、トランスアミナーゼの血漿中レベルを測定した。ALT(アラニントランスアミナーゼ)とAST(アスパラギン酸トランスアミナーゼ)の血漿中レベルを測定し、結果をIU/Lの単位で表して、以下の表に掲載する。肝臓機能のいずれかのマーカーのレベルをアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、血中尿素窒素(BUN)及びクレアチニンの血漿中レベルを測定した。結果をmg/dLの単位で表して、以下の表に掲載する。腎臓機能マーカーのいずれかのレベルをアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
体重測定は39日目に行った。42日目の試験終了時に肝臓、心臓、脾臓及び腎臓の重量を測定した。それらを以下の表に掲載する。臓器重量をアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
9~10週齢の雄スプレーグ・ドーリーラットを12時間明/暗周期で飼育し、Purina通常ラット飼料ダイエット5001を不断給餌した。スプレーグ・ドーリーラット各4匹の群に、週1回、6週にわたって、100mg/kgのMOEギャップマーを皮下注射した。ラット6匹の対照群1つには、週1回、6週にわたって、PBSを皮下注射した。最後の投薬の48時間後に、ラットを安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、42日目に、トランスアミナーゼの血漿中レベルを測定した。ALT(アラニントランスアミナーゼ)とAST(アスパラギン酸トランスアミナーゼ)の血漿中レベルを測定し、結果をIU/Lの単位で表して、以下の表に掲載する。肝臓機能のいずれかのマーカーのレベルをアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、血中尿素窒素(BUN)及びクレアチニンの血漿中レベルを測定した。結果をmg/dLの単位で表して、以下の表に掲載する。腎臓機能マーカーのいずれかのレベルをアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
体重測定は39日目に行った。42日目の試験終了時に肝臓、心臓、脾臓及び腎臓の重量を測定した。それらを以下の表に掲載する。臓器重量をアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
9~10週齢の雄スプレーグ・ドーリーラットを12時間明/暗周期で飼育し、Purina通常ラット飼料ダイエット5001を不断給餌した。スプレーグ・ドーリーラット各4匹の群に、週1回、6週にわたって、100mg/kgのMOEギャップマーまたは50mg/kgのデオキシ、MOE及び(S)-cEtオリゴヌクレオチドを皮下注射した。ラット4匹の対照群1つには、週1回、6週にわたって、PBSを皮下注射した。最後の投薬の48時間後に、ラットを安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、42日目に、トランスアミナーゼの血漿中レベルを測定した。ALT(アラニントランスアミナーゼ)とAST(アスパラギン酸トランスアミナーゼ)の血漿中レベルを測定し、結果をIU/Lの単位で表して、以下の表に掲載する。肝臓機能のいずれかのマーカーのレベルをアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、血中尿素窒素(BUN)及びクレアチニンの血漿中レベル及び尿中レベルを測定した。結果をmg/dLの単位で表して以下の表に掲載する。腎臓機能マーカーのいずれかのレベルをアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
体重測定は39日目に行った。42日目の試験終了時に肝臓、心臓、脾臓及び腎臓の重量を測定した。それらを以下の表に掲載する。臓器重量をアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
雄ラットを12時間明/暗周期で飼育し、Purina通常ラット飼料ダイエット5001を不断給餌した。ラット各4匹の群に、週1回、6週にわたって、100mg/kgのMOEギャップマーまたは50mg/kgのデオキシ、MOE及び(S)-cEtオリゴヌクレオチドもしくは(S)-cEtギャップマーを皮下注射した。ラット4匹の対照群1つには、週1回、6週にわたって、PBSを皮下注射した。最後の投薬の48時間後に、ラットを安楽死させ、さらなる分析のために臓器及び血漿を収集した。
肝機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、42日目に、トランスアミナーゼの血漿中レベルを測定した。ALT(アラニントランスアミナーゼ)とAST(アスパラギン酸トランスアミナーゼ)の血漿中レベルを測定し、結果をIU/Lの単位で表して、以下の表に掲載する。
腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、自動臨床化学分析装置(Hitachi Olympus AU400e,ニューヨーク州メルビル)を使って、総タンパク質及びクレアチニンの尿中レベルを測定した。結果を以下の表に掲載する。腎臓機能マーカーのいずれかのレベルをアンチセンスオリゴヌクレオチドに予想される範囲外にまで変化させたISISオリゴヌクレオチドを、その後の試験では除外した。
体重測定は39日目に行った。42日目の試験終了時に肝臓、心臓、脾臓及び腎臓の重量を測定した。それらを以下の表に掲載する。臓器重量に関する結果を体重に対する比として表し、PBS対照比に対して標準化した。
選ばれた化合物を、ヒトCFBトランスジェニックマウス樹立系統#6における効力について試験した。ヒトCFB遺伝子は第6染色体の位置31913721-31919861に位置する。ヒトCFB遺伝子を発現するトランスジェニックマウスを作製するために、CFB配列を含有するフォスミド(ABC14-50933200C23)を選択した。Cla I(31926612)及びAge I(31926815)制限酵素を使って、CFB遺伝子を含有する前核注入用の22,127bpフラグメントを生成させた。PvuIを使った制限酵素解析によってDNAを確認した。前記22,127bpのDNAフラグメントをC57BL/6NTac胚に注入した。6つの陽性ファウンダーを育てた。肝臓ヒトCFB mRNAを発現するファウンダー#6を第3世代まで交雑した。第3世代マウスからの子孫を使って、ヒトCFB ASOをヒトCFB mRNAの低減について評価した。
マウス各3匹の群に、第1週は週に2回、50mg/kgのISISオリゴヌクレオチドを皮下注射し、次に、さらに3週にわたって、週に1回、50mg/kgのISISオリゴヌクレオチドを投与した。マウス4匹の対照群1つに、第1週は週に2回、その後さらに3週にわたって週に1回、PBSを皮下注射した。最後の投薬の48時間後にマウスを安楽死させ、さらなる分析のために臓器及び血漿を収集した。
投薬期間の終了時に、CFB mRNAレベルのリアルタイムPCR分析用に、肝臓と腎臓からRNAを抽出した。ヒトCFB mRNAレベルはヒトプライマープローブセットRTS3459を使って測定した。CFB mRNAレベルをRIBOGREEN(登
録商標)及びハウスキーピング遺伝子シクロフィリンに対して標準化した。結果は対照と比較したCFB mRNA発現の阻害パーセントとして算出した。すべてのアンチセンスオリゴヌクレオチドが肝臓においてヒトCFB mRNAレベルの阻害を達成した。
マウスCFB mRNA(GENBANKアクセッション番号NM_008198.2,本明細書には配列番号5として組み込まれる)を標的とするアンチセンスオリゴヌクレオチドをいくつか設計した。各オリゴヌクレオチドの標的開始部位と配列を以下の表に記載する。以下の表のキメラアンチセンスオリゴヌクレオチドは5-10-5MOEギャップマーとして設計された。これらのギャップマーは20ヌクレオシド長であり、中央のギャップセグメントは10個の2’-デオキシヌクレオシドで構成され、両側(5’側及び3’側)にそれぞれ5ヌクレオシドを含むウイングが隣接している。5’ウイングセグメント中の各ヌクレオシド及び3’ウイングセグメント中の各ヌクレオシドは2’-MOE修飾を有する。ヌクレオシド間連結部は、各ギャップマーの全体を通して、ホスホロチオエート(P=S)連結部である。シトシン残基は、各ギャップマーの全体を通してすべて、5-メチルシトシンである。
C57BL/6マウス各4匹の群に、3週にわたる週1回の投与で、50mg/kgの
ISIS516269、ISIS516272、ISIS516323、ISIS516330、またはISIS516341を注射した。対照マウス群には、3週にわたる週1回の投与で、リン酸緩衝食塩水(PBS)を注射した。
試験の最後に、プライマープローブセットRTS3430(フォワード配列GGGCAAACAGCAATTTGTGA,本明細書では配列番号816と呼ぶ;リバース配列TGGCTACCCACCTTCCTTGT,本明細書では配列番号817と呼ぶ;プローブ配列CTGGATACTGTCCCAATCCCGGTATTCCX,本明細書では配列番号818と呼ぶ)を用いるCFBのリアルタイムPCR分析用に、肝臓組織からRNAを抽出した。RIBOGREEN(登録商標)を使ってmRNAレベルを標準化した。以下の表に示すとおり、一部のアンチセンスオリゴヌクレオチドはPBS対照と比較してマウスCFBの低減を達成した。結果を、対照と比較したCFBの阻害パーセントとして表す。
ヤギ抗CFB抗体(Sigma Aldrich)を用いるウェスタンブロットによって、腎臓、肝臓、血漿、及び眼におけるCFBタンパク質レベルを測定した。結果を、PBS対照と比較したCFBの阻害パーセントとして表す。「n/a」は,当該試料では測定が行われなかったことを示す。以下の表に示すとおり、ISISオリゴヌクレオチドによるCFBのアンチセンス阻害は、さまざまな組織においてCFBタンパク質の低減をもたらした。以下の表に示すとおり、ISISオリゴヌクレオチドの全身性投与は、眼におけるCFBレベルを低減するのに有効であった。
C57BL/6マウス各4匹の群に、6週にわたる週1回の投与で、25mg/kg、50mg/kg、または100mg/kgのISIS516272、及びISIS516323を注射した。別の2つのマウス群に、6週にわたる週1回の投与で、100mg/
kgのISIS516330またはISIS516341を注射した。2つの対照マウス群には、6週にわたる週1回の投与で、リン酸緩衝食塩水(PBS)を注射した。
プライマープローブセットRTS3430を用いるCFBのリアルタイムPCR分析のために、肝臓組織と腎臓組織からRNAを抽出した。RIBOGREEN(登録商標)を使ってmRNAレベルを標準化した。以下の表に示すとおり、アンチセンスオリゴヌクレオチドはPBS対照との比較でマウスCFBの用量依存的低減を達成した。結果を、対照と比較したCFBの阻害パーセントとして表す。
ヤギ抗CFB抗体(Sigma Aldrich)を用いるウェスタンブロットにより、血漿中のCFBタンパク質レベルを測定した。以下の表に示すように、ISISオリゴヌクレオチドによるCFBのアンチセンス阻害は、CFBタンパク質の低減をもたらした。結果を、PBS対照と比較したCFBの阻害パーセントとして表す。「n/a」は、当該試料で測定が行われなかったことを示す。
NZB/W F1は狼瘡の最も古い古典的モデルであり、これらのマウスは、狼瘡患者の表現型に匹敵する重度の狼瘡様表現型を発症する(Theofilopoulos,A.N. and Dixon,F.J. Advances in Immunology,vol.37、pp.269-390,1985).これらの狼瘡様表現型には、リンパ節腫脹、脾腫、抗dsDNA IgG(その大半はIgG2a及びIgG3である)を含む血清中抗核自己抗体(ANA)の上昇、及び5~6月齢で明白になり10~12月齢で腎不全及び死亡につながる免疫複合体媒介性糸球体腎炎(GN)が含まれる。
CFBを標的とするアンチセンスオリゴヌクレオチドによる処置が、前記マウスモデルにおける腎臓病理を改善することを実証するための試験を行った。17週齢の雌NZB/W F1マウスをJackson Laboratoriesから購入した。マウス各16匹の群に用量100μg/kg/週のISIS516272またはISIS516323を20週にわたって与えた。マウス16匹のもう一つの群には、用量100μg/kg/週の対照オリゴヌクレオチドISIS141923を20週にわたって与えた。マウス10匹のもう一つの群にはPBSを20週にわたって投与し、それを対照群として、他のすべての群をこの対照群と比較した。最後の注射を行った48時間後に、最終エンドポイントを収集した。
プライマープローブセットRTS3430を用いるCFBのリアルタイムPCR分析用に、肝臓組織と腎臓組織からRNAを抽出した。RIBOGREEN(登録商標)を使ってmRNAレベルを標準化した。以下の表に示すとおり、一部のアンチセンスオリゴヌクレオチドは、PBS対照に対してマウスCFBの低減を達成した。結果を、対照と比較したCFBの阻害パーセントとして表す。
このマウスモデルでは60%の動物にタンパク尿が予想される。臨床分析装置を使って総タンパク質対クレアチニン比を算出することにより、重症タンパク尿の累積発生率を測定した。結果を以下の表に掲載する。これらの結果は、CFBを標的とするアンチセンスオリゴヌクレオチドによる処置が、PBS対照マウス及び対照オリゴヌクレオチド処置マウスと比較して、マウスにおけるタンパク質尿の低減を達成したことを実証している。
マウスの数を処置開始時に記録し、20週目に再び記録することにより、マウスの生存率を監視した。結果を以下の表に掲載する。これらの結果は、CFBを標的とするアンチオリゴヌクレオチドによる処置が、マウスの生存率を、PBS対照マウス及び対照オリゴヌクレオチド処置マウスと比較して増加させたことを実証している。
腎臓の糸球体におけるC3沈着及びIgG沈着の量を、抗C3抗体を用いる免疫組織化学によって測定した。結果を以下の表に掲載する。これらの結果は、CFBを標的とするアンチオリゴヌクレオチドによる処置が、PBS対照マウス及び対照オリゴヌクレオチド処置マウスと比較して、腎臓糸球体におけるC3沈着の低減とIgG沈着の低減をどちらも達成したことを実証している。
16週齢の雌NZB/W F1マウスをJackson Laboratoriesから購入した。マウス10匹の群に、用量100μg/kg/週のISIS516323を12週にわたって与えた。マウス10匹のもう一つの群には、用量100μg/kg/週の対照オリゴヌクレオチドISIS141923を12週にわたって与えた。マウス10匹のもう一つの群には、PBSを12週にわたって投与し、それを対照群として、他のすべての群をこの対照群と比較した。最後の注射を行った48時間後に、最終エンドポイントを収集した。
プライマープローブセットRTS3430を用いるCFBのリアルタイムPCR分析用に、肝臓組織と腎臓組織からRNAを抽出した。以下の表に示すように、ISIS516323による処置はPBS対照に対してマウスCFBの低減を達成した。結果を、対照と比較したCFBの阻害パーセントとして表す。
尿中総タンパク質対クレアチニン比を測定すると共に、総ミクロアルブミンレベルを測定することにより、重症タンパク尿の累積発生率を評価した。結果を以下の表に掲載する。これらの結果は、CFBを標的とするアンチオリゴヌクレオチドによる処置が、PBS対照マウス及び対照オリゴヌクレオチド処置マウスと比較して、マウスにおけるタンパク尿を低減したことを実証している。
マウスの数を処置開始時に記録し、12週目に再び記録することにより、マウスの生存
率を監視した。結果を以下の表に掲載する。これらの結果は、CFBを標的とするアンチオリゴヌクレオチドによる処置が、マウスにおける生存率を、PBS対照マウス及び対照オリゴヌクレオチド処置マウスと比較して増加させたことを実証している。
MRL/lprループス腎炎マウスモデルは、二重陰性(CD4-CD8-)及びB220+ T細胞の蓄積に起因するリンパ節腫脹を特徴とするSLE様表現型を発症する。これらのマウスは死亡率の増進を呈する。加えて、これらのマウスは循環免疫グロブリン濃度が高く、それらには、ANA、抗ssDNA、抗dsDNA、抗Sm、及びリウマトイド因子などといった自己抗体レベルの上昇も含まれていて、多量の免疫複合体をもたらす(Andrews,B.et al.,J.Exp.Med.148:1198-1215,1978)。
CFBを標的とするアンチオリゴヌクレオチドによる処置が前記マウスモデルにおける腎病理を逆転させるかどうかを調べるための試験を行った。14週齢の雌MRL/lprマウスをJackson Laboratoriesから購入した。マウス10匹の1群に用量50μg/kg/週のISIS516323を7週にわたって与えた。マウス10匹のもう一つの群には用量50μg/kg/週の対照オリゴヌクレオチドISIS141923を7週にわたって与えた。マウス10匹のもう一つの群にはPBSを7週にわたって投与し、それを対照群として、他のすべての群をこの対照群と比較した。最後の注射を行った48時間後に、最終エンドポイントを収集した。
プライマープローブセットRTS3430を用いるCFBのリアルタイムPCR用に、肝臓組織からRNAを抽出した。以下の表に示すとおり、ISIS516323は、PBS対照と比較してCFBを低減した。結果を、対照と比較したCFBの阻害パーセントとして表す。
腎病理を2つの方法で評価した。腎臓の組織切片をヘマトキシリンとエオシンで染色した。PBS対照は、糸球体硬化症の一症状である多数の糸球体半月体及び管状円柱(multiglomerular crescents tubular casts)の存在を示す。これに対し、ISIS516323で処置したマウスからの切片には、半月体及び管状円柱(crescents tubular casts)が存在せず、ボウマン嚢のごくわずかな線維性変化、中等度~重度の分節性メサンギウム細胞増殖及び糸球体基底膜肥厚を示した。
CFBの低減は代替補体経路の活性化を阻害する。これは、C3消費を防止し、血漿中C3レベルの見掛け上の上昇につながる。終末採血により、臨床分析装置で血漿中C3レベルを測定した。結果を以下の表に掲載する。これらの結果は、ISIS516323による処置が血漿中のC3レベルを対照群と比較して増加させたこと(p<0.001)を実証している。
CFHヘテロ接合(CFH Het,CFH+/-)マウスモデルは、突然変異型H因子タンパク質を完全長マウスタンパク質と共に発現する(Pickering,M.C.et al.,J.Exp.Med.2007.204:1249-56)。これらのマウスでは、6月齢までは腎組織構造が正常な状態を保っている。
6週齢のCFH+/-マウス各8匹の群に用量75mg/kg/週のISIS516323またはISIS516341を6週にわたって与えた。マウス8匹のもう一つの群には用量75mg/kg/週の対照オリゴヌクレオチドISIS141923を6週にわたって与えた。マウス8匹のもう一つの群にはPBSを6週にわたって投与し、それを対照群として、他のすべての群をこの対照群と比較した。最後の注射を行った48時間後に、最終エンドポイントを収集した。
プライマープローブセットRTS3430を用いるCFBのリアルタイムPCR分析用に、肝臓組織と腎臓組織からRNAを抽出した。以下の表に示すとおり、アンチセンスオ
リゴヌクレオチドは、PBS対照と比較して、CFBを低減した。結果を、対照と比較したCFBの阻害パーセントとして表す。
CFBの低減は代替補体経路の活性化を阻害する。これは、C3消費を防止し、血漿中C3レベルの見掛け上の上昇につながる。終末採血により、臨床分析装置で、血漿中C3レベルを測定した。結果を以下の表に掲載する。これらの結果は、ISIS516323による処置が血漿中のC3レベルを正常レベルまで増加させたことを実証している。
CFH+/-マウス各5匹の群に、用量12.5mg/kg/週、25mg/kg/週、50mg/kg/週、75mg/kg/週、または100mg/kg/週のISIS516323またはISIS516341を、6週にわたって与えた。マウス5匹のもう一つの群には用量75μg/kg/週の対照オリゴヌクレオチドISIS141923を6週にわたって与えた。マウス5匹のもう一つの群には、PBSを6週にわたって投与し、それを対照群として、他のすべての群をこの対照群と比較した。最後の注射を行った48時間後に、最終エンドポイントを収集した。
プライマープローブセットRTS3430を用いるCFBのリアルタイムPCR分析用に、肝臓組織と腎臓組織からRNAを抽出した。以下の表に示すとおり、前記アンチセンスオリゴヌクレオチドは、CFBをPBS対照と比較して用量依存的に低減した。結果を、対照と比較したCFBの阻害パーセントとして表す。
CFBの低減は代替補体経路の活性化を阻害する。これは、C3消費を防止し、血漿中C3レベルの見掛け上の上昇につながる。終末血漿収集により、臨床分析装置で血漿中C3レベルを測定した。結果を以下の表に掲載する。これらの結果は、CFBを標的とするISISオリゴヌクレオチドによる処置が、血漿中のC3レベルを増加させることを実証している。
カニクイザルを、上記実施例で述べた試験から選択したISISアンチセンスオリゴヌクレオチドで処置した。アンチセンスオリゴヌクレオチドの効力と耐容性、ならびに肝臓
及び腎臓におけるそれらの薬物動態プロファイルを評価した。
試験に先だって、サルを少なくとも30日間にわたって隔離し続け、その期間中は全身の健康状態について動物を毎日観察した。サルは2~4歳で、体重は2~4kgであった。ランダムに割り当てた雄カニクイザル各4~6匹の11群に対し、背中の四ヶ所に時計回りに(すなわち左、上、右、及び下)、ISISオリゴヌクレオチドまたはPBSを、各回1部位ずつ、皮下注射した。最初の1週間はサルに初回負荷量のPBSまたは40mg/kgのISIS532800、ISIS532809、ISIS588540、ISIS588544、ISIS588548、ISIS588550、ISIS588553、ISIS588555、ISIS588848、またはISIS594430を4回(1日目、3日目、5日目、及び7日目)与え、次にPBSまたは40mg/kgのISISオリゴヌクレオチドを、週1回、12週にわたって投与した(14日目、21日目、28日目、35日目、42日目、49日目、56日目、63日目、70日目、77日目、及び84日目)。ISIS532770は、2匹の雄カニクイザル及び2匹の雌カニクイザルを含む群による別個の試験において、類似する条件で調べた。
RNA分析
86日目に、肝臓試料及び腎臓試料を、二つ一組(それぞれ約250mg)にして、CFB mRNA分析用に採取した。屠殺から約10分以内の剖検時に試料を液体窒素中で急速冷凍した。
85日目に利用可能なすべての動物から約1mLの血液を採取して、EDTAのカリウム塩が入っているチューブに入れた。その血液試料を氷またはKryorackに直ちに入れ、遠心分離(3000rpm、4℃で10分間)することにより、採取から60分以内に血漿(約0.4mL)を得た。ポリクローナル抗B因子抗体を用いる放射状免疫拡散法(RID)により、CFBの血漿中レベルを血漿で測定した。結果を以下の表に掲載する。ISIS532770は別個の試験で調べ、その群では血漿中タンパク質レベルを91日目または92日目に測定した。
体重測定
動物の総合的健康に対するISISオリゴヌクレオチドの効果を評価するために、体重及び臓器重量を測定した。それを以下の表に掲載する。「*」は、当該オリゴヌクレオチドが別個の試験において類似の条件で調べられたこと、そして雄サルと雌サルから得られた測定値の平均であることを示す。これらの結果は、アンチセンスオリゴヌクレオチドによる処置が体重及び臓器重量に及ぼす効果は、アンチセンスオリゴヌクレオチドに予想される範囲内であったことを示している。
肝機能に対するISISオリゴヌクレオチドの効果を評価するために、すべての試験群から血液試料を集めた。血液試料は、橈側皮静脈、伏在静脈、または大腿静脈から、投薬の48時間後に集めた。採血に先だってサルを終夜絶食させた。血清を分離するために、抗凝固剤が入っていないチューブに血液(1.5mL)を集めた。そのチューブを最低90分間室温に保ってから、遠心分離(約3,000rpmで10分間)することにより、血清を得た。東芝200FR NEO化学分析装置(東芝、日本)を使って、さまざまな肝臓機能マーカーのレベルを測定した。
腎臓機能に対するISISオリゴヌクレオチドの効果を評価するために、すべての試験群から血液試料を集めた。血液試料は、橈側皮静脈、伏在静脈、または大腿静脈から、投薬の48時間後に集めた。採血に先だってサルを終夜絶食させた。血清を分離するために、抗凝固剤が入っていないチューブに血液を集めた。そのチューブを最低90分間室温に保ってから、遠心分離(約3,000rpmで10分間)することにより、血清を得た。東芝200FR NEO化学分析装置(東芝、日本)を使って、BUN及びクレアチニンのレベルを測定した。結果をmg/dLの単位で表して、以下の表に掲載する。「*」は、当該オリゴヌクレオチドが別個の試験において類似の条件で調べられたこと、そして雄サルと雌サルから得られた測定値の平均であることを示す。
カニクイザル中のISISオリゴヌクレオチドが血液学的パラメータに及ぼす影響を評価するために、利用可能な試験動物のそれぞれから、血液約0.5mLの血液試料を、K2-EDTAが入っているチューブに集めた。ADVIA120血液分析装置(Bayer、米国)を使って、試料を、赤血球(RBC)数、白血球(WBC)数、個別白血球数、例えば単球、好中球、リンパ球の数、ならびに血小板数、ヘモグロビン含量及びヘマトクリットについて分析した。データを以下の表に掲載する。「*」は、当該オリゴヌクレオチドが別個の試験において類似の条件で調べられたこと、そして雄サルと雌サルから得られた測定値の平均であることを示す。
を示している。
腎臓組織及び肝臓組織における完全長オリゴヌクレオチドの濃度を測定した。使用した方法は、以前に公表された方法(Leeds et al.,1996;Geary et al.,1999)の変法であり、フェノール-クロロホルム(液-液)抽出と、それに続く固相抽出からなる。組織試料中濃度は、定量下限(LLOQ)が約1.14μg/gである検量線を使って算出した。結果を、μg/g-肝臓または腎臓組織の単位で、以下の表に掲載する。
同じ核酸塩基配列を有する2つのアンチセンスオリゴヌクレオチド、すなわち非共役アンチセンスオリゴヌクレオチドISIS588540と、5’-THA-GalNAc3-共役アンチセンスオリゴヌクレオチドISIS696844とを、ヒトCFBトランスジェニックマウス(hCFB-Tgマウス)で調べた。
結果を以下の表に掲載する。これらの結果は、CFBを標的とする5’-THA-GalNAc3-共役アンチセンスオリゴヌクレオチドの方が同じ配列を持つ非共役アンチセンスオリゴヌクレオチドよりも強力であることを実証している。
肝臓mRNAレベルを、同mRNAの異なる領域を標的とする2つの異なるプライマープローブセットで測定し、RIBOGREEN(登録商標)(RGB)またはシクロフィリンのどちらかに対して標準化した。プライマープローブセットは上述のRTS3459、及びRTS3460(フォワード配列CGAAGCAGCTCAATGAAATCAA,本明細書では配列番号813と呼ぶ;リバース配列TGCCTGGAGGGCCTTC
TT,本明細書では配列番号814と呼ぶ;プローブ配列AGACCACAAGTTGAAGTC,本明細書では配列番号815と呼ぶ)であった。結果を以下の表に掲載する。これらの結果は、使用したプライマープローブセットとは無関係に、CFBを標的とする5’-THA-GalNAc3-共役アンチセンスオリゴヌクレオチドの方が同じ配列を持つ非共役アンチセンスオリゴヌクレオチドより強力であることを実証している。
〔項1〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号1の核酸塩基30~49、48~63、150~169、151~170、152~171、154~169、154~173、156~171、156~175、157~176、158~173、158~177、480~499、600~619、638~657、644~663、738~757、1089~1108、1135~1154、1141~1160、1147~1166、1150~1169、1153~1172、1159~1178、1162~1181、1165~1184、1171~1186、1171~1190、1173~1188、1173~1192、1175~1190、1175~1194、1177~1196、1183~1202、1208~1227、1235~1254、1298~1317、1304~1323、1310~1329、1316~1335、1319~1338、1322~1341、1328~
1347、1349~1368、1355~1374、1393~1412、1396~1415、1399~1418、1405~1424、1421~1440、1621~1640、1646~1665、1646~1665、1647~1666、1689~1708、1749~1768、1763~1782、1912~1931、2073~2092、2085~2104、2166~2185、2172~2191、2189~2208、2191~2210、2193~2212、2195~2210、2195~2214、2196~2215、2197~2212、2197~2216、2202~2221、2223~2238、2223~2242、2225~2240、2226~2245、2227~2242、2227~2246、2238~2257、2241~2260、2267~2286、2361~2380、2388~2407、2397~2416、2448~2467、2453~2472、2455~2474、2457~2472、2457~2476、2459~2474、2459~2478、2461~2476、2461~2480、2532~2551、2550~2569、2551~2566、2551~2570、2552~2568、2552~2570、2552~2571、2553~2568、2553~2570、2553~2571、2553~2572、2554~2571、2554~2572、2554~2573、2555~2570、2555~2572、2555~2574、2556~2573、2556~2574、2556~2575、2557~2573、2557~2574、2557~2575、2557~2576、2558~2575、2558~2576、2558~2577、2559~2576、2559~2577、2559~2578、2560~2577、2560~2578、2560~2579、2561~2576、2561~2578、2561~2579、2561~2580、2562~2577、2562~2579、2562~2581、2563~2578、2563~2580、2563~2582、2564~2581、2564~2583、2565~2584、2566~2583、2566~2585、2567~2582、2567~2584、2567~2586、2568~2583、2568~2585、2568~2587、2569~2586、2569~2588、2570~2585、2570~2587、2570~2589、2571~2586、2571~2588、2571~2590、2572~2589、2572~2590、2572~2591、2573~2590、2573~2592、2574~2590、2574~2591、2574~2593、2575~2590、2575~2591、2575~2592、2575~2594、2576~2593、2576~2595、2577~2594、2577~2595、2577~2596、2578~2594、2578~2596、2578~2597、2579~2598、2580~2596、2580~2597、2580~2598、2580~2599、2581~2597、2581~2598、2581~2599、2581~2600、2582~2598、2582~2599、2582~2600、2582~2601、2583~2599、2583~2600、2583~2601、2583~2602、2584~2600、2584~2601、2584~2602、2584~2603、2585~2601、2585~2603、2585~2604、2586~2601、2586~2602、2586~2604、2586~2605、2587~2602、2587~2603、2587~2605、2587~2606、2588~2603、2588~2604、2588~2605、2588~2606、2588~2607、2589~2604、2589~2605、2589~2606、2589~2607、2589~2608、2590~2605、2590~2606、2590~2607、2590~2608、2590~2609、2590~2609、2591~2607、2591~2608、2591~2609、2591~2610、2592~2607、2592~2608、2592~2609、2592~2610、2592~2611、2593~2608、2593~2609、2593~2610、2593~2612、2594~2609、2594~2610、2594~2611、2594~2612、2594~2613、2595~2610、2595~2611、2595~
2612、2595~2613、2595~2614、2596~2611、2596~2612、2596~2613、2596~2614、2596~2615、2597~2612、2597~2612、2597~2613、2597~2614、2597~2615、2597~2616、2598~2613、2598~2614、2598~2615、2598~2616、2598~2617、2599~2614、2599~2615、2599~2616、2599~2617、2599~2618、2600~2615、2600~2616、2600~2617、2600~2618、2600~2619、2601~2616、2601~2617、2601~2618、2601~2619、2601~2620、2602~2617、2602~2618、2602~2619、2602~2620、2602~2621、2603~2618、2603~2619、2603~2620、2603~2621、2603~2622、2604~2619、2604~2620、2604~2621、2604~2622、2604~2623、2605~2620、2605~2621、2605~2622、2605~2623、2605~2624、2606~2621、2606~2622、2606~2623、2606~2624、2606~2625、2607~2622、2607~2623、2607~2624、2607~2625、2607~2626、2608~2623、2608~2624、2608~2625、2608~2626、2608~2627、2609~2624、2609~2625、2609~2626、2609~2627、2609~2628、2610~2625、2610~2626、2610~2627、2610~2628、2610~2629、2611~2626、2611~2627、2611~2628、2611~2629、2611~2630、2612~2627、2612~2628、2612~2629、2612~2630、2612~2631、2613~2628、2613~2629、2613~2630、2613~2631、2614~2629、2614~2630、2614~2631、2615~2630、2615~2631、または2616~2631内で相補的な8~80個の連結されたヌクレオシドからなり、かつ該修飾オリゴヌクレオチドが、配列番号1に対して少なくとも85%、90%、95%、または100%相補的である、前記化合物。
〔項2〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号1の核酸塩基30~49、48~63、150~169、151~170、152~171、154~169、154~173、156~171、156~175、157~176、158~173、158~177、480~499、600~619、638~657、644~663、738~757、1089~1108、1135~1154、1141~1160、1147~1166、1150~1169、1153~1172、1159~1178、1162~1181、1165~1184、1171~1186、1171~1190、1173~1188、1173~1192、1175~1190、1175~1194、1177~1196、1183~1202、1208~1227、1235~1254、1298~1317、1304~1323、1310~1329、1316~1335、1319~1338、1322~1341、1328~1347、1349~1368、1355~1374、1393~1412、1396~1415、1399~1418、1405~1424、1421~1440、1621~1640、1646~1665、1646~1665、1647~1666、1689~1708、1749~1768、1763~1782、1912~1931、2073~2092、2085~2104、2166~2185、2172~2191、2189~2208、2191~2210、2193~2212、2195~2210、2195~2214、2196~2215、2197~2212、2197~2216、2202~2221、2223~2238、2223~2242、2225~2240、2226~2245、2227~2242、2227~2246、2238~2257、2241~2260、2267~2286、2361~2380、2388~2407、2397~2416、2448~2467、2453~2472、2455~2474、2457~
2472、2457~2476、2459~2474、2459~2478、2461~2476、2461~2480、2532~2551、2550~2569、2551~2566、2551~2570、2552~2568、2552~2570、2552~2571、2553~2568、2553~2570、2553~2571、2553~2572、2554~2571、2554~2572、2554~2573、2555~2570、2555~2572、2555~2574、2556~2573、2556~2574、2556~2575、2557~2573、2557~2574、2557~2575、2557~2576、2558~2575、2558~2576、2558~2577、2559~2576、2559~2577、2559~2578、2560~2577、2560~2578、2560~2579、2561~2576、2561~2578、2561~2579、2561~2580、2562~2577、2562~2579、2562~2581、2563~2578、2563~2580、2563~2582、2564~2581、2564~2583、2565~2584、2566~2583、2566~2585、2567~2582、2567~2584、2567~2586、2568~2583、2568~2585、2568~2587、2569~2586、2569~2588、2570~2585、2570~2587、2570~2589、2571~2586、2571~2588、2571~2590、2572~2589、2572~2590、2572~2591、2573~2590、2573~2592、2574~2590、2574~2591、2574~2593、2575~2590、2575~2591、2575~2592、2575~2594、2576~2593、2576~2595、2577~2594、2577~2595、2577~2596、2578~2594、2578~2596、2578~2597、2579~2598、2580~2596、2580~2597、2580~2598、2580~2599、2581~2597、2581~2598、2581~2599、2581~2600、2582~2598、2582~2599、2582~2600、2582~2601、2583~2599、2583~2600、2583~2601、2583~2602、2584~2600、2584~2601、2584~2602、2584~2603、2585~2601、2585~2603、2585~2604、2586~2601、2586~2602、2586~2604、2586~2605、2587~2602、2587~2603、2587~2605、2587~2606、2588~2603、2588~2604、2588~2605、2588~2606、2588~2607、2589~2604、2589~2605、2589~2606、2589~2607、2589~2608、2590~2605、2590~2606、2590~2607、2590~2608、2590~2609、2590~2609、2591~2607、2591~2608、2591~2609、2591~2610、2592~2607、2592~2608、2592~2609、2592~2610、2592~2611、2593~2608、2593~2609、2593~2610、2593~2612、2594~2609、2594~2610、2594~2611、2594~2612、2594~2613、2595~2610、2595~2611、2595~2612、2595~2613、2595~2614、2596~2611、2596~2612、2596~2613、2596~2614、2596~2615、2597~2612、2597~2612、2597~2613、2597~2614、2597~2615、2597~2616、2598~2613、2598~2614、2598~2615、2598~2616、2598~2617、2599~2614、2599~2615、2599~2616、2599~2617、2599~2618、2600~2615、2600~2616、2600~2617、2600~2618、2600~2619、2601~2616、2601~2617、2601~2618、2601~2619、2601~2620、2602~2617、2602~2618、2602~2619、2602~2620、2602~2621、2603~2618、2603~2619、2603~2620、2603~2621、2603~2622、2604~
2619、2604~2620、2604~2621、2604~2622、2604~2623、2605~2620、2605~2621、2605~2622、2605~2623、2605~2624、2606~2621、2606~2622、2606~2623、2606~2624、2606~2625、2607~2622、2607~2623、2607~2624、2607~2625、2607~2626、2608~2623、2608~2624、2608~2625、2608~2626、2608~2627、2609~2624、2609~2625、2609~2626、2609~2627、2609~2628、2610~2625、2610~2626、2610~2627、2610~2628、2610~2629、2611~2626、2611~2627、2611~2628、2611~2629、2611~2630、2612~2627、2612~2628、2612~2629、2612~2630、2612~2631、2613~2628、2613~2629、2613~2630、2613~2631、2614~2629、2614~2630、2614~2631、2615~2630、2615~2631、または2616~2631のうちの長さが等しい部分に100%相補的な少なくとも8個の連続する核酸塩基部分を含む核酸塩基配列を有する8~80個の連結されたヌクレオシドからなり、かつ前記修飾オリゴヌクレオチドの前記核酸塩基配列が、配列番号1に対して少なくとも85%、90%、95%、または100%相補的である、前記化合物。
〔項3〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号2の核酸塩基1608~1627、1685~1704、1686~1705、1751~1770、1769~1784、1871~1890、1872~1891、1873~1892、1875~1890、1875~1894、1877~1892、1877~1896、1878~1897、1879~1894、1879~1898、2288~2307、2808~2827、2846~2865、2852~2871、2946~2965、3773~3792、3819~3838、3825~3844、3831~3850、3834~3853、3837~3856、3843~3862、4151~4166、4151~4170、4153~4172、4159~4178、4184~4203、4211~4230、4609~4628、4612~4631、4615~4634、4621~4640、4642~4661、4648~4667、4686~4705、4689~4708、4692~4711、4698~4717、4714~4733、5270~5289、5295~5314、5296~5315、5830~5849、5890~5909、5904~5923、6406~6425、6662~6681、6674~6693、6954~6973、6960~6979、6977~6996、6979~6998、6981~7000、6983~6998、6983~7002、6984~7003、6985~7000、6985~7004、6990~7009、7122~7141、7125~7144、7151~7170、7353~7372、7362~7381、7683~7702、7688~7707、7690~7709、7692~7707、7692~7711、7694~7709、7694~7713、7696~7711、7696~7715、7767~7786、7785~7804、7786~7801、7787~7803、7787~7805、7787~7806、7788~7803、7788~7805、7788~7806、7788~7807、7789~7806、7789~7807、7789~7808、7790~7805、7790~7807、7790~7809、7791~7808、7791~7809、7791~7810、7792~7808、7792~7809、7792~7810、7792~7811、7793~7810、7793~7811、7793~7812、7794~7811、7794~7812、7794~7813、7795~7812、7795~7813、7795~7814、7796~7811、7796~7813、7796~7814、7796~7815、7797~7812、7797~7814、7797~7816、7798~7813、7798~78
15、7798~7817、7799~7816、7799~7818、7800~7819、7801~7818、7801~7820、7802~7817、7802~7819、7802~7821、7803~7818、7803~7820、7803~7822、7804~7821、7804~7823、7805~7820、7805~7822、7805~7824、7806~7821、7806~7823、7806~7825、7807~7824、7807~7825、7807~7826、7808~7825、7808~7827、7809~7825、7809~7826、7809~7828、7810~7825、7810~7826、7810~7827、7810~7829、7811~7828、7811~7830、7812~7829、7812~7830、7812~7831、7813~7829、7813~7831、7813~7832、7814~7833、7815~7831、7815~7832、7815~7833、7815~7834、7816~7832、7816~7833、7816~7834、7816~7835、7817~7833、7817~7834、7817~7835、7817~7836、7818~7834、7818~7835、7818~7836、7818~7837、7819~7835、7819~7836、7819~7837、7819~7838、7820~7836、7820~7838、7820~7839、7821~7836、7821~7837、7821~7839、7821~7840、7822~7837、7822~7838、7822~7840、7822~7841、7823~7838、7823~7839、7823~7839、7823~7840、7823~7841、7823~7842、7824~7839、7824~7840、7824~7840、7824~7841、7824~7842、7824~7843、7825~7840、7825~7841、7825~7842、7825~7843、7825~7844、7826~7842、7826~7843、7826~7844、7826~7845、7827~7842、7827~7843、7827~7844、7827~7845、7827~7846、7828~7843、7828~7844、7828~7845、7828~7847、7829~7844、7829~7845、7829~7846、7829~7847、7829~7848、7830~7845、7830~7846、7830~7847、7830~7848、7830~7849、7831~7846、7831~7847、7831~7848、7831~7849、7831~7850、7832~7847、7832~7848、7832~7849、7832~7850、7832~7851、7833~7848、7833~7849、7833~7850、7833~7851、7833~7852、7834~7849、7834~7850、7834~7851、7834~7852、7834~7853、7835~7850、7835~7851、7835~7852、7835~7853、7835~7854、7836~7851、7836~7852、7836~7853、7836~7854、7836~7855、7837~7852、7837~7853、7837~7854、7837~7855、7837~7856、7838~7853、7838~7854、7838~7855、7838~7856、7838~7857、7839~7854、7839~7855、7839~7856、7839~7857、7839~7858、7840~7855、7840~7856、7840~7857、7840~7858、7840~7859、7841~7856、7841~7857、7841~7858、7841~7859、7841~7860、7842~7857、7842~7858、7842~7859、7842~7860、7842~7861、7843~7858、7843~7859、7843~7860、7843~7861、7843~7862、7844~7859、7844~7860、7844~7861、7844~7862、7845~7860、7845~7861、7845~7862、7846~7861、または7846~7862内で相補的な8~80個の連結されたヌクレオシドからなり、かつ該修飾オリゴヌクレオチドが、配列番号2に対して少なくとも85%、90%、95%、または100%相補的である、前記化合物。
〔項4〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号2の核酸塩基1608~1627、1685~1704、1686~1705、1751~1770、1769~1784、1871~1890、1872~1891、1873~1892、1875~1890、1875~1894、1877~1892、1877~1896、1878~1897、1879~1894、1879~1898、2288~2307、2808~2827、2846~2865、2852~2871、2946~2965、3773~3792、3819~3838、3825~3844、3831~3850、3834~3853、3837~3856、3843~3862、4151~4166、4151~4170、4153~4172、4159~4178、4184~4203、4211~4230、4609~4628、4612~4631、4615~4634、4621~4640、4642~4661、4648~4667、4686~4705、4689~4708、4692~4711、4698~4717、4714~4733、5270~5289、5295~5314、5296~5315、5830~5849、5890~5909、5904~5923、6406~6425、6662~6681、6674~6693、6954~6973、6960~6979、6977~6996、6979~6998、6981~7000、6983~6998、6983~7002、6984~7003、6985~7000、6985~7004、6990~7009、7122~7141、7125~7144、7151~7170、7353~7372、7362~7381、7683~7702、7688~7707、7690~7709、7692~7707、7692~7711、7694~7709、7694~7713、7696~7711、7696~7715、7767~7786、7785~7804、7786~7801、7787~7803、7787~7805、7787~7806、7788~7803、7788~7805、7788~7806、7788~7807、7789~7806、7789~7807、7789~7808、7790~7805、7790~7807、7790~7809、7791~7808、7791~7809、7791~7810、7792~7808、7792~7809、7792~7810、7792~7811、7793~7810、7793~7811、7793~7812、7794~7811、7794~7812、7794~7813、7795~7812、7795~7813、7795~7814、7796~7811、7796~7813、7796~7814、7796~7815、7797~7812、7797~7814、7797~7816、7798~7813、7798~7815、7798~7817、7799~7816、7799~7818、7800~7819、7801~7818、7801~7820、7802~7817、7802~7819、7802~7821、7803~7818、7803~7820、7803~7822、7804~7821、7804~7823、7805~7820、7805~7822、7805~7824、7806~7821、7806~7823、7806~7825、7807~7824、7807~7825、7807~7826、7808~7825、7808~7827、7809~7825、7809~7826、7809~7828、7810~7825、7810~7826、7810~7827、7810~7829、7811~7828、7811~7830、7812~7829、7812~7830、7812~7831、7813~7829、7813~7831、7813~7832、7814~7833、7815~7831、7815~7832、7815~7833、7815~7834、7816~7832、7816~7833、7816~7834、7816~7835、7817~7833、7817~7834、7817~7835、7817~7836、7818~7834、7818~7835、7818~7836、7818~7837、7819~7835、7819~7836、7819~7837、7819~7838、7820~7836、7820~7838、7820~7839、7821~7836、7821~7837、7821~7839、7821~7840、7822~7837、7822~7838、7822~7840、7822~7841、7823~7838、7823~7839、7823~7839、7823~78
40、7823~7841、7823~7842、7824~7839、7824~7840、7824~7840、7824~7841、7824~7842、7824~7843、7825~7840、7825~7841、7825~7842、7825~7843、7825~7844、7826~7842、7826~7843、7826~7844、7826~7845、7827~7842、7827~7843、7827~7844、7827~7845、7827~7846、7828~7843、7828~7844、7828~7845、7828~7847、7829~7844、7829~7845、7829~7846、7829~7847、7829~7848、7830~7845、7830~7846、7830~7847、7830~7848、7830~7849、7831~7846、7831~7847、7831~7848、7831~7849、7831~7850、7832~7847、7832~7848、7832~7849、7832~7850、7832~7851、7833~7848、7833~7849、7833~7850、7833~7851、7833~7852、7834~7849、7834~7850、7834~7851、7834~7852、7834~7853、7835~7850、7835~7851、7835~7852、7835~7853、7835~7854、7836~7851、7836~7852、7836~7853、7836~7854、7836~7855、7837~7852、7837~7853、7837~7854、7837~7855、7837~7856、7838~7853、7838~7854、7838~7855、7838~7856、7838~7857、7839~7854、7839~7855、7839~7856、7839~7857、7839~7858、7840~7855、7840~7856、7840~7857、7840~7858、7840~7859、7841~7856、7841~7857、7841~7858、7841~7859、7841~7860、7842~7857、7842~7858、7842~7859、7842~7860、7842~7861、7843~7858、7843~7859、7843~7860、7843~7861、7843~7862、7844~7859、7844~7860、7844~7861、7844~7862、7845~7860、7845~7861、7845~7862、7846~7861、及び7846~7862のうちの長さが等しい部分に100%相補的な少なくとも8個の連続する核酸塩基部分を含む核酸塩基配列を有する8~80個の連結されたヌクレオシドからなり、かつ前記修飾オリゴヌクレオチドの前記核酸塩基配列は、配列番号2に対して少なくとも85%、90%、95%、または100%相補的である、前記化合物。
〔項5〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドがCFB核酸の3’UTRを標的とする、前記化合物。
〔項6〕
前記修飾オリゴヌクレオチドが、配列番号1の核酸塩基配列を有するCFB核酸のヌクレオチド2574~2626内を標的とする、請求項5に記載の化合物。
〔項7〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドは、配列番号1の核酸塩基配列を有するCFB核酸の核酸塩基2457~2631、2457~2472、2457~2474、2457~2476、2457~2566、2457~2570、2457~2571、2457~2572、2457~2573、2457~2574、2457~2575、2457~2576、2457~2577、2457~2578、2457~2579、2457~2580、2457~2581、2457~2582、2457~2583、2457~2584、2457~2585、2457~2586、2457~2587、2457~2588、2457~2589、2457~2590、2457~2591、2457~2592、2457~2593、2457~2594、2457~2595、2457~2596、2457~2597、2457~2598、2457~2599、2457~2600、2457~2601、2
457~2602、2457~2603、2457~2604、2457~2605、2457~2606、2457~2607、2457~2608、2457~2609、2457~2610、2457~2611、2457~2612、2457~2613、2457~2614、2457~2615、2457~2616、2457~2617、2457~2618、2457~2619、2457~2620、2457~2621、2457~2622、2457~2623、2457~2624、2457~2625、2457~2626、2457~2627、2457~2628、2457~2629、2457~2630、2457~2631、2459~2474、2459~2476、2459~2566、2459~2570、2459~2571、2459~2572、2459~2573、2459~2574、2459~2575、2459~2576、2459~2577、2459~2578、2459~2579、2459~2580、2459~2581、2459~2582、2459~2583、2459~2584、2459~2585、2459~2586、2459~2587、2459~2588、2459~2589、2459~2590、2459~2591、2459~2592、2459~2593、2459~2594、2459~2595、2459~2596、2459~2597、2459~2598、2459~2599、2459~2600、2459~2601、2459~2602、2459~2603、2459~2604、2459~2605、2459~2606、2459~2607、2459~2608、2459~2609、2459~2610、2459~2611、2459~2612、2459~2613、2459~2614、2459~2615、2459~2616、2459~2617、2459~2618、2459~2619、2459~2620、2459~2621、2459~2622、2459~2623、2459~2624、2459~2625、2459~2626、2459~2627、2459~2628、2459~2629、2459~2630、2459~2631、2461~2476、2461~2566、2461~2570、2461~2571、2461~2572、2461~2573、2461~2574、2461~2575、2461~2576、2461~2577、2461~2578、2461~2579、2461~2580、2461~2581、2461~2582、2461~2583、2461~2584、2461~2585、2461~2586、2461~2587、2461~2588、2461~2589、2461~2590、2461~2591、2461~2592、2461~2593、2461~2594、2461~2595、2461~2596、2461~2597、2461~2598、2461~2599、2461~2600、2461~2601、2461~2602、2461~2603、2461~2604、2461~2605、2461~2606、2461~2607、2461~2608、2461~2609、2461~2610、2461~2611、2461~2612、2461~2613、2461~2614、2461~2615、2461~2616、2461~2617、2461~2618、2461~2619、2461~2620、2461~2621、2461~2622、2461~2623、2461~2624、2461~2625、2461~2626、2461~2627、2461~2628、2461~2629、2461~2630、2461~2631、2551~2566、2551~2570、2551~2571、2551~2572、2551~2573、2551~2574、2551~2575、2551~2576、2551~2577、2551~2578、2551~2579、2551~2580、2551~2581、2551~2582、2551~2583、2551~2584、2551~2585、2551~2586、2551~2587、2551~2588、2551~2589、2551~2590、2551~2591、2551~2592、2551~2593、2551~2594、2551~2595、2551~2596、2551~2597、2551~2598、2551~2599、2551~2600、2551~2601、2551~2602、2551~2603、2551~2604、2551~2605、2551~2606、2551~2607、2551~2608、2551~2609、2
551~2610、2551~2611、2551~2612、2551~2613、2551~2614、2551~2615、2551~2616、2551~2617、2551~2618、2551~2619、2551~2620、2551~2621、2551~2622、2551~2623、2551~2624、2551~2625、2551~2626、2551~2627、2551~2628、2551~2629、2551~2630、2551~2631、2553~2570、2553~2571、2553~2572、2553~2573、2553~2574、2553~2575、2553~2576、2553~2577、2553~2578、2553~2579、2553~2580、2553~2581、2553~2582、2553~2583、2553~2584、2553~2585、2553~2586、2553~2587、2553~2588、2553~2589、2553~2590、2553~2591、2553~2592、2553~2593、2553~2594、2553~2595、2553~2596、2553~2597、2553~2598、2553~2599、2553~2600、2553~2601、2553~2602、2553~2603、2553~2604、2553~2605、2553~2606、2553~2607、2553~2608、2553~2609、2553~2610、2553~2611、2553~2612、2553~2613、2553~2614、2553~2615、2553~2616、2553~2617、2553~2618、2553~2619、2553~2620、2553~2621、2553~2622、2553~2623、2553~2624、2553~2625、2553~2626、2553~2627、2553~2628、2553~2629、2553~2630、2553~2631、2554~2573、2554~2574、2554~2575、2554~2576、2554~2577、2554~2578、2554~2579、2554~2580、2554~2581、2554~2582、2554~2583、2554~2584、2554~2585、2554~2586、2554~2587、2554~2588、2554~2589、2554~2590、2554~2591、2554~2592、2554~2593、2554~2594、2554~2595、2554~2596、2554~2597、2554~2598、2554~2599、2554~2600、2554~2601、2554~2602、2554~2603、2554~2604、2554~2605、2554~2606、2554~2607、2554~2608、2554~2609、2554~2610、2554~2611、2554~2612、2554~2613、2554~2614、2554~2615、2554~2616、2554~2617、2554~2618、2554~2619、2554~2620、2554~2621、2554~2622、2554~2623、2554~2624、2554~2625、2554~2626、2554~2627、2554~2628、2554~2629、2554~2630、2554~2631、2555~2572、2555~2573、2555~2574、2555~2575、2555~2576、2555~2577、2555~2578、2555~2579、2555~2580、2555~2581、2555~2582、2555~2583、2555~2584、2555~2585、2555~2586、2555~2587、2555~2588、2555~2589、2555~2590、2555~2591、2555~2592、2555~2593、2555~2594、2555~2595、2555~2596、2555~2597、2555~2598、2555~2599、2555~2600、2555~2601、2555~2602、2555~2603、2555~2604、2555~2605、2555~2606、2555~2607、2555~2608、2555~2609、2555~2610、2555~2611、2555~2612、2555~2613、2555~2614、2555~2615、2555~2616、2555~2617、2555~2618、2555~2619、2555~2620、2555~2621、2555~2622、2555~2623、2555~2624、2555~2625、2555~2626、2555~2627、2555~2628、2
555~2629、2555~2630、2555~2631、2556~2573、2556~2574、2556~2575、2556~2576、2556~2577、2556~2578、2556~2579、2556~2580、2556~2581、2556~2582、2556~2583、2556~2584、2556~2585、2556~2586、2556~2587、2556~2588、2556~2589、2556~2590、2556~2591、2556~2592、2556~2593、2556~2594、2556~2595、2556~2596、2556~2597、2556~2598、2556~2599、2556~2600、2556~2601、2556~2602、2556~2603、2556~2604、2556~2605、2556~2606、2556~2607、2556~2608、2556~2609、2556~2610、2556~2611、2556~2612、2556~2613、2556~2614、2556~2615、2556~2616、2556~2617、2556~2618、2556~2619、2556~2620、2556~2621、2556~2622、2556~2623、2556~2624、2556~2625、2556~2626、2556~2627、2556~2628、2556~2629、2556~2630、2556~2631、2557~2574、2557~2575、2557~2576、2557~2577、2557~2578、2557~2579、25
57~2580、2557~2581、2557~2582、2557~2583、2557~2584、2557~2585、2557~2586、2557~2587、2557~2588、2557~2589、2557~2590、2557~2591、2557~2592、2557~2593、2557~2594、2557~2595、2557~2596、2557~2597、2557~2598、2557~2599、2557~2600、2557~2601、2557~2602、2557~2603、2557~2604、2557~2605、2557~2606、2557~2607、2557~2608、2557~2609、2557~2610、2557~2611、2557~2612、2557~2613、2557~2614、2557~2615、2557~2616、2557~2617、2557~2618、2557~2619、2557~2620、2557~2621、2557~2622、2557~2623、2557~2624、2557~2625、2557~2626、2557~2627、2557~2628、2557~2629、2557~2630、2557~2631、2558~2575、2558~2576、2558~2577、2558~2578、2558~2579、2558~2580、2558~2581、2558~2582、2558~2583、2558~2584、2558~2585、2558~2586、2558~2587、2558~2588、2558~2589、2558~2590、2558~2591、2558~2592、2558~2593、2558~2594、2558~2595、2558~2596、2558~2597、2558~2598、2558~2599、2558~2600、2558~2601、2558~2602、2558~2603、2558~2604、2558~2605、2558~2606、2558~2607、2558~2608、2558~2609、2558~2610、2558~2611、2558~2612、2558~2613、2558~2614、2558~2615、2558~2616、2558~2617、2558~2618、2558~2619、2558~2620、2558~2621、2558~2622、2558~2623、2558~2624、2558~2625、2558~2626、2558~2627、2558~2628、2558~2629、2558~2630、2558~2631、2559~2576、2559~2577、2559~2578、2559~2579、2559~2580、2559~2581、2559~2582、2559~2583、2559~2584、2559~2585、2559~2586、25
59~2587、2559~2588、2559~2589、2559~2590、2559~2591、2559~2592、2559~2593、2559~2594、2559~2595、2559~2596、2559~2597、2559~2598、2559~2599、2559~2600、2559~2601、2559~2602、2559~2603、2559~2604、2559~2605、2559~2606、2559~2607、2559~2608、2559~2609、2559~2610、2559~2611、2559~2612、2559~2613、2559~2614、2559~2615、2559~2616、2559~2617、2559~2618、2559~2619、2559~2620、2559~2621、2559~2622、2559~2623、2559~2624、2559~2625、2559~2626、2559~2627、2559~2628、2559~2629、2559~2630、2559~2631、2560~2577、2560~2578、2560~2579、2560~2580、2560~2581、2560~2582、2560~2583、2560~2584、2560~2585、2560~2586、2560~2587、2560~2588、2560~2589、2560~2590、2560~2591、2560~2592、2560~2593、2560~2594、2560~2595、2560~2596、2560~2597、2560~2598、2560~2599、2560~2600、2560~2601、2560~2602、2560~2603、2560~2604、2560~2605、2560~2606、2560~2607、2560~2608、2560~2609、2560~2610、2560~2611、2560~2612、2560~2613、2560~2614、2560~2615、2560~2616、2560~2617、2560~2618、2560~2619、2560~2620、2560~2621、2560~2622、2560~2623、2560~2624、2560~2625、2560~2626、2560~2627、2560~2628、2560~2629、2560~2630、2560~2631、2561~2578、2561~2579、2561~2580、2561~2581、2561~2582、2561~2583、2561~2584、2561~2585、2561~2586、2561~2587、2561~2588、2561~2589、2561~2590、2561~2591、2561~2592、2561~2593、2561~2594、2561~2595、2561~2596、2561~2597、2561~2598、2561~2599、2561~2600、2561~2601、2561~2602、2561~2603、2561~2604、2561~2605、2561~2606、2561~2607、2561~2608、2561~2609、2561~2610、2561~2611、2561~2612、2561~2613、2561~2614、2561~2615、2561~2616、2561~2617、2561~2618、2561~2619、2561~2620、2561~2621、2561~2622、2561~2623、2561~2624、2561~2625、2561~2626、2561~2627、2561~2628、2561~2629、2561~2630、2561~2631、2562~2577、2562~2578、2562~2579、2562~2580、2562~2581、2562~2582、2562~2583、2562~2584、2562~2585、2562~2586、2562~2587、2562~2588、2562~2589、2562~2590、2562~2591、2562~2592、2562~2593、2562~2594、2562~2595、2562~2596、2562~2597、2562~2598、2562~2599、2562~2600、2562~2601、2562~2602、2562~2603、2562~2604、2562~2605、2562~2606、2562~2607、2562~2608、2562~2609、2562~2610、2562~2611、2562~2612、2562~2613、2562~2614、2562~2615、2562~2616、2562~2617、2562~2618、2562~2619、2562~2620、2562~2621、2562~2622、25
62~2623、2562~2624、2562~2625、2562~2626、2562~2627、2562~2628、2562~2629、2562~2630、2562~2631、2563~2580、2563~2581、2563~2582、2563~2583、2563~2584、2563~2585、2563~2586、2563~2587、2563~2588、2563~2589、2563~2590、2563~2591、2563~2592、2563~2593、2563~2594、2563~2595、2563~2596、2563~2597、2563~2598、2563~2599、2563~2600、2563~2601、2563~2602、2563~2603、2563~2604、2563~2605、2563~2606、2563~2607、2563~2608、2563~2609、2563~2610、2563~2611、2563~2612、2563~2613、2563~2614、2563~2615、2563~2616、2563~2617、2563~2618、2563~2619、2563~2620、2563~2621、2563~2622、2563~2623、2563~2624、2563~2625、2563~2626、2563~2627、2563~2628、2563~2629、2563~2630、2563~2631、2564~2581、2564~2582、2564~2583、2564~2584、2564~2585、2564~2586、2564~2587、2564~2588、2564~2589、2564~2590、2564~2591、2564~2592、2564~2593、2564~2594、2564~2595、2564~2596、2564~2597、2564~2598、2564~2599、2564~2600、2564~2601、2564~2602、2564~2603、2564~2604、2564~2605、2564~2606、2564~2607、2564~2608、2564~2609、2564~2610、2564~2611、2564~2612、2564~2613、2564~2614、2564~2615、2564~2616、2564~2617、2564~2618、2564~2619、2564~2620、2564~2621、2564~2622、2564~2623、2564~2624、2564~2625、2564~2626、2564~2627、2564~2628、2564~2629、2564~2630、2564~2631、2565~2584、2565~2585、2565~2586、2565~2587、2565~2588、2565~2589、2565~2590、2565~2591、2565~2592、2565~2593、2565~2594、2565~2595、2565~2596、2565~2597、2565~2598、2565~2599、2565~2600、2565~2601、2565~2602、2565~2603、2565~2604、2565~2605、2565~2606、2565~2607、2565~2608、2565~2609、2565~2610、2565~2611、2565~2612、2565~2613、2565~2614、2565~2615、2565~2616、2565~2617、2565~2618、2565~2619、2565~2620、2565~2621、2565~2622、2565~2623、2565~2624、2565~2625、2565~2626、2565~2627、2565~2628、2565~2629、2565~2630、2565~2631、2566~2583、2566~2584、2566~2585、2566~2586、2566~2587、2566~2588、2566~2589、2566~2590、2566~2591、2566~2592、2566~2593、2566~2594、2566~2595、2566~2596、2566~2597、2566~2598、2566~2599、2566~2600、2566~2601、2566~2602、2566~2603、2566~2604、2566~2605、2566~2606、2566~2607、2566~2608、2566~2609、2566~2610、2566~2611、2566~2612、2566~2613、2566~2614、256
6~2615、2566~2616、2566~2617、2566~2618、2566~2619、2566~2620、2566~2621、2566~2622、2566~2623、2566~2624、2566~2625、2566~2626、2566~2627、2566~2628、2566~2629、2566~2630、2566~2631、2567~2584、2567~2585、2567~2586、2567~2587、2567~2588、2567~2589、2567~2590、2567~2591、2567~2592、2567~2593、2567~2594、2567~2595、2567~2596、2567~2597、2567~2598、2567~2599、2567~2600、2567~2601、2567~2602、2567~2603、2567~2604、2567~2605、2567~2606、2567~2607、2567~2608、2567~2609、2567~2610、2567~2611、2567~2612、2567~2613、2567~2614、2567~2615、2567~2616、2567~2617、2567~2618、2567~2619、2567~2620、2567~2621、2567~2622、2567~2623、2567~2624、2567~2625、2567~2626、2567~2627、2567~2628、2567~2629、2567~2630、2567~2631、2568~2585、2568~2586、2568~2587、2568~2588、2568~2589、2568~2590、2568~2591、2568~2592、2568~2593、2568~2594、2568~2595、2568~2596、2568~2597、2568~2598、2568~2599、2568~2600、2568~2601、2568~2602、2568~2603、2568~2604、2568~2605、2568~2606、2568~2607、2568~2608、2568~2609、2568~2610、2568~2611、2568~2612、2568~2613、2568~2614、2568~2615、2568~2616、2568~2617、2568~2618、2568~2619、2568~2620、2568~2621、2568~2622、2568~2623、2568~2624、2568~2625、2568~2626、2568~2627、2568~2628、2568~2629、2568~2630、2568~2631、2569~2586、2569~2587、2569~2588、2569~2589、2569~2590、2569~2591、2569~2592、2569~2593、2569~2594、2569~2595、2569~2596、2569~2597、2569~2598、2569~2599、2569~2600、2569~2601、2569~2602、2569~2603、2569~2604、2569~2605、2569~2606、2569~2607、2569~2608、2569~2609、2569~2610、2569~2611、2569~2612、2569~2613、2569~2614、2569~2615、2569~2616、2569~2617、2569~2618、2569~2619、2569~2620、2569~2621、2569~2622、2569~2623、2569~2624、2569~2625、2569~2626、2569~2627、2569~2628、2569~2629、2569~2630、2569~2631、2569~2586、2569~2587、2569~2588、2569~2589、2569~2590、2569~2591、2569~2592、2569~2593、2569~2594、2569~2595、2569~2596、2569~2597、2569~2598、2569~2599、2569~2600、2569~2601、2569~2602、2569~2603、2569~2604、2569~2605、2569~2606、2569~2607、2569~2608、2569~2609、2569~2610、2569~2611、2569~2612、2569~2613、2569~2614、2569~2615、2569~2616、2569~2617、2569~2618、2569~2619、2569~2620、2569~2621、2569~2622、2569~2623、256
9~2624、2569~2625、2569~2626、2569~2627、2569~2628、2569~2629、2569~2630、2569~2631、2571~2588、2571~2589、2571~2590、2571~2591、2571~2592、2571~2593、2571~2594、2571~2595、2571~2596、2571~2597、2571~2598、2571~2599、2571~2600、2571~2601、2571~2602、2571~2603、2571~2604、2571~2605、2571~2606、2571~2607、2571~2608、2571~2609、2571~2610、2571~2611、2571~2612、2571~2613、2571~2614、2571~2615、2571~2616、2571~2617、2571~2618、2571~2619、2571~2620、2571~2621、2571~2622、2571~2623、2571~2624、2571~2625、2571~2626、2571~2627、2571~2628、2571~2629、2571~2630、2571~2631、2572~2589、2572~2590、2572~2591、2572~2592、2572~2593、2572~2594、2572~2595、2572~2596、2572~2597、2572~2598、2572~2599、2572~2600、2572~2601、2572~2602、2572~2603、2572~2604、2572~2605、2572~2606、2572~2607、2572~2608、2572~2609、2572~2610、2572~2611、2572~2612、2572~2613、2572~2614、2572~2615、2572~2616、2572~2617、2572~2618、2572~2619、2572~2620、2572~2621、2572~2622、2572~2623、2572~2624、2572~2625、2572~2626、2572~2627、2572~2628、2572~2629、2572~2630、2572~2631、2573~2590、2573~2591、2573~2592、2573~2593、2573~2594、2573~2595、2573~2596、2573~2597、2573~2598、2573~2599、2573~2600、2573~2601、2573~2602、2573~2603、2573~2604、2573~2605、2573~2606、2573~2607、2573~2608、2573~2609、2573~2610、2573~2611、2573~2612、2573~2613、2573~2614、2573~2615、2573~2616、2573~2617、2573~2618、2573~2619、2573~2620、2573~2621、2573~2622、2573~2623、2573~2624、2573~2625、2573~2626、2573~2627、2573~2628、2573~2629、2573~2630、2573~2631、2574~2591、2574~2592、2574~2593、2574~2594、2574~2595、2574~2596、2574~2597、2574~2598、2574~2599、2574~2600、2574~2601、2574~2602、2574~2603、2574~2604、2574~2605、2574~2606、2574~2607、2574~2608、2574~2609、2574~2610、2574~2611、2574~2612、2574~2613、2574~2614、2574~2615、2574~2616、2574~2617、2574~2618、2574~2619、2574~2620、2574~2621、2574~2622、2574~2623、2574~2624、2574~2625、2574~2626、2574~2627、2574~2628、2574~2629、2574~2630、2574~2631、2575~2592、2575~2593、2575~2594、2575~2595、2575~2596、2575~2597、2575~2598、2575~2599、2575~2600、2575~2601、2575~2602、2575~2603、2575~2604、2575~2605、2575~2606、2575~2607、2575~2608、2575~2609、2575~2610、2575~2611、2575~2612、2575~2613、257
5~2614、2575~2615、2575~2616、2575~2617、2575~2618、2575~2619、2575~2620、2575~2621、2575~2622、2575~2623、2575~2624、2575~2625、2575~2626、2575~2627、2575~2628、2575~2629、2575~2630、2575~2631、2576~2593、2576~2594、2576~2595、2576~2596、2576~2597、2576~2598、2576~2599、2576~2600、2576~2601、2576~2602、2576~2603、2576~2604、2576~2605、2576~2606、2576~2607、2576~2608、2576~2609、2576~2610、2576~2611、2576~2612、2576~2613、2576~2614、2576~2615、2576~2616、2576~2617、2576~2618、2576~2619、2576~2620、2576~2621、2576~2622、2576~2623、2576~2624、2576~2625、2576~2626、2576~2627、2576~2628、2576~2629、2576~2630、2576~2631、2577~2594、2577~2595、2577~2596、2577~2597、2577~2598、2577~2599、2577~2600、2577~2601、2577~2602、2577~2603、2577~2604、2577~2605、2577~2606、2577~2607、2577~2608、2577~2609、2577~2610、2577~2611、2577~2612、2577~2613、2577~2614、2577~2615、2577~2616、2577~2617、2577~2618、2577~2619、2577~2620、2577~2621、2577~2622、2577~2623、2577~2624、2577~2625、2577~2626、2577~2627、2577~2628、2577~2629、2577~2630、2577~2631、2578~2597、2578~2598、2578~2599、2578~2600、2578~2601、2578~2602、2578~2603、2578~2604、2578~2605、2578~2606、2578~2607、2578~2608、2578~2609、2578~2610、2578~2611、2578~2612、2578~2613、2578~2614、2578~2615、2578~2616、2578~2617、2578
~2618、2578~2619、2578~2620、2578~2621、2578~2622、2578~2623、2578~2624、2578~2625、2578~2626、2578~2627、2578~2628、2578~2629、2578~2630、2578~2631、2579~2598、2579~2599、2579~2600、2579~2601、2579~2602、2579~2603、2579~2604、2579~2605、2579~2606、2579~2607、2579~2608、2579~2609、2579~2610、2579~2611、2579~2612、2579~2613、2579~2614、2579~2615、2579~2616、2579~2617、2579~2618、2579~2619、2579~2620、2579~2621、2579~2622、2579~2623、2579~2624、2579~2625、2579~2626、2579~2627、2579~2628、2579~2629、2579~2630、2579~2631、2580~2598、2580~2599、2580~2600、2580~2601、2580~2602、2580~2603、2580~2604、2580~2605、2580~2606、2580~2607、2580~2608、2580~2609、2580~2610、2580~2611、2580~2612、2580~2613、2580~2614、2580~2615、2580~2616、2580~2617、2580~2618、2580~2619、2580~2620、2580~2621、2580
~2622、2580~2623、2580~2624、2580~2625、2580~2626、2580~2627、2580~2628、2580~2629、2580~2630、2580~2631、2581~2597、2581~2598、2581~2599、2581~2600、2581~2601、2581~2602、2581~2603、2581~2604、2581~2605、2581~2606、2581~2607、2581~2608、2581~2609、2581~2610、2581~2611、2581~2612、2581~2613、2581~2614、2581~2615、2581~2616、2581~2617、2581~2618、2581~2619、2581~2620、2581~2621、2581~2622、2581~2623、2581~2624、2581~2625、2581~2626、2581~2627、2581~2628、2581~2629、2581~2630、2581~2631、2582~2600、2582~2601、2582~2602、2582~2603、2582~2604、2582~2605、2582~2606、2582~2607、2582~2608、2582~2609、2582~2610、2582~2611、2582~2612、2582~2613、2582~2614、2582~2615、2582~2616、2582~2617、2582~2618、2582~2619、2582~2620、2582~2621、2582~2622、2582~2623、2582~2624、2582~2625、2582~2626、2582~2627、2582~2628、2582~2629、2582~2630、2582~2631、2583~2601、2583~2602、2583~2603、2583~2604、2583~2605、2583~2606、2583~2607、2583~2608、2583~2609、2583~2610、2583~2611、2583~2612、2583~2613、2583~2614、2583~2615、2583~2616、2583~2617、2583~2618、2583~2619、2583~2620、2583~2621、2583~2622、2583~2623、2583~2624、2583~2625、2583~2626、2583~2627、2583~2628、2583~2629、2583~2630、2583~2631、2585~2603、2585~2604、2585~2605、2585~2606、2585~2607、2585~2608、2585~2609、2585~2610、2585~2611、2585~2612、2585~2613、2585~2614、2585~2615、2585~2616、2585~2617、2585~2618、2585~2619、2585~2620、2585~2621、2585~2622、2585~2623、2585~2624、2585~2625、2585~2626、2585~2627、2585~2628、2585~2629、2585~2630、2585~2631、2586~2604、2586~2605、2586~2606、2586~2607、2586~2608、2586~2609、2586~2610、2586~2611、2586~2612、2586~2613、2586~2614、2586~2615、2586~2616、2586~2617、2586~2618、2586~2619、2586~2620、2586~2621、2586~2622、2586~2623、2586~2624、2586~2625、2586~2626、2586~2627、2586~2628、2586~2629、2586~2630、2586~2631、2587~2605、2587~2606、2587~2607、2587~2608、2587~2609、2587~2610、2587~2611、2587~2612、2587~2613、2587~2614、2587~2615、2587~2616、2587~2617、2587~2618、2587~2619、2587~2620、2587~2621、2587~2622、2587~2623、2587~2624、2587~2625、2587~2626、2587~2627、2587~2628、2587~2629、2587~2630、2587~2631、2588~2606、2588~2607、2588~2608、2588~2609、2588~2610、2588~2611、2588~2612、2588~2613、2588
~2614、2588~2615、2588~2616、2588~2617、2588~2618、2588~2619、2588~2620、2588~2621、2588~2622、2588~2623、2588~2624、2588~2625、2588~2626、2588~2627、2588~2628、2588~2629、2588~2630、2588~2631、2589~2607、2589~2608、2589~2609、2589~2610、2589~2611、2589~2612、2589~2613、2589~2614、2589~2615、2589~2616、2589~2617、2589~2618、2589~2619、2589~2620、2589~2621、2589~2622、2589~2623、2589~2624、2589~2625、2589~2626、2589~2627、2589~2628、2589~2629、2589~2630、2589~2631、2590~2606、2590~2607、2590~2608、2590~2609、2590~2610、2590~2611、2590~2612、2590~2613、2590~2614、2590~2615、2590~2616、2590~2617、2590~2618、2590~2619、2590~2620、2590~2621、2590~2622、2590~2623、2590~2624、2590~2625、2590~2626、2590~2627、2590~2628、2590~2629、2590~2630、2590~2631、2591~2610、2591~2611、2591~2612、2591~2613、2591~2614、2591~2615、2591~2616、2591~2617、2591~2618、2591~2619、2591~2620、2591~2621、2591~2622、2591~2623、2591~2624、2591~2625、2591~2626、2591~2627、2591~2628、2591~2629、2591~2630、2591~2631、2592~2611、2592~2612、2592~2613、2592~2614、2592~2615、2592~2616、2592~2617、2592~2618、2592~2619、2592~2620、2592~2621、2592~2622、2592~2623、2592~2624、2592~2625、2592~2626、2592~2627、2592~2628、2592~2629、2592~2630、2592~2631、2593~2608、2593~2612、2593~2613、2593~2614、2593~2615、2593~2616、2593~2617、2593~2618、2593~2619、2593~2620、2593~2621、2593~2622、2593~2623、2593~2624、2593~2625、2593~2626、2593~2627、2593~2628、2593~2629、2593~2630、2593~2631、2594~2612、2594~2613、2594~2614、2594~2615、2594~2616、2594~2617、2594~2618、2594~2619、2594~2620、2594~2621、2594~2622、2594~2623、2594~2624、2594~2625、2594~2626、2594~2627、2594~2628、2594~2629、2594~2630、2594~2631、2595~2611、2595~2612、2595~2613、2595~2614、2595~2615、2595~2616、2595~2617、2595~2618、2595~2619、2595~2620、2595~2621、2595~2622、2595~2623、2595~2624、2595~2625、2595~2626、2595~2627、2595~2628、2595~2629、2595~2630、2595~2631、2596~2614、2596~2615、2596~2616、2596~2617、2596~2618、2596~2619、2596~2620、2596~2621、2596~2622、2596~2623、2596~2624、2596~2625、2596~2626、2596~2627、2596~2628、2596~2629、2596~2630、2596~2631、2597~2612、2597~2613、2597~2614、2597~2615、2597~2616、2597~2617、2597~2618、2597~2619、2597
~2620、2597~2621、2597~2622、2597~2623、2597~2624、2597~2625、2597~2626、2597~2627、2597~2628、2597~2629、2597~2630、2597~2631、2598~2613、2598~2614、2598~2615、2598~2616、2598~2617、2598~2618、2598~2619、2598~2620、2598~2621、2598~2622、2598~2623、2598~2624、2598~2625、2598~2626、2598~2627、2598~2628、2598~2629、2598~2630、2598~2631、2599~2614、2599~2615、2599~2616、2599~2617、2599~2618、2599~2619、2599~2620、2599~2621、2599~2622、2599~
2623、2599~2624、2599~2625、2599~2626、2599~2627、2599~2628、2599~2629、2599~2630、2599~2631、2600~2615、2600~2616、2600~2617、2600~2618、2600~2619、2600~2620、2600~2621、2600~2622、2600~2623、2600~2624、2600~2625、2600~2626、2600~2627、2600~2628、2600~2629、2600~2630、2600~2631、2601~2616、2601~2617、2601~2618、2601~2619、2601~2620、2601~2621、2601~2622、2601~2623、2601~2624、2601~2625、2601~2626、2601~2627、2601~2628、2601~2629、2601~2630、2601~2631、2602~2618、2602~2619、2602~2620、2602~2621、2602~2622、2602~2623、2602~2624、2602~2625、2602~2626、2602~2627、2602~2628、2602~2629、2602~2630、2602~2631、2603~2620、2603~2621、2603~2622、2603~2623、2603~2624、2603~2625、2603~2626、2603~2627、2603~2628、2603~2629、2603~2630、2603~2631、2604~2619、2604~2620、2604~2621、2604~2622、2604~2623、2604~2624、2604~2625、2604~2626、2604~2627、2604~2628、2604~2629、2604~2630、2604~2631、2605~2620、2605~2621、2605~2622、2605~2623、2605~2624、2605~2625、2605~2626、2605~2627、2605~2628、2605~2629、2605~2630、2605~2631、2606~2621、2606~2622、2606~2623、2606~2624、2606~2625、2606~2626、2606~2627、2606~2628、2606~2629、2606~2630、2606~2631、2607~2622、2607~2623、2607~2624、2607~2625、2607~2626、2607~2627、2607~2628、2607~2629、2607~2630、2607~2631、2608~2623、2608~2624、2608~2625、2608~2626、2608~2627、2608~2628、2608~2629、2608~2630、2608~2631、2609~2624、2609~2625、2609~2626、2609~2627、2609~2628、2609~2629、2609~2630、2609~2631、2610~2625、2610~2626、2610~2627、2610~2628、2610~2629、2610~2630、2610~2631、2611~2626、2611~2627、2611~2628、2611~2629、2611~2630、2611~2631、2612~2627、2612~2628、2612~2629、2612~2630、2612~
2631、2613~2628、2613~2629、2613~2630、2613~2631、2614~2629、2614~2630、2614~2631、2615~2630、2615~2631、または2616~2631のうちの長さが等しい部分に相補的な少なくとも8個の連続する核酸塩基部分を含む核酸塩基配列を有する8~80個の連結されたヌクレオシドからなり、かつ前記修飾オリゴヌクレオチドの前記核酸塩基配列が配列番号1に相補的である、前記化合物。
〔項8〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号1のヌクレオチド2193~2212、2195~2210、2457~2476、2571~2590、2584~2603、2588~2607、2592~2611、2594~2613、2597~2616、2600~2619、または2596~2611内で相補的な8~80個の連結されたヌクレオシドからなる、前記化合物。
〔項9〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号198、228、237、440、444、448、450、453、455、549、及び598のいずれか一つを含む核酸塩基配列を有する8~80個の連結されたヌクレオシドからなる、前記化合物。
〔項10〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号198、228、237、440、444、448、450、453、455、549、及び598のいずれか一つからなる核酸塩基配列を有する、前記化合物。〔項11〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが10~30個の連結されたヌクレオシドからなり、かつ配列番号6~808の核酸塩基配列のいずれかの少なくとも8個の連続する核酸塩基を含む核酸塩基配列を有する、前記化合物。
〔項12〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが10~30個の連結されたヌクレオシドからなり、かつ配列番号6~808の核酸塩基配列のいずれかの少なくとも9個の連続する核酸塩基を含む核酸塩基配列を有する、前記化合物。
〔項13〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが10~30個の連結されたヌクレオシドからなり、かつ配列番号6~808の核酸塩基配列のいずれかの少なくとも10個の連続する核酸塩基を含む核酸塩基配列を有する、前記化合物。
〔項14〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが10~30個の連結されたヌクレオシドからなり、かつ配列番号6~808の核酸塩基配列のいずれかの少なくとも11個の連続する核酸塩基を含む核酸塩基配列を有する、前記化合物。
〔項15〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが10~30個の連結されたヌクレオシドからなり、かつ配列番号6~808の核酸塩基配列のいずれかの少なくとも12個の連続する核酸塩基を含む核酸塩基配列を有する、前記化合物。
〔項16〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが10~30個の連結されたヌクレオシドからなり、かつ配列番号6~808のいずれ
か一つの核酸塩基配列を含む核酸塩基配列を有する、前記化合物。
〔項17〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが配列番号6~808のいずれか一つの核酸塩基配列からなる、前記化合物。
〔項18〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号84、238、239、317、412、413、420、421、426、434、436、437、438、439、440、442、443、444、445、446、448、451、452、453、454、455、456、457、458、459、460、461、462、464、465、472、473、514、515、542、543、544、545、546、551、553、555、556、599、600、601、602、610、616、617、618、662、666、670、676、677、678、688、689、713、723、729、730、740、741、742、743、744、745、746、747、748、749、755、756、768、783、793、833、及び867のいずれか一つの少なくとも8核酸塩基部分を含む核酸塩基配列を有する、前記化合物。
〔項19〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号198、228、237、440、444、448、450、453、455、549、及び598のいずれか一つを含む核酸塩基配列を有する10~30個の連結されたヌクレオシドからなり、前記修飾オリゴヌクレオチドが、
連結されたデオキシヌクレオシドからなるギャップセグメント、
連結されたヌクレオシドからなる5’ウイングセグメント、及び
連結されたヌクレオシドからなる3’ウイングセグメント
を含み、前記ギャップセグメントは前記5’ウイングセグメントと前記3’ウイングセグメントの間に配置されており、かつ各ウイングセグメントの各ヌクレオシドが修飾糖を含む、前記化合物。
〔項20〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号198、228、237、440、444、448、450、453、または455に示す配列からなる核酸塩基配列を有する20個の連結されたヌクレオシドからなり、前記修飾オリゴヌクレオチドが
10個の連結されたデオキシヌクレオシドからなるギャップセグメント、
5個の連結されたヌクレオシドからなる5’ウイングセグメント、及び
5個の連結されたヌクレオシドからなる3’ウイングセグメント
を含み、前記ギャップセグメントは前記5’ウイングセグメントと前記3’ウイングセグメントの間に配置されており、各ウイングセグメントの各ヌクレオシドは2’-O-メトキシエチル糖を含み、各ヌクレオシド間連結部はホスホロチオエート連結部であり、かつ各シトシンが5-メチルシトシンである、前記化合物。
〔項21〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号598に示す配列からなる核酸塩基配列を有する16個の連結されたヌクレオシドからなり、前記修飾オリゴヌクレオチドが
10個の連結されたデオキシヌクレオシドからなるギャップセグメント、
3個の連結されたヌクレオシドからなる5’ウイングセグメント、及び
3個の連結されたヌクレオシドからなる3’ウイングセグメント
を含み、前記ギャップセグメントは前記5’ウイングセグメントと前記3’ウイングセグメントの間に配置されており、前記5’ウイングセグメントは2’-O-メトキシエチル糖、2’-O-メトキシエチル糖、及びcEt糖を5’→3’方向に含み、前記3’ウイングセグメントはcEt糖、cEt糖、及び2’-O-メトキシエチル糖を5’→3’方
向に含み、各ヌクレオシド間連結部はホスホロチオエート連結部であり、かつ各シトシンが5-メチルシトシンである、前記化合物。
〔項22〕
修飾オリゴヌクレオチドと共役基とを含む化合物であって、前記修飾オリゴヌクレオチドが、配列番号549に示す配列からなる核酸塩基配列を有する16個の連結されたヌクレオシドからなり、前記修飾オリゴヌクレオチドが
10個の連結されたデオキシヌクレオシドからなるギャップセグメント、
3個の連結されたヌクレオシドからなる5’ウイングセグメント、及び
3個の連結されたヌクレオシドからなる3’ウイングセグメント
を含み、前記ギャップセグメントは前記5’ウイングセグメントと前記3’ウイングセグメントの間に配置されており、各ウイングセグメントの各ヌクレオシドはcEt糖を含み、各ヌクレオシド間連結部はホスホロチオエート連結部であり、かつ各シトシンが5-メチルシトシンである、前記化合物。
〔項23〕
前記オリゴヌクレオチドが、配列番号1または配列番号2に少なくとも80%、85%、90%、95%または100%相補的である、請求項1~22のいずれか一項に記載の化合物。
〔項24〕
前記修飾オリゴヌクレオチドが、少なくとも1つの修飾ヌクレオシド間連結部、少なくとも1つの修飾糖、または少なくとも1つの修飾核酸塩基を含む、請求項1~23のいずれか一項に記載の化合物。
〔項25〕
前記修飾ヌクレオシド間連結部がホスホロチオエートヌクレオシド間連結部である、請求項24に記載の化合物。
〔項26〕
前記修飾オリゴヌクレオチドが、少なくとも1つのホスホジエステルヌクレオシド間連結部を含む、請求項25に記載の化合物。
〔項27〕
前記修飾オリゴヌクレオチドが、少なくとも2つのホスホジエステルヌクレオシド間連結部を含む、請求項25に記載の化合物。
〔項28〕
前記修飾オリゴヌクレオチドが、少なくとも3つのホスホジエステルヌクレオシド間連結部を含む、請求項25に記載の化合物。
〔項29〕
前記修飾オリゴヌクレオチドが、少なくとも4つのホスホジエステルヌクレオシド間連結部を含む、請求項25に記載の化合物。
〔項30〕
前記修飾オリゴヌクレオチドが、少なくとも5つのホスホジエステルヌクレオシド間連結部を含む、請求項25に記載の化合物。
〔項31〕
前記修飾オリゴヌクレオチドが、少なくとも6つのホスホジエステルヌクレオシド間連結部を含む、請求項25に記載の化合物。
〔項32〕
前記修飾オリゴヌクレオチドが、少なくとも7つのホスホジエステルヌクレオシド間連結部を含む、請求項25に記載の化合物。
〔項33〕
前記修飾オリゴヌクレオチドの各ヌクレオシド間連結部が、ホスホジエステルヌクレオシド間連結部及びホスホロチオエートヌクレオシド間連結部から選択される、請求項26~32のいずれか一項に記載の化合物。
〔項34〕
前記修飾オリゴヌクレオチドの各ヌクレオシド間連結部がホスホロチオエートヌクレオシド間連結部を含む、請求項25に記載の化合物。
〔項35〕
前記修飾糖が二環式糖である、請求項24~34のいずれか一項に記載の化合物。
〔項36〕
前記二環式糖が、4’-(CH2)-O-2’(LNA)、4’-(CH2)2-O-2’(ENA)、及び4’-CH(CH3)-O-2’(cEt)からなる群より選択される、請求項35に記載の化合物。
〔項37〕
前記修飾糖が2’-O-メトキシエチルである、請求項24~34のいずれか一項に記載の化合物。
〔項38〕
前記修飾核酸塩基が5-メチルシトシンである、請求項24~37のいずれか一項に記載の化合物。
〔項39〕
前記修飾オリゴヌクレオチドが
(a)連結されたデオキシヌクレオシドからなるギャップセグメント、
(b)連結されたヌクレオシドからなる5’ウイングセグメント、及び
(c)連結されたヌクレオシドからなる3’ウイングセグメント;
を含み、前記ギャップセグメントが前記5’ウイングセグメント及び前記3’ウイングセグメントに直接隣り合うように、前記5’ウイングセグメントと前記3’ウイングセグメントの間に配置され、各ウイングセグメントの各ヌクレオシドが修飾糖を含む、請求項1~38のいずれか一項に記載の化合物。
〔項40〕
一本鎖である、請求項1~39のいずれか一項に記載の化合物。
〔項41〕
二本鎖である、請求項1~39のいずれか一項に記載の化合物。
〔項42〕
リボヌクレオチドを含む、請求項1~41のいずれか一項に記載の化合物。
〔項43〕
デオキシリボヌクレオチドを含む、請求項1~41のいずれか一項に記載の化合物。
〔項44〕
前記修飾オリゴヌクレオチドが10~30個の連結されたヌクレオシドからなる、請求項1~43のいずれか一項に記載の化合物。
〔項45〕
前記修飾オリゴヌクレオチドが12~30個の連結されたヌクレオシドからなる、請求項1~43のいずれか一項に記載の化合物。
〔項46〕
前記修飾オリゴヌクレオチドが15~30個の連結されたヌクレオシドからなる、請求項1~43のいずれか一項に記載の化合物。
〔項47〕
ISIS532770、ISIS532800、ISIS532809、ISIS588540、ISIS588544、ISIS588548、ISIS588550、ISIS588553、ISIS588555、ISIS588848、またはISIS594430と、共役基とからなる化合物。
〔項48〕
前記共役基が前記修飾オリゴヌクレオチドの5’端で前記修飾オリゴヌクレオチドに連結されている、請求項1~47のいずれか一項に記載の化合物。
〔項49〕
前記共役基が前記修飾オリゴヌクレオチドの3’端で前記修飾オリゴヌクレオチドに連
結されている、請求項1~47のいずれか一項に記載の化合物。
〔項50〕
前記共役基が厳密に1つのリガンドを含む、請求項1~49のいずれか一項に記載の化合物。
〔項51〕
前記共役基が厳密に2つのリガンドを含む、請求項1~49のいずれか一項に記載の化合物。
〔項52〕
前記共役基が3つ以上のリガンドを含む、請求項1~49のいずれか一項に記載の化合物。
〔項53〕
前記共役基が厳密に3つのリガンドを含む、請求項1~49のいずれか一項に記載の化合物。
〔項54〕
各リガンドが多糖、修飾多糖、マンノース、ガラクトース、マンノース誘導体、ガラクトース誘導体、D-マンノピラノース、L-マンノピラノース、D-アラビノース、L-ガラクトース、D-キシロフラノース、L-キシロフラノース、D-グルコース、L-グルコース、D-ガラクトース、L-ガラクトース、α-D-マンノフラノース、β-D-マンノフラノース、α-D-マンノピラノース、β-D-マンノピラノース、α-D-グルコピラノース、β-D-グルコピラノース、α-D-グルコフラノース、β-D-グルコフラノース、α-D-フルクトフラノース、α-D-フルクトピラノース、α-D-ガラクトピラノース、β-D-ガラクトピラノース、α-D-ガラクトフラノース、β-D-ガラクトフラノース、グルコサミン、シアル酸、α-D-ガラクトサミン、N-アセチルガラクトサミン、2-アミノ-3-O-[(R)-1-カルボキシエチル]-2-デオキシ-β-D-グルコピラノース、2-デオキシ-2-メチルアミノ-L-グルコピラノース、4,6-ジデオキシ-4-ホルムアミド-2,3-ジ-O-メチル-D-マンノピラノース、2-デオキシ-2-スルホアミノ-D-グルコピラノース、N-グリコロイル-α-ノイラミン酸、5-チオ-β-D-グルコピラノース、メチル2,3,4-トリ-O-アセチル-1-チオ-6-O-トリチル-α-D-グルコピラノシド、4-チオ-β-D-ガラクトピラノース、エチル3,4,6,7-テトラ-O-アセチル-2-デオキシ-1,5-ジチオ-α-D-グルコ-ヘプトピラノシド、2,5-アンヒドロ-D-アロノニトリル、リボース、D-リボース、D-4-チオリボース、L-リボース、L-4-チオリボースのなかから選択される、請求項50~53のいずれか一項に記載の化合物。
〔項55〕
各リガンドがN-アセチルガラクトサミンである、請求項54に記載の化合物。
〔項56〕
前記共役基が
を含む、請求項1~55のいずれか一項に記載の化合物。
〔項57〕
前記共役基が
を含む、請求項1~55のいずれか一項に記載の化合物。
〔項58〕
前記共役基が
を含む、請求項1~55のいずれか一項に記載の化合物。
〔項59〕
前記共役基が
を含む、請求項1~55のいずれか一項に記載の化合物。
〔項60〕
前記共役基が
を含む、請求項1~55のいずれか一項に記載の化合物。
〔項61〕
前記共役基が少なくとも1つのリン連結基または中性連結基を含む、請求項49~60のいずれか一項に記載の化合物。
〔項62〕
前記共役基が
[式中、
nは1~12であり、かつ
mは1~12である]
のなかから選択される構造を含む、請求項1~61のいずれか一項に記載の化合物。
〔項63〕
前記共役基が、
[式中、
Lは、リン連結基または中性連結基のどちらかであり、
Z1は、C(=O)O-R2であり、
Z2は、H、C1-C6アルキルまたは置換C1-C6アルキルであり、
R2は、H、C1-C6アルキルまたは置換C1-C6アルキルであり、かつ
各m1は、独立して、0~20であって、各テザーにつき少なくとも1つのm1は0より大きい]
のなかから選択される構造を有するテザーを有する、請求項1~62のいずれか一項に記載の化合物。
〔項64〕
前記共役基が、
[式中、
Z2は、HまたはCH3であり、かつ
各m1は、独立して、0~20であって、各テザーにつき少なくとも1つのm1は0より大きい]
のなかから選択される構造を有するテザーを有する、請求項63に記載の化合物。
〔項65〕
前記共役基が
[式中、
nは1~12であり、かつ
mは1~12である]
のなかから選択される構造を有するテザーを有する、請求項1~64のいずれか一項に記載の化合物。
〔項66〕
前記共役基が、前記修飾オリゴヌクレオチドに共有結合で取り付けられている、請求項1~65のいずれか一項に記載の化合物。
〔項67〕
式:
[式中、
Aは前記修飾オリゴヌクレオチドであり、
Bは前記切断可能部分であり、
Cは前記共役リンカーであり、
Dは前記分岐基であり、
各Eはテザーであり、
各Fはリガンドであり、かつ
qは1と5の間の整数である]
によって表される構造を有する、請求項1~66のいずれか一項に記載の化合物。
〔項68〕
式:
[式中、
Aは前記修飾オリゴヌクレオチドであり、
Bは前記切断可能部分であり、
Cは前記共役リンカーであり、
Dは前記分岐基であり、
各Eはテザーであり、
各Fはリガンドであり、
各nは独立して0または1であり、かつ
qは1と5の間の整数である]
によって表される構造を有する、請求項1~66のいずれか一項に記載の化合物。
〔項69〕
式:
[式中、
Aは前記修飾オリゴヌクレオチドであり、
Bは前記切断可能部分であり、
Cは前記共役リンカーであり、
各Eはテザーであり、
各Fはリガンドであり、かつ
qは1と5の間の整数である]
によって表される構造を有する、請求項1~66のいずれか一項に記載の化合物。
〔項70〕
式:
[式中、
Aは前記修飾オリゴヌクレオチドであり、
Cは前記共役リンカーであり、
Dは前記分岐基であり、
各Eはテザーであり、
各Fはリガンドであり、かつ
qは1と5の間の整数である]
によって表される構造を有する、請求項1~66のいずれか一項に記載の化合物。
〔項71〕
式:
[式中、
Aは前記修飾オリゴヌクレオチドであり、
Cは前記共役リンカーであり、
各Eはテザーであり、
各Fはリガンドであり、かつ
qは1と5の間の整数である]
によって表される構造を有する、請求項1~66のいずれか一項に記載の化合物。
〔項72〕
式:
[式中、
Aは前記修飾オリゴヌクレオチドであり、
Bは前記切断可能部分であり、
Dは前記分岐基であり、
各Eはテザーであり、
各Fはリガンドであり、かつ
qは1と5の間の整数である]
によって表される構造を有する、請求項1~66のいずれか一項に記載の化合物。
〔項73〕
式:
[式中、
Aは前記修飾オリゴヌクレオチドであり、
Bは前記切断可能部分であり、
各Eはテザーであり、
各Fはリガンドであり、かつ
qは1と5の間の整数である]
によって表される構造を有する、請求項1~66のいずれか一項に記載の化合物。
〔項74〕
式:
[式中、
Aは前記修飾オリゴヌクレオチドであり、
Dは前記分岐基であり、
各Eはテザーであり、
各Fはリガンドであり、かつ
qは1と5の間の整数である]
によって表される構造を有する、請求項1~66のいずれか一項に記載の化合物。
〔項75〕
前記共役リンカーが
各Lは、独立して、リン連結基または中性連結基であり、かつ
各nは、独立して、1~20である]
のなかから選択される構造を有する、請求項1~74のいずれか一項に記載の化合物。〔項76〕
前記共役リンカーが
のなかから選択される構造を有する、請求項1~74のいずれか一項に記載の化合物。〔項77〕
前記共役リンカーが以下の構造を有する、請求項1~74のいずれか一項に記載の化合物:
。
〔項78〕
前記共役リンカーが
のなかから選択される構造を有する、請求項1~74のいずれか一項に記載の化合物。
〔項79〕
前記共役リンカーが
〔項80〕
前記共役リンカーが
のなかから選択される構造を有する、請求項1~74のいずれか一項に記載の化合物。
〔項81〕
前記共役リンカーがピロリジンを含む、請求項1~80のいずれか一項に記載の化合物。
〔項82〕
前記共役リンカーがピロリジンを含まない、請求項1~80のいずれか一項に記載の化合物。
〔項83〕
前記共役リンカーがPEGを含む、請求項1~82のいずれか一項に記載の化合物。
〔項84〕
前記共役リンカーがアミドを含む、請求項1~83のいずれか一項に記載の化合物。
〔項85〕
前記共役リンカーが少なくとも2つのアミドを含む、請求項1~84のいずれか一項に記載の化合物。
〔項86〕
前記共役リンカーがアミドを含まない、請求項1~83のいずれか一項に記載の化合物。
〔項87〕
前記共役リンカーがポリアミドを含む、請求項1~86のいずれか一項に記載の化合物。
〔項88〕
前記共役リンカーがアミンを含む、請求項1~87のいずれか一項に記載の化合物。
〔項89〕
前記共役リンカーが1つ以上のジスルフィド結合を含む、請求項1~88のいずれか一項に記載の化合物。
〔項90〕
前記共役リンカーがタンパク質結合部分を含む、請求項1~89のいずれか一項に記載の化合物。
〔項91〕
前記タンパク質結合部分が脂質を含む、請求項90に記載の化合物。
〔項92〕
前記タンパク質結合部分が、コレステロール、コール酸、アダマンタン酢酸、1-ピレン酪酸、ジヒドロテストステロン、1,3-ビス-O(ヘキサデシル)グリセロール、ゲラニルオキシヘキシル基、ヘキサデシルグリセロール、ボルネオール、メントール、1,3-プロパンジオール、ヘプタデシル基、パルミチン酸、ミリスチン酸、O3-(オレオイル)リトコール酸、O3-(オレオイル)コレン酸、ジメトキシトリチル、またはフェノキサジン)、ビタミン(例えば葉酸、ビタミンA、ビタミンE、ビオチン、ピリドキサール)、ペプチド、炭水化物(例えば単糖、二糖、三糖、四糖、オリゴ糖、多糖)、エンドソーム溶解成分、ステロイド(例えばウバオール、ヘシゲニン(hecigenin)、ジオスゲニン)、テルペン(例えばトリテルペン、例えばサルササポゲニン、フリーデ
リン、エピフリーデラノール誘導体化リトコール酸)、またはカチオン性脂質のなかから選択される、請求項90に記載の化合物。
〔項93〕
前記タンパク質結合部分が、C16~C22長鎖飽和または不飽和脂肪酸、コレステロール、コール酸、ビタミンE、アダマンタンまたは1-ペンタフルオロプロピルのなかから選択される、請求項90に記載の化合物。
〔項94〕
前記共役リンカーが
[式中、各nは、独立して、1~20であり、かつpは1~6である]
のなかから選択される構造を有する、請求項1~93のいずれか一項に記載の化合物。
〔項95〕
前記共役リンカーが
[式中、各nは、独立して、1~20である]
のなかから選択される構造を有する、請求項1~94のいずれか一項に記載の化合物。〔項96〕
前記共役リンカーが
のなかから選択される構造を有する、請求項1~94のいずれか一項に記載の化合物。〔項97〕
前記共役リンカーが
[式中、nは1~20である]
のなかから選択される構造を有する、請求項1~94のいずれか一項に記載の化合物。〔項98〕
前記共役リンカーが
のなかから選択される構造を有する、請求項1~94のいずれか一項に記載の化合物。〔項99〕
前記共役リンカーが
[式中、各nは、独立して、0、1、2、3、4、5、6、または7である]
のなかから選択される構造を有する、請求項1~94のいずれか一項に記載の化合物。〔項100〕
前記共役リンカーが以下の構造を有する、請求項1~94のいずれか一項に記載の化合物:
。
〔項101〕
前記分岐基が以下の構造のうちの一つを有する、請求項1~100のいずれか一項に記載の化合物:
[式中、
各A1は、独立して、O、S、C=OまたはNHであり、かつ
各nは、独立して、1~20である]。
〔項102〕
前記分岐基が以下の構造のうちの一つを有する、請求項1~100のいずれか一項に記載の化合物:
[式中、
各A1は、独立して、O、S、C=OまたはNHであり、かつ
各nは、独立して、1~20である]。
〔項103〕
前記分岐基が以下の構造を有する、請求項1~100のいずれか一項に記載の化合物:
。
〔項104〕
前記分岐基が以下の構造を有する、請求項1~100のいずれか一項に記載の化合物:
。
〔項105〕
前記分岐基が以下の構造を有する、請求項1~100のいずれか一項に記載の化合物:
。
〔項106〕
前記分岐基が以下の構造を有する、請求項1~100のいずれか一項に記載の化合物:
。
〔項107〕
前記分岐基がエーテルを含む、請求項1~100のいずれか一項に記載の化合物。
〔項108〕
前記分岐基が以下の構造を有する、請求項1~100のいずれか一項に記載の化合物:
[各nは、独立して、1~20であり、かつ
mは2~6である]。
〔項109〕
前記分岐基が以下の構造を有する、請求項1~100のいずれか一項に記載の化合物:
。
〔項110〕
前記分岐基が以下の構造を有する、請求項1~100のいずれか一項に記載の化合物:
。
〔項111〕
前記分岐基が
、
、
、
、または
[式中、
各jは1~3の整数であり、かつ
各nは1~20の整数である]
を含む、請求項1~100のいずれか一項に記載の化合物。
〔項112〕
前記分岐基が
、
、
、
、または
を含む、請求項1~100のいずれか一項に記載の化合物。
〔項113〕
各テザーが
[式中、
Lは、リン連結基及び中性連結基から選択され、
Z1は、C(=O)O-R2であり、
Z2は、H、C1-C6アルキルまたは置換C1-C6アルキルであり、
R2は、H、C1-C6アルキルまたは置換C1-C6アルキルであり、かつ
各m1は、独立して、0~20であって、各テザーにつき少なくとも1つのm1は0より大きい]
のなかから選択される、請求項1~112のいずれか一項に記載の化合物。
〔項114〕
各テザーが
[式中、
Z2は、HまたはCH3であり、
各m2は、独立して、0~20であって、各テザーにつき少なくとも1つのm2は0より大きい]
のなかから選択される、請求項1~112のいずれか一項に記載の化合物。
〔項115〕
各テザーが
[式中、
nは1~12であり、かつ
mは1~12である]
のなかから選択される、請求項1~112のいずれか一項に記載の化合物。
〔項116〕
少なくとも1つのテザーがエチレングリコールを含む、請求項1~112のいずれか一項に記載の化合物。
〔項117〕
少なくとも1つのテザーがアミドを含む、請求項1~116のいずれか一項に記載の化合物。
〔項118〕
少なくとも1つのテザーがポリアミドを含む、請求項1~117のいずれか一項に記載の化合物。
〔項119〕
少なくとも1つのテザーがアミンを含む、請求項1~118のいずれか一項に記載の化合物。
〔項120〕
少なくとも2つのテザーが互いに異なる、請求項1~119のいずれか一項に記載の化合物。
〔項121〕
すべてのテザーが互いに同じである、請求項1~120のいずれか一項に記載の化合物。
〔項122〕
各テザーが
[式中、
各nは、独立して、1~20であり、かつ
各pは1~約6である]
のなかから選択される、請求項1~121のいずれか一項に記載の化合物。
〔項123〕
各テザーが
のなかから選択される、請求項1~122のいずれか一項に記載の化合物。
〔項124〕
各テザーが以下の構造を有する、請求項1~123のいずれか一項に記載の化合物:
[式中、各nは、独立して、1~20である]。
〔項125〕
各テザーが以下の構造を有する、請求項1~124のいずれか一項に記載の化合物:
〔項126〕
前記テザーが、
、または
[式中、各nは、独立して、0、1、2、3、4、5、6、または7である]
のなかから選択される構造を有する、請求項1~125のいずれか一項に記載の化合物。〔項127〕
前記テザーが構造:
〔項128〕
nが3である、請求項126に記載の化合物。
〔項129〕
前記リガンドがガラクトースである、請求項1~128のいずれか一項に記載の化合物。
〔項130〕
前記リガンドがマンノース-6-ホスフェートである、請求項1~128のいずれか一項に記載の化合物。
〔項131〕
各リガンドが、
[式中、各R1はOH及びNHCOOHから選択される]
のなかから選択される、請求項1~128のいずれか一項に記載の化合物。
〔項132〕
各リガンドが、
のなかから選択される、請求項1~128のいずれか一項に記載の化合物。
〔項133〕
各リガンドが以下の構造を有する、請求項1~128のいずれか一項に記載の化合物:
。
〔項134〕
各リガンドが以下の構造を有する、請求項124~127のいずれか一項に記載の共役アンチセンス化合物:
。
〔項135〕
前記共役基が細胞ターゲティング部分を含む、請求項1~134のいずれか一項に記載の化合物。
〔項136〕
前記共役基が以下の構造を有する細胞ターゲティング部分を含む、請求項135に記載の化合物:
[式中、各nは、独立して、1~20である]。
〔項137〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項138〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
[式中、各nは、独立して、1~20である]。
〔項139〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項140〕
前記細胞ターゲティング部分が、
を含む、請求項135に記載の化合物。
〔項141〕
前記細胞ターゲティング部分が
を含む、請求項135に記載の化合物。
〔項142〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項143〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項144〕
前記細胞ターゲティング部分が
を含む、請求項135に記載の化合物。
〔項145〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項146〕
前記細胞ターゲティング部分が
を含む、請求項135に記載の化合物。
〔項147〕
前記細胞ターゲティング部分が
を含む、請求項135に記載の化合物。
〔項148〕
前記細胞ターゲティング部分が
を含む、請求項135に記載の化合物。
〔項149〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項150〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項151〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項152〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項153〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項154〕
前記細胞ターゲティング部分が
を含む、請求項135に記載の化合物。
〔項155〕
前記細胞ターゲティング部分が
を含む、請求項135に記載の化合物。
〔項156〕
前記細胞ターゲティング部分が
を含む、請求項135に記載の化合物。
〔項157〕
前記細胞ターゲティング部分が
を含む、請求項135に記載の化合物。
〔項158〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項159〕
前記細胞ターゲティング部分が
を含む、請求項135に記載の化合物。
〔項160〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
。
〔項161〕
前記細胞ターゲティング部分が
[式中、各Yは、O、S、置換または無置換C1-C10アルキル、アミノ、置換アミノ、アジド、アルケニルまたはアルキニルから選択される]
を含む、請求項135に記載の化合物。
〔項162〕
前記共役基が
[式中、各Yは、O、S、置換または無置換C1-C10アルキル、アミノ、置換アミノ、アジド、アルケニルまたはアルキニルから選択される]
を含む、請求項135に記載の化合物。
〔項163〕
前記細胞ターゲティング部分が以下の構造を有する、請求項135に記載の化合物:
[式中、各Yは、O、S、置換または無置換C1-C10アルキル、アミノ、置換アミノ、アジド、アルケニルまたはアルキニルから選択される]。
〔項164〕
前記共役基が
を含む、請求項1~163のいずれか一項に記載の化合物。
〔項165〕
前記共役基が
を含む、請求項1~164のいずれか一項に記載の化合物。
〔項166〕
前記共役基が
を含む、請求項1~164のいずれか一項に記載の化合物。
〔項167〕
前記共役基が
を含む、請求項166に記載の化合物。
〔項168〕
前記共役基が、ホスホジエステル、アミド、またはエステルから選択される切断可能部分を含む、請求項1~167のいずれか一項に記載の化合物。
〔項169〕
前記共役基がホスホジエステル切断可能部分を含む、請求項1~168のいずれか一項に記載の化合物。
〔項170〕
前記共役基が切断可能部分を含まず、かつ前記共役基が前記共役基と前記オリゴヌクレオチドとの間にホスホロチオエート連結部を含む、請求項1~169のいずれか一項に記
載の化合物。
〔項171〕
前記共役基がアミド切断可能部分を含む、請求項1~170のいずれか一項に記載の化合物。
〔項172〕
前記共役基がエステル切断可能部分を含む、請求項1~171のいずれか一項に記載の化合物。
〔項173〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
各nは、独立して、1~20であり、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項174〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
各nは、独立して、1~20であり、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項175〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
各nは、独立して、1~20であり、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、
Zは、Hまたは連結された固体支持体であり、かつ
Bxは、複素環式塩基部分である]。
〔項176〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
各nは、独立して、1~20であり、
Q13は、HまたはO(CH2)2-OCH3;
Aは、前記修飾オリゴヌクレオチドであり、
Zは、Hまたは連結された固体支持体であり、かつ
Bxは、複素環式塩基部分である]。
〔項177〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項178〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項179〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項180〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項181〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項182〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項183〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項184〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項185〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項186〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項187〕
以下の構造を有する、請求項1~172のいずれか一項に記載の化合物:
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]。
〔項188〕
前記共役基が
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]
を含む、請求項1~172のいずれか一項に記載の化合物。
〔項189〕
前記共役基が
[式中、
Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]
を含む、請求項1~172のいずれか一項に記載の化合物。
〔項200〕
前記共役基が
[式中、Q13は、HまたはO(CH2)2-OCH3であり、
Aは、前記修飾オリゴヌクレオチドであり、かつ
Bxは、複素環式塩基部分である]
を含む、請求項1~172のいずれか一項に記載の化合物。
〔項201〕
Bxが、アデニン、グアニン、チミン、ウラシル、またはシトシンもしくは5-メチルシトシンのなかから選択される、請求項173~200のいずれか一項に記載の化合物。〔項202〕
Bxがアデニンである、請求項173~200のいずれか一項に記載の化合物。
〔項203〕
Bxがチミンである、請求項173~200のいずれか一項に記載の化合物。
〔項204〕
Q13がO(CH2)2-OCH3である、請求項173~200のいずれか一項に記載の化合物。
〔項205〕
Q13がHである、請求項173~200のいずれか一項に記載の化合物。
〔項206〕
ISIS696844、ISIS696845、ISIS698969、またはISIS698970を含む化合物。
〔項207〕
ISIS696844、ISIS696845、ISIS698969、またはISIS698970からなる化合物。
〔項208〕
請求項1~207のいずれか一項に記載の化合物またはその塩と、医薬上許容される担体または希釈剤の少なくとも1つとを含む組成物。
〔項209〕
請求項1~208のいずれか一項に記載の化合物を含むプロドラッグ。
〔項210〕
対象における補体代替経路の調節異常に関連する疾患を処置し、防止し、または改善する方法であって、前記対象に、請求項1~207のいずれか一項に記載の化合物、請求項208に記載の組成物、または請求項209に記載のプロドラッグを投与し、それによって前記疾患を処置し、防止し、または改善することを含む、前記方法。
〔項211〕
前記補体代替経路が正常より強く活性化されている、請求項210に記載の方法。
〔項212〕
前記疾患が黄斑変性である、請求項210または211に記載の方法。
〔項213〕
前記黄斑変性が加齢黄斑変性(AMD)である、請求項212に記載の方法。
〔項214〕
前記AMDが滲出型AMDである、請求項213に記載の方法。
〔項215〕
前記AMDが乾性AMDである、請求項213に記載の方法。
〔項216〕
前記乾性AMDが地図状萎縮である、請求項215に記載の方法。
〔項217〕
前記疾患が腎臓疾患である、請求項210または211に記載の方法。
〔項218〕
前記腎臓疾患がループス腎炎である、請求項217に記載の方法。
〔項219〕
前記腎臓疾患が全身性エリテマトーデス(SLE)である、請求項217に記載の方法。
〔項220〕
前記腎臓疾患がデンスデポジット病(DDD)である、請求項217に記載の方法。
〔項221〕
前記腎臓疾患がC3糸球体腎炎(C3GN)である、請求項217に記載の方法。
〔項222〕
前記腎臓疾患がCFHR5ネフロパシーである、請求項217に記載の方法。
〔項223〕
前記腎臓疾患が非典型溶血性尿毒症症候群(aHUS)である、請求項217に記載の方法。
〔項224〕
前記aHUSが血栓性微小血管症を特徴とする、請求項223に記載の方法。
〔項225〕
前記腎臓疾患がC3沈着に関連する、請求項217~224のいずれか一項に記載の方法。
〔項226〕
前記腎臓疾患が糸球体におけるC3沈着に関連する、請求項225に記載の方法。
〔項227〕
前記腎臓疾患が正常値未満の循環C3レベルに関連する、請求項217~226のいずれか一項に記載の方法。
〔項228〕
前記循環C3レベルが血清中C3レベルまたは血漿中C3レベルである、請求項227に記載の方法。
〔項229〕
前記化合物または組成物を投与することによって、眼C3レベルが低減し、または眼C3レベルの蓄積が阻害される、請求項210~216のいずれか一項に記載の方法。
〔項230〕
前記C3レベルがC3タンパク質レベルである、請求項229に記載の方法。
〔項231〕
前記化合物または組成物を投与することによって、眼C3沈着のレベルが低減するか、眼C3沈着の蓄積が阻害される、請求項210~216のいずれか一項に記載の方法。
〔項232〕
前記化合物または組成物が前記対象に非経口投与される、請求項229~231のいずれか一項に記載の方法。
〔項233〕
前記化合物または組成物を投与することによって、腎臓におけるC3レベルが低減し、または腎臓におけるC3レベルの蓄積が阻害される、請求項217~228のいずれか一項に記載の方法。
〔項234〕
前記C3レベルがC3タンパク質レベルである、請求項233に記載の方法。
〔項235〕
前記化合物または組成物を投与することによって、腎臓C3沈着のレベルが低減するか、腎臓C3沈着の蓄積が阻害される、請求項233または234に記載の方法。
〔項236〕
腎臓における前記C3レベルが糸球体におけるC3レベルである、請求項233~235のいずれか一項に記載の方法。
〔項237〕
前記化合物または組成物が前記対象に非経口投与される、請求項233~236のいずれか一項に記載の方法。
〔項238〕
前記対象が、補体代替経路の調節異常に関連する疾患を有するか、または前記疾患を有するリスクがあると同定される、請求項210~237のいずれか一項に記載の方法。
〔項239〕
前記同定が、前記対象の血清における補体レベルまたは膜侵襲複合体レベルを検出することを含む、請求項238に記載の方法。
〔項240〕
前記同定が、前記疾患に関連する補体因子の遺伝子変異に関する遺伝子検査を実行することを含む、請求項238に記載の方法。
〔項241〕
補体代替経路の調節異常に関連する疾患を有するかまたは前記疾患を有するリスクがある対象における補体B因子(CFB)の発現を阻害する方法であって、請求項1~207のいずれか一項に記載の化合物、請求項208に記載の組成物、または請求項209に記載のプロドラッグを前記対象に投与し、それによって前記対象におけるCFBの発現を阻害することを含む、前記方法。
〔項242〕
前記補体代替経路が正常より強く活性化されている、請求項241に記載の方法。
〔項243〕
前記化合物または組成物を投与することによって、眼におけるCFBの発現が阻害される、請求項241または242に記載の方法。
〔項244〕
前記対象が加齢黄斑変性(AMD)を有するか、加齢黄斑変性(AMD)を有するリスクがある、請求項243に記載の方法。
〔項245〕
前記化合物または組成物を投与することによって、腎臓におけるCFBの発現が阻害される、請求項241または242に記載の方法。
〔項246〕
前記化合物または組成物を投与することによって、糸球体におけるCFBの発現が阻害される、請求項245に記載の方法。
〔項247〕
前記対象が、ループス腎炎、デンスデポジット病(DDD)、C3糸球体腎炎(C3GN)、CFHR5ネフロパシー、もしくは非典型溶血性尿毒症症候群(aHUS)、またはそれらの任意の組み合わせを有するか、それらを有するリスクがある、請求項245または246に記載の方法。
〔項248〕
補体代替経路の調節異常に関連する疾患を有するかまたは前記疾患を有するリスクがある対象の眼におけるC3沈着を低減しまたはC3沈着の蓄積を阻害する方法であって、請求項1~207のいずれか一項に記載の化合物、請求項208に記載の組成物、または請求項209に記載のプロドラッグを前記対象に投与し、それによって前記対象の眼におけるC3沈着を低減しまたはC3沈着の蓄積を阻害することを含む、前記方法。
〔項249〕
前記補体代替経路が正常より強く活性化されている、請求項248に記載の方法。
〔項250〕
前記対象が加齢黄斑変性(AMD)を有するか、または加齢黄斑変性(AMD)を有するリスクがある、請求項248または249に記載の方法。
〔項251〕
補体代替経路の調節異常に関連する疾患を有するかまたは前記疾患を有するリスクがある対象の腎臓におけるC3沈着を低減しまたはC3沈着の蓄積を阻害する方法であって、請求項1~207のいずれか一項に記載の化合物、請求項208に記載の組成物、または請求項209に記載のプロドラッグを前記対象に投与し、それによって前記対象の腎臓におけるC3沈着を低減しまたはC3沈着の蓄積を阻害することを含む、前記方法。
〔項252〕
前記補体代替経路が正常より強く活性化されている、請求項251に記載の方法。
〔項253〕
前記対象が、ループス腎炎、デンスデポジット病(DDD)、C3糸球体腎炎(C3GN)、CFHR5ネフロパシー、もしくは非典型溶血性尿毒症症候群(aHUS)、またはそれらの任意の組み合わせを有するか、またはそれらを有するリスクがある、請求項251または252に記載の方法。
〔項254〕
前記化合物または組成物が前記対象に非経口投与される、請求項241~253のいずれか一項に記載の方法。
〔項255〕
補体代替経路の調節異常に関連する疾患を処置し、防止し、または改善するための、請求項1~207のいずれか一項に記載の化合物、請求項208に記載の組成物、または請求項209に記載のプロドラッグの使用。
〔項256〕
前記補体代替経路が正常より強く活性化されている、請求項255に記載の使用。
〔項257〕
前記疾患が黄斑変性である、請求項255または256に記載の使用。
〔項258〕
前記黄斑変性が加齢黄斑変性(AMD)である、請求項257に記載の使用。
〔項259〕
前記AMDが滲出型AMDである、請求項258に記載の使用。
〔項260〕
前記AMDが乾性AMDである、請求項258に記載の使用。
〔項261〕
前記乾性AMDが地図状萎縮である、請求項260に記載の使用。
〔項262〕
前記疾患が腎臓疾患である、請求項255または256に記載の使用。
〔項263〕
前記腎臓疾患が、ループス腎炎、デンスデポジット病(DDD)、C3糸球体腎炎(C3GN)、CFHR5ネフロパシー、もしくは非典型溶血性尿毒症症候群(aHUS)、またはそれらの任意の組み合わせである、請求項262に記載の使用。
Claims (15)
- 請求項1~3のいずれか一項に記載のオリゴマー化合物またはその塩と、医薬上許容される担体または希釈剤の少なくとも1つを含む組成物。
- 組成物が、40センチポアズ(cP)未満、30センチポアズ(cP)未満、20センチポアズ(cP)未満、15センチポアズ(cP)未満、または10センチポアズ(cP)未満の粘度を有する、請求項4に記載の組成物。
- 対象における補体代替経路の調節異常に関連する疾患を治療するための医薬であって、請求項1~3のいずれか一項に記載のオリゴマー化合物または請求項4または5に記載の組成物を含む、前記医薬。
- 前記補体代替経路が正常より強く活性化されている、請求項6に記載の医薬。
- 前記疾患が黄斑変性、加齢黄斑変性(AMD)、滲出型AMD、乾性AMDまたは地図状萎縮である、請求項6に記載の医薬。
- 前記疾患が腎臓疾患である、請求項6に記載の医薬。
- 前記腎臓疾患がIgAネフロパシー、ループス腎炎、全身性エリテマトーデス(SLE)、デンスデポジット病(DDD)、C3糸球体腎炎(C3GN)、CFHR5ネフロパシー、または非典型溶血性尿毒症症候群(aHUS)である、請求項9に記載の医薬。
- 補体代替経路の調節異常に関連する疾患を治療するための医薬の製造における、請求項1~3のいずれか一項に記載のオリゴマー化合物または請求項4または5に記載の組成物の使用。
- 前記補体代替経路が正常より強く活性化されている、請求項11に記載の医薬の製造におけるオリゴマー化合物または組成物の使用。
- 前記疾患が黄斑変性、加齢黄斑変性(AMD)、滲出型AMD、乾性AMDまたは地図状萎縮である、請求項11に記載の医薬の製造におけるオリゴマー化合物または組成物の使用。
- 前記疾患が腎臓疾患である、請求項11に記載の医薬の製造におけるオリゴマー化合物または組成物の使用。
- 前記腎臓疾患がIgAネフロパシー、ループス腎炎、全身性エリテマトーデス(SLE)、デンスデポジット病(DDD)、C3糸球体腎炎(C3GN)、CFHR5ネフロパシー、または非典型溶血性尿毒症症候群(aHUS)である、請求項14に記載の医薬の製造におけるオリゴマー化合物または組成物の使用。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201461987471P | 2014-05-01 | 2014-05-01 | |
| US61/987,471 | 2014-05-01 | ||
| US201462076273P | 2014-11-06 | 2014-11-06 | |
| US62/076,273 | 2014-11-06 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016565465A Division JP6637442B2 (ja) | 2014-05-01 | 2015-05-01 | 補体b因子発現を調節するための組成物及び方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2020058368A JP2020058368A (ja) | 2020-04-16 |
| JP2020058368A5 JP2020058368A5 (ja) | 2020-05-28 |
| JP7001663B2 true JP7001663B2 (ja) | 2022-02-04 |
Family
ID=54359510
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016565465A Active JP6637442B2 (ja) | 2014-05-01 | 2015-05-01 | 補体b因子発現を調節するための組成物及び方法 |
| JP2019228789A Active JP7001663B2 (ja) | 2014-05-01 | 2019-12-19 | 補体b因子発現を調節するための組成物及び方法 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016565465A Active JP6637442B2 (ja) | 2014-05-01 | 2015-05-01 | 補体b因子発現を調節するための組成物及び方法 |
Country Status (29)
| Country | Link |
|---|---|
| US (5) | US10280423B2 (ja) |
| EP (3) | EP4219718A3 (ja) |
| JP (2) | JP6637442B2 (ja) |
| KR (1) | KR102369736B1 (ja) |
| CN (2) | CN110724687B (ja) |
| AU (1) | AU2015252858C1 (ja) |
| BR (1) | BR112016022593B1 (ja) |
| CA (2) | CA2943894C (ja) |
| CL (2) | CL2016002764A1 (ja) |
| CR (2) | CR20200228A (ja) |
| DK (1) | DK3137596T3 (ja) |
| DO (1) | DOP2016000291A (ja) |
| EA (1) | EA036496B1 (ja) |
| ES (2) | ES2941742T3 (ja) |
| HR (1) | HRP20191664T1 (ja) |
| HU (1) | HUE046272T2 (ja) |
| IL (2) | IL247883B (ja) |
| LT (1) | LT3137596T (ja) |
| MX (1) | MX380866B (ja) |
| PE (2) | PE20190626A1 (ja) |
| PH (1) | PH12016502062B1 (ja) |
| PL (2) | PL3608406T3 (ja) |
| PT (1) | PT3137596T (ja) |
| RS (1) | RS59182B1 (ja) |
| RU (1) | RU2701645C2 (ja) |
| SG (2) | SG10201809953QA (ja) |
| SI (1) | SI3137596T1 (ja) |
| UA (1) | UA121656C2 (ja) |
| WO (1) | WO2015168635A2 (ja) |
Families Citing this family (27)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013159108A2 (en) * | 2012-04-20 | 2013-10-24 | Isis Pharmaceuticals, Inc. | Oligomeric compounds comprising bicyclic nucleotides and uses thereof |
| DK2992098T3 (da) | 2013-05-01 | 2019-06-17 | Ionis Pharmaceuticals Inc | Sammensætninger og fremgangsmåder til modulering af hbv- og ttr-ekspression |
| MY181251A (en) * | 2013-09-13 | 2020-12-21 | Ionis Pharmaceuticals Inc | Modulators of complement factor b |
| EA036496B1 (ru) | 2014-05-01 | 2020-11-17 | Ионис Фармасьютикалз, Инк. | Конъюгированные олигонуклеотиды для модулирования экспрессии фактора комплемента b |
| BR112016022742B1 (pt) | 2014-05-01 | 2022-06-14 | Ionis Pharmaceuticals, Inc | Composto químico, composição compreendendo o composto e uso dos mesmos |
| CN106795200B (zh) | 2014-10-10 | 2020-06-19 | 豪夫迈·罗氏有限公司 | Galnac亚磷酰胺、其核酸缀合物及其用途 |
| KR20250078597A (ko) | 2015-11-06 | 2025-06-02 | 아이오니스 파마수티컬즈, 인코포레이티드 | 아포리포프로테인 (a) 발현 조정 |
| US10781175B2 (en) | 2016-07-15 | 2020-09-22 | Am Chemicals Llc | Solid supports and phosphoramidite building blocks for oligonucleotide conjugates |
| JOP20190215A1 (ar) * | 2017-03-24 | 2019-09-19 | Ionis Pharmaceuticals Inc | مُعدّلات التعبير الوراثي عن pcsk9 |
| WO2020109343A1 (en) | 2018-11-29 | 2020-06-04 | F. Hoffmann-La Roche Ag | Combination therapy for treatment of macular degeneration |
| JP7720788B2 (ja) * | 2019-06-25 | 2025-08-08 | アムジエン・インコーポレーテツド | 炭水化物に連結されたオリゴヌクレオチドのための精製方法 |
| JP7672394B2 (ja) | 2019-09-03 | 2025-05-07 | アークトゥラス・セラピューティクス・インコーポレイテッド | 治療的に活性な複合体のアシアロ糖タンパク質受容体媒介送達 |
| WO2021081026A1 (en) | 2019-10-22 | 2021-04-29 | Alnylam Pharmaceuticals, Inc. | Complement component c3 irna compositions and methods of use thereof |
| BR112022010742A2 (pt) | 2019-12-26 | 2022-08-16 | Eisai R&D Man Co Ltd | Composição farmacêutica contendo ácido ribonucleico de fita dupla que inibe a expressão de c5 complementar |
| JP2023523790A (ja) * | 2020-04-30 | 2023-06-07 | アルナイラム ファーマシューティカルズ, インコーポレイテッド | 補体因子B(CFB)iRNA組成物およびその使用方法 |
| EP4373940A4 (en) * | 2021-07-17 | 2025-10-01 | Sirnaomics Inc | PRODUCTS AND COMPOSITIONS |
| WO2023031359A1 (en) | 2021-09-02 | 2023-03-09 | Silence Therapeutics Gmbh | Nucleic acids for inhibiting expression of complement factor b (cfb) in a cell |
| CN118302525A (zh) | 2021-10-29 | 2024-07-05 | 阿尔尼拉姆医药品有限公司 | 补体因子B(CFB)iRNA组合物及其使用方法 |
| AU2022396536A1 (en) | 2021-11-24 | 2024-06-06 | Adarx Pharmaceuticals, Inc. | Complement factor b-modulating compositions and methods of use thereof |
| WO2024097861A1 (en) * | 2022-11-02 | 2024-05-10 | Ionis Pharmaceuticals, Inc. | Methods for modulating complement factor b expression |
| WO2024137590A2 (en) * | 2022-12-19 | 2024-06-27 | Sanegene Bio Usa Inc. | Small interfering rna targeting cfb and uses thereof |
| EP4684015A2 (en) * | 2023-03-21 | 2026-01-28 | Arrowhead Pharmaceuticals, Inc. | Rnai agents for inhibiting expression of complement factor b (cfb), pharmaceutical compositions thereof, and methods of use |
| TW202513799A (zh) * | 2023-06-02 | 2025-04-01 | 大陸商維亞臻生物技術(蘇州)有限公司 | 用於免疫類疾病的雙鏈核苷酸化合物及其用途 |
| WO2025002401A1 (zh) * | 2023-06-28 | 2025-01-02 | 百奥赛图(北京)医药科技股份有限公司 | 一种cfb基因修饰的非人动物 |
| CN121532510A (zh) * | 2023-07-28 | 2026-02-13 | 苏州炫景生物科技有限公司 | Cfb抑制剂组合物及其应用 |
| WO2025151250A2 (en) * | 2024-01-09 | 2025-07-17 | Adarx Pharmaceuticals, Inc. | Complement factor b-modulating compositions and methods of use thereof |
| WO2026046277A1 (zh) * | 2024-08-28 | 2026-03-05 | 倍臻生物技术(苏州)有限公司 | 用于抑制补体因子b(cfb)基因表达的双链核糖核酸及其缀合体 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005504522A (ja) | 2001-06-21 | 2005-02-17 | アイシス・ファーマシューティカルス・インコーポレーテッド | トランスフォーム増殖因子β受容体II発現のアンチセンスモジュレーション |
| JP2006507841A (ja) | 2002-11-14 | 2006-03-09 | ダーマコン, インコーポレイテッド | 機能的siRNAおよび超機能的siRNA |
| JP2007505605A (ja) | 2003-09-16 | 2007-03-15 | サーナ・セラピューティクス・インコーポレイテッド | 低分子干渉核酸(siNA)を使用したRNA干渉により媒介される血管内皮増殖因子遺伝子発現および血管内皮増殖因子遺伝子受容体遺伝子発現のRNA干渉媒介性抑制 |
| WO2012177947A2 (en) | 2011-06-21 | 2012-12-27 | Alnylam Pharmaceuticals, Inc. | Compositions and methods for inhibition of expression of apolipoprotein c-iii (apoc3) genes |
| WO2013166121A1 (en) | 2012-05-02 | 2013-11-07 | Merck Sharp & Dohme Corp. | Novel tetragalnac containing conjugates and methods for delivery of oligonucleotides |
Family Cites Families (292)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2699508A (en) | 1951-12-21 | 1955-01-11 | Selectronics Inc | Method of mounting and construction of mounting for low frequency piezoelectric crystals |
| US3687808A (en) | 1969-08-14 | 1972-08-29 | Univ Leland Stanford Junior | Synthetic polynucleotides |
| US4458066A (en) | 1980-02-29 | 1984-07-03 | University Patents, Inc. | Process for preparing polynucleotides |
| US4500707A (en) | 1980-02-29 | 1985-02-19 | University Patents, Inc. | Nucleosides useful in the preparation of polynucleotides |
| US5132418A (en) | 1980-02-29 | 1992-07-21 | University Patents, Inc. | Process for preparing polynucleotides |
| US4469863A (en) | 1980-11-12 | 1984-09-04 | Ts O Paul O P | Nonionic nucleic acid alkyl and aryl phosphonates and processes for manufacture and use thereof |
| US4973679A (en) | 1981-03-27 | 1990-11-27 | University Patents, Inc. | Process for oligonucleo tide synthesis using phosphormidite intermediates |
| US4668777A (en) | 1981-03-27 | 1987-05-26 | University Patents, Inc. | Phosphoramidite nucleoside compounds |
| US4415732A (en) | 1981-03-27 | 1983-11-15 | University Patents, Inc. | Phosphoramidite compounds and processes |
| US5023243A (en) | 1981-10-23 | 1991-06-11 | Molecular Biosystems, Inc. | Oligonucleotide therapeutic agent and method of making same |
| US4476301A (en) | 1982-04-29 | 1984-10-09 | Centre National De La Recherche Scientifique | Oligonucleotides, a process for preparing the same and their application as mediators of the action of interferon |
| DE3329892A1 (de) | 1983-08-18 | 1985-03-07 | Köster, Hubert, Prof. Dr., 2000 Hamburg | Verfahren zur herstellung von oligonucleotiden |
| US5118800A (en) | 1983-12-20 | 1992-06-02 | California Institute Of Technology | Oligonucleotides possessing a primary amino group in the terminal nucleotide |
| USRE34036E (en) | 1984-06-06 | 1992-08-18 | National Research Development Corporation | Data transmission using a transparent tone-in band system |
| US5550111A (en) | 1984-07-11 | 1996-08-27 | Temple University-Of The Commonwealth System Of Higher Education | Dual action 2',5'-oligoadenylate antiviral derivatives and uses thereof |
| FR2567892B1 (fr) | 1984-07-19 | 1989-02-17 | Centre Nat Rech Scient | Nouveaux oligonucleotides, leur procede de preparation et leurs applications comme mediateurs dans le developpement des effets des interferons |
| US5367066A (en) | 1984-10-16 | 1994-11-22 | Chiron Corporation | Oligonucleotides with selectably cleavable and/or abasic sites |
| FR2575751B1 (fr) | 1985-01-08 | 1987-04-03 | Pasteur Institut | Nouveaux nucleosides de derives de l'adenosine, leur preparation et leurs applications biologiques |
| US4751219A (en) | 1985-02-05 | 1988-06-14 | Nederlandse Centrale Organisatie Voor Toegepast-Natuur-Wetenschappelijk Onderzoek | Synthetic glycolipides, a process for the preparation thereof and several uses for these synthetic glycolipides |
| US5185444A (en) | 1985-03-15 | 1993-02-09 | Anti-Gene Deveopment Group | Uncharged morpolino-based polymers having phosphorous containing chiral intersubunit linkages |
| US5506337A (en) | 1985-03-15 | 1996-04-09 | Antivirals Inc. | Morpholino-subunit combinatorial library and method |
| US5235033A (en) | 1985-03-15 | 1993-08-10 | Anti-Gene Development Group | Alpha-morpholino ribonucleoside derivatives and polymers thereof |
| US5166315A (en) | 1989-12-20 | 1992-11-24 | Anti-Gene Development Group | Sequence-specific binding polymers for duplex nucleic acids |
| US5034506A (en) | 1985-03-15 | 1991-07-23 | Anti-Gene Development Group | Uncharged morpholino-based polymers having achiral intersubunit linkages |
| US5405938A (en) | 1989-12-20 | 1995-04-11 | Anti-Gene Development Group | Sequence-specific binding polymers for duplex nucleic acids |
| EP0260032B1 (en) | 1986-09-08 | 1994-01-26 | Ajinomoto Co., Inc. | Compounds for the cleavage at a specific position of RNA, oligomers employed for the formation of said compounds, and starting materials for the synthesis of said oligomers |
| US5276019A (en) | 1987-03-25 | 1994-01-04 | The United States Of America As Represented By The Department Of Health And Human Services | Inhibitors for replication of retroviruses and for the expression of oncogene products |
| US5264423A (en) | 1987-03-25 | 1993-11-23 | The United States Of America As Represented By The Department Of Health And Human Services | Inhibitors for replication of retroviruses and for the expression of oncogene products |
| EP0366685B1 (en) | 1987-06-24 | 1994-10-19 | Howard Florey Institute Of Experimental Physiology And Medicine | Nucleoside derivatives |
| US4924624A (en) | 1987-10-22 | 1990-05-15 | Temple University-Of The Commonwealth System Of Higher Education | 2,',5'-phosphorothioate oligoadenylates and plant antiviral uses thereof |
| US5188897A (en) | 1987-10-22 | 1993-02-23 | Temple University Of The Commonwealth System Of Higher Education | Encapsulated 2',5'-phosphorothioate oligoadenylates |
| ATE151467T1 (de) | 1987-11-30 | 1997-04-15 | Univ Iowa Res Found | Durch modifikationen an der 3'-terminalen phosphodiesterbindung stabilisierte dna moleküle, ihre verwendung als nukleinsäuresonden sowie als therapeutische mittel zur hemmung der expression spezifischer zielgene |
| US5403711A (en) | 1987-11-30 | 1995-04-04 | University Of Iowa Research Foundation | Nucleic acid hybridization and amplification method for detection of specific sequences in which a complementary labeled nucleic acid probe is cleaved |
| JPH03503894A (ja) | 1988-03-25 | 1991-08-29 | ユニバーシィティ オブ バージニア アランミ パテンツ ファウンデイション | オリゴヌクレオチド n‐アルキルホスホラミデート |
| US5278302A (en) | 1988-05-26 | 1994-01-11 | University Patents, Inc. | Polynucleotide phosphorodithioates |
| US5216141A (en) | 1988-06-06 | 1993-06-01 | Benner Steven A | Oligonucleotide analogs containing sulfur linkages |
| US5175273A (en) | 1988-07-01 | 1992-12-29 | Genentech, Inc. | Nucleic acid intercalating agents |
| US5194599A (en) | 1988-09-23 | 1993-03-16 | Gilead Sciences, Inc. | Hydrogen phosphonodithioate compositions |
| US5256775A (en) | 1989-06-05 | 1993-10-26 | Gilead Sciences, Inc. | Exonuclease-resistant oligonucleotides |
| US5134066A (en) | 1989-08-29 | 1992-07-28 | Monsanto Company | Improved probes using nucleosides containing 3-dezauracil analogs |
| US5591722A (en) | 1989-09-15 | 1997-01-07 | Southern Research Institute | 2'-deoxy-4'-thioribonucleosides and their antiviral activity |
| US5399676A (en) | 1989-10-23 | 1995-03-21 | Gilead Sciences | Oligonucleotides with inverted polarity |
| US5721218A (en) | 1989-10-23 | 1998-02-24 | Gilead Sciences, Inc. | Oligonucleotides with inverted polarity |
| US5264562A (en) | 1989-10-24 | 1993-11-23 | Gilead Sciences, Inc. | Oligonucleotide analogs with novel linkages |
| US5264564A (en) | 1989-10-24 | 1993-11-23 | Gilead Sciences | Oligonucleotide analogs with novel linkages |
| DE69034150T2 (de) | 1989-10-24 | 2005-08-25 | Isis Pharmaceuticals, Inc., Carlsbad | 2'-Modifizierte Oligonukleotide |
| US5177198A (en) | 1989-11-30 | 1993-01-05 | University Of N.C. At Chapel Hill | Process for preparing oligoribonucleoside and oligodeoxyribonucleoside boranophosphates |
| US5130302A (en) | 1989-12-20 | 1992-07-14 | Boron Bilogicals, Inc. | Boronated nucleoside, nucleotide and oligonucleotide compounds, compositions and methods for using same |
| US5459255A (en) | 1990-01-11 | 1995-10-17 | Isis Pharmaceuticals, Inc. | N-2 substituted purines |
| US5681941A (en) | 1990-01-11 | 1997-10-28 | Isis Pharmaceuticals, Inc. | Substituted purines and oligonucleotide cross-linking |
| US5623065A (en) | 1990-08-13 | 1997-04-22 | Isis Pharmaceuticals, Inc. | Gapped 2' modified oligonucleotides |
| US7101993B1 (en) | 1990-01-11 | 2006-09-05 | Isis Pharmaceuticals, Inc. | Oligonucleotides containing 2′-O-modified purines |
| US5646265A (en) | 1990-01-11 | 1997-07-08 | Isis Pharmceuticals, Inc. | Process for the preparation of 2'-O-alkyl purine phosphoramidites |
| US5587470A (en) | 1990-01-11 | 1996-12-24 | Isis Pharmaceuticals, Inc. | 3-deazapurines |
| US5457191A (en) | 1990-01-11 | 1995-10-10 | Isis Pharmaceuticals, Inc. | 3-deazapurines |
| US5670633A (en) | 1990-01-11 | 1997-09-23 | Isis Pharmaceuticals, Inc. | Sugar modified oligonucleotides that detect and modulate gene expression |
| US5859221A (en) | 1990-01-11 | 1999-01-12 | Isis Pharmaceuticals, Inc. | 2'-modified oligonucleotides |
| US6005087A (en) | 1995-06-06 | 1999-12-21 | Isis Pharmaceuticals, Inc. | 2'-modified oligonucleotides |
| US5587361A (en) | 1991-10-15 | 1996-12-24 | Isis Pharmaceuticals, Inc. | Oligonucleotides having phosphorothioate linkages of high chiral purity |
| US5149797A (en) | 1990-02-15 | 1992-09-22 | The Worcester Foundation For Experimental Biology | Method of site-specific alteration of rna and production of encoded polypeptides |
| US5220007A (en) | 1990-02-15 | 1993-06-15 | The Worcester Foundation For Experimental Biology | Method of site-specific alteration of RNA and production of encoded polypeptides |
| US5321131A (en) | 1990-03-08 | 1994-06-14 | Hybridon, Inc. | Site-specific functionalization of oligodeoxynucleotides for non-radioactive labelling |
| US5470967A (en) | 1990-04-10 | 1995-11-28 | The Dupont Merck Pharmaceutical Company | Oligonucleotide analogs with sulfamate linkages |
| GB9009980D0 (en) | 1990-05-03 | 1990-06-27 | Amersham Int Plc | Phosphoramidite derivatives,their preparation and the use thereof in the incorporation of reporter groups on synthetic oligonucleotides |
| ES2116977T3 (es) | 1990-05-11 | 1998-08-01 | Microprobe Corp | Soportes solidos para ensayos de hibridacion de acidos nucleicos y metodos para inmovilizar oligonucleotidos de modo covalente. |
| US5541307A (en) | 1990-07-27 | 1996-07-30 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogs and solid phase synthesis thereof |
| US5386023A (en) | 1990-07-27 | 1995-01-31 | Isis Pharmaceuticals | Backbone modified oligonucleotide analogs and preparation thereof through reductive coupling |
| US5618704A (en) | 1990-07-27 | 1997-04-08 | Isis Pharmacueticals, Inc. | Backbone-modified oligonucleotide analogs and preparation thereof through radical coupling |
| US5602240A (en) | 1990-07-27 | 1997-02-11 | Ciba Geigy Ag. | Backbone modified oligonucleotide analogs |
| US5608046A (en) | 1990-07-27 | 1997-03-04 | Isis Pharmaceuticals, Inc. | Conjugated 4'-desmethyl nucleoside analog compounds |
| JPH0874B2 (ja) | 1990-07-27 | 1996-01-10 | アイシス・ファーマシューティカルス・インコーポレーテッド | 遺伝子発現を検出および変調するヌクレアーゼ耐性、ピリミジン修飾オリゴヌクレオチド |
| US5677437A (en) | 1990-07-27 | 1997-10-14 | Isis Pharmaceuticals, Inc. | Heteroatomic oligonucleoside linkages |
| US5378825A (en) | 1990-07-27 | 1995-01-03 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogs |
| US5610289A (en) | 1990-07-27 | 1997-03-11 | Isis Pharmaceuticals, Inc. | Backbone modified oligonucleotide analogues |
| US5489677A (en) | 1990-07-27 | 1996-02-06 | Isis Pharmaceuticals, Inc. | Oligonucleoside linkages containing adjacent oxygen and nitrogen atoms |
| US5623070A (en) | 1990-07-27 | 1997-04-22 | Isis Pharmaceuticals, Inc. | Heteroatomic oligonucleoside linkages |
| US5223618A (en) | 1990-08-13 | 1993-06-29 | Isis Pharmaceuticals, Inc. | 4'-desmethyl nucleoside analog compounds |
| MY107332A (en) | 1990-08-03 | 1995-11-30 | Sterling Drug Inc | Compounds and methods for inhibiting gene expression. |
| US5177196A (en) | 1990-08-16 | 1993-01-05 | Microprobe Corporation | Oligo (α-arabinofuranosyl nucleotides) and α-arabinofuranosyl precursors thereof |
| US5214134A (en) | 1990-09-12 | 1993-05-25 | Sterling Winthrop Inc. | Process of linking nucleosides with a siloxane bridge |
| US5561225A (en) | 1990-09-19 | 1996-10-01 | Southern Research Institute | Polynucleotide analogs containing sulfonate and sulfonamide internucleoside linkages |
| JPH06505704A (ja) | 1990-09-20 | 1994-06-30 | ギリアド サイエンシズ,インコーポレイテッド | 改変ヌクレオシド間結合 |
| US5432272A (en) | 1990-10-09 | 1995-07-11 | Benner; Steven A. | Method for incorporating into a DNA or RNA oligonucleotide using nucleotides bearing heterocyclic bases |
| US6582908B2 (en) | 1990-12-06 | 2003-06-24 | Affymetrix, Inc. | Oligonucleotides |
| US5948903A (en) | 1991-01-11 | 1999-09-07 | Isis Pharmaceuticals, Inc. | Synthesis of 3-deazapurines |
| US5672697A (en) | 1991-02-08 | 1997-09-30 | Gilead Sciences, Inc. | Nucleoside 5'-methylene phosphonates |
| US7015315B1 (en) | 1991-12-24 | 2006-03-21 | Isis Pharmaceuticals, Inc. | Gapped oligonucleotides |
| US5571799A (en) | 1991-08-12 | 1996-11-05 | Basco, Ltd. | (2'-5') oligoadenylate analogues useful as inhibitors of host-v5.-graft response |
| EP0538194B1 (de) | 1991-10-17 | 1997-06-04 | Novartis AG | Bicyclische Nukleoside, Oligonukleotide, Verfahren zu deren Herstellung und Zwischenprodukte |
| US5594121A (en) | 1991-11-07 | 1997-01-14 | Gilead Sciences, Inc. | Enhanced triple-helix and double-helix formation with oligomers containing modified purines |
| AU3222793A (en) | 1991-11-26 | 1993-06-28 | Gilead Sciences, Inc. | Enhanced triple-helix and double-helix formation with oligomers containing modified pyrimidines |
| TW393513B (en) | 1991-11-26 | 2000-06-11 | Isis Pharmaceuticals Inc | Enhanced triple-helix and double-helix formation with oligomers containing modified pyrimidines |
| US5484908A (en) | 1991-11-26 | 1996-01-16 | Gilead Sciences, Inc. | Oligonucleotides containing 5-propynyl pyrimidines |
| US5792608A (en) | 1991-12-12 | 1998-08-11 | Gilead Sciences, Inc. | Nuclease stable and binding competent oligomers and methods for their use |
| US5359044A (en) | 1991-12-13 | 1994-10-25 | Isis Pharmaceuticals | Cyclobutyl oligonucleotide surrogates |
| JP3131222B2 (ja) * | 1991-12-24 | 2001-01-31 | アイシス・ファーマシューティカルス・インコーポレーテッド | ギャップを有する2′修飾オリゴヌクレオチド |
| US5700922A (en) | 1991-12-24 | 1997-12-23 | Isis Pharmaceuticals, Inc. | PNA-DNA-PNA chimeric macromolecules |
| FR2687679B1 (fr) | 1992-02-05 | 1994-10-28 | Centre Nat Rech Scient | Oligothionucleotides. |
| US5633360A (en) | 1992-04-14 | 1997-05-27 | Gilead Sciences, Inc. | Oligonucleotide analogs capable of passive cell membrane permeation |
| US20030206887A1 (en) * | 1992-05-14 | 2003-11-06 | David Morrissey | RNA interference mediated inhibition of hepatitis B virus (HBV) using short interfering nucleic acid (siNA) |
| US5434257A (en) | 1992-06-01 | 1995-07-18 | Gilead Sciences, Inc. | Binding compentent oligomers containing unsaturated 3',5' and 2',5' linkages |
| EP0577558A2 (de) | 1992-07-01 | 1994-01-05 | Ciba-Geigy Ag | Carbocyclische Nukleoside mit bicyclischen Ringen, Oligonukleotide daraus, Verfahren zu deren Herstellung, deren Verwendung und Zwischenproduckte |
| US5652355A (en) | 1992-07-23 | 1997-07-29 | Worcester Foundation For Experimental Biology | Hybrid oligonucleotide phosphorothioates |
| ATE162198T1 (de) | 1992-07-27 | 1998-01-15 | Hybridon Inc | Oligonukleotid alkylphosphonothiate |
| ATE138384T1 (de) | 1993-01-25 | 1996-06-15 | Hybridon Inc | Olionukleotidalkylphosphonate und - phosphonothioate |
| US5476925A (en) | 1993-02-01 | 1995-12-19 | Northwestern University | Oligodeoxyribonucleotides including 3'-aminonucleoside-phosphoramidate linkages and terminal 3'-amino groups |
| GB9304620D0 (en) | 1993-03-06 | 1993-04-21 | Ciba Geigy Ag | Compounds |
| GB9304618D0 (en) | 1993-03-06 | 1993-04-21 | Ciba Geigy Ag | Chemical compounds |
| CA2159631A1 (en) | 1993-03-30 | 1994-10-13 | Sanofi | Acyclic nucleoside analogs and oligonucleotide sequences containing them |
| HU9501974D0 (en) | 1993-03-31 | 1995-09-28 | Sterling Winthrop Inc | Oligonucleotides with amide linkages replacing phosphodiester linkages |
| US5502177A (en) | 1993-09-17 | 1996-03-26 | Gilead Sciences, Inc. | Pyrimidine derivatives for labeled binding partners |
| US5801154A (en) | 1993-10-18 | 1998-09-01 | Isis Pharmaceuticals, Inc. | Antisense oligonucleotide modulation of multidrug resistance-associated protein |
| US5457187A (en) | 1993-12-08 | 1995-10-10 | Board Of Regents University Of Nebraska | Oligonucleotides containing 5-fluorouracil |
| DE733059T1 (de) | 1993-12-09 | 1997-08-28 | Univ Jefferson | Verbindungen und verfahren zur ortsspezifischen mutation in eukaryotischen zellen |
| US5446137B1 (en) | 1993-12-09 | 1998-10-06 | Behringwerke Ag | Oligonucleotides containing 4'-substituted nucleotides |
| US5519134A (en) | 1994-01-11 | 1996-05-21 | Isis Pharmaceuticals, Inc. | Pyrrolidine-containing monomers and oligomers |
| US5596091A (en) | 1994-03-18 | 1997-01-21 | The Regents Of The University Of California | Antisense oligonucleotides comprising 5-aminoalkyl pyrimidine nucleotides |
| US5627053A (en) | 1994-03-29 | 1997-05-06 | Ribozyme Pharmaceuticals, Inc. | 2'deoxy-2'-alkylnucleotide containing nucleic acid |
| US5625050A (en) | 1994-03-31 | 1997-04-29 | Amgen Inc. | Modified oligonucleotides and intermediates useful in nucleic acid therapeutics |
| US5646269A (en) | 1994-04-28 | 1997-07-08 | Gilead Sciences, Inc. | Method for oligonucleotide analog synthesis |
| US5525711A (en) | 1994-05-18 | 1996-06-11 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Pteridine nucleotide analogs as fluorescent DNA probes |
| US5597909A (en) | 1994-08-25 | 1997-01-28 | Chiron Corporation | Polynucleotide reagents containing modified deoxyribose moieties, and associated methods of synthesis and use |
| US5681940A (en) * | 1994-11-02 | 1997-10-28 | Icn Pharmaceuticals | Sugar modified nucleosides and oligonucleotides |
| US6172045B1 (en) | 1994-12-07 | 2001-01-09 | Neorx Corporation | Cluster clearing agents |
| US6908903B1 (en) | 1994-12-07 | 2005-06-21 | Aletheon Pharmaceuticals, Inc. | Cluster clearing agents |
| US5652356A (en) | 1995-08-17 | 1997-07-29 | Hybridon, Inc. | Inverted chimeric and hybrid oligonucleotides |
| CN1120707C (zh) | 1995-11-22 | 2003-09-10 | 约翰斯·霍普金斯大学 | 增强生物分子的细胞摄取的配体 |
| US20030119724A1 (en) | 1995-11-22 | 2003-06-26 | Ts`O Paul O.P. | Ligands to enhance cellular uptake of biomolecules |
| US5998203A (en) | 1996-04-16 | 1999-12-07 | Ribozyme Pharmaceuticals, Inc. | Enzymatic nucleic acids containing 5'-and/or 3'-cap structures |
| US20080119427A1 (en) | 1996-06-06 | 2008-05-22 | Isis Pharmaceuticals, Inc. | Double Strand Compositions Comprising Differentially Modified Strands for Use in Gene Modulation |
| CN1231675A (zh) | 1996-09-26 | 1999-10-13 | 味之素株式会社 | 修饰的生理活性蛋白及含有该蛋白的药物组合物 |
| US6770748B2 (en) | 1997-03-07 | 2004-08-03 | Takeshi Imanishi | Bicyclonucleoside and oligonucleotide analogue |
| USRE44779E1 (en) | 1997-03-07 | 2014-02-25 | Santaris Pharma A/S | Bicyclonucleoside and oligonucleotide analogues |
| JP3756313B2 (ja) | 1997-03-07 | 2006-03-15 | 武 今西 | 新規ビシクロヌクレオシド及びオリゴヌクレオチド類縁体 |
| US6794499B2 (en) | 1997-09-12 | 2004-09-21 | Exiqon A/S | Oligonucleotide analogues |
| US7572582B2 (en) | 1997-09-12 | 2009-08-11 | Exiqon A/S | Oligonucleotide analogues |
| JP4236812B2 (ja) | 1997-09-12 | 2009-03-11 | エクシコン エ/エス | オリゴヌクレオチド類似体 |
| US20030228597A1 (en) | 1998-04-13 | 2003-12-11 | Cowsert Lex M. | Identification of genetic targets for modulation by oligonucleotides and generation of oligonucleotides for gene modulation |
| US6300319B1 (en) | 1998-06-16 | 2001-10-09 | Isis Pharmaceuticals, Inc. | Targeted oligonucleotide conjugates |
| US6043352A (en) | 1998-08-07 | 2000-03-28 | Isis Pharmaceuticals, Inc. | 2'-O-Dimethylaminoethyloxyethyl-modified oligonucleotides |
| US6166239A (en) | 1998-09-04 | 2000-12-26 | Isis Pharmaceuticals, Inc. | Oligonucleotide protecting groups |
| AU1705100A (en) | 1998-10-09 | 2000-05-01 | Musc Foundation For Research Development | Blocking factor b to treat complement-mediated immune disease |
| ES2234563T5 (es) | 1999-02-12 | 2018-01-17 | Daiichi Sankyo Company, Limited | Nuevos análogos de nucleósidos y oligonucleótidos |
| US20030170249A1 (en) | 1999-02-19 | 2003-09-11 | Hakomori Sen-Itiroh | Vaccines directed to cancer-associated carbohydrate antigens |
| US7084125B2 (en) | 1999-03-18 | 2006-08-01 | Exiqon A/S | Xylo-LNA analogues |
| KR20070118315A (ko) | 1999-04-21 | 2007-12-14 | 와이어쓰 | 폴리뉴클레오티드 서열의 기능을 억제하기 위한 조성물 |
| US7053207B2 (en) | 1999-05-04 | 2006-05-30 | Exiqon A/S | L-ribo-LNA analogues |
| US6525191B1 (en) | 1999-05-11 | 2003-02-25 | Kanda S. Ramasamy | Conformationally constrained L-nucleosides |
| US6383812B1 (en) | 1999-05-28 | 2002-05-07 | Academia Sinica | Anti liver disease drug R-YEEE and method of synthesizing branched galactose-terminal glycoproteins |
| US20080281041A1 (en) | 1999-06-07 | 2008-11-13 | Rozema David B | Reversibly Masked Polymers |
| US8541548B2 (en) | 1999-06-07 | 2013-09-24 | Arrowhead Madison Inc. | Compounds and methods for reversible modification of biologically active molecules |
| JP4151751B2 (ja) | 1999-07-22 | 2008-09-17 | 第一三共株式会社 | 新規ビシクロヌクレオシド類縁体 |
| DE19935303A1 (de) * | 1999-07-28 | 2001-02-08 | Aventis Pharma Gmbh | Oligonukleotide zur Inhibierung der Expression von humanem eg5 |
| US20020082227A1 (en) * | 1999-09-30 | 2002-06-27 | Scott Henry | Use of oligonucleotides for inhibition of complement activation |
| EP1244667B1 (en) | 1999-12-30 | 2006-04-05 | K.U. Leuven Research & Development | Cyclohexene nucleic acids |
| US7491805B2 (en) * | 2001-05-18 | 2009-02-17 | Sirna Therapeutics, Inc. | Conjugates and compositions for cellular delivery |
| US7833992B2 (en) | 2001-05-18 | 2010-11-16 | Merck Sharpe & Dohme | Conjugates and compositions for cellular delivery |
| US7053199B2 (en) | 2000-08-29 | 2006-05-30 | Takeshi Imanishi | Nucleoside analogs and oligonucleotide derivatives containing these analogs |
| US6426220B1 (en) | 2000-10-30 | 2002-07-30 | Isis Pharmaceuticals, Inc. | Antisense modulation of calreticulin expression |
| CN100406065C (zh) | 2000-12-01 | 2008-07-30 | 细胞工厂治疗公司 | 糖基化/半乳糖基化肽、双官能接头和核苷酸单体/多聚体的缀合物以及相关的组合物和使用方法 |
| WO2002087541A1 (en) | 2001-04-30 | 2002-11-07 | Protiva Biotherapeutics Inc. | Lipid-based formulations for gene transfer |
| CA2452458A1 (en) | 2001-07-03 | 2003-01-16 | Isis Pharmaceuticals, Inc. | Nuclease resistant chimeric oligonucleotides |
| US20030158403A1 (en) | 2001-07-03 | 2003-08-21 | Isis Pharmaceuticals, Inc. | Nuclease resistant chimeric oligonucleotides |
| US20030175906A1 (en) | 2001-07-03 | 2003-09-18 | Muthiah Manoharan | Nuclease resistant chimeric oligonucleotides |
| US6964950B2 (en) | 2001-07-25 | 2005-11-15 | Isis Pharmaceuticals, Inc. | Antisense modulation of C-reactive protein expression |
| US20030073623A1 (en) * | 2001-07-30 | 2003-04-17 | Drmanac Radoje T. | Novel nucleic acid sequences obtained from various cDNA libraries |
| CA2459347C (en) | 2001-09-04 | 2012-10-09 | Exiqon A/S | Locked nucleic acid (lna) compositions and uses thereof |
| US7439043B2 (en) | 2001-10-10 | 2008-10-21 | Neose Technologies, Inc. | Galactosyl nucleotide sugars |
| US20100240730A1 (en) | 2002-02-20 | 2010-09-23 | Merck Sharp And Dohme Corp. | RNA Interference Mediated Inhibition of Gene Expression Using Chemically Modified Short Interfering Nucleic Acid (siNA) |
| EP1540004A4 (en) | 2002-07-31 | 2007-10-03 | Nucleonics Inc | DOUBLE-STRING RNA STRUCTURES AND CONSTRUCTS AND METHOD FOR THE PRODUCTION AND USE THEREOF |
| AU2003261449A1 (en) * | 2002-08-07 | 2004-02-25 | Compositions for rna interference and methods of use thereof | |
| CA2498772A1 (en) | 2002-09-11 | 2004-03-25 | Santaris Pharma A/S | Modified pna molecules |
| CA2502649A1 (en) | 2002-10-18 | 2004-04-29 | Nucleonics Inc. | Double-stranded rna structures and constructs, and methods for generating and using the same |
| WO2004041889A2 (en) | 2002-11-05 | 2004-05-21 | Isis Pharmaceuticals, Inc. | Polycyclic sugar surrogate-containing oligomeric compounds and compositions for use in gene modulation |
| AU2003291755A1 (en) | 2002-11-05 | 2004-06-07 | Isis Pharmaceuticals, Inc. | Oligomers comprising modified bases for binding cytosine and uracil or thymine and their use |
| US6673661B1 (en) | 2002-12-20 | 2004-01-06 | Taiwan Semiconductor Manufacturing Co., Ltd. | Self-aligned method for forming dual gate thin film transistor (TFT) device |
| US20070015927A1 (en) | 2003-01-09 | 2007-01-18 | Kim Byeang H | New phosphoramidite compounds |
| CA2518475C (en) | 2003-03-07 | 2014-12-23 | Alnylam Pharmaceuticals, Inc. | Irna agents comprising asymmetrical modifications |
| US7851615B2 (en) | 2003-04-17 | 2010-12-14 | Alnylam Pharmaceuticals, Inc. | Lipophilic conjugated iRNA agents |
| ES2702942T3 (es) | 2003-04-17 | 2019-03-06 | Alnylam Pharmaceuticals Inc | Agentes de ARNi modificados |
| US7723509B2 (en) | 2003-04-17 | 2010-05-25 | Alnylam Pharmaceuticals | IRNA agents with biocleavable tethers |
| US20070123466A1 (en) | 2003-05-13 | 2007-05-31 | New York Society For The Ruptured And Crippled Maintaining The Hospital For Special Surgery | Method of treating recurrent miscarriages |
| WO2004101619A1 (ja) | 2003-05-15 | 2004-11-25 | Shionogi Co., Ltd. | 機能的糖ペプチドの合理的設計および合成 |
| WO2004106356A1 (en) | 2003-05-27 | 2004-12-09 | Syddansk Universitet | Functionalized nucleotide derivatives |
| EP1661905B9 (en) | 2003-08-28 | 2012-12-19 | IMANISHI, Takeshi | Novel artificial nucleic acids of n-o bond crosslinkage type |
| CA2538252C (en) | 2003-09-18 | 2014-02-25 | Isis Pharmaceuticals, Inc. | 4'-thionucleosides and oligomeric compounds |
| US7959919B2 (en) | 2003-11-19 | 2011-06-14 | Novelmed Therapeutics, Inc. | Method of inhibiting factor B-mediated complement activation |
| US20060019941A1 (en) | 2003-12-23 | 2006-01-26 | Infinity Pharmaceuticals, Inc. | Analogs of benzoquinone-containing ansamycins and methods of use thereof |
| JPWO2005061707A1 (ja) | 2003-12-24 | 2007-07-12 | 協和醗酵工業株式会社 | 癌細胞のEg5阻害剤に対する感受性を判定する方法 |
| US20050244851A1 (en) | 2004-01-13 | 2005-11-03 | Affymetrix, Inc. | Methods of analysis of alternative splicing in human |
| PL1713503T3 (pl) | 2004-02-10 | 2014-02-28 | Univ Colorado Regents | Hamowanie czynnika B, alternatywny szlak dopełniacza i związane z tym sposoby |
| US20050244869A1 (en) | 2004-04-05 | 2005-11-03 | Brown-Driver Vickie L | Modulation of transthyretin expression |
| JPWO2005097155A1 (ja) | 2004-04-08 | 2008-02-28 | タカラバイオ株式会社 | 神経突起伸長誘導剤 |
| EP1791567B1 (en) | 2004-08-10 | 2015-07-29 | Alnylam Pharmaceuticals Inc. | Chemically modified oligonucleotides |
| US20090203132A1 (en) | 2004-09-09 | 2009-08-13 | Swayze Eric E | Pyrrolidinyl groups for attaching conjugates to oligomeric compounds |
| US7919472B2 (en) | 2004-09-17 | 2011-04-05 | Isis Pharmaceuticals, Inc. | Enhanced antisense oligonucleotides |
| WO2006047842A2 (en) | 2004-11-08 | 2006-05-11 | K.U. Leuven Research And Development | Modified nucleosides for rna interference |
| US20060148740A1 (en) | 2005-01-05 | 2006-07-06 | Prosensa B.V. | Mannose-6-phosphate receptor mediated gene transfer into muscle cells |
| US20080206869A1 (en) | 2005-01-24 | 2008-08-28 | Avaris Ab | Nucleic Acid Complex |
| KR20080065617A (ko) | 2005-09-19 | 2008-07-14 | 존슨 앤드 존슨 파머슈티컬 리서치 앤드 디벨로프먼트 엘엘씨 | 글루코코티코이드 수용체 발현의 조절 |
| WO2007056111A1 (en) * | 2005-11-02 | 2007-05-18 | The Government Of The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Method evolved for recognition and testing of age related macular degeneration (mert-armd) |
| WO2007090071A2 (en) | 2006-01-27 | 2007-08-09 | Isis Pharmaceuticals, Inc. | 6-modified bicyclic nucleic acid analogs |
| US7569686B1 (en) | 2006-01-27 | 2009-08-04 | Isis Pharmaceuticals, Inc. | Compounds and methods for synthesis of bicyclic nucleic acid analogs |
| JP2009536222A (ja) * | 2006-05-05 | 2009-10-08 | アイシス ファーマシューティカルズ, インコーポレーテッド | Pcsk9の発現を調節するための化合物および方法 |
| US7666854B2 (en) | 2006-05-11 | 2010-02-23 | Isis Pharmaceuticals, Inc. | Bis-modified bicyclic nucleic acid analogs |
| AU2007249349B2 (en) | 2006-05-11 | 2012-03-08 | Isis Pharmaceuticals, Inc. | 5'-Modified bicyclic nucleic acid analogs |
| US8658211B2 (en) | 2006-08-18 | 2014-02-25 | Arrowhead Madison Inc. | Polyconjugates for in vivo delivery of polynucleotides |
| CN101500548A (zh) | 2006-08-18 | 2009-08-05 | 弗·哈夫曼-拉罗切有限公司 | 用于体内递送多核苷酸的多缀合物 |
| AU2007299705B2 (en) | 2006-09-22 | 2012-09-06 | Dharmacon, Inc. | Duplex oligonucleotide complexes and methods for gene silencing by RNA interference |
| ES2526295T5 (es) | 2006-10-18 | 2021-05-04 | Ionis Pharmaceuticals Inc | Compuestos antisentido |
| WO2008101157A1 (en) | 2007-02-15 | 2008-08-21 | Isis Pharmaceuticals, Inc. | 5'-substituted-2'-f modified nucleosides and oligomeric compounds prepared therefrom |
| US9216228B2 (en) | 2007-02-16 | 2015-12-22 | KTB Tumorforschungsgesellschaft MBM | Receptor and antigen targeted prodrug |
| JP5332064B2 (ja) | 2007-03-01 | 2013-11-06 | ウェルスタット イムノセラピューティクス, エルエルシー | 炎症により特徴付けられる疾患の治療 |
| US20100055782A1 (en) * | 2007-03-02 | 2010-03-04 | Mdrna, Inc. | Nucleic acid compounds for inhibiting myc gene expression and uses thereof |
| CA2685127C (en) | 2007-04-23 | 2019-01-08 | Alnylam Pharmaceuticals, Inc. | Glycoconjugates of rna interference agents |
| CA2688321A1 (en) | 2007-05-30 | 2008-12-11 | Isis Pharmaceuticals, Inc. | N-substituted-aminomethylene bridged bicyclic nucleic acid analogs |
| DK2173760T4 (en) | 2007-06-08 | 2016-02-08 | Isis Pharmaceuticals Inc | Carbocyclic bicyclic nukleinsyreanaloge |
| US20090004140A1 (en) | 2007-06-26 | 2009-01-01 | Yao-Ling Qiu | 4-substituted pyrrolidine as anti-infectives |
| AU2008272918B2 (en) | 2007-07-05 | 2012-09-13 | Isis Pharmaceuticals, Inc. | 6-disubstituted bicyclic nucleic acid analogs |
| KR101654007B1 (ko) | 2007-08-15 | 2016-09-05 | 아이오니스 파마수티컬즈, 인코포레이티드 | 테트라하이드로피란 핵산 유사체 |
| US20090123928A1 (en) | 2007-10-11 | 2009-05-14 | The Johns Hopkins University | Genomic Landscapes of Human Breast and Colorectal Cancers |
| WO2009067647A1 (en) | 2007-11-21 | 2009-05-28 | Isis Pharmaceuticals, Inc. | Carbocyclic alpha-l-bicyclic nucleic acid analogs |
| WO2009073809A2 (en) | 2007-12-04 | 2009-06-11 | Alnylam Pharmaceuticals, Inc. | Carbohydrate conjugates as delivery agents for oligonucleotides |
| CA2713379A1 (en) | 2008-01-31 | 2009-11-05 | Alnylam Pharmaceuticals, Inc. | Optimized methods for delivery of dsrna targeting the pcsk9 gene |
| WO2009100320A2 (en) | 2008-02-07 | 2009-08-13 | Isis Pharmaceuticals, Inc. | Bicyclic cyclohexitol nucleic acid analogs |
| US20110130440A1 (en) | 2008-03-26 | 2011-06-02 | Alnylam Pharmaceuticals, Inc. | Non-natural ribonucleotides, and methods of use thereof |
| CA2721183C (en) | 2008-04-11 | 2019-07-16 | Alnylam Pharmaceuticals, Inc. | Site-specific delivery of nucleic acids by combining targeting ligands with endosomolytic components |
| WO2009143369A2 (en) | 2008-05-22 | 2009-11-26 | Isis Pharmaceuticals, Inc. | Method of preparing nucleosides and analogs thereof without using chromatography |
| NZ591057A (en) | 2008-07-10 | 2012-11-30 | Az Univ Amsterdam | Complement antagonists and uses thereof |
| EP2323667A4 (en) | 2008-08-07 | 2012-07-25 | Isis Pharmaceuticals Inc | MODULATION OF TRANSTHYRETIN EXPRESSION BY TREATMENT OF CNS DISEASES |
| AU2009298802A1 (en) | 2008-09-23 | 2010-04-08 | Alnylam Pharmaceuticals, Inc. | Chemical modifications of monomers and oligonucleotides with cycloaddition |
| DK2356129T3 (da) | 2008-09-24 | 2013-05-13 | Isis Pharmaceuticals Inc | Substituerede alpha-L-bicykliske nukleosider |
| DK2361256T3 (da) | 2008-09-24 | 2013-07-01 | Isis Pharmaceuticals Inc | Cyclohexenyl-nukleinsyreanaloger |
| MX360460B (es) | 2008-10-20 | 2018-11-05 | Alnylam Pharmaceuticals Inc | Composiciones y metodos para inhibir la expresion de transtiretina. |
| US20120059045A1 (en) | 2008-10-24 | 2012-03-08 | Isis Pharmaceuticals, Inc. | Methods of using oligomeric compounds comprising 2'-substituted nucleosides |
| EP2447274B1 (en) | 2008-10-24 | 2017-10-04 | Ionis Pharmaceuticals, Inc. | Oligomeric compounds and methods |
| CN111808084A (zh) | 2008-11-10 | 2020-10-23 | 阿布特斯生物制药公司 | 用于递送治疗剂的新型脂质和组合物 |
| EP3243504A1 (en) | 2009-01-29 | 2017-11-15 | Arbutus Biopharma Corporation | Improved lipid formulation |
| AU2010221419B2 (en) | 2009-03-02 | 2015-10-01 | Alnylam Pharmaceuticals, Inc. | Nucleic acid chemical modifications |
| FR2943060B1 (fr) | 2009-03-13 | 2013-01-04 | Commissariat Energie Atomique | Agents chelatants d'ions metalliques, leurs procedes de preparation et leurs applications |
| SG10201911942UA (en) | 2009-05-05 | 2020-02-27 | Muthiah Manoharan | Lipid compositions |
| KR101766408B1 (ko) | 2009-06-10 | 2017-08-10 | 알닐람 파마슈티칼스 인코포레이티드 | 향상된 지질 조성물 |
| JP5894913B2 (ja) | 2009-06-15 | 2016-03-30 | アルナイラム ファーマシューティカルズ, インコーポレイテッドAlnylam Pharmaceuticals, Inc. | Pcsk9遺伝子を標的とする、脂質で製剤化されたdsrna |
| US9512164B2 (en) | 2009-07-07 | 2016-12-06 | Alnylam Pharmaceuticals, Inc. | Oligonucleotide end caps |
| WO2011005860A2 (en) | 2009-07-07 | 2011-01-13 | Alnylam Pharmaceuticals, Inc. | 5' phosphate mimics |
| US9012421B2 (en) | 2009-08-06 | 2015-04-21 | Isis Pharmaceuticals, Inc. | Bicyclic cyclohexose nucleic acid analogs |
| TWI458493B (zh) | 2009-09-25 | 2014-11-01 | Iner Aec Executive Yuan | 新穎肝標靶藥劑與合成方法 |
| BR112012008865A2 (pt) | 2009-10-16 | 2019-09-24 | Glaxo Group Ltd | inibidores de hbv anti-sentido. |
| TWI391144B (zh) | 2009-10-26 | 2013-04-01 | Iner Aec Executive Yuan | 一種定量肝殘餘功能的檢驗方法與其新穎肝受體造影檢驗藥劑 |
| TWI388338B (zh) | 2009-10-26 | 2013-03-11 | Iner Aec Executive Yuan | 對聚合醣鏈進行放射標誌以作為肝受體造影劑之方法 |
| WO2011072290A2 (en) | 2009-12-11 | 2011-06-16 | The Regents Of The University Of Michigan | Targeted dendrimer-drug conjugates |
| US9198972B2 (en) | 2010-01-28 | 2015-12-01 | Alnylam Pharmaceuticals, Inc. | Monomers and oligonucleotides comprising cycloaddition adduct(s) |
| SI2539451T1 (sl) | 2010-02-24 | 2016-04-29 | Arrowhead Research Corporation | Sestavki za ciljano dostavo sirna |
| US9193752B2 (en) | 2010-03-17 | 2015-11-24 | Isis Pharmaceuticals, Inc. | 5′-substituted bicyclic nucleosides and oligomeric compounds prepared therefrom |
| EP2553019A1 (en) | 2010-03-26 | 2013-02-06 | Mersana Therapeutics, Inc. | Modified polymers for delivery of polynucleotides, method of manufacture, and methods of use thereof |
| US20130109817A1 (en) | 2010-03-26 | 2013-05-02 | Mersana Therapeutics, Inc. | Modified Polymers for Delivery of Polynucleotides, Method of Manufacture, and Methods of Use Thereof |
| US9102938B2 (en) | 2010-04-01 | 2015-08-11 | Alnylam Pharmaceuticals, Inc. | 2′ and 5′ modified monomers and oligonucleotides |
| WO2011133871A2 (en) | 2010-04-22 | 2011-10-27 | Alnylam Pharmaceuticals, Inc. | 5'-end derivatives |
| US10913767B2 (en) | 2010-04-22 | 2021-02-09 | Alnylam Pharmaceuticals, Inc. | Oligonucleotides comprising acyclic and abasic nucleosides and analogs |
| EP2601204B1 (en) | 2010-04-28 | 2016-09-07 | Ionis Pharmaceuticals, Inc. | Modified nucleosides and oligomeric compounds prepared therefrom |
| PL2563920T3 (pl) | 2010-04-29 | 2017-08-31 | Ionis Pharmaceuticals, Inc. | Modulacja ekspresji transtyretyny |
| US20130236968A1 (en) | 2010-06-21 | 2013-09-12 | Alnylam Pharmaceuticals, Inc. | Multifunctional copolymers for nucleic acid delivery |
| CA2812046A1 (en) | 2010-09-15 | 2012-03-22 | Alnylam Pharmaceuticals, Inc. | Modified irna agents |
| WO2012068187A1 (en) | 2010-11-19 | 2012-05-24 | Merck Sharp & Dohme Corp. | Poly(amide) polymers for the delivery of oligonucleotides |
| AU2011343664B2 (en) | 2010-12-17 | 2015-10-08 | Arrowhead Pharmaceuticals, Inc. | Galactose cluster-pharmacokinetic modulator targeting moiety for siRNA |
| US8501930B2 (en) | 2010-12-17 | 2013-08-06 | Arrowhead Madison Inc. | Peptide-based in vivo siRNA delivery system |
| CA3131967A1 (en) | 2010-12-29 | 2012-07-05 | F. Hoffman-La Roche Ag | Small molecule conjugates for intracellular delivery of nucleic acids |
| EP2673361B1 (en) | 2011-02-08 | 2016-04-13 | Ionis Pharmaceuticals, Inc. | Oligomeric compounds comprising bicyclic nucleotides and uses thereof |
| CN103562215B (zh) | 2011-04-01 | 2017-04-26 | 埃西斯药品公司 | 信号转导及转录激活蛋白3(stat3)表达的调节 |
| WO2012145674A1 (en) | 2011-04-21 | 2012-10-26 | Isis Pharmaceuticals, Inc. | Modulation of hepatitis b virus (hbv) expression |
| RS61447B1 (sr) | 2011-04-21 | 2021-03-31 | Glaxo Group Ltd | Modulacija ekspresije virusa hepatitisa b (hbv) |
| EP2723758B1 (en) | 2011-06-21 | 2018-06-20 | Alnylam Pharmaceuticals, Inc. | Angiopoietin-like 3 (angptl3) irna compostions and methods of use thereof |
| WO2013032829A1 (en) | 2011-08-26 | 2013-03-07 | Arrowhead Research Corporation | Poly(vinyl ester) polymers for in vivo nucleic acid delivery |
| WO2013033230A1 (en) | 2011-08-29 | 2013-03-07 | Isis Pharmaceuticals, Inc. | Oligomer-conjugate complexes and their use |
| EP3730618A1 (en) * | 2011-11-18 | 2020-10-28 | Alnylam Pharmaceuticals, Inc. | Rnai agents, compositions and methods of use thereof for treating transthyretin (ttr) associated diseases |
| WO2013119979A1 (en) | 2012-02-08 | 2013-08-15 | Isis Pharmaceuticals, Inc. | Methods and compositions for modulating factor vii expression |
| WO2013159108A2 (en) | 2012-04-20 | 2013-10-24 | Isis Pharmaceuticals, Inc. | Oligomeric compounds comprising bicyclic nucleotides and uses thereof |
| US20150299696A1 (en) | 2012-05-02 | 2015-10-22 | Sirna Therapeutics, Inc. | SHORT INTERFERING NUCLEIC ACID (siNA) COMPOSITIONS |
| US20160002624A1 (en) | 2012-05-17 | 2016-01-07 | Isis Pharmaceuticals, Inc. | Antisense oligonucleotide compositions |
| US9695418B2 (en) | 2012-10-11 | 2017-07-04 | Ionis Pharmaceuticals, Inc. | Oligomeric compounds comprising bicyclic nucleosides and uses thereof |
| CN104837996A (zh) | 2012-11-15 | 2015-08-12 | 罗氏创新中心哥本哈根有限公司 | 抗apob反义缀合物化合物 |
| WO2014118272A1 (en) | 2013-01-30 | 2014-08-07 | Santaris Pharma A/S | Antimir-122 oligonucleotide carbohydrate conjugates |
| AU2014211406B2 (en) | 2013-01-30 | 2019-07-18 | Roche Innovation Center Copenhagen A/S | LNA oligonucleotide carbohydrate conjugates |
| IL288931B2 (en) * | 2013-03-14 | 2025-05-01 | Alnylam Pharmaceuticals Inc | Compositions comprising a complementary portion of C5 IRNA and methods of using them |
| DK2992098T3 (da) | 2013-05-01 | 2019-06-17 | Ionis Pharmaceuticals Inc | Sammensætninger og fremgangsmåder til modulering af hbv- og ttr-ekspression |
| EP3564374A1 (en) | 2013-06-21 | 2019-11-06 | Ionis Pharmaceuticals, Inc. | Compositions and methods for modulation of target nucleic acids |
| HUE048738T2 (hu) | 2013-06-27 | 2020-08-28 | Roche Innovation Ct Copenhagen As | Antiszensz oligomerek és konjugátumok, amelyek a PCK9-t célozzák meg |
| DE102013106985A1 (de) * | 2013-07-03 | 2015-01-22 | Osram Oled Gmbh | Optoelektronische Bauelementevorrichtung und Verfahren zum Herstellen einer optoelektronischen Bauelementevorrichtung |
| WO2015006740A2 (en) * | 2013-07-11 | 2015-01-15 | Alnylam Pharmaceuticals, Inc. | Oligonucleotide-ligand conjugates and process for their preparation |
| MY181251A (en) * | 2013-09-13 | 2020-12-21 | Ionis Pharmaceuticals Inc | Modulators of complement factor b |
| SG10201804960RA (en) * | 2013-12-12 | 2018-07-30 | Alnylam Pharmaceuticals Inc | Complement component irna compositions and methods of use thereof |
| EA036496B1 (ru) | 2014-05-01 | 2020-11-17 | Ионис Фармасьютикалз, Инк. | Конъюгированные олигонуклеотиды для модулирования экспрессии фактора комплемента b |
-
2015
- 2015-05-01 EA EA201692204A patent/EA036496B1/ru unknown
- 2015-05-01 AU AU2015252858A patent/AU2015252858C1/en active Active
- 2015-05-01 MX MX2016014294A patent/MX380866B/es unknown
- 2015-05-01 RS RSP20191141 patent/RS59182B1/sr unknown
- 2015-05-01 PE PE2019000234A patent/PE20190626A1/es unknown
- 2015-05-01 SI SI201530821T patent/SI3137596T1/sl unknown
- 2015-05-01 EP EP23154909.8A patent/EP4219718A3/en active Pending
- 2015-05-01 PL PL19184459.6T patent/PL3608406T3/pl unknown
- 2015-05-01 US US15/307,526 patent/US10280423B2/en active Active
- 2015-05-01 LT LTEP15786214.5T patent/LT3137596T/lt unknown
- 2015-05-01 BR BR112016022593-7A patent/BR112016022593B1/pt active IP Right Grant
- 2015-05-01 CA CA2943894A patent/CA2943894C/en active Active
- 2015-05-01 ES ES19184459T patent/ES2941742T3/es active Active
- 2015-05-01 PL PL15786214T patent/PL3137596T3/pl unknown
- 2015-05-01 KR KR1020167032652A patent/KR102369736B1/ko active Active
- 2015-05-01 PT PT15786214T patent/PT3137596T/pt unknown
- 2015-05-01 HR HRP20191664 patent/HRP20191664T1/hr unknown
- 2015-05-01 UA UAA201612124A patent/UA121656C2/uk unknown
- 2015-05-01 ES ES15786214T patent/ES2745825T3/es active Active
- 2015-05-01 CA CA3289039A patent/CA3289039A1/en active Pending
- 2015-05-01 CN CN201910898718.XA patent/CN110724687B/zh active Active
- 2015-05-01 SG SG10201809953QA patent/SG10201809953QA/en unknown
- 2015-05-01 RU RU2016147047A patent/RU2701645C2/ru active
- 2015-05-01 PH PH1/2016/502062A patent/PH12016502062B1/en unknown
- 2015-05-01 DK DK15786214.5T patent/DK3137596T3/da active
- 2015-05-01 CN CN201580020852.XA patent/CN106232804B/zh active Active
- 2015-05-01 HU HUE15786214A patent/HUE046272T2/hu unknown
- 2015-05-01 CR CR20200228A patent/CR20200228A/es unknown
- 2015-05-01 WO PCT/US2015/028916 patent/WO2015168635A2/en not_active Ceased
- 2015-05-01 EP EP19184459.6A patent/EP3608406B1/en active Active
- 2015-05-01 PE PE2016002157A patent/PE20170010A1/es unknown
- 2015-05-01 JP JP2016565465A patent/JP6637442B2/ja active Active
- 2015-05-01 CR CR20160554A patent/CR20160554A/es unknown
- 2015-05-01 EP EP15786214.5A patent/EP3137596B1/en active Active
- 2015-05-01 SG SG11201608502TA patent/SG11201608502TA/en unknown
-
2016
- 2016-09-18 IL IL247883A patent/IL247883B/en active IP Right Grant
- 2016-10-28 DO DO2016000291A patent/DOP2016000291A/es unknown
- 2016-11-02 CL CL2016002764A patent/CL2016002764A1/es unknown
-
2018
- 2018-07-23 CL CL2018001996A patent/CL2018001996A1/es unknown
-
2019
- 2019-03-18 US US16/357,018 patent/US20200048638A1/en not_active Abandoned
- 2019-12-19 JP JP2019228789A patent/JP7001663B2/ja active Active
- 2019-12-23 IL IL271659A patent/IL271659A/en unknown
-
2021
- 2021-05-07 US US17/314,537 patent/US11732265B2/en active Active
-
2023
- 2023-05-19 US US18/320,948 patent/US20230357776A1/en not_active Abandoned
-
2025
- 2025-06-30 US US19/256,127 patent/US20260022382A1/en active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005504522A (ja) | 2001-06-21 | 2005-02-17 | アイシス・ファーマシューティカルス・インコーポレーテッド | トランスフォーム増殖因子β受容体II発現のアンチセンスモジュレーション |
| JP2006507841A (ja) | 2002-11-14 | 2006-03-09 | ダーマコン, インコーポレイテッド | 機能的siRNAおよび超機能的siRNA |
| JP2007505605A (ja) | 2003-09-16 | 2007-03-15 | サーナ・セラピューティクス・インコーポレイテッド | 低分子干渉核酸(siNA)を使用したRNA干渉により媒介される血管内皮増殖因子遺伝子発現および血管内皮増殖因子遺伝子受容体遺伝子発現のRNA干渉媒介性抑制 |
| WO2012177947A2 (en) | 2011-06-21 | 2012-12-27 | Alnylam Pharmaceuticals, Inc. | Compositions and methods for inhibition of expression of apolipoprotein c-iii (apoc3) genes |
| WO2013166121A1 (en) | 2012-05-02 | 2013-11-07 | Merck Sharp & Dohme Corp. | Novel tetragalnac containing conjugates and methods for delivery of oligonucleotides |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7001663B2 (ja) | 補体b因子発現を調節するための組成物及び方法 | |
| JP6882411B2 (ja) | 成長ホルモン受容体発現を調節するための組成物及び方法 | |
| JP6665111B2 (ja) | Pkk発現を調節するための組成物及び方法 | |
| HK40022441A (en) | Compositions and methods for modulating complement factor b expression | |
| HK1234433A1 (en) | Compositions and methods for modulating complement factor b expression | |
| HK1234433B (en) | Compositions and methods for modulating complement factor b expression |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200117 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200310 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210201 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20210412 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210802 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20211206 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20211224 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7001663 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |