JP2013527022A - 液体混合物の自動形成及び操作システムと方法。 - Google Patents
液体混合物の自動形成及び操作システムと方法。 Download PDFInfo
- Publication number
- JP2013527022A JP2013527022A JP2012549966A JP2012549966A JP2013527022A JP 2013527022 A JP2013527022 A JP 2013527022A JP 2012549966 A JP2012549966 A JP 2012549966A JP 2012549966 A JP2012549966 A JP 2012549966A JP 2013527022 A JP2013527022 A JP 2013527022A
- Authority
- JP
- Japan
- Prior art keywords
- liquid
- fluid duct
- fluid
- valve
- duct
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502715—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by interfacing components, e.g. fluidic, electrical, optical or mechanical interfaces
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01F—MIXING, e.g. DISSOLVING, EMULSIFYING OR DISPERSING
- B01F25/00—Flow mixers; Mixers for falling materials, e.g. solid particles
- B01F25/40—Static mixers
- B01F25/42—Static mixers in which the mixing is affected by moving the components jointly in changing directions, e.g. in tubes provided with baffles or obstructions
- B01F25/43—Mixing tubes, e.g. wherein the material is moved in a radial or partly reversed direction
- B01F25/433—Mixing tubes wherein the shape of the tube influences the mixing, e.g. mixing tubes with varying cross-section or provided with inwardly extending profiles
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01F—MIXING, e.g. DISSOLVING, EMULSIFYING OR DISPERSING
- B01F25/00—Flow mixers; Mixers for falling materials, e.g. solid particles
- B01F25/40—Static mixers
- B01F25/42—Static mixers in which the mixing is affected by moving the components jointly in changing directions, e.g. in tubes provided with baffles or obstructions
- B01F25/43—Mixing tubes, e.g. wherein the material is moved in a radial or partly reversed direction
- B01F25/433—Mixing tubes wherein the shape of the tube influences the mixing, e.g. mixing tubes with varying cross-section or provided with inwardly extending profiles
- B01F25/4331—Mixers with bended, curved, coiled, wounded mixing tubes or comprising elements for bending the flow
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01F—MIXING, e.g. DISSOLVING, EMULSIFYING OR DISPERSING
- B01F33/00—Other mixers; Mixing plants; Combinations of mixers
- B01F33/30—Micromixers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502769—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by multiphase flow arrangements
- B01L3/502784—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by multiphase flow arrangements specially adapted for droplet or plug flow, e.g. digital microfluidics
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2200/00—Solutions for specific problems relating to chemical or physical laboratory apparatus
- B01L2200/02—Adapting objects or devices to another
- B01L2200/028—Modular arrangements
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0809—Geometry, shape and general structure rectangular shaped
- B01L2300/0816—Cards, e.g. flat sample carriers usually with flow in two horizontal directions
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2300/00—Additional constructional details
- B01L2300/08—Geometry, shape and general structure
- B01L2300/0861—Configuration of multiple channels and/or chambers in a single devices
- B01L2300/0867—Multiple inlets and one sample wells, e.g. mixing, dilution
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2400/00—Moving or stopping fluids
- B01L2400/04—Moving fluids with specific forces or mechanical means
- B01L2400/0475—Moving fluids with specific forces or mechanical means specific mechanical means and fluid pressure
- B01L2400/0487—Moving fluids with specific forces or mechanical means specific mechanical means and fluid pressure fluid pressure, pneumatics
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2400/00—Moving or stopping fluids
- B01L2400/04—Moving fluids with specific forces or mechanical means
- B01L2400/0475—Moving fluids with specific forces or mechanical means specific mechanical means and fluid pressure
- B01L2400/0487—Moving fluids with specific forces or mechanical means specific mechanical means and fluid pressure fluid pressure, pneumatics
- B01L2400/049—Moving fluids with specific forces or mechanical means specific mechanical means and fluid pressure fluid pressure, pneumatics vacuum
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L2400/00—Moving or stopping fluids
- B01L2400/06—Valves, specific forms thereof
- B01L2400/0633—Valves, specific forms thereof with moving parts
- B01L2400/0655—Valves, specific forms thereof with moving parts pinch valves
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01L—CHEMICAL OR PHYSICAL LABORATORY APPARATUS FOR GENERAL USE
- B01L3/00—Containers or dishes for laboratory use, e.g. laboratory glassware; Droppers
- B01L3/50—Containers for the purpose of retaining a material to be analysed, e.g. test tubes
- B01L3/502—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures
- B01L3/5027—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip
- B01L3/502738—Containers for the purpose of retaining a material to be analysed, e.g. test tubes with fluid transport, e.g. in multi-compartment structures by integrated microfluidic structures, i.e. dimensions of channels and chambers are such that surface tension forces are important, e.g. lab-on-a-chip characterised by integrated valves
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T436/00—Chemistry: analytical and immunological testing
- Y10T436/25—Chemistry: analytical and immunological testing including sample preparation
- Y10T436/2575—Volumetric liquid transfer
Abstract
第1バルブ (14, 29, 46) と,第1流体ダクト (10, 25, 28)とを備え、該第1バルブ (14, 29, 46)を上記マイクロ流体サブシステムと接続して第1液を供給し、第2流体ダクト(11)を備え、上記マイクロ流体サブシステムとを接続し、第2液を供給するようになっており、
上記第1流体バルブ (14, 29. 46)は100msecより悪くない時間分解能でもって閉鎖するに適し,そして1流体ダクト (10, 25, 28)のパラメータはXl[Paー1]の値が
Xl [Paー1] = (0.5 x 10-9+ l/E1) (αRl 2 L1 2/ A1) で定義され、104 Paー1より小さいことを特徴とする。
ここで El は材料のヤング率で、この材料で第1流体ダクト (10, 25, 28)は製造され、L1は第1流体ダクト (10, 25, 28)の長さで、A1は第1流体ダクト (10, 25, 28)の内腔面積で、αRlは第1流体ダクト (10, 25, 28)の流体抵抗Rlを示す式:Rl = αRl (LIμ/ A1 2) における幾何学的構造を特徴づける定数であり、μはRlの測定における第1流体ダクト (10, 25, 28)を満たす流体の動的粘性係数である。本発明はかかるシステムでマイクロ液滴をオンデマンドで作成する方法でもある。
Description
本発明に従って構成されたシステムはまた、微生物学では、時間と費用対効果の高い研究を実行するために使用される。
i)チャネル内での液体の要素の滞留時間が分散しない、ii)効率的かつ迅速混合、iii)動態を制御する能力、iv)並行してマルチ反応を行わせる能力、v)試薬の低消費である。これらの特性は、マイクロ流体システムでのマイクロ液滴形成の化学分析と合成のための潜在的に貴重なツールを 生化学及びフォルム微生物学のために提供する。既に液滴の使用上の既存のレポートには、化学反応の区分のためのマイクロ流体システムの使用[A.Griffithsらのマイクロ流体制御による区別コンビナトリアルケミストリー米国特許出願US20060078893]、および生化学的反応における使用[A.Hsiehら、迅速な核酸分析のための方法および装置、米国特許出願US20080166720]が提案されている。
上記供給パーツは第1バルブと第1流体ダクトとを備え,第1バルブと上記マイクロ流体サブシステムとを接続し、第1液体を供給し、
第2流体ダクトを備え、上記マイクロ流体サブシステムと接続し、第2液体を供給し、、
上記第1流体バルブは100msecより悪くない時間分解能でもって閉鎖し,そして第1流体ダクト のパラメータはΧl [Paー1]の値が
Xl[Paー1] = (0.5 x 10-9 + l/E1) (αRl L1 2/ A1) で定義され、104 Paー1より小さいことを特徴とする。
ここで El は第1流体ダクトの材料のヤング率で、L1は第1流体ダクトの長さで、A1は第1流体ダクト の内腔面積、αRlは第1流体ダクト の流体抵抗Rlを示す式:Rl = αRl (LIμ/ A1 2) における幾何学的構造を特徴づける定数であり、但し、μはRlを測定する第1流体ダクト (10, 25, 28)を満たす流体の動的粘性係数である。
X2 [Paー1] = (0.5 x 10-9+ l/E2) (αR2 L2 2/ A2) で定義され、104 Paー1より小さいことを特徴とする。
ここで E2は第2流体ダクト材料のヤング率で、L2は第2流体ダクトの長さで、A2は第2流体ダクト の内腔面積、αR2は第2流体ダクト の流体抵抗R2を示す式:R2= αR2 (L2μ/ A2 2) における幾何学的構造を特徴づける定数であり、但し、μはR2を測定する第2流体ダクト を満たす流体の動的粘性係数である。
・ 第1バルブと第1流体ダクトを通して第1液を前記マイクロサブシステムに供給する工程と、
・ 第2バルブを通しての第2液と第2流体ダクトとを備える前記マイクロサブシステムを供給する工程とからなり、
前記第1液の流れは第1及び第2流体ダクトの接合部においてマイクロ液滴を発生させるように制御される。
好ましくは、前記第1流体ダクト (10, 25, 28)のパラメータはXl [Paー1]の値が
Xl[Paー1] = (0.5 x 10-9 + l/E1) (αRl L1 2/ A1) で定義され、104 Paー1より小さくなるように選択されることを特徴とする。
ここで El は第1流体ダクト の材料のヤング率で、L1は第1流体ダクト の長さで、A1は第1流体ダクト の内腔面積、αRlは第1流体ダクト の流体抵抗Rlを示す式:Rl = αRl (LIμ/ A1 2) における幾何学的構造を特徴づける定数であり、但し、μはRlを測定する第1流体ダクト を満たす流体の動的粘性係数である。
そして第2流体ダクト のパラメータはX2 [Paー1]値が
X2 [Paー1] = (0.5 x 10-9+ l/E2) (αR2 L2 2/ A2) で定義され、104 Paー1より小さくなるように選択される。
ここで E2は第2流体ダクト (11)の材料のヤング率で、L2は第2流体ダクト (11)の長さで、A2は第2流体ダクト (11)の内腔面積、αR2は第2流体ダクト (11)の流体抵抗R2を示す式:R2= αR2 (L2μ/ A2 2) における幾何学的構造を特徴づける定数であり、但し、μはR2を測定する第2流体ダクト (11)を満たす流体の動的粘性係数である。
本発明においては マイクロ液滴はマイクロ流体システム内で形成される。該システムは液体の輸送のための少なくとも2本の相互接続した流路を備える。制限を加えるものでないが、実施例では流路は数十マイクロメータ、数百マイクロメータから1ミリメータまで幅及び高さを有する。
(1)ダクト10及び 11内の液体の流れの切り替えに必要な最小間隔
(ii) ダクト10 及び11 の、 液圧抵抗のi) バルブ 14 及び15の入口の液圧抵抗比率, 及びii) マイクロ流体 チップ1の液圧抵抗に対する比率
(iii) ダクト10 及び11の液圧コンプライアンス
関係式:t=r2/(γ1 2 v)
ここで、r はダクトルーメンの半径, γ= 2.4048は第1種のベッセル関数の第1根、vは液体の動的粘性係数である。
ダクトが非円形、コンパクトな断面 (e. g. 矩形の幅の高さに対するアスペクト比が 1/2より大きく、2以下で, 同一の式が近似として使用できる。
R = (αR L/ A2)μ
ここで、Lはダクトの長さで、Aはダクトの内腔(ルーメン)面積、αRはダクトの内腔に依存する定数であり、μはダクトを満たす流体の動的粘性係数である。その αR 値はダクトを満たす液体のパラメータに依存せず、当業者には円形パイプではαR = 8πであることが知られている。他の断面の値は例えば(Mortensen等著, Phys. Rev. E 71, 057301 (2005))に記載がある。
C=Cf+ Cc,
ここで、 Cfはキャピラリーを満たす液体の圧縮率と関連する液圧コンプライアンスを示し、Ccはキャピラリー壁の弾性と関連する液圧コンプライアンスを示す。
ΔV=ΔP(Cf+ Cc)
Cf = V0 * βrと見積られる。ここで、βrはキャピラリーを満たす液体の等温圧縮率を示す。
Cc=2Vo・(1+σ)/E.
他方、キャピラリーが薄い壁を備える場合 (h< r)、同じコンプライアンスが次のように見積もられる:
Cc=2Vo・(r / h) /E.
ここで、キャピラリー容量は V0 =πr2・Lで示される。本発明の主題は液圧コンプライアンスを減少させることにあるが、我々は厚い壁(図示せず)を備える流体ダクトの使用を考えており、円形断面と非円形断面(マイクロ流体システムに対し典型的に矩形断面)のダクトを含む。
ΔV=ΔpV0βr+2ΔpVo・(1+σ)/E = ΔVf + ΔVc
減少する圧力Δp時のキャピラリーから押し出される容量は寄与ΔVfを有し、液体の圧縮率と関連し、ΔVcはキャピラリーの壁の弾性と関連する。
ΔV= ΔVf + ΔVc
ここで、ΔVf〜(Δp/2)V0βr、ΔVc〜ΔpV0(1+σ)/Eである。
また、バルブ 14 の連続する閉鎖後キャピラリーの圧力は Pchipに減少し、キャピラリーからマイクロ流体チップに容量ΔVが押し出される。
ホ゜アソン比は0.4としてヤング率の最小値のための次の近似式を得、必要な精度を与える。
Emin = 1,4 * Vo * Δp / ΔVmax. ,
Δp = 5 バールの実施例では:
Emin = 27.489 GPa ( Vmin = I nL); 1/Emin = 0,04 x 10-9 Pa-1
Emin = 2.749 GPa ( Vmin = 10 nL); 1/Emin = 0.36 x10-9 Pa-1
Emin = 0.275 GPa ( Vmim = 100 nL); 1/Emin = 3.6 x10-9 Pa-1
Δp = 0.5 バールの実施例では
Emin = 2,749 GPa ( Vmin = I nL); 1/Emin = 0.36 x 10-9 Pa-1
Emin= 0.275 GPa ( Vmin = 10 nL); 1/Emin = 3.6 x 10-9 Pa-1
E min= 0.027 GPa ( Vmin = 100 nL); 1/Emin= 36 x 10-9 Pa-1.
Δp = 0.05 バールの実施例では:
Emin = 0.275 GPa ( Vmin = I nL); 1/Emin = 3.6 x 10-9 Pa-1
Emin = 0.027 GPa ( Vin = 10 nL); 1/Emin = 36 x 10-9 Pa-1
Emin = 0.003 GPa ( Vmin = 100 nL); 1/Emin = 360 x 10-9 Pa-1.
いくつのかの弾性パラメータを以下の表1に示す。
ΔV = ΔpA Lβ
ここで、Δpはバルブ上流のPvalveとマイクロ液体チップの圧力Pchipの差であり、Aはマイクロ流体流路でバルブと接続する流体ダクトの断面積で、Lは上記ダクトの長さ、
βはダクトのコンプライアンスを示す近似された定数で、
β=(βt/2)+(1+σ)/Eである。βt は通常の状態ではほとんどの液体で同様であり、材料の広い範囲で20%以下の範囲で変化し(スチールで1.3、シリコンゴムで1.5)、単位の50%以下であるので、簡略化のため、β=1.5X10-9+1/E と見積もられる。
ここでEはPaの単位で示され、βはPa-1の単位で示される。さらに、
オンデマンドで生成されるマイクロ液滴の最小容量Vminに対するΔVの比率は実際的に興味あるもので、
Vmin=t openQ=t openΔp/R=t openΔA2/αRμLと表現される。
そのとき、比率 ΔV/Vmin は次のように簡略化される:
(ΔV/Vmin)=(βαR L2/A) (μ/topen)
ここでβ、αR、Lは液圧ダクトを特徴つけるパラメータであり、μ及びtopenは方法のパラメータである。本発明の好ましい実施態様ではtopenは1sより大きくないと算定され、より好ましくは100ms、最も好ましくは10 msと算定される。動的粘性係数は100 mPa、10 mPaまたは1mPa(水溶液では)と算定する事ができる。
βαR L2/ A=(0.5X10-9 +1/E)(αR L2/ A) < Χ[ Pa-1]
ここで、Χ=(ΔV/Vmin)(topen /μ)である。
.上記 topen 及びμの値を挿入すると、Χ = 104 Pa-1 ,好ましくは Χ = 103 Pa-1 、より好ましくはΧ= 100 Pa-1,、最も好ましくはΧ = 10 Pa-1 が得られる。
チップ1は流路 3を含み、該流路には連続液体 26がポート 9を介して供給される。.
この連続液体は液体の加圧容器から液圧ダクト 28を介して図示しない電気制御機によって制御されているバルブ 29から送られ、バルブが開放されると,上記液体の有効な一定量が得られる。 好ましくは、流路 3の出口がマイクロ流体チップ,又は他のマイクロ流体チップに流体ダクトを介して接続されると、流路 3を通して バルブ 31によって液体流れを制御することができる。バルブは液圧ダクト 32上に位置し、該ダクトは大気圧力 33の貯槽を備えるマイクロ流体チップに接続している. 好ましくは流路3 は追加の入口ポート 7を備え, ピペット先端35の終端をマイクロ流体チップ内に挿入することを可能とする。本発明の好ましい実施態様では、マイクロ流体チップの流体ダクトはまず、連続する、湿潤液体26で入口ポート 9を介して満たされ、その後. 連続液体の流れをバルブ 29を介して停止させる。その後ピペットの先端の終端をポート 7に差し込む。好ましくはこのピッペットの先端は. 少なくとも連続液体 26, 37と混和せず、非混和性連続液体に懸濁している少なくとも一つの液体サンプル36を含む。バルブの制御により流路3からの出流(例えば31)を制御することによってピペット先端35の懸濁液体サンプルは流路に移送され、移送後はサンプル36はポート7の下流38に位置する。好ましくは液体サンプル36、38が流路内に移送され、流路3からの出流が閉じられ、そして流路3内への流入が開放されると、連続液体26でポート7が満たされ、気泡のトラップが回避される。本発明の好ましい実施例ではピペット先端35からのサンプル36の流路3への移送操作は、必要な液体サンプル38の列が流路3内に供給されるまで繰り返すことができる。好ましくは、液体サンプルの流路3内への供給が終わると、ポート7はきっちりと閉鎖され、連続液体26の流れによってサンプルの列を移送させることができる。この連続液体は入力(例えば29)と出力(例えば31)バルブの状態を制御する図示しない電気制御器からの信号を使用して制御される。
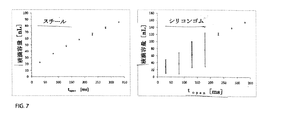
この実験的システムにおいては、すべてのマイクロ流体チャンネルは200×200マイクロメーターの公称寸法の均一な正方形断面を有する。この実施例のシステムでは、マイクロ流体チップに液体が電磁ソレノイドバルブ、大きな絵気圧抵抗を特徴とするキャピラリーを介して、供給される。分散される液体の貯槽に適応される圧力は50ミリバールに設定された。第1実験ではバルブはマイクロ流体チップと内径200μm長さ100cmのスチールキャピラリーを介してマイクロ流体チップに接続された。第2実施例ではキャピラリーはシリコンゴムで製造され、内径190μmであって長さ74cmであり、上記スチールキャピラリーとして流れる同様の液圧抵抗が存在した。スチールキャピラリーの液圧コンプライアンスはCK=3.89×10−19m3/Paに等しく、シリコンゴムの液圧コンプライアンスはCK=3.15×10−14m3/Paに等しい。図7に示すグラフは本発明によって構成されたシステムがスチールキャプラリーを備え、マイクロ液滴の容量を正確にコントロールする限り、シリコンゴムのキャプラリーを備える第2システムは満足な精度を与えないを明示している。
たとえば電界は2つの電極78および79を使用することによって発生させることができる。マイクロ液滴はより大きなマイクロ液滴を形成するように混合され、次の処理のための溶液混合物を含む。そして、それらの混合物の内容物を加工、培養又は検出するか、あるいはポート80を介して他のマイクロ流体システム又は流体ダクトに移送される。接合部73および74から接合部77にマイクロ液滴をガイドする流路はマイクロ液滴の存在を検出する検出器81および82を備えることができる。このような検出器からの信号は連続液体の流れを制御し、接合部77のマイクロ液滴の発現に同期させるようにする。
1つは、検出器のウィンドウ部102を連続的に通過するマイクロ液滴上で、又は、もう1つは検出器のウィンドウ部102に一定の間隔で停止させるマイクロ液滴上で行われる。
流路94内でマイクロ液滴104の列を前方に送る能力又はこれらのマイクロ液滴の流れを必要な間隔の間、停止させる能力はこれらの列104中のすべてのマイクロ液滴(たとえば103)に対し単一又は複数の測定を行わせる。また、マイクロ液滴のすべての列104上で測定を行うことおよび上記列での単一の液滴(例えば103)の測定の間隔を調整することが出来る。
本発明の例示的な実施形態は、図1に示すようなシステムであり、任意の入口ポート7なしで、オンデマンドでマイクロ液滴を生成するために役立てることができ、バルブ14、
ポート9及び油圧ダクト10を介して、供給源12から供給される液体から形成される。この実施例では、マイクロ流体サブシステムは正方形の断面公称寸法100×100μmのマイクロ流体流路を備える。この例では、分散される液体は蒸留水で、マイクロ流体流路の壁を濡らさないで、ソース13から供給され、バルブ15及び流体ダクト11を介してポート4に入る連続相はヘキサデカンのスパン80界面活性剤(1重量%)溶液である。この実施例では、ダクト10および11は長さ2mで内径200μmの鋼製キャピラリーである。油の貯槽に適用される圧力は1バールで、水の貯槽に加えられる圧力は333ミリバールである。液体を供給するシステムは、100 Hzのペースで駆動され、各10msでマイクロ液滴が接合部8で形成される。これらのマイクロ液滴の体積はtopenの間隔の長さによって制御され、その間、バルブ14が開かれ、バルブ15が閉じられる。図12に示すグラフはマイクロ液滴の量が直線的に変化することを示し,topenの1msから9msまでの変更時〜0.45 nLから〜4nLに変化する。topenの同じ値で生成された10個のマイクロ液滴から計算された偏差は、所定量の1%未満である(図12)。
接合部73へのヘキサデカンの連続的な液体の流れに押され、topenを50msから500ms(図14)の間で変更することにより、330nLに80 nLの容量のマイクロ液滴を生成することに使用される。同じ実施例では、流路76は、断面(800×800μm)有している。青インクの水溶液のサンプル(〜100μL)を流路76に供給する。このサンプルは、ヘキサデカンの連続的な流れに押され、topenを150msから2.8s図14)の間でtopenを変更することにより、〜0.8μLから〜9.8μLに容量の範囲でマイクロ液滴を生成するのに使用され、各接合部で生成されたマイクロ液滴の誤差は平均容量の1%未満であった。
本発明の例示的な実施形態は、図 15に示し、反応混合物の化学組成の急激なスクリーングを実行するために使用される。
システムはマイクロ液滴の形成のための3つの独立した接合部を含み、各接合部には異なる溶液が供給される。この実施例では、接合部に送られる液体は赤インクのきれいな水溶液、青インクの水溶液で、このシステムは電子制御ユニットによって制御され、三つの接合部で同期されて液滴を発生させるプロトコールを実行し、これらのボリュームのすべての可能な組み合わせを合計で1.5μLの一定体積になるようにスクリーニングする。同期
されるパケットは、3 Hzのレートで生成され、パケットの各々は3つの液滴発生器の接合部に集合される。集合された液滴は溶液とクリーン水の所定の組み合わせを含む。図15に示すグラフは入力流れを10%とする工程における二つのインキの濃度のすべての可能な組み合わせのスクリーンを示す。
本件発明の典型的な実施例は、アルブミンを量的に測定して人間又は動物の血清中におけるアルブミンの濃度を決定するものである。その典型的な測定は連続液体に作用する2つの加圧された貯槽から構成されるシステムによって実行され、前記の貯槽は電気的な制御バルブ及び流路を経てマイクロ流体チップに接続され、液圧抵抗及び液圧コンプライアンスについての要求を満たすようになっている。このマイクロ流体システムは2つの流路を有するモジュール(例えば、83)で構成され、血清及び試薬のサンプルを供給し、要求に応じて血清及び試薬を含むマイクロ液滴を生成し、これらのマイクロ液滴を反応混合物を含むより大きなマイクロ液滴に混入できるようになっている。また、このシステムは混合モジュール(例えば、84)及び分光光度計87によって構成することができる。この検出モジュール87の幾何学的な形状は、必要な光学的な流路がマイクロ液滴を通って得られるように選択することができる。本件発明によれば、連続流体をチップ83に分配するバルブを適切に操作することによって、正確に決定され望ましい容積のマイクロ液滴を生成するができる。これによって反応混合物内の血清と試薬の相対濃度を正確に決定することができる。また、これによって測定中の試薬の相対濃度を精査(screen)することができる。さらに、モジュール83内の適切な流路に最初に供給された(血清及び試薬)の各サンプルから同一の又は異なる容積の複数のマイクロ液滴を形成することが可能となる。マイクロ液滴を形成し、混入し、混合し及びモジュール83、84、87を通過する流速をコントロールすることによって、反応混合物へのマイクロ液滴の混入の実行と反応結果の分光光度計の動作の間における時間間隔を調整することができる。従って、この典型的な測定によって、比色計による測定を通して血清中のアルブミンの濃度を決定することができ、アルブミンの測定を最適化すること、例えば混合と、最適な測定感度及び分析のための測定との間における時間間隔、試験を実行するために必要な血清の容積及び試薬の容積の最小化、試薬の混入と結果の検出との間における培養の時間を短縮化することができる。
異なる実施例においては、モジュール83に血清の複数の異なるサンプルを供給し、血清の複数の異なるサンプルについて複数の測定を自動的に行うことができる。
異なる実施例においては、図16に概略的に示されるシステムが用いられ、動的測定が実行される。例えば、血清のサンプルはモジュール125に供給され、αアミラーゼの濃度を動的に測定するための試薬が同じモジュール125の第2のマイクロ液滴の生成器に供給される。これらのサンプルを用いて、モジュール125内で要求に応じてマイクロ液滴が生成される。これらのマイクロ液滴は同じモジュール125内に混入され、モジュール126内で混合され、モジュール127、128を経て、流路が接続されたモジュール129、139に流れ込み、反復測定のために用いられる。同一の又は異なる濃度の血清及び試薬を含むマイクロ液滴の連続列がダクトが接続されたモジュール129、139に移送されると、バルブ130、131、132、133がいずれかに位置され、検出モジュール134の検出器の窓に連続してマイクロ液滴を保持し、いずれかのマイクロ液滴について一連の分光光度の測定が実行される。また、(バルブ130、131、132、133によって)マイクロ液滴138の連続列が検出器の窓135を順方向及び逆方向に反復して移送され、これによってマイクロ液滴138の列の全て又は一部について一連の分光光度の測定を行うことができる。
本発明を限定するものではないが、他の実施例においては、本件発明に従って設計されたシステムを用いて、化学合成物の有毒性の決定、特にこれらの合成物の最小阻害濃度(MIC)を決定することができる。MICは微生物の成長を阻害する殺菌剤又は静菌剤の最小濃度である。実施例において、マイクロ流体のシステムはモジュール125に類似のモジュールを備え、このモジュールには2つではないがN個の接合部(ジャンクション)が設けられ、異なる供給源又はモジュールに供給されたサンプルから要求に応じて(オンデマンドで)マイクロ液滴を生成するようになっている。実施例においては、このシステムは所定の容積のN個のマイクロ液滴を効率よく同期的に成形し、各マイクロ液滴には微生物の懸濁物及び殺菌剤又は静菌剤の溶液、成長媒体及び微生物の成長の比色測定又は蛍光測定のための溶液が含まれている。本発明を限定するものではないが、好ましい実施例において、細胞の懸濁物は5×105・CFU(群生成単位)の濃度を有し、媒体はミューラ・ヒントン又はルリア・バータニ媒体、微生物の精査や所定の有毒性の検査に特に有用な異なる媒体が含まれる。微生物の成長の検出には吸収測定あるいは代謝マーカー(例えばアラマーブルー(Alamar Blue))からの蛍光の強さの測定を通じて行う光濃度計が含まれる。そのような実施例において、要求に応じて生成されたN個のマイクロ液滴は培養混合物に混入され、得られたマイクロ液滴はモジュール126に類似のモジュール内で混合され、次に培養混合物の列が流路に送られ、そこで必要な時間だけ培養される。次に、マイクロ液滴の列は検出モジュールを通過し、マイクロ液滴中の微生物の群の成長(又は代謝のレベル)が検出される。
Claims (43)
- マイクロ流体サブシステムと該マイクロ流体サブシステムに液体を供給する供給パーツとからなるシステム(1)であって、
上記供給パーツは第1バルブ (14, 29, 46) と,該第1バルブ (14, 29, 46)と上記マイクロ流体サブシステムとを接続し、第1液体を供給する第1流体ダクト (10, 25, 28)と、上記マイクロ流体サブシステムとを接続し、第2液体を供給する第2流体ダクト(11)とからなり、
上記第1流体バルブ (14, 29. 46)は100msecより悪くない時間分解能でもって閉鎖し,そして第1流体ダクト (10, 25, 28)のパラメータはXl[Paー1]の値が
Xl [Paー1] = (0.5 x 10-9+ l/E1) (αRl L1 2/ A1) で定義され、104 Paー1より小さいことを特徴とするシステム。
ここで El は第1流体ダクト (10, 25, 28)の材料のヤング率で、L1は第1流体ダクト (10, 25, 28)の長さで、A1は第1流体ダクト (10, 25, 28)の内腔面積、αRlは第1流体ダクト (10, 25, 28)の流体抵抗Rlを示す式:Rl = αRl (LIμ/ A1 2) における幾何学的構造を特徴づける定数であり、μはRlを測定する第1流体ダクト (10, 25, 28)を満たす流体の動的粘性係数である。 - 上記供給パーツが上記第2流体ダクト(11)の流れを閉じるための第2バルブ(15)をさらに備え、第2バルブ(15) は100msecより悪くない時間分解能でもって閉鎖し,そして第2流体ダクト (11)のパラメータはX2 [Paー1]値が
X2 [Paー1] = (0.5 x 10-9 + l/E2) (αR2 L2 2/ A2) で定義され、104 Paー1より小さいことを特徴とする請求項1記載のシステム。
ここで E2は第2流体ダクト (11)の材料のヤング率で、L2は第2流体ダクト (11)の長さで、A2は第2流体ダクト (11)の内腔面積、αR2は第2流体ダクト (11)の流体抵抗R2を示す式:R2= αR2 (L2μ/ A2 2) における幾何学的構造を特徴づける定数であり、μはR2を測定する第2流体ダクト (11)を満たす流体の動的粘性係数である。 - 前記X1[Pa~1]又は X2 [Pa−l]値が 103 Pa−lより低く、好ましくは102Pa−1より低く、最も好ましくは10 Pa−1.より低い請求項1又は2記載のシステム。
- 第1流体ダクト(1 O, 25, 28)の弾性 Cc1 又は第2流体ダクト(11)の弾性 Cc2 が10-16 m3/Paより高くなく、好ましくは, 10−18 m3/Paより高くなく、最も好ましくは10-20m3/Paより高くない前記請求項のいずれかに記載のシステム。
- 第1流体ダクト(lO, 25, 28)又は最2流体ダクト (1 1) の流体抵抗Routが 第1流体ダクト(l4, 29, 46)又は最2流体ダクト (1 1)の入口の流体抵抗Rinより高く、好ましくは10倍高く、最も好ましくは100倍高い前記請求項のいずれかに記載のシステム。
- 第1流体ダクト(lO, 25, 28)又は最2流体ダクト (1 1) の流体抵抗Routが マイクロ流体サブシステムの流体抵抗より高く、好ましくは10倍高く、最も好ましくは100倍高い前記請求項のいずれかに記載のシステム。」
- 第1流体ダクト(lO, 25, 28)又は最2流体ダクト (1 1) がヤング率0.5Gpaより高く、好ましくは10Gpaより高く最も好ましくは100Gpaより高く、例えば金属、スチール、セラミックス、ガラス又は硬質ポリマーから製造される前記請求項のいずれかに記載のシステム。
- 前記バルブ(14、15、29、46)の少なくとも一つが10msecより悪くない時間分解能で閉鎖するに適当である前記請求項のいずれかに記載のシステム。
- 前記バルブ(14、15、29、46)の少なくとも一つの電気コントローラ(124)をさらに備える前記請求項のいずれかに記載のシステム。
- 前記バルブ(14、15、29、46)の少なくとも一つがピエゾ電気バルブ、メンブレンバルブ、又はマイクロバルブである前記請求項のいずれかに記載のシステム。
- 前記最1液体および第2液体と混和しない第3液体の連続液滴(47、49)を前記マイクロ流体サブシステムに供給するに適するセットを備え、該セットは第3液体の液滴(47)の入口ポートを低圧又は真空に貯槽に接続し、前記バルブ(43)の開放により第3液体の液滴(47)を入口ポート(40)からシステムに引き入れるようにする請求項1〜10のいずれかに記載のシステム。
- 前記最1液体および第2液体と混和せず、懸濁する第3液体の連続液滴(36、38)を前記マイクロ流体サブシステムに供給するに適するセットを備え、第3液体の液滴(36、38)をソース(36、38)に接続する入口ポート(7、9)を備える請求項1〜10のいずれかに記載のシステム。
- 連続液滴のソースが流体ダクト(39)又はピペット(35)である請求項12記載のシステム。
- 前記第1流体ダクト(51)と第2流体ダクト(61)の接合部(54)を備えるとともに、第3流体ダクト(60)にポート(61)を介して接続するバルブを備え、前記接続部(54)からポート(57)に導き、そこで前記バルブを低圧又は真空の貯槽に接続し、前期バルブの開放により前記第3流体ダクト(60)の少なくとも一部の流体抵抗を減少させるようになっている前記請求項のいずれかに記載のシステム。
- 流体ダクトの流れの少なくことも一つの検出器(56、81、82、121、122、136、137)を備え、好ましくはホト検出器であって、前記電気コントローラ(124)と接続し、前記検出器(56、81、82、121、122、136、137)からの信号により前記バルブ(14、15、29、46)を開放または閉鎖することができるようになっている前記請求項11又は12に記載のシステム。
- 前記検出器(56)は、前記液滴(50)の一つのヘッドにより第1流体ダクト(51)と第2流体ダクト(61)の接続部(54)への接近について電気コントローラへの検出時に信号を検出して伝達するように、配置され、かつ形成されている請求項15に記載のシステム。
- 少なくとも2つの追加バルブ(98、109、113、130、132、100、111、115、131、133)を備え、そこで、前記バルブの第1(98、109、113、130、132)は前記バルブ第2(100、111、115、131、133)より高い圧力の供給源(97、108、112)に接続するとともに、流体ダクト(94)の同一部分に接続し、前記バルブの双方(98、109、113、130、132、100、111、115、131、133)の開放によって流体ダクト(94)の一部にある液体をバルブ第1(98、109、113、130、132)からバルブ第2(100、111、115、131、133)の方向に流し、前記バルブの双方(98、109、113、130、132、100、111、115、131、133)の閉鎖によって流体ダクト(94)の一部にある液体の流れを停止させることを特徴とする前記請求項のいずれかに記載のシステム。
- 2対のバルブ(109、113、130、132、111、115、131、133)を備え、そこで、前記バルブの第1対(109、113、130、132)は前記バルブの第2対(100、111、115、131、133)より高い圧力の供給源(108、112)に接続するとともに、前記各対は流体ダクトの同一部分に接続し、前記バルブの第1対の双方(109と115、130と133)を開放する一方、バルブ第2対の双方(113と115、132と131)を閉鎖することによって流体ダクトの一部にある液体を一方向に流し、、バルブ第2対の双方(113と115、132と131)を開放する一方、前記バルブ第1対の双方(109と115、130と133)を閉鎖することにより流体ダクトの一部にある液体を反対方向に流すことを特徴とする前記請求項17に記載のシステム。
- システム(84,86,126,128)は、前記マイクロ流体サブシステムが液体混合のための流体ダクトの蛇行部分を構成していることを特徴とする前記請求項のいずれかに記載のシステム。
- 検出モジュール(116、134)、好ましくは、分光光度検出器を備え、液体を有する流体ダクトに放射線ビームを提供する手段、、好ましくは導波路を構成し、前記液体を通過した放射線の検出器を備えることを特徴とする前記請求項のいずれかに記載のシステム。
- 前記マイクロ流体サブシステムが使い捨てであることを特徴とする前記請求項のいずれかに記載のシステム。
- 前記マイクロ流体サブシステムが2またはそれ以上の取り外し可能な接続可能なパーツを備えることを特徴とする前記請求項のいずれかに記載のシステム。
- 前記第1バルブ、前記第2バルブ、前記第1流体ダクト、または前記第2流体ダクトが前記マイクロ流体サブシステムと一体となっていることを特徴とする前記請求項のいずれかに記載のシステム。
- 接合部で出会う第1流体ダクトと第2流体ダクトとからなるシステムでオンデマンドで微小液滴を提供する方法であって、以下に述べるステップからなる;
・ 第1バルブと第1流体ダクトを通して第1液を前記マイクロサブシステムに供給する工程と、
・ 第2バルブを通しての第2液と第2流体ダクトとを備える前記マイクロサブシステムを供給する工程とからなり、
前記第1液の流れは第1及び第2流体ダクトの接合部においてマイクロ液滴を発生させるように制御されることを特徴とする方法。 - 前記第1流体ダクト (10, 25, 28)のパラメータはXl[Paー1]の値が
Xl [Paー1] = (0.5 x 10-9+ l/E1) (αRl L1 2/ A1) で定義され、104 Paー1より小さくなるように選択されることを特徴とする請求項24に記載の方法。
ここで El は第1流体ダクト (10, 25, 28)の材料のヤング率で、L1は第1流体ダクト (10, 25, 28)の長さで、A1は第1流体ダクト (10, 25, 28)の内腔面積、αRlは第1流体ダクト (10, 25, 28)の流体抵抗Rlを示す式:Rl = αRl (LIμ/ A1 2) における幾何学的構造を特徴づける定数であり、μはRlを測定する第1流体ダクト (10, 25, 28)を満たす流体の動的粘性係数である。 - 第2液が第2バルブ及び第2流体ダクtを介して前記マイクロ流体サブシステムに供給される工程を備え,そして第2流体ダクト (11)のパラメータはX2 [Paー1]値が
X2 [Paー1] = (0.5 x 10-9 + l/E2) (αR2 L2 2/ A2) で定義され、104 Paー1より小さくなるように選択されることを特徴とする請求項24」又は25記載の方法。
ここで E2は第2流体ダクト (11)の材料のヤング率で、L2は第2流体ダクト (11)の長さで、A2は第2流体ダクト (11)の内腔面積、αR2は第2流体ダクト (11)の流体抵抗R2を示す式:R2= αR2 (L2μ/ A2 2) における幾何学的構造を特徴づける定数であり、μはR2を測定する第2流体ダクト (11)を満たす流体の動的粘性係数である。 - 更に第2液の流れは第1及び第2流体ダクトの接合部にマイクロ液滴を発生させるように制御される請求項24、25又は26に記載の方法。
- 前記第2液は連続液でマイクロ流体サブシステムのマイクロ流路の壁面を湿潤させる請求項27に記載の方法。
- 前記第1液は連続液でマイクロ流体サブシステムのマイクロ流路の壁面を湿潤させず、第2液と混和しない請求項28に記載の方法。
- 液体が流れる流体ダクトの接合部を通しての第1液及び第2液の流れによりマイクロ液滴をオンデマンドで発生させる請求項29記載の方法。
- 前記第1液は連続液でマイクロ流体サブシステムのマイクロ流路の壁面を湿潤させ、
さらに第1液及び第2液と混和せず、マイクロ流体サブシステムのマイクロ流路の壁面を湿潤させない第3液をシステムに供給する工程を含む請求項28記載の方法。 - 前記第3液はポートを通して流体ダクトに液滴の形態で提供され、該液滴は前記流体ダクトに移動させた後流体ダクトからの流出を停止し、前記流体ダクトへの流入を開放して連続液でポートを満たすことを特徴とする請求項31記載の方法。
- 前記第1及び第2液に懸濁させた第3液の液滴の連続をシステムに供給する工程を含む請求項32記載の方法。
- 前記第3液と第1又は第2液の流れにより流体ダクト接合部を通してオンデマンドでマイクロ液体を発生させ、流体ダクト接合部を通して前記液が流れることを特徴とする請求項32又は33記載の方法。
- 前記第1液と第2液が同一液である請求項32、33又は33に記載の方法。
- 前記第1及び第2液の流れ、選択的に第3液の流れが第1及び第2バルブの開閉により制御される請求項28〜35のいずれか記載の方法。
- 前記第1及び第2バルブの開閉モーメントが所定のパルス関係に対応する請求項36記載の方法。
- 前記第1バルブが開放されると時間間隔の始期及び終期を、前記第2バルブの閉鎖した時の時間間隔の始期及び終期に関連して時間シフトさせる請求項37記載の方法。
- 前記第1バルブを開放したとき第2バルブが閉じられ、第1バルブが閉じられたとき第2バルブが開放される請求項37記載の方法。
- 第1及び第2バルブの開閉のために第1及び最2バルブに送られるステアリングインパルス間で時間シフトが、前記バルブの電気機械慣性を補償又は利用するように選択され,前記バルブが実際に開放又は閉鎖されるときその時間間隔が基本的に同期されることを特徴とする請求項36〜39のいずれかに記載の方法。
- ステアリングインパルスが方形インパルスである請求項36〜40のいずれかに記載の方法。
- 必要な濃度の反応物を有する反応混合物を製造する工程がオンデマンドで発生させる反応物のマイクロ液滴が必要な体積を有し、これを混合させることにより行われる請求項24ないし41のいずれかに記載の方法。
- オンデマンドで発生させるマイクロ液滴が0.01nLから10mLの容量を有する請求項24ないし41のいずれかに記載の方法。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PL390251A PL390251A1 (pl) | 2010-01-24 | 2010-01-24 | Metoda i układ do wytwarzania kropli na żądanie w układzie mikroprzepływowym oraz tworzenia sekwencji kropli o arbitralnie zadanych kombinacjach stężeń roztworów wejściowych |
| PL390250A PL216402B1 (pl) | 2010-01-24 | 2010-01-24 | Zawór do zamykania przepływu płynu |
| PLP-390250 | 2010-01-24 | ||
| PLP-390251 | 2010-01-24 | ||
| PL393619A PL393619A1 (pl) | 2011-01-11 | 2011-01-11 | Układ do zasilania podukładu mikroprzepływowego płynami i odpowiedni podukład mikroprzepływowy |
| PLP-393619 | 2011-01-11 | ||
| PCT/PL2011/050002 WO2011090396A1 (en) | 2010-01-24 | 2011-01-21 | System and method for automated generation and handling of liquid mixtures |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015204571A Division JP2016047528A (ja) | 2010-01-24 | 2015-10-16 | 液体混合物の自動形成及び操作システムと方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2013527022A true JP2013527022A (ja) | 2013-06-27 |
| JP2013527022A5 JP2013527022A5 (ja) | 2013-08-15 |
Family
ID=43969415
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2012549966A Pending JP2013527022A (ja) | 2010-01-24 | 2011-01-21 | 液体混合物の自動形成及び操作システムと方法。 |
| JP2015204571A Pending JP2016047528A (ja) | 2010-01-24 | 2015-10-16 | 液体混合物の自動形成及び操作システムと方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015204571A Pending JP2016047528A (ja) | 2010-01-24 | 2015-10-16 | 液体混合物の自動形成及び操作システムと方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US9132396B2 (ja) |
| EP (2) | EP2570187A3 (ja) |
| JP (2) | JP2013527022A (ja) |
| BR (1) | BRPI1106097A2 (ja) |
| RU (1) | RU2583068C2 (ja) |
| WO (1) | WO2011090396A1 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016047528A (ja) * | 2010-01-24 | 2016-04-07 | インスチチュート・ケミィ・フィジズネジ・ポルスキージ・アカデミィ・ナウク | 液体混合物の自動形成及び操作システムと方法 |
| JP2017532186A (ja) * | 2014-08-06 | 2017-11-02 | エタブリセマン・ジ・スフレ | マイクロ流体またはミリ流体デバイス内で、反応体と試薬液滴とを融合させ、または接触させるための方法 |
| JP2019525139A (ja) * | 2016-06-14 | 2019-09-05 | セルプライ・ソチエタ・ア・レスポンサビリタ・リミタータCELLPLY S.r.l. | スクリーニングキットおよび方法 |
| JP2019529081A (ja) * | 2016-09-02 | 2019-10-17 | フルイディック・アナリティクス・リミテッド | マイクロ流体デバイスのための流体流制御器の改良またはそれに関する改良 |
Families Citing this family (35)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2972198B1 (fr) | 2011-03-04 | 2017-02-10 | Centre Nat Rech Scient | Procede de suivi de reaction et systeme reactionnel pour sa mise en oeuvre |
| GB201115895D0 (en) | 2011-09-14 | 2011-10-26 | Embl | Microfluidic device |
| PL397071A1 (pl) | 2011-11-21 | 2013-05-27 | Scope Fluidics Spólka Z Ograniczona Odpowiedzialnoscia | Sposób oznaczania parametrów biochemicznych plynu ustrojowego |
| EP2785460B1 (en) * | 2011-11-29 | 2021-01-27 | Caliper Life Sciences, Inc. | Systems and methods for sampling of amplification products |
| US9689029B2 (en) | 2011-12-02 | 2017-06-27 | Caliper Life Sciences, Inc. | Systems and methods for sampling of amplification products |
| PL398979A1 (pl) | 2012-04-25 | 2013-10-28 | Scope Fluidics Spólka Z Ograniczona Odpowiedzialnoscia | Urzadzenie mikroprzeplywowe i uklad mikroprzeplywowy obejmujacy jedno lub wiecej urzadzen mikroprzeplywowych |
| US10209246B2 (en) | 2012-06-26 | 2019-02-19 | Curiosity Diagnostics Sp. Z.O.O. | Method for performing quantitation assays |
| DE102013217959A1 (de) * | 2013-09-09 | 2015-03-12 | Efficient Robotics Gmbh | Mikrofluidikanalyse-Bauelement und Herstellungsverfahren |
| US9656221B2 (en) * | 2014-01-24 | 2017-05-23 | Baker Hughes Incorporated | Systems and methods for treating fluids |
| US10775370B2 (en) * | 2015-07-17 | 2020-09-15 | Stat-Diagnostica & Innovation, S.L. | Fluidic system for performing assays |
| US10252239B2 (en) | 2015-08-14 | 2019-04-09 | Massachusetts Institute Of Technology | Multi-phase oscillatory flow reactor |
| CN105670929B (zh) * | 2016-03-14 | 2017-11-17 | 江苏大学 | 一种用于细胞培养条件优化控制的微流控实验装置与方法 |
| SG11201809482TA (en) * | 2016-05-04 | 2018-11-29 | Clearbridge Biomedics Pte Ltd | Systems and methods for enriching target cells in a sample |
| CN109789383A (zh) * | 2016-10-21 | 2019-05-21 | 惠普发展公司,有限责任合伙企业 | 微滴发生器 |
| CN107321398B (zh) * | 2017-06-27 | 2019-11-26 | 中国科学院长春光学精密机械与物理研究所 | 一种液滴自发形成与控制的系统及方法 |
| JP6936085B2 (ja) * | 2017-09-06 | 2021-09-15 | 株式会社日立プラントサービス | マイクロリアクタシステム |
| CN107446820B (zh) * | 2017-09-28 | 2021-01-05 | 清华大学 | 基于微流控芯片的单细胞采样与原位检测质谱接口装置 |
| GB201717103D0 (en) * | 2017-10-18 | 2017-11-29 | Tech Partnership Plc | Fluid ejector system |
| CN107930710A (zh) * | 2017-11-27 | 2018-04-20 | 深圳华炎微测医疗科技有限公司 | 化学发光检测微流控芯片和化学发光检测微流控芯片体系以及它们的应用 |
| CN210427605U (zh) * | 2018-06-07 | 2020-04-28 | 洛阳华清天木生物科技有限公司 | 一种微液滴处理装置 |
| CN110575851A (zh) * | 2018-06-07 | 2019-12-17 | 洛阳华清天木生物科技有限公司 | 一种用于微液滴定量分割与融合的装置、芯片以及微液滴定量分割与融合的方法 |
| CN210151104U (zh) * | 2018-06-07 | 2020-03-17 | 洛阳华清天木生物科技有限公司 | 一种微流控芯片及包括其的系统 |
| EP3613498A1 (en) * | 2018-08-24 | 2020-02-26 | Université de Liège | Microfluidic module for co-encapsulation in droplets |
| US11298701B2 (en) | 2018-11-26 | 2022-04-12 | King Instrumentation Technologies | Microtiter plate mixing control system |
| EP3921081A4 (en) | 2019-02-04 | 2022-11-30 | Illumina Inc | MICROFLUIDIC DROPLET GENERATORS |
| CN112403538A (zh) * | 2019-08-23 | 2021-02-26 | 无锡源清天木生物科技有限公司 | 一种液滴生成与融合的装置及其方法 |
| CN112403539A (zh) * | 2019-08-23 | 2021-02-26 | 无锡源清天木生物科技有限公司 | 一种微流控芯片 |
| CN110787851B (zh) * | 2019-10-25 | 2020-12-04 | 浙江大学 | 基于压力驱动的多通道液滴定量量取装置与量取方法 |
| US11376812B2 (en) | 2020-02-11 | 2022-07-05 | Helicoid Industries Inc. | Shock and impact resistant structures |
| CN111804354B (zh) * | 2020-04-07 | 2021-09-21 | 苏州大学 | 液滴无损转移装置及方法、液滴微反应方法 |
| US11346499B1 (en) | 2021-06-01 | 2022-05-31 | Helicoid Industries Inc. | Containers and methods for protecting pressure vessels |
| US11852297B2 (en) | 2021-06-01 | 2023-12-26 | Helicoid Industries Inc. | Containers and methods for protecting pressure vessels |
| CN113797986B (zh) * | 2021-10-11 | 2023-05-26 | 苏州美翎生物医学科技有限公司 | 一种可微调毛细管同轴排列的微流控芯片 |
| WO2024006078A1 (en) | 2022-06-27 | 2024-01-04 | Helicoid Industries Inc. | High impact-resistant, reinforced fiber for leading edge protection of aerodynamic structures |
| KR102524384B1 (ko) * | 2022-10-11 | 2023-04-24 | 한국표준과학연구원 | 동기화 동작 이중밸브를 사용한 미세유체 유속 정밀제어 장치 및 이를 이용한 미세유체 유속 정밀제어 방법 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003190751A (ja) * | 2001-12-25 | 2003-07-08 | Minolta Co Ltd | 混合方法、混合装置、及び該混合装置を用いた検査装置 |
| JP2005199164A (ja) * | 2004-01-15 | 2005-07-28 | Hitachi Industries Co Ltd | マイクロ流体システム |
| JP2006275023A (ja) * | 2005-03-30 | 2006-10-12 | Ebara Corp | 流量制御機構 |
| JP2007029909A (ja) * | 2005-07-29 | 2007-02-08 | Hitachi Plant Technologies Ltd | 乳化方法とその装置 |
| JP2007304045A (ja) * | 2006-05-15 | 2007-11-22 | Nippon Sheet Glass Co Ltd | 試料供給機構、それを用いた試料供給方法、マイクロ化学システム、評価システム、及びインジェクターシステム |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB2097692B (en) | 1981-01-10 | 1985-05-22 | Shaw Stewart P D | Combining chemical reagents |
| EP1099483B1 (en) | 1999-11-11 | 2009-02-11 | Allegro Technologies Limited | Liquid droplet dispensing |
| US7351376B1 (en) * | 2000-06-05 | 2008-04-01 | California Institute Of Technology | Integrated active flux microfluidic devices and methods |
| TW593122B (en) * | 2001-02-13 | 2004-06-21 | Qinetiq Ltd | Microchannel device |
| EP2278338B1 (en) * | 2002-05-09 | 2020-08-26 | The University of Chicago | Device and method for pressure-driven plug transport and reaction |
| US20060078893A1 (en) | 2004-10-12 | 2006-04-13 | Medical Research Council | Compartmentalised combinatorial chemistry by microfluidic control |
| JP2009513365A (ja) * | 2003-07-16 | 2009-04-02 | ベーリンガー インゲルハイム マイクロパーツ ゲゼルシャフト ミット ベシュレンクテル ハフツング | 板状の複合構造から微笑流体装置を製造する方法 |
| JP4551123B2 (ja) * | 2004-05-28 | 2010-09-22 | 株式会社日立プラントテクノロジー | マイクロ流体システム及びそれを用いる処理方法 |
| US20080166720A1 (en) | 2006-10-06 | 2008-07-10 | The Regents Of The University Of California | Method and apparatus for rapid nucleic acid analysis |
| JP4997571B2 (ja) * | 2006-12-19 | 2012-08-08 | 有限会社フルイド | マイクロ流体デバイスおよびそれを用いた分析装置 |
| EP2040073A1 (en) * | 2007-09-20 | 2009-03-25 | Iline Microsystems, S.L. | Microfluidic device and method for fluid clotting time determination |
| US9011777B2 (en) | 2008-03-21 | 2015-04-21 | Lawrence Livermore National Security, Llc | Monodisperse microdroplet generation and stopping without coalescence |
| WO2011090396A1 (en) * | 2010-01-24 | 2011-07-28 | Instytut Chemii Fizycznej Polskiej Akademii Nauk | System and method for automated generation and handling of liquid mixtures |
-
2011
- 2011-01-21 WO PCT/PL2011/050002 patent/WO2011090396A1/en active Application Filing
- 2011-01-21 US US13/263,229 patent/US9132396B2/en not_active Expired - Fee Related
- 2011-01-21 EP EP12158774.5A patent/EP2570187A3/en not_active Withdrawn
- 2011-01-21 BR BRPI1106097A patent/BRPI1106097A2/pt not_active IP Right Cessation
- 2011-01-21 JP JP2012549966A patent/JP2013527022A/ja active Pending
- 2011-01-21 RU RU2011139195/13A patent/RU2583068C2/ru not_active IP Right Cessation
- 2011-01-21 EP EP11705053A patent/EP2451577A1/en not_active Withdrawn
-
2015
- 2015-10-16 JP JP2015204571A patent/JP2016047528A/ja active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003190751A (ja) * | 2001-12-25 | 2003-07-08 | Minolta Co Ltd | 混合方法、混合装置、及び該混合装置を用いた検査装置 |
| JP2005199164A (ja) * | 2004-01-15 | 2005-07-28 | Hitachi Industries Co Ltd | マイクロ流体システム |
| JP2006275023A (ja) * | 2005-03-30 | 2006-10-12 | Ebara Corp | 流量制御機構 |
| JP2007029909A (ja) * | 2005-07-29 | 2007-02-08 | Hitachi Plant Technologies Ltd | 乳化方法とその装置 |
| JP2007304045A (ja) * | 2006-05-15 | 2007-11-22 | Nippon Sheet Glass Co Ltd | 試料供給機構、それを用いた試料供給方法、マイクロ化学システム、評価システム、及びインジェクターシステム |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016047528A (ja) * | 2010-01-24 | 2016-04-07 | インスチチュート・ケミィ・フィジズネジ・ポルスキージ・アカデミィ・ナウク | 液体混合物の自動形成及び操作システムと方法 |
| JP2017532186A (ja) * | 2014-08-06 | 2017-11-02 | エタブリセマン・ジ・スフレ | マイクロ流体またはミリ流体デバイス内で、反応体と試薬液滴とを融合させ、または接触させるための方法 |
| JP2019525139A (ja) * | 2016-06-14 | 2019-09-05 | セルプライ・ソチエタ・ア・レスポンサビリタ・リミタータCELLPLY S.r.l. | スクリーニングキットおよび方法 |
| JP7212523B2 (ja) | 2016-06-14 | 2023-01-25 | セルプライ・ソチエタ・ア・レスポンサビリタ・リミタータ | スクリーニングキットおよび方法 |
| JP2019529081A (ja) * | 2016-09-02 | 2019-10-17 | フルイディック・アナリティクス・リミテッド | マイクロ流体デバイスのための流体流制御器の改良またはそれに関する改良 |
Also Published As
| Publication number | Publication date |
|---|---|
| US9132396B2 (en) | 2015-09-15 |
| WO2011090396A1 (en) | 2011-07-28 |
| US20120040472A1 (en) | 2012-02-16 |
| EP2570187A2 (en) | 2013-03-20 |
| RU2011139195A (ru) | 2013-04-10 |
| RU2583068C2 (ru) | 2016-05-10 |
| BRPI1106097A2 (pt) | 2017-06-27 |
| JP2016047528A (ja) | 2016-04-07 |
| EP2451577A1 (en) | 2012-05-16 |
| EP2570187A3 (en) | 2014-08-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2016047528A (ja) | 液体混合物の自動形成及び操作システムと方法 | |
| Kaminski et al. | Controlled droplet microfluidic systems for multistep chemical and biological assays | |
| US11674170B2 (en) | Droplet generating method | |
| CN100503838C (zh) | 用于分析核酸的微流系统 | |
| US7389879B2 (en) | Sorting particles | |
| JP4543986B2 (ja) | マイクロ総合分析システム | |
| CN108139418B (zh) | 受试体处理芯片、受试体处理装置及受试体处理方法 | |
| US20150125947A1 (en) | Microfluidic device | |
| CN101995477B (zh) | 用于液体样品分析的系统 | |
| JP2013524171A (ja) | 液滴ベースのアッセイのための液滴の発生 | |
| EP3366375B1 (en) | Liquid sending method using sample processing chip and liquid sending device for sample processing chip | |
| US20180221881A1 (en) | Specimen treatment chip, specimen treatment apparatus, and specimen treatment method | |
| CN108883413A (zh) | 微流体网络装置 | |
| CN112076807B (zh) | 一种自发形成油包水液滴的微流控芯片及装置 | |
| EP2307882B1 (en) | System and method to prevent cross-contamination in assays performed in a microfludic channel | |
| CN116157500A (zh) | 采样设备和系统 | |
| CN117063071A (zh) | 非接触式分配器组件以及相关系统和方法 | |
| CN110116028A (zh) | 微流控实验装置及方法 | |
| CN114602368B (zh) | 液滴生成装置及方法 | |
| CN114752479A (zh) | 液滴生成方法及装置 | |
| PL216402B1 (pl) | Zawór do zamykania przepływu płynu |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A072 | Dismissal of procedure [no reply to invitation to correct request for examination] |
Free format text: JAPANESE INTERMEDIATE CODE: A072 Effective date: 20130516 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20130701 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20131025 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131112 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140210 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140218 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140310 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140317 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20140414 |
|
| A602 | Written permission of extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A602 Effective date: 20140421 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20140512 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20141125 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20150224 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20150324 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20150424 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20150522 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20150616 |