JP2012158593A - テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 - Google Patents
テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 Download PDFInfo
- Publication number
- JP2012158593A JP2012158593A JP2012043433A JP2012043433A JP2012158593A JP 2012158593 A JP2012158593 A JP 2012158593A JP 2012043433 A JP2012043433 A JP 2012043433A JP 2012043433 A JP2012043433 A JP 2012043433A JP 2012158593 A JP2012158593 A JP 2012158593A
- Authority
- JP
- Japan
- Prior art keywords
- formula
- compound
- independently
- liquid crystal
- alkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- GBLVEEGAUSKYLP-UHFFFAOYSA-N CCC(C(CC1)CCC1C(CC1)COC1C=C)I Chemical compound CCC(C(CC1)CCC1C(CC1)COC1C=C)I GBLVEEGAUSKYLP-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D309/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings
- C07D309/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
- C07D309/04—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having no double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D309/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings
- C07D309/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
- C07D309/04—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having no double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
- C07D309/06—Radicals substituted by oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D309/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings
- C07D309/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
- C07D309/08—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only ring hetero atom, not condensed with other rings having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D309/10—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/34—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring
- C09K19/3402—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring having oxygen as hetero atom
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
- G02F1/137—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells characterised by the electro-optical or magneto-optical effect, e.g. field-induced phase transition, orientation effect, guest-host interaction or dynamic scattering
- G02F1/139—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells characterised by the electro-optical or magneto-optical effect, e.g. field-induced phase transition, orientation effect, guest-host interaction or dynamic scattering based on orientation effects in which the liquid crystal remains transparent
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K19/00—Liquid crystal materials
- C09K19/04—Liquid crystal materials characterised by the chemical structure of the liquid crystal components, e.g. by a specific unit
- C09K19/06—Non-steroidal liquid crystal compounds
- C09K19/34—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring
- C09K19/3402—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring having oxygen as hetero atom
- C09K2019/3422—Non-steroidal liquid crystal compounds containing at least one heterocyclic ring having oxygen as hetero atom the heterocyclic ring being a six-membered ring
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2323/00—Functional layers of liquid crystal optical display excluding electroactive liquid crystal layer characterised by chemical composition
Abstract
【解決手段】 式(1)で表される化合物とする。
式(1)において、例えば、R1およびR2は炭素数1〜10のアルキルであり;T1、T2、およびT3はテトラヒドロピラン−2,5−ジイルまたはテトラヒドロピラン−3,6−ジイルであり;A1およびA2は1,4−シクロヘキシレンまたは1,4−フェニレンであり;Z1、Z2、Z3、およびZ4は単結合または炭素数1〜4のアルキレンであり;nおよびiは0または1であり;j、kおよびmは0、1、または2である。
【選択図】 なし
Description
現在、液晶表示素子の高性能化を達成するため、液晶組成物の特性に対する要求が非常に厳しくなってきている。このような要求を満足させる目的で、液晶組成物の物性を高度に調整するための液晶化合物が必要とされている。
式(1)において、R1およびR2は独立して水素または炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、任意の−(CH2)2−は−CH=CH−、または−C≡C−で置き換えられてもよく;T1、T2、およびT3は独立してテトラヒドロピラン−2,5−ジイルまたはテトラヒドロピラン−3,6−ジイルであり、A1およびA2は独立して1,4−シクロヘキシレン、1,4−フェニレン、デカヒドロナフタレン−2,6−ジイル、1,2,3,4−テトラヒドロナフタレン−2,6−ジイル、またはナフタレン−2,6−ジイルであり、これらの環において一つの−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、任意の−(CH2)2−は−CH=CH−で置き換えられてもよく、1,4−フェニレンにおいて一つの−CH=は−N=で置き換えられてもよく、そしてこれらの環において一つの水素はハロゲン、−CF3、−CHF2、−CH2F、−OCF3、−OCHF2、または−OCH2Fで置き換えられてもよく;Z1、Z2、Z3、およびZ4は独立して単結合または炭素数1〜4のアルキレンであり、このアルキレンにおいて任意の−CH2−は−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、そして任意の−(CH2)2−は−CH=CH−または−C≡C−で置き換えられてもよく;iは0または1であり;j、kおよびmは独立して0、1、または2であり;nは独立して0または1であり;i+j+k+m+nは2、3、または4であり;そしてi+k+nは1、2、3、または4であり;i+j+k+m+nが2または3のとき、j、kおよびmは独立して0または1であり;i+j+k+m+nが4、j+mが3であり、nが1のとき、jは1であり;iが0のとき、jは1または2であり;nが0のとき、mは1または2であり;iが1のとき、R1は炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、任意の−(CH2)2−は−CH=CH−、または−C≡C−で置き換えられてもよく;
nが0のときZ4は単結合であり;i+k+nが1のとき、T1、T2およびT3はテトラヒドロピラン−2,5−ジイルであり;i+j+k+m+nが2のとき、A1およびA2は独立して1,4−シクロヘキシレンまたはデカヒドロナフタレン−2,6−ジイルであり、これらの環において一つの−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく;i+j+k+m+nが3のとき、独立したA1およびA2の少なくとも1つは1,4−シクロヘキシレンまたはデカヒドロナフタレン−2,6−ジイルであり、これらの環において一つの−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく;i+j+k+m+nが4のとき、独立したA1およびA2の少なくとも2つは1,4−シクロヘキシレンまたはデカヒドロナフタレン−2,6−ジイルであり、これらの環において一つの−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく;i+j+k+m+nが3、i+kが0、A1が1,4−シクロヘキシレン、そしてA2が1,4−フェニレンのとき、R1およびR2の少なくとも一つはアルケニルであり;i+j+k+m+nが3、i+kが0、A1が1,4−シクロヘキシレン、そしてA2が2−フルオロ−1,4−フェニレンのとき、R2はアルコキシまたはアルケニルである。
式(1−1)、式(1−2)、式(1−4)〜式(1−6)、および式(1−11)〜式(1−14)において、R1、R2、およびR4は独立して水素または炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、任意の−(CH2)2−は−CH=CH−または−C≡C−で置き換えられてもよく;R3およびR5は独立して炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、任意の−(CH2)2−は−CH=CH−または−C≡C−で置き換えられてもよく;A1およびA2は独立して1,4−シクロヘキシレン、1,4−フェニレン、デカヒドロナフタレン−2,6−ジイル、1,2,3,4−テトラヒドロナフタレン−2,6−ジイル、またはナフタレン−2,6−ジイルであり、これらの環において一つの−CH2−は−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、任意の−(CH2)2−は−CH=CH−で置き換えられてもよく、1,4−フェニレンにおいて一つの−CH=は−N=で置き換えられてもよく、そしてこれらの環において一つの水素はハロゲン、−CF3、−CHF2、−CH2F、−OCF3、−OCHF2、または−OCH2Fで置き換えられてもよく;Z1、Z2、Z3、およびZ4は独立して単結合または炭素数1〜4のアルキレンであり、このアルキレンにおいて任意の−CH2−は−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、そして任意の−(CH2)2−は−CH=CH−または、−C≡C−で置き換えられてもよく;式(1−1)においてA2が1,4−フェニレンのとき、R3およびR4の少なくとも一つはアルケニルであり;式(1−2)においてA1が1,4−フェニレンのとき、R3およびR4の少なくとも一つはアルケニルであり;式(1−4)においてA1およびA2が1,4−フェニレンのとき、R3およびR4の少なくとも一つはアルケニルであり;式(1−6)においてA1が1,4−シクロヘキシレン、そしてA2が1,4−フェニレンのとき、R3およびR4の少なくとも一つはアルケニルであり;式(1−6)においてA1が1,4−シクロヘキシレン、そしてA2が2−フルオロ−1,4−フェニレンのとき、R3はアルコキシまたはアルケニルであり;式(1−6)においてA1、A2が1,4−フェニレンのとき、R3およびR4の少なくとも一つはアルケニルであり;式(1−14)においてA1が1,4−シクロヘキシレンであり、A2が1,4−フェニレンのとき、R3およびR4の少なくとも一つはアルケニルである。
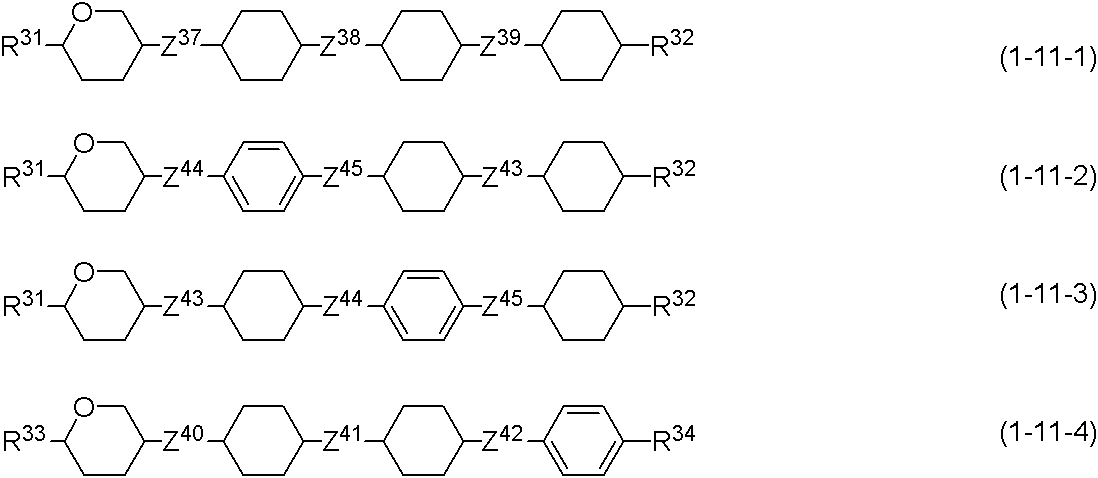
式(1−1−1)、式(1−2−1)、式(1−4−1)〜式(1−4−3)、式(1−5−1)〜式(1−5−3)、式(1−6−1)〜式(1−6−3)、式(1−11−1)〜式(1−11−4)、式(1−12−1)〜式(1−12−4)、式(1−13−1)〜式(1−13−4)、式(1−14−1)〜式(1−14−4)において、R31、R32、およびR33は独立して炭素数2〜10のアルキル、炭素数1〜9のアルコキシまたは炭素数2〜10のアルケニルであり;R34は炭素数2〜10のアルキル、炭素数1〜9のアルコキシ、または1−アルケニル以外の炭素数2〜10のアルケニルであり;R31およびR32のいずれか1つはアルキルであり;R33またはR34のいずれか1つはアルキルであり;Z31,Z32,Z33,Z37,Z38,Z39,Z40,Z41,またはZ43は独立して単結合、−(CH2)2−、または−CH=CH−であり;Z34,Z35,Z36,Z42,Z44,またはZ45は独立して単結合、または−(CH2)2−であり;Z31およびZ32のいずれか1つは単結合であり;Z33およびZ34のいずれか1つは単結合であり;Z35およびZ36のいずれか1つは単結合であり;Z37,Z38,およびZ39のいずれか2つは単結合であり;Z40,Z41,およびZ42のいずれか2つは単結合であり;Z43,Z44,およびZ45のいずれか2つは単結合である。
式(1−1−1)、式(1−2−1)において、R31、およびR32は独立して炭素数2〜10のアルキル、炭素数1〜9のアルコキシまたは炭素数2〜10のアルケニルであり;R31およびR32の一方はアルキルである。
式(1−4−1)、式(1−5−1)、式(1−6−1)において、R31、およびR32は独立して炭素数2〜10のアルキル、炭素数1〜9のアルコキシまたは炭素数2〜10のアルケニルであり;R31およびR32の一方はアルキルであり;Z31,またはZ32は独立して単結合、−(CH2)2−、または−CH=CH−であり;そしてZ31またはZ32のいずれか1つは単結合である。
式中、R7は炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は−O−または−CH=CH−で置き換えられてもよく、そして任意の水素はフッ素で置き換えられてもよく;X1はフッ素、塩素、−OCF3、−OCHF2、−CF3、−CHF2、−CH2F、−OCF2CHF2、または−OCF2CHFCF3であり;環B、Dおよび環Dは独立して1,4−シクロヘキシレン、1,3−ジオキサン−2,5−ジイルまたは任意の水素がフッ素で置き換えられてもよい1,4−フェニレンであり、環Eは1,4−シクロヘキシレンまたは任意の水素がフッ素で置き換えられてもよい1,4−フェニレンであり;Z5、およびZ6は独立して−(CH2)2−、−(CH2)4−、−COO−、−CF2O−、−OCF2−、−CH=CH−、または単結合であり;そしてL1およびL2は独立して水素またはフッ素である。
式中、R8およびR9は独立して炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は−O−または−CH=CH−で置き換えられてもよく、そして任意の水素はフッ素で置き換えられてもよく;X2は−CNまたは−C≡C−CNであり;環Gは1,4−シクロヘキシレン、1,4−フェニレン、1,3−ジオキサン−2,5−ジイル、またはピリミジン−2,5−ジイルであり;環Jは1,4−シクロヘキシレン、ピリミジン−2,5−ジイルまたは任意の水素がフッ素で置き換えられてもよい1,4−フェニレンであり;環Kは1,4−シクロヘキシレンまたは1,4−フェニレンであり;Z7は−(CH2)2−、−COO−、−CF2O−、−OCF2−、または単結合であり;L3、L4およびL5は独立して水素またはフッ素であり;そしてb、cおよびdは独立して0または1である。
式中、R10およびR11は独立して炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は−O−または−CH=CH−で置き換えられてもよく、そして任意の水素はフッ素で置き換えられてもよく、あるいはR10はフッ素であってもよく;環Mおよび環Pは独立して1,4−シクロヘキシレン、1,4−フェニレンまたはデカヒドロ−2,6−ナフチレンであり;Z8およびZ9は独立して−(CH2)2−、−COO−または単結合であり;そしてL6およびL7は独立して水素またはフッ素であり、L6とL7の少なくとも一つはフッ素である。
式中、R12およびR13は独立して炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は−O−または−CH=CH−で置き換えられてもよく、そして任意の水素はフッ素で置き換えられてもよく;環Q、環Tおよび環Uは独立して1,4−シクロヘキシレン、ピリミジン−2、5−ジイル、または任意の水素がフッ素で置き換えられてもよい1,4−フェニレンであり;そしてZ10およびZ11は独立して−C≡C−、−COO−、−(CH2)2−、−CH=CH−、または単結合である。
アリールホウ酸(21)と公知の方法で合成される化合物(22)とを、炭酸塩水溶液とテトラキス(トリフェニルホスフィン)パラジウムのような触媒の存在下で反応させて化合物(1A)を合成する。この化合物(1A)は、公知の方法で合成される化合物(23)にn−ブチルリチウムを、次いで塩化亜鉛を反応させ、ジクロロビス(トリフェニルホスフィン)パラジウムのような触媒の存在下で化合物(22)を反応させることによっても合成される。
化合物(23)にn−ブチルリチウムを、続いて二酸化炭素を反応させてカルボン酸(24)を得る。化合物(24)と、公知の方法で合成されるフェノール(25)とをDDC(1,3−ジシクロヘキシルカルボジイミド)とDMAP(4−ジメチルアミノピリジン)の存在下で脱水させて−COO−を有する化合物(1B)を合成する。この方法によって−OCO−を有する化合物も合成する。
化合物(1B)をローソン試薬のような硫黄化剤で処理して化合物(26)を得る。化合物(26)をフッ化水素ピリジン錯体とNBS(N−ブロモスクシンイミド)でフッ素化し、−CF2O−を有する化合物(1C)を合成する。M. Kuroboshi et al., Chem. Lett., 1992,827.を参照。化合物(1C)は化合物(26)を(ジエチルアミノ)サルファートリフルオリド(DAST)でフッ素化しても合成される。W. H. Bunnelle et al., J. Org. Chem. 1990, 55, 768.を参照。この方法によって−OCF2−を有する化合物も合成する。Peer. Kirsch et al., Anbew. Chem. Int. Ed. 2001, 40, 1480.に記載の方法によってこれらの結合基を生成させることも可能である。
化合物(23)をn−ブチルリチウムで処理した後、N,N−ジメチルホルムアミド(DMF)などのホルムアミドと反応させてアルデヒド(28)を得る。公知の方法で合成されるホスホニウム塩(27)をカリウムtert−ブトキシドのような塩基で処理して発生させたリンイリドを、アルデヒド(28)に反応させて化合物(1D)を合成する。反応条件によってはシス体が生成するので、必要に応じて公知の方法によりシス体をトランス体に異性化する。
化合物(1D)をパラジウム炭素のような触媒の存在下で水素化することにより、化合物(1E)を合成する。
ホスホニウム塩(27)の代わりにホスホニウム塩(29)を用い、項(IV)の方法に従って−(CH2)2−CH=CH−を有する化合物を得る。これを接触水素化して化合物(1F)を合成する。
ジクロロパラジウムとハロゲン化銅との触媒存在下で、化合物(23)に2−メチル−3−ブチン−2−オールを反応させたのち、塩基性条件下で脱保護して化合物(30)を得る。ジクロロパラジウムとハロゲン化銅との触媒存在下、化合物(30)を化合物(22)と反応させて、化合物(1G)を合成する。
化合物(23)をn−ブチルリチウムで処理したあと、テトラフルオロエチレンを反応させて化合物(31)を得る。化合物(22)をn−ブチルリチウムで処理したあと化合物(31)と反応させて化合物(1H)を合成する。
化合物(28)を水素化ホウ素ナトリウムなどの還元剤で還元して化合物(32)を得る。これを臭化水素酸などでハロゲン化して化合物(33)を得る。炭酸カリウムなどの存在下で、化合物(33)を化合物(25)と反応させて化合物(1J)を合成する。
化合物(32)の代わりに化合物(34)を用いて、項(IX)の方法に従って化合物(1K)を合成する。
J. Am. Chem. Soc., 2001, 123, 5414.に記載された方法に従い、ジケトン(−COCO−)をフッ化水素触媒の存在下、四フッ化硫黄でフッ素化して−(CF2)2−を有する化合物を得る。
出発物である化合物(36)は有機合成化学の方法に従って容易に合成することができる。
化合物(39)〜(42)において、Q1またはQ2は式(1)の構造単位である。構造単位はスキームに示した。これらの化合物におけるR1、R2、A1、A2、Z2、およびZ3の記号の意味は、項1に記載した記号の意味と同一である。
化合物(40)は有機合成化学の方法に従って容易に合成することができる。
化合物(43)〜(46)において、Q1またはQ2は式(1)の構造単位である。構造単位はスキームに示した。これらの化合物におけるR1、R2、A1、A2、Z2、およびZ3の記号の意味は、項1に記載した記号の意味と同一である。
化合物(45)は有機合成化学の方法に従って容易に合成することができる。
△εの値が正の組成物の場合:2枚のガラス基板の間隔(セルギャップ)が9μmであり、そしてツイスト角が80度のTN素子に試料を入れた。このTN素子に10ボルトを印加して、液晶分子の長軸方向における誘電率(ε‖)を測定した。0.5ボルトを印加して、液晶分子の短軸方向における誘電率(ε⊥)を測定した。誘電率異方性の値は、Δε=ε‖−ε⊥、の式から計算した。正の誘電率異方性を有する組成物をこの方法によって測定した。試料が化合物のときは、化合物を適切な組成物に混合したあと誘電率異方性を測定した。化合物の誘電率異方性は外挿値である。
(4−ペンチルシクロヘキシル)アセトアルデヒド(30.1g)をジエチルエーテ(40ml)に溶解し、シクロヘキシルアミン(15.2g)と炭酸カリウム(12g)を加え、室温で一晩撹拌した。この懸濁液をセライトろ過し、ろ液を減圧下で濃縮した。得られた黄色油状のシクロヘキシル−[2−(4−ペンチルシクロヘキシル)エチリデン]アミン(40.6g)を精製することなく第二工程に用いた。
第一工程で得られた粗製のシクロヘキシル−[2−(4−ペンチルシクロヘキシル)エチリデン]アミン(40.6g)をアクリル酸エチル(40ml)に溶解し、ヒドロキノン(0.6g)を加え、105℃で10時間加熱還流した。室温まで冷却し、THF(500ml)を加え、飽和シュウ酸水溶液(300ml)を徐々に加え、ジエチルエーテルで抽出した。有機層を水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた褐色の残渣(44.93g)をシリカゲルカラムクロマトグラフィーにて精製し、黄色油状の5−オキサ−4−(4−ペンチルシクロヘキシル)ペンタン酸エチル(27.4g)を得た。
第二工程で得られた5−オキサ−4−(4−ペンチルシクロヘキシル)ペンタン酸エチル(27.4g)をイソプロパノール(200ml)に溶解し、シアノ水素化ホウ素ナトリウム(6.5g)を加え、HCl(2N)で常にphが約3になるよう調整しながら室温で3時間撹拌した。反応液に水(100ml)を加え、トルエンで抽出した。有機層を水で洗浄し、減圧下に濃縮した。得られた橙色の残渣(23.3g)をシリカゲルカラムクロマトグラフィーにて精製し、淡黄色油状の5−(4−ペンチルシクロヘキシル)テトラヒドロピラン−2−オン(14.0g)を得た。
トリメチルシリルアセチレン(16.8ml)をTHF(300ml)に溶解した後、−70℃でn−ブチルリチウム(1.5M、ヘキサン溶液、74.2ml)を滴下し、同温度で1時間撹拌した。この溶液に第三工程で得られた5−(4−ペンチルシクロヘキシル)テトラヒドロピラン−2−オン(14.0g)を−70℃で滴下し、さらに1時間同温度で撹拌し、その後徐々に室温まで昇温した。反応物を飽和塩化アンモニウム水溶液300mlに注ぎ、ジエチルエーテルで抽出した。有機層を水で洗浄し、減圧下に濃縮した。得られた褐色の残渣(20.2g)をシリカゲルカラムクロマトグラフィーにて精製し、褐色固体5−(4−ペンチルシクロヘキシル)−2−トリメチルシラニルエチニルテトラヒドロピラン−2−オール(13.9g)を得た。
第四工程で得られた5−(4−ペンチルシクロヘキシル)−2−トリメチルシラニルエチニルテトラヒドロピラン−2−オール(13.9g)をジクロロメタン(150ml)とアセトニトリル(30ml)に溶解し、−50℃でトリエチルシラン(11.8ml)を滴下し、続けて3フッ化ホウ素−ジエチルエーテル錯体(7ml)を滴下した。ゆっくり0℃に昇温した後、氷水300ml中に注ぎ、n−ヘプタンで抽出した。有機層を水で洗浄し、減圧下に濃縮した。得られた褐色の残渣(11.0g)をシリカゲルカラムクロマトグラフィーにて精製し、黄色油状の2−エチニル−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(8.9g)を得た。
第五工程で得られた2−エチニル−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(2.9g)をイソプロパノール(50ml)に溶解し、Pd−C触媒0.15gを加えた。真空ポンプで反応容器を減圧にした後、水素を常圧で導入し、常温で一晩撹拌した。反応液をろ過し、触媒を取り除いた後、減圧下に濃縮した。得られた無色の残渣(2.7g)をシリカゲルカラムクロマトグラフィーにて精製し、無色油状の2−エチル−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(2.4g)を得た。このものをさらに再結晶を繰り返すことにより精製し、純粋な2−エチル−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(0.5g)をえた。
塩化メトキシメチルトリフェニルホスホニウム(17.9g)をTHF(150ml)に懸濁し、−20℃でカリウム−t−ブトキシド(5.8g)のTHF(150ml)溶液を滴下した。−20℃で30分撹拌した後、同温度で4’−ビニルビシクロヘキシルー4−カルボアルデヒド(9.0g)のTHF100ml溶液を滴下し、同温度で1時間撹拌した。室温まで昇温し、反応液に水(300ml)を加え、トルエンで抽出した。有機層を水で洗浄し、減圧下に約300mlまで濃縮し、n−ヘプタン(1000ml)に強く撹拌しながら投入し、減圧ろ過した。ろ液を減圧下に濃縮し、得られた淡黄色の残渣をシリカゲルカラムクロマトグラフィーにて精製し、淡黄色油状の4−(2−メトキシビニル)−4’−ビニルビシクロヘキシル(8.9g)を得た。
第一工程で得られた4−(2−メトキシビニル)−4’−ビニルビシクロヘキシル(8.9g)をアセトン(100ml)に溶解し、HCl(2N)6mlを加え室温で2時間撹拌した。反応液に水(100ml)を加え、トルエンで抽出した。有機層を水で洗浄し、減圧下に濃縮し、得られた淡黄色の残渣をシリカゲルカラムクロマトグラフィーにて精製し、淡黄色油状の(4’−ビニル−ビシクロヘキシル−4−イル)−アセトアルデヒド(8.2g)を得た。
第一工程で得られた(4’−ビニル−ビシクロヘキシル−4−イル)−アセトアルデヒド(8.2g)をTHF(100ml)に溶解し、シクロヘキシルアミン(3.5g)と炭酸カリウム(3g)を加え、室温で一晩撹拌した。この懸濁液をセライトろ過し、ろ液を減圧下で濃縮した。得られた黄色油状のシクロヘキシル−[2−(4’−ビニルシクロヘキシル−4−イル)エチリデン]アミン(11.3g)を精製することなく第四工程に用いた。
第一工程で得られた粗製のシクロヘキシル−[2−(4’−ビニルシクロヘキシル−4−イル)エチリデン]アミン(11.3g)をアクリル酸エチル(20ml)に溶解し、ヒドロキノン(0.2g)を加え、110℃で15時間加熱還流した。室温まで冷却し、THF(50ml)を加え、飽和シュウ酸水溶液(100ml)を徐々に加え、ジエチルエーテルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた黄色の残渣(11.9g)をシリカゲルカラムクロマトグラフィーにて精製し、無色油状の5−オキサ−4−(4’−ビニルビシクロヘキシル−4−イル)ペンタン酸エチル(7.8g)を得た。
第四工程で得られた5−オキサ−4−(4’−ビニルビシクロヘキシル−4−イル)ペンタン酸エチル(7.8g)イソプロパノール(40ml)に溶解し、シアノ水素化ホウ素ナトリウム(1.2g)を加え、HCl(2N)で常にphが約3になるよう調整しながら室温で3時間撹拌した。反応液に水(100ml)を加え、トルエンで抽出した。有機層を水で洗浄し、減圧下に濃縮した。得られた無色の残渣(7.3g)をシリカゲルカラムクロマトグラフィーにて精製し、無色油状の5−(4’−ビニルビシクロヘキシル−4−イル)テトラヒドロピラン−2−オン(6.0g)を得た。
細かく切り分けた金属リチウム(0.85g)をジエチルエーテル(50ml)にくわえ、室温で1−ブロモプロパン(7.4g)のTHF(30ml)溶液を反応液が緩やかに還流するようゆっくり滴下し、同温度で1時間撹拌したのち、室温で静置し固体を沈殿させ、上澄みを次の反応に用いた。別の反応装置に第五工程で得られた5−(4’−ビニルビシクロヘキシル−4−イル)テトラヒドロピラン−2−オン(6.0g)のTHF溶液を投入し、−70℃に冷却し、先ほど得られた上澄みを滴下、さらに1時間同温度で撹拌し、その後徐々に室温まで昇温した。反応物を飽和塩化アンモニウム水溶液100mlに注ぎ、ジエチルエーテルで抽出した。有機層を水で洗浄し、減圧下に濃縮した。得られた白色の固体(5.4g)をシリカゲルカラムクロマトグラフィーにて精製し、白色固体2−プロピル−5−(4’−ビニルビシクロヘキシル−4−イル)−2−テトラヒドロピラン−2−オール(1.8g)を得た。
第六工程で得られた2−プロピル−5−(4’−ビニルビシクロヘキシル−4−イル)−2−テトラヒドロピラン−2−オール(1.8g)をジクロロメタン(50ml)とアセトニトリル(10ml)に溶解し、−50℃でトリエチルシラン(1.5ml)を滴下し、続けて3フッ化ホウ素−ジエチルエーテル錯体(0.9ml)を滴下した。ゆっくり0℃に昇温した後、氷水50ml中に注ぎ、ジエチルエーテルで抽出した。有機層を水で洗浄し、減圧下に濃縮した。得られた白色固体(1.8g)をシリカゲルカラムクロマトグラフィーにて精製し、白色固体の2−プロピル−5−(4’−ビニルビシクロヘキシル−4−イル)−テトラヒドロピラン(1.4g)を得た。このものをさらに再結晶を繰り返すことにより精製し、純粋な2−プロピル−5−(4’−ビニルビシクロヘキシル−4−イル)−テトラヒドロピラン(0.6g)を得た。
2−[2−(4−エチルシクロヘキシル)エチル]−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(化合物No.1−5−1−10)の合成
第一工程
1−エチル−4−エチニルシクロヘキサン(3.5g)をTHF(100ml)に溶解した後、−70℃でn−ブチルリチウム(1.5M、ヘキサン溶液、16.0ml)を滴下し、同温度で1時間撹拌した。この溶液に実施例1の第三工程で得られた5−(4−ペンチルシクロヘキシル)テトラヒドロピラン−2−オン(5.4g)を−70℃で滴下し、さらに1時間同温度で撹拌し、その後徐々に室温まで昇温した。反応物を飽和塩化アンモニウム水溶液100mlに注ぎ、ジエチルエーテルで抽出した。有機層を水で洗浄し、減圧下に濃縮した。得られた褐色の残渣(7.9g)をシリカゲルカラムクロマトグラフィーにて精製し、褐色固体2−(4−エチルシクロヘキシルエチニル)−5−(4−ペンチルシクロヘキシル)−テトラヒドロピラン−2−オール(7.4g)を得た。
第一工程で得られた2−(4−エチルシクロヘキシルエチニル)−5−(4−ペンチルシクロヘキシル)−テトラヒドロピラン−2−オール(7.4g)をジクロロメタン(50ml)とアセトニトリル(10ml)に溶解し、−50℃でトリエチルシラン(5.4ml)を滴下し、続けて3フッ化ホウ素−ジエチルエーテル錯体(3.2ml)を滴下した。ゆっくり0℃に昇温した後、氷水50ml中に注ぎ、n−ヘプタンで抽出した。有機層を水で洗浄し、減圧下に濃縮した。得られた褐色の残渣(7.2g)をシリカゲルカラムクロマトグラフィーにて精製し、黄色油状の2−(4−エチルシクロヘキシルエチニル)−5−(4−ペンチルシクロヘキシル)−テトラヒドロピラン(6.6g)を得た。
第二工程で得られた2−(4−エチルシクロヘキシルエチニル)−5−(4−ペンチルシクロヘキシル)−テトラヒドロピラン(3.0g)をn−ヘプタン(30ml)に溶解し、Pd−C触媒0.15gを加えた。真空ポンプで反応容器を減圧にした後、水素を常圧で導入し、常温で一晩撹拌した。反応液をろ過し、触媒を取り除いた後、減圧下に濃縮した。得られた淡黄色の残渣(2.8g)をシリカゲルカラムクロマトグラフィーにて精製し、無色固体の2−[2−(4−エチルシクロヘキシル)−エチル]−5−(4−ペンチルシクロヘキシル)−テトラヒドロピラン(2.5g)を得た。このものをさらに再結晶を繰り返すことにより精製し、純粋な2−[2−(4−エチルシクロヘキシル)エチル]−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(1.5g)を得た。
、チッソ気流下アンモニアを系内から除去した。残渣に飽和塩化アンモニウム水溶液100mlを加え、ジクロロメタンで抽出した。有機層を水で洗浄し、減圧下に濃縮した。得られた黄色の残渣(3.3g)をシリカゲルカラムクロマトグラフィーにて精製し、無色固体の2−[2−(4−エチルシクロヘキシル)ビニル]−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(2.9g)を得た。このものをさらに再結晶を繰り返すことにより精製し、純粋な2−[2−(4−エチルシクロヘキシル)ビニル]−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(1.8g)を得た。
実施例1〜4、さらに記載した合成法をもとに、下記の化合物No.1−1−1−1〜1−6−3−27を合成する。実施例1〜4で得られた化合物(No.1−1−1−1、No.1−1−1−4、No.1−5−1−10、No.1−5−1−19)もリストアップした。
4つの化合物を混合して、ネマチック相を有する組成物A(母液晶)を調製した。4つの化合物は、4−(4−プロピルシクロヘキシル)ベンゾニトリル(24%)、4−(4−ペンチルシクロヘキシル)ベンゾニトリル(36%)、4−(4−ヘプチルシクロヘキシル)ベンゾニトリル(25%)、4−(4−(4−ペンチルシクロヘキシル)フェニルベンゾニトリル(15%)である。組成物Aの物性値は次のとおりであった。上限温度(NI)=71.7℃、粘度(η20)=27.0mPa・s、誘電率異方性(Δε)=11.0、光学異方性(Δn)=0.137。
調製例に記載した組成物Aの85%と実施例1で得られた2−エチル−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(化合物No.1−1−1−1)の15%とからなる組成物Bを調製した。測定した組成物Bの物性値を外挿して化合物No.1−1−1−1の物性値を算出した。上限温度(NI)=31.0、誘電率異方性(Δε)=−0.6、光学異方性(Δn)=0.024。
調製例に記載した組成物Aの85%と実施例2で得られた2−ビニル−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(化合物No.1−1−1−4)の15%とからなる組成物Cを調製した。測定した組成物Cの物性値を外挿して化合物No.1−1−1−4の物性値を算出した。上限温度(NI)=51.0、粘度(η;mPa・s)−2.8、誘電率異方性(Δε)=0.3、光学異方性(Δn)=0.050。
調製例に記載した組成物Aの85%と実施例3で得られた2−ビニル−5−(4−プロピルシクロヘキシル)テトラヒドロピラン(化合物No.1−1−1−5)の15%とからなる組成物Dを調製した。測定した組成物Dの物性値を外挿して化合物No.1−1−1−5の物性値を算出した。上限温度(NI)=37.7、誘電率異方性(Δε)=−0.4、光学異方性(Δn)=0.044。
調製例に記載した組成物Aの85%と実施例4で得られた2−エチル−5−(4’−プロピル−ビシクロヘキシル−4−イル)テトラヒドロピラン(化合物No.1−4−1−2)の15%とからなる組成物Eを調製した。測定した組成物Eの物性値を外挿して化合物No.1−4−1−2の物性値を算出した。上限温度(NI)=175.0、粘度(η;mPa・s)45.5、誘電率異方性(Δε)=0.3、光学異方性(Δn)=0.077。
調製例に記載した組成物Aの85%と実施例5で得られた5−(4’−プロピルビシクロヘキシル−4−イル)−2−ビニル−テトラヒドロピラン(化合物No.1−4−1−6)の15%とからなる組成物Fを調製した。測定した組成物Fの物性値を外挿して化合物No.1−4−1−6の物性値を算出した。上限温度(NI)=196.4、誘電率異方性(Δε)=2.1、光学異方性(Δn)=0.097。
調製例に記載した組成物Aの85%と実施例6で得られた2−プロピル−5−(4’−ビニルビシクロヘキシル−4−イル)−テトラヒドロピラン(化合物No.1−4−1−4)の15%とからなる組成物Gを調製した。測定した組成物Gの物性値を外挿して化合物No.1−4−1−4の物性値を算出した。上限温度(NI)=182.4、誘電率異方性(Δε)=1.4、光学異方性(Δn)=0.084。
調製例に記載した組成物Aの85%と実施例7で得られた2−[2−(4−エチルシクロヘキシル)エチル]−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(化合物No.1−5−1−10)の15%とからなる組成物Hを調製した。測定した組成物Hの物性値を外挿して化合物No.1−5−1−10の物性値を算出した。上限温度(NI)=141.0、粘度(η;mPa・s)36.5、誘電率異方性(Δε)=−1.7、光学異方性(Δn)=0.044。
調製例に記載した組成物Aの85%と実施例8で得られた2−[2−(4−エチルシクロヘキシル)ビニル]−5−(4−ペンチルシクロヘキシル)テトラヒドロピラン(化合物No.1−5−1−19)の15%とからなる組成物Iを調製した。測定した組成物Iの物性値を外挿して化合物No.1−5−1−19の物性値を算出した。上限温度(NI)=174.4、粘度(η;mPa・s)34.3、誘電率異方性(Δε)=1.4、光学異方性(Δn)=0.070
5−Hdh2H−2 (1−5−1−10) 10%
2−HdhH−3 (1−5−1−3) 5%
5−HB−CL (2−1) 16%
3−HH−4 (12−1) 12%
3−HH−5 (12−1) 4%
3−HHB−F (3−1) 4%
3−HHB−CL (3−1) 3%
4−HHB−CL (3−1) 4%
3−HHB(F)−F (3−2) 5%
4−HHB(F)−F (3−2) 5%
5−HHB(F)−F (3−2) 5%
7−HHB(F)−F (3−2) 5%
5−HBB(F)−F (3−23) 5%
1O1−HBBH−5 (14−1) 3%
3−HHBB(F,F)−F (4−6) 2%
4−HHBB(F,F)−F (4−6) 3%
5−HHBB(F,F)−F (4−6) 3%
3−HH2BB(F,F)−F (4−15) 3%
4−HH2BB(F,F)−F (4−15) 3%
NI=121.2℃;Δn=0.087;η(20℃)=20.8mPa・s;Δε=2.7;Vth=2.84V.
上記組成物100部にOp−05を0.25部添加したときのピッチは60.0μmであった。
5−Hdh−V (1−1−1−4) 3%
V−Hdh−5 (1−1−1−7) 3%
V−HdhVH−3 (1−5−1−23) 3%
3−HHB(F,F)−F (3−3) 9%
3−H2HB(F,F)−F (3−15) 9%
4−H2HB(F,F)−F (3−15) 8%
5−H2HB(F,F)−F (3−15) 8%
3−HBB(F,F)−F (3−24) 20%
5−HBB(F,F)−F (3−24) 14%
3−H2BB(F,F)−F (3−27) 7%
5−HHBB(F,F)−F (4−6) 3%
5−HHEBB−F (4) 2%
3−HH2BB(F,F)−F (4−15) 3%
1O1−HBBH−4 (14−1) 4%
1O1−HBBH−5 (14−1) 4%
5−Hdh−2 (1−1−1−1) 5%
5−Hdh2B−2 (1−5−2−8) 5%
5−HB−F (2−1) 12%
6−HB−F (2−1) 9%
7−HB−F (2−1) 7%
2−HHB−OCF3 (3−1) 7%
3−HHB−OCF3 (3−1) 7%
4−HHB−OCF3 (3−1) 7%
5−HHB−OCF3 (3−1) 5%
3−HH2B−OCF3 (3−4) 4%
5−HH2B−OCF3 (3−4) 4%
3−HHB(F,F)−OCF2H (3−3) 4%
3−HHB(F,F)−OCF3 (3−3) 5%
3−HH2B(F)−F (3−5) 3%
3−HBB(F)−F (3−23) 5%
5−HBB(F)−F (3−23) 5%
5−HBBH−3 (14−1) 3%
3−HB(F)BH−3 (14−2) 3%
5−Hdh−1V (1−1−1−6) 5%
3−HdhB−2 (1−5−2) 4%
5−HB−CL (2−1) 7%
3−HH−4 (12−1) 8%
3−HHB−1 (13−1) 5%
3−HHB(F,F)−F (3−3) 8%
3−HBB(F,F)−F (3−24) 20%
5−HBB(F,F)−F (3−24) 10%
3−HHEB(F,F)−F (3−12) 10%
4−HHEB(F,F)−F (3−12) 3%
5−HHEB(F,F)−F (3−12) 3%
2−HBEB(F,F)−F (3−36) 3%
3−HBEB(F,F)−F (3−36) 5%
5−HBEB(F,F)−F (3−36) 3%
3−HHBB(F,F)−F (4−6) 6%
V−Hdh2H−3 (1−5−1−13) 4%
5−Hdh2B−2 (1−5−2−8) 6%
3−HB−CL (2−1) 3%
5−HB−CL (2−1) 2%
3−HHB−OCF3 (3−1) 5%
3−H2HB−OCF3 (3−13) 5%
5−H4HB−OCF3 (3−19) 15%
V−HHB(F)−F (3−2) 5%
3−HHB(F)−F (3−2) 5%
5−HHB(F)−F (3−2) 5%
3−H4HB(F,F)−CF3 (3−21) 8%
5−H4HB(F,F)−CF3 (3−21) 10%
5−H2HB(F,F)−F (3−15) 5%
5−H4HB(F,F)−F (3−15) 7%
2−H2BB(F)−F (3−26) 5%
3−H2BB(F)−F (3−26) 5%
3−HBEB(F,F)−F (3−36) 5%
5−Hdh−V (1−1−1−4) 4%
5−Hdh2H−2 (1−5−1−10) 5%
3−HdhB−2 (1−5−2) 5%
5−HB−CL (2−1) 13%
7−HB(F,F)−F (2−3) 3%
3−HH−4 (12−1) 10%
3−HH−5 (12−1) 5%
3−HB−O2 (12−5) 5%
3−HHB−1 (13−1) 8%
3−HHB−O1 (13−1) 5%
2−HHB(F)−F (3−2) 7%
3−HHB(F)−F (3−2) 7%
5−HHB(F)−F (3−2) 7%
3−HHB(F,F)−F (3−3) 6%
3−H2HB(F,F)−F (3−15) 5%
4−H2HB(F,F)−F (3−15) 5%
2−HdhH−3 (1−5−1−3) 5%
V−HdhVH−3 (1−5−1−23) 5%
5−HB−CL (2−1) 3%
7−HB(F)−F (2−2) 7%
3−HH−4 (12−1) 9%
3−HH−EMe (−) 13%
3−HHEB−F (3−10) 8%
5−HHEB−F (3−10) 8%
3−HHEB(F,F)−F (3−12) 10%
4−HHEB(F,F)−F (3−12) 5%
4−HGB(F,F)−F (3−91) 5%
5−HGB(F,F)−F (3−91) 6%
2−H2GB(F,F)−F (3−94) 4%
3−H2GB(F,F)−F (3−94) 5%
5−GHB(F,F)−F (3−97) 7%
5−Hdh−1V (1−1−1−6) 5%
5−HdhVH−2 (1−5−1−19) 5%
3−HH−4 (12−1) 8%
3−HHB−1 (13−1) 6%
3−HHB(F,F)−F (3−3) 10%
3−H2HB(F,F)−F (3−15) 9%
3−HBB(F,F)−F (3−24) 15%
3−BB(F,F)XB(F,F)−F (3−85) 25%
1O1−HBBH−5 (14−1) 7%
2−HHBB(F,F)−F (4−6) 3%
3−HHBB(F,F)−F (4−6) 3%
3−HH2BB(F,F)−F (4−15) 4%
NI=90.6℃;Δn=0.108;η(20℃)=26.3mPa・s;Δε=9.6;Vth=1.52V.
5−Hdh2H−2 (1−5−1−10) 4%
2−HdhH−3 (1−5−1−3) 4%
3−HH−4 (12−1) 5%
3−HH−5 (12−1) 5%
3−HH−O1 (12−1) 6%
3−HH−O3 (12−1) 6%
3−HB−O1 (12−5) 5%
3−HB−O2 (12−5) 5%
3−HB(2F,3F)−O2 (7−1) 10%
5−HB(2F,3F)−O2 (7−1) 10%
3−HHEH−3 (13−20) 4%
3−HHEH−5 (13−20) 3%
4−HHEH−3 (13−20) 3%
2−HHB(2F,3F)−1 (8−1) 4%
3−HHB(2F,3F)−2 (8−1) 4%
3−HHB(2F,3F)−O2 (8−1) 12%
5−HHB(2F,3F)−O2 (8−1) 10%
NI=85.6℃;Δn=0.075;η(20℃)=27.4mPa・s;Δε=−3.3.
2−HdhH−3 (1−5−1−3) 5%
3−dh2BH−2 (1−6−3−20) 5%
5−HB−CL (2−1) 3%
7−HB(F)−F (5−3) 7%
3−HH−4 (12−1) 9%
3−HH−EMe (−) 13%
3−HHEB−F (3−10) 8%
5−HHEB−F (3−10) 8%
3−HHEB(F,F)−F (3−12) 10%
4−HHEB(F,F)−F (3−12) 5%
4−HGB(F,F)−F (3−91) 5%
5−HGB(F,F)−F (3−91) 6%
2−H2GB(F,F)−F (3−94) 4%
3−H2GB(F,F)−F (3−94) 5%
5−GHB(F,F)−F (3−97) 7%
3−dhdh−V (1−3) 5%
3−HdhB−2 (1−5−2) 4%
5−HB−CL (2−1) 7%
3−HH−4 (12−1) 8%
3−HHB−1 (13−1) 5%
3−HHB(F,F)−F (3−3) 8%
3−HBB(F,F)−F (3−24) 20%
5−HBB(F,F)−F (3−24) 10%
3−HHEB(F,F)−F (3−12) 10%
4−HHEB(F,F)−F (3−12) 3%
5−HHEB(F,F)−F (3−12) 3%
2−HBEB(F,F)−F (3−36) 3%
3−HBEB(F,F)−F (3−36) 5%
5−HBEB(F,F)−F (3−36) 3%
3−HHBB(F,F)−F (4−6) 6%
5−Hdh−1V (1−1−1−6) 4%
5−Hdh2H−2 (1−5−1−10) 4%
5−HdhVH−2 (1−5−1−19) 3%
2−BEB(F)−C (5) 5%
3−BEB(F)−C (5) 4%
4−BEB(F)−C (5) 12%
1V2−BEB(F,F)−C (5) 16%
3−HB−O2 (12−5) 3%
3−HH−4 (12−1) 3%
3−HHB−F (3−1) 3%
3−HHB−1 (13−1) 4%
3−HHB−O1 (13−1) 4%
3−HBEB−F (3−34) 4%
3−HHEB−F (3−34) 7%
5−HHEB−F (3−34) 7%
3−H2BTB−2 (13−15) 4%
3−H2BTB−3 (13−15) 4%
3−H2BTB−4 (13−15) 4%
3−HB(F)TB−2 (13−14) 5%
NI=92.7℃;Δn=0.138;η(20℃)=41.7mPa・s;Δε=28.0;Vth=1.07V.
V−Hdh−5 (1−1−1−7) 10%
5−Hdh2B−2 (1−5−2−8) 5%
3−BEB(F)−C (5) 8%
3−HB−C (5−2) 8%
V−HB−C (5−2) 8%
1V−HB−C (5−2) 8%
3−HB−O2 (12−5) 3%
3−HH−2V (12−1) 9%
3−HH−2V1 (12−1) 3%
V2−HHB−1 (13−1) 9%
3−HHB−1 (13−1) 5%
3−HHEB−F (3−10) 7%
3−H2BTB−2 (13−15) 6%
3−H2BTB−3 (13−15) 6%
3−H2BTB−4 (13−15) 5%
V−Hdh2H−3 (1−5−1−13)10%
V−HdhVH−3 (1−5−1−23) 8%
5−BEB(F)−C (5) 5%
V−HB−C (5−2) 11%
5−PyB−C (5−8) 6%
4−BB−3 (12−8) 11%
3−HH−2V (12−1) 10%
5−HH−V (12−1) 11%
V−HHB−1 (13−3) 7%
V2−HHB−1 (13−3) 3%
3−HHB−1 (13−3) 3%
1V2−HBB−2 (13−4) 10%
3−HHEBH−3 (14−6) 5%
5−Hdh−2 (1−1−1−1) 5%
V−Hdh−5 (1−1−1−7) 6%
1V2−BEB(F,F)−C (5) 8%
3−HB−C (5−2) 18%
2−BTB−1 (12−10) 10%
5−HH−VFF (12−1) 20%
3−HHB−1 (13−1) 6%
VFF−HHB−1 (13−1) 6%
VFF2−HHB−1 (13−1) 6%
3−H2BTB−2 (13−15) 5%
3−H2BTB−3 (13−15) 5%
3−H2BTB−4 (13−15) 5%
Claims (21)
- 式(1)で表される化合物。
式(1)において、R1およびR2は独立して炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、任意の−(CH2)2−は−CH=CH−、または−C≡C−で置き換えられてもよく;T1、T2、およびT3は独立してテトラヒドロピラン−2,5−ジイルであり、A1およびA2は独立して1,4−シクロヘキシレンまたは1,4−フェニレンであり、;ただし、A 1 およびA 2 の少なくとも1つは1,4−シクロヘキシレンであり;Z1、Z2、Z3、およびZ4は独立して単結合または炭素数1〜2のアルキレンであり、このアルキレンにおいて−(CH2)2−は−CH=CH−で置き換えられてもよく;iは0または1であり;j、kおよびmは独立して0または1であり;nは0または1であり;i+j+k+m+nは3であり;そしてi+k+nは1であり;iが0のとき、jは1であり;nが0のとき、mは1または2であり;iが1のとき、R1は炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、任意の−(CH2)2−は−CH=CH−、または−C≡C−で置き換えられてもよく;nが0のときZ4は単結合であり;i+kが0、A1が1,4−シクロヘキシレン、そしてA2 が1,4−フェニレンのとき、R 1 およびR2 の少なくとも一つはアルケニルである。 - 式(1−4)〜式(1−6)で表される請求項1に記載の化合物。
式(1−4)〜式(1−6)において、R1、R2、およびR4は独立して炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、任意の−(CH2)2−は−CH=CH−または−C≡C−で置き換えられてもよく;R3 は炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は、−O−、−S−、−CO−、または−SiH2−で置き換えられてもよく、任意の−(CH2)2−は−CH=CH−または−C≡C−で置き換えられてもよく;A1およびA2は独立して1,4−シクロヘキシレンまたは1,4−フェニレンであり、;ただし、A 1 およびA 2 の少なくとも1つは1,4−シクロヘキシレンであり;Z1、Z2、Z3、およびZ4は独立して単結合または炭素数2のアルキレンであり、このアルキレンにおいて任意の−(CH2)2−は−CH=CH−で置き換えられてもよく;式(1−6)においてA1が1,4−シクロヘキシレン、そしてA2が1,4−フェニレンのとき、R3およびR4の少なくとも一つはアルケニルである。 - 請求項2に記載の式(1−4)〜式(1−6)において、R1〜R 4 が独立して炭素数2から10のアルキル、炭素数2から10のアルケニル、炭素数1から9のアルコキシ、炭素数2から9のアルコキシアルキル、炭素数3から9のアルケニルオキシであり;A1およびA2が独立して1,4−シクロヘキシレンまたは1,4−フェニレンであり;Z1、Z2、Z3、およびZ4が独立して単結合、−(CH2)2−、または−CH=CH−である請求項2に記載の化合物。
- 請求項2に記載の式(1−4)〜式(1−6)において、A1およびA2が独立して1,4−シクロヘキシレンである請求項2に記載の化合物。
- 式(1−4−1)〜式(1−4−3)、式(1−5−1)〜式(1−5−3)、式(1−6−1)〜式(1−6−3)のいずれか1つで表される請求項2〜4のいずれか1項に記載の化合物。
式(1−4−1)〜式(1−4−3)、式(1−5−1)〜式(1−5−3)、式(1−6−1)〜式(1−6−3)において、R31、R32、およびR33は独立して炭素数2〜10のアルキル、炭素数1〜9のアルコキシまたは炭素数2〜10のアルケニルであり;R34は炭素数2〜10のアルキル、炭素数1〜9のアルコキシ、または1−アルケニル以外の炭素数2〜10のアルケニルであり;R31およびR32のいずれか1つはアルキルであり;R33またはR34のいずれか1つはアルキルであり;Z31,Z32 またはZ33は独立して単結合、−(CH2)2−、または−CH=CH−であり;Z34,Z35 またはZ36は独立して単結合、または−(CH2)2−であり;Z31およびZ32のいずれか1つは単結合であり;Z33およびZ34のいずれか1つは単結合であり;Z35およびZ36のいずれか1つは単結合であり;式(1−6−3)において、R 31 またはR 32 の少なくともひとつはアルケニルである。 - 式中のR31およびR32の一方がアルキルであり、もう一方がアルケニルである請求項6記載の化合物。
- 請求項1〜7のいずれか1項に記載した少なくとも1つの化合物を含有する液晶組成物。
- 下記の式(2)、(3)および(4)で表される化合物の群から選択された少なくとも一つの化合物をさらに含有する請求項8に記載の液晶組成物。
式中、R7は炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は−O−または−CH=CH−で置き換えられてもよく、そして任意の水素はフッ素で置き換えられてもよく;X1はフッ素、塩素、−OCF3、−OCHF2、−CF3、−CHF2、−CH2F、−OCF2CHF2、または−OCF2CHFCF3であり;環B、Dおよび環Dは独立して1,4−シクロヘキシレン、1,3−ジオキサン−2,5−ジイルまたは任意の水素がフッ素で置き換えられてもよい1,4−フェニレンであり、環Eは1,4−シクロヘキシレンまたは任意の水素がフッ素で置き換えられてもよい1,4−フェニレンであり;Z5、およびZ6は独立して−(CH2)2−、−(CH2)4−、−COO−、−CF2O−、−OCF2−、−CH=CH−、または単結合であり;そしてL1およびL2は独立して水素またはフッ素である。 - 下記の式(5)および(6)で表される化合物の群から選択された少なくとも一つの化合物をさらに含有する請求項8に記載の液晶組成物。
式中、R8およびR9は独立して炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は−O−または−CH=CH−で置き換えられてもよく、そして任意の水素はフッ素で置き換えられてもよく;X2は−CNまたは−C≡C−CNであり;環Gは1,4−シクロヘキシレン、1,4−フェニレン、1,3−ジオキサン−2,5−ジイル、またはピリミジン−2,5−ジイルであり;環Jは1,4−シクロヘキシレン、ピリミジン−2,5−ジイルまたは任意の水素がフッ素で置き換えられてもよい1,4−フェニレンであり;環Kは1,4−シクロヘキシレンまたは1,4−フェニレンであり;Z7は−(CH2)2−、−COO−、−CF2O−、−OCF2−、または単結合であり;L3、L4およびL5は独立して水素またはフッ素であり;そしてb、cおよびdは独立して0または1である。 - 下記の式(7)、(8)、(9)、(10)、および(11)で表される化合物の群から選択された少なくとも一つの化合物をさらに含有する請求項8に記載の液晶組成物。
式中、R10およびR11は独立して炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は−O−または−CH=CH−で置き換えられてもよく、そして任意の水素はフッ素で置き換えられてもよく、あるいはR10はフッ素であってもよく;環Mおよび環Pは独立して1,4−シクロヘキシレン、1,4−フェニレンまたはデカヒドロ−2,6−ナフチレンであり;Z8およびZ9は独立して−(CH2)2−、−COO−または単結合であり;そしてL6およびL7は独立して水素またはフッ素であり、L6とL7の少なくとも一つはフッ素である。 - 下記の式(12)、(13)および(14)で表される化合物の群から選択された少なくとも一つの化合物をさらに含有する請求項8に記載の液晶組成物。
式中、R12およびR13は独立して炭素数1〜10のアルキルであり、このアルキルにおいて任意の−CH2−は−O−または−CH=CH−で置き換えられてもよく、そして任意の水素はフッ素で置き換えられてもよく;環Q、環Tおよび環Uは独立して1,4−シクロヘキシレン、ピリミジン−2、5−ジイル、または任意の水素がフッ素で置き換えられてもよい1,4−フェニレンであり;そしてZ10およびZ11は独立して−C≡C−、−COO−、−(CH2)2−、−CH=CH−、または単結合である。 - 請求項10に記載の式(5)および(6)で表される化合物の群から選択された少なくとも一つの化合物をさらに含有する請求項9に記載の組成物。
- 請求項12に記載の式(12)、(13)および(14)で表される化合物の群から選択された少なくとも1つの化合物をさらに含有する請求項9に記載の組成物。
- 請求項12に記載の式(12)、(13)および(14)で表される化合物の群から選択された少なくとも1つの化合物をさらに含有する請求項10に記載の組成物。
- 請求項12に記載の式(12)、(13)および(14)で表される化合物の群から選択された少なくとも1つの化合物をさらに含有する請求項11に記載の組成物。
- 少なくとも一つの光学活性化合物をさらに含有する請求項8〜16のいずれか1項に記載の液晶組成物。
- 液晶性化合物の全重量に基づいて、請求項1〜7のいずれかに記載の化合物の割合が5〜90重量%の範囲である請求項8〜17のいずれか1項に記載の液晶組成物。
- 請求項8〜18のいずれか1項に記載の液晶組成物を含有する液晶表示素子。
- VAまたはECB効果に基づくアクティブマトリックス駆動を有する請求項19に記載の液晶表示素子。
- 請求項8〜18のいずれか1項に記載の液晶組成物の液晶表示素子における使用。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012043433A JP5488628B2 (ja) | 2004-10-04 | 2012-02-29 | テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004291570 | 2004-10-04 | ||
| JP2004291570 | 2004-10-04 | ||
| JP2012043433A JP5488628B2 (ja) | 2004-10-04 | 2012-02-29 | テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006539246A Division JP4997972B2 (ja) | 2004-10-04 | 2005-09-29 | テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2012158593A true JP2012158593A (ja) | 2012-08-23 |
| JP5488628B2 JP5488628B2 (ja) | 2014-05-14 |
Family
ID=36124641
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006539246A Expired - Fee Related JP4997972B2 (ja) | 2004-10-04 | 2005-09-29 | テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 |
| JP2012043433A Expired - Fee Related JP5488628B2 (ja) | 2004-10-04 | 2012-02-29 | テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006539246A Expired - Fee Related JP4997972B2 (ja) | 2004-10-04 | 2005-09-29 | テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US7842357B2 (ja) |
| EP (2) | EP2128149B1 (ja) |
| JP (2) | JP4997972B2 (ja) |
| KR (2) | KR101258384B1 (ja) |
| CN (2) | CN101560398B (ja) |
| TW (1) | TWI373515B (ja) |
| WO (1) | WO2006038522A1 (ja) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4997972B2 (ja) * | 2004-10-04 | 2012-08-15 | Jnc石油化学株式会社 | テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 |
| JP5098250B2 (ja) | 2006-08-10 | 2012-12-12 | Jnc株式会社 | 液晶組成物および液晶表示素子 |
| ATE494350T1 (de) * | 2006-10-04 | 2011-01-15 | Merck Patent Gmbh | Flüssigkristallines medium |
| EP2272837B1 (en) * | 2008-05-09 | 2014-12-17 | JNC Corporation | Liquid crystalline compound with negative dielectric anisotropy, liquid crystal composition, and liquid crystal display device |
| CN102718736B (zh) * | 2012-06-07 | 2014-08-06 | 北京八亿时空液晶科技股份有限公司 | 一种吡喃类含氟化合物、制备方法及其用途 |
| KR101555596B1 (ko) * | 2012-08-22 | 2015-09-24 | 디아이씨 가부시끼가이샤 | 네마틱 액정 조성물 |
| CN104736670A (zh) * | 2012-10-23 | 2015-06-24 | Dic株式会社 | 液晶组合物、液晶显示元件以及液晶显示器 |
| KR102019189B1 (ko) * | 2013-03-19 | 2019-09-06 | 엘지디스플레이 주식회사 | 액정표시장치 |
| CN104560054B (zh) * | 2013-10-22 | 2017-05-03 | 江苏和成显示科技股份有限公司 | 液晶组合物及液晶显示器件 |
| WO2016017535A1 (ja) * | 2014-07-31 | 2016-02-04 | シャープ株式会社 | 液晶表示装置及びその製造方法 |
| KR20160052898A (ko) | 2014-10-29 | 2016-05-13 | 삼성디스플레이 주식회사 | 액정 조성물 및 이를 포함하는 액정 표시 장치 |
| KR102312261B1 (ko) | 2015-04-30 | 2021-10-13 | 삼성디스플레이 주식회사 | 액정 조성물 및 이를 포함하는 액정 표시 장치 |
| JP2017214589A (ja) * | 2017-07-03 | 2017-12-07 | Dic株式会社 | 液晶組成物、液晶表示素子および液晶ディスプレイ |
Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS59164788A (ja) * | 1983-02-28 | 1984-09-17 | メルク・パテント・ゲゼルシヤフト・ミツト・ベシユレンクテル・ハフツング | テトラヒドロピラン誘導体 |
| JPH0725866A (ja) * | 1993-05-19 | 1995-01-27 | Basf Ag | カイラル化合物 |
| US5443755A (en) * | 1991-12-26 | 1995-08-22 | Kashima Oil Company | Optically active tetrahydropyrane derivatives, liquid crystal composition and liquid crystal device containing the same |
| WO1998032721A1 (fr) * | 1997-01-22 | 1998-07-30 | Chisso Corporation | Composes et composition a cristaux liquides et element graphique a cristaux liquides contenant lesdits composes |
| JPH10237000A (ja) * | 1997-02-25 | 1998-09-08 | Chisso Corp | 誘電率異方性値が負の液晶性化合物、この液晶性化合物を含有する液晶組成物、及びこの液晶組成物を用いた液晶表示素子 |
| JPH10236989A (ja) * | 1997-02-27 | 1998-09-08 | Chisso Corp | 誘電率異方性値が負の液晶性化合物、この液晶性化合物を含有する液晶組成物、及びこの液晶組成物を用いた液晶表示素子 |
| JPH10236990A (ja) * | 1997-02-27 | 1998-09-08 | Chisso Corp | 誘電率異方性値が負の液晶性化合物、この液晶性化合物を含有する液晶組成物、及びこの液晶組成物を用いた液晶表示素子 |
| WO1999021816A1 (fr) * | 1997-10-24 | 1999-05-06 | Chisso Corporation | Nouveaux composes a cristaux liquides presentant une grande valeur negative d'anisotropie de permittivite, composition a cristaux liquides et element d'affichage a cristaux liquides |
| JP2000008040A (ja) * | 1998-06-25 | 2000-01-11 | Chisso Corp | 誘電率異方性値が負の液晶性化合物、この液晶性化合物を含有する液晶組成物、及びこの液晶組成物を用いた液晶表示素子 |
| JP2001115161A (ja) * | 1999-10-13 | 2001-04-24 | Chisso Corp | 液晶組成物および液晶表示素子 |
| JP2001262145A (ja) * | 2000-03-15 | 2001-09-26 | Chisso Corp | 液晶組成物及び液晶表示素子 |
| JP4997972B2 (ja) * | 2004-10-04 | 2012-08-15 | Jnc石油化学株式会社 | テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR900009936A (ko) | 1988-12-28 | 1990-07-06 | 우메모토 요시마사 | 광학활성 화합물, 이 화합물을 함유하는 액정조성물 및 이 조성물을 사용한 액정 광 변조장치 |
| JP2962825B2 (ja) | 1989-10-02 | 1999-10-12 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフトング | 電気光学液晶系 |
| WO1992013928A1 (de) | 1991-02-12 | 1992-08-20 | MERCK Patent Gesellschaft mit beschränkter Haftung | Flüssigkristalline verbindungen |
| DE4222371A1 (de) | 1991-08-20 | 1994-01-13 | Merck Patent Gmbh | Flüssigkristalline Verbindungen |
| DE4132006A1 (de) | 1991-09-26 | 1993-04-01 | Merck Patent Gmbh | Heterocyclen und fluessigkristallines medium |
| DE4238377B4 (de) | 1992-11-13 | 2006-07-27 | Merck Patent Gmbh | Flüssigkristallines Medium |
| JPH10512914A (ja) | 1995-02-03 | 1998-12-08 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフトング | 電気光学的液晶ディスプレイ |
| FI97197C (fi) | 1995-04-19 | 1996-11-11 | Olavi Penttinen | Menetelmä savustusmarinadin tekemiseksi |
| GB2310669B (en) | 1996-02-27 | 2000-09-27 | Merck Patent Gmbh | An electrooptical liquid crystal display of the IPS type containing a liquid crystalline medium having positive dielectric anisotropy and such a medium |
| DE19611096B4 (de) | 1996-03-21 | 2005-09-08 | Merck Patent Gmbh | Flüssigkristallines Medium und seine Verwendung |
| DE19625100A1 (de) | 1996-06-24 | 1998-01-08 | Merck Patent Gmbh | Elektrooptische Flüssigkristallanzeige |
| EP0959060A1 (en) * | 1996-11-28 | 1999-11-24 | Chisso Corporation | Chlorobenzene derivatives, liquid-crystal composition, and liquid-crystal display elements |
| DE19733199A1 (de) | 1997-08-01 | 1999-02-04 | Merck Patent Gmbh | Nematische Flüssigkristallzusammensetzung |
| DE19950194A1 (de) | 1998-10-20 | 2000-05-18 | Merck Patent Gmbh | Elektrooptische Flüssigkristallanzeige |
| JP2002020344A (ja) * | 2000-07-07 | 2002-01-23 | Chisso Corp | ジフルオロビニル化合物、液晶組成物および液晶表示素子 |
| DE10150198A1 (de) | 2001-10-12 | 2003-04-24 | Merck Patent Gmbh | Flüssigkristallines Medium |
| DE50306433D1 (de) * | 2002-12-21 | 2007-03-22 | Merck Patent Gmbh | Flüssigkristallines Medium |
-
2005
- 2005-09-29 JP JP2006539246A patent/JP4997972B2/ja not_active Expired - Fee Related
- 2005-09-29 WO PCT/JP2005/017990 patent/WO2006038522A1/ja active Application Filing
- 2005-09-29 EP EP09010278.1A patent/EP2128149B1/en not_active Not-in-force
- 2005-09-29 KR KR1020127016121A patent/KR101258384B1/ko active IP Right Grant
- 2005-09-29 CN CN2009101364235A patent/CN101560398B/zh not_active Expired - Fee Related
- 2005-09-29 EP EP05787513A patent/EP1798228B1/en not_active Not-in-force
- 2005-09-29 KR KR1020077007050A patent/KR101226396B1/ko active IP Right Grant
- 2005-09-29 CN CN200580031337.8A patent/CN101035779B/zh not_active Expired - Fee Related
- 2005-10-03 TW TW094134475A patent/TWI373515B/zh not_active IP Right Cessation
- 2005-10-04 US US11/244,243 patent/US7842357B2/en not_active Expired - Fee Related
-
2012
- 2012-02-29 JP JP2012043433A patent/JP5488628B2/ja not_active Expired - Fee Related
Patent Citations (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS59164788A (ja) * | 1983-02-28 | 1984-09-17 | メルク・パテント・ゲゼルシヤフト・ミツト・ベシユレンクテル・ハフツング | テトラヒドロピラン誘導体 |
| US5443755A (en) * | 1991-12-26 | 1995-08-22 | Kashima Oil Company | Optically active tetrahydropyrane derivatives, liquid crystal composition and liquid crystal device containing the same |
| JPH0725866A (ja) * | 1993-05-19 | 1995-01-27 | Basf Ag | カイラル化合物 |
| WO1998032721A1 (fr) * | 1997-01-22 | 1998-07-30 | Chisso Corporation | Composes et composition a cristaux liquides et element graphique a cristaux liquides contenant lesdits composes |
| JPH10237000A (ja) * | 1997-02-25 | 1998-09-08 | Chisso Corp | 誘電率異方性値が負の液晶性化合物、この液晶性化合物を含有する液晶組成物、及びこの液晶組成物を用いた液晶表示素子 |
| JPH10236989A (ja) * | 1997-02-27 | 1998-09-08 | Chisso Corp | 誘電率異方性値が負の液晶性化合物、この液晶性化合物を含有する液晶組成物、及びこの液晶組成物を用いた液晶表示素子 |
| JPH10236990A (ja) * | 1997-02-27 | 1998-09-08 | Chisso Corp | 誘電率異方性値が負の液晶性化合物、この液晶性化合物を含有する液晶組成物、及びこの液晶組成物を用いた液晶表示素子 |
| WO1999021816A1 (fr) * | 1997-10-24 | 1999-05-06 | Chisso Corporation | Nouveaux composes a cristaux liquides presentant une grande valeur negative d'anisotropie de permittivite, composition a cristaux liquides et element d'affichage a cristaux liquides |
| JP2000008040A (ja) * | 1998-06-25 | 2000-01-11 | Chisso Corp | 誘電率異方性値が負の液晶性化合物、この液晶性化合物を含有する液晶組成物、及びこの液晶組成物を用いた液晶表示素子 |
| JP2001115161A (ja) * | 1999-10-13 | 2001-04-24 | Chisso Corp | 液晶組成物および液晶表示素子 |
| JP2001262145A (ja) * | 2000-03-15 | 2001-09-26 | Chisso Corp | 液晶組成物及び液晶表示素子 |
| JP4997972B2 (ja) * | 2004-10-04 | 2012-08-15 | Jnc石油化学株式会社 | テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 |
Non-Patent Citations (3)
| Title |
|---|
| AYALA, L., ET AL.: ""Stereochemistry of Nucleophilic Substitution Reactions Depending upon Substituent: Evidence for Ele", JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 125, no. 50, JPN6011046042, 2003, pages 15521 - 15528, ISSN: 0002731277 * |
| ROMERO, J. A. C., ET AL.: ""Stereochemical Reversal of Nucleophilic Substitution Reactions Depending upon Substituent: Reaction", JOURNAL OF THE AMERICAN CHEMICAL SOCIETY, vol. 122, no. 1, JPN6011046044, 2000, pages 168 - 169, XP002995212, ISSN: 0002731278, DOI: 10.1021/ja993366o * |
| TVAROSKA, I., ET AL.: ""One-bond carbon-proton coupling constants: angular dependence in α-linked oligosaccharides"", CARBOHYDRATE RESEARCH, vol. 221, no. 1, JPN6011046048, 1991, pages 83 - 94, XP026730674, ISSN: 0002731279, DOI: 10.1016/0008-6215(91)80050-W * |
Also Published As
| Publication number | Publication date |
|---|---|
| US7842357B2 (en) | 2010-11-30 |
| KR20070074556A (ko) | 2007-07-12 |
| KR101226396B1 (ko) | 2013-01-24 |
| KR101258384B1 (ko) | 2013-04-30 |
| TWI373515B (en) | 2012-10-01 |
| JP4997972B2 (ja) | 2012-08-15 |
| EP2128149A1 (en) | 2009-12-02 |
| EP1798228B1 (en) | 2012-11-14 |
| EP2128149B1 (en) | 2013-07-24 |
| CN101035779A (zh) | 2007-09-12 |
| JPWO2006038522A1 (ja) | 2008-05-15 |
| WO2006038522A1 (ja) | 2006-04-13 |
| TW200613528A (en) | 2006-05-01 |
| CN101560398B (zh) | 2013-11-13 |
| JP5488628B2 (ja) | 2014-05-14 |
| KR20120079486A (ko) | 2012-07-12 |
| CN101035779B (zh) | 2015-06-03 |
| EP1798228A4 (en) | 2009-06-03 |
| US20060071194A1 (en) | 2006-04-06 |
| EP1798228A1 (en) | 2007-06-20 |
| CN101560398A (zh) | 2009-10-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4997972B2 (ja) | テトラヒドロピラン化合物、液晶組成物およびこの液晶組成物を含有する液晶表示素子 | |
| JP5582035B2 (ja) | 含窒素複素環を有する5環液晶化合物、液晶組成物および液晶表示素子 | |
| JP5817734B2 (ja) | シクロヘキセン−3,6−ジイル化合物、液晶組成物および液晶表示素子 | |
| JP4244556B2 (ja) | ビス(トリフルオロメチル)フェニル環を持つ液晶性化合物、液晶組成物および液晶表示素子 | |
| JP5145753B2 (ja) | フルオロイソプロピル基を側鎖として有する化合物およびこれを用いた液晶組成物 | |
| JP4961700B2 (ja) | 末端が水素であるナフタレン誘導体、この誘導体を含有する液晶組成物およびこの液晶組成物を含有する液晶表示素子 | |
| JP4186493B2 (ja) | ナフタレン環を有する液晶性化合物、液晶組成物および液晶表示素子 | |
| JP2004115475A (ja) | ジフルオロメチルおよびトリフルオロメチル基をベンゼン環上にあわせ持つ液晶性化合物、液晶組成物および液晶表示素子 | |
| JP4492206B2 (ja) | パーフルオロプロペニルを有する化合物、液晶組成物および液晶表示素子 | |
| JP4442179B2 (ja) | アリルエーテル化合物、この化合物を含有する液晶組成物およびこの液晶組成物を含有する液晶表示素子 | |
| JP4513351B2 (ja) | 結合基にフッ素化されたアルキル基を有する液晶性化合物、液晶組成物および液晶表示素子 | |
| JP4311055B2 (ja) | 末端基の一つが水素である液晶性化合物、その組成物およびこれを含有する液晶表示素子 | |
| KR20060071318A (ko) | 크로만환을 가지는 액정 화합물, 액정 조성물 및 이 액정조성물을 함유하는 액정 표시소자 | |
| JP5544940B2 (ja) | インドール環を有する化合物、液晶組成物、及び液晶表示素子 | |
| JP2006232727A (ja) | クマリン誘導体、この化合物を含有する液晶組成物およびこの液晶組成物を含有する液晶表示素子 | |
| JP4892853B2 (ja) | カーボネート結合基を有する液晶性化合物、この化合物を含有する液晶組成物およびこの液晶組成物を含有する液晶表示素子 | |
| JP4423877B2 (ja) | 2−トリフルオロメチルジヒドロピラン誘導体、液晶組成物および液晶表示素子 | |
| JP4042423B2 (ja) | フルオロアゾメチン化合物、液晶組成物および液晶表示素子 | |
| JP4774950B2 (ja) | ジヒドロクマリン誘導体、これを含む液晶組成物および液晶表示素子 | |
| JP4432320B2 (ja) | 液晶性3,4−置換ピロール | |
| JP4978017B2 (ja) | ベンゾジオキシン誘導体、これを含む液晶組成物および液晶表示素子 | |
| JP4419457B2 (ja) | ジヒドロピラン化合物、この化合物を含有する液晶組成物およびこの液晶組成物を含有する液晶表示素子 | |
| JP4774963B2 (ja) | クマリン誘導体、この化合物を含有する液晶組成物およびこの液晶組成物を含有する液晶表示素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20131119 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20131226 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20140128 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20140210 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 5488628 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |