JP2007517841A5 - - Google Patents
Download PDFInfo
- Publication number
- JP2007517841A5 JP2007517841A5 JP2006548344A JP2006548344A JP2007517841A5 JP 2007517841 A5 JP2007517841 A5 JP 2007517841A5 JP 2006548344 A JP2006548344 A JP 2006548344A JP 2006548344 A JP2006548344 A JP 2006548344A JP 2007517841 A5 JP2007517841 A5 JP 2007517841A5
- Authority
- JP
- Japan
- Prior art keywords
- dimethylphenyl
- prop
- carboxydimethylmethyloxy
- butyloxycarbonyldimethylmethyloxy
- tert
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 6
- 239000007858 starting material Substances 0.000 description 4
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- OTDVWQGHXPRNQA-UHFFFAOYSA-N 1-[4-(2-cyclohexylethoxy)-3,5-dimethylphenyl]ethanone Chemical compound CC1=CC(C(=O)C)=CC(C)=C1OCCC1CCCCC1 OTDVWQGHXPRNQA-UHFFFAOYSA-N 0.000 description 2
- QJQZRLXDLORINA-UHFFFAOYSA-N 2-cyclohexylethanol Chemical compound OCCC1CCCCC1 QJQZRLXDLORINA-UHFFFAOYSA-N 0.000 description 2
- TXFPEBPIARQUIG-UHFFFAOYSA-N 4'-hydroxyacetophenone Chemical compound CC(=O)C1=CC=C(O)C=C1 TXFPEBPIARQUIG-UHFFFAOYSA-N 0.000 description 2
- YZJHPDOUIGUCCH-UHFFFAOYSA-N 4-[3-(2,5-dimethoxyphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound COC1=C(C=C(C=C1)OC)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O YZJHPDOUIGUCCH-UHFFFAOYSA-N 0.000 description 2
- -1 4-cyclohexylethyloxy-3,5-dimethylphenyl Chemical group 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- VSCWAEJMTAWNJL-UHFFFAOYSA-K aluminium trichloride Chemical compound Cl[Al](Cl)Cl VSCWAEJMTAWNJL-UHFFFAOYSA-K 0.000 description 2
- IIEWJVIFRVWJOD-UHFFFAOYSA-N ethyl cyclohexane Natural products CCC1CCCCC1 IIEWJVIFRVWJOD-UHFFFAOYSA-N 0.000 description 2
- 238000007429 general method Methods 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- BTOQTQDGOKEIOV-UHFFFAOYSA-N 1-[4-(2-cyclohexylethoxy)phenyl]ethanone Chemical compound C1=CC(C(=O)C)=CC=C1OCCC1CCCCC1 BTOQTQDGOKEIOV-UHFFFAOYSA-N 0.000 description 1
- FWWJTQRUGFNVQN-UHFFFAOYSA-N 2,6-dimethyl-4-[3-[4-(2-morpholin-4-ylethoxy)phenyl]-3-oxoprop-1-enyl]-3-propan-2-yloxybenzoic acid Chemical compound N1(CCOCC1)CCOC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O FWWJTQRUGFNVQN-UHFFFAOYSA-N 0.000 description 1
- WGANMSWMGHTEJI-UHFFFAOYSA-N 2,6-dimethyl-4-[3-oxo-3-(2,3,4,5,6-pentamethylphenyl)prop-1-enyl]-3-propan-2-yloxybenzoic acid Chemical compound CC1=C(C(=C(C(=C1C)C)C)C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O WGANMSWMGHTEJI-UHFFFAOYSA-N 0.000 description 1
- VRLJEZHONSHEJI-UHFFFAOYSA-N 2,6-dimethyl-4-[3-oxo-3-(2,4,5-trimethylphenyl)prop-1-enyl]-3-propan-2-yloxybenzoic acid Chemical compound CC1=C(C=C(C(=C1)C)C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O VRLJEZHONSHEJI-UHFFFAOYSA-N 0.000 description 1
- QKYXLSKXTQGCIA-UHFFFAOYSA-N 2,6-dimethyl-4-[3-oxo-3-(4-phenoxyphenyl)prop-1-enyl]-3-propan-2-yloxybenzoic acid Chemical compound C1(=CC=CC=C1)OC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O QKYXLSKXTQGCIA-UHFFFAOYSA-N 0.000 description 1
- RZHDVSWGAHATAI-UHFFFAOYSA-N 2,6-dimethyl-4-[3-oxo-3-[4-(2-pentylsulfanylethoxy)phenyl]prop-1-enyl]-3-propan-2-yloxybenzoic acid Chemical compound C(CCCC)SCCOC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O RZHDVSWGAHATAI-UHFFFAOYSA-N 0.000 description 1
- ZIVPDLRSYMEFGX-UHFFFAOYSA-N 2,6-dimethyl-4-[3-oxo-3-[4-(2-phenylethoxy)phenyl]prop-1-enyl]-3-propan-2-yloxybenzoic acid Chemical compound C1(=CC=CC=C1)CCOC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O ZIVPDLRSYMEFGX-UHFFFAOYSA-N 0.000 description 1
- BIGVLJCQZYEIPT-UHFFFAOYSA-N 2-fluoro-3-methoxy-5,6-dimethyl-4-[3-(4-methylthiophen-2-yl)-3-oxoprop-1-enyl]benzoic acid Chemical compound COC1=C(F)C(C(O)=O)=C(C)C(C)=C1C=CC(=O)C1=CC(C)=CS1 BIGVLJCQZYEIPT-UHFFFAOYSA-N 0.000 description 1
- HPGBIPCQIAZBBS-UHFFFAOYSA-N 4-[3-(2,5-dihydroxy-3,4,6-trimethylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound OC1=C(C(=C(C(=C1C)C)O)C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O HPGBIPCQIAZBBS-UHFFFAOYSA-N 0.000 description 1
- OLPHHMFCWNLPDM-UHFFFAOYSA-N 4-[3-(2,5-dihydroxyphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound OC1=C(C=C(C=C1)O)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O OLPHHMFCWNLPDM-UHFFFAOYSA-N 0.000 description 1
- DJEQRLAVSGJJPD-UHFFFAOYSA-N 4-[3-(2,5-dimethoxy-3,4,6-trimethylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound COC1=C(C(=C(C(=C1C)C)OC)C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O DJEQRLAVSGJJPD-UHFFFAOYSA-N 0.000 description 1
- SEQIYSPDTWOPHP-UHFFFAOYSA-N 4-[3-(3,5-dimethyl-4-methylsulfanylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound CSC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O)C SEQIYSPDTWOPHP-UHFFFAOYSA-N 0.000 description 1
- UOCURAROBOPCBI-UHFFFAOYSA-N 4-[3-(3,5-dimethyl-4-propoxyphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound C(CC)OC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O)C UOCURAROBOPCBI-UHFFFAOYSA-N 0.000 description 1
- PEARMUHAMCHBLA-UHFFFAOYSA-N 4-[3-(3,5-dimethyl-4-sulfanylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound SC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O)C PEARMUHAMCHBLA-UHFFFAOYSA-N 0.000 description 1
- YOVCEOQWBFDKNI-UHFFFAOYSA-N 4-[3-(3-fluoro-4-methoxyphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound COC1=C(C=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O)F YOVCEOQWBFDKNI-UHFFFAOYSA-N 0.000 description 1
- XKJCULKMXSGXEM-UHFFFAOYSA-N 4-[3-(4-bromophenyl)-3-oxoprop-1-enyl]-2,6-difluoro-3-propan-2-yloxybenzoic acid Chemical compound BrC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)F)C(=O)O)F)OC(C)C)=O XKJCULKMXSGXEM-UHFFFAOYSA-N 0.000 description 1
- YORBFUDUTSDBBV-UHFFFAOYSA-N 4-[3-(4-hexoxy-3,5-dimethylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound C(CCCCC)OC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O)C YORBFUDUTSDBBV-UHFFFAOYSA-N 0.000 description 1
- DSFKLZVTSHKPSL-UHFFFAOYSA-N 4-[3-(4-hexylsulfanyl-3,5-dimethylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound C(CCCCC)SC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O)C DSFKLZVTSHKPSL-UHFFFAOYSA-N 0.000 description 1
- LAERXLUDQDUJTC-UHFFFAOYSA-N 4-[3-(4-methoxy-3,5-dimethylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound COC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O)C LAERXLUDQDUJTC-UHFFFAOYSA-N 0.000 description 1
- ILGUAFCUMJUUJQ-UHFFFAOYSA-N 4-[3-(4-methoxy-3-methylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound COC1=C(C=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O)C ILGUAFCUMJUUJQ-UHFFFAOYSA-N 0.000 description 1
- PZYRDJYDJFZLAG-UHFFFAOYSA-N 4-[3-[3,5-dimethyl-4-(2-morpholin-4-ylethoxy)phenyl]-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound CC=1C=C(C=C(C=1OCCN1CCOCC1)C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O PZYRDJYDJFZLAG-UHFFFAOYSA-N 0.000 description 1
- DUVKKJZMTVRDSZ-UHFFFAOYSA-N 4-[3-[4-(2-cyclohexylethoxy)phenyl]-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound C1(CCCCC1)CCOC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O DUVKKJZMTVRDSZ-UHFFFAOYSA-N 0.000 description 1
- DLZBWJHPPWRVRO-UHFFFAOYSA-N 4-[3-[4-(2-cyclohexylethylsulfanyl)-3,5-dimethylphenyl]-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound C1(CCCCC1)CCSC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O)C DLZBWJHPPWRVRO-UHFFFAOYSA-N 0.000 description 1
- GQZBNUSQJKXGFQ-UHFFFAOYSA-N 4-[3-[4-(2-cyclohexylsulfanylethoxy)-3,5-dimethylphenyl]-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound C1(CCCCC1)SCCOC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O)C GQZBNUSQJKXGFQ-UHFFFAOYSA-N 0.000 description 1
- ZFVXGPKTFCDLLA-UHFFFAOYSA-N 4-[3-[4-(2-cyclohexylsulfanylethoxy)phenyl]-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound C1(CCCCC1)SCCOC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O ZFVXGPKTFCDLLA-UHFFFAOYSA-N 0.000 description 1
- ZZYKBBXKEDPZNK-UHFFFAOYSA-N 4-[3-[4-methoxy-3-(trifluoromethyl)phenyl]-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoic acid Chemical compound COC1=C(C=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)=O)C(F)(F)F ZZYKBBXKEDPZNK-UHFFFAOYSA-N 0.000 description 1
- SCUYIKCQQBPACX-VQHVLOKHSA-N CC(C)(C(O)=O)Oc1c(C)cc(/C=C/C(c(cc(cc2)OC)c2OC)=O)cc1C Chemical compound CC(C)(C(O)=O)Oc1c(C)cc(/C=C/C(c(cc(cc2)OC)c2OC)=O)cc1C SCUYIKCQQBPACX-VQHVLOKHSA-N 0.000 description 1
- JDSSPBTXEBYGMB-BQYQJAHWSA-N CC(C)(C(O)=O)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2O)=O)cc1C Chemical compound CC(C)(C(O)=O)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2O)=O)cc1C JDSSPBTXEBYGMB-BQYQJAHWSA-N 0.000 description 1
- XJSOGJDPQGOHLV-CMDGGOBGSA-N CC(C)(C(O)=O)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2OC)=O)cc1C Chemical compound CC(C)(C(O)=O)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2OC)=O)cc1C XJSOGJDPQGOHLV-CMDGGOBGSA-N 0.000 description 1
- OQLHXOPMRXMXSC-VAWYXSNFSA-N CC(C)(C(O)=O)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2OCCCCCC2SSCC2)=O)cc1C Chemical compound CC(C)(C(O)=O)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2OCCCCCC2SSCC2)=O)cc1C OQLHXOPMRXMXSC-VAWYXSNFSA-N 0.000 description 1
- RQXVNEDIKFHCJV-CMDGGOBGSA-N CC(C)(C(O)=O)Oc1c(C)cc(/C=C/C(c2c(C)cc(C)c(C)c2)=O)cc1C Chemical compound CC(C)(C(O)=O)Oc1c(C)cc(/C=C/C(c2c(C)cc(C)c(C)c2)=O)cc1C RQXVNEDIKFHCJV-CMDGGOBGSA-N 0.000 description 1
- PIODZEHSWKEENA-KPKJPENVSA-N CC(C)(C)OC(C(C)(C)Oc(c(Br)cc(/C=C/C(c(cc1)ccc1SC)=O)c1)c1Br)=O Chemical compound CC(C)(C)OC(C(C)(C)Oc(c(Br)cc(/C=C/C(c(cc1)ccc1SC)=O)c1)c1Br)=O PIODZEHSWKEENA-KPKJPENVSA-N 0.000 description 1
- MWHAXDSBGVQNHS-ZRDIBKRKSA-N CC(C)(C)OC(C(C)(C)Oc1c(C)cc(/C=C/C(c(cc(cc2)OC)c2OC)=O)cc1C)=O Chemical compound CC(C)(C)OC(C(C)(C)Oc1c(C)cc(/C=C/C(c(cc(cc2)OC)c2OC)=O)cc1C)=O MWHAXDSBGVQNHS-ZRDIBKRKSA-N 0.000 description 1
- ZARGIPYWZPJQJN-FOCLMDBBSA-N CC(C)(C)OC(C(C)(C)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2OCCC2CCCCC2)=O)cc1C)=O Chemical compound CC(C)(C)OC(C(C)(C)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2OCCC2CCCCC2)=O)cc1C)=O ZARGIPYWZPJQJN-FOCLMDBBSA-N 0.000 description 1
- SVDVUHRBSRYSIH-VAWYXSNFSA-N CC(C)(C)OC(C(C)(C)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2SC)=O)cc1C)=O Chemical compound CC(C)(C)OC(C(C)(C)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2SC)=O)cc1C)=O SVDVUHRBSRYSIH-VAWYXSNFSA-N 0.000 description 1
- HVUVNYQJFVNPLB-UHFFFAOYSA-N CC=1C(=C(C=C(C=1C(=O)O)C)C(C=C)=O)OC(C)C Chemical compound CC=1C(=C(C=C(C=1C(=O)O)C)C(C=C)=O)OC(C)C HVUVNYQJFVNPLB-UHFFFAOYSA-N 0.000 description 1
- TZESXPMYWNQANF-OUKQBFOZSA-N CCCCCCOc(c(C)c1)c(C)cc1C(/C=C/c(cc1C)cc(C)c1OC(C)(C)C(O)=O)=O Chemical compound CCCCCCOc(c(C)c1)c(C)cc1C(/C=C/c(cc1C)cc(C)c1OC(C)(C)C(O)=O)=O TZESXPMYWNQANF-OUKQBFOZSA-N 0.000 description 1
- XGULARGABDGBLZ-MDZDMXLPSA-N CCOC(C(C)(C)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2OCCN2CCOCC2)=O)cc1C)=O Chemical compound CCOC(C(C)(C)Oc1c(C)cc(/C=C/C(c(cc2C)cc(C)c2OCCN2CCOCC2)=O)cc1C)=O XGULARGABDGBLZ-MDZDMXLPSA-N 0.000 description 1
- UKWGUNJZWVOVHD-UHFFFAOYSA-N CSC1=CC=C(C=C1)CC=CC1=C(C(=C(C(=C1)Br)C(=O)O)Br)OC(C)C Chemical compound CSC1=CC=C(C=C1)CC=CC1=C(C(=C(C(=C1)Br)C(=O)O)Br)OC(C)C UKWGUNJZWVOVHD-UHFFFAOYSA-N 0.000 description 1
- DCHZUJHLWKZEAO-UHFFFAOYSA-N CSC1=CC=C(C=C1)CC=CC1=C(C(=C(C(=C1)Br)C(=O)OC(C)(C)C)Br)OC(C)C Chemical compound CSC1=CC=C(C=C1)CC=CC1=C(C(=C(C(=C1)Br)C(=O)OC(C)(C)C)Br)OC(C)C DCHZUJHLWKZEAO-UHFFFAOYSA-N 0.000 description 1
- QZQAMBJPNMFNNK-UHFFFAOYSA-N Cl.CC=1C=C(C=C(C1OCCN1CCOCC1)C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OCC)C)OC(C)C)=O Chemical compound Cl.CC=1C=C(C=C(C1OCCN1CCOCC1)C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OCC)C)OC(C)C)=O QZQAMBJPNMFNNK-UHFFFAOYSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- SXAKQEFXADCVHU-UHFFFAOYSA-N OC1=C(C=C(C=C1C)CC=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)C Chemical compound OC1=C(C=C(C=C1C)CC=CC1=C(C(=C(C(=C1)C)C(=O)O)C)OC(C)C)C SXAKQEFXADCVHU-UHFFFAOYSA-N 0.000 description 1
- ZSSKJWHOUXDLHB-UHFFFAOYSA-N OC1=C(C=C(C=C1C)CC=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)C Chemical compound OC1=C(C=C(C=C1C)CC=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)C ZSSKJWHOUXDLHB-UHFFFAOYSA-N 0.000 description 1
- FXXACINHVKSMDR-UHFFFAOYSA-N acetyl bromide Chemical compound CC(Br)=O FXXACINHVKSMDR-UHFFFAOYSA-N 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 125000000217 alkyl group Chemical group 0.000 description 1
- 125000004414 alkyl thio group Chemical group 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 125000003118 aryl group Chemical group 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- 125000005843 halogen group Chemical group 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 239000012074 organic phase Substances 0.000 description 1
- 150000002923 oximes Chemical class 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- XJBAEHOHLGGTFL-UHFFFAOYSA-N tert-butyl 2,6-dimethyl-4-[3-oxo-3-(2,3,4,5,6-pentamethylphenyl)prop-1-enyl]-3-propan-2-yloxybenzoate Chemical compound CC1=C(C(=C(C(=C1C)C)C)C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O XJBAEHOHLGGTFL-UHFFFAOYSA-N 0.000 description 1
- GOQNQORJHRZGDQ-UHFFFAOYSA-N tert-butyl 2,6-dimethyl-4-[3-oxo-3-(2,4,5-trimethylphenyl)prop-1-enyl]-3-propan-2-yloxybenzoate Chemical compound CC1=C(C=C(C(=C1)C)C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O GOQNQORJHRZGDQ-UHFFFAOYSA-N 0.000 description 1
- AGEZNSCDVHGFRZ-UHFFFAOYSA-N tert-butyl 2,6-dimethyl-4-[3-oxo-3-(4-phenoxyphenyl)prop-1-enyl]-3-propan-2-yloxybenzoate Chemical compound C1(=CC=CC=C1)OC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O AGEZNSCDVHGFRZ-UHFFFAOYSA-N 0.000 description 1
- KTTRJOMYYFSOAG-UHFFFAOYSA-N tert-butyl 2,6-dimethyl-4-[3-oxo-3-[4-(2-pentylsulfanylethoxy)phenyl]prop-1-enyl]-3-propan-2-yloxybenzoate Chemical compound C(CCCC)SCCOC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O KTTRJOMYYFSOAG-UHFFFAOYSA-N 0.000 description 1
- LVORARIMJQPAJK-UHFFFAOYSA-N tert-butyl 2-fluoro-3-methoxy-5,6-dimethyl-4-[3-(4-methylthiophen-2-yl)-3-oxoprop-1-enyl]benzoate Chemical compound COC1=C(F)C(C(=O)OC(C)(C)C)=C(C)C(C)=C1C=CC(=O)C1=CC(C)=CS1 LVORARIMJQPAJK-UHFFFAOYSA-N 0.000 description 1
- IZJNHAQNQVUGGL-UHFFFAOYSA-N tert-butyl 4-[3-(2,5-dimethoxyphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound COC1=C(C=C(C=C1)OC)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O IZJNHAQNQVUGGL-UHFFFAOYSA-N 0.000 description 1
- NCSVDKCQMKOCIZ-UHFFFAOYSA-N tert-butyl 4-[3-(3,5-dimethyl-4-methylsulfanylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound CSC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O)C NCSVDKCQMKOCIZ-UHFFFAOYSA-N 0.000 description 1
- IQDDZCWTVVLUDE-UHFFFAOYSA-N tert-butyl 4-[3-(3,5-dimethyl-4-propoxyphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound C(CC)OC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O)C IQDDZCWTVVLUDE-UHFFFAOYSA-N 0.000 description 1
- APZRCYQNMFRGHS-UHFFFAOYSA-N tert-butyl 4-[3-(3-fluoro-4-methoxyphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound COC1=C(C=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O)F APZRCYQNMFRGHS-UHFFFAOYSA-N 0.000 description 1
- XNLMSJYHCPPVRZ-UHFFFAOYSA-N tert-butyl 4-[3-(4-bromophenyl)-3-oxoprop-1-enyl]-2,6-difluoro-3-propan-2-yloxybenzoate Chemical compound BrC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)F)C(=O)OC(C)(C)C)F)OC(C)C)=O XNLMSJYHCPPVRZ-UHFFFAOYSA-N 0.000 description 1
- FHVRJHDWWXGGLG-UHFFFAOYSA-N tert-butyl 4-[3-(4-hexoxy-3,5-dimethylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound C(CCCCC)OC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O)C FHVRJHDWWXGGLG-UHFFFAOYSA-N 0.000 description 1
- WOVLRQBTZQPGPD-UHFFFAOYSA-N tert-butyl 4-[3-(4-hexylsulfanyl-3,5-dimethylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound C(CCCCC)SC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O)C WOVLRQBTZQPGPD-UHFFFAOYSA-N 0.000 description 1
- XTODTFMCNIFADA-UHFFFAOYSA-N tert-butyl 4-[3-(4-methoxy-3,5-dimethylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound COC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O)C XTODTFMCNIFADA-UHFFFAOYSA-N 0.000 description 1
- KUPDWGRPVFZKTP-UHFFFAOYSA-N tert-butyl 4-[3-(4-methoxy-3-methylphenyl)-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound COC1=C(C=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O)C KUPDWGRPVFZKTP-UHFFFAOYSA-N 0.000 description 1
- XLACVUYLJSYURZ-UHFFFAOYSA-N tert-butyl 4-[3-[4-(2-cyclohexylethoxy)-3,5-dimethylphenyl]-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound C1(CCCCC1)CCOC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O)C XLACVUYLJSYURZ-UHFFFAOYSA-N 0.000 description 1
- APDIOXRLTUKUFW-UHFFFAOYSA-N tert-butyl 4-[3-[4-(2-cyclohexylethoxy)phenyl]-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound C1(CCCCC1)CCOC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O APDIOXRLTUKUFW-UHFFFAOYSA-N 0.000 description 1
- YKNSNPBQSPTECB-UHFFFAOYSA-N tert-butyl 4-[3-[4-(2-cyclohexylsulfanylethoxy)-3,5-dimethylphenyl]-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound C1(CCCCC1)SCCOC1=C(C=C(C=C1C)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O)C YKNSNPBQSPTECB-UHFFFAOYSA-N 0.000 description 1
- AHOZKQCGEXHOAV-UHFFFAOYSA-N tert-butyl 4-[3-[4-(2-cyclohexylsulfanylethoxy)phenyl]-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound C1(CCCCC1)SCCOC1=CC=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O AHOZKQCGEXHOAV-UHFFFAOYSA-N 0.000 description 1
- BOPBPTCRNPKJSI-UHFFFAOYSA-N tert-butyl 4-[3-[4-methoxy-3-(trifluoromethyl)phenyl]-3-oxoprop-1-enyl]-2,6-dimethyl-3-propan-2-yloxybenzoate Chemical compound COC1=C(C=C(C=C1)C(C=CC1=C(C(=C(C(=C1)C)C(=O)OC(C)(C)C)C)OC(C)C)=O)C(F)(F)F BOPBPTCRNPKJSI-UHFFFAOYSA-N 0.000 description 1
- 150000003573 thiols Chemical class 0.000 description 1
- 238000007738 vacuum evaporation Methods 0.000 description 1
Description
本発明に従えば、用語「アリール」は、少なくとも1個のハロゲン原子、アルキル、ヒドロキシル、チオール、アルキルオキシ、アルキルチオ、オキシムもしくはチオニトロソ基によって置換されたまたは特に置換されていない芳香族炭化水素基を示す。フェニル基はかなり特に好適である。
本発明の特定の実施形態に従って、以下に、それらの対応する式で好適な化合物を示す:
1−(4−((R,S)−5−[1,2]ジチオラン−3−イルペンチルオキシ)−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メルカプト−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−シクロヘキシルエチルチオ−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(2,5−ジヒドロキシ−3,4,6−トリメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(2,5−ジメトキシ−3,4,6−トリメチルフェニル)−3−(4−カルボキシジメチルメトキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(2,5−ジヒドロキシフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(2,5−ジメトキシフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−フェニルエチルオキシフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
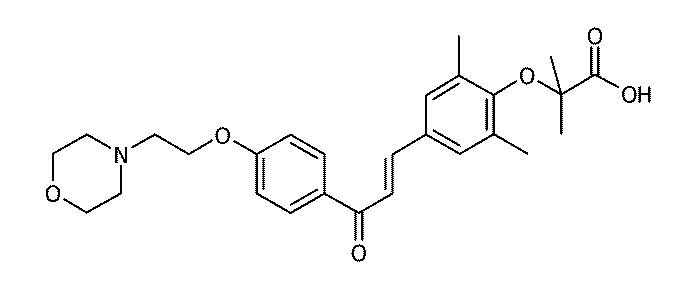
1−(4−(モルホリン−4−イルエチルオキシ)フェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−(ペンチルチオエチルオキシ)フェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−(ペンチルチオエチルオキシ)フェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−ヒドロキシ−3,5−ジメチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン(ene)−1−オン:
1−(4−ヒドロキシ−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン(ene)−1−オン:
1−(4−((R,S)−5−[1,2]ジチオラン−3−イルペンチルオキシ)フェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−((R,S)−5−[1,2]ジチオラン−3−イルペンチルオキシ)フェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メチルチオフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジブロモフェニル)プロプ−2−エン(ene)−1−オン:
1−(4−メチルチオフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジブロモフェニル)プロプ−2−エン(ene)−1−オン:
1−(4−シクロヘキシルエチルオキシフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−シクロヘキシルエチルオキシフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メチルチオ−3,5−ジメチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メチルチオ−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−プロピルオキシ−3,5−ジメチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−プロピルオキシ−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メトキシ−3,5−ジメチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メトキシ−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−ヘキシルオキシ−3,5−ジメチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−ヘキシルオキシ−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−シクロヘキシルエチルオキシ−3,5−ジメチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−シクロヘキシルエチルオキシ−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−シクロヘキシルチオエチルオキシフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−シクロヘキシルチオエチルオキシフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(2,4,5−トリメチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(2,4,5−トリメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−シクロヘキシルチオエチルオキシ−3,5−ジメチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−シクロヘキシルチオエチルオキシ−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メチルチオフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3−フルオロフェニル)プロプ−2−エン−1−オン:
1−(4−メチルチオフェニル)−3−(4−カルボキシジメチルメチルオキシ−3−フルオロフェニル)プロプ−2−エン−1−オン:
1−(2,3,4,5,6−ペンタメチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(2,3,4,5,6−ペンタメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−フェニルオキシフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−フェニルオキシフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メトキシ−3−フルオロフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メトキシ−3−フルオロフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メトキシ−3−メチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メトキシ−3−メチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−ヘキシルチオ−3,5−ジメチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−ヘキシルチオ−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(2,5−ジメトキシフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(2,5−ジメトキシフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(3,5−ジメチル−4−(モルホリン−4−イルエチルオキシ)フェニル)−3−(4−エチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン塩酸塩:
1−(3,5−ジメチル−4−(モルホリン−4−イルエチルオキシ)フェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−ブロモフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジフルオロフェニル)プロプ−2−エン−1−オン:
1−(4−ブロモフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジフルオロフェニル)プロプ−2−エン−1−オン:
1−(4−メトキシ−3−トリフルオロメチルフェニル)−3−(4−tert−ブチルオキシカルボニルジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−メトキシ−3−トリフルオロメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
1−(4−((R,S)−5−[1,2]ジチオラン−3−イルペンチルオキシ)−3,5−ジメチルフェニル)−3−(4−カルボキシジメチルメチルオキシ−3,5−ジメチルフェニル)プロプ−2−エン−1−オン:
出発物質4:
4’−ヒドロキシ−3’,5’−ジメチルアセトフェノン
2,6−ジメチルフェノール(1eq)を塩化メチレンに溶解し、溶液を0℃に冷却した。次いで、塩化アルミニウム(3eq)および臭化アセチル(2eq)を添加した。混合物を、3時間、室温で撹拌し、次いで、氷上に注いだ。水相をジクロロメタンで抽出し、有機相を中性まで水で洗浄し、硫酸マグネシウム上で乾燥させ、溶媒を減圧エバポレーションにより除去した。得られた中間体エステルをシリカゲルクロマトグラフィー(溶出:シクロヘキサン/酢酸エチル9:1)によって精製し、次いで、2N水酸化ナトリウム水溶液(2.5eq)中に採取した。混合物を48時間、室温で撹拌し、次いで、希塩酸で酸性にした。沈殿物を、洗浄水が中性のpHに達するまで、水で洗浄した。
4’−ヒドロキシ−3’,5’−ジメチルアセトフェノン
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0400123A FR2864956B1 (fr) | 2004-01-08 | 2004-01-08 | Compose derive de 1,3-diphenylprop-2-en-1-one, preparation et utilisations |
| FR0409257 | 2004-09-01 | ||
| PCT/FR2005/000040 WO2005073184A1 (fr) | 2004-01-08 | 2005-01-07 | Composes derives de 1,3-diphenylprop-2-en-1-one, preparation et utilisations |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2007517841A JP2007517841A (ja) | 2007-07-05 |
| JP2007517841A5 true JP2007517841A5 (ja) | 2008-03-06 |
Family
ID=34828644
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2006548344A Pending JP2007517841A (ja) | 2004-01-08 | 2005-01-07 | 1,3−ジフェニルプロプ−2−エン−1−オン誘導体化合物、その調製方法およびその使用 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US7547729B2 (ja) |
| EP (1) | EP1701938B1 (ja) |
| JP (1) | JP2007517841A (ja) |
| KR (1) | KR20060132903A (ja) |
| AU (1) | AU2005209446A1 (ja) |
| BR (1) | BRPI0506718A (ja) |
| CA (1) | CA2550576A1 (ja) |
| EA (1) | EA011305B1 (ja) |
| IL (1) | IL176515A0 (ja) |
| NO (1) | NO20062824L (ja) |
| WO (1) | WO2005073184A1 (ja) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2841900B1 (fr) * | 2002-07-08 | 2007-03-02 | Genfit S A | Nouveaux derives de 1,3-diphenylprop-2-en-1-one substitues, preparation et utilisations |
| US7816385B2 (en) * | 2002-12-20 | 2010-10-19 | High Point Pharmaceuticals, Llc | Dimeric dicarboxylic acid derivatives, their preparation and use |
| FR2910892A1 (fr) * | 2006-12-29 | 2008-07-04 | Genfit Sa | Derives de 1,3-diphenylpropane substitues, preparations et utilisations. |
| FR2910894A1 (fr) * | 2006-12-29 | 2008-07-04 | Genfit Sa | Derives de 3-phenyl-1-(phenylthienyl)propan-1-one et de 3-phenyl-1-(phenylfuranyl)propan-1-one substitues, preparation et utilisation. |
| WO2009120891A2 (en) * | 2008-03-27 | 2009-10-01 | Geron Corporation | Differentiation of primate pluripotent stem cells to hematopoietic lineage cells |
| US8772342B2 (en) * | 2009-11-26 | 2014-07-08 | Genfit | Use of 1,3-diphenylprop-2-en-1-one derivatives for treating liver disorders |
| WO2011080276A1 (en) | 2009-12-29 | 2011-07-07 | Genfit | Pharmaceutical combinations comprising a dpp-4 inhibitor and a 1,3-diphenylprop-2-en-1-one derivative |
| CN103025703B (zh) | 2010-05-17 | 2015-10-14 | 金菲特公司 | 查耳酮衍生物的改进制备 |
| DE102011114780A1 (de) * | 2011-10-01 | 2013-04-04 | Merck Patent Gmbh | Verwendung von Propanol- und Propenolderivaten als Antioxidantien |
| JP6140729B2 (ja) * | 2011-12-28 | 2017-05-31 | ジェンフィットGenfit | 1,3−ジフェニルプロパン誘導体、その製造および使用 |
| KR101601685B1 (ko) * | 2015-08-24 | 2016-03-09 | 여명바이오켐 주식회사 | 항산화 효과가 우수한 택시폴린 유도체 및 이를 함유하는 화장료 조성물 |
| JP7266531B2 (ja) * | 2017-04-18 | 2023-04-28 | ジェンフィ | エラフィブラノール又はその誘導体と抗nash剤、抗線維化剤又は抗胆汁うっ滞性剤の組合せ |
| CN108658908B (zh) * | 2017-07-31 | 2019-05-10 | 广州必贝特医药技术有限公司 | 1,3-二取代烯酮类化合物及其应用 |
| CN111148742B (zh) * | 2017-11-30 | 2021-11-16 | 四川科伦博泰生物医药股份有限公司 | 芳香族化合物及其药物组合物和用途 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3994955A (en) * | 1975-01-20 | 1976-11-30 | G. D. Searle & Co. | Substituted phenoxydialkylacetic acids and esters |
| US4190671A (en) * | 1977-03-17 | 1980-02-26 | Biorex Laboratories Limited | Chalcone derivatives |
| GB8426424D0 (en) * | 1984-10-19 | 1984-11-28 | Biorex Laboratories Ltd | Chalcone derivatives |
| DE4327365A1 (de) | 1993-08-14 | 1995-02-16 | Boehringer Mannheim Gmbh | Verwendung von Phenolen und Phenolderivaten als Arzneimittel mit fibrinogensenkender Wirkung |
| US5523302A (en) * | 1993-11-24 | 1996-06-04 | The Du Pont Merck Pharmaceutical Company | Aromatic compounds containing basic and acidic termini useful as fibrinogen receptor antagonists |
| EP0659743A1 (en) * | 1993-12-27 | 1995-06-28 | Hoechst Aktiengesellschaft | Piperidine derivatives as inhibitors of platelet aggregation and their preparation |
| NZ523443A (en) * | 2000-06-20 | 2004-11-26 | Atherogenics Inc | 1,3-bis-(substituted-phenyl)-2-propen-1-ones and their use to treat VCAM-1 mediated disorders |
| JPWO2003037316A1 (ja) | 2001-10-11 | 2005-02-17 | 株式会社カネカ | ペルオキシソーム増殖剤応答性受容体リガンド剤及びその製造法 |
| FR2841784B1 (fr) * | 2002-07-08 | 2007-03-02 | Composition a base de derives de 1,3-diphenylprop-2en-1-one substitues, preparation et utilisations | |
| FR2841900B1 (fr) * | 2002-07-08 | 2007-03-02 | Genfit S A | Nouveaux derives de 1,3-diphenylprop-2-en-1-one substitues, preparation et utilisations |
-
2005
- 2005-01-07 US US10/585,329 patent/US7547729B2/en not_active Expired - Lifetime
- 2005-01-07 JP JP2006548344A patent/JP2007517841A/ja active Pending
- 2005-01-07 BR BRPI0506718-9A patent/BRPI0506718A/pt not_active IP Right Cessation
- 2005-01-07 WO PCT/FR2005/000040 patent/WO2005073184A1/fr not_active Ceased
- 2005-01-07 KR KR1020067015988A patent/KR20060132903A/ko not_active Withdrawn
- 2005-01-07 CA CA002550576A patent/CA2550576A1/fr not_active Abandoned
- 2005-01-07 AU AU2005209446A patent/AU2005209446A1/en not_active Abandoned
- 2005-01-07 EA EA200601288A patent/EA011305B1/ru not_active IP Right Cessation
- 2005-01-07 EP EP05717386A patent/EP1701938B1/fr not_active Expired - Lifetime
-
2006
- 2006-06-16 NO NO20062824A patent/NO20062824L/no not_active Application Discontinuation
- 2006-06-22 IL IL176515A patent/IL176515A0/en unknown
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP2007517841A5 (ja) | ||
| JPS58185553A (ja) | α−保護されたオキシイミノ−β−ケト−γ−ハロゲノ酪酸類 | |
| CN103221401A (zh) | 制备5位被取代的苯并呋喃衍生物的方法 | |
| JPWO2006006496A1 (ja) | アズレン誘導体の製造方法及びその合成中間体 | |
| JP5016575B2 (ja) | ストロンチウムラネレートおよびその水和物の新規な合成法 | |
| WO1991011433A1 (fr) | Procede de production d'un compose de diphenylsulfone | |
| CN1378529A (zh) | 4-羟基联苯基酰肼衍生物 | |
| TWI316939B (en) | Process for the preparation of organic compounds | |
| CN103596917B (zh) | 环戊酮化合物的制造方法、及中间体化合物 | |
| JP2012214405A (ja) | N,n’−メチレンビス(1,2−ベンズイソチアゾリン−3−オン)化合物及びその製造方法 | |
| CN1942434B (zh) | 茚衍生物及其制备方法 | |
| JPS60172975A (ja) | エリスロ−3−(3,4−メチレンジオキシフエニル)セリンの製造方法 | |
| JP2003534243A (ja) | 抗菌キノロン薬のための有用な中間物としてのアルキル3−シクロプロピルアミノ−2−[2,4−ジブロモ−3−(ジフルオロメトキシ)ベンゾイル]−2−プロペノエートのワンポット合成法 | |
| CN112745284B (zh) | 一种天然查尔酮衍生物及其制备方法和用途 | |
| WO2008139057A2 (fr) | Procede de preparation de 2-(n-butyl)-3-(4-hydroxybenzoyl)-5-nitrobenzofurane | |
| JP2641002B2 (ja) | ジフェニルスルホン化合物 | |
| JP2000169407A (ja) | 3−ブテン−1−オール誘導体の製造方法 | |
| JP2008505189A (ja) | アズトレオナムの製造方法 | |
| WO2017152539A1 (zh) | 一种4-五氟化硫苯酚类化合物及制备方法以及五氟化硫取代苯并吡喃类化合物的制备方法 | |
| JP4194984B2 (ja) | フェニルナフチルイミダゾール化合物 | |
| JP3533567B2 (ja) | 置換アニリンから置換キノリンを製造する新規合成法 | |
| JP2004026671A (ja) | チアゾール類の製造方法 | |
| JP3907713B2 (ja) | 4−ヒドロキシ−4′−イソプロポキシジフェニルスルホンの製造方法 | |
| JP3569877B2 (ja) | m−置換−α−ヒドロキシメチルスチレン誘導体の製造法および3−クロロ−α−ブロモスチレン | |
| JP2008517902A (ja) | アルキルアリルサルファイド誘導体の製造方法及び新規なサルファイド化合物 |