JP2005294079A - 二次電池用負極、その製造方法及び二次電池 - Google Patents
二次電池用負極、その製造方法及び二次電池 Download PDFInfo
- Publication number
- JP2005294079A JP2005294079A JP2004108436A JP2004108436A JP2005294079A JP 2005294079 A JP2005294079 A JP 2005294079A JP 2004108436 A JP2004108436 A JP 2004108436A JP 2004108436 A JP2004108436 A JP 2004108436A JP 2005294079 A JP2005294079 A JP 2005294079A
- Authority
- JP
- Japan
- Prior art keywords
- secondary battery
- composite particles
- negative electrode
- carbon
- metal
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 22
- 239000011246 composite particle Substances 0.000 claims abstract description 148
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims abstract description 139
- 229910052799 carbon Inorganic materials 0.000 claims abstract description 131
- 239000002184 metal Substances 0.000 claims abstract description 93
- 229910052751 metal Inorganic materials 0.000 claims abstract description 90
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims abstract description 70
- 229910052814 silicon oxide Inorganic materials 0.000 claims abstract description 69
- 239000011149 active material Substances 0.000 claims abstract description 45
- 239000002245 particle Substances 0.000 claims description 56
- 238000000034 method Methods 0.000 claims description 53
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 claims description 27
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 claims description 22
- 229910001416 lithium ion Inorganic materials 0.000 claims description 22
- 239000002131 composite material Substances 0.000 claims description 18
- 229910052744 lithium Inorganic materials 0.000 claims description 15
- 239000002002 slurry Substances 0.000 claims description 15
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 claims description 14
- 229910052710 silicon Inorganic materials 0.000 claims description 14
- 239000010703 silicon Substances 0.000 claims description 13
- 239000011248 coating agent Substances 0.000 claims description 12
- 238000000576 coating method Methods 0.000 claims description 12
- 238000013329 compounding Methods 0.000 claims description 12
- 238000005229 chemical vapour deposition Methods 0.000 claims description 9
- 229910052742 iron Inorganic materials 0.000 claims description 9
- 238000003466 welding Methods 0.000 claims description 9
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims description 8
- 150000001875 compounds Chemical class 0.000 claims description 8
- 239000001301 oxygen Substances 0.000 claims description 8
- 229910052760 oxygen Inorganic materials 0.000 claims description 8
- 229910052759 nickel Inorganic materials 0.000 claims description 7
- 238000004544 sputter deposition Methods 0.000 claims description 6
- 238000001771 vacuum deposition Methods 0.000 claims description 6
- 229910052802 copper Inorganic materials 0.000 claims description 5
- 229910052737 gold Inorganic materials 0.000 claims description 5
- 229910052750 molybdenum Inorganic materials 0.000 claims description 5
- 229910052719 titanium Inorganic materials 0.000 claims description 5
- 229910052721 tungsten Inorganic materials 0.000 claims description 5
- 229910052804 chromium Inorganic materials 0.000 claims description 4
- 229910052748 manganese Inorganic materials 0.000 claims description 4
- 229910052758 niobium Inorganic materials 0.000 claims description 4
- 229910052697 platinum Inorganic materials 0.000 claims description 4
- 229910052720 vanadium Inorganic materials 0.000 claims description 4
- 229910052741 iridium Inorganic materials 0.000 claims description 3
- 229910052762 osmium Inorganic materials 0.000 claims description 3
- 229910052763 palladium Inorganic materials 0.000 claims description 3
- 239000005518 polymer electrolyte Substances 0.000 claims description 3
- 229910052702 rhenium Inorganic materials 0.000 claims description 3
- 229910052703 rhodium Inorganic materials 0.000 claims description 3
- 229910052707 ruthenium Inorganic materials 0.000 claims description 3
- 229910052727 yttrium Inorganic materials 0.000 claims description 3
- 229910052725 zinc Inorganic materials 0.000 claims description 3
- 229910052726 zirconium Inorganic materials 0.000 claims description 3
- 229910052746 lanthanum Inorganic materials 0.000 claims description 2
- 238000005868 electrolysis reaction Methods 0.000 claims 1
- 239000011244 liquid electrolyte Substances 0.000 claims 1
- 239000007773 negative electrode material Substances 0.000 abstract description 21
- 238000010298 pulverizing process Methods 0.000 abstract description 11
- 150000002739 metals Chemical class 0.000 abstract description 2
- 238000002847 impedance measurement Methods 0.000 description 26
- 239000002033 PVDF binder Substances 0.000 description 17
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 17
- -1 etc.) Inorganic materials 0.000 description 16
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 13
- 239000003795 chemical substances by application Substances 0.000 description 12
- 239000008151 electrolyte solution Substances 0.000 description 10
- 239000000463 material Substances 0.000 description 10
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 10
- 230000000052 comparative effect Effects 0.000 description 9
- 230000002427 irreversible effect Effects 0.000 description 9
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 8
- 238000011049 filling Methods 0.000 description 7
- 229910002804 graphite Inorganic materials 0.000 description 7
- 239000010439 graphite Substances 0.000 description 7
- 230000008569 process Effects 0.000 description 7
- 229920005989 resin Polymers 0.000 description 7
- 239000011347 resin Substances 0.000 description 7
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 description 6
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 6
- 229910052782 aluminium Inorganic materials 0.000 description 6
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 6
- 239000000843 powder Substances 0.000 description 6
- 239000011230 binding agent Substances 0.000 description 5
- 239000010949 copper Substances 0.000 description 5
- 238000007599 discharging Methods 0.000 description 5
- 238000001035 drying Methods 0.000 description 5
- 239000010931 gold Substances 0.000 description 5
- 238000010438 heat treatment Methods 0.000 description 5
- 239000004743 Polypropylene Substances 0.000 description 4
- MCMNRKCIXSYSNV-UHFFFAOYSA-N Zirconium dioxide Chemical compound O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 description 4
- 239000004020 conductor Substances 0.000 description 4
- 239000013078 crystal Substances 0.000 description 4
- 239000011888 foil Substances 0.000 description 4
- 238000003701 mechanical milling Methods 0.000 description 4
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 4
- 229920001155 polypropylene Polymers 0.000 description 4
- 229910001220 stainless steel Inorganic materials 0.000 description 4
- 239000010935 stainless steel Substances 0.000 description 4
- 229920005992 thermoplastic resin Polymers 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- 229910013870 LiPF 6 Inorganic materials 0.000 description 3
- 239000004698 Polyethylene Substances 0.000 description 3
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 239000010419 fine particle Substances 0.000 description 3
- 239000003273 ketjen black Substances 0.000 description 3
- 229910044991 metal oxide Inorganic materials 0.000 description 3
- 150000004706 metal oxides Chemical class 0.000 description 3
- 239000000203 mixture Substances 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- 238000007500 overflow downdraw method Methods 0.000 description 3
- 229920000573 polyethylene Polymers 0.000 description 3
- 238000003825 pressing Methods 0.000 description 3
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 description 3
- 238000007789 sealing Methods 0.000 description 3
- ZZXUZKXVROWEIF-UHFFFAOYSA-N 1,2-butylene carbonate Chemical compound CCC1COC(=O)O1 ZZXUZKXVROWEIF-UHFFFAOYSA-N 0.000 description 2
- VAYTZRYEBVHVLE-UHFFFAOYSA-N 1,3-dioxol-2-one Chemical compound O=C1OC=CO1 VAYTZRYEBVHVLE-UHFFFAOYSA-N 0.000 description 2
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 description 2
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 description 2
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 2
- 229920000049 Carbon (fiber) Polymers 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- 229920000181 Ethylene propylene rubber Polymers 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- 229910000733 Li alloy Inorganic materials 0.000 description 2
- 229920002125 Sokalan® Polymers 0.000 description 2
- 229910045601 alloy Inorganic materials 0.000 description 2
- 239000000956 alloy Substances 0.000 description 2
- RDOXTESZEPMUJZ-UHFFFAOYSA-N anisole Chemical compound COC1=CC=CC=C1 RDOXTESZEPMUJZ-UHFFFAOYSA-N 0.000 description 2
- 229910021383 artificial graphite Inorganic materials 0.000 description 2
- 239000004917 carbon fiber Substances 0.000 description 2
- 239000001768 carboxy methyl cellulose Substances 0.000 description 2
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 2
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 2
- 239000006258 conductive agent Substances 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- VUPKGFBOKBGHFZ-UHFFFAOYSA-N dipropyl carbonate Chemical compound CCCOC(=O)OCCC VUPKGFBOKBGHFZ-UHFFFAOYSA-N 0.000 description 2
- KLKFAASOGCDTDT-UHFFFAOYSA-N ethoxymethoxyethane Chemical compound CCOCOCC KLKFAASOGCDTDT-UHFFFAOYSA-N 0.000 description 2
- FKRCODPIKNYEAC-UHFFFAOYSA-N ethyl propionate Chemical compound CCOC(=O)CC FKRCODPIKNYEAC-UHFFFAOYSA-N 0.000 description 2
- 229910021385 hard carbon Inorganic materials 0.000 description 2
- 238000004898 kneading Methods 0.000 description 2
- 239000005001 laminate film Substances 0.000 description 2
- 239000001989 lithium alloy Substances 0.000 description 2
- AMXOYNBUYSYVKV-UHFFFAOYSA-M lithium bromide Chemical compound [Li+].[Br-] AMXOYNBUYSYVKV-UHFFFAOYSA-M 0.000 description 2
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 2
- 229910003002 lithium salt Inorganic materials 0.000 description 2
- 159000000002 lithium salts Chemical class 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 230000008018 melting Effects 0.000 description 2
- 238000002844 melting Methods 0.000 description 2
- TZIHFWKZFHZASV-UHFFFAOYSA-N methyl formate Chemical compound COC=O TZIHFWKZFHZASV-UHFFFAOYSA-N 0.000 description 2
- 239000012046 mixed solvent Substances 0.000 description 2
- 238000007747 plating Methods 0.000 description 2
- 239000004584 polyacrylic acid Substances 0.000 description 2
- 229920000098 polyolefin Polymers 0.000 description 2
- 239000004810 polytetrafluoroethylene Substances 0.000 description 2
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 239000011232 storage material Substances 0.000 description 2
- PYOKUURKVVELLB-UHFFFAOYSA-N trimethyl orthoformate Chemical compound COC(OC)OC PYOKUURKVVELLB-UHFFFAOYSA-N 0.000 description 2
- 239000011701 zinc Substances 0.000 description 2
- VFRGATWKSPNXLT-UHFFFAOYSA-N 1,2-dimethoxybutane Chemical compound CCC(OC)COC VFRGATWKSPNXLT-UHFFFAOYSA-N 0.000 description 1
- CYSGHNMQYZDMIA-UHFFFAOYSA-N 1,3-Dimethyl-2-imidazolidinon Chemical compound CN1CCN(C)C1=O CYSGHNMQYZDMIA-UHFFFAOYSA-N 0.000 description 1
- FSSPGSAQUIYDCN-UHFFFAOYSA-N 1,3-Propane sultone Chemical compound O=S1(=O)CCCO1 FSSPGSAQUIYDCN-UHFFFAOYSA-N 0.000 description 1
- IZXIZTKNFFYFOF-UHFFFAOYSA-N 2-Oxazolidone Chemical compound O=C1NCCO1 IZXIZTKNFFYFOF-UHFFFAOYSA-N 0.000 description 1
- JWUJQDFVADABEY-UHFFFAOYSA-N 2-methyltetrahydrofuran Chemical compound CC1CCCO1 JWUJQDFVADABEY-UHFFFAOYSA-N 0.000 description 1
- PPDFQRAASCRJAH-UHFFFAOYSA-N 2-methylthiolane 1,1-dioxide Chemical compound CC1CCCS1(=O)=O PPDFQRAASCRJAH-UHFFFAOYSA-N 0.000 description 1
- 229910019001 CoSi Inorganic materials 0.000 description 1
- 229920002943 EPDM rubber Polymers 0.000 description 1
- 229910005347 FeSi Inorganic materials 0.000 description 1
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 229910010238 LiAlCl 4 Inorganic materials 0.000 description 1
- 229910015015 LiAsF 6 Inorganic materials 0.000 description 1
- 229910013063 LiBF 4 Inorganic materials 0.000 description 1
- 229910013684 LiClO 4 Inorganic materials 0.000 description 1
- 229910012851 LiCoO 2 Inorganic materials 0.000 description 1
- 229910012513 LiSbF 6 Inorganic materials 0.000 description 1
- 229910017326 LixMn Inorganic materials 0.000 description 1
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000005062 Polybutadiene Substances 0.000 description 1
- 229920000265 Polyparaphenylene Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 229910008484 TiSi Inorganic materials 0.000 description 1
- BEKPOUATRPPTLV-UHFFFAOYSA-N [Li].BCl Chemical compound [Li].BCl BEKPOUATRPPTLV-UHFFFAOYSA-N 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- 239000006230 acetylene black Substances 0.000 description 1
- 150000007933 aliphatic carboxylic acids Chemical class 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 229910003481 amorphous carbon Inorganic materials 0.000 description 1
- 229910021417 amorphous silicon Inorganic materials 0.000 description 1
- 239000010405 anode material Substances 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- 239000003575 carbonaceous material Substances 0.000 description 1
- 150000005678 chain carbonates Chemical class 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 150000005676 cyclic carbonates Chemical class 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- 210000001787 dendrite Anatomy 0.000 description 1
- 229920005994 diacetyl cellulose Polymers 0.000 description 1
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 description 1
- 150000004862 dioxolanes Chemical class 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000007606 doctor blade method Methods 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- HQQADJVZYDDRJT-UHFFFAOYSA-N ethene;prop-1-ene Chemical group C=C.CC=C HQQADJVZYDDRJT-UHFFFAOYSA-N 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 229940052303 ethers for general anesthesia Drugs 0.000 description 1
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 239000011737 fluorine Substances 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 125000000457 gamma-lactone group Chemical group 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 150000003949 imides Chemical class 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 238000005304 joining Methods 0.000 description 1
- 238000010030 laminating Methods 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- UZKWTJUDCOPSNM-UHFFFAOYSA-N methoxybenzene Substances CCCCOC=C UZKWTJUDCOPSNM-UHFFFAOYSA-N 0.000 description 1
- 239000011733 molybdenum Substances 0.000 description 1
- 239000004570 mortar (masonry) Substances 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 229910021382 natural graphite Inorganic materials 0.000 description 1
- 239000010955 niobium Substances 0.000 description 1
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 description 1
- 239000011255 nonaqueous electrolyte Substances 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-N phosphoric acid Substances OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 1
- 229920001197 polyacetylene Polymers 0.000 description 1
- 229920002857 polybutadiene Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 229920000915 polyvinyl chloride Polymers 0.000 description 1
- 239000004800 polyvinyl chloride Substances 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- FVSKHRXBFJPNKK-UHFFFAOYSA-N propionitrile Chemical compound CCC#N FVSKHRXBFJPNKK-UHFFFAOYSA-N 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 239000005060 rubber Substances 0.000 description 1
- 238000010008 shearing Methods 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 229920003048 styrene butadiene rubber Polymers 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 1
- 229920005608 sulfonated EPDM Polymers 0.000 description 1
- 229910052715 tantalum Inorganic materials 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 229910052723 transition metal Inorganic materials 0.000 description 1
- 150000003624 transition metals Chemical class 0.000 description 1
- WFKWXMTUELFFGS-UHFFFAOYSA-N tungsten Chemical compound [W] WFKWXMTUELFFGS-UHFFFAOYSA-N 0.000 description 1
- 239000010937 tungsten Substances 0.000 description 1
- 238000001291 vacuum drying Methods 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 239000013585 weight reducing agent Substances 0.000 description 1
- 238000004804 winding Methods 0.000 description 1
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Secondary Cells (AREA)
- Battery Electrode And Active Subsutance (AREA)
Abstract
【解決手段】
活物質層が集電体上に形成された二次電池用負極において、活物質層に、ケイ素酸化物と少なくとも1種の金属とを含む無機複合粒子が炭素で被覆されている炭素複合粒子を含有させることにより、上記課題を解決した。
【選択図】 図1
Description
ホング・リー(Hong Li)他著、「ア ハイ キャパシティ ナノ−シリコン コンポジット アノード マテリアル フォー リチウム リチャージャブル バッテリーズ(A High Capacity Nano-Si Composite Anode Material for Lithium Rechargeable Batteries)」、エレクトロケミカル アンド ソリッドステイト レターズ(Electrochemical and Solid-State Letters)、第2巻、第11号、p547−549
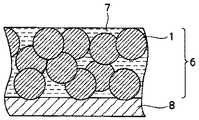
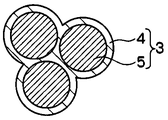
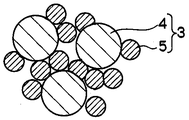
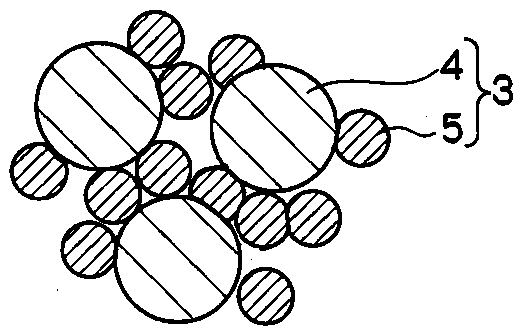
本発明の二次電池用負極について、図面を参照して詳細に説明する。図1は本発明の二次電池用負極の断面拡大図である。本発明の二次電池用負極は、図1に示すように、活物質層6と集電体8とからなり、活物質層6は、炭素複合粒子1、導電付与剤及び結着剤を含有する。本発明の二次電池用負極を用いて二次電池を作製した際は、電解液7が活物質層の空隙を埋めることにより電子のやり取りが行われる。
本発明の二次電池用負極は、ケイ素酸化物と金属とを複合化して無機複合粒子を作製する工程と、無機複合粒子を炭素で被覆して炭素複合粒子を作製する工程と、炭素複合粒子を含むスラリーを集電体上に塗布し乾燥して活物質層を形成する工程と、を含む。以下に、それぞれの工程について説明する。
ケイ素酸化物と金属とを複合化して無機複合粒子が作製されるので、炭素複合粒子が微粉化し難い構造となる。
炭素複合粒子は、無機複合粒子を炭素で被覆して作製されるので、微粉化が起こり難い構造となる。無機複合粒子を炭素で被覆する方法としては、CVD法及び圧接法が挙げられる。CVD法又は圧接法を行った後に、熱処理を施してもよい。こうした方法を用いることにより、無機複合粒子と炭素とが複合化され、無機複合粒子と炭素とが互いに分離し難い構造となるので、二次電池の充放電の際に炭素複合粒子の微粉化が抑制される。
上述した炭素複合粒子及び炭素と、導電付与剤及び結着剤とを混合し、混練してスラリーを作製する。このスラリーを集電体上に塗布して乾燥した後、活物質層の体積充填率が上述した範囲となるようプレスして二次電池用負極とする。スラリーを集電体上に塗布する方法としては、ドクターブレード法及びスプレー塗布等公知の方法を用いることができる。スラリー乾燥する方法としては、真空乾燥及び加熱乾燥等公知の方法を用いることができる。活物質層をプレスする方法としては、ローラープレス等の装置を用いてプレスする方法を用いることができる。
本発明の二次電池は、正極と上述した二次電池用負極とを、セパレータを介して、乾燥空気又は不活性気体雰囲気において積層又は積層したものを捲回した後に、容器に封入して作製される。
平均粒径15μmのケイ素酸化物(酸素:ケイ素=1:1)と、金属として平均粒径1μmのFe粒子を用い、ケイ素酸化物中のケイ素と金属との原子数比が3:1となるように配合し、これを遊星型ボールミル装置を用いて、複合化処理を100時間行った。このとき、遊星型ボールミル装置中のボールミル容器及び直径10mmのボールはジルコニア製であった。ケイ素酸化物と金属の配合処理及び複合化処理はAr雰囲気で行った。次に、Ar雰囲気中、1100℃で1時間、熱処理を施し、無機複合粒子を得た。その後、メタンガスを用いてCVD法で炭素被覆を行い、無機複合粒子に炭素からなる層を形成した後、分級し、粒径10μmの炭素複合粒子を得た。炭素複合粒子中の無機複合粒子と炭素の質量比は、無機複合粒子:炭素=4:1とした。
実施例1において、金属として平均粒径1μmのNi粒子を用いた以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのTi粒子を用い、無機複合粒子と炭素の質量比を1:5とした以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのW粒子を用い、ケイ素酸化物中のケイ素と金属との原子数比を1:0.05とした以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのCo粒子を用い、ケイ素酸化物中のケイ素と金属との原子数比を1:1とした以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのV粒子を用い、無機複合粒子と炭素の質量比を1:10とした以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのMo粒子を用い、ケイ素酸化物として酸素のケイ素に対する元素比が0.8であるケイ素酸化物を用いた以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのCr粒子を用い、ケイ素酸化物として酸素のケイ素に対する元素比が1.9であるケイ素酸化物を用いた以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのMn粒子を用いた以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのTa粒子を用い、無機複合粒子と炭素の質量比と1:3とした以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのNb粒子を用い、分級により炭素複合粒子の平均粒径を3μmとした以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのPd粒子を用い、ケイ素酸化物中のケイ素と金属との原子数比を1:2とした以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのAu粒子を用い、CVD法の代わりに、メカノフュージョン法にて炭素被覆を行った以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのAg粒子を用いた以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのCu粒子を用いた以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、金属として平均粒径1μmのPt粒子を用いた以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、無機複合粒子と炭素の質量比が19:1となるように炭素複合体を作製した以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、無機複合粒子と炭素の質量比が5:1となるように炭素複合体を作製した以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、無機複合粒子と炭素の質量比が1:1となるように炭素複合体を作製した以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
ケイ素酸化物として、平均粒径5μmのケイ素酸化物(酸素:ケイ素=1:1)を用い、金属として平均粒径1μmのFe粒子を用いた。このケイ素酸化物粒子と金属を、SiとFeの原子数の比が4:1となるように配合し、これを遊星型ボールミル装置で複合化処理を12時間行って、無機複合粒子を得た。このとき、遊星型ボールミル装置中のボールミル容器及び直径10mmのボールはジルコニア製で、配合処理及び複合化処理はAr雰囲気で行った。
実施例20において、無機複合粒子と炭素の質量比を1:2とした以外は、実施例20と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例20において、無機複合粒子と炭素の質量比を1:3とした以外は、実施例20と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、無機複合粒子の代わりに、金属を添加していないケイ素酸化物粒子を用いた以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
実施例1において、無機複合粒子に炭素被覆を行わないでそのまま無機複合粒子を活物質層に用いて二次電池用負極を作製した以外は、実施例1と同様の方法にて、二次電池の作製、充放電サイクル試験及びインピーダンス測定を行った。
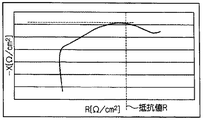
実施例1〜16及び比較例1〜2のサイクル試験及びインピーダンス測定の結果を表1に示す。このとき、100サイクル後の容量維持率は、(各サイクルにおける放電容量)/(5サイクル目における放電容量)の計算式にて算出した。また、インピーダンス測定の結果は、100サイクル後の界面抵抗Rを比較例1の界面抵抗Rの値で除した結果で示す。界面抵抗Rは20KHzから50MHzまでの周波数でコールコールプロットを作製した際に虚軸の−Xの値が最大値となるときの実軸の値とした(図8に示す)。
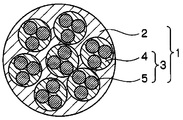
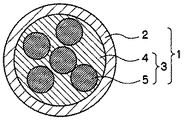
2 炭素
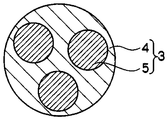
3 無機複合粒子
4 ケイ素酸化物
5 金属
6 活物質層
7 電解液
8 集電体
Claims (10)
- 活物質層が集電体上に形成された二次電池用負極において、前記活物質層は、ケイ素酸化物と少なくとも1種の金属とを含む無機複合粒子が炭素で被覆されている炭素複合粒子を含有することを特徴とする二次電池用負極。
- 前記金属が、Ti、V、Cr、Mn、Fe、Co、Ni、Cu、Zn、Y、Zr、Nb、Mo、Ru、Rh、Pd、Ag、Ta、W、Re、Os、Ir、Pt、Au又はLaであることを特徴とする請求項1に記載の二次電池用負極。
- 前記無機複合粒子中のケイ素の原子数を1としたとき、当該無機複合粒子に含まれる金属の原子数が0.05以上であることを特徴とする請求項1又は2に記載の二次電池用負極。
- 前記炭素複合粒子の質量を1としたとき、前記炭素複合粒子に含まれる前記炭素の質量が0.05以上であることを特徴とする請求項1〜3のいずれか1項に記載の二次電池用負極。
- 前記ケイ素酸化物を構成する酸素のケイ素に対する元素比が、0.8以上2未満であることを特徴とする請求項1〜4のいずれか1項に記載の二次電池用負極。
- 前記炭素複合粒子の平均粒径が10μm以下であることを特徴とする請求項1〜5のいずれか1項に記載の二次電池用負極。
- ケイ素酸化物と金属とを複合化して無機複合粒子を作製する工程と、該無機複合粒子を炭素で被覆して炭素複合粒子を作製する工程と、該炭素複合粒子を含むスラリーを用いて集電体上に活物質層を形成する工程と、を含むことを特徴とする二次電池用負極の製造方法。
- ケイ素酸化物と金属との複合化が、圧接法、スパッタ法又は真空蒸着法を用いて行われることを特徴とする請求項7に記載の二次電池用負極の製造方法。
- 無機複合粒子の炭素による被覆が、CVD法又は圧接法を用いて行われることを特徴とする請求項7又は8に記載の二次電池用負極の製造方法。
- 電気化学的にリチウムイオンを取り出せるリチウム含有化合物を含む正極と、リチウムイオンを吸蔵及び放出することのできる活物質層が集電体上に形成されてなる負極と、リチウムイオン導電性の非水系電解液又はポリマー電解質とを有する二次電池において、
前記活物質層は、ケイ素酸化物と少なくとも1種の金属とを含む無機複合粒子が炭素で被覆されている炭素複合粒子を含有することを特徴とする二次電池。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004108436A JP4547963B2 (ja) | 2004-03-31 | 2004-03-31 | 二次電池用負極、その製造方法及び二次電池 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004108436A JP4547963B2 (ja) | 2004-03-31 | 2004-03-31 | 二次電池用負極、その製造方法及び二次電池 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2005294079A true JP2005294079A (ja) | 2005-10-20 |
| JP4547963B2 JP4547963B2 (ja) | 2010-09-22 |
Family
ID=35326772
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004108436A Expired - Lifetime JP4547963B2 (ja) | 2004-03-31 | 2004-03-31 | 二次電池用負極、その製造方法及び二次電池 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP4547963B2 (ja) |
Cited By (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007141504A (ja) * | 2005-11-15 | 2007-06-07 | Hitachi Chem Co Ltd | リチウムイオン二次電池用負極材 |
| JP2008004460A (ja) * | 2006-06-26 | 2008-01-10 | Nec Tokin Corp | 非水電解質二次電池 |
| JP2011065983A (ja) * | 2009-08-21 | 2011-03-31 | Oike Ind Co Ltd | 鱗片状薄膜微粉末分散液又は鱗片状薄膜微粉末、及びこれを用いたペースト、電池用電極、並びにリチウム二次電池 |
| JP2011233497A (ja) * | 2009-12-24 | 2011-11-17 | Sony Corp | リチウムイオン二次電池、リチウムイオン二次電池用負極、電動工具、電気自動車および電力貯蔵システム |
| US20110294014A1 (en) * | 2010-05-25 | 2011-12-01 | Samsung Sdi Co., Ltd. | Negative electrode for secondary lithium battery, and secondary lithium battery |
| JP2012028345A (ja) * | 2011-11-07 | 2012-02-09 | Hitachi Chem Co Ltd | リチウムイオン二次電池用負極材の製造方法 |
| JP2012033311A (ja) * | 2010-07-29 | 2012-02-16 | Toyota Industries Corp | 非水系二次電池用負極活物質およびその製造方法 |
| US8507133B2 (en) | 2006-09-07 | 2013-08-13 | Toyota Jidosha Kabushiki Kaisha | Anode active material, anode, and lithium secondary battery |
| JP2014032964A (ja) * | 2012-08-06 | 2014-02-20 | Samsung Sdi Co Ltd | リチウム二次電池用負極活物質、その製造方法およびこれを含むリチウム二次電池 |
| KR101514202B1 (ko) | 2012-05-04 | 2015-04-23 | 주식회사 엘지화학 | 전기화학 소자용 음극 활물질 |
| JP2016081709A (ja) * | 2014-10-16 | 2016-05-16 | Tdk株式会社 | リチウムイオン二次電池用負極活物質、およびそれを含む負極並びにリチウムイオン二次電池 |
| WO2017081854A1 (ja) * | 2015-11-09 | 2017-05-18 | 株式会社豊田自動織機 | 負極活物質 |
| KR20170077845A (ko) | 2015-12-28 | 2017-07-06 | 주식회사 엘지화학 | 이차 전지용 음극 재료 및 그것을 이용한 비수 전해질 이차 전지 |
| WO2019107990A1 (ko) * | 2017-12-01 | 2019-06-06 | 주식회사 엘지화학 | 리튬이차전지용 음극 및 이를 포함하는 리튬이차전지 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005259697A (ja) * | 2004-03-08 | 2005-09-22 | Samsung Sdi Co Ltd | リチウム二次電池用負極活物質、リチウム二次電池用負極活物質、およびリチウム二次電池 |
-
2004
- 2004-03-31 JP JP2004108436A patent/JP4547963B2/ja not_active Expired - Lifetime
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2005259697A (ja) * | 2004-03-08 | 2005-09-22 | Samsung Sdi Co Ltd | リチウム二次電池用負極活物質、リチウム二次電池用負極活物質、およびリチウム二次電池 |
Cited By (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007141504A (ja) * | 2005-11-15 | 2007-06-07 | Hitachi Chem Co Ltd | リチウムイオン二次電池用負極材 |
| JP2008004460A (ja) * | 2006-06-26 | 2008-01-10 | Nec Tokin Corp | 非水電解質二次電池 |
| US8507133B2 (en) | 2006-09-07 | 2013-08-13 | Toyota Jidosha Kabushiki Kaisha | Anode active material, anode, and lithium secondary battery |
| JP2011065983A (ja) * | 2009-08-21 | 2011-03-31 | Oike Ind Co Ltd | 鱗片状薄膜微粉末分散液又は鱗片状薄膜微粉末、及びこれを用いたペースト、電池用電極、並びにリチウム二次電池 |
| JP2011233497A (ja) * | 2009-12-24 | 2011-11-17 | Sony Corp | リチウムイオン二次電池、リチウムイオン二次電池用負極、電動工具、電気自動車および電力貯蔵システム |
| US8999583B2 (en) | 2009-12-24 | 2015-04-07 | Sony Corporation | Lithium-ion secondary battery, anode for lithium-ion secondary battery, power tool, electric vehicle and energy storage system |
| US9525175B2 (en) * | 2010-05-25 | 2016-12-20 | Samsung Sdi Co., Ltd. | Negative electrode for secondary lithium battery, and secondary lithium battery |
| US20110294014A1 (en) * | 2010-05-25 | 2011-12-01 | Samsung Sdi Co., Ltd. | Negative electrode for secondary lithium battery, and secondary lithium battery |
| KR101147200B1 (ko) | 2010-05-25 | 2012-05-25 | 삼성에스디아이 주식회사 | 리튬 이차 전지용 음극 및 이를 포함하는 리튬 이차 전지 |
| JP2012033311A (ja) * | 2010-07-29 | 2012-02-16 | Toyota Industries Corp | 非水系二次電池用負極活物質およびその製造方法 |
| JP2012028345A (ja) * | 2011-11-07 | 2012-02-09 | Hitachi Chem Co Ltd | リチウムイオン二次電池用負極材の製造方法 |
| KR101514202B1 (ko) | 2012-05-04 | 2015-04-23 | 주식회사 엘지화학 | 전기화학 소자용 음극 활물질 |
| JP2018152348A (ja) * | 2012-08-06 | 2018-09-27 | 三星エスディアイ株式会社Samsung SDI Co., Ltd. | リチウム二次電池用負極活物質、その製造方法およびこれを含むリチウム二次電池 |
| JP2014032964A (ja) * | 2012-08-06 | 2014-02-20 | Samsung Sdi Co Ltd | リチウム二次電池用負極活物質、その製造方法およびこれを含むリチウム二次電池 |
| US10096820B2 (en) | 2012-08-06 | 2018-10-09 | Samsung Sdi Co., Ltd. | Negative active material for rechargeable lithium battery, method preparing the same and rechargeable lithium battery including the same |
| JP2016081709A (ja) * | 2014-10-16 | 2016-05-16 | Tdk株式会社 | リチウムイオン二次電池用負極活物質、およびそれを含む負極並びにリチウムイオン二次電池 |
| WO2017081854A1 (ja) * | 2015-11-09 | 2017-05-18 | 株式会社豊田自動織機 | 負極活物質 |
| CN108352516A (zh) * | 2015-11-09 | 2018-07-31 | 株式会社丰田自动织机 | 负极活性物质 |
| JPWO2017081854A1 (ja) * | 2015-11-09 | 2018-09-13 | 株式会社豊田自動織機 | 負極活物質 |
| US10833325B2 (en) | 2015-11-09 | 2020-11-10 | Kabushiki Kaisha Toyota Jidoshokki | Negative electrode active material |
| CN108352516B (zh) * | 2015-11-09 | 2021-07-06 | 株式会社丰田自动织机 | 负极活性物质 |
| KR20170077845A (ko) | 2015-12-28 | 2017-07-06 | 주식회사 엘지화학 | 이차 전지용 음극 재료 및 그것을 이용한 비수 전해질 이차 전지 |
| WO2019107990A1 (ko) * | 2017-12-01 | 2019-06-06 | 주식회사 엘지화학 | 리튬이차전지용 음극 및 이를 포함하는 리튬이차전지 |
| US11575123B2 (en) | 2017-12-01 | 2023-02-07 | Lg Energy Solution, Ltd. | Negative electrode for lithium secondary battery and lithium secondary battery including the same |
Also Published As
| Publication number | Publication date |
|---|---|
| JP4547963B2 (ja) | 2010-09-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN107210442B (zh) | 非水电解质二次电池用负极活性物质和非水电解质二次电池 | |
| JP4752508B2 (ja) | 二次電池用負極材料、二次電池用負極およびそれを用いた二次電池 | |
| JP5360871B2 (ja) | 非水系電解質リチウムイオン二次電池 | |
| JP5133020B2 (ja) | 非水電解液二次電池用正極板の製造方法およびその正極板を用いた非水電解液二次電池 | |
| CN107660316B (zh) | 锂电化学发电装置的正电极 | |
| JP2000156229A (ja) | 非水電解質リチウム二次電池 | |
| JP2012190786A (ja) | 正極活物質、並びにそれを採用した正極及びリチウム電池 | |
| JP2011090876A (ja) | リチウム二次電池および該電池の製造方法 | |
| CN111540894B (zh) | 锂离子电池用负极活性材料、锂离子电池用负极和锂离子电池 | |
| JP4547963B2 (ja) | 二次電池用負極、その製造方法及び二次電池 | |
| JP6278870B2 (ja) | 炭素質被覆黒鉛粒子の製造方法、および、それを含有するリチウムイオン二次電池負極の製造方法 | |
| US10930929B2 (en) | Negative-electrode material for Li-ion secondary cell, method for manufacturing said material, negative electrode for Li-ion-secondary-cell, and Li-ion secondary cell | |
| JP4945906B2 (ja) | 二次電池用負極及びそれを用いた二次電池 | |
| JP4513385B2 (ja) | 二次電池用負極及び二次電池 | |
| WO2012063765A1 (ja) | 非水電解質二次電池 | |
| JP5207282B2 (ja) | リチウム二次電池 | |
| JP5855737B2 (ja) | リチウムイオン電池 | |
| JP5213011B2 (ja) | リチウム二次電池用負極、およびそれを用いたリチウム二次電池 | |
| JPH11204145A (ja) | リチウム二次電池 | |
| JP4029224B2 (ja) | 非水電解質電池 | |
| JP2005071938A (ja) | 二次電池用負極活物質、それを用いた二次電池用負極および二次電池、ならびに二次電池用負極活物質およびそれを用いた二次電池用負極の製造方法 | |
| JPH11111342A (ja) | リチウム二次電池 | |
| WO2014115322A1 (ja) | リチウムイオン二次電池用負極活物質及びそれらを用いたリチウムイオン二次電池 | |
| JP3972454B2 (ja) | リチウム二次電池 | |
| JP2016072031A (ja) | 蓄電素子用正極とそれを用いた蓄電素子及び蓄電装置 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20070213 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20100224 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20100323 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20100521 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20100615 |
|
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20100628 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 4547963 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20130716 Year of fee payment: 3 |
|
| EXPY | Cancellation because of completion of term |