ES2807528T3 - Complejos macrocíclicos pentaaza que poseen biodisponibilidad oral - Google Patents
Complejos macrocíclicos pentaaza que poseen biodisponibilidad oral Download PDFInfo
- Publication number
- ES2807528T3 ES2807528T3 ES16835928T ES16835928T ES2807528T3 ES 2807528 T3 ES2807528 T3 ES 2807528T3 ES 16835928 T ES16835928 T ES 16835928T ES 16835928 T ES16835928 T ES 16835928T ES 2807528 T3 ES2807528 T3 ES 2807528T3
- Authority
- ES
- Spain
- Prior art keywords
- solution
- administration
- pharmaceutical composition
- compounds
- substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- XARGIVYWQPXRTC-DTWKUNHWSA-N CC[C@H]1[C@@H](C)CCCC1 Chemical compound CC[C@H]1[C@@H](C)CCCC1 XARGIVYWQPXRTC-DTWKUNHWSA-N 0.000 description 1
- KVZJLSYJROEPSQ-GVHYBUMESA-N C[C@H]1C(C)CCCC1 Chemical compound C[C@H]1C(C)CCCC1 KVZJLSYJROEPSQ-GVHYBUMESA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F13/00—Compounds containing elements of Groups 7 or 17 of the Periodic System
- C07F13/005—Compounds without a metal-carbon linkage
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/28—Compounds containing heavy metals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/555—Heterocyclic compounds containing heavy metals, e.g. hemin, hematin, melarsoprol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/14—Esters of carboxylic acids, e.g. fatty acid monoglycerides, medium-chain triglycerides, parabens or PEG fatty acid esters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/44—Oils, fats or waxes according to two or more groups of A61K47/02-A61K47/42; Natural or modified natural oils, fats or waxes, e.g. castor oil, polyethoxylated castor oil, montan wax, lignite, shellac, rosin, beeswax or lanolin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/286—Polysaccharides, e.g. gums; Cyclodextrin
- A61K9/2866—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4816—Wall or shell material
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D257/00—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms
- C07D257/02—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms not condensed with other rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F1/00—Compounds containing elements of Groups 1 or 11 of the Periodic System
- C07F1/08—Copper compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System
- C07F15/02—Iron compounds
- C07F15/025—Iron compounds without a metal-carbon linkage
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic System
- C07F15/04—Nickel compounds
- C07F15/045—Nickel compounds without a metal-carbon linkage
Abstract
Un complejo macrocíclico pentaaza con la siguiente fórmula: **(Ver fórmula)** Una composición farmacéutica que comprende un complejo macrocíclico pentaaza según la reivindicación 1 y un excipiente farmacéuticamente aceptable adecuado para la administración.
Description
DESCRIPCIÓN
Complejos macrocíclicos pentaaza que poseen biodisponibilidad oral
[0001] La presente descripción por lo general se refiere a complejos macrocíclicos pentaaza de un metal de transición de 15 eslabones que tienen mejores propiedades, incluida una biodisponibilidad oral significativa.
[0002] Se ha demostrado que los complejos macrocíclicos pentaaza de un metal de transición de 15 eslabones que tienen el sistema macrocíclico que corresponde a la Fórmula A muestran eficacia en varios modelos animales y celulares de enfermedad humana, así como en el tratamiento de afecciones que afligen a pacientes humanos.
Por ejemplo, en un modelo de colitis en roedores, se ha afirmado que un compuesto de ese tipo, GC4403, cuando se administra por inyección intraperitoneal (i.p.), reduce significativamente las lesiones al colon de ratas sometidas a un modelo experimental de colitis (véase Cuzzocrea et al., Europ. J. Pharmacol., 432, 79-89 (2001)).
Se ha reportado que GC4403 administrado por vía i.p. también atenúa el daño producido por la radiación en un modelo relevante desde el punto de vista clínico de mucositis oral aguda inducida por radiación en hámsteres (Murphy et al., Clin. Can. Res., 14(13), 4292 (2008)), y por irradiación letal de todo el cuerpo en ratones adultos (Thompson et al., Free Radical Res., 44(5), 529-40 (2010)). De manera similar, se ha demostrado que otro compuesto de ese tipo, GC4419, cuando se administra por vía i.p., mitiga la enfermedad pulmonar inducida por un inhibidor del VEGFr en un modelo en ratas (Tuder, et al., Am. J. Respir. Cell Mol. Biol., 29, 88-97 (2003)), y aumenta la actividad antitumoral de agentes antimetabólitos y antimitóticos en modelos de cáncer en ratones (véase, por ejemplo, la patente WO2009/143454). Asimismo, se ha demostrado que otro compuesto de ese tipo, GC4401, cuando se administra por vía i.p., proporciona efectos protectores en modelos en animales de choque séptico (S. Cuzzocrea, et. al., Crit. Care Med., 32(1), 157 (2004) y pancreatitis (S. Cuzzocrea, et. al., Shock, 22(3), 254-61 (2004)).
[0003] También se ha demostrado que algunos de estos compuestos poseen una potente actividad antiinflamatoria y evitan el daño oxidativo in vivo. Por ejemplo, se ha afirmado que GC4403, cuando se administra por vía i.p., inhibe la inflamación en un modelo de inflamación en ratas (Salvemini, et. al., Science, 286, 304 (1999)) y evita la artropatía en un modelo de artritis inducida con colágeno en ratas (Salvemini et. al., Arthritis & Rheumatism, 44(12), 2009-2021 (2001)). Además, se ha afirmado que estos compuestos poseen actividad analgésica y reducen la inflamación y el edema en el modelo de hiperalgesia inducida por carragenina en pata de rata, véase, por ejemplo, la patente de EE. UU. n.° 6.180.620.
[0004] También se ha demostrado que compuestos de esta clase son inocuos y eficaces en la prevención y el tratamiento de enfermedades en sujetos humanos. Por ejemplo, se ha demostrado que GC4419, cuando se administra por infusión intravenosa (i.v.), reduce la mucositis oral en pacientes con cáncer de cabeza y cuello que siguen un tratamiento con quimiorradiación. (Anderson, C., Phase 1 Trial of Superoxide Dismutase (SOD) Mimetic GC4419 to Reduce Chemoradiotherapy (CRT)-Induced Mucositis (OM) in Patients (pts) with Mouth or Oropharyngeal Carcinoma (OCC), Oral Mucositis Research Workshop, MAs Cc / iSo O Annual Meeting on Supportive Care in Cancer, Copenhague, Dinamarca (25 de junio de 2015)).
[0005] En cada uno de estos compuestos que comprenden el anillo macrocíclico pentaaza de 15 eslabones con la fórmula A, cada uno de los cinco nitrógenos contenidos en el anillo macrocíclico forma un enlace covalente de coordinación con el manganeso (u otro metal de transición coordinado por el macrociclo) al centro de la molécula. Además, el manganeso (u otro metal de transición apropiado coordinado al macrociclo) forma enlaces covalentes de coordinación con «ligandos axiales» en posiciones perpendiculares al macrociclo aproximadamente plano. Dichos enlaces covalentes de coordinación se caracterizan por tener un par de electrones «libre» disponible en un ligando que forma un enlace con un metal de transición mediante donación y compartición del par de electrones, formando así un enlace con dos electrones entre el metal y el átomo donador del ligando (Cotton, F.A. & G. Wilkinson, Advanced Inorganic Chemistry, capítulo 5, Coordination Compounds, 2.a edición revisada, Interscience Publishers, pág. 139 (1966); IUPAC Gold Book, versión en línea http://goldbook.iupac.org/C01329.html). La naturaleza covalente y coordinada de los enlaces entre el manganeso (u otro metal de transición adecuado de este tipo) y los cinco nitrógenos del anillo macrocíclico y entre el manganeso (u otro metal de transición adecuado de este tipo) y cada uno de los dos ligandos axiales de cloro se demuestra, por ejemplo, en la estructura obtenida por rayos X de un «único cristal» de GC4403 (Fig. 11) y GC4419 (Fig. 12).
[0006] Los compuestos de coordinación son distintos a los compuestos iónicos como, por ejemplo, las sales, en los que en el estado sólido las fuerzas entre aniones y cationes son estrictamente fuerzas electrostáticas de tipo culómbico de atracción entre iones de carga opuesta. Por lo tanto, en las sales, los cationes y los aniones discretos proporcionan la fuerza para mantener la estructura en el estado sólido; por ejemplo, como el ion cloruro y el ion sodio en una sal común como el cloruro de sodio (Cotton, F.A. & G. Wilkinson, Advanced Inorganic Chemistry, capítulo 5, "The Nature of Ionic Substances", 2.a edición revisada, Interscience Publishers, págs. 35-36, 45-49 (1966).
[0007] Aunque los complejos macrocíclicos pentaaza de 15 eslabones se han dado a conocer en la bibliografía para varias indicaciones, los complejos dados a conocer hasta la fecha tienen una disponibilidad oral limitada (sustancialmente inferior al 5% cuando se administran en solución acuosa, con una biodisponibilidad algo mayor, aunque todavía insuficiente, cuando se administran en formulaciones oleosas adecuadas; véase, por ejemplo, el Cuadro 1). En general, la asimilación de un fármaco desde el tubo gastrointestinal tiene lugar mediante absorción pasiva de manera que la asimilación está favorecida cuando el fármaco se encuentra en su forma no ionizada (neutra) y lipofílica. Véase, por ejemplo, Goodmun & Gilman: The Pharmacological Basis of Therapeutics, 9.a edición, págs. 5 9 (1996). Sin querer estar limitados por ninguna teoría concreta, en la actualidad esto también se cree que es el caso para esta clase de compuestos, según está ejemplificado por GC4419, en donde los ligandos axiales son ambos residuos de cloro que forman un enlace covalente de coordinación con el manganeso, formándose un complejo neutro:
[0008] También se entiende que una buena solubilidad en agua puede mejorar la velocidad de absorción del fármaco y la biodisponibilidad global (Goodmun & Gilmun's: The Pharmacological Basis of Therapeutics, 9.a edición, pág. 5 (1996)). GC4419 y sus análogos estructurales se disuelven todos en agua con relativa facilidad, pero es posible que en agua no permanezcan en su forma neutra no ionizada. En su lugar, cuando están disueltos en agua, los enlaces covalentes de coordinación se rompen y un ligando axial de agua reemplaza uno o más de los ligandos axiales de cloro, lo que da lugar a complejos monocatiónicos o dicatiónicos, tal y como se ilustra en el Esquema 1. Se prevé que los compuestos catiónicos tengan una capacidad menor de cruzar la barrera intestinal con respecto al complejo neutro.
Monocatión Dicatión
[0009] En la patente WO 2006/083508 A2 se dan a conocer combinaciones de catalizadores sintéticos de bajo peso molecular para la dismutación de superóxido y fármacos analgésicos/antiinflamatorios no esteroideos para aumentar el umbral de dolor en condiciones de hiperalgesia.
[0010] En la patente WO 96/39396 A1 se dan a conocer miméticos de la superóxido dismutasa de bajo peso molecular que se usan como agentes terapéuticos en trastornos y estados patológicos inflamatorios, lesión por reperfusión/isquemia, accidente cerebrovascular, ateroesclerosis y otras afecciones de lesiones o daño tisular inducidos por oxidación.
[0011] En la patente WO 02/071054 A1 se da a conocer un método para detectar y hacer el análisis cualitativo de complejos metálicos. El método comprende depositar una solución de un complejo metálico en una columna, eluir el complejo metálico con una fase móvil, comprendiendo la fase móvil un exceso de una sal de un anión coordinador en un sistema de disolventes y detectar el complejo metálico con un detector.
[0012] En la patente WO 93/02090 A1 se dan a conocer miméticos de la superóxido dismutasa de bajo peso molecular, que se usan como agentes terapéuticos en trastornos y estados patológicos inflamatorios, lesión por reperfusión/isquemia, accidente cerebrovascular, ateroesclerosis, hipertensión y otras afecciones de lesiones o daño tisular inducidos por oxidación.
[0013] En la patente WO 94/15925 A1 se dan a conocer miméticos de la superóxido dismutasa de bajo peso molecular que se usan como agentes terapéuticos en trastornos y estados patológicos inflamatorios, lesión por reperfusión/isquemia, infarto de miocardio, accidente cerebrovascular, ateroesclerosis y otras afecciones de lesiones o daño tisular inducidos por oxidación.
[0014] Por lo tanto, entre los diversos aspectos de la presente descripción se encuentra la provisión de complejos de metales de transición de ligandos macrocíclicos pentaaza que comprenden el anillo macrocíclico de 15 eslabones con la Fórmula A que se puede administrar a un sujeto por vía oral y otras vías de administración, lográndose de este modo elevadas concentraciones sistémicas del fármaco, inclusive mediante administración por vía oral. En una realización preferida en la actualidad, el metal de transición es manganeso.
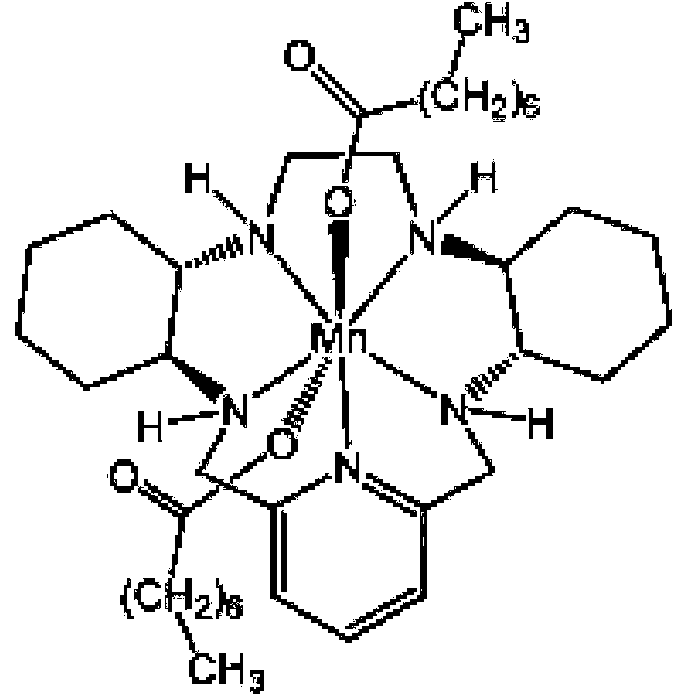
[0015] Un aspecto de la presente descripción es un complejo de un metal de transición que comprende un metal de transición coordinado por un macrociclo que comprende el anillo macrocíclico pentaaza de 15 eslabones que corresponde a la Fórmula A y dos ligandos axiales que tienen la fórmula -OC(O)X1, en donde el macrociclo comprende el anillo pentaaza de 15 eslabones que corresponde a la Fórmula A y en donde la Fórmula A puede tener más sustituyentes, en donde
cada uno de los dos ligandos axiales tiene la fórmula -OC(O)X1, en donde
cada X1 es independientemente fenilo sustituido o no sustituido o -C(-X2)(-X3 )(-X4);
cada X2 es independientemente fenilo sustituido o no sustituido, o alquilo sustituido o no sustituido;
cada X3 es independientemente hidrógeno, hidroxilo, alquilo, amino, -XsC(O)R13, donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es =O; y
cada X4 es independientemente hidrógeno o junto con X3 es =O.
[0016] Un aspecto adicional de la presente descripción es un complejo de manganeso que comprende Mn2+ o Mn3+ coordinado por un macrociclo que comprende el anillo macrocíclico pentaaza de 15 eslabones que corresponde a la Fórmula A y dos ligandos axiales que tienen la fórmula -OC(O)X-i, en donde
cada X1 es independientemente fenilo sustituido o no sustituido o -C(-X2)(-X3 )(-X4);
cada X2 es independientemente fenilo sustituido o no sustituido, o alquilo sustituido o no sustituido;
cada X3 es independientemente hidrógeno, hidroxilo, alquilo, amino, -XsC(O)R13, donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -0 R14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es =O; y
cada X4 es independientemente hidrógeno o junto con X3 es =O.
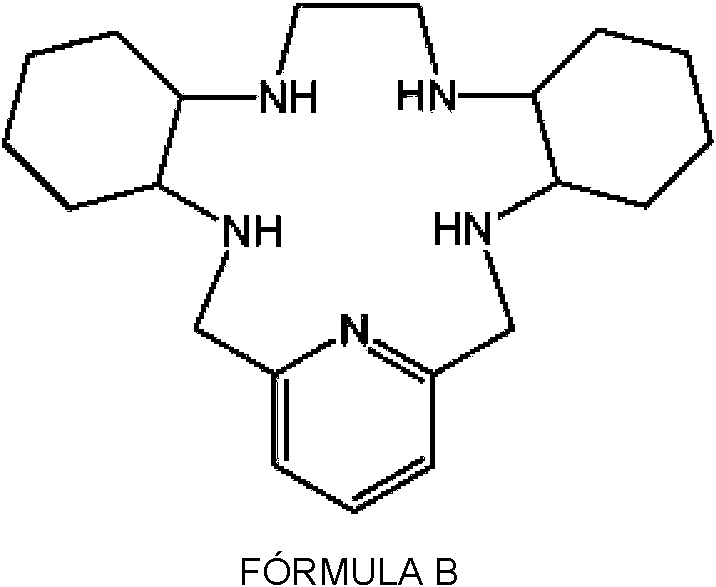
[0017] Un aspecto adicional de la presente descripción es un complejo de un metal de transición que comprende un metal de transición coordinado por los cinco átomos de nitrógeno en el anillo de un macrociclo que comprende el sistema de anillos fusionados con la Fórmula B (que opcionalmente pueden tener más sustituyentes según se describe en otra parte de la presente memoria) y dos ligandos axiales que tienen la fórmula -OC(O)X1, en donde la Fórmula B tiene la siguiente fórmula
cada X1 es independientemente fenilo sustituido o no sustituido o -C(-X2)(-X3 )(-X4);
cada X2 es independientemente fenilo sustituido o no sustituido, o alquilo sustituido o no sustituido;
cada X3 es independientemente hidrógeno, hidroxilo, alquilo, amino, -XsC(O)R13, donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -0 R14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es =O; y
cada X4 es independientemente hidrógeno o junto con X3 es =O.
[0018] Un aspecto adicional de la presente descripción es un complejo de un metal de transición que comprende Mn2+ o Mn3+ coordinado por un macrociclo que comprende el sistema de anillos fusionados con la Fórmula B (que opcionalmente pueden tener más sustituyentes) y dos ligandos axiales que tienen la fórmula -OC(O)X1, en donde cada X1 es independientemente fenilo sustituido o no sustituido o -C(-X2)(-X3 )(-X4);
cada X2 es independientemente fenilo sustituido o no sustituido, o alquilo sustituido o no sustituido;
cada X3 es independientemente hidrógeno, hidroxilo, alquilo, amino, -XsC(O)R13, donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es =O; y
cada X4 es independientemente hidrógeno o junto con X3 es =O.
[0019] Un aspecto adicional de la presente descripción es un complejo de un metal de transición que corresponde a la Fórmula (I):
M es un metal de transición (por ejemplo, Mn2+, Mn3+, Mn4+, Mn6+, Mn7+, Fe2+, Fe3+, Fe4+, Fe6+, Ni2+, Ni3+, Cu1+, Cu2+, V2+, V3+, V4+ o V5+);
R1A, R1B, R2A, R2B, R3A, R3B, R4A, R4B, R5A, R5B, R6a, R6b, R7A, R7B, R8a, R8b, R9A, R9B, R10A y R10B son independientemente:
(i) hidrógeno;
(ii) una porción independientemente seleccionada del grupo que consiste en radicales alquenilo, alquenilcicloalquenilo, alquenilcicloalquilo, alquilo, alquilcicloalquenilo, alquilcicloalquilo, alquinilo, aralquilo, arilo, cicloalquenilo, cicloalquilo, cicloalquilalquilo, cicloalquilcicloalquilo, cicloalquenilalquilo, heterociclo y aralquilo, y radicales unidos al carbono a de aminoácidos (es decir, a-aminoácidos); o (iii) una porción independientemente seleccionada del grupo que consiste en -OR11, -NR11R12, -COR11, -CO2R11, -CONR11R12, -SR11, -SOR11, -SO2R11, -SO2NR11R12, -N(ORh )(R12), -P(O)(ORn)(OR12), -P(O)(ORn)(R12), -OP(O)(ORn)(OR12) y sustituyentes unidos al carbono a de aminoácidos (es decir, aaminoácidos), en donde R11 y R12 son independientemente hidrógeno o alquilo;
(iv) un miembro de un ciclo o heterociclo sustituido o no sustituido, saturado, parcialmente saturado o insaturado que contiene de 3 a 20 átomos de carbono en el anillo que comprende
(a) R1a o R1b y R2A o R2b; R3A o R3B y R4A o R4B; R5A o R5B y R6a o R6b; R7A o R7B y R8a o R8b; o R9A o R9B y R10A o R10B, junto con los átomos de carbono a los que están respectivamente unidos; (b) R10A o R10B y R1A o R1b; R2A o R2B y R3A o R3B; R4a o R4B y R5A o R5B, R6a o R6b y R7A o R7B; o R8a o R8b y R9A o R9B, junto con los átomos de carbono a los que están respectivamente unidos; o (c) R1A y R1b; R2A y R2b; R3A y R3b; R4A y R4b; R5A y R5B, R6a y R6b; R7A y R7b; R8a y R8b; R9A y R9b; o R10A y R10B, junto con los átomos de carbono a los que están respectivamente unidos; o (v) una combinación de cualquiera de (i) a (iv) más arriba;
cada X1 es independientemente fenilo sustituido o no sustituido o -C(-X2)(-X3 )(-X4);
cada X2 es independientemente fenilo sustituido o no sustituido, o alquilo sustituido o no sustituido;
cada X3 es independientemente hidrógeno, hidroxilo, alquilo, amino, -XsC(O)R13, donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es =O;
cada X4 es independientemente hidrógeno o junto con X3 es =O; y
los enlaces entre el metal de transición M y los átomos de nitrógeno del macrociclo y los enlaces entre el metal de transición M y los átomos de oxígeno de los ligandos axiales -OC(O)X1 son enlaces covalentes de coordinación.
[0020] Otro aspecto de la presente descripción es un complejo macrocíclico pentaaza con la Fórmula (I) que corresponde a las Fórmulas (IDr) o (IDs):
en donde
M es Mn2+ o Mn3+
Ría , Rib, R2 , R3, R4A, R4B, R5, R6, R7A, R7B, R8, R9, R10A y R10B son independientemente hidrógeno, metilo, etilo o propilo;
W í , W 2 y W 3 son independientemente haluro o hidrógeno;
cada Xi es independientemente fenilo sustituido o no sustituido o -C(-X2)(-X3 )(-X4);
cada X2 es independientemente fenilo sustituido o no sustituido, metilo, etilo o propilo;
cada X3 es independientemente hidrógeno, hidroxilo, metilo, etilo o propilo, amino, -XsC(O)Ri3, donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -0 R14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es =O;
cada X4 es independientemente hidrógeno o junto con X3 es =O; y
los enlaces entre el manganeso y los átomos de nitrógeno del macrociclo y los enlaces entre el manganeso y los átomos de oxígeno de los ligandos axiales -OC(O)Xi son enlaces covalentes de coordinación.
[0021] Otro aspecto de la descripción es una composición farmacéutica que comprende cualquiera de los complejos macrocíclicos pentaaza mencionados anteriormente y un excipiente aceptable desde el punto de vista farmacéutico adecuado para la administración.
[0022] Otro aspecto de la descripción es un método para administrar a un sujeto un complejo macrocíclico pentaaza, comprendiendo el método la administración a un sujeto humano de una composición farmacéutica que comprende cualquiera de los complejos macrocíclicos pentaaza mencionados anteriormente.
[0023] Otras finalidades y características resultarán en parte evidentes y en parte se señalarán a continuación. La invención está definida por las reivindicaciones.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
[0024]
La Figura 1 es una serie de representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados (donde todos los compuestos que se muestran son derivados de GC4419) por vía intravenosa (i.v.) o intraduodenal (i.d.), estando los artículos ensayados por vía i.d. formulados en Capmul MCM, según se describe en los ejemplos.
La Figura 2 es una serie de representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados (donde todos los compuestos que se muestran son derivados de GC4419) por vía i.v. o i.d., estando los artículos ensayados por vía i.d. formulados en Peceol, según se describe en los ejemplos.
La Figura 3 es una serie de representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados (donde todos los compuestos que se muestran son derivados de GC4419) por vía i.v. o por vía i.d., estando los artículos ensayados por vía i.d. formulados en Labrafil M2125 CS, según se describe en los ejemplos.
La Figura 4 es una serie de representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados (donde todos los compuestos que se muestran son derivados de GC4419) por vía i.v. o por vía i.d., estando los artículos ensayados por vía i.d. formulados en Labrafil M2125 CS, según se describe en los ejemplos.
La Figura 5 es una serie de representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4401 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados (donde todos los compuestos que se muestran son derivados de GC4401) por vía i.v. o por vía i.d., estando los artículos ensayados por vía i.d. formulados en Capmul MCM, según se describe en los ejemplos.
La Figura 6 es una serie de representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4444 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados (donde todos los compuestos que se muestran son derivados de GC4444) por vía i.v. o por vía i.d., estando los artículos ensayados por vía i.d. formulados en Capmul MCM, según se describe en los ejemplos.
La Figura 7 es una serie de representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados (donde todos los compuestos que se muestran son derivados de GC4419) por vía i.v. o por vía i.d., estando los artículos ensayados por vía i.d. formulados en Capmul MCM, según se describe en los ejemplos.
La Figura 8 es una serie de representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados (donde todos los compuestos que se muestran son derivados de GC4419) por vía i.v. o por vía i.d., estando los artículos ensayados por vía i.d. formulados en Maisine 35-1, según se describe en los ejemplos.
La Figura 9 es una serie de representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4403 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados (donde todos los compuestos que se muestran son derivados de GC4403) por vía i.v. o por vía i.d., estando los artículos ensayados por vía i.d. formulados en Capmul MCM, según se describe en los ejemplos.
La Figura 10 es una ilustración de un subconjunto de estructuras de ligandos axiales que proporcionan una mayor biodisponibilidad oral.
La Figura 11 es una estructura cristalina de GC4403 obtenida por rayos X (según está publicado en Advances in Inorganic Chemistry, Riley et al., Vol. 59, págs. 233-263 (2007)).
La Figura 12 es una estructura cristalina de GC4419 obtenida por rayos X mediante el método publicado en Advances in Inorganic Chemistry, Riley et al., Vol. 59, págs. 233-263 (2007).
ABREVIATURAS Y DEFINICIONES
[0025] Las siguientes definiciones y métodos se proporcionan para definir mejor la presente invención y para guiar a los expertos en la técnica en la práctica de la presente invención. A menos que se indique lo contrario, los términos se deben entender de acuerdo con el uso convencional por los expertos en la técnica pertinente.
[0026] El término «acilo» significa una porción de -COR, en donde R es alquilo, haloalquilo, opcionalmente arilo sustituido u opcionalmente heteroarilo sustituido, según se define en la presente memoria, por ejemplo, acetilo, trifluoracetilo, benzoílo y similares.
[0027] El término «aciloxi» significa una porción de -OCOR, en donde R es alquilo, haloalquilo, opcionalmente arilo sustituido u opcionalmente heteroarilo sustituido, según se define en la presente memoria, por ejemplo, acetilo, trifluoracetilo, benzoílo y similares.
[0028] El término «alcoxi» significa una porción de -OR donde R es alquilo, según se define más arriba, por ejemplo, metoxi, etoxi, propoxi o 2-propoxi, n-, iso- o terf-butoxi, y similares.
[0029] El término «alquilo» significa una porción hidrocarbonada saturada lineal monovalente, como de uno a seis átomos de carbono, o una porción hidrocarbonada saturada ramificada monovalente, como de tres a seis átomos de carbono, por ejemplo, grupos alquilo de C1-C6, como metilo, etilo, propilo, 2-propilo, butilo (incluidas todas las formas isoméricas), pentilo (incluidas todas las formas isoméricas) y similares.
[0030] Además, a menos que se indique lo contrario, con el término «alquilo», tal y como se utiliza en la presente memoria, se pretende incluir tanto a «alquilos no sustituidos» como a «alquilos sustituidos», haciendo referencia estos últimos a las porciones de alquilo que tienen sustituyentes que reemplazan a un hidrógeno en uno o más carbonos del esqueleto hidrocarbonado. En efecto, a menos que se indique lo contrario, con todos los grupos mencionados en la presente memoria se pretende incluir a opciones tanto sustituidas como no sustituidas.
[0031] Con el término «Cx-y», cuando se usa junto con una porción química, como alquilo y aralquilo, se pretende incluir grupos que contienen de x a y átomos de carbono en la cadena. Por ejemplo, el término «alquilo de Cx-y» hace referencia a grupos hidrocarbonados saturados sustituidos o no sustituidos, incluidos grupos alquilo de cadena recta y grupos alquilo de cadena ramificada que contienen de x a y átomos de carbono en la cadena.
[0032] El término «alquileno» significa una porción hidrocarbonada saturada lineal divalente, como de uno a seis átomos de carbono, o una porción hidrocarbonada saturada ramificada divalente, como de tres a seis átomos de carbono, a menos que se indique lo contrario, por ejemplo, metileno, etileno, propileno, 1-metilpropileno, 2-metilpropileno, butileno, pentileno y similares.
[0033] El término «alquenilo» significa una porción hidrocarbonada insaturada lineal monovalente, como de dos a seis átomos de carbono, o una porción hidrocarbonada saturada ramificada monovalente, como de tres a seis átomos de carbono, por ejemplo, etenilo (vinilo), propenilo, 2-propenilo, butenilo (incluidas todas las formas isoméricas), pentenilo (incluidas todas las formas isoméricas) y similares.
[0034] El término «alcarilo» significa una porción monovalente derivada de una porción arílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo alquilo.
[0035] El término «alquenilcicloalquenilo» significa una porción monovalente derivada de una porción alquenílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo cicloalquenilo.
[0036] El término «alquenilcicloalquilo» significa una porción monovalente derivada de una porción cicloalquílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo alquenilo.
[0037] El término «alquilcicloalquenilo» significa una porción monovalente derivada de una porción cicloalquenílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo alquilo.
[0038] El término «alquilcicloalquilo» significa una porción monovalente derivada de una porción cicloalquílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo alquilo.
[0039] El término «alquinilo» significa una porción hidrocarbonada insaturada lineal monovalente, como de dos a seis átomos de carbono, o una porción hidrocarbonada saturada ramificada monovalente, como de tres a seis átomos de carbono, por ejemplo, etinilo, propinilo, butinilo, isobutinilo, hexinilo y similares.
[0040] El término «alcoxi» significa una porción monovalente derivada de una porción alquílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo hidroxilo.
[0041] El término «amino» significa un grupo -NRaRb, en donde Ra y Rb son independientemente hidrógeno, alquilo o arilo.
[0042] El término «aralquilo» significa una porción monovalente derivada de una porción alquílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo arilo.
[0043] El término «arilo» significa una porción hidrocarbonada aromática monocíclica o bicíclica monovalente de 6 a 10 átomos en el anillo, por ejemplo, fenilo o naftilo.
[0044] El término «ciclo» significa una porción hidrocarbonada saturada carbocíclica monovalente de tres a diez átomos de carbono.
[0045] El término «cicloalquilo» significa una porción hidrocarbonada saturada cíclica monovalente de tres a diez átomos de carbono, por ejemplo, ciclopropilo, ciclobutilo, ciclopentilo o ciclohexilo y similares.
[0046] El término «cidoalquilalquilo» significa una porción monovalente derivada de una porción alquílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo cicloalquilo, por ejemplo, ciclopropilmetilo, ciclobutilmetilo, ciclopentiletilo o ciclohexiletilo y similares.
[0047] El término «cicloalquilcicloalquilo» significa una porción monovalente derivada de una porción cicloalquílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo cicloalquilo.
[0048] El término «cicloalquenilo» significa una porción hidrocarbonada monoinsaturada cíclica monovalente de tres a diez átomos de carbono, por ejemplo, ciclopropenilo, ciclobutenilo, ciclopentenilo o ciclohexenilo y similares.
[0049] El término «cicloalquenilalquilo» significa una porción monovalente derivada de una porción alquílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo cicloalquenilo, por ejemplo, ciclopropenilmetilo, ciclobutenilmetilo, ciclopenteniletilo o ciclohexeniletilo, y similares.
[0050] El término «capa de recubrimiento entérico» comprende uno o más polímeros entéricos y un excipiente más aceptable desde el punto de vista farmacéutico comprende, entre otros, agentes de liberación mantenida, como copolímero de acrilato de etilo-ácido metacrílico, etilcelulosa.
[0051] El término «éter» significa una porción monovalente derivada de una porción alquílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo alcoxi.
[0052] El término «haluro» significa flúor, cloro, bromo o yodo, preferentemente flúor o cloro.
[0053] El término «heterociclo» o «heterocíclico» significa un grupo monocíclico monovalente saturado o insaturado de 4 a 8 átomos en el anillo, en donde uno o dos átomos en el anillo son heteroátomos seleccionados de entre N, O o S(O)n, en donde n es un número entero del 0 al 2, siendo los átomos restantes C. El anillo heterocíclico está opcionalmente fusionado a (un) anillo arílico o heteroarílico según se define en la presente memoria con la condición de que los anillos arílicos y heteroarílicos sean monocíclicos. En esta solicitud, al anillo heterocíclico fusionado con el anillo monocíclico arílico o heteroarílico también se le denomina anillo «heterocíclico bicíclico». Asimismo, uno o dos átomos de carbono del anillo en el anillo heterocíclico se pueden opcionalmente reemplazar con un grupo -CO-. Más específicamente, el término «heterocíclico» incluye, entre otros, pirrolidino, piperidino, homopiperidino, 2-oxopirrolidinilo, 2-oxopiperidinilo, morfolino, piperazino, tetrahidropiranilo, tiomorfolino y similares. Cuando el anillo heterocíclico es insaturado, este puede contener uno o dos dobles enlaces en el anillo con la condición de que el anillo no sea aromático. Cuando el grupo heterocíclico es un anillo saturado y no está fusionado con el anillo arílico o heteroarílico, como se indica más arriba, en la presente memoria también se le denomina heterociclo monocíclico saturado.
[0054] El término «heteroarilo» significa una porción aromática monovalente monocíclica o bicíclica de 5 a 10 átomos en el anillo, en donde uno o más, preferentemente uno, dos o tres átomos del anillo son heteroátomos seleccionados de entre N, O o S, siendo carbono los restantes átomos del anillo. Algunos ejemplos representativos incluyen, entre otros, pirrolilo, pirazolilo, tienilo, tiazolilo, imidazolilo, furanilo, indolilo, isoindolilo, oxazolilo, isoxazolilo, benzotiazolilo, benzoxazolilo, benzimidazolilo, quinolinilo, isoquinolinilo, piridinilo, pirimidinilo, pirazinilo, piridazinilo, triazolilo, tetrazolilo y similares.
[0055] El término «nitro» significa -NO2.
[0056] El término «organosulfuro» significa una porción monovalente, un grupo -SR donde R es hidrógeno, alquilo o arilo.
[0057] Los términos «alquilo sustituido», «ciclo sustituido», «fenilo sustituido», «arilo sustituido», «heterociclo sustituido» y «heterociclos sustituidos con nitrógeno» significan un alquilo, ciclo, fenilo, arilo, heterociclo o heterociclo que contiene nitrógeno, respectivamente, opcionalmente sustituido con uno, dos, o tres sustituyentes, como los seleccionados independientemente de entre alquilo, alcoxi, alcoxialquilo, haluro, hidroxilo, hidroxialquilo u organosulfuro.
[0058] El término «tioéter» significa una porción monovalente derivada de una porción alquílica que se obtiene al reemplazar uno o más átomos de hidrógeno con un grupo -SR, en donde R es alquilo.
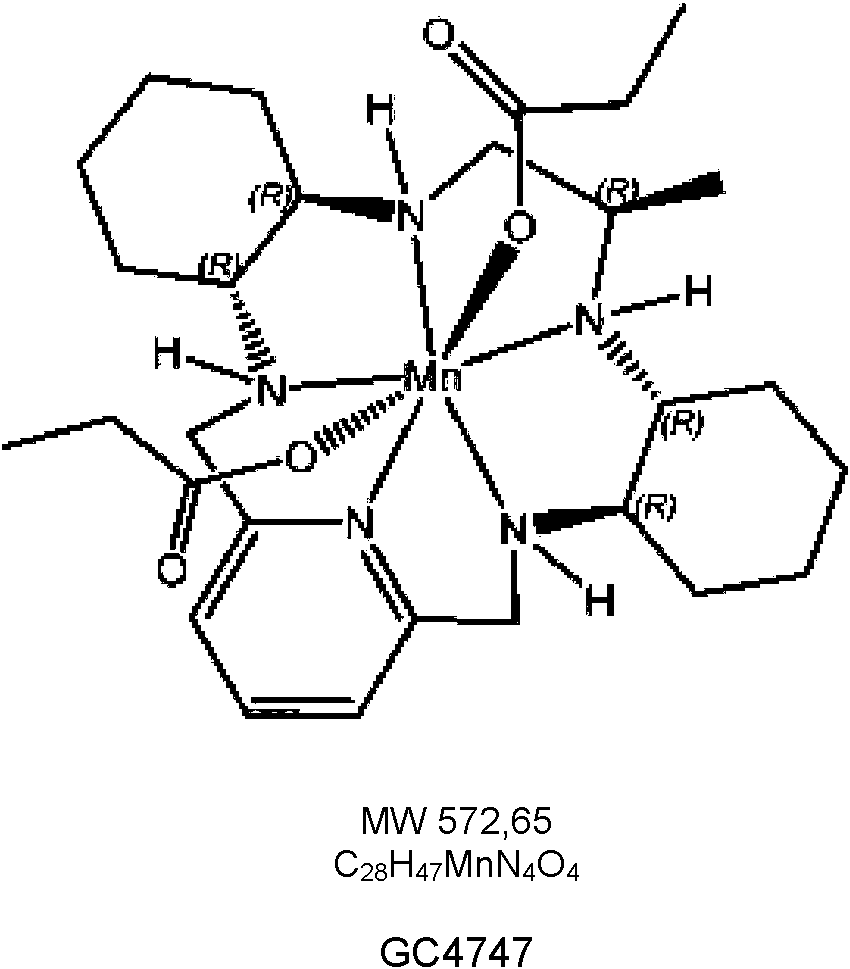
[0059] Tal y como se utiliza en la presente memoria, (i) el compuesto mencionado en la presente memoria y en las figuras como compuesto 401,4401 o GC4401 hace referencia al mismo compuesto, (ii) el compuesto mencionado en la presente memoria y en las figuras como compuesto 403, 4403 o GC4403 hace referencia al mismo compuesto, (iii) el compuesto mencionado en la presente memoria y en las figuras como compuesto 419, 4419 o GC4419 hace referencia al mismo compuesto y (iv) el compuesto mencionado en la presente memoria y en las figuras como compuesto 444, 4444 o GC4444 hace referencia al mismo compuesto.
DESCRIPCIÓN DETALLADA
[0060] Algunos aspectos de la presente descripción incluyen complejos macrocíclicos pentaaza de metales de transición novedosos que también poseen ligandos axiales y que tienen la capacidad, en circulación, de transformarse a las mismas especies a las que los complejos análogos con ligandos axiales de bis-cloro se transforman en circulación. Por lo tanto, los compuestos o complejos descritos en la presente memoria poseen una eficacia terapéutica similar a la de los análogos de bis-cloro, pero son significativamente más versátiles en cuanto a vías de administración. Dicho de otro modo, los compuestos de la descripción poseen una mayor biodisponibilidad oral con respecto a sus análogos de bis-cloro y en algunas realizaciones, y además poseen otras propiedades ventajosas seleccionadas de entre uno o más de mejor permeabilidad intestinal, solubilidad en formas farmacéuticas oleosas y/o acuosas, facilidad de fabricación y/o estabilidad.
[0061] Por lo tanto, la presente descripción está dirigida a complejos macrocíclicos pentaaza de Mn (II) (u otro metal de transición) de 15 eslabones, en donde los ligandos que no forman parte del anillo macrocíclico (es decir, los ligandos axiales) unidos mediante enlaces covalentes al manganeso (II) (u otro metal de transición) se seleccionan de un grupo de porciones que dan lugar al complejo que tiene una versatilidad mejorada en cuanto a vía de administración, inclusive la administración por vía oral, con respecto a, por ejemplo, el complejo conocido de bis-cloro. En determinadas realizaciones, por ejemplo, los complejos descritos en la presente memoria muestran una mayor absorción a través de la pared intestinal, pero mantienen la capacidad de perder el ligando o los ligandos axiales mediante intercambio con agua para dar especies similares en circulación a las obtenidas con los complejos de biscloro que se ilustran en el Esquema 1 más arriba. En estas y/o otras realizaciones, por ejemplo, los complejos también pueden mostrar una mayor solubilidad en disolventes oleosos o acuosos (u otros), en comparación con los complejos de bis-cloro.
[0062] En un primer aspecto, se proporcionad un complejo metálico de coordinación que corresponde a la Fórmula (I):
independientemente:
(i) hidrógeno;
(ii) una porción independientemente seleccionada del grupo que consiste en radicales alquenilo, alquenilcicloalquenilo, alquenilcicloalquilo, alquilo, alquilcicloalquenilo, alquilcicloalquilo, alquinilo, aralquilo, arilo, cicloalquenilo, cicloalquilo, cicloalquilalquilo, cicloalquilcicloalquilo, cicloalquenilalquilo, heterociclo y aralquilo, y radicales unidos al carbono a de aminoácidos (es decir, a-aminoácidos); o (iii) una porción independientemente seleccionada del grupo que consiste en -OR11, -NR11R12, COR11, -CO2R11, -CONR11R12, -SR11, -SOR11, -SO2R11, -SO2NR11R12, -N(ORii)(R i2), -P(=O)(ORii)(ORi2), -P(=O)(ORii)(Ri2), -OP(=O)(ORii)(ORi2 ) y sustituyentes unidos al carbono a de aminoácidos (es decir, a-aminoácidos), en donde R11 y R12 son independientemente hidrógeno o alquilo;
(iv) un miembro de un ciclo o heterociclo sustituido o no sustituido, saturado, parcialmente saturado o insaturado que contiene de 3 a 20 átomos de carbono en el anillo que comprende
(a) Ria o Rib y R2A o R2b; R3A o R3B y R4A o R4B; R5A o R5B y R6a o R6b; R7A o R7B y R8a o R8b; o R9A o R9B y R10A o R10B junto con los átomos de carbono a los que están respectivamente unidos; (b) R10A o R10B y Ría o Rib ; R2A o R2B y R3A o R3B; R4A o R4B y R5A o R5B, R6a o R6b y R7A o R7B; o R8a o R8b y R9A o R9B, junto con los átomos de carbono a los que están respectivamente unidos; o (c) Ría y Ríb ; R2A y R2b; R3A y R3b; R4A y R4b; R5A y R5B, R6a y R6b; R7A y R7b; R8a y R8b; R9A y R9b; o R10A y R10B, junto con los átomos de carbono a los que están respectivamente unidos; o
(v) una combinación de cualquiera de (i) a (iv) más arriba;
cada Xi es independientemente fenilo sustituido o no sustituido o -C(-X2)(-X3 )(-X4);
cada X2 es independientemente fenilo sustituido o no sustituido, o alquilo sustituido o no sustituido;
cada X3 es independientemente hidrógeno, hidroxilo, alquilo, amino, -X5C(=O)Ri3, en donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de Ci-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es (=O);
cada X4 es independientemente hidrógeno o junto con X3 es (=O); y
los enlaces entre el metal de transición M y los átomos de nitrógeno del macrociclo y los enlaces entre el metal de transición M y los átomos de oxígeno de los ligandos axiales -OC(=O)Xi son enlaces covalentes de coordinación.
[0063] En un segundo aspecto, esta descripción está destinada a composiciones farmacéuticas y formulaciones de dosis unitarias que comprenden un compuesto con la Fórmula (I) (o cualquiera de las realizaciones de la misma descritas en la presente memoria) y un excipiente aceptable desde el punto de vista farmacéutico. En una realización, la composición farmacéutica está formulada para administración por vía oral. En otra realización, la composición farmacéutica está formulada para administración por vía parenteral. En otra realización, la composición farmacéutica está formulada para administración por vía tópica. Las composiciones farmacéuticas y las formulaciones de dosis unitarias de este segundo aspecto se comentan con más detalle más abajo.
Realizaciones (no se deben entender como «la invención», la cual está definida por las reivindicaciones)
Realización (IA)
[0064] En la realización (IA), el complejo macrocíclico pentaaza con la Fórmula (I) corresponde a la Fórmula (IA):
en donde
M es un metal de transición (por ejemplo, Mn2+, Mn3+, Mn4+, Mn6+, Mn7+, Fe2+, Fe3+, Fe4+, Fe6+, Ni2+, Ni3+, Cu1+, Cu2+, V2+, V3+, V4+ o V5+);
Ría , Rib , R2 , R3, R4A, R4b, R5 , R6, R7A, R7B, R8, R9 , Rioa y Riob son independientemente hidrógeno, hidrocarbilo, hidrocarbilo sustituido, heterociclo, una porción de cadena lateral aminoacídica o una porción independientemente seleccionada del grupo que consiste en -OR11, -NR11R12, -COR11, -CO2R11, -C(=0)NR i í Rí2, -SR11, -SOR11, -SO2R11, -SO2NR11R12,
-N(ORii)(Ri2),
-P(=O)(0 Ri í )(ORí 2 ), -P(=0 )(ORi í )(Rí 2) y -OP(=0 )(ORi í )(ORí 2), en donde R11 y R12 son independientemente hidrógeno o alquilo;
U, junto con los átomos de carbono adyacentes del macrociclo, forma un ciclo o heterociclo fusionado, sustituido o no sustituido, saturado, parcialmente saturado o insaturado que tiene de 3 a 20 átomos de carbono en el anillo; V, junto con los átomos de carbono adyacentes del macrociclo, forma un ciclo o heterociclo fusionado, sustituido o no sustituido, saturado, parcialmente saturado o insaturado que tiene de 3 a 20 átomos de carbono en el anillo; W, junto con el nitrógeno del macrociclo y los átomos de carbono del macrociclo a los que está unido, forma un heterociclo fusionado que contiene nitrógeno, aromático o alicíclico, sustituido o no sustituido, saturado, parcialmente saturado o insaturado que tiene de 2 a 20 átomos de carbono en el anillo, con la condición de que cuando W es un heterociclo aromático fusionado el hidrógeno unido al nitrógeno que forma parte tanto del heterociclo como del macrociclo, y R5 y R6 unidos a los átomos de carbono que forman parte tanto del heterociclo como del macrociclo, están ausentes; en donde
cada Xi es independientemente fenilo sustituido o no sustituido, o -C(-X2 )(-X3)(-X4);
cada X2 es independientemente fenilo sustituido o no sustituido, o alquilo;
cada X3 es independientemente hidrógeno, hidroxilo, alquilo, amino, -X5C(=O)Ri3, donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18,
arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es (=O);
cada X4 es independientemente hidrógeno o junto con X3 es (=O); y
los enlaces entre el metal de transición M y los átomos de nitrógeno del macrociclo y los enlaces entre el metal de transición M y los átomos de oxígeno de los ligandos axiales -OC(=O)X1 son enlaces covalentes de coordinación.
[0065] Dentro de la realización (IA), en un grupo de compuestos, U y V, junto con los átomos de carbono adyacentes del macrociclo, forman un ciclo o heterociclo fusionado saturado, sustituido o no sustituido, que tiene 6 átomos en el anillo, y R2, R3, R8y Rgson hidrógeno, y W, junto con el nitrógeno del macrociclo y los átomos de carbono del macrociclo a los que está unido, forma un heterociclo fusionado que contiene nitrógeno aromático o alicíclico, sustituido o no sustituido, saturado, parcialmente saturado o insaturado que tiene 6 átomos en el anillo, con la condición de que, cuando W es un heterociclo aromático fusionado, el hidrógeno unido al nitrógeno que forma parte tanto del heterociclo como del macrociclo, y R5 y R6 unidos a los átomos de carbono que forman parte tanto del heterociclo como del macrociclo, están ausentes.
[0066] Dentro de la realización (IA), y los grupos contenidos en la misma, en un grupo de compuestos M es Mn2+, Mn3+, Mn4+, Mn6+, Mn7+, Fe2+, Fe3+, Fe4+, Fe6+.
[0067] Dentro de la realización (IA), y los grupos contenidos en la misma, en un grupo de compuestos X1 es fenilo. Dentro de la realización (IA) y los grupos contenidos en la misma, en un grupo de compuestos X1 es -C(-X2 )(-X3)(-X4) y cada X2, X3 y X4, en combinación, corresponden a cualquiera de las combinaciones identificadas en el cuadro siguiente:
[0068] Además, dentro de la realización (IA) y los grupos contenidos en la misma, en un grupo de compuestos X1 es C(-X2)(-X3 )(-X4), y X3 es -XsC(=O)R13, de tal manera que las combinaciones de X2 , X3 y X4 incluyen cualquiera de las combinaciones identificadas en el cuadro siguiente:
donde R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18.
Realización (IB)
[0069] En la realización (IB), el complejo macrocíclico pentaaza con la Fórmula (I) corresponde a la Fórmula (IB):
en donde
M es Fe2+, Fe3+, Mn2+ o Mn3+;
Ría , Rib, R2 , R3, R4A, R4B, R5, R6, R7A, R7B, R8, R9, Rioa y Riob son según se define en relación con la realización (IA) más arriba;
Wi, W 2 , y W 3 son independientemente haluro, hidrógeno, alquilo sustituido o no sustituido, alquenilo, alquinilo, arilo, aralquilo, alcarilo, acilo, aciloxi, alcoxi, un éter, un tioéter o nitro;
cada Xi es independientemente fenilo sustituido o no sustituido o -C(-X2)(-X3 )(-X4 );
cada X2 es independientemente fenilo sustituido o no sustituido, metilo, etilo o propilo;
cada X3 es independientemente hidrógeno, hidroxilo, metilo, etilo, propilo, amino, -X5 C(=O)Ri3 , donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es (=O);
cada X4 es independientemente hidrógeno o junto con X3 es (=O); y
los enlaces entre el metal de transición M y los átomos de nitrógeno del macrociclo y los enlaces entre el metal de transición M y los átomos de oxígeno de los ligandos axiales -OC(=O)Xi son enlaces covalentes de coordinación.
[0070] Dentro de la realización (IB), cuando uno o más de Wi, W2 y W 3 son alquilo, alquenilo, alquinilo, arilo, aralquilo o alcarilo sustituidos, estos sustituyentes pueden contener de 1 a 20 átomos de carbono (preferentemente de 1 a 6 átomos de carbono) y pueden ser lineales, ramificados o cíclicos, estando uno o más átomos de hidrógeno de las porciones sustituidas reemplazados con un sustituyente distinto, como, por ejemplo, -OH, -OR, -C(=O)OH,
[0071] -C(=O)NH2, -NH2 , -NHR, -NRR, -SH, -SR, -SO2R, -SO2H, -SOR, heterociclo y/o haluro (incluidos F, CI, Br y I), entre otros, en donde cada existencia de R puede ser alquilo sustituido o no sustituido, arilo sustituido o no sustituido, o aralquilo sustituido o no sustituido.
[0072] Dentro de la realización (IB) y los grupos contenidos en la misma, en un grupo de compuestos, M es Mn2+ o Mn3+. Dentro de la realización (IB) y los grupos contenidos en la misma, en otro grupo de compuestos, M es Fe2+ o Fe3+.
[0073] Dentro de la realización (IB), y los grupos contenidos en la misma, en un grupo de compuestos Xi es fenilo. Dentro de la realización (IB) y los grupos contenidos en la misma, en un grupo de compuestos Xi es -C(-X2 )(-X3 )(-X4 ) y cada X2, X3 y X4, en combinación, corresponden a cualquiera de las combinaciones identificadas en el cuadro siguiente:
[0074] Además, dentro de la realización (IB) y los grupos contenidos en la misma, en un grupo de compuestos, Xi
es C(-X2)(-X3)(-X4 ) y X3 es -XsC(O)Ri3 , de tal manera que las combinaciones de X2, X3 y X4 incluyen cualquiera de las combinaciones identificadas en el cuadro siguiente:
donde R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18.
Realización (IC)
[0075] En la realización (IC), el complejo macrocíclico pentaaza con la Fórmula (I) corresponde a las fórmulas (ICr) o (ICS)
en donde
M es Fe2+, Fe3+, Mn2+ o Mn3+;
R1A, R1B, R2, R3 , R4A, R4B, R5, R6, R7A, R7B, R8, R9, R10A y R10B son independientemente hidrógeno o alquilo sustituido o no sustituido;
W 1, W 2 y W 3 son independientemente haluro o hidrógeno;
cada X1 es independientemente fenilo sustituido o no sustituido, o -C(-X2 )(-X3)(-X4);
cada X2 es independientemente fenilo sustituido o no sustituido, metilo, etilo o propilo;
cada X3 es independientemente hidrógeno, hidroxilo, metilo, etilo, propilo, amino, -XsC(=O)R13, donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es (=O);
cada X4 es independientemente hidrógeno o junto con X3 es (=O); y
los enlaces entre el metal de transición M y los átomos de nitrógeno del macrociclo y los enlaces entre el metal de transición M y los átomos de oxígeno de los ligandos axiales -OC(O)X1 son enlaces covalentes de coordinación.
[0076] Dentro de la realización (IC), en un grupo de compuestos M es Mn2+. Dentro de la realización (IC), en otro grupo de compuestos M es Mn3+.
[0077] Dentro de la realización (IC), y los grupos contenidos en la misma, en un grupo de compuestos X1 es fenilo. Dentro de la realización (IC) y los grupos contenidos en la misma, en un grupo de compuestos X1 es -C(-X2 )(-X3)(-X4) y cada X2, X3 y X4, en combinación, corresponden a cualquiera de las combinaciones identificadas en el cuadro siguiente:
[0078] Además, dentro de la realización (IC) y los grupos contenidos en la misma, en un grupo de compuestos, Xi es C(-X2)(-X3)(-X4 ) y X3 es -XsC(O)R13, de tal manera que las combinaciones de X2, X3 y X4 incluyen cualquiera de las combinaciones identificadas en el cuadro siguiente:
donde R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18.
Realización (ID)
[0079] En la realización (ID), el complejo macrocíclico pentaaza con la Fórmula (I) corresponde a las Fórmulas (IDr) o (IDs):
en donde
M es Mn2+ o Mn3+;
R1A, R1B, R2 , R3, R4A, R4B, R5, R6, R7A, R7B, R8, R9, R10A y R10B son independientemente hidrógeno, metilo, etilo o propilo;
W 1, W 2 y W 3 son independientemente haluro o hidrógeno;
cada X1 es independientemente fenilo sustituido o no sustituido o -C(-X2)(-X3 )(-X4);
cada X2 es independientemente fenilo sustituido o no sustituido, metilo, etilo o propilo;
cada X3 es independientemente hidrógeno, hidroxilo, metilo, etilo, propilo, amino, -X5C(=O)R13, donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es (=O);
cada X4 es independientemente hidrógeno o junto con X3 es (=O); y
los enlaces entre el metal de transición M (Mn2+ o Mn3+) y los átomos de nitrógeno del macrociclo y los enlaces entre el metal de transición M y los átomos de oxígeno de los ligandos axiales -OC(=O)Xi son enlaces covalentes de coordinación.
[0080] Dentro de la realización (ID), en un grupo de compuestos M es Mn2+. Dentro de la realización (ID), en otro
grupo de compuestos M es Mn3+.
[0081] Dentro de la realización (ID) y los grupos contenidos en la misma, en un grupo de compuestos, Ría , R-m, R4a, R4b, R7a, R7b, Rioa y Riob son todos hidrógeno. Dentro de la realización (ID), y los grupos contenidos en la misma, en un grupo de compuestos Ríb, R4a, R4b, R7a, R7b, Ríoa, y Ríob son todos hidrógeno y Ría es metilo. Dentro de la realización (ID), y los grupos contenidos en la misma, en un grupo de compuestos Ría , R4A, R4b, R7a, R7b, Ríoa y Ríob son todos hidrógeno y Ríb es metilo. Dentro de la realización (ID), y los grupos contenidos en la misma, en un grupo de compuestos Ría , Ríb , R4b, R7a, Ríoa, y Ríob son todos hidrógeno y R4A y R7B son todos metilo. Dentro de la realización (ID), y los grupos contenidos en la misma, en un grupo de compuestos Ría , Ríb, R4a, R7b, Ríoa y Ríob son todos hidrógeno, y R4B y R7A son todos metilo.
[0082] Dentro de la realización (ID), y los grupos contenidos en la misma, en un grupo de compuestos Xi es fenilo. Dentro de la realización (ID) y los grupos contenidos en la misma, en un grupo de compuestos Xi es -C(-X2 )(-X3X-X4 ) y cada X2, X3 y X4 , en combinación, corresponden a cualquiera de las combinaciones identificadas en el cuadro siguiente:
[0083] Además, dentro de la realización (ID) y los grupos contenidos en la misma, en un grupo de compuestos, Xi es C(-X2)(-X3)(-X4 ) y X3 es -XsC(O)Ri3 , de tal manera que las combinaciones de X2, X3 y X4 incluyen cualquiera de las combinaciones identificadas en el cuadro siguiente:
donde R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18.
Realización (IE)
[0084] En la realización (IE), el complejo macrocíclico pentaaza con la Fórmula (I) corresponde a las Fórmulas (IErí), (IEsí), (IEr2), (IEs2), (IEr3) o (IEs3):
Mn es Mn2+ o Mn3+;
cada Xi es independientemente fenilo sustituido o no sustituido o -C(-X2)(-X3 )(-X4);
cada X2 es independientemente hidrógeno, hidroxilo, metilo, etilo, propilo, amino, -XsC(=O)R13, donde X5 es NH u O, y R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, o junto con X4 es (=O);
cada X4 es independientemente hidrógeno o junto con X3 es (=O); y
los enlaces entre el manganeso y los átomos de nitrógeno del macrociclo y los enlaces entre el manganeso y los átomos de oxígeno de los ligandos axiales -OC(=O)Xi son enlaces covalentes de coordinación.
[0085] Dentro de la realización (IE), y los grupos contenidos en la misma, en un grupo de compuestos Xi es fenilo. Dentro de la realización (IE) y los grupos contenidos en la misma, en un grupo de compuestos Xi es -C(-X2 )(-X3)(-X4) y cada X2, X3 y X4, en combinación, corresponden a cualquiera de las combinaciones identificadas en el cuadro siguiente:
[0086] Además, dentro de la realización (IE) y los grupos contenidos en la misma, en un grupo de compuestos, Xi es C(-X2)(-X3)(-X4 ) y X3 es -X5C(O)Ri3 , de tal manera que las combinaciones de X2, X3 y X4 incluyen cualquiera de las
combinaciones identificadas en el cuadro siguiente:
donde R13 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18, u -OR14, donde R14 es alquilo de C1-C18, arilo sustituido o no sustituido, o aralquilo de C1-C18.
Formulaciones de dosis unitarias y composiciones farmacéuticas
[0087] Como se ha indicado anteriormente, un segundo aspecto de la presente descripción se refiere a las formulaciones de dosis unitarias y a composiciones farmacéuticas que comprenden los compuestos descritos en la presente memoria, comúnmente junto con un vehículo o excipiente aceptables desde el punto de vista farmacéutico, y opcionalmente en combinación con otro compuesto o compuestos con actividad farmacológica. Las composiciones farmacéuticas incluyen el complejo macrocíclico pentaaza que corresponde a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos que se exponen en el Cuadro I del apartado de ejemplos), comúnmente formulado como forma farmacéutica, opcionalmente en combinación con un vehículo, aditivo o excipiente aceptables desde el punto de vista farmacéutico. En una realización, por ejemplo, la composición farmacéutica comprende el compuesto con la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos que se exponen en el Cuadro I del apartado de ejemplos) y un vehículo o excipiente aceptables desde el punto de vista farmacéutico. Se pueden usar formulaciones de dosis unitaria y composiciones farmacéuticas según la presente descripción, por ejemplo, en el tratamiento de varios trastornos cardiovasculares, trastornos cerebrovasculares, trastornos dermatológicos, trastornos fibróticos, trastornos gastrointestinales, trastornos inmunitarios, trastornos inflamatorios, trastornos metabólicos, trastornos neurológicos, trastornos oftálmicos, trastornos pulmonares, enfermedades infecciosas, daño tisular y combinaciones de los mismos. Entre las enfermedades y afecciones concretas se incluyen la fibrosis, las enfermedades y afecciones inflamatorias (incluidas, por ejemplo, la enfermedad inflamatoria intestinal, la artritis reumatoide, el asma, la EPOC, la pancreatitis y similares), la dermatitis, la psoriasis y similares, así como para proteger el tejido frente al daño producido por un tratamiento anticancerígeno u otra exposición a radiación, tal y como se explica en más detalle más abajo.
[0088] Las formulaciones que contienen los compuestos pueden ser sólidas, semisólidas, polvos liofilizados o formas farmacéuticas líquidas como, por ejemplo, aerosoles, cápsulas, cremas, emulsiones, espumas, geles/gelatinas, inyectables, lociones, ungüentos, pastas, polvos, jabones, soluciones, esprais, supositorios, suspensiones, formulaciones de liberación mantenida, comprimidos, tinturas, parches transdérmicos y similares, preferentemente en formas farmacéuticas unitarias adecuadas para la administración sencilla de tomas precisas. Si se formulan como dosis fijas, en dichas composiciones farmacéuticas o productos formulados preferentemente se usan los compuestos en determinados intervalos de dosis. Por lo tanto, dependiendo del modo de administración previsto, en algunas realizaciones las composiciones pueden estar en forma sólida, semisólida o líquida, como, por ejemplo, inyectables, comprimidos, píldoras, cápsulas de liberación temporizada, elixires, tinturas, emulsiones, jarabes, líquidos, suspensiones o similares, algunas veces en tomas unitarias y conforme a las prácticas farmacéuticas convencionales. De manera similar, en algunas realizaciones, también se pueden administrar por vía intravenosa (tanto en bolo como en infusión), intraperitoneal, subcutánea, tópica o intramuscular, o por otras vías descritas en la presente memoria, todas con formas conocidas para los expertos en ciencias farmacéuticas.
[0089] Una realización particular de la presente descripción está destinada a una formulación de dosis unitarias que comprende el compuesto que corresponde a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos que se exponen en el Cuadro I del apartado de ejemplos) en una forma farmacéutica por vía oral según se describe en la presente memoria. Otra realización concreta de la presente descripción está destinada a una formulación de dosis unitarias que comprende el compuesto que corresponde a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos que se exponen en el Cuadro I del apartado de ejemplos) en una forma farmacéutica por vía parenteral según se describe en la presente memoria.
[0090] Para las formas farmacéuticas de administración por vía oral y no oral, los compuestos descritos más arriba (o cualquiera de las realizaciones de los mismos u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos que se exponen en el Cuadro I del apartado de ejemplos) se pueden dispersar en un vehículo aceptable desde el punto de vista farmacéutico antes de la administración al mamífero. El vehículo, que en la técnica también se conoce como excipiente, auxiliar, adyuvante o diluyente, es cualquier sustancia inerte desde el punto de vista farmacéutico que confiere una consistencia o forma adecuada a la composición, y que no reduce la eficacia del compuesto. El vehículo por lo general se considera «aceptable desde el punto de vista farmacéutico o farmacológico» si cuando se administra a un mamífero, especialmente un humano, no produce reacciones adversas
o alérgicas inaceptables, ni ninguna otra reacción no deseada.
[0091] La selección de un vehículo aceptable desde el punto de vista farmacéutico también dependerá, en parte, de la vía de administración. En general, las composiciones de los descritos en la presente memoria se pueden formular para cualquier vía de administración siempre y cuando se pueda acceder al aparato circulatorio por esa vía y conforme a las vías de administración convencionales del componente (por ejemplo, el compuesto). Por ejemplo, entre las vías de administración adecuadas se incluyen, entre otras, oral, parenteral (por ejemplo, administración intravenosa, intraarterial, subcutánea, intramuscular, intraorbital, intracapsular, intravertebral, intraperitoneal o intraesternal), tópica (nasal, transdérmica, bucal, oftálmica), intravesical, intratecal, entérica, pulmonar, intralinfática, intracavitaria, vaginal, rectal, transuretral, intradérmica, intraocular, auricular, intramamaria, ortotópica, intratraqueal, intralesional, percutánea, endoscópica, transmucosal, sublingual e intestinal. En una realización particularmente preferida, el compuesto (o una composición farmacéutica o formulación de dosis unitarias que incluye el compuesto) (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se formula para administración por vía oral.
[0092] Los expertos en la técnica conocen bien los vehículos aceptables desde el punto de vista farmacéuticos para su uso en combinación con los compuestos y las composiciones de la presente descripción y se seleccionan basándose en varios factores: el compuesto o los compuestos y el agente o los agentes concretos utilizados, y su concentración, estabilidad y biodisponibilidad prevista; la seguridad; el sujeto, su edad, tamaño y estado general; y la vía de administración.
[0093] Entre los componentes adecuados (por ejemplo, vehículos y/o excipientes) que se usan para formular formas farmacéuticas sólidas o semisólidas, como comprimidos, cápsulas de gelatina o geles/suspensiones se pueden incluir, por ejemplo, diluyentes (como agua, glicéridos o mezclas de los mismos, aceite de maíz, aceite de oliva, aceite de girasol, aceite de cártamo, lactosa, dextrosa, sucrosa, manitol, sorbitol, celulosa, sodio, sacarina, glucosa y/o glicina); lubricantes (como sílice, talco, su sal de magnesio o calcio, oleato de sodio, estearato de sodio, estearato de magnesio, benzoato de sodio, acetato de sodio, cloruro de sodio y/o polietilenglicol); aglutinantes (como silicato de magnesio y aluminio, pasta de almidón, gelatina, tragacanto, metilcelulosa, carboximetilcelulosa de sodio, carbonato de magnesio, glúcidos naturales como la glucosa o la p-lactosa, edulcorantes de maíz, gomas naturales y sintéticas, como la acacia, el tragacanto o el alginato de sodio, ceras y/o polivinilpirrolidona); disgregantes (como almidones, agar, metilcelulosa, bentonita, goma de xantano o mezclas efervescentes; absorbentes, colorantes, saborizantes y/o edulcorantes; y combinaciones de los mismos. Los métodos para preparar dichas formas farmacéuticas sólidas y semisólidas usando los principios activos farmacéuticos y otros componentes son bien conocidos en la técnica. Por ejemplo, las composiciones en forma líquida, semisólida o en pasta se pueden introducir en cápsulas de gelatina dura o de gelatina blanda mediante máquinas de llenado adecuadas. Como otra posibilidad, la composición también puede ser extruida, pulverizada, granulada o depositada en capa sobre un sustrato para transformarse en un polvo, gránulo o microesfera que además se puede encapsular o comprimir con o sin la adición de aglutinantes o solidificantes adecuados. Este enfoque también permite la creación de una «mezcla fundida», una «solución sólida» o una «mezcla eutéctica». Estos y otros métodos para fabricar formulaciones para administración por vía oral se pueden encontrar, por ejemplo, en «Remington: The Science and Practice of Pharmacy», 20.a edición. A.R. Gennaro, 2000, Lippincott Williams & Wilkins.
[0094] Algunos componentes adecuados (por ejemplo, vehículos y/o excipientes) usados en la formulación de formas farmacéuticas líquidas, por ejemplo, incluyen disolventes polares no acuosos aceptables desde el punto de vista farmacéutico, como aceites, alcoholes, amidas, ésteres, éteres, cetonas, hidrocarburos y mezclas de los mismos, así como agua, soluciones salinas (por ejemplo, soluciones de la USP y de cloruro de sodio isotónica), soluciones de dextrosa (por ejemplo, D5W), soluciones de electrolitos o cualquier otro líquido acuoso aceptable desde el punto de vista farmacéutico. En determinadas realizaciones preferidas, la composición farmacéutica está en forma de solución acuosa que comprende el compuesto que corresponde a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) y suero salino (por ejemplo, suero salino normal, que es una solución acuosa estéril de NaCl al 0.9% en p/v). En estas y otras realizaciones, por ejemplo, el suero salino es preferentemente suero salino fisiológico amortiguado (es decir, suero salino amortiguado). El agente amortiguador puede proporcionar una capacidad de amortiguación adecuada a un pH de aproximadamente 7-8,5, o a un pH de aproximadamente 7,8, o en el intervalo de pH de 7,3-8. El agente amortiguador es preferentemente inerte desde el punto de vista químico y aceptable desde el punto de vista fisiológico y farmacéutico. Entre los ejemplos de agentes amortiguadores se incluyen los agentes amortiguadores de fosfato, los agentes amortiguadores de carbonato, los agentes amortiguadores de tris, los agentes amortiguadores de aminoácidos (por ejemplo, arginina, lisina y otros aminoácidos naturales) y los agentes amortiguadores de citrato. Los agentes amortiguadores de carbonato (como el carbonato de sodio o calcio, o los agentes amortiguadores de bicarbonato) pueden ser particularmente útiles en algunas realizaciones debido a que son fácilmente obtenibles, y a su fuerte capacidad de amortiguación y compatibilidad. Un agente amortiguador particularmente preferido es el bicarbonato de sodio. En una realización preferida, por ejemplo, el vehículo aceptable desde el punto de vista farmacéutico comprende suero salino amortiguado; más preferentemente, en esta realización, el suero salino amortiguado es suero salino amortiguado con bicarbonato.
[0095] En una realización particular, la formulación de dosis unitarias para administración por vía oral que incluye el compuesto (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) además comprende al menos uno de un tensioactivo lipofílico y un aceite.
[0096] Entre determinados tensioactivos lipofílicos adecuados y/o aceites se incluyen los mono-, di- y/o triglicéridos de ácidos grasos, como Imwitor 988 (mono-/dicaprilato de glicerilo), Imwitor 742 (mono-di-caprilato/caprato de glicerilo), Imwitor 308 (monocaprilato de glicerilo), Imwitor 191 (monoestearato de glicerilo), Softigen 701 (mono-/diricinoleato de glicerilo), Capmul MCM (caprilato/caprato de glicerilo), Capmul MCM(L) (forma líquida de Capmul MCM), Capmul GMO (monooleato de glicerilo), Capmul GDL (dilaurato de glicerilo), Maisine (monolinoleato de glicerilo), Peceol (monooleato de glicerilo), Myverol 18-92 (monoglicéridos destilados del aceite de girasol) y Myverol 18-06 (monoglicéridos destilados del aceite de soja hidrogenado), Precirol ATO 5 (palmitoestearato de glicerilo), Gelucire 39/01 (glicéridos semisintéticos, es decir, mono-, di- y tri-glicéridos de C12-18) y Miglyol 812 N (mezcla de triglicéridos del ácido caprílico/cáprico); ésteres del ácido acético, succínico, láctico, cítrico y/o tartárico y mono- y/o di-glicéridos de ácidos grasos, por ejemplo, Myvacet 9-45 (monoglicéridos acetilados destilados), Miglyol 829 (caprilato/caprato de diglicerilsuccinato), Myverol SMG (monoglicéridos mono/di-succinilados), Imwitor 370 (citrato de estearato de glicerilo), Imwitor 375 (lactato/citrato/monoestearato de glicerilo) y Crodatem T22 (ésteres del ácido diacetiltartárico y monoglicéridos); mono- y/o di-ésteres de ácidos grasos y propilenglicol, por ejemplo, Lauroglycol (monolaurato de propilenglicol), Mirpyl (monomiristato de propilenglicol), Captex 200 (dicaprilato/dicaprato de propilenglicol), Miglyol 840 (dicaprilato/dicaprato de propilenglicol) y Neobee M-20 (dicaprilato/dicaprato de propilenglicol); ésteres de ácidos grasos y poliglicerol, como Plurol oleico (oleato de poliglicerilo), Caprol eT (mezcla de ésteres de ácidos grasos y poliglicerilo) y Drewpol 10.10.10 (oleato de poliglicerilo); etoxilados del aceite de ricino con un contenido bajo en etoxilados (HLB<10) como Etocas 5 (5 moles de óxido de etileno reaccionados con 1 mol de aceite de ricino) y Sandoxylate 5 (5 moles de óxido de etileno reaccionados con 1 mol de aceite de ricino; etoxilados de ácidos y ésteres formados mediante reacción del óxido de etileno con ácidos grasos o ésteres de ácidos grasos y glicerol (HLB<10) como Crodet 04 (ácido láurico polioxietilenado (4)), Cithrol 2MS (ácido esteárico polioxietilenado (2)), Marlosol 183 (ácido esteárico polioxietilenado (3)) y Marlowet G 12DO (dioleato de glicerilo polioxietilenado (12 OE)); ésteres de sorbitano y ácidos grasos, por ejemplo, Span 20 (monolaurato de sorbitano), Crill 1 (monolaurato de sorbitano) y Crill 4 (monooleato de sorbitano); productos de transesterificación de un triglicérido de aceites vegetales hidrogenados o naturales y un poliol polialquilénico (HLB<10), por ejemplo, Labrafil M1944CS (aceite de almendra de albaricoque polioxietilado), Labrafil M2125CS (aceite de maíz polioxietilado) y Gelucire 37/06 (coco hidrogenado polioxietilado); etoxilados de alcohol (HLB<10), por ejemplo, Volpo N3 (oleil éter polioxietilado (3)), Brij 93 (oleil éter polioxietilado (2)), Marlowet LA4 (lauril éter polioxietilado (4)); y Pluronics, por ejemplo, copolímeros de polioxietileno-polioxipropileno y copolímeros en bloque (HLB<10), por ejemplo, Synperonic p E L42 (HLB=8) y Synperonic PE L61 (Hl B=3).
[0097] En otra realización particular, la formulación de dosis unitarias para administración por vía oral que incluye el compuesto (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) además comprende un aceite digerible (es decir, un aceite que puede sufrir una desesterificación o hidrólisis en presencia de lipasa pancreática in vivo en condiciones fisiológicas normales). Los aceites digeribles pueden ser triésteres de glicerol y ácidos grasos de cadena media (C7-C13) o de cadena larga (C14-C22) con alcoholes mono-, di- o polihídricos de bajo peso molecular (hasta Ce). Entre los ejemplos adecuados de aceites digeribles se incluyen, por ejemplo, los aceites vegetales (por ejemplo, aceite de soja, aceite de semillas de cártamo, aceite de maíz, aceite de oliva, aceite de ricino, aceite de semillas de algodón, aceite de cacahuete, aceite de semillas de girasol, aceite de coco, aceite de palma, aceite de colza, aceite de grosella, aceite de onagra, aceite de semillas de uva, aceite de germen de trigo, aceite de sésamo, aceite de aguacate, aceites de almendra, borraja, menta y almendra de albaricoque) y aceites animales (por ejemplo, aceite de hígado de pescado, aceite de tiburón y aceite de visón). En determinadas realizaciones, el aceite digerible es un aceite vegetal, por ejemplo, aceite de soja, aceite de semillas de cártamo, aceite de maíz, aceite de oliva, aceite de ricino, aceite de semillas de algodón, aceite de cacahuete, aceite de semillas de girasol, aceite de coco, aceite de palma, aceite de colza, aceite de onagra, aceite de semillas de uva, aceite de germen de trigo, aceite de sésamo, aceite de aguacate, aceite de almendras, aceite de borraja, aceite de menta, aceite de almendras de albaricoque y combinaciones de los mismos.
[0098] Cuando se usan formulaciones farmacéuticas inyectables, estas son preferentemente estériles. Las formulaciones inyectables se pueden esterilizar, por ejemplo, mediante filtración a través de un filtro que retiene las bacterias o mediante la incorporación de agentes esterilizantes en forma de composiciones sólidas estériles que se pueden disolver o dispersar en agua esterilizada u otro medio estéril inyectable justo antes de usar. Las composiciones se pueden proporcionar, preparar, conservar o transportar en cualquier recipiente adecuado para mantener la esterilidad. El recipiente puede incorporar medios para dispensar una composición acuosa como, por ejemplo, un sello perforable o retirable. Las composiciones se pueden dispensar, por ejemplo, mediante extracción con una jeringa o vertiendo la composición directamente en un dispositivo (por ejemplo, una jeringa, bolsa intravenosa (IV) o máquina) para su administración a un paciente. Los expertos en la técnica conocen otros medios para proporcionar, preparar, conservar, transportar y dispensar composiciones farmacéuticas estériles.
[0099] Otros vehículos y excipientes aceptables desde el punto de vista farmacéuticos para su uso en las composiciones farmacéuticas y formas farmacéuticas descritas en la presente memoria son bien conocidos por los
expertos en la técnica, y se identifican en The Chemotherapy Source Book (Williams & Wilkens Publishing), The Handbook of Pharmaceutical Excipients, (American Pharmaceutical Association, Washington, D.C., and The Pharmaceutical Society of Great Britain, London, England, 1968), Modern Pharmaceutics, (G. Banker et al., eds., 3d ed.) (Marcel Dekker, Inc., New York, New York, 1995), The Pharmacological Basis of Therapeutics, (Goodman & Gilman, McGraw Hill Publishing), Pharmaceutical Dosage Forms, (H. Lieberman et al., eds.) (Marcel Dekker, Inc., New York, New York, 1980), Remington’s Pharmaceutical Sciences (A. Gennaro, ed., 19th ed.) (Mack Publishing, Easton, PA, 1995), The United States Pharmacopeia 24, The National Formulary 19, (National Publishing, Philadelphia, PA, 2000), y A.J. Spiegel et al., Use of Nonaqueous Solvents in Parenteral Products, Journal of Pharmaceutical Sciences, Vol. 52, N.° 10, págs. 917-927 (1963).
[0100] En determinadas realizaciones, la composición farmacéutica administrada al sujeto según los métodos descritos en la presente memoria consiste esencialmente en el compuesto que corresponde a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos que se exponen en el Cuadro I del apartado de ejemplos) y un vehículo aceptable desde el punto de vista farmacéutico. En otras realizaciones, la composición farmacéutica comprende el compuesto, un vehículo aceptable desde el punto de vista farmacéutico, y uno o más compuestos o agentes adicionales con actividad farmacológica. En estas realizaciones, las composiciones farmacéuticas descritas en la presente memoria son productos que se forman al mezclar o combinar más de un principio activo, e incluyen tanto combinaciones fijas como combinaciones no fijas de los principios activos. Las combinaciones fijas son aquellas en las que los principios activos, por ejemplo, el compuesto y otro agente o compuesto con actividad farmacológica descritos en la presente memoria, se administran ambos a un paciente simultáneamente en forma de una sola entidad o toma. Las combinaciones no fijas son aquellas en las que los principios activos, por ejemplo, el compuesto y otro agente o compuesto con actividad farmacológica se administran a un sujeto como entidades separadas, ya sea simultáneamente, concurrentemente o secuencialmente sin límites específicos de tiempos entre administraciones, en donde dicha administración proporciona concentraciones eficaces de los dos compuestos en el cuerpo del paciente. Esto último también se aplica a la politerapia, por ejemplo, la administración de tres o más principios activos.
[0101] Se prevé que en las coformulaciones del compuesto (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos que se exponen en el Cuadro I del apartado de ejemplos) y uno o más agentes o compuestos adicionales con actividad farmacológica se pueden emplear técnicas de formulación convencionales para estos componentes individualmente, o vías de formulación alternativas, dependiendo de la compatibilidad y la eficacia de los diversos componentes, en combinación.
[0102] En una realización, un compuesto y/o formulación de la presente descripción (incluidos cualquiera de los compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se formulan para administración por vía oral y la formulación comprende una composición o capa de liberación entérica. Por ejemplo, la forma farmacéutica oral puede ser un comprimido recubierto entérico, una cápsula o comprimido con partículas múltiples o capas múltiples; una gelatina, una gelatina blanda o un equivalente de las mismas; un vinilo o un ftalato de acetato de polivinilo o equivalente de los mismos; un ACRYL-EZE™, SURETERIC™ NUTRATERIC II®, PHTHALAVIN® (Colorcon, Inc. Harleysville, Pensilvania, EE. UU.); una hidroxipropilmetilcelulosa (HPMC), una HPMC de viscosidad elevada, una HPMC de viscosidad ultraelevada; una polivinilpirrolidona (PVP) o una PVP-K90; una celulosa, una celulosa microcristalina (MCC), una metilcelulosa, una hidroximetilcelulosa, una hidroxipropilmetilcelulosa (HPMC), o una etilcelulosa; un copolímero de acrilato de etilo, un poli(met)acrilato, por ejemplo, un copolímero B del ácido metacrílico, un metilmetacrilato y/o un éster del ácido metacrílico con grupos amonio cuaternarios; EUDRAGIT® RLPO™; EUDRAGIT® RL 100™ (Evonik Industries AG, Essen, Alemania).
[0103] En una realización alternativa, un compuesto y/o formulación de la presente descripción (incluidos cualquiera de los compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se formulan para administración por vía oral y la formulación comprende un recubrimiento o, si no, comprende ftalato de acetato de celulosa, ftalato de hidroxipropilmetilcelulosa, ftalato de acetato de polivinilo, succinato de acetato de hidroxipropilmetilcelulosa, trimelitato de acetato de celulosa, succinato de hidroxipropilmetilcelulosa, succinato de acetato de celulosa, hexahidroftalato de acetato de celulosa, ftalato de propionato de celulosa, maleato de acetato de celulosa, butirato de acetato de celulosa, propionato de acetato de celulosa, copolímero de ácido metacrílico y metilmetacrilato, copolímero de metilacrilato, metilmetacrilato y ácido metacrílico, copolímero de metilvinil éter y anhídrido maleico, copolímero de etil metilacrilato-metilmetacrilatoetilacrilato de clorotrimetilamonio, resinas naturales, ceína, goma laca, coloforia, copal o un copolímero acrílico, o cualquier combinación o mezcla de los mismos.
[0104] En realizaciones alternativas, un compuesto y/o formulación de la presente descripción (incluidos cualquiera de los compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se formulan para administración por vía oral y comprende un recubrimiento de liberación mantenida, y opcionalmente el recubrimiento de liberación mantenida comprende una cera mezclada con un monoestearato de glicerilo, un ácido esteárico, un ácido palmítico, un monopalmitato de glicerilo, un alcohol cetílico, una goma laca, una ceína, una etilcelulosa, una resina acrílica, un acetato de celulosa o un elastómero
de silicona, o cualquier combinación o mezcla de los mismos.
MÉTODOS E INDICACIONES
[0105] Como se ha indicado anteriormente, en un tercer aspecto los compuestos descritos en relación con la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se pueden usar para tratar el daño tisular y/o una variedad de enfermedades y afecciones. El tratamiento de enfermedades y afecciones (con inclusión del tejido dañado), según se describe en la presente memoria, por lo general puede suponer no solo la inhibición de la enfermedad en un paciente que está experimentando o presentando las características anatomopatológicas o la sintomatología de la enfermedad o afección (es decir, detener el desarrollo adicional de las características anatomopatológicas y/o la sintomatología), sino también mejorar la enfermedad o afección en un paciente que está experimentando o presentando las características anatomopatológicas o la sintomatología de la enfermedad o afección (es decir, revertir las características anatomopatológicas y/o la sintomatología). El tratamiento en un paciente humano de una enfermedad o afección según se describe en la presente memoria, por ejemplo, daño tisular producido por la administración de radioterapia o quimioterapia, o exposición a radiación, también equivale a la inhibición o profilaxis de dicho daño en un paciente que no está necesariamente experimentando o presentando las características anatomopatológicas o la sintomatología de la enfermedad o afección.
[0106] Los métodos de la presente descripción se pueden usar de manera ventajosa para tratar (por ejemplo, inhibir, aliviar o mitigar) una diversidad de enfermedades o afecciones en una diversidad de sujetos (es decir, pacientes). El sujeto puede ser, por ejemplo, un mamífero bovino, aviar, canino, equino, felino, ovino, porcino o un primate (incluidos primates humanos y no humanos). Un sujeto también puede incluir mamíferos de importancia debido a estar en peligro de extinción, o por tener una importancia económica, como animales que se crían en granjas para consumo por seres humanos o animales de importancia social para los seres humanos, como animales que se tienen como animales de compañía o en zoos. Entre los ejemplos de dichos animales se incluyen, entre otros: gatos, perros, cerdos, rumiantes o ungulados, como ganado vacuno, bueyes, ovejas, jirafas, ciervos, cabras, bisones, camellos o caballos. En una realización, el sujeto es bovino, aviar, canino, equino, felino, ovino, porcino o primate no humano. En una realización preferida, el sujeto es un paciente humano.
TRATAMIENTO DEL DAÑO TISULAR
[0107] Según una realización del tercer aspecto de la presente descripción, se describen métodos en la presente memoria para tratar el daño tisular producido por un tratamiento anticancerígeno (por ejemplo, radioterapia o quimioterapia) administrada a un sujeto que lo necesite. Según otra realización, en la presente memoria se describen métodos para tratar en un paciente humano el daño tisular producido por exposición a radiación. De esta manera, en diversas realizaciones, por ejemplo, la exposición a radiación en varias realizaciones puede ser una exposición accidental a radiación, una exposición involuntaria a radiación o una exposición voluntaria a radiación. Como se ha indicado anteriormente, el tratamiento del daño tisular según se describe en la presente memoria puede incluir tanto la inhibición (es decir, la profilaxis) como la mejora de cualquier daño tisular que pueda producirse por un incidente o actividad. En general, los métodos suponen administrar al sujeto una cantidad eficaz, desde el punto de vista terapéutico, de un compuesto descrito en la presente memoria (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos).
[0108] El tratamiento del daño tisular producido por un tratamiento anticancerígeno u otra exposición a radiación, según los métodos descritos en la presente memoria, supone la administración de una cantidad eficaz desde el punto de vista terapéutico del compuesto descrito en la presente memoria (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos). En general, se puede usar un intervalo de cantidades eficaces desde el punto de vista terapéutico, dependiendo, por ejemplo, del compuesto seleccionado y su seguridad y eficacia, el tipo, la ubicación y la gravedad del daño tisular, entre otros factores.
[0109] En general, los aspectos temporales de la administración del compuesto (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) pueden depender, por ejemplo, del compuesto concreto, la radioterapia o quimioterapia que se seleccione, o el tipo, carácter y/o duración de la exposición a la radiación. Otras consideraciones pueden incluir la enfermedad o trastorno que se está tratando y la gravedad de la enfermedad o trastorno; la actividad del compuesto específico empleado; la composición específica empleada; la edad, el peso corporal, el estado de salud general, el sexo y la dieta del sujeto; el tiempo de administración, la vía de administración y la velocidad de excreción del compuesto específico empleado; la duración del tratamiento; los fármacos utilizados en combinación o al mismo tiempo que el compuesto específico empleado; y factores similares. Por ejemplo, el compuesto se puede administrar en varias realizaciones antes, durante y/o después de la administración del tratamiento anticancerígeno (por ejemplo, radioterapia o quimioterapia). A título de otro ejemplo, los compuestos se pueden administrar en diversas realizaciones antes, durante y/o tras una
exposición a radiación.
[0110] Si se desea, la dosis eficaz se puede dividir en múltiples dosis para fines de administración; en consecuencia, las composiciones de una sola dosis pueden contener dichas cantidades o submúltiplos de las mismas para constituir la dosis.
[0111] En una realización, por ejemplo, el compuesto (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se administra al paciente antes del tratamiento anticancerígeno o al mismo tiempo. En otra realización, por ejemplo, el compuesto (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se administra al paciente antes, pero no después, del tratamiento anticancerígeno. En otra realización adicional, el compuesto se administra al paciente al menos 15 minutos, 30 minutos, 45 minutos, 60 minutos, 90 minutos, 180 minutos, 0,5 días, 1 día, 3 días, 5 días, una semana, dos semanas, tres semanas, cuatro semanas, cinco semanas, seis semanas, siete semanas, ocho semanas, nueve semanas, diez semanas, once semanas, doce semanas, o durante más tiempo, antes del tratamiento anticancerígeno. En otras realizaciones adicionales, por ejemplo, el compuesto (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se administra al paciente tras el tratamiento anticancerígeno; Por lo tanto, por ejemplo, el compuesto se puede administrar hasta 15 minutos, 30 minutos, 45 minutos, 60 minutos, 90 minutos, o 180 minutos, 0,5 días, 1 día, 3 días, 5 días, una semana, dos semanas, tres semanas, cuatro semanas, cinco semanas, seis semanas, siete semanas, ocho semanas, nueve semanas, diez semanas, once semanas, doce semanas, o durante más tiempo, tras el tratamiento anticancerígeno.
[0112] En otra realización, por ejemplo, el compuesto (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se administra al paciente antes de la exposición a la radiación o al mismo tiempo. En otra realización, por ejemplo, el compuesto (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se administra al paciente antes, pero no después, de la exposición a la radiación. En otra realización adicional, el compuesto (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se administra al paciente al menos 15 minutos, 30 minutos, 45 minutos, 60 minutos, 90 minutos, 180 minutos, 0,5 días, 1 día, 3 días, 5 días, una semana, dos semanas, tres semanas, cuatro semanas, cinco semanas, seis semanas, siete semanas, ocho semanas, nueve semanas, diez semanas, once semanas, doce semanas, o durante más tiempo, antes de la exposición a la radiación. En otras realizaciones adicionales, por ejemplo, el compuesto (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se administra al paciente tras la exposición a radiación; así, por ejemplo, el compuesto se puede administrar hasta 15 minutos, 30 minutos, 45 minutos, 60 minutos, 90 minutos, o 180 minutos, 0,5 días, 1 día, 3 días, 5 días, una semana, dos semanas, tres semanas, cuatro semanas, cinco semanas, seis semanas, siete semanas, ocho semanas, nueve semanas, diez semanas, once semanas, doce semanas, o durante más tiempo, tras la exposición a radiación.
[0113] En una realización, por ejemplo, el tratamiento anticancerígeno comprende la administración de radioterapia; por ejemplo, una exposición voluntaria a radiación. Según esta realización, el método proporciona un método inocuo y eficaz para tratar el daño producido por radiación e inhibir o mejorar cánceres relacionados con radiación o daño tisular relacionado con radiación en un paciente que lo necesite mediante la administración al paciente de una cantidad eficaz desde el punto de vista terapéutico de los compuesto descritos en la presente memoria (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos).
[0114] En otra realización, la exposición a radiación es una exposición accidental o involuntaria. Por ejemplo, la exposición a radiación puede producirse por una amplia diversidad de actividades comerciales y no comerciales, incluidas, entre otras, actividades en industrias como las de servicios públicos y energía, petroquímica del petróleo/gas, química/plásticos, control automático de la ventilación (cocinar, fumar, etc.), fabricación en la industria pesada, toxicología y saneamiento medioambiental, biomedicina, cosmética/perfumes, farmacéutica, transporte, respuesta a emergencias y cumplimiento de la ley, actividades militares o terroristas, y detección (por ejemplo, fugas o derrames peligrosos). En una realización, por ejemplo, la exposición a radiación puede producirse por la excavación y/o la limpieza de material radioactivo del aire, aguas subterráneas, aguas superficiales, sedimentos y/o suelo.
[0115] En diversas realizaciones, la fuente de radiación puede ser electromagnética, incluida luz visible o ultravioleta, o nuclear, incluida radiación a, p, y o cósmica. Entre los tipos de daño se pueden incluir, entre otros,
diversas formas de daño dermatológico o mucoso, como mucositis oral, esofagitis y similares, así como pérdida celular interna, fibrosis, formación de quistes, neuropatías y diversos tipos de tumores benignos y malignos.
Tratamiento de enfermedades y afecciones
[0116] Según otra realización del tercer aspecto de la presente descripción, en la presente memoria se describen métodos para tratar una variedad de enfermedades y afecciones moduladas por la superóxido en un sujeto que lo necesite. Como se ha indicado anteriormente, el tratamiento de enfermedades y afecciones como las descritas en la presente memoria pueden incluir tanto la inhibición (es decir, profilaxis) como la mejora de dicha enfermedad o afección. En general, los métodos suponen administrar al sujeto una cantidad eficaz desde el punto de vista terapéutico de un compuesto descrito en la presente memoria (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos).
[0117] En general, los aspectos temporales de la administración del compuesto pueden depender, por ejemplo, del compuesto concreto, o de la enfermedad o afección que se esté tratando. Otras consideraciones pueden incluir la gravedad de la enfermedad o afección; la actividad del compuesto específico empleado; la composición específica empleada; la edad, el peso corporal, el estado de salud general, el sexo y la dieta del sujeto; el tiempo de administración, la vía de administración y la velocidad de excreción del compuesto específico empleado; la duración del tratamiento; los fármacos utilizados en combinación o al mismo tiempo que el compuesto específico empleado; y factores similares.
[0118] Si se desea, la dosis eficaz se puede dividir en múltiples dosis para fines de administración; en consecuencia, las composiciones de una sola dosis pueden contener dichas cantidades o submúltiplos de las mismas para constituir la dosis.
VÍAS DE ADMINISTRACIÓN
[0119] En general, los compuestos descritos en la presente memoria (o composiciones farmacéuticas que incluyen los compuestos) (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) se pueden administrar a sujetos (por ejemplo, humanos y otros mamíferos) y están adaptados para su administración por vía oral; sorprendentemente, los compuestos de la presente descripción son significativamente más biodisponibles cuando se administran por vía oral que otros análogos, por ejemplo, los análogos de b/s-cloro. Por lo tanto, de manera ventajosa, los compuestos de la presente descripción proporcionan un abanico más amplio de vías de administración, entre otras, administración por vía oral, parenteral (por ejemplo, intravenosa, intraarterial, subcutánea, rectal, subcutánea, intramuscular, intraorbitaria, intracapsular, intravertebral, intraperitoneal o intraesternal), tópica (nasal, transdérmica, intraocular), intravesical, intratecal, entérica, pulmonar, intralinfática, intracavitaria, vaginal, transuretral, intradérmica, auricular, intramamaria, bucal, ortotópica, intratraqueal, intralesional, percutánea, endoscópica, transmucosal, sublingual e intestinal. En una realización, el compuesto se introduce al paciente mediante administración por vía oral. En otra realización, el compuesto se introduce al paciente mediante inyección, inclusive mediante inyección intravenosa, subcutánea, intramuscular, intraperitoneal, intraarterial e intradérmica. De manera adicional o alternativa, los compuestos descritos en la presente memoria (o composiciones farmacéuticas que incluyen los compuestos) descritos en la presente memoria se pueden administrar a sujetos por vía tópica (como mediante parches (por ejemplo, parches transdérmicos), polvos, lociones, ungüentos o gotas aplicadas a la piel), por vía bucal o por inhalación, en forma de esprai nasal u oral. Los compuestos descritos en la presente memoria (o composiciones farmacéuticas que incluyen los compuestos) también se pueden administrar a humanos y otros mamíferos por vía intrarrectal o intravaginal. En una realización, el compuesto (o una composición farmacéutica o formulación de dosis unitarias que incluye el compuesto) se administra al sujeto por vía oral. En otra realización, el compuesto (o una composición farmacéutica o formulación de dosis unitarias que incluye el compuesto) se administra al sujeto por vía parenteral. Por lo general, se entenderá que la administración por vía parenteral hace referencia a modos de administración que incluyen la administración por vía intravenosa, intramuscular, intraperitoneal, subcutánea e intraarticular.
[0120] En algunas realizaciones, la administración por vía oral es un método preferido de administración de los presentes compuestos (por ejemplo, los correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos)).
AGENTES ADICIONALES CON ACTIVIDAD FARMACOLÓGICA
[0121] Como se ha indicado anteriormente, los métodos y composiciones farmacéuticas descritos más arriba que incluyen el compuesto pueden además incluir la administración de uno o más componentes o agentes con actividad farmacológica. Aunque los compuestos descritos en la presente memoria se pueden administrar como el único agente farmacéutico activo, también se pueden usar en combinación con uno o más compuestos de la invención u otros agentes. Cuando se administran en una combinación, los agentes terapéuticos se pueden formular como
composiciones independientes que se administran al mismo tiempo o secuencialmente en distintos tiempos (por ejemplo, una o varias horas o días más tarde), o los agentes terapéuticos se pueden administrar en una composición única. Por lo tanto, se pretende que la descripción abarque la administración de cada agente de una manera secuencial en un régimen que proporcionará efectos beneficiosos de la combinación de fármacos. Asimismo, también se pretende que la descripción abarque la coadministración de estos agentes de una manera sustancialmente simultánea, como en una sola cápsula que tiene una relación fija de estos agentes activos o en cápsulas múltiples e independientes para cada agente.
Kits/artículos de fabricación
[0122] Para su uso en las aplicaciones terapéuticas descritas en la presente memoria, también se describen kits y artículos de fabricación. Dichos kits pueden incluir un vehículo, un envase o un recipiente que está compartimentalizado para recibir uno o más recipientes, como viales, tubos y similares, en donde cada uno del recipiente o los recipientes incluye uno de los elementos independientes que se usarán en un método descrito en la presente memoria (como, por ejemplo, los compuestos correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma descritas en la presente memoria), un vehículo aceptable desde el punto de vista farmacéutico, o un compuesto o agente adicional con actividad farmacológica, ya sea por sí solos o en combinación). Entre los recipientes adecuados se incluyen, por ejemplo, botellas, viales, jeringas y tubos de ensayo. Los recipientes pueden estar formados de diversos materiales, como vidrio o plástico.
[0123] Las composiciones que contienen uno o más compuestos proporcionados en la presente memoria (por ejemplo, los compuestos correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos) formulados en un vehículo farmacéutico compatible también se pueden preparar, colocar en un recipiente adecuado y etiquetar para el tratamiento de una condición indicada.
[0124] Según una realización, el artículo de fabricación comprende material de embalaje y dentro de dicho material de embalaje está contenida una formulación oral para tratar una enfermedad o afección, o para proteger el tejido frente al daño producido por la exposición a un tratamiento anticancerígeno en un paciente que lo necesite, que comprende los compuestos correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos). Según esta realización, la formulación por vía parenteral comprende una formulación de dosis unitarias según se describe en la presente memoria, y el material de embalaje comprende una etiqueta o prospecto con instrucciones para la administración por vía oral de la dosis al paciente. Por ejemplo, la formulación oral puede estar en forma de comprimido, píldora, cápsula, o gel o suspensión, y puede estar contenida en un recipiente o vial adecuado.
[0125] Según otra realización, el artículo de fabricación comprende material de embalaje y dentro de dicho material de embalaje está contenida una formulación parenteral para tratar una enfermedad o afección, o para proteger el tejido frente al daño producido por la exposición a un tratamiento anticancerígeno en un paciente que lo necesite, que comprende los compuestos correspondientes a la Fórmula (I) (o cualquiera de las realizaciones de la misma u otros compuestos descritos en la presente memoria, como cualquiera de los compuestos y/o formulaciones que se exponen en el Cuadro I del apartado de ejemplos). Según esta realización, la formulación parenteral comprende una formulación de dosis unitarias según se describe en la presente memoria, y el material de embalaje comprende una etiqueta o prospecto con instrucciones para la administración por vía parenteral de la dosis al paciente. Por ejemplo, la formulación parenteral puede estar en forma de solución y puede estar contenida en un vial o recipiente adecuado.
[0126] Habiendo descrito las realizaciones en detalle, será evidente que es posible hacer modificaciones y variaciones sin apartarse del alcance de la descripción. La invención está definida por las reivindicaciones anexas. Además, se debe apreciar que todos los ejemplos de la presente descripción se proporcionan a título de ejemplo no limitativo.
EJEMPLOS:
[0127] (Solo el compuesto «G4711» (ejemplo 9, página 65) es un ejemplo de acuerdo con las reivindicaciones; los otros ejemplos son ejemplos de referencia).
[0128] Para ilustrar mejor la presente invención se proporcionan los siguientes ejemplos no limitativos. Los expertos en la materia apreciarán que las técnicas dadas a conocer en los ejemplos que se exponen a continuación representan los enfoques que los inventores han encontrado que funcionan bien en la práctica de la invención y, por lo tanto, se pueden considerar que constituyen ejemplos de modos para su puesta en práctica. Sin embargo, los expertos en la materia deberán, en vista de la presente descripción, apreciar que se pueden hacer muchas modificaciones a las realizaciones específicas dadas a conocer.
EJEMPLO 1
Introducción
[0129] Se analizó la biodisponibilidad oral de los compuestos mediante inyección de los profármacos formulados directamente al duodeno (administración intraduodenal o i.d.) de los cerdos enanos usados como sujetos del ensayo, evitándose así el entorno ácido del estómago y de este modo eliminándose posibles resultados engañosos de biodisponibilidad oral que pudieran deberse a la alteración del artículo farmacológico ensayado en el entorno ácido del estómago.
[0130] Como especie para el modelo de ensayo para la evaluación de la biodisponibilidad oral se seleccionó el cerdo enano de Gottingen, ya que: 1) es bien sabido que los cerdos enanos (y los cerdos en general) simulan la fisiología y la farmacología del intestino humano, en particular en lo que respecta a la asimilación de fármacos1 y 2) en estudios previos con GC4403 (el enantiómero de GC4419) en los que se usaron cerdos enanos de Gottingen se demostró una biodisponibilidad oral que concordaba con la experiencia clínica en estudios con humanos.
[0131] Los estudios se llevaron a cabo en Xenometrics LLC (Stillwell, Kansas, EE. UU.) y la biodisponibilidad por vía i.d. se determinó con diversos complejos derivados con ligandos axiales de GC4419, GC4444, GC4403 y GC4401. En cada caso los compuestos precursores (GC4419, GC4403, GC4444 y GC4401) con sus ligandos de cloro axiales se administraron por vía intravenosa (i.v.) con el fin de obtener una referencia para calcular la biodisponibilidad del 100%, determinada mediante el AUCü->24 h (área bajo la curva de 0 a 24 h (ng-h/ml)). El cálculo del porcentaje de biodisponibilidad oral de una formulación de un compuesto administrado por vía i.d. requiere el cálculo del AUCü->24 h por esta vía y la comparación con el AUCü->24 h obtenida mediante administración por vía i.v. A continuación, con la siguiente fórmula se calcula el porcentaje de biodisponibilidad oral mediante asimilación intestinal del complejo como artículo farmacológico ensayado:
Porcentaje (%) de biodisponibilidad oral = AUC0->24 h (i.d.) x (1/dosis (mg/kg)) AUC0->24 h (i.v.)*
[0132] *Donde la dosis por vía i.v. es de 1 mg de artículo farmacológico ensayado por kilogramo de peso corporal del cerdo enano, y la dosis administrada por vía i.d. es de 10 mg de artículo farmacológico ensayado por kilogramo de peso corporal del cerdo enano.
[0133] Todas las instalaciones de Xenometrics están plenamente certificadas por la Asociación para la Evaluación y Acreditación del Cuidado de Animales de Laboratorio (AAALAC, Association for Assessment and Accreditation of Laboratory Animal Care). Todos los experimentos y el cuidado de los animales se llevaron a cabo conforme a las estrictas directrices establecidas y aplicadas por el Comité Institucional de Xenometrics para el uso y el cuidado de animales.
Métodos
[0134] Los cerdos enanos macho de Gottingen (4-5 meses de edad, peso de 9-12 kg) se adquirieron a Marshall BioResources y se alojaron en Xenometrics. Después de un mínimo de 14 días de aclimatación, a cada animal se le implantó una cánula intraduodenal (i.d.) mediante cirugía abdominal con la suficiente anestesia. El extremo distal se exteriorizó con un cono accesible reutilizable (véanse los pormenores de la cirugía más abajo). Durante un período de recuperación de 2 semanas como mínimo los cerdos enanos se manejaron a diario para aclimatarlos a los procedimientos del ensayo, es decir, la administración por vía i.d. y la recogida de muestras de sangre. En cada experimento, a cada cerdo enano se le administró un artículo farmacológico ensayado disuelto o suspendido en un vehículo como excipiente. No fue necesario sujetar a los cerdos enanos para la administración. Todos los experimentos de administración se llevaron a cabo con los animales en ayunas. La comida se retiró de los cerdos enanos 16 horas antes de la administración. Los cerdos enanos tenían libre acceso a agua. Los cerdos enanos a los que se había practicado la administración tenían acceso a alimentos 6 horas tras la administración. El artículo ensayado se administró a una dosis de 10 mg/kg de fármaco precursor en 0,1 ml/kg vehículo (por ejemplo, 1,5 ml en 15 kg de cerdo enano) en inyección en embolada (~1 minuto) por medio de la cánula i.d. La cantidad real total de artículo farmacológico ensayado que se administraba era distinta dependiendo del peso molecular del profármaco. Se usó un volumen idéntico de vehículo como excipiente para irrigar la cánula tras la administración del artículo ensayado. Aproximadamente 6 horas más tarde, se usó aceite de maíz para irrigar la cánula. Aproximadamente 24 horas después de la dosis, el catéter se irrigó con suero salino estéril y se tapó. En los siguientes puntos temporales de 0,25, 0,5, 1, 2, 4, 8, 24 y 48 horas tras la inyección, se recogieron muestras de sangre de 2 ml mediante punción de la vena cava anterior (Vacutainer con heparina de sodio, 4 ml, aguja con un calibre de 20 G de 1,5 pulgadas) después de limpiar con etanol la superficie de la piel. Para la recogida de muestras de sangre, el cerdo enano se colocó en un cabestrillo en posición recostada sin anestesia. Los cerdos enanos nunca se usaron más de una vez en un espacio de 7 días de experimentación. Las muestras de sangre se mantuvieron en hielo hasta que se procesaron para obtener el plasma. Las muestras de sangre se centrifugaron a 1200xg durante diez minutos a 4 °C y las muestras de plasma se transfirieron a tubos para placa de 96 pocillos, se taparon y se conservaron a 20 °C hasta su envío en nieve carbónica al laboratorio de análisis en el que se determinó la concentración de fármaco en el plasma. La concentración de complejo macrocíclico pentaaza de manganeso precursor (independientemente de la composición de los ligandos axiales) se determinó en el plasma mediante un método validado de HPLC/MS/MS cuyo intervalo de linealidad estaba
comprendido entre 50 ng/ml y 20000 ng/ml.
Procedimiento quirúrgico de Xenometrics para la implantación en los cerdos de catéteres duodenales como vía de acceso: Preparación quirúrgica del sistema de ensayo
Preparación de los animales
[0135] Los cerdos se mantienen en ayunas durante la noche antes de la intervención quirúrgica. La administración de medicación previa y la inducción de la anestesia general en los cerdos se realiza según la pauta de medicación y esquema de dosis adjuntos. Se introduce un tubo endotraqueal y se mantiene la anestesia general con isoflurano administrado en oxígeno mediante un vaporizador de precisión y un circuito anestésico de reinhalación. Durante la intervención quirúrgica se administra solución de Ringer lactato a aproximadamente 100 ml por hora a través de un catéter periférico. La intervención quirúrgica se lleva a cabo en una sala quirúrgica designada y se siguen técnicas asépticas durante todos los procedimientos quirúrgicos.
Colocación de la vía de acceso
[0136] Se afeita una zona en la región dorsal derecha del tórax y se prepara con una solución antiséptica de clorhexidina.
[0137] Se hace una laparotomía media, se aísla el duodeno, se canula conforme a la descripción que figura más abajo y se exterioriza en un sitio a lo largo de la región dorsal del tórax. La cánula exteriorizada a continuación se acopla a una vía de acceso individual y se implanta subcutáneamente utilizando un hilo de sutura no reabsorbible adecuado. La incisión para la vía de acceso se cierra adecuadamente asegurando la eliminación del espacio muerto y la piel se cierra con hilo de sutura reabsorbible. Se lleva a cabo la aposición del peritoneo y la capa muscular de la laparotomía mediante sutura discontinua con hilo de sutura reabsorbible de un grosor adecuado. La aposición de los tejidos subcutáneos se hace con hilo de sutura reabsorbible. La piel se cierra mediante sutura intradérmica con hilo de sutura reabsorbible.
Canulación del duodeno con una vía de acceso vascular
[0138] Se afeita una zona del abdomen ventral y se prepara con solución antiséptica de clorhexidina.
[0139] Para canular el duodeno se usa un catéter con válvula de escape de presión con un disco Dacron de 5 mm fijado a 1 cm de la punta (Access Technologies, Chicago, Illinois, EE. UU.). La cánula con válvula de escape de presión se irriga antes de la implantación para garantizar que la válvula de escape de presión no esté obstruida y funcione adecuadamente. Se localiza el duodeno y se aísla el sitio para la introducción de la cánula (es decir, 5-8 cm distalmente al ángulo duodenal anterior). En la superficie mucosa de este sitio se hace una sutura en bolsa de tabaco con Prolene 4-0 en cuyo centro se perfora el intestino con una aguja de 18 G. A continuación, la aguja se retira y se reemplaza con un adaptador de mangueta de 16 G para dilatar aún más el sitio de introducción existente. A continuación, se retira el adaptador de mangueta y se coloca la punta de la válvula de escape de presión en el defecto intestinal hasta que el disco de Dacron quede al ras de la superficie mucosa. La punta se ancla cerrando la bolsa de tabaco y atando en su sitio. El disco se ancla en su sitio a la superficie mucosa mediante 7-8 puntos de sutura discontinuos con Prolene 4-0. Se forma un pequeño bucle y el cuerpo del catéter (aproximadamente 5-6 cm desde el disco) se ancla a la mucosa mediante la técnica del túnel de Weitzel.
[0140] Nota: La técnica del túnel de Weitzel se lleva a cabo colocando el cuerpo del catéter a lo largo del intestino con la cara distal dirigida hacia el ángulo duodenal anterior. Se dan 4-6 puntos de sutura individuales con Prolene 5-0 separados aproximadamente 0,5 cm para formar el «túnel». Este túnel se forma fijando cada una de las suturas a la superficie mucosa al lado de la cánula y a continuación fijando el extremo libre a la superficie mucosa en el otro lado de la cánula asegurando que la sutura quede ENCIMA de la cánula. Cuando las suturas individuales se atan, estas tiran de la mucosa sobre la cánula formando el «túnel».
[0141] Tras finalizar la técnica del túnel de Weitzel se hace una pequeña incisión (2-3 mm) en el peritoneo, aproximadamente 1 cm por debajo de las costillas en el lado derecho del animal y el catéter se exterioriza al sitio de la vía mediante un trócar. Se hace una incisión en la cara lateral dorsal de la región derecha del tórax y se forma una bolsa para aceptar la vía. A continuación, la cánula se mueve a la bolsa mediante el trócar y se une a la vía. A continuación, la vía se ancla a la musculatura subyacente con hilo de sutura monofilamento no reabsorbible de un grosor adecuado y se cierra el músculo, la fascia y la piel de manera adecuada. La vía se irriga con suero salino. El abdomen se cierra mediante sutura discontinua con hilo monofilamento reabsorbible adecuado. La fascia se cierra por separado mediante sutura con hilo reabsorbible adecuado según un patrón de sutura adecuado. La piel se cerró de manera adecuada con grapas o hilo de sutura adecuados. Durante la recuperación de la anestesia los animales se vigilan para comprobar que sus funciones fisiológicas vuelvan a la normalidad.
[0142] Los sitios donde se practicaron las incisiones se examinan a diario durante un mínimo de 14 días. Se administran antibióticos si es necesario. A los animales no se les pone un chaleco durante un mínimo de 14 días tras
la intervención quirúrgica.
Mantenimiento del sistema
[0143] Se accede a las vías mediante una técnica aséptica. El pelo situado por encima de la vía se recorta si es necesario. Se aplican alternadamente al menos 3 frotamientos con solución antiséptica de clorhexidina antes de acceder a la vía mediante una aguja con punta de Huber. Tras la administración, la vía duodenal se irriga con una solución irrigadora adecuada, como suero salino o agua estéril.
Sección experimental
Preparación de las formulaciones para administración
[0144] Los aceites utilizados para preparar las soluciones para la administración se usaron tal y como se recibieron de fuentes comerciales. Capmul MCM (NF), una mezcla de mono/diglicéridos del ácido caprílico/cáprico, fue suministrado por ABITEC Corporation (Janesville, Wisconsin, EE. UU.). Miglyol 812 N, una mezcla de triglicéridos del ácido caprílico/cáprico, fue suministrado por Cremer Oleo Division (Eatontown, Nueva Jersey, EE. UU.). Labrafil M 2125 CS (NF), que se define químicamente como glicéridos de linoleoílo polioxilados 6 (NF), fue suministrado por Gattefose (SAINT-PRIEST Cedex, Francia). Peceol, que se define químicamente como monooleato de glicerilo (Nf , monoglicérido), fue suministrado por Gattefose (SAINT-PRIEST Cedex, Francia). Maisine 35-1, que se define químicamente como monolinoleato de glicerilo (NF, monoglicérido), fue suministrado por Gattefose, SAINT-PRIEST Cedex (Francia). Labrasol (NF), que se define químicamente como glicéridos de caprilocaproílo polioxilados 8 (NF), fue suministrado por Gattefose, SAINT-PRIEST Cedex (Francia). Labrafil M 1944 Cs , que se define químicamente como glicéridos de oleoílo polioxilados 6 (NF), fue suministrado por Gattefose, SAINT-PRIEST Cedex (Francia). Todas las soluciones para administración se prepararon pesando todos los componentes de cada formulación en una balanza analítica de cuatro decimales de manera que el principio activo ensayado representaba un 10% en peso de la formulación y el aceite usado para esa formulación representaba un 90% en peso.
Método bioanalítico
[0145] En el método bioanalítico, la estructura macrocíclica de Mn (II) con ligandos precursora se cuantificó en el plasma mediante HPLC acoplada a un detector de MS/MS examinando la presencia del complejo monocatiónico [monoformatoMn(pentaazamacrociclo)]+. Las muestras bioanalíticas se analizaron en ABC Laboratories mediante el método bioanalítico de Galera validado en ABC como método de ABC número 81201-MI-02, el cual es similar al método descrito en la patente de EE. UU. n.° 8.444.856 concedida a Slomczynska et al.
SÍNTESIS
[0146] Todos los reactivos que se usaron en la síntesis de los compuestos dados a conocer en la presente memoria se adquirieron en Sigma-Aldrich y se usaron sin purificarlos, a menos que se indique lo contrario. Todos los análisis elementales junto con sus informes se hicieron en Galbraith Laboratories, Inc. (Knoxville, Tennessee, EE. UU.).
[0147] Los complejos macrocíclicos pentaaza diclorados de Mn (II) precursores, como GC4419, GC4401, GC4444 y GC4403 (las estructuras se muestran más abajo), se sintetizaron mediante procedimientos publicados en la bibliografía. Para la síntesis de GC4403, como producto de partida2 se usa el R,R-diaminociclohexano quiral, mientras que para la síntesis de GC4419, en su lugar se usa el enantiómero que es la imagen especular de GC4403, el S,S-diaminociclohexano quiral. El resto de la síntesis de GC4419 puede ser idéntica en todos los sentidos al método publicado para GC4403. La síntesis del complejo GC4401 se había publicado previamente en la referencia 5.
[0148] La síntesis de GC4444, que contiene el sustituyeme adicional 11-R-metilo, lo que genera un quinto centro quiral en el carbono (y también se deriva de R,R-diaminociclohexano), se lleva a cabo a partir de la tetraamina quiral correspondiente cuya síntesis se publicó en la referencia 6 como Ejemplo 5C.
Síntesis de derivados de ligandos axiales
[0149] Los mismos complejos macrocíclicos pentaaza diclorados de Mn (II) precursores (GC4419, GC4403, GC4444 y GC4401) también se usaron como producto de partida precursor para la síntesis de otros derivados con ligandos axiales enlazados mediante un esquema genérico de síntesis en el que un gran exceso de una sal de un anión se usa para desplazar el ligando cloro, de este modo generándose el nuevo compuesto.
EJEMPLO 2
[0150] Síntesis de b/s-acetato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20,21, 21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [b/s-Acetato(GC4419)]. GC4701.
[b/s-Acetato(GC4419)]
C25H4-iMnN5O4
MW 530,57
GC4701
[0151] En un matraz Erlenmeyer de 500 ml, se añadieron 100 ml de agua desionizada a 5,3 g de GC4419; la mezcla se agitó vigorosamente durante 15-20 min y a continuación se sonicó durante 5 min. La suspensión resultante de un color amarronado claro se filtró a través de un embudo con frita de 10-20 p (aproximadamente 0,3 g de material sólido permanecieron en el embudo). La solución límpida resultante se añadió en chorro de una sola vez a una solución de acetato de sodio (aproximadamente 429 mmol, 21 eq. en 100 ml de agua desionizada). No se separó ningún sólido y la solución amarillenta se agitó durante 5 min adicionales. La solución se transfirió a un embudo de decantación y se extrajo (3*50 ml) con diclorometano. Las fases orgánicas se separaron, se combinaron y se transfirieron de vuelta al embudo de decantación. La solución de diclorometano se retroextrajo (2*50 ml) con solución acuosa de acetato de sodio (32 g/100 ml). La fase de diclorometano se secó con MgSO4 (aproximadamente 10 g) durante 30 min (con agitación), se filtró a través de un embudo con frita de 10-20 p y la solución se llevó a sequedad en un rotavapor. Al sólido amarillo aceitoso que se obtuvo tras llevar la solución a sequedad se añadió metanol (50 ml). Esta solución a continuación se llevó a sequedad de nuevo en el rotavapor, obteniéndose una espuma/vidrio de color amarillo claro. Este material se secó al vacío a temperatura ambiente durante dos días.
[0152] El material quebradizo de color amarillento que se aisló (4,11 g, rendimiento del 75% calculado a partir de GC4419) se analizó por HPLC, siendo la pureza del 99,7%, y el análisis elemental mostró un 0,98% en peso de cloro residual. El análisis elemental concordaba con la estructura prevista de b/s-(acetato), C25H4-iMnN5O4-2H2O. Análisis teórico: C, 53,00%; H, 8,01%; N, 12,36% y Mn, 9,70%. Análisis experimental: C, 53,10%; H, 8,34%; Mn, 9,86%, N, 12,56% y Cl (representa el contenido de halógenos totales), 0,98% en peso.
EJEMPLO 3
[0153] Síntesis de b/s-octanoato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20, 21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [£vs-Octanoato(GC4419)]. GC4710.
[b/s-Octanoato(GC4419)]
CayH65MnN5O4
MW 698,90
GC4710
[0154] En un matraz Erlenmeyer de 500 ml, se añadieron 200 ml de agua desionizada a 10,2 g de GC4419, se agitó vigorosamente durante 15-20 min y a continuación se sonicó durante 5 min. La suspensión resultante de color beige se filtró a través de un lecho de celite de 45*20 mm (lavado previamente con agua desionizada) en un embudo con frita de 25-50 p. La solución límpida resultante se añadió lentamente en chorro durante 5 min a 250 ml de una solución de octanoato de sodio (75 g, aproximadamente 450 mmol, 11 eq.). No se separó ningún sólido y la solución beige se agitó durante 5 min adicionales. La solución se transfirió a un embudo de decantación y se extrajo (2*100 ml) con DCM. Las fases orgánicas se separaron, se combinaron, se secaron con MgSO4 (10 g), se filtraron y se llevaron a sequedad a presión reducida. Se usó MeOH (75 ml) para coevaporar el DCM residual, obteniéndose una goma de un color beige-amarillo claro. Esta goma se secó al vacío a 40 °C durante 19 h. Se aisló un sólido amarillento con un rendimiento del 73% (10,8 g) calculado a partir de GC4419 como producto de partida. Este sólido se envió para su análisis elemental (Galbraith Labs) y también se analizó por HPLC mediante el método cromatográfico descrito en la referencia 4.
[0155] La pureza por HPLC fue del 99,5% (0,14% de monoamina GC4520). El análisis elemental concordaba con la estructura del hemihidrato, C25H4-iMnN5O4-0,5H2O, FW 734,93 (anhidro). Análisis teórico: C, 63,05%; H, 9,39%; N,
9,94% y Mn, 7,79%. Análisis experimental: C, 63,21%; H, 9,80%; Mn, 7,97%, N, 9,63% y Cl (representa el contenido de halógenos totales), <150 ppm.
EJEMPLO 4
[0156] Síntesis de b/s-pivaloato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20,21, 21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [b/s-pivaloato(GC4419)]. g C4709.
[S/s-Pivaloato (GC4419)]
C3iH53MnN5O4
MW 614,73
GC4709
[0157] La sal de pivaloato de sodio (6,4 g) se añadió a un matraz Erlenmeyer de 125 ml y se disolvió (calentando a aproximadamente 40 °C) en 50 ml de EtOH absoluto (la solución era prácticamente incolora). Una vez la solución de pivaloato de sodio se había enfriado a temperatura ambiente, se añadió una solución que contenía 5,3 g de GC4419 disuelto en 30 ml de EtOH absoluto (la solución era de color beige). Al mezclar, se observó inmediatamente la precipitación del NaCl. La suspensión, de color beige, se agitó durante 1 h a temperatura ambiente bajo Ar, y a continuación se colocó en un frigorífico (2-8 °C) durante la noche. La suspensión resultante, de color beige, se filtró a través de un embudo con frita tarado de 10-20 p (aproximadamente 1,1 g de sal sólida de cloruro de sodio permanecieron en el embudo) y el disolvente se eliminó del filtrado en un rotavapor. El residuo húmedo procedente del rotavapor se secó adicionalmente al vacío durante 15 min. Se añadió IPA (100 ml), la mezcla se agitó suavemente durante una hora y a continuación se colocó en el frigorífico durante la noche. Al día siguiente, al filtrar, se aislaron 1,28 g de un sólido blanco, que se desechó. El filtrado límpido de color amarillo-beige claro se concentró en un rotavapor hasta obtener un sólido húmedo.
[0158] Al sólido húmedo se añadió diclorometano (100 ml). La mezcla se transformó en una suspensión de consistencia gelosa y se mezcló agitando durante 1 h a 37 °C. La suspensión se filtró a través de un embudo con frita tarado de 10-20 p, y se aislaron otros 1,7 g de sólido blanco, que se desechó. El disolvente del filtrado se eliminó en un rotavapor, obteniéndose un almíbar de color beige. Al almíbar beige se añadió MeOH (75 ml) y tras eliminar el disolvente en un rotavapor se obtuvo un semisólido beige. Este material se secó al vacío durante 72 h para dar GC4709 en forma de sólido beige, que se envió para su análisis elemental. La pureza por HPLC fue del 99,5%. El análisis elemental concordaba con la estructura, C3-iH53MnN5O4-0,5H2O, FW 614,73 (anhidro). Análisis teórico: C, 59,69%; H, 8,73%; N, 11,23% y Mn, 8,81%. Análisis experimental: C, 59,87%; H, 8,44%; Mn, 8,45%, N, 10.88%, y Cl (representa el contenido de halógenos totales), aproximadamente 0,08% (784 ppm).
EJEMPLO 5
[0159] Síntesis de b/s-ciclohexanobutirato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a, 18,19,20,21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,ft][1,4,7,10]tetraazaciclo-heptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [b/s-ciclohexanobutirato(GC4419)]. Gc 4707.
GC4707
[0160] Se añadió ciclohexanobutirato de sodio (5,77 g) a un matraz Erlenmeyer de 125 ml y a continuación se trató de disolverlo mientras se agitaba en 50 ml de EtOH absoluto durante 15 min. La mezcla adoptó una consistencia gelosa y se añadieron otros 50 ml de EtOH absoluto, con un total de 100 ml. Con esta cantidad adicional de disolvente no se logró obtener una solución límpida al calentar/sonicar (aproximadamente 40 °C). Se añadió MeOH (10 ml) y tras 15 min de agitación/sonicación se formó una solución límpida. Esta solución se añadió en una porción a una solución que contenía 3,6 g de GC4419 disuelto en 15 ml de EtOH absoluto (la solución era de color beige). Se obtuvo una suspensión fina inmediatamente. La suspensión se agitó durante 15 min y a continuación se colocó en un congelador durante 1 h. En este punto la suspensión se filtró a través de un embudo con frita de 10-15 p y el filtrado límpido de color beige se evaporó a sequedad en un rotavapor. El sólido resultante se secó al vacío a temperatura ambiente durante la noche. A la mañana siguiente, el sólido beige se agitó en 100 ml de diclorometano (DCM) a fin de disolver el producto deseado a la vez que se dejaba el exceso de sal de ciclohexanobutirato de sodio. Esta suspensión se agitó durante 3 h antes de filtrarla a través de un embudo con frita de 10-15 p y se lavó en el embudo con DCM (2*30 ml). El filtrado resultante de color amarillo se evaporó en un rotavapor y a continuación se añadieron 100 ml de MeOH. La solución resultante de color amarillo se evaporó otra vez en el rotavapor y el residuo se dejó al vacío a temperatura ambiente durante la noche. Al día siguiente, se aisló un sólido de color beige. El material se deshizo más y se secó al vacío durante la noche y a continuación se molió con un mortero de ágata.
[0161] El sólido beige aislado (5,4 g, rendimiento del 96% calculado a partir de GC4419) se analizó por HPLC, siendo la pureza del 99,6%. El análisis elemental concordaba con la fórmula de [b/s-(ciclohexanobutirato)GC4419]: C41H6gMnN5O4, FW 750,97 (anhidro). Análisis teórico: C, 65,58%; H, 9,26%; N, 9,33% y Mn 7,32%. Análisis experimental: C, 65,29%; H, 8,83%; Mn, 6,95%, N, 9,42% y Cl (representa el contenido de halógenos totales), 0,22% en peso.
EJEMPLO 6
[0162] Síntesis de b/s-dodecanoato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19, 20,21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,ft][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [b/s-dodecanoato(GC4419)]. GC4708.
[b/s-Dodecanoato(GC4419)]
C45H8iMnN5O4
MW 811,11
GC4708
[0163] Se añadió dodecanoato de sodio (6,17 g) a 300 ml de EtOH absoluto en un matraz Erlenmeyer de 500 ml. La suspensión resultante de color blanco se agitó (300 rpm) a la vez que se calentaba (aproximadamente a 50 °C) en una placa caliente. Tras 15 min la suspensión se espesó un poco. Se añadieron otros 100 ml de EtOH absoluto y la suspensión resultante se sonicó durante 10 min. A continuación, se añadieron 15 ml de agua desionizada (dando EtOH aproximadamente al 96%) mientras se agitaba y la mezcla se transformó en una solución límpida en menos de un minuto. A esta solución, se añadieron 3,6 g de GC4419 disueltos en 30 ml de EtOH absoluto. La solución resultante, turbia y de un color beige claro, se agitó durante 2 h y a continuación se puso en un rotavapor. Se eliminó aproximadamente la mitad del disolvente, formándose un precipitado a medida que el volumen disminuía. En este punto, tanto el sólido como el disolvente se transfirieron a un embudo con filtro de 25-50 p, junto con el aclarado con EtOH (50 ml) del matraz, y se filtró. El filtrado, de color beige claro, se colocó de nuevo en el rotavapor. Tras una evaporación adicional, se obtuvo un sólido de color beige claro, que se colocó al vacío a temperatura ambiente durante la noche. Al día siguiente, se aislaron aproximadamente 4,7 g de un sólido de color beige. Se añadió DCM (100 ml), la suspensión se agitó durante 1 h y a continuación se filtró, obteniéndose un filtrado de color amarillo claro. Tras eliminar el DCM en un rotavapor, se obtuvo una espuma de color beige claro que también se secó al vacío a temperatura ambiente durante 48 h.
[0164] El sólido quebradizo de color beige (2,9 g, rendimiento del 44%) se analizó por HPLC, siendo la pureza del 96,8%.
EJEMPLO 7
[0165] Síntesis de b/s-fenilacetato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20, 21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraazaciclo-heptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [b/s-fenilacetato(GC4419)]. GC4718.
GC4718
[0166] Se disolvió parcialmente ácido fenilacético (47,3 g) en agua desionizada (1 l) y el pH se ajustó a 7,6 con NaOH sólido, seguido de la adición gota a gota de una solución acuosa de NaOH 0,5 M para aumentar el pH a aproximadamente 8,5. El volumen final de solución de fenilacetato de sodio era de aproximadamente 1 l. Se añadió GC4419 en forma sólida (3,5 g) a 400 ml de la solución de fenilacetato mientras se agitaba, tras lo cual se formaron algunos sólidos. Se añadió DCM (50 ml) y se extrajo la fase acuosa. Esta extracción se repitió otras dos veces y los tres extractos de diclorometano se agruparon (aproximadamente 150 ml) y se retroextrajeron con la solución restante de fenilacetato (4*150 ml). La solución de DCM de color amarillo claro se secó con MgSO4 durante 30 min (agitando), se filtró a través de un embudo con frita de 10-20 p y se llevó a sequedad en un rotavapor. La espuma resultante se disolvió en 50 ml de MeOH y se llevó de nuevo a sequedad para eliminar las trazas de DCM. El residuo espumoso resultante se puso al vacío a temperatura ambiente durante la noche. Se aislaron 4,57 g (rendimiento del 93%) de sólido semicristalino de color amarillo-beige claro, que se analizó por HPLC, siendo la pureza del 99,6%. El análisis elemental concordaba con la estructura prevista del b/s-(fenilacetato), C37H4gMnN5O4. Análisis teórico: C, 65,09%; H, 7,23%; N, 10,26% y Mn, 8,05%. Análisis experimental: C, 65,17%; H, 7,26%; Mn, 7,67%, N, 10.08% y Cl (representa el contenido de halógenos totales), 63 ppm.
EJEMPLO 8
[0167] Síntesis de b/s-fenilglioxaloto[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19, 20,21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraazaciclohepta-decino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [b/s-fenilglioxilato(GC4419)]. GC4719.
GC4719
[0168] Se añadió ácido fenilglioxílico (12,4 g) a 200 ml de agua desionizada en un matraz Erlenmeyer de 500 ml. Tras agitar durante 5 min, se obtuvo una solución incolora y límpida. Esta se trató con 3,2 g de NaOH en pelets y la mezcla se agitó vigorosamente. El pH se determinó una vez todo el NaOH se había disuelto. El pH era de 3,61 y se ajustó a ~8,5-9 con solución acuosa de NaOH al 5% en peso.
[0169] Una solución turbia de 5 g de GC4419 en 75 ml de agua desionizada se filtró a través de un embudo de filtro de 10-20 p y se añadió en una porción a aproximadamente una mitad de la solución acuosa (aproximadamente 110 ml) de fenilglioxilato de sodio cuyo pH se había ajustado. El precipitado blanco se agitó durante 15 min adicionales antes de añadir 100 ml de DCM. Se produjo inmediatamente una fase amarilla de DCM. Las capas se separaron y la fase de DCM se extrajo con la segunda mitad de la solución de fenilglioxilato de sodio. Tras agitar vigorosamente y dejar sedimentar durante 10 min, la fase de DCM se secó con MgSO4 , se filtró y el disolvente se eliminó en un rotavapor. Se añadió MeOH (50 ml) al matraz que había en el rotavapor y la solución amarilla se continuó evaporando para eliminar el DCM residual. El sólido resultante se secó al vacío a 30 °C durante la noche.
[0170] El sólido semicristalino de color amarillo claro que se aisló (7,1 g, rendimiento del 96% calculado a partir de GC4419) se analizó por HPLC, siendo la pureza del 99,3%. El análisis elemental dio el siguiente resultado: C, 62,05%; H, 6,38%; Mn, 7,73%; y N, 9,85%. Análisis experimental: C, 62,50%; H, 6,29%; Mn, 7,73%; N, 9,85% y Cl (representa el contenido de halógenos totales), 55 ppm.
EJEMPLO 9
[0171] Síntesis de bs-propionato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20, 21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraaza-cicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [b/s-propionato(GC4419)]. GC4711.
[bis-Propionato(GC4419)]
C27H45MnN5O4
MW 558,63
GC4711
[0172] Se añadió GC4419 (11,0 g) a un matraz Erlenmeyer de 500 ml que contenía 200 ml de agua desionizada. La mezcla se agitó vigorosamente durante 15-20 min mientras se calentaba a 40 °C durante 10 min. La suspensión resultante, de un color amarronado claro, se filtró a través de un embudo con frita de 10-20 |j, obteniéndose una solución límpida de color beige claro. En un matraz aparte se preparó una solución acuosa de 80 g de propionato de sodio en 200 ml de agua desionizada. En un matraz Erlenmeyer de 500 ml, la solución de GC4419 se combinó con 200 ml de la solución de propionato de sodio. La solución resultante de color beige se agitó durante 5 min. La solución de color amarillo-beige claro se transfirió a un embudo de decantación de 1 l y se extrajo con DCM (3*75 ml). Las tres fases de DCM resultantes se combinaron y se transfirieron de vuelta al embudo de decantación. La solución resultante de DCM se retroextrajo con más solución acuosa de propionato de sodio (3*70 ml). La fase de DCM se secó con MgSO4 durante 15 min (con agitación), se filtró a través de un embudo con frita de 20-50 j y se llevó a sequedad (obteniéndose una espuma) en un rotavapor. Se añadió metanol (100 ml) y la solución resultante se llevó a sequedad en un rotavapor para eliminar el DCM residual, obteniéndose un sólido de color amarillo-beige claro. Este material se secó al vacío a 30 °C durante 20 h.
[0173] Se obtuvieron 11,45 g del sólido amarillento aislado, lo que corresponde a un rendimiento del 94% calculado a partir de GC4419, La pureza por HPLC fue del 99,6% y el análisis elemental mostró únicamente 873 ppm de cloro residual, expresado en contenido de halógenos totales, lo que concordaba con la estructura de [bis-propionato(GC4419)]. Análisis teórico: C, 58,05%; H, 8,12%; Mn, 9,83%; y N, 12,54%. Análisis experimental: C, 57,64%; H, 8,05%; Mn, 9,91%; N, 12,51% y Cl (representa el contenido de halógenos totales), 873 ppm.
EJEMPLO 10
[0174] Síntesis de bis-L-fenilglicinato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19, 20,21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,ft][1,4,7,10]tetraazaciclo-heptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II). [bis-(L)-Fenilglicinato(GC4419)]. GC4702.
GC4702
[0175] Se añadió GC4419 (1,5 g) a un matraz Erlenmeyer de 250 ml que contenía 100 ml de agua desionizada y se agitó durante 15 minutos. La suspensión resultante de un color amarronado claro se filtró a través de un embudo con frita de 20-50 p. A un segundo matraz Erlenmeyer, en el que se disolvieron 31,3 g de L-fenilglicina en 400 ml de agua desionizada, se añadieron 8,3 g de NaOH en pelets y la mezcla se agitó vigorosamente. El pH se determinó una vez todo el NaOH se había disuelto. El pH era de 2,30 y se ajustó con solución acuosa de NaOH al 5% en peso (pH resultante = 9,6). En un matraz Erlenmeyer de 250 ml, la solución de GC4419 se combinó con aproximadamente la mitad (200 ml) de la solución de sal sódica de L-fenilglicina. La solución resultante de color beige se agitó durante 5 min. La solución de color amarillo-beige claro se transfirió a un embudo de decantación de 1 l y se extrajo con DCM (3*50 ml). Las tres fases orgánicas de DCM resultantes se combinaron y se transfirieron de vuelta al embudo de decantación. La solución resultante de DCM se retroextrajo con la solución acuosa restante de sal sódica de L-fenilglicina (4*50 ml). La fase de DCM se secó con MgSO4 durante 15 min (con agitación), se filtró a través de un embudo con frita de 20-50 p y se concentró a sequedad en un rotavapor. Se añadió metanol (50 ml) y la solución resultante se llevó a sequedad en un rotavapor para eliminar el DCM residual, obteniéndose un sólido de color amarillobeige claro. Este material se secó al vacío a 30 °C durante 20 h. Se obtuvieron 5,42 g del sólido aislado de color amarillento (rendimiento del 74%). La pureza por HPLC fue del 99,5%. El análisis elemental indicó la presencia de cloro residual a 188 ppm. El análisis elemental concordaba con la estructura prevista de GC4702, con 1,5 moléculas de agua: C37H51MnNyO4-1,5H2O, análisis teórico: C, 60,07%; H, 7,36%; Mn, 7,43%; y N, 13,25%. Análisis experimental: C, 60,20%; H, 7,11%; Mn, 7,72%; N, 13,30% y Cl (representa el contenido de halógenos totales), 188 ppm.
EJEMPLO 11
[0176] Síntesis de rac-b/s-fenilglicinato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18, 19,20,21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,ft][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [(rac)-b/s-fenilglicinato(GC4419)]. g C4720.
GC4720
[0177] En un matraz Erlenmeyer de 500 ml, se añadió GC4419 (10,0 g) a 250 ml de agua desionizada mientras se agitaba vigorosamente durante 15-20 min. La suspensión resultante, de un color amarronado claro, se filtró a través de un embudo con frita de 20-50 p. A un segundo matraz Erlenmeyer que contenía 62,7 g de rac-feniiglicina en 350 ml de agua desionizada, se añadieron 16,6 g de NaOH (dos porciones aproximadamente iguales en pelets) y la mezcla se agitó vigorosamente. El pH se midió una vez todo el NaOH se había disuelto y se había obtenido una solución límpida. El pH que se midió fue de 12,3, y se ajustó a 9 mediante la adición de pequeñas porciones de fenilglicina racémica en polvo. En un matraz Erlenmeyer de 500 ml, la solución de GC4419 se combinó con la mitad (~200 ml) de la solución de fenilglicinato de sodio racémico (aproximadamente 105 mmol). La solución resultante de color marrón claro se agitó durante 5 min. La solución se transfirió a un embudo de decantación de 1 l y se extrajo con 150 ml de DCM. La fase orgánica se separó y se retroextrajo con la solución acuosa restante de fenilglicinato de sodio racémico (2*100 ml). La fase de DCM se secó con MgSO4 durante 15 min (con agitación), se filtró a través de un embudo con frita de 20-50 p y se llevó a sequedad en un rotavapor. Se añadió metanol (75 ml) y la solución resultante se llevó a sequedad en un rotavapor para eliminar el DCM residual, obteniéndose un sólido de color amarillo-beige claro. Este material se secó al vacío a 30 °C durante 20 h. El material amarillento aislado (5,42 g, rendimiento del 74%) se analizó por HPLC, siendo la pureza del 99,5%. El análisis elemental concordaba con la estructura prevista de GC4720, C37H5-iMnN7O4'2H2O. Análisis teórico: C, 62,35%; H, 7,21%; N, 13,76% y Mn, 7,71%. Análisis experimental: C, 56,89%; H, 7,02%; Mn, 7,68%, N, 13,76% y Cl (representa el contenido de halógenos totales), 0,20%.
EJEMPLO 12
[0178] Síntesis de b/s-L-fenilalaninato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19, 20,21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraazaciclo-heptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [b/s-(L)-fenilalaninato(GC4419)]. GC4704.
GC4704
[0179] En un matraz Erlenmeyer de 500 ml, se añadió GC4419 (10,0 g) a 200 ml de agua desionizada mientras se agitaba vigorosamente. La suspensión resultante de un color amarronado claro se filtró a través de un embudo con frita de 20-50 p. Por separado, se añadió (L)-fenilalanina (68,39 g) a 200 ml de agua desionizada en un matraz Erlenmeyer de 500 ml. La suspensión de fenilalanina se trató con NaOH sólido (16,6 g) en pelets y la mezcla se agitó vigorosamente. El pH se determinó una vez todo el NaOH se había disuelto. El pH era de 11,1 y se ajustó hasta un pH de 10,24 mediante la adición de L-fenilalanina. La solución de GC4419 y la mitad (aproximadamente 100 ml) de la solución de sal sódica de L-fenilalanina se combinaron en un matraz Erlenmeyer de 500 ml mientras se agitaba. La solución resultante de color beige se agitó durante 5 min tras haber añadido 100 ml de DCM. La solución bifásica de color amarillo-beige claro se transfirió a un embudo de decantación de 1 l, la fase orgánica se eliminó y la fase acuosa se extrajo con otros 50 ml de DCM. Las fases orgánicas se combinaron y se transfirieron de vuelta al embudo de decantación. La solución de DCM resultante se retroextrajo con la solución acuosa restante de propionato de sodio (2 x aproximadamente 50 ml). La fase de DCM se secó con MgSO4 durante 15 min (con agitación), se filtró a través de un embudo con frita de 20-50 p y se llevó a sequedad (obteniéndose una espuma) en un rotavapor. Se añadió metanol (50 ml) y la solución resultante se llevó a sequedad en un rotavapor para eliminar el DCM residual, obteniéndose un sólido de color amarillo-beige claro. Este material se secó al vacío a 30 °C durante 40 h.
[0180] El polvo amorfo de color amarillo-beige que se aisló (4,1 g, rendimiento del 55%) se analizó por HPLC, siendo la pureza del 99,6%. El análisis elemental concordaba con la estructura prevista del complejo GC4704 como trihidrato, C3gH55MnNyO4-3H2O, con los siguientes resultados: C, 59,19%; H, 7,22%; Mn, 6,52%; N, 12,09% y Cl, 0,20%.
EJEMPLO 13
[0181] Síntesis de rac-b/s-2-fenilpropionato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a, 18,19,20,21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [(rac)-b/s-2-fenilpropionato(GC4419)]. GC4705.
GC4705
[0182] Se añadieron 27,5 g de rac-ácido 2-fenilpropiónico a un matraz Erlenmeyer de 500 ml que contenía 200 ml de agua desionizada. Tras agitar durante 5 min, se obtuvo una dispersión. Esta se trató con NaOH sólido (6,84 g) en pelets y la mezcla se agitó vigorosamente. El pH se determinó una vez todo el NaOH se había disuelto. Antes de la adición de NaOH el pH era de 2,97 (dispersión) y tras la adición el pH se ajustó a ~9 con solución acuosa de NaOH al 5% en peso, obteniéndose una solución algo turbia. Se preparó una solución nebulosa de 10 g de GC4419 en 350 ml de agua desionizada mediante agitación vigorosa. Una porción de 100 ml de la solución acuosa de 2-fenilpropionato cuyo pH se había ajustado se añadió lentamente en chorro durante un minuto. Precipitó un semisólido blanquecino y toda la mezcla se agitó con DCM (100 ml) durante 15 min Transcurrido este tiempo, las dos fases se transfirieron a un embudo de decantación de 500 ml. El matraz Erlenmeyer se aclaró con DCM (10 ml) y el aclarado se añadió al embudo. La fase orgánica se separó y la fase acuosa (superior) se extrajo con más diclorometano (50 ml). Las soluciones de diclorometano, de color beige, se combinaron en el embudo de decantación y se extrajeron con la segunda mitad de la solución acuosa de rac-fenilpropionato (2*50 ml). Tras agitar vigorosamente y dejar sedimentar durante 10 min cada vez, la fase de DCM se secó con MgSO4 (20 g), se filtró y el disolvente se eliminó. Se añadió metanol (75 ml) y la solución resultante se llevó a sequedad en un rotavapor para eliminar el DCM residual. El material resultante se secó al vacío a 35 °C durante la noche.
[0183] El sólido de color beige claro que se aisló (14,6 g, rendimiento del 95%) se analizó por HPLC, siendo la pureza del 99,7%. El análisis elemental concordaba con la estructura prevista de GC4705, C3gH53MnN5O4 C, 65,74%; H, 7,54%; Mn, 7,57%; N, 9,76% y Cl, 60 ppm.
EJEMPLO 14
[0184] Síntesis de rac-b/s-fenilglicinato[2S,21S-dimetil(4aR,13aR,17aR,21aR)-1,2,3,4,4a,5,6,12,13,13a,14,15, 16,17,17a,18,19,20,21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,h][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II). [(rac)-b/s-Fenilglicinato(GC4401)]. GC4715.
GC4715
[0185] Se añadió GC4401 (5 g, 9,78 mmol) a 50 ml de agua desionizada en un matraz Erlenmeyer de 125 ml y se agitó vigorosamente durante 5 min, obteniéndose una solución amarillenta ligeramente turbia. A continuación, esta solución se filtró y la solución del filtrado se guardó. A un segundo matraz Erlenmeyer, se añadió fenilglicina racémica (30 g, 198,5 mmol) a 200 ml de agua desionizada para dar una solución incolora. Esta solución se trató con 7,9 g de NaOH en pelets y la mezcla se agitó vigorosamente. El pH se midió una vez todo el NaOH se había disuelto, siendo de 11,2. La solución ligeramente turbia se filtró (20-50 |j). En un matraz Erlenmeyer de 250 ml, la solución de GC4401 se combinó con la mitad (100 ml) de la solución de fenilglicinato de sodio (aproximadamente 105 mmol/10 eq.) añadiéndolas en chorro. No se separó ningún sólido y la solución resultante de color amarillo-beige se agitó durante otros 15 min, a continuación, se transfirió a un embudo de decantación de 250 ml y se extrajo con diclorometano (50 ml, tiempo de agitación de aproximadamente 1-2 min). La fase orgánica se separó y se transfirió de vuelta al embudo de decantación. Esta solución de diclorometano se retroextrajo con la solución acuosa restante de fenilglicinato de sodio (agitando durante 1-2 min cada vez). La fase de diclorometano se secó con MgSO4 durante 15 min, se filtró a través de un embudo con frita de 20-50 j y se llevó a sequedad (obteniéndose una espuma) en un rotavapor. A continuación, se añadió metanol (50 ml) al sólido amarillo y la solución se llevó a sequedad para coevaporar el diclorometano residual, obteniéndose un sólido de color amarillo claro. Este material se secó al vacío a 30 °C durante 24 h. El sólido amarillento aislado (6,5 g, rendimiento del 90% calculado a partir de GC4401) se analizó por HPLC, siendo la pureza del 99,5%. El análisis elemental concordaba con la estructura prevista de GC4715, C39H55MnNyO4 -H2O. Análisis teórico: C, 63,23%; H, 7,48%; N, 13,23% y Mn, 7,42%. Análisis experimental: C, 60,68%; H, 7,31%; Mn, 7,06%, N, 12,68% y cloro (representa el contenido de halógenos totales), 974 ppm.
EJEMPLO 15
[0186] Síntesis de rac-b/s-fenilglicinato[6R-metil(4aR,13aR,17aR,21aR)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17, 17a,18,19,20,21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,h][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II). [(rac)-b/s-2-Fenilglic¡nato (GC4444)]. GC4716.
[0187] Se añadió GC4444 (1 g, 2 mmol) a 40 ml de agua desionizada en un matraz Erlenmeyer de 125 ml y se agitó vigorosamente durante 5 min para dar una solución de color amarillo claro. A un segundo matraz Erlenmeyer de 250 ml, se añadió rac-fenilglicina (6 g, 40 mmol) a 100 ml de agua desionizada para dar una solución incolora. La solución se trató con NaOH en pelets (1,6 g) y la mezcla se agitó vigorosamente. El pH se midió una vez todo el NaOH se había disuelto, siendo de 12.
[0188] En un matraz Erlenmeyer de 250 ml, la solución de GC4444 se combinó con la mitad (50 ml) de la solución de fenilglicinato de sodio (aproximadamente 20 mmol/10 eq.). La solución resultante de color amarillo-beige se agitó vigorosamente con diclorometano (50 ml) durante 15 min y a continuación se transfirió a un embudo de decantación de 250 ml. La fase orgánica se separó y se transfirió de vuelta al embudo de decantación. La solución de diclorometano se extrajo con la solución acuosa restante de fenilglicinato de sodio (agitando durante 1-2 min cada vez). La fase de diclorometano se secó con MgSO4 durante 15 min, se filtró a través de un embudo con frita de 20-50 p y se llevó a sequedad en un rotavapor. Se añadió metanol (25 ml) al sólido residual aceitoso para dar una solución de color amarillo-beige claro que se llevó a sequedad en el rotavapor, obteniéndose un sólido amarillento. Este material se secó al vacío a 35 °C durante 24 h. El análisis elemental concordaba con la estructura prevista de GC4716, C3sH53MnN7O4 -H2O. Análisis teórico: C, 62,80%; H, 7,35%; N, 13,49%. Análisis experimental: C, 61,14%; H, 7,44%; N, 13,08.
[0189] Se aislaron 6,5 g de un polvo amarillento, lo que corresponde a un rendimiento del 90% calculado a partir de GC4444. El material se analizó por HPLC, siendo la pureza del 99%.
EJEMPLO 16
[0190] Síntesis de rac-b/s-fenilglicinato[(4aR,13aR,17aR,21aR)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18, 19,20,21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,h][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [(rac)-b/s-2-fenilglicinato(GC4403)]. GC4717.
GC4717
[0191] Se añadió GC4403 (3 g, 6,2 mmol) a 75 ml de agua desionizada en un matraz Erlenmeyer de 125 ml y se agitó vigorosamente durante 15-20 min para dar una solución de color naranja claro. En otro matraz Erlenmeyer de 250 ml, 18,76 g (124 mmol) de fenilglicina racémica se añadieron a 125 ml de agua desionizada mientras se agitaba vigorosamente. A esta solución se añadieron 4,9 g de NaOH sólido. Al agitar vigorosamente durante 10 min, se formó una solución incolora con un pH de 12. En un matraz Erlenmeyer de 500 ml, la solución de GC4403 se combinó con 75 ml de la solución de fenilglicinato de sodio racémico. La solución de color marrón claro se agitó durante otros 5 min. La solución se transfirió a un embudo de decantación de 250 ml y se extrajo con diclorometano (75 ml, aproximadamente 1-2 min de agitación). La fase orgánica se separó y se retroextrajo con la solución acuosa restante de fenilglicinato de sodio racémico. La fase de diclorometano se secó con MgSO4 durante 15 min, se filtró a través de un embudo con frita de 20-50 p y se llevó a sequedad (obteniéndose una goma) en un rotavapor. Se usó MeOH (25 ml) para coevaporar el diclorometano residual, obteniéndose un sólido de color naranja claro. Este material se secó al vacío a 37 °C durante 20 h. Se aislaron 5,42 g de un material sólido amarillento, con un rendimiento del 100% calculado a partir de GC4403. La pureza por HPLC de este material fue del 99,5%. El análisis elemental concordaba con la estructura prevista de g C4717, C37H5-iMnN7O4 -H2O. Análisis teórico: C, 62,35%; H, 7,21%; N, 13,76% y Mn, 7,71%. Análisis experimental: C, 60,72%; H, 7,26%; Mn, 7,44%, N, 13,34% y cloro (representa el contenido de halógenos totales), 364 ppm.
EJEMPLO 17
[0192] Síntesis de b/s-n-butirato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20, 21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II). [£>/s-n-Butirato(
[0193] Se añadió GC4419 (5,0 g, 10,34 mmol) a un matraz Erlenmeyer de 500 ml que contenía 100 ml de agua desionizada. La mezcla se agitó vigorosamente durante 15-20 min y a continuación se sonicó/calentó (con una pistola de aire caliente) durante 10 min para dar una solución beige y nebulosa, que a continuación se filtró para eliminar las trazas de sustancias insolubles, quedando una solución límpida. Por separado, en un matraz Erlenmeyer de 500 ml se disolvió butirato de sodio (92 g, 0,835 mmol) en 200 ml de agua desionizada. Al matraz que contenía la solución de GC4419 se añadieron 100 ml de la solución de butirato de sodio. La solución beige se agitó durante otros 5 min, a continuación, se transfirió a un embudo de decantación de 500 ml y se extrajo con DCM (75 ml). La fase orgánica se transfirió de vuelta al embudo de decantación y se retroextrajo con la solución acuosa restante de butirato de sodio (100 ml). La fase de DCM se secó con MgSO4 durante 15 min (con agitación), se filtró a través de un embudo con frita de 20-50 |j y se llevó a sequedad (formándose una espuma) en un rotavapor. Se usó metanol (50 ml) para disolver el sólido y a continuación esta solución se llevó a sequedad en el rotavapor, obteniéndose un aceite de color amarillo claro. Este material se continuó secando al vacío a 30 °C durante 48 h, obteniéndose un sólido beige (4,5 g, rendimiento del 76% calculado a partir de GC4419 como producto de partida). La pureza por HPLC fue del 99,6% (área de pico). El análisis elemental es compatible con la estructura prevista de GC4713, C29H4gMnNsO4 Análisis teórico: C, 59,37%; H, 8,42%; N, 11,94% y Mn, 9,36%. Análisis experimental: C, 59,32%; H, 8,55%; Mn, 8,80%, N, 11,94% y cloro (representa el contenido de halógenos totales), 546 ppm.
EJEMPLO 18
[0194] Síntesis de b/s-benzoato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20,21, 21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II). [£v's-Benzoato(GC4419)]: GC4712.
[0195] En un matraz Erlenmeyer de 500 ml que contenía 200 ml de agua desionizada se añadieron 10 g de GC4419 mientras se agitaba vigorosamente. La solución resultante límpida de un color beige claro se filtró para eliminar las trazas de sustancias insolubles y esta solución a continuación se añadió lentamente en chorro durante 5 min a 100 ml de una solución acuosa de benzoato de sodio (66 g, aproximadamente 458 mmol, 11 eq.). Hacia el final de la adición se separó un sólido blanco gelatinoso. Se añadió diclorometano (100 ml) a la mezcla mientras se agitaba vigorosamente, disolviéndose todo el material sólido. La mezcla resultante de dos fases a continuación se transfirió a un embudo de decantación. La fase orgánica se separó, se secó con MgSO4 (10 g), se filtró y se llevó a sequedad a presión reducida en un rotavapor. Se añadió metanol al matraz que contenía el sólido aceitoso residual y esta solución también se llevó a sequedad en el rotavapor, obteniéndose un sólido de color amarillo claro. Este material se secó al vacío a 30 °C durante 40 h, obteniéndose 7,8 g (rendimiento del 57% calculado a partir de GC4419) de un sólido amarillo-beige claro que se analizó por HPLC, siendo la pureza del 99,6%. El análisis elemental concordaba con la estructura prevista de GC4712, C35H45MnN5O4-0,5H2O. Análisis teórico: C, 63,34%; H, 6,99%; N, 10.55%; Mn, 8,28%. Análisis experimental: C, 63,07%; H, 7,38%; N, 10.54%, Mn, 8,16% y Cl en trazas (211 ppm).
Ejemplo 19
[0196] Síntesis de b/s-L-lactato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20,21, 21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,ft][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II). [b/s-L-Lactato (GC4419)]: GC4714.
GC4714
[0197] En un matraz Erlenmeyer de 500 ml que contenía 100 ml de agua desionizada se añadieron 5 g (10,34 mmol) de GC4419 mientras se agitaba vigorosamente. La solución límpida resultante de color beige claro se filtró para eliminar las trazas de sustancias insolubles y a continuación, a esta solución se añadieron lentamente 125 ml de una solución acuosa de Hactato de sodio (23,4 g) en chorro durante 5 min. La solución beige resultante se agitó durante otros 5 min, a continuación, se transfirió a un embudo de decantación de 500 ml y se extrajo con DCM (75 ml). La fase orgánica se transfirió de vuelta al embudo de decantación y se retroextrajo con la solución acuosa restante de (L)-lactato de sodio (125 ml). La fase de diclorometano se secó con MgSO4 durante 15 min (con agitación), se filtró a través de un embudo con frita de 20-50 p y se llevó a sequedad (formándose una espuma) en un rotavapor para eliminar el disolvente. A continuación, al matraz se añadió metanol (50 ml), que se usó para coevaporar el d Cm residual en el rotavapor, obteniéndose un almíbar de color beige. Este material se continuó secando al vacío a 30 °C durante 48 h, obteniéndose un sólido beige.
[0198] El sólido amorfo de color beige que se aisló se analizó por HPLC, siendo la pureza del 99,7%. El análisis elemental concordaba con la estructura prevista de GC4714, C27H45MnN5O6 'H 2O. Análisis teórico: C, 53,28%; H, 7,78%; N, 11.51%; Mn, 9,03%. Análisis experimental: C, 53,12%; H, 7,77%; N, 11,91%, Mn, 9,06% y Cl (0,87%).
Ejemplo 20
[0199] Síntesis de rac-bis-mandelato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19, 20,21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II). [rac-£vs-Mandelato(
GC4706
[0200] A un matraz Erlenmeyer de 500 ml se añadieron 200 ml de agua desionizada y 12,4 g de rac-ácido
mandélico. Tras agitar esta mezcla durante 5 min se obtuvo una solución límpida e incolora. Esta se trató con 3,2 g de NaOH en pelets y la mezcla se agitó vigorosamente. El pH se determinó una vez todo el NaOH se había disuelto. El pH, que era de 3,61, se ajustó a un pH débilmente alcalino con una solución acuosa de NaOH al 5% en peso (pH resultante = 9,67). Una solución nebulosa de 5 g de GC4419 en 100 ml de agua desionizada se filtró (20-50 |j) y se añadió en una porción a la mitad de la solución acuosa de sal de sodio cuyo pH se había ajustado. El material blanco pegajoso que precipitó se agitó durante otros 5 min y se colocó en un frigorífico a 2-8 °C durante la noche. A la mañana siguiente, la suspensión se transfirió a un embudo de decantación de 250 ml y el matraz Erlenmeyer se aclaró con 100 ml de diclorometano; la suspensión y el aclarado de diclorometano se combinaron en el embudo de decantación. La fase de diclorometano adoptó inmediatamente un color amarillo-beige claro. Las fases se separaron y la fase de diclorometano se extrajo con la segunda mitad de solución acuosa de mandelato de sodio. Tras agitar vigorosamente y dejar sedimentar durante 10 min, la fase de diclorometano se secó con MgSO4 (10 g), se filtró y el disolvente se eliminó. Se añadió metanol (50 ml) y la solución amarilla se evaporó con el fin de codestilar el diclorometano residual en el rotavapor. La espuma resultante se secó al vacío a 30 °C durante la noche. El polvo blanquecino que se aisló (6,7 g, rendimiento del 91%) se analizó por HPLC, siendo la pureza del 99,5%.
[0201] El análisis elemental concordaba con la estructura prevista de GC4706, con los siguientes resultados: C, 61,64%; H, 7,04%; Mn, 7,16%; N, 9,30% y Cl, 66 ppm (0,0066%). Valores de delta (A) correspondientes a las especies con 0,333 (1/3) moléculas de agua: C, 0,52%; H, 0,04%; Mn, 0,07%; N, 0,08% y Cl, 0%.
EJEMPLO 21
[0202] Síntesis de b/s-L-valinato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20, 21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo[b,fr][1,4,7,10]tetraazaciclo-heptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [b/s-(L)-valinato (GC4419)]: g C4746.
[0203] Se añadió GC4419 (3,0 g, 6,2 mmol) a un matraz Erlenmeyer de 250 ml que contenía 100 ml de agua desionizada. La mezcla se agitó vigorosamente durante 15-20 min para dar una solución de un color amarronado claro. En un matraz aparte se preparó una solución acuosa de L-(+)-valina (58,6 g, 0,5 mol) y NaOH (20 g, 0,5 mol) en 200 ml de agua desionizada. El pH de esta solución era de 11,7. En un matraz Erlenmeyer de 500 ml, la solución de GC4419 se combinó con la mitad de la solución de valinato de sodio. La solución resultante se agitó durante otros 5 min, se transfirió a un embudo de decantación de 0,5 l y se extrajo con 100 ml de diclorometano. La fase orgánica se separó, se transfirió de vuelta a un embudo de decantación y se retroextrajo con la solución acuosa restante de valinato de sodio. La fase de diclorometano se separó y el disolvente se eliminó en un rotavapor. El diclorometano residual se coevaporó con MeOH (50 ml), obteniéndose un sólido de color marrón claro. Este material se secó al vacío a 40 °C durante 20 h.
[0204] Se obtuvieron 3,4 g del sólido gris claro aislado, lo que corresponde a un rendimiento del 83% calculado a partir de GC4419. La pureza por HPLC fue del 99,6%. El análisis elemental mostró un 0,67% de cloro residual, expresado en contenido de halógenos totales, y concordaba con la estructura de GC4746 0,5H2O. Análisis teórico: C, 56,87%; H, 8,77%; Mn, 8,39%; y N, 14,97%. Análisis experimental: C, 57,22%; H, 8,70%; Mn, 7,88%; N, 14,12% y Cl (representa el contenido de halógenos totales), 0,67%.
EJEMPLO 22
[0205] Síntesis de b/s-propionato[6R-metN(4aR,13aR,17aR,21aR)-1,2,3,4,4a,5,6,12,13,13a,H15,16,17,17a, 18,19,20,21,21a-e¡cosah¡dro-l1,7-mtrilo-7H-d¡benzo[b,fr][1,4,7,10]tetraazacidoheptadedno-KN5, kN13, kN18, kN21, kN22] de manganeso (II). [b/s-Propionato(GC4444)]: GC4747.
[0206] Se añadió GC4444 (1,6 g, 3,2 mmol) a un matraz Erlenmeyer de 125 ml que contenía 50 ml de agua desionizada. La mezcla se agitó vigorosamente durante 15-20 min para dar una solución de un color amarillo claro. En un matraz aparte se preparó una solución acuosa de 6,15 g de propionato de sodio en 100 ml de agua desionizada. En un matraz Erlenmeyer de 250 ml, la solución de GC4444 se combinó con la solución de propionato de sodio. La solución resultante se agitó durante 15 min, se transfirió a un embudo de decantación de 0,25 l y se extrajo con 50 ml de diclorometano. La fase orgánica se separó y el disolvente se eliminó en un rotavapor. El diclorometano residual se coevaporó con MeOH (25 ml), obteniéndose un sólido de color marrón claro. Este material se secó al vacío a 40 °C durante 24 h.
[0207] Se obtuvieron 1,1 g del sólido beige claro aislado, lo que corresponde a un rendimiento del 60% calculado a partir de GC4444. La pureza por HPLC fue del 99,5%. El análisis elemental mostró un 1,44% de cloro residual, expresado en contenido de halógenos totales, y concordaba con la estructura de GC4747 0,5H2O. Análisis teórico: C, 57,82%; H, 8,32%; Mn, 9,45%; y N, 12,04%. Análisis experimental: C, 58,19%; H, 8,50%; Mn, 9,39%; N, 12,36% y Cl (representa el contenido de halógenos totales), 1,44%.
EJEMPLO 23
[0208] Síntesis de b/s-propionato[(4aR,13aR,17aR,21aR)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20, 21,21a-e¡cosah¡dro-11,7-n¡tr¡lo-7H-d¡benzo[b,h][1,4,7,10]tetraazac¡doheptadec¡no-KN5, kN13, kN18, kN21, kN22] de manganeso (II). [b/s-Propionato(GC4403)]: GC4748.
MW 558,63
GC4748
[0209] Se añadió GC4403 (3,0 g, 6,2 mmol) a un matraz Erlenmeyer de 250 ml que contenía 75 ml de agua desionizada. La mezcla se agitó vigorosamente durante 15-20 min para dar una solución de un color amarronado claro. En un matraz aparte se preparó una solución acuosa de 23,8 g de propionato de sodio en 75 ml de agua desionizada. En un matraz Erlenmeyer de 500 ml, la solución de GC4403 se combinó con 40 ml de la solución de propionato de sodio. La solución resultante se agitó durante otros 5 min, se transfirió a un embudo de decantación de 0,5 l y se extrajo con 50 ml de diclorometano. La fase orgánica se separó, se transfirió de vuelta al embudo de decantación y se retroextrajo con la solución acuosa restante de propionato de sodio (35 ml). La fase de diclorometano se separó y el disolvente se eliminó en un rotavapor. El diclorometano residual se coevaporó con MeOH (25 ml), obteniéndose un sólido de color marrón claro. Este material se secó al vacío a 40 °C durante el fin de semana.
[0210] Se obtuvieron 2,7 g del sólido marrón claro aislado, lo que corresponde a un rendimiento del 78% calculado a partir de GC4403. La pureza por HPLC fue del 97,3% (1,2% de la monoamina GC4520). El análisis elemental mostró un 0,356% de cloro residual, expresado en contenido de halógenos totales, y concordaba con la estructura de GC4748. Análisis teórico: C, 58,05%; H, 8,12%; Mn, 9,83%; y N, 12,54%. Análisis experimental: C, 58,00%; H, 8,45%; Mn, 9,57%; N, 12,53% y Cl (representa el contenido de halógenos totales), 0,356%.
EJEMPLO 24
[0211] Síntesis de b/s-piruvato[(4aS,13aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20,21,21aeicosahidro-11,7-nitrilo-7H-dbenzo[b,h][1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II), [b/s-piruvato(GC4419)]: GC4749.
[0212] En un matraz Erlenmeyer de 500 ml, se añadieron 150 ml de agua desionizada a GC4419 (FW, 483,38, 5 g, 10,34 mmol) y se agitó vigorosamente durante 15-20 min para disolver. En un segundo Erlenmeyer, se añadió ácido pirúvico (72,83 g, 0,827 mmol) a 400 ml de agua desionizada. Mientras se agitaba la suspensión, se añadió NaOH (33,2 g, 0,83 mol) y se continuó agitando hasta que se formó una solución incolora y límpida. El pH de esta solución era de aproximadamente 12. En un matraz Erlenmeyer de 500 ml, la solución de GC4419 se combinó con la mitad de la solución de piruvato de sodio. No se separó ningún sólido y la mezcla beige se agitó durante otros 5 min. La solución de color amarillo-beige claro se transfirió a un embudo de decantación de 1 l y se extrajo con DCM (100 ml) agitando de 1 a 2 min cada vez. La solución acuosa tenía un color violeta rosáceo. La fase de DCM se retroextrajo con la solución acuosa restante de piruvato de sodio. La fase de DCM se secó con MgSO4 durante 15 min (con agitación), se filtró a través de un embudo con frita de 20-50 p y a continuación se llevó a sequedad en un rotavapor. A continuación, se puede usar MeOH (50 ml) para coevaporar el DCM residual y obtener un sólido. Este material se puede secar al vacío a 30 °C durante al menos 20 h. El sólido se puede caracterizar mediante análisis elemental, MS y HPLC.
EJEMPLO 25
[0213] Síntesis de b/s-L-alaninato[(4aS,13aS,17aS,21aS)-1,2,3,4,4a,5,6,12,13,13a,14,15,16,17,17a,18,19,20, 21,21a-eicosahidro-11,7-nitrilo-7H-dibenzo [b, h] [1,4,7,10]tetraazacicloheptadecino-KN5, kN13, kN18, kN21, kN22] de manganeso (II). [bis-L-Alaninato(GC4419)]: Gc 4750
[0214] En un matraz Erlenmeyer de 500 ml, se añadieron 150 ml de agua desionizada a GC4419 (FW, 483,38, 5 g. 10,34 mmol) y se agitó vigorosamente durante 15-20 min para disolver. En un segundo Erlenmeyer, se añadió L-(+)-alanina (73,7 g, 0,827 mol) a 400 ml de agua desionizada. Mientras se agitaba la suspensión, se añadió NaOH (33,2 g, 0,83 mol) y se continuó agitando hasta formar una solución incolora y límpida. El pH de esta solución era de 12,1. En un matraz Erlenmeyer de 500 ml, la solución de GC4419 se combinó con la mitad de la solución de alaninato de sodio. No se separó ningún sólido y la mezcla beige se agitó durante otros 5 min. La solución de color amarillobeige claro se transfirió a un embudo de decantación de 1 l y se extrajo con DCM (100 ml) agitando de 1 a 2 min cada vez. La solución acuosa tenía un color violeta rosáceo. La fase de DCM se retroextrajo con la solución acuosa restante de alaninato de sodio. La fase de DCM se secó con MgSO4 durante 15 min (con agitación), se filtró a través de un embudo con frita de 20-50 p y a continuación se llevó a sequedad en un rotavapor. Se puede usar MeOH (50 ml) para coevaporar el DCM residual y obtener un sólido. Este material se puede secar al vacío a 30 °C durante al menos 20 h. El sólido se puede caracterizar mediante análisis elemental, MS y HPLC.
Resultados
[0215] En el Cuadro I de abajo se resumen los datos de biodisponibilidad obtenidos tras la administración por vía i. d. a cerdos enanos de diversas formulaciones puras oleosas con diversos derivados con ligandos axiales de diversos complejos macrocíclicos pentaaza de Mn (II). En cada ejemplo, la concentración del artículo farmacológico ensayado era de un 10% en peso de la formulación total.
Cuadro I
[0216] En los siguientes ejemplos se muestran representaciones de las concentraciones plasmáticas del complejo macrocíclico pentaaza de Mn (II) precursor tras la administración por vía intraduodenal (i.d.) o por vía i.v. de diversos artículos derivados ensayados frente al tiempo tras la administración de los artículos ensayados. Estos ejemplos se seleccionan de entre los ejemplos que figuran en el Cuadro I (más arriba). En todos los ejemplos el porcentaje de biodisponibilidad se obtiene comparando las concentraciones plasmáticas del artículo farmacológico ensayado obtenidas con la administración por vía i.d. a los mismos cerdos a los que se practicó la administración por vía i.v. con el fin de calcular el valor de AUC correspondiente a una biodisponibilidad del 100%.
[0217] En la Figura 1 se muestran las representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados por vía i.v. o por vía i.d. Se considera que la concentración de GC4419 en la sangre tras la administración por vía i.v. de una dosis de 1 mg/kg de peso corporal (mpk) equivale a una biodisponibilidad del 100% y la concentración plasmática tras la administración por vía i.v. de una formulación acuosa de GC4419 también se muestra. En este ejemplo, la administración por vía intraduodenal de una dosis de 10 mg/kg de formulaciones con un 10% en peso de 1) el derivado de b/'s-L-fenilglicina de GC4419 (GC4702), 2) el derivado de b/'s-L-fenilalanina de GC4419 (GC4704) y 3) el derivado de rac-b/'s-fenilglicina de GC4419 (GC4720) formulados en Capmul MCM se compara con la administración por vía i.v. del propio GC4419 a una dosis de 1 mg/kg.
[0218] En la Figura 2 se muestran las representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados formulados en Peceol para administración por vía i.d. Se considera que la concentración del fármaco precursor (en este caso GC4419) en la sangre tras la administración por vía i.v. de una dosis de 1 mg/kg de peso corporal (mpk) equivale a una biodisponibilidad del 100% y la concentración plasmática tras la administración por vía i.v. de una formulación acuosa de GC4419 también se muestra. En este ejemplo, la administración por vía intraduodenal de una dosis de 10 mg/kg de formulaciones con un 10% en peso de 1) g C4419, 2) el derivado de b/s-acetato de GC4419 (GC4701), 3) el derivado de b/s-fenilglioxilato de GC4419 (GC4719) y 4) el derivado rac-b/s-2-fenilpropionato de GC4419 (GC4705) formulados en Peceol se compara con la administración por vía i.v. del propio GC4419.
[0219] En la Figura 3 se muestran las representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados formulados en Labrafil M2125 CS para administración por vía i.d. Se considera que la concentración del fármaco precursor (en este caso GC4419) en la sangre tras la administración por vía i.v. de una dosis de 1 mg/kg de peso corporal (mpk) equivale a una biodisponibilidad del 100% y la concentración plasmática tras la administración por vía i.v. de una formulación acuosa de GC4419 también se muestra. En esta figura, la administración por vía intraduodenal de una dosis de 10 mg/kg de formulaciones con un 10% en peso de 1) GC4419, 2) el derivado de b/s-acetato de GC4419 (GC4701) y 3) el derivado de b/s-octanoato de GC4419 (GC4710) formulados en M2125 CS se compara con la administración por vía i.v. del propio GC4419 en el mismo conjunto de cerdos.
[0220] En la Figura 4 se muestran las representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos
axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados formulados en Labrafil M2125 CS para administración por vía i.d. Se considera que la concentración del fármaco precursor (en este caso GC4419) en la sangre tras la administración por vía i.v. de una dosis de 1 mg/kg de peso corporal (mpk) equivale a una biodisponibilidad del 100% y la concentración plasmática tras la administración por vía i.v. de una formulación acuosa de GC4419 también se muestra. En este ejemplo, la administración por vía intraduodenal de una dosis de 10 mg/kg de formulaciones con un 10% en peso de 1) el derivado de bis-pivaloato de GC4419 (GC4709), 2) el derivado de bis-propionato de GC4419 (GC4711) y 3) el derivado de bis-butirato de GC4419 (GC4713) formulados en Labrafil M2125 CS se compara con la administración por vía i.v. del propio GC4419 en el mismo conjunto de cerdos.
[0221] En la Figura 5 se muestran las representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4401 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados formulados en Capmul MCM para administración por vía i.d. Se considera que la concentración del fármaco precursor (en este caso GC4401) en la sangre tras la administración por vía i.v. de una dosis de 1 mg/kg de peso corporal (mpk) equivale a una biodisponibilidad del 100% y la concentración plasmática tras la administración por vía i.v. de una formulación acuosa de GC4401 también se muestra. En este ejemplo, la administración por vía intraduodenal de una dosis de 10 mg/kg de formulaciones con un 10% en peso de 1) GC4401 y 2) el derivado de rac-bis-fenilglicina de GC4401 (GC4715) formulados en Capmul MCM se compara con la administración por vía i.v. del propio GC4401 en el mismo conjunto de cerdos.
[0222] En la Figura 6 se muestran las representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4444 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados formulados en Capmul MCM para administración por vía i.d. Se considera que la concentración del fármaco precursor (en este caso GC4444) en la sangre tras la administración por vía i.v. de una dosis de 1 mg/kg de peso corporal (mpk) equivale a una biodisponibilidad del 100% y la concentración plasmática tras la administración por vía i.v. de una formulación acuosa de GC4444 también se muestra. En este ejemplo, la administración por vía intraduodenal de una dosis de 10 mg/kg de formulaciones con un 10% en peso de 1) GC4444 y 2) el derivado de rac-b/'s-fenilglicina de GC4444 (GC4716) formulados en Capmul MCM se compara con la administración por vía i.v. del propio GC4444 en el mismo conjunto de cerdos.
[0223] En la Figura 7 se muestran las representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados formulados en Capmul MCM para administración por vía i.d. Se considera que la concentración del fármaco precursor (en este caso GC4419) en la sangre tras la administración por vía i.v. de una dosis de 1 mg/kg de peso corporal (mpk) equivale a una biodisponibilidad del 100% y la concentración plasmática tras la administración por vía i.v. de una formulación acuosa de GC4419 también se muestra. En este ejemplo, la administración por vía intraduodenal de una dosis de 10 mg/kg de formulaciones del 10% en peso de 1) GC4419, 2) el derivado de bis-acetato de GC4419 (GC4701) y 3) el derivado de rac-bis-mandelato de GC4419 (GC4706) formulados en Capmul MCM se compara con la administración por vía i.v. del propio GC4419 en el mismo conjunto de cerdos.
[0224] En la Figura 8 se muestran las representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4419 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de los artículos farmacológicos ensayados formulados en Maisine 35-1 para administración por vía i.d. Se considera que la concentración del fármaco precursor (en este caso GC4419) en la sangre tras la administración por vía i.v. de una dosis de 1 mg/kg de peso corporal (mpk) equivale a una biodisponibilidad del 100% y la concentración plasmática tras la administración por vía i.v. de una formulación acuosa de GC4419 también se muestra. En este ejemplo, la administración por vía intraduodenal de una dosis de 10 mg/kg de formulaciones del 10% en peso de 1) GC4419, 2) el derivado de bis-fenilacetato de GC4419 (GC4718) y 3) el derivado de bis-acetato de GC4419 (GC4701) formulados en Maisine 35-1 se compara con la administración por vía i.v. del propio GC4419 en el mismo conjunto de cerdos.
[0225] En la Figura 9 se muestran las representaciones del perfil de concentraciones plasmáticas del complejo macrocíclico pentaaza de manganeso precursor de GC4403 (independientemente de la composición de los ligandos axiales) en el plasma de cerdos enanos a partir de muestras de sangre obtenidas en puntos temporales de hasta 24 h tras la administración de rac-bis-fenilglicinato-GC4403 para administración por vía i.d. Se considera que la concentración del fármaco precursor (en este caso GC4403) en la sangre tras la administración por vía i.v. de una dosis de 1 mg/kg de peso corporal (mpk) equivale a una biodisponibilidad del 100% y la concentración plasmática tras la administración por vía i.v. de una formulación acuosa de GC4403 también se muestra. En este ejemplo, la administración por vía intraduodenal de una dosis de 10 mg/kg de una formulación con un 10% en peso del derivado de rac-bis-fenilglicina de GC4403 (GC4717) en una suspensión en Capmul MCM se compara con la administración por vía i.v. del propio GC4403 en el mismo conjunto de cerdos.
[0226] En los ejemplos citados más arriba se demuestra que los ligandos axiales enlazados al ion Mn (II) pueden ejercer un efecto muy profundo y previamente impredecible en la capacidad de estos complejos de penetrar el tubo GI y pasar a estar biodisponibles por vía oral. Hemos descubierto que existe un subconjunto estructural bastante estrecho de ligandos que pueden aportar una absorción gastrointestinal (GI) mucho mayor y, por lo tanto, una biodisponibilidad oral mucho mayor. En este subconjunto de estructuras con ligandos axiales que proporcionan una mayor biodisponibilidad oral se incluyen las que se muestran en la Figura 10.
[0227] Existen varias características estructurales importantes que afectan a la biodisponibilidad. En primer lugar, se analizó un amplio abanico de estructuras de ácidos carboxílicos alquílicos para determinar su biodisponibilidad oral en diversos aceites y se observó que no son igual de eficaces en aportar una elevada biodisponibilidad oral. De hecho, el ligando propionato (y el ligando relacionado lactato, un ligando de propionato en el que e1H se ha sustituido con un OH, y probablemente otros ligandos basados en el ligando propionato) aporta una biodisponibilidad mucho más elevada que cualquiera de los otros ligandos de carboxilato; como la cadena con un átomo menos de carbono, el acetato o los ligandos de carboxilato con una cadena más larga, como butirato u octanoato. En segundo lugar, hay una clase única de ligandos axiales que se derivan del ácido fenilacético; es decir, el ligando fenilacetato. Estos derivados se muestran en la Fig. 10. Todos los complejos que se derivan de esta clase de ligandos de fenilacetato poseen una biodisponibilidad mucho mayor en comparación con el complejo precursor de dicloro o los otros complejos de alquilcarboxilato, incluidos los complejos de acetato u otros complejos derivados con ligandos carboxilato con un peso molecular más elevado. En tercer lugar, uno de estos derivados está basado en el aminoácido fenilglicina. El ligando de fenilglicinato racémico aumenta la biodisponibilidad con todos los diversos ligandos pentaazamacrocíclicos ensayados, lo que demuestra que no se trata de un efecto aislado con el complejo macrocíclico pentaaza de manganeso precursor de GC4419, sino que se aplica a toda esta familia de complejos de Mn (II). Asimismo, el derivado de ^-fenilglicinato de GC4419, GC4702, en realidad se absorbe mucho mejor que otros ligandos aminoacídicos, como los complejos con L-fenilalaninato o L-valininato, o el complejo con rac-fenilglicinato, GC4720. Además, esta propiedad con una mayor biodisponibilidad puede estar restringida a los derivados con ligandos de fenilglicinato (una vez más un derivado del ácido fenilacético) según está ejemplificado por la sumamente escasa biodisponibilidad de los complejos derivados del congénere de L-fenilalanina o el congénere de L-valina, aunque es posible que otros ligandos aminoacídicos, en particular el congénere de L-alanina que pertenece a la clase de ligandos de propionato descritos más arriba, también pueda proporcionar una buena biodisponibilidad.
REFERENCIAS
[0228]
1. Suenderhauf, C., Parrott, N.; "A Physiologically Based Pharmacokinetic Model of the Minipig: Data Compilation and Model Implementation", Pharm. Res., 30(1), 1-15 (2013).
2. Salvemini, D., Wang, Z-Q., Zweier, J.L., Samouilov, A., Macarthur, H., Misko, T.P., Currue, M.G., Cuzzocrea, S., Sikorski, J.A., Riley, D.P., "A Nonpeptidyl Mimic of Superoxide Dismutase with Therapeutic Activity in Rats", Science, 286, Oct. 8, 304-6 (1999).
3. Patente de EE. UU. n.° 8.263.568.
4. Patente de EE. UU. n.° 8.444.856.
5. Aston, K., Rath, N., Naik, A., Slomczynska, U., Schall, O.F., Riley, D.P., "Computer-Aided Design (CAD) of Mn (II) Complexes: Superoxide Dismutase Mimetics with Catalytic Activity Exceeding the Native Enzyme", Inorg. Chem., 40, 1779-89 (2001).
Claims (12)
2. Una composición farmacéutica que comprende un complejo macrocíclico pentaaza según la reivindicación 1 y un excipiente farmacéuticamente aceptable adecuado para la administración.
3. La composición farmacéutica según la reivindicación 2, en donde la composición farmacéutica es adecuada para administración por vía oral a un sujeto humano.
4. La composición farmacéutica según cualquiera de las reivindicaciones 2 y 3, que comprende al menos uno de un tensioactivo lipofílico y un aceite.
5. La composición farmacéutica según la reivindicación 4, en donde al menos uno del tensioactivo lipofílico y el aceite comprende al menos uno de mono- y/o di-glicéridos de ácidos grasos, ésteres del ácido acético, succínico, láctico, cítrico y/o tartárico y mono- y/o di-glicéridos de ácidos grasos, mono- y/o di-ésteres de propilenglicol y ácidos grasos, ésteres de poliglicerol y ácidos grasos, etoxilados de aceite de ricino, etoxilados de ácidos y ésteres formados mediante reacción del óxido de etileno con ácidos grasos o ésteres de ácidos grasos y glicerol, ésteres de sorbitano de ácidos grasos, productos de transesterificación de un triglicérido de aceites vegetales hidrogenados o naturales y un poliol polialquilénico, etoxilados de alcohol y copolímeros de polioxietileno-polioxipropileno.
6. La composición farmacéutica según la reivindicación 5, en donde al menos uno del tensioactivo lipofílico y el aceite comprende al menos uno de una mezcla de 93 mono/diglicéridos de ácidos caprílico/cáprico, una mezcla de triglicéridos de ácidos caprílico/cáprico, glicéridos de linoleoílo polioxilados 6 (NF), glicéridos de oleoílo polioxilados 6 (NF), monooleato de glicerilo (NF), monolinoleato de glicerilo (NF) (monoglicérido) y glicéridos de caprilocaproílo polioxilados 8 (NF).
7. La composición farmacéutica según cualquiera de las reivindicaciones 2 a 6, en donde la composición farmacéutica está en forma farmacéutica sólida o semisólida.
8. La composición farmacéutica según cualquiera de las reivindicaciones 2 a 6, en donde la composición farmacéutica está en forma de comprimidos, cápsulas de gelatina, gel o suspensión adecuados para administración por vía oral.
9. La composición farmacéutica según cualquiera de las reivindicaciones 2 a 8, en donde la composición farmacéutica comprende una capa de recubrimiento entérico.
10. La composición farmacéutica según cualquiera de las reivindicaciones 2 a 9, en donde la composición está en forma de una forma farmacéutica por vía oral que comprende hidroxipropilmetilcelulosa (HPMC).
11. Una composición farmacéutica según cualquiera de las reivindicaciones 2 a 10 para uso en un método para administrar a un sujeto un complejo macrocíclico pentaaza, comprendiendo el método la administración de una composición de cualquiera de las reivindicaciones 2 a 10 a un sujeto humano.
12. El complejo o composición de cualquiera de las reivindicaciones precedentes para uso en un método para la prevención y el tratamiento del daño tisular, opcionalmente en donde dicho daño tisular se ha producido por un tratamiento anticancerígeno u otra exposición a radiación.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562203761P | 2015-08-11 | 2015-08-11 | |
| PCT/US2016/046599 WO2017027728A1 (en) | 2015-08-11 | 2016-08-11 | Pentaaza macrocyclic ring complexes possessing oral bioavailability |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2807528T3 true ES2807528T3 (es) | 2021-02-23 |
Family
ID=57984526
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16835928T Active ES2807528T3 (es) | 2015-08-11 | 2016-08-11 | Complejos macrocíclicos pentaaza que poseen biodisponibilidad oral |
Country Status (29)
| Country | Link |
|---|---|
| US (5) | US10597415B2 (es) |
| EP (2) | EP3334744B1 (es) |
| JP (3) | JP7041959B2 (es) |
| KR (1) | KR20180064380A (es) |
| CN (3) | CN113416170A (es) |
| AU (3) | AU2016306568B2 (es) |
| CA (1) | CA2994845A1 (es) |
| CL (1) | CL2018000371A1 (es) |
| CO (1) | CO2018002544A2 (es) |
| CY (1) | CY1123960T1 (es) |
| DK (1) | DK3334744T3 (es) |
| EA (1) | EA201890471A1 (es) |
| ES (1) | ES2807528T3 (es) |
| HK (1) | HK1257313A1 (es) |
| HR (1) | HRP20201092T1 (es) |
| HU (1) | HUE049926T2 (es) |
| IL (3) | IL297735B1 (es) |
| LT (1) | LT3334744T (es) |
| MX (2) | MX2018001605A (es) |
| MY (1) | MY196401A (es) |
| PH (1) | PH12018500296A1 (es) |
| PL (1) | PL3334744T3 (es) |
| PT (1) | PT3334744T (es) |
| RS (1) | RS60558B1 (es) |
| SG (1) | SG10202002859QA (es) |
| SI (1) | SI3334744T1 (es) |
| UA (1) | UA126788C2 (es) |
| WO (1) | WO2017027728A1 (es) |
| ZA (2) | ZA201801546B (es) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2056675B1 (en) | 2006-10-12 | 2019-01-09 | Galera Labs, LLC | Methods of treating oral mucositis |
| JP6267638B2 (ja) | 2011-09-26 | 2018-01-24 | ガレラ・ラブス・リミテッド・ライアビリティ・カンパニーGalera Labs, Llc | 疾患の治療方法 |
| SG10202002859QA (en) | 2015-08-11 | 2020-05-28 | Galera Labs Llc | Pentaaza macrocyclic ring complexes possessing oral bioavailability |
| CN109906081A (zh) | 2016-09-01 | 2019-06-18 | 加莱拉实验室有限责任公司 | 利用五氮杂大环络合物和抗坏血酸类化合物的联合癌症疗法 |
| AU2018221043A1 (en) | 2017-02-15 | 2019-09-12 | Galera Labs, Llc | Pentaaza macrocyclic ring complexes for local intestinal delivery |
| IL269915B (en) | 2017-04-13 | 2022-09-01 | Galera Labs Llc | Cancer immunotherapy combined with a macrocyclic ring pentase complex |
| IL305082A (en) * | 2017-04-13 | 2023-10-01 | Galera Labs Llc | Cancer immunotherapy combined with a macrocyclic ring pentase complex |
| JP2022551494A (ja) * | 2019-10-10 | 2022-12-09 | ガレラ・ラブス・リミテッド・ライアビリティ・カンパニー | マンガン含有配位錯体の水性製剤の製造方法、製剤および処置方法 |
Family Cites Families (55)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4001212A (en) | 1973-10-03 | 1977-01-04 | E. I. Du Pont De Nemours And Company | Macrocyclic polyamines |
| US3930867A (en) | 1974-01-07 | 1976-01-06 | E. I. Du Pont De Nemours And Company | Macrocyclic polyamines as sensitizers for silver halide emulsions |
| JPS61226751A (ja) | 1985-03-30 | 1986-10-08 | Konishiroku Photo Ind Co Ltd | ハロゲン化銀写真感光材料用処理液及びその処理方法 |
| US5096724A (en) | 1988-06-03 | 1992-03-17 | Aquanautics Corporation | Methods, compositions, and systems for ligand extraction |
| GB9001245D0 (en) | 1990-01-19 | 1990-03-21 | Salutar Inc | Compounds |
| KR0145953B1 (ko) | 1991-07-19 | 1998-08-17 | 제임스 클리프튼 보올딩 | 슈퍼옥사이드의 불균화촉매로서 효과적인 질소를 포함하는 마크로사이클 릭리간드의 망간착물 |
| CA2072934C (en) * | 1991-07-19 | 2007-08-28 | Karl William Aston | Manganese complexes of nitrogen-containing macrocyclic ligands effective as catalysts for dismutating superoxide |
| US6204259B1 (en) | 1993-01-14 | 2001-03-20 | Monsanto Company | Manganese complexes of nitrogen-containing macrocyclic ligands effective as catalysts for dismutating superoxide |
| EP0756495A1 (en) | 1994-04-22 | 1997-02-05 | Monsanto Company | Diagnostic image analysis with metal complexes |
| US6245758B1 (en) | 1994-05-13 | 2001-06-12 | Michael K. Stern | Methods of use for peroxynitrite decomposition catalysts, pharmaceutical compositions therefor |
| US6525041B1 (en) | 1995-06-06 | 2003-02-25 | Pharmacia Corporation | Manganese or iron complexes of nitrogen-containing macrocyclic ligands effective as catalysts for dismutating superoxide |
| BR9610241A (pt) | 1995-08-17 | 1999-06-29 | Monsanto Co | Processos para análise de imagem de diagnóstico utilizando bioconjgados de complexos de metal de ligandos macrocíclicos contendo nitrogênio |
| US5976498A (en) | 1995-08-17 | 1999-11-02 | Neumann; William L. | Methods of diagnostic image analysis using metal complexes of nitrogen-containing macrocyclic ligands |
| US20060270639A1 (en) | 1997-06-20 | 2006-11-30 | Daniela Salvemini | Combinations of superoxide dismutase mimetics and nonsteroidal analgesic/anti-inflammatory drugs |
| US6180620B1 (en) | 1997-06-20 | 2001-01-30 | G.D. Searle & Co. | Analgesic methods using synthetic catalysts for the dismutation of superoxide radicals |
| US6214817B1 (en) | 1997-06-20 | 2001-04-10 | Monsanto Company | Substituted pyridino pentaazamacrocyle complexes having superoxide dismutase activity |
| US20020128248A1 (en) | 1997-06-20 | 2002-09-12 | Metaphore Pharmaceuticals, Inc | SODm therapy for prevention and/or treatment of inflammatory disease |
| US20050171198A1 (en) | 1997-06-20 | 2005-08-04 | Metaphore Pharmaceuticals, Inc. | SODm therapy for treatment, prevention, inhibition and reversal of inflammatory disease |
| EP1045851B1 (en) | 1997-11-03 | 2003-04-23 | Duke University | Substituted porphyrins |
| GB9817845D0 (en) | 1998-08-17 | 1998-10-14 | Glaxo Group Ltd | Chemical compounds |
| US6040330A (en) | 1999-01-08 | 2000-03-21 | Bionumerik Pharmaceuticals, Inc. | Pharmaceutical formulations of taxanes |
| EP1185312B1 (en) | 1999-05-27 | 2005-03-23 | Monsanto Company | Biomaterials modified with superoxide dismutase mimics |
| US6448239B1 (en) | 1999-06-03 | 2002-09-10 | Trustees Of Princeton University | Peroxynitrite decomposition catalysts and methods of use thereof |
| AU3679801A (en) | 2000-02-08 | 2001-08-20 | Rice University | Optically-active nanoparticles for use in therapeutic and diagnostic methods |
| US7279160B2 (en) | 2000-05-02 | 2007-10-09 | The Uab Research Foundation | Combinations of DR5 antibodies and other therapeutic agents |
| US20020072512A1 (en) | 2000-12-08 | 2002-06-13 | Metaphore Pharmaceuticals, Inc | Method of preventing and treating HIV-mediated central nervous system damage |
| US20050175580A1 (en) | 2001-01-05 | 2005-08-11 | Daniela Salvemini | Compositions and methods for enhancing cytokine activity and treating hypotension associated with the administration of cytokines |
| DE60233317D1 (de) | 2001-01-19 | 2009-09-24 | Nat Jewish Med & Res Center | Medikament zum schutz in der radiotherapie |
| WO2002058686A2 (en) | 2001-01-26 | 2002-08-01 | Metaphore Pharmaceuticals, Inc. | Method of treatment of neurodegenerative disorders using pentaaza-macrocyclic ligand complexes |
| US20040137638A1 (en) | 2002-03-04 | 2004-07-15 | Slomczynska Urszula J. | Chromatography of metal complexes |
| WO2002071054A1 (en) * | 2001-03-02 | 2002-09-12 | Metaphore Pharmaceuticals, Inc. | Chromatography of metal complexes |
| WO2002100395A1 (en) | 2001-06-08 | 2002-12-19 | Genzyme Corporation | Bismuth salts of anti-oxidants and radical scavengers for prevention and treatment of mucous membrane ulcers |
| US20040132706A1 (en) | 2001-10-05 | 2004-07-08 | Daniela Salvemini | Composition comprising a catalyst for the dismutation of superoxide and use of the composition for preventing and treating hypotension |
| BRPI0213846B8 (pt) | 2001-11-01 | 2021-05-25 | Uab Research Foundation | composição que compreende um anticorpo que liga especificamente uma dr5 do receptor de trail e um ou mais agentes terapêuticos |
| JP2005530738A (ja) | 2002-04-16 | 2005-10-13 | アイシス・イノヴェイション・リミテッド | 組織障害の予防及び/又は治療のためのクルクミン |
| US20050101581A1 (en) | 2002-08-28 | 2005-05-12 | Reading Christopher L. | Therapeutic treatment methods 2 |
| WO2005042718A2 (en) | 2003-10-31 | 2005-05-12 | Metaphore Pharmaceuticals, Inc. | Compositions and methods for treating, preventing, reversing and inhibiting pain |
| WO2005070126A2 (en) | 2004-01-08 | 2005-08-04 | The Regents Of The University Of Colorado | Methods and compositions for treating human diseases and wounds with ucp and fas inhibitors |
| GB0412893D0 (en) * | 2004-06-10 | 2004-07-14 | Univ Hull | Novel antiviral macrocycle derivatives and metal complexes, incorporating bridged macrocycles |
| US8217166B2 (en) | 2005-05-05 | 2012-07-10 | Galera Therapeutics, Llc | Polyethylene glycolated superoxide dismutase mimetics |
| WO2006083508A2 (en) | 2005-01-10 | 2006-08-10 | Metaphore Pharmaceuticals Inc. | Combinations of superoxide dismutase mimetics and nonsteroidal analgesic/anti-inflammatory drugs |
| WO2006078713A2 (en) | 2005-01-19 | 2006-07-27 | Metaphore Pharmaceuticals, Inc. | Methotrexate combinations for treating inflammatory diseases |
| CA2601575A1 (en) | 2005-03-31 | 2006-10-05 | Schering Corporation | Spirocyclic thrombin receptor antagonists |
| US20100158857A1 (en) | 2006-05-23 | 2010-06-24 | University Of Utah Research Foundation | Compositions and methods for the inhibition of endothelial nitric oxide synthase activity |
| US20080139525A1 (en) | 2006-08-31 | 2008-06-12 | The Brigham And Women's Hospital, Inc. | Antioxidant therapies |
| EP2056675B1 (en) | 2006-10-12 | 2019-01-09 | Galera Labs, LLC | Methods of treating oral mucositis |
| WO2009065059A2 (en) * | 2007-11-14 | 2009-05-22 | Kereos, Inc. | Super-oxide dismutase mimetics |
| WO2009111294A1 (en) | 2008-02-29 | 2009-09-11 | Eagle Pharmaceuticals, Inc. | Topotecan ready to use solutions |
| CA2720846A1 (en) | 2008-04-15 | 2009-11-05 | Intermune, Inc. | Novel inhibitors of hepatitis c virus replication |
| WO2009143454A2 (en) | 2008-05-22 | 2009-11-26 | Kereos, Inc. | Combination antitumor therapy |
| KR20130049775A (ko) | 2010-03-12 | 2013-05-14 | 애브비 바이오테라퓨틱스 인크. | Ctla4 단백질 및 이의 용도 |
| JP6267638B2 (ja) | 2011-09-26 | 2018-01-24 | ガレラ・ラブス・リミテッド・ライアビリティ・カンパニーGalera Labs, Llc | 疾患の治療方法 |
| US9238659B2 (en) | 2012-11-19 | 2016-01-19 | The University Of Hong Kong | Method of using binuclear gold (I) compounds for cancer treatment |
| SG10202002859QA (en) | 2015-08-11 | 2020-05-28 | Galera Labs Llc | Pentaaza macrocyclic ring complexes possessing oral bioavailability |
| BR112018072560A2 (pt) | 2016-05-03 | 2019-02-19 | Galera Labs, Llc | terapia de combinação para tratamento do câncer |
-
2016
- 2016-08-11 SG SG10202002859QA patent/SG10202002859QA/en unknown
- 2016-08-11 CN CN202110688812.XA patent/CN113416170A/zh active Pending
- 2016-08-11 HU HUE16835928A patent/HUE049926T2/hu unknown
- 2016-08-11 MX MX2018001605A patent/MX2018001605A/es unknown
- 2016-08-11 US US15/751,495 patent/US10597415B2/en active Active
- 2016-08-11 UA UAA201802349A patent/UA126788C2/uk unknown
- 2016-08-11 PT PT168359289T patent/PT3334744T/pt unknown
- 2016-08-11 ES ES16835928T patent/ES2807528T3/es active Active
- 2016-08-11 PL PL16835928T patent/PL3334744T3/pl unknown
- 2016-08-11 KR KR1020187006846A patent/KR20180064380A/ko not_active Application Discontinuation
- 2016-08-11 IL IL297735A patent/IL297735B1/en unknown
- 2016-08-11 CN CN201680058867.XA patent/CN108350009B/zh active Active
- 2016-08-11 MY MYPI2018700525A patent/MY196401A/en unknown
- 2016-08-11 LT LTEP16835928.9T patent/LT3334744T/lt unknown
- 2016-08-11 JP JP2018506866A patent/JP7041959B2/ja active Active
- 2016-08-11 DK DK16835928.9T patent/DK3334744T3/da active
- 2016-08-11 EP EP16835928.9A patent/EP3334744B1/en active Active
- 2016-08-11 AU AU2016306568A patent/AU2016306568B2/en active Active
- 2016-08-11 RS RS20200860A patent/RS60558B1/sr unknown
- 2016-08-11 CA CA2994845A patent/CA2994845A1/en active Pending
- 2016-08-11 WO PCT/US2016/046599 patent/WO2017027728A1/en active Application Filing
- 2016-08-11 CN CN202110688814.9A patent/CN113402560A/zh active Pending
- 2016-08-11 EP EP20168046.9A patent/EP3738967A1/en active Pending
- 2016-08-11 SI SI201630852T patent/SI3334744T1/sl unknown
- 2016-08-11 EA EA201890471A patent/EA201890471A1/ru unknown
- 2016-08-25 US US15/246,788 patent/US9738669B2/en active Active
- 2016-08-25 US US15/246,830 patent/US9738670B2/en active Active
-
2018
- 2018-02-04 IL IL257346A patent/IL257346B/en unknown
- 2018-02-07 MX MX2022010230A patent/MX2022010230A/es unknown
- 2018-02-09 PH PH12018500296A patent/PH12018500296A1/en unknown
- 2018-02-09 CL CL2018000371A patent/CL2018000371A1/es unknown
- 2018-03-06 ZA ZA2018/01546A patent/ZA201801546B/en unknown
- 2018-03-09 CO CONC2018/0002544A patent/CO2018002544A2/es unknown
- 2018-12-21 HK HK18116470.5A patent/HK1257313A1/zh unknown
-
2020
- 2020-03-04 ZA ZA2020/01373A patent/ZA202001373B/en unknown
- 2020-03-09 US US16/812,740 patent/US11066433B2/en active Active
- 2020-07-13 HR HRP20201092TT patent/HRP20201092T1/hr unknown
- 2020-07-21 CY CY20201100665T patent/CY1123960T1/el unknown
- 2020-12-15 AU AU2020289730A patent/AU2020289730B2/en active Active
-
2021
- 2021-07-19 US US17/378,852 patent/US20210347796A1/en active Pending
- 2021-10-25 IL IL287546A patent/IL287546B2/en unknown
- 2021-10-28 JP JP2021176312A patent/JP2022023183A/ja active Pending
-
2023
- 2023-02-10 AU AU2023200738A patent/AU2023200738A1/en active Pending
- 2023-10-27 JP JP2023184571A patent/JP2024012401A/ja active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2807528T3 (es) | Complejos macrocíclicos pentaaza que poseen biodisponibilidad oral | |
| JP6404242B2 (ja) | がんの治療のための併用療法としてのエリブリンおよびレンバチニブの使用 | |
| JP2019514962A (ja) | 癌治療のための組み合わせ療法 | |
| CN102821605B (zh) | 改进的稳定的(e)-4-羧基苯乙烯基-4-氯苄基砜水性制剂 | |
| US20210361701A1 (en) | Pentaaza macrocyclic ring complexes for local delivery | |
| IL263950B (en) | A motorcycle containing an auxiliary lighting device for parking operations | |
| CN103772245A (zh) | 取代的l-半胱氨酸类化合物及其制法和用途 | |
| ES2852623T3 (es) | Formulaciones que contienen domperidona deuterada | |
| ES2757060T3 (es) | Composición que contiene apomorfina y un catión metálico divalente | |
| CN117769416A (zh) | Bak激活剂、药物组合物和在治疗癌症中的用途 |