ES2770860T3 - Métodos de purificación y/o inactivación viral - Google Patents
Métodos de purificación y/o inactivación viral Download PDFInfo
- Publication number
- ES2770860T3 ES2770860T3 ES16734237T ES16734237T ES2770860T3 ES 2770860 T3 ES2770860 T3 ES 2770860T3 ES 16734237 T ES16734237 T ES 16734237T ES 16734237 T ES16734237 T ES 16734237T ES 2770860 T3 ES2770860 T3 ES 2770860T3
- Authority
- ES
- Spain
- Prior art keywords
- glycoprotein
- caprylic acid
- ethanol
- recombinant
- cell
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000034 method Methods 0.000 title claims abstract description 77
- 230000002779 inactivation Effects 0.000 title claims description 27
- 230000003612 virological effect Effects 0.000 title claims description 26
- 238000000746 purification Methods 0.000 title abstract description 20
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims abstract description 247
- WWZKQHOCKIZLMA-UHFFFAOYSA-N octanoic acid Chemical compound CCCCCCCC(O)=O WWZKQHOCKIZLMA-UHFFFAOYSA-N 0.000 claims abstract description 164
- 102000003886 Glycoproteins Human genes 0.000 claims abstract description 112
- 108090000288 Glycoproteins Proteins 0.000 claims abstract description 112
- 239000005635 Caprylic acid (CAS 124-07-2) Substances 0.000 claims abstract description 82
- 229960002446 octanoic acid Drugs 0.000 claims abstract description 82
- 210000004027 cell Anatomy 0.000 claims description 97
- 239000000203 mixture Substances 0.000 claims description 25
- 238000001914 filtration Methods 0.000 claims description 20
- 238000011282 treatment Methods 0.000 claims description 20
- 238000003306 harvesting Methods 0.000 claims description 19
- 238000011534 incubation Methods 0.000 claims description 19
- 239000000872 buffer Substances 0.000 claims description 15
- 239000003365 glass fiber Substances 0.000 claims description 8
- 238000009472 formulation Methods 0.000 claims description 5
- 210000004962 mammalian cell Anatomy 0.000 claims description 5
- 238000003756 stirring Methods 0.000 claims description 3
- 102000012673 Follicle Stimulating Hormone Human genes 0.000 description 57
- 108010079345 Follicle Stimulating Hormone Proteins 0.000 description 57
- 229940028334 follicle stimulating hormone Drugs 0.000 description 57
- 102000004169 proteins and genes Human genes 0.000 description 36
- 108090000623 proteins and genes Proteins 0.000 description 36
- 238000001556 precipitation Methods 0.000 description 35
- 239000002253 acid Substances 0.000 description 32
- 239000000243 solution Substances 0.000 description 30
- 102000009151 Luteinizing Hormone Human genes 0.000 description 27
- 108010073521 Luteinizing Hormone Proteins 0.000 description 27
- 239000012535 impurity Substances 0.000 description 27
- 229940040129 luteinizing hormone Drugs 0.000 description 27
- 102000006771 Gonadotropins Human genes 0.000 description 26
- 108010086677 Gonadotropins Proteins 0.000 description 26
- 239000002622 gonadotropin Substances 0.000 description 26
- -1 hCG Proteins 0.000 description 23
- 239000000047 product Substances 0.000 description 20
- 239000006228 supernatant Substances 0.000 description 17
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 16
- 241000700605 Viruses Species 0.000 description 16
- 239000002609 medium Substances 0.000 description 16
- 150000003839 salts Chemical class 0.000 description 10
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 8
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 8
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 8
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 8
- 239000011780 sodium chloride Substances 0.000 description 8
- 210000002700 urine Anatomy 0.000 description 8
- 230000001580 bacterial effect Effects 0.000 description 7
- 239000003755 preservative agent Substances 0.000 description 7
- 238000000108 ultra-filtration Methods 0.000 description 7
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 6
- 239000005695 Ammonium acetate Substances 0.000 description 6
- 102000001708 Protein Isoforms Human genes 0.000 description 6
- 108010029485 Protein Isoforms Proteins 0.000 description 6
- 235000019257 ammonium acetate Nutrition 0.000 description 6
- 229940043376 ammonium acetate Drugs 0.000 description 6
- 208000000509 infertility Diseases 0.000 description 6
- 230000036512 infertility Effects 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- 239000002244 precipitate Substances 0.000 description 6
- 230000002378 acidificating effect Effects 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 230000008030 elimination Effects 0.000 description 5
- 238000003379 elimination reaction Methods 0.000 description 5
- 231100000535 infertility Toxicity 0.000 description 5
- RLSSMJSEOOYNOY-UHFFFAOYSA-N m-cresol Chemical compound CC1=CC=CC(O)=C1 RLSSMJSEOOYNOY-UHFFFAOYSA-N 0.000 description 5
- 244000309711 non-enveloped viruses Species 0.000 description 5
- 230000002335 preservative effect Effects 0.000 description 5
- 101100468640 Danio rerio rhcgl2 gene Proteins 0.000 description 4
- 238000004113 cell culture Methods 0.000 description 4
- 238000005119 centrifugation Methods 0.000 description 4
- 238000012258 culturing Methods 0.000 description 4
- 238000011026 diafiltration Methods 0.000 description 4
- 238000000502 dialysis Methods 0.000 description 4
- 239000012528 membrane Substances 0.000 description 4
- 239000008194 pharmaceutical composition Substances 0.000 description 4
- 239000012460 protein solution Substances 0.000 description 4
- 238000011084 recovery Methods 0.000 description 4
- 101150053759 rhcg gene Proteins 0.000 description 4
- 239000011734 sodium Substances 0.000 description 4
- 239000000725 suspension Substances 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- 108010080982 Formate-tetrahydrofolate ligase Proteins 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 229920002684 Sepharose Polymers 0.000 description 3
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 3
- 210000004978 chinese hamster ovary cell Anatomy 0.000 description 3
- 238000002474 experimental method Methods 0.000 description 3
- 229940094892 gonadotropins Drugs 0.000 description 3
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 3
- 102000011022 Chorionic Gonadotropin Human genes 0.000 description 2
- 108010062540 Chorionic Gonadotropin Proteins 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 239000007832 Na2SO4 Substances 0.000 description 2
- 229920001213 Polysorbate 20 Polymers 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 238000005571 anion exchange chromatography Methods 0.000 description 2
- 239000013622 capto Q Substances 0.000 description 2
- 238000005277 cation exchange chromatography Methods 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- 229940015047 chorionic gonadotropin Drugs 0.000 description 2
- 239000012228 culture supernatant Substances 0.000 description 2
- 239000002158 endotoxin Substances 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 239000011152 fibreglass Substances 0.000 description 2
- 230000002209 hydrophobic effect Effects 0.000 description 2
- 229910052588 hydroxylapatite Inorganic materials 0.000 description 2
- 239000007972 injectable composition Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- XYJRXVWERLGGKC-UHFFFAOYSA-D pentacalcium;hydroxide;triphosphate Chemical compound [OH-].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O XYJRXVWERLGGKC-UHFFFAOYSA-D 0.000 description 2
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 2
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 2
- 229940068977 polysorbate 20 Drugs 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 230000000717 retained effect Effects 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 239000012723 sample buffer Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 229910052938 sodium sulfate Inorganic materials 0.000 description 2
- 235000011152 sodium sulphate Nutrition 0.000 description 2
- FJKROLUGYXJWQN-UHFFFAOYSA-N 4-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 238000013449 Capto Q chromatography Methods 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- 241000699802 Cricetulus griseus Species 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 241000710188 Encephalomyocarditis virus Species 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000012614 Q-Sepharose Substances 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 238000003916 acid precipitation Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 238000005377 adsorption chromatography Methods 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000000844 anti-bacterial effect Effects 0.000 description 1
- 238000011091 antibody purification Methods 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 239000008365 aqueous carrier Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 238000004925 denaturation Methods 0.000 description 1
- 230000036425 denaturation Effects 0.000 description 1
- 238000011033 desalting Methods 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 239000002270 dispersing agent Substances 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 239000006196 drop Substances 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 238000001647 drug administration Methods 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 108010006578 follitropin alfa Proteins 0.000 description 1
- 108010081934 follitropin beta Proteins 0.000 description 1
- 238000007429 general method Methods 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 210000002149 gonad Anatomy 0.000 description 1
- 229940057854 gonal f Drugs 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 238000004191 hydrophobic interaction chromatography Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000009027 insemination Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 239000007951 isotonicity adjuster Substances 0.000 description 1
- 239000012669 liquid formulation Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 239000007922 nasal spray Substances 0.000 description 1
- 229940097496 nasal spray Drugs 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 150000002895 organic esters Chemical class 0.000 description 1
- 210000001672 ovary Anatomy 0.000 description 1
- 230000016087 ovulation Effects 0.000 description 1
- 238000010979 pH adjustment Methods 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 230000000144 pharmacologic effect Effects 0.000 description 1
- 238000009522 phase III clinical trial Methods 0.000 description 1
- 229960003742 phenol Drugs 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920005862 polyol Polymers 0.000 description 1
- 150000003077 polyols Chemical class 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 229940071643 prefilled syringe Drugs 0.000 description 1
- 230000001850 reproductive effect Effects 0.000 description 1
- 239000001488 sodium phosphate Substances 0.000 description 1
- 229910000162 sodium phosphate Inorganic materials 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000008247 solid mixture Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 230000002195 synergetic effect Effects 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- 230000002485 urinary effect Effects 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/14—Extraction; Separation; Purification
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/14—Peptides containing saccharide radicals; Derivatives thereof, e.g. bleomycin, phleomycin, muramylpeptides or vancomycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/06—Drugs for disorders of the endocrine system of the anterior pituitary hormones, e.g. TSH, ACTH, FSH, LH, PRL, GH
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/24—Drugs for disorders of the endocrine system of the sex hormones
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/32—Bonded phase chromatography
- B01D15/325—Reversed phase
- B01D15/327—Reversed phase with hydrophobic interaction
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/36—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving ionic interaction
- B01D15/361—Ion-exchange
- B01D15/362—Cation-exchange
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D15/00—Separating processes involving the treatment of liquids with solid sorbents; Apparatus therefor
- B01D15/08—Selective adsorption, e.g. chromatography
- B01D15/26—Selective adsorption, e.g. chromatography characterised by the separation mechanism
- B01D15/36—Selective adsorption, e.g. chromatography characterised by the separation mechanism involving ionic interaction
- B01D15/361—Ion-exchange
- B01D15/363—Anion-exchange
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D21/00—Separation of suspended solid particles from liquids by sedimentation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D39/00—Filtering material for liquid or gaseous fluids
- B01D39/14—Other self-supporting filtering material ; Other filtering material
- B01D39/20—Other self-supporting filtering material ; Other filtering material of inorganic material, e.g. asbestos paper, metallic filtering material of non-woven wires
- B01D39/2003—Glass or glassy material
- B01D39/2017—Glass or glassy material the material being filamentary or fibrous
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D61/00—Processes of separation using semi-permeable membranes, e.g. dialysis, osmosis or ultrafiltration; Apparatus, accessories or auxiliary operations specially adapted therefor
- B01D61/14—Ultrafiltration; Microfiltration
- B01D61/145—Ultrafiltration
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/14—Extraction; Separation; Purification
- C07K1/30—Extraction; Separation; Purification by precipitation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K1/00—General methods for the preparation of peptides, i.e. processes for the organic chemical preparation of peptides or proteins of any length
- C07K1/14—Extraction; Separation; Purification
- C07K1/34—Extraction; Separation; Purification by filtration, ultrafiltration or reverse osmosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/575—Hormones
- C07K14/59—Follicle-stimulating hormone [FSH]; Chorionic gonadotropins, e.g. HCG; Luteinising hormone [LH]; Thyroid-stimulating hormone [TSH]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Abstract
Un método de purificación de una glucoproteína, comprendiendo el método un paso de tratamiento de la glucoproteína con una combinación de ácido caprílico y etanol.
Description
DESCRIPCIÓN
Métodos de purificación y/o inactivación viral
La presente invención se refiere a métodos de purificación de glucoproteínas (o productos glucoproteicos) y/o métodos de desactivación viral de glucoproteínas (o productos glucoproteicos). Las proteínas/glucoproteínas pueden ser, por ejemplo, glucoproteínas recombinantes tales como FSH, hCG o LH, producidas en células hospedadoras. Las proteínas/glucoproteínas pueden obtenerse de la orina.
Brodsky et al. (2012) Biotechnology and Bioengineering 1009(10):2589-2598 divulgan un método de precipitación con ácido caprílico para reducir impurezas y eliminar virus durante la purificación de anticuerpos.
Se utilizan muchas glucoproteínas en los tratamientos terapéuticos. Por ejemplo, las gonadotropinas son una clase de glucoproteínas que son útiles para el tratamiento de la infertilidad. Las gonadotropinas son un grupo de hormonas glucoproteicas heterodiméricas que regulan la función de las gónadas en el sexo masculino y femenino. Incluyen la hormona estimulante del folículo (FSH, por sus siglas en inglés), la hormona luteinizante (LH, por sus siglas en inglés) y la gonadotropina coriónica (CG, por sus siglas en inglés).
Las FSH y hCG extraídas de la orina de mujeres embarazadas y posmenopáusicas se han utilizado durante muchos años en el tratamiento de la infertilidad. La producción de FSH y hCG extraídas de la orina conlleva la recogida de procesamiento de grandes cantidades de orina.
Como una alternativa a los productos obtenidos de la orina, hay disponibles versiones recombinantes de la FSH y hCG. Los productos aprobados en la actualidad (Gonal-F, Ovitrelle de Merck Serono; Puregon de MSD) se producen (expresan) en células de ovario de hámster chino (CHO).
Los presentes solicitantes han desarrollado una FSH recombinante y una hCG recombinante, y ambas de las cuales se expresan en una línea celular PER.C6®. El producto de tipo FSH obtenido a partir de la línea celular PER.C6®, y los métodos para su producción, se divulgan en la solicitud de patente internacional N.os PCT/GB2009/000978 (publicada como WO2009/127826A) y PCT/EP2012/065507 (publicada como WO2013/020996). Este producto (FE999049) ha completado los ensayos clínicos de fase III en Europa. El producto de tipo hCG recombinante obtenido a partir de la línea celular PER.C6®, y un método para su producción, se divulgan en el documento PCT/GB2010/001854 (publicado como WO2011/042688).
Los presentes solicitantes han desarrollado técnicas que se pueden utilizar para la purificación de, por ejemplo, FSH recombinante y hCG recombinante producidas en líneas de células de mamíferos (por ejemplo, la FSH recombinante divulgada en el documento WO2009/127826A y el documento WO2013/020996, y la hCG recombinante divulgada en el documento WO 2011/042688).
De acuerdo con la presente divulgación, en un primer aspecto se proporciona un método de purificación de una glucoproteína [por ejemplo, una glucoproteína recombinante, una gonadotropina (por ejemplo, recombinante), una FSH, hCG o LH (por ejemplo, recombinante)], comprendiendo el método un paso de tratamiento de la glucoproteína [por ejemplo, una glucoproteína recombinante, una gonadotropina (por ejemplo, recombinante), una FSH, hCG o LH (por ejemplo, recombinante)] con una combinación de ácido caprílico y etanol.
El método puede comprender tratar una solución de la glucoproteína [por ejemplo, en agua, tampón u otro medio (por ejemplo, un tampón; acetato de amonio 100 mM, NaCl 30-50 mM, pH 9-pH 9,5)] con una combinación de ácido caprílico y etanol. El método puede comprender tratar una solución de la glucoproteína en un tampón (por ejemplo, tampón de acetato de amonio) a pH de 6,5 a 12, por ejemplo, pH de 7,5 a 10, por ejemplo, pH de 9 a 9,5.
El paso de tratar la glucoproteína con una combinación de ácido caprílico y etanol puede tener lugar a pH ácido, por ejemplo, de pH 2 a pH 6,5, por ejemplo, de pH 3 pH 6,5, por ejemplo, de pH 4 a pH 6 (por ejemplo, pH 5,5 ± 0,1) preferentemente, de pH 4,5 a pH 5,5]. El uso de condiciones ácidas (por ejemplo, pH 4 - pH 6) se debe a la actividad del ácido caprílico. El ácido caprílico puede inactivar los virus con envoltura al alterar la membrana del virus; esto es posible gracias a la forma no cargada del ácido caprílico, que puede penetrar en la membrana hidrófoba del virus. El ácido caprílico no está cargado a un pH que está cercano a su pKa (pH 4,9). Con un ApH de 1 unidad (~pH 5,9), un 100% de las moléculas de ácido caprílico tienen carga negativa y, por lo tanto, son menos eficaces para la inactivación viral.
La glucoproteína puede ser una proteína recombinante o una proteína procedente de la orina. La glucoproteína puede ser una gonadotropina, por ejemplo, FSH, hCG o LH. La glucoproteína puede ser una glucoproteína recombinante, por ejemplo, una gonadotropina recombinante, por ejemplo, FSH, hCG o LH recombinante. Preferentemente, la glucoproteína es una glucoproteína recombinante (por ejemplo, gonadotropina recombinante, por ejemplo, FSH, hCG o LH recombinante) producida en una célula (línea celular) mediante un método que comprende cultivar la célula (línea celular) en un medio adecuado y recolectar la glucoproteína recombinante de dicha célula (línea celular) y/o dicho medio (por ejemplo, recolectar la proteína recombinante del sobrenadante del
cultivo celular). La célula (línea celular) puede ser una célula (línea celular) de mamíferos, por ejemplo, una célula (línea celular) CHO, una célula (línea celular) PER.C6®, una célula (línea celular) HEK293, una célula (línea celular) HT1080, una célula (línea celular) COS, una célula (línea celular) NOS, una célula (línea celular) Sp20, etc. Preferentemente la una célula (línea celular) es una célula (línea celular) PER.C6®.
Las glucoproteínas (gonadotropinas, FSH, hCG, LH, etc.), ya sean urinarias o recombinantes, se encuentran por lo general en forma de una solución/suspensión en un medio. La glucoproteína puede estar presente como una única isoforma o como una mezcla de isoformas, como se sabe en la técnica. En la presente los términos proteína, glucoproteína, gonadotropina, FSH, hCG, LH, etc., engloban una solución o suspensión que comprende la proteína, glucoproteína, gonadotropina, FSH, hCG, LH, etc. En la presente, los términos proteína, glucoproteína, gonadotropina, FSH, hCG, LH, etc., engloban una solución o suspensión que comprende la proteína, glucoproteína, gonadotropina, FSH, hCG, LH, etc., donde la proteína, glucoproteína, gonadotropina, FSH, hCG, LH, etc. está presente como una única isoforma o como una mezcla de isoformas. Por lo tanto, el término FSH engloba una solución o suspensión que comprende FSH (por ejemplo, donde FSH está presente como una única isoforma o como una mezcla de isoformas).
En la presente, la frase “tratar la proteína (una glucoproteína, gonadotropina, FHS, hCG, LH, etc.) con una combinación de ácido caprílico y etanol” se refiere a la aplicación de tanto ácido caprílico como etanol a la proteína (glucoproteína, gonadotropina, FSH, hCG, LH, etc.) de manera que la proteína (glucoproteína, gonadotropina, FSH, hCG, LH, etc.) esté expuesta tanto al ácido caprílico como al etanol a la vez. Por lo tanto, esta frase engloba técnicas donde se añaden ácido caprílico y etanol, ya sea como una mezcla o como dos reactivos independientes, a una solución de la proteína (glucoproteína, gonadotropina, FSH, hCG, LH, etc.), de manera que la solución se convierta en una mezcla de ácido caprílico, etanol y la proteína (glucoproteína, gonadotropina, FSH, hCG, LH, etc.); esta frase también engloba otras técnicas en las que tanto el ácido caprílico como el etanol actúan a la vez en la proteína (glucoproteína, gonadotropina, FSH, hCG, LH, etc.).
Para los solicitantes resultado sorprendente observar que tratar una solución que contiene proteína/glucoproteína recombinante (por ejemplo, FSH recombinante, hCG recombinante) con etanol y ácido caprílico, por ejemplo, una combinación de ácido caprílico 20 mM/30% de etanol, a pH ácido, puede conllevar la desnaturalización de algunos virus (lo que provoca su inactivación) y/o precipitación de otros virus y proteínas de la célula hospedadora (impurezas). La solución se puede centrifugar o filtrar a continuación (para eliminar los virus y/o proteínas de la célula hospedadora que han precipitado, por ejemplo, utilizando un filtro de lecho profundo tal como un filtro de vidrio), de manera que el sobrenadante incluya la glucoproteína (por ejemplo, FSH recombinante, hCG recombinante) purificada para un posterior procesamiento y uso. Los solicitantes han observado que el tratamiento de una solución que contiene la glucoproteína recombinante (por ejemplo, FSH recombinante, hCG recombinante) con etanol y ácido caprílico puede (i) inactivar virus con envoltura; y/o (ii) eliminar virus sin envoltura por precipitación (el virus precipitado se puede retirar entonces mediante un paso posterior de centrifugación o filtración mediante, por ejemplo, un filtro de fibra de vidrio); y/o (iii) retirar las proteínas relacionadas con el hospedador mediante precipitación (las proteínas relacionadas con el hospedador precipitadas se pueden retirar mediante un paso posterior de centrifugación o filtración mediante, por ejemplo, un filtro de fibra de vidrio). Este tratamiento y proceso de filtración relativamente simple proporciona una retirada notable de impurezas (en este proceso se retiran de un 64% a un 79% de las impurezas relacionadas con el hospedador) con una pérdida mínima de glucoproteína producto (es decir, rendimiento elevado).
El uso de ácido caprílico y etanol (en, por ejemplo, purificación/inactivación viral de FSH recombinante y/o hCG recombinante) tiene otras ventajas. En primer lugar, la combinación de ácido caprílico y etanol puede acortar el proceso de purificación debido a que el paso único puede tener una función doble: inactivación viral y precipitación, así como también la precipitación de las proteínas de la célula hospedadora. En segundo lugar, tal como se ha descrito anteriormente, el ácido caprílico tiene su actividad máxima en lo que se refiere a la inactivación viral a un pH ~4,9, pero este pH bajo podría en teoría dañar el producto de tipo FSH recombinante (por la disociación de la molécula, etc.). De acuerdo con la ecuación de Henderson-Hasselbalch, a pH 5,5 aproximadamente un 20% del AC no tiene carga, lo que proporciona un buen equilibrio de inactivación viral y reducción del riesgo del daño a la FSH recombinante; la adición de EtOH (por ejemplo, 30% de EtOH) compensa la pérdida de actividad del ácido caprílico en estas condiciones, que son menos nocivas para la proteína. En último lugar, la combinación de ácido caprílico/EtOH permite el uso de una concentración menor de EtOH (por ejemplo, 30%), lo que es extremadamente importante en el proceso de producción, debido a problemas de seguridad.
La concentración de ácido caprílico puede ser ácido caprílico de 10 mM a 30 mM, por ejemplo, ácido caprílico de 18 mM a 25 mM, por ejemplo, ácido caprílico de 19 mM a 23 mM, por ejemplo, ácido caprílico 20 mM. El EtOH puede ser de un 20% a un 50% de EtOH, por ejemplo, de un 25% a un 50% de EtOH, por ejemplo, de un 30% a un 50% de EtOH, por ejemplo, un 30% de EtOH. El método puede comprender un paso de tratar la glucoproteína con de un 30% a un 50% de etanol y ácido caprílico de 18 mM a 25 mM, por ejemplo, ácido caprílico 20 mM y 30% de etanol.
El método puede comprender tratar la glucoproteína con etanol y ácido caprílico durante una incubación de 1 minuto a 6 h a una temperatura de 23 ± 2 °C con agitación (por ejemplo, para la inactivación viral, donde se observa
precipitación), por ejemplo, tratar la glucoproteína con etanol y ácido caprílico durante una incubación de 0,5 a 1 h a una temperatura de 23 ± 2 °C con agitación (por ejemplo, para la inactivación viral, donde se observa precipitación). El método puede comprender tratar la glucoproteína con etanol y ácido caprílico a una temperatura de 4-8 °C durante una incubación de 1 minuto a 32 h, sin agitación (este paso puede continuar/permitir la precipitación de las proteínas de la célula hospedadora (PCH) y virus sin envoltura), por ejemplo, tratar la glucoproteína con etanol y ácido caprílico a una temperatura de 4-8 °C durante una incubación de 14 h a 16 h, sin agitación (este paso puede continuar/permitir la precipitación de PCH y virus sin envoltura). En un ejemplo preferido, el método comprende tratar la glucoproteína con etanol y ácido caprílico durante una incubación de 0,5 a 1 h a una temperatura de 23 ± 2 °C con agitación, seguida por una reducción hasta una temperatura de 4-8 °C e incubación posterior durante 16 ± 2 horas, por ejemplo, de 14 h a 16 h, sin agitación.
El método puede comprender tratar la glucoproteína con etanol y ácido caprílico durante una duración de 1 h ± 10 min a un pH de 5,5 ± 0,1 y a una temperatura de 23 ± 2 °C.
El método puede comprender un paso adicional de centrifugar o filtrar la (solución de) glucoproteína tras el tratamiento con ácido caprílico y etanol (por ejemplo, a través de un filtro de lecho profundo, por ejemplo, un filtro de fibra de vidrio).
El método puede comprender un paso adicional de concentrar la (solución de) glucoproteína hasta la concentración (de glucoproteína) deseada y/u otros pasos de purificación/formulación (por ejemplo, posteriores).
De acuerdo con la presente invención, en un aspecto adicional se proporciona un método de inactivación viral de una glucoproteína [por ejemplo, una glucoproteína recombinante, una gonadotropina (por ejemplo, recombinante), una FSH, hCG o lH (por ejemplo, recombinante)], comprendiendo el método un paso de tratar la glucoproteína [por ejemplo, una glucoproteína recombinante, una gonadotropina (por ejemplo, recombinante), una FSH, hCG o LH (por ejemplo, recombinante)] con una combinación de ácido caprílico y etanol.
El método puede comprender tratar una solución de la glucoproteína [por ejemplo, en agua, tampón u otro medio (por ejemplo, un tampón; acetato de amonio 100 mM, NaCl 30-50 mM, pH 9-pH 9,5)] con una combinación de ácido caprílico y etanol. El método puede comprender tratar una solución de la glucoproteína en un tampón (por ejemplo, tampón de acetato de amonio) a un pH de 6,5 a 12, por ejemplo, pH de 7,5 a 10, por ejemplo, pH de 9 a 9,5.
El paso de tratar la glucoproteína con una combinación de ácido caprílico y etanol puede tener lugar a pH ácido, por ejemplo, de pH 2 a pH 6,5, por ejemplo, de pH 3 pH 6,5, por ejemplo, de pH 4 a pH 6 (por ejemplo, pH 5,5 ± 0,1) preferentemente, de pH 4,5 a pH 5,5]. El uso de condiciones ácidas (por ejemplo, pH 4 - pH 6) se debe a la actividad del ácido caprílico. El ácido caprílico puede inactivar los virus con envoltura al alterar la membrana del virus; esto es posible gracias a la forma no cargada del ácido caprílico, que puede penetrar en la membrana hidrófoba del virus. El ácido caprílico no está cargado a un pH que está cercano a su pKa (pH 4,9). Con un ApH de 1 unidad (~pH 5,9), un 100% de las moléculas de ácido caprílico tienen carga negativa y, por lo tanto, son menos eficaces para la inactivación viral.
La concentración de ácido caprílico puede ser ácido caprílico de 10 mM a 30 mM, por ejemplo, ácido caprílico de 18 mM a 25 mM, por ejemplo, ácido caprílico de 19 mM a 23 mM, por ejemplo, ácido caprílico 20 mM. El EtOH puede ser de un 20% a un 50% de EtOH, por ejemplo, de un 25% a un 50% de EtOH, por ejemplo, de un 30% a un 50% de EtOH, por ejemplo, un 30% de EtOH. El método puede comprender un paso de tratar la glucoproteína con de un 30% a un 50% de etanol y ácido caprílico de 18 mM a 25 mM, por ejemplo, ácido caprílico 20 mM y 30% de etanol. El método puede comprender tratar la glucoproteína con etanol y ácido caprílico durante una incubación de 1 minuto a 6 h a una temperatura de 23 ± 2 °C con agitación, por ejemplo, tratar la proteína (glucoproteína) con etanol y ácido caprílico durante una incubación de 0,5 a 1 h a una temperatura de 23 ± 2 °C con agitación. El método puede comprender tratar la glucoproteína con etanol y ácido caprílico a una temperatura de 4-8 °C durante una incubación de 1 minuto a 32 h, sin agitación, por ejemplo, tratar la glucoproteína con etanol y ácido caprílico a una temperatura de 4-8 °C durante una incubación de 14 h a 16 h, sin agitación. En un ejemplo preferido, el método comprende tratar la glucoproteína con etanol y ácido caprílico durante una incubación de 0,5 a 1 h a una temperatura de 23 ± 2 °C con agitación, seguida por una reducción hasta una temperatura de 4-8 °C e incubación posterior durante de 14 h a 16 h, sin agitación.
El método puede comprender tratar la glucoproteína con etanol y ácido caprílico durante una duración de 1 h ± 10 min a un pH de 5,5 ± 0,1 y a una temperatura de 23 ± 2 °C.
El método puede comprender un paso adicional de centrifugar o filtrar la (solución de) glucoproteína tras el tratamiento con ácido caprílico y etanol (por ejemplo, a través de un filtro de fibra de vidrio).
El método puede comprender un paso adicional de concentrar la (solución de) glucoproteína hasta la concentración (de glucoproteína) deseada y/u otros pasos de purificación/formulación (por ejemplo, posteriores).
La glucoproteína puede ser una proteína recombinante o una proteína procedente de la orina. La glucoproteína puede ser una gonadotropina, por ejemplo, FSH, hCG o LH.
La glucoproteína puede ser una glucoproteína recombinante, por ejemplo, una gonadotropina recombinante, por ejemplo, FSH, hCG o LH recombinante. Preferentemente, la glucoproteína es una glucoproteína recombinante (por ejemplo, gonadotropina recombinante, por ejemplo, FSH, hCG o LH recombinante) producida en una célula (línea celular) mediante un método que comprende cultivar la célula (línea celular) en un medio adecuado y recolectar la glucoproteína recombinante de dicha célula (línea celular) y/o dicho medio (por ejemplo, recolectar la proteína recombinante del sobrenadante del cultivo celular). La célula (línea celular) puede ser una célula (línea celular) de mamíferos, por ejemplo, una célula (línea celular) CHO, una célula (línea celular) PER.C6®, una célula (línea celular) HEK293, una célula (línea celular) HT1080, una célula (línea celular) COS, una célula (línea celular) NOS, una célula (línea celular) Sp20, etc.
Preferentemente la una célula (línea celular) es una célula (línea celular) PER.C6®.
En la presente se divulga una proteína que ha sido purificada y/o sometida a inactivación viral mediante un método descrito anteriormente. La proteína puede ser una proteína recombinante o una proteína procedente de la orina. La proteína es una glucoproteína. La glucoproteína puede ser una glucoproteína recombinante, por ejemplo, una gonadotropina recombinante, por ejemplo, FSH, hCG o LH recombinante. Preferentemente, la glucoproteína es una glucoproteína recombinante (por ejemplo, gonadotropina recombinante, por ejemplo, FHS, hCG o LH recombinante) producida en una célula (línea celular) mediante un método que comprende cultivar la célula (línea celular) en un medio adecuado y recolectar la glucoproteína recombinante de dicha célula (línea celular) y/o dicho medio (por ejemplo, recolectar la proteína recombinante del sobrenadante del cultivo celular). La célula (línea celular) puede ser una célula (línea celular) de mamíferos, por ejemplo, una célula (línea celular) CHO, una célula (línea celular) PER.C6®, una célula (línea celular) HEK293, una célula (línea celular) HT1080, una célula (línea celular) COS, una célula (línea celular) NOS, una célula (línea celular) Sp20, etc. Preferentemente la una célula (línea celular) es una célula (línea celular) PER.C6®.
En la presente, se divulga además una composición farmacéutica [por ejemplo, para (su uso) en el tratamiento de la infertilidad] que comprende una glucoproteína (por ejemplo, una glucoproteína recombinante, por ejemplo, FSH recombinante, hCG recombinante) que se ha purificado y/o sometido a inactivación viral mediante un método descrito anteriormente.
En la presente, se divulga además un método de tratamiento (por ejemplo, de la infertilidad) que comprende un paso de administración a un paciente que lo necesite una composición farmacéutica que comprende una glucoproteína (por ejemplo, una glucoproteína recombinante, por ejemplo, FSH recombinante, hCG recombinante) que se ha purificado y/o sometido a inactivación viral mediante un método descrito anteriormente.
El tratamiento de la infertilidad puede comprender tecnologías de reproducción asistida (TRA), inducción de la ovulación o inseminación intrauterina (IIU). La composición farmacéutica se puede utilizar, por ejemplo, en indicaciones médicas donde se han utilizado preparados conocidos de FSH, LH, hCG.
El producto o composición se puede formular en composiciones muy conocidas para cualquier vía de administración de fármacos, por ejemplo, oral, rectal, parenteral, transdérmica (por ejemplo, tecnología de parches), intravenosa, intramuscular, subcutánea, intracisternal, intravaginal, intraperitoneal, local (polvos, ungüentos o gotas) o como un pulverizado bucal o nasal. Una composición típica comprende un portador farmacéuticamente aceptable, tal como una solución acuosa, excipientes atóxicos, incluidos sales y conservantes, tampones y similares, tal como se describe en Remington's Pharmaceutical Sciences, decimoquinta edición (Matt Publishing Company, 1975) en las páginas 1405 a 1412 y 1461-87, y el Formulario Nacional XIV decimocuarta edición (American Pharmaceutial Association, 1975), entre otros.
Los ejemplos de portadores, diluyentes, disolventes o vehículos acuosos y no acuosos adecuados incluyen el agua, etanol, polioles (tales como glicerol, propilenglicol, polietilenglicol y similares), carboximetilcelulosa y mezclas adecuadas de estos, aceites vegetales (tal como aceite de oliva) y ésteres orgánicos inyectables tales como el oleato de etilo. Las composiciones también pueden contener aditivos tales como, sin carácter limitante, conservantes, agentes humectantes, agentes emulsionantes, surfactantes y agentes de dispersión. Se pueden incluir agentes antibacterianos y antifúngicos para prevenir el crecimiento de microbios e incluyen, por ejemplo, m-cresol, alcohol bencílico, parabeno, clorobutanol, fenol, ácido sórbico y similares. Si se incluye un conservante, se prefieren el alcohol bencílico, fenol y/o m-cresol; sin embargo, el conservante no se limita a estos ejemplos de ninguna manera. Además, puede resultar deseable incluir agentes isotónicos tales como azúcares, cloruro de sodio y similares. El producto o composición puede comprender además una sal que comprende un catión de un metal alcalino farmacéuticamente aceptable seleccionado a partir del grupo constituido por sales de Na+ o K+, o una combinación de estas. Preferentemente, la sal es una sal de Na+, por ejemplo, NaCl o Na2SO4.
Preferentemente, el producto o composición comprende una glucoproteína y uno o más de Polisorbato 20, L
metionina, fenol, tampón de fosfato de sodio y sulfato de disodio, tampones de citrato y sacarosa.
Las formulaciones inyectables se pueden esterilizar, por ejemplo, mediante filtración a través de un filtro que retenga bacterias, o incorporando agentes estabilizantes en forma de composiciones sólidas estériles que se pueden disolver o dispersar en agua estéril u otro medio inyectable estéril justo antes de su uso. Las formulaciones inyectables se pueden suministrar en cualquier recipiente adecuado, por ejemplo, vial, jeringuilla rellenada previamente, cartuchos de inyección y similares.
La composición se puede formular para un único uso o para un uso múltiple (dosis múltiple). Si el producto o composición se formula para un uso múltiple, se prefiere que se incluya un conservante. Si se incluye un conservante, se prefieren el alcohol bencílico, fenol y/o m-cresol; sin embargo, el conservante no se limita a estos ejemplos de ninguna manera. La composición o producto formulados para un único uso o un uso múltiple puede comprender además una sal que comprende un catión de un metal alcalino farmacéuticamente aceptable seleccionado a partir del grupo constituido por sales de Na+ o K+, o una combinación de estas. Preferentemente, la sal es una sal de Na+, por ejemplo, NaCl o Na2SO4.
El producto o composición se puede incluir en un recipiente tal como un vial, cartucho rellenado previamente (por ejemplo, para la administración única o uso múltiple) o un dispositivo de inyección tal como un “bolígrafo” para, por ejemplo, la administración de dosis múltiples.
Los viales se pueden empaquetar en un envase de tipo blíster o mediante otros medios para mantener la esterilidad. Cualquier producto puede contener opcionalmente instrucciones para utilizar las formulaciones de FSH (y, por ejemplo, hCG si está presente). El pH y la concentración exacta de los diversos componentes de la composición farmacéutica se ajustan de acuerdo con la práctica habitual en este campo. Remítase a GOODMAN and GILMAN’s THE PHARMACOLOGICAL BASIS FOR THERAPEUTICS, 7.a ed. Preferentemente, las composiciones se suministran como composiciones para la administración parenteral. Existe constancia en la técnica de métodos generales para la preparación de las formulaciones parenterales y estos se describen en REMINGTON; THE SCIENCE AND PRACTICE OF PHARMACY, mencionado anteriormente, en las páginas 780-820. Las composiciones parenterales se pueden suministrar en una formulación líquida o como un sólido que se mezclará con un medio inyectable estéril justo antes de la administración. Preferentemente, las composiciones parenterales se suministran en una forma farmacéutica unitaria para facilitar la administración y la uniformidad de la dosis.
A continuación, se describirá la presente invención haciendo referencia a los dibujos adjuntos en los cuales:
La Figura 1 muestra un esquema del proceso de purificación (desactivación viral) de FSH recombinante de acuerdo con una realización de la presente invención;
La Figura 2 muestra el patrón en gel tras la estimación cualitativa de la eliminación de impurezas para diversas muestras de FSH UF2-DD (ultrafiltración después de la diálisis) tratadas analizadas en PAGE (electroforesis en gel de poliacrilamida) reducida al 12%, donde en el carril 1 están los marcadores BPM (bajo peso molecular), el carril 2 es el tampón de muestra, el carril 3 es UF2-DD, el carril 4 es UF2-DD AC 10 mM, pH 5,5, el carril 5 es UF2-DD AC 10 mM, 30% de etanol, pH 5,5, el carril 6 es tampón de muestra, el carril 7 es PM en el intervalo bajo, el carril 8 es UF2-DD, el carril 9 es UF2-DD 20 mM AC, pH 5,5 y el carril 10 es UF2-DD AC 20 mM, 30% de etanol, pH 5,5 (remítase al Ejemplo 3); y
La Figura 3 muestra el patrón en gel después de la estimación cuantitativa de la eliminación de impurezas para diversas muestras de hGC tratadas analizadas en PAGE (electroforesis en gel de poliacrilamida) reducida al 12%, donde en el carril 1 están los marcadores de BPM (bajo peso molecular), el carril 2 es el Recolectado-DD que contiene hGC, el carril 3 es NR-No Relevante, el carril 4 es el sobrenadante de [Recolectado-DD CA 15 mM pH 5,0] y el carril 5 es el sobrenadante de [Recolectado-DD CA 20 mM 10% de etanol pH 5,0], remítase al Ejemplo 4.
Ejemplo 1
La Figura 1 muestra un resumen de todo el proceso de purificación de FSH recombinante. Como se puede apreciar en la Figura 1, la FHS recombinante se expresa en una línea celular PER.C6® modificada mediante los métodos divulgados en el documento WO 2013/020996 y el documento WO 2009/127826A utilizando un biorreactor.
El biorreactor se siembra y se fomenta el crecimiento celular mediante métodos conocidos por los expertos en la técnica, y el reactor funciona en modo de perfusión para producir y recolectar de manera continua FSH recombinante, utilizando un sistema Hollofibre (ATF4) que se puede adquirir de Repligen. La siembra de al menos 1 x 106 células/mL en un volumen total de 4 ± 1 litros tiene lugar en medio 6GRO. La producción tiene lugar en el medio ProPer-1, y el recolectado del biorreactor se recoge en bolsas de polietileno. Por ejemplo, en este ejemplo la proteína (glucoproteína) es una glucoproteína recombinante (FSH recombinante) producida en una línea celular PER.C6® mediante un método que comprende cultivar la línea celular en un medio adecuado (medio ProPer-1) y recolectar la glucoproteína recombinante del medio (recolectando la proteína recombinante del sobrenadante del
cultivo celular).
El recolectado del bioreactor se combina y se somete a un paso de ultrafiltración/diafiltración de 10 kDa (UF1) que reduce la concentración del recolectado, acondiciona el recolectado (en lo que se refiere al pH y conductividad) para la cromatografía Capto-Q y elimina pigmentos y componentes de bajo peso molecular del medio de cultivo. La fracción retenida se filtra a través de un filtro de fibra de vidrio de 0,8 0,65 pm para aclarar la solución del proceso (remítase a la Fig. 1) y posteriormente se somete a una filtración de 0,2 pm como un control de la carga bacteriana. A continuación, se utiliza cromatografía de intercambio aniónico Capto-Q, mediante métodos muy conocidos en la técnica, para capturar la FSH recombinante y para eliminar el ADN, endotoxina, proteínas de la célula hospedadora e impurezas relacionadas con el proceso. Se realiza una filtración de 0,2 pm adicional como un control de la carga bacteriana.
El eluido de Capto-Q filtrado se somete a una ultrafiltración/diafiltración de 10 kDa adicional (UF2) con el objetivo de desalar y reducir el volumen antes de la purificación/inactivación viral, mediante métodos muy conocidos en la técnica.
Paso de AC/EtOH
La fracción retenida de UF2 es una solución de FSH recombinante en un tampón (acetato de amonio 100 mM, NaCl 30 mM, pH 9,3 - pH 9,7). El pH de la solución proteica se reduce en primer lugar desde pH 9,3 - pH 9,7 hasta pH 6,3 ± 0,3 a 32 ± 2 °C con agitación, a continuación se trata con una combinación de ácido caprílico 20 mM/30% de etanol (AC/EtOH) seguida por un ajuste adicional del pH hasta 4,5 - 5,6 (el pH se ajusta con HCl 1 M). Después de este tratamiento la solución proteica permanece durante una incubación de 0,5 a 1 h a 23 ± 2° con agitación (durante este tiempo tiene lugar la inactivación viral y se observa una precipitación blanca que se asemeja a copos). Al final de la 0,5 - 1 h, la temperatura de la solución proteica se reduce hasta 4 - 8 °C, y la solución se incuba durante de 14 h a 18 h más, por ejemplo, de 14 a 16 h, sin agitación (esto permite que continúe precipitación de PCH y virus sin envoltura). El paso de tratamiento con AC/EtOH tiene una actividad triple: (i) inactivación de los virus con envoltura; (ii) aclaramiento de virus en envoltura mediante precipitación seguido por un paso de aclaramiento que tiene como objetivo eliminar el precipitado; y (iii) eliminación por precipitación de proteínas relacionadas con el hospedador. Las impurezas precipitadas (virus sin envoltura y proteínas relacionadas con el hospedador) se eliminan mediante un paso de filtración a través de un filtro de fibra de vidrio de 0,8 0,65 micrómetros, un paso de filtración que también aclara la solución de FSH recombinante.
Se realiza una filtración de 0,2 pm adicional como un control de la carga bacteriana.
La solución se somete a continuación a cromatografía de intercambio catiónico con sulfopropil-Sepharose (SP-FF) mediante métodos muy conocidos en la técnica para eliminar el ácido caprílico, etanol y más proteínas de la célula hospedadora. Se realiza una filtración de 0,2 pm adicional como un control de la carga bacteriana, seguida por un paso adicional de purificación utilizando cromatografía de interacción hidrófoba con fenil-Sepharose (PS-FF) para eliminar subunidades de FSH recombinantes libres y proteínas de la célula hospedadora.
El eluido de PS se somete a un tercer paso de ultrafiltración/diafiltración de 10 kDa (UF3) para eliminar la sal y acondicionar la solución para el siguiente paso. Se realiza una filtración de 0,2 pm adicional como un control de la carga bacteriana, antes de la cromatografía por adsorción con hidroxiapatita (HyA) que tiene como objetivo eliminar subunidades de FSH disociadas y heterodímeros básicos, seguida por una filtración de 0,2 pm adicional realizada como un control de la carga bacteriana.
Se realiza un “paso de purificación final” por cromatografía de intercambio aniónico con Q-Sepharose (QS-FF) en modo unir/eluir para eliminar proteínas del hospedador, ADN, endotoxinas y posibles virus. A continuación, tiene lugar una filtración de 0,2 pm adicional para el control de la carga bacteriana, antes de combinar los QS MP y nanofiltrar para eliminar posibles virus. El sobrenadante se somete a un cuarto paso de ultrafiltración/diafiltración de 10 kDa (UF4) para concentrar la FSH recombinante hasta de 0,5 a 1,1 mg/mL, seguido por la adición de polisorbato 20 hasta una concentración final de 0,005 mg/mL. Estos son pasos de diálisis y ajuste del tampón, que son muy conocidos en la técnica. La FSH recombinante se somete a un paso de filtración de 0,2 pm final antes de la división en alícuotas en un envase primario y almacenamiento a -20 °C hasta su envío.
Los solicitantes han observado que el tratamiento con ácido caprílico/etanol es capaz de reducir de manera notable las impurezas relacionadas con el hospedador. De acuerdo con diversos ciclos de producción (datos que no se muestran) de un 64 a un 79% de las impurezas relacionadas con el hospedador se eliminan con el paso de AC/EtOH (y filtración con fibra de vidrio posterior) descrito anteriormente, a la vez que se recupera un rendimiento elevado de aproximadamente un 90 a un 95% de la FSH. Esto es una reducción significativa de impurezas relacionadas con el hospedador que se consigue mediante un proceso simple, con una pérdida mínima de proteína producto (glucoproteína producto).
La notable eficacia de aclaramiento viral de este paso se resume en la Tabla 1, que muestra un resumen de los
factores de reducción logio, que están en la región de >4,25 a >5,41. Un factor de reducción-log (FRL) >4 Logio (por ejemplo, hasta 8 Log10 o superior) se considera por lo general elevado, robusto y eficaz.
Tabla 1 Resumen de los factores de reducción log i o (rFSH)
(1)El estudio con EMCV contiene filtración con fibra de vidrio después del tratamiento
El Ejemplo anterior se refiere a rFSH, pero los expertos en la técnica apreciarán que el proceso (por ejemplo el paso con AC/EtOH (y la posterior filtración con fibra de vidrio)) descrito anteriormente se puede aplicar fácilmente a la purificación/inactivación viral de otras proteínas (por ejemplo, glucoproteínas), por ejemplo, rhCG [por ejemplo, rhCG producida en una línea celular PER.C6® mediante el método del documento PCT/GB2010/001854 (publicado como WO2011/042688)].
Ejemplo 2
En otro ejemplo de un método de la invención, se proporciona un proceso de purificación de hCG/inactivación viral. Se utilizó un método similar al del Ejemplo 1 anterior (menos el paso de cromatografía por intercambio catiónico con sulfopropil-Sepharose (SP-FF)) para la purificación/inactivación viral de rhCG producida en una línea celular PER.C6 mediante el método del documento PCT/GB2010/001854 (publicado como WO2011/042688). Los solicitantes observaron que la inactivación química por ácido caprílico y etanol a pH ácido, es decir, utilizando el paso con AC/EtOH descrito en el Ejemplo 1, eliminó aproximadamente un 65% de impurezas que no son hCG (por precipitación), a la vez que se recuperó un rendimiento elevado de aproximadamente un 90% de la hCG.
La excelente eficacia de aclaración viral del paso con AC/EtOH en el Ejemplo se resume en la Tabla 2. La inactivación viral de MuLV fue eficaz tal como se determinó mediante el elevado FRL obtenido, en un intervalo de >5,31 a >5,48. Se obtuvieron FRL entre >2,03 y >2,74 para el tratamiento con AC/EtOH y eliminación del precipitado.
Tabla 2. Resumen de los factores de reducción log1o (rhCG)
Ejemplo 3: Evaluación de las condiciones de precipitación para eliminar impurezas en una solución que contiene rFSH
Descripción del experimento:
El intermedio de UF2-DD (ultrafiltración después de la diálisis) obtenido utilizando el proceso de purificación de rFSH del Ejemplo 1 (hasta el paso con AC/EtOH) contuvo acetato de amonio 100 mM NaCl 30 mM pH 9,50 ± 0,20, 11,00 ± 0,50 mS/cm. Este se dividió en alícuotas y cada alícuotas se sometió a diferentes condiciones de precipitación para eliminar impurezas (rFSH es soluble en la solución). Las condiciones de precipitación estudiadas
fueron las siguientes:
1. UF2-DD sin tratamiento (control)
2. UF2-DD ácido caprílico (AC) 10 mM, pH 5,5
3. UF2-DD CA 10 mM, 30% de etanol, pH 5,5
4. UF2-DD CA 20 mM, pH 5,5
5. UF2-DD CA 20 mM, 30% de etanol, pH 5,5
Todas las muestras tratadas se incubaron durante 30 min a TA con agitación a lo que siguió una incubación adicional de 30 min sin agitación. Se realizó una incubación adicional a 2-8 °C durante 16-20 h. Los precipitados generados se eliminaron por centrifugación mientras que los sobrenadantes se recogieron.
Parámetros de desempeño del proceso de precipitación:
Recuperación de rFSH
La concentración de rFSH en todas las muestras se determinó mediante ELISA FSH y los rendimientos de cada muestra después del tratamiento se calcularon y se exponen en la Tabla 3.
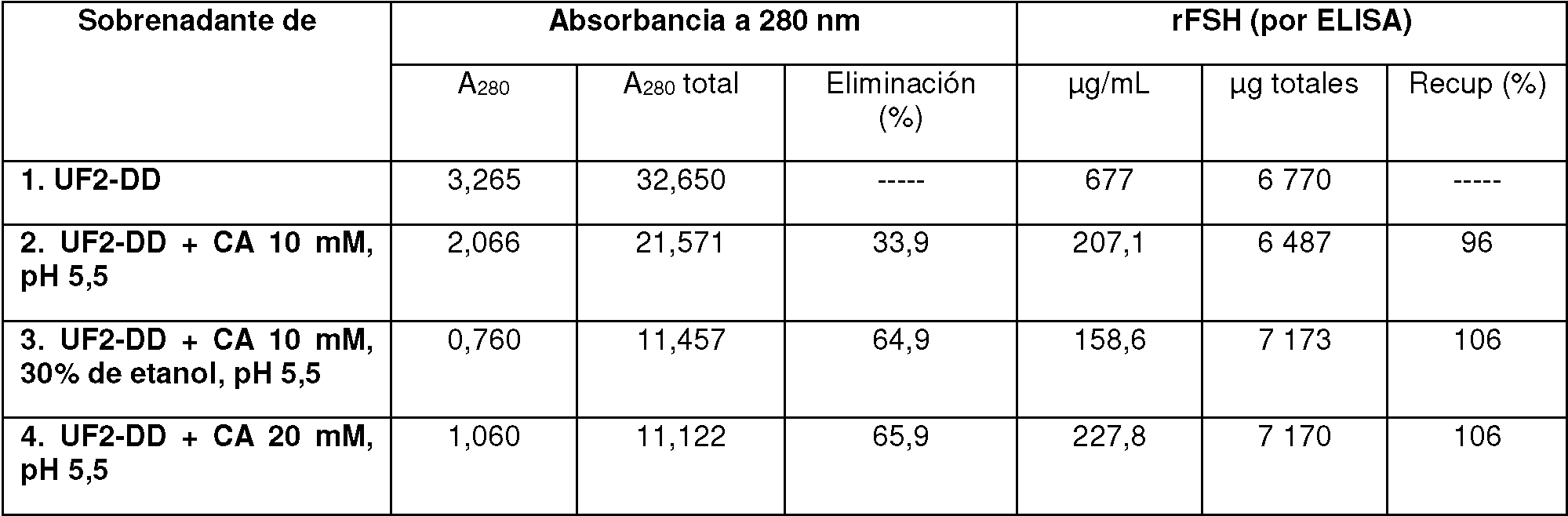
Tal como se aprecia en la Tabla 3, se recuperaron un 96%, 106%, 106% y un 98% de la rFSH en las soluciones del proceso UF2-DD tras la precipitación con AC 10 mM, CA 10 mM 30% de etanol, AC 20 mM y AC 20 mM 30% de etanol, respectivamente. Esto indica que la rFSH no precipita y sigue solubilizada en la solución.
Eliminación de impurezas
Se midió la absorbancia a 280 nm en UF2-DD no tratado y en cada uno de los sobrenadantes de los UF2-DD tratados y se calculó la eliminación de impurezas, tal como se expone en la Tabla 3. Un 33,9%, 64,9%, 65,9% y 68,8% de la impureza A280 total en UF2-DD se eliminó después de la precipitación con AC 10 mM, CA 10 mM 30% de etanol, AC 20 mM y AC 20 mM 30% de etanol, respectivamente.
El UF2-DD no tratado y los sobrenadantes de los diversos UF2-DD tratados se analizaron en PAGE (electroforesis en gel de poliacrilamida) reducida al 12% para la estimación cualitativa de la eliminación de impurezas. El patrón en gel se muestra en la Figura 2. El sobrenadante obtenido tras la precipitación con CA 10 mM 30% de etanol (carril 5) y CA 20 mM 30% de etanol pH 5,5 (carril 10) es sustancialmente más puro respecto al sobrenadante obtenido tras la precipitación con CA 10 mM pH 5,5 (carril 4) y AC 20 mM (carril 9), respectivamente. Esto muestra el efecto sinérgico de la adición de etanol al ácido caprílico en el paso de precipitación.
Conclusiones del experimento:
1. La precipitación de UF2-DD con etanol y ácido caprílico dio como resultado un producto más puro en comparación con el obtenido utilizando solo ácido caprílico.
2. La combinación de etanol y ácido caprílico no precipita la rFSH que sigue solubilizada en la solución, y esto significa un paso de purificación e inactivación viral con un rendimiento elevado.
Tabla 3. los Resultados obtenidos con las diferentes condiciones de precipitación para la eliminación de impurezas en una solución con rFSH intermedia
Ejemplo 4: Evaluación de las condiciones de precipitación para eliminar impurezas en el recolectado que contiene hCG
Descripción del experimento:
Se concentró el recolectado que contenía hCG ~40 veces y se dializó con tampón con glicina 100 mM, NaCI 50 mM pH 9,0, 6 mS/cm mediante un sistema de ultrafiltración (UF) de 10 kDa. Al final de la UF, la solución proteica recuperada, material del Recolectado-DD (después de la diálisis), se dividió en alícuotas y cada alícuota se sometió a condiciones de precipitación diferentes para eliminar impurezas (mientras que la hCG es soluble en la solución). Las condiciones de precipitación estudiadas fueron las siguientes (Tabla 4):
1. Recolectado-DD sin tratamiento como un control;
2. Recolectado-DD AC 15 mM, pH 5,0
3. Recolectado-DD AC 20 mM, pH 5,0
4. Recolectado-DD AC 20 mM 10% de etanol, pH 5,0.
Todas las muestras tratadas se incubaron durante 1 h a TA sin agitación. Los precipitados generados se eliminaron por centrifugación mientras que los sobrenadantes se recogieron.
Parámetros de desempeño del proceso de precipitación:
Recuperación de hCG
Se determinó la concentración de hCG en el recolectado no tratado y en cada uno de los sobrenadantes de los Recolectados DD y se calcularon las recuperaciones tal como se detalla en la Tabla 4.
Eliminación de impurezas
Se determinó la absorbancia a 280 nm (A280) en el recolectado no tratado y en cada uno de los sobrenadantes de los Recolectados DD tratados y se calcularon las eliminaciones de impurezas tal como se detalla en la Tabla 4.
El recolectado no tratado y los sobrenadantes de los diversos Recolectados DD tratados se analizaron en PAGE (electroforesis en gel de poliacrilamida) reducida al 12% para la estimación cualitativa de la eliminación de impurezas. El patrón en gel se muestra en la Figura 3.
Análisis:
1. Recuperación de hCG - Se recuperó un 91%, 86% y 83% de la hCG en el Recolectado-DD después de la precipitación con AC 15 mM, AC 20 mM y AC 20 mM 10% de etanol, respectivamente.
2. Eliminación de impurezas según A280 - Se eliminó un 56,6%, 55,8% y un 63,0% de la A280 total en el Recolectado-DD después de la precipitación con AC 15 mM, AC 20 mM y AC 20 mM 10% de etanol, respectivamente.
3. Eliminación de impurezas por gel - El sobrenadante obtenido tras la precipitación con CA 20 mM 10% de etanol pH 5,0 (carril 5) es sustancialmente más puro respecto al sobrenadante obtenido tras la precipitación con CA 15 mM pH 5,0 (carril 4).
Conclusiones:
1. La precipitación de Recolectado que contiene hCG al que se le ha añadido etanol y ácido caprílico dio como resultado un producto más puro en comparación con el obtenido utilizando solo ácido caprílico.
Tabla 4. Resultados obtenidos a partir de diferentes condiciones de precipitación para eliminar impurezas en recolectado que contiene hCG
Claims (13)
1. Un método de purificación de una glucoproteína, comprendiendo el método un paso de tratamiento de la glucoproteína con una combinación de ácido caprílico y etanol.
2. Un método de inactivación viral de una glucoproteína, comprendiendo el método un paso de tratamiento de la glucoproteína con una combinación de ácido caprílico y etanol.
3. Un método de acuerdo con la reivindicación 1 o la reivindicación 2 que comprende tratar una solución de la glucoproteína (por ejemplo, en un tampón) con una combinación de ácido caprílico y etanol.
4. Un método de acuerdo con cualquier reivindicación anterior donde la glucoproteína es FSH, hCG o LH.
5. Un método de acuerdo con cualquier reivindicación anterior donde la glucoproteína es una glucoproteína recombinante.
6. Un método de acuerdo con cualquier reivindicación anterior donde la glucoproteína es una glucoproteína recombinante producida en una célula mediante un método que comprende cultivar la célula en un medio adecuado y recolectar la glucoproteína recombinante de dicha célula y/o dicho medio.
7. Un método de acuerdo con la reivindicación 7 donde la célula es una célula de mamífero.
8. Un método de acuerdo con cualquier reivindicación anterior donde el tratamiento de la glucoproteína con una combinación de ácido caprílico y etanol tiene lugar de pH 2 a pH 6,5, por ejemplo, de pH 3 a pH 6,5, por ejemplo, de pH 4 a pH 6, por ejemplo, de pH 4,5 a pH 5,5.
9. Un método de acuerdo con cualquier reivindicación anterior donde la concentración de ácido caprílico es ácido caprílico de 10 mM a 30 mM y/o el etanol es de un 20% a un 50% de EtOH.
10. Un método de acuerdo con cualquier reivindicación anterior que comprende: (a) tratar la glucoproteína con etanol y ácido caprílico durante una incubación de 1 minuto a 6 h a una temperatura de 23 ± 2 °C con agitación; (b) tratar la glucoproteína con etanol y ácido caprílico a una temperatura de 4-8 °C durante una incubación de 1 minuto a 32 h, sin agitación; (c) tratar la glucoproteína con etanol y ácido caprílico durante una incubación de 0,5 h a 1 h a una temperatura de 23 ± 2 °C con agitación, seguida por una reducción hasta una temperatura de 4-8 °C y una incubación posterior de 14 h a 18 h, sin agitación; o (d) tratar la glucoproteína con etanol y ácido caprílico durante una duración de 1 h ± 10 min a un pH de 5,5 ± 0,1 y a una temperatura de 23 ± 2 °C.
11. Un método de acuerdo con cualquier reivindicación anterior que comprende un paso adicional de filtrado de la glucoproteína tras el tratamiento con ácido caprílico y etanol.
12. Un método de acuerdo con la reivindicación 12 donde la glucoproteína se filtra utilizando un filtro de fibra de vidrio.
13. Un método de acuerdo con cualquier reivindicación anterior que comprende un paso adicional de concentración de la glucoproteína hasta la concentración deseada y/o pasos posteriores de formulación.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP15174029 | 2015-06-26 | ||
| PCT/EP2016/064668 WO2016207353A1 (en) | 2015-06-26 | 2016-06-24 | Methods of purification and/or viral inactivation |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2770860T3 true ES2770860T3 (es) | 2020-07-03 |
Family
ID=53510646
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES16734237T Active ES2770860T3 (es) | 2015-06-26 | 2016-06-24 | Métodos de purificación y/o inactivación viral |
Country Status (16)
| Country | Link |
|---|---|
| US (1) | US10906953B2 (es) |
| EP (2) | EP3628675A1 (es) |
| JP (2) | JP6845813B2 (es) |
| KR (1) | KR20180020982A (es) |
| CN (2) | CN107709350A (es) |
| AU (1) | AU2016282916B2 (es) |
| CA (1) | CA2990311A1 (es) |
| CL (1) | CL2017003309A1 (es) |
| CO (1) | CO2018000171A2 (es) |
| ES (1) | ES2770860T3 (es) |
| HK (1) | HK1253557A1 (es) |
| MX (1) | MX2017016437A (es) |
| MY (1) | MY179524A (es) |
| PH (1) | PH12017502386A1 (es) |
| RU (1) | RU2719468C2 (es) |
| WO (1) | WO2016207353A1 (es) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2018326556A1 (en) | 2017-09-01 | 2020-03-05 | Ferring B.V. | Composition for controlled ovarian stimulation |
| CN110563832A (zh) * | 2019-07-31 | 2019-12-13 | 江苏璟泽生物医药有限公司 | 一种高纯度重组促卵泡刺激素纯化方法 |
| CN110305903B (zh) * | 2019-07-31 | 2021-10-01 | 江苏璟泽生物医药有限公司 | 重组人促卵泡激素及其制备方法 |
| KR200493431Y1 (ko) | 2019-10-23 | 2021-03-29 | (주)에르젠아웃도어 | 다기능 캠핑용 타프 |
| KR20220020526A (ko) | 2020-08-12 | 2022-02-21 | 주식회사 엘지화학 | 유체 흐름 분배기가 구비된 열교환기 |
Family Cites Families (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR1311764A (fr) | 1959-12-29 | 1962-12-14 | Procédé de purification de la gonadotropine folliculo-stimulante | |
| FR2580503B1 (fr) | 1985-04-23 | 1988-02-19 | Limousin Inst Bio | Perfectionnements apportes a la preparation des inhibiteurs de l'adhesion cellulaire, anti-adhesines ainsi obtenues et medicaments et aliments les contenant |
| US4939176A (en) * | 1988-12-20 | 1990-07-03 | Miles Inc. | Viral inactivation process |
| EP0452753B1 (en) * | 1990-04-19 | 2004-06-23 | Bayer Corporation | Method for preparing essentially monomeric normal serum albumin (human) |
| US5561115A (en) * | 1994-08-10 | 1996-10-01 | Bayer Corporation | Low temperature albumin fractionation using sodium caprylate as a partitioning agent |
| WO2000056768A2 (en) | 1999-03-19 | 2000-09-28 | Bayer Corporation | Chromatographic albumin process |
| RS20060077A (en) * | 2003-08-12 | 2008-08-07 | Octapharma Ag., | Process for preparing an alpha-1-antitrypsin solution |
| TWI488640B (zh) * | 2008-04-16 | 2015-06-21 | Ferring Int Ct Sa | 藥學製劑 |
| CN101397339B (zh) | 2008-09-24 | 2012-07-25 | 上海天伟生物制药有限公司 | 糖蛋白中去除/灭活病毒的方法 |
| TWI532495B (zh) * | 2009-10-05 | 2016-05-11 | 菲瑞茵國際中心股份有限公司 | 藥學製劑 |
| US10562958B2 (en) * | 2011-04-08 | 2020-02-18 | Universidad De Costa Rica | Method for producing injectable formulations of blood-derived protein materials, and materials obtained using said method |
| JO3092B1 (ar) | 2011-08-08 | 2017-03-15 | Ferring Bv | مركب لتحفيز مسيطر عليه للمبيض |
| CN103275206B (zh) | 2013-03-17 | 2014-09-10 | 赤峰博恩药业有限公司 | 孕马血清促性腺激素的提纯方法 |
| KR102356757B1 (ko) | 2013-10-18 | 2022-02-03 | 노바셉 이큅먼트 솔루션즈 | 단백질 정제 |
-
2016
- 2016-06-24 EP EP19206053.1A patent/EP3628675A1/en not_active Withdrawn
- 2016-06-24 AU AU2016282916A patent/AU2016282916B2/en active Active
- 2016-06-24 JP JP2017567128A patent/JP6845813B2/ja active Active
- 2016-06-24 EP EP16734237.7A patent/EP3313859B1/en active Active
- 2016-06-24 RU RU2017145983A patent/RU2719468C2/ru active
- 2016-06-24 US US15/737,524 patent/US10906953B2/en active Active
- 2016-06-24 CA CA2990311A patent/CA2990311A1/en active Pending
- 2016-06-24 CN CN201680037620.XA patent/CN107709350A/zh active Pending
- 2016-06-24 CN CN202210499038.2A patent/CN115028675A/zh active Pending
- 2016-06-24 MX MX2017016437A patent/MX2017016437A/es unknown
- 2016-06-24 KR KR1020177036747A patent/KR20180020982A/ko not_active Application Discontinuation
- 2016-06-24 MY MYPI2017704932A patent/MY179524A/en unknown
- 2016-06-24 WO PCT/EP2016/064668 patent/WO2016207353A1/en active Application Filing
- 2016-06-24 ES ES16734237T patent/ES2770860T3/es active Active
-
2017
- 2017-12-21 PH PH12017502386A patent/PH12017502386A1/en unknown
- 2017-12-21 CL CL2017003309A patent/CL2017003309A1/es unknown
-
2018
- 2018-01-10 CO CONC2018/0000171A patent/CO2018000171A2/es unknown
- 2018-10-08 HK HK18112761.2A patent/HK1253557A1/zh unknown
-
2020
- 2020-10-30 JP JP2020182008A patent/JP7061654B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CO2018000171A2 (es) | 2018-04-30 |
| EP3313859A1 (en) | 2018-05-02 |
| HK1253557A1 (zh) | 2019-06-21 |
| PH12017502386B1 (en) | 2018-06-25 |
| AU2016282916B2 (en) | 2022-01-20 |
| US20190002518A1 (en) | 2019-01-03 |
| MX2017016437A (es) | 2018-03-02 |
| RU2017145983A3 (es) | 2019-09-05 |
| CN115028675A (zh) | 2022-09-09 |
| EP3313859B1 (en) | 2019-11-20 |
| JP2018521049A (ja) | 2018-08-02 |
| MY179524A (en) | 2020-11-10 |
| AU2016282916A1 (en) | 2017-12-21 |
| US10906953B2 (en) | 2021-02-02 |
| KR20180020982A (ko) | 2018-02-28 |
| JP2021036876A (ja) | 2021-03-11 |
| RU2719468C2 (ru) | 2020-04-17 |
| CL2017003309A1 (es) | 2018-04-20 |
| JP6845813B2 (ja) | 2021-03-24 |
| CA2990311A1 (en) | 2016-12-29 |
| CN107709350A (zh) | 2018-02-16 |
| WO2016207353A1 (en) | 2016-12-29 |
| PH12017502386A1 (en) | 2018-06-25 |
| RU2017145983A (ru) | 2019-07-29 |
| EP3628675A1 (en) | 2020-04-01 |
| JP7061654B2 (ja) | 2022-04-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2770860T3 (es) | Métodos de purificación y/o inactivación viral | |
| KR100900753B1 (ko) | 인터페론-베타의 무-hsa 조제물 | |
| KR100617648B1 (ko) | 혈장 또는 혈청을 함유하는 아벨리노 각막 이영양증 치료용약학 조성물 | |
| EA007967B1 (ru) | Защита, восстановление и усиление эритропоэтинреактивных клеток, тканей и органов | |
| CN103052398A (zh) | 稳定fsh | |
| NO324659B1 (no) | Utvinning av von Willebrand-faktor ved kationebytterkromatografi samt preparat inneholdende slik faktor og anvendelse derav. | |
| ES2278722T3 (es) | Hlh purificada recombinante que tiene una bioactividad especifica y procedimiento para su purificacion. | |
| BR112013015802A2 (pt) | método para extrair albumina de soro humano a partir de grão de arroz transgênico | |
| CN116023466B (zh) | 纯化PEG修饰重组人干扰素β1b蛋白的方法 | |
| JPS6289627A (ja) | 経鼻投与用貧血治療剤 | |
| ES2525381T3 (es) | Péptidos cíclicos para la regulación de canales iónicos vectoriales | |
| WO2012104355A1 (de) | Antivirales mittel enthaltend rekombinante mistellektine | |
| EA033742B1 (ru) | ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ПОДКОЖНОГО ВВЕДЕНИЯ, СОДЕРЖАЩАЯ РАСТВОРИМЫЙ Fc-РЕЦЕПТОР, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЛЕКАРСТВЕННУЮ ФОРМУ, И ПРИМЕНЕНИЕ ЛЕКАРСТВЕННОЙ ФОРМЫ И ФАРМАЦЕВТИЧЕСКОЙ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ АУТОИММУННЫХ ЗАБОЛЕВАНИЙ | |
| ES2843685T3 (es) | Composición farmacéutica líquida de eritropoyetina conjugada | |
| JP2632014B2 (ja) | 骨髄機能障害性貧血治療剤 | |
| WO2021257523A1 (en) | Use of arginase for treatment of influenza infections | |
| ES2540862T3 (es) | Formulaciones para el factor estimulante de colonias de granulocitos bovino y sus variantes | |
| JPS6231A (ja) | 腎性貧血治療剤 | |
| US20090047239A1 (en) | Stabilised IL-21 Compositions | |
| RU2438680C1 (ru) | Способ получения препарата фолликулостимулирующего гормона из аденогипофизов животных | |
| JP5628395B1 (ja) | 免疫グロブリン液状組成物 | |
| CN101671388A (zh) | 血脑屏障穿透性促红细胞生成素及其应用 |