EP0233145A1 - Polymerzusammensetzungen enthaltend einen gelösten Dibenzalaceton-Palladiumkomplex - Google Patents
Polymerzusammensetzungen enthaltend einen gelösten Dibenzalaceton-Palladiumkomplex Download PDFInfo
- Publication number
- EP0233145A1 EP0233145A1 EP87810046A EP87810046A EP0233145A1 EP 0233145 A1 EP0233145 A1 EP 0233145A1 EP 87810046 A EP87810046 A EP 87810046A EP 87810046 A EP87810046 A EP 87810046A EP 0233145 A1 EP0233145 A1 EP 0233145A1
- Authority
- EP
- European Patent Office
- Prior art keywords
- polymer
- oder
- photoresist
- complex
- hydrogen
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C23—COATING METALLIC MATERIAL; COATING MATERIAL WITH METALLIC MATERIAL; CHEMICAL SURFACE TREATMENT; DIFFUSION TREATMENT OF METALLIC MATERIAL; COATING BY VACUUM EVAPORATION, BY SPUTTERING, BY ION IMPLANTATION OR BY CHEMICAL VAPOUR DEPOSITION, IN GENERAL; INHIBITING CORROSION OF METALLIC MATERIAL OR INCRUSTATION IN GENERAL
- C23C—COATING METALLIC MATERIAL; COATING MATERIAL WITH METALLIC MATERIAL; SURFACE TREATMENT OF METALLIC MATERIAL BY DIFFUSION INTO THE SURFACE, BY CHEMICAL CONVERSION OR SUBSTITUTION; COATING BY VACUUM EVAPORATION, BY SPUTTERING, BY ION IMPLANTATION OR BY CHEMICAL VAPOUR DEPOSITION, IN GENERAL
- C23C18/00—Chemical coating by decomposition of either liquid compounds or solutions of the coating forming compounds, without leaving reaction products of surface material in the coating; Contact plating
- C23C18/16—Chemical coating by decomposition of either liquid compounds or solutions of the coating forming compounds, without leaving reaction products of surface material in the coating; Contact plating by reduction or substitution, e.g. electroless plating
- C23C18/18—Pretreatment of the material to be coated
- C23C18/20—Pretreatment of the material to be coated of organic surfaces, e.g. resins
- C23C18/28—Sensitising or activating
- C23C18/30—Activating or accelerating or sensitising with palladium or other noble metal
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S430/00—Radiation imagery chemistry: process, composition, or product thereof
- Y10S430/145—Infrared
Definitions
- the invention relates to polymer compositions in which a dibenzalacetone-palladium complex is dissolved, a process for electroless metal deposition on substrate surfaces and the use of said polymer compositions in the production of metallized surfaces or of conductive patterns on substrate surfaces.
- EP-A 125 617 describes mixtures of polymers and organometallic complexes. Pd-II complexes but no Pd ° complexes, for example dibenzalacetone-palladium complexes, are mentioned. Pd metal can be deposited from such Pd-II complexes either reductively or by heating to relatively high temperatures. The thermally activated polymer surfaces are suitable according to EP-A 125 617
- R 1 , R 2 , R 4 and R 5 as alkyl and alkoxy groups can be straight-chain or branched. Examples include: methyl, ethyl, n-propyl, isopropyl, n-butyl, sec-butyl, tert.
- R 1 , R 2 , R 4 and R 5 carry non-polar substituents, for example C 1 -C 4 alkyl or alkoxy radicals, as substituted phenyl. Examples include methyl, ethyl or methoxy.
- Examples of preferred substituted phenyl radicals R 1 , R 2 , R 4 and R 5 are o-, m- or p-tolyl, o-, m- or p-methoxyphenyl or 2,3-, 2,4-, 2,5 -, 2,6- or 3,5-dimethylphenyl.
- m is preferably a number from 2-4 and n is preferably a number from 0-10, particularly preferably 0-6.
- group C m H 2m means ethylene, 1,2- or 1,3-propylene or 1,4-butylene.
- the halogen atom R 2 can be fluorine, chlorine, bromine or iodine. Chlorine and bromine, in particular chlorine, are preferred.
- R 2 is a glycidyl ether radical, it is preferably a group of the formula II wherein R 6 and R 8 each represent a hydrogen atom, where R 7 is then a hydrogen atom or a methyl group, or wherein R 6 and R 8 together represent -CH 2 CH 2 -, where R 7 is then a hydrogen atom.
- R 2 as glycidyl ether radical is preferably a group of the formula III
- R 3 as C 1 -C 4 -alkyl is preferably straight-chain. Examples of such radicals are methyl, ethyl, propyl or butyl, but particularly preferably methyl.
- R 3 is preferably hydrogen.
- R 3 groups together form a C 2 -C 4 polymethylene chain, these are, for example, ethylene, trimethylene and tetramethylene.
- R 4 and R 5 are preferably hydrogen.
- the compounds of the formula can also be in the form of mixtures with different meanings of q.
- q is preferably 2 to 3.5.
- compositions containing compounds of the formula 1 in which R 1 is hydrogen, R 2 is C 1 -C 12 alkyl, C 1 -C 4 alkoxy, halogen or a glycidyl ether radical are preferred, R 3 is hydrogen and q is a number from 2 to 3, 5 is.
- compositions containing compounds of the formula I in which R 1 is hydrogen, R 2 is C 1 -C 5 alkyl, in particular isopropyl, R 3 is hydrogen and q is a number from 2 to 3.5 are particularly preferred.
- the groups R 2 are preferably each in the p-position.
- the palladium complexes of the formula dissolve in high concentrations in many commercially available polymers.
- the polymers can be soluble or insoluble in organic solvents; i.e. linear or cross-linked polymers.
- the cross-linked polymer precursors must be soluble in organic solvents.
- the solvents used are those which do not decompose the palladium complex I, preferably apolar organic solvents.
- solvents examples include aliphatic or aromatic hydrocarbons, such as n-hexane, n-heptane, cyclohexane, benzene, toluene or xylene, ethers, such as di-n-butyl ether, diethyl ether, diphenyl ether, 1,4-dioxane, anisole tetrahydrofuran , diethylene glycol diethyl ether, Ethylenglykoldimethyl ether or triethylene glycol dimethyl ether, halogenated hydrocarbons such as carbon tetrachloride, chlorobenzene, bromobenzene, chloroform, dichloromethane or 1,2-dichloroethane, ketones such as cyclohexanone, methyl ethyl ketone, acetophenone or acetone, and esters such as ethyl acetate.
- the respective polymers are considered soluble if they dissolve in the solvent in question at room temperature to at least 1 mg / l, preferably at least 10 mg / l.
- the polymers preferably have a glass transition temperature of more than 90 ° C.
- the polymer component in the mixtures according to the invention must be free from olefinic double bonds or conjugated, non-aromatic double bond systems.
- the palladium complex is selected such that it is not polymerized into the polymer matrix in the subsequent crosslinking step.
- compositions containing as component a) a polymer (mixture) which is soluble in organic solvents are preferred.
- compositions in which the polymer is selected from the group consisting of polystyrene, polyvinyl chloride, polycarbonate, polyarylate and polyimide soluble in organic solvents are particularly preferred.
- compositions according to the invention may equally well contain, as component a), a crosslinked or crosslinkable polymer, for example an epoxy resin.
- a crosslinked or crosslinkable polymer for example an epoxy resin.
- the palladium complex should be chosen so that it is not polymerized into the polymer structure, but only remains dissolved in it.
- the invention therefore preferably relates to compositions as defined above, containing as component a) an epoxy resin.
- epoxy resins which are suitable for the construction of crosslinked substrates and of hardeners for these resins can be found in Ullmann's Encyclopedia of Industrial Chemistry, Volume 10, 2. 563-580 (4th edition, Verlag Chemie, Weinheim / Bergstr .; 1975).
- the proportion of dibenzalacetone-palladium complex of the formula 1 in the compositions according to the invention is generally 0.1-25% by weight, preferably 0.5-10% by weight, based on the total mixture.
- the mixtures according to the invention can also contain other known customary additives.
- additives are pigments, dyes, reinforcing materials such as glass fibers, flame retardants, antistatic agents, flow control agents, release agents, adhesion promoters, antioxidants and light stabilizers.
- the mixtures according to the invention can also contain electrically conductive fillers c), expediently in amounts of 1-90% by weight, particularly 40-80% by weight, based on the total weight of the mixture, components a) to c) add up to 100% by weight.
- electrically conductive fillers are those of an organic or inorganic type, e.g. Carbon black and graphite or metals of groups Vb, Vlb, VIII and Ib of the periodic table, alloys and salts thereof, such as halides, oxides and sulfides.
- suitable metals and metal compounds are: vanadium, niobium, tantalum, molybdenum, tungsten, copper, noble metals, such as Pt, Pd, Ag and Au, AgPd alloys, silver oxide, silver iodide, copper (il) sulfide, copper (1) iodide, Copper (II) oxide, gold (III) bromide, iodide and oxide, molybdenum (IV) sulfide, niobium (V) chloride and oxide, palladium iodide, palladium oxide, platinum (VI) bromide and chloride, vanadium (III) chloride, vanadium (IV) oxide, tungsten (VI) chloride and oxide.
- Silver, copper, silver / palladium alloys, palladium, platinum, gold, tungsten and molybdenum are preferred.
- Au, Pt AgPd and especially Ag and Cu powder are particularly preferred.
- compositions according to the invention can be prepared in a simple manner by dissolving the polymer or its crosslinkable precursor combined with a suitable crosslinking agent and the complex together and then pouring this solution into films in a manner known per se or applying it to a suitable substrate and optionally then hardens.
- Suitable substrates are common materials, which are preferably electrically non-conductive. Examples include paper, wood, glass, ceramics, semiconductors such as silicon, germanium or gallium arsenide, and in particular plastics, preferably hardened epoxy resins.
- metallic substrates such as aluminum or copper, can also be coated with the mixtures.
- the substrate is coated using customary methods, for example by immersion, brushing and spraying processes, spin coating, cascade casting or curtain casting coating.
- the polymer or its crosslinkable precursor and complex I can be dissolved together in a solvent. However, it is also possible to use mixtures of different solvents or to combine separate solutions of polymer or crosslinkable precursor and complex in different solvents.
- an adhesion promoter can be added to the solution.
- an adhesion promoter you can e.g. use a linear, soluble epoxy polymer.
- the compounds of formula 1 can be prepared by processes known per se (cf., for example, J. Chem.Soc. D, 1970, 1065 and US Pat. No. 4,347,323) by q mol of a compound of formula IV in the presence of a base and optionally an H donor with a soluble palladium salt.
- R 1 , R 2 , R 3 and q have the meaning given under formula I.
- Alkali metal salts of aliphatic monocarboxylic acids can be used as bases.
- Suitable palladium salts are, for example, PdBr 2 , PdCl 2 and Na 2 PdCl 4 .
- Na 2 PdC 1 4 and especially PdCl 2 are particularly preferably used.
- the reaction is expediently carried out in an organic solvent which also acts as an H donor. Suitable for this purpose are, for example, alkanols with up to 6 carbon atoms, especially ethanol and particularly preferably methanol.
- the compounds of the formula IV can be prepared in a manner known per se, for example analogously to the process described in US Pat. No. 3,295,974.
- composition according to the invention can be used for the electroless metallization of plastics or for the production of structured metal surfaces on plastics.
- the activation for the electroless metal deposition is carried out by heating to temperatures above 100 ° C., preferably to 100-250 ° C., particularly preferably to 150-200 ° C.
- the heating can be carried out, for example, by annealing the sample or by irradiation with IR radiation.
- Sources such as IR lasers, or the IR component of actinic radiation sources (for example xenon lamps, argon lamps, tungsten lamps, carbon arcs, metal halide and metal arc lamps, such as mercury lamps) take place.
- the temperature treatment releases finely dispersed, catalytically active palladium.
- Irradiation with IR sources can also take place in an image, e.g. by a laser beam that is guided over the surface.
- the annealing process can take between 1 and 60 minutes depending on the temperature; the tempering times are surprisingly very short.
- the Pd ° clusters formed are catalytically active and catalyze the electroless metallization (eg nickel plating, copper plating) of the polymer surface, for example according to the following scheme:
- Electroless metal deposition can be carried out using metallization baths known per se and by customary methods.
- suitable metals are copper, nickel, cobalt, silver, gold and tin or cobalt-phosphorus and cobalt-nickel alloys.
- composition according to the invention in a structured manner to a substrate, for example by means of a screen printing or a selectively controlled spray mist recording method. Suitable recording methods are described for example in DE-OS 3,326,508.
- the structuring can also be carried out using a photoresist.
- a substrate is coated with a photoresist in a manner known per se.
- the palladium complex 1 can either be dissolved in the photoresist or in an underlying polymer substrate, preferably a polymer layer.
- the sample is annealed and immersed in a metallizing bath.
- the metal deposition now takes place either on the structured photoresist or on the polymer substrate structured by the photoresist.
- stage (iii) and (iv) you can switch on a tempering step between stage (iii) and (iv) to pre-harden the exposed photoresist.
- the materials customary in technology can be used as photoresists.
- photoresist also includes olefinically unsaturated compounds. P.S. gives an overview of imaging processes with such varnishes and selected compound classes. Pappas in “UV Curing: Science and Technology", Chapter 9, pp. 230-253 (1973).
- the photoresist must of course be chosen so that a structure created by the irradiation and development step survives the annealing step without major distortions.
- Such systems are known to the person skilled in the art or can be selected using routine methods.
- a radiation-sensitive polymer system is chosen as the photoresist, the polymer having no olefinic double bonds.
- good results can already be achieved with relatively small amounts of the Pd compound.
- less than 10% by weight of the complex of the formula I, based on the polymer solution is sufficient in order to obtain a catalytically active surface after the exposure and tempering step.
- preference is given to using 1-5% by weight of the complex of the formula 1, based on the polymer solution.
- Examples of radiation-sensitive polymer systems with polymers without olefinic double bonds are combination ions of epoxy resins with photoinitiators of cationic polymerization.
- exposure to a predetermined pattern of actinic radiation means both exposure through a photomask that contains a predetermined pattern, such as a slide, and exposure through a laser beam that is moved, for example, computer-controlled, over the surface, and thus Image created.
- actinic radiation When generating images using a photoresist, actinic radiation of 200 to 600 nm is preferably used. Suitable sources of actinic radiation include carbon arcs, mercury vapor lamps, fluorescent lamps with ultraviolet light-emitting phosphors, argon and xenon incandescent lamps, tungsten lamps and photographic floodlight lamps. However, X-rays or electron beams as well as high-energy radiation can also be used.
- developers can take place, for example, with water, aqueous or aqueous-organic solutions of a base or acid, organic solvents or solvent mixtures.
- Another object of the invention is the use of the mixtures according to the invention for electroless metal deposition, in particular for producing electrically conductive patterns on plastic surfaces.
- patterns according to the invention patterns with high resolution can be achieved.
- Such products can be used, for example, as printed circuits.
- Example 1 Tris (dibenzalacetone-p, p'-diglycidyl ether) palladium.
- a precipitate is formed which is filtered off under argon and washed once with 100 ml of methanol, three times with 100 ml of water and twice with 100 ml of methanol. The product is then dried at 50 ° C in a vacuum. To completely remove residual dibenzalacetone-bis-p, p'-diglycidyl ether, the crystals are suspended again in 700 ml of methanol and filtered off under argon. It is then dried in vacuo. 100.7 g of violet crystals (97% of theory) are obtained. Decomposition range: 120-160 ° C. The analysis gives a value of 3.2 for q.
- Example 2 Tris (p, p'-diisopropyldibenzalacetone) palladium.
- Example 3 Bis (dibenzalacetone) palladium.
- Examples BE One works as described in example A.
- the working conditions of the experiments AE are described in the following table.
- Well-adhering nickel or copper coatings are obtained in each case.
- Example F An epoxy resin plate (60x40x2mm) is coated with a 50 ⁇ m thick polymer film of the composition according to Example C. After the solvent has evaporated, the plate 6 min. heated to 170 ° C and then immersed in one of the nickel plating baths described in Example A. The surface is covered with a well-adhering nickel film.
- Example G Execution as described in Example F. A glass plate is used as the substrate.
- Example H Execution as described in Example F. An aluminum plate is used as the substrate.
- Example 1 0.25 g of the complex according to Example 1 is dissolved in 20 g of 1,2-dichloroethane in a solution of 5 g of a linear polyepoxide * ). With this solution a 50 ⁇ m thick polymer film is produced on an epoxy resin plate (60x40x2mm). After the solvent has evaporated, the coated epoxy resin plate is 6 min. heated to 170 ° C and then immersed in one of the nickel deposition baths described in Example A. A well adhering nickel film is formed on the coated resin surface.
- the epoxy polymer is a linear addition copolymer consisting of a diglycidyl ether based on bisphenol A (epoxy value: 5.3 Val / kg) and benzylamine in a molar ratio of 1: 1.
- the production follows the in J. Polym. Sci. Polym. Chem. Ed., 22 249 (1984).
- Example J 0.5 g of the complex according to Example 1, 0.5 g of the linear polyepoxide according to Example 1 and 10.0 g Makrolon® (cf. Example C) are dissolved in 70 g 1,2 dichloroethane. An epoxy resin plate is treated with the solution obtained as described in Example I. A well adhering nickel film is obtained on the coated resin surface.
- Example K 11.2 g (56.0% by weight) of a diglycidyl ether based on bisphenol A (epoxy value: 5.25-5.4 Vat / kg), 7.8 g (39.0% by weight) of hexahydropthalic anhydride and 1.0 g (5.0% by weight) of the complex according to Example 2 are mixed at 90 ° C. for 15 minutes. Then 0.06 g of benzyldimethylamine is added as an accelerator. After a further 5 minutes at 90 ° C., the mixture is poured into a mold preheated to 100 ° C. and cured for 4 hours at 100 ° C. and for a further 4 hours at 120 ° C.
- the molded body is tempered for a further 2 hours at 240 ° C. and then coated with nickel in a commercial nickel plating bath (Shipley Niposit® 468 or Niposit® PM 980). A well adhering nickel coating is obtained.
- the nickel plating can also be carried out using the nickel plating bath according to example A. Comparable results are achieved.
- Example L 22.4 g (50.8 wt.%) Of a diglycidyl ether based on bisphenol A (epoxy value: 5.25-5.4 val / kg), 15.4 g (34.9 wt.%) Hexahydrophthalic anhydride and 6. 3 g (14.3% by weight) of the complex according to Example 3 are mixed at 90 ° C. for 15 minutes. Then 0.1 g of benzyldimethylamine is added as an accelerator. After a further 5 minutes at 90 ° C., the mixture is poured into a mold preheated to 100 ° C. and cured for 4 hours at 100 ° C. and for a further 4 hours at 120 ° C.
- the molded body is annealed at 240 ° C. for 1 hour and then coated with nickel in a commercial nickel plating bath (Shipley Nisposit® 468 or Nisposit® PM 980). A well adhering nickel coating is obtained.
- the nickel plating can also be carried out with comparably good results using the nickel plating bath described in Example A.
- Example M 0.25 g tris (p, p'-diisopropyldibenzalacetone) palladium and 0.2 g polystyrene are dissolved in 20 ml toluene. This solution is used as a writing ink in a Hewlett-Packard "Thinkjet" printer with a modified writing head * ). With the printer, a text is written on a transparency for normal copiers (Folex® X-100). The film is then 15 min. annealed at 170 ° C. The film is then immersed in one of the nickel deposition baths written in Example A (duration 15 minutes). A nickel coating adheres well to the film at the printed areas.
- the ink reservoir is made of aluminum to increase resistance to organic solvents. In addition, all bonds are made with the solvent-resistant Araldit® adhesive.
- Example N 20 g of a photoresist from 120 parts by weight of a technical epoxy cresol novolak (epoxy content 4.5 equivalents / kg), 50 parts by weight a technical bisphenol A epoxy resin (epoxy content 0.5 eq./kg), 20 parts by weight Talc, 1 part by weight Irgatith green, 2 parts by weight ( ⁇ 6 -stylbene) ( ⁇ 5 -cyclopentadienyl) iron (II) hexafluorophosphate and 200 parts by weight Cyclohexanone is mixed with a solution of 0.5 g of the complex according to Example 2 in 15 ml of dichloroethane and mixed well.
- a technical epoxy cresol novolak epoxy content 4.5 equivalents / kg
- a technical bisphenol A epoxy resin epoxy content 0.5 eq./kg
- Talc 1 part by weight Irgatith green
- ⁇ 6 -stylbene ⁇ 5 -cyclopentadie
- This mixture is applied to a glass plate (200x100x4 mm) using a 70 ⁇ squeegee.
- the applied lacquer is dried for one hour at 80 ° C.
- the paint is exposed through a mask (5000 W Hg high-pressure lamp Berner M 061), 20 min. hardened at 135 ° C, and then developed by immersion in cyclohexanone for 1 1/2 min.
- annealing is carried out at 230 ° C in a forced air oven for one hour.
- the plate is then nickel-plated in a metallizing bath described in Example A. A well adhering nickel coating is created on the structured surface of the photoresist.
- Example 0 The procedure is as in Example N. Instead of a glass plate, an epoxy carbon fiber laminate is used as the substrate. After the irradiation, 10 min. hardened at 135 ° C. After development and metallization, a well-adhering nickel coating is created on the structured surface of the photoresist.
Abstract
- a) mindestens ein organisches Polymeres und
- b) in diesem Polymeren einheitlich gelöst aber nicht damit copolymerisierbar einen Komplex der Formel 1
Description
- Die Erfindung betrifft Polymerzusammensetzungen, in denen ein Dibenzalaceton-Palladiumkomplex gelöst ist, ein Verfahren zur stromlosen Metallabscheidung auf Substratoberflächen sowie die Verwendung besagter Polymerzusammensetzungen bei der Herstellung von metallisiserten Oberflächen oder von leitfähigen Mustern auf Substratoberflächen.
- Aus der US-PS 3,993,807 ist es bekannt, dass Lösungen von Komplexen aus Palladium, Triphenylphosphit und einer olefinisch oder acetylenisch ungesättigten organischen Verbindung mit 3-16 C-Atomen oder von Dibenzalaceton-Palladium-Komplexen für die stromlose Metallabscheidung auf Substraten, wie Metallen, oxidierten Metallen und Kunststoffen, eingesetzt werden können. Dabei werden die zu beschichtenden Substrate ein oder mehrere Male in eine Lösung der Palladium-Komplexe getaucht, bevorzugt in Benzol oder Toluol-Lösungen, und auf 100-300° C erhitzt, wobei Palladium auf der Substrat-Oberfläche abgeschieden wird. Die so beschichteten Substrate eignen sich zur stromlosen Metallabscheidung. Eine Vorbehandlung des zu metallisierenden Substrates mit einem Aktivierbad kann allerdings zu Problemen führen (ungenügende Benetzung, Quellung der Oberfläche).
- In der EP-A 125 617 sind Mischungen aus Polymeren und Organometallkomplexen beschrieben. Es werden Pd-II-Komplexe aber keine Pd°-Komplexe, beispielsweise Dibenzalaceton-Palladiumkomplexe, erwähnt. Aus solchen Pd-II-Komplexen lässt sich Pd-Metall entweder reduktiv oder durch Erhitzen auf relativ hohe Temperaturen abscheiden. Die thermisch aktivierten Polymeroberflächen eignen sich nach der EP-A 125 617
- zur stromlosen Metallabscheidung.
- Die vorliegende Erfindung betrifft Zusammensetzungen enthaltend
- a) mindestens ein organisches Polymeres und
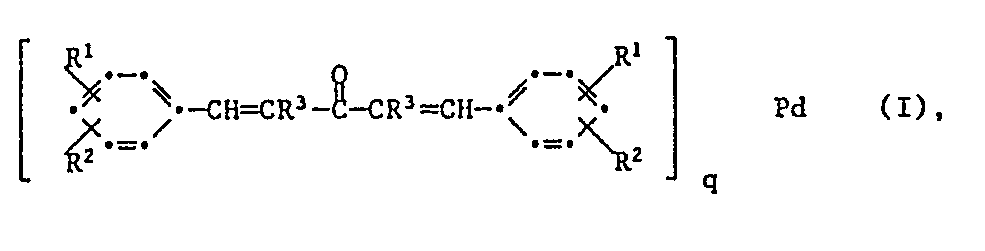
- b) in diesem Polymeren einheitlich gelöst aber nicht damit copolymerisierbar einen Dibenzalaceton-Palladiumkomplex der Formel 1
R3 Wasserstoff oder C1-C4Alkyl ist oder die beiden Gruppen R3 zusammen eine Polymethylenkette von 2-4 Kohlenstoffatomen bilden, R4 und R5 eine der Bedeutungen von R1 besitzen und
q eine Zahl von 1 bis 3,5 ist, m für eine Zahl von 2 bis 6 und n für eine Zahl von 0 bis 20 steht, mit der Massgabe, dass die Zusammensetzung kein Polymeres mit einer olefinischen Doppelbindung enthält. - R1, R2, R4 und R5 als Alkyl- und Alkoxygruppen können geradkettig oder verzweigt sein. Als Beispiele seien genannt: Methyl, Ethyl, n-Propyl, Isopropyl, n- Butyl, sek.Butyl, tert. Butyl, n-Pentyl, n-Hexyl, n-Heptyl, n-Octyl, 2-Ethylhexyl, n-Decyl, n-Dodecyl, n-Tetradecyl, n-Hexadecyl oder n-Octadecyl, sowie Methoxy, Ethoxy, n-Propoxy, Isopropoxy, n-Butoxy, sek. Butoxy, tert.Butoxy, Pentoxy oder Hexoxy.
- Als substituiertes Phenyl tragen Rl, R2, R4 bzw. R5 nichtpolare Substituenten, beispielsweise C1-C4-Alkyl-oder -Alkoxyreste. Beispiele dafür sind insbesondere Methyl, Ethyl oder Methoxy.
- Beispiele für bevorzugte substitutierte Phenylreste R1, R2, R4 und R5 sind o-, m- oder p-Tolyl, o-, m- oder p-Methoxyphenyl oder 2,3-, 2,4-, 2,5-, 2,6- oder 3,5-Dimethylphenyl.
- In der Gruppe -(O-CmH2m-)n-OR4 ist m bevorzugt eine Zahl von 2-4 und n bevorzugt eine Zahl von 0-10, besonders bevorzugt 0-6. Insbesondere bedeutet die Gruppe CmH2m Ethylen, 1,2- oder 1,3-Propylen oder 1,4-Butylen.
- Als Halogenatom kann R2 Fluor, Chlor, Brom oder lod bedeuten. Bevorzugt werden Chlor und Brom, insbesondere Chlor.
-
-
- Bilden beide Reste R3 zusammen eine C2-C4Polymethylenkette, so handelt es sich dabei beispielsweise um Ethylen, Trimethylen und Tetramethylen. R4 und R5 sind vorzugsweise Wasserstoff.
- Die Verbindungen der Formel können auch in Form von Gemischen mit unterschiedlicher Bedeutung von q vorliegen. q ist vorzugsweise 2 bis 3,5.
- Bevorzugt werden Zusammensetzungen enthaltend Verbindungen der Formel 1, worin R1 Wasserstoff ist, R2 C1-C12Alkyl, C1-C4Alkoxy, Halogen oder ein Glycidyletherrest ist, R3 Wasserstoff bedeutet und q eine Zahl von 2 bis 3,5 ist.
- Besonders bevorzugt werden Zusammensetzungen enthaltend Verbindungen der Formel I, worin R1 Wasserstoff ist, R2 C1-C5Alkyl, insbesondere Isopropyl, ist, R3 Wasserstoff bedeutet und q eine Zahl von 2 bis 3, 5 ist.
- Vorzugsweise befinden sich die Gruppen R2 jeweils in p-Position.
- Ueberraschenderweise lösen sich die Palladiumkomplexe der Formel in hohen Konzentrationen in vielen handelsüblichen Polymeren. Die Polymeren können löslich oder unlöslich in organischen Lösungsmitteln sein; d.h., es handelt sich um lineare oder um vernetzte Polymere. Jedoch müssen die Vorstufen der vernetzten Polymeren in organischen Lösungsmitteln löslich sein.
- Bei den verwendeten Lösungsmitteln handelt es sich um solche, die den Palladiumkomplex I nicht zersetzen, bevorzugt um apolare organische Lösungsmittel.
- Beispiele für solche Lösungsmittel sind aliphatische oder aromatische Kohlenwasserstoffe, wie beispielsweise n-Hexan, n-Heptan, Cyclohexan, Benzol, Toluol oder Xylol, Ether, wie beispielsweise Di-n-butylether, Diethylether, Diphenylether, 1,4-Dioxan, Anisol Tetrahydrofuran, Diethylenglykoldiethylether, Ethylenglykoldimethyl ether oder Triethylenglykoldimethylether, halogenierte Kohlenwasserstoffe, wie beispielsweise Tetrachlorkohlenstoff, Chlorbenzol, Brombenzol, Chloroform, Dichlormethan oder 1,2-Dichlorethan, Ketone, wie beispielsweise Cyclohexanon, Methylethylketon, Acetophenon oder Aceton, sowie Ester, wie beispielsweise Essigsäureethylester. Bevorzugt werden Zusammensetzungen enthaltend als Komponente a) ein in organischen Lösungsmitteln lösliches Polymer(gemisch).
- Als löslich werden die jeweiligen Polymeren dann angesehen, wenn sie sich in dem betreffenden Lösungsmittel bei Raumtemperatur zu wenigstens 1 mg/I, vorzugsweise mindestens 10 mg/I, lösen.
- Als Polymersubstrate können die unterschiedlichsten Verbindungsklassen bzw. Gemische davon eingesetzt werden, sofern sie unter die oben angegebene Definition fallen.
- Vorzugsweise haben die Polymeren eine Glasübergangstemperatur von mehr als 90°C.
- Die Polymerkomponente in den erfindungsgemässen Mischungen muss frei von olefinischen Doppelbindungen oder konjugierten, nichtaromatischen Doppelbindungssystemen sein.
- Enthält die Polymerkomponente vernetzbare Gruppen für eine nach der Herstellung der Palladiumkomplex- /Präpolymerenmischung durchzuführende Vernetzungsreaktion, so wird der Palladiumkomplex so gewählt, dass er im anschliessenden Vernetzungsschritt nicht in die Polymermatrix einpolymerisiert wird.
- Beispiele für brauchbare Polymerklassen sind:
- 1. Polymere von Mono- und Diolefinen, beispielsweise Polyethylen (das gegebenenfalls vernetzt sein kann), Polypropylen, Polyisobutylen, Polybuten-1 oder Polymethylpenten-1, sowie Polymerisate von Cycloolefinen wie z.B. von Cyclopenten oder Norbornen.
- 2. Mischungen der unter 1) genannten Polymeren, z.B. Mischungen von Polypropylen mit Polyisobutylen.
- 3. Copolymere von Mono- und Diolefinen untereinander oder mit anderen Vinylmonomeren, wie z.B. Ethylen-Propylen-Copolymere, Propylen-Buten-1-Copolymere, Propylen-Isobutylen-Copolymere, Ethylen-Buten-1-Copolymere, Ethylen-Alkyacrylat-Copolymere oder Ethylen-Alkylmethacrylat-Copolymere oder Ethylen-Vinylacetat-Copolymere.
- 4. Polystyrol, Poly-(p-methylstyrol).
- 5. Copolymere von Styrol oder a-Methylstyrol mit Acrylderivaten, wie z.B. Styrol-Acrylnitril, Styrol-Alkylmethacrylat, Styrol-Maleinanhydrid, Styrol-Acrylnitril-Methylacrylat; Mischungen von hoher Schlagzähigkeit aus Styrol-Copolymeren und einem anderen Polymer wie z.B. einem Polyacrylat; sowie Block-Copolymere des Styrols, wie z.B. Styrol-Ethylen/Butylen-Styrol oder Styrol-Ethylen/Propylen-Styrol.
- 6. Pfropfcopolymere von Styrol, wie z.B. Styrol und Acrylnitril auf Polyalkylacrylaten oder Polyalkylmethacrylaten.
- 7. Halogenhaltige Polymere, wie z.B. Polychloropren, chloriertes oder chlorsulfoniertes Polyethylen, Epichlorhydrinhomo- und copolymere, insbesondere Polymere aus halogenhaltigen Vinylverbindungen, wie z.B. Polyvinylchlorid, Polyvinylidenchlorid, Polyvinylfluorid, Polyvinylidenfluorid; sowie deren Copolymere wie Vinylchlorid-Vinylchlorid-Vinylidenchlorid, Vinylchlorid-Vinylacetat oder Vinylidenchlorid-Vinylacetat; sowie chlorierter Kautschuk.
- 8. Polymere, die sich von Derviaten (Estern) a,ß-ungesättigter Säuren ableiten, wie Polyacrylate, Polymethacrylate und Polyacrylnitrile.
- 9. Copolymere der unter 8) genannten Monomeren untereinander oder mit anderen ungesättigten Monomeren, wie z.B. Acrylnitril-Alkylacrylat- Copolymere, Acrylnitril-Alkoxyalkylacrylat-Copolymere oder Acylnitril-Vinylhalogenid-Copolymere.
- 10. Homo- und Copolymere von cyclischen Ethern, wie Polyalklenglykole, Polyethylenoxyd, Polypropylenoxyd oder deren Copolymere mit Bisglycidylethern.
- 11. Polyphenyloxide und -sulfide und deren Mischungen mit Styrolpolymeren.
- 12. Polyimide, Polyetherimide, Polyesterimide und Polybenzimidazole.
- 13. Polyester, die sich von Dicarbonsäuren und Dialkoholen und/oder von Hydroxycarbonsäuren oder den entsprechenden Lactonen ableiten, wie Polyethylenterephthalat, Polybutylenterephthalat, Poly-1,4-dimethylotcyclohexanterephthalat, Polyhydroxybenzoate, sowie Block-Polyether-ester, die sich von Polyethern mit Hydroxylendgruppen ableiten.
- 14. Polycarabonate.
- 15. Polysulfone, Polyethersulfone und Polyetherketone.
- 16. Vernetzte oder vernetzbare Polymere, die sich von Aldehyden einerseits und Phenolen andererseits ableiten, wie Phenol-Formaldehydharze.
- 17. Nicht-trocknende Alkydharze.
- 18. Vernetzbare Acrylharze, die sich von substituierten Acrylsäureestern ableiten wie z.B. Epoxygruppen enthaltende Polyacrylate.
- 19. Alkydharze, Polyesterharze und Acrylatharze, die mit Epoxidharzen vernetzt sind.
- 20. Vernetzte oder vernetzbare Epoxidharze, die sich von Polyepoxiden ableiten, z.B. von Bis-glycidylethern oder von cycloaliphatischen Diepoxiden, sowie lineare Epoxidharze, beispielsweise solche auf Bisphenol A Basis.
- 21. Polymerhomolog chemisch agbewandelte Derivate von natürlichen Polymeren, wie Celluloseacetate, -propionate und -butyrate, bzw. die Celluloseether, wie Methylcellulose.
- 22. Mischungen (Polyblends) der vorgenannten Polymeren wie z.B. PVC/EVA.
- Bevorzugt werden Zusammensetzungen enthaltend als Komponente a) ein in organische Lösungsmitteln lösliches Polymer(gemisch).
- Besonders bevorzugt werden Zusammensetzungen, worin das Polymere ausgewählt wird aus der Gruppe bestehend aus Polystyrol, Polyvinylchlorid, Polycarbonat, Polyarylat und in organischen Lösungsmitteln löslichem Polyimid.
- Die erfindungsgemässen Zusammensetzungen können aber ebensogut als Komponente a) ein vernetztes oder vernetzbares Polymeres enthalten, beispielsweise ein Epoxidharz. In einem solchen Fall sollte der Palladiumkomplex so gewählt werden, dass er nicht in das Polymergerüst einpolymerisiert wird, sondern lediglich darin gelöst bleibt.
- Die Erfindung betrifft daher bevorzugt Zusammensetzungen, wie oben definiert, enthaltend als Komponente a) ein Epoxidharz.
- Beispiele für Epoxidharze, die sich zum Aufbau von vernetzten Substraten eignen, sowie von Härtern für diese Harze, findet man in Ullmanns Enzyklopädie der technischen Chemie, Band 10, 2. 563-580 (4. Auflage, Verlag Chemie, Weinheim/Bergstr.; 1975).
- Der Anteil an Dibenzalaceton-Palladiumkomplex der Formel 1 in den erfindungsgemässen Zusammensetzungen beträgt in der Regel 0,1-25 Gew.%, vorzugsweise 0,5-10 Gew.%, bezogen auf die Gesamtmischung.
- Die erfindungsgemässen Gemische können auch weitere bekannte übliche Zusatzstoffe enthalten. Beispiele für solche Zusatzstoffe sind Pigmente, Farbstoffe, Verstärkungsmaterialien, wie Glasfasern, Flammhemmer, Antistatika, Verlaufmittel, Trennmittel, Haftvermittler, Antioxidantien und Lichtschutzmittel.
- Die erfindungsgemässen Gemische können - neben weiteren üblichen Zusätzen - auch elektrisch leitende Füllstoffe c) enthalten, zweckmässig in Mengen von 1-90 Gew.%, besonders 40-80 Gew.%, bezogen auf das Gesamtgewicht des Gemisches, wobei sich die Komponenten a) bis c) auf 100 Gew.% ergänzen. Als elektrisch leitende Füllstoffe eignen sich solche organischer oder anorganischer Art, wie z.B. Russ und Graphit oder Metalle der Gruppen Vb, Vlb, VIII und Ib des periodischen Systems, Legierungen und Salze davon, wie Halogenide, Oxide und Sulfide.
- Beispiele geeigneter Metalle und Metallverbindungen sind: Vanadium, Niob, Tantal, Molybdän, Wolfram, Kupfer, Edelmetalle, wie Pt, Pd, Ag und Au, AgPd-Legierungen, Silberoxid, Silberjodid, Kupfer(il)sulfid, Kupfer(1)jodid, Kupfer(II)oxid, Gold(III)bromid, -jodid und-oxid, Molybdän(lV)sulfid, Niob(V)chlorid und -oxid, Palladiumjodid, Palladiumoxid, Platin (Vl)bromid und -chlorid, Vanadium(III)chlorid, Vanadium(lV)oxid, Wolfram(Vl)chlorid und-oxid. Bevorzugt sind Silber, Kupfer, Silber/Palladiumlegierungen, Palladium, Platin, Gold, Wolfram und Molybdän. Besonders bevorzugt sind Au, Pt AgPd und vor allem Ag und Cu-Pulver.
- Die erfindungsgemässen Zusammensetzungen lassen sich in einfacher Weise dadurch herstellen, indem man das Polymere oder dessen vernetzbare Vorstufe kombiniert mit einem geeigneten Vernetzungs mittel und den Komplex gemeinsam löst und diese Lösung anschliessend in an sich bekannter Weise zu Filmen vergiesst oder auf ein geeignetes Substrat aufträgt und gegebenenfalls anschliessend härtet.
- Geeignete Substrate sind übliche Werkstoffe, die vorzugsweise elektrisch nicht leitend sind. Beispiele dafür sind Papier, Holz, Glas, Keramik, Halbleiter, wie Silizium, Germanium oder Galliumarsenid, und insbesondere Kunststoffe, bevorzugt gehärtete Epoxidharze.
- Selbstverständlich können auch metallische Substrate, wie beispielsweise Aluminium oder Kupfer, mit den Mischungen beschichtet werden.
- Die Beschichtung des Substrates erfolgt mit üblichen Methoden, beispielsweise durch Tauch-, Streich- und Sprühverfahren, Schleuder-, Kaskadenguss- oder Vorhanggussbeschichtung.
- Man kann allerdings auch eine Folie aus der erfindungsgemässen Mischung giessen und diese dann anschliessend auf ein geeignetes Substrat aufkleben.
- Das Polymere bzw. dessen vernetzbare Vorstufe und der Komplex I können gemeinsam in einem Lösungsmittel gelöst werden. Man kann aber auch Mischungen unterschiedlicher Lösungsmittel einsetzen oder getrennte Lösungen von Polymer bzw. vernetzbarer Vorstufe und Komplex in unterschiedlichen Lösungsmitteln zusammengeben.
- Die Wahl des jeweiligen Lösungsmittelgemisches richtet sich nach den jeweils verwendeten Polymeren und Komplexen und kann vom Fachmann anhand von Routineversuchen bestimmt werden.
- Zur Haftverbesserung von Beschichtungen kann der Lösung ein Haftvermittler zugesetzt sein. Als Haftvermittler kann man z.B. ein lineares, lösliches Epoxidpolymeres einsetzen.
- Die Wahl der jeweiligen Polymer(mischungen) und der Palladiumkomplexe 1 richtet sich nach der Löslichkeit der Komponenten ineinander und kann vom Fachmann ebenfalls anhand von Routineversuchen ermittelt werden.
- Die Verbindungen der Formel 1 können nach an sich bekannten Verfahren hergestellt werden (vgl. z.B. J.Chem.Soc. D, 1970, 1065 und US-PS 4,347,323), indem man q Mol einer Verbindung der Formel IV
- Als Basen können z.B. Alkalimetallsalze aliphatischer Monocarbonsäuren, besonders Kalium- und Natriumacetat, verwendet werden. Geeignete Palladiumsalze sind beispielsweise PdBr2, PdCl2 und Na2PdCl4. Besonders bevorzugt verwendet man Na2PdC14 und vor allem PdCl2. Die Umsetzung wird zweckmässig in einem organischen Lösungsmittel durchgeführt, das gleichzeitig auch als H-Donor fungiert. Dazu eignen sich z.B. Alkanole mit bis zu 6 C-Atomen, vor allem Ethanol und besonders bevorzugt Methanol.
- Die Verbindungen der Formel IV können auf an sich bekannte Weise hergestellt werden, beispielsweise analog dem in der US-PS 3,295,974 beschriebenen Verfahren.
- Die erfindungsgemässe Zusammensetzung kann zur stromlosen Metallisierung von Kunststoffen oder zur Herstellung von strukurierten Metalloberflächen auf Kunststoffen eingesetzt werden.
- Als besonders vorteilhaft ist anzusehen, dass keine Vorbehandlung der zu metallisierenden Oberfläche (Aktivierbad, Reduktionsbad) notwendig ist, dass die Metallabscheidung auf beschichteten Substra ten durchgeführt werden kann, dass der Komplex 1 keine aggressiven Bestandteile enthält, die ihrerseits das Polymere angreifen können und dass bereits relativ geringe Mengen an Komplex 1 für die stromlose Metallisierung der Kunststoffoberfläche ausreichen.
- Die Aktivierung der Zusammensetzung für die stromlose Metallabscheidung erfolgt durch Erwärmen auf Temperaturen oberhalb von 100°C, vorzugsweise auf 100-250° C, besonders bevorzugt auf 150-200° C, die Erwärmung kann beispielsweise durch Tempern der Probe oder durch Bestrahlung mit IR-Quellen, wie beispielsweise IR-Lasern, oder dem IR-Anteil von aktinischen Strahlungsquellen (beispielsweise Xenonlampen, Argonlampen, Wolframlampen, Kohlelichtbogen, Metallhalogenid- und Metallichtbogenlampen, wie Quecksilberlampen) erfolgen.
- Durch die Temperaturbehandlung wird eine Freisetzung von fein dispergiertem, katalytisch aktivem Palladium bewirkt.
- Die Bestrahlung mit IR-Quellen kann auch bildmässig erfolgen, z.B. durch einen Laserstrahl der über die Oberfläche geführt wird.
-
- Gegenstand der Erfindung ist daher auch ein Verfahren zur Aktivierung von Polymeroberflächen zum Zwecke der stromlosen Metallisierung wobei
- i) eine Lösung des Komplexes der Formel 1 in einem Polymeren, wie oben definiert, auf ein Substrat aufgebracht wird oder als freitragender Film hergestellt wird und
- ii) die Anordnung auf Temperaturen über 100°C erhitzt wird, wobei der Komplex 1 sich zersetzt und fein verteiltes, katalytisch aktives Pd° entsteht.
-
- Die Haftung des Metallfilms ist ausgezeichnet. Die stromlose Metallabscheidung kann mit an sich bekannten Metallisierungsbädern und nach üblichen Methoden erfolgen. Als Metalle eignen sich beispielsweise Kupfer, Nickel, Kobalt, Silber, Gold und Zinn oder Kobalt-Phosphor- und Kobalt-Nickel-Legierungen.
- Die Erfindung betrifft daher auch ein Verfahren zur stromlosen Metallabscheidung auf Polymeroberflächen umfassend eine Aktiverung der Polymeroberfläche, wie oben definiert (Schritte i und ii), und daran anschliessend
- iii) die stromlose Metallisierung der aktivierten Polymeroberfläche in an sich bekannter Weise.
- Soll ein Metallmuster auf einer Substratoberfläche hergestellt werden, so bietet es sich an, die erfindungsgemässe Zusammensetzung struckturiert auf ein Substrat aufzubringen, beispielsweise mittels eines Siebdruck- oder eines selektiv gesteuerten Sprühnebel-Aufzeichnungsverfahren. Geeignete Aufzeichnungsverfahren sind beispielsweise in der DE-OS 3,326,508 beschrieben.
- Die Erfindung betrifft daher auch ein Verfahren zur Erzeugung von metallischen Mustern auf Substratoberflächen umfassend
- i) strukturiertes Aufbringen einer Lösung eines Komplexes in einem Polymeren, wie oben definiert, auf ein Substrat,
- ii) Erhitzen der Anordnung auf Temperaturen von über 100° C, wobei der Komplex I sich zersetzt und fein verteiltes, katalytisch aktives Pd° entsteht und
- iii) stromlose Metallisierung der aktivierten Polymeroberfläche in an sich bekannter Weise.
- Die Strukturierung kann auch mittels eines Photolackes erfolgen. Zu diesem Zweck wird ein Substrat in an sich bekannter Weise mit einem Photolack beschichtet. Der Palladiumkomplex 1 kann entweder in dem Photolack oder in einem darunterliegenden Polymersubstrat, vorzugsweise einer Polymerschicht, gelöst sein. Nach dem Bestrahlen der Anordnung mit aktinischem Licht und der anschliessenden Entwicklung des Photolackes (positiv oder negativ arbeitend) wird die Probe getempert und in ein Metallisierbad getaucht. Die Metallabscheidung erfolgt nun entweder auf dem strukturierten Photolack oder auf dem durch den Photolack strukturierten Polymersubstrat.
- Die Erfindung betrifft daher ferner ein Verfahren zur Erzeugung von metallischen Mustern auf Polymeroberflächen umfassend
- i) das Aufbringen einer Lösung des Komplexes 1 in einem Polymeren, wie oben definiert, auf ein Substrat oder Herstellung eines freitragenden Films auf besagter Lösung,
- ii) Beschichten der Polymeroberfläche mit einem positiv oder negativ arbeitendem Photolack,
- iii) Belichten der Anordnung mit einem vorbestimmten Muster aktinischer Strahlung,
- iv) Entwickeln des Photolackes in an sich bekannter Weise,
- v) Erhitzen der Anordnung auf Temperaturen von mehr als 100°C, wobei der Komplex 1 sich zersetzt und fein verteiltes, katalytisch aktives Pd° entsteht, und
- vi) stromloses Metallisieren des aktivierten vom Photolack nicht mehr bedeckten Teils der Polymeroberfläche in an sich bekannter Weise.
- Selbstverständlich kann man zwischen Stufe (iii) und (iv) noch einen Temperschritt einschalten, um den belichteten Photolack vorzuhärten. Als Photolacke lassen sich die in der Technik üblichen Materialien einsetzen. Der Begriff "Photolack" umfasst auch olefinisch ungesättigte Verbindungen. Eine Uebersicht über Abbildungsverfahren mit solchen Lacken und über ausgewählte Verbindungsklassen gibt P.S. Pappas in "UV Curing: Science and Technology", Kapitel 9, S. 230-253 (1973).
- Der Photolack muss natürlich so gewählt werden, dass eine durch den Bestrahlungs- und Entwicklungsschritt erzeugte Strucktur den Temperschritt ohne grössere Verzerrungen übersteht. Solche Systeme sind dem Fachmann bekannt oder können mittels Routineverfahren ausgewählt werden.
- Verfährt man nach der Variante, bei der ein in einem Photolack gelöster Komplex der Formel I vorliegt, so wählt man als Photolack ein strahlungsempfindliches Polymersystem, wobei das Polymere keine olefinischen Doppelbindungen besitzt. In diesem Verfahren lassen sich bereits mit relativ geringen Mengen der Pd-Verbindung gute Ergebnisse erzielen. Hier genügen in der Regel weniger als 10 Gew.% des Komplexes der Formel I, bezogen auf die Polymerlösung, um nach erfolgter Belichtung und Temperstufe eine katalytisch aktive Oberfläche zu erhalten. Bevorzugt verwendet man bei dieser Variante 1 - 5 Gew.% des Komplexes der Formel 1 bezogen auf die Polymerlösung.
- Beispiele für strahlungsempfindliche Polymersysteme mit Polymeren ohne olefinische Doppelbindungen sind Kombinationion von Epoxidharzen mit Photoinitiatoren der kationischen Polymerisation.
-
- - Bevorzugte Kombinationen dieses Typs sind in der EP-A 153,904 bechrieben; diese Kombinationen sind ebenfalls Gegenstand der vorliegenden Beschreibung. Ganz besonders bevorzugt setzt man Kombinationen von Epoxidharzen auf Bisphenol-A Basis oder auf Basis von Phenol- oder Kresol-Novolacken mit Eisen-Aren Photoinitiatoren ein. Solche Gemische sind ebenfalls in der EP-A 153,904 beschrieben.
- Gegenstand der Erfindung ist also ferner ein Verfahren zur Erzeugung von metallischen Mustern auf Polymeroberflächen umfassend
- i) das Aufbringen einer Zusammensetzung enthaltend
- a) einen positiv oder negativ arbeitenden Photolack und
- b) in diesem Photolack einheitlich gelöst aber nicht damit copolymerisierbar einen Dibenzalacetonkomplex der Formel I, wie oben definiert,
auf eine Substratoberfläche, mit der Massgabe, dass der Photolack kein Polymeres mit einer olefinischen Doppelbindung enthält, - ii) Belichten der Anordnung mit einem vorbestimmten Muster aktinischer Strahlung,
- iii) Entwickeln des Photolackes in an sich bekannter Weise, iv) Erhitzen der Anordnung auf Temperaturen von mehr als 100°C, wobei der Komplex 1 sich zersetzt und fein verteiltes, katalytisch aktives Pd° entsteht und v) stromloses Metallisieren der vom Photolack bedeckten Teile der Anordnung in an sich bekannter Weise. Auch bei dieser Ausführungsform wird zwischen Schritt ii) und iii) vorzugsweise ein Temperschritt geschaltet, um den belichteten Photolack vorzuhärten.
- Der Ausdruck "Belichtung mit einem vorbestimmten Muster aktinischer Strahlung" bedeutet sowohl eine Belichtung durch eine Photomaske, die ein vorbestimmtes Muster enthält, beispielsweise ein Diapositiv, sowie die Belichtung durch einen Laserstrahl, der beispielsweise computergesteuert über die Oberfläche bewegt wird, und auf diese Weise ein Bild erzeugt.
- Bei der Bilderzeugung mittels eines Photolackes wird vorzugsweise aktinische Strahlung von 200 bis 600 nm verwendet. Geeignete Quellen aktinischer Strahlung umfassen Kohlebögen, Quecksilberdampflampen, fluoreszierende Lampen mit ultraviolettes Licht emittierenden Phosphoren, Argon- und Xenonglühlampen, Wolframlampen und photographische Flutlichtlampen. Es lassen sich aber auch Röntgen- oder Elektronenstrahlen sowie hochenergetische Strahlung verwenden.
- Als Entwickler kommen je nach Art des gewählten Photolackes unterschiedlichste Materialien in Frage. Die Entwicklung kann beispielsweise mit Wasser, wässrigen oder wässrig-organischen Lösungen einer Base oder Säure, organischen Lösungsmitteln oder Lösungsmittelgemischen erfolgen.
- Ein weiterer Gegenstand der Erfindung ist die Verwendung der erfindungsgemässen Mischungen zur stromlosen Metallabscheidung, insbesondere zur Erzeugung von elektrisch leitfähigen Mustern auf Kunststoffoberflächen. Mit dem erfindungsgemässen Verfahren können Muster mit hoher Auflösung erzielt werden. Solche Produkte können beispielsweise als gedruckte Schaltungen verwendet werden.
- Die nachfolgenden Beispiele erläutern die Erfindung näher.
- 15 g PdC12 werden in einer Lösung aus 10,7 g NaC1 in 65 ml Wasser unter kräftigem Rührem zum Sieden erhitzt, bis das Palladiumchlorid vollständig gelöst ist. Dann wird das Wasser abdestilliert. Der Rückstand wird in 200 ml Methanol aufgenommen und auf 60° C erwärmt. 105,9 g Dibenzalaceton-bis-p,p'-diglycidylether und 42,8 g Natriumacetat·3H20 werden zugesetzt und es werden nochmals 175 ml Methanol zugegeben. Nach weiteren 15 Minuten bei 60°C wird die Mischung abgekühlt. Es entsteht ein Niederschlag, der unter Argon abfiltriert und einmal mit 100 ml Methanol, dreimal mit je 100 ml Wasser und noch zweimal mit 100 ml Methanol gewaschen wird. Anschliessend wird das Produkt bei 50° C im Vakuum getrocknet. Zur völligen Entfernung von restlichem Dibenzalaceton-bis-p,p'-diglycidylether werden die Kristalle nochmals in 700 ml Methanol suspendiert und unter Argon abfiltriert. Anschliessend wird im Vakuum getrocknet. Man erhält 100,7 g violetter Kristalle (97 % der Theorie). Zersetzungsbereich: 120-160°C. Die Analyse ergibt für q einen Wert von 3,2.
- Die Herstellung dieser Verbindung erfolgt gemäss US-PS 4,347,232.
- Die Herstellung erfolgt gemäss J.Chem. Soc. D 1970, 1065.
- Beispiel A: 20 g PVC werden in 80 g Tetrahydrofuran gelöst und mit einer Lösung von 0,6 g des Komplexes aus Beispiel 2 in 30 g Tetrahydrofuran versetzt. Die Lösung wird zu einem Film von 200 µm Dicke vergossen. Nach dem Abdunsten des Lösungsmittels wird der Film 15 min. bei 170°C getempert und anschliessend in einem kommerziellen Vernickelungsbad (SHIPLEY Nisposit® 468 bzw. PM 980) mit Nickel beschichtet. Es wird ein gut haftender Nickelüberzug erhalten. Ein weiterer Film wird in ein kommerzielles Verkupferungsbad gehalten (SHIPLEY Cuposit® CP 78 bzw. 328). Es wird ein gut haftender Kupferüberzug erhalten. Vergleichbare Ergebnisse werden mit den folgenden Metallisierungsbädern erhalten.
- a) Verkupferungsbad. Badzusammensetzung entsprechend "Printed Circuits Handbook", 2. Auflage, C.F. Coombs, jr. et al., McGraw Hill Book Co., New York, 1979, S. 7-5:
25 g/I CuSO4·5 H20
60 g/I Natriumgluconat
20 g/I NaOH
25 g/l 37%ige wässrige Formaldehydlösung, unter Sauerstoff-Strom.
Arbeitstemperatur: 20° C. - b) Vernickelungsbad. Badzusammensetzung entsprechend J. Appl., Electrochem., 1 (1971) 167:
30 g/I NiCl2·6 H20
10 g/I NaH2PO2·H2O -
- Beispiel F: Eine Epoxidharzplatte (60x40x2mm) wird mit einem 50 µm dicken Polymerfilm der Zusammensetzung nach Beispiel C beschichtet. Nach dem Abdunsten des Lösungsmittels wird die Platte 6 min. auf 170°C erwärmt und anschliessend in eines der in Beispiel A beschriebenen Vernickelungsbäder getaucht. Die Oberfläche überzieht sich mit einem gut haftenden Nickelfilm.
- Beispiel G: Durchführung wie in Beispiel F beschrieben. Als Substrat wird eine Glasplatte verwendet.
- Beispiel H: Durchführung wie in Beispiel F beschrieben. Als Substrat wird eine Aluminiumplatte verwendet.
- Beispiel 1: 0,25 g des Komplexes gemäss Beispiel 1 werden in einer Lösung von 5 g eines linearen Polyepoxids*) in 20 g 1,2-Dichlorethan gelöst. Mit dieser Lösung wird auf einer Epoxidharzplatte (60x40x2mm) ein 50 µm dicker Polymerfilm erzeugt. Nach dem Abdunsten des Lösungsmittels wird die beschichtete Epoxidharzplatte 6 min. auf 170°C erwärmt und anschliessend in eines der in Beispiel A beschriebenen Nickelabscheidungsbäder getaucht. Es entsteht ein gut haftender Nickelfilm auf der beschichteten Harzoberfläche.
- *) Das Epoxidpolymere ist ein lineares Additionscopolymeres bestehend aus einem Diglycidylether auf Bisphenol A Basis (Epoxidwert:5,3 Val/kg) und Benzylamin im Molverhältnis 1:1. Die Herstellung erfolgt nach der in J. Polym. Sci. Polym. Chem. Ed., 22 249 (1984) beschriebenen Methode.
- Beispiel J: 0,5 g des Komplexes gemäss Beispiel 1, 0,5 g des linearen Polyepoxids gemäss Beispiel 1 und 10,0 g Makrolon® (vgl. Beispiel C) werden in 70 g 1,2 Dichlorethan gelöst. Mit der erhaltenen Lösung wird eine Epoxidharzplatte wie in Beispiel I beschrieben behandelt. Es wird ein gut haftender Nickelfilm auf beschichteten Harzoberfläche erhalten.
- Beispiel K: 11,2 g (56,0 Gew.%) eines Diglycidylethers auf Bisphenol A Basis (Epoxidwert: 5,25-5,4 Vat/kg), 7,8 g (39,0 Gew.%) Hexahydropthafsäureanhydrid und 1,0 g (5,0 Gew.%) des Komplexes gemäss Beispiel 2 werden bei 90° C während 15 Minuten vermischt. Dann gibt man 0,06 g Benzyldimethylamin als Beschleuniger zu. Nach weiteren 5 Minuten bei 90°C wird die Mischung in eine auf 100°C vorgeheizte Form gegossen und 4 Stunden bei 100°C sowie weitere 4 Stunden bei 120°C gehärtet. Nach dem Entfernen der Form wird der Formkörper weitere 2 Stunden bei 240°C getempert und anschliessend in einem kommerziellen Vernickelungsbad (Shipley Niposit® 468 bzw. Niposit® PM 980) mit Nickel beschichtet. Es wird ein gut haftender Nickelüberzug erhalten.
- Die Vernickelung lässt sich auch mit dem Vernickelungsbad gemäss Beispiel A durchführen. Es werden vergleichbare Ergebnisse erzielt.
- Beispiel L: 22,4 g (50,8 Gew.%) eines Diglycidylethers auf Bisphenol A Basis (Epoxidwert:5,25-5,4 Val/kg), 15.4 g (34,9 Gew.%) Hexahydrophthalsäureanhydrid und 6,3 g (14,3 Gew.%) des Komplexes gemäss Beispiel 3 werden bei 90°C während 15 Minuten vermischt. Dann gibt man 0,1 g Benzyldimethylamin als Beschleuniger zu. Nach weiteren 5 Minuten bei 90°C wird die Mischung in eine auf 100°C vorgeheizte Form gegossen und 4 Stunden bei 100°C sowie weitere 4 Stunden bei 120°C gehärtet. Nach dem Entfernen der Form wird der Formkörper 1 Stunde bei 240° C getempert und anschliessend in einem kommerziellen Vernickelungsbad (Shipley Nisposit® 468 bzw. Nisposit® PM 980) mit Nickel beschichtet. Es wird ein gut haftender Nickelüberzug erhalten.
- Die Vernickelung lässt sich mit vergleichbar guten Ergebnissen auch mit dem in Beispiel A beschriebenen Vernickelungsbad durchführen.
- Beispiel M: 0,25 g Tris(p,p'-diisopropyldibenzalaceton)-Palladium und 0.2 g Polystyrol werden in 20 ml Toluol gelöst. Diese Lösung wird als Schreibtinte in einem Hewlett-Packard "Thinkjet"-Printer mit modifiziertem Schreibkopf*) verwendet. Mit dem Printer wird auf eine Transparentfolie für Normalkopierer (Folex® X-100) ein Text geschrieben. Anschliessend wird die Folie 15 min. bei 170°C getempert. Danach wird die Folie in eines der in Beispiel A geschriebenen Nickelabscheidungsbäder getaucht (Dauer 15 min.). An den bedruckten Stellen entsteht ein gut auf der Folie haftender Nickelüberzug.
- *) Das Tintenvorratsgefäss ist aus Aluminium gefertigt, um die Resistenz gegen organische Lösungsmittel zu erhöhen. Ferner sind alle Verklebungen mit dem ebenfalls lösungsmittelresistenten Araldit®-Kleber ausgeführt.
- Beispiel N: 20 g eines Photolacks aus 120 Gew.T. eines technischen Epoxidkresol-Novolaks (Epoxidgehalt 4,5 Aequ./kg), 50 Gew.T. eines technischen Bisphenol A Epoxidharzes (Epoxidgehalt 0,5 Aequ./kg), 20 Gew.T. Talkum, 1 Gew.T. Irgatithgrün, 2 Gew.T. (η6-Stilben)(η5-cyclopentadienyl)eisen(II)-hexafluorophosphat und 200 Gew.T. Cyclohexanon werden mit einer Lösung von 0,5 g des Komplexes gemäss Beispiel 2 in 15 ml Dichlorethan versetzt und gut durchmischt. Diese Mischung wird mit einer 70µ-Rakel auf eine Glasplatte (200x100x4 mm) aufgetragen. Der aufgetragene Lack wird eine Stunde bei 80°C getrocknet. Zur Strukturierung wird der Lack durch eine Maske belichtet (5000 W Hg-Hochdrucklampe Berner M 061), 20 min. bei 135°C gehärtet, und anschliessend durch 1 1/2 min Eintauchen in Cyclohexanon entwickelt. Zur Pd°-Abscheidung wird eine Stunde bei 230° C in einem Umluftofen getempert. Danach wird die Platte in einem unter Beispiel A beschriebenen Metallisierbad vernickelt. Auf der strukturierten Oberflächen des Photolacks entsteht ein gut haftender Nickelüberzug.
- Beispiel 0: Es wird wie in Beispiel N verfahren. Anstelle einer Glasplatte wird ein Epoxy-Kohlefasser-Laminat als Substrat verwendet. Nach der Bestrahlung wird 10 min. bei 135°C gehärtet. Nach Entwicklung und Metallisierung entsteht auf der strukturierten Oberfläche des Photolacks ein gut haftender Nickelüberzug.
Claims (14)
R2 eine der Bedeutungen von R1 annimmt oder zusätzlich eine Amino-, Nitro- oder Cyangruppe darstellt, ein Rest -(-O-CmH2m-)nOR4 oder -O-CH2-CH·OR4-CH2·OR5 oder ein Halogenatom oder ein Glycidyletherrest ist,
R3 Wasserstoff oder C1-C4Alkyl ist oder die beiden Gruppen R3 zusammen eine Polymethylenkette von 2-4 Kohlenstoffatomen bilden,
R4 und R5 eine der Bedeutung von R besitzen und
q eine Zahl von 1 bis 3,5 ist,
m für eine Zahl von 2 bis 6 und n für eine Zahl von 0 bis 20 steht,
mit der Massgabe, dass die Zusammensetzung kein Polymeres mit einer olefinischen Doppelbindung enthält.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CH34886 | 1986-01-30 | ||
| CH348/86 | 1986-01-30 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP0233145A1 true EP0233145A1 (de) | 1987-08-19 |
| EP0233145B1 EP0233145B1 (de) | 1989-10-18 |
Family
ID=4184967
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP87810046A Expired EP0233145B1 (de) | 1986-01-30 | 1987-01-26 | Polymerzusammensetzungen enthaltend einen gelösten Dibenzalaceton-Palladiumkomplex |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US5045436A (de) |
| EP (1) | EP0233145B1 (de) |
| JP (1) | JPS62192584A (de) |
| DE (1) | DE3760813D1 (de) |
| PH (1) | PH23902A (de) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5030742A (en) * | 1988-12-16 | 1991-07-09 | Ciba-Geigy Corporation | Ultrathin layers of palladium(O) complexes |
| WO1991009986A1 (en) * | 1989-12-21 | 1991-07-11 | Monsanto Company | Catalytic, water-soluble polymeric films for metal coatings |
| US5082734A (en) * | 1989-12-21 | 1992-01-21 | Monsanto Company | Catalytic, water-soluble polymeric films for metal coatings |
| WO2002059209A1 (fr) * | 2001-01-24 | 2002-08-01 | Toray Engineering Company,Limited | Solution de precurseur de resines polyimides, lamines pour composants electroniques fabriques a l'aide desdites solutions, et procede de production desdits lamines |
| DE102005015454A1 (de) * | 2005-04-04 | 2006-10-05 | Infineon Technologies Ag | Halbleitersensorbauteil mit Hohlraumgehäuse und Sensorchip sowie Verfahren zur Herstellung desselben |
| DE102005037321A1 (de) * | 2005-08-04 | 2007-02-15 | Infineon Technologies Ag | Halbleiterbauteil mit Leiterbahnen zwischen Halbleiterchip und Schaltungsträger und Verfahren zur Herstellung desselben |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5389496A (en) * | 1987-03-06 | 1995-02-14 | Rohm And Haas Company | Processes and compositions for electroless metallization |
| US5506091A (en) * | 1990-04-20 | 1996-04-09 | Nisshinbo Industries, Inc. | Photosensitive resin composition and method of forming conductive pattern |
| US5310580A (en) * | 1992-04-27 | 1994-05-10 | International Business Machines Corporation | Electroless metal adhesion to organic dielectric material with phase separated morphology |
| US5419954A (en) * | 1993-02-04 | 1995-05-30 | The Alpha Corporation | Composition including a catalytic metal-polymer complex and a method of manufacturing a laminate preform or a laminate which is catalytically effective for subsequent electroless metallization thereof |
| US6141870A (en) | 1997-08-04 | 2000-11-07 | Peter K. Trzyna | Method for making electrical device |
| EP1537913B1 (de) * | 2002-09-13 | 2009-07-01 | Wako Pure Chemical Industies, Ltd. | Palladiumkatalysatorzusammensetzung |
| US8435603B2 (en) | 2003-12-05 | 2013-05-07 | Conductive Inkjet Technology Limited | Formation of solid layers on substrates |
| EP1689909B1 (de) * | 2003-12-05 | 2017-10-11 | CIT Technology Limited | Ausbildung von festen schichten auf trägern |
| DE102005015455B4 (de) | 2005-04-04 | 2021-03-18 | Infineon Technologies Ag | Kunststoffgehäuse und Halbleiterbauteil mit derartigem Kunststoffgehäuse sowie ein Verfahren zur Herstellung eines Kunststoffgehäuses |
| US8436197B2 (en) * | 2007-10-25 | 2013-05-07 | West Chester University Of Pennsylvania Of The State System Of Higher Education | Palladium complexes and polymerization and coupling processes thereof |
| SG11202104359PA (en) * | 2018-12-14 | 2021-05-28 | Univ Nanyang Tech | Metallization of three-dimensional printed structures |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2289629A1 (fr) * | 1974-10-29 | 1976-05-28 | Basf Ag | Activation de substrats pour la metallisation sans courant electrique |
| EP0125617A2 (de) * | 1983-05-11 | 1984-11-21 | Nissan Chemical Industries Ltd. | Verfahren zur Herstellung eines metallisierten Polymers aus der Polymerzusammensetzung |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3900320A (en) * | 1971-09-30 | 1975-08-19 | Bell & Howell Co | Activation method for electroless plating |
| US3950570A (en) * | 1974-05-02 | 1976-04-13 | Western Electric Company, Inc. | Method of depositing a metal on a surface |
| DE2451276C2 (de) * | 1974-10-29 | 1982-12-30 | Basf Ag, 6700 Ludwigshafen | Verfahren zur Herstellung starrer magnetischer Aufzeichnungsträger |
| GB2085874B (en) * | 1980-09-04 | 1984-08-08 | Johnson Matthey Plc | Hydroformylation of olefins |
| DD157989A3 (de) * | 1980-10-10 | 1982-12-22 | Lothar Gierth | Verfahren zur strukturierten chemisch-reduktiven metallabscheidung |
| US4347232A (en) * | 1981-06-17 | 1982-08-31 | Fmc Corporation | Preparation of hydrogen peroxide from its elements |
| DE3148280A1 (de) * | 1981-12-05 | 1983-06-09 | Bayer Ag, 5090 Leverkusen | Verfahren zur aktivierung von substratoberflaechen fuer die stromlose metallisierung |
| DE3326508A1 (de) * | 1983-07-22 | 1985-02-07 | Bayer Ag, 5090 Leverkusen | Verfahren zum aktivieren von substratoberflaechen fuer die direkte partielle metallisierung von traegermaterialien |
| US4469714A (en) * | 1983-09-02 | 1984-09-04 | Okuno Chemical Industry Co., Ltd. | Composition for bonding electroconductive metal coating to electrically nonconductive material |
| US4574095A (en) * | 1984-11-19 | 1986-03-04 | International Business Machines Corporation | Selective deposition of copper |
-
1987
- 1987-01-26 DE DE8787810046T patent/DE3760813D1/de not_active Expired
- 1987-01-26 EP EP87810046A patent/EP0233145B1/de not_active Expired
- 1987-01-29 PH PH34785A patent/PH23902A/en unknown
- 1987-01-30 JP JP62020351A patent/JPS62192584A/ja active Pending
-
1989
- 1989-03-03 US US07/319,884 patent/US5045436A/en not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2289629A1 (fr) * | 1974-10-29 | 1976-05-28 | Basf Ag | Activation de substrats pour la metallisation sans courant electrique |
| EP0125617A2 (de) * | 1983-05-11 | 1984-11-21 | Nissan Chemical Industries Ltd. | Verfahren zur Herstellung eines metallisierten Polymers aus der Polymerzusammensetzung |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5030742A (en) * | 1988-12-16 | 1991-07-09 | Ciba-Geigy Corporation | Ultrathin layers of palladium(O) complexes |
| WO1991009986A1 (en) * | 1989-12-21 | 1991-07-11 | Monsanto Company | Catalytic, water-soluble polymeric films for metal coatings |
| US5082734A (en) * | 1989-12-21 | 1992-01-21 | Monsanto Company | Catalytic, water-soluble polymeric films for metal coatings |
| WO2002059209A1 (fr) * | 2001-01-24 | 2002-08-01 | Toray Engineering Company,Limited | Solution de precurseur de resines polyimides, lamines pour composants electroniques fabriques a l'aide desdites solutions, et procede de production desdits lamines |
| DE102005015454A1 (de) * | 2005-04-04 | 2006-10-05 | Infineon Technologies Ag | Halbleitersensorbauteil mit Hohlraumgehäuse und Sensorchip sowie Verfahren zur Herstellung desselben |
| DE102005015454B4 (de) * | 2005-04-04 | 2010-02-18 | Infineon Technologies Ag | Halbleitersensorbauteil mit Hohlraumgehäuse und Sensorchip sowie Verfahren zur Herstellung desselben |
| DE102005037321A1 (de) * | 2005-08-04 | 2007-02-15 | Infineon Technologies Ag | Halbleiterbauteil mit Leiterbahnen zwischen Halbleiterchip und Schaltungsträger und Verfahren zur Herstellung desselben |
| DE102005037321B4 (de) * | 2005-08-04 | 2013-08-01 | Infineon Technologies Ag | Verfahren zur Herstellung von Halbleiterbauteilen mit Leiterbahnen zwischen Halbleiterchips und einem Schaltungsträger |
Also Published As
| Publication number | Publication date |
|---|---|
| US5045436A (en) | 1991-09-03 |
| JPS62192584A (ja) | 1987-08-24 |
| PH23902A (en) | 1989-12-18 |
| DE3760813D1 (en) | 1989-11-23 |
| EP0233145B1 (de) | 1989-10-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0233145B1 (de) | Polymerzusammensetzungen enthaltend einen gelösten Dibenzalaceton-Palladiumkomplex | |
| EP0233567B1 (de) | Härtbare Mischungen, enthaltend N-Sulfonylaminosulfoniumsalze als kationisch wirksame Katalysatoren | |
| DE3717199C2 (de) | ||
| EP0006561B1 (de) | Lichtempfindliches Gemisch | |
| EP0153904B1 (de) | Verfahren zur Herstellung einer Schutzschicht oder einer Reliefabbildung | |
| EP0072780B1 (de) | Imidylverbindungen, Polymere daraus und Verwendung der Polymeren | |
| EP0302019B1 (de) | Negativ-Photoresist auf Basis von Polyphenolen und ausgewählten Epoxid-oder Vinyletherverbindungen | |
| EP0101587A2 (de) | Positiv arbeitendes Verfahren zur Herstellung von Reliefbildern oder Resistmustern | |
| EP0119959B1 (de) | Verfahren zur Bilderzeugung | |
| EP0182744B1 (de) | Photohärtbare gefüllte Expoxidharz-Zusammensetzungen und deren Verwendung | |
| EP0562393B1 (de) | Verfahren zur Verbesserung der Haftfestigkeit von stromlos abgeschiedenen Metallschichten | |
| DE2834791A1 (de) | Durch hochenergetische strahlung haertbares resistmaterial und herstellungsverfahren | |
| EP0295211B1 (de) | Photoresistzusammensetzungen | |
| EP0683435B1 (de) | Positiv arbeitendes strahlungsempfindliches Gemisch | |
| EP0153683A2 (de) | Verfahren zur Herstellung von Leiterplatten | |
| EP0214097B1 (de) | Mischung aus Olefin und Dibenzalaceton-Palladiumkomplex und deren Verwendung | |
| DE2507008A1 (de) | Polymerisierbare ester | |
| EP0717317B1 (de) | Strahlungsempfindliches Gemisch | |
| EP0126029B1 (de) | Verfahren zur Bilderzeugung | |
| DE3510133A1 (de) | Strahlungsempfindliche, metallkomplex bildende polymere, verfahren zur polymerisation von acetylen und beschichtetes material | |
| DE2806928B2 (de) | Strahlungsempfindliches Material und seine Verwendung als Resistmaterial | |
| DE2450381C3 (de) | Strahlungsempfindliches Material und dessen Verwendung | |
| EP0521826A1 (de) | Verfahren zur Herstellung von elektrisch leitenden Schichten | |
| DE19546140A1 (de) | Photoempfindliche Zusammensetzung | |
| EP0510441A1 (de) | Positiv arbeitendes strahlungsempfindliches Gemisch und damit hergestelltes strahlungsempfindliches Aufzeichnungsmaterial |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| 17P | Request for examination filed |
Effective date: 19870128 |
|
| AK | Designated contracting states |
Kind code of ref document: A1 Designated state(s): CH DE FR GB IT LI NL SE |
|
| 17Q | First examination report despatched |
Effective date: 19890314 |
|
| GRAA | (expected) grant |
Free format text: ORIGINAL CODE: 0009210 |
|
| AK | Designated contracting states |
Kind code of ref document: B1 Designated state(s): CH DE FR GB IT LI NL SE |
|
| REF | Corresponds to: |
Ref document number: 3760813 Country of ref document: DE Date of ref document: 19891123 |
|
| ITF | It: translation for a ep patent filed |
Owner name: BARZANO' E ZANARDO MILANO S.P.A. |
|
| ET | Fr: translation filed | ||
| GBT | Gb: translation of ep patent filed (gb section 77(6)(a)/1977) | ||
| PLBE | No opposition filed within time limit |
Free format text: ORIGINAL CODE: 0009261 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: NO OPPOSITION FILED WITHIN TIME LIMIT |
|
| 26N | No opposition filed | ||
| ITTA | It: last paid annual fee | ||
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: FR Payment date: 19921119 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: DE Payment date: 19921203 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: GB Payment date: 19921207 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: SE Payment date: 19930129 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: NL Payment date: 19930131 Year of fee payment: 7 |
|
| PGFP | Annual fee paid to national office [announced via postgrant information from national office to epo] |
Ref country code: CH Payment date: 19930311 Year of fee payment: 7 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: GB Effective date: 19940126 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: SE Effective date: 19940127 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: LI Effective date: 19940131 Ref country code: CH Effective date: 19940131 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: NL Effective date: 19940801 |
|
| NLV4 | Nl: lapsed or anulled due to non-payment of the annual fee | ||
| GBPC | Gb: european patent ceased through non-payment of renewal fee |
Effective date: 19940126 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: FR Effective date: 19940930 |
|
| REG | Reference to a national code |
Ref country code: CH Ref legal event code: PL |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: DE Effective date: 19941001 |
|
| REG | Reference to a national code |
Ref country code: FR Ref legal event code: ST |
|
| EUG | Se: european patent has lapsed |
Ref document number: 87810046.0 Effective date: 19940810 |
|
| PG25 | Lapsed in a contracting state [announced via postgrant information from national office to epo] |
Ref country code: IT Free format text: LAPSE BECAUSE OF NON-PAYMENT OF DUE FEES;WARNING: LAPSES OF ITALIAN PATENTS WITH EFFECTIVE DATE BEFORE 2007 MAY HAVE OCCURRED AT ANY TIME BEFORE 2007. THE CORRECT EFFECTIVE DATE MAY BE DIFFERENT FROM THE ONE RECORDED. Effective date: 20050126 |