-
Die
vorliegende Erfindung betrifft ein Verfahren zur Herstellung von
Hydroxylaminderivaten, die als Antioxidationsmittel in farbfotografischen
Entwicklungszusammensetzungen verwendbar sind. Die vorliegende Erfindung
betrifft zudem Farbentwicklungszusammensetzungen, die die Antioxidationsmittel
enthalten.
-
Farbentwicklungslösungen werden
verwendet, um farbfotografische Materialien, wie farbfotografische Filme
und Papiere zur Erzeugung der gewünschten Farbbilder zu verarbeiten.
Derartige Lösungen
enthalten im Allgemeinen Farbentwicklungsmittel, beispielsweise
4-Amin-3-Methyl-N-(β-Methansulfonamidoethyl)anilin, als
Reduktionsmittel zur Reaktion mit Farberzeugungskupplern in den
fotografischen Materialien zwecks Ausbildung der gewünschten
Farbstoffe. Derartige Farbentwicklungsmittel unterliegen jedoch
einer Oxidation durch gelösten
Sauerstoff. Herkömmlicherweise
ist in Farbentwicklungslösungen
ein Antioxidationsmittel enthalten, um den Oxidationszustand des
Farbentwicklungsmittels zu bewahren und dadurch die Entwicklungsaktivität zu erhalten.
-
Als
Farbentwicklungs-Antioxidationsmittel finden zahlreiche Klassen
von Verbindungen Verwendung, u.a. Hydroxylamine, Hydroxaminsäuren, Oxime,
Nitroxyradikale, Hydrazine, Hydrazide, Phenole, Saccharide, verschiedene
einfache Amine, Polyamine, quaternäre Ammoniumsalze, α-Hydroxyketone,
Alkohole, Diamide und Disulfonamide. Für die Verwendung in der Praxis
müssen
Antioxidationsmittel in wässrigem
Medium löslich
sein, dürfen
für lebendige
Organismen nicht toxisch sein, müssen
kostengünstig
und silberhalogenidfreie Entwickler sein. Es ist zudem wünschenswert,
dass Antioxidationsmittel langsam mit Sauerstoff und schnell mit
oxidiertem Farbentwicklungsmittel reagieren, jedoch nicht so schnell,
dass sich die Farbentwicklung verzögert. Das Antioxidationsmittel
darf zudem kein bakterielles Wachstum fördern. Vorzugsweise sind derartige Verbindungen
zudem geruchlos.
-
Alle
diese Überlegungen
begrenzen die Anzahl und Klasse von Verbindungen wesentlich, die
in der Praxis als Antioxidationsmittel oder Stabilisatoren in Farbentwicklungszusammensetzungen
verwendbar sind. Die auf diese Weise am häufigsten verwendeten Verbindungen
sind Hydroxylamin- und Mono- sowie Dialkylhydroxylaminderivate.
Diese weisen sehr gute Eigenschaften insofern auf, als dass sie
als silberhalogenidfreie Entwickler einer nur langsamen Flächenoxidation
unterliegen und relativ kostengünstig
herzustellen sind. Es gibt zahlreiche Publikationen, die derartige
Verbindungen beschreiben, wie US-A-4,892,804 und US-A-5,354,646.
-
Leider
weisen viele Hydroxylaminderivate bei Raumtemperatur einen erheblichen
Dampfdruck und somit einen charakteristischen, unangenehmen Geruch
auf. Es sind erhebliche Arbeiten unternommen worden, um verschiedene
Merkmale dieser Verbindungen zu verbessern, u.a. in Bezug auf die
Wasserlöslichkeit,
so dass die Dämpfe
minimiert werden. Beispielsweise sind verschiedene Lösungsgruppen,
wie u.a. Hydroxyl-, Carboxyl- und Sulfonylgruppen, in diese Verbindungen
durch einfache Reaktion eingebracht worden, um das Geruchsproblem
zu minimieren.
-
Bekannte
Verfahren zur Herstellung von Hydroxylaminderivaten mit Lösungsgruppen,
wie u.a. Hydroxylgruppen, umfassen typischerweise einen oder mehrere
synthetische Reaktionsschritte und die Isolierung des Produkts,
das dann den Farbentwicklungslösungen
hinzugefügt
wird. Ein vereinfachtes Verfahren zur Herstellung geruchsloser Farbentwicklungs-Antioxidationsmittel
wird in US-A-5,508,155 sowie in den zugehörigen Patenten beschrieben.
Das Verfahren umfasst die Reaktion eines Salzes von Hydroxylamin
oder eines monosubstituierten Hydroxylaminderivates mit einem bestimmten
Epoxid bei Raumtemperatur für
mindestens 8 Stunden (vorzugsweise bis zu 24 Stunden). Das resultierende
Produkt ist in einer Farbentwicklungszusammensetzung ohne Isolation
verwendbar.
-
Zwar
stellt dieses Vorbereitungsverfahren einen wichtigen Fortschritt
der Technik dar, aber es erzeugt neben dem gewünschten Produkt eine Anzahl
von Nebenprodukten. Zudem erfordert es eine zu lange Reaktionszeit
für eine
kostengünstige
Massenherstellung. Es besteht somit Bedarf nach Mitteln zur kostengünstigeren
Herstellung hydroxysubstituierter Hydroxylaminderivate bei reduziertem
Anfall von Nebenprodukten.
-
Die
zuvor genannten Probleme werden mit einem Verfahren zur Herstellung
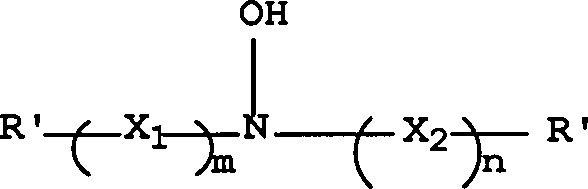
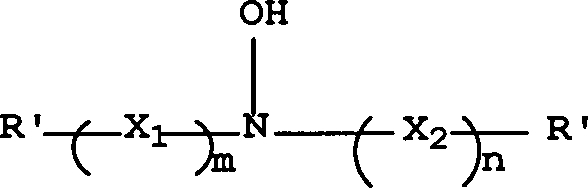
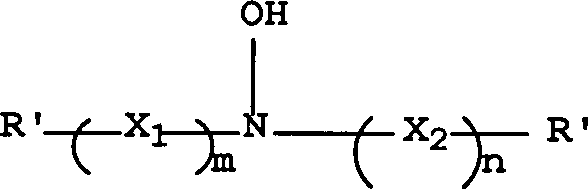
eines Antioxidationsmittels mit folgender Struktur I gelöst:
worin R' für
Wasserstoff, eine Alkylgruppe, eine Haloalkylgruppe, eine Hydroxyalkylgruppe,
eine Cycloalkylgruppe oder eine Arylgruppe steht und X
1 für -C(OH)R
2CHR
1-,
X
2 für
-CHR
1C(OH)R
2-, R
1 und R
2 jeweils
unabhängig
für Wasserstoff,
eine Alkylgruppe oder eine Hydroxyalkylgruppe stehen oder R
1 und R
2 zusammen
die Kohlenstoffatome darstellen, die notwendig sind, um einen 5- bis
8-gliedrigen carbozyklischen Ring zu bilden, und worin m und n jeweils
für 1 stehen,
-
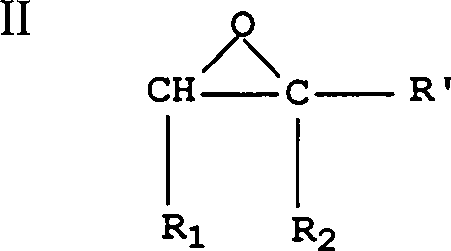
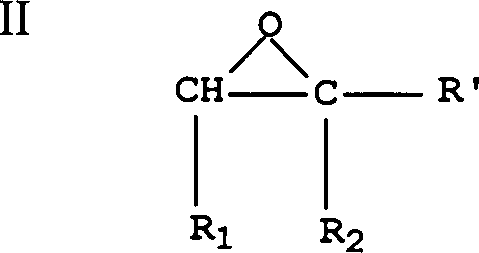
Hinzufügen eines
Epoxids mit folgender Struktur II:
worin R', R
1 und R
2 wie zuvor definiert sind,
zu einer
wässrigen
Lösung
von Hydroxylamin oder einem monosubstituierten Hydroxylamin in freier
Basenform mit einer Menge derart, dass die Reaktionstemperatur der
Reaktionslösung
bei mindestens 50°C
bleibt und dass das Molverhältnis
der Gesamtmenge des Epoxids, das dem Hydroxylamin oder dem monosubstituierten
Hydroxylamin zugesetzt wird, zwischen 2:1 und 2:1,2 beträgt.
-
Die
vorliegende Erfindung stellt zudem die aus dem genannten Produktionsverfahren
resultierende wässrige
Reaktionslösung
bereit und eine gebrauchsfertige Farbentwicklungslösung mit einem
fotografischen Farbentwicklungsmittel sowie eine Reaktionlösung eines
Hydroxylamin-Antioxidationsmittels, das wie zuvor beschrieben herstellbar
ist.
-
Die
vorliegende Erfindung stellt zudem ein Verfahren zur Herstellung
einer fotografischen Farbentwicklungszusammensetzung bereit, das
folgende Schritte umfasst:
- A) Herstellen des
substituierten Hydroxylamin-Antioxidationsmittels in einer Reaktionslösung, wie
zuvor beschrieben, und
- B) Mischen des Hydroxylamin-Antioxidationsmittels mit einem
fotografischen Farbentwicklungsmittel, ohne das Hydroxylamin-Antioxidationsmittel
von der Reaktionslösung
zu trennen.
-
Zudem
umfasst das Verfahren zur fotografischen Verarbeitung die Behandlung
eines bildweise belichteten, farbfotografischen Silberhalogenidelements
mit der zuvor beschriebenen Farbentwicklungszusammensetzung.
-
Die
vorliegende Erfindung stellt eine gebrauchsfähige Farbentwicklungszusammensetzung
bereit, die aufgrund des Vorhandenseins eines geeigneten, hydroxysubstituierten
Hydroxylamins als Antioxidationsmittel gegen Flächenoxidation stabil ist. Zudem
ist dieses Antioxidationsmittel sehr gut wasserlöslich, was den unangenehmen
Geruch reduziert, der ansonsten auftreten könnte. Die Lösungsgruppen werden dem Hydroxylaminausgangsmaterial
in einem schnellen und einfachen synthetischen Verfahren unter Verwendung
eines Epoxids als Co-Reaktionsmittel
zugesetzt. Die resultierende Reaktionslösung enthält weniger Nebenprodukte und lässt sich
mit einem Farbentwicklungsmittel mischen, ohne dass das Antioxidationsmittel
aus seiner Reaktionslösung
isoliert werden muss. Wegen der geringeren Anzahl von Nebenprodukten
kann die Reaktionslösung
mit Titrier- und Chromatographieverfahren leichter auf das Produkt
analysiert werden.
-
Die
zuvor beschriebenen Vorteile werden durch Verwendung einer freien
Basenform des Hydroxylamins (oder des monosubstituierten Derivats)
in der Reaktion statt des üblicheren
Hydroxylaminsalzes (wie z.B. ein Hydroxylaminsulfat) erzielt. Das
Epoxid wird zudem einer wässrigen
Reaktionslösung
in einer Menge zugesetzt, die ausreicht, um aufgrund der exo thermen
Wärmeentwicklung
aus der Reaktion eine höhere
Reaktionstemperatur zu wahren. Die Gesamtmenge der Reaktionsmittel
wird derart gesteuert, dass die höchste Stabilität bei einer
Reduzierung der Nebenprodukte erzielt wird, so dass das Molverhältnis des
Epoxids zum Hydroxylaminreaktionsmittel zwischen 2:1 und 2:1,2 beträgt.
-
Die
Erfindung wird im folgenden anhand in der Zeichnung dargestellter
Ausführungsbeispiele
näher erläutert.
-
Es
zeigen
-
1 eine
grafische Darstellung einer bei 0-22°C durchgeführten Reaktion, wie in Beispiel
1 nachfolgend beschrieben.
-
2 eine
grafische Darstellung einer bei 25-48°C durchgeführten Reaktion, wie in Beispiel
1 nachfolgend beschrieben.
-
3 eine
grafische Darstellung einer bei 50-62°C durchgeführten Reaktion, wie in Beispiel
1 nachfolgend beschrieben.
-
4 eine
grafische Darstellung einer bei 60-100°C durchgeführten Reaktion, wie in Beispiel
1 nachfolgend beschrieben.
-
Wie
zuvor erwähnt,
werden die erfindungsgemäßen Farbentwicklungszusammensetzungen
durch Mischen eines fotografischen Farbentwicklungsmittels mit einem
hydroxysubstituierten Hydroxylamin-Antioxidationsmittel hergestellt,
wie nachfolgend beschrieben wird. Im Allgemeinen wird das Antioxidationsmittel
aus den Reaktionsteilnehmern in einer Reaktionslösung hergestellt und in dieser
Reaktionslösung
ohne Trennung verwendet. Auf diese Weise wurde das Antioxidationsmittel
in situ hergestellt, und brauchte in keiner Weise vor der Verwendung
von der Reaktionslösung
getrennt zu werden. Es ist allerdings nicht notwendig, dass die die
Reaktionsteilnehmer enthaltende Reaktionslösung auf Anhieb verwendet wird.
Statt dessen kann sie zur späteren
Verwendung gelagert oder zunächst
mit dem Farbentwicklungsmittel gemischt und zur späteren Verwendung
gelagert werden. Unter "Trennung" ist ein physikalisches
oder chemisches Mittel zu verstehen, um das Produkt der hydroxysubstituierten
Hydroxylaminreaktion vor der Verwendung mit dem Farbentwicklungsmittel
aus der Reak tionslösung
zu entfernen. Diese kosten- und zeitaufwändigen Trennschritte werden
durch die praktische Verwertung der vorliegenden Erfindung vermieden.
-
Die
Farbentwicklungszusammensetzung als eine Mischung aus Antioxidationsmittel
und Farbentwicklungsmittel (und anderen geeigneten Komponenten)
lässt sich
entweder als arbeitsfertiges fotografisches Bad oder als Regenerator
verwenden oder in konzentrierter Form formulieren.
-
Monosubstituierte
Hydroxylamine, die als ein Reaktionsmittel in der praktischen Verwertung
der vorliegenden Erfindung verwendbar sind, lassen sich im Allgemeinen
als "Hydroxylamine" definieren, die
einen monovalenten aliphatischen oder aromatischen Substituenten
aufweisen, der mit dem Stickstoffatom verbunden ist. Derartige Substituenten
enthalten monovalente Acryl- oder zyklische Kohlenwasserstoffgruppen,
aromatische carbozyklische Gruppen sowie monovalente heterozyklische
Gruppen. Monosubstituierte Hydroxylamine werden beispielsweise in
US-A-5,091,292, US-A-5,094,937 und US-A-5,100, 765 beschrieben.
-
Geeignete
Hydroxylamine lassen sich beispielsweise als R''N(OH)H
definieren, wobei R" für Wasserstoff,
eine substituierte oder unsubstituierte Alkylgruppe aus 1 bis 10
Kohlenstoffatomen (wie Methyl, Ethyl, Propyl, Isopropyl, Hydroxymethyl,
2-Hydroxyethyl, Pentyl, t-Butyl, Benzyl und Octyl), eine substituierte
oder unsubstituierte Cycloalkylgruppe aus 5 bis 10 Kohlenstoffatomen
(wie Cyclopentyl, Cyclohexyl, 4-Methyl-Cyclohexyl und Cyclooctyl)
oder substituierte oder unsubstituierte Arylgruppe aus 6 bis 10
Kohlenstoffatomen (wie Phenyl, Naphthyl, Xylyl, 4-Hydroxyphenyl
und Tolyl) steht. Andere substituierte Alkyl-, Cycloalkyl- und Arylgruppen
werden Fachleuten selbstverständlich
bekannt sein. Vorzugsweise steht R'' für Wasserstoff
oder Alkylgruppe mit 1 bis 4 Kohlenstoffatomen. Am besten steht
R'' für Wasserstoff.
-
Besonders
geeignete, monosubstituierte Hydroxylamine umfassen beispielsweise,
aber nicht abschließend,
N-Methylhydroxylamin, N-Isopropylhydroxylamin und N-Ethylhydroxylamin.
-
Für die Verwendung
in der Erfindung müssen
Hydroxylamin- oder die monosubstituierten Derivate in freier Basenform
vorliegen, was bedeutet, dass sie nicht als saure Salze vorhanden sind,
wie beispielsweise Sulfate oder Hydrochloride. Zur Verwendung in
der vorliegenden Erfindung sind also keine Hydroxylaminsalze vorgesehen,
und es brauchen der Reaktionsmischung keine chemischen Basen zugesetzt
zu werden, um die Reaktionssalze zu neutralisieren.
-
Das
zuvor beschriebene Hydroxylamine oder die monosubstituierten Hydroxylamine
werden also unter geeigneten Bedingungen (siehe unten) mit mono-,
di-, tri- oder tetrasubstituiertem Epoxid reagiert, d.h. Epoxide
mit einem bis vier Substituenten auf den beiden Kohlenstoffatomen
im Epoxidring. Derartige Substituenten beinhalten die zuvor in der
Definition der Hydroxylamine beschriebenen.
-
Insbesondere
lassen sich diese Epoxide so definieren, dass sie folgende Struktur
(II) aufweisen:
wobei R' für
Wasserstoff oder eine Alkylgruppe von 1 bis 10 Kohlenstoffatomen
(wie Methyl, Ethyl, Isopropyl, t-Butyl, Pentyl, Hexyl, Benzyl, Octyl,
Decyl und 3-Methylhexyl) steht. Unter "Alkylgruppe" ist eine unsubstituierte lineare oder
verzweigte Alkylgruppe mit den genannten Kohlenstoffatomen zu verstehen
sowie eine lineare oder verzweigte Alkylgruppe, die mit einer oder
mehreren Phenylgruppen oder Hydroxyphenylgruppen substituiert ist,
solange die maximale Zahl von Kohlenstoffatomen nicht überschritten
wird. Vorzugsweise steht R' für eine substituierte
oder unsubstituierte Alkylgruppe aus 1 bis 7 Kohlenstoffatomen und
am besten weisen die Alkylgruppen 1 bis 3 Kohlenstoffatome auf.
-
R' kann zudem eine
substituierte oder unsubstituierte Haloalkylgruppe aus 1 bis 10
Kohlenstoffatomen sein (wie die zuvor beschriebenen Alkylgruppen,
bei denen ein oder mehrere Wasserstoffatome durch ein oder mehrere
Haloatome ersetzt sind). Die Haloalkylgruppe kann einen oder mehrere
Halosubstituenten aufweisen, die aus Chlor und Brom auswählbar sind.
Vorzugsweise weist die Haloalkylgruppe 1 bis 3 Kohlenstoffatome und
einen oder zwei Chlorsubstituenten und am besten eine einzelne Chlorgruppe
auf. In dieser Kategorie von R' Gruppen
ist dies vorzugsweise Chlormethyl oder 2-Chlorethyl.
-
R' kann zudem eine
substituierte oder unsubstituierte Hydroxyalkylgruppe von 1 bis
10 Kohlenstoffatomen sein (wie Hydroxymethyl, 2-Hydroxyethyl, 1-Hydroxyethyl,
2-Hydroxypropyl, 2,3-Dihydroxypropyl, 1-Hydroxyoctyl und 1,3-Dihydroxydecyl).
Mit "Hydroxyalkylgruppe" ist eine Alkylgruppe
gemeint, bei der die genannten Kohlenstoffatome durch eine oder
mehrere Hydroxygruppen an einer beliebigen Stelle des Moleküls substituiert
sind, an der dies technisch möglich
ist, und wahlweise durch einen oder mehrere Substituenten, wie zuvor
für die "Alkylgruppe" beschrieben. Vorzugsweise
ist in diesem Ausführungsbeispiel
R' eine unsubstituierte
Hydroxyalkylgruppe aus 1 bis 3 Kohlenstoffatomen mit nur einer Hydroxylgruppe
und vorzugsweise ist dies Hydroxymethyl.
-
In
der oben genannten Formel II kann R' zudem für eine Arylgruppe mit 6 bis
10 Kohlenstoffatomen in der Ringstruktur stehen (wie Phenyl, Xylyl,
Tolyl, Naphthyl und 4-Hydroxyphenyl). Mit "Arylgruppe" ist eine substituierte oder unsubstituierte
Naphthylgruppe gemeint oder eine dieser Gruppen, bei denen eine
oder mehrere Alkylgruppen (wie zuvor definiert) oder Hydroxygruppen
an einer beliebigen Position des Rings stehen, die nicht mit den
Reaktionseigenschaften oder der Löslichkeit des Epoxids kollidieren.
Die Arylgruppe kann zudem einen Phenylring mit nicht aromatischen
ankondensierten carbozyklischen oder heterozyklischen Ringstrukturen
umfassen. Wenn R' für eine Arylgruppe
steht, ist dies vorzugsweise eine substituierte oder unsubstituierte Phenylgruppe
und am besten Phenyl.
-
R' kann zudem eine
Cycloalkylgruppe mit 5 bis 10 Kohlenstoffatomen in der Ringstruktur
sein (wie Cyclopentyl, Cyclohexyl, 4-Methylcyclohexyl und 3-Hydroxycyclohexyl).
Unter "Cycloalkylgruppe" ist ein unsubstituiertes
Cycloalkyl mit den erforderlichen Kohlenstoffatomen zu verstehen,
sowie Cycloalkylringe, die mit einem oder mehreren Alkylguppen (wie
zuvor definiert) oder Hydroxylgruppen substituiert sind. Als Cycloalkylgruppe
steht R' vorzugsweise
für Cyclohexyl.
-
R1 und R2 stehen unabhängig voneinander
für eine
substituierte oder unsubstituierte Alkylgruppe aus 1 bis 2 Kohlenstoffatomen
(d.h. eine Methyl- oder Ethylgruppe, die, wie beschrieben, an die
Stelle einer "Alkylgruppe" treten kann), oder
für eine
substituierte oder unsubstituierte Hydroxyalkylgruppe aus 1 bis
2 Kohlenstoffatomen (d.h. Methyl oder Ethyl mit einem oder mehreren
Hydroxysubstituenten).
-
Alternativ
hierzu können
R1 und R2 zusammen
für die
Kohlenstoffatome stehen, die notwendig sind, um eine 5- bis 8-gliedrige
gesättigte
oder teilgesättigte,
carbozyklische Ringstruktur zu bilden (aus einem oder mehreren kondensierten
Ringen), die durch eine oder mehrere Alkylgruppen von 1 bis 3 Kohlenstoffatomen (wie
zuvor definiert) oder durch einen oder mehrere Hydroxyalkylgruppen
aus 1 bis 3 Kohlenstoffatomen (wie zuvor definiert) substituierbar
sind. Unter "teilgesättigt" sind Ringstrukturen
zu verstehen, die mindestens eine Doppelbindung enthalten, wobei
die Ringstruktur aber nicht aromatisch ist.
-
Besonders
geeignete Epoxide zur praktischen Verwertung der vorliegenden Erfindung
sind u.a. folgende Verbindungen: Glycidol, Ethylenoxid, Propylenoxid,
2-Methyl-2,3-Epoxy-1-Propanol,
4-Phenyl-2,3-Epoxy-1-Butanol, 1,4-Butandioldiglycidylether, Epichlorhydrin
und 1,2,7,8-Diepoxyoctan. Glycidol wird am meisten bevorzugt.
-
Die
zur praktischen Verwertung der vorliegenden Erfindung geeigneten
Hydroxylamin-Antioxidationsmittel werden mithilfe der folgenden
allgemeinen Verfahren und Bedingungen hergestellt.
-
Eines
oder mehrere Hydroxylamine (in freier Basenform), wie zuvor definiert,
werden in einer wässrigen
Lösung
bereitgestellt. Die Konzentration in der Lösung kann variieren, beträgt im Allgemeinen
aber bis zu 17 Mol/l und typischerweise von 1 bis 5 Mol/l. Ein oder
mehrere Epoxide, wie zuvor definiert, werden dann der Lösung zur
Reaktion zugesetzt. Die Reaktionsgeschwindigkeit wird derart gesteuert,
dass die Reaktion so schnell wie möglich erfolgt, aber langsam
genug ist, um die erwartete exotherme Wärmeentwicklung zu steuern und
ein Rücklaufen
zu verhindern. Im Allgemeinen werden die Epoxide zur Reaktionslösung mit
mindestens 0,1 Mol%/Min und vorzugsweise mit 0,1 bis 4 Mol%/min
zugegeben. Die Zugabemenge kann somit erheblich je nach Reaktionsgeschwindigkeit
eines bestimmten Satzes von Reaktionsteilnehmern, der gewünschten
Reaktionstemperatur und dem gewünschten
Ertrag variieren. Die Angabe "Mol%/min" bezieht sich auf
die gesamte Stoffmenge von Epoxid zur Verwendung in der Reaktion.
Epoxidzugaben können
kontinuierlich oder intermittie rend erfolgen, je nach verwendeten
Geräten
und Reaktionsmitteln und der Fähigkeit
des Bedieners, die Reaktionstemperatur zu steuern.
-
Die
Reaktion beginnt sofort bei Zugabe von Epoxid und kann sich über dessen
Zugabe hinaus fortsetzen. Der Zeitpunkt der Reaktion ist von vielen
Faktoren abhängig,
u.a. den Reaktionsmitteln, der Reaktionstemperatur, dem gewünschten
Ertrag und der Art der Epoxidzugabe. Im Allgemeinen wird die Reaktion
in möglichst
so kurzer Zeit durchgeführt,
wie das unter den gegebenen Umständen
sinnvoll ist. Vorzugsweise wird die Reaktion innerhalb von 8 Stunden
abgeschlossen (und am besten innerhalb von 4 Stunden). Die Lösung kann jederzeit
während
der Reaktion in geeigneter Weise umgerührt werden.
-
Die
Reaktion kann bei jeder geeigneten Temperatur durchgeführt werden,
wobei niedrigere Reaktionstemperaturen zu einer impraktikabel langsamen
Reaktion (ihren. Die Reaktionstemperatur wird daher im Allgemeinen
bei mindestens 50°C
gehalten und beträgt
vorzugsweise zwischen 70 und 95°C.
Eine höhere
Reaktionstemperatur ermöglicht
eine schnellere Reaktion und kann durch die exotherme Wärmeentwicklung
der Reaktion oder unter Verwendung einer externen Wärmezufuhr
bereitgestellt werden. Die Reaktion kann also bei deutlich niedrigerer
Temperatur beginnen, während
die exotherme Wärmeentwicklung
einen Anstieg der Temperatur der Reaktionsmischung auf den gewünschten
Wert bewirkt. Alternativ hierzu kann die Reaktionslösung auf
die gewünschte
Reaktionstemperatur vor Zugabe des Epoxids oder der Epoxide vorgewärmt werden.
-
Die
das Antioxidans-Reaktionsprodukt enthaltende Reaktionslösung ist
zur Zubereitung von Farbentwicklungszusammensetzungen ohne Trennung
oder Isolierung verwendbar, oder sie kann verdünnt oder zur Lagerung konzentriert
und später
verwendet werden.
-
Die
zur Herstellung des Antioxidans verwendeten Reaktionsmittel können aus
einer Anzahl kommerzieller Quellen bezogen werden, beispielsweise,
aber nicht abschließend,
von Nissin Chemical Company, Dixie Chemical Company, Angus Chemicals,
BASF und Aldrich Chemical Company. Alternativ hierzu wäre es für einen
Fachmann nicht schwierig, die genannten Epoxide oder monosubstituierten
Hydroxylamine anhand bekannter Verfahren und leicht zugänglicher
Ausgangsmaterialien herzustellen.
-
Die
resultierenden Hydroxylamin-Antioxidantien lassen sich durch folgende
Struktur (I) definieren:
worin R', R
1, R
2, X
1, X
2,
m und n wie zuvor definiert sind.
-
Die
in der vorliegenden Erfindung hergestellten und darin verwendbaren
disubstituierten Hydroxylamin-Antioxidantien umfassen beispielsweise,
aber nicht abschließend:
N,N-Bis(2,3-Dihydroxypropyl)-Hydroxylamin,
N,N-Bis(2-Methyl-2,3-Dihydroxypropyl)hydroxylamin und N,N-Bis(1-Hydroxymethyl-2-Hydroxy-3-Phenylpropyl)hydroxylamin.
Die erste Verbindung ist die bevorzugte.
-
Mehr
als ein Antioxidans kann gleichzeitig hergestellt und in die erfindungsgemäßen Farbentwicklungszusammensetzungen
eingebracht werden, indem die entsprechenden mehrfachen Epoxide
und monosubstituierten Hydroxylamine in der Reaktionslösung zur
Reaktion gebracht werden. Vorzugsweise wird allerdings nur ein Antioxidans
hergestellt und für
jede Farbentwicklungszusammensetzung verwendet.
-
Die
erfindungsgemäßen Farbentwicklungszusammensetzungen
umfassen ein oder mehrere Farbentwicklungsmittel, von denen es wiederum
hunderte von Möglichkeiten
gibt. Verwendbare Klassen dieser Materialien beinhalten beispielsweise,
aber nicht abschließend,
Ainophenole, p-Phenylendiamine (insbesondere N,N-Dialkyl p-Phenylendiamine)
sowie andere in der Technik bekannte Stoffe. Weitere Angaben zu
diesen Materialien sind in Research Disclosure, Publikation 38957,
Seite 592-639 (September 1996) und den darin genannten Quellen aufgeführt. Research
Disclosure ist eine Publikation von Kenneth Mason Publications Ltd., Dudley
House, 12 North Street, Emsworth, Hampshire PO10 7DQ, England (auch
von Emsworth Design Inc., 121 West 19th Street, New York, N.Y. 10011,
USA zu beziehen). Diese Quellen werden im Folgenden als Forschungsveröffentlichung "Research Disclosure" bezeichnet.
-
Besonders
geeignete Farbentwicklungsmittel umfassen beispielsweise, aber nicht
abschließend, N,N-Diethyl
p-Phenylenediaminsulfat (KODAK Farbentwicklungsmittel CD-2), 4-Amino-3-Methyl-N-(2-Methansulfonamidoethyl)anilinsulfat,
4-(N-Ethyl-N-β-Hydroxyethylamin)-2-Methylanilinsulfat
(KODAK Farbentwicklungsmittel CD-4), p-Hydroxyethylethylaminoanilinsulfat,
4-(N-Ethyl-N-2-Methansulfonylaminoethyl)-2-Methylphenylenediaminsesquisulfat
oder 4-Amin-3-Methyl-N-Ethyl-N-(β-Methansulfonamidoethyl)anilin
(KODAK Farbentwicklungsmittel CD-3), 4-(N-Ethyl-N-2-Methansulfonylaminoethyl)-2-Methylphenylenediaminsesquisulfat
sowie weitere, wie Technikern bekannt sein wird. Das KODAK Farbentwicklungsmittel
CD-3 wird zur praktischen Verwertung der vorliegenden Erfindung
bevorzugt.
-
Die
Farbentwicklungszusammensetzung lässt sich leicht durch Mischen
eines geeigneten Farbentwicklungsmittels (in einer geeigneten Lösung) mit
einem Teil der originalen Reaktionslösung (verdünnt oder konzentriert) herstellen,
die das zuvor beschriebene Antioxidationsmittel enthält. Der
resultierenden Zusammensetzung kann Wasser zugesetzt werden, um
die gewünschten
Konzentrationen zu erhalten, und der pH-Wert kann mit einer geeigneten
chemischen Base (wie Natriumhydroxid) auf den gewünschten
Wert eingestellt werden.
-
Die
Mengen des Hydroxylamin-Antioxidationsmittels und des Farbentwicklungsmittels,
die in der erfindungsgemäßen Farbentwicklungszusammensetzung
im Allgemeinen und vorzugsweise vorhanden sind, werden in der folgenden
Tabelle aufgeführt.
Diese Bereichsangaben sind ungefähre
Angaben. Im Allgemeinen kann das Stoffmengenverhältnis (Molverhältnis) von
Antioxidationsmittel zu Farbentwicklungsmittel stark schwanken,
liegt aber vorzugsweise im Bereich von 0,1:1 bis 4:1.
-
-
Die
erfindungsgemäße Farbentwicklungszusammensetzung
kann zudem einen oder mehrere weiterer Zusätze enthalten, die in derartigen
Zusammensetzungen üblich
sind, wie beispielsweise Alkalimetallhalogenide (wie z.B. Kaliumchlorid,
Kaliumbromid, Natriumbromid und Natriumiodid), Metallmaskierungsmittel
(wie Aminopolycarboxylsäuren),
Puffer zur Einstellung des pH-Werts auf 9 bis 13 (vorzugsweise auf
9 bis 11), wie Carbonate, Phosphate und Borate, Sulfate, Entwicklungsbeschleuniger,
Duftstoffe, optische Aufheller, Netzmittel, Surfactants und wasserlösliche oder
wasserdispergierbare Kuppler, wie einschlägigen Fachleuten bekannt ist
(siehe beispielsweise oben genannte Forschungsveröffentlichung "Research Disclosure"). Die Mengen dieser
Additive sind in der Technik bekannt.
-
Eine
weitere geeignete Komponente der Farbentwicklungszusammensetzung,
insbesondere bei Formulierung in konzentrierter Form, ist ein fotografisch
inaktives, wassermischbares oder wasserlösliches, geradkettiges organisches
Lösemittel,
das Farbentwicklungsmittel in ihrer freien Basenform zu lösen vermag. Derartige
organische Lösemittel
sind einzeln oder in Kombination verwendbar, wobei jedes vorzugsweise
eine Molmasse von mindestens 50 aufweist und vorzugsweise von mindestens
100 und im Allgemeinen von 200 oder weniger und vorzugsweise von
150 oder weniger. Derartige bevorzugte Lösemittel weisen im Allgemeinen
2 bis 10 Kohlenstoffatome auf (vorzugsweise 2 bis 6 Kohlenstoffatome
und vorzugsweise 4 bis 6 Kohlenstoffatome) und können zudem mindestens zwei
Stickstoff- oder Sauerstoffatome oder mindestens ein jeweiliges
Heteroatom enthalten. Die organischen Lösemittel sind durch mindestens
eine hydroxyfunktionale Gruppe und vorzugsweise durch mindestens
zwei derartiger Gruppen substituiert. Dabei handelt es sich um geradkettige
Moleküle,
nicht um zyklische Moleküle.
-
Mit "fotografisch inaktiv" ist gemeint, dass
die organischen Lösemittel
im Wesentlichen keine positive oder negative Wirkung auf die Farbentwicklungsfunktion
des Konzentrats ausüben.
-
Geeignete
organische Lösemittel
umfassen beispielsweise, aber nicht abschließend, Polyole, wie u.a. Glycole
(wie Ethylenglycol, Diethylenglycol und Triethylenglycol), Polyhydroxyamine
(inkl. Polyalkoholamine) und Alkohole (wie Ethanol und Benzylalkohol).
Bevorzugt werden Glycole, wobei Ethylenglycol, Diethylenglycol und
Triethylenglycol besonders bevorzugt werden. Bei den Alkoholen werden
Ethanol und Benzylalkohol besonders bevorzugt. Das am meisten bevorzugte
organische Lösemittel
ist Diethylenglycol.
-
Die
erfindungsgemäße Farbentwicklungszusammensetzung
kann als gebrauchsfertig konzentrierte Lösung in Verarbeitungstanks,
als Regenerat oder in Form von Konzentraten für jede geeignete Verwendung in
der fotografischen Verarbeitung angesetzt werden.
-
Die
erfindungsgemäße Farbentwicklungszusammensetzung
ist für
die Farbentwicklung in einem bildweise belichteten fotografischen
Silberhalogenidelement verwendbar, das einen Träger und eine oder mehrere Silberhalogenid-Emulsionsschichten
umfasst, die eine bildweise Verteilung entwickelbarer Silberhalogenid-Emulsionskörner enthalten.
Eine große
Vielzahl von fotografischen Elementen (sowohl Farbfilme und Farbpapiere
als auch Laufbild-Farbfilme
und Prints), die verschiedene Emulsionsarten enthalten, können unter Verwendung
der vorliegenden Erfindung verarbeitet werden, wobei die Arten der
jeweiligen Elemente in der Technik bekannt sind (siehe oben genannte
Forschungsveröffentlichung "Research Disclosure"). Insbesondere ist
die vorliegende Erfindung zur Verarbeitung farbfotografischer Silberhalogenidpapiere
oder anderer "Anzeigeelemente" verwendbar, insbesondere
Farbpapiere mit stark silberchloridhaltigen (mehr als 90 Mol% Chlorid,
bezogen auf den Gesamtsilbergehalt), lichtempfindlichen Emulsionen.
Die Farbentwicklungszusammensetzungen sind auch zur Verarbeitung
von Farbumkehrfilmen und Papieren verwendbar.
-
Die
Farbentwicklung ist im Allgemeinen durch Inkontaktbringen des Elements
unter geeigneten Zeit- und Temperaturbedingungen sowie in einem
geeigneten Entwicklungsgerät
zur Erzeugung des gewünschten Farbbildes
durchführbar.
Weitere Verarbeitungsschritte sind dann durch Verwendung konventioneller
Verfahren durchführbar,
beispielsweise, aber nicht abschließend, mit Schritten zur Entsilberung
des Elements (Bleichen und Fixieren oder Bleichen/Fixieren), Wässern (oder
Spülen),
Stabilisieren und Trocknen, die in einer gewünschten Reihenfolge durchgeführt werden.
Geeignete Verarbeitungsschritte, Bedingungen und Materialien sind
in der Technik bekannt (siehe beispielsweise die oben genannte Forschungsveröffentlichung "Research Disclosure").
-
Die
folgenden Beispiele zeigen die praktische Verwertung der Erfindung
und sind in keiner Weise einschränkend
zu verstehen. Soweit nicht anders angegeben, beziehen sich die Prozentangaben
auf Gew.-%.
-
Beispiel 1: Herstellung
von Hydroxylamin-Antioxidationsmittel im Labormaßstab
-
Das
Beispiel zeigt ein typisches Verfahren zur Herstellung von erfindungsgemäßen Antioxidationsmitteln.
-
Ein
2-Liter-Dreihalskolben mit mechanischem Rührwerk, Rücklaufkondensator, Thermometer,
Stickstoffeinlass und zusätzlichem
Trichter wurde mit einer 50% wässrigen
Hydroxylaminlösung
((209,4 ml, 234,53 g, 3,547 Mol) befüllt und mit 5647 ml entsalztem
Wasser aufgefüllt.
Die Lösung
wurde mithilfe eines Ölbads auf
60°C erwärmt. Die
Reaktion wurde mit einer FTIR-Sonde überwacht. Hierzu zirkulierte
die Lösung
durch eine IR-Zelle, wobei in Abständen von jeweils drei Minuten
Messspektren ermittelt wurden. Die Konzentration jedes Stoffes wurde
nach jeder Probennahme aus einem deutlichen Messwert für jeden
Stoff ermittelt und auf einer Zeitachse abgetragen (siehe 4).
-
Der
Lösung
wurde Glycidol (96%, 490 ml, 547,33 g, 7,094 Mol) mit 2,1 ml/min
zugegeben. Die Temperatur der resultierenden Reaktionsmischung stieg
an, und die Mischung begann zurückzulaufen.
Die Epoxidzugabe war innerhalb von 1,5 Stunden abgeschlossen, worauf
die Reaktion für
weitere 30 Minuten fortgesetzt wurde. Nach dem Abkühlen betrug
das Reaktionsmischungsvolumen 1143 ml bei einer Masse von 1293,1
g.
-
Der
theoretische Analyse des gewünschten
Produkts N,N-Bis-(2,3-Dihydroxypropyl)hydroxylamin betrug 49,37%
(3,1 Mol), die tatsächlich
berechnete Analyse ergab 49,1 %, wie durch titrimetrische und chromatografische
Verfahren ermittelt. Der Gesamtertrag betrug 99%. Wässrige Lösungen der
genannten Verbindung wiesen keinen unangenehmen Geruch auf.
-
Ähnliche
Reaktionsverfahren wurden bei unterschiedlichen Reaktionstemperaturen
durchgeführt,
wobei nach jedem Reaktionslauf eine FTIR-Sonde in den Kolben eingebracht
wurde, um das Verschwinden von Reaktionsteilnehmern und das Entstehen
des gewünschten
Produkts zu überwachen.
Alle Reaktionen wurden mit demselben Verhältnis von Reaktionsteilnehmern
durchgeführt,
wie im vorausgehenden Beispiel beschrieben. In den 1-4 zeigen
die mit "X" bezeichneten Kurven
die Konzentrationsänderung
des Hydroxylamin-Reaktionsmittels. Auf gleiche Weise zeigen die
mit "B" bezeichneten Kurven
die Konzentrationsänderung des
Glycidol-Reaktionsmittels, und die mit "C" bezeichneten
Kurven zeigen die Änderung
der Konzentration an substituiertem Hydroxylamin.
-
Die
Ergebnisse einer bei einer Reaktionstemperatur von 0-22°C durchgeführten Reaktion
sind in 1 dargestellt. Auf der Zeitskala
begann die Glycidolzugabe bei Punkt "A" (10
Minuten) bei einer Reaktionstemperatur von 10°C. Bei Punkt "B" (25 Minuten) war die Reaktionstemperatur
auf 12°C
angestiegen, und die Glycidolzugabe wurde erhöht. Bei Punkt "C" (60 Minuten) war die Glycidolzugabe
abgeschlossen, und die Reaktionstemperatur betrug 19°C. "Punkt" bezeichnet eine
Reaktionszeit von 225 Minuten. Zu diesem Zeitpunkt betrug die Reaktionstemperatur
22°C. Es
ist ersichtlich, dass die Glycidolkonzentration in der Reaktionsmischung
erheblich war, bevor eine deutliche Reaktion einsetzte. Diese lange
Induktionsperiode ist unter bestimmten Umständen nicht akzeptabel (beispielsweise
in der Massenproduktion), da Nebenreaktionen auftreten könnten, die
zu unerwünschten
Nebenprodukten führen,
wenn die Glycidolkonzentration steigt.
-
2 zeigt
die Ergebnisse für
eine Reaktion, die bei 25°C
begann, wobei allerdings ein Anstieg der Reaktionstemperatur auf
48°C zugelassen
wurde, die anschließend
gehalten wurde. Die Reaktion begann wesentlich schneller als bei
einer Reaktionstemperatur im Bereich von 0-22°C (1). In 2 bezeichnet
Punkt "A" (10 Minuten) den
Punkt, bei dem die Glycidolzugabe bei einer Reaktionstemperatur
von 25°C
begann. Bei Punkt "B" (50 Minuten) betrug
die Reaktionstemperatur 48°C.
Bei Punkt "C" (80 Minuten) war
die Glycidolzugabe abgeschlossen, und die Reaktionstemperatur betrug
48°C. Bei
Punkt "D" (225 Minuten) war
die Reaktion beendet, und die Reaktionstemperatur war auf 25°C gefallen.
-
Die
Auswirkung der Temperatur ist in 3 noch deutlicher
zu sehen, wo die Ergebnisse für
eine Reaktionsmischung gezeigt werden, die vor der Glycidolzugabe
auf 50°C
erwärmt
wurde. Das Hydroxylaminreaktionsmittel blieb bei dieser Temperatur
stabil und zeigte eine stetige Reaktion bei Exposidzugabe. Die Glycidolkonzentration
wurde während
der gesamten Reaktion gering gehalten, wodurch kaum Zeit zur Bildung
unerwünschter
Nebenprodukte verblieb. Punkt "A" (40 Minuten) bezeichnet
den Startzeitpunkt der Glycidolzugabe. Bei Punkt "B" (95 Minuten) war die Glycidolzugabe
abgeschlossen, und die Reaktionstemperatur war auf 62°C gestiegen.
Bei Punkt "C" (220 Minuten) war
die Reaktion beendet, und die Reaktionstemperatur war auf 50°C gefallen.
-
4 zeigt
die Ergebnisse aus Beispiel 1, bei dem die Reaktionsmischung auf
60°C vorgewärmt worden
war, gefolgt von einer Glycidolzugabe, die schnell genug erfolgte,
um ein Refluxieren der Reaktionsmischung zu gestatten. Die Reaktion
erfolgte im Wesentlichen spontan, wobei kein weiteres Reaktionsprodukt nach
Abschluss der Glycidolzugabe gebildet wurde. Obwohl es nicht in
jedem Fall wünschenswert
ist, die Reaktionsmischung zum Refluxieren zu bringen, lässt sich
die Reaktionstemperatur leicht überwachen,
um eine optimale Reaktionstemperatur für diesen Satz von Reaktionsteilnehmern
zwischen 60 und 90°C
zu halten. Bei Punkt "A" (40 Minuten) begann
die Glycidolzugabe. Bei Punkt "B" (60 Minuten) war
die Reaktionstemperatur auf 80°C
angestiegen, und die Glycidolzugabe wurde erhöht. Bei Punkt "C" (80 Minuten) war die Reaktionstemperatur
auf 100°C
angestiegen, bei Punkt "D" (140 Minuten) war
die Glycidolzugabe abgeschlossen, und die Reaktionstemperatur bleibt
bei 100°C
konstant.
-
Beispiel 2: Massenherstellung
von Hydroxylamin-Antioxidationsmittel
-
Ein
12-Liter-Dreihalskolben mit mechanischem Rührwerk, Rücklaufkondensator, Thermometer,
Stickstoffeinlass und zusätzlichem
Trichter wurde mit einer 50% wässrigen
Hydroxylaminlösung
(1,675 ml, 1,875 kg, 28,375 Mol) befällt und mit 4375 ml entsalztem
Wasser aufgefüllt.
-
Der
wässrigen
Lösung
wurde Glycidol (96%, 3919 ml, 4377,5 g, 56,75 Mol) bei Raumtemperatur
zugegeben. Bei fortgesetzter Zugabe begann die Temperatur der resultierenden
Reaktionsmischung anzusteigen, und die Epoxidzugabe wurde bei mit
einer Menge fortgesetzt, die ausreichte, um die Temperatur zwischen 80
und 95°C
zu halten. Die Epoxidzugabe war innerhalb von 3 Stunden abgeschlossen,
worauf man die Mischung auf Raumtemperatur abkühlen ließ. Das Reaktionsmischungsvolumen
betrug 9,2 Liter mit einer Masse von 10,516 kg.
-
Die
theoretische Analyse des gewünschten
Produkts N,N-Bis-(2,3-Dihydroxypropyl)hydroxylamin betrug 48,56%
(3,08 Mol), die tatsächlich
berechnete Analyse ergab 48,5%, wie durch titrimetrische und chromatografische
Verfahren ermittelt (im Wesentlichen ein Ertrag von 100%). Wässrige Lösungen der
genannten Verbindung wiesen keinen unangenehmen Geruch auf.
-
Beispiel 3: alternative
Herstellung der Farbentwicklungszusammensetzung
-
Beispiel
1 wurde wiederholt, mit dem Unterschied, dass Propylenoxid anstelle
von Glycidol bei gleicher Molmasse relativ zum Hydroxylamin-Reaktionsmittel
verwendet wurde. Die Analyse ergab, dass das gewünschte, substituierte Hydroxylaminprodukt
erzeugt wurde.
-
Beispiel 4: Herstellung
der Farbentwicklungszusammensetzung
-
Das
Beispiel zeigt die Herstellung einer geeigneten fotografischen,
erfindungsgemäßen Farbentwicklungszusammensetzung.
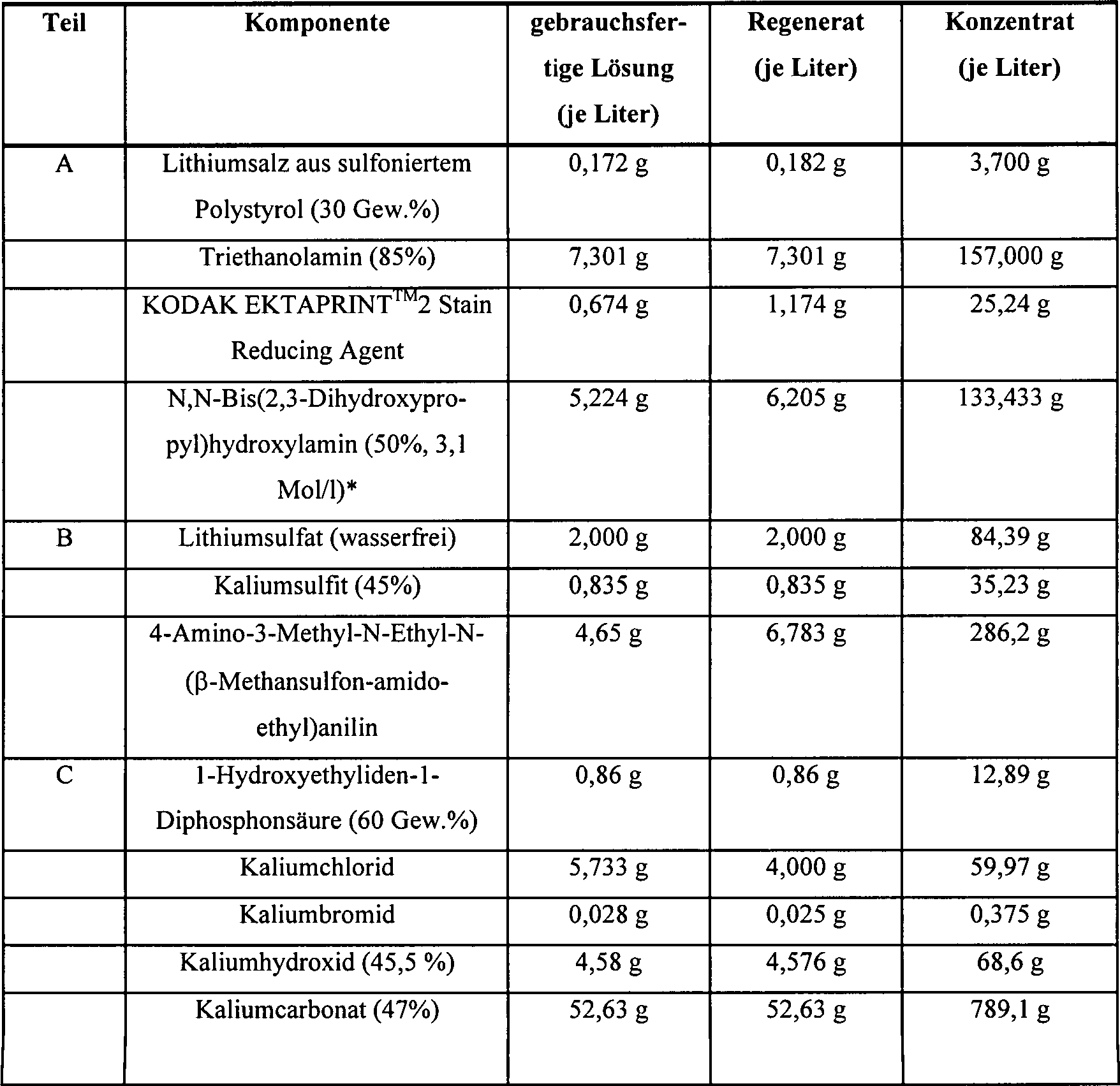
Die Komponenten der Zusammensetzung, wie in der folgenden Tabelle
1 gezeigt, wurden in drei Teilen zugegeben und dann gemischt, um
eine erfindungsgemäße, gebrauchsfertige
Zusammensetzung, ein Regenerat sowie eine konzentrierte Farbentwicklungszusammensetzung
zu erzeugen. Tabelle
I
-
Beispiel 5: Verarbeitung
des fotografischen Elements
-
Die
Farbentwicklungszusammensetzung aus Beispiel 3 wurde zur Verarbeitung
von Proben eines bildweise belichteten farbfotografischen Silberhalogenidpapiers
des Typs KODAK EDGE 7 verwendet. Nach dem Bleichen/Fixieren mithilfe
der kommerziell verfügbaren
EKTACOLOR Bleich-/Fixierlösung
und anschließendem
Wässern
erhielt man geeignete Farbbilder.