CN1204102C - 2,3-二氯-1-丙醇和表氯醇的生产方法 - Google Patents
2,3-二氯-1-丙醇和表氯醇的生产方法 Download PDFInfo
- Publication number
- CN1204102C CN1204102C CN 02801406 CN02801406A CN1204102C CN 1204102 C CN1204102 C CN 1204102C CN 02801406 CN02801406 CN 02801406 CN 02801406 A CN02801406 A CN 02801406A CN 1204102 C CN1204102 C CN 1204102C
- Authority
- CN
- China
- Prior art keywords
- reactor
- chlorine
- degassing tower
- trimethylewne chlorohydrin
- solution
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Lifetime
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C29/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring
- C07C29/62—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring by introduction of halogen; by substitution of halogen atoms by other halogen atoms
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Epoxy Compounds (AREA)
Abstract
本发明公开了以高收率和长时间稳定的方式连续生产2,3-二氯-1-丙醇(2,3-DCH)和表氯醇的方法。在其中使烯丙醇在盐酸溶液中氯化并将反应溶液引入到脱气塔中以便释出氯化氢、再从剩余溶液中获取2,3-DCH的方法中,通过监控和/或控制在脱气塔之前紧接的反应器出口处的溶液的氯浓度和/或存在于反应器气相部分中的氯气的分压和在脱气塔之前的氯气的流速,将在所要引入到脱气塔的反应混合物中的氯的浓度保持在0.015g/ml或0.015g/ml以下和/或将在脱气塔之前紧接的反应器中的氯气的分压保持在0.08MPa或0.08MPa以下。
Description
技术领域
本发明涉及2,3-二氯-1-丙醇(下文有时缩写为“2,3-DCH”)的生产方法,它是制备作为溶剂、环氧树脂生产用原料、合成橡胶生产用原料、氯化橡胶原料稳定剂等使用的表氯醇的中间产物,以及由2,3-DCH制备表氯醇(下文有时缩写为“ECH”)的方法。本发明涉及通过使烯丙醇与氯在盐酸溶液中反应来生产2,3-二氯-1-丙醇的方法。
背景技术
对于通过在盐酸溶液中用氯使烯丙醇氯化来制备2,3-二氯-1-丙醇(2,3-DCH)的生产方法已经提出了许多建议。尤其,已知的是,烯丙醇与氯在高浓度盐酸溶液中的反应能够以高收率生产2,3-DCH(日本专利申请公报Nos.59-128340,59-128341和3-74342等)。
作为2,3-DCH的工业有用的连续生产方法,例如,日本专利申请公报Nos.59-128340,60-258171(US Pat 4634784)和3-74342等公开了将通过烯丙醇在盐酸溶液中的氯化获得的溶液引入到脱气塔中和将该溶液加热以释出氯化氢,随后回收氯化氢和将其送入反应器来生产2,3-DCH的方法。至于在这些方法中使用的烯丙醇和氯之间的比例,日本专利申请公报No.3-74342描述了以相对于烯丙醇的10mol%或10mol%以下的过量供给氯,以及日本专利申请公报No.59-128340描述了大约1.05mol或1.05mol以下的氯/mol烯丙醇的量是足够的。
然而,在将通过烯丙醇在盐酸溶液中的氯化获得的溶液引入到脱气塔中和将该溶液加热以释出氯化氢,随后回收氯化氢和将其送入反应器来生产2,3-DCH的连续方法中,存在的问题是,氯以相对于烯丙醇的超过化学计量比例的量连续供给不仅导致了过量供给的氯的损失,而且导致了气相氯化氢在氯化氢吸收器和/或反应器中的分压降低,这进而引起2,3-DCH的收率下降。相反,烯丙醇以相对于氯的超过化学计量比例的量连续供给不仅引起了未反应的烯丙醇的损失,而且由于聚合物的积累,招致脱气塔的加热器的堵塞,使得操作不能以稳定方式持续长时间。
此外,日本专利申请公报No.3-74342描述了烯丙醇在从系统连续排出的反应混合物中的浓度应该基本为零。然而,它没有关于怎样使烯丙醇的浓度为零的具体描述。
本发明的公开
因此,本发明的目的是提供2,3-DCH的连续生产方法,包括将通过烯丙醇在盐酸溶液中的氯化获得的溶液引入到脱气塔中和将该溶液加热以释出氯化氢,随后回收氯化氢和将其送入反应器,其中使保留在引入脱气塔的反应混合物中的烯丙醇浓度基本为零,使得2,3-DCH和表氯醇能够以高收率和长期稳定的方式连续生产。
在此情况下,进行了大量的研究,结果,现在发现在将通过烯丙醇在盐酸溶液中的氯化获得的溶液引入到脱气塔中和将该溶液加热以释出氯化氢,随后回收氯化氢和将其送入反应器来生产2,3-DCH的连续方法中,为了使保留在引入脱气塔的反应混合物中的烯丙醇的浓度基本为零和连续以高收率获得2,3-二氯-1-丙醇,必须将在所要引入脱气塔的反应混合物中溶解的氯的浓度控制至特定浓度或特定浓度以下和/或将存在于脱气塔之前紧接的反应器气相部分中的氯气分压控制至特定分压或特定分压以下。进一步认识到,重要的是设置用于测定在脱气塔之前紧接的反应器的出口处的溶液中的氯浓度和/或存在于反应器的气相部分中的氯气浓度(分压)的自动分析仪,作为用于将在脱气塔之前紧接的反应器的反应混合物中溶解的氯的浓度和/或在脱气塔之前紧接的反应器的气相部分的分压控制在特定范围内的装置,并且根据该分析仪的读数来控制引入脱气塔之前紧接的反应器的氯气的流速。这样,完成了本发明。
也就是说,本发明提供了如以下所述的用于生产23-二氯-1-丙醇的方法和用于生产表氯醇的方法:
1)通过将含有由烯丙醇在盐酸溶液中的氯化获得的2,3-二氯-1-丙醇的溶液引入到脱气塔以便释出氯化氢,使该氯化氢返回到反应器以供氯化用,以及从剩余溶液中获取2,3-二氯-1-丙醇来生产2,3-二氯-1-丙醇的方法,特征在于该方法包括将在马上要引入到脱气塔中的反应器出口处的溶液中溶解的氯的浓度保持在0.015g/ml或0.015g/ml以下。
2)如在以上1)中所述的通过将含有由烯丙醇在盐酸溶液中的氯化获得的2,3-二氯-1-丙醇的溶液引入到脱气塔以便释出氯化氢,使该氯化氢返回到反应器以供氯化用,以及从剩余溶液中获取2,3-二氯-1-丙醇来生产2,3-二氯-1-丙醇的方法,特征在于该方法包括在脱气塔之前紧接的反应器中设置用于监控反应器出口处的溶液中的氯浓度的分析仪和控制所要引入到反应器的氯气的流速,使得氯的浓度能够保持在0.015g/ml或0.015g/ml以下。
3)通过将含有由烯丙醇在盐酸溶液中的氯化获得的2,3-二氯-1-丙醇的溶液引入到脱气塔以便释出氯化氢,使该氯化氢返回到反应器以供氯化用,以及从剩余溶液中获取2,3-二氯-1-丙醇来生产2,3-二氯-1-丙醇的方法,特征在于该方法包括将脱气塔之前紧接的反应器的气相部分中的氯的分压保持在0.08MPa(绝对压力)或0.08MPa以下。
4)如在以上3)中所述的通过将含有由烯丙醇在盐酸溶液中的氯化获得的2,3-二氯-1-丙醇的溶液引入到脱气塔以便释出氯化氢,使该氯化氢返回到反应器以供氯化用,以及从剩余溶液中获取2,3-二氯-1-丙醇来生产2,3-二氯-1-丙醇的方法,特征在于该方法包括在脱气塔之前紧接的反应器中设置用于监控在反应器气相部分中氯气浓度的分析仪和控制所要引入到反应器的氯气的流速,使得氯气的分压能够保持在0.08MPa(绝对压力)或0.08MPa以下。
5)如在以上1)-4)的任一项中所述的生产2,3-二氯-1-丙醇的方法,其中使用含有40-75质量%的氯化氢(按HCl/(H2O+HCl)计算)的盐酸水溶液。
6)如在以上1)-4)的任一项中所述的生产2,3-二氯-1-丙醇的方法,其中烯丙醇的氯化反应在-30℃到+20℃的温度下进行。
7)如在以上1)-4)的任一项中所述的生产2,3-二氯-1-丙醇的方法,其中烯丙醇的氯化反应在1MPa(表压)或1MPa以下的压力下进行。
8)生产表氯醇的方法,特征在于该方法包括使在以上1)-7)的任一项中所生产的2,3-二氯-1-丙醇进行皂化反应。
附图简述
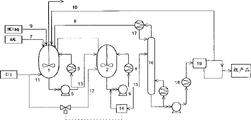
图1是说明使用单段式反应装置的根据本发明的生产2,3-二氯-1-丙醇的方法的实施方案的流程图。
图2是说明使用串联连接的两段式反应装置的根据本发明的生产2,3-二氯-1-丙醇的方法的实施方案的流程图。
图3是说明使用并联连接的两段式反应装置的根据本发明的生产2,3-二氯-1-丙醇的方法的实施方案的流程图。
图4是说明使用串联连接的两段式反应器的根据本发明的生产2,3-二氯-1-丙醇的方法的一个实施方案的流程图。
实施本发明的最佳方式
以下将更详细地描述本发明。
在本发明中用作反应溶剂的盐酸可以是下列的任一种:35质量%浓盐酸水溶液,通过将烯丙醇的氯化的反应混合物脱气、冷却并然后将所获得的液体进行相分离而作为上相溶液获得的盐酸水溶液,在作为后续步骤的2,3-二氯-1-丙醇的纯化步骤中获得的盐酸水溶液,和它们的混合物。作为原料烯丙醇,可以使用无水烯丙醇或水溶液。氯气可以通过液体氯的蒸发来获得或者可以是包括大约1-3%氢、空气和其它气体的氯气。
在脱气塔中分离的氯化氢气体可以被回收和输送到反应器中,或者通过设置在反应器前一段的氯化氢气体吸收器来回收。在其中设置氯化氢气体吸收器的情况下,氯化氢气体能够通过使用反应溶剂和/或由反应溶剂和原料烯丙醇组成的混合溶液作为吸收剂溶液来回收。在其中将原料烯丙醇供给设置在反应器的前一段的氯化氢气体吸收器的情况下,吸收的温度优选是-30℃到+20℃。如果它是在20℃以上,由于氯化氢和烯丙醇之间反应产生的副产物如烯丙基氯和2-氯-1-丙醇增加。另一方面,虽然它对于减少副产物是有利的,但在-30℃以下的温度不是优选的,因为反应混合物的粘度增加,冷却所需的成本太高。
用于烯丙醇和氯之间的反应的已知反应器的实例包括与外部冷凝器结合的搅拌釜式反应器,同时进行反应和冷却的湿壁式反应器,环形管式反应器等。已知的是,氯与烯丙醇的加成反应是非常快的,反应将在大约30秒的停留时间下完成。由此可以得出,本发明中使用的任何反应器可以是能够确保30秒的停留时间的任何反应器,以及可以使用上述反应器的任何一种。反应器可以是单段式反应器或多段式反应器。
在反应在单段式反应装置中进行的情况下,该反应器配有氯浓度分析仪,以及所要供给的氯气的流速通过所设置的氯浓度分析仪的指示值来控制。
在其中反应在多段式反应装置中进行的情况下,所要设置的氯浓度分析仪的反应器将是不同的,这取决于反应溶剂或在吸收氯化氢气体之后的溶液被加入到反应器中的添加方式。也就是说,当将反应溶剂或吸收氯化氢溶液之后的溶液并行供给n个反应器,以及将n个反应器的出口溶液分别或作为混合物供给脱气塔时,所有的n个反应器必须各自配有氯浓度分析仪,以及所要供给各反应器的氯气的流速必须通过其中设置的氯浓度分析仪的指示值来控制。另一方面,在其中将反应溶剂或吸收氯化氢气体之后的溶液供给串联的n个反应器和将第n个反应器的出口溶液供给脱气塔时,可以只在第n个反应器中配置氯浓度分析仪,以及所要供给第n个反应器的氯气的流速可以通过所配置的氯浓度分析仪的指示值来控制。原料烯丙醇的添加方法可以是按总量供给上述氯化氢气体吸收器或在n个反应器的每一个之前分开供给。
在使用并联连接的多个反应器的多段式反应装置的情况下,必须在各反应器中配置氯浓度分析仪。然而,可以使得烯丙醇的浓度在各反应器中基本为零,从而能够抑制由于烯丙醇和氯化氢之间的副反应形成的烯丙基氯、2-氯-1-丙醇等的副产物。相比之下,使用串联连接的反应器的多段式反应装置的优点在于可以仅在最终阶段的反应器配置氯浓度分析仪和控制氯气流速,使得运行该系统的操作是简单的。
在下文中,将参照附图来详细说明单段反应,以及作为多段反应的代表性实例的使用两个反应器的串联和并联类型的反应。
图1是说明使用单段式反应装置的根据本发明的烯丙醇的氯化反应的流程图。氯化反应装置由具有装有搅拌器的反应器1、热交换器3和通过环形管连接的循环泵5的装置构成。在反应器1的气相部分中配置用于将气相气体排出到系统之外的管道。这些管道分别配有阀门。循环泵5的出口管分支出用于供给脱气塔16的管道13,以便将溶液由反应器1供给脱气塔16。将氯浓度分析仪14配置在气体抽提管或循环泵5的抽提管中。整个装置保持充分冷却,以及冷冻剂在热交换器中循环以便冷却。将烯丙醇引入管7、用于引入由脱气塔回收的氯化氢气体的管道8、盐酸水溶液引入管9和回收反应溶剂引入管10连接于氯化氢气体吸收器20,在那里,氯化氢气体被吸收,再供给反应器1。让冷冻剂在氯化氢吸收器中循环以便使之冷却。配置氯引入管11,以便将氯供给反应器1。
在本发明中使用的氯浓度分析仪14可以是任何类型的,只要它是通常在盐酸的存在下使用的分析型仪器,如吸光分析法和滴定法。对在气相部分或液相部分中配置的氯浓度分析仪14的测量值和由氯引入管11供给的氯气流速进行级联控制,使得所要供给反应器1的氯气的流速能够被控制,使得在反应器1的气相部分中的氯分压或在反应器1的反应混合物中的氯浓度是恒定的。脱气塔16通常是蒸馏塔,塔顶气体被通入冷凝器17。将冷凝物回流,再在氯化氢气体吸收器20中回收氯化氢气体。在塔的底部配置加热器,以便加热反应混合物。脱气塔底部之上的液体通过冷却器18来冷却,然后引入到分离罐19中。分离罐19具有液体供给口及上相和下相抽提口,在静置之后,液体分离为上相和下相。从上相抽提预定量,再通过引入管10回收到氯化氢气体吸收器20中。上相和下相的剩余物作为2,3-二氯-1-丙醇的粗产物回收。
图2是使用具有串联连接的两个反应器的氯化反应装置的根据本发明的烯丙醇的氯化反应的流程图。
该氯化反应装置由具有各自装有搅拌器的反应器1和2,热交换器3和4,以及通过环形管道连接的循环泵5和6的装置构成。反应器1和2的气相部分通过管道互相连接。反应器1的气相部分配有用于将气相气体排出到系统之外的管道。这些管道分别具备阀门。循环泵5的出口管分支出用于供给反应器2的管道13,以便将液体由反应器1供给反应器2。整个装置保持充分冷却,以及让冷冻剂在热交换器中循环,用于冷却。将烯丙醇(引入管7)、由脱气塔回收的氯化氢气体(引入管8)、盐酸(引入管9)和回收的反应溶剂(引入管10)供给氯化氢气体吸收器20,在那里,氯化氢气体被吸收,再供给反应器1。让冷冻剂在氯化氢吸收器中循环,以便使之冷却。配置氯引入管11和12,以便将氯分别供给反应器1和2。循环泵6的出口管分支成用于供给脱气塔16的管道15,并将液体由反应器2供给脱气塔16。在用于将气相气体由反应器2的气相部分抽提到反应器1的管道中或在循环泵6的抽提管中配置氯浓度分析仪14。作为氯浓度分析仪14,可以使用上述那些。
对在气相部分或液相部分中配置的氯浓度分析仪14的测量值和由氯引入管12供给的氯气流速进行级联控制,使得所要供给反应器2的氯气的流速能够被控制,致使在反应器2的气相部分中的氯分压或在反应器2的反应混合物中的氯浓度是恒定的。脱气塔16通常是蒸馏塔,塔顶气体被通入冷凝器17。将冷凝物回流,再在氯化氢气体吸收器20中回收氯化氢气体。在塔的底部配置加热器,以便加热反应混合物。脱气塔底部之上的液体通过冷却器18来冷却,然后引入到分离罐19中。分离罐19具有液体供给口及上相和下相抽提口,以及在静置之后,液体分离为上相和下相。从上相抽提预定量的液体,再通过引入管10回收到氯化氢气体吸收器20中。上相和下相的剩余物作为2,3-二氯-1-丙醇的粗产物回收。
图3是使用具有并联连接的两个反应器的氯化反应装置的根据本发明的烯丙醇的氯化反应的流程图。
该氯化反应装置由具有各自配备搅拌器的反应器1和2,热交换器3和4,以及通过环形管道连接的循环泵5和6的装置构成。在反应器1和2的气相部分中配置用于将气相气体排出到系统之外的管道。这些管道分别具备阀门。循环泵5和6的出口管分别分支出用于供给脱气塔16的管道13和15,将液体由反应器1和2分别供给脱气塔16。整个装置保持充分冷却,以及让冷冻剂在热交换器中循环,用于冷却。将烯丙醇(引入管7)、由脱气塔回收的氯化氢气体(引入管8)、盐酸(引入管9)和回收的反应溶剂(引入管10)供给氯化氢气体吸收器20,在那里,氯化氢气体被吸收,再供给反应器1和2。让冷冻剂在氯化氢吸收器中循环,以便使之冷却。设置氯引入管11和12,以便将氯供给反应器1和2。在用于从反应器1的气相部分中抽提气相气体的管道或循环泵5的抽提管中和在用于从反应器2的气相部分中抽提气相气体的管道或循环泵6的抽提管中配置氯浓度分析仪14。作为氯浓度分析仪14,可以各自使用上述那些。
对在反应器1的气相部分或液相部分中配置的氯浓度分析仪14的测量值和由氯引入管11供给的氯气流速进行级联控制,使得所要供给反应器1的氯气的流速能够被控制,致使在反应器1的气相部分中的氯分压或在反应器1的反应混合物中的氯浓度是恒定的。还有,对在反应器2的气相部分或液相部分中配置的氯浓度分析仪14的测量值和由氯引入管12供给的氯气流速进行级联控制,使得所要供给反应器2的氯气的流速能够被控制,致使在反应器2的气相部分中的氯分压或在反应器2的反应混合物中的氯浓度是恒定的。
脱气塔16通常是蒸馏塔,塔顶气体被通入冷凝器17。将冷凝物回流,再在氯化氢气体吸收器20中回收氯化氢气体。在塔的底部配置加热器,以便加热反应混合物。脱气塔底部之上的液体通过冷却器18来冷却,然后引入到分离罐19中。分离罐19具有液体供给口及上相和下相抽提口,以及在静置之后,液体分离为上相和下相。从上相抽提预定量的液体,再通过引入管10回收到氯化氢气体吸收器20中。上相和下相的剩余物一起作为2,3-二氯-1-丙醇的粗产物回收。
在本发明的方法中,必要的是将氯溶解在脱气塔之前紧接的反应器出口溶液中,即使是以少量。然而,其中溶解太多氯的状态不是优选的。溶解氯的量优选是高于0g/ml且不多于0.015g/ml的浓度。高于0.015g/ml的浓度不是优选的,因为在该浓度下,溶解在反应混合物中的氯加速了由醇到醛的氧化反应,反应器的压力明显增加。更优选的氯浓度是0.001g/ml-0.005g/ml。至于在脱气塔之前紧接的反应器的气相部分中的氯分压,基于上述相同的理由,必要的是在气相中存在氯,即使是以少量存在。优选的是,氯以0.08MPa(绝对压力)或0.08MPa以下的氯分压和更优选以0.005MPa-0.025MPa(绝对压力)的氯分压存在。
在本发明中,优选的是所要在烯丙醇和氯之间的反应中用作反应溶剂的盐酸是含有40-75质量%氯化氢的水溶液,按HCl/(H2O+HCl)计算。这里定义的“氯化氢浓度”还包括由作为原料的烯丙醇带入反应系统的水量。低于40质量%的氯化氢浓度(按HCl/(H2O+HCl)计算)是不优选的,因为副产物如3-氯-1,2-丙二醇和醚类将会增加。另一方面,超过75质量%的氯化氢浓度(按HCl/(H2O+HCl)计算)是不优选的,因为副产物如烯丙基氯、2-氯-1-丙醇和1,2,3-三氯丙烷将会增加。反应温度优选是20℃或20℃以下,因为20℃以上的反应温度将使副产物如烯丙基氯、2-氯-1-丙醇和1,2,3-三氯丙烷增加。另一方面,低于-30℃的温度是不优选的,因为虽然这样的温度对于改进收率是有利的,但反应混合物的粘度将增加,冷却所需的成本太高。优选的是在0-1MPa(表压)的反应压力下进行反应。高于1MPa(计示压力)的反应压力是不优选的,因为这样的压力将引起氯化氢浓度增加,从而增加了副产物如烯丙基氯、2-氯-1-丙醇和1,2,3-三氯丙烷。
根据本发明的用于生产表氯醇(ECH)的方法的特征在于使2,3-二氯-1-丙醇(2,3-DCH)进行皂化。2,3-DCH的皂化反应可以在2,3-DCH的纯化之后进行。
皂化反应是通过2,3-DCH和碱之间的反应来生产ECH,该反应通过使用相对于2,3-DCH的1.0-1.5当量的碱来进行。在皂化反应中使用的碱例如包括Ca(OH)2,NaOH,KOH,Na2CO3,K2CO3等。它们可以作为水溶液或淤浆溶液使用。
对反应条件没有特别限制。反应例如可以在40-110℃的温度下在减压或在增压下进行。至于反应的方式,可以使用各种方法。
实施本发明的最佳方式
下文,将通过实施例和对比实施例来更具体地描述本发明。
实施例1:级联控制氯气供给量的生产2,3-DCH的方法
烯丙醇的氯化反应通过使用如图4所示的具有串联连接的两个反应器的反应装置来进行。
如图4所示的该装置与在图2的流程图中所示的结构相同,只是省去氯化氢气体吸收器20,以及烯丙醇引入管7、由脱气塔回收的氯化氢气体的引入管8、盐酸溶液的引入管9和回收反应溶剂的引入管10直接供给反应器1,不需通过氯化氢气体吸收器20。
仅将氯浓度分析仪14配置于循环泵6的抽提管,对液相部分中氯浓度的测量浓度和由氯引入管12供给的氯气的流速进行级联控制,和控制供给反应器2的氯气的流速,使得在反应器2的反应混合物中的氯浓度能够保持恒定。气相部分中的氯分压通过手工分析来测量。
作为反应器1和2,分别使用各自装有搅拌器的300L容积搪玻璃反应器。作为热交换器3和4,使用各自具有20m2的热传递面积的石墨制热交换器。所使用的氯浓度分析仪14是通过电流滴定方法测量氯的XT-1315(商品名,由Denki Kagaku Keiki Co.,Ltd.生产)。
使用装有陶瓷制联锁座板的石墨制蒸馏塔作为脱气塔16,将塔顶气体通入石墨制冷凝器17和使冷凝物回流,以便回收反应器1中的氯化氢气体。塔底部用来自石墨制加热器的蒸汽加热。脱气塔底部之上的液体通过冷却器18来冷却,然后引入到300L容积搪玻璃容器的分离罐19中。分离罐19具有液体供给口及上相和下相抽提口,在该分离罐中,让液体静置,以便分离为上相和下相。从分离的上相中抽提预定量的液体,再通过引入管10在反应器1中回收,上相和下相的剩余物用作2,3-二氯-1-丙醇的粗产物。
使用上述反应装置,在反应器1中由管道7以16.0kg/hr的速率供给70质量%烯丙醇水溶液,由管道9以5.0kg/hr的速率供给35质量%盐酸水溶液,由管道10以25.0kg/hr的速率供给含有21质量%的2,3-二氯-1-丙醇、60质量%的水和16质量%氯化氢的回收反应溶剂,由管道8以22.4kg/hr的速率供给回收的氯化氢气体,以及由管道8以6.8kg/hr的速率供给氯气。将供给反应器1的氯气的流速设定到相对于烯丙醇的50mol%。控制反应器1,使得反应压力是0.10MPa(计示压力)和反应温度是0℃。以75.3kg/hr的速率由管道13抽提反应器1中的反应混合物,再供给反应器2。在此场合下,反应混合物含有37质量%氯化氢和31质量%水,其中HCl/(H2O+HCl)占大约55质量%。由管道12向反应器2供给氯气,使得氯浓度分析仪14的指示值是0.002-0.004g/ml。在此场合下,在反应器2的气相部分中的氯分压是0.01-0.02MPa(绝对压力)。控制反应器2,使得反应压力是0.13MPa(计示压力)和反应温度是0℃。以82.1kg/hr的速率从管道15中抽提反应混合物,再供给脱气塔16。脱气塔16在0.11MPa(计示压力)的塔顶压力和130℃的塔底温度下运行,以22.4kg/hr的速率从塔的顶部抽提主要由氯化氢组成的气体,再通过管道8引入到反应器1中。从塔的底部以59.7kg/hr的速率抽提塔底部组分,在冷却器18中冷却到大约25℃,然后引入到分离罐19中。在分离罐中静置之后,以28.1kg/hr的速率抽提分离的上相(水相),其中的25.0kg/hr引入到反应器1中。剩余的上相与下相(油相)合并,以36.6kg/hr的速率获得了粗产物。粗产物用液相色谱法分析,显示在粗产物当中以23.4kg/hr的份额产生了2,3-二氯-1-丙醇,收率是94%,基于所供给的烯丙醇。
在上述反应条件下,连续操作进行30天,但2,3-二氯-1-丙醇的收率没有改变,也没有发生脱气塔加热器的堵塞。供给反应器1和2的氯气的总和与供给反应器1的烯丙醇的量的摩尔比在0.99-1.01的范围内变化。
实施例2:级联控制氯气供给量的生产2,3-DCH的方法
以与实施例1相同的方式,使用在图4中所示的反应装置进行烯丙醇的氯化反应。向反应器1中由管道7以16.0kg/hr的速率供给70质量%烯丙醇水溶液,由管道9以5.0kg/hr的速率供给35质量%盐酸水溶液,由管道10以25.0kg/hr的速率供给含有21质量%的2,3-二氯-1-丙醇、60质量%的水和16质量%氯化氢的回收反应溶剂,由管道8以17.3kg/hr的速率供给回收的氯化氢气体,以及由管道11以6.8kg/hr的速率供给氯气。将供给反应器1的氯气的流速设定到相对于烯丙醇的50mol%。控制反应器1,使得反应压力是0MPa(计示压力)和反应温度是0℃。以70.1kg/hr的速率由管道13抽提反应器1中的反应混合物,再供给反应器2。在此场合下,反应混合物含有33质量%氯化氢和33质量%水,其中HCl/(H2O+HCl)占大约50质量%。由管道12向反应器2供给氯气,使得氯浓度分析仪14的指示值是0.002-0.004g/ml。在此场合下,在反应器2的气相部分中的氯分压是0.01-0.02MPa(绝对压力)。控制反应器2,使得反应压力是0.03MPa(计示压力)和反应温度是0℃。以77.0kg/hr的速率从管道15中抽提反应混合物,再供给脱气塔16。脱气塔16在0.01MPa(计示压力)的塔顶压力和120℃的塔底温度下运行,以17.3kg/hr的速率从塔的顶部抽提主要由氯化氢组成的气体,再通过管道8引入到反应器1中。从塔的底部以59.7kg/hr的速率抽提塔底部组分,在冷却器18中冷却到大约25℃,然后引入到分离罐19中。在分离罐中静置之后,以28.6kg/hr的速率抽提分离的上相(水相),其中的25.0kg/hr引入到反应器1中。剩余的上相与下相(油相)合并,以34.7kg/hr的速率获得了粗产物。粗产物用液相色谱法分析,显示在粗产物当中以23.2kg/hr的份额生产出2,3-二氯-1-丙醇,收率是93.5%,基于所供给的烯丙醇。
在上述反应条件下,连续操作进行30天,但2,3-二氯-1-丙醇的收率没有改变,也没有发生脱气塔加热器的堵塞。供给反应器1和2的氯气的总和与供给反应器1的烯丙醇的量的摩尔比在0.99-1.01的范围内变化。
对比实施例1:没有级联控制的通过以相对于烯丙醇稍过量的量供给氯气来生产2,3-DCH的方法
烯丙醇的氯化反应通过使用与在实施例1中所用相同的反应装置来进行,只是不进行在实施例1中的氯浓度分析仪14的测量值和由管道12引入氯的流速的级联控制。将供给反应器1和2的氯气的流速控制至相对于烯丙醇供给量的大约1.02mol当量。氯化反应在以下所述的条件下引发。在反应器1中由管道7以16.0kg/hr的速率供给70质量%烯丙醇水溶液,由管道9以5.0kg/hr的速率供给35质量%盐酸水溶液,由管道10以25.0kg/hr的速率供给含有21质量%的2,3-二氯-1-丙醇、60质量%的水和16质量%氯化氢的回收反应溶剂,以及由管道11以7.0kg/hr的速率供给氯气。将回收的氯化氢气体由管道8供给反应器1。将供给反应器1的氯气的流速设定到相对于所供给氯气总量的50mol%。控制反应器1,使得反应压力是0MPa(计示压力)和反应温度是0℃。由管道13抽提反应器1中的反应混合物,使得在反应器1中的液体水平是恒定的,再供给反应器2。以与反应器1的情况相同的方式以7.0kg/hr由管道12向反应器2供给氯气。控制反应器2,使得反应压力是0.03MPa(计示压力)和反应温度是0℃。通过管道15从反应器2中抽提反应混合物,使得反应器2中的液体水平是恒定的,再供给脱气塔16。脱气塔16在0.01MPa(计示压力)的塔顶压力和125℃的塔底温度下运行,从塔的顶部抽提主要由氯化氢组成的气体,再通过管道8引入到反应器1中。从塔的底部抽提塔底部组分,在冷却器18中冷却到大约25℃,然后引入到分离罐19中。在分离罐中静置之后,将分离的上相(水相)中的25.0kg/hr引入到反应器1中。剩余的上相与下相(油相)合并,获得粗产物。
在上述条件下的连续反应导致过量供给的氯气由连接反应器1和2的气相部分和管道8的管道涌入到反应器1,以及在反应条件稳定之后,氯气通过用于将氯气从气相部分排出到外部的管道以0.2kg/hr的速度排出到系统之外。这种氯量对应于供给反应器的氯量总和的1.4%。在此场合下,溶解在反应器2的反应混合物中的氯浓度是0.018g/ml,存在于反应器2的气相部分中的氯分压是0.09MPa(绝对压力)。粗产物用液相色谱法分析显示,在粗产物中,以22.1kg/hr的份额生产出了2,3-二氯-1-丙醇,收率是89%,基于所供给的烯丙醇。
对比实施例2:没有级联控制的通过以相对于烯丙醇的稍微不足的量供给氯气来生产2,3-DCH的方法
烯丙醇的氯化反应通过使用与在实施例1中所用相同的反应装置来进行,只是不进行在实施例1中的氯浓度分析仪14的测量值和由管道12引入氯的流速的级联控制。将供给反应器1和2的氯气的流速控制至相对于烯丙醇供给量的大约0.98mol当量。向反应器1中由管道7以16.0kg/hr的速率供给70质量%烯丙醇水溶液,由管道9以5.0kg/hr的速率供给35质量%盐酸水溶液,由管道10以25.0kg/hr的速率供给含有21质量%的2,3-二氯-1-丙醇、60质量%的水和16质量%氯化氢的回收反应溶剂,由管道8以17.3kg/hr的流速供给回收的氯化氢气体,以及由管道11以6.7kg/hr的速率供给氯气。将供给反应器1的氯气的流速设定到相对于所供给氯气总量的50mol%。控制反应器1,使得反应压力是0MPa(计示压力)和反应温度是0℃。通过管道13以70.0kg/hr的速率抽提反应器1中的反应混合物,再供给反应器2。在此场合下,反应混合物含有33质量%的氯化氢和33质量%的水,其中HCl/(H2O+HCl)占大约50质量%。以在反应器1的情况下相同的方式以6.7kg/hr由管道12向反应器2供给氯气。在此场合下,在反应器2的气相部分中存在的氯的分压是0MPa(绝对压力)和在反应器2的反应混合物中的氯浓度为0.0g/ml。控制反应器2,使得反应压力是0.03MPa(计示压力)和反应温度是0℃。通过管道15以76.7kg/hr的速率从反应器2中抽提反应混合物,再供给脱气塔16。供给的液体含有0.2kg/hr的烯丙醇,该量对应于供给反应器的烯丙醇总量的1.8%。脱气塔16在0.01MPa(计示压力)的塔顶压力和120℃的塔底温度下运行,以17.3kg/hr的速率从塔的顶部抽提主要由氯化氢组成的气体,再通过管道8引入到反应器1中。从塔的底部以59.4kg/hr的速率抽提塔底部组分,在冷却器18中冷却到大约25℃,然后引入到分离罐19中。在分离罐中静置之后,以28.9kg/hr的速率抽提分离的上相(水相),将其中的25.0kg/hr引入到反应器1中。剩余的上相与下相(油相)合并,以34.5kg/hr的速率获得了粗产物。粗产物用液相色谱法分析显示,在粗产物当中,以22.7kg/hr的份额生产出了2,3-二氯-1-丙醇,收率是91%,基于所供给的烯丙醇。
在上述条件下的连续反应导致加热器的热效率在10天之后开始下降,以及在20天之后通过停止反应来检测加热器,显示加热器管子的大约60%被聚合产物堵塞。
工业应用性
根据本发明,在通过将含有由烯丙醇在盐酸溶液中的氯化获得的2,3-二氯-1-丙醇的溶液引入到加热的脱气塔中以便释出氯化氢,将该氯化氢返回到反应器以供氯化用,再从剩余溶液中获取2,3-二氯-1-丙醇来连续生产2,3-二氯-1-丙醇的方法中,通过将在引入到脱气塔的反应混合物中溶解的氯浓度控制到特定浓度(0.015g/ml)或特定浓度以下,和/或将在脱气塔之前紧接的反应器的气相部分中的氯分压控制到特定分压(0.08MPa(绝对压力))或特定分压以下,和此外通过设置用于测量在脱气塔之前紧接的反应器的出口处溶液的氯浓度和/或存在于反应器的气相部分中的氯气浓度(分压)的分析仪,作为将在脱气塔之前紧接的反应器的反应混合物中溶解的氯的浓度和/或在脱气塔之前紧接的反应器的气相部分中的分压控制在必需范围内的装置,再根据该分析仪的指示值来控制引入到脱气塔之前紧接的反应器的氯气的流速,从而能够使在引入脱气塔的反应混合物中保留的烯丙醇的浓度基本上为零,并且能够以高收率和长时间稳定的方式连续生产2,3-DCH和表氯醇。
Claims (8)
1、通过将含有由烯丙醇在盐酸溶液中的氯化获得的2,3-二氯-1-丙醇的溶液引入到脱气塔以便释出氯化氢,使该氯化氢返回到反应器以供氯化用,以及从剩余溶液中获取2,3-二氯-1-丙醇来生产2,3-二氯-1-丙醇的方法,特征在于该方法包括将在马上要引入到脱气塔的反应器出口处的溶液中溶解的氯的浓度保持在0.015g/ml或0.015g/ml以下。
2、如在权利要求1中所述的通过将含有由烯丙醇在盐酸溶液中的氯化获得的2,3-二氯-1-丙醇的溶液引入到脱气塔以便释出氯化氢,使该氯化氢返回到反应器以供氯化用,以及从剩余溶液中获取2,3-二氯-1-丙醇来生产2,3-二氯-1-丙醇的方法,特征在于该方法包括在脱气塔之前紧接的反应器中设置用于监控反应器出口处的溶液中的氯浓度的分析仪和控制所要引入反应器的氯气的流速,使得氯的浓度能够保持在0.015g/ml或0.015g/ml以下。
3、通过将含有由烯丙醇在盐酸溶液中的氯化获得的2,3-二氯-1-丙醇的溶液引入到脱气塔以便释出氯化氢,使该氯化氢返回到反应器以供氯化用,以及从剩余溶液中获取2,3-二氯-1-丙醇来生产2,3-二氯-1-丙醇的方法,特征在于该方法包括将脱气塔之前紧接的反应器的气相部分中的氯的分压保持在绝对压力0.08MPa或0.08MPa以下。
4、如在权利要求3中所述的通过将含有由烯丙醇在盐酸溶液中的氯化获得的2,3-二氯-1-丙醇的溶液引入到脱气塔以便释出氯化氢,使该氯化氢返回到反应器以供氯化用,以及从剩余溶液中获取2,3-二氯-1-丙醇来生产2,3-二氯-1-丙醇的方法,特征在于该方法包括在脱气塔之前紧接的反应器中设置用于监控在反应器气相部分中氯气浓度的分析仪和控制所要引入到反应器的氯气的流速,使得氯气的分压能够保持在绝对压力0.08MPa或0.08MPa以下。
5、如在权利要求1-4的任一项中所述的生产2,3-二氯-1-丙醇的方法,其中使用含有40-75质量%氯化氢的盐酸水溶液,按HCl/(H2O+HCl)计算。
6、如在权利要求1-4的任一项中所述的生产2,3-二氯-1-丙醇的方法,其中烯丙醇的氯化反应在-30℃到+20℃的温度下进行。
7、如在权利要求1-4的任一项中所述的生产2,3-二氯-1-丙醇的方法,其中烯丙醇的氯化反应在表压1MPa或1MPa以下的压力下进行。
8、生产表氯醇的方法,特征在于,在通过将含有由烯丙醇在盐酸溶液中的氯化获得的2,3-二氯-1-丙醇的溶液引入到脱气塔以便释出氯化氢,使该氯化氢返回到反应器以供氯化用,以及从剩余溶液中获取2,3-二氯-1-丙醇来生产2,3-二氯-1-丙醇的方法中,将在马上要引入到脱气塔的反应器出口处的溶液中溶解的氯的浓度保持在0.015g/ml或0.015g/ml以下,和/或将脱气塔之前紧接的反应器的气相部分中的氯的分压保持在绝对压力0.08MPa或0.08MPa以下来生产2,3-二氯-1-丙醇,接着使所生产的2,3-二氯-1-丙醇进行皂化反应。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP128670/2001 | 2001-04-26 | ||
| JP2001128670A JP4721311B2 (ja) | 2001-04-26 | 2001-04-26 | 2,3−ジクロル−1−プロパノール及びエピクロルヒドリンの製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1462265A CN1462265A (zh) | 2003-12-17 |
| CN1204102C true CN1204102C (zh) | 2005-06-01 |
Family
ID=18977333
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN 02801406 Expired - Lifetime CN1204102C (zh) | 2001-04-26 | 2002-04-24 | 2,3-二氯-1-丙醇和表氯醇的生产方法 |
Country Status (3)
| Country | Link |
|---|---|
| JP (1) | JP4721311B2 (zh) |
| CN (1) | CN1204102C (zh) |
| TW (1) | TWI227223B (zh) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CZ20032346A3 (cs) * | 2003-09-01 | 2005-04-13 | Spolek Pro Chemickou A Hutní Výrobu,A.S. | Způsob přípravy dichlorpropanolů z glycerinu |
| US20100032617A1 (en) * | 2007-02-20 | 2010-02-11 | Solvay (Societe Anonyme) | Process for manufacturing epichlorohydrin |
| JP5294144B2 (ja) * | 2008-04-03 | 2013-09-18 | ダイソー株式会社 | ジクロロヒドリンの製造法 |
| CN104059031A (zh) * | 2014-06-20 | 2014-09-24 | 中国天辰工程有限公司 | 一种二氯丙醇脱除气相氯化氢生产环氧氯丙烷的方法 |
| TWI547470B (zh) * | 2015-12-18 | 2016-09-01 | 長春人造樹脂廠股份有限公司 | 製造二氯丙醇之方法 |
| CN108059586B (zh) * | 2017-12-12 | 2021-08-17 | 浙江镇洋发展股份有限公司 | 一种甘油氯化制备二氯丙醇的方法 |
| CN111925300B (zh) * | 2020-08-12 | 2022-10-14 | 上海应用技术大学 | 一种4-氯-2-甲氧基亚氨基乙酰乙酸乙酯的合成方法及装置 |
| CN111978205B (zh) * | 2020-08-12 | 2023-04-28 | 上海应用技术大学 | 一种连续合成4-氯-2-甲氧基亚氨基乙酰乙酸乙酯的方法及装置 |
| CN112010776B (zh) * | 2020-08-12 | 2023-04-28 | 上海应用技术大学 | 一种连续合成4-氯-2-甲氧基亚氨基乙酰乙酸乙酯的方法及装置 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS60258171A (ja) * | 1984-06-04 | 1985-12-20 | Showa Denko Kk | エピクロルヒドリンの製造方法 |
| JPH0643354B2 (ja) * | 1989-08-10 | 1994-06-08 | ダイソー株式会社 | 2,3―ジクロロ―1―プロパノールの連続的製法及びその装置 |
| JPH0725711B2 (ja) * | 1990-07-17 | 1995-03-22 | 昭和電工株式会社 | 2,3―ジクロル―1―プロパノールの精製法 |
| JP2705521B2 (ja) * | 1993-07-22 | 1998-01-28 | 昭和電工株式会社 | 2,3−ジクロル−1−プロパノールの精製法 |
-
2001
- 2001-04-26 JP JP2001128670A patent/JP4721311B2/ja not_active Expired - Fee Related
-
2002
- 2002-04-24 CN CN 02801406 patent/CN1204102C/zh not_active Expired - Lifetime
- 2002-04-25 TW TW91108584A patent/TWI227223B/zh not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| TWI227223B (en) | 2005-02-01 |
| JP2002322106A (ja) | 2002-11-08 |
| CN1462265A (zh) | 2003-12-17 |
| JP4721311B2 (ja) | 2011-07-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN100439305C (zh) | 从甘油中制备二氯丙醇的方法 | |
| US8721842B2 (en) | Catalytic reaction-rectification integrated process and specialized device thereof | |
| CN1204102C (zh) | 2,3-二氯-1-丙醇和表氯醇的生产方法 | |
| JP2022554215A (ja) | 気液バブリング床反応器、反応系、及びカーボネートエステルを合成するための方法 | |
| CN107033107A (zh) | 一种制备环氧氯丙烷的方法 | |
| CN101184715A (zh) | 一种由甘油和盐酸生产α,γ-二氯丙醇的生产方法 | |
| CN114315767A (zh) | 一种5-羟甲基糠醛的制备方法及其制备装置 | |
| CN110467595A (zh) | 一种无硫酸法三聚甲醛合成装置及其合成工艺路线 | |
| CN106588590A (zh) | 聚甲醛二甲基醚的精制方法 | |
| CN100564335C (zh) | 一种甲酸的制备方法 | |
| CN117105759B (zh) | 一种连续制备2-氯-1-(1-氯环丙基)乙酮的方法 | |
| CN102887816B (zh) | 一种化学反应-渗透汽化耦合法制备二氯丙醇的方法 | |
| CN211814210U (zh) | 一种基于乙烯水合法制备乙二醇的微界面强化反应系统 | |
| CN1045432C (zh) | 甲代烯丙基磺酸钠生产方法及设备 | |
| CN105480948A (zh) | 一种脂肪酸或脂肪酰氯氯化生产过程中副产物氯化氢循环利用方法及系统 | |
| CN114874069B (zh) | 一种制备电子级乙二醇的方法及装置 | |
| CN212425922U (zh) | 三聚甲醛和二氧五环联产制备聚甲醛的装置 | |
| CN110563754B (zh) | 一种用于生产氯甲基三乙氧基硅烷的醇解反应系统 | |
| CN103360213B (zh) | 一种氯代甘油提纯装置及其生产方法 | |
| CN220070749U (zh) | 一种3-氯丙酰氯合成连续化反应装置 | |
| CN111848889B (zh) | 三聚甲醛和二氧五环联产制备聚甲醛的方法 | |
| EP1280751B1 (en) | Method for producing 2, 3 dichloro-1-propahol and epichlorohyrin | |
| CN1709845A (zh) | 一种连续法生产取代苄基醇的方法及其装置 | |
| CN219023274U (zh) | 一种生产HCFC-112a的设备 | |
| CN112694639B (zh) | Evoh生产过程中聚合液净化的方法和装置 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| CX01 | Expiry of patent term |
Granted publication date: 20050601 |
|
| CX01 | Expiry of patent term |