CN103201386A - 皮肤穿透及细胞进入(space)肽及其使用方法 - Google Patents
皮肤穿透及细胞进入(space)肽及其使用方法 Download PDFInfo
- Publication number
- CN103201386A CN103201386A CN2011800532510A CN201180053251A CN103201386A CN 103201386 A CN103201386 A CN 103201386A CN 2011800532510 A CN2011800532510 A CN 2011800532510A CN 201180053251 A CN201180053251 A CN 201180053251A CN 103201386 A CN103201386 A CN 103201386A
- Authority
- CN
- China
- Prior art keywords
- seq
- peptide
- composition
- sirna
- described method
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1136—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against growth factors, growth regulators, cytokines, lymphokines or hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/08—Peptides having 5 to 11 amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/12—Cyclic peptides, e.g. bacitracins; Polymyxins; Gramicidins S, C; Tyrocidins A, B or C
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/164—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/69—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit
- A61K47/6921—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere
- A61K47/6927—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores
- A61K47/6929—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the conjugate being characterised by physical or galenical forms, e.g. emulsion, particle, inclusion complex, stent or kit the form being a particulate, a powder, an adsorbate, a bead or a sphere the form being a solid microparticle having no hollow or gas-filled cores the form being a nanoparticle, e.g. an immuno-nanoparticle
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K49/00—Preparations for testing in vivo
- A61K49/001—Preparation for luminescence or biological staining
- A61K49/0013—Luminescence
- A61K49/0017—Fluorescence in vivo
- A61K49/005—Fluorescence in vivo characterised by the carrier molecule carrying the fluorescent agent
- A61K49/0056—Peptides, proteins, polyamino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/127—Liposomes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/44—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material not provided for elsewhere, e.g. haptens, metals, DNA, RNA, amino acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/46—Hybrid immunoglobulins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/06—Linear peptides containing only normal peptide links having 5 to 11 amino acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/08—Linear peptides containing only normal peptide links having 12 to 20 amino acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/64—Cyclic peptides containing only normal peptide links
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
- C12N15/1137—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing against enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/14—Type of nucleic acid interfering N.A.
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/30—Chemical structure
- C12N2310/35—Nature of the modification
- C12N2310/351—Conjugate
- C12N2310/3513—Protein; Peptide
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
- C12N2320/32—Special delivery means, e.g. tissue-specific
Abstract
本公开提供促进递送活性剂或活性剂载体的肽以及肽组合物,其中所述组合物能够穿透角质层(SC)和/或活细胞的细胞膜。
Description
相关申请的交叉引用
本申请要求以下美国临时专利申请号的优先权:2010年11月9日提交的标题为“Peptides to Facilitate Drug Delivery”(促进药物递送的肽)的61/411,884;2011年8月25日提交的标题为“Skin Permeatingand Cell Entering(SPACE)Peptides and Methods of Use Thereof”(皮肤穿透及细胞进入(SPACE)肽及其使用方法)的61/527,574;以及2011年8月26日提交的标题为“Skin Permeating and Cell Entering(SPACE)Peptides and Methods of Use Thereof”(皮肤穿透及细胞进入(SPACE)肽及其使用方法)的61/528,036,这些专利申请全文且出于所有目以引用方式并入本文。
政府权利
本发明根据国立卫生研究院(National Institutes of Health)授予的联邦资助号1UO1 HL080718以及国家资源研究中心(National Centerfor Research Resources)授予的联邦资助号1S10RR017753-01在政府支持下完成。政府享有本发明的某些权利。
背景
皮肤作为人体最大的器官是许多皮肤疾病的宿主,这些疾病共同地代表了一大类人类健康疾患。因此,将治疗剂例如大分子(例如siRNA)成功地递送至皮肤内已成为活跃研发的课题。然而,实现局部siRNA递送这一目标极具挑战性,除了一些例外已经非常难以实现。主要挑战是大分子的皮肤穿透力差。在人们所提出的增强大分子穿透的多种物理-化学方法中,肽载体已作为潜在的候选物而出现,原因在于它们的易用性、多样性以及靶向皮肤内细胞亚型的潜力。人们已对最初被鉴定为可将药物递送入细胞质的多种肽(包括TAT、多聚精氨酸、爪蟾抗菌肽(meganin)和果蝇穿膜肽(penetratin))进行了跨角质层(SC)的穿透测试,少数已经显示出可将小分子递送入表皮的一定效果。相比之下,只有一种肽TD-1具体表明可穿透SC,并具有增强局部用药的全身吸收的能力。虽然已知多种肽可穿透细胞膜以及少数可穿透SC,但是需要能同时增强跨SC和/或跨活表皮和真皮细胞细胞膜的大分子穿透及其他活动的肽。
发明概述
本公开提供促进递送活性剂或活性剂载体的肽以及肽组合物,其中该组合物能够穿透SC和/或活细胞的细胞膜。
在第一方面,本公开提供包含包括氨基酸序列TGSTQHQ(SEQID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中该肽偶联到活性剂或包含该活性剂的活性剂载体,并且其中该组合物在与角质层(SC)接触时能够穿透角质层或与细胞接触时穿透细胞。
在该第一方面的一个实施方案中,该组合物能够穿透角质层(SC)以及穿透细胞。
在该第一方面的一个实施方案中,该氨基酸序列包括CTGSTQHQC(SEQ ID NO:7)、CHSALTKHC(SEQ ID NO:8)、CKTGSHNQC(SEQ ID NO:9)、CMGPSSMLC(SEQ ID NO:10)、CTDPNQLQC(SEQ ID NO:11)或CSTHFIDTC(SEQ ID NO:12)。
在该第一方面的一个实施方案中,该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。在一个实施方案中,其中该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18),该肽为包含Cys-Cys二硫键的环肽。
在该第一方面的一个实施方案中,该组合物能够穿透活非人类动物细胞的细胞膜。
在该第一方面的一个实施方案中,该组合物能够穿透活人类细胞的细胞膜。
在该第一方面的一个实施方案中,该组合物能够穿透活表皮或真皮细胞的细胞膜。
在该第一方面的一个实施方案中,该组合物能够穿透活免疫细胞的细胞膜。
在该第一方面的一个实施方案中,该活性剂包括大分子。在一个实施方案中,该大分子包括蛋白质。在一个实施方案中,该蛋白质包括含有至少一个互补位(paratope)的抗体或其片段。
在该第一方面的一个实施方案中,其中活性剂包括大分子,该大分子包括核酸。在一个实施方案中,该核酸为DNA。在一个实施方案中,该核酸为RNA。在一个实施方案中,其中该核酸为RNA,该RNA为干扰RNA。在一个实施方案中,其中该RNA为干扰RNA,该干扰RNA为shRNA。在一个实施方案中,其中该RNA为干扰RNA,该干扰RNA为miRNA。在一个实施方案中,其中该RNA为干扰RNA,该干扰RNA为siRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为IL-10siRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为CD86siRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为KRT6a siRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为TNFR1 siRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为TACEsiRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为突变特异性siRNA。
在该第一方面的一个实施方案中,该活性剂为药物化合物。
在该第一方面的一个实施方案中,该活性剂包括可检测剂。在一个实施方案中,其中该活性剂包括可检测剂,该可检测剂包括荧光标记。在一个实施方案中,其中该活性剂包括可检测剂,该可检测剂包括放射性标记。
在该第一方面的一个实施方案中,该活性剂为纳米粒子。
在该第一方面的一个实施方案中,该活性剂为低分子量化合物。
在该第一方面的一个实施方案中,该活性剂为IL-10生物活性抑制剂。在一个实施方案中,其中该活性剂为IL-10生物活性抑制剂,该活性剂选自IL-10siRNA以及结合IL-10的抗体或其片段。
在该第一方面的一个实施方案中,该肽偶联到该活性剂。
在该第一方面的一个实施方案中,该肽偶联到包含该活性剂的活性剂载体。在一个实施方案中,其中该肽偶联到包含该活性剂的活性剂载体,该活性剂载体为脂质体。在一个实施方案中,其中该肽偶联到包含该活性剂的活性剂载体,该活性剂载体为纳米粒子。在一个实施方案中,其中该肽偶联到包含该活性剂的活性剂载体,该活性剂载体为聚合物胶束。
在第二方面,本公开提供包含包括氨基酸序列TGSTQHQ(SEQID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中该肽与活性剂或包含该活性剂的活性剂载体缔合,其中该缔合由疏水、静电或范德华相互作用产生,并且其中该组合物能够在与角质层(SC)接触时穿透角质层或与细胞接触时穿透细胞。
在该第二方面的一个实施方案中,该组合物能够穿透角质层(SC)以及穿透细胞。
在该第二方面的一个实施方案中,该氨基酸序列包括CTGSTQHQC(SEQ ID NO:7)、CHSALTKHC(SEQ ID NO:8)、CKTGSHNQC(SEQ ID NO:9)、CMGPSSMLC(SEQ ID NO:10)、CTDPNQLQC(SEQ ID NO:11)或CSTHFIDTC(SEQ ID NO:12)。
在该第二方面的一个实施方案中,该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。在一个实施方案中,其中该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18),该肽为包含Cys-Cys二硫键的环肽。
在第三方面,本公开提供包含包括这样的氨基酸序列的肽的组合物,该氨基酸序列包含三个连续氨基酸的片段,该连续氨基酸选自以下氨基酸序列之一:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ IDNO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6),其中该肽偶联到活性剂或包含该活性剂的活性剂载体,并且其中该组合物能够在与角质层(SC)接触时穿透角质层或与细胞接触时穿透细胞。
在该第三方面的一个实施方案中,该组合物能够穿透角质层(SC)以及穿透细胞。
在该第三方面的一个实施方案中,该氨基酸序列包含四个连续氨基酸的片段,该连续氨基酸选自以下氨基酸序列之一:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ IDNO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)。
在该第三方面的一个实施方案中,该氨基酸序列包含五个连续氨基酸的片段,该连续氨基酸选自以下氨基酸序列之一:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ IDNO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)。
在该第三方面的一个实施方案中,该氨基酸序列包含六个连续氨基酸的片段,该连续氨基酸选自以下氨基酸序列之一:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ IDNO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)。
在第四方面,本公开提供包含包括这样的氨基酸序列的肽的组合物,该氨基酸序列包含三个连续氨基酸的片段,该连续氨基酸选自以下氨基酸序列之一:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ IDNO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6),其中该肽与活性剂或包含该活性剂的活性剂载体缔合,其中该缔合由疏水、静电或范德华相互作用产生,并且其中该组合物能够在与角质层(SC)接触时穿透角质层或与细胞接触时穿透细胞。
在该第四方面的一个实施方案中,该组合物能够穿透角质层(SC)以及穿透细胞。
在该第四方面的一个实施方案中,该氨基酸序列包含四个连续氨基酸的片段,该连续氨基酸选自以下氨基酸序列之一:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ IDNO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)。
在该第四方面的一个实施方案中,该氨基酸序列包含五个连续氨基酸的片段,该连续氨基酸选自以下氨基酸序列之一:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ IDNO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)。
在该第四方面的一个实施方案中,该氨基酸序列包含六个连续氨基酸的片段,该连续氨基酸选自以下氨基酸序列之一:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ IDNO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)。
在第五方面,本公开提供分离肽,其包含选自以下序列之一的氨基酸序列:ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQID NO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQ ID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)和ACSTHFIDTCG(SEQ ID NO:18)。
在该第五方面的一个实施方案中,该肽包含ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ ID NO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQ IDNO:16)、ACTDPNQLQCG(SEQ ID NO:17)和ACSTHFIDTCG(SEQID NO:18)一者或多者的重复单元。在一个实施方案中,其中该肽包含ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)和ACSTHFIDTCG(SEQ ID NO:18)一者或多者的重复单元,该单元重复2至50次。在一个实施方案中,其中该肽包含ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ ID NO:14)、ACKTGSHNQCG(SEQ IDNO:15)、ACMGPSSMLCG(SEQ ID NO:16)、ACTDPNQLQCG(SEQID NO:17)和ACSTHFIDTCG(SEQ ID NO:18)一者或多者的重复单元,每个单元由插入肽序列(intervening peptide sequence)分离。
在该第五方面的一个实施方案中,该肽为包含Cys-Cys二硫键的环肽。
在第六方面,本公开提供分离多肽,其包含以下一者或多者的重复单元:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)和STHFIDT(SEQ ID NO:6)。
在该第六方面的一个实施方案中,该单元重复2至50次。
在该第六方面的一个实施方案中,每个单元由插入肽序列分离。
在第七方面,本公开提供分离多肽,其基本上由以下一者或多者的重复单元组成:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ IDNO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)和STHFIDT(SEQ ID NO:6)。在一个实施方案中,其中该分离多肽基本上由以下一者或多者的重复单元组成:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)和STHFIDT(SEQ ID NO:6)。
在第八方面,本公开提供将活性剂递送至受试者的方法,包括:向受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中该肽偶联到活性剂或包含该活性剂的活性剂载体,并且其中该组合物能够穿透受试者的角质层(SC)或穿透受试者的细胞。
在该第八方面的一个实施方案中,该组合物能够穿透受试者的角质层(SC)以及穿透受试者的细胞。
在该第八方面的一个实施方案中,该施用为局部施用。
在该第八方面的一个实施方案中,该氨基酸序列包括CTGSTQHQC(SEQ ID NO:7)、CHSALTKHC(SEQ ID NO:8)、CKTGSHNQC(SEQ ID NO:9)、CMGPSSMLC(SEQ ID NO:10)、CTDPNQLQC(SEQ ID NO:11)或CSTHFIDTC(SEQ ID NO:12)。
在该第八方面的一个实施方案中,该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。在一个实施方案中,其中该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18),该肽为包含Cys-Cys二硫键的环肽。
在该第八方面的一个实施方案中,该组合物能够穿透活非人类动物细胞的细胞膜。
在该第八方面的一个实施方案中,该组合物能够穿透活人类细胞的细胞膜。
在该第八方面的一个实施方案中,该组合物能够穿透活表皮或真皮细胞的细胞膜。
在该第八方面的一个实施方案中,该组合物能够穿透活免疫细胞的细胞膜。
在该第八方面的一个实施方案中,该活性剂包括大分子。在一个实施方案中,该大分子包括蛋白质。在一个实施方案中,该蛋白质包括含有至少一个互补位的抗体或其片段。
在该第八方面的一个实施方案中,其中活性剂包括大分子,该大分子包括核酸。在一个实施方案中,该核酸为DNA。在一个实施方案中,该核酸为RNA。在一个实施方案中,其中该核酸为RNA,该RNA为干扰RNA。在一个实施方案中,其中该RNA为干扰RNA,该干扰RNA为shRNA。在一个实施方案中,其中该RNA为干扰RNA,该干扰RNA为miRNA。在一个实施方案中,其中该RNA为干扰RNA,该干扰RNA为siRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为IL-10siRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为CD86siRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为KRT6a siRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为TNFR1siRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为TACEsiRNA。在一个实施方案中,其中该干扰RNA为siRNA,该siRNA为突变特异性siRNA。
在该第八方面的一个实施方案中,该活性剂为药物化合物。
在该第八方面的一个实施方案中,该活性剂包括可检测剂。在一个实施方案中,其中该活性剂包括可检测剂,该可检测剂包括荧光标记。在一个实施方案中,其中该活性剂包括可检测剂,该可检测剂包括放射性标记。
在该第八方面的一个实施方案中,该活性剂为纳米粒子。
在该第八方面的一个实施方案中,该活性剂为低分子量化合物。
在该第八方面的一个实施方案中,该活性剂为IL-10生物活性抑制剂。在一个实施方案中,其中该活性剂为IL-10生物活性抑制剂,该活性剂选自IL-10siRNA以及结合IL-10的抗体或其片段。
在该第八方面的一个实施方案中,该肽偶联到该活性剂。
在该第八方面的一个实施方案中,该肽偶联到包含该活性剂的活性剂载体。在一个实施方案中,其中该肽偶联到包含该活性剂的活性剂载体,该活性剂载体为脂质体。在一个实施方案中,其中该肽偶联到包含该活性剂的活性剂载体,该活性剂载体为纳米粒子。在一个实施方案中,其中该肽偶联到包含该活性剂的活性剂载体,该活性剂载体为聚合物胶束。
在第九方面,本公开提供将活性剂递送至受试者的方法,包括:向受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中该肽与活性剂或包含该活性剂的活性剂载体缔合,其中该缔合由疏水、静电或范德华相互作用产生,并且其中该组合物能够穿透受试者的角质层(SC)或穿透受试者的细胞。
在该第九方面的一个实施方案中,该组合物能够穿透受试者的角质层(SC)以及穿透受试者的细胞。
在该第九方面的一个实施方案中,该施用为局部施用。
在该第九方面的一个实施方案中,该氨基酸序列包括CTGSTQHQC(SEQ ID NO:7)、CHSALTKHC(SEQ ID NO:8)、CKTGSHNQC(SEQ ID NO:9)、CMGPSSMLC(SEQ ID NO:10)、CTDPNQLQC(SEQ ID NO:11)或CSTHFIDTC(SEQ ID NO:12)。
在该第九方面的一个实施方案中,该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。在一个实施方案中,其中该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18),该肽为包含Cys-Cys二硫键的环肽。
在第十方面,本公开提供治疗患有皮肤疾病的受试者的方法,包括:向受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中该肽偶联到皮肤病活性剂或包含该活性剂的皮肤病活性剂载体,并且其中该组合物能够穿透受试者的角质层(SC)或穿透受试者的细胞。
在该第十方面的一个实施方案中,该组合物能够穿透受试者的角质层(SC)以及穿透受试者的细胞。
在该第十方面的一个实施方案中,该施用为局部施用。
在该第十方面的一个实施方案中,该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。在一个实施方案中,其中该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18),该肽为包含Cys-Cys二硫键的环肽。
在第十一方面,本公开提供治疗患有皮肤疾病的受试者的方法,包括:向受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中该肽与皮肤病活性剂或包含该活性剂的皮肤病活性剂载体缔合,其中该缔合由疏水、静电或范德华相互作用产生,并且其中该组合物能够穿透受试者的角质层(SC)或穿透受试者的细胞。
在该第十一方面的一个实施方案中,该组合物能够穿透受试者的角质层(SC)以及穿透受试者的细胞。
在该第十一方面的一个实施方案中,该施用为局部施用。
在该第十一方面的一个实施方案中,该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。在一个实施方案中,其中该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18),该肽为包含Cys-Cys二硫键的环肽。
在第十二方面,本公开提供治疗患有、疑似患有或易患至少部分地由mRNA的表达所导致的疾病的受试者的方法,包括向受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中该肽偶联到靶向该mRNA的干扰RNA或包含该干扰RNA的载体,其中该组合物能够穿透受试者的角质层(SC)或受试者的细胞,并且其中该mRNA的表达因而得以减弱。
在该第十二方面的一个实施方案中,该组合物能够穿透受试者的角质层(SC)以及穿透受试者的细胞。
在该第十二方面的一个实施方案中,该施用为局部施用。
在该第十二方面的一个实施方案中,该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。在一个实施方案中,其中该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18),该肽为包含Cys-Cys二硫键的环肽。
在第十三方面,本公开提供治疗患有、疑似患有或易患至少部分地由mRNA的表达所导致的疾病的受试者的方法,包括向受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中该肽与靶向该mRNA的干扰RNA或包含该干扰RNA的载体缔合,其中该缔合由疏水、静电或范德华相互作用产生,其中该组合物能够穿透受试者的角质层(SC)或受试者的细胞,并且其中该mRNA的表达因而得以减弱。
在该第十三方面的一个实施方案中,该组合物能够穿透受试者的角质层(SC)以及穿透受试者的细胞。
在该第十三方面的一个实施方案中,该施用为局部施用。
在该第十三方面的一个实施方案中,该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。在一个实施方案中,其中该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18),该肽为包含Cys-Cys二硫键的环肽。
在第十四方面,本公开提供减弱对其有需要的受试者中mRNA表达的方法,包括向受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ IDNO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中该肽偶联到靶向该mRNA的siRNA或包含靶向该mRNA的siRNA的载体,其中该组合物能够穿透受试者的角质层(SC)或受试者的细胞,并且其中该mRNA的表达因而得以减弱。
在该第十四方面的一个实施方案中,该mRNA为IL-10mRNA并且该siRNA为IL-10siRNA。
在该第十四方面的一个实施方案中,该mRNA为CD86mRNA并且该siRNA为CD86siRNA。
在该第十四方面的一个实施方案中,该mRNA为KRT6a mRNA并且该siRNA为KRT6a siRNA。
在该第十四方面的一个实施方案中,该mRNA为TNFR1mRNA并且该siRNA为TNFR1siRNA。
在该第十四方面的一个实施方案中,该mRNA为TACE mRNA并且该siRNA为TACE siRNA。
在该第十四方面的一个实施方案中,该组合物能够穿透受试者的角质层(SC)以及穿透受试者的细胞。
在该第十四方面的一个实施方案中,该施用为局部施用。
在该第十四方面的一个实施方案中,该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。在一个实施方案中,其中该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18),该肽为包含Cys-Cys二硫键的环肽。
在第十五方面,本公开提供减弱对其有需要的受试者中mRNA表达的方法,包括向受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ IDNO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中该肽与靶向该mRNA的siRNA或包含靶向该mRNA的siRNA的载体缔合,其中该缔合由疏水、静电或范德华相互作用产生,其中该组合物能够穿透受试者的角质层(SC)或受试者的细胞,并且其中该mRNA的表达因而得以减弱。
在该第十五方面的一个实施方案中,该mRNA为IL-10mRNA并且该siRNA为IL-10siRNA。
在该第十五方面的一个实施方案中,该mRNA为CD86mRNA并且该siRNA为CD86siRNA。
在该第十五方面的一个实施方案中,该mRNA为KRT6a mRNA并且该siRNA为KRT6a siRNA。
在该第十五方面的一个实施方案中,该mRNA为TNFR1mRNA并且该siRNA为TNFR1siRNA。
在该第十五方面的一个实施方案中,该mRNA为TACE mRNA并且该siRNA为TACE siRNA。
在该第十五方面的一个实施方案中,该组合物能够穿透受试者的角质层(SC)以及穿透受试者的细胞。
在该第十五方面的一个实施方案中,该施用为局部施用。
在该第十五方面的一个实施方案中,该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。在一个实施方案中,其中该氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18),该肽为包含Cys-Cys二硫键的环肽。
在第十六方面,本公开提供包含基本上由氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ IDNO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)组成的肽的组合物,其中该肽偶联到活性剂或包含该活性剂的活性剂载体,并且其中该组合物在与角质层(SC)接触时能够穿透角质层或与细胞接触时穿透细胞。
普通技术人员在阅读本说明书后将对其他方面和实施方案显而易见。
附图简述
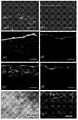
图1显示了在猪皮中通过体外噬菌体展示鉴定皮肤穿透肽。(a)将噬菌体文库应用于FDC的供体室。采集据发现可穿透皮肤进入受体室的噬菌体,扩增,并用于后续数轮筛选。通过扩散实验和共焦显微术确认了各个克隆的皮肤穿透能力。为了确认肽穿透皮肤的能力,将肽与噬菌体分离,通过共焦显微术在视觉上确认其穿透进入皮肤;(b)噬菌体展示筛选第3至5轮中各高频肽序列的出现百分比;(c,d)分别为SPACE和对照肽进入猪皮的皮肤穿透情况的共焦显微图像;(e,f)偶联到生物素化SPACE肽的Alexa Fluor488标记链霉亲和素和单独的Alexa Fluor488链霉亲和素的皮肤穿透情况。插图示出了在主图像中突出显示部分的放大视图。比例尺=200μm。
图2显示了共焦显微图像,示出了荧光标记分子穿过皮肤。(a,b)荧光标记的噬菌体展示肽穿透进入猪皮。(c,d)生物素化肽-链霉亲和素包被量子点穿透进入猪皮。(e,f)荧光标记肽穿透进入人体皮肤。(g,h)人体皮肤中荧光标记肽的顶视图(俯视SC)。(a,c,e,g)代表SPACE肽的图像,而(b,d,f,h)则代表对照肽的图像。比例尺=200μm。
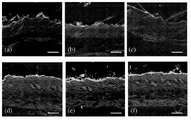
图3显示了荧光标记肽穿透进入活体小鼠皮肤30分钟后的图像。三个代表性图像针对每种情况而提供。(a-c)为荧光标记对照肽的穿透,而(d-f)为荧光标记SPACE肽的穿透。比例尺=50μm。
图4显示了荧光标记肽穿透进入活体小鼠皮肤2小时后的图像。三个代表性图像针对每种情况而提供。(a-c)为荧光标记对照肽的穿透,而(d-f)为荧光标记SPACE肽的穿透。比例尺=50μm。
图5显示了荧光标记肽结合到脱脂角质层的图像结果(a,b)和肽处理前后角质层的FTIR光谱(c-f)。在紫外(a)和可见光(不同的样品)(b)下的脱脂SC图像。(i,ii,iii)分别代表SPACE肽、对照肽和无肽。比例尺=1cm。注意,上面所示的角质层样品进行了脱脂处理,以确保对肽的结合能力而非转运能力进行比较。因此,如上所见的对照与SPACE肽之间的差异可能并不直接转化成它们对皮肤穿透的影响。(c,d)分别为SPACE肽和对照肽光谱的1400-1700cm-1区。(e,f)分别为SPACE肽和对照肽光谱的2800-3000cm-1区。初始和最终光谱用箭头表示。
图6提供了无肽处理前后角质层的酰胺I和酰胺II区的FTIR光谱。
图7显示了用对照(CP)和SPACE肽共孵育后猪皮的菊粉穿透性和电导率增强的图形结果。
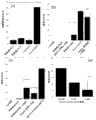
图8显示了SPACE肽穿透进入多种细胞系。(a,c,e)无肽处理的细胞的共焦图像,(b,d,f)用荧光标记SPACE肽孵育24小时的细胞的共焦图像。(a,b)人角质形成细胞,(c,d)人成纤维细胞,以及(e,f)人脐静脉内皮细胞(HUVEC)。(g)人角质形成细胞中SPACE肽内化的放大图像。(h)HUVEC、成纤维细胞和角质形成细胞中对照肽(空心条)和SPACE肽(实心条)内化24小时后的平均荧光强度。误差条表示标准偏差(N>或=30)。比例尺=100μm(a-f)和20μm(g)。
图9显示了荧光标记肽穿透进入MDA-MBA-231人乳腺癌细胞6小时后的图像结果(a-c)。无肽(a)、对照肽(b)和SPACE肽(c)处理细胞的图像。比例尺=50μm,图7还显示了在用与Lipofectamine络合的GFP siRNA处理后GFP表达内皮细胞的共焦图像(d-f)。(d)仅用Lipofectamine(无siRNA)处理细胞,(e)用与GFP siRNA络合的Lipofectamine处理细胞,以及(f)用与SPACE-GFP siRNA络合的Lipofectamine处理细胞。比例尺=200μm。
图10显示了细胞机制和毒性研究的结果。(a)4℃下以及采用内吞抑制剂脱氧-D-葡萄糖、氯丙嗪、制霉菌素和EIPA时人角质形成细胞中对照肽和SPACE肽的肽内化(对照%)。(b)在存在0.1mg/mL和1.0mg/mL对照肽(空心条)或SPACE肽(实心条)的情况下人角质形成细胞的细胞增殖。误差条表示标准偏差(N=4)。
图11显示使用SPACE肽递送siRNA的结果。(a)GFP表达内皮细胞中GPF的敲低百分比。误差条表示SD(N>或=30),(b)处理后24小时小鼠中IL-10蛋白水平的百分比。误差条表示SE(N>或=3),NS表示没有显著差异(p>0.15),(c)处理后72小时小鼠中GAPDH蛋白水平的敲低百分比。误差条表示SE(N>或=3),(d)局部应用siRNA后GAPDH敲低的剂量依赖性。误差条表示SE(N>或=3)。
图12显示使用肽偶联GAPDH siRN在不同施加时间时GAPDH敲低的结果。SPACE-GAPDH siRNA应用后4小时、24小时和72小时GAPDH蛋白水平的降低。
定义
在进一步描述本发明前,应当理解本发明不限于所述的特定实施方案,因此当然可以发生变化。还应当理解,本文所用的术语只是为了描述特定实施方案,并非旨在进行限制,因为本发明的范围将只由所附权利要求书限定。
如果提供了值的范围,则应当理解,介于该范围上限与下限之间的每个居间值(直至下限单位的十分之一,除非上下文另有明确指出)以及该所述范围内的任何其他所述值或居间值均涵盖在本发明内。这些较小范围的上限和下限可独立地包含在所述较小范围内,并且也涵盖在本发明内,受所述范围内任何具体排除的限值的约束。如果所述范围包含所述限值的一个或两个,则排除这些所含限值一者或两者的范围也包括在本发明内。
除非另有定义,否则本文所用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常所理解的相同含义。虽然类似于或等同于本文所述的那些的任何方法和材料也可用于实践或检验本发明,但现在描述示例性方法和材料。本文提及的所有出版物和申请以引用方式并入以公开和描述与所引述的出版物相关的方法和/或材料。在以引用方式并入本文的任何申请或出版物与本公开发生冲突的情况下,以本公开为准。
必须注意,如本文和所附权利要求书中所用,单数形式“一个”、“一种”和“该/所述”包括复数指代物,除非上下文另有明确指出。因此,例如,提及“一种肽”包括多个这样的肽,而提及“该药剂”包括提及一种或多种药剂以及本领域技术人员已知的其等同物,等等。
本文所论述的出版物仅针对它们在本申请提交日之前的公开内容而提供。此处的任何信息都不应解释为承认本发明不能因为是在先发明而先于这些出版物。另外,所提供的公开日可能不同于实际的公开日,这可能需要独立地进行确认。
应理解,在整个本公开中,根据单字母或三字母编码提及氨基酸。为使读者方便,如下提供单字母和三字母氨基酸代码:
G 甘氨酸 Gly P 脯氨酸 Pro
A 丙氨酸 Ala V 缬氨酸 Val
L 亮氨酸 Leu I 异亮氨酸 Ile
M 甲硫氨酸 Met C 半胱氨酸 Cys
F 苯丙氨酸 Phe Y 酪氨酸 Tyr
W 色氨酸 Trp H 组氨酸 His
K 赖氨酸 Lys R 精氨酸 Arg
Q 谷氨酰胺 Gln N 天冬酰胺 Asn
E 谷氨酸 Glu D 天冬氨酸 Asp
S 丝氨酸 Ser T 苏氨酸 Thr
如本文所用,术语“活性剂”是指单独地或联合其他活性或惰性组分施用给诸如人或非人动物的受试者后提供所需药理作用的药剂,例如蛋白质、肽、核酸(包括例如核苷酸、核苷及其类似物)或小分子药物。以上定义包括活性剂的前体、衍生物、类似物和前药。术语“活性剂”在本文也可用于泛指与本文所述的穿透肽偶联或缔合或连接到本文所述的活性剂载体或由其包含的任何药剂,例如蛋白质、肽、核酸(包括例如核苷酸、核苷及其类似物)或小分子药物。
在本文所述的穿透肽组合物背景下所用的术语“偶联”是指两个实体(例如分子、化合物或其组合)之间的共价或离子相互作用。
在本文所述的穿透肽组合物背景下所用的术语“缔合”是指由疏水、静电和范德华相互作用一者或多者介导的两个实体(例如分子、化合物或其组合)之间的非共价相互作用。
本文可互换使用的术语“多肽”和“蛋白质”是指任何长度的氨基酸(可包括编码和非编码氨基酸、化学或生物化学修饰或衍生的氨基酸)的聚合物形式,以及具有修饰肽主链的多肽。该术语包括融合蛋白质,包括但不限于与异源氨基酸序列形成的融合蛋白质、与异源和天然前导序列形成的融合体,含或不含N端甲硫氨酸残基;免疫标记蛋白;与可检测的融合配偶体形成的融合蛋白质,例如包含荧光蛋白、β-半乳糖苷酶、萤光素酶等作为融合配偶体的融合蛋白质;等等。
术语“抗体”和“免疫球蛋白”包括任何同种型的抗体或免疫球蛋白、保持与抗原特异性结合的抗体片段(包括但不限于Fab、Fv、scFv和Fd片段)、嵌合抗体、人源化抗体、单链抗体以及包含抗体的抗原结合部分和非抗体蛋白质的融合蛋白质。抗体可例如用放射性同位素、生成可检测产物的酶、荧光蛋白等进行可检测标记。抗体可进一步偶联到其他部分,例如特异性结合对的成员,例如生物素(生物素-亲和素特异性结合对的成员)等。这些术语还涵盖Fab’、Fv、F(ab’)2以及保持与抗原特异性结合的其他抗体片段。
抗体可以多种其他形式存在,包括例如Fv、Fab和(Fab′)2以及双官能(即,双特异性)杂交抗体(如Lanzavecchia等,Eur.J.Immunol.17,105(1987))以及以单链存在(如Huston等,Proc.Natl.Acad.Sci.U.S.A.,85,5879-5883(1988)和Bird等,Science,242,423-426(1988),这些文献以引用方式并入本文)。(一般参见Hood等,Immunology,Benjamin,N.Y.,第2版(1984),以及Hunkapiller和Hood,Nature,323,15-16(1986))。
术语“核酸”、“核酸分子”和“多核苷酸”可互换使用,并指任何长度的核苷酸(脱氧核糖核苷酸或核糖核苷酸或其类似物)的聚合物形式。这些术语涵盖例如DNA、RNA及其修饰形式。多核苷酸可具有任何三维结构,并可执行任何已知或未知的功能。多核苷酸的非限制性实例包括基因、基因片段、外显子、内含子、信使RNA(mRNA)、转移RNA、核糖体RNA、核糖酶、cDNA、重组多核苷酸、支链多核苷酸、质粒、载体、分离的任何序列的DNA、控制区、分离的任何序列的RNA、核酸探针和引物。核酸分子可以为线性或环状的。
“RNA干扰”(RNAi)是双链RNA(dsRNA)借以用来沉默基因表达的过程。不希望受任何特定理论的束缚,RNAi以较长dsRNA被RNaseIII样酶切丁酶(dicer)裂解成小干扰RNA(siRNA)开始。siRNA是长度通常为约19至28个核苷酸,或20至25个核苷酸,或21至23个核苷酸的dsRNA,并通常包含2-3个核苷酸3′突出端以及5′磷酸和3′羟基末端。siRNA的一条链结合到称为RNA诱导沉默复合物(RISC)的核糖核蛋白复合物中。RISC使用这条siRNA链来识别至少部分地与所结合的siRNA链互补的mRNA分子,然后裂解这些目标mRNA或抑制它们的翻译。结合到RISC中的siRNA链称为引导链或反义链。称为过客链或有义链的另一条siRNA链从siRNA中消除,并至少部分地与目标mRNA同源。本领域的技术人员应理解,原则上siRNA的任一条链均可结合到RISC中并用作引导链。然而,siRNA可以被设计(例如,通过在反义链5′端使siRNA双链体稳定性降低)为有利于反义链结合到RISC中。
RISC介导的序列至少部分地与引导链互补的mRNA的裂解导致该mRNA以及mRNA编码的相应蛋白质的稳态水平降低。可选地,RISC还可通过翻译抑制而不裂解目标mRNA使相应蛋白质的表达降低。其他RNA分子可与RISC相互作用并沉默基因表达。可与RISC相互作用的其他RNA分子的实例包括短发夹RNA(shRNA)、单链siRNA、微RNA(miRNA)和切丁酶底物27-mer双链体,即含一个或多个化学修饰核苷酸、一个或多个脱氧核糖核苷酸和/或一个或多个非磷酸二酯键合的RNA分子。如本文所用的术语“siRNA”是指双链干扰RNA,除非另外指明。为了便于本发明的讨论,将可与RISC相互作用并参与RISC介导的基因表达变化的所有RNA分子称为“干扰RNA”。因此,siRNA、shRNA、miRNA和切丁酶底物27-mer双链体是“干扰RNA”的子集。
“置换”由与多肽氨基酸序列或核苷酸序列相比时一个或多个氨基酸或核苷酸分别被不同的氨基酸或核苷酸取代而产生。如果置换为保守的,则置换到多肽中的氨基酸具有与其置换的氨基酸相似的结构或化学性质(如,电荷、极性、疏水性等)。天然存在的氨基酸的保守置换通常导致第一氨基酸被与第一氨基酸处于相同组中的第二氨基酸置换,其中示例性氨基酸组如下所示:(1)酸性(带负电)氨基酸,例如天冬氨酸和谷氨酸;(2)碱性(带正电),例如精氨酸、组氨酸和赖氨酸;(3)中性极性氨基酸,例如甘氨酸、丝氨酸、苏氨酸、半胱氨酸、酪氨酸、天冬酰胺和谷氨酰胺;以及(4)中性非极性氨基酸,例如丙氨酸、亮氨酸、异亮氨酸、缬氨酸、脯氨酸、苯丙氨酸、色氨酸和甲硫氨酸。在一些实施方案中,多肽变体可具有“非保守”变化,其中被置换的氨基酸在结构和/或化学性质方面不同。
“缺失”定义为氨基酸或核苷酸序列的变化,其中与天然存在的多肽的氨基酸序列或核苷酸序列相比时一个或多个氨基酸或核苷酸残基分别不存在。在多肽或多核苷酸序列的背景下,考虑到被修饰的多肽或多核苷酸序列的长度,缺失可涉及2个、5个、10个、至多20个、至多30个或至多50个或更多个氨基酸的缺失。
“插入”或“添加”在于与天然存在的多肽的氨基酸序列或核苷酸序列相比时分别导致添加一个或多个氨基酸或核苷酸残基的氨基酸或核苷酸序列变化。“插入”通常是指添加到多肽氨基酸序列内的一个或多个氨基酸残基,而“添加”可以是插入或指在N或C末端添加的氨基酸残基。在多肽或多核苷酸序列的背景下,插入或添加可以具有至多10个、至多20个、至多30个或至多50个或更多个氨基酸。
在多肽背景下的“非天然”、“非内源”和“异源”在本文可互换使用,以指代氨基酸序列与天然存在的不同的多肽,或在表达系统或病毒颗粒的背景下所处的环境与天然存在的不同的多肽。
在核酸或多肽背景下的“外源”用于指代已引入宿主细胞的核酸或多肽。“外源”核酸和多肽可以是宿主细胞天然或非天然的,其中相对于引入外源分子前宿主细胞中存在的编码基因产物或多肽水平而言,外源天然核酸或多肽使重组宿主细胞中的编码基因产物或多肽水平升高。
如本文所用,术语“测定”、“测量”、“评估”和“分析”可互换使用,并同时包括定量和定性测定。
如本文所用,术语“分离的”当用在分离化合物的背景下时是指所处的环境与该化合物天然存在的环境不同的所关注化合物。“分离的”旨在包括处于大体上富含所关注化合物和/或其中所关化合物得以部分或大体上纯化的样品内的化合物。
如本文所用,术语“大体上纯的”是指从其天然环境中移除并至少60%不含、75%不含或90%不含与其天然相关的其他组分的化合物。
“编码序列”或“编码”选定多肽的序列是例如当置于合适的调控序列(或“控制元件”)控制下在体内转录(就DNA而言)和翻译(就mRNA而言)成多肽的核酸分子。编码序列的边界通常由5′(氨基)末端的起始密码子和3′(羧基)末端的翻译终止密码子决定。编码序列可包括但不限于来自病毒、原核或真核mRNA的cDNA,来自病毒或原核DNA的基因组DNA序列,以及合成的DNA序列。转录终止序列可位于编码序列的3′。其他“控制元件”也可与编码序列相关。编码多肽的DNA序列可通过使用选定细胞所偏好的密码子进行优化以在该选定细胞中表达,从而代表所需多肽编码序列的DNA拷贝。
“由...编码的”是指编码基因产物(例如多肽)的核酸序列。如果该基因产物为多肽,则该多肽序列或其部分包含来自由该核酸序列编码的多肽的至少3至5个氨基酸、8至10个氨基酸或至少15至20个氨基酸的氨基酸序列。
“可操作地连接”是指元件的排列,其中所述组分被构造为执行它们通常的功能。就启动子而言,可操作地连接到编码序列的启动子将对编码序列的表达产生影响。启动子或其他控制元件不必与编码序列邻接,只要它们发挥作用指导其表达即可。例如,可以在启动子序列和编码序列之间存在插入未翻译但转录的序列,而启动子序列仍可被视为“可操作地连接”到编码序列。
所谓“核酸构建体”是指被构造成包含一个或多个合在一起不存在于自然界中的功能单元的核酸序列。实例包括环状、线性、双链、染色体外DNA分子(质粒)、粘粒(包含来自λ噬菌体的COS序列的质粒)、包含非天然核酸序列的病毒基因组等等。
“载体”能够将基因序列转移到目标细胞。通常,“载体构建体”、“表达载体”和“基因转移载体”是指能够指导所关注基因表达并可将基因序列转移到目标细胞的任何核酸构建体,这可通过载体的全部或一部分的基因组整合或载体作为染色体外元件而瞬时或可遗传性维持来实现。因此,该术语包括克隆和表达运载体以及整合载体。
“表达盒”包括能够指导可操作地连接到表达盒启动子的所关注基因/编码序列表达的任何核酸构建体。此类表达盒可被构建到“载体”、“载体构建体”、“表达载体”或“基因转移载体”中,以便将表达盒转移到目标细胞中。因此,该术语包括克隆和表达运载体以及病毒载体。
测定核酸和氨基酸“序列同一性”的技术在本领域中是已知的。通常,此类技术包括测定基因mRNA的核苷酸序列和/或测定因此编码的氨基酸序列,并将这些序列与第二核苷酸或氨基酸序列进行比较。一般来讲,“同一性”分别指两个多核苷酸或多肽序列精确的核苷酸与核苷酸或氨基酸与氨基酸对应性。两个或更多个序列(多核苷酸或氨基酸)可通过测定它们的“百分比同一性”而进行比较。无论核酸还是氨基酸序列,两个序列的百分比同一性都是两比对序列之间的精确匹配数除以较短序列的长度再乘以100。核酸序列的近似比对由以下文献中的局部同源性算法提供:Smith和Waterman,Advances in AppliedMathematics,2:482-489(1981)。该算法可通过使用由Dayhoff,Atlas ofProtein Sequences and Structure,M.O.Dayhoff编辑,第5次增补,3:353-358,National Biomedical Research Foundation,Washington,D.C.,USA开发以及由Gribskov,Nucl.Acids Res.14(6):6745-6763(1986)归一化的评分矩阵而应用于氨基酸序列。
该算法测定序列百分比同一性的示例性实施由GeneticsComputer Group(Madison,WI)在“BestFit”应用程序中提供。该方法的默认参数见述于Wisconsin Sequence Analysis Package Program Manual第8版(1995)(可得自Genetics Computer Group,Madison,WI)。在本发明背景下确立百分比同一性的另一种方法是使用版权归Universityof Edinburgh所有的程序的MPSRCH包,其由John F.Collins和ShaneS.Sturrok开发,并由IntelliGenetics,Inc.(Mountain View,CA)分销。通过这套软件包,可以采用Smith-Waterman算法,其中将默认参数用于评分表(例如,空位开放罚分为12,空位延伸罚分为1,空位为6)。通过生成的数据,“匹配”值反映“序列同一性”。其他计算序列间百分比同一性或相似性的合适程序在本领域中是熟知的,例如,另一比对程序为BLAST,使用默认参数。例如,可以通过以下默认参数使用BLASTN和BLASTP:遗传密码=标准;过滤器=无;链=两条;截止值=60;预期值=10;矩阵=BLOSUM62;说明=50个序列;排序方式=高分;数据库=非冗余,GenBank+EMBL+DDBJ+PDB+GenBank CDS翻译库+Swiss蛋白数据库+Spupdate+PIR。这些程序的详细信息可见于互联网,网址为http://in front ofblast.ncbi.nlm.nih.gov/Blast.cgi。
可选地,在多核苷酸的背景下,同源性可通过以下方式测定:在同源区之间形成稳定双链体的条件下使多核苷酸杂交,然后用单链特异性核酸酶消化,以及进行消化片段的大小测定。
两个DNA或两个多肽序列在使用上述方法测定时若所述序列在分子的限定长度上表现出至少约80%-85%、至少约85%-90%、至少约90%-95%或至少约95%-98%序列同一性则彼此“大体同源”。如本文所用,大体上同源也指表现出与指定的DNA或多肽序列完全同一性的序列。大体上同源的DNA序列可在DNA杂交实验中在例如严格条件(如针对该特定系统而定义)下鉴定。定义合适的杂交条件在本领域的技术范围内。参见例如Sambrook和Russel,MolecularCloning:ALaboratory Manual第三版,(2001)Cold Spring HarborLaboratory Press,Cold Spring Harbor,NY。
第一多核苷酸在具有与第二多核苷酸的区域、其cDNA、其补体相同或大体上相同的核苷酸序列时或在表现出如上所述的序列同一性时则“衍生自”第二多核苷酸。该术语不意味着要求或暗示该多核苷酸必须得自所述的来源(虽然也涵盖这种情况),而是可以通过任何合适的方法制得。
第一多肽(或肽)在(i)由衍生自第二多核苷酸的第一多核苷酸编码时,或(ii)显示出如上所述的与第二多肽的序列同一性时则“衍生自”第二多肽(或肽)。该术语不意味着要求或暗示该多肽必须得自所述的来源(虽然也涵盖这种情况),而是可以通过任何合适的方法制得。
如本文所用的术语“联合”是指如下使用,其中例如在第二治疗的整个施用过程中施用第一治疗;其中第一治疗的施用时间段与第二治疗的施用重叠,例如,第一治疗的施用在第二治疗的施用前开始并且第一治疗的施用在第二治疗的施用结束前结束;其中第二治疗的施用在第一治疗的施用前开始并且第二治疗的施用在第一治疗的施用结束前结束;其中第一治疗的施用在第二治疗的施用开始前开始并且第二治疗的施用在第一治疗的施用结束前结束;其中第二治疗的施用在第一治疗的施用开始前开始并且第一治疗的施用在第二治疗的施用结束前结束。因此,“联合”也可指涉及施用两种或更多种治疗的方案。如本文所用的“联合”也指两种或更多种治疗的施用,它们可以在相同的或不同的制剂中施用,通过相同或不同的途径施用,以及以相同的或不同的剂型施用。
术语“治疗”、“处理”等是指获得所需的药理和/或生理效应。该效应在完全或部分防止疾病或其症状方面可以是预防性的,和/或在部分或完全治愈疾病和/或由该疾病引起的不利影响方面可以是治疗性的。如本文所用的“治疗”涵盖对哺乳动物尤其是人类中的疾病的任何治疗,并包括:(a)防止可能有患病倾向但尚未诊断为患有该疾病的受试者中的疾病发生;(b)抑制疾病,即阻止其发展或进展;以及(c)缓解疾病,即,使疾病逆转和/或缓解一种或多种疾病症状。“治疗”也旨在涵盖药剂递送,以便提供药理效应,甚至在不存在疾病或疾患的情况下。例如,“治疗”涵盖穿透肽组合物的递送,其可在不存在病情的情况下引起免疫反应或产生免疫力,例如就疫苗而言。
“受试者”、“宿主”和“患者”在本文可互换使用,以指代可根据本公开的方法接受治疗或可向其施用根据本公开的肽组合物以实现所需效应的动物、人类或非人类。一般来讲,受试者为哺乳动物受试者。
如本文所用的术语“皮炎”是指皮肤炎症并包括例如过敏性接触性皮炎、荨麻疹、缺脂性皮炎(小腿皮肤干燥)、特应性皮炎、接触性皮炎(包括刺激性接触性皮炎和漆酚引起的接触性皮炎)、湿疹、重力性皮炎、钱币状皮炎、外耳炎、口周皮炎和脂溢性皮炎。
术语“角质层”是指表皮的角质外层,由扁平、角化、无核、死亡或剥离细胞组成。
如权利要求书中所用,与“包括”、“含有”和“特征在于”同义的术语“包含”是包含性或开放式的,并且不会排除另外的、未列举的要素和/或方法步骤。“包含”是一个专门术语,是指存在所述的要素和/或步骤,但也可添加其他要素和/或步骤,并仍落在相关主题的范围内。
如本文所用,短语“由...组成”排除未具体列举的任何要素、步骤和/或成分。例如,当短语“由...组成”出现在权利要求主体的条款中而不是紧跟前序时,则其只限制该条款中所述的要素;其他要素作为整体不排除在权利要求之外。
如本文所用,短语“基本上由...组成”将相关公开内容或权利要求的范围限制到指定的材料和/或步骤,以及不实质性影响所公开的和/或要求保护的主题的基本和新颖特征的那些。例如,在一些实施方案中本发明所公开的主题的肽可“基本上由”核心氨基酸序列“组成”,这表示该肽可包含一个或多个(如1、2、3、4、5、6或更多个)N端和/或C端氨基酸,其存在不实质性影响肽的所需生物活性。
至于术语“包含”、“基本上由...组成”和“由...组成”,如果在本文使用这三个术语之一,则本发明所公开的主题可包括使用其他两个术语的任一者。例如,本发明所公开的主题在一些实施方案中涉及包含氨基酸序列TGSTQHQ(SEQ ID NO:1)的组合物。应当理解,本发明所公开的主题因此也涵盖在一些实施方案中基本上由氨基酸序列TGSTQHQ(SEQ ID NO:1)组成的肽;以及在一些实施方案中由氨基酸序列TGSTQHQ(SEQ ID NO:1)组成的肽。类似地,还应当理解,本发明所公开的主题的方法在一些实施方案中包括本文所公开的和/或权利要求中所列举的步骤,它们在一些实施方案中基本上由本文所公开的和/或权利要求中所列举的步骤组成,以及它们在一些实施方案中由本文所公开的和/或权利要求中所列举的步骤组成。
本发明的示例性实施方案的详述
本公开涉及单独时以及偶联到活性剂或活性剂载体或者与活性剂或活性剂载体缔合时均能够穿透SC和/或活细胞(例如表皮和真皮细胞)细胞膜的肽。相关的组合物和方法也在本文进行了描述。
穿透肽
本公开提供在施用后能够穿透SC和/或穿透活细胞的肽。这些肽在本文称为“穿透肽”。在一些实施方案中,这些穿透肽能够穿透活表皮和真皮细胞的细胞膜。根据本公开的穿透肽可包括例如下表1中提供的氨基酸序列的一者或多者。
表1
在一些实施方案中,根据本公开的穿透肽包含包括3、4、5、6或7个连续氨基酸的片段的氨基酸序列,所述连续氨基酸选自以下氨基酸序列之一:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ IDNO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)和STHFIDT(SEQ ID NO:6)。
在一些实施方案中,根据本公开的穿透肽具有长度为8至11、12至15或16至19个氨基酸的氨基酸序列,所述氨基酸包含选自以下氨基酸序列之一的氨基酸序列:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)和STHFIDT(SEQ IDNO:6)。在一些实施方案中,根据本公开的穿透肽具有至少10个、至少20个、至少30个、至少40个、至少50个、至少60个、至少70个、至少80个、至少90或至少100个氨基酸的氨基酸序列。根据本公开的穿透肽可通过任何多种已知的交联方法环化。在一些实施方案中,根据本公开的穿透肽可以环化构象(即,作为环肽)提供,其中存在Cys-Cys二硫键。在一些实施方案中,根据本公开的穿透肽具有包含选自以下氨基酸序列之一的内部氨基酸序列的氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)和STHFIDT(SEQ ID NO:6),其中该肽的氨基酸序列包含在N端方向位于内部序列外部的至少第一Cys以及在C端方向位于内部序列外部的至少第二Cys。
在一些实施方案中,根据本公开的穿透肽包含包括选自以下氨基酸序列之一的3、4、5或6个连续氨基酸内部片段的氨基酸序列:TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)和STHFIDT(SEQ ID NO:6),并进一步包含在N端方向位于内部序列外部的至少第一Cys以及在C端方向位于内部序列外部的至少第二Cys。
本文所公开的穿透肽包括具有所提供的氨基酸序列的那些,以及相对于所提供的序列而言具有一个或多个氨基酸置换(例如一个或多个保守氨基酸置换)的肽,其中该肽保持穿透SC或穿透细胞的能力。
活性剂
上述肽在与分子货物(molecular cargo)(例如低分子量化合物或大分子)偶联或缔合的同时经局部施用后穿透SC和/或穿透活细胞(例如表皮和真皮细胞)细胞膜的能力使得它们适于促进本领域已知的多种活性剂的递送。
可以递送的活性的一般类别包括例如蛋白质、肽、核酸、核苷酸、核苷及其类似物;以及药物化合物,例如低分子量化合物。
可使用本文所公开的穿透肽递送的活性剂包括作用于以下方面的药剂:外周神经、肾上腺素能受体、胆碱能受体、骨骼肌、心血管系统、平滑肌、血液循环系统、突触点、神经效应器连接点、内分泌和激素系统、免疫系统、生殖系统、骨骼系统、自体有效物质系统(autacoid system)、消化及排泄系统、组胺系统以及中枢神经系统。
合适的活性剂可例如选自:皮肤病药剂、抗肿瘤剂、心血管药剂、肾药剂、胃肠药剂、风湿病药剂、免疫药剂和神经药剂等。
合适的皮肤病药剂可包括例如:局部麻醉剂、抗炎剂、抗感染剂、痤疮治疗剂、抗病毒剂、抗真菌剂、银屑病药剂(例如局部用皮质类固醇)等。
在一些实施方案中,合适的皮肤病药剂选自以下列表:16-17A-环氧孕酮(CAS登记号:1097-51-4)、对甲氧基肉桂酸/4-甲氧基肉桂酸(CAS登记号:830-09-1)、甲氧基肉桂酸辛酯(CAS登记号:5466-77-3)、甲氧基肉桂酸辛酯(CAS登记号:5466-77-3)、对甲氧基肉桂酸甲酯(CAS登记号:832-01-9)、4-雌甾烯-17β-醇-3-酮(CAS登记号:62-90-8)、对茴香酰乙酸乙酯(CAS登记号:2881-83-6)、二氢尿嘧啶(CAS登记号:1904-98-9)、洛匹那韦(CAS登记号:192725-17-0)、利坦色林(CAS登记号:87051-43-2)、尼洛替尼(CAS登记号:641571-10-0)、罗库溴铵(CAS登记号:119302-91-9)、6-(1-羟乙基)-1-氮杂双环(3.2.0)庚烷-3,7-二酮-2-羧酸对硝基苄基酯(CAS登记号:74288-40-7)、阿巴克丁(CAS登记号:71751-41-2)、帕利哌酮(CAS登记号:144598-75-4)、吉米沙星(CAS登记号:175463-14-6)、戊柔比星(CAS登记号:56124-62-0)、咪唑立宾(CAS登记号:50924-49-7)、琥珀酸索利那新(CAS登记号:242478-38-2)、拉帕替尼(CAS登记号:231277-92-2)、地屈孕酮(CAS登记号:152-62-5)、2,2-二氯-N-[(1R,2S)-3-氟-1-羟基-1-(4-甲基磺酰基苯基)丙-2-基]乙酰胺(CAS登记号:73231-34-2)、替米考星(CAS登记号:108050-54-0)、依法韦仑(CAS登记号:154598-52-4)、吡柔比星(CAS登记号:72496-41-4)、那格列奈(CAS登记号:105816-04-4)、表柔比星(CAS登记号:56420-45-2)、恩替卡韦(CAS登记号:142217-69-4)、依托考昔(CAS登记号:202409-33-4)、西尼地平(CAS登记号:132203-70-4)、盐酸多柔比星(CAS登记号:25316-40-9)、依地普仑(CAS登记号:128196-01-0)、磷酸西格列汀一水合物(CAS登记号:654671-77-9)、阿维A(CAS登记号:55079-83-9)、苯甲酸利扎曲坦(CAS登记号:145202-66-0)、多尼培南(CAS登记号:148016-81-3)、苯磺酸阿曲库铵(CAS登记号:64228-81-5)、尼鲁米特(CAS登记号:63612-50-0)、3,4-二羟基苯乙醇(CAS登记号:10597-60-1)、酒石酸酮色林(CAS登记号:83846-83-7)、奥扎格雷(CAS登记号:82571-53-7)、甲磺酸依普沙坦(CAS登记号:144143-96-4)、盐酸雷尼替丁(CAS登记号:66357-35-5)、6,7-二氢-6-巯基-5H-吡唑并[1,2-a][1,2,4]三唑鎓氯化物(CAS登记号:153851-71-9)、磺胺吡啶(CAS登记号:144-83-2)、替考拉宁(CAS登记号:61036-62-2)、他克莫司(CAS登记号:104987-11-3)、罗美昔布(CAS登记号:220991-20-8)、烯丙醇(CAS登记号:107-18-6)、保护美罗培南(CAS登记号:96036-02-1)、奈拉滨(CAS登记号:121032-29-9)、吡美莫司(CAS登记号:137071-32-0)、4-[6-甲氧基-7-(3-哌啶-1-基丙氧基)喹唑啉-4-基]-N-(4-丙-2-基氧苯基)哌嗪-1-甲酰胺(CAS登记号:387867-13-2)、利托那韦(CAS登记号:155213-67-5)、阿达帕林(CAS登记号:106685-40-9)、阿瑞匹坦(CAS登记号:170729-80-3)、依普利酮(CAS登记号:107724-20-9)、甲磺酸雷沙吉兰(CAS登记号:161735-79-1)、米替福新(CAS登记号:58066-85-6)、拉替拉韦钾(CAS登记号:871038-72-1)、达沙替尼一水合物(CAS登记号:863127-77-9)、奥索马嗪(CAS登记号:3689-50-7)、普拉克索(CAS登记号:104632-26-0)、帕瑞昔布钠(CAS登记号:198470-85-8)、替加环素(CAS登记号:220620-09-7)、托曲珠利(CAS登记号:69004-03-1)、长春氟宁(CAS登记号:162652-95-1)、屈螺酮(CAS登记号:67392-87-4)、达托霉素(CAS登记号:103060-53-3)、孟鲁司特钠(CAS登记号:151767-02-1)、布林佐胺(CAS登记号:138890-62-7)、马拉韦罗(CAS登记号:376348-65-1)、度骨化醇(CAS登记号:54573-75-0)、奥索利酸(CAS登记号:14698-29-4)、盐酸柔红霉素(CAS登记号:23541-50-6)、尼扎替丁(CAS登记号:76963-41-2)、伊达比星(CAS登记号:58957-92-9)、盐酸氟西汀(CAS登记号:59333-67-4)、子囊霉素(CAS登记号:11011-38-4)、β-甲基乙烯基磷酸酯(MAP)(CAS登记号:90776-59-3)、阿莫罗芬(CAS登记号:67467-83-8)、盐酸非索非那定(CAS登记号:83799-24-0)、酮康唑(CAS登记号:65277-42-1)、9,10-二氟-2,3-二氢-3-甲基-7-氧-7H-吡啶并-1(CAS登记号:82419-35-0)、酮康唑(CAS登记号:65277-42-1)、盐酸特比萘芬(CAS登记号:78628-80-5)、阿莫罗芬(CAS登记号:78613-35-1)、甲氧沙林(CAS登记号:298-81-7)、盐酸奥洛他定(CAS登记号:113806-05-6)、吡硫翁锌(CAS登记号:13463-41-7)、盐酸奥洛他定(CAS登记号:140462-76-6)、环孢霉素(CAS登记号:59865-13-3)以及肉毒杆菌毒素及其类似物和疫苗组分。
作为活性剂的蛋白质、多肽和肽
可用于本发明所公开的储库(depot)制剂的蛋白质可包括例如:例如细胞因子及其受体的分子,以及包含细胞因子或其受体的嵌合蛋白质,包括例如肿瘤坏死因子α和β,其受体及其衍生物;肾素;生长激素,包括人生长激素、牛生长激素、蛋氨酰人生长激素、脱苯丙氨酸人生长激素和猪生长激素;生长激素释放因子(GRF);甲状旁腺和垂体激素;促甲状腺激素;人胰腺激素释放因子;脂蛋白;秋水仙碱;催乳激素;促肾上腺皮质激素;促甲状腺激素;催产素;加压素;促生长素抑制素;赖氨酸加压素;促胰酶素;亮丙瑞林;α-1-抗胰蛋白酶;胰岛素A链;胰岛素B链;胰岛素原;促卵泡激素;降钙素;促黄体激素;促黄体激素释放激素(LHRH);LHRH激动剂和拮抗剂;高血糖素;凝血因子,例如因子VIIIC、因子IX、组织因子和血管性假血友病因子(von Willebrands factor);抗凝血因子,例如蛋白质C;心钠素;肺表面活性物质;除组织型纤溶酶原激活剂(t-PA)以外的纤溶酶原激活剂,例如尿激酶;铃蟾肽;凝血酶;造血生长因子;脑啡肽酶;RANTES(受激活调节正常T细胞表达和分泌因子);人巨噬细胞炎性蛋白(MIP-1-α);血清白蛋白,例如人血清白蛋白;苗勒抑制物质(mullerian-inhibiting substance);松弛素A链;松弛素B链;松弛素原;小鼠促性腺激素相关肽;绒毛膜促性腺激素;促性腺激素释放激素;牛生长激素;猪生长激素;微生物蛋白,例如β-内酰胺酶;DNA酶;抑制素;激活素;血管内皮生长因子(VEGF);激素或生长因子受体;整联蛋白;蛋白质A或D;类风湿因子;神经营养因子,例如骨源性神经营养因子(BDNF)、神经营养因子-3、4、-5或-6(NT-3、NT-4、NT-5或NT-6)或神经生长因子,例如NGF-β;血小板源性生长因子(PDGF);成纤维细胞生长因子,例如酸性FGF和碱性FGF;表皮生长因子(EGF);转化生长因子(TGF),例如TGF-α和TGF-β,包括TGF-β1、TGF-β2、TGF-β3、TGF-β4或TGF-β5;胰岛素样生长因子I和II(IGF-I和IGF-II);des(1-3)-IGF-I(脑IGF-I)、胰岛素样生长因子结合蛋白;CD蛋白,例如CD-3、CD-4、CD-8和CD-19;促红细胞生成素;骨生成诱导因子;免疫毒素;骨形态发生蛋白(BMP);干扰素,例如干扰素-α(如干扰素α2A)、-β、-γ、-λ和复合干扰素;集落刺激因子(CSF),如M-CSF、GM-CSF和G-CSF;白介素(IL),如IL-1至IL-10;超氧化物歧化酶;T细胞受体;表面膜蛋白;衰变加速因子;病毒抗原,例如HIV-1包膜糖蛋白的一部分、gp120、gp160或其片段;转运蛋白;归巢受体;地址素;生育抑制剂,例如前列腺素;生育促进剂;调控蛋白;抗体(包括其片段)和嵌合蛋白质,例如免疫粘附素;这些化合物的前体、衍生物、前药和类似物,以及这些化合物的药学上可接受的盐,或它们的前体、衍生物、前药和类似物。
合适的蛋白质或肽可以是天然的或重组的,并包括例如融合蛋白质。
在一些实施方案中,蛋白质为生长激素,例如人生长激素(hGH)、重组人生长激素(rhGH)、牛生长激素、蛋氨酰人生长激素、脱苯丙氨酸人生长激素和猪生长激素;胰岛素、胰岛素A链、胰岛素B链和胰岛素原;或生长因子,例如血管内皮生长因子(VEGF)、神经生长因子(NGF)、血小板源性生长因子(PDGF)、成纤维细胞生长因子(FGF)、表皮生长因子(EGF)、转化生长因子(TGF)以及胰岛素样生长因子I和II(IGF-I和IGF-II)。
适于在本文所公开的注射用可生物降解递送储库中用作活性剂的肽包括但不限于胰高血糖素样肽1(GLP-1)及其前体、衍生物、前药和类似物。
作为活性剂的核酸
核酸活性剂包括核酸及其前体、衍生物、前药和类似物,例如治疗性核苷酸、核苷及其类似物;治疗性寡核苷酸;以及治疗性多核苷酸。选自该组的活性剂可尤其用作抗癌剂和抗病毒剂。合适的核酸活性剂可包括例如核糖酶、反义寡脱氧核苷酸、适配子和siRNA。合适的核苷类似物的实例包括但不限于阿糖胞苷(araCTP)、吉西他滨(dFdCTP)和氟尿苷(FdUTP)。在一些实施方案中,合适的核酸活性剂为干扰RNA,例如shRNA、miRNA或siRNA。合适的siRNA包括例如IL-7(白介素7)siRNA、IL-10(白介素10)siRNA、IL-22(白介素22)siRNA、IL-23(白介素23)siRNA、CD86siRNA、KRT6a(角蛋白6A)siRNA、K6a N171K(角蛋白6a N171K)siRNA、TNFα(肿瘤坏死因子α)siRNA、TNFR1(肿瘤坏死因子受体1)siRNA、TACE(肿瘤坏死因子(TNF)-α转化酶)siRNA、RRM2(核糖核苷酸还原酶亚单位2)siRNA和VEGF(血管内皮生长因子)siRNA。这些siRNA的人基因靶标的mRNA序列在本领域中是已知的。对于IL-7,参见例如GenBank登录号:NM_000880.3、GenBank登录号:NM_001199886.1、GenBank登录号:NM_001199887.1和GenBank登录号:NM_001199888.1;对于IL-10,参见例如GenBank登录号:NM_000572.2;对于IL-22,参见例如GenBank登录号:NM_020525.4;对于IL-23,参见例如GenBank登录号:NM_016584.2和GenBank登录号:AF301620.1;对于CD86,参见例如GenBank登录号:NM_175862.4、GenBank登录号:NM_006889.4、GenBank登录号:NM_176892.1、GenBank登录号:NM_001206924.1和GenBank登录号:NM_001206925.1;对于KRT6a,参见例如GenBank登录号:NM_005554.3;对于TNFα,参见例如GenBank登录号:NM_000594.2;对于TNFR1,参见例如GenBank登录号:NM_001065.3;对于TACE,参见例如GenBank登录号:NM_003183.4;对于RRM2,参见例如GenBank登录号:NM_001165931.1和GenBank登录号:NM_001034.3;对于VEGF,参见例如GenBank登录号:NM_001025366.2、GenBank登录号:NM_001025367.2、GenBank登录号:NM_001025368.2、GenBank登录号:NM_001025369.2、GenBank登录号:NM_001025370.2、NM_001033756.2、GenBank登录号:NM_001171622.1和GenBank登录号:NM_003376.5。
此外,用于在siRNA设计期间选择特定mRNA目标序列的多种方法和技术在本领中是已知的。参见例如由MIT的Whitehead Instituteof Biomedical Research所提供的公用siRNA设计工具。该工具可在网站上找到,网址为http://directly precedingjura.wi.mit.edu/bioc/siRNAext/。
另外的活性剂化合物
多种另外的活性剂化合物可用于本文所公开的注射用储库组合物。合适的化合物可包括涉及以下药物靶标中的一者或多者的化合物:三环域、羧肽酶、羧酸酯水解酶、糖基化酶、视紫质样多巴胺受体、视紫质样肾上腺素受体、视紫质样组胺受体、视紫质样血清素受体、视紫质样短肽受体、视紫质样乙酰胆碱受体、视紫质样核苷酸样受体、视紫质样脂质样配体受体、视紫质样褪黑素受体、金属蛋白酶、转运体ATP酶、羧酸酯水解酶、过氧化物酶、脂肪氧合酶、多巴脱羧酶、A/G环化酶、甲基转移酶、磺酰脲受体、其他转运体(如多巴胺转运体、GABA转运体1、去甲肾上腺素转运体、钾转运ATP酶α链1、钠-(钾)-氯共转运体2、血清素转运体、突触囊泡胺转运体和噻嗪敏感性钠-氯共转运体)、电化学核苷转运体、电压门控离子通道、GABA受体(Cys-环)、乙酰胆碱受体(Cys-环)、NMDA受体、5-HT3受体(Cys-环)、配体门控离子通道Glu:钾盐镁矾、AMPA Glu受体、酸敏感性离子通道醛固酮、兰尼碱受体(Ryanodine receptor)、维生素K环氧化物还原酶、MetGluR样GABAB受体、内向整流K+通道、NPC1L1、MetGluR样钙敏感受体、醛脱氢酶、酪氨酸3-羟化酶、醛糖还原酶、黄嘌呤脱氢酶、核糖核苷还原酶、二氢叶酸还原酶、IMP脱氢酶、硫氧还蛋白还原酶、双加氧酶、肌醇单磷酸酶、磷酸二酯酶、腺苷脱氨酶、肽基脯氨酰异构酶、胸苷酸合成酶、氨基转移酶、法呢基焦磷酸合成酶、蛋白激酶、碳酸酐酶、微管蛋白、肌钙蛋白、IκB激酶-β抑制剂、胺氧化酶、环氧合酶、细胞色素P450、甲状腺素5-脱碘酶、类固醇脱氢酶、HMG-CoA还原酶、类固醇还原酶、二氢乳清酸氧化酶、环氧化物水解酶、转运体ATP酶、易位蛋白、糖基转移酶、核受体:NR3受体、核受体:NR1受体以及拓扑异构酶。
在一些实施方案中,该活性剂为靶向以下之一的化合物:视紫质样GPCR、核受体、配体门控离子通道、电压门控离子通道、青霉素结合蛋白、髓过氧物酶样、钠:神经递质共运输蛋白家族、DNA拓扑异构酶类II型、纤连蛋白III型和细胞色素P450。
在一些实施方案中,该活性剂为抗癌剂。合适的抗癌剂包括但不限于:放线菌素D、阿仑珠单抗、别嘌醇钠、氨磷汀、安吖啶、阿那曲唑、单磷酸阿糖胞苷(Ara-CMP)、门冬酰胺酶、氮杂胞苷(Azacytadine)、苯达莫司汀、贝伐珠单抗、比卡鲁胺、博莱霉素(如博莱霉素A2和B2)、硼替佐米、白消安、喜树碱钠盐、卡培他滨、卡铂、卡莫司汀、西妥昔单抗、苯丁酸氮芥、顺铂、克拉屈滨、氯法拉滨、环磷酰胺、阿糖胞苷、达卡巴嗪、更生霉素、柔红霉素、柔红霉素脂质体、达卡巴嗪、地西他滨、多西他赛、多柔比星、多柔比星脂质体、表柔比星、雌莫司汀、依托泊苷、磷酸依托泊苷、依西美坦、氟尿苷、氟达拉滨、磷酸氟达拉滨、5-氟尿嘧啶、福莫司汀、氟维司群、吉西他滨、戈舍瑞林、六甲蜜胺、羟基脲、伊达比星、异环磷酰胺、伊马替尼、伊立替康、伊沙匹隆、拉帕替尼、来曲唑、醋酸亮丙瑞林、洛莫司汀、氮芥、美法仑、6-巯嘌呤、甲氨蝶呤、光辉霉素、丝裂霉素C、米托坦、米托蒽醌、尼莫司汀、奥法木单抗(Ofatumumab)、奥沙利铂、紫杉醇、帕尼单抗、培门冬酶、培美曲塞、喷司他丁、帕妥珠单抗、吡铂、哌泊溴烷、普乐沙福、丙卡巴肼、雷替曲塞、利妥昔单抗、链脲佐菌素、替莫唑胺、替尼泊苷、6-硫鸟嘌呤、塞替派、托泊替康、曲妥珠单抗、曲奥舒凡、曲他胺、三甲曲沙、尿嘧啶氮芥、戊柔比星、长春碱、长春新碱、长春地辛、长春瑞滨及其类似物、前体、衍生物和前药。应该指出的是,上述化合物中的两种或更多种可以联合用于本公开的穿透肽组合物。
用于本发明所公开的穿透肽组合物的所关注活性剂还可包括阿片类物质及其衍生物以及阿片受体激动剂和拮抗剂,例如纳曲酮、纳洛酮、纳布啡、芬太尼、舒芬太尼、羟考酮及其药学上可接受的盐和衍生物。
在一些实施方案中,该活性剂为小分子或低分子量化合物,如分子量小于或等于约1000道尔顿(例如小于或等于约800道尔顿)的分子或化合物。
在一些实施方案中,该活性剂为标记物。合适的标记物包括例如放射性同位素、荧光剂、化学发光剂、生色团、酶、酶底物、酶辅因子、酶抑制剂、生色团、染料、金属离子、磁性粒子、纳米粒子和量子点。
活性剂可以任何合适的浓度存在于本文所公开的组合物中。合适的浓度可根据活性剂效力、活性剂半衰期等而变化。此外,根据本公开的穿透肽组合物可包含一种或多种活性剂,例如,上述活性剂中两种或更多种的组合。
活性剂载体
如本文此前所述,一种或多种活性剂可偶联到穿透肽或与穿透肽缔合,以提供根据本公开的穿透肽组合物。可选地,根据本公开的穿透肽组合物可包含与活性剂载体偶联或缔合的如本文所公开的穿透肽,而活性剂载体继而包含与其连接的和/或放置在其中的活性剂。
合适的活性剂载体包括例如脂质体、纳米粒子、胶束、微泡等等。用于将活性剂掺入此类载体的技术在本领域中是已知的。例如,脂质体或脂质粒子可根据美国专利号5,077,057(Szoka,Jr.)制备。由具有脂质双层形成潜力的非磷酰脂质(nonphosphal lipid)组分形成的脂质体在Biochim.Biophys.Acta.,19:227-232(1982)中有所公开。对于脂质体的制备、纯化、修饰和载药,一般参见New,R.C.C.,Liposomes:APractical Approach,(1990)Oxford University Press Inc.,N.Y。
制备脂质体和药物包封脂质体的技术的一般性讨论可见于美国专利号4,224,179(Schneider)。另见Mayer等,Chemistry andPhysics ofLipids,40:333-345(1986)。有关活性剂干粉组合物的包封,另见美国专利号6,083,539。对于将活性剂掺入纳米粒子,参见例如M.M.deVilliers等(编辑),Nanotechnology in Drug Delivery,(2009)AmericanAssociate of Pharmaceutical Scientists。对于将活性剂掺入胶束,参见例如D.R.Lu和S.Oie,Cellular Drug Delivery:Principles and Practice,(2004)Humana Press Inc.Totowa,NJ。
将肽连接到活性剂和活性剂载体
如本文所述的穿透肽可偶联到活性剂或与活性剂缔合。可选地,如本文所公开的穿透肽可偶联到活性剂载体或与活性剂载体缔合,活性剂载体继而包含与其连接的和/或放置在其中的活性剂(其实例如上所讨论)。偶联技术一般导致在穿透肽与活性剂或活性剂载体之间形成一个或多个共价键,而缔合技术则通常利用疏水、静电或范德华相互作用中的一种或多种。
多种技术可用于将肽偶联或缔合到活性剂。类似地,多种技术可用于将肽偶联或缔合到活性剂载体,例如,如本文所述的脂质体、纳米粒子或胶束。
例如,如果活性剂为肽或多肽,则包含穿透肽的整个组合物可使用标准氨基酸合成技术合成。包括标准分子生物学技术的其他方法可用于表达和纯化包含穿透肽的整个多肽序列。将肽偶联到其他肽或多肽的另外方法包括:如Rostovtsev等(2002)Angew.Chem.Int.Ed.41:2596-2599和Tornoe等(2002)J.Org.Chem.67:3057-3064所述的铜催化叠氮/炔[3+2]环加成“点击化学”;如Baskin等(2007)PNAS第104卷,第43期:167393-16797所述的叠氮/DIFO(二氟环辛炔)无铜点击化学;如Lin等(2005)J.Am.Chem.Soc.127:2686-2695所述的叠氮/膦“Staudinger反应”;如Saxon和Bertozzi(2000)3月17日Science287(5460):2007-10所述的叠氮/三芳基膦“改良Staudinger反应”;以及如Casey(2006)J.of Chem.Edu.第83卷,第2期:192-195,Lynn等(2000)J.Am.Chem.Soc.122:6601-6609和Chen等(2003)Progress inChemistry15:401-408所述的催化烯烃交叉复分解反应。
如果活性剂为低分子量化合物或小分子,则可使用多种技术将低分子量化合物或小分子偶联到如本文所述的穿透肽,如Loh等,ChemCommun(Camb),2010年11月28日;46(44):8407-9(2010年10月7日电子出版)中所述的点击化学。另见Thomson S.,Methods MolMed.,(2004);94:255-65,其中描述了将小分子羧基、羟基和胺残基偶联到蛋白质上的胺和巯基残基。
本领域中也有将肽偶联到活性剂载体(例如脂质体)的方法。参见例如G.Gregoriadis(编辑),Liposome Technology第三版第II卷Entrapment of Drugs and Other materials into Liposomes,(2007),Informa Healthcare,New York,NY,其描述了将肽偶联到脂质体表面的技术。对于蛋白质与脂质体的共价连接,参见New,R.C.C.,Liposomes:APractical Approach,(1990)Oxford University Press Inc.,N.Y.第163-182页。
作为药物制剂施用穿透肽组合物
本领域的技术人员应理解,有多种合适的方法可将穿透肽组合物施用给对其有需要的受试者或宿主,例如患者,并且虽然不止一种途径可用于施用特定的组合物,但是特定的途径可比另一种途径提供更即时和更有效的反应。药学上可接受的赋形剂也是本领域技术人员熟知的,并可容易地获得。赋形剂的选择将部分地由特定的化合物以及由用于施用组合物的特定方法决定。因此,存在多种合适的穿透肽组合物制剂。以下方法和赋形剂仅仅是示例性的,绝不是进行限制。
适于经口施用的制剂可包括:(a)液体溶液剂,例如溶于稀释剂(例如水、盐水或橙汁)中的有效量的化合物;(b)胶囊剂、小药囊或片剂,各自包含作为固体或颗粒的预定量的活性剂;(c)处于合适液体中的混悬剂;(d)合适的乳剂以及(e)水凝胶。片剂可包含以下一者或多者:乳糖、甘露醇、玉米淀粉、马铃薯淀粉、微晶纤维素、阿拉伯胶、明胶、胶态二氧化硅、交联羧甲基纤维素钠、滑石、硬脂酸镁、硬脂酸和其他赋形剂,着色剂,稀释剂,缓冲剂,润湿剂,防腐剂,调味剂以及药理学相容的赋形剂。锭剂可在调味剂(通常为蔗糖和阿拉伯胶或黄蓍胶)中包含活性成分,而糖果锭剂在惰性基质(例如明胶和甘油,或蔗糖和阿拉伯胶、乳剂、凝胶等)中包含活性成分,除了活性成分以外,还包含本领域已知的赋形剂。
穿透肽制剂可制成气溶胶制剂以通过吸入施用。这些气溶胶制剂可置于加压的可接受的抛射剂中,例如二氯二氟甲烷、丙烷、氮气等。它们也可被配制为非加压制剂的药剂,例如用于喷雾器或雾化器。
适于非肠道施用的制剂包括水性和非水性等渗无菌注射溶液,其可包含抗氧化剂、缓冲剂、抑菌剂以及使制剂与预期受体的血液等渗的溶质;以及水性和非水性无菌混悬剂,其可包含助悬剂、增溶剂、增稠剂、稳定剂和防腐剂。制剂可存在于单位剂量或多剂量密封容器中,例如安瓿和小瓶,并可储存在冷冻干燥(冻干)条件下,只需在即将使用前添加无菌液体赋形剂,例如注射用水。临时的注射溶液剂和混悬剂可通过之前所述种类的无菌粉末、颗粒和片剂制备。
适于局部施用的制剂可以霜剂、凝胶剂、糊剂、贴剂、喷雾剂或泡沫剂存在。
还通过与多种基质例如乳化基质或水溶性基质混合提供栓剂。适于阴道施用的制剂可以阴道栓、止血栓、霜剂、凝胶剂、糊剂、泡沫剂存在。
可提供经口或经直肠施用的单位剂型例如糖浆剂、酏剂和混悬剂,其中每个剂量单位例如茶匙、汤匙、片或栓包含预定量的组合物。类似地,供注射或静脉内施用的单位剂型可作为无菌水、生理盐水或另一种药学上可接受的载体中的溶液形式在制剂中包含穿透肽。
如本文所用的术语“单位剂型”是指作为单位剂量供人和动物受试者使用的物理上分离的单位,每个单位含预定量的穿透肽组合物,该量经计算为与药学上可接受的稀释剂、载体或媒介物相结合时足以产生所需的效果。穿透肽组合物的新单位剂型的技术规范取决于所采用的特定活性剂和要实现的效果,以及在宿主中与每种化合物相关的药效动力学。
本领域的技术人员应容易理解,剂量水平可根据具体的化合物、递送媒介物的性质等而变化。给定化合物的合适剂量可容易地由本领域的技术人员通过多种方法确定。
任选地,药物组合物可包含其他药学上可接受的组分,例如缓冲剂、表面活性剂、抗氧化剂、粘度改性剂、防腐剂等等。这些组分的每一种均是本领域所熟知的。参见例如美国专利号5,985,310,该专利的公开内容以引用方式并入本文。
适用于穿透肽制剂的其他组分可见于Remington′s PharmaceuticalSciences,Mack Pub.Co.,第18版(1995年6月)。在一个实施方案中,环糊精水溶液进一步包含右旋糖,例如约5%的右旋糖。
作为医疗器械组分施用穿透肽组合物
在一些实施方案中,本公开的穿透肽组合物中的一种或多种可结合到本领域已知的医疗器械中,例如药物洗脱支架、导管、织物、粘固剂、绷带(液体或固体)、生物可降解聚合物储库等。在一些实施方案中,该医疗器械为可植入的或可部分植入的医疗器械。
治疗方法
穿透肽组合物的术语“有效量”(或,在治疗背景下,“药学有效量”)一般是指穿透肽组合物有效实现所需疗效的量,例如,就穿透肽-siRNA组合物而言,即有效降低靶向mRNA表达以产生所需疗效的量。
穿透肽组合物的有效量、合适的递送媒介物以及方案可通过常规方法确定。例如,在治疗背景下,医师可在对其有需要的受试者或患者中以低剂量的一种或多种穿透肽组合物开始治疗,然后提高剂量或系统性改变剂量方案,监测其对患者或受试者的效果,以及调整剂量或治疗方案以使所需的疗效最大化。优化剂量和治疗方案的进一步论述可见于Benet等,Goodman & Gilman’s The Pharmacological Basis ofTherapeutics,第九版,Hardman等编辑,McGraw-Hill,New York,(1996),第1章第3-27页,和L.A.Bauer,Pharmacotherapy,APathophysiologic Approach,第四版,DiPiro等编辑,Appleton&Lange,Stamford,Connecticut,(1999),第3章第21-43页,以及其中引用以供读者参考的参考文献。
剂量水平和施用模式将取决于多种因素,例如所用的穿透肽、活性剂、使用背景(例如,待治疗的患者)等。优化施用模式、剂量水平以及调整方案(包括对系统进行监测以评估效果)是本领域普通技术人员熟知的常规事项。
在一个实施方案中,本公开提供治疗患有皮肤疾病的受试者的方法,包括:向受试者施用药学有效量的包含本文所公开的穿透肽的组合物,其中该肽与皮肤病活性剂(例如本文所公开的皮肤病活性剂)或包含活性剂的皮肤病活性剂载体偶联或缔合。
在一个实施方案中,本公开提供治疗患有、疑似患有或易患至少部分地由mRNA的表达所导致的疾病的受试者的方法,包括向受试者施用药学有效量的包含本文所述的穿透肽的组合物,其中该穿透肽与干扰RNA或包含干扰RNA的活性剂载体偶联或缔合,例如靶向mRNA的shRNA、miRNA或siRNA,或包含干扰RNA的载体。
在一个实施方案中,干扰RNA为siRNA,例如选自以下一者的siRNA:Il-10siRNA、IL-17siRNA、IL-22siRNA、IL-23siRNA、CD86siRNA、KRT6a siRNA、TNFR1 siRNA、TNFα siRNA和TACE siRNA。
体外用途
除了治疗方法和其他体内用途外,本文所公开的穿透肽组合物还可用于体外实验的背景下。例如,本文所公开的穿透肽可用于将本文所讨论的多种活性剂以及潜在的活性剂的任何一种在体外递送入活细胞,以确定所述活性剂或潜在活性剂的潜在疗效、毒性等。为此,本公开的穿透肽和穿透肽组合物可用于药物测试和/或筛选的背景下。
在一些实施方案中,如本文所述的穿透肽组合物可用于体外基因沉默实验,例如通过引入涉及基因靶标的穿透肽-干扰RNA偶联物,并监测对基因表达的作用。
另外的体外用途可包括使用与一种或多种标记剂(如,荧光剂或放射性标记)或一种或多种标记剂载体偶联或缔合的如本文所公开的穿透肽,以便在体外标记活细胞。
实施例
提出以下实施例以便为本领域的普通技术人员提供如何完成和使用本发明的完整公开内容与说明,这些实施例不旨在限制发明人视为的发明范围,也不旨在表示下文的实验是所执行的全部或唯一实验。已试图确保所用数字(例如,量、温度等)的准确性,但是应考虑一些实验误差和偏差。除非另外指明,否则份数均为重量份,分子量均为重均分子量,温度单位均为摄氏度,以及压力均为大气压或接近大气压。
实施例1
使用如下以及大致如图1中的A图所示的体外噬菌体展示鉴定穿透SC的肽。
噬菌体展示
采用了Ph.D.-C7C噬菌体展示肽文库(New England Biolabs)。在Franz扩散池(FDC,Permegear)中对猪皮进行研究。将2×1011pfu(10μL)噬菌体文库连同1mL磷酸缓冲盐水(PBS,pH7.4)置于FDC的供体室内。24小时后,将受体室中的液体移除,通过将受体溶液的等分试样加到200μL大肠杆菌(E.Coli)菌株ER2738(New England Biolabs)中并平铺到IPTG/Xgal板上而测定滴度。对37℃下孵育18小时后形成的蓝色菌斑数计数,随机选择20个菌斑进行测序。对于后续数轮筛选,将1mL受体溶液加到20mL ER2738的1∶100稀释过夜培养物中,生长4.5小时以扩增噬菌体。通过PEG/NaCl沉淀法纯化噬菌体,并重悬在PBS中。然后将扩增的噬菌体用于下一轮筛选。置于供体室中的噬菌体数2×1011pfu对于所有5轮筛选均保持恒定。
五轮筛选导致展示文库缩小,如图1的B图所示。一个序列AC-TGSTQHQ-CG(SEQ ID NO:13)在较高的轮数中高频出现,被指定为皮肤穿透及细胞进入(SPACE)肽。第二个序列(AC-HSALTKH-CG)(SEQ ID NO:14)也以高频率出现。第三个序列(AC-STHFIDT-CG)(SEQ ID NO:18)在第4和5轮中以相对高的频率出现。注意,如本文在肽序列背景下所用的“AC-”和“-CG”是指源于噬菌体展示系统的序列的AC和CG部分。
噬菌体穿透
按照如上所述的相同程序(无扩增和后续筛选步骤),使用在受体样品中检测到的噬菌体集落数和确定穿透的标准方程,测定了多种噬菌体样品的穿透,包括无肽文库的噬菌体、完整噬菌体文库、SPACE肽展示噬菌体和七甘氨酸噬菌体。
噬菌体克隆
为了确认噬菌体穿透皮肤的能力,将Ph.D.肽展示克隆系统(M13KE载体,New England Biolabs)用于构建噬菌体,其展示所关注的特定肽序列。将所关注的肽序列克隆到Ph.D.肽展示克隆系统中(M13KE载体,New England Biolabs)。该肽序列被插入KpnI和EagI限制位点之间。为了区分含有插入肽的修饰M13KE载体中的原始M13KE载体,将反向引物工程化以通过两个位点突变将EagI限制位点(5’-CGGCCG-3’)(SEQ ID NO:19)改为SacII限制位点(5’-CCGCGG-3’)(SEQ ID NO:20)。将正向引物和反向引物均用于复制整个载体。正向引物为5’-GTTCCGCGGAAACTGTTGAAAGTTGTTTAGCAAAATCCC-3’(SEQ ID NO:21)。TGSTQHQ(SEQ ID NO:1)和THGQTQS(SEQ IDNO:22)的反向引物分别为5’-TTTCCGCGGAACCTCCACCGCACTGATGCTGCTCGAACCAGTACAAGCAGAGTGAGAATAGAAAGGTACTACTAAAGGAATTGCGAATAATAATTTTTTCAC-3’(SEQ ID NO:23)和5’-TTTCCGCGGAACCTCCACCGCA(AGACTGAGTCTGCCCATGAGT)ACAAGCAGAGTGAGAATAGAAAGGTACTACTAAAGGAATTGCGAATAATAATTTTTTCAC-3’(SEQ ID NO:24)。
纯化复制产物,然后用SacII消化以产生连接载体所需的平端。将修饰后的载体电穿孔到电感受态ER2738细胞中,然后立即置于1mL SOC培养基(New England Biolabs)中,在37℃下生长45分钟。然后将所得的培养物置于50mL1∶100稀释的过夜培养物中,生长4.5小时。使用上述方案纯化经扩增的噬菌体,并测定滴度。18小时后挑取菌斑,测序,以确认肽在噬菌体表面上展示。
肽合成
SPACE肽的肽序列为ACTGSTQHQCG(SEQ ID NO:13),对照肽(CP)的肽序列为ACTHGQTQSCG(SEQ ID NO:25),在半胱氨酸之间形成有二硫键以产生环肽。5-羧基荧光素(5-FAM)或异硫氰基荧光素(FITC)偶联肽由ChinaTech Peptide Co.和RS Synthesis合成。将该染料置于肽的N端上。两种肽的生物素化形式由ChinaTech Peptide Co.合成,无修饰的肽由RS Synthesis合成。
实施例2
数学模型
噬菌体SC的穿透鉴于其大小而出人意料(Potts RO和Guy RH(1992)Predicting skin permeability.Pharm Res9(5):663-669;Magnusson B、Pugh W和Roberts M(2004)Simple rules defining thepotential of compounds for transdermal delivery or toxicity.Pharm Res21(6):1047-1054;Mitragotri S(2003)Modeling skin permeability tohydrophilic and hydrophobic solutes based on four permeation pathways.J Control Release86(1):69-92.)。大溶质(通常MW>500Da)表现出不良的皮肤穿透,测量其经皮穿透通常受它们的检测灵敏度的限制。用于本研究的M13噬菌体为长丝状颗粒,约8nm宽、900nm长。高供体浓度(约2x1011pfu/ml)、低检测限(约1pfu)和扩增潜力有利于对噬菌体真皮穿透的评估。噬菌体跨猪皮的穿透性测量值非常低;对照噬菌体(无肽文库的噬菌体)为10-9cm/h,对于SPACE噬菌体则为10-7-10-6cm/h。噬菌体的穿透虽然比低分子量溶质小得多,但仍然显著且出人意外。最重要的是,噬菌体的穿透具有序列特异性。
穿过细胞间脂质的扩散代表了分子经皮穿透的经典机制。然而,该机制通常限于小亲脂性分子。对大亲水性分子穿透的研究相对较少。此类溶质的经皮转运归因于两个途径:(i)极性或多孔途径,以及(ii)附属器(毛囊)。数学模型已在文献中有所描述,以阐述两种途径对经皮穿透的作用(Tang H、Mitragotri S、Blankschtein D和Langer R(2001)Theoretical description of transdermal transport of hydrophilicpermeants:application to low-frequency sonophoresis.J Pharm Sci90(5):545-568;Peck KD、Ghanem AH和Higuchi WI(1994)Hindereddiffusion of polar molecules through and effective pore radii estimates ofintact and ethanol treated human epidermal membrane.Pharm Res11(9):1306-1314.)。将这些模型应用到噬菌体转运及其与实验观测值的比较在下文给出。
这些模型的基本原理已有公开(Tang H、Mitragotri S、BlankschteinD和Langer R(2001)Theoretical description of transdermal transport ofhydrophilic permeants:application to low-frequency sonophoresis.(由英语翻译)J Pharm Sci90(5):545-568(英语);Peck KD、Ghanem AH和Higuchi WI(1994)Hindered diffusion of polar molecules through andeffective pore radii estimates of intact and ethanol treated humanepidermal membrane.(由英语翻译)Pharm Res11(9):1306-1314(英语)),这些模型的概要在下文提供。这些模型已应用于描述大分子例如流体力学半径为2.6nm的葡聚糖的转运,其虽然小于噬菌体的半径(约4nm),但具有相同的数量级。以下分析基于这些模型的外推,并提供解读噬菌体穿过皮肤的信息背景。
极性通路:极性(或多孔)通路已用于描述多种亲水性溶质(包括大分子)的透皮扩散(Tang H、Mitragotri S、Blankschtein D和LangerR(2001)Theoretical description of transdermal transport of hydrophilicpermeants:application to low-frequency sonophoresis.(由英语翻译)JPharm Sci90(5):545-568(英语);Mitragotri S等(Mathematical modelsof skin permeability:An overview.(由英语翻译)Int J Pharm(英语);Tezel A、Sens A和Mitragotri S(2003)Description of transdermaltransport of hydrophilic solutes during low-frequency sonophoresis basedon a modified porous pathway model.(由英语翻译)J Pharm Sci92(2):381-393(英语);Tezel A、Sens A和Mitragotri S(2002)Atheoretical analysis of low-frequency sonophoresis:dependence oftransdermal transport pathways on frequency and energy density.(由英语翻译)Pharm Res19(12):1841-1846(英语);TezelA和Mitragotri S(2003)On the origin of size-dependent tortuosity for permeation of hydrophilicsolutes across the stratum corneum.(由英语翻译)J Control Release86(1):183-186(英语);Polat BE、Seto JE、Blankschtein D和Langer R(Application of the aqueous porous pathway model to quantify the effectof sodium lauryl sulfate on ultrasound-induced skin structuralperturbation.(由英语翻译)J Pharm Sci(英语);Seto JE、Polat BE、Lopez RF、Blankschtein D和Langer R(Effects of ultrasound and sodiumlauryl sulfate on the transdermal delivery of hydrophilic permeants:Comparative in vitro studies with full-thickness and split-thickness pigand human skin.(由英语翻译)J Control Release145(1):26-32(英语);Tang H、Blankschtein D和Langer R(2002)Prediction of steady-state skinpermeabilities of polar and nonpolar permeants across excised pig skinbased on measurements of transient diffusion:characterization ofhydration effects on the skin porous pathway.(由英语翻译)J Pharm Sci91(8):1891-1907(英语);Tang H、Blankschtein D和Langer R(2002)Effects of low-frequency ultrasound on the transdermal permeation ofmannitol:comparative studies with in vivo and in vitro skin.(由英语翻译)J Pharm Sci91(8):1776-1794)(英语)。
为了跨过角质层(SC),亲水性溶质需要穿过多个脂质双层。然而,鉴于亲水性溶质跨过脂质双层的低穿透性,亲水性分子要通过对疏水性溶质发挥着重要作用的经典分配-扩散过程扩散跨过SC似乎是不可能的。已有人提出,此类溶质的经皮穿透主要通过角质层中的缺陷发生,这些缺陷以多种物理形式存在,包括晶粒边界、位错、纳米级孔或皮肤结构中的其他异常。角质层的水合可进一步增加此类缺陷的发生。这些缺陷的精确大小取决于缺陷的类型,并可跨越1-100nm的长度尺度。
其中ε、τ和L分别为膜的孔隙度、弯曲度和厚度,以及D∞为无限稀释的溶质扩散系数。H(λ)为立体阻碍因子,其中λ为渗透物质的流体动力学半径rh与皮肤的有效孔径r的比值(即,λ=rh/r)。H(λ)和λ之间的相对关系由阻碍转运理论给出,并在文献(11)中有所描述。γ(r)是皮肤中的孔径分布,已由以下函数(4)对猪皮进行了描述。
γ(r)=0.024exp(-0.00045r2) [2]
方程[2]考虑介质例如皮肤中孔(或空隙)形成的能量学。孔形成的可能性根据以下一般方程可与孔形成的自由能相关。
其中E为每单位面积每单位孔的孔形成自由能。方程[2]和[3]的比较表明,猪皮中4nm半径孔的E值<1kT,这是一个相对小的值。
经测定猪皮的ε值为约2x10-5(4)。类似地,已表明,猪SC中大亲水溶质的扩散弯曲度τ为约1(4)。Dp ∞是水中的溶质扩散系数,已使用如下例如Wilke-Chang或Stoke-Einstein方程的相互关系进行了计算。
附属器的贡献:大溶质还能够通过附属器跨皮肤扩散。虽然毛囊的密度随解剖位置而变化巨大,但是据估算猪皮毛囊的平均密度为约10/cm2。然而,大部分的毛囊被毛发占据,不能用于转运。由下式给出皮肤穿透性分流的贡献。
其中,φs为可用于转运的毛囊所占据的皮肤面积分数。Ds是溶质在毛囊内含物中的扩散系数,Lshunt是通过毛囊的扩散路径长度。可用于转运的毛囊中的皮肤面积分数为约10-4cm2/cm2。Ds可使用Wilke-Change方程或Stoke-Einstein关系估算。假设毛囊被粘性液体填充并鉴于噬菌体的大尺寸,Ds可近似为约10-8cm2/s。Lshunt为约500μm。通过代入φs和Lshunt的上述值,可以得到以下约10-7cm/h的表达。
因此,以上方程估算出噬菌体跨猪皮的穿透性在10-7-10-8cm/h的范围内。
为了将这些估计值与实验数据进行比较,如本文之前所述测量了跨猪皮的噬菌体穿透。对照噬菌体(未展示任何肽的噬菌体)表现出约10-9cm/h的穿透性。展示七甘氨酸的噬菌体也表现出约10-10cm/h的低穿透性。整个噬菌体展示文库表现出约10-8-10-7cm/h的穿透性,展示SPACE序列的噬菌体的穿透性为10-7-10-6cm/h。这些数值大致与理论预测值相符。注意,测得的穿透性值可能不代表稳态值,并且可能不满足穿透性的经典定义,尽管如此,这些值仍提供了合理的值以便与理论预测值进行比较。
鉴于研究中所用的所有噬菌体颗粒具有相同的大小,SPACE噬菌体相对于对照噬菌体(未展示肽)的穿透性较高的可能解释是由于在噬菌体表面上展示的肽。多孔途径模型假设皮肤中溶质的分配是一个整体,也就是说,溶质不表现出向皮肤的亲和力。如果SPACE噬菌体会表现出向皮肤的较高亲和力,则会导致较高比例的噬菌体穿过皮肤。实验观测值确实表明,SPACE增加了货物向皮肤组分尤其是角蛋白的亲和力。不希望受任何特定理论的束缚,我们假设该增加的亲和力是SPACE噬菌体相对于对照噬菌体穿透增强背后的主要原因。
为了进一步确证这一假设,开展了实验,其中评估了过量SPACE肽对SPACE噬菌体跨皮肤穿透的影响。具体地讲,将SPACE肽展示噬菌体在存在约100,000倍过量SPACE肽(噬菌体上每个SPACE肽对应约105个游离SPACE肽)的情况下置于皮肤上。过量SPACE肽显著减少了SPACE噬菌体的穿透,在此情况下SPACE噬菌体的穿透性接近七甘氨酸噬菌体(约10-10cm/h)。
实施例3
真皮筛选
在单独的实验中,进行了噬菌体筛选以分离位于真皮中的噬菌体。对于真皮筛选,将噬菌体展示文库也置于FDC的供体室内。24小时后,将供体室中的液体移除,将皮肤置于60℃下90秒。然后从真皮移除表皮。为了从真皮中提取噬菌体,将真皮切成小片,然后匀化(IKA分散机)。将匀浆在5,000rpm下离心5分钟,然后重悬在PBS中,于室温下孵育5分钟。然后将样品再次离心,再洗涤两次。最后一次离心后,将匀浆重悬在1%NP40(Sigma)中以从真皮中洗脱出剩余的噬菌体。根据上面列出的方法将洗脱液铺到板上并进行扩增。将此总共重复5轮。第五轮筛选结束时,从真皮中回收到约1.9x105个噬菌体。对噬菌体测序,第五轮中的三个先导序列为AC-KTGSHNQ-CG(SEQ ID NO:15)(30%)、AC-MGPSSML-CG(SEQID NO:16)(30%)和AC-TDPNQLQ-CG(SEQ ID NO:17)(20%)。考虑到AC-KTGSHNQ-CG(SEQ ID NO:15)肽与上文鉴定的SPACE肽之间的相似性,选择了SPACE肽进行进一步的研究。
实施例4
荧光标记噬菌体的穿透
将展示SPACE肽的噬菌体克隆进行荧光标记,并测试它们穿透进入皮肤的能力。将噬菌体粒子用Alexa Fluor488蛋白标记试剂盒(Invitrogen)进行标记。Alexa Fluor488包含与噬菌体外壳蛋白上的伯胺基团反应的TFP酯。将2×1012pfu的DI水或PBS溶液加到DI水中,得到500μL的总体积。然后将噬菌体溶液加到50μL1M的碳酸氢钠溶液中,将所得的溶液置于装有荧光染料的小瓶中,置于室温下1小时。然后使用PEG/NaCl纯化噬菌体以移除多余的未反应的染料,并测定滴度。
从约克夏猪的腹侧区获得全厚猪皮。将皮肤储存在-80℃下,在即将使用前解冻。测量皮肤的电导率以确保皮肤屏障的完整性。将电阻高于50kΩ的皮肤样品用于实验。将展示SPACE肽的荧光标记噬菌体克隆或乱序重排肽序列(AC-THGQTQS-CG)(SEQ ID NO:25)置于FDC的供体室内。为了模拟噬菌体筛选实验,将2×1011pfu加到供体室中,24小时后收获皮肤。制备皮肤样品,以通过共焦显微术成像。
用于共焦显微术成像的皮肤样品的制备
收获后立即将皮肤样品置于4℃的4%低聚甲醛(ElectronMicroscopy Sciences)中过夜,再用DI水漂洗。然后将皮肤样品冷冻在OCT冰冻切片包埋剂中,在冷冻切片机(Leica)上以20μm的厚度切片。将组织固定在带正电的载玻片上,以便将组织附着到载玻片(Fisher Scientific)上。将载玻片在DI水中洗涤5分钟,再用5μg/mLHoechest33342(Invitrogen)染色5分钟。然后将载玻片在DI水中再洗涤5分钟,接着在室温下于暗处使其完全干燥。将10μLPermount封片剂(Fisher Scientific)连同盖玻片置于皮肤切片顶部,然后密封载玻片。在共焦显微镜(Leica and Olympus Fluoview500)上对所有样品成像。
上述实验的成像结果在图2的(a)和(b)图中示出。展示SPACE肽的荧光标记噬菌体克隆表现出小但可检测的皮肤穿透进入(a)。相比之下,乱序重排肽序列(AC-THGQTQS-CG)(SEQ ID NO:25)仅表现出浅表穿透(b)。
实施例5
肽穿透进入猪皮
如下测试了当从噬菌体移除时SPACE肽穿透猪皮的能力。如上所述获得并制备全厚猪皮。将荧光标记肽(200μL1mg/mL的溶液)置于FDC的供体室内。24小时后,将供体室中的剩余溶液移除,拆卸FDC。取回皮肤样品,用DI水漂洗,以移除皮肤表面上多余的肽或肽复合物。然后如上所述制备皮肤样品,用于共焦显微术成像。
上述实验的成像结果在图1的(c)和(d)图中示出。SPACE肽在从噬菌体移除时穿透进入了皮肤(c)。与通过完整噬菌体获得的观测值一致,据发现SPACE肽主要集中在真皮。未观察到对照肽的显著穿透(d)。
实施例6
肽和大分子在猪皮中的穿透
如下测试了SPACE肽携带大分子货物跨过SC的能力。如上所述获得并制备全厚猪皮。首先如下更详细所述将肽偶联到大分子,然后将肽-大分子复合物置于FDC的供体室内。24小时后,将供体室中的剩余溶液移除,拆卸FDC。取回皮肤样品,用DI水漂洗,以移除皮肤表面上多余的肽复合物。然后如上所述制备皮肤样品,用于共焦显微术成像。
为了将肽偶联到大分子链霉亲和素,将80μL1mg/mL的生物素化肽溶液用20μL2mg/mL的链霉亲和素-Alexa Fluor488偶联物(Invitrogen)溶液在室温下孵育30分钟。然后将所得的溶液置于FDC的供体室内。24小时后收获皮肤样品,如上所述进行成像。
链霉亲和素当偶联到生物素化SPACE肽时远远穿过了SC,一些链霉亲和素存在于表皮和真皮中(图1的(e)图)。未偶联到SPACE肽的链霉亲和素表现出极微的表皮穿透进入(图1的(f)图)。
还测试了SPACE肽携带量子点跨过SC的能力。对于将量子点递送至皮肤内,将198μL100ng/mL的生物素化肽溶液用2μL QDot525链霉亲和素偶联物(Invitrogen)在室温下孵育1小时。然后将200μL悬浮液置于FDC的供体室内。24小时后收获皮肤样品,如上所述进行共焦显微术成像。
SPACE肽当偶联到链霉亲和素包被的量子点时导致了可检测但较小的转运量。未观察到偶联到对照肽的量子点的显著穿透。分别参见图2的(c)和(d)图。不希望受任何特定理论的束缚,转运量降低可能是由于量子点的尺寸相对较大。
实施例7
肽在人体皮肤中的穿透
如下测试了当从噬菌体移除并偶联到荧光标记形式的示例性小分子时SPACE肽穿透人体皮肤的能力。从National Disease ResearchInterchange获得全厚人体皮肤。将皮肤储存在-80℃下,在即将使用前解冻。测量皮肤的电导率以确保皮肤屏障的完整性。将电阻高于50kΩ的皮肤样品用于实验。将荧光标记肽(200μL1mg/mL的溶液)置于FDC的供体室内。24小时后,将供体室中的剩余溶液移除,拆卸FDC。取回皮肤样品,用DI水漂洗,以移除皮肤表面上多余的肽或肽复合物。然后如上所讨论制备皮肤样品,用于共焦显微术成像。
经证实SPACE肽成功地跨过人体皮肤,并表现出与存在于猪皮中相似的穿透。参见图2的(e)图(SPACE)和(f)图(对照)。当从上观察时,发现了角质细胞内SPACE肽的高度定位,而未观察到对照肽的显著穿透。分别参见图2的(g)图和(h)图。
实施例8
肽穿透进入活体小鼠皮肤
如下测试了SPACE肽穿透活体小鼠皮肤的能力。将200μl荧光标记肽(1mg/ml)施加到小鼠皮肤上。通过收获皮肤、切片并在显微镜下观察,评估了多个时间点的穿透。
SPACE肽以显著高于对照肽的水平穿透进入了活体小鼠皮肤(分别参见图3的(a)-(f)图和图4的(a)-(f)图)。将SPACE肽施加到小鼠皮肤上30分钟(图3)导致了穿透,施加两小时(图4)导致了显著的皮肤穿透并位于真皮深层,与猪皮和人体皮肤中所见的一致。
实施例9
角质层研究
为了进一步表征SPACE肽穿透SC的能力,使用分离的SC如下进行了实验。为了从全厚皮肤中分离SC,将皮肤置于60℃的水浴中90秒。从水浴中取出后,将表皮与真皮分离。然后将SC以表皮侧向下置于含0.25%胰蛋白酶的培养皿中,以从SC去除表皮。将SC在DI水中洗涤,然后使其在室温下使其完全干燥。为了使SC脱脂,将SC置于以下氯仿∶甲醇溶剂混合物中各15分钟:2∶1(v/v)、1∶1(v/v)和1∶2(v/v)。为了确认去除了脂质,在暴露于溶剂混合物前后对SC样品进行了FTIR。
SC的傅立叶变换红外(FTIR)光谱
对SC样品进行了FTIR以观察不同肽溶液对SC结构的作用。将SC切成1.5×1.5cm的片,在暴露于肽前获得每片的对照光谱。然后将2mL肽溶液与SC孵育24小时。接着将SC样品用DI水漂洗,并使其在室温下完全干燥。再次读取每个SC样品的光谱,将前后光谱进行比较以确定各肽对SC结构的作用。使用Nicolet Magna850光度计以2cm-1的分辨率获得光谱,并通过400次扫描求平均值。
采用分离的人SC的实验表明SPACE肽结合到角质细胞蛋白,最可能结合到角蛋白(图5的(a)和(b)图)。傅里叶变换红外光谱(FTIR)研究也确认了SPACE肽对角蛋白的作用。具体地讲,暴露于SPACE肽的SC表现出FTIR光谱的变化,从而表明角蛋白发生了结构变化(图5的(c)图)。与不存在任何肽的情况下所见相比,FTIR表明对照肽对蛋白结构无显著影响(图5的(d)图以及图6)。FTIR还表明SPACE肽对SC脂质无可检测的影响(图5的(e)和(f)图)。既未发现对称CH2拉伸峰的峰面积发生变化也未发现中心频率的偏移,从而表明SPACE肽未引起SC脂质的提取或流化。与FTIR数据一致,暴露于SPACE肽未引起皮肤电导率的显著变化(图7)。具体地讲,皮肤电导率在用SPACE肽孵育24小时后增加了约1.7(+/-0.6)倍。该提高虽然高于对照肽的观测值但仍相对温和。类似地,SPACE肽与大亲水分子菊粉的共孵育仅导致了其穿透性的温和增加(图7),从而表明SPACE肽主要对增强偶联货物但非共施用货物的穿透性有效。
不希望受任何特定理论的束缚,SPACE肽的主要作用可能是增强SC主要是角质细胞中的分配,其继而增强SPACE肽和偶联物跨过皮肤屏障的能力。还可预期肽对穿透的附加作用,因为其能够影响角蛋白结构。
实施例10
SPACE肽穿透进入活细胞
已经确认了SPACE肽穿透SC的能力,还测试了其在细胞培养中穿透进入活细胞包括角质形成细胞、成纤维细胞和内皮细胞(HUVEC)的能力。
对于细胞穿透研究,将1.2×104个细胞接种到多聚右旋赖氨酸包被的玻璃底培养皿(MatTek)上。对于HUVEC细胞,在细胞接种前将培养皿包被上1%的明胶。在37℃下孵育4小时后,移除培养基,将20μL1mg/mL的荧光肽溶液加到180μL培养基中,随后加到细胞培养皿中。对于对照,加入等量的PBS以代替肽溶液。加入肽后,将细胞培养物在合适的条件下孵育以研究细胞穿透(4℃或37℃)并孵育6或24小时。制备细胞进行共焦显微术成像。
细胞培养条件
将成人表皮角质形成细胞(Invitrogen)在补充了人角质形成细胞生长添加剂(Invitrogen)的EpiLife培养基(Invitrogen)中培养,将人皮肤成纤维细胞(ATCC)在补充了10%胎牛血清的DMEM培养基(ATCC)中培养,将混合人脐带静脉内皮细胞(HUVEC,Lonza)在补充了15%胎牛血清、15μg/mL内皮细胞生长添加剂、100μg/mL肝素和2mM L-谷氨酰胺的M199培养基中在1%明胶包被培养瓶中培养,以及将MDA-MB-231乳腺癌细胞在补充了10%胎牛血清的DMEM培养基(ATCC)中培养。将所有细胞培养基补充100U/mL青霉素和100μg/mL链霉素,让培养物在标准细胞培养条件(37℃,含5%CO2)下生长。
用于共焦显微术成像的细胞培养样品的制备
孵育后,将细胞用汉克平衡盐缓冲液(HBSS,Lonza)洗涤,再用1%台盼蓝孵育5分钟以猝灭细胞表面上的任何荧光。然后将细胞用4%低聚甲醛固定3分钟,接着在HBSS中再次洗涤。接下来将细胞用Hoechest33342(5μg/mL)孵育5分钟,然后在HBSS中洗涤。然后将细胞培养皿充满HBSS,使用共焦显微镜(Olympus Fluoview500)成像。
经证实SPACE肽对所有细胞系均显著穿透(图8的(a)-(f)图),图8的(g)图显示了角质形成细胞中SPACE肽内化的放大视图。在所有情况下,SPACE肽的内化程度均高于对照肽的内化程度,表明细胞穿透以序列特异性方式发生(图8的(h)图)。SPACE肽在乳腺癌细胞中也表现出内化(MD-MB-23,图9的(a)-(c)图)。穿透所有类型的测试细胞的能力表明,SPACE进入细胞的模式通过所有研究细胞系共同的途径而进行,而不是由于角质形成细胞特有的特定膜蛋白。
实施例11
细胞穿透机制研究
为了确定SPACE肽的细胞穿透的潜在机制,在人角质形成细胞中测试了多种内吞抑制剂(包括在4℃下孵育)对内化的影响(参见图10的(a)图)。
内吞抑制剂
对于细胞机制研究,将细胞与多种内吞抑制剂一起孵育或在4℃孵育1小时,然后添加荧光标记肽。所用的内吞抑制剂为EIPA(Invitrogen)以及氯丙嗪、制霉菌素和脱氧-D-葡萄糖(Sigma)。将EIPA溶于DMSO,以100μM的浓度使用。将氯丙嗪、制霉菌素和脱氧-D-葡萄糖溶于无菌水中,并分别以10μg/mL、25μg/mL和5mM的浓度使用。将细胞用荧光标记肽孵育3小时,然后收获以使用流式细胞术进行分析。
用于流式细胞术的样品的制备
用荧光标记肽孵育后,移除培养基,将细胞在HBSS中洗涤3次,每次5分钟,以移除残余的荧光。将0.25%胰蛋白酶(HyClone)用于从细胞培养板上移除细胞。然后将细胞以5,000rpm离心处理5分钟,以沉淀细胞。将细胞沉淀在冰上重悬在PBS(pH7.4)中,将样品使用FACS Aria流式细胞仪进行分析。
4℃下的孵育显著减少了SPACE肽(与37℃下相比约5%的摄取)以及对照肽的内化,表明两者均通过主动机制进入细胞(图10的(a)图)。这通过使用脱氧-D-葡萄糖进一步确认,其也导致了两种肽内化的减少(约52%)(图10的(a)图)。为了进一步评估主动摄取的性质,将细胞用网格蛋白介导的内吞抑制剂氯丙嗪和胞膜窖介导的内吞抑制剂制霉菌素孵育。两者均未减少SPACE肽或对照肽的细胞内化(图10的(a)图)。最后,测试了巨胞饮抑制剂5-(N-乙基-N-异丙基)阿米洛利(EIPA)的影响。将细胞暴露于EIPA导致了约50%的SPACE内化减少(图10的(a)图)。相比之下,EIPA对对照肽内化无影响。总之,这些结果表明巨胞饮在SPACE肽的内化中发挥着重要作用,这一结论也适用于其他细胞穿透肽,具体参见相关文献(Nakase I等(2004)Cellular uptake of arginine-rich peptides:roles for macropinocytosis andactin rearrangement.Mol Ther10(6):1011-1022;Patel LN、Zaro JL和Shen WC(2007)Cell penetrating peptides:intracellular pathways andpharmaceutical perspectives.Pharm Res24(11):1977-1992)。已有研究报道,巨胞饮内化的货物通常不与核内体/溶酶体共定位,这意味着有可能避免它们进入降解溶酶体室(Tamaru M、Akita H、Fujiwara T、Kajimoto K和Harashima H(2010)Leptin-derived peptide,a targetingligand for mouse brain-derived endothelial cells via macropinocytosis.Biochem Biophys Res Commun394(3):587-592;Walsh M等(2006)Evaluation of cellular uptake and gene transfer efficiency of pegylatedpoly-L-lysine compacted DNA:implications for cancer gene therapy.MolPharm3(6):644-653)。对角质细胞培养物的MTT分析表明,SPACE肽在这里研究的浓度范围内对细胞无毒性(0.1-1.0mg/mL,图10的(b)图)。
实施例12
使用SPACE肽偶联的siRNA敲低GFP
SPACE肽穿透进入多种细胞的能力使其成为siRNA递送的优异候选物。使用表达绿荧光蛋白(GFP)的内皮细胞作为模型细胞系在体外探究了这一可能性。
使表达GFP的内皮细胞(ATCC)在补充了10%胎牛血清的DMEM培养基中生长。将GFP siRNA即5’-GAC GUAAAC GGC CAC AAGUUC N6-3’(SEQ ID NO:26)(Dharmacon)通过EDC化学反应偶联到荧光标记肽(含游离羧基)。
将10mM肽溶液在MES缓冲液(pH5.5)中用等份的10mM N-(3-二甲氨基丙基)-N’-乙基碳二亚胺盐酸盐溶液(EDAC,Sigma)和9.5mM N-羟基硫代琥珀酰亚胺钠盐溶液(NHS,Sigma)孵育15分钟。然后将胺改性的siRNA加入混合物中以将肽偶联到siRNA,并使其混合过夜。
将肽-siRNA复合物加入合适的细胞培养基中,得到1μM siRNA的最终浓度。然后将连同肽-siRNA的培养基加入细胞中,并使其孵育48小时。将细胞使用共焦显微镜成像,再使用ImageJ进行图像分析以确定各细胞的总体荧光强度。将敲低确定为测试例中强度低于对照例(未处理)细胞群的平均强度观测值至少30%的细胞的百分比。
SPACE肽偶联的siRNA引起了GFP的显著敲低(图11的(a)图)。相比之下,对于单独的siRNA、单独的SPACE、偶联到对照siRNA的SPACE或偶联到siRNA的对照肽,未观察到显著的敲低。为了确定siRNA偶联到SPACE肽对siRNA的效能是否有不利影响,将未偶联的siRNA和SPACE-siRNA两者与LipofectmineTM复合,并评估敲低。在两种情况下,敲低与对照即无siRNA处理相比均是显著的(图9的(d)-(f)图)。
实施例13
使用肽偶联的IL-10siRNA进行活体真皮穿透
如下评估了SPACE肽增强IL-10siRNA真皮穿透的能力。选择该siRNA是因为其治疗特应性皮炎(一种主要的皮肤病)的潜力。由于与SPACE肽相比时对照肽所见的敲低不显著以及活体皮肤穿透能力不足,因此在活体siRNA研究中未评估对照肽。
在活体研究中所用的siRNA序列如下:IL-10:5’-GAA UGAAUUUGA CAU CUU CUU N6-3’(SEQ ID NO:27),以及萤光素酶(对照):5’-UAA GGC UAU GAA GAG AUA CUU N6-3’(SEQ ID NO:28)。对于IL-10,在所有碱基上均进行2-O-甲基修饰。所有siRNA均购自Dharmacon。
根据实验动物照护及使用委员会(Institutional Animal Care andUse Committee)批准的方案,在6-8周龄的雌性Balb/C小鼠(CharlesRiver Laboratories)中进行了siRNA递送。将小鼠置于麻醉下(1-2%异氟烷),轻轻刮去其背部的毛。将200μL10μM的肽-siRNA溶液或相应的对照局部施加在动物背部的3cm2大小的区域上。然后将溶液用无菌纱布和透气绷带覆盖。24小时后,将小鼠用CO2处死,使用4mm活检穿孔器立即采集皮肤样品。从处理区随机采集两个4mm的活检样本,立即冷冻在液氮中。然后将皮肤置于0.5%(w/v)3-(癸基二甲基铵基)丙烷磺酸盐(DPS)和Brij30的表面活性剂组合中,在冰上匀化(IKA分散机)1分钟以从皮肤样品中提取出蛋白质。然后将匀浆在10,000rpm下离心5分钟,收集上清液。使用微量BCA蛋白定量试剂盒(Pierce)测定总蛋白浓度,使用小鼠IL-10ELISA(Raybiotech)测定IL-10水平。
与未接受处理、接受单独的SPACE肽或接受偶联到萤光素酶siRNA(对照siRNA)的SPACE的小鼠相比,施加无肽的单独的IL-10siRNA未对IL-10水平产生显著影响。相比之下,用偶联到IL-10siRNA的SPACE以及偶联到2-O-甲基修饰IL-10siRNA的SPACE处理动物显示出IL-10水平的显著降低(图11的(b)图)。
实施例14
使用肽偶联的GAPDH siRNA进行活体真皮穿透
作为另一个实例,将SPACE肽偶联到3-磷酸甘油醛脱氢酶(GAPDH)siRNA,并如下评估了其对皮肤GAPDH水平的作用。选择此靶标是因为GAPDH是一种常见的看家蛋白并提供常见siRNA靶标的一个实例。
在活体研究中所用的siRNA序列如下:GAPDH:5’-GUG UGAACC ACG AGAAAU AUU N6-3’(SEQ ID NO:29),以及萤光素酶(对照):5’-UAA GGC UAU GAA GAG AUA CUU N6-3’(SEQ ID NO:28)。所有siRNA均购自Dharmacon。
根据实验动物照护及使用委员会批准的方案,在6-8周龄的雌性Balb/C小鼠(Charles River Laboratories)中进行了siRNA递送。将小鼠置于麻醉下(1-2%异氟烷),轻轻刮去其背部的毛。将200μL10μM的肽-siRNA溶液或相应的对照局部施加在动物背部的3cm2大小的区域上。然后将溶液用无菌纱布和透气绷带覆盖。72小时后,将小鼠用CO2处死,使用4mm活检穿孔器立即采集皮肤样品。从处理区随机采集两个4mm的活检样本,立即冷冻在液氮中。然后将皮肤置于0.5%(w/v)3-(癸基二甲基铵基)丙烷磺酸盐(DPS)和Brij30的表面活性剂组合中,在冰上匀化(IKA分散机)1分钟以从皮肤样品中提取出蛋白质。然后将匀浆在10,000rpm下离心5分钟,收集上清液。使用微量BCA蛋白定量试剂盒(Pierce)测定总蛋白浓度。使用KdalertTMGAPDH测定试剂盒(Ambion)测量GAPDH水平。
与对照(未处理、单独的siRNA、单独的SPACE肽和偶联到对照siRNA的SPACE,图11的(c)图)相比,用SPACE-GAPDH siRNA偶联物处理的动物引起了蛋白水平的显著降低。皮肤中GAPDH的敲低是剂量依赖性的;在10μM下观察到43%的敲低,在5μM下观察到21%的敲低,以及在1μM下观察到10%的敲低(图11的(d)图)。敲低还取决于施加时间,更长的施加时间导致了更高的敲低(图12)。
Claims (138)
1.一种组合物,其包含包括氨基酸序列TGSTQHQ(SEQ IDNO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽,其中所述肽偶联到活性剂或包含所述活性剂的活性剂载体,并且其中所述组合物能够在与角质层(SC)接触时穿透所述角质层或与细胞接触时穿透所述细胞。
2.根据权利要求1所述的组合物,其中所述组合物能够穿透所述SC层以及穿透所述细胞。
3.根据权利要求1所述的组合物,其中所述氨基酸序列包括CTGSTQHQC(SEQ ID NO:7)、CHSALTKHC(SEQ ID NO:8)、CKTGSHNQC(SEQ ID NO:9)、CMGPSSMLC(SEQ ID NO:10)、CTDPNQLQC(SEQ ID NO:11)或CSTHFIDTC(SEQ ID NO:12)。
4.根据权利要求1所述的组合物,其中所述氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。
5.根据权利要求4所述的组合物,其中所述肽为包含Cys-Cys二硫键的环肽。
6.根据权利要求1所述的组合物,其中所述组合物能够穿透所述活非人类动物细胞的细胞膜。
7.根据权利要求1所述的组合物,其中所述组合物能够穿透所述活人类细胞的细胞膜。
8.根据权利要求1所述的组合物,其中所述组合物能够穿透活表皮或真皮细胞的细胞膜。
9.根据权利要求1所述的组合物,其中所述组合物能够穿透活免疫细胞的细胞膜。
10.根据权利要求1所述的组合物,其中所述活性剂包括大分子。
11.根据权利要求10所述的组合物,其中所述大分子包括蛋白质。
12.根据权利要求11所述的组合物,其中所述蛋白质包括含有至少一个互补位的抗体或其片段。
13.根据权利要求10所述的组合物,其中所述大分子包括核酸。
14.根据权利要求13所述的组合物,其中所述核酸为DNA。
15.根据权利要求13所述的组合物,其中所述核酸为RNA。
16.根据权利要求15所述的组合物,其中所述RNA为干扰RNA。
17.根据权利要求16所述的组合物,其中所述干扰RNA为shRNA。
18.根据权利要求16所述的组合物,其中所述干扰RNA为miRNA。
19.根据权利要求16所述的组合物,其中所述干扰RNA为siRNA。
20.根据权利要求19所述的组合物,其中所述siRNA为IL-10siRNA。
21.根据权利要求19所述的组合物,其中所述siRNA为CD86siRNA。
22.根据权利要求19所述的组合物,其中所述siRNA为KRT6asiRNA。
23.根据权利要求19所述的组合物,其中所述siRNA为TNFR1siRNA。
24.根据权利要求19所述的组合物,其中所述siRNA为TACEsiRNA。
25.根据权利要求19所述的组合物,其中所述siRNA为突变特异性siRNA。
26.根据权利要求1所述的组合物,其中所述活性剂为药物化合物。
27.根据权利要求1所述的组合物,其中所述活性剂包括可检测剂。
28.根据权利要求27所述的组合物,其中所述可检测剂包括荧光标记。
29.根据权利要求27所述的组合物,其中所述可检测剂包括放射性标记。
30.根据权利要求1所述的组合物,其中所述活性剂为纳米粒子。
31.根据权利要求1所述的组合物,其中所述活性剂为低分子量化合物。
32.根据权利要求1所述的组合物,其中所述活性剂为IL-10生物活性抑制剂。
33.根据权利要求32所述的组合物,其中所述活性剂选自IL-10siRNA以及结合IL-10的抗体或其片段。
34.根据权利要求1所述的组合物,其中所述肽偶联到所述活性剂。
35.根据权利要求1所述的组合物,其中所述肽偶联到包含所述活性剂的活性剂载体。
36.根据权利要求35所述的组合物,其中所述活性剂载体为脂质体。
37.根据权利要求35所述的组合物,其中所述活性剂载体为纳米粒子。
38.根据权利要求35所述的组合物,其中所述活性剂载体为聚合物胶束。
39.一种组合物,其包含包括氨基酸序列TGSTQHQ(SEQ IDNO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽,其中所述肽与活性剂或包含所述活性剂的活性剂载体缔合,其中所述缔合由疏水、静电或范德华相互作用产生,并且其中所述组合物能够在与角质层(SC)接触时穿透所述角质层或与细胞接触时穿透所述细胞。
40.根据权利要求39所述的组合物,其中所述组合物能够穿透所述SC层以及穿透所述细胞。
41.根据权利要求39所述的组合物,其中所述氨基酸序列包括CTGSTQHQC(SEQ ID NO:7)、CHSALTKHC(SEQ ID NO:8)、CKTGSHNQC(SEQ ID NO:9)、CMGPSSMLC(SEQ ID NO:10)、CTDPNQLQC(SEQ ID NO:11)或CSTHFIDTC(SEQ ID NO:12)。
42.根据权利要求39所述的组合物,其中所述氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。
43.根据权利要求42所述的组合物,其中所述肽为包含Cys-Cys二硫键的环肽。
44.一种分离肽,其包含选自以下序列之一的氨基酸序列:ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)和ACSTHFIDTCG(SEQ ID NO:18)。
45.根据权利要求44所述的分离肽,其中所述肽包含ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)和ACSTHFIDTCG(SEQ ID NO:18)一者或多者的重复单元。
46.根据权利要求45所述的分离肽,其中所述单元重复2至50次。
47.根据权利要求45所述的分离肽,其中每个单元由插入肽序列分离。
48.根据权利要求44所述的分离肽,其中所述肽为包含Cys-Cys二硫键的环肽。
49.一种分离多肽,其包含TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ IDNO:4)、TDPNQLQ(SEQ ID NO:5)和STHFIDT(SEQ ID NO:6)一者或多者的重复单元。
50.根据权利要求49所述的分离肽,其中所述单元重复2至50次。
51.根据权利要求49所述的分离肽,其中每个单元由插入肽序列分离。
52.一种分离多肽,其基本上由TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)和STHFIDT(SEQ ID NO:6)一者或多者的重复单元组成。
53.一种将活性剂递送至受试者的方法,其包括:向受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ IDNO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中所述肽偶联到活性剂或包含所述活性剂的活性剂载体,并且其中所述组合物能够穿透所述受试者的角质层(SC)或穿透所述受试者的细胞。
54.根据权利要求53所述的方法,其中所述组合物能够穿透所述受试者的SC以及穿透所述受试者的细胞。
55.根据权利要求53所述的方法,其中所述施用为局部施用。
56.根据权利要求53所述的方法,其中所述氨基酸序列包括CTGSTQHQC(SEQ ID NO:7)、CHSALTKHC(SEQ ID NO:8)、CKTGSHNQC(SEQ ID NO:9)、CMGPSSMLC(SEQ ID NO:10)、CTDPNQLQC(SEQ ID NO:11)或CSTHFIDTC(SEQ ID NO:12)。
57.根据权利要求56所述的方法,其中所述氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。
58.根据权利要求57所述的方法,其中所述肽为包含Cys-Cys二硫键的环肽。
59.根据权利要求53所述的方法,其中所述组合物能够穿透所述活非人类动物细胞的细胞膜。
60.根据权利要求53所述的方法,其中所述组合物能够穿透所述活人类细胞的细胞膜。
61.根据权利要求53所述的方法,其中所述组合物能够穿透所述活表皮或真皮细胞的细胞膜。
62.根据权利要求53所述的方法,其中所述组合物能够穿透所述活免疫细胞的细胞膜。
63.根据权利要求53所述的方法,其中所述活性剂包括大分子。
64.根据权利要求63所述的方法,其中所述大分子包括蛋白质。
65.根据权利要求64所述的方法,其中所述蛋白质包括含有至少一个互补位的抗体或其片段。
66.根据权利要求64所述的方法,其中所述大分子包括核酸。
67.根据权利要求66所述的方法,其中所述核酸为DNA。
68.根据权利要求66所述的方法,其中所述核酸为RNA。
69.根据权利要求68所述的方法,其中所述RNA为干扰RNA。
70.根据权利要求69所述的方法,其中所述干扰RNA为shRNA。
71.根据权利要求69所述的方法,其中所述干扰RNA为miRNA。
72.根据权利要求69所述的方法,其中所述干扰RNA为siRNA。
73.根据权利要求72所述的方法,其中所述siRNA为IL-10siRN。
74.根据权利要求72所述的方法,其中所述siRNA为CD86siRNA。
75.根据权利要求72所述的方法,其中所述siRNA为KRT6asiRNA。
76.根据权利要求72所述的方法,其中所述siRNA为TNFR1siRNA。
77.根据权利要求72所述的方法,其中所述siRNA为TACEsiRNA。
78.根据权利要求72所述的方法,其中所述siRNA为突变特异性siRNA。
79.根据权利要求53所述的方法,其中所述活性剂为药物化合物。
80.根据权利要求53所述的方法,其中所述活性剂包括可检测剂。
81.根据权利要求53所述的方法,其中所述可检测剂包括荧光标记。
82.根据权利要求53所述的方法,其中所述可检测剂包括放射性标记。
83.根据权利要求53所述的方法,其中所述活性剂为纳米粒子。
84.根据权利要求53所述的方法,其中所述活性剂为低分子量化合物。
85.根据权利要求1所述的方法,其中所述活性剂为IL-10生物活性抑制剂。
86.根据权利要求85所述的方法,其中所述活性剂选自IL-10siRNA以及结合IL-10的抗体或其片段。
87.根据权利要求53所述的方法,其中所述肽偶联到所述活性剂。
88.根据权利要求53所述的方法,其中所述肽偶联到包含所述活性剂的活性剂载体。
89.根据权利要求88所述的方法,其中所述活性剂载体为脂质体。
90.根据权利要求88所述的方法,其中所述活性剂载体为纳米粒子。
91.根据权利要求88所述的方法,其中所述活性剂载体为聚合物胶束。
92.一种将活性剂递送至受试者的方法,其包括:向受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ IDNO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中所述肽与活性剂或包含所述活性剂的活性剂载体缔合,其中所述缔合由疏水、静电或范德华相互作用产生,并且其中所述组合物能够穿透所述受试者的角质层(SC)或穿透所述受试者的细胞。
93.根据权利要求92所述的方法,其中所述组合物能够穿透所述受试者的SC以及穿透所述受试者的细胞。
94.根据权利要求92所述的方法,其中所述施用为局部施用。
95.根据权利要求92所述的方法,其中所述氨基酸序列包括CTGSTQHQC(SEQ ID NO:7)、CHSALTKHC(SEQ ID NO:8)、CKTGSHNQC(SEQ ID NO:9)、CMGPSSMLC(SEQ ID NO:10)、CTDPNQLQC(SEQ ID NO:11)或CSTHFIDTC(SEQ ID NO:12)。
96.根据权利要求95所述的方法,其中所述氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。
97.根据权利要求96所述的方法,其中所述肽为包含Cys-Cys二硫键的环肽。
98.一种治疗患有皮肤疾病的受试者的方法,其包括:向所述受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ IDNO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中所述肽偶联到皮肤病活性剂或包含所述活性剂的皮肤病活性剂载体,并且其中所述组合物能够穿透所述受试者的角质层(SC)或穿透所述受试者的细胞。
99.根据权利要求98所述的方法,其中所述组合物能够穿透所述受试者的SC以及穿透所述受试者的细胞。
100.根据权利要求98所述的方法,其中所述施用为局部施用。
101.根据权利要求98所述的方法,其中所述氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。
102.根据权利要求101所述的方法,其中所述肽为包含Cys-Cys二硫键的环肽。
103.一种治疗患有皮肤疾病的受试者的方法,其包括:向受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ IDNO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中所述肽与皮肤病活性剂或包含所述活性剂的皮肤病活性剂载体缔合,其中所述缔合由疏水、静电或范德华相互作用产生,并且其中所述组合物能够穿透所述受试者的角质层(SC)或穿透所述受试者的细胞。
104.根据权利要求103所述的方法,其中所述组合物能够穿透所述受试者的SC以及穿透所述受试者的细胞。
105.根据权利要求103所述的方法,其中所述施用为局部施用。
106.根据权利要求103所述的方法,其中所述氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。
107.根据权利要求106所述的方法,其中所述肽为包含Cys-Cys二硫键的环肽。
108.一种治疗患有、疑似患有或易患至少部分地由mRNA的表达所导致的疾病的受试者的方法,其包括向所述受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中所述肽偶联到靶向所述mRNA的干扰RNA或包含所述干扰RNA的载体,其中所述组合物能够穿透所述受试者的角质层(SC)或所述受试者的细胞,并且其中所述mRNA的表达因而得以减弱。
109.根据权利要求108所述的方法,其中所述组合物能够穿透所述受试者的SC以及穿透所述受试者的细胞。
110.根据权利要求108所述的方法,其中所述施用为局部施用。
111.根据权利要求108所述的方法,其中所述氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。
112.根据权利要求111所述的方法,其中所述肽为包含Cys-Cys二硫键的环肽。
113.一种治疗患有、疑似患有或易患至少部分地由mRNA的表达所导致的疾病的受试者的方法,其包括向所述受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中所述肽与靶向所述mRNA的干扰RNA或包含所述干扰RNA的载体缔合,其中所述缔合由疏水、静电或范德华相互作用产生,其中所述组合物能够穿透所述受试者的角质层(SC)或所述受试者的细胞,并且其中所述mRNA的表达因而得以减弱。
114.根据权利要求113所述的方法,其中所述组合物能够穿透所述受试者的SC以及穿透所述受试者的细胞。
115.根据权利要求113所述的方法,其中所述施用为局部施用。
116.根据权利要求113所述的方法,其中所述氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。
117.根据权利要求116所述的方法,其中所述肽为包含Cys-Cys二硫键的环肽。
118.一种减弱对其有需要的受试者中mRNA表达的方法,其包括向所述受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中所述肽偶联到靶向所述mRNA的siRNA或包含靶向所述mRNA的siRNA的载体,其中所述组合物能够穿透所述受试者的角质层(SC)或所述受试者的细胞,并且其中所述mRNA的表达因而得以减弱。
119.根据权利要求118所述的方法,其中所述mRNA为IL-10mRNA并且所述siRNA为IL-10siRNA。
120.根据权利要求118所述的方法,其中所述mRNA为CD86mRNA并且所述siRNA为CD86 siRNA。
121.根据权利要求118所述的方法,其中所述mRNA为KRT6amRNA并且所述siRNA为KRT6a siRNA。
122.根据权利要求118所述的方法,其中所述mRNA为TNFR1mRNA并且所述siRNA为TNFR1 siRNA。
123.根据权利要求118所述的方法,其中所述mRNA为TACEmRNA并且所述siRNA为TACE siRNA。
124.根据权利要求118所述的方法,其中所述组合物能够穿透所述受试者的SC以及穿透所述受试者的细胞。
125.根据权利要求118所述的方法,其中所述施用为局部施用。
126.根据权利要求118所述的方法,其中所述氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。
127.根据权利要求126所述的方法,其中所述肽为包含Cys-Cys二硫键的环肽。
128.一种减弱对其有需要的受试者中mRNA表达的方法,其包括向所述受试者施用包含包括氨基酸序列TGSTQHQ(SEQ ID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)的肽的组合物,其中所述肽与靶向所述mRNA的siRNA或包含靶向所述mRNA的siRNA的载体缔合,其中所述缔合由疏水、静电或范德华相互作用产生,其中所述组合物能够穿透所述受试者的角质层(SC)或所述受试者的细胞,并且其中所述mRNA的表达因而得以减弱。
129.根据权利要求128所述的方法,其中所述mRNA为IL-10mRNA并且所述siRNA为IL-10 siRNA。
130.根据权利要求128所述的方法,其中所述mRNA为CD86mRNA并且所述siRNA为CD86 siRNA。
131.根据权利要求128所述的方法,其中所述mRNA为KRT6amRNA并且所述siRNA为KRT6a siRNA。
132.根据权利要求128所述的方法,其中所述mRNA为TNFR1mRNA并且所述siRNA为TNFR1 siRNA。
133.根据权利要求128所述的方法,其中所述mRNA为TACEmRNA并且所述siRNA为TACE siRNA。
134.根据权利要求128所述的方法,其中所述组合物能够穿透所述受试者的SC以及穿透所述受试者的细胞。
135.根据权利要求128所述的方法,其中所述施用为局部施用。
136.根据权利要求128所述的方法,其中所述氨基酸序列包括ACTGSTQHQCG(SEQ ID NO:13)、ACHSALTKHCG(SEQ IDNO:14)、ACKTGSHNQCG(SEQ ID NO:15)、ACMGPSSMLCG(SEQID NO:16)、ACTDPNQLQCG(SEQ ID NO:17)或ACSTHFIDTCG(SEQ ID NO:18)。
137.根据权利要求136所述的方法,其中所述肽为包含Cys-Cys二硫键的环肽。
138.一种组合物,其包含基本上由氨基酸序列TGSTQHQ(SEQID NO:1)、HSALTKH(SEQ ID NO:2)、KTGSHNQ(SEQ ID NO:3)、MGPSSML(SEQ ID NO:4)、TDPNQLQ(SEQ ID NO:5)或STHFIDT(SEQ ID NO:6)组成的肽,其中所述肽偶联到活性剂或包含所述活性剂的活性剂载体,并且其中所述组合物能够在与角质层(SC)接触时穿透所述角质层或与细胞接触时穿透所述细胞。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US41188410P | 2010-11-09 | 2010-11-09 | |
| US61/411,884 | 2010-11-09 | ||
| US201161527574P | 2011-08-25 | 2011-08-25 | |
| US61/527,574 | 2011-08-25 | ||
| US201161528036P | 2011-08-26 | 2011-08-26 | |
| US61/528,036 | 2011-08-26 | ||
| PCT/US2011/054967 WO2012064429A2 (en) | 2010-11-09 | 2011-10-05 | Skin permeating and cell entering (space) peptides and methods of use thereof |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN103201386A true CN103201386A (zh) | 2013-07-10 |
Family
ID=46051476
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2011800532510A Pending CN103201386A (zh) | 2010-11-09 | 2011-10-05 | 皮肤穿透及细胞进入(space)肽及其使用方法 |
Country Status (8)
| Country | Link |
|---|---|
| US (4) | US8518871B2 (zh) |
| EP (1) | EP2638162B1 (zh) |
| JP (1) | JP2014500867A (zh) |
| KR (1) | KR20130139254A (zh) |
| CN (1) | CN103201386A (zh) |
| AU (1) | AU2011326732B2 (zh) |
| CA (1) | CA2811113A1 (zh) |
| WO (1) | WO2012064429A2 (zh) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105491982A (zh) * | 2013-08-12 | 2016-04-13 | 3M创新有限公司 | 用于增强透皮递送的肽 |
| CN105504066A (zh) * | 2016-01-16 | 2016-04-20 | 广州市科玮生物技术有限公司 | 一种融合蛋白在化妆品中的应用 |
| CN111803652A (zh) * | 2020-08-04 | 2020-10-23 | 北京瀚梅生物科技有限公司 | 治疗痤疮的化合物在制备治疗痤疮的药物组合物或化妆品组合物中的用途 |
| CN113943778A (zh) * | 2020-07-17 | 2022-01-18 | 通用电气医疗集团股份有限公司 | 用于核酸检测的分子探针及其制备方法和用途 |
| CN114315960A (zh) * | 2021-12-31 | 2022-04-12 | 深圳市维琪医药研发有限公司 | 一种经修饰的肽及其美容组合物或药用组合物和用途 |
Families Citing this family (47)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8834423B2 (en) | 2009-10-23 | 2014-09-16 | University of Pittsburgh—of the Commonwealth System of Higher Education | Dissolvable microneedle arrays for transdermal delivery to human skin |
| EP3578205A1 (en) | 2010-08-06 | 2019-12-11 | ModernaTX, Inc. | A pharmaceutical formulation comprising engineered nucleic acids and medical use thereof |
| RU2013120302A (ru) | 2010-10-01 | 2014-11-20 | Модерна Терапьютикс, Инк. | Сконструированные нуклеиновые кислоты и способы их применения |
| KR20130139254A (ko) * | 2010-11-09 | 2013-12-20 | 더 리젠츠 오브 더 유니버시티 오브 캘리포니아 | 피부 침투 및 세포 진입(space) 펩타이드 및 그의 사용방법 |
| JP2014511687A (ja) | 2011-03-31 | 2014-05-19 | モデルナ セラピューティクス インコーポレイテッド | 工学操作された核酸の送達および製剤 |
| US9464124B2 (en) | 2011-09-12 | 2016-10-11 | Moderna Therapeutics, Inc. | Engineered nucleic acids and methods of use thereof |
| US9428535B2 (en) | 2011-10-03 | 2016-08-30 | Moderna Therapeutics, Inc. | Modified nucleosides, nucleotides, and nucleic acids, and uses thereof |
| LT2791160T (lt) | 2011-12-16 | 2022-06-10 | Modernatx, Inc. | Modifikuotos mrnr sudėtys |
| WO2013112488A2 (en) * | 2012-01-23 | 2013-08-01 | Kythera Biopharmaceuticals, Inc. | Dermal filling compositions and methods |
| US9572897B2 (en) | 2012-04-02 | 2017-02-21 | Modernatx, Inc. | Modified polynucleotides for the production of cytoplasmic and cytoskeletal proteins |
| US9283287B2 (en) | 2012-04-02 | 2016-03-15 | Moderna Therapeutics, Inc. | Modified polynucleotides for the production of nuclear proteins |
| US9254311B2 (en) | 2012-04-02 | 2016-02-09 | Moderna Therapeutics, Inc. | Modified polynucleotides for the production of proteins |
| US9192651B2 (en) | 2012-04-02 | 2015-11-24 | Moderna Therapeutics, Inc. | Modified polynucleotides for the production of secreted proteins |
| EP4112112A1 (en) | 2012-05-01 | 2023-01-04 | University of Pittsburgh - Of the Commonwealth System of Higher Education | Tip-loaded microneedle arrays for transdermal insertion |
| JP2015523966A (ja) * | 2012-05-16 | 2015-08-20 | アーディジェン, エルエルシー | 線維症および炎症状態を処置するための多標的調整 |
| KR101329411B1 (ko) | 2012-05-31 | 2013-11-14 | 주식회사 엘지생활건강 | 피부투과성 펩타이드 |
| WO2014081507A1 (en) | 2012-11-26 | 2014-05-30 | Moderna Therapeutics, Inc. | Terminally modified rna |
| CN103897043A (zh) * | 2012-12-28 | 2014-07-02 | 天津药物研究院 | 一种穿膜多肽连接拉帕替尼的制备及应用 |
| WO2014123543A2 (en) * | 2013-02-11 | 2014-08-14 | Convoy Therapeutics | Skin permeating and cell entering (space) peptides and methods of use therefor |
| US20140227174A1 (en) * | 2013-02-11 | 2014-08-14 | The Regents Of The University Of California | Skin permeating and cell entering (space) peptides and methods of use therefor |
| US8980864B2 (en) | 2013-03-15 | 2015-03-17 | Moderna Therapeutics, Inc. | Compositions and methods of altering cholesterol levels |
| EP3052106A4 (en) | 2013-09-30 | 2017-07-19 | ModernaTX, Inc. | Polynucleotides encoding immune modulating polypeptides |
| CA2926218A1 (en) | 2013-10-03 | 2015-04-09 | Moderna Therapeutics, Inc. | Polynucleotides encoding low density lipoprotein receptor |
| US9321821B2 (en) | 2013-11-14 | 2016-04-26 | Lg Household & Health Care Ltd. | Cosmetic composition for improving skin conditions comprising fusion protein |
| KR101602690B1 (ko) * | 2013-11-14 | 2016-03-11 | 주식회사 엘지생활건강 | 염기성 섬유모세포성장인자 융합단백질을 포함하는 피부개선용 화장료 조성물 |
| WO2016033314A1 (en) * | 2014-08-27 | 2016-03-03 | The Regents Of The University Of California | Skin penetrating peptides (spps) and methods of use therefor |
| WO2016048246A1 (en) | 2014-09-25 | 2016-03-31 | Nanyang Technological University | Targeting of melanocytes for delivering therapeutic or diagnostic agents using protein nanocages |
| WO2016071814A1 (en) | 2014-11-04 | 2016-05-12 | Università Degli Studi Di Milano | A promoter for cutaneous absorption of active ingredients having peptidic structure |
| US10441768B2 (en) | 2015-03-18 | 2019-10-15 | University of Pittsburgh—of the Commonwealth System of Higher Education | Bioactive components conjugated to substrates of microneedle arrays |
| EP3336098B1 (en) * | 2015-09-10 | 2021-08-11 | IUCF-HYU (Industry-University Cooperation Foundation Hanyang University) | Skin permeable peptide and method for using same |
| WO2017043920A1 (ko) * | 2015-09-10 | 2017-03-16 | 한양대학교 산학협력단 | 피부 투과성 펩티드 및 그 이용방법 |
| WO2017048812A1 (en) * | 2015-09-15 | 2017-03-23 | The Regents Of The University Of California | Skin-penetrating peptides and compositions and methods of use thereof |
| WO2017066768A1 (en) | 2015-10-16 | 2017-04-20 | University Of Pittsburgh-Of The Commonwealth System Of Higher Education | Mullti-component biio-active drug delivery and controlled release to the skin by microneedle array devices |
| CN108350457B (zh) | 2015-10-30 | 2021-10-01 | 株式会社博纳克 | 稳定地含有抑制TGF-β1基因的表达的单链核酸分子的组合物 |
| WO2017082690A1 (ko) * | 2015-11-12 | 2017-05-18 | 주식회사 펩트론 | 미백, 피부 탄력, 주름 개선 및 상처치유 활성을 갖는 다기능성 피부투과 펩타이드 |
| US11744889B2 (en) | 2016-01-05 | 2023-09-05 | University of Pittsburgh—of the Commonwealth System of Higher Education | Skin microenvironment targeted delivery for promoting immune and other responses |
| KR20180105199A (ko) * | 2016-01-23 | 2018-09-27 | 앰퍼샌드 바이오파마슈티컬스, 인크. | 활성 제제의 경피 전달 증대 |
| MX2019012385A (es) * | 2017-04-17 | 2022-03-15 | Ampersand Biopharmaceuticals Llc | Administración parenteral no sistémica de agentes amortiguadores para inhibir la metástasis de tumores sólidos, hiperpigmentación y gota. |
| KR102083976B1 (ko) * | 2017-12-18 | 2020-03-03 | 주식회사 엘지생활건강 | 혈관내피세포 성장인자의 융합 단백질을 포함하는 피부개선용 화장료 조성물 |
| KR102083978B1 (ko) * | 2017-12-18 | 2020-03-03 | 주식회사 엘지생활건강 | 혈소판유래 성장인자 a서브유닛의 융합 단백질을 포함하는 피부개선용 화장료 조성물 |
| JP2020534285A (ja) | 2017-09-15 | 2020-11-26 | アンパサンド バイオファーマシューティカルズ インコーポレイテッドAmpersand Biopharmaceuticals Inc. | 投与および処置の方法 |
| GB2566516A (en) | 2017-09-15 | 2019-03-20 | Univ Oxford Innovation Ltd | Electrochemical recognition and quantification of cytochrome c oxidase expression in bacteria |
| US10905738B2 (en) | 2018-07-05 | 2021-02-02 | Biozeus Desenvolvimento De Produtos Biofarmacêuticos | Synthetic peptides, prodrugs, pharmaceutical compositions and uses |
| CN113710225A (zh) | 2019-04-19 | 2021-11-26 | 范德生物公司 | 活性剂在皮肤内的递送和保留 |
| WO2021113410A1 (en) * | 2019-12-02 | 2021-06-10 | Ampersand Biopharmaceuticals, Inc. | Transdermal penetrant formulations for vitamins, minerals and supplements |
| KR102301572B1 (ko) * | 2020-02-06 | 2021-09-10 | 인천대학교 산학협력단 | 신규한 핵산 분자 전달용 조성물 및 그 용도 |
| KR20230135586A (ko) | 2021-01-24 | 2023-09-25 | 마이클 데이비드 포레스트 | Atp 합성효소 억제제 - 미용 및 치료 용도 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20090186802A1 (en) * | 2005-12-16 | 2009-07-23 | Diatos | Cell Penetrating Peptide Conjugates for Delivering of Nucleic Acids into a Cell |
| CN101812439A (zh) * | 2009-02-25 | 2010-08-25 | 张舒羽 | 一种透皮结构域及其衍生的具有透皮作用的融合蛋白和其制备方法 |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CH624011A5 (zh) | 1977-08-05 | 1981-07-15 | Battelle Memorial Institute | |
| US5077057A (en) | 1989-04-05 | 1991-12-31 | The Regents Of The University Of California | Preparation of liposome and lipid complex compositions |
| US6083539A (en) | 1994-12-16 | 2000-07-04 | Sakuma Ebisu Kabushiki Kaisha | Buckwheat starch syrup, method for preparing the same, and foods containing the same |
| US6747137B1 (en) * | 1998-02-13 | 2004-06-08 | Genome Therapeutics Corporation | Nucleic acid sequences relating to Candida albicans for diagnostics and therapeutics |
| US20090070897A1 (en) * | 2006-01-12 | 2009-03-12 | Goldman Barry S | Genes and uses for plant improvement |
| JP4596391B2 (ja) * | 2005-02-10 | 2010-12-08 | 国立大学法人大阪大学 | 細胞透過性ペプチド |
| US7659252B2 (en) | 2005-09-15 | 2010-02-09 | Novomed Technologies, Inc. (Shanghai) | Transdermal delivery peptides and method of use thereof |
| WO2007035474A2 (en) | 2005-09-15 | 2007-03-29 | Novomed Technologies, Inc. (Shanghai) | Transdermal delivery peptides and method of use thereof |
| JP2007143454A (ja) * | 2005-11-25 | 2007-06-14 | Toray Ind Inc | 細胞膜通過性ペプチド |
| GB0606415D0 (en) | 2006-03-31 | 2006-05-10 | Univ Southampton | Topical drug delivery |
| CA2671850A1 (en) | 2006-12-08 | 2008-06-19 | Massachusetts Institute Of Technology | Delivery of nanoparticles and/or agents to cells |
| JP2008200011A (ja) * | 2007-02-22 | 2008-09-04 | Toray Ind Inc | 細胞内移行性ペプチド、それを含有する医薬組成物及びその使用方法 |
| AU2008295509A1 (en) | 2007-08-29 | 2009-03-12 | Tufts University | Methods of making and using a cell penetrating peptide for enhanced delivery of nucleic acids, proteins, drugs, and adenovirus to tissues and cells, and compositions and kits |
| US20090233993A1 (en) * | 2008-03-06 | 2009-09-17 | Burnham Institute For Medical Research | Compositions and methods for inhibiting gsk3 activity and uses thereof |
| EP2355852A4 (en) * | 2008-09-16 | 2015-06-24 | Ge Healthcare Bio Sciences Ab | CHEMICALLY MODIFIED CELL-PENETRATING PEPTIDES FOR IMPROVED DELIVERY OF GENE MODULATING COMPOUNDS |
| US8389481B2 (en) * | 2008-11-12 | 2013-03-05 | University Of Medicine And Dentistry Of New Jersey | Glutamate-enhanced cell-penetrating peptides and methods of using same |
| EP2421505A4 (en) * | 2009-04-22 | 2014-01-01 | Univ Texas | HYDROGELS FOR COMBINATORY ADMINISTRATION OF BIOMOLECULES MODULATING IMMUNITY |
| WO2010129023A2 (en) | 2009-04-28 | 2010-11-11 | President And Fellows Of Harvard College | Supercharged proteins for cell penetration |
| KR20130139254A (ko) | 2010-11-09 | 2013-12-20 | 더 리젠츠 오브 더 유니버시티 오브 캘리포니아 | 피부 침투 및 세포 진입(space) 펩타이드 및 그의 사용방법 |
| JP2014511687A (ja) | 2011-03-31 | 2014-05-19 | モデルナ セラピューティクス インコーポレイテッド | 工学操作された核酸の送達および製剤 |
-
2011
- 2011-10-05 KR KR1020137008413A patent/KR20130139254A/ko not_active Application Discontinuation
- 2011-10-05 EP EP11839394.1A patent/EP2638162B1/en not_active Not-in-force
- 2011-10-05 AU AU2011326732A patent/AU2011326732B2/en not_active Expired - Fee Related
- 2011-10-05 CN CN2011800532510A patent/CN103201386A/zh active Pending
- 2011-10-05 JP JP2013537678A patent/JP2014500867A/ja active Pending
- 2011-10-05 US US13/253,796 patent/US8518871B2/en active Active
- 2011-10-05 CA CA2811113A patent/CA2811113A1/en not_active Abandoned
- 2011-10-05 WO PCT/US2011/054967 patent/WO2012064429A2/en active Application Filing
-
2013
- 2013-07-26 US US13/952,525 patent/US8791062B2/en active Active
-
2014
- 2014-04-25 US US14/262,453 patent/US9441014B2/en active Active
-
2016
- 2016-08-04 US US15/228,852 patent/US20170173173A1/en not_active Abandoned
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20090186802A1 (en) * | 2005-12-16 | 2009-07-23 | Diatos | Cell Penetrating Peptide Conjugates for Delivering of Nucleic Acids into a Cell |
| CN101812439A (zh) * | 2009-02-25 | 2010-08-25 | 张舒羽 | 一种透皮结构域及其衍生的具有透皮作用的融合蛋白和其制备方法 |
Non-Patent Citations (4)
| Title |
|---|
| HEITZ ET AL.: "Twenty years of cell-penetrating peptides:from molecular mechanisms to therapeutics", 《BRITISH JOURNAL OF PHARMACOLOGY》 * |
| HSU ET AL: "Peptides as Penetration Enhancers for Transdermal Drug Delivery", 《2009 AAPS ANNUAL MEETING AND EXPOSITION》 * |
| YEU-CHUN KIM ET AL.: "Transdermal delivery enhanced by magainin pore-forming peptide", 《JOURNAL OF CONTROLLED RELEASE》 * |
| 陈勇平: "通过噬菌体文库鉴定透皮输运蛋白质肽", 《中国博士学位论文全文数据库 医药卫生科技辑》 * |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN105491982A (zh) * | 2013-08-12 | 2016-04-13 | 3M创新有限公司 | 用于增强透皮递送的肽 |
| CN105491982B (zh) * | 2013-08-12 | 2019-09-10 | 3M创新有限公司 | 用于增强透皮递送的肽 |
| CN105504066A (zh) * | 2016-01-16 | 2016-04-20 | 广州市科玮生物技术有限公司 | 一种融合蛋白在化妆品中的应用 |
| CN113943778A (zh) * | 2020-07-17 | 2022-01-18 | 通用电气医疗集团股份有限公司 | 用于核酸检测的分子探针及其制备方法和用途 |
| CN111803652A (zh) * | 2020-08-04 | 2020-10-23 | 北京瀚梅生物科技有限公司 | 治疗痤疮的化合物在制备治疗痤疮的药物组合物或化妆品组合物中的用途 |
| CN111803652B (zh) * | 2020-08-04 | 2021-09-14 | 南通康是美生物科技有限公司 | 治疗痤疮的化合物在制备治疗痤疮的药物组合物或化妆品组合物中的用途 |
| CN114315960A (zh) * | 2021-12-31 | 2022-04-12 | 深圳市维琪医药研发有限公司 | 一种经修饰的肽及其美容组合物或药用组合物和用途 |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2011326732B2 (en) | 2016-07-21 |
| KR20130139254A (ko) | 2013-12-20 |
| US8518871B2 (en) | 2013-08-27 |
| EP2638162B1 (en) | 2016-08-10 |
| US20120128756A1 (en) | 2012-05-24 |
| US20170173173A1 (en) | 2017-06-22 |
| AU2011326732A1 (en) | 2013-05-02 |
| US8791062B2 (en) | 2014-07-29 |
| US9441014B2 (en) | 2016-09-13 |
| CA2811113A1 (en) | 2012-05-18 |
| EP2638162A2 (en) | 2013-09-18 |
| WO2012064429A2 (en) | 2012-05-18 |
| US20150025221A1 (en) | 2015-01-22 |
| WO2012064429A3 (en) | 2012-08-02 |
| EP2638162A4 (en) | 2014-05-28 |
| US20140161871A1 (en) | 2014-06-12 |
| JP2014500867A (ja) | 2014-01-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN103201386A (zh) | 皮肤穿透及细胞进入(space)肽及其使用方法 | |
| Accardo et al. | Peptide-modified liposomes for selective targeting of bombesin receptors overexpressed by cancer cells: a potential theranostic agent | |
| Kang et al. | A brain tumor-homing tetra-peptide delivers a nano-therapeutic for more effective treatment of a mouse model of glioblastoma | |
| CN108473555A (zh) | 条件活性多肽 | |
| KR101647804B1 (ko) | 신규 세포투과 펩타이드 및 이의 용도 | |
| CN106619515A (zh) | 脂质体组合物及其用途 | |
| CN108289966A (zh) | 用于减少转移的方法和组合物 | |
| CN110121506A (zh) | 条件活性多肽及产生它们的方法 | |
| CN108473541A (zh) | 通过受体介导的化学疗法治疗癌症的肽化合物和肽缀合物 | |
| Noguchi et al. | Effects of lyophilization of arginine-rich cell-penetrating peptide-modified extracellular vesicles on intracellular delivery | |
| US9687563B2 (en) | Ph-sensitive peptides and their nanoparticles for drug delivery | |
| CN103626846B (zh) | 与MDSCs特异性结合的配体多肽及药物输送系统 | |
| Ye et al. | Self-reinforced cancer targeting (SRCT) depending on reciprocally enhancing feedback between targeting and therapy | |
| JP6009154B2 (ja) | 細胞膜透過型ホウ素ペプチド | |
| US10046022B2 (en) | Synthetic peptide that increases radiosensitivity of tumor cells and use of same | |
| EP2108698A1 (en) | Vascular endothelial cell-binding peptide | |
| US20140227174A1 (en) | Skin permeating and cell entering (space) peptides and methods of use therefor | |
| WO2014123543A2 (en) | Skin permeating and cell entering (space) peptides and methods of use therefor | |
| US20170258930A1 (en) | Skin penetrating peptides (spps) and methods of use therefor | |
| CN108752426A (zh) | 带中性电荷的细胞穿透肽及作为细胞内运送载体的用途 | |
| CN108727472A (zh) | 带负电荷的细胞穿透肽及作为细胞内运送载体的用途 | |
| CN114805594B (zh) | 一种能够透过生物屏障且聚集核周的动力蛋白结合肽及其应用 | |
| JP2016204378A (ja) | 細胞膜透過型ホウ素ペプチド | |
| WO2024026444A1 (en) | Methods and compositions for using leucine zippers for crosslinking of cells and drug carriers | |
| Lebl | Peptides Across the Pacific: Proceedings of the 23rd American Peptide Symposium and the 6th International Peptide Symposium |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: DE Ref document number: 1187074 Country of ref document: HK |
|
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |
Application publication date: 20130710 |
|
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: WD Ref document number: 1187074 Country of ref document: HK |