CN102807520A - 离子液体及使用离子液体的蓄电装置 - Google Patents
离子液体及使用离子液体的蓄电装置 Download PDFInfo
- Publication number
- CN102807520A CN102807520A CN2012101745667A CN201210174566A CN102807520A CN 102807520 A CN102807520 A CN 102807520A CN 2012101745667 A CN2012101745667 A CN 2012101745667A CN 201210174566 A CN201210174566 A CN 201210174566A CN 102807520 A CN102807520 A CN 102807520A
- Authority
- CN
- China
- Prior art keywords
- ionic liquid
- storage devices
- electrical storage
- general formula
- alkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000002608 ionic liquid Substances 0.000 title claims abstract description 117
- 238000003860 storage Methods 0.000 title claims abstract description 115
- -1 methoxyethyl group Chemical group 0.000 claims abstract description 85
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 27
- 150000001450 anions Chemical class 0.000 claims abstract description 20
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 claims abstract description 19
- 150000003949 imides Chemical class 0.000 claims abstract description 15
- LGRLWUINFJPLSH-UHFFFAOYSA-N methanide Chemical compound [CH3-] LGRLWUINFJPLSH-UHFFFAOYSA-N 0.000 claims abstract description 15
- 150000002500 ions Chemical class 0.000 claims description 81
- 239000008151 electrolyte solution Substances 0.000 claims description 69
- HBBGRARXTFLTSG-UHFFFAOYSA-N Lithium ion Chemical compound [Li+] HBBGRARXTFLTSG-UHFFFAOYSA-N 0.000 claims description 50
- 229910001416 lithium ion Inorganic materials 0.000 claims description 50
- 239000003990 capacitor Substances 0.000 claims description 48
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 33
- 229910052799 carbon Inorganic materials 0.000 claims description 29
- 150000003839 salts Chemical class 0.000 claims description 18
- 239000002253 acid Substances 0.000 claims description 15
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 claims description 3
- 238000002844 melting Methods 0.000 abstract description 9
- 230000008018 melting Effects 0.000 abstract description 2
- 125000004432 carbon atom Chemical group C* 0.000 abstract 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 abstract 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 abstract 1
- 239000000463 material Substances 0.000 description 49
- 239000007788 liquid Substances 0.000 description 47
- 238000000034 method Methods 0.000 description 42
- 230000000052 comparative effect Effects 0.000 description 37
- 239000007774 positive electrode material Substances 0.000 description 37
- 150000001875 compounds Chemical class 0.000 description 33
- 150000001408 amides Chemical class 0.000 description 27
- 229910052744 lithium Inorganic materials 0.000 description 27
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 26
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 24
- 239000007773 negative electrode material Substances 0.000 description 23
- 238000004519 manufacturing process Methods 0.000 description 19
- 125000002091 cationic group Chemical group 0.000 description 18
- 229910052731 fluorine Inorganic materials 0.000 description 17
- 239000011737 fluorine Substances 0.000 description 17
- 125000001453 quaternary ammonium group Chemical group 0.000 description 15
- 238000006243 chemical reaction Methods 0.000 description 13
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 13
- 238000005160 1H NMR spectroscopy Methods 0.000 description 12
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 12
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 12
- 239000004020 conductor Substances 0.000 description 12
- 239000012467 final product Substances 0.000 description 12
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 12
- 239000002904 solvent Substances 0.000 description 12
- 238000004821 distillation Methods 0.000 description 11
- 230000009467 reduction Effects 0.000 description 11
- 230000008595 infiltration Effects 0.000 description 10
- 238000001764 infiltration Methods 0.000 description 10
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical group C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 9
- 230000001590 oxidative effect Effects 0.000 description 9
- XYFCBTPGUUZFHI-UHFFFAOYSA-N Phosphine Chemical compound P XYFCBTPGUUZFHI-UHFFFAOYSA-N 0.000 description 8
- 239000000956 alloy Substances 0.000 description 8
- 239000003125 aqueous solvent Substances 0.000 description 8
- 238000005893 bromination reaction Methods 0.000 description 8
- 238000007600 charging Methods 0.000 description 8
- 229910052736 halogen Inorganic materials 0.000 description 8
- 150000002367 halogens Chemical class 0.000 description 8
- 238000003756 stirring Methods 0.000 description 8
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 7
- 238000000605 extraction Methods 0.000 description 7
- 239000012212 insulator Substances 0.000 description 7
- 239000000203 mixture Substances 0.000 description 7
- 229910052710 silicon Inorganic materials 0.000 description 7
- 239000010703 silicon Substances 0.000 description 7
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 6
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 6
- 230000009471 action Effects 0.000 description 6
- 150000001412 amines Chemical group 0.000 description 6
- 239000002585 base Substances 0.000 description 6
- 230000031709 bromination Effects 0.000 description 6
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Chemical compound C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 6
- 235000019253 formic acid Nutrition 0.000 description 6
- 238000001819 mass spectrum Methods 0.000 description 6
- 239000000758 substrate Substances 0.000 description 6
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 5
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 5
- 239000004411 aluminium Substances 0.000 description 5
- 229910052782 aluminium Inorganic materials 0.000 description 5
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 5
- 239000012752 auxiliary agent Substances 0.000 description 5
- 238000004364 calculation method Methods 0.000 description 5
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 5
- 238000000576 coating method Methods 0.000 description 5
- 239000010949 copper Substances 0.000 description 5
- 238000001035 drying Methods 0.000 description 5
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 5
- 239000013081 microcrystal Substances 0.000 description 5
- 229910052759 nickel Inorganic materials 0.000 description 5
- 229910052700 potassium Inorganic materials 0.000 description 5
- 239000011591 potassium Substances 0.000 description 5
- 239000007787 solid Substances 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- 229920003048 styrene butadiene rubber Polymers 0.000 description 5
- 229910052723 transition metal Inorganic materials 0.000 description 5
- 150000003624 transition metals Chemical class 0.000 description 5
- XPDWGBQVDMORPB-UHFFFAOYSA-N trifluoromethane acid Natural products FC(F)F XPDWGBQVDMORPB-UHFFFAOYSA-N 0.000 description 5
- IBZJNLWLRUHZIX-UHFFFAOYSA-N 1-ethyl-3-methyl-2h-imidazole Chemical compound CCN1CN(C)C=C1 IBZJNLWLRUHZIX-UHFFFAOYSA-N 0.000 description 4
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 4
- 238000003775 Density Functional Theory Methods 0.000 description 4
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 4
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 4
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 4
- 229910045601 alloy Inorganic materials 0.000 description 4
- 150000001728 carbonyl compounds Chemical class 0.000 description 4
- 229920006184 cellulose methylcellulose Polymers 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 150000002460 imidazoles Chemical class 0.000 description 4
- 239000012528 membrane Substances 0.000 description 4
- 229910000073 phosphorus hydride Inorganic materials 0.000 description 4
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 4
- 230000004044 response Effects 0.000 description 4
- 229910052708 sodium Inorganic materials 0.000 description 4
- 239000011734 sodium Substances 0.000 description 4
- 238000004544 sputter deposition Methods 0.000 description 4
- 239000010936 titanium Substances 0.000 description 4
- 238000001075 voltammogram Methods 0.000 description 4
- 238000005406 washing Methods 0.000 description 4
- KAESVJOAVNADME-UHFFFAOYSA-N 1H-pyrrole Natural products C=1C=CNC=1 KAESVJOAVNADME-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 3
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 3
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 3
- 229920002943 EPDM rubber Polymers 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 239000005030 aluminium foil Substances 0.000 description 3
- 239000012298 atmosphere Substances 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 235000013495 cobalt Nutrition 0.000 description 3
- 229910052802 copper Inorganic materials 0.000 description 3
- 230000007423 decrease Effects 0.000 description 3
- 239000003792 electrolyte Substances 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 3
- 229910052751 metal Inorganic materials 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
- 239000007769 metal material Substances 0.000 description 3
- KTQDYGVEEFGIIL-UHFFFAOYSA-N n-fluorosulfonylsulfamoyl fluoride Chemical compound FS(=O)(=O)NS(F)(=O)=O KTQDYGVEEFGIIL-UHFFFAOYSA-N 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 3
- 229920005989 resin Polymers 0.000 description 3
- 239000011347 resin Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 238000001291 vacuum drying Methods 0.000 description 3
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- 229920003026 Acene Polymers 0.000 description 2
- 229910018182 Al—Cu Inorganic materials 0.000 description 2
- 229910018507 Al—Ni Inorganic materials 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- ZSQNVDXIAIHROP-UHFFFAOYSA-N C(CC)C=1NC=CC1.CC1(C(=O)O)CC(C(=O)O)=CC=C1 Chemical compound C(CC)C=1NC=CC1.CC1(C(=O)O)CC(C(=O)O)=CC=C1 ZSQNVDXIAIHROP-UHFFFAOYSA-N 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 description 2
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 2
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 2
- 239000004677 Nylon Substances 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 2
- 206010040844 Skin exfoliation Diseases 0.000 description 2
- 239000002174 Styrene-butadiene Substances 0.000 description 2
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 2
- 239000006230 acetylene black Substances 0.000 description 2
- 239000011149 active material Substances 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 229910001413 alkali metal ion Inorganic materials 0.000 description 2
- 150000001340 alkali metals Chemical class 0.000 description 2
- 229910001420 alkaline earth metal ion Inorganic materials 0.000 description 2
- 230000002152 alkylating effect Effects 0.000 description 2
- 230000029936 alkylation Effects 0.000 description 2
- 238000005804 alkylation reaction Methods 0.000 description 2
- 125000000129 anionic group Chemical group 0.000 description 2
- 229910052786 argon Inorganic materials 0.000 description 2
- 125000004429 atom Chemical group 0.000 description 2
- 229910052788 barium Inorganic materials 0.000 description 2
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 2
- 229910052728 basic metal Inorganic materials 0.000 description 2
- 150000003818 basic metals Chemical class 0.000 description 2
- 229910052790 beryllium Inorganic materials 0.000 description 2
- ATBAMAFKBVZNFJ-UHFFFAOYSA-N beryllium atom Chemical compound [Be] ATBAMAFKBVZNFJ-UHFFFAOYSA-N 0.000 description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- RDHPKYGYEGBMSE-UHFFFAOYSA-N bromoethane Chemical compound CCBr RDHPKYGYEGBMSE-UHFFFAOYSA-N 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 150000001721 carbon Chemical group 0.000 description 2
- 239000003575 carbonaceous material Substances 0.000 description 2
- 239000002322 conducting polymer Substances 0.000 description 2
- 229920001940 conductive polymer Polymers 0.000 description 2
- 230000002596 correlated effect Effects 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 229910021419 crystalline silicon Inorganic materials 0.000 description 2
- 230000018044 dehydration Effects 0.000 description 2
- 238000006297 dehydration reaction Methods 0.000 description 2
- 230000035618 desquamation Effects 0.000 description 2
- 238000007599 discharging Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 229920001971 elastomer Polymers 0.000 description 2
- KTWOOEGAPBSYNW-UHFFFAOYSA-N ferrocene Chemical compound [Fe+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KTWOOEGAPBSYNW-UHFFFAOYSA-N 0.000 description 2
- 239000007789 gas Substances 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 239000010439 graphite Substances 0.000 description 2
- 229910002804 graphite Inorganic materials 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 150000004678 hydrides Chemical class 0.000 description 2
- 229910052740 iodine Inorganic materials 0.000 description 2
- 239000011630 iodine Substances 0.000 description 2
- 229910052742 iron Inorganic materials 0.000 description 2
- 238000003475 lamination Methods 0.000 description 2
- 238000004768 lowest unoccupied molecular orbital Methods 0.000 description 2
- 229920002521 macromolecule Polymers 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- WPBNNNQJVZRUHP-UHFFFAOYSA-L manganese(2+);methyl n-[[2-(methoxycarbonylcarbamothioylamino)phenyl]carbamothioyl]carbamate;n-[2-(sulfidocarbothioylamino)ethyl]carbamodithioate Chemical compound [Mn+2].[S-]C(=S)NCCNC([S-])=S.COC(=O)NC(=S)NC1=CC=CC=C1NC(=S)NC(=O)OC WPBNNNQJVZRUHP-UHFFFAOYSA-L 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 239000004745 nonwoven fabric Substances 0.000 description 2
- 229920001778 nylon Polymers 0.000 description 2
- 230000003534 oscillatory effect Effects 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 238000005268 plasma chemical vapour deposition Methods 0.000 description 2
- 229910052697 platinum Inorganic materials 0.000 description 2
- 229920003214 poly(methacrylonitrile) Polymers 0.000 description 2
- 229920000570 polyether Polymers 0.000 description 2
- 229920000642 polymer Polymers 0.000 description 2
- 229920000098 polyolefin Polymers 0.000 description 2
- 230000001376 precipitating effect Effects 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 239000004627 regenerated cellulose Substances 0.000 description 2
- 239000005060 rubber Substances 0.000 description 2
- 239000004065 semiconductor Substances 0.000 description 2
- 229910052712 strontium Inorganic materials 0.000 description 2
- CIOAGBVUUVVLOB-UHFFFAOYSA-N strontium atom Chemical compound [Sr] CIOAGBVUUVVLOB-UHFFFAOYSA-N 0.000 description 2
- HJUGFYREWKUQJT-UHFFFAOYSA-N tetrabromomethane Chemical compound BrC(Br)(Br)Br HJUGFYREWKUQJT-UHFFFAOYSA-N 0.000 description 2
- 229910052719 titanium Inorganic materials 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- 229920002554 vinyl polymer Polymers 0.000 description 2
- RNFJDJUURJAICM-UHFFFAOYSA-N 2,2,4,4,6,6-hexaphenoxy-1,3,5-triaza-2$l^{5},4$l^{5},6$l^{5}-triphosphacyclohexa-1,3,5-triene Chemical compound N=1P(OC=2C=CC=CC=2)(OC=2C=CC=CC=2)=NP(OC=2C=CC=CC=2)(OC=2C=CC=CC=2)=NP=1(OC=1C=CC=CC=1)OC1=CC=CC=C1 RNFJDJUURJAICM-UHFFFAOYSA-N 0.000 description 1
- PUAQLLVFLMYYJJ-UHFFFAOYSA-N 2-aminopropiophenone Chemical compound CC(N)C(=O)C1=CC=CC=C1 PUAQLLVFLMYYJJ-UHFFFAOYSA-N 0.000 description 1
- DUAXLVGFFDFSAG-UHFFFAOYSA-N 4-amino-2-methylbutan-1-ol Chemical class OCC(C)CCN DUAXLVGFFDFSAG-UHFFFAOYSA-N 0.000 description 1
- IGNGFGXAWDQJGP-UHFFFAOYSA-O CC1C[NH+](C)CC1 Chemical compound CC1C[NH+](C)CC1 IGNGFGXAWDQJGP-UHFFFAOYSA-O 0.000 description 1
- BHPQYMZQTOCNFJ-UHFFFAOYSA-N Calcium cation Chemical compound [Ca+2] BHPQYMZQTOCNFJ-UHFFFAOYSA-N 0.000 description 1
- 229920003043 Cellulose fiber Polymers 0.000 description 1
- 238000004057 DFT-B3LYP calculation Methods 0.000 description 1
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 1
- 229920002449 FKM Polymers 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 229910015015 LiAsF 6 Inorganic materials 0.000 description 1
- 229910013063 LiBF 4 Inorganic materials 0.000 description 1
- 229910012820 LiCoO Inorganic materials 0.000 description 1
- 229910012851 LiCoO 2 Inorganic materials 0.000 description 1
- 229910010707 LiFePO 4 Inorganic materials 0.000 description 1
- 229910013870 LiPF 6 Inorganic materials 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- 229920002319 Poly(methyl acrylate) Polymers 0.000 description 1
- 239000005062 Polybutadiene Substances 0.000 description 1
- 229920001328 Polyvinylidene chloride Polymers 0.000 description 1
- NPYPAHLBTDXSSS-UHFFFAOYSA-N Potassium ion Chemical compound [K+] NPYPAHLBTDXSSS-UHFFFAOYSA-N 0.000 description 1
- 229910000676 Si alloy Inorganic materials 0.000 description 1
- BQCADISMDOOEFD-UHFFFAOYSA-N Silver Chemical compound [Ag] BQCADISMDOOEFD-UHFFFAOYSA-N 0.000 description 1
- FKNQFGJONOIPTF-UHFFFAOYSA-N Sodium cation Chemical compound [Na+] FKNQFGJONOIPTF-UHFFFAOYSA-N 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- 229920002978 Vinylon Polymers 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 150000001414 amino alcohols Chemical class 0.000 description 1
- 229910001422 barium ion Inorganic materials 0.000 description 1
- 229920005601 base polymer Polymers 0.000 description 1
- 229910001423 beryllium ion Inorganic materials 0.000 description 1
- PWOSZCQLSAMRQW-UHFFFAOYSA-N beryllium(2+) Chemical compound [Be+2] PWOSZCQLSAMRQW-UHFFFAOYSA-N 0.000 description 1
- 229910001424 calcium ion Inorganic materials 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 229940105329 carboxymethylcellulose Drugs 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- CZKMPDNXOGQMFW-UHFFFAOYSA-N chloro(triethyl)germane Chemical compound CC[Ge](Cl)(CC)CC CZKMPDNXOGQMFW-UHFFFAOYSA-N 0.000 description 1
- 229910017052 cobalt Inorganic materials 0.000 description 1
- 239000010941 cobalt Substances 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 150000005676 cyclic carbonates Chemical class 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- 229920005994 diacetyl cellulose Polymers 0.000 description 1
- QHGJSLXSVXVKHZ-UHFFFAOYSA-N dilithium;dioxido(dioxo)manganese Chemical compound [Li+].[Li+].[O-][Mn]([O-])(=O)=O QHGJSLXSVXVKHZ-UHFFFAOYSA-N 0.000 description 1
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N dimethylmethane Natural products CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 1
- 238000005530 etching Methods 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 239000003063 flame retardant Substances 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- 230000005283 ground state Effects 0.000 description 1
- 125000001145 hydrido group Chemical group *[H] 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 150000002466 imines Chemical class 0.000 description 1
- 238000009434 installation Methods 0.000 description 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 1
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 description 1
- GELKBWJHTRAYNV-UHFFFAOYSA-K lithium iron phosphate Chemical compound [Li+].[Fe+2].[O-]P([O-])([O-])=O GELKBWJHTRAYNV-UHFFFAOYSA-K 0.000 description 1
- MHCFAGZWMAWTNR-UHFFFAOYSA-M lithium perchlorate Chemical compound [Li+].[O-]Cl(=O)(=O)=O MHCFAGZWMAWTNR-UHFFFAOYSA-M 0.000 description 1
- 229910001425 magnesium ion Inorganic materials 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 150000003003 phosphines Chemical class 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 230000010287 polarization Effects 0.000 description 1
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 1
- 229920002239 polyacrylonitrile Polymers 0.000 description 1
- 229920002857 polybutadiene Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 239000004926 polymethyl methacrylate Substances 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 229910001414 potassium ion Inorganic materials 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 230000000630 rising effect Effects 0.000 description 1
- 239000002210 silicon-based material Substances 0.000 description 1
- 229910052709 silver Inorganic materials 0.000 description 1
- 239000004332 silver Substances 0.000 description 1
- QRUBYZBWAOOHSV-UHFFFAOYSA-M silver trifluoromethanesulfonate Chemical compound [Ag+].[O-]S(=O)(=O)C(F)(F)F QRUBYZBWAOOHSV-UHFFFAOYSA-M 0.000 description 1
- 229910001415 sodium ion Inorganic materials 0.000 description 1
- 238000009987 spinning Methods 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 229910001427 strontium ion Inorganic materials 0.000 description 1
- PWYYWQHXAPXYMF-UHFFFAOYSA-N strontium(2+) Chemical compound [Sr+2] PWYYWQHXAPXYMF-UHFFFAOYSA-N 0.000 description 1
- 229920005608 sulfonated EPDM Polymers 0.000 description 1
- 230000002195 synergetic effect Effects 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 229920003002 synthetic resin Polymers 0.000 description 1
- 239000000057 synthetic resin Substances 0.000 description 1
- BFKJFAAPBSQJPD-UHFFFAOYSA-N tetrafluoroethene Chemical group FC(F)=C(F)F BFKJFAAPBSQJPD-UHFFFAOYSA-N 0.000 description 1
- 229910052718 tin Inorganic materials 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0569—Liquid materials characterised by the solvents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D207/04—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D207/06—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with radicals, containing only hydrogen and carbon atoms, attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C309/00—Sulfonic acids; Halides, esters, or anhydrides thereof
- C07C309/01—Sulfonic acids
- C07C309/02—Sulfonic acids having sulfo groups bound to acyclic carbon atoms
- C07C309/03—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton
- C07C309/06—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of an acyclic saturated carbon skeleton containing halogen atoms, or nitro or nitroso groups bound to the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C311/00—Amides of sulfonic acids, i.e. compounds having singly-bound oxygen atoms of sulfo groups replaced by nitrogen atoms, not being part of nitro or nitroso groups
- C07C311/48—Amides of sulfonic acids, i.e. compounds having singly-bound oxygen atoms of sulfo groups replaced by nitrogen atoms, not being part of nitro or nitroso groups having nitrogen atoms of sulfonamide groups further bound to another hetero atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01G—CAPACITORS; CAPACITORS, RECTIFIERS, DETECTORS, SWITCHING DEVICES, LIGHT-SENSITIVE OR TEMPERATURE-SENSITIVE DEVICES OF THE ELECTROLYTIC TYPE
- H01G11/00—Hybrid capacitors, i.e. capacitors having different positive and negative electrodes; Electric double-layer [EDL] capacitors; Processes for the manufacture thereof or of parts thereof
- H01G11/04—Hybrid capacitors
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01G—CAPACITORS; CAPACITORS, RECTIFIERS, DETECTORS, SWITCHING DEVICES, LIGHT-SENSITIVE OR TEMPERATURE-SENSITIVE DEVICES OF THE ELECTROLYTIC TYPE
- H01G11/00—Hybrid capacitors, i.e. capacitors having different positive and negative electrodes; Electric double-layer [EDL] capacitors; Processes for the manufacture thereof or of parts thereof
- H01G11/04—Hybrid capacitors
- H01G11/06—Hybrid capacitors with one of the electrodes allowing ions to be reversibly doped thereinto, e.g. lithium ion capacitors [LIC]
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01G—CAPACITORS; CAPACITORS, RECTIFIERS, DETECTORS, SWITCHING DEVICES, LIGHT-SENSITIVE OR TEMPERATURE-SENSITIVE DEVICES OF THE ELECTROLYTIC TYPE
- H01G11/00—Hybrid capacitors, i.e. capacitors having different positive and negative electrodes; Electric double-layer [EDL] capacitors; Processes for the manufacture thereof or of parts thereof
- H01G11/52—Separators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01G—CAPACITORS; CAPACITORS, RECTIFIERS, DETECTORS, SWITCHING DEVICES, LIGHT-SENSITIVE OR TEMPERATURE-SENSITIVE DEVICES OF THE ELECTROLYTIC TYPE
- H01G11/00—Hybrid capacitors, i.e. capacitors having different positive and negative electrodes; Electric double-layer [EDL] capacitors; Processes for the manufacture thereof or of parts thereof
- H01G11/54—Electrolytes
- H01G11/58—Liquid electrolytes
- H01G11/60—Liquid electrolytes characterised by the solvent
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01G—CAPACITORS; CAPACITORS, RECTIFIERS, DETECTORS, SWITCHING DEVICES, LIGHT-SENSITIVE OR TEMPERATURE-SENSITIVE DEVICES OF THE ELECTROLYTIC TYPE
- H01G11/00—Hybrid capacitors, i.e. capacitors having different positive and negative electrodes; Electric double-layer [EDL] capacitors; Processes for the manufacture thereof or of parts thereof
- H01G11/54—Electrolytes
- H01G11/58—Liquid electrolytes
- H01G11/62—Liquid electrolytes characterised by the solute, e.g. salts, anions or cations therein
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/02—Details
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2220/00—Batteries for particular applications
- H01M2220/20—Batteries in motive systems, e.g. vehicle, ship, plane
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2220/00—Batteries for particular applications
- H01M2220/30—Batteries in portable systems, e.g. mobile phone, laptop
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
- H01M2300/0028—Organic electrolyte characterised by the solvent
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
- H01M2300/0045—Room temperature molten salts comprising at least one organic ion
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/13—Energy storage using capacitors
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02T—CLIMATE CHANGE MITIGATION TECHNOLOGIES RELATED TO TRANSPORTATION
- Y02T10/00—Road transport of goods or passengers
- Y02T10/60—Other road transportation technologies with climate change mitigation effect
- Y02T10/70—Energy storage systems for electromobility, e.g. batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Power Engineering (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- Microelectronics & Electronic Packaging (AREA)
- General Chemical & Material Sciences (AREA)
- Manufacturing & Machinery (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- General Physics & Mathematics (AREA)
- Inorganic Chemistry (AREA)
- Electric Double-Layer Capacitors Or The Like (AREA)
- Secondary Cells (AREA)
- Pyrrole Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
技术领域
本发明涉及一种离子液体及使用离子液体的蓄电装置。
背景技术
近年来,由于对移动电话或笔记本型个人电脑等便携式电子设备的需求的增加及电动汽车(EV:Electric Vehicle)等的开发,对双电层电容器、锂离子二次电池、锂离子电容器等蓄电装置的需求显著增加。另外,蓄电装置需要高电容、高性能化及各种工作环境下的安全性等。
为了满足上述那样的要求,对蓄电装置的电解液积极地进行开发。作为用于蓄电装置的电解液有环状碳酸酯,尤其是,通常使用具有高介电常数及优良的离子传导性的碳酸乙烯酯。
然而,不仅是碳酸乙烯酯,有机溶剂大多具有挥发性及低闪点。因此,在将有机溶剂用作蓄电装置的电解液时,有可能由于内部短路或过充电等而内部温度上升,从而导致发生锂离子二次电池的破裂或发火等。
于是,考虑到上述危险性,对将具有非挥发性及阻燃性的离子液体用作蓄电装置的电解液进行了研讨。离子液体还被称为室温熔融盐,是指由阳离子和阴离子的组合构成的盐。作为离子液体,例如可以举出包含季铵类阳离子的离子液体及包含咪唑类阳离子的离子液体等(参照专利文献1及非专利文献1)。
[专利文献1]日本专利申请公开2003-331918号公报
[非专利文献1]
Hajime Matsumoto等,含基于二(氟磺酰基)亚胺[FSI]-的低粘度离子液体的Li/LiCoO2电池的快速循环(Fast cycling of Li/LiCoO2 cellwith low-viscosity ionic liquids based onbis(fluorosulfonyl)imide[FSI]-),Journal of PowerSources,160,2006,第1308-1313页
在将离子液体用作蓄电装置的电解液的情况下,该离子液体被要求具有很宽的电位窗及高电化学稳定性。另外,由于蓄电装置在很多情况下被要求-30°C至70°C的工作温度,因此当蓄电装置在各种环境下,特别在低温环境下使用时,该离子液体的熔点优选低。
但是,因为专利文献1所示的包含季铵类阳离子的离子液体的熔点是10°C左右,所以当在低温环境下使用蓄电装置时,有可能离子液体凝固而导致离子液体的电阻增大。另外,因为在低温环境下使用蓄电装置是很困难的,所以发生蓄电装置的工作温度范围变窄的问题。
另外,如非专利文献1所示那样,包含咪唑类阳离子的离子液体与包含季铵类阳离子的离子液体相比,电位窗窄,不能说具有充分的电化学稳定性。因此,包含咪唑类阳离子的离子液体对正极材料及负极材料不稳定,从而有可能蓄电装置的可靠性被降低。
发明内容
鉴于上述问题,本发明的一个方式的目的之一是提供一种电化学稳定性良好且熔点低的离子液体。另外,本发明的一个方式的目的之一是提供一种电解液包含该离子液体的蓄电装置。
本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G0)表示的离子液体。
通式(G0)中,R0至R5分别表示碳数为1至20的烷基、甲氧基、甲氧基甲基、甲氧基乙基和氢原子中的任一个,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、四氟硼酸盐(BF4-)或六氟磷酸盐(PF6 -)。
本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G1)表示的离子液体。
通式(G1)中,R1至R4中的一种或两种表示碳数为1至20的烷基、甲氧基、甲氧基甲基和甲氧基乙基中的任一个,其他两种或三种表示氢原子,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、BF4 -或PF6 -。
通式(G1)中,R1至R4中的一种或两种优选为碳数为1至4的烷基。
另外,本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G2)表示的离子液体。
通式(G2)中,R1或R2表示碳数为1至20的烷基、甲氧基、甲氧基甲基和甲氧基乙基中的任一个,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、BF4 -或PF6 -。
通式(G2)中,R1或R2分别优选为碳数为1至4的烷基。
另外,本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G3)表示的离子液体。
通式(G3)中,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、BF4 -或PF6 -。
另外,本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G4)表示的离子液体。
通式(G4)中,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、BF4 -或PF6 -。
另外,本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G5)表示的离子液体。
通式(G5)中,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、BF4 -或PF6 -。
通式(G0)至通式(G5)中,A-优选为选自(CnF2n+1SO2)2N-(n=0至4)、(CmF2m+1SO3)-(m=0至4)和CF2(CF2SO2)2N-中的任一种的一价阴离子。
另外,本发明的一个方式是一种包括正极、负极、隔离体以及电解液的蓄电装置,所述电解液包括由通式(G0)至通式(G5)中任一个表示的离子液体。
另外,本发明的一个方式是一种包括正极、负极、隔离体以及电解液的蓄电装置,所述电解液包括由通式(G0)至通式(G5)中任一个表示的离子液体及包含锂离子的电解质盐。
在本说明书等中,蓄电装置是指具有蓄电功能的所有元件及装置。例如,锂离子二次电池、锂离子电容器以及双电层电容器等都包括在蓄电装置的范畴内。
有关本发明的一个方式可以提供一种电化学稳定性良好且熔点低的离子液体。另外,还可以提供一种包括包含有关本发明的一个方式的离子液体的电解液的蓄电装置。
附图说明
图1A和1B是示出蓄电装置的截面图;
图2A和2B分别是蓄电装置的俯视图和透视图;
图3A和3B是示出蓄电装置的制造方法的透视图;
图4是示出蓄电装置的制造方法的透视图;
图5A和5B是示出蓄电装置的应用方式的图;
图6A和6B是示出蓄电装置的应用方式的图;
图7是1,3-二甲基-1-丙基吡咯烷双(三氟甲磺酰)酰胺(简称为3mP13-TFSA)的NMR谱图;
图8是1,3-二甲基-1-丙基吡咯烷双(氟磺酰)酰胺(简称为3mP13-FSA)的NMR谱图;
图9是1,2-二甲基-1-丙基吡咯烷双(氟磺酰)酰胺(简称为2mP13-FSA)的NMR谱图;
图10是示出样品1至样品3及对比样品1至对比样品3的线性扫描伏安图的图;
图11是双电层电容器的俯视图;
图12A和12B是示出样品4及对比样品4的液电阻及单元电阻的图;
图13是示出样品5、对比样品5及对比样品6的输出特性的图;
图14是1-乙基-1,3-二甲基吡咯烷双(氟磺酰)酰胺(简称为3mP12-FSA)的NMR谱图;
图15是示出3mP12-FSA的线性扫描伏安图的图;
图16是锂离子二次电池的斜视图;
图17A和17B是示出样品6及样品7的输出特性的图。
具体实施方式
下面,将参照附图说明本发明的实施方式。注意,本发明不局限于以下说明,所属技术领域的普通技术人员可以很容易地理解一个事实就是其方式和详细内容可以被变换为各种各样的形式,而不脱离本发明的宗旨及其范围。因此,本发明不应该被解释为仅限定在以下所示的实施方式及实施例所记载的内容中。
实施方式1
本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G0)表示的离子液体。
通式(G0)中,R0至R5分别表示碳数为1至20的烷基、甲氧基、甲氧基甲基、甲氧基乙基和氢原子中的任一个,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、BF4 -或PF6 -。
本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G1)表示的离子液体。
通式(G1)中,R1至R4中的一种或两种表示碳数为1至20的烷基、甲氧基、甲氧基甲基和甲氧基乙基中的任一个,其他两种或三种表示氢原子,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、BF4 -或PF6 -。
通式(G1)中,R1至R4中的一种或两种优选为碳数为1至4的烷基。
另外,本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G2)表示的离子液体。
通式(G2)中,R1或R2表示碳数为1至20的烷基、甲氧基、甲氧基甲基和甲氧基乙基中的任一个,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、BF4 -或PF6 -。
通式(G2)中,R1或R2分别优选为碳数为1至4的烷基。
另外,本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G3)表示的离子液体。
通式(G3)中,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、BF4 -或PF6 -。
另外,本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G4)表示的离子液体。
通式(G4)中,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、BF4 -或PF6 -。
另外,本发明的一个方式是包括环季铵阳离子和一价阴离子且由以下通式(G5)表示的离子液体。
通式(G5)中,A-表示一价酰亚胺类阴离子、一价甲基化物类阴离子、全氟烷基磺酸阴离子、BF4 -或PF6 -。
作为环季铵阳离子,具体地说,可以举出由结构式(100)至结构式(117)表示的有机化合物。但是,本发明的一个方式不局限于此。
在此,示出关于由具有电子给予性的取代基引起的耐还原性的提高的计算结果。
下面,作为有关本发明的一个方式的离子液体中的阳离子,示出:由结构式(100)表示的1,2-二甲基-1-丙基吡咯烷阳离子(简称为2mP13);由结构式(101)表示的1,3-二甲基-1-丙基吡咯烷阳离子(简称为3mP13);以及由结构式(110)表示的1-乙基-1,3-二甲基吡咯烷阳离子(简称为3mP12),并且作为用来对比的离子液体中的阳离子示出:由结构式(301)表示的1-甲基-1-丙基吡咯烷阳离子(简称为P13);以及由结构式(302)表示的1-乙基-3-甲基咪唑阳离子(简称为EMI)。
对于有关本发明的一个方式的离子液体中的阳离子(结构式(100)、(101)、(110))及用来对比的离子液体中的阳离子(结构式(301)、(302)),作为量子化学计算利用密度泛函理论法(DFT)计算了单重基态的最佳分子结构。以电势能、电子间静电能、电子的运动能及包括所有的其他复杂的电子间的互相作用的交换相关能的总和表示DFT的总能量。在DFT中,由于使用以电子密度表示的单电子势的泛函(函数的函数之意)来近似表示交换相关作用,所以计算速度快且精度高。在此,利用作为混合泛函的B3LYP来规定涉及交换和相关能的各参数的权重。此外,作为基底函数使用6-311G(对每个原子价轨道使用三个缩短函数的三重分裂价层(triple split valence)基底类的基底函数)而将它应用到所有原子上。通过上述基底函数,例如关于氢原子,考虑到1s至3s的轨道,而关于碳原子,考虑到1s至4s、2p至4p的轨道。再者,为了提高计算精度作为极化基底类,对氢原子加上p函数,对氢原子以外的原子加上d函数。
此外,作为量子化学计算程序,使用Gaussian09。使用高性能计算机(SGI株式会社制造,Altix ICE8400EX)来进行计算。注意,假设由结构式(100)、(101)、(110)、(301)及(302)表示的所有离子液体中的阳离子具有最稳定的结构并处于真空中而进行量子化学计算。
表1示出通过量子化学计算算出的由结构式(100)、(101)及(110)表示的三种离子液体中的阳离子的最低未占据分子轨道能级(LUMO能级)。此外,作为对比,表1还示出由结构式(301)及(302)表示的两种离子液体中的阳离子的最低未占据分子轨道能级(LUMO能级)。
[表1]
在用于蓄电装置中的电解液包含离子液体的情况下,离子液体的耐还原性起因于离子液体中的阳离子的从负极的电子接受性。
例如,在离子液体中的阳离子的LUMO能级高于负极材料的导带时,包含该阳离子的离子液体不被还原。通过将阳离子的LUMO能级与由结构式(302)表示的EMI阳离子的LUMO能级进行比较来可以相对地评价对于锂的阳离子的耐还原性,所述由结构式(302)表示的EMI阳离子的还原电位与典型的低电位负极材料的锂的氧化还原电位大致相同。就是说,在有关本发明的一个方式的离子液体中的阳离子的LUMO能级至少高于由结构式(302)表示的EMI阳离子的LUMO能级时,可以说有关本发明的一个方式的离子液体具有优良的耐还原性。
表1所示那样,虽然由结构式(301)表示的P13阳离子的LUMO能级是-3.50eV,但是由结构式(100)表示的2mP13阳离子、由结构式(101)表示的3mP13阳离子及由结构式(110)表示的3mP12阳离子的LUMO能级都高于-3.50eV。因此,可以说有关本发明的一个方式的离子液体具有优良的耐还原性。
以上计算结果示出通过对离子液体中的阳离子导入具有电子给予性的取代基提高离子液体的耐还原性。
在通式(G0)至(G5)中,A-优选是选自(CnF2n+1SO2)2N-(n=0至4)、(CmF2m+1SO3)-(m=0至4)和CF2(CF2SO2)2N-中的任一种一价阴离子。但是,不局限于此,A-是与环季铵阴离子配成对而形成离子液体的阴离子即可。
离子液体中的氧化电位根据阴离子种类而变化。通过使用选自(CnF2n+1SO2)2N-(n=0至4)、(CmF2m+1SO3)-(m=0至4)和CF2(CF2SO2)2N-中的任一种一价阴离子,可以由于与上述阴离子相互作用而提高离子液体的氧化电位。就是说,这意味着能够提高离子液体的耐氧化性。
接下来,对有关本发明的一个方式的离子液体的合成方法进行说明。作为有关本发明的一个方式的离子液体的合成方法可以应用各种反应。例如,通过进行以下所示的合成方法能够合成由通式(G1)表示的离子液体。注意,有关本发明的一个方式的离子液体的合成方法不局限于以下所示的合成方法。
〈由通式(G1)表示的离子液体的合成方法〉
对有关本发明的一个方式的离子液体的合成方法可以应用各种反应。这里,作为一个例子参照合成方案(S-1)进行说明。
在上述合成方案(S-1)中,从通式(α-1)到通式(α-2)的反应是经过利用三烷基膦等三取代膦和卤素源的卤化的氨基醇的闭环反应。PR’表示三取代膦,X1表示卤素源。作为卤素源可以使用四氯化碳、四溴化碳、碘、碘代甲烷等。在本发明的一个方式的离子液体中,作为三取代膦使用三烷基膦,并且作为卤素源使用四氯化碳。
在上述合成方案(S-1)中,从通式(α-2)到通式(α-3)的反应是在氢化物离子(hydrido)的存在下,利用胺化合物和羰基化合物进行胺的烷基化的反应。例如,可以使用过剩的甲酸作为氢化物源。在本发明的一个方式的离子液体中,作为羰基化合物使用CH2O。
在上述合成方案(S-1)中,从通式(α-3)到通式(α-4)的反应是利用叔胺化合物和卤化烷基化合物进行烷基化而合成季铵盐的反应。作为卤化烷基化合物可以使用卤代丙烷(propane halide)或溴乙烷。此外,X2表示卤素。作为卤素,由于反应性高,所以优选使用溴或碘,更优选使用碘。
通过利用由通式(α-4)表示的季铵盐和所希望的金属盐进行离子交换,可以得到由通式(G1)表示的离子液体。作为金属盐,例如可以使用锂金属盐。
〈由通式(G4)表示的离子液体的合成方法〉
接下来,作为有关本发明的一个方式的离子液体的合成方法参照合成方案(S-2)进行说明。
在上述合成方案(S-2)中,从通式(α-5)到通式(α-6)的反应是在氢化物离子的存在下,利用胺化合物和羰基化合物进行胺的烷基化的反应。例如,可以使用过剩的甲酸作为氢化物源。在本发明的一个方式的离子液体中,作为羰基化合物使用CH2O。
在上述合成方案(S-2)中,从通式(α-6)到通式(α-7)的反应是利用叔胺化合物和卤化烷基化合物进行烷基化而合成季铵盐的反应。作为卤化烷基化合物可以使用卤代丙烷或溴乙烷。此外,X3表示卤素。作为卤素,由于反应性高,所以优选使用溴或碘,更优选使用碘。
通过利用由通式(α-7)表示的季铵盐和所希望的金属盐进行离子交换,可以得到由通式(G4)表示的离子液体。作为金属盐,例如可以使用锂金属盐。
有关本发明的一个方式的离子液体具有很宽的电位窗,即为0.2以上且5.4以下,优选为-0.1以上且5.8以下,并且电化学稳定性良好。
另外,通过对环季铵导入取代基,可以降低离子液体的熔点。例如,通过对吡咯烷骨架导入甲基,可以降低熔点。有关本发明的一个方式的离子液体可以实现-10°C以下的熔点,优选实现-30°C以下的熔点。熔点的降低起因于对环季铵导入取代基而使环季铵分子的对称性破坏。
另外,本实施方式可以与其他实施方式适当地组合而实施。
实施方式2
在本实施方式中,参照图1A和1B至图4对将有关本发明的一个方式的离子液体用作电解液的蓄电装置进行说明。
有关本发明的一个方式的蓄电装置至少包括正极、负极、隔离体及电解液。例如,锂离子二次电池及锂离子电容器中的电解液包括非水溶剂及电解质盐。有关本发明的一个方式的离子液体可以用作溶解电解质盐的非水溶剂。另外,作为双电层电容器中的电解液,可以只使用有关本发明的一个方式的离子液体而不使用电解质盐。
图1A示出蓄电装置100的结构。以下,作为蓄电装置的一个例子,对锂离子二次电池进行说明。
图1A所示的蓄电装置100包括:具有正极集电体101及正极活性物质层102的正极103;具有负极集电体104及负极活性物质层105的负极106;隔离体107;电解液108;以及框体109。在设置于框体109内的正极103和负极106之间设置有隔离体107。此外,在框体109内充满有电解液108。
作为正极集电体101,例如可以使用导电材料等。作为导电材料,例如可以使用铝(Al)、铜(Cu)、镍(Ni)或钛(Ti)。此外,作为正极集电体101,也可以使用由上述导电材料中的多种构成的合金材料,并且作为该合金材料例如可以使用Al-Ni合金或Al-Cu合金等。此外,作为正极集电体101,可以适当地采用箔状、板状、网状等形状。此外,也可以将形成在制造衬底上的导电层从该制造衬底剥离而用作正极集电体101。
作为正极活性物质层102,例如可以使用包含成为载流子的离子及过渡金属的材料。作为包含成为载流子的离子及过渡金属的材料,例如可以举出通式AhMiPOj(h>0、i>0、j>0)所示的材料。在此,A例如为如锂、钠、钾等碱金属、如钙、锶、钡等碱土金属、铍或镁。M例如为如铁、镍、锰、钴等过渡金属。作为通式AhMiPOj(h>0、i>0、j>0)所示的材料,例如可以举出磷酸铁锂、磷酸铁钠等。作为由A表示的材料及由M表示的材料,选择上述材料中的一种或多种即可。
或者,作为正极活性物质层102,可以使用通式AhMiOj(h>0、i>0、j>0)所示的材料。在此,A例如为如锂、钠、钾等碱金属、如钙、锶、钡等碱土金属、铍或镁。M例如为如铁、镍、锰、钴等过渡金属。作为通式AhMiOj(h>0、i>0、j>0)所示的材料,例如可以举出钴酸锂、锰酸锂或镍酸锂等。作为由A表示的材料及由M表示的材料,选择上述材料中的一种或多种即可。
在锂离子二次电池中,作为正极活性物质层102,优选选择包含锂的材料。换言之,上述通式AhMiPOj(h>0、i>0、j>0)或通式AhMiOj(h>0、i>0、j>0)中的A优选为锂。
在此,活性物质仅是指有关作为载流子的离子的嵌入及脱嵌的物质。但是,在本说明书等中,有时正极活性物质层102不但包括上述材料(实际上是“正极活性物质”的材料)而且还包括导电助剂或粘合剂等。
作为导电助剂,使用不会在蓄电装置中引起化学变化的电子导电材料即可。例如,可以使用:乙炔黑、黑铅、碳纤维等碳类材料;铜、镍、铝或银等金属材料;或上述物质的混合物的粉末、纤维等。
作为粘结剂,有淀粉、羧甲基纤维素、羟丙基纤维素、再生纤维素、二乙酰纤维素等多糖类;聚氯乙烯、聚乙烯、聚丙烯、聚乙烯醇、聚乙烯吡咯烷酮、聚四氟乙烯、聚偏氟乙烯、EPDM(Ethylene PropyleneDiene Monomer;乙烯丙烯二烯单体)橡胶、磺化EPDM橡胶、丁苯橡胶、丁二稀橡胶、氟化橡胶等乙烯基聚合物;聚氧化乙烯等聚醚;等等。
作为负极集电体104,例如可以使用导电材料等。作为导电材料,例如可以使用铝(Al)、铜(Cu)、镍(Ni)或钛(Ti)。此外,作为负极集电体104,也可以使用由上述导电材料中的多种构成的合金材料,并且作为该合金材料例如可以使用Al-Ni合金或Al-Cu合金等。此外,作为正极集电体101,可以适当地采用箔状、板状、网状等形状。此外,也可以将形成在制造衬底上的导电层从该制造衬底剥离而用作负极集电体104。
作为负极活性物质层105,只要是能够溶解且析出金属或嵌入且脱嵌金属离子的材料,就没有特别的限制。作为负极活性物质层105,例如可以使用锂金属、碳材料、硅、硅合金、锡等。作为能够嵌入且脱嵌锂离子的碳材料,可以使用粉末状或纤维状的黑铅或石墨(graphite)等。
另外,也可以用锂对负极活性物质层105进行预掺杂。作为锂的预掺杂的方法,也可以使用利用溅射法在负极活性物质层105表面形成锂层的方法。或者,通过在负极活性物质层105的表面设置锂箔,能够用锂对负极活性物质层105进行预掺杂。
电解液108包括非水溶剂及电解质盐。作为非水溶剂,可以使用有关本发明的一个方式的离子液体的一种或多种。注意,非水溶剂不一定是有关本发明的一个方式的离子液体的单一溶剂,也可以是有关本发明的一个方式的离子液体和其他离子液体的混合溶剂。
用于蓄电装置的电解液越具有低还原电位和高氧化电位,即宽的氧化还原的电位窗,越可以增大用于正极及负极的材料的选择范围。另外,氧化还原的电位窗越宽,对所选的正极材料及负极材料越稳定。通过将具有很宽的电位窗的有关本发明的一个方式的离子液体用作电解液,可以提高锂离子二次电池的可靠性。
溶解于非水溶剂的电解质盐是包含作为载体子的离子且适合正极活性物质层102的电解质盐即可。电解质盐是包含碱金属离子、碱土金属离子、铍离子或镁离子的电解质盐即可。作为碱金属离子,例如有锂离子、钠离子或钾离子。此外,作为碱土金属离子,例如有钙离子、锶离子或钡离子。在将包含锂的材料用于正极活性物质层102时,选择包含锂的电解质盐(以下,也称为含锂电解质盐)即可,并且在将包含钠的材料用于正极活性物质层102时,优选选择包含钠的电解质盐。
作为含锂电解质盐,可以使用氯化锂(LiCl)、氟化锂(LiF)、过氯酸锂(LiClO4)、氟硼酸锂(LiBF4)、LiAsF6、LiPF6、Li(CF3SO2)2N等。
作为隔离体107,使用纸、无纺布、玻璃纤维、或者合成纤维如尼龙(聚酰胺)、维尼纶(聚乙烯醇类纤维)、聚酯、丙烯酸树脂、聚烯烃、聚氨酯等即可。但是,需要选择不溶解在电解液108中的材料。
作为隔离体107,例如可以使用选自氟化类聚合物、聚醚如聚环氧乙烷及聚环氧丙烷等、聚烯烃如聚乙烯及聚丙烯等、聚丙烯腈、聚偏二氯乙烯、聚甲基丙烯酸甲酯、聚丙烯酸甲酯、聚乙烯醇、聚甲基丙烯腈(polymethacrylonitrile)、聚乙酸乙烯酯、聚乙烯吡咯烷酮、聚乙烯亚胺、聚丁二烯、聚苯乙烯、聚异戊二烯、以及聚氨酯类高分子及上述物质的衍生物;纤维素;纸;以及无纺布中的一种或两种以上的组合。
作为框体109,可以使用选自层压薄膜、高分子薄膜、金属薄膜、金属壳、塑料壳等中的一种或两种以上的组合。
接下来,参照图1B对与图1A所示的蓄电装置100的结构不同的蓄电装置110进行说明。
图1B所示的蓄电装置110与图1A所示的蓄电装置100相同之处在于包括:具有正极集电体101及正极活性物质层102的正极103;具有负极集电体104及负极活性物质层105的负极106;隔离体107;电解液;以及框体109。图1B所示的蓄电装置在设置于框体109内的正极103和负极106之间设置有浸渗有电解液的隔离体107。
在蓄电装置110中,正极集电体101、正极活性物质层102、负极集电体104、负极活性物质层105、框体109的材料分别可以使用与蓄电装置100相同的材料。
在蓄电装置110中,隔离体107优选为多孔膜。作为该多孔膜的材料,可以使用玻璃纤维、合成树脂材料或陶瓷材料等。此外,作为浸渗在隔离体107中的电解液,可以使用与蓄电装置100相同的材料。
接下来,对蓄电装置100的制造方法进行说明。以下,作为蓄电装置的一个例子,对锂离子二次电池进行说明。
首先,通过在正极集电体101上形成正极活性物质层102,而形成正极103。正极活性物质层102可以使用上述材料并利用涂敷法、溅射法形成。在通过涂敷法形成正极活性物质层102的情况下,通过对包含作为载体子的离子及过渡金属的材料混合导电助剂或粘合剂等来形成膏,并将该膏涂敷在正极集电体101上而使其干燥。在通过涂敷法形成正极活性物质层102的情况下,当需要时,进行加压成形即可。
接下来,通过在负极集电体104上形成负极活性物质层105,而形成负极106。负极活性物质层105可以使用上述材料并利用涂敷法、等离子体CVD法、溅射法形成。在作为负极活性物质层105使用硅的情况下,也可以使用如下材料:形成微晶硅,然后通过蚀刻去除该微晶硅中存在的非晶硅而得到的硅材料。通过去除微晶硅中存在的非晶硅,残留的微晶硅的表面积增大。作为微晶硅的成膜方法,可以使用等离子体CVD法或溅射法等。此外,在通过涂敷法形成负极活性物质层105的情况下,通过对能够溶解且析出金属或嵌入且脱嵌金属离子的材料混合导电助剂或粘合剂等以与正极活性物质层102相同的方式形成。注意,作为导电助剂及粘合剂,可以使用上述材料。
在本实施方式中,将锂箔用于负极106。因为有关本发明的一个方式的离子液体具有高耐还原性并对具有最低电位的负极材料的锂稳定,所以通过将该离子液体用作电解液,可以制造具有高能量密度和高可靠性的蓄电装置。
作为电解液108及浸渗在隔离体107中的电解液的制造方法,对实施方式1所示的离子液体混合包含金属离子的电解质盐。在本实施方式中,作为含锂电解质盐使用Li(CF3SO2)2N。
有关本发明的一个方式的离子液体因为氧化还原的电位窗宽,所以对正极材料及负极材料稳定。因此,通过将有关本发明的一个方式的离子液体用作电解液108及浸渗在隔离体107中的电解液,可以提高蓄电装置的可靠性。
接下来,通过在框体109内在正极103和负极106之间设置隔离体107并充满电解液108,可以制造蓄电装置100。另外,通过在框体109内在正极103和负极106之间设置浸渗有电解液的隔离体107,可以制造蓄电装置110。
接着,参照图2A对层压型蓄电装置的一个例子进行说明。
图2A所示的层压型蓄电装置120包括:具有正极集电体101及正极活性物质层102的正极103;具有负极集电体104及负极活性物质层105的负极106;隔离体107;电解液108;以及框体109。在设置于框体109内的正极103和负极106之间设置有隔离体107。此外,在框体109内充满有电解液108。
在图2A所示的蓄电装置120中,正极集电体101及负极集电体104还用作与外部电接触的端子。因此,正极集电体101及负极集电体104的一部分露出到框体109的外侧。
在层压型蓄电装置120中,作为框体109优选使用层压薄膜、高分子薄膜、金属薄膜等。
接下来,参照图2B对硬币型蓄电装置的一个例子进行说明。
图2B所示的硬币型蓄电装置130与图1A所示的蓄电装置100等相同之处在于包括:具有正极集电体101及正极活性物质层102的正极103;具有负极集电体104及负极活性物质层105的负极106;隔离体107;电解液108;以及框体109。在图2B所示的蓄电装置130中,框体由第一框体109a和第二框体109b构成。此外,在设置于第一框体109a和第二框体109b内的正极103和负极106之间设置有浸渗有电解液108的隔离体107。
接下来,参照图3A和3B及图4对蓄电装置130的制造方法的一个例子进行说明。
首先,准备第一框体109a。第一框体109a的形状为没有一方底面的圆柱状。此外,为了使外部和正极103电连接,第一框体109a的材料优选为导电材料。第一框体109a例如由金属材料形成即可。在第一框体109a内部设置具有正极集电体101及正极活性物质层102的正极103(参照图3A)。
另一方面,准备第二框体109b。第二框体109b的形状为没有面积小一侧的底面的圆锥台状。此外,为了使外部和负极106电连接,第二框体109b的材料优选为导电材料。第二框体109b例如由金属材料形成即可。在第二框体109b内部设置具有负极集电体104及负极活性物质层105的负极106(参照图3B)。
图4示出设置有具有正极集电体101及正极活性物质层102的正极103的第一框体109a、环状绝缘体131、浸渗有电解液108的隔离体107、以及设置有具有负极集电体104及负极活性物质层105的负极106的第二框体109b。
以覆盖设置在第一框体109a内的正极103的外侧的方式设置环状绝缘体131。环状绝缘体131具有使正极103和负极106彼此绝缘的作用。此外,环状绝缘体131优选使用绝缘树脂形成。
隔着预先浸渗有电解液的隔离体107将图3B所示的设置有负极106的第二框体109b设置在设置有环状绝缘体131的第一框体109a内部。由于第二框体109b的直径小于第一框体109a底面的直径,所以将第二框体109b嵌入第一框体109a内部。另外,由于正极103及负极106通过环状绝缘体131彼此绝缘,所以不会短路。
通过上述步骤,可以制造图2B所示的硬币型蓄电装置130。
因为有关本发明的一个方式的离子液体具有很宽的电位窗及良好的电化学稳定性,所以对所选的正极材料及负极材料稳定。因此,通过将有关本发明的一个方式的离子液体用作锂离子二次电池的电解液,可以提高锂离子二次电池的可靠性。
另外,本发明的离子液体具有熔点低的特征。因此,通过将有关本发明的一个方式的离子液体用作锂离子二次电池的电解液,可以使锂离子二次电池在低温环境下工作并实现很宽的工作温度。
参照图1A至图4说明了锂离子二次电池的结构及制造方法,但是有关本发明的一个方式的蓄电装置不局限于此。作为有关本发明的一个方式的蓄电装置,可以举出电容器。作为电容器,可以举出锂离子电容器及双电层电容器等。
在将蓄电装置100至130用作锂离子电容器时,作为正极活性物质层102使用能够可逆地插入并脱离锂离子及/或阴离子的材料即可。作为正极活性物质层102及负极活性物质层105,例如可以使用活性炭、黑铅、导电高分子、多并苯有机半导体(PAS)等。
因为有关本发明的一个方式的离子液体具有很宽的电位窗及良好的电化学稳定性,所以对所选的正极材料及负极材料稳定。因此,通过将有关本发明的一个方式的离子液体用作锂离子电容器的电解液,可以提高锂离子电容器的可靠性。
另外,本发明的离子液体具有熔点低的特征。因此,通过将有关本发明的一个方式的离子液体用作锂离子电容器的电解液,可以使锂离子电容器在低温环境下工作并实现宽的工作温度。
在将蓄电装置100至130用作双电层电容器时,作为正极活性物质层102及负极活性物质层105,例如可以使用活性炭、导电高分子、多并苯有机半导体(PAS)等。
另外,在将蓄电装置100至130用作双电层电容器时,电解液108可以只由非水溶剂构成而不使用电解质盐。作为非水溶剂可以使用有关本发明的一个方式的离子液体的一种或多种。
因为有关本发明的一个方式的离子液体具有很宽的电位窗及良好的电化学稳定性,所以对所选的正极材料及负极材料稳定。因此,通过将有关本发明的一个方式的离子液体用作双电层电容器的电解液,可以提高双电层电容器的可靠性。
另外,本发明的离子液体具有熔点低的特征。因此,通过将有关本发明的一个方式的离子液体用作双电层电容器的电解液,可以使双电层电容器在低温环境下工作并实现宽的工作温度。
在本实施方式中,虽然示出层压型蓄电装置及硬币型蓄电装置的例子,但是有关本发明的一个方式的蓄电装置不局限于此。例如,可以制造叠层式、筒式等各种结构的蓄电装置。
此外,本实施方式可以与其他实施方式所记载的结构适当地组合而实施。
实施方式3
在本实施方式中,对有关本发明的一个方式的蓄电装置的应用方式进行说明。
有关本发明的一个方式的蓄电装置可以安装在多种电子装置中。例如,蓄电装置可以安装在影像拍摄装置例如数字照相机或摄像机等、移动电话、便携式信息终端、电子书籍用终端、便携式游戏机、数字相框、声音再现装置等。此外,有关本发明的一个方式的蓄电装置可以安装在电力推动车辆例如电动汽车、混合动力汽车、铁路用电动车厢、工作车、卡丁车、轮椅或自行车等。
有关本发明的一个方式的蓄电装置的电解液包括有关本发明的一个方式的离子液体。因为有关本发明的一个方式的离子液体具有很宽的电位窗及良好的电化学稳定性,所以对所选的正极材料及负极材料稳定。因此,通过将有关本发明的一个方式的离子液体用作蓄电装置的电解液,可以提高蓄电装置的可靠性。
另外,本发明的离子液体具有熔点低的特征。因此,通过将有关本发明的一个方式的离子液体用作锂离子二次电池的电解液,可以使锂离子二次电池在低温环境下工作并实现宽的工作温度。
图5A示出移动电话的一个例子。在移动电话3010中,显示部3012安装在框体3011中。框体3011还具备操作按钮3013、操作按钮3017、外部连接端口3014、扬声器3015及麦克风3016等。通过将有关本发明的一个方式的蓄电装置安装在上述移动电话中,可以实现高可靠性和宽的工作温度。注意,作为蓄电装置,可以使用锂离子二次电池、锂离子电容器及双电层电容器中的一种或多种的组合。
图5B示出电子书籍用终端的一个例子。电子书籍用终端3030包括第一框体3031及第二框体3033的两个框体,并且两个框体由轴部3032连为一体。第一框体3031及第二框体3033可以以轴部3032为轴进行开闭工作。第一框体3031安装有第一显示部3035,而第二框体3033安装有第二显示部3037。另外,第二框体3033具备操作按钮3039、电源3043及扬声器3041等。通过将有关本发明的一个方式的蓄电装置安装在上述电子书籍用终端,可以实现高可靠性和宽的工作温度。注意,作为蓄电装置,可以使用锂离子二次电池、锂离子电容器及双电层电容器中的一种或多种的组合。
图6A示出电动汽车的一个例子。电动汽车3050安装有蓄电装置3051。蓄电装置3051的电力由控制电路3053调整输出而供给到驱动装置3057。控制电路3053由计算机3055控制。
驱动装置3057利用直流电动机或交流电动机或者将电动机和内燃机组合而构成。计算机3055根据电动汽车3050的驾驶员的操作信息(加速、减速、停止等)或行车时的信息(上坡路或下坡路等的信息、施加到驱动轮的负荷信息等)的输入信息对控制电路3053输出控制信号。控制电路3053根据计算机3055的控制信号调整从蓄电装置3051供给的电能而控制驱动装置3057的输出。当安装有交流电动机时,还安装有将直流转换为交流的转换器。
作为蓄电装置3051,可以使用锂离子二次电池、锂离子电容器及双电层电容器中的一种或多种的组合。通过利用插件技术从外部供给电力来可以给蓄电装置3051充电。通过将有关本发明的一个方式的蓄电装置安装在电动汽车中,可以缩短充电时间等,从而可以提高方便性。此外,可以实现高可靠性和宽的工作温度。
图6B示出电动轮椅的一个例子。轮椅3070具备具有蓄电装置、电力控制部、控制单元等的控制部3073。通过控制部3073控制输出的蓄电装置的电力供应到驱动部3075。此外,控制部3073与控制器3077连接。通过操作控制器3077,可以通过控制部3073驱动驱动部3075,并且可以控制轮椅3070的向前、向后、转弯等工作以及速度。
作为蓄电装置,可以使用锂离子二次电池、锂离子电容器及双电层电容器中的一种或多种的组合。通过利用插件技术从外部供给电力来可以给蓄电装置充电。通过将有关本发明的一个方式的蓄电装置安装在电动轮椅3070中,可以缩短充电时间等,从而可以提高方便性。此外,可以实现高可靠性和宽的工作温度。
另外,当将蓄电装置安装在作为电力推动车辆的铁路用电动车厢时,可以从架空电缆或导电轨供给电力来进行充电。
本实施方式可以与其他实施方式及实施例的结构适当地组合。
实施例1
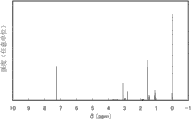
在本实施例中,将说明由结构式(200)表示的1,3-二甲基-1-丙基吡咯烷双(三氟甲磺酰)酰胺(简称为3mP13-TFSA)的制造方法。
首先,在室温的氮气气氛下,混合4-氨基-2-甲基-1-丁醇(24.8g,240mmol)和四氯化碳(111g,720mmol),接着将三苯基膦(69.2g,264mmol)溶解并加入到脱水二氯甲烷(150ml)中。在40°C下搅拌1小时至1.5小时,然后对反应溶液加入纯水(50ml)充分地搅拌而分成水层和二氯甲烷层。然后,利用纯水从二氯甲烷层萃取黄色油状物质(50ml×2次)。然后,利用甲苯洗涤水层(50ml×3次),然后通过减压蒸馏而去除溶剂而得到黄色油状物质。
将氢氧化钠(19.2g,480mmol)溶解于纯水(20ml),将氢氧化钠水溶液逐渐加入到所得到的黄色油状物质,搅拌12小时。然后,通过蒸馏得到了无色透明液体;3-甲基吡咯烷(18.7g,219mmol)。
对在水冷下的甲酸(21.6g,470mmol)缓慢加入3-甲基吡咯烷(18.7g,219mmol)。接着,对该溶液加入37%甲醛液(26ml,330mmol),在100°C下加热并回流,在产生气泡之后冷却至室温,并搅拌约30分钟。然后,再次加热并回流1小时。
在使用氢氧化钠中和甲酸之后,利用二乙醚萃取目的物,利用硫酸镁干燥,然后蒸馏而去除溶剂。然后,通过蒸馏得到了无色透明液体;1,3-二甲基吡咯烷(13.3g,134mmol)。
对添加有1,3-二甲基吡咯烷(12.0g,121mmol)的二氯甲烷(10ml)中加入溴丙烷(22.3g,182mmol)加热并回流24小时。蒸馏而去除溶剂来得到白色残渣,利用乙醇/乙酸乙酯对该白色残渣进行再结晶。进一步,在80°C下减压干燥24小时,从而得到白色固体;1,3-二甲基-1-丙基溴化吡咯烷(13.9g,63.4mmol)。
在纯水中,混合并搅拌1,3-二甲基-1-丙基溴化吡咯烷(5.30g,23.9mmol)和锂双(三氟甲磺酰)酰胺(7.55g,26.3mmol),从而立即得到不溶于水的离子液体。然后,在利用二氯甲烷萃取所得到的离子液体之后,利用纯水洗涤6次。通过蒸馏而去除溶剂并在100°C下进行真空干燥,得到了1,3-二甲基-1-丙基吡咯烷-双(三氟甲磺酰)酰胺(9.37g,22.2mmol)。
通过利用核磁共振(NMR)方法和质谱确认到通过上述步骤合成的化合物是目的物1,3-二甲基-1-丙基吡咯烷-双(三氟甲磺酰)酰胺。
下面示出所得到的化合物的1H NMR数据。
1H-NMR(CDCl3,400MHz,298K):δ=0.97-1.05(3H),1.15-1.21(3H),1.67-1.99(3H),2.28-2.48(1H),2.58-2.78(1H),2.94-3.08(1H),3.06,3.13(3H),3.18-3.34(2H),3.47-3.87(3H)
图7示出所得到的化合物的1H-NMR谱图。
下面示出所得到的化合物的的电喷雾电离质谱(ESI-MS)的测试结果。
MS(ESI-MS):m/z=142.22(M)+;C9H20N(142.16),m/z=279.95(M)-;C2F6NO4S2(279.92)
接下来,通过以下所示的方法求得所得到的化合物的物性值。
在25°C下使用株式会社SEKONIC(塞康聂克)制造的振动式粘度计(VM-10A)测定粘度。由于振动式粘度计的测定值是“粘度(mPa·s)×密度(g/ml)”,测定值除以密度来求得粘度。
在由氟树脂制作的框体内具备SUS株式会社制造的平板电极的传导单元(conductivity cell)中封入样品,进行交流阻抗测定来求得导电率。
交流阻抗测定是指使用由恒电位仪(potentiostat)和频率响应分析仪(FRA:frequency response analyzer)构成的阻抗测定系统来分析对测定对象施加的微小电压振幅的响应电流的方法。
对北斗电工株式会社制造的电化学测定系统HZ-5000连接株式会社NF回路设计制造的频率响应分析器FRA5022,并且在AC(交流)振幅为10mV、温度为25°C的条件下进行交流阻抗测定。
利用SII Nano Technology株式会社制造的示差扫描量热计DSC200,并且在测定温度范围为-100°C至100°C,升温速度为10°C/min的条件下测定熔点。
所得到的化合物的粘度是68mPa·s,导电率是3.4mS/cm。此外,熔点是-14°C。
实施例2
在本实施例中,将说明由结构式(201)表示的1,3-二甲基-1-丙基吡咯烷双(氟磺酰)酰胺(简称为3mP13-FSA)的制造方法。
首先,通过与实施例1同样的步骤合成1,3-二甲基-1-丙基溴化吡咯烷。
在纯水中,混合并搅拌1,3-二甲基-1-丙基溴化吡咯烷(11.4g,51.3mmol)和钾双(氟磺酰)酰胺(12.3g,56.1mmol),从而立即得到不溶于水的离子液体。然后,在利用二氯甲烷萃取所得到的离子液体之后,利用纯水洗涤6次。通过蒸馏而去除溶剂并在100°C下进行真空干燥,得到了1,3-二甲基-1-丙基吡咯烷-双(氟磺酰)酰胺(12.2g,37.8mmol)。
通过利用核磁共振(NMR)方法和质谱确认到通过上述步骤合成的化合物是目的物1,3-二甲基-1-丙基吡咯烷-双(氟磺酰)酰胺。
下面示出所得到的化合物的1H NMR数据。
1H-NMR(CDCl3,400MHz,298K):δ=0.99-1.08(3H),1.17-1.24(3H),1.74-1.97(3H),2.33-2.50(1H),2.60-2.78(1H),2.97-3.08(1H),3.09,3.16(3H),3.20-3.37(2H),3.48-3.88(3H)
图8示出所得到的化合物的1H-NMR谱图。
下面示出所得到的化合物的电子轰击质谱(electron impact massspectrometry;EI-MS)的测试结果。
MS(EI-MS):m/z=142.23(M)+;C9H20N(142.16),m/z=180.00(M)-;F2NO4S2(179.92)
通过与实施例1所示的方法同样的方法求得所得到的化合物的物性值。
所得到的化合物的粘度是50mPa·s,导电率是6.4mS/cm。此外,在-101°C处表示玻璃化转变点,确认不到明显的熔点。
实施例3
在本实施例中,将说明由结构式(202)表示的1,2-二甲基-1-丙基吡咯烷双(氟磺酰)酰胺(简称为2mP13-FSA)的制造方法。
首先,对在水冷下的甲酸(12.8g,250mmol)缓慢加入2-甲基吡咯烷(8.52g,100mmol)。接着,对该溶液加入37%甲醛液(11ml,150mmol),在100°C下加热并回流,在产生气泡之后冷却至室温,并搅拌约30分钟。然后,再次加热并回流1小时。
在使用氢氧化钠中和甲酸之后,利用二乙醚萃取目的物,利用硫酸镁干燥,然后蒸馏而去除溶剂。然后,通过蒸馏得到了无色透明液体;1,2-二甲基吡咯烷(6.97g,70.3mmol)。
对添加有1,2-二甲基吡咯烷(6.97g,70.3mmol)的二氯甲烷(10ml)中加入溴丙烷(12.9g,105mmol)加热并回流24小时。蒸馏而去除溶剂来得到白色残渣,利用乙醇/乙酸乙酯对该白色残渣进行再结晶。然后,在80°C下减压干燥24小时,从而得到白色固体;1,2-二甲基-1-丙基溴化吡咯烷(8.36g,37.6mmol)。
在纯水中,混合并搅拌1,2-二甲基-1-丙基溴化吡咯烷(6.44g,29.0mmol)和钾双(氟磺酰)酰胺(6.99g,3.19mmol),从而立即得到不溶于水的离子液体。然后,在利用二氯甲烷萃取所得到的离子液体之后,利用纯水洗涤6次。通过蒸馏而去除溶剂并在100°C下进行真空干燥,得到了1,2-二甲基-1-丙基吡咯烷-双(氟磺酰)酰胺(7.61g,23.6mmol)。
通过利用核磁共振(NMR)方法和质谱确认到通过上述步骤合成的化合物是目的物1,2-二甲基-1-丙基吡咯烷-双(氟磺酰)酰胺。
下面示出所得到的化合物的1H NMR数据。
1H-NMR(CDCl3,400MHz,298K):δ=1.05-1.11(3H),1.44-1.47(3H),1.75-1.96(3H),2.04-2.20(1H),2.22-2.35(1H),2.44-2.58(1H),2.81,3.09(3H),2.94-3.89(5H)
图9示出所得到的化合物的1H-NMR谱图。
下面示出所得到的化合物的电子轰击质谱(EI-MS)的测试结果。
MS(EI-MS):m/z=142.22(M)+;C9H20N(142.16),m/z=180.00(M)-;F2NO4S2(179.92)
通过与实施例1所示的方法同样的方法求得所得到的化合物的物性值。
所得到的化合物的粘度是82mPa·s,导电率是3.6mS/cm。此外,熔点是-34°C。
实施例4
在本实施例中,将说明对实施例1至3分别所示的3mP13-TFSA、2mP13-FSA及3mP13-FSA进行线性扫描伏安测定而算出电位窗的结果。
对在本实施例中使用的样品进行说明。作为样品1使用实施例1所说明的3mP13-TFSA,作为样品2使用2mP13-FSA,并且作为样品3使用3mP13-FSA。另外,作为对比样品1使用关东化学株式会社制造的1-甲基-1-丙基吡咯烷-双(氟磺酰)酰胺(简称为P13-FSA),作为对比样品2使用岸田化学株式会社制造的1-甲基-1-丙基吡咯烷-双(三氟甲基磺酰)酰胺(简称为P13-TFSA),并且作为对比样品3使用关东化学株式会社制造的1-乙基-3-甲基咪唑双(氟磺酰)酰胺(简称为EMI-FSA)。
通过使用北斗电工株式会社制造的电化学测定系统HZ-5000在氩气气氛下的手套箱中进行测定。作为工作电极使用玻碳电极,而作为对置电极使用铂线。作为参考电极,在以0.1M的浓度将三氟甲基磺酸银溶解于1-乙基-3-甲基咪唑双(三氟甲基磺酰)酰胺而成的溶液中浸渗银线。以二茂铁的氧化还原电位(Fc/Fc+)为基准补正离子液体的氧化还原电位。另外,电位扫描速度是50mV/s。
图10示出样品1至样品3及对比样品1至对比样品3的线性扫描伏安图。在图10中,粗线表示样品1至样品3,细线表示对比样品1至对比样品3。在粗线中,实线表示样品1,虚线表示样品2,并且链条线表示样品3。在细线中,实线表示对比样品1,虚线表示对比样品2,并且双点划线表示对比样品3。表2示出样品1至样品3及对比样品1至对比样品3的每个还原电位、氧化电位及电位窗。在本实施例中的电位窗是氧化电位和还原电位之间的差。在图10中,作为还原电位算出在扫描电位过程中检测到电流密度为-1mA/cm2的电位。另外,在图10中,作为氧化电位算出在扫描电位过程中检测到电流密度为1mA/cm2的电位。从“氧化电位”减去“还原电位”算出电位窗。
[表2]
由此可知,有关本发明的一个方式的离子液体的样品1至样品3与包含咪唑类阳离子的离子液体的对比样品3相比具有低还原电位和高氧化电位。另外,有关本发明的一个方式的离子液体的样品1至样品3具有不逊色于包含环季铵类阳离子的离子液体的对比样品1及对比样品2的电位窗。
接下来,参照图11及图12说明离子液体的液电阻和电解液中包含离子液体的双电层电容器的单元电阻的测定结果。
首先,参照图11说明双电层电容器的制造方法。
如图11所示那样,在本实施例中制造的双电层电容器是层压型双电层电容器。
层压型双电层电容器320包括:具有正极集电体301及正极活性物质层302的正极303;具有负极集电体304及负极活性物质层305的负极306;隔离体307;电解液308;以及框体309。
对在本实施例中使用的层压型双电层电容器的制造方法进行说明。
在本实施例中,至于除了电解液308以外的正极303、负极306、隔离体307以及框体309,使用市场上出售的产品。具体而言,作为正极303使用有限公司TAKUMI技研出售的电极,其中正极集电体301由铝箔形成,并且正极活性物质层302由活性炭/导电材料/SBR(Styrene-Butadiene Rubber:丁苯橡胶)/CMC(Carboxy MethylCellulose:羧甲基纤维素)(=90/10/2/2)形成。另外,作为负极306,与正极303同样地使用有限公司TAKUMI技研出售的电极,其中负极集电体304由铝箔形成,并且负极活性物质层305由活性炭/导电材料/SBR/CMC(=90/10/2/2)形成。另外,作为隔离体307使用日本高度纸工业株式会社制造的溶剂纺丝再生纤维素纤维(TF40)。另外,作为框体309使用由宝泉株式会社制造的铝层压薄膜(外层:尼龙+铝层/膜厚度25μm+40μm、内层:酸变性聚丙烯+聚丙烯/膜厚度22.5μm+22.5μm)构成的具有阀门的外装体。在正极303与负极306之间夹持隔离体307,将他们插入到框体309内,注入电解液308,最后进行密封。
这里,将作为电解液308使用3mP13-FSA的双电层电容器用作样品4,并且将作为电解液308使用关东化学株式会社制造的P13-FSA的双电层电容器用作对比样品4。
接下来,对样品4及对比样品4测定液电阻及单元电阻。通过进行交流阻抗测定来求得液电阻及单元电阻。
在将样品4及对比样品4在日本爱斯佩客(ESPEC)株式会社制造的恒温槽中分别保持为25°C、20°C、10°C、0°C、-10°C、-20°C、-30°C及-40°C的状态下,测定各个双电层电容器的阻抗。这里,使用北斗电工株式会社制造的多通道恒电位仪(multi-potentiostat)VSP进行恒电位交流阻抗测定。采用如下测定条件:起始频率为200kHz;AC(交流)振幅为10mV;以及终止频率为20mHz,并且以1.25V保持15分钟,然后进行测定。
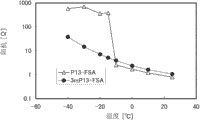
图12A示出样品4及对比样品4的液电阻,图12B示出样品4及对比样品4的单元电阻。注意,图12A所示的液电阻是频率为200kHz时的电阻,图12B所示的单元电阻是频率为20mHz时的电阻。在图12A及图12B中,横轴表示温度[°C],纵轴表示阻抗[Ω]。另外,在图12A及图12B中,圆圈表示样品4,三角表示对比样品4。
如图12A及图12B所示那样,对比样品4随着温度下降电阻值上升,并且在温度是-20°C以下时,电阻值急剧上升。另一方面,样品4虽然随着温度下降电阻值上升,但是没有发生电阻值急剧上升。
可以认为对比样品4由于在温度是-20°C以下时从液体相转变到固体而导致电阻值急剧上升。另一方面,可以认为样品4即使温度下降也没有从液体转变到固体,因此没有发生电阻值急剧上升。
接下来,参照图13说明对电解液包含离子液体的双电层电容器的负荷特性进行评价的结果。
用来测定负荷特性的双电层电容器是图11所示的层压型双电层电容器。另外,制造了具有与样品4及对比样品4相同的结构的双电层电容器。这里,将具有与样品4相同的结构的双电层电容器用作样品5,并且将具有与对比样品4相同的结构的双电层电容器用作对比样品5。另外,将作为电解液308使用岸田化学株式会社制造的1.0M的Et4NBF4/PC的双电层电容器用作对比样品6。注意,在对比样品6中,除了电解液308以外的结构与其他双电层电容器的结构相同。
接下来,对样品5、对比样品5及对比样品6进行充放电测试。通过使用北斗电工株式会社制造的电池充放电测试仪HJ-1010D8在25°C下进行充放电测试。以4mA(10C)进行CC充电,然后以2.5V进行CV充电(终止条件为0.4mA)。另外,以0.4mA至400mA(1C至1000C)进行放电。
图13示出样品5、对比样品5及对比样品6的输出特性。横轴表示电流密度,纵轴表示电容。另外,在图13中,圆圈表示样品5,三角表示对比样品5,并且四角表示对比样品6。
如图13所示那样,将有关本发明的一个方式的离子液体用于电解液的样品5具有不逊色于将有机溶剂用于电解液的对比样品6的输出特性。
由图10至图13的结果可知,有关本发明的一个方式的离子液体是电位窗宽、电化学稳定性良好且熔点低的离子液体。
实施例5
在本实施例中,将说明由结构式(203)表示的1-乙基-1,3-二甲基吡咯烷双(氟磺酰)酰胺(简称为3mP12-FSA)的制造方法。
首先,在N2气氛下对添加有1,3-二甲基吡咯烷(12.0g,121mmol)的脱水四氢呋喃(10ml)中加入溴丙烷(19.77g,182mmol)加热并回流24小时。接着,蒸馏而去除溶剂来得到白色残渣,利用乙醇/乙酸乙酯对该白色残渣进行再结晶。然后,在80°C下减压干燥24小时,从而得到白色固体;1-乙基-1,3-二甲基溴化吡咯烷(12.90g,62mmol)。
接下来,在纯水中,混合并搅拌1-乙基-1,3-二甲基溴化吡咯烷(12.90g,62mmol)和钾双(氟磺酰)酰胺(10.08g,46mmol),从而立即得到不溶于水的离子液体。然后,在利用二氯甲烷萃取所得到的离子液体之后,利用纯水洗涤6次。通过蒸馏而去除溶剂并在60°C下减压干燥约8小时,得到了1-乙基-1,3-二甲基吡咯烷双(氟磺酰)酰胺(16.26g,53mmol)。
通过利用核磁共振(NMR)方法和质谱确认到通过上述步骤合成的化合物是目的物1-乙基-1,3-二甲基吡咯烷双(氟磺酰)酰胺。
下面示出所得到的化合物的1H NMR数据。
1H-NMR(CDCl3,400MHz,298K):δ=1.15-1.25(3H),1.35-1.55(3H),1.83-1.89(1H),2.31-2.50(1H),2.58-2.78(1H),2.94-3.09(1H),2.99,3.05,3.09,3.15(3H),3.31-3.62(2H),3.45-3.62(2H),3.62,3.83(1H)
图14示出所得到的化合物的1H-NMR谱图。
下面示出所得到的化合物的电喷雾电离质谱(ESI-MS)的测试结果。
MS(EI-MS):m/z=142.23(M)+;C9H20N(142.16),m/z=180.00(M)-;F2NO4S2(179.92)
通过与实施例1所示的方法同样的方法求得所得到的化合物的物性值。
所得到的化合物的粘度是42mPa·s,导电率是8.9mS/cm。此外,熔点是-26°C。
接下来,将说明对3mP12-FSA进行线性扫描伏安测定而算出电位窗的结果。
通过使用北斗电工株式会社制造的电化学测定系统HZ-5000在氩气气氛下的手套箱中进行测定。作为工作电极使用玻碳电极,而作为对置电极使用铂线。作为参考电极,在以0.1M的浓度将三氟甲磺酸银溶解于1-乙基-3-甲基咪唑双(三氟甲基磺酰)酰胺而成的溶液中浸渗银线。以二茂铁的氧化还原电位(Li/Li+)为基准补正离子液体的氧化还原电位。另外,电位扫描速度是50mV/s。
图15示出3mP12-FSA的线性扫描伏安图。在图15中,作为还原电位算出在扫描电位过程中检测到电流密度为-1mA/cm2的电位。另外,在图15中,作为氧化电位算出在扫描电位过程中检测到电流密度为1mA/cm2的电位。从“氧化电位”减去“还原电位”算出电位窗。从图15的结果可知,还原电位是0.2V,氧化电位是5.6V,并且电位窗是5.4V。由以上结果可知,3mP12-FSA是电位窗宽的离子液体。
实施例6
在本实施例中,将说明对有关本发明的一个方式的锂离子二次电池进行充放电测试的结果。
首先,参照图16说明锂离子二次电池的制造方法。
如图16所示那样,在本实施例中制造的锂离子二次电池是硬币型锂离子二次电池。
硬币型锂离子二次电池330包括:具有正极集电体331及正极活性物质层332的正极333;具有负极集电体334及负极活性物质层335的负极336;隔离体337;以及框体339a、339b。
对在本实施例中使用的硬币型锂离子二次电池的制造方法进行说明。
本实施例中,至于除了电解液以外的正极333、负极336、隔离体337以及框体339a、339b,使用市场上出售的产品。具体而言,作为正极集电体331使用铝箔,并且在正极集电体331上形成由LiFePO4/乙炔黑/PVDF(聚偏氟乙烯)(=85/7/8)构成的正极活性物质层332,将它们用作正极333。另外,作为负极336使用锂电极。另外,作为隔离体337使用默克(Merck)株式会社制造的滤膜(membrane filter)(Durapore VVLP04700)。
另外,作为框体339a、339b使用宝泉株式会社出售的2032型硬币单元。将正极333插入到框体339a内,注入电解液,层叠负极336及框体339b,利用“硬币单元压合器(coin cell crimper)”使框体339a和339b嵌合,来制造硬币型锂离子二次电池。
这里,将使用对3mP13-FSA溶解约1M的锂双(三氟甲基磺酰)酰胺(简称为LiTFSA)而成的电解液的锂离子二次电池用作样品6。另外,将使用对3mP12-FSA溶解LiTFSA而成的电解液的锂离子二次电池用作样品7。
对样品6及样品7进行充放电测试。在通过使用北斗电工株式会社制造的电池充放电测试仪HJ-1010D8在日本爱斯佩客株式会社制造的恒温槽中保持为-25°C的状态下进行充放电测试。以0.04mA(0.02C)直到4.0V进行CC充电。另外,以0.04mA至0.2mA(0.02C至0.1C)进行放电。
图17A和17B示出样品6及样品7的输出特性。横轴表示电容,纵轴表示电压。
如图17A和17B所示那样,使用包含有关本发明的一个方式的离子液体的电解液的样品6及样品7是即使在-25°C的低温环境下也能够进行充放电的锂离子二次电池。就是说,这意味着有关本发明的一个方式的离子液体即使在-25°C的低温环境下也保持液体状态而不凝固。
符号说明
100 蓄电装置
101 正极集电体
102 正极活性物质层
103 正极
104 负极集电体
105 负极活性物质层
106 负极
107 隔离体
108 电解液
109 框体
109a 框体
109b 框体
110 蓄电装置
120 蓄电装置
130 蓄电装置
131 环状绝缘体
301 正极集电体
302 正极活性物质层
303 正极
304 负极集电体
305 负极活性物质层
306 负极
307 隔离体
308 电解液
309 框体
320 双电层电容器
330 锂离子二次电池
331 正极集电体
332 正极活性物质层
333 正极
334 负极集电体
335 负极活性物质层
336 负极
337 隔离体
339a 框体
339b 框体
3010 移动电话
3011 框体
3012 显示部
3013 操作按钮
3014 外部连接端口
3015 扬声器
3016 麦克风
3017 操作按钮
3030 电子书籍用终端
3031 框体
3032 轴部
3033 框体
3035 显示部
3037 显示部
3039 操作按钮
3041 扬声器
3043 电源
3050 电动汽车
3051 蓄电装置
3053 控制电路
3055 计算机
3057 驱动装置
3070 轮椅
3073 控制部
3075 驱动部
3077 控制器
Claims (22)
2.根据权利要求1所述的离子液体,其中A-是选自(CnF2n+1SO2)2N-(n=0至4)、(CmF2m+1SO3)-(m=0至4)和CF2(CF2SO2)2N-中的任一种的一价阴离子。
3.根据权利要求1所述的离子液体,
其中:
所述离子液体由通式(G1)表示;
R1至R4中的一种或两种是碳数为1至20的烷基、甲氧基、甲氧基甲基和甲氧基乙基中的任一个;
并且所述R1至R4中的其他三种或两种都是氢原子。
4.根据权利要求3所述的离子液体,其中所述R1至R4中的一种或两种都是碳数为1至4的烷基。
6.根据权利要求5所述的离子液体,其中所述R1和R2分别是碳数为1至4的烷基。
7.根据权利要求1所述的离子液体,
其中:
所述离子液体由通式(G3)表示;
并且R1是碳数为1至20的烷基、甲氧基、甲氧基甲基和甲氧基乙基中的任一个。
9.根据权利要求1所述的离子液体,
其中:
所述离子液体由通式(G5)表示;
并且R2是碳数为1至20的烷基、甲氧基、甲氧基甲基和甲氧基乙基中的任一个。
11.根据权利要求10所述的蓄电装置,其中A-是选自(CnF2n+1SO2)2N-(n=0至4)、(CmF2m+1SO3)-(m=0至4)和CF2(CF2SO2)2N-中的任一种的一价阴离子。
13.根据权利要求12所述的蓄电装置,其中所述R1至R4中的一种或两种都是碳数为1至4的烷基。
15.根据权利要求14所述的蓄电装置,其中所述R1和所述R2分别是碳数为1至4的烷基。
19.根据权利要求10所述的蓄电装置,
其中所述电解液还包括具有锂离子的电解质盐。
20.根据权利要求10所述的蓄电装置,其中所述蓄电装置是电容器。
21.根据权利要求20所述的蓄电装置,其中所述电容器是锂离子电容器或双电层电容器。
22.根据权利要求10所述的蓄电装置,其中所述蓄电装置是锂离子二次电池。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2011125116 | 2011-06-03 | ||
| JP2011-125116 | 2011-06-03 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN102807520A true CN102807520A (zh) | 2012-12-05 |
Family
ID=47231408
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2012101745667A Pending CN102807520A (zh) | 2011-06-03 | 2012-05-30 | 离子液体及使用离子液体的蓄电装置 |
Country Status (5)
| Country | Link |
|---|---|
| US (4) | US8951664B2 (zh) |
| JP (2) | JP5778625B2 (zh) |
| KR (1) | KR101945316B1 (zh) |
| CN (1) | CN102807520A (zh) |
| TW (2) | TWI577660B (zh) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103936677A (zh) * | 2013-01-21 | 2014-07-23 | 中国科学院大连化学物理研究所 | 一种基于全氟烷基磺酸根阴离子的磺酸功能化离子液体及其制备方法 |
| CN109074965A (zh) * | 2016-03-09 | 2018-12-21 | Zapgo有限公司 | 减少超级电容器排气的方法 |
| CN109155435A (zh) * | 2016-08-08 | 2019-01-04 | 株式会社日立制作所 | 固体电解质、全固态电池 |
| CN113169294A (zh) * | 2018-10-09 | 2021-07-23 | 科罗拉多大学董事会 | 改进锂离子电池中的离子液体电解质的性能的方法 |
| CN114008832A (zh) * | 2019-05-15 | 2022-02-01 | 原子能和替代能源委员会 | 用于在热失控的情况下熄灭电化学发生器的方法 |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5778625B2 (ja) | 2011-06-03 | 2015-09-16 | 株式会社半導体エネルギー研究所 | イオン液体、及びイオン液体を含む蓄電装置 |
| JP6151910B2 (ja) | 2011-12-23 | 2017-06-21 | 株式会社半導体エネルギー研究所 | イオン液体、非水溶媒、電解液、蓄電装置 |
| KR20130073822A (ko) | 2011-12-23 | 2013-07-03 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 이온 액체, 비수 전해질 및 축전 장치 |
| JP2014088361A (ja) | 2012-04-27 | 2014-05-15 | Semiconductor Energy Lab Co Ltd | 環状4級アンモニウム塩、非水溶媒、非水電解質及び蓄電装置 |
| KR20140045880A (ko) | 2012-10-09 | 2014-04-17 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 축전 장치 |
| JP6260209B2 (ja) * | 2013-11-08 | 2018-01-17 | 住友電気工業株式会社 | アルカリ金属イオンキャパシタ、その製造方法および充放電方法 |
| US10147556B2 (en) | 2014-03-31 | 2018-12-04 | Semiconductor Energy Laboratory Co., Ltd. | Power storage device and electronic device |
| JP6478775B2 (ja) * | 2014-05-15 | 2019-03-06 | キヤノン株式会社 | アミン化合物及びイオン導電剤、導電性樹脂組成物 |
| CN105578811B (zh) * | 2014-10-17 | 2018-09-04 | 小米科技有限责任公司 | 电子设备以及电子设备使用方法 |
| US10158108B2 (en) | 2014-10-24 | 2018-12-18 | Semiconductor Energy Laboratory Co., Ltd. | Power storage device including separator surrounding electrode |
| JP6592891B2 (ja) * | 2014-12-22 | 2019-10-23 | 日清紡ホールディングス株式会社 | 二次電池用電解液および二次電池 |
| JP2017178792A (ja) * | 2016-03-28 | 2017-10-05 | Tdk株式会社 | アンモニウム塩、リチウム二次電池用電解液およびこれを用いたリチウム二次電池 |
| JP7012660B2 (ja) | 2016-04-01 | 2022-02-14 | ノームズ テクノロジーズ インコーポレイテッド | リン含有修飾イオン性液体 |
| EP4087005A1 (en) | 2017-07-17 | 2022-11-09 | Nohms Technologies, Inc. | Phosphorus-containing electrolytes |
| JP6759173B2 (ja) * | 2017-09-20 | 2020-09-23 | 株式会社東芝 | 二次電池、電池パック及び車両 |
| WO2019135624A1 (ko) | 2018-01-03 | 2019-07-11 | 주식회사 엘지화학 | 겔 폴리머 전해질 조성물, 이에 의해 제조된 겔 폴리머 전해질 및 이를 포함하는 리튬 이차전지 |
| EP3694040A4 (en) * | 2018-01-03 | 2020-12-16 | Lg Chem, Ltd. | COMPOSITION OF POLYMERIC ELECTROLYTE GEL, POLYMERIC ELECTROLYTE GEL PREPARED FROM THE LATTER, AND SECONDARY LITHIUM BATTERY CONTAINING THE SAID COMPOSITION |
| WO2019225404A1 (ja) * | 2018-05-24 | 2019-11-28 | 日本ゼオン株式会社 | 電極材料、電極、蓄電デバイス、およびスラリー組成物 |
| US11784350B2 (en) * | 2019-12-20 | 2023-10-10 | Uchicago Argonne, Llc | Ionic liquid electrolyte for lithium-ion batteries |
Citations (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003331918A (ja) * | 2002-05-16 | 2003-11-21 | National Institute Of Advanced Industrial & Technology | 常温溶融塩及び常温溶融塩を用いたリチウム二次電池 |
| JP2005139100A (ja) * | 2003-11-05 | 2005-06-02 | Tosoh Corp | 常温溶融塩 |
| JP2005225843A (ja) * | 2004-02-16 | 2005-08-25 | Tosoh Corp | アルコキシアルキル基含有4級アンモニウム塩の製造方法 |
| CN1802362A (zh) * | 2003-07-01 | 2006-07-12 | 大塚化学株式会社 | 季铵盐与电解质及电化学装置 |
| JP2007051219A (ja) * | 2005-08-18 | 2007-03-01 | Koei Chem Co Ltd | 帯電防止性環状オレフィン系重合体組成物 |
| WO2007104144A1 (en) * | 2006-03-10 | 2007-09-20 | Transfert Plus, S.E.C. | Compounds, ionic liquids, molten salts and uses thereof |
| US20070235696A1 (en) * | 2002-06-21 | 2007-10-11 | Burrell Anthony K | Preparation and purification of ionic liquids and precursors |
| CN101103009A (zh) * | 2005-01-12 | 2008-01-09 | 大塚化学株式会社 | 季铵盐、电解质、电解液以及电化学装置 |
| JP2008084664A (ja) * | 2006-09-27 | 2008-04-10 | Sony Corp | 電気化学発光素子及び電気化学発光装置 |
| US20080084158A1 (en) * | 2006-10-05 | 2008-04-10 | Yan Shao | Hybrid polymer light-emitting devices |
| JP2009138254A (ja) * | 2007-02-13 | 2009-06-25 | Teijin Pharma Ltd | 電気化学的酸素発生素子 |
| WO2010022353A1 (en) * | 2008-08-21 | 2010-02-25 | Innova Meterials, Llc | Enhanced surfaces, coatings, and related methods |
| CN101679899A (zh) * | 2007-06-20 | 2010-03-24 | 慕尼黑克吕伯尔润滑器两合公司 | 润滑脂组合物 |
| EP2202826A1 (en) * | 2008-12-23 | 2010-06-30 | SMR PATENTS S.à.r.l. | Polymer Electrolytes and Devices containing them |
| WO2010095082A1 (en) * | 2009-02-18 | 2010-08-26 | Universita' Degli Studi Di Roma La Sapienza | High safety lithium-ion battery |
| CN101821892A (zh) * | 2007-06-29 | 2010-09-01 | 联邦科学及工业研究组织 | 锂储能装置 |
| CN101910263A (zh) * | 2007-05-29 | 2010-12-08 | 伊诺瓦材料有限责任公司 | 具有粒子的表面以及相关方法 |
| WO2011026993A1 (de) * | 2009-09-07 | 2011-03-10 | Xolution Gmbh | Behälterdeckel mit druckausgleichseinrichtung |
| CN103250297A (zh) * | 2010-10-12 | 2013-08-14 | 丰田自动车株式会社 | 离子液体、包含所述离子液体的锂二次电池电解质和包含所述电解质的锂二次电池 |
Family Cites Families (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0711966B2 (ja) * | 1986-03-17 | 1995-02-08 | 三洋電機株式会社 | 非水電解液電池 |
| US5202042A (en) | 1987-03-09 | 1993-04-13 | Nippon Chemi-Con Corporation | Heterocyclic electrolyte salts for electrolytic capacitors |
| JPH0810663B2 (ja) * | 1987-03-09 | 1996-01-31 | 日本ケミコン株式会社 | 電解コンデンサ用電解液 |
| EP0281994A1 (en) | 1987-03-09 | 1988-09-14 | Nippon Chemi-Con Corporation | An electrolyte for electrolytic capacitor |
| EP1380569B1 (en) | 2001-03-26 | 2013-02-20 | Nisshinbo Industries, Inc. | Ionic liquid of dimethylethyl(methoxyethyl)ammonium for an electric double layer capacitor and a secondary battery |
| JP4641646B2 (ja) * | 2001-04-06 | 2011-03-02 | 株式会社トクヤマ | 非水電解液用電解質 |
| US20050106440A1 (en) * | 2003-11-19 | 2005-05-19 | Honda Motor Co., Ltd. | Proton conductor and method for producing the same |
| EP1698631B1 (en) | 2003-12-26 | 2011-08-10 | National Institute of Advanced Industrial Science and Technology | Ionic liquid, method for producing same, double layer capacitor comprising same, and lithium battery |
| JP4070734B2 (ja) * | 2004-03-03 | 2008-04-02 | 株式会社東芝 | 電解液及び電気化学デバイス |
| CN101297434B (zh) | 2005-10-27 | 2010-05-26 | 株式会社Lg化学 | 包含低共熔混合物的二次电池及其制备方法 |
| SG174024A1 (en) * | 2006-08-02 | 2011-09-29 | Ada Techonologies Inc | High performance ultracapacitors with carbon nanomaterials and ionic liquids |
| ES2433206T3 (es) * | 2007-06-01 | 2013-12-09 | Invista Technologies S.À.R.L. | Líquidos iónicos como electrolitos |
| KR101002566B1 (ko) * | 2008-07-29 | 2010-12-17 | 삼성에스디아이 주식회사 | 리튬 이온 이차 전지용 전해액 및 이를 포함하는 리튬 이온이차 전지 |
| US20110070486A1 (en) | 2008-09-10 | 2011-03-24 | National Institute Of Advanced Industrial Science And Technology | Ionic liquid |
| FR2942235B1 (fr) | 2009-02-13 | 2011-07-22 | Centre Nat Rech Scient | Gels conducteurs ioniques, leur procede de preparation et leur utilisation comme electrolyte |
| US8927156B2 (en) | 2009-02-19 | 2015-01-06 | Semiconductor Energy Laboratory Co., Ltd. | Power storage device |
| JP2010239122A (ja) | 2009-03-09 | 2010-10-21 | Semiconductor Energy Lab Co Ltd | 蓄電デバイス |
| EP2287946A1 (en) | 2009-07-22 | 2011-02-23 | Belenos Clean Power Holding AG | New electrode materials, in particular for rechargeable lithium ion batteries |
| AU2011220397B2 (en) | 2010-02-27 | 2015-09-03 | Nuovo Film Suzhou China Inc. | Structures with surface-embedded additives and related manufacturing methods |
| US20110294005A1 (en) | 2010-05-28 | 2011-12-01 | Semiconductor Energy Laboratory Co., Ltd. | Power storage device, electrode, and electric device |
| US8795544B2 (en) | 2010-06-30 | 2014-08-05 | Semiconductor Energy Laboratory Co., Ltd. | Power storage device, lithium-ion secondary battery, electric double layer capacitor and lithium-ion capacitor |
| DE112011102750T5 (de) | 2010-08-19 | 2013-07-04 | Semiconductor Energy Laboratory Co., Ltd. | Elektrisches Gerät |
| US20120088151A1 (en) | 2010-10-08 | 2012-04-12 | Semiconductor Energy Laboratory Co., Ltd. | Positive-electrode active material and power storage device |
| CN106229475B (zh) | 2010-10-08 | 2019-12-17 | 株式会社半导体能源研究所 | 储能装置用正极活性材料的制造方法及储能装置 |
| JP5778625B2 (ja) * | 2011-06-03 | 2015-09-16 | 株式会社半導体エネルギー研究所 | イオン液体、及びイオン液体を含む蓄電装置 |
| US20120328960A1 (en) | 2011-06-24 | 2012-12-27 | Semiconductor Energy Laboratory Co., Ltd. | Nonaqueous solvent and power storage device |
| JP6151910B2 (ja) | 2011-12-23 | 2017-06-21 | 株式会社半導体エネルギー研究所 | イオン液体、非水溶媒、電解液、蓄電装置 |
| KR20130073822A (ko) | 2011-12-23 | 2013-07-03 | 가부시키가이샤 한도오따이 에네루기 켄큐쇼 | 이온 액체, 비수 전해질 및 축전 장치 |
| EP3332865B1 (en) * | 2016-12-11 | 2021-02-03 | Fast&Fluid Management B.V. | Stirrer for a viscous liquid |
-
2012
- 2012-05-24 JP JP2012118224A patent/JP5778625B2/ja not_active Expired - Fee Related
- 2012-05-24 US US13/479,582 patent/US8951664B2/en active Active
- 2012-05-29 TW TW101119123A patent/TWI577660B/zh not_active IP Right Cessation
- 2012-05-29 TW TW105133565A patent/TWI624456B/zh not_active IP Right Cessation
- 2012-05-30 KR KR1020120057797A patent/KR101945316B1/ko active IP Right Grant
- 2012-05-30 CN CN2012101745667A patent/CN102807520A/zh active Pending
-
2015
- 2015-01-20 US US14/600,135 patent/US9171677B2/en active Active
- 2015-05-04 JP JP2015094494A patent/JP6002807B2/ja not_active Expired - Fee Related
- 2015-10-21 US US14/918,830 patent/US9583276B2/en active Active
-
2017
- 2017-02-23 US US15/440,964 patent/US9997806B2/en not_active Expired - Fee Related
Patent Citations (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003331918A (ja) * | 2002-05-16 | 2003-11-21 | National Institute Of Advanced Industrial & Technology | 常温溶融塩及び常温溶融塩を用いたリチウム二次電池 |
| US20070235696A1 (en) * | 2002-06-21 | 2007-10-11 | Burrell Anthony K | Preparation and purification of ionic liquids and precursors |
| CN1802362A (zh) * | 2003-07-01 | 2006-07-12 | 大塚化学株式会社 | 季铵盐与电解质及电化学装置 |
| JP2005139100A (ja) * | 2003-11-05 | 2005-06-02 | Tosoh Corp | 常温溶融塩 |
| JP2005225843A (ja) * | 2004-02-16 | 2005-08-25 | Tosoh Corp | アルコキシアルキル基含有4級アンモニウム塩の製造方法 |
| CN101103009A (zh) * | 2005-01-12 | 2008-01-09 | 大塚化学株式会社 | 季铵盐、电解质、电解液以及电化学装置 |
| JP2007051219A (ja) * | 2005-08-18 | 2007-03-01 | Koei Chem Co Ltd | 帯電防止性環状オレフィン系重合体組成物 |
| WO2007104144A1 (en) * | 2006-03-10 | 2007-09-20 | Transfert Plus, S.E.C. | Compounds, ionic liquids, molten salts and uses thereof |
| JP2008084664A (ja) * | 2006-09-27 | 2008-04-10 | Sony Corp | 電気化学発光素子及び電気化学発光装置 |
| US20080084158A1 (en) * | 2006-10-05 | 2008-04-10 | Yan Shao | Hybrid polymer light-emitting devices |
| JP2009138254A (ja) * | 2007-02-13 | 2009-06-25 | Teijin Pharma Ltd | 電気化学的酸素発生素子 |
| CN101910263A (zh) * | 2007-05-29 | 2010-12-08 | 伊诺瓦材料有限责任公司 | 具有粒子的表面以及相关方法 |
| CN101679899A (zh) * | 2007-06-20 | 2010-03-24 | 慕尼黑克吕伯尔润滑器两合公司 | 润滑脂组合物 |
| CN101821892A (zh) * | 2007-06-29 | 2010-09-01 | 联邦科学及工业研究组织 | 锂储能装置 |
| WO2010022353A1 (en) * | 2008-08-21 | 2010-02-25 | Innova Meterials, Llc | Enhanced surfaces, coatings, and related methods |
| EP2202826A1 (en) * | 2008-12-23 | 2010-06-30 | SMR PATENTS S.à.r.l. | Polymer Electrolytes and Devices containing them |
| WO2010095082A1 (en) * | 2009-02-18 | 2010-08-26 | Universita' Degli Studi Di Roma La Sapienza | High safety lithium-ion battery |
| WO2011026993A1 (de) * | 2009-09-07 | 2011-03-10 | Xolution Gmbh | Behälterdeckel mit druckausgleichseinrichtung |
| CN103250297A (zh) * | 2010-10-12 | 2013-08-14 | 丰田自动车株式会社 | 离子液体、包含所述离子液体的锂二次电池电解质和包含所述电解质的锂二次电池 |
Non-Patent Citations (1)
| Title |
|---|
| 田鹏,等编著: "《绿色溶剂—离子液体的相平衡和微观结构》", 31 August 2009, 科学出版社 * |
Cited By (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103936677A (zh) * | 2013-01-21 | 2014-07-23 | 中国科学院大连化学物理研究所 | 一种基于全氟烷基磺酸根阴离子的磺酸功能化离子液体及其制备方法 |
| CN103936677B (zh) * | 2013-01-21 | 2016-06-29 | 中国科学院大连化学物理研究所 | 一种基于全氟烷基磺酸根阴离子的磺酸功能化离子液体及其制备方法 |
| CN109074965A (zh) * | 2016-03-09 | 2018-12-21 | Zapgo有限公司 | 减少超级电容器排气的方法 |
| CN109074965B (zh) * | 2016-03-09 | 2021-08-13 | Zapgo有限公司 | 减少超级电容器排气的方法 |
| CN109155435A (zh) * | 2016-08-08 | 2019-01-04 | 株式会社日立制作所 | 固体电解质、全固态电池 |
| CN109155435B (zh) * | 2016-08-08 | 2021-06-15 | 株式会社日立制作所 | 固体电解质、全固态电池 |
| CN113169294A (zh) * | 2018-10-09 | 2021-07-23 | 科罗拉多大学董事会 | 改进锂离子电池中的离子液体电解质的性能的方法 |
| CN114008832A (zh) * | 2019-05-15 | 2022-02-01 | 原子能和替代能源委员会 | 用于在热失控的情况下熄灭电化学发生器的方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| US9997806B2 (en) | 2018-06-12 |
| KR20120135067A (ko) | 2012-12-12 |
| JP6002807B2 (ja) | 2016-10-05 |
| US20160042876A1 (en) | 2016-02-11 |
| US20150132665A1 (en) | 2015-05-14 |
| TWI577660B (zh) | 2017-04-11 |
| US20170229739A1 (en) | 2017-08-10 |
| TWI624456B (zh) | 2018-05-21 |
| TW201706243A (zh) | 2017-02-16 |
| JP2013010745A (ja) | 2013-01-17 |
| US8951664B2 (en) | 2015-02-10 |
| US9583276B2 (en) | 2017-02-28 |
| JP5778625B2 (ja) | 2015-09-16 |
| JP2015178509A (ja) | 2015-10-08 |
| US9171677B2 (en) | 2015-10-27 |
| TW201311641A (zh) | 2013-03-16 |
| US20120308882A1 (en) | 2012-12-06 |
| KR101945316B1 (ko) | 2019-02-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN102807520A (zh) | 离子液体及使用离子液体的蓄电装置 | |
| JP6634415B2 (ja) | 蓄電装置 | |
| US10581118B2 (en) | Co-solvents with high coulombic efficiency in propylene carbonate based electrolytes | |
| CN103172556B (zh) | 离子液体、非水电解质及蓄电装置 | |
| CN103178299B (zh) | 非水溶剂、非水电解质及蓄电装置 | |
| CN104245703B (zh) | 环状季铵盐、非水溶剂、非水电解质及蓄电装置 | |
| KR20150056481A (ko) | 화합물, 비수 전해질 및 축전 장치 | |
| Patterson | Chemical shuttle additives in lithium ion batteries | |
| JP2017183237A (ja) | 二次電池用有機正極活物質、二次電池および有機化合物 | |
| Krishnan et al. | Organic solvents containing zwitterion as electrolyte for Li ion cells | |
| JP2022164578A (ja) | 電極活物質、電極及びその製造方法、二次電池、並びに化合物 | |
| JP2006048972A (ja) | 二次電池 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| RJ01 | Rejection of invention patent application after publication |
Application publication date: 20121205 |
|
| RJ01 | Rejection of invention patent application after publication |