CN101948552B - 线型聚苯乙烯支载手性噁唑烷-2-硒酮及其制备方法 - Google Patents
线型聚苯乙烯支载手性噁唑烷-2-硒酮及其制备方法 Download PDFInfo
- Publication number
- CN101948552B CN101948552B CN2010102652707A CN201010265270A CN101948552B CN 101948552 B CN101948552 B CN 101948552B CN 2010102652707 A CN2010102652707 A CN 2010102652707A CN 201010265270 A CN201010265270 A CN 201010265270A CN 101948552 B CN101948552 B CN 101948552B
- Authority
- CN
- China
- Prior art keywords
- compound
- oxazolidine
- reaction
- selenone
- organic solvent
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 238000002360 preparation method Methods 0.000 title description 5
- 239000011669 selenium Substances 0.000 title description 5
- 229910052711 selenium Inorganic materials 0.000 title 1
- 238000006243 chemical reaction Methods 0.000 claims abstract description 36
- 239000004793 Polystyrene Substances 0.000 claims abstract description 16
- 229920002223 polystyrene Polymers 0.000 claims abstract description 16
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 claims description 57
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 claims description 40
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 33
- 150000001875 compounds Chemical class 0.000 claims description 33
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 21
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical group ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 claims description 20
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 claims description 16
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 claims description 14
- -1 lithium aluminum hydride Chemical compound 0.000 claims description 14
- 239000003960 organic solvent Substances 0.000 claims description 14
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 claims description 12
- 230000035484 reaction time Effects 0.000 claims description 11
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical group N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 claims description 10
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 claims description 10
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 claims description 9
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 8
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 claims description 8
- 238000000034 method Methods 0.000 claims description 7
- ZRZHXNCATOYMJH-UHFFFAOYSA-N 1-(chloromethyl)-4-ethenylbenzene Chemical compound ClCC1=CC=C(C=C)C=C1 ZRZHXNCATOYMJH-UHFFFAOYSA-N 0.000 claims description 6
- ZSXGLVDWWRXATF-UHFFFAOYSA-N N,N-dimethylformamide dimethyl acetal Chemical compound COC(OC)N(C)C ZSXGLVDWWRXATF-UHFFFAOYSA-N 0.000 claims description 6
- BUGBHKTXTAQXES-UHFFFAOYSA-N Selenium Chemical compound [Se] BUGBHKTXTAQXES-UHFFFAOYSA-N 0.000 claims description 6
- WETWJCDKMRHUPV-UHFFFAOYSA-N acetyl chloride Chemical compound CC(Cl)=O WETWJCDKMRHUPV-UHFFFAOYSA-N 0.000 claims description 6
- 239000012346 acetyl chloride Substances 0.000 claims description 6
- 230000003197 catalytic effect Effects 0.000 claims description 6
- 229940126214 compound 3 Drugs 0.000 claims description 6
- 229940125898 compound 5 Drugs 0.000 claims description 6
- 239000012280 lithium aluminium hydride Substances 0.000 claims description 6
- YNESATAKKCNGOF-UHFFFAOYSA-N lithium bis(trimethylsilyl)amide Chemical compound [Li+].C[Si](C)(C)[N-][Si](C)(C)C YNESATAKKCNGOF-UHFFFAOYSA-N 0.000 claims description 6
- 229910000027 potassium carbonate Inorganic materials 0.000 claims description 6
- 239000003999 initiator Substances 0.000 claims description 5
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 claims description 4
- 229940125782 compound 2 Drugs 0.000 claims description 4
- YNQLUTRBYVCPMQ-UHFFFAOYSA-N alpha-methyl toluene Natural products CCC1=CC=CC=C1 YNQLUTRBYVCPMQ-UHFFFAOYSA-N 0.000 claims description 2
- 150000003983 crown ethers Chemical class 0.000 claims description 2
- 238000006798 ring closing metathesis reaction Methods 0.000 claims description 2
- 239000003153 chemical reaction reagent Substances 0.000 abstract description 18
- 238000001514 detection method Methods 0.000 abstract description 5
- 238000007867 post-reaction treatment Methods 0.000 abstract description 3
- 239000002994 raw material Substances 0.000 abstract description 3
- 238000004064 recycling Methods 0.000 abstract description 3
- GWLYOSPGFKDZAH-UHFFFAOYSA-N [Se]=C1NCCO1 Chemical compound [Se]=C1NCCO1 GWLYOSPGFKDZAH-UHFFFAOYSA-N 0.000 abstract description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 24
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 16
- 239000000047 product Substances 0.000 description 15
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 13
- 239000011780 sodium chloride Substances 0.000 description 12
- 239000007787 solid Substances 0.000 description 12
- 239000002904 solvent Substances 0.000 description 12
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical class O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 10
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- 239000003208 petroleum Substances 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- 238000003786 synthesis reaction Methods 0.000 description 8
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 6
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 6
- 239000012141 concentrate Substances 0.000 description 6
- 239000000706 filtrate Substances 0.000 description 6
- 229920000642 polymer Polymers 0.000 description 6
- 238000000926 separation method Methods 0.000 description 6
- 238000000746 purification Methods 0.000 description 5
- MXZROAOUCUVNHX-UHFFFAOYSA-N 2-Aminopropanol Chemical compound CCC(N)O MXZROAOUCUVNHX-UHFFFAOYSA-N 0.000 description 4
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 4
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 4
- 238000004440 column chromatography Methods 0.000 description 4
- 229910001873 dinitrogen Inorganic materials 0.000 description 4
- 238000004458 analytical method Methods 0.000 description 3
- 239000007791 liquid phase Substances 0.000 description 3
- 239000007790 solid phase Substances 0.000 description 3
- CNBUSIJNWNXLQQ-NSHDSACASA-N (2s)-3-(4-hydroxyphenyl)-2-[(2-methylpropan-2-yl)oxycarbonylamino]propanoic acid Chemical compound CC(C)(C)OC(=O)N[C@H](C(O)=O)CC1=CC=C(O)C=C1 CNBUSIJNWNXLQQ-NSHDSACASA-N 0.000 description 2
- XEZNGIUYQVAUSS-UHFFFAOYSA-N 18-crown-6 Chemical compound C1COCCOCCOCCOCCOCCO1 XEZNGIUYQVAUSS-UHFFFAOYSA-N 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 2
- ZCQWOFVYLHDMMC-UHFFFAOYSA-N Oxazole Chemical compound C1=COC=N1 ZCQWOFVYLHDMMC-UHFFFAOYSA-N 0.000 description 2
- 235000004279 alanine Nutrition 0.000 description 2
- 238000011914 asymmetric synthesis Methods 0.000 description 2
- 230000008033 biological extinction Effects 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 238000007664 blowing Methods 0.000 description 2
- 239000000969 carrier Substances 0.000 description 2
- 238000007877 drug screening Methods 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 235000019256 formaldehyde Nutrition 0.000 description 2
- 239000000178 monomer Substances 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 239000012074 organic phase Substances 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- GYSDUVRPSWKYDJ-UHFFFAOYSA-N selinone Chemical compound C1=CC(OCC=C(C)C)=CC=C1C1OC2=CC(O)=CC(O)=C2C(=O)C1 GYSDUVRPSWKYDJ-UHFFFAOYSA-N 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- MMGCJLGQCXYAAW-KRWDZBQOSA-N C=Cc1ccc(COc2ccc(C[C@@H](CO)N)cc2)cc1 Chemical compound C=Cc1ccc(COc2ccc(C[C@@H](CO)N)cc2)cc1 MMGCJLGQCXYAAW-KRWDZBQOSA-N 0.000 description 1
- DURZGLLNSJDUGF-FQEVSTJZSA-N CC(C)(C)OC(N[C@@H](Cc(cc1)ccc1OCc1ccc(C=C)cc1)CO)=O Chemical compound CC(C)(C)OC(N[C@@H](Cc(cc1)ccc1OCc1ccc(C=C)cc1)CO)=O DURZGLLNSJDUGF-FQEVSTJZSA-N 0.000 description 1
- 238000007259 addition reaction Methods 0.000 description 1
- 238000005575 aldol reaction Methods 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 239000012752 auxiliary agent Substances 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 238000001212 derivatisation Methods 0.000 description 1
- ROBXZHNBBCHEIQ-BYPYZUCNSA-N ethyl (2s)-2-aminopropanoate Chemical compound CCOC(=O)[C@H](C)N ROBXZHNBBCHEIQ-BYPYZUCNSA-N 0.000 description 1
- 125000000524 functional group Chemical group 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 230000036632 reaction speed Effects 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 238000010008 shearing Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
Landscapes
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
Abstract
本发明涉及线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮,其结构如下:
Description
技术领域
本发明涉及一种线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮及其制备方法。
背景技术
有机合成反应中产物的分离和纯化一直都是棘手的难题。固相有机合成法将反应底物支载到不溶性载体上,再通过“分子剪切”得到高纯的产物,已经广泛应用到组合化学和高通量药物筛选中。但固相有机合成存在非均相反应、反应时间长、反应速度和方式难以预计、不能用常规的分析方法进行在线检测等不足。经过探索研究,人们发现利用可溶性载体进行液相合成不仅具有固相有机合成的优点,还兼具经典液相反应的均相反应、反应快、便于在线检测等优点。因此可溶性聚合物被广泛地应用,并逐渐替代不可溶聚合物支载合成大量的小分子化合物库,进一步提高了药物筛选的效率。
线型聚苯乙烯(NCPS)是一类应用广泛的可溶性聚合物载体,容易制备,通过改变单体物质量比,可调节其支载容量。NCPS在二氯甲烷、苯、乙酸乙酯、四氢呋喃等溶剂中具有很好的溶解性,但在水、甲醇、乙醇等溶剂中不溶,反应完成后用甲醇等溶剂将聚合物沉淀,通过过滤并用甲醇等溶剂洗涤除去过量的小分子物质,方便分离纯化。线型聚苯乙烯支载的液相有机合成,可以用TLC、HPLC、IR及NMR等测定其骨架结构、功能基及支载容量,监测分离纯度,广泛地应用于有机合成中。
利用手性辅助试剂进行不对称合成是一类重要的不对称合成方法。手性噁唑硒酮是一类新颖的手性辅助试剂,用来诱导不对称Aldol反应、烷基化反应和共轭加成反应等多种不对称反应,与其他手性助剂相比,具有较高的立体选择性。手性噁唑硒酮同时也是一类优良的手性衍生试剂,常被用来测定手性化合物的绝对构型和ee值,但价格较为昂贵,难以回收重复使用。
聚合物支载合成具有易于分离纯化、可回收重复使用等优点,将手性辅助试剂支载在聚合物载体上诱导不对称反应能使反应产物容易从体系中分离,而且昂贵的手性辅助试剂可以回收重复使用,甚至有望发展成为一个连续的产生手性产物的体系。
在本发明中,我们将(4S)-噁唑烷-2-硒酮支载在线型聚苯乙烯上,制得线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮手性辅助试剂,不仅保留了该类手性辅助试剂诱导不对称反应的高收率以及高立体选择性,同时实现了手性辅助试剂的回收循环使用。
发明内容
本发明所要解决的问题是提供能作为手性辅助试剂在诱导不对称反应中进行均相反应,反应快,便于在线检测且能够回收循环使用的线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮及其制备方法,本发明原料及试剂价廉易得,路线可行,反应后处理简单。
本发明提供的技术方案是,线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮,其结构如下:
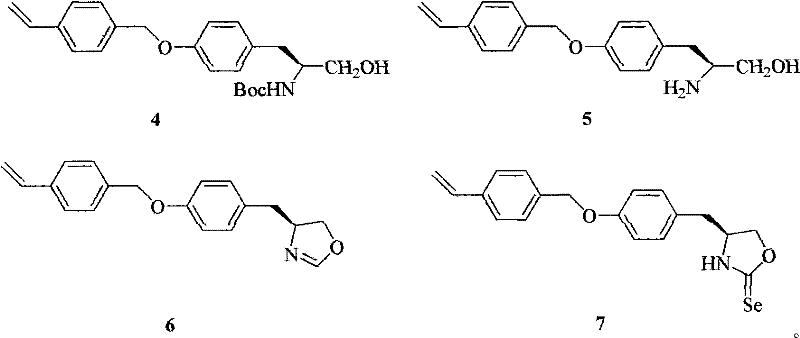
式中m∶n=1∶1~4,Mw=8100~13500。
本发明还提供了线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮的制备方法:
(1)在有机溶剂中,碳酸钾和催化量的冠醚的作用下,化合物2和对乙烯基苄氯反应得到化合物3,反应温度为20~60℃,反应时间为12~48h,上述化合物的摩尔比为化合物2∶碳酸钾∶对乙烯基苄氯=1∶1~3∶1~1.5;
(2)在有机溶剂中,化合物3在氢化铝锂作用下还原得到化合物4,反应温度为0~25℃,反应时间为8~12h,上述化合物的摩尔比为化合物3∶氢化铝锂=1∶1~1.5;
(3)在有机溶剂中,化合物4和乙酰氯反应得到化合物5,反应温度为20~40℃,反应时间为12~24h,上述化合物的摩尔比为化合物4∶乙酰氯=1∶2~4;
(4)在有机溶剂中,催化量的对甲基苯磺酸作用下,化合物5和N,N-二甲基甲酰胺二甲缩醛反应关环得到化合物6,反应温度为90~120℃,反应时间为24~36h,上述化合物的摩尔比为化合物5∶N,N-二甲基甲酰胺二甲缩醛=1∶1~1.5;
(5)在有机溶剂中,化合物6在六甲基二硅胺基锂的作用下与硒粉反应得到化合物7,反应温度为-78~25℃,反应时间为2~3h,上述化合物的摩尔比为化合物6∶六甲基二硅胺基锂∶硒粉=1∶1~1.5∶1~1.5;
(6)在有机溶剂中,化合物7和苯乙烯在引发剂的作用下共聚得到线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮,反应温度为60~80℃,反应时间为72~96h,上述化合物的摩尔比为化合物7∶苯乙烯=1∶1~4,所述的引发剂是偶氮二异丁腈,用量为两单体总量的2mol%;
上述化合物2,3,4,5,6,7具有下列的结构式:
所述有机溶剂为二氯甲烷、三氯甲烷、N,N-二甲基甲酰胺、四氢呋喃、甲醇、乙醇、乙酸乙酯、苯或甲苯。
上述反应过程由如下反应式表示:
本发明提出了一种线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮及其制备方法。将(4S)-噁唑烷-2-硒酮支载在线型聚苯乙烯上,作为手性辅助试剂诱导不对称反应为均相反应,反应快,便于在线检测。该手性辅助试剂不仅保留了噁唑烷-2-硒酮类手性辅助试剂诱导不对称反应的高收率以及高立体选择性,同时实现了(4S)-噁唑烷-2-硒酮的回收循环使用。本发明原料及试剂价廉易得,路线可行,反应后处理简单。
具体实施方式
通过以下实施例将有助于理解本发明,但并不限制本发明的内容。
实施例1
N-叔丁氧羰基-L-酪氨酸乙酯(5.0g,16.17mmol)溶于N,N-二甲基甲酰胺(50mL),加入催化量18-冠-6和无水碳酸钾(6.69g,48.51mmol),以2滴/秒逐滴(每滴约0.05mL,下同)滴加对乙烯基苄氯(3.42mL,24.26mmol)的N,N-二甲基甲酰胺(15mL)溶液,20℃反应48h。减压蒸馏除去溶剂后,加入乙酸乙酯(100mL),用饱和食盐水洗涤(3×10mL),无水硫酸镁干燥,除去溶剂后用乙酸乙酯和石油醚(1∶3,体积比)重结晶得白色固体,即产物(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-(N-叔丁氧羰基)氨基丙酸乙酯(5.73g,83.3%)。m.p.76.6-77.8℃;[α]D 20=+0.9(c 0.09,THF);IR(NaCl):υ3377,2978,1716cm-1;1H NMR(CDCl3,600MHz):δ7.42(2H,d,J=7.8Hz,ArH),7.37(2H,d,J=7.8Hz,ArH),7.04(2H,d,J=7.8Hz,ArH),6.88(2H,d,J=8.4Hz,ArH),6.73(1H,dd,J1=10.8Hz,J2=17.4Hz,CH2=CH),5.75(1H,d,J=17.4Hz,CH2=CH),5.25(1H,d,J=11.4Hz,CH2=CH),5.02(2H,s,ArCH2O),4.97(1H,d,J=7.2Hz,Boc-NH),4.51(1H,d,J=7.2Hz,CHN),4.15(2H,q,J=6.6Hz,OCH2),3.02(2H,q,J=6.0Hz,ArCH2),1.42(9H,s,Boc),1.23(3H,t,J=7.2Hz,CH3);13C NMR(CDCl3,150MHz):δ171.9,157.8,155.1,137.3,136.5,136.4,130.3,128.3(2C),127.6(2C),126.4(2C),114.8,114.0(2C),79.8,69.7,61.2,54.5,37.5,28.3(3C),14.1.
实施例2
N-叔丁氧羰基-L-酪氨酸乙酯(5.0g,16.17mmol)溶于N,N-二甲基甲酰胺(50mL),加入催化量18-冠-6和无水碳酸钾(2.23g,16.17mmol),以2滴/秒逐滴滴加对乙烯基苄氯(2.28mL,16.17mmol)的N,N’-二甲基甲酰胺(15mL)溶液,60℃搅拌12h。减压蒸馏除去溶剂后,加入乙酸乙酯(100mL)稀释,用饱和食盐水洗涤(3×10mL),无水硫酸镁干燥,除去溶剂后用乙酸乙酯和石油醚(1∶3,体积比)重结晶得白色固体,即产物(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-(N-叔丁氧羰基)氨基丙酸乙酯(5.79g,84.2%)。m.p.76.6-77.8℃;[α]D 20=+0.9(c 0.09,THF);IR(NaCl):υ3377,2978,1716cm-1;1H NMR(CDCl3,600MHz):δ7.42(2H,d,J=7.8Hz,ArH),7.37(2H,d,J=7.8Hz,ArH),7.04(2H,d,J=7.8Hz,ArH),6.88(2H,d,J=8.4Hz,ArH),6.73(1H,dd,J1=10.8Hz,J2=17.4Hz,CH2=CH),5.75(1H,d,J=17.4Hz,CH2=CH),5.25(1H,d,J=11.4Hz,CH2=CH),5.02(2H,s,ArCH2O),4.97(1H,d,J=7.2Hz,Boc-NH),4.51(1H,d,J=7.2Hz,CHN),4.15(2H,q,J=6.6Hz,OCH2),3.02(2H,q,J=6.0Hz,ArCH2),1.42(9H,s,Boc),1.23(3H,t,J=7.2Hz,CH3);13C NMR(CDCl3,150MHz):δ171.9,157.8,155.1,137.3,136.5,136.4,130.3,128.3(2C),127.6(2C),126.4(2C),114.8,114.0(2C),79.8,69.7,61.2,54.5,37.5,28.3(3C),14.1.
实施例3
干燥的(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-(N-叔丁氧羰基)氨基丙酸乙酯(5.5g,12.93mmol)溶于无水四氢呋喃(50mL),保持温度在-10℃以下以1滴/秒滴加氢化铝锂(0.74g,19.40mmol)的四氢呋喃悬浮液(10mL),室温下搅拌8h。用10%HCl溶液调节pH至6-7,过滤,沉淀反复用丙酮洗涤,滤液浓缩。加入乙酸乙酯(100mL),用饱和食盐水洗涤(3×10mL),无水硫酸镁干燥,除去溶剂后用乙酸乙酯和石油醚(1∶5,体积比)重结晶得白色固体,即产物(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-(N-叔丁氧羰基)氨基丙醇(4.14g,83.5%)。m.p.101.7-102.6℃;[α]D 20=-2.1(c 0.26,THF);IR(NaCl):υ3359,2927,1686cm-1;1H NMR(CDCl3,600MHz):δ7.41(2H,d,J=8.4Hz,ArH),7.37(2H,d,J=7.8Hz,ArH),7.10(2H,d,J=8.4Hz,ArH),6.89(2H,d,J=8.4Hz,ArH),6.73(1H,dd,J1=10.8Hz,J2=18Hz,CH2=CH),5.75(1H,d,J=17.4Hz,CH2=CH),5.24(1H,d,J=11.4Hz,CH2=CH),5.02(2H,s,ArCH2O),4.78(1H,s,Boc-NH),3.80(1H,s,CH-N),3.68(1H,m,CH2-O-),3.55(1H,m,CH2-O-),2.76(2H,d,J=7.2Hz,ArCH2),1.6(1H,s,OH),1.40(9H,s,Boc);13C NMR(CDCl3,150MHz):δ157.5,137.3,136.6,136.4(2C),130.2(2C),130.0,127.6(2C),126.4(2C),115.0(2C),114.0,79.5,69.8,65,54,36.7,28.3(3C).
实施例4
干燥的(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-(N-叔丁氧羰基)氨基丙酸乙酯(5.5g,12.93mmol)溶于无水四氢呋喃(50mL),保持温度在-10℃以下以1滴/秒滴加氢化铝锂(0.49g,12.93mmol)的四氢呋喃悬浮液(10mL),室温下搅拌12h。用10%HCl溶液调节pH至6-7,过滤,沉淀反复用丙酮洗涤,滤液浓缩。加入乙酸乙酯(100mL),用饱和食盐水洗涤(3×10mL),无水硫酸镁干燥,除去溶剂后用乙酸乙酯和石油醚(1∶5,体积比)重结晶得白色固体,即产物(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-(N-叔丁氧羰基)氨基丙醇(4.05g,81.8%)。m.p.101.7-102.6℃;[α]D 20=-2.1(c 0.26,THF);IR(NaCl):υ3359,2927,1686cm-1;1H NMR(CDCl3,600MHz):δ7.41(2H,d,J=8.4Hz,ArH),7.37(2H,d,J=7.8Hz,ArH),7.10(2H,d,J=8.4Hz,ArH),6.89(2H,d,J=8.4Hz,ArH),6.73(1H,dd,J1=10.8Hz,J2=18Hz,CH2=CH),5.75(1H,d,J=17.4Hz,CH2=CH),5.24(1H,d,J=11.4Hz,CH2=CH),5.02(2H,s,ArCH2O),4.78(1H,s,Boc-NH),3.80(1H,s,CH-N),3.68(1H,m,CH2-O-),3.55(1H,m,CH2-O-),2.76(2H,d,J=7.2Hz,ArCH2),1.6(1H,s,OH),1.40(9H,s,Boc);13C NMR(CDCl3,150MHz):δ157.5,137.3,136.6,136.4(2C),130.2(2C),130.0,127.6(2C),126.4(2C),115.0(2C),114.0,79.5,69.8,65,54,36.7,28.3(3C).
实施例5
(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-(N-叔丁氧羰基)氨基丙醇(4.0g,10.44mmol),溶于乙酸乙酯(20mL)和无水甲醇(40mL),冰盐浴下以1滴/秒滴加乙酰氯(2.60mL,20.88mmol),20℃搅拌24h,用5%的NaOH溶液调节pH至9,浓缩。加入二氯甲烷(100mL),用饱和食盐水洗涤(3×10mL),无水硫酸镁干燥,除去溶剂后用甲醇和乙酸乙酯(1∶10,体积比)重结晶得白色固体,即产物(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-氨基丙醇(2.51g,85.0%)。m.p.145.5-146.1℃;[α]D 20=-0.8(c 0.12,MeOH);IR(NaCl):υ3334,1509,1176cm-1;1H NMR(CDCl3,600MHz):δ7.41(2H,d,J=7.2Hz,ArH),7.37(2H,d,J=7.8Hz,ArH),7.09(2H,d,J=7.8Hz,ArH),6.90(2H,d,J=7.8Hz,ArH),6.71(1H,dd,J1=10.8Hz,J2=18Hz,CH2=CH),5.75(1H,d,J=18.0Hz,CH2=CH),5.26(1H,t,J1=10.8Hz,J2=19.8Hz,CH2=CH),5.03(2H,s,ArCH2O),3.61(1H,t,J1=3.6Hz,J2=6.6Hz,CH2O),3.49(1H,s,OH),3.35(1H,d,J=3.6Hz,CH2O),3.04(1H,m,CHN),2.72(1H,m,ArCH2),2.47(1H,m,ArCH2),1.5(2H,s,NH);13C NMR(CDCl3,150MHz):δ158.0,140.3,136.2(2C),130.4,129.2(2C),127.1(2C),126.5(2C),114.4(2C),114.3,70.9,68.5,54.0,41.9.
实施例6
(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-(N-叔丁氧羰基)氨基丙醇(4.0g,10.44mmol),溶于乙酸乙酯(20mL)和无水甲醇(40mL),冰盐浴下以1滴/秒滴加乙酰氯(5.2mL,41.76mmol),40℃搅拌12h,用5%的NaOH溶液调节pH至9,浓缩。加入二氯甲烷(100mL),饱和食盐水洗涤(3×10mL),无水硫酸镁干燥,除去溶剂后用甲醇和乙酸乙酯(1∶10,体积比)重结晶得白色固体,即产物(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-氨基丙醇(2.39g,81.2%)。m.p.145.5-146.1℃;[α]D 20=-0.8(c 0.12,MeOH);IR(NaCl):υ3334,1509,1176cm-1;1H NMR(CDCl3,600MHz):δ7.41(2H,d,J=7.2Hz,ArH),7.37(2H,d,J=7.8Hz,ArH),7.09(2H,d,J=7.8Hz,ArH),6.90(2H,d,J=7.8Hz,ArH),6.71(1H,dd,J1=10.8Hz,J2=18Hz,CH2=CH),5.75(1H,d,J=18.0Hz,CH2=CH),5.26(1H,t,J1=10.8Hz,J2=19.8Hz,CH2=CH),5.03(2H,s,ArCH2O),3.61(1H,t,J1=3.6Hz,J2=6.6Hz,CH2O),3.49(1H,s,OH),3.35(1H,d,J=3.6Hz,CH2O),3.04(1H,m,CHN),2.72(1H,m,ArCH2),2.47(1H,m,ArCH2),1.5(2H,s,NH);13C NMR(CDCl3,150MHz):δ158.0,140.3,136.2(2C),130.4,129.2(2C),127.1(2C),126.5(2C),114.4(2C),114.3,70.9,68.5,54.0,41.9.
实施例7
(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-氨基丙醇(2.0g,7.06mmol)溶于干燥的甲苯(80mL),氮气保护下,依次加入对甲基苯磺酸(50mg)和N,N-二甲基甲酰胺二甲缩醛(0.94mL,7.06mmol),120℃下索氏提取器中回流24h,用10%NaHCO3(30mL)猝灭反应。分离出有机相,用饱和食盐水洗涤(3×10mL),无水硫酸钠干燥,除去溶剂后经柱层析(石油醚∶乙酸乙酯∶三乙胺=4∶1∶1,体积比)分离提纯得白色固体,即产物(4S)-4-[4′-(对乙烯基苄氧)苯基]-4,5-二氢噁唑啉(1.66g,80.5%)。m.p.144.4-145.0℃;[α]D 20=-33.1(c 0.13,THF);IR(NaCl):3047,1635,1116cm-1;1H NMR(CDCl3,600MHz):δ8.17(1H,s,CH=N),7.42(2H,d,J=8.4Hz,ArH),7.38(2H,d,J=7.8Hz,ArH),7.09(2H,d,J=9.0Hz,ArH),6.91(2H,d,J=9.0Hz,ArH),6.72(1H,dd,J1=10.8Hz,J2=18.0Hz,CH2=CH),5.75(1H,d,J=7.8Hz,CH2=CH),5.25(1H,d,J=10.8Hz,CH2=CH),5.03(2H,s,ArCH2O),4.54(1H,s,CH-N),3.65(1H,dd,J1=3.6Hz,J2=11.4Hz,OCH2),3.54(1H,m,OCH2),2.88(2H,m,ArCH2);13C NMR(CDCl3,150MHz):δ160.5,137.4,136.5,136.4(2C),130.4(2C),130.2,128.7,127.7(2C),126.4(2C),115.2(2C),114.1,69.8,49.4,46.4.
实施例8
(2S)-3-[4′-(对乙烯基苄氧基)苯基]-2-氨基丙醇(2.0g,7.06mmol)溶于干燥的苯(80mL),氮气保护下,依次加入对甲基苯磺酸(50mg)和N,N-二甲基甲酰胺二甲缩醛(1.41mL,10.59mmol),90℃下索氏提取器中回流36h,用10%NaHCO3(30mL)猝灭反应。分离出有机相,用饱和食盐水洗涤(3×10mL),无水硫酸钠干燥,除去溶剂后经柱层析(石油醚∶乙酸乙酯∶三乙胺=4∶1∶1,体积比)分离提纯得白色固体,即产物(4S)-4-[4′-(对乙烯基苄氧)苯基]-4,5-二氢噁唑啉(1.72g,83.4%)。m.p.144.4-145.0℃;[α]D 20=-33.1(c 0.13,THF);IR(NaCl):3047,1635,1116cm-1;1H NMR(CDCl3,600MHz):δ8.17(1H,s,CH=N),7.42(2H,d,J=8.4Hz,ArH),7.38(2H,d,J=7.8Hz,ArH),7.09(2H,d,J=9.0Hz,ArH),6.91(2H,d,J=9.0Hz,ArH),6.72(1H,dd,J1=10.8Hz,J2=18.0Hz,CH2=CH),5.75(1H,d,J=7.8Hz,CH2=CH),5.25(1H,d,J=10.8Hz,CH2=CH),5.03(2H,s,ArCH2O),4.54(1H,s,CH-N),3.65(1H,dd,J1=3.6Hz,J2=11.4Hz,OCH2),3.54(1H,m,OCH2),2.88(2H,m,ArCH2);13C NMR(CDCl3,150MHz):δ160.5,137.4,136.5,136.4(2C),130.4(2C),130.2,128.7,127.7(2C),126.4(2C),115.2(2C),114.1,69.8,49.4,46.4.
实施例9
(4S)-4-[4′-(对乙烯基苄氧)苯基]-4,5-二氢噁唑啉(1.5g,5.12mmol)溶于THF(30mL),通入氮气,-78℃下加入新制的六甲基二硅胺基锂(5.12mmol)溶液。-78℃下搅拌0.5h后,分批加入硒粉(0.4g,5.12mmol),升温至25℃,继续反应3h。加入饱和柠檬酸水溶液调节pH至4-5,过滤,滤液浓缩。加入二氯甲烷(100mL),饱和食盐水洗涤(3×10mL),无水硫酸钠干燥,过滤,滤液浓缩后经柱层析(石油醚∶乙酸乙酯=3∶1,体积比)分离提纯得白色固体,即产物(4S)-4-[4′-(对乙烯基苄氧基)苯基]噁唑烷-2-硒酮(1.63g,85.2%)。m.p.156.3-156.7℃;[α]D 20=-56.8(c 0.05,THF);IR(NaCl):3325,1530,1501cm-1;77Se NMR(CDCl3,150MHz):δ-319.84;1H NMR(CDCl3,600MHz):δ7.60(1H,s,NH),7.44(2H,d,J=7.8Hz,ArH),7.39(2H,d,J=8.4Hz,ArH),7.08(2H,d,J=8.4Hz,ArH),6.95(2H,d,J=8.4Hz,ArH),6.72(1H,dd,J1=10.8Hz,J2=18.0Hz,CH2=CH),5.77(1H,d,J=17.4Hz,CH2=CH),5.26(1H,d,J=10.8Hz,CH2=CH),5.05(2H,s,ArCH2O),4.74(1H,m,CH-N),4.44(1H,dd,J1=6.0Hz,J2=9.0Hz,ArCH2),4.22(1H,m,ArCH2),2.86(2H,m,OCH2);13C NMR(CDCl3,150MHz):δ188.2,158.2,137.4,136.4,136.3,130.0(2C),127.7(2C),127.1,126.5(2C),126.3,115.7(2C),114.2,76.2,69.8,58.9,39.6.
实施例10
(4S)-4-[4′-(对乙烯基苄氧)苯基]-4,5-二氢噁唑啉(1.5g,5.12mmol)溶于THF(30mL),通入氮气,-78℃下加入新制的六甲基二硅胺基锂(7.68mmol)溶液。-78℃下搅拌0.5h后,分批加入硒粉(0.6g,7.68mmol),升温至25℃,继续反应2h。加入饱和柠檬酸水溶液调节pH至4-5,过滤,滤液浓缩。加入二氯甲烷(100mL),饱和食盐水洗涤(3×10mL),无水硫酸钠干燥,过滤,滤液浓缩后经柱层析(石油醚∶乙酸乙酯=3∶1,体积比)分离提纯得白色固体,即产物(4S)-4-[4′-(对乙烯基苄氧基)苯基]噁唑烷-2-硒酮(1.67g,87.5%)。m.p.156.3-156.7℃;[α]D 20=-56.8(c 0.05,THF);IR(NaCl):3325,1530,1501cm-1;77Se NMR(CDCl3,150MHz):δ-319.84;1H NMR(CDCl3,600MHz):δ7.60(1H,s,NH),7.44(2H,d,J=7.8Hz,ArH),7.39(2H,d,J=8.4Hz,ArH),7.08(2H,d,J=8.4Hz,ArH),6.95(2H,d,J=8.4Hz,ArH),6.72(1H,dd,J1=10.8Hz,J2=18.0Hz,CH2=CH),5.77(1H,d,J=17.4Hz,CH2=CH),5.26(1H,d,J=10.8Hz,CH2=CH),5.05(2H,s,ArCH2O),4.74(1H,m,CH-N),4.44(1H,dd,J1=6.0Hz,J2=9.0Hz,ArCH2),4.22(1H,m,ArCH2),2.86(2H,m,OCH2);13C NMR(CDCl3,150MHz):δ188.2,158.2,137.4,136.4,136.3,130.0(2C),127.7(2C),127.1,126.5(2C),126.3,115.7(2C),114.2,76.2,69.8,58.9,39.6.
实施例11
干燥的(4S)-4-[4′-(对乙烯基苄氧基)苯基]噁唑烷-2-硒酮(1.5g,4.02mmol)溶于无水四氢呋喃(30mL),加入苯乙烯(0.46mL,4.02mmol)和偶氮二异丁腈(0.026g),通入氮气,60℃反应96h。反应混合液以3滴/秒逐滴滴加到冰乙醇(100mL)中,过滤并用冰乙醇洗涤得白色固体,即产物线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮(1.58g,82.4%)。Mw=8100;IR(NaCl):3340,1510,1261,698cm-1;77Se NMR(CDCl3,150MHz):δ-319.84;1H NMR(CDCl3,600MHz):δ7.35-6.20(bm,polymer-ArH),5.17(s,ArCH2O),4.84(br s,CH-N),4.11(m,CH2O),3.64(1H,m,CH2O),3.00-2.75(br s,ArCH2),2.1-0.92(bm,polymer-CH2);13C NMR(CDCl3,150MHz):δ188.2,158.0,137.4,136.4,136.3,130.1,127.7,127.1,126.5,126.3,115.7,114.2,75.5,68.8,56.9,52.2,39.3;Elementary analysis:C,68.15%;H,5.75%;N,2.81%.
实施例12
干燥的(4S)-4-[4′-(对乙烯基苄氧基)苯基]噁唑烷-2-硒酮(1.5g,4.02mmol)溶于无水四氢呋喃(30mL),加入苯乙烯(1.84mL,16.08mmol)和偶氮二异丁腈(0.066g),通入氮气,80℃反应72h。反应混合液以3滴/秒逐滴滴加到冰乙醇(100mL)中,过滤并用冰乙醇洗涤得白色固体,即产物线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮(2.58g,81.5%)。Mw=13500;IR(NaCl):3340,1510,1261,698cm-1;77Se NMR(CDCl3,150MHz):δ-319.84;1H NMR(CDCl3,600MHz):δ7.35-6.20(bm,polymer-ArH),5.17(s,ArCH2O),4.84(br s,CH-N),4.11(m,CH2O),3.64(1H,m,CH2O),3.00-2.75(br s,ArCH2),2.1-0.92(bm,polymer-CH2);13C NMR(CDCl3,150MHz):δ188.2,158.1,137.6,136.4,136.3,130.1,127.7,127.1,126.5,126.3,115.7,114.2,75.5,68.8,56.9,52.2,39.2;Elementary analysis:C,77.71%;H,6.58%;N,1.69%.
Claims (4)
2.一种制备权利要求1所述的线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮的方法,该方法包括下述步骤:
(1)在有机溶剂中,碳酸钾和催化量的冠醚的作用下,化合物2和对乙烯基苄氯反应得到化合物3,反应温度为20~60℃,反应时间为12~48h,上述化合物的摩尔比为化合物2∶碳酸钾∶对乙烯基苄氯=1∶1~3∶1~1.5;
(2)在有机溶剂中,化合物3在氢化铝锂作用下还原得到化合物4,反应温度为0~25℃,反应时间为8~12h,上述化合物的摩尔比为化合物3∶氢化铝锂=1∶1~1.5;
(3)在有机溶剂中,化合物4和乙酰氯反应得到化合物5,反应温度为20~40℃,反应时间为12~24h,上述化合物的摩尔比为化合物4∶乙酰氯=1∶2~4;
(4)在有机溶剂中,催化量的对甲基苯磺酸作用下,化合物5和N,N-二甲基甲酰胺二甲缩醛反应关环得到化合物6,反应温度为90~120℃,反应时间为24~36h,上述化合物的摩尔比为化合物5∶N,N-二甲基甲酰胺二甲缩醛=1∶1~1.5;
(5)在有机溶剂中,化合物6在六甲基二硅胺基锂的作用下与硒粉反应得到化合物7,反应温度为-78℃~25℃,反应时间为2~3h,上述化合物的摩尔比为化合物6∶六甲基二硅胺基锂∶硒粉=1∶1~1.5∶1~1.5;
(6)在有机溶剂中,化合物7和苯乙烯在引发剂的作用下共聚得到线型聚苯乙烯支载(4S)-噁唑烷-2-硒酮,反应温度为60~80℃,反应时间为72~96h,上述化合物的摩尔比为化合7∶苯乙烯=1∶1~4,所述的引发剂是偶氮二异丁腈;
上述化合物2,3,4,5,6,7具有下列的结构式:
3.如权利要求2所述的方法,其特征是:所述有机溶剂为二氯甲烷、三氯甲烷、N,N-二甲基甲酰胺、四氢呋喃、甲醇、乙醇、乙酸乙酯、苯或甲苯。
4.如权利要求2或3所述的方法,其特征是:步骤(6)中引发剂偶氮二异丁腈用量为化合物7和苯乙烯总量的2mol%。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN2010102652707A CN101948552B (zh) | 2010-08-27 | 2010-08-27 | 线型聚苯乙烯支载手性噁唑烷-2-硒酮及其制备方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN2010102652707A CN101948552B (zh) | 2010-08-27 | 2010-08-27 | 线型聚苯乙烯支载手性噁唑烷-2-硒酮及其制备方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN101948552A CN101948552A (zh) | 2011-01-19 |
| CN101948552B true CN101948552B (zh) | 2012-04-18 |
Family
ID=43452190
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2010102652707A Expired - Fee Related CN101948552B (zh) | 2010-08-27 | 2010-08-27 | 线型聚苯乙烯支载手性噁唑烷-2-硒酮及其制备方法 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN101948552B (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103467641B (zh) * | 2013-09-17 | 2016-02-03 | 湖北大学 | 线型聚苯乙烯支载(s)-5-(4-氧苄基)-3-苯基-1-丙酰基海因及其制备方法和用途 |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1237056C (zh) * | 2002-12-25 | 2006-01-18 | 中国科学院上海药物研究所 | 噁唑烷酮类化合物、其制备方法和用途 |
| CN100395270C (zh) * | 2006-05-25 | 2008-06-18 | 湖北大学 | 线型聚苯乙烯支载的(4s)-5,5-二取代基噁唑烷酮及其制备方法和用途 |
-
2010
- 2010-08-27 CN CN2010102652707A patent/CN101948552B/zh not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| CN101948552A (zh) | 2011-01-19 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN117603081A (zh) | N-(2-((2-(3-甲氧基苯氧基)苯基)氨基)-2-乙酰氧基)-1-萘胺的制备方法 | |
| CN110305018B (zh) | 一种3-溴-2-氟硝基苯的制备方法 | |
| CN108558692B (zh) | 一种酰胺类化合物的制备方法 | |
| CN110511193B (zh) | 一种α-酮硫代酰胺类化合物及其合成方法 | |
| CN102942511B (zh) | 一种环戊二烯的制备方法 | |
| CN101948552B (zh) | 线型聚苯乙烯支载手性噁唑烷-2-硒酮及其制备方法 | |
| CN105148988B (zh) | 一种手性吡哆醛类催化剂及其合成方法与应用 | |
| CN106977489A (zh) | 一种制备多取代占吨酮类衍生物的方法 | |
| CN109096162B (zh) | 一种钪催化硫醇对邻亚甲基苯醌的亲核加成反应方法 | |
| CN102675415B (zh) | 制备硼替佐米的方法 | |
| US8222429B2 (en) | Photodissociable protective group | |
| CN1696094A (zh) | 4,4'-二羟基二苯甲酮的制备方法 | |
| JPH1045656A (ja) | フルオレン誘導体の製造法 | |
| WO2016115962A1 (zh) | 一种奈必洛尔中间体的制备方法及奈必洛尔的制备方法 | |
| CN113045463B (zh) | 一种(e)-3-芳硫基-2-碘丙烯酸乙酯化合物的合成方法 | |
| CN111548257B (zh) | 一种(4-异丙氧基-2-甲基)苯基异丙基酮的制备方法 | |
| CN100395270C (zh) | 线型聚苯乙烯支载的(4s)-5,5-二取代基噁唑烷酮及其制备方法和用途 | |
| CN115232020A (zh) | 一种合成n,n-二乙基-2-羟基苯乙酰胺及其类似物的方法及其应用 | |
| CN110845445A (zh) | 一种连接体及制备方法和应用、基于沙利度胺的PROTACs的中间体及应用 | |
| KR101856566B1 (ko) | 4'-히드록시-4-비페닐카르복실산의 신규 제조 방법 | |
| CN103755852B (zh) | 线型聚苯乙烯支载(4s)-(4’-氧苄基)-2-正丁基环磺酰胺及其制备方法和用途 | |
| CN102267946B (zh) | 高光学纯度含手性联萘骨架的α-季碳氨基酸酯类化合物、其制备方法及用途 | |
| CN117700356A (zh) | 一种制备药物lumacaftor中间体的新方法 | |
| CN121517343A (zh) | L-脯氨酸杂环中间体、α-甲基-L-脯氨酸盐酸盐及制备方法 | |
| CN103819357B (zh) | (-)-有效霉醇叠氮四乙酸酯的制备方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C17 | Cessation of patent right | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20120418 Termination date: 20120827 |