BRPI0922641B1 - Método de integração de uma ou mais sequências de ácido nucleico exógenas no genoma de uma célula vegetal - Google Patents
Método de integração de uma ou mais sequências de ácido nucleico exógenas no genoma de uma célula vegetal Download PDFInfo
- Publication number
- BRPI0922641B1 BRPI0922641B1 BRPI0922641-9A BRPI0922641A BRPI0922641B1 BR PI0922641 B1 BRPI0922641 B1 BR PI0922641B1 BR PI0922641 A BRPI0922641 A BR PI0922641A BR PI0922641 B1 BRPI0922641 B1 BR PI0922641B1
- Authority
- BR
- Brazil
- Prior art keywords
- sequence
- dna
- gene
- cleavage
- zinc finger
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 115
- 230000010354 integration Effects 0.000 title claims abstract description 55
- 150000007523 nucleic acids Chemical group 0.000 title claims description 78
- 108090000623 proteins and genes Proteins 0.000 claims description 221
- 238000003776 cleavage reaction Methods 0.000 claims description 146
- 241000196324 Embryophyta Species 0.000 claims description 136
- 230000007017 scission Effects 0.000 claims description 124
- 230000027455 binding Effects 0.000 claims description 111
- 238000009739 binding Methods 0.000 claims description 111
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 claims description 86
- 229910052725 zinc Inorganic materials 0.000 claims description 86
- 239000011701 zinc Substances 0.000 claims description 85
- 108020001507 fusion proteins Proteins 0.000 claims description 82
- 102000037865 fusion proteins Human genes 0.000 claims description 82
- 102000004169 proteins and genes Human genes 0.000 claims description 65
- 108010017070 Zinc Finger Nucleases Proteins 0.000 claims description 51
- 102000040430 polynucleotide Human genes 0.000 claims description 46
- 108091033319 polynucleotide Proteins 0.000 claims description 46
- 239000002157 polynucleotide Substances 0.000 claims description 46
- 240000008042 Zea mays Species 0.000 claims description 45
- 235000002017 Zea mays subsp mays Nutrition 0.000 claims description 41
- 239000004009 herbicide Substances 0.000 claims description 32
- 230000002363 herbicidal effect Effects 0.000 claims description 29
- 108091028043 Nucleic acid sequence Proteins 0.000 claims description 28
- 230000004927 fusion Effects 0.000 claims description 27
- 108091026890 Coding region Proteins 0.000 claims description 19
- 101710163270 Nuclease Proteins 0.000 claims description 15
- 239000013604 expression vector Substances 0.000 claims description 14
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 claims description 13
- 235000005822 corn Nutrition 0.000 claims description 13
- 241000238631 Hexapoda Species 0.000 claims description 8
- 230000001965 increasing effect Effects 0.000 claims description 8
- 230000001131 transforming effect Effects 0.000 claims description 4
- 208000035240 Disease Resistance Diseases 0.000 claims description 2
- 229920002494 Zein Polymers 0.000 claims description 2
- 201000010099 disease Diseases 0.000 claims description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 2
- 239000005019 zein Substances 0.000 claims description 2
- 229940093612 zein Drugs 0.000 claims description 2
- 230000014509 gene expression Effects 0.000 abstract description 46
- 108090000765 processed proteins & peptides Proteins 0.000 abstract description 40
- 229920001184 polypeptide Polymers 0.000 abstract description 39
- 102000004196 processed proteins & peptides Human genes 0.000 abstract description 39
- 239000000203 mixture Substances 0.000 abstract description 26
- 210000004027 cell Anatomy 0.000 description 127
- 108020004414 DNA Proteins 0.000 description 111
- 239000002773 nucleotide Substances 0.000 description 108
- 125000003729 nucleotide group Chemical group 0.000 description 105
- 235000018102 proteins Nutrition 0.000 description 63
- 239000012634 fragment Substances 0.000 description 61
- 102000039446 nucleic acids Human genes 0.000 description 59
- 108020004707 nucleic acids Proteins 0.000 description 59
- 238000006243 chemical reaction Methods 0.000 description 53
- 239000013612 plasmid Substances 0.000 description 52
- 230000004568 DNA-binding Effects 0.000 description 46
- 239000013615 primer Substances 0.000 description 45
- 239000000047 product Substances 0.000 description 38
- 239000013598 vector Substances 0.000 description 36
- 108091008146 restriction endonucleases Proteins 0.000 description 33
- 235000016383 Zea mays subsp huehuetenangensis Nutrition 0.000 description 28
- 235000009973 maize Nutrition 0.000 description 28
- 238000009396 hybridization Methods 0.000 description 25
- 101150113864 pat gene Proteins 0.000 description 22
- 210000003483 chromatin Anatomy 0.000 description 21
- 238000005215 recombination Methods 0.000 description 21
- 230000006798 recombination Effects 0.000 description 21
- 230000009466 transformation Effects 0.000 description 21
- 108010077544 Chromatin Proteins 0.000 description 20
- 238000005516 engineering process Methods 0.000 description 19
- 238000003780 insertion Methods 0.000 description 19
- 230000037431 insertion Effects 0.000 description 19
- 230000006801 homologous recombination Effects 0.000 description 18
- 238000002744 homologous recombination Methods 0.000 description 18
- 210000000349 chromosome Anatomy 0.000 description 17
- 101710185494 Zinc finger protein Proteins 0.000 description 16
- 102100023597 Zinc finger protein 816 Human genes 0.000 description 16
- 125000003275 alpha amino acid group Chemical group 0.000 description 16
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 15
- 230000000694 effects Effects 0.000 description 15
- 239000000499 gel Substances 0.000 description 15
- 108091034117 Oligonucleotide Proteins 0.000 description 14
- 230000003321 amplification Effects 0.000 description 13
- 238000010367 cloning Methods 0.000 description 13
- 230000006870 function Effects 0.000 description 13
- 238000003199 nucleic acid amplification method Methods 0.000 description 13
- 210000001519 tissue Anatomy 0.000 description 13
- 235000001014 amino acid Nutrition 0.000 description 12
- 230000008569 process Effects 0.000 description 12
- 239000000523 sample Substances 0.000 description 12
- 102000053602 DNA Human genes 0.000 description 11
- 108010042407 Endonucleases Proteins 0.000 description 11
- 150000001413 amino acids Chemical class 0.000 description 11
- 230000001413 cellular effect Effects 0.000 description 11
- 102000004190 Enzymes Human genes 0.000 description 10
- 108090000790 Enzymes Proteins 0.000 description 10
- 238000012408 PCR amplification Methods 0.000 description 10
- 238000003556 assay Methods 0.000 description 10
- 230000000875 corresponding effect Effects 0.000 description 10
- 238000001976 enzyme digestion Methods 0.000 description 10
- 230000001404 mediated effect Effects 0.000 description 10
- 230000002441 reversible effect Effects 0.000 description 10
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 9
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 9
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 9
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 9
- 238000012181 QIAquick gel extraction kit Methods 0.000 description 9
- 230000035772 mutation Effects 0.000 description 9
- 230000008929 regeneration Effects 0.000 description 9
- 238000011069 regeneration method Methods 0.000 description 9
- 238000012546 transfer Methods 0.000 description 9
- 240000007594 Oryza sativa Species 0.000 description 8
- 235000007164 Oryza sativa Nutrition 0.000 description 8
- 108700019146 Transgenes Proteins 0.000 description 8
- 239000011230 binding agent Substances 0.000 description 8
- 238000013461 design Methods 0.000 description 8
- 238000001514 detection method Methods 0.000 description 8
- -1 for example Substances 0.000 description 8
- 230000002068 genetic effect Effects 0.000 description 8
- 238000012423 maintenance Methods 0.000 description 8
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 8
- 230000002103 transcriptional effect Effects 0.000 description 8
- 239000003155 DNA primer Substances 0.000 description 7
- 102100031780 Endonuclease Human genes 0.000 description 7
- 241000588724 Escherichia coli Species 0.000 description 7
- 108091092584 GDNA Proteins 0.000 description 7
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 7
- 238000012300 Sequence Analysis Methods 0.000 description 7
- 230000002759 chromosomal effect Effects 0.000 description 7
- 238000006471 dimerization reaction Methods 0.000 description 7
- 230000001105 regulatory effect Effects 0.000 description 7
- 230000008439 repair process Effects 0.000 description 7
- 238000013518 transcription Methods 0.000 description 7
- 230000035897 transcription Effects 0.000 description 7
- 241000894006 Bacteria Species 0.000 description 6
- 108090001060 Lipase Proteins 0.000 description 6
- 102000004882 Lipase Human genes 0.000 description 6
- 239000004367 Lipase Substances 0.000 description 6
- 230000004075 alteration Effects 0.000 description 6
- 230000001580 bacterial effect Effects 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 210000004899 c-terminal region Anatomy 0.000 description 6
- 238000004113 cell culture Methods 0.000 description 6
- 239000002299 complementary DNA Substances 0.000 description 6
- 238000012217 deletion Methods 0.000 description 6
- 230000037430 deletion Effects 0.000 description 6
- 238000004520 electroporation Methods 0.000 description 6
- 230000003993 interaction Effects 0.000 description 6
- 235000019421 lipase Nutrition 0.000 description 6
- 108020004999 messenger RNA Proteins 0.000 description 6
- 210000001938 protoplast Anatomy 0.000 description 6
- 238000012216 screening Methods 0.000 description 6
- 238000012163 sequencing technique Methods 0.000 description 6
- 230000009261 transgenic effect Effects 0.000 description 6
- 230000003612 virological effect Effects 0.000 description 6
- 230000007018 DNA scission Effects 0.000 description 5
- 102000004533 Endonucleases Human genes 0.000 description 5
- 108700007698 Genetic Terminator Regions Proteins 0.000 description 5
- 108700026244 Open Reading Frames Proteins 0.000 description 5
- 239000011543 agarose gel Substances 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 230000008859 change Effects 0.000 description 5
- 238000012512 characterization method Methods 0.000 description 5
- 239000003795 chemical substances by application Substances 0.000 description 5
- 150000001875 compounds Chemical class 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 239000003550 marker Substances 0.000 description 5
- 239000013600 plasmid vector Substances 0.000 description 5
- 241000894007 species Species 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- 241000589158 Agrobacterium Species 0.000 description 4
- 241000589155 Agrobacterium tumefaciens Species 0.000 description 4
- 241001515826 Cassava vein mosaic virus Species 0.000 description 4
- 102000016680 Dioxygenases Human genes 0.000 description 4
- 108010028143 Dioxygenases Proteins 0.000 description 4
- 108010033040 Histones Proteins 0.000 description 4
- 108010077850 Nuclear Localization Signals Proteins 0.000 description 4
- IAJOBQBIJHVGMQ-UHFFFAOYSA-N Phosphinothricin Natural products CP(O)(=O)CCC(N)C(O)=O IAJOBQBIJHVGMQ-UHFFFAOYSA-N 0.000 description 4
- 235000002595 Solanum tuberosum Nutrition 0.000 description 4
- 244000061456 Solanum tuberosum Species 0.000 description 4
- 241000700605 Viruses Species 0.000 description 4
- PTFCDOFLOPIGGS-UHFFFAOYSA-N Zinc dication Chemical compound [Zn+2] PTFCDOFLOPIGGS-UHFFFAOYSA-N 0.000 description 4
- JLCPHMBAVCMARE-UHFFFAOYSA-N [3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[3-[[3-[[3-[[3-[[3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-[[5-(2-amino-6-oxo-1H-purin-9-yl)-3-hydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxyoxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(5-methyl-2,4-dioxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(6-aminopurin-9-yl)oxolan-2-yl]methoxy-hydroxyphosphoryl]oxy-5-(4-amino-2-oxopyrimidin-1-yl)oxolan-2-yl]methyl [5-(6-aminopurin-9-yl)-2-(hydroxymethyl)oxolan-3-yl] hydrogen phosphate Polymers Cc1cn(C2CC(OP(O)(=O)OCC3OC(CC3OP(O)(=O)OCC3OC(CC3O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c3nc(N)[nH]c4=O)C(COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3COP(O)(=O)OC3CC(OC3CO)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3ccc(N)nc3=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cc(C)c(=O)[nH]c3=O)n3cc(C)c(=O)[nH]c3=O)n3ccc(N)nc3=O)n3cc(C)c(=O)[nH]c3=O)n3cnc4c3nc(N)[nH]c4=O)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)n3cnc4c(N)ncnc34)O2)c(=O)[nH]c1=O JLCPHMBAVCMARE-UHFFFAOYSA-N 0.000 description 4
- 125000000539 amino acid group Chemical group 0.000 description 4
- 230000003115 biocidal effect Effects 0.000 description 4
- 238000010276 construction Methods 0.000 description 4
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 4
- 230000001419 dependent effect Effects 0.000 description 4
- 230000029087 digestion Effects 0.000 description 4
- 239000003623 enhancer Substances 0.000 description 4
- 238000001502 gel electrophoresis Methods 0.000 description 4
- 125000000487 histidyl group Chemical group [H]N([H])C(C(=O)O*)C([H])([H])C1=C([H])N([H])C([H])=N1 0.000 description 4
- 239000003446 ligand Substances 0.000 description 4
- 230000004048 modification Effects 0.000 description 4
- 238000012986 modification Methods 0.000 description 4
- 238000010369 molecular cloning Methods 0.000 description 4
- 230000008488 polyadenylation Effects 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 210000003705 ribosome Anatomy 0.000 description 4
- 235000009566 rice Nutrition 0.000 description 4
- 238000010561 standard procedure Methods 0.000 description 4
- 230000010474 transient expression Effects 0.000 description 4
- 238000013519 translation Methods 0.000 description 4
- 230000014616 translation Effects 0.000 description 4
- 102000007469 Actins Human genes 0.000 description 3
- 108010085238 Actins Proteins 0.000 description 3
- 235000004977 Brassica sinapistrum Nutrition 0.000 description 3
- 108091007914 CDKs Proteins 0.000 description 3
- 102000014914 Carrier Proteins Human genes 0.000 description 3
- 102000012410 DNA Ligases Human genes 0.000 description 3
- 108010061982 DNA Ligases Proteins 0.000 description 3
- 102000052510 DNA-Binding Proteins Human genes 0.000 description 3
- 238000002965 ELISA Methods 0.000 description 3
- 230000010337 G2 phase Effects 0.000 description 3
- 241000209510 Liliopsida Species 0.000 description 3
- 241000227653 Lycopersicon Species 0.000 description 3
- 241001465754 Metazoa Species 0.000 description 3
- 102000011931 Nucleoproteins Human genes 0.000 description 3
- 108010061100 Nucleoproteins Proteins 0.000 description 3
- 238000009004 PCR Kit Methods 0.000 description 3
- 235000008331 Pinus X rigitaeda Nutrition 0.000 description 3
- 241000018646 Pinus brutia Species 0.000 description 3
- 235000011613 Pinus brutia Nutrition 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- 108091027967 Small hairpin RNA Proteins 0.000 description 3
- 108091023040 Transcription factor Proteins 0.000 description 3
- 102000040945 Transcription factor Human genes 0.000 description 3
- 241000209140 Triticum Species 0.000 description 3
- 235000021307 Triticum Nutrition 0.000 description 3
- 230000004913 activation Effects 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 125000004104 aryloxy group Chemical group 0.000 description 3
- 108091008324 binding proteins Proteins 0.000 description 3
- 230000022131 cell cycle Effects 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 230000018109 developmental process Effects 0.000 description 3
- 230000005782 double-strand break Effects 0.000 description 3
- 238000009510 drug design Methods 0.000 description 3
- 238000001962 electrophoresis Methods 0.000 description 3
- 241001233957 eudicotyledons Species 0.000 description 3
- IAJOBQBIJHVGMQ-BYPYZUCNSA-N glufosinate-P Chemical compound CP(O)(=O)CC[C@H](N)C(O)=O IAJOBQBIJHVGMQ-BYPYZUCNSA-N 0.000 description 3
- 230000000670 limiting effect Effects 0.000 description 3
- 239000002502 liposome Substances 0.000 description 3
- 239000011159 matrix material Substances 0.000 description 3
- 238000000520 microinjection Methods 0.000 description 3
- 239000002105 nanoparticle Substances 0.000 description 3
- 210000001623 nucleosome Anatomy 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 230000010076 replication Effects 0.000 description 3
- 238000011160 research Methods 0.000 description 3
- 239000004055 small Interfering RNA Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- 230000005030 transcription termination Effects 0.000 description 3
- 239000003981 vehicle Substances 0.000 description 3
- 101710159080 Aconitate hydratase A Proteins 0.000 description 2
- 101710159078 Aconitate hydratase B Proteins 0.000 description 2
- 101710197633 Actin-1 Proteins 0.000 description 2
- 108091093088 Amplicon Proteins 0.000 description 2
- 244000075850 Avena orientalis Species 0.000 description 2
- 241000219310 Beta vulgaris subsp. vulgaris Species 0.000 description 2
- 240000002791 Brassica napus Species 0.000 description 2
- 241000701489 Cauliflower mosaic virus Species 0.000 description 2
- 108050006400 Cyclin Proteins 0.000 description 2
- 102000016736 Cyclin Human genes 0.000 description 2
- 108700020911 DNA-Binding Proteins Proteins 0.000 description 2
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 2
- AOJJSUZBOXZQNB-TZSSRYMLSA-N Doxorubicin Chemical compound O([C@H]1C[C@@](O)(CC=2C(O)=C3C(=O)C=4C=CC=C(C=4C(=O)C3=C(O)C=21)OC)C(=O)CO)[C@H]1C[C@H](N)[C@H](O)[C@H](C)O1 AOJJSUZBOXZQNB-TZSSRYMLSA-N 0.000 description 2
- 241001057636 Dracaena deremensis Species 0.000 description 2
- 241000206602 Eukaryota Species 0.000 description 2
- 108091029865 Exogenous DNA Proteins 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 241000219146 Gossypium Species 0.000 description 2
- 244000020551 Helianthus annuus Species 0.000 description 2
- 235000003222 Helianthus annuus Nutrition 0.000 description 2
- 102000003964 Histone deacetylase Human genes 0.000 description 2
- 108090000353 Histone deacetylase Proteins 0.000 description 2
- 102000006947 Histones Human genes 0.000 description 2
- 101000687346 Homo sapiens PR domain zinc finger protein 2 Proteins 0.000 description 2
- 240000005979 Hordeum vulgare Species 0.000 description 2
- 235000007340 Hordeum vulgare Nutrition 0.000 description 2
- 206010021929 Infertility male Diseases 0.000 description 2
- 235000003228 Lactuca sativa Nutrition 0.000 description 2
- 240000008415 Lactuca sativa Species 0.000 description 2
- 102000003960 Ligases Human genes 0.000 description 2
- 108090000364 Ligases Proteins 0.000 description 2
- 235000007688 Lycopersicon esculentum Nutrition 0.000 description 2
- 208000007466 Male Infertility Diseases 0.000 description 2
- 241000220225 Malus Species 0.000 description 2
- 240000004658 Medicago sativa Species 0.000 description 2
- 235000017587 Medicago sativa ssp. sativa Nutrition 0.000 description 2
- 241000589195 Mesorhizobium loti Species 0.000 description 2
- 241000244206 Nematoda Species 0.000 description 2
- 241000208125 Nicotiana Species 0.000 description 2
- 238000000636 Northern blotting Methods 0.000 description 2
- 108020004711 Nucleic Acid Probes Proteins 0.000 description 2
- 108010047956 Nucleosomes Proteins 0.000 description 2
- 102100024885 PR domain zinc finger protein 2 Human genes 0.000 description 2
- 101001091422 Physarum polycephalum Intron-encoded endonuclease I-PpoI Proteins 0.000 description 2
- 108700001094 Plant Genes Proteins 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 2
- 241000220324 Pyrus Species 0.000 description 2
- 102000044126 RNA-Binding Proteins Human genes 0.000 description 2
- 101710105008 RNA-binding protein Proteins 0.000 description 2
- 108091030071 RNAI Proteins 0.000 description 2
- 241000209056 Secale Species 0.000 description 2
- 108020004459 Small interfering RNA Proteins 0.000 description 2
- 235000011684 Sorghum saccharatum Nutrition 0.000 description 2
- 244000062793 Sorghum vulgare Species 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 235000021536 Sugar beet Nutrition 0.000 description 2
- IQFYYKKMVGJFEH-XLPZGREQSA-N Thymidine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 IQFYYKKMVGJFEH-XLPZGREQSA-N 0.000 description 2
- 241000723873 Tobacco mosaic virus Species 0.000 description 2
- 230000021736 acetylation Effects 0.000 description 2
- 238000006640 acetylation reaction Methods 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 238000000246 agarose gel electrophoresis Methods 0.000 description 2
- 230000033228 biological regulation Effects 0.000 description 2
- 230000005540 biological transmission Effects 0.000 description 2
- 229910000389 calcium phosphate Inorganic materials 0.000 description 2
- 239000001506 calcium phosphate Substances 0.000 description 2
- 235000011010 calcium phosphates Nutrition 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 230000006369 cell cycle progression Effects 0.000 description 2
- 108091092356 cellular DNA Proteins 0.000 description 2
- 230000007248 cellular mechanism Effects 0.000 description 2
- 235000013339 cereals Nutrition 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 210000003763 chloroplast Anatomy 0.000 description 2
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 2
- 238000007796 conventional method Methods 0.000 description 2
- 238000012937 correction Methods 0.000 description 2
- 230000002596 correlated effect Effects 0.000 description 2
- 244000038559 crop plants Species 0.000 description 2
- 235000018417 cysteine Nutrition 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 238000011033 desalting Methods 0.000 description 2
- 239000000539 dimer Substances 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 230000034431 double-strand break repair via homologous recombination Effects 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 230000000408 embryogenic effect Effects 0.000 description 2
- 230000007613 environmental effect Effects 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 210000003527 eukaryotic cell Anatomy 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- 230000002538 fungal effect Effects 0.000 description 2
- 238000002523 gelfiltration Methods 0.000 description 2
- 238000012239 gene modification Methods 0.000 description 2
- 230000009368 gene silencing by RNA Effects 0.000 description 2
- 238000003205 genotyping method Methods 0.000 description 2
- 210000004602 germ cell Anatomy 0.000 description 2
- 238000001114 immunoprecipitation Methods 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 208000015181 infectious disease Diseases 0.000 description 2
- 230000002458 infectious effect Effects 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- 230000002452 interceptive effect Effects 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 125000001909 leucine group Chemical group [H]N(*)C(C(*)=O)C([H])([H])C(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 229920002521 macromolecule Polymers 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 230000011987 methylation Effects 0.000 description 2
- 238000007069 methylation reaction Methods 0.000 description 2
- 239000002480 mineral oil Substances 0.000 description 2
- 235000010446 mineral oil Nutrition 0.000 description 2
- 230000009871 nonspecific binding Effects 0.000 description 2
- 239000002853 nucleic acid probe Substances 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- 238000002823 phage display Methods 0.000 description 2
- 125000002467 phosphate group Chemical group [H]OP(=O)(O[H])O[*] 0.000 description 2
- 108010082527 phosphinothricin N-acetyltransferase Proteins 0.000 description 2
- 210000001236 prokaryotic cell Anatomy 0.000 description 2
- 238000000746 purification Methods 0.000 description 2
- 238000007634 remodeling Methods 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 230000035939 shock Effects 0.000 description 2
- 150000003384 small molecules Chemical class 0.000 description 2
- 239000000243 solution Substances 0.000 description 2
- 238000010186 staining Methods 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 230000035882 stress Effects 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- RYYWUUFWQRZTIU-UHFFFAOYSA-K thiophosphate Chemical group [O-]P([O-])([O-])=S RYYWUUFWQRZTIU-UHFFFAOYSA-K 0.000 description 2
- 238000011426 transformation method Methods 0.000 description 2
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 2
- 230000001960 triggered effect Effects 0.000 description 2
- 238000010396 two-hybrid screening Methods 0.000 description 2
- 235000013311 vegetables Nutrition 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- 102000040650 (ribonucleotides)n+m Human genes 0.000 description 1
- VSNHCAURESNICA-NJFSPNSNSA-N 1-oxidanylurea Chemical compound N[14C](=O)NO VSNHCAURESNICA-NJFSPNSNSA-N 0.000 description 1
- ZBMRKNMTMPPMMK-UHFFFAOYSA-N 2-amino-4-[hydroxy(methyl)phosphoryl]butanoic acid;azane Chemical compound [NH4+].CP(O)(=O)CCC(N)C([O-])=O ZBMRKNMTMPPMMK-UHFFFAOYSA-N 0.000 description 1
- ASJSAQIRZKANQN-CRCLSJGQSA-N 2-deoxy-D-ribose Chemical compound OC[C@@H](O)[C@@H](O)CC=O ASJSAQIRZKANQN-CRCLSJGQSA-N 0.000 description 1
- 108010020183 3-phosphoshikimate 1-carboxyvinyltransferase Proteins 0.000 description 1
- 230000005730 ADP ribosylation Effects 0.000 description 1
- 108010013043 Acetylesterase Proteins 0.000 description 1
- 244000291564 Allium cepa Species 0.000 description 1
- 235000002732 Allium cepa var. cepa Nutrition 0.000 description 1
- 235000003840 Amygdalus nana Nutrition 0.000 description 1
- 244000296825 Amygdalus nana Species 0.000 description 1
- 244000099147 Ananas comosus Species 0.000 description 1
- 235000007119 Ananas comosus Nutrition 0.000 description 1
- 108020000948 Antisense Oligonucleotides Proteins 0.000 description 1
- 108020005544 Antisense RNA Proteins 0.000 description 1
- 241000219194 Arabidopsis Species 0.000 description 1
- 235000005340 Asparagus officinalis Nutrition 0.000 description 1
- 235000005781 Avena Nutrition 0.000 description 1
- 235000007319 Avena orientalis Nutrition 0.000 description 1
- 241000194110 Bacillus sp. (in: Bacteria) Species 0.000 description 1
- DWRXFEITVBNRMK-UHFFFAOYSA-N Beta-D-1-Arabinofuranosylthymine Natural products O=C1NC(=O)C(C)=CN1C1C(O)C(O)C(CO)O1 DWRXFEITVBNRMK-UHFFFAOYSA-N 0.000 description 1
- 241000219198 Brassica Species 0.000 description 1
- 235000011331 Brassica Nutrition 0.000 description 1
- 235000014698 Brassica juncea var multisecta Nutrition 0.000 description 1
- 235000006008 Brassica napus var napus Nutrition 0.000 description 1
- 235000006618 Brassica rapa subsp oleifera Nutrition 0.000 description 1
- 244000188595 Brassica sinapistrum Species 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 235000002566 Capsicum Nutrition 0.000 description 1
- 240000008574 Capsicum frutescens Species 0.000 description 1
- 108090000994 Catalytic RNA Proteins 0.000 description 1
- 102000053642 Catalytic RNA Human genes 0.000 description 1
- 101710151663 Cationic peroxidase Proteins 0.000 description 1
- 102220584160 Cellular tumor antigen p53_P75R_mutation Human genes 0.000 description 1
- 235000007516 Chrysanthemum Nutrition 0.000 description 1
- 244000189548 Chrysanthemum x morifolium Species 0.000 description 1
- 241000219109 Citrullus Species 0.000 description 1
- 241000207199 Citrus Species 0.000 description 1
- 235000013162 Cocos nucifera Nutrition 0.000 description 1
- 244000060011 Cocos nucifera Species 0.000 description 1
- 108700010070 Codon Usage Proteins 0.000 description 1
- 240000004270 Colocasia esculenta var. antiquorum Species 0.000 description 1
- 108020004635 Complementary DNA Proteins 0.000 description 1
- 241000218631 Coniferophyta Species 0.000 description 1
- 235000009091 Cordyline terminalis Nutrition 0.000 description 1
- 244000289527 Cordyline terminalis Species 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 244000241257 Cucumis melo Species 0.000 description 1
- 235000015510 Cucumis melo subsp melo Nutrition 0.000 description 1
- 241000219122 Cucurbita Species 0.000 description 1
- 102100026398 Cyclic AMP-responsive element-binding protein 3 Human genes 0.000 description 1
- HMFHBZSHGGEWLO-SOOFDHNKSA-N D-ribofuranose Chemical compound OC[C@H]1OC(O)[C@H](O)[C@@H]1O HMFHBZSHGGEWLO-SOOFDHNKSA-N 0.000 description 1
- 238000007399 DNA isolation Methods 0.000 description 1
- 102100027828 DNA repair protein XRCC4 Human genes 0.000 description 1
- 230000006820 DNA synthesis Effects 0.000 description 1
- 101710096438 DNA-binding protein Proteins 0.000 description 1
- 241000208175 Daucus Species 0.000 description 1
- 244000000626 Daucus carota Species 0.000 description 1
- 235000002767 Daucus carota Nutrition 0.000 description 1
- 108010054576 Deoxyribonuclease EcoRI Proteins 0.000 description 1
- 108010008532 Deoxyribonuclease I Proteins 0.000 description 1
- 102000007260 Deoxyribonuclease I Human genes 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 235000002723 Dioscorea alata Nutrition 0.000 description 1
- 235000007056 Dioscorea composita Nutrition 0.000 description 1
- 235000009723 Dioscorea convolvulacea Nutrition 0.000 description 1
- 235000005362 Dioscorea floribunda Nutrition 0.000 description 1
- 235000004868 Dioscorea macrostachya Nutrition 0.000 description 1
- 235000005361 Dioscorea nummularia Nutrition 0.000 description 1
- 235000005360 Dioscorea spiculiflora Nutrition 0.000 description 1
- 238000012286 ELISA Assay Methods 0.000 description 1
- 241000132521 Erigeron Species 0.000 description 1
- 108700024394 Exon Proteins 0.000 description 1
- 108060002716 Exonuclease Proteins 0.000 description 1
- GHASVSINZRGABV-UHFFFAOYSA-N Fluorouracil Chemical compound FC1=CNC(=O)NC1=O GHASVSINZRGABV-UHFFFAOYSA-N 0.000 description 1
- 235000016623 Fragaria vesca Nutrition 0.000 description 1
- 240000009088 Fragaria x ananassa Species 0.000 description 1
- 235000011363 Fragaria x ananassa Nutrition 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 102000053187 Glucuronidase Human genes 0.000 description 1
- 108010060309 Glucuronidase Proteins 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 235000010469 Glycine max Nutrition 0.000 description 1
- 244000068988 Glycine max Species 0.000 description 1
- 102000003886 Glycoproteins Human genes 0.000 description 1
- 108090000288 Glycoproteins Proteins 0.000 description 1
- 235000009438 Gossypium Nutrition 0.000 description 1
- 108091027305 Heteroduplex Proteins 0.000 description 1
- 229920000209 Hexadimethrine bromide Polymers 0.000 description 1
- 102100039869 Histone H2B type F-S Human genes 0.000 description 1
- 108010036115 Histone Methyltransferases Proteins 0.000 description 1
- 102000011787 Histone Methyltransferases Human genes 0.000 description 1
- 102100022893 Histone acetyltransferase KAT5 Human genes 0.000 description 1
- 101710116149 Histone acetyltransferase KAT5 Proteins 0.000 description 1
- 102000003893 Histone acetyltransferases Human genes 0.000 description 1
- 108090000246 Histone acetyltransferases Proteins 0.000 description 1
- 102100024594 Histone-lysine N-methyltransferase PRDM16 Human genes 0.000 description 1
- 101000855520 Homo sapiens Cyclic AMP-responsive element-binding protein 3 Proteins 0.000 description 1
- 101000649315 Homo sapiens DNA repair protein XRCC4 Proteins 0.000 description 1
- 101001035372 Homo sapiens Histone H2B type F-S Proteins 0.000 description 1
- 101000686942 Homo sapiens Histone-lysine N-methyltransferase PRDM16 Proteins 0.000 description 1
- 101000615488 Homo sapiens Methyl-CpG-binding domain protein 2 Proteins 0.000 description 1
- 101000904868 Homo sapiens Transcriptional regulator ATRX Proteins 0.000 description 1
- 241000209219 Hordeum Species 0.000 description 1
- 102000012330 Integrases Human genes 0.000 description 1
- 108010061833 Integrases Proteins 0.000 description 1
- 108091092195 Intron Proteins 0.000 description 1
- 235000006350 Ipomoea batatas var. batatas Nutrition 0.000 description 1
- 241000208822 Lactuca Species 0.000 description 1
- 108091036060 Linker DNA Proteins 0.000 description 1
- 108090001030 Lipoproteins Proteins 0.000 description 1
- 102000004895 Lipoproteins Human genes 0.000 description 1
- 241000209082 Lolium Species 0.000 description 1
- 108060001084 Luciferase Proteins 0.000 description 1
- 239000005089 Luciferase Substances 0.000 description 1
- 235000002262 Lycopersicon Nutrition 0.000 description 1
- 101710180598 Lysosomal cobalamin transporter ABCD4 Proteins 0.000 description 1
- 241000218922 Magnoliophyta Species 0.000 description 1
- 235000011430 Malus pumila Nutrition 0.000 description 1
- 235000015103 Malus silvestris Nutrition 0.000 description 1
- 240000003183 Manihot esculenta Species 0.000 description 1
- 102100021299 Methyl-CpG-binding domain protein 2 Human genes 0.000 description 1
- 108060004795 Methyltransferase Proteins 0.000 description 1
- 108010059724 Micrococcal Nuclease Proteins 0.000 description 1
- 240000005561 Musa balbisiana Species 0.000 description 1
- 235000018290 Musa x paradisiaca Nutrition 0.000 description 1
- 101100093450 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) ubi::crp-6 gene Proteins 0.000 description 1
- 235000002637 Nicotiana tabacum Nutrition 0.000 description 1
- KYRVNWMVYQXFEU-UHFFFAOYSA-N Nocodazole Chemical compound C1=C2NC(NC(=O)OC)=NC2=CC=C1C(=O)C1=CC=CS1 KYRVNWMVYQXFEU-UHFFFAOYSA-N 0.000 description 1
- 102000043276 Oncogene Human genes 0.000 description 1
- 108700020796 Oncogene Proteins 0.000 description 1
- 241001233986 Orychophragmus Species 0.000 description 1
- 241000209094 Oryza Species 0.000 description 1
- 238000002944 PCR assay Methods 0.000 description 1
- 229930012538 Paclitaxel Natural products 0.000 description 1
- 102000001406 Perilipin Human genes 0.000 description 1
- 108060006002 Perilipin Proteins 0.000 description 1
- 241000218196 Persea Species 0.000 description 1
- 240000007377 Petunia x hybrida Species 0.000 description 1
- 241000219833 Phaseolus Species 0.000 description 1
- 235000010627 Phaseolus vulgaris Nutrition 0.000 description 1
- 244000046052 Phaseolus vulgaris Species 0.000 description 1
- 102000045595 Phosphoprotein Phosphatases Human genes 0.000 description 1
- 108700019535 Phosphoprotein Phosphatases Proteins 0.000 description 1
- 102000004160 Phosphoric Monoester Hydrolases Human genes 0.000 description 1
- 108090000608 Phosphoric Monoester Hydrolases Proteins 0.000 description 1
- 241000219843 Pisum Species 0.000 description 1
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 description 1
- 229920000776 Poly(Adenosine diphosphate-ribose) polymerase Polymers 0.000 description 1
- 108010043400 Protamine Kinase Proteins 0.000 description 1
- 102000001253 Protein Kinase Human genes 0.000 description 1
- 108700040121 Protein Methyltransferases Proteins 0.000 description 1
- 102000055027 Protein Methyltransferases Human genes 0.000 description 1
- 235000011432 Prunus Nutrition 0.000 description 1
- 235000014443 Pyrus communis Nutrition 0.000 description 1
- 230000004570 RNA-binding Effects 0.000 description 1
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 1
- 241000220259 Raphanus Species 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 102000018120 Recombinases Human genes 0.000 description 1
- 108010091086 Recombinases Proteins 0.000 description 1
- 108700008625 Reporter Genes Proteins 0.000 description 1
- 241000589187 Rhizobium sp. Species 0.000 description 1
- 241000220010 Rhode Species 0.000 description 1
- 108091028664 Ribonucleotide Proteins 0.000 description 1
- PYMYPHUHKUWMLA-LMVFSUKVSA-N Ribose Natural products OC[C@@H](O)[C@@H](O)[C@@H](O)C=O PYMYPHUHKUWMLA-LMVFSUKVSA-N 0.000 description 1
- 241000220317 Rosa Species 0.000 description 1
- 230000018199 S phase Effects 0.000 description 1
- 101001025539 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) Homothallic switching endonuclease Proteins 0.000 description 1
- 240000000111 Saccharum officinarum Species 0.000 description 1
- 235000007201 Saccharum officinarum Nutrition 0.000 description 1
- 241000607142 Salmonella Species 0.000 description 1
- 235000007238 Secale cereale Nutrition 0.000 description 1
- 241000589127 Sinorhizobium fredii NGR234 Species 0.000 description 1
- 241000207763 Solanum Species 0.000 description 1
- 235000002634 Solanum Nutrition 0.000 description 1
- 240000006394 Sorghum bicolor Species 0.000 description 1
- 238000002105 Southern blotting Methods 0.000 description 1
- 241001292337 Sphingobium herbicidovorans Species 0.000 description 1
- 235000009337 Spinacia oleracea Nutrition 0.000 description 1
- 244000300264 Spinacia oleracea Species 0.000 description 1
- 241000187191 Streptomyces viridochromogenes Species 0.000 description 1
- 241001648840 Thosea asigna virus Species 0.000 description 1
- 108091036066 Three prime untranslated region Proteins 0.000 description 1
- 101710183280 Topoisomerase Proteins 0.000 description 1
- 108010073062 Transcription Activator-Like Effectors Proteins 0.000 description 1
- 102100023931 Transcriptional regulator ATRX Human genes 0.000 description 1
- 102000004357 Transferases Human genes 0.000 description 1
- 108090000992 Transferases Proteins 0.000 description 1
- RTKIYFITIVXBLE-UHFFFAOYSA-N Trichostatin A Natural products ONC(=O)C=CC(C)=CC(C)C(=O)C1=CC=C(N(C)C)C=C1 RTKIYFITIVXBLE-UHFFFAOYSA-N 0.000 description 1
- 108091023045 Untranslated Region Proteins 0.000 description 1
- 229910052770 Uranium Inorganic materials 0.000 description 1
- 241000219977 Vigna Species 0.000 description 1
- JXLYSJRDGCGARV-WWYNWVTFSA-N Vinblastine Natural products O=C(O[C@H]1[C@](O)(C(=O)OC)[C@@H]2N(C)c3c(cc(c(OC)c3)[C@]3(C(=O)OC)c4[nH]c5c(c4CCN4C[C@](O)(CC)C[C@H](C3)C4)cccc5)[C@@]32[C@H]2[C@@]1(CC)C=CCN2CC3)C JXLYSJRDGCGARV-WWYNWVTFSA-N 0.000 description 1
- 235000009392 Vitis Nutrition 0.000 description 1
- 241000219095 Vitis Species 0.000 description 1
- 102100036976 X-ray repair cross-complementing protein 6 Human genes 0.000 description 1
- 101710124907 X-ray repair cross-complementing protein 6 Proteins 0.000 description 1
- 241000589634 Xanthomonas Species 0.000 description 1
- 241000607479 Yersinia pestis Species 0.000 description 1
- 241000209149 Zea Species 0.000 description 1
- FJJCIZWZNKZHII-UHFFFAOYSA-N [4,6-bis(cyanoamino)-1,3,5-triazin-2-yl]cyanamide Chemical compound N#CNC1=NC(NC#N)=NC(NC#N)=N1 FJJCIZWZNKZHII-UHFFFAOYSA-N 0.000 description 1
- 125000000218 acetic acid group Chemical group C(C)(=O)* 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 244000193174 agave Species 0.000 description 1
- 230000009418 agronomic effect Effects 0.000 description 1
- HMFHBZSHGGEWLO-UHFFFAOYSA-N alpha-D-Furanose-Ribose Natural products OCC1OC(O)C(O)C1O HMFHBZSHGGEWLO-UHFFFAOYSA-N 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000000074 antisense oligonucleotide Substances 0.000 description 1
- 238000012230 antisense oligonucleotides Methods 0.000 description 1
- IQFYYKKMVGJFEH-UHFFFAOYSA-N beta-L-thymidine Natural products O=C1NC(=O)C(C)=CN1C1OC(CO)C(O)C1 IQFYYKKMVGJFEH-UHFFFAOYSA-N 0.000 description 1
- 238000002306 biochemical method Methods 0.000 description 1
- 239000003139 biocide Substances 0.000 description 1
- 238000003766 bioinformatics method Methods 0.000 description 1
- 239000002981 blocking agent Substances 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 238000009395 breeding Methods 0.000 description 1
- 230000001488 breeding effect Effects 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000001390 capsicum minimum Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 230000025084 cell cycle arrest Effects 0.000 description 1
- 230000007910 cell fusion Effects 0.000 description 1
- 230000010307 cell transformation Effects 0.000 description 1
- 230000007073 chemical hydrolysis Effects 0.000 description 1
- 238000001311 chemical methods and process Methods 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 229960004316 cisplatin Drugs 0.000 description 1
- 235000020971 citrus fruits Nutrition 0.000 description 1
- 238000000749 co-immunoprecipitation Methods 0.000 description 1
- 238000000975 co-precipitation Methods 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 239000003184 complementary RNA Substances 0.000 description 1
- 238000012790 confirmation Methods 0.000 description 1
- 238000009402 cross-breeding Methods 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 239000005547 deoxyribonucleotide Substances 0.000 description 1
- 125000002637 deoxyribonucleotide group Chemical group 0.000 description 1
- 229960002086 dextran Drugs 0.000 description 1
- 229960000633 dextran sulfate Drugs 0.000 description 1
- 150000004985 diamines Chemical class 0.000 description 1
- 239000005546 dideoxynucleotide Substances 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 235000004879 dioscorea Nutrition 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 229960004679 doxorubicin Drugs 0.000 description 1
- 235000013399 edible fruits Nutrition 0.000 description 1
- 210000002257 embryonic structure Anatomy 0.000 description 1
- 230000007071 enzymatic hydrolysis Effects 0.000 description 1
- 238000006047 enzymatic hydrolysis reaction Methods 0.000 description 1
- 238000001952 enzyme assay Methods 0.000 description 1
- ZMMJGEGLRURXTF-UHFFFAOYSA-N ethidium bromide Chemical compound [Br-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CC)=C1C1=CC=CC=C1 ZMMJGEGLRURXTF-UHFFFAOYSA-N 0.000 description 1
- 229960005542 ethidium bromide Drugs 0.000 description 1
- VJJPUSNTGOMMGY-MRVIYFEKSA-N etoposide Chemical compound COC1=C(O)C(OC)=CC([C@@H]2C3=CC=4OCOC=4C=C3[C@@H](O[C@H]3[C@@H]([C@@H](O)[C@@H]4O[C@H](C)OC[C@H]4O3)O)[C@@H]3[C@@H]2C(OC3)=O)=C1 VJJPUSNTGOMMGY-MRVIYFEKSA-N 0.000 description 1
- 229960005420 etoposide Drugs 0.000 description 1
- 102000013165 exonuclease Human genes 0.000 description 1
- 230000001036 exonucleolytic effect Effects 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 229960002949 fluorouracil Drugs 0.000 description 1
- 239000004459 forage Substances 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 230000008014 freezing Effects 0.000 description 1
- 238000007710 freezing Methods 0.000 description 1
- 238000010363 gene targeting Methods 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- 102000034356 gene-regulatory proteins Human genes 0.000 description 1
- 108091006104 gene-regulatory proteins Proteins 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 230000005017 genetic modification Effects 0.000 description 1
- 235000013617 genetically modified food Nutrition 0.000 description 1
- 238000010362 genome editing Methods 0.000 description 1
- 150000004676 glycans Chemical class 0.000 description 1
- 230000013595 glycosylation Effects 0.000 description 1
- 238000006206 glycosylation reaction Methods 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 229910001385 heavy metal Inorganic materials 0.000 description 1
- 241000411851 herbal medicine Species 0.000 description 1
- 239000000833 heterodimer Substances 0.000 description 1
- 235000014304 histidine Nutrition 0.000 description 1
- 239000000710 homodimer Substances 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 238000012744 immunostaining Methods 0.000 description 1
- 238000007901 in situ hybridization Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 239000012212 insulator Substances 0.000 description 1
- 238000005304 joining Methods 0.000 description 1
- 229930027917 kanamycin Natural products 0.000 description 1
- 229960000318 kanamycin Drugs 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 229930182823 kanamycin A Natural products 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 235000005739 manihot Nutrition 0.000 description 1
- 108010083942 mannopine synthase Proteins 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000029115 microtubule polymerization Effects 0.000 description 1
- 235000019713 millet Nutrition 0.000 description 1
- 229950002289 mimosine Drugs 0.000 description 1
- 210000003470 mitochondria Anatomy 0.000 description 1
- 230000002438 mitochondrial effect Effects 0.000 description 1
- 102000035118 modified proteins Human genes 0.000 description 1
- 108091005573 modified proteins Proteins 0.000 description 1
- 238000001823 molecular biology technique Methods 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 238000002703 mutagenesis Methods 0.000 description 1
- 231100000350 mutagenesis Toxicity 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 229950006344 nocodazole Drugs 0.000 description 1
- 238000007899 nucleic acid hybridization Methods 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 210000003463 organelle Anatomy 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- 230000036542 oxidative stress Effects 0.000 description 1
- 229960001592 paclitaxel Drugs 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 230000000737 periodic effect Effects 0.000 description 1
- PTMHPRAIXMAOOB-UHFFFAOYSA-L phosphoramidate Chemical compound NP([O-])([O-])=O PTMHPRAIXMAOOB-UHFFFAOYSA-L 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 238000000053 physical method Methods 0.000 description 1
- 229930195732 phytohormone Natural products 0.000 description 1
- 244000000003 plant pathogen Species 0.000 description 1
- 230000027086 plasmid maintenance Effects 0.000 description 1
- 230000004983 pleiotropic effect Effects 0.000 description 1
- 229960000502 poloxamer Drugs 0.000 description 1
- 229920001983 poloxamer Polymers 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 102000021127 protein binding proteins Human genes 0.000 description 1
- 108091011138 protein binding proteins Proteins 0.000 description 1
- 230000004853 protein function Effects 0.000 description 1
- 108060006633 protein kinase Proteins 0.000 description 1
- 238000001742 protein purification Methods 0.000 description 1
- 230000004850 protein–protein interaction Effects 0.000 description 1
- 235000014774 prunus Nutrition 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000014493 regulation of gene expression Effects 0.000 description 1
- 102000037983 regulatory factors Human genes 0.000 description 1
- 108091008025 regulatory factors Proteins 0.000 description 1
- 230000003362 replicative effect Effects 0.000 description 1
- 230000000754 repressing effect Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 239000002336 ribonucleotide Substances 0.000 description 1
- 125000002652 ribonucleotide group Chemical group 0.000 description 1
- 108091092562 ribozyme Proteins 0.000 description 1
- 102200108201 rs1042522 Human genes 0.000 description 1
- 102220050701 rs193920857 Human genes 0.000 description 1
- 102220059906 rs786202575 Human genes 0.000 description 1
- 102220103308 rs878854065 Human genes 0.000 description 1
- 238000010517 secondary reaction Methods 0.000 description 1
- 238000010187 selection method Methods 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 238000002864 sequence alignment Methods 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- 239000013605 shuttle vector Substances 0.000 description 1
- HBMJWWWQQXIZIP-UHFFFAOYSA-N silicon carbide Chemical compound [Si+]#[C-] HBMJWWWQQXIZIP-UHFFFAOYSA-N 0.000 description 1
- 229910010271 silicon carbide Inorganic materials 0.000 description 1
- MFBOGIVSZKQAPD-UHFFFAOYSA-M sodium butyrate Chemical compound [Na+].CCCC([O-])=O MFBOGIVSZKQAPD-UHFFFAOYSA-M 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 230000009870 specific binding Effects 0.000 description 1
- 210000000130 stem cell Anatomy 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- RCINICONZNJXQF-MZXODVADSA-N taxol Chemical compound O([C@@H]1[C@@]2(C[C@@H](C(C)=C(C2(C)C)[C@H](C([C@]2(C)[C@@H](O)C[C@H]3OC[C@]3([C@H]21)OC(C)=O)=O)OC(=O)C)OC(=O)[C@H](O)[C@@H](NC(=O)C=1C=CC=CC=1)C=1C=CC=CC=1)O)C(=O)C1=CC=CC=C1 RCINICONZNJXQF-MZXODVADSA-N 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 229940104230 thymidine Drugs 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 238000003151 transfection method Methods 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- RTKIYFITIVXBLE-QEQCGCAPSA-N trichostatin A Chemical compound ONC(=O)/C=C/C(/C)=C/[C@@H](C)C(=O)C1=CC=C(N(C)C)C=C1 RTKIYFITIVXBLE-QEQCGCAPSA-N 0.000 description 1
- 238000010798 ubiquitination Methods 0.000 description 1
- 230000034512 ubiquitination Effects 0.000 description 1
- 238000002604 ultrasonography Methods 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 229960003048 vinblastine Drugs 0.000 description 1
- JXLYSJRDGCGARV-XQKSVPLYSA-N vincaleukoblastine Chemical compound C([C@@H](C[C@]1(C(=O)OC)C=2C(=CC3=C([C@]45[C@H]([C@@]([C@H](OC(C)=O)[C@]6(CC)C=CCN([C@H]56)CC4)(O)C(=O)OC)N3C)C=2)OC)C[C@@](C2)(O)CC)N2CCC2=C1NC1=CC=CC=C21 JXLYSJRDGCGARV-XQKSVPLYSA-N 0.000 description 1
- 239000013603 viral vector Substances 0.000 description 1
- 230000001018 virulence Effects 0.000 description 1
- 238000011179 visual inspection Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/82—Vectors or expression systems specially adapted for eukaryotic hosts for plant cells, e.g. plant artificial chromosomes (PACs)
- C12N15/8201—Methods for introducing genetic material into plant cells, e.g. DNA, RNA, stable or transient incorporation, tissue culture methods adapted for transformation
- C12N15/8213—Targeted insertion of genes into the plant genome by homologous recombination
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01H—NEW PLANTS OR NON-TRANSGENIC PROCESSES FOR OBTAINING THEM; PLANT REPRODUCTION BY TISSUE CULTURE TECHNIQUES
- A01H5/00—Angiosperms, i.e. flowering plants, characterised by their plant parts; Angiosperms characterised otherwise than by their botanic taxonomy
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N63/00—Biocides, pest repellants or attractants, or plant growth regulators containing microorganisms, viruses, microbial fungi, animals or substances produced by, or obtained from, microorganisms, viruses, microbial fungi or animals, e.g. enzymes or fermentates
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/10—Cells modified by introduction of foreign genetic material
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A40/00—Adaptation technologies in agriculture, forestry, livestock or agroalimentary production
- Y02A40/10—Adaptation technologies in agriculture, forestry, livestock or agroalimentary production in agriculture
- Y02A40/146—Genetically Modified [GMO] plants, e.g. transgenic plants
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Biotechnology (AREA)
- Biomedical Technology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Chemical & Material Sciences (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Biochemistry (AREA)
- Plant Pathology (AREA)
- Biophysics (AREA)
- Physics & Mathematics (AREA)
- Molecular Biology (AREA)
- Environmental Sciences (AREA)
- Agronomy & Crop Science (AREA)
- Developmental Biology & Embryology (AREA)
- Botany (AREA)
- Physiology (AREA)
- Pest Control & Pesticides (AREA)
- Virology (AREA)
- Dentistry (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Breeding Of Plants And Reproduction By Means Of Culturing (AREA)
- Peptides Or Proteins (AREA)
- Ultra Sonic Daignosis Equipment (AREA)
- Oscillators With Electromechanical Resonators (AREA)
Abstract
integração objetivada no locus de zp15. a invenção refere-se a métodos e composições para integração objetivada de uma sequência oxógena em um locus de zp de planta, por exemplo, para a expressão de um polipeptídeo de interesse.
Description
[001] Não aplicável.
[002] A presente invenção está no campo de engenharia genômica de planta, particularmente integração objetivada de um transgene em um gene Zp15 de planta.
[003] A biotecnologia tem emergido como uma ferramenta essencial em esforços para ir de encontro ao desafio de aumento da demanda global pela produção de alimento. Abordagens convencionais para aprimoramento da produtividade agrícola, por exemplo, rendimento intensificado ou resistência manipulada a pestes, contam com melhoramento por mutação ou introdução de novos genes nos genomas de espécies de safra por meio de transformação. Ambos os processos são inerentemente não específicos e relativamente ineficientes. Por exemplo, métodos convencionais de transformação de planta distribuem DNA exógeno que se integram no genoma em locais aleatórios. Assim, de forma a identificar e isolar linhagens transgênicas com atributos desejáveis, é necessário gerar milhares de eventos de integração aleatória única e subsequentemente realizar triagem quanto aos indivíduos desejados. Como um resultado, a manipulação convencional de traços de uma planta é trabalhosa, consome tempo e imprevisível. Além disso, a natureza aleatória dessas integrações torna difícil prever se efeitos pleiotrópicos em virtude de ruptura não intencional do genoma ocorreu. Como um resultado, a geração, isolamento e caracterização de linhagens de planta com genes ou traços manipulados têm sido um processo extremamente trabalhoso e de alto custo, com uma baixa probabilidade de sucesso.
[004] A modificação gênica objetivada supera os desafios logísticos de práticas convencionais em sistemas de planta e, como tal, tem sido um objetivo há muito desejado, mas elusivo em pesquisa de biologia de planta básica e biotecnologia agrícola. Contudo, foi provado até recentemente que, com exceção de "objetivação gênica" via seleção de fármaco positiva-negativa em arroz ou o uso de sítios de restrição pré- manipulados, modificação genômica objetivada em todas as espécies de planta, modelo e safra, é muito difícil. Terada etal. (2002) NatBiotechnol 20(10): 1030; Terada et al. (2007) Plant Physiol 144(2): 846; D'Halluin et al. (2008) Plant Biotechnology J. 6(1): 93.
[005] Recentemente, métodos e composições para clivagem objeti vada de DNA genômico foram descritos. T ais eventos de clivagem objetivada podem ser usados, por exemplo, para induzir à mutagênese objetivada, induzir a deleções objetivadas de sequências de DNA celular e facilitar a recombinação objetivada em um locus cromossômico predeterminado. Vide, por exemplo, Publicações de Patente dos Estados Unidos 20030232410; 20050208489; 20050026157; 20050064474; e 20060188987 e Publicação Internacional WO 2007/014275, as divulgações das quais são incorporadas por referência em suas totalidades para todas as finalidades. A Publicação de Patente U.S. No. 20080182332 descreve o uso de nucleases do dedo de zinco (Zinc Finger Nucleases - ZFNs) não canônicas para modificação objetivada de genomas de planta e o Pedido de Patente U.S. No. 12/284.888 descreve a interação objetivada ZFN-mediada em um locus EPSPS de planta.
[006] Contudo, permanece uma necessidade por composições e métodos para integração objetivada estável em loci adicionais dentro do genoma de uma planta para estabelecimento de modificações genéticas estáveis, hereditárias na planta e sua prole.
[007] A presente invenção proporciona métodos e composições pa ra expressão de um ou mais produtos de uma sequência de ácido nucleico exógena (isto é, uma proteína ou uma molécula de RNA) que tenha sido integrada em um gene Zp15 em uma célula vegetal. Conforme mostrado aqui, a integração de uma ou mais sequências exógenas em ou próximo do locus de Zp15 não parece prejudicar a capacidade da planta hospedeira de regenerar, florescer ou produzir sementes e, opcionalmente, permite transmissão hereditária da(s) sequências(s) exógena(s) durante as gerações. As sequências de ácido nucleico exógenas podem compreender, por exemplo, um ou mais genes ou moléculas de cDNA ou qualquer tipo de sequência de codificação ou não codificação, bem como um ou mais elementos de controle (por exemplo, promotores). Por exemplo, genes de tolerância ao herbicida podem ser integrados nesse locus para produzir plantas de safra com a resistência ao herbicida desejada. Células contendo ácidos nucleicos exógenos em ou próximo do locus de Zp15 também podem contribuir para o gametófito (linhagem germinativa) e, portanto, ser transmitidas para a prole em gerações subsequentes.
[008] A integração da sequência de ácido nucleico exógena em um gene Zp15 é facilitada por clivagem de fita dupla objetivada do genoma no locus de Zp15. Clivagem é objetivada a um gene Zp15 mediante o uso de proteínas de fusão compreendendo um domínio de ligação a DNA, tal como um domínio de ligação a DNA de meganuclease, um domínio de ligação a DNA de zíper de leucina, uma proteína do dedo de zinco (Zinc Finger Protein - ZFP) ou combinações quiméricas dos antes mencionados, o qual é manipulado para se ligar a uma sequência dentro do locus de Zp15 selecionado e um domínio de clivagem ou um meio-domínio de clivagem. Tal clivagem estimula a integração de sequências de polinucle- otídeo exógenas em ou próximo do sítio de clivagem. Integração de sequências exógenas pode se processar por meio de mecanismos dependentes de homologia e independentes de homologia.
[009] Em um aspecto, são divulgados aqui domínios de ligação a DNA manipulados (por exemplo, ZFPs, meganucleases ou zíperes de leucina) que se ligam a um sítio-alvo em um gene Zp15. O domínio de ligação a DNA pode compreender, por exemplo, qualquer um dos domínios de ligação a DNA de dedo de zinco manipulados compreendendo as hélices de reconhecimento mostradas na Tabela 1. Qualquer um dos domínios de ligação a DNA descritos aqui pode ainda compreender um domínio funcional, por exemplo, um domínio de clivagem ou meio-domínio de clivagem. Em algumas modalidades, o meio-domínio de clivagem pode ser de uma endonuclease de restrição do tipo IIS, tal como FokI ou StsI. Em outras modalidades, o domínio de clivagem pode compreender uma endonuclease "homing", por exemplo, uma endonuclease "homing" com um domínio de ligação a DNA modificado.
[0010] Em outro aspecto, são divulgadas aqui plantas ou sementes compreendendo uma sequência exógena integrada no locus de Zp15. Em determinadas modalidades, a sequência exógena é integrada no gametó- fito da planta.
[0011] Em outro aspecto, é divulgado aqui um método para expres são do produto de uma sequência de ácido nucleico exógena em uma célula, o método compreendendo: (a) expressão de uma primeira proteína de fusão na célula, a primeira proteína de fusão compreendendo um primeiro domínio de ligação a DNA (por exemplo, uma ZFP) e um primeiro meio-domínio de clivagem, em que o domínio de ligação a DNA tenha sido manipulado para se ligar a um primeiro sítio-alvo em um gene Zp15 do genoma da célula; (b) expressão de uma segunda proteína de fusão na célula, a segunda proteína de fusão compreendendo um segundo domínio de ligação a DNA e um segundo meio-domínio de clivagem, em que o segundo domínio de ligação a DNA se liga a um segundo sítio-alvo no gene Zp15 do genoma da célula, em que o segundo sítio-alvo é diferente do primeiro sítio-alvo; e (c) contato da célula com um polinucleotí- deo compreendendo uma sequência de ácido nucleico exógena e uma primeira sequência de nucleotídeo que é homóloga à primeira sequência em um gene Zp15; em que ligação da primeira proteína de fusão ao primeiro sítio-alvo e ligação da segunda proteína de fusão ao segundo sítio- alvo posiciona os meio-domínios de clivagem de modo que o genoma da célula seja clivado no gene Zp15, desse modo, resultando em integração da sequência exógena no genoma da célula no gene Zp15 e expressão do produto da sequência exógena.
[0012] A sequência de ácido nucleico exógena pode compreender uma sequência que codifica um ou mais polipeptídeos funcionais (por exemplo, um cDNA), com ou sem um ou mais promotores e/ou pode produzir uma ou mais sequências de RNA (por exemplo, via um ou mais cassetes de expressão de shRNA) as quais conferem traços desejáveis à planta. Tais traços incluem, mas não estão limitados a, resistência ou tolerância ao herbicida; resistência ou tolerância a insetos; resistência ou tolerância a doenças (virais, bacterianas, fúngicas, por nematoide); tolerância e/ou resistência a estresse, conforme exemplificado por resistência ou tolerância à estiagem, calor, frio, congelamento, umidade excessiva, estresse por sal; estresse oxidativo; rendimentos aumentados; teor e composição alimentícia; aparência física; esterilidade masculina; velocidade de secagem; sustentabilidade; abundância; quantidade e qualidade de amido; quantidade e qualidade de óleo; qualidade e quantidade de proteína; composição de aminoácido; e semelhantes. Naturalmente, quaisquer dois ou mais ácidos nucleicos exógenos de qualquer descrição, tais como aqueles que conferem resistência ao herbicida, insetos, doenças (virais, bacterianas, fúngicas, por nematoide) ou estiagem, esterilidade masculina, velocidade de secagem, sustentabilidade, abundância, propriedades de amido, quantidade e qualidade de óleo ou aqueles que aumentam o rendimento ou qualidade nutricional podem ser empregados, conforme desejado. Em determinadas modalidades, a sequência de ácido nucleico compreende uma sequência que codifica uma proteína de resistência a herbicida (por exemplo, o gene AAD-1 (Aryloxy Alkanoate Dioxygenase - Dioxigenase de Arilóxi Alcanoato), o gene AAD-12 ou o gene de acetil transferase de fosfinotricina (Phosphinothricin Acetyl Transferase - PAT) e/ou fragmentos funcionais dos mesmos. Expressão da sequência integrada pode ser acionada por um promotor operativamente ligado à sequência integrada. Alternativamente, a sequência integrada é sem promotor e a transcrição é acionada pelo promotor de Zp15 endógeno.
[0013] Em determinadas modalidades, o polinucleotídeo ainda com preende uma segunda sequência de nucleotídeo que é homóloga a uma segunda sequência no gene Zp15. A segunda sequência de nucleotídeo pode ser idêntica à segunda sequência no gene Zp15. Além disso, em modalidades compreendendo primeira e segunda sequências de nucleotídeo, a primeira sequência de nucleotídeo pode ser idêntica à primeira sequência no gene Zp15 e a segunda sequência de nucleotídeo pode ser homóloga, mas não idêntica, a uma segunda sequência no gene Zp15. Em qualquer um dos métodos descritos aqui, as primeira e segunda sequências de nucleotídeo flanqueiam a sequência exógena. Em determinadas modalidades, o polinucleotídeo é um plasmídeo. Em outras modalidades, o polinucleotídeo é uma molécula de DNA linear.
[0014] Em outro aspecto, é proporcionado aqui um método para inte gração de uma sequência exógena no gene Zp15 no genoma de uma célula, o método compreendendo: (a) expressão de uma primeira proteína de fusão na célula, a primeira proteína de fusão compreendendo um primeiro domínio de ligação a DNA (por exemplo, uma ZFP) e um primeiro meio-domínio de clivagem, em que o primeiro domínio de ligação a DNA foi manipulado para se ligar a um primeiro sítio-alvo no locus de Zp15 no genoma da célula; (b) expressão de uma segunda proteína de fusão na célula, a segunda proteína de fusão compreendendo um segun- do domínio de ligação a DNA (por exemplo, uma ZFP) e um segundo meio-domínio de clivagem, em que o segundo domínio de ligação a DNA se liga a um segundo sítio-alvo no locus de Zp15 no genoma da célula, em que o segundo sítio-alvo é diferente do primeiro sítio-alvo; e (c) contato da célula com um polinucleotídeo compreendendo uma sequência de ácido nucleico exógena; em que ligação da primeira proteína de fusão ao primeiro sítio-alvo e ligação da segunda proteína de fusão ao segundo sítio-alvo posicionam os meio-domínios de clivagem de modo que o genoma da célula seja clivado no locus de Zp15, desse modo, resultando em integração dependente de homologia da sequência exógena no genoma da célula dentro do locus de Zp15. Em determinadas modalidades, uma sequência exógena que codifica um polipeptídeo funcional é inserida no gene Zp15.
[0015] Em qualquer um dos métodos descritos aqui, os primeiro e segundo meio-domínios de clivagem podem ser de uma endonuclease de restrição do tipo IIS, por exemplo, Fok I ou Sfs I. Além disso, em qualquer um dos métodos descritos aqui, pelo menos uma das proteínas de fusão pode compreender uma alteração na sequência de aminoácido da interface de dimerização do meio-domínio de clivagem, por exemplo, de modo que heterodímeros obrigatórios dos meio-domínios de clivagem sejam formados.
[0016] Em qualquer um dos métodos descritos aqui, a célula vegetal pode compreender uma célula vegetal monocotiledônea ou dicotiledônea. Em determinadas modalidades, a célula vegetal é uma planta de safra, por exemplo, milho.
[0017] A Figura 1 representa os resultados de análise de sequência exemplificativos de produtos da amplificação de Zp15 a partir de gDNA de milho HiII derivado de células submetidas à expressão transitória do par de ZFP #25 (sítios de ligação sublinhados) e revela uma inserção NHEJ de 6 bp (negrito) no sítio de clivagem esperado.
[0018] A Figura 2 representa resultados de análise de sequência exemplificativos de produtos da amplificação de Zp15 de gDNA de milho HiII derivado de células submetidas à expressão transitória do par de ZFP #24 (sítios de ligação sublinhados) e revela uma deleção de 3 bp no sítio de clivagem esperado.
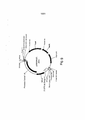
[0019] A Figura 3 é uma representação esquemática do construto designado pDAB7489.
[0020] A Figura 4 é um esquema representando um cassete de ex pressão de gene de tolerância a herbicida exemplificativo que codifica um gene AAD.
[0021] A Figura 5 é um esquema representando o construto desig nado pDAB7490.
[0022] A Figura 6 representa o alinhamento de um evento de inte gração objetivada (Targeted Integration - TI) em que o fragmento doador de Zp15 de milho do tipo silvestre (Wild Type - WT), bem como as regiões de borda 5' e 3' que unem as sequências doadoras integradas, são alinhados.
[0023] A Figura 7 é um esquema mostrando o construto designado pDAB104101.
[0024] A Figura 8 é um esquema representando o cassete de ex pressão de PAT.
[0025] A Figura 9 é um esquema representando o construto desig nado pDAB104107.
[0026] A Figura 10 é um esquema representando o construto desig nado pDAB104104.
[0027] A Figura 11 é um esquema representando o construto desig nado pDAB104105.
[0028] A Figura 12 é um esquema representando o construto desig nado pDAB104106.
[0029] A Figura 13 é um esquema representando o construto desig nado pDAB104100.
[0030] A Figura 14 é um esquema representando o construto desig nado pDAB104103.
[0031] A Figura 15 é um esquema representando o construto desig nado pDAB104102.
[0032] A presente invenção se refere a métodos e composições para integração objetivada (TI) em um gene Zp15 de planta, o qual reside sobre o cromossomo 6 em milho. Usando proteínas de fusão compreendendo domínios de ligação a DNA (por exemplo, ZFPs, meganucleases ou zíperes de leucina) e domínios de nuclease, uma sequência inserida (doadora) pode ser operativamente ligada a um promotor exógeno ou pode ser sem promotor. Se sem promotor, transcrição do quadro de leitura aberto integrado pode ocorrer a partir do promotor do gene Zp15 endógeno nos tecidos promotor-especificados. Uso de um doador sem promotor diminui a probabilidade de integração aleatória do doador e/ou ativação supérflua de um gene endógeno pelo promotor trazido sobre o doador.
[0033] Composições úteis para clivagem e recombinação objetivada em um gene Zp15 incluem proteínas de fusão compreendendo um domínio de clivagem (ou um meio-domínio de clivagem) e um domínio de ligação a DNA (por exemplo, uma ZFP), polinucleotídeos que codificam essas proteínas e combinações de polipeptídeos e polinucleotídeos que codificam polipeptídeos. Um domínio de ligação de dedo de zinco pode compreender um ou mais dedos de zinco (por exemplo, 2, 3, 4, 5, 6, 7, 8, 9 ou mais dedos de zinco) e pode ser manipulado para se ligar a qualquer sequência dentro de um gene Zp15. A presença de tal proteína (ou proteínas) de fusão em uma célula resultará em ligação da(s) proteína(s) de fusão a seu(s) sítio(s) de ligação e clivagem dentro do gene Zp15 en- dógeno. Geral
[0034] A prática dos métodos, bem como preparo e uso das compo sições divulgadas aqui empregam, a menos que de outro modo indicado, técnicas convencionais em biologia molecular, bioquímica, estrutura e análise de cromatina, química computacional, cultura de célula, DNA re- combinante e campos relacionados, conforme dentro da capacidade no campo. Essas técnicas são totalmente explicadas na literatura. Vide, por exemplo, Sambrook et al. MOLECULAR CLONING: A LABORATORY MANUAL, Segunda edição, Cold Spring Harbor Laboratory Press, 1989 e Terceira edição, 2001; Ausubel et al, CURRENT PROTOCOLS IN MOLECULAR BIOLOGY, John Wiley & Sons, New York, 1987 e atualizações periódicas; a série METHODS IN ENZYMOLOGY, Academic Press, San Diego; Wolffe, CHROMATIN STRUCTURE AND FUNCTION, Terceira edição, Academic Press, San Diego, 1998; METHODS IN ENZYMOLOGY, Vol. 304, "Chromatin" (P.M. Wassarman e A. P. Wolffe, eds.), Academic Press, San Diego, 1999; e METHODS IN MOLECULAR BIOLOGY, Vol. 119, "Chromatin Protocols" (P.B. Becker, ed.) Humana Press, Totowa, 1999. Definições
[0035] Os termos "ácido nucleico", "polinucleotídeo" e "oligonucleotí- deo" são usados permutavelmente e referem-se a um polímero de deoxir- ribonucleotídeo ou ribonucleotídeo, em conformação linear ou circular e na forma fita simples ou dupla. Para fins da presente invenção, esses termos não devem ser construídos como limitativos com relação ao comprimento de um polímero. Os termos podem abranger análogos conhecidos de nucleotídeos naturais, bem como nucleotídeos que são modificados nas porções de base, açúcar e/ou fosfato (por exemplo, partes principais de fosforotioato). Em geral, um análogo de um nucleotídeo em particular tem a mesma especificidade de pareamento de base; isto é, um análogo de A realizará pareamento de base com T.
[0036] Os termos "polipeptídeo", "peptídeo" e "proteína" são usados permutavelmente para referir-se a um polímero de resíduos de aminoácido. O termo também se aplica a polímeros de aminoácido nos quais um ou mais aminoácidos são análogos químicos ou derivados modificados de um aminoácido que ocorre naturalmente correspondente.
[0037] "Ligação" se refere a uma interação não covalente, sequência- específica entre macromoléculas (por exemplo, entre uma proteína e um ácido nucleico). Nem todos os componentes de uma interação de ligação precisam ser sequência-específicos (por exemplo, contatos com resíduos de fosfato em uma parte principal de DNA), contanto que a interação como um todo seja sequência-específica. Tais interações são, em geral, caracterizadas por uma constante de dissociação (Kd) de 10-6 M-1 ou menor. "Afinidade" se refere à intensidade de ligação: a afinidade de ligação aumentada estando correlacionada a uma menor Kd.
[0038] Uma "proteína de ligação" é uma proteína que é capaz de li gação não covalentemente à outra molécula. Uma proteína de ligação pode se ligar, por exemplo, a uma molécula de DNA (uma proteína de ligação a DNA), uma molécula de RNA (uma proteína de ligação a RNA) e/ou uma molécula de proteína (uma proteína de ligação à proteína). No caso de uma proteína de ligação à proteína, ela pode se ligar a si mesma (para formar homodímeros, homotrímeros, etc.) e/ou ela pode se ligar a uma ou mais moléculas de uma proteína ou proteínas diferentes. Uma proteína de ligação pode ter mais de um tipo de atividade de ligação. Por exemplo, proteínas do dedo de zinco têm atividade de ligação a DNA, ligação a RNA e ligação à proteína.
[0039] Uma "proteína de ligação a DNA de dedo de zinco" (ou domí nio de ligação) é uma proteína ou um domínio dentro de uma proteína maior que se liga ao DNA de uma maneira sequência-específica através de um ou mais dedos de zinco, os quais são regiões de sequência de aminoácido dentro do domínio de ligação cuja estrutura é estabilizada mediante coordenação de um íon de zinco. O termo proteína de ligação a DNA de dedo de zinco é, frequentemente, abreviado como proteína de dedo de zinco ou ZFP.
[0040] Domínios de ligação de dedo de zinco podem ser "manipula dos" para se ligar a uma sequência de nucleotídeo predeterminada. Exemplos não limitativos de métodos para manipulação de proteínas de dedo de zinco são design e seleção. Uma proteína de dedo de zinco projetada é uma proteína que não ocorre na natureza cujo de- sign/composição resulta principalmente de critérios racionais. Critérios racionais para design incluem aplicação de regras de substituição e algoritmos computadorizados para processamento de informação em um banco de dados que armazena informação de designs de ZFP e dados de ligação existentes. Vide, por exemplo, Patentes US 6.140.081; 6.453.242; e 6.534.261; vide também documentos WO 98/53058; WO 98/53059; WO 98/53060; WO 02/016536 e WO 03/016496.
[0041] Uma proteína de dedo de zinco "selecionada" é uma proteína não encontrada na natureza cuja produção resulta primariamente de um processo empírico, tal como exibição de fago (“phage display"), contenção para interação ou seleção de híbrido. Vide, por exemplo, documentos US 5.789.538; US 5.925.523; US 6.007.988; US 6.013.453; US 6.200.759; WO 95/19431; WO 96/06166; WO 98/53057; WO 98/54311; WO 00/27878; WO 01/60970 WO 01/88197 e WO 02/099084.
[0042] O termo "sequência" se refere a uma sequência de nucleotí deo de qualquer comprimento, a qual pode ser DNA ou RNA; pode ser linear, circular ou ramificada e pode ser fita simples ou fita dupla. O termo "sequência doadora" se refere a uma sequência de nucleotídeo que é inserida em um genoma. Uma sequência doadora pode ser de qualquer comprimento, por exemplo, entre 2 e 10.000 nucleotídeos de comprimento (ou qualquer valor inteiro entre os mesmos ou acima dos mesmos), de preferência entre cerca de 100 e 1.000 nucleotídeos de comprimento (ou qualquer inteiro entre os mesmos), mais preferivelmente entre cerca de 200 e 500 nucleotídeos de comprimento.
[0043] Uma "sequência homóloga, não idêntica" se refere a uma pri meira sequência a qual compartilha um grau de identidade de sequência com uma segunda sequência, mas cuja sequência não é idêntica àquela da segunda sequência. Por exemplo, um polinucleotídeo compreendendo a sequência do tipo silvestre de um gene mutante é homólogo e não idêntico à sequência do gene mutante. Em determinadas modalidades, o grau de homologia entre as duas sequências é suficiente para permitir recombinação homóloga entre as mesmas, utilizando mecanismos celulares normais. Duas sequências homólogas não idênticas podem ser de qualquer comprimento e seu grau de não homologia pode ser tão pequeno quanto um único nucleotídeo (por exemplo, para correção de uma mutação de ponto genética por meio de recombinação homóloga objetivada) ou tão grande quanto 10 ou mais quilobases (por exemplo, para inserção de um gene em um sítio ectópico predeterminado em um cromossomo). Dois polinucleotídeos compreendendo as sequências homólogas não idênticas não precisam ser do mesmo comprimento. Por exemplo, um polinucleotídeo exógeno (isto é, polinucleotídeo doador) de entre 20 e 10.000 nucleotídeos ou pares de nucleotídeo pode ser usado.
[0044] Técnicas para determinação de identidade de sequência de ácido nucleico e aminoácido são conhecidas no campo. Tipicamente, tais técnicas incluem determinação da sequência de nucleotídeo do mRNA para um gene e/ou determinação da sequência de aminoácido codificada pelo menos e comparação dessas sequências com uma segunda sequência de nucleotídeo ou aminoácido. Sequências genômicas podem também ser determinadas e comparadas desse modo. Em geral, identidade se refere a uma correspondência nucleotídeo-a-nucleotídeo ou ami- noácido-a-aminoácido exata de duas sequências de polinucleotídeo ou polipeptídeo, respectivamente. Duas ou mais sequências (polinucleotídeo ou aminoácido) podem ser comparadas determinando-se sua identidade percentual. A identidade percentual de duas sequências, quer sequências de ácido nucleico ou aminoácido, é o número de combinações exatas entre duas sequências alinhadas dividido pelo comprimento das sequências mais curtas e multiplicado por 100. Um alinhamento aproximado para sequências de ácido nucleico é proporcionado pelo algoritmo de homologia local de Smith e Waterman, Advances in Applied Mathematics 2: 482-489 (1981). Esse algoritmo pode ser aplicado a sequências de aminoácido usando a matriz de escore desenvolvida por Dayhoff, Atlas of Protein Sequences and Structure, M.O. Dayhoff ed., supl. 3: 353-358, National Biomedical Research Foundation, Washington, D.C., EUA e normalizada por Gribskov, Nucl. Acids Res. 14(6): 6745-6763 (1986). Uma implementação exemplificativa desse algoritmo para determinar a identidade percentual de uma sequência é fornecida pelo Genetics Computer Group (Madison, WI) no aplicativo "BestFit". Programas adequados para cálculo da identidade ou similaridade percentual entre sequências são, em geral, conhecidos na técnica, por exemplo. Outro programa de alinhamento é o BLAST, usado com os parâmetros de default. Por exemplo, o BLASTN e BLASTP podem ser usados utilizando os seguintes parâmetros de default: código genético = padrão; filtro = nenhum; fita = ambas; corte = 60; esperado = 10; Matriz = BLOSUM62; Descrições = 50 sequência; escolhido por = HIGH SCORE; Bancos de Dados = não redundante, traduções no GenBank + EMBL + DDBJ + PDB + GenBank CDS + Swiss Protein + Spupdate + PIR. Detalhes desses programas podem ser encontrados na internet. Com relação às sequências descritas aqui, a faixa de graus de-sejados de identidade de sequência é aproximadamente 80% a 100% e qualquer valor inteiro entre os mesmos. Tipicamente, as identidades per-centuais entre as sequências são pelo menos 70-75%, de preferência 8082%, mais preferivelmente 85-90%, ainda mais preferivelmente 92%, mais preferivelmente 95% e, ainda mais preferivelmente, 98% de identidade de sequência.
[0045] Alternativamente, o grau de similaridade de sequência entre polinucleotídeos pode ser determinado por meio de hibridização de poli-nucleotídeos sob condições que permitam a formação de duplas estáveis entre regiões homólogas, seguido por digestão com nuclease(s) específi- ca(s) para fita simples e determinação de tamanho dos fragmentos digeridos. Duas sequências de ácido nucleico ou duas de polipeptídeo são substancialmente homólogas uma à outra quando as sequências exibem pelo menos cerca de 70%-75%, de preferência 80%-82%, mais preferivelmente 85%-90%, ainda mais preferivelmente 92%, mais preferivelmente 95% e, ainda mais preferivelmente, 98% de identidade de sequência sobre um comprimento definido das moléculas, conforme determinado usando os métodos acima. Conforme usado aqui, substancialmente homólogo se refere também à sequências mostrando identidade completa a uma sequência de DNA ou polipeptídeo especificada. Sequências de DNA que são substancialmente homólogas podem ser identificadas em um experimento de hibridização de Southern, por exemplo, sob condições estringentes, conforme definido para esse sistema em particular. Definição de condições de hibridização apropriadas está dentro da capacidade no campo. Vide, por exemplo, Sambrook etal, supra; Nucleic Acid Hybridization: A Practical Approach, editores B.D. Hames e S.J. Higgins, (1985) Oxford; Washington, DC; IRL Press).
[0046] Hibridização seletiva de dois fragmentos de ácido nucleico po de ser determinada como segue. O grau de identidade de sequência entre duas moléculas de ácido nucleico afeta a eficiência e resistência de eventos de hibridização entre tais moléculas. Uma sequência de ácido nucleico parcialmente idêntica inibirá, pelo menos parcialmente, a hibridização de uma sequência completamente idêntica a uma molécula-alvo. Inibição de hibridização da sequência completamente idêntica pode ser avaliada usando ensaios de hibridização que são bem-conhecidos no campo (por exemplo, Southern (DNA) blot, Northern (RNA) blot, hibridização em solução ou semelhante; vide Sambrook, et al, Molecular Cloning: A Laboratory Manual, Segunda Edição, (1989) Cold Spring Harbor, N.Y.). Tais ensaios podem ser conduzidos usando graus variados de seletividade, por exemplo, usando condições variáveis de baixa à alta estringência. Se condições de baixa estringência são empregadas, a ausência de ligação não específica pode ser avaliada usando uma sonda secundária que carece mesmo de um grau parcial de identidade de sequência (por exemplo, uma sonda tendo menos de cerca de 30% de identidade de sequência com a molécula-alvo) de modo que, na ausência de eventos de ligação não específica, a sonda secundária não se hibridize ao alvo.
[0047] Quando de utilização de um sistema de detecção baseado em hibridização, uma sonda de ácido nucleico é escolhida que é complementar a uma sequência de ácido nucleico de referência e, então, através de seleção de condições apropriadas, a sonda e a sequência de referência hibridizam seletivamente ou se ligam uma à outra para formar uma molécula dupla. Uma molécula de ácido nucleico que é capaz de hibridização seletiva a uma sequência de referência sob condições de hibridização moderadamente estringentes se hibridiza, tipicamente, sob condições que permitem a detecção de uma sequência de ácido nucleico-alvo de pelo menos cerca de 10-14 nucleotídeos de comprimento tendo pelo menos aproximadamente 70% de identidade de sequência com a sequência da sonda de ácido nucleico selecionada. Condições de hibridização estringentes permitem, tipicamente, a detecção de sequências de ácido nu- cleico-alvo de pelo menos cerca de 10-14 nucleotídeos de comprimento tendo uma identidade de sequência de mais de cerca de 90-95% com a sequência da sonda de ácido nucleico selecionada. Condições de hibridização úteis para hibridização de sonda/sequência de referência, onde a sonda e a sequência de referência têm um grau específico de identidade de sequência, podem ser determinadas conforme é conhecido no campo (vide, por exemplo, Nucleic Acid Hvbridization: A Practical Approach, editores B.D. Hames e S.J. Higgins, (1985) Oxford; Washington, DC; IRL Press).
[0048] Condições para hibridização são bem-conhecidas por aqueles versados no campo. Estringência de hibridização se refere ao grau até o qual as condições de hibridização desfavorecem a formação de híbridos contendo nucleotídeos erroneamente correspondentes, com maior estringência correlacionada a uma menor tolerância para híbridos erroneamente correspondentes. Fatores que afetam a estringência de hibridização são bem-conhecidos por aqueles versados no campo e incluem, mas não estão limitados a, temperatura, pH, resistência iônica e concentração de solventes orgânicos tais como, por exemplo, formamida e sulfóxido de dimetila. Conforme é conhecido por aqueles versados no campo, a estringência de hibridização pode ser aumentada por maiores temperaturas, menor resistência iônica e menores concentrações de solvente.
[0049] Com relação às condições de estringência para hibridização, é bem-conhecido no campo que numerosas condições equivalentes podem ser empregadas para estabelecer uma estringência particular variando, por exemplo, os seguintes fatores: o comprimento e natureza das sequências, composição de base das várias sequências, concentrações de sais e outros componentes de hibridização, a presença ou ausência de agentes de bloqueio nas soluções de hibridização (por exemplo, sulfato de dextrana e polietileno glicol), temperatura da reação de hibridização e parâmetros de tempo, bem como variando as condições de lavagem. A seleção de um conjunto particular de condições de hibridização é selecionada seguindo métodos padrões no campo (vide, por exemplo, Sam- brook, et al., Molecular Cloning: A Laboratory Manual. Segunda Edição, (1989) Cold Spring Harbor, N.Y.).
[0050] "Recombinação" se refere a um processo de troca de informa- ção genética entre dois polinucleotídeos. Para fins da presente invenção, "recombinação homóloga (Homologous Recombination - HR)" se refere à forma especializada de tal troca que ocorre, por exemplo, durante reparo de rupturas de fita dupla em células. Esse processo requer homologia de sequência de nucleotídeo, usa uma molécula "doadora" como molde para reparo de uma molécula-"alvo" (isto é, uma que experimentou a ruptura de fita dupla) e é variadamente conhecido como "conversão gênica sem cruzamento" ou "conversão gênica de trato curto" porque ele leva à transferência de informação genética do doador para o alvo. Sem desejar estar preso por qualquer teoria em particular, tal transferência pode envolver correção de correspondência errônea de DNA heteroduplex que se forma entre o alvo rompido e o doador e/ou "anelamento de fita síntese- dependente", no qual o doador é usado para ressintetizar informação ge-nética que se tornará parte do alvo e/ou processos relacionados. Tal HR especializada frequentemente resulta em uma alteração da sequência da molécula-alvo, de modo que parte ou toda a sequência do polinucleotídeo doador é incorporada no polinucleotídeo-alvo.
[0051] "Clivagem" se refere à ruptura da parte principal covalente de uma molécula de DNA. Clivagem pode ser iniciada através de uma variedade de métodos incluindo, mas não limitado a, hidrólise enzimática ou química de uma ligação de fosfodiéster. Clivagem de fita simples e clivagem de fita dupla são possíveis e clivagem de fita dupla pode ocorrer como um resultado de dois eventos de clivagem de fita simples distintos. Clivagem de DNA pode resultar na produção de extremidades cegas ou extremidades alternadas. Em determinadas modalidades, polipeptídeos de fusão são usados para clivagem de DNA fita dupla-alvo.
[0052] Um "domínio de clivagem" compreende uma ou mais sequên cias polipeptídicas as quais possuem atividade catalitica para clivagem de DNA. Um domínio de clivagem pode estar contido em uma única cadeia polipeptídica ou atividade de clivagem pode resultar da associação de dois (ou mais) polipeptídeos.
[0053] Um "meio-domínio de clivagem" é uma sequência polipeptídica a qual, em conjunto com um segundo polipeptídeo (quer idêntico ou diferente) forma um complexo tendo atividade de clivagem (de preferência atividade de clivagem de fita dupla).
[0054] "Cromatina" é a estrutura de nucleoproteína compreendendo o genoma celular. Cromatina celular compreende ácido nucleico, primariamente DNA e proteína, incluindo proteínas cromossômicas de histona e não-histona. A maioria da cromatina celular eucariota existe na forma de nucleossomas, em que um núcleo de nucleossoma compreende aproximadamente 150 pares de base de DNA associado a um octâmero compreendendo duas de cada uma das histonas H2A, H2B, H3 e H4; e DNA ligante (de comprimento variável, dependendo do organismo) se estende entre os núcleos de nucleossoma. Uma molécula de histona H1 está, em geral, associada ao DNA ligante. Para fins da presente invenção, o termo "cromatina" se destina a abranger todos os tipos de nucleoproteína celular, procariota e eucariota. A cromatina celular inclui cromatina cromossômica e epissomal.
[0055] Um "cromossomo" é um complexo de cromatina compreen dendo todo ou uma parte do genoma de uma célula. O genoma de uma célula é, frequentemente, caracterizado por seu cariótipo, o qual é a coleção de todos os cromossomos que compreendem o genoma da célula. O genoma de uma célula pode compreender um ou mais cromossomos.
[0056] Um "epissoma" é um ácido nucleico de replicação, complexo de nucleoproteína ou outra estrutura compreendendo um ácido nucleico que não é parte do cariótipo cromossômico de uma célula. Exemplos de epissomas incluem plasmídeos e determinados genomas virais.
[0057] Uma "região acessível" é um local na cromatina celular no qual um sítio-alvo presente no ácido nucleico pode ser ligado por uma molécula exógena a qual reconhece o sítio-alvo. Sem desejar estar preso por qualquer teoria em particular, acredita-se que uma região acessível é uma que não está engolfada em uma estrutura nucleossômica. A estrutura distinta de uma região acessível pode, frequentemente, ser detectada por sua sensibilidade a sondas químicas e enzimáticas, por exemplo, nucleases.
[0058] Um "sítio-alvo" ou "sequência-alvo" é uma sequência de ácido nucleico que define uma porção de um ácido nucleico à qual uma molécula de ligação se ligará, contanto que existam condições suficientes para ligação. Por exemplo, a sequência 5'-GAATTC-3' é o sítio-alvo para a endonuclease de restrição EcoRI.
[0059] Uma molécula "exógena" é uma molécula que normalmente não está presente em uma célula, mas pode ser introduzida em uma célula através de um ou mais métodos genéticos, bioquímicos ou outros. A "presença normal na célula" é determinada com relação ao estágio de desenvolvimento e condições ambientais particulares da célula. Assim, por exemplo, uma molécula que está presente apenas durante desenvolvimento embriônico do músculo é uma molécula exógena com relação a uma célula muscular em adultos. Similarmente, uma molécula induzida por choque térmico é uma molécula exógena com relação a uma célula não induzida por choque térmico. Uma molécula exógena pode compreender, por exemplo, uma sequência de codificação para qualquer polipeptídeo ou fragmento do mesmo, uma versão funcional de uma molécula endógena não funcional ou uma versão não funcional de uma molécula endógena normalmente funcional. Adicionalmente, uma molécula exógena pode compreender uma sequência de codificação de outra espécie que é um ortólogo de um gene endógeno na célula hospedeira.
[0060] Uma molécula exógena pode ser, dentre outras coisas, uma pequena molécula, tal como gerada em um processo químico combinatorial ou uma macromolécula, tal como uma proteína, ácido nucleico, carboidrato, lipídio, glicoproteína, lipoproteína, polissacarídeo, qualquer deri- vado modificado das moléculas acima ou qualquer complexo compreendendo uma ou mais das moléculas acima. Ácidos nucleicos incluem DNA e RNA, podem ser fita simples ou dupla; podem ser lineares, ramificados ou circulares; e podem ser de qualquer comprimento. Ácidos nucleicos incluem aqueles capazes de formação de duplas, bem como ácidos nucleicos que formam tripletos. Vide, por exemplo, Patentes U.S. Nos. 5.176.996 e 5.422.251. Proteínas incluem, mas não estão limitadas a, proteínas de ligação a DNA, fatores de transcrição, fatores de remodela- mento de cromatina, proteínas de ligação a DNA metilado, polimerases, metilases, demetilases, acetilases, deacetilases, quinases, fosfatases, integrases, recombinases, ligases, topoisomerases, girases e helicases.
[0061] Uma molécula exógena pode ser do mesmo tipo de molécula que uma molécula endógena, por exemplo, uma proteína ou ácido nucleico exógeno. Por exemplo, um ácido nucleico exógeno pode compreender um genoma viral infeccioso, um plasmídeo ou epissoma introduzido em uma célula ou um cromossomo que normalmente não está presente na célula. Métodos para a introdução de moléculas exógenas em células são conhecidos por aqueles versados no campo e incluem, mas não estão limitados a, transferência lipídio-mediada (isto é, lipossomas, incluindo lipídios neutros e catiônicos), eletroporação, injeção direta, fusão celular, bombardeamento de partícula, coprecipitação com fosfato de cálcio, transformação de nanopartícula, transferência mediada por DEAE- dextrana e transferência mediada por vetor viral.
[0062] Ao contrário, uma molécula "endógena" é uma que normal mente está presente em uma célula em particular em um estágio de de-senvolvimento em particular sob condições ambientais particulares. Por exemplo, um ácido nucleico endógeno pode compreender um cromossomo, o genoma de uma mitocôndria, cloroplasto ou outra organela ou um ácido nucleico epissomal que ocorre naturalmente. Moléculas endógenas adicionais podem incluir proteínas, por exemplo, fatores de transcrição e enzimas.
[0063] Conforme usado aqui, o termo "produto de um ácido nucleico exógeno" inclui produtos de polinucleotídeo e polipeptídeo, por exemplo, produtos de transcrição (polinucleotídeos, tal como RNA) e produtos de tradução (polipeptídeos).
[0064] Uma molécula de "fusão" é uma molécula na qual duas ou mais moléculas subunitárias são ligadas, por exemplo, covalentemente. As moléculas subunitárias podem ser o mesmo tipo de molécula ou podem ser tipos químicos diferentes de moléculas. Exemplos do primeiro tipo de molécula de fusão incluem, mas não estão limitados a, proteínas de fusão (por exemplo, uma fusão entre um domínio de ligação a DNA de ZFP e um domínio de clivagem) e ácidos nucleicos de fusão (por exemplo, um ácido nucleico que codifica a proteína de fusão descrita supra). Exemplos do segundo tipo de molécula de fusão incluem, mas não estão limitados a, uma fusão entre um ácido nucleico de formação de tripleto e um polipeptídeo e uma fusão entre um ligante da ranhura menor e um ácido nucleico.
[0065] Expressão de uma proteína de fusão em uma célula pode re sultar de distribuição da proteína de fusão à célula ou distribuição de um polinucleotídeo que codifica a proteína de fusão a uma célula, em que o polinucleotídeo é transcrito e o transcrito é traduzido, para gerar a proteína de fusão. Trans-junção, clivagem de polipeptídeo e ligação de polipeptídeo também podem estar envolvidos em expressão de uma proteína em uma célula. Métodos para distribuição de polinucleotídeo e polipeptídeo a células são apresentados em alguma parte na presente invenção.
[0066] Um "gene", para fins da presente invenção, inclui uma região de DNA que codifica um produto gênico (vide infra), bem como todas as regiões de DNA as quais regulam a produção do produto gênico, quer tais sequências regulatórias estejam ou não adjacentes a sequências de codificação e/ou transcritas. Consequentemente, um gene inclui, mas não está necessariamente limitado a, sequências promotoras, terminadores, sequências regulatórias de tradução, tais como sítios de ligação ribossô- mica e sítios de entrada ribossômica internos, intensificadores, silenciadores, isoladores, elementos limítrofes, origens de replicação, sítios de fixação de matriz e regiões de controle de locus.
[0067] "Expressão gênica" se refere à conversão da informação, con tida em um gene, em um produto gênico. Um produto gênico pode ser o produto direto de um gene (por exemplo, mRNA, tRNA, rRNA, RNA antissenso, RNA de interferência, ribozima, RNA estrutural ou qualquer outro tipo de RNA) ou uma proteína produzida através de tradução de um mRNA. Produtos gênicos também incluem RNAs os quais são modificados através de processos tais como "capeamento", poliadenilação, meti- lação e edição e proteínas modificadas, por exemplo, através de metila- ção, acetilação, fosforilação, ubiquitinação, ADP-ribosilação, miristilação e glicosilação.
[0068] "Modulação" de expressão gênica se refere a uma alteração na atividade de um gene. Modulação de expressão pode incluir, mas não está limitada a, ativação gênica e repressão gênica.
[0069] Células de "planta" incluem, mas não estão limitadas a, célu las de plantas monocotiledôneas (monocots) ou dicotiledôneas (dicots). Exemplos não limitativos de monocots incluem plantas de cereal, tais como milho, arroz, cevada, aveia, trigo, sorgo, centeio, cana-de-açúcar, abacaxi, cebola, banana e coco. Exemplos não limitativo de dicots incluem tabaco, tomate, girassol, algodão, beterraba sacarínica, batata, alface, melão, soja, canola (colza) e alfafa. Células de planta podem ser de qualquer parte da planta e/ou de qualquer estágio de desenvolvimento de uma planta.
[0070] Uma "região de interesse" é qualquer região de cromatina ce lular tal como, por exemplo, um gene ou uma sequência de não codifica- ção dentro ou adjacente a um gene, na qual é desejável ligar uma molécula exógena. Ligação pode ser para fins de clivagem de DNA objetivada e/ou recombinação objetivada. Uma região de interesse pode estar presente em um cromossomo, um epissoma, um genoma organelar (por exemplo, mitocondrial, cloroplasto) ou um genoma viral infeccioso, por exemplo. Uma região de interesse pode estar dentro da região de codificação de um gene, dentro de regiões de não codificação transcritas tais como, por exemplo, sequências líderes, sequências "trailer" ou íntrons ou dentro de regiões não transcritas, quer a montante ou a jusante da região de codificação. Uma região de interesse pode ser tão pequena quanto um único par de nucleotídeo ou até 2.000 pares de nucleotídeo de compri-mento ou qualquer valor integral de pares de nucleotídeo.
[0071] Os termos "ligação operativa" e "operativamente ligado" (ou "operativamente ligado" são usados permutavelmente com referência a uma justaposição de dois ou mais componentes (tais como elementos de sequência) na qual os componentes estão dispostos de modo que ambos os componentes funcionam normalmente e permitem a possibilidade de que pelo menos um dos componentes possa mediar uma função que é exercida sobre pelo menos um dos outros componentes. À guisa de ilustração, uma sequência regulatória de transcrição, tal como um promotor, é operativamente ligada a uma sequência de codificação se a sequência regulatória de transcrição controla o nível de transcrição da sequência de codificação em resposta à presença ou ausência de um ou mais fatores regulatórios de transcrição. Uma sequência regulatória de transcrição é, em geral, operativamente ligada em cis com uma sequência de codificação, mas não precisa ser diretamente adjacente à mesma. Por exemplo, um intensificador é uma sequência regulatória de transcrição que é operativamente ligada a uma sequência de codificação, mesmo embora eles não sejam contíguos.
[0072] Com relação a polipeptídeos de fusão, o termo "operativamen te ligado" pode referir-se ao fato de que cada um dos componentes desempenha a mesma função em ligação ao outro componente conforme seria se não estivessem ligados. Por exemplo, com relação a um polipeptídeo de fusão no qual um domínio de ligação a DNA de ZFP é fundido a um domínio de clivagem, o domínio de ligação a DNA de ZFP e o domínio de clivagem estão em ligação operativa se, no polipeptídeo de fusão, a porção de domínio de ligação a DNA de ZFP é capaz de se ligar a seu sítio-alvo e/ou seu sítio de ligação, enquanto que o domínio de clivagem é capaz de clivar o DNA na proximidade do sítio-alvo.
[0073] Um "fragmento funcional" de uma proteína, polipeptídeo ou ácido nucleico é uma proteína, polipeptídeo ou ácido nucleico cuja sequência não é idêntica à proteína, polipeptídeo ou ácido nucleico de comprimento total, ainda que retenha a mesma função que a proteína, polipeptídeo ou ácido nucleico de comprimento total. Um fragmento funcional pode possuir mais, menos ou o mesmo número de resíduos que a molécula nativa correspondente e/ou pode conter uma ou mais substituições de aminoácido ou nucleotídeo. Métodos para determinação da função de um ácido nucleico (por exemplo, função de codificação, capacidade de hibridização a outro ácido nucleico) são bem-conhecidos no campo. Similarmente, métodos para determinação de função de proteína são bem-conhecidos. Por exemplo, a função de ligação a DNA de um polipeptídeo pode ser determinada, por exemplo, através de ensaios de ligação a filtro, desvio de mobilidade eletroforética ou imunoprecipitação. Clivagem de DNA pode ser avaliada por meio de eletroforese em gel. Vide Ausubel et al., supra. A capacidade de uma proteína de interagir com outra proteína pode ser determinada, por exemplo, através de coimuno- precipitação, ensaios com dois híbridos ou complementação, genética e bioquímica. Vide, por exemplo, Fields et al. (1989) Nature 340: 245-246; Patente U.S. No. 5.585.245 e documento PCT WO 98/44350. Sítios-Alvo
[0074] Os métodos e composições divulgados incluem proteínas de fusão compreendendo um domínio de clivagem (ou um meio-domínio de clivagem) e um domínio de ligação a DNA (por exemplo, ZFP, meganuclease ou zíper de leucina), nas quais o domínio de ligação a DNA (por exemplo, domínio de dedo de zinco, meganuclease ou zíper de leucina), através de ligação a uma sequência em um locus de Zp15 em uma planta, direciona a atividade do domínio de clivagem (ou meio-domínio de clivagem) para a proximidade da sequência e, consequentemente, induz à clivagem (por exemplo, uma ruptura em fita dupla) em Zp15. Conforme apresentado em alguma parte na presente invenção, um domínio de dedo de zinco pode ser manipulado para se ligar a virtualmente qualquer sequência desejada. Consequentemente, um ou mais domínios de ligação a DNA (por exemplo, ZFPs) podem ser manipulados para se ligar a uma ou mais sequências em um gene Zp15 de planta. Expressão de uma proteína de fusão compreendendo um domínio de ligação a DNA (por exemplo, ZFP) e um domínio de clivagem (ou de duas proteínas de fusão, cada uma compreendendo um domínio de ligação a DNA e um meio-domínio de clivagem), em uma célula, realiza clivagem no gene Zp15.
[0075] Seleção de uma sequência em um Zp15 para ligação através de um domínio de dedo de zinco (por exemplo, um sítio-alvo) pode ser realizada, por exemplo, de acordo com os métodos divulgados na Patente US cocedida No. 6.453.242 (17 de setembro de 2002), a qual também divulga métodos para design de ZFPs que se ligam a uma sequência selecionada. Será evidente para aqueles versados no campo que simples inspeção visual de uma sequência de nucleotídeo também pode ser usada para seleção de um sítio-alvo. Consequentemente, qualquer meio para seleção de sítio-alvo pode ser usado nos métodos descritos aqui.
[0076] Para domínios de ligação a DNA de ZFP, sítios-alvo são, em geral, compostos de uma pluralidade de subsítios-alvo adjacentes. Um subsítio-alvo se refere à sequência (usualmente um tripleto de nucleotí- deo ou uma quadrupleto de nucleotídeo que pode se sobrepor por um nucleotídeo com uma quadrupleto adjacente) ligada por um dedo de zinco individual. Vide, por exemplo, documento WO 02/077227. Se a fita com a qual uma proteína de dedo de zinco faz a maioria dos contatos é designada como a "fita de reconhecimento primário" de fita-alvo ou "fita de contato primário", algumas proteínas do dedo de zinco se ligam a um tripleto de três bases na fita-alvo e uma quarta base sobre a fita não-alvo. Um sítio-alvo geralmente tem um comprimento de pelo menos 9 nucleotídeos e, consequentemente, é ligado através de um domínio de ligação de dedo de zinco compreendendo pelo menos três dedos de zinco. Contudo, ligação, por exemplo, de um domínio de ligação com 4 dedos a um sítio- alvo de 12 nucleotídeos, um domínio de ligação de 5 dedos a um sítio- alvo de 15 nucleotídeos ou um domínio de ligação de 6 dedos a um sítio- alvo de 18 nucleotídeos também é possível. Conforme será evidente, a ligação de domínios de ligação maiores (por exemplo, 7, 8, 9 ou mais dedos) a sítios-alvo maiores também é possível.
[0077] Não é necessário que um sítio-alvo seja um múltiplo de três nucleotídeos. Por exemplo, em casos nos quais interações fita-cruzada ocorrem (vide, por exemplo, Patente U.S. No. 6.453.242 e documento WO 02/077227), um ou mais dos dedos de zinco individuais de um domínio de ligação a múltiplos dedos podem se ligar a subsítios de um quadrupleto em sobreposição. Como um resultado, uma proteína com três dedos pode se ligar a uma sequência de 10 nucleotídeos, em que o décimo nucleotídeo é parte de um quadrupleto ligado por um dedo terminal, uma proteína com quatro dedos pode se ligar a uma sequência de 13 nucleotídeos, em que o décimo terceiro nucleotídeo é parte de um quadrupleto ligado por um dedo terminal, etc.
[0078] O comprimento e natureza de sequências ligantes de aminoá cido entre dedos de zinco individuais em um domínio de ligação a múltiplos dedos também afetam a ligação a uma sequência-alvo. Por exemplo, a presença de um assim denominado "ligante não canônico", "ligante longo" ou "ligante estruturado" entre dedos de zinco adjacentes em um domínio de ligação a múltiplos dedos pode permitir que esses dedos se liguem a subsítios os quais não são imediatamente adjacentes. Exemplos não limitativos de tais ligantes são descritos, por exemplo, na Patente U.S. No. 6.479.626 e documento WO 01/53480. Consequentemente, um ou mais subsítios, em um sítio-alvo para um domínio de ligação a dedo de zinco, podem ser separados uns dos outros por 1, 2, 3, 4, 5 ou mais nucleotídeos. Para proporcionar mais um exemplo, um domínio de ligação de quatro dedos pode se ligar a um sítio-alvo de 13 nucleotídeos compreendendo, em sequência, dois subsítios de 3 nucleotídeos contíguos, um nucleotídeo interveniente e dois subsítios de tripleto contíguos.
[0079] A distância entre sequências (por exemplo, sítios-alvo) se re fere ao número de nucleotídeos ou pares de nucleotídeo intervenientes entre duas sequências, conforme medido a partir das bordas das sequências mais próximas umas das outras.
[0080] Em determinadas modalidades nas quais a clivagem depende da ligação de duas moléculas de fusão de domínio de dedo de zin- co/meio-domínio de clivagem a sítios-alvo distintos, os dois sítios-alvo podem estar sobre fitas de DNA opostas. Em outras modalidades, ambos os sítios-alvo estão sobre a mesma fita de DNA. Domínios de Ligação a DNA
[0081] Qualquer domínio de ligação a DNA pode ser usado nos mé todos divulgados aqui. Em determinadas modalidades, o domínio de ligação a DNA compreende uma proteína do dedo de zinco. Um domínio de ligação de dedo de zinco compreende um ou mais dedos de zinco. Miller et al. (1985) EMBOJ. 4: 1609-1614; Rhodes (1993) Scientific American Fev.: 56-65; Patente U.S. No. 6.453.242. Os domínios de ligação de dedo de zinco descritos geralmente incluem 2, 3, 4, 5, 6 ou mesmo mais dedos de zinco.
[0082] Tipicamente, um único domínio de dedo de zinco tem cerca de 30 aminoácidos de comprimento. Estudos estruturais demonstraram que cada domínio de dedo de zinco (motivo) contém duas beta folhas (mantida em um beta giro o qual contém os dois resíduos de cisteína invariáveis) e uma alfa hélice (contendo os dois resíduos de histidina invariáveis), os quais são mantidos em uma conformação particular através de coordenação de um átomo de zinco pelas duas cisteínas e as duas histi- dinas.
[0083] Dedos de zinco incluem dedos de zinco C2H2 canônicos (isto é, aqueles nos quais o íon de zinco é coordenado por dois resíduos de cisteína e dois de histidina) e dedos de zinco não canônicos tais como, por exemplo, dedos de zinco C3H (aqueles nos quais o íon de zinco é coordenado por três resíduos de cisteína e um resíduo de histidina) e dedos de zinco C4 (aqueles nos quais o íon de zinco é coordenado por quatro resíduos de cisteína). Vide também documento WO 02/057293 e também Publicação de Patente U.S. No. 20080182332 com relação a ZFPs não canônicas para uso em plantas.
[0084] Um domínio de ligação de dedo de zinco manipulado pode ter uma nova especificidade de ligação, comparado com uma proteína de dedo de zinco que ocorre naturalmente. Métodos de manipulação incluem, mas não estão limitados a, design racional e vários tipos de seleção. Design racional inclui, por exemplo, uso de bancos de dados compreendendo sequências de nucleotídeo tripletos (ou quadrupletos) e sequências de aminoácido de dedo de zinco individuais, nas quais cada sequência de nucleotídeo tripleto ou quadrupleto está associada a uma ou mais sequências de aminoácido de dedos de zinco as quais se ligam à sequência tripleto ou quadrupleto em particular.
[0085] Métodos de seleção exemplificativos, incluindo exibição de fago (“phage display") e sistemas com dois híbridos, são divulgados nas Patentes U.S. Nos. 5.789.538; 5.925.523; 6.007.988; 6.013.453; 6.410.248; 6.140.466; 6.200.759; e 6.242.568; bem como documentos WO 98/37186; WO 98/53057; WO 00/27878; WO 01/88197 e GB 2.338.237.
[0086] Intensificação de especificidade de ligação para domínios de dedo de zinco foi descrita, por exemplo, no documento concedido WO 02/077227.
[0087] Uma vez que um dedo de zinco individual se liga a uma se quência de três nucleotídeos (isto é, tripleto) (ou uma sequência de quatro nucleotídeos a qual pode se sobrepor, por um nucleotídeo, com o sítio de ligação de quatro nucleotídeos de um dedo de zinco adjacente), o comprimento de uma sequência à qual um domínio de ligação de dedo de zinco se liga (por exemplo, uma sequência-alvo) determinará o número de dedos de zinco em um domínio de ligação de dedo de zinco manipulado. Por exemplo, para ZFPs nas quais os motivos de dedo não se ligam a subsítios em sobreposição, uma sequência-alvo de seis nucleotídeos é ligada por domínios de ligação com dois dedos; uma sequência-alvo de nove nucleotídeos é ligada por um domínio de ligação com três dedos; uma sequência-alvo de seis nucleotídeos é ligada por um domínio de ligação com dois dedos; uma sequência-alvo de nove nucleotídeos é ligada por um domínio de ligação com três dedos, etc. Conforme mencionado aqui, sítios de ligação para dedos de zinco individuais (isto é, subsítios) em um sítio-alvo não precisam ser contíguos, mas podem ser separados por um ou vários nucleotídeos, dependendo do comprimento e natureza de sequência de aminoácido entre os dedos de zinco (isto é, os ligantes interdedo) em um domínio de ligação de múltiplos dedos.
[0088] Em um domínio de ligação de dedo de zinco a múltiplos de dos, dedos de zinco adjacentes podem ser separados por sequências ligantes de aminoácido de aproximadamente 5 aminoácidos (os assim denominados ligantes interdedo "canônicos") ou, alternativamente, por um ou mais ligantes não canônicos. Vide, por exemplo, Patentes U.S. concedidas Nos. 6.453.242 e 6.534.261. Para domínios de dedo de zinco manipulados compreendendo mais de três dedos, inserção de ligantes interdedo mais longos (não canônicos) entre alguns dos dedos de zinco pode ser desejável em alguns casos, uma vez que isso pode aumentar a afinidade e/ou especificidade de ligação pelo domínio de ligação. Vide, por exemplo, Patente U.S. No. 6.479.626 e documento WO 01/53480. Consequentemente, domínios de ligação de dedo de zinco com múltiplos dedos podem também ser caracterizados com relação à presença e localização de ligantes interdedo não canônicos. Por exemplo, a um domínio de ligação de dedo de zinco com seis dedos compreendendo três dedos (unidos por dois ligantes interdedo canônicos), um ligante longo e três dedos adicionais (unidos por dois ligantes interdedo canônicos) são denotados uma configuração 2x3. Similarmente, a um domínio de ligação compreendendo dois dedos (com um ligante canônico entre os mesmos), um ligante longo e dois dedos adicionais (unidos por um ligante canônico) são denotados uma configuração 2x2. Uma proteína compreendendo três unidades com dois dedos (em cada uma das quais os dois dedos são unidos por um ligante canônico) e na qual cada unidade com dois dedos é unida à unidade com dois dedos adjacentes por um ligante longo é referida como uma configuração 3x2.
[0089] A presença de um ligante interdedo longo ou não canônico entre dois dedos de zinco adjacentes em um domínio de ligação a múltiplos dedos frequentemente permite que os dois dedos se liguem a subsítios os quais não são imediatamente contíguos na sequência-alvo. Con-sequentemente, podem haver vãos de um ou mais nucleotídeos entre subsítios em um sítio-alvo; isto é, um sítio-alvo pode conter um ou mais nucleotídeos que não são contatados por um dedo de zinco. Por exemplo, um domínio de ligação de dedo de zinco 2x2 pode se ligar a duas sequências com seis nucleotídeos separadas por um nucleotídeo, isto é, ele se liga a um sítio-alvo de 13 nucleotídeos. Vide também Moore et al. (2001a) Proc. Natl. Acad. Sci. USA 98: 1432-1436; Moore et al. (2001b) Proc. Natl. Acad. Sci. USA 98: 1437-1441 e documento WO 01/53480.
[0090] Conforme mencionado anteriormente, um subsítio-alvo é uma sequência de três ou quatro nucleotídeos que é ligada por um único dedo de zinco. Para determinadas finalidades, uma unidade com dois dedos é denotada um "módulo de ligação". Um módulo de ligação pode ser obtido, por exemplo, selecionando dois dedos adjacentes no contexto de uma proteína de múltiplos dedos (geralmente três dedos) a qual se liga a uma sequência-alvo de seis nucleotídeos em particular. Alternativamente, módulos podem ser construídos por meio de montagem de dedos de zinco individuais. Vide também documentos WO 98/53057 e WO 01/53480.
[0091] Alternativamente, o domínio de ligação a DNA pode ser deri vado de uma nuclease. Por exemplo, as sequências de reconhecimento das endonucleases e meganucleases "homing", tais como I-Sce l, l-Ceu l, Vl-Psp l, Pl-Sce, I-Sce IV, l-Csm l, l-Pan l, I-Sce ll, I -Ppo I, l-Sce lll, l-Cre l, l- Tev l, l-Tevll e I-Tev III são conhecidas. Vide também Patente U.S. No. 5.420.032; Patente U.S. No. 6.833.252; Belfort et al. (1997) Nucleic Acids Res. 25: 3379-3388; Dujon et al. (1989) Gene 82: 115-118; Verier et al. (1994) Nucleic Acids Res. 22, 1125-1127; Jasin (1996) Trends Genet. 12: 224-228; Gimble et al. (1996) J. Mol. Biol. 263: 163-180; Argast et al. (1998) J. Mol. Biol. 280: 345-353 e o catálogo da New England Biolabs. Além disso, a especificidade de ligação a DNA de endonucleases e meganucleases "homing" pode ser manipulada para se ligar a sítios-alvo não naturais. Vide, por exemplo, Chevalier et al. (2002) Molec. Cell 10: 895905; Epinat et al. (2003) Nucleic Acids Res. 31: 2952-2962; Ashworth et al. (2006) Nature 441: 656-659; Paques et al. (2007) Current Gene Therapy 7: 49-66; Publicação de Patente U.S. No. 20070117128.
[0092] Como outra alternativa, o domínio de ligação a DNA pode ser derivado de uma proteína de zíper de leucina. Zíperes de leucina são uma classe de proteínas que estão envolvidas em interações proteína- proteína em muitas proteínas regulatórias eucariotas que são fatores transcricionais importantes associados à expressão gênica. O zíper de leucina se refere a um motivo estrutural em comum compartilhado nesses fatores de transcrição através de vários reinos, incluindo animais, plantas, leveduras, etc. O zíper de leucina é formado por dois polipeptídeos (ho- modímero ou heterodímero) que se ligam a sequências de DNA específicas de uma maneira onde os resíduos de leucina são uniformemente espaçados através de uma a-hélice, de modo que os resíduos de leucina dos dois polipeptídeos terminam sobre a mesma face da hélice. A especificidade de ligação a DNA de zíperes de leucina pode ser utilizada nos domínios de ligação a DNA divulgados aqui.
[0093] Em algumas modalidades, o domínio de ligação a DNA é um domínio manipulado a partir de um efetuador TAL derivado do patógeno de planta Xanthomonas (vide Boch et al, (2009) Science, 29 de outubro de 2009 (10.1126/science.117881) e Moscou e Bogdanove, (2009) Science , 29 de outubro de 2009 (10.1126/science.1178817). Domínios de Clivagem
[0094] Conforme mencionado acima, o domínio de ligação a DNA pode estar associado a um domínio de clivagem (nuclease). Por exemplo, endonucleases "homing" podem ser modificadas quanto à sua especificidade de ligação a DNA, ao mesmo tempo em que retêm a função de nuclease. Além disso, proteínas do dedo de zinco também podem ser fundidas a um domínio de clivagem para formar uma nuclease de dedo de zinco (ZFN). A porção de domínio de clivagem das proteínas de fusão divulgadas aqui pode ser obtida a partir de qualquer endonuclease ou exonuclease. Endonucleases exemplificativas das quais um domínio de clivagem pode ser derivado incluem, mas não estão limitadas a, endonucleases de restrição e endonucleases "homing". Vide, por exemplo, Catálogo de 2002-2003, New England Biolabs, Beverly, MA; e Belfort et al. (1997) Nucleic Acids Res. 25: 3379-3388. Enzimas adicionais as quais clivam DNA são conhecidas (por exemplo, Nuclease SI; nuclease de feijão-da- China; DNase I pancreática; nuclease microcócica; endonuclease HO de levedura; vide também Linn et al. (eds.) Nucleases, Cold Spring Harbor Laboratory Press, 1993). Exemplos não limitativos de endonucleases e meganucleases "homing" incluem I-Sce l, l-Ceu l, Vl-Psp l, Pl-Sce, I-Sce IV, l-Csm l, l-Pan l, I-Sce ll, I -Ppo I, l-Sce lll, l-Cre l, l-TeV, l-Tev ll e I-Tev III são conhecidos. Vide também Patente U.S. No. 5.420.032; Patente U.S. No. 6.833.252; Belfort et al. (1997) Nucleic Acids Res. 25: 3379-3388; Dujon et al. (1989) Gene 82: 115-118; Perler et al. (1994) Nucleic Acids Res. 22, 1125-1127; Jasin (1996) Trends Genet. 12: 224-228; Gimble et al. (1996) J. Mol. Biol. 263: 163-180; Argast et al. (1998) J. Mol. Biol. 280: 345-353 e o catálogo da New England Biolabs. Uma ou mais dessas enzimas (ou fragmentos funcionais das mesmas) podem ser usadas como uma fonte de domínios de clivagem e meio-domínios de clivagem.
[0095] Endonucleases de restrição (enzimas de restrição) estão pre sentes em muitas espécies e são capazes de ligação sequência- específica ao DNA (em um sítio de reconhecimento) e clivagem de DNA em ou próximo do sítio de ligação. Determinadas enzimas de restrição (por exemplo, Tipo ISS) clivam o DNA em sítios removidos do sítio de reconhecimento e têm domínios de ligação e clivagem separáveis. Por exemplo, a enzima FokI do tipo IIS catalisa a clivagem de DNA fita dupla em 9 nucleotídeos a partir de seu sítio de reconhecimento sobre uma fita e 13 nucleotídeos a partir de seu sítio de reconhecimento sobre a outra. Vide, por exemplo, Patentes US 5.356.802; 5.436.150 e 5.487.994; bem como Li et al. (1992) Proc. Natl. Acad. Sci. USA 89: 4275-4279; Li et al. (1993) Proc. Natl. Acad. Sci. USA 90: 2764-2768; Kim et al. (1994a) Proc. Natl. Acad. Sci. USA 91: 883-887; Kim et al. (1994b) J. Biol. Chem. 269: 31, 978-31, 982. Assim, em uma modalidade, proteínas de fusão compreendem o domínio de clivagem (ou meio-domínio de clivagem) de pelo menos uma enzima de restrição do Tipo IIS e um ou mais domínios de ligação a dedo de zinco, os quais podem ou não ser manipulados.
[0096] Uma enzima de restrição do Tipo IIS exemplificativa, cujo do mínio de clivagem é separável do domínio de ligação é Fok I. Essa enzima em particular é ativa como um dímero. Bitinaite et al. (1998) Proc. Natl. Acad. Sci. USA 95: 10.570-10.575. Consequentemente, para fins da presente invenção, a porção da enzima Fok I usada nas proteínas de fusão divulgadas é considerada um meio-domínio de clivagem. Assim, para clivagem de fita dupla objetivada e/ou substituição objetivada de sequências celulares usando fusões de dedo de zinco-Fok I, duas proteínas de fusão, cada uma compreendendo um meio-domínio de clivagem de Fok I, podem ser usadas para reconstituir um domínio de clivagem catalitica- mente ativo. Alternativamente, uma única molécula polipeptídica contendo um domínio de ligação de dedo de zinco e dois meio-domínios de clivagem de Fok I também pode ser usada. Parâmetros para clivagem objetivada e alteração de sequência objetivada usando fusões de dedo de zinco-FokI são proporcionados em alguma parte na presente invenção.
[0097] Um domínio de clivagem ou meio-domínio de clivagem pode ser qualquer porção de uma proteína que retém a atividade de clivagem ou que retém a capacidade de multimerizar (por exemplo, dimerizar) para formar um domínio de clivagem funcional.
[0098] Enzimas de restrição do Tipo IIS exemplificativas são descritas na Publicação Internacional cocedida WO 2007/014275, incorporada por referência aqui na íntegra.
[0099] Para intensificar a especificidade de clivagem, domínios de clivagem também podem ser modificados. Em determinadas modalidades, variantes do meio-domínio de clivagem são empregadas onde essas variantes minimizam ou previnem a homodimerização dos meio-domínios de clivagem. Exemplos não limitativos de tais meio-domínios de clivagem modificados são descritos em detalhes no documento WO 2007/014275, aqui incorporado por referência na íntegra. Vide, também, Exemplos. Em determinadas modalidades, o domínio de clivagem compreende um meio- domínio de clivagem manipulado (também referido como mutantes com domínio de dimerização) que minimizam ou previnem a homodimerização são conhecidos por aqueles versados no campo e descritos, por exemplo, nas Publicações de Patente U.S. Nos. 20050064474 e 20060188987, incorporadas por referência aqui na íntegra. Resíduos de aminoácido nas posições 446, 447, 479, 483, 484, 486, 487, 490, 491, 496, 498, 499, 500, 531,534, 537 e 538 de Fok I são todos alvo para influenciar a dimerização dos meio-domínios de clivagem de Fok I. Vide, por exemplo, Publicações de Patente U.S. Nos. 20050064474 e 20060188987; Publicação de Patente Internacional WO 07/139898; Miller etal. (2007) Nat. Bio- technol. 25(7): 778-785.
[00100] Meio-domínios de clivagem de Fok I manipulados adicionais que formam heterodímeros obrigatórios também podem ser usados nas ZFNs descritas aqui. Em uma modalidade, o primeiro meio-domínio de clivagem inclui mutações em resíduos de aminoácido nas posições 490 e 528 de Fok I e o segundo meio-domínio de clivagem inclui mutações em resíduos de aminoácido 486 e 499.
[00101] Em determinadas modalidades, o domínio de clivagem compreende dois meio-domínios de clivagem, ambos os quais são parte de um único polipeptídeo compreendendo um domínio de ligação, um primeiro meio-domínio de clivagem e um segundo meio-domínio de clivagem. Os meio-domínios de clivagem podem ter a mesma sequência de aminoácido ou diferentes sequências de aminoácido, na medida em que eles funcionem para clivar o DNA.
[00102] Em geral, duas proteínas de fusão são requeridas para clivagem se as proteínas de fusão compreendem meio-domínios de clivagem. Alternativamente, uma única proteína compreendendo dois meio- domínios de clivagem pode ser usada. Os dois meio-domínios de cliva- gem podem ser derivados da mesma endonuclease (ou fragmentos funcionais da mesma) ou cada meio-domínio de clivagem pode ser derivado de uma endonuclease diferente (ou fragmentos funcionais das mesmas). Além disso, os sítios-alvo para as duas proteínas de fusão são, de preferência, dispostos, um com relação ao outro, de modo que ligação das duas proteínas de fusão a seus respectivos sítios-alvo coloca os meio- domínios de clivagem em uma orientação espacial um com relação ao outro, de modo a permitir que a clivagem dos meio-domínios forme um domínio de clivagem funcional, por exemplo, através de dimerização. Assim, em determinadas modalidades, as bordas próximas dos sítios-alvo são separadas por 5-8 nucleotídeos ou por 15-18 nucleotídeos. Contudo, qualquer número integral de nucleotídeos ou pares de nucleotídeo podem estar intervenientes entre dois sítios-alvo (por exemplo, de 2 a 50 nucleotídeos ou mais). Em geral, o ponto de clivagem reside entre os sítios-alvo. Proteínas de Fusão
[00103] Métodos para design e construção de proteínas de fusão (e polinucleotídeos que codificam as mesmas) são conhecidos por aqueles versados no campo. Por exemplo, métodos para o design e construção de proteínas de fusão compreendendo domínios de ligação de DNA (por exemplo, domínios de dedo de zinco) e domínios regulatórios ou de clivagem (ou meio-domínios de clivagem) e polinucleotídeos que codificam tais proteínas de fusão são descritos nas Patentes U.S. cocedidas Nos. 6.453.242 e 6.534.261 e Publicações de Pedido de Patente U.S. 2007/0134796 e 2005/0064474; aqui incorporados por referência na íntegra. Em determinadas modalidades, polinucleotídeos que codificam as proteínas de fusão são construídos. Esses polinucleotídeos podem ser inseridos em um vetor e o vetor pode ser introduzido em uma célula (vide abaixo para divulgação adicional com relação a vetores e métodos para introdução de polinucleotídeos em células).
[00104] Em determinadas modalidades dos métodos descritos aqui, uma nuclease de dedo de zinco compreende uma proteína de fusão compreendendo um domínio de ligação de dedo de zinco e um meio- domínio de clivagem da enzima de restrição Fok I e duas de tais proteínas de fusão são expressas em uma célula. Expressão de duas proteínas de fusão em uma célula pode resultar de distribuição das duas proteínas à célula; distribuição de uma proteína e um ácido nucleico que codifica uma das proteínas à célula; distribuição de dois ácidos nucleicos, cada um codificando uma das proteínas, à célula; ou através de distribuição de um único ácido nucleico, que codifica ambas as proteínas, à célula. Em modalidades adicionais, uma proteína de fusão compreende uma única cadeia polipeptídica compreendendo dois meio-domínios de clivagem e um domínio de ligação de dedo de zinco. Nesse caso, uma única proteína de fusão é expressa em uma célula e, sem desejar estar preso pela teoria, acredita-se que clive o DNA como um resultado de formação de um dímero intramolecular dos meio-domínios de clivagem.
[00105] Em determinadas modalidades, os componentes das proteínas de fusão (por exemplo, fusões de ZFP-Fok I) são dispostos de modo que o domínio de dedo de zinco esteja mais próximo do amino término da proteína de fusão e o meio-domínio de clivagem esteja mais próximo do carbóxi término. Isso espelha a orientação relativa do domínio de clivagem em domínios de clivagem de dimerização que ocorrem naturalmente, tais como aqueles derivados da enzima Fok I, nos quais o domínio de ligação a DNA está mais próximo do amino término e o meio- domínio de clivagem está mais próximo do carbóxi término. Nessas modalidades, acredita-se que dimerização dos meio-domínios de clivagem para formar uma nuclease funcional ocorra mediante ligação das proteínas de fusão a sítios sobre fitas de DNA opostas, com as extremidades 5' dos sítios de ligação estão próximas umas das outras.
[00106] Em modalidades adicionais, os componentes das proteínas de fusão (por exemplo, fusões ZFN-Fok I) são dispostos de modo que o meio-domínio de clivagem esteja mais próximo do amino término da proteína de fusão e o domínio de dedo de zinco esteja mais próximo do carbóxi término. Nessas modalidades, acredita-se que dimerização dos meio-domínios de clivagem forme uma nuclease funcional através de ligação das proteínas de fusão a sítios sobre fitas de DNA opostas, com as extremidades 3' dos sítios de ligação estando próximas uma da outra.
[00107] Em outras modalidades adicionais, uma primeira proteína de fusão contém o meio-domínio de clivagem mais próximo do amino término da proteína de fusão e o domínio de dedo de zinco mais próximo do carbóxi término e uma segunda proteína de fusão está disposta de modo que o domínio de dedo de zinco esteja mais próximo do amino término da proteína de fusão e o meio-domínio de clivagem esteja mais próximo do carbóxi término. Nessas modalidades, ambas as proteínas de fusão se ligam à mesma fita de DNA, com o sítio de ligação da primeira proteína de fusão contendo o domínio de dedo de zinco mais próximo do carbóxi término localizado no lado 5' do sítio de ligação da segunda proteína de fusão contendo o domínio de dedo de zinco mais próximo do amino término.
[00108] Em determinadas modalidades das proteínas de fusão divulgadas, a sequência de aminoácido entre o domínio de dedo de zinco e o domínio de clivagem (ou meio-domínio de clivagem) é denotada o "ligante ZC". O ligante ZC deve ser distinguido dos ligantes interdedo discutidos acima. Vide, por exemplo, Publicações de Patente U.S. 20050064474A1 e 20030232410 e Publicação de Patente Internacional WO05/084190 para detalhes sobre a obtenção de ligantes ZC que otimizam a clivagem.
[00109] Em uma modalidade, a invenção proporciona uma ZFN com-preendendo uma proteína de dedo de zinco tendo uma ou mais das sequências de aminoácido de hélice de reconhecimento mostradas na Tabela 1. Em outra modalidade, é proporcionado aqui um vetor de expres- são de ZFP compreendendo uma sequência de nucleotídeo que codifica uma ZFP tendo uma ou mais hélices de reconhecimento mostradas na Tabela 1. Integração Objetivada
[00110] Os métodos e composições divulgados podem ser usados para clivar DNA em um gene Zp15 da cromatina celular de planta, o que facilita a integração objetivada estável de uma sequência exógena no locus . Conforme descrito aqui, perda de função de genes Zp15 endógenos é bem tolerada por células de planta e sequências integradas dentro desse gene são amplamente descritas e geram plantas com modificações na linhagem germinativa para transmissão hereditária da sequência integrada. Consequentemente, o Zp15 é um sítio desejável para integração objetivada de sequências exógenas.
[00111] Para integração objetivada em Zp15, um ou mais domínios de ligação a DNA (por exemplo, ZFPs) são manipulados para se ligar a um sítio-alvo em ou próximo do sítio de clivagem predeterminado e uma proteína de fusão compreendendo o domínio de ligação a DNA manipulado e um domínio de clivagem é expresso em uma célula. Quando de ligação da porção de ligação a DNA (por exemplo, dedo de zinco) da proteína de fusão ao sítio-alvo, o DNA é clivado, de preferência via uma ruptura de fita dupla, próximo do sítio-alvo pelo domínio de clivagem.
[00112] A presença de uma ruptura de fita dupla no locus de Zp15 facilita a integração de sequências exógenas via recombinação homóloga. Assim, o polinucleotídeo compreendendo a sequência exógena a ser inserida no gene Zp15 incluirá uma ou mais regiões de homologia com um gene Zp15 para facilitar a recombinação homóloga.
[00113] Qualquer sequência de interesse (sequência exógena) pode ser introduzida em um locus de Zp15 conforme descrito aqui. Sequências exógenas exemplificativas incluem, mas não estão limitadas a, qualquer sequência de codificação polipeptídica (por exemplo, cDNAs), promotores, intensificadores e outras sequências regulatórias (por exemplo, sequências de RNA de interferência, cassetes de expressão de shRNA, tags de epitopo, genes marcadores, sítios de reconhecimento de enzima de clivagem, sítios e vários tipos de construtos de expressão. Tais sequências podem ser prontamente obtidas usando técnicas de biologia molecular padrões (clonagem, síntese, etc.) e/ou estão comercialmente disponíveis.
[00114] Além das moléculas de fusão descritas aqui, substituição objetivada de uma sequência genômica selecionada também envolve a introdução da sequência de substituição (ou doadora). A sequência doadora pode ser introduzida na célula antes de, concorrentemente com ou subsequentemente à expressão da(s) proteína(s) de fusão. O polinucleotídeo doador contém homologia suficiente ao Zp15 para sustentar recombinação homóloga (ou reparo homologia-dirigido) entre o mesmo e a sequência genômica de Zp15 com a qual ele tem homologia. Aproximadamente 25, 50, 100, 200, 500, 750, 1.000, 1.500, 2.000 nucleotídeos ou mais de homologia de sequência entre uma sequência doadora e uma genômica (ou qualquer valor integral entre 10 e 2.000 nucleotídeos ou mais) sustentarão a recombinação homóloga entre as mesmas. Em determinadas modalidades, os braços de homologia têm menos de 1.000 pares de base de comprimento. Em outras modalidades, os braços de homologia têm menos de 750 pares de base de comprimento. Vide também Pedido de Patente Provisória U.S. No. 61/124.047, a qual é incorporada aqui por referência.
[00115] Sequências doadoras podem oscilar, quanto ao comprimento, de 10 a 5.000 nucleotídeos (ou qualquer valor integral de nucleotídeos entre os mesmos) ou mais. Será prontamente evidente que a sequência doadora, tipicamente, não é idêntica à sequência genômica que ela substitui. Por exemplo, a sequência do polinucleotídeo doador pode conter uma ou mais alterações, inserções, deleções, inversões ou reestrutura- ções de uma base com relação à sequência genômica, contanto que ho- mologia suficiente com as sequências cromossômicas esteja presente. Alternativamente, uma sequência doadora pode conter uma sequência não homóloga flanqueada por duas regiões de homologia. Adicionalmente, sequências doadoras podem compreender uma molécula de vetor contendo sequências que não são homólogas à região de interesse na cromatina celular. Geralmente, a(s) região(ões) homóloga(s) de uma sequência doadora terá(ão) pelo menos 50% de identidade de sequência a uma sequência genômica com a qual recombinação é desejada. Em determinadas modalidades, 60%, 70%, 80%, 90%, 95%, 98%, 99% ou 99,9% de identidade de sequência estão presentes. Qualquer valor entre 1% e 100% de identidade de sequência pode estar presente, dependendo do comprimento do polinucleotídeo doador.
[00116] Uma molécula doadora pode conter várias regiões descontinuas de homologia à cromatina celular. Por exemplo, para inserção objetivada de sequências normalmente não presentes em uma região de interesse, as referidas sequências podem estar presentes em uma molécula de ácido nucleico e flanqueada por regiões de homologia a uma sequência gênica na região de interesse.
[00117] Moléculas doadoras também podem ser inseridas no locus de Zp15 para servir como um reservatório para uso posterior. Por exemplo, uma molécula doadora homóloga a um gene endógeno, mas contendo uma mutação de interesse, pode ser inserida no locus de Zp15. Em seguida, ZFNs específicas ao gene endógeno podem ser introduzidas, as quais clivarão o locus endógeno e a molécula doadora no locus de Zp15 o qual contém a mutação de interesse. O DSB resultante no genoma pode, então, se tornar o sítio de integração para a molécula doadora liberada do locus de Zp15. Dessa forma, a eficiência de integração objetivada de uma sequência doadora em qualquer região de interesse pode ser grandemente aumentada, uma vez que o método não conta com capta ção simultânea de ácidos nucleicos que codificam as ZFNs e aqueles das sequências doadoras.
[00118] Moléculas doadoras também podem ser inseridas no locus de Zp15 para servir como um sítio-alvo para subsequentes inserções. Por exemplo, uma molécula doadora compreendida de sequências de DNA que contêm sítios de reconhecimento para designs de ZFN adicionais pode ser inserida no locus de Zp15. Subsequentemente, designs de ZFN adicionais podem ser gerados e expressos em células, de modo que a molécula doadora original seja clivada e modificada através de reparo ou recombinação homóloga. Dessa forma, integrações reiterativas de moléculas doadoras podem ocorrer no locus de Zp15.
[00119] Para simplificar os ensaios (por exemplo, hibridização, PCR, digestão com enzima de restrição) para determinação de inserção com sucesso da sequência doadora, determinadas diferenças de sequência podem estar presentes na sequência doadora quando comparado com a sequência genômica de Zp15. De preferência, se localizadas em uma região de codificação, tais diferenças de sequência de nucleotídeo não alterarão a sequência de aminoácido ou farão alterações de aminoácido silenciosas (isto é, alterações as quais não afetam a estrutura ou função da proteína). O polinucleotídeo doador pode, opcionalmente, conter alterações em sequências correspondendo aos sítios de ligação com domínio de ligação a DNA na região de interesse para impedir clivagem de sequências doadoras que tenham sido introduzidas na cromatina celular por meio de recombinação homóloga.
[00120] O polinucleotídeo doador pode ser DNA ou RNA, fita simples ou fita dupla e pode ser introduzido em uma célula na forma linear ou circular. Se introduzido na forma linear, as extremidades da sequência doadora podem ser protegidas (por exemplo, contra degradação exonucleolí- tica) através de métodos conhecidos por aqueles versados no campo. Por exemplo, um ou mais resíduos de dideoxinucleotídeo são adiciona dos ao 3' término de uma molécula linear e/ou oligonucleotídeos auto- complementares são ligados a uma ou ambas as extremidades. Vide, por exemplo, Chang et al. (1987) Proc. Natl. Acad. Sci. USA 84: 4959-4963; Nehls et al. (1996) Science 272: 886-889. Métodos adicionais para proteção de polinucleotídeos exógenos contra degradação incluem, mas não estão limitados a, adição de grupo(s) amino terminal(is) e o uso de ligações internucleotídeo modificadas tais como, por exemplo, resíduos de fosforotioatos, fosforamidatos e O-metil ribose ou deoxirribose.
[00121] Um polinucleotídeo pode ser introduzido em uma célula como parte de uma molécula de vetor tendo sequências adicionais tais como, por exemplo, origens de replicação, promotores e genes que codificam resistência a antibiótico. Além disso, os polinucleotídeos doadores podem ser introduzidos como ácido nucleico "nu", como um ácido nucleico em complexo com um agente, tal como uma nanopartícula, lipossoma ou po- loxâmero ou pode ser distribuído por bactérias ou vírus (por exemplo, Agrobacterium, Rhizobium sp. NGR234, Sinorhizoboium meliloti, Me- sorhizobium loti, vírus mosaico do tabaco, vírus X da batata, vírus mosaico da couve-flor e vírus mosaico do veio de cassava). Vide, por exemplo, Chung et al. (2006) Trends Plant Sci. 11(1): 1-4.
[00122] Parece que a presença de uma ruptura de fita dupla em uma sequência celular, acoplada à presença de uma molécula de DNA exógena tendo homologia a uma região adjacente a ou que envolve a ruptura, ativa mecanismos celulares os quais reparam a ruptura por meio de transferência de informação de sequência da molécula doadora para a sequência celular (por exemplo, genômica ou cromossômica); isto é, através de um processo de reparo homologia-dirigido, também conhecido como "conversão gênica". Os métodos da Requerente combinam, vantajosamente, as poderosas capacidades de objetivação de ZFPs manipuladas com um domínio de clivagem (ou meio-domínio de clivagem) para objetivar especificamente genes parálogos, tais como genes Zp15, de modo que clivagem da sequência-alvo produz uma ruptura de fita dupla na região do genoma onde inserção de sequências exógenas é desejada.
[00123] Para alteração de uma sequência cromossômica, não é necessário que toda a sequência do doador seja copiada para o cromossomo, contanto que o bastante da sequência doadora seja copiado para realizar a alteração de sequência desejada.
[00124] A eficiência de inserção de sequências doadoras através de recombinação homóloga é inversamente relacionada à distância, no DNA celular, entre a ruptura de fita dupla e o sítio no qual recombinação é desejada. Em outras palavras, maiores eficiências de recombinação homóloga são observadas quando a ruptura de fita dupla está mais próxima do sítio no qual recombinação é desejada. Em casos nos quais um sítio preciso de recombinação não é predeterminado (por exemplo, o evento de recombinação desejado pode ocorrer sobre um intervalo de sequência genômica), o comprimento e sequência do ácido nucleico doador, junto com o(s) sítio(s) de clivagem, são selecionados para obter o evento de recombinação desejado. Em casos nos quais o evento desejado é projetado para alterar a sequência de um único par de nucleotídeo em uma sequência genômica, a cromatina celular é clivada dentro de 10.000 nucleotídeos sobre qualquer lado desse par de nucleotídeo. Em determinadas modalidades, clivagem ocorre dentro de 1,000, 500, 200, 100, 90, 80, 70, 60, 50, 40, 30, 20, 10, 5 ou 2 nucleotídeos ou qualquer valor integral entre 2 e 1.000 nucleotídeos, sobre qualquer lado do par de nucleotídeo cuja sequência tem de ser alterada.
[00125] Conforme detalhado acima, os sítios de ligação para duas proteínas de fusão, cada uma compreendendo um domínio de ligação de dedo de zinco e um meio-domínio de clivagem, podem estar localizados 5-8 ou 15-18 nucleotídeos de distância, conforme medido a partir da borda de cada sítio de ligação mais próximo do outro sítio de ligação e clivagem ocorre entre os sítios de ligação. Se clivagem ocorre em um único sítio ou em múltiplos sítios entre os sítios de ligação não é relevante, uma vez que as sequências genômicas clivadas são substituídas pelas sequências doadoras. Assim, para alteração eficiente da sequência de um único par de nucleotídeo através de recombinação objetivada, o ponto mediano da região entre os sítios de ligação está dentro de 10.000 nucleotídeos desse par de nucleotídeo, de preferência dentro de 1.000 nucleotídeos ou 500 nucleotídeos ou 200 nucleotídeos ou 100 nucleotídeos ou 50 nucleotídeos ou 20 nucleotídeos ou 10 nucleotídeos ou 5 nucleotídeos ou 2 nucleotídeos ou um nucleotídeo ou no par de nucleotídeo de interesse.
[00126] Em determinadas modalidades, um cromossomo homólogo pode servir como o polinucleotídeo doador. Assim, por exemplo, correção de uma mutação em um heterozigoto pode ser obtida manipulando proteínas de fusão as quais se ligam a e clivam a sequência mutante sobre um cromossomo, mas não clivam a sequência do tipo silvestre sobre o cromossomo homólogo. A ruptura de fita dupla sobre o cromossomo trazendo a mutação estimula um processo de "conversão gênica" baseado em homologia no qual a sequência do tipo silvestre do cromossomo homólogo é copiada para o cromossomo clivado, assim, restaurando duas cópias da sequência do tipo silvestre.
[00127] São também proporcionados métodos e composições que podem intensificar os níveis de recombinação objetivada incluindo, mas não limitado a, o uso de fusões de domínio funcional-ZFP adicionais para ativar a expressão de genes envolvidos em recombinação homóloga tais como, por exemplo, genes de planta do grupo de epistase RAD54 (por exemplo, AtRad54, AtRad51) e genes cujos produtos interagem com os produtos gênicos antes mencionados. Vide, por exemplo, Klutstein M, et al. Genetics. Abril de 2008; 178(4): 2389-97.
[00128] Similarmente, fusões de domínio funcional-ZFP podem ser usadas, em combinação com os métodos e composições divulgados aqui, para reprimir a expressão de genes envolvidos em união terminal não homóloga (por exemplo, Ku70/80, XRCC4, poli(ADP ribose) polime- rase, DNA ligase 4). Vide, por exemplo, Riha et al. (2002) EMBO 21: 2819-2826; Freisner et al. (2003) Plant J. 34: 427-440; Chen et al. (1994) European Journal of Biochemistry 224: 135-142. Métodos para ativação e repressão de expressão gênica usando fusões entre um domínio de ligação de dedo de zinco e um domínio funcional são divulgados, por exemplo, nas Patentes US cocedidas 6.534.261; 6.824.978 e 6.933.113. Métodos de repressão adicionais incluem o uso de oligonucleotídeos antissenso e/ou pequeno RNA de interferência (siRNA ou RNAi) ou shR- NAs objetivados à sequência do gene a ser reprimido.
[00129] Como uma alternativa a ou além disso, ativação de expressão de produtos gênicos envolvidos em recombinação homóloga, fusões dessa proteína (ou fragmentos funcionais da mesma) com um domínio de ligação de dedo de zinco objetivo ao Zp15, pode ser usada para recrutar essas proteínas (proteínas de recombinação) à região de interesse, desse modo, aumentando sua concentração local e ainda estimulando processos de recombinação homóloga. Alternativamente, um polipeptídeo envolvido em recombinação homóloga, conforme descrito acima (ou um fragmento funcional do mesmo) pode ser parte de uma proteína de fusão tripla compreendendo um domínio de ligação de dedo de zinco, um domínio de clivagem (ou meio-domínio de clivagem) e a proteína de recombinação (ou fragmento funcional da mesma). Proteínas adicionais envolvidas em conversão gênica e remodelamento de cromatina relacionado à recombinação, as quais podem ser usadas nos métodos e composições antes mencionados, incluem acetil transferases de histona (por exemplo, Esalp, Tip60), metil transferases de histona (por exemplo, Dotlp), quina- ses de histona e fosfatases de histona. Vide também Bhat et al. (1999) Plant 7.33: 455-469.
[00130] Aumentos adicionais na eficiência de recombinação objetivada em células compreendendo uma molécula de fusão de dedo de zin- co/nuclease e uma molécula de DNA doadora são obtidos bloqueando as células na fase G2 do ciclo celular, quando processos de reparo acionados por homologia estão maximamente ativos. Tal interrupção pode ser obtida através de uma série de formas. Por exemplo, as células podem ser tratadas, por exemplo, com fármacos, compostos e/ou pequenas moléculas as quais influenciam a progressão do ciclo celular, de forma a interromper as células na fase G2. Moléculas exemplificativas desse tipo incluem, mas não estão limitadas a, compostos os quais afetam a polime- rização de microtúbulo (por exemplo, vinblastina, nocodazol, Taxol), compostos que interagem com o DNA (por exemplo, cis-platina(II), diclo- reto de diamina, Cisplatina, doxorrubicina) e/ou compostos que afetam a síntese de DNA (por exemplo, timidina, hidroxiureia, L-mimosina, etopo- sídeo, 5-fluorouracila). Aumentos adicionais na eficiência de recombinação são obtidos mediante o uso de inibidores de deacetilase de histona (HDAC) (por exemplo, butirato de sódio, tricostatina A), os quais alteram a estrutura da cromatina para tornar o DNA genômico mais acessível à máquina de recombinação celular.
[00131] Métodos adicionais para interrupção do ciclo celular incluem superexpressão de proteínas as quais inibem a atividade das quinases CDK do ciclo celular, por exemplo, mediante introdução de um cDNA que codifica a proteína na célula ou por meio de introdução, na célula, de uma ZFP manipulada a qual ativa expressão do gene que codifica a proteína. Interrupção do ciclo celular é também obtida inibindo a atividade de cicli- nas e CDKs, por exemplo, usando métodos de RNAi (por exemplo, Patente U.S. No. 6.506.559) ou mediante introdução, na célula, de uma ZFP manipulada a qual reprime a expressão de um ou mais genes envolvidos em progressão do ciclo celular tais como, por exemplo, genes de ciclina e/ou CDK. Vide, por exemplo, Patente U.S. cocedida No. 6.534.261 para métodos de síntese de proteínas do dedo de zinco manipuladas para re- gulação de expressão gênica.
[00132] Alternativamente, em determinados casos, clivagem objetivada é conduzida na ausência de um polinucleotídeo doador (de preferência na fase S ou G2) e recombinação ocorre entre cromossomos homólogos. Vetores de Expressão
[00133] Um ácido nucleico que codifica uma ou mais proteínas de fusão (por exemplo, ZFNs), conforme descrito aqui, pode ser clonado em um vetor para transformação em células procariotas ou eucariotas para replicação e/ou expressão. Vetores podem ser vetores procariotas, por exemplo, plasmídeos ou vetores "shuttle", vetores de inseto ou vetores eucariotas. Um ácido nucleico que codifica uma proteína de fusão também pode ser clonado em um vetor de expressão para administração a uma célula vegetal.
[00134] Para expressar as proteínas de fusão (por exemplo, ZFNs), sequências que codificam as proteínas de fusão são, tipicamente, sub- clonadas em um vetor de expressão que contém um promotor para dirigir a transcrição. Promotores bacterianos e eucariotas adequados são bem- conhecidos na técnica e descritos, por exemplo, em Sambrook et al, Molecular Cloning, A Laboratory Manual (2a ed. 1989; 3a ed., 2001); Kriegler, Gene Transfer and Expression: A Laboratory Manual (1990); e Current Protocols in Molecular Biology (Ausubel et al., supra). Sistemas de expressão bacterianos para expressão da ZFP estão disponíveis, por exemplo, em E. coli, Bacillus sp e Salmonella (Palva et al, Gene 22: 229235 (1983)). Kits para tais sistemas de expressão estão comercialmente disponíveis. Sistemas de expressão para células de mamífero, levedura e células de inseto são bem-conhecidos por aqueles versados no campo e também estão comercialmente disponíveis.
[00135] O promotor usado para dirigir a expressão de um ácido nucleico que codifica proteína de fusão depende da aplicação em particular. Por exemplo, um promotor constitutivo forte adequado para a célula hos-pedeira é, tipicamente, usado para expressão e purificação de proteínas de fusão.
[00136] Em contraste, quando uma proteína de fusão é administrada in vivo para regulação de um gene de planta (vide a seção "Distribuição de Ácido Nucleico a células de Planta" abaixo), um promotor constitutivo ou induzível é usado, dependendo do uso particular da proteína de fusão. Exemplos não limitativos de promotores de planta incluem sequências derivadas de ubiquitina-3 de A. thaliana (ubi-3) (Callis, etal, 1990, J. Biol. Chem. 265: 12486-12493); sintase de manopina de A. Tumefaciens (Amas) (Petolino et al, Patente U.S. No. 6.730.824); e/ou Vírus Mosaico do Veio de Cassava (CsVMV) (Verdaguer et al., 1996, Plant Molecular Biology 31: 1129-1139). Vide também Exemplos.
[00137] Além do promotor, o vetor de expressão contém, tipicamente, uma unidade de transcrição ou cassete de expressão que contém todos os elementos adicionais requeridos para a expressão do ácido nucleico em células hospedeiras, quer procariotas ou eucariotas. Um cassete de expressão típico, assim, contém um promotor operativamente ligado, por exemplo, a uma sequência de ácido nucleico que codifica a proteína de fusão e sinais requeridos, por exemplo, para poliadenilação eficiente do transcrito, término de transcrição, sítios de ligação ribossômica ou término de tradução. Elementos adicionais do cassete podem incluir, por exemplo, intensificadores, sinais de junção heterólogos e/ou um sinal de localização nuclear (Nuclear Localization Signal - NLS).
[00138] O vetor de expressão usado em particular para transportar a informação genética para a célula é selecionado com relação ao uso pre-tendido das proteínas de fusão, por exemplo, expressão em plantas, animais, bactérias, fungos, protozoários, etc. (vide vetores de expressão descritos acima). Vetores de expressão bacterianos e animais padrões são conhecidos na técnica e são descritos em detalhes, por exemplo, Publicação de Patente U.S. 20050064474A1 e Publicações de Patente Internacionais WO05/084190, WO05/014791 e WO03/080809.
[00139] Métodos padrões de transfecção podem ser usados para produzir linhagens de células bacterianas, de mamífero, levedo ou inseto que expressam grandes quantidades de proteína as quais podem, então, ser purificadas usando técnicas padrões (vide, por exemplo, Colley et al., J. Biol. Chem. 264: 17619-17622 (1989); Guide to Protein Purification, in Methods in Enzymology, vol. 182 (Deutscher, ed., 1990)). Transformação de células eucariotas e procariotas é realizada de acordo com técnicas padrões (vide, por exemplo, Morrison, J. Bact. 132: 349-351 (1977); Clark-Curtiss & Curtiss, Methods in Enzymology 101: 347-362 (Wu et al., eds., 1983).
[00140] Qualquer um dos procedimentos bem-conhecidos para introdução de sequências de nucleotídeo estranhas em tais células hospedeiras pode ser usado. Esses incluem o uso de transfecção com fosfato de cálcio, polibreno, fusão de protoplasto, eletroporação, métodos de ultrassom (por exemplo, sonoporação), lipossomas, microinjeção, DNA "nu", vetores de plasmídeo, vetores virais, epissomais e integrativos e qualquer um dos outros métodos bem-conhecidos para introdução de DNA genô- mico, cDNA, DNA sintético clonado ou outro material genético estranho em uma célula hospedeira (vide, por exemplo, Sambrook et al., supra). É necessário apenas que o procedimento de engenharia genética usado em particular seja capaz de introduzir com sucesso pelo menos um gene na célula hospedeira capaz de expressão da proteína de escolha. Distribuição de Ácido Nucleico a Células de Planta
[00141] Conforme notado acima, construtos de DNA podem ser introduzidos (por exemplo, no genoma) em um hospedeiro vegetal desejado através de uma variedade de técnicas convencionais. Para revisões de tais técnicas vide, por exemplo, Weissbach & Weissbach Methods for Plant Molecular Biology (1988, Academic Press, N.Y.) Seção VIII, páginas 421-463; e Grierson & Corey, Plant Molecular Biology (1988, 2a Ed.), Blackie, Londres, Capítulos 7-9.
[00142] Por exemplo, o construto de DNA pode ser introduzido diretamente no DNA genômico da célula vegetal usando técnicas tais como eletroporação e microinjeção de protoplastos de células de planta ou os construtos de DNA podem ser introduzidos diretamente no tecido de planta usando métodos biolísticos, tal como bombardeamento de partícula de DNA (vide, por exemplo, Klein et al. (1987) Nature 327: 70-73). Alternativamente, o construto de DNA pode ser introduzido na célula vegetal via transformação de nanopartícula (vide, por exemplo, Pedido de Patente US No. 12/245.685, o qual é incorporado aqui por referência em sua totalidade). Alternativamente, os construtos de DNA podem ser combinados com regiões de flanqueamento/borda de T-DNA adequadas e introduzidos em um vetor hospedeiro Agrobacterium tumefaciens convencional. Técnicas de transformação mediadas por Agrobacterium tumefaciens, incluindo desarme e uso de vetores binários, são bem descritas na literatura científica. Vide, por exemplo, Horsch et al. (1984) Science 233: 496498 e Fraley et al. (1983) Proc. Natl Acad. Sci. USA 80: 4803.
[00143] Além disso, transferência gênica pode ser obtida usando bactérias que não Agrobacterium ou vírus, tais como Rhizobium sp. NGR234, Sinorhizoboium meliloti, Mesorhizobium loti, vírus X de batata, vírus mosaico da couve-flor e vírus mosaico do veio de cassava e/ou vírus mosaico de tabaco. Vide, por exemplo, Chung et al. (2006) Trends Plant Sci. 11(1): 1-4.
[00144] As funções de virulência do hospedeiro Agrobacterium tumefaciens dirigirão a inserção de uma T-fita contendo o construto e marcador adjacente ao DNA de célula vegetal quando a célula é infectada pela bactéria usando vetor de T DNA binário (Bevan (1984) Nuc. Acid Res. 12: 8711-8721) ou o procedimento de cocultura (Horsch et al. (1985) Science 227: 1229-1231). Em geral, o sistema de transformação com Agrobacterium é usado para manipular plantas dicotiledôneas (Bevan et al. (1982) Ann. Rev. Genet 16: 357-384; Rogers et al. (1986) Methods Enzymol. 118: 627-641). O sistema de transformação de Agrobacterium pode também ser usado para transformar, bem como transferir, DNA para plantas e células de plantas monocotiledôneas. Vide Patente U.S. No. 5.591.616; Hernalsteen et al. (1984) EMBO 73: 3039-3041; Hooykass-Van Slogteren et al. (1984) Nature 311: 763-764; Grimsley et al. (1987) Nature 325: 1677-179; Boulton et al. (1989) Plant Mol. Biol. 12: 31-40; e Gould et al. (1991) Plant Physiol. 95: 426-434.
[00145] Métodos alternativos de transferência e transformação gênica incluem, mas não estão limitados a, transformação de protoplasto através de captação mediada por eletroporação, cálcio ou polietileno glicol (PEG) de DNA "nu" (vide Paszkowski et al. (1984) EMBO J 3: 2717-2722, Po- trykus etal. (1985) Molec. Gen. Genet. 199: 169-177; Fromm etal. (1985) Proc. Nat. Acad. Sci. USA 82: 5824-5828; e Shimamoto (1989) Nature 338: 274-276) e eletroporação de tecidos de planta (D'Halluin et al. (1992) Plant Cell 4: 1495-1505). Métodos adicionais para transformação de célula vegetal incluem microinjeção, captação de DNA mediada por carbureto de silício (Kaeppler et al. (1990) Plant Cell Reporter9: 415-418) e bombardeamento de microprojétil (vide Klein et al. (1988) Proc. Nat. Acad. Sci. USA 85: 4305-4309; e Gordon-Kamm et al. (1990) Plant Cell 2: 603-618).
[00146] Os métodos e composições divulgados podem ser usados para inserir sequências exógenas em um local predeterminado (por exemplo, um gene Zp15) em um genoma de célula vegetal. Isso é útil uma vez que expressão de um transgene introduzido em um genoma de planta depende criticamente de seu sítio de integração. Consequentemente, genes que codificam, por exemplo, tolerância a herbicida, resistência a inseto, nutrientes, antibióticos ou moléculas terapêuticas podem ser inseridos, através de recombinação objetivada, em regiões do genoma de uma planta favoráveis à sua expressão.
[00147] Células de planta transformadas as quais são produzidas através de qualquer uma dessas técnicas de transformação podem ser cultivadas para regenerar uma planta inteira a qual possui o genótipo transformado e, assim, o fenótipo desejado. Tais técnicas de regeneração contam com manipulação de determinados fitormônios em um meio de crescimento de cultura tecidual, tipicamente contando com um marcador biocida e/ou herbicida o qual tenha sido introduzido junto com as sequências de nucleotídeo desejadas. A regeneração de planta a partir de proto- plastos cultivados é descrita em Evans et al., "Protoplasts Isolation and Culture" em Handbook of Plant Cell Culture, páginas 124-176, Macmillian Publishing Company, New York, 1983; e Binding, Regeneration of Plants, Plant Protoplasts, páginas 21-73, CRC Press, Boca Raton, 1985. Regeneração também pode ser obtida a partir de caule, explante, órgãos, po- lens, embriões de planta ou partes dos mesmos. Tais técnicas de regeneração são descritas, em geral, em Klee et al. (1987) Ann. Rev. of Plant Phys. 38: 467-486.
[00148] Ácidos nucleicos introduzidos em uma célula vegetal podem ser usados para conferir traços desejados a essencialmente qualquer planta. Uma ampla variedade de plantas e sistemas de célula vegetal podem ser manipulados quanto às características fisiológicas e agronômicas desejadas descritas aqui usando os construtos de ácido nucleico da presente invenção e os vários métodos de transformação mencionados acima. Em modalidades preferidas, plantas e células de planta-alvo para manipulação incluem, mas não estão limitadas a, aquelas plantas mono- cotiledôneas e dicotiledôneas, tais como safras, incluindo safras de grãos (por exemplo, trigo, milho, arroz, painço, cevada), safras de fruta (por exemplo, tomate, maçã, pêra, morango, laranja), safras de forragem (por exemplo, alfafa), safras de vegetais de raiz (por exemplo, cenoura, bata ta, beterrabas sacarínicas, inhame), safras de vegetais folhosos (por exemplo, alface, espinafre); plantas de floração (por exemplo, petúnia, rosa, crisântemo), coníferas e pinheiros (por exemplo, pinheiro, pinho); plantas usadas em fitoterapia (por exemplo, plantas que acumulam metal pesada); safras oleosas (por exemplo, girassol, colza) e plantas usadas para fins experimentais (por exemplo, Arabidopsis). Assim, os métodos e composições divulgados têm uso sobre uma ampla faixa de plantas incluindo, mas não limitado a, espécies dos gêneros Asparagus, Avena, Brassica, Citrus, Citrullus, Capsicum, Cucurbita, Daucus, Erigeron, Glycine, Gossypium, Hordeum, Lactuca, Lolium, Lycopersicon, Malus, Manihot, Nicotiana, Orychophragmus, Oryza, Persea, Phaseolus, Pisum, Pyrus, Prunus, Raphanus, Secale, Solanum, Sorghum, Triticum, Vitis, Vigna e Zea.
[00149] Aqueles versados no campo reconhecerão que, após a sequência exógena ser estavelmente incorporada em plantas transgênica e confirmada como sendo operável, ela pode ser introduzida em outras plantas através de cruzamento sexual. Qualquer uma de uma série de técnicas padrões de melhoramento pode ser usada, dependendo da espécie a ser cruzada.
[00150] Uma célula, caule, tecido de planta ou planta transformada pode ser identificado e isolado por meio de seleção ou triagem do material vegetal manipulado quanto a traços codificados pelos genes marcadores presentes sobre o DNA de transformação. Por exemplo, seleção pode ser realizada crescendo o material vegetal manipulado sobre meios contendo uma quantidade inibitória do antibiótico ou herbicida ao qual o construto gênico de transformação confere resistência. Ainda, plantas e células de planta transformadas também podem ser identificadas por meio de triagem das atividades de quaisquer genes marcadores visíveis (por exemplo, os genes de β-glucuronidase, luciferase, B ou Cl) que possam estar presentes sobre os construtos de ácido nucleico recombinante. Tais metodologias de seleção e triagem são bem-conhecidas por aqueles versados no campo.
[00151] Métodos físicos e bioquímicos também podem ser usados para identificar transformantes de planta ou célula vegetal contendo constru- tos gênicos inseridos. Esses métodos incluem, mas não estão limitados a: 1) análise de Southern ou amplificação por PCR para detecção e determinação da estrutura do inserto de DNA recombinante; 2) Northern blot, proteção com SIRNase, extensão de iniciador ou amplificação por PCR com transcriptase reversa para detecção e exame dos transcritos de RNA dos construtos gênicos; 3) eletroforese em gel de proteína, técnicas de Western blot, imunoprecipitação ou imunoensaios enzima-ligados (ELISA), onde os produtos do construto gênico são proteínas. Técnicas adicionais, tais como hibridização in situ, coloração enzimática e imu- nocoloração, também podem ser usados para detectar a presença ou expressão do construto recombinante em órgãos e tecidos específicos de uma planta. Os métodos para fazer todos esses ensaios são bem- conhecidos por aqueles versados no campo.
[00152] Os efeitos de manipulação gênica usando os métodos divulgados aqui podem ser observados, por exemplo, através de Northern blots do RNA (por exemplo, mRNA) isolado dos tecidos de interesse. Tipicamente, se o mRNA está presente ou a quantidade de mRNA aumentou, pode se admitir que o transgene correspondente está sendo expresso. Outros métodos de medição de atividade do polipeptídeo codificado e/ou gene podem ser usados. Diferentes tipos de ensaios enzimáticos podem ser usados, dependendo do substrato usado e do método de detecção de aumento ou diminuição de um produto ou subproduto de reação. Além disso, os níveis de polipeptídeo expresso podem ser medidos imunoquimicamente, isto é, ELISA, RIA, ELA e outros ensaios baseados em anticorpo bem-conhecidos por aqueles versados no campo, tal como através de ensaios de detecção eletroforéticos (com coloração ou Wes- tern blotting). Como um exemplo não limitativo, a detecção das proteínas AAD-1 e PAT usando um ensaio ELISA é descrita no Pedido de Patente U.S. No. 11/587.893, referência a qual é aqui incorporada por referência na íntegra. O transgene pode ser seletivamente expresso em alguns tecidos da planta ou em alguns estágios de desenvolvimento ou o transgene pode ser expresso em substancialmente todos os tecidos de planta, substancialmente ao longo de todo o ciclo de vida. Contudo, qualquer modo de expressão combinatorial é também aplicável.
[00153] A presente invenção também abrange sementes das plantas transgênicas descritas acima em que a semente tem o transgene ou construto gênico. A presente invenção ainda abrange a prole, clones, linhagens de célula ou células das plantas transgênicas descritas acima, em que a referida prole, clone, linhagem de célula ou célula tem o transgene ou produto gênico.
[00154] Proteínas de fusão (por exemplo, ZFNs) e vetores de expressão que codificam proteínas de fusão podem ser administrados diretamente à planta para regulação gênica, clivagem objetivada e/ou recombinação. Em determinadas modalidades, a planta contém múltiplos genesalvo parálogos. Sabe-se que plantas podem conter múltiplos genes pará- logos. Assim, uma ou mais proteínas de fusão ou vetores de expressão que codificam proteínas de fusão diferentes podem ser administrados a uma planta de forma a objetivar um ou mais genes Zp15 na planta.
[00155] A administração de quantidades eficazes é através de qualquer uma das vias normalmente usadas para introdução de proteínas de fusão em contato com a célula vegetal a ser tratada. As ZFPs são administradas através de muitas maneiras adequadas, de preferência com veículos aceitáveis. Métodos adequados de administração de tais modula- dores estão disponíveis e bem-conhecidos por aqueles versados no campo e, embora mais de uma via possa ser usada para administrar uma composição em particular, um via particular pode, frequentemente, pro porcionar uma reação mais imediata e mais eficaz do que outra via.
[00156] Veículos também podem ser usados e são determinados, em parte, pela composição que está sendo administrada, bem como pelo método usado para administrar a composição em particular. Consequentemente, há uma ampla variedade de formulações adequadas de veículos que estão disponíveis. EXEMPLOS
[00157] Abaixo estão exemplos de modalidades específicas para realização da presente invenção. Os exemplos são oferecidos para fins ilustrativos apenas e não se destinam a limitar o escopo da presente invenção de qualquer forma.
[00158] Esforços foram feitos para assegurar precisão com relação aos números usados (por exemplo, quantidades, temperaturas, etc.), mas algum erro e desvio experimental pode, naturalmente, ser permitido. Exemplo 1: Identificação e Caracterização do Locus Alvo de Zp15
[00159] Baseado em mapas genéticos publicamente disponíveis (Lawrence, C. et al. (2004) NAR 32: 393-397; banco de dados de milho na internet) e na sequência de genoma extraída de milho, o locus de Zp15 sobre o braço curto do cromossomo 6 foi escolhido como um alvo para modificação usando ZFNs baseado em localização e informação disponível sobre o gene Zp15. A estrutura e sequência genômica de um gene que codifica beta zeína de 15 kD (Zp15) de milho foram descritas e anotadas no domínio público (Woo et al. (2001) Plant Cell 13(10): 22972313). A sequência para o gene Zp15 é descrita no número de acesso ao GenBank AF371264, o qual é incorporado aqui por referência.
[00160] A sequência genômica do Zp15 foi usada como "query" em bancos de dados de genoma TIGR e Maize GDB usando algoritmos BLAST. Várias sequências com homologia de sobreposição ao Zp15 incluindo, mas não limitado a, dois contigs (AZM5_16782 e ZmGSStuc11- 12-04.8785.1) e vários ESTs (M72708, M13507, M12147, AY103640 e AF371264) foram identificados. Baseado na sequência desses acessos, bem como na sequência do Zp15, múltiplos oligonucleotídeos curtos foram projetados para uso como iniciadores de PCR usando o programa Primer3 (Rozen, S. e Skaletsky, H.J. (2000) Primeri on the WWW for general users and for biologist programmers. Em: Krawetz S, Misener S (eds.) Bioinformatics Methods and Protocols: Methods in Molecular Biology. Humana Press, Totowa, NJ, páginas 365-386; também disponível na internet).
[00161] Esses iniciadores incluem, mas não estão limitados a, os seguintes oligonucleotídeos na orientação para frente: PÓ7F 5T -CGTATGAATTCATTGACAACC-3* (SEQ ID NO: 1) P68F 5’ - ATGATCTATCTGTAAATCC - 3* (SEQIDNO:2) P69F 5 ’ - CGTC ATGC A ACGC A AC ATTCC - 3 ’ (SEQ ID NO:3) P73F 5’ -AAGAACATCACAAGTTATGC-3’ (SEQ ID NO >4) P74F 51 -TCATGTGGATCCAAGGCATC-3’ (SEQ1DNO:5)
[00162] Além disso, os iniciadores incluem, mas não estão limitados a, os seguintes oligonucleotídeos na orientação reversa: P70R 5’ - ATGTGTGTCGTCTTACTGC - 3“ (SEQIDNO:ó) P71R 5* -CAGTAGTAGGGCGGAATG-3’ (SEQ ID NO: 7) P72R 5’-GGGCAGCTGGTACTG-r (SEQIDNO:£) P75R 5’ - CTATAATCGATGTAGAGC - 3* (SEQ ID NO:9) P76R 5’ - CTATGCTTTGTCTATAGTCG - 3' (SEQ ]D NO: 10)
[00163] Todos os iniciadores de oligonucleotídeo foram sintetizados por e adquiridos da Integrated DNA Technologies (IDT, Coralville, LA). Amplificações de gDNA da variedade de milho Hi-II foram realizadas sobre um PCR Thermal Cycler usando 30 ng de gDNA. Um fragmento de amplificação de 2.215 bp, correspondendo ao gene Zp15 de Hi-II, foi isolado e clonado no plasmídeo pCR2.1 (Invitrogen, Carlsbad, CA). Análise de sequência desse fragmento revelou que a estrutura genômica de Zp15 da variedade de milho Hi-II contém dois éxons e um pequeno íntron de 31 bp (SEQ ID NO: 126). Designs para ZFN objetivada ao Zp15 são focalizados sobre as regiões de codificação do gene Zp15 da variedade de milho Hi-II. Exemplo 2: Design de Nucleases de Dedo de Zinco Objetivadas ao Gene Zp15 de Milho
[00164] De forma a montar vetores de expressão para ZFNs, um esquema de clonagem modular em etapas foi projetado o qual é aplicável para qualquer determinado par de genes que codificam ZFN selecionados do arquivo de biblioteca ou sintetizados de novo.
[00165] ZFNs objetivadas ao Zp15, primeiro, sofreram triagem usando a triagem por ensaio com levedura conforme descrito em Doyon et al. (2008) Nature Biotechnology 26(6): 702 e Pedido de Patente U.S. No. 12/284.887. Resumidamente, todo o locus de Zp15 foi introduzido no locus HO no genoma de levedura de forma a comparar diretamente a atividade de ZFN em diferentes sítios de ligação dentro do gene-alvo; ZFNs sofreram triagem quanto à sua capacidade de induzir a DSB no gene repórter usando um ensaio repórter (MEL1), conforme descrito em Doyon et al.
[00166] Baseado nos resultados desses ensaios de sistema proxy, foi confirmado que vários pares de ZFN testados eram capazes de induzir a DSBs dentro do Zp15.
[00167] Após pré-triagem de levedo, os pares de ZFN foram, então, subclonados em vetores de expressão de milho específicos. Conforme descrito na Publicação de Patente U.S. No. 20080182332, um vetor incluindo segmentos reprojetados e sintetizados de um sinal de localização nuclear (NLS) derivado do domínio de nuclease op-2 e Fokl de milho utilizando a tendência de códon para milho foi modificado com uma única inserção de nucleotídeo (C) a jusante do sítio Xho I único para criar um sítio Sac I extra. Um vetor similar foi modificado para incluir a sequência ribossômica 2A do vírus Thosea asigna. Os cassetes gênicos que codifi- cam ORFs de proteínas do dedo de zinco individuais foram clonados em qualquer um desses vetores via sítios de restrição Kpn I e BamH I e sub-sequentemente os dois vetores foram combinados via sítios de restrição Bgl IV - Xho I, proporcionando um construto intermediário que continha um cassete incluindo 2 domínios de codificação de ZFN flanqueados por sítios de restrição Nco I e Sac I.
[00168] O cassete Nco VSac I dessa construção intermediária foi exci- sado via digestão com enzima de restrição e ligado na parte principal de plasmídeo pDAB3872, o qual contém um promotor do gene de ubiquitina- 1 de milho (Sharrock et al. (1992) Plant Mol Biol. 18(4): 675) e sequências terminadoras do gene de peroxidase catiônica raiz de milho preferencial (Patente US No. 7.179.902).
[00169] Os plasmídeos resultantes incluem os genes de ZFN, mais os marcadores selecionáveis relevantes para manutenção de plasmídeo e sítios de flanqueamento attL para manipulação conveniente usando o sistema GATEWAY™ da Invitrogen (Carlsbad, CA). Cada um dos construtos de ZFN gerados usando esse esquema de clonagem foi transformado em células DH5a de E. coli e subsequentemente mantidos sob a seleção apropriada.
[00170] A Tabela 1 mostra ZFNs objetivadas ao Zp15 exemplificativas que foram usadas para experimentos de integração objetivada no locus de Zp15. A sequência de DNA-alvo para a ZFN é mostrada na segunda coluna (sítios-alvo de DNA indicados em letras maiúsculas; nucleotídeos não contatados indicados em letras minúsculas) e as terceira à sexta coluna mostram a sequência de aminoácido da região de reconhecimento (aminoácidos =1 a +6, com relação ao início da hélice) de cada um dos dedos de zinco (F1 a F4) na proteína. Também fornecido na primeira coluna da Tabela 1 é um número de identificação para cada proteína. Tabela 1
[00171] Será evidente que ZFNs podem ser prontamente inseridas em partes principais de C2H2 ou C3H e que uma variedade de sequências pode ser usada para unir a proteína de dedo de zinco e o domínio de clivagem. Vide Publicação de Patente U.S. 20080182332, particularmente Tabela 6, com relação a tais sequências, referência a qual é incorporada aqui por referência na íntegra. Exemplo 3: Ruptura ZFN-mediada de Zp15 em células de milho
[00172] Indução de DSB por pares de ZFN foi testada. Pares de ZFN que são capazes de produção eficiente de DSB no sítio-alvo pretendido do gene Zp15 endógeno foram identificados. A natureza propensa a erro de reparo DSB através de união terminal não homóloga (NHEJ), a qual é conhecida por gerar pequenas deleções/inserções de DNA no local de uma ruptura induzida por ZFN, foi utilizada para selecionar pares de ZFN os quais se ligam e clivam eficientemente o sítio-alvo do gene Zp15 endógeno.
[00173] ZFNs foram transitoriamente expressas em células de milho cultivadas e análise de sequência do locus alvo no sítio de clivagem previsto foi conduzida. Por exemplo, um plasmídeo pDAB7468 que codifica o par de ZFN # 25 (11768/11766 hélices de reconhecimento mostradas acima) foi distribuído via transformação WHISKERS™-mediada em culturas de célula de milho Hi-II, conforme descrito no Pedido de Patente U.S. No. 12/001.939, o qual é incorporado aqui por referência na íntegra. Após 24 ou 72 horas de expressão transitória, a sequência-alvo de ZFN rompida resultante foi amplificada do DNA genômico isolado e clonada no vetor de plasmídeo pCR2.1. O gDNA foi submetido à digestão por restrição usando a enzima Bsu361, seguido por amplificação da sequência-alvo de Zp15 e clonagem dos produtos de PCR no vetor de plasmídeo pCR2.1. Colônias individuais do produto da amplificação clonado foram analisadas por meio de digestões por restrição do DNA de plasmídeo, seguido por eletroforese em gel de agarose (produtos da amplificação clonados que mostraram resistência à clivagem pela enzima de restrição Bsu361 foram considerados como contendo mutações que destroem o sítio de restrição associado ao sítio de clivagem de ZFN).
[00174] Análise de sequência direta de 192 clones revelou uma inserção de 6 bp (Figura 1). Em outro exemplo, o plasmídeo pDAB7467 que codifica o par de ZFN # 24 (11753 /11750 hélices de reconhecimento mostradas acima) foi distribuído diretamente em culturas de célula de milho e, após 24 ou 72 horas de expressão transitória, a sequência-alvo de ZFN foi amplificada e clonada no vetor de plasmídeo pCR2.1. Análise de sequência direta de 192 clones revelou uma deleção de 3 bp (Figura 2) no sítio de clivagem preciso. A inserção e deleção descritas aqui são o início de reparo NHEJ de um DSB induzido no sítio-alvo e indica que as ZFNs 24 e 25 têm atividade de clivagem no locus de Zp15 endógeno em células de milho.
[00175] O mesmo processo foi realizado usando ZFN 25 ou 28, mas antes de triagem de colônias através de digestão com enzima de restrição, 192 clones independentes foram diretamente sequenciados. Uma inserção de 6 bp foi detectada (Figura 2, superior).
[00176] Tomados juntos, esses dados demonstram que uma exposição transitória a ZFNs é insuficiente para induzir a um DSB objetivado no locus de Zp15 em células de milho cultivadas. Exemplo 4: Integração Objetivada no locus de Zp15
[00177] De forma a testar se ZFNs projetadas com atividade em Zp15 poderiam acionar a integração de sequências exógenas, foram construídas moléculas de DNA doadoras trazendo um cassete gênico autônomo que codifica um gene de resistência a herbicida exógeno exemplificativo, AAD-1 de Sphingomonas herbicidovorans (ATCC 700291). AAD-1 codifica a enzima dioxigenase de arilóxi alcanoato e confere resistência a herbicidas de ariloxifenóxi propionato (Patentes Internacionais WO 2005/107437, WO2008141154 A2). Aqueles versados no campo apreciarão que outros ácidos nucleicos exógenos poderiam ser similarmente incorporados em moléculas doadoras de DNA incluindo, mas não limitado a, outros genes de tolerância a herbicida, tal como o gene AAD-12 relacionado. Nesse doador de gene de tolerância a herbicida, a sequência promotora é derivada de actina de O. sativa (números de acesso ao GenBank S44221 e X63830) e sequências terminadoras são derivadas de lipase de Z. mays (Número de Acesso ao GenBank L35913). A. Construção de Molécula de DNA Doadora
[00178] Construtos doadores contendo regiões de homologia ao Zp15 foram gerados como segue. Uma parte principal de plasmídeo contendo flancos de homologia para o gene Zp15 foi manipulada para permitir a integração de qualquer sequência de DNA doadora no sítio-alvo correspondente do gene Zp15. A parte principal de plasmídeo exemplificada aqui se originou com o vetor de plasmídeo de base fagemídeo pBC SK(-) (3,4 kbp) (Stratagene, La Jolla, CA). Houveram quatro etapas nesse processo.
[00179] Primeiro, o plasmídeo de base foi preparado linearizando 3 μg de pBC SK(-) usando as endonucleases de restrição Spe I e Sal I (New England Biolabs, Beverly, MA). O vetor de subclonagem de 3,3 kbp digerido com Spe I/Sal I, pBC SK(-), foi excisado em gel e purificado de acordo com as orientações do fabricante usando o kit QIAQUICK Gel Extraction (QIAGEN Inc., Valencia, CA).
[00180] Segundo, os flancos de 5'- & 3'-homologia foram isolados do Zp15 usando os seguintes iniciadores de oligonucleotídeo, que foram sintetizados pela Integrated DNA Technologies, Inc. (Coralville, IA): ZplSHRDoador NotI(2O5)F: 5’- GCGCHXGCATGCAAGAGCTGTTGATC -3’ (SEQ ID NO:97) MH Doador Mlul; lU/' ,.R- ?■- CAATTGCCGGCGTAGTAGGGCGCCGCCGCCAGC -3’ (SEQ [D NQ:98) /r15lll{Doador : .V- CAATTGGTGTGGGCAGCCGAGCGCCATGTTCCAG - 3’ (SEQ ID NO:99) /r15ll|ÍDoador S.ili22^JlK V GTCGACCGATACTGATGCGGACCGTCCACCrTGTC - 3’ (SEQ ID NO: 100).
[00181] Reações de amplificação por PCR foram realizadas usando reagentes fornecidos com o kit LA TAQ PCR (TaKaRa Biotechnology Inc. Otsu, Shiga, Japão). O coquetel de reação de PCR consistia em: 5 uL de 10X Tampão LA PCR™ II (Mg2+), 20 ng de molde de fita dupla (DNA ge- nômico de milho Hi-II), 10 pmol de iniciador de oligonucleotídeo para a frente, 10 pmol de iniciador de oligonucleotídeo reverso, 8 uL de mistura de dNTP (2,5 mM cada dNTP), 33,5 uL de H2O, 0,5 uL (2,5 unidades) de DNA Polimerase TaKaRa LA Taq™, 1 gota de óleo mineral. Os iniciadores Zp15HRDoadorNotI(205)F e Zp15HRDoadorMfeI(1025)R foram usados para uma reação e os iniciadores Zp15HRDoadorMfeI(1025)F e Zp15HRDoadorSalI(2270)R foram usados para a segunda reação. Reações de PCR foram realizadas usando um Perkin-Elmer Cetus, 48- Sample DNA Thermal Cycler (Norwalk, CT) sob as seguintes condições de ciclo: 94°C, 4 min/1 ciclo; 98°C, 20 seg, 65°C, 1 min, 68°C, 1 min/30 ciclos; 72°C, 5 min/1 ciclo; 4°C/manutenção.
[00182] Quinze (15) μL de cada reação de PCR foram submetidos à eletroporação e os fragmentos amplificados foram visualizados com luz UV e os tamanhos de fragmento estimados por meio de comparação com "ladder" de DNA de 1 kbp. Clones de plasmídeo esperados foram diagnosticados pela presença de fragmentos de DNA de 825 bp para o 5'- fragmento ou 1.250 bp para o 3'-fragmento. Esses fragmentos foram ex- cisados em gel e purificados de acordo com as orientações do fabricante usando o kit QIAquick Gel Extraction (QIAGEN Inc., Valencia, CA). Fragmentos purificados foram, então, clonados no plasmídeo pCR2.1 usando o kit TOPO TA CLONING® e transformados em células de E. coli quimicamente competentes ONE SHOT® TOP 10 (Invitrogen Life Technologies, Carlsbad, CA) de acordo com o protocolo do fabricante.
[00183] Colônias individuais contendo o fragmento 5' de 825 bp ou o fragmento 3' de 1.250 bp foram identificadas e confirmadas via digestão com enzima de restrição e dados de sequenciamento. Colônias contendo o fragmento 5' de 825 bp foram confirmadas via uma digestão com enzima de restrição Mfe I e Not I (New England Biolabs, Beverly, MA). Colônias contendo o fragmento 3' de 1.250 bp foram identificadas e confirmadas via digestão com enzima de restrição usando Sal I (New England Biolabs, Beverly, MA). Clones de plasmídeo esperados foram diagnosticados pela presença de fragmentos de DNA inseridos de 825 bp (5'-fragmento) ou 1.250 bp (3'-fragmento), além do vetor pCR®2.1 de 3,9 kbp. Reações de sequenciamento de fita dupla dos clones de plasmídeo foram realizadas conforme descrito pelo fabricante usando o kit CEQ™ DTCS-Quick Start (Beckman-Coulter, Palo Alto, CA). As reações foram purificadas usando Performa DTR Gel Filtration Cartridges (Edge BioSystems, Gaithersburg, MD), conforme descrito pelos protocolos do fabricante. Reações de sequência foram analisadas sobre um Beckman-Coulter CEQ™ 2000 XL DNA Analysis System e caracterização de nucleotídeo realizada usando um SEQUENCHER™ versão 4.1.4 (Gene Codes Corporation, Ann Arbor, MI). As sequências de fragmentos de 5'- e 3'-homologia de Zp15 são indicadas em SEQ ID NO: 127 e SEQ ID NO: 128.
[00184] Terceiro, o flanco de 3'-homologia foi ligado no plasmídeo de base, como segue. Clones que continham a sequência do flanco de 3'- homologia correta foram digeridos com enzimas de restrição e um fragmento de DNA foi excisado em gel e purificado usando o kit QIAquick Gel Extraction (QIAGEN Inc., Valencia, CA). Esses fragmentos foram ligados em um plasmídeo de base purificado, previamente digerido com Spe I/Sal I (vide acima), em uma proporção de vetor:inserto de 1:5 usando 500 unidades de DNA Ligase T4 (Invitrogen Life Technologies, Carlsbad, CA) em um volume de reação de 20 uL sob condições de incubação de 16 horas em um banho de água a 16°C. Cinco (5) uL da reação de ligação foram subsequentemente transformados em células de E. coli quimicamente competentes One SHOT® Top 10 (Invitrogen Life Technologies, Carlsbad, CA) e colocados sobre meios contendo seleção por antibiótico. Colônias putativas foram isoladas e digeridas com as enzimas de restrição Spe I e Sal I (New England Biolabs, Beverly, MA) para identificar clones os quais continham o fragmento 3' ligado.
[00185] Quarto, o flanco de 5'-homologia foi ligado no plasmídeo contendo o flanco de 3'-homologia. O plasmídeo contendo o flanco de 3'- homologia, descrito na etapa três acima, foi digerido com endonucleases de restrição Mfe I e Not I (New England Biolabs, Beverly, MA) durante 1 hora a 37°C. O plasmídeo digerido com Not I/ Mfe I contendo o flanco de 3' -homologia foi excisado em gel e purificado de acordo com as orientações do fabricante usando o kit QIAquick Gel Extraction (QIAGEN Inc., Valencia, CA).
[00186] Fragmentos isolados do doador de flanco de 5'-homologia gerados através de digestão com enzima de restrição usando as enzimas de restrição Mfe I e Not I foram produzidos e ligados com o plasmídeo contendo o flanco de 3'-homologia em uma reação de ligação de 20 μL usando uma proporção de vetor:inserto de 1:5 e 500 unidades de DNA Ligase T4 (Invitrogen Life Technologies, Carlsbad, CA). As reações de ligação foram incubadas durante 16 horas em um banho de água a 16°C.
[00187] Após a ligação, 5 μL da reação de ligação foram transformados em células DH5a™ Quimicamente Competentes MAX EFFICIENCY® (Invitrogen Life Technologies, Carlsbad, CA), conforme as recomendações do fabricante. Colônias individuais foram selecionadas e DNA de plasmídeo foi isolado e digerido com a enzima de restrição Not I (New England Biolabs, Beverly, MA) para identificar plasmídeos os quais continham um fragmento integrado do doador do flanco de 5'-homologia. Ao plasmídeo resultante foi fornecido o nome pDAB7489 (Figura 3).
[00188] Um cassete de expressão de gene de tolerância a herbicida compreendendo uma unidade transcricional de planta (PTU) contendo promotor, gene de tolerância a herbicida e sequências de término de po- liadenilação (poliA) foi construído. A sequência promotora é derivada de actina 1 de O. sativa (McElroy et al. (1990) Plant Cell 2, 163-171; Acesso ao GenBank S44221 e Acesso ao GenBank X63830). O gene de tolerância a herbicida compreendia o gene AAD-1 (dioxigenase de arilóxi alca- noato), o qual confere resistência a herbicidas de ariloxifenóxi propionato (WO 2005/107437). A versão do gene utilizada foi a versão #3, a qual inclui uma sequência códon-otimizada para expressão em plantas. As sequências terminadoras são derivadas de lipase de Z. mays (clone de cDNA de lipase de milho com Número de Acesso ao GenBank L35913). Essa sequência de milho compreende a região não traduzida 3'/região de término de transcrição para o gene AAD-1. O cassete de expressão de gene de tolerância a herbicida é mostrado na Figura 4.
[00189] Para gerar esse cassete, os seguintes iniciadores de oligonu- cleotídeo foram sintetizados pela Integrated DNA Technologies, Inc. (Co-ralville, LA) sob condições de dessalinização padrão e diluídos com água para uma concentração de 0,125 μg/uL: OsActAüd 1 vJZmLipMfelF 5’ - CAATTGGTCATTCATATGCTTGAGAAGAG - 3’ (SEQIDNO: 101) Os Ac t Aad 1 vJZmLipMfeJR 5 ’ - C AATTG AGC ACTT A A AG ATCTTT AG A AG - 3’ (SEQ ID NO: 102)
[00190] Reações de amplificação por PCR foram realizadas usando o kit LA TAQ PCR (TaKaRa Biotechnology Inc., Otsu, Shiga,, Japão). O coquetel de reação de PCR compreendia: 5 uL de 10X Tampão LA PCR™ II (Mg2+), 20 ng de molde de fita dupla (DNA de plasmídeo pDAB3878), 10 pmol de iniciador de oligonucleotídeo para a frente, 10 pmol de iniciador de oligonucleotídeo reverso, 8 uL de mistura de dNTP (2,5 mM cada), 33,5 uL de H2O, 0,5 uL (2,5 unidades) de DNA Polimerase TaKaRa LA Taq™, 1 gota de óleo mineral. As reações de PCR foram realizadas usando um Perkin-Elmer Cetus, 48-Sample DNA Thermal Cycler (Norwalk, CT) sob as seguintes condições de ciclo: 94°C, 4 min/1 ciclo; 98°C, 20 seg, 55°C, 1 min, 68°C, 3 min/30 ciclos; 72°C, 5 min/1 ciclo; 4°C/manutenção. Quinze (15) μL de cada reação de PCR foram submetidos à eletroforese a 100 V durante 1 hora em géis de agarose TAE a 1,0% suplementados com brometo de etídio a 0,5%. Fragmentos amplificados foram visualizados com luz UV e o tamanho do fragmento estimado por meio de comparação com o "ladder" de DNA de 1 kbp.
[00191] Produtos de PCR esperados foram diagnosticados pela presença de um fragmento de DNA de 2,7 kbp (AAD-1 PTU). Esse fragmento foi excisado em gel e purificado de acordo com as orientações do fabricante usando o kit QIAquick Gel Extraction (QIAGEN Inc., Valencia, CA). Fragmentos purificados foram, então, clonados no plasmídeo pCR2.1 usando o kit TOPO TA Cloning® (com o vetor pCR®2.1) e células de E. coliquimicamente competentes One Shot® TOP 10 (Invitrogen Life Technologies, Carlsbad, CA) de acordo com o protocolo do fabricante.
[00192] Colônias individuais foram selecionadas, DNA de plasmídeo foi isolado e digerido com a enzima de restrição Mfe I (New England Biolabs, Beverly, MA). Clones de plasmídeo esperados foram diagnosticados pela presença de um fragmento de DNA inserido de 2.674 bp (AAD-1 PTU), além do vetor pCR®2.1 de 3,9 kbp. Reações de sequenciamento de fita dupla de clones de plasmídeo foram realizadas conforme descrito pelo fabricante usando o kit CEQ™ DTCS-Quick Start (Beckman-Coulter, Palo Alto, CA). As reações foram purificadas usando Performa DTR Gel Filtration Cartridges (Edge BioSystems, Gaithersburg, MD), conforme descrito pelos protocolos do fabricante. Reações de sequência foram analisadas sobre um Beckman-Coulter CEQ™ 2000 XL DNA Analysis System e caracterização de nucleotídeo realizada usando o SEQUENCHER versão 4.1.4 (Gene Codes Corporation, Ann Arbor, MI).
[00193] O fragmento restrito de um clone que continha a sequência de 2.674 bp correta foi excisado em gel e purificado de acordo com as orientações do fabricante usando o kit QIAquick Gel Extraction (QIAGEN Inc., Valencia, CA). Esse fragmento foi, então, combinado em uma reação de ligação com pDAB7489 purificado (parte principal de plasmídeo) o qual tinha sido digerido com a enzima de restrição Mfe I e subsequentemente desfosforilado. Ligação foi realizada sob as seguintes condições: proporção de vetor:inserto de 1:5 e 500 unidades de DNA Ligase T4 (Invitrogen Life Technologies, Carlsbad, CA) em um volume de reação de 20 uL sob condições de 16 horas de incubação em um banho de água a 16°C. Cinco (5) uL da reação de ligação foram subsequentemente transformados em células E. coliMAX EFFICIENCY® DH5a™ quimicamente competentes (Invitrogen Life Technologies, Carlsbad, CA) e colocados em lâminas sob condições de seleção descritas pelo fabricante.
[00194] Colônias individuais foram selecionadas, DNA de plasmídeo foi isolado e digerido com a enzima de restrição Mfe I (New England Biolabs, Beverly, MA). Os clones de plasmídeo esperados continham fragmentos de DNA de 2.674 bp (AAD-1 PTU) e 5.413bp (vetor pDAB7489). O plasmídeo resultante foi denominado pDAB7490 (Figura 5).
[00195] Culturas de célula embriogênica da variedade de milho Hi-II (Armstrong et al (1991) Maize Genet Crop Newsletter 65: 92-93) foram geradas, mantidas e submetidas à simultânea transformação de plasmí- deos que codificam ZFN24 e a molécula doadora pDAB7490. A transformação e seleção de tecido de caule e subsequente regeneração de transformantes são descritas no Pedido de Patente U.S. No. 12/001.939, referência a qual é incorporada aqui por referência na íntegra. Para orientação adicional com relação a protocolos de transformação e seleção vide Petolino et al. (2000) Plant Cell Rept. 19: 781-786. Após antese, as plantas foram autopolinizadas ou cruzadas com a variedade de milho DAS5XH751. Semente de prole resultante foi colhida e seca. A regeneração de caule em plantas de milho férteis intactas é descrita no Pedido de Patente U.S. No. 12/001.939, particularmente Exemplo 22, referência a qual é aqui incorporada por referência na íntegra. B. Integração objetivada do cassete do gene AAD-1 no locus de Zp15
[00196] Dos eventos tolerantes a herbicida contendo uma molécula de DNA doadora integrada que codifica um cassete gênico de tolerância a herbicida, espera-se que alguma proporção dos referidos eventos seja o produto de integração objetivada de DNA doador no sítio de ruptura de fita dupla induzida por ZFN. De forma a diferenciar esses eventos de in tegração objetivada daqueles derivados de integração aleatória do cassete gênico de tolerância a herbicida, uma estratégia de genotipificação baseada em PCR usando uma combinação de iniciadores de PCR genoma- específicos e subsequentemente genoma-específicos mais doador- específicos foi utilizada.
[00197] Genotipificação diferencial de integração objetivada versus aleatória do transgene AAD-1 em todos os eventos transformados tolerantes a herbicida foi realizada usando ensaios de PCR específicos ao locus de Zp15 e ao gene AAD-1. Nos exemplos apresentados aqui, todos os iniciadores de oligonucleotídeo foram sintetizados pela Integrated DNA Technologies, Inc. (Coralville, LA) sob condições de dessalinização padrão e diluídos com água até uma concentração de 100 μM. O conjunto a seguir de iniciadores de oligonucleotídeo para a frente e reverso foi projetado para se anelar a sequências de gDNA específicas para o gene Zp15 alvo que reside fora dos limites das sequências de DNA doadoras: HB501f: 5’- AAGGTCCCAAATCTGAGGCATACTGTTGCT -3’ (SEQ ID NO: 103) HB502T; S’- GAGGTCCTATGCTTTGTCTATAGTCGGCAG -35 (SEQ ID NO;104)
[00198] Um segundo conjunto de iniciadores de oligonucleotídeo para a frente e reverso foi também criado para se anelar à sequência de gDNA específica para o gene-alvo Zp15 fora dos limites das sequências doadoras de DNA, ainda que agrupadas dentro do primeiro par: HB503 f5F- GGCATACTGTTGCTGCCCTGCTGGAA -3’ (SEQ TD NO: 105) HB504r 5’- GACACCTATAATCGATGTAGAGCCGAAGAG -3’ (SEQ ID NO; 106)
[00199] Iniciadores de oligonucleotídeo para a frente e reverso foram adicionalmente criados para se anelar especificamente ao DNA doador correspondendo à região de codificação do gene de tolerância a herbicida AAD-1: HB5O5f 5’- AGTCCACCCCAGTGATCTCAGCACCA -3’ (SEQ ID NO: 107) HB506f S’- AGTGGCTGGACAGCTATTCTCTCAAAGCQT -3’ (SEQ ID NO: 108) HB5O7r 5’- ACGCTTTGAGAGAATAGCTGTCCAGCCACT -3’ (SEQ ID NO: 109) HB503r 5 TGGTGCTGAGATCACTGGGGTGGACT -3’ (SEQ ID NO: 110)
[00200] Duas reações de amplificação primária distintas foram realizadas utilizando iniciadores que se ligam à região genômica de Zp15 e à molécula doadora, dando origem a um amplicon que abrange o limite de integração entre o genoma e o doador. A primeira reação se focalizou sobre o limite 5'- entre o genoma e o doador e usou o conjunto de iniciadores HB501f e HB507r. A segunda reação se focalizou sobre o limite 3'- entre o doador e o genoma e usou o conjunto de iniciadores HB505f e HB502r. DNA genômico foi isolado dos eventos de milho Hi-II transformados. Reações de amplificação por PCR primária foram realizadas usando reagentes fornecidos com o kit LA TAQ PCR (TaKaRa Biotechnology Inc., Otsu, Shiga, Japão). O coquetel de reação de PCR consistia em: 2,5 μL de 10X Tampão La Taq PCR™, 40-200 ng de molde de DNA genômico fita dupla, iniciador de oligonucleotídeo para a frente a 10 μM, iniciador de oligonucleotídeo reverso a 10 μM, 2 μL de mistura de dNTP (2,5 mM cada), 16,25 μL de H2O, 0,25 μL (1,25 unidades) de DNA poli- merase LA Taq™. As reações de PCR foram realizadas usando um BioRad, 96-Sample DNA Engine Tetrad2, Peltier Thermal Cycler (Hercules, CA) sob as seguintes condições de ciclo: 94°C, 2 min/1 ciclo; 94°C, 30 seg, 62°C, 30 seg, 68°C, 5 min/30 ciclos; 4°C/manutenção.
[00201] Os produtos da reação de PCR primária foram subsequentemente diluídos a 1:100 em H2O e usados como molde de DNA para duas reações de PCR secundárias distintas. As reações secundárias também utilizam iniciadores que se ligam na região genômica de Zp15 e à molécula doadora, dando origem a um amplicon que abrange o limite de integração entre o genoma e o doador. A identidade dos iniciadores específicos determina se a amplificação está focalizada sobre o limite 5'- ou 3'- entre o genoma e o doador. A primeira reação se focalizou sobre o limite 5'- entre o genoma e o doador e usou o conjunto de iniciadores HB503f e HB508r. A segunda reação se focalizou sobre o limite 3'- entre o doador e o genoma e usou o conjunto de iniciadores HB506f e HB504r. Ambas as reações consistiam no seguinte: 2,5 μL de 10X Tampão La Taq PCR™, 1 μL de molde [diluição a 1:50 da 1a Reação de PCR], iniciador de oligonucleotídeo para a frente a 10 μM, iniciador de oligonucleotídeo reverso a 10 μM, 2 μL de mistura de dNTP (2,5 mM cada), 16,25 μL de H2O, 0,25 μL (1,25 unidades) de DNA polimerase LA Taq™. As reações de PCR foram realizadas usando um Bio-Rad, 96-Sample DNA Engine Tetrad2, Peltier Thermal Cycler (Hercules, CA) sob as seguintes condições de ciclo: 94°C, 2 min/1 ciclo; 94°C, 0 seg, 62°C, 30 seg, 68°C, 5 min/30 ciclos; 4°C/manutenção. Fragmentos de amplificação por PCR esperados de 2.180 bp para o limite 5'- ou 2.980 bp para o limite 3'- foram observados.
[00202] Esses fragmentos foram excisados em gel e purificados de acordo com as orientações do fabricante usando o kit QIAquick Gel Extraction (QIAGEN Inc., Valencia, CA). Fragmentos purificados foram subsequentemente clonados no plasmídeo pCR2.1 usando o kit TOPO TA CLONING® (com o vetor pCR®2.1) e células de E. coli quimicamente competentes ONE SHOT® TOP 10 (Invitrogen Life Technologies, Carlsbad, CA) de acordo com o protocolo do fabricante.
[00203] Clones individuais foram selecionados, DNA de plasmídeo foi isolado e digerido com a enzima de restrição Eco RI (New England Biolabs, Beverly, MA). Clones de plasmídeo esperados foram diagnosticados pela presença dos fragmentos de DNA inseridos de tamanho apropriado, além do vetor pCR®2.1 de 3,9 kbp.
[00204] Reações de sequenciamento de fita dupla dos clones de plasmídeo foram realizadas e caracterização e alinhamento de nucleotídeo foram realizados usando o SEQUENCHER™ versão 4.1.4 (Gene Codes Corporation, Ann Arbor, MI).
[00205] Dados de sequência selecionados derivados de um evento de integração objetivado (evento #147) do cassete gênico doador de AAD-1 inserido no gene alvo Zp15 são mostrados no alinhamento da Figura 6.
[00206] Produtos de PCR cuja amplificação primária se focalizou sobre o limite 5' ou 3' entre o genoma e o doador foram submetidos à amplificação secundária também focalizada sobre o limite 5'- ou 3'- entre o genoma e o doador. Alinhamento de fragmentos clonados correspondendo a esses produtos de amplificação secundária com a sequência genômica de Zp15 do tipo silvestre, bem como a sequência esperada de um evento de integração objetivada, indica claramente que a integração precisa de DNA doador no sítio-alvo ocorreu. A sequência de nucleotídeo do locus genômico de Zp15, do limite genoma/doador, sequência de nucleotídeo das regiões doadoras correspondendo a flancos de homologia ao Zp15 e a sequência de nucleotídeo do cassete de tolerância a herbicida foram todas preservadas em múltiplos produtos de PCR clonados derivados desse evento. Portanto, esse evento representa um genoma no qual o reparo homologia-acionado de uma ruptura de fita dupla mediada por ZFN e integração objetivada de um DNA doador em um alvo gênico específico ocorreram. Na Figura 6, foram mostrados dados de alinhamento de sequência derivados de um único caule de milho transformado isolado representativo (evento #147).
[00207] Eventos transformados adicionais que representam ocorrências de integração objetivada únicas foram obtidos, demonstrando que os métodos ensinados aqui são reproduzíveis em caule de milho. Exemplo 5: Integração objetivada de PAT no locus de Zp15
[00208] Como uma outra exemplificação de métodos para integração objetivada de polinucleotídeos exógenos selecionados em loci objetivados divulgados aqui, moléculas de DNA doadoras adicionais trazendo um cassete gênico autônomo que codifica PAT foram criadas e construídas para testar a integração de uma sequência doadora exógena dentro do lócus-alvo de Zp15 endógeno. ZFNs com atividade de clivagem específica do gene alvo Zp15 endógeno foram empregadas para criar um DSB nesse locus. Moléculas de DNA doadoras trazendo um cassete gênico autônomo que codifica PATde Streptomyces viridochromogenes e sequências de flanqueamento homólogas ao Zp15 foram subsequentemente integradas no DSB induzido por ZFN do alvo Zp15. O PAT codifica a enzima acetil transferase de fosfinotricina e confere resistência ao composto herbicida fosfinotricina (PPT) através de acetilação (Patente U.S. No. 5.633.434). a fosfinotricina é o ingrediente ativo dos herbicidas LIBERTY, BASTA e IGNITE. A sequência de codificação de PAT foi construída como uma unidade de transcrição de planta (Plant Transcription Unit - PTU) e continha uma sequência promotora derivada de actina de O. sativa (números de acesso ao GenBank S44221 e X63830) e uma sequência terminadora derivada de lipase de Z. mays (número de acesso ao GenBank L35913). A. Construção de molécula de DNA doadora
[00209] Um construto doador de Zp15 contendo regiões de homologia ao Zp15 foi gerado sinteticamente como segue. Uma região de homologia ao Zp15 compreendendo os nucleotídeos 4595-5346 (sequência de homologia 5'; SEQ ID NO: 111) e nucleotídeos 21-796 (sequência de homologia 3'; SEQ ID NO: 112) a partir do pDAB7489 foi projetado. Essa região de homologia incluía sítios de clonagem Mfe I entre os elementos 5' e 3' - homólogos e sítios de restrição Not I nas extremidades 5' e 3'. Essa sequência de DNA (SEQ ID NO: 113) foi sintetizada e inserida no plasmídeo do tipo ColE1 resistente à canamicina, pMK nos sítios de clonagem Sac I e Kpn I (Gene Art Ag, Regensburg, Alemanha). O plasmídeo doador resultante foi designado pDAB104101 (Figura 7) e contém flancos de homologia para o gene Zp15 a fim de permitir a integração de qualquer sequência de DNA de interesse no sítio-alvo correspondente do gene Zp15.
[00210] Um cassete de expressão de gene de tolerância a herbicida compreendendo um promotor contento PTU completo, gene de tolerância a herbicida e sequências de término de poliadenilação (poliA) foi construído. A sequência do promotor é derivada de actina 1 de O. sativa (McElroy et al. (1990) Plant Cell 2: 163-171). Acesso ao GenBank S44221 e Acesso ao GenBank X63830). O gene de tolerância a herbicida era o PAT. As sequências terminadoras são derivadas de lipase de Z. mays (clone de cDNA de lipase de milho com Número de Acesso ao GenBank L35913). Essa sequência de milho compreende a região de término de transcrição/região não traduzida 3' para o gene PAT. O cassete de expressão de gene PAT de tolerância a herbicida é mostrado na Figura 8.
[00211] O cassete do gene PAT foi amplificado de um plasmídeo pDAB102256 através de PCR usando iniciadores sintetizados pela Integrated DNA Technologies, Inc. (Coralville, IA): DC0015’- CCAGTGCA ATTGGGTCATTCATATGCTTGAGAAG - 3 ’ (SEQ [D NO: 114) DC002 5’ - CCAGTGCAATTGAATTCAGCACTTAAAGATCTTTAG -3’ (SEQID NO; 115)
[00212] Reações de amplificação por PCR foram realizadas usando DNA Polimerase PHUSION™ (New England Biolabs, Beverly, MA) sob as seguintes condições de ciclo: 98°C, 30 seg/1 ciclo; 98°C 10 seg, 60°C, 20 seg, 72°C, 45 seg/9 ciclos; 98°C, 10 seg, 72°C, 60 seg/24 ciclos; 72°C, 10 min/1 ciclo; 4°C/manutenção. A reação de PCR foi submetida à eletroforese em um gel de agarose TAE a 1,0%.
[00213] Produtos de PCR esperados foram diagnosticados pela presença de um fragmento de DNA de 2,3 kbp (PAT PUT). Esse fragmento foi excisado em gel e purificado de acordo com as orientações do fabricante usando o kit QIAquick Gel Extraction (QIAGEN Inc., Valencia, CA). Fragmentos purificados foram, então, clonados no vetor pCR-BluntII- TOPO usando o kit Zero Blunt TOPO PCR Cloning e células de E. coli quimicamente competentes One Shot® TOP 10 (Invitrogen Life Technologies, Carlsbad, CA) de acordo com o protocolo do fabricante.
[00214] Colônias individuais foram selecionadas e o DNA de plasmídeo foi isolado e submetido à digestão com enzima de restrição e análise de sequência. Os insertos de PAT clonados foram sequenciados para demonstrar a identidade e fidelidade de sequência dos produtos de PCR clonados (SEQ ID NO: 116). Um de tais plasmídeos foi designado pDAB104107 (Figura 9) e foi subsequentemente usado como a fonte do cassete do gene PAT para inserção nos novos vetores doadores de homologia de Zp15.
[00215] O fragmento do gene PAT de 2,3 kbp foi recuperado do pDAB104107 através de digestão com Mfe I, seguido por eletroforese em gel, excisão e purificação. O plasmídeo doador de homologia de Zp15, pDAB104101, foi também digerido com Mfe I e purificado em gel.Ligação do fragmento do gene PAT no pDAB104101 proporcionou clones nos quais o gene PATfoi inserido no sítio Mfe I em qualquer uma de duas orientações com relação às sequências do gene Zp15, conforme determinado por meio de digestão com enzima de restrição diferencial. O pDAB104104 (Figura 10) compreendia o gene PAT inserido na mesma orientação transcricional que o gene Zp15. O pDAB104105 (Figura 11) compreendia o gene PAT inserido na orientação oposta com relação ao gene Zp15. B. Construção de molécula de DNA doadora adicional
[00216] Outro construto doador contendo regiões de homologia ao Zp15 foi gerado, no qual a sequência de homologia 3' de Zp15 no pDAB7489 foi alterada por meio de truncamento, enquanto que a sequência de homologia 5' de Zp15 no pDAB7489 permaneceu a mesma.
[00217] A região de homologia 3' truncada foi gerada a partir do pDAB7489 através de PCR usando iniciadores sintetizados pela Integrated DNA Technologies, Inc. (Coralville, LA): DC003 5* - CTAATCGTCGACTCGTCAAGCCCCGCCTTTAAAT - 3’ (SEQ ID NO: 117} DC004 5’ - CTAATCCAATTGGTGTGGGCAGCCGAGCG - 3’ (SEQ ID NO: 118}
[00218] Reações de amplificação por PCR foram realizadas usando DNA Polimerase PHUSION HOT START (New England Biolabs, Beverly, MA) sob as seguintes condições de ciclo: 98°C, 30 s/1 ciclo; 98°C 10 seg, 72°C, 15 seg/33 ciclos; 72°C, 5 min/1 ciclo; 4°C/manutenção. A reação de PCR foi submetida à eletroforese em um gel de agarose TAE a 1,0%.
[00219] Produtos de PCR esperados foram diagnosticados pela presença de um fragmento de DNA de 0,8 kbp (homologia-3' de Zp15). Esse fragmento foi excisado em gel e purificado de acordo com as orientações do fabricante usando o kit QIAquick Gel Extraction (QIAGEN Inc., Valencia, CA). Fragmentos purificados foram, então, clonados no vetor pCR- BluntI I-TOPO usando o kit Zero Blunt TOPO PCR Cloning e células de E. coli quimicamente competentes One Shot® TOP 10 (Invitrogen Life Technologies, Carlsbad, CA) de acordo com o protocolo do fabricante.
[00220] Colônias individuais foram selecionadas e submetidas a isolamento de DNA de plasmídeo e confirmação por meio de digestão com enzima de restrição. Insertos de homologia 3' de Zp15 foram sequencia- dos para demonstrar a identidade e fidelidade de sequência dos produtos de PCR clonados (SEQ ID NO: 119). Um de tais plasmídeos foi designado pDAB104106 (Figura 12) e foi subsequentemente usado como a fonte da nova sequência de homologia 3' de Zp15 para substituição no pDAB7489 a fim de criar um novo vetor doador de homologia de Zp15.
[00221] pDAB7489 foi digerido sequencialmente com Mfe I e Sal I e o fragmento de vetor de 4,2 kbp foi purificado em gel. O pDAB104106 foi também digerido com Mfe I e Sal I e o fragmento de 0,8 kbp compreendendo a sequência de homologia 3' de Zp15 truncada foi purificado em gel. Ligação e transformação desses fragmentos purificados em gel proporcionaram clones nos quais a sequência de homologia 3' de Zp15 trun cada foi substituída pela sequência de homologia 3' de Zp15 original. Esse plasmídeo foi designado pDAB104100 (Figura 13) e foi usado como o recipiente para o gene PAT.
[00222] O gene PAT foi removido do pDAB104107 por meio de digestão com Mfe I. Após eletroforese em gel, o fragmento gênico de PATde 2,3 kbp foi purificado em gel. O plasmídeo doador de homologia de Zp15, pDAB104100, também foi digerido com Mfe I e purificado em gel. Ligação do gene PAT no pDAB104100 proporcionou clones nos quais o gene PAT estava inserido no sítio Mfe I em qualquer uma de duas orientações com relação ao gene Zp15, conforme determinado por meio de digestão com enzima de restrição diferencial. O pDAB104103 (Figura 14) compreendia o gene PAT inserido na mesma orientação transcricional que o gene Zp15. O pDAB104102 (Figura 15) compreendia o gene PAT inserido na orientação oposta com relação ao gene Zp15. C. Transformação de milho e recuperação de inserções Zp15 - PAT objetivadas
[00223] Culturas de célula embriogênica da variedade de milho Hi-II (Armstrong et al (1991) Maize Genet Crop Newsletter 65: 92-93) foram geradas, mantidas e submetidas à transformação simultânea de plasmí- deos que codificam ZFN24 e molécula doadora. Moléculas doadoras incluem aquelas descritas aqui; pDAB104102, pD AB 104103, pD AB 104104 e pD AB 104105. A transformação e seleção de tecido de caule e subsequente regeneração de transformantes são descritas no Pedido de Patente U.S. No. 12/001.939, particularmente Exemplo 19, referência a qual é aqui incorporada por referência na íntegra. Para orientação adicional com relação ao protocolo de transformação e seleção vide Petolino et al. (2000) Plant Cell Rept. 19: 781-786. Após antese, as plantas são au- topolinizadas ou cruzadas com uma variedade de milho, tal como DAS5XH751. A semente de prole resultante pode ser colhida e seca e plantas dessas sementes podem ser analisadas para demonstrar a here- ditariedade de eventos de integração objetivados. A regeneração de caule em plantas de milho férteis intactas é descrita no Pedido de Patente U.S. No. 12/001.939, particularmente Exemplo 22, referência a qual é aqui incorporada por referência na íntegra. D. Identificação de inserções de PAT Zp15-objetivadas
[00224] Inserções de PAT Zp15-objetivadas em tecido de caule transformado são detectadas através de PCR. Molde de DNA genômico é extraído do tecido de caule via métodos bem-conhecidos e comumente usados, tais como o kit Plant DNEASY (QIAGEN Inc., Valencia, CA) ou o método de Dellaporta (Dellaporta et al, (1983) Plant Mol. Biol. Rep. 1; 1921). Uso de iniciadores específicos para PAT em conjunto com os iniciadores de sequência de flanqueamento de Zp15 já usados para detectar integração objetivada de AAD-1 no locus de Zp15 resulta na amplificação das junções de inserção objetivada de PAT nas regiões de homologia 5' e 3' de Zp15. Os iniciadores específicos para PAT podem ser: DC013 5’ - CAATCGTA AGCGTTCCTAGCCTTCCAG - 3’ (SEQ ID NO: 120) DC014 5’ - CTGGAAGGCTAGGAACGCTTACGATTG -3’ (SEQ ID NO: 121)
[00225] Especificamente, iniciadores HB501f ou HB503f na região genômica que flanqueia o DNA doador da sequência de homologia 5' de Zp15 são usados em conjunto com o iniciador DC013 (SEQ ID NO: 120) na região de codificação da proteína PAT para detectar junções de inserção PAT-Zp15 5' quando os DNAs doadores têm o gene PAT na orientação direta com relação ao gene Zp15. Da mesma forma, os iniciadores HB501f ou HB503f são usados em conjunto com o iniciador DC014 (SEQ ID NO: 121) na região de codificação da proteína PAT para detectar junções de inserção PAT-Zp15 5' quando os DNAs doadores têm o gene PAT na orientação indireta com relação ao gene Zp15. Para detecção de junções de inserção PAT-Zp15 3', os iniciadores HB502r ou HB504r são usados em conjunto com o iniciador DC013 (SEQ ID NO: 120) para de- tectar junções de inserção quando os DNAs doadores têm o gene PAT na orientação indireta com relação ao gene Zp15. Da mesma forma, os inici-adores HB502r ou HB504r são usados em conjunto com o iniciador DC014 (SEQ ID NO: 121) para detectar junções de inserção PAT-Zp15 3' quando os DNAs doadores têm o gene PAT na orientação direta com relação ao gene Zp15.
[00226] Reações de amplificação por PCR foram realizadas usando DNA Polimerase PHUSION HOT START (New England Biolabs, Beverly, MA) sob as seguintes condições de ciclo: 98°C, 30 s/1 ciclo; 98°C 10 seg, 72°C, 15 seg/33 ciclos; 72°C, 5 min/1 ciclo; 4°C/manutenção. Os produtos de PCR foram decompostos e identificados usando eletroforese em gel de agarose TAE. Os tamanhos esperados de fragmento do gel para os produtos de PCR de eventos de integração objetivada PAT - Zp15 em caule transgênico gerados usando os diferentes DNAs doadores de PAT- Zp15 são como segue: HB501f/HB503f + DC013 (5') = 2,6 kbp (pDAB104103), 2,6 kbp (pDAB 104104) HB501f/HB503f + DC014 (5') = 1,6 kbp (pDAB104105), 1,7 kbp (pDAB 104102) HB502r/HB504r + DC013 (3') = 3,2 kbp (pDAB104105), 3,2 kbp (pDAB 104102) HB502r/HB504r + DC014 (3') = 1,2 kbp (pDAB104103), 1,2 kbp (pDAB 104104)
[00227] Os produtos de PCR compreendendo as junções de integração objetivada PAT- Zp15 5' e 3' são clonados e sequenciados usando métodos padrões conhecidos por aqueles versados no campo. Por exemplo, os produtos de PCR são purificados do gel de agarose e clonados no plasmídeo pCR-BluntII TOPO usando o kit TOPO BLUNT CLONING® e células de E. coliquimicamente competentes ONE SHOT® TOP 10 (Invitrogen Life Technologies, Carlsbad, CA) de acordo com o protocolo do fabricante.
[00228] As junções de integração clonadas são, então, sequenciadas para demonstrar que o gene PAT está inserido no genoma de milho no locus de Zp15 por meio de recombinação homóloga via as sequências de homologia de Zp15 5' e 3' que são incorporadas nos vetores de transformação doadores. Além do vetor TOPO, iniciadores específicos M13 para a frente e M13 reverso, iniciadores específicos ao cassete do gene PAT são usados para obter sequência completa dos clones de integração objetivados. Iniciadores de PCR SEQ ID NO: 120 e SEQ ID NO: 121, os quais são específicos à sequência de codificação da proteína PAT, também são usados como iniciadores de sequenciamento. Além disso, outros iniciadores também podem ser usados para sequenciamento. Esses incluem, mas não estão limitados a, aqueles que são específicos para o elemento promotor actina de arroz do cassete de PAT: DC-S1 51 -CCAACTGG AC AAT AGTCTCC AC-3 ’ (SEQ ID NO: 122) DC-S2 5* ’CATCGCCACTATATACATACC-3’ (SEQ ID NO: 123)
[00229] e aqueles que são específicos para a sequência de codificação da proteína PAT: DC-S 3 5 ’ -CGTCTC AATGT A ATGGTT A ACG-3 ’ (SEQID NO; 124) DC-S4 5* -GCCC AGCGT AAGC AAT ACC AG -3 ’ (SEQID NO: 125) Exemplo 6: Hereditariedade de integração objetivada de AAD-1 no locus de Zp15
[00230] Um evento com caule transgênico trazendo o cassete do gene AAD-1 objetivado ao locus de Zp15 foi gerado (Evento 138). Plantas TO do Evento 138 foram regeneradas e cruzadas como fêmeas com os machos DAS5XH751. Sementes T1 resultantes foram plantadas e plantas T1 foram crescidas.
[00231] Plantas T1 foram analisadas através de PCR para demonstrar a ocorrência da integração objetivada AAD-1 - Zp15. Reações de amplificação por PCR foram realizadas usando DNA Polimerase PHUSION HOT START (New England Biolabs, Beverly, MA) sob as seguintes condições de ciclo: 98°C, 30 s/1 ciclo; 98°C 10 seg, 72°C 15 seg/33 ciclos; 72°C, 5 min/1 ciclo; 4°C/manutenção. As reações de PCR foram analisadas através de eletroforese em géis de agarose TAE a 1,0%. DNA genô- mico foi extraído de uma planta Ti e usado como molde de DNA em reações de PCR com iniciadores agrupados criados para detectar a junção de integração AAD-1 / Zp15 5'. Reações de PCR primárias e secundárias foram conduzidas usando os mesmos iniciadores usados antes na análise do evento 147 com caule. Para PCR primária, os iniciadores HB501f e HB507r foram usados. PCR primária proporcionou uma banda no tamanho esperado de 2,2 kbp. Uma alíquota da reação de PCR primária foi diluída a 1:100 e usada como molde em PCR secundária usando iniciadores agrupados HB503f e HB508r. PCR secundária também proporcionou uma banda no tamanho esperado de 2,2 kbp.
[00232] O produto de PCR secundário de 2,2 kbp foi clonado no pCR- BluntII-TOPO usando o kit ZERO BLUNT TOPO PCR Cloning e células de E. coliquimicamente competentes ONE SHOT TOP 10 (Invitrogen Life Technologies, Carlsbad, CA) de acordo com o protocolo do fabricante. O DNA clonado foi sequenciado usando iniciadores específicos ao vetor de flanqueamento (M13 para a frente e M13 reverso). Descobriu-se que a sequência era idêntica àquela esperada para uma integração objetivada de AAD-1 no locus de Zp15.
[00233] Todas as patentes, pedidos de patente e publicações mencionados aqui são incorporados por referência na íntegra para todas as finalidades.
[00234] Embora divulgação tenha sido fornecida em alguns detalhes à guisa de ilustração e exemplo para fins de clareza de compreensão, será evidente para aqueles versados no campo que várias alterações e modi-ficações podem ser praticadas sem se desviar do espírito ou escopo da divulgação. Consequentemente, as descrições e exemplos precedentes não deverão ser construídos como limitativos.
Claims (13)
1. Método de integração de uma ou mais sequências de ácido nucleico exógenas no genoma de uma célula vegetal, caracterizado pelo fato de que compreende: transformar a célula vegetal com um ou mais polinucleotídeos que codificam uma nuclease que produz uma clivagem de fita dupla no genoma da célula vegetal em um locus beta zein de15kD Zp15 (Zp15), a nuclease compreendendo um domínio de ligação de dedo de zinco que se liga a um sítio alvo no locus Zp15, o domínio de ligação de dedo de zinco compreendendo 4 dedos de zinco ordenados e designados F1 a F4, cada dedo de zinco compreendendo uma região de reconhecimento, em que as regiões de reconhecimento do domínio de ligação de dedo de zinco e o sítio alvo são mostrados em linhas individuais da Tabela a se guir:
resultando assim na in tegração de um polinucleotídeo com- preendendo uma ou mais sequências exógenas no genoma da célula no ou próximo ao locus Zp15, em que a planta obtida com o referido método é excluída da proteção.
2. Método, de acordo com a reivindicação 1, caracterizado pelo fato de que compreende ainda expressar um produto da uma ou mais sequências exógenas.
3. Método, de acordo com a reivindicação 1 ou 2, caracterizado pelo fato de que a clivagem de fita dupla é feita por meio de: (a) transformar a célula vegetal com um vetor de expressão compreendendo uma sequência que codifica uma primeira proteína de fusão na célula, a primeira proteína de fusão compreendendo o primeiro domínio de ligação de dedo de zinco compreendendo 4 dedos de zinco ordenados e designados de F1 a F4, cada dedo de zinco compreendendo uma região de reconhecimento, em que o domínio de ligação de dedo de zinco é selecionado a partir do grupo que consiste em um domínio de ligação de dedo de zinco designado 11742, 11743, 11750, 11753, 11754, 11755, 11756, 11757, 11758, 11759, 11760, 11761, 11762, 11763, 11766, 11767, 11768, 11769, 11770 , 11771, 11772, 11773, 11774, 11775, 11776, 11777, 11778, 11779, 11780, 11781,11782, 11783, 11784 e 11785 conforme estabelecido na Tabela a seguir:
e um primeiro meio-domínio de clivagem, em que o primeiro domínio de ligação de dedo de zinco foi projetado para se ligar a um primeiro sítio alvo, conforme estabelecido na Tabela acima em ou próximo a um locus Zp15 no genoma da célula vegetal; e (b) transformar a célula vegetal com um vetor de expressão compreendendo uma sequência que codifica uma segunda proteína de fusão na célula, a segunda proteína de fusão compreendendo um segundo domínio de ligação de dedo de zinco e um segundo meio domínio de clivagem, em que o segundo domínio de ligação de dedo de zinco se liga a um segundo sítio alvo no ou próximo ao locus Zp15 no genoma da célula vegetal, em que o segundo sítio alvo é diferente do primeiro sítio alvo; e em que a ligação da primeira proteína de fusão ao primeiro sítio alvo e a ligação da segunda proteína de fusão ao segundo sítio alvo posiciona os meios-domínios de clivagem de modo que o genoma da célula vegetal em ou próximo ao locus Zp15 é clivado.
4. Método, de acordo com qualquer uma das reivindicações 1 a 3, caracterizado pelo fato de que os meio-domínios de clivagem ocorrem naturalmente ou não ocorrem naturalmente.
5. Método, de acordo com a reivindicação 1 ou 2, caracterizado pelo fato de que a nuclease de dedo de zinco compreende um par de nucleases de dedo de zinco.
6. Método, de acordo com a reivindicação 1 ou 2, caracterizado pelo fato de que a uma ou mais sequências de ácido nucleico exógenas compreende uma sequência de codificação.
7. Método, de acordo com a reivindicação 6, caracterizado pelo fato de que a sequência de codificação codifica um produto que confe- re: resistência a herbicida; tolerância a herbicida; resistência a insetos; tolerância a insetos; resistência a doenças; tolerância a doenças; rendimentos aumentados de óleo ou combinações dos mesmos.
8. Método, de acordo com qualquer uma das reivindicações 1 a 7, caracterizado pelo fato de que o polinucleotídeo compreende ainda sequências de nucleotídeo que são homólogas às sequências no locus Zp15.
9. Método, de acordo com a reivindicação 8, caracterizado pelo fato de que as sequências de nucleotídeo homólogas flanqueiam a sequência exógena.
10. Método, de acordo com qualquer uma das reivindicações 1 a 9, caracterizado pelo fato de que o polinucleotídeo compreende ainda um promotor.
11. Método, de acordo com qualquer uma das reivindicações 1 a 10, caracterizado pelo fato de que uma ou mais das sequências exógenas integradas são transmitidas à progênie em gerações subsequentes.
12. Método, de acordo com qualquer uma das reivindicações 1 a 11, caracterizado pelo fato de que a célula vegetal é uma célula vegetal monocotiledônea.
13. Método, de acordo com a reivindicação 12, caracterizado pelo fato de que a célula vegetal é uma célula de milho.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US20194608P | 2008-12-17 | 2008-12-17 | |
| US61/201946 | 2008-12-17 | ||
| PCT/US2009/006606 WO2010077319A1 (en) | 2008-12-17 | 2009-12-17 | Targeted integration into the zp15 locus |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0922641A2 BRPI0922641A2 (pt) | 2020-10-20 |
| BRPI0922641B1 true BRPI0922641B1 (pt) | 2021-10-26 |
Family
ID=42310058
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0922641-9A BRPI0922641B1 (pt) | 2008-12-17 | 2009-12-17 | Método de integração de uma ou mais sequências de ácido nucleico exógenas no genoma de uma célula vegetal |
Country Status (18)
| Country | Link |
|---|---|
| US (1) | US8329986B2 (pt) |
| EP (1) | EP2370575B1 (pt) |
| JP (2) | JP2012511926A (pt) |
| KR (1) | KR101683928B1 (pt) |
| CN (1) | CN102333868B (pt) |
| AR (1) | AR074783A1 (pt) |
| AU (1) | AU2009333863B2 (pt) |
| BR (1) | BRPI0922641B1 (pt) |
| CA (1) | CA2747124C (pt) |
| DK (1) | DK2370575T3 (pt) |
| ES (1) | ES2654923T3 (pt) |
| HR (1) | HRP20180074T1 (pt) |
| HU (1) | HUE037911T2 (pt) |
| IL (1) | IL213557A (pt) |
| PT (1) | PT2370575T (pt) |
| SI (1) | SI2370575T1 (pt) |
| WO (1) | WO2010077319A1 (pt) |
| ZA (1) | ZA201104014B (pt) |
Families Citing this family (50)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2010226313B2 (en) | 2009-03-20 | 2014-10-09 | Sangamo Therapeutics, Inc. | Modification of CXCR4 using engineered zinc finger proteins |
| EP2467010B1 (en) * | 2009-08-19 | 2018-11-28 | Dow AgroSciences LLC | Aad-1 event das-40278-9, related transgenic corn lines, and event-specific identification thereof |
| EA031322B1 (ru) | 2010-01-22 | 2018-12-28 | Дау Агросайенсиз Ллс | Клетка или клеточная линия для экспрессии экзогенных нуклеотидных последовательностей и применение клетки или клеточной линии |
| AR085533A1 (es) | 2011-03-23 | 2013-10-09 | Pioneer Hi Bred Int | Metodos de produccion de un locus de rasgos transgenicos complejo |
| JP6188703B2 (ja) | 2011-10-27 | 2017-08-30 | サンガモ セラピューティクス, インコーポレイテッド | Hprt遺伝子座を修飾するための方法および組成物 |
| TW201341394A (zh) * | 2012-02-01 | 2013-10-16 | Dow Agrosciences Llc | 合成之葉綠體輸送胜肽 |
| BR112014026203A2 (pt) | 2012-04-23 | 2017-07-18 | Bayer Cropscience Nv | engenharia do genoma direcionado nas plantas |
| MX369788B (es) | 2012-05-02 | 2019-11-21 | Dow Agrosciences Llc | Modificacion dirigida de deshidrogenasa de malato. |
| BR112014027813A2 (pt) | 2012-05-07 | 2017-08-08 | Dow Agrosciences Llc | métodos e composições para integração de transgenes direcionada mediada por nuclease |
| US10648001B2 (en) | 2012-07-11 | 2020-05-12 | Sangamo Therapeutics, Inc. | Method of treating mucopolysaccharidosis type I or II |
| RU2665811C2 (ru) | 2012-09-07 | 2018-09-04 | ДАУ АГРОСАЙЕНСИЗ ЭлЭлСи | Локусы fad3 для выполнения операций и соответствующие связывающиеся со специфическими сайтами-мишенями белки, способные к вызову направленных разрывов |
| UA118090C2 (uk) | 2012-09-07 | 2018-11-26 | ДАУ АГРОСАЙЄНСІЗ ЕлЕлСі | Спосіб інтегрування послідовності нуклеїнової кислоти, що представляє інтерес, у ген fad2 у клітині сої та специфічний для локусу fad2 білок, що зв'язується, здатний індукувати спрямований розрив |
| US9756871B2 (en) * | 2012-11-20 | 2017-09-12 | J.R. Simplot Company | TAL-mediated transfer DNA insertion |
| CA2895117A1 (en) | 2012-12-13 | 2014-06-19 | James W. Bing | Precision gene targeting to a particular locus in maize |
| EP3679785A3 (en) | 2013-04-05 | 2020-09-16 | Dow AgroSciences LLC | Methods and compositions for integration of an exogenous sequence within the genome of plants |
| JP2016518142A (ja) | 2013-05-10 | 2016-06-23 | サンガモ バイオサイエンシーズ, インコーポレイテッド | ヌクレアーゼ媒介ゲノム遺伝子操作のための送達方法および組成物 |
| CN105683376A (zh) | 2013-05-15 | 2016-06-15 | 桑格摩生物科学股份有限公司 | 用于治疗遗传病状的方法和组合物 |
| ES2729635T3 (es) | 2013-08-22 | 2019-11-05 | Pioneer Hi Bred Int | Modificación genómica usando sistemas de polinucleótido guía/endonucleasa Cas y métodos de uso |
| EP3988654A1 (en) | 2013-08-28 | 2022-04-27 | Sangamo Therapeutics, Inc. | Compositions for linking dna-binding domains and cleavage domains |
| KR20150026336A (ko) * | 2013-09-02 | 2015-03-11 | 엘지전자 주식회사 | 웨어러블 디바이스 및 그 컨텐트 출력 방법 |
| BR102014021800B1 (pt) | 2013-09-04 | 2022-03-29 | Dow Agrosciences Llc | Método para detectar a integração específica de sítio de uma sequência de doador de polinucleotídeo dentro de um sítio-alvo genômico |
| WO2015057980A1 (en) | 2013-10-17 | 2015-04-23 | Sangamo Biosciences, Inc. | Delivery methods and compositions for nuclease-mediated genome engineering |
| EP3057432B1 (en) | 2013-10-17 | 2018-11-21 | Sangamo Therapeutics, Inc. | Delivery methods and compositions for nuclease-mediated genome engineering in hematopoietic stem cells |
| AU2014341928B2 (en) | 2013-11-04 | 2017-11-30 | Corteva Agriscience Llc | A universal donor system for gene targeting |
| UY35812A (es) | 2013-11-04 | 2015-05-29 | Dow Agrosciences Llc | ?loci de maíz óptimos?. |
| CN106232821A (zh) | 2013-11-04 | 2016-12-14 | 美国陶氏益农公司 | 最优大豆座位 |
| WO2015066634A2 (en) | 2013-11-04 | 2015-05-07 | Dow Agrosciences Llc | Optimal soybean loci |
| CA2928855A1 (en) | 2013-11-04 | 2015-05-07 | Dow Agrosciences Llc | Optimal maize loci |
| US10774338B2 (en) | 2014-01-16 | 2020-09-15 | The Regents Of The University Of California | Generation of heritable chimeric plant traits |
| WO2015116969A2 (en) * | 2014-01-30 | 2015-08-06 | The Board Of Trustees Of The University Of Arkansas | Method, vectors, cells, seeds and kits for stacking genes into a single genomic site |
| US9522936B2 (en) | 2014-04-24 | 2016-12-20 | Sangamo Biosciences, Inc. | Engineered transcription activator like effector (TALE) proteins |
| WO2015188056A1 (en) | 2014-06-05 | 2015-12-10 | Sangamo Biosciences, Inc. | Methods and compositions for nuclease design |
| MX2017000422A (es) | 2014-07-11 | 2017-05-01 | Du Pont | Composiciones y metodos para producir plantas resistentes al herbicida glifosato. |
| WO2016014794A1 (en) | 2014-07-25 | 2016-01-28 | Sangamo Biosciences, Inc. | Methods and compositions for modulating nuclease-mediated genome engineering in hematopoietic stem cells |
| WO2016014837A1 (en) | 2014-07-25 | 2016-01-28 | Sangamo Biosciences, Inc. | Gene editing for hiv gene therapy |
| US9616090B2 (en) | 2014-07-30 | 2017-04-11 | Sangamo Biosciences, Inc. | Gene correction of SCID-related genes in hematopoietic stem and progenitor cells |
| EP3191595B1 (en) | 2014-09-12 | 2019-12-25 | E. I. du Pont de Nemours and Company | Generation of site-specific-integration sites for complex trait loci in corn and soybean, and methods of use |
| PL3194570T3 (pl) | 2014-09-16 | 2021-12-20 | Sangamo Therapeutics, Inc. | Sposoby i kompozycje do inżynierii genomowej w której pośredniczy nukleaza i korekty hematopoetycznych komórek macierzystych |
| EP3237624B1 (en) | 2014-12-23 | 2020-01-29 | Syngenta Participations AG | Methods and compositions for identifying and enriching for cells comprising site specific genomic modifications |
| US10450576B2 (en) | 2015-03-27 | 2019-10-22 | E I Du Pont De Nemours And Company | Soybean U6 small nuclear RNA gene promoters and their use in constitutive expression of small RNA genes in plants |
| JP6954890B2 (ja) | 2015-07-13 | 2021-10-27 | サンガモ セラピューティクス, インコーポレイテッド | ヌクレアーゼ媒介ゲノム遺伝子操作のための送達方法及び組成物 |
| JP6113310B2 (ja) * | 2016-01-15 | 2017-04-12 | ダウ アグロサイエンシィズ エルエルシー | Aad−1イベントdas−40278−9、関連するトランスジェニックトウモロコシ系統およびそのイベント特異的同定 |
| US10724020B2 (en) | 2016-02-02 | 2020-07-28 | Sangamo Therapeutics, Inc. | Compositions for linking DNA-binding domains and cleavage domains |
| US11020492B2 (en) | 2016-10-31 | 2021-06-01 | Sangamo Therapeutics, Inc. | Gene correction of SCID-related genes in hematopoietic stem and progenitor cells |
| JP2020518245A (ja) | 2017-05-03 | 2020-06-25 | サンガモ セラピューティクス, インコーポレイテッド | 嚢胞性線維症膜貫通コンダクタンス制御因子(cftr)遺伝子の改変のための方法および組成物 |
| US11661611B2 (en) | 2017-11-09 | 2023-05-30 | Sangamo Therapeutics, Inc. | Genetic modification of cytokine inducible SH2-containing protein (CISH) gene |
| WO2019204457A1 (en) | 2018-04-18 | 2019-10-24 | Sangamo Therapeutics, Inc. | Zinc finger protein compositions for modulation of huntingtin (htt) |
| US11690921B2 (en) | 2018-05-18 | 2023-07-04 | Sangamo Therapeutics, Inc. | Delivery of target specific nucleases |
| AU2019398351A1 (en) | 2018-12-14 | 2021-06-03 | Pioneer Hi-Bred International, Inc. | Novel CRISPR-Cas systems for genome editing |
| EP4313122A1 (en) | 2021-03-23 | 2024-02-07 | Iovance Biotherapeutics, Inc. | Cish gene editing of tumor infiltrating lymphocytes and uses of same in immunotherapy |
Family Cites Families (62)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5422251A (en) | 1986-11-26 | 1995-06-06 | Princeton University | Triple-stranded nucleic acids |
| US5176996A (en) | 1988-12-20 | 1993-01-05 | Baylor College Of Medicine | Method for making synthetic oligonucleotides which bind specifically to target sites on duplex DNA molecules, by forming a colinear triplex, the synthetic oligonucleotides and methods of use |
| US5633434A (en) | 1990-02-02 | 1997-05-27 | Hoechst Aktiengesellschaft | Transgenic plants displaying virus and phosphinothricin resistance |
| US5420032A (en) | 1991-12-23 | 1995-05-30 | Universitge Laval | Homing endonuclease which originates from chlamydomonas eugametos and recognizes and cleaves a 15, 17 or 19 degenerate double stranded nucleotide sequence |
| US5356802A (en) | 1992-04-03 | 1994-10-18 | The Johns Hopkins University | Functional domains in flavobacterium okeanokoites (FokI) restriction endonuclease |
| US5487994A (en) * | 1992-04-03 | 1996-01-30 | The Johns Hopkins University | Insertion and deletion mutants of FokI restriction endonuclease |
| US5436150A (en) * | 1992-04-03 | 1995-07-25 | The Johns Hopkins University | Functional domains in flavobacterium okeanokoities (foki) restriction endonuclease |
| US5792632A (en) * | 1992-05-05 | 1998-08-11 | Institut Pasteur | Nucleotide sequence encoding the enzyme I-SceI and the uses thereof |
| EP0604662B1 (en) | 1992-07-07 | 2008-06-18 | Japan Tobacco Inc. | Method of transforming monocotyledon |
| US6242568B1 (en) * | 1994-01-18 | 2001-06-05 | The Scripps Research Institute | Zinc finger protein derivatives and methods therefor |
| ATE310812T1 (de) | 1994-01-18 | 2005-12-15 | Scripps Research Inst | Derivate von zinkfingerproteinen und methoden |
| US6140466A (en) | 1994-01-18 | 2000-10-31 | The Scripps Research Institute | Zinc finger protein derivatives and methods therefor |
| US5585245A (en) | 1994-04-22 | 1996-12-17 | California Institute Of Technology | Ubiquitin-based split protein sensor |
| JP4118327B2 (ja) | 1994-08-20 | 2008-07-16 | ゲンダック・リミテッド | Dna認識のための結合タンパク質におけるまたはそれに関連する改良 |
| GB9824544D0 (en) | 1998-11-09 | 1999-01-06 | Medical Res Council | Screening system |
| US5789538A (en) | 1995-02-03 | 1998-08-04 | Massachusetts Institute Of Technology | Zinc finger proteins with high affinity new DNA binding specificities |
| US5925523A (en) | 1996-08-23 | 1999-07-20 | President & Fellows Of Harvard College | Intraction trap assay, reagents and uses thereof |
| GB2338237B (en) | 1997-02-18 | 2001-02-28 | Actinova Ltd | In vitro peptide or protein expression library |
| GB9703369D0 (en) | 1997-02-18 | 1997-04-09 | Lindqvist Bjorn H | Process |
| US6342345B1 (en) | 1997-04-02 | 2002-01-29 | The Board Of Trustees Of The Leland Stanford Junior University | Detection of molecular interactions by reporter subunit complementation |
| GB9710807D0 (en) | 1997-05-23 | 1997-07-23 | Medical Res Council | Nucleic acid binding proteins |
| GB9710809D0 (en) | 1997-05-23 | 1997-07-23 | Medical Res Council | Nucleic acid binding proteins |
| US6506559B1 (en) | 1997-12-23 | 2003-01-14 | Carnegie Institute Of Washington | Genetic inhibition by double-stranded RNA |
| AR014491A1 (es) | 1998-01-29 | 2001-02-28 | Dow Agrosciences Llc | Metodo para obtener plantas transgenicas fertiles de gossypium hirsutum. |
| US6410248B1 (en) * | 1998-01-30 | 2002-06-25 | Massachusetts Institute Of Technology | General strategy for selecting high-affinity zinc finger proteins for diverse DNA target sites |
| US6479626B1 (en) | 1998-03-02 | 2002-11-12 | Massachusetts Institute Of Technology | Poly zinc finger proteins with improved linkers |
| US6140081A (en) | 1998-10-16 | 2000-10-31 | The Scripps Research Institute | Zinc finger binding domains for GNN |
| US6453242B1 (en) | 1999-01-12 | 2002-09-17 | Sangamo Biosciences, Inc. | Selection of sites for targeting by zinc finger proteins and methods of designing zinc finger proteins to bind to preselected sites |
| US6534261B1 (en) * | 1999-01-12 | 2003-03-18 | Sangamo Biosciences, Inc. | Regulation of endogenous gene expression in cells using zinc finger proteins |
| US6794136B1 (en) | 2000-11-20 | 2004-09-21 | Sangamo Biosciences, Inc. | Iterative optimization in the design of binding proteins |
| US7030215B2 (en) * | 1999-03-24 | 2006-04-18 | Sangamo Biosciences, Inc. | Position dependent recognition of GNN nucleotide triplets by zinc fingers |
| AU772110B2 (en) * | 1999-08-05 | 2004-04-08 | Icon Genetics, Inc. | Method of making plant artificial chromosomes |
| EP1250424B1 (en) | 2000-01-24 | 2007-02-28 | Gendaq, Ltd. | Nucleic acid binding polypeptides characterized by flexible linkers connected nucleic acid binding modules |
| US20020061512A1 (en) | 2000-02-18 | 2002-05-23 | Kim Jin-Soo | Zinc finger domains and methods of identifying same |
| AU2001263155A1 (en) | 2000-05-16 | 2001-11-26 | Massachusetts Institute Of Technology | Methods and compositions for interaction trap assays |
| JP2002060786A (ja) | 2000-08-23 | 2002-02-26 | Kao Corp | 硬質表面用殺菌防汚剤 |
| US9234187B2 (en) | 2001-01-22 | 2016-01-12 | Sangamo Biosciences, Inc. | Modified zinc finger binding proteins |
| GB0108491D0 (en) | 2001-04-04 | 2001-05-23 | Gendaq Ltd | Engineering zinc fingers |
| JP2005500061A (ja) | 2001-08-20 | 2005-01-06 | ザ スクリップス リサーチ インスティテュート | Cnnについての亜鉛フィンガー結合ドメイン |
| ATE347593T1 (de) * | 2002-01-23 | 2006-12-15 | Univ Utah Res Found | Zielgerichtete chromosomale mutagenese mit zinkfingernukleasen |
| EP2368982A3 (en) | 2002-03-21 | 2011-10-12 | Sangamo BioSciences, Inc. | Methods and compositions for using zinc finger endonucleases to enhance homologous recombination |
| WO2004003177A2 (en) | 2002-06-27 | 2004-01-08 | Dow Agrosciences Llc | Use of regulatory sequences in transgenic plants |
| WO2004037977A2 (en) * | 2002-09-05 | 2004-05-06 | California Institute Of Thechnology | Use of chimeric nucleases to stimulate gene targeting |
| US7888121B2 (en) * | 2003-08-08 | 2011-02-15 | Sangamo Biosciences, Inc. | Methods and compositions for targeted cleavage and recombination |
| US8409861B2 (en) * | 2003-08-08 | 2013-04-02 | Sangamo Biosciences, Inc. | Targeted deletion of cellular DNA sequences |
| DK2927318T3 (da) | 2003-08-08 | 2020-08-03 | Sangamo Therapeutics Inc | Fremgangsmåde og sammensætninger til målrettet spaltning og rekombination |
| US8729341B2 (en) | 2004-02-23 | 2014-05-20 | University Of Chicago | Plants modified with mini-chromosomes |
| JP5285906B2 (ja) * | 2004-04-30 | 2013-09-11 | ダウ アグロサイエンシズ リミテッド ライアビリティー カンパニー | 除草剤抵抗性遺伝子 |
| AU2004326206B2 (en) * | 2004-12-28 | 2011-03-17 | Pioneer Hi-Bred International, Inc. | Improved grain quality through altered expression of seed proteins |
| WO2006097854A1 (en) * | 2005-03-15 | 2006-09-21 | Cellectis | Heterodimeric meganucleases and use thereof |
| US20090263900A1 (en) * | 2008-04-14 | 2009-10-22 | Sangamo Biosciences, Inc. | Linear donor constructs for targeted integration |
| SG10201508995QA (en) * | 2005-07-26 | 2015-11-27 | Sangamo Biosciences Inc | Targeted integration and expression of exogenous nucleic acid sequences |
| DK1945762T3 (da) * | 2005-10-18 | 2013-07-29 | Prec Biosciences | Rationelt konstruerede meganucleaser med ændret sekvensspecificitet og DNA-bindingsaffinitet |
| KR100740694B1 (ko) * | 2006-02-09 | 2007-07-18 | 한국생명공학연구원 | 색소체 게놈 내에 삽입된 외래유전자의 이차 재조합을방지하기 위한 벡터개발 |
| CA2651494C (en) | 2006-05-25 | 2015-09-29 | Sangamo Biosciences, Inc. | Engineered cleavage half-domains |
| KR101613624B1 (ko) * | 2006-12-14 | 2016-04-29 | 다우 아그로사이언시즈 엘엘씨 | 최적화된 비-정규 아연 손가락 단백질 |
| ATE489465T1 (de) | 2007-04-26 | 2010-12-15 | Sangamo Biosciences Inc | Gezielte integration in die ppp1r12c-position |
| JP5907657B2 (ja) | 2007-05-09 | 2016-04-26 | ダウ アグロサイエンシィズ エルエルシー | 新規な除草剤抵抗性遺伝子 |
| JP2009047247A (ja) | 2007-08-20 | 2009-03-05 | Yamaha Motor Co Ltd | エアクリーナ、無段変速機のケース、エンジンユニット及び鞍乗型車両 |
| AR068559A1 (es) * | 2007-09-27 | 2009-11-18 | Sangamo Biosciences Inc | Proteinas de dedo de zinc obtenidas por ingenieria dirigidas a genes de 5-enolpiruvilshikimato-3-fosfatosintetasa |
| WO2009042163A2 (en) | 2007-09-27 | 2009-04-02 | Sangamo Biosciences, Inc. | Rapid in vivo identification of biologically active nucleases |
| CA2701636C (en) * | 2007-10-05 | 2019-10-15 | Dow Agrosciences Llc | Methods for transferring molecular substances into plant cells |
-
2009
- 2009-12-17 AR ARP090104955A patent/AR074783A1/es unknown
- 2009-12-17 DK DK09836506.7T patent/DK2370575T3/en active
- 2009-12-17 AU AU2009333863A patent/AU2009333863B2/en active Active
- 2009-12-17 PT PT98365067T patent/PT2370575T/pt unknown
- 2009-12-17 KR KR1020117016519A patent/KR101683928B1/ko active IP Right Grant
- 2009-12-17 EP EP09836506.7A patent/EP2370575B1/en active Active
- 2009-12-17 SI SI200931795T patent/SI2370575T1/en unknown
- 2009-12-17 WO PCT/US2009/006606 patent/WO2010077319A1/en active Application Filing
- 2009-12-17 CN CN200980156926.7A patent/CN102333868B/zh active Active
- 2009-12-17 HU HUE09836506A patent/HUE037911T2/hu unknown
- 2009-12-17 US US12/653,735 patent/US8329986B2/en active Active
- 2009-12-17 JP JP2011542133A patent/JP2012511926A/ja not_active Withdrawn
- 2009-12-17 CA CA2747124A patent/CA2747124C/en active Active
- 2009-12-17 BR BRPI0922641-9A patent/BRPI0922641B1/pt active IP Right Grant
- 2009-12-17 ES ES09836506.7T patent/ES2654923T3/es active Active
-
2011
- 2011-05-31 ZA ZA2011/04014A patent/ZA201104014B/en unknown
- 2011-06-14 IL IL213557A patent/IL213557A/en active IP Right Grant
-
2015
- 2015-07-02 JP JP2015133818A patent/JP6127297B2/ja active Active
-
2018
- 2018-01-16 HR HRP20180074TT patent/HRP20180074T1/hr unknown
Also Published As
| Publication number | Publication date |
|---|---|
| JP2012511926A (ja) | 2012-05-31 |
| PT2370575T (pt) | 2017-12-11 |
| EP2370575A4 (en) | 2012-05-09 |
| US8329986B2 (en) | 2012-12-11 |
| CN102333868A (zh) | 2012-01-25 |
| SI2370575T1 (en) | 2018-07-31 |
| JP6127297B2 (ja) | 2017-05-17 |
| DK2370575T3 (en) | 2018-02-05 |
| CA2747124A1 (en) | 2010-07-08 |
| ZA201104014B (en) | 2013-05-29 |
| AU2009333863B2 (en) | 2015-02-05 |
| ES2654923T3 (es) | 2018-02-15 |
| AR074783A1 (es) | 2011-02-09 |
| AU2009333863A1 (en) | 2011-07-07 |
| EP2370575B1 (en) | 2017-11-01 |
| IL213557A0 (en) | 2011-07-31 |
| EP2370575A1 (en) | 2011-10-05 |
| HUE037911T2 (hu) | 2018-09-28 |
| KR101683928B1 (ko) | 2016-12-07 |
| US20100199389A1 (en) | 2010-08-05 |
| WO2010077319A1 (en) | 2010-07-08 |
| KR20110095420A (ko) | 2011-08-24 |
| JP2015226537A (ja) | 2015-12-17 |
| IL213557A (en) | 2015-02-26 |
| CA2747124C (en) | 2018-09-04 |
| BRPI0922641A2 (pt) | 2020-10-20 |
| HRP20180074T1 (hr) | 2018-04-06 |
| CN102333868B (zh) | 2015-01-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CA2747124C (en) | Targeted integration into the zp15 locus | |
| US11198883B2 (en) | Methods and compositions for integration of an exogenous sequence within the genome of plants | |
| US11085092B2 (en) | Targeted modification of malate dehydrogenase | |
| US10260062B2 (en) | Targeted genomic alteration | |
| US9428756B2 (en) | Zinc finger nuclease-mediated homologous recombination | |
| US20230374529A1 (en) | Reconstruction of site specific nuclease binding sites | |
| AU2017216446A1 (en) | Zinc finger nuclease-mediated homologous recombination | |
| BRPI0716427B1 (pt) | Method for introducing an exogenous sequence in the genome of a plant cell |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 17/12/2009, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |