WO2022064744A1 - 硫化物系固体電解質及び全固体リチウムイオン電池 - Google Patents
硫化物系固体電解質及び全固体リチウムイオン電池 Download PDFInfo
- Publication number
- WO2022064744A1 WO2022064744A1 PCT/JP2021/015220 JP2021015220W WO2022064744A1 WO 2022064744 A1 WO2022064744 A1 WO 2022064744A1 JP 2021015220 W JP2021015220 W JP 2021015220W WO 2022064744 A1 WO2022064744 A1 WO 2022064744A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- sulfide
- solid electrolyte
- based solid
- ion battery
- state lithium
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B19/00—Selenium; Tellurium; Compounds thereof
- C01B19/007—Tellurides or selenides of metals
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0561—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of inorganic materials only
- H01M10/0562—Solid materials
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01B—CABLES; CONDUCTORS; INSULATORS; SELECTION OF MATERIALS FOR THEIR CONDUCTIVE, INSULATING OR DIELECTRIC PROPERTIES
- H01B1/00—Conductors or conductive bodies characterised by the conductive materials; Selection of materials as conductors
- H01B1/06—Conductors or conductive bodies characterised by the conductive materials; Selection of materials as conductors mainly consisting of other non-metallic substances
- H01B1/10—Conductors or conductive bodies characterised by the conductive materials; Selection of materials as conductors mainly consisting of other non-metallic substances sulfides
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0065—Solid electrolytes
- H01M2300/0068—Solid electrolytes inorganic
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Definitions
- the present invention relates to a sulfide-based solid electrolyte and an all-solid-state lithium-ion battery.
- lithium ion batteries are attracting attention from the viewpoint of high energy density. Further, high energy density and improvement of battery characteristics are also required for lithium secondary batteries in large-scale applications such as power sources for automobiles and road leveling.
- Non-Patent Document 1 discloses a technique of substituting a pentavalent P in an algyrodite type Li 7 PS 6 with a tetravalent Ge.
- the present inventor can replace phosphorus (P) with 100% germanium (Ge) by adopting a structure containing tellurium (Te) in a lithium ion conductor having an algyrodite type structure. It was found that the ionic conductivity could be improved by this. They have found that a sulfide-based solid electrolyte having an argylodite-type structure and having a predetermined composition solves the above-mentioned problems.
- a sulfide-based solid electrolyte having an argylodite-type structure and has a composition.
- Formula: Li 8 GeS 5-x Te 1 + x (In the formula, ⁇ 0.5 ⁇ x ⁇ 0, 0 ⁇ x ⁇ 0.375.) It is a sulfide-based solid electrolyte represented by.
- the sulfide-based solid electrolyte of the present invention has ⁇ 0.375 ⁇ x ⁇ 0 in the above formula.
- the present invention is an all-solid lithium ion battery including a solid electrolyte layer composed of the sulfide-based solid electrolyte according to the embodiment of the present invention, a positive electrode layer, and a negative electrode layer.
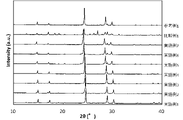
- 5 is an X-ray diffraction (XRD) graph according to Examples 1 to 7, Comparative Example 1 and Reference Example 1.
- the sulfide-based solid electrolyte of the present embodiment is a sulfide-based solid electrolyte having an Argyrodite type structure. It can be confirmed by, for example, X-ray diffraction measurement using CuK ⁇ ray that the sulfide-based solid electrolyte has an algyrodite type structure.
- the sulfide-based solid electrolyte of the present embodiment may have these peaks.
- the sulfide-based solid electrolyte of the present embodiment may contain an amorphous component as long as it has an X-ray diffraction pattern having an algyrodite-type structure, and has a structure or a raw material other than the algyrodite-type structure. May include.
- the sulfide-based solid electrolyte of the present embodiment has a composition of the formula: Li 8 GeS 5-x Te 1 + x (in the formula, ⁇ 0.5 ⁇ x ⁇ 0, 0 ⁇ x ⁇ 0.375). It is represented by.
- the sulfur (S) in the solid electrolyte is replaced with Te, which has a large ionic radius, so that the stability of the crystal structure is improved, and phosphorus (P) is contained in germanium (Ge). ) Is completely (100%) replaced. According to such a configuration, the substitution amount of germanium (Ge) is increased, so that a sulfide-based solid electrolyte having good ionic conductivity can be obtained.
- the sulfide-based solid electrolyte of the present embodiment if x is less than ⁇ 0.5 in the above composition formula, a Li 4 GeS 4 phase having low ion conductivity may occur. Further, when x exceeds 0.375, the crystal lattice becomes large, so that the distance between Li sites becomes long, and the ionic conductivity may decrease.
- the sulfide-based solid electrolyte of the present embodiment preferably has ⁇ 0.375 ⁇ x ⁇ 0 in the above composition formula. With such a configuration, a sulfide-based solid electrolyte having better ionic conductivity can be obtained.
- the average particle size of the sulfide-based solid electrolyte according to the embodiment of the present invention is not particularly limited, but may be 0.01 to 100 ⁇ m, 0.1 to 100 ⁇ m, or 0.1 to 50 ⁇ m. There may be.
- the ionic conductivity of the sulfide-based solid electrolyte according to the embodiment of the present invention is preferably 10 -4 S / cm or more, and more preferably 10 -3 S / cm or more.
- 0.2 g of the sulfide-based solid electrolyte powder was pressed at a pressure of 550 MPa to form a plate, and then gold electrodes were attached to both sides of the plate. It can be obtained by preparing pellets having a diameter of 10 mm and measuring AC impedance from 1 Hz to 10 MHz at 25 ° C.
- the raw materials are weighed so as to have a predetermined composition in a glove box having an atmosphere of an inert gas such as argon gas or nitrogen gas.
- an inert gas such as argon gas or nitrogen gas.
- the raw materials used here include Li, Li 2 S, Li 2 Te, LiTe 3 , Ge, GeS, GeS 2 , GeTe, S, Te and the like.
- the mixed powder is made into pellets, vacuum-sealed in a quartz ampoule, and baked together with the quartz ampoule at 400 to 800 ° C. for 1 to 20 hours to obtain the composition: Li 8 GeS 5-x Te 1+ .
- the sulfide-based solid electrolyte according to the embodiment of the present invention represented by x (in the formula, ⁇ 0.5 ⁇ x ⁇ 0, 0 ⁇ x ⁇ 0.375) can be produced.
- An all-solid lithium ion battery including the solid electrolyte layer, the positive electrode layer, and the negative electrode layer can be produced by forming a solid electrolyte layer with the sulfide-based solid electrolyte according to the embodiment of the present invention.
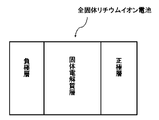
- the positive electrode layer and the negative electrode layer constituting the all-solid-state lithium-ion battery according to the embodiment of the present invention are not particularly limited and can be formed of a known material, and may have a known configuration as shown in FIG. can.
- the positive electrode layer of the lithium ion battery is formed by layering a positive electrode mixture formed by mixing a known positive electrode active material for a lithium ion battery with a sulfide-based solid electrolyte or another sulfide-based solid electrolyte according to the embodiment of the present invention. It was formed in.
- the positive electrode mixture may further contain a conductive auxiliary agent.
- a conductive auxiliary agent a carbon material, a metal material, or a mixture thereof can be used.
- Conductive aids consist of, for example, carbon, nickel, copper, aluminum, indium, silver, cobalt, magnesium, lithium, chromium, gold, ruthenium, platinum, beryllium, iridium, molybdenum, niobium, osnium, rhodium, tungsten and zinc. It may contain at least one element selected from the group.
- the conductive auxiliary agent is preferably a simple substance of carbon, a simple substance of metal containing carbon, nickel, copper, silver, cobalt, magnesium, lithium, ruthenium, gold, platinum, niobium, osnium or rhodium, a mixture or a compound. ..
- the carbon material for example, carbon black such as Ketjen black, acetylene black, denka black, thermal black, channel black, graphite, carbon fiber, activated carbon and the like can be used.
- the negative electrode layer of the lithium ion battery may be a layered layer of a known negative electrode active material for a lithium ion battery. Further, the negative electrode layer is formed by layering a negative electrode mixture formed by mixing a known negative electrode active material for a lithium ion battery with a sulfide-based solid electrolyte or another sulfide-based solid electrolyte according to the embodiment of the present invention. It may be formed.
- the negative electrode layer may contain a conductive auxiliary agent in the same manner as the positive electrode layer. As the conductive auxiliary agent, the same material as that described for the positive electrode layer can be used.
- the negative electrode active material examples include carbon materials, specifically, artificial graphite, graphite carbon fiber, resin calcined carbon, thermally decomposed vapor phase grown carbon, coke, mesocarbon microbeads (MCMB), and furfuryl alcohol resin calcined carbon. , Polyacene, pitch-based carbon fiber, vapor-phase grown carbon fiber, natural graphite, non-graphitizable carbon, etc., or a mixture thereof can be used. Further, as the negative electrode material, for example, an alloy combined with a metal itself such as metallic lithium, metallic indium, metallic aluminum, metallic silicon, or other elements or compounds can be used.
- Example 1 The raw materials were weighed in a glove box in an argon atmosphere so as to have a predetermined composition, and mixed for 15 minutes using a mortar to prepare a mixed powder. Next, the mixed powder was made into 1 g pellets, vacuum-sealed in a quartz ampoule, and baked together with the quartz ampoule at 700 ° C. for 8 hours to obtain a sulfide-based solid electrolyte having a composition of Li 8 GeS 5.5 Te 0.5 . Obtained.
- the Integrity of "Intensity (a.u.)" represents the intensity of the X-ray detected by the XRD measurement, and a. u. Is an abbreviation for arbitrary unit and indicates that it is an arbitrary unit.
- "2 ⁇ ” indicates the angle (diffraction angle) formed by the incident X-ray direction and the diffracted X-ray direction.
- Example 2 The procedure was carried out in the same manner as in Example 1 except that the composition of the prepared sulfide-based solid electrolyte was Li 8 GeS 5.375 Te 0.625 .
- Example 3 The procedure was carried out in the same manner as in Example 1 except that the composition of the prepared sulfide-based solid electrolyte was Li 8 GeS 5.25 Te 0.75 .
- Example 4 The procedure was carried out in the same manner as in Example 1 except that the composition of the prepared sulfide-based solid electrolyte was Li 8 GeS 5.125 Te 0.875 .
- Example 5 The procedure was carried out in the same manner as in Example 1 except that the composition of the prepared sulfide-based solid electrolyte was Li 8 GeS 4.875 Te 1.125 .
- Example 6 The procedure was carried out in the same manner as in Example 1 except that the composition of the prepared sulfide-based solid electrolyte was Li 8 GeS 4.75 Te 1.25 .
- Example 7 The procedure was carried out in the same manner as in Example 1 except that the composition of the prepared sulfide-based solid electrolyte was Li 8 GeS 4.625 Te 1.375 .
- Example 1 The procedure was carried out in the same manner as in Example 1 except that the composition of the produced sulfide-based solid electrolyte was Li 8 GeS 5.625 Te 0.375 .
- the solid electrolytes of Examples 1 to 7 and Reference Example 1 have the formula: Li 8 GeS 5-x Te 1 + x (in the formula, ⁇ 0.5 ⁇ x ⁇ 0, 0 ⁇ x ⁇ 0.375. ), But Comparative Example 1 did not have the composition. Therefore, the solid electrolytes according to Examples 1 to 7 and Reference Example 1 did not have an argylodite-type structure, and had better ionic conductivity than Comparative Example 1 which did not have the above composition. Therefore, it is expected that the battery capacity of the all-solid-state lithium-ion battery using the solid electrolyte according to Examples 1 to 7 and Reference Example 1 will be improved.
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Manufacturing & Machinery (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- Inorganic Chemistry (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- General Physics & Mathematics (AREA)
- Organic Chemistry (AREA)
- Secondary Cells (AREA)
- Conductive Materials (AREA)
Abstract
イオン伝導度が良好な硫化物系固体電解質、及び、それを用いた全固体リチウムイオン電池を提供する。アルジロダイト型構造を有する硫化物系固体電解質であって、組成が、 式:Li8GeS5-xTe1+x (式中、-0.5≦x<0、0<x≦0.375である。) で表される硫化物系固体電解質。
Description
本発明は、硫化物系固体電解質及び全固体リチウムイオン電池に関する。
近年におけるパソコン、ビデオカメラ、及び携帯電話等の情報関連機器や通信機器等の急速な普及に伴い、その電源として利用される電池の開発が重要視されている。該電池の中でも、エネルギー密度が高いという観点から、リチウムイオン電池が注目を浴びている。また、車載用等の動力源やロードレベリング用といった大型用途におけるリチウム二次電池についても、高エネルギー密度、電池特性向上が求められている。
ただ、リチウムイオン電池の場合は、電解液は有機化合物が大半であり、たとえ難燃性の化合物を用いたとしても火災に至る危険性が全くなくなるとは言いきれない。こうした液系リチウムイオン電池の代替候補として、電解質を固体とした全固体リチウムイオン電池が近年注目を集めている。その中でも、固体電解質としてLi2S-P2S5などの硫化物やそれにハロゲン化リチウムを添加した全固体リチウムイオン電池が主流となりつつある。
また、全固体リチウムイオン電池の特性改善のため、イオン伝導度の高い固体電解質が求められている。一般的に、電荷担体であるリチウムイオンを増やすことで、リチウムイオン伝導性の向上が期待される。このような技術として、例えば、非特許文献1には、アルジロダイト型Li7PS6中の五価のPを、四価のGeで置換する技術が開示されている。
J.Mater.Chem.A,7(2019)2717.
硫化物系固体電解質中の五価のPを、四価の元素で置換する量が増えると、それに従いイオン伝導度が向上する。この点について、上述の非特許文献1に記載された技術では、アルジロダイト型Li7PS6中の五価のPを、四価のGeで置換しているが、Pを35%置換しているに過ぎず、完全に置換することができていない。このため、硫化物系固体電解質のイオン伝導度については未だ改善の余地がある。本発明の実施形態では、イオン伝導度が良好な硫化物系固体電解質、及び、それを用いた全固体リチウムイオン電池を提供することを目的とする。
本発明者は、種々の検討を行った結果、アルジロダイト型構造を有するリチウムイオン伝導体において、テルル(Te)を含む構造とすることで、リン(P)を100%ゲルマニウム(Ge)に置換可能となり、これによってイオン伝導度を向上させることができることを見出した。そして、アルジロダイト型構造を有し、所定の組成で構成された硫化物系固体電解質によれば、上述の課題が解決されることを見出した。
上記知見を基礎にして完成した本発明は実施形態において、アルジロダイト型構造を有する硫化物系固体電解質であって、組成が、
式:Li8GeS5-xTe1+x
(式中、-0.5≦x<0、0<x≦0.375である。)
で表される硫化物系固体電解質である。
式:Li8GeS5-xTe1+x
(式中、-0.5≦x<0、0<x≦0.375である。)
で表される硫化物系固体電解質である。
本発明の硫化物系固体電解質は別の実施形態において、前記式中、-0.375≦x<0である。
本発明は更に別の実施形態において、本発明の実施形態に係る硫化物系固体電解質で構成された固体電解質層と、正極層と、負極層とを含む全固体リチウムイオン電池である。
本発明によれば、イオン伝導度が良好な硫化物系固体電解質、及び、それを用いた全固体リチウムイオン電池を提供することができる。
(硫化物系固体電解質)
本実施形態の硫化物系固体電解質は、アルジロダイト(Argyrodite)型構造を有する硫化物系固体電解質である。硫化物系固体電解質が、アルジロダイト型構造を有していることは、例えば、CuKα線を用いたX線回折測定により確認できる。アルジロダイト型構造は、2θ=24.3±1.0°及び28.7±1.0°に強い回折ピークを有する。なお、アルジロダイト型構造の回折ピークは、例えば、2θ=14.8±1.0°、17.2±1.0°、30.0±1.0°、42.9±1.0°又は45.6±1.0°にも現れることがある。本実施形態の硫化物系固体電解質は、これらのピークを有していてもよい。
本実施形態の硫化物系固体電解質は、アルジロダイト(Argyrodite)型構造を有する硫化物系固体電解質である。硫化物系固体電解質が、アルジロダイト型構造を有していることは、例えば、CuKα線を用いたX線回折測定により確認できる。アルジロダイト型構造は、2θ=24.3±1.0°及び28.7±1.0°に強い回折ピークを有する。なお、アルジロダイト型構造の回折ピークは、例えば、2θ=14.8±1.0°、17.2±1.0°、30.0±1.0°、42.9±1.0°又は45.6±1.0°にも現れることがある。本実施形態の硫化物系固体電解質は、これらのピークを有していてもよい。
本実施形態の硫化物系固体電解質は、アルジロダイト型構造のX線回折パターンを有していれば、その一部に非晶質成分が含まれていてもよく、アルジロダイト型構造以外の構造や原料を含んでいてもよい。
本実施形態の硫化物系固体電解質は、組成が、式:Li8GeS5-xTe1+x(式中、-0.5≦x<0、0<x≦0.375である。)で表される。本実施形態の硫化物系固体電解質は、固体電解質中の硫黄(S)を、イオン半径が大きいTeで置換することにより、結晶構造の安定性が高くなり、リン(P)が、ゲルマニウム(Ge)によって完全に(100%)置換されている。このような構成によれば、ゲルマニウム(Ge)の置換量が増大するため、良好なイオン伝導度を有する硫化物系固体電解質が得られる。
本実施形態の硫化物系固体電解質は、上記組成式において、xが-0.5未満であると、イオン伝導性の低いLi4GeS4相が生じるおそれがある。また、xが0.375超であると、結晶格子が大きくなるためLiサイト間距離が長くなり、イオン伝導度が低下するおそれがある。本実施形態の硫化物系固体電解質は、上記組成式において、-0.375≦x<0であるのが好ましい。このような構成によれば、より良好なイオン伝導度を有する硫化物系固体電解質が得られる。このように硫化物系固体電解質のイオン伝導度が良好であると、放電時の電圧の低下(IRドロップ)が小さくなるため、それを用いた全固体リチウムイオン電池の電池容量が高くなる。また、この効果は、全固体リチウムイオン電池が、特に高レートの際に顕著となる。なお、上記式中、「-0.5≦x<0、0<x≦0.375である」とは、-0.5≦x<0、または、0<x≦0.375であることを示す。
本発明の実施形態に係る硫化物系固体電解質の平均粒径は特に限定されないが、0.01~100μmであってもよく、0.1~100μmであってもよく、0.1~50μmであってもよい。
本発明の実施形態に係る硫化物系固体電解質のイオン伝導度は、10-4S/cm以上であることが好ましく、10-3S/cm以上であることがより好ましい。硫化物系固体電解質のイオン伝導度は、例えば、当該硫化物系固体電解質の粉末0.2gを、550MPaの圧力で押圧してプレート状に成形した後、当該プレートの両面に金電極を取り付けた直径10mmのペレットを作製し、25℃において、1Hz~10MHzまでの交流インピーダンス測定を行うことで求めることができる。
(硫化物系固体電解質の製造方法)
次に、本発明の実施形態に係る硫化物系固体電解質の製造方法について説明する。
まず、アルゴンガスまたは窒素ガスなどの不活性ガス雰囲気のグローブボックス内で所定の組成となるように原料を秤量する。ここで用いる各原料は、例えば、Li、Li2S、Li2Te、LiTe3、Ge、GeS、GeS2、GeTe、S、Te等が挙げられる。
次に、本発明の実施形態に係る硫化物系固体電解質の製造方法について説明する。
まず、アルゴンガスまたは窒素ガスなどの不活性ガス雰囲気のグローブボックス内で所定の組成となるように原料を秤量する。ここで用いる各原料は、例えば、Li、Li2S、Li2Te、LiTe3、Ge、GeS、GeS2、GeTe、S、Te等が挙げられる。
次に、乳鉢などにより、5~30分混合して混合粉を作製する。このとき、混合粉の平均粒径が5~40μmとなるような時間だけ混合することが好ましい。
次に、当該混合粉をペレットにして石英アンプル中に真空封管し、石英アンプルごと400~800℃で1~20時間焼成することで、組成が、式:Li8GeS5-xTe1+x(式中、-0.5≦x<0、0<x≦0.375である。)で表される、本発明の実施形態に係る硫化物系固体電解質を作製することができる。
(全固体リチウムイオン電池)
本発明の実施形態に係る硫化物系固体電解質によって固体電解質層を形成し、当該固体電解質層と、正極層と、負極層とを含む全固体リチウムイオン電池を作製することができる。本発明の実施形態に係る全固体リチウムイオン電池を構成する正極層及び負極層は、特に限定されず、公知の材料で形成することができ、図1に示すような公知の構成とすることができる。
本発明の実施形態に係る硫化物系固体電解質によって固体電解質層を形成し、当該固体電解質層と、正極層と、負極層とを含む全固体リチウムイオン電池を作製することができる。本発明の実施形態に係る全固体リチウムイオン電池を構成する正極層及び負極層は、特に限定されず、公知の材料で形成することができ、図1に示すような公知の構成とすることができる。
リチウムイオン電池の正極層は、公知のリチウムイオン電池用正極活物質と、本発明の実施形態に係る硫化物系固体電解質または別の硫化物系固体電解質とを混合してなる正極合材を層状に形成したものである。正極合材は、さらに導電助剤を含んでもよい。当該導電助剤としては、炭素材料、金属材料、または、これらの混合物を用いることができる。導電助剤は、例えば、炭素、ニッケル、銅、アルミニウム、インジウム、銀、コバルト、マグネシウム、リチウム、クロム、金、ルテニウム、白金、ベリリウム、イリジウム、モリブデン、ニオブ、オスニウム、ロジウム、タングステン及び亜鉛からなる群より選択される少なくとも1種の元素を含んでもよい。導電助剤は、好ましくは、導電性が高い炭素単体、炭素、ニッケル、銅、銀、コバルト、マグネシウム、リチウム、ルテニウム、金、白金、ニオブ、オスニウム又はロジウムを含む金属単体、混合物又は化合物である。炭素材料としては、例えば、ケッチェンブラック、アセチレンブラック、デンカブラック、サーマルブラック、チャンネルブラック等のカーボンブラック、黒鉛、炭素繊維、活性炭等を用いることができる。
リチウムイオン電池の負極層は、公知のリチウムイオン電池用負極活物質を層状に形成したものであってもよい。また、当該負極層は、公知のリチウムイオン電池用負極活物質と、本発明の実施形態に係る硫化物系固体電解質または別の硫化物系固体電解質とを混合してなる負極合材を層状に形成したものであってもよい。負極層は、正極層と同様に、導電助剤を含んでもよい。当該導電助剤は、正極層において説明した材料と同じ材料を用いることができる。負極活物質としては、例えば、炭素材料、具体的には、人造黒鉛、黒鉛炭素繊維、樹脂焼成炭素、熱分解気相成長炭素、コークス、メソカーボンマイクロビーズ(MCMB)、フルフリルアルコール樹脂焼成炭素、ポリアセン、ピッチ系炭素繊維、気相成長炭素繊維、天然黒鉛及び難黒鉛化性炭素等、または、その混合物を用いることができる。また、負極材としては、例えば、金属リチウム、金属インジウム、金属アルミ、金属ケイ素等の金属自体や他の元素、化合物と組み合わせた合金を用いることができる。
以下、本発明及びその利点をより良く理解するための実施例を提供するが、本発明はこれらの実施例に限られるものではない。
(実施例1)
アルゴン雰囲気のグローブボックス内で所定の組成となるように原料を秤量し、乳鉢を用いて15分間混合して混合粉を作製した。次に、当該混合粉を1gのペレットにして石英アンプル中に真空封管し、石英アンプルごと700℃で8時間焼成することで、Li8GeS5.5Te0.5の組成を有する硫化物系固体電解質を得た。
この硫化物系固体電解質の粉末0.2gを、550MPaの圧力で押圧してプレート状に成形した後、当該プレートの両面に金電極を取り付けた直径10mmのペレットを作製し、25℃において、1Hz~10MHzまでの交流インピーダンス測定を行い、イオン伝導度を求めた。
また、サンプルの硫化物系固体電解質について、CuKα線を用いたX線回折測定により、X線回折(XRD:X-Ray Diffraction)グラフを得た。図2に、実施例1~7、比較例1及び参考例1に係るXRDグラフを示す。XRDグラフにおいて、「Intensity(a.u.)」のIntensityはXRD測定で検出したX線の強度を表しており、a.u.はarbitrary unitの略で任意単位であることを表す。XRDグラフにおいて、「2θ」は、入射X線方向と回折X線方向がなす角度(回折角)を示す。当該XRDグラフに基づき、アルジロダイト型構造の回折ピークの有無を確認することにより、サンプルの硫化物系固体電解質がアルジロダイト型構造を有するか否かを評価した。
アルゴン雰囲気のグローブボックス内で所定の組成となるように原料を秤量し、乳鉢を用いて15分間混合して混合粉を作製した。次に、当該混合粉を1gのペレットにして石英アンプル中に真空封管し、石英アンプルごと700℃で8時間焼成することで、Li8GeS5.5Te0.5の組成を有する硫化物系固体電解質を得た。
この硫化物系固体電解質の粉末0.2gを、550MPaの圧力で押圧してプレート状に成形した後、当該プレートの両面に金電極を取り付けた直径10mmのペレットを作製し、25℃において、1Hz~10MHzまでの交流インピーダンス測定を行い、イオン伝導度を求めた。
また、サンプルの硫化物系固体電解質について、CuKα線を用いたX線回折測定により、X線回折(XRD:X-Ray Diffraction)グラフを得た。図2に、実施例1~7、比較例1及び参考例1に係るXRDグラフを示す。XRDグラフにおいて、「Intensity(a.u.)」のIntensityはXRD測定で検出したX線の強度を表しており、a.u.はarbitrary unitの略で任意単位であることを表す。XRDグラフにおいて、「2θ」は、入射X線方向と回折X線方向がなす角度(回折角)を示す。当該XRDグラフに基づき、アルジロダイト型構造の回折ピークの有無を確認することにより、サンプルの硫化物系固体電解質がアルジロダイト型構造を有するか否かを評価した。
(実施例2)
作製した硫化物系固体電解質の組成がLi8GeS5.375Te0.625であること以外は実施例1と同様に実施した。
作製した硫化物系固体電解質の組成がLi8GeS5.375Te0.625であること以外は実施例1と同様に実施した。
(実施例3)
作製した硫化物系固体電解質の組成がLi8GeS5.25Te0.75であること以外は実施例1と同様に実施した。
作製した硫化物系固体電解質の組成がLi8GeS5.25Te0.75であること以外は実施例1と同様に実施した。
(実施例4)
作製した硫化物系固体電解質の組成がLi8GeS5.125Te0.875であること以外は実施例1と同様に実施した。
作製した硫化物系固体電解質の組成がLi8GeS5.125Te0.875であること以外は実施例1と同様に実施した。
(実施例5)
作製した硫化物系固体電解質の組成がLi8GeS4.875Te1.125であること以外は実施例1と同様に実施した。
作製した硫化物系固体電解質の組成がLi8GeS4.875Te1.125であること以外は実施例1と同様に実施した。
(実施例6)
作製した硫化物系固体電解質の組成がLi8GeS4.75Te1.25であること以外は実施例1と同様に実施した。
作製した硫化物系固体電解質の組成がLi8GeS4.75Te1.25であること以外は実施例1と同様に実施した。
(実施例7)
作製した硫化物系固体電解質の組成がLi8GeS4.625Te1.375であること以外は実施例1と同様に実施した。
作製した硫化物系固体電解質の組成がLi8GeS4.625Te1.375であること以外は実施例1と同様に実施した。
(比較例1)
作製した硫化物系固体電解質の組成がLi8GeS5.625Te0.375であること以外は実施例1と同様に実施した。
作製した硫化物系固体電解質の組成がLi8GeS5.625Te0.375であること以外は実施例1と同様に実施した。
(参考例1)
作製した硫化物系固体電解質の組成がLi8GeS5Teであること以外は実施例1と同様に実施した。
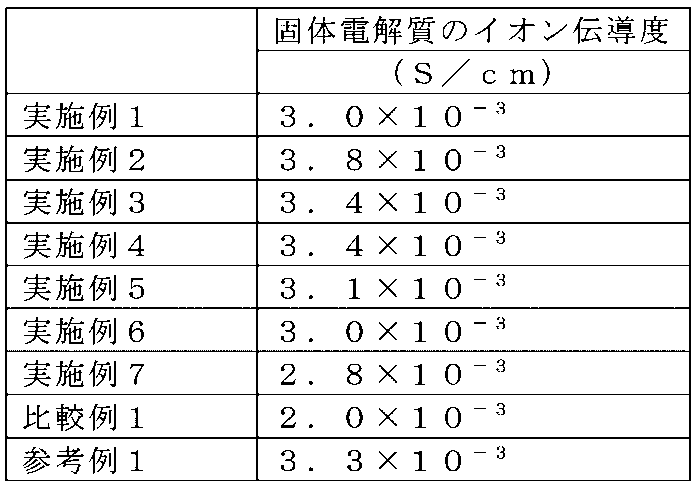
上記結果を表1に示す。
作製した硫化物系固体電解質の組成がLi8GeS5Teであること以外は実施例1と同様に実施した。
上記結果を表1に示す。
(評価結果)
実施例1~7、参考例1の固体電解質については、いずれもXRDグラフにおいて、2θ=24.3±1.0°及び28.7±1.0°に強い回折ピークが確認され、アルジロダイト型構造を有していた。比較例1の固体電解質は、XRDグラフにおいて、2θ=24.3±1.0°及び28.7±1.0°に実施例1~7、参考例1ほどの強い回折ピークが確認されなかった。
また、実施例1~7、参考例1の固体電解質は、式:Li8GeS5-xTe1+x(式中、-0.5≦x<0、0<x≦0.375である。)で示す組成を有していたが、比較例1は当該組成を有していなかった。
このため、実施例1~7、参考例1に係る固体電解質は、アルジロダイト型構造を有さず、また、上記組成を有さない比較例1よりも、イオン伝導度が良好であった。従って、実施例1~7、参考例1に係る固体電解質を用いた全固体リチウムイオン電池の電池容量の向上が期待できる。
実施例1~7、参考例1の固体電解質については、いずれもXRDグラフにおいて、2θ=24.3±1.0°及び28.7±1.0°に強い回折ピークが確認され、アルジロダイト型構造を有していた。比較例1の固体電解質は、XRDグラフにおいて、2θ=24.3±1.0°及び28.7±1.0°に実施例1~7、参考例1ほどの強い回折ピークが確認されなかった。
また、実施例1~7、参考例1の固体電解質は、式:Li8GeS5-xTe1+x(式中、-0.5≦x<0、0<x≦0.375である。)で示す組成を有していたが、比較例1は当該組成を有していなかった。
このため、実施例1~7、参考例1に係る固体電解質は、アルジロダイト型構造を有さず、また、上記組成を有さない比較例1よりも、イオン伝導度が良好であった。従って、実施例1~7、参考例1に係る固体電解質を用いた全固体リチウムイオン電池の電池容量の向上が期待できる。
Claims (3)
- アルジロダイト型構造を有する硫化物系固体電解質であって、組成が、
式:Li8GeS5-xTe1+x
(式中、-0.5≦x<0、0<x≦0.375である。)
で表される硫化物系固体電解質。 - 前記式中、-0.375≦x<0である請求項1に記載の硫化物系固体電解質。
- 請求項1または2に記載の硫化物系固体電解質で構成された固体電解質層と、正極層と、負極層とを含む全固体リチウムイオン電池。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US17/925,206 US20230198006A1 (en) | 2020-09-24 | 2021-04-12 | Sulfide-based solid electrolyte and all-solid lithium ion battery |
| EP21871880.7A EP4122880A4 (en) | 2020-09-24 | 2021-04-12 | SULFIDE-BASED SOLID ELECTROLYTE AND LITHIUM-ION SOLID-STATE BATTERY |
| CN202180039056.6A CN115699391A (zh) | 2020-09-24 | 2021-04-12 | 硫化物系固体电解质和全固态锂离子电池 |
| KR1020237008654A KR20230051249A (ko) | 2020-09-24 | 2021-04-12 | 황화물계 고체 전해질 및 전고체 리튬 이온 전지 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020160154A JP7477414B2 (ja) | 2020-09-24 | 2020-09-24 | 硫化物系固体電解質及び全固体リチウムイオン電池 |
| JP2020-160154 | 2020-09-24 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2022064744A1 true WO2022064744A1 (ja) | 2022-03-31 |
Family
ID=80845151
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2021/015220 WO2022064744A1 (ja) | 2020-09-24 | 2021-04-12 | 硫化物系固体電解質及び全固体リチウムイオン電池 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20230198006A1 (ja) |
| EP (1) | EP4122880A4 (ja) |
| JP (1) | JP7477414B2 (ja) |
| KR (1) | KR20230051249A (ja) |
| CN (1) | CN115699391A (ja) |
| WO (1) | WO2022064744A1 (ja) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017007030A1 (ja) * | 2015-07-09 | 2017-01-12 | 国立大学法人東京工業大学 | リチウム固体電解質 |
| JP2018029058A (ja) * | 2016-08-12 | 2018-02-22 | 出光興産株式会社 | 硫化物固体電解質 |
-
2020
- 2020-09-24 JP JP2020160154A patent/JP7477414B2/ja active Active
-
2021
- 2021-04-12 US US17/925,206 patent/US20230198006A1/en active Pending
- 2021-04-12 EP EP21871880.7A patent/EP4122880A4/en active Pending
- 2021-04-12 CN CN202180039056.6A patent/CN115699391A/zh active Pending
- 2021-04-12 KR KR1020237008654A patent/KR20230051249A/ko unknown
- 2021-04-12 WO PCT/JP2021/015220 patent/WO2022064744A1/ja unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017007030A1 (ja) * | 2015-07-09 | 2017-01-12 | 国立大学法人東京工業大学 | リチウム固体電解質 |
| JP2018029058A (ja) * | 2016-08-12 | 2018-02-22 | 出光興産株式会社 | 硫化物固体電解質 |
Non-Patent Citations (1)
| Title |
|---|
| J. MATER. CHEM. A, vol. 7, 2019, pages 2717 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20230051249A (ko) | 2023-04-17 |
| CN115699391A (zh) | 2023-02-03 |
| EP4122880A1 (en) | 2023-01-25 |
| JP7477414B2 (ja) | 2024-05-01 |
| JP2022053358A (ja) | 2022-04-05 |
| US20230198006A1 (en) | 2023-06-22 |
| EP4122880A4 (en) | 2024-05-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP3454405B1 (en) | Sulfide-based solid electrolyte for lithium secondary battery | |
| US11760649B2 (en) | Solid electrolyte material and battery | |
| US11427477B2 (en) | Solid electrolyte material and battery | |
| KR101807583B1 (ko) | 리튬이온 전지용 황화물계 고체 전해질 | |
| KR101826407B1 (ko) | 황화물 고체 전해질 재료, 전지 및 황화물 고체 전해질 재료의 제조 방법 | |
| KR101665465B1 (ko) | 리튬 이온 전지용 황화물계 고체 전해질 | |
| JPWO2019135317A1 (ja) | 固体電解質材料、および、電池 | |
| CN111295721B (zh) | 固体电解质材料及电池 | |
| EP3754774A1 (en) | Sulfide-type compound particles, solid electrolyte, and lithium secondary battery | |
| JP6798477B2 (ja) | 硫化物固体電解質 | |
| JP7164939B2 (ja) | 全固体型二次電池 | |
| WO2022064744A1 (ja) | 硫化物系固体電解質及び全固体リチウムイオン電池 | |
| JP7301005B2 (ja) | 硫化物系固体電解質及び全固体リチウムイオン電池 | |
| CN115152068A (zh) | 固体电解质、锂离子蓄电元件和蓄电装置 | |
| WO2024105906A1 (ja) | 硫化物系固体電解質及び全固体リチウムイオン電池 | |
| JP2022126504A (ja) | 硫化物系固体電解質及び全固体リチウムイオン電池 | |
| JP2021132019A (ja) | 固体電解質材料、その製造方法及び電池 | |
| JP7301013B2 (ja) | 硫化物系固体電解質及び全固体リチウムイオン電池 | |
| JP2023051467A (ja) | 硫化物系固体電解質及び全固体リチウムイオン電池 | |
| JP2024073233A (ja) | 硫化物系固体電解質及び全固体リチウムイオン電池 | |
| WO2024024823A1 (ja) | 固体電解質組成物、固体電解質層又は電極合材、及びリチウムイオン電池 | |
| KR20190051519A (ko) | 고체 전해질 재료, 이의 제조방법, 및 이를 포함하는 전고체 전지 | |
| TW202126575A (zh) | 硫化物系化合物粒子、固體電解質及鋰二次電池 | |
| KR20230040519A (ko) | 황화물계 고체전해질, 이의 제조방법 및 이를 포함하는 전고체 전지 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 21871880 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2021871880 Country of ref document: EP Effective date: 20221018 |
|
| ENP | Entry into the national phase |
Ref document number: 20237008654 Country of ref document: KR Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |