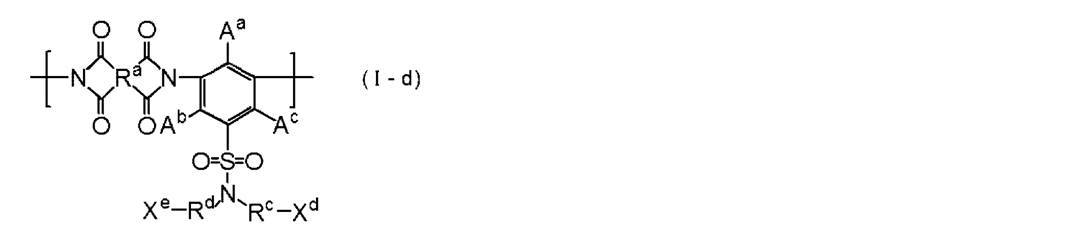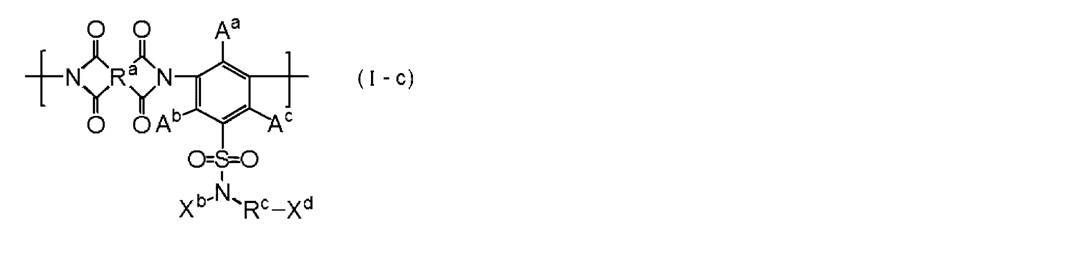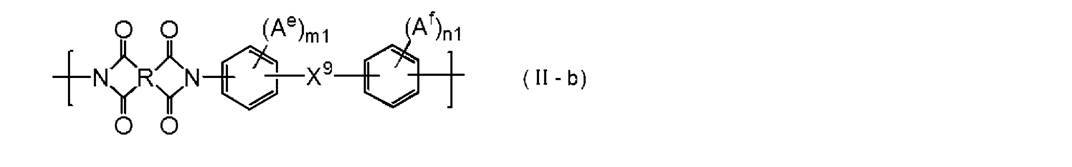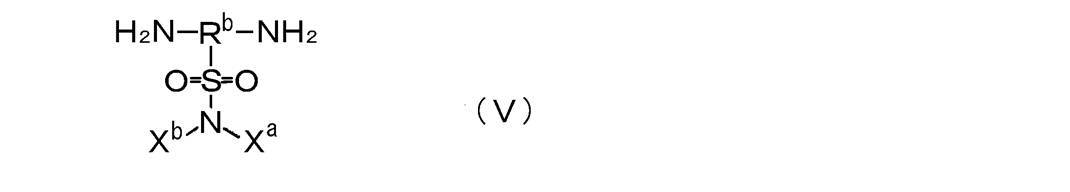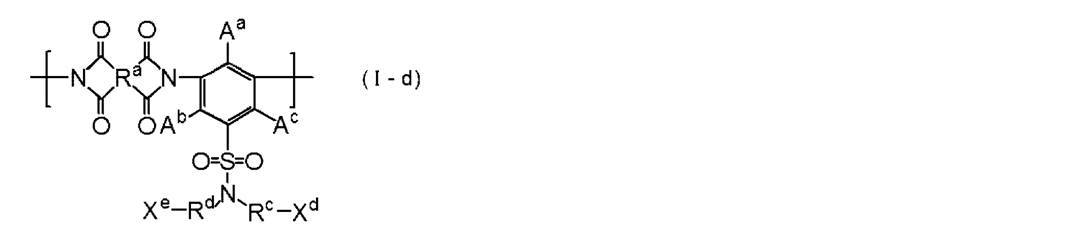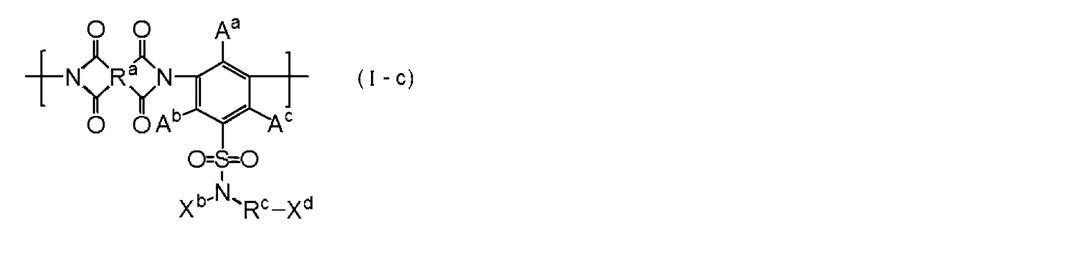WO2018043149A1 - ガス分離膜、ガス分離モジュール、ガス分離装置、ガス分離方法及びポリイミド化合物 - Google Patents
ガス分離膜、ガス分離モジュール、ガス分離装置、ガス分離方法及びポリイミド化合物 Download PDFInfo
- Publication number
- WO2018043149A1 WO2018043149A1 PCT/JP2017/029540 JP2017029540W WO2018043149A1 WO 2018043149 A1 WO2018043149 A1 WO 2018043149A1 JP 2017029540 W JP2017029540 W JP 2017029540W WO 2018043149 A1 WO2018043149 A1 WO 2018043149A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- gas separation
- formula
- carbon atoms
- substituent
- Prior art date
Links
- 238000000926 separation method Methods 0.000 title claims abstract description 258
- 239000004642 Polyimide Substances 0.000 title claims abstract description 144
- 229920001721 polyimide Polymers 0.000 title claims abstract description 144
- 239000012528 membrane Substances 0.000 title claims abstract description 143
- 150000001875 compounds Chemical class 0.000 title claims abstract description 107
- 239000007789 gas Substances 0.000 claims abstract description 321
- 125000001424 substituent group Chemical group 0.000 claims abstract description 105
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims abstract description 56
- 125000004432 carbon atom Chemical group C* 0.000 claims description 218
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 claims description 104
- 125000000217 alkyl group Chemical group 0.000 claims description 82
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 claims description 60
- 229910002092 carbon dioxide Inorganic materials 0.000 claims description 52
- 125000003118 aryl group Chemical group 0.000 claims description 43
- 239000001569 carbon dioxide Substances 0.000 claims description 40
- 239000002131 composite material Substances 0.000 claims description 37
- 229910052731 fluorine Inorganic materials 0.000 claims description 26
- 125000001153 fluoro group Chemical group F* 0.000 claims description 26
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 claims description 23
- 125000002947 alkylene group Chemical group 0.000 claims description 14
- 239000004745 nonwoven fabric Substances 0.000 claims description 14
- 125000000732 arylene group Chemical group 0.000 claims description 13
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 13
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 12
- 125000002993 cycloalkylene group Chemical group 0.000 claims description 11
- 239000000463 material Substances 0.000 claims description 11
- 229910052757 nitrogen Inorganic materials 0.000 claims description 11
- 125000004434 sulfur atom Chemical group 0.000 claims description 11
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims description 8
- 239000000470 constituent Substances 0.000 claims description 6
- 125000005462 imide group Chemical group 0.000 claims description 3
- 230000035699 permeability Effects 0.000 abstract description 35
- 239000002994 raw material Substances 0.000 abstract description 8
- -1 thiocarbamoyl group Chemical group 0.000 description 199
- 239000010410 layer Substances 0.000 description 143
- 230000015572 biosynthetic process Effects 0.000 description 61
- 238000003786 synthesis reaction Methods 0.000 description 55
- 239000000126 substance Substances 0.000 description 47
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 46
- 125000005647 linker group Chemical group 0.000 description 46
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 35
- 229920000642 polymer Polymers 0.000 description 34
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 33
- 239000000543 intermediate Substances 0.000 description 33
- 125000003277 amino group Chemical group 0.000 description 32
- 238000006243 chemical reaction Methods 0.000 description 31
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 30
- 239000000243 solution Substances 0.000 description 29
- 238000000034 method Methods 0.000 description 25
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 24
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 22
- 239000003431 cross linking reagent Substances 0.000 description 22
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical group [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 21
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 19
- 125000003700 epoxy group Chemical group 0.000 description 19
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 18
- 239000003960 organic solvent Substances 0.000 description 18
- 150000004985 diamines Chemical class 0.000 description 17
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 16
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 15
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 15
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 14
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 14
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 14
- 239000011241 protective layer Substances 0.000 description 14
- 125000002252 acyl group Chemical group 0.000 description 13
- 125000004429 atom Chemical group 0.000 description 13
- 230000000052 comparative effect Effects 0.000 description 13
- 239000010408 film Substances 0.000 description 13
- 239000007788 liquid Substances 0.000 description 13
- 239000000203 mixture Substances 0.000 description 13
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 12
- 125000004442 acylamino group Chemical group 0.000 description 12
- 125000000753 cycloalkyl group Chemical group 0.000 description 12
- 125000000623 heterocyclic group Chemical group 0.000 description 12
- 229910052751 metal Inorganic materials 0.000 description 12
- 239000002184 metal Substances 0.000 description 12
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 11
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 11
- 125000005843 halogen group Chemical group 0.000 description 11
- 239000002904 solvent Substances 0.000 description 11
- 238000012360 testing method Methods 0.000 description 11
- 125000003396 thiol group Chemical group [H]S* 0.000 description 11
- 229910052799 carbon Inorganic materials 0.000 description 10
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 10
- 229910052739 hydrogen Inorganic materials 0.000 description 10
- 239000001257 hydrogen Substances 0.000 description 10
- 238000005259 measurement Methods 0.000 description 10
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 9
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 9
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 9
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 9
- 125000003545 alkoxy group Chemical group 0.000 description 9
- 239000011248 coating agent Substances 0.000 description 9
- 238000000576 coating method Methods 0.000 description 9
- 239000012535 impurity Substances 0.000 description 9
- 238000004519 manufacturing process Methods 0.000 description 9
- 125000000020 sulfo group Chemical group O=S(=O)([*])O[H] 0.000 description 9
- ALYNCZNDIQEVRV-UHFFFAOYSA-N 4-aminobenzoic acid Chemical compound NC1=CC=C(C(O)=O)C=C1 ALYNCZNDIQEVRV-UHFFFAOYSA-N 0.000 description 8
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 8
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 8
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 8
- 125000003342 alkenyl group Chemical group 0.000 description 8
- 238000001816 cooling Methods 0.000 description 8
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 8
- BGTOWKSIORTVQH-UHFFFAOYSA-N cyclopentanone Chemical compound O=C1CCCC1 BGTOWKSIORTVQH-UHFFFAOYSA-N 0.000 description 8
- SWXVUIWOUIDPGS-UHFFFAOYSA-N diacetone alcohol Chemical compound CC(=O)CC(C)(C)O SWXVUIWOUIDPGS-UHFFFAOYSA-N 0.000 description 8
- 238000007654 immersion Methods 0.000 description 8
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 8
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 8
- 229920006294 polydialkylsiloxane Polymers 0.000 description 8
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 7
- 125000000304 alkynyl group Chemical group 0.000 description 7
- 239000000460 chlorine Substances 0.000 description 7
- 238000005345 coagulation Methods 0.000 description 7
- 230000015271 coagulation Effects 0.000 description 7
- 229920001577 copolymer Polymers 0.000 description 7
- 238000001035 drying Methods 0.000 description 7
- 239000012510 hollow fiber Substances 0.000 description 7
- 229920002239 polyacrylonitrile Polymers 0.000 description 7
- 229920001296 polysiloxane Polymers 0.000 description 7
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 7
- GQHTUMJGOHRCHB-UHFFFAOYSA-N 2,3,4,6,7,8,9,10-octahydropyrimido[1,2-a]azepine Chemical compound C1CCCCN2CCCN=C21 GQHTUMJGOHRCHB-UHFFFAOYSA-N 0.000 description 6
- 125000005619 boric acid group Chemical group 0.000 description 6
- 150000004696 coordination complex Chemical class 0.000 description 6
- 238000011156 evaluation Methods 0.000 description 6
- 238000012423 maintenance Methods 0.000 description 6
- 230000002829 reductive effect Effects 0.000 description 6
- 229920005989 resin Polymers 0.000 description 6
- 239000011347 resin Substances 0.000 description 6
- 239000007787 solid Substances 0.000 description 6
- 229910052717 sulfur Inorganic materials 0.000 description 6
- 229920002554 vinyl polymer Polymers 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 125000004423 acyloxy group Chemical group 0.000 description 5
- 125000004104 aryloxy group Chemical group 0.000 description 5
- 125000001951 carbamoylamino group Chemical group C(N)(=O)N* 0.000 description 5
- 229910052801 chlorine Inorganic materials 0.000 description 5
- 125000001309 chloro group Chemical group Cl* 0.000 description 5
- 235000014113 dietary fatty acids Nutrition 0.000 description 5
- 239000004205 dimethyl polysiloxane Substances 0.000 description 5
- 239000000194 fatty acid Substances 0.000 description 5
- 229930195729 fatty acid Natural products 0.000 description 5
- 230000003993 interaction Effects 0.000 description 5
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 5
- 239000003446 ligand Substances 0.000 description 5
- 125000003566 oxetanyl group Chemical group 0.000 description 5
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 5
- 239000011148 porous material Substances 0.000 description 5
- 125000000547 substituted alkyl group Chemical group 0.000 description 5
- ARXJGSRGQADJSQ-UHFFFAOYSA-N 1-methoxypropan-2-ol Chemical compound COCC(C)O ARXJGSRGQADJSQ-UHFFFAOYSA-N 0.000 description 4
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical group [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 4
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical group [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 4
- DKPFZGUDAPQIHT-UHFFFAOYSA-N Butyl acetate Natural products CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- 239000004593 Epoxy Substances 0.000 description 4
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 4
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 4
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 4
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 4
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 4
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 4
- GTDPSWPPOUPBNX-UHFFFAOYSA-N ac1mqpva Chemical compound CC12C(=O)OC(=O)C1(C)C1(C)C2(C)C(=O)OC1=O GTDPSWPPOUPBNX-UHFFFAOYSA-N 0.000 description 4
- 239000002253 acid Substances 0.000 description 4
- 229910052782 aluminium Inorganic materials 0.000 description 4
- 150000001408 amides Chemical class 0.000 description 4
- 229960004050 aminobenzoic acid Drugs 0.000 description 4
- FZFAMSAMCHXGEF-UHFFFAOYSA-N chloro formate Chemical compound ClOC=O FZFAMSAMCHXGEF-UHFFFAOYSA-N 0.000 description 4
- 235000013870 dimethyl polysiloxane Nutrition 0.000 description 4
- 150000002148 esters Chemical class 0.000 description 4
- 125000005842 heteroatom Chemical group 0.000 description 4
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 4
- 229930195733 hydrocarbon Natural products 0.000 description 4
- 150000002430 hydrocarbons Chemical class 0.000 description 4
- 229910052740 iodine Inorganic materials 0.000 description 4
- ZXEKIIBDNHEJCQ-UHFFFAOYSA-N isobutanol Chemical compound CC(C)CO ZXEKIIBDNHEJCQ-UHFFFAOYSA-N 0.000 description 4
- 125000001624 naphthyl group Chemical group 0.000 description 4
- 125000000843 phenylene group Chemical group C1(=C(C=CC=C1)*)* 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 4
- 230000005855 radiation Effects 0.000 description 4
- 238000006467 substitution reaction Methods 0.000 description 4
- 239000004094 surface-active agent Substances 0.000 description 4
- 125000006158 tetracarboxylic acid group Chemical group 0.000 description 4
- 239000010936 titanium Substances 0.000 description 4
- QAEDZJGFFMLHHQ-UHFFFAOYSA-N trifluoroacetic anhydride Chemical compound FC(F)(F)C(=O)OC(=O)C(F)(F)F QAEDZJGFFMLHHQ-UHFFFAOYSA-N 0.000 description 4
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 4
- SBASXUCJHJRPEV-UHFFFAOYSA-N 2-(2-methoxyethoxy)ethanol Chemical compound COCCOCCO SBASXUCJHJRPEV-UHFFFAOYSA-N 0.000 description 3
- NEAQRZUHTPSBBM-UHFFFAOYSA-N 2-hydroxy-3,3-dimethyl-7-nitro-4h-isoquinolin-1-one Chemical compound C1=C([N+]([O-])=O)C=C2C(=O)N(O)C(C)(C)CC2=C1 NEAQRZUHTPSBBM-UHFFFAOYSA-N 0.000 description 3
- PKKGGWLTUCMSSD-UHFFFAOYSA-N 3,5-diamino-2,4,6-trimethylbenzenesulfonic acid Chemical compound CC1=C(N)C(C)=C(S(O)(=O)=O)C(C)=C1N PKKGGWLTUCMSSD-UHFFFAOYSA-N 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- 239000004215 Carbon black (E152) Substances 0.000 description 3
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 3
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 3
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 125000003282 alkyl amino group Chemical group 0.000 description 3
- 125000004103 aminoalkyl group Chemical group 0.000 description 3
- 125000001769 aryl amino group Chemical group 0.000 description 3
- 229910052796 boron Inorganic materials 0.000 description 3
- 238000004132 cross linking Methods 0.000 description 3
- 125000006310 cycloalkyl amino group Chemical group 0.000 description 3
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 3
- 230000018044 dehydration Effects 0.000 description 3
- 238000006297 dehydration reaction Methods 0.000 description 3
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 3
- 239000000835 fiber Substances 0.000 description 3
- 125000000524 functional group Chemical group 0.000 description 3
- ANSXAPJVJOKRDJ-UHFFFAOYSA-N furo[3,4-f][2]benzofuran-1,3,5,7-tetrone Chemical compound C1=C2C(=O)OC(=O)C2=CC2=C1C(=O)OC2=O ANSXAPJVJOKRDJ-UHFFFAOYSA-N 0.000 description 3
- 238000001641 gel filtration chromatography Methods 0.000 description 3
- 125000005417 glycidoxyalkyl group Chemical group 0.000 description 3
- 230000020169 heat generation Effects 0.000 description 3
- 238000010438 heat treatment Methods 0.000 description 3
- 125000000717 hydrazino group Chemical group [H]N([*])N([H])[H] 0.000 description 3
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 3
- 229910052738 indium Inorganic materials 0.000 description 3
- SKTCDJAMAYNROS-UHFFFAOYSA-N methoxycyclopentane Chemical compound COC1CCCC1 SKTCDJAMAYNROS-UHFFFAOYSA-N 0.000 description 3
- 238000002156 mixing Methods 0.000 description 3
- 230000004048 modification Effects 0.000 description 3
- 238000012986 modification Methods 0.000 description 3
- 239000003345 natural gas Substances 0.000 description 3
- MWUXSHHQAYIFBG-UHFFFAOYSA-N nitrogen oxide Inorganic materials O=[N] MWUXSHHQAYIFBG-UHFFFAOYSA-N 0.000 description 3
- 230000036961 partial effect Effects 0.000 description 3
- ABLZXFCXXLZCGV-UHFFFAOYSA-N phosphonic acid group Chemical group P(O)(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 3
- 229920003023 plastic Polymers 0.000 description 3
- 239000004033 plastic Substances 0.000 description 3
- 238000006116 polymerization reaction Methods 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 125000000213 sulfino group Chemical group [H]OS(*)=O 0.000 description 3
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 3
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 3
- 229910052719 titanium Inorganic materials 0.000 description 3
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 3
- CYSGHNMQYZDMIA-UHFFFAOYSA-N 1,3-Dimethyl-2-imidazolidinon Chemical compound CN1CCN(C)C1=O CYSGHNMQYZDMIA-UHFFFAOYSA-N 0.000 description 2
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 2
- PLIKAWJENQZMHA-UHFFFAOYSA-N 4-aminophenol Chemical compound NC1=CC=C(O)C=C1 PLIKAWJENQZMHA-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 2
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 2
- OTMSDBZUPAUEDD-UHFFFAOYSA-N Ethane Chemical compound CC OTMSDBZUPAUEDD-UHFFFAOYSA-N 0.000 description 2
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical class C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 2
- YCKRFDGAMUMZLT-UHFFFAOYSA-N Fluorine atom Chemical compound [F] YCKRFDGAMUMZLT-UHFFFAOYSA-N 0.000 description 2
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical group OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 239000004698 Polyethylene Substances 0.000 description 2
- 239000004743 Polypropylene Substances 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 2
- 229910018557 Si O Inorganic materials 0.000 description 2
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 2
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 2
- 239000000370 acceptor Substances 0.000 description 2
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 2
- 230000009471 action Effects 0.000 description 2
- 125000003158 alcohol group Chemical group 0.000 description 2
- 125000006323 alkenyl amino group Chemical group 0.000 description 2
- 125000004466 alkoxycarbonylamino group Chemical group 0.000 description 2
- 125000004414 alkyl thio group Chemical group 0.000 description 2
- 125000006319 alkynyl amino group Chemical group 0.000 description 2
- 235000011114 ammonium hydroxide Nutrition 0.000 description 2
- 125000005100 aryl amino carbonyl group Chemical group 0.000 description 2
- 125000005162 aryl oxy carbonyl amino group Chemical group 0.000 description 2
- 125000005161 aryl oxy carbonyl group Chemical group 0.000 description 2
- 125000005110 aryl thio group Chemical group 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 230000005540 biological transmission Effects 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 150000001721 carbon Chemical group 0.000 description 2
- 125000004181 carboxyalkyl group Chemical group 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 125000004965 chloroalkyl group Chemical group 0.000 description 2
- 239000011651 chromium Substances 0.000 description 2
- 238000004440 column chromatography Methods 0.000 description 2
- 239000010949 copper Substances 0.000 description 2
- OPQARKPSCNTWTJ-UHFFFAOYSA-L copper(ii) acetate Chemical compound [Cu+2].CC([O-])=O.CC([O-])=O OPQARKPSCNTWTJ-UHFFFAOYSA-L 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 230000007547 defect Effects 0.000 description 2
- 239000002270 dispersing agent Substances 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- 125000003709 fluoroalkyl group Chemical group 0.000 description 2
- 238000005187 foaming Methods 0.000 description 2
- 229910052733 gallium Inorganic materials 0.000 description 2
- 230000014509 gene expression Effects 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 229910052742 iron Inorganic materials 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 239000011572 manganese Substances 0.000 description 2
- 125000005358 mercaptoalkyl group Chemical group 0.000 description 2
- 229940098779 methanesulfonic acid Drugs 0.000 description 2
- 239000000178 monomer Substances 0.000 description 2
- 229910052759 nickel Inorganic materials 0.000 description 2
- 239000002736 nonionic surfactant Substances 0.000 description 2
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- 125000001820 oxy group Chemical group [*:1]O[*:2] 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 238000012856 packing Methods 0.000 description 2
- 125000005010 perfluoroalkyl group Chemical group 0.000 description 2
- 238000005191 phase separation Methods 0.000 description 2
- 229920005575 poly(amic acid) Polymers 0.000 description 2
- 238000012643 polycondensation polymerization Methods 0.000 description 2
- 229920000573 polyethylene Polymers 0.000 description 2
- 229920001155 polypropylene Polymers 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 2
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- LIVNPJMFVYWSIS-UHFFFAOYSA-N silicon monoxide Inorganic materials [Si-]#[O+] LIVNPJMFVYWSIS-UHFFFAOYSA-N 0.000 description 2
- 125000004469 siloxy group Chemical group [SiH3]O* 0.000 description 2
- 125000003808 silyl group Chemical group [H][Si]([H])([H])[*] 0.000 description 2
- 238000004528 spin coating Methods 0.000 description 2
- 125000000475 sulfinyl group Chemical group [*:2]S([*:1])=O 0.000 description 2
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 2
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 2
- 239000011593 sulfur Substances 0.000 description 2
- 125000004149 thio group Chemical group *S* 0.000 description 2
- FYSNRJHAOHDILO-UHFFFAOYSA-N thionyl chloride Chemical compound ClS(Cl)=O FYSNRJHAOHDILO-UHFFFAOYSA-N 0.000 description 2
- VXUYXOFXAQZZMF-UHFFFAOYSA-N titanium(IV) isopropoxide Chemical compound CC(C)O[Ti](OC(C)C)(OC(C)C)OC(C)C VXUYXOFXAQZZMF-UHFFFAOYSA-N 0.000 description 2
- HVLLSGMXQDNUAL-UHFFFAOYSA-N triphenyl phosphite Chemical compound C=1C=CC=CC=1OP(OC=1C=CC=CC=1)OC1=CC=CC=C1 HVLLSGMXQDNUAL-UHFFFAOYSA-N 0.000 description 2
- 229910052727 yttrium Inorganic materials 0.000 description 2
- 229910052725 zinc Inorganic materials 0.000 description 2
- 239000011701 zinc Substances 0.000 description 2
- JIAARYAFYJHUJI-UHFFFAOYSA-L zinc dichloride Chemical compound [Cl-].[Cl-].[Zn+2] JIAARYAFYJHUJI-UHFFFAOYSA-L 0.000 description 2
- 229910052726 zirconium Inorganic materials 0.000 description 2
- ZVYYAYJIGYODSD-LNTINUHCSA-K (z)-4-bis[[(z)-4-oxopent-2-en-2-yl]oxy]gallanyloxypent-3-en-2-one Chemical compound [Ga+3].C\C([O-])=C\C(C)=O.C\C([O-])=C\C(C)=O.C\C([O-])=C\C(C)=O ZVYYAYJIGYODSD-LNTINUHCSA-K 0.000 description 1
- YOBOXHGSEJBUPB-MTOQALJVSA-N (z)-4-hydroxypent-3-en-2-one;zirconium Chemical compound [Zr].C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O YOBOXHGSEJBUPB-MTOQALJVSA-N 0.000 description 1
- KEQGZUUPPQEDPF-UHFFFAOYSA-N 1,3-dichloro-5,5-dimethylimidazolidine-2,4-dione Chemical compound CC1(C)N(Cl)C(=O)N(Cl)C1=O KEQGZUUPPQEDPF-UHFFFAOYSA-N 0.000 description 1
- WZCQRUWWHSTZEM-UHFFFAOYSA-N 1,3-phenylenediamine Chemical compound NC1=CC=CC(N)=C1 WZCQRUWWHSTZEM-UHFFFAOYSA-N 0.000 description 1
- 125000006219 1-ethylpentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 description 1
- IBLKWZIFZMJLFL-UHFFFAOYSA-N 1-phenoxypropan-2-ol Chemical compound CC(O)COC1=CC=CC=C1 IBLKWZIFZMJLFL-UHFFFAOYSA-N 0.000 description 1
- YQTCQNIPQMJNTI-UHFFFAOYSA-N 2,2-dimethylpropan-1-one Chemical group CC(C)(C)[C]=O YQTCQNIPQMJNTI-UHFFFAOYSA-N 0.000 description 1
- WCZNKVPCIFMXEQ-UHFFFAOYSA-N 2,3,5,6-tetramethylbenzene-1,4-diamine Chemical compound CC1=C(C)C(N)=C(C)C(C)=C1N WCZNKVPCIFMXEQ-UHFFFAOYSA-N 0.000 description 1
- CUDYYMUUJHLCGZ-UHFFFAOYSA-N 2-(2-methoxypropoxy)propan-1-ol Chemical compound COC(C)COC(C)CO CUDYYMUUJHLCGZ-UHFFFAOYSA-N 0.000 description 1
- XNWFRZJHXBZDAG-UHFFFAOYSA-N 2-METHOXYETHANOL Chemical group COCCO XNWFRZJHXBZDAG-UHFFFAOYSA-N 0.000 description 1
- QCDWFXQBSFUVSP-UHFFFAOYSA-N 2-phenoxyethanol Chemical compound OCCOC1=CC=CC=C1 QCDWFXQBSFUVSP-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- SZRDJHHKIJHJHQ-UHFFFAOYSA-N 3,4,5-trifluoroaniline Chemical compound NC1=CC(F)=C(F)C(F)=C1 SZRDJHHKIJHJHQ-UHFFFAOYSA-N 0.000 description 1
- WAKMMQSMEDJRRI-UHFFFAOYSA-N 3,5-bis(trifluoromethyl)benzoyl chloride Chemical compound FC(F)(F)C1=CC(C(Cl)=O)=CC(C(F)(F)F)=C1 WAKMMQSMEDJRRI-UHFFFAOYSA-N 0.000 description 1
- XBIUWALDKXACEA-UHFFFAOYSA-N 3-[bis(2,4-dioxopentan-3-yl)alumanyl]pentane-2,4-dione Chemical compound CC(=O)C(C(C)=O)[Al](C(C(C)=O)C(C)=O)C(C(C)=O)C(C)=O XBIUWALDKXACEA-UHFFFAOYSA-N 0.000 description 1
- FLROJJGKUKLCAE-UHFFFAOYSA-N 3-amino-2-methylphenol Chemical compound CC1=C(N)C=CC=C1O FLROJJGKUKLCAE-UHFFFAOYSA-N 0.000 description 1
- DKIDEFUBRARXTE-UHFFFAOYSA-N 3-mercaptopropanoic acid Chemical compound OC(=O)CCS DKIDEFUBRARXTE-UHFFFAOYSA-N 0.000 description 1
- QJENIOQDYXRGLF-UHFFFAOYSA-N 4-[(4-amino-3-ethyl-5-methylphenyl)methyl]-2-ethyl-6-methylaniline Chemical compound CC1=C(N)C(CC)=CC(CC=2C=C(CC)C(N)=C(C)C=2)=C1 QJENIOQDYXRGLF-UHFFFAOYSA-N 0.000 description 1
- 125000000590 4-methylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 1
- ODGIMMLDVSWADK-UHFFFAOYSA-N 4-trifluoromethylaniline Chemical compound NC1=CC=C(C(F)(F)F)C=C1 ODGIMMLDVSWADK-UHFFFAOYSA-N 0.000 description 1
- VQVIHDPBMFABCQ-UHFFFAOYSA-N 5-(1,3-dioxo-2-benzofuran-5-carbonyl)-2-benzofuran-1,3-dione Chemical compound C1=C2C(=O)OC(=O)C2=CC(C(C=2C=C3C(=O)OC(=O)C3=CC=2)=O)=C1 VQVIHDPBMFABCQ-UHFFFAOYSA-N 0.000 description 1
- QHHKLPCQTTWFSS-UHFFFAOYSA-N 5-[2-(1,3-dioxo-2-benzofuran-5-yl)-1,1,1,3,3,3-hexafluoropropan-2-yl]-2-benzofuran-1,3-dione Chemical compound C1=C2C(=O)OC(=O)C2=CC(C(C=2C=C3C(=O)OC(=O)C3=CC=2)(C(F)(F)F)C(F)(F)F)=C1 QHHKLPCQTTWFSS-UHFFFAOYSA-N 0.000 description 1
- 125000003341 7 membered heterocyclic group Chemical group 0.000 description 1
- 229920000178 Acrylic resin Polymers 0.000 description 1
- 239000004925 Acrylic resin Substances 0.000 description 1
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 1
- KZMGYPLQYOPHEL-UHFFFAOYSA-N Boron trifluoride etherate Chemical compound FB(F)F.CCOCC KZMGYPLQYOPHEL-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical compound S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 1
- GYHNNYVSQQEPJS-UHFFFAOYSA-N Gallium Chemical compound [Ga] GYHNNYVSQQEPJS-UHFFFAOYSA-N 0.000 description 1
- 229910021578 Iron(III) chloride Inorganic materials 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- PWHULOQIROXLJO-UHFFFAOYSA-N Manganese Chemical compound [Mn] PWHULOQIROXLJO-UHFFFAOYSA-N 0.000 description 1
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 239000004695 Polyether sulfone Substances 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004721 Polyphenylene oxide Substances 0.000 description 1
- 229920001214 Polysorbate 60 Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 229920001800 Shellac Polymers 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 238000004833 X-ray photoelectron spectroscopy Methods 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 125000000738 acetamido group Chemical group [H]C([H])([H])C(=O)N([H])[*] 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 125000005595 acetylacetonate group Chemical group 0.000 description 1
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 description 1
- 150000008065 acid anhydrides Chemical class 0.000 description 1
- 125000003647 acryloyl group Chemical group O=C([*])C([H])=C([H])[H] 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 125000005599 alkyl carboxylate group Chemical group 0.000 description 1
- 150000005215 alkyl ethers Chemical class 0.000 description 1
- 125000005037 alkyl phenyl group Chemical group 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- SMZOGRDCAXLAAR-UHFFFAOYSA-N aluminium isopropoxide Chemical compound [Al+3].CC(C)[O-].CC(C)[O-].CC(C)[O-] SMZOGRDCAXLAAR-UHFFFAOYSA-N 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- MHDLAWFYLQAULB-UHFFFAOYSA-N anilinophosphonic acid Chemical compound OP(O)(=O)NC1=CC=CC=C1 MHDLAWFYLQAULB-UHFFFAOYSA-N 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- 125000005427 anthranyl group Chemical group 0.000 description 1
- 150000001491 aromatic compounds Chemical class 0.000 description 1
- 125000006615 aromatic heterocyclic group Chemical group 0.000 description 1
- 229920003235 aromatic polyamide Polymers 0.000 description 1
- 125000002785 azepinyl group Chemical group 0.000 description 1
- 125000000043 benzamido group Chemical group [H]N([*])C(=O)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 1
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 1
- 229910052790 beryllium Inorganic materials 0.000 description 1
- ATBAMAFKBVZNFJ-UHFFFAOYSA-N beryllium atom Chemical compound [Be] ATBAMAFKBVZNFJ-UHFFFAOYSA-N 0.000 description 1
- 230000001588 bifunctional effect Effects 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 239000010796 biological waste Substances 0.000 description 1
- 229920001400 block copolymer Polymers 0.000 description 1
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 1
- 239000004327 boric acid Substances 0.000 description 1
- WKDNYTOXBCRNPV-UHFFFAOYSA-N bpda Chemical compound C1=C2C(=O)OC(=O)C2=CC(C=2C=C3C(=O)OC(C3=CC=2)=O)=C1 WKDNYTOXBCRNPV-UHFFFAOYSA-N 0.000 description 1
- 239000001273 butane Substances 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- QAZYYQMPRQKMAC-FDGPNNRMSA-L calcium;(z)-4-oxopent-2-en-2-olate Chemical compound [Ca+2].C\C([O-])=C\C(C)=O.C\C([O-])=C\C(C)=O QAZYYQMPRQKMAC-FDGPNNRMSA-L 0.000 description 1
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 1
- 150000001718 carbodiimides Chemical class 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- 239000003093 cationic surfactant Substances 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 239000012461 cellulose resin Substances 0.000 description 1
- 239000004568 cement Substances 0.000 description 1
- 239000007806 chemical reaction intermediate Substances 0.000 description 1
- XTHPWXDJESJLNJ-UHFFFAOYSA-N chlorosulfonic acid Substances OS(Cl)(=O)=O XTHPWXDJESJLNJ-UHFFFAOYSA-N 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 230000001112 coagulating effect Effects 0.000 description 1
- 229910017052 cobalt Inorganic materials 0.000 description 1
- 239000010941 cobalt Substances 0.000 description 1
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 1
- FJDJVBXSSLDNJB-LNTINUHCSA-N cobalt;(z)-4-hydroxypent-3-en-2-one Chemical compound [Co].C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O FJDJVBXSSLDNJB-LNTINUHCSA-N 0.000 description 1
- 230000008094 contradictory effect Effects 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- DMSZORWOGDLWGN-UHFFFAOYSA-N ctk1a3526 Chemical group NP(N)(N)=O DMSZORWOGDLWGN-UHFFFAOYSA-N 0.000 description 1
- 125000004093 cyano group Chemical group *C#N 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000000280 densification Methods 0.000 description 1
- NBAUUSKPFGFBQZ-UHFFFAOYSA-N diethylaminophosphonic acid Chemical compound CCN(CC)P(O)(O)=O NBAUUSKPFGFBQZ-UHFFFAOYSA-N 0.000 description 1
- 229940028356 diethylene glycol monobutyl ether Drugs 0.000 description 1
- 230000029087 digestion Effects 0.000 description 1
- RXKJFZQQPQGTFL-UHFFFAOYSA-N dihydroxyacetone Chemical compound OCC(=O)CO RXKJFZQQPQGTFL-UHFFFAOYSA-N 0.000 description 1
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 229910001873 dinitrogen Inorganic materials 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000000578 dry spinning Methods 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 239000003822 epoxy resin Substances 0.000 description 1
- 239000004210 ether based solvent Substances 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- 125000003754 ethoxycarbonyl group Chemical group C(=O)(OCC)* 0.000 description 1
- 125000004705 ethylthio group Chemical group C(C)S* 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 238000000855 fermentation Methods 0.000 description 1
- 230000004151 fermentation Effects 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000012847 fine chemical Substances 0.000 description 1
- YLQWCDOCJODRMT-UHFFFAOYSA-N fluoren-9-one Chemical compound C1=CC=C2C(=O)C3=CC=CC=C3C2=C1 YLQWCDOCJODRMT-UHFFFAOYSA-N 0.000 description 1
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 1
- 125000002541 furyl group Chemical group 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 238000001891 gel spinning Methods 0.000 description 1
- 125000003055 glycidyl group Chemical group C(C1CO1)* 0.000 description 1
- 229920000578 graft copolymer Polymers 0.000 description 1
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 1
- 239000001307 helium Substances 0.000 description 1
- 229910052734 helium Inorganic materials 0.000 description 1
- SWQJXJOGLNCZEY-UHFFFAOYSA-N helium atom Chemical compound [He] SWQJXJOGLNCZEY-UHFFFAOYSA-N 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229910000037 hydrogen sulfide Inorganic materials 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 125000001841 imino group Chemical group [H]N=* 0.000 description 1
- NBZBKCUXIYYUSX-UHFFFAOYSA-N iminodiacetic acid Chemical compound OC(=O)CNCC(O)=O NBZBKCUXIYYUSX-UHFFFAOYSA-N 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- SKWCWFYBFZIXHE-UHFFFAOYSA-K indium acetylacetonate Chemical compound CC(=O)C=C(C)O[In](OC(C)=CC(C)=O)OC(C)=CC(C)=O SKWCWFYBFZIXHE-UHFFFAOYSA-K 0.000 description 1
- APFVFJFRJDLVQX-UHFFFAOYSA-N indium atom Chemical compound [In] APFVFJFRJDLVQX-UHFFFAOYSA-N 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 229910010272 inorganic material Inorganic materials 0.000 description 1
- 239000011147 inorganic material Substances 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- RBTARNINKXHZNM-UHFFFAOYSA-K iron trichloride Chemical compound Cl[Fe](Cl)Cl RBTARNINKXHZNM-UHFFFAOYSA-K 0.000 description 1
- 230000001678 irradiating effect Effects 0.000 description 1
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- AKTIAGQCYPCKFX-FDGPNNRMSA-L magnesium;(z)-4-oxopent-2-en-2-olate Chemical compound [Mg+2].C\C([O-])=C\C(C)=O.C\C([O-])=C\C(C)=O AKTIAGQCYPCKFX-FDGPNNRMSA-L 0.000 description 1
- 229910052748 manganese Inorganic materials 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 125000001160 methoxycarbonyl group Chemical group [H]C([H])([H])OC(*)=O 0.000 description 1
- 125000006626 methoxycarbonylamino group Chemical group 0.000 description 1
- 125000002816 methylsulfanyl group Chemical group [H]C([H])([H])S[*] 0.000 description 1
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 229910052750 molybdenum Inorganic materials 0.000 description 1
- 239000011733 molybdenum Substances 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 230000004899 motility Effects 0.000 description 1
- 239000010813 municipal solid waste Substances 0.000 description 1
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- OFBQJSOFQDEBGM-UHFFFAOYSA-N n-pentane Natural products CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 1
- 239000000025 natural resin Substances 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- CXQXSVUQTKDNFP-UHFFFAOYSA-N octamethyltrisiloxane Chemical compound C[Si](C)(C)O[Si](C)(C)O[Si](C)(C)C CXQXSVUQTKDNFP-UHFFFAOYSA-N 0.000 description 1
- 239000003895 organic fertilizer Substances 0.000 description 1
- 239000011368 organic material Substances 0.000 description 1
- 229920000620 organic polymer Polymers 0.000 description 1
- 125000004043 oxo group Chemical group O=* 0.000 description 1
- JCGNDDUYTRNOFT-UHFFFAOYSA-N oxolane-2,4-dione Chemical compound O=C1COC(=O)C1 JCGNDDUYTRNOFT-UHFFFAOYSA-N 0.000 description 1
- 230000000149 penetrating effect Effects 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 239000012466 permeate Substances 0.000 description 1
- 238000000614 phase inversion technique Methods 0.000 description 1
- 239000005011 phenolic resin Substances 0.000 description 1
- 125000003356 phenylsulfanyl group Chemical group [*]SC1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- PTMHPRAIXMAOOB-UHFFFAOYSA-N phosphoric acid amide group Chemical group P(N)(O)(O)=O PTMHPRAIXMAOOB-UHFFFAOYSA-N 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 125000005936 piperidyl group Chemical group 0.000 description 1
- 238000004987 plasma desorption mass spectroscopy Methods 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 229920002037 poly(vinyl butyral) polymer Polymers 0.000 description 1
- 229920002432 poly(vinyl methyl ether) polymer Polymers 0.000 description 1
- 229920001921 poly-methyl-phenyl-siloxane Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920006122 polyamide resin Polymers 0.000 description 1
- 229920005668 polycarbonate resin Polymers 0.000 description 1
- 239000004431 polycarbonate resin Substances 0.000 description 1
- 229920000647 polyepoxide Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920001225 polyester resin Polymers 0.000 description 1
- 239000004645 polyester resin Substances 0.000 description 1
- 229920006393 polyether sulfone Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 230000000379 polymerizing effect Effects 0.000 description 1
- 229920005672 polyolefin resin Polymers 0.000 description 1
- 229920006380 polyphenylene oxide Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920001343 polytetrafluoroethylene Polymers 0.000 description 1
- 239000004810 polytetrafluoroethylene Substances 0.000 description 1
- 229920002635 polyurethane Polymers 0.000 description 1
- 239000004814 polyurethane Substances 0.000 description 1
- 229920005749 polyurethane resin Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 229920002620 polyvinyl fluoride Polymers 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- TYJJADVDDVDEDZ-UHFFFAOYSA-M potassium hydrogencarbonate Chemical compound [K+].OC([O-])=O TYJJADVDDVDEDZ-UHFFFAOYSA-M 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000005554 pyridyloxy group Chemical group 0.000 description 1
- 125000005030 pyridylthio group Chemical group N1=C(C=CC=C1)S* 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 229920005604 random copolymer Polymers 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 238000007363 ring formation reaction Methods 0.000 description 1
- 239000005060 rubber Substances 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 229910052706 scandium Inorganic materials 0.000 description 1
- SIXSYDAISGFNSX-UHFFFAOYSA-N scandium atom Chemical compound [Sc] SIXSYDAISGFNSX-UHFFFAOYSA-N 0.000 description 1
- VSZWPYCFIRKVQL-UHFFFAOYSA-N selanylidenegallium;selenium Chemical compound [Se].[Se]=[Ga].[Se]=[Ga] VSZWPYCFIRKVQL-UHFFFAOYSA-N 0.000 description 1
- 239000010865 sewage Substances 0.000 description 1
- 239000004208 shellac Substances 0.000 description 1
- ZLGIYFNHBLSMPS-ATJNOEHPSA-N shellac Chemical compound OCCCCCC(O)C(O)CCCCCCCC(O)=O.C1C23[C@H](C(O)=O)CCC2[C@](C)(CO)[C@@H]1C(C(O)=O)=C[C@@H]3O ZLGIYFNHBLSMPS-ATJNOEHPSA-N 0.000 description 1
- 229940113147 shellac Drugs 0.000 description 1
- 235000013874 shellac Nutrition 0.000 description 1
- 238000009987 spinning Methods 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 125000004079 stearyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 229940124530 sulfonamide Drugs 0.000 description 1
- 150000003456 sulfonamides Chemical class 0.000 description 1
- 125000000542 sulfonic acid group Chemical group 0.000 description 1
- 125000006296 sulfonyl amino group Chemical group [H]N(*)S(*)(=O)=O 0.000 description 1
- 150000003462 sulfoxides Chemical class 0.000 description 1
- XTQHKBHJIVJGKJ-UHFFFAOYSA-N sulfur monoxide Chemical class S=O XTQHKBHJIVJGKJ-UHFFFAOYSA-N 0.000 description 1
- 229910052815 sulfur oxide Inorganic materials 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000002344 surface layer Substances 0.000 description 1
- JBQYATWDVHIOAR-UHFFFAOYSA-N tellanylidenegermanium Chemical compound [Te]=[Ge] JBQYATWDVHIOAR-UHFFFAOYSA-N 0.000 description 1
- 125000001544 thienyl group Chemical group 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- 125000002088 tosyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1C([H])([H])[H])S(*)(=O)=O 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- ZIBGPFATKBEMQZ-UHFFFAOYSA-N triethylene glycol Chemical compound OCCOCCOCCO ZIBGPFATKBEMQZ-UHFFFAOYSA-N 0.000 description 1
- JLGLQAWTXXGVEM-UHFFFAOYSA-N triethylene glycol monomethyl ether Chemical group COCCOCCOCCO JLGLQAWTXXGVEM-UHFFFAOYSA-N 0.000 description 1
- 229930195735 unsaturated hydrocarbon Natural products 0.000 description 1
- LEONUFNNVUYDNQ-UHFFFAOYSA-N vanadium atom Chemical compound [V] LEONUFNNVUYDNQ-UHFFFAOYSA-N 0.000 description 1
- 238000010792 warming Methods 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 238000002166 wet spinning Methods 0.000 description 1
- 239000002759 woven fabric Substances 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
- VWQVUPCCIRVNHF-UHFFFAOYSA-N yttrium atom Chemical compound [Y] VWQVUPCCIRVNHF-UHFFFAOYSA-N 0.000 description 1
- 239000011592 zinc chloride Substances 0.000 description 1
- 235000005074 zinc chloride Nutrition 0.000 description 1
- NHXVNEDMKGDNPR-UHFFFAOYSA-N zinc;pentane-2,4-dione Chemical compound [Zn+2].CC(=O)[CH-]C(C)=O.CC(=O)[CH-]C(C)=O NHXVNEDMKGDNPR-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D53/00—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols
- B01D53/22—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols by diffusion
- B01D53/228—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols by diffusion characterised by specific membranes
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D53/00—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols
- B01D53/22—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols by diffusion
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D71/00—Semi-permeable membranes for separation processes or apparatus characterised by the material; Manufacturing processes specially adapted therefor
- B01D71/06—Organic material
- B01D71/56—Polyamides, e.g. polyester-amides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D71/00—Semi-permeable membranes for separation processes or apparatus characterised by the material; Manufacturing processes specially adapted therefor
- B01D71/06—Organic material
- B01D71/58—Other polymers having nitrogen in the main chain, with or without oxygen or carbon only
- B01D71/62—Polycondensates having nitrogen-containing heterocyclic rings in the main chain
- B01D71/64—Polyimides; Polyamide-imides; Polyester-imides; Polyamide acids or similar polyimide precursors
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/06—Polycondensates having nitrogen-containing heterocyclic rings in the main chain of the macromolecule
- C08G73/10—Polyimides; Polyester-imides; Polyamide-imides; Polyamide acids or similar polyimide precursors
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/06—Polycondensates having nitrogen-containing heterocyclic rings in the main chain of the macromolecule
- C08G73/10—Polyimides; Polyester-imides; Polyamide-imides; Polyamide acids or similar polyimide precursors
- C08G73/1039—Polyimides; Polyester-imides; Polyamide-imides; Polyamide acids or similar polyimide precursors comprising halogen-containing substituents
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/06—Polycondensates having nitrogen-containing heterocyclic rings in the main chain of the macromolecule
- C08G73/10—Polyimides; Polyester-imides; Polyamide-imides; Polyamide acids or similar polyimide precursors
- C08G73/1075—Partially aromatic polyimides
- C08G73/1078—Partially aromatic polyimides wholly aromatic in the diamino moiety
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/06—Polycondensates having nitrogen-containing heterocyclic rings in the main chain of the macromolecule
- C08G73/10—Polyimides; Polyester-imides; Polyamide-imides; Polyamide acids or similar polyimide precursors
- C08G73/1075—Partially aromatic polyimides
- C08G73/1082—Partially aromatic polyimides wholly aromatic in the tetracarboxylic moiety
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2256/00—Main component in the product gas stream after treatment
- B01D2256/24—Hydrocarbons
- B01D2256/245—Methane
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2257/00—Components to be removed
- B01D2257/50—Carbon oxides
- B01D2257/504—Carbon dioxide
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D67/00—Processes specially adapted for manufacturing semi-permeable membranes for separation processes or apparatus
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D69/00—Semi-permeable membranes for separation processes or apparatus characterised by their form, structure or properties; Manufacturing processes specially adapted therefor
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02C—CAPTURE, STORAGE, SEQUESTRATION OR DISPOSAL OF GREENHOUSE GASES [GHG]
- Y02C20/00—Capture or disposal of greenhouse gases
- Y02C20/40—Capture or disposal of greenhouse gases of CO2
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/151—Reduction of greenhouse gas [GHG] emissions, e.g. CO2
Definitions
- the present invention relates to a gas separation membrane, a gas separation module, a gas separation device, a gas separation method, and a polyimide compound.
- a material composed of a polymer compound has gas permeability specific to each material. Based on the properties of the gas separation membrane, a desired gas component can be selectively permeated and separated by a membrane made of a specific polymer compound.
- gas separation membranes As an industrial application of gas separation membranes, it is considered to separate and recover carbon dioxide from large-scale carbon dioxide generation sources in thermal power plants, cement plants, steelworks blast furnaces, etc., in connection with the problem of global warming.
- Natural gas and biogas gas generated by fermentation or anaerobic digestion, such as biological waste, organic fertilizer, biodegradable substances, sewage, garbage, or energy crops
- use of a gas separation membrane has been studied (Patent Document 1).
- the membrane In an actual plant, the membrane is plasticized due to high pressure conditions or the influence of impurities (for example, benzene, toluene, xylene) present in natural gas, and this causes a problem in that gas separation selectivity is lowered. Therefore, the gas separation membrane is not only improved in gas permeability and gas separation selectivity, but also has a plasticity that can continuously exhibit good gas permeability and gas separation selectivity under high pressure conditions and in the presence of the impurities. Resistance to crystallization is also required.
- Patent Document 3 employs a 1,3-phenylenediamine component having a substituent at the 2-position and at least one 4- to 6-position as the diamine component of the polyimide compound.
- the gas separation membrane using this polyimide compound in the gas separation layer has gas permeability even under high pressure by making at least one of the substituents at the position and the substituents at the 4-6 position a specific polar group. And gas separation selectivity and high resistance against impurities such as toluene.
- the gas separation layer In order to obtain a practical gas separation membrane, the gas separation layer must be made thin to ensure sufficient gas permeability, and a higher degree of gas separation selectivity must be realized.
- a method for thinning the gas separation layer there is a method in which a polymer compound such as a polyimide compound is made into an asymmetric membrane by a phase separation method, and a portion contributing to separation is made into a thin layer called a dense layer or a skin layer.
- a portion other than the dense layer is allowed to function as a support layer that bears the mechanical strength of the membrane.
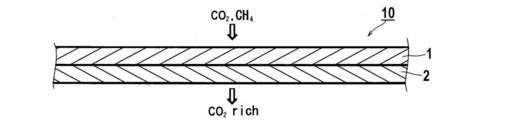
- the gas separation layer responsible for the gas separation function and the support layer responsible for the mechanical strength are made of different materials, and the gas separation layer having gas separation ability is thinly formed on the gas permeable support layer.
- the form of the composite film formed in the above is also known.
- the present invention relates to a gas separation membrane that realizes both gas permeability and gas separation selectivity at a sufficient level even when used under high pressure conditions, and enables high-speed and highly selective gas separation.
- the present invention also relates to a gas separation membrane that can maintain good gas separation performance even when it comes into contact with toluene, which is an impurity component.
- the present invention relates to a gas separation module, a gas separation device, and a gas separation method using the gas separation membrane.
- the present invention also relates to a polyimide compound suitable as a constituent material of the gas separation layer of the gas separation membrane.
- the present inventors have a gas separation membrane having a gas separation layer using a polyimide compound, and the diamine component of this polyimide compound has a ring having a substituted sulfamoyl group having a specific structure.
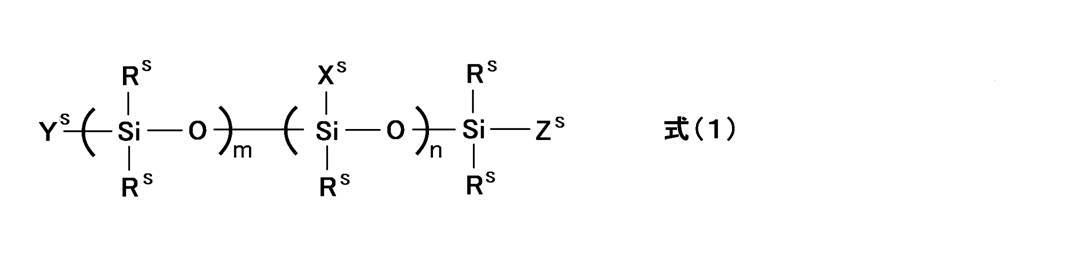
- a gas separation membrane having a gas separation layer containing a polyimide compound as a constituent material The gas separation membrane in which the said polyimide compound contains the repeating unit represented by following formula (I).
- Xa represents an oxygen atom, a nitrogen atom and / or a sulfur atom group, or an aryl group having a fluorine atom in the substituent.
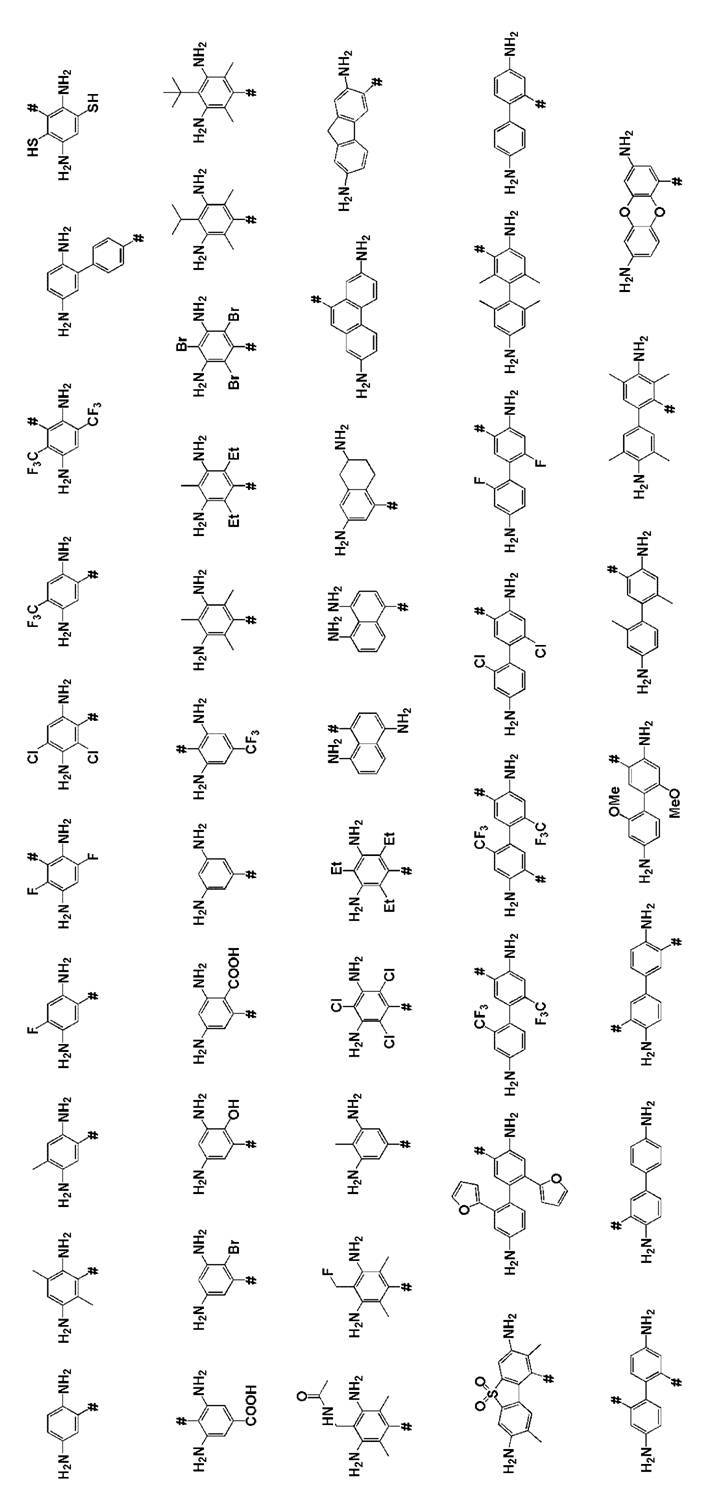
- Xb represents a hydrogen atom or a substituent.
- X a is a structure selected from OH, NH and SH At least one part.
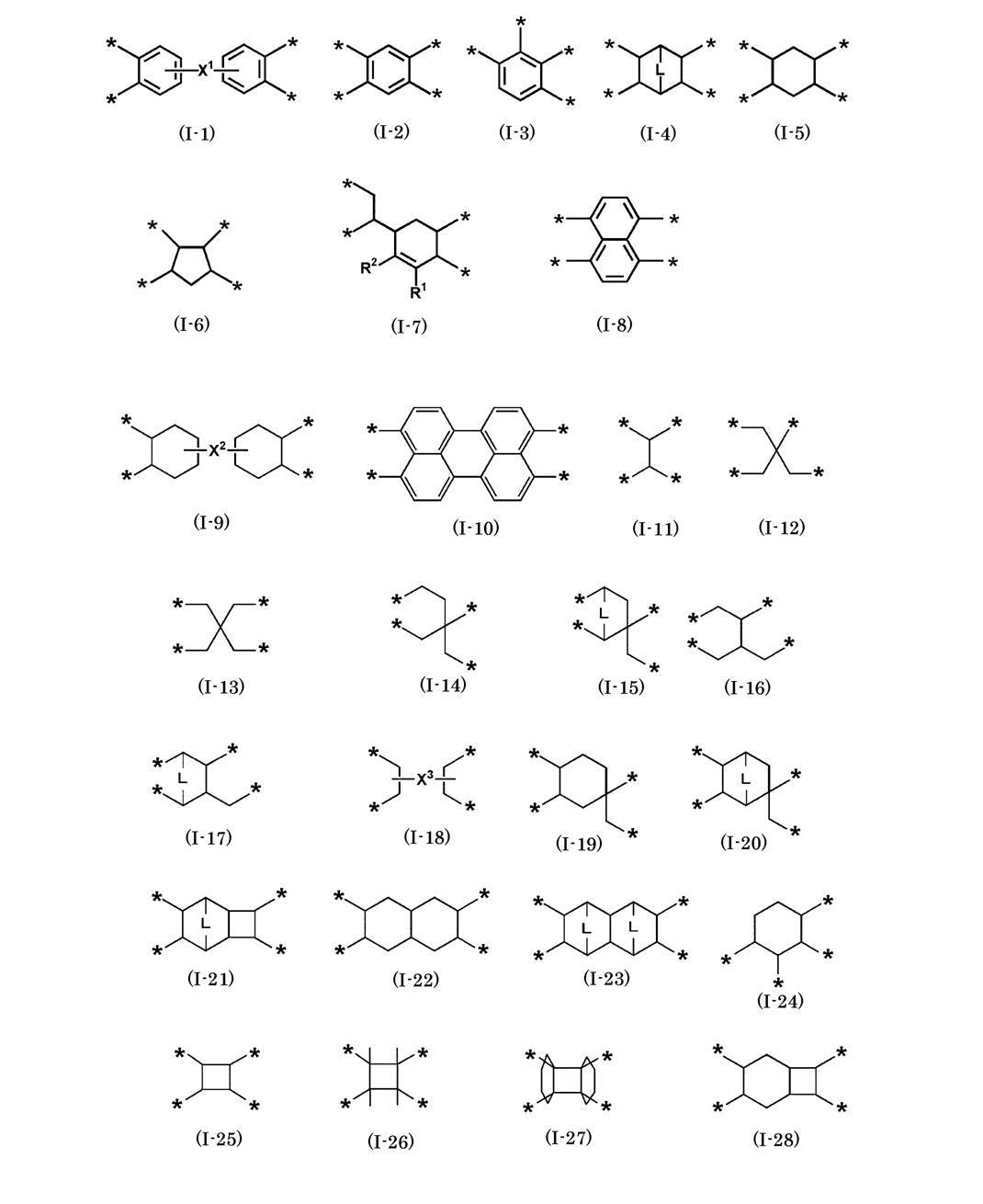
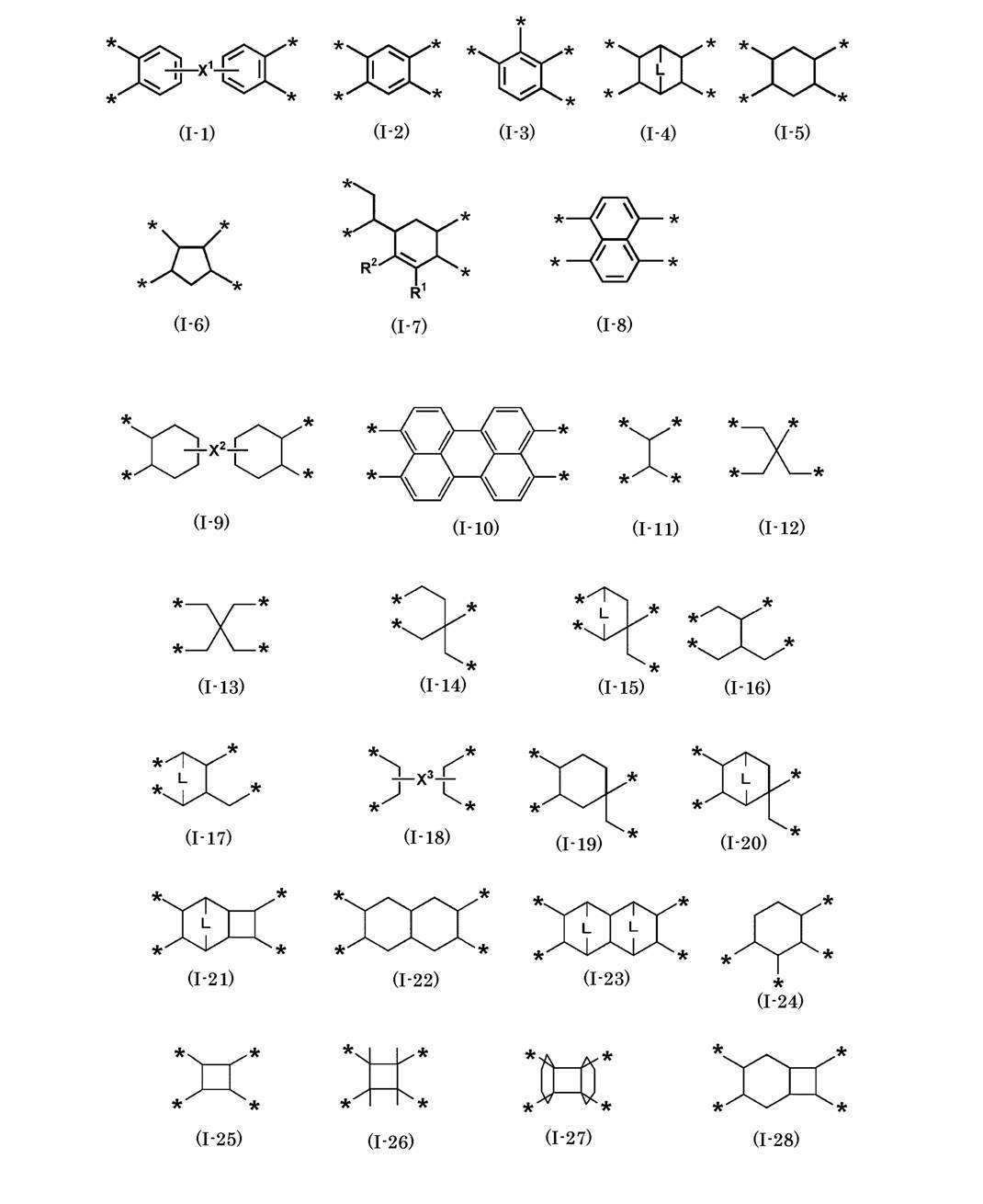
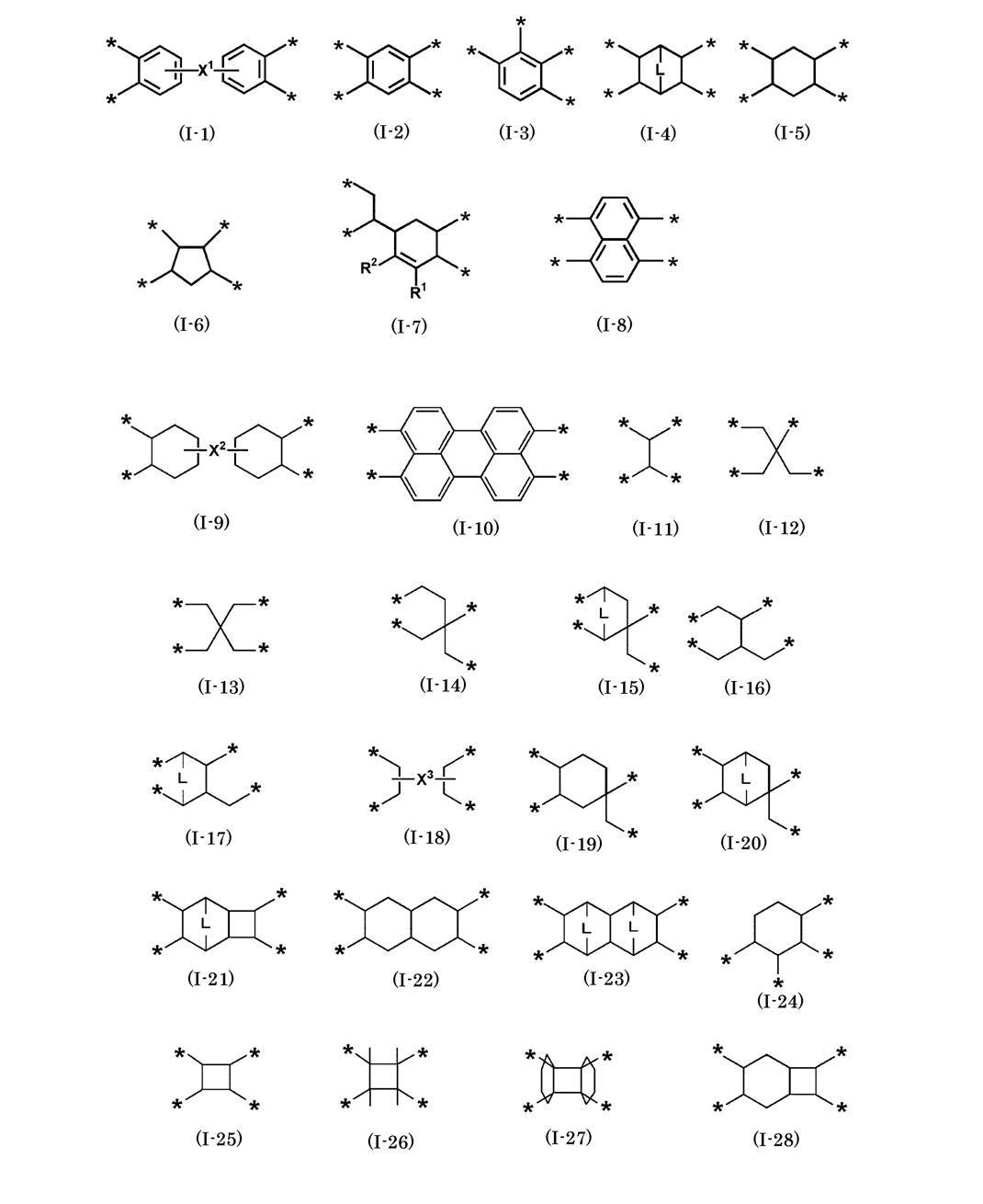
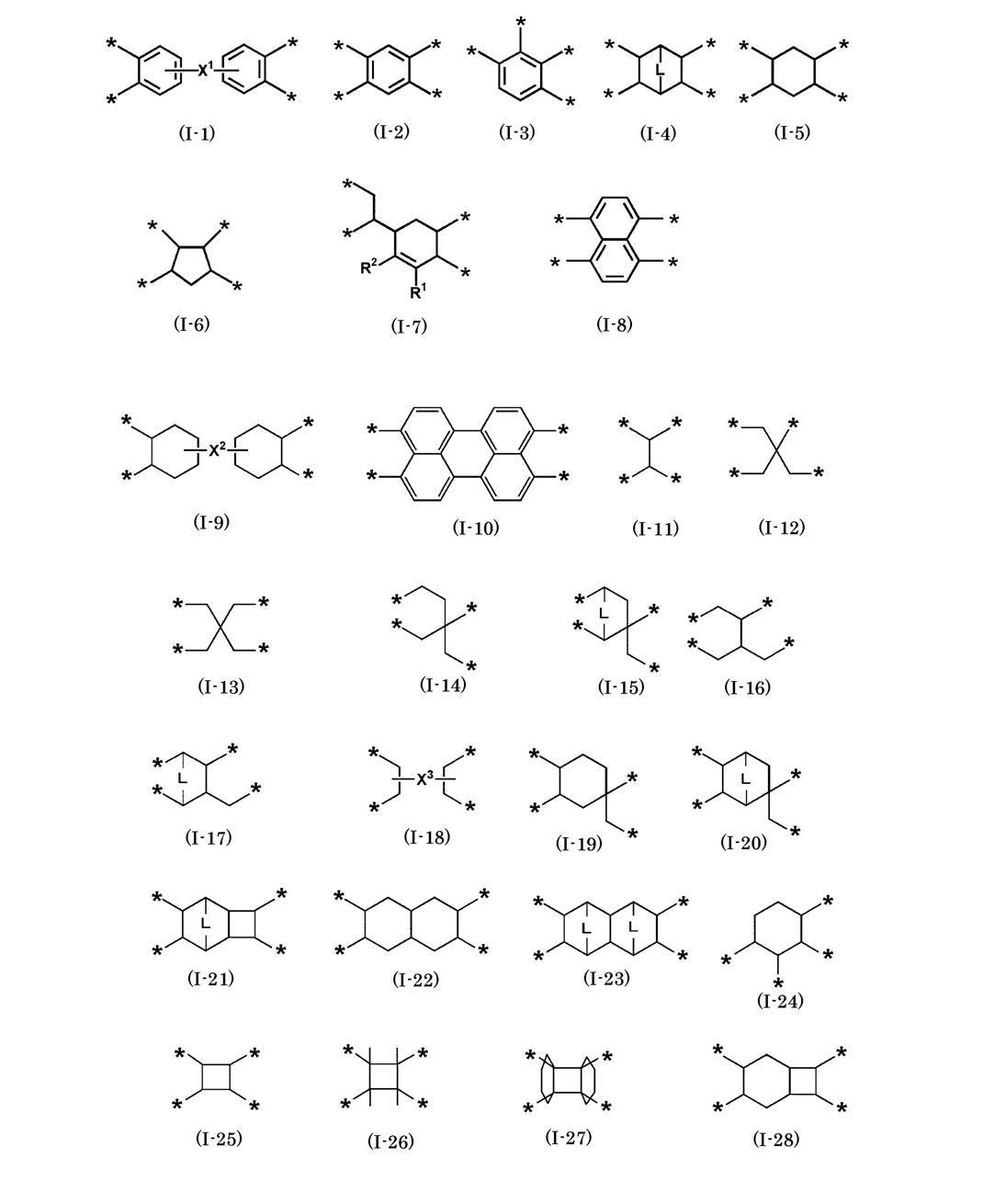
- R a represents a group represented by any of the following formulas (I-1) to (I-28).
- X 1 to X 3 each represents a single bond or a divalent group
- L independently represents —CH ⁇ CH— or —CH 2 —
- R 1 and R 2 each represents a hydrogen atom or a substituent.
- * Indicates a binding site with the carbonyl group shown in formula (I).
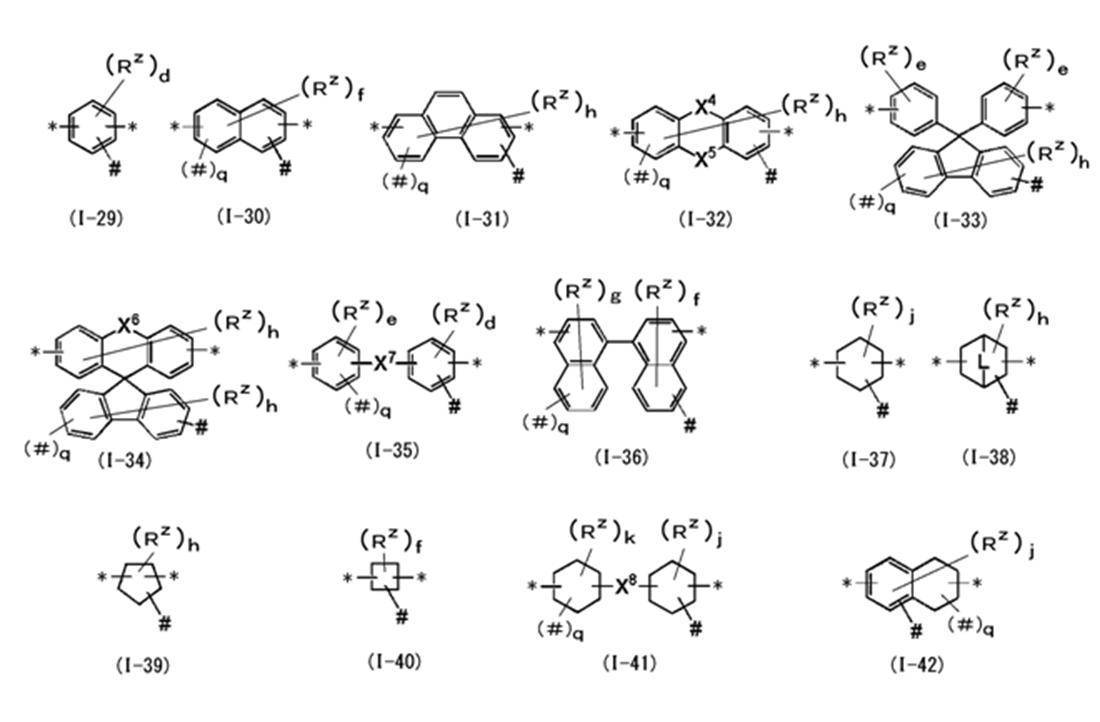
- R b represents a group represented by any of the following formulas (I-29) to (I-42).
- X 4 to X 8 represent a single bond or a divalent group
- L represents —CH ⁇ CH— or —CH 2 —
- R Z represents a substituent
- * represents in the formula (I).
- d is each independently an integer of 0 to 3
- e is independently an integer of 0 to 4
- f is independently of an integer of 0 to 5
- g is 0 to 6
- H represents an integer of 0 to 7
- each independently represents an integer of 0 to 9
- k represents an integer of 0 to 10.
- q represents 0 or 1 each independently.
- R a , X b, A a, A b and A c are respectively the formula (I-a) in the R a, X b, A a , A b and A c synonymous It is.
- Xc represents a substituent.
- X c is selected from OH, NH and SH Having at least one structure.
- the support layer is composed of a porous layer and a nonwoven fabric layer, The gas separation membrane according to [10], wherein the nonwoven fabric layer, the porous layer, and the gas separation layer are provided in this order.
- the gas to be separated is a mixed gas of carbon dioxide and methane
- the permeation rate of carbon dioxide at 40 ° C. and 5 MPa is 20 GPU or more
- the permeation rate ratio of carbon dioxide and methane R CO2 / R CH4
- R a represents a group represented by any of the following formulas (I-1) to (I-28).
- X 1 to X 3 each represents a single bond or a divalent group
- L independently represents —CH ⁇ CH— or —CH 2 —
- R 1 and R 2 each represents a hydrogen atom or a substituent.
- * Represents a binding site with the carbonyl group shown in formula (Ib).
- a a , A b and Ac represent a hydrogen atom or a substituent.
- Xb represents a hydrogen atom or a substituent.
- Xc represents a substituent.
- R a represents a group represented by any of the following formulas (I-1) to (I-28).
- X 1 to X 3 each represents a single bond or a divalent group
- L independently represents —CH ⁇ CH— or —CH 2 —
- R 1 and R 2 each represents a hydrogen atom or a substituent.
- a a , A b and Ac represent a hydrogen atom or a substituent.
- Xb represents a hydrogen atom or a substituent.
- R c represents an alkylene group, a cycloalkylene group or an arylene group.
- X d represents a group having 0 to 2 carbon atoms and having a structural part selected from OH, NH and SH.
- substituents, etc. when there are a plurality of substituents, linking groups, etc. (hereinafter referred to as “substituents, etc.”) designated by specific symbols, or when a plurality of substituents etc. are specified simultaneously or alternatively
- each substituent and the like may be the same as or different from each other.
- each partial structure or repeating unit may be the same or different.
- the gas separation membrane, the gas separation module, the gas separation apparatus, and the gas separation method of the present invention realize high-speed and high selectivity by realizing both gas permeability and gas separation selectivity at a sufficient level even under high pressure conditions. Allows gas separation.
- the gas separation membrane, gas separation module, gas separation apparatus, and gas separation method of the present invention can maintain good gas separation performance even when the gas separation membrane is exposed to toluene, which is an impurity component.
- the polyimide compound of this invention can be used suitably as a constituent material of the gas separation layer in the said gas separation membrane.
- the gas separation membrane of this invention contains the polyimide compound of a specific structure in a gas separation layer as the constituent material.
- polyimide compound used in the present invention contains at least a repeating unit represented by the following formula (I).
- R a represents a group represented by any of the following formulas (I-1) to (I-28).
- * represents a binding site with a carbonyl group in the formula (I).
- R a is preferably a group represented by the formula (I-1), (I-2) or (I-4), and is a group represented by (I-1) or (I-4). It is more preferable that the group represented by (I-1) is particularly preferable.
- X 1 to X 3 represent a single bond or a divalent group.
- the divalent group includes —C (R x ) 2 — (R x represents a hydrogen atom or a substituent.
- R x When R x is a substituent, they may be linked to each other to form a ring), — O—, —SO 2 —, —C ( ⁇ O) —, —S—, —NR Y —, —Si (R Y ) 2 — (R Y is a hydrogen atom, an alkyl group (preferably methyl or ethyl) or An aryl group (preferably a phenyl group)), —C 6 H 4 — (phenylene), a heterocyclic group or a combination thereof is preferable, and a single bond or —C (R x ) 2 — is more preferable.
- R x represents a substituent
- substituent group Z an alkyl group (preferable range is synonymous with the alkyl group shown in the substituent group Z described later).
- an alkyl group having a halogen atom as a substituent is more preferable, and trifluoromethyl is particularly preferable.
- X 3 is connected to one of the two carbon atoms described on the left side and one of the two carbon atoms described on the right side thereof.
- Means that X 1 to X 3 preferably have a molecular weight of 500 or less, more preferably 350 or less, and more preferably 10 to 200.
- L is independently —CH ⁇ CH -Or -CH 2 -is shown.
- R 1 and R 2 represent a hydrogen atom or a substituent.
- substituent include a group selected from the substituent group Z described later.
- R 1 and R 2 may be bonded to each other to form a ring.
- R 1 and R 2 are preferably a hydrogen atom or an alkyl group, more preferably a hydrogen atom, a methyl group or an ethyl group, and even more preferably a hydrogen atom.
- the carbon atoms shown in the formulas (I-1) to (I-28) may further have a substituent. That is, in the present invention, a form in which the carbon atom shown in the formulas (I-1) to (I-28) further has a substituent is also included in the repeating unit represented by the formula (I). Specific examples of this substituent include groups selected from the substituent group Z described later, and among them, an alkyl group or an aryl group is preferable.
- R b represents a group represented by any of the following formulas (I-29) to (I-42).
- * represents a bonding site with the imide group shown in formula (I)
- X a ) represents a binding site.
- R b is preferably a group represented by the formula (I-29), (I-33), (I-34) or (I-35), and the formula (I-29) or (I-34) Is more preferable.
- X 4 to X 8 each represents a single bond or a divalent group.
- Examples of the divalent group which can be taken as X 4 , X 5 and X 6 include —O—, —S—, —NR N — ( RN represents a hydrogen atom, an alkyl group or an aryl group), —S. ( ⁇ O) 2 —, —C ( ⁇ O) —, or —C (R x ) 2 — (R x represents a hydrogen atom or a substituent. When R x is a substituent, they are linked to each other to form a ring.
- the preferred form of the divalent group that can be taken as X 7 and X 8 is the same as the preferred form of the divalent group that can be taken as X 1 described above.
- L in formula (I-38) has the same meaning as L in formula (I-4).
- R Z each independently represents a substituent.
- R Z is preferably an alkyl group (preferably an alkyl group having 1 to 10 carbon atoms, more preferably 1 to 6 carbon atoms, still more preferably 1 to 3 carbon atoms, and preferred specific examples include methyl, ethyl and isopropyl.
- This alkyl group preferably has a fluorine atom as a substituent.
- An aryl group preferably an aryl group having 6 to 20 carbon atoms, more preferably 6 to 15 carbon atoms, and still more preferably 6 to 10 carbon atoms).
- Preferred examples include phenyl and naphthyl.
- An alkoxy group preferably an alkoxy group having 1 to 10 carbon atoms, more preferably 1 to 6 carbon atoms, and still more preferably 1 to 3 carbon atoms, Preferable specific examples include methoxy and ethoxy.
- a heterocyclic group preferably an oxygen atom as a ring-constituting heteroatom, A nitrogen atom and / or a sulfur atom, preferably a 3- to 8-membered ring, more preferably a 5- or 6-membered ring, and a halogen atom (specifically, a fluorine atom, a chlorine atom, a bromine atom, and an iodine atom) .
- a hydroxy group, and a carboxy group, and a group selected from an alkyl group, an aryl group, and a halogen atom is more preferable.
- D is an integer of 0 to 3, preferably an integer of 0 to 2.
- e is an integer of 0 to 4, preferably an integer of 0 to 3, and more preferably an integer of 0 to 2.
- f is an integer of 0 to 5, preferably an integer of 0 to 4, more preferably an integer of 0 to 3, and still more preferably an integer of 0 to 2.
- g is an integer of 0 to 6, preferably an integer of 0 to 5, more preferably an integer of 0 to 4, and still more preferably an integer of 0 to 3.
- h is an integer of 0 to 7, preferably an integer of 0 to 6, more preferably an integer of 0 to 5, and particularly preferably an integer of 0 to 4.
- j is an integer of 0 to 9, preferably an integer of 0 to 8, more preferably an integer of 0 to 7, still more preferably an integer of 0 to 6, and particularly preferably an integer of 0 to 4.
- k is an integer of 0 to 10, preferably an integer of 0 to 8, more preferably an integer of 0 to 6, and further preferably an integer of 0 to 4.
- q represents 0 or 1; In the present invention, the case where q is 1 means that there are two sulfamoyl groups shown in the formula (1) in the repeating unit of the formula (1). And included in the repeating unit represented by the formula (1).
- X a represents an oxygen atom, a nitrogen atom and / or a sulfur atom group, or an aryl group having a fluorine atom in the substituent.
- aryl group having a fluorine atom in the substituent does not have any oxygen atom, a nitrogen atom and a sulfur atom.
- Xb represents a hydrogen atom or a substituent.
- X a is a structure selected from OH, NH and SH At least one part.
- the polyimide compound represented by the formula (I) has a sulfamoyl group which is a highly polar group in the diamine component, and this sulfamoyl group has a structure part selected from OH, NH and SH in the structure. With such a structure, the electronic interaction between the polymer chains, the hydrogen bonding interaction, etc.
- X a is, when an aryl group having a fluorine atom in the substituent is a gap due to the repulsion between the fluorine atom while the gas permeability is enhanced, higher by [pi-[pi stacking such aryl groups It is presumed that the gas separation selectivity can be maintained well.
- Xa preferably has a molecular weight of 10 to 400, more preferably 30 to 250. It can take as X a, group having an oxygen atom, a nitrogen atom and / or sulfur atoms are not particularly limited as long as it has an oxygen atom, a nitrogen atom and / or sulfur atoms. Oxygen atoms, nitrogen atoms and / or sulfur atoms function as hydrogen atom acceptors in hydrogen bonding interactions.
- X a group having an oxygen atom, a nitrogen atom and / or sulfur atoms, preferably an acyl group, a carbamoyl group, a thiocarbamoyl group, a sulfamoyl group, a carboxy group, a sulfo group, a phosphoric acid group (-P ( ⁇ O) (OH) 2 ), boric acid group (—B (OH) 2 ), and a group having a group selected from hydroxy groups.
- X a an oxygen atom, a group having a nitrogen atom and / or sulfur atoms, an alkyl group (preferably having 1 to 12 carbon atoms, more preferably 1 to 8 carbon atoms, more preferably 1 to 4 carbon atoms Alkyl group), a cycloalkyl group (preferably a cycloalkyl group having 3 to 10 carbon atoms, more preferably a cycloalkyl group having 3 to 8 carbon atoms), an aryl group (preferably having 6 to 20 carbon atoms, more preferably 6 to 15 carbon atoms, More preferably an aryl group having 6 to 12 carbon atoms), an acyl group (preferably an acyl group having 2 to 20 carbon atoms, more preferably an acyl group having 2 to 15 carbon atoms, and still more preferably an acyl group having 2 to 10 carbon atoms), an arylaminocarbonyl group (Preferably an arylaminocarbonyl group having 7 to 20 carbon atoms, an
- These groups preferably have a fluorine atom, an amino group, an acylamino group, a hydroxy group, a carboxy group, a carbamoyl group, a boric acid group, and a sulfamoyl group as a substituent. More preferred is a form having a group selected from a carboxy group, a carbamoyl group, a boric acid group and a sulfamoyl group as a substituent, and a group selected from a fluorine atom, an acylamino group, a hydroxy group, a carboxy group, a carbamoyl group and a sulfamoyl group is substituted.
- a form having a group is particularly preferable.
- Preferred forms of the amino group, acylamino group, carbamoyl group and sulfamoyl group are the same as the preferred forms of the corresponding groups in the substituent group Z described later.
- the molecular weight of the substituent is preferably 10 to 400, more preferably 30 to 250.
- substituent that can be adopted as Xb and examples thereof include an alkyl group, an alkenyl group, an alkynyl group, an acyl group, a cycloalkyl group, and an aryl group.
- the substituent includes a fluorine atom, an amino group (preferably a monoalkylamino group), an acylamino group, a hydroxy group, a carboxy group, a carbamoyl group, a mercapto group, a boric acid group, phosphorus It is also preferable that a group selected from an acid group, a sulfo group, a sulfino group, a sulfamoyl group, a ureido group, a hydroxamic acid group and a hydrazino group is included.
- alkyl group Preferred forms of the alkyl group, alkenyl group, alkynyl group, acyl group, cycloalkyl group, aryl group, amino group, acylamino group, carbamoyl group, sulfamoyl group, and ureido group are the corresponding groups of the substituent group Z described later. It is the same as the preferable form in.
- Xb is more preferably a hydrogen atom, an alkyl group, an aryl group or an acyl group, further preferably a hydrogen atom, an alkyl group or an aryl group, and particularly preferably a hydrogen atom.
- the repeating unit represented by the formula (I) is preferably a repeating unit represented by the following formula (Ia).
- R a , X a and X b are respectively synonymous with R a , X a and X b in the formula (I), and preferred forms are also the same.
- a a , A b and Ac represent a hydrogen atom or a substituent.
- a a is not particularly limited to substituents which can be taken as A b and A c, for example, it includes groups selected from substituent group Z to be described later.
- an alkyl group preferably an alkyl group having 1 to 12 carbon atoms, more preferably 1 to 6 carbon atoms, still more preferably 1 to 3 carbon atoms, and this alkyl group is preferably an unsubstituted form.
- Methyl, ethyl, isopropyl and t-butyl) and aryl groups preferably aryl groups having 6 to 20 carbon atoms, more preferably 6 to 15 carbon atoms, still more preferably 6 to 10 carbon atoms.
- Examples include phenyl and naphthyl.
- An alkoxy group preferably an alkoxy group having 1 to 10 carbon atoms, more preferably 1 to 6 carbon atoms, and still more preferably 1 to 3 carbon atoms
- a halogen atom for example, a fluorine atom
- a chlorine atom, a bromine atom or an iodine atom a carboxy group, a hydroxy group
- an acylamino group preferably having 2 to 10 carbon atoms, Ri preferably 2 to 6 carbon atoms, and more preferably preferably a group selected from acylamino groups having 2 or 3 carbon atoms, an alkyl group or a halogen atom is more preferable.
- At least one of A a , A b and A c is a substituent, and it is more preferable that at least one of A a , A b and A c is an alkyl group.
- hydrogen atoms other than the alkyl group among A a , A b and A c are preferable.
- the repeating unit represented by the above formula (Ia) is preferably a repeating unit represented by the following formula (Ib).
- R a , X b, A a, A b and A c are respectively the formula (I-a) in the R a, X b, A a , A b and A c synonymous
- Xc represents a substituent.
- X c is selected from OH, NH and SH Having at least one structure.
- group chosen from the substituent group Z mentioned later is mentioned.
- Xc is preferably an alkyl group, an alkenyl group, an alkynyl group, a cycloalkyl group, an aryl group or an amino group.
- the alkyl group that can be taken as X c is preferably an alkyl group having 1 to 10 carbon atoms, more preferably 1 to 6 carbon atoms, and still more preferably 1 to 3 carbon atoms. Preferred specific examples include methyl, ethyl, isopropyl , T-butyl.
- the alkenyl group that can be taken as Xc is preferably an alkenyl group having 2 to 10 carbon atoms, more preferably 2 to 6 carbon atoms, and still more preferably 2 or 3 carbon atoms.
- the alkynyl group that can be taken as X c is preferably an alkynyl group having 2 to 10 carbon atoms, more preferably 2 to 6 carbon atoms, and still more preferably 2 or 3 carbon atoms.
- the cycloalkyl group that can be taken as Xc is preferably a cycloalkyl group having 3 to 10 carbon atoms, more preferably 3 to 8 carbon atoms, and specific examples thereof include cyclopentyl and cyclohexyl.
- the aryl group that can be taken as Xc is preferably an aryl group having 6 to 20 carbon atoms, more preferably 6 to 15 carbon atoms, and still more preferably 6 to 10 carbon atoms.
- the amino group that can be taken as Xc is preferably an alkylamino group (preferably an alkylamino group having 1 to 10, more preferably 1 to 6, more preferably 1 to 3 carbon atoms), an alkenylamino group (preferably Is an alkenylamino group having 2 to 10 carbon atoms, more preferably 2 to 6 carbon atoms, more preferably 2 to 3 carbon atoms, and an alkynylamino group (preferably 2 to 10 carbon atoms, more preferably 2 to 6 carbon atoms, Preferably an alkynylamino group having 2 or 3 carbon atoms), a cycloalkylamino group (preferably a cycloalkylamino group having 3 to 10 carbon atoms, more preferably a cycloalkylamino group having 4 to 8 carbon atoms), or an arylamino group (preferably having a carbon number)
- Xc is more preferably an alkyl group, a cycloalkyl group or an aryl group. Xc is also preferably in a form having at least one fluorine atom as a substituent. Xc is also preferably in a form having a group selected from a carboxy group, a hydroxy group, a carbamoyl group and a sulfamoyl group as a substituent.
- X b is particularly preferably a hydrogen atom.
- the acyl group (—C ( ⁇ O) X c ) in the repeating unit represented by the formula (Ib) serves as a hydrogen bond acceptor (site that interacts with a hydrogen atom).
- the electron withdrawing property can also increase the donor property of hydrogen (X b ) in —N (X b ) —, and the denseness of the polyimide compound will increase, leading to improved gas separation selectivity and plastic resistance. .
- X c has a fluorine atom
- the donor property of —N (X b ) — hydrogen is further enhanced by the electron withdrawing property of the fluorine atom, and at the same time, appropriate vacancies are generated by the repulsive force between the fluorine atoms.
- gas separation selectivity, gas permeability, and plastic resistance can be compatible at a higher level.
- a fluorine atom contributes also to the hydrolysis suppression of a polyimide compound by the water repellency.
- the repeating unit represented by the above formula (Ia) is also preferably a repeating unit represented by the following formula (Ic).
- R a , X b, A a, A b and A c are respectively the formula (I-a) in the R a, X b, A a , A b and A c synonymous
- the preferred form is also the same.
- R c represents an alkylene group, a cycloalkylene group or an arylene group.
- the alkylene group which can be adopted as R c may be linear or branched.
- the alkylene group preferably has 1 to 12 carbon atoms, more preferably 1 to 8 carbon atoms, and still more preferably 1 to 4 carbon atoms.
- the cycloalkylene group that can be employed as R c preferably has 3 to 12 carbon atoms, more preferably 3 to 9 carbon atoms, and particularly preferably 3 to 6 carbon atoms.
- the arylene group that can be used as R c preferably has 6 to 18 carbon atoms, more preferably 6 to 14, more preferably 6 to 10, and still more preferably phenylene.
- X d is a group having a structural part selected from OH, NH and SH, and X d has 0 to 2 carbon atoms.
- Preferred examples of Xd include amino group, monoalkylamino group, acylamino group, hydroxy group, carboxy group, carbamoyl group, mercapto group, boric acid group, phosphoric acid group, sulfo group, sulfino group, sulfamoyl group, ureido group, And a hydroxamic acid group and a hydrazino group, and an amino group, an acylamino group, a hydroxy group, a carboxy group, a carbamoyl group, a boric acid group or a sulfamoyl group is more preferable, and an acylamino group, a hydroxy group, a carboxy group, a carbamoyl group, or a sulfamoyl group.
- the group is
- the repeating unit represented by the formula (Ic) can increase motility by the action of R c which is a linker site, and can realize sufficient gas permeability more reliably.
- R c which is a linker site
- Xd has a structural part selected from OH, NH and SH
- hydrogen bonding interaction between polyimide chains can be enhanced. Therefore, it is considered that good gas separation selectivity and plastic resistance can be realized.
- the repeating unit represented by the above formula (Ic) is also preferably a repeating unit represented by the following formula (Id).
- R a , R c , X d , A a , A b and A c are the same as R a , R c , X d , A a and A in formula (Ic), respectively. It has the same meaning as b and a c, which is the preferred form also the same.
- R d represents an alkylene group, a cycloalkylene group or an arylene group.
- Preferred forms of the alkylene group, cycloalkylene group, and arylene group that can be taken as R d are the same as the preferred forms of the alkylene group, cycloalkylene group, and arylene group that can be taken as R c , respectively.
- X e is a group having a structural part selected from OH, NH and SH, and X e has 0 to 2 carbon atoms.
- a preferred form of X e are the same as the preferred mode of the X d.
- the polyimide compound constituting the gas separation layer is in a dense packing state, and appropriate pores are also generated. It is estimated that gas separation selectivity and gas permeability can be compatible at a high level.
- the polyimide compound used in the present invention may have a repeating unit represented by the following formula (II-a) and / or (II-b) in addition to the repeating unit represented by the above formula (I). .
- R has the same meaning as R a in formula (I), and the preferred range is also the same.
- a d , A e and A f each independently represent a substituent. Examples of the substituent include a group selected from the substituent group Z described later.
- Ad is preferably an alkyl group, a carboxy group, or a halogen atom.
- K1 indicating the number of A d is an integer of 0 to 4, when A d is an alkyl group, preferably k1 is 1-4, more preferably 2-4, more preferably 3 or 4.
- Ad is a carboxy group, k1 is preferably 1 to 2, more preferably 1.
- the alkyl group preferably has 1 to 10 carbon atoms, more preferably 1 to 5, more preferably 1 to 3, and still more preferably methyl, ethyl Or trifluoromethyl.
- the two linking sites for incorporation into the polyimide compound of the diamine component are preferably located at the meta position or the para position relative to each other. More preferably, it is located at a position.
- the structure represented by the formula (II-a) does not include the structure represented by the formula (I).
- a e and A f each preferably represents an alkyl group or a halogen atom, or a group that forms a ring together with X 9 by being linked to each other.
- a form in which two Ae are connected to form a ring and a form in which two Af are connected to form a ring are also preferable.
- the structure in which A e and A f are connected is not particularly limited, but a single bond, —O— or —S— is preferable.
- M1 and n1 representing the numbers of Ae and Af are integers of 0 to 4, preferably 1 to 4, more preferably 2 to 4, and more preferably 3 or 4.
- the alkyl group preferably has 1 to 10 carbon atoms, more preferably 1 to 5 carbon atoms, still more preferably 1 to 3 carbon atoms, and still more preferably Is methyl, ethyl or trifluoromethyl.
- X 9 has the same meaning as X 1 in formula (I-1), and the preferred range is also the same.
- the content of the repeating unit represented by the above formula (I) is preferably 30 to 100 mol%, more preferably 50 to 100 mol%, It is more preferably 70 to 100 mol%, particularly preferably 80 to 100 mol%.
- the repeating unit represented by the above formula (I), the repeating unit represented by the above formula (II-a), and the above formula (II-b) are represented.
- the proportion of the molar amount of the repeating unit represented by the formula (I) in the total molar amount of the repeating unit is preferably 30 to 100 mol%, more preferably 50 to 100 mol%, and more preferably 70 to 100 mol%.
- the repeating unit represented by the above formula (I), the repeating unit represented by the above formula (II-a), and the repeating unit represented by the above formula (II-b) account for the total molar amount.
- the ratio of the molar amount of the repeating unit represented by the formula (I) is 100 mol% means that the polyimide compound contains the repeating unit represented by the above formula (II-a) and the above formula (II-b). ) Means that none of the repeating units represented.
- the polyimide compound used in the present invention comprises a repeating unit represented by the above formula (I), or a repeating unit represented by the above formula (I), and the above formula (II-a) and / or the above formula It is preferably composed of a repeating unit represented by (II-b).
- repeating unit represented by the above formula (II-a) and / or the above formula (II-b) means an embodiment comprising the repeating unit represented by the above formula (II-a), An embodiment comprising a repeating unit represented by the above formula (II-b) or an embodiment comprising a repeating unit represented by the above formula (II-a) and a repeating unit represented by the above formula (II-b) It is the meaning including these three aspects.
- Substituent group Z An alkyl group (preferably an alkyl group having 1 to 30 carbon atoms, more preferably 1 to 20 carbon atoms, particularly preferably 1 to 10 carbon atoms, such as methyl, ethyl, iso-propyl, tert-butyl, n-octyl) , N-decyl, n-hexadecyl), a cycloalkyl group (preferably a cycloalkyl group having 3 to 30 carbon atoms, more preferably 3 to 20 carbon atoms, particularly preferably 3 to 10 carbon atoms, such as cyclopropyl, Cyclopentyl, cyclohexyl, etc.), an alkenyl group (preferably an alkenyl group having 2 to 30 carbon atoms, more preferably 2 to 20 carbon atoms, particularly preferably 2 to 10 carbon atoms, such as vinyl, allyl, -Butenyl, 3-pentenyl, etc.), alky
- an aryl group having 6 to 12 carbon atoms such as phenyl, p-methylphenyl, naphthyl, anthranyl, etc.
- amino group amino group, alkylamino group, arylamino group, hetero
- a cyclic amino group preferably an amino group having 0 to 30 carbon atoms, more preferably 0 to 20 carbon atoms, still more preferably 0 to 10 carbon atoms, and particularly preferably 0 to 6 carbon atoms.
- a alkoxy group (preferably an alkoxy group having 1 to 30 carbon atoms, more preferably 1 to 20 carbon atoms, particularly preferably 1 to 10 carbon atoms, and examples thereof include methoxy, ethoxy, butoxy, 2-ethylhexyloxy and the like.
- An aryloxy group preferably an aryloxy group having 6 to 30 carbon atoms, more preferably 6 to 20 carbon atoms, particularly preferably 6 to 12 carbon atoms, such as phenyloxy, 1-naphthyloxy, 2-naphthyl Oxy and the like
- a heterocyclic oxy group preferably a heterocyclic oxy group having 1 to 30 carbon atoms, more preferably 1 to 20 carbon atoms, particularly preferably 1 to 12 carbon atoms, such as pyridyloxy, Pyrazyloxy, pyrimidyloxy, quinolyloxy, etc.
- An acyl group (preferably an acyl group having 1 to 30 carbon atoms, more preferably 1 to 20 carbon atoms, still more preferably 1 to 12 carbon atoms, and particularly preferably 2 to 8 carbon atoms.
- alkoxycarbonyl groups preferably C2-C30, more preferably C2-C20, particularly preferably C2-C12 alkoxycarbonyl groups such as methoxycarbonyl, ethoxycarbonyl, etc.
- An aryloxycarbonyl group (preferably an aryloxycarbonyl group having 7 to 30 carbon atoms, more preferably 7 to 20 carbon atoms, particularly preferably 7 to 12 carbon atoms, such as phenyloxycarbonyl)
- An acyloxy group (preferably having 2 to 30 carbon atoms, An acyloxy group having 2 to 20 carbon atoms, particularly preferably 2 to 10 carbon atoms, preferably acetoxy,
- alkoxycarbonylamino group preferably an alkoxycarbonylamino group having 2 to 30 carbon atoms, more preferably 2 to 20 carbon atoms, particularly preferably 2 to 12 carbon atoms, such as methoxycarbonylamino
- aryl Oxycarbonylamino group preferably an aryloxycarbonylamino group having 7 to 30 carbon atoms, more preferably 7 to 20 carbon atoms, particularly preferably 7 to 12 carbon atoms, and examples thereof include phenyloxycarbonylamino group
- a sulfonylamino group preferably having 1 to 30 carbon atoms, more preferably 1 to 20 carbon atoms, particularly preferably 1 to 12 carbon atoms, such as methanesulfonylamino, benzenesulfonylamino, etc.
- a sulfamoyl group Preferably 0-30 carbon atoms, more preferred Is a sulfamoyl group having 0 to 20 carbon
- a carbamoyl group (preferably a carbamoyl group having 1 to 20 carbon atoms, more preferably 1 to 16, more preferably 1 to 12, particularly preferably 1 to 7 carbon atoms, such as a carbamoyl group, methylcarbamoyl group, Group, diethylcarbamoyl group, phenylcarbamoyl group, etc.)
- An alkylthio group preferably an alkylthio group having 1 to 30 carbon atoms, more preferably 1 to 20 carbon atoms, particularly preferably 1 to 12 carbon atoms, such as methylthio and ethylthio
- an arylthio group preferably An arylthio group having 6 to 30 carbon atoms, more preferably 6 to 20 carbon atoms, particularly preferably 6 to 12 carbon atoms, such as phenylthio, and a heterocyclic thio group (preferably having 1 to 30 carbon atoms).
- heterocyclic thio group having 1 to 20 carbon atoms, particularly preferably 1 to 12 carbon atoms, such as pyridylthio, 2-benzimidazolylthio, 2-benzoxazolylthio, 2-benzthiazolylthio and the like.
- a sulfonyl group (preferably a sulfonyl group having 1 to 30 carbon atoms, more preferably 1 to 20 carbon atoms, particularly preferably 1 to 12 carbon atoms, such as mesyl, tosyl, etc.), a sulfinyl group (preferably A sulfinyl group having 1 to 30 carbon atoms, more preferably 1 to 20 carbon atoms, particularly preferably 1 to 12 carbon atoms, such as methanesulfinyl, benzenesulfinyl, etc.), ureido group (preferably having 1 carbon atom) -30, more preferably a ureido group having 1 to 20 carbon atoms, particularly preferably 1 to 12 carbon atoms, such as ureido, methylureido, phenylureido, etc.), a phosphoramide group (preferably having a carbon number) A phosphoric acid amide group having 1 to 30, more preferably 1 to 20 carbon
- the heteroatom may be a heterocycle, and examples of the heteroatom constituting the heterocycle include a nitrogen atom, an oxygen atom and a sulfur atom, preferably 0 to 30 carbon atoms, more preferably a heterocycle having 1 to 12 carbon atoms.
- Specific examples include imidazolyl, pyridyl, quinolyl, furyl, thienyl, piperidyl, morpholino, benzoxazolyl, benzimidazolyl, benzthiazolyl, carbazolyl, azepinyl, and the like, and a silyl group (preferably having a carbon number).
- a silyl group having 3 to 40 carbon atoms, more preferably 3 to 30 carbon atoms, particularly preferably 3 to 24 carbon atoms For example, trimethylsilyl, triphenylsilyl, etc.), a silyloxy group (preferably a silyloxy group having 3 to 40 carbon atoms, more preferably 3 to 30 carbon atoms, and particularly preferably 3 to 24 carbon atoms. , Triphenylsilyloxy, etc.).
- These substituents may be further substituted with any one or more substituents selected from the above substituent group Z.
- substituents when one structural site has a plurality of substituents, these substituents are connected to each other to form a ring, or condensed with a part or all of the above structural sites to form an aromatic group.
- a ring or an unsaturated heterocyclic ring may be formed.
- a compound or a substituent when a compound or a substituent includes an alkyl group, an alkenyl group, etc., these may be linear or branched, and may be substituted or unsubstituted. When an aryl group, a heterocyclic group, or the like is included, they may be monocyclic or condensed, and may be substituted or unsubstituted.
- the molecular weight of the polyimide compound used in the present invention is preferably 10,000 to 1,000,000 as a weight average molecular weight, more preferably 15,000 to 500,000, and still more preferably 20,000 to 200,000. It is.
- the molecular weight and the dispersity are values measured using a GPC (gel filtration chromatography) method, and the molecular weight is a weight average molecular weight in terms of polystyrene.
- the gel packed in the column used in the GPC method is preferably a gel having an aromatic compound as a repeating unit, and examples thereof include a gel made of a styrene-divinylbenzene copolymer. Two to six columns are preferably connected and used.
- the solvent used include ether solvents such as tetrahydrofuran and amide solvents such as N-methylpyrrolidinone.
- the measurement is preferably performed at a solvent flow rate in the range of 0.1 to 2 mL / min, and most preferably in the range of 0.5 to 1.5 mL / min. By performing the measurement within this range, the apparatus is not loaded and the measurement can be performed more efficiently.
- the measurement temperature is preferably 10 to 50 ° C, most preferably 20 to 40 ° C. Note that the column and carrier to be used can be appropriately selected according to the physical properties of the polymer compound that is symmetrical to the measurement.
- the polyimide compound used in the present invention can be synthesized by condensation polymerization of a specific bifunctional acid anhydride (tetracarboxylic dianhydride) and a specific diamine.
- a general book for example, Ikuo Imai, edited by Rikio Yokota, “Latest Polyimide: Fundamentals and Applications”, NTS Corporation, August 25, 2010, p. 3-49). , Etc.
- Etc. can be carried out with appropriate reference to the methods described in the above.
- At least one tetracarboxylic dianhydride as one raw material is represented by the following formula (IV). All of the tetracarboxylic dianhydrides used as raw materials are preferably represented by the following formula (IV).
- R a has the same meaning as R a in the formula (I).
- tetracarboxylic dianhydrides that can be used in the present invention include the following.
- At least one diamine compound as the other raw material is represented by the following formula (V).
- R b, X a and X b are respectively the same as R b, X a and X b in the formula (I).
- diamine compound represented by the formula (V) include, for example, those shown below, but the present invention is not limited thereto.
- # indicates a linking site with —S ( ⁇ O) 2 N (X b ) X a in the formula (V). Specific examples of this —S ( ⁇ O) 2 N (X b ) X a are shown below.
- a d and k1 are respectively synonymous with A d and k1 in the above formula (II-a).
- the diamine compound represented by the formula (VI-a) does not include the diamine compound represented by the formula (V).
- a e , A f, X 9, m1 and n1 are A e, A f in each of the above formulas (II-b), and X 9, m1 and n1 synonymous.
- the diamine compound represented by the formula (VI-b) does not include the diamine compound represented by the formula (V).
- the monomer represented by the above formula (IV) and the monomer represented by the above formula (V), (VI-a) or (VI-b) may be used in advance as an oligomer or a prepolymer.
- the polyimide compound used in the present invention may be any of a block copolymer, a random copolymer, and a graft copolymer.
- the polyimide compound used in the present invention can be obtained by mixing each of the above raw materials in a solvent and performing condensation polymerization by a conventional method as described above.
- the solvent is not particularly limited, but ester organic solvents such as methyl acetate, ethyl acetate, and butyl acetate; aliphatics such as acetone, methyl ethyl ketone, methyl isobutyl ketone, diacetone alcohol, cyclopentanone, and cyclohexanone.
- Ether organic solvents such as ketone, ethylene glycol dimethyl ether, dibutyl butyl ether, tetrahydrofuran, methylcyclopentyl ether, dioxane, amide organic solvents such as N-methylpyrrolidone, 2-pyrrolidone, dimethylformamide, dimethylimidazolidinone, dimethylacetamide, dimethyl And sulfur-containing organic solvents such as sulfoxide and sulfolane. These organic solvents are appropriately selected as long as it is possible to dissolve tetracarboxylic dianhydride as a reaction substrate, diamine compound, polyamic acid as a reaction intermediate, and polyimide compound as a final product.
- ester type preferably butyl acetate
- aliphatic ketone preferably methyl ethyl ketone, methyl isobutyl ketone, diacetone alcohol, cyclopentanone, cyclohexanone
- ether type diethylene glycol monomethyl ether, methyl cyclopentyl) Ether
- amide preferably N-methylpyrrolidone
- sulfur-containing dimethyl sulfoxide, sulfolane
- the polymerization reaction temperature is not particularly limited, and a temperature that can be usually employed in the synthesis of a polyimide compound can be employed. Specifically, it is preferably ⁇ 40 to 60 ° C., more preferably ⁇ 30 to 50 ° C.
- a polyimide compound is obtained by imidizing the polyamic acid produced by the above polymerization reaction by a dehydration ring-closing reaction in the molecule.
- a method for dehydrating and ring-closing a general book (for example, Ikuo Imai, edited by Rikio Yokota, “Latest Polyimide: Fundamentals and Applications”), NTS Corporation, August 25, 2010, p. 3 to 49, etc.) can be referred to.
- acetic anhydride or dicyclohexyl is heated in the presence of a basic catalyst such as pyridine, triethylamine or DBU by heating to 120 ° C to 200 ° C for reaction while removing by-product water out of the system.
- a technique such as so-called chemical imidization using a dehydration condensing agent such as carbodiimide and triphenyl phosphite is preferably used.
- the total concentration of tetracarboxylic dianhydride and diamine compound in the polymerization reaction solution of the polyimide compound is not particularly limited, but is preferably 5 to 70% by mass, more preferably 5 to 50% by mass. And more preferably 5 to 30% by mass.
- FIG. 1 is a longitudinal sectional view schematically showing a gas separation composite membrane 10 which is a preferred embodiment of the present invention.
- 1 is a gas separation layer
- 2 is a support layer which consists of a porous layer.
- FIG. 2 is a cross-sectional view schematically showing a gas separation composite membrane 20 which is a preferred embodiment of the present invention.
- the support layer includes the nonwoven fabric layer 3
- the gas separation composite membrane 20 includes the gas separation layer 1, the porous layer 2, and the nonwoven fabric layer 3.
- 1 and 2 show an embodiment in which carbon dioxide is selectively permeated from a mixed gas of carbon dioxide and methane to make the permeated gas rich in carbon dioxide.
- “on the support layer” means that another layer may be interposed between the support layer and the gas separation layer.
- the side of the gas separation membrane to which the gas to be separated is supplied is “upper”, and the side from which the separated gas is discharged is “lower”.
- the gas separation composite membrane of the present invention may be formed or disposed on the surface or inner surface of a porous support (support layer), or at least formed on the surface of the porous support.
- a composite membrane can be easily formed.
- a composite membrane having both high separation selectivity, high gas permeability, and mechanical strength can be obtained.
- the film thickness of the gas separation layer is preferably as thin as possible from the viewpoint of gas permeability as long as the mechanical strength and gas separation selectivity can be maintained at desired levels.
- the thickness of the gas separation layer is not particularly limited, but is preferably 0.01 to 5.0 ⁇ m, more preferably 0.05 to 2.0 ⁇ m.
- the support layer is not particularly limited as long as the mechanical strength and gas permeability are at desired levels, and either an organic material or an inorganic material may be used.
- This support layer is preferably a porous layer of an organic polymer, and the thickness thereof is preferably 1 to 3000 ⁇ m, more preferably 5 to 500 ⁇ m, still more preferably 5 to 150 ⁇ m.
- the average pore diameter is usually preferably 10 ⁇ m or less, more preferably 0.5 ⁇ m or less, and still more preferably 0.2 ⁇ m or less.
- the porosity is preferably 20 to 90%, more preferably 30 to 80%.
- the support layer is “gas permeable” means that carbon dioxide is supplied to the support layer (membrane consisting of only the support layer) at a temperature of 40 ° C. with the total pressure on the gas supply side being 4 MPa.
- the permeation rate of carbon dioxide is 1 ⁇ 10 ⁇ 5 cm 3 (STP) / cm 2 ⁇ sec ⁇ cmHg (10 GPU) or more.
- the gas permeability of the support layer is such that when carbon dioxide is supplied at a temperature of 40 ° C.
- the carbon dioxide permeation rate is 3 ⁇ 10 ⁇ 5 cm 3 (STP) / It is preferably cm 2 ⁇ sec ⁇ cmHg (30 GPU) or more, more preferably 100 GPU or more, and further preferably 200 GPU or more.
- the material for the porous layer examples include conventionally known polymers such as polyolefin resins such as polyethylene and polypropylene, fluorine-containing resins such as polytetrafluoroethylene, polyvinyl fluoride, and polyvinylidene fluoride, polystyrene, cellulose acetate, Various resins such as polyurethane, polyacrylonitrile, polyphenylene oxide, polysulfone, polyethersulfone, polyimide, polyaramid, and the like can be given.
- the shape of the porous layer may be any shape such as a flat plate shape, a spiral shape, a tubular shape, and a hollow fiber shape.
- a support is formed to further impart mechanical strength to the lower part of the support layer forming the gas separation layer.
- a support include woven fabrics, nonwoven fabrics, nets, and the like, but nonwoven fabrics are preferably used in terms of film forming properties and cost.
- the nonwoven fabric fibers made of polyester, polypropylene, polyacrylonitrile, polyethylene, polyamide or the like may be used alone or in combination.
- the nonwoven fabric can be produced, for example, by making a main fiber and a binder fiber uniformly dispersed in water with a circular net or a long net and drying with a dryer. Further, for the purpose of removing the fluff or improving the mechanical properties, it is also preferable to apply a heat treatment with the nonwoven fabric sandwiched between two rolls.
- the method for producing a gas separation composite membrane of the present invention is preferably a production method including forming a gas separation layer by applying a coating liquid containing the polyimide compound on a porous support.
- the content of the polyimide compound in the coating solution is not particularly limited, but is preferably 0.1 to 30% by mass, and more preferably 0.5 to 10% by mass.
- the gas separation membrane of the present invention can be produced by adjusting the molecular weight, structure, composition, and solution viscosity of the polyimide compound used for forming the gas separation layer according to the purpose.
- the organic solvent used as a medium for the coating solution is not particularly limited, and hydrocarbon organic solvents such as n-hexane and n-heptane, ester organic solvents such as methyl acetate, ethyl acetate and butyl acetate, methanol Alcohol organic solvents such as ethanol, n-propanol, isopropanol, n-butanol, isobutanol, tert-butanol, aliphatic ketones such as acetone, methyl ethyl ketone, methyl isobutyl ketone, diacetone alcohol, cyclopentanone and cyclohexanone, ethylene Glycol, diethylene glycol, triethylene glycol, glycerin, propylene glycol, ethylene glycol monomethyl or monoethyl ether, propylene glycol methyl ether, dipropylene glycol methyl ether, Ethers such as propylene glycol methyl ether,
- organic solvents are appropriately selected as long as they do not adversely affect the support, such as ester-based organic solvents (preferably butyl acetate), alcohol-based organic solvents (preferably methanol). , Ethanol, isopropanol, isobutanol), aliphatic ketones (preferably methyl ethyl ketone, methyl isobutyl ketone, diacetone alcohol, cyclopentanone, cyclohexanone), ether organic solvents (ethylene glycol, diethylene glycol monomethyl ether, methylcyclopentyl ether) More preferred are aliphatic ketones, alcohol-based organic solvents, and ether-based organic solvents. Moreover, these can be used 1 type or in combination of 2 or more types.
- siloxane compound layer By providing the siloxane compound layer, the unevenness on the outermost surface of the support can be smoothed, and the separation layer can be easily thinned.
- siloxane compound forming the siloxane compound layer include those having a main chain made of polysiloxane and compounds having a siloxane structure and a non-siloxane structure in the main chain.
- siloxane compound means an organopolysiloxane compound unless otherwise specified.
- siloxane compound having a main chain made of polysiloxane examples include one or more polyorganosiloxanes represented by the following formula (1) or (2). Moreover, these polyorganosiloxanes may form a crosslinking reaction product.
- a cross-linking reaction for example, a compound represented by the following formula (1) is crosslinked by a polysiloxane compound having a group capable of linking by reacting with the reactive group X S of the formula (1) at both ends The compound of the form is mentioned.
- R S is a non-reactive group and is an alkyl group (preferably an alkyl group having 1 to 18 carbon atoms, more preferably an alkyl group having 1 to 12 carbon atoms) or an aryl group (preferably having 6 to 6 carbon atoms). 15, more preferably an aryl group having 6 to 12 carbon atoms, and still more preferably phenyl).
- X S is a reactive group selected from a hydrogen atom, a halogen atom, a vinyl group, a hydroxyl group, and a substituted alkyl group (preferably an alkyl group having 1 to 18 carbon atoms, more preferably an alkyl group having 1 to 12 carbon atoms). It is preferably a group.
- Y S and Z S are the above R S or X S.
- m is a number of 1 or more, preferably 1 to 100,000.
- n is a number of 0 or more, preferably 0 to 100,000.
- X S, Y S, Z S, R S, m and n are X S of each formula (1), Y S, Z S, R S, and m and n synonymous.
- examples of the alkyl group include methyl, ethyl, hexyl, octyl, decyl, and octadecyl.
- examples of the fluoroalkyl group include —CH 2 CH 2 CF 3 and —CH 2 CH 2 C 6 F 13 .
- examples of the alkyl group include a hydroxyalkyl group having 1 to 18 carbon atoms and an aminoalkyl group having 1 to 18 carbon atoms.
- the number of carbon atoms of the alkyl group constituting the hydroxyalkyl group is preferably an integer of 1 to 10, for example, —CH 2 CH 2 CH 2 OH.
- the number of carbon atoms of the alkyl group constituting the aminoalkyl group is preferably an integer of 1 to 10, and examples thereof include —CH 2 CH 2 CH 2 NH 2 .
- the number of carbon atoms of the alkyl group constituting the carboxyalkyl group is preferably an integer of 1 to 10.
- Examples of the hydroxyalkyl group include —CH 2 CH 2 CH 2 COOH.
- the number of carbon atoms of the alkyl group constituting the chloroalkyl group is preferably an integer of 1 to 10.
- the aminoalkyl group include —CH 2 Cl.
- a preferable carbon number of the alkyl group constituting the glycidoxyalkyl group is an integer of 1 to 10.
- Examples of the glycidoxyalkyl group include 3-glycidyloxypropyl.
- the preferable number of carbon atoms of the epoxy cyclohexyl alkyl group having 7 to 16 carbon atoms is an integer of 8 to 12.
- a preferable carbon number of the (1-oxacyclobutan-3-yl) alkyl group having 4 to 18 carbon atoms is an integer of 4 to 10.
- a preferable carbon number of the alkyl group constituting the methacryloxyalkyl group is an integer of 1 to 10.
- Examples of the methacryloxyalkyl group include —CH 2 CH 2 CH 2 —OOC—C (CH 3 ) ⁇ CH 2 .
- a preferable carbon number of the alkyl group constituting the mercaptoalkyl group is an integer of 1 to 10.
- examples of the methacryloxyalkyl group include —CH 2 CH 2 CH 2 SH.
- m and n are preferably numbers that give a molecular weight of 5,000 to 1,000,000 of the compound.
- a reactive group-containing siloxane unit (wherein the number is a structural unit represented by n) and a siloxane unit having no reactive group (wherein the number is m)
- the distribution of the structural unit represented by That is, in the formulas (1) and (2), the (Si (R S ) (R S ) —O) unit and the (Si (R S ) (X S ) —O) unit may be randomly distributed. Good.
- R S, m and n are respectively the same as R S, m and n in formula (1).
- R L is —O— or —CH 2 —
- R S1 is a hydrogen atom or methyl. Both ends of Formula (3) are preferably an amino group, a hydroxyl group, a carboxy group, a trimethylsilyl group, an epoxy group, a vinyl group, a hydrogen atom, or a substituted alkyl group.
- n and n are synonymous with m and n in Formula (1), respectively.
- m and n have the same meanings as m and n in formula (1), respectively.
- m and n are synonymous with m and n in Formula (1), respectively. It is preferable that the both ends of Formula (6) have an amino group, a hydroxyl group, a carboxy group, a trimethylsilyl group, an epoxy group, a vinyl group, a hydrogen atom, or a substituted alkyl group bonded thereto.
- m and n are synonymous with m and n in formula (1), respectively. It is preferable that an amino group, a hydroxyl group, a carboxy group, a trimethylsilyl group, an epoxy group, a vinyl group, a hydrogen atom, or a substituted alkyl group is bonded to both ends of the formula (7).
- the siloxane structural unit and the non-siloxane structural unit may be randomly distributed.
- the compound having a siloxane structure and a non-siloxane structure in the main chain preferably contains 50 mol% or more of siloxane structural units, more preferably 70 mol% or more, based on the total number of moles of all repeating structural units. .
- the weight average molecular weight of the siloxane compound used in the siloxane compound layer is preferably 5,000 to 1,000,000 from the viewpoint of achieving both a thin film and durability.
- the method for measuring the weight average molecular weight is as described above.
- siloxane compound which comprises a siloxane compound layer is enumerated below.
- the thickness of the siloxane compound layer is preferably 0.01 to 5 ⁇ m and more preferably 0.05 to 1 ⁇ m from the viewpoint of smoothness and gas permeability.
- the gas permeability at 40 ° C. and 4 MPa of the siloxane compound layer is preferably 100 GPU or more, more preferably 300 GPU or more, and further preferably 1000 GPU or more in terms of carbon dioxide transmission rate.
- the gas separation membrane of the present invention may be an asymmetric membrane.
- the asymmetric membrane can be formed by a phase change method using a solution containing a polyimide compound.
- the phase inversion method is a known method for forming a film while bringing a polymer solution into contact with a coagulation liquid to cause phase conversion.
- a so-called dry / wet method is suitably used.
- the polymer solution in the shape of a film is evaporated to form a thin dense layer, which is then immersed in a coagulation liquid, and micropores are formed by utilizing the phase separation phenomenon that occurs.
- the thickness of the surface layer that contributes to gas separation is not particularly limited, but is 0.01 to 5.0 ⁇ m from the viewpoint of imparting practical gas permeability. And more preferably 0.05 to 1.0 ⁇ m.
- the porous layer below the dense layer lowers the gas permeability resistance and at the same time imparts mechanical strength, and its thickness is particularly limited as long as it is self-supporting as an asymmetric membrane. It is not a thing.
- the thickness of the lower porous layer in the asymmetric membrane is preferably 5 to 500 ⁇ m, more preferably 5 to 200 ⁇ m, and even more preferably 5 to 100 ⁇ m.
- the gas separation asymmetric membrane of the present invention may be a flat membrane or a hollow fiber membrane.
- the asymmetric hollow fiber membrane can be produced by a dry and wet spinning method.
- the dry-wet spinning method is a method for producing an asymmetric hollow fiber membrane by applying a dry-wet method to a polymer solution that is discharged from a spinning nozzle to have a hollow fiber-like target shape. More specifically, the polymer solution is discharged from a nozzle into a hollow fiber-like target shape, and is passed through an air or nitrogen gas atmosphere immediately after the discharge. Thereafter, the polymer is not substantially dissolved and is immersed in a coagulation liquid having compatibility with the solvent of the polymer solution to form an asymmetric structure. Thereafter, the separation membrane is produced by drying and further heat-treating as necessary.
- the solution viscosity of the solution containing the polyimide compound discharged from the nozzle is preferably 2 to 17000 Pa ⁇ s, more preferably 10 to 1500 Pa ⁇ s, particularly 20 to 1000 Pa ⁇ s at the discharge temperature (for example, 10 ° C.),
- the shape after discharge such as a hollow fiber shape, can be stabilized.
- the film is immersed in the primary coagulation liquid and solidified to such an extent that the shape of the hollow fiber or the like can be maintained, wound on a guide roll, and then immersed in the secondary coagulation liquid to fully saturate the entire film. It is preferable to solidify. It is efficient to dry the coagulated film after replacing the coagulating liquid with a solvent such as hydrocarbon.
- the heat treatment for drying is preferably performed at a temperature lower than the softening point or secondary transition point of the used polyimide compound.
- a siloxane compound layer may be provided as a protective layer on the gas separation layer.
- the siloxane compound layer used as the protective layer preferably has a Si ratio before and after immersion in chloroform represented by the following formula (I) in the range of 0.6 to 1.0.
- Si ratio (Si-K ⁇ X-ray intensity after chloroform immersion) / (Si-K ⁇ X-ray intensity before chloroform immersion)
- a method for measuring the Si-K ⁇ X-ray intensity is described in, for example, Japanese Patent Application Laid-Open No. 6-88792.
- the Si-K ⁇ X-ray intensity is reduced by immersion in chloroform as compared with that before immersion, it means that a low molecular weight component is present and eluted. Therefore, the smaller the degree of decrease in the Si-K ⁇ X-ray intensity after immersion in chloroform, the higher the polymer constituting the siloxane compound layer, and the more difficult it is to elute in chloroform.
- the Si ratio of the siloxane compound layer is in the range of 0.6 to 1.0, the siloxane compound can be present in the layer with high density and uniformity, effectively preventing film defects and gas separation. The performance can be further increased. In addition, use under high pressure, high temperature and high humidity conditions, and plasticization of the gas separation layer due to impurity components such as toluene can be further suppressed.
- the Si ratio of the siloxane compound layer constituting the protective layer is preferably 0.7 to 1.0, more preferably 0.75 to 1.0, still more preferably 0.8 to 1.0, and 0.85 to 1 0.0 is more preferable.
- the siloxane compounds are composed of * —O—M—O— * , * —SMS— * , * —NR a1 C ( ⁇ O) — * , * —NR.
- M represents a divalent to tetravalent metal atom.
- R a1 , R b1 , R c1 , R d1 , R e1 , and R f1 represent a hydrogen atom or an alkyl group. * Indicates a linking site.
- Examples of the metal atom M include aluminum (Al), iron (Fe), beryllium (Be), gallium (Ga), vanadium (V), indium (In), titanium (Ti), zirconium (Zr), and copper. (Cu), cobalt (Co), nickel (Ni), zinc (Zn), calcium (Ca), magnesium (Mg), yttrium (Y), scandium (Sc), chromium (Cr), manganese (Mn), molybdenum
- Examples include metal atoms selected from (Mo) and boron (B), and among these, metal atoms selected from Ti, In, Zr, Fe, Zn, Al, Ga, and B are preferable, and selected from Ti, In, and Al. The metal atom is more preferable, and Al is more preferable.
- the alkyl group that can be adopted as R a1 , R b1 , R c1 , R d1 , R e1 , and R f1 is preferably 1 to 20 carbon atoms, more preferably 1 to 10 carbon atoms, still more preferably 1 to carbon atoms. 7, more preferably an alkyl group having 1 to 4 carbon atoms.
- This alkyl group may be linear or branched, but is more preferably linear.
- Specific examples of preferred alkyl groups include methyl, ethyl, isopropyl, n-butyl, t-butyl, pentyl, hexyl, heptyl, octyl and 1-ethylpentyl.
- the Si ratio of the siloxane compound layer can be easily increased to the range defined in the present invention.
- the linking group * —O—M—O— * is represented by, for example, a siloxane compound having a group having —OH (an active hydrogen-containing group) such as a hydroxy group, a carboxy group, or a sulfo group, and the following formula (B): It can be formed by a ligand exchange reaction with a metal complex (crosslinking agent).
- L L each independently represents an alkoxy group, an aryloxy group, an acetylacetonato group, an acyloxy group, a hydroxy group or a halogen atom.
- y represents an integer of 2 to 4.
- the alkoxy group that can be taken as L L preferably has 1 to 10 carbon atoms, more preferably 1 to 4 carbon atoms, and still more preferably 1 to 3 carbon atoms.
- Specific examples of the alkoxy group that can be taken as L L include, for example, methoxy, ethoxy, tert-butoxy, and isopropoxy.
- the aryloxy group that can be taken as L L preferably has 6 to 10 carbon atoms, more preferably 6 to 8 carbon atoms, and still more preferably 6 to 7 carbon atoms.
- Specific examples of the aryloxy group that can be taken as L L include, for example, phenoxy, 4-methoxyphenoxy, and naphthoxy.
- the acyloxy group that can be taken as L L preferably has 2 to 10 carbon atoms, more preferably 2 to 6 carbon atoms, and still more preferably 2 to 4 carbon atoms.
- Specific examples of the acyloxy group that can be taken as L L include, for example, acetoxy, propanoyloxy, pivaloyloxy, and acetyloxy.
- the halogen atom which can be taken as L L is not particularly limited, and examples thereof include a fluorine atom, a chlorine atom, a bromine atom and an iodine atom. Of these, a chlorine atom is preferable.
- the metal complex represented by the above formula (B) is soluble in an organic solvent used for a coating solution when forming a siloxane compound layer. More specifically, the solubility of the metal complex represented by the above formula (B) with respect to 100 g of tetrahydrofuran at 25 ° C. is preferably 0.01 to 10 g, and preferably 0.1 to 1.0 g. Is more preferable. When the metal complex represented by the formula (B) is soluble in the organic solvent, a more homogeneous metal-crosslinked siloxane compound layer can be formed.
- Preferred examples of the metal complex represented by the formula (B) include aluminum acetylacetonate, gallium acetylacetonate, indium acetylacetonate, zirconium acetylacetonate, cobalt acetylacetonate, calcium acetylacetonate, nickel acetyl.
- ligand exchange reaction is as follows. The following examples show the case where the siloxane compound has a hydroxy group, but when the siloxane compound has an active hydrogen-containing group such as a carboxy group or a sulfo group, the same ligand exchange reaction proceeds, * ⁇ A linking group represented by O—M—O— * is formed.
- R P represents a siloxane compound residue (that is, R P —OH represents a siloxane compound having a hydroxy group).
- R P —OH can usually coordinate up to 4 to one M (form (a) above).
- M is a tetravalent metal atom
- two forms of R P —OH are coordinated (form (c) above), and three are coordinated (form (b) above) )
- 4-coordinated form (form (a) above) are all encompassed by the form having a linking group represented by * —O—M—O— * .
- R P —OH is represented by R P1 — (OH) h
- R P1 is a siloxane compound residue
- h is an integer of 2 or more, that is, one molecule 2 or more OH present in one molecule of R P1 — (OH) h may be coordinated to one M.
- This embodiment also * intended to be encompassed by embodiments having a -O-M-O-* a linking group represented.
- R P —OH can usually be coordinated to one M up to three (form (d) above).
- M is a trivalent metal atom
- two forms of R P —OH are coordinated (form (e) above), and three are coordinated (form (d) above) any form of) are also intended to be encompassed in the form having a linking group represented by * -O-M-O- *.
- R P —OH is represented by R P1 — (OH) h
- R P1 is a siloxane compound residue
- h is an integer of 2 or more, that is, one molecule 2 or more OH present in one molecule of R P1 — (OH) h may be coordinated to one M.
- This embodiment also * intended to be encompassed by embodiments having a -O-M-O-* a linking group represented.
- the form of the (f) is in the form having a linking group represented by the present invention defined by * -O-M-O- *.
- R P —OH is represented by R P1 — (OH) h
- R P1 is a siloxane compound residue
- h is an integer of 2 or more, that is, one molecule 2 or more OH present in one molecule of R P1 — (OH) h may be coordinated to one M.
- This embodiment also * intended to be encompassed by embodiments having a -O-M-O-* a linking group represented.
- the linking structure * -SMS— * can be formed by, for example, a ligand exchange reaction between a siloxane compound having a thiol group and the metal complex represented by the above formula (B). .
- This reaction is a reaction form in which R P —OH is replaced with R P —SH in the above-described reaction for forming * —O—M—O— * . Since —SH is also an active hydrogen-containing group, a ligand exchange reaction can be performed in the same manner as described above.
- the linking group * —NR a C ( ⁇ O) — * is obtained, for example, by reacting a siloxane compound having a carboxy group with a siloxane compound having an amino group in the presence of a dehydration condensing agent (for example, a carbodiimide compound). Can be formed.
- a dehydration condensing agent for example, a carbodiimide compound.
- This reaction can be represented by the following formula.
- RP represents a siloxane compound residue.
- R a linked to one N on the left side is a hydrogen atom, and the rest is a hydrogen atom or an alkyl group. That is, R a on the right side is a hydrogen atom or an alkyl group.
- the linking group can also be formed by reacting a siloxane compound having a carboxy group with a compound having two or more amino groups as a crosslinking agent.
- the said coupling group can also be formed by making the siloxane compound which has an amino group, and the compound which has two or more carboxy groups as a crosslinking agent react.
- the linking group * —NR b1 C ( ⁇ O) NR b1 — * can be formed, for example, by reacting a siloxane compound having an amino group with a chloroformate as a crosslinking agent.
- This reaction can be represented by the following formula. 2R P —N (R b1 ) 2 + Cl—C ( ⁇ O) —O—R Cl ⁇ R P —R b1 N—C ( ⁇ O) —NR b1 —R P + HCl + HO—R Cl
- RP represents a siloxane compound residue
- R Cl represents an alcohol residue of chloroformate.
- R b1 groups connected to one N atom on the left side is a hydrogen atom, and the rest is a hydrogen atom or an alkyl group (that is, R b1 on the right side is a hydrogen atom or an alkyl group).
- the linking group * —O—CH 2 —O— * can be formed, for example, by reacting a siloxane compound having a hydroxy group with formaldehyde as a crosslinking agent. This reaction can be represented by the following formula. 2R P —OH + HC ( ⁇ O) —H ⁇ R P —O—CH (O—R P ) —H + H 2 O
- RP represents a siloxane compound residue.
- the linking group * —S—CH 2 CH 2 — * can be formed, for example, by reacting a siloxane compound having a thiol group with a siloxane compound having a vinyl group.
- This reaction can be represented by the following formula.
- RP represents a siloxane compound residue.
- the linking group can also be formed when a siloxane compound having a thiol group is reacted with a compound having two or more vinyl groups as a crosslinking agent.
- the linking group can be formed by reacting a siloxane compound having a vinyl group with a compound having two or more thiol groups as a crosslinking agent.
- the linking group * —OC ( ⁇ O) O— * can be formed, for example, by reacting a siloxane compound having a hydroxy group with a chloroformate as a crosslinking agent. This reaction can be represented by the following formula. 2R P —OH + Cl—C ( ⁇ O) —O—R Cl ⁇ R P —O—C ( ⁇ O) —O—R P + HCl + HO—R Cl
- RP represents a siloxane compound residue
- R Cl represents an alcohol residue of chloroformate.
- the linking group * —C ( ⁇ O) O — N + (R d1 ) 3 ⁇ * can be formed, for example, by reacting a siloxane compound having a carboxy group with a siloxane compound having an amino group. .
- This reaction can be represented by the following formula.
- RP represents a siloxane compound residue.
- R d1 represents a hydrogen atom or an alkyl group.
- connection structure can also be formed by making the siloxane compound which has a carboxy group, and the compound which has two or more amino groups as a crosslinking agent react.
- said coupling group can also be formed by making the siloxane compound which has an amino group, and the compound which has two or more carboxy groups as a crosslinking agent react.
- the linking group * -SO 3 - N + (R e1) 3 - * can be formed by reacting a siloxane compound having a sulfo group, a siloxane compound having an amino group.
- This reaction can be represented by the following formula.
- RP represents a siloxane compound residue.
- R e1 represents a hydrogen atom or an alkyl group.
- the linking group can also be formed by reacting a siloxane compound having a sulfo group with a compound having two or more amino groups as a crosslinking agent.
- the linking group can also be formed by reacting a siloxane compound having an amino group with a compound having two or more sulfo groups as a crosslinking agent.
- connection structure * —PO 3 H — N + (R f1 ) 3 ⁇ * can be formed, for example, by reacting a cellulose resin having a phosphonic acid group with a siloxane compound having an amino group.
- This reaction can be represented by the following formula.
- R P —PO 3 H 2 + R P —N (R f1 ) 2 ⁇ R P -P ( O) (OH) -O -- N + H (R f1 ) 2 -R P
- RP represents a siloxane residue.
- R f1 represents a hydrogen atom or an alkyl group.
- the linking group can also be formed by reacting a siloxane compound having a phosphonic acid group with a compound having two or more amino groups as a crosslinking agent.
- the linking group can also be formed by reacting a siloxane compound having an amino group with a compound having two or more sulfonic acid groups as a crosslinking agent.
- the linking group * —CH (OH) CH 2 OCO— * can be formed, for example, by reacting a siloxane compound having an epoxy group with a siloxane compound having a carboxy group.
- the linking group is obtained by reacting a siloxane compound having an epoxy group with a compound having two or more carboxy groups as a crosslinking agent, or a siloxane compound having a carboxy group and an epoxy group as a crosslinking agent. It can also be formed by reacting with two or more compounds.
- the linking group * —CH (OH) CH 2 O— * can be formed, for example, by reacting a siloxane compound having an epoxy group with a siloxane compound having a hydroxy group.
- the linking group is obtained by reacting a siloxane compound having an epoxy group with a compound having two or more hydroxy groups as a crosslinking agent, or a siloxane compound having a hydroxy group and an epoxy group as a crosslinking agent. It can also be formed by reacting with two or more compounds.
- the linking group * —CH (OH) CH 2 S— * can be formed, for example, by reacting a siloxane compound having an epoxy group with a siloxane compound having a thiol group.
- the linking group is obtained by reacting a siloxane compound having an epoxy group with a compound having two or more thiol groups as a crosslinking agent, or a siloxane compound having a thiol group and an epoxy group as a crosslinking agent. It can also be formed by reacting with two or more compounds.
- the linking group * —CH (OH) CH 2 NR c1 ⁇ * can be formed, for example, by reacting a siloxane compound having an epoxy group with a siloxane compound having an amino group.
- the linking group includes a reaction between a siloxane compound having an epoxy group and a compound having two or more amino groups as a crosslinking agent, or a siloxane compound having an amino group and an epoxy group as a crosslinking agent. It can also be formed by reacting with two or more compounds.
- the linking group * —CH (CH 2 OH) CH 2 OCO— * can be formed by replacing the epoxy group with an oxetanyl group in the above-described formation of * —CH (OH) CH 2 OCO— * .
- the linking group * —CH (CH 2 OH) CH 2 O— * can be formed by replacing the epoxy group with an oxetanyl group in the above-described formation of * —CH (OH) CH 2 O— * .
- the linking group * —CH (CH 2 OH) CH 2 S— * can be formed by replacing the epoxy group with an oxetanyl group in the above-described formation of * —CH (OH) CH 2 S— * .
- the linking group * —CH (CH 2 OH) CH 2 NR c1 ⁇ * can be formed by replacing the epoxy group with an oxetanyl group in the above-described formation of * —CH (OH) CH 2 NR c — *. it can.
- the linking group * —CH 2 CH 2 — * can be formed, for example, by polymerizing siloxane compounds having a vinyl group (such as a (meth) acryloyl group). It can also be formed by reacting a vinyl group of a siloxane compound having a vinyl group with a hydrosilyl group of a siloxane compound having a hydrosilyl group.
- the structure linked via * —CH 2 CH 2 — * does not include the structure linked via * —S—CH 2 CH 2 — * .
- the siloxane compound layer constituting the protective layer may have one or more of the above-mentioned connection structures.
- connection structure between the siloxane compounds is the above-described * -O-MO- * , from the viewpoint of the reactivity for forming the connection structure and the chemical stability of the connection structure.
- * —SMS— * , * —O—CH 2 —O— * , * —S—CH 2 CH 2 — * , * —OC ( ⁇ O) O— * , * —CH 2 CH 2 — * , And * -C ( ⁇ O) O ⁇ N + (R d1 ) 3 ⁇ * are preferably one or more of a linking structure through a linking group selected from the group * -O—M—O— * , * -S-M-S- * , * -O-CH 2 -O- * and * -S-CH 2 CH 2 - *, * -CH 2 CH 2 - * linked via a linking group selected from one or more preferably two or more structures, * -O-M-
- the siloxane compound used as a raw material for the siloxane compound layer is not particularly limited as long as it is a siloxane compound having a functional group that gives the connecting structure.
- this siloxane compound examples include methacrylate-modified polydialkylsiloxane, methacrylate-modified polydiarylsiloxane, methacrylate-modified polyalkylarylsiloxane, thiol-modified polydialkylsiloxane, thiol-modified polydiarylsiloxane, thiol-modified polyalkylarylsiloxane, hydroxy-modified polysiloxane.
- the modification site by each functional group may be a terminal or a side chain. Moreover, it is preferable that there are two or more modified sites in one molecule. Each functional group introduced by the modification may further have a substituent. Moreover, there is no restriction
- the alkyl group preferably has 1 to 10 carbon atoms, more preferably 1 to 5, more preferably 1 to 3, and still more preferably methyl.
- the aryl group preferably has 6 to 20 carbon atoms, more preferably 6 to 15 carbon atoms, still more preferably 6 to 12 carbon atoms, and even more preferably phenyl.
- the siloxane compound layer constituting the protective layer preferably has at least one structure selected from the following (a) and (b).
- R SL shows an alkyl group or an aryl group each independently.
- L A independently represents a single bond or a divalent linking group.
- X A is * -OM 1 -O- * , * -SM 1 -S- * , * -O-CH 2 -O- * , * -S-CH 2 CH 2- * , * -OC A linking group selected from ( ⁇ O) O— * , * —CH 2 CH 2 — * , and * —C ( ⁇ O) O — N + (R d ) 3 — * .
- M 1 represents Zr, Fe, Zn, B, Al, or Ga
- R d represents a hydrogen atom or an alkyl group.
- a1 and b1 are integers of 2 or more (preferably integers of 5 or more).
- “ * ” Indicates a linking site.
- “**” represents a linking site in the siloxane bond. That is, in the general formulas (1a) to (3a), when ** is an O atom, ** indicates a connecting site with a Si atom, and when ** is a Si atom, ** is an O atom. And the linking site.
- the terminal structure of the general formula (4a) is preferably a group selected from a hydrogen atom, a mercapto group, an amino group, a vinyl group, a carboxy group, an oxetanyl group, a sulfo group, and a phosphonic acid group.
- R SL and R d are alkyl groups, they are preferably alkyl groups having 1 to 10 carbon atoms, more preferably 1 to 5 carbon atoms, still more preferably 1 to 3 carbon atoms, and particularly preferably methyl.
- R SL is an aryl group, the carbon number thereof is preferably 6 to 20, more preferably 6 to 15, further preferably 6 to 12, and still more preferably a phenyl group.
- L A is a divalent linking group
- an alkylene group preferably having 1 to 10 carbon atoms, more preferably an alkylene group having 1 to 5 carbon atoms
- an arylene group preferably having 6 to 20 carbon atoms, more preferably arylene group having 6 to 15 carbon atoms, more preferably has the same meaning as R SL phenylene group
- -Si (R SL) 2 -O- is preferred (R SL is the general formula (2a), the preferred form be the same “O” in —Si (R SL ) 2 —O— is linked to Si shown in the above general formula).
- the structure (a) preferably has a repeating unit represented by the following formula (5a) in addition to the structure represented by any one of the above general formulas (1a) to (3a).
- repeating unit represented by the above formula (5a) is present in the siloxane compound layer with a structure in which the repeating units represented by the above formula (5a) are connected to each other by a siloxane bond.
- the content of the repeating unit represented by the above formula (5a) is preferably 0.01 to 0.55, and preferably 0.03 to 0.40. More preferably, it is 0.05 to 0.25.
- the content of the repeating unit represented by the formula (5a) was determined by using a siloxane compound layer cut into a 2.5 cm square as a measurement sample, and the measurement sample was subjected to X-ray photoelectron spectroscopy (apparatus: Quantra SXM manufactured by Ulvac-PHI).
- the fluorescent X-ray intensity [SA] of the Si—O bond energy peak of the repeating unit (Q component) represented by the formula (5a) and the structure (T component) other than the repeating unit represented by the formula (5a) [SA] / ([SA] + [ST]) is calculated on the basis of the total intensity [ST] of Si—O bond energy peaks, and is defined as the content of the repeating unit represented by the formula (5a).
- the thickness of the siloxane compound layer as the protective layer is preferably 10 to 3000 nm, more preferably 100 to 1500 nm.
- the gas separation membrane (composite membrane and asymmetric membrane) of the present invention can be suitably used as a gas separation recovery method and gas separation purification method.
- a gas separation membrane that selectively permeates and separates carbon dioxide from a gas mixture containing carbon dioxide and hydrocarbon (methane) is preferable.
- the permeation rate of carbon dioxide at 40 ° C. and 5 MPa is preferably 20 GPU or more, more preferably 30 GPU or more, More preferably, it is 35 to 500 GPU.
- the permeation rate ratio of carbon dioxide to methane (R CO2 / R CH4 ) is preferably 15 or more, more preferably 20 or more, further preferably 23 or more, and preferably 25 to 50. Particularly preferred.
- R CO2 represents the permeation rate of carbon dioxide
- R CH4 represents the permeation rate of methane.
- 1 GPU is 1 ⁇ 10 ⁇ 6 cm 3 (STP) / cm 2 ⁇ sec ⁇ cmHg, STP stands for Standard Temperature and Pressure, and GPU stands for Gas Permeation Unit.
- Various polymer compounds can be added to the gas separation layer of the gas separation membrane of the present invention in order to adjust the membrane properties.
- High molecular compounds include acrylic polymers, polyurethane resins, polyamide resins, polyester resins, epoxy resins, phenol resins, polycarbonate resins, polyvinyl butyral resins, polyvinyl formal resins, shellac, vinyl resins, acrylic resins, rubber resins. Waxes and other natural resins can be used. Two or more of these may be used in combination.
- nonionic surfactants, cationic surfactants, organic fluoro compounds, and the like can be added to adjust liquid properties.
- the surfactant include alkylbenzene sulfonate, alkylnaphthalene sulfonate, higher fatty acid salt, sulfonate of higher fatty acid ester, sulfate ester of higher alcohol ether, sulfonate of higher alcohol ether, higher alkyl
- Anionic surfactants such as alkyl carboxylates of sulfonamides, alkyl phosphates, polyoxyethylene alkyl ethers, polyoxyethylene alkyl phenyl ethers, polyoxyethylene fatty acid esters, sorbitan fatty acid esters, ethylene oxide adducts of acetylene glycol,
- Nonionic surfactants such as ethylene oxide adducts of glycerin and polyoxyethylene sorbitan fatty acid esters, and other amphoteric boundaries such as alkyl betaines and amide betaines
- a polymer dispersant may be included, and specific examples of the polymer dispersant include polyvinyl pyrrolidone, polyvinyl alcohol, polyvinyl methyl ether, polyethylene oxide, polyethylene glycol, polypropylene glycol, and polyacrylamide. Of these, polyvinylpyrrolidone is preferably used.
- the conditions for forming the gas separation membrane of the present invention are not particularly limited, but the temperature is preferably ⁇ 30 to 100 ° C., more preferably ⁇ 10 to 80 ° C., and particularly preferably 5 to 50 ° C.
- a gas such as air or oxygen may coexist at the time of forming the film, but it is preferably in an inert gas atmosphere.
- the content of the polyimide compound in the gas separation layer is not particularly limited as long as desired gas separation performance can be obtained. From the viewpoint of further improving the gas separation performance, the content of the polyimide compound in the gas separation layer is preferably 20% by mass or more, more preferably 40% by mass or more, and 60% by mass or more. Is preferable, and it is more preferable that it is 70 mass% or more.
- the content of the polyimide compound in the gas separation layer may be 100% by mass, but is usually 99% by mass or less.
- the gas separation method of the present invention is a method including selectively permeating carbon dioxide from a mixed gas containing carbon dioxide and methane.
- the pressure during gas separation is preferably 0.5 to 10 MPa, more preferably 1 to 10 MPa, and further preferably 2 to 7 MPa.
- the gas separation temperature is preferably ⁇ 30 to 90 ° C., more preferably 15 to 70 ° C.
- a gas separation module can be prepared using the gas separation membrane of the present invention.
- modules include spiral type, hollow fiber type, pleated type, tubular type, plate & frame type and the like.
- a gas separation apparatus having means for separating and recovering or purifying gas can be obtained using the gas separation composite membrane or gas separation module of the present invention.
- the gas separation composite membrane of the present invention may be applied to, for example, a gas separation and recovery device as a membrane / absorption hybrid method used in combination with an absorbing solution as described in JP-A-2007-297605.
- the reaction solution was cooled, diluted with acetone (Wako Pure Chemical Industries, Ltd.), and then isopropyl alcohol (Wako Pure Chemical Industries, Ltd.) was added to obtain a polymer as a solid.
- the operation of dissolving the obtained polymer with acetone and reprecipitating with isopropyl alcohol was repeated twice, followed by drying at 80 ° C. to obtain polyimide (P-1) (18 g).
- Polyimide (P-4) was obtained in the same manner as the synthesis of polyimide (P-2) except that pyromellitic anhydride was used in place of 6FDA in the synthesis of polyimide (P-2).
- polyimide (P-6) was synthesized in the same manner as the synthesis of polyimide (P-5) except that 4,4′-biphthalic anhydride was used instead of pyromellitic anhydride. -6) was obtained.
- Polyimides (P-8), (P-9) and (P-10) are the same as the synthesis of the polyimide (P-1) except that the raw materials used are changed to those corresponding to the following polyimide structures. Got.
- polyimide (P-11a) In the synthesis of the polyimide (P-1), polyimide (P-11a) was obtained in the same manner as the synthesis of the polyimide (P-1) except that 4-aminophenol was used instead of 4-aminobenzoic acid. It was.
- a polyimide (P-13) was obtained in the same manner as the polyimide (P-1) except that iminodiacetic acid was used instead of 4-aminobenzoic acid in the synthesis of the polyimide (P-1). .
- the gas separation composite membrane shown in FIG. 2 was produced (the smooth layer is not shown in FIG. 2).
- 0.08 g of polyimide (P-1) and 7.92 g of tetrahydrofuran were mixed and stirred for 30 minutes, and the resulting mixture was placed on the porous support on which the above smooth layer was formed.
- a gas separation layer was formed by spin coating to obtain a composite film.
- the thickness of the polyimide (P-1) layer was about 100 nm.
- the molecular weight cut off of the used polyacrylonitrile porous layer was 100,000 or less.
- the permeability of carbon dioxide at 40 ° C. and 5 MPa of this porous layer was 25000 GPU.
- the protective layer was provided in the following procedure with respect to the gas separation layer surface of the composite membrane created above. That is, vinyl Q resin (manufactured by Gelest, product number VQM-135) (10 g), hydrosilyl PDMS (manufactured by Gelest, product number HMS-301) (1 g), Karstedt catalyst (manufactured by Aldrich, product number 479527) (5 mg), heptane
- vinyl Q resin manufactured by Gelest, product number VQM-135
- hydrosilyl PDMS manufactured by Gelest, product number HMS-301
- Karstedt catalyst manufactured by Aldrich, product number 479527
- heptane The mixture obtained by mixing (90 g) was spin-coated on the gas separation layer surface of the composite membrane prepared above. The mixed solution was dried and cured at 80 ° C. for 5 hours to obtain a gas separation composite membrane having a 500 nm thick siloxane compound layer (protective layer) on the gas separation layer.
- Example 2 to 13 Production of Composite Film In the same manner as in Example 1 except that polyimide (P-1) was changed to polyimides (P-2) to (P-13) in Example 1 above, Gas separation composite membranes having protective layers of Examples 2 to 13 were produced.
- the measurement is performed under the conditions of carbon dioxide (CO 2 ): methane (CH 4 ) 13:87 (volume ratio) mixed gas, the total pressure on the gas supply side is 5 MPa (CO 2 partial pressure: 0.3 MPa), flow rate The adjustment was carried out so as to be 500 mL / min and 40 ° C.
- the permeated gas was analyzed by gas chromatography.
- the gas permeability of the membrane was compared by calculating the gas permeation rate as gas permeability (Permeance).
- the gas separation selectivity was calculated as the ratio of the CO 2 permeation rate R CO2 to the CH 4 permeation rate R CH4 of this membrane (R CO2 / R CH4 ).
- the above measurement results were evaluated based on the following evaluation criteria.
- R CO2 / R CH4 is 30 or more B: R CO2 / R CH4 is 25 or more and less than 30 C: R CO2 / R CH4 is 20 or more and less than 25 D: R CO2 / R CH4 is 15 or more and less than 20 E: R CO2 / R CH4 is less than 15
- the gas separation membrane in which the gas separation layer was formed using comparative polyimide (C-1) had many membrane defects in the gas separation layer and did not function as a gas separation membrane.
- a gas separation membrane in which a gas separation layer is formed using comparative polyimide (C-2) is inferior in both gas permeability and gas separation selectivity, and is easily plasticized by exposure to toluene and inferior in durability. there were.
- a gas separation membrane in which a gas separation layer is formed using the polyimide compound defined in the present invention has a high gas permeation rate and an enhanced gas separation selectivity. Further, it was found that these gas separation membranes are not easily deteriorated in gas separation performance even when exposed to toluene, and are excellent in plasticization resistance (Examples 1 to 13).
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Analytical Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Separation Using Semi-Permeable Membranes (AREA)
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
Abstract
高圧条件下の使用においてもガス透過性とガス分離選択性の両立を十分なレベルで実現し、可塑化耐性にも優れたガス分離膜、このガス分離膜を用いたガス分離モジュール、ガス分離装置及びガス分離方法を提供する。上記ガス分離膜のガス分離層の原料として好適なポリイミド化合物を提供する。ガス分離膜は、ポリイミド化合物を含むガス分離層を有し、ポリイミド化合物が式(I)で表される繰り返し単位を含む。ガス分離モジュール、ガス分離装置及びガス分離方法は上記ガス分離膜を用いる。Raは特定の4価の基を示し、Rbは特定の環を有する3価の基を示す。Xaは特定の置換基を示し、Xbは水素原子又は置換基を示す。 式(1-b)又は(1-c)で表されるポリイミド化合物。Raは特定の4価の基を示し、Rcは特定の2価の基を示す。Aa、Ab、Ac及びXbは水素原子又は置換基を示し、Xc及びXdは特定の置換基を示す。
Description
本発明は、ガス分離膜、ガス分離モジュール、ガス分離装置、ガス分離方法及びポリイミド化合物に関する。
高分子化合物からなる素材には、その素材ごとに特有の気体透過性がある。ガス分離膜は、その性質に基づき、特定の高分子化合物から構成された膜によって、所望の気体成分を選択的に透過させて分離することができる。ガス分離膜の産業上の利用態様として、地球温暖化の問題と関連し、火力発電所、セメントプラント、製鉄所高炉等において、大規模な二酸化炭素発生源から二酸化炭素を分離回収することが検討されている。また、天然ガスやバイオガス(生物の排泄物、有機質肥料、生分解性物質、汚水、ゴミ、又はエネルギー作物などの、発酵又は嫌気性消化により発生するガス)は主としてメタンと二酸化炭素とを含む混合ガスであり、この混合ガスから不純物である二酸化炭素等を除去する手段としてガス分離膜の利用が検討されている(特許文献1)。
膜分離方法を用いた天然ガスの精製では、より効率的にガスを分離するために、優れたガス透過性とガス分離選択性が求められる。しかし一般に、ガス透過性とガス分離選択性は互いにいわゆるトレードオフの関係にある。それ故、ガス分離層に用いる高分子化合物の分子構造を調整することにより、ガス分離層のガス透過性及びガス分離選択性のいずれかを改善することはできても、これらの特性を高いレベルで両立するのは困難とされる。これを克服するために種々の膜素材が検討されており、その一環としてポリイミド化合物を用いたガス分離膜が検討されてきた。例えば、特許文献2には、特定構造のジアミンからなるポリイミド化合物を用いることで、ガス透過性とガス分離選択性を向上させたことが記載されている。
実際のプラントにおいては、高圧条件、あるいは天然ガス中に存在する不純物(例えば、ベンゼン、トルエン、キシレン)の影響等によって膜が可塑化し、これによるガス分離選択性の低下が問題となる。したがって、ガス分離膜には、ガス透過性とガス分離選択性を高めるだけでなく、高圧条件下や、上記不純物存在下においても良好なガス透過性とガス分離選択性を持続的に発現できる可塑化耐性も求められる。特許文献3には、ポリイミド化合物のジアミン成分として、2位の部位と4~6位の少なくとも1つの部位に置換基を有する1,3-フェニレンジアミン成分を採用し、さらにこのジアミン成分の上記2位の置換基及び4~6位の置換基のうち少なくとも1つの置換基を特定の極性基とすることにより、このポリイミド化合物をガス分離層に用いたガス分離膜が、高圧下でもガス透過性とガス分離選択性のいずれにも優れ、トルエン等の不純物に対しても高い耐性を示したことが記載されている。
実際のプラントにおいては、高圧条件、あるいは天然ガス中に存在する不純物(例えば、ベンゼン、トルエン、キシレン)の影響等によって膜が可塑化し、これによるガス分離選択性の低下が問題となる。したがって、ガス分離膜には、ガス透過性とガス分離選択性を高めるだけでなく、高圧条件下や、上記不純物存在下においても良好なガス透過性とガス分離選択性を持続的に発現できる可塑化耐性も求められる。特許文献3には、ポリイミド化合物のジアミン成分として、2位の部位と4~6位の少なくとも1つの部位に置換基を有する1,3-フェニレンジアミン成分を採用し、さらにこのジアミン成分の上記2位の置換基及び4~6位の置換基のうち少なくとも1つの置換基を特定の極性基とすることにより、このポリイミド化合物をガス分離層に用いたガス分離膜が、高圧下でもガス透過性とガス分離選択性のいずれにも優れ、トルエン等の不純物に対しても高い耐性を示したことが記載されている。
実用的なガス分離膜とするためには、ガス分離層を薄層にして十分なガス透過性を確保した上で、さらに高度なガス分離選択性も実現しなければならない。ガス分離層を薄層化する手法としては、ポリイミド化合物等の高分子化合物を相分離法により非対称膜とし、分離に寄与する部分を緻密層あるいはスキン層と呼ばれる薄層にする方法がある。この非対称膜では、緻密層以外の部分を膜の機械的強度を担う支持層として機能させる。
また、上記非対称膜の他に、ガス分離機能を担うガス分離層と機械強度を担う支持層とを別素材とし、ガス透過性の支持層上に、ガス分離能を有するガス分離層を薄層に形成する複合膜の形態も知られている。
また、上記非対称膜の他に、ガス分離機能を担うガス分離層と機械強度を担う支持層とを別素材とし、ガス透過性の支持層上に、ガス分離能を有するガス分離層を薄層に形成する複合膜の形態も知られている。
本発明は、高圧条件下の使用においてもガス透過性とガス分離選択性の両立を十分なレベルで実現して高速かつ高選択性のガス分離を可能とするガス分離膜に関する。また本発明は、不純物成分であるトルエン等と接触してもガス分離性能を良好に維持することができるガス分離膜に関する。さらに本発明は、上記ガス分離膜を用いたガス分離モジュール、ガス分離装置及びガス分離方法に関する。また本発明は、上記ガス分離膜のガス分離層の構成材料として好適なポリイミド化合物に関する。
本発明者らは上記課題に鑑み鋭意検討を重ねた結果、ポリイミド化合物を用いたガス分離層を有するガス分離膜において、このポリイミド化合物のジアミン成分を、特定構造の置換スルファモイル基を持つ環を有する形態とすることにより、高速かつ高選択性のガス分離が実現できること、また、このガス分離膜を不純物成分であるトルエン等に曝してもガス分離層が可塑化しにくく、良好なガス分離性能の持続的な発現が可能になることを見出した。本発明は、これらの知見に基づきさらに検討を重ね、完成させるに至ったものである。
上記の課題は以下の手段により達成された。
〔1〕
ポリイミド化合物を構成材料として含むガス分離層を有するガス分離膜であって、
上記ポリイミド化合物が下記式(I)で表される繰り返し単位を含む、ガス分離膜。
式(I)中、Xaは酸素原子、窒素原子及び/もしくは硫黄原子を有する基、又は、置換基中にフッ素原子を有するアリール基を示す。Xbは水素原子又は置換基を示す。但し、式(I)中の-N(Xb)-で表される構造中にOH、NH及びSHから選ばれる構造部が含まれない場合、XaはOH、NH及びSHから選ばれる構造部を少なくとも1つ有する。
Raは下記式(I-1)~(I-28)のいずれかで表される基を示す。ここでX1~X3は単結合又は2価の基を示し、Lは、それぞれ独立に、-CH=CH-又は-CH2-を示し、R1及びR2は水素原子又は置換基を示し、*は式(I)中に示されたカルボニル基との結合部位を示す。
Rbは下記式(I-29)~(I-42)のいずれかで表される基を示す。ここでX4~X8は単結合又は2価の基を示し、Lは-CH=CH-又は-CH2-を示し、RZは置換基を示し、*は式(I)中に示されたイミド基との結合部位を示し、#は式(I)中に示されたスルファモイル基との結合部位を示す。dは、それぞれ独立に、0~3の整数を示し、eは、それぞれ独立に、0~4の整数を示し、fは、それぞれ独立に、0~5の整数を示し、gは0~6の整数を示し、hは、それぞれ独立に、0~7の整数を示し、jは、それぞれ独立に、0~9の整数を示し、kは0~10の整数を示す。qは、それぞれ独立に、0又は1を示す。
〔1〕
ポリイミド化合物を構成材料として含むガス分離層を有するガス分離膜であって、
上記ポリイミド化合物が下記式(I)で表される繰り返し単位を含む、ガス分離膜。
式(I)中、Xaは酸素原子、窒素原子及び/もしくは硫黄原子を有する基、又は、置換基中にフッ素原子を有するアリール基を示す。Xbは水素原子又は置換基を示す。但し、式(I)中の-N(Xb)-で表される構造中にOH、NH及びSHから選ばれる構造部が含まれない場合、XaはOH、NH及びSHから選ばれる構造部を少なくとも1つ有する。
Raは下記式(I-1)~(I-28)のいずれかで表される基を示す。ここでX1~X3は単結合又は2価の基を示し、Lは、それぞれ独立に、-CH=CH-又は-CH2-を示し、R1及びR2は水素原子又は置換基を示し、*は式(I)中に示されたカルボニル基との結合部位を示す。
Rbは下記式(I-29)~(I-42)のいずれかで表される基を示す。ここでX4~X8は単結合又は2価の基を示し、Lは-CH=CH-又は-CH2-を示し、RZは置換基を示し、*は式(I)中に示されたイミド基との結合部位を示し、#は式(I)中に示されたスルファモイル基との結合部位を示す。dは、それぞれ独立に、0~3の整数を示し、eは、それぞれ独立に、0~4の整数を示し、fは、それぞれ独立に、0~5の整数を示し、gは0~6の整数を示し、hは、それぞれ独立に、0~7の整数を示し、jは、それぞれ独立に、0~9の整数を示し、kは0~10の整数を示す。qは、それぞれ独立に、0又は1を示す。
〔2〕
上記Rbが上記式(I-29)又は(I-34)で表される基を示す、〔1〕記載のガス分離膜。
〔3〕
上記式(I)で表される繰り返し単位が下記式(I-a)で表される繰り返し単位である、〔1〕又は〔2〕記載のガス分離膜。
式(I-a)中、Ra、Xa及びXbは、それぞれ上記式(I)中のRa、Xa及びXbと同義である。Aa、Ab及びAcは水素原子又は置換基を示す。
〔4〕
上記式(I-a)で表される繰り返し単位が下記式(I-b)で表される繰り返し単位である、〔3〕記載のガス分離膜。
式(I-b)中、Ra、Xb、Aa、Ab及びAcは、それぞれ上記式(I-a)中のRa、Xb、Aa、Ab及びAcと同義である。Xcは置換基を示す。但し、式(I-b)中の-N(Xb)-で表される構造中にOH、NH及びSHから選ばれる構造部が含まれない場合、XcはOH、NH及びSHから選ばれる構造部を少なくとも1つ有する。
〔5〕
上記Xcがフッ素原子を少なくとも1つ有する置換基である、〔4〕記載のガス分離膜。
〔6〕
上記式(I-a)で表される繰り返し単位が下記式(I-c)で表される繰り返し単位である、〔3〕記載のガス分離膜。
式(I-c)中、Ra、Xb、Aa、Ab及びAcは、それぞれ上記式(I-a)中のRa、Xb、Aa、Ab及びAcと同義である。Rcはアルキレン基、シクロアルキレン基又はアリーレン基を示す。XdはOH、NH及びSHから選ばれる構造部を有する、炭素数が0~2の基を示す。
〔7〕
上記式(I-c)で表される繰り返し単位が下記式(I-d)で表される繰り返し単位である、〔6〕記載のガス分離膜。
式(I-d)中、Ra、Rc、Xd、Aa,Ab及びAcは、それぞれ上記式(I-c)中のRa、Rc、Xd、Aa,Ab及びAcと同義である。Rdはアルキレン基、シクロアルキレン基又はアリーレン基を示す。XeはOH、NH及びSHから選ばれる構造部を有する、炭素数が0~2の基を示す。
〔8〕
上記Aa、Ab及びAcのうち少なくとも1つがアルキル基である、〔3〕~〔7〕のいずれかに記載のガス分離膜。
〔9〕
上記ポリイミド化合物中、上記式(I)で表される繰り返し単位の含有量が30~100モル%である、〔1〕~〔8〕のいずれか記載のガス分離膜。
〔10〕
ガス透過性の支持層上に、上記ガス分離層が設けられるガス分離複合膜である、〔1〕~〔9〕のいずれか記載のガス分離膜。
〔11〕
上記支持層が、多孔質層と、不織布層とからなり、
上記不織布層、上記多孔質層および上記ガス分離層がこの順に設けられる、〔10〕に記載のガス分離膜。
〔12〕
分離処理されるガスが二酸化炭素とメタンの混合ガスである場合において、40℃、5MPaにおける二酸化炭素の透過速度が20GPU以上であり、二酸化炭素とメタンとの透過速度比(RCO2/RCH4)が15以上である、〔1〕~〔11〕のいずれか記載のガス分離膜。
〔13〕
二酸化炭素及びメタンを含むガスから二酸化炭素を選択的に透過させるために用いられる、〔1〕~〔12〕のいずれか記載のガス分離膜。
〔14〕
〔1〕~〔13〕のいずれか記載のガス分離膜を具備するガス分離モジュール。
〔15〕
〔14〕に記載のガス分離モジュールを備えたガス分離装置。
〔16〕
〔1〕~〔13〕のいずれか1項に記載のガス分離膜を用いて、二酸化炭素及びメタンを含むガスから二酸化炭素を選択的に透過させるガス分離方法。
上記Rbが上記式(I-29)又は(I-34)で表される基を示す、〔1〕記載のガス分離膜。
〔3〕
上記式(I)で表される繰り返し単位が下記式(I-a)で表される繰り返し単位である、〔1〕又は〔2〕記載のガス分離膜。
式(I-a)中、Ra、Xa及びXbは、それぞれ上記式(I)中のRa、Xa及びXbと同義である。Aa、Ab及びAcは水素原子又は置換基を示す。
〔4〕
上記式(I-a)で表される繰り返し単位が下記式(I-b)で表される繰り返し単位である、〔3〕記載のガス分離膜。
式(I-b)中、Ra、Xb、Aa、Ab及びAcは、それぞれ上記式(I-a)中のRa、Xb、Aa、Ab及びAcと同義である。Xcは置換基を示す。但し、式(I-b)中の-N(Xb)-で表される構造中にOH、NH及びSHから選ばれる構造部が含まれない場合、XcはOH、NH及びSHから選ばれる構造部を少なくとも1つ有する。
〔5〕
上記Xcがフッ素原子を少なくとも1つ有する置換基である、〔4〕記載のガス分離膜。
〔6〕
上記式(I-a)で表される繰り返し単位が下記式(I-c)で表される繰り返し単位である、〔3〕記載のガス分離膜。
式(I-c)中、Ra、Xb、Aa、Ab及びAcは、それぞれ上記式(I-a)中のRa、Xb、Aa、Ab及びAcと同義である。Rcはアルキレン基、シクロアルキレン基又はアリーレン基を示す。XdはOH、NH及びSHから選ばれる構造部を有する、炭素数が0~2の基を示す。
〔7〕
上記式(I-c)で表される繰り返し単位が下記式(I-d)で表される繰り返し単位である、〔6〕記載のガス分離膜。
式(I-d)中、Ra、Rc、Xd、Aa,Ab及びAcは、それぞれ上記式(I-c)中のRa、Rc、Xd、Aa,Ab及びAcと同義である。Rdはアルキレン基、シクロアルキレン基又はアリーレン基を示す。XeはOH、NH及びSHから選ばれる構造部を有する、炭素数が0~2の基を示す。
〔8〕
上記Aa、Ab及びAcのうち少なくとも1つがアルキル基である、〔3〕~〔7〕のいずれかに記載のガス分離膜。
〔9〕
上記ポリイミド化合物中、上記式(I)で表される繰り返し単位の含有量が30~100モル%である、〔1〕~〔8〕のいずれか記載のガス分離膜。
〔10〕
ガス透過性の支持層上に、上記ガス分離層が設けられるガス分離複合膜である、〔1〕~〔9〕のいずれか記載のガス分離膜。
〔11〕
上記支持層が、多孔質層と、不織布層とからなり、
上記不織布層、上記多孔質層および上記ガス分離層がこの順に設けられる、〔10〕に記載のガス分離膜。
〔12〕
分離処理されるガスが二酸化炭素とメタンの混合ガスである場合において、40℃、5MPaにおける二酸化炭素の透過速度が20GPU以上であり、二酸化炭素とメタンとの透過速度比(RCO2/RCH4)が15以上である、〔1〕~〔11〕のいずれか記載のガス分離膜。
〔13〕
二酸化炭素及びメタンを含むガスから二酸化炭素を選択的に透過させるために用いられる、〔1〕~〔12〕のいずれか記載のガス分離膜。
〔14〕
〔1〕~〔13〕のいずれか記載のガス分離膜を具備するガス分離モジュール。
〔15〕
〔14〕に記載のガス分離モジュールを備えたガス分離装置。
〔16〕
〔1〕~〔13〕のいずれか1項に記載のガス分離膜を用いて、二酸化炭素及びメタンを含むガスから二酸化炭素を選択的に透過させるガス分離方法。
〔17〕
下記式(I-b)で表される繰り返し単位を含むポリイミド化合物。
式(I-b)中、Raは下記式(I-1)~(I-28)のいずれかで表される基を示す。ここでX1~X3は単結合又は2価の基を示し、Lは、それぞれ独立に、-CH=CH-又は-CH2-を示し、R1及びR2は水素原子又は置換基を示し、*は式(I-b)中に示されたカルボニル基との結合部位を示す。
Aa、Ab及びAcは水素原子又は置換基を示す。Xbは水素原子又は置換基を示す。Xcは置換基を示す。但し、式(I-b)中の-N(Xb)-で表される構造中にOH、NH及びSHから選ばれる構造部が含まれない場合、XcはOH、NH及びSHから選ばれる構造部を少なくとも1つ有する。
〔18〕
下記式(I-c)で表される繰り返し単位を含むポリイミド化合物。
式(I-c)中、Raは下記式(I-1)~(I-28)のいずれかで表される基を示す。ここでX1~X3は単結合又は2価の基を示し、Lは、それぞれ独立に、-CH=CH-又は-CH2-を示し、R1及びR2は水素原子又は置換基を示し、*は式(I-c)中に示されたカルボニル基との結合部位を示す。
Aa、Ab及びAcは水素原子又は置換基を示す。Xbは水素原子又は置換基を示す。Rcはアルキレン基、シクロアルキレン基又はアリーレン基を示す。XdはOH、NH及びSHから選ばれる構造部を有する、炭素数が0~2の基を示す。
下記式(I-b)で表される繰り返し単位を含むポリイミド化合物。
式(I-b)中、Raは下記式(I-1)~(I-28)のいずれかで表される基を示す。ここでX1~X3は単結合又は2価の基を示し、Lは、それぞれ独立に、-CH=CH-又は-CH2-を示し、R1及びR2は水素原子又は置換基を示し、*は式(I-b)中に示されたカルボニル基との結合部位を示す。
Aa、Ab及びAcは水素原子又は置換基を示す。Xbは水素原子又は置換基を示す。Xcは置換基を示す。但し、式(I-b)中の-N(Xb)-で表される構造中にOH、NH及びSHから選ばれる構造部が含まれない場合、XcはOH、NH及びSHから選ばれる構造部を少なくとも1つ有する。
〔18〕
下記式(I-c)で表される繰り返し単位を含むポリイミド化合物。
式(I-c)中、Raは下記式(I-1)~(I-28)のいずれかで表される基を示す。ここでX1~X3は単結合又は2価の基を示し、Lは、それぞれ独立に、-CH=CH-又は-CH2-を示し、R1及びR2は水素原子又は置換基を示し、*は式(I-c)中に示されたカルボニル基との結合部位を示す。
Aa、Ab及びAcは水素原子又は置換基を示す。Xbは水素原子又は置換基を示す。Rcはアルキレン基、シクロアルキレン基又はアリーレン基を示す。XdはOH、NH及びSHから選ばれる構造部を有する、炭素数が0~2の基を示す。
本明細書において、特定の符号で表示された置換基、連結基等(以下、「置換基等」という。)が複数あるとき、あるいは複数の置換基等を同時もしくは択一的に規定するときには、それぞれの置換基等は互いに同一でも異なっていてもよいことを意味する。このことは、置換基等の数の規定についても同様である。また、式中に同一の表示で表された複数の部分構造の繰り返しがある場合は、各部分構造ないし繰り返し単位は同一でも異なっていてもよい。また、特に断らない場合であっても、複数の置換基等が近接するときにはそれらが互いに連結したり縮環したりして環を形成していてもよい意味である。
本明細書において化合物ないし基の表示については、化合物ないし基そのもののほか、それらの塩、それらのイオンを含む意味に用いる。また、目的の効果を奏する範囲で、構造の一部を変化させたものを含む意味である。
本明細書において置換又は無置換を明記していない置換基(連結基についても同様)については、所望の効果を奏する範囲で、その基に任意の置換基を有していてもよい意味である。これは置換又は無置換を明記していない化合物についても同義である。
本明細書において置換基というときには、特に断らない限り、後記置換基群Zをその好ましい範囲とする。また、特定の範囲を有する置換基が記載されているだけの場合(例えば「アルキル基」と記載されているだけの場合)は、下記置換基群Zの対応する基(上記の場合はアルキル基)における好ましい範囲、具体例が適用される。
本明細書において、ある基の炭素数を規定する場合、この炭素数は、基全体の炭素数を意味する。つまり、この基がさらに置換基を有する形態である場合、この置換基を含めた全体の炭素数を意味する。
本明細書において置換又は無置換を明記していない置換基(連結基についても同様)については、所望の効果を奏する範囲で、その基に任意の置換基を有していてもよい意味である。これは置換又は無置換を明記していない化合物についても同義である。
本明細書において置換基というときには、特に断らない限り、後記置換基群Zをその好ましい範囲とする。また、特定の範囲を有する置換基が記載されているだけの場合(例えば「アルキル基」と記載されているだけの場合)は、下記置換基群Zの対応する基(上記の場合はアルキル基)における好ましい範囲、具体例が適用される。
本明細書において、ある基の炭素数を規定する場合、この炭素数は、基全体の炭素数を意味する。つまり、この基がさらに置換基を有する形態である場合、この置換基を含めた全体の炭素数を意味する。
本発明のガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法は、高圧条件下においてもガス透過性とガス分離選択性の両立を十分なレベルで実現して高速かつ高選択性のガス分離を可能とする。また、本発明のガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法は、ガス分離膜が不純物成分であるトルエン等に曝されてもガス分離性能を良好に維持することができる。また、本発明のポリイミド化合物は、上記ガス分離膜におけるガス分離層の構成材料として好適に用いることができる。
以下、本発明について詳細に説明する。
本発明のガス分離膜は、その構成材料としてガス分離層に特定構造のポリイミド化合物を含む。
本発明のガス分離膜は、その構成材料としてガス分離層に特定構造のポリイミド化合物を含む。
[ポリイミド化合物]
本発明に用いるポリイミド化合物は、下記式(I)で表される繰り返し単位を少なくとも含む。
本発明に用いるポリイミド化合物は、下記式(I)で表される繰り返し単位を少なくとも含む。
式(I)中、Raは下記式(I-1)~(I-28)のいずれかで表される基を示す。下記式(I-1)~(I-28)において、*は式(I)中のカルボニル基との結合部位を示す。Raは式(I-1)、(I-2)又は(I-4)で表される基であることが好ましく、(I-1)又は(I-4)で表される基であることがより好ましく、(I-1)で表される基であることが特に好ましい。
上記式(I-1)、(I-9)及び(I-18)中、X1~X3は、単結合又は2価の基を示す。この2価の基としては、-C(Rx)2-(Rxは水素原子又は置換基を示す。Rxが置換基の場合、互いに連結して環を形成してもよい)、-O-、-SO2-、-C(=O)-、-S-、-NRY-、-Si(RY)2-(RYは水素原子、アルキル基(好ましくはメチル又はエチル)又はアリール基(好ましくはフェニル基))、-C6H4-(フェニレン)、ヘテロ環基又はこれらの組み合わせが好ましく、単結合又は-C(Rx)2-がより好ましい。Rxが置換基を示すとき、その具体例としては、後記置換基群Zから選ばれる基が挙げられ、なかでもアルキル基(好ましい範囲は後記置換基群Zに示されたアルキル基と同義である)が好ましく、ハロゲン原子を置換基として有するアルキル基がより好ましく、トリフルオロメチルが特に好ましい。なお、式(I-18)は、X3が、その左側に記載された2つの炭素原子のいずれか一方、及び、その右側に記載された2つの炭素原子のうちいずれか一方と連結していることを意味する。
X1~X3は分子量が500以下が好ましく、350以下がより好ましく、10~200がより好ましい。
X1~X3は分子量が500以下が好ましく、350以下がより好ましく、10~200がより好ましい。
上記式(I-4)、(I-15)、(I-17)、(I-20)、(I-21)及び(I-23)中、Lは、それぞれ独立に、-CH=CH-又は-CH2-を示す。
上記式(I-7)中、R1及びR2は水素原子又は置換基を示す。この置換基としては、後述する置換基群Zから選ばれる基が挙げられる。R1及びR2は互いに結合して環を形成していてもよい。
R1、R2は水素原子又はアルキル基であることが好ましく、水素原子、メチル基又はエチル基であることがより好ましく、水素原子であることが更に好ましい。
式(I-1)~(I-28)中に示された炭素原子はさらに置換基を有していてもよい。つまり、本発明においては、式(I-1)~(I-28)中に示された炭素原子がさらに置換基を有した形態も、式(I)で表される繰り返し単位に含まれる。この置換基の具体例としては、後記置換基群Zから選ばれる基が挙げられ、なかでもアルキル基又はアリール基が好ましい。
Rbは下記式(I-29)~(I-42)のいずれかで表される基を示す。下記式(I-29)~(I-42)において、*は式(I)中に示されたイミド基との結合部位を示し、#は式(I)中に示されたスルファモイル基(-S(=O)2N(Xb)Xa)との結合部位を示す。Rbは式(I-29)、(I-33)、(I-34)又は(I-35)で表される基であることが好ましく、式(I-29)又は(I-34)で表される基がより好ましい。
X4~X8は単結合又は2価の基を示す。X4、X5及びX6として採り得る2価の基としては、-O-、-S-、-NRN-(RNは水素原子、アルキル基、又はアリール基を示す。)、-S(=O)2-、-C(=O)-、又は-C(Rx)2-(Rxは水素原子又は置換基を示す。Rxが置換基の場合、互いに連結して環を形成してもよい)が好ましく、-O-、-C(=O)-、又は-C(Rx)2-がより好ましい。
X7及びX8として採り得る2価の基の好ましい形態は、上述したX1として採り得る2価の基の好ましい形態と同じである。
X7及びX8として採り得る2価の基の好ましい形態は、上述したX1として採り得る2価の基の好ましい形態と同じである。
式(I-38)におけるLは上記式(I-4)におけるLと同義である。
RZは、それぞれ独立に、置換基を示す。RZは好ましくはアルキル基(好ましくは炭素数1~10、より好ましくは炭素数1~6、さらに好ましくは炭素数1~3のアルキル基であり、好ましい具体例としてメチル、エチル及びイソプロピルが挙げられる。このアルキル基はフッ素原子を置換基として有することも好ましい。)、アリール基(好ましくは炭素数6~20、より好ましくは炭素数6~15、さらに好ましくは炭素数6~10のアリール基であり、好ましい具体例としてフェニル及びナフチルが挙げられる。)、アルコキシ基(好ましくは炭素数1~10、より好ましくは炭素数1~6、さらに好ましくは炭素数1~3のアルコキシ基であり、好ましい具体例としてメトキシ及びエトキシが挙げられる。)、ヘテロ環基(環構成ヘテロ原子として好ましくは酸素原子、窒素原子及び/又は硫黄原子を含む。3~8員環が好ましく、5又は6員環がより好ましい。)、ハロゲン原子(具体的にはフッ素原子、塩素原子、臭素原子及びヨウ素原子が挙げられる。)、ヒドロキシ基、及びカルボキシ基から選ばれる基であり、アルキル基、アリール基、及びハロゲン原子から選ばれる基がより好ましい。
dは0~3の整数であり、0~2の整数が好ましい。eは0~4の整数であり、0~3の整数が好ましく、0~2の整数がより好ましい。fは0~5の整数であり、0~4の整数が好ましく、0~3の整数がより好ましく、0~2の整数がさらに好ましい。gは0~6の整数であり、0~5の整数が好ましく、0~4の整数がより好ましく、0~3の整数がさらに好ましい。hは0~7の整数であり、0~6の整数が好ましく、0~5の整数がさらに好ましく、0~4の整数が特に好ましい。jは0~9の整数であり、0~8の整数が好ましく、0~7の整数がより好ましく、0~6の整数がさらに好ましく、0~4の整数が特に好ましい。kは0~10の整数であり、0~8の整数が好ましく、0~6の整数がより好ましく、0~4の整数がさらに好ましい。qは0又は1を示す。なお、本発明においてqが1の場合とは、式(1)の繰り返し単位において、式(1)中に示されたスルファモイル基が2つ存在することを意味し、本発明においてはかかる形態も、式(1)で表される繰り返し単位に含まれるものとする。
Xaは酸素原子、窒素原子及び/もしくは硫黄原子を有する基、又は、置換基中にフッ素原子を有するアリール基を示す。ここで、本発明においてXaとして採り得る「置換基中にフッ素原子を有するアリール基」は、酸素原子、窒素原子及び硫黄原子のいずれも有しない。Xbは水素原子又は置換基を示す。但し、式(I)中の-N(Xb)-で表される構造中にOH、NH及びSHから選ばれる構造部が含まれない場合、XaはOH、NH及びSHから選ばれる構造部を少なくとも1つ有する。
式(I)で表される繰り返し単位を有するポリイミド化合物をガス分離膜のガス分離層に用いることにより、ガス透過性とガス分離選択性という互いに相反する特性を高いレベルで両立することができ、また可塑化耐性も向上させることが可能となる。その理由は定かではないが、一因として次のことが考えられる。
式(I)で表されるポリイミド化合物は、ジアミン成分中に極性の高い基であるスルファモイル基を有し、さらにこのスルファモイル基はその構造中にOH、NH及びSHから選ばれる構造部を有する。このような構造により、ポリマー鎖間の電子的相互作用、水素結合性相互作用等が複合的に作用してポリマー同士がほどよく緻密化し、適度な自由体積分率を有しながらも、動的分子径の大きな分子についてはその透過性を効果的に抑えることができるものと考えられる。さらに、この緻密化と極性基の存在とが相俟って、不純物成分であるトルエン等との相互作用性が効果的に抑制され、可塑化耐性も向上するものと考えられる。また、Xaが、置換基中にフッ素原子を有するアリール基である場合には、フッ素原子同士の反発に伴う空隙によりガス透過性が高められる一方で、アリール基のπ-πスタッキング等により高いガス分離選択性も良好に維持することができると推定される。
式(I)で表される繰り返し単位を有するポリイミド化合物をガス分離膜のガス分離層に用いることにより、ガス透過性とガス分離選択性という互いに相反する特性を高いレベルで両立することができ、また可塑化耐性も向上させることが可能となる。その理由は定かではないが、一因として次のことが考えられる。
式(I)で表されるポリイミド化合物は、ジアミン成分中に極性の高い基であるスルファモイル基を有し、さらにこのスルファモイル基はその構造中にOH、NH及びSHから選ばれる構造部を有する。このような構造により、ポリマー鎖間の電子的相互作用、水素結合性相互作用等が複合的に作用してポリマー同士がほどよく緻密化し、適度な自由体積分率を有しながらも、動的分子径の大きな分子についてはその透過性を効果的に抑えることができるものと考えられる。さらに、この緻密化と極性基の存在とが相俟って、不純物成分であるトルエン等との相互作用性が効果的に抑制され、可塑化耐性も向上するものと考えられる。また、Xaが、置換基中にフッ素原子を有するアリール基である場合には、フッ素原子同士の反発に伴う空隙によりガス透過性が高められる一方で、アリール基のπ-πスタッキング等により高いガス分離選択性も良好に維持することができると推定される。
Xaは分子量が10~400が好ましく、30~250がより好ましい。
Xaとして採り得る、酸素原子、窒素原子及び/もしくは硫黄原子を有する基は、酸素原子、窒素原子及び/もしくは硫黄原子を有していれば特に制限はない。酸素原子、窒素原子及び/もしくは硫黄原子は水素結合性相互作用において、水素原子のアクセプターとして機能する。Xaとして採り得る、酸素原子、窒素原子及び/もしくは硫黄原子を有する基は、好ましくは、アシル基、カルバモイル基、チオカルバモイル基、スルファモイル基、カルボキシ基、スルホ基、リン酸基(-P(=O)(OH)2)、ホウ酸基(-B(OH)2)及びヒドロキシ基から選ばれる基を有する形態である。
Xaとして採り得る、酸素原子、窒素原子及び/もしくは硫黄原子を有する基は、酸素原子、窒素原子及び/もしくは硫黄原子を有していれば特に制限はない。酸素原子、窒素原子及び/もしくは硫黄原子は水素結合性相互作用において、水素原子のアクセプターとして機能する。Xaとして採り得る、酸素原子、窒素原子及び/もしくは硫黄原子を有する基は、好ましくは、アシル基、カルバモイル基、チオカルバモイル基、スルファモイル基、カルボキシ基、スルホ基、リン酸基(-P(=O)(OH)2)、ホウ酸基(-B(OH)2)及びヒドロキシ基から選ばれる基を有する形態である。
Xaとして採り得る、酸素原子、窒素原子及び/もしくは硫黄原子を有する基は、アルキル基(好ましくは炭素数1~12、より好ましくは炭素数1~8、さらに好ましくは炭素数1~4のアルキル基)、シクロアルキル基(好ましくは炭素数3~10、より好ましくは炭素数3~8のシクロアルキル基)、アリール基(好ましくは炭素数6~20、より好ましくは炭素数6~15、さらに好ましくは炭素数6~12のアリール基)、アシル基(好ましくは炭素数2~20、より好ましくは炭素数2~15、さらに好ましくは炭素数2~10のアシル基)、アリールアミノカルボニル基(好ましくは炭素数7~20、より好ましくは炭素数7~16、さらに好ましくは炭素数7~13のアリールアミノカルボニル基)又はアリールアミノチオカルボニル基(好ましくは炭素数7~20、より好ましくは炭素数7~15、さらに好ましくは炭素数7~12のアリールアミノチオカルボニル基)の形態が好ましく、アルキル基、シクロアルキル基、アリール基又はアシル基がより好ましく、アルキル基、アリール基又はアシル基であることが特に好ましい。
これらの基は、フッ素原子、アミノ基、アシルアミノ基、ヒドロキシ基、カルボキシ基、カルバモイル基、ホウ酸基及びスルファモイル基から選ばれる基を置換基として有する形態が好ましく、フッ素原子、アシルアミノ基、ヒドロキシ基、カルボキシ基、カルバモイル基、ホウ酸基及びスルファモイル基から選ばれる基を置換基として有する形態がより好ましく、フッ素原子、アシルアミノ基、ヒドロキシ基、カルボキシ基、カルバモイル基及びスルファモイル基から選ばれる基を置換基として有する形態が特に好ましい。上記アミノ基、アシルアミノ基、カルバモイル基及びスルファモイル基の好ましい形態は、後述する置換基群Zの対応する基における好ましい形態と同じである。
これらの基は、フッ素原子、アミノ基、アシルアミノ基、ヒドロキシ基、カルボキシ基、カルバモイル基、ホウ酸基及びスルファモイル基から選ばれる基を置換基として有する形態が好ましく、フッ素原子、アシルアミノ基、ヒドロキシ基、カルボキシ基、カルバモイル基、ホウ酸基及びスルファモイル基から選ばれる基を置換基として有する形態がより好ましく、フッ素原子、アシルアミノ基、ヒドロキシ基、カルボキシ基、カルバモイル基及びスルファモイル基から選ばれる基を置換基として有する形態が特に好ましい。上記アミノ基、アシルアミノ基、カルバモイル基及びスルファモイル基の好ましい形態は、後述する置換基群Zの対応する基における好ましい形態と同じである。
Xaとして採り得る、置換基中にフッ素原子を有するアリール基は、その炭素数が6~18が好ましく、6~14がより好ましく、6~10がさらに好ましい。
Xaとして採り得る、置換基中にフッ素原子を有するアリール基は、フッ素原子を置換基として有するアリール基であるか、又はフッ化アルキル基を置換基として有するアリール基が好ましく、パーフルオロアリール基であるか、又はパーフルオロアルキル基を置換基として有するアリール基がより好ましく、パーフルオロアルキル基を置換基として有するアリール基が特に好ましい。
Xaとして採り得る、置換基中にフッ素原子を有するアリール基は、フッ素原子を置換基として有するアリール基であるか、又はフッ化アルキル基を置換基として有するアリール基が好ましく、パーフルオロアリール基であるか、又はパーフルオロアルキル基を置換基として有するアリール基がより好ましく、パーフルオロアルキル基を置換基として有するアリール基が特に好ましい。
Xbが置換基の場合、この置換基の分子量は10~400が好ましく、30~250がより好ましい。Xbとして採り得る置換基に特に制限はなく、例えばアルキル基、アルケニル基、アルキニル基、アシル基、シクロアルキル基及びアリール基を挙げることができる。またXbが置換基の場合、この置換基中には、フッ素原子、アミノ基(好ましくはモノアルキルアミノ基)、アシルアミノ基、ヒドロキシ基、カルボキシ基、カルバモイル基、メルカプト基、ホウ酸基、リン酸基、スルホ基、スルフィノ基、スルファモイル基、ウレイド基、ヒドロキサム酸基及びヒドラジノ基から選ばれる基が含まれることも好ましい。上記アルキル基、アルケニル基、アルキニル基、アシル基、シクロアルキル基、アリール基、アミノ基、アシルアミノ基、カルバモイル基、スルファモイル基、及びウレイド基の好ましい形態は、後述する置換基群Zの対応する基における好ましい形態と同じである。
Xbは水素原子、アルキル基、アリール基又はアシル基がより好ましく、水素原子、アルキル基又はアリール基であることがさらに好ましく、特に好ましくは水素原子である。
Xbは水素原子、アルキル基、アリール基又はアシル基がより好ましく、水素原子、アルキル基又はアリール基であることがさらに好ましく、特に好ましくは水素原子である。
上記式(I)で表される繰り返し単位は下記式(I-a)で表される繰り返し単位であることが好ましい。
式(I-a)中、Ra、Xa及びXbは、それぞれ上記式(I)中のRa、Xa及びXbと同義であり、好ましい形態も同じである。
Aa、Ab及びAcは水素原子又は置換基を示す。Aa、Ab及びAcとして採り得る置換基に特に制限はなく、例えば、後述する置換基群Zから選ばれる基が挙げられる。なかでもアルキル基(好ましくは炭素数1~12、より好ましくは炭素数1~6、さらに好ましくは炭素数1~3のアルキル基、このアルキル基は無置換の形態が好ましい。好ましい具体例として、メチル、エチル、イソプロピル、t-ブチルが挙げられる)、アリール基(好ましくは炭素数6~20、より好ましくは炭素数6~15、さらに好ましくは炭素数6~10のアリール基であり、好ましい具体例としてフェニル及びナフチルが挙げられる。)、アルコキシ基(好ましくは炭素数1~10、より好ましくは炭素数1~6、さらに好ましくは炭素数1~3のアルコキシ基)、ハロゲン原子(例えばフッ素原子、塩素原子、臭素原子又はヨウ素原子)、カルボキシ基、ヒドロキシ基、及びアシルアミノ基(好ましくは炭素数2~10、より好ましくは炭素数2~6、さらに好ましくは炭素数2又は3のアシルアミノ基)から選ばれる基が好ましく、アルキル基又はハロゲン原子がより好ましい。
Aa、Ab及びAcのうち少なくとも1つが置換基であることが好ましく、Aa、Ab及びAcのうち少なくとも1つがアルキル基であることがより好ましい。この場合、Aa、Ab及びAcのうちアルキル基以外のものは水素原子が好ましい。
Aa、Ab及びAcは水素原子又は置換基を示す。Aa、Ab及びAcとして採り得る置換基に特に制限はなく、例えば、後述する置換基群Zから選ばれる基が挙げられる。なかでもアルキル基(好ましくは炭素数1~12、より好ましくは炭素数1~6、さらに好ましくは炭素数1~3のアルキル基、このアルキル基は無置換の形態が好ましい。好ましい具体例として、メチル、エチル、イソプロピル、t-ブチルが挙げられる)、アリール基(好ましくは炭素数6~20、より好ましくは炭素数6~15、さらに好ましくは炭素数6~10のアリール基であり、好ましい具体例としてフェニル及びナフチルが挙げられる。)、アルコキシ基(好ましくは炭素数1~10、より好ましくは炭素数1~6、さらに好ましくは炭素数1~3のアルコキシ基)、ハロゲン原子(例えばフッ素原子、塩素原子、臭素原子又はヨウ素原子)、カルボキシ基、ヒドロキシ基、及びアシルアミノ基(好ましくは炭素数2~10、より好ましくは炭素数2~6、さらに好ましくは炭素数2又は3のアシルアミノ基)から選ばれる基が好ましく、アルキル基又はハロゲン原子がより好ましい。
Aa、Ab及びAcのうち少なくとも1つが置換基であることが好ましく、Aa、Ab及びAcのうち少なくとも1つがアルキル基であることがより好ましい。この場合、Aa、Ab及びAcのうちアルキル基以外のものは水素原子が好ましい。
式(I-a)で表される繰り返し単位は、ジアミン成分がポリイミド化合物主鎖中に組み込まれるための2つの連結部位が互いにメタ位の関係にある。それ故、スルファモイル基がポリイミド主鎖から張り出した構造となり、スルファモイル基の上述した作用をより効果的に引き出すことができるものと推定される。また、Aa,Ab及びAcの少なくとも1つが置換基を有する形態である場合には、ポリイミド化合物の緻密なパッキング状態を保ちながらもほどよい空孔を生じ、ガス透過性をより高めることができると考えられる。
上記式(I-a)で表される繰り返し単位は、下記式(I-b)で表される繰り返し単位であることが好ましい。
式(I-b)中、Ra、Xb、Aa、Ab及びAcは、それぞれ上記式(I-a)中のRa、Xb、Aa、Ab及びAcと同義であり、好ましい形態も同じである。
Xcは置換基を示す。但し、式(I-b)中の-N(Xb)-で表される構造中にOH、NH及びSHから選ばれる構造部が含まれない場合、XcはOH、NH及びSHから選ばれる構造部を少なくとも1つ有する。
Xcとして採り得る置換基に特に制限はなく、例えば後述する置換基群Zから選ばれる基が挙げられる。なかでも、Xcはアルキル基、アルケニル基、アルキニル基、シクロアルキル基、アリール基又はアミノ基が好ましい。
Xcとして採り得るアルキル基は、好ましくは炭素数1~10、より好ましくは炭素数1~6、さらに好ましくは炭素数1~3のアルキル基であり、好ましい具体例として、メチル、エチル、イソプロピル、t-ブチルが挙げられる。
Xcとして採り得るアルケニル基は、好ましくは炭素数2~10、より好ましくは炭素数2~6、さらに好ましくは炭素数2又は3のアルケニル基である。
Xcとして採り得るアルキニル基は、好ましくは炭素数2~10、より好ましくは炭素数2~6、さらに好ましくは炭素数2又は3のアルキニル基である。
Xcとして採り得るシクロアルキル基は、好ましくは炭素数3~10、より好ましくは炭素数3~8のシクロアルキル基であり、好ましい具体例としてはシクロペンチル及びシクロヘキシルが挙げられる。
Xcとして採り得るアリール基は、好ましくは炭素数6~20、より好ましくは炭素数6~15、さらに好ましくは炭素数6~10のアリール基であり、好ましい具体例としてフェニル及びナフチルが挙げられる。
Xcとして採り得るアミノ基は、好ましくはアルキルアミノ基(好ましくは炭素数1~10、より好ましく炭素数1~6、さらに好ましくは炭素数1~3のアルキルアミノ基)、アルケニルアミノ基(好ましくは炭素数2~10、より好ましく炭素数2~6、さらに好ましくは炭素数2~3のアルケニルアミノ基)、アルキニルアミノ基(好ましくは炭素数2~10、より好ましく炭素数2~6、さらに好ましくは炭素数2又は3のアルキニルアミノ基)、シクロアルキルアミノ基(好ましくは炭素数3~10、より好ましくは炭素数4~8のシクロアルキルアミノ基)、又はアリールアミノ基(好ましくは炭素数6~20、より好ましくは炭素数6~15、さらに好ましくは炭素数6~10のアリールアミノ基)である。
Xcはアルキル基、シクロアルキル基又はアリール基がより好ましい。また、Xcはフッ素原子を置換基として少なくとも1つ有する形態であることも好ましい。また、Xcはカルボキシ基、ヒドロキシ基、カルバモイル基及びスルファモイル基から選ばれる基を置換基として有する形態であることも好ましい。
Xcは置換基を示す。但し、式(I-b)中の-N(Xb)-で表される構造中にOH、NH及びSHから選ばれる構造部が含まれない場合、XcはOH、NH及びSHから選ばれる構造部を少なくとも1つ有する。
Xcとして採り得る置換基に特に制限はなく、例えば後述する置換基群Zから選ばれる基が挙げられる。なかでも、Xcはアルキル基、アルケニル基、アルキニル基、シクロアルキル基、アリール基又はアミノ基が好ましい。
Xcとして採り得るアルキル基は、好ましくは炭素数1~10、より好ましくは炭素数1~6、さらに好ましくは炭素数1~3のアルキル基であり、好ましい具体例として、メチル、エチル、イソプロピル、t-ブチルが挙げられる。
Xcとして採り得るアルケニル基は、好ましくは炭素数2~10、より好ましくは炭素数2~6、さらに好ましくは炭素数2又は3のアルケニル基である。
Xcとして採り得るアルキニル基は、好ましくは炭素数2~10、より好ましくは炭素数2~6、さらに好ましくは炭素数2又は3のアルキニル基である。
Xcとして採り得るシクロアルキル基は、好ましくは炭素数3~10、より好ましくは炭素数3~8のシクロアルキル基であり、好ましい具体例としてはシクロペンチル及びシクロヘキシルが挙げられる。
Xcとして採り得るアリール基は、好ましくは炭素数6~20、より好ましくは炭素数6~15、さらに好ましくは炭素数6~10のアリール基であり、好ましい具体例としてフェニル及びナフチルが挙げられる。
Xcとして採り得るアミノ基は、好ましくはアルキルアミノ基(好ましくは炭素数1~10、より好ましく炭素数1~6、さらに好ましくは炭素数1~3のアルキルアミノ基)、アルケニルアミノ基(好ましくは炭素数2~10、より好ましく炭素数2~6、さらに好ましくは炭素数2~3のアルケニルアミノ基)、アルキニルアミノ基(好ましくは炭素数2~10、より好ましく炭素数2~6、さらに好ましくは炭素数2又は3のアルキニルアミノ基)、シクロアルキルアミノ基(好ましくは炭素数3~10、より好ましくは炭素数4~8のシクロアルキルアミノ基)、又はアリールアミノ基(好ましくは炭素数6~20、より好ましくは炭素数6~15、さらに好ましくは炭素数6~10のアリールアミノ基)である。
Xcはアルキル基、シクロアルキル基又はアリール基がより好ましい。また、Xcはフッ素原子を置換基として少なくとも1つ有する形態であることも好ましい。また、Xcはカルボキシ基、ヒドロキシ基、カルバモイル基及びスルファモイル基から選ばれる基を置換基として有する形態であることも好ましい。
なお、式(1-b)においてはXbが水素原子であることが特に好ましい。この場合、式(I-b)で表される繰り返し単位中のアシル基(-C(=O)Xc)が水素結合のアクセプター(水素原子と相互作用する部位)となり、また、アシル基の電子求引性により-N(Xb)-における水素(Xb)のドナー性をより高めることもでき、ポリイミド化合物の緻密性がより高まりガス分離選択性と耐可塑性の向上に繋がると考えられる。さらに、Xcがフッ素原子を有すると、フッ素原子の電子求引性により-N(Xb)-の水素のドナー性がさらに高められ、同時にフッ素原子同士の反発力により適度な空孔が生じ、ガス分離選択性、ガス透過性、耐可塑性をより高度なレベルで両立することが可能になると推定される。また、フッ素原子はその撥水性により、ポリイミド化合物の加水分解抑制にも寄与すると考えられる。
上記式(I-a)で表される繰り返し単位は下記式(I-c)で表される繰り返し単位であることも好ましい。
式(I-c)中、Ra、Xb、Aa、Ab及びAcは、それぞれ上記式(I-a)中のRa、Xb、Aa、Ab及びAcと同義であり、好ましい形態も同じである。
Rcはアルキレン基、シクロアルキレン基又はアリーレン基を示す。Rcとして採り得るアルキレン基は、直鎖でも分岐を有してもよい。このアルキレン基の炭素数は1~12が好ましく、1~8がより好ましく、1~4がさらに好ましい。Rcとして採り得るシクロアルキレン基は、その炭素数が3~12が好ましく、3~9がより好ましく、3~6が特に好ましい。Rcとして採り得るアリーレン基は、その炭素数が6~18が好ましく、6~14がより好ましく、6~10がさらに好ましく、さらに好ましくはフェニレンである。
XdはOH、NH及びSHから選ばれる構造部を有する基であり、Xdの炭素数は0~2である。Xdの好ましい例として、アミノ基、モノアルキルアミノ基、アシルアミノ基、ヒドロキシ基、カルボキシ基、カルバモイル基、メルカプト基、ホウ酸基、リン酸基、スルホ基、スルフィノ基、スルファモイル基、ウレイド基、ヒドロキサム酸基、及びヒドラジノ基が挙げられ、アミノ基、アシルアミノ基、ヒドロキシ基、カルボキシ基、カルバモイル基、ホウ酸基又はスルファモイル基がより好ましく、アシルアミノ基、ヒドロキシ基、カルボキシ基、カルバモイル基、又はスルファモイル基が特に好ましい。
式(I-c)で表される繰り返し単位は、リンカー部位であるRcの作用により運動性を高めることができ、十分なガス透過性をより確実に実現することが可能になると推定される。他方、XdがOH、NH及びSHから選ばれる構造部を有することにより、ポリイミド鎖間の水素結合性相互作用等も高めることができると推定される、結果、ポリイミド鎖に緻密性を付与して良好なガス分離選択性と耐可塑性も実現できるものと考えられる。
上記式(I-c)で表される繰り返し単位は下記式(I-d)で表される繰り返し単位であることも好ましい。
式(I-d)中、Ra、Rc、Xd、Aa,Ab及びAcは、それぞれ上記式(I-c)中のRa、Rc、Xd、Aa,Ab及びAcと同義であり、好ましい形態も同じである。
Rdはアルキレン基、シクロアルキレン基又はアリーレン基を示す。Rdとして採り得るアルキレン基、シクロアルキレン基及びアリーレン基の好ましい形態は、それぞれ、上記Rcとして採り得るアルキレン基、シクロアルキレン基及びアリーレン基の好ましい形態と同じである。
Rdはアルキレン基、シクロアルキレン基又はアリーレン基を示す。Rdとして採り得るアルキレン基、シクロアルキレン基及びアリーレン基の好ましい形態は、それぞれ、上記Rcとして採り得るアルキレン基、シクロアルキレン基及びアリーレン基の好ましい形態と同じである。
XeはOH、NH及びSHから選ばれる構造部を有する基であり、Xeの炭素数は0~2である。Xeの好ましい形態は、上記Xdの好ましい形態と同じである。
上記式(I-d)で表される繰り返し単位を有するポリイミド化合物をガス分離層に用いることにより、ガス分離層を構成するポリイミド化合物を緻密なパッキング状態としながらも適度な空孔も生じさせることができガス分離選択性とガス透過性を高いレベルで両立することが可能になると推定される。
本発明に用いるポリイミド化合物は、上記式(I)で表される繰り返し単位に加えて、下記式(II-a)及び/又は(II-b)で表される繰り返し単位を有してもよい。
上記式(II-a)及び(II-b)中、Rは式(I)中のRaと同義であり、好ましい範囲も同じである。Ad、Ae及びAfは、それぞれ独立に、置換基を示す。置換基としては、後述する置換基群Zから選ばれる基が挙げられる。
Adはアルキル基、カルボキシ基、又はハロゲン原子であることが好ましい。Adの数を示すk1は0~4の整数であり、Adがアルキル基の場合、k1は1~4であることが好ましく、2~4であることがより好ましく、より好ましくは3又は4である。Adがカルボキシ基の場合、k1は1~2であることが好ましく、より好ましくは1である。Adがアルキルである場合、このアルキル基の炭素数は1~10であることが好ましく、1~5であることがより好ましく、1~3であることがさらに好ましく、さらに好ましくはメチル、エチル又はトリフルオロメチルである。
式(II-a)において、ジアミン成分(すなわちR4を有しうるフェニレン基)のポリイミド化合物に組み込まれるための2つの連結部位は、互いにメタ位又はパラ位に位置することが好ましく、互いにパラ位に位置することがより好ましい。
本発明において、上記式(II-a)で表される構造には、上記式(I)で表される構造は含まれないものとする。
Adはアルキル基、カルボキシ基、又はハロゲン原子であることが好ましい。Adの数を示すk1は0~4の整数であり、Adがアルキル基の場合、k1は1~4であることが好ましく、2~4であることがより好ましく、より好ましくは3又は4である。Adがカルボキシ基の場合、k1は1~2であることが好ましく、より好ましくは1である。Adがアルキルである場合、このアルキル基の炭素数は1~10であることが好ましく、1~5であることがより好ましく、1~3であることがさらに好ましく、さらに好ましくはメチル、エチル又はトリフルオロメチルである。
式(II-a)において、ジアミン成分(すなわちR4を有しうるフェニレン基)のポリイミド化合物に組み込まれるための2つの連結部位は、互いにメタ位又はパラ位に位置することが好ましく、互いにパラ位に位置することがより好ましい。
本発明において、上記式(II-a)で表される構造には、上記式(I)で表される構造は含まれないものとする。
Ae及びAfはアルキル基もしくはハロゲン原子を示すか、又は互いに連結してX9と共に環を形成する基を示すことが好ましい。また、2つのAeが連結して環を形成している形態や、2つのAfが連結して環を形成している形態も好ましい。Ae及びAfが連結した構造に特に制限はないが、単結合、-O-又は-S-が好ましい。Ae及びAfの数を示すm1及びn1は0~4の整数であるが、1~4であることが好ましく、2~4であることがより好ましく、より好ましくは3又は4である。Ae及びAfがアルキル基である場合、このアルキル基の炭素数は1~10であることが好ましく、1~5であることがより好ましく、1~3であることがさらに好ましく、さらに好ましくはメチル、エチル又はトリフルオロメチルである。
X9は上記式(I-1)におけるX1と同義であり、好ましい範囲も同一である。
本発明に用いるポリイミド化合物は、その構造中、上記式(I)で表される繰り返し単位の含有量が30~100モル%であることが好ましく、50~100モル%であることがより好ましく、70~100モル%であることがさらに好ましく、80~100モル%であることが特に好ましい。
本発明に用いるポリイミド化合物は、その構造中、上記式(I)で表される繰り返し単位と、上記式(II-a)で表される繰り返し単位と、上記式(II-b)で表される繰り返し単位の総モル量中に占める、式(I)で表される繰り返し単位のモル量の割合が30~100モル%であることが好ましく、50~100モル%がより好ましく、70~100モル%がさらに好ましく、80~100モル%がさらに好ましい。なお、上記式(I)で表される繰り返し単位と、上記式(II-a)で表される繰り返し単位と、上記式(II-b)で表される繰り返し単位の総モル量中に占める、式(I)で表される繰り返し単位のモル量の割合が100モル%であるとは、ポリイミド化合物が、上記式(II-a)で表される繰り返し単位と、上記式(II-b)で表される繰り返し単位のいずれも有しないことを意味する。
本発明に用いるポリイミド化合物は、その構造中、上記式(I)で表される繰り返し単位と、上記式(II-a)で表される繰り返し単位と、上記式(II-b)で表される繰り返し単位の総モル量中に占める、式(I)で表される繰り返し単位のモル量の割合が30~100モル%であることが好ましく、50~100モル%がより好ましく、70~100モル%がさらに好ましく、80~100モル%がさらに好ましい。なお、上記式(I)で表される繰り返し単位と、上記式(II-a)で表される繰り返し単位と、上記式(II-b)で表される繰り返し単位の総モル量中に占める、式(I)で表される繰り返し単位のモル量の割合が100モル%であるとは、ポリイミド化合物が、上記式(II-a)で表される繰り返し単位と、上記式(II-b)で表される繰り返し単位のいずれも有しないことを意味する。
本発明に用いるポリイミド化合物は、上記式(I)で表される繰り返し単位からなるか、又は、上記式(I)で表される繰り返し単位と、上記式(II-a)及び/又は上記式(II-b)で表される繰り返し単位とからなることが好ましい。ここで、「上記式(II-a)及び/又は上記式(II-b)で表される繰り返し単位からなる」とは、上記式(II-a)で表される繰り返し単位からなる態様、上記式(II-b)で表される繰り返し単位からなる態様、又は、上記式(II-a)で表される繰り返し単位と上記式(II-b)で表される繰り返し単位とからなる態様の3つの態様を含む意味である。
置換基群Z:
アルキル基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~10のアルキル基であり、例えばメチル、エチル、iso-プロピル、tert-ブチル、n-オクチル、n-デシル、n-ヘキサデシル)、シクロアルキル基(好ましくは炭素数3~30、より好ましくは炭素数3~20、特に好ましくは炭素数3~10のシクロアルキル基であり、例えばシクロプロピル、シクロペンチル、シクロヘキシルなどが挙げられる。)、アルケニル基(好ましくは炭素数2~30、より好ましくは炭素数2~20、特に好ましくは炭素数2~10のアルケニル基であり、例えばビニル、アリル、2-ブテニル、3-ペンテニルなどが挙げられる。)、アルキニル基(好ましくは炭素数2~30、より好ましくは炭素数2~20、特に好ましくは炭素数2~10のアルキニル基であり、例えばプロパルギル、3-ペンチニルなどが挙げられる。)、アリール基(好ましくは炭素数6~30、より好ましくは炭素数6~20、特に好ましくは炭素数6~12のアリール基であり、例えばフェニル、p-メチルフェニル、ナフチル、アントラニルなどが挙げられる。)、アミノ基(アミノ基、アルキルアミノ基、アリールアミノ基、ヘテロ環アミノ基を含み、好ましくは炭素数0~30、より好ましくは炭素数0~20、さらに好ましくは炭素数0~10、特に好ましくは炭素数0~6のアミノ基であり、例えばアミノ、メチルアミノ、ジメチルアミノ、ジエチルアミノ、ジベンジルアミノ、ジフェニルアミノ、ジトリルアミノなどが挙げられる。)、アルコキシ基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~10のアルコキシ基であり、例えばメトキシ、エトキシ、ブトキシ、2-エチルヘキシルオキシなどが挙げられる。)、アリールオキシ基(好ましくは炭素数6~30、より好ましくは炭素数6~20、特に好ましくは炭素数6~12のアリールオキシ基であり、例えばフェニルオキシ、1-ナフチルオキシ、2-ナフチルオキシなどが挙げられる。)、ヘテロ環オキシ基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~12のヘテロ環オキシ基であり、例えばピリジルオキシ、ピラジルオキシ、ピリミジルオキシ、キノリルオキシなどが挙げられる。)、
アルキル基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~10のアルキル基であり、例えばメチル、エチル、iso-プロピル、tert-ブチル、n-オクチル、n-デシル、n-ヘキサデシル)、シクロアルキル基(好ましくは炭素数3~30、より好ましくは炭素数3~20、特に好ましくは炭素数3~10のシクロアルキル基であり、例えばシクロプロピル、シクロペンチル、シクロヘキシルなどが挙げられる。)、アルケニル基(好ましくは炭素数2~30、より好ましくは炭素数2~20、特に好ましくは炭素数2~10のアルケニル基であり、例えばビニル、アリル、2-ブテニル、3-ペンテニルなどが挙げられる。)、アルキニル基(好ましくは炭素数2~30、より好ましくは炭素数2~20、特に好ましくは炭素数2~10のアルキニル基であり、例えばプロパルギル、3-ペンチニルなどが挙げられる。)、アリール基(好ましくは炭素数6~30、より好ましくは炭素数6~20、特に好ましくは炭素数6~12のアリール基であり、例えばフェニル、p-メチルフェニル、ナフチル、アントラニルなどが挙げられる。)、アミノ基(アミノ基、アルキルアミノ基、アリールアミノ基、ヘテロ環アミノ基を含み、好ましくは炭素数0~30、より好ましくは炭素数0~20、さらに好ましくは炭素数0~10、特に好ましくは炭素数0~6のアミノ基であり、例えばアミノ、メチルアミノ、ジメチルアミノ、ジエチルアミノ、ジベンジルアミノ、ジフェニルアミノ、ジトリルアミノなどが挙げられる。)、アルコキシ基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~10のアルコキシ基であり、例えばメトキシ、エトキシ、ブトキシ、2-エチルヘキシルオキシなどが挙げられる。)、アリールオキシ基(好ましくは炭素数6~30、より好ましくは炭素数6~20、特に好ましくは炭素数6~12のアリールオキシ基であり、例えばフェニルオキシ、1-ナフチルオキシ、2-ナフチルオキシなどが挙げられる。)、ヘテロ環オキシ基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~12のヘテロ環オキシ基であり、例えばピリジルオキシ、ピラジルオキシ、ピリミジルオキシ、キノリルオキシなどが挙げられる。)、
アシル基(好ましくは炭素数1~30、より好ましくは炭素数1~20、さらに好ましくは炭素数1~12、特に好ましくは炭素数2~8のアシル基であり、例えばアセチル、ベンゾイル、ホルミル、ピバロイルなどが挙げられる。)、アルコキシカルボニル基(好ましくは炭素数2~30、より好ましくは炭素数2~20、特に好ましくは炭素数2~12のアルコキシカルボニル基であり、例えばメトキシカルボニル、エトキシカルボニルなどが挙げられる。)、アリールオキシカルボニル基(好ましくは炭素数7~30、より好ましくは炭素数7~20、特に好ましくは炭素数7~12のアリールオキシカルボニル基であり、例えばフェニルオキシカルボニルなどが挙げられる。)、アシルオキシ基(好ましくは炭素数2~30、より好ましくは炭素数2~20、特に好ましくは炭素数2~10のアシルオキシ基であり、例えばアセトキシ、ベンゾイルオキシなどが挙げられる。)、アシルアミノ基(好ましくは炭素数2~30、より好ましくは炭素数2~20、さらに好ましくは炭素数2~10、特に好ましくは炭素数2~5のアシルアミノ基であり、例えばアセチルアミノ、ベンゾイルアミノなどが挙げられる。)、
アルコキシカルボニルアミノ基(好ましくは炭素数2~30、より好ましくは炭素数2~20、特に好ましくは炭素数2~12のアルコキシカルボニルアミノ基であり、例えばメトキシカルボニルアミノなどが挙げられる。)、アリールオキシカルボニルアミノ基(好ましくは炭素数7~30、より好ましくは炭素数7~20、特に好ましくは炭素数7~12のアリールオキシカルボニルアミノ基であり、例えばフェニルオキシカルボニルアミノなどが挙げられる。)、スルホニルアミノ基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~12であり、例えばメタンスルホニルアミノ、ベンゼンスルホニルアミノなどが挙げられる。)、スルファモイル基(好ましくは炭素数0~30、より好ましくは炭素数0~20、さらに好ましくは炭素数0~12、特に好ましくは炭素数0~6のスルファモイル基であり、例えばスルファモイル、メチルスルファモイル、ジメチルスルファモイル、フェニルスルファモイルなどが挙げられる。)、カルバモイル基(好ましくは炭素原子数1~20、より好ましくは1~16、さらに好ましくは1~12、特に好ましくは炭素数1~7のカルバモイル基であり、例えばカルバモイル基、メチルカルバモイル基、ジエチルカルバモイル基、フェニルカルバモイル基などが挙げられる。)
アルキルチオ基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~12のアルキルチオ基であり、例えばメチルチオ、エチルチオなどが挙げられる。)、アリールチオ基(好ましくは炭素数6~30、より好ましくは炭素数6~20、特に好ましくは炭素数6~12のアリールチオ基であり、例えばフェニルチオなどが挙げられる。)、ヘテロ環チオ基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~12のヘテロ環チオ基であり、例えばピリジルチオ、2-ベンズイミゾリルチオ、2-ベンズオキサゾリルチオ、2-ベンズチアゾリルチオなどが挙げられる。)、
スルホニル基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~12のスルホニル基であり、例えばメシル、トシルなどが挙げられる。)、スルフィニル基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~12のスルフィニル基であり、例えばメタンスルフィニル、ベンゼンスルフィニルなどが挙げられる。)、ウレイド基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~12のウレイド基であり、例えばウレイド、メチルウレイド、フェニルウレイドなどが挙げられる。)、リン酸アミド基(好ましくは炭素数1~30、より好ましくは炭素数1~20、特に好ましくは炭素数1~12のリン酸アミド基であり、例えばジエチルリン酸アミド、フェニルリン酸アミドなどが挙げられる。)、ヒドロキシ基、メルカプト基、ハロゲン原子(例えばフッ素原子、塩素原子、臭素原子、ヨウ素原子であり、より好ましくはフッ素原子が挙げられる)、
シアノ基、カルボキシ基、オキソ基、ニトロ基、ヒドロキサム酸基、スルフィノ基、ヒドラジノ基、イミノ基、ヘテロ環基(好ましくは3~7員環のヘテロ環基で、芳香族ヘテロ環でも芳香族でないヘテロ環であってもよく、ヘテロ環を構成するヘテロ原子としては、窒素原子、酸素原子、硫黄原子が挙げられる。炭素数は0~30が好ましく、より好ましくは炭素数1~12のヘテロ環基であり、具体的には例えばイミダゾリル、ピリジル、キノリル、フリル、チエニル、ピペリジル、モルホリノ、ベンズオキサゾリル、ベンズイミダゾリル、ベンズチアゾリル、カルバゾリル、アゼピニルなどが挙げられる。)、シリル基(好ましくは炭素数3~40、より好ましくは炭素数3~30、特に好ましくは炭素数3~24のシリル基であり、例えばトリメチルシリル、トリフェニルシリルなどが挙げられる。)、シリルオキシ基(好ましくは炭素数3~40、より好ましくは炭素数3~30、特に好ましくは炭素数3~24のシリルオキシ基であり、例えばトリメチルシリルオキシ、トリフェニルシリルオキシなどが挙げられる。)などが挙げられる。これらの置換基は、更に上記置換基群Zより選択されるいずれか1つ以上の置換基により置換されてもよい。
なお、本発明において、1つの構造部位に複数の置換基があるときには、それらの置換基は互いに連結して環を形成していたり、上記構造部位の一部又は全部と縮環して芳香族環もしくは不飽和複素環を形成していたりしてもよい。
なお、本発明において、1つの構造部位に複数の置換基があるときには、それらの置換基は互いに連結して環を形成していたり、上記構造部位の一部又は全部と縮環して芳香族環もしくは不飽和複素環を形成していたりしてもよい。
化合物ないし置換基等がアルキル基、アルケニル基等を含むとき、これらは直鎖状でも分岐状でもよく、置換されていても無置換でもよい。またアリール基、ヘテロ環基等を含むとき、それらは単環でも縮環でもよく、置換されていても無置換でもよい。
本発明に用いるポリイミド化合物の分子量は、重量平均分子量として10,000~1000,000であることが好ましく、より好ましくは15,000~500,000であり、さらに好ましくは20,000~200,000である。
本明細書において分子量及び分散度は特に断らない限りGPC(ゲルろ過クロマトグラフィー)法を用いて測定した値とし、分子量はポリスチレン換算の重量平均分子量とする。GPC法に用いるカラムに充填されているゲルは芳香族化合物を繰り返し単位に持つゲルが好ましく、例えばスチレン-ジビニルベンゼン共重合体からなるゲルが挙げられる。カラムは2~6本連結させて用いることが好ましい。用いる溶媒は、テトラヒドロフラン等のエーテル系溶媒、N-メチルピロリジノン等のアミド系溶媒が挙げられる。測定は、溶媒の流速が0.1~2mL/minの範囲で行うことが好ましく、0.5~1.5mL/minの範囲で行うことが最も好ましい。この範囲内で測定を行うことで、装置に負荷がかからず、さらに効率的に測定ができる。測定温度は10~50℃で行うことが好ましく、20~40℃で行うことが最も好ましい。なお、使用するカラム及びキャリアは測定対称となる高分子化合物の物性に応じて適宜選定することができる。
(ポリイミド化合物の合成)
本発明に用いるポリイミド化合物は、特定の2官能酸無水物(テトラカルボン酸二無水物)と特定のジアミンとを縮合重合させることで合成することができる。その方法としては一般的な成書(例えば、今井淑夫、横田力男編著、「最新ポリイミド~基礎と応用~」、株式会社エヌ・ティー・エス、2010年8月25日、p.3~49、など)に記載の手法を適宜参照して実施することができる。
本発明に用いるポリイミド化合物は、特定の2官能酸無水物(テトラカルボン酸二無水物)と特定のジアミンとを縮合重合させることで合成することができる。その方法としては一般的な成書(例えば、今井淑夫、横田力男編著、「最新ポリイミド~基礎と応用~」、株式会社エヌ・ティー・エス、2010年8月25日、p.3~49、など)に記載の手法を適宜参照して実施することができる。
本発明に用いるポリイミド化合物の合成において、一方の原料であるテトラカルボン酸二無水物の少なくとも1種は、下記式(IV)で表される。原料とするテトラカルボン酸二無水物のすべてが下記式(IV)で表されることが好ましい。
式(IV)中、Raは上記式(I)におけるRaと同義である。
本発明に用いうるテトラカルボン酸二無水物の具体例としては、例えば以下に示すものが挙げられる。
本発明に用いうるポリイミド化合物の合成において、他方の原料であるジアミン化合物の少なくとも1種は、下記式(V)で表される。
式(V)中、Rb、Xa及びXbは、それぞれ上記式(I)におけるRb、Xa及びXbと同義である。
式(V)で表されるジアミン化合物の具体例としては、例えば、下記に示すものを挙げることができるが、本発明はこれらに限定されるものではない。
上記各構造式において、#は式(V)中の-S(=O)2N(Xb)Xaとの連結部位を示す。この-S(=O)2N(Xb)Xaの具体例を以下に示す。
また、本発明に用いうるポリイミド化合物の合成において、原料とするジアミン化合物として、上記式(V)で表されるジアミン化合物に加えて、下記式(VI-a)又は下記式(VI-b)で表されるジアミン化合物を用いてもよい。
式(VI-a)中、Ad及びk1は、それぞれ上記式(II-a)におけるAd及びk1と同義である。式(VI-a)で表されるジアミン化合物には、式(V)で表されるジアミン化合物は含まれない。
式(VI-b)中、Ae、Af、X9、m1及びn1は、それぞれ上記式(II-b)におけるAe、Af、X9、m1及びn1と同義である。式(VI-b)で表されるジアミン化合物には、式(V)で表されるジアミン化合物は含まれない。
式(VI-b)中、Ae、Af、X9、m1及びn1は、それぞれ上記式(II-b)におけるAe、Af、X9、m1及びn1と同義である。式(VI-b)で表されるジアミン化合物には、式(V)で表されるジアミン化合物は含まれない。
式(VI-a)又は(VI-b)で表されるジアミンとして、例えば下記に示すものを用いることができる。
上記式(IV)で表されるモノマーと、上記式(V)、(VI-a)又は(VI-b)で表されるモノマーは、予めオリゴマー又はプレポリマーとして用いてもよい。本発明に用いるポリイミド化合物は、ブロック共重合体、ランダム共重合体、グラフト共重合体のいずれでもよい。
本発明に用いるポリイミド化合物は、上記各原料を溶媒中に混合して、上記のように通常の方法で縮合重合させて得ることができる。
上記溶媒としては、特に限定されるものではないが、酢酸メチル、酢酸エチル、酢酸ブチル等のエステル系有機溶剤、アセトン、メチルエチルケトン、メチルイソブチルケトン、ジアセトンアルコール、シクロペンタノン、シクロヘキサノン等の脂肪族ケトン、エチレングリコールジメチルエーテル、ジブチルブチルエーテル、テトラヒドロフラン、メチルシクロペンチルエーテル、ジオキサン等のエーテル系有機溶剤、N-メチルピロリドン、2-ピロリドン、ジメチルホルムアミド、ジメチルイミダゾリジノン、ジメチルアセトアミド等のアミド系有機溶剤、ジメチルスルホキシド、スルホラン等の含硫黄系有機溶剤などが挙げられる。これらの有機溶剤は反応基質であるテトラカルボン酸二無水物、ジアミン化合物、反応中間体であるポリアミック酸、さらに最終生成物であるポリイミド化合物を溶解させることを可能とする範囲で適切に選択されるものであるが、好ましくは、エステル系(好ましくは酢酸ブチル)、脂肪族ケトン(好ましくは、メチルエチルケトン、メチルイソブチルケトン、ジアセトンアルコール、シクロペンタノン、シクロヘキサノン)、エーテル系(ジエチレングリコールモノメチルエーテル、メチルシクロペンチルエーテル)、アミド系(好ましくはN-メチルピロリドン)、含硫黄系(ジメチルスルホキシド、スルホラン)が好ましい。また、これらは、1種又は2種以上を組み合わせて用いることができる。
上記溶媒としては、特に限定されるものではないが、酢酸メチル、酢酸エチル、酢酸ブチル等のエステル系有機溶剤、アセトン、メチルエチルケトン、メチルイソブチルケトン、ジアセトンアルコール、シクロペンタノン、シクロヘキサノン等の脂肪族ケトン、エチレングリコールジメチルエーテル、ジブチルブチルエーテル、テトラヒドロフラン、メチルシクロペンチルエーテル、ジオキサン等のエーテル系有機溶剤、N-メチルピロリドン、2-ピロリドン、ジメチルホルムアミド、ジメチルイミダゾリジノン、ジメチルアセトアミド等のアミド系有機溶剤、ジメチルスルホキシド、スルホラン等の含硫黄系有機溶剤などが挙げられる。これらの有機溶剤は反応基質であるテトラカルボン酸二無水物、ジアミン化合物、反応中間体であるポリアミック酸、さらに最終生成物であるポリイミド化合物を溶解させることを可能とする範囲で適切に選択されるものであるが、好ましくは、エステル系(好ましくは酢酸ブチル)、脂肪族ケトン(好ましくは、メチルエチルケトン、メチルイソブチルケトン、ジアセトンアルコール、シクロペンタノン、シクロヘキサノン)、エーテル系(ジエチレングリコールモノメチルエーテル、メチルシクロペンチルエーテル)、アミド系(好ましくはN-メチルピロリドン)、含硫黄系(ジメチルスルホキシド、スルホラン)が好ましい。また、これらは、1種又は2種以上を組み合わせて用いることができる。
重合反応温度に特に制限はなくポリイミド化合物の合成において通常採用されうる温度を採用することができる。具体的には-40~60℃であることが好ましく、より好ましくは-30~50℃である。
上記の重合反応により生成したポリアミック酸を分子内で脱水閉環反応させることによりイミド化することで、ポリイミド化合物が得られる。脱水閉環させる方法としては、一般的な成書(例えば、今井淑夫、横田力男編著、「最新ポリイミド~基礎と応用~」、株式会社エヌ・ティー・エス、2010年8月25日、p.3~49、など)に記載の方法を参考とすることができる。例えば、120℃~200℃に加熱して、副生する水を系外に除去しながら反応させる熱イミド化法や、ピリジンやトリエチルアミン、DBUのような塩基性触媒共存下で、無水酢酸やジシクロヘキシルカルボジイミド、亜リン酸トリフェニルのような脱水縮合剤を用いるいわゆる化学イミド化等の手法が好適に用いられる。
本発明において、ポリイミド化合物の重合反応液中のテトラカルボン酸二無水物及びジアミン化合物の総濃度は特に限定されるものではないが、5~70質量%が好ましく、より好ましくは5~50質量%が好ましく、さらに好ましくは5~30質量%である。
[ガス分離膜]
(ガス分離複合膜)
本発明のガス分離膜の好ましい態様であるガス分離複合膜は、ガス透過性の支持層上に、特定のポリイミド化合物を構成材料として含むガス分離層が設けられる。この複合膜は、多孔質の支持体の少なくとも表面に、上記ポリイミド化合物を含有する塗布液(ドープ)を塗布して、上記ガス分離層を設けることが好ましい。なお、本明細書において「塗布」とは、塗布液に浸漬する態様を含む。
図1は、本発明の好ましい実施形態であるガス分離複合膜10を模式的に示す縦断面図である。1はガス分離層、2は多孔質層からなる支持層である。図2は、本発明の好ましい実施形態であるガス分離複合膜20を模式的に示す断面図である。この実施形態では、ガス分離層1及び多孔質層2に加え、支持層に不織布層3を含み、ガス分離複合膜20は、ガス分離層1と、多孔質層2と、不織布層3とが、この順に設けられる。
図1及び2は、二酸化炭素とメタンとの混合ガスから二酸化炭素を選択的に透過させることにより、透過ガスを二酸化炭素リッチにした態様を示す。
(ガス分離複合膜)
本発明のガス分離膜の好ましい態様であるガス分離複合膜は、ガス透過性の支持層上に、特定のポリイミド化合物を構成材料として含むガス分離層が設けられる。この複合膜は、多孔質の支持体の少なくとも表面に、上記ポリイミド化合物を含有する塗布液(ドープ)を塗布して、上記ガス分離層を設けることが好ましい。なお、本明細書において「塗布」とは、塗布液に浸漬する態様を含む。
図1は、本発明の好ましい実施形態であるガス分離複合膜10を模式的に示す縦断面図である。1はガス分離層、2は多孔質層からなる支持層である。図2は、本発明の好ましい実施形態であるガス分離複合膜20を模式的に示す断面図である。この実施形態では、ガス分離層1及び多孔質層2に加え、支持層に不織布層3を含み、ガス分離複合膜20は、ガス分離層1と、多孔質層2と、不織布層3とが、この順に設けられる。
図1及び2は、二酸化炭素とメタンとの混合ガスから二酸化炭素を選択的に透過させることにより、透過ガスを二酸化炭素リッチにした態様を示す。
本明細書において「支持層上」とは、支持層とガス分離層との間に他の層が介在してもよい意味である。また、上下の表現については、特に断らない限り、ガス分離膜の、分離対象となるガスが供給される側を「上」とし、分離されたガスが排出される側を「下」とする。
本発明のガス分離複合膜は、多孔質性の支持体(支持層)の表面ないし内面にガス分離層を形成ないしは配置するようにしてもよく、少なくとも多孔質性の支持体表面に形成して簡便に複合膜とすることができる。多孔質性の支持体の少なくとも表面にガス分離層を形成することで、高分離選択性と高ガス透過性、更には機械的強度を兼ね備えた複合膜とすることができる。ガス分離層の膜厚は、ガス透過性の観点から、機械的強度及びガス分離選択性を所望のレベルに維持できる範囲で可能な限り薄膜とすることが好ましい。
本発明のガス分離複合膜において、ガス分離層の厚さは特に限定されないが、0.01~5.0μmであることが好ましく、0.05~2.0μmであることがより好ましい。
支持層は、機械的強度及び気体透過性が所望のレベルにあるものであれば、特に限定されるものではなく、有機素材又は無機素材のいずれを用いてもよい。この支持層は好ましくは有機高分子の多孔質層であり、その厚さは1~3000μmが好ましく、5~500μmがより好ましく、さらに好ましくは5~150μmである。この多孔質層の細孔構造は、通常平均細孔直径が好ましくは10μm以下、より好ましくは0.5μm以下、さらに好ましくは0.2μm以下である。空孔率は好ましくは20~90%であり、より好ましくは30~80%である。
ここで、支持層が「ガス透過性」であるとは、支持層(支持層のみからなる膜)に対して、40℃の温度下、ガス供給側の全圧力を4MPaにして二酸化炭素を供給した際に、二酸化炭素の透過速度が1×10-5cm3(STP)/cm2・sec・cmHg(10GPU)以上であることを意味する。さらに、支持層のガス透過性は、40℃の温度下、ガス供給側の全圧力を4MPaにして二酸化炭素を供給した際に、二酸化炭素透過速度が3×10-5cm3(STP)/cm2・sec・cmHg(30GPU)以上であることが好ましく、100GPU以上であることがより好ましく、200GPU以上であることがさらに好ましい。上記多孔質層の素材としては、従来公知の高分子、例えばポリエチレン、ポリプロピレン等のポリオレフィン系樹脂等、ポリテトラフルオロエチレン、ポリフッ化ビニル、ポリフッ化ビニリデン等の含フッ素樹脂等、ポリスチレン、酢酸セルロース、ポリウレタン、ポリアクリロニトリル、ポリフェニレンオキシド、ポリスルホン、ポリエーテルスルホン、ポリイミド、ポリアラミド等の各種樹脂を挙げることができる。上記多孔質層の形状としては、平板状、スパイラル状、管状、中空糸状などいずれの形状をとることもできる。
ここで、支持層が「ガス透過性」であるとは、支持層(支持層のみからなる膜)に対して、40℃の温度下、ガス供給側の全圧力を4MPaにして二酸化炭素を供給した際に、二酸化炭素の透過速度が1×10-5cm3(STP)/cm2・sec・cmHg(10GPU)以上であることを意味する。さらに、支持層のガス透過性は、40℃の温度下、ガス供給側の全圧力を4MPaにして二酸化炭素を供給した際に、二酸化炭素透過速度が3×10-5cm3(STP)/cm2・sec・cmHg(30GPU)以上であることが好ましく、100GPU以上であることがより好ましく、200GPU以上であることがさらに好ましい。上記多孔質層の素材としては、従来公知の高分子、例えばポリエチレン、ポリプロピレン等のポリオレフィン系樹脂等、ポリテトラフルオロエチレン、ポリフッ化ビニル、ポリフッ化ビニリデン等の含フッ素樹脂等、ポリスチレン、酢酸セルロース、ポリウレタン、ポリアクリロニトリル、ポリフェニレンオキシド、ポリスルホン、ポリエーテルスルホン、ポリイミド、ポリアラミド等の各種樹脂を挙げることができる。上記多孔質層の形状としては、平板状、スパイラル状、管状、中空糸状などいずれの形状をとることもできる。
本発明のガス分離複合膜においては、ガス分離層を形成する支持層の下部にさらに機械的強度を付与するために支持体が形成されていることが好ましい。このような支持体としては、織布、不織布、ネット等が挙げられるが、製膜性及びコスト面から不織布が好適に用いられる。不織布としてはポリエステル、ポリプロピレン、ポリアクリロニトリル、ポリエチレン、ポリアミド等からなる繊維を単独あるいは複数を組み合わせて用いてもよい。不織布は、例えば、水に均一に分散した主体繊維とバインダー繊維とを円網や長網等で抄造し、ドライヤーで乾燥することにより製造できる。また、毛羽を除去したり機械的性質を向上させたりする目的で、不織布を2本のロール挟んで圧熱加工を施すことも好ましい。
<ガス分離複合膜の製造方法>
本発明のガス分離複合膜の製造方法は、好ましくは、上記ポリイミド化合物を含有する塗布液を多孔質支持体上に塗布してガス分離層を形成することを含む製造方法が好ましい。塗布液中のポリイミド化合物の含有量は特に限定されないが、0.1~30質量%であることが好ましく、0.5~10質量%であることがより好ましい。ポリイミド化合物の含有量をこの範囲とすることで、多孔質支持体上にガス分離層を形成した際に、塗布液が下層へと浸透することを抑制できるので、形成するガス分離層に欠陥が生じにくくなる。また、多孔質支持体上にガス分離層を形成した際に、塗布液が孔内に高濃度に充填されることを抑制できるので、優れた透過性を有するガス分離複合膜が得られる。本発明のガス分離膜は、ガス分離層の形成に用いるポリイミド化合物の分子量、構造、組成さらには溶液粘度を目的に応じて調整し、製造することができる。
本発明のガス分離複合膜の製造方法は、好ましくは、上記ポリイミド化合物を含有する塗布液を多孔質支持体上に塗布してガス分離層を形成することを含む製造方法が好ましい。塗布液中のポリイミド化合物の含有量は特に限定されないが、0.1~30質量%であることが好ましく、0.5~10質量%であることがより好ましい。ポリイミド化合物の含有量をこの範囲とすることで、多孔質支持体上にガス分離層を形成した際に、塗布液が下層へと浸透することを抑制できるので、形成するガス分離層に欠陥が生じにくくなる。また、多孔質支持体上にガス分離層を形成した際に、塗布液が孔内に高濃度に充填されることを抑制できるので、優れた透過性を有するガス分離複合膜が得られる。本発明のガス分離膜は、ガス分離層の形成に用いるポリイミド化合物の分子量、構造、組成さらには溶液粘度を目的に応じて調整し、製造することができる。
塗布液の媒体とする有機溶剤としては、特に限定されるものではなく、n-ヘキサン、n-ヘプタン等の炭化水素系有機溶剤、酢酸メチル、酢酸エチル、酢酸ブチル等のエステル系有機溶剤、メタノール、エタノール、n-プロパノール、イソプロパノール、n-ブタノール、イソブタノール、tert-ブタノール等のアルコール系有機溶剤、アセトン、メチルエチルケトン、メチルイソブチルケトン、ジアセトンアルコール、シクロペンタノン、シクロヘキサノン等の脂肪族ケトン、エチレングリコール、ジエチレングリコール、トリエチレングリコール、グリセリン、プロピレングリコール、エチレングリコールモノメチル又はモノエチルエーテル、プロピレングリコールメチルエーテル、ジプロピレングリコールメチルエーテル、トリプロピレングリコールメチルエーテル、エチレングリコールフェニルエーテル、プロピレングリコールフェニルエーテル、ジエチレングリコールモノメチル又はモノエチルエーテル、ジエチレングリコールモノブチルエーテル、トリエチレングリコールモノメチル又はモノエチルエーテル、ジブチルブチルエーテル、テトラヒドロフラン、メチルシクロペンチルエーテル、ジオキサン等のエーテル系有機溶剤、N-メチルピロリドン、2-ピロリドン、ジメチルホルムアミド、ジメチルイミダゾリジノン、ジメチルスルホキシド、ジメチルアセトアミドなどが挙げられる。これらの有機溶剤は支持体を浸蝕するなどの悪影響を及ぼさない範囲で適切に選択されるものであるが、好ましくは、エステル系有機溶剤(好ましくは酢酸ブチル)、アルコール系有機溶剤(好ましくはメタノール、エタノール、イソプロパノール、イソブタノール)、脂肪族ケトン(好ましくは、メチルエチルケトン、メチルイソブチルケトン、ジアセトンアルコール、シクロペンタノン、シクロヘキサノン)、エーテル系有機溶剤(エチレングリコール、ジエチレングリコールモノメチルエーテル、メチルシクロペンチルエーテル)であり、さらに好ましくは脂肪族ケトン、アルコール系有機溶剤、エーテル系有機溶剤である。またこれらは、1種又は2種以上を組み合わせて用いることができる。
<支持層とガス分離層の間の他の層>
本発明のガス分離複合膜において、支持層とガス分離層との間には他の層が存在していてもよい。他の層の好ましい例として、シロキサン化合物層が挙げられる。シロキサン化合物層を設けることで、支持体最表面の凹凸を平滑化することができ、分離層の薄層化が容易になる。シロキサン化合物層を形成するシロキサン化合物としては、主鎖がポリシロキサンからなるものと、主鎖にシロキサン構造と非シロキサン構造とを有する化合物とが挙げられる。
本明細書において「シロキサン化合物」という場合、特に断りのない限り、オルガノポリシロキサン化合物を意味する。
本発明のガス分離複合膜において、支持層とガス分離層との間には他の層が存在していてもよい。他の層の好ましい例として、シロキサン化合物層が挙げられる。シロキサン化合物層を設けることで、支持体最表面の凹凸を平滑化することができ、分離層の薄層化が容易になる。シロキサン化合物層を形成するシロキサン化合物としては、主鎖がポリシロキサンからなるものと、主鎖にシロキサン構造と非シロキサン構造とを有する化合物とが挙げられる。
本明細書において「シロキサン化合物」という場合、特に断りのない限り、オルガノポリシロキサン化合物を意味する。
-主鎖がポリシロキサンからなるシロキサン化合物-
シロキサン化合物層に用いうる、主鎖がポリシロキサンからなるシロキサン化合物としては、下記式(1)又は(2)で表されるポリオルガノシロキサンの1種又は2種以上が挙げられる。また、これらのポリオルガノシロキサンは架橋反応物を形成していてもよい。この架橋反応物としては、例えば、下記式(1)で表される化合物が、下記式(1)の反応性基XSと反応して連結する基を両末端に有するポリシロキサン化合物により架橋された形態の化合物が挙げられる。
シロキサン化合物層に用いうる、主鎖がポリシロキサンからなるシロキサン化合物としては、下記式(1)又は(2)で表されるポリオルガノシロキサンの1種又は2種以上が挙げられる。また、これらのポリオルガノシロキサンは架橋反応物を形成していてもよい。この架橋反応物としては、例えば、下記式(1)で表される化合物が、下記式(1)の反応性基XSと反応して連結する基を両末端に有するポリシロキサン化合物により架橋された形態の化合物が挙げられる。
式(1)中、RSは非反応性基であって、アルキル基(好ましくは炭素数1~18、より好ましくは炭素数1~12のアルキル基)又はアリール基(好ましくは炭素数6~15、より好ましくは炭素数6~12のアリール基、さらに好ましくはフェニル)であることが好ましい。
XSは反応性基であって、水素原子、ハロゲン原子、ビニル基、ヒドロキシル基、及び置換アルキル基(好ましくは炭素数1~18、より好ましくは炭素数1~12のアルキル基)から選ばれる基であることが好ましい。
YS及びZSは上記RS又はXSである。
mは1以上の数であり、好ましくは1~100,000である。
nは0以上の数であり、好ましくは0~100,000である。
XSは反応性基であって、水素原子、ハロゲン原子、ビニル基、ヒドロキシル基、及び置換アルキル基(好ましくは炭素数1~18、より好ましくは炭素数1~12のアルキル基)から選ばれる基であることが好ましい。
YS及びZSは上記RS又はXSである。
mは1以上の数であり、好ましくは1~100,000である。
nは0以上の数であり、好ましくは0~100,000である。
式(2)中、XS、YS、ZS、RS、m及びnは、それぞれ式(1)のXS、YS、ZS、RS、m及びnと同義である。
上記式(1)及び(2)において、非反応性基RSがアルキル基である場合、このアルキル基の例としては、メチル、エチル、へキシル、オクチル、デシル、及びオクタデシルを挙げることができる。また、非反応性基RSがフルオロアルキル基である場合、このフルオロアルキル基としては、例えば、-CH2CH2CF3、-CH2CH2C6F13が挙げられる。
上記式(1)及び(2)において、反応性基XSが置換アルキル基である場合、このアルキル基の例としては、炭素数1~18のヒドロキシアルキル基、炭素数1~18のアミノアルキル基、炭素数1~18のカルボキシアルキル基、炭素数1~18のクロロアルキル基、炭素数1~18のグリシドキシアルキル基、グリシジル基、炭素数7~16のエポキシシクロへキシルアルキル基、炭素数4~18の(1-オキサシクロブタン-3-イル)アルキル基、メタクリロキシアルキル基、及びメルカプトアルキル基が挙げられる。
上記ヒドロキシアルキル基を構成するアルキル基の炭素数は1~10の整数であることが好ましく、例えば、-CH2CH2CH2OHが挙げられる。
上記アミノアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数であることが好ましく、例えば、-CH2CH2CH2NH2が挙げられる。
上記カルボキシアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数であることが好ましい。ヒドロキシアルキル基は、例えば、-CH2CH2CH2COOHが挙げられる。
上記クロロアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数であることが好ましい。アミノアルキル基は、例えば、-CH2Clが挙げられる。
上記グリシドキシアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数である。グリシドキシアルキル基は、例えば、3-グリシジルオキシプロピルが挙げられる。
上記炭素数7~16のエポキシシクロへキシルアルキル基の好ましい炭素数は8~12の整数である。
炭素数4~18の(1-オキサシクロブタン-3-イル)アルキル基の好ましい炭素数は4~10の整数である。
上記メタクリロキシアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数である。メタクリロキシアルキル基は、例えば、-CH2CH2CH2-OOC-C(CH3)=CH2が挙げられる。
上記メルカプトアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数である。メタクリロキシアルキル基は、例えば、-CH2CH2CH2SHが挙げられる。
m及びnは、化合物の分子量が5,000~1,000,000になる数であることが好ましい。
上記ヒドロキシアルキル基を構成するアルキル基の炭素数は1~10の整数であることが好ましく、例えば、-CH2CH2CH2OHが挙げられる。
上記アミノアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数であることが好ましく、例えば、-CH2CH2CH2NH2が挙げられる。
上記カルボキシアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数であることが好ましい。ヒドロキシアルキル基は、例えば、-CH2CH2CH2COOHが挙げられる。
上記クロロアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数であることが好ましい。アミノアルキル基は、例えば、-CH2Clが挙げられる。
上記グリシドキシアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数である。グリシドキシアルキル基は、例えば、3-グリシジルオキシプロピルが挙げられる。
上記炭素数7~16のエポキシシクロへキシルアルキル基の好ましい炭素数は8~12の整数である。
炭素数4~18の(1-オキサシクロブタン-3-イル)アルキル基の好ましい炭素数は4~10の整数である。
上記メタクリロキシアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数である。メタクリロキシアルキル基は、例えば、-CH2CH2CH2-OOC-C(CH3)=CH2が挙げられる。
上記メルカプトアルキル基を構成するアルキル基の好ましい炭素数は1~10の整数である。メタクリロキシアルキル基は、例えば、-CH2CH2CH2SHが挙げられる。
m及びnは、化合物の分子量が5,000~1,000,000になる数であることが好ましい。
上記式(1)及び(2)において、反応性基含有シロキサン単位(式中、その数がnで表される構成単位)と反応性基を有さないシロキサン単位(式中、その数がmで表される構成単位)の分布に特に制限はない。すなわち、式(1)及び(2)中、(Si(RS)(RS)-O)単位と(Si(RS)(XS)-O)単位とはランダムに分布していてもよい。
-主鎖にシロキサン構造と非シロキサン構造とを有する化合物-
シロキサン化合物層に用いうる、主鎖にシロキサン構造と非シロキサン構造を有する化合物としては、例えば、下記式(3)~(7)で表される化合物が挙げられる。
シロキサン化合物層に用いうる、主鎖にシロキサン構造と非シロキサン構造を有する化合物としては、例えば、下記式(3)~(7)で表される化合物が挙げられる。
式(3)中、RS、m及びnは、それぞれ式(1)のRS、m及びnと同義である。RLは-O-又は-CH2-であり、RS1は水素原子又はメチルである。式(3)の両末端はアミノ基、水酸基、カルボキシ基、トリメチルシリル基、エポキシ基、ビニル基、水素原子、又は置換アルキル基であることが好ましい。
式(4)中、m及びnは、それぞれ式(1)におけるm及びnと同義である。
式(5)中、m及びnは、それぞれ式(1)におけるm及びnと同義である。
式(6)中、m及びnは、それぞれ式(1)におけるm及びnと同義である。式(6)の両末端はアミノ基、水酸基、カルボキシ基、トリメチルシリル基、エポキシ基、ビニル基、水素原子、又は置換アルキル基が結合していることが好ましい。
式(7)中、m及びnは、それぞれ式(1)におけるm及びnと同義である。式(7)の両末端はアミノ基、水酸基、カルボキシ基、トリメチルシリル基、エポキシ基、ビニル基、水素原子、又は置換アルキル基が結合していることが好ましい。
上記式(3)~(7)において、シロキサン構造単位と非シロキサン構造単位とは、ランダムに分布していてもよい。
主鎖にシロキサン構造と非シロキサン構造を有する化合物は、全繰り返し構造単位の合計モル数に対して、シロキサン構造単位を50モル%以上含有することが好ましく、70モル%以上含有することがさらに好ましい。
シロキサン化合物層に用いるシロキサン化合物の重量平均分子量は、薄膜化と耐久性の両立の観点から、5,000~1000,000であることが好ましい。重量平均分子量の測定方法は上述したとおりである。
さらに、シロキサン化合物層を構成するシロキサン化合物の好ましい例を以下に列挙する。
ポリジメチルシロキサン、ポリメチルフェニルシロキサン、ポリジフェニルシロキサン、ポリスルホン-ポリヒドロキシスチレン-ポリジメチルシロキサン共重合体、ジメチルシロキサン-メチルビニルシロキサン共重合体、ジメチルシロキサン-ジフェニルシロキサン-メチルビニルシロキサン共重合体、メチル-3,3,3-トリフルオロプロピルシロキサン-メチルビニルシロキサン共重合体、ジメチルシロキサン-メチルフェニルシロキサン-メチルビニルシロキサン共重合体、ジフェニルシロキサン-ジメチルシロキサン共重合体末端ビニル、ポリジメチルシロキサン末端ビニル、ポリジメチルシロキサン末端H、及びジメチルシロキサン-メチルハイドロシロキサン共重合体から選ばれる1種又は2種以上。なお、これらの化合物は架橋反応物を形成している形態も含まれる。
ポリジメチルシロキサン、ポリメチルフェニルシロキサン、ポリジフェニルシロキサン、ポリスルホン-ポリヒドロキシスチレン-ポリジメチルシロキサン共重合体、ジメチルシロキサン-メチルビニルシロキサン共重合体、ジメチルシロキサン-ジフェニルシロキサン-メチルビニルシロキサン共重合体、メチル-3,3,3-トリフルオロプロピルシロキサン-メチルビニルシロキサン共重合体、ジメチルシロキサン-メチルフェニルシロキサン-メチルビニルシロキサン共重合体、ジフェニルシロキサン-ジメチルシロキサン共重合体末端ビニル、ポリジメチルシロキサン末端ビニル、ポリジメチルシロキサン末端H、及びジメチルシロキサン-メチルハイドロシロキサン共重合体から選ばれる1種又は2種以上。なお、これらの化合物は架橋反応物を形成している形態も含まれる。
本発明のガス分離複合膜において、シロキサン化合物層の厚さは、平滑性及びガス透過性の観点から、0.01~5μmであることが好ましく、0.05~1μmであることがより好ましい。
また、シロキサン化合物層の40℃、4MPaにおける気体透過率は二酸化炭素透過速度で100GPU以上であることが好ましく、300GPU以上であることがより好ましく、1000GPU以上であることがさらに好ましい。
また、シロキサン化合物層の40℃、4MPaにおける気体透過率は二酸化炭素透過速度で100GPU以上であることが好ましく、300GPU以上であることがより好ましく、1000GPU以上であることがさらに好ましい。
(ガス分離非対称膜)
本発明のガス分離膜は、非対称膜であってもよい。非対称膜は、ポリイミド化合物を含む溶液を用いて相転換法によって形成することができる。相転換法は、ポリマー溶液を凝固液と接触させて相転換させながら膜を形成する公知の方法であり、本発明ではいわゆる乾湿式法が好適に用いられる。乾湿式法は、膜形状にしたポリマー溶液の表面の溶液を蒸発させて薄い緻密層を形成し、ついで凝固液に浸漬し、その際生じる相分離現象を利用して微細孔を形成して多孔質層を形成させる方法であり、ロブ・スリラージャンらが提案(例えば、米国特許第3,133,132号明細書)したものである。なお、凝固液はポリマー溶液の溶媒とは相溶し、ポリマーは不溶な溶剤である。
本発明のガス分離膜は、非対称膜であってもよい。非対称膜は、ポリイミド化合物を含む溶液を用いて相転換法によって形成することができる。相転換法は、ポリマー溶液を凝固液と接触させて相転換させながら膜を形成する公知の方法であり、本発明ではいわゆる乾湿式法が好適に用いられる。乾湿式法は、膜形状にしたポリマー溶液の表面の溶液を蒸発させて薄い緻密層を形成し、ついで凝固液に浸漬し、その際生じる相分離現象を利用して微細孔を形成して多孔質層を形成させる方法であり、ロブ・スリラージャンらが提案(例えば、米国特許第3,133,132号明細書)したものである。なお、凝固液はポリマー溶液の溶媒とは相溶し、ポリマーは不溶な溶剤である。
ガス分離非対称膜において、緻密層あるいはスキン層と呼ばれるガス分離に寄与する表層の厚さは特に限定されないが、実用的なガス透過性を付与する観点から、0.01~5.0μmであることが好ましく、0.05~1.0μmであることがより好ましい。一方、緻密層より下部の多孔質層はガス透過性の抵抗を下げると同時に機械強度を付与するものであり、その厚さは非対称膜としての自立性が付与される限りにおいては特に限定されるものではない。非対称膜における下部多孔質層の厚さは5~500μmであることが好ましく、5~200μmであることがより好ましく、5~100μmであることがさらに好ましい。
本発明のガス分離非対称膜は、平膜であってもあるいは中空糸膜であってもよい。非対称中空糸膜は乾湿式紡糸法により製造することができる。乾湿式紡糸法は、紡糸ノズルから吐出して中空糸状の目的形状としたポリマー溶液に、乾湿式法を適用して非対称中空糸膜を製造する方法である。より詳しくは、ポリマー溶液をノズルから中空糸状の目的形状に吐出させ、吐出直後に空気又は窒素ガス雰囲気中を通す。その後、ポリマーを実質的には溶解せず且つポリマー溶液の溶媒とは相溶性を有する凝固液に浸漬して非対称構造を形成する。その後乾燥し、さらに必要に応じて加熱処理して分離膜を製造する方法である。
ノズルから吐出させるポリイミド化合物を含む溶液の溶液粘度は、吐出温度(例えば10℃)で2~17000Pa・sが好ましく、より好ましくは10~1500Pa・sであり、特に20~1000Pa・sであり、中空糸状などの吐出後の形状を安定化することができる。凝固液への浸漬は、一次凝固液に浸漬して中空糸状等の膜の形状が保持出来る程度に凝固させた後、案内ロールに巻き取り、ついで二次凝固液に浸漬して膜全体を十分に凝固させることが好ましい。凝固した膜の乾燥は、凝固液を炭化水素などの溶媒に置換してから行うのが効率的である。乾燥のための加熱処理は、用いたポリイミド化合物の軟化点又は二次転移点よりも低い温度で実施することが好ましい。
<保護層>
本発明のガス分離膜は、上記ガス分離層上にシロキサン化合物層が保護層として設けられていてもよい。
保護層として用いるシロキサン化合物層は、下記数式(I)で表されるクロロホルム浸漬前後のSi比が0.6~1.0の範囲内にあることが好ましい。
本発明のガス分離膜は、上記ガス分離層上にシロキサン化合物層が保護層として設けられていてもよい。
保護層として用いるシロキサン化合物層は、下記数式(I)で表されるクロロホルム浸漬前後のSi比が0.6~1.0の範囲内にあることが好ましい。
数式(I)
Si比=(クロロホルム浸漬後のSi-KαX線強度)/(クロロホルム浸漬前のSi-KαX線強度)
Si比=(クロロホルム浸漬後のSi-KαX線強度)/(クロロホルム浸漬前のSi-KαX線強度)
Si比は、シロキサン化合物層をクロロホルム中に、25℃で12時間浸漬し、この浸漬前後のシロキサン化合物層表面にX線を照射し、そのSi-KαX線(1.74keV)のピーク(2θ=144.6deg)の強度を測定することにより算出される。Si-KαX線強度の測定方法は、例えば特開平6-88792号公報に記載されている。クロロホルム中への浸漬により、浸漬前に比べてSi-KαX線強度が低下する場合、低分子量成分が存在し、これが溶出していることを意味する。したがって、クロロホルム中への浸漬後において、Si-KαX線強度の低下度合が小さい程、シロキサン化合物層を構成するポリマーがより高分子化され、クロロホルム中に溶出しにくくなっていることを意味する。
シロキサン化合物層のSi比が0.6~1.0の範囲内であることにより、シロキサン化合物を層中に、高密度且つ均質に存在させることができ、膜欠陥を効果的に防ぎ、ガス分離性能をより高めることができる。また、高圧、高温且つ高湿条件下における使用や、トルエン等の不純物成分によるガス分離層の可塑化をより抑えることが可能となる。
保護層を構成するシロキサン化合物層のSi比は、0.7~1.0が好ましく、0.75~1.0がより好ましく、0.8~1.0がさらに好ましく、0.85~1.0がさらに好ましい。
保護層を構成するシロキサン化合物層のSi比は、0.7~1.0が好ましく、0.75~1.0がより好ましく、0.8~1.0がさらに好ましく、0.85~1.0がさらに好ましい。
保護層を構成するシロキサン化合物層は、シロキサン化合物同士が、*-O-M-O-*、*-S-M-S-*、*-NRa1C(=O)-*、*-NRb1C(=O)NRb1-*、*-O-CH2-O-*、*-S-CH2CH2-*、*-OC(=O)O-*、*-CH(OH)CH2OCO-*、*-CH(OH)CH2O-*、*-CH(OH)CH2S-*、*-CH(OH)CH2NRc1-*、*-CH(CH2OH)CH2OCO-*、*-CH(CH2OH)CH2O-*、*-CH(CH2OH)CH2S-*、*-CH(CH2OH)CH2N(Rc1)2-*、*-CH2CH2-*、*-C(=O)O-N+(Rd1)3-*、*-SO3
-N+(Re1)3-*及び*-PO3
-N+(Rf1)3-*から選ばれる連結基を介して連結した構造を有することが好ましい。
式中、Mは2~4価の金属原子を示す。Ra1、Rb1、Rc1 、Rd1、Re1、及びRf1は水素原子又はアルキル基を示す。*は連結部位を示す。
式中、Mは2~4価の金属原子を示す。Ra1、Rb1、Rc1 、Rd1、Re1、及びRf1は水素原子又はアルキル基を示す。*は連結部位を示す。
上記金属原子Mとしては、例えば、アルミニウム(Al)、鉄(Fe)、ベリリウム(Be)、ガリウム(Ga)、バナジウム(V)、インジウム(In)、チタン(Ti)、ジルコニウム(Zr)、銅(Cu)、コバルト(Co)、ニッケル(Ni)、亜鉛(Zn)、カルシウム(Ca)、マグネシウム(Mg)、イットリウム(Y)、スカンジウム(Sc)、クロム(Cr)、マンガン(Mn)、モリブデン(Mo)及びホウ素(B)から選ばれる金属原子が挙げられ、なかでもTi、In、Zr、Fe、Zn、Al、Ga及びBから選ばれる金属原子が好ましく、Ti、In、及びAlから選ばれる金属原子がより好ましく、Alがさらに好ましい。
上記Ra1、Rb1、Rc1
、Rd1、Re1、及びRf1として採り得るアルキル基は、好ましくは炭素数1~20、より好ましくは炭素数1~10、さらに好ましくは炭素数1~7、さらに好ましくは炭素数1~4のアルキル基である。このアルキル基は直鎖でも分岐を有してもよいが、直鎖であることがより好ましい。このアルキル基の好ましい具体例として、例えばメチル、エチル、イソプロピル、n-ブチル、t-ブチル、ペンチル、ヘキシル、ヘプチル、オクチル、及び1-エチルペンチルを挙げることができる。
シロキサン化合物同士が上記連結基を介して連結した構造を有することにより、シロキサン化合物層のSi比を本発明で規定する範囲内にまでより高めやすくなる。
シロキサン化合物同士を、上記連結基を介して連結する反応について以下に説明する。
<*-O-M-O-*>
上記連結基*-O-M-O-*は、例えば、ヒドロキシ基、カルボキシ基、スルホ基等の-OHを有する基(活性水素含有基)を有するシロキサン化合物と、下記式(B)で表される金属錯体(架橋剤)との間の配位子交換反応により形成することができる。
上記連結基*-O-M-O-*は、例えば、ヒドロキシ基、カルボキシ基、スルホ基等の-OHを有する基(活性水素含有基)を有するシロキサン化合物と、下記式(B)で表される金属錯体(架橋剤)との間の配位子交換反応により形成することができる。
式中、Mは上記金属原子Mと同義であり、好ましい形態も同じである。LLは、それぞれ独立に、アルコキシ基、アリールオキシ基、アセチルアセトナト基、アシルオキシ基、ヒドロキシ基又はハロゲン原子を示す。yは2~4の整数を示す。
LLとして採りうるアルコキシ基は、その炭素数が1~10が好ましく、1~4がより好ましく、1~3がさらに好ましい。LLとして採りうるアルコキシ基の具体例としては、例えば、メトキシ、エトキシ、tert-ブトキシ、及びイソプロポキシが挙げられる。
LLとして採りうるアリールオキシ基は、その炭素数が6~10が好ましく、6~8がより好ましく、6~7がさらに好ましい。LLとして採りうるアリールオキシ基の具体例としては、例えば、フェノキシ、4-メトキシフェノキシ、及びナフトキシを挙げることができる。
LLとして採りうるアシルオキシ基は、その炭素数が、2~10が好ましく、2~6がより好ましく、2~4がさらに好ましい。LLとして採りうるアシルオキシ基の具体例としては、例えば、アセトキシ、プロパノイルオキシ、ピバロイルオキシ、及びアセチルオキシを挙げることができる。
LLとして採りうるハロゲン原子は特に制限はなく、フッ素原子、塩素原子、臭素原子及びヨウ素原子が挙げられる。なかでも塩素原子が好ましい。
LLとして採りうるアルコキシ基は、その炭素数が1~10が好ましく、1~4がより好ましく、1~3がさらに好ましい。LLとして採りうるアルコキシ基の具体例としては、例えば、メトキシ、エトキシ、tert-ブトキシ、及びイソプロポキシが挙げられる。
LLとして採りうるアリールオキシ基は、その炭素数が6~10が好ましく、6~8がより好ましく、6~7がさらに好ましい。LLとして採りうるアリールオキシ基の具体例としては、例えば、フェノキシ、4-メトキシフェノキシ、及びナフトキシを挙げることができる。
LLとして採りうるアシルオキシ基は、その炭素数が、2~10が好ましく、2~6がより好ましく、2~4がさらに好ましい。LLとして採りうるアシルオキシ基の具体例としては、例えば、アセトキシ、プロパノイルオキシ、ピバロイルオキシ、及びアセチルオキシを挙げることができる。
LLとして採りうるハロゲン原子は特に制限はなく、フッ素原子、塩素原子、臭素原子及びヨウ素原子が挙げられる。なかでも塩素原子が好ましい。
上記式(B)で表される金属錯体は、シロキサン化合物層を形成する際の塗布液に用いる有機溶媒に対して可溶であることが好ましい。より具体的には、25℃において、テトラヒドロフラン100gに対して上記式(B)で表される金属錯体の溶解度が0.01~10gであることが好ましく、0.1~1.0gであることがより好ましい。上記式(B)で表される金属錯体が上記有機溶媒に対して可溶であることにより、より均質な金属架橋シロキサン化合物層を形成することができる。
上記式(B)で表される金属錯体の好ましい具体例としては、アルミニウムアセチルアセトナト、ガリウムアセチルアセトナト、インジウムアセチルアセトナト、ジルコニウムアセチルアセトナト、コバルトアセチルアセトナト、カルシウムアセチルアセトナト、ニッケルアセチルアセトナト、亜鉛アセチルアセトナト、マグネシウムアセチルアセトナト、塩化第二鉄、酢酸銅(II)、アルミニウムイソプロポキシド、チタニウムイソプロポキシド、ホウ酸、及び三フッ化ホウ素・ジエチルエーテル錯体から選ばれる金属錯体が挙げられる。
上記配位子交換反応の一例を示すと下記の通りである。なお、下記例はシロキサン化合物がヒドロキシ基を有する場合を示すが、シロキサン化合物がカルボキシ基やスルホ基等の活性水素含有基を有する場合にも、同様の配位子交換反応が進行し、*-O-M-O-*で表される連結基が形成される。
式中、RPはシロキサン化合物残基を示す(すなわちRP-OHはヒドロキシ基を有するシロキサン化合物を示す)。
Mが4価の金属原子(y=4)の場合、RP-OHは1つのMに対して通常4つまで配位しうる(上記(a)の形態)。本発明においては、Mが4価の金属原子の場合には、RP-OHが2つ配位した形態(上記(c)の形態)、3つ配位した形態(上記(b)の形態)、及び4つ配位した形態(上記(a)の形態)いずれの形態も、*-O-M-O-*で表される連結基を有する形態に包含されるものとする。
また、上記式には示していないが、上記シロキサン化合物RP-OHがRP1-(OH)hで表される場合(RP1はシロキサン化合物残基、hは2以上の整数、すなわち1分子中にヒドロキシ基を2つ以上有する形態である場合)、RP1-(OH)hの1分子中に存在する2つ以上のOHが1つのMに配位していてもよい。この形態も*-O-M-O-*で表される連結基を有する形態に包含されるものとする。
Mが4価の金属原子(y=4)の場合、RP-OHは1つのMに対して通常4つまで配位しうる(上記(a)の形態)。本発明においては、Mが4価の金属原子の場合には、RP-OHが2つ配位した形態(上記(c)の形態)、3つ配位した形態(上記(b)の形態)、及び4つ配位した形態(上記(a)の形態)いずれの形態も、*-O-M-O-*で表される連結基を有する形態に包含されるものとする。
また、上記式には示していないが、上記シロキサン化合物RP-OHがRP1-(OH)hで表される場合(RP1はシロキサン化合物残基、hは2以上の整数、すなわち1分子中にヒドロキシ基を2つ以上有する形態である場合)、RP1-(OH)hの1分子中に存在する2つ以上のOHが1つのMに配位していてもよい。この形態も*-O-M-O-*で表される連結基を有する形態に包含されるものとする。
Mが3価の金属原子の場合(y=3)、RP-OHは1つのMに対して通常3つまで配位しうる(上記(d)の形態)。本発明においては、Mが3価の金属原子の場合には、RP-OHが2つ配位した形態(上記(e)の形態)、3つ配位した形態(上記(d)の形態)のいずれの形態も、*-O-M-O-*で表される連結基を有する形態に包含されるものとする。
また、上記式には示していないが、上記シロキサン化合物RP-OHがRP1-(OH)hで表される場合(RP1はシロキサン化合物残基、hは2以上の整数、すなわち1分子中にヒドロキシ基を2つ以上有する形態である場合)、RP1-(OH)hの1分子中に存在する2つ以上のOHが1つのMに配位していてもよい。この形態も*-O-M-O-*で表される連結基を有する形態に包含されるものとする。
また、上記式には示していないが、上記シロキサン化合物RP-OHがRP1-(OH)hで表される場合(RP1はシロキサン化合物残基、hは2以上の整数、すなわち1分子中にヒドロキシ基を2つ以上有する形態である場合)、RP1-(OH)hの1分子中に存在する2つ以上のOHが1つのMに配位していてもよい。この形態も*-O-M-O-*で表される連結基を有する形態に包含されるものとする。
Mが2価の金属原子の場合(y=2)、上記(f)の形態が、本発明で規定する*-O-M-O-*で表される連結基を有する形態である。
また、上記式には示していないが、上記シロキサン化合物RP-OHがRP1-(OH)hで表される場合(RP1はシロキサン化合物残基、hは2以上の整数、すなわち1分子中にヒドロキシ基を2つ以上有する形態である場合)、RP1-(OH)hの1分子中に存在する2つ以上のOHが1つのMに配位していてもよい。この形態も*-O-M-O-*で表される連結基を有する形態に包含されるものとする。
また、上記式には示していないが、上記シロキサン化合物RP-OHがRP1-(OH)hで表される場合(RP1はシロキサン化合物残基、hは2以上の整数、すなわち1分子中にヒドロキシ基を2つ以上有する形態である場合)、RP1-(OH)hの1分子中に存在する2つ以上のOHが1つのMに配位していてもよい。この形態も*-O-M-O-*で表される連結基を有する形態に包含されるものとする。
<*-S-M-S-*>
上記連結構造*-S-M-S-*は、例えば、チオール基を有するシロキサン化合物と、上記式(B)で表される金属錯体との間の配位子交換反応により形成することが出来る。この反応は、上述した*-O-M-O-*を形成するための反応においてRP-OHをRP-SHに代えた反応形態である。-SHも活性水素含有基であるため、上記と同様に配位子交換反応を行うことができる。
上記連結構造*-S-M-S-*は、例えば、チオール基を有するシロキサン化合物と、上記式(B)で表される金属錯体との間の配位子交換反応により形成することが出来る。この反応は、上述した*-O-M-O-*を形成するための反応においてRP-OHをRP-SHに代えた反応形態である。-SHも活性水素含有基であるため、上記と同様に配位子交換反応を行うことができる。
<*-NRaC(=O)-*>
上記連結基*-NRaC(=O)-*は、例えば、カルボキシ基を有するシロキサン化合物と、アミノ基を有するシロキサン化合物とを、脱水縮合剤(例えばカルボジイミド化合物)の存在下で反応させることにより形成することができる。この反応は下記式で表すことができる。
RP-COOH + RP-N(Ra)2
⇒ RP-C(=O)-NRa-RP + H2O
上記式中、RPはシロキサン化合物残基を示す。左辺において1つのNに連結する2つのRaのうち1つは水素原子であり、残りは水素原子又はアルキル基である。つまり、右辺のRaは水素原子又はアルキル基である。
また、上記連結基は、カルボキシ基を有するシロキサン化合物と、架橋剤としての、アミノ基を2つ以上有する化合物とを反応させることで形成することもできる。また、アミノ基を有するシロキサン化合物と、架橋剤としての、カルボキシ基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成させることができる。
上記連結基*-NRaC(=O)-*は、例えば、カルボキシ基を有するシロキサン化合物と、アミノ基を有するシロキサン化合物とを、脱水縮合剤(例えばカルボジイミド化合物)の存在下で反応させることにより形成することができる。この反応は下記式で表すことができる。
RP-COOH + RP-N(Ra)2
⇒ RP-C(=O)-NRa-RP + H2O
上記式中、RPはシロキサン化合物残基を示す。左辺において1つのNに連結する2つのRaのうち1つは水素原子であり、残りは水素原子又はアルキル基である。つまり、右辺のRaは水素原子又はアルキル基である。
また、上記連結基は、カルボキシ基を有するシロキサン化合物と、架橋剤としての、アミノ基を2つ以上有する化合物とを反応させることで形成することもできる。また、アミノ基を有するシロキサン化合物と、架橋剤としての、カルボキシ基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成させることができる。
<*-NRb1C(=O)NRb1-*>
上記連結基*-NRb1C(=O)NRb1-*は、例えば、アミノ基を有するシロキサン化合物と、架橋剤としてのクロロギ酸エステルとを反応させることにより形成することができる。この反応は下記式で表すことができる。
2RP-N(Rb1)2 + Cl-C(=O)-O-RCl
⇒ RP-Rb1N-C(=O)-NRb1-RP + HCl + HO-RCl
上記式中、RPはシロキサン化合物残基を示し、RClはクロロギ酸エステルのアルコール残基を示す。左辺において1つのN原子に連結する2つのRb1のうち1つは水素原子であり、残りは水素原子又はアルキル基である(つまり、右辺のRb1は水素原子又はアルキル基である)。
上記連結基*-NRb1C(=O)NRb1-*は、例えば、アミノ基を有するシロキサン化合物と、架橋剤としてのクロロギ酸エステルとを反応させることにより形成することができる。この反応は下記式で表すことができる。
2RP-N(Rb1)2 + Cl-C(=O)-O-RCl
⇒ RP-Rb1N-C(=O)-NRb1-RP + HCl + HO-RCl
上記式中、RPはシロキサン化合物残基を示し、RClはクロロギ酸エステルのアルコール残基を示す。左辺において1つのN原子に連結する2つのRb1のうち1つは水素原子であり、残りは水素原子又はアルキル基である(つまり、右辺のRb1は水素原子又はアルキル基である)。
<*-O-CH2-O-*>
上記連結基*-O-CH2-O-*は、例えば、ヒドロキシ基を有するシロキサン化合物と、架橋剤としてのホルムアルデヒドとを反応させることにより形成することができる。この反応は下記式で表すことができる。
2RP-OH + H-C(=O)-H
⇒ RP-O-CH(O-RP)-H + H2O
上記式中、RPはシロキサン化合物残基を示す。
上記連結基*-O-CH2-O-*は、例えば、ヒドロキシ基を有するシロキサン化合物と、架橋剤としてのホルムアルデヒドとを反応させることにより形成することができる。この反応は下記式で表すことができる。
2RP-OH + H-C(=O)-H
⇒ RP-O-CH(O-RP)-H + H2O
上記式中、RPはシロキサン化合物残基を示す。
<*-S-CH2CH2-*>
上記連結基*-S-CH2CH2-*は、例えば、チオール基を有するシロキサン化合物と、ビニル基を有するシロキサン化合物とを反応させることにより形成することができる。この反応は下記式で表すことができる。
RP-SH + RP-CH=CH2
⇒ RP-S-CH2-CH2-RP
上記式中、RPはシロキサン化合物残基を示す。
なお、チオール基を有するシロキサン化合物と、架橋剤としての、ビニル基を2つ以上有する化合物とを反応させた場合にも、上記連結基を形成させることができる。また、ビニル基を有するシロキサン化合物と、架橋剤としての、チオール基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。
上記連結基*-S-CH2CH2-*は、例えば、チオール基を有するシロキサン化合物と、ビニル基を有するシロキサン化合物とを反応させることにより形成することができる。この反応は下記式で表すことができる。
RP-SH + RP-CH=CH2
⇒ RP-S-CH2-CH2-RP
上記式中、RPはシロキサン化合物残基を示す。
なお、チオール基を有するシロキサン化合物と、架橋剤としての、ビニル基を2つ以上有する化合物とを反応させた場合にも、上記連結基を形成させることができる。また、ビニル基を有するシロキサン化合物と、架橋剤としての、チオール基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。
<*-OC(=O)O-*>
上記連結基*-OC(=O)O-*は、例えば、ヒドロキシ基を有するシロキサン化合物と、架橋剤としてのクロロギ酸エステルとを反応させることにより形成することができる。この反応は下記式で表すことができる。
2RP-OH + Cl-C(=O)-O-RCl
⇒ RP-O-C(=O)-O-RP + HCl + HO-RCl
上記式中、RPはシロキサン化合物残基を示し、RClはクロロギ酸エステルのアルコール残基を示す。
上記連結基*-OC(=O)O-*は、例えば、ヒドロキシ基を有するシロキサン化合物と、架橋剤としてのクロロギ酸エステルとを反応させることにより形成することができる。この反応は下記式で表すことができる。
2RP-OH + Cl-C(=O)-O-RCl
⇒ RP-O-C(=O)-O-RP + HCl + HO-RCl
上記式中、RPはシロキサン化合物残基を示し、RClはクロロギ酸エステルのアルコール残基を示す。
<*-C(=O)O-N+(Rd1)3-*>
上記連結基*-C(=O)O-N+(Rd1)3-*は、例えば、カルボキシ基を有するシロキサン化合物と、アミノ基を有するシロキサン化合物とを反応させることにより形成することができる。この反応は下記式で表すことができる。
RP-COOH + RP-N(Rd1)2
⇒ RP-CO-O--N+H(Rd1)2-RP
上記式中、RPはシロキサン化合物残基を示す。Rd1は水素原子又はアルキル基を示す。
なお、カルボキシ基を有するシロキサン化合物と、架橋剤としての、アミノ基を2つ以上有する化合物とを反応させることによっても、上記連結構造を形成することができる。また、アミノ基を有するシロキサン化合物と、架橋剤としての、カルボキシ基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。
上記連結基*-C(=O)O-N+(Rd1)3-*は、例えば、カルボキシ基を有するシロキサン化合物と、アミノ基を有するシロキサン化合物とを反応させることにより形成することができる。この反応は下記式で表すことができる。
RP-COOH + RP-N(Rd1)2
⇒ RP-CO-O--N+H(Rd1)2-RP
上記式中、RPはシロキサン化合物残基を示す。Rd1は水素原子又はアルキル基を示す。
なお、カルボキシ基を有するシロキサン化合物と、架橋剤としての、アミノ基を2つ以上有する化合物とを反応させることによっても、上記連結構造を形成することができる。また、アミノ基を有するシロキサン化合物と、架橋剤としての、カルボキシ基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。
<*-SO3
-N+(Re1)3-*>
上記連結基*-SO3 -N+(Re1)3-*は、例えば、スルホ基を有するシロキサン化合物と、アミノ基を有するシロキサン化合物とを反応させることにより形成することができる。この反応は下記式で表すことができる。
RP-SO3H + RP-N(Re1)2
⇒ RP-SO2-O--N+H(Re1)2-RP
上記式中、RPはシロキサン化合物残基を示す。Re1は水素原子又はアルキル基を示す。
なお、スルホ基を有するシロキサン化合物と、架橋剤としての、アミノ基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。また、アミノ基を有するシロキサン化合物と、架橋剤としての、スルホ基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。
上記連結基*-SO3 -N+(Re1)3-*は、例えば、スルホ基を有するシロキサン化合物と、アミノ基を有するシロキサン化合物とを反応させることにより形成することができる。この反応は下記式で表すことができる。
RP-SO3H + RP-N(Re1)2
⇒ RP-SO2-O--N+H(Re1)2-RP
上記式中、RPはシロキサン化合物残基を示す。Re1は水素原子又はアルキル基を示す。
なお、スルホ基を有するシロキサン化合物と、架橋剤としての、アミノ基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。また、アミノ基を有するシロキサン化合物と、架橋剤としての、スルホ基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。
<*-PO3H-N+(Rf1)3-*>
上記連結構造*-PO3H-N+(Rf1)3-*は、例えば、ホスホン酸基を有するセルロース樹脂と、アミノ基を有するシロキサン化合物とを反応させることにより形成することができる。この反応は下記式で表すことができる。
RP-PO3H2 + RP-N(Rf1)2
⇒ RP-P(=O)(OH)-O--N+H(Rf1)2-RP
上記式中、RPはシロキサン残基を示す。Rf1は水素原子又はアルキル基を示す。
なお、ホスホン酸基を有するシロキサン化合物と、架橋剤としてのアミノ基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。また、アミノ基を有するシロキサン化合物と、架橋剤としての、スルホン酸基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。
上記連結構造*-PO3H-N+(Rf1)3-*は、例えば、ホスホン酸基を有するセルロース樹脂と、アミノ基を有するシロキサン化合物とを反応させることにより形成することができる。この反応は下記式で表すことができる。
RP-PO3H2 + RP-N(Rf1)2
⇒ RP-P(=O)(OH)-O--N+H(Rf1)2-RP
上記式中、RPはシロキサン残基を示す。Rf1は水素原子又はアルキル基を示す。
なお、ホスホン酸基を有するシロキサン化合物と、架橋剤としてのアミノ基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。また、アミノ基を有するシロキサン化合物と、架橋剤としての、スルホン酸基を2つ以上有する化合物とを反応させることによっても、上記連結基を形成することができる。
<*-CH(OH)CH2OCO-*>
上記連結基*-CH(OH)CH2OCO-*は、例えば、エポキシ基を有するシロキサン化合物と、カルボキシ基を有するシロキサン化合物とを反応させることで形成することができる。
また、上記連結基は、エポキシ基を有するシロキサン化合物と、架橋剤としての、カルボキシ基を2つ以上有する化合物とを反応させたり、カルボキシ基を有するシロキサン化合物と、架橋剤としての、エポキシ基を2つ以上有する化合物とを反応させたりすることで形成することもできる。
上記連結基*-CH(OH)CH2OCO-*は、例えば、エポキシ基を有するシロキサン化合物と、カルボキシ基を有するシロキサン化合物とを反応させることで形成することができる。
また、上記連結基は、エポキシ基を有するシロキサン化合物と、架橋剤としての、カルボキシ基を2つ以上有する化合物とを反応させたり、カルボキシ基を有するシロキサン化合物と、架橋剤としての、エポキシ基を2つ以上有する化合物とを反応させたりすることで形成することもできる。
<*-CH(OH)CH2O-*>
上記連結基*-CH(OH)CH2O-*は、例えば、エポキシ基を有するシロキサン化合物と、ヒドロキシ基を有するシロキサン化合物とを反応させることで形成することができる。
また、上記連結基は、エポキシ基を有するシロキサン化合物と、架橋剤としての、ヒドロキシ基を2つ以上有する化合物とを反応させたり、ヒドロキシ基を有するシロキサン化合物と、架橋剤としての、エポキシ基を2つ以上有する化合物とを反応させたりすることで形成することもできる。
上記連結基*-CH(OH)CH2O-*は、例えば、エポキシ基を有するシロキサン化合物と、ヒドロキシ基を有するシロキサン化合物とを反応させることで形成することができる。
また、上記連結基は、エポキシ基を有するシロキサン化合物と、架橋剤としての、ヒドロキシ基を2つ以上有する化合物とを反応させたり、ヒドロキシ基を有するシロキサン化合物と、架橋剤としての、エポキシ基を2つ以上有する化合物とを反応させたりすることで形成することもできる。
<*-CH(OH)CH2S-*>
上記連結基*-CH(OH)CH2S-*は、例えば、エポキシ基を有するシロキサン化合物と、チオール基を有するシロキサン化合物とを反応させることで形成することができる。
また、上記連結基は、エポキシ基を有するシロキサン化合物と、架橋剤としての、チオール基を2つ以上有する化合物とを反応させたり、チオール基を有するシロキサン化合物と、架橋剤としての、エポキシ基を2つ以上有する化合物とを反応させたりすることで形成することもできる。
上記連結基*-CH(OH)CH2S-*は、例えば、エポキシ基を有するシロキサン化合物と、チオール基を有するシロキサン化合物とを反応させることで形成することができる。
また、上記連結基は、エポキシ基を有するシロキサン化合物と、架橋剤としての、チオール基を2つ以上有する化合物とを反応させたり、チオール基を有するシロキサン化合物と、架橋剤としての、エポキシ基を2つ以上有する化合物とを反応させたりすることで形成することもできる。
<*-CH(OH)CH2NRc1-*>
上記連結基*-CH(OH)CH2NRc1-*は、例えば、エポキシ基を有するシロキサン化合物と、アミノ基を有するシロキサン化合物とを反応させることで形成することができる。
また、上記連結基は、エポキシ基を有するシロキサン化合物と、架橋剤としての、アミノ基を2つ以上有する化合物とを反応させたり、アミノ基を有するシロキサン化合物と、架橋剤としての、エポキシ基を2つ以上有する化合物とを反応させたりすることで形成することもできる。
上記連結基*-CH(OH)CH2NRc1-*は、例えば、エポキシ基を有するシロキサン化合物と、アミノ基を有するシロキサン化合物とを反応させることで形成することができる。
また、上記連結基は、エポキシ基を有するシロキサン化合物と、架橋剤としての、アミノ基を2つ以上有する化合物とを反応させたり、アミノ基を有するシロキサン化合物と、架橋剤としての、エポキシ基を2つ以上有する化合物とを反応させたりすることで形成することもできる。
<*-CH(CH2OH)CH2OCO-*>
上記連結基*-CH(CH2OH)CH2OCO-*は、上述した*-CH(OH)CH2OCO-*の形成において、エポキシ基をオキセタニル基に代えることで形成することができる。
上記連結基*-CH(CH2OH)CH2OCO-*は、上述した*-CH(OH)CH2OCO-*の形成において、エポキシ基をオキセタニル基に代えることで形成することができる。
<*-CH(CH2OH)CH2O-*>
上記連結基*-CH(CH2OH)CH2O-*は、上述した*-CH(OH)CH2O-*の形成において、エポキシ基をオキセタニル基に代えることで形成することができる。
上記連結基*-CH(CH2OH)CH2O-*は、上述した*-CH(OH)CH2O-*の形成において、エポキシ基をオキセタニル基に代えることで形成することができる。
<*-CH(CH2OH)CH2S-*>
上記連結基*-CH(CH2OH)CH2S-*は、上述した*-CH(OH)CH2S-*の形成において、エポキシ基をオキセタニル基に代えることで形成することができる。
上記連結基*-CH(CH2OH)CH2S-*は、上述した*-CH(OH)CH2S-*の形成において、エポキシ基をオキセタニル基に代えることで形成することができる。
<*-CH(CH2OH)CH2NRc1-*>
上記連結基*-CH(CH2OH)CH2NRc1-*は、上述した*-CH(OH)CH2NRc-*の形成において、エポキシ基をオキセタニル基に代えることで形成することができる。
上記連結基*-CH(CH2OH)CH2NRc1-*は、上述した*-CH(OH)CH2NRc-*の形成において、エポキシ基をオキセタニル基に代えることで形成することができる。
<*-CH2CH2-*>
上記連結基*-CH2CH2-*は、例えば、ビニル基((メタ)アクリロイル基等)を有するシロキサン化合物同士を重合反応させることにより形成することができる。また、ビニル基を有するシロキサン化合物のビニル基と、ヒドロシリル基を有するシロキサン化合物のヒドロシリル基とを反応させることにより形成することもできる。
本発明において、*-CH2CH2-*を介して連結した構造には、*-S-CH2CH2-*を介して連結した構造は含まれないものとする。
上記連結基*-CH2CH2-*は、例えば、ビニル基((メタ)アクリロイル基等)を有するシロキサン化合物同士を重合反応させることにより形成することができる。また、ビニル基を有するシロキサン化合物のビニル基と、ヒドロシリル基を有するシロキサン化合物のヒドロシリル基とを反応させることにより形成することもできる。
本発明において、*-CH2CH2-*を介して連結した構造には、*-S-CH2CH2-*を介して連結した構造は含まれないものとする。
保護層を構成するシロキサン化合物層は、上記連結構造を1種有してもよいし、2種以上有してもよい。
保護層を構成するシロキサン化合物層中、シロキサン化合物同士の連結構造は、連結構造を形成するための反応性、連結構造の化学的安定性の観点から、上記*-O-M-O-*、*-S-M-S-*、*-O-CH2-O-*、*-S-CH2CH2-*、*-OC(=O)O-*、*-CH2CH2-*、及び*-C(=O)O-N+(Rd1)3-*から選ばれる連結基を介した連結構造の1種又は2種以上が好ましく、*-O-M-O-*、*-S-M-S-*、*-O-CH2-O-*及び*-S-CH2CH2-*、*-CH2CH2-*から選ばれる連結基を介した連結構造の1種又は2種以上がより好ましく、*-O-M-O-*及び*-CH2CH2-*から選ばれる連結基を介した連結構造の1種又は2種がさらに好ましい。
シロキサン化合物層の原料として用いるシロキサン化合物(上記連結基を介した連結構造が形成される前のシロキサン化合物)は、上記連結構造を与える官能基を有するシロキサン化合物であれば特に制限はない。このシロキサン化合物の好ましい例としては、メタクリレート変性ポリジアルキルシロキサン、メタクリレート変性ポリジアリールシロキサン、メタクリレート変性ポリアルキルアリールシロキサン、チオール変性ポリジアルキルシロキサン、チオール変性ポリジアリールシロキサン、チオール変性ポリアルキルアリールシロキサン、ヒドロキシ変性ポリジアルキルシロキサン、ヒドロキシ変性ポリジアリールシロキサン、ヒドロキシ変性ポリアルキルアリールシロキサン、アミン変性ポリジアルキルシロキサン、アミン変性ポリジアリールシロキサン、アミン変性ポリアルキルアリールシロキサン、ビニル変性ポリジアルキルシロキサン、ビニル変性ポリジアリールシロキサン、ビニル変性ポリアルキルアリールシロキサン、カルボキシ変性ポリジアルキルシロキサン、カルボキシ変性ポリジアリールシロキサン、カルボキシ変性ポリアルキルアリールシロキサン、ヒドロシリル変性ポリジアルキルシロキサン、ヒドロシリル変性ポリジアリールシロキサン、ヒドロシリル変性ポリアルキルアリールシロキサン、エポキシ変性ポリジアルキルシロキサン、エポキシ変性ポリジアリールシロキサン、エポキシ変性ポリアルキルアリールシロキサン、オキセタニル変性ポリジアルキルシロキサン、オキセタニル変性ポリジアリールシロキサン、及びオキセタニル変性ポリアルキルアリールシロキサンから選ばれる1種又は2種以上が挙げられる。
また、上記例示のポリシロキサン化合物において、各官能基による変性部位は末端でもよく側鎖であってもよい。また、1分子中に2つ以上の変性部位があることが好ましい。また、上記変性により導入された各官能基はさらに置換基を有してもよい。
また、上記「ポリアルキルアリールシロキサン」におけるアルキル基とアリール基の量比に特に制限はない。すなわち、「ポリアルキルアリールシロキサン」はその構造中に、ジアルキルシロキサン構造やジアリールシロキサン構造を有していてもよい。
上記例示のシロキサン化合物において、アルキル基の炭素数は1~10が好ましくは、1~5がより好ましく、1~3がさらに好ましく、メチルがさらに好ましい。また、上記例示のシロキサン化合物において、アリール基の炭素数は6~20が好ましくは、6~15がより好ましく、6~12がさらに好ましく、フェニルがさらに好ましい。
また、上記例示のポリシロキサン化合物において、各官能基による変性部位は末端でもよく側鎖であってもよい。また、1分子中に2つ以上の変性部位があることが好ましい。また、上記変性により導入された各官能基はさらに置換基を有してもよい。
また、上記「ポリアルキルアリールシロキサン」におけるアルキル基とアリール基の量比に特に制限はない。すなわち、「ポリアルキルアリールシロキサン」はその構造中に、ジアルキルシロキサン構造やジアリールシロキサン構造を有していてもよい。
上記例示のシロキサン化合物において、アルキル基の炭素数は1~10が好ましくは、1~5がより好ましく、1~3がさらに好ましく、メチルがさらに好ましい。また、上記例示のシロキサン化合物において、アリール基の炭素数は6~20が好ましくは、6~15がより好ましく、6~12がさらに好ましく、フェニルがさらに好ましい。
保護層を構成するシロキサン化合物層は、下記(a)及び(b)から選ばれる少なくとも1つの構造を有することが好ましい。
(a)下記一般式(1a)で表される構造と、下記一般式(2a)又は(3a)で表される構造とを有する構造
(a)下記一般式(1a)で表される構造と、下記一般式(2a)又は(3a)で表される構造とを有する構造
式中、RSLは、それぞれ独立に、アルキル基又はアリール基を示す。LAは、それぞれ独立に、単結合又は2価の連結基を示す。XAは*-O-M1-O-*、*-S-M1-S-*、*-O-CH2-O-*、*-S-CH2CH2-*、*-OC(=O)O-*、*-CH2CH2-*、及び*-C(=O)O-N+(Rd)3-*から選ばれる連結基を示す。M1は、Zr、Fe、Zn、B、Al又はGaを示し、Rdは水素原子又はアルキル基を表す。a1及びb1は2以上の整数(好ましくは5以上の整数)である。「*」は連結部位を示す。「**」はシロキサン結合中の連結部位を示す。すなわち、一般式(1a)~(3a)において、**の隣がO原子の場合、**はSi原子との連結部位を示し、**の隣がSi原子の場合、**はO原子と連結部位を示す。
また、一般式(4a)の末端構造は、水素原子、メルカプト基、アミノ基、ビニル基、カルボキシ基、オキセタニル基、スルホ基、及びホスホン酸基から選ばれる基であることが好ましい。
また、一般式(4a)の末端構造は、水素原子、メルカプト基、アミノ基、ビニル基、カルボキシ基、オキセタニル基、スルホ基、及びホスホン酸基から選ばれる基であることが好ましい。
上記RSL及びRdがアルキル基の場合、好ましくは炭素数1~10、より好ましくは炭素数1~5、さらに好ましくは炭素数1~3のアルキル基であり、メチルであることが特に好ましい。
上記RSLがアリール基の場合、その炭素数は6~20が好ましく、6~15がより好ましく、6~12がさらに好ましく、さらに好ましくはフェニル基である。
上記RSLがアリール基の場合、その炭素数は6~20が好ましく、6~15がより好ましく、6~12がさらに好ましく、さらに好ましくはフェニル基である。
上記LAが2価の連結基の場合、アルキレン基(好ましくは炭素数1~10、より好ましくは炭素数1~5のアルキレン基)、アリーレン基(好ましくは炭素数6~20、より好ましくは炭素数6~15のアリーレン基、さらに好ましくはフェニレン基)又は-Si(RSL)2-O-が好ましい(RSLは一般式(2a)のRSLと同義であり、好ましい形態も同じである。-Si(RSL)2-O-中の「O」が、上記一般式に示されたSiと連結する)。
上記(a)の構造は、上記一般式(1a)~(3a)のいずれかで表される構造の他に、下記式(5a)で表される繰り返し単位を有することが好ましい。
上記式(5a)で表される繰り返し単位は、シロキサン化合物層中において、上記式(5a)で表される繰り返し単位同士が互いにシロキサン結合で連結した構造をとって存在することも好ましい。
保護層を構成するシロキサン化合物層中、上記式(5a)で表される繰り返し単位の含有率は、0.01~0.55であることが好ましく、0.03~0.40であることがより好ましく、さらに好ましくは0.05~0.25である。
式(5a)で表される繰り返し単位の含有率は、2.5cm四方に切り出したシロキサン化合物層を測定用試料とし、この測定用試料をX線光電子分光法(装置:Ulvac-PHI社製QuantraSXM)により、X線源:Al-Kα線(1490eV,25W,100umφ)、測定領域:300μm×300μm、Pass Energy 55eV、 Step 0.05eVの条件で、Si2p(98~104eV付近)を測定し、T成分(103eV)とQ成分(104eV)のピークを分離・定量し、比較することで求められる。すなわち、式(5a)で表される繰り返し単位(Q成分)のSi-O結合エネルギーピークの蛍光X線強度[SA]と、式(5a)で表される繰り返し単位以外の構造(T成分)のSi-O結合エネルギーピークの強度の合計[ST]に基づき[SA]/([SA]+[ST])を算出し、式(5a)で表される繰り返し単位の含有率とする。
式(5a)で表される繰り返し単位の含有率は、2.5cm四方に切り出したシロキサン化合物層を測定用試料とし、この測定用試料をX線光電子分光法(装置:Ulvac-PHI社製QuantraSXM)により、X線源:Al-Kα線(1490eV,25W,100umφ)、測定領域:300μm×300μm、Pass Energy 55eV、 Step 0.05eVの条件で、Si2p(98~104eV付近)を測定し、T成分(103eV)とQ成分(104eV)のピークを分離・定量し、比較することで求められる。すなわち、式(5a)で表される繰り返し単位(Q成分)のSi-O結合エネルギーピークの蛍光X線強度[SA]と、式(5a)で表される繰り返し単位以外の構造(T成分)のSi-O結合エネルギーピークの強度の合計[ST]に基づき[SA]/([SA]+[ST])を算出し、式(5a)で表される繰り返し単位の含有率とする。
本発明において、保護層であるシロキサン化合物層の厚さは10~3000nmであることが好ましく、100~1500nmであることがより好ましい。
(ガス分離膜の用途と特性)
本発明のガス分離膜(複合膜及び非対称膜)は、ガス分離回収法、ガス分離精製法として好適に用いることができる。例えば、水素、ヘリウム、一酸化炭素、二酸化炭素、硫化水素、酸素、窒素、アンモニア、硫黄酸化物、窒素酸化物、メタン、エタン及びブタンなどの炭化水素、プロピレンなどの不飽和炭化水素、テトラフルオロエタンなどのパーフルオロ化合物などのガスを含有する気体混合物から特定の気体を効率よく分離し得るガス分離膜とすることができる。特に二酸化炭素及び炭化水素(メタン)を含む気体混合物から二酸化炭素を選択的に透過して分離するガス分離膜とすることが好ましい。
本発明のガス分離膜(複合膜及び非対称膜)は、ガス分離回収法、ガス分離精製法として好適に用いることができる。例えば、水素、ヘリウム、一酸化炭素、二酸化炭素、硫化水素、酸素、窒素、アンモニア、硫黄酸化物、窒素酸化物、メタン、エタン及びブタンなどの炭化水素、プロピレンなどの不飽和炭化水素、テトラフルオロエタンなどのパーフルオロ化合物などのガスを含有する気体混合物から特定の気体を効率よく分離し得るガス分離膜とすることができる。特に二酸化炭素及び炭化水素(メタン)を含む気体混合物から二酸化炭素を選択的に透過して分離するガス分離膜とすることが好ましい。
とりわけ、分離処理されるガスが二酸化炭素とメタンとの混合ガスである場合においては、40℃、5MPaにおける二酸化炭素の透過速度が20GPU以上であることが好ましく、30GPU以上であることがより好ましく、35~500GPUであることがより好ましい。二酸化炭素とメタンとの透過速度比(RCO2/RCH4)は15以上であることが好ましく、20以上であることがより好ましく、23以上であることがさらに好ましく、25~50であることが特に好ましい。RCO2は二酸化炭素の透過速度、RCH4はメタンの透過速度を示す。
なお、1GPUは1×10-6cm3(STP)/cm2・sec・cmHgであり、STPは、Standard Temperature and Pressureを意味し、GPUは、Gas Permeation Unit を意味する。
なお、1GPUは1×10-6cm3(STP)/cm2・sec・cmHgであり、STPは、Standard Temperature and Pressureを意味し、GPUは、Gas Permeation Unit を意味する。
(その他の成分等)
本発明のガス分離膜のガス分離層には、膜物性を調整するため、各種高分子化合物を添加することもできる。高分子化合物としては、アクリル系重合体、ポリウレタン樹脂、ポリアミド樹脂、ポリエステル樹脂、エポキシ樹脂、フェノール樹脂、ポリカーボネート樹脂、ポリビニルブチラール樹脂、ポリビニルホルマール樹脂、シェラック、ビニル系樹脂、アクリル系樹脂、ゴム系樹脂、ワックス類、その他の天然樹脂等が使用できる。また、これらは2種以上併用してもよい。
また、液物性調整のためにノニオン性界面活性剤、カチオン性界面活性剤や、有機フルオロ化合物などを添加することもできる。
本発明のガス分離膜のガス分離層には、膜物性を調整するため、各種高分子化合物を添加することもできる。高分子化合物としては、アクリル系重合体、ポリウレタン樹脂、ポリアミド樹脂、ポリエステル樹脂、エポキシ樹脂、フェノール樹脂、ポリカーボネート樹脂、ポリビニルブチラール樹脂、ポリビニルホルマール樹脂、シェラック、ビニル系樹脂、アクリル系樹脂、ゴム系樹脂、ワックス類、その他の天然樹脂等が使用できる。また、これらは2種以上併用してもよい。
また、液物性調整のためにノニオン性界面活性剤、カチオン性界面活性剤や、有機フルオロ化合物などを添加することもできる。
界面活性剤の具体例としては、アルキルベンゼンスルホン酸塩、アルキルナフタレンスルホン酸塩、高級脂肪酸塩、高級脂肪酸エステルのスルホン酸塩、高級アルコールエーテルの硫酸エステル塩、高級アルコールエーテルのスルホン酸塩、高級アルキルスルホンアミドのアルキルカルボン酸塩、アルキルリン酸塩などのアニオン界面活性剤、ポリオキシエチレンアルキルエーテル、ポリオキシエチレンアルキルフェニルエーテル、ポリオキシエチレン脂肪酸エステル、ソルビタン脂肪酸エステル、アセチレングリコールのエチレンオキサイド付加物、グリセリンのエチレンオキサイド付加物、ポリオキシエチレンソルビタン脂肪酸エステルなどの非イオン性界面活性剤、また、この他にもアルキルベタインやアミドベタインなどの両性界面活性剤、シリコン系界面活性剤、フッソ系界面活性剤などを含めて、従来公知である界面活性剤及びその誘導体から適宜選ぶことができる。
また、高分子分散剤を含んでいてもよく、この高分子分散剤として、具体的にはポリビニルピロリドン、ポリビニルアルコール、ポリビニルメチルエーテル、ポリエチレンオキシド、ポリエチレングリコール、ポリプロピレングリコール、ポリアクリルアミド等が挙げられ、中でもポリビニルピロリドンを用いることが好ましい。
本発明のガス分離膜を形成する条件に特に制限はないが、温度は-30~100℃が好ましく、-10~80℃がより好ましく、5~50℃が特に好ましい。
本発明においては、膜の形成時に空気や酸素などの気体を共存させてもよいが、不活性ガス雰囲気下であることが望ましい。
本発明のガス分離膜において、ガス分離層中のポリイミド化合物の含有量は、所望のガス分離性能が得られれば特に制限はない。ガス分離性能をより向上させる観点から、ガス分離層中のポリイミド化合物の含有量は、20質量%以上であることが好ましく、40質量%以上であることがより好ましく、60質量%以上であることが好ましく、70質量%以上であることがさらに好ましい。また、ガス分離層中のポリイミド化合物の含有量は、100質量%であってもよいが、通常は99質量%以下である。
本発明のガス分離膜において、ガス分離層中のポリイミド化合物の含有量は、所望のガス分離性能が得られれば特に制限はない。ガス分離性能をより向上させる観点から、ガス分離層中のポリイミド化合物の含有量は、20質量%以上であることが好ましく、40質量%以上であることがより好ましく、60質量%以上であることが好ましく、70質量%以上であることがさらに好ましい。また、ガス分離層中のポリイミド化合物の含有量は、100質量%であってもよいが、通常は99質量%以下である。
[ガス混合物の分離方法]
本発明のガス分離方法では、二酸化炭素及びメタンを含む混合ガスから二酸化炭素を選択的に透過させることを含む方法である。ガス分離の際の圧力は0.5~10MPaであることが好ましく、1~10MPaであることがより好ましく、2~7MPaであることがさらに好ましい。また、ガス分離温度は、-30~90℃であることが好ましく、15~70℃であることがさらに好ましい。二酸化炭素とメタンとを含む混合ガスにおいて、二酸化炭素とメタンの混合比に特に制限はないが、二酸化炭素:メタン=1:99~99:1(体積比)であることが好ましく、二酸化炭素:メタン=5:95~90:10であることがより好ましい。
本発明のガス分離方法では、二酸化炭素及びメタンを含む混合ガスから二酸化炭素を選択的に透過させることを含む方法である。ガス分離の際の圧力は0.5~10MPaであることが好ましく、1~10MPaであることがより好ましく、2~7MPaであることがさらに好ましい。また、ガス分離温度は、-30~90℃であることが好ましく、15~70℃であることがさらに好ましい。二酸化炭素とメタンとを含む混合ガスにおいて、二酸化炭素とメタンの混合比に特に制限はないが、二酸化炭素:メタン=1:99~99:1(体積比)であることが好ましく、二酸化炭素:メタン=5:95~90:10であることがより好ましい。
[ガス分離モジュール及びガス分離装置]
本発明のガス分離膜を用いてガス分離モジュールを調製することができる。モジュールの例としては、スパイラル型、中空糸型、プリーツ型、管状型、プレート&フレーム型などが挙げられる。
また、本発明のガス分離複合膜又はガス分離モジュールを用いて、ガスを分離回収又は分離精製させるための手段を有する気体分離装置を得ることができる。本発明のガス分離複合膜は、例えば、特開2007-297605号公報に記載のような吸収液と併用した膜・吸収ハイブリッド法としての気体分離回収装置に適用してもよい。
本発明のガス分離膜を用いてガス分離モジュールを調製することができる。モジュールの例としては、スパイラル型、中空糸型、プリーツ型、管状型、プレート&フレーム型などが挙げられる。
また、本発明のガス分離複合膜又はガス分離モジュールを用いて、ガスを分離回収又は分離精製させるための手段を有する気体分離装置を得ることができる。本発明のガス分離複合膜は、例えば、特開2007-297605号公報に記載のような吸収液と併用した膜・吸収ハイブリッド法としての気体分離回収装置に適用してもよい。
以下に実施例に基づき本発明を更に詳細に説明するが、本発明はこれらの実施例により限定されるものではない。下記実施例において、各構造式中のMeはメチルを示す。
[合成例]
<ポリイミド(P-1)の合成>
<ポリイミド(P-1)の合成>
(中間体1-1の合成)
ジアミノメシチレンスルホン酸(和光純薬工業社製)(60g)、アセトニトリル(和光純薬工業社製)(380g)、ピリジン(和光純薬工業社製)(23g)を1Lフラスコに入れた。そこに、氷冷下、トリフルオロ酢酸無水物(和光純薬工業社製)(115g)を慎重に滴下した後、70℃で2時間反応させた。反応溶液を冷却後、メタノール(和光純薬工業社製)(30g)を加え、1時間攪拌した。減圧濃縮後、塩酸を用いて精製し、中間体1-1(110g)得た。
ジアミノメシチレンスルホン酸(和光純薬工業社製)(60g)、アセトニトリル(和光純薬工業社製)(380g)、ピリジン(和光純薬工業社製)(23g)を1Lフラスコに入れた。そこに、氷冷下、トリフルオロ酢酸無水物(和光純薬工業社製)(115g)を慎重に滴下した後、70℃で2時間反応させた。反応溶液を冷却後、メタノール(和光純薬工業社製)(30g)を加え、1時間攪拌した。減圧濃縮後、塩酸を用いて精製し、中間体1-1(110g)得た。
(中間体1-2の合成)
アセトニトリル(和光純薬工業社製)(440mL)、中間体1-1(68g)を1Lフラスコに入れた。塩化チオニル(和光純薬工業社製)(115g)、ジメチルホルムアミド(和光純薬工業社製)(0.9g)を慎重に加えた後、発熱、発泡に注意しながら内温を70℃まで上昇させた。減圧留去後、反応混合物を氷に注ぎ、精製し中間体1-2(65g)を得た。
アセトニトリル(和光純薬工業社製)(440mL)、中間体1-1(68g)を1Lフラスコに入れた。塩化チオニル(和光純薬工業社製)(115g)、ジメチルホルムアミド(和光純薬工業社製)(0.9g)を慎重に加えた後、発熱、発泡に注意しながら内温を70℃まで上昇させた。減圧留去後、反応混合物を氷に注ぎ、精製し中間体1-2(65g)を得た。
(中間体1-3の合成)
4-アミノ安息香酸(Sigma-Aldrich社製)(19g)、ピリジン(和光純薬工業社製)
(29mL)、アセトニトリル(和光純薬工業社製)(120mL)を500mLフラスコに入れた。そこに、氷冷下、中間体1-2(53g)を慎重に加えた。60℃で6時間攪拌した後、攪拌後の溶液に塩酸(和光純薬工業社製)と酢酸エチル(和光純薬工業社製)を加えて分液し、有機層を減圧濃縮、精製して中間体1-3(84g)を得た。
4-アミノ安息香酸(Sigma-Aldrich社製)(19g)、ピリジン(和光純薬工業社製)
(29mL)、アセトニトリル(和光純薬工業社製)(120mL)を500mLフラスコに入れた。そこに、氷冷下、中間体1-2(53g)を慎重に加えた。60℃で6時間攪拌した後、攪拌後の溶液に塩酸(和光純薬工業社製)と酢酸エチル(和光純薬工業社製)を加えて分液し、有機層を減圧濃縮、精製して中間体1-3(84g)を得た。
(ジアミン1の合成)
中間体1-3(60g)、メタノール(和光純薬工業社製)(200g)を500mLフラスコに入れた。メタンスルホン酸(和光純薬工業社製)(60g)を慎重に加え、発熱に注意しながら昇温し、120℃で30分間攪拌した。反応溶液を、冷却した後、炭酸カリウム溶液に注ぎ、次いで、カラムクロマトグラフィー(展開溶媒:メタノール)により精製してジアミン1(25g)を得た。
中間体1-3(60g)、メタノール(和光純薬工業社製)(200g)を500mLフラスコに入れた。メタンスルホン酸(和光純薬工業社製)(60g)を慎重に加え、発熱に注意しながら昇温し、120℃で30分間攪拌した。反応溶液を、冷却した後、炭酸カリウム溶液に注ぎ、次いで、カラムクロマトグラフィー(展開溶媒:メタノール)により精製してジアミン1(25g)を得た。
(ポリイミド(P-1)の合成)
1-メチルー2-ピロリドン(和光純薬工業社製)(60g)、ジアミン1(8.80g)、4,4’-(ヘキサフルオロイソプロピリデン)ジフタル酸無水物(6FDA、東京化成工業社製)(12.44g)を200mLフラスコに入れた。そこに、トルエン(和光純薬工業社製)(10g)を加えた後、180℃まで加熱し、6時間反応させた。反応溶液を冷却後、アセトン(和光純薬工業社製)で希釈し、次いで、イソプロピルアルコール(和光純薬工業社製)を加えてポリマーを固体として得た。得られたポリマーをアセトンで溶解し、イソプロピルアルコールで再沈殿する操作を2回繰り返した後、80℃で乾燥し、ポリイミド(P-1)(18g)を得た。
1-メチルー2-ピロリドン(和光純薬工業社製)(60g)、ジアミン1(8.80g)、4,4’-(ヘキサフルオロイソプロピリデン)ジフタル酸無水物(6FDA、東京化成工業社製)(12.44g)を200mLフラスコに入れた。そこに、トルエン(和光純薬工業社製)(10g)を加えた後、180℃まで加熱し、6時間反応させた。反応溶液を冷却後、アセトン(和光純薬工業社製)で希釈し、次いで、イソプロピルアルコール(和光純薬工業社製)を加えてポリマーを固体として得た。得られたポリマーをアセトンで溶解し、イソプロピルアルコールで再沈殿する操作を2回繰り返した後、80℃で乾燥し、ポリイミド(P-1)(18g)を得た。
1H NMR(400MHz,DMSO-d6):δ=12.79(brs,1H),11.17(brs,1H),8.19(d,2H),7.92(brs,4H),7.82(d,2H),7.06(d,2H),2.50(s,6H),1.99(s,3H)
<ポリイミド(P-2)の合成>
上記ポリイミド(P-1)の合成において、4-アミノ安息香酸に代えて4-トリフルオロメチルアニリンを用いた以外は上記ポリイミド(P-1)の合成と同様にして、下記繰り返し単位からなるポリイミド(P-2)を得た。
上記ポリイミド(P-1)の合成において、4-アミノ安息香酸に代えて4-トリフルオロメチルアニリンを用いた以外は上記ポリイミド(P-1)の合成と同様にして、下記繰り返し単位からなるポリイミド(P-2)を得た。
<ポリイミド(P-3)の合成>
(中間体3-1の合成)
上記中間体1-1の合成において、ジアミノメシチレンスルホン酸に代えて4,4’-メチレンビス(2-エチル-6-メチルアニリン)を用いた以外は上記中間体1-1の合成と同様にして、中間体3-1を得た。
上記中間体1-1の合成において、ジアミノメシチレンスルホン酸に代えて4,4’-メチレンビス(2-エチル-6-メチルアニリン)を用いた以外は上記中間体1-1の合成と同様にして、中間体3-1を得た。
(中間体3-2の合成)
クロロホルム(和光純薬工業社製)(300mL)、中間体3-1(67g)を1Lフラスコに入れた。そこに、氷冷下、クロロスルホン酸(和光純薬工業社製)(79g)を慎重に滴下した後、発熱、発泡に注意しながら内温を50℃まで上昇させた。冷却後、反応混合物を氷に注ぎ、吸引ろ過し、水で洗浄することにより中間体3-2(59g)を得た。
クロロホルム(和光純薬工業社製)(300mL)、中間体3-1(67g)を1Lフラスコに入れた。そこに、氷冷下、クロロスルホン酸(和光純薬工業社製)(79g)を慎重に滴下した後、発熱、発泡に注意しながら内温を50℃まで上昇させた。冷却後、反応混合物を氷に注ぎ、吸引ろ過し、水で洗浄することにより中間体3-2(59g)を得た。
(中間体3-3~ポリイミドP-3の合成)
中間体3-2を用いたこと以外は、上記ポリイミド(P-1)の合成と同様にして、ポリイミド(P-3)を得た。
中間体3-2を用いたこと以外は、上記ポリイミド(P-1)の合成と同様にして、ポリイミド(P-3)を得た。
<ポリイミド(P-4)の合成>
上記ポリイミド(P-2)の合成において、6FDAに代えてピロメリット酸無水物を用いた以外は上記ポリイミド(P-2)の合成と同様にして、ポリイミド(P-4)を得た。
上記ポリイミド(P-2)の合成において、6FDAに代えてピロメリット酸無水物を用いた以外は上記ポリイミド(P-2)の合成と同様にして、ポリイミド(P-4)を得た。
<ポリイミド(P-5)の合成>
(中間体5-1の合成)
上記中間体3-2の合成において、中間体3-1に代えて9-フルオレノンを用いた以外は上記中間体3-2の合成と同様にして、中間体5-1を得た。
上記中間体3-2の合成において、中間体3-1に代えて9-フルオレノンを用いた以外は上記中間体3-2の合成と同様にして、中間体5-1を得た。
(中間体5-2の合成)
アンモニア水(和光純薬工業社製)(90g)を500mLフラスコに入れた。そこに、氷冷下、中間体5-1(27g)をテトラヒドロフラン(和光純薬工業社製)(130g)に懸濁させた液を慎重に加えた。混合液を40℃で2時間攪拌した後、減圧濃縮し、吸引ろ過、水でかけ洗いして中間体5-2(21g)を得た。
アンモニア水(和光純薬工業社製)(90g)を500mLフラスコに入れた。そこに、氷冷下、中間体5-1(27g)をテトラヒドロフラン(和光純薬工業社製)(130g)に懸濁させた液を慎重に加えた。混合液を40℃で2時間攪拌した後、減圧濃縮し、吸引ろ過、水でかけ洗いして中間体5-2(21g)を得た。
(ジアミン5の合成)
中間体5-2(19.4g)、3-アミノ-o-クレゾール(東京化成工業社製)(9.2g)、3-メルカプトプロピオン酸(和光純薬工業社製)(318.4mg)、トルエン(75mL)を500mLフラスコに入れた。そこに、室温下、メタンスルホン酸(和光純薬工業社製)(108.1g)を慎重に滴下した後、120℃で3時間反応させた。冷却後、反応溶液を水(375mL)とNaHCO3(95g)をいれたビーカーに注ぎ、酢酸エチル(600mL)を加えた。有機層を分液し減圧濃縮し、得られた固体をヘキサンで洗浄することで黄色固体(28.2g)を得た。カラムクロマトグラフィー(ヘキサン/酢酸エチル=50/50(v/v))で精製することでジアミン(16.5g)を得た。
中間体5-2(19.4g)、3-アミノ-o-クレゾール(東京化成工業社製)(9.2g)、3-メルカプトプロピオン酸(和光純薬工業社製)(318.4mg)、トルエン(75mL)を500mLフラスコに入れた。そこに、室温下、メタンスルホン酸(和光純薬工業社製)(108.1g)を慎重に滴下した後、120℃で3時間反応させた。冷却後、反応溶液を水(375mL)とNaHCO3(95g)をいれたビーカーに注ぎ、酢酸エチル(600mL)を加えた。有機層を分液し減圧濃縮し、得られた固体をヘキサンで洗浄することで黄色固体(28.2g)を得た。カラムクロマトグラフィー(ヘキサン/酢酸エチル=50/50(v/v))で精製することでジアミン(16.5g)を得た。
(ポリイミド(P-5a)の合成)
上記ポリイミド(P-1)の合成において、ジアミン1に代えてジアミン5を用い、6FDAに代えてピロメリット酸無水物を用いた以外は上記ポリイミド(P-1)の合成と同様にして、ポリイミド(P-5a)を得た。
上記ポリイミド(P-1)の合成において、ジアミン1に代えてジアミン5を用い、6FDAに代えてピロメリット酸無水物を用いた以外は上記ポリイミド(P-1)の合成と同様にして、ポリイミド(P-5a)を得た。
(ポリイミド(P-5)の合成)
ポリイミド(P-5a)(2.0g)、塩化亜鉛(和光純薬工業社製)(40.9mg)、無水酢酸(和光純薬工業社製)(15.0mL)を50mLフラスコに入れた。50℃まで加熱し、4時間反応させた。反応溶液を冷却後、アセトン(和光純薬工業社製)で希釈した後、そこにイソプロピルアルコール(和光純薬工業社製)を加えてポリマーを固体として得た。得られたポリマーをアセトンで溶解し、イソプロピルアルコールで再沈殿する操作を2回繰り返した後、80℃で乾燥し、ポリイミド(P-5)(2.1g)を得た。
ポリイミド(P-5a)(2.0g)、塩化亜鉛(和光純薬工業社製)(40.9mg)、無水酢酸(和光純薬工業社製)(15.0mL)を50mLフラスコに入れた。50℃まで加熱し、4時間反応させた。反応溶液を冷却後、アセトン(和光純薬工業社製)で希釈した後、そこにイソプロピルアルコール(和光純薬工業社製)を加えてポリマーを固体として得た。得られたポリマーをアセトンで溶解し、イソプロピルアルコールで再沈殿する操作を2回繰り返した後、80℃で乾燥し、ポリイミド(P-5)(2.1g)を得た。
1H NMR(400MHz,DMSO-d6):δ=12.56(brs,1H),8.54(brs,2H),8.24(d,1H),8.15(m,1H),7.62(s,1H),7.52(brs,1H),7.40(m,2H),7.28(d,1H),6.97(d,2H),6.28(d,2H),2.37(s,6H),2.02(s,3H)
<ポリイミド(P-6)の合成>
上記ポリイミド(P-5)の合成において、ピロメリット酸無水物に代えて4,4’-ビフタル酸無水物を用いた以外は上記ポリイミド(P-5)の合成と同様にして、ポリイミド(P-6)を得た。
上記ポリイミド(P-5)の合成において、ピロメリット酸無水物に代えて4,4’-ビフタル酸無水物を用いた以外は上記ポリイミド(P-5)の合成と同様にして、ポリイミド(P-6)を得た。
ポリイミド(P-6)
1H NMR(400MHz,DMSO-d6):δ=12.55(brs,1H),8.49(s,1H),8.41(brs,1H),8.19(m,3H),7.63(s,1H),7.52(brs,1H),7.40(m,2H),7.29(d,1H),6.97(d,2H),6.28(d,2H),2.37(s,6H),2.03(s,3H)
<ポリイミド(P-7)の合成>
上記中間体1-3の合成と同様にして、中間体5-1と3,4,5-トリフルオロアニリンとを反応させて中間体7-1を得た後、上記ポリイミド(P-5)の合成と同様にして、ポリイミド(P-7)を得た。
<ポリイミド(P-8)、(P-9)及び(P-10)の合成>
用いる原料を下記ポリイミドの構造と対応したものに変更したこと以外は、上記ポリイミド(P-1)の合成と同様にして、ポリイミド(P-8)、(P-9)及び(P-10)を得た。
用いる原料を下記ポリイミドの構造と対応したものに変更したこと以外は、上記ポリイミド(P-1)の合成と同様にして、ポリイミド(P-8)、(P-9)及び(P-10)を得た。
<ポリイミド(P-11)の合成>
(ポリイミド(P-11a)の合成)
上記ポリイミド(P-1)の合成において、4-アミノ安息香酸に代えて4-アミノフェノールを用いた以外は上記ポリイミド(P-1)の合成と同様にして、ポリイミド(P-11a)を得た。
上記ポリイミド(P-1)の合成において、4-アミノ安息香酸に代えて4-アミノフェノールを用いた以外は上記ポリイミド(P-1)の合成と同様にして、ポリイミド(P-11a)を得た。
(ポリイミド(P-11)の合成)
テトラヒドロフラン(和光純薬工業社製)(144mL)、ポリイミド(P-11a)(13.7g)を300mLフラスコに入れた。そこへ、トリフルオロ酢酸無水物(和光純薬工業社製)(12.7mL)、トリエチルアミン(和光純薬工業社製)(9.1g)を加えた後、室温で6時間反応させた。反応溶液をアセトン(和光純薬工業社製)で希釈した後、そこにメタノール(和光純薬工業社製)を加えてポリマーを固体として得た。得られたポリマーをアセトンで溶解し、イソプロピルアルコールで再沈殿する操作を2回繰り返した後、80℃で乾燥し、ポリイミド(P-11)(6.8g)を得た。
テトラヒドロフラン(和光純薬工業社製)(144mL)、ポリイミド(P-11a)(13.7g)を300mLフラスコに入れた。そこへ、トリフルオロ酢酸無水物(和光純薬工業社製)(12.7mL)、トリエチルアミン(和光純薬工業社製)(9.1g)を加えた後、室温で6時間反応させた。反応溶液をアセトン(和光純薬工業社製)で希釈した後、そこにメタノール(和光純薬工業社製)を加えてポリマーを固体として得た。得られたポリマーをアセトンで溶解し、イソプロピルアルコールで再沈殿する操作を2回繰り返した後、80℃で乾燥し、ポリイミド(P-11)(6.8g)を得た。
1H NMR(400MHz,DMSO-d6):δ=9.43(brs,1H),8.17(d,2H),7.89(brs,4H),7.14(d,2H),6.80(d,2H),2.50(s,6H),1.99(s,3H)
<ポリイミド(P-12)(x:y=31:69(モル比))の合成>
(ポリイミド(P-12a)の合成)
上記ポリイミド(P-1)の合成において、中間体1-2に、上記中間体5-2の合成と同様にしてアンモニア水を作用させて中間体12-1を得た後、上記ポリイミド(P-1)の合成と同様にして、ポリイミド(P-12a)を得た。
上記ポリイミド(P-1)の合成において、中間体1-2に、上記中間体5-2の合成と同様にしてアンモニア水を作用させて中間体12-1を得た後、上記ポリイミド(P-1)の合成と同様にして、ポリイミド(P-12a)を得た。
(ポリイミド(P-12)(x:y=31:69(モル比))の合成)
1-メチル-2-ピロリドン(和光純薬工業社製)(20mL)、ポリイミド(P-12a)(3.2g)を100mLフラスコに入れた。3,5-ビス(トリフルオロメチル)ベンゾイルクロリド(東京化成工業社製)(1.8mL)、トリエチルアミン(和光純薬工業社製)(1.0g)を加えた後、80℃で6時間反応させた。反応溶液をアセトン(和光純薬工業社製)で希釈した後、そこにメタノール(和光純薬工業社製)を加えてポリマーを固体として得た。得られたポリマーをアセトンで溶解し、イソプロピルアルコールで再沈殿する操作を2回繰り返した後、80℃で乾燥し、ポリイミド(P-12)(2.8g)を得た。
1-メチル-2-ピロリドン(和光純薬工業社製)(20mL)、ポリイミド(P-12a)(3.2g)を100mLフラスコに入れた。3,5-ビス(トリフルオロメチル)ベンゾイルクロリド(東京化成工業社製)(1.8mL)、トリエチルアミン(和光純薬工業社製)(1.0g)を加えた後、80℃で6時間反応させた。反応溶液をアセトン(和光純薬工業社製)で希釈した後、そこにメタノール(和光純薬工業社製)を加えてポリマーを固体として得た。得られたポリマーをアセトンで溶解し、イソプロピルアルコールで再沈殿する操作を2回繰り返した後、80℃で乾燥し、ポリイミド(P-12)(2.8g)を得た。
1H NMR(400MHz,DMSO-d6):δ=8.51(brs,2H*0.31),8.19(brs,2H+1H*0.31),7.95(brs,4H),7.75(brs,2H*0.69),2.50(s,6H),1.99(s,3H)
<ポリイミド(P-13)の合成>
上記ポリイミド(P-1)の合成において、4-アミノ安息香酸に代えてイミノ二酢酸を用いた以外は上記ポリイミド(P-1)の合成と同様にして、ポリイミド(P-13)を得た。
ポリイミド(P-13)
1H NMR(400MHz,DMSO-d6):δ=8.19(brs,2H),7.95(brs,4H),2.90(s,4H),2.44(s,6H),1.99(s,3H)
<比較ポリイミド(C-1)>
上記ポリイミド(P-1)の合成において、ジアミン1に代えて、ジアミン1と同モル量のジアミノメシチレンスルホン酸(和光純薬工業社製)を用い、更に、トリエチルアミン(4.41g)を添加し、ポリマーの精製時、塩酸を用いた以外は、上記ポリイミド(P-1)の合成と同様にして、比較ポリイミド(C-1)(13g)を合成した。
上記ポリイミド(P-1)の合成において、ジアミン1に代えて、ジアミン1と同モル量のジアミノメシチレンスルホン酸(和光純薬工業社製)を用い、更に、トリエチルアミン(4.41g)を添加し、ポリマーの精製時、塩酸を用いた以外は、上記ポリイミド(P-1)の合成と同様にして、比較ポリイミド(C-1)(13g)を合成した。
比較ポリイミド(C-1)
<比較ポリイミド(C-2)>
2,3,5,6-テトラメチル-1,4-フェニレンジアミン(2.97g)、N-メチルピロリドン(50mL)を300mLフラスコに入れた。そこへ、氷冷下、4,4'-カルボニルジフタル酸無水物(東京化成工業社製)(5.83g)を添加し、N-メチルピロリドン(6mL)で洗い込んだ。混合物を40℃で5時間攪拌した後、そこにピリジン(和光純薬工業社製)(0.43g)、無水酢酸(和光純薬工業社製)(6.10g)を加え、反応溶液を80℃まで昇温させ、3時間攪拌した。攪拌後の溶液を冷却し、アセトンを加えた後、メタノールを加え、比較ポリマー(C-2)を粉体として析出させた。メタノール洗浄を2回繰り返した後、40℃で乾燥し、比較ポリイミド(C-2)(8.09g)を得た。
2,3,5,6-テトラメチル-1,4-フェニレンジアミン(2.97g)、N-メチルピロリドン(50mL)を300mLフラスコに入れた。そこへ、氷冷下、4,4'-カルボニルジフタル酸無水物(東京化成工業社製)(5.83g)を添加し、N-メチルピロリドン(6mL)で洗い込んだ。混合物を40℃で5時間攪拌した後、そこにピリジン(和光純薬工業社製)(0.43g)、無水酢酸(和光純薬工業社製)(6.10g)を加え、反応溶液を80℃まで昇温させ、3時間攪拌した。攪拌後の溶液を冷却し、アセトンを加えた後、メタノールを加え、比較ポリマー(C-2)を粉体として析出させた。メタノール洗浄を2回繰り返した後、40℃で乾燥し、比較ポリイミド(C-2)(8.09g)を得た。
比較ポリイミド(C-2)
[実施例1] ガス分離複合膜の作製
<平滑層付PAN(ポリアクリロニトリル)多孔質層の作製>
(ジアルキルシロキサン基を有する放射線硬化性ポリマーの調製)
150mLの3口フラスコに、39gのUV9300(Momentive社製)、10gのX-22-162C(信越化学工業社製)およびDBU(1,8-ジアザビシクロ[5.4.0]ウンデカ-7-エン)0.007gを加え、n-ヘプタン50gに溶解させた。これを95℃で168時間維持させて、ポリ(シロキサン)基を有する放射線硬化性ポリマー溶液(25℃で粘度22.8mPa・s)を得た。
<平滑層付PAN(ポリアクリロニトリル)多孔質層の作製>
(ジアルキルシロキサン基を有する放射線硬化性ポリマーの調製)
150mLの3口フラスコに、39gのUV9300(Momentive社製)、10gのX-22-162C(信越化学工業社製)およびDBU(1,8-ジアザビシクロ[5.4.0]ウンデカ-7-エン)0.007gを加え、n-ヘプタン50gに溶解させた。これを95℃で168時間維持させて、ポリ(シロキサン)基を有する放射線硬化性ポリマー溶液(25℃で粘度22.8mPa・s)を得た。
(重合性の放射線硬化性組成物の調製)
上記放射線硬化性ポリマー溶液5gを20℃まで冷却し、n-ヘプタン95gで希釈した。得られた溶液に対し、光重合開始剤であるUV9380C(Momentive社製)0.5g及びオルガチックスTA-10(マツモトファインケミカル社製)0.1gを添加し、重合性の放射線硬化性組成物を調製した。
上記放射線硬化性ポリマー溶液5gを20℃まで冷却し、n-ヘプタン95gで希釈した。得られた溶液に対し、光重合開始剤であるUV9380C(Momentive社製)0.5g及びオルガチックスTA-10(マツモトファインケミカル社製)0.1gを添加し、重合性の放射線硬化性組成物を調製した。
(平滑層の形成)
PAN多孔質層(不織布上にポリアクリロニトリル多孔質層を有する支持体、不織布を含め、膜厚は約180μm)に、上記の重合性の放射線硬化性組成物をスピンコートした後、UV強度24kW/m、処理時間10秒間のUV処理条件でUV処理(Fusion UV System社製、Light Hammer 10、D-バルブ)を行った後、乾燥させた。このようにして、多孔質支持体上にジアルキルシロキサン基を有する厚み1μmの平滑層を形成した。
PAN多孔質層(不織布上にポリアクリロニトリル多孔質層を有する支持体、不織布を含め、膜厚は約180μm)に、上記の重合性の放射線硬化性組成物をスピンコートした後、UV強度24kW/m、処理時間10秒間のUV処理条件でUV処理(Fusion UV System社製、Light Hammer 10、D-バルブ)を行った後、乾燥させた。このようにして、多孔質支持体上にジアルキルシロキサン基を有する厚み1μmの平滑層を形成した。
<複合膜の作製>
図2に示すガス分離複合膜を作製した(図2には平滑層は図示していない)。
30ml褐色バイアル瓶に、ポリイミド(P-1)を0.08g、テトラヒドロフラン7.92gを混合して30分間攪拌した後、得られた混合液を、上記平滑層を形成した多孔質支持体上にスピンコートしてガス分離層を形成し、複合膜を得た。ポリイミド(P-1)層の厚さは約100nmであった。
なお、使用したポリアクリロニトリル多孔質層の分画分子量は100,000以下であった。また、この多孔質層の40℃、5MPaにおける二酸化炭素の透過性は、25000GPUであった。
図2に示すガス分離複合膜を作製した(図2には平滑層は図示していない)。
30ml褐色バイアル瓶に、ポリイミド(P-1)を0.08g、テトラヒドロフラン7.92gを混合して30分間攪拌した後、得られた混合液を、上記平滑層を形成した多孔質支持体上にスピンコートしてガス分離層を形成し、複合膜を得た。ポリイミド(P-1)層の厚さは約100nmであった。
なお、使用したポリアクリロニトリル多孔質層の分画分子量は100,000以下であった。また、この多孔質層の40℃、5MPaにおける二酸化炭素の透過性は、25000GPUであった。
上記で作成した複合膜のガス分離層表面に対し、下記手順で保護層を設けた。
すなわち、ビニルQレジン(Gelest製、製品番号VQM-135)(10g)、ヒドロシリルPDMS(Gelest製、製品番号HMS-301)(1g)、Karstedt触媒(Aldrich製、製品番号479527)(5mg)、ヘプタン(90g)を混合して得た混合液を、上記で作製した複合膜のガス分離層表面にスピンコートした。混合液を、80℃で5時間乾燥して硬化させることにより、ガス分離層上に、厚さ500nmのシロキサン化合物層(保護層)を有するガス分離複合膜を得た。
すなわち、ビニルQレジン(Gelest製、製品番号VQM-135)(10g)、ヒドロシリルPDMS(Gelest製、製品番号HMS-301)(1g)、Karstedt触媒(Aldrich製、製品番号479527)(5mg)、ヘプタン(90g)を混合して得た混合液を、上記で作製した複合膜のガス分離層表面にスピンコートした。混合液を、80℃で5時間乾燥して硬化させることにより、ガス分離層上に、厚さ500nmのシロキサン化合物層(保護層)を有するガス分離複合膜を得た。
[実施例2~13] 複合膜の作製
上記実施例1において、ポリイミド(P-1)をポリイミド(P-2)~(P-13)に変更したこと以外は実施例1と同様にして、実施例2~13の、保護層を有するガス分離複合膜を作製した。
上記実施例1において、ポリイミド(P-1)をポリイミド(P-2)~(P-13)に変更したこと以外は実施例1と同様にして、実施例2~13の、保護層を有するガス分離複合膜を作製した。
[比較例1及び2] ガス分離複合膜の作製
上記実施例1において、ポリイミド(P-1)を比較ポリイミド(C-1)及び(C-2)に変更したこと以外は実施例1と同様にして、比較例1及び2の、保護層を有するガス分離複合膜を作製した。なお、比較ポリマー(C-1)はメチルエチルケトンに溶解しなかったため、溶媒として、メチルエチルケトンに代えてメタノールを用いた。
上記実施例1において、ポリイミド(P-1)を比較ポリイミド(C-1)及び(C-2)に変更したこと以外は実施例1と同様にして、比較例1及び2の、保護層を有するガス分離複合膜を作製した。なお、比較ポリマー(C-1)はメチルエチルケトンに溶解しなかったため、溶媒として、メチルエチルケトンに代えてメタノールを用いた。
[試験例1] ガス分離膜のCO2透過速度及びガス分離選択性の評価-透過試験1
上記各実施例及び比較例のガス分離膜(複合膜)を用いて、ガス分離性能を以下のように評価した。
ガス分離膜を多孔質支持体(支持層)ごと直径5cmに切り取り、透過試験サンプルを作製した。GTRテック株式会社製ガス透過率測定装置を用い、透過試験サンプルのガス透過率を測定した。測定は、条件を二酸化炭素(CO2):メタン(CH4)が13:87(体積比)の混合ガスをガス供給側の全圧力が5MPa(CO2の分圧:0.3MPa)、流量500mL/min、40℃となるように調整して行った。透過してきたガスをガスクロマトグラフィーにより分析した。膜のガス透過性は、ガス透過率(Permeance)としてガス透過速度を算出することにより比較した。ガス透過率(ガス透過速度)の単位はGPU(ジーピーユー)単位〔1GPU=1×10-6cm3(STP)/cm2・sec・cmHg〕で表した。ガス分離選択性は、この膜のCH4の透過速度RCH4に対するCO2の透過速度RCO2の比率(RCO2/RCH4)として計算した。
上記の測定結果を下記評価基準に基づき評価した。
上記各実施例及び比較例のガス分離膜(複合膜)を用いて、ガス分離性能を以下のように評価した。
ガス分離膜を多孔質支持体(支持層)ごと直径5cmに切り取り、透過試験サンプルを作製した。GTRテック株式会社製ガス透過率測定装置を用い、透過試験サンプルのガス透過率を測定した。測定は、条件を二酸化炭素(CO2):メタン(CH4)が13:87(体積比)の混合ガスをガス供給側の全圧力が5MPa(CO2の分圧:0.3MPa)、流量500mL/min、40℃となるように調整して行った。透過してきたガスをガスクロマトグラフィーにより分析した。膜のガス透過性は、ガス透過率(Permeance)としてガス透過速度を算出することにより比較した。ガス透過率(ガス透過速度)の単位はGPU(ジーピーユー)単位〔1GPU=1×10-6cm3(STP)/cm2・sec・cmHg〕で表した。ガス分離選択性は、この膜のCH4の透過速度RCH4に対するCO2の透過速度RCO2の比率(RCO2/RCH4)として計算した。
上記の測定結果を下記評価基準に基づき評価した。
-ガス透過速度の評価基準-
A:60GPU以上
B:40GPU以上60GPU未満
C:20GPU以上40GPU未満
D:10GPU以上20GPU未満
E:10GPU未満
-ガス分離選択性の評価基準-
A:RCO2/RCH4が30以上
B:RCO2/RCH4が25以上30未満
C:RCO2/RCH4が20以上25未満
D:RCO2/RCH4が15以上20未満
E:RCO2/RCH4が15未満
A:60GPU以上
B:40GPU以上60GPU未満
C:20GPU以上40GPU未満
D:10GPU以上20GPU未満
E:10GPU未満
-ガス分離選択性の評価基準-
A:RCO2/RCH4が30以上
B:RCO2/RCH4が25以上30未満
C:RCO2/RCH4が20以上25未満
D:RCO2/RCH4が15以上20未満
E:RCO2/RCH4が15未満
[試験例2] 可塑化耐性試験(トルエン暴露試験)
トルエン溶媒を張ったシャーレをステンレス製容器内に入れ、そこへ、実施例及び比較例において作製したガス分離膜を入れ、密閉系とした。その後、25℃条件下で10分間保存した後、上記[試験例1]と同様に、ガス分離膜を直径5cmに切り取り、耐性試験サンプルを作製した。得られた耐性試験サンプルを用いて、上記[試験例1]と同様にしてガス分離選択性(RCO2/RCH4)を調べ、トルエン曝露前後におけるガス分離選択性の変化を可塑化耐性の指標とした。具体的には、[トルエン曝露後のガス分離選択性]/[トルエン曝露前のガス分離選択性]を算出し、得られた値(選択性維持率)を下記評価基準に当てはめ、可塑化耐性を評価した。
トルエン溶媒を張ったシャーレをステンレス製容器内に入れ、そこへ、実施例及び比較例において作製したガス分離膜を入れ、密閉系とした。その後、25℃条件下で10分間保存した後、上記[試験例1]と同様に、ガス分離膜を直径5cmに切り取り、耐性試験サンプルを作製した。得られた耐性試験サンプルを用いて、上記[試験例1]と同様にしてガス分離選択性(RCO2/RCH4)を調べ、トルエン曝露前後におけるガス分離選択性の変化を可塑化耐性の指標とした。具体的には、[トルエン曝露後のガス分離選択性]/[トルエン曝露前のガス分離選択性]を算出し、得られた値(選択性維持率)を下記評価基準に当てはめ、可塑化耐性を評価した。
-可塑化耐性の評価基準-
A:選択性維持率が0.5以上
B:選択性維持率が0.4以上0.5未満
C:選択性維持率が0.3以上0.4未満
D:選択性維持率が0.15以上0.3未満
E:選択性維持率が0.15未満
A:選択性維持率が0.5以上
B:選択性維持率が0.4以上0.5未満
C:選択性維持率が0.3以上0.4未満
D:選択性維持率が0.15以上0.3未満
E:選択性維持率が0.15未満
上記の結果を下記表1に示す。
比較ポリイミド(C-1)を用いてガス分離層を形成したガス分離膜は、ガス分離層に膜欠陥が多く生じ、ガス分離膜として機能しないものであった。また、比較ポリイミド(C-2)を用いてガス分離層を形成したガス分離膜は、ガス透過性とガス分離選択性の両特性に劣り、またトルエン曝露により可塑化しやすく耐久性に劣るものであった。
これに対し、本発明で規定するポリイミド化合物を用いてガス分離層を形成したガス分離膜は、ガス透過速度が速く、かつガス分離選択性にも高められていることがわかる。またこれらのガス分離膜は、トルエンに曝してもガス分離性能が低下しにくく、可塑化耐性にも優れることがわかった(実施例1~13)。
これに対し、本発明で規定するポリイミド化合物を用いてガス分離層を形成したガス分離膜は、ガス透過速度が速く、かつガス分離選択性にも高められていることがわかる。またこれらのガス分離膜は、トルエンに曝してもガス分離性能が低下しにくく、可塑化耐性にも優れることがわかった(実施例1~13)。
以上の結果から、本発明のガス分離膜を用いると、優れた気体分離方法、ガス分離モジュール、このガス分離モジュールを備えたガス分離装置を提供できることが分かった。
1 ガス分離層
2 多孔質層
3 不織布層
10、20 ガス分離複合膜
2 多孔質層
3 不織布層
10、20 ガス分離複合膜
Claims (18)
- ポリイミド化合物を構成材料として含むガス分離層を有するガス分離膜であって、
前記ポリイミド化合物が下記式(I)で表される繰り返し単位を含む、ガス分離膜。
式(I)中、Xaは酸素原子、窒素原子及び/もしくは硫黄原子を有する基、又は、置換基中にフッ素原子を有するアリール基を示す。Xbは水素原子又は置換基を示す。但し、式(I)中の-N(Xb)-で表される構造中にOH、NH及びSHから選ばれる構造部が含まれない場合、XaはOH、NH及びSHから選ばれる構造部を少なくとも1つ有する。
Raは下記式(I-1)~(I-28)のいずれかで表される基を示す。ここでX1~X3は単結合又は2価の基を示し、Lは、それぞれ独立に、-CH=CH-又は-CH2-を示し、R1及びR2は水素原子又は置換基を示し、*は式(I)中に示されたカルボニル基との結合部位を示す。
Rbは下記式(I-29)~(I-42)のいずれかで表される基を示す。ここでX4~X8は単結合又は2価の基を示し、Lは-CH=CH-又は-CH2-を示し、RZは、それぞれ独立に、置換基を示し、*は式(I)中に示されたイミド基との結合部位を示し、#は式(I)中に示されたスルファモイル基との結合部位を示す。dは、それぞれ独立に、0~3の整数を示し、eは、それぞれ独立に、0~4の整数を示し、fは、それぞれ独立に、0~5の整数を示し、gは0~6の整数を示し、hは、それぞれ独立に、0~7の整数を示し、jは、それぞれ独立に、0~9の整数を示し、kは0~10の整数を示す。qは、それぞれ独立に、0又は1を示す。
- 前記Rbが前記式(I-29)又は(I-34)で表される基を示す、請求項1記載のガス分離膜。
- 前記Xcがフッ素原子を少なくとも1つ有する置換基である、請求項4記載のガス分離膜。
- 前記Aa、Ab及びAcのうち少なくとも1つがアルキル基である、請求項3~7のいずれか1項記載のガス分離膜。
- 前記ポリイミド化合物中、上記式(I)で表される繰り返し単位の含有量が30~100モル%である、請求項1~8のいずれか1項に記載のガス分離膜。
- ガス透過性の支持層上に、前記ガス分離層が設けられるガス分離複合膜である、請求項1~9のいずれか1項に記載のガス分離膜。
- 前記支持層が、多孔質層と、不織布層とからなり、
前記不織布層、前記多孔質層および前記ガス分離層がこの順に設けられる、請求項10に記載のガス分離膜。 - 分離処理されるガスが二酸化炭素とメタンの混合ガスである場合において、40℃、5MPaにおける二酸化炭素の透過速度が20GPU以上であり、二酸化炭素とメタンとの透過速度比(RCO2/RCH4)が15以上である、請求項1~11のいずれか1項に記載のガス分離膜。
- 二酸化炭素及びメタンを含むガスから二酸化炭素を選択的に透過させるために用いられる、請求項1~12のいずれか1項に記載のガス分離膜。
- 請求項1~13のいずれか1項に記載のガス分離膜を具備するガス分離モジュール。
- 請求項14に記載のガス分離モジュールを備えたガス分離装置。
- 請求項1~13のいずれか1項に記載のガス分離膜を用いて、二酸化炭素及びメタンを含むガスから二酸化炭素を選択的に透過させるガス分離方法。
- 下記式(I-b)で表される繰り返し単位を含むポリイミド化合物。
式(I-b)中、Raは下記式(I-1)~(I-28)のいずれかで表される基を示す。ここでX1~X3は単結合又は2価の基を示し、Lは、それぞれ独立に、-CH=CH-又は-CH2-を示し、R1及びR2は水素原子又は置換基を示し、*は式(I-b)中に示されたカルボニル基との結合部位を示す。
Aa、Ab及びAcは水素原子又は置換基を示す。Xbは水素原子又は置換基を示す。Xcは置換基を示す。但し、式(I-b)中の-N(Xb)-で表される構造中にOH、NH及びSHから選ばれる構造部が含まれない場合、XcはOH、NH及びSHから選ばれる構造部を少なくとも1つ有する。
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018537123A JPWO2018043149A1 (ja) | 2016-08-31 | 2017-08-17 | ガス分離膜、ガス分離モジュール、ガス分離装置、ガス分離方法及びポリイミド化合物 |
| US16/281,127 US20190176081A1 (en) | 2016-08-31 | 2019-02-21 | Gas separation membrane, gas separation module, gas separation device, gas separation method, and polyimide compound |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016-168768 | 2016-08-31 | ||
| JP2016168768 | 2016-08-31 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US16/281,127 Continuation US20190176081A1 (en) | 2016-08-31 | 2019-02-21 | Gas separation membrane, gas separation module, gas separation device, gas separation method, and polyimide compound |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2018043149A1 true WO2018043149A1 (ja) | 2018-03-08 |
Family
ID=61305252
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2017/029540 WO2018043149A1 (ja) | 2016-08-31 | 2017-08-17 | ガス分離膜、ガス分離モジュール、ガス分離装置、ガス分離方法及びポリイミド化合物 |
Country Status (3)
| Country | Link |
|---|---|
| US (1) | US20190176081A1 (ja) |
| JP (1) | JPWO2018043149A1 (ja) |
| WO (1) | WO2018043149A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201510648D0 (en) * | 2015-06-17 | 2015-07-29 | Fujifilm Mfg Europe Bv | Composite membranes |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08333452A (ja) * | 1995-06-06 | 1996-12-17 | Ube Ind Ltd | 芳香族ポリイミド及び半透膜及びその製法 |
| JP2014024939A (ja) * | 2012-07-26 | 2014-02-06 | Fujifilm Corp | ポリイミド樹脂の製造方法、ガス分離膜、ガス分離モジュール、及びガス分離装置、並びにガス分離方法 |
| JP2015051407A (ja) * | 2013-09-09 | 2015-03-19 | 富士フイルム株式会社 | ガス分離複合膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 |
| JP2015083296A (ja) * | 2013-09-20 | 2015-04-30 | 富士フイルム株式会社 | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 |
-
2017
- 2017-08-17 WO PCT/JP2017/029540 patent/WO2018043149A1/ja active Application Filing
- 2017-08-17 JP JP2018537123A patent/JPWO2018043149A1/ja not_active Ceased
-
2019
- 2019-02-21 US US16/281,127 patent/US20190176081A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH08333452A (ja) * | 1995-06-06 | 1996-12-17 | Ube Ind Ltd | 芳香族ポリイミド及び半透膜及びその製法 |
| JP2014024939A (ja) * | 2012-07-26 | 2014-02-06 | Fujifilm Corp | ポリイミド樹脂の製造方法、ガス分離膜、ガス分離モジュール、及びガス分離装置、並びにガス分離方法 |
| JP2015051407A (ja) * | 2013-09-09 | 2015-03-19 | 富士フイルム株式会社 | ガス分離複合膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 |
| JP2015083296A (ja) * | 2013-09-20 | 2015-04-30 | 富士フイルム株式会社 | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2018043149A1 (ja) | 2019-03-28 |
| US20190176081A1 (en) | 2019-06-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2014087928A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| WO2015041250A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| JP6038058B2 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| US10537848B2 (en) | Gas separation asymmetric membrane, gas separation module, gas separation device, and gas separation method | |
| WO2016136404A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| JP2015073980A (ja) | ガス分離膜およびガス分離膜モジュール | |
| WO2017130604A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| US10537859B2 (en) | Gas separation membrane, gas separation module, gas separation device, gas separation method, and polyimide compound | |
| WO2017145747A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| WO2015129553A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| WO2015033772A1 (ja) | ガス分離複合膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| WO2017145432A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、ガス分離方法、ガス分離層形成用組成物、ガス分離膜の製造方法、ポリイミド化合物及びジアミンモノマー | |
| JP6355058B2 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| WO2018043149A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、ガス分離方法及びポリイミド化合物 | |
| WO2017175598A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| WO2017145728A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、ガス分離方法及びポリイミド化合物 | |
| WO2017179393A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、ガス分離方法、ガス分離膜用組成物及びガス分離膜の製造方法 | |
| WO2017145905A1 (ja) | ポリイミド化合物、ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| JP2019010631A (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| WO2017179396A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、ガス分離方法、ガス分離膜用組成物及びガス分離膜の製造方法 | |
| WO2019044215A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、ガス分離方法、及びポリイミド化合物 | |
| WO2017175695A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置及びガス分離方法 | |
| WO2016136396A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| JP2017131856A (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びガス分離方法 | |
| WO2021256237A1 (ja) | ガス分離膜、ガス分離モジュール、ガス分離装置、及びポリイミド化合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ENP | Entry into the national phase |
Ref document number: 2018537123 Country of ref document: JP Kind code of ref document: A |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 17846157 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 17846157 Country of ref document: EP Kind code of ref document: A1 |