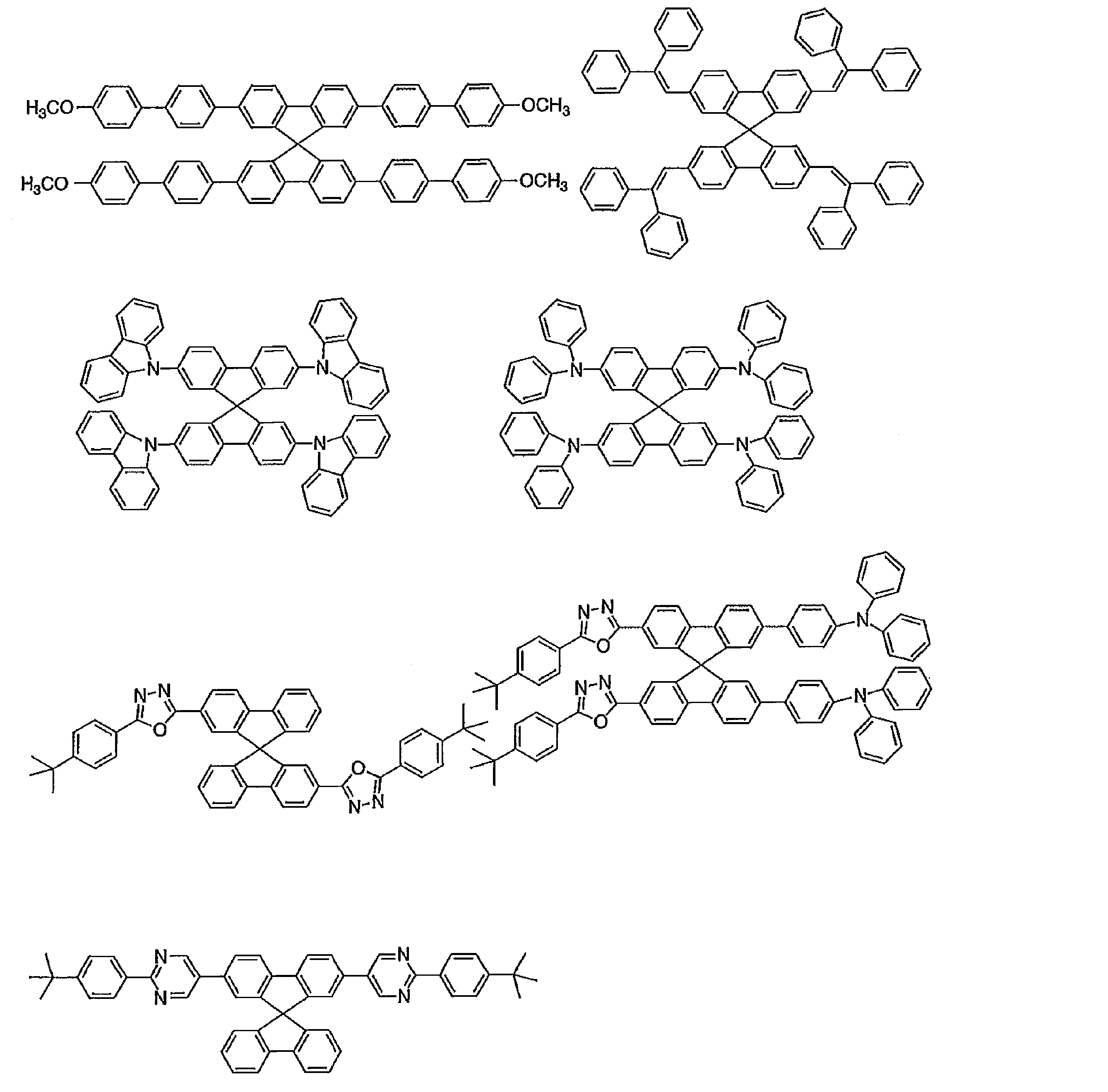WO2015016200A1 - 化合物、発光材料および有機発光素子 - Google Patents
化合物、発光材料および有機発光素子 Download PDFInfo
- Publication number
- WO2015016200A1 WO2015016200A1 PCT/JP2014/069891 JP2014069891W WO2015016200A1 WO 2015016200 A1 WO2015016200 A1 WO 2015016200A1 JP 2014069891 W JP2014069891 W JP 2014069891W WO 2015016200 A1 WO2015016200 A1 WO 2015016200A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- general formula
- group
- compound
- substituent
- represented
- Prior art date
Links
- 0 Cc(c(*)c(*)c(*)c1*)c1N(C)c1c(*)c(*)c(*)c(*)c1* Chemical compound Cc(c(*)c(*)c(*)c1*)c1N(C)c1c(*)c(*)c(*)c(*)c1* 0.000 description 7
- JTGATYXNIYQVHC-AIJYBYDHSA-N C1C=CC=CC1/C(/c1ccccc1)=C/c(cc1)cc(C23c4cc(C=C(c5ccccc5)c5ccccc5)ccc4-c4ccc(C=C(c5ccccc5)c5ccccc5)cc24)c1-c1c3cc(C=C(c2ccccc2)c2ccccc2)cc1 Chemical compound C1C=CC=CC1/C(/c1ccccc1)=C/c(cc1)cc(C23c4cc(C=C(c5ccccc5)c5ccccc5)ccc4-c4ccc(C=C(c5ccccc5)c5ccccc5)cc24)c1-c1c3cc(C=C(c2ccccc2)c2ccccc2)cc1 JTGATYXNIYQVHC-AIJYBYDHSA-N 0.000 description 1
- IOVMXJRMJURPKW-UHFFFAOYSA-N C=Cc1cccc(-[n](c(cccc2)c2c2c3)c2cc(c2ccccc22)c3[n]2-c2c(cccc3)c3ccc2)c1C=C Chemical compound C=Cc1cccc(-[n](c(cccc2)c2c2c3)c2cc(c2ccccc22)c3[n]2-c2c(cccc3)c3ccc2)c1C=C IOVMXJRMJURPKW-UHFFFAOYSA-N 0.000 description 1
- JWTJCIYHZFCEPU-IKVQWSBMSA-N CC[n]1c(ccc(/C=C/c2cc(/C=C/c(cc3)cc4c3[n](CC)c3ccccc43)cc(/C=C/c(cc3)cc4c3[n](CC)c3ccccc43)c2)c2)c2c2c1cccc2 Chemical compound CC[n]1c(ccc(/C=C/c2cc(/C=C/c(cc3)cc4c3[n](CC)c3ccccc43)cc(/C=C/c(cc3)cc4c3[n](CC)c3ccccc43)c2)c2)c2c2c1cccc2 JWTJCIYHZFCEPU-IKVQWSBMSA-N 0.000 description 1
- NJPVAQIVXCSFHI-UHFFFAOYSA-N c(cc1)ccc1-c1cc(-c(cc2)ccc2-[n]2c3ccccc3c3c2cccc3)nc(-c(cc2)ccc2-[n]2c(cccc3)c3c3c2cccc3)c1 Chemical compound c(cc1)ccc1-c1cc(-c(cc2)ccc2-[n]2c3ccccc3c3c2cccc3)nc(-c(cc2)ccc2-[n]2c(cccc3)c3c3c2cccc3)c1 NJPVAQIVXCSFHI-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/10—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/10—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic System
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
- C07F7/0812—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring
- C07F7/0816—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring said ring comprising Si as a ring atom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B15/00—Acridine dyes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B17/00—Azine dyes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B17/00—Azine dyes
- C09B17/02—Azine dyes of the benzene series
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B19/00—Oxazine dyes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B21/00—Thiazine dyes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B67/00—Influencing the physical, e.g. the dyeing or printing properties of dyestuffs without chemical reactions, e.g. by treating with solvents grinding or grinding assistants, coating of pigments or dyes; Process features in the making of dyestuff preparations; Dyestuff preparations of a special physical nature, e.g. tablets, films
- C09B67/0033—Blends of pigments; Mixtured crystals; Solid solutions
- C09B67/0041—Blends of pigments; Mixtured crystals; Solid solutions mixtures containing one azo dye
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B67/00—Influencing the physical, e.g. the dyeing or printing properties of dyestuffs without chemical reactions, e.g. by treating with solvents grinding or grinding assistants, coating of pigments or dyes; Process features in the making of dyestuff preparations; Dyestuff preparations of a special physical nature, e.g. tablets, films
- C09B67/0071—Process features in the making of dyestuff preparations; Dehydrating agents; Dispersing agents; Dustfree compositions
- C09B67/0084—Dispersions of dyes
- C09B67/0085—Non common dispersing agents
- C09B67/009—Non common dispersing agents polymeric dispersing agent
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B69/00—Dyes not provided for by a single group of this subclass
- C09B69/008—Dyes containing a substituent, which contains a silicium atom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent, e.g. electroluminescent, chemiluminescent materials
- C09K11/06—Luminescent, e.g. electroluminescent, chemiluminescent materials containing organic luminescent materials
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/40—Organosilicon compounds, e.g. TIPS pentacene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/655—Aromatic compounds comprising a hetero atom comprising only sulfur as heteroatom
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B32—LAYERED PRODUCTS
- B32B—LAYERED PRODUCTS, i.e. PRODUCTS BUILT-UP OF STRATA OF FLAT OR NON-FLAT, e.g. CELLULAR OR HONEYCOMB, FORM
- B32B2457/00—Electrical equipment
- B32B2457/20—Displays, e.g. liquid crystal displays, plasma displays
- B32B2457/206—Organic displays, e.g. OLED
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
- C09K2211/1033—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom with oxygen
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
- C09K2211/1037—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom with sulfur
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
- C09K2211/104—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom with other heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1092—Heterocyclic compounds characterised by ligands containing sulfur as the only heteroatom
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
- G02F1/133—Constructional arrangements; Operation of liquid crystal cells; Circuit arrangements
- G02F1/1333—Constructional arrangements; Manufacturing methods
- G02F1/1335—Structural association of cells with optical devices, e.g. polarisers or reflectors
- G02F1/1336—Illuminating devices
- G02F1/133614—Illuminating devices using photoluminescence, e.g. phosphors illuminated by UV or blue light
-
- G—PHYSICS
- G02—OPTICS
- G02F—OPTICAL DEVICES OR ARRANGEMENTS FOR THE CONTROL OF LIGHT BY MODIFICATION OF THE OPTICAL PROPERTIES OF THE MEDIA OF THE ELEMENTS INVOLVED THEREIN; NON-LINEAR OPTICS; FREQUENCY-CHANGING OF LIGHT; OPTICAL LOGIC ELEMENTS; OPTICAL ANALOGUE/DIGITAL CONVERTERS
- G02F1/00—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics
- G02F1/01—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour
- G02F1/13—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells
- G02F1/137—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells characterised by the electro-optical or magneto-optical effect, e.g. field-induced phase transition, orientation effect, guest-host interaction or dynamic scattering
- G02F1/13762—Devices or arrangements for the control of the intensity, colour, phase, polarisation or direction of light arriving from an independent light source, e.g. switching, gating or modulating; Non-linear optics for the control of the intensity, phase, polarisation or colour based on liquid crystals, e.g. single liquid crystal display cells characterised by the electro-optical or magneto-optical effect, e.g. field-induced phase transition, orientation effect, guest-host interaction or dynamic scattering containing luminescent or electroluminescent additives
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
Abstract
Description
[2] Ar1~Ar3が置換アリール基を表すとき、アリール基に置換している置換基は、前記一般式(2)で表される置換基、炭素数1~6のアルキル基、炭素数6~14のアリール基、および炭素数7~15のアラルキル基からなる群より選択されることを特徴とする[1]に記載の化合物。
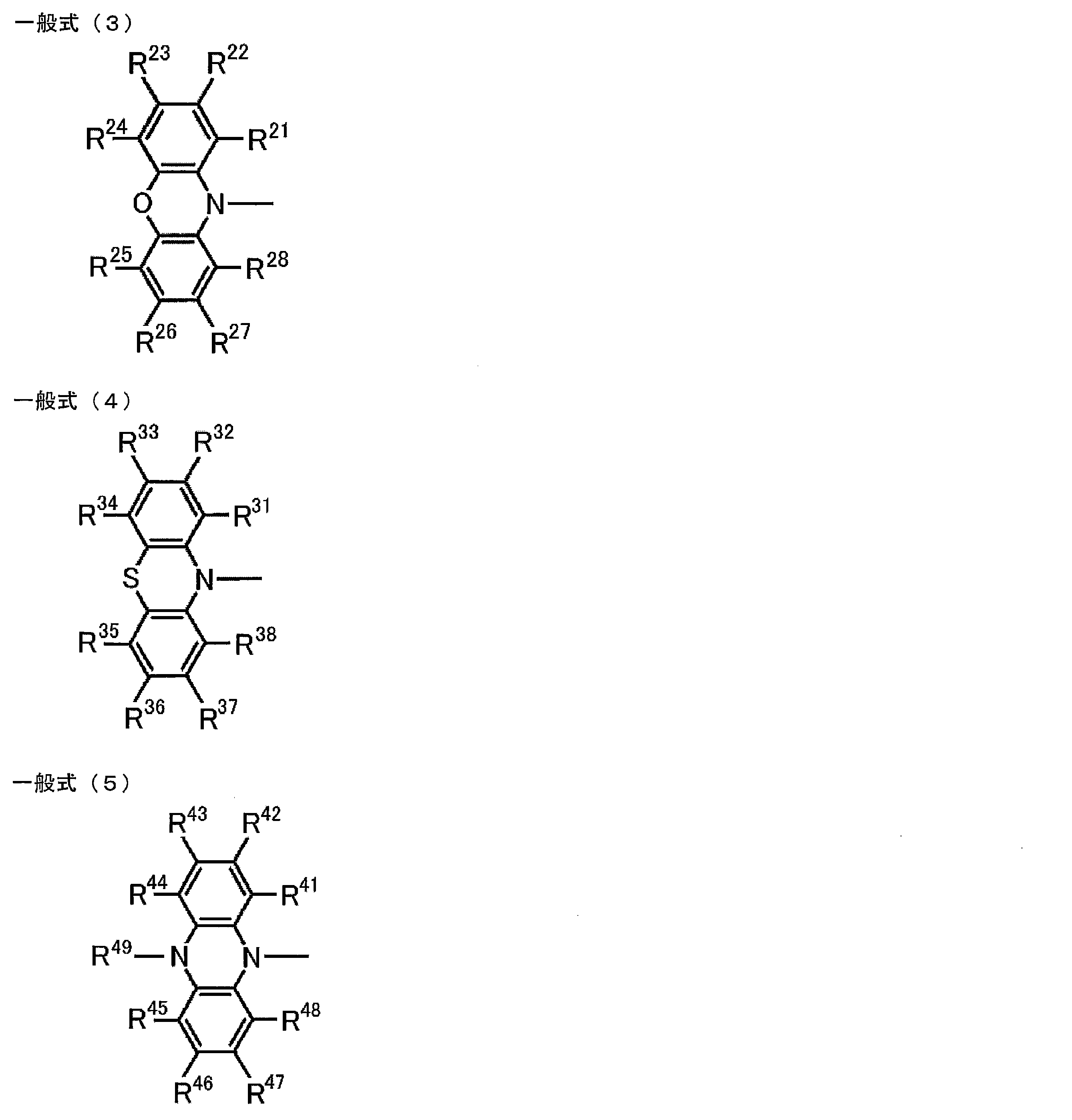
[3] 一般式(1)のAr1~Ar3の少なくとも1つは下記一般式(3)で表される基で置換されたアリール基であることを特徴とする[1]に記載の化合物。
[4] 一般式(1)のAr1~Ar3の少なくとも1つは下記一般式(4)で表される基で置換されたアリール基であることを特徴とする[1]に記載の化合物。
[5] 一般式(1)のAr1~Ar3の少なくとも1つは下記一般式(5)で表される基で置換されたアリール基であることを特徴とする[1]に記載の化合物。
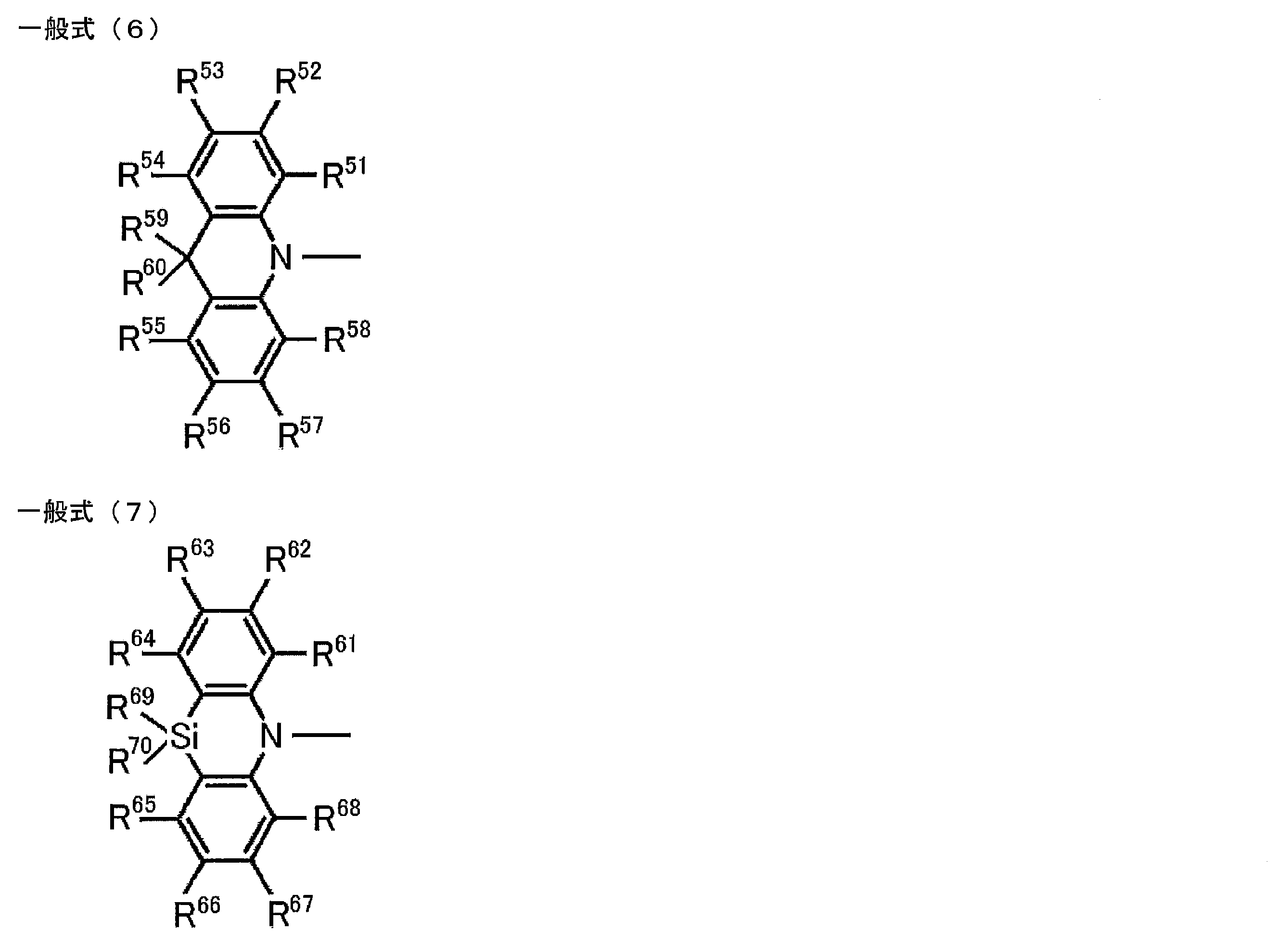
[6] 一般式(1)のAr1~Ar3の少なくとも1つは下記一般式(6)で表される基で置換されたアリール基であることを特徴とする[1]に記載の化合物。
[7] 一般式(1)のAr1~Ar3の少なくとも1つは下記一般式(7)で表される基で置換されたアリール基であることを特徴とする[1]に記載の化合物。
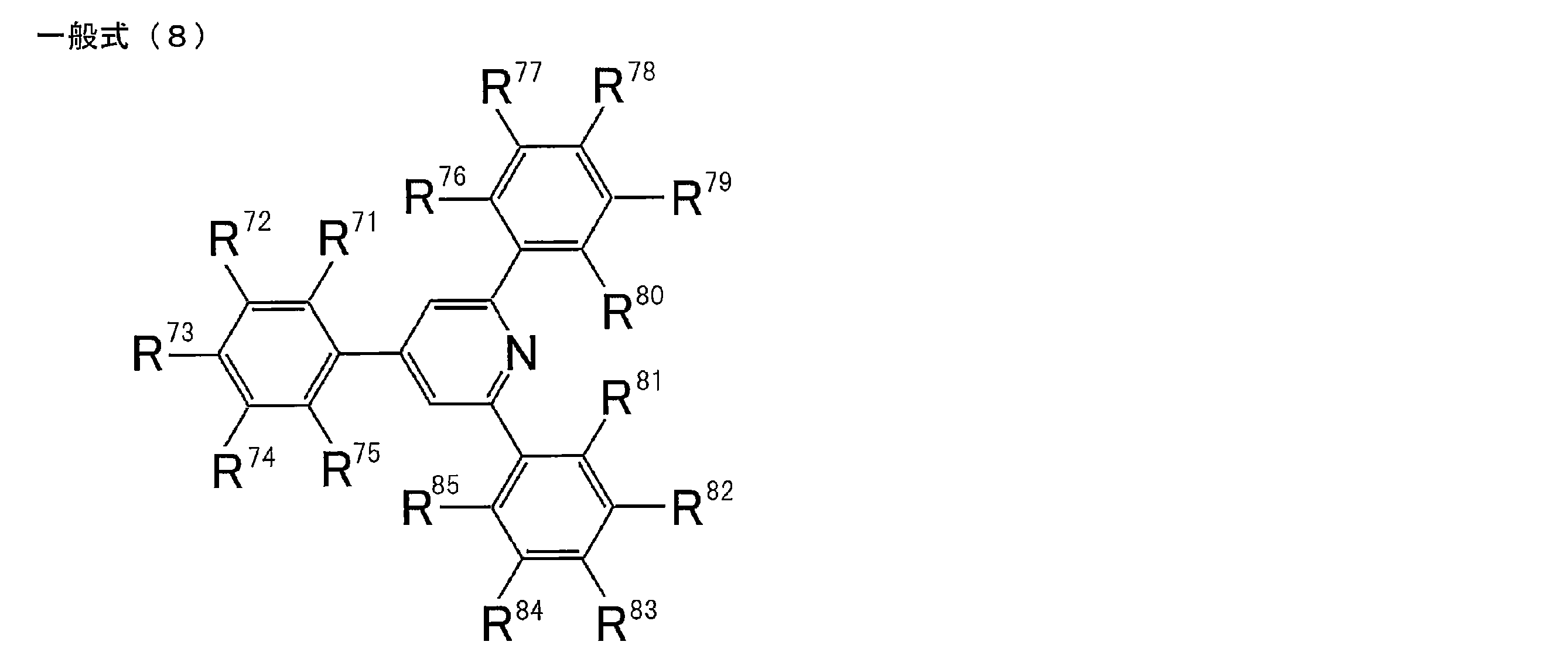
[8] 下記一般式(8)で表される構造を有することを特徴とする[1]に記載の化合物。
[9] 一般式(8)のR71~R85の少なくとも1つは下記一般式(3)で表される基であることを特徴とする[8]に記載の化合物。
[10] 一般式(8)のR71~R85の少なくとも1つは下記一般式(4)で表される基であることを特徴とする[8]に記載の化合物。
[11] 一般式(8)のR71~R85の少なくとも1つは下記一般式(5)で表される基であることを特徴とする[8]に記載の化合物。
[12] 一般式(8)のR71~R85の少なくとも1つは下記一般式(6)で表される基であることを特徴とする[8]に記載の化合物。
[13] 一般式(8)のR71~R85の少なくとも1つは下記一般式(7)で表される基であることを特徴とする[8]に記載の化合物。
[15] 下記一般式(1)で表される構造を有する遅延蛍光体。
[16] [14]に記載の発光材料を含む発光層を基板上に有することを特徴とする有機発光素子。
[17] 遅延蛍光を放射することを特徴とする[16]に記載の有機発光素子。
[18] 有機エレクトロルミネッセンス素子であることを特徴とする[16]または[17]に記載の有機発光素子。
本発明の化合物は、下記一般式(1)で表される構造を有することを特徴とする。
R1~R8は、これら置換基のうち前記一般式(2)で表される置換基、炭素数1~6のアルキル基、炭素数6~14のアリール基、または炭素数7~15のアラルキル基であることが好ましい。
一般式(3)~(7)における置換基の数は制限されず、R21~R28、R31~R38、R41~R49、R51~R60、R61~R70のすべてが無置換(すなわち水素原子)であってもよい。また、一般式(3)~(7)のそれぞれにおいて置換基が2つ以上ある場合、それらの置換基は同一であっても異なっていてもよい。一般式(3)~(7)に置換基が存在している場合、その置換基は一般式(3)であればR22~R27のいずれかであることが好ましく、一般式(4)であればR32~R37のいずれかであることが好ましく、一般式(5)であればR42~R47、R49のいずれかであることが好ましく、一般式(6)であればR52、R53、R56、R57、R59、R60のいずれかであることが好ましく、一般式(7)であればR62、R63、R66、R67、R69、R70のいずれかであることが好ましい。
一般式(1)中に存在する一般式(3)~(5)で表される基は、すべてが一般式(3)~(5)のいずれか1つの一般式で表される基であることが好ましい。例えば、一般式(3)で表される基である場合や、すべてが一般式(4)で表される場合を好ましく例示することができる。
一般式(1)で表される化合物は、分子量にかかわらず塗布法で成膜してもよい。塗布法を用いれば、分子量が比較的大きな化合物であっても成膜することが可能である。
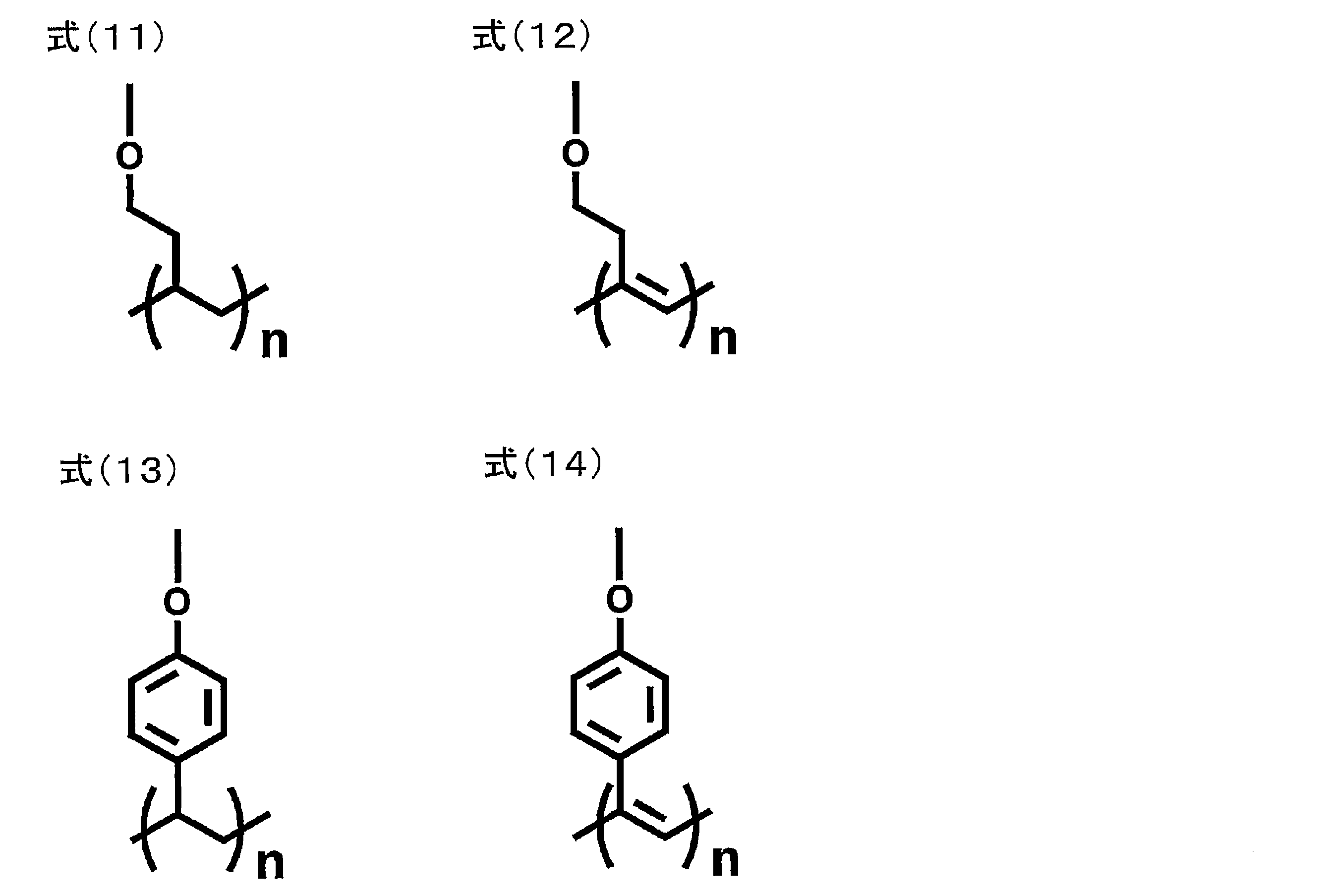
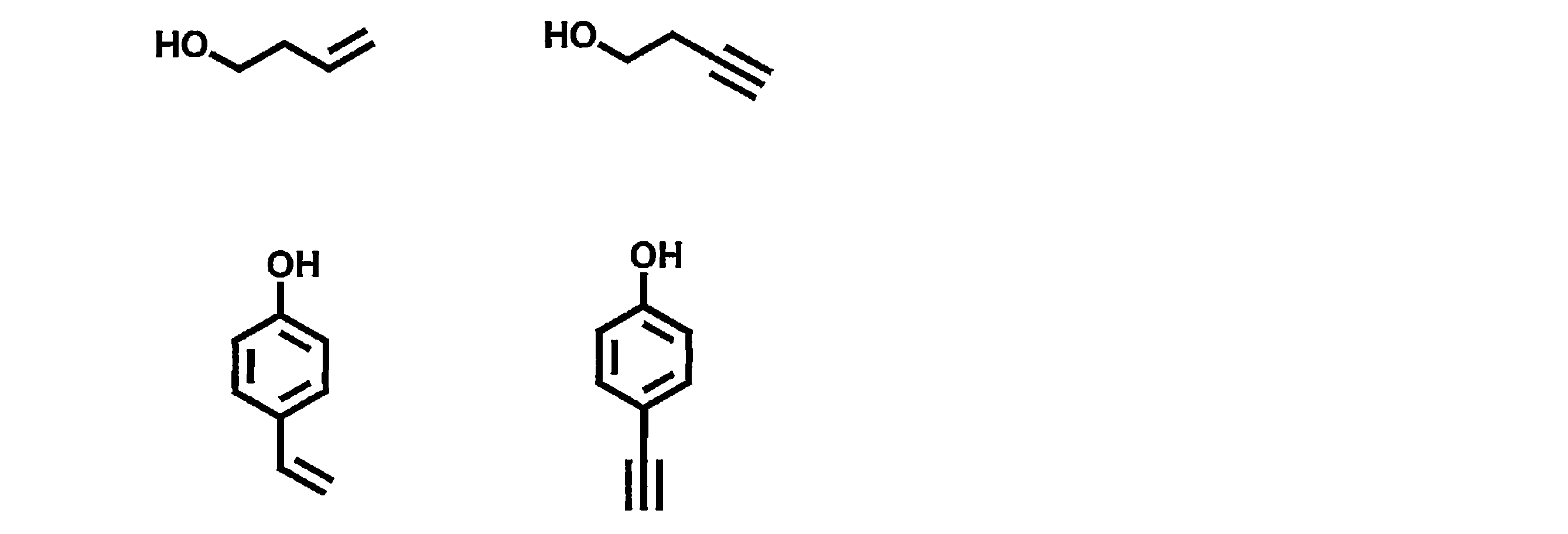
例えば、一般式(1)で表される構造中にあらかじめ重合性基を存在させておいて、その重合性基を重合させることによって得られる重合体を、発光材料として用いることが考えられる。具体的には、一般式(1)のAr1~Ar3のいずれかに重合性官能基を含むモノマーを用意して、これを単独で重合させるか、他のモノマーとともに共重合させることにより、繰り返し単位を有する重合体を得て、その重合体を発光材料として用いることが考えられる。あるいは、一般式(1)で表される構造を有する化合物どうしを反応させることにより、二量体や三量体を得て、それらを発光材料として用いることも考えられる。
一般式(9)および(10)において、R101、R102、R103およびR104は、各々独立に置換基を表す。好ましくは、炭素数1~6の置換もしくは無置換のアルキル基、炭素数1~6の置換もしくは無置換のアルコキシ基、ハロゲン原子であり、より好ましくは炭素数1~3の無置換のアルキル基、炭素数1~3の無置換のアルコキシ基、フッ素原子、塩素原子であり、さらに好ましくは炭素数1~3の無置換のアルキル基、炭素数1~3の無置換のアルコキシ基である。
L1およびL2で表される連結基は、Qを構成する一般式(1)の構造のAr1~Ar1のいずれかに結合する。1つのQに対して連結基が2つ以上連結して架橋構造や網目構造を形成していてもよい。
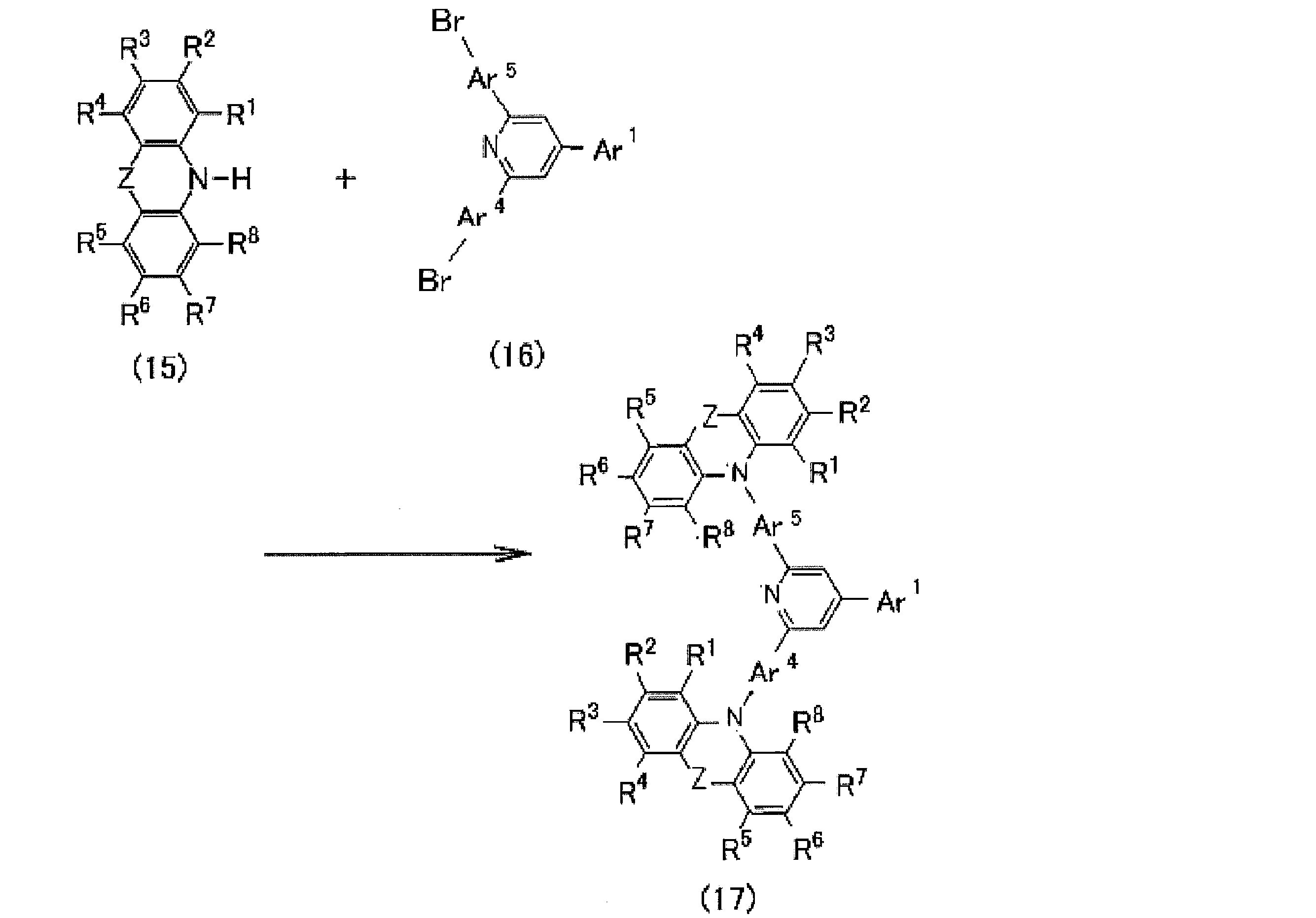
一般式(1)で表される化合物は、既知の反応を組み合わせることによって合成することができる。例えば、一般式(1)のAr2とAr3が、一般式(2)で表される基で置換されたアリール基である場合の合成は、以下のスキームにしたがって一般式(15)で表される化合物と一般式(16)で表される化合物を反応させることにより行うことができる。この反応自体は公知の反応であり、公知の反応条件を適宜選択して用いることができる。また、一般式(16)で表される化合物は、例えば、対応する塩化物をアミンに変換し、さらに臭化物へと変換することにより合成することが可能である。
上記スキームにおいて用いる一般式(16)で表される化合物を、臭素による多置換体に変更することにより、一般式(2)で表される基を複数導入した化合物を合成することが可能である。
上記の反応の詳細については、後述の合成例を参考にすることができる。また、一般式(1)で表される化合物は、その他の公知の合成反応を組み合わせることによっても合成することができる。
本発明の一般式(1)で表される化合物は、有機発光素子の発光材料として有用である。このため、本発明の一般式(1)で表される化合物は、有機発光素子の発光層に発光材料として効果的に用いることができる。一般式(1)で表される化合物の中には、遅延蛍光を放射する遅延蛍光材料(遅延蛍光体)が含まれている。すなわち本発明は、一般式(1)で表される構造を有する遅延蛍光体の発明と、一般式(1)で表される化合物を遅延蛍光体として使用する発明と、一般式(1)で表される化合物を用いて遅延蛍光を発光させる方法の発明も提供する。そのような化合物を発光材料として用いた有機発光素子は、遅延蛍光を放射し、発光効率が高いという特徴を有する。その原理を、有機エレクトロルミネッセンス素子を例にとって説明すると以下のようになる。
有機フォトルミネッセンス素子は、基板上に少なくとも発光層を形成した構造を有する。また、有機エレクトロルミネッセンス素子は、少なくとも陽極、陰極、および陽極と陰極の間に有機層を形成した構造を有する。有機層は、少なくとも発光層を含むものであり、発光層のみからなるものであってもよいし、発光層の他に1層以上の有機層を有するものであってもよい。そのような他の有機層として、正孔輸送層、正孔注入層、電子阻止層、正孔阻止層、電子注入層、電子輸送層、励起子阻止層などを挙げることができる。正孔輸送層は正孔注入機能を有した正孔注入輸送層でもよく、電子輸送層は電子注入機能を有した電子注入輸送層でもよい。具体的な有機エレクトロルミネッセンス素子の構造例を図1に示す。図1において、1は基板、2は陽極、3は正孔注入層、4は正孔輸送層、5は発光層、6は電子輸送層、7は陰極を表わす。
以下において、有機エレクトロルミネッセンス素子の各部材および各層について説明する。なお、基板と発光層の説明は有機フォトルミネッセンス素子の基板と発光層にも該当する。
本発明の有機エレクトロルミネッセンス素子は、基板に支持されていることが好ましい。この基板については、特に制限はなく、従来から有機エレクトロルミネッセンス素子に慣用されているものであればよく、例えば、ガラス、透明プラスチック、石英、シリコンなどからなるものを用いることができる。
有機エレクトロルミネッセンス素子における陽極としては、仕事関数の大きい(4eV以上)金属、合金、電気伝導性化合物およびこれらの混合物を電極材料とするものが好ましく用いられる。このような電極材料の具体例としてはAu等の金属、CuI、インジウムチンオキシド(ITO)、SnO2、ZnO等の導電性透明材料が挙げられる。また、IDIXO(In2O3-ZnO)等非晶質で透明導電膜を作製可能な材料を用いてもよい。陽極はこれらの電極材料を蒸着やスパッタリング等の方法により、薄膜を形成させ、フォトリソグラフィー法で所望の形状のパターンを形成してもよく、あるいはパターン精度をあまり必要としない場合は(100μm以上程度)、上記電極材料の蒸着やスパッタリング時に所望の形状のマスクを介してパターンを形成してもよい。あるいは、有機導電性化合物のように塗布可能な材料を用いる場合には、印刷方式、コーティング方式等湿式成膜法を用いることもできる。この陽極より発光を取り出す場合には、透過率を10%より大きくすることが望ましく、また陽極としてのシート抵抗は数百Ω/□以下が好ましい。さらに膜厚は材料にもよるが、通常10~1000nm、好ましくは10~200nmの範囲で選ばれる。
一方、陰極としては、仕事関数の小さい(4eV以下)金属(電子注入性金属と称する)、合金、電気伝導性化合物およびこれらの混合物を電極材料とするものが用いられる。このような電極材料の具体例としては、ナトリウム、ナトリウム-カリウム合金、マグネシウム、リチウム、マグネシウム/銅混合物、マグネシウム/銀混合物、マグネシウム/アルミニウム混合物、マグネシウム/インジウム混合物、アルミニウム/酸化アルミニウム(Al2O3)混合物、インジウム、リチウム/アルミニウム混合物、希土類金属等が挙げられる。これらの中で、電子注入性および酸化等に対する耐久性の点から、電子注入性金属とこれより仕事関数の値が大きく安定な金属である第二金属との混合物、例えば、マグネシウム/銀混合物、マグネシウム/アルミニウム混合物、マグネシウム/インジウム混合物、アルミニウム/酸化アルミニウム(Al2O3)混合物、リチウム/アルミニウム混合物、アルミニウム等が好適である。陰極はこれらの電極材料を蒸着やスパッタリング等の方法により薄膜を形成させることにより、作製することができる。また、陰極としてのシート抵抗は数百Ω/□以下が好ましく、膜厚は通常10nm~5μm、好ましくは50~200nmの範囲で選ばれる。なお、発光した光を透過させるため、有機エレクトロルミネッセンス素子の陽極または陰極のいずれか一方が、透明または半透明であれば発光輝度が向上し好都合である。
また、陽極の説明で挙げた導電性透明材料を陰極に用いることで、透明または半透明の陰極を作製することができ、これを応用することで陽極と陰極の両方が透過性を有する素子を作製することができる。
発光層は、陽極および陰極のそれぞれから注入された正孔および電子が再結合することにより励起子が生成した後、発光する層であり、発光材料を単独で発光層に使用しても良いが、好ましくは発光材料とホスト材料を含む。発光材料としては、一般式(1)で表される本発明の化合物群から選ばれる1種または2種以上を用いることができる。本発明の有機エレクトロルミネッセンス素子および有機フォトルミネッセンス素子が高い発光効率を発現するためには、発光材料に生成した一重項励起子および三重項励起子を、発光材料中に閉じ込めることが重要である。従って、発光層中に発光材料に加えてホスト材料を用いることが好ましい。ホスト材料としては、励起一重項エネルギー、励起三重項エネルギーの少なくとも何れか一方が本発明の発光材料よりも高い値を有する有機化合物を用いることができる。その結果、本発明の発光材料に生成した一重項励起子および三重項励起子を、本発明の発光材料の分子中に閉じ込めることが可能となり、その発光効率を十分に引き出すことが可能となる。もっとも、一重項励起子および三重項励起子を十分に閉じ込めることができなくても、高い発光効率を得ることが可能な場合もあるため、高い発光効率を実現しうるホスト材料であれば特に制約なく本発明に用いることができる。本発明の有機発光素子または有機エレクトロルミネッセンス素子において、発光は発光層に含まれる本発明の発光材料から生じる。この発光は蛍光発光および遅延蛍光発光の両方を含む。但し、発光の一部或いは部分的にホスト材料からの発光があってもかまわない。
ホスト材料を用いる場合、発光材料である本発明の化合物が発光層中に含有される量は0.1重量%以上であることが好ましく、1重量%以上であることがより好ましく、また、50重量%以下であることが好ましく、20重量%以下であることがより好ましく、10重量%以下であることがさらに好ましい。
発光層におけるホスト材料としては、正孔輸送能、電子輸送能を有し、かつ発光の長波長化を防ぎ、なおかつ高いガラス転移温度を有する有機化合物であることが好ましい。
注入層とは、駆動電圧低下や発光輝度向上のために電極と有機層間に設けられる層のことで、正孔注入層と電子注入層があり、陽極と発光層または正孔輸送層の間、および陰極と発光層または電子輸送層との間に存在させてもよい。注入層は必要に応じて設けることができる。
阻止層は、発光層中に存在する電荷(電子もしくは正孔)および/または励起子の発光層外への拡散を阻止することができる層である。電子阻止層は、発光層および正孔輸送層の間に配置されることができ、電子が正孔輸送層の方に向かって発光層を通過することを阻止する。同様に、正孔阻止層は発光層および電子輸送層の間に配置されることができ、正孔が電子輸送層の方に向かって発光層を通過することを阻止する。阻止層はまた、励起子が発光層の外側に拡散することを阻止するために用いることができる。すなわち電子阻止層、正孔阻止層はそれぞれ励起子阻止層としての機能も兼ね備えることができる。本明細書でいう電子阻止層または励起子阻止層は、一つの層で電子阻止層および励起子阻止層の機能を有する層を含む意味で使用される。
正孔阻止層とは広い意味では電子輸送層の機能を有する。正孔阻止層は電子を輸送しつつ、正孔が電子輸送層へ到達することを阻止する役割があり、これにより発光層中での電子と正孔の再結合確率を向上させることができる。正孔阻止層の材料としては、後述する電子輸送層の材料を必要に応じて用いることができる。
電子阻止層とは、広い意味では正孔を輸送する機能を有する。電子阻止層は正孔を輸送しつつ、電子が正孔輸送層へ到達することを阻止する役割があり、これにより発光層中での電子と正孔が再結合する確率を向上させることができる。
励起子阻止層とは、発光層内で正孔と電子が再結合することにより生じた励起子が電荷輸送層に拡散することを阻止するための層であり、本層の挿入により励起子を効率的に発光層内に閉じ込めることが可能となり、素子の発光効率を向上させることができる。励起子阻止層は発光層に隣接して陽極側、陰極側のいずれにも挿入することができ、両方同時に挿入することも可能である。すなわち、励起子阻止層を陽極側に有する場合、正孔輸送層と発光層の間に、発光層に隣接して該層を挿入することができ、陰極側に挿入する場合、発光層と陰極との間に、発光層に隣接して該層を挿入することができる。また、陽極と、発光層の陽極側に隣接する励起子阻止層との間には、正孔注入層や電子阻止層などを有することができ、陰極と、発光層の陰極側に隣接する励起子阻止層との間には、電子注入層、電子輸送層、正孔阻止層などを有することができる。阻止層を配置する場合、阻止層として用いる材料の励起一重項エネルギーおよび励起三重項エネルギーの少なくともいずれか一方は、発光材料の励起一重項エネルギーおよび励起三重項エネルギーよりも高いことが好ましい。
正孔輸送層とは正孔を輸送する機能を有する正孔輸送材料からなり、正孔輸送層は単層または複数層設けることができる。
正孔輸送材料としては、正孔の注入または輸送、電子の障壁性のいずれかを有するものであり、有機物、無機物のいずれであってもよい。使用できる公知の正孔輸送材料としては例えば、トリアゾール誘導体、オキサジアゾール誘導体、イミダゾール誘導体、カルバゾール誘導体、インドロカルバゾール誘導体、ポリアリールアルカン誘導体、ピラゾリン誘導体およびピラゾロン誘導体、フェニレンジアミン誘導体、アリールアミン誘導体、アミノ置換カルコン誘導体、オキサゾール誘導体、スチリルアントラセン誘導体、フルオレノン誘導体、ヒドラゾン誘導体、スチルベン誘導体、シラザン誘導体、アニリン系共重合体、また導電性高分子オリゴマー、特にチオフェンオリゴマー等が挙げられるが、ポルフィリン化合物、芳香族第3級アミン化合物およびスチリルアミン化合物を用いることが好ましく、芳香族第3級アミン化合物を用いることがより好ましい。
電子輸送層とは電子を輸送する機能を有する材料からなり、電子輸送層は単層または複数層設けることができる。
電子輸送材料(正孔阻止材料を兼ねる場合もある)としては、陰極より注入された電子を発光層に伝達する機能を有していればよい。使用できる電子輸送層としては例えば、ニトロ置換フルオレン誘導体、ジフェニルキノン誘導体、チオピランジオキシド誘導体、カルボジイミド、フレオレニリデンメタン誘導体、アントラキノジメタンおよびアントロン誘導体、オキサジアゾール誘導体等が挙げられる。さらに、上記オキサジアゾール誘導体において、オキサジアゾール環の酸素原子を硫黄原子に置換したチアジアゾール誘導体、電子吸引基として知られているキノキサリン環を有するキノキサリン誘導体も、電子輸送材料として用いることができる。さらにこれらの材料を高分子鎖に導入した、またはこれらの材料を高分子の主鎖とした高分子材料を用いることもできる。
一方、りん光については、本発明の化合物のような通常の有機化合物では、励起三重項エネルギーは不安定で熱等に変換され、寿命が短く直ちに失活するため、室温では殆ど観測できない。通常の有機化合物の励起三重項エネルギーを測定するためには、極低温の条件での発光を観測することにより測定可能である。
4-ブロモアセトフェノン(11.2g,56.3mmol)、ベンズアルデヒド(2.87mL,28.1mmol)、酢酸アンモニウム(27.8g,0.366mol)を酢酸(60mL)中で混合し、5時間還流した。室温に冷却後、ろ別した固形分を酢酸で洗浄し、乾燥後に酢酸エチルで再結晶することにより、無色固体の2,6-ビス(4-ブロモフェニル)-4-フェニルピリジン(2.9g,収率22%)を得た。
1H NMR (CDCl3, 400 MHz)δ7.47-7.57(m,3H), 7.62-7.66(m,4H), 7.71-7.75(m,2H), 7.87(s,2H), 8.04-8.09(m,4H).
13C NMR (CDCl3, 100 MHz) δ117.15, 123.65, 127.16, 128.65, 129.19, 131.88, 136.40, 138.21, 138.66, 150.63, 156.44.
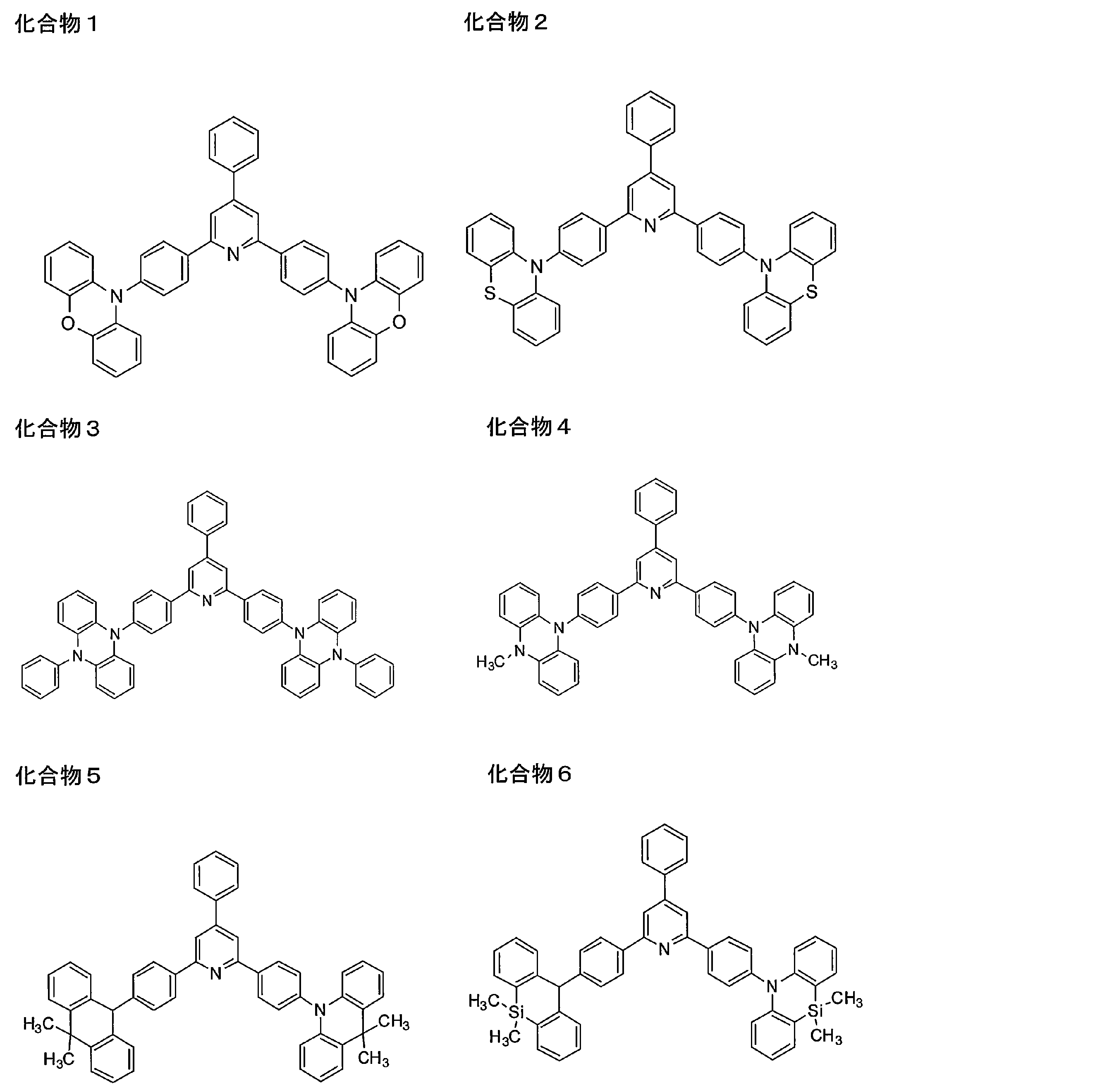
2,6-ビス(4-ブロモフェニル)-4-フェニルピリジン(1.03g,2.24mmol),10H-フェノキサジン(1.02g,5.57mmol)、炭酸カリウム(1.57g,11.2mmol)をトルエン(50mL)中で混合し、15分間窒素でバブリングした後に酢酸パラジウム(15mg,0.07mmol)とトリ-tert-ブチルリン(ヘキサンの10重量%溶液,0.56mL,0.27mmol)を添加して、48時間還流した。室温に冷却してシリカゲルでろ過し、酢酸エチル/塩化メチレン/トルエン(1:5:5)で洗浄した。ろ液を濃縮して得た固形物をシリカゲルカラムクロマトグラフィー(酢酸エチル/トルエン/ペトロール(2.5:20:77.5)、次いで塩化メチレン/ペトロール(35:65)、次いで塩化メチレン/トルエン(60:40))で精製して、淡黄色固体として化合物1(1.34g,収率89%)を得た。さらにトルエンで再結晶し、昇華精製(320℃,10―6mBar)することにより精製した。
m.p.325-331℃(DSC).
1H NMR (CDCl3,400 MHz)δ6.05(d,J7.7Hz,4H), 6.58-6.74(m,12H), 7.50-7.61(m,7H), 7.79-7.84(m,2H), 8.02(s,2H), 8.44(d,J8.3Hz,4H).
13C NMR (CDCl3, 100 MHz) δ113.33, 115.49, 117.79, 121.42, 123.26, 127.20, 129.28, 129.37, 129.91, 131.21, 134.23, 138.54, 139.46, 139.88, 143.97, 150.84, 156.80.
HRMS(EI) m/z670.2483 C47H32O2N3 [M+H]+ requires 670.2489.
2,6-ビス(4-ブロモフェニル)-4-フェニルピリジン(2.87g,6.21mmol),10H-フェノチアジン(3.03g,15.5mmol)、炭酸カリウム(4.35g,31.1mmol)をトルエン(70mL)中で混合し、15分間窒素でバブリングした後に酢酸パラジウム(84mg,0.37mmol)とトリ-tert-ブチルリン(トルエンの10重量%溶液,3.60mL,1.49mmol)を添加して、48時間還流した。室温に冷却してシリカゲルでろ過し、酢酸エチル/塩化メチレン/トルエン(1:5:5)で洗浄した。ろ液を濃縮して得た固形物をシリカゲルカラムクロマトグラフィー(酢酸エチル/トルエン/ペトロール(2.5:20:77.5)、次いで塩化メチレン/ペトロール(30:70)で精製して、淡黄色固体として化合物2(4.13g,収率95%)を得た。さらにトルエンで再結晶し、昇華精製(315℃,10-6mBar)することにより精製した。
m.p.254-260℃(DSC).
1H NMR (C6D6,400 MHz)δ6.41(dd,J1.2,8.1Hz,4H), 6.64(dt,J1.3,7.4Hz,4H), 6.68-6.74(m,4H), 7.01(dd,J1.6,7.5Hz,4H), 7.20-7.30(m,7H), 7.46-7.50(m,2H), 7.69(s,2H), 8.19-8.22(m,4H).
13C NMR (C6D6,100 MHz) δ121.46, 123.13, 127.13, 127.30, 127.53, 127.88, 128.12, 129.29, 129.86, 130.84, 139.15, 139.31, 142.48, 144.70, 150.73, 157.21; HRMS (EI) m/z701.1949 C47H32N3S2 [M]+ requires 701.1954.
2,6-ビス(4-ブロモフェニル)-4-フェニルピリジン(1.0g,2.16mmol),9,9-ジメチルー9,10-ジヒドロアクリジン(1.04g,4.98mmol)、ナトリウム-tert-ブトキシド(520mg,5.4mmol)をトルエン(40mL)中で混合し、15分間窒素でバブリングした後にトリス(ジベンジリデンアセトン)ジパラジウム(0)(20mg,0.022mmol)と1,1‘-ビス(ジフェニルホスフィノ)フェロセン(24mg,0.044mmol)を添加して、72時間還流した。室温に冷却してシリカゲルでろ過し、酢酸エチル/塩化メチレン/トルエン(1:5:5)で洗浄した。ろ液を濃縮して得た固形物をシリカゲルカラムクロマトグラフィー(トルエン/ペトロール/塩化メチレン(25:75:0)、次いで(30:60:10)、次いで(30:50:20))で精製して、無色固体として化合物5(1.45g,収率93%)を得た。さらにトルエン/ペトロールで再結晶し、昇華精製(320℃,10-6mBar)することにより精製した。
m.p.338-343℃(DSC).
1H NMR (CDCl3, 400 MHz) δ 1.74 (s, 12H), 6.42 (dd, J 1.3, 8.0 Hz, 4H), 6.94 - 7.04 (m, 8H), 7.48 - 7.63 (m, 11H), 7.83 - 7.88 (m, 2H), 8.08 (s, 2H), 8.49 - 8.53 (m, 4H); 13C NMR (CDCl3, 100 MHz) δ 31.33, 35.99, 114.12, 117.70, 120.62, 125.28, 126.38, 127.21, 129.24, 129.71, 130.01, 131.71, 138.69, 139.37, 140.79, 142.14, 150.68, 157.02; HRMS (APCI) m/z 721.3452 C53H43N3[M]+・ requires 721.3451.
アセトフェノン(9.71mL,83.2mmol),4-ブロモベンズアルデヒド(7.7g,41.8mmol)、酢酸アンモニウム(41g,0.54mol)を酢酸(80mL)中で混合し、24時間還流した。室温に冷却後、ろ別した固形分を酢酸で洗浄し、酢酸エチルに不溶性の成分を取りだして飽和炭酸水素ナトリウム水溶液と飽和塩化ナトリウム水溶液で洗浄して乾燥した。その後、シリカゲルカラムクロマトグラフィー(酢酸エチル/ペトロール(2:98)を行い、エタノールで再結晶することにより、無色固体の4-(4-ブロモフェニル)-2,6-ジフェニルピリジン(3.0g,収率19%)を得た。
1H NMR (CDCl3,400MHz)δ7.43-7.56(m,6H), 7.59-7.69(m,4H), 7.85(s,2H), 8.12-8.22(m,4H).
13C NMR (CDCl3,100 MHz)δ116.74, 123.39, 127.11, 128.73, 129.16, 131.82, 132.28, 137.95, 139.37, 148.96, 157.69.
4-(4-ブロモフェニル)-2,6-ジフェニルピリジン(2.18g,5.67mmol),10H-フェノキサジン(1.19g,6.52mmol)、炭酸カリウム(1.59g,11.3mmol)をトルエン(50mL)中で混合し、15分間窒素でバブリングした後に酢酸パラジウム(76mg,0.34mmol)とトリ-tert-ブチルリン(ヘキサンの10重量%溶液,2.83mL,1.36mmol)を添加して、48時間還流した。室温に冷却してシリカゲルでろ過し、酢酸エチル/塩化メチレン/トルエン(1:5:5)で洗浄した。ろ液を濃縮して得た固形物をシリカゲルカラムクロマトグラフィー(酢酸エチル/トルエン/ペトロール(2.5:5:92.5))で精製して、淡黄色固体として化合物19(2.6g,収率94%)を得た。さらに塩化メチレン/酢酸エチルで再結晶し、昇華精製(245℃,10-6mBar)することにより精製した。
m.p.235-242℃(DSC).
1H NMR(CDCl3,400MHz)δ6.03(dd,J1.6,7.8Hz,2H), 6.63(dt,J1.8,7.3Hz,2H), 6.68(dt,J1.4,7.3Hz,2H), 6.73(dd,J1.8,7.8Hz,2H), 7.44-7.57(m,8H), 7.96(s,2H), 7.96-8.00(m,2H), 8.22-8.27(m,4H).
13C NMR(CDCl3,100MHz)δ113.25, 115.57, 117.01, 121.54, 123.28, 127.13, 128.76, 129.20, 129.88, 131.61, 134.16, 139.25, 139.37, 139.76, 143.96, 149.12, 157.69.
HRMS(EI) m/z488.1884 C35H24N2O [M]+ requires 488.1884.
4-(4-ブロモフェニル)-2,6-ジフェニルピリジン(750mg,1.95mmol),9,9-ジメチルー9,10-ジヒドロアクリジン(410g,1.95mmol)、ナトリウム-tert-ブトキシド(280mg,2.92mmol)をトルエン(40mL)中で混合し、15分間窒素でバブリングした後にトリス(ジベンジリデンアセトン)ジパラジウム(0)(36mg,0.04mmol)と1,1‘-ビス(ジフェニルホスフィノ)フェロセン(43mg,0.08mmol)を添加して、48時間還流した。室温に冷却してシリカゲルでろ過し、酢酸エチル/トルエン(5:95)で洗浄した。ろ液を濃縮して得た固形物をシリカゲルカラムクロマトグラフィー(トルエン/ペトロール(27:73))で精製して、無色固体として化合物20(795mg,収率79%)を得た。さらにトルエン/ペトロールで再結晶し、昇華精製(230℃,10-6mBar)することにより精製した。
m.p.200-205℃(DSC).
1H NMR (CDCl3, 400 MHz) δ 1.57 (s, 6H), 6.37 (dd, J 1.3, 8.0 Hz, 2H), 6.94 - 7.05 (m, 4H), 7.45 - 7.58 (m, 10H), 8.01 (s, 2H), 8.01 - 8.04 (m, 2H), 8.25 - 8.29 (m, 4H); 13C NMR (CDCl3, 100 MHz) δ 31.30, 36.00, 114.01, 117.07, 120.74, 125.34, 126.41, 127.14, 128.75, 129.17, 129.69, 130.10, 132.09, 138.95, 139.42, 140.74, 142.06, 149.29, 157.67; HRMS (APCI) m/z 514.2408 C38H30N2[M]+・ requires 514.2404.
4-(4-ブロモフェニル)-2,6-ジフェニルピリジン(720mg,1.87mmol),9,9-ジフェニルー9,10-ジヒドロアクリジン(620g,1.87mmol)、ナトリウム-tert-ブトキシド(210mg,2.2mmol)をトルエン(40mL)中で混合し、15分間窒素でバブリングした後にトリス(ジベンジリデンアセトン)ジパラジウム(0)(18mg,0.02mmol)と1,1‘-ビス(ジフェニルホスフィノ)フェロセン(22mg,0.04mmol)を添加して、48時間還流した。室温に冷却してシリカゲルでろ過し、酢酸エチル/トルエン(5:95)で洗浄した。ろ液を濃縮して得た固形物をシリカゲルカラムクロマトグラフィー(塩化メチレン/ペトロール(15:85)、次いで(20:80)、次いで(30:70))で精製して、無色固体として化合物21(1.45g,収率93%)を得た。さらにトルエン/ペトロールで再結晶し、昇華精製(285℃,10-6mBar)することにより精製した。
m.p.288-293℃(DSC).
1H NMR (CDCl3, 400 MHz) δ 6.52 (dd, J 0.7, 8.6 Hz, 2H), 6.89 - 6.96 (m, 4H), 7.01 - 7.06 (m, 4H), 7.10 (ddd, J2.4, 6.4, 8.4 Hz, 2H), 7.23 - 7.32 (m, 8H), 7.45 - 7.50 (m, 2H), 7.51 - 7.57 (m, 4H), 7.89 - 7.94 (m, 2H), 7.96 (s, 2H), 8.22 - 8.26 (m, 4H); 13C NMR (CDCl3, 100 MHz) δ 56.76, 114.03, 117.05, 120.34, 126.30, 126.90, 127.12, 127.64, 128.75, 129.16, 129.32, 129.73, 130.10, 130.39, 132.02, 138.93, 139.41, 141.60, 142.04, 146.38, 149.28, 157.65; HRMS (APCI) m/z 638.2716 C48H34N2[M]+・ requires 638.2717.
2,6-ビス(4-ブロモフェニル)-4-フェニルピリジン(340mg,0.74mmol),9,9-ジフェニルー9,10-ジヒドロアクリジン(540g,1.62mmol)、ナトリウム-tert-ブトキシド(200mg,2.06mmol)をトルエン(40mL)中で混合し、15分間窒素でバブリングした後にトリス(ジベンジリデンアセトン)ジパラジウム(0)(27mg,0.03mmol)と1,1‘-ビス(ジフェニルホスフィノ)フェロセン(33mg,0.06mmol)を添加して、24時間還流した。室温に冷却してシリカゲルでろ過し、酢酸エチル/トルエン(5:95)で洗浄した。ろ液を濃縮して得た固形物をシリカゲルカラムクロマトグラフィー(トルエン/ペトロール/塩化メチレン(25:75:0)、次いで(30:40:30))で精製して、無色固体として化合物22(610mg,収率86%)を得た。さらにトルエン/塩化メチレンで再結晶し、昇華精製(380℃,10-6mBar)することにより精製した。
1H NMR (CDCl3, 400 MHz) δ 6.54 (dd, J 0.9, 8.4 Hz, 4H), 6.86 - 6.94 (m, 8H), 7.01 - 7.09 (m, 12H), 7.21 - 7.30 (m, 16H), 7.47 - 7.58 (m, 3H), 7.76 - 7.81 (m, 2H), 7.98 (s, 2H), 8.34 - 8.39 (m, 4H); 13C NMR (CDCl3, 100 MHz) δ 56.75, 114.1, 117.59, 120.21, 126.25, 126.86, 127.17, 127.62, 129.22, 129.30, 129.54, 130.04, 130.40, 131.62, 138.68, 139.32, 141.67, 142.08, 146.45, 150.62, 156.91; HRMS (APCI) m/z 969.4073 C73H51N3[M]+・ requires 969.4078.
2,6-ビス(4-ブロモフェニル)-4-フェニルピリジン(480mg,1.04mmol),9,9-ビス-(5-メチルチオフェン-2-イル)-9,10-ジヒドロアクリジン(850g,2.28mmol)、ナトリウム-tert-ブトキシド(280mg,2.91mmol)をトルエン(40mL)中で混合し、15分間窒素でバブリングした後にトリス(ジベンジリデンアセトン)ジパラジウム(0)(38mg,0.04mmol)と1,1‘-ビス(ジフェニルホスフィノ)フェロセン(46mg,0.08mmol)を添加して、8時間還流した。室温に冷却してシリカゲルでろ過し、酢酸エチル/ぺトロール(10:90)で洗浄した。ろ液を濃縮して得た固形物をシリカゲルカラムクロマトグラフィー(トルエン/ペトロール(20:80)、次いで(30:70)、次いで(40:60))で精製して、淡黄色固体として化合物23(840mg,収率74%)を得た。さらにトルエン/塩化メチレン/ペトロールで再結晶した。
1H NMR (CDCl3, 400 MHz) δ 2.43(2, 12H), 6.46 - 6.50 (m, 8H), 6.56 - 6.60 (m, 4H), 6.93 (dt, J 1.2, 7.7 Hz, 4H), 7.08 (ddd, J1.6, 8.3, 8.5 Hz, 4H), 7.27 (dd, J1.5, 7.8 Hz, 4H), 7.38 - 7.42 (m, 4H), 7.49 - 7.61 (m, 3H), 7.80 - 7.84 (m, 2H), 8.03 (s, 2H), 8.41 - 8.45 (m, 4H); 13C NMR (CDCl3, 100 MHz) δ 15.46, 50.75, 114.15, 117.68, 120.23, 123.94, 127.19, 127.55, 127.65, 128.50, 129.23, 129.28, 129.49, 131.72, 138.68, 139.45, 140.07, 140.75, 141.70, 150.53, 150.67, 156.95; HRMS (APCI) m/z 1050.3040 C73H51N3[M+H]+・ requires 1050.3039.
合成例1で合成した化合物1のトルエン溶液(濃度10-4mol/L)を調製して、窒素をバブリングしながら300Kで紫外光を照射したところ、図2に示すようにピーク波長が475nmの蛍光が観測された。また、窒素バブル前後に小型蛍光寿命測定装置(浜松ホトニクス(株)製Quantaurus-tau)による測定を行って、図3に示す過渡減衰曲線を得た。窒素バブル前の化合物1のトルエン溶液では励起寿命が4.56nsの蛍光が観測され、窒素バブル後の化合物1のトルエン溶液では励起寿命が5.80nsの蛍光と、17.1nsの遅延蛍光が観測された。化合物1のトルエン溶液中でのフォトルミネッセンス量子効率を絶対PL量子収率測定装置(浜松ホトニクス(株)製Quantaurus-QY)により励起波長330nmで測定したところ、窒素バブル前が21.8%であり、窒素バブル後が37.5%であった。
化合物1のかわりに合成例2で合成した化合物2を用いて実施例1と同様にトルエン溶液の作製と評価を行った。図4に発光スペクトルを示し、図5に過渡減衰曲線を示す。窒素バブル前の化合物2のトルエン溶液では励起寿命が2.58nsの蛍光が観測され、窒素バブル後の化合物2のトルエン溶液では励起寿命が2.85nsの蛍光と、20.6nsの遅延蛍光が観測された。フォトルミネッセンス量子効率は、窒素バブル前が3.4%であり、窒素バブル後が3.8%であった。
化合物1のかわりに合成例3で合成した化合物5を10-5Mの濃度で用いて実施例1と同様にトルエン溶液の作製と評価を行った。図6に励起波長354nmでの吸収発光スペクトルを示し、図7に励起波長340nmでの過渡減衰曲線を示す。435nmをピークとする発光が観測された。また、窒素バブル前の化合物5のトルエン溶液では励起寿命が4.6nsの蛍光が観測され、窒素バブル後の化合物5のトルエン溶液では励起寿命が6.1nsの蛍光が観測された。励起波長320nmでのフォトルミネッセンス量子効率は、窒素バブル前が16.2%であり、窒素バブル後が25.7%であった。
化合物1のかわりに合成例4で合成した化合物19を用いて実施例1と同様にトルエン溶液の作製と評価を行った。図8に発光スペクトルを示し、図9に過渡減衰曲線を示す。窒素バブル前の化合物19のトルエン溶液では励起寿命が5.94nsの蛍光が観測され、窒素バブル後の化合物19のトルエン溶液では励起寿命が8.39nsの蛍光と、1.56μsの遅延蛍光が観測された。フォトルミネッセンス量子効率は、窒素バブル前が14.8%であり、窒素バブル後が24.8%であった。
化合物1のかわりに合成例5で合成した化合物20を10-5Mの濃度で用いて実施例1と同様にトルエン溶液の作製と評価を行った。図10に励起波長356nmでの吸収発光スペクトルを示し、図11に励起波長340nmでの過渡減衰曲線を示す。445nmをピークとする発光が観測された。また、窒素バブル前の化合物20のトルエン溶液では励起寿命が4.4nsの蛍光が観測され、窒素バブル後の化合物20のトルエン溶液では励起寿命が5.6nsの蛍光が観測された。励起波長320nmでのフォトルミネッセンス量子効率は、窒素バブル前が12.1%であり、窒素バブル後が20.3%であった。
化合物1のかわりに合成例6で合成した化合物21を10-5Mの濃度で用いて実施例1と同様にトルエン溶液の作製と評価を行った。図12に励起波長356nmでの吸収発光スペクトルを示し、図13に励起波長340nmでの過渡減衰曲線を示す。430nmをピークとする発光が観測された。また、窒素バブル前の化合物21のトルエン溶液では励起寿命が4.0nsの蛍光が観測され、窒素バブル後の化合物21のトルエン溶液では励起寿命が4.9nsの蛍光が観測された。励起波長320nmでのフォトルミネッセンス量子効率は、窒素バブル前が15.1%であり、窒素バブル後が23.5%であった。
化合物1のかわりに合成例7で合成した化合物22を10-5Mの濃度で用いて実施例1と同様にトルエン溶液の作製と評価を行った。図14に励起波長346nmでの吸収発光スペクトルを示し、図15に励起波長340nmでの過渡減衰曲線を示す。422nmをピークとする発光が観測された。また、窒素バブル前の化合物22のトルエン溶液では励起寿命が4.3nsの蛍光が観測され、窒素バブル後の化合物22のトルエン溶液では励起寿命が5.5nsの蛍光が観測された。励起波長320nmでのフォトルミネッセンス量子効率は、窒素バブル前が21.7%であり、窒素バブル後が30.8%であった。
石英基板上に真空蒸着法にて、真空度10-4Pa以下の条件にて化合物1とmCPとを異なる蒸着源から蒸着し、化合物1の濃度が6.0重量%である共蒸着薄膜を100nmの厚さで形成した。この薄膜の吸収発光スペクトルを図16に示す。479nmをピークとする発光が確認された。
膜厚100nmのインジウム・スズ酸化物(ITO)からなる陽極が形成されたガラス基板上に、各薄膜を真空蒸着法にて、真空度5.0×10-4Paで積層した。まず、ITO上にHATCNを10nmの厚さに形成し、TrisPCzを20nmの厚さに形成し、mCPを10nmの厚さに形成した。次に、化合物1とmCPを異なる蒸着源から共蒸着し、15nmの厚さの層を形成して発光層とした。この時、化合物1の濃度は6.0重量%とした。次に、PPTを10nmの厚さに形成し、BPyTp2を40nmの厚さに形成した。さらにフッ化リチウム(LiF)を0.8nm真空蒸着し、次いでアルミニウム(Al)を80nmの厚さに蒸着することにより陰極を形成し、有機エレクトロルミネッセンス素子とした。
製造した有機エレクトロルミネッセンス素子の発光スペクトルを図17に示し、電圧-電流密度特性を図18に示し、電流密度-外部量子効率特性を図19に示す。488nmをピークとする発光が確認され、7.9%の高い外部量子効率を達成した。
2 陽極
3 正孔注入層
4 正孔輸送層
5 発光層
6 電子輸送層
7 陰極
Claims (18)
- Ar1~Ar3が置換アリール基を表すとき、アリール基に置換している置換基は、前記一般式(2)で表される置換基、炭素数1~6のアルキル基、炭素数6~14のアリール基、および炭素数7~15のアラルキル基からなる群より選択されることを特徴とする請求項1に記載の化合物。
- 下記一般式(8)で表される構造を有することを特徴とする請求項1に記載の化合物。
- 請求項1~13のいずれか1項に記載の化合物からなる発光材料。
- 下記一般式(1)で表される構造を有する遅延蛍光体。
- 請求項14に記載の発光材料を含む発光層を基板上に有することを特徴とする有機発光素子。
- 遅延蛍光を放射することを特徴とする請求項16に記載の有機発光素子。
- 有機エレクトロルミネッセンス素子であることを特徴とする請求項16または17に記載の有機発光素子。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US14/909,182 US10439148B2 (en) | 2013-08-01 | 2014-07-29 | Compound, light emitting material, and organic light emitting device |
| EP14831835.5A EP3029033B1 (en) | 2013-08-01 | 2014-07-29 | Compound, light-emitting material, and organic light-emitting device |
| CN201480043477.6A CN105531271B (zh) | 2013-08-01 | 2014-07-29 | 化合物、发光材料及有机发光元件 |
| JP2015529573A JP6318155B2 (ja) | 2013-08-01 | 2014-07-29 | 化合物、発光材料および有機発光素子 |
| KR1020167005042A KR102034341B1 (ko) | 2013-08-01 | 2014-07-29 | 화합물, 발광 재료 및 유기 발광 소자 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013-160826 | 2013-08-01 | ||
| JP2013160826 | 2013-08-01 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2015016200A1 true WO2015016200A1 (ja) | 2015-02-05 |
Family
ID=52431733
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2014/069891 WO2015016200A1 (ja) | 2013-08-01 | 2014-07-29 | 化合物、発光材料および有機発光素子 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US10439148B2 (ja) |
| EP (1) | EP3029033B1 (ja) |
| JP (1) | JP6318155B2 (ja) |
| KR (1) | KR102034341B1 (ja) |
| CN (1) | CN105531271B (ja) |
| TW (1) | TWI641599B (ja) |
| WO (1) | WO2015016200A1 (ja) |
Cited By (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN106221691A (zh) * | 2016-04-25 | 2016-12-14 | 中节能万润股份有限公司 | 一种含有氮杂苯基类化合物的有机电致发光器件及其应用 |
| CN106220609A (zh) * | 2016-04-25 | 2016-12-14 | 中节能万润股份有限公司 | 一种以氮杂苯为核心的化合物及其在有机电致发光器件上的应用 |
| JP2016210913A (ja) * | 2015-05-11 | 2016-12-15 | 国立大学法人九州大学 | 発光材料、有機発光素子および化合物 |
| DE102016108327B3 (de) * | 2016-05-04 | 2017-03-02 | Cynora Gmbh | Organische Moleküle, insbesondere zur Verwendung in organischen optoelektronischen Vorrichtungen |
| JP2017210464A (ja) * | 2016-05-26 | 2017-11-30 | 三星ディスプレイ株式會社Samsung Display Co.,Ltd. | 含窒素化合物及び含窒素化合物を含む有機電界発光素子 |
| CN109575039A (zh) * | 2017-09-29 | 2019-04-05 | 江苏三月光电科技有限公司 | 一种氮杂苯类有机化合物及其应用 |
| WO2020076796A1 (en) | 2018-10-09 | 2020-04-16 | Kyulux, Inc. | Novel composition of matter for use in organic light-emitting diodes |
| WO2021157642A1 (ja) | 2020-02-04 | 2021-08-12 | 株式会社Kyulux | ホスト材料、組成物および有機発光素子 |
| US11101440B2 (en) | 2015-07-01 | 2021-08-24 | Kyushu University, National University Corporation | Organic electroluminescent device |
| WO2021235549A1 (ja) | 2020-05-22 | 2021-11-25 | 株式会社Kyulux | 化合物、発光材料および発光素子 |
| WO2022025248A1 (ja) | 2020-07-31 | 2022-02-03 | 株式会社Kyulux | 化合物、発光材料および発光素子 |
| US11271169B2 (en) | 2017-08-24 | 2022-03-08 | Samsung Display Co., Ltd. | Nitrogen-containing compound and organic electroluminescence device including the same |
| US11335872B2 (en) | 2016-09-06 | 2022-05-17 | Kyulux, Inc. | Organic light-emitting device |
| WO2022168956A1 (ja) | 2021-02-04 | 2022-08-11 | 株式会社Kyulux | 化合物、発光材料および有機発光素子 |
| US11476435B2 (en) | 2017-08-24 | 2022-10-18 | Kyushu University, National University Corporation | Film and organic light-emitting device containing perovskite-type compound and organic light-emitting material |
| US11482679B2 (en) | 2017-05-23 | 2022-10-25 | Kyushu University, National University Corporation | Compound, light-emitting lifetime lengthening agent, use of n-type compound, film and light-emitting device |
| WO2022244503A1 (ja) | 2021-05-20 | 2022-11-24 | 株式会社Kyulux | 有機発光素子 |
| WO2022270354A1 (ja) | 2021-06-23 | 2022-12-29 | 株式会社Kyulux | 化合物、発光材料および有機発光素子 |
| WO2022270602A1 (ja) | 2021-06-23 | 2022-12-29 | 株式会社Kyulux | 有機発光素子および膜 |
| WO2022270113A1 (ja) | 2021-06-23 | 2022-12-29 | 株式会社Kyulux | 有機エレクトロルミネッセンス素子 |
| WO2023282224A1 (ja) | 2021-07-06 | 2023-01-12 | 株式会社Kyulux | 有機発光素子およびその設計方法 |
| WO2023053835A1 (ja) | 2021-09-28 | 2023-04-06 | 株式会社Kyulux | 化合物、組成物、ホスト材料、電子障壁材料および有機発光素子 |
| RU2812517C1 (ru) * | 2023-11-20 | 2024-01-30 | Федеральное государственное бюджетное учреждение науки Пермский федеральный исследовательский центр Уральского отделения Российской академии наук | 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридин, проявляющий флуоресцентные свойства и способ его получения |
| US11930654B2 (en) | 2017-07-06 | 2024-03-12 | Kyulux, Inc. | Organic light-emitting element |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102631944B1 (ko) * | 2016-08-03 | 2024-02-02 | 삼성디스플레이 주식회사 | 방향족 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| JP6789195B2 (ja) * | 2016-08-24 | 2020-11-25 | サイノラ ゲゼルシャフト ミット ベシュレンクテル ハフツング | 特に有機光電子デバイスに使用するための有機分子 |
| KR20180054963A (ko) | 2016-11-14 | 2018-05-25 | 삼성디스플레이 주식회사 | 헤테로환 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR20180062561A (ko) | 2016-11-30 | 2018-06-11 | 삼성디스플레이 주식회사 | 다환 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| CN109721595A (zh) * | 2017-10-27 | 2019-05-07 | 苏州大学 | 一种三联吡啶衍生物、制备方法及其在有机电致发光器件中的应用 |
| US11778904B2 (en) * | 2018-05-09 | 2023-10-03 | Kyulux, Inc. | Composition of matter for use in organic light-emitting diodes |
| CN110079305A (zh) * | 2019-05-24 | 2019-08-02 | 武汉华星光电半导体显示技术有限公司 | 深蓝色热活化延迟荧光材料和其制作方法、电致发光器件 |
Citations (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH06312982A (ja) * | 1993-04-30 | 1994-11-08 | Bando Chem Ind Ltd | ヘテロ環基を有するフェニル置換ベンゼン誘導体 |
| JP2000186066A (ja) * | 1998-12-22 | 2000-07-04 | Minolta Co Ltd | 新規アミノ化合物とその製造方法、及び用途 |
| JP2010031259A (ja) * | 2008-06-30 | 2010-02-12 | Sumitomo Chemical Co Ltd | フェノキサジン系高分子化合物及びそれを用いた発光素子 |
| JP2010180204A (ja) * | 2009-01-06 | 2010-08-19 | Fujifilm Corp | 電荷輸送材料及び有機電界発光素子 |
| JP2011210749A (ja) * | 2010-03-26 | 2011-10-20 | Fujifilm Corp | 有機電界発光素子及び電荷輸送材料 |
| WO2012067415A2 (ko) * | 2010-11-19 | 2012-05-24 | 덕산하이메탈(주) | 화합물 및 이를 이용한 유기전기소자, 그 단말 |
| WO2012108879A1 (en) | 2011-02-11 | 2012-08-16 | Universal Display Corporation | Organic light emitting device and materials for use in same |
| KR20120095832A (ko) * | 2012-08-10 | 2012-08-29 | 주식회사 두산 | 신규 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| US20120248968A1 (en) * | 2011-03-25 | 2012-10-04 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| WO2012149999A1 (de) * | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| US20130020558A1 (en) * | 2011-01-20 | 2013-01-24 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| WO2013100603A1 (ko) * | 2011-12-28 | 2013-07-04 | 주식회사 두산 | 유기발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| KR20130115160A (ko) * | 2012-04-10 | 2013-10-21 | 에스에프씨 주식회사 | 이형고리 화합물 및 이를 포함하는 유기전계발광소자 |
| KR20140076521A (ko) * | 2012-12-12 | 2014-06-20 | 에스에프씨 주식회사 | 유기발광 화합물 및 이를 포함하는 유기전계발광소자 |
| KR20140079315A (ko) * | 2012-12-18 | 2014-06-26 | 에스에프씨 주식회사 | 유기발광 화합물 및 이를 포함하는 유기전계발광소자 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4776639B2 (ja) * | 2008-01-18 | 2011-09-21 | 三井化学株式会社 | ピリジン誘導体、およびそれを含む有機電界発光素子 |
| KR101899497B1 (ko) | 2011-03-23 | 2018-09-19 | 박한영 | 원터치 도어 개폐장치 |
| CN103503187B (zh) | 2011-05-05 | 2016-11-02 | 默克专利有限公司 | 用于电子器件的化合物 |
| CN104396042B (zh) * | 2012-06-28 | 2016-10-12 | 新日铁住金化学株式会社 | 有机电致发光元件用材料及有机电致发光元件 |
-
2014
- 2014-07-29 JP JP2015529573A patent/JP6318155B2/ja active Active
- 2014-07-29 CN CN201480043477.6A patent/CN105531271B/zh active Active
- 2014-07-29 WO PCT/JP2014/069891 patent/WO2015016200A1/ja active Application Filing
- 2014-07-29 EP EP14831835.5A patent/EP3029033B1/en active Active
- 2014-07-29 US US14/909,182 patent/US10439148B2/en active Active
- 2014-07-29 KR KR1020167005042A patent/KR102034341B1/ko active IP Right Grant
- 2014-08-01 TW TW103126495A patent/TWI641599B/zh not_active IP Right Cessation
Patent Citations (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH06312982A (ja) * | 1993-04-30 | 1994-11-08 | Bando Chem Ind Ltd | ヘテロ環基を有するフェニル置換ベンゼン誘導体 |
| JP2000186066A (ja) * | 1998-12-22 | 2000-07-04 | Minolta Co Ltd | 新規アミノ化合物とその製造方法、及び用途 |
| JP2010031259A (ja) * | 2008-06-30 | 2010-02-12 | Sumitomo Chemical Co Ltd | フェノキサジン系高分子化合物及びそれを用いた発光素子 |
| JP2010180204A (ja) * | 2009-01-06 | 2010-08-19 | Fujifilm Corp | 電荷輸送材料及び有機電界発光素子 |
| JP2011210749A (ja) * | 2010-03-26 | 2011-10-20 | Fujifilm Corp | 有機電界発光素子及び電荷輸送材料 |
| WO2012067415A2 (ko) * | 2010-11-19 | 2012-05-24 | 덕산하이메탈(주) | 화합물 및 이를 이용한 유기전기소자, 그 단말 |
| US20130020558A1 (en) * | 2011-01-20 | 2013-01-24 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| WO2012108879A1 (en) | 2011-02-11 | 2012-08-16 | Universal Display Corporation | Organic light emitting device and materials for use in same |
| US20120248968A1 (en) * | 2011-03-25 | 2012-10-04 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| WO2012149999A1 (de) * | 2011-05-05 | 2012-11-08 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen |
| WO2013100603A1 (ko) * | 2011-12-28 | 2013-07-04 | 주식회사 두산 | 유기발광 화합물 및 이를 이용한 유기 전계 발광 소자 |
| KR20130115160A (ko) * | 2012-04-10 | 2013-10-21 | 에스에프씨 주식회사 | 이형고리 화합물 및 이를 포함하는 유기전계발광소자 |
| KR20120095832A (ko) * | 2012-08-10 | 2012-08-29 | 주식회사 두산 | 신규 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR20140076521A (ko) * | 2012-12-12 | 2014-06-20 | 에스에프씨 주식회사 | 유기발광 화합물 및 이를 포함하는 유기전계발광소자 |
| KR20140079315A (ko) * | 2012-12-18 | 2014-06-26 | 에스에프씨 주식회사 | 유기발광 화합물 및 이를 포함하는 유기전계발광소자 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP3029033A4 |
Cited By (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2016210913A (ja) * | 2015-05-11 | 2016-12-15 | 国立大学法人九州大学 | 発光材料、有機発光素子および化合物 |
| US11101440B2 (en) | 2015-07-01 | 2021-08-24 | Kyushu University, National University Corporation | Organic electroluminescent device |
| CN106221691B (zh) * | 2016-04-25 | 2020-02-21 | 中节能万润股份有限公司 | 一种含有氮杂苯基类化合物的有机电致发光器件及其应用 |
| CN106220609A (zh) * | 2016-04-25 | 2016-12-14 | 中节能万润股份有限公司 | 一种以氮杂苯为核心的化合物及其在有机电致发光器件上的应用 |
| CN106221691A (zh) * | 2016-04-25 | 2016-12-14 | 中节能万润股份有限公司 | 一种含有氮杂苯基类化合物的有机电致发光器件及其应用 |
| DE102016108327B3 (de) * | 2016-05-04 | 2017-03-02 | Cynora Gmbh | Organische Moleküle, insbesondere zur Verwendung in organischen optoelektronischen Vorrichtungen |
| US10686139B2 (en) | 2016-05-26 | 2020-06-16 | Samsung Display Co., Ltd. | Nitrogen-containing compound and organic electroluminescence device including the same |
| JP2021001175A (ja) * | 2016-05-26 | 2021-01-07 | 三星ディスプレイ株式會社Samsung Display Co.,Ltd. | 含窒素化合物及び含窒素化合物を含む有機電界発光素子 |
| KR20170134841A (ko) | 2016-05-26 | 2017-12-07 | 삼성디스플레이 주식회사 | 함질소 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| JP7078961B2 (ja) | 2016-05-26 | 2022-06-01 | 三星ディスプレイ株式會社 | 含窒素化合物及び含窒素化合物を含む有機電界発光素子 |
| JP2017210464A (ja) * | 2016-05-26 | 2017-11-30 | 三星ディスプレイ株式會社Samsung Display Co.,Ltd. | 含窒素化合物及び含窒素化合物を含む有機電界発光素子 |
| US11335872B2 (en) | 2016-09-06 | 2022-05-17 | Kyulux, Inc. | Organic light-emitting device |
| US11482679B2 (en) | 2017-05-23 | 2022-10-25 | Kyushu University, National University Corporation | Compound, light-emitting lifetime lengthening agent, use of n-type compound, film and light-emitting device |
| US11930654B2 (en) | 2017-07-06 | 2024-03-12 | Kyulux, Inc. | Organic light-emitting element |
| US11476435B2 (en) | 2017-08-24 | 2022-10-18 | Kyushu University, National University Corporation | Film and organic light-emitting device containing perovskite-type compound and organic light-emitting material |
| US11271169B2 (en) | 2017-08-24 | 2022-03-08 | Samsung Display Co., Ltd. | Nitrogen-containing compound and organic electroluminescence device including the same |
| CN109575039A (zh) * | 2017-09-29 | 2019-04-05 | 江苏三月光电科技有限公司 | 一种氮杂苯类有机化合物及其应用 |
| CN109575039B (zh) * | 2017-09-29 | 2022-02-08 | 江苏三月科技股份有限公司 | 一种氮杂苯类有机化合物及其应用 |
| WO2020076796A1 (en) | 2018-10-09 | 2020-04-16 | Kyulux, Inc. | Novel composition of matter for use in organic light-emitting diodes |
| WO2021157593A1 (ja) | 2020-02-04 | 2021-08-12 | 株式会社Kyulux | 組成物、膜、有機発光素子、発光組成物を提供する方法およびプログラム |
| WO2021157642A1 (ja) | 2020-02-04 | 2021-08-12 | 株式会社Kyulux | ホスト材料、組成物および有機発光素子 |
| WO2021235549A1 (ja) | 2020-05-22 | 2021-11-25 | 株式会社Kyulux | 化合物、発光材料および発光素子 |
| WO2022025248A1 (ja) | 2020-07-31 | 2022-02-03 | 株式会社Kyulux | 化合物、発光材料および発光素子 |
| WO2022168956A1 (ja) | 2021-02-04 | 2022-08-11 | 株式会社Kyulux | 化合物、発光材料および有機発光素子 |
| WO2022244503A1 (ja) | 2021-05-20 | 2022-11-24 | 株式会社Kyulux | 有機発光素子 |
| WO2022270602A1 (ja) | 2021-06-23 | 2022-12-29 | 株式会社Kyulux | 有機発光素子および膜 |
| WO2022270113A1 (ja) | 2021-06-23 | 2022-12-29 | 株式会社Kyulux | 有機エレクトロルミネッセンス素子 |
| WO2022270354A1 (ja) | 2021-06-23 | 2022-12-29 | 株式会社Kyulux | 化合物、発光材料および有機発光素子 |
| WO2023282224A1 (ja) | 2021-07-06 | 2023-01-12 | 株式会社Kyulux | 有機発光素子およびその設計方法 |
| WO2023053835A1 (ja) | 2021-09-28 | 2023-04-06 | 株式会社Kyulux | 化合物、組成物、ホスト材料、電子障壁材料および有機発光素子 |
| RU2812517C1 (ru) * | 2023-11-20 | 2024-01-30 | Федеральное государственное бюджетное учреждение науки Пермский федеральный исследовательский центр Уральского отделения Российской академии наук | 2,6-бис-(4-(9H-карбазол-9-ил)фенил)-4-(4-N,N-дифениламинофенил)пиридин, проявляющий флуоресцентные свойства и способ его получения |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3029033B1 (en) | 2021-06-16 |
| JP6318155B2 (ja) | 2018-04-25 |
| US10439148B2 (en) | 2019-10-08 |
| KR102034341B1 (ko) | 2019-10-18 |
| CN105531271A (zh) | 2016-04-27 |
| EP3029033A4 (en) | 2017-04-05 |
| TWI641599B (zh) | 2018-11-21 |
| JPWO2015016200A1 (ja) | 2017-03-02 |
| CN105531271B (zh) | 2019-04-12 |
| US20160172600A1 (en) | 2016-06-16 |
| KR20160035062A (ko) | 2016-03-30 |
| EP3029033A1 (en) | 2016-06-08 |
| TW201520203A (zh) | 2015-06-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6318155B2 (ja) | 化合物、発光材料および有機発光素子 | |
| JP5594750B2 (ja) | 化合物、発光材料および有機発光素子 | |
| JP6225111B2 (ja) | 発光材料、化合物、およびそれらを用いた有機発光素子 | |
| JP6277182B2 (ja) | 化合物、発光材料および有機発光素子 | |
| JP5679496B2 (ja) | 有機発光素子ならびにそれに用いる遅延蛍光材料および化合物 | |
| JP6263524B2 (ja) | 化合物、発光材料および有機発光素子 | |
| JP6668152B2 (ja) | 化合物、発光材料および有機発光素子 | |
| KR102168905B1 (ko) | 유기 발광 소자 그리고 그것에 사용하는 발광 재료 및 화합물 | |
| JP6326050B2 (ja) | 化合物、発光材料および有機発光素子 | |
| JP6293417B2 (ja) | 化合物、発光材料および有機発光素子 | |
| JP6367189B2 (ja) | 発光材料、有機発光素子および化合物 | |
| JP6600298B2 (ja) | 発光材料、有機発光素子および化合物 | |
| WO2015080183A1 (ja) | 発光材料、有機発光素子および化合物 | |
| WO2015002213A1 (ja) | 発光材料、遅延蛍光体、有機発光素子および化合物 | |
| WO2013161437A1 (ja) | 発光材料および有機発光素子 | |
| JPWO2018159662A1 (ja) | 化合物、発光材料および有機発光素子 | |
| JP2017119663A (ja) | 化合物、発光材料および有機発光素子 | |
| WO2017115834A1 (ja) | 化合物、発光材料および有機発光素子 | |
| JP2016084283A (ja) | 化合物、発光材料および有機発光素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201480043477.6 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 14831835 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2015529573 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14909182 Country of ref document: US |
|
| ENP | Entry into the national phase |
Ref document number: 20167005042 Country of ref document: KR Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2014831835 Country of ref document: EP |