WO2011122418A1 - 水素製造装置及び燃料電池システム - Google Patents
水素製造装置及び燃料電池システム Download PDFInfo
- Publication number
- WO2011122418A1 WO2011122418A1 PCT/JP2011/057013 JP2011057013W WO2011122418A1 WO 2011122418 A1 WO2011122418 A1 WO 2011122418A1 JP 2011057013 W JP2011057013 W JP 2011057013W WO 2011122418 A1 WO2011122418 A1 WO 2011122418A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- reformed gas
- selective oxidation
- oxidation reaction
- gas
- flow path
- Prior art date
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/06—Combination of fuel cells with means for production of reactants or for treatment of residues
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J8/00—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes
- B01J8/02—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds
- B01J8/04—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds the fluid passing successively through two or more beds
- B01J8/0446—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds the fluid passing successively through two or more beds the flow within the beds being predominantly vertical
- B01J8/0461—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds the fluid passing successively through two or more beds the flow within the beds being predominantly vertical in two or more cylindrical annular shaped beds
- B01J8/0465—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds the fluid passing successively through two or more beds the flow within the beds being predominantly vertical in two or more cylindrical annular shaped beds the beds being concentric
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J7/00—Apparatus for generating gases
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J8/00—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes
- B01J8/02—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds
- B01J8/04—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds the fluid passing successively through two or more beds
- B01J8/0446—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds the fluid passing successively through two or more beds the flow within the beds being predominantly vertical
- B01J8/0461—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds the fluid passing successively through two or more beds the flow within the beds being predominantly vertical in two or more cylindrical annular shaped beds
- B01J8/0469—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds the fluid passing successively through two or more beds the flow within the beds being predominantly vertical in two or more cylindrical annular shaped beds the beds being superimposed one above the other
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J8/00—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes
- B01J8/02—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds
- B01J8/04—Chemical or physical processes in general, conducted in the presence of fluids and solid particles; Apparatus for such processes with stationary particles, e.g. in fixed beds the fluid passing successively through two or more beds
- B01J8/0496—Heating or cooling the reactor
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B3/00—Hydrogen; Gaseous mixtures containing hydrogen; Separation of hydrogen from mixtures containing it; Purification of hydrogen
- C01B3/02—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen
- C01B3/32—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air
- C01B3/34—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air by reaction of hydrocarbons with gasifying agents
- C01B3/38—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air by reaction of hydrocarbons with gasifying agents using catalysts
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B3/00—Hydrogen; Gaseous mixtures containing hydrogen; Separation of hydrogen from mixtures containing it; Purification of hydrogen
- C01B3/02—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen
- C01B3/32—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air
- C01B3/34—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air by reaction of hydrocarbons with gasifying agents
- C01B3/48—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air by reaction of hydrocarbons with gasifying agents followed by reaction of water vapour with carbon monoxide
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B3/00—Hydrogen; Gaseous mixtures containing hydrogen; Separation of hydrogen from mixtures containing it; Purification of hydrogen
- C01B3/50—Separation of hydrogen or hydrogen containing gases from gaseous mixtures, e.g. purification
- C01B3/56—Separation of hydrogen or hydrogen containing gases from gaseous mixtures, e.g. purification by contacting with solids; Regeneration of used solids
- C01B3/58—Separation of hydrogen or hydrogen containing gases from gaseous mixtures, e.g. purification by contacting with solids; Regeneration of used solids including a catalytic reaction
- C01B3/583—Separation of hydrogen or hydrogen containing gases from gaseous mixtures, e.g. purification by contacting with solids; Regeneration of used solids including a catalytic reaction the reaction being the selective oxidation of carbon monoxide
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2208/00—Processes carried out in the presence of solid particles; Reactors therefor
- B01J2208/00008—Controlling the process
- B01J2208/00017—Controlling the temperature
- B01J2208/00106—Controlling the temperature by indirect heat exchange
- B01J2208/00168—Controlling the temperature by indirect heat exchange with heat exchange elements outside the bed of solid particles
- B01J2208/00212—Plates; Jackets; Cylinders
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2208/00—Processes carried out in the presence of solid particles; Reactors therefor
- B01J2208/00008—Controlling the process
- B01J2208/00017—Controlling the temperature
- B01J2208/00106—Controlling the temperature by indirect heat exchange
- B01J2208/00265—Part of all of the reactants being heated or cooled outside the reactor while recycling
- B01J2208/00283—Part of all of the reactants being heated or cooled outside the reactor while recycling involving reactant liquids
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2208/00—Processes carried out in the presence of solid particles; Reactors therefor
- B01J2208/00008—Controlling the process
- B01J2208/00017—Controlling the temperature
- B01J2208/00504—Controlling the temperature by means of a burner
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/02—Processes for making hydrogen or synthesis gas
- C01B2203/0205—Processes for making hydrogen or synthesis gas containing a reforming step
- C01B2203/0227—Processes for making hydrogen or synthesis gas containing a reforming step containing a catalytic reforming step
- C01B2203/0233—Processes for making hydrogen or synthesis gas containing a reforming step containing a catalytic reforming step the reforming step being a steam reforming step
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/02—Processes for making hydrogen or synthesis gas
- C01B2203/0283—Processes for making hydrogen or synthesis gas containing a CO-shift step, i.e. a water gas shift step
- C01B2203/0288—Processes for making hydrogen or synthesis gas containing a CO-shift step, i.e. a water gas shift step containing two CO-shift steps
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/04—Integrated processes for the production of hydrogen or synthesis gas containing a purification step for the hydrogen or the synthesis gas
- C01B2203/0435—Catalytic purification
- C01B2203/044—Selective oxidation of carbon monoxide
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/04—Integrated processes for the production of hydrogen or synthesis gas containing a purification step for the hydrogen or the synthesis gas
- C01B2203/0465—Composition of the impurity
- C01B2203/047—Composition of the impurity the impurity being carbon monoxide
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/06—Integration with other chemical processes
- C01B2203/066—Integration with other chemical processes with fuel cells
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/08—Methods of heating or cooling
- C01B2203/0805—Methods of heating the process for making hydrogen or synthesis gas
- C01B2203/0811—Methods of heating the process for making hydrogen or synthesis gas by combustion of fuel
- C01B2203/0816—Heating by flames
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/08—Methods of heating or cooling
- C01B2203/0805—Methods of heating the process for making hydrogen or synthesis gas
- C01B2203/0811—Methods of heating the process for making hydrogen or synthesis gas by combustion of fuel
- C01B2203/0827—Methods of heating the process for making hydrogen or synthesis gas by combustion of fuel at least part of the fuel being a recycle stream
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/08—Methods of heating or cooling
- C01B2203/0872—Methods of cooling
- C01B2203/0888—Methods of cooling by evaporation of a fluid
- C01B2203/0894—Generation of steam
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/12—Feeding the process for making hydrogen or synthesis gas
- C01B2203/1258—Pre-treatment of the feed
- C01B2203/1264—Catalytic pre-treatment of the feed
- C01B2203/127—Catalytic desulfurisation
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/12—Feeding the process for making hydrogen or synthesis gas
- C01B2203/1288—Evaporation of one or more of the different feed components
- C01B2203/1294—Evaporation by heat exchange with hot process stream
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/80—Aspect of integrated processes for the production of hydrogen or synthesis gas not covered by groups C01B2203/02 - C01B2203/1695
- C01B2203/82—Several process steps of C01B2203/02 - C01B2203/08 integrated into a single apparatus
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/06—Combination of fuel cells with means for production of reactants or for treatment of residues
- H01M8/0606—Combination of fuel cells with means for production of reactants or for treatment of residues with means for production of gaseous reactants
- H01M8/0612—Combination of fuel cells with means for production of reactants or for treatment of residues with means for production of gaseous reactants from carbon-containing material
- H01M8/0618—Reforming processes, e.g. autothermal, partial oxidation or steam reforming
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M8/00—Fuel cells; Manufacture thereof
- H01M8/06—Combination of fuel cells with means for production of reactants or for treatment of residues
- H01M8/0662—Treatment of gaseous reactants or gaseous residues, e.g. cleaning
- H01M8/0675—Removal of sulfur
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/30—Hydrogen technology
- Y02E60/50—Fuel cells
Definitions
- the present invention relates to a hydrogen production apparatus and a fuel cell system.
- an apparatus including a selective oxidation reaction unit that selectively oxidizes carbon monoxide in a reformed gas generated by reforming raw fuel such as hydrocarbon is known (for example, , See Patent Document 1).
- an external heater such as a heater is usually used.
- water for generating steam at a position adjacent to the inner peripheral side of the cylindrical selective oxidation reaction unit is used.
- the temperature of the selective oxidation reaction unit can be controlled by the water temperature supplied to the water evaporation unit without using a heater.
- the selective oxidation reaction section since the flow path through which water or water vapor flows is provided at a position adjacent to the selective oxidation reaction section, when the water temperature in the flow path is low, the selective oxidation reaction section The temperature of the selective oxidation catalyst is lowered. When the temperature of the selective oxidation catalyst becomes too low, there is a problem in that the selective oxidation catalyst is oxidized and deteriorated and the life of the catalyst is shortened. On the other hand, when an appropriate cooling structure for the selective oxidation reaction section is not provided, the temperature of the selective oxidation catalyst is increased so that the methanation reaction of carbon monoxide and carbon dioxide proceeds and the temperature exceeds the heat resistance temperature of the member. There was a problem that risend. From the above, it has been required to keep the temperature of the selective oxidation reaction part at an optimum temperature.
- a hydrogen production apparatus includes a selective oxidation reaction unit that selectively oxidizes carbon monoxide in a reformed gas containing hydrogen, an evaporation channel that circulates water to generate water vapor, and a gas channel that circulates the reformed gas
- the gas flow path is disposed between the selective oxidation reaction section and the evaporation flow path, and the reformed gas flows through the gas flow path and then flows into the selective oxidation reaction section.
- a gas flow path through which the reformed gas flows is disposed between the evaporation flow path for flowing water to generate water vapor and the selective oxidation reaction section.
- the selective oxidation reaction unit can cause the gas flow channel to function as a heat medium without directly contacting the evaporation flow channel through which water flows. This can prevent the temperature of the selective oxidation catalyst in the selective oxidation reaction section from becoming too low.
- the gas flow path can circulate the reformed gas supplied to the selective oxidation reaction unit, that is, the inlet gas of the selective oxidation reaction unit.
- the reformed gas as the inlet gas of the selective oxidation reaction section is cooled by supplying heat to water and water vapor in the evaporation channel when the temperature is higher than necessary, but does not become lower than necessary. In addition, it is kept at an appropriate temperature by water or water vapor in the evaporation channel. As a result, the reformed gas that has flowed through the gas flow path is supplied to the selective oxidation reaction section at an optimum temperature.
- the temperature of the selective oxidation reaction unit can be maintained at an optimum temperature with a simple structure without using an external heater such as a heater, and the life of the selective oxidation catalyst can be extended. Is possible.
- the hydrogen production apparatus further includes an exhaust gas passage through which the exhaust gas of the burner used to generate the reformed gas flows, and the exhaust gas passage is disposed at a position adjacent to the evaporation passage on the opposite side of the gas passage. It may be. Since the exhaust gas flow channel is disposed at a position adjacent to the evaporation flow channel, the water in the evaporation flow channel can be efficiently evaporated by receiving heat from the high temperature exhaust gas. Furthermore, the evaporating channel can reliably maintain the reformed gas at the optimum temperature without overcooling the reformed gas in the gas channel.
- a shift reaction unit that removes carbon monoxide in the reformed gas by a shift reaction
- an air supply unit that supplies air to the reformed gas from the shift reaction unit toward the selective oxidation reaction unit
- the shift reaction unit has an outlet through which the reformed gas after the shift reaction flows out, and the air supply unit opposes the flow of the reformed gas with respect to the reformed gas flowing out from the outlet. Air may be supplied from the direction.
- the reformed gas from which carbon monoxide has been removed by the shift reaction is collected at the outlet when it flows out of the shift reaction section.
- the air supply unit can supply air to the reformed gas collected at the outlet. Thereby, the air and the reformed gas can be mixed efficiently.
- the air supply unit can supply air from the direction opposite to the flow of the reformed gas, the reformed gas and the air collide and are mixed more efficiently.
- the fuel cell system includes the hydrogen production apparatus and a fuel cell stack that generates power using the reformed gas generated by the hydrogen production apparatus.
- This fuel cell system also includes the above-described hydrogen production apparatus, and therefore the above-described effect that the temperature of the selective oxidation reaction section can be maintained at an optimum temperature with a simple structure without using an external heater such as a heater. Is played.
- the present invention it is possible to keep the temperature of the selective oxidation reaction section at an optimum temperature with a simple structure without using an external heater such as a heater.
- FIG. 3 is an enlarged view of a configuration around a selective oxidation reaction unit shown in FIG. 2. It is a block diagram which shows the flow of the heat
- FIG. 1 is a schematic block diagram showing a part of a fuel cell system according to an embodiment.
- a hydrogen production apparatus (FPS: Fuel Processing System) 1 is used as a hydrogen supply source in a fuel cell system 100 for home use, for example.
- the hydrogen production apparatus 1 here uses petroleum-based hydrocarbons as a raw fuel, and supplies a reformed gas containing hydrogen to a cell stack (fuel cell stack) 20.
- alcohols, ethers, biofuels, natural gas, and city gas may be used as raw fuel.
- petroleum-based hydrocarbons, naphtha, light oil, etc. can be used as raw fuel in addition to kerosene and LP gas.
- various types such as a solid polymer type, an alkaline electrolyte type, a phosphoric acid type, a molten carbonate type, or a solid oxide type may be used.
- FIG. 2 is a schematic front end view showing the hydrogen production apparatus of FIG.
- the hydrogen production apparatus 1 includes a desulfurization part 2 having a cylindrical outer shape with a central axis as an axis G, and a main body part 3 with a cylindrical outer shape having a central axis as an axis G. These are accommodated in the housing 4. Further, in the casing 4, the surroundings of the desulfurization part 2 and the main body part 3 are filled with a powdery heat insulating material (not shown) to be insulated.
- the desulfurization unit 2 may be installed outside the housing 4.
- the desulfurization unit 2 desulfurizes raw fuel introduced from the outside with a desulfurization catalyst to remove sulfur, and supplies the raw fuel to a feed unit 5 described later.
- the desulfurization part 2 is fixed to the side plate 4x of the housing 4 by a pipe 21 and is held so as to surround the upper part of the main body part 3 with a predetermined gap.
- the main body 3 includes a feed unit 5, a reforming unit 6, a shift reaction unit 7, a selective oxidation reaction unit 8, and an evaporation unit 9, which are integrally configured.
- the main body 3 is fixed and held on a floor plate 4 y of the housing 4 by a cylindrical stay 22.
- the feed unit 5 mixes the raw fuel and steam (steam) desulfurized in the desulfurization unit 2 and supplies them to the reforming unit 6.
- the feed unit 5 includes a mixing unit 5x that combines and mixes raw fuel and water vapor to generate a mixed gas (mixed fluid), and a mixed gas channel 5y that distributes the mixed gas to the reforming unit 6. , Including.
- the reforming section (SR: Steam Reforming) 6 steam-reforms the mixed gas supplied from the feed section 5 with a reforming catalyst (reforming catalyst section) 6x to generate a reformed gas.
- the reforming part 6 has a cylindrical outer shape with the central axis as the axis G, and is provided on the upper end side of the main body part 3 so as to be located in the cylinder of the desulfurization part 2.
- the burner 10 is used as a heat source for heating the reforming catalyst 6x of the reforming section 6.
- raw fuel is supplied as burner fuel from the outside and burned.
- the burner 10 is attached to a combustion cylinder 11 provided at the upper end of the main body 3 and having the axis G as a central axis so that a flame by the burner 10 is surrounded.
- a part of the raw fuel desulfurized in the desulfurization unit 2 may be supplied as burner fuel and burned.
- the shift reaction unit 7 is for lowering the carbon monoxide concentration (CO concentration) of the reformed gas supplied from the reforming unit 6, and shifts the carbon monoxide in the reformed gas to generate hydrogen and Convert to carbon dioxide.
- the shift reaction section 7 can perform the shift reaction in two stages, and performs a high temperature shift reaction that is a shift reaction at a high temperature (for example, 400 ° C. to 600 ° C.).
- HTS High Temperature Shift
- LTS LowTemperature Shift 13 for performing a low temperature shift reaction that is a shift reaction at a temperature lower than the temperature of the high temperature shift reaction (for example, 150 ° C to 350 ° C).
- the high temperature shift reaction unit 12 is not necessarily provided.
- the high temperature shift reaction unit 12 causes the carbon monoxide in the reformed gas supplied from the reforming unit 6 to undergo a high temperature shift reaction with the high temperature shift catalyst 12x, thereby reducing the CO concentration of the reformed gas.
- the high temperature shift reaction section 12 has a cylindrical outer shape with the central axis as the axis G, and is disposed adjacent to the radially outer side of the reforming section 6 so that the high temperature shift catalyst 12x surrounds the lower end of the reforming catalyst 6x. ing.
- the high temperature shift reaction unit 12 supplies the reformed gas having a reduced CO concentration to the low temperature shift reaction unit 13.
- the low temperature shift reaction unit 13 causes the carbon monoxide in the reformed gas subjected to the high temperature shift reaction in the high temperature shift reaction unit 12 to undergo a low temperature shift reaction by the low temperature shift catalyst 13x, thereby reducing the CO concentration of the reformed gas.
- the low temperature shift reaction part 13 has a cylindrical outer shape with the central axis as the axis G, and is disposed on the lower end side of the main body part 3.
- the low temperature shift reaction unit 13 supplies the reformed gas having a reduced CO concentration to the selective oxidation reaction unit 8 via the reformed gas pipe 14x.
- a selective oxidation reaction unit (PROX) 8 further reduces the CO concentration in the reformed gas subjected to the low temperature shift reaction in the low temperature shift reaction unit 13. This is because if a high concentration of carbon monoxide is supplied to the cell stack 20, the catalyst of the cell stack 20 is poisoned and the performance is greatly reduced. Specifically, the selective oxidation reaction section 8 reacts carbon monoxide in the reformed gas with air introduced through the air pipe 15 by the selective oxidation catalyst 8x, thereby converting hydrogen in the reformed gas. Without oxidizing, carbon monoxide is selectively oxidized and converted to carbon dioxide.
- the selective oxidation reaction portion 8 has a cylindrical outer shape with the central axis as the axis G, and is disposed so as to constitute the outermost peripheral side of the main body portion 3 from the lower end of the main body portion 3 to the upper end side of a predetermined length. .
- the selective oxidation reaction unit 8 guides the reformed gas whose CO concentration is further reduced to the outside through the reformed gas pipe 14y provided with the heat exchange unit 16.
- the heat exchanging unit 16 exchanges heat between the reformed gas flowing through the reformed gas pipe 14y and the water introduced from the outside through the water pipe 17x, and supplies the water to the evaporator 9 Supply via the pipe 17y.
- the evaporation unit 9 stores the water supplied from the heat exchange unit 16 and moves the water from the low temperature shift reaction unit 13 and the selective oxidation reaction unit 8 (the low temperature shift reaction unit 13 and the selective oxidation reaction unit). Steam is generated by vaporizing with heat (obtained by cooling 8) and heat of exhaust gas from the burner 10.
- the evaporator 9 is of a jacket type and has a cylindrical shape with the central axis as the axis G.
- the evaporation unit 9 is located radially outside the high temperature shift reaction unit 12 and the low temperature shift reaction unit 13 and inside the selective oxidation reaction unit 8 (that is, between the shift reaction unit 7 and the selective oxidation reaction unit 8). It is arranged to be located.
- the evaporation unit 9 supplies the generated water vapor to the mixing unit 5x of the feed unit 5 via the water vapor pipe 17z.
- the raw fuel desulfurized in the desulfurization unit 2 and the water vapor from the evaporation unit 9 are mixed in the mixing unit 5x to generate a mixed gas.
- This mixed gas is supplied to the reforming unit 6 via the mixed gas flow path 5y and steam reformed by the reforming catalyst 6x, thereby generating a reformed gas.
- the generated reformed gas has its carbon monoxide concentration lowered to, for example, about several thousand ppm by the shift reaction unit 7, and after its carbon monoxide concentration has been lowered to about 10 ppm or less by the selective oxidation reaction unit 8. Then, it is cooled by the heat exchange unit 16 and led out to the cell stack 20 at the subsequent stage.
- the temperature of each part is set as follows in order to suitably perform the catalytic reaction with the respective catalysts 6x, 12x, 13x, and 8x. That is, the temperature of the mixed gas flowing into the reforming unit 6 is set to about 300 to 550 ° C., and the temperature of the reformed gas flowing out of the reforming unit 6 is set to 550 ° C. to 800 ° C. and flows into the high temperature shift reaction unit 12 The temperature of the reformed gas is 400 to 600 ° C., and the temperature of the reformed gas flowing out from the high temperature shift reaction unit 12 is 300 to 500 ° C. Further, the temperature of the reformed gas flowing into the low temperature shift reaction unit 13 is set to 150 ° C.
- the temperature of the reformed gas flowing out from the low temperature shift reaction unit 13 is set to 150 ° C. to 250 ° C.
- the temperature of the reformed gas flowing into 8 is set to 90 ° C. to 210 ° C. (120 ° C. to 190 ° C.).
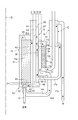
- FIG. 3 is an enlarged view of the configuration around the selective oxidation reaction section shown in FIG.
- the carbon monoxide removal structure of the hydrogen production apparatus 1 has a low-temperature shift reaction unit 13, a shift reaction inlet gas flow path 31, an exhaust gas flow from the axis G side toward the outer peripheral side.
- the channel 32, the water evaporation channel 33, the selective oxidation reaction inlet gas channel 34, and the selective oxidation reaction unit 8 are provided in this order.
- the low temperature shift reaction section 13, the shift reaction inlet gas flow path 31, the exhaust gas flow path 32, the water evaporation flow path 33, the selective oxidation reaction inlet gas flow path 34, and the selective oxidation reaction section 8 all have the axis G as the central axis. It has a cylindrical shape and is arranged so as to be adjacent to each other in the radial direction.
- the low temperature shift reaction unit 13 includes a peripheral wall 41, a peripheral wall 42, a lower end wall 43, a punching plate 44, a punching plate 45, and a low temperature shift catalyst 13x.
- the peripheral wall 41 and the peripheral wall 42 have a cylindrical shape (circular tube shape) having the axis G as a central axis.
- a gap for filling the low temperature shift catalyst 13x is formed between the peripheral wall 41 and the peripheral wall 42.
- the lower end wall 43 has a disk shape extending along the radial direction, and blocks the lower side of the low temperature shift reaction unit 13 continuously from the lower ends of the peripheral wall 41 and the peripheral wall 42.
- the peripheral wall 42 extends further upward than the peripheral wall 41.
- the punching plate 44 has a disk shape extending along the radial direction, and is provided between the peripheral wall 41 and the peripheral wall 42 at a position spaced upward from the lower end wall 43.
- the punching plate 45 has a disk shape extending along the radial direction, and is provided between the peripheral wall 41 and the peripheral wall 42 at a position on the upper end side of the peripheral wall 41.
- the low temperature shift catalyst 13x is filled in a space formed by the peripheral wall 41, the peripheral wall 42, the punching plate 44, and the punching plate 45.
- the low temperature shift reaction part 13 has the exit 52 which flows out the reformed gas after shift reaction.
- the low temperature shift reaction part 13 is good also as a structure which does not use a punching board.
- a mixing structure 50 for efficiently mixing the reformed gas and the air after the shift reaction is provided below the low temperature shift reaction unit 13.
- the mixing structure 50 includes an internal space 51, an outlet 52, a reformed gas pipe 14x, and an air pipe (air supply unit) 15.
- the internal space 51 is an annular space formed between the lower end wall 43 and the punching plate 44.
- the internal space 51 can efficiently collect the reformed gas after the shift reaction at the outlet 52.
- the outlet 52 is a through hole formed in the lower end wall 43 of the low temperature shift reaction unit 13. Since the outlet 52 is formed only at one place on the lower end wall 43, the reformed gas after the shift reaction can be collected at one place.
- the reformed gas pipe 14 x is a pipe connected to the outlet 52. The reformed gas pipe 14 x allows the reformed gas after the shift reaction to flow to the selective oxidation reaction inlet gas channel 34.
- the reformed gas pipe 14 x includes a pipe portion 14 a that extends upward from below the low temperature shift reaction portion 13 with the axis G as the central axis and is connected to the outlet 52.
- the tip of the air pipe 15 is inserted into the reformed gas pipe 14x.
- the distal end portion of the air pipe 15 is disposed coaxially with the pipe portion 14 a inside the pipe portion 14 a of the reformed gas pipe 14 x and extends upward toward the outlet 52.
- the outlet 52 can collect the reformed gas after the shift reaction in one place and flow the reformed gas downward into the pipe portion 14a of the reformed gas pipe 14x.
- the air pipe 15 can supply air to the reformed gas passing through the outlet 52 from the lower side to the upper side (that is, from the direction facing the flow of the reformed gas).
- the mixing structure 50 can efficiently mix the reformed gas and air after the shift reaction in the vicinity of the outlet 52.
- the mixing position of the reformed gas and air is not particularly limited, and may be a position away from the outlet 52, but the position closer to the outlet 52 is preferable because the flow rate of the reformed gas is high and the mixing efficiency is good.
- the shift reaction inlet gas channel 31 is a channel through which the inlet gas to the low temperature shift reaction unit 13 circulates, and includes a peripheral wall 42 and a peripheral wall 61.
- the peripheral wall 61 has a cylindrical shape (circular tube shape) having the axis G as a central axis.
- the shift reaction inlet gas flow path 31 is constituted by a gap between the peripheral wall 41 and the peripheral wall 61.
- the peripheral wall 61 is connected to a lower end wall 62 arranged so as to be spaced downward from the lower end wall 43 of the low temperature shift reaction unit 13.
- the reformed gas flowing through the shift reaction inlet gas channel 31 flows so as to wrap around the lower end wall 43 and the peripheral wall 41 of the low temperature shift reaction unit 13 and is supplied to the low temperature shift reaction unit 13 from above.
- the reformed gas supplied to the low temperature shift reaction unit 13 is not limited to such a flow, and may be supplied to the low temperature shift reaction unit 13 through any flow path. Therefore, the shift reaction inlet gas flow path 31 may not be provided in such an arrangement.
- the exhaust gas channel 32 is a channel through which the exhaust gas from the burner is circulated, and includes a peripheral wall 61, a peripheral wall 63, a lower end wall 64, and an outer peripheral wall 66.
- the peripheral wall 63 has a cylindrical shape (circular tube shape) having the axis G as a central axis.
- the exhaust gas flow path 32 is configured by a gap between the peripheral wall 61 and the peripheral wall 63.
- a lower end portion of the peripheral wall 63 is connected to an annular lower end wall 64 spaced upward from the lower end wall 62. Further, the outer peripheral end portions of the lower end wall 64 and the lower end wall 62 are closed by a cylindrical outer peripheral wall 66.
- the exhaust gas flow channel 32 circulates the exhaust gas from the reforming unit 6 side from above to below.
- the water evaporation channel 33 is a channel through which water or water vapor of the evaporation unit 9 is circulated, and includes a peripheral wall 63, a lower end wall 64, a peripheral wall 67, and an upper end wall 68.
- the peripheral wall 67 has a cylindrical shape (circular tube shape) having the axis G as a central axis.
- the water evaporation channel 33 is constituted by a gap between the peripheral wall 63 and the peripheral wall 67.
- a lower end portion of the peripheral wall 67 is connected to the lower end wall 64.
- the lower end wall 64 has a disk shape extending in the radial direction, and closes the lower side of the water evaporation channel 33 continuously to the lower ends of the peripheral wall 63 and the peripheral wall 67.
- the upper end wall 68 has a disk shape extending in the radial direction, and continuously closes the upper ends of the peripheral wall 63 and the peripheral wall 67 and closes the upper side of the water evaporation channel 33. Near the lower end of the peripheral wall 67, a water pipe 17x is connected.
- the water evaporation channel 33 circulates the water supplied from the water pipe 17x from below to above. Since water evaporates in the water evaporation channel 33, the water evaporation channel 33 has a lower water layer and an upper steam layer.
- the position of the water surface in the water evaporation channel 33 is not particularly limited, but is preferably at least above the upper end position of the selective oxidation catalyst 8x. Further, the upper end of the water evaporation channel 33, that is, the position of the upper end wall 68 is not particularly limited, and may be arranged at a position higher than the position shown in the figure.
- the selective oxidation reaction inlet gas flow path 34 is a flow path for circulating the inlet gas to the selective oxidation reaction portion 8 and is constituted by a peripheral wall 67, a peripheral wall 69, a lower end wall 71, and an upper end wall 72.
- the lower end wall 71 has a disk shape extending along the radial direction, and is provided on the outer peripheral surface of the peripheral wall 67.
- the lower end wall 71 is disposed above the connection position of the water pipe 17x.
- the upper end wall 72 has a disk shape extending along the radial direction, and is provided on the outer peripheral surface of the peripheral wall 67.
- the peripheral wall 69 has a cylindrical shape (circular tubular shape) with the axis G as the central axis, and extends between the lower end wall 71 and the upper end wall 72.
- the lower end of the peripheral wall 69 is separated from the lower end wall 71, and the upper end of the peripheral wall 69 is separated from the upper end wall 72.
- the selective oxidation reaction inlet gas channel 34 is formed by a gap between the peripheral wall 67 and the peripheral wall 69.
- the outer peripheral end of the lower end wall 71 and the outer peripheral end of the upper end wall 72 are connected by a peripheral wall 73.
- the peripheral wall 73 has a cylindrical shape (circular tube) with the axis G as the central axis on the outer peripheral side of the peripheral wall 69.
- a reformed gas pipe 14 x is connected near the lower end of the peripheral wall 73.
- the selective oxidation reaction inlet gas flow path 34 allows the reformed gas supplied from the reformed gas pipe 14x to flow from below to above.
- the positions of the upper end and the lower end of the selective oxidation reaction inlet gas channel 34, that is, the positions of the upper end wall 72 and the lower end wall 71 are not limited to the positions shown in the figure.
- the selective oxidation reaction section 8 includes a peripheral wall 69, a peripheral wall 73, a punching plate 74, a punching plate 76, a lower end wall 77, and a selective oxidation catalyst 8x.
- a gap for filling the selective oxidation catalyst 8x is formed between the peripheral wall 69 and the peripheral wall 73.
- the punching plate 74 has a disk shape extending in the radial direction, and is provided between the peripheral wall 69 and the peripheral wall 73 at a position on the lower end side of the peripheral wall 69.
- the punching plate 76 has a disk shape extending along the radial direction, and is provided between the peripheral wall 69 and the peripheral wall 73 at a position on the upper end side of the peripheral wall 69.
- the selective oxidation catalyst 8x is filled in a space constituted by the peripheral wall 69, the peripheral wall 73, the punching plate 74, and the punching plate 76.
- the lower end wall 77 has a disk shape extending along the radial direction, and closes the lower side of the selective oxidation reaction unit 8 continuously from the lower end of the peripheral wall 69 and the inner peripheral surface of the peripheral wall 73.
- a reformed gas pipe 14 y is connected to the peripheral wall 73 at a position between the lower end wall 77 and the punching plate 74. Note that the selective oxidation reaction unit 8 may be configured not to use a punching plate.
- FIG. 4 is a block diagram showing the heat flow around the selective oxidation reaction unit 8 shown in FIG.
- the reformed gas RG flows through the shift reaction inlet gas flow path 31 and is supplied to the low temperature shift reaction unit 13.
- the reformed gas RG whose carbon monoxide concentration has been reduced by the low temperature shift catalyst 13x is collected at one location in the internal space 51 toward the outlet 52.
- the temperature of the reformed gas RG flowing out from the low temperature shift reaction unit 13 is 150 ° C. to 250 ° C. as described above.
- the reformed gas RG collected at the outlet 52 flows downward toward the pipe portion 14a of the reformed gas pipe 14x.
- the reformed gas RG collides with the air supplied upward from the air pipe 15 and is efficiently mixed with the air.
- the reformed gas RG mixed with air flows through the reformed gas pipe 14 x and is supplied to the selective oxidation reaction inlet gas channel 34.
- the reformed gas RG supplied to the selective oxidation reaction inlet gas channel 34 flows through the selective oxidation reaction inlet gas channel 34 from below to above. At this time, the reformed gas RG exchanges heat with water (or water vapor) in the water evaporation channel 33 adjacent to the inner peripheral side of the selective oxidation reaction inlet gas channel 34. As a result, when the reformed gas RG is hotter than necessary, the reformed gas RG is cooled by supplying heat to the water evaporation channel 33, but is maintained at an appropriate temperature so as not to become unnecessarily low. That is, the selective oxidation reaction inlet gas channel 34 can function as a heat exchange part A that performs heat exchange with the water evaporation channel 33. The temperature of the reformed gas RG is kept at 100 to 200 ° C. immediately before flowing into the selective oxidation reaction unit 8.
- Carbon monoxide is removed from the reformed gas RG flowing into the selective oxidation reaction unit 8 by the selective oxidation catalyst 8x.
- the selective oxidation reaction is an exothermic reaction, heat is generated from the selective oxidation catalyst 8x.
- the selective oxidation reaction unit 8 can exchange heat with the water evaporation channel 33 via the selective oxidation reaction inlet gas channel 34. Thereby, it is possible to prevent the vicinity of the inlet of the selective oxidation reaction unit 8 from becoming unnecessarily high.
- the selective oxidation reaction inlet gas channel 34 can function as a heat exchange unit B that performs heat exchange between the selective oxidation reaction unit 8 and the water evaporation channel 33.
- the temperature of the reformed gas RG is set to 100 to 180 ° C. immediately after flowing out of the selective oxidation reaction unit 8.
- the reformed gas RG flowing out from the selective oxidation reaction unit 8 is heat-exchanged with the water supplied to the water evaporation channel 33 by the heat exchange unit 16.
- the heat exchange part 16 functions as the heat exchange part C shown in FIG.
- the reformed gas RG is finally set to 80 to 130 ° C.
- the selective oxidation reaction inlet gas flow channel 34 can function as the two heat exchange parts A and B while being a single flow channel.
- Water W is supplied from the water pipe 17 x and receives heat from the reformed gas RG by the heat exchange unit 16.
- the water W heat-exchanged by the heat exchange part 16 flows into the water evaporation flow path 33, and flows upward from the bottom.
- the water W can receive heat from the exhaust gas EG in the exhaust gas channel 32 adjacent to the water evaporation channel 33 on the inner peripheral side.
- the water W can receive the heat of the reformed gas RG from the selective oxidation reaction inlet gas flow path 34 that functions as the heat exchange part A.
- the water W can receive heat from the selective oxidation reaction from the selective oxidation reaction inlet gas flow path 34 functioning as the heat exchange part B.
- the temperature of the water W is 80 to 500 ° C. in the region in contact with the selective oxidation reaction inlet gas flow path 34, and particularly 100 to 300 ° C. near the inlet of the selective oxidation reaction unit 8. .
- the water W evaporates while flowing upward, becomes steam, and goes to the reforming unit 6.
- a selective oxidation reaction inlet gas flow path 34 through which the reformed gas RG flows is disposed between the selective oxidation reaction unit 8 and the water evaporation flow path 33.
- the selective oxidation reaction unit 8 can cause the selective oxidation reaction inlet gas flow path 34 to function as a heat medium without directly contacting the water evaporation flow path 33 through which water or water vapor flows. Thereby, it is possible to prevent the temperature of the selective oxidation catalyst 8x of the selective oxidation reaction unit 8 from becoming too low.
- the selective oxidation reaction inlet gas flow path 34 can flow the reformed gas RG supplied to the selective oxidation reaction unit 8, that is, the inlet gas of the selective oxidation reaction unit 8.
- the reformed gas RG as the inlet gas of the selective oxidation reaction section 8 is cooled by supplying heat to water and water vapor in the water evaporation channel 33 when the temperature is higher than necessary, but more than necessary.
- the temperature is kept at an appropriate temperature by water or water vapor in the water evaporation channel 33 so that the temperature is not low.
- the reformed gas RG flowing through the selective oxidation reaction inlet gas flow path 34 is supplied to the selective oxidation reaction unit 8 in a state where the reformed gas RG is at an optimum temperature.
- the temperature of the selective oxidation reaction unit 8 can be maintained at an optimum temperature with a simple structure without using an external heater such as a heater. It is possible to extend the life of the catalyst.
- the exhaust gas flow channel 32 is disposed at a position adjacent to the water evaporation flow channel 33 on the opposite side of the selective oxidation reaction inlet gas flow channel 34. Since the exhaust gas flow path 32 is disposed at a position adjacent to the water evaporation flow path 33, the water in the water evaporation flow path 33 can be efficiently evaporated by receiving heat from the high temperature exhaust gas EG. Furthermore, the water evaporation channel 33 can reliably keep the reformed gas RG at the optimum temperature without overcooling the reformed gas RG in the selective oxidation reaction inlet gas channel 34.
- the low temperature shift reaction unit 13 has an outlet 52 through which the reformed gas RG after the shift reaction passes.
- the air pipe 15 can supply air to the reformed gas RG passing through the outlet 52 from the direction facing the flow of the reformed gas RG.
- the reformed gas RG is collected at the outlet 52 when it flows out of the low temperature shift reaction unit 13.
- the air pipe 15 can supply air to the reformed gas RG collected at the outlet 52.
- air and the reformed gas RG can be mixed efficiently.
- the air pipe 15 can supply air from the direction opposite to the flow of the reformed gas RG, the reformed gas RG and the air collide and are mixed more efficiently.
- the temperature of the selective oxidation reaction unit 8 can be maintained at an optimum temperature with a simple structure without using an external heater such as a heater. The above effect is exhibited.
- the hydrogen production apparatus and the fuel cell system according to the present invention are not limited to the hydrogen production apparatus 1 and the fuel cell system 100 according to the embodiment.
- the gist described in the claims may be modified within a range not changing, or applied to other things.
- the configuration of the hydrogen production apparatus shown in the above embodiment is an example, and the configuration of the portion excluding the positional relationship of the selective oxidation reaction unit 8, the selective oxidation reaction inlet gas flow channel 34, and the water evaporation flow channel 33 is as follows.
- the positional relationship and configuration of each flow path, pipe, and component may be changed as appropriate.
- one having a different structure of the reforming part may be adopted, and the desulfurization part 2 may not be provided.
- the said embodiment is equipped with the high temperature shift reaction part 12 and the low temperature shift reaction part 13 as what carries out the shift reaction of the carbon monoxide in reformed gas, as shown in FIG. You may have only.
- tubular shape includes not only a substantially cylindrical shape but also a substantially polygonal tubular shape.
- substantially cylindrical shape and the substantially polygonal cylindrical shape mean a cylindrical shape and a polygonal cylindrical shape in a broad sense such as those substantially equal to the cylindrical shape and the polygonal cylindrical shape, and those including at least a cylindrical shape and a polygonal cylindrical shape. ing.
- the present invention can be used for a hydrogen production apparatus and a fuel cell system.
- SYMBOLS 1 Hydrogen production apparatus, 10 ... Burner, 20 ... Cell stack (fuel cell stack), 8 ... Selective oxidation reaction part, 13 ... Shift reaction part, 15 ... Air piping (air supply part), 32 ... Exhaust gas flow path, 33 ... water evaporation channel (evaporation channel), 34 ... selective oxidation reaction inlet gas channel (gas channel), 52 ... outlet, 100 ... fuel cell system, G ... axis.
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Combustion & Propulsion (AREA)
- Inorganic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Manufacturing & Machinery (AREA)
- Sustainable Development (AREA)
- Sustainable Energy (AREA)
- Electrochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Hydrogen, Water And Hydrids (AREA)
- Fuel Cell (AREA)
Abstract
水素製造装置1は、水素を含有する改質ガス中の一酸化炭素を選択酸化する選択酸化反応部8と、水を流通させて水蒸気を生成する蒸発流路33と、改質ガスが流通するガス流路34と、を備え、ガス流路34は、選択酸化反応部8と蒸発流路33との間に配置されており、改質ガスは、ガス流路34を流通した後、選択酸化反応部8へ流入する。
Description
本発明は、水素製造装置及び燃料電池システムに関する。
従来の水素製造装置としては、炭化水素等の原燃料を改質することによって生成された改質ガス中の一酸化炭素を選択酸化する選択酸化反応部を備えたものが知られている(例えば、特許文献1参照)。選択酸化反応部の温度を制御するためには通常ヒータ等の外部加熱器が用いられるが、例えば、筒状の選択酸化反応部の内周側に隣接する位置に、水蒸気を生成するための水蒸発部が配置されている水素製造装置では、水蒸発部に供給された水温により、加熱器を用いることなく、選択酸化反応部の温度を制御することが可能である。
ここで、上述したような水素製造装置では、水または水蒸気が流通する流路が、選択酸化反応部に隣接する位置に設けられているため流路中の水温が低い場合、選択酸化反応部の選択酸化触媒の温度が低下してしまう。選択酸化触媒の温度が低くなりすぎた場合、選択酸化触媒の酸化劣化が生じ触媒の寿命が短くなるという問題があった。一方、選択酸化反応部に対する適切な冷却構造が設けられていない場合は、選択酸化触媒の温度が高くなることにより、一酸化炭素および二酸化炭素のメタン化反応が進行し部材の耐熱温度以上に温度が急上昇するという問題があった。以上より、選択酸化反応部の温度を最適な温度に保つことが要求されていた。
そこで、本発明は、ヒータ等の外部加熱器を用いることなく、簡便な構造で選択酸化反応部の温度を最適な温度に保つことができる水素製造装置及び燃料電池システムを提供することを課題とする。
水素製造装置は、水素を含有する改質ガス中の一酸化炭素を選択酸化する選択酸化反応部と、水を流通させて水蒸気を生成する蒸発流路と、改質ガスが流通するガス流路と、を備え、ガス流路は、選択酸化反応部と蒸発流路との間に配置されており、改質ガスは、ガス流路を流通した後、選択酸化反応部へ流入する。
この水素製造装置では、水を流通させて水蒸気を生成する蒸発流路と選択酸化反応部との間には、改質ガスが流通するガス流路が配置される。このような構成により、選択酸化反応部は、水が流通する蒸発流路と直接接触することなく、ガス流路を熱媒として機能させることができる。これによって、選択酸化反応部の選択酸化触媒の温度が低くなりすぎることを防止することができる。更に、ガス流路は、選択酸化反応部へ供給される改質ガス、すなわち選択酸化反応部の入口ガスを流通させることができる。これによって、選択酸化反応部の入口ガスとしての改質ガスは、必要以上に高温な場合は蒸発流路の水や水蒸気に熱を供給することで冷却されつつも、必要以上に低温とならないように蒸発流路の水や水蒸気によって適切な温度に保たれる。これによって、ガス流路を流通した改質ガスは、最適な温度にされた状態で選択酸化反応部へ供給される。以上によって、水素製造装置によれば、ヒータ等の外部加熱器を用いることなく、簡便な構造で選択酸化反応部の温度を最適な温度に保つことができ、選択酸化触媒の寿命を長くすることが可能となる。
また、水素製造装置において、改質ガスの生成に用いられるバーナの排ガスが流通する排ガス流路を更に備え、排ガス流路は、ガス流路の反対側で蒸発流路と隣接する位置に配置されていてもよい。排ガス流路が蒸発流路と隣接する位置に配置されているため、蒸発流路内の水は、高温の排ガスからの熱を受けて効率よく蒸発することができる。更に、蒸発流路は、ガス流路内の改質ガスを冷やしすぎることなく、確実に改質ガスを最適な温度に保つことができる。
また、水素製造装置において、改質ガス中の一酸化炭素をシフト反応により除去するシフト反応部と、シフト反応部から選択酸化反応部へ向かう改質ガスに対して空気を供給する空気供給部と、を更に備え、シフト反応部は、シフト反応後の改質ガスを流出させる出口を有し、空気供給部は、出口から流出する改質ガスに対して、当該改質ガスの流れに対向する方向から空気を供給してもよい。シフト反応により一酸化炭素が除去された改質ガスは、シフト反応部から流出する際に出口に集められる。このとき、空気供給部は、出口に集められた改質ガスに対して空気を供給することができる。これによって、空気と改質ガスとが効率よく混合することができる。更に、空気供給部は、改質ガスの流れに対向する方向から空気を供給することができるため、改質ガスと空気とが衝突し、一層効率よく混合される。
また、燃料電池システムは、上記水素製造装置と、水素製造装置によって生成された改質ガスを用いて発電を行う燃料電池スタックと、を備える。
この燃料電池システムにおいても、上記水素製造装置を備えているため、ヒータ等の外部加熱器を用いることなく、簡便な構造で選択酸化反応部の温度を最適な温度に保つことができるという上記効果が奏される。
本発明によれば、ヒータ等の外部加熱器を用いることなく、簡便な構造で選択酸化反応部の温度を最適な温度に保つことが可能となる。
以下、図面を参照しながら、本発明の好適な実施形態について詳細に説明する。なお、以下の説明では、同一又は相当要素には同一符号を付し、重複する説明は省略する。また、「上」「下」の語は、図面の上下方向に対応するものであり便宜的なものである。
図1は、一実施形態に係る燃料電池システムの一部を示す概略ブロック図である。図1に示すように、水素製造装置(FPS:Fuel Processing System)1は、例えば家庭用の燃料電池システム100において水素供給源として利用されるものである。ここでの水素製造装置1は、原燃料として石油系炭化水素が用いられ、水素を含有する改質ガスをセルスタック(燃料電池スタック)20に供給する。
なお、原燃料としては、アルコール類、エーテル類、バイオ燃料、天然ガス、都市ガスを用いてもよい。また、石油系炭化水素としては、灯油、LPガスのほか、ナフサ、軽油などを原燃料として使用することができる。また、セルスタック20としては、固体高分子形、アルカリ電解質形、リン酸形、溶融炭酸塩形或いは固体酸化物形等の種々のものを用いてもよい。
図2は、図1の水素製造装置を示す概略正面端面図である。図1,2に示すように、水素製造装置1は、中心軸を軸Gとする円筒状外形の脱硫部2と、中心軸を軸Gとする円柱状外形の本体部3と、を備え、これらが筐体4に収容されている。また、筐体4内において脱硫部2及び本体部3の周囲には、粉状の断熱材(不図示)が充填されて断熱されている。脱硫部2は筐体4の外に設置されてもよい。
脱硫部2は、外部から導入された原燃料を脱硫触媒によって脱硫して硫黄分を除去し、この原燃料を後述のフィード部5へ供給する。脱硫部2は、筐体4の側板4xにパイプ21で固定され、本体部3の上部を所定の隙間を有して囲繞するよう保持されている。本体部3は、フィード部5、改質部6、シフト反応部7、選択酸化反応部8及び蒸発部9を備え、これらが一体で構成されている。この本体部3は、筐体4の床板4yに筒状のステー22により固定され保持されている。
フィード部5は、脱硫部2で脱硫した原燃料及び水蒸気(スチーム)を混合し、これらを改質部6に供給する。具体的には、フィード部5は、原燃料及び水蒸気を合流・混合させて混合ガス(混合流体)を生成する混合部5xと、混合ガスを改質部6へ流通させる混合ガス流路5yと、を含んでいる。
改質部(SR:Steam Reforming)6は、フィード部5により供給された混合ガスを改質触媒(改質触媒部)6xによって水蒸気改質して改質ガスを生成し、この改質ガスをシフト反応部7へ供給する。改質部6は、中心軸を軸Gとする円筒状外形を呈し、脱硫部2の筒内に位置するよう本体部3の上端側に設けられている。この改質部6にあっては、水蒸気改質反応が高温を必要としかつ吸熱反応であるため、改質部6の改質触媒6xを加熱するための熱源としてバーナ10を利用している。
バーナ10では、外部から原燃料がバーナ燃料として供給されて燃焼される。このバーナ10は、本体部3の上端部に設けられ軸Gを中心軸とする燃焼筒11に、バーナ10による火炎が取り囲まれるよう取り付けられている。なお、バーナ10においては、脱硫部2で脱硫した原燃料の一部が、バーナ燃料として供給されて燃焼される場合もある。
シフト反応部7は、改質部6から供給された改質ガスの一酸化炭素濃度(CO濃度)を低下させるためのものであり、改質ガス中の一酸化炭素をシフト反応させて水素及び二酸化炭素に転換する。ここでのシフト反応部7は、シフト反応を2段階に分けて行うことも可能であり、高温(例えば400°C~600°C)でのシフト反応である高温シフト反応を行う高温シフト反応部(HTS:High Temperature Shift)12と、高温シフト反応の温度よりも低温(例えば150°C~350°C)でのシフト反応である低温シフト反応を行う低温シフト反応部(LTS:LowTemperature Shift)13と、を有している。ただし、高温シフト反応部12は、必ずしも設けなくともよい。
高温シフト反応部12は、改質部6から供給された改質ガス中の一酸化炭素を高温シフト触媒12xによって高温シフト反応させ、改質ガスのCO濃度を低下させる。高温シフト反応部12は、中心軸を軸Gとする円筒状外形を呈しており、高温シフト触媒12xが改質触媒6xの下端部を囲繞するよう改質部6の径方向外側に隣接配置されている。この高温シフト反応部12は、CO濃度を低下させた改質ガスを低温シフト反応部13へ供給する。
低温シフト反応部13は、高温シフト反応部12で高温シフト反応させた改質ガス中の一酸化炭素を低温シフト触媒13xによって低温シフト反応させ、改質ガスのCO濃度を低下させる。低温シフト反応部13は、中心軸を軸Gとする円筒状外形を呈しており、本体部3の下端側に配設されている。この低温シフト反応部13は、CO濃度を低下させた改質ガスを改質ガス配管14xを介して選択酸化反応部8へ供給する。
選択酸化反応部(PROX:Preferential Oxidation)8は、低温シフト反応部13で低温シフト反応させた改質ガス中のCO濃度をさらに低下させる。これは、セルスタック20に高濃度の一酸化炭素を供給すると、セルスタック20の触媒が被毒して大きく性能低下するためである。この選択酸化反応部8は、具体的には、改質ガス中の一酸化炭素と空気配管15を介して導入される空気とを選択酸化触媒8xで反応させて、改質ガス中の水素を酸化させることなく、一酸化炭素を選択的に酸化し、二酸化炭素に転換する。選択酸化反応部8は、中心軸を軸Gとする円筒状外形を呈しており、本体部3の下端から所定長上端側に該本体部3の最外周側を構成するよう配設されている。
この選択酸化反応部8は、CO濃度をさらに低下させた改質ガスを、熱交換部16が設けられた改質ガス配管14yを介して外部へ導出する。熱交換部16は、改質ガス配管14y内を流通する改質ガスと、外部から水配管17xを介して導入された水との間で熱交換を行うと共に、この水を蒸発部9に水配管17yを介して供給する。
蒸発部9は、熱交換部16から供給された水を内部に貯留させると共に、この水を低温シフト反応部13及び選択酸化反応部8から移動させた(低温シフト反応部13及び選択酸化反応部8を冷却して得た)熱、及びバーナ10の排ガスの熱で気化させて水蒸気を生成する。蒸発部9は、ジャケット型のものであり、中心軸を軸Gとする円筒状を呈している。この蒸発部9は、高温シフト反応部12及び低温シフト反応部13の径方向外側で且つ選択酸化反応部8の径方向内側(つまり、シフト反応部7と選択酸化反応部8との間)に位置するよう配設されている。この蒸発部9は、生成した水蒸気をフィード部5の混合部5xに水蒸気配管17zを介して供給する。
このような水素製造装置1では、まず、バーナ燃料及びセルスタック20からのオフガス(セルスタック20で反応に使用されない残ガス)の少なくとも一方と空気とがバーナ10に供給されて燃焼され、かかる燃焼によって改質触媒6xが加熱される。そして、バーナ10の排ガスが排ガス流路L1及びガス配管18を流通して外部へ排気される。
これと共に、脱硫部2で脱硫された原燃料と蒸発部9からの水蒸気とが混合部5xで混合され、混合ガスが生成される。この混合ガスは、混合ガス流路5yを介して改質部6に供給されて改質触媒6xで水蒸気改質され、これにより、改質ガスが生成される。そして、生成された改質ガスは、シフト反応部7によってその一酸化炭素濃度が例えば数千ppm程度まで低下され、選択酸化反応部8によってその一酸化炭素濃度が10ppm程度以下まで低下された後、熱交換部16で冷却され、後段のセルスタック20へ導出される。
なお、本実施形態においては、例えば各触媒6x,12x,13x,8xにて触媒反応を好適に行うため、次のように各部位の温度が設定されている。すなわち、改質部6に流入する混合ガスの温度が約300~550℃とされ、改質部6から流出する改質ガスの温度が550℃~800℃とされ、高温シフト反応部12に流入する改質ガスの温度が400℃~600℃とされ、高温シフト反応部12から流出する改質ガスの温度が300℃~500℃とされている。また、低温シフト反応部13に流入する改質ガスの温度が150℃~350℃とされ、低温シフト反応部13から流出する改質ガスの温度が150℃~250℃とされ、選択酸化反応部8に流入する改質ガスの温度が90℃~210℃(120℃~190℃)とされている。
次に、本実施形態における低温シフト反応部13及び選択酸化反応部8の周辺構成について、より詳細に説明する。
図3は、図2に示す選択酸化反応部周辺の構成の拡大図である。図3に示すように、本実施形態に係る水素製造装置1の一酸化炭素除去構造は、軸G側から外周側へ向かって、低温シフト反応部13、シフト反応入口ガス流路31、排ガス流路32、水蒸発流路33、選択酸化反応入口ガス流路34、選択酸化反応部8を、この順番で備えている。低温シフト反応部13、シフト反応入口ガス流路31、排ガス流路32、水蒸発流路33、選択酸化反応入口ガス流路34、選択酸化反応部8は、いずれも軸Gを中心軸とする円筒状をなしており、径方向に互いに隣接するようにそれぞれ配置されている。
低温シフト反応部13は、周壁41、周壁42、下端壁43、パンチング板44、パンチング板45及び低温シフト触媒13xを備えている。周壁41及び周壁42は、軸Gを中心軸とする円筒状(円管状)を呈している。周壁41と周壁42との間には、低温シフト触媒13xを充填するための隙間が形成されている。下端壁43は、径方向に沿って延在する円板状を呈し、周壁41及び周壁42それぞれの下端に連続して低温シフト反応部13の下方側を閉塞する。周壁42は、周壁41よりも更に上方へ延びている。パンチング板44は、径方向に沿って延在する円板状を呈し、下端壁43から上方へ離間する位置に、周壁41と周壁42との間に設けられている。パンチング板45は、径方向に沿って延在する円板状を呈し、周壁41の上端側の位置に、周壁41と周壁42との間に設けられている。低温シフト触媒13xは、周壁41、周壁42、パンチング板44、パンチング板45で構成される空間に充填される。また、低温シフト反応部13は、シフト反応後の改質ガスを流出させる出口52を有している。なお、低温シフト反応部13は、パンチング板を用いない構成としてもよい。この低温シフト反応部13の下方側には、シフト反応後の改質ガスと空気とを効率よく混合するための混合構造50が設けられている。
混合構造50は、内部空間51、出口52、改質ガス配管14x、空気配管(空気供給部)15によって構成されている。内部空間51は、下端壁43とパンチング板44との間に形成される円環状の空間である。内部空間51は、シフト反応後の改質ガスを効率よく出口52へ集めることができる。出口52は、低温シフト反応部13の下端壁43に形成された貫通孔である。出口52は、下端壁43に一箇所のみ形成されているため、シフト反応後の改質ガスを一箇所に集めることができる。改質ガス配管14xは、出口52に接続された配管である。改質ガス配管14xは、シフト反応後の改質ガスを選択酸化反応入口ガス流路34へ流通させる。改質ガス配管14xは、軸Gを中心軸として低温シフト反応部13の下方から上方へ延び、出口52に接続される管部14aを備えている。空気配管15は、先端部分が改質ガス配管14xの内部に挿入されている。空気配管15の先端部分は、改質ガス配管14xの管部14aの内部で当該管部14aと同軸上に配置され、出口52へ向かって上方へ延びている。
このような構成によって、出口52は、シフト反応後の改質ガスを一箇所に集めると共に、当該改質ガスを改質ガス配管14xの管部14a内へ下方に向けて流すことができる。一方、空気配管15は、出口52を通過する改質ガスに対して、下方から上方へ向かって(すなわち、改質ガスの流れに対向する方向から)空気を供給することができる。これによって、混合構造50は、シフト反応後の改質ガスと空気とを出口52付近で効率よく混合することができる。なお、改質ガスと空気との混合位置は、特に限定されず、出口52から離れた位置でもよいが、出口52に近い方が改質ガスの流速が高く混合効率が良いので好適である。
シフト反応入口ガス流路31は、低温シフト反応部13に対する入口ガスを流通させる流路であり、周壁42及び周壁61によって構成されている。周壁61は、軸Gを中心軸とする円筒状(円管状)を呈している。シフト反応入口ガス流路31は、周壁41と周壁61との間の隙間によって構成されている。周壁61は、低温シフト反応部13の下端壁43から下方へ離間するように配置された下端壁62に接続されている。シフト反応入口ガス流路31を流通する改質ガスは、低温シフト反応部13の下端壁43と周壁41の外側を回り込むように流れ低温シフト反応部13へ上側から供給される。なお、低温シフト反応部13へ供給される改質ガスはこのような流れに限定されず、どのような流路で低温シフト反応部13へ供給されてもよい。従って、シフト反応入口ガス流路31がこのような配置で設けられていなくてもよい。
排ガス流路32は、バーナからの排ガスを流通させる流路であり、周壁61、周壁63、下端壁64、外周壁66によって構成されている。周壁63は、軸Gを中心軸とする円筒状(円管状)を呈している。排ガス流路32は、周壁61と周壁63との間の隙間によって構成されている。周壁63の下端部は、下端壁62から上方へ離間した円環状の下端壁64に接続されている。また、下端壁64と下端壁62の外周側の端部は円筒状の外周壁66によって閉塞されている。排ガス流路32は、改質部6側からの排ガスを上方から下方へ向けて流通させる。
水蒸発流路33は、蒸発部9の水または水蒸気を流通させる流路であり、周壁63、下端壁64、周壁67、上端壁68によって構成されている。周壁67は、軸Gを中心軸とする円筒状(円管状)を呈している。水蒸発流路33は、周壁63と周壁67との間の隙間によって構成されている。周壁67の下端部は、下端壁64に接続されている。下端壁64は、径方向に沿って延在する円板状を呈し、周壁63及び周壁67それぞれの下端に連続して水蒸発流路33の下方側を閉塞する。上端壁68は、径方向に沿って延在する円板状を呈し、周壁63及び周壁67それぞれの上端に連続して水蒸発流路33の上方側を閉塞する。周壁67の下端付近には、水配管17xが接続されている。水蒸発流路33は、水配管17xから供給された水を下方から上方へ向けて流通させる。なお、水は水蒸発流路33内で蒸発するため、水蒸発流路33は下側の水層と上側のスチーム層を有している。水蒸発流路33内の水の水面の位置は特に限定されないが、少なくとも選択酸化触媒8xの上端位置よりも上方であることが好ましい。また、水蒸発流路33の上端、すなわち上端壁68の位置は特に限定されず、図に示す位置より更に高い位置に配置してよい。
選択酸化反応入口ガス流路34は、選択酸化反応部8に対する入口ガスを流通させる流路であり、周壁67、周壁69、下端壁71、上端壁72によって構成されている。下端壁71は、径方向に沿って延在する円板状を呈し、周壁67の外周面に設けられている。下端壁71は、水配管17xの接続位置よりも上方に配置されている。上端壁72は、径方向に沿って延在する円板状を呈し、周壁67の外周面に設けられている。周壁69は、軸Gを中心軸とする円筒状(円管状)を呈し、下端壁71と上端壁72との間を延在している。周壁69の下端は下端壁71から離間し、周壁69の上端は上端壁72から離間している。選択酸化反応入口ガス流路34は、周壁67と周壁69との間の隙間によって構成されている。下端壁71の外周側の端部と上端壁72の外周側の端部とは、周壁73で連結されている。周壁73は、周壁69よりも外周側で、軸Gを中心軸とする円筒状(円管状)を呈している。周壁73の下端付近には、改質ガス配管14xが接続されている。選択酸化反応入口ガス流路34は、改質ガス配管14xから供給された改質ガスを下方から上方へ向かって流通させる。選択酸化反応入口ガス流路34の上端及び下端の位置、すなわち上端壁72及び下端壁71の位置は、図に示す位置に限定されない。
選択酸化反応部8は、周壁69、周壁73、パンチング板74、パンチング板76、下端壁77、及び選択酸化触媒8xを備えている。周壁69と周壁73との間には、選択酸化触媒8xを充填するための隙間が形成されている。パンチング板74は、径方向に沿って延在する円板状を呈し、周壁69の下端側の位置に、周壁69と周壁73との間に設けられている。パンチング板76は、径方向に沿って延在する円板状を呈し、周壁69の上端側の位置に、周壁69と周壁73との間に設けられている。選択酸化触媒8xは、周壁69、周壁73、パンチング板74、及びパンチング板76で構成される空間に充填される。下端壁77は、径方向に沿って延在する円板状を呈し、周壁69の下端と周壁73の内周面に連続して選択酸化反応部8の下方側を閉塞する。周壁73には、下端壁77とパンチング板74との間の位置に改質ガス配管14yが接続されている。なお、選択酸化反応部8は、パンチング板を用いない構成としてもよい。
次に、選択酸化反応部8周辺における改質ガスRG、水(または水蒸気)W、排ガスEGの流れ、及び熱の流れについて図3及び図4を参照しながら説明する。図4は、図3に示す選択酸化反応部8周辺の熱の流れを示すブロック図である。
まず、改質ガスRGは、シフト反応入口ガス流路31を流通し、低温シフト反応部13へ供給される。低温シフト触媒13xで一酸化炭素濃度が低下した改質ガスRGは、内部空間51内で出口52へ向かって一箇所に集められる。低温シフト反応部13から流出する改質ガスRGの温度は、上述のように150℃~250℃である。出口52へ集められた改質ガスRGは、改質ガス配管14xの管部14aへ向かって下方へ流通する。このとき、改質ガスRGは、空気配管15から上方へ向かって供給された空気と衝突し、効率よく空気と混合される。空気と混合された改質ガスRGは、改質ガス配管14xを流通して、選択酸化反応入口ガス流路34へ供給される。
選択酸化反応入口ガス流路34へ供給された改質ガスRGは、当該選択酸化反応入口ガス流路34を下方から上方へ向かって流通する。このとき、改質ガスRGは、選択酸化反応入口ガス流路34の内周側に隣接する水蒸発流路33内の水(あるいは水蒸気)との間で熱交換を行う。これによって、改質ガスRGは、必要以上に高温な場合は水蒸発流路33に熱を供給することで冷却されつつも、必要以上に低温とならないように適切な温度に保たれる。すなわち、選択酸化反応入口ガス流路34は、水蒸発流路33との間で熱交換を行う熱交換部Aとして機能することができる。改質ガスRGの温度は、選択酸化反応部8へ流入する直前では、100~200℃に保たれる。
選択酸化反応部8へ流入した改質ガスRGは、選択酸化触媒8xによって一酸化炭素が除去される。ここで、選択酸化反応は発熱反応であるため、選択酸化触媒8xから熱が生じる。このとき、選択酸化反応部8は、選択酸化反応入口ガス流路34を介して水蒸発流路33との間で熱交換をすることができる。これによって、選択酸化反応部8の入口付近が必要以上に高温となることを防止できる。このとき、選択酸化反応入口ガス流路34は、選択酸化反応部8と水蒸発流路33との間で熱交換を行う熱交換部Bとして機能することができる。改質ガスRGの温度は、選択酸化反応部8から流出した直後では、100~180℃とされる。選択酸化反応部8から流出した改質ガスRGは、熱交換部16によって、水蒸発流路33へ供給される水との間で熱交換が行われる。このとき、熱交換部16は、図4に示す熱交換部Cとして機能する。改質ガスRGは、最終的に80~130℃とされる。以上のように、選択酸化反応入口ガス流路34は、一本の流路でありながら、二つの熱交換部A,Bとして機能することができる。
水Wは、水配管17xから供給され、熱交換部16によって改質ガスRGから熱を受ける。熱交換部16で熱交換された水Wは、水蒸発流路33へ流入し、下方から上方へ向かって流れる。このとき、水Wは、水蒸発流路33と内周側で隣接する排ガス流路32の排ガスEGから熱を受けることができる。また、水Wは、熱交換部Aとして機能する選択酸化反応入口ガス流路34から改質ガスRGの熱を受けることができる。更に、水Wは、熱交換部Bとして機能する選択酸化反応入口ガス流路34から選択酸化反応による熱を受けることができる。水W(または水蒸気)の温度は、選択酸化反応入口ガス流路34と接している領域では80~500℃とされ、特に、選択酸化反応部8の入口付近においては100~300℃とされる。水Wは、上方へ流通する間に蒸発することでスチームとなり、改質部6へ向かう。
次に、本実施形態に係る水素製造装置1及び燃料電池システム100の作用・効果について説明する。
本実施形態に係る水素製造装置1では、選択酸化反応部8と水蒸発流路33との間には、改質ガスRGが流通する選択酸化反応入口ガス流路34が配置される。このような構成により、選択酸化反応部8は、水や水蒸気が流れる水蒸発流路33と直接接触することなく、選択酸化反応入口ガス流路34を熱媒として機能させることができる。これによって、選択酸化反応部8の選択酸化触媒8xの温度が低くなりすぎることを防止することができる。更に、選択酸化反応入口ガス流路34は、選択酸化反応部8へ供給される改質ガスRG、すなわち選択酸化反応部8の入口ガスを流通させることができる。これによって、選択酸化反応部8の入口ガスとしての改質ガスRGは、必要以上に高温な場合は水蒸発流路33の水や水蒸気に熱を供給することで冷却されつつも、必要以上に低温とならないように水蒸発流路33の水や水蒸気によって適切な温度に保たれる。これによって、選択酸化反応入口ガス流路34を流通した改質ガスRGは、最適な温度にされた状態で選択酸化反応部8へ供給される。以上によって、本実施形態に係る水素製造装置1によれば、ヒータ等の外部加熱器を用いることなく、簡便な構造で選択酸化反応部8の温度を最適な温度に保つことができ、選択酸化触媒の寿命を長くすることが可能となる。
また、本実施形態に係る水素製造装置1において、排ガス流路32は、選択酸化反応入口ガス流路34の反対側で水蒸発流路33と隣接する位置に配置されている。排ガス流路32が水蒸発流路33と隣接する位置に配置されているため、水蒸発流路33内の水は、高温の排ガスEGからの熱を受けて効率よく蒸発することができる。更に、水蒸発流路33は、選択酸化反応入口ガス流路34内の改質ガスRGを冷やしすぎることなく、確実に改質ガスRGを最適な温度に保つことができる。
また、本実施形態に係る水素製造装置1において、低温シフト反応部13は、シフト反応後の改質ガスRGが通過する出口52を有している。また、空気配管15は、出口52を通過する改質ガスRGに対して、当該改質ガスRGの流れに対向する方向から空気を供給することができる。改質ガスRGは、低温シフト反応部13から流出する際は出口52に集められる。このとき、空気配管15は、出口52に集められた改質ガスRGに対して空気を供給することができる。これによって、空気と改質ガスRGとが効率よく混合することができる。更に、空気配管15は、改質ガスRGの流れに対向する方向から空気を供給することができるため、改質ガスRGと空気とが衝突し、一層効率よく混合される。
また、燃料電池システム100は、上記水素製造装置1を備えているため、ヒータ等の外部加熱器を用いることなく、簡便な構造で選択酸化反応部8の温度を最適な温度に保つことができるという上記効果が奏される。
以上、本発明の好適な実施形態について説明したが、本発明に係る水素製造装置及び燃料電池システムは、実施形態に係る上記水素製造装置1及び上記燃料電池システム100に限られるものではなく、各請求項に記載した要旨を変更しない範囲で変形し、又は他のものに適用したものであってもよい。
例えば、上記実施形態で示された水素製造装置の構成は、一例であり、選択酸化反応部8、選択酸化反応入口ガス流路34、水蒸発流路33の位置関係を除く部分の構成は、特に限定されず、各流路や配管や構成要素の位置関係や構成を適宜変更してもよい。例えば、改質部の構造が異なるものを採用してもよく、また、脱硫部2がなくともよい。
また、上記実施形態は、改質ガス中の一酸化炭素をシフト反応させるものとして高温シフト反応部12及び低温シフト反応部13を備えているが、図5に示すように、低温シフト反応部13のみ備えていてもよい。
ちなみに、上記の「筒状」とは、略円筒状だけでなく、略多角筒状を含むものである。また、略円筒状及び略多角筒状とは、円筒状及び多角筒状に概略等しいものや、円筒状及び多角筒状の部分を少なくとも含むもの等の広義の円筒状及び多角筒状を意味している。
本発明は、水素製造装置及び燃料電池システムに利用可能である。
1…水素製造装置、10…バーナ、20…セルスタック(燃料電池スタック)、8…選択酸化反応部、13…シフト反応部、15…空気配管(空気供給部)、32…排ガス流路、33…水蒸発流路(蒸発流路)、34…選択酸化反応入口ガス流路(ガス流路)、52…出口、100…燃料電池システム、G…軸。
Claims (4)
- 水素を含有する改質ガス中の一酸化炭素を選択酸化する選択酸化反応部と、
水を流通させて水蒸気を生成する蒸発流路と、
前記改質ガスが流通するガス流路と、を備え、
前記ガス流路は、前記選択酸化反応部と前記蒸発流路との間に配置されており、
前記改質ガスは、前記ガス流路を流通した後、前記選択酸化反応部へ流入することを特徴とする水素製造装置。 - 前記改質ガスの生成に用いられるバーナの排ガスが流通する排ガス流路を更に備え、
前記排ガス流路は、前記ガス流路の反対側で前記蒸発流路と隣接する位置に配置されていることを特徴とする請求項1記載の水素製造装置。 - 前記改質ガス中の一酸化炭素をシフト反応により除去するシフト反応部と、
前記シフト反応部から前記選択酸化反応部へ向かう前記改質ガスに対して空気を供給する空気供給部と、を更に備え、
前記シフト反応部は、シフト反応後の前記改質ガスを流出させる出口を有し、
前記空気供給部は、前記出口から流出する前記改質ガスに対して、当該改質ガスの流れに対向する方向から前記空気を供給することを特徴とする請求項1または2記載の水素製造装置。 - 請求項1~3の何れか一項記載の水素製造装置と、
前記水素製造装置によって生成した前記改質ガスを用いて発電を行う燃料電池スタックと、を備えたことを特徴とする燃料電池システム。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN2011800164684A CN102834349A (zh) | 2010-03-30 | 2011-03-23 | 氢制造装置以及燃料电池系统 |
| US13/637,793 US20130065144A1 (en) | 2010-03-30 | 2011-03-23 | Hydrogen production apparatus and fuel cell system |
| EP11762650.7A EP2554512A4 (en) | 2010-03-30 | 2011-03-23 | DEVICE FOR HYDROGEN PRODUCTION AND FUEL CELL SYSTEM |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2010-078763 | 2010-03-30 | ||
| JP2010078763A JP5600460B2 (ja) | 2010-03-30 | 2010-03-30 | 水素製造装置及び燃料電池システム |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2011122418A1 true WO2011122418A1 (ja) | 2011-10-06 |
Family
ID=44712128
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2011/057013 WO2011122418A1 (ja) | 2010-03-30 | 2011-03-23 | 水素製造装置及び燃料電池システム |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20130065144A1 (ja) |
| EP (1) | EP2554512A4 (ja) |
| JP (1) | JP5600460B2 (ja) |
| CN (1) | CN102834349A (ja) |
| WO (1) | WO2011122418A1 (ja) |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9312554B2 (en) * | 2011-05-27 | 2016-04-12 | Panasonic Intellectual Property Management Co., Ltd. | Hydrogen generator and fuel cell system |
| CN104203397A (zh) * | 2011-12-06 | 2014-12-10 | Hy9公司 | 催化剂容纳反应器系统以及相关方法 |
| JP6089210B2 (ja) * | 2013-03-19 | 2017-03-08 | パナソニックIpマネジメント株式会社 | 水素生成装置 |
| GB201501952D0 (en) | 2015-02-05 | 2015-03-25 | Johnson Matthey Plc | Process |
| KR101771303B1 (ko) * | 2015-02-16 | 2017-08-24 | 한국가스공사 | 연료처리장치 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004149403A (ja) * | 2002-10-10 | 2004-05-27 | Matsushita Electric Ind Co Ltd | 水素発生装置及び燃料電池発電システム |
| JP2008088049A (ja) * | 2006-09-05 | 2008-04-17 | Matsushita Electric Ind Co Ltd | 水素生成装置及び燃料電池システム |
| JP2009280408A (ja) | 2006-09-01 | 2009-12-03 | Panasonic Corp | 水素生成装置及び燃料電池システム |
| JP2010001187A (ja) * | 2008-06-20 | 2010-01-07 | Aisin Seiki Co Ltd | 改質装置 |
Family Cites Families (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE275529T1 (de) * | 1996-06-28 | 2004-09-15 | Matsushita Electric Works Ltd | Reformierungsvorrichtung zum erzeugen eines spaltgases mit verringertem co-gehalt. |
| US7338644B2 (en) * | 2000-04-17 | 2008-03-04 | Shell Oil Company | Fuel processor |
| US8257668B2 (en) * | 2006-09-05 | 2012-09-04 | Panasonic Corporation | Hydrogen generator and fuel cell system |
| JP4542205B2 (ja) * | 2008-05-30 | 2010-09-08 | パナソニック株式会社 | 燃料処理装置 |
-
2010
- 2010-03-30 JP JP2010078763A patent/JP5600460B2/ja not_active Expired - Fee Related
-
2011
- 2011-03-23 CN CN2011800164684A patent/CN102834349A/zh active Pending
- 2011-03-23 US US13/637,793 patent/US20130065144A1/en not_active Abandoned
- 2011-03-23 EP EP11762650.7A patent/EP2554512A4/en not_active Withdrawn
- 2011-03-23 WO PCT/JP2011/057013 patent/WO2011122418A1/ja active Application Filing
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004149403A (ja) * | 2002-10-10 | 2004-05-27 | Matsushita Electric Ind Co Ltd | 水素発生装置及び燃料電池発電システム |
| JP2009280408A (ja) | 2006-09-01 | 2009-12-03 | Panasonic Corp | 水素生成装置及び燃料電池システム |
| JP2008088049A (ja) * | 2006-09-05 | 2008-04-17 | Matsushita Electric Ind Co Ltd | 水素生成装置及び燃料電池システム |
| JP2010001187A (ja) * | 2008-06-20 | 2010-01-07 | Aisin Seiki Co Ltd | 改質装置 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP2554512A4 * |
Also Published As
| Publication number | Publication date |
|---|---|
| US20130065144A1 (en) | 2013-03-14 |
| CN102834349A (zh) | 2012-12-19 |
| EP2554512A4 (en) | 2014-01-22 |
| EP2554512A1 (en) | 2013-02-06 |
| JP2011207703A (ja) | 2011-10-20 |
| JP5600460B2 (ja) | 2014-10-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US9012098B2 (en) | Hydrogen production apparatus and fuel cell system | |
| JP5476392B2 (ja) | 燃料電池システム | |
| JP5600460B2 (ja) | 水素製造装置及び燃料電池システム | |
| JP5534900B2 (ja) | 水素製造装置及び燃料電池システム | |
| JP4870499B2 (ja) | 水素製造装置及び燃料電池発電装置 | |
| JP5895169B2 (ja) | 水素生成装置 | |
| JP5538025B2 (ja) | 水素製造装置及び燃料電池システム | |
| JP5534899B2 (ja) | 水素製造装置及び燃料電池システム | |
| JP2011207726A (ja) | 水素製造装置及び燃料電池システム | |
| JP2014009129A (ja) | 水素製造装置及び燃料電池システム | |
| JP5634729B2 (ja) | 水素製造装置及び燃料電池システム | |
| JP5538028B2 (ja) | 水素製造装置及び燃料電池システム | |
| JP5534901B2 (ja) | 水素製造装置及び燃料電池システム | |
| JP2011207713A (ja) | 水素製造装置及び燃料電池システム | |
| JP5513210B2 (ja) | 水素製造装置及び燃料電池システム | |
| JP5948605B2 (ja) | 水素生成装置 | |
| JP5462687B2 (ja) | 水素製造装置及び燃料電池システム | |
| JP2011207707A (ja) | 水素製造装置及び燃料電池システム | |
| JP2011207729A (ja) | 水素製造装置及び燃料電池システム | |
| JP2006143558A (ja) | 改質装置 | |
| JP2014009130A (ja) | 水素製造装置及び燃料電池システム | |
| WO2011122419A1 (ja) | 水素製造装置及び燃料電池システム | |
| JP6089210B2 (ja) | 水素生成装置 | |
| JP5135606B2 (ja) | 定置型水素製造装置の起動方法 | |
| JP2011146170A (ja) | 燃料電池システム |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201180016468.4 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 11762650 Country of ref document: EP Kind code of ref document: A1 |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2011762650 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 13637793 Country of ref document: US |