明 細 書
環状アミン化合物
技術分野
[0001] 本発明は、アンドロゲン受容体モジュレーターとして有用な環状アミン化合物などに 関する。
発明の背景
[0002] アンドロゲンは精巣および副腎皮質で合成され、標的臓器でアンドロゲン受容体に 結合し、様々な生理活性を発揮する。天然のアンドロゲンは化学的にはすべて C19ス テロイドに属する。その中で主要なアンドロゲンは、主として精巣で合成されるテストス テロンであり、標的細胞への取り込み、生理活性が強い。女性では副腎皮質が主要 なアンドロゲンの供給原となってレ、る。
アンドロゲンは生殖器官 (前立腺、精嚢、副精巣、精管など)の発育'機能維持、胎 生期の性分化、精子形成、二次性徴の発現 (筋肉骨格、音声、脂肪分布などの雄性 化の誘起など)、筋肉などでのタンパク質同化の促進作用、骨代謝への作用などが ある。したがって、精巣機能障害や去勢などによりアンドロゲンが不足するとこのよう な作用が不十分となり、種々の疾病や QOL (quality of life,生活の質)の低下につな がる。これに対して、通常、アンドロゲンを補充する治療法が行われる。テストステロン 以外にも、アンドロゲンの作用のバランスが異なる合成アンドロゲンも研究され、臨床 で用いられている。
[0003] 一方、アンドロゲンが病態の進行に関わっている場合には、アンドロゲンを低下させ る治療が行われる。例えば、アンドロゲン依存性の前立腺癌では、去勢術や GnRH ァゴニスト投与により、テストステロンを低下させ、治療効果を上げている。
アンドロゲンを補充する場合、通常、テストステロンや合成アンドロゲンが用いられて いる。し力もながら、それらはステロイド骨格を有しており、肝臓への負担が大きかつ たり、他のステロイドホルモン作用を示すことがあったりする。したがって、非ステロイド 骨格を有するアンドロゲン受容体モジュレーター(特にァゴニスト)は、アンドロゲン作 用が不足している病態 (ハイポゴナディズム、男性更年期障害など)の改善やアンド口
ゲンが有する作用により改善が期待できる病態 (骨粗鬆症など)に有用であると考え られる。
ピロリジン環を有するナフタレン誘導体が優れたアンドロゲン受容体モジュレーター 作用を有することが知られている(特許文献 1)。し力もながらこの文献には、ピロリジ ン環 3位に置換基を有するピロリジノベンゼン誘導体は開示されて!/、な!/、。
また、抗アンドロゲン作用を有する、ピロリジン環を有するベンゼン誘導体(特許文 献 2および 3)、および骨粗鬆症等に用いられる、ピロリジン環を有するベンゼン誘導 体が知られているが(特許文献 4)、ピロリジン環の 3位に置換基を有する化合物は開 示されていない。
特許文献 1:国際特許出願第 2004/16576号パンフレット
特許文献 2:特開 2002— 88073号公報
特許文献 3:国際特許出願第 2005/090282号パンフレット
特許文献 4 :国際特許出願第 2005/108351号パンフレット
発明の開示
発明が解決しょうとする課題
[0004] 本発明は、さらに優れたアンドロゲン受容体調節作用を有する化合物を提供するこ とを目的とする。
課題を解決するための手段
[0005] 本発明者らは、上記の課題に鑑み、鋭意検討を重ねた結果、式 (I)で表わされる環 状ァミノベンゼン化合物が、予想外にも優れたアンドロゲン受容体調節作用を有する ことを見出し、本発明を完成するに至った。
すなわち、本発明は、
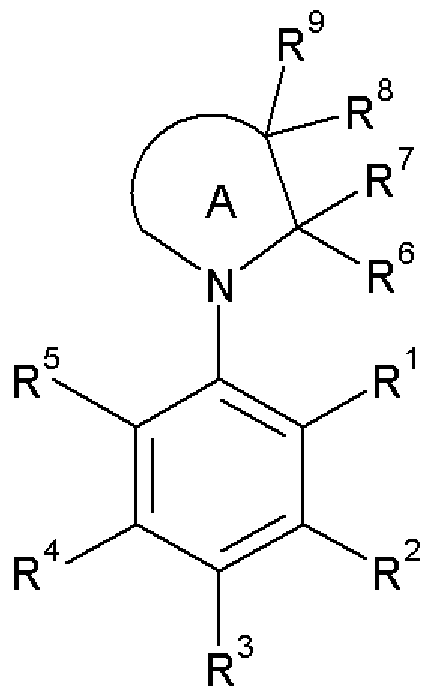
〔1〕式 (I)
[0006] [化 1]
R1は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R2は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R3は電子吸引性基;
R4は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R5は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R6は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R7は置換基を有して!、てもよ!/、アルキル;
R8は水素原子、置換基を有していてもよいアルキル、置換基を有していてもよいアル ケニルまたは置換基を有してレ、てもよ!/、シクロアルキル;
R9は酸素原子を介する基;および
環 Aは R6〜R9以外の置換基を有して!/、てもよい 5または 6員環を示す(但し、
2—クロ口一 4— [ (2S, 3S)— 3—ヒドロキシ一 2—メチルピロリジン一 1—ィル]—3— メチルベンゾニトリル、
2—クロ口一 4— [ (2S, 3S)— 3—ヒドロキシ一 2—メチルピロリジン一 1—ィル]ベンゾ
二トリル、
4- [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]ベンゾニトリル、 2 クロ口一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]—5— メチルベンゾニトリル、
2 クロ口一 3 ェチノレ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1 ィル]ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]—2— (トリフルォロ メチノレ)ベンゾニトリル、
2, 3 ジクロロ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル] 5—メチルベンゾニトリル、
2, 3 ジクロロ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル] ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2—メチルピロリジン一 1—ィル]—3— (トリフルォロ メチノレ)ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 イソプロピルピロリジン一 1—ィル]—2— (トリフ ノレオロメチノレ)ベンゾニトリル、
4— [ (2S, 3R)— 3 ヒドロキシ一 2 イソプロピルピロリジン一 1—ィル]—2— (トリフ ノレオロメチル)ベンゾニトリル、および
2 クロ口一 4— [ (2S)— 3 ヒドロキシ一 2 メチルビペリジン一 1—ィノレ]ベンゾニト リルを除く)。〕で表される化合物(以下、化合物(I)と略記する)またはその塩、 〔2〕 R1が水素原子または置換基を有して!/、てもよ!/、アルキル;
R2が水素原子、ハロゲン原子、置換基を有していてもよいアルキルまたは置換基を 有して!/、てもよ!/、アルコキシ;
R3がシァノ;
R4が水素原子またはハロゲン原子;
R5が水素原子;
R6が水素原子;
R7が置換基を有して!/、てもよ!/、アルキル;
R8が水素原子、置換基を有していていてもよいアルキル、置換基を有していてもよい アルケニルまたは置換基を有してレ、てもよ!/、シクロアルキル;
R9がヒドロキシ;および
環 Aが R6〜R9以外に、 C アルキルを有していてもよい 5員環である上記〔1〕記載
1 -6
の化合物、
〔3〕 R1が (i)水素原子または (ii)ハロゲン原子を有して!/、てもよ!/、C アルキル;
1 -6
R2が水素原子、ハロゲン原子、ハロゲン原子を有して!/、てもよ!/、C アルキルまたは
1 -6
C ァノレコキシ;
1 -6
R3がシァノ;
R4が水素原子またはハロゲン原子;
R5が水素原子;
R6が水素原子;
R7が C ァノレキノレ;
1 - 6
R8が水素原子、ハロゲン原子を有していてもよい C アルキル、 C アルケニルま
1 -6 2-6
たは C シクロアルキル;
3-8
R9がヒドロキシ;
環 Aが R6〜R9以外に、 C アルキルを 1または 2個有していてもよいピロリジン環で
1 -6
ある請求項 1記載の化合物。
〔4〕下記化合物またはその塩。
2 フルオロー 4— [ (2S, 3S)— 3 ヒドロキシー 2, 3 ジメチルピロリジン一 1—ィル ]ベンゾニトリル、
2 フルオロー 4— [ (2S, 3S)— 3 ヒドロキシー 2, 3 ジメチルピロリジン一 1—ィル ]一 3—メチルベンゾニトリル、
4- [ (2S, 3S)— 3 ェチルー 3 ヒドロキシー2 メチルピロリジン 1ーィル ]—2, 6—ジフルォロベンゾニトリル、
2 クロロー 4—[ (2S, 3S)— 3 ヒドロキシー2—メチルー 3 (トリフルォロメチル) ピロリジン 1 ィル]ベンゾニトリル、
2, 6 ジフルオロー 4—[ (2S, 3S)— 3 ヒドロキシー2 イソプロピルー3 メチル
ピロリジン 1 ィル]ベンゾニトリル、
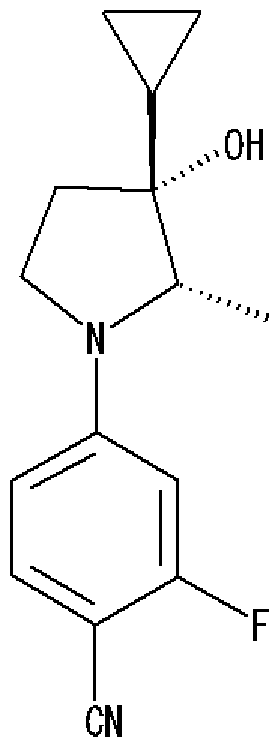
4— [ (2 S , 3R)— 3 シクロプロピル 3—ヒドロキシ 2 メチルピロリジン 1—ィ ル ] 2—フルォロベンゾニトリル、
〔5〕式 (I)
[0009] [化 2]
[0010] 〔式中、
R1は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R2は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R3は電子吸引性基;
R4は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R5は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R6は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R7は置換基を有してレ、てもよ!/、アルキル;
R8は水素原子、置換基を有していてもよいアルキル、置換基を有していてもよいアル ケニルまたは置換基を有してレ、てもよ!/、シクロアルキル;
R9は酸素原子を介する基;および
環 Aは 〜 以外の置換基を有して!/、てもよい 5または 6員環を示す(但し、
2—クロ 4— [ (2S , 3S)— 3—ヒドロキシ一 2—メチルピロリジン一 1—ィル]—3— メチルベンゾニトリル、
2 クロ口一 4— [ (2S , 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]ベンゾ 二トリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]ベンゾニトリル、 2 クロ 4— [ (2S , 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]—5— メチルベンゾニトリル、
2 クロ 3 ェチ 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1 ィル]ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]—2— (トリフルォロ メチノレ)ベンゾニトリル、
2, 3 ジクロロ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル] 5—メチルベンゾニトリル、
2, 3 ジクロロ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル] ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2—メチルピロリジン一 1—ィル]—3— (トリフルォロ メチノレ)ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 イソプロピルピロリジン一 1—ィル]—2— (トリフ ノレオロメチノレ)ベンゾニトリル、
4— [ (2S, 3R)— 3 ヒドロキシ一 2 イソプロピルピロリジン一 1—ィル]—2— (トリフ レオロメチル)ベンゾニトリル、および
2 クロ 4— [ (2S)— 3 ヒドロキシ一 2 メチルビペリジン一 1—ィ ]ベンゾニト リルを除く)。〕で表される化合物のプロドラッグ、
〔6〕式 (I)
[化 3]
R1は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R2は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R3は電子吸引性基;
R4は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R5は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R6は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R7は置換基を有して!/、てもよ!/、アルキル;
R8は水素原子、置換基を有していてもよいアルキル、置換基を有していてもよいアル ケニルまたは置換基を有してレ、てもよ!/、シクロアルキル;
R9は酸素原子を介する基;および
環 Aは R6〜R9以外の置換基を有して!/、てもよい 5または 6員環を示す(但し、
2—クロ口一 4— [ (2S, 3S)— 3—ヒドロキシ一 2—メチルピロリジン一 1—ィル]—3— メチルベンゾニトリル、
2—クロ口一 4— [ (2S, 3S)— 3—ヒドロキシ一 2—メチルピロリジン一 1—ィル]ベンゾ
二トリル、
4 - [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]ベンゾニトリル、 2 クロ口一 4— [ (2S , 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]—5— メチルベンゾニトリル、
2 クロ口一 3 ェチノレ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1 ィル]ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]—2— (トリフルォロ メチノレ)ベンゾニトリル、
2, 3 ジクロロ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル] 5—メチルベンゾニトリル、
2, 3 ジクロロ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル] ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2—メチルピロリジン一 1—ィル]—3— (トリフルォロ メチノレ)ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 イソプロピルピロリジン一 1—ィル]—2— (トリフ ルォロメチル)ベンゾニトリル、
4— [ (2S, 3R)— 3 ヒドロキシ一 2 イソプロピルピロリジン一 1—ィル]—2— (トリフ ルォロメチル)ベンゾニトリル、および
2 クロ口一 4— [ (2S)— 3 ヒドロキシ一 2 メチルビペリジン一 1—ィノレ]ベンゾニト リルを除く)。〕で表される化合物もしくはその塩またはそのプロドラッグを含有してなる 医薬、
〔7〕アンドロゲン受容体調節剤である上記〔6〕記載の医薬、
〔8〕アンドロゲン受容体ァゴニストである上記〔6〕記載の医薬、
〔9〕臓器選択的アンドロゲン受容体調節剤である上記〔6〕記載の医薬、
〔10〕ハイポゴナディズム、男性更年期障害、体力低下、悪液質または骨粗鬆症の予 防'治療剤である上記〔6〕記載の医薬、
〔11〕体力低下抑制剤、筋力増強剤、筋肉増加剤、悪質液抑制剤、体重減少抑制剤 、前立腺肥大症、筋萎縮障害、疾患に起因する筋肉減少の予防 ·治療剤、前立腺の
重量低下剤である上記〔6〕記載の医薬、
〔12〕哺乳動物に対して、式 (I)
[0013] [化 4]
[0014] 〔式中、
R1は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R2は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R3は電子吸引性基;
R4は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R5は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R6は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R7は置換基を有して!/、てもよ!/、アルキル;
R8は水素原子、置換基を有していてもよいアルキル、置換基を有していてもよいアル ケニルまたは置換基を有してレ、てもよ!/、シクロアルキル;
R9は酸素原子を介する基;および
環 Aは R6〜R9以外の置換基を有して!/、てもよレ、5または 6員環を示す(但し、
2 クロ 4— [ (2S , 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]—3— メチルベンゾニトリル、
2 クロ口一 4— [ (2S , 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]ベンゾ 二トリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]ベンゾニトリル、 2 クロ 4— [ (2S , 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]—5— メチルベンゾニトリル、
2 クロ 3 ェチ 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1 ィル]ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]—2— (トリフルォロ メチノレ)ベンゾニトリル、
2, 3 ジクロロ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル] 5—メチルベンゾニトリル、
2, 3 ジクロロ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル] ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2—メチルピロリジン一 1—ィル]—3— (トリフルォロ メチノレ)ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 イソプロピルピロリジン一 1—ィル]—2— (トリフ ノレオロメチノレ)ベンゾニトリル、
4— [ (2S, 3R)— 3 ヒドロキシ一 2 イソプロピルピロリジン一 1—ィル]—2— (トリフ レオロメチル)ベンゾニトリル、および
2 クロ 4— [ (2S)— 3 ヒドロキシ一 2 メチルビペリジン一 1—ィ ]ベンゾニト リルを除く)。〕で表される化合物もしくはその塩またはそのプロドラッグの有効量を投 与することを特徴とするハイポゴナディズム、男性更年期障害、体力低下、悪液質ま たは骨粗鬆症の予防 ·治療方法。
〔13〕ハイポゴナディズム、男性更年期障害、体力低下、悪液質または骨粗鬆症の予 防 ·治療剤を製造するための式 (I)
[化 5]
R1は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R2は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R3は電子吸引性基;
R4は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R5は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R6は水素原子、ハロゲン原子、炭素原子を介する基、窒素原子を介する基、酸素原 子を介する基または硫黄原子を介する基;
R7は置換基を有して!、てもよ!/、アルキル;
R8は水素原子、置換基を有していてもよいアルキル、置換基を有していてもよいアル ケニルまたは置換基を有してレ、てもよ!/、シクロアルキル;
R9は酸素原子を介する基;および
環 Aは R6〜R9以外の置換基を有して!/、てもよい 5または 6員環を示す(但し、
2—クロ口一 4— [ (2S, 3S)— 3—ヒドロキシ一 2—メチルピロリジン一 1—ィル]—3— メチルベンゾニトリル、
2—クロ口一 4— [ (2S, 3S)— 3—ヒドロキシ一 2—メチルピロリジン一 1—ィル]ベンゾ
二トリル、
4 - [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]ベンゾニトリル、 2 クロ口一 4— [ (2S , 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]—5— メチルベンゾニトリル、
2 クロ口一 3 ェチノレ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1 ィル]ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル]—2— (トリフルォロ メチノレ)ベンゾニトリル、
2, 3 ジクロロ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル] 5—メチルベンゾニトリル、
2, 3 ジクロロ一 4— [ (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン一 1—ィル] ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2—メチルピロリジン一 1—ィル]—3— (トリフルォロ メチノレ)ベンゾニトリル、
4— [ (2S, 3S)— 3 ヒドロキシ一 2 イソプロピルピロリジン一 1—ィル]—2— (トリフ ノレオロメチノレ)ベンゾニトリル、
4— [ (2S, 3R)— 3 ヒドロキシ一 2 イソプロピルピロリジン一 1—ィル]—2— (トリフ ノレオロメチル)ベンゾニトリル、および
2 クロ口一 4— [ (2S)— 3 ヒドロキシ一 2 メチルビペリジン一 1—ィノレ]ベンゾニト リルを除く)。〕で表される化合物もしくはその塩またはそのプロドラッグの使用、等に 関する。
[0017] 以下、化合物(I)の置換基の定義について説明する。
R
2、 R
4、 R
5および R
6で 表される「ハロゲン原子」とは、フッ素原子、塩素原子、臭素原子およびヨウ素原子が あげられる。
[0018] R2、 R4、 R5および R6で表される「炭素原子を介する基」とは、例えば、シァノ、 置換基を有していてもよい炭化水素基、ァシル、エステル化されていてもよいカルボ キシル、置換基を有していてもよいイミドイル、置換基を有していてもよいアミジノ、置 換基を有して!/、てもよ!/、力ルバモイル、置換基を有して!/、てもよ!/、チォ力ルバモイル
、置換基を有してレ、てもよ!/、炭素原子を介する複素環基などがあげられる。
[0019] 上記の「置換基を有して!/、てもよ!/、炭化水素基」としては、置換基を有してレ、てもよ いアルキル、置換基を有していてもよいアルケニル、置換基を有していてもよいアル キニル、置換基を有していてもよいシクロアルキル、置換基を有していてもよいァリー ノレ、置換基を有してレ、てもよ!/、ァラルキルなどがあげられる。
[0020] 上記の「置換基を有していてもよいアルキル」の「アルキル」とは、例えば、 C アル
1 - 6 キノレ(例、メチル、ェチル、プロピル、イソプロピル、ブチル、イソブチル、 sec-ブチル、 tert-ブチル、ペンチル、へキシル等)等があげられる。
上記の「置換基を有して!/、てもよ!/、アルキル」が有して!/、てもよ!/、置換基としては、 例えば、
(0ハロゲン原子(例、フッ素原子、塩素原子、臭素原子およびヨウ素原子)、
(ii) C アルコキシ(例、メトキシ、エトキシ、プロポキシ、イソプロポキシ、ブトキシ、ィ
1 - 6
ソブトキシ、 sec-ブトキシ、 tert-ブトキシ等)、
(iii) C アルケニル(例、ビュル、ァリル等)、
2- 6
(iv) C アルキニル(例、ェチュル、プロパルギル等)、
2-6
(V)アミ入
(vi)モノ C アルキルアミノ(例、メチノレアミノ、ェチノレアミノ、プロピルアミノ等)、
1 -6
(vii)ジ C アルキルアミノ(例、ジメチルァミノ、ジェチルァミノ、ジプロピルアミノ等)、
1 -6
(viii)モノ C アルキル カルボニルァミノ(例、ァセチルァミノ、ェチルカルボニルァ
1 -6
ミノ等)、
(ix)ジ(C アルキル—カルボニル)ァミノ(例、ジ(ァセチル)アミ入ジ(ェチルカルポ
1 -6
ニル)ァミノ、ジ(プロピルカルボニル)アミノ等)、
(X)ヒドロキシ、
(xi)シァノ、
(xii)アミジノ、
(xiii)力ノレボキシノレ、
(xiv) C アルコキシ カルボニル(例、メトキシカルボニル、エトキシカルボニル、プ
1 - 6
口ポキシカノレポ二ノレ等)、
(xv)力ルバモイル、
(xvi)モノ C アルキル一力ルバモイル(例、メチルカルバモイル、ェチルカルバモイ
1 - 6
ル等)、
(xvii)ジ C アルキル一力ルバモイル(例、ジメチルカルバモイル、ジェチルカルバ
1 -6
モイル等)、
(xviii)環状アミノカルボニル(例、 1ーァゼチュルカルボニル、ピペリジノカルボニル、 モルホリノカルボニル等)、
(xix)ウレイド、
(XX) C アルキル ウレイド(例、メチルウレイド、ェチルウレイド等)等があげられ、
1 -6
置換可能な位置に 1な!/、し 3個有して!/、てもよ!/、。
[0021] 上記の「置換基を有していてもよいアルケニル」の「ァルケニル」とは、例えば、 C
2-6 アルケニル(例、ビュル、ァリル等)等があげられる。
上記の「置換基を有して!/、てもよ!/、ァルケニル」が有して!/、てもよ!/、置換基としては 、例えば、上記の「置換基を有していてもよいアルキル」が有していてもよい置換基と 同様のものおよび C アルキル(例、メチル、ェチル、プロピル、イソプロピル、ブチ
1 -6
ノレ、イソブチル、 sec-ブチル、 tert-ブチル、ペンチル、へキシル等)等があげられ、置 換可能な位置に 1な!/、し 3個有して!/、てもよ!/、。
[0022] 上記の「置換基を有していてもよいアルキニル」の「アルキニル」とは、例えば、 C
2- 6 アルキニル(例、ェチュル、プロパルギル等)等があげられる。
上記の「置換基を有して!/、てもよ!/、アルキニル」が有して!/、てもよ!/、置換基としては 、例えば、上記の「置換基を有していてもよいアルケニル」が有していてもよい置換基 と同様のもの等があげられ、置換可能な位置に 1な!/、し 3個有して!/、てもよ!/、。
[0023] 上記の「置換基を有して!/、てもよ!/、シクロアルキル」の「シクロアルキル」とは、例え ば、 C シクロアルキニル(例、シクロプロピル、シクロブチル、シクロペンチル、シクロ
3-8
へキシル、シクロへプチル、シクロオタチル等)等があげられる。
上記の「置換基を有して!/、てもよ!/、シクロアルキル」が有して!/、てもよ!/、置換基とし ては、例えば、上記の「置換基を有していてもよいアルケニル」が有していてもよい置 換基と同様のもの等があげられ、置換可能な位置に 1な!/、し 3個有して!/、てもよ!/、。
[0024] 上記の「置換基を有していてもよいァリール」の「ァリール」とは、例えば、 C ァリ
6- 14 ール(例、フエニル、ナフチル、アントリル等)等があげられる。
上記の「置換基を有して!/、てもよ!/、ァリール」が有して!/、てもよ!/、置換基としては、 例えば、上記の「置換基を有して!/、てもよ!/、ァルケニル」が有して!/、てもよ!/、置換基と 同様のもの等があげられ、置換可能な位置に 1な!/、し 3個有して!/、てもよ!/、。
[0025] 上記の「置換基を有して!/、てもよ!/、ァラルキル」の「ァラルキル」とは、例えば、 C
7- 14 ァラルキル(例、ベンジル、フエニルェチル、ナフチルメチル等)等があげられる。 上記の「置換基を有して!/、てもよ!/、ァラルキル」が有して!/、てもよ!/、置換基としては 、例えば、上記の「置換基を有していてもよいアルケニル」が有していてもよい置換基 と同様のもの等があげられ、置換可能な位置に 1な!/、し 3個有して!/、てもよ!/、。
[0026] 上記の「ァシル」としては、上記の「置換基を有して!/、てもよ!/、炭化水素基」がカルボ ニルと結合してなる基があげられる。
上記の「エステル化されて!/、てもよ!/、カルボキシル」としては、上記の「置換基を有し て!/、てもよ!/、炭化水素基」でエステル化されて!/、てもよ!/、カルボキシルがあげられる。 上記の「置換基を有して!/、てもよ!/、イミドィノレ」としては、上記の「置換基を有してレヽ てもよレ、炭化水素基」を 1または 2個有して!/、てもよ!/、イミドイルがあげられる。
上記の「置換基を有して!/、てもよ!/、アミジノ」としては、上記の「置換基を有して!/、て もよレ、炭化水素基」を 1なレ、し 3個有して!/、てもよ!/、アミジノがあげられる。
[0027] 上記の「置換基を有して!/、てもよ!/、力ルバモイル」としては、上記の「置換基を有し て!/、てもよ!/、炭化水素基」を 1または 2個有して!/、てもよ!/、力ルバモイルがあげられる 上記の「置換基を有して!/、てもよ!/、チォ力ルバモイル」としては、上記の「置換基を 有して!/、てもよ!/、炭化水素基」を 1または 2個有して!/、てもよ!/、チォ力ルバモイルがぁ げられる。
[0028] 上記の「置換基を有していてもよい炭素原子を介する複素環基」の、「炭素原子を 介する複素環基」としては、例えば環系を構成する原子(環原子)として、酸素原子、 硫黄原子および窒素原子等から選ばれたヘテロ原子 1ないし 3種 (好ましくは 1ないし 2種)を少なくとも 1個(好ましくは 1ないし 4個、さらに好ましくは 1ないし 2個)含む芳香
族複素環基、飽和あるいは不飽和の非芳香族複素環基 (脂肪族複素環基)であり、 炭素原子に結合基を有する基などが用いられる。
該「芳香族複素環基」としては、例えば、フリル、チェニル、ピロリル、ォキサゾリル、 イソォキサゾリル、チアゾリル、イソチアゾリル、イミダゾリル、ピラゾリル、 1 , 2, 3—ォ キサジァゾリル、 1 , 2, 4—ォキサジァゾリル、 1 , 3, 4—ォキサジァゾリル、フラザニル 、 1 , 2, 3 チ ジ ゾ、リノレ、 1 , 2, 4 チ ジ ゾ、リノレ、 1 , 3, 4 チ ジ ゾ、リノレ、 1 , 2, 3—卜リ ゾ 'リノレ、 1 , 2, 4—卜リ ゾ 'リノレ、テ卜ラゾ'リノレ、ピリジノレ、ピリダジニノレ、ピリミ ジニル、ピラジュル、トリアジニルなどの 5ないし 6員の単環式芳香族複素環基、およ び、例えばベンゾフラニル、イソベンゾフラニル、ベンゾ〔b〕チェニル、インドリル、イソ インドリル、 1H—インダゾリル、ベンズイミダゾリル、ベンゾォキサゾリル、 1 , 2—ベン ゾイソォキサゾリル、ベンゾチアゾリル、ベンゾピラニル、 1 , 2—べンゾイソチアゾリル、 1H—べンゾトリァゾリル、キノリル、イソキノリル、シンノリニル、キナゾリニル、キノキサ リニル、フタラジュル、ナフチリジニル、プリニル、プテリジニル、カルノ ゾリル、 α—力 ノレボリ二ノレ、 β カルボリニル、 γ カルボリニル、アタリジニル、フエノキサジニル、 フエノチアジニル、フエナジニル、フエノキサチイニル、チアントレニル、フエナントリジ ニル、フエナトロリニル、インドリジニル、ピロ口〔1 , 2— b〕ピリダジニル、ピラゾ口〔1 , 5 a〕ピリジル、イミダゾ〔1 , 2— a〕ピリジル、イミダゾ〔1 , 5— a〕ピリジル、イミダゾ〔1 , 2 — 〕ピリダジニル、イミダゾ〔1 , 2— a〕ピリミジニル、 1 , 2, 4 トリァゾロ〔4, 3— a〕ピリ ジル、 1 , 2, 4 トリァゾロ〔4, 3 〕ピリダジニルなどの 8〜; 12員の縮合多環式芳香 族複素環基などが用いられる。
該「非芳香族複素環基」としては、例えば、ォキシラエル、ァゼチジュル、ォキセタ ニル、チェタニル、ピロリジニル、テトラヒドロフリノレ、チオラニル、ピペリジル、テトラヒド ロビラニル、モルホリニル、チオモルホリニル、ピペラジニルなどの 3〜8員(好ましくは 5〜6員)の飽和あるいは不飽和(好ましくは飽和)の非芳香族複素環基 (脂肪族複素 環基)など、あるレヽ (ま 1 , 2, 3, 4 テトラヒドロキノリノレ、 1 , 2, 3, 4 テトラヒドロイソキ ノリルなどのように上記した単環式芳香族複素環基又は縮合多環式芳香族複素環 基の一部又は全部の二重結合が飽和した非芳香族複素環基などが用いられる。 上記の「置換基を有して!/、てもよ!/、炭素原子を介する複素環基」が有して!/、てもよ
い置換基としては、例えば、上記の「置換基を有していてもよいアルケニル」が有して いてもよい置換基と同様のもの等があげられ、置換可能な位置に 1ないし 3個有して いてもよい。
[0030] R2、 R4、 R5および R6で表される「窒素原子を介する基」とは、例えば、(i)アミ入( ii)上記の「炭素原子を介する基」でモノ置換されたァミノおよび (iii)上記の「炭素原子 を介する基」および C アルキル (例、メチル、ェチル、プロピル等)でジ置換された
1 -6
ァミノ等があげられる。
[0031] R2、 R4、 R5、 R6および R9で表される「酸素原子を介する基」とは、例えば、上記 の「炭素原子を介する基」で置換されて!/、てもよ!/、ヒドロキシ等があげられる。
R2、 R4、 R5および R6で表される「硫黄原子を介する基」とは、例えば、上記の「 炭素原子を介する基」で置換されていてもよいメルカプト等があげられる。なお、該メ ルカプトは酸化されて!/、てもよ!/、。
[0032] R3で表される電子吸引性基とは、一般に分子内で水素を標準としたとき、他から電 子を引きつける傾向のある基をいい、有機化学上用いられるものであれば特に限定 されない。例えば、シァ入ニトロ、ハロゲン原子(例えば、フッ素原子、塩素原子、臭 素原子、ヨウ素原子)、ァシル(上記の「ァシル」と同様のものを示す)、エステル化さ れて!/、てもよ!/、カルボキシル(上記の「エステル化されて!/、てもよ!/、カルボキシル」と 同様のものを示す)、置換されて!/、てもよ!/、力ルバモイル(上記の「置換されて!/、ても よい力ルバモイル」と同様のものを示す)または 1ないし 5個のハロゲン原子で置換さ れた C アルキル(例、フルォロメチル、クロロメチル、ジフルォロメチル、ジクロロメチ
1 -6
ノレ、トリフルォロメチル、トリクロロメチル等)等があげられる。
[0033] R7および R8で表される「置換基を有して!/、てもよ!/、アルキル」とは、上記の「置換基 を有して!/、てもよ!/、アルキル」と同様のものがあげられる。
[0034] R8で表される「置換基を有して!/、てもよ!/、ァルケニル」とは、上記の「置換基を有し てレ、てもよ!/ヽァルケニル」と同様のものがあげられる。
[0035] R8で表される「置換基を有して!/、てもよ!/、シクロアルキル」とは、上記の「置換基を有 して!/、てもよ!/ヽシクロアルキル」と同様のものがあげられる。
[0036] 環 Aは R6〜R9以外の置換基を有していてもよい 5または 6員環を示す。環 Aとして
は、ピロリジン環およびピぺリジン環があげられる。
[0037] 環 Aがさらに有していてもよい置換基としては、例えば、上記の「置換基を有してい てもよ!/、ァルケニル」が有して!/、てもよ!/、置換基と同様のもの等があげられ、置換可 能な位置に 1な!/、し 3個有して!/、てもよ!/、。
[0038] R1としては、水素原子または置換基を有していてもよいアルキルが好ましぐなかで も (i)水素原子または (ii)ハロゲン原子を有していてもよい C アルキルが好ましい。と
1 - 6
りわけ、(i)水素原子または (ii)フッ素原子を有してレ、てもよ!/、メチルが好まし!/、。
[0039] R2としては、水素原子、ハロゲン原子、置換基を有して!/、てもよ!/、アルキルまたは 置換基を有していてもよいアルコキシが好ましい。なかでも、水素原子、ハロゲン原子 、ハロゲン原子を有していてもよい C アルキルまたは C アルコキシが好ましい。
1 -6 1 -6
とりわけ、水素原子、フッ素原子、塩素原子、フッ素原子を有していてもよいメチルま たはメトキシが好ましい。
R3としては、シァノが好ましい。
R4としては、水素原子またはハロゲン原子が好ましい。なかでも、水素原子またはフ ッ素原子が好ましい。
R5としては、水素原子が好ましい。
R6としては、水素原子が好ましい。
[0040] R7としては、置換基を有していてもよいアルキルが好ましい。なかでも、 C アルキ
1 -6 ルが好ましい。とりわけ、メチル、ェチルまたはイソプロピルが好ましい。
R8としては、水素原子、置換基を有していてもよいアルキル、置換基を有していても よ!/、アルケニルまたは置換基を有して!/、てもよ!/、シクロアルキルが好まし!/、。なかでも 、水素原子、ハロゲン原子を有していてもよい C アルキル、 C アルケニルまたは
1 -6 2- 6
C シクロアルキルが好まし!/、。とりわけ、水素原子、フッ素原子を有して!/、てもよ!/ヽ
3 -8
メチル、ェチル、プロピル、ビュルまたはシクロプロピルが好ましい。
R9としては、ヒドロキシが好ましい。
環 Aとしては、 R6〜R9以外に、ハロゲン原子および C アルキルから選ばれる置換
1 -6
基を 1ないし 3個有していてもよい 5員環(ピロリジン環)が好ましい。なかでも、 R6〜R9 以外に、メチルを 1または 2個有して!/、てもよ!/、5員環(ピロリジン環)が好ましレ、。
[0041] 化合物(I)としては、
R1が水素原子または置換基を有して!/、てもよ!/、アルキル;
R2が水素原子、ハロゲン原子、置換基を有していてもよいアルキルまたは置換基を 有して!/、てもよ!/、アルコキシ;
R3がシァノ;
R4が水素原子またはハロゲン原子;
R5が水素原子;
R6が水素原子;
R7が置換基を有して!/、てもよ!/、アルキル;
R8が水素原子、置換基を有していていてもよいアルキル、置換基を有していてもよい アルケニルまたは置換基を有してレ、てもよ!/、シクロアルキル;
R9がヒドロキシ;
環 Aが R6〜R9以外に、 C アルキルを有して!/、てもよい 5員環であるものが好まし!/ヽ
1 -6
〇
[0042] なかでも、
R1が (i)水素原子または (ii)ハロゲン原子を有して!/、てもよ!/、C アルキル;
1 -6
R2が水素原子、ハロゲン原子、ハロゲン原子を有して!/、てもよ!/、C ァノレキノレまたは
1 -6
C ァノレコキシ;
1 -6
R3がシァノ;
R4が水素原子またはハロゲン原子;
R5が水素原子;
R6が水素原子;
R7が C ァノレキノレ;
1 - 6
R8が水素原子、 C アルキル、 C アルケニルまたは C シクロアルキル;
1 -6 2-6 3 -8
R9がヒドロキシ;
環 Aが R6〜R9以外に、メチルを 1または 2個有していてもよいピロリジン環であるもの が好ましい。
[0043] とりわけ、
R1が (i)水素原子または (ii)フッ素原子を有して!/、てもよ!/、メチル;
R2が水素原子、フッ素原子、塩素原子、フッ素原子を有していてもよいメチルまたは メトキシ;
R3がシァノ;
R4が水素原子またはフッ素原子;
R5が水素原子;
R6が水素原子;
R7がメチル、ェチルまたはイソプロピル;
R8が水素原子、メチル、ェチル、プロピル、ビュルまたはシクロプロピル;
R9がヒドロキシ;
環 Aが R6〜R9以外に、メチルを 1または 2個有していてもよいピロリジン環であるもの が好ましい。
[0044] より具体的には、後述の実施例 1〜63に記載の化合物またはその塩が好ましい。
特に、
2 フルオロー 4— [ (2S, 3S)— 3 ヒドロキシー 2, 3 ジメチルピロリジン一 1—ィル ]ベンゾニトリル (実施例 1)、
2 フルオロー 4— [ (2S, 3S)— 3 ヒドロキシー 2, 3 ジメチルピロリジン一 1—ィル ]一 3 メチルベンゾニトリル(実施例 2)、
4- [ (2S, 3S)— 3 ェチルー 3 ヒドロキシー2 メチルピロリジン 1ーィル ]—2, 6—ジフルォロベンゾニトリル(実施例 7)、
2 クロロー 4—[ (2S, 3S)— 3 ヒドロキシー2—メチルー 3 (トリフルォロメチル) ピロリジン— 1 ィル]ベンゾニトリル(実施例 18)、
2, 6 ジフルオロー 4—[ (2S, 3S)— 3 ヒドロキシー2 イソプロピルー3 メチル ピロリジン— 1—ィル]ベンゾニトリル(実施例 20)、
4— [ (2 S , 3R)— 3 シクロプロピル 3—ヒドロキシ 2 メチルピロリジン 1—ィ ノレ ] 2 フルォロベンゾニトリル(実施例 32)、またはそれらの塩が好ましい。
[0045] 以下に化合物 (I)の製造法につ!/、て記載する。化合物 (I)は一般有機合成法を用 いることにより、または公知の合成法(例、 WO2004/016576号パンフレット)に準
じて製造すること力でさる。
化合物(I)は、例えば式 (II)
[0046] [化 6]
[0047] 〔式中、 Mは脱離基を、他の記号は上記と同意義を示す。〕で表される化合物または その塩と、式 (III)
[0048] [化 7]
[0049] 〔式中、各記号は上記と同意義を示す。〕で表される化合物またはその塩とを反応さ せ、保護基を有する場合は保護基を除去することにより製造することができる。
[0050] Mで示される「脱離基」としては、例えばフッ素、塩素、臭素、ヨウ素等のハロゲン、ト リフルォロメタンスルホニルォキシ、 p—トルエンスルホニルォキシ、メタンスルホニル ォキシ等を用いることができる。
化合物(III)またはその塩は、化合物(II) 1モルに対して通常 1から 3モルを用いる 。この反応は必要に応じ、炭酸リチウム、炭酸カリウム、炭酸ナトリウム、炭酸セシウム 、炭酸水素ナトリウム、水酸化ナトリウム、ナトリウム tert—ブトキシド、カリウム tert—ブ トキシド、トリエチルァミン、ジイソプロピルェチルァミン(DIEA)、ピリジン、 4— (ジメ チルァミノ)ピリジン(DMAP)、 1,8—ジァザビシクロ [5· 4. 0]ゥンデクー 7—ェン(D BU)、 1,5—ジァザビシクロ [4· 3. 0]ノンー5—ェン(DBN)等の塩基を添加すること
により、円滑に反応を進行させることもできる。更に触媒として遷移金属触媒 (例えば 、 J.O.C., 1997, 62, ppl264-1267)を用いることも好適である。
反応は、不活性溶媒、例えばメタノール、エタノール、プロパノール、イソプロパノー ノレ、 n ブタノール、テトラヒドロフラン、ジェチルエーテル、ァセトニトリノレ、アセトン、 酢酸ェチノレ、 1 , 2 ジメトキシェタン、 1 , 4 ジォキサン、トノレェン、ベンゼン、キシレ ン、ジクロロメタン、クロ口ホルム、 1 , 2—ジクロロェタン、 N, N ジメチルホルムアミド (DMF)、ジメチルスルホキシド(DMSO)等、あるいはこれらの混合溶媒中で行うこと ができる。反応は約 0°Cないし 180°Cの温度範囲で行われる。反応時間は特に限定 されないが、通常 0. 1時間から 100時間、好ましくは、 0. 5時間から 72時間である。
[0051] さらに、化合物(I)中の A環上の 1個またはそれより多くの置換基を、他の置換基に 変換すること力できる。例えばそれ自体公知の方法に準じて、カルボニルを還元して アルコールへと導き、アルコールを脱水してォレフィンへと導き、または、アルコール をアルキル化してエーテルに導くこともできる。出発物質として用いる化合物(11)、 (II I)は、公知の方法またはそれに準じた方法により合成することができ、例えば後記の 参考例に示す方法により製造することができる。
ここで、上記式中の基は、一般有機合成上用いられる保護基で保護されていてもよ ぐ反応後所望により公知の方法で保護基を除去することができる。
力べして得られた化合物 (I)は、 自体公知の分離手段、例えば濃縮、減圧濃縮、溶 媒抽出、液性変換、塩析、晶出、再結晶、転溶、クロマトグラフィー等により単離、精 製すること力 Sでさる。
化合物(I)が遊離体で得られた場合には、自体公知の方法あるいはそれに準じる 方法によって目的とする塩に変換することができ、逆に塩で得られた場合には、自体 公知の方法あるいはそれに準ずる方法により、遊離体または、 目的とする他の塩に 変換すること力でさる。
[0052] 化合物(I)は、水和物であってもよぐ非水和物であってもよい。
化合物 (I)が光学活性体の混合物として得られる場合には、 自体公知の光学分割 手段により目的とする光学活性体に分離することができる。
化合物 (I)は同位元素 (例、 2H、 3H、 14C等)等で標識されていてもよい。
化合物(I)のプロドラッグは、生体内における生理条件下で酵素や胃酸等による反 応により化合物(I)に変換する化合物、即ち酵素的に酸化、還元、加水分解等を起こ して化合物(I)に変化する化合物、胃酸等により加水分解等を起こして化合物(I)に 変化する化合物をいう。化合物(I)のプロドラッグとしては、化合物(I)のァミノがァシ ノレ化、アルキル化、リン酸化された化合物(例、化合物(I)のァミノがエイコサノィル化 、ァラニル化、ペンチルァミノカルボニル化、(5 メチルー 2 ォキソ 1 , 3 ジォキ ソレン一 4—ィル)メトキシカルボニル化、テトラヒドロフラニル化、ピロリジルメチル化、 ビバロイルォキシメチル化、 tert ブチル化された化合物等);化合物(I)のヒドロキシ がァシル化、アルキル化、リン酸化、ホウ酸化された化合物(例、化合物(I)のヒドロキ シがァセチル化、パルミトイル化、プロパノィル化、ビバロイル化、スクシ二ル化、フマ リル化、ァラニル化、ジメチルァミノメチルカルボニル化された化合物等);化合物(I) のカルボキシルがエステル化、アミド化された化合物(例、化合物(I)のカルボキシル がェチルエステル化、フエニルエステル化、カルボキシメチルエステル化、ジメチルァ ミノメチルエステル化、ピバロィルォキシメチルエステル化、エトキシカルボ二ルォキ シェチルエステル化、フタリジルエステル化、(5 メチルー 2 ォキソ 1 , 3 ジォ キソレンー4 ィル)メチルエステル化、シクロへキシルォキシカルボニルェチルエス テル化、メチルアミド化された化合物等)等が用いられる。これらの化合物は自体公 知の方法によって化合物(I)力、ら製造すること力 Sできる。
また、化合物(I)のプロドラッグは、広川書店 1990年刊「医薬品の開発」第 7巻分子 設計 163頁から 198頁に記載されているような生理的条件で化合物(I)に変化するも のであってもよい。
本発明中の化合物(プロドラッグを含む)は塩を形成していてもよい。化合物の塩と しては反応を阻害しないものであれば特に限定されないが、例えば無機塩基との塩 、アンモニゥム塩、有機塩基との塩、無機酸との塩、有機酸との塩、アミノ酸との塩な どが用いられる。無機塩基との塩の好適な例としては、例えばナトリウム塩、カリウム 塩などのアルカリ金属塩、カルシウム塩、マグネシウム塩などのアルカリ土類金属塩、 並びにアルミニウム塩、アンモニゥム塩などが用いられる。有機塩基との塩の好適な 例としては、例えばトリメチルァミン、トリェチルァミン、ピリジン、ピコリン、 2, 6 ルチ
ジン、エタノールァミン、ジエタノールァミン、トリエタノールァミン、シクロへキシルアミ ン、ジシクロへキシルァミン、 N, N'—ジベンジルエチレンジァミンなどとの塩が用い られる。無機酸との塩の好適な例としては、例えば塩酸、臭化水素酸、硝酸、硫酸、リ ン酸などとの塩が用いられる。有機酸との塩の好適な例としては、例えばギ酸、酢酸 、トリフルォロ酢酸、フタル酸、フマル酸、シユウ酸、酒石酸、マレイン酸、クェン酸、コ ハク酸、リンゴ酸、メタンスルホン酸、ベンゼンスルホン酸、 p—トルエンスルホン酸な どとの塩が用いられる。塩基性アミノ酸との塩の好適な例としては、例えばアルギニン 、リジン、オル二チンなどとの塩が挙げられ、酸性アミノ酸との塩の好適な例としては、 例えばァスパラギン酸、グルタミン酸などとの塩が用いられる。
本発明の化合物(I)もしくはその塩またはそのプロドラッグ (以下、本発明の化合物 と略記する場合がある)は、アンドロゲン受容体調節作用、特にアンドロゲン受容体ァ ゴニスト作用を有し、哺乳動物におけるアンドロゲン受容体ァゴニストの投与が有効 な疾患の予防または治療に用いることができる。アンドロゲン受容体ァゴニストの投与 が有効な疾患には、ハイポゴナディズム、骨粗鬆症、ホルモン抵抗性癌(特に LHRH ァゴニスト抵抗性癌)、更年期障害 (特に男性更年期障害)、体力低下 (frailty)、悪液 質 (カケタシァ)、貧血、動脈硬化、アルツハイマー病、勃起不全、うつ病または消耗 性疾患および高 TG血症(高脂血症)などが含まれる。特にハイポゴナディズム、男性 更年期障害、体力低下、悪液質または骨粗鬆症の予防 ·治療に用いられる。
本発明の化合物は、臓器選択的アンドロゲン受容体調節作用を有し、例えば、前 立腺に対してはアンタゴニスト、筋肉に対してはァゴニスト作用を有する。具体的には 、本発明の化合物は筋肉(例えば、肛門挙筋など)の重量を増加する投与量で、前 立腺の重量を増加させない作用を有する。より具体的には、肛門挙筋重量を約 20% 以上 (好ましくは約 20%〜約 50%)増加させる投与量で、前立腺重量の増加が約 1 0%以下 (好ましくは 0%以下)である。ここで「前立腺重量の増加が 0%以下」とは、 前立腺重量の増加が 0%の場合、前立腺重量の増減がないことを意味し、前立腺重 量の増加が 0%未満の場合、前立腺重量がその絶対値の分減少することを意味する 。従って、本発明の化合物は以下のような医薬として用いることができる。
(1)体力低下の抑制剤。
(2)筋力増強剤または筋肉増加剤(高齢入院患者を寝たきりにさせない、リハビリ期 間を短縮できる等の効果を有する)。
(3)例えば、 AIDSや癌などに起因する悪液質の抑制剤。
(4)体重減少抑制剤。
(5)前立腺肥大症の予防 ·治療剤(前立腺重量を低下させる)。
(6)筋萎縮障害の予防'治療剤。
(7)前立腺の重量低下剤。
(8)疾患(例えば、筋ジストロフィー、筋萎縮症、 X—連鎖脊髄延髄筋萎縮症(SBMA) 、悪液質、栄養不良、ハンセン病、糖尿病、腎疾患、 COPD (慢性閉塞性肺疾患)、癌 、末期腎不全、サルコぺユア(高齢による筋損失)、肺気腫、骨軟化症、 HIV感染、 AI DS、心筋症など)に起因する筋肉減少の予防 ·治療剤。
(9)閉経後女性の筋力低下の抑制剤。
(10)閉経後女性の骨塩量低下の抑制剤。
(11)閉経後女性のホットフラッシュ(例、ほてり'発汗など)の抑制剤。
(12) LHRHァゴニスト(リュープロレリン、ゴセレリン、ブセレリン、ナファレリン、トリプト レリン、ゴナドレリンなど)、 LHRHアンタゴニスト(ガユレリックス、セトロレリックス、アン タレリックス、ァバレリックス、スフォゴリックスなど)などの LHRH調節薬の副作用軽減 剤。
(13) LHRH調節薬などの薬剤投与後の筋力低下の抑制剤。
(14) LHRH調節薬などの薬剤投与後の骨塩量低下の抑制剤。
(15) LHRH調節薬などの薬剤投与後のホットフラッシュ(例、ほてり'発汗など)の抑 制剤。
また、本発明の化合物は、前立腺肥大症の予防治療剤または前立腺重量低下剤 として用いながら、体力低下の抑制剤、筋力増強剤または筋肉増加剤として効果を 有し、高齢入院患者を寝たきりにさせずリハビリ期間を短縮することが期待できる。前 立腺重量を増加する副作用がないので、前立腺癌の可能性が高い患者に対する前 立腺癌の治療または予防剤が期待できる。さらに、男性化の副作用がなぐ女性へ の適用が可能であり閉経後女性の筋力低下または骨塩量低下の抑制剤または閉経
後女性のホットフラッシュ(ほてり'発汗等)抑制剤も期待できる。さらに、 LHRHァゴ 二スト(リュープロレリン、ゴセレリン、ブセレリン、ナファレリン、トリプトレリン、ゴナドレリ ンなど)、 LHRHアンタゴニスト(ガユレリックス、セトロレリックス、アンタレリックス、アバ レリックス、スフォゴリックスなど)の副作用軽減剤、これらの薬剤投与後の筋力低下ま たは骨塩量低下の抑制剤、これらの薬剤投与後のホットフラッシュ(ほてり'発汗など) の抑制剤としても期待される。
本発明の化合物は、アンドロゲンに高感受性になることでホルモン治療に抵抗性を 獲得した癌に対して逆に過剰の刺激を与えることで増殖阻害や細胞死を導くことによ り、種々の癌のなかでもホルモン抵抗性を獲得した、乳癌、前立腺癌、子宮体癌、子 宮頸癌、卵巣癌、膀胱癌、甲状腺癌、骨腫瘍、陰茎癌に対する予防または治療剤と して用いることができ、特に前立腺癌の予防または治療剤として有用である。
ホルモン抵抗性癌としては、例えば LHRH誘導体抵抗性癌が挙げられ、好ましくは LHRHァゴニスト抵抗性癌である。
本発明の化合物は、毒性が低ぐそのまま医薬として、または自体公知の薬学的に 許容しうる担体等と混合して哺乳動物 (例、ヒト、ゥマ、ゥシ、犬、猫、ラット、マウス、ゥ サギ、ブタ、サル等)に対して医薬組成物として用いることができる。
医薬組成物の中に本発明の化合物とともに他の活性成分、例えば下記のホルモン 療法剤、抗癌剤(例えば、化学療法剤、免疫療法剤、または細胞増殖因子ならびに その受容体の作用を阻害する薬剤等)、制吐剤等を含有させてもよい。
本発明の化合物を医薬として、ヒト等の哺乳動物に投与するにあたって、投与方法 は通常例えば錠剤、カプセル剤(ソフトカプセル、マイクロカプセルを含む)、散剤、 顆粒剤等として経口的、あるいは注射剤、坐剤、ペレット等として非経口的に投与で きる。「非経口」には、静脈内、筋肉内、皮下、臓器内、鼻腔内、皮内、点眼、脳内、 直腸内、膣内および腹腔内、腫瘍内部、腫瘍の近位等への投与あるいは直接病巣 への投与を含む。
本発明の化合物の投与量は、投与ルート、症状等によって異なる力 例えば乳癌、 前立腺癌を持つ患者(体重 40な!/、し 80kg)に抗癌剤として経口投与する場合、例え ば 1曰 0· ;!〜 200mg/kg体重、好ましくは 1曰;!〜 100mg/kg体重、さらに好ましく
は 1日 l〜50mg/kg体重である。この量を 1日 1回または 2〜3回に分けて投与する こと力 Sでさる。
本発明の化合物は、薬学的に許容される担体と配合し、錠剤、カプセル剤、顆粒剤 、散剤等の固形製剤;またはシロップ剤、注射剤等の液状製剤として経口または非経 口的に投与することができる。
薬学的に許容される担体としては、製剤素材として慣用されている各種有機あるい は無機担体物質が用いられ、固形製剤における賦形剤、滑沢剤、結合剤、崩壊剤; 液状製剤における溶剤、溶解補助剤、懸濁化剤、等張化剤、緩衝剤、無痛化剤等と して配合される。また必要に応じて、防腐剤、抗酸化剤、着色剤、甘味剤等の製剤添 加物を用いることもできる。
賦形剤の好適な例としては、例えば乳糖、白糖、 D—マンニトール、デンプン、結晶 セルロース、軽質無水ケィ酸等が用いられる。
滑沢剤の好適な例としては、例えばステアリン酸マグネシウム、ステアリン酸カルシ ゥム、タルク、コロイドシリカ等が用いられる。
結合剤の好適な例としては、例えば結晶セルロース、白糖、 D—マンニトール、デキ ルピロリドン等が用いられる。
崩壊剤の好適な例としては、例えばデンプン、カルボキシメチルセルロース、カルボ キシメチルセルロースカルシウム、クロスカルメロースナトリウム、カルボキシメチルスタ ーチナトリウム等が用いられる。
溶剤の好適な例としては、例えば注射用水、アルコール、プロピレングリコール、マ クロゴール、ゴマ油、トウモロコシ油等が用いられる。
溶解補助剤の好適な例としては、例えばポリエチレングリコール、プロピレングリコ ール、 D—マンニトール、安息香酸べンジル、エタノール、トリスァミノメタン、コレステ ロール、トリエタノールァミン、炭酸ナトリウム、クェン酸ナトリウム等が用いられる。 懸濁化剤の好適な例としては、例えばステアリルトリエタノールァミン、ラウリル硫酸 ナトリウム、ラウリルアミノプロピオン酸、レシチン、塩化ベンザルコニゥム、塩化べンゼ トニゥム、モノステアリン酸グリセリン等の界面活性剤;例えばポリビュルアルコール、
ポリビュルピロリドン、カルボキシメチルセルロースナトリウム、メチルセルロース、ヒドロ キシメチノレセノレロース、ヒドロキシェチノレセノレロース、ヒドロキシプロピノレセノレロース等 の親水性高分子等が用いられる。
[0058] 等張化剤の好適な例としては、例えば塩化ナトリウム、グリセリン、 D—マンニトーノレ 等が用いられる。
緩衝剤の好適な例としては、例えばリン酸塩、酢酸塩、炭酸塩、クェン酸塩等の緩 衝液等が用いられる。
無痛化剤の好適な例としては、例えばべンジルアルコール等が用いられる。 防腐剤の好適な例としては、例えば、パラォキシ安息香酸エステル類、クロロブタノ ール、ベンジルアルコール、フエネチルアルコール、デヒドロ酢酸、ソルビン酸等が用 いられる。
抗酸化剤の好適な例としては、例えば亜硫酸塩、ァスコルビン酸等が用いられる。 医薬組成物は、剤型、投与方法、担体等により異なるが、本発明の化合物を製剤 全量に対して通常 0. ;!〜 95% (w/w)含有させることにより、常法に従って製造する こと力 Sでさる。
また、(1)本発明の化合物の有効量を投与することと、(2) (i)他の抗癌剤の有効量 を投与すること、(ii)他のホルモン療法剤の有効量を投与すること、および (iii)非薬剤 療法からなる群から選ばれる 1〜3種とを組み合わせることにより、より効果的に癌を 予防 ·治療することができる。非薬剤療法としては、例えば、手術、アンジォテンシン II 等を用いる昇圧化学療法、放射線療法、遺伝子療法、温熱療法、凍結療法、レーザ 一灼熱療法等が用いられ、これらを 2種以上組み合わせることもできる。
例えば、本発明化合物は、他のホルモン療法剤、他の抗癌剤(例えば、化学療法 剤、免疫療法剤(ワクチンを含む)、抗体、遺伝子治療薬、細胞増殖因子ならびにそ の受容体の作用を阻害する薬剤、血管新生を阻害する薬剤)、制吐剤等 (以下、併 用薬物と略記する)と併用して使用すること力 Sできる。
[0059] 本発明の化合物は単剤として使用しても優れた抗癌作用を示すが、さらに上記併 用薬物の一つまたは幾つかと併用(多剤併用)することによって、その効果をより一層 増強または患者の QOLを改善させることができる。
該「ホルモン療法剤」としては、例えば、ホスフェストロール、ジェチルスチルベスト口 ール、クロロトリアニセリン、酢酸メドロキシプロゲステロン、酢酸メゲストロール、酢酸ク ロルマジノン、酢酸シプロテロン、ダナゾール、ジエノゲスト、ァソプリスニル、ァリルェ ストレノール、ゲストリノン、ノメゲストロール、タデナン、メノ ルトリシン、ラロキシフェン、 オルメロキフェン、レボルメロキシフェン、抗エストロゲン(例、タエン酸タモキシフェン、 タエン酸トレミフェン等)、 ERダウンレギュレーター (例えばフルべストラント等)、ヒト閉 経ゴナドトロピン、卵胞刺激ホルモン、ピル製剤、メピチォスタン、テスト口ラタトン、アミ ノグルテチイミド、 LH— RH誘導体(例、 LH— RHァゴニスト(例、酢酸ゴセレリン、ブ セレリン、リュープロレリン等)、 LH— RHアンタゴニスト)、ドロロキシフェン、ェピチォ スタノール、スルホン酸ェチュルエストラジオール、ァロマターゼ阻害薬(例、塩酸フ アドロゾーノレ、アナストロゾーノレ、レトロゾーノレ、ェキセメスタン、ボロゾーノレ、フォノレメス タン等)、抗アンドロゲン薬(例、フルタミド、ビカルタミド、ニルタミド等)、 5 a—レダク ターゼ阻害薬 (例、フィナステリド、デュタステリド、エブリステリド等)、副腎皮質ホルモ ン系薬剤(例、デキサメタゾン、プレドニゾロン、ベタメタゾン、トリアムシノロン等)、ァ ンドロゲン合成阻害薬 (例、アビラテロン等)、レチノイドおよびレチノイドの代謝を遅ら せる薬剤(例、リアロゾール等)等が用いられる。好ましくは LH— RH誘導体である。 該「化学療法剤」としては、例えばアルキル化剤、代謝拮抗剤、抗癌性抗生物質、 植物由来抗癌剤、その他の化学療法剤等が用いられる。
「アルキル化剤」としては、例えば、ナイトロジェンマスタード、塩酸ナイトロジエンマ スタードー N—ォキシド、クロラムブチル、シクロフォスフアミド、ィホスフアミド、チォテ ノ 、カルボコン、トシル酸インプロスルファン、ブスルファン、塩酸二ムスチン、ミトブロ 二トール、メルファラン、ダカルバジン、ラニムスチン、リン酸エストラムスチンナトリウム 、トリエチレンメラミン、力ノレムスチン、口ムスチン、ストレプトゾシン、ピポブロマン、エト ダルシド、カルポプラチン、シスプラチン、ミポプラチン、ネダプラチン、ォキサリプラチ ン、アルトレタミン、アンバムスチン、塩酸ジブロスビジゥム、フォテムスチン、プレドニ ムスチン、プミテパ、リボムスチン、テモゾ口ミド、トレォスルファン、トロフォスフアミド、 ジノスタチンスチマラマー、カルボコン、アドゼレシン、システムスチン、ビゼレシン等 が用いられる。
「代謝拮抗剤」としては、例えば、メルカプトプリン、 6—メルカプトプリンリボシド、チ 塩酸アンシタビン、 5— FU系薬剤(例、フルォロウラシル、テガフール、 UFT、ドキシ フルリジン、カルモフール、ガロシタビン、エミテフール等)、アミノプテリン、ロイコボリ
、クラドリビン、エミテフール、フルダラビン、ゲムシタビン、ヒドロキシカルバミド、ペント スタチン、ピリトレキシム、イドキシゥリジン、ミトグァゾン、チアゾフリン、アンバムスチン 等が用いられる。
「抗癌性抗生物質」としては、例えば、ァクチノマイシン D、ァクチノマイシン C、マイ トマイシン C、クロモマイシン A3、塩酸ブレオマイシン、硫酸ブレオマイシン、硫酸ぺ プロマイシン、塩酸ダウノルビシン、塩酸ドキソルビシン、塩酸アクラルビシン、塩酸ピ ラルビシン、塩酸ェピルビシン、ネオカルチノスタチン、ミスラマイシン、ザルコマイシ ン、カルチノフィリン、ミトタン、塩酸ゾルビシン、塩酸ミトキサントロン、塩酸イダルビシ ン等が用いられる。
「植物由来抗癌剤」としては、例えば、エトポシド、リン酸エトポシド、硫酸ビンブラス チン、硫酸ビンクリスチン、硫酸ビンデシン、テニポシド、パクリタキセル、ドセタキセル 、 DJ-927、ビノレノレビン、イリノテカン、トポテカン等が用いられる。
「その他の化学療法剤」としては、ソブゾキサン等が用いられる。
該「免疫療法剤(BRM)」としては、例えば、ピシバニール、クレスチン、シゾフィラン 、レンチナン、ウベニメタス、インターフェロン、インターロイキン、マクロファージコロニ 一刺激因子、顆粒球コロニー刺激因子、エリスロポイエチン、リンホトキシン、コリネバ クテリゥムパルブム、レバミゾール、ポリサッカライド K、プロコダゾール等が用いられる 。またワクチンとしては BCGワクチン、 PROVENGE、 Onyvax_P、 PROSTVAC_VF、 G VAX, DCVax_Prostate、 SAPOIMMUNE, VPM-4-001などが用いられる。
該「抗体」としては EpiCAMに対する抗体、 PSCAに対する抗体、 PSMAに対する抗 体が用いられる。
該「細胞増殖因子ならびにその受容体の作用を阻害する薬剤」における、「細胞増 殖因子」としては、細胞の増殖を促進する物質であればどのようなものでもよぐ通常
、分子量が 20,000以下のペプチドで、受容体との結合により低濃度で作用が発揮さ れる因子が用いられ、具体的には、(l ) EGF (印 idermal growth factor)またはそれと 実質的に同一の活性を有する物質〔例、 EGF、ハレダリン、 TGF— a、 HB— EGF 等〕、(2)インシュリンまたはそれと実質的に同一の活性を有する物質〔例、インシユリ ン、 IGF unsulin- like growth factor)—1、 IGF— 2 ]、 ^ό) FGF (fibroblast growth fa ctor)またはそれと実質的に同一の活性を有する物質〔例、酸性 FGF、塩基性 FGF、 KGF (keratinocyte growth factor)、 FGF- 10等〕、(4)その他の細胞増殖因子〔例、 CSF (colony stimulating factor)、 EPO (erythropoietin)、 IL— 2 (interleukin-2)、 N GF(nerve growth factor) PDGF (platelet-derived growth factor)、 TGF β (transfor ming growth factor β )、 HGF (hepatocyte growth factor)、 VEGF (vascular endothel ial growth factor)等〕等があげられる。
該「細胞増殖因子の受容体」としては、上記の細胞増殖因子と結合能を有する受容 体であればいかなるものであってもよぐ具体的には、 EGF受容体およびそれと同じ ファミリーに属する受容体である HER2、 HER3および HER4、インシュリン受容体、 I GF受容体、 FGF受容体 1または FGF受容体 2等があげられる。
該「細胞増殖因子ならびにその受容体の作用を阻害する薬剤」としては、トラスッズ マブ(ノヽーセプチン(商標); HER2抗体)、メシル酸ィマチニブ、 ZD 1839、セツキシ マブ、ゲフイチニブ、エノレロチニブ等があげられる。
該「血管新生を阻害する薬剤」としては、 VEGFに対する抗体 (例、べバシツマブ) 、 VEGF受容体に対する抗体、 VEGF受容体キナーゼ阻害剤(例、 SU 11248等)、 P DGF受容体キナーゼ阻害剤、 Tie2キナーゼ阻害剤、サリドマイド等が用いられる。 前記の薬剤の他に、 Lーァスパラギナーゼ、ァセグラトン、塩酸プロカルバジン、プ ロトポルフィリン'コバルト錯塩、水銀へマトポルフィリン'ナトリウム、分化誘導剤(例、 レチノイド、ビタミン D類等)、 a ブロッカー(例、塩酸タムスロシン、ナフトビジル、ゥ ラビジル、アルフゾシン、テラゾシン、プラゾシン、シロドシン等)セリン.スレオニンキナ ーゼ阻害薬、エンドセリン受容体拮抗薬 (例、アトラセンタン等)、プロテアゾーム阻害 薬(例、ボルテゾミブ等)、 Hsp90阻害薬 (例、 17-AAG等)、スピロノラタトン、ミノキシジ ノレ、 11 α—ヒドロキシプロゲステロン、骨吸収阻害'転移抑制薬 (例、ゾレドロン酸、ァ
レンドロン酸、ノ ミドロン酸、ェチドロン酸、ィバンドロン酸、クロドロン酸)等も用いるこ と力 Sできる。
[0062] 「制吐剤」としては、オンダンセトロン、塩酸トロピセトロン、ァザセトロン、ラモセトロン 、ダラニセトロン、ドラセトロンメシレート、パロノセトロンなどの 5— HT拮抗剤、ドンぺ
3
リドン、モサプリド、メトクロブラミドなどの 5— HT拮抗剤などの消化管運動促進薬;ト
4
リメブチンなどの消化管運動調律薬;マレイン酸プロクロルペラジン、プロメタジン, チ ェチルペラジンなどのフエノチアジン系薬剤;ノヽロペリドーノレ、フエノールフタレイン酸 クロルプロマジン、ジァゼパム、ドロペリドールなどの精神安定剤;デキサメタゾン、プ レドニゾロン、ベタメタゾン、トリアムシノロン等などのステロイド剤;その他、ジメチルヒ ドリン酸、ジフェンヒドラミン、ヒヨスチン、臭酸ヒヨスチン、テトラべナジンなどを用いるこ と力 sできる。
[0063] 上記 LH— RH誘導体としては、ホルモン依存性疾患、特に性ホルモン依存性癌( 例、前立腺癌、子宮癌、乳癌、下垂体腫瘍、肝癌など)、前立腺肥大症、子宮内膜症 、子宮筋腫、思春期早発症、月経困難症、無月経症、月経前症候群、多房性卵巣 症候群等の性ホルモン依存性の疾患および避妊 (もしくは、その休薬後のリバウンド 効果を利用した場合には、不妊症)に有効な LH— RH誘導体またはその塩が用いら れる。さらに性ホルモン非依存性である力 SLH— RH感受性である良性または悪性腫 瘍などに有効な LH— RH誘導体またはその塩も用いられる。
LH— RH誘導体またはその塩の具体例としては、例えば、トリートメント ウイズ G nRH アナログ:コントラバーシス アンド パースペクティブス(Treatment with GnR ri analogs: Controversies and perspectives) [ノヽノレアノン ノヽノリッンング グノレーフ ° ( 株)(The Parthenon Publishing Group Ltd.)発行 1996年]、特表平 3— 503165号公 報、特開平 3— 101695号、特開平 7— 97334号および特開平 8— 259460号公報 などに記載されてレ、るペプチド類が用いられる。
[0064] LH— RH誘導体としては、 LH— RHァゴニストまたは LH— RHアンタゴニストが挙 げられる力 LH— RHアンタゴニストとしては、例えば、式
X-D2Nal-D4ClPhe-D3Pal-Ser-A-B-Leu-C-Pro-DAlaNH
〔式中、 Xは N(4H - fbroyl)Glyまたは NAcを、 Aは NMeTyr、 Tyr、 Aph(Atz)、 NMeAph(A
tz)から選ばれる残基を、 Bは DLys(Nic)、 DCit、 DLys(AzaglyNic), DLys(AzaglyFur), DhArg(Et )、 DAph(Atz)および DhCiから選ばれる残基を、 Cは Lys(Nisp)、 Argまたは h Arg(Et )をそれぞれ示す〕で表わされる生理活性ペプチドまたはその塩などが用いら れ、特に好ましくはアバレリタス、ガニレリタス、セトロレリタス、 5— (N ベンジル一 N ーメチルァミノメチル)ー1 (2 , 6—ジフルォロベンジル)ー6—[4一(3—メトキシゥ レイド)フエ二ル]— 3 フエニルチエノ [2 , 3— d]ピリミジン一 2 , 4 ( 1 H, 3H) ジォ ン、 5—(N べンジルー N メチルァミノメチル)ー1 (2 , 6 ジフルォロベンジル) 6— [4一(3 ェチルウレイド)フエニル] 3 フエニルチエノ [2 , 3 - d]ピリミジン —2 , 4 ( 1 H, 3H)—ジオン、 5— (N ベンジル一 N メチルアミノメチル)一 1— (2 , 6—ジフルォロベンジル)ー6— [4一(3—ェチルウレイド)フエニル ] 3—フエニルチ エノ [2 , 3— d]ピリミジン 2 , 4 ( 1 H, 3H)—ジオン 塩酸塩などが用いられる。
[0065] LH— RHァゴニストとしては、例えば、式
5_oxo_Pro_His_ lYp-Ser-l yr— f_Leu_Arg_Pro_Z
〔式中、 Yは DLeu、 DAla、 DTrp、 DSer(tBu)、 D2Nalおよび DHis(ImBzl)から選ばれる 残基を、 Zは NH-C Hまたは Gly_NH2をそれぞれ示す〕で表わされる生理活性ぺプチ ドまたはその塩などが用いられる。例えば、酢酸ゴセレリン、ブセレリンなどである。特 に、 Yが DLeuで、 Z力 SNH-C Hであるペプチド(即ち、 5-oxo-Pro-His-Trp-Ser_Tyr-
DLeu-Leu-Arg-Pro-NH-C Hで表されるペプチド A ;リュープロレリン)またはその塩
(例、酢酸塩)が好適である。
[0066] 本明細書中に記載されるポリペプチドにおけるアミノ酸、ペプチド、保護基等に関し 、略号で表示する場合、 IUPAC— IUB Commission on Biochemical Nomenclature による略号あるいは当該分野における慣用略号に基づくものとし、また、アミノ酸に関 し光学異性体がありうる場合は、特に明示しなければ L体を示すものとする。
[0067] 略号の例を以下に示す。
Abu :ァミノ酪酸
Aibu : 2—ァミノ酪酸
Ala :ァラニン
Arg :アルギニン
Gly :グリシン
His :ヒスチジン
lie :ィソロイシン
Leu :ロイシン
Met :メチォニン
Nle :ノノレロイシン
Nval :カレバリン
Phe :フエ二ルァラニン
Phg :フエニルダリシン
Pro :プロリン
(Pyr) Glu :ピログルタミン酸
Ser :セリン
Thr :スレ才ニン
Trp :トリブトファン
Tyr :チロシン
Val :バリン
D2Nal : D-3_(2-ナフチル)ァラニン残基
DSer (tBu): O-tert-ブチノレー D—セリン
DHis(ImBzl) : Nim-ベンジル一 D -ヒスチジン
PAM :フエ二ルァセタミドメチル
Boc : tーブチノレオキシカノレポ二ノレ
Fmoc : 9—フノレオレニノレメチノレオキシカノレボニノレ
C1-Z : 2—クロ口一ペンジノレオキシカノレポ二ノレ
Br— Z : 2—ブロモーべンジルォキシカルボニル
Bzl :ベンジノレ
CI -Bzl : 2,6—ジクロロべンジル
Tos : p—トノレエンスノレホニノレ
HONb : N—ヒドロキシー 5—ノルボルネンー 2, 3—ジカルボキシイミド
HOBt 1ーヒドロキシベンゾトリァゾーノレ
HOOBt 3 ヒドロキシ 3, 4 ジヒドロー 4 ォキソ 1 , 2, 3 べンゾトリア
MeBzl : 4 メチルベンジル
Bom :ベンジノレォキシメチノレ
Bum : tーブトキシメチノレ
Trt :トリチノレ
DNP :ジニトロフエ二ノレ
DCC : N, N'—ジシクロへキシノレ力ノレポジイミド
上記した中でも、併用薬としては、 LH— RHァゴニスト(例、酢酸ゴセレリン、ブセレ リン、リュープロレリン等)等が好ましい。
本発明の化合物と併用薬物との併用に際しては、本発明の化合物と併用薬物の投 与時期は限定されず、本発明の化合物と併用薬物とを、投与対象に対し、同時に投 与してもよいし、時間差をおいて投与してもよい。併用薬物の投与量は、臨床上用い られている投与量に準ずればよぐ投与対象、投与ルート、疾患、組み合わせ等によ り適宜選択することができる。
本発明の化合物と併用薬物の投与形態は、特に限定されず、投与時に、本発明の 化合物と併用薬物とが組み合わされていればよい。このような投与形態としては、例 えば、(1)本発明の化合物と併用薬物とを同時に製剤化して得られる単一の製剤の 投与、(2)本発明の化合物と併用薬物とを別々に製剤化して得られる 2種の製剤の 同一投与経路での同時投与、(3)本発明の化合物と併用薬物とを別々に製剤化し て得られる 2種の製剤の同一投与経路での時間差をおいての投与、(4)本発明の化 合物と併用薬物とを別々に製剤化して得られる 2種の製剤の異なる投与経路での同 時投与、(5)本発明の化合物と併用薬物とを別々に製剤化して得られる 2種の製剤 の異なる投与経路での時間差をおいての投与 (例えば、本発明の化合物→併用薬 物の順序での投与、あるいは逆の順序での投与)等が用いられる。以下、これらの投 与形態をまとめて、本発明の併用剤と略記する。
本発明の併用剤は、毒性が低ぐ例えば、本発明の化合物または(および)上記併
用薬物を自体公知の方法に従って、薬理学的に許容される担体と混合して医薬組 成物、例えば錠剤(糖衣錠、フィルムコーティング錠を含む)、散剤、顆粒剤、カプセ ノレ剤、(ソフトカプセルを含む)、液剤、注射剤、坐剤、徐放剤等として、経口的又は 非経口的 (例、局所、直腸、静脈投与等)に安全に投与することができる。注射剤は、 静脈内、筋肉内、皮下、臓器内、鼻腔内、皮内、点眼、脳内、直腸内、膣内および腹 腔内、腫瘍内部、腫瘍の近位等への投与あるいは直接病巣に投与することができる 本発明の併用剤の製造に用いられてもよい薬理学的に許容される担体としては、 上記した本発明の医薬組成物に使用されるものと同様のものを使用することができる 本発明の併用剤における本発明の化合物と併用薬物との配合比は、投与対象、投 与ルート、疾患等により適宜選択することができる。
例えば、本発明の併用剤における本発明の化合物の含有量は、製剤の形態によつ て相違する力、通常製剤全体に対して約 0. 01ないし 100重量%、好ましくは約 0. 1 ないし 50重量%、さらに好ましくは約 0. 5ないし 20重量%程度である。
本発明の併用剤における併用薬物の含有量は、製剤の形態によって相違するが、 通常製剤全体に対して約 0. 01ないし 100重量%、好ましくは約 0. 1ないし 50重量 %、さらに好ましくは約 0. 5ないし 20重量%程度である。
本発明の併用剤における担体等の添加剤の含有量は、製剤の形態によって相違 する力 通常製剤全体に対して約 1ないし 99. 99重量%、好ましくは約 10ないし 90 重量%程度である。
また、本発明の化合物および併用薬物をそれぞれ別々に製剤化する場合も同様の 含有量でよい。
これらの製剤は、製剤工程にお!/、て通常一般に用いられる自体公知の方法により 製造すること力 Sでさる。
例えば、本発明の化合物または併用薬物は、分散剤(例、ツイーン (Tween) 80 ( アトラスパウダー社製、米国)、 HCO 60 (日光ケミカノレズ製) ポリエチレングリコー
ノレロース、デキストリン等)、安定化剤(例、ァスコルビン酸、ピロ亜硫酸ナトリウム等)、 界面活性剤(例、ポリソルベート 80、マクロゴール等)、可溶剤(例、グリセリン、ェタノ ール等)、緩衝剤(例、リン酸及びそのアルカリ金属塩、クェン酸及びそのアルカリ金 属塩等)、等張化剤(例、塩化ナトリウム、塩化カリウム、マンニトール、ソルビトール、 ブドウ糖等)、 pH調節剤 (例、塩酸、水酸化ナトリウム等)、保存剤 (例、ノ ラオキシ安 息香酸ェチル、安息香酸、メチルパラベン、プロピルパラベン、ベンジルアルコール 等)、溶解剤(例、濃グリセリン、メダルミン等)、溶解補助剤(例、プロピレングリコール 、白糖等)、無痛化剤(例、ブドウ糖、ベンジルアルコール等)等と共に水性注射剤に 、あるいはォリーブ油、ゴマ油、綿実油、コーン油等の植物油、プロピレングリコール 等の溶解補助剤に溶解、懸濁あるいは乳化して油性注射剤に成形し、注射剤とする こと力 Sでさる。
[0070] 経口投与用製剤とするには、自体公知の方法に従い、本発明の化合物または併用 薬物を例えば、賦形剤 (例、乳糖、白糖、デンプン等)、崩壊剤 (例、デンプン、炭酸 カルシウム等)、結合剤(例、デンプン、アラビアゴム、カルボキシメチルセルロース、 ポリビュルピロリドン、ヒドロキシプロピルセルロース等)又は滑沢剤(例、タルク、ステ アリン酸マグネシウム、ポリエチレングリコール 6000等)等を添加して圧縮成形し、 次いで必要により、味のマスキング、腸溶性あるいは持続性の目的のため自体公知 の方法でコーティングすることにより経口投与製剤とすることができる。そのコーティン グ剤としては、例えば、ヒドロキシプロピルメチルセルロース、ェチルセルロース、ヒドロ キシメチノレセノレロース、ヒドロキシプロピノレセノレロース、ポリ才キシエチレングリコーノレ 、ツイーン 80、プル口ニック F68、セルロースアセテートフタレート、ヒドロキシプロ ピルメチルセルロースフタレート、ヒドロキシメチルセルロースアセテートサクシネート、 オイドラギット(ローム社製、ドイツ,メタアクリル酸 'アクリル酸共重合)および色素(例 、ベンガラ,二酸化チタン等)等が用いられる。経口投与用製剤は速放性製剤、徐放 性製剤の!/、ずれであってもよレ、。
[0071] 例えば、坐剤とするには、 自体公知の方法に従い、本発明の化合物または併用薬 物を油性又は水性の固状、半固状あるいは液状の坐剤とすることができる。上記組 成物に用いる油性基剤としては、例えば、高級脂肪酸のグリセリド〔例、カカオ脂、ゥ
ィテプゾル類 (ダイナマイトノーベル社製,ドイツ)等〕、中級脂肪酸〔例、ミグリオール 類 (ダイナマイトノーベル社製,ドイツ)等〕、あるいは植物油(例、ゴマ油、大豆油、綿 実油等)等が用いられる。また、水性基剤としては、例えばポリエチレングリコール類 、プロピレングリコール、水性ゲル基剤としては、例えば天然ガム類、セルロース誘導 体、ビュル重合体、アクリル酸重合体等が用いられる。
[0072] 上記徐放性製剤としては、徐放性マイクロカプセル剤等が用いられる。
徐放型マイクロカプセルとするには、自体公知の方法を採用できる力 例えば、下 記〔2〕に示す徐放性製剤に成型して投与するのが好まし!/、。
本発明の化合物は、固形製剤 (例、散剤、顆粒剤、錠剤、カプセル剤)等の経口投 与用製剤に成型するか、坐剤等の直腸投与用製剤に成型するのが好ましい。特に 経口投与用製剤が好ましい。
併用薬物は、薬物の種類に応じて上記した剤形とすることができる。
以下に、〔1〕本発明の化合物または併用薬物の注射剤およびその調製、〔2〕本発 明の化合物または併用薬物の徐放性製剤又は速放性製剤およびその調製、〔3〕本 発明の化合物または併用薬物の舌下錠、パッカル又は口腔内速崩壊剤およびその 調製について具体的に示す。
[0073] 〔1〕注射剤およびその調製
本発明の化合物または併用薬物を水に溶解してなる注射剤が好ましい。該注射剤 には安息香酸塩又は/およびサリチル酸塩を含有させてもよい。
該注射剤は、本発明の化合物または併用薬物と所望により安息香酸塩又は/およ びサリチル酸塩の双方を水に溶解することにより得られる。
上記安息香酸、サリチル酸の塩としては、例えばナトリウム,カリウム等のアルカリ金 属塩、カルシウム,マグネシウム等のアルカリ土類金属塩、アンモニゥム塩、メダルミン 塩、その他トロメタモール等の有機酸塩等が用いられる。
注射剤中の本発明の化合物または併用薬物の濃度は 0.5〜50w/v%、好ましく は 3〜20w/v%程度である。また安息香酸塩又は/およびサリチル酸塩の濃度は 0 .5〜50w/v%、好ましくは 3〜20w/v%が好ましい。
また、本剤には一般に注射剤に使用される添加剤、例えば安定化剤(ァスコルビン
酸、ピロ亜硫酸ナトリウム等)、界面活性剤(ポリソルベート 80、マクロゴール等)、可 溶剤(グリセリン、エタノール等)、緩衝剤(リン酸及びそのアルカリ金属塩、クェン酸 及びそのアルカリ金属塩等)、等張化剤 (塩化ナトリウム、塩化カリウム等)、分散剤(ヒ ドロキシプロピルメチルセルロース、デキストリン)、 pH調節剤 (塩酸、水酸化ナトリウ ム等)、保存剤 (パラォキシ安息香酸ェチル、安息香酸等)、溶解剤 (濃グリセリン、メ ダルミン等)、溶解補助剤(プロピレングリコール、白糖等)、無痛化剤(ブドウ糖、ベン ジルアルコール等)等を適宜配合することができる。これらの添加剤は一般に注射剤 に通常用いられる割合で配合される。
注射剤は pH調節剤の添加により pH2〜12、好ましくは ρΗ2·5〜8·0に調整するの がよい。
注射剤は本発明の化合物または併用薬物と所望により安息香酸塩又は/および サリチル酸塩の双方を、また必要により上記添加剤を水に溶解することにより得られ る。これらの溶解はどのような順序で行ってもよぐ従来の注射剤の製法と同様に適 宜 fiうこと力 Sできる。
注射用水溶液は加温するのがよぐまた通常の注射剤と同様にたとえば濾過滅菌, 高圧加熱滅菌等を行うことにより注射剤として供することができる。
注射用水溶液は、例えば 100°C〜; 121°Cの条件で 5分〜 30分高圧加熱滅菌する のがよい。
さらに多回分割投与製剤として使用できるように、溶液に抗菌性を付与した製剤と してもよい。
〔2〕徐放性製剤又は速放性製剤およびその調製
本発明の化合物または併用薬物を含んでなる核を所望により水不溶性物質ゃ膨 潤性ポリマー等の被膜剤で被覆してなる徐放性製剤が好ましい。例えば、 1日 1回投 与型の経口投与用徐放性製剤が好まし!/、。
被膜剤に用いられる水不溶性物質としては、例えばェチルセルロース、ブチルセル ロース等のセノレロースエーテノレ類、セノレロースアセテート、セノレロースプロピオネート 等のセルロースエステル類、ポリビュルアセテート、ポリビュルブチレート等のポリビニ ルエステル類、アクリル酸/メタクリル酸共重合体、メチルメタタリレート共重合体、ェ
トキシェチルメタタリレート/シンナモェチルメタタリレート/アミノアルキルメタタリレー ト共重合体、ポリアクリル酸、ポリメタクリル酸、メタクリル酸アルキルアミド共重合体、 ポリ(メタクリル酸メチル)、ポリメタタリレート、ポリメタクリルアミド、アミノアルキルメタク リレート共重合体、ポリ(メタクリル酸アンヒドリド)、グリシジルメタタリレート共重合体、 とりわけオイドラギット RS— 100, RL- 100, RS - 30D, RL— 30D, RL— PO, RS PO (アクリル酸ェチル 'メタアクリル酸メチル 'メタアクリル酸塩化トリメチル ·ァンモ 二ゥムェチル共重合体)、オイドラギット NE— 30D (メタアクリル酸メチル.アクリル酸 ェチル共重合体)等のオイドラギット類(ローム'ファーマ社)等のアクリル酸系ポリマ 一、硬化ヒマシ油(例、ラブリーワックス(フロイント産業)等)等の硬化油、カルナバヮ ッタス、脂肪酸グリセリンエステル、ノ ラフィン等のワックス類、ポリグリセリン脂肪酸ェ ステル等が用いられる。
膨潤性ポリマーとしては、酸性の解離基を有し、 pH依存性の膨潤を示すポリマー が好ましぐ胃内のような酸性領域では膨潤が少なぐ小腸や大腸等の中性領域で 膨潤が大きくなる酸性の解離基を有するポリマーが好ましい。
このような酸性の解離基を有し pH依存性の膨潤を示すポリマーとしては、例えば力 一ボマ一(Carbomer) 934P、 940、 941、 974P、 980、 1342等、ポリカーボフィノレ(p olycarbophil)、カノレシゥムポリカーボフィノレ (carcium polycarbophil) (上記はいずれも BFグッドリッチ社製)、ハイビスヮコー 103、 104、 105、 304 (いずれも和光純薬(株) 製)等の架橋型ポリアクリル酸重合体が用いられる。
徐放性製剤に用いられる被膜剤は親水性物質をさらに含んで!/、てもよレ、。
該親水性物質としては、例えばプルラン、デキストリン、アルギン酸アルカリ金属塩 等の硫酸基を有していてもよい多糖類、ヒドロキシプロピルセルロース、ヒドロキシプロ ピノレメチノレセノレロース、カノレポキシメチノレセノレロースナトリウム等のヒドロキシァノレキノレ 又はカルボキシアルキルを有する多糖類、メチルセルロース、ポリビュルピロリドン、 ポリビュルアルコール、ポリエチレンダリコール等が用いられる。
徐放性製剤の被膜剤における水不溶性物質の含有率は約 30な!/、し約 90% (w/ w)、好ましくは約 35ないし約 80% (w/w)、さらに好ましくは約 40ないし 75% (w/ w)、膨潤性ポリマーの含有率は約 3ないし約 30% (w/w)、好ましくは約 3ないし約
15%(w/w)である。被膜剤は親水性物質をさらに含んでいてもよぐその場合被膜 剤における親水性物質の含有率は約 50%(w/w)以下、好ましくは約 5〜約 40% ( w/w)、さらに好ましくは約 5〜約 35% (w/w)である。ここで上記% (w/w)は被 膜剤液から溶媒 (例、水、メタノール、エタノール等の低級アルコール等)を除いた被 膜剤組成物に対する重量%を示す。
徐放性製剤は、以下に例示するように薬物を含む核を調製し、次いで得られた核を 、水不溶性物質や膨潤性ポリマー等を加熱溶解あるいは溶媒に溶解又は分散させ た被膜剤液で被覆することにより製造される。
I.薬剤を含む核の調製
被膜剤で被覆される薬物を含む核 (以下、単に核と称することがある)の形態は特 に制限されないが、好ましくは顆粒あるいは細粒等の粒子状に形成される。
核が顆粒又は細粒の場合、その平均粒子径は、好ましくは約 150ないし 2,000 m、さらに好ましくは約 500ないし約 1 ,400 μ mである。
核の調製は通常の製造方法で実施することができる。例えば、薬物に適当な賦形 剤、結合剤、崩壊剤、滑沢剤、安定化剤等を混合し、湿式押し出し造粒法、流動層 造粒法等により調製する。
核の薬物含量は、約 0.5ないし約 95% (w/w)、好ましくは約 5.0ないし約 80% (w /w)、さらに好ましくは約 30ないし約 70% (w/w)である。
核に含まれる賦形剤としては、例えば白糖、乳糖、マンニトール、グルコース等の糖 類、澱粉、結晶セルロース、リン酸カルシウム、コーンスターチ等が用いられる。中で も、結晶セルロース、コーンスターチが好ましい。
結合剤としては、例えばポリビュルアルコール、ヒドロキシプロピルセルロース、ポリ エチレングリコール、ポリビュルピロリドン、プル口ニック F68、アラビアゴム、ゼラチン、 澱粉等が用いられる。崩壊剤としては、例えばカルボキシメチルセルロースカルシゥ ム (ECG505)、クロスカルメロースナトリウム (Ac— Di— Sol)、架橋型ポリビュルピロリ ドン(クロスポビドン)、低置換度ヒドロキシプロピルセルロース(L— HPC)等が用いら れる。 中でも、ヒドロキシプロピルセルロース、ポリビュルピロリドン、低置換度ヒドロキ シプロピルセルロースが好ましい。滑沢剤、凝集防止剤としては例えばタルク、ステア
リン酸マグネシゥムおよびその無機塩、また潤滑剤としてポリエチレンダリコール等が 用いられる。安定化剤としては酒石酸、クェン酸、コハク酸、フマル酸、マレイン酸等 の酸が用いられる。
核は上記製造法以外にも、例えば核の中心となる不活性担体粒子上に水、低級ァ ルコール (例、メタノール、エタノール等)等の適当な溶媒に溶解した結合剤をスプレ 一しながら、薬物あるいはこれと賦形剤、滑沢剤等との混合物を少量づっ添加して行 なう転動造粒法、パンコーティング法、流動層コーティング法や溶融造粒法によって も調製すること力できる。不活性担体粒子としては、例えば白糖、乳糖、澱粉、結晶 セルロース、ワックス類で製造されたものが使用でき、その平均粒子径は約 100〃 m ないし約 1 ,500〃 mであるものが好ましい。
核に含まれる薬物と被膜剤とを分離するために、防護剤で核の表面を被覆してもよ い。防護剤としては、例えば上記親水性物質や、水不溶性物質等が用いられる。防 護剤は、好ましくはポリエチレングリコールゃヒドロキシアルキル又はカルボキシアル キルを有する多糖類、より好ましくはヒドロキシプロピルメチルセルロース、ヒドロキシ プロピルセルロースが用いられる。該防護剤には安定化剤として酒石酸、クェン酸、 コハク酸、フマル酸、マレイン酸等の酸や、タルク等の滑沢剤を含んでいてもよい。防 護剤を用いる場合、その被覆量は核に対して約 1ないし約 15% (w/w)、好ましくは 約 1ないし約 10% (w/w)、さらに好ましくは約 2ないし約 8% (w/w)である。
防護剤は通常のコーティング法により被覆することができ、具体的には、防護剤を 例えば流動層コーティング法、パンコーティング法等により核にスプレーコーティング することで被覆すること力でさる。
II.核の被膜剤による被覆
上記 Iで得られた核を、上記水不溶性物質及び pH依存性の膨潤性ポリマー、およ び親水性物質を加熱溶解あるいは溶媒に溶解又は分散させた被膜剤液により被覆 することにより徐放性製剤が製造される。
核の被膜剤液による被覆方法として、例えば噴霧コーティングする方法等が用いら れる。
被膜剤液中の水不溶性物質、膨潤性ポリマー又は親水性物質の組成比は、被膜
中の各成分の含有率がそれぞれ上記含有率となるように適宜選ばれる。
被膜剤の被覆量は、核(防護剤の被覆量を含まない)に対して約 1ないし約 90% ( w/w)、好ましくは約 5ないし約 50% (w/w)、さらに好ましくは約 5ないし 35% (w Z w)でめる。
被膜剤液の溶媒としては水又は有機溶媒を単独であるいは両者の混液を用いるこ とができる。混液を用いる際の水と有機溶媒との混合比(水/有機溶媒:重量比)は、 1ないし 100%の範囲で変化させることができ、好ましくは 1ないし約 30%である。該 有機溶媒としては、水不溶性物質を溶解するものであれば特に限定されないが、例 えばメチルアルコール、エチルアルコール、イソプロピルアルコール、 n-ブチルアルコ ール等の低級アルコール、アセトン等の低級アルカノン、ァセトニトリル、クロ口ホルム 、メチレンクロライド等が用いられる。このうち低級アルコールが好ましぐェチルアル コール、イソプロピルアルコールが特に好ましい。水及び水と有機溶媒との混液が被 膜剤の溶媒として好ましく用いられる。この時、必要であれば被膜剤液中に被膜剤液 安定化のために酒石酸、クェン酸、コハク酸、フマル酸、マレイン酸等の酸を加えて あよい。
噴霧コーティングにより被覆する場合の操作は通常のコーティング法により実施す ること力 Sでき、具体的には、被膜剤液を例えば流動層コーティング法、バンコ一ティン グ法等により核にスプレーコーティングすることで実施することができる。この時必要 であれば、タルク、酸化チタン、ステアリン酸マグネシウム、ステアリン酸カルシウム、 軽質無水ケィ酸等を滑沢剤として、グリセリン脂肪酸エステル、硬化ヒマシ油、クェン 酸トリエチル、セチルアルコール、ステアリルアルコール等を可塑剤として添加しても よい。
被膜剤による被膜後、必要に応じてタルク等の帯電防止剤を混合してもよい。 速放性製剤は、液状 (溶液、懸濁液、乳化物等)であっても固形状 (粒子状、丸剤、 錠剤等)であってもよい。経口投与剤、注射剤等非経口投与剤が用いられるが、経口 投与剤が好ましい。
速放性製剤は、通常、活性成分である薬物に加えて、製剤分野で慣用される担体 、添加剤や賦形剤(以下、賦形剤と略称することがある)を含んでいてもよい。用いら
れる製剤賦形剤は、製剤賦形剤として常用される賦形剤であれば特に限定されない 。例えば経口固形製剤用の賦形剤としては、乳糖、デンプン、コーンスターチ、結晶 セルロース(旭化成(株)製、アビセル PH101等)、粉糖、ダラ二ユウ糖、マンニトール 、軽質無水ケィ酸、炭酸マグネシウム、炭酸カルシウム、 L—システィン等が用いられ 、好ましくはコーンスターチおよびマンニトール等が用いられる。これらの賦形剤は一 種又は二種以上を組み合わせて使用できる。賦形剤の含有量は速放性製剤全量に 対して、例えば約 4· 5〜約 99. 4% (w/w)、好ましくは約 20〜約 98· 5% (w/w) 、さらに好ましくは約 30〜約 97% (w/w)である。
速放性製剤における薬物の含量は、速放性製剤全量に対して、約 0. 5〜約 95% 、好ましくは約 1〜約 60%の範囲から適宜選択することができる。
速放性製剤が経口固型製剤の場合、通常上記成分に加えて、崩壊剤を含有する。 このような崩壊剤としては、例えばカルボキシメチルセルロースカルシウム(五徳薬品 製、 ECG— 505)、クロスカノレメロースナトリウム(例えば、旭化成 (株)製、ァクジゾル) 、クロスポビドン (例えば、 BASF社製、コリドン CL)、低置換度ヒドロキシプロピルセル ロース(信越化学 (株))、カルボキシメチルスターチ(松谷化学 (株))、カルボキシメチ ルスターチナトリウム(木村産業製、エキスプロタブ)、部分 α化デンプン (旭化成 (株) 製、 PCS)等が用いられ、例えば水と接触して吸水、膨潤、あるいは核を構成してい る有効成分と賦形剤との間にチャネルを作る等により顆粒を崩壊させるものを用いる ことができる。これらの崩壊剤は、一種又は二種以上を組み合わせて使用できる。崩 壊剤の配合量は、用いる薬物の種類や配合量、放出性の製剤設計等により適宜選 択されるが、速放性製剤全量に対して、例えば約 0. 05〜約 30% (w/w)、好ましく は約 0. 5〜約 15% (w/w)である。
速放性製剤が経口固型製剤である場合、経口固型製剤の場合には上記の組成に 加えて、所望により固型製剤において慣用の添加剤をさらに含んでいてもよい。この ような添加剤としては、例えば結合剤(例えば、ショ糖、ゼラチン、アラビアゴム末、メ
、カルボキシメチルセルロース、ポリビュルピロリドン、プルラン、デキストリン等)、滑沢 剤(例えば、ポリエチレングリコール、ステアリン酸マグネシウム、タルク、軽質無水ケ
ィ酸 (例えば、ァエロジル(日本ァエロジル) )、界面活性剤(例えば、アルキル硫酸ナ トリウム等のァニオン系界面活性剤、ポリオキシエチレン脂肪酸エステルおよびポリオ キシエチレンソルビタン脂肪酸エステル、ポリオキシエチレンヒマシ油誘導体等の非 イオン系界面活性剤等)、着色剤(例えば、タール系色素、カラメル、ベンガラ、酸化 チタン、リボフラビン類)、必要ならば、矯味剤 (例えば、甘味剤、香料等)、吸着剤、 防腐剤、湿潤剤、帯電防止剤等が用いられる。また、安定化剤として酒石酸、クェン 酸、コハク酸、フマル酸等の有機酸を加えてもよい。
[0079] 上記結合剤としては、ヒドロキシプロピルセルロース、ポリエチレングリコールおよび ポリビュルピロリドン等が好ましく用いられる。
速放性製剤は、通常の製剤の製造技術に基づき、上記各成分を混合し、必要によ り、さらに練合し、成型することにより調製すること力 Sできる。上記混合は、一般に用い られる方法、例えば、混合、練合等により行われる。具体的には、例えば速放性製剤 を粒子状に形成する場合、上記徐放性製剤の核の調製法と同様の手法により、バー チカルグラニュレーター、万能練合機 (畑鉄工所製)、流動層造粒機 FD— 5S (パウレ ック社製)等を用いて混合しその後、湿式押し出し造粒法、流動層造粒法等により造 粒することにより調製すること力 Sでさる。
このようにして得られた速放性製剤と徐放性製剤とは、そのままあるいは適宜、製剤 賦形剤等と共に常法により別々に製剤化後、同時あるいは任意の投与間隔を挟んで 組み合わせて投与する製剤としてもよぐまた両者をそのままあるいは適宜、製剤賦 形剤等と共に一つの経口投与製剤 (例、顆粒剤、細粒剤、錠剤、カプセル等)に製剤 化してもよい。両製剤を顆粒あるいは細粒に製して、同一のカプセル等に充填して経 口投与用製剤としてもよい。
[0080] 〔3〕舌下錠、バッカル又は口腔内速崩壊剤およびその調製
舌下錠、バッカル製剤、口腔内速崩壊剤は錠剤等の固形製剤であってもよいし、 口腔粘膜貼付錠 (フィルム)であってもよ!/、。
舌下錠、バッカル又は口腔内速崩壊剤としては、本発明の化合物または併用薬物 と賦形剤とを含有する製剤が好ましい。また、滑沢剤、等張化剤、親水性担体、水分 散性ポリマー、安定化剤等の補助剤を含有していてもよい。また、吸収を容易にし、
生体内利用率を高めるために /3—シクロデキストリン又は /3—シクロデキストリン誘導 体(例、ヒドロキシプロピル一 β—シクロデキストリン等)等を含有していてもよい。 上記賦形剤としては、乳糖、白糖、 D—マンニトール、デンプン、結晶セルロース、 軽質無水ケィ酸等が用いられる。滑沢剤としてはステアリン酸マグネシウム、ステアリ ン酸カルシウム、タルク、コロイドシリカ等が用いられ、特に、ステアリン酸マグネシウム やコロイドシリカが好ましい。等張化剤としては塩化ナトリウム、グルコース、フルクトー ス、マンニトーノレ、ソノレビトーノレ、ラタトース、サッカロース、グリセリン、尿素等が用いら れ、特にマンニトールが好ましい。親水性担体としては結晶セルロース、ェチルセル ロース、架橋性ポリビュルピロリドン、軽質無水珪酸、珪酸、リン酸二カルシウム、炭酸 カルシウム等の膨潤性親水性担体が用いられ、特に結晶セルロース(例、微結晶セ ルロース等)が好ましい。水分散性ポリマーとしてはガム(例、トラガカントガム、ァカシ ァガム、グァーガム)、アルギン酸塩(例、アルギン酸ナトリウム)、セルロース誘導体( 例、メチノレセノレロース、カノレポキシメチノレセノレロース、ヒドロキシメチノレセノレロース、ヒド ロキシプロピルセルロース、ヒドロキシプロピルメチルセルロース)、ゼラチン、水溶性 デンプン、ポリアクリル酸(例、カーボマー)、ポリメタクリル酸、ポリビュルアルコール、 ポリエチレングリコール、ポリビュルピロリドン、ポリカーボフィル、ァスコルビン酸パノレ ミチン酸塩等が用いられ、ヒドロキシプロピルメチルセルロース、ポリアクリル酸、アル ギン酸塩、ゼラチン、カルボキシメチルセルロース、ポリビュルピロリドン、ポリエチレン グリコール等が好ましい。特にヒドロキシプロピルメチルセルロースが好ましい。安定 化剤としては、システィン、チォソルビトール、酒石酸、クェン酸、炭酸ナトリウム、ァス コルビン酸、グリシン、亜硫酸ナトリウム等が用いられ、特に、クェン酸ゃァスコルビン 酸が好ましい。
舌下錠、バッカル又は口腔内速崩壊剤は、本発明の化合物または併用薬物と賦形 剤とを自体公知の方法により混合することにより製造することができる。さらに、所望 により上記した滑沢剤、等張化剤、親水性担体、水分散性ポリマー、安定化剤、着色 剤、甘味剤、防腐剤等の補助剤を混合してもよい。上記成分を同時に若しくは時間 差をおいて混合した後、加圧打錠成形することにより舌下錠、ノ ッカル錠又は口腔内 速崩壊錠が得られる。適度な硬度を得るため、打錠成形の過程の前後において必要
に応じ水やアルコール等の溶媒を用いて加湿'湿潤させ、成形後、乾燥させて製造 してもよい。
粘膜貼付錠 (フィルム)に成型する場合は、本発明の化合物または併用薬物および 上記した水分散性ポリマー(好ましくは、ヒドロキシプロピルセルロース、ヒドロキシプロ ピルメチルセルロース)、賦形剤等を水等の溶媒に溶解させ、得られる溶液を流延さ せて(cast)フィルムとする。さらに、可塑剤、安定剤、酸化防止剤、保存剤、着色剤、 緩衝剤、甘味剤等の添加物を加えてもよい。フィルムに適度の弾性を与えるためポリ エチレングリコールやプロピレングリコール等のグリコール類を含有させたり、 口腔の 粘膜ライニングへのフィルムの接着を高めるため生物接着性ポリマー(例、ポリカーボ フィル、カルボポール)を含有させたりしてもよい。流延は、非接着性表面に溶液を注 ぎ、ドクターブレード等の塗布用具で均一な厚さ(好ましくは 10〜; 1000ミクロン程度) にそれを広げ、次いで溶液を乾燥してフィルムを形成することにより達成される。この ように形成されたフィルムは室温若しくは加温下乾燥させ、所望の表面積に切断す れば'よい。
好ましい口腔内速崩壊剤としては、本発明の化合物または併用薬物と、本発明の 化合物または併用薬物とは不活性である水溶性若しくは水拡散性キヤリヤーとの網 状体からなる固体状の急速拡散投与剤が用いられる。該網状体は、本発明の化合 物または併用薬物を適当な溶媒に溶解した溶液とから構成されている固体状の該組 成物から溶媒を昇華することによって得られる。
該口腔内速崩壊剤の組成物中には、本発明の化合物または併用薬物に加えて、 マトリックス形成剤と二次成分とを含んでレ、るのが好ましレ、。
該マトリックス形成剤としてはゼラチン類、デキストリン類ならびに大豆、小麦ならび にォォバコ(psyllium)種子タンパク等の動物性タンパク類若しくは植物性タンパク 類;アラビアゴム、ガーガム、寒天ならびにキサンタン等のゴム質物質;多糖類;アル ギン酸類;カノレポキシメチノレセノレロース類;力ラゲナン類;デキストラン類;ぺクチン類; ポリビュルピロリドン等の合成ポリマー類;ゼラチン アラビアゴムコンプレックス等か ら誘導される物質が含まれる。さらに、マンニトール、デキストロース、ラタトース、ガラ クトースならびにトレハロース等の糖類;シクロデキストリン等の環状糖類;リン酸ナトリ
ゥム、塩化ナトリウムならびにケィ酸アルミニウム等の無機塩類;グリシン、 L—ァラニン 、 L—ァスパラギン酸、 L—グルタミン酸、 L—ヒドロキシプロリン、 L—イソロイシン、 L —ロイシンならびに L—フエ二ルァラニン等の炭素原子数が 2から 12までのアミノ酸 等が含まれる。
マトリックス形成剤は、その 1種若しくはそれ以上を、固形化の前に、溶液又は懸濁 液中に導入することができる。力、かるマトリックス形成剤は、界面活性剤に加えて存在 していてもよく、また界面活性剤が排除されて存在していてもよい。マトリックス形成剤 はそのマトリックスを形成することに加えて、本発明の化合物または併用薬物の拡散 状態をその溶液又は懸濁液中に維持する助けをすることができる。
保存剤、酸化防止剤、界面活性剤、増粘剤、着色剤、 pH調整剤、香味料、甘味料 若しくは食味マスキング剤等の二次成分を組成物中に含有して!/、てよレ、。適当な着 色剤としては、赤色、黒色ならびに黄色酸化鉄類およびエリス 'アンド ' ·エベラールド 社の FD&Cブルー 2号ならびに FD&Cレッド 40号等の FD&C染料が用いられる。 適当な香味料には、ミント、ラズベリー、甘草、オレンジ、レモン、グレープフルーツ、 カラメル、バニラ、チェリーならびにグレープフレーバーおよびその組合せたものが含 まれる。適当な pH調整剤は、クェン酸、酒石酸、リン酸、塩酸およびマレイン酸が含 まれる。適当な甘味料としてはアスパルテーム、アセスルフエーム Kならびにタウマチ ン等が含まれる。適当な食味マスキング剤としては、重炭酸ナトリウム、イオン交換樹 脂、シクロデキストリン包接化合物、吸着質物質ならびにマイクロカプセル化アポモル フィンが含まれる。
製剤には通常約 0. 1〜約 50重量%、好ましくは約 0. 1〜約 30重量%の本発明の 化合物または併用薬物を含み、約 1分〜約 60分の間、好ましくは約 1分〜約 15分の 間、より好ましくは約 2分〜約 5分の間に(水に)本発明の化合物または併用薬物の 9 0%以上を溶解させることが可能な製剤(上記、舌下錠、パッカル等)や、口腔内に入 れられて 1ないし 60秒以内に、好ましくは 1ないし 30秒以内に、さらに好ましくは 1な V、し 10秒以内に崩壊する口腔内速崩壊剤が好まし!/、。
上記賦形剤の製剤全体に対する含有量は、約 10〜約 99重量%、好ましくは約 30 〜約 90重量0 /0である。 β—シクロデキストリン又は /3—シクロデキストリン誘導体の製
剤全体に対する含有量は 0〜約 30重量%である。滑沢剤の製剤全体に対する含有 量は、約 0. 01〜約 10重量%、好ましくは約 1〜約 5重量%である。等張化剤の製剤 全体に対する含有量は、約 0. 1〜約 90重量%、好ましくは、約 10〜約 70重量%で ある。親水性担体の製剤全体に対する含有量は約 0. 1〜約 50重量%、好ましくは 約 10〜約 30重量%である。水分散性ポリマーの製剤全体に対する含有量は、約 0. 1〜約 30重量%、好ましくは約 10〜約 25重量%である。安定化剤の製剤全体に対 する含有量は約 0. 1〜約 10重量%、好ましくは約 1〜約 5重量%である。上記製剤 はさらに、着色剤、甘味剤、防腐剤等の添加剤を必要に応じ含有していてもよい。 本発明の併用剤の投与量は、本発明の化合物の種類、年齢、体重、症状、剤形、 投与方法、投与期間等により異なるが、例えば、前立腺癌の患者 (成人、体重約 60k g)—人あたり、通常、本発明の化合物および併用薬物として、それぞれ 1日約 0.01 〜約 1000mg/kg、好ましくは約 0. 01〜約 100mg/kg、より好ましくは約 0. 1 ~ 約 100mg/kg、とりわけ約 0· 1〜約 50mg/kgを、な力、でも約 1 · 5〜約 30mg/kg を 1日 1回から数回に分けて静脈投与される。もちろん、上記したように投与量は種々 の条件で変動するので、上記投与量より少ない量で十分な場合もあり、また範囲を超 えて投与する必要のある場合もある。
併用薬物は、副作用が問題とならない範囲でどのような量を設定することも可能で ある。併用薬物としての一日投与量は、症状の程度、投与対象の年齢、性別、体重、 感受性差、投与の時期、間隔、医薬製剤の性質、調剤、種類、有効成分の種類等に よって異なり、特に限定されないが、薬物の量として通常、たとえば経口投与で哺乳 動物 lkg体重あたり約 0.00;!〜 2000mg、好ましくは約 0.0;!〜 500mg、さらに好まし くは、約 0.;!〜 lOOmg程度であり、これを通常 1日 1〜4回に分けて投与する。
本発明の併用剤を投与するに際しては、同時期に投与してもよいが、併用薬物を 先に投与した後、本発明の化合物を投与してもよいし、本発明の化合物を先に投与 し、その後で併用薬物を投与してもよい。時間差をおいて投与する場合、時間差は 投与する有効成分、剤形、投与方法により異なるが、例えば、併用薬物を先に投与 する場合、併用薬物を投与した後 1分〜 3日以内、好ましくは 10分〜 1日以内、より 好ましくは 15分〜 1時間以内に本発明の化合物を投与する方法が用いられる。本発
明の化合物を先に投与する場合、本発明の化合物を投与した後、 1分〜 1日以内、 好ましくは 10分〜 6時間以内、より好ましくは 15分から 1時間以内に併用薬物を投与 する方法が用いられる。
好ましい投与方法としては、例えば、経口投与製剤に製形された併用薬物約 0.00 l〜200mg/kgを経口投与し、約 15分後に経口投与製剤に製形された本発明の 化合物約 0.005〜; 100mg/kgを 1日量として経口投与する。
[0084] また、本発明の医薬組成物または本発明の併用剤を、例えば(1)手術、(2)アンジ ォテンシン II等を用いる昇圧化学療法、(3)遺伝子療法、(4)温熱療法、(5)凍結療 法、(6)レーザー焼灼法、(7)放射線療法等の非薬剤療法と組み合わせることもでき 例えば、本発明の医薬組成物または本発明の併用剤を手術等の前または後に、あ るいはこれら 2、 3種を組み合わせた治療前または後に使用することによって、耐性発 現の阻止、無病期(Disease-Free Survival)の延長、癌転移あるいは再発の抑制、延 命等の効果が得られる。
[0085] また、本発明の医薬組成物または本発明の併用剤による治療と、支持療法〔(i)各 種感染病の併発に対する抗生物質 (例えば、パンスポリン等の /3—ラタタム系、クラリ スロマイシン等のマクロライド系等)の投与、(ii)栄養障害改善のための高カロリー輸 液、アミノ酸製剤、総合ビタミン剤の投与、(iii)疼痛緩和のためのモルヒネ投与、(iv) 悪心、嘔吐、食欲不振、下痢、白血球減少、血小板減少、ヘモグロビン濃度低下、 脱毛、肝障害、腎障害、 DIC、発熱等のような副作用を改善する薬剤の投与および( V)癌の多剤耐性を抑制するための薬剤の投与等〕を組み合わせることもできる。 このような目的のための薬剤、例えば「制吐剤」としての具体例を挙げれば、オンダ ンセトロン、塩酸トロピセトロン、ァザセトロン、ラモセトロン、グラニセトロン、ドラセトロ ンメシレート、パロノセトロンなどの 5— HT拮抗剤; sendide、 CP— 99994、 CP— 1
3
00263、 CP— 122721— 1、 CP— 96345、 FK224、 RPR100893、 NKP608、 ap repitant (EMEND (商標))などの NKl受容体拮抗薬;ドンペリドン、モサプリド、メト クロブラミドなどの 5— HT拮抗剤などの消化管運動促進薬;トリメブチンなどの消化
4
管運動調律薬;マレイン酸プロクロルペラジン、プロメタジン、チェチルペラジンなど
のフエノチアジン系薬剤;ノヽロペリドーノレ、フエノールフタレイン酸クロルプロマジン、 ジァゼパム、ドロペリドールなどの精神安定剤;デキサメタゾン、プレドニゾロン、ベタメ タゾン、トリアムシノロン等などのステロイド剤;その他、ジメチルヒドリン酸、ジフェンヒド ラミン、ヒヨスチン、臭酸ヒヨスチン、テトラべナジンなどを用いることができる。
[0086] 上記の処置を施す前または施した後に、本発明の医薬組成物または本発明の併 用剤を経口投与 (徐放性を含む)、静脈内投与 (bolus、 infusion,包接体を含む)、皮 下および筋注 (bolus、 infusion,徐放性を含む)、経皮、腫瘍内および近位投与によ つて投与するのが好ましい。
手術等の前に本発明の医薬組成物または本発明の併用剤を投与する場合の時期 としては、例えば、手術等の約 30分〜 24時間前に 1回投与することもできるし、ある いは手術等の約 3ヶ月〜6ヶ月前に 1〜3サイクルに分けて投与することもできる。この ように、手術等の前に本発明の医薬組成物または本発明の併用剤を投与することに より、例えば癌組織を縮小させることができるので、手術等がしゃすくなる。
手術等の後に本発明の医薬組成物または本発明の併用剤を投与する場合の時期 としては、手術等の約 30分〜 24時間後に、例えば数週間〜 3ヶ月単位で反復投与 すること力 Sできる。このように、手術等の後に本発明の医薬組成物または本発明の併 用剤を投与することにより、手術等の効果を高めることができる。
実施例
[0087] 以下に参考例、実施例、製剤例および試験例を挙げて、本発明を詳しく説明する 力 本発明はこれらに限定されるものではない。
参考例および実施例のカラムクロマトグラフィーにおける溶出は、 TLC (Thin Layer Chromatography,薄層クロマトグラフィー)による観察下に行われた。 TLCの観察に おいては、 TLCプレートとしてメルク社製のキーゼルゲル 60F プレートを使用し、
254
展開溶媒としてはカラムクロマトグラフィーで溶出溶媒として用いられた溶媒を、検出 法として UV検出器を採用した。カラム用シリカゲルは、同じくメルク社製のキーゼル ゲノレ 60F (70〜230メッシュ)を用いた。 NMRスペクトルは、プロトン NMRを示し、
254
内部標準としてテトラメチルシランを用いて VARIAN Gemini— 200 (200MHz型ス ぺクトロメーター)、 VARIAN Mercury— 300 (300MHz)または日本電子株式会
社 JMTCO400/54 (400MHz)型にて測定し、 δ値を ppmで表した。マイクロウ エーブ反応装置を用いた反応は Biotage社製 Emrys Optimizerを用いて実施した。 赤外吸収スペクトル(IR)はパーキンエルマ一社製 Paragon 1000を用いて測定し た。
参考例および実施例で用いる略号は、次のような意義を有する。
S :ンングレツ卜
br : :ブロード(幅広い)
d :ダブレット
t :トリプレット
q :クヮノレテツ卜
dd :ダブノレダブレット
ddd :ダブノレダブルダフ
dt :ダブルトリプレット
m :マルチプレット
J : :カップリング定数
Hz :へノレツ
THF :テトラヒドロフラン
DMSO:ジメチノレスノレホキシド
DMF : N,N ジメチルホルムアミド
[0088] 参考例 1
(2S, 3S) 3 ヒドロキシー 2 メチノレピロリジン-
[0089] [化 10]
[0090] (4S, 5S)— 4 ヒドロキシ一 5 メチルピロリジン一 2 オン(10· 45g)の脱水 TH F懸濁液(418mUに氷冷、窒素気流下、 Red— Al (104. 9g : 363mmol : 70%トル ェン溶液)を滴下した。室温で 20分攪拌し、さらに 3時間還流した。反応液を再度氷 冷し、窒素気流下、炭酸ナトリウム · 10水和物(41. 6g)を添加した。室温終夜攪拌 後、セライトを用いて不溶物を濾去し、 THFで洗浄した。濾液、洗浄液を合わせて減 圧下濃縮し、(2S, 3S)— 3 ヒドロキシー2 メチルピロリジンを得た。本化合物はこ れ以上精製することなく DMSOで希釈し 0· 9mol/L— DMSO溶液とした。 (2S, 3 S)— 3 ヒドロキシ一 2 メチルピロリジンの 0· 9mol/L— DMSO溶液(170mUを 水(200mUで希釈し、炭酸水素ナトリウム(24. 6g)とクロロギ酸べンジル(15mU を加え、室温で 18時間攪拌した。反応液に水を加え、酢酸ェチルで抽出し、抽出液 を飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、減圧濃縮することで表題化合 物を淡黄色油状物として得た(収量: 20. 64g、収率:84%)。
'H-NMR CCDCl ) δ : 1. 10- 1. 30 (3Η, br) , 1. 60— 2. 20 (3Η, m) , 3. 40
3
—4. 40 (5Η, m) , 7. 20— 7. 40 (5Η, m) .
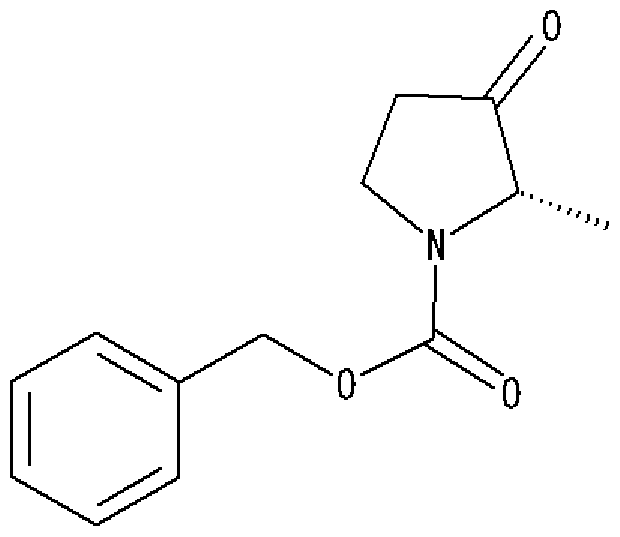
[0091] 参考例 2
(2S)— 2 メチルー 3 ォキソピロリジン 1一力ルボン酸べンジル
[0092] [化 11]
[0093] (2S, 3S)— 3 ヒドロキシー2 メチルピロリジン 1一力ルボン酸べンジル(20· 5 g)のァセトニトリル溶液(150mUに粉末モレキュラーシーブス 4A(25g)、 4 メチル モルホリン一 N ォキシド(20· 4g)を加え、 0°Cに冷却した後、テトラ一 n プロピル
アンモニゥムぺルルテナート(3. Og)を加え、 0°Cで 1時間攪拌した後、室温で 18時 間攪拌した。反応液を減圧濃縮した後、残留物を酢酸ェチルで懸濁し、不溶物をハ ィフロスーパーセルで濾過した。濾液を減圧濃縮した後、残留物をシリカゲルカラム クロマトグラフィー(展開溶媒:へキサン/酢酸ェチル = 9/1→2/1)にて精製し、 表題化合物を無色油状物として得た(収量: 18. 0g、収率: 89%)。
'H-NMR CCDCl ) δ : 1. 34 (3Η, d, J = 6. 6Hz) , 2. 50— 2. 70 (2H, m) , 3.
3
60 - 3. 75 (1H, m) , 3. 90— 4. 10 (2H, m) , 5. 15 (1H, d, J= 12. 3Hz) , 5. 2 0 (1H, d, J= 12. 3Hz) , 7. 30— 7. 40 (5H, m) .
[0094] 参考例 3
(2S, 3S)— 3 ヒドロキシー 2, 3 ジメチルピロリジン 1一力ルボン酸べンジル
[0095] [化 12]
[0096] 塩化セリウム(47g)の THF懸濁液(300mL)を— 78°Cに冷却し、 3mol/Lメチル マグネシウムブロミドージェチルエーテル溶液(56mL)を溶液温度が 70°C以下と なるように調節しながら滴下した。滴下終了後、 78°Cで 30分間攪拌し、(2S)— 2 ーメチルー 3 ォキソピ口リジン 1 カルボン酸べンジル( 18 g)の THF溶液(60m Uを溶液温度が一 70°C以下となるように調節しながら滴下した。反応液を 2時間か けて 0°Cに昇温した後、酢酸ェチル(1L)を加え、不溶物を濾去した。濾液に水をカロ え、分液操作を行い、有機層を飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、 減圧濃縮した。残留物をシリカゲルカラムクロマトグラフィー(展開溶媒:へキサン/酢 酸ェチル = 9/1→1/1)にて精製し、表題化合物を無色油状物として得た(収量: 1 6. 2g、収率: 84%)。
H-NMR(CDC1 ) δ :1.10— 1.35(3H, br) , 1.34 (3H, s) , 1.47(1H, s) ,
3
1.75-1.90(1H, m), 1.91— 2.00(1H, m) , 3.49 (2H, t, J = 7.2Hz) , 3.
55-3.65(1H, m), 5.05— 5.20 (2H, m) , 7.20— 7.40 (5H, m) .
[0097] 参考例 4
(2S, 3S)— 2, 3 ジメチルピロリジン一 3—オール 0.5シユウ酸塩
[0098] [化 13]
[0099] (2S, 3S)— 3 ヒドロキシー 2, 3 ジメチルピロリジン 1一力ルボン酸べンジル( 16. lg)のメタノール溶液(200mUに 50%含水 10%Pd/C(0.4g)を加え、水 素雰囲気下、激しく攪拌した。触媒を濾去し、濾液にシユウ酸 (2.90g)を加え、減圧 濃縮した。残留固体に酢酸ェチルを加え懸濁させた後、濾過することで表題化合物 を無色固体として得た(収量: 9.09g、収率: 88%)。
'H-NMRCDMSO-d ) δ :1.05(3H, d, J = 6.6Hz) , 1.18(3H, s), 1.74
6
-1.86 (2H, m), 2.80— 2.95(2H, m) , 2.98— 3.10(1H, m) , 4.00— 5. 20 (3H, m).
[0100] 参考例 5
(2S, 3S)— 3 ェチルー 3 ヒドロキシー2 メチルピロリジン 1一力ルボン酸ベン ジル
[0101] [化 14]
[0102] 塩化セリウム(7· 94g)、 3mol/Lェチルマグネシウムブロミドージェチルエーテル 溶液(9.46mL)、(2S)— 2 メチルー 3 ォキソピロリジンー1一力ルボン酸べンジ ル(3. Og)を用いて、参考例 3と同様の操作を行い、表題化合物を淡黄色油状物とし て得た(収量: 1.96g、収率: 58%)。
'H-NMRCCDCl ) δ :0.98 (3Η, t, J = 7.5Hz) , 1.10— 1.35(3H, br) , 1.
3
39(1H, s), 1.40-1.70 (2H, m) , 1.75— 1.95(2H, m) , 3.40— 3.58(2 H, m), 3.60-3.70(1H, m) , 5.00— 5.20 (2H, m) , 7.20— 7.40 (5H, m ).
[0103] 参考例 6
(2S, 3S)— 3 ェチルー 2 メチルピロリジンー3 オール 0· 5シユウ酸塩
[0104] [化 15]
[0105] (2S, 3S)— 3 ェチルー 3 ヒドロキシー2 メチルピロリジン 1一力ルボン酸べ ンジル(1.95g)、 50%含水 10%Pd/C(0.05g)を用いて、参考例 4と同様の操 作を行い、表題化合物を無色固体として得た(収量: 1.20g、収率: 93%)。
'H-NMRCDMSO-d ) δ :0.91 (3Η, t, J = 7.5Hz) , 1.07(3H, d, J = 6.6
6
Hz), 1.30-1.45(1H, m) , 1.46— 1.60(1H, m) , 1.78— 1.83(2H, m) , 2.90-3.15(3H, m) .
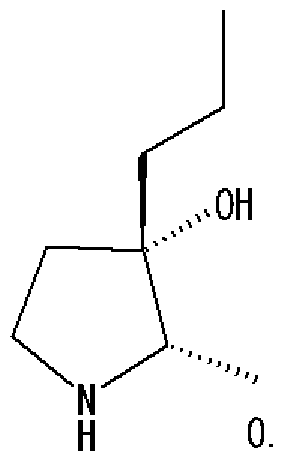
[0106] 参考例 7
(2S, 3S)— 3 ヒドロキシー2 メチルー 3 プロピルピロリジン 1一力ルボン酸べ ンジル
[0107] [化 16]
[0108] 塩化セリウム(12· 9g)、 2mol/Lプロピルマグネシウムブロミドー THF溶液(20m L)、(2S)— 2—メチルー 3—ォキソピロリジン 1一力ルボン酸べンジル(3· 5g)を用 いて、参考例 3と同様の操作を行い、表題化合物を淡黄色油状物として得た (収量: 2.32g、収率: 56%)。
'H-NMRCCDCl ) δ :0.90-1.00 (3Η, m) , 1.10— 1.35(3Η, br) , 1.30
3
-1.70 (5Η, m), 1.75— 1.95(2Η, m) , 3.40— 3.70 (3Η, m) , 5.00— 5. 20 (2Η, m), 7.20— 7.40 (5Η, m) .
[0109] 参考例 8
(2S, 3S)— 2—メチル—3 プロピルピロリジン— 3—オール 0· 5シユウ酸塩
[0110] [化 17]
(2S, 3S)— 3—ヒドロキシー 2—メチノレー 3—プロピルピ口リジン一 1—力ルボン酸 ベンジル(2· 32g)、 50%含水 10%Pd/C(0.10g)を用いて、参考例 4と同様の 操作を行い、表題化合物を無色固体として得た(収量: 1.50g、収率: 96%)。
'H-NMRCDMSO-d ) δ :0.90 (3Η, t, J = 6.6Hz) , 1.15(3H, d, J=6.6
Hz), 1.20-1.60 (4H, m) , 1.80— 2.00 (2H, m) , 3.05— 3.25(3H, m) .
[0112] 参考例 9
(2S, 3S)— 3—ヒドロキシー2—メチルー 3—(トリフルォロメチル)ピロリジン 1一力 ノレボン酸べ:
[0113] [化 18]
[0114] (2S)— 2 メチル 3 ォキソピロリジン一 1—カルボン酸べンジル(1.0g)の TH F溶液(10mUに氷冷下、トリフルォロメチルトリメチルシラン(0.95mUと lmol/L テトラプチルアンモニゥムフルオリドー THF溶液(0· 43mL)を加え、室温で 18時間 攪拌した。反応液に lmol/Lテトラプチルアンモニゥムフルオリド— THF溶液(8· 5 6mUを加え、 50°Cで 1時間攪拌した。反応液に水を加え、酢酸ェチルで抽出し、抽 出液を飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、減圧濃縮した。残留物を シリカゲルカラムクロマトグラフィー(展開溶媒:へキサン 酢酸ェチル =9: 1→2:1) にて精製し、表題化合物を無色油状物として得た (収量: 1.06g、収率: 81%)。 'H-NMRCCDCl ) δ :1.20-1.40 (3Η, br) , 1.95— 2.05(1Η, m) , 2. 17
3
-2.35(1Η, m), 3.45— 3.56(1Η, m) , 3.66— 3.80(1Η, m) , 4.10— 4. 25(1Η, m), 5.05— 5.20 (2Η, m) , 7.20— 7.40 (5Η, m) .
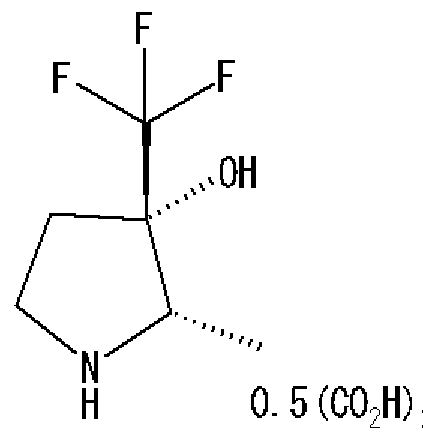
[0115] 参考例 10
(2S, 3S)— 2—メチルー 3 (トリフルォロメチル)ピロリジンー3 オール 0· 5シュ ク酸塩
[0117] (2S, 3S)—3 ヒドロキシー2 メチノレー 3—
カルボン酸べンジル(1.05g)、 50%含水 10%Pd/C(0.05g)を用いて、参考 例 4と同様の操作を行い、表題化合物を無色固体として得た(収量: 0.65g、収率: 8
8%) o
'H-NMRCDMSO-d ) δ :1.16(3H, d, J = 6.6Hz) , 1.90— 2.08(1H, m)
6
, 2.15-2.30(1H, m), 2.95— 3.05(1H, m) , 3. 10— 3.20(1H, m) , 3.3
4(1H, q, J = 6.6Hz), 6.00— 7.00(1H, br) .
[0118] 参考例 11
(2S)— 2 イソプロピル 3 ォキソピロリジン 1一力ルボン酸べ:
[0119] [化 20]
[0120] アルゴン雰囲気下、ジイソプロピルアミン(31.2g)の脱水 THF溶液(315mUを— 10°Cに冷却し、 1.6mol/L ブチルリチウム一へキサン溶液(175· 3mUを 5°C 以下で加え、同温度で 30分攪拌した。次いで— 78°Cに冷却し、酢酸ェチル(24.7 g)の脱水 THF溶液(65mL)を— 70°C以下で滴下し、同温度で 1時間攪拌後、 [(1 S)— 1—ホルミルー2 メチルプロピル]力ルバミン酸べンジル(16· 5g)の脱水 THF 溶液(70mL)を— 65°C以下で滴下した。 70°Cで 1時間攪拌した後、酢酸(36g)
を加え、 0°Cに昇温した。反応混合物を氷水に注ぎ、酢酸ェチルで抽出し、有機層を 飽和食塩水で洗浄後、無水硫酸マグネシウムで乾燥し、濃縮した。残留物をシリカゲ ルカラムクロマトグラフィー(展開溶媒:へキサン/酢酸ェチル = 19/1→3/2)にて 精製し、(4S)— 4— { [ (ベンジルォキシ)カルボニル]アミノ}— 3—ヒドロキシ— 5—メ チルへキサン酸ェチルを無色油状物として得た(収量: 15. 4g)。
アルゴン雰囲気下、 (4S)— 4 { [ (ベンジルォキシ)カルボニル]アミノ} 3—ヒド 口キシ一 5 メチルへキサン酸ェチル(14· 74g)の脱水 THF溶液(228mL)に 2, 6 —ルチジン(7. 33g)を加え、氷冷攪拌下、トリフルォロメタンスルホン酸 tert ブチ ルジメチルシリル(14. 46g)を滴下した。徐々に室温に戻し 1. 5時間攪拌後、反応 混合物を氷水に注ぎ、酢酸ェチルで抽出し、有機層を飽和食塩水で洗浄し、無水硫 酸マグネシウムで乾燥後、濃縮した。残留物をシリカゲルカラムクロマトグラフィー(展 開溶媒:へキサン/酢酸ェチル = 19/1→4/1)にて精製し、(4S)— 4— { [ (ベン ジルォキシ)カルボニル]アミノ } 3— { [tert ブチル(ジメチル)シリル]ォキシ } 5 ーメチルへキサン酸ェチルを無色油状物として得た(収量: 17. 7g)。
アルゴン雰囲気下、 (4S)— 4 { [ (ベンジルォキシ)カルボニル]アミノ} 3— { [te rt ブチル(ジメチル)シリル]ォキシ } 5 メチルへキサン酸ェチル(17· 7g)、塩 化カルシウム(6. 73g)、水素化ホウ素ナトリウム(4. 58g)の脱水 THF懸濁液(303 mL)に氷冷攪拌下、脱水エタノール(152mL)を加え、徐々に室温に戻して 15時間 攪拌した。反応混合物を酢酸ェチル /氷水(lmol/L塩酸, 122mLを含む)にゆつ くり注いだ後、分配した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾 燥後、濃縮した。残留物をシリカゲルカラムクロマトグラフィー (展開溶媒:へキサン/ 酢酸ェチル = 19/ 1→ 1 / 1 )にて精製し、 (( 1 S ) 2 { [tert ブチル (ジメチル) シリル]ォキシ } 4ーヒドロキシー 1 イソプロピルブチル)力ルバミン酸ベンジルを無 色油状物として得た(収量: 14. 9g)。
( ( 1 S)— 2— { [tert ブチル(ジメチル)シリル]ォキシ } 4ーヒドロキシー 1 イソ プロピルブチル)力ルバミン酸べンジル(14· 9g)の脱水 THF溶液(188mUにトリエ チルァミン(5. 07g)を加え、氷冷攪拌下、メタンスルホユルクロリド(4. 96g)の脱水 THF溶液(lOmL)を滴下した。同温度で 1時間攪拌後、反応混合物を酢酸ェチル
/氷水に注ぎ、分配した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで 乾燥後、濃縮した。残留物の脱水 THF溶液(188mUに氷冷攪拌下、 lmol/L-t ert ブトキシカリウム THF溶液(37. 7mUを加え、同温度で 1時間攪拌した。反 応混合物を酢酸ェチル /氷水に注ぎ、分配した。有機層を飽和食塩水で洗浄、無 水硫酸マグネシウムで乾燥、濃縮した。残留物の脱水 THF溶液(188mL)に氷冷攪 拌下、 lmol/L テトラブチルアンモニゥムフルオリドー THF溶液(37. 7mUを加 え、同温度で 1時間、室温に戻して 5時間攪拌した。反応混合物を酢酸ェチル /氷 水に注いだ後、分配した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで 乾燥後、濃縮した。残留物をシリカゲルカラムクロマトグラフィー (展開溶媒:へキサン 酢酸ェチル /19/1→2/3)にて精製し、(2S)— 3 ヒドロキシー 2 イソプロピ ルピロリジン 1一力ルボン酸ベンジルを無色油状物として得た(収量:3. 22g)。
[0122] (2S)— 3—ヒドロキシー2—イソプロピルピロリジンー1一力ルボン酸べンジル(3· 2 2g)の脱水ァセトニトリル溶液(26mUに粉末モレキュラーシーブス 4Α(2· 31g)、 4 —メチルモルホリン一 N ォキシド(2· 86g)を加え、 0°Cに冷却した後、テトラ一 n— プロピルアンモニゥムぺルルテナート(0. 16g)を加え、 0°Cで 1時間攪拌した後、室 温で 18時間攪拌した。反応液を減圧濃縮した後、残留物を酢酸ェチルで懸濁し、不 溶物をハイフロスーパーセルで濾過した。濾液を減圧濃縮した後、残留物をシリカゲ ルカラムクロマトグラフィー(展開溶媒:へキサン一酢酸ェチル = 19 : 1→4: 1)にて精 製し、表題化合物を無色油状物として得た (収量: 2. 74g)。
'H-NMR CCDCl ) δ : 0. 93 (3Η, d, J = 6. 9Hz) , 1. 02 (3H, d, J = 6. 9Hz) ,
3
2. 14- 2. 39 (1H, brs) , 2. 40— 2. 65 (2H, m) , 3. 56— 3. 73 (1H, m) , 3. 8 9 (1H, brs) , 3. 97— 4. 20 (1H, brs) , 5. 17 (2H, s) , 7. 36 (5H, brs) .
IR (KBr) : 2963, 1753, 1703, 1414cm—1.
[0123] 参考例 12
(2S, 3S)— 3—ヒドロキシー2—イソプロピルー3—メチルピロリジン 1一力ルボン 酸べンジル
[0124] [化 21]
[0125] 塩化セリウム(6· 35g)、 3mol/Lメチルマグネシウムブロミドージェチルエーテル 溶液(7.55mL)、(2S)— 2—イソプロピルー3—ォキソピロリジンー1一力ルボン酸 ベンジル(2.7g)を用いて、参考例 3と同様の操作を行い、表題化合物を淡黄色油 状物として得た (収量: 1.78g、収率: 62%)。
'H-NMRCCDCl ) δ :0.87-1. 13(6H, m) , 1.34 (3H, s) , 1.62(1H, s) ,
3
1.76-1.89(1H, m), 1.99— 2.09 (2H, m) , 3.34— 3.54 (3H, m) , 5.13 (2H, s), 7.34 (5H, brs) .
IR(KBr) :3432, 2965, 1682, 1416cm—1.
[0126] 参考例 13
(2S, 3S)— 2—イソプロピル一 3—メチルピロリジン一 3—オール 0.5シユウ酸塩 [0127] [化 22]
[0128] (2S, 3S)— 3—ヒドロキシ一 2—イソプロピル一 3—メチルピロリジン一 1—カルボン 酸べンジル(1· 78g)、 50%含水— 10%Pd/C(0.09g)を用いて、参考例 4と同様 の操作を行い、表題化合物を無色固体として得た(収量: 1.07g、収率: 89%)。 'H-NMRCDMSO-d +TFA) δ :0.98 (3Η, d, J = 6.6Hz) , 1.03 (3H, d, J
6
=6.6Hz), 1.37(3H, s) , 1.91— 1.97(2H, m) , 2.00— 2.12(1H, m) , 2 .75-2.83(1H, m), 3.06— 3.18(2H, m) , 8.58(1H, brs), 9.32(1H, br
[0129] 参考例 14
(2S, 3S)— 3 ェチル 3 ヒドロキシ一 2 リジン 1一力ノレボン 酸べンジル
[0130] [化 23]
[0131] 塩化セリウム(9· 25g)、 3mol/Lェチルマグネシウムブロミドージェチルエーテル 溶液(11. OmU、(2S)— 2—イソプロピルー3—ォキソピロリジンー1一力ルボン酸 ベンジル(3.92g)を用いて、参考例 3と同様の操作を行い、表題化合物を無色油状 物として得た(収量: 2· 21g、収率: 51%)。
'H-NMRCCDCl ) δ :0.92-1. 10(9H, m) , 1.43(1H, s) , 1.50— 1.60(
3
2H, m), 1.91-2.14(3H, m) , 3.30— 3.60 (3H, m) , 5.12(2H, s) , 7.3 4(5H, brs).
IR(KBr) :3434, 2963, 1680, 1416cm—1.
[0132] 参考例 15
(2S, 3S)— 3 ェチルー 2 イソプロピルピロリジンー3 オール 0· 5シユウ酸塩 [0133] [化 24]
(2S, 3S)— 3 ェチルー 3 ヒドロキシー2 イソプロピルピロリジン 1 カルボ ン酸べンジル(2· 2g)、 50%含水 10%Pd/C(0. llg)を用いて、参考例 4と同 様の操作を行い、表題化合物を無色固体として得た(収量: 1.33g、収率: 83%)。 'H-NMRCDMSO-d +TFA) δ :0.92 (3Η, t, J = 7.2Hz) , 0.99 (3H, d, J
=6.6Hz), 1.01 (3H, d, J = 6.6Hz) , 1.49— 1.61(1H, m) , 1.70— 1.80( 1H, m), 1.88-1.95(2H, m) , 1.99— 2.13(1H, m) , 2.78— 2.86(1H, m), 3.06-3.20 (2H, m) , 8.55(1H, brs) , 9.18(1H, brs) .
[0135] 参考例 16
(2S , 3R)— 3—シクロプロピル 3—ヒドロキシ 2—イソプロピルピロリジン 1—力 ノレボン酸べンジル
[0136] [化 25]
[0137] 塩化セリウム(7· 40g)、 0.5molZLシクロプロピルマグネシウムブロミドー THF溶 液(52.8mU、(2S)— 2 イソプロピルー3 ォキソピロリジンー1一力ルボン酸べ ンジル(3.14g)を用いて、参考例 3と同様の操作を行い、表題化合物を無色油状物 として得た(収量: 2.31g、収率: 63%)。
'H-NMRCCDCl ) δ :0.32-0.47 (4Η, m) , 0.92— 1.08 (7Η, m) , 1.29(
3
1Η, s), 1.84-1.92(1Η, m) , 1.95— 2. 12(2Η, br) , 3.35— 3.62(3Η, m ), 5.14(2Η, s), 7.34 (5Η, brs).
IR(KBr) :3414, 2959, 1680, 1416cm—1.
[0138] 参考例 17
(2S, 3R)—3 シクロプロピノレー 2 イソプロピノレピロリジンー3 ォーノレ 0· 5シュ
ク酸塩
[0139] [化 26]
[0140] (2S, 3S)—3 シクロプロピル一 3 ヒドロキシ一 2 イソプロピルピロリジン一 1— カルボン酸べンジル(1.98g)、 50%含水 10%Pd/C(0.10g)を用いて、参考 例 4と同様の操作を行い、表題化合物を無色固体として得た(収量: 1.22g、収率: 8
'H-NMRCDMSO-d +TFA) δ :0.34— 0.45(3H, m) , 0.50— 0.57(1Η
6
, m), 0.93-1.03(1Η, m) , 0.99 (3Η, d, J = 6.6Hz) , 1.08 (3Η, d, J = 6. 6Hz), 1.75-1.97(2Η, m) , 2.00— 2.12(1Η, m) , 2.87— 2.95(1Η, m) , 3.06-3.18(2Η, m) , 8.58(1Η, brs) , 9.22(1Η, brs) .
[0141] 参考例 18
(2S , 3R) 3—シクロプロピノレー 3—ヒドロキシ 2—メチルピロリジン 1—カルボ ン酸べンジノレ
[0142] [化 27]
[0143] 塩化セリウム(11· lg)、0.5molZLシクロプロピルマグネシウムブロミドー THF溶
液(72· OmU、(2S)— 2 メチルー 3 ォキソピロリジン 1一力ルボン酸べンジル (3. Og)を用いて、参考例 3と同様の操作を行い、表題化合物を無色油状物として得 た(収量: 1.64g、収率: 46%)。
'H-NMRCCDCl ) δ :0.28-0.57 (4Η, m) , 0.92— 1.10(1Η, m) , 1.16
3
-1.36 (4Η, m), 1.74— 1.89(2Η, m) , 3.41— 3.75(3Η, m) , 5.04— 5. 23 (2Η, m), 7.28— 7.43(5Η, m) .
[0144] 参考例 19
(2S, 3S)— 3 ヒドロキシー2 メチルピロリジン 1一力ルボン酸 tert ブチル [0145] [化 28]
[0146] (2S, 3S)— 3 ヒドロキシ一 2 メチルピロリジン(69mmol)の THF溶液( 15 OmL )を水(70mUで希釈し,炭酸ナトリウム(14· 83g)と二炭酸ジー tert ブチル(17· 43mL)を加え、室温で 24時間攪拌した。反応液を酢酸ェチル /水で分配し、有機 層を無水硫酸マグネシウムで乾燥した後、減圧濃縮した。残留物をシリカゲルカラム クロマトグラフィー(展開溶媒:へキサン/酢酸ェチル =3/1→1/3)にて精製し、 表題化合物を薄黄色油状物として得た(収量: 11.09g、収率: 80%)。
'H-NMRCCDCl ) δ :1.15-1.22 (3Η, m) , 1.47(9Η, s) , 1.56— 1.63(
3
1Η, m), 1.77-1.93(1Η, m) , 1.96— 2.11(1Η, m) , 3.28— 3.54 (2Η, m), 3.76-3.96(1Η, m) , 4.26— 4.37(1Η, m) .
[0147] 参考例 20
(2S)— 2 メチルー 3 ォキソピロリジン 1一力ルボン酸 tert ブチル
[0148] [化 29]
[0149] (2S, 3S)—3—ヒドロキシー2—メチルピロリジンー1一力ルボン酸 tert ブチル( 9. 04g)の脱水ァセトニトリル溶液(75mUに粉末モレキュラーシーブス 4Α(11 · 5g )、 4 メチルモルホリン一 N ォキシド(10· 5g)を加え、 0°Cに冷却した後、テトラー n—プロピルアンモニゥムぺルルテナート(0. 80g)を加え、室温で 4時間半攪拌した 。反応液を減圧濃縮した後、残留物を酢酸ェチルで懸濁し、不溶物をハイフロス一 パーセルで濾過した。濾液を減圧濃縮した後、残留物をシリカゲルカラムクロマトダラ フィー(展開溶媒:へキサン/酢酸ェチル = 15/1→1/1)にて精製し、表題化合 物を無色油状物として得た(収量: 7. 67g、収率: 85. 7%)。
'H-NMR CCDCl ) δ : 1. 32 (3Η, d, J = 7. 2Hz) , 1. 50 (9H, s) , 2. 47— 2. 6
3
7 (2H, m) , 3. 50- 3. 65 (1H, m) , 3. 82— 4. 00 (2H, m) .
[0150] 参考例 21
(2S, 3R)— 3—ヒドロキシ一 2—メチル 3—ビュルピロリジン一 1—カルボン酸 ter tーブチノレ
[0151] [化 30]
塩化セリウム(3· 95g)、 lmol/Lビュルマグネシウムブロミドー THF溶液(12· 5m L)、 (2S)— 2—メチルー 3—ォキソピロリジン 1一力ルボン酸 tert ブチル(1 · 0
g)を用いて、参考例 3と同様の操作を行い、表題化合物を無色油状物として得た (収 量: 0.648g、収率: 57%)。
'H-NMRCCDCl ) δ :1.21 (3Η, d, J = 6.4Hz) , 1.42— 1.51(1H, m) , 1.
3
48 (9H, s), 1.84-1.97(2H, m) , 3.39— 3.54(1H, m) , 3.44— 3.60(1 H, m), 3.58-3.71(1H, m) , 5. 19(1H, dd, J=10.7, 1.0Hz) , 5.36(1H , dd, J=17.3, 1. OHz), 5.94(1H, dd, J=17.3, 10.7Hz) .
[0153] 参考例 22
( 2 S )— 2—ェチル 3—ォキソピロリジン一 1—カルボン酸べンジル
[0154] [化 31]
[0155] [(1S)— 1 ホルミルプロピル]力ルバミン酸べンジノレを用いて、参考例 11と同様の 操作を行い、表題化合物を無色油状物として得た。
'H-NMRCCDCl ) δ :0.85(3H, t, J = 7.6Hz) , 1.75— 2.06 (2H, m) , 2.3
3
9-2.73 (2H, m), 3.55— 3.73(1H, m) , 3.91-4.13(2H, m) , 5.11— 5 .26 (2H, m), 7.26— 7.47(5H, m) .
[0156] 参考例 23
(2S, 3S)— 2 ェチルー 3 ヒドロキシー3 メチルピロリジン 1一力ルボン酸ベン ジル
[0157] [化 32]
[0158] 塩化セリウム(11· 69g)、 3mol/Lのメチルマグネシウムブロミドージェチルエーテ ル溶液(13· 55mL)、(2S)—2 ェチルー 3 ォキソピロリジン 1一力ルボン酸べ ンジル(3.35g)を用いて、参考例 3と同様の操作を行い、表題化合物を無色油状物 として得た(収量: 2.84g、収率: 84%)。
'H-NMRCCDCl ) δ :0.88-1.07(3H, m) , 1.36 (3H, s) , 1.42(1H, s) ,
3
1.47-1.90 (3H, m), 1.91— 2.07(1H, m) , 3.34— 3.58 (3H, m) , 5.07 -5. 19(2H, m), 7.27— 7.40 (5H, m) .
[0159] 参考例 24
(2S, 3S)— 2 ェチルー 3 メチルピロリジンー3 オール 0· 5シユウ酸塩
[0160] [化 33]
0.5 (C0?H)
[0161] (2S, 3S)— 2 ェチルー 3 ヒドロキシー3 メチルピロリジン 1一力ルボン酸べ ンジル(2· 84g)、 50%含水 10%Pd/C(0.31g)を用いて、参考例 4と同様の操 作を行い、表題化合物を無色固体として得た(収量: 1.77g、収率: 88%)。
'H-NMRCDMSO-d ) δ :0.82— 1.02 (4Η, m) , 1.24 (3Η, s) , 1.38— 1.
6
76 (2Η, m), 1.81— 1.97(2Η, m) , 2.81— 2.91(1Η, m) , 3.01— 3.20(2 Η, m), 4.94-6.34(1Η, m) .
[0162] 参考例 25
(2S, 3S)— 2, 3 ジェチルー 3 ヒドロキシピロリジン 1一力ルボン酸べンジル [0163] [化 34]
[0164] 塩化セリウム(8.58g)、 3mol/Lのェチルマグネシウムブロミドージェチルエーテ ル溶液(9.6mL)、(2S)— 2 ェチルー 3 ォキソピロリジンー1一力ルボン酸ベン ジル(2.37g)を用いて、参考例 3と同様の操作を行い、表題化合物を無色油状物と して得た(収量: 2.19g、収率: 82%)。
'H-NMRCCDCl ) δ :0.96 (6Η, t, J = 7.4Hz) , 1.28— 1.71 (4H, m) , 1.6
3
6-1.86(1H, m), 1.84— 1.96 (2H, m) , 3.35— 3.51 (2H, m) , 3.50— 3 .67(1H, m), 5.02— 5.21 (2H, m) , 7.27— 7.42(5H, m) .
[0165] 参考例 26
(2S, 3S)— 2, 3 ジェチルピロリジンー3 オール 0· 5シユウ酸塩
[0166] [化 35]
0.5(C02H)2
(2S, 3S)— 2, 3 ジェチルー 3 ヒドロキシピロリジン 1一力ルボン酸べンジル( 2. 19g)、 50%含水— 10%Pd/C(0.22g)を用いて、参考例 4と同様の操作を行 い、表題化合物を無色固体として得た(収量: 1.40g、収率:94%)。
'H-NMRCDMSO-d ) δ :0.80— 1.01 (6Η, m) , 1.27— 1.66 (5Η, m) , 1
.74-1.88 (2H, m), 2.69— 2.84(1H, m) , 2.90— 3. 14(2H, m) , 4.57 -5.31(1H, m).
[0168] 参考例 27
(2S , 3R)— 3—シクロプロピル 2—ェチル 3—ヒドロキシピロリジン 1—カルボ ン酸べンジノレ
[0169] [化 36]
[0170] 塩化セリウム(8· 64g)、0.5molZLのシクロプロピルマグネシウムブロミドー THF 溶液(58. OmU、(2S)— 2 ェチルー 3 ォキソピロリジンー1一力ルボン酸べンジ ル(2.37g)を用いて、参考例 3と同様の操作を行い、表題化合物を無色油状物とし て得た(収量: 2. Olg、収率: 73%)。
'H-NMRCCDCl ) δ :0.29-0.53 (4Η, m) , 0.86— 1.14 (4Η, m) , 1.20
3
-1.32(1Η, m), 1.49— 1.73(1Η, m) , 1.65— 1.85(1Η, m) , 1.80— 2. 00 (2Η, m), 3.36-3.60 (3Η, m) , 5.05— 5.22 (2Η, m) , 7.26— 7.43(5 Η, m).
[0171] 参考例 28
(2S, 3R)—3 シクロプロピル一 2 ェチルピロリジン一 3 オール 0· 5シユウ酸 塩
0.5(C02H)2
[0173] (2S, 3R)—3 シクロプロピル一 2 ェチル 3 ヒドロキシピロリジン一 1—カル ボン酸べンジル(2· 01g)、 50%含水 10%Pd/C(0.20g)を用いて、参考例 4と 同様の操作を行い、表題化合物を無色固体として得た(収量: 1.35g、収率: 96%)
'H-NMRCDMSO-d +TFA) δ :0.22— 0.51 (4Η, m) , 0.79— 1.10 (4Η
6
, m), 1.49-2.01 (4Η, m) , 3.00— 3.26 (3Η, m) , 8.63(1Η, brs) , 9.16 (1Η, brs).
[0174] 参考例 29
4-{[ (ベンジルォキシ)カルボ二ノレ]アミノ}—2, 2 ジメチル一 3 ヒドロキシペンタ ン酸ェチノレ
[0176] 4 { [(ベンジルォキシ)カルボニル]アミノ}ー2, 2 ジメチルー 3 ォキソペンタン 酸ェチル(5.76g)のメタノール溶液(lOOmUに 0°Cで水素化ホウ素ナトリウム(940 mg)を加えた後、室温で 17時間攪拌した。反応液に飽和塩化アンモニゥム水溶液を 加え、酢酸ェチルで抽出した。抽出液を飽和食塩水で洗浄し、無水硫酸マグネシゥ ムで乾燥後、減圧濃縮した。残留物をシリカゲルカラムクロマトグラフィー (展開溶媒: へキサン/酢酸ェチル = 50/1→1/3)にて精製することで表題化合物を無色固 体として得た(収量: 4.26g、収率: 74%)。
H-NMR(CDC1 ) δ :1.01 (3H, d, J = 6.8Hz) , 1.12— 1.40(10H, m) , 3
3
.39-3.64(1H, m), 3.76— 4.24 (3H, m) , 4.85— 5.33 (3H, m) , 7.22 -7.42(5H, m).
[0177] 参考例 30
4 { [(ベンジルォキシ)カルボニル]アミノ}ー2, 2 ジメチルー 3 (tert ブチルジ メチルシリルォキシ)ペンタン酸ェチル
[0178] [化 57]
[0179] 4 { [(ベンジルォキシ)カルボニル]アミノ}ー2, 2 ジメチルー 3 ヒドロキシペン タン酸ェチル(5.7g)と 2, 6 ルチジン(2· 27mUの THF溶液(80mUに氷冷下 、トリフルォロメタンスルホン酸 tert ブチルジメチルシリル(3.44mL)をカロえ、室温 に昇温した後、 17時間攪拌した。反応液を水に加え、酢酸ェチルで抽出した。抽出 液を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥後、減圧濃縮した。残留物 をシリカゲルカラムクロマトグラフィー(展開溶媒:へキサン/酢酸ェチル = 50/1→2 /1)にて精製することで表題化合物を無色油状物として得た(収量: 5.42g、収率: 70%) 0
'H-NMRCCDCl ) δ :0.03-0.20 (6Η, m) , 0.88— 0.95(9H, m) , 1.06
3
-1.33(12H, m), 3.73— 4. 19(4H, m) , 4.55— 5.22 (3H, m) , 7.26— 7 .41 (5H, m).
[0180] 参考例 31
[2— (tert ブチルジメチルシリルォキシ)ー4ーヒドロキシ 1, 3, 3 トリメチルブチ ノレ]力ルバミン酸べンジル
[0182] 4 { [ (ベンジルォキシ)カルボニル]アミノ}ー2, 2 ジメチルー 3—(tert ブチル ジメチルシリルォキシ)ペンタン酸ェチル(5· 42g)、塩化カノレシゥム(2. 06g)の TH F (50mL) エタノール(25mU混合溶液に水素化ホウ素ナトリウム(1. 56g)を加 え室温で 13時間攪拌した。反応液を水に加え、酢酸ェチルで抽出した。抽出液を飽 和食塩水で洗浄し、無水硫酸マグネシウムで乾燥後、減圧濃縮した。残留物をシリカ ゲルカラムクロマトグラフィー(展開溶媒:へキサン/酢酸ェチル = 50/1→1/1)に て精製することで表題化合物を無色固体として得た (収量: 1. 38g、収率: 28%)。
'H-NMR CCDCl ) δ : 0. 04-0. 06 (6Η, m) , 0. 86 (3Η, s) , 0. 93 (9Η, s) ,
3
0. 98 (3Η, s) , 1. 14 (3Η, d, J = 6. 8Hz) , 3. 34— 3. 46 (1H, m) , 3. 50— 3. 66 (2H, m) , 3. 77— 3. 82 (1H, m) , 3. 92— 4. 03 (1H, m) , 4. 68— 4. 80 (1 H, m) , 5. 03- 5. 17 (2H, m) , 7. 28— 7. 42 (5H, m) .
[0183] 参考例 32
ベンジル (2RS, 3SR)— 3—ヒドロキシー 2, 4, 4—トリメチルピロリジン一 1—カル ボキシラート
[0184] [化 59]
[0185] [2— (tert ブチルジメチルシリルォキシ)ー4ーヒドロキシ 1 , 3, 3 トリメチルブ チル]力ルバミン酸べンジル(1. 38g)とトリエチノレアミン(0. 73mUの THF溶液(20
mL)を 0°Cに冷却し、塩化メシル(0. 352mL)を加え、さらに 0°Cで 45分間攪拌した 。反応液を水に加え、酢酸ェチルで抽出した。抽出液を飽和食塩水で洗浄し、無水 硫酸マグネシウムで乾燥後、減圧濃縮した。残留物の THF溶液(20mL)に 1M 力 リウム tert ブトキシド THF溶液(3. 8mL)を加え、室温で 1時間攪拌した後、水を 加え酢酸ェチルで抽出した。抽出液を飽和食塩水で洗浄し、無水硫酸マグネシウム で乾燥後、減圧濃縮した。残留物の THF溶液(10mUに 1M テトラプチルアンモニ ゥムフルオリドー THF溶液(4mUを加え、室温で 17時間攪拌した。反応液を水に加 え、酢酸ェチルで抽出した。抽出液を飽和食塩水で洗浄し、無水硫酸マグネシウム で乾燥後、減圧濃縮した。残留物をシリカゲルカラムクロマトグラフィー(展開溶媒:へ キサン/酢酸ェチル = 50/1→1/2)にて精製することで表題化合物を無色固体と して得た(収量: 842mg、収率: 92%)。
'H-NMR CCDCl ) δ : 0. 96 (3Η, s) , 1. 06 (3H, s) , 1. 32— 1. 48 (1H, m) ,
3
3. 01 - 3. 15 (1H, m) , 3. 40— 3. 61 (3H, m) , 5. 07— 5. 20 (2H, m) , 7. 26 - 7. 40 (5H, m) .
[0186] 参考例 33
(2RS, 3SR)— 2, 4, 4 トリメチルピロリジン一 3 オール 0· 5シユウ酸塩
[0187] [化 60]
ベンジノレ (2RS, 3SR)— 3 ヒドロキシー 2, 4, 4 トリメチノレピロリジン 1一力ノレ ボキシラート(842mg)と 10%パラジウム炭素(50%含水、 110mg)のメタノール懸濁 液(20mL)を水素雰囲気下 1. 5時間攪拌した。反応液を濾過し、濾液にシユウ酸(1 44mg)を加えた後、減圧濃縮することで表題化合物を無色固体として得た (収量: 5 12mg、収率: 92%)。
'H-NMR Cd— DMSO + TFA) δ : 0. 92 (3Η, s) , 1. 03 (3Η, s) , 1. 31 (3Η,
d, J = 6.8Hz), 2.88-3.11 (2H, m) , 3.12— 3.33(1H, m) , 3.40(1H, d J = 9. 1Hz), 8.49(1H, brs) , 9.05(1H, brs) .
[0189] 参考例 34
ベンジル (2S, 3S, 5R)— 3—ヒドロキシ一 2, 5—ジメチルピロリジン一 1—カルボ キシラート
[0190] [化 61]
[0191] Journal of Organic Chemistry,第 59巻、 1958〜 1960ページ、 1994年 記載の方法 に従って合成したベンジル (2S, 3S, 5S)— 3 ヒドロキシー2 メチルー 5 [(トリ メチルシリル)メチル]ピロリジンー1 カルボキシラート(222mg)、カリウム tert ブト キシド( 130mg)、 18 クラウン一 6—エーテル(53mg)の DMSO溶液( 12mUに 水(0.6mL)を加え、 100°Cで 17時間攪拌した。反応液に水を加え、酢酸ェチルで 抽出した。抽出液を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥後、減圧濃 縮した。残留物をシリカゲルカラムクロマトグラフィー(展開溶媒:へキサン/酢酸ェチ ル = 50/1→2/3)にて精製することで表題化合物を無色油状物として得た (収量: 112mg、収率: 65%)。
'H-NMRCCDCl ) δ :1.23 (3Η, d, J = 6.4Hz) , 1.35(3H, d, J = 6.1Hz),
3
1.52-1.73(1H, m), 2.25— 2.40(1H, m) , 3.79— 3.94(1H, m) , 3.95 —4. 10(1H, m), 4.22— 4.36(1H, m) , 5.06— 5.19(2H, m) , 7.26— 7. 42 (5H, m).
[0192] 参考例 35
(2S, 3S, 5R)— 2, 5 ジメチルピロリジンー3 オール 0.5シユウ酸塩
[0193] [化 62]
0.5(CO2H)2
[0194] ベンジノレ (2S, 3S, 5R)— 3 ヒドロキシ一 2, 5 ジメチルピロリジン一 1—カルボ キシラート(785mg)、 10%パラジウム炭素(50%含水、 80mg)、シユウ酸(142mg) を用いて参考例 33と同様の操作を行うことで、表題化合物を無色固体として得た(収 量: 485mg、収率: 96%)。
'H-NMRCd— DMSO + TFA) δ :1. 16— 1.40(1H, m) , 1.22 (3H, d, J = 6
6
.8Hz), 1.32(3H, d, J = 6.8 Hz), 1.42-1.57(1H, m) , 2.33— 2.52(1H , m), 3.28-3.47(1H, m) , 3.46— 3.66(1H, m) , 4.05— 4.22(1H, m) , 8.21(1H, brs), 9.13(1H, brs) .
[0195] 参考例 36
ベンジル (2S, 5R)— 2, 5 ジメチルー 3 ォキソピロリジン一 1—カルボキシラート [0196] [化 63]
[0197] ベンジノレ (2S, 3S, 5R)— 3 ヒドロキシ一 2, 5 ジメチルピロリジン一 1—力ルポ キシラー Hi.30g)のァセトニトリル溶液(20mUにテトラプロピルアンモニゥムペル ルテナート(92mg)、 4 メチルモルホリン N ォキシド(1.22g)、モレキュラシーブ ス 4A粉末(1.32g)を加え、室温で 2時間攪拌した。反応液を濃縮し、残留物を酢酸
ェチルに懸濁し、セライトを用いて濾過した。濾液を減圧濃縮し、残留物をシリカゲル カラムクロマトグラフィー(展開溶媒:へキサン/酢酸ェチル =30/1→1/1)にて精 製することで表題化合物を無色油状物として得た (収量: 1.30g、収率: 100%)。 'H-NMRCCDCl ) δ :1.30 (3Η, d, J = 6.6Hz) , 1.39 (3H, d, J = 7.0Hz) ,
3
2. 18-2.32(1H, m) , 2.77— 2.92(1H, m) , 3.96— 4. 10(1H, m) , 4.41 —4.55(1H, m), 5.15— 5.25(2H, m) , 7.29— 7.42(5H, m) .
[0198] 参考例 37
ベンジノレ (2S, 3S, 5R)— 3—ヒドロキシ一 2, 3, 5—トリメチノレピロリジン一 1—力ノレ ボキシラート
[0199] [化 64]
塩化セリウム(2· 09g)の THF懸濁液(8mUを— 78°Cに冷却し、 1M メチルマグ ネシゥムブロミド— THF溶液(7.2mL)を滴下した。反応液を— 78°Cで 30分間攪拌 した後、ベンジル (2S, 3S, 5R)-2, 5—ジメチルー 3—ォキソピロリジンー1一力 ルポキシラート(600mg)の THF溶液(4mL)を滴下した。滴下終了後、反応液を 2. 5時間かけて室温まで昇温した。反応液に 1M塩酸を加え、酢酸ェチルで抽出した。 抽出液を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥後、減圧濃縮した。残 留物をシリカゲルカラムクロマトグラフィー(展開溶媒:へキサン/酢酸ェチル = 50/ 1→1/1)にて精製することで表題化合物を無色油状物として得た(収量 :450mg、 収率: 70%)。
'H-NMRCCDCl ) δ :1.24 (3Η, d, J = 6.6Hz) , 1.31 (3H, s), 1.34 (3H,
3
d, J = 6.2Hz), 1.36-1.49(1H, m) , 1.77(1H, dd, J=12.7, 7.4Hz) , 1
.98-2.12(1H, m), 3.58— 3.75(1H, m) , 3.76— 3.92(1H, m) , 5.03 -5.23 (2H, m), 7.27— 7.43(5H, m) .
[0201] 実施例 1
2 フルオロー 4— [(2S, 3S)— 3 ヒドロキシー 2, 3 ジメチルピロリジン一 1—ィル ]ベンゾニトリノレ
[0202] [化 73]
[0203] (2S, 3S)— 2, 3 ジメチルピロリジン— 3 オール 0· 5シユウ酸塩(228mg)、 2 , 4ージフルォロベンゾニトリル(292mg)、炭酸リチウム(206mg)の DMSO溶液(2 mL)を 80°Cで 18時間攪拌した。反応液に水を加え、酢酸ェチルで抽出し、抽出液 を飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥し、減圧濃縮した。残留物をシリ 力ゲルカラムクロマトグラフィー(展開溶媒:へキサン 酢酸ェチル =9: 1→2: 1)にて 精製した後、へキサン イソプロピルエーテルから再結晶することで表題化合物を無 色固体として得た(収量: 188mg、収率: 57 % )。
'H-NMRCCDCl ) δ :1.21 (3Η, d, J = 6.6Hz) , 1.37(3H, s), 1.59(1H, s
3
), 1.95-2.04(1H, m), 2.14— 2.26(1H, m) , 6.23(1H, dd, J=12.9,2 . 1Hz), 6.31(1H, dd, J = 8.7, 2. 1Hz), 7.35(1H, dd, J = 8.7, 7.8Hz) . IR(KBr) :3324, 2973, 2209, 1609cm—1.
mp:103-104°C.
[0204] 実施例 2
2 フルオロー 4— [(2S, 3S)— 3 ヒドロキシー 2, 3 ジメチルピロリジン一 1—ィル
]一 3—メチルベンゾニトリル
[0205] [化 74]
[0206] (2S, 3S)— 2, 3—ジメチルピロリジン— 3—オール 0· 5シユウ酸塩(228mg)、 2 , 4—ジフルォロ— 3—メチルベンゾニトリル(321mg)、炭酸リチウム(206mg)を用 いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 194 mg、収率: 56%)。
'H-NMRCCDCl ) δ :1.08 (3Η, d, J = 6. 3Hz) , 1.41 (3H, s), 1. 66(1H, s
3
), 1. 84-2.02 (2H, m) , 2. 19(3H, d, J = 2.4Hz) , 2. 95(1H, dt, J = 9. 6, 2. 1Hz), 3. 50(1H, q, J = 6. 3Hz) , 3. 85— 3. 95(1H, m) , 6. 60(1H, d, J =8. 6Hz), 7. 30(1H, t, J = 8. 6Hz) .
IR(KBr) :3470, 2976, 2224, 1613cm—1.
mp:68-69°C.
[0207] 実施例 3
4-[(2S, 3S)— 3—ヒドロキシー 2, 3—ジメチルピロリジン一 1—ィル]—3— (トリフ ノレオロメチノレ)ベンゾニトリノレ
[0209] (2S, 3S)— 2, 3 ジメチルピロリジン— 3 オール 0· 5シユウ酸塩(228mg)、 4 —フルォロ 3 (トリフルォロメチル)ベンゾニトリル (397mg)、炭酸リチウム(206m g)を用いて、実施例 1と同様の操作を行い、表題化合物を無色油状物として得た (収 量: 220mg、収率: 55%)。
'H-NMRCCDCl ) δ :1.09 (3Η, d, J = 6. OHz) , 1.40 (3H, s), 1.71(1H, s
3
), 1.85-2.08 (2H, m) , 3.10— 3.20(1H, m) , 3.53(1H, q, J = 6.3Hz) , 3.80-3.95(1H, m) , 7.02(1H, d, J = 8.7Hz) , 7.61(1H, dd, J = 8.7, 2 . OHz), 7.87(1H, d, J = 2. OHz).
IR(KBr) :3441, 2975, 2222, 1615cm—1.
[0210] 実施例 4
4-[(2S, 3S)— 3 ヒドロキシー 2, 3 ジメチルピロリジン一 1—ィル]—2 メトキシ ベンゾニトリノレ
[0211] [化 76]
[0212] (2S, 3S)— 2, 3 ジメチルピロリジン— 3 オール 0· 5シユウ酸塩(228mg)、 4 —フルォロ 2 メトキシベンゾニトリル(317mg)、炭酸リチウム(206mg)を用いて、 実施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 170mg、収 率: 49%)。
'H-NMRCCDCl ) δ :1.22 (3Η, d, J = 6.6Hz) , 1.38 (3H, s), 1.92— 2.0
3
3(1H, m), 2.12-2.25(1H, m) , 3.20— 3.30(1H, m) , 3.45— 3.60 (2H , m), 3.89(3H, s), 5.96(1H, d, J = 2.4Hz) , 6.12(1H, dd, J = 9.0, 2.4 Hz), 7.31(1H, d, J = 9.0Hz) .
IR(KBr) :3441, 2975, 2218, 1622cm—1.
mp:117-118°C.
[0213] 実施例 5
2, 6—ジフルオロー 4— [(2S, 3S)— 3—ヒドロキシー 2, 3—ジメチルピロリジン 1 ィル]ベンゾニトリノレ
[0214] [化 77]
(2S, 3S)— 2, 3 ジメチノレピロリジン一 3 才一ノレ 0.5シユウ酸塩(300mg)、 2 , 4, 6 トリフルォロベンゾニトリル(882mg)、炭酸リチウム(276mg)を用いて、実 施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 263mg、収率 :56%)。
'H-NMRCCDCI ) δ :1.21 (3Η, d, J = 6.6Hz) , 1.38 (3H, s), 1.95— 2. 1
5(1H, m), 2.16-2.30(1H, m) , 3.15— 3.26(1H, m) , 3.40— 3.55(2H , m), 6.07(2H, d, J=10.8Hz) .
IR(KBr) :3526, 2982, 2226, 1651cm—1.
mp:142-143°C.
[0216] 実施例 6
4-[(2S, 3S)—3—ェチルー 3—ヒドロキシー2—メチルピロリジン 1ーィル ]—2 ーフノレオ口べンゾニトリノレ
[0217] [化 78]
[0218] (2S, 3S)— 3 ェチルー 2 メチルピロリジンー3 オール 0· 5シユウ酸塩(257 mg)、 2, 4 ジフノレ才口べンゾ、二卜リノレ(411mg)、炭酸リチウム(218mg)を用レヽて、 実施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 250mg、収 率: 68%)。
'H-NMRCCDCl ) δ :1.00 (3Η, t, J = 7.5Hz) , 1.21 (3H, d, J = 6.6Hz) ,
3
1.50-1.70 (3H, m), 2.00— 2.20 (2H, m) , 3.19(1H, q, J = 8.1Hz), 3. 40-3.50(1H, m), 3.59(1H, q, J = 6.3Hz) , 6.24(1H, dd, J=12.6, 2. 1Hz), 6.31(1H, dd, J = 8.7, 2.1Hz), 7.36(1H, t, J = 8.7Hz) .
IR(KBr) :3416, 2973, 2218, 1622cm—1.
mp:97— 98。C.
[0219] 実施例 7
4-[(2S, 3S)—3 ェチルー 3 ヒドロキシー2 メチルピロリジン 1ーィル ]—2,
6—ジフルォロベンゾニトリル
[0220] [化 79]
[0221] (2S, 3S)— 3 ェチルー 2 メチルピロリジンー3 オール 0· 5シユウ酸塩(257 mg)、2, 4, 6 トリフノレ才口べンゾ、二トリノレ(464mg)、炭酸リチウム(218mg)を用!/、 て、実施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 207mg 、収率: 53%)。
'H-NMRCCDCl ) δ :1.01 (3Η, t, J = 7.2Hz) , 1.21 (3H, d, J = 6.3Hz) ,
3
1.50-1.70 (3H, m), 2.00— 2.20 (2H, m) , 3.12— 3.26(1H, m) , 3.40 -3.60 (2H, m), 6.08 (2H, d, J = 8. 1Hz).
IR(KBr) :3596, 2942, 2222, 1644cm—1.
mp:140-141°C.
[0222] 実施例 8
4-[(2S, 3S)—3 ェチルー 3 ヒドロキシー2 メチルピロリジン 1ーィル ]—2 ーメトキシベンゾニトリノレ
[0223] [化 80]
[0224] (2S, 3S)— 3 ェチルー 2 メチルピロリジンー3 オール 0· 5シユウ酸塩(257 mg)、 4 フルォロ一 2 メトキシベンゾニトリル(447mg)、炭酸リチウム(218mg)を 用いて、実施例 1と同様の操作を行い、表題化合物を無色油状物として得た(収量: 305mg、収率: 79%)。
'H-NMRCCDCl ) δ :1.01 (3Η, t, J = 7.5Hz) , 1.50— 1.70 (3H, m), 2.0
3
0-2.20 (2H, m), 3.22(1H, q, J = 8. 1Hz), 3.44— 3.54(1H, m) , 3.62( 1H, q, J = 6.0Hz), 3.89(3H, m) , 5.97(1H, d, J = 2.1Hz), 6.13(1H, dd , J = 8.7, 2.1Hz), 7.32(1H, d, J = 8.7Hz) .
IR(KBr) :3615, 2973, 2209, 1613cm—1.
[0225] 実施例 9
4-[(2S, 3S)—3 ェチルー 3 ヒドロキシー2 メチルピロリジン 1ーィル ]—3 (トリフルォロメチル)ベンゾニトリノレ
[0226] [化 81]
(2S, 3S)— 3 ェチルー 2 メチルピロリジンー3 オール 0.5シユウ酸塩(257 mg)、 4 フルオロー 3 (トリフルォロメチノレ)ベンゾニトリノレ(419mg)、炭酸リチウム (218mg)を用いて、実施例 1と同様の操作を行い、表題化合物を無色油状物として 得た(収量: 218mg、収率:49%)。
'H-NMRCCDCl ) δ :1.00-1. 10(6H, m) , 1.50— 2.00 (5H, m) , 3.18(
3
1H, t, J = 8.7Hz), 3.59(1H, q, J = 6.3Hz) , 3.82— 3.98(1H, m) , 6.01
(1H, d, J = 8.7Hz), 7.60(1H, dd, J = 8.7, 2.1Hz), 7.86(1H, d, J = 2. 1 Hz).
IR(KBr) :3497, 2975, 2222, 1613cm—1.
[0228] 実施例 10
4-[(2S, 3S)—3 ェチルー 3 ヒドロキシー2 メチルピロリジン 1ーィル ]—2 フルォロ 3—メチルベンゾニトリノレ
[0229] [化 82]
[0230] (2S, 3S)— 3 ェチルー 2 メチルピロリジンー3 オール 0· 5シユウ酸塩(257 mg)、 2, 4 ジフノレ才ロー 3 メチノレベン、ノ、二卜リノレ(340mg)、炭酸リチウム(218m g)を用いて、実施例 1と同様の操作を行い、表題化合物を無色油状物として得た (収 量: 184mg、収率:47%)。
'H-NMRCCDCl ) δ :1.00-1.09(6H, m) , 1.50— 2.00 (5H, m) , 2.19(
3
3H, d, J = 2.7Hz), 2.98(1H, dt, J = 6.0, 1.5Hz) , 3.54(1H, q, J = 6.3H z), 3.84-3.95(1H, m) , 6.59(1H, d, J = 8.7Hz) , 7.29(1H, t, J = 8.7 Hz).
IR(KBr) :3499, 2971, 2222, 1615cm—1.
[0231] 実施例 11
4-[(2S, 3S)— 3 ヒドロキシ一 2—メチル 3 プロピルピロリジン一 1—ィル]—3 (トリフルォロメチル)ベンゾニトリノレ
[0232] [化 83]
[0233] (2S, 3S)— 2 メチル 3 プロピルピロリジン一 3 オール 0.5シユウ酸塩(25 Omg)、 4—フルオロー 3— (トリフルォロメチル)ベンゾニトリル(499mg)、炭酸リチウ ム(195mg)を用いて、実施例 1と同様の操作を行い、表題化合物を無色油状物とし て得た(収量: 383mg、収率: 93%)。
'H-NMRCCDCl ) δ :1.00 (3Η, t, J = 6.9Hz) , 1.08 (3H, d, J = 6.6Hz) ,
3
1.40-2.05(7H, m), 3. 18(1H, t, J = 9.0Hz) , 3.47(1H, q, J = 6.3Hz) , 3.80-3.92(1H, m) , 7.01(1H, d, J = 8.7Hz) , 7.61(1H, dd, J = 8.7, 2.4Hz), 7.87(1H, d, J = 2.4Hz) .
IR(KBr) :3486, 2961, 2222, 1613cm—1.
[0234] 実施例 12
2 フルオロー 4— [(2S, 3S)— 3 ヒドロキシ一 2—メチル 3 プロピルピロリジン 1 ィル]ベンゾニトリノレ
[0235] [化 84]
[0236] (2S, 3S)— 2 メチル 3 プロピルピロリジン一 3 オール 0.5シユウ酸塩(25 Omg)、 2, 4 ジフルォロベンゾニトリル(367mg)、炭酸リチウム(195mg)を用いて 、実施例 1と同様の操作を行い、表題化合物を無色油状物として得た(収量: 287mg 、収率: 83%)。
'H-NMRCCDCl ) δ :0.96 (3Η, t, J = 6.6Hz) , 1.20 (3H, d, J = 6.3Hz) ,
3
1.40-1.60(5H, m), 2.00— 2.20 (2H, m) , 3.15— 3.25(1H, m) , 3.42 -3.52(1H, m), 3.58(1H, q, J = 6.3Hz) , 6.24(1H, dd, J=12.6, 2. 1H z), 6.31(1H, dd, J = 8.7, 2.1Hz), 7.36(1H, t, J = 8.7Hz) .
IR(KBr) :3459, 2959, 2218, 1622cm—1.
[0237] 実施例 13
4-[(2S, 3S)— 3 ヒドロキシ一 2 メチル 3 プロピルピロリジン一 1—ィル]—2 ーメトキシベンゾニトリノレ
[0238] [化 85]
[0239] (2S, 3S)— 2 メチル 3 プロピルピロリジン一 3 オール 0.5シユウ酸塩(25 Omg)、 4 フルォロ一 2 メトキシベンゾニトリル(399mg)、炭酸リチウム(195mg) を用いて、実施例 1と同様の操作を行い、表題化合物を無色油状物として得た(収量 :303mg、収率: 83%)。
'H-NMRCCDCl ) δ :0.96 (3Η, t, J = 6.6Hz) , 1.21 (3H, d, J = 6.3Hz) ,
3
1.40-1.60(5H, m), 2.00— 2.20 (2H, m) , 3.23(1H, q, J=7.1Hz), 3. 45-3.55(1H, m), 3.62(1H, q, J = 6.3Hz) , 3.89(3H, s) , 5.97(1H, d, J = 2. 1Hz), 6.12(1H, dd, J = 8.7, 2. 1Hz), 7.32(1H, d, J = 8.7Hz) . IR(KBr) :3449, 2959, 2209, 1611cm—1.
[0240] 実施例 14
2, 6 ジフルオロー 4— [(2S, 3S)— 3 ヒドロキシー2—メチルー 3 プロピルピロ リジン 1 ィル]ベンゾニトリノレ
[0241] [化 86]
[0242] (2S, 3S)— 2 メチル 3 プロピルピロリジン一 3 オール 0.5シユウ酸塩(25 Omg)、 2, 4, 6 卜リフノレ才口ベンゾ、二卜リノレ(414mg)、炭酸リチウム(195mg)を用 いて、実施例 1と同様の操作を行い、表題化合物を無色油状物として得た(収量: 23 3mg、収率: 63%)。
'H-NMRCCDCl ) δ :0.96 (3Η, t, J = 6.9Hz) , 1.20 (3H, d, J = 6.6Hz) ,
3
1.40-1.60(5H, m), 2.00— 2.20 (2H, m) , 3.15— 3.25(1H, m) , 3.40 -3.47(1H, m), 3.54(1H, q, J = 6.2Hz) , 6.08 (2H, d, J=10.8Hz) . IR(KBr) :3459, 2963, 2226, 1644cm—1.
[0243] 実施例 15
2 クロ口一 4— [(2S, 3S)— 3 ヒドロキシー 2, 3 ジメチルピロリジン一 1—ィル] 3—メチルベンゾニトリノレ
[0244] [化 87]
[0245] (2S, 3S)— 2, 3—ジメチルピロリジン— 3—オール 0.5シユウ酸塩(260mg)、 2 —クロ口一 4—フルオロー 3—メチルベンゾニトリル(550mg)、炭酸リチウム(240mg )を用いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 320mg、収率: 75%)。
'H-NMRCCDCl ) δ :1.05(3H, d, J = 6.0Hz) , 1.41 (3H, s) , 1.69(1H, s
3
), 1.85-2.10(2H, m), 2.34 (3H, s) , 2.82(1H, dt, J = 9.6, 5.7Hz) , 3 .44(1H, q, J = 6.3Hz) , 3.80— 3.85(1H, m) , 6.78(1H, d, J = 8.7Hz) , 7.40(1H, d, J = 8.7Hz).
IR(KBr) :3609, 2975, 2230, 1586cm—1.
mp:109-110°C.
[0246] 実施例 16
2—クロ口一 4— [(2S, 3S)— 3—ヒドロキシー 2, 3—ジメチルピロリジン一 1—ィル] ベンゾニトリノレ
[0247] [化 88]
[0248] (2S, 3S)— 2, 3—ジメチノレピロリジン一 3—才一ノレ 0.5シユウ酸塩(1.50g)、 2 —クロ口一 4—フルォロベンゾニトリル(3· 04g)、炭酸リチウム(1.04g)を用いて、実 施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 1.70g、収率
:72%)。
'H-NMRCCDCl ) δ :1.21 (3H, d, J = 6.3Hz) , 1.37(3H, s), 1.63(1H, s
3
), 1.90-2.05(1H, m), 2.14— 2.25(1H, m) , 3. 15— 3.26(1H, m) , 3. 40-3.60 (2H, m), 6.41(1H, dd, J = 8.7, 1.8Hz) , 6.54(1H, d, J=l.8 Hz), 7.40(1H, d, J = 8.7Hz) .
IR(KBr) :3406, 2973, 2216, 1601cm—1.
mp:127-128°C.
[0249] 実施例 17
2 フルオロー 4— [(2S, 3S)— 3 ヒドロキシー2—メチルー 3 (トリフルォロメチル )ピロリジン 1 ィル]ベンゾニトリル
[0250] [化 89]
(2S, 3S)— 2—メチルー 3 (トリフルォロメチル)ピロリジンー3 オール 0· 5シ ユウ酸塩(200mg)、 2, 4 ジフルォロベンゾニトリル(258mg)、炭酸リチウム(138 mg)を用いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得た (収 量: 120mg、収率:45%)。
'H-NMRCCDCl ) δ :1.30 (3Η, d, J = 6.3Hz) , 2.20— 2.35(1H, m) , 2.
3
42-2.55(2H, m) , 3.35— 3.45(1H, m) , 3.50— 3.65(1H, m) , 4.10(1 H, q, J = 6.6Hz), 6.25— 6.37(2H, m) , 7.39(1H, dd, J = 8.7, 7.5Hz) .
IR(KBr) :3378, 2988, 2224, 1622cm ·
mp:148-149°C.
[0252] 実施例 18
2 クロロー 4— [(2S, 3S)— 3 ヒドロキシー2—メチルー 3 (トリフルォロメチル) ピロリジン 1 ィル]ベンゾニトリル
[0253] [化 90]
[0254] (2S, 3S)— 2 メチルー 3 (トリフルォロメチル)ピロリジンー3 オール 0.5シ ユウ酸塩(200mg)、 2 クロ口一 4 フルォロベンゾニトリル(289mg)、炭酸リチウム (138mg)を用いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得 た(収量: 100mg、収率: 35%)。
'H-NMRCCDCl ) δ :1.29 (3Η, d, J = 6.6Hz) , 2.20— 2.31(1H, m) , 2.
3
42-2.55(2H, m) , 3.36— 3.45(1H, m) , 3.56— 3.64(1H, m) , 4.12(1 H, q, J = 6.6Hz), 6.45(1H, dd, J = 8.7, 1.5Hz) , 6.58(1H, d, J=l.5Hz ), 7.44(1H, d, J = 8.7Hz).
IR(KBr) :3341, 2986, 2224, 1601cm—1.
mp:149-150°C.
[0255] 実施例 19
2 フルオロー 4— [(2S, 3S)— 3 ヒドロキシ一 2—イソプロピル一 3—メチルピロリ
[0257] (2S, 3S)—2 イソプロピルー3 メチルピロリジンー3 オール 0· 5シユウ酸塩
(150.6mg)、 2, 4 ジフノレ才口べンヽノ、二トリノレ(112mg)、炭酸リチウム(126mg)を 用いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 14 5mg、収率: 69%)。
'H-NMRCCDCl ) δ :0.95(3H, d, J = 6.9Hz) , 1.13(3H, d, J = 6.9Hz) ,
3
1.32 (3H, s), 1.58(1H, s) , 1.93— 2.00(1H, m) , 2.10— 2.34 (2H, m) , 3.10-3.19(1H, m), 3.27(1H, d, J = 5.7Hz) , 3.42— 3.49(1H, m) , 6 .25(1H, dd, J=12.6, 2.4Hz) , 6.32(1H, dd, J = 8.7, 2.4Hz) , 7.33(1 H, t, J = 8.7Hz).
IR(KBr) :3459, 2965, 2218, 1624, 1518cm—1.
[0258] 実施例 20
2, 6 ジフルオロー 4— [(2S, 3S)— 3 ヒドロキシー2 イソプロピルー3 メチル ピロリジン 1 ィル]ベンゾニトリル
[0259] [化 92]
[0260] (2S, 3S)—2 イソプロピルー3 メチルピロリジンー3 オール 0.5シユウ酸塩
(150.6mg)、 2, 4, 6 卜リフノレ才口べンヽノ、二卜リノレ(126mg)、炭酸リチウム(126m g)を用いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得た (収量 :168mg、収率: 75%)。
'H-NMRCCDCl ) δ :0.95(3H, d, J = 6.9Hz) , 1.13(3H, d, J = 6.9Hz) ,
3
1.32 (3H, s), 1.79(1H, s) , 1.94— 2.01(1H, m) , 2.11— 2.35(2H, m) , 3.10-3.19(1H, m), 3.22(1H, d, J = 5.7Hz) , 3.40— 3.48(1H, m) , 6 . 10(2H, d, J=ll.4Hz).
IR(KBr) :3433, 2967, 2226, 1644, 1524cm—1.
[0261] 実施例 21
4-[(2S, 3S)— 3 ヒドロキシ一 2—イソプロピル一 3—メチルピロリジン一 1—ィル] 2—メトキシベンゾニトリノレ
[0262] [化 93]
[0263] (2S, 3S)—2 イソプロピルー3 メチルピロリジンー3 オール 0· 5シユウ酸塩 (150.6mg)、 4ーフノレ才ロー 2 メ卜キシベンゾ、二卜リノレ(121mg)、炭酸リチウム(12 6mg)を用いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得た( 収量: 20mg、収率: 9. 1%)。
'H-NMRCCDCl ) δ :0.96 (3Η, d, J = 6.9Hz) , 1.13(3H, d, J = 6.9Hz) ,
3
1.32 (3H, s), 1.57(1H, s) , 1.92— 1.99(1H, m) , 2.15— 2.33 (2H, m) , 3.13-3.22(1H, m) , 3.31(1H, d, J = 5.4Hz) , 3.45— 3.52(1H, m) , 3 .88 (3H, s), 5.98(1H, d, J = 2.1Hz), 6. 13(1H, dd, J = 8.7, 2.1Hz), 7 .33(1H, d, J = 8.7Hz).
IR(KBr) :3447, 2961, 2211, 1609, 1518cm—1.
[0264] 実施例 22
2 クロ口一 4— [(2S, 3S)— 3 ヒドロキシ一 2—イソプロピル一 3—メチルピロリジン 1 ィル]ベンゾニトリノレ
[0265] [化 94]
(2S, 3S)— 2—イソプロピル一 3—メチルピロリジン一 3—オール 0· 5シユウ酸塩 (132mg)、 2 ク口口 4ーフノレ才口ベン、ノ、二卜リノレ(109mg)、炭酸リチウム(lllmg )を用いて、実施例 1と同様の操作を行い、表題化合物を無色油状物として得た(収
量: 133mg、収率: 68%)。
'H-NMRCCDCl ) δ :0.95(3H, d, J = 6.9Hz) , 1.13(3H, d, J = 6.9Hz) ,
3
1.32 (3H, s), 1.69(1H, s) , 1.93— 2.00(1H, m) , 2.11— 2.34 (2H, m) , 3.10-3.20(1H, m), 3.29(1H, d, J = 5.7Hz) , 3.43— 3.50(1H, m) , 6 .44(1H, dd, J = 9.0, 2.4Hz) , 6.56(1H, d, J = 2.4Hz) , 7.39(1H, d, J = 9.0Hz).
IR(KBr) :3451, 2965, 2218, 1599, 1510cm—1.
[0267] 実施例 23
4-[(2S, 3S)— 3—ェチルー 3—ヒドロキシー2—イソプロピルピロリジン 1ーィル ] 2, 6 ジフルォロベンゾニトリノレ
[0268] [化 95]
(2S, 3S)— 3 ェチル 2—イソプロピルピロリジン一 3—オール 0· 5シユウ酸塩 (203mg)、 2, 4, 6 卜リフノレ才ロベンゾ、二卜リノレ(157mg)、炭酸リチウム(163mg) を用いて、実施例 1と同様の操作を行い、表題化合物を無色油状物として得た(収量 :143mg、収率:49%)。
'H-NMRCCDCl ) δ :0.95(3H, d, J = 6.9Hz) , 0.96 (3H, t, J = 7.5Hz) ,
3
1. 12(3H, d, J = 6.9Hz), 1.47— 1.56 (2H, m) , 1.59(1H, s) , 2.07— 2. 26 (3H, m), 3.05— 3.15(1H, m) , 3.28(1H, d, J = 6.0Hz) , 3.39— 3.46 (1H, m), 6.09 (2H, d, J=ll.4Hz) .
IR(KBr) :3486, 2965, 2226, 1644, 1524cm
[0270] 実施例 24
4-[(2S, 3S)— 3 ェチル 3 ヒドロキシ一 2—
]一 2—メトキシベンゾニトリル
[0271] [化 96]
[0272] (2S, 3S)— 3 ェチルー 2 イソプロピルピロリジンー3 オール 0· 5シユウ酸塩
(203mg)、 4ーフノレ才ロー 2 メ卜キシベンゾ、二卜リノレ(151mg)、炭酸リチウム (163 mg)を用いて、実施例 1と同様の操作を行い、表題化合物を無色油状物として得た( 収量: 22mg、収率: 7.6%)0
'H-NMRCCDCl ) δ :0.95(3H, d, J = 6.6Hz) , 0.95(3H, t, J = 7.2Hz) ,
3
1. 13(3H, d, J = 6.6Hz), 1.47— 1.54 (2H, m) , 1.56(1H, s) , 2.03— 2. 25 (3H, m), 3.09— 3.18(1H, m) , 3.36(1H, d, J = 5.7Hz) , 3.43— 3.50 (1H, m), 3.88 (3H, s) , 5.97(1H, d, J = 2.1Hz), 6.13(1H, dd, J = 8.7, 2. 1Hz), 7.30(1H, d, J = 8.7Hz) .
IR(KBr) :3455, 2963, 2211, 1609, 1518cm—1.
[0273] 実施例 25
4-[(2S, 3S)— 3—ェチルー 3—ヒドロキシー2—イソプロピルピロリジン 1ーィル ]-2- (トリフルォロメチノレ)ベンゾニトリノレ
[0274] [化 97]
[0275] (2S, 3S)— 3 ェチルー 2 イソプロピルピロリジンー3 オール 0· 5シユウ酸塩
(203mg)、 4ーフノレ才ロー 2 (卜リフノレ才ロメチノレ)ベンゾ、二卜リノレ(189mg)、炭酸リ チウム(163mg)を用いて、実施例 1と同様の操作を行い、表題化合物を無色油状物 として得た(収量: 180mg、収率: 55%)。
'H-NMRCCDCl ) δ :0.95(3H, d, J = 6.9Hz) , 0.96 (3H, t, J = 7.2Hz) ,
3
1. 14(3H, d, J = 6.9Hz), 1.47— 1.56 (2H, m) , 1.64(1H, s) , 2.07— 2. 28 (3H, m), 3.11— 3.20(1H, m) , 3.40(1H, d, J = 5.7Hz) , 3.47— 3.54 (1H, m), 6.65(1H, dd, J = 8.7, 2.7Hz) , 6.80(1H, d, J = 2.7Hz) , 7.54 (1H, d, J = 8.7Hz).
IR(KBr) :3476, 2963, 2218, 1613, 1520cm—1.
[0276] 実施例 26
4-[(2S, 3S)— 3—ェチルー 3—ヒドロキシー2—イソプロピルピロリジン 1ーィル ]一 2—フルォロベンゾニトリノレ
[0277] [化 98]
[0278] (2S, 3S)— 3 ェチルー 2 イソプロピルピロリジンー3 オール 0· 5シユウ酸塩
(162mg)、 2, 4 ジフノレ才口ベンゾ、二トリノレ(112mg)、炭酸リチウム(126mg)を用 いて、実施例 1と同様の操作を行い、表題化合物を無色油状物として得た(収量: 13 6mg、収率: 62%)。
'H-NMRCCDCl ) δ :0.95(3H, d, J = 6.9Hz) , 0.95(3H, t, J = 7.3Hz) ,
3
1. 12(3H, d, J = 6.9Hz), 1.44— 1.55(2H, m) , 1.54(1H, s) , 2.04— 2. 26 (3H, m), 3.05— 3.15(1H, m) , 3.33(1H, d, J = 5.7Hz) , 3.40— 3.48 (1H, m), 6.24(1H, dd, J=12.9, 2.4Hz) , 6.32(1H, dd, J = 8.7, 2.4Hz ), 7.33(1H, t, J = 7.8Hz).
IR(KBr) :3472, 2963, 2218, 1624, 1518cm—1.
[0279] 実施例 27
2 クロ口一 4— [(2S, 3S)— 3 ェチル 3 ヒドロキシ一 2—イソプロピルピロリジ ン 1 ィル]ベンゾニトリノレ
[0280] [化 99]
[0281] (2S, 3S)— 3 ェチルー 2 イソプロピルピロリジンー3 オール 0.5シユウ酸塩
(162mg)、 2 ク口口 4ーフノレ才口ベン、ノ、二トリノレ(125mg)、炭酸リチウム(126mg )を用いて、実施例 1と同様の操作を行い、表題化合物を淡褐色油状物として得た( 収量: 151mg、収率: 65%)。
'H-NMRCCDCl ) δ :0.95(3H, d, J = 6.9Hz) , 0.95(3H, t, J = 7.4Hz) ,
3
1. 12(3H, d, J = 6.9Hz), 1.46— 1.55(2H, m) , 1.57(1H, s) , 2.04— 2. 26 (3H, m), 3.06— 3.15(1H, m) , 3.35(1H, d, J = 5.7Hz) , 3.41— 3.48 (1H, m), 6.43(1H, dd, J = 8.7, 2.4Hz) , 6.55(1H, d, J = 2.4Hz) , 7.38 (1H, t, J = 8.7Hz).
IR(KBr) :3465, 2963, 2218, 1599, 1508cm—1.
[0282] 実施例 28
4 [ (2 S , 3R)— 3 シクロプロピル 3—ヒドロキシ 2 イソプロピルピロリジン 1 ーィノレ ]—2, 6—ジフルォロベンゾニトリノレ
[0283] [化 100]
[0284] (2S, 3R)—3 シクロプロピルー2 イソプロピルピロリジンー3 オール 0.5シ ユウ酸塩(215mg)、 2, 4, 6 トリフルォロベンゾニトリル(157mg)、炭酸リチウム(1 63mg)を用いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得た( 収量: 115mg、収率: 38%)。
'H-NMRCCDCl ) δ :0.27-0.48 (4Η, m) , 0.94 (3Η, d, J = 6.9Hz) , 0.
3
94-1.04(1H, m), 1.10(3H, d, J = 6.9Hz) , 1.46(1H, s) , 2.06— 2.21 (2H, m), 2.25-2.36(1H, m) , 3. 16— 3.27(2H, m) , 3.42— 3.50(1H, m), 6.09 (2H, d, J=ll.4Hz) .
IR(KBr) :3486, 2961, 2226, 1644, 1522cm—1.
[0285] 実施例 29
4 [ (2 S , 3R)— 3 シクロプロピル 3—ヒドロキシ 2 イソプロピルピロリジン 1 ーィル ] 2—(トリフルォロメチノレ)ベンゾニトリノレ
[0286] [化 101]
[0287] (2S, 3R)—3 シクロプロピルー2 イソプロピルピロリジンー3 オール 0.5シ ユウ酸塩(215mg)、 4 フルォロ 2 (トリフルォロメチノレ)ベンゾニトリノレ(189mg) 、炭酸リチウム(163mg)を用いて、実施例 1と同様の操作を行い、表題化合物を淡 褐色固体として得た(収量: 227mg、収率: 67%)。
'H-NMRCCDCl ) δ :0.28-0.47 (4Η, m) , 0.94 (3Η, d, J = 6.9Hz) , 0.
3
94-1.07(1H, m), 1.11 (3H, d, J = 6.9Hz) , 1.56(1H, s) , 2.08— 2.25 (2H, m), 2.27-2.37(1H, m) , 3.23— 3.33 (2H, m) , 3.51— 3.58(1H, m), 6.67(1H, dd, J = 8.7, 2.4Hz) , 6.82(1H, d, J = 2.4Hz) , 7.55(1H, d, J = 8.7Hz).
IR(KBr) :3476, 2963, 2218, 1613, 1518cm—1.
[0288] 実施例 30
4 [ (2 S , 3R)— 3 シクロプロピル 3—ヒドロキシ 2 イソプロピルピロリジン 1 ーィル ] 2—フルォロベンゾニトリノレ
[0289] [化 102]
(2S, 3R)—3 シクロプロピノレー 2 イソプロピノレピロリジン一 3 ォーノレ 0.5シ ユウ酸塩(215mg)、 2, 4 ジフルォロベンゾニトリル(139mg)、炭酸リチウム(163 mg)を用いて、実施例 1と同様の操作を行い、表題化合物を淡褐色固体として得た( 収量: 114mg、収率:40%)。
'H-NMRCCDCl ) δ :0.24-0.46 (4Η, m) , 0.94 (3Η, d, J = 7.2Hz) , 0.
3
94-1.03(1H, m), 1.10(3H, d, J = 7.2Hz) , 1.49(1H, s) , 2.04— 2.21
(2H, m), 2.25-2.35(1H, m) , 3. 18— 3.27(2H, m) , 3.44— 3.51(1H: m), 6.25(1H, dd, J=12.9, 2.1Hz), 6.33(1H, dd, J = 8.7, 2.1Hz), 7. 34(1H, t, J = 8.3Hz).
IR(KBr) :3484, 2961, 2218, 1620, 1518cm—1.
[0291] 実施例 31
2 クロ口一 4— [(2S, 3R)—3 シクロプロピル一 3 ヒドロキシ一 2 イソプロピル ピロリジン 1 ィル]ベンゾニトリル
[0292] [化 103]
(2S, 3R)—3 シクロプロピノレー 2 イソプロピノレピロリジン一 3 ォーノレ 0.5シ ユウ酸塩(215mg)、 2 クロロー 4 フルォロベンゾニトリル(156mg)、炭酸リチウム (163mg)を用いて、実施例 1と同様の操作を行い、表題化合物を淡褐色固体として 得た(収量: 130mg、収率:43%)。
'H-NMRCCDCl ) δ :0.25-0.46 (4Η, m) , 0.94 (3Η, d, J = 7.2Hz) , 0.
3
94-1.01(1H, m), 1.10(3H, d, J = 7.2Hz) , 1.48(1H, s) , 2.05— 2.21 (2H, m), 2.24-2.35(1H, m) , 3. 18— 3.28 (2H, m) , 3.45— 3.52(1H, m), 6.44(1H, dd, J = 8.7, 2.4Hz) , 6.56(1H, d, J = 2.4Hz) , 7.39(1H, t, J = 8.7Hz).
IR(KBr) :3480, 2961, 2216, 1599, 1510cm—1.
[0294] 実施例 32
4— [ (2 S , 3R)— 3 シクロプロピル 3—ヒドロキシ 2 メチルピロリジン 1—ィ ノレ 2—フルォロベンゾニトリノレ
[0295] [化 104]
[0296] (2S, 3R)—3 シクロプロピル一 3 ヒドロキシ一 2 メチルピロリジン一 1—カルボ ン酸べンジル(1· 64g)、 50%含水 10%Pd/C(0.30g)を用いて、参考例 4と同 様の操作を行い、 (2S, 3R)— 3 シクロプロピル— 2 メチルピロリジン— 3 ォー ノレ 0· 5シユウ酸塩を無色固体として得た(収量: 677· 5mg、収率: 69%)。
(2S, 3R)— 3 シクロプロピル一 2 メチルピロリジン一 3 オール 0.5シユウ酸 塩(200mg)、 2, 4 ジフノレ才口ベンゾ、二卜リノレ(255mg)、炭酸リチウム(180mg)を 用いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 18 8mg、収率: 59%)。
'H-NMRCCDCl ) δ :0.30-0.58 (4Η, m) , 0.97— 1.13(1Η, m) , 1.20 (
3
3Η, d, J = 6.4Hz), 1.41(1Η, brs) , 1.95— 2.23 (2Η, m) , 3.21— 3.37(1 Η, m), 3.42-3.60 (2Η, m) , 6. 18— 6.39 (2Η, m) , 7.36(1Η, t, J = 8.2 Hz).
IR(KBr) :3443, 2975, 2218, 1549cm—1.
mp:112-113°C
[0297] 実施例 33
4— [ (2 S , 3R)— 3—シクロプロピル 3—ヒドロキシ 2—メチルピロリジン 1—ィ ノレ] 2, 6 ジフルォロベンゾニトリノレ
[0298] [化 105]
[0299] (2S, 3R)— 3 シクロプロピル一 2 メチルピロリジン一 3 オール 0.5シユウ酸 塩(200mg)、 2, 4, 6 卜リフノレ才口ベンゾ、二卜リノレ(288mg)、炭酸リチウム(180mg )を用いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 172mg、収率: 51%)。
'H-NMRCCDCl ) δ :0.31-0.45(2H, m) , 0.42— 0.57(2H, m) , 0.98
3
-1. 14(1H, m), 1.20 (3H, d, J = 6.4Hz) , 1.35(1H, s) , 1.97— 2.23(2 H, m), 3.21-3.35 (1H, m) , 3.40— 3.55 (2H, m) , 6.09 (2H, d, J=10. 9Hz).
IR(KBr) :3443, 2226, 1644, 1526cm—1.
mp:130-131°C
[0300] 実施例 34
4— [ (2 S , 3R)— 3 シクロプロピル 3—ヒドロキシ 2 メチルピロリジン 1—ィ ノレ ] 2—メトキシベンゾニトリノレ
[0301] [化 106]
[0302] (2S, 3R)— 3 シクロプロピル一 2 メチルピロリジン一 3 オール 0.5シユウ酸 塩(200mg)、 2 メ卜キシ 4ーフノレ才口ベンゾ、二卜リノレ(277mg)、炭酸リチウム(18 Omg)を用いて、実施例 1と同様の操作を行い、表題化合物を淡黄色固体として得た (収量: 192mg、収率: 58%)。
'H-NMRCCDCl ) δ :0.32-0.54 (4Η, m) , 1.00— 1.14(1Η, m) , 1.22(
3
3Η, d, J = 6.4Hz), 1.47— 1.55(1Η, m) , 1.96— 2.22 (2Η, m) , 3.24— 3 .39(1Η, m), 3.44— 3.63(2Η, m) , 3.89(3Η, s) , 5.98(1Η, d, J = 2.3Η ζ), 6.14(1Η, dd, J = 8.8, 2.3Hz) , 7.32(1Η, d, J = 8.9Hz) .
IR(KBr) :3486, 2975, 2209, 1615cm—1.
mp:115-116°C
[0303] 実施例 35
4 [ (2 S , 3R) 3—シクロプロピル 3—ヒドロキシ 2—メチルピロリジン 1—ィ ノレ] 2 フルォロ 3 メチルベンゾニトリノレ
[0304] [化 107]
[0305] (2S, 3R)— 3 シクロプロピル一 2 メチルピロリジン一 3 オール 0.5シユウ酸 塩(260mg)、 2, 4 ジフノレ才ロー 3 メチノレべンゾ、二卜リノレ(364mg)、炭酸リチウム (234mg)を用いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得 た(収量: 106mg、収率: 24%)。
'H-NMRCCDCl ) δ :0.34-0.48(1H, m) , 0.43— 0.63(3H, m) , 0.96
3
-1.09(1H, m), 1.11 (3H, d, J = 6.2Hz) , 1.43(1H, s) , 1.69— 1.82(2 H, m), 2.18(3H, d, J = 2.6Hz) , 2.92— 3.06(1H, m) , 3.69(1H, q, J = 6 .2Hz), 3.84-3.98(1H, m) , 6.61(1H, d, J = 8.5Hz) , 7.23— 7.37(1H , m) .
IR(KBr) :3486, 2975, 2224, 1613cm—1.
mp:127-128°C
[0306] 実施例 36
2 フルォロ一 4— [(2S, 3R)—3 ヒドロキシ一 2 メチル 3—ビュルピロリジン一 1 ィル]ベンゾニトリノレ
[0307] [化 108]
[0308] (2S, 3R)—3 ヒドロキシ一 2 メチル 3—ビュルピロリジン一 1—カルボン酸 t ert ブチル(684mg, 2.85mmol)にトリフルォロ酢酸(3. Oml)を加えた。混合液 を室温で 15分間攪拌した後、減圧濃縮し、(2S, 3R)— 2 メチル—3—ビュルピロ リジンー3—オールを得た(収量: 1. llg)。
(2S, 3R)— 2 メチル 3—ビュルピロリジン一 3 オール(554mg)、 2, 4 ジフ ルォ口べンゾニトリル(300mg)、炭酸リチウム(350mg)を用いて、実施例 1と同様の 操作を行い、表題化合物を無色固体として得た(収量: 177mg、収率: 50%)。 'H-NMRCCDCl ) δ :1.23 (3Η, d, J = 6.4Hz) , 1.78— 1.91(1H, m) , 2.
3
02-2.17(1H, m), 2.15— 2.31(1H, m) , 3.19— 3.33(1H, m) , 3.49— 3.62(1H, m), 3.71(1H, q, J = 6.4Hz) , 5.20(1H, d, J=10.7Hz) , 5.31 (1H, d, J=17.3Hz), 6.00(1H, dd, J=17.3, 10.7Hz) , 6.26(1H, dd, J = 12.7, 2.4Hz), 6.34(1H, dd, J = 8.7, 2.4Hz) , 7.30— 7.42(1H, m) . IR(KBr) :3436, 2980, 2218, 1620cm—1.
mp:85-86°C
[0309] 実施例 37
2 フルォロ一 4— [(2S, 3R)—3 ヒドロキシ一 2 メチル 3—ビュルピロリジン一 1 ィル] 3—メチルベンゾニトリノレ
[0310] [化 109]
[0311] (2S, 3R)— 2 メチル 3—ビュルピロリジン一 3 オール(556mg)、 2, 4 ジフ ノレォロ一 3 メチルベンゾニトリル(350mg)、炭酸リチウム(350mg)を用いて、実施 例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 84.6mg、収率 :23%)。
'H-NMRCCDCl ) δ :1.03 (3Η, d, J = 6.4Hz) , 1.75(1H, s) , 1.90— 2. 1
3
4(2H, m), 2.20 (3H, d, J = 2.7Hz) , 2.97— 3.12(1H, m) , 3.66(1H, q, J = 6.4Hz), 3.94-4.08(1H, m) , 5.29(1H, d, J=ll.7Hz) , 5.48(1H, d, J=16.3Hz), 5.88-6.05(1H, m) , 6.60(1H, d, J = 8.7Hz) , 7.23— 7 .36(1H, m).
IR(KBr) :3480, 2976, 2224, 1615cm—1.
mp:114-115°C
[0312] 実施例 38
4-[(2S, 3S)—2 ェチルー 3 ヒドロキシー3 メチルピロリジン 1ーィル ]—2 ーフノレオ口べンゾニトリノレ
[0313] [化 110]
[0314] (2S, 3S)— 2 ェチルー 3 メチルピロリジンー3 オール 0· 5シユウ酸塩(200 mg)、 2, 4 ジフノレ才口べンゾ、二卜リノレ(240mg)、炭酸リチウム(187mg)を用レヽて、 実施例 1と同様の操作を行い、表題化合物を淡黄色油状物として得た (収量: 188. 6mg、収率: 66%)。
'H-NMRCCDCl ) δ :1.02 (3Η, t, J = 7.6Hz) , 1.37(3H, s) , 1.48— 1.7
3
2(2H, m), 1.72-1.91(1H, m) , 1.91— 2.07(1H, m) , 2. 13— 2.32(1H , m), 3.09-3.25(1H, m) , 3.31(1H, dd, J=8.0, 3.8Hz) , 3.39— 3.53 (1H, m), 6.21(1H, dd, J=12.9, 2.3Hz) , 6.29(1H, dd, J = 8.7, 2.3 Hz ), 7.29-7.43(1H, m) .
IR(KBr) :3438, 2969, 2218, 1520cm—1.
[0315] 実施例 39
4-[(2S, 3S)—2 ェチルー 3 ヒドロキシー3 メチルピロリジン 1ーィル ]—2, 6—ジフルォロベンゾニトリノレ
[0317] (2S, 3S)— 2 ェチルー 3 メチルピロリジンー3 オール 0· 5シユウ酸塩(200 mg)、2, 4, 6 トリフノレ才口べンゾ、二トリノレ(270mg)、炭酸リチウム(187mg)を用レヽ て、実施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 187.5 mg、収率: 61%)。
'H-NMRCCDCl ) δ :1.02 (3Η, t, J = 7.4Hz) , 1.37(3H, s) , 1.49— 1.6
3
7(2H, m), 1.73-1.91(1H, m) , 1.92— 2.07(1H, m) , 2. 15— 2.30(1H , m), 3.12-3.24(1H, m) , 3.27(1H, dd, J = 8.0, 3.8Hz) , 3.38— 3.51 (1H, m), 6.06 (2H, d, J=ll.4Hz) .
IR(KBr) :3457, 2971, 2226, 1644cm—1.
mp:104-105°C
[0318] 実施例 40
4-[(2S, 3S)—2 ェチルー 3 ヒドロキシー3 メチルピロリジン 1ーィル ]—2 (トリフルォロメチル)ベンゾニトリノレ
[0319] [化 112]
[0320] (2S, 3S)— 2 ェチルー 3 メチルピロリジンー3 オール 0· 5シユウ酸塩(200 mg)、 4 フルオロー 2 (トリフルォロメチノレ)ベンゾニトリノレ(325mg)、炭酸リチウム (187mg)を用いて、実施例 1と同様の操作を行い、表題化合物を淡黄色油状物とし て得た(収量: 306.6mg、収率: 90%)。
'H-NMRCCDCl ) δ :1.03 (3Η, t, J = 7.6Hz) , 1.38 (3H, s) , 1.48— 1.7
3
4(2H, m), 1.74-1.93(1H, m) , 1.95— 2.07(1H, m) , 2. 17— 2.33(1H , m), 3.14-3.31(1H, m) , 3.38(1H, dd, J=7.6, 3.8Hz) , 3.46— 3.58 (1H, m), 6.61(1H, dd, J = 8.7, 2.3Hz) , 6.78(1H, d, J = 2.3Hz) , 7.57 (1H, d, J=8.7Hz).
IR(KBr) :3438, 2971, 2218, 1615cm—1.
[0321] 実施例 41
2—クロ口一 4— [(2S, 3S)— 2—ェチル 3—ヒドロキシ一 3—メチルピロリジン一 1 ィル]ベンゾニトリノレ
[0322] [化 113]
[0323] (2S, 3S)— 2 ェチルー 3 メチルピロリジンー3 オール 0· 5シユウ酸塩(195 mg)、 2 クロ口一 4 フルォロベンゾニトリル(320mg)、炭酸リチウム(200mg)を用 いて、実施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 221. 4mg、収率: 75%)。
'H-NMRCCDCl ) δ :1.02 (3Η, t, J = 7.4Hz) , 1.37(3H, s) , 1.48— 1.6
3
7(1H, m), 1.63-1.89(2H, m) , 1.91— 2.09(1H, m) , 2. 13— 2.30(1H , m), 3.10-3.25(1H, m) , 3.33(1H, dd, J=7.8, 3.6Hz) , 3.40— 3.54 (1H, m), 6.35-6.45(1H, m) , 6.53(1H, d, J = 2.3Hz) , 7.40(1H, d, J =8.7Hz).
IR(KBr) :3413, 2969, 2216, 1599cm—1.
mp:77-78°C
[0324] 実施例 42
4-[(2S, 3S)—2 ェチルー 3 ヒドロキシー3 メチルピロリジン 1ーィル ]—2 ーメトキシベンゾニトリノレ
[0325] [化 114]
[0326] (2S, 3S)— 2 ェチルー 3 メチルピロリジンー3 オール 0· 5シユウ酸塩(210 mg)、 4 フルォロ一 2 メトキシベンゾニトリル(320mg)、炭酸リチウム(210mg)を 用いて、実施例 1と同様の操作を行い、表題化合物を淡黄色固体として得た(収量: 195.8mg、収率: 62%)。
'H-NMRCCDCl ) δ :1.03 (3Η, t, J = 7.6Hz) , 1.37(3H, s) , 1.51— 1.7
3
2(1H, m), 1.73-1.91 (2H, m) , 1.91— 2.03(1H, m) , 2. 13— 2.29(1H , m), 3.13-3.28(1H, m) , 3.33(1H, dd, J=8.0, 3.4Hz) , 3.42— 3.56 (1H, m), 3.88 (3H, s) , 5.96(1H, d, J=l.9Hz) , 6.10(1H, dd, J = 8.7, 1.9Hz), 7.31(1H, d, J = 8.7Hz) .
IR(KBr) :3439, 2967, 2209, 1613cm—1.
mp:110-lll°C
[0327] 実施例 43
2 クロ口一 4— [(2S, 3S)— 2 ェチル 3 ヒドロキシ一 3 メチルピロリジン一 1 ィル] 3—メチルベンゾニトリノレ
[0328] [化 115]
[0329] (2S, 3S)— 2 ェチルー 3 メチルピロリジンー3 オール 0· 5シユウ酸塩(210 mg)、2 クロ口一 4 フルォロ 3 メチルベンゾニトリル(300mg)、炭酸リチウム( 215mg)を用いて、実施例 1と同様の操作を行い、表題化合物を淡黄色油状物とし て得た(収量: 91.2mg、収率: 27%)。
'H-NMRCCDCl ) δ :0.96 (3Η, t, J = 7.8Hz) , 1.37— 1.53(1H, m) , 1.5
3
0(3H, s), 1.61-1.76 (2H, m) , 1.86— 2.02 (2H, m) , 2.33 (3H, s) , 2. 76-2.88(1H, m), 3.34(1H, dd, J = 8.3, 3.0Hz) , 3.74— 3.92(1H, m) , 6.78(1H, d, J = 8.7Hz), 7.40(1H, d, J = 8.7Hz) .
IR(KBr) :3478, 2969, 2220, 1586cm—1.
[0330] 実施例 44
2 フルオロー 4— [(2S, 3S)— 2 ェチルー 3 ヒドロキシー3 メチルピロリジン 1 ィル] 3—メチルベンゾニトリノレ
[0331] [化 116]
[0332] (2S, 3S)— 2—ェチルー 3—メチルピロリジンー3—オール 0· 5シユウ酸塩(220 mg)、 2, 4—ジフノレ才ロー 3—メチノレベン、ノ、二卜リノレ(290mg)、炭酸リチウム(210m g)を用いて、実施例 1と同様の操作を行い、表題化合物を淡黄色油状物として得た( 収量: 97.3mg、収率: 29%)。
'H-NMRCCDCl ) δ :0.97(3H, t, J = 7.8Hz) , 1.41— 1.55(1H, m) , 1.5
3
0(3H, s), 1.60-1.75(2H, m) , 1.86— 2.00 (2H, m) , 2.18(3H, d, J = 2 .7Hz), 2.89-3.03(1H, m) , 3.40(1H, dd, J = 8.5, 3.2Hz) , 3.80— 3. 95(1H, m), 6.59(1H, d, J = 8.7Hz) , 7.23— 7.35(1H, m) .
IR(KBr) :3478, 2967, 2224, 1615cm—1.
[0333] 実施例 45
4-[(2S, 3S)— 2, 3—ジェチルー 3—ヒドロキシピロリジン一 1—ィル]—2—フルォ 口べンゾニトリノレ
[0334] [化 117]
(2S, 3S)— 2, 3—ジェチルピロリジン— 3—オール 0· 5シユウ酸塩(196mg)、 2 , 4ージフルォロベンゾニトリル(284mg)、炭酸リチウム(202mg)を用いて、実施例 1と同様の操作を行い、表題化合物を淡黄色油状物として得た (収量: 208mg、収率 :76%)。
H-NMR(CDC1 ) δ :0.92— 1.08 (6H, m) , 1.48— 1.67(3H, m) , 1.65
3
-1.93 (2H, m), 2.01— 2.23 (2H, m) , 3.07— 3.22(1H, m) , 3.31— 3. 52 (2H, m), 6.16— 6.26(1H, m) , 6.25— 6.34(1H, m) , 7.34(1H, t, J =8. 1Hz).
IR(KBr) :3470, 2969, 2218, 1520cm—1.
[0336] 実施例 46
4-[(2S, 3S)— 2, 3—ジェチルー 3—ヒドロキシピロリジン一 1—ィル]—2, 6—ジ フノレオ口べンゾニトリノレ
[0337] [化 118]
[0338] (2S, 3S)— 2, 3—ジェチルピロリジン— 3—オール 0· 5シユウ酸塩(197mg)、 2 , 4, 6—トリフルォロベンゾニトリル(295mg)、炭酸リチウム(192mg)を用いて、実 施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 157mg、収率 :54%)。
'H-NMRCCDCl ) δ :0.92-1.08 (6Η, m) , 1.45— 1.76 (4Η, m) , 1.75
3
-1.94(1Η, m), 2.02— 2.23 (2Η, m) , 3.07— 3.22(1Η, m) , 3.32(1Η, dd, J = 7.8, 3.6Hz), 3.36— 3.49(1Η, m) , 6.05(2Η, d, J=ll. ΟΗζ) . IR(KBr) :3457, 2971, 2226, 1644cm—1.
mp: 66— 67°C
[0339] 実施例 47
4-[(2S, 3S)— 2, 3 ジェチルー 3 ヒドロキシピロリジン一 1—ィル]—2— (トリフ ノレオロメチノレ)ベンゾニトリノレ
[0340] [化 119]
[0341] (2S, 3S)—2, 3 ジェチルピロリジンー3 オール 0· 5シユウ酸塩(193mg)、 4 フルォロ 2 (トリフルォロメチノレ)ベンゾニトリノレ(364mg)、炭酸リチウム(221m g)を用いて、実施例 1と同様の操作を行い、表題化合物を淡黄色油状物として得た( 収量: 219mg、収率: 82%)。
'H-NMRCCDCl ) δ :0.93-1.08 (6Η, m) , 1.47— 1.69(3Η, m) , 1.69
3
-1.97(2Η, m), 2.02— 2.25(2Η, m) , 3.13— 3.29(1Η, m) , 3.36— 3. 57 (2Η, m), 6.61(1Η, dd, J = 8.7, 2.7Hz) , 6.78(1Η, d, J = 2.7Hz) , 7. 56(1Η, d, J = 8.7Hz).
IR(KBr) :3457, 2969, 2218, 1615cm—1.
[0342] 実施例 48
2 クロ口一 4— [(2S, 3S)— 2, 3 ジェチルー 3 ヒドロキシピロリジン一 1—ィル] ベンゾニトリノレ
[0343] [化 120]
[0344] (2S, 3S)— 2, 3 ジェチルピロリジンー3 オール 0· 5シユウ酸塩(204mg)、 2 クロロー 4 フルォロベンゾニトリル(314mg)、炭酸リチウム(205mg)を用いて、 実施例 1と同様の操作を行い、表題化合物を淡黄色油状物として得た (収量: 262m g、収率: 87%)。
'H-NMRCCDCl ) δ :0.92-1.06 (6Η, m) , 1.47— 1.66 (3H, m) , 1.62
3
-1.75(1H, m), 1.74— 1.94(1H, m) , 1.99— 2.22 (2H, m) , 3.07— 3. 24(1H, m), 3.33— 3.51 (2H, m) , 6.39(1H, dd, J = 8.8, 2.3Hz) , 6.52 (1H, d, J = 2.3Hz), 7.40(1H, d, J = 8.8Hz) .
IR(KBr) :3478, 2967, 2216, 1599cm—1.
[0345] 実施例 49
4-[(2S, 3S)— 2, 3—ジェチルー 3—ヒドロキシピロリジン一 1—ィル]—2—メトキ シベンゾニトリノレ
[0346] [化 121]
[0347] (2S, 3S)—2, 3 ジェチルピロリジンー3 オール 0· 5シユウ酸塩(201mg)、 4 —フルォロ一 2 メトキシベンゾニトリル(250mg)、炭酸リチウム(180mg)を用いて、 実施例 1と同様の操作を行い、表題化合物を無色固体として得た(収量: 158mg、収 率: 54%)。
'H-NMRCCDCl ) δ :0.93-1.07(6H, m) , 1.49— 1.69(3H, m) , 1.69
3
-1.93 (2H, m), 2.01— 2.22 (2H, m) , 3.10— 3.25(1H, m) , 3.32— 3. 52 (2H, m), 3.88 (3H, s) , 5.91— 5.98(1H, m) , 6.10(1H, dd, J = 8.7, 2.3Hz), 7.24-7.36(1H, m) .
IR(KBr) :3438, 2967, 2209, 1613cm—1.
mp:91-92°C
[0348] 実施例 50
2—クロ口一 4— [(2S, 3S)— 2, 3—ジェチルー 3—ヒドロキシピロリジン一 1—ィル] 3—メチルベンゾニトリノレ
[0349] [化 122]
[0350] (2S, 3S)— 2, 3 ジェチルピロリジンー3 オール 0· 5シユウ酸塩(201mg)、 2 —クロ口一 4 フルオロー 3 メチルベンゾニトリノレ(294mg)、炭酸リチウム(250mg )を用いて、実施例 1と同様の操作を行い、表題化合物を淡黄色油状物として得た( 収量: 95.6mg、収率: 31%)。
'H-NMRCCDCl ) δ :0.93 (3Η, t, J = 7.5Hz) , 1.06 (3H, t, J = 7.5Hz) ,
3
1.33-1.51(1H, m), 1.54-1.78 (3H, m) , 1.78— 1.99 (3H, m) , 2.33 (3H, s), 2.79-2.92(1H, m) , 3.40(1H, dd, J = 8.1, 3.2Hz) , 3.75— 3 .91(1H, m), 6.78(1H, d, J = 8.7Hz) , 7.39(1H, d, J = 8.7Hz) .
IR(KBr) :3476, 2969, 2220, 1586cm—1.
[0351] 実施例 51
2 フルオロー 4— [(2S, 3S)— 2, 3 ジェチルー 3 ヒドロキシピロリジン一 1—ィ ノレ] 3—メチルベンゾニトリノレ
[0352] [化 123]
[0353] (2S, 3S)— 2, 3 ジェチルピロリジンー3 オール 0· 5シユウ酸塩(200mg)、 2 , 4 ジフルォロ 3 メチルベンゾニトリル(279mg)、炭酸リチウム(220mg)を用 いて、実施例 1と同様の操作を行い、表題化合物を淡黄色油状物として得た(収量: 151mg、収率: 52%)。
'H-NMRCCDCl ) δ :0.94 (3Η, t, J = 7.6Hz) , 1.06 (3H, t, J = 7.4Hz) ,
3
1.37-1.53(1H, m), 1.54— 1.78 (3H, m) , 1.78— 2.00 (3H, m) , 2.18 (3H, d, J = 2.4Hz), 2.92— 3.06(1H, m) , 3.46(1H, dd, J = 8.3, 2.2Hz ), 3.79-3.95(1H, m) , 6.59(1H, d, J = 8.7Hz) , 7.23— 7.35(1H, m) . IR(KBr) :3478, 2969, 2224, 1613cm—1.
[0354] 実施例 52
4 [ (2 S , 3R)— 3 シクロプロピル 2 ェチル 3—ヒドロキシピロリジン 1—ィ ノレ 2—メトキシベンゾニトリノレ
[0355] [化 124]
[0356] (2S, 3R)—3 シクロプロピルー2 ェチルピロリジンー3 オール 0.5シユウ酸 塩(185mg)、 4 フルォロ 2 メトキシベンゾニトリル(290mg)、炭酸リチウム(19 8mg)を用いて、実施例 1と同様の操作を行い、表題化合物を淡黄色固体として得た (収量: 144mg、収率: 55%)。
'H-NMRCCDCl ) δ :0.27-0.52 (4Η, m) , 0.95— 1.13(1Η, m) , 1.00 (
3
3Η, t, J = 7.4Hz), 1.32-1.38(1Η, m) , 1.48— 1.66(1Η, m) , 1.72— 1 .89(1Η, m), 2.00— 2.13(1Η, m) , 2.14— 2.29(1Η, m) , 3.19— 3.34 ( 2Η, m), 3.43-3.54(1Η, m) , 3.89(3Η, s) , 5.95(1Η, d, J = 2.3Hz) , 6 . 10(1Η, dd, J=8.7, 2.3Hz) , 7.33(1Η, d, J = 8.7Hz) .
IR(KBr) :3461, 2965, 2211, 1609cm—1.
mp:140-141°C
[0357] 実施例 53
rac-4-[(2R, 3S)— 3—ヒドロキシー 2, 4, 4—トリメチノレピロリジン 1ーィノレ] 2—メトキシベンゾニトリノレ
[0358] [化 139]
[0359] (2R, 3S)— 2, 4, 4 卜リメチノレピロリジン 3 才一ノレ 0.5シユウ酸塩(152mg) 、 4 フルォロ 2 メトキシベンゾニトリノレ(183mg)と炭酸リチウム(155mg)の DM SO懸濁液(5mL)を 100°Cで 15時間攪拌した後、反応液を水に加え、酢酸ェチル で抽出した。抽出液を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥後、減圧 濃縮した。残留物をシリカゲルカラムクロマトグラフィー(展開溶媒:へキサン/酢酸ェ チル = 50/1→2/3)にて精製することで表題化合物を無色固体として得た (収量: 103mg、収率:45%)。
'H-NMRCCDCl ) δ :0.99 (3Η, s), 1.17(3H, s) , 1.39(3H, d, J = 6.0Hz
3
), 1.70(1H, d, J = 6.0Hz), 3.17— 3.33 (2H, m) , 3.54— 3.72 (2H, m) , 3.88 (3H, s), 5.96(1H, d, J = 7.2Hz) , 6. 11(1H, dd, J=8.7, 2.1Hz), 7.32(1H, d, J = 8.7Hz).
IR(KBr) :3418, 2963, 2211, 1609cm—1.
mp:139-142°C.
[0360] 実施例 54
rac-4-[(2R, 3S)— 3 ヒドロキシー 2, 4, 4 トリメチノレピロリジン 1ーィノレ] 2—(トリフルォロメチル)ベンゾニトリノレ
[0361] [化 140]
[0362] (2R, 3S)— 2, 4, 4 トリメチルピロリジン一 3 オール 0· 5シユウ酸塩(146mg) 、 4 フルォロ 2 (トリフルォロメチノレ)ベンゾニトリノレ(255mg)と炭酸リチウム(14 Omg)を用いて、実施例 53と同様の操作を行うことで表題化合物を無色固体として得 た(収量: 106mg、収率: 42%)。
'H-NMRCCDCl ) δ :0.99 (3Η, s), 1.19(3H, s) , 1.40 (3H, d, J = 6. OHz
3
), 1.81(1H, d, J = 5.7Hz), 3.19— 3.38 (2H, m) , 3.57— 3.76 (2H, m) , 6.63(1H, dd, J = 8.5, 2.4Hz) , 6.79(1H, d, J = 2.4Hz) , 7.57(1H, d, J =8.5Hz).
IR(KBr) :3430, 2967, 2220, 1613cm—1.
mp:115-116°C.
[0363] 実施例 55
。ー2—フルォロー4 [(21^, 3S)— 3 ヒドロキシー 2, 4, 4 トリメチルピロリジン 1 ィル] 3—メチルベンゾニトリノレ
[0364] [化 141]
[0365] (2RS, 3SR)— 2, 4, 4 トリメチルピロリジン— 3 オール 0· 5シユウ酸塩(214 mg)、 2, 4 ジフルオロー 3 メチルベンゾニトリノレ(240mg)と炭酸リチウム(246m g)を用いて、実施例 53と同様の操作を行うことで表題化合物を無色固体として得た( 収量: 112mg、収率: 35%)。
'H-NMRCCDCl ) δ :0.95(3H, s) , 1.13(3H, s) , 1.18(3H, d, J = 5.7Hz
3
), 1.68(1H, d, J = 6.1Hz), 2.13(3H, d, J = 2.3Hz) , 2.91(1H, d, J = 9. 5Hz), 3.51(1H, d, J = 9.5Hz) , 3.55— 3.71 (2H, m) , 6.54(1H, d, J = 8 .3Hz), 7.23-7.33(1H, m) .
IR(KBr) :3428, 2967, 2224, 1613cm—1.
mp:118-119°C.
[0366] 実施例 56
4-[(2S, 3S, 5R)— 3—ヒドロキシ一 2, 5—ジメチルピロリジン一 1—ィル]—2—メ トキシベンゾニトリノレ
[0367] [化 142]
(2S, 3S, 5R)— 2, 5 ジメチルピロリジンー3 オール 0· 5シユウ酸塩(62mg) 、 4 フルォロ 2 メトキシベンゾニトリル(70mg)と炭酸リチウム(63mg)を用いて 、実施例 53と同様の操作を行うことで表題化合物を無色固体として得た(収量: 7mg 、収率: 7.3%)。
'H-NMRCCDCI ) δ :1.28 (3Η, d, J = 6.4Hz) , 1.37(3H, d, J = 6.1Hz),
1.75-1.90(1H, m), 1.95— 2.05(1H, m) , 2.43— 2.57(1H, m) , 3.77 -3.96 (2H, m), 3.87(3H, s) , 4.38(1H, q, J = 7.4Hz) , 6.00— 6.05(1 H, m), 6.17(1H, dd, J = 8.7, 1.9Hz) , 7.31(1H, d, J = 8.7Hz).
IR(KBr) :3426, 2973, 2211, 1609cm—1.
[0369] 実施例 57
2—クロ口一 4— [(2S, 3S, 5R)— 3—ヒドロキシ一 2, 5—ジメチルピロリジン一 1—ィ ノレ]ベン 二トリノレ
[0370] [化 143]
[0371] (2S, 3S, 5R)—2, 5—ジメチルピロリジンー3—オール 0· 5シユウ酸塩(144mg )、 2—クロ口一 4—フルォロベンゾニトリル(254mg)と炭酸リチウム(193mg)を用い て、実施例 53と同様の操作を行うことで表題化合物を無色油状物として得た (収量: 61mg、収率: 27%)。
'H-NMRCCDCl ) δ :1.27(3H, d, J = 6.4Hz) , 1.36 (3H, d, J = 6.4Hz) ,
3
1.61-1.71(1H, m), 1.75— 1.91(1H, m) , 2.43— 2.59(1H, m) , 3.74 -3.93 (2H, m), 4.32— 4.45(1H, m) , 6.46(1H, dd, J = 8.8, 2.4Hz) , 6 .59(1H, d, J = 2.4Hz), 7.41(1H, d, J = 8.8Hz) .
IR(KBr) :3401, 2218, 1599cm—1.
[0372] 実施例 58
4-[(2S, 3S, 5R)— 3—ヒドロキシ一 2, 5—ジメチルピロリジン一 1—ィル]—2— ( トリフルォロメチノレ)ベンゾニトリノレ
[0373] [化 144]
[0374] (2S, 3S, 5R)—2, 5 ジメチルピロリジンー3 オール 0· 5シユウ酸塩(153mg )、 4 フルォロ 2 (トリフルォロメチル)ベンゾニトリル(277mg)と炭酸リチウム(2 OOmg)を用いて、実施例 53と同様の操作を行うことで表題化合物を無色油状物して 得た(収量: 121 mg、収率: 45 % )。
'H-NMRCCDCl ) δ :1.30 (3Η, d, J = 6.4Hz) , 1.38 (3H, d, J = 6.4Hz) ,
3
1.65-1.73(1H, m), 1.77— 1.94(1H, m) , 2.43— 2.61(1H, m) , 3.80 -3.98 (2H, m), 4.33— 4.49(1H, m) , 6.68(1H, dd, J = 8.8, 2.5Hz) , 6 .84(1H, d, J = 2.5Hz), 7.57(1H, d, J = 8.8Hz) .
IR(KBr) :3407, 2220, 1611cm-1.
[0375] 実施例 59
2 フルオロー 4— [(2S, 3S, 5R)— 3 ヒドロキシ一 2, 5 ジメチルピロリジン一 1 ィル] 3—メチルベンゾニトリノレ
[0376] [化 145]
[0377] (2S, 3S, 5R)-2, 5 ジメチノレピロリジン一 3 才一ノレ 0.5シユウ酸塩(189mg )、 2, 4 ジフルオロー 3 メチルベンゾニトリル(510mg)と炭酸リチウム(200mg)を 用いて、実施例 53と同様の操作を行うことで表題化合物を無色油状物として得た(収 量: 20mg、収率: 6.8%)。
'H-NMRCCDCl ) δ :0.92 (3Η, d, J = 6.4Hz) , 1.00 (3H, d, J = 6.1Hz),
3
1.50-1.68 (2H, m), 1.72— 1.85(1H, m) , 2.25— 2.36 (3H, m) , 3.02 -3.21 (2H, m), 4.15(1H, brs) , 7.05— 7.16(1H, m) , 7.40(1H, t, J = 8.0Hz).
IR(KBr) :3382, 2222, 1615cm—1.
[0378] 実施例 60
2—クロ口一 4— [(2S, 3S, 5R)— 3—ヒドロキシ一 2, 3, 5—トリメチルピロリジン一 1 ィル]ベンゾニトリノレ
[0379] [化 146]
[0380] ベンジノレ (2S, 3S, 5R)— 3 ヒドロキシ一 2, 3, 5 トリメチノレピロリジン一 1一力 ルポキシラート(450mg)、 10%パラジウム炭素(50%含水、 40mg)、シユウ酸(77m g)を用いて参考例 51と同様の操作を行うことで、(2S, 3S, 5R)— 2, 3, 5 トリメチ ルピロリジン 3 オール 0.5シユウ酸塩を無色固体として得た(収量: 285.3mg 、収率: 960/0)。 (2S, 3S, 5R)-2, 3, 5 トリメチノレピロリジン一 3 才一ノレ 0.5シ ユウ酸塩(50mg)、 2 クロ口一 4 フルォロベンゾニトリル(67mg)と炭酸リチウム(4
6.7mg)を用いて、実施例 53と同様の操作を行うことで表題化合物を無色固体とし て得た(収量: 36.3mg、収率: 48%)。
'H-NMRCCDCl ) δ :1.29 (3Η, d, J = 6.2Hz) , 1.30 (3H, s), 1.35(3H,
3
d, J = 6.0Hz), 1.49-1.54(1H, m) , 1.95(1H, dd, J=12.6, 7.6Hz) , 2 .22(1H, dd, J=12.6, 6.6Hz) , 3.48(1H, q, J = 6.6Hz) , 3.66— 3.82(1 H, m), 6.46(1H, dd, J = 8.8, 2.5Hz) , 6.59(1H, d, J = 2.5Hz) , 7.36—
7.47(1H, m).
mp:132-133°C.
[0381] 実施例 61
2 フノレ才ロー 4 [(2S, 3S, 5R)— 3 ヒドロキシー 2, 3, 5 トリメチノレピロリジン 1 ィル]ベンゾニトリノレ
[0382] [化 147]
(2S, 3S, 5R)— 2, 3, 5 トリメチノレピロリジン一 3 才一ノレ 0.5シユウ酸塩(93 mg)、 2, 4 ジフノレオ口べンゾニトリノレ(120mg)と炭酸リチウム(93mg)を用いて、 実施例 53と同様の操作を行うことで表題化合物を無色固体として得た(収量: 76mg 、収率: 57%)。
'H-NMRCCDCl ) δ :1.29 (3Η, d, J = 6.6Hz) , 1.30 (3H, s), 1.35(3H,
3
d, J = 6.2Hz), 1.54-1.64(1H, m) , 1.96(1H, dd, J=12.6, 7.6Hz) , 2 .22(1H, dd, J=12.6, 7.6Hz) , 3.47(1H, q, J = 6.6Hz) , 3.65— 3.81(1 H, m), 6.28(1H, dd, J=13.0, 2.3Hz) , 6.35(1H, dd, J = 8.8, 2.3Hz) ,
7.35(1H, dd, J = 8.8, 7.7Hz) .
mp:125-128°C.
[0384] 実施例 62
4-[(2S, 3S, 5R)— 3 ヒドロキシー 2, 3, 5 トリメチノレピロリジン 1ーィノレ] 2 (トリフルォロメチル)ベンゾニトリノレ
[0385] [化 148]
[0386] (2S, 3S, 5R)— 2, 3, 5 トリメチルピロリジンー3 オール 0.5シユウ酸塩(83 mg)、 4 フルォロ 2 (トリフルォロメチル)ベンゾニトリル (203mg)と炭酸リチウム (93mg)を用いて、実施例 53と同様の操作を行うことで表題化合物を無色固体とし て得た(収量: 61.9mg、収率: 44%)。
'H-NMRCCDCl ) δ :1.31 (3Η, d, J = 6.6Hz) , 1.32 (3H, s), 1.37(3H,
3
d, J = 6.2Hz), 1.48-1.53(1H, m) , 1.98(1H, dd, J=12.6, 7.7Hz) , 2 .24(1H, dd, J=12.6, 7.7Hz) , 3.46— 3.58(1H, m) , 3.73— 3.89(1H, m), 6.67(1H, dd, J=8.9, 2.5Hz) , 6.83(1H, d, J = 2.5Hz) , 7.58(1H, d, J = 8.9Hz).
mp:115-117°C.
[0387] 実施例 63
4-[(2S, 3S, 5R)— 3—ヒドロキシー 2, 3, 5—トリメチノレピロリジン 1ーィノレ] 2 ーメトキシベンゾニトリノレ
[0388] [化 149]
[0389] 2 フノレ才ロー 4 [(2S, 3S, 5R)— 3 ヒドロキシー 2, 3, 5 トリメチノレピロリジン
1 ィル]ベンゾニトリル(47· 6mg)の DMSO溶液(5mUにナトリウムメトキシド(3 5mg)を加えて 100°Cで 3.5時間攪拌した後、ナトリウムメトキシド(130mg)を追加し て、さらに 100°Cで 4.5時間攪拌した。反応液を水に加え、酢酸ェチルで抽出した。 抽出液を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥後、減圧濃縮した。残 留物をシリカゲルカラムクロマトグラフィー(展開溶媒:へキサン/酢酸ェチル = 50/ 1→2/3)にて精製することで表題化合物を無色固体として得た(収量: 25. lmg、 収率: 50%)。
'H-NMRCCDCl ) δ :1.30 (3Η, d, J = 6.6Hz) , 1.31 (3H, s), 1.36 (3H,
3
d, J = 6.0Hz), 1.48-1.60(1H, m) , 1.95(1H, dd, J=12.5, 7.6Hz) , 2 .21(1H, dd, J=12.5, 7.6Hz) , 3.51(1H, q, J = 6.6Hz) , 3.69— 3.84(1 H, m), 3.88 (3H, s) , 6.02(1H, d, J = 2.2Hz) , 6.16(1H, dd, J = 8.7, 2. 2Hz), 7.32(1H, d, J = 8.7Hz) .
mp:121-123°C.
[0390] 実験例 1 AR結合阻害試験 (野生型)
野生型を有するアンドロゲン受容体 (AR)を含む溶液に 3nMのラジオラベルミボレロ ンおよび ΙΟΟηΜの化合物を加え、 4°Cで 3時間インキュベーションした後、デキストラ ン /チヤ一コール法にて B (Bound) / F (Free)分離した。 Bのラベルカウントを測定し、 化合物の阻害率を算出した。結果を表 1に示す。
[0391] [表 1]
化合物実施例番号 1 0 0 n Mでの阻害率
(%)
1 9 5
7 9 8
1 8 1 0 0
2 0 9 8
3 2 9 8
6 0 9 2
[0392] 実験例 2 Cos7細胞を用いたレポーターアツセィ系での化合物評価
Cos- 7を 150cm2フラスコに 5,000,000 cells播き、培養液(10%Dextran Charcoal ( DCC)-Fetal Bovine Serum (FBS)、 2mM glutamineを含む DMEM培地)中で 24時間 培養後、 AR遺伝子を含むベクター DNA、および MMTV(Mouse Mammary Tumor Vir us)由来のアンドロゲン応答性プロモーターの下流にルシフェラーゼ遺伝子を結合さ せたベクター DNAをリボソーム法によってコトランスフエクシヨンした。 4時間培養後、 細胞を回収し、 96well plateに 10,000 cells播き 2時間培養後、 1 Mの 5 α -ジヒドロ テストステロンまたは Ι ΟΟηΜの化合物を添加して、さらに 24時間培養した後、ルシフ エラーゼ活性を測定した。 1 ^ Mの 5 α -ジヒドロテストステロン添加時に誘導されるル シフェラーゼ活性を 100として、化合物の誘導率を求めた。結果を表 2に示す。
[0393] [表 2]
(1)実施例 1記載の化合物 5.0mg
(2)食塩 20.0mg
(3)蒸留水 全量 2mlとする
実施例 1記載の化合物 5.0mgおよび食塩 20.0mgを蒸留水に溶解させ、水を加え て全量 2.0mlとする。溶液をろ過し、無菌条件下に 2mlのアンプルに充填する。アン プルを滅菌した後、密封し注射用溶液を得る。
産業上の利用可能性
[0395] 本発明化合物は、アンドロゲン受容体調節薬 (特にァゴニスト)として優れた作用を 有し、アンドロゲンの投与が有効なノ、イボゴナデイズム、男性更年期障害、体力低下
、悪液質、骨粗鬆症等の予防 ·治療に有用である。
[0396] 本願は、 日本で出願された特願 2006— 324538及び 2007— 205966を基礎とし ており、その内容は本明細書にすべて包含されるものである。