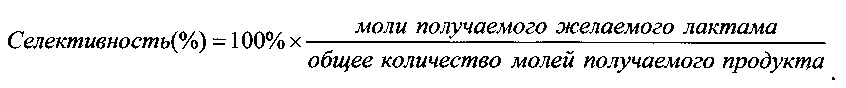RU2609779C2 - Газофазная и жидкофазная каталитическая перегруппировка бекмана оксимов с получением лактамов - Google Patents
Газофазная и жидкофазная каталитическая перегруппировка бекмана оксимов с получением лактамов Download PDFInfo
- Publication number
- RU2609779C2 RU2609779C2 RU2014121157A RU2014121157A RU2609779C2 RU 2609779 C2 RU2609779 C2 RU 2609779C2 RU 2014121157 A RU2014121157 A RU 2014121157A RU 2014121157 A RU2014121157 A RU 2014121157A RU 2609779 C2 RU2609779 C2 RU 2609779C2
- Authority
- RU
- Russia
- Prior art keywords
- catalyst
- sapo
- silicon
- oxime
- reaction
- Prior art date
Links
- 150000002923 oximes Chemical class 0.000 title claims abstract description 44
- 150000003951 lactams Chemical class 0.000 title claims abstract description 36
- 239000007791 liquid phase Substances 0.000 title claims abstract description 27
- 238000006237 Beckmann rearrangement reaction Methods 0.000 title claims abstract description 10
- 230000003197 catalytic effect Effects 0.000 title description 2
- 239000003054 catalyst Substances 0.000 claims abstract description 145
- 238000006243 chemical reaction Methods 0.000 claims abstract description 136
- VEZUQRBDRNJBJY-UHFFFAOYSA-N cyclohexanone oxime Chemical compound ON=C1CCCCC1 VEZUQRBDRNJBJY-UHFFFAOYSA-N 0.000 claims abstract description 63
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 claims abstract description 60
- 229910052710 silicon Inorganic materials 0.000 claims abstract description 57
- 239000010703 silicon Substances 0.000 claims abstract description 54
- JBKVHLHDHHXQEQ-UHFFFAOYSA-N epsilon-caprolactam Chemical compound O=C1CCCCCN1 JBKVHLHDHHXQEQ-UHFFFAOYSA-N 0.000 claims abstract description 48
- 239000002253 acid Substances 0.000 claims abstract description 41
- 238000000034 method Methods 0.000 claims abstract description 39
- 229910052698 phosphorus Inorganic materials 0.000 claims abstract description 21
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 claims abstract description 19
- 239000011574 phosphorus Substances 0.000 claims abstract description 19
- JHWNWJKBPDFINM-UHFFFAOYSA-N Laurolactam Chemical compound O=C1CCCCCCCCCCCN1 JHWNWJKBPDFINM-UHFFFAOYSA-N 0.000 claims abstract description 18
- 239000012071 phase Substances 0.000 claims abstract description 16
- SCRFXJBEIINMIC-UHFFFAOYSA-N n-cyclododecylidenehydroxylamine Chemical compound ON=C1CCCCCCCCCCC1 SCRFXJBEIINMIC-UHFFFAOYSA-N 0.000 claims abstract description 14
- 239000007848 Bronsted acid Substances 0.000 claims abstract description 9
- 239000002904 solvent Substances 0.000 claims description 22
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 11
- 238000006462 rearrangement reaction Methods 0.000 claims description 9
- 125000006552 (C3-C8) cycloalkyl group Chemical group 0.000 claims description 6
- 125000004650 C1-C8 alkynyl group Chemical group 0.000 claims description 6
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 claims description 6
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 6
- 229910052739 hydrogen Inorganic materials 0.000 claims description 6
- 125000003342 alkenyl group Chemical group 0.000 claims description 5
- 125000000217 alkyl group Chemical group 0.000 claims description 5
- MYXKPFMQWULLOH-UHFFFAOYSA-M tetramethylazanium;hydroxide;pentahydrate Chemical compound O.O.O.O.O.[OH-].C[N+](C)(C)C MYXKPFMQWULLOH-UHFFFAOYSA-M 0.000 claims description 5
- LPSKDVINWQNWFE-UHFFFAOYSA-M tetrapropylazanium;hydroxide Chemical compound [OH-].CCC[N+](CCC)(CCC)CCC LPSKDVINWQNWFE-UHFFFAOYSA-M 0.000 claims description 5
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims description 4
- 229910052799 carbon Inorganic materials 0.000 claims description 4
- 229940075614 colloidal silicon dioxide Drugs 0.000 claims description 4
- BGTOWKSIORTVQH-UHFFFAOYSA-N cyclopentanone Chemical compound O=C1CCCC1 BGTOWKSIORTVQH-UHFFFAOYSA-N 0.000 claims description 4
- 150000002825 nitriles Chemical class 0.000 claims description 4
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 claims description 3
- 229910000147 aluminium phosphate Inorganic materials 0.000 claims description 3
- 239000003849 aromatic solvent Substances 0.000 claims description 3
- 125000003118 aryl group Chemical group 0.000 claims description 3
- BVZSQTRWIYKUSF-TWGQIWQCSA-N 4-[(Z)-N-hydroxy-C-methylcarbonimidoyl]phenol Chemical compound C1=C(C=CC(=C1)O)/C(=N\O)/C BVZSQTRWIYKUSF-TWGQIWQCSA-N 0.000 claims description 2
- CGZZMOTZOONQIA-UHFFFAOYSA-N cycloheptanone Chemical compound O=C1CCCCCC1 CGZZMOTZOONQIA-UHFFFAOYSA-N 0.000 claims description 2
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Chemical compound CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 claims 2
- SNOOUWRIMMFWNE-UHFFFAOYSA-M sodium;6-[(3,4,5-trimethoxybenzoyl)amino]hexanoate Chemical compound [Na+].COC1=CC(C(=O)NCCCCCC([O-])=O)=CC(OC)=C1OC SNOOUWRIMMFWNE-UHFFFAOYSA-M 0.000 claims 2
- 239000000126 substance Substances 0.000 abstract description 3
- 230000000694 effects Effects 0.000 abstract description 2
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzonitrile Chemical compound N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 description 52
- MVPPADPHJFYWMZ-UHFFFAOYSA-N chlorobenzene Chemical compound ClC1=CC=CC=C1 MVPPADPHJFYWMZ-UHFFFAOYSA-N 0.000 description 16
- 239000007789 gas Substances 0.000 description 16
- 238000002474 experimental method Methods 0.000 description 13
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 12
- HOPRXXXSABQWAV-UHFFFAOYSA-N anhydrous collidine Natural products CC1=CC=NC(C)=C1C HOPRXXXSABQWAV-UHFFFAOYSA-N 0.000 description 12
- UTBIMNXEDGNJFE-UHFFFAOYSA-N collidine Natural products CC1=CC=C(C)C(C)=N1 UTBIMNXEDGNJFE-UHFFFAOYSA-N 0.000 description 12
- GFYHSKONPJXCDE-UHFFFAOYSA-N sym-collidine Natural products CC1=CN=C(C)C(C)=C1 GFYHSKONPJXCDE-UHFFFAOYSA-N 0.000 description 12
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 description 10
- 230000015572 biosynthetic process Effects 0.000 description 10
- 229910002091 carbon monoxide Inorganic materials 0.000 description 10
- 239000002808 molecular sieve Substances 0.000 description 10
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 10
- 229910052782 aluminium Inorganic materials 0.000 description 9
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 9
- 238000011068 loading method Methods 0.000 description 9
- 239000000203 mixture Substances 0.000 description 9
- 230000008707 rearrangement Effects 0.000 description 9
- 238000001228 spectrum Methods 0.000 description 9
- 238000006467 substitution reaction Methods 0.000 description 9
- 238000005481 NMR spectroscopy Methods 0.000 description 8
- 238000003795 desorption Methods 0.000 description 8
- 239000000463 material Substances 0.000 description 8
- 239000000047 product Substances 0.000 description 8
- 238000004566 IR spectroscopy Methods 0.000 description 7
- 239000001307 helium Substances 0.000 description 7
- 229910052734 helium Inorganic materials 0.000 description 7
- SWQJXJOGLNCZEY-UHFFFAOYSA-N helium atom Chemical compound [He] SWQJXJOGLNCZEY-UHFFFAOYSA-N 0.000 description 7
- 239000007788 liquid Substances 0.000 description 7
- SXVPOSFURRDKBO-UHFFFAOYSA-N Cyclododecanone Chemical compound O=C1CCCCCCCCCCC1 SXVPOSFURRDKBO-UHFFFAOYSA-N 0.000 description 6
- 238000012512 characterization method Methods 0.000 description 6
- 238000010574 gas phase reaction Methods 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- 230000004044 response Effects 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 229910021529 ammonia Inorganic materials 0.000 description 5
- 230000014759 maintenance of location Effects 0.000 description 5
- 239000011148 porous material Substances 0.000 description 5
- 238000012360 testing method Methods 0.000 description 5
- 238000005133 29Si NMR spectroscopy Methods 0.000 description 4
- 238000002441 X-ray diffraction Methods 0.000 description 4
- 239000006227 byproduct Substances 0.000 description 4
- -1 caprolactam Chemical class 0.000 description 4
- 238000006555 catalytic reaction Methods 0.000 description 4
- 238000010586 diagram Methods 0.000 description 4
- 239000011521 glass Substances 0.000 description 4
- 239000008187 granular material Substances 0.000 description 4
- 238000009616 inductively coupled plasma Methods 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 230000007246 mechanism Effects 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 239000007787 solid Substances 0.000 description 4
- 239000010457 zeolite Substances 0.000 description 4
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- 229920000299 Nylon 12 Polymers 0.000 description 3
- 229920002292 Nylon 6 Polymers 0.000 description 3
- 229910004298 SiO 2 Inorganic materials 0.000 description 3
- 229910021536 Zeolite Inorganic materials 0.000 description 3
- 150000001298 alcohols Chemical class 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- HNPSIPDUKPIQMN-UHFFFAOYSA-N dioxosilane;oxo(oxoalumanyloxy)alumane Chemical compound O=[Si]=O.O=[Al]O[Al]=O HNPSIPDUKPIQMN-UHFFFAOYSA-N 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 229910052760 oxygen Inorganic materials 0.000 description 3
- 125000004437 phosphorous atom Chemical group 0.000 description 3
- 238000005070 sampling Methods 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 239000010936 titanium Substances 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- ZTQSAGDEMFDKMZ-UHFFFAOYSA-N Butyraldehyde Chemical compound CCCC=O ZTQSAGDEMFDKMZ-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- AMQJEAYHLZJPGS-UHFFFAOYSA-N N-Pentanol Chemical compound CCCCCO AMQJEAYHLZJPGS-UHFFFAOYSA-N 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 2
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 2
- 239000003377 acid catalyst Substances 0.000 description 2
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 2
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 2
- 235000011130 ammonium sulphate Nutrition 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 239000011324 bead Substances 0.000 description 2
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 2
- BTANRVKWQNVYAZ-UHFFFAOYSA-N butan-2-ol Chemical compound CCC(C)O BTANRVKWQNVYAZ-UHFFFAOYSA-N 0.000 description 2
- 238000004364 calculation method Methods 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- ZSIAUFGUXNUGDI-UHFFFAOYSA-N hexan-1-ol Chemical compound CCCCCCO ZSIAUFGUXNUGDI-UHFFFAOYSA-N 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- ZXEKIIBDNHEJCQ-UHFFFAOYSA-N isobutanol Chemical compound CC(C)CO ZXEKIIBDNHEJCQ-UHFFFAOYSA-N 0.000 description 2
- 125000004430 oxygen atom Chemical group O* 0.000 description 2
- 230000010287 polarization Effects 0.000 description 2
- 238000000634 powder X-ray diffraction Methods 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 2
- 238000004626 scanning electron microscopy Methods 0.000 description 2
- 229910052665 sodalite Inorganic materials 0.000 description 2
- HIFJUMGIHIZEPX-UHFFFAOYSA-N sulfuric acid;sulfur trioxide Chemical compound O=S(=O)=O.OS(O)(=O)=O HIFJUMGIHIZEPX-UHFFFAOYSA-N 0.000 description 2
- 229910052719 titanium Inorganic materials 0.000 description 2
- 238000004438 BET method Methods 0.000 description 1
- 238000003775 Density Functional Theory Methods 0.000 description 1
- 238000001157 Fourier transform infrared spectrum Methods 0.000 description 1
- GSCCALZHGUWNJW-UHFFFAOYSA-N N-Cyclohexyl-N-methylcyclohexanamine Chemical compound C1CCCCC1N(C)C1CCCCC1 GSCCALZHGUWNJW-UHFFFAOYSA-N 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- 239000004809 Teflon Substances 0.000 description 1
- 229920006362 Teflon® Polymers 0.000 description 1
- 238000005263 ab initio calculation Methods 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- VXAUWWUXCIMFIM-UHFFFAOYSA-M aluminum;oxygen(2-);hydroxide Chemical compound [OH-].[O-2].[Al+3] VXAUWWUXCIMFIM-UHFFFAOYSA-M 0.000 description 1
- 150000001491 aromatic compounds Chemical class 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 238000010504 bond cleavage reaction Methods 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- IIRFCWANHMSDCG-UHFFFAOYSA-N cyclooctanone Chemical compound O=C1CCCCCCC1 IIRFCWANHMSDCG-UHFFFAOYSA-N 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 239000008367 deionised water Substances 0.000 description 1
- 229910021641 deionized water Inorganic materials 0.000 description 1
- 230000005595 deprotonation Effects 0.000 description 1
- 238000010537 deprotonation reaction Methods 0.000 description 1
- 238000002050 diffraction method Methods 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 238000006073 displacement reaction Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 239000000446 fuel Substances 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000010931 gold Substances 0.000 description 1
- 229910052737 gold Inorganic materials 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 238000002329 infrared spectrum Methods 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 239000013335 mesoporous material Substances 0.000 description 1
- 239000012229 microporous material Substances 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 229910000069 nitrogen hydride Inorganic materials 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- RVTZCBVAJQQJTK-UHFFFAOYSA-N oxygen(2-);zirconium(4+) Chemical compound [O-2].[O-2].[Zr+4] RVTZCBVAJQQJTK-UHFFFAOYSA-N 0.000 description 1
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 230000005588 protonation Effects 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 239000000376 reactant Substances 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 238000001878 scanning electron micrograph Methods 0.000 description 1
- 150000003376 silicon Chemical class 0.000 description 1
- 239000011973 solid acid Substances 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 238000003419 tautomerization reaction Methods 0.000 description 1
- WGTYBPLFGIVFAS-UHFFFAOYSA-M tetramethylammonium hydroxide Substances [OH-].C[N+](C)(C)C WGTYBPLFGIVFAS-UHFFFAOYSA-M 0.000 description 1
- HGBOYTHUEUWSSQ-UHFFFAOYSA-N valeric aldehyde Natural products CCCCC=O HGBOYTHUEUWSSQ-UHFFFAOYSA-N 0.000 description 1
- 239000012808 vapor phase Substances 0.000 description 1
- 239000011800 void material Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 229910001928 zirconium oxide Inorganic materials 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J29/00—Catalysts comprising molecular sieves
- B01J29/04—Catalysts comprising molecular sieves having base-exchange properties, e.g. crystalline zeolites
- B01J29/06—Crystalline aluminosilicate zeolites; Isomorphous compounds thereof
- B01J29/08—Crystalline aluminosilicate zeolites; Isomorphous compounds thereof of the faujasite type, e.g. type X or Y
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J29/00—Catalysts comprising molecular sieves
- B01J29/82—Phosphates
- B01J29/84—Aluminophosphates containing other elements, e.g. metals, boron
- B01J29/85—Silicoaluminophosphates [SAPO compounds]
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J35/00—Catalysts, in general, characterised by their form or physical properties
- B01J35/30—Catalysts, in general, characterised by their form or physical properties characterised by their physical properties
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B37/00—Compounds having molecular sieve properties but not having base-exchange properties
- C01B37/06—Aluminophosphates containing other elements, e.g. metals, boron
- C01B37/08—Silicoaluminophosphates [SAPO compounds], e.g. CoSAPO
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B39/00—Compounds having molecular sieve and base-exchange properties, e.g. crystalline zeolites; Their preparation; After-treatment, e.g. ion-exchange or dealumination
- C01B39/54—Phosphates, e.g. APO or SAPO compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D201/00—Preparation, separation, purification or stabilisation of unsubstituted lactams
- C07D201/02—Preparation of lactams
- C07D201/04—Preparation of lactams from or via oximes by Beckmann rearrangement
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D223/00—Heterocyclic compounds containing seven-membered rings having one nitrogen atom as the only ring hetero atom
- C07D223/02—Heterocyclic compounds containing seven-membered rings having one nitrogen atom as the only ring hetero atom not condensed with other rings
- C07D223/06—Heterocyclic compounds containing seven-membered rings having one nitrogen atom as the only ring hetero atom not condensed with other rings with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D223/08—Oxygen atoms
- C07D223/10—Oxygen atoms attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D225/00—Heterocyclic compounds containing rings of more than seven members having one nitrogen atom as the only ring hetero atom
- C07D225/02—Heterocyclic compounds containing rings of more than seven members having one nitrogen atom as the only ring hetero atom not condensed with other rings
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/52—Improvements relating to the production of bulk chemicals using catalysts, e.g. selective catalysts
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Materials Engineering (AREA)
- Inorganic Chemistry (AREA)
- Geology (AREA)
- General Life Sciences & Earth Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Crystallography & Structural Chemistry (AREA)
- Catalysts (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
- Other In-Based Heterocyclic Compounds (AREA)
Abstract
Описаны способы получения лактамов из оксимов путем проведения перегруппировки Бекмана с использованием силикоалюминофосфатного катализатора. Данные катализаторы можно использовать в газофазных или жидкофазных реакциях с превращением оксимов в лактамы. Способ проведения реакции перегруппировки Бекмана в жидкой фазе при температуре ниже 250°С включает реакцию оксима в присутствии катализатора с получением лактама, причем указанный катализатор содержит кремнийсодержащий алюмофосфат с кодом каркаса FAU согласно МЦА. Способ проведения реакции перегруппировки Бекмана в газовой фазе включает реакцию оксима в присутствии катализатора, который содержит кремнийсодержащие алюмофосфаты с кодом каркаса FAU согласно МЦА и собой катализатор типа SAPO-37, полученный из геля, характеризующегося соотношением кремния к фосфору от 0,22:1 до 0,63:1. Катализатор для проведения реакции перегруппировки Бекмана содержит кремнийсодержащий алюмофосфат с кодом каркаса FAU согласно МЦА и множество отдельных кислотных центров Бренстеда, расположенных во внутреннем пространстве каркаса, причем кислотные центры содержат кремний, изоморфно замещающий фосфор в каркасе; причем катализатор представляет собой катализатор типа SAPO-37, полученный из геля, характеризующегося соотношением кремния к фосфору от 0,22:1 до 0,63:1. Высокую степень превращения оксима и высокую селективность к желаемым лактамам получают при помощи раскрытых способов, включая высокую степень превращения и селективность к ε-капролактаму, получаемому из циклогексаноноксима, и высокую степень превращения и селективность к ω-лауролактаму, получаемому из циклододеканоноксима. 3 н. и 7 з.п. ф-лы, 14 табл., 22 ил., 4 пр.
Description
Ссылка на родственные заявки
Согласно разделу 35 §119(e) Кодекса законов США настоящая заявка испрашивает приоритет в соответствии с предварительной заявкой на выдачу патента США с серийным номером №61/628419, поданной 28 октября 2011 г., раскрытие которой таким образом включено ссылкой во всей своей полноте.
Область техники
Настоящее изобретение относится к способам получения лактамов, таких как капролактам, например. В частности, настоящее изобретение относится к способу получения капролактама с использованием силикоалюминофосфатных (SAPO) катализаторов.
Уровень техники
Традиционные подходы для получения лактамов, используемых при получении нейлона, включают прохождение оксимом перегруппировки Бекмана в присутствии кислотного катализатора, такого как дымящая серная кислота. Типичные реакции показаны на фиг. 1. Как показано на фиг.1A, циклогексаноноксим реагирует с образованием ε-капролактама. ε-капролактам в свою очередь полимеризуется с образованием нейлона-6. Как показано на фиг. 1B, циклододеканоноксим реагирует с образованием ω-лауролактама. ω-лауролактам в свою очередь полимеризуется с образованием нейлона-12. Нейлон-6 и нейлон-12 широко используются в промышленности и производстве.
Один возможный механизм реакции для реакции с фиг. 1A показан на фиг. 1C. Механизм обычно состоит из протонирования гидроксильной группы, проведения перегруппировки алкила, в тоже время вытеснения гидроксила с образованием иона нитрилия, с последующим гидролизом, таутомеризацией и депротонированием с образованием лактама.
Обычно реакции перегруппировки Бекмана оксимов с образованием лактамов проводят с использованием кислот, таких как дымящая серная кислота. Данные реакции характеризуются полным или практически полным превращением оксима и очень высокой, селективностью к желаемым лактамам. Однако данные реакции также дают побочные продукты, включая сульфат аммония. Хотя сульфат аммония является сам по себе применимым продуктом, минимизация его получения может быть желательной.
Известны газофазная и жидкофазная перегруппировки Бекмана циклогексаноноксимов, в которых используют различные природные и синтетические катализаторы, включая твердые кислотные катализаторы. Однако опубликованные результаты приводят низкую степень превращения оксима и низкую селективность к желаемым лактамовым продуктам.
Желательны усовершенствования в вышеуказанных процессах.
Сущность изобретения
Настоящее раскрытие обеспечивает способы получения лактамов из оксимов путем проведения перегруппировки Бекмана с использованием силикоалюминофосфатного катализатора. Данные катализаторы используют в газофазных и жидкофазных реакциях для превращения оксимов в лактамы. Высокую степень превращения оксима и высокую селективность к желаемым лактамам получают при помощи раскрытых способов, включая высокую степень превращения и селективность к ε-капролактаму, получаемому из циклогексаноноксима, и высокую степень превращения и селективность к ω-лауролактаму, получаемому из циклододеканоноксима.
Согласно одному типичному варианту осуществления настоящее изобретение обеспечивает способ проведения реакции перегруппировки Бекмана. Способ включает реакцию оксима в жидкой фазе в присутствии катализатора с получением лактама, причем указанный катализатор содержит кремнийсодержащий алюмофосфат с кодом каркаса FAU согласно МЦА.
Согласно другому типичному варианту осуществления настоящее изобретение обеспечивает другой способ проведения реакции перегруппировки Бекмана. Способ включает реакцию оксима в газовой фазе в присутствии катализатора с получением лактама, причем указанный катализатор содержит кремнийсодержащие алюмофосфаты с кодом каркаса FAU согласно МЦА; причем указанная стадия реакции дополнительно включает комбинацию степени превращения оксима и селективности лактама, выбранную из группы, состоящей из: степень превращения оксима составляет по меньшей мере 50%, и селективность к лактаму составляет по меньшей мере 90%; и степень превращения оксима составляет по меньшей мере 90%, и селективность к лактаму составляет по меньшей мере 80%.
Согласно еще одному типичному варианту осуществления настоящее изобретение обеспечивает катализатор. Катализатор содержит кремнийсодержащий алюмофосфатный каркас с кодом каркаса FAU согласно МЦА и множество отдельных кислотных центров Бренстеда, расположенных во внутреннем пространстве каркаса, причем кислотные центры содержат кремний, изоморфно замещающий фосфор в каркасе; причем катализатор представляет собой катализатор типа SAPO-37, и по меньшей мере 10% всего количества кислотных центров характеризуются как слабые кислотные центры.
Согласно еще одному типичному варианту осуществления обеспечивают способ проведения реакции перегруппировки Бекмана. Способ включает реакцию оксима в жидкой или газовой фазе в присутствии катализатора с получением лактама, причем указанный катализатор содержит кремнийсодержащий алюмофосфат с кодом каркаса FAU согласно МЦА; причем, когда оксим находится в газовой фазе, указанная стадия реакции дополнительно включает комбинацию степени превращения оксима и селективности лактама, выбранную из группы, состоящей из: степень превращения оксима составляет по меньшей мере 50%, и селективность к лактаму составляет по меньшей мере 90%; и степень превращения оксима составляет по меньшей мере 90%, и селективность к лактаму составляет по меньшей мере 80%.
Указанные выше и другие признаки настоящего изобретения и способ их достижения станут более очевидными, и само настоящее изобретение будет лучше понято, исходя из следующего описания вариантов осуществления настоящего изобретения, взятых совместно с приложенными графическими материалами.
Краткое описание чертежей
На фиг. 1A показана реакция циклогексаноноксима в ε-капролактам;
на фиг. 1B показана реакция циклододеканоноксима в ω-лауролактам;
на фиг. 1C показаны возможные стадии реакции, соответствующей реакции перегруппировки Бекмана из циклогексаноноксима в ε-капролактам;
на фиг. 2A-2G показаны структуры типичного катализатора SAPO-37;
на фиг. 3A представлена диаграмма состояния для тройной системы, показывающая композиционные параметры одного варианта осуществления силикоалюминофосфатов, выраженные в мольных долях кремния, алюминия и фосфора;
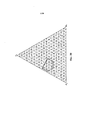
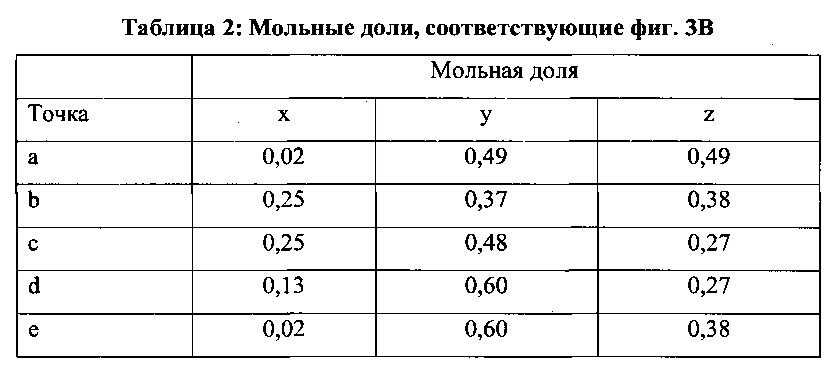
на фиг. 3B представлена диаграмма состояния для тройной системы, показывающая композиционные параметры следующих вариантов осуществления силикоалюминофосфатов, выраженные в мольных долях кремния, алюминия и фосфора;
фиг. 4A-4C соответствуют примеру 2 и представляют результаты определения характеристик катализаторов SAPO-37 при помощи твердофазного 29Si-ЯМР;
фиг. 5 соответствует примеру 2 и представляет результаты определения характеристик катализаторов SAPO-37 при помощи термопрограммированной десорбции NH3;
фиг. 6 соответствует примеру 2 и представляет результаты определения характеристик катализаторов SAPO при помощи рентгеновской дифракции;
фиг. 7 соответствует примеру 2 и представляет результаты определения площади поверхности по БЭТ катализаторов SAPO-37;
фиг. 8A-8C соответствуют примеру 2 и представляют собой СЭМ-изображения катализаторов SAPO-37;
фиг. 9-15 соответствуют примеру 3 и представляют результаты степени превращения и селективности газофазных реакций перегруппировки Бекмана циклогексаноноксима в ε-капролактам с использованием различных катализаторов;
фиг. 16-20 соответствуют примеру 4 и представляют результаты степени превращения и селективности жидкофазных реакций перегруппировки Бекмана циклогексаноноксима в ε-капролактам с использованием различных катализаторов; и
фиг. 21 и 22 соответствуют примеру 5 и представляет результаты степени превращения и селективности жидкофазных реакций перегруппировки Бекмана циклододеканоноксима в ω-лауролактам с использованием различных катализаторов.
Подробное описание изобретения
Настоящее изобретение относится к способу образования лактамов из циклических оксимовых соединений. Типичные реакции показаны на фиг. 1. Как показано на фиг. 1A, циклогексаноноксим реагирует с образованием ε-капролактама, который в свою очередь может полимеризоваться с образованием нейлона-6. Как показано на фиг. 1B, циклододеканоноксим реагирует с образованием ω-лауролактама, который в свою очередь может полимеризоваться с образованием нейлона-12. Согласно другим типичным вариантам осуществления дополнительные лактамы, кроме ε-капролактама и ω-лауролактама, получают из соответствующих оксимов посредством данного способа. Способ согласно настоящему изобретению также пригоден для проведения других реакций перегруппировки Бекмана.
Способы согласно настоящему изобретению включают прохождение оксимовым реагентом реакции перегруппировки Бекмана в присутствии катализатора. Типичные катализаторы включают микропористые и мезопористые природные и синтетические молекулярные сита, цеолиты, алюмофосфатные (AlPO) материалы и силикоалюминофосфатные (SAPO) материалы.
Силикоалюминофосфатные (SAPO) катализаторы представляют собой синтетические молекулярные сита, известные как пригодные в качестве катализаторов. Типичные способы получения конкретных катализаторов SAPO предоставлены в патенте США №4440871, выданном Lok и соавт., и N. Jappar, Y. Tanaka, S. Nakata, and T. Tatsumi, «Synthesis and Characterization of a New Titanium Silicoaluminophospate: TAPSO-37», Microporous and Mesoporous Materials, Vol. 23, Issues 3-4, August 1998, pp. 169-178, раскрытия каждого документа таким образом включены ссылкой.
Типичная структура одного катализатора SAPO, SAPO-37, показана на фиг. 2A-2G. Молекулярные сита, такие как катализатор SAPO-37, показанный на фиг. 2A, представляют собой кристаллические структуры, имеющие геометрические структуры трехмерного каркаса. Каркасы молекулярных сит включают пустоты, полости, каналы и поры в зависимости от типа молекулярного сита. Кислотные центры, находящиеся или на поверхности, или во внутреннем пространстве, или и там, и там, молекулярного сита обеспечивают способность некоторых молекулярных сит выступать в качестве кислотных катализаторов.
В типичной структуре SAPO-37, показанной на фиг. 2A-2G, участок 10 катализатора содержит геометрию кремнийсодержащего алюмофосфата со структурой фоязитного типа. Геометрия содержит множество пор 12, соединяющих внутренние полости катализатора. На фиг. 2A-2G также показано, что кислотный центр содержит атомы 14 кремния во внутренних полостях катализатора. Кислотные центры также содержат атом водорода, т.е. протон 16, который используется при катализе реакции перегруппировки Бекмана. Атом 14 кремния и протон 16 увеличены для сравнения на фиг. 2A-2G. На фиг. 2A-2F показано множество видов в перспективе одной внутренней полости, образованной катализатором 10. На фиг. 2G показан увеличенный вид кислотного центра, содержащего атом 14 кремния и протон 16 во внутреннем пространстве пустоты, образованной катализатором 10.
Как лучше всего показано на фиг. 2G, атом 14 кремния для пояснения присоединен к четырем атомам кислорода 18A, 18B, 18C и 18D, показывая, что он изоморфно заместил атом фосфора в каркасе катализатора. Такое изоморфное замещение называется замещение II типа. Согласно типичным вариантам осуществления катализатор содержит множество таких изоморфно замещенных атомов кремния, образующих кислотные центры, так, что кислотные центры являются отдельными и хорошо отделенными друг от друга. Данное типичное расположение обеспечивает функционирование каждого кислотного центра как хорошо отделенной кислоты Бренстеда с одним кислотным центром. Катализаторы, имеющие большую долю кислотных центров со II типом изоморфного замещения, характеризуются большими долями слабых кислотных центров Бренстеда. Катализаторы с большим содержанием кремния характеризуются большей долей сильных кислотных центров, которые связаны с замещением III типа двумя атомами кремния соседних атомов алюминия и фосфора. Замещение III типа приводит к снижению доступных слабых кислотных центров Бренстеда.
Протон 16 для наглядности присоединен к одному из атомов кислорода 18A. Протон 16 может отдаваться кислотным центром для катализа реакции в полости, такой как перегруппировка Бекмана.
Обычно катализатор представляет собой кремнийсодержащий алюмофосфат со структурой фоязитного типа. Согласно типичному варианту осуществления катализатор представляет собой кремнийсодержащий алюмофосфат или силикоалюминофосфатный катализатор с кодом каркаса FAU согласно Международной цеолитной ассоциации (МЦА), как описано в Atlas of Zeolite Framework Types, 6th ed., Christian Baerlocher, Lynne B. McCusker and David H. Olson, Elsevier, Amsterdam (2007), раскрытие которого таким образом включено ссылкой. Более конкретно, катализатор состоит из пустот содалита, соединенных вместе посредством 6,6 (дважды по 6) вторичных строительных блоков. Двенадцать этих пустот содалита затем используются для создания сверхпустотной структуры, отверстие-пора которой составляет 7,4 Å, и внутренний диаметр сверхпустоты находится в диапазоне 12-14 Å. Катализатор также содержит множество отдельных кислотных центров Бренстеда, расположенных во внутреннем пространстве каркаса, причем кислотные центры содержат кремний, изоморфно замещающий фосфор в каркасе.
Согласно типичным вариантам осуществления катализатор представляет собой силикоалюминофосфат, имеющий микропористую структуру кристаллического каркаса и определяющий эмпирический химический состав которого в синтезированной форме в пересчете на безводную форму представляет собой:
mR:(SixAlyPz)O2,
где:
R представляет собой по меньшей мере одно органическое темплатное средство, находящееся во внутрикристаллической системе пор; m имеет значение от 0,02 до 0,3;
x y и z представляют собой, соответственно, мольную долю кремния, алюминий и фосфора, находящихся в оксидном фрагменте;
согласно одному варианту осуществления значение x, y и z, находящееся в пределах композиционной области, ограниченной точками A, B, C, D и E диаграммы состояния для тройной системы, которая представлена на фиг. 3A, представлено значениями, указанными ниже в таблице 1;
согласно другому варианту осуществления значение x, y и z, находящееся в пределах композиционной области, ограниченной точками a, b, c, d и e диаграммы состояния для тройной системы, которая представлена на фиг. 3B, представлено значениями, указанными ниже в таблице 2;
указанный силикоалюминофосфат имеет характеристическую порошковую рентгенограмму, которая имеет, по меньшей мере, d-расстояние, указанное ниже в таблице 3.
Одной типичной процедурой для получения катализаторов SAPO-37 является следующая. Сначала источник алюминия, такой как оксид алюминия, медленно добавляют в источник фосфора, такой как 85% фосфорная кислота. Структурный раствор темплата получают растворением пентагидрата гидроксида тетраметиламмония (ТМАОН) в гидроксиде тетрапропиламмония (ТРАОН), в который медленно добавляют коллоидную двуокись кремния. Раствор затем добавляют по каплям с энергичным перемешиванием в смесь алюминия/фосфора. Полученный гель нагревают для синтеза желаемой структуры. Полученный продукт отделяют обычно центрифугированием, фильтрацией и промывкой. Продукт затем сушат и прокаливают перед хранением в инертной атмосфере.
Относительные концентрации кремния и алюминия можно регулировать для обеспечения подходящего количества и распределения кислотных центров на поверхности и во внутреннем пространстве катализатора. Типичные процедуры для регулирования количества и распределения кислотных центров включают регулирование соотношения кремния к фосфору, обеспечиваемое при образовании геля. Согласно типичным вариантам осуществления соотношение Si:P в геле составляет от приблизительно 0,1:1 до приблизительно 0,8:1. Согласно более конкретному варианту осуществления соотношение Si:P в геле составляет от приблизительно 0,11:1 до приблизительно 0,63:1. Согласно еще одним вариантам осуществления соотношение Si:P в геле составляет всего лишь 0,1:1, 0,11:1, 0,16:1, 0,17:1, 0,21:1, 0,22:1, или вплоть до 0,42:1, 0,63:1, 0,75:1, 0,8:1, или в любом диапазоне, определенном между любой парой указанных значений.
Массовую процентную концентрацию кремния в образованном катализаторе можно также определить. Типичный способ определения массовой процентной концентрации кремния состоит в использовании индуктивно-связанной плазмы. Обычно кремний составляет от приблизительно 1 масс.% до приблизительно 10 масс.% всей массы катализатора. Согласно более конкретному варианту осуществления кремний составляет от приблизительно 2 масс.% до приблизительно 9,1 масс.% всей массы катализатора. Согласно еще одному варианту осуществления кремний составляет массовый процент от всей массы катализатора от всего лишь 1 масс.%, 1,5 масс.%, 2 масс.%, 2,1 масс.%, 2,5 масс.% вплоть до 6 масс.%, 7 масс.%, 8 масс.%, 9 масс.%, 9,1 масс.%, 10 масс.%, или в любом диапазоне, определенном между любой парой указанных значений.
Оксимы превращаются в лактамы как, например, в примерах, показанных на фиг. 1A и 1B, посредством контакта с катализаторами. Настоящее изобретение, как считается, в общем применимо для любого оксима, образованного из ряда альдегидов и кетонов. Типичные оксимы включают, помимо прочего, циклогексаноноксим, циклододеканоноксим, 4-гидроксиацетофеноноксим и оксимы, образованные из ацеофенона, бутиральдегида, циклопентанона, циклогептанона, циклооктанона, бензальдегида.
Согласно типичным вариантам осуществления реакцию проводят в присутствии растворителя. Хотя рабочие примеры предусмотрены для реакций, проводимых в растворителе, настоящее изобретение, как считается, также применимо для реакций перегруппировки Бекмана, проводимых в отсутствие растворителя. В реакциях, проводимых в отсутствие растворителя, продукт используют для поглощения экзотермического тепла, производимого реакцией. Согласно данным вариантам осуществления большое соотношение лактама к оксиму поддерживают в зоне реакции для поглощения энергии, производимой реакцией.
Типичные растворители включают органические нитрилы формулы:
R1-CN,
где R1 представляет собой C1-C8-алкил, C1-C8-алкенил, C1-C8-алкинил, C3-C8-циклоалкил; C3-C8-аралкил, содержащий C6-ароматическое кольцо. Типичные нитрилы включают ацетонитрил, бензонитрил и смеси любых вышеперечисленных.
Другие типичные растворители включают ароматические соединения формулы:
R2-Ar,
где Ar представляет собой ароматическое кольцо, и R2 представляет собой H, F, Cl или Br. Типичные ароматические растворители включают бензол и хлорбензол.
Еще одни типичные растворители включают воду и спирты формулы:
R3-OH,
где R3 представляет собой водород, C1-C3-алкил, C1-C8-алкенил, C1-C8-алкинил, C3-C8-циклоалкил; C3-C8-арилалкил. Типичные спирты включают спирты с 8 или менее атомами углерода, такие как метанол, этанол, н-пропанол, изопропанол, н-бутанол, втор-бутанол, изобутанол, трет-бутанол, н-амиловый спирт, н-гексанол, фенол и смеси любых вышеперечисленных.
Согласно типичным вариантам осуществления растворитель тщательно сушат перед контактом с катализатором. При использовании в настоящем документе тщательно высушенный понимают как высушенный до уровня 100 частей на миллион воды или менее. Типичные способы сушки включают адсорбцию воды при помощи молекулярных сит, таких как активированные молекулярные сита 4A. При использовании в настоящем документе реакция, проводимая в отсутствие воды, означает реакцию, в которой вода составляет менее 0,01 масс.% массы реагентов.
Реакцию проводят как жидкофазную реакцию или газофазную реакцию. При использовании в настоящем документе жидкофазная реакция представляет собой реакцию, в которой по существу весь оксим находится в жидкой фазе, когда реагирует с образованием лактама. При использовании в настоящем документе газофазная реакция представляет собой реакцию, в которой по существу весь оксим находится в газовой или паровой фазе, когда реагирует с образованием лактама.
При проведении в форме газофазной реакции реакцию обычно проводят при температуре ниже 350°C. Согласно более конкретному варианту осуществления реакцию проводят при температуре от приблизительно 130°C до приблизительно 300°C. Согласно еще одним вариантам осуществления реакцию можно проводить при температуре всего лишь приблизительно 90°C, 100°C, 110°C, 120°C, 130°C, или до приблизительно 140°C, 150°C, 170°C, 180°C, 190°C, 200°C, 210°C, 220°C, 230°C, 240°C 250°C, 275°C, 300°C, 325°C, 350°C, или в любом диапазоне, определенном между любой парой указанных значений.
При проведении в форме газофазной реакции реакцию обычно проводят при давлении от приблизительно 0,1 бар до приблизительно 1 бар. Более конкретно, согласно типичным вариантам осуществления реакции, проводимой в форме газофазной реакции, давление может составлять всего лишь 0,01 бар, 0,02 бар, 0,05 бар, 0,1 бар, до 0,5 бар, 1 бар, или в диапазоне, определенном между любой парой указанных значений.
При проведении в форме жидкофазной реакции реакцию обычно проводят при температуре ниже 250°C. Согласно более конкретному варианту осуществления реакцию проводят при температуре от приблизительно 130°C до приблизительно 190°C. Согласно еще одним вариантам осуществления реакцию можно проводить при температуре всего лишь приблизительно 90°C, 100°C, 110°C, 120°, 130°, или до приблизительно 140°C, 150°C, 170°C, 180°C, 190°C, 200°C, 210°C, 220°C, 230°C, 240°C 250°C, или в любом диапазоне, определенном между любой парой указанных значений.
При проведении в форме жидкофазной реакции реакцию обычно проводят при давлении от приблизительно 1 бар до приблизительно 5 бар. Более конкретно, согласно некоторым типичным вариантам осуществления давление может составлять всего лишь 0,5 бар, 1 бар, до 1 бар, 2 бар, 5 бар, 10 бар, 15 бар, 20 бар, 25 бар, 30 бар, 35 бар, или в любом диапазоне, определенном между любой парой указанных значений. Согласно некоторым типичным вариантам осуществления реакции, проводимой в форме жидкофазной реакции, растворитель обычно представляет собой газ при температуре реакции, однако остается в жидкой фазе при проведении реакции при повышенном давлении.
При проведении в форме жидкофазной реакции реакцию обычно проводят при температуре и давлении ниже критической точки растворителя, где давление может составлять всего лишь 1 бар, до 2 бар, 5 бар, 10 бар, 15 бар, 20 бар, 25 бар, 30 бар, 35 бар, или в любом диапазоне, определенном между любой парой указанных значений.
Эффективность реакции можно выражать на основании степени превращения оксима, селективности к желаемому продукту или выхода. Степень превращения является мерой количества оксимового реагента, которое расходуется в ходе реакции. Более высокие степени превращения являются более желательными. Степень превращения рассчитывают следующим образом:
Селективность является мерой количества желаемого продукта, который получают, относительно всех продуктов реакции. Более высокие селективности являются более желательными. Более низкие селективности показывают, что большая процентная концентрация реагента использовалась для получения продуктов, отличных от желаемого лактама. Селективность рассчитывают следующим образом:
Выход является мерой, которая объединяет селективность и степень превращения. Выход показывает, как много поступающего оксима реагирует с образованием желаемого лактама. Выход рассчитывают следующим образом:
Выход(%) = Селективность(%) × Степень превращениям/о) / 100%.
Способы согласно настоящему изобретению дают высокие степени превращения и селективности.
Согласно типичным вариантам осуществления степень превращения составляет 50% или выше. Согласно более конкретному варианту осуществления степень превращения составляет от приблизительно 50% до приблизительно 100%. Например, степень превращения может составлять всего лишь приблизительно 50%, 60%, 70%, 75%, или до приблизительно 80%, 85%, 90%, 95%, 97,5%, 99%, 99,5%, приближаться к 100% или составлять 100%, или может находиться в любом диапазоне, определенном между любой парой указанных значений.
Согласно типичным вариантам осуществления селективность составляет 50% или выше. Согласно более конкретному варианту осуществления селективность составляет всего лишь приблизительно 50%, 55%, 60%, 65%, или до приблизительно 70%, 75%, 80%, 85%, 90%, 95%, 97,5%, 99%, 99,5%, приближается к 100%, или может находиться в любом диапазоне, определенном между любой парой указанных значений.
Согласно типичным вариантам осуществления степень превращения циклогексаноноксима в ε-капролактам составляет от приблизительно 90% до приблизительно 100%, и селективность составляет от приблизительно 80% до приблизительно 100%. Согласно более конкретным вариантам осуществления степень превращения составляет от приблизительно 95% до приблизительно 100%, и селективность составляет от приблизительно 90% до приблизительно 98%. Согласно еще более конкретным вариантам осуществления степень превращения составляет от приблизительно 98% до приближающейся к 100%, и селективность составляет от приблизительно 95% до приблизительно 98%.
Согласно типичным вариантам осуществления степень превращения циклододеканоноксима в ω-лауролактам составляет от приблизительно 90% до приблизительно 100%, и селективность составляет от приблизительно 80% до приблизительно 100%. Согласно более конкретным вариантам осуществления степень превращения составляет от приблизительно 95% до приблизительно 100%, и селективность составляет от приблизительно 98% до приблизительно 99%.
Пример 1 - Получение катализатора SAPO-37
Фазу псевдобемита оксида алюминия медленно добавляли в разбавленный раствор фосфорной кислоты (85 масс.%) и оставляли при перемешивании на 7 часов. Второй раствор пентагидрата гидроксида тетраметиламмония (ТМАОН), растворенного в гидроксиде тетрапропиламмония (ТРАОН) (40 масс.%), получали, в который медленно добавляли коллоидную двуокись кремния. Его оставляли при перемешивании на 2 часа и затем добавляли по каплям в перемешанный гель алюминия/фосфора. Катализаторы SAPO-37 получали с четырьмя различными загрузками SiO2. Катализаторы маркировали в зависимости от соотношения SiO2 к H3PO4, используемого при получении. Загрузки геля для различных образцов можно найти в таблице 4 ниже.
Смесь перемешивали в течение 68 часов и затем переносили в автоклав. Раствор нагревали под автогенным давлением при 200°C в течение 24 часов. При удалении гель центрифугировали, отфильтровывали и промывали. Материал затем сушили в течение ночи при комнатной температуре. Белое твердое вещество затем прокаливали при 550°C в течение 16 часов и сохраняли в инертной атмосфере.
Пример 2 - Определение характеристик катализаторов
Твердофазный 29Si-ЯМР
Все ЯМР-измерения проводили на спектрометре Chemagnetics Infinity 400 на 4 мм образце с вращением образца под магическим углом (ВМУ) при двойном резонансе. Образец паковали в тонкостенную вращающуюся часть из оксида циркония и вращали при 8 кГц при помощи сжатого азота для предотвращения разложения образца на воздухе. 27Al-ЯМР: все эксперименты проводили при помощи прямого отбора данных. Данные 31P-ЯМР собирали как при помощи прямого отбора данных (120 с выдержкой времени между сканированиями), так и при помощи поперечной поляризации. Данные Si-ЯМР для всех 1D экспериментов проводили при помощи наклонной поперечной поляризации с разрывом связи SPINAL-64 во время отбора данных. Двумерные эксперименты проводили с использованием протон-индуцированной спиновой диффузии (ПИСД) с временем перемешивания 5 мс.
Результаты ЯМР-измерений можно увидеть на фиг. 4. На фиг. 4A показаны результаты 2D 2981-ЯМР с ВМУ SAPO-37(0,21). На фиг. 4B показаны результаты 2D 29Si-ЯМР с ВМУ SAPO-37(0,63). На фиг. 4C показаны результаты 29Si-ЯМР с ВМУ систем SAPO-3 7 с различными соотношениями в геле. На фиг. 4C показано наличие отделенных центров Si(OAl)4 при -93 частях на миллион и центров Si(OAl)3(OSi) при -98 частях на миллион.
На фиг. 4A-4C показано, что кремний начинает группироваться при высоких загрузках. На фиг. 4A показаны от низких до отсутствия пиков при -103 частях на миллион, соответствующих кластеру двух центров, и при -108 частях на миллион, соответствующих кластеру трех центров. Как показано на фиг. 4B и 4C, при более высоких уровнях загрузки кремния кремний начинает группироваться, образуя пики при -103 частях на миллион - Si(OAl)2(OSi)2, и -108 частях на миллион - Si(OAl)(OSi)3. Более низкие загрузки кремния, такие как при использовании SAPO-37(0,21), как показано на фиг. 3A и 3C, снижают пик при -98 частях на миллион, показывая большую распространенность отделенных отдельных центров со слабой кислотностью Бренстеда относительно кластеров нескольких центров.
Термопрограммированная десорбция NH3 (ТПЦ)
Количество и силу кислотных центров исследовали при помощи термопрограммированной десорбции (ТПД) аммиака. Синтезированные материалы предварительно обрабатывали в смеси 20% O2 в He, и нагревали при 10°C/мин до 550°C, и выдерживали при 550°C в течение 2 часов. Десорбцию проводили при 10°C/мин до 600°C в течение 40 минут.
Согласно данному эксперименту аммиак адсорбируется на поверхности катализатора, связываясь с кислотными центрами, дающими определенный пик. Площадь этого пика соответствует количеству аммиака в системе. Систему затем нагревают и аммиак десорбируется при температуре. Чем сильнее кислотный центр, тем большая температура требуется для десорбции аммиака.
Все значения кислотности для SAPO-37(0,21) и SAPO-37(0,42), полученные при помощи NH3-ТПД, находились в пределах погрешности эксперимента. Как показано на фиг. 5, общее количество кислотных центров, что измерено общим количеством ммоль/г десорбированного NH3, показало, что SAPO-37(0,21) и SAPO-37(0,42) имели подобные количества кислотных центров, в то время как SAPO-3 7(0,63) показал значительно меньшее число кислотных центров, чем либо SAPO-37(0,21), либо SAPO-37(0,42). Анализ областей температур показывает относительную силу имеющихся кислотных центров, при этом более сильные центры требуют более высоких температур для десорбции. Как показано на фиг. 5, материалы с более низкой загрузкой SAPO-37(0,21) и SAPO-37(0,42) имели более слабые кислотные центры, что показано более высокими значениями при более низких температурах, однако увеличение загрузки кремния приводит к снижению количества слабых кислотных центров и увеличению сильных кислотных центров. Эти результаты согласуются с результатами образования кластеров кремния, представленными данными ЯМР на фиг. 4A-4C.
ИК-спектроскопия с преобразованием Фурье образца СО
Количество и силу кислотных центров также исследовали при помощи спектров ИК-спектроскопии с преобразованием Фурье образца моноксида углерода (CO). Образцы каждого тестируемого катализатора перемалывали и спрессовывали в самонесущие гранулы. Гранулы затем нагревали при 10°C/мин до 550°C в потоке газа, содержащем 20%O2/80%Ν2, затем выдерживали при температуре в течение 1 часа. Поток газа затем переключали на гелий и выдерживали в течение дополнительного 1 часа. Образцы охлаждали до 30°C и спектр записывали. Девять 0,02 см3 впрысков CO добавляли в образцы с последующим 1 конечным 0,2 см3 впрыском. После каждого впрыска систему приводили в равновесие в течение 3 минут перед тем, как записывали спектр. Все спектры записывали на ИК-спектрометре Nicolet Nexus 870 с 128 сканированиями с использованием охлажденного KPT-детектора. Все спектры обрабатывали при помощи программного обеспечения GRAMS/AI 9, доступного от Thermo Scientific.
Результаты тестирования образца СО при помощи ИК-спектроскопии с преобразованием Фурье представлены в таблице 5.
| Таблица 5: | ||
| Результаты ИК-спектроскопии с преобразованием Фурье образца CO | ||
| Система | Площадь CO/у .е. | Сдвиг пика/см-1 |
| SAPO-37(0,21) | 0,854 | 305 |
| SAPO-37(0,42) | 0,856 | 311 |
| SAPO-37(0,63) | 0,582 | 321 |
В таблице 5 указано, что полная кислотность, показанная площадью СО/условная единица (у.е.), составляет:
SAPO-37(0,21)~SAPO-37(0,42)>SAPO-37(0,63).
Сдвиг пика дает понимание силы кислоты, где больший сдвиг соответствует более сильным кислотным центрам. В таблице 5 показано, что на основании силы кислоты:
SAPO-37(0,63)>SAPO-37(0,42)>SAPO-37(0,21).
Данные как NH3-ТПД, так и ИК-спектроскопии с преобразованием Фурье образца СО показывают, что SAPO-3 7(0,21) имеет такое же количество кислотных центров, как SAPO-37(0,42), и что SAPO-37(0,63) имеет меньше кислотных центров, чем либо SAPO 37(0,21), либо SAPO-37(0,42). Аналогично, данные как NH3-ТПД, так и ИК-спектроскопии с преобразованием Фурье образца СО показывают, что SAPO-37(0,63) имеет самые сильные кислотные центры, и SAPO-37(0,21) имеет самые слабые. NH3-ТПД показывает, что SAPO-37(0,21) и SAPO-37(0,42) имели более слабые центры (десорбция при 200-300°C и 300-400°C), чем SAPO-37(0,63), однако SAPO-37(0,63) имел более сильные кислотные центры (400-500°C), чем либо SAPO-37(0,21), либо SAPO-37(0,42).
ИК-спектроскопия с преобразованием Фурье образца коллидина
Количество и силу кислотных центров также исследовали при помощи спектров ИК-спектроскопии с преобразованием Фурье образца коллидина. Образцы перемалывали и спрессовывали в самонесущие гранулы. Гранулы затем нагревали при 10°C/мин до 550°C в потоке 20%O2/Ν2, затем выдерживали при температуре в течение 2 часов. Образцы охлаждали до 30°C и спектр записывали. Коллидин адсорбировали при 150°C в течение 1 часа. Коллидин затем десорбировали при 150/300/450°C в течение 1 часа для каждой стадии. Все спектры записывали на ИК-спектрометре Nicolet Nexus 870 с 128 сканированиями с использованием охлажденного KPT-детектора. Все спектры обрабатывали при помощи программного обеспечения GRAMS/AI 9, доступного от Thermo Scientific.
Согласно данному эксперименту коллидин адсорбировался на поверхности катализатора, связываясь с кислотными центрами, дающими определенный пик. Площадь этого пика соответствует количеству коллидина в системе. Систему затем нагревали, и коллидин десорбировался при температуре. Чем сильнее кислотный центр, тем более высокая температура требуется для десорбции коллидина. Слабые центры характеризуются, если коллидин десорбируется от 150° до 300°C, средние центры характеризуются, если коллидин десорбируется от 300° до 450°C, и сильные центры характеризуются, если имеют коллидин, все еще адсорбированный при 450°C.
Результаты тестирования образца коллидина при помощи ИК-спектроскопии с преобразованием Фурье представлены в таблице 6.
В таблице 6 показано, что полная кислотность, что измерено общим количеством кислотных центров, составляет:
SAPO-37(0,63)>SAPO-37(0,42)>SAPO-37(0,21).
Касательно силы кислотных центров слабые и средние центры все показали большие количества для SAPO-37(0,21), чем SAPO-37(0,63). Большое количество слабых центров для SAPO-37(0,21), 0,913 из 5,367 общего числа центров, составляют более 15% общего числа. Это было намного больше, чем для SAPO-37(0,42), который имел 0,389 из 4,704 или 8,3% всего числа, и SAPO-37(0,63), который имел 0,382 из 4,303 или 8,9% всего числа, и предполагает большую часть кислотных центров Бренстеда, которые являются отдельными и одноцентровыми по природе. Сила слабых кислотных центров SAPO-37(0,42) и сильных кислотных центров для SAPO-37(0,63) совершенно не согласуется с другими исследованиями кислотности, однако данные для средних центров приблизительно равны для SAPO-37(0,21) и SAPO-37(0,42).
Большая доля слабых кислотных центров Бренстеда связана с большим количеством изоморфных замещений II типа фосфора на кремний в каркасе катализатора. Катализаторы с большими загрузками кремния характеризуются большей долей сильных кислотных центров, которые связаны с замещениями III типа, что приводит к снижению доли слабых кислотных центров Бренстеда.
Определение характеристик согласно теории функционала плотности СТФП) Элементарную ячейку SAPO-37 оптимизировали при помощи пакета CRSTAL09 для проведения ab initio расчетов кристаллической системы, R. Dovesi, R. Orlando, B. Civalleri, C. Roetti, V.R. Saunders, and C.M. Zicovich-Wilson, Z. Kristallogr. 220, 571 (2005). Элементарная ячейка SAPO-37 содержала 577 атомов с формулой H1Si1Al96P95O384. Это соответствует загрузке 1 мольн. % кремния. Элементарную ячейку моделировали при помощи присутствующего NH3 так, что он мог взаимодействовать с кислотным центром (H4N1Si1Al96P95O384). Используя следующее уравнение, энергию связи NH3 с SAPO-37 оценили как 117 кДж моль-1:
Eсвязи=E(SAPO-37+NH3)-E(SAPO-37)-E(NH3).
Вышеуказанный расчет можно использовать как меру кислотности. Результаты находятся в предполагаемом диапазоне для этих расчетов.
Рентгеновская дифракция и определение площади поверхности по БЭТ
Порошковые рентгенограммы получали при помощи дифрактометра Siemens D5000, где λ=1,54056 ангстрем () при излучении Cu Kα1. Кроме того, получали рентгенограмму катализатора SAPO-5 (AFI). Три образца с большей загрузкой, как обнаружили, были чистофазными, однако SAPO-37(0,11) показал значительную примесь фазы AFI. SAPO-3 7(0,11) показал пики, соответствующие как каркасу FAU-типа при 111 и 331, а также каркасу AFI-типа согласно МЦА при 100 и 200. Результаты рентгеновской порошковой дифрактометрии можно найти на фиг. 6.
Измерения площади поверхности по БЭТ для исследования общей площади поверхности катализаторов проводили при помощи анализатора площади поверхности Gemini 2375 и получали при помощи получения в потоке газа. Результаты измерений площади поверхности по БЭТ и предполагаемого содержания кремния в масс.% можно найти на фиг. 7. Определения элементарной ячейки обеспечивали подобные размеры элементарной ячейки для трех измеренных катализаторов SAPO-37, хотя большие загрузки SiO2 давали в результате незначительно большие элементарные ячейки, обеспечивая дополнительное доказательство повышенного замещения кремния в каркасе молекулярного сита.
Результаты рентгеновской дифракции и определения площади поверхности по БЭТ были типичными для данной системы.
Индуктивно-связанная плазма (ИСП)
ИСП измерения проводили для определения количества фактической массовой процентной концентрации кремния в каждом из полученных катализаторов. Perkin-Elmer Optimum 3000 DV использовали для обеспечения результатов ИСП. Прокаленные образцы получали и полностью переносили в 10 мл деионизированной воды и 10 мл сертифицированной ACS Plus серной кислоты, доступной от Fisher Scientific. Растворы стандартных концентраций использовали для калибровки.
Результаты ИСП и соотношение загрузок кремния к фосфору в геле, полученном в примере 1, можно найти в таблице 7 ниже:
| Таблица 7: | ||
| Результаты ИСП | ||
| Система | Соотношение Si/P в геле Из синтезированного геля | Si/Macc.% Из ИСП измерений |
| SAPO-5(AFI) | 0,21 | 1,33 |
| SAPO-34(CHA) | 0,23 | 0,73 |
| SAPO-BER | 0,21 | 0,73 |
| SAPO-37(0,21) | 0,21 | 2 |
| SAPO-37(0,63) | 0,63 | 9,1 |
Соотношение кремния к фосфору в геле, используемом для получения катализаторов, для SAPO-37(0,63) и SAPO-37(0,21) составляло 0,63:0,21 или 3:1. Массовая процентная концентрация кремния SAPO-37(0,63) была выше, чем массовая процентная концентрация кремния SAPO-37(0,21). Соотношение массовой процентной концентрацией кремния между SAPO-37(0,63) и SAPO-37(0,21) составляло 9,1:2 или 4,55:1. Это было выше, чем соотношение загрузки в геле 3:1.
Изображения сканирующей электронной микроскопии
Изображения сканирующей электронной микроскопии катализаторов получали при помощи микроскопа JOEL-JSM5910 с ускоряющим напряжением 0,3-30 кВ. Образцы получали покрытием золотом. СЭМ показала, что все 3 системы состояли из правильных октаэдрических кристаллов приблизительно 1 мкм в длину. Изображение СЭМ SAPO 37(0,21) представлено как фиг. 8A, изображение СЭМ SAPO-37(0,42) представлено как фиг. 8B, и изображение СЭМ SAPO-37(0,63) представлено как фиг. 8C.
Пример 3 - Газофазный катализ
Получение катализаторов
Загрузки в геле для катализаторов, используемых в газофазных примерах, даны в таблице 8.
Катализаторы SAPO-37 получали как в примере 1.
SAPO-5 получали разбавлением 4,7 г H3PO4 (85% в H2O) в тефлоновом химическом стакане с 10 мл H2O и перемешивали до однородности (5 минут). 4,3 г Al(OH)3 медленно добавляли в кислоту, а затем дополнительные 10 мл H2O. Смесь перемешивали в течение 10 минут. 0,76 г коллоидной двуокиси кремния медленно добавляли, а затем 10 мл H2O. Смесь перемешивали в течение 30 минут. Наконец темплатное средство (N-метилдициклогексиламин) добавляли по каплям и добавляли дополнительные 10 мл H2O. Смесь перемешивали в течение 1 часа. Белый гель затем переносили в автоклав и нагревали до 200°C в течение 2 часов. При удалении гель отфильтровывали и промывали H2O и оставляли сушиться при 70°C в течение ночи. Полученное белое твердое вещество прокаливали при 550°C в течение 10 часов перед использованием.
SAPO-TRY получали таким же образом как SAPO-5 выше, за исключением того, что не использовали темплатное средство.
Катализатор SAPO-34 получали согласно способу, представленному D. Dubois, et al., Fuel Process. Technol. 2003, 83, 203, раскрытие которого таким образом включено ссылкой.
TS-1, катализатор на основе цеолита силикалита титана, получали из Национальной химической лаборатории, Пуна, Индия. Образец имел загрузку Ti 2 масс.%. Катализатор TS-1 раскрыт в патенте США №4859785, раскрытие которого таким образом включено ссылкой.
Анализ степени превращения и селективности
Степень превращения и селективность системы анализировали при помощи Claras 400 газового хроматографа с ПИД и с использованием колонки Elite 5, площади пиков калибровали при помощи известных факторов отклика. Способ предполагал: начало на 120°C, удерживание в течение 2 минут, затем увеличение 15°C/мин до 220°C и удерживание в течение 5 минут при 220°C. Способ длился в общем 13 минут и 40 секунд. Циклогексаноноксим имеет пик, соответствующий времени удерживания 4,0 минуты, ε-капролактам имеет пик, соответствующий времени удерживания 5,8 минуты, побочный продукт имеет пик, соответствующий времени удерживания 6,6 минуты. Инжекторный порт устанавливали на 220°C и детектор устанавливали на 250°C. Давление носителя (гелий) составляло 14 фунтов/кв. дюйм. Способу давали 1 минуту для уравновешивания перед введением. Вводили центрифугированный образец 5 мкл.
Образцы калибровали при помощи относительного фактора отклика ε-капролактама относительно циклогексаноноксима, который, как обнаружили, составлял 1,119. Образцы калибровали для внутреннего стандарта хлорбензола для материального баланса. Циклогексаноноксим, как обнаружили, имел относительный фактор отклика 1,2972 относительно хлорбензола, и ε-капролактам, как обнаружили, имел фактор отклика 1,4516 относительно хлорбензола. Материальный баланс при 130°C, как обнаружили, составлял 106% через 6 часов. При помощи следующей формулы факторы отклика использовали для расчета молей циклогексаноноксима, ε-капролактама и побочных продуктов (фактор отклика предполагается равным 1,00):
Экспериментальная процедура
Цилиндрическую стеклянную пробирку (4 мм в диаметре) со стеклообразной фриттой заполняли 5 мм слоем стеклянных шариков, слоем гранулированного катализатора (~0,25 г, 40 мм) и также 60 мм слоем стеклянных шариков, помещали внутрь проточного реактора, нагреваемого рубашкой до 673 K. Образец затем обрабатывали в потоке газообразного гелия в течение 1 часа. Температуру снижали до тестовой температуры как указано ниже и подачу жидкости 10 масс.% циклогексаноноксима в этаноле подавали в реактор, поддерживая экспериментальную объемную скорость (OC) как указано ниже.
Сравнение катализаторов при ОС 0,3 ч-1 и 300°C
Газофазные опыты проводили для различных катализаторов при подобных условиях. Выбранные условия представляли собой OC 0,3 ч-1, подача жидкости 10 масс.% оксима в этаноле, температура 300°C, поток гелия 33,3 мл/мин и 0,25 г катализатора. Каждый катализатор предварительно активировали при 400°C в течение 1 часа в 33,3 мл/мин потоке гелия. Образцы брали для анализа степени превращения и селективности через час.
Результаты можно найти в таблице 9 и фиг. 9.
| Таблица 9: | ||
| Газофазные результаты | ||
| Система | Степень превращения/мольн. % | Селективность к ε-капролактаму/мольн. % |
| SAPO-37(0.42) | 99,7 | 86,2 |
| SAPO-5 | 66,0 | 53,8 |
| SAPO-34 | 78,2 | 75,2 |
| SAPO-TRY | 74,9 | 79,0 |
Катализатор SAPO-37 (0,42) давал намного более высокие результаты степени превращения и селективности, чем любые другие протестированные катализаторы SAPO.
Сравнение катализаторов SAPO-37 с SAPO-41 и TS-1 при различных температурах
В качестве сравнения газофазные опыты проводили для катализаторов SAPO-3 7, SAPO-41 и TS-1 при подобных условиях. Выбранные условия представляли собой объемную скорость 0,3 ч-1, подачу жидкости 10 масс.% оксима в этаноле, поток гелия 33,3 мл/мин и 0,25 г катализатора. Каждый катализатор предварительно активировали при 400°C в течение 1 часа в 33,3 мл/мин потоке гелия. Образцы брали для анализа степени превращения и селективности через час.Результаты для различных температур представлены на фиг. 10-13.
Результаты для SAPO-37(0,22) показаны на фиг. 10. SAPO-37(0,22) давал высокие степени превращения и селективность. Степень превращения повышалась, когда температура повышалась от 300°C до 350°C. Селективность также повышалась, однако была приблизительно 80% при всех трех измеренных температурах.
Результаты для SAPO-37(0,42) показаны на фиг. 11. SAPO-37(0,22) давал высокие степени превращения и селективность. Степень превращения и селективность снижались, когда температура снижалась от 300°C до 325°C. Однако степень превращения оставалась высокой на 94,6%, и селективность оставалась приблизительно 80%.
Как показано на фиг. 12, SAPO-41 обеспечивал высокую степень превращения, однако намного более низкую селективность к ε-капролактаму, чем катализаторы SAPO-37.
Результаты для TS-1 показаны на фиг. 13. Степень превращения и селективность были высокими для TS-1 при 300°C.
На фиг. 14 и 15 сравнивают результаты для различных катализаторов при одних и тех же температурах.
Как можно увидеть на фиг. 14, при 300°C высокая селективность и степень превращения были получены для SAPO-37 (0,42) по сравнению с катализатором SAPO-41.
Как показано на фиг. 15, все три катализатора SAPO давали хорошую степень превращения при 325°C. Однако только катализаторы SAPO-37 давали высокие селективности.
Пример 4 - Жидкофазный катализ
Получение катализаторов
Загрузки в геле для катализаторов, используемых в жидкофазных примерах, даны в таблице 10.
Катализаторы SAPO-3 7 получали, как в примере 1.
Катализаторы SAPO-5 и SAPO-34 получали, как в примере 3.
Катализатор SAPO-11 получали согласно P. Meriaudeau, V.A. Tuan, V.T. Nghiem, S.Y. Lai, L.N. Hung and C. Naccache, Journal of catalysis, 1997, 169, 55-66, раскрытие которого таким образом включено ссылкой.
Катализатор SAPO-41 получали согласно P. Meriaudeau, V.A. Tuan, V.T. Nghiem, S.Y. Lai, L.N. Hung and C. Naccache, Journal of catalysis, 1997, 169, 55-66, раскрытие которого таким образом включено ссылкой.
Экспериментальная процедура
100 мг циклогексаноноксима, 100 мг катализатора и 20 мл бензонитрила в качестве растворителя (Aldrich) добавляли в стеклянный реактор и перемешивали при 500 об/мин при выбранной температуре с обратным холодильником. Образцы брали с заранее определенными интервалами на основе выбранной температуры: 30 минут для 130°C, 15 минут для 150°C, 5 минут для 170°C и 5 минут для 190°C. Все образцы анализировали на газовом хроматографе Varian Star 3400CX с детектором ионизации пламени (ДИП). Образцы вводили в колонку Perkin Elmer HP1 со сшитым метилсилоксаном (30 м × 0,32 мм × 1 мкм толщина пленки). Образцы приводили в баланс по массе при помощи хлорбензола в качестве внутреннего стандарта.
Анализ степени превращения и селективности
Образцы анализировали как в примере 3 с пиком бензонитрильного растворителя, имеющим большой пик, соответствующий времени удерживания 3,5 минуты.
Сравнение катализаторов при 130°C
Жидкофазные опыты проводили для различных катализаторов при подобных условиях. Выбранные условия представляли собой 130°C, с соотношением катализатор:циклогексаноноксим:бензонитрил 1:1:200 и 0,1 г циклогексаноноксима. Образцы анализировали через 7 часов.
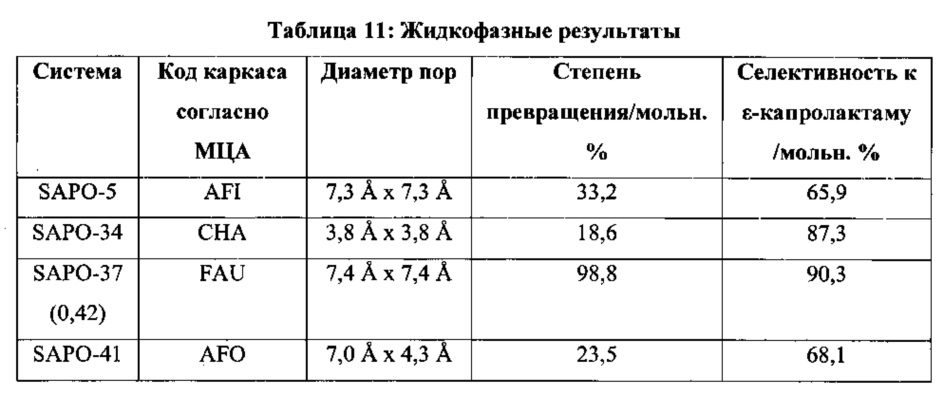
Результаты можно найти в таблице 11 и на фиг. 16.
Каркасы SAPO-3 7 и SAPO-5 имеют подобные диаметры пор, первый 7,4 А, последний 7,3 А, кроме того, они показали очень различные уровни активности, таким образом конфигурации анализировали при помощи техник 29Si-ЯМР при вращении образца под магическим углом. Спектр SAPO-37 показал преобладающий пик при -93 частях на миллион, с меньшим вторичным пиком при -98 частях на миллион, соответствующие конфигурациям Si(OAl)4 и Si(OSi)(OAl)3, соответственно. Конфигурация Si(OAl)4 показывает, что кремний заместил один атом фосфора, таким образом создавая кислотный центр Бренстеда (механизм замещения II типа), конфигурация Si(OSi)(OAl)3 показывает, что два кремния заместили пару фосфора и алюминия, таким образом не создавая кислотность (механизм замещения III типа). Напротив спектр SAPO-5 показал преобладающий пик при -110 частях на миллион, соответствующий конфигурации Si(OSi)4, предполагая, кремний находился главным образом в кремнийсодержащих зонах. Это показало, что отделенные центры кремния представляют собой активный центр для данной реакции. Содержание кремния частиц SAPO-37 изменялось (означая SAPO-37(X), где X представляет собой соотношение в синтезированном геле), давая три различных образца, что показало незначительные различия каталитической активности.
Оба катализатора SAPO-3 7 показали очень высокую степень превращения и селективность, особенно по сравнении с другими катализаторами SAPO.
Жидкофазная перегруппировка Бекмана с использованием хлорбензольного растворителя
Такая же экспериментальная процедура как для реакций в жидкости с бензонитрилом проводили с хлорбензолом в качестве растворителя. Реакцию проводили при 130°C, с 100 мг циклогексаноноксима, 100 мг катализатора SAPO-37(0,21) и 20 мл хлорбензола. Через 7 часов наблюдали 14,6% степень превращения оксима и 95,0% селективность для ε-капролактама.
Изменение реакции с течением времени для различных катализаторов при 130°C
Степень превращения, селективность и выход с течением времени реакции с катализатором SAPO-3 7 (0,16), катализатором SAPO-11 и катализатором SAPO-41 при 130°C показаны на фиг. 17-20. Катализатор SAPO-37 показал очень высокую степень превращения и селективность по сравнению с другими катализаторами SAPO.
На фиг. 17 показана высокая степень превращения и селективность при использовании катализатора SAPO-37(0,16) в жидкофазной реакции с использованием бензонитрила в качестве растворителя. Реакцию проводили при 130°C, с соотношением катализатор : циклогексаноноксим : бензонитрил 1:1:200, с использованием 0,1 г циклогексаноноксима и проводили в течение 7 часов.
На фиг. 18 показана та же реакция с использованием безводного бензонитрила в качестве растворителя. Реакцию проводили при 130°C, с соотношением катализатор:циклогексаноноксим:безводный бензонитрил 1:1:200, с использованием 0,125 г циклогексаноноксим и проводили в течение 7 часов.
Безводный бензонитрил, показанный на фиг. 18, давал в результате большую селективность, но меньшую степень превращения, чем (влажный) бензонитрил, показанный на фиг. 17. Обе фиг. 17 и 18 показывают высокую степень превращения и селективность в жидкофазной реакции.
На фиг. 19 показаны низкая степень превращения и селективность для жидкофазной реакции с SAPO-11 в качестве катализатора. Реакцию проводили при 130°C, с соотношением катализатор:циклогексаноноксим:бензонитрил 1:1:200, с использованием 0,1 г циклогексаноноксима и проводили в течение 7 часов.
На фиг. 20 показаны даже более низкие степень превращения и селективность для жидкофазной реакции с SAPO-41 в качестве катализатора. Реакцию проводили при 130°C, с соотношением катализатор : циклогексаноноксим : бензонитрил 1:1:200, с использованием 0,1 г циклогексаноноксима и проводили в течение 7 часов.
Дополнительные результаты теста в жидкости представлены в таблицах 12 и 13. Таблица 12 представляет степень превращения, селективность и выход для катализаторов SAPO-3 7 с различными загрузками в геле с интервалами времени в ходе реакции. Таблица 13 представляет конечные значения степени превращения и селективности, взятые для каждого катализатора при указанной температуре. Бензонитрил использовали в качестве растворителя в каждом из опытов в таблицах 12 и 13. SAPO-37(0,21)БВ означает использование безводного бензонитрила в качестве растворителя.
Результаты в таблицах 12 и 13 показывают высокие уровни степени превращения и селективности при использовании SAPO-3 7 в качестве катализатора и бензонитрила в качестве растворителя в жидкофазной реакции. Данные в таблицах 12 и 13 показывают степень превращения большую чем 97,5% в пределах измеренного времени, в то время как селективность для ε-капролактама изменялась от приблизительно 80% для SAPO-37(0,63) при 190°C до приблизительно 98% для SAPO-37(0,21) при 130°C в безводном бензонитриле.
Обычно SAPO-3 7(0,21) обеспечивал большую селективность, чем SAPO-37(0,42), что в свою очередь обеспечивал большую селективность, чем SAPO-37(0,63), хотя высокая селективность и степень превращения можно было увидеть у всех трех катализаторов. Эти результаты согласуются с большими количествами кислотных центров, предполагаемых данными, определенными в примере 2.
Жидкофазная перегруппировка Бекмана циклододеканоноксима в ω-лауролактам Перегруппировка Бекмана также известна как пригодная при получении ω-лауролактама из циклододеканона (смотри фиг. 1B).
Такую же экспериментальную процедуру, как для реакций в жидкости с циклогексаноноксимом, проводили с циклододеканоноксимом с использованием катализаторов SAPO-37(0,21) и SAPO-11. Реакцию проводили при 130°C, с 175 мг циклододеканоноксима, 100 мг катализатора и 20 мл бензонитрила. Время удерживания при газовой хроматографии составляло 8,4 минуты для циклододеканона, 10,6 минут для циклододеканоноксима и 11,8 минуты для ω-лауролактама. Результаты при использовании SAPO-3 7 (0,21) представлены на фиг. 19 и в таблице 14. Результаты при использовании SAPO-11 представлены на фиг. 20.
На фиг. 21 показана очень высокая степень превращения и селективность при использовании SAPO-37 в качестве катализатора, в то время как на фиг. 22 показана намного более низкая степень превращения и селективность при использовании SAPO-37 в качестве катализатора. Единственным значительным побочным продуктом, обнаруженным при использовании SAPO-37, был циклододеканон.
Хотя настоящее изобретение в первую очередь относится к производству ε-капролактама и ω-лауролактама, следует понимать, что признаки, раскрытые в настоящем документе, имеют применимость для производства других лактамов и других мономеров.
Хотя настоящее изобретение было описано касательно типичных образцов, настоящее изобретение можно также модифицировать в пределах идеи и объема настоящего изобретения. Кроме того, настоящая заявка предназначена охватывать такие отклонения от настоящего изобретения, которые находятся в области известной или принятой практики в области техники, к которой настоящее изобретение относится.
Claims (28)
1. Способ проведения реакции перегруппировки Бекмана, включающий стадии:
реакции оксима в жидкой фазе при температуре ниже 250°С в присутствии катализатора с получением лактама, причем указанный катализатор содержит кремнийсодержащий алюмофосфат с кодом каркаса FAU согласно МЦА.
2. Способ по п. 1, отличающийся тем, что катализатор представляет собой катализатор SAPO-37.
3. Способ по п. 1, отличающийся тем, что указанную стадию реакции проводят в присутствии растворителя, содержащего по меньшей мере один растворитель, выбранный из группы, состоящей из:
органического нитрила формулы R1-CN;
ароматического растворителя формулы R2-Ar и
спирта формулы R3-OH;
причем:
R1 представляет собой C1-С8-алкил, C1-C8-алкенил, C1-C8-алкинил, С3-C8-циклоалкил или С3-С8-аралкил;
Ar представляет собой ароматическое кольцо, и R2 представляет собой Н, F, Cl, Br; и
R3 представляет собой Н, C1-C8-алкил, C1-С8-алкенил, С1-С8-алкинил, С3-C8-циклоалкил; С3-С8-аралкил.
4. Способ по п. 1, отличающийся тем, что оксим выбирают из циклогексаноноксима и циклододеканоноксима и лактам выбирают из ε-капролактама и ω-лауролактама.
5. Способ по п. 1, отличающийся тем, что оксим выбирают из группы, состоящей из: циклогексаноноксима, циклододеканоноксима, 4-гидроксиацетофеноноксима, и оксимов, образованных из ацетофенона, циклопентанона и циклогептанона.
6. Способ проведения реакции перегруппировки Бекмана, включающий стадии:
реакции оксима в газовой фазе в присутствии катализатора с получением лактама, причем указанный катализатор содержит кремнийсодержащие алюмофосфаты с кодом каркаса FAU согласно МЦА; причем катализатор представляет собой катализатор типа SAPO-37, полученного из геля, характеризующегося соотношением кремния к фосфору от 0,22:1 до 0,63:1.
7. Способ по п. 6, отличающийся тем, что указанный гель получен из оксида алюминия, фосфорной кислоты, пентагидрата гидроксида тетраметиламмония, гидроксида тетрапропиламмония и коллоидной двуокиси кремния.
8. Способ по п. 6, отличающийся тем, что указанную стадию реакции проводят в присутствии растворителя, содержащего по меньшей мере один растворитель, выбранный из группы, состоящей из:
органического нитрила формулы R1-CN;
ароматического растворителя формулы R2-Ar и
спирта формулы R3-OH; причем
R1 представляет собой C1-C8-алкил, C1-С8-алкенил, С1-С8-алкинил, С3-C8-циклоалкил или С3-C8 аралкил;
Ar представляет собой ароматическое кольцо, и R2 представляет собой Н, F, Cl, Br; и
R3 представляет собой Н, C1-C8-алкил, С1-С8-алкенил, C1-C8-алкинил, С3-C8-циклоалкил; С3-С8-аралкил.
9. Способ по п. 6, отличающийся тем, что оксим выбирают из циклогексаноноксима и циклододеканоноксима и лактам выбирают из ε-капролактама и ω-лауролактама.
10. Катализатор для проведения реакции перегруппировки Бекмана, содержащий:
кремнийсодержащий алюмофосфат с кодом каркаса FAU согласно МЦА и
множество отдельных кислотных центров Бренстеда, расположенных во внутреннем пространстве каркаса, причем кислотные центры содержат кремний, изоморфно замещающий фосфор в каркасе;
причем катализатор представляет собой катализатор типа SAPO-37, полученный из геля, характеризующегося соотношением кремния к фосфору от 0,22:1 до 0,63:1.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201161628419P | 2011-10-28 | 2011-10-28 | |
| US61/628,419 | 2011-10-28 | ||
| US13/658,495 US8772476B2 (en) | 2011-10-28 | 2012-10-23 | Gas and liquid phase catalytic Beckmann rearrangement of oximes to produce lactams |
| US13/658,495 | 2012-10-23 | ||
| PCT/US2012/061876 WO2013063244A1 (en) | 2011-10-28 | 2012-10-25 | Gas and liquid phase catalytic beckmann rearrangement of oximes to produce lactams |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2014121157A RU2014121157A (ru) | 2015-12-10 |
| RU2609779C2 true RU2609779C2 (ru) | 2017-02-03 |
Family
ID=48168483
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2014121157A RU2609779C2 (ru) | 2011-10-28 | 2012-10-25 | Газофазная и жидкофазная каталитическая перегруппировка бекмана оксимов с получением лактамов |
Country Status (12)
| Country | Link |
|---|---|
| US (3) | US8772476B2 (ru) |
| EP (1) | EP2771317B1 (ru) |
| JP (2) | JP6243340B2 (ru) |
| KR (1) | KR102002197B1 (ru) |
| CN (1) | CN104039760B (ru) |
| BR (1) | BR112014010194A8 (ru) |
| CO (1) | CO6950487A2 (ru) |
| ES (1) | ES2856699T3 (ru) |
| IN (1) | IN2014DN03074A (ru) |
| MX (1) | MX354802B (ru) |
| RU (1) | RU2609779C2 (ru) |
| WO (1) | WO2013063244A1 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2672912C1 (ru) * | 2014-12-16 | 2018-11-21 | Эдвансикс Ресинс Энд Кемикалс Ллк | Иерархические алюмофосфаты в качестве катализаторов для перегруппировки бекмана |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4136000B2 (ja) * | 1994-06-03 | 2008-08-20 | 三井化学株式会社 | 殺虫性テトラヒドロフラン系化合物 |
| US8772476B2 (en) * | 2011-10-28 | 2014-07-08 | Honeywell International Inc. | Gas and liquid phase catalytic Beckmann rearrangement of oximes to produce lactams |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4440871A (en) * | 1982-07-26 | 1984-04-03 | Union Carbide Corporation | Crystalline silicoaluminophosphates |
| US4873325A (en) * | 1986-06-25 | 1989-10-10 | Uop | Process for the production of amides |
| US5312915A (en) * | 1993-03-04 | 1994-05-17 | Sumitomo Chemical Company, Limited | Process for producing epsilon-caprolactam |
| EP1193251A2 (en) * | 2000-09-29 | 2002-04-03 | Sumitomo Chemical Company, Limited | Method for producing E-caprolactam and reactor for the method |
Family Cites Families (38)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3503958A (en) | 1964-10-29 | 1970-03-31 | Mobil Oil Corp | Molecular rearrangement of oximes |
| DE1545789A1 (de) | 1965-02-10 | 1969-10-02 | Bayer Ag | Verfahren zum Herstellen von Lactamen |
| US4677243A (en) * | 1982-10-04 | 1987-06-30 | Union Carbide Corporation | Production of light olefins from aliphatic hetero compounds |
| US4499327A (en) * | 1982-10-04 | 1985-02-12 | Union Carbide Corporation | Production of light olefins |
| IT1187661B (it) | 1985-04-23 | 1987-12-23 | Enichem Sintesi | Catalizzatore a base di silicio e titanio ad elevata resistenza meccanica |
| JP3066047B2 (ja) | 1990-08-03 | 2000-07-17 | 中外製薬株式会社 | 新規なビタミンd▲下3▼誘導体 |
| DE4125457A1 (de) | 1991-08-01 | 1993-02-04 | Bayer Ag | Verfahren zur herstellung von n-substituierten lactamen |
| KR100224333B1 (ko) | 1991-11-27 | 1999-10-15 | 고오사이 아끼오 | ε-카프로락탐의 제조방법 |
| US5292880A (en) | 1992-05-11 | 1994-03-08 | Mobil Oil Corporation | Synthesis of caprolactam using catalysts |
| US5242676A (en) | 1992-05-11 | 1993-09-07 | Mobil Oil Corp. | Selective surface dealumination of zeolites using dicarboxylic acid |
| JPH09291074A (ja) | 1996-04-26 | 1997-11-11 | Sumitomo Chem Co Ltd | ε−カプロラクタムの製造方法 |
| US6350428B1 (en) * | 1997-05-29 | 2002-02-26 | Exxonmobil Chemical Patents Inc. | Preparation of zeolite-bound FAU structure type zeolite and use thereof |
| US6331500B1 (en) * | 1997-08-25 | 2001-12-18 | California Institute Of Technology | Functionalized molecular sieves |
| JP2001072657A (ja) | 1999-06-28 | 2001-03-21 | Mitsubishi Chemicals Corp | アミド化合物の製造方法 |
| JP2001072658A (ja) | 1999-06-28 | 2001-03-21 | Mitsubishi Chemicals Corp | アミド化合物の製造方法 |
| TW526172B (en) | 1999-06-30 | 2003-04-01 | Sumitomo Chemical Co | A process for producing pentacyl-type crystalline zeolites and a process for producing ε-caprolactam using the same |
| IT1314001B1 (it) | 1999-11-19 | 2002-12-03 | Enichem Spa | Metodo per la rimozione del templante da zeoliti sintetiche |
| IT1314263B1 (it) | 1999-12-03 | 2002-12-06 | Enichem Spa | Processo per la preparazione di catalizzatori zeolitici. |
| US6489474B1 (en) * | 2000-04-21 | 2002-12-03 | Mitsubishi Chemical Corporation | Process for producing amide compound |
| CN1322927A (zh) | 2001-03-05 | 2001-11-21 | 叶声羽 | 大热水量的电热水器及槓杆式上水自动装置 |
| WO2003024927A1 (fr) | 2001-09-12 | 2003-03-27 | Asahi Kasei Chemicals Corporation | Procede de production de lactame |
| ITMI20012470A1 (it) | 2001-11-23 | 2003-05-23 | Enichem Spa | Procediemnto per la preparazione di vitalizzatori zeolitici di tipo mfi |
| JP3969078B2 (ja) | 2001-12-12 | 2007-08-29 | 住友化学株式会社 | ペンタシル型ゼオライトの製造方法およびε−カプロラクタムの製造方法 |
| US6946553B2 (en) | 2002-02-27 | 2005-09-20 | Sumitomo Chemical Company, Limited | Process for producing ε-caprolactam and catalyst for the production |
| US7326332B2 (en) * | 2003-09-25 | 2008-02-05 | Exxonmobil Chemical Patents Inc. | Multi component catalyst and its use in catalytic cracking |
| US20070112189A1 (en) | 2003-11-17 | 2007-05-17 | Takuji Ikeda | High silica cds-1 zeolite |
| JP4461926B2 (ja) | 2004-06-30 | 2010-05-12 | 住友化学株式会社 | ゼオライトの製造方法及びε−カプロラクタムの製造方法 |
| GB2450711A (en) | 2007-07-03 | 2009-01-07 | Univ Southampton | An aluminophosphate based redox catalyst |
| JP2010047499A (ja) | 2008-08-20 | 2010-03-04 | Univ Of Tokyo | ε−カプロラクタムの製造方法及びペンタシル型ゼオライトの製造方法 |
| DE102008060340A1 (de) | 2008-12-03 | 2010-06-10 | Wolfgang F. Prof. Dr. Hölderich | Herstellung von Lactamen und Carbonsäureamide durch Beckmann-Umlagerung von Oximen in Gegenwart von Nb-Katalysatoren |
| GB0900198D0 (en) | 2009-01-07 | 2009-02-11 | Univ Southampton | Ammoximation process |
| CN102050464B (zh) | 2009-10-30 | 2012-07-25 | 中国石油化工股份有限公司 | 硅分子筛的合成方法 |
| GB2475740B (en) * | 2009-11-30 | 2017-06-07 | Johnson Matthey Plc | Catalysts for treating transient NOx emissions |
| JP2012066977A (ja) | 2010-09-27 | 2012-04-05 | Sumitomo Chemical Co Ltd | ゼオライトの製造方法及びε−カプロラクタムの製造方法 |
| JP2012158501A (ja) | 2011-02-02 | 2012-08-23 | Sumitomo Chemical Co Ltd | ゼオライトの製造方法及びε−カプロラクタムの製造方法 |
| CN102188989B (zh) | 2011-03-24 | 2013-08-07 | 中国天辰工程有限公司 | 一种流化床催化剂及制备方法 |
| CN102432032B (zh) | 2011-09-16 | 2013-05-15 | 湖南大学 | 一种纳米全硅分子筛及其制备方法与应用 |
| US8772476B2 (en) * | 2011-10-28 | 2014-07-08 | Honeywell International Inc. | Gas and liquid phase catalytic Beckmann rearrangement of oximes to produce lactams |
-
2012
- 2012-10-23 US US13/658,495 patent/US8772476B2/en active Active
- 2012-10-25 EP EP12842979.2A patent/EP2771317B1/en active Active
- 2012-10-25 ES ES12842979T patent/ES2856699T3/es active Active
- 2012-10-25 KR KR1020147014091A patent/KR102002197B1/ko active IP Right Grant
- 2012-10-25 IN IN3074DEN2014 patent/IN2014DN03074A/en unknown
- 2012-10-25 WO PCT/US2012/061876 patent/WO2013063244A1/en active Application Filing
- 2012-10-25 BR BR112014010194A patent/BR112014010194A8/pt not_active Application Discontinuation
- 2012-10-25 JP JP2014538999A patent/JP6243340B2/ja active Active
- 2012-10-25 RU RU2014121157A patent/RU2609779C2/ru active
- 2012-10-25 MX MX2014005018A patent/MX354802B/es active IP Right Grant
- 2012-10-25 CN CN201280052939.1A patent/CN104039760B/zh active Active
-
2014
- 2014-04-28 CO CO14089762A patent/CO6950487A2/es active IP Right Grant
- 2014-04-28 US US14/263,156 patent/US9662643B2/en active Active
- 2014-05-09 US US14/273,688 patent/US9221762B2/en active Active
-
2017
- 2017-04-07 JP JP2017076432A patent/JP2017200906A/ja active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4440871A (en) * | 1982-07-26 | 1984-04-03 | Union Carbide Corporation | Crystalline silicoaluminophosphates |
| US4873325A (en) * | 1986-06-25 | 1989-10-10 | Uop | Process for the production of amides |
| US5312915A (en) * | 1993-03-04 | 1994-05-17 | Sumitomo Chemical Company, Limited | Process for producing epsilon-caprolactam |
| EP1193251A2 (en) * | 2000-09-29 | 2002-04-03 | Sumitomo Chemical Company, Limited | Method for producing E-caprolactam and reactor for the method |
Non-Patent Citations (1)
| Title |
|---|
| Ramesh B.Borade et al, A comparative study of acidic properties of SAPO-5, -11, -34 and -37 molecular sieves, Journal of molecular catalysis, vol.88, no 2, 1994, pp 249-265. M.Briend et al, Dependence of the acidic properties of SAPO-37 molecular sieves on Si content and heat treatment, Journal of catalysis, 138, 1992, pp 90-100. * |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2672912C1 (ru) * | 2014-12-16 | 2018-11-21 | Эдвансикс Ресинс Энд Кемикалс Ллк | Иерархические алюмофосфаты в качестве катализаторов для перегруппировки бекмана |
| US10537884B2 (en) | 2014-12-16 | 2020-01-21 | Advansix Resins & Chemicals Llc | Hierarchical aluminophosphates as catalysts for the Beckmann rearrangement |
Also Published As
| Publication number | Publication date |
|---|---|
| US8772476B2 (en) | 2014-07-08 |
| JP2015501321A (ja) | 2015-01-15 |
| BR112014010194A2 (pt) | 2017-06-13 |
| CN104039760A (zh) | 2014-09-10 |
| IN2014DN03074A (ru) | 2015-05-15 |
| JP6243340B2 (ja) | 2017-12-06 |
| US20130109851A1 (en) | 2013-05-02 |
| EP2771317B1 (en) | 2020-12-09 |
| MX2014005018A (es) | 2014-07-09 |
| WO2013063244A1 (en) | 2013-05-02 |
| KR102002197B1 (ko) | 2019-07-19 |
| CO6950487A2 (es) | 2014-05-20 |
| BR112014010194A8 (pt) | 2017-06-20 |
| EP2771317A1 (en) | 2014-09-03 |
| US20160279622A9 (en) | 2016-09-29 |
| EP2771317A4 (en) | 2015-10-07 |
| ES2856699T3 (es) | 2021-09-28 |
| MX354802B (es) | 2018-03-22 |
| JP2017200906A (ja) | 2017-11-09 |
| US9221762B2 (en) | 2015-12-29 |
| KR20150000863A (ko) | 2015-01-05 |
| US20150126732A1 (en) | 2015-05-07 |
| US20150306586A1 (en) | 2015-10-29 |
| RU2014121157A (ru) | 2015-12-10 |
| CN104039760B (zh) | 2018-03-09 |
| US9662643B2 (en) | 2017-05-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10537884B2 (en) | Hierarchical aluminophosphates as catalysts for the Beckmann rearrangement | |
| Yun et al. | Mechanistic study of glycerol dehydration on Brønsted acidic amorphous aluminosilicate | |
| EP4249115A2 (en) | Molding for a hydrophobic zeolitic material | |
| Ding et al. | Clean synthesis of acetaldehyde oxime through ammoximation on titanosilicate catalysts | |
| RU2609779C2 (ru) | Газофазная и жидкофазная каталитическая перегруппировка бекмана оксимов с получением лактамов | |
| CN109289902B (zh) | 一种提高成型mfi分子筛催化贝克曼重排反应性能的方法 | |
| EP1101735B1 (en) | Method for the removal of the templating agent from synthetic zeolites | |
| Zhang et al. | In situ synthesis of Pt nanoparticles encapsulated in silicalite-1 zeolite via a steam-assisted dry-gel conversion method | |
| US8450526B2 (en) | Ammoximation process | |
| JP2012514628A (ja) | アンモオキシム化方法 | |
| US7232784B2 (en) | Metal oxide-containing kenyaite catalyst, method for preparing the same, and method for preparing ε-caprolactam using the same | |
| JP4465731B2 (ja) | ε−カプロラクタムの製造方法 | |
| JPH06256304A (ja) | ε−カプロラクタムの製法 |