RU2411945C2 - Комбинированное лекарственное средство, содержащее пробукол и производное тетразолилалкоксидигидрокарбостирила, с эффектами супрессора супероксида - Google Patents
Комбинированное лекарственное средство, содержащее пробукол и производное тетразолилалкоксидигидрокарбостирила, с эффектами супрессора супероксида Download PDFInfo
- Publication number
- RU2411945C2 RU2411945C2 RU2008114512/15A RU2008114512A RU2411945C2 RU 2411945 C2 RU2411945 C2 RU 2411945C2 RU 2008114512/15 A RU2008114512/15 A RU 2008114512/15A RU 2008114512 A RU2008114512 A RU 2008114512A RU 2411945 C2 RU2411945 C2 RU 2411945C2
- Authority
- RU
- Russia
- Prior art keywords
- probucol
- combination
- derivative
- superoxide
- dihydrocarbostyril
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/095—Sulfur, selenium, or tellurium compounds, e.g. thiols
- A61K31/10—Sulfides; Sulfoxides; Sulfones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/095—Sulfur, selenium, or tellurium compounds, e.g. thiols
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4704—2-Quinolinones, e.g. carbostyril
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
- A61P39/06—Free radical scavengers or antioxidants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Diabetes (AREA)
- Cardiology (AREA)
- Hematology (AREA)
- Heart & Thoracic Surgery (AREA)
- Obesity (AREA)
- Urology & Nephrology (AREA)
- Hospice & Palliative Care (AREA)
- Emergency Medicine (AREA)
- Endocrinology (AREA)
- Vascular Medicine (AREA)
- Biochemistry (AREA)
- Toxicology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Изобретение относится к области фармацевтики и касается комбинированного лекарственного средства для предотвращения и лечения церебрального инфаркта, артериосклероза, почечных заболеваний и диабета, включающего комбинацию производного тетразолилалкоксидигидрокарбостирила формулы (1) и пробукола, благодаря синергическим эффектам комбинации в качестве супрессора супероксида. 27 н. и 3 з.п. ф-лы, 6 ил.
Description
Область техники, к которой относится изобретение
Это изобретение касается комбинированного лекарственного средства для лечения и предотвращения церебрального инфаркта, артериосклероза, почечных заболеваний или диабета. Более конкретно, оно касается комбинированного лекарственного средства для лечения и предотвращения церебрального инфаркта, артериосклероза, почечных заболеваний или диабета, которое включает комбинацию по меньшей мере одного из производных тетразолилалкоксидигидрокарбостирила формулы:
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную связь или двойную связь, или его соли, и пробукола.
Комбинированное лекарственное средство согласно настоящему изобретению эффективно при церебральном инфаркте, артериосклерозе, почечных заболеваниях или диабете благодаря активности в подавлении супероксида, основанной на синергических эффектах комбинации вышеупомянутого производного тетразолилалкоксидигидрокарбостирила (1) и пробукола (= 4,4'-изопропилидендитиобис[2,6-ди-трет-бутилфенол]).
Уровень техники, к которой относится изобретение
Церебральный инфаркт, включающий острый церебральный инфаркт и хронический церебральный инфаркт, также известный как инсульт или церебромаляция, вызывается нарушением кровоснабжения части мозга вследствие закупорки или стеноза церебральной артерии и/или вены, имеющих результатом некроз ткани или клеток головного мозга. Наиболее важными факторами риска в этих ситуациях являются повышенное кровяное давление, порок сердца, диабет и курение сигарет. Для лечения церебрального инфаркта важно подавление развития некроза, обусловленного свободными радикалами, и распространения церебрального поражения, и применялись антикоагулянты, тромболитические средства, такие как урокиназа, тканевой активатор плазминогена (tPA).
Артериосклероз, этот термин часто употребляется взаимозаменяемо с атеросклерозом, имеет место в условиях, когда стенки артерий утолщаются и становятся жесткими и кровоснабжение органов и тканей ограничивается. Хотя причина этого неизвестна, предполагается, что он начинается с дефекта или повреждения внутреннего слоя артерии, и повреждение может быть вызвано разнообразными факторами, в том числе высоким кровяным давлением, высоким содержанием холестерина, воздействием раздражителя (например, никотина) и некоторыми болезнями, такими как диабет. Для лечения артериосклероза использовались различные лекарственные средства, например, антихолестериновые препараты (например, пробукол, статины, клофибраты), антитромбоцитарные препараты (например, аспирин), антикоагулянты (например, гепарин, варфарин), средства регулирования кровяного давления (например, ингибиторы ангиотензин-превращающего фермента (АСЕ, АПФ), блокаторы кальциевых каналов).
Почечные заболевания, включая диабетическую нефропатию, почечную недостаточность и нефрит, характеристичны в таких функциональных изменениях, как избыточная клубочковая фильтрация в почках и альбуминурия, и таких гистологических изменениях, как гломерулярный склероз вследствие роста белка внеклеточного матрикса. Считается, что почечные заболевания вызываются продолжительным высоким уровнем сахара в крови, ненормальным внутриклеточным метаболизмом (например, усилением полиольного пути и гексозаминового пути обмена глюкозы, и активации протеинкиназы С (РКС)) вследствие гипергликемии, накоплением конечных продуктов избыточного гликолиза (AGE), повышенным давлением вследствие клубочковой гипертензии, или повышенным оксидантным стрессом, и что многие важные причины возникновения почечных заболеваний обусловливаются повышенным оксидантным стрессом, а также гипергликемией, в свете сообщений, что активный кислород усиливает внутриклеточный ненормальный метаболизм или процесс формирования AGE (см. журнал Nature, том 414, стр. 813-820, 2001), и что все усиления гексозаминового пути, активации протеинкиназы С (РКС) и роста AGE подавляются ингибированием избыточной продукции супероксида в митохондрии (см. журнал Nature, том 404, стр. 787-790, 2000).
Известно, что обострение резистентности к инсулину является важным фактором начала диабета, но обострение резистентности к инсулину становится не только патогенезом метаболического синдрома, такого как диабет, но также способствует возникновению и развитию сердечно-сосудистых заболеваний и почечных заболеваний (см. журнал Arterioscler. Thromb. Vasc. Biol., том 24, стр. 816-823, 2004), и тем самым предполагалось, что преодоление резистентности к инсулину является полезным для лечения диабета и диабетических осложнений. Также сообщалось, что усиленный оксидантный стресс может быть важным фактором индуцирования резистентности к инсулину (см. журнал Nature, том 440, стр. 944-948, 2006), и тем самым ингибитор оксидантного стресса может быть полезным для предотвращения и лечения диабета и возникновения и развития почечных заболеваний в свете улучшения активности резистентности к инсулину.
Хотя численность диабетических пациентов с почечными заболеваниями возрастает год от года, так и не найдено применимой терапии для лечения почечных заболеваний.
Между прочим, было известно, что кислород является исключительно важным для живого организма, чтобы поддерживать жизнь, например, чтобы сохранять стабильными выработку энергии и обмен веществ. Кислород в живом организме может быть изменен в так называемый активный кислород. Активный кислород включает радикальный кислород и нерадикальный кислород. В ряду активного кислорода в широком смысле, включая имеющие отношение к липидам материалы, названный первым радикальный кислород включает гидроксильный радикал (·OH), алкоксильный радикал, пероксидный радикал, гидропероксидный радикал, монооксид азота, диоксид азота, супероксид (О2 ·-) и т.д. Названная последней группа нерадикального кислорода включает синглетный кислород, озон, пероксид водорода (Н2О2), гидропероксиды липида и т.д.
В ряд активного кислорода, который может быть вредным для тканевых клеток, входят радикальные кислородные частицы О2 ·- и ·ОН, и нерадикальное соединение кислорода Н2О2 (см. журнал YAKUGAKU ZASSHI, том 122, № 3, стр. 203-218 (2002)). Частица О2 ·- генерирует кислород и пероксид водорода при действии супероксиддисмутазы (SOD, СОД) в живом организме. Пероксид водорода превращается в радикал ·ОН при каталитическом действии иона железа, иона меди, присутствующих в клетке. Гидроксильный радикал атакует непосредственно ДНК, белки в живом организме. С другой стороны, гидроксильный радикал реагирует с липидами и тем самым преобразует их в липидные радикалы и затем продуцирует гидропероксид липида.
Таким образом, эти активные кислородные частицы, такие как ·ОН, Н2О2, которые имеют отношение к серьезным заболеваниям, главным образом происходят от анион-радикала О2 ·-, и, тем самым, возникла потребность найти субстанцию, способную подавлять частицу О2 ·-.
Сущность изобретения
Изобретатели интенсивно изучали характеристики фармакологической активности комбинации производного тетразолилалкоксидигидрокарбостирила (1), который известен как обладающий активностью супрессора активного кислорода с известным антигиперлипемическим средством, пробуколом, и было обнаружено, что комбинация проявляет превосходную синергическую антиоксидантную активность, а также отличную синергическую активность в подавлении супероксида, который вызывает церебральный инфаркт, артериосклероз и почечные заболевания, и далее проявляет существенное улучшение резистентности к инсулину и заметно снижает выделение глюкозы с мочой, которое является одним из показателей почечных дисфункций, и затем было найдено, что комбинация производного тетразолилалкоксидигидрокарбостирила (1) и пробукола эффективна для предотвращения и/или лечения церебрального инфаркта, артериосклероза, почечных заболеваний (например, диабетической нефропатии, почечной недостаточности, нефрита) или диабета благодаря отличной активности в подавлении супероксида.
Таким образом, целью изобретения является представление комбинированного лекарственного средства для предотвращения и лечения церебрального инфаркта, включающего производное тетразолилалкоксидигидрокарбостирила (1) и пробукол.
Еще одна цель изобретения состоит в представлении комбинированного лекарственного средства для предотвращения и лечения артериосклероза, включающего производное тетразолилалкоксидигидрокарбостирила (1) и пробукол.
Цель изобретения также состоит в представлении комбинированного лекарственного средства для предотвращения и лечения почечных заболеваний, включающего производное тетразолилалкоксидигидрокарбостирила (1) и пробукол.
Дальнейшая цель изобретения состоит в представлении комбинированного лекарственного средства для предотвращения и лечения диабета, включающего производное тетразолилалкоксидигидрокарбостирила (1) и пробукол.
Также цель изобретения состоит в представлении усовершенствованного супрессора супероксида, включающего производное тетразолилалкоксидигидрокарбостирила (1) и пробукол.
Краткое описание чертежей
Фиг.1 представляет собой график, показывающий корреляцию между концентрацией цилостазола и NAD(P)H-зависимой продукцией О2 ·- при ингибировании самим цилостазолом или комбинацией цилостазола и пробукола NAD(P)H-зависимой продукции О2 ·-.
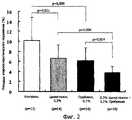
Фиг.2 представляет собой график, показывающий эффекты ингибирования отдельно 0,3%-ным цилостазолом, отдельно 0,1%-ным пробуколом или комбинацией 0,3% цилостазола и 0,1% пробукола для атеросклеротического поражения у мышей с нокаутом рецептора липопротеинов низкой плотности, получавших пищу с высоким содержанием холестерина.
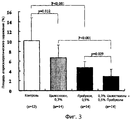
Фиг.3 представляет собой график, показывающий эффекты ингибирования отдельно 0,3%-ным цилостазолом, отдельно 0,5%-ным пробуколом или комбинацией 0,3% цилостазола и 0,5% пробукола для атеросклеротического поражения у мышей с нокаутом рецептора липопротеинов низкой плотности, получавших пищу с высоким содержанием холестерина.
Фиг.4 представляет собой график, показывающий эффекты пробукола и цилостазола по отдельности и комбинации пробукола и цилостазола против фокального церебрального ишемического поражения у крыс.
Фиг.5 представляет собой график, показывающий эффекты пробукола и цилостазола по отдельности и комбинации пробукола и цилостазола против выделения глюкозы с мочой у крыс.
Фиг.6 представляет собой график, показывающий эффекты пробукола и цилостазола по отдельности и комбинации пробукола и цилостазола против резистентности к инсулину у крыс.
Подробное описание изобретения
Производное карбостирила, будучи включенным в качестве одного из компонентов комбинированного лекарственного средства согласно настоящему изобретению, представляет собой производные тетразолилалкоксидигидрокарбостирила формулы:
в которой радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную связь или двойную связь, или его соль.
В вышеуказанной формуле (1) циклоалкильная группа включает С3-С8-циклоалкильные группы, такие как циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Предпочтительной группой является циклогексил. Низшая алкиленовая группа включает С1-С6-алкиленовые группы, такие как метиленовый, этиленовый, пропиленовый, тетраметиленовый, бутиленовый и пентиленовый фрагменты, из которых предпочтительным является тетраметиленовый фрагмент.
Предпочтительным карбостирильным производным является 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирил, который был выведен на рынок под торговым наименованием цилостазол в качестве антитромбоцитарного средства.
Эти производные карбостирила (1) и их соли и способ их получения описаны в патенте США 4277479. В патенте США 6743806 также описано, что производные карбостирила (1) имеют активность подавления активного кислорода.
Другой активный ингредиент, пробукол, представляет собой соединение, имеющее химическое название 4,4'-изопропилидендитиобис[2,6-ди-трет-бутилфенол], уже был выведен на рынок в качестве антигиперлипемического средства. Известно также, что это соединение имеет активность в ингибировании продукции окисленного липопротеина низкой плотности (LDL, ЛПНП) (см. журнал J. Clin. Invest., том 77, стр. 641, 1986).
Эти активные ингредиенты, производное карбостирила (1) и пробукол, могут быть введены вместе или по отдельности, в одно и то же время или в разные моменты времени. Эти ингредиенты обычно могут быть использованы в традиционных фармацевтических препаратах. Далее, эти ингредиенты могут быть приготовлены в фармацевтических препаративных формах в единой лекарственной форме или в отдельных лекарственных формах.
Лекарственные формы не конкретизированы, но могут быть любыми традиционными фармацевтическими препаративными формами, например, препаратами для орального введения, такими как таблетки, капсулы, гранулы, различные жидкие препараты, пригодные для орального употребления, или препаратами для парентерального введения, такими как инъекции, суппозитории.
Дозировка этих активных ингредиентов не ограничивается каким-то конкретным интервалом. Производные карбостирила (1) или их соли могут быть использованы в количестве от 50 до 200 мг/сутки для взрослых (с массой тела 50 кг), которое вводится один раз в день или раздельно на два или несколько приемов в день. Пробукол может быть использован в количестве от 100 до 1000 мг/сутки для взрослых (с массой тела 50 кг), которое может быть введено однократно, но предпочтительно может быть введено с разделением суточной дозы на два или несколько приемов в день. Когда эти ингредиенты готовятся в единой лекарственной форме, они вводятся в соотношении от 0,25 до 10 частей по весу пробукола на 1 часть по весу производного карбостирила (1) или его соли.
Препаративные формы, такие как таблетки, капсулы, жидкости для орального введения, могут быть приготовлены традиционными методами. Таблетки могут быть приготовлены смешением активного(ых) ингредиента(ов) с общеупотребительными носителями, такими как желатин, крахмалы, лактоза, стеарат магния, тальк, гуммиарабик и тому подобные. Капсулы могут быть приготовлены смешением с инертными фармацевтическими наполнителями или разбавителям, и помещены в твердую желатиновую капсулу или в мягкую капсулу. Оральные жидкие составы, такие как сиропы или эликсиры, готовятся смешением активного(ых) ингредиента(ов) и подсластителей (например, сахарозы), консервантов (например, метилпарабена, пропилпарабена), красителей, отдушек и тому подобных. Составы для парентерального введения также могут быть приготовлены общеупотребительным методом, например растворением активного(ых) ингредиента(ов) согласно настоящему изобретению в стерилизованном водном носителе, предпочтительно воде или физиологическом растворе. Предпочтительный водный состав, пригодный для парентерального введения, готовится растворением суточной дозы активных ингредиентов, как упомянутых выше, в воде и органическом растворителе, и далее в полиэтиленгликоле, имеющем молекулярную массу от 300 до 5000, который предпочтительно вводится со смазывающим средством, таким как натриевая соль карбоксиметилцеллюлозы, метилцеллюлоза, поливинилпирролидон и поливиниловый спирт. Вышеназванные жидкие составы предпочтительно могут быть далее введены с дезинфицирующим средством (например, бензиловым спиртом, фенолом, тимеросалом), фунгицидом, и далее по выбору с изотоническим средством (например, сахарозой, хлоридом натрия), местным обезболивающим средством, стабилизатором, буферным раствором и тому подобным. С точки зрения сохранения стабильности, состав для парентерального введения может быть помещен в капсулу, с последующим удалением водной среды с помощью общеупотребительной техники лиофильной сушки, и переведен в жидкий препарат путем растворения в водной среде непосредственно при употреблении.
Согласно настоящему изобретению, при комбинировании производного карбостирила (1), в частности, 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирила, или его соли, с пробуколом, они являются эффективными при церебральном инфаркте, артериосклерозе, почечных заболеваниях (например, диабетической нефропатии, почечной недостаточности, нефрите) или диабете.
Один из механизмов проявления этих эффектов может быть обусловлен отличной активностью в подавлении супероксида, то есть они проявляют отличную синергическую антиоксидантную активность и синергические эффекты подавления супероксида, благодаря которым супероксид, оказывающий вредное воздействие на тканевые клетки, эффективно удаляется. Кроме того, при подавлении супероксида это имеет результатом также ингибирование продукции частиц ·ОН, Н2О2, которые являются производными от супероксида. Комбинированное лекарственное средство согласно настоящему изобретению также может ингибировать продукцию активных кислородных частиц, таких как О2 ·-, ·ОН, Н2О2, которые являются главной причиной серьезных заболеваний. Известно, что супероксид вызывает церебральный инфаркт (например, острый церебральный инфаркт, хронический церебральный инфаркт), артериосклероз, почечные заболевания (например, диабетическую нефтопатию, почечную недостаточность, нефрит) (см. журнал Antioxidants & Redox Signaling, том 5, 2003, стр. 597-607, который описывает участие О2 ·- в церебральном инфаркте; журнал Circ. Res., том 86, 2000, стр. 494-501, который сообщает, что НАДФ(Н)-оксидаза (NAD(P)H) продуцирует супероксид О2 ·- и имеет отношение к болезням системы кровообращения, таким как артериосклероз; журнал Eur. J. Pharmacol., том 450, 2002, стр. 67-76, который описывает участие О2 ·- в почечных заболеваниях).
Таким образом, благодаря синергическим эффектам подавления супероксида комбинация производного карбостирила (1) и пробукола согласно настоящему изобретению может проявлять желаемые эффекты для профилактики и лечения церебрального инфаркта, артериосклероза, почечных заболеваний (например, диабетической нефтопатии, почечной недостаточности, нефрита) или диабета.
Примеры
Настоящее изобретение иллюстрируется нижеследующими примерами приготовления и экспериментами по активности агента в подавлении супероксида согласно настоящему изобретению, но не должно толковаться как ограниченное таковыми.
Состав 1
| Состав таблеток: | |
| Компоненты | Количество (г) |
| 6-[4-(1-Циклогексил-1Н-тетразол-5-ил)бутокси]- | |
| 3,4-дигидрокарбостирил | 100 |
| Пробукол | 250 |
| Лактоза (Японская Фармакопея) | 40 |
| Кукурузный крахмал (Японская Фармакопея) | 40 |
| Кристаллическая целлюлоза (Японская Фармакопея) | 20 |
| Гидроксипропилцеллюлоза (Японская Фармакопея) | 4 |
| Стеарат магния (Японская Фармакопея) | 2 |
Вышеуказанные активные ингредиенты согласно настоящему изобретению, лактоза, кукурузный крахмал и кристаллическая целлюлоза тщательно смешиваются, и смесь гранулируется с 5%-ным водным раствором гидроксипропилцеллюлозы, и гранулированная смесь просеивается через сито с ячейками 200 меш для тщательного высушивания гранул, и затем гранулы таблетируются общеупотребительным способом для формирования таблеток (1000 таблеток).
Фармакологические эксперименты
Эксперимент 1
Синергическое ингибирование комбинацией цилостазола и пробукола NAD(P)H-зависимой продукции О2 ·- из человеческих сосудистых эндотелиальных клеток
(1) Материалы и методы
Клеточные культуры: НСАЕС (эндотелиальные клетки человеческой коронарной артерии) были культивированы в базальной среде-2 эндотелиальных клеток, набор Bulletkit EGM-2. Клетки были выращены до слияния при 37°С в атмосфере с 5% СО2 и использованы для экспериментов при не более чем шестикратном пересеве.
Испытательные материалы были (1) - цилостазол отдельно (n=4), (2) пробукол отдельно (n=4), (3) смесь цилостазола с пробуколом (n=4): конечные концентрации для цилостазола были 0,3, 1,0 и 3,0 микромоля/литр и пробукола 0,01, 0,03 и 0,1 микромоля/литр, которые соответствовали соотношению цилостазола и пробукола между 3:1 и 300:1 по молекулярной массе.
(2) Измерение супероксида
Цилостазол и пробукол были растворены в диметилсульфоксиде с образованием маточных растворов с концентрацией 10 миллимолей/литр. Немедленно после добавления цилостазола и/или пробукола при конечных концентрациях 0, 0,3, 1,0, 3,0 микромолей/литр и 0, 0,01, 0,03, 0,1 микромолей/литр, соответственно, в культуральную среду, был добавлен цитокин TNF-α (50 нг/мл), и клетки НСАЕС были инкубированы в течение 4 часов. После того как клетки были обработаны цитокином TNF-α, эндотелиальные гомогенаты были помещены в люминометр (Microlumat LB96P, фирма EG & G Berthold). Сразу же после записи характеристик хемилюминесценции были добавлены NADH и NADPH (с конечной концентрацией каждого 100 микромолей/литр), и через автоматический дозатор был добавлен адаптированный к темноте люцигенин (динитрат N,N'-диметил-бисакридиния, концентрация 5 микромолей/литр). Интенсивность хемилюминесценции фиксировалась каждые 30 секунд в течение 15 минут, и соответствующий фоновый уровень был вычтен. Хемилюминесценция была выражена в числе отсчетов в секунду на миллиграм белка.
Статистический анализ был проведен следующим образом.
1. Эффекты для отдельного цилостазола или отдельного пробукола были сравнены с эффектами их комбинации с помощью теста Даннетта.
2. Чтобы оценить синергические эффекты их комбинации, двухфакторный анализ отклонений (two-way ANOVA) был проведен между контролем, отдельно цилостазолом, отдельно пробуколом и их комбинацией.
Все испытания были выполнены с помощью двустороннего критерия со значащим уровнем 5%, с помощью программы SAS Software (SAS Institute, Japan, R8.1).
(3) Результаты
Результаты показаны в сопроводительной Фиг.1. В Фиг.1 продольная ось соответствует NAD(P)H-зависимой продукции О2 ·- (% от контроля), и ось абсцисс означает концентрацию цилостазола (микромолей/литр), и линия с ромбическими отметками означает данные для отдельного цилостазола, то есть без пробукола (РО), линия с квадратными отметками означает данные для смеси цилостазола с пробуколом в количестве 0,01 микромоля/литр, линия с треугольными отметками означает данные для смеси цилостазола с пробуколом в количестве 0,03 микромоля/литр, и линия с отметками в виде крестика «×» означает данные для смеси цилостазола с пробуколом в количестве 0,1 микромоля/литр.
Как видно из Фиг.1, когда цилостазол был использован в комбинации с пробуколом, продукция О2 ·- была существенно ингибирована по сравнению с отдельным цилостазолом. Далее, эффект подавления был существенно усилен комбинацией 3 микромолей/литр цилостазола и 0,1 микромоля/литр пробукола (р=0,0322 согласно двухфакторному анализу отклонений (two-way ANOVA)).
Эксперимент 2
Эффекты цилостазола и пробукола по отдельности и в комбинации относительно атеросклероза у мышей-нокаутов с рецептором липопротеина низкой плотности, получающих питание с высоким содержанием холестерина.
(1) Материалы и методы
Были использованы мыши с нокаутом рецептора липопротеинов низкой плотности (LDLR-KO) (журнал J. Clin. Invest., 1993; том 92: стр. 883-893) (самцы, возраст 9 недель, которые были получены и содержались в фирме Otsuka Pharmaceutical Co., Ltd.). Животные были обработаны с разделением на следующие шесть групп.
1) контрольная группа (n=13),
2) группа с введением 0,3% цилостазола (n=14),
3) группа с введением 0,1% пробукола (n= 14),
4) группа с введением 0,5% пробукола (n=14),
5) группа с введением 0,3% цилостазола + 0,1% пробукола (n=14),
6) группа с введением 0,3% цилостазола + 0,5% пробукола (n=14).
Перед началом эксперимента были измерены массы тела животных и общее содержание холестерина, и, основываясь на обоих данных, животные были разделены на шесть групп в произвольном порядке по методу стратифицированной рандомизации (программа SAS Software, R8.1). Дозы пробукола и цилостазола были определены на основе опубликованных данных (журналы Horm. Metab. Res., 2001; том 33: стр. 472-479, и J. Pharmacol. Exp. Ther., 2005; том 313: стр. 502-509), соответственно. В контрольной группе мыши получали рацион с высоким содержанием жира [то есть традиционное питание (CRF-1, приготовленное фирмой Oriental Yeast Industries Co., Ltd.), дополненное холестерином (1,25%), холатом натрия (0,5%) и какао-маслом (15%)], и в группе с введением тестового материала мыши получали рацион с высоким содержанием жира, комбинированный с цилостазолом (0,3%) и/или пробуколом (0,1% или 0,5%). Рацион с высоким содержанием жира получали LDLR-KO-мыши (с возраста 9 недель), чтобы индуцировать атеросклероз (в контрольной группе). В группах с введением тестового материала мыши (с возраста 9 недель) получали рацион с высоким содержанием жира, смешанный с тестовым материалом. Мыши в обеих группах были препарированы через восемь недель после начала введения рациона. Атеросклеротическое поражение было оценено изъятием целой аорты под эфирной анестезией, обнажением внутренней поверхности аорты и окрашиванием жировых отложений красителем Судан IV. Площадь атеросклеротического поражения (содержащего жиры/липиды) в аорте в целом была определена анализом изображений окрашенной зоны и общей площади аорты.
Статистический анализ был проведен следующим образом.
1. Чтобы подтвердить синергические эффекты комбинации цилостазола и пробукола, был проведен двухфакторный анализ отклонений (two-way ANOVA) между контрольной группой и группой, получавшей цилостазол, а также между группой, получавшей пробукол, и группой, получавшей оба средства, и тем самым наблюдалось взаимодействие.
2. Эффекты в группах, получавших цилостазол и пробукол, были сравнены с эффектами в контрольной группе в тесте Даннетта. Далее, эффекты в группах, получавших цилостазол и пробукол, были сравнены с эффектами группы, получавшей цилостазол + пробукол, с помощью теста Даннетта.
Все тесты были выполнены с помощью двустороннего критерия со значащим уровнем 5%, с использованием программы SAS Software (SAS Institute, Japan, R8.1).
(2) Результаты
Площадь атеросклеротического поражения была рассчитана как отношение (%) площади, окрашенной Суданом IV, к общей площади аорты. Значащие величины ± стандартное отклонение составляли 10,1 ±4,7% в контрольной группе, 6,6 ±2,6% в группе, получавшей цилостазол, 6,2 ±2,6% в группе, получавшей 0,1% пробукола, 4,7 ±1,2% в группе, получавшей 0,5% пробукола, 3,8 ±1,2% в группе, получавшей цилостазол + 0,1% пробукола, и 2,9 ±1,5% в группе, получавшей цилостазол + 0,5% пробукола.
Как показано в сопроводительных Фиг.2 и Фиг.3, цилостазол (0,3%) и пробукол (0,1 и 0,5%) существенно ингибировали атеросклеротическое поражение у LDLR-KO-мышей. Кроме того, когда вводились комбинации двух средств, артериосклероз был ингибирован более значительно в каждой комбинации с дозами пробукола.
Эксперимент 3
Эффекты пробукола и цилостазола по отдельности и в комбинации в отношении Фокального церебрального ишемического поражения у крыс.
(1) Материалы и методы
Самцы крыс Спрейга-Доули с массой 280-320 г были анестезированы пентобарбиталом натрия (20 мг/кг, внутрибрюшинным введением) и помещены на нагреваемую подушку (Homeothermic Blanket System, Harvard Apparatus, South Natick, MA) для поддержания постоянной ректальной температуры (37 ±0,5°С). Системное артериальное кровяное давление, кислотно-основный баланс артериальной крови и величина рН измерялись предварительно, во время ишемии и после 22-часовой реперфузии.
Фокальная церебральная ишемия была индуцирована путем временной окклюзии левой средней мозговой артерии (МСА), как было описано ранее (Stroke, 1989; 20:84-91). Хирургическая найлоновая шовная нить (размер 3-0) с скругленным концом была продвинута из внешней сонной артерии в просвет внутренней сонной артерии вплоть до блокирования кровотока в средней церебральной артерии (МСА). Через два часа после окклюзии МСА была обеспечена возможность реперфузии путем удаления шовной нити до очищения просвета внутренней сонной артерии.
Для анализа церебрального инфаркта при 22-часовой реперфузии после двухчасовой окклюзии МСА крысы, которым была введена избыточная доза тиопентала натрия, были декапитированы, и затем мозг был быстро извлечен и заморожен подвешиванием над жидким азотом. Мозг был разрезан на блоки толщиной 2 мм в направлении венечного шва. Мозговые срезы были погружены в 2%-ный раствор хлорида 2,3,5-трифенилтетразолия (ТТС) в нормальном физиологическом растворе при 37°С на 30 минут и затем фиксированы в 10%-ном забуференном фосфатным буфером формалине при 4°С. Окрашенные ТТС мозговые срезы были сфотографированы с использованием CCD-видеокамеры, и размер инсульта был рассчитан с помощью системы анализа изображений (Image-Pro Plus, Media Cybernetics, Maryland) и выражен в форме процентной доли пораженной ткани в отношении ипсилатерального полушария.
Цилостазол и пробукол были растворены в диметилсульфоксиде (ДМСО, DMSO) с образованием маточного раствора с концентрацией 30 мг/мл и разбавлены забуференным фосфатом физиологическим раствором до концентрации 10 мг/мл, соответственно. В одной группе крысы получили орально 20 мг/кг цилостазола два раза через 5 минут и через 4 часа после завершения окклюзии МСА, соответственно. Другая группа крыс получила 30 мг/кг пробукола орально два раза через 5 минут и через 4 часа после завершения окклюзии МСА, соответственно. Группа крыс получила комбинацию 20 мг/кг цилостазола плюс 30 мг/кг пробукола орально два раза, соответственно. Группа «носителя» получила 30%-ный раствор ДМСО (300 мкл) орально без цилостазола/пробукола.
Статистический анализ был проведен следующим образом. Данные были выражены как среднее значение ± S.E.M. (стандартная ошибка среднего). Сравнение результатов площадей полушарного инфаркта между группами анализируется дисперсионным анализом с учетом повторных измерений, согласно Tukey's тестам множественного сравнения в качестве апостериорного (post hoc) сравнения. Значения с P<0,05 расценивались как статистически достоверные.
(2) Результаты
Зона церебральной ишемии была единообразно идентифицирована в коре и полосатом теле мозга левого мозгового полушария как отчетливая тускло-окрашенная область у крыс, подвергнутых двухчасовой ишемии/22-часовой реперфузии. Как показано в сопроводительной Фиг.4, площадь инфаркта была сокращена лишь минимально, когда животные получали орально 20 мг/кг цилостазола два раза через 5 минут и через 4 часа после завершения двухчасовой ишемии, тогда как 30 мг/кг пробукола не дали никакого эффекта. Введение цилостазола (20 мг/кг) и пробукола (30 мг/кг) в комбинации существенно сократило площадь полушарного церебрального инфаркта, будучи сравненным с таковым для носителя, обозначив этим сильный синергический эффект комбинированной терапии.
Эксперимент 4
Эффекты пробукола и цилостазола по отдельности и в комбинации против выделения глюкозы с мочой и резистентности к инсулину у крыс
(1) Материалы и методы
Самцы линии крыс с наследственным ожирением Otsuka Long-Evans Tokushima Fatty (OLETF) (возрастом 6 недель) были произвольно разделены на следующие четыре группы в зависимости от масс тела по методу стратифицированной рандомизации (с использованием программы SAS Software, R8.1):
i) Контрольная группа: n=10,
ii) Группа, получившая 0,3% цилостазола: n=10,
iii) Группа, получившая 0,5% пробукола: n=10,
iv) Группа, получившая 0,3% цилостазола + 0,5% пробукола: n=9.
Сразу же после рандомизированного подразделения на группы мыши в каждой группе получали рацион с высоким содержанием жира (имеющееся в продаже питание (CRF-1, приготовленное фирмой Oriental Yeast Industries Co., Ltd.), дополненный холестерином (1,25%), холатом натрия (0,5%) и какао-маслом (15%), чтобы индуцировать начало почечного заболевания. В группах, получающих тестовый материал, каждая мышь немедленно после разделения на группы получала рацион с высоким содержанием жира, комбинированный с тестовым материалом.
Через одиннадцать недель после начала питания у мышей была взята кровь из хвостовой вены без анестезирования, и были измерены плазменная концентрация глюкозы и уровень инсулина в плазме. Отдельно была взята моча, и был измерен уровень глюкозы в моче. Глюкоза измерялась энзиматическим методом с использованием имеющегося в продаже набора для измерения глюкозы, и инсулин измерялся с помощью имеющегося в продаже набора ELISA.
Статистический анализ был проведен следующим образом.
1. Чтобы подтвердить синергические эффекты комбинации цилостазола и пробукола, двухфакторный анализ отклонений (two-way ANOVA) был проведен между контрольной группой и группой, получавшей цилостазол, а также между группой, получавшей пробукол, и группой, получавшей два средства, и тем самым наблюдалось взаимодействие.
2. Эффекты в группе, получавшей цилостазол, и группе, получавшей пробукол, были сравнены с эффектами в контрольной группе с использованием теста Даннетта. Далее, эффекты в группе, получавшей цилостазол, и группе, получавшей пробукол, были сравнены с эффектами в группе, получавшей цилостазол + пробукол, с использованием теста Даннетта.
Все тесты были проведены с помощью двустороннего критерия со значащим уровнем 5%, с помощью программы SAS Software (SAS Institute, Japan, R8.1). Данные были показаны средним значением ± SD (стандартное отклонение) (n).
(2) Результаты
1. Эффекты комбинации двух средств на уровень глюкозы в моче
Контрольная группа показала уровень глюкозы в моче при 186 ±171 мг/дл (n=10), который был гораздо выше, чем значение для нормальных крыс (менее, чем 10 мг/дл). В группах, получавших цилостазол и пробукол, каждый по отдельности, уровень глюкозы в моче был существенно понижен, каждое значение составляло 11 ±2 мг/дл (n=10) и 11 ±3 мг/дл (n=10), соответственно, но в группе, получавшей комбинацию двух средств, уровень глюкозы в моче был ингибирован более значительно, при величине 8 ±1 мг/дл (n=9). Эти результаты показаны в сопроводительной Фиг.5.
2. Эффекты комбинации двух средств на резистентность к инсулину
Контрольная группа показала нормальный уровень плазменной глюкозы при 162 ±16 мг/дл, но обнаружила более высокий уровень инсулина в плазме при 9,9 ±5,0 нг/мл (n=10) по сравнению с данными для нормальных крыс. В то время как ни цилостазол, ни пробукол не показали никакого эффекта в отношении уровня плазменной глюкозы, комбинация цилостазола и пробукола показала значительные ингибирующие эффекты в отношении уровня инсулина в плазме по сравнению с введением цилостазола или пробукола по отдельности. Результаты показаны в сопроводительной Фиг.6.
Таким образом, комбинированное лекарственное средство из цилостазола и пробукола показало прекрасные улучшенные эффекты в отношении резистентности к инсулину.
Claims (30)
1. Средство для предотвращения и лечения церебрального инфаркта, включающее комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила формулы:
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и пробукола.
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и пробукола.
2. Средство для предотвращения и лечения артериосклероза, включающее комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.1, и пробукола.
3. Средство для предотвращения и лечения почечных заболеваний, включающее комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.1, и пробукола.
4. Средство для предотвращения и лечения диабета, включающее комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.1, и пробукола.
5. Супрессор супероксида, включающий комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.1, и пробукола.
6. Средство для предотвращения и лечения церебрального инфаркта, которое включает супрессор супероксида, включающий комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила формулы:
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и пробукола.
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и пробукола.
7. Средство для предотвращения и лечения артериосклероза, которое включает супрессор супероксида, включающий комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.6, и пробукола.
8. Средство для предотвращения и лечения почечных заболеваний, включающее супрессор супероксида, включающий комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.6, и пробукола.
9. Средство для предотвращения и лечения диабета, включающее супрессор супероксида, включающий комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.6, и пробукола.
10. Средство по любому из пп.1-9, в котором производное тетразолилалкоксидигидрокарбостирила представляет собой 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирил или его соль.
11. Способ предотвращения и лечения церебрального инфаркта, включающий введение комбинации эффективного количества по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила формулы:
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и эффективного количества пробукола нуждающемуся субъекту.
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и эффективного количества пробукола нуждающемуся субъекту.
12. Способ предотвращения и лечения артериосклероза, который включает введение комбинации эффективного количества по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.11, и эффективного количества пробукола нуждающемуся субъекту.
13. Способ предотвращения и лечения почечных заболеваний, который включает введение комбинации эффективного количества по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.11, и эффективного количества пробукола нуждающемуся субъекту.
14. Способ предотвращения и лечения диабета, который включает введение комбинации эффективного количества по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.11, и эффективного количества пробукола нуждающемуся субъекту.
15. Способ подавления супероксида, который включает введение комбинации эффективного количества по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.11, и эффективного количества пробукола нуждающемуся субъекту.
16. Способ предотвращения и лечения церебрального инфаркта, который включает введение эффективного количества супрессора супероксида, включающего комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила формулы:
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и пробукола нуждающемуся субъекту.
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и пробукола нуждающемуся субъекту.
17. Способ предотвращения и лечения артериосклероза, который включает введение эффективного количества супрессора супероксида, включающего комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.16, и пробукола нуждающемуся субъекту.
18. Способ предотвращения и лечения почечных заболеваний, который включает введение эффективного количества супрессора супероксида, включающего комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.16, и пробукола нуждающемуся субъекту.
19. Способ предотвращения и лечения диабета, который включает введение эффективного количества супрессора супероксида, включающего комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.16, и пробукола нуждающемуся субъекту.
20. Способ по любому из пп.11-19, в котором производное тетразолилалкоксидигидрокарбостирила (1) представляет собой 6-[4-(1-циклогексил-1 Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирил или его соль.
21. Применение комбинации по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила формулы:
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и пробукола для изготовления лекарственного средства для предотвращения и лечения церебрального инфаркта.
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и пробукола для изготовления лекарственного средства для предотвращения и лечения церебрального инфаркта.
22. Применение комбинации по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.21, и пробукола для изготовления лекарственного средства для предотвращения и лечения артериосклероза.
23. Применение комбинации по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.21, и пробукола для изготовления лекарственного средства для предотвращения и лечения почечных заболеваний.
24. Применение комбинации по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.21, и пробукола для изготовления лекарственного средства для предотвращения и лечения диабета.
25. Применение комбинации по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.21, и пробукола для приготовления лекарственного средства для подавления супероксида.
26. Применение супрессора супероксида, включающего комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила формулы:
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и пробукола для изготовления лекарственного средства для предотвращения и лечения церебрального инфаркта.
где радикал R представляет собой циклоалкильную группу, А представляет собой низшую алкиленовую группу, и связь между положениями 3 и 4 в карбостирильном ядре означает одинарную или двойную связь, или его соли, и пробукола для изготовления лекарственного средства для предотвращения и лечения церебрального инфаркта.
27. Применение супрессора супероксида, включающего комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.26, и пробукола для изготовления лекарственного средства для предотвращения и лечения артериосклероза.
28. Применение супрессора супероксида, включающего комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.26, и пробукола для изготовления лекарственного средства для предотвращения и лечения почечных заболеваний.
29. Применение супрессора супероксида, включающего комбинацию по меньшей мере одного производного тетразолилалкоксидигидрокарбостирила (1), как определено в п.26, и пробукола для изготовления лекарственного средства для предотвращения и лечения диабета.
30. Применение по любому из пп.21-29, в котором производное тетразолилалкоксидигидрокарбостирила (1) представляет собой 6-[4-(1-циклогексил-1Н-тетразол-5-ил)бутокси]-3,4-дигидрокарбостирил или его соль.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US71695405P | 2005-09-15 | 2005-09-15 | |
| US60/716,954 | 2005-09-15 | ||
| US76177506P | 2006-01-25 | 2006-01-25 | |
| US60/761,775 | 2006-01-25 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2008114512A RU2008114512A (ru) | 2009-10-20 |
| RU2411945C2 true RU2411945C2 (ru) | 2011-02-20 |
Family
ID=37420867
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2008114512/15A RU2411945C2 (ru) | 2005-09-15 | 2006-09-14 | Комбинированное лекарственное средство, содержащее пробукол и производное тетразолилалкоксидигидрокарбостирила, с эффектами супрессора супероксида |
Country Status (21)
| Country | Link |
|---|---|
| US (2) | US8580818B2 (ru) |
| EP (2) | EP1942895B1 (ru) |
| JP (2) | JP5179354B2 (ru) |
| KR (1) | KR101299320B1 (ru) |
| AR (1) | AR057520A1 (ru) |
| AU (1) | AU2006289752B2 (ru) |
| BR (1) | BRPI0616223A2 (ru) |
| CA (1) | CA2620296C (ru) |
| CY (1) | CY1112716T1 (ru) |
| DK (1) | DK1942895T3 (ru) |
| ES (1) | ES2378896T3 (ru) |
| HK (1) | HK1122996A1 (ru) |
| IL (1) | IL189751A0 (ru) |
| MY (1) | MY145787A (ru) |
| NO (1) | NO20081811L (ru) |
| PL (1) | PL1942895T3 (ru) |
| PT (1) | PT1942895E (ru) |
| RU (1) | RU2411945C2 (ru) |
| SG (1) | SG165379A1 (ru) |
| TW (1) | TWI372053B (ru) |
| WO (1) | WO2007032557A1 (ru) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AR065588A1 (es) * | 2007-03-09 | 2009-06-17 | Otsuka Pharma Co Ltd | Un medicamento para tratar enfermedad pulmonar obstructiva cronica |
| AR070816A1 (es) * | 2008-03-14 | 2010-05-05 | Otsuka Pharma Co Ltd | Farmaco de combinacion para tratar trastornos vasculares |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5535019A (en) | 1978-09-01 | 1980-03-11 | Otsuka Pharmaceut Co Ltd | Carbostyryl derivative |
| JPH04193836A (ja) | 1990-11-26 | 1992-07-13 | Banyu Pharmaceut Co Ltd | 抗高脂血症剤 |
| JPH107590A (ja) | 1996-06-24 | 1998-01-13 | Chugai Pharmaceut Co Ltd | 脳循環障害後遺症または脳虚血後の脳神経障害の治療剤 |
| FR2751540B1 (fr) | 1996-07-26 | 1998-10-16 | Sanofi Sa | Composition pharmaceutique antithrombotique |
| JP2001500875A (ja) | 1996-09-18 | 2001-01-23 | メルク エンド カンパニー インコーポレーテッド | 心臓血管系疾患関連の危険性を減らす併用治療法 |
| US6245797B1 (en) | 1997-10-22 | 2001-06-12 | Merck & Co., Inc. | Combination therapy for reducing the risks associated with cardio-and-cerebrovascular disease |
| AU1387399A (en) * | 1997-11-10 | 1999-05-31 | Vyrex Corporation | Probucol esters and uses thereof |
| US6235311B1 (en) | 1998-03-18 | 2001-05-22 | Bristol-Myers Squibb Company | Pharmaceutical composition containing a combination of a statin and aspirin and method |
| WO2000021507A2 (de) | 1998-10-12 | 2000-04-20 | Andreas Bockelmann | Pharmazeutisch wirksame zusammensetzung |
| ES2263604T5 (es) | 2000-04-10 | 2017-02-07 | Nicholas John Wald | Formulación para la Prevención de Enfermedad Cardiovascular |
| US20020115728A1 (en) * | 2000-09-05 | 2002-08-22 | Roland Stocker | Compositions and methods for treating cardiovascular disorders |
| RU2003126186A (ru) * | 2001-01-26 | 2005-03-10 | Шеринг Корпорейшн (US) | Комбинации ингибитора (ингибиторов) всасывания стерина с сердечно-сосудистым агентом (агентами), предназначенные для лечения патологических состояний сосудов |
| US6576256B2 (en) | 2001-08-28 | 2003-06-10 | The Brigham And Women's Hospital, Inc. | Treatment of patients at elevated cardiovascular risk with a combination of a cholesterol-lowering agent, an inhibitor of the renin-angiotensin system, and aspirin |
| JP2003192573A (ja) | 2001-12-25 | 2003-07-09 | Otsuka Pharmaceut Factory Inc | 経口ゲル製剤 |
| US20030181461A1 (en) | 2002-01-25 | 2003-09-25 | Lautt Wilfred Wayne | Use of phosphodiesterase antagonists to treat insulin resistance |
| US6743806B2 (en) * | 2002-10-23 | 2004-06-01 | Otsuka Pharmaceutical Company, Limited | Active oxygen scavenger |
| JP2005232059A (ja) | 2004-02-18 | 2005-09-02 | Iichiro Shimomura | 低アディポネクチン血症予防・治療剤 |
| WO2006132091A1 (ja) | 2005-06-08 | 2006-12-14 | Kowa Company, Ltd. | 新規なトリグリセリド低下剤 |
| JP4193836B2 (ja) | 2005-10-24 | 2008-12-10 | ブラザー工業株式会社 | インク噴射装置の製造方法 |
-
2006
- 2006-09-14 TW TW095134039A patent/TWI372053B/zh not_active IP Right Cessation
- 2006-09-14 JP JP2008514987A patent/JP5179354B2/ja not_active Expired - Fee Related
- 2006-09-14 US US12/065,619 patent/US8580818B2/en not_active Expired - Fee Related
- 2006-09-14 EP EP06810355A patent/EP1942895B1/en not_active Not-in-force
- 2006-09-14 BR BRPI0616223-1A patent/BRPI0616223A2/pt not_active IP Right Cessation
- 2006-09-14 ES ES06810355T patent/ES2378896T3/es active Active
- 2006-09-14 MY MYPI20080610A patent/MY145787A/en unknown
- 2006-09-14 SG SG201006668-6A patent/SG165379A1/en unknown
- 2006-09-14 RU RU2008114512/15A patent/RU2411945C2/ru not_active IP Right Cessation
- 2006-09-14 PL PL06810355T patent/PL1942895T3/pl unknown
- 2006-09-14 EP EP10177619A patent/EP2275106A1/en not_active Withdrawn
- 2006-09-14 AU AU2006289752A patent/AU2006289752B2/en not_active Ceased
- 2006-09-14 DK DK06810355.5T patent/DK1942895T3/da active
- 2006-09-14 WO PCT/JP2006/318675 patent/WO2007032557A1/en active Application Filing
- 2006-09-14 AR ARP060104020A patent/AR057520A1/es unknown
- 2006-09-14 PT PT06810355T patent/PT1942895E/pt unknown
- 2006-09-14 CA CA2620296A patent/CA2620296C/en not_active Expired - Fee Related
- 2006-09-14 KR KR1020087008859A patent/KR101299320B1/ko not_active IP Right Cessation
-
2008
- 2008-02-25 IL IL189751A patent/IL189751A0/en unknown
- 2008-04-14 NO NO20081811A patent/NO20081811L/no not_active Application Discontinuation
-
2009
- 2009-01-09 HK HK09100257.9A patent/HK1122996A1/xx not_active IP Right Cessation
-
2012
- 2012-04-20 CY CY20121100376T patent/CY1112716T1/el unknown
- 2012-09-11 JP JP2012199804A patent/JP5603393B2/ja not_active Expired - Fee Related
-
2013
- 2013-10-21 US US14/059,368 patent/US20140045889A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| AU2006289752A1 (en) | 2007-03-22 |
| TW200744597A (en) | 2007-12-16 |
| CA2620296C (en) | 2013-10-22 |
| EP1942895B1 (en) | 2012-02-01 |
| KR101299320B1 (ko) | 2013-09-03 |
| JP5603393B2 (ja) | 2014-10-08 |
| CA2620296A1 (en) | 2007-03-22 |
| BRPI0616223A2 (pt) | 2011-06-14 |
| SG165379A1 (en) | 2010-10-28 |
| EP2275106A1 (en) | 2011-01-19 |
| US20140045889A1 (en) | 2014-02-13 |
| US20090176826A1 (en) | 2009-07-09 |
| ES2378896T3 (es) | 2012-04-18 |
| JP5179354B2 (ja) | 2013-04-10 |
| AR057520A1 (es) | 2007-12-05 |
| DK1942895T3 (da) | 2012-03-05 |
| EP1942895A1 (en) | 2008-07-16 |
| IL189751A0 (en) | 2008-12-29 |
| AU2006289752B2 (en) | 2011-06-09 |
| MY145787A (en) | 2012-04-30 |
| NO20081811L (no) | 2008-04-14 |
| WO2007032557A1 (en) | 2007-03-22 |
| JP2013014605A (ja) | 2013-01-24 |
| PL1942895T3 (pl) | 2012-07-31 |
| PT1942895E (pt) | 2012-03-29 |
| US8580818B2 (en) | 2013-11-12 |
| HK1122996A1 (en) | 2009-06-05 |
| TWI372053B (en) | 2012-09-11 |
| RU2008114512A (ru) | 2009-10-20 |
| CY1112716T1 (el) | 2016-02-10 |
| JP2009508804A (ja) | 2009-03-05 |
| KR20080049822A (ko) | 2008-06-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10449154B2 (en) | Treatment of NASH with Gemcabene | |
| US11559522B2 (en) | Methods for enhancing liver regeneration | |
| AU2016276951A1 (en) | Methods of using pyruvate kinase activators | |
| KR20110086700A (ko) | 통상의 와파린 요법에 비해 안전성 프로파일이 향상된 다비가트란 에텍실레이트 또는 이의 염을 사용하여 혈전증을 치료하거나 예방하는 방법 | |
| DE112011105169T5 (de) | Neue pharmazeutische Zusammensetzung mit geringen Nebenwirkungen enthaltend anti-Tuberkulose Arzneimittel | |
| KR102017550B1 (ko) | 간에 대한 부작용이 없는 신규의 아세트아미노펜 화합물 조성물 | |
| RU2530645C2 (ru) | Способ лечения или профилактики тромбоза с использованием этексилата дабигатрана или его соли с улучшенной эффективностью по сравнению со стандартным лечением варфарином | |
| RU2411945C2 (ru) | Комбинированное лекарственное средство, содержащее пробукол и производное тетразолилалкоксидигидрокарбостирила, с эффектами супрессора супероксида | |
| CA3218585A1 (en) | Composition for treating autoimmune, alloimmune, inflammatory, and mitochondrial conditions, and uses thereof | |
| Yousif et al. | Role of Ca2+/calmodulin‐dependent protein kinase II in development of vascular dysfunction in diabetic rats with hypertension | |
| CN101267823B (zh) | 具有超氧化物抑制作用的包含普罗布考和四唑基烷氧基-二氢喹诺酮衍生物的组合药物 | |
| WO2022048618A1 (en) | Methods to treat inflammatory bowel disease | |
| TWI552748B (zh) | The use of a compound for the removal of hepatotoxicity against Acetaminophen (APAP) | |
| US20230083417A1 (en) | Therapeutic combination for the treatment of brain ischemia and said therapeutic combination for use in the treatment of brain ischemia | |
| Srivastava et al. | Diabetic Kidney Disease: Routes to drug development, pharmacology and underlying molecular mechanisms | |
| Falah | The role of the cdk5 pathway and NMDA receptor phosphorylation in neurodegeneration in hippocampal sclerosis | |
| WO2002085376A2 (en) | A method for decreasing superoxide anion production and for the treatment of diseases associated with oxidative stress | |
| Bondok et al. | The effect of cholinesterase inhibition on liver dysfunction in experimental acute liver failure: a randomized controlled study. | |
| EP1839675A1 (en) | Novel method of protecting ischemic cardiopathy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20150915 |