KR20180098233A - 록소프로펜을 함유하는 의약 제제 - Google Patents
록소프로펜을 함유하는 의약 제제 Download PDFInfo
- Publication number
- KR20180098233A KR20180098233A KR1020187014745A KR20187014745A KR20180098233A KR 20180098233 A KR20180098233 A KR 20180098233A KR 1020187014745 A KR1020187014745 A KR 1020187014745A KR 20187014745 A KR20187014745 A KR 20187014745A KR 20180098233 A KR20180098233 A KR 20180098233A
- Authority
- KR
- South Korea
- Prior art keywords
- container
- group
- component
- composition
- salts
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/192—Carboxylic acids, e.g. valproic acid having aromatic groups, e.g. sulindac, 2-aryl-propionic acids, ethacrynic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/10—Alcohols; Phenols; Salts thereof, e.g. glycerol; Polyethylene glycols [PEG]; Poloxamers; PEG/POE alkyl ethers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/16—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing nitrogen, e.g. nitro-, nitroso-, azo-compounds, nitriles, cyanates
- A61K47/18—Amines; Amides; Ureas; Quaternary ammonium compounds; Amino acids; Oligopeptides having up to five amino acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/22—Heterocyclic compounds, e.g. ascorbic acid, tocopherol or pyrrolidones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/28—Steroids, e.g. cholesterol, bile acids or glycyrrhetinic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/46—Ingredients of undetermined constitution or reaction products thereof, e.g. skin, bone, milk, cotton fibre, eggshell, oxgall or plant extracts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0087—Galenical forms not covered by A61K9/02 - A61K9/7023
- A61K9/0095—Drinks; Beverages; Syrups; Compositions for reconstitution thereof, e.g. powders or tablets to be dispersed in a glass of water; Veterinary drenches
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/06—Ointments; Bases therefor; Other semi-solid forms, e.g. creams, sticks, gels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/107—Emulsions ; Emulsion preconcentrates; Micelles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/12—Aerosols; Foams
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2121/00—Preparations for use in therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Engineering & Computer Science (AREA)
- Dispersion Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Botany (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicinal Preparation (AREA)
- Medicines Containing Plant Substances (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물의, 고온 보존시에 있어서의 변색을 억제하는 수단의 제공. 다음 성분 (A) 및 (B) : (A) 록소프로펜 또는 그 염 ; (B) 다음 성분 (B-1) ∼ (B-9) 의 어느 것 ; (B-1) 테르펜류 (B-2) 아르니카속의 식물 또는 그 추출물 (B-3) 다가 알코올 (B-4) 셀룰로오스류 (B-5) 토코페롤류 (B-6) 글리시르레틴산류 (B-7) 하기 일반식 (1) 로 나타내는 화합물 (클로르페니라민, 디펜히드라민 등) 또는 그 염 (B-8) 고추 또는 그 추출물 (B-9) 유기 아민을 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제.
Description
본 발명은, 록소닌 (등록상표) 의 유효 성분으로도 알려진 록소프로펜을 함유하는 의약 제제 등에 관한 것이다.
록소프로펜은, 페닐프로피온산계의 비스테로이드성 소염 진통제 (NSAID) 의 일종으로 (비특허문헌 1), 우수한 소염 진통 효과를 발휘한다.
그 때문에, 외용 소염 진통제의 유효 성분으로서 널리 이용되고 있고, 지금까지 변형성 관절증, 근육통, 외상 후의 종창·동통 등의 질환 그리고 증상의 소염·진통 등을 효능 효과로 하는 외용 첩부제 (습포제, 테이프제 등) 나 외용 도포제 (겔제 등) 가 개발·출시되어 있다 (비특허문헌 2).
그런데, 멘톨 등의 테르펜류는, 냉각감을 부여할 목적으로 외용 소염 진통제 등에 배합되어 있고, 록소프로펜과 함께 배합된 외용제도 이미 알려져 있다 (예를 들어, 특허문헌 1 ∼ 5).
또한, 아르니카 등의 국화과 아르니카속의 식물이나 그 추출물에는 소염 작용이 있는 것으로 여겨지고 있고, 록소프로펜과 함께 배합된 외용제도 이미 알려져 있다 (예를 들어, 특허문헌 6).
또한, 1,3-부틸렌글리콜 등의 다가 알코올은 외용 소염 진통제 등에 배합되어 있고, 록소프로펜과 함께 배합된 외용제도 이미 알려져 있다 (예를 들어, 특허문헌 5, 7).
또한, 하이드록시프로필메틸셀룰로오스 등의 셀룰로오스류는 외용 소염 진통제 등에 배합되어 있고, 록소프로펜과 함께 배합된 외용제도 이미 알려져 있다 (예를 들어, 특허문헌 4, 8).
또한, 감초, 글리시르레틴산 등의 글리시르레틴산류는 외용 소염 진통제 등에 배합되어 있고, 록소프로펜과 함께 배합된 외용제도 이미 알려져 있다 (예를 들어, 특허문헌 8).
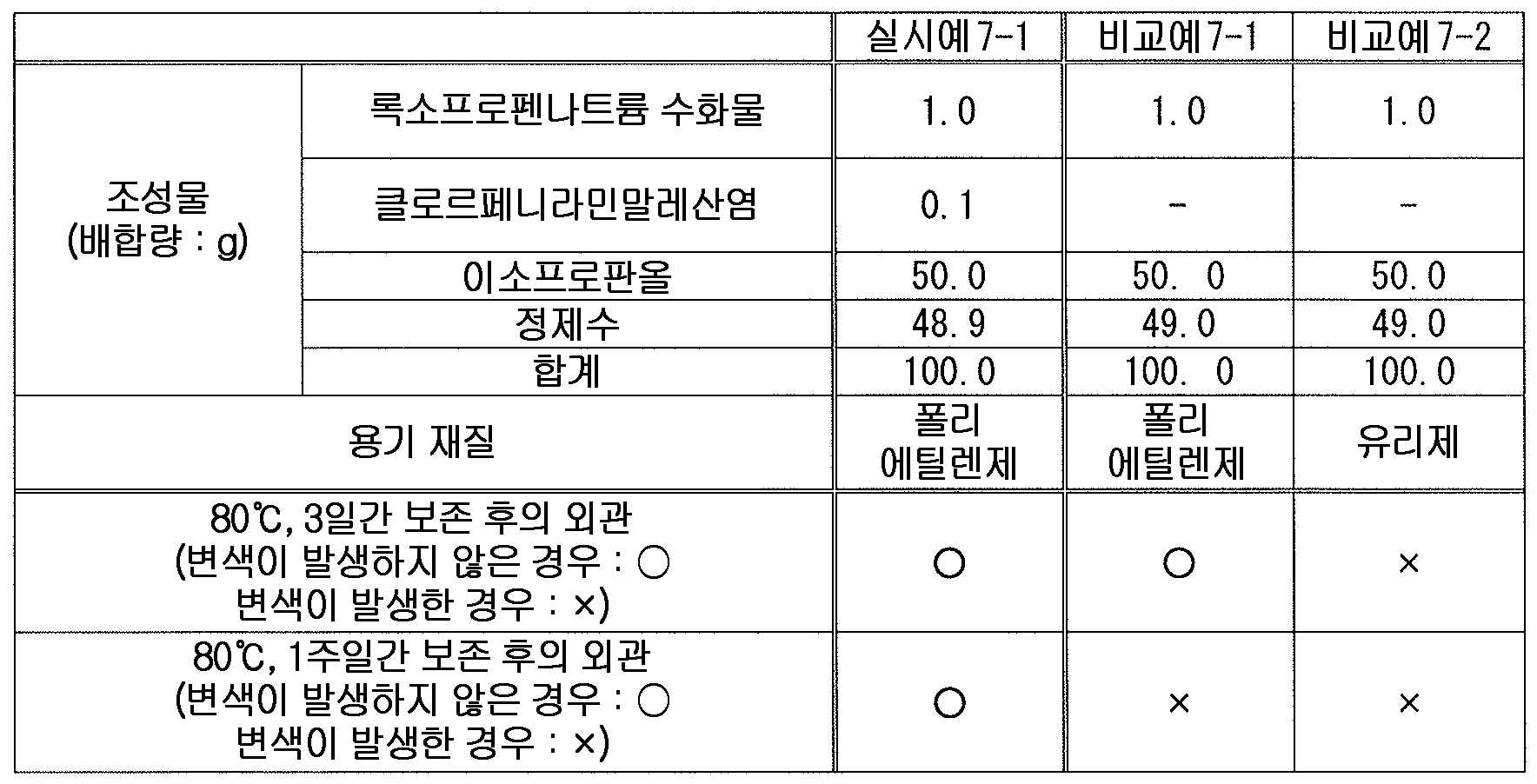
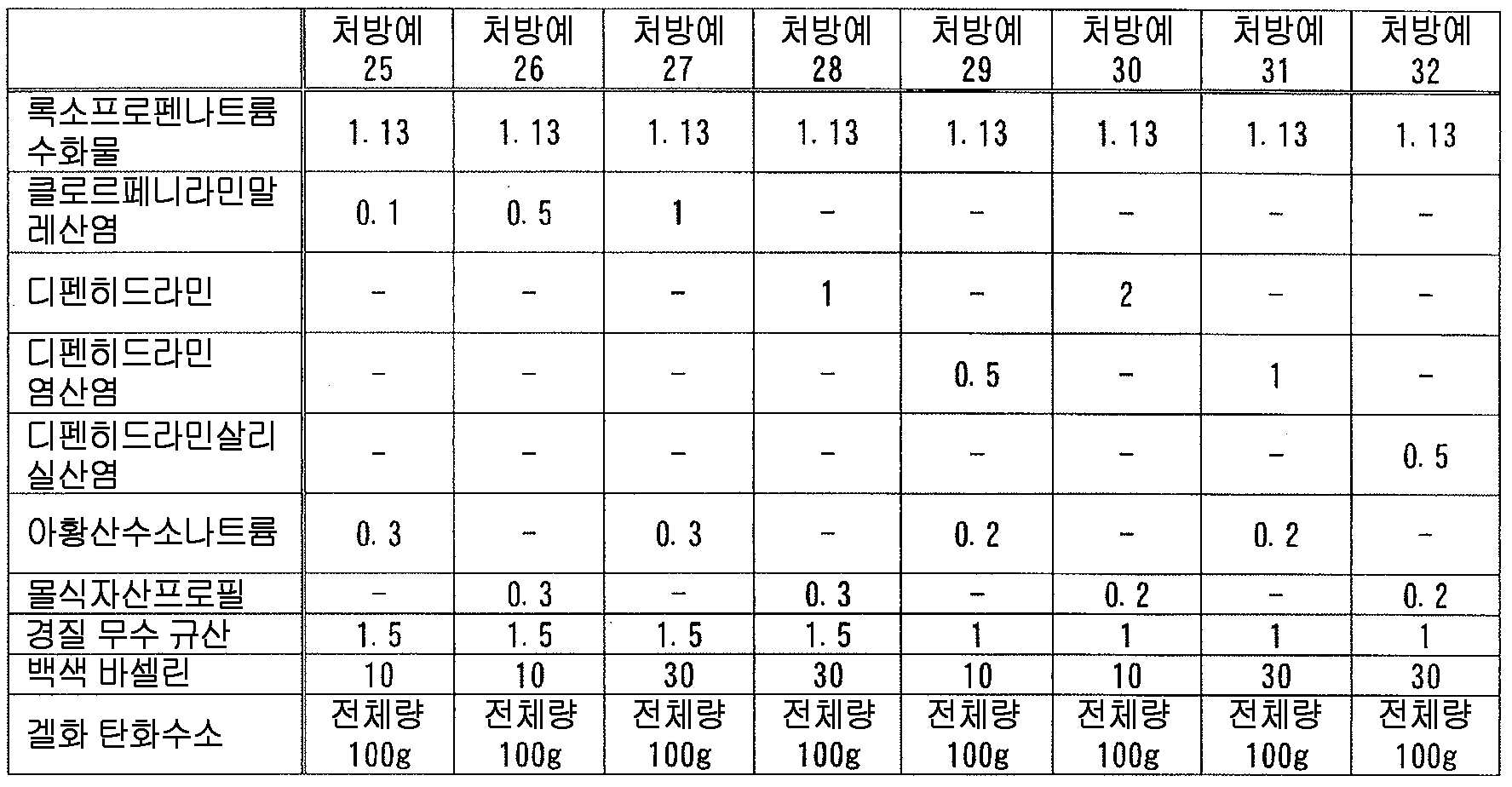
또한, 클로르페니라민말레산염, 디펜히드라민염산염 등의 항히스타민제는 외용 소염 진통제 등에 배합되어 있고, 록소프로펜과 함께 배합된 외용제도 이미 알려져 있다 (예를 들어, 특허문헌 5, 7).
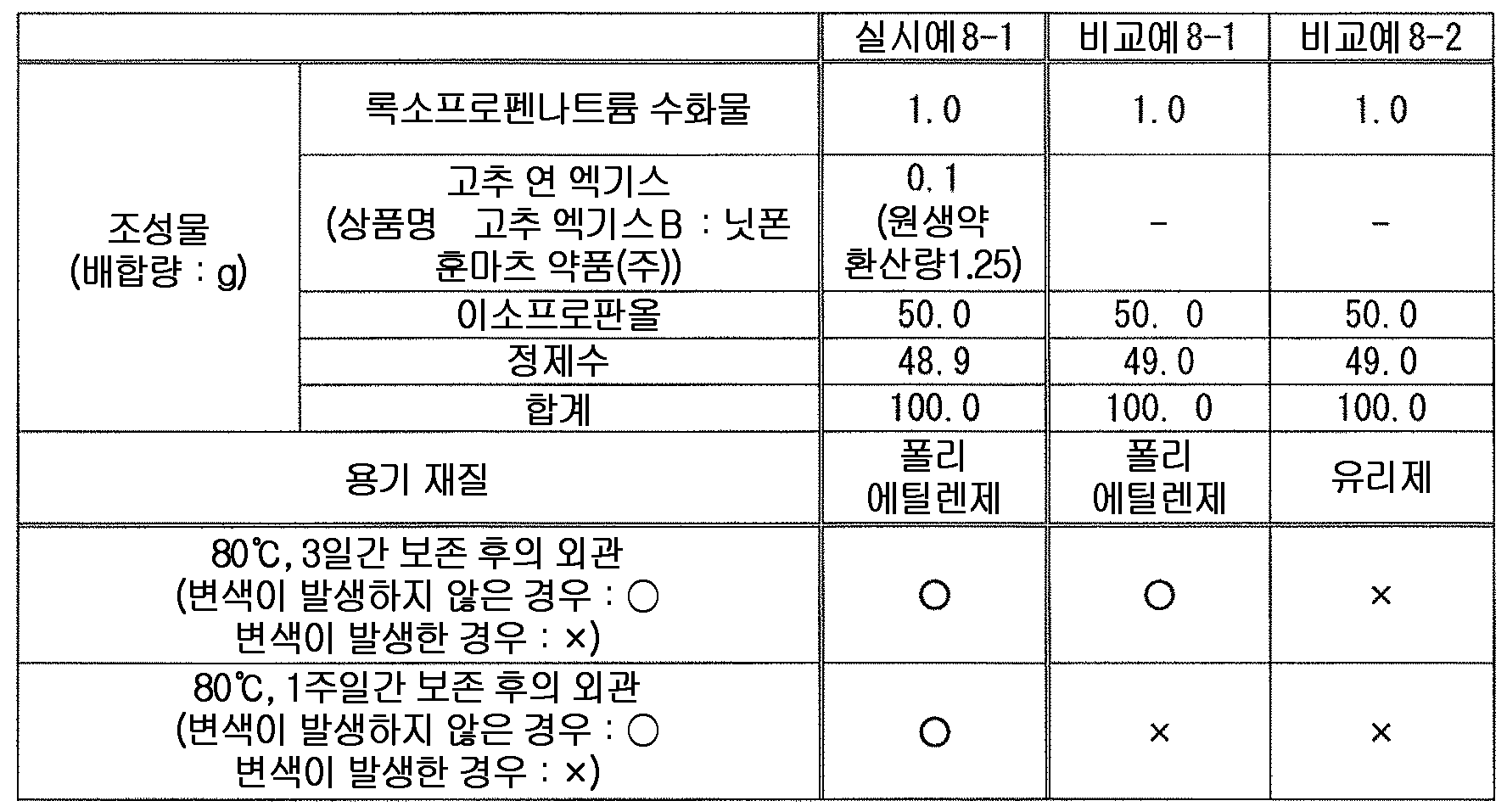
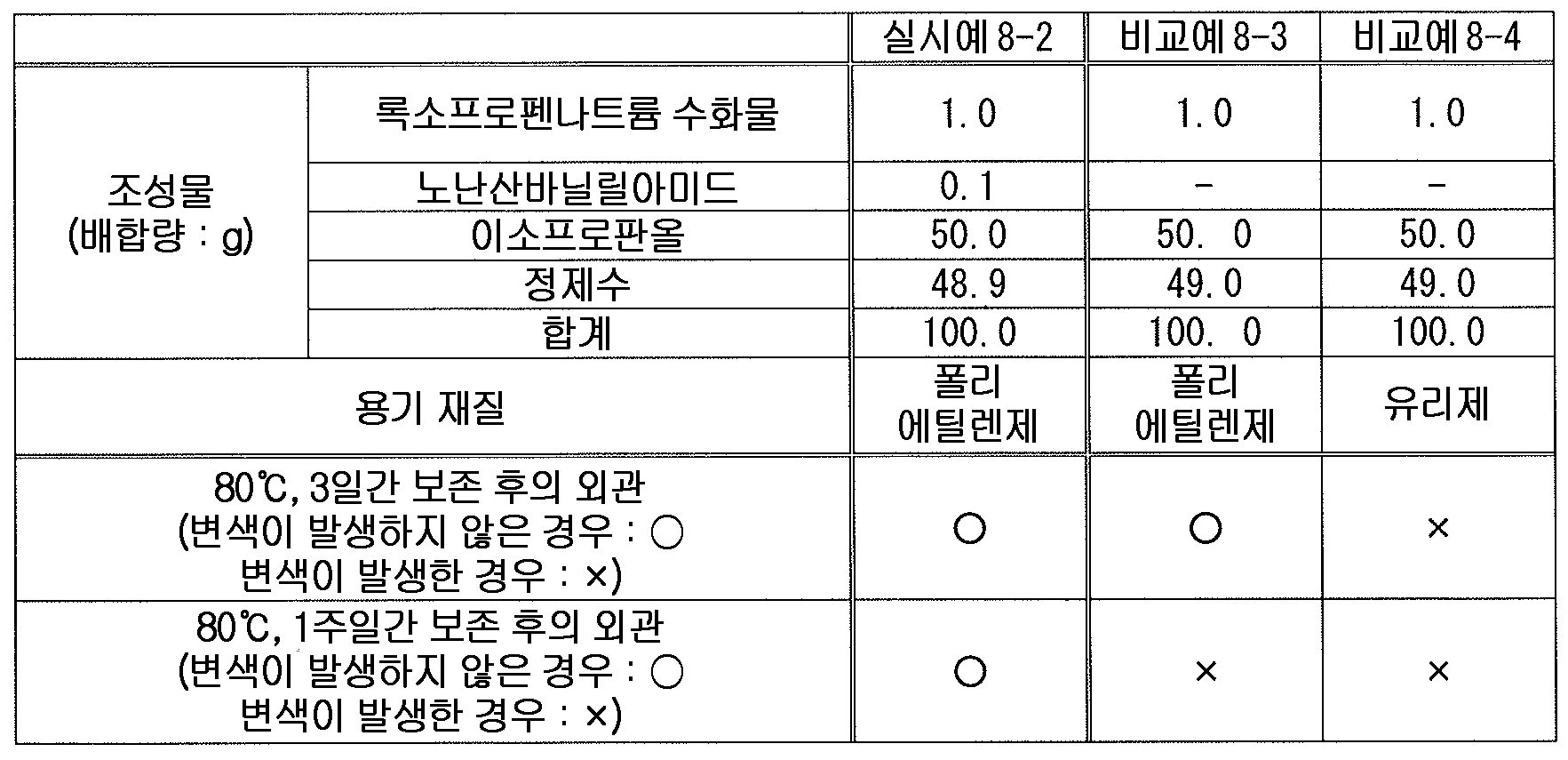
또한, 고추, 노난산바닐릴아미드 (노닐산바닐릴아미드) 등의 고추 또는 그 추출물은 외용 소염 진통제 등에 배합되어 있고, 록소프로펜과 함께 배합된 외용제도 이미 알려져 있다 (예를 들어, 특허문헌 7, 8).
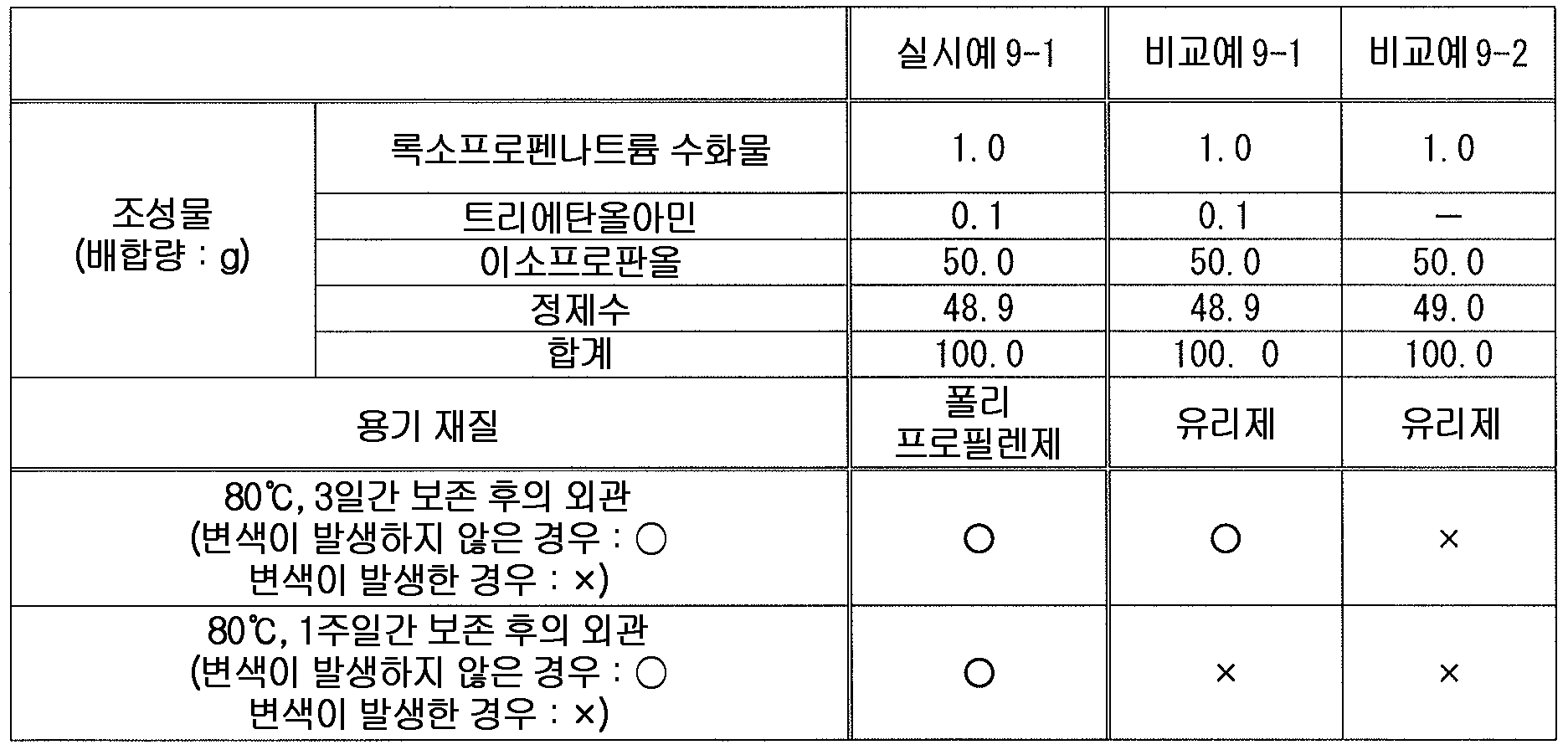
또한, 디이소프로판올아민 등의 유기 아민은 외용 소염 진통제 등에 배합되어 있고, 록소프로펜과 함께 배합된 외용제도 이미 알려져 있다 (예를 들어, 특허문헌 9).
제16 개정 일본 약국방 해설서 주식회사 히로카과 서점 제C-5359 ∼ 5364페이지
록소닌 (등록상표) 겔 1 % 의약품 인터뷰 폼 다이이치산쿄 주식회사 2010년 10월 개정 (제3판)
록소프로펜을 외용제의 유효 성분으로서 이용하는 경우, 로션제, 겔제나 크림제 등의 외용 도포제와 같이, 액상 혹은 반고형상의 조성물로서 환부에 도포 등 함으로써 사용하는 것이, 환부의 위치, 형상이나 범위에 따라 유연하게 필요한 양만큼 투여하는 관점에서 바람직하다. 또한, 록소프로펜을 액상 또는 반고형상의 조성물에 안정적으로 배합하는 기술을 확립할 수 있으면, 외용제뿐만 아니라 내복약 (경구 액제 등) 에 대한 응용도 가능해진다.
그래서 본 발명자가, 록소프로펜을 액상 또는 반고형상의 조성물에 안정적으로 배합하는 기술을 확립하기 위해서, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물을 조제하여 보존 안정성을 평가한 결과, 의외로, 고온 조건하에서의 보존에 의해 시간 경과적으로 변색이 발생할 수 있는 것이 판명되었다.
따라서, 본 발명의 과제는, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물의, 고온 보존시에 있어서의 변색을 억제하는 수단을 제공하는 것이다.
그래서 본 발명자는, 이 과제를 해결하기 위하여 추가로 검토한 결과, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 이하의 성분 1 ∼ 9 중 어느 것 :
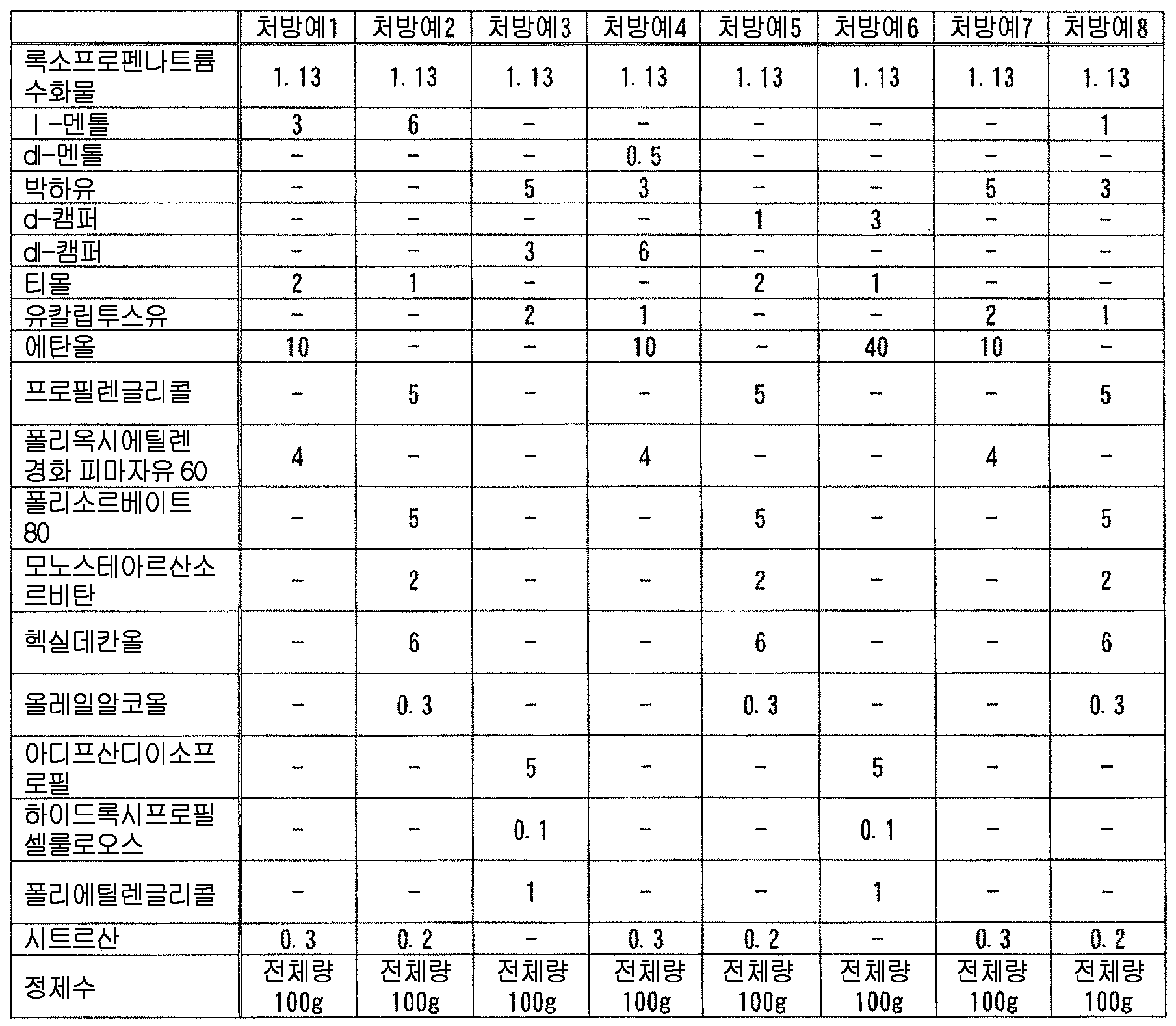
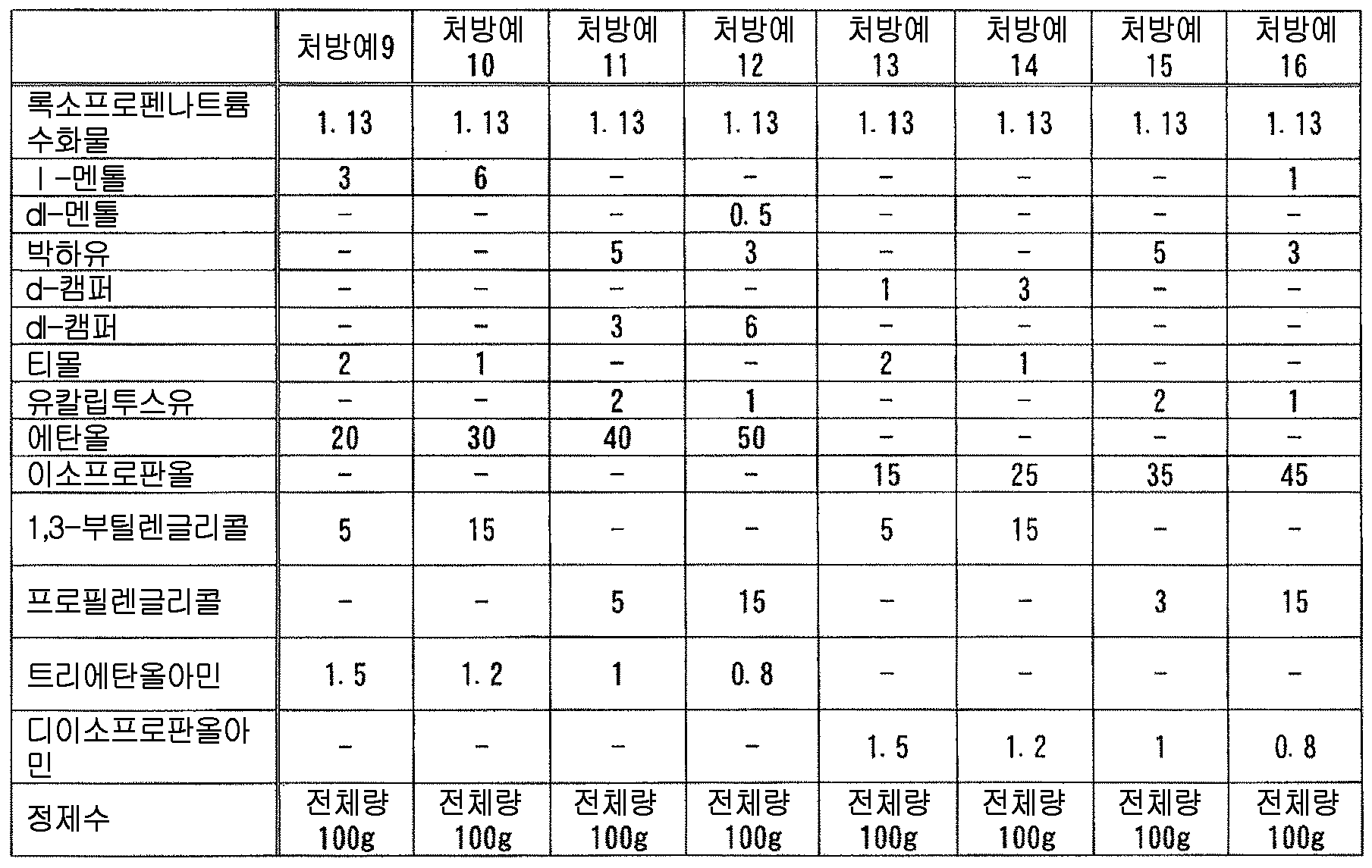
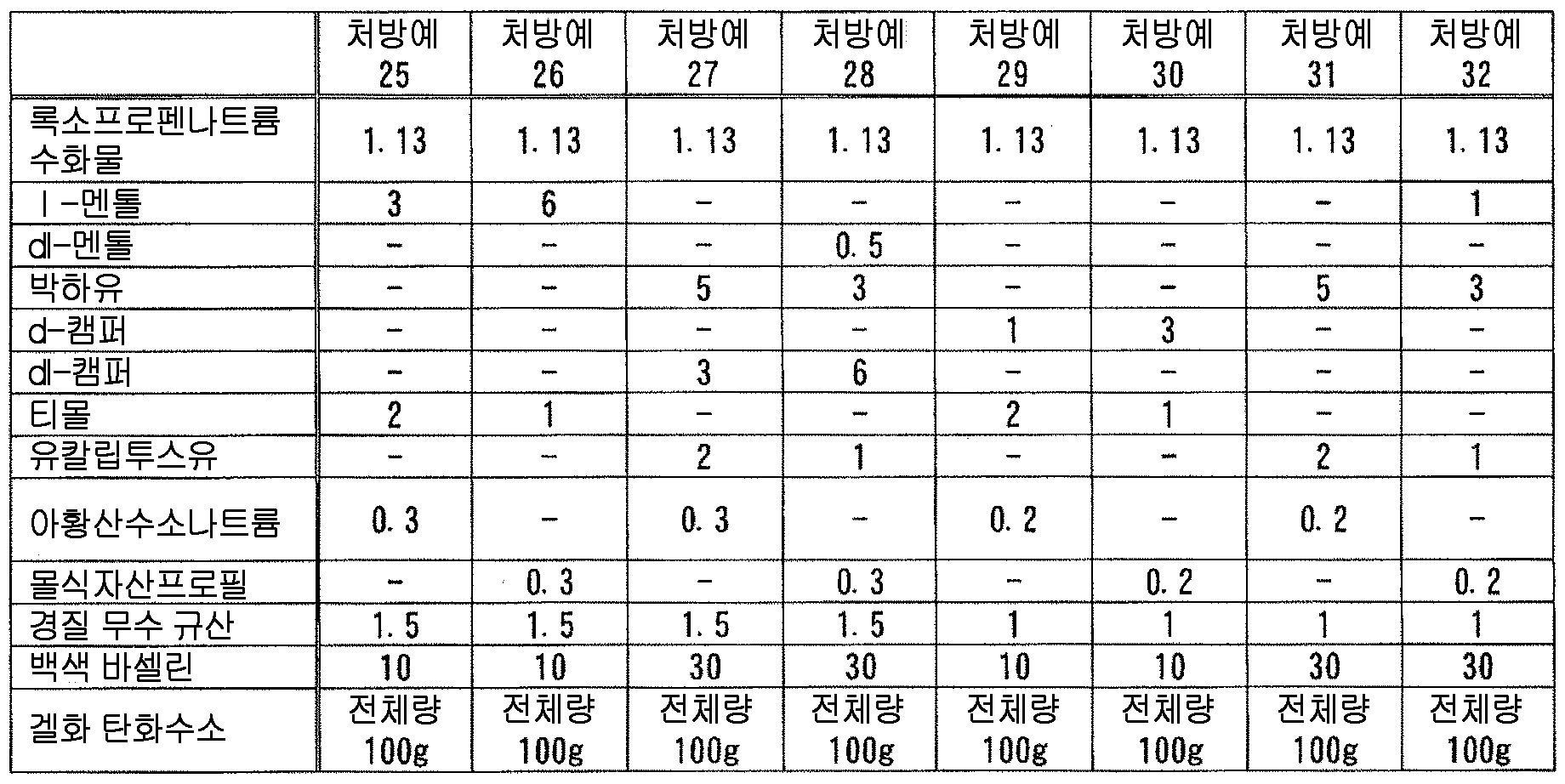
(성분 1) 멘톨, 캠퍼, 티몰로 대표되는 테르펜류
(성분 2) 아르니카 팅크로 대표되는 아르니카속의 식물 또는 그 추출물
(성분 3) 1,3-부틸렌글리콜로 대표되는 다가 알코올
(성분 4) 하이프로멜로스로 대표되는 셀룰로오스류
(성분 5) dl-α-토코페롤아세트산에스테르로 대표되는 토코페롤류
(성분 6) 글리시르레틴산으로 대표되는 글리시르레틴산류
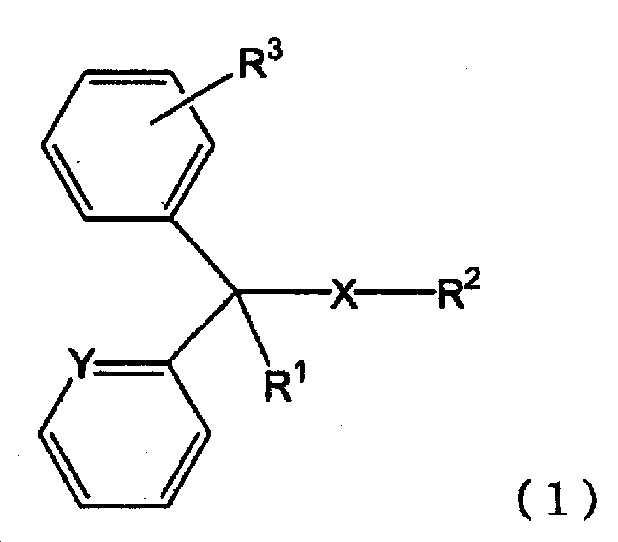
(성분 7) 클로르페니라민 또는 그 염, 디펜히드라민 또는 그 염으로 대표되는 하기 일반식 (1)
[화학식 1]
[식 (1) 중, X 는 단결합 또는 산소 원자를 나타내고, Y 는 메틴기 또는 질소 원자를 나타내고, R1 은 수소 원자, 수산기 또는 알킬기를 나타내고, R2 는 치환기를 가져도 되는 고리형 아미노기, 또는 치환기를 가져도 되는 아미노알킬기를 나타내고, R3 은 수소 원자 또는 할로겐 원자를 나타낸다.]
로 나타내는 화합물 또는 그 염
(성분 8) 고추 연 (軟) 엑기스, 노난산바닐릴아미드로 대표되는 고추 또는 그 추출물
(성분 9) 트리에탄올아민으로 대표되는 유기 아민
을 함유시키고, 또한, 폴리에틸렌, 폴리프로필렌으로 대표되는 폴리올레핀계 수지제의 용기에 수용함으로써, 고온 보존시의 변색을 억제할 수 있는 것을 알아내고, 본 발명을 완성하였다.
즉, 본 발명은, 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 다음 성분 (B-1) ∼ (B-9) 의 어느 것 ;
(B-1) 테르펜류
(B-2) 아르니카속의 식물 또는 그 추출물
(B-3) 다가 알코올
(B-4) 셀룰로오스류
(B-5) 토코페롤류
(B-6) 글리시르레틴산류
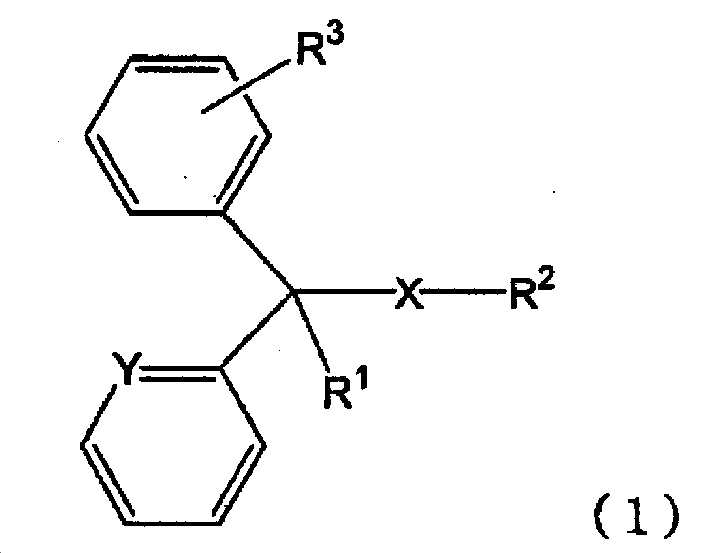
(B-7) 하기 일반식 (1)
[화학식 2]
[식 (1) 중, X 는 단결합 또는 산소 원자를 나타내고, Y 는 메틴기 또는 질소 원자를 나타내고, R1 은 수소 원자, 수산기 또는 알킬기를 나타내고, R2 는 치환기를 가져도 되는 고리형 아미노기, 또는 치환기를 가져도 되는 아미노알킬기를 나타내고, R3 은 수소 원자 또는 할로겐 원자를 나타낸다.]
로 나타내는 화합물 또는 그 염
(B-8) 고추 또는 그 추출물
(B-9) 유기 아민
을 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제를 제공하는 것이다.
또한, 본 발명은, 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 다음 성분 (B-1) ∼ (B-9) 의 어느 것 ;
(B-1) 테르펜류
(B-2) 아르니카속의 식물 또는 그 추출물
(B-3) 다가 알코올
(B-4) 셀룰로오스류
(B-5) 토코페롤류
(B-6) 글리시르레틴산류
(B-7) 상기 일반식 (1) 로 나타내는 화합물 또는 그 염
(B-8) 고추 또는 그 추출물
(B-9) 유기 아민
을 함유하는 액상 또는 반고형상의 조성물을, 폴리올레핀계 수지제 용기에 수용하는 공정을 포함하는, 조성물의 변색의 억제 방법을 제공하는 것이다.
본 발명에 의하면, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물의, 고온 보존시에 있어서의 변색을 억제할 수 있다. 따라서, 보존 안정성이 우수한, 록소프로펜 또는 그 염을 함유하는 의약을 제공할 수 있다.
먼저, 「의약 제제」 의 양태의 발명에 대하여 이하에 설명한다.
<성분 (A)>
본 발명에 있어서, 「록소프로펜 또는 그 염」 에는, 록소프로펜 그 자체 외에, 록소프로펜의 약학 상 허용되는 염, 나아가 록소프로펜이나 그 약학 상 허용되는 염과 물이나 알코올 등의 용매화물도 포함된다. 이들은 공지된 화합물이고, 공지된 방법에 의해 제조할 수 있는 것 외에 시판되는 것을 사용할 수 있다. 본 발명에 있어서, 록소프로펜 또는 그 염으로는, 록소프로펜나트륨 수화물 (화학명 : Monosodium 2-[4-[(2-oxocyclopentyl)methyl]phenyl]propanoate dihydrate) 이 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 록소프로펜 또는 그 염의 함유량은 특별히 한정되지 않고, 원하는 소염 진통 효과에 따라 적절히 검토하여 결정하면 된다. 본 발명에 있어서는, 록소프로펜 또는 그 염을 조성물 전체 질량에 대하여, 록소프로펜나트륨 무수물 환산으로 0.01 ∼ 10 질량% 함유하는 것이 바람직하고, 0.1 ∼ 5 질량% 함유하는 것이 보다 바람직하고, 0.5 ∼ 3 질량% 함유하는 것이 특히 바람직하다.
<성분 (B-1)>
본 발명에 있어서, 「테르펜류」 란, 테르펜탄화수소 외에, 테르펜알코올, 테르펜알데히드, 테르펜케톤, 테르펜옥사이드, 테르펜락톤 등을 포함하는 총칭 (테르페노이드) 을 의미하고, 그 구조는 특별히 한정되는 것이 아니고, 모노테르펜, 세스퀴테르펜 또는 그들의 유도체 등을 들 수 있다. 또한, 고리형이어도 되고 사슬형이어도 된다
이와 같은 테르펜류로는, 구체적으로는 예를 들어, 이소보르네올, 이론, 오시멘, 카르베올, 카르보타나세톤, 카르보멘톤, 카르본, 카렌, 카론, 캄펜, 캠퍼, 게라니올, 사비넨, 사프라날, 시클로시트랄, 시트랄, 시트로넬랄, 시트로넬산, 시트로넬롤, 시네올, 시멘, 실베스트렌, 티몰, 이소투?, 투존, 테르피네올, 테르피넨, 테르피놀렌, 트리시클렌, 네롤, 피넨, 피노캄페올, 피놀, 피페리테논, 펠란드랄, 펠란드렌, 펜첸, 펜칠알코올, 페릴릴알코올, 페릴알데히드, 보르네올, 미르센, 멘톨, 멘톤, 요놀, 요논, 리날로올, 리모넨 등을 들 수 있고, 이들을 단독으로 또는 2 종 이상 조합하여 사용할 수 있다. 또한, 이들 테르펜류에 광학 이성체가 존재하는 경우에는, 특별히 지정하지 않는 한 어느 이성체도 포함된다. 즉, 본 발명에 있어서, 테르펜류의 성분명으로서 특정한 광학 이성체를 지정하지 않는 한, 이러한 성분 표기는 각종 광학 이성체 단독 및 그들의 임의의 비율의 혼합물 모두를 포함하고, 단일의 광학 이성체여도 되고 각종 광학 이성체의 임의의 비율의 혼합물이어도 된다 (예를 들어, 「멘톨」 이라는 기재는 dl-멘톨과 d-멘톨의 어느 것도 포함하는 것이다).
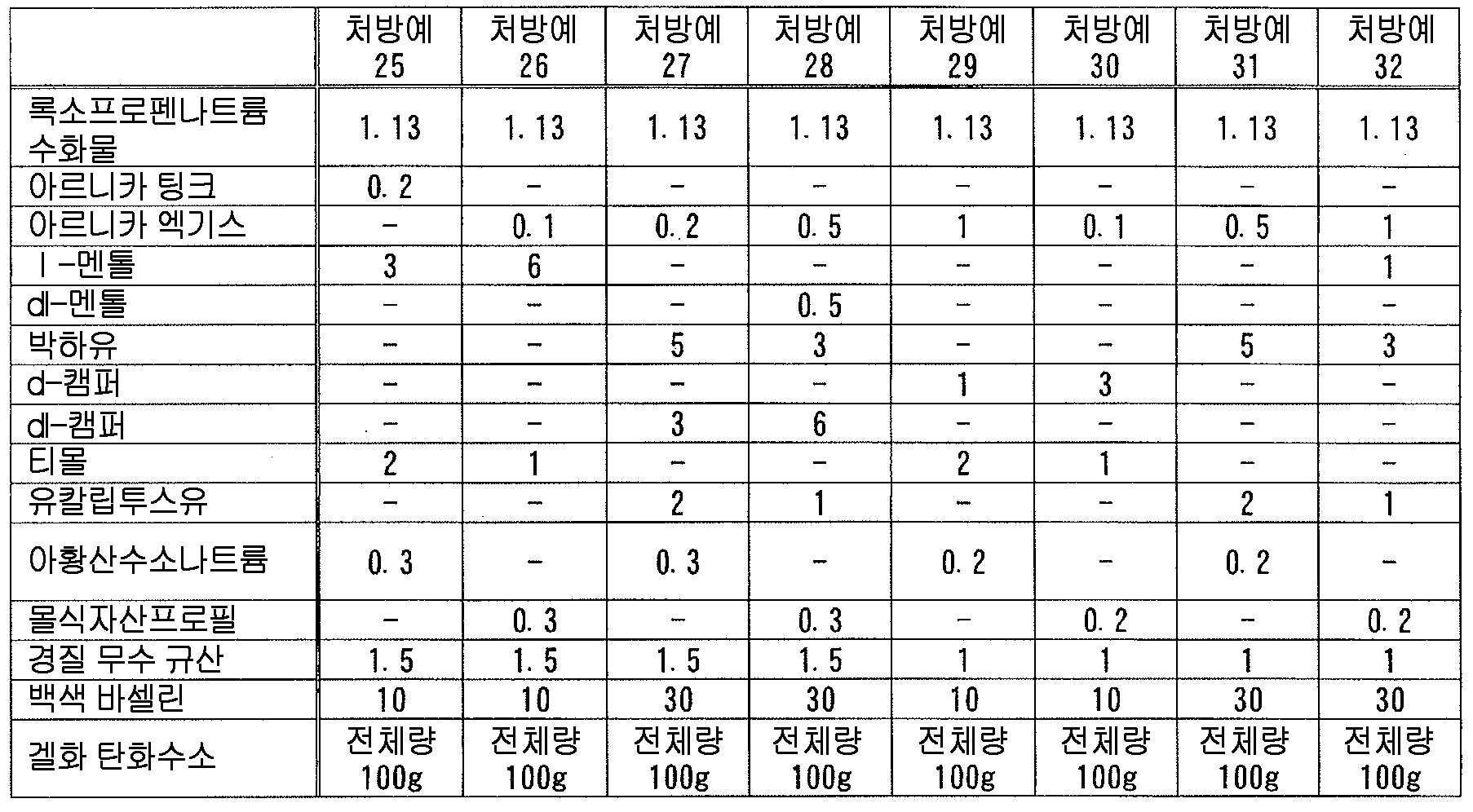
상기 테르펜류 중에서는, 변색 억제 작용의 관점에서, 고리형의 테르페노이드가 바람직하고, 고리형의 모노테르페노이드가 보다 바람직하고, 단고리형 또는 2 고리형의 모노테르페노이드가 더욱 바람직하고, p-멘탄 골격을 갖는 모노테르페노이드 (예를 들어, 시멘, 티몰, 테르피넨, 테르피놀렌, 펠란드렌, 리모넨 등의, p-멘탄의 불포화 유도체 ; 카르베올, 테르피네올, 멘톨 등의 p-멘탄 골격을 갖는 모노테르펜알코올 ; 카르본, 멘톤 등의, p-멘탄 골격을 갖는 모노테르펜케톤 ; 페릴알데히드 등의 p-멘탄 골격을 갖는 모노테르펜알데히드 ; 시네올 등의, p-멘탄 골격을 갖는 모노테르펜에테르 등) 또는 보르난 골격을 갖는 모노테르페노이드 (예를 들어, 보르네올 등의 보르난 골격을 갖는 모노테르펜알코올 ; 캠퍼 등의, 보르난 골격을 갖는 모노테르펜케톤 등) 이 더욱 보다 바람직하고, 시네올, 티몰, 테르피네올, 멘톨, 리모넨, 캠퍼 및 보르네올로 이루어지는 군에서 선택되는 1 종 이상이 더욱 보다 바람직하고, 시네올, 캠퍼, 티몰, 보르네올 및 멘톨로 이루어지는 군에서 선택되는 1 종 이상이 더욱 보다 바람직하고, 시네올, d-캠퍼, dl-캠퍼, 티몰, d-보르네올, l-멘톨 및 dl-멘톨로 이루어지는 군에서 선택되는 1 종 이상이 더욱 보다 바람직하고, 시네올, d-캠퍼, dl-캠퍼, 티몰, l-멘톨 및 dl-멘톨로 이루어지는 군에서 선택되는 1 종 이상이 특히 바람직하다.
또한, 테르펜류를 액상 또는 반고형상의 조성물에 함유시키는 경우, 테르펜류를 그대로 사용하는 것 외에, 테르펜류를 포함하는 정유를 사용해도 된다.
이와 같은 정유로는, 예를 들어, 아니스유, 일랑일랑유, 이리스유, 회향유, 오렌지유, 카낭가유, 캐모마일유, 카유풋유, 캐러웨이유, 쿠베브유, 그레이프후르츠유, 계피유, 코리앤더유, 사프란유, 산초유, 차조기유, 시트리오도라유, 시트로넬라유, 생강유, 카더몬유, 장뇌유, 진저 그래스유, 스피어민트유, 페퍼민트유, 제라늄유, 대회향유, 정자유, 테레빈유, 등피유, 네롤리유, 바질유, 박하유, 팔마로사유, 피멘토유, 페티그레인유, 베이유, 페니로얄유, 헤노포디유, 베르가모트유, 보아드로즈유, 방장유, 마조람유, 만다린유, 멜리사유, 유칼립투스유, 라임유, 라벤더유, 리날로에유, 레몬유, 레몬 그라스유, 로즈유, 로즈마리유, 로먼 캐모마일유 등을 들 수 있고, 이들을 단독으로 또는 2 종 이상 조합하여 사용해도 된다.
이들 중에서도, 일랑일랑유, 회향유, 오렌지유, 캐모마일유, 계피유, 차조기유, 시트로넬라유, 생강유, 장뇌유, 페퍼민트유, 제라늄유, 정자유, 테레빈유, 등피유, 네롤리유, 박하유, 팔마로사유, 베르가모트유, 유칼립투스유, 라벤더유, 리날로에유, 레몬유, 로즈유, 로즈마리유, 로먼 캐모마일유 등이 바람직하고, 장뇌유, 페퍼민트유, 테레빈유, 박하유, 유칼립투스유가 보다 바람직하고, 박하유, 유칼립투스유가 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 테르펜류의 함유량은 특별히 한정되지 않고, 적절히 검토하여 결정하면 되지만, 변색 억제 작용의 관점에서, 테르펜류를 조성물 전체 질량에 대하여 0.01 ∼ 15 질량% 함유하는 것이 바람직하고, 0.1 ∼ 10 질량% 함유하는 것이 보다 바람직하고, 0.5 ∼ 8 질량% 함유하는 것이 특히 바람직하다.
그 중에서도, 테르펜류로서 캠퍼를 사용하는 경우에 있어서는, 변색 억제 작용의 관점에서, 캠퍼를 조성물 전체 질량에 대하여 0.4 ∼ 15 질량% 함유하는 것이 바람직하고, 1 ∼ 10 질량% 함유하는 것이 보다 바람직하고, 3 ∼ 7 질량% 함유하는 것이 특히 바람직하다. 또한, 테르펜류로서 티몰을 사용하는 경우에 있어서는, 변색 억제 작용의 관점에서, 티몰을 조성물 전체 질량에 대하여 0.2 ∼ 3 질량% 함유하는 것이 바람직하고, 0.4 ∼ 2 질량% 함유하는 것이 보다 바람직하고, 0.6 ∼ 1 질량% 함유하는 것이 특히 바람직하다. 또한, 테르펜류로서 멘톨을 사용하는 경우에 있어서는, 변색 억제 작용의 관점에서, 멘톨을 조성물 전체 질량에 대하여 0.3 ∼ 10 질량% 함유하는 것이 바람직하고, 1 ∼ 8 질량% 함유하는 것이 보다 바람직하고, 3 ∼ 6 질량% 함유하는 것이 특히 바람직하다.
또한, 본 발명에 있어서, 액상 또는 반고형상의 조성물에 포함되는 록소프로펜 또는 그 염과 테르펜류의 함유비는 특별히 한정되지 않고, 적절히 검토하여 결정하면 되지만, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜나트륨 무수물 환산으로 1 질량부에 대하여, 테르펜류를 0.01 ∼ 15 질량부 함유하는 것이 바람직하고, 0.1 ∼ 10 질량부 함유하는 것이 보다 바람직하고, 0.5 ∼ 7 질량부 함유하는 것이 특히 바람직하다.
그 중에서도, 테르펜류로서 캠퍼를 사용하는 경우에 있어서는, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜나트륨 무수물 환산으로 1 질량부에 대하여, 캠퍼를 0.2 ∼ 13 질량부 함유하는 것이 바람직하고, 0.3 ∼ 8 질량부 함유하는 것이 보다 바람직하고, 0.4 ∼ 7 질량부 함유하는 것이 특히 바람직하다. 또한, 테르펜류로서 티몰을 사용하는 경우에 있어서는, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜나트륨 무수물 환산으로 1 질량부에 대하여, 티몰을 0.1 ∼ 2 질량부 함유하는 것이 바람직하고, 0.3 ∼ 1 질량부 함유하는 것이 보다 바람직하고, 0.4 ∼ 0.8 질량부 함유하는 것이 특히 바람직하다. 또한 테르펜류로서 멘톨을 사용하는 경우에 있어서는, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜나트륨 무수물 환산으로 1 질량부에 대하여, 멘톨을 0.2 ∼ 11 질량부 함유하는 것이 바람직하고, 1 ∼ 7 질량부 함유하는 것이 보다 바람직하고, 2 ∼ 5 질량부 함유하는 것이 특히 바람직하다.
<성분 (B-2)>
본 발명에 있어서, 「아르니카속의 식물」 이란, 국화과 아르니카속 (아르니카속) 에 속하는 식물체를 의미하고, 당해 속에 속하는 것이면 구체적인 종은 특별히 한정되지 않고, 예를 들어, 이하의 학명의 식물 : Arnica montana (아르니카), Arnica chamissonis, Arnica fulgens, Arnica cordifolia (환엽 아르니카), Arnica latifolia (광엽 아르니카), Arnica longifolia (장엽 아르니카), Arnica sachalinensis 등을 들 수 있다. 본 발명에 있어서는, 아르니카로서, 단일의 종의 식물을 사용해도 되고, 복수의 상이한 종의 식물을 조합하여 사용해도 된다. 본 발명에 있어서는, 변색 억제 작용의 관점에서, Arnica montana (아르니카) 를 사용하는 것이 바람직하다. 또한, 본 발명에 있어서, 아르니카속의 식물의 사용 부위는 특별히 한정되지 않고, 그 전체 식물 혹은 일부 (꽃, 화서, 화수, 꽃봉오리, 잎, 가지, 뿌리 등) 또는 그들 2 종 이상의 조합을 사용할 수 있다.
아르니카속의 식물은 필요에 따라 그 형태를 조절할 수 있고, 소편, 소괴로 절단 혹은 분쇄, 또는 분말로 분쇄할 수 있다. 또한, 조성물·의약 제제의 제조시 취급의 편의 등을 고려하여, 아르니카속의 식물에 어떠한 추출 처리를 실시한 것 (본 명세서에 있어서 「아르니카속의 식물의 추출물」 이라고 칭한다) 을 사용해도 된다.
또한, 「아르니카속의 식물의 추출물」 에는, 추출 처리에 더하여, 가열, 건조, 분쇄 등의 가공 처리를 실시한 것도 포함된다. 구체적으로는, 아르니카속의 식물을 필요에 따라 적당한 크기로 한 후에, 적당한 침출액 (추출 용매) 을 첨가하여 침출한 액이나, 당해 침출액을 농축한 액 (연 엑기스, 팅크 등), 또한 이들을 건조시킨 것 (건조 엑기스 등) 등도 본 발명의 「아르니카속의 식물의 추출물」 에 포함된다.
아르니카속의 식물의 추출물의 제조 방법은 특별히 한정되지 않고, 예를 들어 제16 개정 일본 약국방 제제 총칙의 「엑기스제」, 「침제·탕약제」, 「팅크제」, 「유엑기스제」 의 항의 기재 등, 공지된 식물 추출물의 제조 방법을 참고로 하여 제조할 수 있다. 구체적으로는 예를 들어, 아르니카속의 식물을 필요에 따라 절단, 가열, 건조, 분쇄 등 한 후, 적당한 추출 용매를 첨가하여 추출을 실시함으로써, 제조할 수 있다. 얻어진 추출물은, 필요에 따라 추가로 농축, 건조 등 시켜도 된다.
상기 추출 용매로는 예를 들어, 메탄올, 에탄올, 이소프로판올, n-부탄올 등의 저급 1 가 알코올 ; 에틸렌글리콜, 프로필렌글리콜, 1,3-부틸렌글리콜, 글리세린 등의 저급 다가 알코올 ; 디에틸에테르 등의 에테르류 ; 아세톤, 에틸메틸케톤 등의 케톤류 ; 아세트산에틸 등의 에스테르류 ; 아세토니트릴 등의 니트릴류 ; 펜탄, 헥산, 시클로펜탄, 시클로헥산 등의 알칸류 ; 디클로로메탄, 클로로포름 등의 할로게노알칸류 ; 벤젠, 톨루엔 등의 방향족 탄화수소 ; 디메틸포름아미드 ; 디메틸술폭시드 ; 물 (열수를 포함한다) 등을 들 수 있다. 이들은 각각 단독으로 사용해도 되고, 2 종 이상을 조합하여 사용해도 된다. 본 발명에 있어서는, 물, 에탄올, 프로필렌글리콜, 1,3-부틸렌글리콜 또는 이들의 2 종 이상의 혼액이 바람직하다.
추출 조작은 특별히 한정되지 않고, 식물로부터의 추출 조작에 이용되는 공지된 방법을 적절히 채용할 수 있고, 구체적으로는 예를 들어, 추출 용매에 대한 침지 (냉침, 온침, 퍼콜레이션 등), 초임계 유체나 아임계 유체를 사용한 추출 등을 들 수 있다. 또한, 추출 효율을 높이기 위해서, 교반이나 추출 용매 중에서 호모게나이즈해도 된다.
추출 온도는 특별히 한정되지 않고, 사용하는 추출 용매, 추출 조작 등에 따라 상이하지만, 5 ℃ 정도부터 추출 용매의 비점 이하의 온도로 하는 것이 바람직하다.
추출 시간은 특별히 한정되지 않고, 사용하는 추출 용매, 추출 조작 등에 따라 상이하지만, 1 시간 ∼ 14 일 정도로 하는 것이 바람직하다.
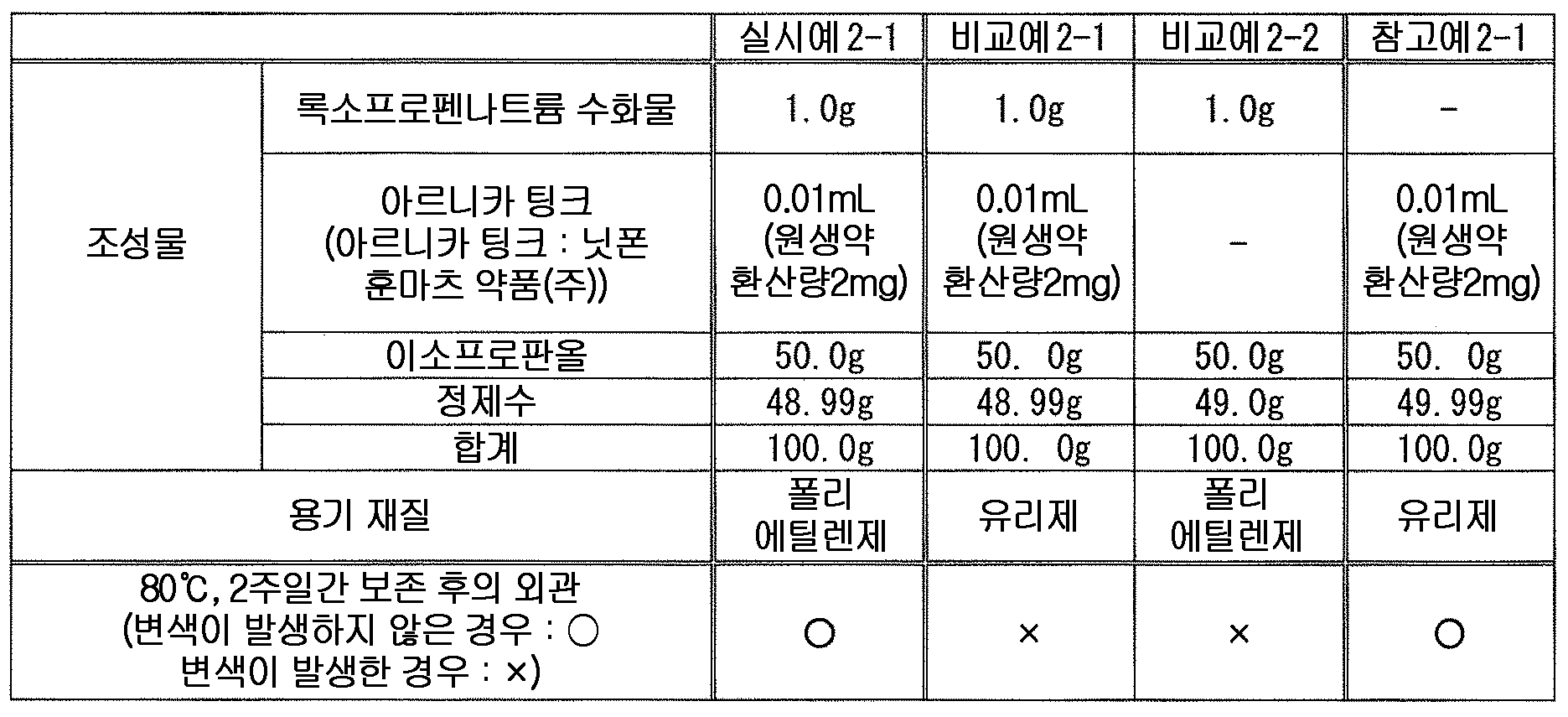
본 발명에 있어서, 「아르니카속의 식물 또는 그 추출물」 로는, 아르니카 (Arnica montana) 또는 그 추출물이 바람직하다. 아르니카의 추출물로는, 아르니카 팅크, 아르니카 엑기스를 들 수 있다. 아르니카속의 식물 또는 그 추출물로는, 아르니카 팅크 및 아르니카 엑기스 (연 엑기스, 건조 엑기스) 에서 선택되는 1 종 이상의 아르니카의 추출물이 보다 바람직하고, 아르니카 팅크, 의약부 외품 원료 규격 2006 에 수재된 아르니카 엑기스가 더욱 바람직하고, 아르니카 팅크가 특히 바람직하다.
본 발명에 있어서, 아르니카속의 식물 또는 그 추출물로는, 시판품을 사용할 수 있고, 구체적인 시판품으로는 예를 들어, 아르니카 팅크 (알프스 약품 공업 (주)), 아르니카 엑기스 (마루젠 제약 (주)), 파르콜렉스 아르니카 (이치마루 파르코스 (주)), 아르니카 엑기스, 아르니카 팅크 (이상, 닛폰 훈마츠 약품 (주)) 등을 들 수 있다.
본 발명에 있어서, 액상 또는 반고형상의 조성물에 있어서의 아르니카속의 식물 또는 그 추출물의 함유량은 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 아르니카속의 식물 또는 그 추출물을 원생약 환산량으로, 조성물 전체 질량에 대하여 0.00001 ∼ 5 질량% 함유하는 것이 바람직하고, 0.00005 ∼ 2 질량% 함유하는 것이 보다 바람직하고, 0.0007 ∼ 0.7 질량% 함유하는 것이 특히 바람직하다. 특히, 아르니카속의 식물로서 아르니카를 사용하는 경우에 있어서는, 변색 억제 작용의 관점에서, 아르니카 또는 그 추출물을 원생약 환산량으로, 조성물 전체 질량에 대하여 0.0001 ∼ 3 질량% 함유하는 것이 바람직하고, 0.0005 ∼ 1 질량% 함유하는 것이 보다 바람직하고, 0.001 ∼ 0.5 질량% 함유하는 것이 특히 바람직하다.
또한, 본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 록소프로펜 또는 그 염과 아르니카속의 식물 또는 그 추출물의 함유비는 특별히 한정되지 않고, 변색 억제 작용의 관점에서 적절히 검토하여 결정하면 되지만, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜 무수물 환산으로 1 질량부에 대하여, 아르니카속의 식물 또는 그 추출물을 원생약 환산량으로 0.00001 ∼ 5 질량부 함유하는 것이 바람직하고, 0.00005 ∼ 2 질량부 함유하는 것이 보다 바람직하고, 0.0007 ∼ 0.7 질량부 함유하는 것이 특히 바람직하다. 특히, 아르니카속의 식물로서 아르니카를 사용하는 경우에 있어서는, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜 무수물 환산으로 1 질량부에 대하여, 아르니카 또는 그 추출물을 원생약 환산량으로 0.0001 ∼ 3 질량부 함유하는 것이 바람직하고, 0.0005 ∼ 1 질량부 함유하는 것이 보다 바람직하고, 0.001 ∼ 0.5 질량부 함유하는 것이 특히 바람직하다.
<성분 (B-3)>
본 발명에 있어서, 「다가 알코올」 이란, 동일 분자 내에 수산기를 2 개 이상 갖는 알코올을 의미하고, 구체적으로는 예를 들어, 에틸렌글리콜, 디에틸렌글리콜, 트리에틸렌글리콜, 프로필렌글리콜, 디프로필렌글리콜, 글리세린, 디글리세린, 3-메틸-1,3-부탄디올, 부틸렌글리콜, 에리트리톨, 자일리톨, 소르비톨, 만니톨, 헥산트리올 등의 저급 다가 알코올 (보다 상세하게는, 탄소수 1 ∼ 6 의 저급 다가 알코올) ; 폴리비닐알코올, 폴리에틸렌글리콜, 폴리글리세린, 폴리프로필렌글리콜 등의 고급 다가 알코올 (보다 상세하게는, 탄소수 7 이상의 고급 다가 알코올) 등을 들 수 있다. 또한, 이들 중 1 종을 단독으로 또는 2 종 이상을 조합하여 이용하면 된다.
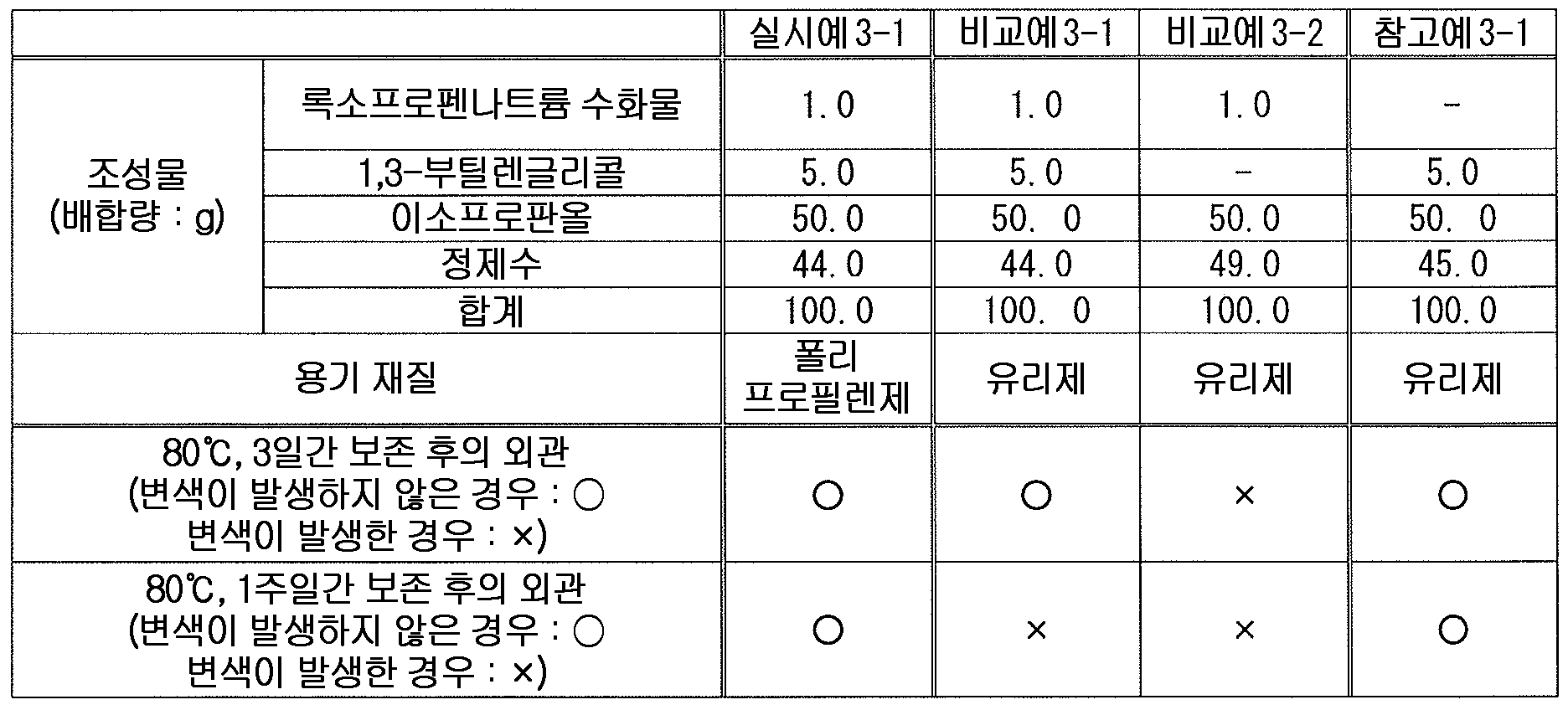
본 발명에 있어서 다가 알코올로는, 변색 억제 작용의 관점에서, 에틸렌글리콜, 트리에틸렌글리콜, 프로필렌글리콜, 디프로필렌글리콜, 글리세린, 1,3-부틸렌글리콜, 에리트리톨, 자일리톨, 소르비톨, 만니톨, 1,2,6-헥산트리올, 폴리비닐알코올, 폴리에틸렌글리콜 및 폴리프로필렌글리콜로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상의 다가 알코올이 바람직하고, 1,3-부틸렌글리콜, 폴리에틸렌글리콜 300, 폴리에틸렌글리콜 400, 폴리에틸렌글리콜 1000, 폴리에틸렌글리콜 1500, 폴리에틸렌글리콜 1540, 폴리에틸렌글리콜 4000, 폴리에틸렌글리콜 6000 및 폴리에틸렌글리콜 20000 으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상의 다가 알코올이 보다 바람직하고, 1,3-부틸렌글리콜이 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 다가 알코올의 함유량은 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 다가 알코올을 조성물 전체 질량에 대하여 0.1 ∼ 70 질량% 함유하는 것이 바람직하고, 0.5 ∼ 50 질량% 함유하는 것이 보다 바람직하고, 1 ∼ 30 질량% 함유하는 것이 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 록소프로펜 또는 그 염과 다가 알코올의 함유비는 특별히 한정되지 않고, 변색 억제 작용의 관점에서 적절히 검토하여 결정하면 되지만, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜 무수물 환산으로 1 질량부에 대하여, 다가 알코올을 1 ∼ 60 질량부 함유하는 것이 바람직하고, 3 ∼ 40 질량부 함유하는 것이 보다 바람직하고, 5 ∼ 20 질량부 함유하는 것이 특히 바람직하다.
<성분 (B-4)>
본 발명에 있어서, 「셀룰로오스류」 란, 셀룰로오스 또는 그 염 그 자체 외에, 셀룰로오스의 하이드록시기의 전부 또는 일부가 에테르 결합을 형성한 유도체 또는 그 염 (이하, 「셀룰로오스에테르 유도체 또는 그 염」 이라고 칭한다. 또한, 당해 셀룰로오스에테르 유도체 또는 그 염은, 에테르 결합 외에, 필요에 따라 추가로 에스테르화, 가교 형성 등, 추가적인 수식이 이루어져 있어도 된다.) 을 포함하는 개념이다. 여기서 염으로는 특별히 한정되지 않고, 구체적으로는 예를 들어, 나트륨염, 칼륨염 등의 알칼리 금속염 ; 칼슘염, 마그네슘염 등의 알칼리 토금속염 등을 들 수 있다.
당해 셀룰로오스류 중, 셀룰로오스 또는 그 염으로는 구체적으로는 예를 들어, 결정 셀룰로오스, 분말 셀룰로오스 등을 들 수 있다.
또한, 셀룰로오스류 중, 셀룰로오스에테르 유도체 또는 그 염으로는 구체적으로는 예를 들어, 메틸셀룰로오스, 에틸셀룰로오스 등의 알킬셀룰로오스 또는 그 염 ; 하이드록시에틸셀룰로오스, 하이드록시프로필셀룰로오스 등의 하이드록시알킬셀룰로오스 또는 그 염 ; 하이드록시에틸메틸셀룰로오스, 하이프로멜로스 등의 알킬(하이드록시알킬)셀룰로오스 또는 그 염 ; 하이프로멜로스아세트산에스테르숙신산에스테르, 하이프로멜로스프탈산에스테르 등의 알킬(하이드록시알킬)셀룰로오스 유도체 또는 그 염 ; 카르복시메틸셀룰로오스, 카르멜로스칼륨, 카르멜로스칼슘, 카르멜로스나트륨 등의 카르복시알킬셀룰로오스 또는 그 염 ; 크로스카르멜로스나트륨 등의 카르복시알킬셀룰로오스 유도체 또는 그 염 등을 들 수 있다. 또한, 당해 셀룰로오스에테르 유도체에 있어서의 알킬기로는 특별히 제한되지 않지만, 탄소수 1 ∼ 6 의 직사슬형 또는 분기형의 알킬기가 바람직하다. 또한, 당해 셀룰로오스에테르 유도체에 있어서의 에테르화율 (알킬기, 하이드록시알킬기 등의 에테르 결합을 형성하는 치환기의 치환율 : %) 은 특별히 제한되지 않지만, 용매에 대한 용해성 등의 관점에서, 10 ∼ 90 % 가 바람직하고, 20 ∼ 80 % 가 특히 바람직하다. 또한, 에테르화율 (%) 은 각 셀룰로오스에테르 유도체에 대하여 제16 개정 일본 약국방에 기재된 방법, 또는 이것에 준한 방법에 의해 측정한다.
이들 셀룰로오스류는, 모두 공지된 화합물이고, 공지된 방법에 의해 제조할 수 있는 것 외에, 시판품을 사용해도 된다.
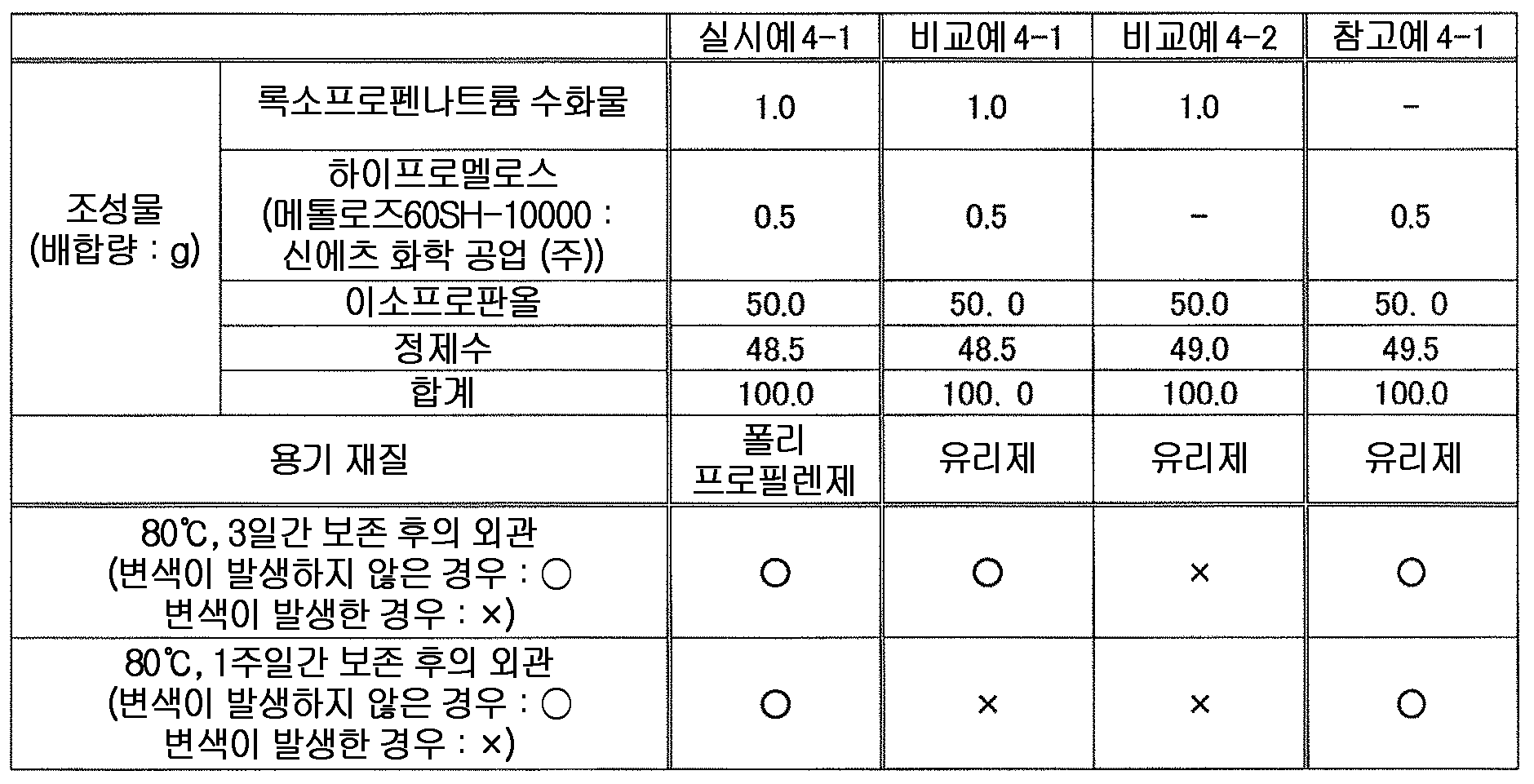
본 발명에 있어서 셀룰로오스류로는, 변색 억제 작용의 관점에서, 셀룰로오스에테르 유도체 또는 그 염이 바람직하고, 알킬셀룰로오스, 하이드록시알킬셀룰로오스, 알킬(하이드록시알킬)셀룰로오스 및 카르복시알킬셀룰로오스 그리고 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상이 보다 바람직하고, C1 - C6 알킬셀룰로오스, 하이드록시 C1 - C6 알킬셀룰로오스, C1 - C6 알킬(하이드록시C1 - C6 알킬)셀룰로오스 및 카르복시 C1 - C6 알킬셀룰로오스 그리고 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상이 더욱 바람직하고, 메틸셀룰로오스, 에틸셀룰로오스, 하이드록시에틸셀룰로오스, 하이드록시프로필셀룰로오스, 하이프로멜로스 및 카르복시메틸셀룰로오스 그리고 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상이 더욱 보다 바람직하고, 하이프로멜로스가 더욱 보다 바람직하고, 제16 개정 일본 약국방에 규정한, 치환도 타입이 2910 인 하이프로멜로스가 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 셀룰로오스류의 함유량은 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 조성물 전체 질량에 대하여 0.01 ∼ 5 질량% 함유하는 것이 바람직하고, 0.05 ∼ 3 질량% 함유하는 것이 보다 바람직하고, 0.1 ∼ 2 질량% 함유하는 것이 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 록소프로펜 또는 그 염과 셀룰로오스류의 함유비는 특별히 한정되지 않고, 변색 억제 작용의 관점에서 적절히 검토하여 결정하면 되지만, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜 무수물 환산으로 1 질량부에 대하여, 셀룰로오스류를 0.02 ∼ 4 질량부 함유하는 것이 바람직하고, 0.2 ∼ 1.5 질량부 함유하는 것이 보다 바람직하고, 0.3 ∼ 1 질량부 함유하는 것이 특히 바람직하다.
<성분 (B-5)>
본 발명에 있어서, 「토코페롤류」 란, 토코페롤, 토코트리에놀 및 그들의 유도체 (예를 들어, 아세트산에스테르, 숙신산에스테르, 니코틴산에스테르 등의 에스테르화 유도체 등) 그리고 그들의 염 (예를 들어, 칼슘염, 마그네슘염 등의 알칼리 토금속염 등) 에서 선택되는 1 종 또는 2 종 이상을 의미한다. 여기서, 토코페롤로는, α-토코페롤, β-토코페롤, γ-토코페롤, δ-토코페롤의 어느 것이어도 되지만, α-토코페롤이 바람직하다. 또한, 토코트리에놀로는, α-토코트리에놀, β-토코트리에놀, γ-토코트리에놀, δ-토코트리에놀의 어느 것이어도 되지만, α-토코트리에놀이 바람직하다. 본 발명에 있어서는, 변색 억제 작용의 관점에서, α-토코페롤, 그 아세트산에스테르, 그 숙신산에스테르 및 그 니코틴산에스테르 그리고 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상이 바람직하다. 또한, 토코페롤이나 토코트리에놀에는 광학 이성체가 존재할 수 있는데, 본 발명에 있어서는, 특별히 지정하지 않는 한 어느 이성체도 포함된다. 즉, 본 발명에 있어서, 토코페롤류의 성분명으로서 특정한 광학 이성체를 지정하지 않는 한, 이러한 성분 표기는 각종 광학 이성체 단독 및 그들의 임의의 비율의 혼합물 모두를 포함하고, 단일의 광학 이성체여도 되고 각종 광학 이성체의 임의의 비율의 혼합물이어도 된다 (예를 들어, 「α-토코페롤의 아세트산에스테르」 라는 기재는, dl-α-토코페롤의 아세트산에스테르, d-α-토코페롤의 아세트산에스테르의 어느 것도 포함하는 것이다). 또한, 본 발명의 토코페롤류로는, 제16 개정 일본 약국방에 수재된 「토코페롤」, 「토코페롤숙신산에스테르칼슘」, 「토코페롤아세트산에스테르」, 「토코페롤니코틴산에스테르」 등을 바람직하게 사용할 수 있다.
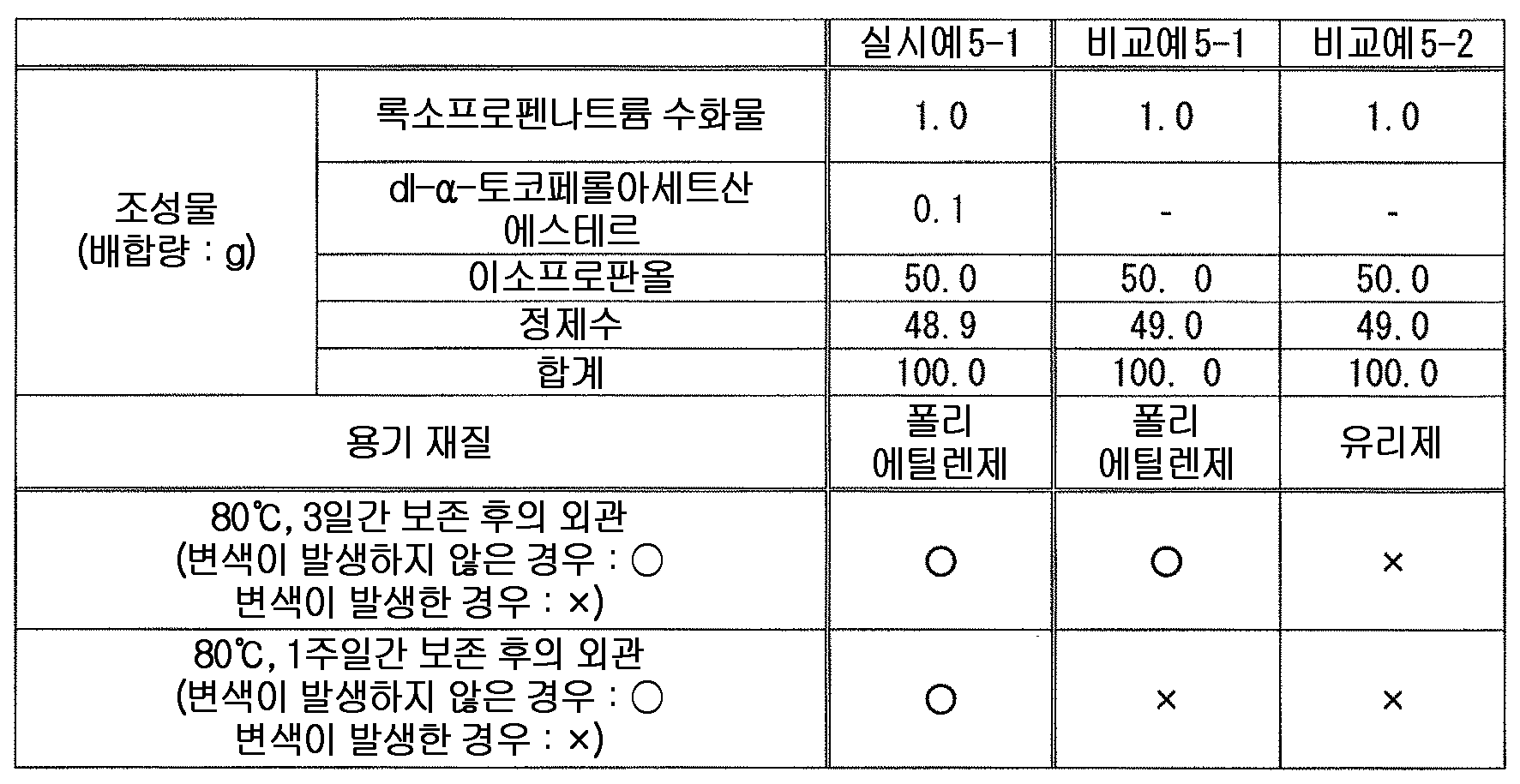
본 발명에 있어서 토코페롤류로는, 변색 억제 작용의 관점에서, 토코페롤, 토코페롤숙신산에스테르, 토코페롤아세트산에스테르 및 토코페롤니코틴산에스테르 그리고 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상이 바람직하고, 토코페롤, 토코페롤숙신산에스테르칼슘, 토코페롤아세트산에스테르 및 토코페롤니코틴산에스테르로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상이 보다 바람직하고, dl-α-토코페롤, dl-α-토코페롤숙신산에스테르칼슘, dl-α-토코페롤아세트산에스테르 및 dl-α-토코페롤니코틴산에스테르로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상이 더욱 바람직하고, dl-α-토코페롤아세트산에스테르가 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 토코페롤류의 함유량은 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 토코페롤류를 조성물 전체 질량에 대하여 0.01 ∼ 8 질량% 함유하는 것이 바람직하고, 0.05 ∼ 4 질량% 함유하는 것이 보다 바람직하고, 0.1 ∼ 2 질량% 함유하는 것이 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 록소프로펜 또는 그 염과 토코페롤류의 함유비는 특별히 한정되지 않고, 변색 억제 작용의 관점에서 적절히 검토하여 결정하면 되지만, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜 무수물 환산으로 1 질량부에 대하여, 토코페롤류를 0.01 ∼ 5 질량부 함유하는 것이 바람직하고, 0.05 ∼ 3 질량부 함유하는 것이 보다 바람직하고, 0.1 ∼ 1 질량부 함유하는 것이 특히 바람직하다.
<성분 (B-6)>
본 발명에 있어서, 「글리시르레틴산류」 란, 글리시르레틴산 및 그 유도체 (예를 들어, 글리실리진산 등의, 글리시르레틴산의 당부가 유도체 등) 그리고 그들의 염 (예를 들어, 칼륨염, 나트륨염 등의 알칼리 금속염 ; 암모늄염 등) 에서 선택되는 1 종 또는 2 종 이상을 의미한다.
본 발명에 있어서 글리시르레틴산류로는, 변색 억제 작용의 관점에서, 글리시르레틴산, 글리실리진산 및 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상이 바람직하고, 글리시르레틴산, 글리실리진산, 글리실리진산이칼륨, 글리실리진산모노암모늄, 글리실리진산이나트륨 및 글리실리진산삼나트륨으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상이 보다 바람직하고, 글리시르레틴산, 글리실리진산 및 글리실리진산이칼륨으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상이 더욱 바람직하고, 글리시르레틴산이 특히 바람직하다.
또한, 글리시르레틴산류를 액상 또는 반고형상의 조성물에 함유시키는 경우, 글리시르레틴산류를 그대로 사용하는 것 외에, 글리시르레틴산류를 함유하는 감초(감초) 나 그 추출물을 사용해도 된다. 여기서, 「감초」 (감초) 란, Glycyrrhiza uralensis Fischer 또는 Glycyrrhiza glabra Linne (Leguminosae) 의 뿌리 및 스톨론을 의미하고, 그 주피를 제거한 것 (껍질 제거 감초) 도 포함하는 개념이다 (제16 개정 일본 약국방). 감초는 필요에 따라 그 형태를 조절할 수 있고, 소편, 소괴로 절단 혹은 파쇄, 또는 분말로 분쇄할 수 있고, 예를 들어, 감초를 분말로 한 「감초 가루」 도 사용할 수 있다. 또한, 의약 조성물의 제조시의 취급의 편의를 고려하여, 감초에 어떠한 추출 처리를 실시한 「감초의 추출물」 을 사용해도 된다. 여기서, 당해 「감초의 추출물」 에는, 추출 처리에 더하여, 가열, 건조, 분쇄 등의 가공 처리를 실시한 것도 포함된다. 구체적으로는, 감초를 필요에 따라 적당한 크기로 한 후에, 적당한 침출액 (추출 용매) 을 첨가하여 침출한 액이나, 당해 침출액을 농축한 액 (연 엑기스, 팅크 등), 또한 이들을 건조시킨 것 (건조 엑기스 등) 등도 「감초의 추출물」 에 포함된다.
본 발명에 있어서, 감초 또는 그 추출물로는, 제16 개정 일본 약국방에 기재된 감초, 감초 가루, 감초 엑기스, 감초 미정제 엑기스가 바람직하다.
감초의 추출물의 제조 방법은 특별히 한정되지 않고, 예를 들어 제16 개정 일본 약국방 제제 총칙의 「엑기스제」, 「침제·탕약제」, 「팅크제」, 「유엑기스제」 의 항의 기재 등, 공지된 식물 추출물의 제조 방법을 참고로 하여 제조할 수 있다. 구체적으로는 예를 들어, 감초를 필요에 따라 절단, 가열, 건조, 분쇄 등 한 후, 적당한 추출 용매를 첨가하여 추출을 실시함으로써, 제조할 수 있다. 얻어진 추출물은, 필요에 따라 추가로 농축, 건조 등 시켜도 된다.
상기 추출 용매로는 예를 들어, 메탄올, 에탄올, 이소프로판올, n-부탄올 등의 저급 1 가 알코올 ; 에틸렌글리콜, 프로필렌글리콜, 1,3-부틸렌글리콜, 글리세린 등의 저급 다가 알코올 ; 디에틸에테르 등의 에테르류 ; 아세톤, 에틸메틸케톤 등의 케톤류 ; 아세트산에틸 등의 에스테르류 ; 아세토니트릴 등의 니트릴류 ; 펜탄, 헥산, 시클로펜탄, 시클로헥산 등의 알칸류 ; 디클로로메탄, 클로로포름 등의 할로게노알칸류 ; 벤젠, 톨루엔 등의 방향족 탄화수소 ; 디메틸포름아미드 ; 디메틸술폭시드 ; 물 (열수를 포함한다) 등을 들 수 있다. 이들은 각각 단독으로 사용해도 되고, 2 종 이상을 조합하여 사용해도 된다. 본 발명에 있어서는, 물, 에탄올, 또는 물/에탄올 혼액이 바람직하다.
추출 조작은 특별히 한정되지 않고, 식물로부터의 추출 조작에 이용되는 공지된 방법을 채용할 수 있고, 구체적으로는 예를 들어, 추출 용매에 대한 침지 (냉침, 온침, 퍼콜레이션 등), 초임계 유체나 아임계 유체를 사용한 추출 등을 들 수 있다. 또한, 추출 효율을 높이기 위해서, 교반이나 추출 용매 중에서 호모게나이즈해도 된다.
추출 온도는 특별히 한정되지 않고, 사용하는 추출 용매, 추출 조작 등에 따라 상이하지만, 5 ℃ 정도부터 추출 용매의 비점 이하의 온도로 하는 것이 바람직하다.
추출 시간은 특별히 한정되지 않고, 사용하는 추출 용매, 추출 조작 등에 따라 상이하지만, 1 시간 ∼ 14 일간 정도로 하는 것이 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 글리시르레틴산류의 함유량은 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 글리시르레틴산류를 프리체 환산으로 조성물 전체 질량에 대하여 0.01 ∼ 1 질량% 함유하는 것이 바람직하고, 0.03 ∼ 0.5 질량% 함유하는 것이 보다 바람직하고, 0.05 ∼ 0.3 질량% 함유하는 것이 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 록소프로펜 또는 그 염과 글리시르레틴산류의 함유비는 특별히 한정되지 않고, 변색 억제 작용의 관점에서 적절히 검토하여 결정하면 되지만, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜 무수물 환산으로 1 질량부에 대하여, 글리시르레틴산류를 프리체 환산으로 0.02 ∼ 0.8 질량부 함유하는 것이 바람직하고, 0.03 ∼ 0.4 질량부 함유하는 것이 보다 바람직하고, 0.04 ∼ 0.25 질량부 함유하는 것이 특히 바람직하다.
<성분 (B-7)>
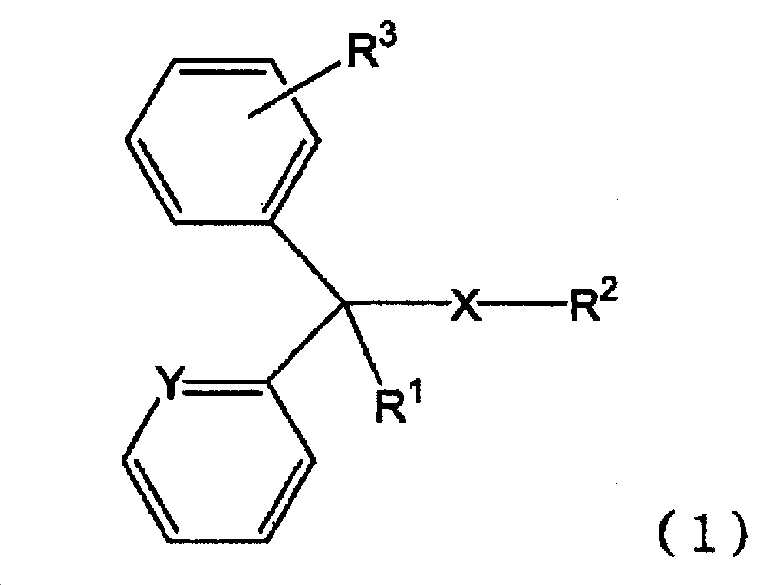
본 발명에 있어서, 「일반식 (1)
[화학식 3]
[식 (1) 중, X 는 단결합 또는 산소 원자를 나타내고, Y 는 메틴기 또는 질소 원자를 나타내고, R1 은 수소 원자, 수산기 또는 알킬기를 나타내고, R2 는 치환기를 가져도 되는 고리형 아미노기, 또는 치환기를 가져도 되는 아미노알킬기를 나타내고, R3 은 수소 원자 또는 할로겐 원자를 나타낸다.]
으로 나타내는 화합물 또는 그 염」 에는, 상기 일반식 (1) 로 나타내는 화합물 그 자체 외에, 일반식 (1) 로 나타내는 화합물의 약학 상 허용되는 염도 포함된다. 일반식 (1) 로 나타내는 화합물 또는 그 염의 구체예로는 예를 들어, 일반식 (1) 로 나타내는 화합물, 일반식 (1) 로 나타내는 화합물의 무기산염이나 유기산염 (예를 들어, 염산염, 말레산염, 푸마르산염, 디페닐디술폰산염, 테오클산염, 살리실산염, 탄닌산염, 베실산염, 인산염 등) 등을 들 수 있다. 또한, 일반식 (1) 로 나타내는 화합물의 화학 구조 중, 부제 탄소가 존재하는 경우에는, 다양한 광학 이성체를 갖는데, 본 발명에 있어서는, 어느 광학 이성체도 포함하고, 단일 광학 이성체여도 되고, 각종 광학 이성체의 혼합물이어도 된다. 또한, 일반식 (1) 로 나타내는 화합물 또는 그 염은 용매화물의 상태로 있어도 되고, 일반식 (1) 로 나타내는 화합물이나 그 염과 물이나 알코올 등의 용매화물도 「일반식 (1) 로 나타내는 화합물 또는 그 염」 에 포함된다.
상기 R1 에 있어서, 알킬기로는, 직사슬 또는 분기 사슬의 탄소수 1 ∼ 3 의 알킬기가 바람직하다. 구체적으로는, 메틸기, 에틸기, n-프로필기, 이소프로필기를 들 수 있지만, 메틸기가 바람직하다.
또한, 상기 R1 로는, 수소 원자, 메틸기가 바람직하다.
상기 R2 에 있어서, 치환기를 가져도 되는 고리형 아미노기에 있어서의 「고리형 아미노기」 란, 고리 구성 원자로서 질소 원자를 적어도 1 개, 바람직하게는 1 또는 2 개 갖는 5 ∼ 7 원의 지환식기를 의미한다.
이와 같은 고리형 아미노기로는, 구체적으로는 예를 들어, 피롤리디닐기, 피라졸리디닐기, 피페리디닐기, 피페라지닐기, 모르폴리닐기, 호모 피페리디닐기, 호모 피페라지닐기 등을 들 수 있다. 그 중에서도, 피페리디닐기, 피페라지닐기, 호모 피페라지닐기가 바람직하고, 피페리디닐기, 피페라지닐기가 보다 바람직하다.
또한, 치환기를 가져도 되는 고리형 아미노기에 있어서의 「치환기」 로는, 예를 들어, 알킬벤조일기, 1,3-디하이드로-2H-벤조이미다졸-2-온-1-일기, 카르복시알콕시기, 카르복실기, 카르복시알킬페닐기 및 수산기에서 선택되는 1 종 이상의 기가 치환되어 있어도 되는 알킬기 등을 들 수 있다. 그 중에서도, 알킬기, 카르복시알콕시알킬기, 카르복시알킬페닐(하이드록시)알킬기가 바람직하다.
상기 「치환기」 의 구체예로는, 예를 들어, 메틸기, 3-(4-tert-부틸벤조일)프로필기, 3-(1,3-디하이드로-2H-벤조이미다졸-2-온-1-일)프로필기, 2-(카르복시메톡시)에틸기, 4-[4-(2-카르복시프로판-2-일)페닐]-4-하이드록시부틸기, 3-카르복시프로필기 등을 들 수 있다.
상기 R2 에 있어서, 「치환기를 가져도 되는 고리형 아미노기」 로는, 1-메틸피페리딘-4-일기, 4-메틸 호모 피페라진-1-일기, 1-[3-(4-tert-부틸벤조일)프로필]피페리딘-4-일기, 4-[3-(1,3-디하이드로-2H-벤조이미다졸-2-온-1-일)프로필]피페라진-1-일기, 4-[2-(카르복시메톡시)에틸]피페라진-1-일기, 1-{4-[4-(2-카르복시프로판-2-일)페닐]-4-하이드록시부틸}피페리딘-4-일기, 1-(3-카르복시프로필)피페리딘-4-일기가 바람직하다.
상기 R2 에 있어서, 치환기를 가져도 되는 아미노알킬기에 있어서의 「아미노알킬기」 는, 아미노기, 모노알킬아미노기, 디알킬아미노기 또는 고리형 아미노기 (당해 「고리형 아미노기」 는, 상기한 「치환기를 가져도 되는 고리형 아미노기」 에 있어서의 「고리형 아미노기」 와 동일한 의미이다) 가 치환된 알킬기를 의미한다. 그 중에서도, 디알킬아미노기 또는 고리형 아미노기가 치환된 알킬기가 바람직하다. 또한, 당해 고리형 아미노기로는, 피롤리디닐기가 바람직하다.
이와 같은 아미노알킬기로는, 구체적으로는 예를 들어, 2-(디메틸아미노)에틸기, 2-(피롤리딘-2-일)에틸기, 2-[(이소프로필)(메틸)아미노]에틸기 등을 들 수 있다. 또한, 치환기를 가져도 되는 아미노알킬기에 있어서의 「치환기」 로는, 예를 들어, 수산기, 페닐기, 알킬기 등을 들 수 있다.
상기 R2 에 있어서, 「치환기를 가져도 되는 아미노알킬기」 로는, 2-(디메틸아미노)에틸기, 2-(1-메틸피롤리딘-2-일)에틸기, 2-[(메틸)(1-페닐-1-하이드록시프로판-2-일)아미노]에틸기가 바람직하다.
또한, 상기 R2 에 있어서, 「알킬기」, 「알킬벤조일기」, 「카르복시알킬페닐기」, 「아미노알킬기」, 「모노알킬아미노기」, 「디알킬아미노기」 에 있어서의 알킬기 부분으로는, 탄소수 1 ∼ 6 의 직사슬 또는 분기 사슬의 알킬기가 바람직하고, 구체예로는, 메틸기, 에틸기, 프로필기, 부틸기, 펜틸기, 헥실기 등을 들 수 있다.
또한, 상기 R2 에 있어서, 「카르복시알콕시기」 에 있어서의 알콕시기 부분으로는, 탄소수 1 ∼ 6 의 직사슬 또는 분기 사슬의 알콕시기가 바람직하고, 구체예로는, 메톡시기, 에톡시기, 프로폭시기, 부톡시기, 펜틸옥시기, 헥실옥시기 등을 들 수 있다.
상기 R3 에 있어서, 「할로겐 원자」 로는, 불소 원자, 염소 원자, 브롬 원자, 요오드 원자 등을 들 수 있고, 본 발명에 있어서는, 염소 원자가 바람직하다. 또한, 일반식 (1) 에 있어서 R3 의 페닐기 상의 치환 위치는 특별히 한정되지 않지만, 4 위치에 치환하는 것이 바람직하다.
본 발명에 있어서, 「일반식 (1) 로 나타내는 화합물 또는 그 염」 으로는, 구체적으로는 예를 들어, 에바스틴 또는 그 염 ; 옥사토미드 또는 그 염 ; 카르비녹사민디페닐디술폰산염, 카르비녹사민말레산염 등의 카르비녹사민 또는 그 염 ; 클레마스틴푸마르산염 등의 클레마스틴 또는 그 염 ; d-클로르페니라민말레산염, dl-클로르페니라민말레산염 등의 클로르페니라민 또는 그 염 ; 디페테롤염산염, 디페테롤인산염 등의 디페테롤 또는 그 염 ; 디페닐피랄린염산염, 디페닐피랄린테오클산염 등의 디페닐피랄린 또는 그 염 ; 디펜히드라민염산염, 디펜히드라민살리실산염, 디펜히드라민탄닌산염 등의 디펜히드라민 또는 그 염 ; 세티리진염산염 등의 세티리진 또는 그 염 ; 펙소페나딘 또는 그 염 ; 베포타스틴베실산염 등의 베포타스틴 또는 그 염 ; 호모클로르시클리진염산염 등의 호모클로르시클리진 또는 그 염 등을 들 수 있다. 또한, 이들 중 1 종을 단독으로 사용해도 되고 2 종 이상을 조합하여 사용해도 된다.
또한, 상기 일반식 (1) 로 나타내는 화합물 및 그 염, 특히 상기한 화합물 및 그 염은 공지이고, 공지된 방법에 의해 제조할 수 있는 것 외에, 시판되는 것을 사용할 수 있다.
본 발명에 있어서, 액상 또는 반고형상의 조성물에 있어서의 일반식 (1) 로 나타내는 화합물 또는 그 염의 합계 함유량은 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 일반식 (1) 로 나타내는 화합물 또는 그 염을 조성물 전체 질량에 대하여 0.01 ∼ 10 질량% 함유하는 것이 바람직하고, 0.05 ∼ 5 질량% 함유하는 것이 보다 바람직하고, 0.1 ∼ 3 질량% 함유하는 것이 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 록소프로펜 또는 그 염과 일반식 (1) 로 나타내는 화합물 또는 그 염의 함유비는 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜 무수물 환산으로 1 질량부에 대하여, 일반식 (1) 로 나타내는 화합물 또는 그 염을 합계로 0.01 ∼ 10 질량부 함유하는 것이 바람직하고, 0.05 ∼ 5 질량부 함유하는 것이 보다 바람직하고, 0.1 ∼ 3 질량부 함유하는 것이 특히 바람직하다.
본 발명에 있어서는, 일반식 (1) 로 나타내는 화합물 또는 그 염으로서, 「클로르페니라민 또는 그 염」 또는 「디펜히드라민 또는 그 염」 을 사용하는 것이 바람직하다.
본 발명에 있어서, 「클로르페니라민 또는 그 염」 에는, 클로르페니라민 그 자체 외에, 클로르페니라민의 약학 상 허용되는 염도 포함된다. 또한, 클로르페니라민은, 하기 식
[화학식 4]
로 나타내는 화합물이다.
클로르페니라민에는 부제 탄소가 존재하기 때문에, 광학 이성체를 갖는데, 본 발명에 있어서는, 어느 광학 이성체도 포함하고, 단일의 광학 이성체여도 되고, 각종 광학 이성체의 혼합물이어도 된다. 이들 중, 본 발명에 있어서는, d-체, dl-체가 바람직하다. 당해 클로르페니라민 또는 그 염의 구체예로는 예를 들어, 클로르페니라민, 클로르페니라민말레산염, d-클로르페니라민말레산염, dl-클로르페니라민말레산염 등을 들 수 있다. 본 발명에 있어서는, 클로르페니라민말레산염이 바람직하고, d-클로르페니라민말레산염, dl-클로르페니라민말레산염이 보다 바람직하고, d-클로르페니라민말레산염이 특히 바람직하다. 이들은 공지된 화합물이고, 공지된 방법에 의해 제조할 수 있는 것 외에, 시판되는 것을 사용할 수 있다.
클로르페니라민 또는 그 염을 사용하는 경우에 있어서, 액상 또는 반고형상의 조성물 중의 클로르페니라민 또는 그 염의 함유량은 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 클로르페니라민 또는 그 염을 조성물 전체 질량에 대하여 0.01 ∼ 5 질량% 함유하는 것이 바람직하고, 0.05 ∼ 3 질량% 함유하는 것이 보다 바람직하고, 0.1 ∼ 2 질량% 함유하는 것이 특히 바람직하다.
클로르페니라민 또는 그 염을 사용하는 경우에 있어서, 액상 또는 반고형상의 조성물에 포함되는 록소프로펜 또는 그 염과 클로르페니라민 또는 그 염의 함유비는 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜나트륨 무수물 환산으로 1 질량부에 대하여, 클로르페니라민 또는 그 염을 0.01 ∼ 5 질량부 함유하는 것이 바람직하고, 0.05 ∼ 3 질량부 함유하는 것이 보다 바람직하고, 0.1 ∼ 2 질량부 함유하는 것이 특히 바람직하다.
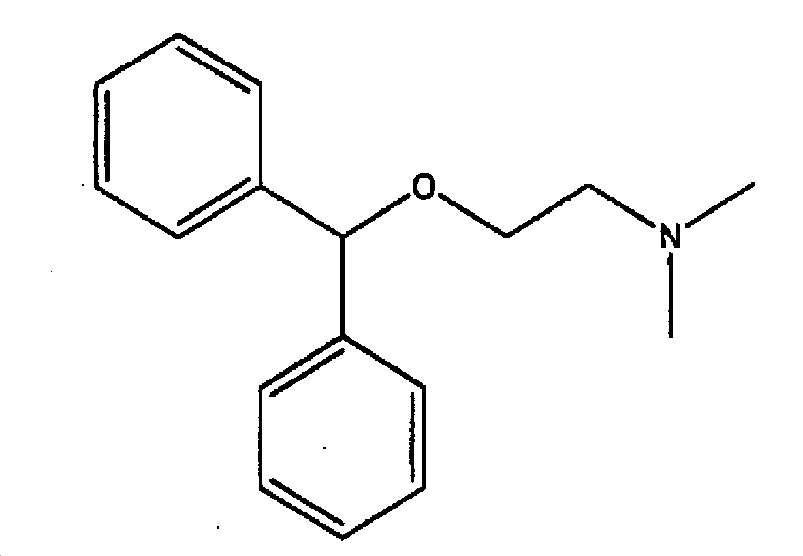
본 발명에 있어서, 「디펜히드라민 또는 그 염」 에는, 디펜히드라민 그 자체 외에, 디펜히드라민의 약학 상 허용되는 염도 포함된다. 또한, 디펜히드라민은, 하기 식
[화학식 5]
로 나타내는 화합물이다. 당해 디펜히드라민 또는 그 염의 구체예로는 예를 들어, 디펜히드라민, 디펜히드라민염산염, 디펜히드라민살리실산염, 디펜히드라민탄닌산염 등을 들 수 있다. 본 발명에 있어서는, 디펜히드라민, 디펜히드라민염산염, 디펜히드라민살리실산염이 바람직하다. 이들은 공지된 화합물이고, 공지된 방법에 의해 제조할 수 있는 것 외에, 시판되는 것을 사용할 수 있다.
디펜히드라민 또는 그 염을 사용하는 경우에 있어서, 액상 또는 반고형상의 조성물 중의 디펜히드라민 또는 그 염의 함유량은 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 디펜히드라민 또는 그 염을 조성물 전체 질량에 대하여 0.05 ∼ 10 질량% 함유하는 것이 바람직하고, 0.1 ∼ 5 질량% 함유하는 것이 보다 바람직하고, 0.3 ∼ 3 질량% 함유하는 것이 특히 바람직하다.
디펜히드라민 또는 그 염을 사용하는 경우에 있어서, 액상 또는 반고형상의 조성물에 포함되는 록소프로펜 또는 그 염과 디펜히드라민 또는 그 염의 함유비는 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜나트륨 무수물 환산으로 1 질량부에 대하여, 디펜히드라민 또는 그 염을 0.05 ∼ 10 질량부 함유하는 것이 바람직하고, 0.1 ∼ 5 질량부 함유하는 것이 보다 바람직하고, 0.3 ∼ 3 질량부 함유하는 것이 특히 바람직하다.
<성분 (B-8)>
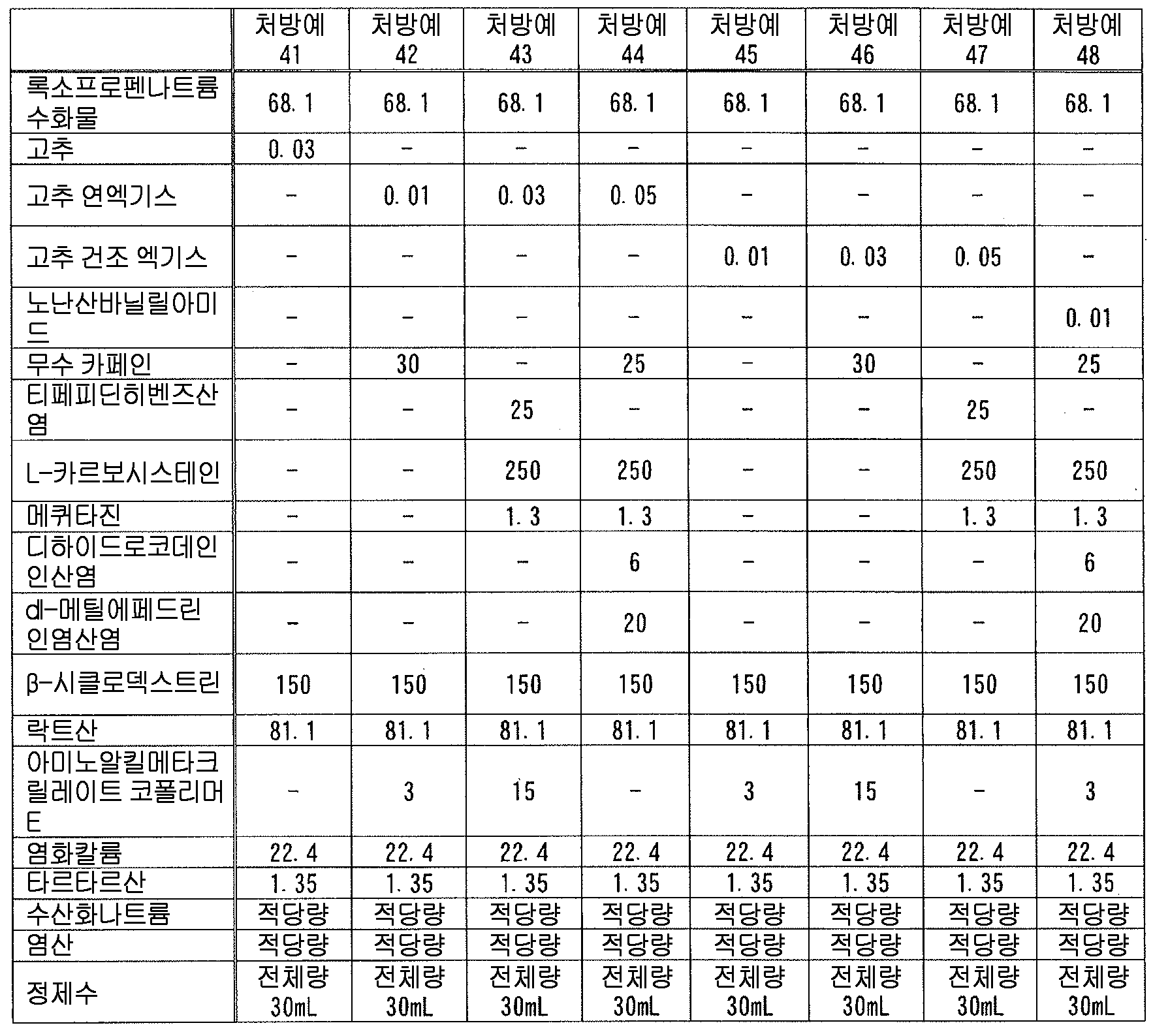
본 발명에 있어서, 「고추」 는 특별히 한정되지 않고, 예를 들어, 제16 개정 일본 약국방에 수재된 고추 (Capsicum annuum Linne (Solanaceae) 의 과실) 등을 바람직하게 사용할 수 있다. 고추는 필요에 따라 그 형태를 조절할 수 있고, 소편, 소괴로 절단 혹은 파쇄, 또는 분말로 분쇄할 수 있고, 예를 들어, 고추를 분말로 한 「고추 가루」 도 본 발명의 「고추」 로서 사용할 수 있다. 또한, 조성물·의약 제제의 제조시 취급의 편의 등을 고려하여, 고추에 어떠한 추출 처리를 실시한 것 (본 명세서에 있어서 「고추의 추출물」 이라고 칭한다) 을 사용해도 된다.
또한, 「고추의 추출물」 에는, 추출 처리에 더하여, 가열, 건조, 분쇄 등의 가공 처리를 실시한 것도 포함된다. 구체적으로는, 고추를 필요에 따라 적당한 크기로 한 후에, 적당한 침출액 (추출 용매) 을 첨가하여 침출한 액이나, 당해 침출액을 농축한 액 (연 엑기스, 팅크 등), 또한 이들을 건조시킨 것 (건조 엑기스 등) 등도 본 발명의 「고추의 추출물」 에 포함된다.
또한 본 발명에 있어서, 「고추의 추출물」 로는, 고추의 주성분인 공지된 캡사이시노이드를 사용해도 된다. 당해 캡사이시노이드로는, 캡사이신, 노난산바닐릴아미드 (별명 : 노닐산바닐릴아미드) 가 바람직하다.
본 발명에 있어서, 「고추 또는 그 추출물」 로는, 고추, 고추 가루, 고추 엑기스 (연 엑기스, 건조 엑기스), 캡사이신, 노난산바닐릴아미드가 바람직하고, 고추 연엑기스, 노난산바닐릴아미드가 특히 바람직하다.
고추의 추출물의 제조 방법은 특별히 한정되지 않고, 예를 들어 제16 개정 일본 약국방 제제 총칙의 「엑기스제」, 「침제·탕약제」, 「팅크제」, 「유엑기스제」 의 항의 기재 등, 공지된 식물 추출물의 제조 방법을 참고로 하여 제조할 수 있다. 구체적으로는 예를 들어, 고추를 필요에 따라 절단, 가열, 건조, 분쇄 등 한 후, 적당한 추출 용매를 첨가하여 추출을 실시함으로써, 제조할 수 있다. 얻어진 추출물은, 필요에 따라 추가로 농축, 건조 등 시켜도 된다.
상기 추출 용매로는 예를 들어, 메탄올, 에탄올, 이소프로판올, n-부탄올 등의 저급 1 가 알코올 ; 에틸렌글리콜, 프로필렌글리콜, 1,3-부틸렌글리콜, 글리세린 등의 저급 다가 알코올 ; 디에틸에테르 등의 에테르류 ; 아세톤, 에틸메틸케톤 등의 케톤류 ; 아세트산에틸 등의 에스테르류 ; 아세토니트릴 등의 니트릴류 ; 펜탄, 헥산, 시클로펜탄, 시클로헥산 등의 알칸류 ; 디클로로메탄, 클로로포름 등의 할로게노알칸류 ; 벤젠, 톨루엔 등의 방향족 탄화수소 ; 디메틸포름아미드 ; 디메틸술폭시드 ; 물 (열수를 포함한다) 등을 들 수 있다. 이들은 각각 단독으로 사용해도 되고, 2 종 이상을 조합하여 사용해도 된다. 본 발명에 있어서는, 물, 에탄올, 또는 물/에탄올 혼액이 바람직하다.
추출 조작은 특별히 한정되지 않고, 식물로부터의 추출 조작에 이용되는 공지된 방법을 적절히 채용할 수 있고, 구체적으로는 예를 들어, 추출 용매에 대한 침지 (냉침, 온침, 퍼콜레이션 등), 초임계 유체나 아임계 유체를 사용한 추출 등을 들 수 있다. 또한, 추출 효율을 높이기 위해서, 교반이나 추출 용매 중에서 호모게나이즈해도 된다.
추출 온도는 특별히 한정되지 않고, 사용하는 추출 용매, 추출 조작 등에 따라 상이하지만, 5 ℃ 정도부터 추출 용매의 비점 이하의 온도로 하는 것이 바람직하다.
추출 시간은 특별히 한정되지 않고, 사용하는 추출 용매, 추출 조작 등에 따라 상이하지만, 1 시간 ∼ 14 일 정도로 하는 것이 바람직하다.
본 발명에 있어서, 고추 또는 그 추출물로는, 시판품을 사용할 수 있고, 구체적인 시판품으로는 예를 들어, 고추 엑기스-B, 고추 엑기스-D, 고추 엑기스-N, 고추 엑기스-S, (국) 고추 팅크, (국) 고추 가루 (이상, 닛폰 훈마츠 약품 주식회사), 노닐산바닐릴아미드 (나가오카 실업 주식회사) 등을 들 수 있다.
본 발명에 있어서, 액상 또는 반고형상의 조성물에 있어서의 고추 또는 그 추출물의 함유량은 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 고추 또는 그 추출물을 원생약 환산량으로, 조성물 전체 질량에 대하여 0.01 ∼ 15 질량% 함유하는 것이 바람직하고, 0.05 ∼ 10 질량% 함유하는 것이 보다 바람직하고, 0.1 ∼ 8 질량% 함유하는 것이 특히 바람직하다. 또한, 특히 고추 또는 그 추출물로서 캡사이신, 노난산바닐릴아미드 등의 캡사이시노이드를 사용하는 경우에 있어서는, 변색 억제 작용의 관점에서, 캡사이시노이드를 조성물 전체 질량에 대하여 0.0001 ∼ 2 질량% 함유하는 것이 바람직하고, 0.0005 ∼ 1 질량% 함유하는 것이 보다 바람직하고, 0.001 ∼ 0.5 질량% 함유하는 것이 더욱 바람직하고, 0.005 ∼ 0.1 질량% 함유하는 것이 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 록소프로펜 또는 그 염과 고추 또는 그 추출물의 함유비는 특별히 한정되지 않고, 변색 억제 작용의 관점에서 적절히 검토하여 결정하면 되지만, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜 무수물 환산으로 1 질량부에 대하여, 고추 또는 그 추출물을 원생약 환산량으로 0.01 ∼ 15 질량부 함유하는 것이 바람직하고, 0.05 ∼ 10 질량부 함유하는 것이 보다 바람직하고, 0.1 ∼ 8 질량부 함유하는 것이 특히 바람직하다. 또한, 특히 고추 또는 그 추출물로서 캡사이신, 노난산바닐릴아미드 등의 캡사이시노이드를 사용하는 경우에 있어서는, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜나트륨 무수물 환산으로 1 질량부에 대하여, 캡사이시노이드를 0.0001 ∼ 2 질량부 함유하는 것이 바람직하고, 0.0005 ∼ 1 질량부 함유하는 것이 보다 바람직하고, 0.001 ∼ 0.2 질량부 함유하는 것이 더욱 바람직하고, 0.005 ∼ 0.1 질량부 함유하는 것이 특히 바람직하다.
<성분 (B-9)>
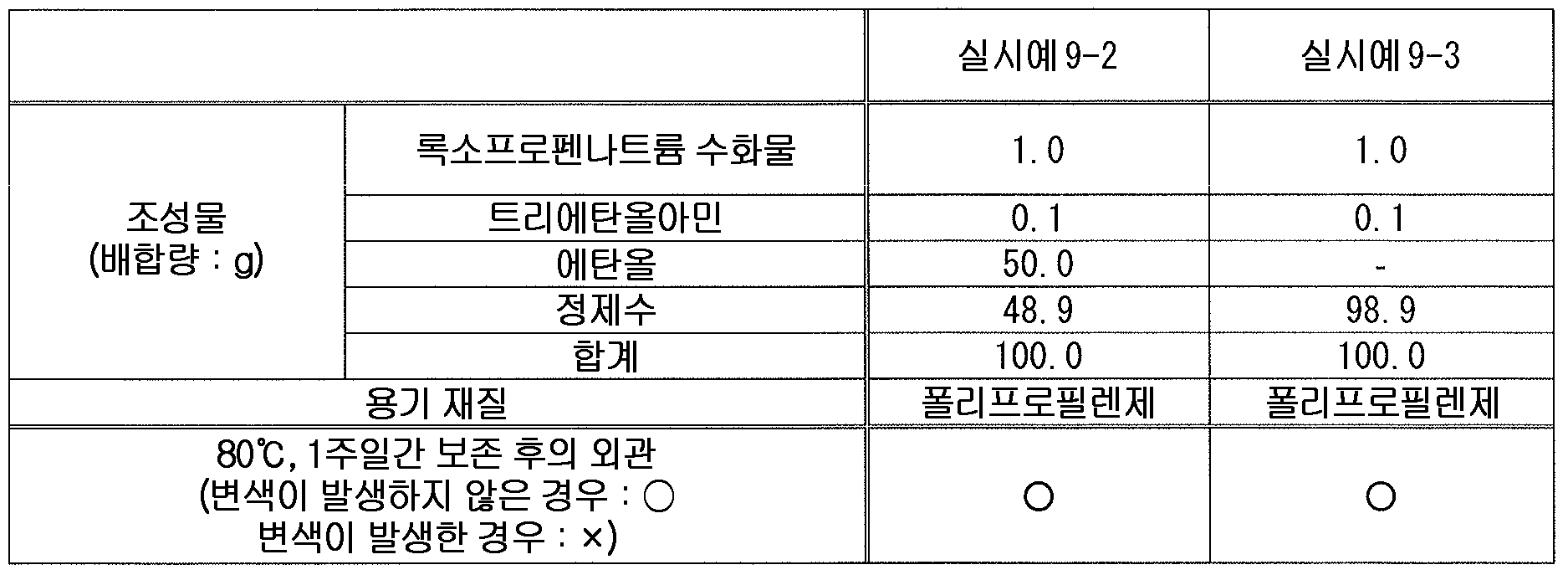
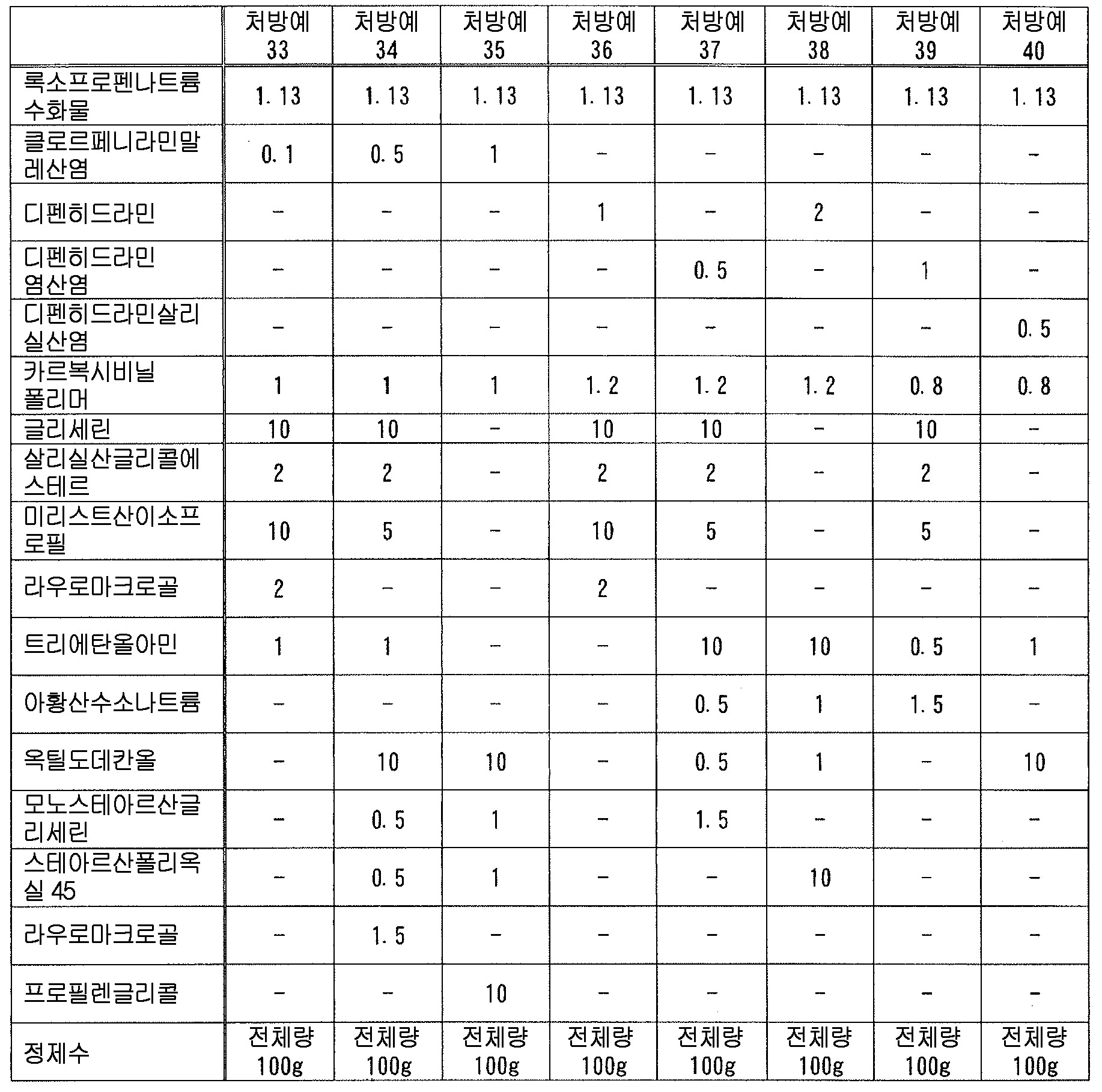
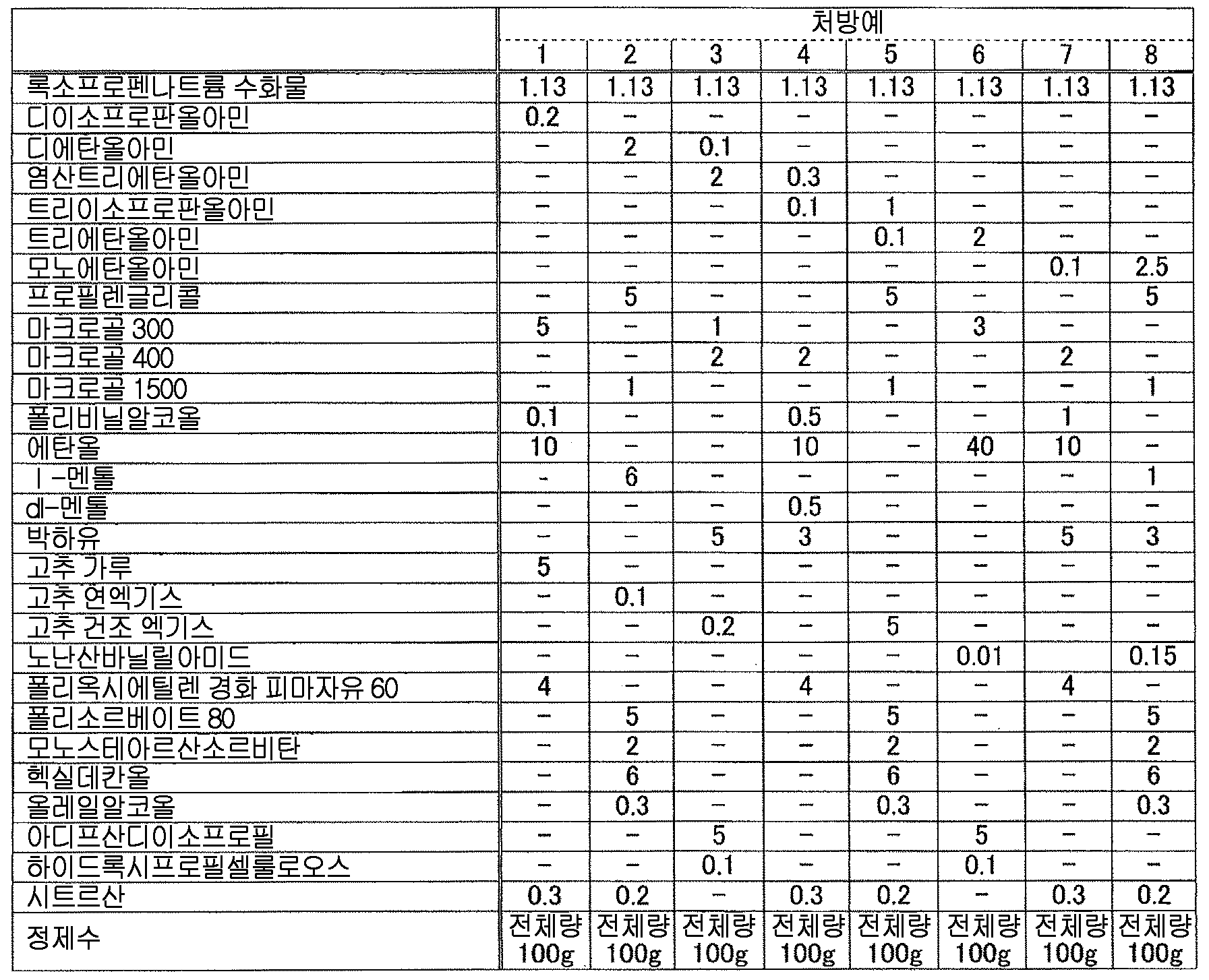
본 발명에 있어서, 「유기 아민」 으로는 다양하게 들 수 있지만, 변색 억제 작용의 관점에서, 알칸올아민이 바람직하다. 알칸올아민으로는, 예를 들어, 디이소프로판올아민, 디에탄올아민, 염산트리에탄올아민, 트리이소프로판올아민, 트리에탄올아민, 트로메타몰, 메글루민, 모노에탄올아민 등을 들 수 있다. 이들 중 1 종을 단독으로 또는 2 종 이상을 조합하여 사용해도 된다.
이들 중에서도, 변색 억제 작용의 관점에서, 에탄올아민류가 바람직하고, 트리에탄올아민 또는 그 염이 보다 바람직하고, 트리에탄올아민 또는 그 유기산염 혹은 무기산염이 더욱 바람직하고, 염산트리에탄올아민, 트리에탄올아민이 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 유기 아민의 함유량은 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 유기 아민을 조성물 전체 질량에 대하여, 0.001 ∼ 5 질량% 함유하는 것이 바람직하고, 0.01 ∼ 1 질량% 함유하는 것이 보다 바람직하고, 0.05 ∼ 0.5 질량% 함유하는 것이 특히 바람직하다.
본 발명에 있어서, 액상 또는 반고형상의 조성물 중의 록소프로펜 또는 그 염과 유기 아민의 함유비는 특별히 한정되지 않지만, 변색 억제 작용의 관점에서, 록소프로펜 또는 그 염을 록소프로펜 무수물 환산으로 1 질량부에 대하여, 유기 아민을 0.03 ∼ 0.6 질량부 함유하는 것이 바람직하고, 0.06 ∼ 0.4 질량부 함유하는 것이 보다 바람직하고, 0.1 ∼ 0.2 질량부 함유하는 것이 특히 바람직하다.
<액상 또는 반고형상의 조성물>
본 발명에 있어서, 「액상 또는 반고형상의 조성물」 이란, 상온 (15 ∼ 25 ℃ 의 범위 내 중 어느 온도) 에 있어서 액상 혹은 반고형상의 조성물을 의미한다.
본 발명에 있어서 조성물의 성상은 특별히 한정되지 않고, 용액, 콜로이드 용액 (졸 (현탁액이나 유탁액)), 겔 등의 어느 것이어도 된다. 또한, 용매 혹은 기제의 종류·성질 등은 특별히 한정되지 않고, 친수성이어도 되고 유성 등의 소수성이어도 되고, 나아가 상이한 복수종의 용매·기제를 적절히 혼합·유화 등 하여 사용해도 된다. 이러한 용매·기제로는, 구체적으로는 예를 들어, 후기하는 첨가물로서 예시된 성분 등을 들 수 있다.
본 발명에 있어서는, 의약 제제의 사용시의 안전성의 관점에서, 액상 또는 반고형상의 조성물이, 물을 함유하는 것이 바람직하다. 여기서, 조성물 중의 물의 함유량은, 특별히 한정되지 않지만, 의약 제제의 사용시의 안전성이나 변색 억제 작용의 관점에서, 조성물 전체 질량에 대하여 1 질량% 이상인 것이 바람직하고, 5 질량% 이상인 것이 보다 바람직하고, 10 질량% 이상인 것이 더욱 바람직하고, 20 질량% 이상인 것이 더욱 보다 바람직하고, 30 질량% 이상인 것이 특히 바람직하다. 또한, 상기와 동일한 관점에서, 조성물 전체 질량에 대하여 100 질량% 미만인 것이 바람직하고, 99 질량% 이하인 것이 보다 바람직하고, 90 질량% 이하인 것이 더욱 바람직하고, 70 질량% 이하인 것이 더욱 보다 바람직하고, 50 질량% 이하인 것이 특히 바람직하다. 또한 상기와 동일한 관점에서, 조성물 전체 질량에 대하여 10 ∼ 90 질량% 인 것이 더욱 바람직하고, 20 ∼ 70 질량% 인 것이 더욱 보다 바람직하고, 30 ∼ 50 질량% 인 것이 특히 바람직하다.
또한, 본 발명에 있어서는, 의약 제제의 사용감의 관점에서, 액상 또는 반고형상의 조성물이, 저급 알코올을 함유하는 것이 바람직하다. 여기서, 「저급 알코올」 이란, 탄소수 1 ∼ 6 의 직사슬 또는 분기 사슬의 1 가의 알코올을 의미하고, 구체적으로는 예를 들어, 에탄올, 이소프로판올, n-프로판올 등을 들 수 있고, 에탄올, 이소프로판올 및 이들의 혼합물이 바람직하다. 조성물 중의 저급 알코올의 함유량은, 특별히 한정되지 않지만, 의약 제제의 사용감이나 변색 억제 작용의 관점에서, 조성물 전체 질량에 대하여 5 질량% 이상인 것이 바람직하고, 10 ∼ 90 질량% 인 것이 보다 바람직하고, 15 ∼ 70 질량% 인 것이 더욱 바람직하고, 17.5 ∼ 60 질량% 인 것이 더욱 보다 바람직하고, 20 ∼ 50 질량% 인 것이 특히 바람직하다.
본 발명에 있어서는, 의약 제제의 사용시의 안전성, 사용감의 관점에서, 액상 또는 반고형상의 조성물이, 물 및 저급 알코올의 양자를 함께 함유하는 것이 바람직하다. 조성물이, 물 또는 저급 알코올의 적어도 일방을 함유하는 조성물 (특히 물 및 저급 알코올의 양자를 함께 함유하는 조성물) 의 경우에도, 변색이 억제된 것이 된다.
본 발명에 있어서, 액상 또는 반고형상의 조성물에는, 의약 성분으로서, 상기 이외의 약물, 예를 들어, 진통 성분, 항염증 성분, 상기 일반식 (1) 로 나타내는 화합물 및 그 염을 제외한 항히스타민 성분, 살균 성분, 수렴·보호 성분, 혈행 촉진 성분, 국소 마취 성분, 진해제, 노스카핀류, 기관지 확장제, 거담제, 최면 진정제, 비타민류, 위 점막 보호제, 제산제, 항콜린제, 생약류, 한방 처방 등으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상을 포함하고 있어도 된다.
진통 성분으로는, 예를 들어, 아스피린, 아스피린알루미늄, 아세트아미노펜, 이소프로필안티피린, 이부프로펜, 에텐자미드, 사자피린, 살리실아미드, 살리실산, 살리실산에틸렌글리콜, 살리실산글리콜, 살리실산나트륨, 살리실산메틸, 티아라미드염산염, 락틸페네티딘 등을 들 수 있다.
항염증 성분으로는, 예를 들어, 구아이아줄렌술폰산나트륨, 세아프로제, 세미알칼리프로테이나제, 세라펩타제, 프록타제, 프로나제, 브로멜라인 등을 들 수 있다.
상기 일반식 (1) 로 나타내는 화합물 및 그 염을 제외한 항히스타민 성분으로는, 예를 들어, 아젤라스틴염산염, 알리메마진타르타르산염, 이소티펜딜염산염, 이프로헵틴염산염, 에피나스틴염산염, 에메다스틴푸마르산염, 케토티펜푸마르산염, 트리프롤리딘염산염, 트리펠레나민염산염, 톤질아민염산염, 페네타진염산염, 프로메타진염산염, 프로메타진메틸렌이살리실산염, 메퀴타진, 메트딜라진염산염, 메브하이드롤린나파디실산염 등을 들 수 있다.
살균 성분으로는, 예를 들어, 염화벤잘코늄 등을 들 수 있다. 수렴·보호 성분으로는, 예를 들어, 산화아연 등을 들 수 있다. 혈행 촉진 성분으로는, 니코틴산벤질, 헤파린 유사 물질, 폴리에틸렌술폰산나트륨 등을 들 수 있다. 국소 마취 성분으로는, 예를 들어, 리도카인, 벨라도나 엑기스 등을 들 수 있다.
진해제로는, 예를 들어, 알로클라미드염산염, 에프라지논염산염, 카르베타펜탄시트르산염, 클로페라스틴염산염, 클로페라스틴펜디조산염, 디부네이트나트륨, 디메모르판인산염, 티페피딘시트르산염, 티페피딘히벤즈산염 등을 들 수 있다.
노스카핀류로는, 예를 들어, 노스카핀염산염, 노스카핀 등을 들 수 있다.
기관지 확장제로는, 예를 들어, 트리메토퀴놀염산염, 페닐레프린염산염, 메톡시페나민염산염 등을 들 수 있다.
거담제로는, 예를 들어, 암모니아·회향정, 염화암모늄 등을 들 수 있다.
최면 진정제로는, 예를 들어, 알릴이소프로필아세틸우레아나 브롬발레릴우레아 등을 들 수 있다.
비타민류로는, 예를 들어, 비타민 B1, 비타민 B2, 비타민 B5, 비타민 B6, 비타민 B12, 비타민 C, 헤스페리딘 및 그 유도체 그리고 그들의 염류 등 (예를 들어, 티아민, 티아민염화물염산염, 티아민질화물, 디세티아민염산염, 세토티아민염산염, 푸르술티아민, 푸르술티아민염산염, 옥토티아민, 시코티아민, 티아민디술피드, 비스이부티아민, 비스벤티아민, 프로술티아민, 벤포티아민, 리보플라빈, 리보플라빈인산에스테르, 리보플라빈부티르산에스테르, 인산리보플라빈나트륨, 판테놀, 판테틴, 판토텐산나트륨, 피리독신염산염, 피리독살인산에스테르, 시아노코발라민, 메코발라민, 아스코르브산, 아스코르브산나트륨, 아스코르브산칼슘, 헤스페리딘 등) 을 들 수 있다.
위 점막 보호제로는, 예를 들어, 게파르나트, 세트락세이트염산염, 소파르콘, 테프레논, 메틸메티오닌술포늄클로라이드 등을 들 수 있다.
제산제로는, 예를 들어, 아미노아세트산, 규산알루민산마그네슘, 규산마그네슘, 합성 규산알루미늄, 합성 하이드로탈사이트, 산화마그네슘, 디하이드록시알루미늄아미노아세테이트, 수산화알루미나마그네슘, 수산화알루미늄겔, 건조 수산화알루미늄겔, 수산화알루미늄·탄산마그네슘 혼합 건조 겔, 수산화알루미늄·탄산수소나트륨의 공침 생성물, 수산화알루미늄·탄산칼슘·탄산마그네슘의 공침 생성물, 수산화마그네슘, 수산화마그네슘·황산알루미늄칼륨의 공침 생성물, 탄산마그네슘, 탄산수소나트륨, 침강 탄산칼슘, 메타규산알루민산마그네슘, 무수 인산수소칼슘, 인산수소칼슘, 오적골, 석결명, 모려 등을 들 수 있다.
항콜린약으로는, 예를 들어, 옥시펜사이클리민염산염, 디사이클로민염산염, 메틱센염산염, 티페피디늄 브롬화물, 메틸베낙티쥼 브롬화물, 피렌제핀염산염, 요오드화이소프로파미드, 요오드화디페닐피페리디노메틸디옥솔란 등을 들 수 있다.
생약류로는, 예를 들어, 예덕나무 (적아백), 갬비어 (아선약), 삼지구엽초 (음양곽), 펜넬 (회향), 터메릭 (울금), 현호색 (연호색), 황금 (황잠), 황정 (황정), 황벽 (황백), 벚나무껍질 (앵피), 황련 (황련), 원지 (원지), 봉출 (아출), 쥐오줌풀 (녹자초), 캐모마일, 하늘타리 (괄루인), 도라지 (길경), 살구씨 (행인), 구기 (구기자), 구기자잎 (구기엽), 정가 (형개), 계피 (계피), 결명초씨 (결명자), 젠티아나, 쥐손이풀 (현증거), 잇꽃 (홍화), 약방동사니 (향부자), 우황 (우황), 오미자 (오미자), 족두리풀 (세신), 치자 (산치자), 분디 (산초), 개미취 (자원), 구기근피 (지골피), 자근 (자근), 작약 (작약), 사미취 (사향), 더덕 (사삼), 질경이 (차전자), 질경이 (차전초), 수담 (웅담을 포함한다), 생강 (생강), 지렁이 (지룡), 목련 (신이), 컨커트리, 꽃무릇 (석산), 세네가, 천궁이 (천궁), 아삼 (전호), 당약 (천진), 삽주 (창출), 상근백피 (상백피), 자소 (소엽), 마늘 (대산), 죽절삼 (죽절인삼), 귤껍질 (진피), 승검초 (당귀), 토근 (토근), 남천 열매 (남천실), 당근 (당근), 패모 (패모), 맥문동 (맥문동), 끼무릇 (반하), 사프란 (번홍화), 살모사 (반비), 구릿대 (백지), 삽주 (백출), 복령 (복령), 모란피 (목단피), 소귀나무 (양매피), 녹용 (녹용) 등의 생약 및 이들의 추출물 (엑기스, 팅크, 건조 엑기스 등) 등을 들 수 있다.
한방 처방으로는, 예를 들어, 계지탕 (계지탕), 향소산 (향소산), 시호계지탕 (시호계지탕), 소시호탕 (소시호탕), 맥문동탕 (맥문동탕), 반하후박탕 (반하후박탕) 등을 들 수 있다.
또한, 본 발명에 있어서, 액상 또는 반고형상의 조성물에는, 상기 성분 이외에, 의약 제제의 제형, 투여 방법 등에 따라 의약품 분야, 화장품 분야 등에 있어서 사용되는 첨가물을 배합해도 된다. 이러한 첨가물로는, 예를 들어, 겔화제, 유지류, 유화제, 가용화제, pH 조정제, 항산화제, 연화제, 증점제, 보습제, 방부제, 안정화제, 경피 흡수 촉진제, 교미제·감미제 등을 들 수 있다.
겔화제로는, 예를 들어, 카르복시비닐 폴리머 등의 아크릴산계 고분자 ; 폴리비닐피롤리돈 등을 들 수 있다.
유지류로는, 예를 들어, 스쿠알란, 파라핀, 유동 파라핀, 경질 유동 파라핀, 바셀린 등의 탄화수소류 ; 미리스트산이소프로필, 미리스트산옥틸도데실 등의 지방산 에스테르류 ; 베헤닐알코올, 라우릴알코올, 미리스틸알코올, 세틸알코올, 스테아릴알코올, 이소스테아릴알코올, 올레일알코올 등의 고급 알코올류 ; 베헤닌산, 라우르산, 미리스트산, 스테아르산, 이소스테아르산, 올레산 등의 고급 지방산 ; 카르나우바납, 경랍, 셸락, 호호바유, 밀랍, 백랍, 몬탄납, 라놀린, 정제 라놀린, 환원 라놀린 등의 납류 ; 실리콘유 등을 들 수 있다.
유화제로는, 예를 들어, 프로필렌글리콜 모노 지방산 에스테르, 에틸렌글리콜 모노 지방산 에스테르, 글리세린 모노 지방산 에스테르, 폴리글리세린 지방산 에스테르, 소르비탄 지방산 에스테르, 자당 지방산 에스테르, 메틸글리코시드 지방산 에스테르, 알킬폴리글리코시드 등의 다가 알코올 지방산 에스테르 또는 다가 알코올알킬에테르 ; 폴리옥시에틸렌알킬에테르, 폴리옥시에틸렌알킬페닐에테르, 폴리옥시에틸렌피토스테롤, 폴리옥시에틸렌피토스타놀, 폴리옥시에틸렌폴리옥시프로필렌알킬에테르 등의 폴리옥시에틸렌에테르 ; 폴리옥시에틸렌모노 지방산 에스테르, 폴리에틸렌글리콜디 지방산 에스테르, 폴리옥시에틸렌글리세린 지방산 에스테르, 폴리옥시에틸렌소르비탄 지방산 에스테르, 폴리옥시에틸렌소르비톨 지방산 에스테르, 폴리옥시에틸렌메틸글리코시드 지방산 에스테르, 폴리옥시에틸렌 경화 피마자유, 폴리옥시에틸렌 피마자유, 폴리옥시에틸렌 식물유, 폴리옥시에틸렌알킬에테르 지방산 에스테르 등의 에테르에스테르 등의 비이온성 계면 활성제 또는 라우릴황산나트륨, 세틸황산나트륨 등의 이온성 계면 활성제 등을 들 수 있다.
가용화제로는, 예를 들어, 상기의 유화제로서 예시한 비이온성 계면 활성제 또는 이온성 계면 활성제에 더하여, 유동 파라핀, 크로타미톤 등을 들 수 있다.
pH 조정제로는, 예를 들어, 시트르산, 시트르산나트륨, 무수 시트르산, 말산, 말레산, 숙신산, 푸마르산, 타르타르산, 타르타르산나트륨, 락트산, 락트산칼슘, 락트산나트륨, 아세트산, 아세트산나트륨, 빙초산 등의 유기산 또는 그 염 ; 염산, 황산, 인산, 인산수소나트륨, 인산이수소칼륨, 인산이수소나트륨, 탄산나트륨, 탄산수소나트륨 등의 무기산 또는 그 염 ; 수산화나트륨, 수산화칼륨, 수산화칼슘, 수산화마그네슘 등의 수산화알칼리 등을 들 수 있다.
항산화제로는, 예를 들어, 아황산나트륨, 아스코르브산, 아황산수소나트륨, 아황산나트륨, 에데트산나트륨, 에리소르브산, 염산시스테인, 시트르산, 대두 레시틴, 몰식자산프로필 등을 들 수 있다.
연화제로는, 예를 들어, 알란토인, 아몬드유, 올리브유, 유동 파라핀, 스쿠알란, 스쿠알렌, 정제 라놀린, 중사슬 지방산 트리글리세리드, 유채씨유, 피마자유, 폴리부텐 등을 들 수 있다.
증점제로는, 예를 들어, 폴리비닐피롤리돈, 콜로이드성 규산알루미늄, 잔탄검, 로커스트빈검, 트라가간트검, 구아검, 젤라틴, 아라비아 고무, 알긴산, 알부민 등을 들 수 있다.
보습제로는, 히알루론산나트륨, 우레아, 자당 등을 들 수 있다.
방부제로는, 예를 들어, 파라옥시벤조산메틸, 파라옥시벤조산에틸, 파라옥시벤조산프로필, 파라옥시벤조산이소프로필, 파라옥시벤조산부틸, 파라옥시벤조산이소부틸, 파라옥시벤조산벤질, 벤조산나트륨, 벤조산, 벤조산벤질, 염화벤잘코늄, 염화세틸피리디늄, 염화벤제토늄, 아미노에틸술폰산 등을 들 수 있다.
안정화제로는, 예를 들어, 아디프산, 아스코르브산, 아황산나트륨, 아황산수소나트륨, 염화나트륨, 경화유, 시스테인 등을 들 수 있다.
경피 흡수 촉진제로는, 예를 들어, 아디프산디이소프로필 등의 지방산 에스테르류를 들 수 있다.
교미제·감미제로는, 예를 들어, 아세설팜칼륨, 스테비아, 타우마틴, 수크랄로스, 파노오스, 트레할로스, 환원 팔라티노오스, 커플링 슈거, 프락토 올리고당, 갈락토 올리고당, 유과 올리고당, 이소말토 올리고당, 팔라티노오스 올리고당, 라피노오스, 아스파탐, 과당, 흑설탕, 사카린 혹은 그 염, 젖당, 백당, 벌꿀, 포도당, 말토오스, 물엿 등을 들 수 있다.
본 발명에 있어서, 액상 또는 반고형상의 조성물의 제조 방법은 특별히 한정되지 않고, 배합하는 성분의 종류나 양, 조성물의 성상, 용기의 형상, 의약 제제의 제형, 투여 경로나 용도 등에 따라, 예를 들어 제16 개정 일본 약국방 제제 총칙 등에 기재된 공지된 방법에 의해 제조할 수 있다.
<폴리올레핀계 수지제 용기>
본 발명에 있어서, 「용기」 란, 액상 또는 반고형상의 조성물을 직접적으로 수용하는 포장체를 의미한다. 용기의 형상은, 액상 또는 반고형상의 조성물을 수용 가능한 것을 한도로 하여 특별히 한정되지 않고, 조성물의 성상, 의약 제제의 제형, 투여 경로나 용도 등에 따라 적절히 검토하여 결정하면 된다.
이와 같은 용기의 형상으로는, 예를 들어, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기 (보다 상세하게는 예를 들어, 스펀지상의 도포 부재 (헤드) 를 구비하는 보틀 용기, 롤 온 용기나 자 보틀 용기 등), 튜브 용기, 점안 용기 등을 들 수 있다. 또한, 이들 용기는 모두 공지이고, 공지된 방법에 의해 제조하면 되고, 또한, 시판품을 사용해도 된다.
본 발명에 있어서, 용기로는, 의약 제제의 취급이나 사용시의 편의 등의 관점에서, 이하의 (1) 또는 (2) :
(1) 스펀지상의 도포 부재를 구비하는 보틀 용기와 같이, 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 튜브 용기와 같이, 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
가 바람직하고, (1) 의 양태의 용기가 특히 바람직하다.
[(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기]
이러한 양태의 용기의 경우, 용기 본체에 수용된 조성물을 도포 부재에 함침·유지시켜, 상기 도포 부재를 피도포부에 접촉시킴으로써, 조성물을 도포할 수 있다. 이 경우에 있어서, 용기 본체와 도포 부재는, 각각 독립적인 부재로서 제작한 후 용기 본체에 도포 부재를 장착해도 되고, 일체적으로 성형해도 된다.
또한, 도포 부재로는, 액상 또는 반고형상의 조성물을 함침·유지 가능한 구성이면 되고, 예를 들어 스펀지상과 같은 다공질의 부재나 솔상의 부재 등을 들 수 있다.
이와 같은 용기로는 예를 들어, 용기 본체의 개구부에 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기를 들 수 있다.
보다 상세한 구체예로는 예를 들어, 개구부를 갖는 용기 본체와, 상기 개구부에 장착된, 다공질 (스펀지상 등) 의 도포 부재를 구비하여 이루어지는 용기 등을 들 수 있다. 이 경우, 용기 본체에 수용된 조성물을, 구멍 직경·공극률 등이 적절히 조정된 다공질의 도포 부재에 함침·유지시킨 후, 당해 도포 부재를 피도포부에 접촉시키는 것에 의해, 조성물을 피도포부에 도포할 수 있다.
또한, 다른 구체예로는 예를 들어, 개구부를 갖는 용기 본체와, 상기 개구부에 장착된, 솔상의 도포 부재를 구비하여 이루어지는 용기 등을 들 수 있다. 이 경우, 용기 본체에 수용된 조성물을, 털의 길이·간격 등이 적절히 조정된 솔에 함침·유지시킨 후, 당해 도포 부재를 피도포부에 접촉시키는 것에 의해, 조성물을 피도포부에 도포할 수 있다.
이러한 양태의 용기는, 도포 부재에 조성물을 함침·유지시켜 사용하기 때문에, 예를 들어 의약 제제가 외용 도포제인 경우에 있어서 피도포부에서 액 흐름의 문제가 잘 발생하지 않거나, 도포 부재를 직접 피도포부에 접촉시켜 사용함으로써 손가락이 오염되지 않거나, 혹은 도포 부재의 형상·크기 등을 조정함으로써 간이하게 조성물을 도포하는 영역을 유연하게 조정 가능한, 등의 장점을 갖는다. 그러나, 도포 부재에 있어서 조성물이 함침·유지되는 것으로 인해 조성물에 변색이 발생한 경우에는 도포 부재 전체에 걸쳐서 변색이 발생하게 된다. 그 때문에, 예를 들어 의약 제제의 사용시 등, 도포 부재를 외부에 노출시킨 경우에 있어서, 외관 상 특히 변색이 눈에 띄게 된다. 이러한 결과, 본 발명에 의하면 조성물의 변색이 억제되기 때문에, 이러한 외관 상의 문제를 해결하여 상기의 장점을 충분히 향수할 수 있다는 우수한 효과를 갖는다. 또한, 이러한 양태의 용기의 경우, 용기 본체 및 도포 부재가 모두 폴리올레핀계 수지제인 것이 특히 바람직하다.
또한, 이러한 용기는, 수용하는 조성물이, 예를 들어 액상의 조성물이나 저점성의 반고형상의 조성물인 경우에 특히 바람직하게 채용할 수 있다.
이러한 양태의 용기는 공지이고, 예를 들어, 일본 특허 제5570089호 등에 개시되어 있다. 또한, 본 발명에 있어서는, 이러한 양태의 용기로서 시판품을 사용해도 되고, 이와 같은 시판품으로는 예를 들어, 도포 부재로서 저밀도 폴리에틸렌제의 연통 다공질체인 MAPS ((주) 이노악 코퍼레이션) 를 사용한 용기 등을 들 수 있다.
[(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기]
이러한 양태의 용기의 경우, 유연성을 갖는 용기 본체를 압압하는 것 등에 의해 용기 내부에 압을 가하여, 용기 내부에 수용된 조성물을 토출구로부터 토출시키는 것에 의해, 조성물을 피도포부에 도포할 수 있다. 또한, 이러한 양태의 용기에 있어서 토출구는 용기에 미리 형성되어 있지 않아도 되고, 사용 개시 전에 용기에 천공 등 하여 토출구를 형성하는 구성으로 해도 되고, 이러한 양태의 용기도 「유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기」 에 포함된다.
이러한 양태의 용기는, 단순한 구조이기 때문에 제조 비용이 낮고, 용기 본체를 압압하는 것 등에 의해 토출구로부터 조성물을 토출시켜 사용하기 때문에 용기 내의 조성물이 오염되지 않는, 등의 장점을 갖는다.
또한, 이러한 양태의 용기는, 수용하는 조성물이, 예를 들어 점성이 높은 반고형상의 조성물인 경우에 특히 바람직하게 채용할 수 있다.
이러한 양태의 용기는 공지이고, 예를 들어, 일본 특허 제5302550호, 일본 특허 제5525135호 등에 개시되어 있다. 또한, 본 발명에 있어서는, 이러한 양태의 용기로서 시판품을 사용해도 된다.
본 발명에 있어서, 「폴리올레핀계 수지」 는 특별히 한정되지 않고, 단일종의 모노머의 중합체 (호모폴리머) 여도 되고, 복수종의 모노머의 공중합체 (코폴리머) 여도 된다. 또한, 코폴리머인 경우, 그 중합 양식은 특별히 한정되지 않고, 랜덤 중합이어도 되고 블록 중합이어도 된다. 또한 그 입체 규칙성 (탁티시티) 은 특별히 한정되지 않는다.
이와 같은 폴리올레핀계 수지로는, 구체적으로는 예를 들어, 폴리에틸렌 (보다 상세하게는 예를 들어, 저밀도 폴리에틸렌 (직사슬형 저밀도 폴리에틸렌을 포함한다), 고밀도 폴리에틸렌, 중밀도 폴리에틸렌 등), 폴리프로필렌, 고리형 폴리올레핀, 폴리(4-메틸펜텐), 폴리테트라플루오로에틸렌, 에틸렌·프로필렌 공중합체, 에틸렌·α-올레핀 공중합체, 에틸렌·아크릴산 공중합체, 에틸렌·메타크릴산 공중합체, 에틸렌·아세트산비닐 공중합체, 에틸렌·아크릴산에틸 공중합체 등을 들 수 있고, 본 발명에 있어서는, 이들의 1 종 또는 2 종 이상을 조합하여 사용할 수 있다.
본 발명에 있어서, 폴리올레핀계 수지로는, 변색 억제 작용의 관점에서, 폴리에틸렌, 폴리프로필렌, 고리형 폴리올레핀이 바람직하고, 폴리에틸렌, 폴리프로필렌이 특히 바람직하다.
또한, 본 발명에 있어서, 「폴리올레핀계 수지제」 란, 그 재질의 적어도 일부에 폴리올레핀계 수지를 포함하고 있는 것을 의미하고, 예를 들어, 폴리올레핀계 수지와 다른 수지의 2 종 이상의 수지의 혼합체 (폴리머 얼로이) 도 「폴리올레핀계 수지제」 에 포함된다.
본 발명에 있어서, 「폴리올레핀계 수지제 용기」 란, 용기에 있어서, 그 내부에 수용된 액상 또는 반고형상의 조성물과 접하는 부분의 적어도 일부 (바람직하게는, 통상적인 보존시에 있어서 조성물과 접하는 부분의 10 % 이상, 보다 바람직하게는, 통상적인 보존시에 있어서 조성물과 접하는 부분의 30 % 이상, 특히 바람직하게는, 통상적인 보존시에 있어서 조성물과 접하는 부분의 전체) 가 「폴리올레핀계 수지제」 인 「용기」 를 의미한다. 따라서, 예를 들어 액상 또는 반고형상의 조성물과 접하는 층 (용기의 최내층) 의 적어도 일부에 폴리올레핀계 수지의 층을 형성하고, 그 외측에 다른 재질의 수지나 알루미늄박 등의 소재를 적층 등 시켜 이루어지는 용기도, 「폴리올레핀계 수지제 용기」 에 해당한다.
이와 같은, 복수종의 소재를 적층 등 시켜 이루어지는 용기로는, 구체적으로는 예를 들어, 폴리올레핀계 수지로 구성된 층을 최내층으로 하고, 그 외측에 직접 혹은 다른 층을 개재하여 알루미늄박을 적층하고, 추가로 그 외측에 필요에 따라 임의로 다른 층을 적층하여 이루어지는 라미네이트 필름제의 용기 등을 들 수 있다.
또한, 본 발명에 있어서, 액상 또는 반고형상의 조성물의, 용기에 대한 수용 수단은 특별히 한정되지 않고, 용기의 형상이나 조성물의 성상 등에 따라, 통상적인 방법에 의해 충전 등 하면 되고, 이에 의해 본 발명의 의약 제제를 제조할 수 있다.
<의약 제제>
본 발명에 있어서, 「의약 제제」 의 투여 방법·적용 방법은 특별히 한정되지 않고, 경구 및 경피, 경질 등의 비경구를 들 수 있다. 본 발명에 있어서는, 액상 또는 반고형상의 조성물의 특성 (환부의 위치, 형상이나 범위에 따라 유연하게 필요한 양만큼 도포 등 하는 것이 가능한 점) 으로부터, 비경구가 바람직하고, 경피 투여가 특히 바람직하다.
본 발명에 있어서, 의약 제제의 제형은, 용기에 수용된 조성물이 액상 또는 반고형상인 한에 있어서 특별히 한정되는 것이 아니고, 그 이용 목적 등에 따라, 예를 들어, 제16 개정 일본 약국방 제제 총칙 등에 기재된 제형으로부터 적절히 선택할 수 있다. 이러한 제형으로는, 구체적으로는 예를 들어, 피부 등에 적용하는 제제 (외용 액제, 스프레이제, 연고제, 크림제, 겔제 등), 경구 투여하는 제제 (경구 액제, 시럽제, 경구 젤리제 등) 등의, 제16 개정 일본 약국방 제제 총칙에 기재된 제형을 들 수 있다.
본 발명에 있어서 의약 제제로는, 외용 액제, 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인 것이 바람직하고, 리니먼트제, 로션제, 외용 에어졸제, 펌프 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인 것이 보다 바람직하고, 로션제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인 것이 특히 바람직하다.
본 발명의 의약 제제는, NSAID 의 일종인 록소프로펜 또는 그 염을 함유하는 점에서, 의료용 의약품이나 OTC 의약품으로서 사용할 수 있고, 구체적으로는 예를 들어 외용 소염 진통제 ; 해열 진통약, 종합 감기약 (감기약) 등의 내복약 ; 등으로서 유용하다.
다음으로, 「방법」 의 양태의 발명에 대하여 이하에 설명한다.
본 발명은, 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 다음 성분 (B-1) ∼ (B-9) 의 어느 것 ;
(B-1) 테르펜류
(B-2) 아르니카속의 식물 또는 그 추출물
(B-3) 다가 알코올
(B-4) 셀룰로오스류
(B-5) 토코페롤류
(B-6) 글리시르레틴산류
(B-7) 상기 일반식 (1) 로 나타내는 화합물 또는 그 염
(B-8) 고추 또는 그 추출물
(B-9) 유기 아민
을 함유하는 액상 또는 반고형상의 조성물을, 폴리올레핀계 수지제 용기에 수용하는 공정을 포함하는, 조성물의 변색의 억제 방법에 관한 것이기도 하다.
이러한 양태의 발명에 있어서, 성분 (A) 를 배합하는 공정, 성분 (B) 를 배합하는 공정, 및 조성물을 폴리올레핀계 수지제 용기에 수용하는 공정의 순서는 특별히 한정되지 않고, 성분 (A) 및 (B) 를 함유하는 액상 또는 반고형상의 조성물이 폴리올레핀계 수지제 용기에 수용된 상태가 직접적 또는 간접적으로 작출되면 된다.
또한, 이러한 양태의 발명에 있어서, 각종 문언의 의의, 각 성분의 배합량 등은 모두 「의약 제제」 에 대하여 설명한 것과 동일하다.
본 명세서는, 이상의 실시형태에 관련하여, 예를 들어 이하에 예시되는 발명을 개시하지만, 이들에 전혀 한정되는 것이 아니다.
[1-1] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 테르펜류 ;
를 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제.
[1-2] 록소프로펜나트륨 1 질량%, l-멘톨 3 질량%, 에탄올 52.3 질량% 및 물 43.7 질량% 를 함유하는 액체 조성물이, 스테인리스 SUS304 제의 볼 1 개를 갖는 폴리프로필렌제의 롤 온 용기에 충전되어 이루어지는 외용 소염 진통제 제품을 포함하지 않는 것인, [1-1] 에 기재된 의약 제제.
[1-3] 성분 (A) 가, 록소프로펜나트륨 수화물인, [1-1] 또는 [1-2] 에 기재된 의약 제제.
[1-4] 성분 (B) 가, 이소보르네올, 이론, 오시멘, 카르베올, 카르보타나세톤, 카르보멘톤, 카르본, 카렌, 카론, 캄펜, 캠퍼, 게라니올, 사비넨, 사프라날, 시클로시트랄, 시트랄, 시트로넬랄, 시트로넬산, 시트로넬롤, 시네올, 시멘, 실베스트렌, 티몰, 이소투?, 투존, 테르피네올, 테르피넨, 테르피놀렌, 트리시클렌, 네롤, 피넨, 피노캄페올, 피놀, 피페리테논, 펠란드랄, 펠란드렌, 펜첸, 펜칠알코올, 페릴릴알코올, 페릴릴알데히드, 보르네올, 미르센, 멘톨, 멘톤, 요놀, 요논, 리날로올 및 리모넨으로 이루어지는 군에서 선택되는 1 종 이상인, [1-1] ∼ [1-3] 의 어느 하나에 기재된 의약 제제.
[1-5] 성분 (B) 가, 고리형의 테르페노이드인, [1-1] ∼ [1-3] 의 어느 하나에 기재된 의약 제제.
[1-6] 성분 (B) 가, 고리형의 모노테르페노이드인, [1-1] ∼ [1-3] 의 어느 하나에 기재된 의약 제제.
[1-7] 성분 (B) 가, 단고리형 또는 2 고리형의 모노테르페노이드인, [1-1] ∼ [1-3] 의 어느 하나에 기재된 의약 제제.
[1-8] 성분 (B) 가, p-멘탄 골격을 갖는 모노테르페노이드 또는 보르난 골격을 갖는 모노테르페노이드인, [1-1] ∼ [1-3] 의 어느 하나에 기재된 의약 제제.
[1-9] 성분 (B) 가, 시네올, 티몰, 테르피네올, 멘톨, 리모넨, 캠퍼 및 보르네올로 이루어지는 군에서 선택되는 1 종 이상인, [1-1] ∼ [1-3] 의 어느 하나에 기재된 의약 제제.
[1-10] 성분 (B) 가, 시네올, 캠퍼, 티몰, 보르네올 및 멘톨로 이루어지는 군에서 선택되는 1 종 이상인, [1-1] ∼ [1-3] 의 어느 하나에 기재된 의약 제제.
[1-11] 성분 (B) 가, 시네올, d-캠퍼, dl-캠퍼, 티몰, d-보르네올, l-멘톨 및 dl-멘톨로 이루어지는 군에서 선택되는 1 종 이상인, [1-1] ∼ [1-3] 의 어느 하나에 기재된 의약 제제.
[1-12] 성분 (B) 가, 시네올, d-캠퍼, dl-캠퍼, 티몰, l-멘톨 및 dl-멘톨로 이루어지는 군에서 선택되는 1 종 이상인, [1-1] ∼ [1-3] 의 어느 하나에 기재된 의약 제제.
[1-13] 조성물이, 물을 함유하는 것인, [1-1] ∼ [1-12] 의 어느 하나에 기재된 의약 제제.
[1-14] 조성물이, 저급 알코올을 함유하는 것인, [1-1] ∼ [1-13] 의 어느 하나에 기재된 의약 제제.
[1-15] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [1-14] 에 기재된 의약 제제.
[1-16] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [1-1] ∼ [1-15] 의 어느 하나에 기재된 의약 제제.
[1-17] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [1-1] ∼ [1-16] 의 어느 하나에 기재된 의약 제제.
[1-18] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [1-1] ∼ [1-16] 의 어느 하나에 기재된 의약 제제.
[1-19] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [1-1] ∼ [1-16] 의 어느 하나에 기재된 의약 제제.
[1-20] 외용 액제, 스프레이제, 연고제, 크림제, 겔제, 경구 액제, 시럽제 및 경구 젤리제로 이루어지는 군에서 선택되는 제형인, [1-1] ∼ [1-19] 의 어느 하나에 기재된 의약 제제.
[1-21] 외용 액제, 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [1-1] ∼ [1-19] 의 어느 하나에 기재된 의약 제제.
[1-22] 리니먼트제, 로션제, 에어졸제, 펌프 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [1-1] ∼ [1-19] 의 어느 하나에 기재된 의약 제제.
[1-23] 로션제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [1-1] ∼ [1-19] 의 어느 하나에 기재된 의약 제제.
[1-24] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 테르펜류 ;
를 함유하는 액상 또는 반고형상의 조성물을, 폴리올레핀계 수지제 용기에 수용하는 공정을 포함하는, 조성물의 변색의 억제 방법.
[1-25] 성분 (A) 가, 록소프로펜나트륨 수화물인, [1-24] 에 기재된 방법.
[1-26] 성분 (B) 가, 이소보르네올, 이론, 오시멘, 카르베올, 카르보타나세톤, 카르보멘톤, 카르본, 카렌, 카론, 캄펜, 캠퍼, 게라니올, 사비넨, 사프라날, 시클로시트랄, 시트랄, 시트로넬랄, 시트로넬산, 시트로넬롤, 시네올, 시멘, 실베스트렌, 티몰, 이소투?, 투존, 테르피네올, 테르피넨, 테르피놀렌, 트리시클렌, 네롤, 피넨, 피노캄페올, 피놀, 피페리테논, 펠란드랄, 펠란드렌, 펜첸, 펜칠알코올, 페릴릴알코올, 페릴릴알데히드, 보르네올, 미르센, 멘톨, 멘톤, 요놀, 요논, 리날로올 및 리모넨으로 이루어지는 군에서 선택되는 1 종 이상인, [1-24] 또는 [1-25] 에 기재된 방법.
[1-27] 성분 (B) 가, 고리형의 테르페노이드인, [1-24] 또는 [1-25] 에 기재된 방법.
[1-28] 성분 (B) 가, 고리형의 모노테르페노이드인, [1-24] 또는 [1-25] 에 기재된 방법.
[1-29] 성분 (B) 가, 단고리형 또는 2 고리형의 모노테르페노이드인, [1-24] 또는 [1-25] 에 기재된 방법.
[1-30] 성분 (B) 가, p-멘탄 골격을 갖는 모노테르페노이드 또는 보르난 골격을 갖는 모노테르페노이드인, [1-24] 또는 [1-25] 에 기재된 방법.
[1-31] 테르펜류가, 시네올, 티몰, 테르피네올, 멘톨, 리모넨, 캠퍼 및 보르네올로 이루어지는 군에서 선택되는 1 종 이상인, [1-24] 또는 [1-25] 에 기재된 방법.
[1-32] 성분 (B) 가, 시네올, 캠퍼, 티몰, 보르네올 및 멘톨로 이루어지는 군에서 선택되는 1 종 이상인, [1-24] 또는 [1-25] 에 기재된 방법.
[1-33] 성분 (B) 가, 시네올, d-캠퍼, dl-캠퍼, 티몰, d-보르네올, l-멘톨 및 dl-멘톨로 이루어지는 군에서 선택되는 1 종 이상인, [1-24] 또는 [1-25] 에 기재된 방법.
[1-34] 성분 (B) 가, 시네올, d-캠퍼, dl-캠퍼, 티몰, l-멘톨 및 dl-멘톨로 이루어지는 군에서 선택되는 1 종 이상인, [1-24] 또는 [1-25] 에 기재된 방법.
[1-35] 조성물이, 물을 함유하는 것인, [1-24] ∼ [1-34] 의 어느 하나에 기재된 방법.
[1-36] 조성물이, 저급 알코올을 함유하는 것인, [1-24] ∼ [1-34] 의 어느 하나에 기재된 방법.
[1-37] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [1-36] 에 기재된 방법.
[1-38] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [1-24] ∼ [1-37] 의 어느 하나에 기재된 방법.
[1-39] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [1-24] ∼ [1-38] 의 어느 하나에 기재된 방법.
[1-40] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [1-24] ∼ [1-38] 의 어느 하나에 기재된 방법.
[1-41] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [1-24] ∼ [1-38] 의 어느 하나에 기재된 방법.
[2-1] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 아르니카속의 식물 또는 그 추출물 ;
을 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제.
[2-2] 성분 (A) 가, 록소프로펜나트륨 수화물인, [2-1] 에 기재된 의약 제제.
[2-3] 성분 (B) 가, Arnica montana, Arnica chamissonis, Arnica fulgens, Arnica cordifolia, Arnica latifolia, Arnica longifolia 및 Arnica sachalinensis 그리고 그들의 추출물로 이루어지는 군에서 선택되는 1 종 이상인, [2-1] 또는 [2-2] 에 기재된 의약 제제.
[2-4] 성분 (B) 가, 아르니카 또는 그 추출물인, [2-1] 또는 [2-2] 에 기재된 의약 제제.
[2-5] 성분 (B) 가, 아르니카, 아르니카 팅크 및 아르니카 엑기스로 이루어지는 군에서 선택되는 1 종 이상인, [2-1] 또는 [2-2] 에 기재된 의약 제제.
[2-6] 조성물이, 물을 추가로 함유하는 것인, [2-1] ∼ [2-5] 의 어느 하나에 기재된 의약 제제.
[2-7] 조성물이, 저급 알코올을 추가로 함유하는 것인, [2-1] ∼ [2-6] 의 어느 하나에 기재된 의약 제제.
[2-8] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [2-7] 에 기재된 의약 제제.
[2-9] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [2-1] ∼ [2-8] 의 어느 하나에 기재된 의약 제제.
[2-10] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [2-1] ∼ [2-9] 의 어느 하나에 기재된 의약 제제.
[2-11] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [2-1] ∼ [2-9] 의 어느 하나에 기재된 의약 제제.
[2-12] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [2-1] ∼ [2-9] 의 어느 하나에 기재된 의약 제제.
[2-13] 외용 액제, 스프레이제, 연고제, 크림제, 겔제, 경구 액제, 시럽제 및 경구 젤리제로 이루어지는 군에서 선택되는 제형인, [2-1] ∼ [2-12] 의 어느 하나에 기재된 의약 제제.
[2-14] 외용 액제, 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [2-1] ∼ [2-12] 의 어느 하나에 기재된 의약 제제.
[2-15] 리니먼트제, 로션제, 에어졸제, 펌프 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [2-1] ∼ [2-12] 의 어느 하나에 기재된 의약 제제.
[2-16] 로션제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [2-1] ∼ [2-12] 의 어느 하나에 기재된 의약 제제.
[2-17] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 아르니카속의 식물 또는 그 추출물 ;
을 함유하는 액상 또는 반고형상의 조성물을, 폴리올레핀계 수지제 용기에 수용하는 공정을 포함하는, 조성물의 변색의 억제 방법.
[2-18] 성분 (A) 가, 록소프로펜나트륨 수화물인, [2-17] 에 기재된 방법.
[2-19] 성분 (B) 가, Arnica montana, Arnica chamissonis, Arnica fulgens, Arnica cordifolia, Arnica latifolia, Arnica longifolia 및 Arnica sachalinensis 그리고 그들의 추출물로 이루어지는 군에서 선택되는 1 종 이상인, [2-17] 또는 [2-18] 에 기재된 방법.
[2-20] 성분 (B) 가, 아르니카 또는 그 추출물인, [2-17] 또는 [2-18] 에 기재된 방법.
[2-21] 성분 (B) 가, 아르니카, 아르니카 팅크 및 아르니카 엑기스로 이루어지는 군에서 선택되는 1 종 이상인, [2-17] 또는 [2-18] 에 기재된 방법.
[2-22] 조성물이, 물을 추가로 함유하는 것인, [2-17] ∼ [2-21] 의 어느 하나에 기재된 방법.
[2-23] 조성물이, 저급 알코올을 추가로 함유하는 것인, [2-17] ∼ [2-22] 의 어느 하나에 기재된 방법.
[2-24] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [2-23] 에 기재된 방법.
[2-25] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [2-17] ∼ [2-24] 의 어느 하나에 기재된 방법.
[2-26] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [2-17] ∼ [2-25] 의 어느 하나에 기재된 방법.
[2-27] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [2-17] ∼ [2-25] 의 어느 하나에 기재된 방법.
[2-28] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [2-17] ∼ [2-25] 의 어느 하나에 기재된 방법.
[3-1] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 다가 알코올 ;
을 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제.
[3-2] 성분 (A) 가, 록소프로펜나트륨 수화물인, [3-1] 에 기재된 의약 제제.
[3-3] 성분 (B) 가, 탄소수 1 ∼ 6 의 저급 다가 알코올 및 탄소수 7 이상의 고급 다가 알코올로 이루어지는 군에서 선택되는 1 종 이상인, [3-1] 또는 [3-2] 에 기재된 의약 제제.
[3-4] 성분 (B) 가, 에틸렌글리콜, 트리에틸렌글리콜, 프로필렌글리콜, 디프로필렌글리콜, 글리세린, 1,3-부틸렌글리콜, 에리트리톨, 자일리톨, 소르비톨, 만니톨, 1,2,6-헥산트리올, 폴리비닐알코올, 폴리에틸렌글리콜 및 폴리프로필렌글리콜로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [3-1] ∼ [3-3] 중 어느 하나에 기재된 의약 제제.
[3-5] 성분 (B) 가, 1,3-부틸렌글리콜인, [3-1] ∼ [3-4] 중 어느 하나에 기재된 의약 제제.
[3-6] 조성물이, 추가로 물을 함유하는 것인, [3-1] ∼ [3-5] 중 어느 하나에 기재된 의약 제제.
[3-7] 조성물이, 추가로 저급 알코올을 함유하는 것인, [3-1] ∼ [3-6] 중 어느 하나에 기재된 의약 제제.
[3-8] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [3-7] 에 기재된 의약 제제.
[3-9] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [3-1] ∼ [3-8] 중 어느 하나에 기재된 의약 제제.
[3-10] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [3-1] ∼ [3-9] 중 어느 하나에 기재된 의약 제제.
[3-11] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [3-1] ∼ [3-9] 중 어느 하나에 기재된 의약 제제.
[3-12] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [3-1] ∼ [3-9] 중 어느 하나에 기재된 의약 제제.
[3-13] 외용 액제, 스프레이제, 연고제, 크림제, 겔제, 경구 액제, 시럽제 및 경구 젤리제로 이루어지는 군에서 선택되는 제형인, [3-1] ∼ [3-12] 중 어느 하나에 기재된 의약 제제.
[3-14] 외용 액제, 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [3-1] ∼ [3-12] 중 어느 하나에 기재된 의약 제제.
[3-15] 리니먼트제, 로션제, 외용 에어졸제, 펌프 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [3-1] ∼ [3-12] 중 어느 하나에 기재된 의약 제제.
[3-16] 로션제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [3-1] ∼ [3-12] 중 어느 하나에 기재된 의약 제제.
[3-17] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 다가 알코올 ;
을 함유하는 액상 또는 반고형상의 조성물을, 폴리올레핀계 수지제 용기에 수용하는 공정을 포함하는, 조성물의 변색의 억제 방법.
[3-18] 성분 (A) 가, 록소프로펜나트륨 수화물인, [3-17] 에 기재된 방법.
[3-19] 성분 (B) 가, 탄소수 1 ∼ 6 의 저급 다가 알코올 및 탄소수 7 이상의 고급 다가 알코올로 이루어지는 군에서 선택되는 1 종 이상인, [3-17] 또는 [3-18] 에 기재된 방법.
[3-20] 성분 (B) 가, 에틸렌글리콜, 트리에틸렌글리콜, 프로필렌글리콜, 디프로필렌글리콜, 글리세린, 1,3-부틸렌글리콜, 에리트리톨, 자일리톨, 소르비톨, 만니톨, 1,2,6-헥산트리올, 폴리비닐알코올, 폴리에틸렌글리콜 및 폴리프로필렌글리콜로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [3-17] ∼ [3-19] 중 어느 하나에 기재된 방법.
[3-21] 성분 (B) 가, 1,3-부틸렌글리콜인, [3-17] ∼ [3-20] 중 어느 하나에 기재된 방법.
[3-22] 조성물이, 추가로 물을 함유하는 것인, [3-17] ∼ [3-21] 중 어느 하나에 기재된 방법.
[3-23] 조성물이, 추가로 저급 알코올을 함유하는 것인, [3-17] ∼ [3-22] 중 어느 하나에 기재된 방법.
[3-24] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [3-23] 에 기재된 방법.
[3-25] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [3-17] ∼ [3-24] 중 어느 하나에 기재된 방법.
[3-26] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [3-17] ∼ [3-25] 중 어느 하나에 기재된 방법.
[3-27] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [3-17] ∼ [3-25] 중 어느 하나에 기재된 방법.
[3-28] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [3-17] ∼ [3-25] 중 어느 하나에 기재된 방법.
[4-1] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 셀룰로오스류 ;
를 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제.
[4-2] 성분 (A) 가, 록소프로펜나트륨 수화물인, [4-1] 에 기재된 의약 제제.
[4-3] 성분 (B) 가, 셀룰로오스에테르 유도체 또는 그 염인, [4-1] 또는 [4-2] 에 기재된 의약 제제.
[4-4] 성분 (B) 가, 알킬셀룰로오스, 하이드록시알킬셀룰로오스, 알킬(하이드록시알킬)셀룰로오스 및 카르복시알킬셀룰로오스 그리고 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [4-1] ∼ [4-3] 중 어느 하나에 기재된 의약 제제.
[4-5] 성분 (B) 가, 하이프로멜로스인, [4-1] ∼ [4-4] 중 어느 하나에 기재된 의약 제제.
[4-6] 조성물이, 추가로 물을 함유하는 것인, [4-1] ∼ [4-5] 중 어느 하나에 기재된 의약 제제.
[4-7] 조성물이, 추가로 저급 알코올을 함유하는 것인, [4-1] ∼ [4-6] 중 어느 하나에 기재된 의약 제제.
[4-8] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [4-7] 에 기재된 의약 제제.
[4-9] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [4-1] ∼ [4-8] 중 어느 하나에 기재된 의약 제제.
[4-10] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [4-1] ∼ [4-9] 중 어느 하나에 기재된 의약 제제.
[4-11] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [4-1] ∼ [4-9] 중 어느 하나에 기재된 의약 제제.
[4-12] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [4-1] ∼ [4-9] 중 어느 하나에 기재된 의약 제제.
[4-13] 외용 액제, 스프레이제, 연고제, 크림제, 겔제, 경구 액제, 시럽제 및 경구 젤리제로 이루어지는 군에서 선택되는 제형인, [4-1] ∼ [4-12] 중 어느 하나에 기재된 의약 제제.
[4-14] 외용 액제, 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [4-1] ∼ [4-12] 중 어느 하나에 기재된 의약 제제.
[4-15] 리니먼트제, 로션제, 외용 에어졸제, 펌프 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [4-1] ∼ [4-12] 중 어느 하나에 기재된 의약 제제.
[4-16] 로션제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [4-1] ∼ [4-12] 중 어느 하나에 기재된 의약 제제.
[4-17] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 셀룰로오스류 ;
를 함유하는 액상 또는 반고형상의 조성물을, 폴리올레핀계 수지제 용기에 수용하는 공정을 포함하는, 조성물의 변색의 억제 방법.
[4-18] 성분 (A) 가, 록소프로펜나트륨 수화물인, [4-17] 에 기재된 방법.
[4-19] 성분 (B) 가, 셀룰로오스에테르 유도체 또는 그 염인, [4-17] 또는 [4-18] 에 기재된 방법.
[4-20] 성분 (B) 가, 알킬셀룰로오스, 하이드록시알킬셀룰로오스, 알킬(하이드록시알킬)셀룰로오스 및 카르복시알킬셀룰로오스 그리고 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [4-17] ∼ [4-19] 중 어느 하나에 기재된 방법.
[4-21] 성분 (B) 가, 하이프로멜로스인, [4-17] ∼ [4-20] 중 어느 하나에 기재된 방법.
[4-22] 조성물이, 추가로 물을 함유하는 것인, [4-17] ∼ [4-21] 중 어느 하나에 기재된 방법.
[4-23] 조성물이, 추가로 저급 알코올을 함유하는 것인, [4-17] ∼ [4-22] 중 어느 하나에 기재된 방법.
[4-24] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [4-23] 에 기재된 방법.
[4-25] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [4-17] ∼ [4-24] 중 어느 하나에 기재된 방법.
[4-26] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [4-17] ∼ [4-25] 중 어느 하나에 기재된 방법.
[4-27] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [4-17] ∼ [4-25] 중 어느 하나에 기재된 방법.
[4-28] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [4-17] ∼ [4-25] 중 어느 하나에 기재된 방법.
[5-1] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 토코페롤류 ;
를 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제.
[5-2] 성분 (A) 가, 록소프로펜나트륨 수화물인, [5-1] 에 기재된 의약 제제.
[5-3] 성분 (B) 가, 토코페롤, 토코페롤숙신산에스테르, 토코페롤아세트산에스테르 및 토코페롤니코틴산에스테르 그리고 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [5-1] 또는 [5-2] 에 기재된 의약 제제.
[5-4] 성분 (B) 가, dl-α-토코페롤, dl-α-토코페롤숙신산에스테르칼슘, dl-α-토코페롤아세트산에스테르 및 dl-α-토코페롤니코틴산에스테르로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [5-1] ∼ [5-3] 중 어느 하나에 기재된 의약 제제.
[5-5] 성분 (B) 가, dl-α-토코페롤아세트산에스테르인, [5-1] ∼ [5-4] 중 어느 하나에 기재된 의약 제제.
[5-6] 조성물이, 추가로 물을 함유하는 것인, [5-1] ∼ [5-5] 중 어느 하나에 기재된 의약 제제.
[5-7] 조성물이, 추가로 저급 알코올을 함유하는 것인, [5-1] ∼ [5-6] 중 어느 하나에 기재된 의약 제제.
[5-8] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [5-7] 에 기재된 의약 제제.
[5-9] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [5-1] ∼ [5-8] 중 어느 하나에 기재된 의약 제제.
[5-10] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [5-1] ∼ [5-9] 중 어느 하나에 기재된 의약 제제.
[5-11] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [5-1] ∼ [5-9] 중 어느 하나에 기재된 의약 제제.
[5-12] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [5-1] ∼ [5-9] 중 어느 하나에 기재된 의약 제제.
[5-13] 외용 액제, 스프레이제, 연고제, 크림제, 겔제, 경구 액제, 시럽제 및 경구 젤리제로 이루어지는 군에서 선택되는 제형인, [5-1] ∼ [5-12] 중 어느 하나에 기재된 의약 제제.
[5-14] 외용 액제, 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [5-1] ∼ [5-12] 중 어느 하나에 기재된 의약 제제.
[5-15] 리니먼트제, 로션제, 외용 에어졸제, 펌프 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [5-1] ∼ [5-12] 중 어느 하나에 기재된 의약 제제.
[5-16] 로션제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [5-1] ∼ [5-12] 중 어느 하나에 기재된 의약 제제.
[5-17] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 토코페롤류 ;
를 함유하는 액상 또는 반고형상의 조성물을, 폴리올레핀계 수지제 용기에 수용하는 공정을 포함하는, 조성물의 변색의 억제 방법.
[5-18] 성분 (A) 가, 록소프로펜나트륨 수화물인, [5-17] 에 기재된 방법.
[5-19] 성분 (B) 가, 토코페롤, 토코페롤숙신산에스테르, 토코페롤아세트산에스테르 및 토코페롤니코틴산에스테르 그리고 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [5-17] 또는 [5-18] 에 기재된 방법.
[5-20] 성분 (B) 가, dl-α-토코페롤, dl-α-토코페롤숙신산에스테르칼슘, dl-α-토코페롤아세트산에스테르 및 dl-α-토코페롤니코틴산에스테르로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [5-17] ∼ [5-19] 중 어느 하나에 기재된 방법.
[5-21] 성분 (B) 가, dl-α-토코페롤아세트산에스테르인, [5-17] ∼ [5-20] 중 어느 하나에 기재된 방법.
[5-22] 조성물이, 추가로 물을 함유하는 것인, [5-17] ∼ [5-21] 중 어느 하나에 기재된 방법.
[5-23] 조성물이, 추가로 저급 알코올을 함유하는 것인, [5-17] ∼ [5-22] 중 어느 하나에 기재된 방법.
[5-24] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [5-23] 에 기재된 방법.
[5-25] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [5-17] ∼ [5-24] 중 어느 하나에 기재된 방법.
[5-26] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [5-17] ∼ [5-25] 중 어느 하나에 기재된 방법.
[5-27] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [5-17] ∼ [5-25] 중 어느 하나에 기재된 방법.
[5-28] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [5-17] ∼ [5-25] 중 어느 하나에 기재된 방법.
[6-1] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 글리시르레틴산류 ;
를 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제.
[6-2] 성분 (A) 가, 록소프로펜나트륨 수화물인, [6-1] 에 기재된 의약 제제.
[6-3] 성분 (B) 가, 글리시르레틴산, 글리실리진산 및 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [6-1] 또는 [6-2] 에 기재된 의약 제제.
[6-4] 성분 (B) 가, 글리시르레틴산, 글리실리진산, 글리실리진산이칼륨, 글리실리진산모노암모늄, 글리실리진산이나트륨 및 글리실리진산삼나트륨으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [6-1] ∼ [6-3] 중 어느 하나에 기재된 의약 제제.
[6-5] 성분 (B) 가, 글리시르레틴산인, [6-1] ∼ [6-4] 중 어느 하나에 기재된 의약 제제.
[6-6] 조성물이, 추가로 물을 함유하는 것인, [6-1] ∼ [6-5] 중 어느 하나에 기재된 의약 제제.
[6-7] 조성물이, 추가로 저급 알코올을 함유하는 것인, [6-1] ∼ [6-6] 중 어느 하나에 기재된 의약 제제.
[6-8] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [6-7] 에 기재된 의약 제제.
[6-9] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [6-1] ∼ [6-8] 중 어느 하나에 기재된 의약 제제.
[6-10] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [6-1] ∼ [6-9] 중 어느 하나에 기재된 의약 제제.
[6-11] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [6-1] ∼ [6-9] 중 어느 하나에 기재된 의약 제제.
[6-12] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [6-1] ∼ [6-9] 중 어느 하나에 기재된 의약 제제.
[6-13] 외용 액제, 스프레이제, 연고제, 크림제, 겔제, 경구 액제, 시럽제 및 경구 젤리제로 이루어지는 군에서 선택되는 제형인, [6-1] ∼ [6-12] 중 어느 하나에 기재된 의약 제제.
[6-14] 외용 액제, 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [6-1] ∼ [6-12] 중 어느 하나에 기재된 의약 제제.
[6-15] 리니먼트제, 로션제, 외용 에어졸제, 펌프 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [6-1] ∼ [6-12] 중 어느 하나에 기재된 의약 제제.
[6-16] 로션제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [6-1] ∼ [6-12] 중 어느 하나에 기재된 의약 제제.
[6-17] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 글리시르레틴산류 ;
를 함유하는 액상 또는 반고형상의 조성물을, 폴리올레핀계 수지제 용기에 수용하는 공정을 포함하는, 조성물의 변색의 억제 방법.
[6-18] 성분 (A) 가, 록소프로펜나트륨 수화물인, [6-17] 에 기재된 방법.
[6-19] 성분 (B) 가, 글리시르레틴산, 글리실리진산 및 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [6-17] 또는 [6-18] 에 기재된 방법.
[6-20] 성분 (B) 가, 글리시르레틴산, 글리실리진산, 글리실리진산이칼륨, 글리실리진산모노암모늄, 글리실리진산이나트륨 및 글리실리진산삼나트륨으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [6-17] ∼ [6-19] 중 어느 하나에 기재된 방법.
[6-21] 성분 (B) 가, 글리시르레틴산인, [6-17] ∼ [6-20] 중 어느 하나에 기재된 방법.
[6-22] 조성물이, 추가로 물을 함유하는 것인, [6-17] ∼ [6-21] 중 어느 하나에 기재된 방법.
[6-23] 조성물이, 추가로 저급 알코올을 함유하는 것인, [6-17] ∼ [6-22] 중 어느 하나에 기재된 방법.
[6-24] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [6-23] 에 기재된 방법.
[6-25] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [6-17] ∼ [6-24] 중 어느 하나에 기재된 방법.
[6-26] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [6-17] ∼ [6-25] 중 어느 하나에 기재된 방법.
[6-27] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [6-17] ∼ [6-25] 중 어느 하나에 기재된 방법.
[6-28] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [6-17] ∼ [6-25] 중 어느 하나에 기재된 방법.
[7-1] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 하기 일반식 (1)
[화학식 6]
[식 (1) 중, X 는 단결합 또는 산소 원자를 나타내고, Y 는 메틴기 또는 질소 원자를 나타내고, R1 은 수소 원자, 수산기 또는 알킬기를 나타내고, R2 는 치환기를 가져도 되는 고리형 아미노기, 또는 치환기를 가져도 되는 아미노알킬기를 나타내고, R3 은 수소 원자 또는 할로겐 원자를 나타낸다.]
로 나타내는 화합물 또는 그 염 ;
을 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제.
[7-2] 성분 (A) 가, 록소프로펜나트륨 수화물인, [7-1] 에 기재된 의약 제제.
[7-3] 성분 (B) 가, 에바스틴 및 그 염, 옥사토미드 및 그 염, 카르비녹사민 및 그 염, 클레마스틴 및 그 염, 클로르페니라민 및 그 염, 디페테롤 및 그 염, 디페닐피랄린 및 그 염, 디펜히드라민 및 그 염, 세티리진 및 그 염, 펙소페나딘 및 그 염, 베포타스틴 및 그 염, 그리고 호모클로르시클리진 및 그 염으로 이루어지는 군에서 선택되는 1 종 이상인, [7-1] 또는 [7-2] 에 기재된 의약 제제.
[7-4] 성분 (B) 가, 클로르페니라민 및 그 염, 그리고 디펜히드라민 및 그 염으로 이루어지는 군에서 선택되는 1 종 이상인, [7-1] 또는 [7-2] 에 기재된 의약 제제.
[7-5] 성분 (B) 가, 클로르페니라민말레산염, 디펜히드라민, 디펜히드라민염산염 및 디펜히드라민살리실산염으로 이루어지는 군에서 선택되는 1 종 이상인, [7-1] 또는 [7-2] 에 기재된 의약 제제.
[7-6] 조성물이, 물을 추가로 함유하는 것인, [7-1] ∼ [7-5] 의 어느 하나에 기재된 의약 제제.
[7-7] 조성물이, 저급 알코올을 추가로 함유하는 것인, [7-1] ∼ [7-6] 의 어느 하나에 기재된 의약 제제.
[7-8] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [7-7] 에 기재된 의약 제제.
[7-9] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [7-1] ∼ [7-8] 의 어느 하나에 기재된 의약 제제.
[7-10] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [7-1] ∼ [7-9] 의 어느 하나에 기재된 의약 제제.
[7-11] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [7-1] ∼ [7-9] 의 어느 하나에 기재된 의약 제제.
[7-12] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [7-1] ∼ [7-9] 의 어느 하나에 기재된 의약 제제.
[7-13] 외용 액제, 스프레이제, 연고제, 크림제, 겔제, 경구 액제, 시럽제 및 경구 젤리제로 이루어지는 군에서 선택되는 제형인, [7-1] ∼ [7-12] 의 어느 하나에 기재된 의약 제제.
[7-14] 외용 액제, 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [7-1] ∼ [7-12] 의 어느 하나에 기재된 의약 제제.
[7-15] 리니먼트제, 로션제, 에어졸제, 펌프 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [7-1] ∼ [7-12] 의 어느 하나에 기재된 의약 제제.
[7-16] 로션제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [7-1] ∼ [7-12] 의 어느 하나에 기재된 의약 제제.
[7-17] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 상기 일반식 (1) 로 나타내는 화합물 또는 그 염 ;
을 함유하는 액상 또는 반고형상의 조성물을, 폴리올레핀계 수지제 용기에 수용하는 공정을 포함하는, 조성물의 변색의 억제 방법.
[7-18] 성분 (A) 가, 록소프로펜나트륨 수화물인, [7-17] 에 기재된 방법.
[7-19] 성분 (B) 가, 에바스틴 및 그 염, 옥사토미드 및 그 염, 카르비녹사민 및 그 염, 클레마스틴 및 그 염, 클로르페니라민 및 그 염, 디페테롤 및 그 염, 디페닐피랄린 및 그 염, 디펜히드라민 및 그 염, 세티리진 및 그 염, 펙소페나딘 및 그 염, 베포타스틴 및 그 염, 그리고 호모클로르시클리진 및 그 염으로 이루어지는 군에서 선택되는 1 종 이상인, [7-17] 또는 [7-18] 에 기재된 방법.
[7-20] 성분 (B) 가, 클로르페니라민 및 그 염, 그리고 디펜히드라민 및 그 염으로 이루어지는 군에서 선택되는 1 종 이상인, [7-17] 또는 [7-18] 에 기재된 방법.
[7-21] 성분 (B) 가, 클로르페니라민말레산염, 디펜히드라민, 디펜히드라민염산염 및 디펜히드라민살리실산염으로 이루어지는 군에서 선택되는 1 종 이상인, [7-17] 또는 [7-18] 에 기재된 방법.
[7-22] 조성물이, 물을 추가로 함유하는 것인, [7-17] ∼ [7-21] 의 어느 하나에 기재된 방법.
[7-23] 조성물이, 저급 알코올을 추가로 함유하는 것인, [7-17] ∼ [7-22] 의 어느 하나에 기재된 방법.
[7-24] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [7-23] 에 기재된 방법.
[7-25] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [7-17] ∼ [7-24] 의 어느 하나에 기재된 방법.
[7-26] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [7-17] ∼ [7-25] 의 어느 하나에 기재된 방법.
[7-27] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [7-17] ∼ [7-25] 의 어느 하나에 기재된 방법.
[7-28] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [7-17] ∼ [7-25] 의 어느 하나에 기재된 방법.
[8-1] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 고추 또는 그 추출물 ;
을 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제.
[8-2] 성분 (A) 가, 록소프로펜나트륨 수화물인, [8-1] 에 기재된 의약 제제.
[8-3] 성분 (B) 가, 고추, 고추 가루, 고추 연엑기스, 고추 건조 엑기스, 캡사이신 및 노난산바닐릴아미드 (노닐산바닐릴아미드) 로 이루어지는 군에서 선택되는 1 종 이상인, [8-1] 또는 [8-2] 에 기재된 의약 제제.
[8-4] 성분 (B) 가, 고추 연엑기스 및 노난산바닐릴아미드 (노닐산바닐릴아미드) 로 이루어지는 군에서 선택되는 1 종 이상인, [8-1] 또는 [8-2] 에 기재된 의약 제제.
[8-5] 조성물이, 물을 추가로 함유하는 것인, [8-1] ∼ [8-4] 의 어느 하나에 기재된 의약 제제.
[8-6] 조성물이, 저급 알코올을 추가로 함유하는 것인, [8-1] ∼ [8-5] 의 어느 하나에 기재된 의약 제제.
[8-7] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [8-6] 에 기재된 의약 제제.
[8-8] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [8-1] ∼ [8-7] 의 어느 하나에 기재된 의약 제제.
[8-9] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [8-1] ∼ [8-8] 의 어느 하나에 기재된 의약 제제.
[8-10] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [8-1] ∼ [8-8] 의 어느 하나에 기재된 의약 제제.
[8-11] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [8-1] ∼ [8-8] 의 어느 하나에 기재된 의약 제제.
[8-12] 외용 액제, 스프레이제, 연고제, 크림제, 겔제, 경구 액제, 시럽제 및 경구 젤리제로 이루어지는 군에서 선택되는 제형인, [8-1] ∼ [8-11] 의 어느 하나에 기재된 의약 제제.
[8-13] 외용 액제, 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [8-1] ∼ [8-11] 의 어느 하나에 기재된 의약 제제.
[8-14] 리니먼트제, 로션제, 에어졸제, 펌프 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [8-1] ∼ [8-11] 의 어느 하나에 기재된 의약 제제.
[8-15] 로션제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [8-1] ∼ [8-11] 의 어느 하나에 기재된 의약 제제.
[8-16] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 고추 또는 그 추출물 ;
을 함유하는 액상 또는 반고형상의 조성물을, 폴리올레핀계 수지제 용기에 수용하는 공정을 포함하는, 조성물의 변색의 억제 방법.
[8-17] 성분 (A) 가, 록소프로펜나트륨 수화물인, [8-16] 에 기재된 방법.
[8-18] 성분 (B) 가, 고추, 고추 가루, 고추 연엑기스, 고추 건조 엑기스, 캡사이신 및 노난산바닐릴아미드 (노닐산바닐릴아미드) 로 이루어지는 군에서 선택되는 1 종 이상인, [8-16] 또는 [8-17] 에 기재된 방법.
[8-19] 성분 (B) 가, 고추 연엑기스 및 노난산바닐릴아미드 (노닐산바닐릴아미드) 로 이루어지는 군에서 선택되는 1 종 이상인, [8-16] 또는 [8-17] 에 기재된 방법.
[8-20] 조성물이, 물을 추가로 함유하는 것인, [8-16] ∼ [8-19] 의 어느 하나에 기재된 방법.
[8-21] 조성물이, 저급 알코올을 추가로 함유하는 것인, [8-16] ∼ [8-20] 의 어느 하나에 기재된 방법.
[8-22] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [8-21] 에 기재된 방법.
[8-23] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [8-16] ∼ [8-22] 의 어느 하나에 기재된 방법.
[8-24] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [8-16] ∼ [8-23] 의 어느 하나에 기재된 방법.
[8-25] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [8-16] ∼ [8-23] 의 어느 하나에 기재된 방법.
[8-26] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [8-16] ∼ [8-23] 의 어느 하나에 기재된 방법.
[9-1] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 유기 아민 ;
을 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제.
[9-2] 성분 (A) 가, 록소프로펜나트륨 수화물인, [9-1] 에 기재된 의약 제제.
[9-3] 성분 (B) 가, 알칸올아민인, [9-1] 또는 [9-2] 에 기재된 의약 제제.
[9-4] 성분 (B) 가, 디이소프로판올아민, 디에탄올아민, 염산트리에탄올아민, 트리이소프로판올아민, 트리에탄올아민, 트로메타몰, 메글루민 및 모노에탄올아민으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [9-1] 또는 [9-2] 에 기재된 의약 제제.
[9-5] 성분 (B) 가, 트리에탄올아민 및 염산트리에탄올아민으로 이루어지는 군에서 선택되는 1 종 이상인, [9-1] 또는 [9-2] 에 기재된 의약 제제.
[9-6] 조성물이, 추가로 물을 함유하는 것인, [9-1] ∼ [9-5] 중 어느 하나에 기재된 의약 제제.
[9-7] 조성물이, 추가로 저급 알코올을 함유하는 것인, [9-1] ∼ [9-6] 중 어느 하나에 기재된 의약 제제.
[9-8] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [9-7] 에 기재된 의약 제제.
[9-9] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [9-1] ∼ [9-8] 중 어느 하나에 기재된 의약 제제.
[9-10] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [9-1] ∼ [9-9] 중 어느 하나에 기재된 의약 제제.
[9-11] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [9-1] ∼ [9-9] 중 어느 하나에 기재된 의약 제제.
[9-12] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [9-1] ∼ [9-9] 중 어느 하나에 기재된 의약 제제.
[9-13] 외용 액제, 스프레이제, 연고제, 크림제, 겔제, 경구 액제, 시럽제 및 경구 젤리제로 이루어지는 군에서 선택되는 제형인, [9-1] ∼ [9-12] 중 어느 하나에 기재된 의약 제제.
[9-14] 외용 액제, 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [9-1] ∼ [9-12] 중 어느 하나에 기재된 의약 제제.
[9-15] 리니먼트제, 로션제, 외용 에어졸제, 펌프 스프레이제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [9-1] ∼ [9-12] 중 어느 하나에 기재된 의약 제제.
[9-16] 로션제, 연고제, 크림제 및 겔제로 이루어지는 군에서 선택되는 제형인, [9-1] ∼ [9-12] 중 어느 하나에 기재된 의약 제제.
[9-17] 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 유기 아민 ;
을 함유하는 액상 또는 반고형상의 조성물을, 폴리올레핀계 수지제 용기에 수용하는 공정을 포함하는, 조성물의 변색의 억제 방법.
[9-18] 성분 (A) 가, 록소프로펜나트륨 수화물인, [9-17] 에 기재된 방법.
[9-19] 성분 (B) 가, 알칸올아민인, [9-17] 또는 [9-18] 에 기재된 방법.
[9-20] 성분 (B) 가, 디이소프로판올아민, 디에탄올아민, 염산트리에탄올아민, 트리이소프로판올아민, 트리에탄올아민, 트로메타몰, 메글루민 및 모노에탄올아민으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, [9-17] 또는 [9-18] 에 기재된 방법.
[9-21] 성분 (B) 가, 트리에탄올아민 및 염산트리에탄올아민으로 이루어지는 군에서 선택되는 1 종 이상인, [9-17] 또는 [9-18] 에 기재된 방법.
[9-22] 조성물이, 추가로 물을 함유하는 것인, [9-17] ∼ [9-21] 중 어느 하나에 기재된 방법.
[9-23] 조성물이, 추가로 저급 알코올을 함유하는 것인, [9-17] ∼ [9-22] 중 어느 하나에 기재된 방법.
[9-24] 저급 알코올이, 에탄올 및 이소프로판올로 이루어지는 군에서 선택되는 1 종 이상인, [9-23] 에 기재된 방법.
[9-25] 폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, [9-17] ∼ [9-24] 중 어느 하나에 기재된 방법.
[9-26] 용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, [9-17] ∼ [9-25] 중 어느 하나에 기재된 방법.
[9-27] 용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, [9-17] ∼ [9-25] 중 어느 하나에 기재된 방법.
[9-28] 용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, [9-17] ∼ [9-25] 중 어느 하나에 기재된 방법.
실시예
이하에 실시예를 들어 본 발명을 상세하게 설명하지만, 본 발명은 이들 실시예에 전혀 한정되는 것은 아니다.
[시험예 1-1] 보존 시험 (테르펜류) 그 1
표 1 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 1-1, 비교예 1-1, 1-2 또는 참고예 1-1 의 의약 제제로 하였다.
얻어진 각종 의약 제제를, 80 ℃ 의 어두운 곳에 1 주일간 보존하고, 보존 후의 변색 (황변) 의 유무를 육안으로 평가하였다. 또한, 결과는, 변색이 발생하지 않은 것을 ○, 변색이 발생한 것을 × 로서 평가하였다.
결과를 표 1 에 나타낸다.
비교예 1-1 과, 참고예 1-1 (록소프로펜 비배합) 의 대비로부터, 80 ℃ 1 주일간의 보존 후에 있어서 확인된 변색은, 록소프로펜을 액상의 조성물에 배합한 것에서 기인하는 것이 분명해졌다.
그리고, 실시예 1-1 과, 비교예 1-1 (유리제 용기 수용), 비교예 1-2 (멘톨 비배합) 의 대비로부터, 액상의 조성물에 추가로 l-멘톨을 배합하고, 또한, 폴리에틸렌제의 용기에 수용함으로써, 이러한 변색을 억제할 수 있는 것이 분명해졌다.
이상의 시험 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 멘톨을 함유시키고, 또한, 이것을 폴리에틸렌제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 1-2] 보존 시험 (테르펜류) 그 2
표 2 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제의 용기에 수용하여 실시예 1-2 의 의약 제제로 하고, 시험예 1-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 2 에 나타낸다.
이상의 시험 결과로부터, 저급 알코올로서 이소프로판올 대신에 에탄올을 사용한 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
[시험예 1-3] 보존 시험 (테르펜류) 그 3
표 3 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제의 용기에 수용하여 실시예 1-3, 1-4 의 의약 제제로 하고, 시험예 1-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 3 에 나타낸다.
이상의 시험 결과로부터, 폴리올레핀계 수지제 용기로서 폴리에틸렌제 용기 대신에 폴리프로필렌제 용기를 사용한 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
[시험예 1-4] 보존 시험 (테르펜류) 그 4
표 4 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제의 용기에 수용하여 실시예 1-5 ∼ 1-8 의 의약 제제로 하고, 시험예 1-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 4 에 나타낸다.
이상의 시험 결과로부터, 테르펜류로서 l-멘톨 대신에 dl-캠퍼, 티몰을 사용한 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다. 또한, l-멘톨, 티몰은 단고리형의 모노테르페노이드이고, dl-캠퍼는 2 고리형의 모노테르페노이드인 것으로부터, 테르펜류가 넓게 변색 억제 작용을 갖는 것으로 합리적으로 추찰되었다.
이상의 시험예 1-1 ∼ 1-4 의 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 멘톨, 캠퍼, 티몰로 대표되는 테르펜류를 함유시키고, 또한, 폴리에틸렌, 폴리프로필렌으로 대표되는 폴리올레핀계 수지제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 1-5] 보존 시험 (테르펜류) 그 5
실시예 1-2, 1-5 ∼ 1-8 의 의약 제제에 수용되어 있는 것과 동일한 액상의 조성물을 조제하고, 이것을, 용기에 있어서 도포 부재로서 사용되는, 저밀도 폴리에틸렌제의 연통 다공질체 (MAPS : (주) 이노악 코퍼레이션) 에 함침시킨 후, 80 ℃ 의 어두운 곳에 1 주일간 보존했지만, 어느 조성물에 있어서도 분명한 변색은 확인되지 않았다.
[시험예 2-1] 보존 시험 (아르니카속의 식물 또는 그 추출물) 그 1
표 5 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 2-1, 비교예 2-1, 2-2 또는 참고예 2-1 의 의약 제제로 하였다.
얻어진 각종 의약 제제를, 80 ℃ 의 어두운 곳에 2 주일간 보존하고, 보존 후의 변색 (황변) 의 유무를 육안으로 평가하였다. 또한, 결과는, 변색이 발생하지 않은 것을 ○, 변색이 발생한 것을 × 로서 평가하였다.
결과를 표 5 에 나타낸다.
비교예 2-1 과, 참고예 2-1 (록소프로펜 비배합) 의 대비로부터, 80 ℃ 2 주일간의 보존 후에 있어서 확인된 변색은, 록소프로펜을 액상의 조성물에 배합한 것에서 기인하는 것이 분명해졌다.
그리고, 실시예 2-1 과, 비교예 2-1 (유리제 용기 수용), 비교예 2-2 (아르니카 팅크 비배합) 의 대비로부터, 액상의 조성물에 추가로 아르니카 팅크를 배합하고, 또한, 폴리에틸렌제의 용기에 수용함으로써, 이러한 변색을 억제할 수 있는 것이 분명해졌다.
이상의 시험 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 아르니카 팅크로 대표되는 아르니카속의 식물 또는 그 추출물을 함유시키고, 또한, 이것을 폴리에틸렌제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 2-2] 보존 시험 (아르니카속의 식물 또는 그 추출물) 그 2
표 6 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제의 용기에 수용하여 실시예 2-2 의 의약 제제로 하고, 시험예 2-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 2 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 6 에 나타낸다.
이상의 시험 결과로부터, 폴리올레핀계 수지제 용기로서 폴리에틸렌제 용기 대신에 폴리프로필렌제 용기를 사용한 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
이상의 시험예 2-1 ∼ 2-2 의 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 아르니카 팅크로 대표되는 아르니카속의 식물 또는 그 추출물을 함유시키고, 또한, 폴리에틸렌, 폴리프로필렌으로 대표되는 폴리올레핀계 수지제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 3-1] 보존 시험 (다가 알코올) 그 1
표 7 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제 또는 유리제의 용기에 수용하여, 각각 실시예 3-1, 비교예 3-1, 3-2 또는 참고예 3-1 의 의약 제제로 하였다.
얻어진 각종 의약 제제를, 80 ℃ 의 어두운 곳에 1 주일간 보존하고, 3 일간 보존 후 및 1 주일간 보존 후의 변색 (황변) 의 유무를 육안으로 평가하였다. 또한, 결과는, 변색이 발생하지 않은 것을 ○, 변색이 발생한 것을 × 로서 평가하였다.
결과를 표 7 에 나타낸다.
비교예 3-1 과, 참고예 3-1 (록소프로펜 비배합) 의 대비로부터, 80 ℃ 1 주일간의 보존 후에 있어서 확인된 변색은, 록소프로펜을 액상의 조성물에 배합한 것에서 기인하는 것이 분명해졌다.
또한, 비교예 3-1 (1,3-부틸렌글리콜 배합) 과 비교예 3-2 (1,3-부틸렌글리콜 비배합) 의 대비로부터, 조성물에 1,3-부틸렌글리콜을 배합함으로써 3 일간 보존 후의 변색이 억제되어 다소의 변색 억제 작용이 발휘되지만, 그 작용은 충분하지 않고, 1 주일간 보존 후에는 변색이 발생하는 것이 확인되었다.
한편, 실시예 3-1 (폴리프로필렌제 용기 수용, 1,3-부틸렌글리콜 배합) 과 비교예 3-1 (유리제 용기 수용, 1,3-부틸렌글리콜 배합) 의 대비로부터, 조성물에 1,3-부틸렌글리콜을 배합한 후에 폴리프로필렌제의 용기에 수용하는 것에 의해, 1 주일간 보존 후의 변색도 억제되어, 충분한 변색 억제 작용이 발휘되는 것이 확인되었다.
[시험예 3-2] 보존 시험 (다가 알코올) 그 2
표 8 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제의 용기에 수용하여 실시예 3-2, 3-3 의 의약 제제로 하고, 시험예 3-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 8 에 나타낸다.
이상의 시험 결과로부터, 저급 알코올로서 이소프로판올 대신에 에탄올을 사용한 경우나 저급 알코올을 배합하지 않는 경우에 있어서도 동일하게, 고온 보존시에 있어서의 변색의 억제가 확인되었다.
이상의 시험예 3-1 ∼ 3-2 의 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 1,3-부틸렌글리콜로 대표되는 다가 알코올을 함유시키고, 또한, 폴리프로필렌으로 대표되는 폴리올레핀계 수지제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 4-1] 보존 시험 (셀룰로오스류) 그 1
표 9 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제 또는 유리제의 용기에 수용하여, 각각 실시예 4-1, 비교예 4-1, 4-2 또는 참고예 4-1 의 의약 제제로 하였다.
얻어진 각종 의약 제제를, 80 ℃ 의 어두운 곳에 1 주일간 보존하고, 3 일간 보존 후 및 1 주일간 보존 후의 변색 (황변) 의 유무를 육안으로 평가하였다. 또한, 결과는, 변색이 발생하지 않은 것을 ○, 변색이 발생한 것을 × 로서 평가하였다.
결과를 표 9 에 나타낸다.
비교예 4-1 과, 참고예 4-1 (록소프로펜 비배합) 의 대비로부터, 80 ℃ 1 주일간의 보존 후에 있어서 확인된 변색은, 록소프로펜을 액상의 조성물에 배합한 것에서 기인하는 것이 분명해졌다.
또한, 비교예 4-1 (하이프로멜로스 배합) 과 비교예 4-2 (하이프로멜로스 비배합) 의 대비로부터, 조성물에 하이프로멜로스를 배합함으로써 3 일간 보존 후의 변색이 억제되어 다소의 변색 억제 작용이 발휘되지만, 그 작용은 충분하지 않고, 1 주일간 보존 후에는 변색이 발생하는 것이 확인되었다.
한편, 실시예 4-1 (폴리프로필렌제 용기 수용, 하이프로멜로스 배합) 과 비교예 4-1 (유리제 용기 수용, 하이프로멜로스 배합) 의 대비로부터, 조성물에 하이프로멜로스를 배합한 후에 폴리프로필렌제의 용기에 수용하는 것에 의해, 1 주일간 보존 후의 변색도 억제되어, 충분한 변색 억제 작용이 발휘되는 것이 확인되었다.
[시험예 4-2] 보존 시험 (셀룰로오스류) 그 2
표 10 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제의 용기에 수용하여 실시예 4-2, 4-3 의 의약 제제로 하고, 시험예 4-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 10 에 나타낸다.
이상의 시험 결과로부터, 저급 알코올로서 이소프로판올 대신에 에탄올을 사용한 경우나 저급 알코올을 배합하지 않는 경우에 있어서도 동일하게, 고온 보존시에 있어서의 변색의 억제가 확인되었다.
이상의 시험예 4-1 ∼ 4-2 의 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 하이프로멜로스로 대표되는 셀룰로오스류를 함유시키고, 또한, 폴리프로필렌으로 대표되는 폴리올레핀계 수지제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 5-1] 보존 시험 (토코페롤류) 그 1
표 11 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 5-1, 비교예 5-1, 5-2 의 의약 제제로 하였다.
얻어진 각종 의약 제제를, 80 ℃ 의 어두운 곳에 1 주일간 보존하고, 3 일간 보존 후 및 1 주일간 보존 후의 변색 (황변) 의 유무를 육안으로 평가하였다. 또한, 결과는, 변색이 발생하지 않은 것을 ○, 변색이 발생한 것을 × 로서 평가하였다.
결과를 표 11 에 나타낸다.
비교예 5-1 (폴리에틸렌제 용기 수용) 과 비교예 5-2 (유리제 용기 수용) 의 대비로부터, 조성물을 폴리에틸렌제의 용기에 수용함으로써 3 일간 보존 후의 변색이 억제되어 다소의 변색 억제 작용이 발휘되지만, 그 작용은 충분하지 않고, 1 주일간 보존 후에는 변색이 발생하는 것이 확인되었다.
한편, 실시예 5-1 (dl-α-토코페롤아세트산에스테르 배합, 폴리에틸렌제 용기 수용) 과 비교예 5-1 (dl-α-토코페롤아세트산에스테르 비배합, 폴리에틸렌제 용기 수용) 의 대비로부터, 조성물에 추가로 dl-α-토코페롤아세트산에스테르를 배합한 후에 폴리에틸렌제의 용기에 수용함으로써, 1 주일간 보존 후의 변색도 억제되어, 충분한 변색 억제 작용이 발휘되는 것이 확인되었다.
이상의 시험 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 토코페롤류를 함유시키고, 또한, 이것을 폴리올레핀계 수지제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 5-2] 보존 시험 (토코페롤류) 그 2
표 12 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 5-2, 비교예 5-3, 5-4 또는 참고예 5-1 의 의약 제제로 하고, 시험예 5-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 2 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 12 에 나타낸다.
비교예 5-3 과, 참고예 5-1 (록소프로펜 비배합) 의 대비로부터, 80 ℃ 2 주일간의 보존 후에 있어서 확인된 변색은, 록소프로펜을 액상의 조성물에 배합한 것에서 기인하는 것이 확인되었다.
그리고, 실시예 5-2 와 비교예 5-3 (유리제 용기 수용), 비교예 5-4 (dl-α-토코페롤아세트산에스테르 비배합) 의 대비로부터, 액상의 조성물에 추가로 dl-α-토코페롤아세트산에스테르를 배합하고, 또한, 폴리에틸렌제의 용기에 수용함으로써, 이러한 변색을 억제할 수 있는 것이 확인되었다.
[시험예 5-3] 보존 시험 (토코페롤류) 그 3
표 13 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제의 용기에 수용하여 실시예 5-3 의 의약 제제로 하고, 시험예 5-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 2 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 13 에 나타낸다.
이상의 시험 결과로부터, 폴리올레핀계 수지제 용기로서 폴리에틸렌제 용기 대신에 폴리프로필렌제 용기를 사용한 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
[시험예 5-4] 보존 시험 (토코페롤류) 그 4
실시예 5-1 의 의약 제제에 수용되어 있는 것과 동일한 액상의 조성물을 조제하고, 이것을, 용기에 있어서 도포 부재로서 사용되는, 저밀도 폴리에틸렌제의 연통 다공질체 (MAPS : (주) 이노악 코퍼레이션) 에 함침시킨 후, 80 ℃ 의 어두운 곳에 1 주일간 보존했지만, 분명한 변색은 확인되지 않았다.
[시험예 6-1] 보존 시험 (글리시르레틴산류) 그 1
표 14 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 6-1, 비교예 6-1, 6-2 의 의약 제제로 하였다.
얻어진 각종 의약 제제를, 80 ℃ 의 어두운 곳에 1 주일간 보존하고, 3 일간 보존 후 및 1 주일간 보존 후의 변색 (황변) 의 유무를 육안으로 평가하였다. 또한, 결과는, 변색이 발생하지 않은 것을 ○, 변색이 발생한 것을 × 로서 평가하였다.
결과를 표 14 에 나타낸다.
비교예 6-1 (폴리에틸렌제 용기 수용) 과 비교예 6-2 (유리제 용기 수용) 의 대비로부터, 조성물을 폴리에틸렌제의 용기에 수용함으로써 3 일간 보존 후의 변색이 억제되어 다소의 변색 억제 작용이 발휘되지만, 그 작용은 충분하지 않고, 1 주일간 보존 후에는 변색이 발생하는 것이 확인되었다.
한편, 실시예 6-1 (글리시르레틴산 배합, 폴리에틸렌제 용기 수용) 과 비교예 6-1 (글리시르레틴산 비배합, 폴리에틸렌제 용기 수용) 의 대비로부터, 조성물에 추가로 글리시르레틴산을 배합한 후에 폴리에틸렌제의 용기에 수용함으로써, 1 주일간 보존 후의 변색도 억제되어, 충분한 변색 억제 작용이 발휘되는 것이 확인되었다.
[시험예 6-2] 보존 시험 (글리시르레틴산류) 그 2
표 15 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제의 용기에 수용하여 실시예 6-2 의 의약 제제로 하고, 시험예 6-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 15 에 나타낸다.
이상의 시험 결과로부터, 저급 알코올로서 이소프로판올 대신에 에탄올을 사용한 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
이상의 시험예 6-1, 6-2 의 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 글리시르레틴산류를 함유시키고, 또한, 이것을 폴리올레핀계 수지제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 6-3] 보존 시험 (글리시르레틴산류) 그 3
표 16 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 6-3, 비교예 6-3, 6-4 또는 참고예 6-1 의 의약 제제로 하고, 시험예 6-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 2 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 16 에 나타낸다.
비교예 6-3 과, 참고예 6-1 (록소프로펜 비배합) 의 대비로부터, 80 ℃ 2 주일간의 보존 후에 있어서 확인된 변색은, 록소프로펜을 액상의 조성물에 배합한 것에서 기인하는 것이 확인되었다.
그리고, 실시예 6-3 과, 비교예 6-3 (유리제 용기 수용), 비교예 6-4 (글리시르레틴산 비배합) 의 대비로부터, 액상의 조성물에 추가로 글리시르레틴산을 배합하고, 또한, 폴리에틸렌제의 용기에 수용함으로써, 이러한 변색을 억제할 수 있는 것이 확인되었다.
[시험예 6-4] 보존 시험 (글리시르레틴산류) 그 4
표 17 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제의 용기에 수용하여 실시예 6-4, 6-5 의 의약 제제로 하고, 시험예 6-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 2 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 17 에 나타낸다.
이상의 시험 결과로부터, 폴리올레핀계 수지제 용기로서 폴리에틸렌제 용기 대신에 폴리프로필렌제 용기를 사용한 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
[시험예 6-5] 보존 시험 (글리시르레틴산류) 그 5
실시예 6-1, 6-2 의 의약 제제에 수용되어 있는 것과 동일한 액상의 조성물을 조제하고, 이것을, 용기에 있어서 도포 부재로서 사용되는, 저밀도 폴리에틸렌제의 연통 다공질체 (MAPS : (주) 이노악 코퍼레이션) 에 함침시킨 후, 80 ℃ 의 어두운 곳에 1 주일간 보존했지만, 분명한 변색은 확인되지 않았다.
[시험예 7-1] 보존 시험 (일반식 (1) 로 나타내는 화합물 또는 그 염) 그 1
표 18 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 7-1, 비교예 7-1, 7-2 의 의약 제제로 하였다.
얻어진 각종 의약 제제를, 80 ℃ 의 어두운 곳에 1 주일간 보존하고, 3 일간 보존 후 및 1 주일간 보존 후의 변색 (황변) 의 유무를 육안으로 평가하였다. 또한, 결과는, 변색이 발생하지 않은 것을 ○, 변색이 발생한 것을 × 로서 평가하였다.
결과를 표 18 에 나타낸다.
비교예 7-1 (폴리에틸렌제 용기 수용) 과 비교예 7-2 (유리제 용기 수용) 의 대비로부터, 조성물을 폴리에틸렌제의 용기에 수용함으로써 3 일간 보존 후의 변색이 억제되어 다소의 변색 억제 작용이 발휘되지만, 그 작용은 충분하지 않고, 1 주일간 보존 후에는 변색이 발생하는 것이 확인되었다.
한편, 실시예 7-1 (클로르페니라민 배합, 폴리에틸렌제 용기 수용) 과 비교예 7-1 (폴리에틸렌제 용기 수용) 의 대비로부터, 조성물에 추가로 클로르페니라민을 배합한 후에 폴리에틸렌제의 용기에 수용함으로써, 1 주일간 보존 후의 변색도 억제되어, 충분한 변색 억제 작용이 발휘되는 것이 확인되었다.
이상의 시험 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 클로르페니라민 또는 그 염을 함유시키고, 또한, 이것을 폴리올레핀계 수지제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 7-2] 보존 시험 (일반식 (1) 로 나타내는 화합물 또는 그 염) 그 2
표 19 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 7-2, 비교예 7-3, 7-4 의 의약 제제로 하고, 시험예 7-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 3 일간 및 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 19 에 나타낸다.
이상의 시험 결과로부터, 클로르페니라민말레산염 대신에 디펜히드라민염산염을 함유시킨 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
[시험예 7-3] 보존 시험 (일반식 (1) 로 나타내는 화합물 또는 그 염) 그 3
표 20 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제의 용기에 수용하여 실시예 7-3, 7-4 의 의약 제제로 하고, 시험예 7-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 20 에 나타낸다.
이상의 시험 결과로부터, 저급 알코올로서 이소프로판올 대신에 에탄올을 사용한 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
이상의 시험예 7-1 ∼ 7-3 의 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 클로르페니라민 또는 그 염, 디펜히드라민 또는 그 염으로 대표되는 상기 일반식 (1) 로 나타내는 화합물 또는 그 염을 함유시키고, 또한, 폴리올레핀계 수지제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 7-4] 보존 시험 (일반식 (1) 로 나타내는 화합물 또는 그 염) 그 4
표 21 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 7-5, 비교예 7-5, 7-6 또는 참고예 7-1 의 의약 제제로 하고, 시험예 7-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 3 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 21 에 나타낸다.
비교예 7-5 와, 참고예 7-1 (록소프로펜 비배합) 의 대비로부터, 80 ℃ 3 주일간의 보존 후에 있어서 확인된 변색은, 록소프로펜을 액상의 조성물에 배합한 것에서 기인하는 것이 확인되었다.
그리고, 실시예 7-5 와, 비교예 7-5 (유리제 용기 수용), 비교예 7-6 (클로르페니라민말레산염 비배합) 의 대비로부터, 액상의 조성물에 추가로 클로르페니라민말레산염을 배합하고, 또한, 폴리에틸렌제의 용기에 수용함으로써, 이러한 변색을 억제할 수 있는 것이 확인되었다.
[시험예 7-5] 보존 시험 (일반식 (1) 로 나타내는 화합물 또는 그 염) 그 5
표 22 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제의 용기에 수용하여, 각각 실시예 7-6 ∼ 7-9 의 의약 제제로 하고, 시험예 7-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 22 에 나타낸다.
이상의 시험 결과로부터, 폴리올레핀계 수지제 용기로서 폴리에틸렌제 용기 대신에 폴리프로필렌제 용기를 사용한 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
[시험예 7-6] 보존 시험 (일반식 (1) 로 나타내는 화합물 또는 그 염) 그 6
실시예 7-3, 7-4 의 의약 제제에 수용되어 있는 것과 동일한 액상의 조성물을 조제하고, 이것을, 용기에 있어서 도포 부재로서 사용되는, 저밀도 폴리에틸렌제의 연통 다공질체 (MAPS : (주) 이노악 코퍼레이션) 에 함침시킨 후, 80 ℃ 의 어두운 곳에 1 주일간 보존했지만, 어느 조성물에 있어서도 분명한 변색은 확인되지 않았다.
[시험예 8-1] 보존 시험 (고추 또는 그 추출물) 그 1
표 23 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 8-1, 비교예 8-1, 8-2 의 의약 제제로 하였다.
얻어진 각종 의약 제제를, 80 ℃ 의 어두운 곳에 1 주일간 보존하고, 3 일간 보존 후 및 1 주일간 보존 후의 변색 (황변) 의 유무를 육안으로 평가하였다. 또한, 결과는, 변색이 발생하지 않은 것을 ○, 변색이 발생한 것을 × 로서 평가하였다.
결과를 표 23 에 나타낸다.
비교예 8-1 (폴리에틸렌제 용기 수용) 과 비교예 8-2 (유리제 용기 수용) 의 대비로부터, 조성물을 폴리에틸렌제의 용기에 수용함으로써 3 일간 보존 후의 변색이 억제되어 다소의 변색 억제 작용이 발휘되지만, 그 작용은 충분하지 않고, 1 주일간 보존 후에는 변색이 발생하는 것이 확인되었다.
한편, 실시예 8-1 (고추 연엑기스 배합, 폴리에틸렌제 용기 수용) 과 비교예 8-1 (폴리에틸렌제 용기 수용) 의 대비로부터, 조성물에 추가로 고추 연엑기스를 배합한 후에 폴리에틸렌제의 용기에 수용함으로써, 1 주일간 보존 후의 변색도 억제되어, 충분한 변색 억제 작용이 발휘되는 것이 확인되었다.
이상의 시험 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 고추 또는 그 추출물을 함유시키고, 또한, 이것을 폴리올레핀계 수지제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 8-2] 보존 시험 (고추 또는 그 추출물) 그 2
표 24 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 8-2, 비교예 8-3, 8-4 의 의약 제제로 하고, 시험예 8-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 3 일간 및 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 24 에 나타낸다.
이상의 시험 결과로부터, 고추 연엑기스 대신에 노난산바닐릴아미드를 함유시킨 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
[시험예 8-3] 보존 시험 (고추 또는 그 추출물) 그 3
표 25 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제의 용기에 수용하여 실시예 8-3 의 의약 제제로 하고, 시험예 8-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 25 에 나타낸다.
이상의 시험 결과로부터, 저급 알코올로서 이소프로판올 대신에 에탄올을 사용한 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
이상의 시험예 8-1 ∼ 8-3 의 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 고추 연엑기스, 노난산바닐릴아미드로 대표되는 고추 또는 그 추출물을 함유시키고, 또한, 폴리올레핀계 수지제의 용기에 수용함으로써, 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
[시험예 8-4] 보존 시험 (고추 또는 그 추출물) 그 4
표 26 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리에틸렌제 또는 유리제의 용기에 수용하여, 각각 실시예 8-4, 비교예 8-5, 8-6 또는 참고예 8-1 의 의약 제제로 하고, 시험예 8-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 2 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 26 에 나타낸다.
비교예 8-5 와, 참고예 8-1 (록소프로펜 비배합) 의 대비로부터, 80 ℃ 2 주일간의 보존 후에 있어서 확인된 변색은, 록소프로펜을 액상의 조성물에 배합한 것에서 기인하는 것이 확인되었다.
그리고, 실시예 8-4 와, 비교예 8-5 (유리제 용기 수용), 비교예 8-6 (노난산바닐릴아미드 비배합) 의 대비로부터, 액상의 조성물에 추가로 노난산바닐릴아미드를 배합하고, 또한, 폴리에틸렌제의 용기에 수용함으로써, 이러한 변색을 억제할 수 있는 것이 확인되었다.
[시험예 8-5] 보존 시험 (고추 또는 그 추출물) 그 5
표 27 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제의 용기에 수용하여 실시예 8-5, 8-6 의 의약 제제로 하고, 시험예 8-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 2 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 27 에 나타낸다.
이상의 시험 결과로부터, 폴리올레핀계 수지제 용기로서 폴리에틸렌제 용기 대신에 폴리프로필렌제 용기를 사용한 경우에도, 동일하게 고온 보존시에 있어서의 변색의 억제가 확인되었다.
[시험예 8-6] 보존 시험 (고추 또는 그 추출물) 그 6
실시예 8-1, 8-3 의 의약 제제에 수용되어 있는 것과 동일한 액상의 조성물을 조제하고, 이것을, 용기에 있어서 도포 부재로서 사용되는, 저밀도 폴리에틸렌제의 연통 다공질체 (MAPS : (주) 이노악 코퍼레이션) 에 함침시킨 후, 80 ℃ 의 어두운 곳에 1 주일간 보존했지만, 어느 조성물에 있어서도 분명한 변색은 확인되지 않았다.
[시험예 9-1] 보존 시험 (유기 아민) 그 1
표 28 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제 또는 유리제의 용기에 수용하여, 각각 실시예 9-1, 비교예 9-1, 9-2 의 의약 제제로 하였다.
얻어진 각종 의약 제제를, 80 ℃ 의 어두운 곳에 1 주일간 보존하고, 3 일간 보존 후 및 1 주일간 보존 후의 변색 (황변) 의 유무를 육안으로 평가하였다. 또한, 결과는, 변색이 발생하지 않은 것을 ○, 변색이 발생한 것을 × 로서 평가하였다.
결과를 표 28 에 나타낸다.
상기 시험 결과의 비교예 9-1 (트리에탄올아민 배합) 과 비교예 9-2 (트리에탄올아민 비배합) 의 대비로부터, 조성물에 트리에탄올아민을 배합함으로써 3 일간 보존 후의 변색이 억제되어 다소의 변색 억제 작용이 발휘되지만, 그 작용은 충분하지 않고, 1 주일간 보존 후에는 변색이 발생하는 것이 확인되었다.
한편, 실시예 9-1 (폴리프로필렌제 용기 수용, 트리에탄올아민 배합) 과 비교예 9-1 (유리제 용기 수용, 트리에탄올아민 배합) 의 대비로부터, 조성물에 트리에탄올아민을 배합한 후에 폴리프로필렌제의 용기에 수용함으로써, 1 주일간 보존 후의 변색도 억제되어, 충분한 변색 억제 작용이 발휘되는 것이 확인되었다.
즉, 조성물에 유기 아민을 배합하고, 폴리올레핀계 수지제 용기에 수용함으로써, 조성물의 시간 경과적인 변색 내지 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 판명되었다.
[시험예 9-2] 보존 시험 (유기 아민) 그 2
표 29 에 나타내는 성분 및 분량을 함유하는 액상의 조성물을 조제하고, 폴리프로필렌제의 용기에 수용하여 실시예 9-2, 9-3 의 의약 제제로 하고, 시험예 9-1 과 동일한 방법에 의해 80 ℃ 의 어두운 곳에 1 주일간 보존한 후의 변색의 유무를 평가하였다.
결과를 표 29 에 나타낸다.
이상의 시험 결과로부터, 저급 알코올로서 이소프로판올 대신에 에탄올을 사용한 경우나 저급 알코올을 배합하지 않는 경우에 있어서도 동일하게, 고온 보존시에 있어서의 변색의 억제가 확인되었다.
이상의 시험예 9-1 ∼ 9-2 의 결과로부터, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물에, 추가로 트리에탄올아민으로 대표되는 유기 아민을 함유시키고, 또한, 폴리프로필렌으로 대표되는 폴리올레핀계 수지제의 용기에 수용함으로써, 조성물의 시간 경과적인 변색 내지 고온 보존시에 있어서의 변색을 억제할 수 있는 것이 분명해졌다.
이하에, 의약 제제의 제조예를 나타낸다. 또한, 아르니카속의 식물의 추출물의 함유량은, 특별히 언급이 없는 한, 원생약 환산량 (g) 을 나타낸다.
제조예 1-1 (로션제)
통상적인 방법에 의해, 하기 표 30 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 1-1-1 ∼ 1-1-8 의 의약 제제 (로션제) 로 하였다.
제조예 1-2 (로션제)
통상적인 방법에 의해, 상기 표 30 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 1-2-1 ∼ 1-2-8 의 의약 제제 (로션제) 로 하였다.
제조예 1-3 (로션제)
통상적인 방법에 의해, 하기 표 31 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 1-3-1 ∼ 1-3-8 의 의약 제제 (로션제) 로 하였다.
제조예 1-4 (로션제)
통상적인 방법에 의해, 상기 표 31 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 1-4-1 ∼ 1-4-8 의 의약 제제 (로션제) 로 하였다.
제조예 1-5 (겔제)
통상적인 방법에 의해, 하기 표 32 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 17 ∼ 24) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 알루미늄박, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 1-5-1 ∼ 1-5-8 의 의약 제제 (겔제) 로 하였다.
제조예 1-6 (연고제)
통상적인 방법에 의해, 하기 표 33 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 25 ∼ 32) 을 제조하고, 고밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 폴리에틸렌테레프탈레이트제의 필름, 추가로 그 외측에 고밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 1-6-1 ∼ 1-6-8 의 의약 제제 (연고제) 로 하였다.
제조예 1-7 (크림제)
통상적인 방법에 의해, 하기 표 34 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 33 ∼ 40) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 나일론제의 필름, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 1-7-1 ∼ 1-7-8 의 의약 제제 (크림제) 로 하였다.
제조예 1-8 (경구 액제)
통상적인 방법에 의해, 하기 표 35 에 기재된 성분 및 분량 (㎎) 을 30 ㎖ 중에 함유하는 액상의 조성물 (처방예 41 ∼ 48) 을 제조하고, 폴리프로필렌제의 보틀 용기에 수용하여, 각각 제조예 1-8-1 ∼ 1-8-8 의 의약 제제 (경구 액제) 로 하였다.
제조예 2-1 (로션제)
통상적인 방법에 의해, 하기 표 36 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 2-1-1 ∼ 2-1-8 의 의약 제제 (로션제) 로 하였다.
제조예 2-2 (로션제)
통상적인 방법에 의해, 상기 표 36 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 2-2-1 ∼ 2-2-8 의 의약 제제 (로션제) 로 하였다.
제조예 2-3 (로션제)
통상적인 방법에 의해, 하기 표 37 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 2-3-1 ∼ 2-3-8 의 의약 제제 (로션제) 로 하였다.
제조예 2-4 (로션제)
통상적인 방법에 의해, 상기 표 37 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 2-4-1 ∼ 2-4-8 의 의약 제제 (로션제) 로 하였다.
제조예 2-5 (겔제)
통상적인 방법에 의해, 하기 표 38 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 17 ∼ 24) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 알루미늄박, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 2-5-1 ∼ 2-5-8 의 의약 제제 (겔제) 로 하였다.
제조예 2-6 (연고제)
통상적인 방법에 의해, 하기 표 39 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 25 ∼ 32) 을 제조하고, 고밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 폴리에틸렌테레프탈레이트제의 필름, 추가로 그 외측에 고밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 2-6-1 ∼ 2-6-8 의 의약 제제 (연고제) 로 하였다.
제조예 2-7 (크림제)
통상적인 방법에 의해, 하기 표 40 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 33 ∼ 40) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 나일론제의 필름, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 2-7-1 ∼ 2-7-8 의 의약 제제 (크림제) 로 하였다.
제조예 2-8 (경구 액제)
통상적인 방법에 의해, 하기 표 41 에 기재된 성분 및 분량 (㎎) 을 30 ㎖ 중에 함유하는 액상의 조성물 (처방예 41 ∼ 48) 을 제조하고, 폴리프로필렌제의 보틀 용기에 수용하여, 각각 제조예 2-8-1 ∼ 2-8-8 의 의약 제제 (경구 액제) 로 하였다.
제조예 3-1 (로션제)
통상적인 방법에 의해, 하기 표 42 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 3-1-1 ∼ 3-1-8 의 의약 제제 (로션제) 로 하였다.
제조예 3-2 (로션제)
통상적인 방법에 의해, 상기 표 42 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 3-2-1 ∼ 3-2-8 의 의약 제제 (로션제) 로 하였다.
제조예 3-3 (로션제)
통상적인 방법에 의해, 하기 표 43 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 3-3-1 ∼ 3-3-8 의 의약 제제 (로션제) 로 하였다.
제조예 3-4 (로션제)
통상적인 방법에 의해, 상기 표 43 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 3-4-1 ∼ 3-4-8 의 의약 제제 (로션제) 로 하였다.
제조예 3-5 (겔제)
통상적인 방법에 의해, 하기 표 44 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 17 ∼ 24) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 알루미늄박, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 3-5-1 ∼ 3-5-8 의 의약 제제 (겔제) 로 하였다.
제조예 3-6 (크림제)
통상적인 방법에 의해, 하기 표 45 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 25 ∼ 32) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 나일론제의 필름, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 3-6-1 ∼ 3-6-8 의 의약 제제 (크림제) 로 하였다.
제조예 3-7 (경구 액제)
통상적인 방법에 의해, 하기 표 46 에 기재된 성분 및 분량 (㎎) 을 30 ㎖ 중에 함유하는 액상의 조성물 (처방예 33 ∼ 40) 을 제조하고, 폴리프로필렌제의 보틀 용기에 수용하여, 각각 제조예 3-7-1 ∼ 3-7-8 의 의약 제제 (경구 액제) 로 하였다.
제조예 4-1 (로션제)
통상적인 방법에 의해, 하기 표 47 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 4-1-1 ∼ 4-1-8 의 의약 제제 (로션제) 로 하였다.
제조예 4-2 (로션제)
통상적인 방법에 의해, 상기 표 47 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 4-2-1 ∼ 4-2-8 의 의약 제제 (로션제) 로 하였다.
제조예 4-3 (로션제)
통상적인 방법에 의해, 하기 표 48 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 4-3-1 ∼ 4-3-8 의 의약 제제 (로션제) 로 하였다.
제조예 4-4 (로션제)
통상적인 방법에 의해, 상기 표 48 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 4-4-1 ∼ 4-4-8 의 의약 제제 (로션제) 로 하였다.
제조예 4-5 (겔제)
통상적인 방법에 의해, 하기 표 49 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 17 ∼ 24) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 알루미늄박, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 4-5-1 ∼ 4-5-8 의 의약 제제 (겔제) 로 하였다.
제조예 4-6 (연고제)
통상적인 방법에 의해, 하기 표 50 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 25 ∼ 32) 을 제조하고, 고밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 폴리에틸렌테레프탈레이트제의 필름, 추가로 그 외측에 고밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 4-6-1 ∼ 4-6-8 의 의약 제제 (연고제) 로 하였다.
제조예 4-7 (크림제)
통상적인 방법에 의해, 하기 표 51 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 33 ∼ 40) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 나일론제의 필름, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 4-7-1 ∼ 4-7-8 의 의약 제제 (크림제) 로 하였다.
제조예 4-8 (경구 액제)
통상적인 방법에 의해, 하기 표 52 에 기재된 성분 및 분량 (㎎) 을 30 ㎖ 중에 함유하는 액상의 조성물 (처방예 41 ∼ 48) 을 제조하고, 폴리프로필렌제의 보틀 용기에 수용하여, 각각 제조예 4-8-1 ∼ 4-8-8 의 의약 제제 (경구 액제) 로 하였다.
제조예 5-1 (로션제)
통상적인 방법에 의해, 하기 표 53 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 5-1-1 ∼ 5-1-8 의 의약 제제 (로션제) 로 하였다.
제조예 5-2 (로션제)
통상적인 방법에 의해, 상기 표 53 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 5-2-1 ∼ 5-2-8 의 의약 제제 (로션제) 로 하였다.
제조예 5-3 (로션제)
통상적인 방법에 의해, 하기 표 54 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 5-3-1 ∼ 5-3-8 의 의약 제제 (로션제) 로 하였다.
제조예 5-4 (로션제)
통상적인 방법에 의해, 상기 표 54 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 5-4-1 ∼ 5-4-8 의 의약 제제 (로션제) 로 하였다.
제조예 5-5 (겔제)
통상적인 방법에 의해, 하기 표 55 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 17 ∼ 24) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 알루미늄박, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 5-5-1 ∼ 5-5-8 의 의약 제제 (겔제) 로 하였다.
제조예 5-6 (연고제)
통상적인 방법에 의해, 하기 표 56 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 25 ∼ 32) 을 제조하고, 고밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 폴리에틸렌테레프탈레이트제의 필름, 추가로 그 외측에 고밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 5-6-1 ∼ 5-6-8 의 의약 제제 (연고제) 로 하였다.
제조예 5-7 (크림제)
통상적인 방법에 의해, 하기 표 57 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 33 ∼ 40) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 나일론제의 필름, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 5-7-1 ∼ 5-7-8 의 의약 제제 (크림제) 로 하였다.
제조예 5-8 (경구 액제)
통상적인 방법에 의해, 하기 표 58 에 기재된 성분 및 분량 (㎎) 을 30 ㎖ 중에 함유하는 액상의 조성물 (처방예 41 ∼ 48) 을 제조하고, 폴리프로필렌제의 보틀 용기에 수용하여, 각각 제조예 5-8-1 ∼ 5-8-8 의 의약 제제 (경구 액제) 로 하였다.
제조예 6-1 (로션제)
통상적인 방법에 의해, 하기 표 59 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 6-1-1 ∼ 6-1-8 의 의약 제제 (로션제) 로 하였다.
제조예 6-2 (로션제)
통상적인 방법에 의해, 상기 표 59 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 6-2-1 ∼ 6-2-8 의 의약 제제 (로션제) 로 하였다.
제조예 6-3 (로션제)
통상적인 방법에 의해, 하기 표 60 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 6-3-1 ∼ 6-3-8 의 의약 제제 (로션제) 로 하였다.
제조예 6-4 (로션제)
통상적인 방법에 의해, 상기 표 60 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 6-4-1 ∼ 6-4-8 의 의약 제제 (로션제) 로 하였다.
제조예 6-5 (겔제)
통상적인 방법에 의해, 하기 표 61 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 17 ∼ 24) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 알루미늄박, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 6-5-1 ∼ 6-5-8 의 의약 제제 (겔제) 로 하였다.
제조예 6-6 (연고제)
통상적인 방법에 의해, 하기 표 62 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 25 ∼ 32) 을 제조하고, 고밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 폴리에틸렌테레프탈레이트제의 필름, 추가로 그 외측에 고밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 6-6-1 ∼ 6-6-8 의 의약 제제 (연고제) 로 하였다.
제조예 6-7 (크림제)
통상적인 방법에 의해, 하기 표 63 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 33 ∼ 40) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 나일론제의 필름, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 6-7-1 ∼ 6-7-8 의 의약 제제 (크림제) 로 하였다.
제조예 6-8 (경구 액제)
통상적인 방법에 의해, 하기 표 64 에 기재된 성분 및 분량 (㎎) 을 30 ㎖ 중에 함유하는 액상의 조성물 (처방예 41 ∼ 48) 을 제조하고, 폴리프로필렌제의 보틀 용기에 수용하여, 각각 제조예 6-8-1 ∼ 6-8-8 의 의약 제제 (경구 액제) 로 하였다.
제조예 7-1 (로션제)
통상적인 방법에 의해, 하기 표 65 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 7-1-1 ∼ 7-1-8 의 의약 제제 (로션제) 로 하였다.
제조예 7-2 (로션제)
통상적인 방법에 의해, 상기 표 65 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 7-2-1 ∼ 7-2-8 의 의약 제제 (로션제) 로 하였다.
제조예 7-3 (로션제)
통상적인 방법에 의해, 하기 표 66 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 7-3-1 ∼ 7-3-8 의 의약 제제 (로션제) 로 하였다.
제조예 7-4 (로션제)
통상적인 방법에 의해, 상기 표 66 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 7-4-1 ∼ 7-4-8 의 의약 제제 (로션제) 로 하였다.
제조예 7-5 (겔제)
통상적인 방법에 의해, 하기 표 67 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 17 ∼ 24) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 알루미늄박, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 7-5-1 ∼ 7-5-8 의 의약 제제 (겔제) 로 하였다.
제조예 7-6 (연고제)
통상적인 방법에 의해, 하기 표 68 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 25 ∼ 32) 을 제조하고, 고밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 폴리에틸렌테레프탈레이트제의 필름, 추가로 그 외측에 고밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 7-6-1 ∼ 7-6-8 의 의약 제제 (연고제) 로 하였다.
제조예 7-7 (크림제)
통상적인 방법에 의해, 하기 표 69 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 33 ∼ 40) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 나일론제의 필름, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 7-7-1 ∼ 7-7-8 의 의약 제제 (크림제) 로 하였다.
제조예 7-8 (경구 액제)
통상적인 방법에 의해, 하기 표 70 에 기재된 성분 및 분량 (㎎) 을 30 ㎖ 중에 함유하는 액상의 조성물 (처방예 41 ∼ 48) 을 제조하고, 폴리프로필렌제의 보틀 용기에 수용하여, 각각 제조예 7-8-1 ∼ 7-8-8 의 의약 제제 (경구 액제) 로 하였다.
제조예 8-1 (로션제)
통상적인 방법에 의해, 하기 표 71 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 8-1-1 ∼ 8-1-8 의 의약 제제 (로션제) 로 하였다.
제조예 8-2 (로션제)
통상적인 방법에 의해, 상기 표 71 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 8-2-1 ∼ 8-2-8 의 의약 제제 (로션제) 로 하였다.
제조예 8-3 (로션제)
통상적인 방법에 의해, 하기 표 72 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 8-3-1 ∼ 8-3-8 의 의약 제제 (로션제) 로 하였다.
제조예 8-4 (로션제)
통상적인 방법에 의해, 상기 표 72 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 8-4-1 ∼ 8-4-8 의 의약 제제 (로션제) 로 하였다.
제조예 8-5 (겔제)
통상적인 방법에 의해, 하기 표 73 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 17 ∼ 24) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 알루미늄박, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 8-5-1 ∼ 8-5-8 의 의약 제제 (겔제) 로 하였다.
제조예 8-6 (연고제)
통상적인 방법에 의해, 하기 표 74 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 25 ∼ 32) 을 제조하고, 고밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 폴리에틸렌테레프탈레이트제의 필름, 추가로 그 외측에 고밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 8-6-1 ∼ 8-6-8 의 의약 제제 (연고제) 로 하였다.
제조예 8-7 (크림제)
통상적인 방법에 의해, 하기 표 75 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 33 ∼ 40) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 나일론제의 필름, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 8-7-1 ∼ 8-7-8 의 의약 제제 (크림제) 로 하였다.
제조예 8-8 (경구 액제)
통상적인 방법에 의해, 하기 표 76 에 기재된 성분 및 분량 (㎎) 을 30 ㎖ 중에 함유하는 액상의 조성물 (처방예 41 ∼ 48) 을 제조하고, 폴리프로필렌제의 보틀 용기에 수용하여, 각각 제조예 8-8-1 ∼ 8-8-8 의 의약 제제 (경구 액제) 로 하였다.
제조예 9-1 (로션제)
통상적인 방법에 의해, 하기 표 77 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 9-1-1 ∼ 9-1-8 의 의약 제제 (로션제) 로 하였다.
제조예 9-2 (로션제)
통상적인 방법에 의해, 상기 표 77 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 1 ∼ 8) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 9-2-1 ∼ 9-2-8 의 의약 제제 (로션제) 로 하였다.
제조예 9-3 (로션제)
통상적인 방법에 의해, 하기 표 78 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리프로필렌제의 용기 본체의 개구부에 스펀지상의 폴리우레탄제 도포 부재를 장착한 보틀 용기에 수용하여, 각각 제조예 9-3-1 ∼ 9-3-8 의 의약 제제 (로션제) 로 하였다.
제조예 9-4 (로션제)
통상적인 방법에 의해, 상기 표 78 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 액상의 조성물 (처방예 9 ∼ 16) 을 제조하고, 폴리에틸렌제의 용기 본체의 개구부에 스펀지상의 저밀도 폴리에틸렌제 도포 부재 (MAPS : (주) 이노악 코퍼레이션) 를 장착한 보틀 용기에 수용하여, 각각 제조예 9-4-1 ∼ 9-4-8 의 의약 제제 (로션제) 로 하였다.
제조예 9-5 (겔제)
통상적인 방법에 의해, 하기 표 79 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 17 ∼ 24) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 알루미늄박, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 9-5-1 ∼ 9-5-8 의 의약 제제 (겔제) 로 하였다.
제조예 9-6 (크림제)
통상적인 방법에 의해, 하기 표 80 에 기재된 성분 및 분량 (g) 을 100 g 중에 함유하는 반고형상의 조성물 (처방예 25 ∼ 32) 을 제조하고, 저밀도 폴리에틸렌제의 필름을 최내층으로 하고 그 외측 (중간층) 에 나일론제의 필름, 추가로 그 외측에 저밀도 폴리에틸렌제의 필름을 적층한 라미네이트 필름제의 튜브 용기 (라미네이트 튜브) 에 수용하여, 각각 제조예 9-6-1 ∼ 9-6-8 의 의약 제제 (크림제) 로 하였다.
제조예 9-7 (경구 액제)
통상적인 방법에 의해, 하기 표 81 에 기재된 성분 및 분량 (㎎) 을 30 ㎖ 중에 함유하는 액상의 조성물 (처방예 33 ∼ 40) 을 제조하고, 폴리프로필렌제의 보틀 용기에 수용하여, 각각 제조예 9-7-1 ∼ 9-7-8 의 의약 제제 (경구 액제) 로 하였다.
산업상 이용가능성
본 발명에 의하면, 록소프로펜 또는 그 염을 함유하는 액상 또는 반고형상의 조성물의, 고온 보존시에 있어서의 변색을 억제할 수 있다. 따라서, 보존 안정성이 우수한, 록소프로펜 또는 그 염을 함유하는 의약을 제공할 수 있고, 의약품 산업 등에 있어서 바람직하게 이용할 수 있다.
Claims (24)
- 다음 성분 (A) 및 (B) :
(A) 록소프로펜 또는 그 염 ;
(B) 다음 성분 (B-1) ∼ (B-9) 의 어느 것 ;
(B-1) 테르펜류
(B-2) 아르니카속의 식물 또는 그 추출물
(B-3) 다가 알코올
(B-4) 셀룰로오스류
(B-5) 토코페롤류
(B-6) 글리시르레틴산류
(B-7) 하기 일반식 (1)
[화학식 1]
[식 (1) 중, X 는 단결합 또는 산소 원자를 나타내고, Y 는 메틴기 또는 질소 원자를 나타내고, R1 은 수소 원자, 수산기 또는 알킬기를 나타내고, R2 는 치환기를 가져도 되는 고리형 아미노기, 또는 치환기를 가져도 되는 아미노알킬기를 나타내고, R3 은 수소 원자 또는 할로겐 원자를 나타낸다.]
로 나타내는 화합물 또는 그 염
(B-8) 고추 또는 그 추출물
(B-9) 유기 아민
을 함유하는 액상 또는 반고형상의 조성물이, 폴리올레핀계 수지제 용기에 수용되어 이루어지는, 의약 제제. - 제 1 항에 있어서,
성분 (B) 가, 고리형의 테르페노이드인, 의약 제제. - 제 1 항 또는 제 2 항에 있어서,
성분 (B) 가, 시네올, 티몰, 테르피네올, 멘톨, 리모넨, 캠퍼 및 보르네올로 이루어지는 군에서 선택되는 1 종 이상인, 의약 제제. - 제 1 항에 있어서,
성분 (B) 가, 아르니카 또는 그 추출물인, 의약 제제. - 제 1 항 또는 제 4 항에 있어서,
성분 (B) 가, 아르니카, 아르니카 팅크 또는 아르니카 엑기스인, 의약 제제. - 제 1 항에 있어서,
성분 (B) 가, 에틸렌글리콜, 트리에틸렌글리콜, 프로필렌글리콜, 디프로필렌글리콜, 글리세린, 1,3-부틸렌글리콜, 에리트리톨, 자일리톨, 소르비톨, 만니톨, 1,2,6-헥산트리올, 폴리비닐알코올, 폴리에틸렌글리콜 및 폴리프로필렌글리콜로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, 의약 제제. - 제 1 항 또는 제 6 항에 있어서,
성분 (B) 가, 1,3-부틸렌글리콜인, 의약 제제. - 제 1 항에 있어서,
성분 (B) 가, 셀룰로오스에테르 유도체 또는 그 염인, 의약 제제. - 제 1 항 또는 제 8 항에 있어서,
성분 (B) 가, 하이프로멜로스인, 의약 제제. - 제 1 항에 있어서,
성분 (B) 가, 토코페롤, 토코페롤숙신산에스테르, 토코페롤아세트산에스테르 및 토코페롤니코틴산에스테르 그리고 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, 의약 제제. - 제 1 항 또는 제 10 항에 있어서,
성분 (B) 가, dl-α-토코페롤아세트산에스테르인, 의약 제제. - 제 1 항에 있어서,
성분 (B) 가, 글리시르레틴산, 글리실리진산 및 그들의 염으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, 의약 제제. - 제 1 항 또는 제 12 항에 있어서,
성분 (B) 가, 글리시르레틴산인, 의약 제제. - 제 1 항에 있어서,
성분 (B) 가, 에바스틴 및 그 염, 옥사토미드 및 그 염, 카르비녹사민 및 그 염, 클레마스틴 및 그 염, 클로르페니라민 및 그 염, 디페테롤 및 그 염, 디페닐피랄린 및 그 염, 디펜히드라민 및 그 염, 세티리진 및 그 염, 펙소페나딘 및 그 염, 베포타스틴 및 그 염, 그리고 호모클로르시클리진 및 그 염으로 이루어지는 군에서 선택되는 1 종 이상인, 의약 제제. - 제 1 항 또는 제 14 항에 있어서,
성분 (B) 가, 클로르페니라민 및 그 염, 그리고 디펜히드라민 및 그 염으로 이루어지는 군에서 선택되는 1 종 이상인, 의약 제제. - 제 1 항에 있어서,
성분 (B) 가, 고추, 고추 가루, 고추 연엑기스, 고추 건조 엑기스, 캡사이신 및 노난산바닐릴아미드로 이루어지는 군에서 선택되는 1 종 이상인, 의약 제제. - 제 1 항 또는 제 16 항에 있어서,
성분 (B) 가, 고추 연엑기스 및 노난산바닐릴아미드로 이루어지는 군에서 선택되는 1 종 이상인, 의약 제제. - 제 1 항에 있어서,
성분 (B) 가, 알칸올아민인, 의약 제제. - 제 1 항 또는 제 18 항에 있어서,
성분 (B) 가, 디이소프로판올아민, 디에탄올아민, 염산트리에탄올아민, 트리이소프로판올아민, 트리에탄올아민, 트로메타몰, 메글루민 및 모노에탄올아민으로 이루어지는 군에서 선택되는 1 종 또는 2 종 이상인, 의약 제제. - 제 1 항 내지 제 19 항 중 어느 한 항에 있어서,
폴리올레핀계 수지가, 폴리에틸렌 및 폴리프로필렌으로 이루어지는 군에서 선택되는 1 종 이상인, 의약 제제. - 제 1 항 내지 제 20 항 중 어느 한 항에 있어서,
용기가, 에어졸제용 용기, 펌프 스프레이제용 용기, 보틀 용기, 튜브 용기 또는 점안 용기인, 의약 제제. - 제 1 항 내지 제 20 항 중 어느 한 항에 있어서,
용기가, 이하의 (1) 또는 (2) :
(1) 용기 본체와 도포 부재를 구비하고, 상기 용기 본체에 수용된 조성물을 상기 도포 부재에 함침시켜 사용하는 용기 ;
(2) 유연성을 갖는 용기 본체와, 토출구를 구비하여 이루어지는 용기 ;
인, 의약 제제. - 제 1 항 내지 제 20 항 중 어느 한 항에 있어서,
용기가, 스펀지상의 도포 부재를 구비하는 보틀 용기, 또는 튜브 용기인, 의약 제제. - 제 1 항 내지 제 23 항 중 어느 한 항에 있어서,
외용 액제, 스프레이제, 연고제, 크림제, 겔제, 경구 액제, 시럽제 및 경구 젤리제로 이루어지는 군에서 선택되는 제형인, 의약 제제.
Applications Claiming Priority (27)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2015253246 | 2015-12-25 | ||
| JPJP-P-2015-253241 | 2015-12-25 | ||
| JP2015253241 | 2015-12-25 | ||
| JPJP-P-2015-253246 | 2015-12-25 | ||
| JP2015253243 | 2015-12-25 | ||
| JPJP-P-2015-253243 | 2015-12-25 | ||
| JP2016015132 | 2016-01-29 | ||
| JPJP-P-2016-015125 | 2016-01-29 | ||
| JP2016015125 | 2016-01-29 | ||
| JPJP-P-2016-015132 | 2016-01-29 | ||
| JPJP-P-2016-035600 | 2016-02-26 | ||
| JP2016035600 | 2016-02-26 | ||
| JPJP-P-2016-035613 | 2016-02-26 | ||
| JP2016035613 | 2016-02-26 | ||
| JPJP-P-2016-087660 | 2016-04-26 | ||
| JP2016087660 | 2016-04-26 | ||
| JPJP-P-2016-143059 | 2016-07-21 | ||
| JP2016143053 | 2016-07-21 | ||
| JPJP-P-2016-143053 | 2016-07-21 | ||
| JP2016143059 | 2016-07-21 | ||
| JP2016145922 | 2016-07-26 | ||
| JPJP-P-2016-145922 | 2016-07-26 | ||
| JPJP-P-2016-159906 | 2016-08-17 | ||
| JP2016159906 | 2016-08-17 | ||
| JPJP-P-2016-170471 | 2016-09-01 | ||
| JP2016170471 | 2016-09-01 | ||
| PCT/JP2016/088739 WO2017111167A1 (ja) | 2015-12-25 | 2016-12-26 | ロキソプロフェンを含有する医薬製剤 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20180098233A true KR20180098233A (ko) | 2018-09-03 |
Family
ID=59090591
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020187014745A Withdrawn KR20180098233A (ko) | 2015-12-25 | 2016-12-26 | 록소프로펜을 함유하는 의약 제제 |
Country Status (3)
| Country | Link |
|---|---|
| JP (5) | JPWO2017111167A1 (ko) |
| KR (1) | KR20180098233A (ko) |
| WO (1) | WO2017111167A1 (ko) |
Families Citing this family (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6847656B2 (ja) * | 2016-12-27 | 2021-03-24 | 小林製薬株式会社 | 外用組成物 |
| JP7412870B2 (ja) * | 2017-06-27 | 2024-01-15 | 小林製薬株式会社 | 外用組成物 |
| JP7412871B2 (ja) * | 2017-06-27 | 2024-01-15 | 小林製薬株式会社 | 外用組成物 |
| JP7086597B2 (ja) * | 2017-12-28 | 2022-06-20 | 小林製薬株式会社 | 外用組成物 |
| JP7098320B2 (ja) * | 2017-12-28 | 2022-07-11 | 小林製薬株式会社 | 外用組成物 |
| JP2019119686A (ja) * | 2017-12-28 | 2019-07-22 | 小林製薬株式会社 | 外用製剤 |
| JP7455509B2 (ja) * | 2017-12-28 | 2024-03-26 | 小林製薬株式会社 | 外用製剤 |
| JP7206043B2 (ja) * | 2017-12-28 | 2023-01-17 | 小林製薬株式会社 | 外用組成物 |
| JP7086596B2 (ja) * | 2017-12-28 | 2022-06-20 | 小林製薬株式会社 | 外用組成物 |
| JP7206042B2 (ja) * | 2017-12-28 | 2023-01-17 | 小林製薬株式会社 | 外用組成物 |
| JP7186026B2 (ja) * | 2018-06-27 | 2022-12-08 | 小林製薬株式会社 | 外用医薬組成物 |
| JP7226957B2 (ja) * | 2018-10-09 | 2023-02-21 | 小林製薬株式会社 | 外用医薬組成物 |
| JP7198625B2 (ja) * | 2018-10-09 | 2023-01-04 | 小林製薬株式会社 | 水性外用医薬組成物 |
| JP7488643B2 (ja) * | 2018-11-30 | 2024-05-22 | 興和株式会社 | ロキソプロフェンを含有する組成物 |
| JP7592396B2 (ja) * | 2019-03-25 | 2024-12-02 | 第一三共ヘルスケア株式会社 | ロキソプロフェン及び可溶化剤を含有する皮膚外用剤 |
| JP7667528B2 (ja) * | 2020-04-15 | 2025-04-23 | 大正製薬株式会社 | 医薬組成物 |
| JP7728228B2 (ja) * | 2021-04-27 | 2025-08-22 | 久光製薬株式会社 | ヘパリン類似物質含有ゲル組成物及びその粘度低下抑制方法 |
| TW202440139A (zh) * | 2022-12-23 | 2024-10-16 | 日商第一三共健康事業股份有限公司 | 含有選自由類肝素物質及洛索洛芬、其鹽及該些的水合物所組成的群組中至少一種的皮膚外用劑 |
| JP7558545B1 (ja) | 2023-05-26 | 2024-10-01 | 株式会社 雪の元本店 | ロキソプロフェン含有皮膚外用剤 |
| JP2025021161A (ja) | 2023-07-31 | 2025-02-13 | ロート製薬株式会社 | 乳化外用組成物 |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10120560A (ja) | 1996-08-26 | 1998-05-12 | Sankyo Co Ltd | ロキソプロフェン含有外用製剤 |
| JP2001199883A (ja) | 1999-11-10 | 2001-07-24 | Toko Yakuhin Kogyo Kk | 消炎鎮痛外用剤 |
| WO2006048939A1 (ja) | 2004-11-05 | 2006-05-11 | Lead Chemical Co., Ltd. | 非ステロイド消炎鎮痛薬を含有する非水系経皮吸収製剤 |
| WO2010103844A1 (ja) | 2009-03-11 | 2010-09-16 | 興和株式会社 | 鎮痛・抗炎症剤含有外用剤 |
| WO2013191293A1 (ja) | 2012-06-22 | 2013-12-27 | 興和株式会社 | ロキソプロフェンを含有する医薬組成物 |
| WO2014002599A1 (ja) | 2012-06-25 | 2014-01-03 | 興和株式会社 | 生薬等含有医薬組成物 |
| JP2014185132A (ja) | 2012-03-29 | 2014-10-02 | Kowa Company Ltd | ロキソプロフェンを含有する医薬組成物 |
| JP2015098469A (ja) | 2013-10-16 | 2015-05-28 | 興和株式会社 | トウガラシ含有医薬組成物 |
| JP2015110557A (ja) | 2013-11-01 | 2015-06-18 | 第一三共ヘルスケア株式会社 | ロキソプロフェンを配合する外用剤組成物 |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2001309986A (ja) * | 2000-05-01 | 2001-11-06 | Lion Corp | 塗布容器入り皮膚外用剤組成物 |
| US20100029704A1 (en) * | 2007-01-29 | 2010-02-04 | Medrx Co., Ltd. | Salt of nonsteroidal anti-inflammatory drug and organic amine compound and use thereof |
| JP6131522B2 (ja) * | 2011-03-25 | 2017-05-24 | 大正製薬株式会社 | ロキソプロフェン含有外用剤 |
| JP6224578B2 (ja) * | 2012-02-29 | 2017-11-01 | 興和株式会社 | ロキソプロフェン含有外用固形剤 |
| JP6114646B2 (ja) * | 2012-06-28 | 2017-04-12 | 興和株式会社 | ロキソプロフェン含有外用固形剤 |
| JP2014224110A (ja) * | 2013-04-25 | 2014-12-04 | 第一三共ヘルスケア株式会社 | ロキソプロフェン含有外用剤組成物 |
| JP6253495B2 (ja) * | 2013-04-25 | 2017-12-27 | 第一三共ヘルスケア株式会社 | ロキソプロフェンを含有する外用剤組成物 |
| JP6189668B2 (ja) * | 2013-07-31 | 2017-08-30 | 興和株式会社 | ロキソプロフェン含有外用塗布剤 |
| JP6467167B2 (ja) * | 2013-08-23 | 2019-02-06 | 第一三共ヘルスケア株式会社 | ロキソプロフェン配合外用剤組成物 |
| JP6420102B2 (ja) * | 2013-09-04 | 2018-11-07 | 興和株式会社 | ロキソプロフェン含有外用固形剤及び該外用固形剤の保存安定化剤 |
| JP2015083563A (ja) * | 2013-09-18 | 2015-04-30 | 第一三共ヘルスケア株式会社 | ロキソプロフェン配合皮膚外用液剤 |
-
2016
- 2016-12-26 WO PCT/JP2016/088739 patent/WO2017111167A1/ja not_active Ceased
- 2016-12-26 KR KR1020187014745A patent/KR20180098233A/ko not_active Withdrawn
- 2016-12-26 JP JP2017558332A patent/JPWO2017111167A1/ja active Pending
-
2022
- 2022-06-01 JP JP2022089588A patent/JP7367124B2/ja active Active
-
2023
- 2023-10-11 JP JP2023175697A patent/JP2023171546A/ja active Pending
-
2024
- 2024-02-19 JP JP2024023001A patent/JP2024045618A/ja active Pending
-
2026
- 2026-01-13 JP JP2026003806A patent/JP2026043010A/ja active Pending
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10120560A (ja) | 1996-08-26 | 1998-05-12 | Sankyo Co Ltd | ロキソプロフェン含有外用製剤 |
| JP2001199883A (ja) | 1999-11-10 | 2001-07-24 | Toko Yakuhin Kogyo Kk | 消炎鎮痛外用剤 |
| WO2006048939A1 (ja) | 2004-11-05 | 2006-05-11 | Lead Chemical Co., Ltd. | 非ステロイド消炎鎮痛薬を含有する非水系経皮吸収製剤 |
| WO2010103844A1 (ja) | 2009-03-11 | 2010-09-16 | 興和株式会社 | 鎮痛・抗炎症剤含有外用剤 |
| JP2014185132A (ja) | 2012-03-29 | 2014-10-02 | Kowa Company Ltd | ロキソプロフェンを含有する医薬組成物 |
| WO2013191293A1 (ja) | 2012-06-22 | 2013-12-27 | 興和株式会社 | ロキソプロフェンを含有する医薬組成物 |
| WO2014002599A1 (ja) | 2012-06-25 | 2014-01-03 | 興和株式会社 | 生薬等含有医薬組成物 |
| JP2015098469A (ja) | 2013-10-16 | 2015-05-28 | 興和株式会社 | トウガラシ含有医薬組成物 |
| JP2015110557A (ja) | 2013-11-01 | 2015-06-18 | 第一三共ヘルスケア株式会社 | ロキソプロフェンを配合する外用剤組成物 |
Non-Patent Citations (2)
| Title |
|---|
| 록소닌 (등록상표) 겔 1 % 의약품 인터뷰 폼 다이이치산쿄 주식회사 2010년 10월 개정 (제3판) |
| 제16 개정 일본 약국방 해설서 주식회사 히로카과 서점 제C-5359 ∼ 5364페이지 |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2017111167A1 (ja) | 2017-06-29 |
| JP2026043010A (ja) | 2026-03-11 |
| JP2022107739A (ja) | 2022-07-22 |
| JP2023171546A (ja) | 2023-12-01 |
| JP2024045618A (ja) | 2024-04-02 |
| JPWO2017111167A1 (ja) | 2018-11-29 |
| JP7367124B2 (ja) | 2023-10-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7367124B2 (ja) | ロキソプロフェンを含有する医薬製剤(弐) | |
| JP2025085789A (ja) | ロキソプロフェンを含有してなる医薬製剤(肆) | |
| JP6397100B2 (ja) | ロキソプロフェンを含有する医薬組成物3 | |
| JP6425767B2 (ja) | ロキソプロフェンを含有する医薬組成物<弐> | |
| JP2024098085A (ja) | トウガラシ含有医薬組成物(ご) | |
| JP7600294B2 (ja) | ロキソプロフェン含有の医薬製剤(さん) | |
| JP6189668B2 (ja) | ロキソプロフェン含有外用塗布剤 | |
| JP2022009982A (ja) | ロキソプロフェンを含有する医薬製剤(さん) | |
| JP2025092756A (ja) | ロキソプロフェンを含有する医薬製剤 | |
| JP7488643B2 (ja) | ロキソプロフェンを含有する組成物 | |
| JP2017155042A (ja) | ロキソプロフェン含有的医薬製剤 | |
| JP7260992B2 (ja) | 組成物 | |
| JP2018021027A (ja) | ロキソプロフェンを含有する医薬製剤 | |
| JP2018021004A (ja) | ロキソプロフェンを含有してなる医薬製剤 | |
| JP6420101B2 (ja) | ロキソプロフェンを含有する外用塗布剤 | |
| JP6114646B2 (ja) | ロキソプロフェン含有外用固形剤 | |
| JP2017197537A (ja) | ロキソプロフェン含む医薬の製剤 | |
| JP2018039775A (ja) | ロキソプロフェン含有医薬製剤 | |
| JP6876017B2 (ja) | オロパタジン含有水性組成物 | |
| JP2022028643A (ja) | 組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20180524 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PC1203 | Withdrawal of no request for examination | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |