KR20150036102A - 혈청 및 조직 생화학 마커로서 bag3 - Google Patents
혈청 및 조직 생화학 마커로서 bag3 Download PDFInfo
- Publication number
- KR20150036102A KR20150036102A KR20157001228A KR20157001228A KR20150036102A KR 20150036102 A KR20150036102 A KR 20150036102A KR 20157001228 A KR20157001228 A KR 20157001228A KR 20157001228 A KR20157001228 A KR 20157001228A KR 20150036102 A KR20150036102 A KR 20150036102A
- Authority
- KR
- South Korea
- Prior art keywords
- bag3
- seq
- rna
- cancer
- nucleotide
- Prior art date
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6893—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids related to diseases not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/46—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- C07K14/47—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
- C12Q1/686—Polymerase chain reaction [PCR]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6883—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material
- C12Q1/6886—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for diseases caused by alterations of genetic material for cancer
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57407—Specifically defined cancers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57407—Specifically defined cancers
- G01N33/57434—Specifically defined cancers of prostate
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57407—Specifically defined cancers
- G01N33/57438—Specifically defined cancers of liver, pancreas or kidney
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/574—Immunoassay; Biospecific binding assay; Materials therefor for cancer
- G01N33/57484—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites
- G01N33/57496—Immunoassay; Biospecific binding assay; Materials therefor for cancer involving compounds serving as markers for tumor, cancer, neoplasia, e.g. cellular determinants, receptors, heat shock/stress proteins, A-protein, oligosaccharides, metabolites involving intracellular compounds
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
- G01N33/6887—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids from muscle, cartilage or connective tissue
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2527/00—Reactions demanding special reaction conditions
- C12Q2527/101—Temperature
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/118—Prognosis of disease development
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/158—Expression markers
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2333/00—Assays involving biological materials from specific organisms or of a specific nature
- G01N2333/435—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans
- G01N2333/46—Assays involving biological materials from specific organisms or of a specific nature from animals; from humans from vertebrates
- G01N2333/47—Assays involving proteins of known structure or function as defined in the subgroups
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/32—Cardiovascular disorders
- G01N2800/324—Coronary artery diseases, e.g. angina pectoris, myocardial infarction
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/32—Cardiovascular disorders
- G01N2800/325—Heart failure or cardiac arrest, e.g. cardiomyopathy, congestive heart failure
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/70—Mechanisms involved in disease identification
- G01N2800/7095—Inflammation
Abstract
본 발명은 진단 생물학적 마커 분야에 대한 것이다. 특히 본 발명은 병리 상태의 진단용 생물학적 마커로서 BAG3 RNA 또는 그 단편의 용도에 대한 것이다. 게다가, 본 발명은 생물학적 샘플에서 BAG3 RNA 또는 그 단편의 레벨의 검출 및/또는 평가를 위한 특정 키트 및 방법에 대한 것이다.
Description
본 발명은 병리 상태의 진단에서 생화학 마커로서의 용도인 BAG3 RNA 또는 그 단편에 대한 것이다.
BAG3 (RefSeq: NP_ 004272; Gene ID 9531)는 특히 조면 소포체(rough endoplasmic reticulum)내에 농축된 74 kDa의 세포질 단백질(cytoplasmic protein)이다. BAG3 단백질은 BAG 도메인 (110-124 아미노산)으로 알려진 구조적 도메인을 통하여 열충격 단백질(heat shock protein) HSP70의 ATPase 도메인과 상호작용하는 코-샤페론(co-chaperones) 패밀리에 속한다. 상기 BAG 도메인에 추가하여, BAG3는 WW 도메인과 프롤린-풍부 반복 (proline-rich repeat, PXXP)을 포함하여 다른 단백질들과의 결합을 매개할 수 있다. 게다가, 두 개의 보존된 IPV (Ile-Pro-Val) 모티프(motif)는 상기 WW 및 PXXP 영역 사이에 위치하여 BAG3의 분자 샤페론의 HspB 패밀리의 멤버인 HspB8에의 결합을 매개할 수 있다. 그러므로, BAG3는, 그 멀티도메인 구조의 어댑터 특성(adaptor nature)으로 인하여, 다른 파트너 단백질과 상호작용할 수 있다. bag3 유전자 발현은 근세포(myocytes)를 포함하는 몇몇 정상 세포 타입(normal cell type)에서 항시적(constitutive)이며, 몇몇 일차 종양(primary tumour) 또는 종양 세포주(tumour cell line)에서 항시적이다. 게다가, 다양한 스트레스 인자(stressors)에 의하여 유도될 수 있다: 스트레스가 많은 자극은 스테레스-활성화 유전자들, 예를 들어 bag3의 발현에 관여하는 열충격 전사인자(heat shock transcription factor, HSF) 1을 활성화시킨다(Rosati A, Graziano V, De Laurenzi V, Pascale M, Turco MC. BAG3: a multifaceted protein that regulates major cell pathways. Cell Death Dis. 2011; 2: e141). BAG3는 세포 컨택스트(cell context)에 따라, Hsp70- 의존 또는 -비의존 방식으로, IKKγ, Bax 또는 BRAF와 같은 세포사멸(apoptosis)-조절 단백질의 레벨 또는 위치(localisation)를 조절함으로써 세포 생존 유지 역할을 수행하는 것이 밝혀졌다.
BAG3 단백질은 심근모세포 분화(cardiomyoblasts differentiation) 동안 발현되고 미오게닌(myogenin) 발현을 유지하는 것으로 보여진다. 이러한 발견은 후반 심장 발전(late heart development)에서 BAG3의 관여를 의미한다 (De Marco M, Turco MC, Rosati A. BAG3 protein is induced during cardiomyoblast differentiation and modulates myogenin expression. Cell Cycle. 2011; 10: 850-852). 게다가, 심장근육세포(cardiomyocytes)에서 BAG3는 Z-판(Z-disc)에서 위치하고, 근원섬유(myofibril) 구조를 안정화시키고 기계적 스트레스 동안 근원섬유의 인테그리티(myofibrillar integrity)를 가능한 한 보존시키는 액틴 캐핑 단백질(actin capping protein), CapZβ1과 상호작용한다. BAG3 돌연변이는 Z-판 어셈블리를 손상시킬 수 있고 스트레스-유도 세포사멸에 대한 민감성을 증가시킬 수 있다. 심장세포(cardiocytes) 및, 일반적으로 근육 세포(muscle cells)에서의 생존 및 근원섬유의 인테그리티(myofibrillar integrity)에 있어서의 BAG3의 역할과 부합하게, bag3 유전자에서의 돌연변이는 근원섬유 근질환(myofibrillar myopathy) 및 확장성 심근병증(dilated cardiomyopathy)의 몇몇 형태와 관련되어 있다.
지금까지, 세포질 BAG3 및 BAG3의 가용성 시리얼 형태 모두가 일반적으로 세포 생존뿐만 아니라 상이한 병리와 관련되는 것으로 발견되었다.
놀랍도록 특이적이고 민감한 방법에서 침습적 진단과 관련된 단점을 가지지 않고/않거나 그 병리의 조기 검출, 치료 효과 모니터, 합병증의 위험 예측, 유익한 후속 조치 수행이 가능하도록 하는, 그러한 병리의 빠른 동정이 가능하도록 하는 생물학적 마커의 동적에 대한 요구 및 중요성이 증가된다.
본 발명은 병리 상태(pathological state)의 진단에서 생화학 마커로서의 용도인 BAG3 RNA 또는 그 단편에 대한 것이다.
바람직하게, 상기 BAG3 RNA는 BAG3 mRNA이다.
본 발명의 바람직한 실시예에 따라 상기 진단은 인비트로(in vitro) 또는 엑스비보(ex vivo)이다.
본 발명의 다른 측면은 상기 진단의 수용체는 포유동물, 바람직하게 인간이다.
본 발명의 상세 설명에서 설명될 것이지만, 본 발명의 BAG-3 RNA 또는 그 단편의 용도는 심장병, 암, 당뇨병, 염증 및 피부, 신경, 뼈, 혈관 및 연결 조직의 염증관련질환으로부터 구성된 군으로부터 선택되는 병리 상태에 특이적인 이점을 가진다.
본 발명의 바람직한 실시예에 따라, 상기 심장병은 다음으로부터 선택된다: 협심증(angina pectoris), 경색전 협심증(pre-infarction angina), 심근경색증( myocardial infarction), 심부전(heart failure), 국소 빈혈(ischemia), 급성 관상동맥 질환(acute coronary disease), 급성심부전(acute heart failure), 만성심부전(chronic heart failure), 및 의인성 심장질환(iatrogenic heart disease).
본 발명의 다른 바람직한 실시예에 따라 상기 암은 다음으로부터 선택된다: 췌장암, 방광암 및 전립선암.
본 발명의 다른 실시예는 생물학적 샘플에서 BAG3 유전자 발현의 검출 및/또는 정량을 위한 키트로서, bag3 뉴클레오티드 서열 (SEQ ID NO 18)에 포함된 한 쌍의 단일-가닥 올리고뉴클레오티드 프라이머를 포함하는 것을 특징으로 한다.
바람직하게 상기 키트는 상기 bag3 뉴클레오티드 서열의 뉴클레오티드 1 내지 뉴클레오티드 360, 뉴클레오티드 466 내지 뉴클레오티드 1570, 또는 뉴클레오티드 1801 내지 뉴클레오티드 2533 중 어느 한 영역에 포함되는 뉴클레오티드 서열을 가지는 것으로부터 선택된 한 쌍의 프라이머를 포함한다.
본 발명의 더 바람직한 실시예는 상기 키트는 다음 서열을 갖는 것으로부터 선택된 한 쌍의 프라이머를 포함한다: SEQ ID NO. 1 및 SEQ ID NO. 2; SEQ ID NO. 3 및 SEQ ID NO. 4; SEQ ID NO. 5 및 SEQ ID NO. 6; SEQ ID NO. 7 및 SEQ ID NO. 8; SEQ ID NO. 9 및 SEQ ID NO. 10.
바람직하게, 상기 프라이머는 60 내지 75℃, 바람직하게 72℃의 어닐링 온도(annealing temperature)를 가진다.
바람직하게, 상기 프라이머 세트는 정량적 실시간 RT-PCR(quantitative real-time RT-PCR)에 의하여 BAG3 RNA 또는 그 단편의 검출 및/또는 정량에 적절하다.
본 발명의 바람직한 실시예에서, 상기 생물학적 샘플은 혈청, 혈장, 소변, 타액 또는 조직 샘플이다.
바람직하게, 상기 혈청, 혈장, 소변, 타액 또는 조직 샘플은 포유동물, 바람직하게 인간으로부터 획득된다.
본 발명의 다른 실시예에 따라, 상기 키트는 심장병, 암, 당뇨병, 염증, 및 피부, 신경, 뼈, 혈관 및 결합조직(connective tissues)의 염증관련질환으로 구성된 군으로부터 선택된 병리 상태의 진단에 특이적이다.
본 발명의 바람직한 실시예에 따라, 상기 심장병은 다음으로부터 선택된다: 협심증(angina pectoris), 경색전 협심증(pre-infarction angina), 심근경색증( myocardial infarction), 심부전(heart failure), 국소 빈혈(ischemia), 급성 관상동맥 질환(acute coronary disease), 급성심부전(acute heart failure), 만성심부전(chronic heart failure), 및 의인성 심장질환(iatrogenic heart disease).
본 발명의 다른 바람직한 실시예에 따라, 상기 암은 다음으로부터 선택된다: 췌장암, 방광암 및 전립선암.
본 발명의 다른 실시예는 생물학적 샘플에서 BAG3 RNA 또는 그 단편의 레벨을 검출 및 정량화 방법이고, 이는 다음 단계들을 포함한다:
a. 혈청, 혈장, 소변, 타액 또는 조직샘플로 구성된 생물학적 샘플 획득단계.
b. 상기 생물학적 샘플로부터 전체 RNA(total RNA) 추출 단계.
c. 정량적 실시간 RT-PCR에 의하여 상기 BAG3 RNA 또는 그 단편을 정량하는 단계.
바람직한 실시예에 따라, 본 발명의 방법은 다음의 추가 단계를 더 포함한다:
c. 생물학적 샘플로부터 획득된 수치를 참조 수치 또는 건강한 기증자로부터 획득된 수치와 비교하는 단계.
본 발명의 다른 바람직한 실시예에 따라 상기 혈청, 혈장, 소변, 타액 또는 조직샘플은 포유동물, 바람직하게 인간으로부터 획득된다.
본 발명의 방법에서 바람직한 실시예에 따라 상기 BAG3 RNA 또는 그 단편의 존재는 병리 상태와 관련된다.
바람직하게, 상기 병리 상태는 심장병, 암, 당뇨병, 염증 및 피부, 신경, 뼈, 혈관, 및 결합조직의 염증관련질환으로 구성된 군으로부터 선택된다.
바람직하게 상기 심장병은 다음으로부터 선택된다: 협심증(angina pectoris), 경색전 협심증(pre-infarction angina), 심근경색증( myocardial infarction), 심부전(heart failure), 국소 빈혈(ischemia), 급성 관상동맥 질환(acute coronary disease), 급성심부전(acute heart failure), 만성심부전(chronic heart failure), 및 의인성 심장질환(iatrogenic heart disease).
바람직하게 상기 암 질환은 다음으로부터 선택된다: 췌장암, 방광암 및 전립선암.
본 발명은 생물학적 샘플에서 BAG3 단백질의 검출을 위한 면역조직화학(IHC) 키트에 대한 것으로서, 여기에서 상기 생물학적 샘플은 바람직하게 BAG3-특이적 항체 및 상기 염색에 요구되는 프로브를 포함하는 시약을 포함하는 조직샘플이다.
본 발명의 특징 및 효과는 설명적이고 비-제한적 목적으로 주어된 실시예들로부터, 그리고 첨부된 도 1-9으로부터 하기 기재된 상세 설명에서 더 자세히 기재될 것이고, 여기에서:
도 1.
도 1a: 배양된 심장근육세포(cardiomyocytes)의 상청액(supernatant)에서 BAG3 단백질의 검출. 80%의 컨플루언시(confluency)로 인간(HCMa) 및 래트(H9c2) 심장근육세포가 10% FBS 존재 또는 부존재로 5% CO2 분위기, 37℃에서 16시간 동안 배양되었다. 상청액은 50 mM NaCl 및 0.05% IGEPAL 함유 버퍼에서 투석되고(dialyzed), 동결건조되고(lyophilized), 1 ml의 RIPA 버퍼(50 mM Tris HCl pH 7.6, 150 mM 염화나트륨(sodium chloride), 2 mM 소듐 오르소바나데이트(sodium orthovanadate), 4 mM EDTA, 10mM 소듐 피로포스페이트(sodium pyrophosphate), 1% NP-40, 0.1% 소듐 디옥시콜레이트(sodium deoxycholat))에서 재현탁되고, 웨스턴 블로팅(western blotting)에 의하여 항-BAG3 또는 항-GAPDH 항체로 분석되었다.
도 1b: 엑소사이트 소포(exocytic vesicle)에서 BAG3 단백질의 검출. H9c2 세포로부터 획득된 상청액은 순차적 원심분리가 수행되었다: (i) 세포 제거를 위하여, 2’000×g로 15분; (ii) 세포 파편(cellular debris)의 제거를 위하여, 10’000×g로 30분; (iii) 엑소사이트 소포를 침전시키기 위하여, 150’000×g로 90분. 상기 침전물은 150’000×g에서 90분 동안 PBS에서 한번 세척되고 웨스턴 블럿에 의하여 전체-세포 용해물(whole-cell lysate)와 비교로 항-BAG3 TOS-2 폴리클로날 항체로 분석되었다. Rab-4는 엑소사이트 소포를 위한 마커로서 분석되었다. 시토졸 단백질(cytosolic protein)인 GAPDH이 대조군으로 분석되었다.
도 1c: 두 명의 건강한 기증자(donor) 및 두 명의 만성심부전 환자의 혈청이 웨스턴 블로팅에서 항-BAG3 항체 TOS-2 폴리클로날 항체로 분석되었다.
도 1d: 두 명의 만성심부전 환자에서 획득된 밴드(Bands)가 겔로부터 추출되고 프로그램 MASCOT를 이용하여 질량분석(mass spectrometry)에 의하여 그것의 아이덴티티(identity)가 분석되었다.
도 2.
도 2a: CHF 환자로부터의 혈청에서 BAG3 단백질의 검출. BAG3 재조합 단백질 및 HCMa 세포의 전체 세포 용해물(whole-cell lysate)이 심부전 환자로부터 획득된 혈청 (1:40)으로 웨스턴 블로팅에 의하여 분석되었다. 건강한 기증자로부터의 혈청으로의 분석이 음성 대조군으로 수행되었다.
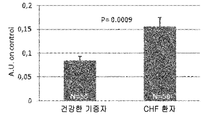
도 2b: ELISA 테스트에 의한 항-BAG3 항체의 검출. 50명의 (박출률 < 60%) CHF 환자들의 혈청을 특정 ELISA 테스트에서 항-BAG3 항체의 존재를 확인하기 위하여 50명의 건강한 기증자로부터의 혈청과 비교하였다. 결과는 임의 단위(arbitrary units)로서 표시되었다.
도 2c: ELISA 테스트 결과의 ROC 분석. 0.083 A.U. 에서의 컷-오프(cut-off)는 74% 민감도(sensitivity) 및 68% 특이성(specificity)으로 결론났다.
도 3.
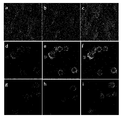
도 3a: HCMa 세포 (a, b, c) 및 J774 A1 세포 (d, e, f, g, h, i)에 결합하는 rBAG3-FITC의 검출을 위하여 수행된 직접 형광 공초점 현미경 분석(Confocal microscopy analysis). BAG3 재조합 단백질 및 정제된 BSA (SIGMA로부터 구입된 소혈청으로부터의 알부민)이 SIGMA로부터 구입된 FluoroTag FITC Conjugation Kit를 이용하여 제조자 지시에 따라 FITC에 결합되었다. 제조자 지시에 따라 계산된, 동량의 rBAG3-FITC (b, e) 및 BSA-FITC (h) 단백질이 0.1 % NaN3를 갖는 HCM 및 J774 A1 배양 미디어에 1시간 동안 첨가되었다. β-인테그린(integrin)이 대조군(a, d, g)으로서 분석되었다. 세포가 Zeiss LSM 공초점 현미경으로 분석되었다. 합성 이미지가 c, f 및 i으로 도시된다.
도 3b: BAG3는 대식세포(macrophages)에 결합한다. J774 A1 대식세포 (1×106 cells/ml)가 다른 농도의 Fitc-BAG3 단백질(7, 14 및 70 nm)로 배양되었다. FITC-BSA (70 nM)가 음성 대조군(회색)으로서 사용되었다. 세포 형광이 흐름세포측정(flow cytometry)으로 분석되었다.
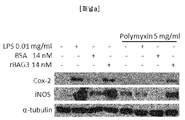
도 3c[패널 a] - BAG3로 배양된 J774 A1 대식세포에서 Cox-2 및 iNOS 레벨 분석. 80% 컨플루언시(confluency)에서 J774 A1 세포는 대조 배지(medium), BSA, LPS 또는 rBAG3으로 20시간 동안 배양되었다. 폴리믹신(Polymixin)이 대장균(E. coli)-유래 rBAG3의 효과가 내독소 오염의 존재로부터 독립적임을 증명하기 위하여 추가되었다. Cox-2 및 iNOS 발현은 웨스턴 블로팅에 의하여 세포 용해물(cell lysates)에서 분석되었다.
도 3d[패널 b] - BAG3로 배양된 J774 A1 대식세포로부터 방출된 아질산염(Nitrite)의 분석. 80% 컨플루언시에서 J774 A1 세포가 대조 배지, BSA, LPS 또는 rBAG3로 24시간 동안 배양되었다. 각 샘플로부터 100 μl의 상청액을 100 μl의 그리스 시약(Griess reagent)으로 배양하였고; 550 nm(OD550)에서 광학 밀도가 Beckman DU62 분광 측광기(spectrophotometer)로 측정되었다. 아질산염(Nitrite) 농도는 샘플의 OD550과 아질산나트륨(sodium nitrite)의 표준 곡선의 그것과 비교하여 평가하였다.
도 3e[패널 c] - BAG3로 배양된 J774 A1 대식세포로부터 방출된 IL-6의 분석. 80% 컨플루언시에서 J774 A1 세포가 대조 배지, BSA, LPS 또는 rBAG3로 5시간 동안 배양되었다. BAG3 펩티드 (펩티드 1, 펩티드 2, 펩티드 3, 펩티드 4, 또는 스크램블 펩티드(scrambled peptide)) 625 nM 가 추가되어 BAG3 활성 차단에 대한 그들의 능력을 증명하였다. IL-6 생산이 ELISA 테스트를 이용하여 세포 배양 배지에서 측정되었다. IL-6 농도는 샘플의 OD와 재조합 IL-6의 표준 곡선의 그것과 비교함으로써 평가되었다.
도 4.
도 4a:
정상 췌장 조직에서 모노클로날 항-BAG3 항체 AC-1을 이용한 BAG3 염색의 대표 이미지. 섹션들이 헤마톡실린로 대비염색되었다. 염색이 랑게르한스섬(Langerhans islets)의 보통의 확실성(moderate positivity)을 보여주고, 반면 정상 췌관(pancreatic ducts) 및 췌장 소엽 세포(pancreatic acinar cells)은 어떠한 BAG3 발현을 가지지 않았다.
도 4b: 바이오틴 부착 2차 항체(biotinylated secondary antibody)로 드러난 모노클로날 항-BAG3 항체를 이용하여 염색된 BAG3 낮은 양성(low positive) 및 BAG3 높은 양성(high positive) 종양 세포의 대표 이미지. 섹션들이 헤마톡실린로 대비염색되었다. 두 개의 서로 다른 확대배율이 도시된다: 100×(좌측 패널) 및 400× (우측 패널). 400× 확대배율을 이용하여 10개의 오버랩핑되지 않는 필드에서 전체 암 세포에 대한 양성 세포의 개수를 카운팅함으로써 상기 샘플에서 양성 암 세포의 비율에 기초하여 점수를 할당하였다. 상기 기재한 것처럼 계산된, BAG3 양성 세포의 중간 퍼센티지는 40%였고, 이 수치는 낮은 및 높은 양성 샘플을 분리하기 위한 컷-오프(cut-off)로서 이용되었다.
도 4c:
생존 곡선(Survival curves)이 낮은 BAG3 염색(양성 세포의 ≤40%)을 갖는 39명의 환자와 높은 BAG3 염색(양성 세포의 >40%)을 갖는 27명의 환자를 비교하여 작성되었다. 모든 환자들에 대하여 상기 췌장 선암 세포(pancreatic adenocarcinoma)의 RO 절제(R0 resection)가 수행되어 분석되었다. 생존 중앙값(Median survival)은 높은 양성 그룹에서 12개월부터 낮은 양성 그룹에서 23개월까지 증가한다. 로그-랭크 테스트 p-수치=0.0013
도 5.
몇몇 류마티스 관절염의 활액막 조직(synovial tissues)에서 염색된 BAG3 대표 이미지. BAG3 양성이 활액막 섬유아세포(synovial fibroblasts) 및 염증 침윤(inflammatory infiltrates)에서 관찰되었다. 섹션들이 헤마톡실린로 대비염색되었다.
도 6.
음성 판정된 정상 유로시스티스(normal urocystis)에서, 그리고 종양 세포의 세포질의 BAG3에 대하여 높은 양성으로 판정된 이행 세포 방광 암종(transitional cell bladder carcinoma)에서 BAG3 염색의 대표 이미지. 섹션들이 헤마톡실린로 대비염색되었다.
도 7.
도 7a.
qRT-PCRd 의하여 평가된 bag3 mRNA 상대적 발현이 그래프에서 도시된다. 여기서 값은 평균 + S.D로 보고된다. 푸른선은 계산된 중앙값을 대표한다.
도 7b.
생존 분석이 모든 환자들에 있어서 qRT-PCRd로 분석되었다. 높은 bag3 발현을 갖는 13명의 환자들이 낮은 bag3 발현을 갖는 12명의 환자들(생존 중앙값 = 32.0 개월)에 비하여 더 짧은 생존 (생존 중앙값 = 19.0 개월)을 가졌다. 로그-랭크 테스트 p-수치 = 0.0198.
도 8.
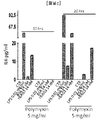
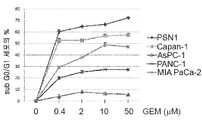
도 8a:
췌장암 세포주(PSN1, Capan-1, AsPC-1, PANC-1 및 MIA PaCa-2)가 그래프에서 표시된 것처럼 서로 다른 농도의 젬사이타빈(gemcitabine)으로 처리되었다. 48시간 후에, 아포프토시스 세포사멸(apoptotic cell death)이 분석되었다. 그래프는 Sub G0/G1 세포 (± S.D.)의 평균 퍼센티지를 도시한다. 데이터는 세 개의 독립된 실험을 대표한다.
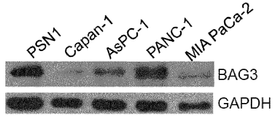
도 8b:
췌장암 세포주에서 BAG3의 웨스턴 블럿 분석; GAPDH 관리 단백질(housekeeping protein) 컨텐츠가 동일 로딩 조건을 모니터링하기 위하여 사용되었다.
도 8c:
MIA PaCa-2 및 PANC-1 세포주는 지시된 시간 동안 2 μM 젬사이타빈(GEM)으로 처리되어 BAG3 단백질 발현 레벨이 웨스턴 블럿으로 모니터링되었다.
도 8d:
bag3 mRNA 레벨이 RT-PCR에 의하여 분석되었다; 그래프는 상대적인 bag3 mRNA 레벨 (± S.D.)을 나타내고 데이터는 세 개의 독립된 실험을 대표한다.
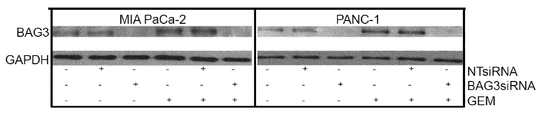
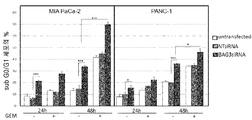
도 8e:
MIA PaCa-2 및 PANC-1 세포주는 72시간 동안 BAG3 siRNA 또는 비-타켓 siRNA (NTsiRNA)로 세포 감염시키고, 그 후 24시간 동안 2 μM 젬사이타빈(GEM)으로 처리되었다. BAG3 레벨이 웨스턴 블럿으로 분석되고 GAPDH 레벨이 동일 로딩 조건을 모니터링하기 위하여 측정되었다.
도 8f:
MIA PaCa-2 및 PANC-1 세포주는 상기 기재한 바와 같이 감염(transfected)되었고 24시간 또는 48시간 동안 2 μM 젬사이타빈(GEM)으로 처리되었다. 아포프토시스 세포사멸(apoptotic cell death) 상기 기재한 것과 같이 분석되었다. 그래프는 Sub G0/G1 세포 (± S.D.)의 평균 퍼센티지를 나타낸다. 데이터는 세 개의 독립된 실험을 대표한다.
도 9.
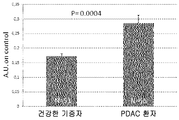
도 9a: ELISA 테스트에 의한 BAG3 특이적 면역-복합체의 검출. 특이적 ELISA 테스트에서 BAG3 특이적 면역-복합체의 존재를 위하여, 55명의 췌장 선암(pancreatic adenocarcinoma) 환자의 혈청이 51명의 건강한 기증자의 혈청과 비교하였다. 결과는 임의 단위 +S. E.로서 표시되었다.
도 9b: ELISA 테스트 결과의 ROC 분석. 0.183 A.U.의 컷-오프(Cut-off)는 65% 민감도 및 78% 특이성으로 나타났다.
도 10.
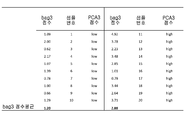
Bag3 점수는 내생 GAPDHdml 발현을 위하여 표준화(normalizing)한 후에, 상기 비교방법을 이용하여 상대 발현 레벨으로서, 각 샘플에서 계산되었다. 상기 bag3 점수의 평균은 2 그룹의 환자들에서 평가되었다: 낮은 PCA3 점수 환자들 및 높은 PCA3 점수 환자들. 상기 두 그룹 사이의 차이는 스튜던트 t 테스트(student t test)에 의하여 측정되어 중요하게 결론지어졌다: P = 0.001.
도 1.
도 1a: 배양된 심장근육세포(cardiomyocytes)의 상청액(supernatant)에서 BAG3 단백질의 검출. 80%의 컨플루언시(confluency)로 인간(HCMa) 및 래트(H9c2) 심장근육세포가 10% FBS 존재 또는 부존재로 5% CO2 분위기, 37℃에서 16시간 동안 배양되었다. 상청액은 50 mM NaCl 및 0.05% IGEPAL 함유 버퍼에서 투석되고(dialyzed), 동결건조되고(lyophilized), 1 ml의 RIPA 버퍼(50 mM Tris HCl pH 7.6, 150 mM 염화나트륨(sodium chloride), 2 mM 소듐 오르소바나데이트(sodium orthovanadate), 4 mM EDTA, 10mM 소듐 피로포스페이트(sodium pyrophosphate), 1% NP-40, 0.1% 소듐 디옥시콜레이트(sodium deoxycholat))에서 재현탁되고, 웨스턴 블로팅(western blotting)에 의하여 항-BAG3 또는 항-GAPDH 항체로 분석되었다.
도 1b: 엑소사이트 소포(exocytic vesicle)에서 BAG3 단백질의 검출. H9c2 세포로부터 획득된 상청액은 순차적 원심분리가 수행되었다: (i) 세포 제거를 위하여, 2’000×g로 15분; (ii) 세포 파편(cellular debris)의 제거를 위하여, 10’000×g로 30분; (iii) 엑소사이트 소포를 침전시키기 위하여, 150’000×g로 90분. 상기 침전물은 150’000×g에서 90분 동안 PBS에서 한번 세척되고 웨스턴 블럿에 의하여 전체-세포 용해물(whole-cell lysate)와 비교로 항-BAG3 TOS-2 폴리클로날 항체로 분석되었다. Rab-4는 엑소사이트 소포를 위한 마커로서 분석되었다. 시토졸 단백질(cytosolic protein)인 GAPDH이 대조군으로 분석되었다.
도 1c: 두 명의 건강한 기증자(donor) 및 두 명의 만성심부전 환자의 혈청이 웨스턴 블로팅에서 항-BAG3 항체 TOS-2 폴리클로날 항체로 분석되었다.
도 1d: 두 명의 만성심부전 환자에서 획득된 밴드(Bands)가 겔로부터 추출되고 프로그램 MASCOT를 이용하여 질량분석(mass spectrometry)에 의하여 그것의 아이덴티티(identity)가 분석되었다.
도 2.
도 2a: CHF 환자로부터의 혈청에서 BAG3 단백질의 검출. BAG3 재조합 단백질 및 HCMa 세포의 전체 세포 용해물(whole-cell lysate)이 심부전 환자로부터 획득된 혈청 (1:40)으로 웨스턴 블로팅에 의하여 분석되었다. 건강한 기증자로부터의 혈청으로의 분석이 음성 대조군으로 수행되었다.
도 2b: ELISA 테스트에 의한 항-BAG3 항체의 검출. 50명의 (박출률 < 60%) CHF 환자들의 혈청을 특정 ELISA 테스트에서 항-BAG3 항체의 존재를 확인하기 위하여 50명의 건강한 기증자로부터의 혈청과 비교하였다. 결과는 임의 단위(arbitrary units)로서 표시되었다.
도 2c: ELISA 테스트 결과의 ROC 분석. 0.083 A.U. 에서의 컷-오프(cut-off)는 74% 민감도(sensitivity) 및 68% 특이성(specificity)으로 결론났다.
도 3.
도 3a: HCMa 세포 (a, b, c) 및 J774 A1 세포 (d, e, f, g, h, i)에 결합하는 rBAG3-FITC의 검출을 위하여 수행된 직접 형광 공초점 현미경 분석(Confocal microscopy analysis). BAG3 재조합 단백질 및 정제된 BSA (SIGMA로부터 구입된 소혈청으로부터의 알부민)이 SIGMA로부터 구입된 FluoroTag FITC Conjugation Kit를 이용하여 제조자 지시에 따라 FITC에 결합되었다. 제조자 지시에 따라 계산된, 동량의 rBAG3-FITC (b, e) 및 BSA-FITC (h) 단백질이 0.1 % NaN3를 갖는 HCM 및 J774 A1 배양 미디어에 1시간 동안 첨가되었다. β-인테그린(integrin)이 대조군(a, d, g)으로서 분석되었다. 세포가 Zeiss LSM 공초점 현미경으로 분석되었다. 합성 이미지가 c, f 및 i으로 도시된다.
도 3b: BAG3는 대식세포(macrophages)에 결합한다. J774 A1 대식세포 (1×106 cells/ml)가 다른 농도의 Fitc-BAG3 단백질(7, 14 및 70 nm)로 배양되었다. FITC-BSA (70 nM)가 음성 대조군(회색)으로서 사용되었다. 세포 형광이 흐름세포측정(flow cytometry)으로 분석되었다.
도 3c[패널 a] - BAG3로 배양된 J774 A1 대식세포에서 Cox-2 및 iNOS 레벨 분석. 80% 컨플루언시(confluency)에서 J774 A1 세포는 대조 배지(medium), BSA, LPS 또는 rBAG3으로 20시간 동안 배양되었다. 폴리믹신(Polymixin)이 대장균(E. coli)-유래 rBAG3의 효과가 내독소 오염의 존재로부터 독립적임을 증명하기 위하여 추가되었다. Cox-2 및 iNOS 발현은 웨스턴 블로팅에 의하여 세포 용해물(cell lysates)에서 분석되었다.
도 3d[패널 b] - BAG3로 배양된 J774 A1 대식세포로부터 방출된 아질산염(Nitrite)의 분석. 80% 컨플루언시에서 J774 A1 세포가 대조 배지, BSA, LPS 또는 rBAG3로 24시간 동안 배양되었다. 각 샘플로부터 100 μl의 상청액을 100 μl의 그리스 시약(Griess reagent)으로 배양하였고; 550 nm(OD550)에서 광학 밀도가 Beckman DU62 분광 측광기(spectrophotometer)로 측정되었다. 아질산염(Nitrite) 농도는 샘플의 OD550과 아질산나트륨(sodium nitrite)의 표준 곡선의 그것과 비교하여 평가하였다.
도 3e[패널 c] - BAG3로 배양된 J774 A1 대식세포로부터 방출된 IL-6의 분석. 80% 컨플루언시에서 J774 A1 세포가 대조 배지, BSA, LPS 또는 rBAG3로 5시간 동안 배양되었다. BAG3 펩티드 (펩티드 1, 펩티드 2, 펩티드 3, 펩티드 4, 또는 스크램블 펩티드(scrambled peptide)) 625 nM 가 추가되어 BAG3 활성 차단에 대한 그들의 능력을 증명하였다. IL-6 생산이 ELISA 테스트를 이용하여 세포 배양 배지에서 측정되었다. IL-6 농도는 샘플의 OD와 재조합 IL-6의 표준 곡선의 그것과 비교함으로써 평가되었다.
도 4.
도 4a:
정상 췌장 조직에서 모노클로날 항-BAG3 항체 AC-1을 이용한 BAG3 염색의 대표 이미지. 섹션들이 헤마톡실린로 대비염색되었다. 염색이 랑게르한스섬(Langerhans islets)의 보통의 확실성(moderate positivity)을 보여주고, 반면 정상 췌관(pancreatic ducts) 및 췌장 소엽 세포(pancreatic acinar cells)은 어떠한 BAG3 발현을 가지지 않았다.
도 4b: 바이오틴 부착 2차 항체(biotinylated secondary antibody)로 드러난 모노클로날 항-BAG3 항체를 이용하여 염색된 BAG3 낮은 양성(low positive) 및 BAG3 높은 양성(high positive) 종양 세포의 대표 이미지. 섹션들이 헤마톡실린로 대비염색되었다. 두 개의 서로 다른 확대배율이 도시된다: 100×(좌측 패널) 및 400× (우측 패널). 400× 확대배율을 이용하여 10개의 오버랩핑되지 않는 필드에서 전체 암 세포에 대한 양성 세포의 개수를 카운팅함으로써 상기 샘플에서 양성 암 세포의 비율에 기초하여 점수를 할당하였다. 상기 기재한 것처럼 계산된, BAG3 양성 세포의 중간 퍼센티지는 40%였고, 이 수치는 낮은 및 높은 양성 샘플을 분리하기 위한 컷-오프(cut-off)로서 이용되었다.
도 4c:
생존 곡선(Survival curves)이 낮은 BAG3 염색(양성 세포의 ≤40%)을 갖는 39명의 환자와 높은 BAG3 염색(양성 세포의 >40%)을 갖는 27명의 환자를 비교하여 작성되었다. 모든 환자들에 대하여 상기 췌장 선암 세포(pancreatic adenocarcinoma)의 RO 절제(R0 resection)가 수행되어 분석되었다. 생존 중앙값(Median survival)은 높은 양성 그룹에서 12개월부터 낮은 양성 그룹에서 23개월까지 증가한다. 로그-랭크 테스트 p-수치=0.0013
도 5.
몇몇 류마티스 관절염의 활액막 조직(synovial tissues)에서 염색된 BAG3 대표 이미지. BAG3 양성이 활액막 섬유아세포(synovial fibroblasts) 및 염증 침윤(inflammatory infiltrates)에서 관찰되었다. 섹션들이 헤마톡실린로 대비염색되었다.
도 6.
음성 판정된 정상 유로시스티스(normal urocystis)에서, 그리고 종양 세포의 세포질의 BAG3에 대하여 높은 양성으로 판정된 이행 세포 방광 암종(transitional cell bladder carcinoma)에서 BAG3 염색의 대표 이미지. 섹션들이 헤마톡실린로 대비염색되었다.
도 7.
도 7a.
qRT-PCRd 의하여 평가된 bag3 mRNA 상대적 발현이 그래프에서 도시된다. 여기서 값은 평균 + S.D로 보고된다. 푸른선은 계산된 중앙값을 대표한다.
도 7b.
생존 분석이 모든 환자들에 있어서 qRT-PCRd로 분석되었다. 높은 bag3 발현을 갖는 13명의 환자들이 낮은 bag3 발현을 갖는 12명의 환자들(생존 중앙값 = 32.0 개월)에 비하여 더 짧은 생존 (생존 중앙값 = 19.0 개월)을 가졌다. 로그-랭크 테스트 p-수치 = 0.0198.
도 8.
도 8a:
췌장암 세포주(PSN1, Capan-1, AsPC-1, PANC-1 및 MIA PaCa-2)가 그래프에서 표시된 것처럼 서로 다른 농도의 젬사이타빈(gemcitabine)으로 처리되었다. 48시간 후에, 아포프토시스 세포사멸(apoptotic cell death)이 분석되었다. 그래프는 Sub G0/G1 세포 (± S.D.)의 평균 퍼센티지를 도시한다. 데이터는 세 개의 독립된 실험을 대표한다.
도 8b:
췌장암 세포주에서 BAG3의 웨스턴 블럿 분석; GAPDH 관리 단백질(housekeeping protein) 컨텐츠가 동일 로딩 조건을 모니터링하기 위하여 사용되었다.
도 8c:
MIA PaCa-2 및 PANC-1 세포주는 지시된 시간 동안 2 μM 젬사이타빈(GEM)으로 처리되어 BAG3 단백질 발현 레벨이 웨스턴 블럿으로 모니터링되었다.
도 8d:
bag3 mRNA 레벨이 RT-PCR에 의하여 분석되었다; 그래프는 상대적인 bag3 mRNA 레벨 (± S.D.)을 나타내고 데이터는 세 개의 독립된 실험을 대표한다.
도 8e:
MIA PaCa-2 및 PANC-1 세포주는 72시간 동안 BAG3 siRNA 또는 비-타켓 siRNA (NTsiRNA)로 세포 감염시키고, 그 후 24시간 동안 2 μM 젬사이타빈(GEM)으로 처리되었다. BAG3 레벨이 웨스턴 블럿으로 분석되고 GAPDH 레벨이 동일 로딩 조건을 모니터링하기 위하여 측정되었다.
도 8f:
MIA PaCa-2 및 PANC-1 세포주는 상기 기재한 바와 같이 감염(transfected)되었고 24시간 또는 48시간 동안 2 μM 젬사이타빈(GEM)으로 처리되었다. 아포프토시스 세포사멸(apoptotic cell death) 상기 기재한 것과 같이 분석되었다. 그래프는 Sub G0/G1 세포 (± S.D.)의 평균 퍼센티지를 나타낸다. 데이터는 세 개의 독립된 실험을 대표한다.
도 9.
도 9a: ELISA 테스트에 의한 BAG3 특이적 면역-복합체의 검출. 특이적 ELISA 테스트에서 BAG3 특이적 면역-복합체의 존재를 위하여, 55명의 췌장 선암(pancreatic adenocarcinoma) 환자의 혈청이 51명의 건강한 기증자의 혈청과 비교하였다. 결과는 임의 단위 +S. E.로서 표시되었다.
도 9b: ELISA 테스트 결과의 ROC 분석. 0.183 A.U.의 컷-오프(Cut-off)는 65% 민감도 및 78% 특이성으로 나타났다.
도 10.
Bag3 점수는 내생 GAPDHdml 발현을 위하여 표준화(normalizing)한 후에, 상기 비교방법을 이용하여 상대 발현 레벨으로서, 각 샘플에서 계산되었다. 상기 bag3 점수의 평균은 2 그룹의 환자들에서 평가되었다: 낮은 PCA3 점수 환자들 및 높은 PCA3 점수 환자들. 상기 두 그룹 사이의 차이는 스튜던트 t 테스트(student t test)에 의하여 측정되어 중요하게 결론지어졌다: P = 0.001.
본 발명은 병리 상태의 진단에서 생화학적 마커로서의 용도로서 BAG3 RNA 또는 그 단편에 대한 것이다.
본 발명에서 용어 "BAG3 RNA 단편(BAG3 RNA fragment)"은 150-300 뉴클레오티드의 단편을 의미한다.
본 발명에서 용어 "진단(diagnosis)" 은 가능한 질병 또는 질환을 결정 또는 확인하기 위하여 시도되는 절차를 의미하는 의료적 진단(종종 단순히 진단으로 기재됨)을 의미한다. 본 발명의 진단은 또한 초기 진단(early diagnosis)을 포함한다.
용어 "초기 진단"은 특이적 또는 비특이전 증상 전에 병리 상태를 식별하기 위한 테스트의 능력을 의미한다.
항-BAG3 항체는 혈청에서 현저하게 검출되었다. 지금까지 그러한 항체들이 생리학적 또는 병리 상태의 혈청에서 발견되지 않았다. 혈청 내의 항-BAG3 항체의 검출은 치료 모니터링 및 식별을 위한 툴로서, 진단, 초기 진단 및 예후 목적(prognostic purposes), 예후 판정(risk stratification)을 위하여 이용되는 빠르고 비-침습적 기술의 이점을 가진다.
본 발명에 있어서, 혈청(serum)은 혈액 세포(blood cell) 또는 응혈 인자(clotting factor)가 아닌 혈액의 성분인 것으로 의도된다; 그것은 피브리노겐(fibrinogens)이 제거된 혈장(blood plasma)이다. 혈청은 혈액 응고(blood clotting, coagulation)에 사용되지 않는 모든 단백질과 모든 전해액(electrolytes), 항체, 항원, 호르몬 및 어떠한 외인성 물질(exogenous substances)을 포함한다.
본 발명에 있어서, 혈장(plasma)은 상청액의 전체 혈액에서 상기 혈액 세포를 정상적으로 가지는 혈액의 밀짚-컬러/옅은-황색(straw-colored/pale-yellow) 액체 성분인 것으로 의도된다. 이는 피브리노겐과 같은 응혈 인자를 포함한다.
다른 실시예에서, 본 발명은 생화학적 마커로서 항-BAG3 항체의 용도를 제공하고, 여기에서 상기 항-BAG3 항체는 가용성 BAG3(soluble BAG3)에 결합하여 면역 복합체를 형성한다.
가용성 BAG3에 결합하거나 결합하지 않고 면역 복합체를 형성하는 항-BAG3 항체는 생물학적 샘플에서 지금 효과적으로 검출될 수 있고, 병리 상태의 진단에서 마커로서 사용될 수 있다. 생물학적 샘플 내의 그러한 항체 및/또는 면역 복합체의 검출은 또한 진단 및/또는 예후 목적을 위한 빠르고 비-침습적 기술의 효과를 가진다.
본 발명에서, 면역 복합체 또는 단백질/항체 복합체는 항체의 가용성 항원에대한 필수적 결합으로 의도되고, 상기 결합된 항원은 특이적 에피토프(epitope)로서 작용하고, 항체로의 결합은 단일 면역 복합체로 지칭된다.
그러한 면역 복합체는 항체 검출을 위한 것으로 보여진 것과 동일한 이점을 가지는데, 혈청의 매우 적은 양이 상기 면역 복합체의 검출에 요구되기 때문이다. 상기 가용성 BAG3의 검출에 요구되는 혈청의 양은, 상기 단백질/항체 (면역) 복합체의 검출에 요구되는 것보다 훨씬 더 크다. 자유 항체뿐만 아니라 면역 복합체는 특이적 질환의 초기 단계에서 검출가능하고 합병증의 위험을 효과적으로 예측가능하며 치료의 효과를 모니터링할 수 있도록 한다.
본 발명의 또 다른 실시예는 항-BAg3 항체 또는 상기 면역 복합체의 병리 상태의 생물학적 마커로서의 용도로서, 여기에서 상기 병리 상태는 심장병, 암, 당뇨병, 염증 및 피부, 신경, 뼈, 혈관 및 연결조직의 염증관련질환이다.
바람직하게 상기 심장병은 다음으로 구성되는 군으로부터 선택된다: 협심증(angina pectoris), 경색전 협심증(pre-infarction angina), 국소 빈혈(ischemia), 심근경색증( myocardial infarction), 심부전(heart failure), 급성 관상동맥 질환(acute coronary disease), 급성심부전(acute heart failure), 만성심부전(chronic heart failure), 및 의인성 심장질환(iatrogenic heart disease).
본 발명의 다른 실시예는 생물학적 샘플에서 항-BAG3 항체 또는 가용성 BAG3에 결합되어 면역 복합체를 형성하는 항-BAG3 항체의 존재 검출 방법으로서 다음 단계들을 포함한다:
a. 혈청, 혈장으로 구성된 생물학적 샘플을 획득하는 단계,
b. 상기 생물학적 샘플에서 항-BAG3 또는 BAG3 관련 항체의 존재를 결정하는 단계.
본 발명에 따른 방법은 건강한 대상자와 BAG3-관련 질환(병리)에 의하여 영향받은 환자 사이에서 항-BAG3 항체 및/또는 BAG3/항체 복합체 사이의 현저한 차이점을 검출하도록 하는 이점을 갖는다. 상기 제안된 분석 방법은 건강한 사람이 속한 집단으로부터 심장병 환자(cardiac patients) 집단을 통계적으로 현저히 구분이 되도록 한다. 또한 그러한 심장 질환을 가진 환자들을 위험도(심부전, HF)가 높은 서브 그룹의 환자들로 계층화할 수 있다.
다른 측면에서, 본 발명은 생물학적 샘플 내에서 항-BAG3 항체 또는 가용성 BAG3에 결합되어 면역 복합체를 형성하는 항-BAG3 항체의 존재 검출 방법으로서 다음 단계를 포함한다:
c. 상기 생물학적 샘플로부터 획득된 수치를 참조 수치 또는 건강한 기증자로부터 획득된 수치와 비교하는 단계.
바람직한 측면에서, 본 발명에 따른 방법은, 상기 결정 단계 b는 ELISA 테스트에 의하여 수행되는 방법이다.
본 발명에 따른 방법은 질환(병증, 또는 병리, pathologies)의 평가, 질환 위험 및/또는 그들의 합병증, 및 치료 모니터링을 가능하도록 하는 생물학적 마커의 빠르고 비-침습적 검출이 가능하도록 하는 이점을 가진다.
다른 측면에 따르면, 본 발명은 검출 방법에 대한 것으로서, 여기에서 상기 항-BAG3 항체 또는 가용성 BAG3에 결합되어 면역 복합체를 형성하는 상기 항-BAG3 항체의 존재는 병리 상태(pathological condition)와 관련된다.
바람직한 실시예에서, 상기 병리 상태는 심장병, 암, 당뇨병, 염증 및 피부, 신경, 뼈, 혈관 및 연결 조직의 염증 관련 질환으로 구성된 군으로부터 선택된다. 특히, 상기 심장병은 다음으로 구성되는 군으로부터 선택된다: 협심증(angina pectoris), 경색전 협심증(pre-infarction angina), 심근경색증( myocardial infarction), 심부전(heart failure), 급성 관상동맥 질환(acute coronary disease), 급성심부전(acute heart failure), 만성심부전(chronic heart failure), 또는 의인성 심장질환(iatrogenic heart disease).
본 발명은 또한 생물학적 샘플 내에서 항-BAG3 항체 또는 가용성 BAG3에 결합되어 면역 복합체를 형성하는 항-BAG3 항체의 검출을 위한 ELISA 키트에 대한 것이다.
본 발명에 따른 상기 ELISA 키트는 가용성 BAG3 및 인간 면역글로불린의 인식 가능한 항체를 캡쳐하기 위하여, 항-BAG3 항체 또는 BAG3-특이적 마우스 모노클로날 항체 AC-1, AC-2, AC-3, AC-4 및 AC-5의 캡쳐를 위한 BAG3 재조합 단백질을 포함한다.
상기 항체는 인간 면역글로불린의 인식 가능한 효소-링크 항체일 수 있다.
본 발명은 또한 생물학적 샘플에서 BAG3-관련 항체의 검출을 위한 키트에 대한 것이고, 인간 면역글로불린을 인식할 수 있는 검출을 위하여 가용성 BAG3 및 효소-링크 항체를 캡쳐링하는, BAG3-특이적 마우스 모노클로날 항체 AC-1, AC-2, AC-3, AC-4 및 AC-5로 ELISA에 의하여 수행된다.
본 발명은 또한 생물학적 샘플 내에서 BAG3 단백질의 검출을 위한 면역조직화학(Immunohistochemistry, IHC) 키트에 대한 것으로서, 여기에서 상기 생물학적 샘플은 바람직하게 조직 샘플이다. 조직 샘플은 생검(biopsies), 동결 조직(frozen tissues), 파라핀 포매 조직(paraffin embedded tissues)이다.
본 발명에 따른 상기 IHC 키트는 BAG3-특이적 항체 및 상기 염색에 요구되는 프로브를 포함하는 시약을 포함한다.
상기 BAG3-특이적 항체는 상기 검출을 위하여 마우스 면역글로불린을 인식할 수 있는 검출을 위한 마우스 모노클로날 항체(mouse monoclonal antibody) AC-1, AC-2 및 AC-3 및/또는 효소-링크 항체(enzyme-linked antibody)일 수 있다.
특히, 상기 IHC 키트는 췌장 절제(pancreas resection)를 겪은 환자로부터의 췌장 암종(pancreatic carcinoma) 조직 샘플 100%에서 BAG3 단백질을 효과적으로 드러내도록 하고, 방광 암종(bladder carcinoma) 샘플에서 가장 잘 발현된다.
게다가, BAG3 단백질은, 또한 랑게르한스섬(Langerhans islet)에 있는 정상 췌장 조직 내에서 IHC에 의한 BAG3 검출을 위한 키트로 드러나질 수 있는데, 반면, 다른 정상 조직(예를 들어 정상 유로시스티스(urocystis))은 음성으로 나타난다.
BAG3 양성은 또한 시노비알 섬유아세포(synovial fibroblasts) 및 류마티스 관절염(rheumatoid arthritis) 조직 샘플의 염증 침윤물(inflammatory infiltrates)에서 관찰될 수 있다.
PDAC이 발병된 환자들의 장기간 생존이 매우 미미하다: 오직 환자의 약 4%가 진단 후 5년 생존할 것이다. 정말로, 외과적 절제가 현재 유일한 치료 방법이고, 그러나 약 20%의 환자들만이 절제가능한 질환(resectable disease)으로 진단된다; 게다가, 그러한 환자들의 큰 부분 집합(약 80%)에서 전이 과정이 이미 진단에서 일어나고, 외과적 절제 후에 정말로 원격 전이(distant metastases)가 나타난다. 그러므로 췌장암의 발전에서 초기 단계에 대한 더 나은 이해가 요구되고 그들을 검출하도록 할 수 있는 분자를 동정할 필요가 있다. 또한, 더 나은 예후(prognosis)와 치료 선택을 도와줄 수 있는 마커들이 많이 요구된다.
상기 BAG3 IHC 키트는 PDAC 환자의 예후(prognosis)를 효과적으로 식별하도록 한다. IHC에 의하여 식별된 BAG3 발현의 강도는 환자의 생존과 상관관계 있는 것으로 확인되었다. 그러므로 이는 예후 및 치료 선택을 위하여 사용될 수 있다.
본 발명의 다른 실시예는 병리 상태의 진단에서 생화학적 마커로서의 용도를 가지는 BAG3 RNA 또는 그 단편이다.
바람직하게, 상기 BAG3 RNA는 BAG3 mRNA이다.
상기 BAG3 RNA는 SEQ ID N. 18(Reference: NCBI PubMed, XM 055575.1 Homo sapiens BCL2-associated athanogene 3 (BAG3) mRNA)의 BAG3 뉴클레오티드 서열에 대응한다.
SEQ ID NO: 18.
1gcggagctcc gcatccaacc ccgggccgcg gccaactttt
ttggactgga ccagaagttt ctagccggcc agttgctacc
tccctttatc tcctccttcc cctctggcag cgaggaggct
atttccagac acttccaccc ctctctggcc acgtcacccc
cgcctttaat tcataaaggt gcccggcgcc ggcttcccgg
acacgtcggc ggcggagagg ggcccacggc ggcggcccgg
ccagagactc ggcgcccgga gccagcgccc cgcacccgcg
ccccagcggg cagaccccaa cccagcatga gcgccgccac
ccactcgccc atgatgcagg tggcgtccgg caacggtgac
cgcgaccctt tgccccccgg atgggagatc aagatcgacc
cgcagaccgg ctggcccttc ttcgtggacc acaacagccg
caccactacg tggaacgacc cgcgcgtgcc ctctgagggc
cccaaggaga ctccatcctc tgccaatggc ccttcccggg
agggctctag gctgccgcct gctagggaag gccaccctgt
gtacccccag ctccgaccag gctacattcc cattcctgtg
ctccatgaag gcgctgagaa ccggcaggtg caccctttcc
atgtctatcc ccagcctggg atgcagcgat tccgaactga
ggcggcagca gcggctcctc agaggtccca gtcacctctg
cggggcatgc cagaaaccac tcagccagat aaacagtgtg
gacaggtggc agcggcggcg gcagcccagc ccccagcctc
ccacggacct gagcggtccc agtctccagc tgcctctgac
tgctcatcct catcctcctc ggccagcctg ccttcctccg
gcaggagcag cctgggcagt caccagctcc cgcgggggta
catctccatt ccggtgatac acgagcagaa cgttacccgg
ccagcagccc agccctcctt ccaccaagcc cagaagacgc
actacccagc gcagcagggg gagtaccaga cccaccagcc
tgtgtaccac aagatccagg gggatgactg ggagccccgg
cccctgcggg cggcatcccc gttcaggtca tctgtccagg
gtgcatcgag ccgggagggc tcaccagcca ggagcagcac
gccactccac tccccctcgc ccatccgtgt gcacaccgtg
gtcgacaggc ctcagcagcc catgacccat cgagaaactg
cacctgtttc ccagcctgaa aacaaaccag aaagtaagcc
aggcccagtt ggaccagaac tccctcctgg acacatccca
attcaagtga tccgcaaaga ggtggattct aaacctgttt
cccagaagcc cccacctccc tctgagaagg tagaggtgaa
agttccccct gctccagttc cttgtcctcc tcccagccct
ggcccttctg ctgtcccctc ttcccccaag agtgtggcta
cagaagagag ggcagccccc agcactgccc ctgcagaagc
tacacctcca aaaccaggag aagccgaggc tcccccaaaa
catccaggag tgctgaaagt ggaagccatc ctggagaagg
tgcaggggct ggagcaggct gtagacaact ttgaaggcaa
gaagactgac aaaaagtacc tgatgatcga agagtatttg
accaaagagc tgctggccct ggattcagtg gaccccgagg
gacgagccga tgtgcgtcag gccaggagag acggtgtcag
gaaggttcag accatcttgg aaaaacttga acagaaagcc
attgatgtcc caggtcaagt ccaggtctat gaactccagc
ccagcaacct tgaagcagat cagccactgc aggcaatcat
ggagatgggt gccgtggcag cagacaaggg caagaaaaat
gctggaaatg cagaagatcc ccacacagaa acccagcagc
cagaagccac agcagcagcg acttcaaacc ccagcagcat
gacagacacc cctggtaacc cagcagcacc gtagcctctg
ccctgtaaaa atcagactcg gaaccgatgt gtgctttagg
gaattttaag ttgcatgcat ttcagagact ttaagtcagt
tggtttttat tagctgcttg gtatgcagta acttgggtgg
aggcaaaaca ctaataaaag ggctaaaaag gaaaatgatg
cttttcttct atattcttac tctgtacaaa taaagaagtt
gcttgttgtt tcagaagttt aaccccgttg cttgttctgc
agccctgtct acttgggcac ccccaccacc tgttagctgt
ggttgtgcac tgtcttttgt agctctggac tggaggggta
gatggggagt caattaccca tcacataaat atgaaacatt
tatcagaaat gttgccattt taatgagatg attttcttca
tctcataatt aaaatacctg actttagaga gagtaaaatg
tgccaggagc cataggaata tctgtatgtt ggatgacttt
aatgctacat ttt
BAG3 RNA 또는 그 단편은 혈청, 혈장, 소변, 타액 또는 조직 샘플에서 유리하게 검출된다. 지금까지 그러한 BAG3 RNA는 생리학적 또는 병리 상태에서 상기 언급된 생물학적 샘플에서 발견되지 못하였다. 혈청, 및 다른 생물학적 샘플, 예를 들어 혈장, 소변, 타액 또는 조직에서 BAG3 RNA 또는 그 단편의 검출은 상기 식별의 툴로서, 진단적, 초기 진단 및 예후 목적, 위험 계층 및 치료 모니터링을 위하여 활용되는 빠르고 비-침습적 기술의 이점을 가진다.
BAG3 RNA 또는 그 단편의 검출 및 정량의 다른 이점은 매우 적은 양의 샘플이 상기 검출에 요구되는 점이다.
본 발명의 바람직한 실시예에 따라 상기 진단은 인비트로(in vitro) 또는 엑스비보(ex vivo)이다.
본 발명의 다른 측면은 상기 진단의 수용자는 포유동물, 바람직하게 인간이다.
상세한 설명에 더 기재될 것이나, 본 발명의 BAG-3 RNA 또는 그 단편의 용도는 심장병, 암, 당뇨병, 염증, 및 피부, 신경, 뼈, 혈관 및 결합조직의 염증관련질환으로 구성된 군으로부터 선택되는 병리 상태에 특이적인 효과를 가진다.
본 발명의 바람직한 실시예에 따라, 상기 심장병은 다음으로부터 선택된다: 협심증(angina pectoris), 경색전 협심증(pre-infarction angina), 심근경색증( myocardial infarction), 심부전(heart failure), 국소빈혈(ischemia), 급성 관상동맥 질환(acute coronary disease), 급성심부전(acute heart failure), 만성심부전(chronic heart failure), 및 의인성 심장질환(iatrogenic heart disease).
본 발명의 다른 바람직한 실시예에 따라, 상기 암은 다음으로부터 선택된다: 췌장암, 방광암, 및 전립선암.
본 발명의 다른 실시예는, bag3 뉴클레오티드 서열 (SEQ ID NO 18)에 포함된 한 쌍의 단일-가닥 올리고뉴클레오티드 프라이머를 포함하는 것을 특징으로 하는 생물학적 샘플에서 BAG3 유전자 발현의 검출 및/또는 정량을 위한 키트이다.
바람직하게 상기 키트는, 상기 bag3 뉴클레오티드 서열의 뉴클레오티드 1 내지 뉴클레오티드 360, 뉴클레오티드 466 내지 뉴클레오티드 1570, 또는 뉴클레오티드 1801 내지 뉴클레오티드 2533 중 어느 하나의 영역(region)에 포함된 뉴클레오티드 서열을 가지는 것으로부터 선택된 한 쌍의 프라이머를 포함한다.
본 발명의 다른 바람직한 실시예는, 상기 키트는 다음 서열을 가지는 것으로부터 선택되는 한 쌍의 프라이머를 포함한다: SEQ ID NO. 1 및 SEQ ID NO. 2; SEQ ID NO. 3 및 SEQ ID NO. 4; SEQ ID NO. 5 및 SEQ ID NO. 6; SEQ ID NO. 7 및 SEQ ID NO. 8; SEQ ID NO. 9 및 SEQ ID NO. 10.
하기 기재되고 SEQ ID NO. 1 내지 SEQ ID NO. 10에 의하여 식별되는, 프라이머 세트 1 내지 5에 따른 특이적 프라이머 bag3 프라이머는 정량적 실시간 PCR(quantitative real-time PCR)에 의하여 BAG3 발현의 검출 및 정량이 가능하도록 한다.
프라이머 세트 1
fw: SEQ ID NO. 1: AACGGTGACCGCGACCCTTT;
rev: SEQ ID NO. 2: CCTTCCCTAGCAGGCGGCAG
프라이머 세트 2
fw: SEQ ID NO. 3: CCGGCTGGCCCTTCTTCGTG;
rev: SEQ ID NO. 4: CAGCCTAGAGCCCTCCCGGG
프라이머 세트 3
fw: SEQ ID NO. 5: GTCACCTCTGCGGGGCATGC;
rev: SEQ ID NO. 6: GGTGACTGCCCAGGCTGCTC
Primer set 4
fw: SEQ ID NO. 7: CCAGCCTCCCACGGACCTGA;
rev: SEQ ID NO. 8: CTGGTGACTGCCCAGGCTGC
프라이머 세트 5
fw: SEQ ID NO. 9: CAGGAGCAGCACGCCACTCC;
rev: SEQ ID NO. 10: TGGTCCAACTGGGCCTGGCT.
생물학적 샘플에서 bag3 mRNA 검출을 위한 RT-PCR 키트는, 환자의 생존과 bag3 유전자 발현 레벨을 연관짓도록 하며, 예후 및 치료 선택을 위하여 사용될 수 있다. 바람직하게 상기 생물학적 샘플은 혈청, 혈장, 소변, 타액 및 조직 샘플이다.
바람직하게, 상기 프라이머는 60 내지 75℃, 더욱 바람직하게 72℃의 어닐링 온도(annealing temperature)를 가진다.
바람직하게, 상기 프라이머 세트는 정량적 실시간 RT-PCR에 의하여 BAG3 RNA 또는 그 단편의 검출 및/또는 정량에 적절하다.
본 발명의 바람직한 실시예에서, 상기 생물학적 샘플은 혈청, 혈장, 소변, 타액 또는 조직 샘플이다.
바람직하게, 상기 혈청, 혈장, 소변, 타액 또는 조직 샘플은 포유동물, 바람직하게 인간으로부터 획득된다.
본 발명의 다른 실시예에 따라, 상기 키트는 심장병, 암, 당뇨병, 염증, 피부, 신경, 뼈, 혈관 및 결합조직의 염증관련질환으로 구성되는 군으로부터 선택된 병리 상태의 진단에 특이적이다.
본 발명의 바람직한 실시예에 따라, 상기 심장병은 다음으로부터 선택된다: 협심증(angina pectoris), 경색전 협심증(pre-infarction angina), 심근경색증( myocardial infarction), 심부전(heart failure), 국소 빈혈(ischemia), 급성 관상 동맥질환(acute coronary disease), 급성심부전(acute heart failure), 만성심부전(chronic heart failure), 및 의인성 심장질환(iatrogenic heart disease).
본 발명의 다른 바람직한 실시예에 따라, 상기 암은 다음으로부터 선택된다: 췌장암, 방광암 및 전립선암.
본 발명의 다른 실시예는, 생물학적 샘플에서 BAG3 RNA 또는 그 단편의 레벨을 검출 및 정량하는 방법으로서, 다음 단계들을 포함한다:
a. 혈청, 혈장, 소변, 타액 또는 조직으로 구성된 생물학적 샘플을 획득하는 단계.
b. 상기 생물학적 샘플로부터 전체 RNA를 추출하는 단계.
c. 정량적 실시간 RT-PCR에 의하여 상기 BAG3 RNA 또는 그 단편을 정량하는 단계.
분자 생물학에서, 생물학저 샘플에서 상기 RNA 레벨의 검출 또는 정량을 위한 다른 방법이 존재한다: 노던 블럿(Northern blot), RT-PCR, qRT-PCR, DNA-마이크로어레이(DNA-microarray).
실시간 폴리머라아제 연쇄 반응(real-time polymerase chain reaction), 또한 소위 정량적 실시간 폴리머라아제 연쇄 반응(quantitative real time polymerase chain reaction, qPCR) 또는 키네틱 폴리머라아제 연쇄 반응(kinetic polymerase chain reaction)은 폴리머라아제 연쇄 반응(PCR)에 기초한 실험실 기술로서, 타겟 DNA 분자의 증폭 및 동시에 정량하기 위하여 사용된다. DNA 샘플에서 하나 이상의 특이적 서열의 경우, 실시간-PCR은 검출 및 정량이 모두 가능하다. 상기 정량은 카피(copy)의 절대적인 개수 또는 DNA 입력 또는 추가적인 정규화 유전자로 정규화될 때 상대적인 양일 수 있다.
상기 절차는 폴리머라아제 연쇄 반응의 일반적인 원칙을 따른다; 그 핵심 특징은 증폭된 DNA는 실시간으로 반응 진행으로서 검출된다. 이는 상기 반응의 산물이 그 마지막에 검출되는 표준 PCR과 비교하여 새로운 접근이다. 실시간 PCR에서 산물의 검출을 위한 두 가지 일반적인 방법은: (1) 어떠한 이중-가닥 DNA에 삽입되는 비-특이적 형광 염색 및 (2) 상보적 DNA 타겟을 갖는 프로브의 혼성화(hybridization) 후에 오직 검출을 허여하는 형광 리포터로 레이블링된 올리고뉴클레오티드를 구성하는 서열-특이적 DNA 프로브이다.
빈번하게, 실시간 PCR은 세포, 조직 또는 생물학적 샘플 내에서 메신저 RNA(mRNA) 및 비-코딩 RNA을 정량하기 위하여 역전사(reverse transcription)와 결합된다.
실시간 역전사 PCR은 다음으로 나타낸다: qRT-PCR. 상기 약어 "RT-PCR"은 일반적으로 역전자 폴리머라아제 연쇄 반응을 의미한다.
바람직한 실시예에 따라, 본 발명의 방법은 다음의 추가 단계를 더 포함한다:
d. 생물학적 샘플로부터 획득된 수치를 참조 수치 또는 건강한 기증자로부터 획득된 수치와 비교하는 단계.
본 발명의 다른 실시예에 따라, 상기 혈청, 혈장, 소변, 타액 또는 조직 샘플은 포유동물, 바람직하게 인간으로부터 획득된다.
본 발명의 방법에서 바람직한 실시예에 따라, 상기 BAG3 RNA 또는 그 단편의 존재는 병리 상태와 관련된다.
바람직하게, 상기 병리 상태는 심장병, 암, 당뇨병, 염증 및 피부, 신경, 뼈, 혈관 및 결합조직의 염증관련질환으로 구성된 군으로부터 선택된다.
바람직하게 상기 심장병은 다음으로부터 선택된다: 협심증(angina pectoris), 경색전 협심증(pre-infarction angina), 심근경색증( myocardial infarction), 심부전(heart failure), 국소 빈혈(ischemia), 급성 관상동맥 질환(acute coronary disease), 급성심부전(acute heart failure), 만성심부전(chronic heart failure), 및 의인성 심장질환(iatrogenic heart disease).
바람직하게 상기 암은 다음으로부터 선택된다: 췌장암, 방광암 및 전립선암.
본 발명의 또 다른 측면은 항-BAG3 모노클로날 항체, 그 단편, 및 대식세포 활동을 차단할 수 있는 BAG3 단백질의 특이적 아미노산 서열에 대응하는 펩티드로 대표되고, 이에 따라 염증, 종양, 대식세포 활동 관련 다른 질환의 치료를 위하여 사용될 수 있다. 특히 도 3 및 표 I을 참조하라.
본 발명은 BAG3-특이적 마우스 모노클로날 항체 AC-1, AC-2 및 AC-3 또는 F(ab), F(ab’)2, F(ab)로 변형되거나 인간화(humanized)된 상기 항체들; 또는 다음과 같은 서열을 포함하는 펩티들의 용도에 대한 것이다:
PEP 1: DRDPLPPGWEIKIDPQ (SEQ ID NO. 11)
PEP2: SSPKSVATEERAAPS (SEQ ID NO. 12)
PEP3: DKGKKNAGNAEDPHT (SEQ ID NO. 13)
PEP4: NPSSMTDTPGNPAAP (SEQ ID NO. 14)
로서 가용성 BAG3 효과에 결합하거나 차단할 수 있는 분자들이다.
실시예들
실시예 1.
배양된 인간 주요 심장근육세포(human primary cardiomyocyte) 및 래트(rat) 심장근육세포 세포주 H9c2에서의 혈청 박탈(Serum deprivation)-유도 스트레스
심장근육세포(Cardiomyocytes)는 스트레스 요소에 대한 반응을 증가시키는 보호 요소를 방출하는 것으로 알려져 있다. 스트레스-유도 단백질, 예를 들어 Hsp70, Hp27, Hsp90 및 다른 것들이 비록 세포내 활성을 행사하더라도 스트레스에 대한 응답으로 분비될 수 있기에, 심장근육세포에 의한 BAG3 방출은 스트레스 조건에서 분석되었다. 이러한 목적을 위하여, 우리는 배양된 인간 주요 심장근육세포 또는 래트 심장근육세포 세포주 H9c2에서 혈청 박탈-유도 스트레스의 효과를 분석하였다. 도 1에서 도시된 바와 같이, 우리는 16시간 동안 혈청 박탈에 노출된 심장근육세포의 상청액에서 BAG3 단백질을 검출할 수 있었다(도 1a). 그 시점에, 세포 생존은 혈청 박탈에 의하여 영향을 받지 않았기에(결과 미기재), 우리는 BAG3 방출이 세포 괴사(cell necrosis) 때문일 것이라는 가설을 버렸다. 그럼에 따라, 우리는 엑소사이트 소포(exocytic vesicles)에 BAG3가 존재하는지 여부를 확인하였다. 분별 원심분리(differential centrifugation) 절차 (16)를 통하여 세포외 소포(extracellular vesicle)를 분리함으로써, 우리는 그들이 BAG3 단백질을 포함하고 있음을 발견하였다(도 1b).
BAG3의 가용성 형태의 존재를 증명하기 위하여, 우리는 만성 심부전(chronic heart failure, CHF)을 앓고 있는 환자들의 두 개의 혈청에서 그 존재를 조사하였다. 웨스턴 블럿 분석을 통하여, 우리는 항-BAG3 항체에 의하여 인식되는 밴드를 식별할 수 있었다. 우리는 상기 밴드를 잘라내어 그것을 질량 분석을 수행하여 그것의 정체를 확인하였다(도 1c). 이 증거는 상기 단백질이 세포외 형태(extracellular form)에서 검출될 수 있음을 확인하였다. 우리는 상기 단백질을 건강한 기증자의 혈청에선 검출할 수 없었다(도 1c).
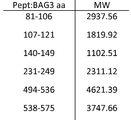
상기 전체 BAG3 단백질 서열 상에서 질량 분석에 의하여 인식되고 매치된 펩티들은 굵게 표시되었다:
MSAATHSPMM QVASGNGDRD PLPPGWEIKI DPQTGWPFFV
DHNSRTTTWN DPRVPSEGPK ETPSSANGPS REGSRLPPAR
EGHPVYPQLR PGYIPIPVLH EGAENRQVHP FHVYPQPGMQ
RFRTEAAAAA PQRSQSPLRG MPETTQPDKQ CGQVAAAAAA
QPPASHGPER SQSPAASDCS SSSSSASLPS SGRSSLGSHQ
LPRGYISIPV IHEQNVTRPA AQPSFHQAQK THYPAQQGEY
QTHQPVYHKI QGDDWEPRPL RAASPFRSSV QGASSREGSP
ARSSTPLHSP SPIRVHTVVD RPQQPMTHRE TAPVSQPENK
PESKPGPVGP ELPPGHIPIQ VIRKEVDSKP VSQKPPPPSE
KVEVKVPPAP VPCPPPSPGP SAVPSSPKSV ATEERAAPST
APAEATPPKP GEAEAPPKHP GVLKVEAILE KVQGLEQAVD
NFEGKKTDKK YLMIEEYLTK ELLALDSVDP EGRADVRQAR
RDGVRKVQTI LEKLEQKAID VPGQVQVYEL QPSNLEADQP
LQAIMEMGAV AADKGKKNAG NAEDPHTETQ QPEATAAATS
NPSSMTDTPG NPAAP(SEQ ID NO: 15).
인간 BAG3 단백질은 SEQ ID NO:15에 따른 아미노산 서열을 가진다.
실시예 2.
CHF 환자들의 혈청에서 항-BAG3 항체
우리는 제2 항체로서 항-인간 IgG를 이용하여, CHF 환자들의 혈청이 웨스턴 블럿팅으로 BAG3 단백질을 인식함을 발견하였다(세 명의 환자들로부터의 혈청에 대한 대표 실험의 결과가 도 2a에 도시된다). 상기 결과는 CHF 환자들의 혈청에서 항-BAG3 항체의 존재를 지시한다. 이 발견을 확인하기 위하여, 우리는 특정 ELISA 테스트로 항-BAG3 항체의 존재를 위하여, 50명의 건강한 기증자로부터의 혈청과 50 명의 CHF 환자들의 혈청(박출율 < 60%)를 분석하였다. 도 2b에서 도시된 바와 같이, 우리는 대조군의 혈청에 대비하여 환자들에서 현저하게 높은 항-BAG3 항체의 수치를 검출하였다. 컷-오프로서 0.083 A.U.를 이용하여, ELISA 테스트의 ROC 분석 결과는 74% 민감도 및 68% 특이성을 보였다(도 2c).
실시예 3.
대식세포에 결합하는 BAG3
우리는 심장근육세포에 의한 BAG3 방출의 기능적 중요성을 다루었다. 우리는 상기 단백질이 자가분비경로(autocrine pathway)에 관련될 수 있는 것을 배제하였다. 왜냐하면, 그것은 명확히 상기 심장근육세포의 표면에 결합하지 않았기에 우리는 형광 이소티오시아네이트(fluorescein isothiocyanate, FITC)-접합 BAG3를 이용한 실험에서 평가하였다(도 3a). 그러므로 우리는 BAG3가 혈액 세포와 상호작용할 수 있는지 여부를 조사하였다. 우리는 세포주 J774의 대식세포에 결합된 FITC-BAG3를 발견하였다(도 3b). 대식세포에 결합된 BAG3는 특이적으로 BAG3 펩티드 경쟁에 의하여 또는 항-BAG3 모노클로날 항체로부터 BAG3-격리 F(ab’)2 단편에 의하여 손상되었다 (표 I).
표 I
특히 J774 세포는 14 nM FITC-BAG3 단백질과 625nM의 BAG3 단백질 (펩티드 1, 펩티드 2, 펩티드 3, 펩티드 4 또는 스크램블 펩티드), 또는 항-BAG3 모노클로날 및 폴리클로날 항체(마우스 모노클로날 AC1, AC2 및 래빗 폴리클로날 TOS2)의 F(ab')2 단편 420nM으로 배양되었다. 마우스 IgG의 F(ab')2 단편 또는 래빗 IgG의 F(ab’)2 단편이 음성 대조군으로서 이용되었다.
대식세포에 결합하는 BAG3의 기능적 결과를 알아보기 위하여, 우리는 상기 세포에서 유도성 일산화질소 합성효소(inducible nitric oxide synthase, iNOS) 및 시클로옥시게나아제(cyclooxygenase, Cox)-2의 발현에 대한 재조합 BAG3의 효과를 시험하였다. 도 3c[패널 a]에서 도시된 바와 같이, 이들 효소들의 레벨이 BAG3-처리 대식세포에서 강화되었다. 게다가 BAG3는, 아질산염(nitrite) 및 인터루킨(IL)-6의 방출(도 3d[패널 b] 및 도 3e[패널 c])을 유도하였고, 이 결과는 상기 단백질에 대한 그들의 결합에 따라 대식세포가 활성되는 것을 확인시켜주었다.
CHF 환자들로부터의 혈청에서 우리는 항-BAG3 항체의 현저한 양을 검출할 수 있었다(도 2a, b). 자가항체 생산은, 예를 들어 항-트로포닌 자가항체(anti- troponin autoantibodies)를 생산하는 만성 국소빈혈 환자들에서 일어나는 것처럼, 정상적으로 세포내 단백질의 세포외 방출에 관련될 가능성이 있다. CHF 환자들의 혈청에서 항-BAG3 항체의 ELISA 수치는 건강한 대조군 혈청에서 검출된 것보다 현저히 높다.
그러므로, ELISA에 의하여 검출된, 항-BAG3 항체의 생산은 만성 심부전의 바이오마커가 된다. 위험 계층화(risk stratification) 및 치료 모니터링에 대한 그 유용성이 매우 가치있는 것으로 조사되었다.
스트레스받은 심장근육세포에 의한 BAG3 방출 및 대식세포의 연이은 활성이 NO의 국소적 방출을 이끌어 심장 허혈(heart ischemia)에서 보호회로(protective circuit)를 구성할 수 있다. 혈관확장(vasodilation), 혈관신생(neoangiogenesis) 및 리모델링이 타겟될 수 있다. BAG3 방출 및 그 일시적 또는 만성적 효과는 조사될 만하고 국소빈혈(ischemia) 및 다른 심장 스트레스 상태의 우리의 이해에 도움을 줄 수 있다.
게다가, BAG3-특이적 마우스 모노클로날 항체 AC-1, AC-2 및 AC-3 및/또는 F(ab), F(ab’)2, F(ab) 또는 인간화로 변형된 동일한 또는 다른 항체들; PEP 1 내지 4의 서열을 포함하는 펩티드 및/또는 다른 것들이 가용성 BAG3 효과에 결합 및/또는 차단할 수 있는 분자로서 염증, 종양, 대식세포 활동 관련 다른 질환의 치료를 위하여 사용될 수 있다.
실시예 4.
면역조직화학(immunohistochemistry)에 의한 PDAC에서 BAG3 발현
우리는 우리의 항-BAG3 모노클로날 항체를 포함하여 면역조직화학(IHC)에 의하여 BAG3 단백질의 검출이 가능한, 면역조직화학(IHC) 키트를 개발하였다. 상기 키트는 우리가 분석했던 모든 346 PDAC 생검(100%)에서 BAG3 발현을 드러냈다. 정상 췌장관(pancreatic ducts) 및 췌장 소엽(pancreatic acinar) 세포는 BAG3 발현을 가지지 않는 반면, BAG3 염색(staining)이 랑게르한스섬의 보통의 양성을 드러냈다. 이는 정상 췌장 및 종양 덩어리(tumor mass)에 인접한 비-종양(non-neoplastic) 췌장 조직에서도 마찬가지이다. BAG3 염색이 종양 세포의 세포질에서 우세하게 관찰되었다. BAG3 염색의 강도는 양성 암 세포의 개수만큼이나 다양하다. 게다가, 랑게르한스섬(Langerhans insulae)이 양성이고 IHC의 좋은 내부 대조군을 구성한다(도 4a). 그러므로 우리 키트는 IHC에 의하여 PDAC에서 BAG3 단백질의 검출이 가능하도록 한다. 게다가, 그것은 또한 다른 종양 또는 정상 조직에서 IHC에 의하여 BAG3 단백질이 검출되도록 한다.
우리는 또한 환자의 생존과의 상관관계에서, 치료에 대한 응답에서 BAG3의 발현을 조사하였다. 우리는 면역조직화학에 의하여 분석된 모든 종양 샘플의 데이터 및 생존 데이터로 분석된 RO 환자들의 서브그룹의 데이터를 표현하는, 같은 수의 환자들로부터 346 PDAC 샘플 집단(표 II)을 분석하였다; 우리는 400× 배율을 이용하여 10개의 비-오버랩 필드에서 총 암 세포에 대한 양성 세포의 개수를 카운팅함으로써 상기 샘플에서 양성 암 세포의 비율에 기초하여 점수를 할당하였다.
표 II
상기 기재한 것처럼 계산된 BAG3 양성 세포의 중앙 퍼센티지(median percentage)는 40%였고 이 수치는 낮은 및 높은 양성 샘플에 컷-오프로서 이용되었다. 이 분류에 기초하여 190개의 환자 샘플들 (55%)이 낮은 양성으로서 분류되고 (≤40%의 양성세포), 156 (45%)가 높은 양성으로 분류되었다(>40%의 양성 세포) (도 4, 패널 B). 상기 생존 분석은 시험된 모든 병변이 종양 세포 (RO)로부터 절제 경계가 없는 66명의 환자 집단에서 수행되었고, 오직 3.7%만이 떨어진 기관에 대한 전이(metastases)를 보였다 (표 II). 획득 데이터는 높은 BAG3 발현을 갖는 환자들이 낮은 BAG3 발현을 갖는 이들(생존 중앙값=23.0개월)(p=0.0013)보다 현저하게 짧은 생존 (생존 중앙값 = 12.0개월)을 보였다(도 4, 패널 C). 콕스 비례 분석(Cox proportional analysis)에 기초하여 높은 BAG3 발현이 두 배 이상의 더 높은 사망 위험과 관련되었다(표 III).
표 III
실시예 5.
치료에 대한 응답에서
BAG3
단백질
췌장암의 치료로 제1-라인 화학요법(first-line chemotherapy)이 젬시타빈(gemcitabine)이다. 치료에 따른 BAG3 단백질의 역할을 조사하기 위하여, 우리는 인간 PDAC 세포에서 BAG3-다운 조절의 효과를 분석하였다. 우리는 상기 세포를 bag3 mRNA을 타겟팅하는 특이적 siRNA로, 또는 비특이적(NT) siRNA로 감염시키고, 지시된 시간 동안 젬시타빈으로 세포를 처리하였다. BAG3 침묵이 상기 의약에 대한 응답에서 세포 사멸(cell apoptosis)을 강화하였다(도 8).
이러한 결과는, 췌장 선암(pancreatic adenocarcinoma)에서 BAG3 단백질 및 mRNA의 과발현을 나타내고, 높은 발현 레벨은 높은 사망 위험과 관계 있음을 나타내며, 따라서 BAG3는 예후 및 치료 선택에 유용한 마커의 역할을 담당한다. 게다가 이러한 결과는, BAG3 다운 조절이 PDAC 세포에서 사멸을 증대시킨다는 점을 보여준다. 모든 테스트된 병변에서 그것의 넓은 발현 및 췌장암 세포 생존의 유지에서의 그것의 관련성때문에, BAG3는 PDAC에서 혁신적인 치료를 위한 가치있는 타겟을 대표한다.
실시예 6.
췌장암 환자들의 혈청에서 BAG3 단백질
췌장아 환자들에서 그것의 넓은 발현으로 인하여, 우리는 BAG3가 췌장암 환자들의 형청에 존재하는지 여부를 조사하였다. 우리는 BAG3가 검출될 수 있음을 발견하였다. 또한 비록 널리 BAG3와 복합되지만 항-BAG3 항체가 검출가능하였다. 그러므로 우리는 BAG3/항체 복합체를 검출하기 위하여 ELISA를 개발하였다. 우리는 51명의 건강한 기증자로부터의 혈청과 PDAC를 앓고 있는 55명의 환자의 혈청을 분석하였다(표 IV).
표 IV
도 9a에서 도시된 바와 같이, (임의 단위로 측정된) 면역 복합체가 건강한 기증자로부터의 혈청에서보다 환자로부터의 혈청에서 현저하게 높았다. 게다가 ELISA 테스트의 ROC 분석 결과는, 컷-오프 0.183 A.U.를 이용하여, 65% 민감도 및 78% 특이성을 보였다(도 9b).
실시예 7.
정량적 실시간
PCR
(
quantitative
real
-
time
PCR
)에 의한
BAG3
발현
BAG3 발현에 대한 면역조직화학 데이터가 또한 25개의 PDAC 조직 샘플에서 bag3 mRNA 레벨을 측정하여 확인되었다 (표 V).
표 V
특히, 상기 분석 시에, 26명의 환자 중 16명이 생존한 반면, 췌장암 진행으로 9명의 환자가 사망하였다. 분석된 종양에서 bag3 mRNA의 발현 중앙값은 0.0068 (Q1=0.004; Q3=0.010)으로 세팅되었다(도 7, 패널 A).
PDAC 환자들의 고려된 모든 통계 및 임상 특징이 bag3 mRNA 레벨과 관련이 없었다. 그러므로, 생존과의 상호관련성이 평가되었고 PDAC 샘플에서 bag3 발현 레벨의 중앙값이 컷-오프로서 이용되어 높은 bag3 발현을 갖는 이들로부터 낮은 발현을 갖는 환자들을 구분하였다. 13개의 샘플 (52%)이 높은 bag3 양성으로 분류되고 12개의 샘플(48%)이 낮은 bag3 양성으로서 분류되었다. 높은 bag3 발현을 갖는 환자들은 낮은 bag3 발현을 갖는 이들(생존 중앙값 = 32.0 개월)보다 더 짧은 생존 (생존 중앙값 = 19.0 개월)을 가졌고, p-수치=0.0198이다 (도 7, 패널 B). 콕스 비례 분석에 기초하여 높은 bag3 발현은 6배 이상의 더 높은 사망 위험과 관련되었다(univariate: HR=6.094; 95% CI=1.105-33.597, p=0.038).
정량적 실시간 RT-PCR에 의한 BAG3 발현을 검출하는 bag3 프라이머. 우리는 bage mRNA 검출 및 정량을 위하여 특이적 프라이머를 함유하는 RT-PCR 키트를 개발하였다.
실시예
8
전립샘마사지(prostatic massage) 후에 1ml의 소변을 전립선암으로 진단된 남성 환자로부터 수집하였다. 전체 RNA는 소변으로부터 획득되고 bag3 RNA 레벨은 RT-PCR에 의하여 측정되었다. Bag3 점수는 내생 GAPDH의 발현을 위하여 정규화한 후에 비교법을 이용하여 상대적인 발현 레벨으로서 각 샘플에서 측정되었다. 보고된 표에서 bag3는 다른 PCA3 점수를 나타내는 두 개의 그룹 사이에서 비교되었다.
PCA3는 전립선암 조직에서 특이적으로 과발현되는 전립선 특이적 비-코딩 mRNA이다.
비뇨기의 PCA3 RNA 레벨은 전립선암 진단에서 중요한 역할을 제시하는 전립선암 등급과 관련되어 있다. PCA3 점수는 정량 폴리머라아제 연쇄 반응(qPCR) 기술을 이용하여 계산되었다; 특히 PCA3 및 PSA (전립선 특이적 항원, Prostate Specific Antigen) mRNA 분자는 증폭되어 상기 PCA3 점수는 1000 x [mRNA PCA3]/[mRNA PSA]와 동일하게 계산되었다 (참조: Bussemakers MJ, van Bokhoven A, Verhaegh GW, Smit FP, Karthaus HF, Schalken JA et al. DD3: a new prostate-specific gene, highly overexpressed in prostate cancer. Cancer Res 1999;59: 5975-9).
PCA3 점수 ≥ 35를 가지는 환자는 PCA를 가질 개연성이 높으며, 반복적 생검이 추천될 수 있다. 만약 결과가 음성 (PCA3 점수 < 35) 이면, 상기 환자는 PCA를 가질 개연성이 낮으며 반복적 생검이 환자의 적극적 감시/후속 조치(follow-up)로 지연될 수 있다. BAG3 점수는 bag3 점수 및 PCA3 점수 사이에서 유사한 트랜드를 보여준 두 개의 샘플 그룹에서 분석되고, 낮은 PCA3 점수를 갖는 환자들이 1.20의 BAG3 점수 평균과 관련있는 반면, 높은 PCA3 점수 환자들이 2.88의 BAG3 점수 평균과 관련된다. 상기 두 그룹 사이의 차이는 스튜던트 t 테스트(student t test)에 의하여 측정되고 현저하게 결론났다: P = 0.001.
상기 결론은 소변 샘플에서 bag3 RNA 결정이 전립선암으로 발전되는 위험 평가를 위한 신규한 툴을 대표할 수 있는 가능성을 제시한다.
방법들
세포 배양(
Cell
cultures
)
HCMa (Human Cardiac Myocytes-adult)는 사이언셀 연구소(Sciencell Research Laboratories, San Diego, CA)로부터 구입하여 심장 근세포 메디엄(Cardiac Myocyte Medium) (CMM, FBS 5%, 심장 근세포 성장 보충제(Cardiac Myocyte Growth Supplement) 1%, 페니실린/스트렙토마이신 용액 1%) (Sciencell Research Laboratories, San Diego, CA)에서 성장시켰다. 모든 실험들이 낮은-통과 세포 배양(low-passage cell cultures)으로 수행되었다. 배아 랫트(embryonic rat) 심근세포(라인 H9c2)는 American Type Culture Collection (ATCC, Manassas, VA, USA)로부터 구입하여 10% FBS(fetal bovine serum), 100 U/mL 페니실린 및 100 μg/mL 스트렙토마이신으로 보충된 DMEM (Dulbecco's Modified Eagle's Medium)에서 성장시켰다. J774A.1, 쥐과의 단핵구 대식세포주 (murine monocyte macrophage cell line ) (ATCC, Manassas, VA, USA), 는 10% FBS (fetal bovine serum), 25mM HEPES, 2mM 글루타민, 100u/mL 페니실린 및 100 μg/mL 스트렙토마이신으로 보충된 DMEM에서 성장시켰다.
췌장암 세포주 (MIA PaCa-2, AsPC-1, PSN1, Capan-1 및 PANC-1)는 ATCC 세포 뱅크(American Type Culture Collection; Manassas, VA)로 부터 수취하였다. MIA PaCa-2 세포는 10% FBS 및 2.5% 말 혈청으로 보충된 DMEM (Dulbecco’s Modified Eagle’s Medium)으로 배양되었다. AsPC-1 및 PSN1 세포는 10% FBS로 보충된 RPMI-1640 메디엄에서 성장시켰다. PANC-1가 10% FBS로 보충된 DMEM에서 배양되는 반면, Capan-1는 20% FBS를 함유하는 RPMI-1640에서 배양되었다.
상기 세포주를 위한 모든 배지(media)는 BioWhittaker-Lonza (Bergamo, Italy) MediaTech (Manassas, VA)로부터 구입하였고, 100 유닛(units)의 페니실린/mL 및 2 μg 스트렙토마이신/mL (Sigma-Aldrich, St. Louis, MO)으로 보충하였다. 상기 세포들은 5% CO2 환경에서 37℃에서 배양되었다. 세포들은 지시된 농도로 Eli Lilly (Sesto Fiorentino, Italy)에 의하여 공급된 젬시타빈 (2′,2′-difluorodeoxycytidine; GEM, Gemzar®)으로 처리되었다.
인간 혈청에서 BAG3 항체의 분리
혈청은 분리 버퍼 (1.5% BSA 및 0.2M 글리신-아세테이트 pH 2.5를 갖는 PBS)로 1:40으로 희석되어 500㎕의 최종 부피가 되고 실온에서 20분 동안 배양되었다. 상기 혈청은 마이크로콘 원심분리 필터 장치(Microcon centrifugal filter device), YM-100 (100,000 MW cut-off; Millipore, Billerica, MA, USA)로 피펫팅되고 실온에서 20분 동안 14,100 rpm으로 원심분리되었다. 상기 샘플 저장기(reservoir)가 통과액(flow through)으로부터 분리되어 제2 튜브 내로 정반대로 위치시켜 실온에서 3분 동안 5,000rpm에서 원심분리하였다. 분리된 항체를 함유하는 수집 용액이 1M 트리스 버퍼(Tris buffer), pH 9.0로 pH 7.0로 조정되었다. 농축 부피(retentate volume)는 희석 버퍼(PBS with 1.5% BSA and 0.1% Tween-20). 14로 초기 부피(500㎕)로 재구성되었다. 면역블로팅(immunoblotting)에 의하여 BAG3 단백질의 검출을 위하여, 상기 분리된 항체들은 5% 소 혈청 알부민(bovine serum albumin)을 함유하는 TBST로 1:200으로 희석되어 4℃에서 하룻밤 두었다.
웨스턴 블럿 분석
세포들을 수확하여 20mM HEPEs (pH 7.5), 150 mM NaCl, 프로티아제 억제제 칵테일(protease inhibitors cocktail) (1 mM 페닐메틸술포닐 플루오라이드(phenylmethylsulfonyl fluoride), 1 mg/ml 펩스타틴(pepstatin) A, 2 mg/ml 아프로티닌(aprotinin))으로 보충된 0.1% 트리톤(Triton) (TNN buffer)를 함유하는 버퍼에서 3회 동결 및 해동하여 용해시켰다. 가용성 단백질은 15분 동안 10,000g에서 원심분리한 후 수집되고, 그 양이 브래드포드 분석(Bradford assay) (Bio-Rad, Hercules, CA)에 의하여 결정되었다. 총 단백질의 25㎍ 및 혈청 샘플 (PBS-T 0.05%에서 1:2)을 8% 또는 10% SDS-PAGE 겔 상에서 러닝시켜 전기영동적으로 니트로섬유소막(nitrocellulose membrane)으로 트랜스퍼시켰다. 니트로셀룰로스 블럿이 TBST buffer (20 mM Tris-HCl pH 7.4, 500 mM NaCl, 및 0.1% Tween 20)에서 10% 무-지방 건조 우유로 차단되고 5% 소혈청 알부민 또는 5% 무-지방 건조 우유를 함유하는 TBST에서 1차 항체(primary antibodies)로, 4℃에서 밤새도록 배양시켰다.
면역반응성이 아머샴 생명과학(Amersham Life Sciences Inc.) (Arlington Heights, IL, USA)으로부터 구입한 ECL 검출 시약 및 피얼스(Pierce) (Rockford, IL)로부터 구입한 서양고추냉이 과산화수소(horseradish peroxidase)-접합 2차 항체로 연속 배양에 의하여 측정되었다.
상기 밴드의 농도계측 스캐닝(Scanning densitometry)이 이미지 스캔 (SnapScan 1212; Agfa-Gevaert NV)으로 수행되었다. 각 밴드와 관련된 곡선 아래의 영역이 Gimp2 소프트웨어를 이용하여 결정되었다. 배경을 계산된 수치에서 뺐다.
질량 분석(Mass spectrometry)
단백질 밴드가 추출되었고 겔 피스가 연이어 밀리큐 워터(MilliQ Water) 및 아세토나이트릴(Acetonitrile)로 세척되었고, 상기 단백질이 세우첸코 프로토콜(Shevchenko protocol)에 기재된 것처럼 인시츄(in situ)로 소화되었다. 간단히, 겔 슬라이스는 1,4-디티오트레이톨(1,4-dithiothreitol) (10mM) 및 아킬화된 요오드아세트아미드(iodoacetamide) (50 mM)에서 환원(reduced)되고, 1시간 동안 얼음에서 트립신 용액 (12 ng/μL)에서 세척 및 재수화되었다. 30㎕의 중탄산 암모늄(ammonium bicarbonate) (10 mM, pH 7.5)의 첨가 후에, 샘플들이 25℃에서 하룻밤 동안 소화되었다. 상기 획득된 펩티드 혼합물의 5㎕를 나노 액큐이티 LC 시스템 (nano Acquity LC system) (Waters Corp. Manchester, United Kingdom) 상으로 주입시켰다. 상기 펩티드는 1.7㎛ BEH C-18 컬럼 (Waters Corp. Manchester, United Kingdom) 상에서 유속 200 nl/min으로 분리되었다. 기울기 (용액 A: 0.1% 포름산, 용액 B: 0.1% 포름산, 100% ACN)은 5%에서 시작되고 55분 후에 50% B에서 종료되었다. MS 및 MS/MS 데이터는 Q-TOF 프리미어 질량 분석기 (Waters Corp., Micromass, Manchester, United Kingdom)를 이용하여 획득되었다. 두 배 및 세 배로 충진된 펩티드-이온이 매스린스 소프트웨어(MassLynx software)에 의하여 자동적으로 선택되어 분획되었다. MS 데이터는 자동적으로 처리되어 데이터베이스 서치에 의한 단백질 식별을 위한 피크리스트가 프로테인린스 소프트웨어(ProteinLynx software)에 의하여 생성되었다. 데이터베이스 서치는 스위스포트 단백질 데이터베이스(SwissProt protein database)을 이용하여 MASCOT 서버로 수행되었다. 상기 스위스포트 인간 데이터베이스 (405506 서열; 146166984 잔기)가 1 미스된 굴곡(cleavage), 고정된 변형으로서 카바미도메틸(carbamidomethyl)(C )을 허용하면서 서치되었다. 상기 펩티드의 톨러런스는 60ppm으로 세팅되고 MS/MS 톨러런스는 0.8Da이다.
분별 초원심분리(differential ultracentrifugation)에 의한 엑소사이트 소포(exocytic vesicles)의 정제
H9c2의 무혈청 메디엄(medium)에서 4℃에서 연속 원심분리 (2000 ×g 15분, 10,000 ×g 30분)에 의하여 세포 및 큰 데브리스가 제거되었다. 최초 두 번의 원심분리 각각 이후에, 펠릿들이 제거되고, 상청액(supernatant)이 다음 단계를 위하여 취하여졌다. 최종 상청액은 4℃에서 90분 동안 150,000×g에서 원심분리(SW50.1 rotor, 및 옵티머 L-90K 초원심분리기(Optima L-90K Ultracentrifuge), Beckman Coulter)되어 엑소섬(exosome)으로 펠릿화되었다. 상기 펠릿은 PBS로 세척되어 오염 단백질을 제거하고 4℃에서 90분 동안 150,000×g에서 마지막으로 원심분리되었다. 세척 후에, 상기 펠릿(엑소섬)은 20㎕의 PBS로 재현탁되고 웨스턴 블럿에 의하여 전체-세포 용해물과 비교하여 항-BAG3 TOS-2 폴리클로날 항체로 분석되었다. Rab-4가 엑소사이트 소포를 위한 마커로서 분석되었다.
FACS 분석
rBAG3 결합 - J774 A.1 세포가 얼음 상에서 PBS에서 2% FBS + 0.1% NaN3로 15분 동안 블러킹되고 상이한 농도의 FITC-rBAG3 단백질 (7, 14, 및 70nm) 또는 2% FBS + 0.1% NaN3을 함유하는 PBS에서 FITC-BSA (70nM)로 암실에서 4℃에서 30분 동안 배양되었다. PBS로 세척한 후, 상기 세포는 PBS + 2% FBS + 0.1% NaN3에서 재현탁시켜 FACScan (BD Biosceiences) 플로우 사이토미터로 분석되었다.
경쟁(competition) - J774 A.1 세포 (2.5x105/100㎕)는 625nM의 BAG3 펩티드(펩티드 1, 펩티드 2, 펩티드 3, 펩티드 4 또는 스크램블 펩티드)로 또는 항-BAG3 모노클로날 및 폴리클로날 항체 (마우스 모노클로날 AC1, AC2 및 래빗 폴리클로날 TOS2)로부터 F(ab')2 단편 또는 마우스 IgG로부터 F(ab’)2 단편 또는 래빗 IgG로부터의 F(ab’)2 단편의 420nM로 2% FBS + 0.1% NaN3를 함유하는 PBS에서 얼음 상에서 30분동안 배양시켰다. 배양 후에, 상기 세포는 PBS로 세척되고 FITC-rBAG3 단백질 (14 nM)로 2% FBS + 0.1% NaN3를 함유하는 PBS에서 암실의 4℃에서 배양되었고, 플로우 사이토미터 (BD Biosciences)에 의하여 분석되었다.
ELISA에 의한 IL6 검출
IL6는 폴리믹신 B 설페이트(polymyxin B sulfate) (5㎍/ml)의 존재 또는 부존재 하에서 LPS(10 ng/ml) 또는 rBAG3 (14 nM) 또는 BSA (14 nM)로 10시간 또는 20시간 동안 처리된 J774 A.1 세포 (5x104/96-웰 마이크로플레이트에서)의 상청액에서 측정되었다. 상기 처리 후에, 50㎕의 세포 배양 배지가 수집되고 마우스 IL6 키트 (eBioscience)로 세 차례 분석되었다.
형광(Fluorescence)
세포들이 60-70% 컨플루언시까지 6-웰 플레이트에서 커버슬립(coverslips) 상에서 배양되고 동량의 rBAG3-FITC 및 BSA-FITC 단백질이 0.1 % NaN3가 포함된 HCMa 및 J774 A1 배양 메디어(media)에 1시간 동안 첨가되었다. 커버슬립이 1x PBS로 세척되고, 실온에서 30분 동안 1x PBS에서 3.7% 포름알데히드에서 고정시키고, 1x PBS 0.1M 글리신으로 5분 동안 배양시켰다.
4℃에서 항-β-인터그린(integrin) 모노클로날 항체의 1:100 희석으로 뱅양하고, 커버슬립은 1x PBS로 3회 세척되었다. 염소 항-마우스 IgG DyLight 594-접합 항체 (Jackson ImmunoResearch, West Grove, PA, USA)의 1:500 희석으로 실온에서 45분 동안 배양한 후, 커버스립은 다시 1x PBS로 3회 세척되었다. 실온에서 10분 동안 Hoechst 33342 (Sigma Aldrich, 2 μg/ml)으로 배양하고, 커버슬립은 다시 PBS로 3회 세척되고 증류수로 세척되었다. 상기 커버슬립은 47% (v/v) 글리세롤 함유 인터스페이스로 슬라이드 상에 마운트시켰다. 샘플들은 공초점 레이저 스캐닝 현미경(Zeiss LSM confocal microscope, Germany)을 이용하여 분석되었다. 이미지는 실험 및 대조 물질을 비교할 때 상기 동일한 자료취득 변수(레이저 강도, 광전자 배증관 이득(gain photomultipliers), 핀홀 구멍(pinhole aperture), 오브젝티브 63X, 줌 2)를 이용하여 연속 스캔 모드에서 획득되었다. 도면의 획득을 위하여, 이미지의 밝기 및 콘트라스트는 가장 낮은 형광 강도 특징의 시각적 공감 및 상이한 실험 그룹들 사이에서의 비교를 돕기 위하여 빛 세포 형광 배경을 남겨놓으면서 조정되었다. 최종 도면은 아도비 포토샵 7 및 아도비 일러스트레이트 10을 이용하여 집합시켰다. 레이카 Q9 공초점 소프트웨어 및 이미지J(Leica Q9 Confocal Software and ImageJ)가 데이터 분석을 위하여 사용되었다.
ELISA에 의한 항체 역가(antibody titers)의 측정
NUNC 맥시소르프 96 웰 ELISA 플레이트(NUNC Maxisorp 96 well ELISA)는 pH7, PBS에서 재조합 BAG3 단백질 1μg/ml (50μl/well)로 코팅되어 4℃에서 하룻밤 동안 배양되었다. 플레이트는 세척 버퍼(PBS + 0.05% Tween-20)로 2회 세척하고 PBS에서 0.5% 피쉬 겔라틴으로 실온에서 1시간 동안 차단되었다(150 μl/well). 차단 이후, 상기 플레이트는 세척 버퍼로 2회 세척되고 혈청은 세척 버퍼에서 0.5% 피쉬 겔라틴으로 1:170으로 희석되어 세 배로 적용되고(50 μl/well) 2시간 동안 실온에서 배양되었다. 상기 플레이트는 세척 버퍼로 6회 세척되었다. 항-인간 IgG (H+L) 항체 (Sigma Aldrich)가 세척 버퍼에서 0.5% 피쉬 겔라틴으로 1:20,000으로 희석되고, 50 μl/well로 첨가되어 30분 동안 4℃에서 배양되었다. 배양 후, 상기 플레이트는 6회 세척되고 TMB (50 μl/well) (eBioscience)으로 디벨로프시키고, 상기 반응은 4.5 M 황산 (25 μl/well)으로 중단시키고 상기 플레이트는 450nm에서 분광측색적으로 분석되었다.
NO
2
-
분석
상기 배양 상청액에서 세포로부터 방출되는 NO의 안정한 대사산물인 아질산염 함량(NO2 -)을 폴리믹신 B 설페이트(Sigma-Aldrich, St. Louis, MO, USA) 5㎍/ml의 존재 또는 부존재에서 LPS (10 ng/ml) 또는 rBAG3 (7, 14 및 28 nM) 또는 BSA (28 nM)로 24시간 동안 처리된 J774 A.1 세포 (5x104/ 96-웰 마이크로플레이트에서)에서 측정되었다. NO2 - 양은 그리스 반응(Griess reaction)으로 측정되었다. 간단히 100 μL의 세포 배양 메디엄이 100 μL 의 그리스 시약 - 5% (v:v) 인산(phosphoric acid) 및 0.1% (w:v) 나프틸에틸렌디아민-HCl 에서 동량의 1% (w:v) 술파닐아미드(sulphanilamide)-로 혼합되었고, 마이크로플레이트 리더 티터텍 (Dasit, Cornaredo, Milan, Italy)에서 550nm에서 흡광도가 측정되었다. 상기 샘플들에서 NO2 - 의 양(γM로)은 아질산나트륨 표준곡선으로부터 계산되었다.
ELISA에 의한 BAG3/항체 면역복합체의 측정
NUNC 맥시소르프 96 웰 ELISA 플레이트(NUNC Maxisorp 96 well ELISA)는 pH 7, PBS에서 항-BAG3 모노클로날 항체 AC-1, AC-2 또는 AC-3로 코팅시켜 4℃에서 하룻밤동안 배양시켰다. 플레이트는 세척 버퍼 (PBS + 0.05% Tween-20)로 2회 세척되고, PBS에서 0.5% 피쉬 겔라틴으로 실온에서 한 시간 동안 차단되었다(150 μl/well). 차단 후, 상기 플레이트는 세척 버퍼로 2회 세척되고 혈청은 세척 버퍼에서 0.5% 피쉬 겔라틴으로 1:70으로 희석시키고 3배 적용시켜 (50 μl/well) 두 시간 동안 실온에서 배양시켰다. 상기 플레이트는 세척 버퍼로 6회 세척되었다. 항-인간 IgG (H+L) 항체 (Sigma Aldrich)는 세척 버퍼에서 0.5% 피쉬 겔라틴으로 1:20,000으로 희석시켜 50 μl/well에서 첨가하고 30분 동안 4℃에서 배양시켰다. 배양 후에, 상기 플레이트는 6회 세척되고 TMB (50 μl/well) (eBioscience)으로 디벨로프시키고, 상기 반응은 4.5 M 황산 (25 μl/well)으로 중단시키고 상기 플레이트는 450nm에서 분광측색적으로 분석되었다.
면역조직화학(Immunohistochemistry)
면역조직화학 프로토콜은 다음을 포함한다: 크실렌(xylene)에서 탈파라핀(deparaffination), 알콜의 농도를 순수 물까지 하향시켜 재수화, pH 6.0, 구연산염 버퍼(citrate buffer)에서 95℃에서 30분 동안, 비-효소 항원 회수 및 20분 동안 메탄올에서 H2O2으로 내생 페록시다아제(endogenous peroxidase) 담금질(quenching). PBS로 린스 후, 상기 샘플은 0.1% PBS/BSA에서 5% 정상 말 형청으로 차단되었다. BAG3 검출을 위하여, 샘플들은 3 ㎍/ml의 농도에서 BAG3 모노클로날 항체 AC-1, AC-2 또는 AC-3로 실온에서 1시간 동안 배양되었다. PBS로 거칠게 세척 후, 섹션들은 20분 동안 바이오티닐부착 2차 항-마우스 IgG로 배양되고, 린스된 후, 아비딘-비오틴-복합체 페록시다아제(avidin-biotin-complexes peroxidase) (Novocastra-Leica Microsystems, Milano, IT에서 구입)로 배양시키고, 다이아미노벤지딘 (Sigma-Aldrich, St. Louis,MO)으로 디벨로프시켰다. 마지막으로, 상기 섹션들은 헤마톡실린(hematoxylin)으로 대비염색되고, 알코올로 탈수되고, 크실렌으로 세척되고, 퍼마운트(Permount)(Fisher Scientific, Milan, IT)로 마운트시켰다.
정량적 실시간
RT
-PCR(
Quantitative
Real
-
time
RT
-
PCR
)
절개된 췌장암의 조직 생검을 취하여 즉시 액체 질소에서 동결시켜 RNA 추출때까지 -80℃에서 보관하였다. 총 RNA가 페놀 추출의 수단으로 동결 조직 및 췌장암세포로부터 분리되었다 (TRIzol Reagent, Invitrogen Corporation, Carlsbad, CA, USA). 조직 샘플에서 암 세포질(Cancer cellularity)은 동결 절편(cryostat sectioning) 및 대부분의 세포 영역의 절개로 강화되었다. RNA 농도 및 순도 (A260:A280>2.0; A260/A230>1.8)는 나노드롭 분광광도계 (NanoDrop Spectrophotometer) (Thermo Fisher, Waltham, MA, USA)에 의하여 입증되었다. 총 RNA의 1.0 μg 은 제조자의 지시에 따라 고-용량 cDNA 역전사 키트(High-Capacity cDNA Reverse Transcription Kit)(Applied Biosystems, Applera, Foster City, CA, USA)을 이용하여 역-전사시켰다. 정량적 실시간 PCR 분석은 종양 조직 샘플에서 BAG3의 차분 발현을 평가하기 위하여 사용되었다. 인간 bag3 유전자을 위한 프라이머는 Primm srl (Milano, Italy) (정방향 프라이머(foward primer): (SEQ ID NO:16) CCT GTT AGC TGT GGT TG; 역방향 프라이머(reverse primer): (SEQ ID NO:17) AAC ATA CAG ATA TTC CTA TGG C)에 의하여 합성되었다.
소변 샘플의 경우, 전립선마사지 후 취득되고 RNA 프로텍터 버퍼로 안정화된 1ml의 소변이 15ml의 팔콘 튜브(falcon tube)로 옮기고 2ml의 트리졸 시약(Trizol Reagent ®)과 1ml의 클로로포름(chloroform)과 혼합하였다. 샘플들은 4℃, 8000 rpm에서 15분 동안 원심분리되었다. 수층(Aqueous phase)은 새로운 팔콘 튜브로 옮기고 1ml의 순수 에탄올을 첨가하였다. 샘플들이 혼합되고 RNAeasy 퀴아겐 컬럼(RNAeasy qiagen column) 상으로 (4단계로) 옮기고, RNA 정제에 적절한 공급 프로토콜을 따랐다. RNA는 15㎕의 유출 버퍼(elution buffer)에서 유출시켰다. 12㎕의 유출된 RNA는 최종 부피 20㎕에서 역전사 반응(Quantitect reverse transcription kit, Qiagen)을 수행하기 위하여 사용되었다. 2㎕의 합성 cDNA는 라이트 사이클러 480 로쉐 장비(Light Cycler 480 Roche instrument) 상에서 실시간 PCR 스크리닝을 위하여 사용되었다.
Bag3 프라이머는 다음과 같다: fw 5’-CAGGAGCAGCACGCCACTCC-3’(SEQ ID NO:16); rev 5’-TGGTCCAACTGGGCCTGGCT-3’(SEQ ID NO:17).
GAPDH mRNA는 다음 프라이머로 측정된 bag3 RNA 수치를 정규화하기 위하여 측정되었다 : fw 5’- AGCCTCCCGCTTCGCTCTCT-3’; rev 5’- CCAGGCGCCCAATACGACCA-3’.
모든 qPCRs는 QuantiFast SYBR 그린 PCR 키트(QIAGEN, Hamburg, Germany)를 이용하여 25-㎕ 최종 부피에서 수행되고, 샘플 당 3회 반복되고, 다음 조건을 따라서 ABI PRISM® 7700 서열 검출 시스템(Applied Biosystems, Applera, Foster City, CA, USA)에서 또는 라이트 사이클러 480 로쉐 장비(Light Cycler 480 Roche instrument)에서 러닝된다: 95℃에서 5분, 95℃ 에서 10분 동안 40 사이클 및 60℃ 에서 30분. 데이터는 S.D.S 소프트웨어 v 2.1을 이용하여 임계 사이클(Ct) 수치로서 획득되었다. 각 샘플에서, bag3 mRNA 상대 발현 레벨은 상기 내생 GAPDH의 발현을 위하여 정규화한 후, 상기 비교법을 이용하여 획득되었다.
상기 기재 및 상기 설명된 실시예들로부터, 본 발명에 따라 기재되고 획득된 생물학적 마커에 의하여 이루어지는 효과는 명백하다.
SEQUENCE LISTING
<110> Biouniversa S.r.l.
<120> BAG3 RNA as biochemical markers
<130> 13MG06E
<150> EP12172531.1
<151> 2012-06-19
<160> 20
<170> BiSSAP 1.2
<210> 1
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="Forward primer"
/organism="Homo sapiens"
<400> 1
aacggtgacc gcgacccttt 20
<210> 2
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="Reverse primer"
/organism="Homo sapiens"
<400> 2
ccttccctag caggcggcag 20
<210> 3
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="Forward primer"
/organism="Homo sapiens"
<400> 3
ccggctggcc cttcttcgtg 20
<210> 4
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="Reverse primer"
/organism="Homo sapiens"
<400> 4
cagcctagag ccctcccggg 20
<210> 5
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="forward primer"
/organism="Homo sapiens"
<400> 5
gtcacctctg cggggcatgc 20
<210> 6
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="Reverse primer"
/organism="Homo sapiens"
<400> 6
ggtgactgcc caggctgctc 20
<210> 7
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="Forward primer"
/organism="Homo sapiens"
<400> 7
ccagcctccc acggacctga 20
<210> 8
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="Reverse primer"
/organism="Homo sapiens"
<400> 8
ctggtgactg cccaggctgc 20
<210> 9
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="Forward primer"
/organism="Homo sapiens"
<400> 9
caggagcagc acgccactcc 20
<210> 10
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="Reverse primer"
/organism="Homo sapiens"
<400> 10
tggtccaact gggcctggct 20
<210> 11
<211> 16
<212> PRT
<213> Homo sapiens
<220>
<223> protein
<400> 11
Asp Arg Asp Pro Leu Pro Pro Gly Trp Glu Ile Lys Ile Asp Pro Gln
1 5 10 15
<210> 12
<211> 15
<212> PRT
<213> Homo sapiens
<220>
<223> Protein
<400> 12
Ser Ser Pro Lys Ser Val Ala Thr Glu Glu Arg Ala Ala Pro Ser
1 5 10 15
<210> 13
<211> 15
<212> PRT
<213> Homo sapiens
<220>
<223> Protein
<400> 13
Asp Lys Gly Lys Lys Asn Ala Gly Asn Ala Glu Asp Pro His Thr
1 5 10 15
<210> 14
<211> 15
<212> PRT
<213> Homo sapiens
<220>
<223> Protein
<400> 14
Asn Pro Ser Ser Met Thr Asp Thr Pro Gly Asn Pro Ala Ala Pro
1 5 10 15
<210> 15
<211> 575
<212> PRT
<213> Homo sapiens
<220>
<223> BAG3
<400> 15
Met Ser Ala Ala Thr His Ser Pro Met Met Gln Val Ala Ser Gly Asn
1 5 10 15
Gly Asp Arg Asp Pro Leu Pro Pro Gly Trp Glu Ile Lys Ile Asp Pro
20 25 30
Gln Thr Gly Trp Pro Phe Phe Val Asp His Asn Ser Arg Thr Thr Thr
35 40 45
Trp Asn Asp Pro Arg Val Pro Ser Glu Gly Pro Lys Glu Thr Pro Ser
50 55 60
Ser Ala Asn Gly Pro Ser Arg Glu Gly Ser Arg Leu Pro Pro Ala Arg
65 70 75 80
Glu Gly His Pro Val Tyr Pro Gln Leu Arg Pro Gly Tyr Ile Pro Ile
85 90 95
Pro Val Leu His Glu Gly Ala Glu Asn Arg Gln Val His Pro Phe His
100 105 110
Val Tyr Pro Gln Pro Gly Met Gln Arg Phe Arg Thr Glu Ala Ala Ala
115 120 125
Ala Ala Pro Gln Arg Ser Gln Ser Pro Leu Arg Gly Met Pro Glu Thr
130 135 140
Thr Gln Pro Asp Lys Gln Cys Gly Gln Val Ala Ala Ala Ala Ala Ala
145 150 155 160
Gln Pro Pro Ala Ser His Gly Pro Glu Arg Ser Gln Ser Pro Ala Ala
165 170 175
Ser Asp Cys Ser Ser Ser Ser Ser Ser Ala Ser Leu Pro Ser Ser Gly
180 185 190
Arg Ser Ser Leu Gly Ser His Gln Leu Pro Arg Gly Tyr Ile Ser Ile
195 200 205
Pro Val Ile His Glu Gln Asn Val Thr Arg Pro Ala Ala Gln Pro Ser
210 215 220
Phe His Gln Ala Gln Lys Thr His Tyr Pro Ala Gln Gln Gly Glu Tyr
225 230 235 240
Gln Thr His Gln Pro Val Tyr His Lys Ile Gln Gly Asp Asp Trp Glu
245 250 255
Pro Arg Pro Leu Arg Ala Ala Ser Pro Phe Arg Ser Ser Val Gln Gly
260 265 270
Ala Ser Ser Arg Glu Gly Ser Pro Ala Arg Ser Ser Thr Pro Leu His
275 280 285
Ser Pro Ser Pro Ile Arg Val His Thr Val Val Asp Arg Pro Gln Gln
290 295 300
Pro Met Thr His Arg Glu Thr Ala Pro Val Ser Gln Pro Glu Asn Lys
305 310 315 320
Pro Glu Ser Lys Pro Gly Pro Val Gly Pro Glu Leu Pro Pro Gly His
325 330 335
Ile Pro Ile Gln Val Ile Arg Lys Glu Val Asp Ser Lys Pro Val Ser
340 345 350
Gln Lys Pro Pro Pro Pro Ser Glu Lys Val Glu Val Lys Val Pro Pro
355 360 365
Ala Pro Val Pro Cys Pro Pro Pro Ser Pro Gly Pro Ser Ala Val Pro
370 375 380
Ser Ser Pro Lys Ser Val Ala Thr Glu Glu Arg Ala Ala Pro Ser Thr
385 390 395 400
Ala Pro Ala Glu Ala Thr Pro Pro Lys Pro Gly Glu Ala Glu Ala Pro
405 410 415
Pro Lys His Pro Gly Val Leu Lys Val Glu Ala Ile Leu Glu Lys Val
420 425 430
Gln Gly Leu Glu Gln Ala Val Asp Asn Phe Glu Gly Lys Lys Thr Asp
435 440 445
Lys Lys Tyr Leu Met Ile Glu Glu Tyr Leu Thr Lys Glu Leu Leu Ala
450 455 460
Leu Asp Ser Val Asp Pro Glu Gly Arg Ala Asp Val Arg Gln Ala Arg
465 470 475 480
Arg Asp Gly Val Arg Lys Val Gln Thr Ile Leu Glu Lys Leu Glu Gln
485 490 495
Lys Ala Ile Asp Val Pro Gly Gln Val Gln Val Tyr Glu Leu Gln Pro
500 505 510
Ser Asn Leu Glu Ala Asp Gln Pro Leu Gln Ala Ile Met Glu Met Gly
515 520 525
Ala Val Ala Ala Asp Lys Gly Lys Lys Asn Ala Gly Asn Ala Glu Asp
530 535 540
Pro His Thr Glu Thr Gln Gln Pro Glu Ala Thr Ala Ala Ala Thr Ser
545 550 555 560
Asn Pro Ser Ser Met Thr Asp Thr Pro Gly Asn Pro Ala Ala Pro
565 570 575
<210> 16
<211> 17
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..17
<223> /mol_type="unassigned DNA"
/note="Forward primer"
/organism="Homo sapiens"
<400> 16
cctgttagct gtggttg 17
<210> 17
<211> 22
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..22
<223> /mol_type="unassigned DNA"
/note="Reverse primer"
/organism="Homo sapiens"
<400> 17
aacatacaga tattcctatg gc 22
<210> 18
<211> 2533
<212> RNA
<213> Homo sapiens
<220>
<221> source
<222> 1..2533
<223> /mol_type="mRNA"
/note="Homo sapiens BCL2-associated athanogene 3 (BAG3) mRNA"
/organism="Homo sapiens"
<400> 18
gcggagctcc gcatccaacc ccgggccgcg gccaactttt ttggactgga ccagaagttt 60
ctagccggcc agttgctacc tccctttatc tcctccttcc cctctggcag cgaggaggct 120
atttccagac acttccaccc ctctctggcc acgtcacccc cgcctttaat tcataaaggt 180
gcccggcgcc ggcttcccgg acacgtcggc ggcggagagg ggcccacggc ggcggcccgg 240
ccagagactc ggcgcccgga gccagcgccc cgcacccgcg ccccagcggg cagaccccaa 300
cccagcatga gcgccgccac ccactcgccc atgatgcagg tggcgtccgg caacggtgac 360
cgcgaccctt tgccccccgg atgggagatc aagatcgacc cgcagaccgg ctggcccttc 420
ttcgtggacc acaacagccg caccactacg tggaacgacc cgcgcgtgcc ctctgagggc 480
cccaaggaga ctccatcctc tgccaatggc ccttcccggg agggctctag gctgccgcct 540
gctagggaag gccaccctgt gtacccccag ctccgaccag gctacattcc cattcctgtg 600
ctccatgaag gcgctgagaa ccggcaggtg caccctttcc atgtctatcc ccagcctggg 660
atgcagcgat tccgaactga ggcggcagca gcggctcctc agaggtccca gtcacctctg 720
cggggcatgc cagaaaccac tcagccagat aaacagtgtg gacaggtggc agcggcggcg 780
gcagcccagc ccccagcctc ccacggacct gagcggtccc agtctccagc tgcctctgac 840
tgctcatcct catcctcctc ggccagcctg ccttcctccg gcaggagcag cctgggcagt 900
caccagctcc cgcgggggta catctccatt ccggtgatac acgagcagaa cgttacccgg 960
ccagcagccc agccctcctt ccaccaagcc cagaagacgc actacccagc gcagcagggg 1020
gagtaccaga cccaccagcc tgtgtaccac aagatccagg gggatgactg ggagccccgg 1080
cccctgcggg cggcatcccc gttcaggtca tctgtccagg gtgcatcgag ccgggagggc 1140
tcaccagcca ggagcagcac gccactccac tccccctcgc ccatccgtgt gcacaccgtg 1200
gtcgacaggc ctcagcagcc catgacccat cgagaaactg cacctgtttc ccagcctgaa 1260
aacaaaccag aaagtaagcc aggcccagtt ggaccagaac tccctcctgg acacatccca 1320
attcaagtga tccgcaaaga ggtggattct aaacctgttt cccagaagcc cccacctccc 1380
tctgagaagg tagaggtgaa agttccccct gctccagttc cttgtcctcc tcccagccct 1440
ggcccttctg ctgtcccctc ttcccccaag agtgtggcta cagaagagag ggcagccccc 1500
agcactgccc ctgcagaagc tacacctcca aaaccaggag aagccgaggc tcccccaaaa 1560
catccaggag tgctgaaagt ggaagccatc ctggagaagg tgcaggggct ggagcaggct 1620
gtagacaact ttgaaggcaa gaagactgac aaaaagtacc tgatgatcga agagtatttg 1680
accaaagagc tgctggccct ggattcagtg gaccccgagg gacgagccga tgtgcgtcag 1740
gccaggagag acggtgtcag gaaggttcag accatcttgg aaaaacttga acagaaagcc 1800
attgatgtcc caggtcaagt ccaggtctat gaactccagc ccagcaacct tgaagcagat 1860
cagccactgc aggcaatcat ggagatgggt gccgtggcag cagacaaggg caagaaaaat 1920
gctggaaatg cagaagatcc ccacacagaa acccagcagc cagaagccac agcagcagcg 1980
acttcaaacc ccagcagcat gacagacacc cctggtaacc cagcagcacc gtagcctctg 2040
ccctgtaaaa atcagactcg gaaccgatgt gtgctttagg gaattttaag ttgcatgcat 2100
ttcagagact ttaagtcagt tggtttttat tagctgcttg gtatgcagta acttgggtgg 2160
aggcaaaaca ctaataaaag ggctaaaaag gaaaatgatg cttttcttct atattcttac 2220
tctgtacaaa taaagaagtt gcttgttgtt tcagaagttt aaccccgttg cttgttctgc 2280
agccctgtct acttgggcac ccccaccacc tgttagctgt ggttgtgcac tgtcttttgt 2340
agctctggac tggaggggta gatggggagt caattaccca tcacataaat atgaaacatt 2400
tatcagaaat gttgccattt taatgagatg attttcttca tctcataatt aaaatacctg 2460
actttagaga gagtaaaatg tgccaggagc cataggaata tctgtatgtt ggatgacttt 2520
aatgctacat ttt 2533
<210> 19
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="Forward primer"
/organism="Homo sapiens"
<400> 19
agcctcccgc ttcgctctct 20
<210> 20
<211> 20
<212> DNA
<213> Homo sapiens
<220>
<221> source
<222> 1..20
<223> /mol_type="unassigned DNA"
/note="Reverse primer"
/organism="Homo sapiens"
<400> 20
ccaggcgccc aatacgacca 20
Claims (25)
- 병리 상태(pathological state)의 진단에서의 BAG3 RNA 또는 그 단편의 용도.
- 제1항에 있어서,
상기 BAG3 RNA는,
BAG3 mRNA인 것인, BAG3 RNA 또는 그 단편의 용도. - 제1항에 있어서,
상기 진단은,
인비트로(in vitro) 또는 엑스비보(ex vivo)인 것인, BAG3 RNA 또는 그 단편의 용도. - 제1항 내지 제3항 중 어느 한 항에 있어서,
상기 진단의 수용자(recipient)는,
포유동물, 바람직하게 인간인 것인, BAG3 RNA 또는 그 단편의 용도. - 제1항 내지 제4항 중 어느 한 항에 있어서,
상기 병리 상태는,
심장병, 암, 당뇨병, 염증 및 피부, 신경, 뼈, 혈관 및 결합조직의 염증관련질환 중에서 선택되는 것인 BAG3 RNA 또는 그 단편의 용도. - 제5항에 있어서,
상기 심장병은,
협심증(angina pectoris), 경색전 협심증(pre-infarction angina), 심근경색증(myocardial infarction), 심부전(heart failure), 국소 빈혈(ischemia), 급성 관상동맥 질환(acute coronary disease), 급성심부전(acute heart failure), 만성심부전(chronic heart failure), 및 의인성 심장질환(iatrogenic heart disease) 중에서 선택되는 것인, BAG3 RNA 또는 그 단편의 용도. - 제5항에 있어서,
상기 암은,
췌장암, 방광암 및 전립선암 중에서 선택되는 것인, BAG3 RNA 또는 그 단편의 용도. - 생물학적 샘플에서 BAG3 유전자 발현의 검출 및/또는 정량용 키트에 있어서,
bag3 뉴클레오티드 서열 (SEQ ID NO 18)에 포함된 한 쌍의 단일-가닥 올리고뉴클레오티드 프라이머를 포함하는 것을 특징으로 하는, 키트. - 제8항에 있어서,
상기 bag3 뉴클레오티드 서열의 뉴클레오티드 1 내지 뉴클레오티드 360, 뉴클레오티드 466 내지 뉴클레오티드 1570 또는 뉴클레오티드 1801 내지 뉴클레오티드 2533의 영역 중 어느 하나에 포함된 뉴클레오티드 서열을 가지는 것으로부터 선택되는 한 쌍의 프라이머를 포함하는 것을 특징으로 하는, 키트. - 제8항 또는 제9항에 있어서,
다음 서열을 가지는 것들로부터 선택된 한 쌍의 프라이머를 포함하는 것을 특징으로 하는 키트:
SEQ ID NO. 1 및 SEQ ID NO. 2; SEQ ID NO. 3 및 SEQ ID NO. 4; SEQ ID NO. 5 및 SEQ ID NO. 6; SEQ ID NO. 7 및 SEQ ID NO. 8; SEQ ID NO. 9 및 SEQ ID NO. 10. - 제8항 내지 제10항 중 어느 한 항에 있어서,
상기 프라이머는,
60 내지 75℃, 바람직하게는 72℃의 어닐링 온도(annealing temperature)를 가지는 것을 특징으로 하는, 키트. - 제8항 내지 제11항 중 어느 한 항에 있어서,
상기 프라이머 세트는,
정량적 실시간 RT-PCR에 의하여 BAG3 RNA 또는 그 단편의 검출 및/또는 정량에 적절한 것인, 키트. - 제8항에 있어서,
상기 생물학적 샘플은,
혈청(serum), 혈장(plasma), 소변(urine), 타액(saliva) 또는 조직 샘플(tissue sample)인 것인, 키트. - 제13항에 있어서,
상기 혈청, 혈장, 소변, 타액 또는 조직 샘플은,
포유동물, 바람직하게 인간으로부터 획득되는 것인, 키트. - 제8항 내지 제14항 중 어느 한 항에 있어서,
상기 키트는,
병리 상태의 진단에서 사용되는 것인 키트. - 제15항에 있어서,
상기 병리 상태는,
심장병, 암, 당뇨병, 염증 및 피부, 신경, 뼈, 혈관 및 결합조직의 염증관련질환 중에서 선택되는 것인, 키트. - 제16항에 있어서,
상기 심장병은,
협심증(angina pectoris), 경색전 협심증(pre-infarction angina), 심근경색증(myocardial infarction), 심부전(heart failure), 국소 빈혈(ischemia), 급성 관상동맥 질환(acute coronary disease), 급성심부전(acute heart failure), 만성심부전(chronic heart failure), 및 의인성 심장질환(iatrogenic heart disease) 중에서 선택되는 것인, 키트. - 제16항에 있어서,
상기 암은,
췌장암, 방광암, 및 전립선암 중에서 선택되는 것인, 키트 - 생물학적 샘플에서 BAG3 RNA 또는 그 단편의 레벨을 검출 및/또는 정량하는 방법에 있어서,
a. 혈청, 혈장, 소변, 타액 또는 조직으로 구성된 생물학적 샘플을 획득하는단계;
b. 상기 생물학적 샘플로부터 전체 RNA를 추출하는 단계;
c. 정량적 실시간 RT-PCR(quantitative real-time RT-PCR)에 의하여 상기 BAG3 RNA 또는 그 단편을 정량하는 단계;를 포함하는, 방법. - 제19항에 있어서,
d. 상기 생물학적 샘플로부터 획득된 수치를 참조 수치 또는 건강한 기증자로부터 획득된 수치와의 비교하는 단계;를 더 포함하는, 방법. - 제19항 또는 제20항에 있어서,
상기 혈청, 혈장, 소변, 타액 또는 조직 샘플은 포유동물, 바람직하게 인간으로부터 획득되는 것인, 방법. - 제19항 내지 제21항 중 어느 한 항에 있어서,
상기 BAG3 RNA 또는 그 단편의 존재는 병리 상태와 관련되는 것인, 방법. - 제22항에 있어서,
상기 병리 상태는,
심장병, 암, 당뇨병, 염증 및 피부, 신경, 뼈, 혈관 및 결합조직의 염증관련질환 중에서 선택되는 것인, 방법. - 제23항에 있어서,
상기 심장병은,
협심증(angina pectoris), 경색전 협심증(pre-infarction angina), 심근경색증(myocardial infarction), 심부전(heart failure), 국소 빈혈(ischemia), 급성 관상동맥 질환(acute coronary disease), 급성심부전(acute heart failure), 만성심부전(chronic heart failure), 및 의인성 심장질환(iatrogenic heart disease) 중에서 선택되는 것인, 방법. - 제23항에 있어서,
상기 암은,
췌장암, 방광암 및 전립선암 중에서 선택되는 것인, 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP12172531.1 | 2012-06-19 | ||
| EP12172531.1A EP2676966A1 (en) | 2012-06-19 | 2012-06-19 | BAG3 as biochemical serum and tissue marker |
| PCT/EP2013/061971 WO2013189775A1 (en) | 2012-06-19 | 2013-06-11 | Bag3 as biochemical serum and tissue marker |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20150036102A true KR20150036102A (ko) | 2015-04-07 |
Family
ID=48607259
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR20157001228A KR20150036102A (ko) | 2012-06-19 | 2013-06-11 | 혈청 및 조직 생화학 마커로서 bag3 |
| KR1020157001313A KR102150903B1 (ko) | 2012-06-19 | 2013-06-11 | 혈청 및 조직 생화학 마커로서 bag3 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020157001313A KR102150903B1 (ko) | 2012-06-19 | 2013-06-11 | 혈청 및 조직 생화학 마커로서 bag3 |
Country Status (12)
| Country | Link |
|---|---|
| US (2) | US20150132764A1 (ko) |
| EP (3) | EP2676966A1 (ko) |
| JP (2) | JP2015521475A (ko) |
| KR (2) | KR20150036102A (ko) |
| CN (2) | CN104507965B (ko) |
| AU (2) | AU2013279604B2 (ko) |
| BR (2) | BR112014031958A2 (ko) |
| CA (2) | CA2876922C (ko) |
| ES (1) | ES2795981T3 (ko) |
| IN (2) | IN2014DN10561A (ko) |
| PL (1) | PL2861618T3 (ko) |
| WO (2) | WO2013189778A1 (ko) |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ITMI20130403A1 (it) * | 2013-03-18 | 2014-09-19 | Biouniversa Srl | Anticorpi anti-bag3 per uso terapeutico |
| CN105021825B (zh) * | 2015-07-09 | 2016-08-17 | 陈勇 | 一种检测胰腺癌相关多肽dap44的elisa试剂盒 |
| CN105769900A (zh) * | 2016-03-22 | 2016-07-20 | 山西大学 | Bag3基因在制备抗膀胱癌药物中的应用 |
| IT201600069391A1 (it) * | 2016-07-04 | 2016-10-04 | Univ Degli Studi Di Salerno | Uso della proteina bag3 e suoi frammenti peptidici per il controllo dell’omeostasi vascolare |
| WO2021140173A1 (en) | 2020-01-10 | 2021-07-15 | Biouniversa S.R.L. | Methods and uses for treating fibrotic solid tumors with bags inhibitors |
| US11940450B2 (en) | 2021-03-16 | 2024-03-26 | University Of Connecticut | Biomarker panel for non-invasive diagnosis of congenital renal dysfunction |
| CN113862361B (zh) * | 2021-10-25 | 2023-08-15 | 中山大学孙逸仙纪念医院 | 一种诊断和治疗膀胱癌的分子标志物hsf1及其用途 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5652223A (en) * | 1994-03-14 | 1997-07-29 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | DNA encoding CAI resistance proteins and uses thereof |
| AU5789500A (en) * | 1999-07-09 | 2001-01-30 | Burnham Institute, The | A method for determining the prognosis of cancer patients by measuring levels ofbag expression |
| US20030073623A1 (en) * | 2001-07-30 | 2003-04-17 | Drmanac Radoje T. | Novel nucleic acid sequences obtained from various cDNA libraries |
| EP2131198B1 (en) * | 2001-09-20 | 2013-03-27 | Board of Regents, The University of Texas System | Measuring circulating therapeutic antibody, antigen and antigen/antibody complexes using ELISA assays |
| EP1323733A1 (en) * | 2001-12-28 | 2003-07-02 | Arturo Leone | BAG3 nucleotide and protein sequences to be used in research, diagnostics and therapy for cell death-involving diseases |
| US20090047689A1 (en) * | 2007-06-20 | 2009-02-19 | John Kolman | Autoantigen biomarkers for early diagnosis of lung adenocarcinoma |
| WO2011044927A1 (en) * | 2009-10-12 | 2011-04-21 | INSERM (Institut National de la Santé et de la Recherche Médicale) | A method for the diagnosis or prognosis of an advanced heart failure |
| IT1397083B1 (it) * | 2009-12-04 | 2012-12-28 | Biouniversa Srl | Marcatore biochimico serico |
| GB201017520D0 (en) * | 2010-10-15 | 2010-12-01 | Sense Proteomic Ltd | Biomarkers |
-
2012
- 2012-06-19 EP EP12172531.1A patent/EP2676966A1/en not_active Withdrawn
-
2013
- 2013-06-11 KR KR20157001228A patent/KR20150036102A/ko not_active Application Discontinuation
- 2013-06-11 AU AU2013279604A patent/AU2013279604B2/en not_active Ceased
- 2013-06-11 PL PL13728180T patent/PL2861618T3/pl unknown
- 2013-06-11 AU AU2013279601A patent/AU2013279601A1/en not_active Abandoned
- 2013-06-11 KR KR1020157001313A patent/KR102150903B1/ko active IP Right Grant
- 2013-06-11 CN CN201380032138.3A patent/CN104507965B/zh active Active
- 2013-06-11 CA CA2876922A patent/CA2876922C/en active Active
- 2013-06-11 BR BR112014031958A patent/BR112014031958A2/pt not_active IP Right Cessation
- 2013-06-11 WO PCT/EP2013/061976 patent/WO2013189778A1/en active Application Filing
- 2013-06-11 ES ES13728180T patent/ES2795981T3/es active Active
- 2013-06-11 CA CA2876872A patent/CA2876872A1/en not_active Abandoned
- 2013-06-11 CN CN201380032196.6A patent/CN104619861A/zh active Pending
- 2013-06-11 JP JP2015517669A patent/JP2015521475A/ja active Pending
- 2013-06-11 BR BR112014031957A patent/BR112014031957A2/pt not_active IP Right Cessation
- 2013-06-11 WO PCT/EP2013/061971 patent/WO2013189775A1/en active Application Filing
- 2013-06-11 EP EP13728375.0A patent/EP2861754A1/en not_active Ceased
- 2013-06-11 EP EP13728180.4A patent/EP2861618B1/en active Active
- 2013-06-11 JP JP2015517672A patent/JP6654432B2/ja not_active Expired - Fee Related
-
2014
- 2014-12-11 IN IN10561DEN2014 patent/IN2014DN10561A/en unknown
- 2014-12-11 IN IN10562DEN2014 patent/IN2014DN10562A/en unknown
- 2014-12-16 US US14/572,445 patent/US20150132764A1/en not_active Abandoned
- 2014-12-16 US US14/572,654 patent/US10359433B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| AU2013279601A1 (en) | 2015-01-15 |
| EP2861618A1 (en) | 2015-04-22 |
| BR112014031958A2 (pt) | 2017-08-01 |
| EP2676966A1 (en) | 2013-12-25 |
| KR20150036111A (ko) | 2015-04-07 |
| PL2861618T3 (pl) | 2020-09-21 |
| CN104507965B (zh) | 2019-04-26 |
| AU2013279604A1 (en) | 2014-12-18 |
| IN2014DN10561A (ko) | 2015-08-28 |
| CN104507965A (zh) | 2015-04-08 |
| US20150132764A1 (en) | 2015-05-14 |
| JP2015529633A (ja) | 2015-10-08 |
| CA2876922C (en) | 2022-09-20 |
| WO2013189775A1 (en) | 2013-12-27 |
| WO2013189778A1 (en) | 2013-12-27 |
| IN2014DN10562A (ko) | 2015-08-28 |
| AU2013279604B2 (en) | 2018-03-29 |
| BR112014031957A2 (pt) | 2017-08-01 |
| JP6654432B2 (ja) | 2020-02-26 |
| US10359433B2 (en) | 2019-07-23 |
| JP2015521475A (ja) | 2015-07-30 |
| CA2876872A1 (en) | 2013-12-27 |
| CN104619861A (zh) | 2015-05-13 |
| CA2876922A1 (en) | 2013-12-27 |
| EP2861754A1 (en) | 2015-04-22 |
| EP2861618B1 (en) | 2020-03-11 |
| KR102150903B1 (ko) | 2020-09-03 |
| ES2795981T3 (es) | 2020-11-25 |
| US20150147767A1 (en) | 2015-05-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20150036102A (ko) | 혈청 및 조직 생화학 마커로서 bag3 | |
| WO2015089575A1 (en) | Method of diagnosis and treatment | |
| JP2011501741A (ja) | がんの診断および治療のためのtaz/wwtr1 | |
| CN106461681B (zh) | 用于诊断血管疾病的生物标志物及其用途 | |
| US20210077577A1 (en) | Blockade of ccl18 signaling via ccr6 as a therapeutic option in fibrotic diseases and cancer | |
| WO2020081556A2 (en) | Non-canonical swi/snf complex and uses thereof | |
| EP3217175B1 (en) | Arteriosclerosis detection method using deoxyhypusine synthase gene as indicator | |
| KR101983435B1 (ko) | Rnf20의 신장암 또는 간암 진단, 치료 및 치료제 스크리닝 용도 | |
| EP2799546B1 (en) | Radiation exposure diagnostic marker igfbp-5 and method for diagnosing radiation exposure by measuring the expression level of the marker | |
| US20080219981A1 (en) | Diagnostic Kit for Solid Cancer and Medicament for Solid Cancer Therapy | |
| KR102258977B1 (ko) | CDK1-Cyclin B1의 결합 억제제를 이용한 암 치료물질의 스크리닝 방법 | |
| EP2816354B1 (en) | Biomarker for complex regional pain syndrome (CRPS) | |
| KR20190020364A (ko) | 혈액 내 gastrokine 1 단백을 이용하는 위암 진단 | |
| JP2007267660A (ja) | 抗癌剤のスクリーニング方法 | |
| KR20200062460A (ko) | CDK1-Cyclin B1의 결합 억제제를 이용한 암 치료물질의 스크리닝 방법 | |
| KR20200135994A (ko) | 심장 근육 손상의 진단 방법 | |
| KR101179651B1 (ko) | 피부 편평세포암 진단 또는 예후 마커인 nqo-1 및 이의 용도 | |
| CN115976196A (zh) | ErbB3作为肺动脉高压生物标志物和治疗靶点的应用 | |
| EP2721410A2 (en) | Biomarkers for epithelial cancer diagnosis and treatment | |
| JP2007139656A (ja) | 食道癌診断キット | |
| KR20210073226A (ko) | Wasf2 자가항체를 이용한 간세포암종 조기진단용 조성물 | |
| TW200827718A (en) | Alpha-enolase specific antibody and method of use | |
| WO2017023649A1 (en) | Detection of elevated levels of phosphorylated mcm and method of increasing mcm phosphorylation capacity |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |