KR20140113931A - 디알킬 카르보네이트와 알켈렌 글리콜을 수득하는 방법 - Google Patents
디알킬 카르보네이트와 알켈렌 글리콜을 수득하는 방법 Download PDFInfo
- Publication number
- KR20140113931A KR20140113931A KR1020147018561A KR20147018561A KR20140113931A KR 20140113931 A KR20140113931 A KR 20140113931A KR 1020147018561 A KR1020147018561 A KR 1020147018561A KR 20147018561 A KR20147018561 A KR 20147018561A KR 20140113931 A KR20140113931 A KR 20140113931A
- Authority
- KR
- South Korea
- Prior art keywords
- carbonate
- stream
- alkylene
- alkylene glycol
- dialkyl carbonate
- Prior art date
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D3/00—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping
- B01D3/009—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping in combination with chemical reactions
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D3/00—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping
- B01D3/14—Fractional distillation or use of a fractionation or rectification column
- B01D3/141—Fractional distillation or use of a fractionation or rectification column where at least one distillation column contains at least one dividing wall
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D3/00—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping
- B01D3/34—Distillation or related exchange processes in which liquids are contacted with gaseous media, e.g. stripping with one or more auxiliary substances
- B01D3/36—Azeotropic distillation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C29/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring
- C07C29/74—Separation; Purification; Use of additives, e.g. for stabilisation
- C07C29/76—Separation; Purification; Use of additives, e.g. for stabilisation by physical treatment
- C07C29/80—Separation; Purification; Use of additives, e.g. for stabilisation by physical treatment by distillation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C29/00—Preparation of compounds having hydroxy or O-metal groups bound to a carbon atom not belonging to a six-membered aromatic ring
- C07C29/74—Separation; Purification; Use of additives, e.g. for stabilisation
- C07C29/76—Separation; Purification; Use of additives, e.g. for stabilisation by physical treatment
- C07C29/86—Separation; Purification; Use of additives, e.g. for stabilisation by physical treatment by liquid-liquid treatment
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C68/00—Preparation of esters of carbonic or haloformic acids
- C07C68/06—Preparation of esters of carbonic or haloformic acids from organic carbonates
- C07C68/065—Preparation of esters of carbonic or haloformic acids from organic carbonates from alkylene carbonates
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C68/00—Preparation of esters of carbonic or haloformic acids
- C07C68/08—Purification; Separation; Stabilisation
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/10—Process efficiency
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/582—Recycling of unreacted starting or intermediate materials
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
본 발명은 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림으로부터 디알킬 카르보네이트와 알킬렌 글리콜을 수득하는 방법으로서, 하기 단계를 포함하는 방법에 관한 것이다:
(a) 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림으로부터 제1 증류 스테이지(1)에서 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림(5)을 증류로 빼내는 단계,
(b) 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림(5)을 상 분리용 장치(25)에서 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림(27)과 실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림(29)으로 분리하는 단계.
(a) 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림으로부터 제1 증류 스테이지(1)에서 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림(5)을 증류로 빼내는 단계,
(b) 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림(5)을 상 분리용 장치(25)에서 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림(27)과 실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림(29)으로 분리하는 단계.
Description
본 발명은 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림(stream)으로부터 디알킬 카르보네이트와 알킬렌 글리콜을 수득하는 방법에 관한 것이다.
디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림은 전형적으로 촉매 존재하에 알코올과 시클릭 알킬렌 카르보네이트의 에스테르 교환에 의해 주생성물로서 디알킬 카르보네이트 및 부산물로서 알킬렌 글리콜의 제조에서 발생한다.
알킬렌 글리콜이 부산물로서 동시에 형성되는, 시클릭 알킬렌 카르보네이트와 알코올로부터 디알킬 카르보네이트의 제조는 공지되어 있고 이전에 여러 번 기재된 바 있다. 합성은 디알킬 카르보네이트와 알킬렌 글리콜의 생성물 혼합물이 또한 항상 미전환 알킬렌 카르보네이트와 알코올의 비율을 포함하는 가역적 평형 반응이다. 여러 증류 컬럼에서 생성물의 하류 정제와 함께 반응기 중 에스테르 교환 반응은 예를 들어 WO-A 제2001/058168호에 기재되어 있다. 여기서 기재한 에스테르 교환 반응에서, 평형에서 가능한 전환을 이룰 수 있을 뿐이다. 미전환 출발 물질은 생성물로부터 최대 순도로 제거되어야 하며, 그 이유는 에스테르 교환 반응으로 재순환된 생성물이 바람직하지 않게 평형에 영향을 미치고 생산성을 떨어트리기 때문이다.
별도 반응기에서 에스테르 교환 반응에 더하여, 공지된 대안은 알코올과 알킬렌 카르보네이트가 공급되고, 성분의 에스테르 교환과 분별이 컬럼에서 동시에 진행되는 반응성 증류를 사용하는 것이다. 이러한 반응성 증류는 예를 들어 JP-A 2005/357704, US 6,346,638, EP-A 1 967 507 또는 DE-A 10 2009 030 680에 기재되어 있다. 반응성 증류에서 생성물의 증류 제거는 유용하게는 반응의 평형에 영향을 미친다. 그러나, 이러한 반응성 증류는 반응 또는 필요한 전환에 요구된 체류 시간이 컬럼에서 성립될 수 있는 때에만 가능하다. 반응성 증류 컬럼에서 체류 시간에 대한 유용한 영향은 예를 들어 US-A 2009/030223에 기재된 적합한 길이/직경 비에 의해 또는 DE-A 10 2009 030 680에 기재된 바와 같이, 알코올 및 워크업(workup)으로부터 재순환된 스트림으로서 알코올과 디알킬 카르보네이트를 포함하는 혼합물의 공급물 지점 사이의 특정 거리 비에 의해 성취될 수 있다. 그러나, 디알킬 카르보네이트를 포함하고 상단을 통해 빼낸 저비등 혼합물이 또한 미전환 알코올을 포함하며, 하부에서 빼낸 알킬렌 글리콜이 추가로 또한 미전환 알킬렌 카르보네이트를 포함한다는 단점이 있다. 이들 경우에, 디알킬 카르보네이트는 하나 이상의 추가 증류 컬럼에서 정제된다. 이 부분은 장치 면에서 에너지 집약적이고 복잡하며, 그 이유는 형성되는 알코올과 디알킬 카르보네이트가 일반적으로 공비혼합물을 형성하기 때문이다. 이러한 분리용 증류의 성능은 예를 들어 US-A 2005/0080287에 기재되어 있다. 개시된 또다른 대안은 추출 증류에 의해 혼합물을 분리하는 것이며, 이 경우 알킬렌 카르보네이트는 추출제로서 사용된다. 이는 예를 들어 US-A 2007/197816에 개시되어 있다. 그 후 디알킬 카르보네이트는 추가 증류에서 추출제로부터 제거된다.
반응 중 조기에 평형으로부터 디알킬 카르보네이트를 빼내기 위해, US 5,489,703에서는 반응 존 내에서 조기에 추출제를 첨가하는 것을 개시하고 있다. 미전환 알코올이 합성으로 재순환된다면, 이 경우에도 생성물의 일부가 포함된다. 그러나, 에스테르 교환 반응으로 생성물의 재순환은 평형에 대해 바람직하지 못한 효과를 가지며, 그 이유는 출발 물질의 형성이 촉진되고 따라서 생산성이 악화되기 때문이다. 더 높은 전환율을 얻기 위해, US 5,847,189에서는 반응기가 외부에 있고, 따라서 알코올과 디알킬 카르보네이트를 포함하는 혼합물의 공급이 또한 고전환율로 유도될 수 있는 구조를 제안하고 있다. 그러나, 생성물을 얻기 위해, 알코올 디알킬 카르보네이트 공비혼합물의 하류 증류 정제가 여기서 역시 필요하다.
알킬렌 글리콜이 부산물로서 얻어지는, 선행 기술로부터 공지되어 있는 모든 공정에서, 추가 정제 단계가 필요하며, 여기서 알킬렌 글리콜은 미정제 생성물로부터 제거되며 미전환 알킬렌 카르보네이트는 합성으로 재순환된다. 그러나, 고온에서 장기 체류 시간으로, 특히 에스테르 교환 반응에 사용된 촉매의 존재하에 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 혼합물의 워크업은 부반응을 야기시켜 폴리알킬렌 글리콜 예컨대 디알킬렌 글리콜 및 트리알킬렌 글리콜을 제공한다. 이들 부반응을 피하기 위해, 불가피하게 알킬렌 카르보네이트-알킬렌 글리콜 공비혼합물을 형성하는 감압하 적당한 조건하에 증류를 수행할 필요가 있다. 이러한 공비혼합물은 고함량의 알킬렌 글리콜을 포함한다. 그러나, 알킬렌 글리콜과 함께 미전환 알킬렌 카르보네이트의 동시 재순환은 다시 에스테르 교환 반응의 평형에 대해 바람직하지 못한 효과가 있고 생산성을 감소시킨다.
알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 혼합물의 워크업과 고순도 알킬렌 글리콜의 제조는 예를 들어 US 5,847,189에 기재되어 있다. 워크업에 대해, 알킬렌 카르보네이트와 물 스트림을 포함하는 고비등 혼합물을 함께 연속으로 가수분해 반응기로 통과시키고, 형성된 알킬렌 글리콜을 연속으로 빼낸다. 물의 공급으로 알킬렌 카르보네이트의 알킬렌 글리콜과 이산화탄소로 분해를 초래한다.
대안으로서, US-A 2003/0078448에서는 알킬렌 글리콜을 정제하는 방법을 기재하고 있으며, 여기서 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 혼합물을 처음에 증류하고 알킬렌 카르보네이트-알킬렌 글리콜 공비혼합물 분획과 순수 알킬렌 글리콜로 분리한다. 알킬렌 카르보네이트-알킬렌 글리콜 공비혼합물을 순수 알킬렌 글리콜과 이산화탄소로 알킬렌 카르보네이트의 가수분해에 의해 전환시킨다. 그러나, 가수분해의 단점은 알킬렌 카르보네이트가 분해되어서 더 이상 가치 있는 디알킬 카르보네이트로 전환될 수 없다는 것이다. 이 부분은 이산화탄소로서 얻어지고 공정에서 상실된다.
가수분해를 방지하기 위해, JP-A 2006/023065에서는 다단계 정제를 수행하는 것을 개시하고 있으며, 여기서 알킬렌 글리콜과 알킬렌 카르보네이트를 포함하는 하부 스트림을 추가 컬럼에서 증류하고 알킬렌 글리콜을 측면 유출(side draw)로부터 얻는다.
알킬렌 글리콜의 정제를 위해, US 6,479,689에서는 시클릭 알킬렌 카르보네이트와 알킬렌 글리콜의 부분 사이의 에테르 형성 반응을 기재하고 있다. 반응 후 컬럼에서 상단을 통해 제거되는 이산화탄소 포함 저비등 혼합물, 및 알킬렌 글리콜을 포함하는 하부 분획으로 분리가 이어진다. 이산화탄소를 추가 컬럼에서 질소에 의해 저비등 혼합물로부터 휘산시키고 디알킬 카르보네이트가 존재하거나 부재한 알코올을 포함하는 저비등 혼합물을 반응성 증류 컬럼으로 복귀시킨다. 그러나, 이 실시형태는 비슷하게 알킬렌 글리콜의 정제를 위해 다단계 워크업 시퀀스를 필요로 하며 에테르 화합물로서 알킬렌 카르보네이트의 손실을 초래한다.
선행 기술로부터 공지된 모든 공정에서, 불리하게도 에스테르 교환에서 유래하는 생성물 혼합물의 분리는 복잡한 장치에 의해 에너지 집약적인 방식으로만 수행될 수 있다. 이는 특히 디알킬 카르보네이트가 사용된 알코올과 공비혼합물을 형성하는 경우이다. 이의 결과는, 출발 물질이 추가의 복잡한 분리 조작 없이 합성으로 재순환되는 경우, 또한 생성물의 일부가 항상 회송되어서, 에스테르 교환 반응에 바람직하지 못하게 영향을 미친다는 것이다. 또한, 선행 기술로부터 공지된 공정에서, 형성된 미전환 알킬렌 카르보네이트와 알킬렌 글리콜의 호모공비혼합물(homoazeotrope)의 분리는 분해 또는 반응에 의해만 가능하며 따라서 알킬렌 카르보네이트의 손실이 있거나, 다단계에 의해서만 가능하며 따라서 에너지 집약적 증류이다.
따라서 본 발명의 목적은 디알킬 카르보네이트를 제조하는 연속 방법을 제공하는 것이며, 이 방법은 선행 기술로부터 알려진 단점이 없으며 생성물과 미전환 반응물은 에너지적으로 유리한 방식으로 그리고 장치 복잡성이 더 낮은 수준으로서 분리될 수 있다.
본 목적은 하기 단계를 포함하는, 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림으로부터 디알킬 카르보네이트와 알킬렌 글리콜을 수득하는 방법에 의해 달성된다:
(a) 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림으로부터 제1 증류 스테이지(stage)에서 헤테로공비혼합물(heteroazeotrope)로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림을 증류로 빼내는 단계,
(b) 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림을 상 분리용 장치에서 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림과 실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림으로 분리하는 단계.
도 1은 제1 실시형태에서 본 발명에 따른 공정의 플로우 다이어그램이며;
도 2는 제2 실시형태에서 본 발명에 따른 공정의 플로우 다이어그램이다.
도 2는 제2 실시형태에서 본 발명에 따른 공정의 플로우 다이어그램이다.
본 발명의 본문에서, "실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림"은 이 스트림에서 디알킬 카르보네이트의 비율이 70 중량% 이상, 바람직하게는 90 중량% 이상 및 특히 95 중량% 이상인 것을 의미한다. 디알킬 카르보네이트에 더해, 제1 미정제 생성물 스트림은 일반적으로 또한 알킬렌 글리콜의 잔류물을 포함한다.
"실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림"은 이 미정제 생성물 스트림이 70 중량% 이상의 알킬렌 글리콜, 더 바람직하게는 90 중량% 이상의 알킬렌 글리콜 및 특히 95 중량% 이상의 알킬렌 글리콜을 포함하는 것을 의미한다. 알킬렌 글리콜에 더해, 제2 미정제 생성물 스트림은 일반적으로 또한 디알킬 카르보네이트의 잔류물을 포함한다.
본 발명에 따른 방법 및 상 분리용 장치에 의해 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림의 분리는 선행 기술로부터 알려진 공정에서보다 장치 복잡성이 더 낮은 수준으로 에너지 조건이 더 낮게 생성물 혼합물을 분리할 수 있게 한다.
본 발명에 따른 방법을 수행할 수 있기 위해, 형성되는 알킬렌 글리콜과 함께 헤테로공비혼합물을 형성하는 디알킬 카르보네이트를 알킬렌 카르보네이트의 에스테르 교환의 결과로서 형성하는 알코올을 이용하여 디알킬 카르보네이트를 제조할 필요가 있다. 헤테로공비혼합물의 형성으로 에너지 비용 없이 상 분리용 장치에서 분리가 가능하다. 사용된 알코올이 반응에서 형헝되는 디알킬 카르보네이트와 공비혼합물을 형성하지 않는 경우가 더 바람직하다.
디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림으로서, 이로부터 헤테로공비혼합물로서 디알킬 카르보네이트 및 알킬렌 글리콜을 포함하는 스트림이 증류에 의해 제거되는 스트림은 알킬렌 카르보네이트를 알코올과 에스테르 교환반응시켜 디알킬 카르보네이트를 제공하는 에스테르 교환 반응에서 유래한다. 알킬렌 글리콜은 부산물로서 얻어진다.
에스테르 교환은 일반적으로 균일 또는 비균일 촉매하에 수행된다. 균일 촉매의 경우에, 촉매는 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림에 비슷하게 존재한다. 적합한 촉매는 당업자에게 알려져 있으며 예를 들어 DE-A 10 2009 053 370, EP-A 1 961 721 및 WO-A 201 1/058168에 기재되어 있다. 적합한 균일 촉매의 일예는 알칼리 금속, 유기산 예컨대 아세트산, 프로피온산, 부티르산, 벤조산, 스테아르산의 알칼리 금속염, 알칼리 금속의 수소화물, 산화물, 수산화물, 알콕시드, 아미드, 카르보네이트 또는 디카르보네이트 또는 무기산, 예를 들어 염산, 브롬화수소산 또는 요오드화수소산, 질산, 황산, 불산, 인산, 시안화수소, 시안화수소산 또는 티오시안산에서 유도되는 알칼리 금속염을 포함한다.
수산화칼륨, 수산화나트륨 또는 에스테르 교환에서 사용된 알코올의 칼륨 또는 나트륨염을 사용하는 것이 바람직하다.
균일 촉매의 양은 전형적으로 10 중량% 미만, 일반적으로 0.0001 내지 5 중량%의 범위 및 특히 0.001 내지 2 중량%의 범위이며, 각 경우 반응 혼합물의 양을 기준으로 한다.
원칙적으로, 또한 비균일 촉매하에 에스테르 교환을 수행할 수 있다. 촉매 반응은 상류 반응기에서 또는 제1 증류 스테이지에서 수행될 수 있다. 적합한 비균일 촉매는 예를 들어 3차 아민으로부터 형성된 작용기, 사차 암모늄 기(이 경우 짝이온의 일예는 염화물, 황산수소염 또는 수산화물이다)가 있는 이온교환수지, 암모늄 교환 제올라이트 또는 이산화규소 지지체상에 함침된 알칼리 금속 또는 알칼리 토금속 실리케이트이다.
반응은 별도 반응기에서 수행될 수 있으며, 이 경우 알킬렌 카르보네이트 및 알코올과 촉매는 반응기에 공급되고 에스테르 교환은 반응기에서 수행된다. 그 후 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림을 반응기에서 빼내 단계 (a)에서 제1 증류 스테이지로 공급한다. 대안으로, 단계 (a)에서 제1 증류 스테이지는 알킬렌 카르보네이트와 알코올이 반응물로서 첨가되고 평형 반응에서 디알킬 카르보네이트와 알킬렌 글리콜로 전환되어, 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 모노알코올을 포함하는 스트림을 제공하는 반응성 증류물(distillation)을 포함하는 것이 또한 가능하다. 반응성 증류 컬럼에서, 헤테로공비혼합물로서 알킬렌 글리콜과 디알킬 카르보네이트를 포함하는 스트림은 그 후 이 스트림으로부터 제거된다.
제1 실시형태에서, 제1 증류 스테이지는 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림이 알코올 포함 상단 스트림, 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하고 하부 스트림으로서 호모공비혼합물을 형성하는 스트림, 및 디알킬 카르보네이트와 알킬렌 글리콜을 헤테로공비혼합물로서 포함하고 사이드 스트림으로서 빼내는 스트림으로 분리되는 격벽 컬럼(dividing wall column)을 포함한다. 알코올 포함 상단 스트림은 반응물로서 반응기로 또는 반응성 증류 컬럼으로 바로 재순환될 수 있다. 하부 스트림은 호모공비혼합물을 형성하는 알킬렌 카르보네이트와 알킬렌 글리콜에 더해 일반적으로 추가로 또한 에스테르 교환에 사용된 촉매를 포함한다. 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하고 격벽 컬럼으로부터 측면 유출을 통해 빼내는 스트림은 촉매가 존재하지 않는다.
격벽 컬럼에 대안으로, 또한 제1 증류 스테이지가 2개의 증류 컬럼을 포함하는 것이 가능하며, 이 경우 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림은 디알킬 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 상단 스트림, 및 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 호모공비혼합물 형성 하부 스트림으로 분리된다. 제2 증류 컬럼에서, 제1 증류 컬럼으로부터 디알킬 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 상단 스트림은 알코올을 포함하는 상단 스트림과 하부 스트림으로서 디알킬 카르보네이트와 알킬렌 글리콜을 헤테로공비혼합물로서 포함하는 스트림으로 분리된다.
격벽 컬럼으로부터 측면 유출로서 또는 제2 증류 컬럼으로부터 하부 스트림으로서 얻어지고 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림을 그 후 단계 (b)에서 상 분리용 장치에서 분리를 위해 이송한다.
바람직한 실시형태에서, 호모공비혼합물 형성 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하고, 제1 증류 스테이지에서 얻어지며 격벽 컬럼의 하부 스트림으로서 또는 제1 증류 컬럼의 하부 스트림으로서 얻어지는 스트림을 제2 증류 스테이지로 이송한다. 연행제(entraining agent)로서 단계 (b)로부터 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림의 일부는 추가로 제2 증류 스테이지에 공급된다. 알킬렌 카르보네이트를 포함하는 하부 스트림과 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 상단 스트림을 그 후 제2 증류 스테이지로부터 빼낸다. 그 후 알킬렌 카르보네이트를 포함하는 하부 스트림을 비슷하게 반응물로서 에스테르 교환으로 재순환시킨다. 에스테르 교환이 균일 촉매 반응하에 수행되는 경우, 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하고 제2 증류 스테이지로 이송되는 호모공비혼합물 형성 스트림은 추가로 또한 촉매를 포함한다. 이는 비슷하게 제2 증류 스테이지의 하부에서 얻어지며 알킬렌 카르보네이트와 함께 에스테르 교환으로 재순환될 수 있다. 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 상단 스트림을 디알킬 카르보네이트와 알킬렌 글리콜이 생성물로서 얻어지도록 단계 (b)에서 상 분리용 장치에 공급한다. 이 과정의 결과, 미전환 알킬렌 카르보네이트는 손실 없이 에스테르 교환으로 재순환된다.
제1 증류 스테이지가 격벽 컬럼에서 수행되는 경우, 격벽 컬럼은 압력 0.01 내지 0.5 바의 범위에서, 바람직하게는 0.02 내지 0.2 바의 범위에서 그리고 더 바람직하게는 0.03 내지 0.1 바의 범위에서 운전되는 것이 바람직하다. 격벽 컬럼의 하부에서 온도는 바람직하게는 120 내지 200℃의 범위, 더 바람직하게는 130 내지 190℃의 범위 및 특히 140 내지 180℃의 범위이고 격벽 컬럼의 상단에서 온도는 10 내지 100℃의 범위, 더 바람직하게는 20 내지 80℃의 범위 및 특히 25 내지 60℃의 범위이다.
상기에 그리고 하기에 제시된 압력 수치는 명백히 다르게 언급되지 않는 한 절대 압력 수치이다.
제1 증류 스테이지가 2개의 증류 컬럼에서 수행되는 경우, 제1 증류 컬럼은 압력 0.01 내지 0.5 바의 범위에서, 더 바람직하게는 0.01 내지 0.1 바의 범위에서 그리고 특히 0.01 내지 0.05 바의 범위에서 운전되는 것이 바람직하며, 하부 온도는 바람직하게는 120 내지 200℃의 범위, 더 바람직하게는 130 내지 190℃의 범위 및 특히 150 내지 185℃의 범위이고 상부 온도는 20 내지 100℃의 범위, 더 바람직하게는 30 내지 80℃의 범위 및 특히 40 내지 70℃의 범위이다. 제2 증류 컬럼에서 압력은 바람직하게는 0.05 내지 0.5 바의 범위, 더 바람직하게는 0.1 내지 0.3 바의 범위 및 특히 0.1 내지 0.2 바의 범위이다. 제2 증류 컬럼의 하부에서 온도는 바람직하게는 80 내지 200℃의 범위, 더 바람직하게는 100 내지 150℃의 범위 및 특히 110 내지 130℃의 범위이고, 제2 증류 컬럼의 상단에서 온도는 10 내지 100℃, 더 바람직하게는 20 내지 80℃의 범위 및 특히 25 내지 70℃의 범위이다.
알킬렌 카르보네이트와 알킬렌 글리콜의 호모공비혼합물이 연행제로서 디알킬 카르보네이트의 존재하에 분리되는 제2 증류 스테이지는 압력 0.01 내지 0.5 바의 범위, 더 바람직하게는 0.02 내지 0.2 바의 범위 및 특히 0.05 내지 0.1 바의 범위에서 운전되는 것이 바람직하며, 하부 온도는 바람직하게는 100 내지 200℃, 더 바람직하게는 130 내지 190℃ 및 특히 140 내지 180℃의 범위이며, 상부 온도는 50 내지 150℃의 범위, 더 바람직하게는 80 내지 120℃의 범위 및 특히 바람직하게는 90 내지 110℃의 범위이다.
대안적인 실시형태에서, 제1 증류 스테이지는, 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림이 알킬렌 카르보네이트를 포함하는 하부 스트림, 알코올을 포함하는 상단 스트림, 및 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하고 사이드 스트림으로서 빼내는 스트림으로 분리되는 격벽 컬럼을 포함한다. 대안으로, 이 경우 제1 증류 스테이지는, 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림이 알킬렌 카르보네이트를 포함하는 하부 스트림과 디알킬 카르보네이트, 알코올 및 알킬렌 글리콜을 포함하는 상단 스트림으로 분리되는 제1 증류 컬럼, 및 제1 증류 컬럼으로부터 디알킬 카르보네이트, 알코올 및 알킬렌 글리콜을 포함하는 상단 스트림이 알코올 포함 상단 스트림과 하부 스트림으로서 디알킬 카르보네이트와 알킬렌 글리콜을 헤테로공비혼합물로서 포함하는 스트림으로 분리되는 제2 증류 컬럼을 포함한다. 제1 증류 스테이지가 격벽 컬럼에서 또는 2개의 증류 컬럼에서 수행되는 지에 관계 없이, 단계 (b)로부터 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림의 일부는 연행제로서 추가로 첨가된다. 연행제로서 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림의 첨가로 알킬렌 카르보네이트가 무알킬렌 글리콜 형태로 제거되고 반응에 재순환될 수 있도록, 알킬렌 카르보네이트와 알킬렌 글리콜의 호모공비혼합물을 파괴한다. 이는 평형시 반응에 재순환된 알킬렌 글리콜의 부작용을 피한다. 또한, 이는 알킬렌 글리콜을 포함하는 상단 스트림에서 알킬렌 카르보네이트의 부재와 하류 공정 스테이지로 알킬렌 카르보네이트의 통행 금지를 달성한다.
단계 (b)로부터 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림의 일부가 연행제로서 제1 증류 스테이지로 첨가되는 경우, 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림의 일부를 제1 증류 스테이지로 공급물에 첨가할 수 있다. 대안으로, 또한 디알킬 카르보네이트를 포함하는 제1 미정제 스트림의 일부를 별도 공급물로서 격벽 컬럼 또는 제1 증류 컬럼에 공급할 수 있으며, 이 경우 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림의 일부는 격벽 컬럼의 공급물 측에 또는 제1 증류 컬럼에 알킬렌 카르보네이트와 알코올의 공급물, 또는 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림의 공급물 위로 첨가된다.
생성물의 품질을 향상시키기 위해, 실질적으로 디알킬 카르보네이트를 포함하고 단계 (b)에서 상 분리용 장치로부터 빼내는 제1 미정제 생성물 스트림을, 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림에 아직 존재한 알킬렌 글리콜이 이로부터 제거되는 증류 조작에 공급되는 경우 추가로 바람직하다. 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림으로부터 제거된 알킬렌 글리콜은 아직 디알킬 카르보네이트를 포함하며 따라서 바람직학는 단계 (b)의 상 분리용 장치로 재순환된다. 이는 이것을 비슷하게 생성물로서 증류에서 제거된 디알킬 카르보네이트를 얻을 수 있게 한다.
실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림으로부터 알킬렌 글리콜의 제거를 위한 증류 스테이지는 바람직하게는 0.05 내지 1 바 범위의 압력에서, 더 바람직하게는 0.09 내지 0.5 바 범위의 압력에서 그리고 특히 0.1 내지 0.2 바 범위의 압력에서 수행된다. 상부 온도는 바람직하게는 10 내지 150℃ 범위, 더 바람직하게는 50 내지 145℃ 범위 및 특히 90 내지 140℃ 범위이며, 하부 온도는 80 내지 200℃ 범위, 더 바람직하게는 90 내지 160℃ 범위 및 특히 95 내지 140℃ 범위이다.
비슷하게 생성물로서 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림에 존재한 디알킬 카르보네이트를 얻을 수 있기 위해, 실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물은 바람직하게는 또한 증류 조작(distillative operation)에 이송되어 이로부터 실질적으로 알킬렌 글리콜을 포함하는 미정제 생성물 스트림에 아직 존재한 디알킬 카르보네이트를 제거한다. 일반적으로 디알킬 카르보네이트는 이에 존재한 알킬렌 글리콜과 공비혼합물의 형태로 제거되기 때문에, 또한 단계 (b)에서 상 분리용 장치로 제거된 디알킬 카르보네이트를 재순환시키는 것이 바람직하다. 이는 이것을 비슷하게 생성물로서 증류에서 제거된 알킬렌 글리콜을 얻을 수 있게 한다.
실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림의 처리를 위한 증류는 바람직하게는 0.05 내지 1 바 범위의 압력에서, 더 바람직하게는 0.09 내지 0.3 바 범위의 압력에서 그리고 특히 0.1 내지 0.2 바 범위의 압력에서 수행된다. 하부 온도는 바람직하게는 80 내지 200℃ 범위, 더 바람직하게는 90 내지 180℃ 범위 및 특히 110 내지 150℃ 범위이다. 상부 온도는 바람직하게는 20 내지 180℃ 범위, 더 바람직하게는 50 내지 170℃ 범위 및 특히 80 내지 160℃ 범위이다.
단계 (b)에서 상 분리용 장치는 당업자에게 공지된 임의의 적합한 액체 상분리기, 예를 들어 문헌[Perry's Chemical Engineers' Handbook, seventh edition, 1998, p. 15- 26 내지 15- 27, Gravity Settiers, decanters, 및 Liquid Extraction, second edition, McGraw-Hill Book Company 1963, p. 440- 450]에 언급된 것들일 수 있다.
상 분리용 장치는 바람직하게는 1 내지 5 바 범위, 더 바람직하게는 1 내지 3 바 범위 및 특히 1 내지 2 바 범위의 압력에서 그리고 1 내지 90℃ 범위, 더 바람직하게는 1 내지 50℃ 범위 및 특히 5 내지 40℃ 범위의 온도에서 운전된다.
본 발명에 따른 방법은 연속으로 또는 배치로 수행될 수 있다. 방법을 연속으로 조작하는 것이 바람직하다. 이 목적을 위해, 더 구체적으로는 연속 운전가능한 상 분리용 장치를 사용하는 것이 필요하다.
본 발명에 따른 방법에 적합한 알코올은 하기 화학식(I)의 것들이다:
R-OH (I)
상기 식에서, R은 임의로 또한 고리를 포함하는, 직쇄 또는 분지된 C2-C8-알킬, 직쇄 또는 분지된 C3-C8-알켄일, 직쇄 또는 분지된 C3-C8-알킨일 또는 C3-C8-시클로알킬이며,
1 또는 2개의 비말단 CH2 기는 임의로 기 O로부터 헤테로원자에 의해 치환되고,
C2-알킬을 제외한 R은 비치환되거나 할로겐, C1-C4-알킬, C1-C4-알콕시, C6-C10-아릴, 디-(C1-C4-알킬)-아미노 및 푸릴메틸의 군에서 1 내지 3개의 치환기(할로겐의 경우 가능한 최대수까지)에 의해 치환되며, C2-알킬에 대해 항상 할로겐, C1-C4-알킬, C1-C4-알콕시, C6-C10-아릴, 디-(C1-C4-알킬)-아미노 및 푸릴메틸의 군에서 1 내지 3개의 치환기(할로겐의 경우 가능한 최대수까지)에 의해 치환된다.
일 실시형태에서, R은 직쇄 또는 분지된 C2-C8-알킬이다.
바람직한 실시형태에서, R은 비치환되거나 1개의 메톡시 치환기에 의해 치환되는 직쇄 또는 분지된 C3-C8-알킬이며, 특히 비치환되거나 1개의 메톡시 치환기에 의해 치환되는 직쇄 또는 분지된 C3-C6-알킬이다.
R이 분지된 C2-C8-알킬인 경우, 분지는 바람직하게는 β 및/또는 γ 위치, 더 구체적으로는 β 위치에 있다.
R이 C3-C8-알킨일인 경우, 이것은 바람직하게는 프로파르길이다.
R이 C3-C8-시클로알킬인 경우, 이것은 바람직하게는 시클로펜틸, 시클로헥실 또는 시클로헵틸이며, 특히 시클로펜틸 또는 시클로헥실이다.
비말단 CH2 기가 헤테로원자에 의해 치환되는 경우, 하나의 비말단 CH2 기는 바람직하게는 산소 원자에 의해 치환된다.
특정 실시형태에서 R은 직쇄 C3-C6-알킬이며, 이는 β 위치에 산소 원자를 포함한다.
R이 치환되는 경우, 바람직하게는 β 및/또는 γ 위치, 더 구체적으로는 β 위치가 치환된다.
R이 기 할로겐으로부터의 치환기에 의해 치환되는 경우, 이것은 바람직하게는 1-8개 불소 또는 1-3개 염소 치환기에 의해 치환된다.
R이 기 C1-C4-알킬로부터의 치환기에 의해 치환되는 경우, 이것은 바람직하게는 메틸 또는 에틸 치환기, 특히 메틸 치환기에 의해 치환된다.
R이 기 C1-C4-알콕시로부터의 치환기에 의해 치환되는 경우, 이것은 바람직하게는 1개의 메톡시 또는 에톡시 치환기에 의해 치환된다.
적합한 알코올은 예를 들어 2,2,2-트리플루오로에탄올, 1,1,2,2-테트라플루오로에탄올, 1,1,2,2,2-펜타플루오로에탄올, 1,1,1-트리플루오로-2-프로판올, 1,1-디메틸-1-에탄올, 2-프로판올, 2,2,3,3,4,4,4-헵타플루오로-l-부탄올, 2,2,3,3,3-펜타플루오로-l-프로판올, 1-프로판올, 2-부탄올, 1,1-디메틸-1-프로판올, 이소부탄올, 3-메틸-2-부탄올, 2-프로핀-1-올, 2,2-디메틸-1-프로판올, 3-펜탄올, 1-부탄올, 2,3-디메틸-2-부탄올, 2-펜탄올, 3,3-디메틸-2-부탄올, 2-메틸-2-펜탄올, 3-메틸-3-펜탄올, 2-클로로-1-프로판올, 2-메틸-3-펜탄올, 2-클로로-1-에탄올, 1-클로로-2-프로판올, 2-메틸-1-부탄올, 2,3,3-트리메틸-2-부탄올! 3-메틸-1-부탄올, 4-메틸-2-펜탄올, 2,4-디메틸-2-펜탄올, 3-메틸-2-펜탄올, 1-메틸시클로펜탄올, 3-헥산올, 2,2-디메틸-3-펜탄올, 2,2-디메틸-1-부탄올, 1-펜탄올, 4,4-디메틸-2-펜탄올, 2,4-디메틸-3-펜탄올, 2,3-디메틸-3-펜탄올, 2,3-디메틸-2-펜탄올, 2-헥산올, 시클로펜탄올, 2-메틸-2-헥산올, 3-에틸-3-펜탄올, 3,3-디메틸-1-부탄올, 3-메틸-3-헥산올, 2-에틸-1-부탄올, 2-메틸-3-헥산올, 5-메틸-3-헥산올, 2-메틸-1-펜탄올, 2,3-디메틸-1- 부탄올, 2,4-디메틸-2-헥산올, 5-메틸-2-헥산올, 3,4-디메틸-3-헥산올, 4-메틸-1-펜탄올, 3-메틸-2-헥산올, 3-에틸-2-펜탄올, 2,4-디메틸-4-헥산올, 3-메틸-1-펜탄올, 1-에틸시클로펜탄올, 5-메틸-3-헵탄올, 4-헵탄올, 4-메틸-3-헵탄올, 2,2-디메틸-3-헥산올, 2-메틸-2-헵탄올, 3-헵탄올, 1-헥산올, 2,3-디메틸-3-헥산올, 2-헵탄올, 3-에틸-3-헥산올, 2,5-디메틸-3-헥산올, 4,4-디메틸-1-펜탄올, 2,4-디메틸-3-헥산올, 3-메틸-3-헵탄올, 시클로헥산올, 3-클로로-1-프로판올, 4-메틸-4-헵탄올, 시클로헵탄올, 2,4-디메틸-1-펜탄올, 2-메틸-1-헥산올, 3-메틸-4-헵탄올, 시스-2-메틸시클로헥산올, 3-메틸-2-헵탄올, 2-메틸-4-헵탄올, 트란스-2-메틸시클로헥산올, 2-메틸-3-헵탄올, 2,2,4-트리메틸-1-펜탄올, 1-메틸시클로헥산올, 1-에틸시클로헥산올, 푸르푸릴 알코올, 시스-4-메틸시클로헥산올, 트란스-4-메틸시클로헥산올, 4-메틸-2-헵탄올, 5-메틸-2-헵탄올, 5-메틸-1-헥산올, 3-메틸-1-헥산올, 6-메틸-2-헵탄올, 2,4,4-트리메틸-1-펜탄올, 4-메틸-1-헥산올, 3-옥탄올, 시스-3-메틸시클로헥산올, 1,3-디클로로-2-프로판올, 트란스-3-메틸시클로헥산올, 2,6-디메틸시클로헥산올, 2-메톡시-1-에탄올 또는 2-에톡시-1-에탄올이다.
바람직한 알코올은 1-프로판올, 1-부탄올, 1-펜탄올, 1-헥산올, 이소부탄올, 2-메틸-1-부탄올, 3-메틸-1-부탄올, 또는 2-메톡시에탄올이며, 특히 바람직한 알코올은 1-프로판올, 1-부탄올, 1-펜탄올, 이소부탄올 또는 3-메틸-1-부탄올이다.
본 발명에 따른 방법에 적합한 알킬렌 카르보네이트는 하기 화학식(II)의 알킬렌 카르보네이트이다:
상기 식에서, R1 및 R2는 각각 독립적으로-(CR3R4)m-이며, 여기서 m=1-3이고, R3 및 R4 는 각각 독립적으로, 수소, C1-C10-알킬 또는 C6-C10-아릴이거나 R4 라디칼 둘 다 함께 C5-C10 고리를 형성한다.
사용된 알킬렌 카르보네이트는 더 바람직하게는 에틸렌 카르보네이트 및 프로필렌 카르보네이트이다.
에스테르 교환 반응에서, 알킬렌 카르보네이트의 고리 구조는 파괴되어 열리고 알킬렌 카르보네이트의 R1 및 R2 라디칼은 각각 사용된 알코올의 R 라디칼에 의해 치환된다. 이 경우에, 또한 R1 및 R2 라디칼이 알코올의 상이한 라디칼에 의해 치환되도록, 몇몇 알코올의 혼합물을 사용할 수 있다.
에스테르 교환에서 형성된 디알킬 카르보네이트는 일반적으로 하기 화학식(III)의 것들이다:
상기 식에서, R은 같거나 상이하며 화학식(I)의 알코올의 R 라디칼의 상기 정의에 상응한다.
R은 바람직하게는 같다.
카르보네이트는 대칭이거나 그렇지 않으면 비대칭일 수 있다. 언급된 카르보네이트는 상이한 알코올의 가능한 조합의 선택이다.
에스테르 교환 반응에서 제조가능한 디알킬 카르보네이트는 예를 들어 디-(2,2,2-트리플루오로에틸)-카르보네이트, 디-(1,1,2,2-테트라플루오로에틸)-카르보네이트, 디-(1,1,2,2,2-펜타플루오로에틸)-카르보네이트, 디-(1,1,1-트리플루오로-2-프로필)카르보네이트, 디-1,1-디메틸-1-에틸카르보네이트, 디-2-프로필카르보네이트, 디-(2,2,3,3,4,4,4-헵타플루오로-1-부틸)-카르보네이트, 디-(2,2,3,3,3-펜타플루오로-1-프로필)카르보네이트, 디-1-프로필카르보네이트, 디-2-부틸카르보네이트, 디-1,1-디메틸-1-프로필카르보네이트, 디이소부틸카르보네이트, 디-(3-메틸-2-부틸)-카르보네이트, 디-(2-프로핀-1-올)-카르보네이트, 디-(2,2-디메틸-1-프로필)-카르보네이트, 디-3-펜틸카르보네이트, 디-1-부틸카르보네이트, 디-(2,3-디메틸-2-부틸)-카르보네이트, 디-2-펜틸카르보네이트, 디-(3,3-디메틸-2-부틸)-카르보네이트, 디-(2-메틸-2-펜틸)-카르보네이트, 디-(3-메틸-3-펜틸)-카르보네이트, 디-(2-클로로-1-프로필)-카르보네이트, 디-(2-메틸-3-펜틸)-카르보네이트, 디-(2-클로로-1-에틸)-카르보네이트, 디-(1-클로로-2-프로필)-카르보네이트, 디-(2-메틸-1-부틸)-카르보네이트, 디-(2,3,3-트리메틸-2-부틸)-카르보네이트, 디-(3-메틸-1-부틸)-카르보네이트, 디-(4-메틸-2-펜틸)-카르보네이트, 디-(2,4-디메틸-2-펜틸)-카르보네이트, 디-(3-메틸-2-펜틸)-카르보네이트, 디-(1-메틸시클로펜틸)-카르보네이트, 디-(3-헥실)-카르보네이트, 디-(2,2-디메틸-3-펜틸)-카르보네이트, 디-(2,2-디메틸-1-부틸)-카르보네이트, 디-1-펜틸카르보네이트, 디-(4,4-디메틸-2-펜틸)-카르보네이트, 디-(2,4-디메틸-3-펜틸)-카르보네이트, 디-(2,3-디메틸-3-펜틸)-카르보네이트, 디-(2,3-디메틸-2-펜틸)-카르보네이트, 디-2-헥실카르보네이트, 디-시클로펜틸카르보네이트, 디-(2-메틸-2-헥실)-카르보네이트, 디-(3-에틸-3-펜틸)-카르보네이트, 디-(3,3-디메틸-1-부틸)-카르보네이트, 디-(3-메틸-3-헥실)-카르보네이트, 디-(2-에틸-1-부틸)-카르보네이트, 디-(2-메틸-3-헥실)-카르보네이트, 디-(5-메틸-3-헥실)-카르보네이트, 디-(2-메틸-1-펜틸)-카르보네이트, 디-(2,3-디메틸-1-부틸)-카르보네이트, 디-(2,4-디메틸-2-헥실)-카르보네이트, 디-(5-메틸-2-헥실)-카르보네이트, 디-(3,4-디메틸-3-헥실)-카르보네이트, 디-(4-메틸-1-펜틸)-카르보네이트, 디-(3-메틸-2-헥실)-카르보네이트, 디-(3-에틸-2-펜틸)-카르보네이트, 디-(2,4-디메틸-4-헥실)-카르보네이트, 디-(3-메틸-1-펜틸)-카르보네이트, 디-(1-에틸시클로펜틸)-카르보네이트, 디-(5-메틸-3-헵틸)-카르보네이트, 디-(4-헵틸)-카르보네이트, 디-(4-메틸-3-헵틸)-카르보네이트, 디-(2,2-디메틸-3-헥실)-카르보네이트, 디-(2-메틸-2-헵틸)-카르보네이트, 디-(3-헵틸)-카르보네이트, 디-(1-헥실)-카르보네이트, 디-(2,3-디메틸-3-헥실)-카르보네이트, 디-(2-헵틸)-카르보네이트, 디-(3-에틸-3-헥실)-카르보네이트, 디-(2,5-디메틸-3-헥실)-카르보네이트, 디-(4,4-디메틸-1-펜틸)-카르보네이트, 디-(2,4-디메틸-3-헥실)-카르보네이트, 디-(3-메틸-3-헵틸)-카르보네이트, 디-(시클로헥실)-카르보네이트, 디-(3-클로로-1-프로필)-카르보네이트, 디-(4-메틸-4-헵틸)-카르보네이트, 디-(시클로헵틸)-카르보네이트, 디-(2,4-디메틸-1-펜틸)-카르보네이트, 디-(2-메틸-1-헥실)-카르보네이트, 디-(3-메틸-4-헵틸)-카르보네이트, 디-(시스-2-메틸시클로헥실)-카르보네이트, 디-(2-메틸시클로헥실)-카르보네이트, 디-(3-메틸-2-헵틸)-카르보네이트, 디-(2-메틸-4-헵틸)-카르보네이트, 디-(트란스-2-메틸시클로헥실)-카르보네이트, 디-(3-히드록시-2-메틸 프로피온알데히드)-카르보네이트, 디-(2-메틸-헵틸-3)-카르보네이트, 디-(2,2,4-트리메틸-1-펜틸)-카르보네이트, 디-(1-메틸시클로-헥실)-카르보네이트, 디-(1-에틸시클로헥산올)-카르보네이트, 디-(2-헥신-1-올)-카르보네이트, 디-(2-푸란메틸)-카르보네이트, 디-(시스-4-메틸시클로헥실)-카르보네이트, 디-(트란스-4-메틸시클로-헥실)-카르보네이트, 디-(4-메틸-2-헵틸)-카르보네이트, 디-(5-메틸-2-헵틸)-카르보네이트, 디-(5-메틸-1-헥실)-카르보네이트, 디-(3-메틸-1-헥실)-카르보네이트, 디-(6-메틸-2-헵틸)-카르보네이트, 디-(2,4,4-트리메틸-1-펜틸)-카르보네이트, 디-(4-메틸-1-헥실)-카르보네이트, 디-(3-옥틸)-카르보네이트, 디-(시스-3-메틸시클로헥실)-카르보네이트, 디-(1,3-디클로로-2-프로필)-카르보네이트, 디-(트란스-3-메틸시클로헥실)-카르보네이트, 디-(2,6-디메틸시클로헥실)-카르보네이트, 디-2-메톡시에틸카르보네이트 또는 디-2-에톡시에틸카르보네이트이다.
바람직한 디알킬 카르보네이트는 디-1-프로필카르보네이트, 디-1-부틸카르보네이트, 디-1-펜틸카르보네이트, 디-1-헥실카르보네이트, 디이소부틸카르보네이트, 디-2-메틸-1-부틸카르보네이트, 디-3-메틸부틸카르보네이트 또는 디-2-메톡시에틸카르보네이트이다.
더 바람직한 디알킬 카르보네이트 디-1-프로필카르보네이트, 디-1-부틸카르보네이트, 디-1-펜틸카르보네이트, 디이소부틸카르보네이트, 디-3-메틸-1-부틸카르보네이트 또는 디-2-메톡시에틸카르보네이트이다.
사용된 알코올의 히드록실 기와 에스테르 교환에서 유리된 R1 및 R2 라디칼은 하기 화학식(IV)의 알킬렌 글리콜을 형성한다:
HO-R1R2-OH (IV)
여기서 R1 및 R2 라디칼은 알킬렌 카르보네이트에 대해 상기에 기재한 것과 같다.
디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림이 공정에 공급되는 경우, 일반적으로 0.5 내지 70 중량%의 디알킬 카르보네이트, 1 내지 50 중량%의 알킬렌 카르보네이트, 1 내지 40 중량%의 알킬렌 글리콜 및 10 내지 95 중량%의 알코올을 포함한다. 스트림은 더 바람직하게는 1 내지 50 중량%의 디알킬 카르보네이트, 2 내지 30 중량%의 알킬렌 카르보네이트, 2 내지 30 중량%의 알킬렌 글리콜 및 20 내지 90 중량%의 알코올을 포함한다. 더 구체적으로는, 스트림은 5 내지 40 중량%의 디알킬 카르보네이트, 5 내지 30 중량%의 알킬렌 카르보네이트, 2 내지 15 중량%의 알킬렌 글리콜 및 40 내지 80 중량%의 알코올을 포함한다.
또한, 스트림은 특히 균일하게 촉매 작용을 한 에스테르 교환 반응의 경우 10 중량% 미만, 더 바람직하게는 5 내지 0.0001 중량% 및 특히 2 내지 0.001 중량%의 촉매를 포함할 수 있다.
본 발명의 실시예는 도면에 제시되어 있고 하기 상세한 설명에 예시된다.
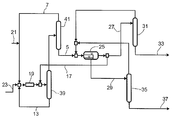
도 1에서는 제1 실시형태로 본 발명에 따른 방법의 플로우 다이어그램을 보여준다.
디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하고 처리될 스트림을 제1 증류 스테이지로 이송한다. 제1 증류 스테이지는 도 1에 도시된 실시형태에서, 격벽 컬럼(1)을 포함한다. 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림의 공급물은 측면 공급물(3)으로서 격벽 컬럼(1)으로 구성된다. 격벽 컬럼(1)에서, 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림은 증류에 의해 제거된다. 이 스트림을 측면 유출(5)로 빼낸다. 격벽 컬럼의 상단에서, 알코올 포함 상단 스트림(7)을 얻는다. 격벽 컬럼(1)의 하부에서 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하고 호모공비혼합물을 형성하는 스트림을 하부 스트림(9)으로서 빼낸다. 하부 스트림(9)으로서 빼낸 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 호모공비혼합물 형성 스트림을 제2 증류 스테이지(11)로 이송한다. 제2 증류 스테이지(11)는 증류 컬럼을 포함한다. 제2 증류 스테이지(11)에서, 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 스트림을, 알킬렌 카르보네이트를 포함하는 하부 스트림(13)과 알킬렌 글리콜과 디알킬 카르보네이트를 포함하는 상단 스트림(15)으로 분리한다. 제2 증류 스테이지(11)에서 호모공비혼합물로서 존재한 알킬렌 카르보네이트와 알킬렌 글리콜의 혼합물을 분리하기 위해, 디알킬 카르보네이트를 추가로 제2 증류 스테이지(11)에 공급한다. 여기서 기재한 실시형태에서, 공급은 알킬렌 글리콜과 알킬렌 카르보네이트의 혼합물의 공급물(9) 위 측면 공급물(17)을 통한다. 제2 증류 스테이지(11)의 하부에서 얻어진 알킬렌 카르보네이트는 격벽 컬럼(1)의 상단에서 얻어진 알코올과 같이 알킬렌 카르보네이트와 알코올이 에스테르 교환 반응으로 반응하여 디알킬 카르보네이트와 알킬렌 글리콜을 제공하는 반응기(19)로 재순환된다. 반응은 평형 반응이며, 따라서 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림을 반응기(19)에서 빼내어 격벽 컬럼(1)로 재순환시킨다. 반응에서 전환된 알코올을 반응기(19)에 제1 공급물(21)을 통해 공급하고, 전환된 알킬렌 카르보네이트를 제2 공급물(23)을 통해 공급한다. 도 1에 도시한 바와 같이, 알코올을 상단 스트림(7)의 환류에 공급할 수 있고, 알킬렌 카르보네이트를 제2 증류 스테이지(11)로부터 알킬렌 카르보네이트의 환류에 공급할 수 있다. 또한 반응기와 별도로 개별 스트림 각각을 공급할 수 있다. 그러나, 반응기(19)로 공급된 모든 스트림을 혼합 지점에서 혼합하고 이들을 함께 반응기(19)로 도입하는 것이 바람직하다. 혼합은 중앙 공급 라인으로 개방되어 있는 파이프라인에 의해 간단한 방식으로 반응기(19)로 수행될 수 있다. 디알킬 카르보네이트와 알킬렌 카르보네이트를 헤테로공비혼합물의 형태로 포함하고 격벽 컬럼(1)으로부터 측면 유출(5)로서 빼내는 스트림을 상 분리용 장치(25)로 공급한다. 상분리를 위해 사용된 장치(25)는 예를 들어 세틀러(settler)일 수 있다. 상 분리용 장치(25)에서, 디알킬 카르보네이트와 알킬렌 글리콜의 헤테로공비혼합물을 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림(27)과 실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림(29)으로 분리한다. 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림(27)의 일부를 분기시켜 디알킬 카르보네이트용 공급물(17)을 통해 제2 증류 스테이지(11)로 통과시킨다.
실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림(27)을 추가 처리를 위해 증류 컬럼(31)으로 통과시킨다. 증류 컬럼(31)에서 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림을, 증류 컬럼(31)으로부터 하부 스트림으로서 빼내는, 디알킬 카르보네이트를 포함하는 생성물 스트림(33) 및 상 분리용 장치(25)로 재순환되는, 실질적으로 디알킬 카르보네이트를 포함하는 상단 스트림으로 증류에 의해 분리한다. 증류 컬럼(31)에서 제거된 알킬렌 글리콜은 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림(27)에서 불순물로서 존재한다.
실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림(29)이 또한 불순물로서 디알킬 카르보네이트를 포함하므로, 이것은 비슷하게 증류 컬럼(35)으로 공급된다. 증류 컬럼(35)에서 알킬렌 글리콜을 포함하는 생성물 스트림(37)이 제거되고, 실질적으로 디알킬 카르보네이트를 포함하는 스트림이 상 분리용 장치(25)로 재순환된다. 여기서 증류 컬럼(31, 35)으로부터 재순환 스트림을 혼합하고 이들을 함께 상 분리용 장치(25)로 잰순환시킬 수 있다. 증류 컬럼(31, 35)으로부터 재순환된 스트림은 추가로 또한 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하고 격벽 컬럼(1)으로부터 제거되는 스트림과 혼합될 수 있다. 비슷하게 알킬렌 글리콜과 디알킬 카르보네이트를 포함하고 제2 증류 스테이지(11)의 상단에서 빼내는 상단 스트림이 상 분리용 장치(25)로 재순환된다. 각 경우에 상 분리용 장치(25)로 공급된 스트림은 공급되기 전에 혼합될 수 있거나 별도 공급물로서 공급될 수 있다. 또한 개별 스트림을 혼합하고 몇몇 공급물을 제공할 수 있다.
제1 증류 스테이지가 격벽 컬럼(1)의 형태로 구성되는, 도 1에 도시된 실시형태의 대안으로, 또한 격벽 컬럼(1)을 2개의 증류 컬럼으로 대체할 수 있다. 이 경우, 디알킬 카르보네이트, 알킬렌 글리콜, 알킬렌 카르보네이트 및 알코올을 포함하는 스트림을 제1 증류 컬럼으로 공급하고 디알킬 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 상단 스트림, 및 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 호모공비혼합물 형성 하부 스트림으로 분리하고, 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 호모공비혼합물 형성 하부 스트림은 제2 증류 스테이지로 공급된다. 디알킬 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 상단 스트림을 제1 증류 스테이지의 제2 증류 컬럼으로 통과시키고, 이 스트림을 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하고 하부 스트림으로서 상 분리용 장치(25)로 공급되는 스트림, 및 반응기(19)로 재순환되는 알코올 포함 상단 스트림으로 분리한다.
별도 반응기(19) 대신에, 반응성 증류를 추가로 구비할 수 있으며, 이 경우 알코올과 알킬렌 카르보네이트를 반응성 증류에 공급하고, 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하고 분리될 스트림을 생성하고 반응성 증류 컬럼에서 직접 분리한다.
도 2에서는 대안적인 실시형태에서 본 발명에 따른 방법을 보여준다.
도 1에 도시된 실시형태로부터 도 2에 도시된 실시형태의 차이는 디알킬 카르보네이트를 포함하는 미정제 생성물 스트림(27)의 일부가 연행제로서 스트림(17)의 형태로 제1 증류 스테이지에 공급된다는 사실을 포함한다. 이 결과로서, 제1 증류 스테이지의 제1 증류 컬럼(39)에서 알킬렌 카르보네이트를 포함하는 스트림(13)을 이미 제거할 수 있으며, 알킬렌 글리콜과 알킬렌 카르보네이트의 호모공비혼합물이 얻어지지 않는다. 따라서 제2 증류 스테이지(11)를 생략할 수 있다. 도 2에서는 2개의 증류 컬럼(39 및 41)이 있는 제1 증류 스테이지를 보여준다. 대안으로서 또한 도 2에 도시된 2개의 증류 컬럼(39 및 41)을 격벽 컬럼(1)으로 대체할 수 있다. 이 경우 디알킬 카르보네이트를 포함하는 스트림을 공급물로 격벽 컬럼으로 공급하고, 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림을 제2 증류 컬럼으로부터 탑저물로서가 아니라, 오히려 도 1에 도시한 바와 같이, 격벽 컬럼으로부터 측면 유출로서 얻는다.
실시예
실시예에서 제공된 퍼센트는 다르게 지정되지 않는 한 중량%이다.
실시예 1:
관형 반응기에서 촉매로서 0.5 몰%(에틸렌 카르보네이트 기준)의 나트륨 이소부톡시드의 존재하에 140℃에서 2.63 kg/h의 에틸렌 카르보네이트를 6.65 kg/h의 이소부탄올(이소부탄올 대 에틸렌 카르보네이트의 몰비 3:1)과 반응시켜 2.5 kg/h의 디이소부틸 카르보네이트와 0.93 kg/h의 모노에틸렌 글리콜을 제공한다.
반응 산출량을 상부 압력 80 mbar(절대)에서 운전되는 격벽 컬럼으로 통과시킨다. 하부 온도 170℃ 및 환류비 0.76 g/g에서 증류를 연속으로 수행한다.
조성이 57.5%의 에틸렌 카르보네이트, 20.5%의 모노에틸렌 글리콜, 15.1%의 디이소부틸 카르보네이트 및 0.55%의 나트륨 이소부톡시드인 2.38 kg/h의 액체 하부 생성물을 얻는다. 나머지는 주로 고급 에틸렌 글리콜로 이루어진다.
상단에서, 조성이 99.91%의 이소부탄올, 100 ppm의 디이소부틸 카르보네이트 및 물인 7.97 kg/h의 증기 스트림을 얻으며, 이를 응축시키고 반응기로, 또는 환류로서 컬럼으로 재순환시킨다. 스트림 일부를 배출시켜 시스템으로부터 물을 제거한다.
격벽 컬럼의 측면 유출에서, 2.58 kg/h의 액체 이상 스트림을 빼내며, 이는 조성 83%의 디이소부틸 카르보네이트와 17%의 모노에틸렌 글리콜을 포함한다. 이 스트림을 상분리기에 공급한다. 98.5%의 디이소부틸 카르보네이트가 있는 디이소부틸 카르보네이트 농후 상과 97.6%의 모노에틸렌 글리콜이 있는 모노에틸렌 농후 상으로의 상분리를 40℃에서 수행한다.
3.15 kg/h의 디이소부틸 카르보네이트 농후 상을 컬럼으로 안내하여 하부 온도 125℃ 및 상부 압력 130 mbar에서 증류시킨다. 조성이 99.94%의 디이소부틸 카르보네이트 및 600 ppm의 모노에틸렌 글리콜인 2.5 kg/h의 액체 하부 생성물을 얻는다. 상단에서, 조성이 2.2%의 이소부탄올, 4.9%의 모노에틸렌 글리콜 및 92.9%의 디이소부틸 카르보네이트인 0.65 kg/h의 증기 스트림을 빼내, 응축하여 상 분리로 재순환시킨다.
격벽 컬럼으로부터 모노에틸렌 글리콜과 에틸렌 카르보네이트를 포함하는 하부 스트림의 분리를 위해 2.82 kg/h의 디이소부틸 카르보네이트 농후 상을 컬럼의 상부로 통과시킨다. 컬럼을 상부 압력 70 mbar 및 하부 온도 159℃에서 운전한다. 조성이 89.2%의 에틸렌 카르보네이트와 0.9%의 촉매, 및 또한 고급 에틸렌 글리콜인 1.53 kg/h의 액체 하부 스트림을 얻고, 이를 반응기로 재순환시킨다. 시스템으로부터 고급 에틸렌 글리콜을 제거하기 위해 하부 스트림 일부를 배출한다.
컬럼 상단에서, 조성이 85.6%의 디이소부틸 카르보네이트, 14.0%의 모노에틸렌 글리콜 및 0.4%의 이소부탄올인 3.67 kg/h의 증기 스트림을 얻고, 이를 응축하여 상 분리로 공급한다.
모노에틸렌 글리콜 농후 상을 상부 압력 130 mbar 및 하부 온도 139℃에서의 컬럼에서 질량 유량 0.95 kg/h에서 증류에 의해 정제한다. 이로서 조성이 99.9%의 모노에틸렌 글리콜 및 0.1%의 에틸렌 카르보네이트인 0.93 kg/h의 액체 하부 스트림을 제공한다.
상단에서, 조성이 39%의 이소부탄올, 40.1%의 디이소부틸 카르보네이트 및 20.9%의 모노에틸렌 글리콜인 0.03 kg/h의 증기 스트림을 빼내서, 응축시키고 상 분리로 재순환시킨다.
실시예 2:
반응은 실시예 1에 기재된 것과 동일한 조건하에 일어난다. 반응 산출량을 4 kg/h의 디이소부틸 카르보네이트 농후 상과 함께 상 분리기로부터 상부 압력 25 mbar에서 운전되는 증류 컬럼으로 통과시킨다. 하부 온도 178℃ 및 환류비 0.44 g/g에서 연속으로 증류 조작된다.
컬럼 하부에서, 조성이 92.3%의 에틸렌 카르보네이트, 0.3%의 디이소부틸 카르보네이트, 0.49%의 나트륨 이소부톡시드 및 잔류 고급 에틸렌 글리콜인 2.17 kg/h의 액체 하부 스트림을 얻고, 이를 반응기로 재순환시킨다.
컬럼 상단에서, 조성이 35.1%의 이소부탄올, 57.5%의 디이소부틸 카르보네이트 및 7.4%의 모노에틸렌 글리콜인 15 kg/h의 증기 스트림을 얻고, 이를 응축시키고 이소부탄올과 디이소부틸 카르보네이트 모노에틸렌 글리콜 공비혼합물의 분리를 위해 컬럼으로 통과시킨다.
상부 압력 200 mbar 및 하부 온도 124℃에서 컬럼의 증류를 수행한다. 이로서 조성이 99%의 이소부탄올, 0.9%의 디이소부틸 카르보네이트 및 물인 4.1 kg/h의 증기 스트림을 제공하고, 이를 응축시키고 반응기(1)로 재순환시킨다. 상단 스트림의 일부를 배출하여 시스템으로부터 물을 제거한다.
컬럼 하부에서, 조성이 87.7%의 디이소부틸 카르보네이트, 11.3%의 모노에틸렌 글리콜 및 1%의 이소부탄올인 6.79 kg/h의 이상 하부 스트림을 얻고, 이를 상 분리기로 통과시킨다. 97.02%의 디이소부틸 카르보네이트가 있는 디이소부틸 카르보네이트 농후 상과 94.5%의 모노에틸렌 글리콜이 있는 모노에틸렌 글리콜 농후 상으로의 상 분리를 40℃에서 수행한다.
2.57 kg/h의 디이소부틸 카르보네이트 농후 상을 컬럼으로 안내하여 하부 온도 124℃ 및 상부 압력 130 mbar에서 증류시킨다. 이로서 조성이 99.99%의 디이소부틸 카르보네이트 및 30 ppm의 에틸렌 카르보네이트인 2.0 kg/h의 액체 하부 생성물을 제공한다. 상단에서, 조성이 7.6%의 이소부탄올, 87.2%의 디이소부틸 카르보네이트 및 5.2%의 모노에틸렌 글리콜인 0.57 kg/h의 증기 스트림을 빼내어, 응축시키고 상 분리로 재순환시킨다.
에틸렌 카르보네이트로부터 모노에틸렌 글리콜의 제거를 위해 상 분리기로부터 4.1 kg/h의 디이소부틸 카르보네이트 농후 상을 컬럼의 공급물로 통과시킨다.
상 분리기로부터 모노에틸렌 글리콜 농후 상을, 상부 압력 130 mbar 및 하부 온도 139℃에서의 컬럼에서 질량 유량 0.76 kg/h에 증류에 의해 정제한다. 이로서 조성이 99.99%의 모노에틸렌 글리콜 및 60 ppm의 에틸렌 카르보네이트인 0.72 kg/h의 액체 하부 스트림을 제공한다. 컬럼 상단에서, 조성이 23.8%의 디이소부틸 카르보네이트, 66%의 이소부탄올 및 10.2%의 모노에틸렌 글리콜인 0.05 kg/h의 증기 스트림을 빼내어, 응축시키고 상 분리로 재순환시킨다.
실시예 3:
관형 반응기에서 촉매로서 0.5 몰%(에틸렌 카르보네이트 기준)의 나트륨 이소부톡시드의 존재하에 140℃에서 2.45 kg/h의 에틸렌 카르보네이트를 5 kg/h의 1-프로판올(1-프로판올 대 에틸렌 카르보네이트의 몰비 3:1)과 반응시켜 2.1 kg/h의 디프로필 카르보네이트와 0.89 kg/h의 모노에틸렌 글리콜을 제공한다.
반응 산출량을 상부 압력 150 mbar에서 운전되는 격벽 컬럼으로 통과시킨다. 하부 온도 152℃ 및 환류비 0.76 g/g에서 증류를 연속으로 수행한다.
격벽 컬럼의 하부에서, 조성이 62.4%의 에틸렌 카르보네이트 및 37.6%의 모노에틸렌 글리콜인 1.89 kg/h의 액체 하부 생성물을 얻는다.
격벽 컬럼의 상단에서, 조성이 99.9%의 1-프로판올 및 0.1%의 디이소부틸 카르보네이트인 5.8 kg/h의 증기 스트림을 얻으며, 이를 응축시키고 반응기로, 또는 환류로서 컬럼으로 재순환시킨다.
격벽 컬럼의 측면 유출에서, 2.28 kg/h의 액체 이상 스트림을 빼내며, 이는 조성 92%의 디이소부틸 카르보네이트와 8%의 모노에틸렌 글리콜을 포함한다. 이 스트림을 상분리기에 공급한다. 98.2%의 디이소부틸 카르보네이트가 있는 디이소부틸 카르보네이트 농후 상과 97%의 모노에틸렌 글리콜이 있는 모노에틸렌 농후 상으로의 상분리를 40℃에서 수행한다.
상 분리기로부터 3.36 kg/h의 디이소부틸 카르보네이트 농후 상을 컬럼으로 안내하여 하부 온도 127℃ 및 상부 압력 300 mbar에서 증류시킨다. 조성이 99.9%의 디프로필 카르보네이트 및 100 ppm의 모노에틸렌 글리콜인 2.1 kg/h의 액체 하부 생성물을 얻는다. 컬럼의 상단에서, 조성이 0.1%의 1-프로판올, 4.4%의 모노에틸렌 글리콜 및 95.5%의 디이소부틸 카르보네이트인 1.3 kg/h의 증기 스트림을 빼내, 응축하여 상 분리로 재순환시킨다.
격벽 컬럼의 하부에서 얻어지는 에틸렌 카르보네이트 모노에틸렌 글리콜 혼합물의 분리를 위해 상 분리기로부터 14 kg/h의 디프로필 카르보네이트 농후 상을 컬럼의 상부로 안내한다.
컬럼을 상부 압력 70 mbar 및 하부 온도 159℃에서 운전한다. 조성이 99.9%의 에틸렌 카르보네이트와 0.1%의 촉매, 및 또한 고급 에틸렌 글리콜인 1.2 kg/h의 액체 하부 스트림을 얻고, 이를 반응기로 재순환시킨다. 하부 스트림 일부를 배출하여 시스템으로부터 고급 에틸렌 글리콜을 제거한다.
컬럼 상단에서, 조성이 93.5%의 디프로필 카르보네이트, 6.4%의 모노에틸렌 글리콜, 800 ppm의 에틸렌 카르보네이트 및 440 ppm의 1-프로판올인 15.8 kg/h의 증기 스트림을 얻고, 이를 응축하여 상 분리로, 또는 환류로서 컬럼으로 재순환시킨다.
상 분리기로부터 모노에틸렌 글리콜 농후 상을 상부 압력 100 mbar 및 하부 온도 161℃에서의 컬럼에서 질량 유량 0.92 kg/h에서 증류에 의해 정제한다. 하부에서, 조성이 99.9%이고 0.1%의 에틸렌 카르보네이트인 0.89 kg/h의 모노에틸렌 글리콜을 얻는다. 컬럼의 상단에서, 조성이 89.6%의 디프로필 카르보네이트, 7.2%의 모노에틸렌 글리콜, 및 3.2%의 1-프로판올인 0.03 kg/h의 증기 스트림을 빼내서, 응축시키고 상 분리로 재순환시킨다.
1 격벽 컬럼
3 측면 공급물
5 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림
7 알코올을 포함하는 상단 스트림
9 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 호모공비혼합물 형성 하부 스트림
11 제2 증류 스테이지
13 알킬렌 카르보네이트를 포함하는 하부 스트림
15 알킬렌 글리콜과 디알킬 카르보네이트를 포함하는 상단 스트림
17 측면 공급물
19 반응기
21 제1 공급물
23 제2 공급물
25 상 분리용 장치
27 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림
29 실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림
31 증류 컬럼
33 디알킬 카르보네이트를 포함하는 생성물 스트림
35 증류 컬럼
37 알킬렌 글리콜을 포함하는 생성물 스트림
39 제1 증류 컬럼
41 제2 증류 컬럼
3 측면 공급물
5 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림
7 알코올을 포함하는 상단 스트림
9 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 호모공비혼합물 형성 하부 스트림
11 제2 증류 스테이지
13 알킬렌 카르보네이트를 포함하는 하부 스트림
15 알킬렌 글리콜과 디알킬 카르보네이트를 포함하는 상단 스트림
17 측면 공급물
19 반응기
21 제1 공급물
23 제2 공급물
25 상 분리용 장치
27 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림
29 실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림
31 증류 컬럼
33 디알킬 카르보네이트를 포함하는 생성물 스트림
35 증류 컬럼
37 알킬렌 글리콜을 포함하는 생성물 스트림
39 제1 증류 컬럼
41 제2 증류 컬럼
Claims (14)
- 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림(stream)으로부터 디알킬 카르보네이트와 알킬렌 글리콜을 수득하는 방법으로서,
(a) 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림으로부터 제1 증류 스테이지(stage)(1)에서 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림(5)을 증류로 빼내는 단계,
(b) 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 스트림(5)을 상 분리용 장치(25)에서 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림(27)과 실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림(29)으로 분리하는 단계
를 포함하는 방법. - 제1항에 있어서, 제1 증류 스테이지는 알킬렌 카르보네이트와 알코올이 반응물로서 첨가되고 평형 반응에서 디알킬 카르보네이트와 알킬렌 글리콜로 전환되어, 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림을 제공하는 반응성 증류물(distillation)을 포함하는 것인 방법.
- 제1항에 있어서, 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림을 제1 증류 스테이지(1)로 공급하는 것인 방법.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 제1 증류 스테이지(1)는, 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림이 알코올 포함 상단 스트림(7), 하부 스트림으로서 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 호모공비혼합물 형성 스트림(9) 및 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하고 측면 스트림으로서 빼내는 스트림(5)으로 분리되는 격벽 컬럼(1)을 포함하거나, 상기 제1 증류 스테이지는 2개의 증류 컬럼을 포함하며, 제1 증류 컬럼에서 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림이 디알킬 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 상단 스트림, 및 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 호모공비혼합물 형성 하부 스트림으로 분리되고, 제1 증류 컬럼으로부터 디알킬 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 상단 스트림은 제2 증류 컬럼에서 알코올 포함 상당 스트림과 하부 스트림으로서 디알킬 카르보네이트와 알킬렌 글리콜을 헤테로공비혼합물로서 포함하는 스트림으로 분리되는 것인 방법.
- 제4항에 있어서, 알킬렌 카르보네이트와 알킬렌 글리콜을 포함하는 호모공비혼합물 형성 스트림(9)과 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림의 일부를 연행제로서 제2 증류 스테이지(11)로 공급하고, 알킬렌 카르보네이트를 포함하는 하부 스트림(13)과 디알킬 카르보네이트와 알킬렌 글리콜을 포함하는 상단 스트림(15)을 제2 증류 스테이지(11)로부터 빼내는 것인 방법.
- 제1항 내지 제3항 중 어느 한 항에 있어서, 제1 증류 스테이지는, 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림이 알킬렌 카르보네이트를 포함하는 하부 스트림, 알코올을 포함하는 상단 스트림, 및 헤테로공비혼합물로서 디알킬 카르보네이트와 알킬렌 글리콜을 포함하며 측면 스트림으로서 빼내는 스트림으로 분리되는 격벽 컬럼을 포함하거나, 제1 증류 스테이지는, 디알킬 카르보네이트, 알킬렌 카르보네이트, 알킬렌 글리콜 및 알코올을 포함하는 스트림이 알킬렌 카르보네이트를 포함하는 하부 스트림(13) 및 디알킬 카르보네이트, 알코올 및 알킬렌 글리콜을 포함하는 상단 스트림으로 분리되는 제1 증류 컬럼(39), 및 제1 증류 컬럼(39)으로부터 디알킬 카르보네이트, 알코올 및 알킬렌 글리콜을 포함하는 상단 스트림이 알코올 포함 상단 스트림(7) 및 하부 스트림으로서 디알킬 카르보네이트와 알킬렌 글리콜을 헤테로공비혼합물로서 포함하는 스트림(5)으로 분리되는 제2 증류 컬럼(41)을 포함하며, 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림의 일부는 연행제로서 제1 증류 스테이지로 추가 첨가되는 것인 방법.
- 제6항에 있어서, 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림의 일부를 공급물로 제1 증류 스테이지에 첨가하는 것인 방법.
- 제6항에 있어서, 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림의 일부를 격벽 컬럼의 공급물 측면 상에 또는 제1 증류 컬럼에 첨가하는 것인 방법.
- 제1항 내지 제8항 중 어느 한 항에 있어서, 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림(27)을, 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림(27)에 아직 존재한 알킬렌 글리콜을 빼내 디알킬 카르보네이트를 포함하는 생성물 스트림(33)을 얻는 증류 조작(distillative operation)(31)에 공급하는 것인 방법.
- 제9항에 있어서, 실질적으로 디알킬 카르보네이트를 포함하는 제1 미정제 생성물 스트림(27)으로부터 빼낸 알킬렌 글리콜을 단계 (b)에서 상 분리용 장치(25)로 공급하는 것인 방법.
- 제1항 내지 제10항 중 어느 한 항에 있어서, 실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림(29)을, 실질적으로 알킬렌 글리콜을 포함하는 미정제 생성물 스트림(29)에 아직 존재한 디알킬 카르보네이트를 빼내 알킬렌 글리콜을 포함하는 생성물 스트림(37)을 얻는 증류 조작(35)에 공급하는 것인 방법.
- 제11항에 있어서, 실질적으로 알킬렌 글리콜을 포함하는 제2 미정제 생성물 스트림(29)으로부터 빼낸 디알킬 카르보네이트를 단계 (b)에서 상 분리용 장치(25)로 공급하는 것인 방법.
- 제1항 내지 제12항 중 어느 한 항에 있어서, 알코올은 n-프로판올, n-부탄올, 이소부탄올, n-펜탄올, n-헥산올, 2-메틸-1-부탄올, 3-메틸-1-부탄올 또는 2-메톡시-1-에탄올인 방법.
- 제1항 내지 제13항 중 어느 한 항에 있어서, 알킬렌 카르보네이트가 에틸렌 카르보네이트 또는 프로필렌 카르보네이트인 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP11191894.2 | 2011-12-05 | ||
| EP11191894 | 2011-12-05 | ||
| PCT/EP2012/074478 WO2013083618A1 (de) | 2011-12-05 | 2012-12-05 | Verfahren zur gewinnung eines dialkylcarbonats und eines alkylenglykols |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20140113931A true KR20140113931A (ko) | 2014-09-25 |
Family
ID=47351616
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020147018561A KR20140113931A (ko) | 2011-12-05 | 2012-12-05 | 디알킬 카르보네이트와 알켈렌 글리콜을 수득하는 방법 |
Country Status (7)
| Country | Link |
|---|---|
| EP (1) | EP2788315A1 (ko) |
| JP (1) | JP2015504855A (ko) |
| KR (1) | KR20140113931A (ko) |
| CN (1) | CN104203899A (ko) |
| BR (1) | BR112014013557A2 (ko) |
| IN (1) | IN2014CN04151A (ko) |
| WO (1) | WO2013083618A1 (ko) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2013150989A1 (ja) * | 2012-04-04 | 2013-10-10 | 旭硝子株式会社 | ジオールおよびジブチルカーボネートの分離方法、精製方法、ならびに製造方法 |
| EP3915613A1 (en) | 2015-10-28 | 2021-12-01 | SHL Medical AG | Medicament container holder |
| US10399004B2 (en) | 2016-09-08 | 2019-09-03 | Eastman Chemical Company | Thermally integrated distillation systems and processes using the same |
| CN108440297A (zh) * | 2017-03-23 | 2018-08-24 | 秦燕雯 | 一种用于碳酸二甲酯装置节能降耗的装置 |
| CN114555553B (zh) * | 2019-10-03 | 2024-04-05 | 国际壳牌研究有限公司 | 用于制备碳酸二烷基酯和链烷二醇的方法 |
| EP3831805A1 (en) * | 2019-12-06 | 2021-06-09 | Shell Internationale Research Maatschappij B.V. | Process for the preparation of a dialkyl carbonate and an alkanediol |
| WO2021110627A1 (en) * | 2019-12-06 | 2021-06-10 | Shell Internationale Research Maatschappij B.V. | Process for removing an ether alkanol impurity from an organic carbonate stream |
| CN115594585B (zh) * | 2022-12-13 | 2023-04-07 | 江苏华盛锂电材料股份有限公司 | 一种一步合成并提纯甲基三氟乙基碳酸酯的方法 |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3642858A (en) * | 1969-02-12 | 1972-02-15 | Dow Chemical Co | Carbonate synthesis from alkylene carbonates |
| US5489703A (en) | 1995-05-19 | 1996-02-06 | Amoco Corporation | Reaction extraction of alkyl carbonate |
| ES2174126T3 (es) | 1995-12-22 | 2002-11-01 | Asahi Chemical Ind | Metodo para la produccion en continuo de dialquil carbonato y dioles. |
| JP4565742B2 (ja) | 1998-06-10 | 2010-10-20 | 旭化成ケミカルズ株式会社 | ジアルキルカーボネートとジオールを連続的に製造する方法 |
| CN1172889C (zh) | 1999-03-03 | 2004-10-27 | 旭化成株式会社 | 连续生产碳酸二烷基酯和二醇的方法 |
| US6166240A (en) * | 2000-02-22 | 2000-12-26 | Mobil Oil Corporation | Process for co-production of dialkyl carbonate and alkanediol |
| US6573396B2 (en) * | 2001-10-12 | 2003-06-03 | Exxonmobil Chemical Patents Inc. | Co-production of dialkyl carbonates and diols with treatment of hydroxy alkyl carbonate |
| JP2003300918A (ja) * | 2002-04-11 | 2003-10-21 | Mitsui Chemicals Inc | ジアルキルカーボネートとグリコールの連続同時製造方法 |
| US6620959B1 (en) | 2002-04-16 | 2003-09-16 | Exxonmobil Chemical Patents Inc. | Process for the production of unsymmetric and/or symmetric dialkyl carbonates and diols |
| JP4000912B2 (ja) * | 2002-05-30 | 2007-10-31 | 三菱化学株式会社 | ジメチルカーボネートの製造方法 |
| JP4424898B2 (ja) * | 2002-10-08 | 2010-03-03 | 旭化成ケミカルズ株式会社 | ジアルキルカーボネートおよびジオールを製造する方法 |
| JP2006023065A (ja) | 2004-06-10 | 2006-01-26 | Mitsubishi Electric Corp | 換気機能付き空気調和機及び換気機能付き空気調和機の換気装置及び換気機能付き空気調和機の換気方法 |
| JP2006206497A (ja) * | 2005-01-28 | 2006-08-10 | Asahi Kasei Chemicals Corp | ジアルキルカーボネートおよびジオールを製造する方法 |
| US20090326257A1 (en) | 2005-12-12 | 2009-12-31 | Shinsuke Fukuoka | Process for industrially producing dialkyl carbonate and diol |
| TW200732291A (en) | 2005-12-14 | 2007-09-01 | Asahi Kasei Chemicals Corp | Process for production of dialkyl carbonate and diol in industrial scale and with high yield |
| TWI383976B (zh) | 2006-02-22 | 2013-02-01 | Shell Int Research | 製備碳酸二烷酯及烷二醇的方法 |
| JP5094459B2 (ja) | 2007-03-09 | 2012-12-12 | ローム アンド ハース カンパニー | アルカンを不飽和カルボン酸に変換するための改良法 |
| DE102009030680A1 (de) | 2009-06-26 | 2010-12-30 | Bayer Materialscience Ag | Verfahren zur Herstellung von Dialkylcarbonaten aus Alkylencarbonaten und Alkoholen |
| DE102009053370A1 (de) | 2009-11-14 | 2011-05-19 | Bayer Materialscience Ag | Verfahren zur Reinigung von Dialkylcarbonaten |
| TWI473786B (zh) | 2009-11-16 | 2015-02-21 | Shell Int Research | 製備烷二醇及碳酸二烷酯的方法 |
-
2012
- 2012-12-05 CN CN201280069004.4A patent/CN104203899A/zh active Pending
- 2012-12-05 WO PCT/EP2012/074478 patent/WO2013083618A1/de unknown
- 2012-12-05 EP EP12799132.1A patent/EP2788315A1/de not_active Withdrawn
- 2012-12-05 BR BR112014013557A patent/BR112014013557A2/pt not_active IP Right Cessation
- 2012-12-05 KR KR1020147018561A patent/KR20140113931A/ko not_active Application Discontinuation
- 2012-12-05 JP JP2014545236A patent/JP2015504855A/ja not_active Ceased
- 2012-12-05 IN IN4151CHN2014 patent/IN2014CN04151A/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| IN2014CN04151A (ko) | 2015-07-17 |
| EP2788315A1 (de) | 2014-10-15 |
| BR112014013557A2 (pt) | 2017-06-13 |
| WO2013083618A1 (de) | 2013-06-13 |
| JP2015504855A (ja) | 2015-02-16 |
| CN104203899A (zh) | 2014-12-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20140113931A (ko) | 디알킬 카르보네이트와 알켈렌 글리콜을 수득하는 방법 | |
| EP2432758B1 (en) | The production of n,n-dialkylaminoethyl (meth)acrylates | |
| EP2231572B1 (en) | Production of propylene glycol monoalkyl ether | |
| KR20110105379A (ko) | 디알킬카보네이트의 제조 방법 | |
| CA2185821A1 (en) | Continuous preparation of alkyl esters of (meth)acrylic acid and apparatus for this purpose | |
| US20030018216A1 (en) | Method for producing anhydrous formic acid | |
| US7750192B2 (en) | Purification of Fluoromethyl 1,1,1,3,3,3-hexafluoroisopropyl ether (sevoflurane) | |
| CN108473412A (zh) | 用于纯化(甲基)丙烯酸酯的方法 | |
| KR20180015632A (ko) | 공액 디엔의 제조 방법 | |
| US20060205972A1 (en) | Process for preparing alkyl esters of (meth)acrylic acid | |
| US5074967A (en) | Separation of methoxyisopropylamine from methoxyisopropylamine-water azeotrope | |
| US20060205973A1 (en) | Process for preparing alkyl esters of (meth)acrylic acid | |
| US8558021B2 (en) | Process for the catalytic halogenation of a diol | |
| US9133094B2 (en) | Apparatus and process for nitration selectivity flexibility enabled by azeotropic distillation | |
| US6838579B2 (en) | Utilization of an extracting agent as antifoaming agent in the production of anhydrous formic acid | |
| CN112262119B (zh) | 纯化轻质丙烯酸酯的方法 | |
| US20130144080A1 (en) | Process for obtaining a dialkyl carbonate and an alkylene glycol | |
| US9192877B2 (en) | Apparatus and process for using a nitroalkane as an entrainer for azeotropic removal of water from aqueous acid solution | |
| US3860495A (en) | Process for the purification of crude acrolein by extractive distillation | |
| JPS6039049B2 (ja) | アルコ−ルの製造方法 | |
| KR20020029131A (ko) | 지방산 아미드의 제조방법 | |
| US20220227627A1 (en) | Improved process for preparing hydrazine hydrate with pyrazoline recycling | |
| US6414204B1 (en) | Process for producing allyl chloride | |
| JP6270476B2 (ja) | ジトリメチロールプロパンの製造方法 | |
| JP2002003458A (ja) | ホルムアミドの製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WITN | Withdrawal due to no request for examination |