KR20120030570A - 디펩티딜 펩티다아제 4 저해 화합물과 감미료와의 병용 - Google Patents
디펩티딜 펩티다아제 4 저해 화합물과 감미료와의 병용 Download PDFInfo
- Publication number
- KR20120030570A KR20120030570A KR1020127002221A KR20127002221A KR20120030570A KR 20120030570 A KR20120030570 A KR 20120030570A KR 1020127002221 A KR1020127002221 A KR 1020127002221A KR 20127002221 A KR20127002221 A KR 20127002221A KR 20120030570 A KR20120030570 A KR 20120030570A
- Authority
- KR
- South Korea
- Prior art keywords
- sweetener
- glp
- pharmaceutical composition
- promoting action
- secretion promoting
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/426—1,3-Thiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/047—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates having two or more hydroxy groups, e.g. sorbitol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/496—Non-condensed piperazines containing further heterocyclic rings, e.g. rifampin, thiothixene
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/54—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one sulfur as the ring hetero atoms, e.g. sulthiame
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7004—Monosaccharides having only carbon, hydrogen and oxygen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/702—Oligosaccharides, i.e. having three to five saccharide radicals attached to each other by glycosidic linkages
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Abstract
본 발명은 우수한 항비만 효과(체중 감소 효과 및/또는 체지방 감소 효과)를 발휘하는 신규한 치료 또는 예방 방법, 의약 조성물, 및 이들의 사용을 제공한다. 본 발명은 디펩티딜 펩티다아제 4 저해 화합물과 GLP-1 분비 촉진 작용을 갖는 감미료를 조합하여 포함하는 의약 조성물, 및 의약의 제조에 있어서의 그의 사용을 제공한다. 또한, 비만의 증상을 갖는 환자에게, (a) 디펩티딜 펩티다아제 4 저해 화합물 및 (b) GLP-1 분비 촉진 작용을 갖는 감미료를 유효량 투여하는 것을 특징으로 하는 비만의 치료 또는 예방 방법을 제공한다.
Description
본 발명은 체중 감소(reduction of body weight), 체지방 감소(reduction of body fat mass), 및/또는 비만의 치료 또는 예방을 위한 방법, 이들을 위한 의약 조성물, 및 이들의 사용에 관한 것이다.
보다 상세하게는, 본 발명은 (1) 디펩티딜 펩티다아제 4 저해 화합물과 (2) GLP-1 분비 촉진 작용을 갖는 감미료를 병용한 체중 감소, 체지방 감소, 및/또는 비만의 치료 또는 예방을 위한 방법, 의약 조성물, 및 이들의 사용에 관한 것이다.
비만은 현대의 사회에서 큰 사회 문제로 되어 있지만, 기존의 비만 치료약(오리스타트, 덱스펜플루라민, 시부트라민, 펜테르민 등)의 효과는 반드시 충분하지 않고, 또한 부작용의 문제가 있다.
비만은 그것 자체에 의해서, 또는 다른 질병과의 관계에 의해서, 많은 건강상의 문제를 야기한다. 비만에 관련하여 생명을 위협할 수 있는 질환으로서는 고혈압, 2형 당뇨병, 혈장 인슐린 농도 상승, 인슐린 저항성, 이상 지질혈증, 고지혈증, 동맥 경화증, 심장병 등을 들 수 있다.
이들 중에서, 2형 당뇨병과 비만과의 사이에는 밀접한 관계가 있다.
2형 당뇨병이 이루어지는 원인으로서는 췌장 인슐린 분비 장해와 함께, 인슐린 저항성을 들 수 있지만, 비만에 있어서 지방 조직이 비대하면, 지방 세포의 인슐린 수용체 수가 감소하는 것 외에, 지방 세포로부터 TNF-α 등의 인슐린 저항성 야기성의 사이토카인 분비가 항진되는 것 등에 의해서, 인슐린 저항성이 야기된다.
따라서, 2형 당뇨병 환자 및 그의 리스크가 높은 사람에게 있어서는, 비만의 예방이 중요하고, 또한 비만이 발병한 2형 당뇨병 환자에 있어서는 비만의 개선이 강하게 요구된다.
한편, 디펩티딜 펩티다아제 4(DPP 4)는 폴리펩티드쇄의 N 말단에서 Xaa-Pro 또는 Xaa-Ala(Xaa는 어떠한 아미노산일 수도 있음)의 디펩티드를 특이적으로 가수분해하는 세린프로테아제의 1종이다.
또한, GLP-1(글루카곤 유사 펩티드 1)은 주로 글루코오스 의존적으로 인슐린 분비를 증폭시키는 기능을 갖는 펩티드 호르몬이고, 주로 소장 하부에서 식후에 분비되어, 췌장에서 작용한다. DPP 4는 이 GLP-1을 가수분해하여 불활성시킴과 동시에, GLP-1 수용체의 길항제로서 작용하는 펩티드를 생기게 한다.
DPP 4의 효소 활성을 저해하는 화합물(DPP 4 저해 화합물)은 그의 저해 작용을 통해 내재성 GLP-1의 작용을 높임으로써, 글루코오스 의존적인 인슐린 분비(glucose-stimulated insulin secretion)를 높여, 혈당 강하 작용을 발휘함과 동시에, 손상된 내당능(impaired glucose tolerance)을 개선시킨다.
이 때문에, DPP 4 저해 화합물은 당뇨병 등의 예방ㆍ치료에 유용하다고 생각되고 있고, 많은 DPP 4 저해 화합물이 당뇨병(특히 2형 당뇨병)의 치료약으로서, 개발되고 있다.
문헌〔Augustyns et al., Expert Opin. Ther. Patents, 2003, 13:499-510;
Campbell, Ann. Pharmacother., 2007, 41:51-60
GLP-1의 아날로그도 또한, 당뇨병의 치료약으로서 개발되고 있다. 또한, GLP-1이 섭식 억제 작용을 갖는 것을 시사하는 보고가 있고, GLP-1의 아날로그에 대해서는 인간에서의 임상 시험에 있어서, 항비만 효과가 얻어졌다는 보고가 있다.
문헌〔Zander et al., Lancet, 2002, 359:824-830;
Iltz JL et al., Clin Ther., 2006, 28(5):652-65;
Mack et al., Int. J. Obes. 2006, 30(9):1332-40;
DeFronzo et al., Diabetes Care. 2005, 28(5):1092-100
DPP 4 저해 화합물도 또한, 비만 등의 치료 또는 예방에 있어서의 효과가 기대되고 있지만, 지금까지 DPP 4 저해 화합물의 단독 투여에 의해, 유의한 항비만 효과가 얻어졌다고 하는 전임상 또는 임상의 보고는 나타나지 않았다.
당류에 대해서는 이하와 같은 것이 알려져 있다.
다양한 당류에 의해, GLP-1의 레벨이 상승하는 것이 알려져 있다. 또한 몇 가지의 당류에 대해서는 그의 투여에 의해 체중 증가가 억제되는 것이 알려져 있다.
예를 들면, 시마(Shima) 등의 문헌[Acta Endocrinologica, 1990, 123:464-470]에는 D-글루코오스, D-갈락토오스, 말토오스, 수크로오스, 말티톨 등의 당류의 투여에 의해, 혈중의 GLP-1 레벨이 상승하는 것이 개시되어 있다.
도쿠나가(Tokunaga) 등의 문헌[J. Nutri. Sci. Vitaminol., 1986, 32:111-121] 및 일본 특허 공고 (소)62-60369에는 프락토올리고당(fructooligosaccharide)을 래트에 투여함으로써, 체중 증가의 억제가 나타났다는 것이 개시되어 있다.
또한, 카니(Cani) 등의 문헌에는 올리고프락토스(Oligofructose)〔라프틸로스; glucosyl-(fructosyl)n-fructose 및 (fructosyl)m-fructose의 혼합물; 평균 중합 4.5〕에 대해서, 이것을 래트 또는 마우스에게 투여함으로써, 혈중 및 장내의 GLP-1 농도가 증가하는 것, 당 부하시의 혈당 레벨이 저하하는 것, 고지방식 부하 래트에 있어서 체중 감소 효과가 얻어진 것 등이 개시되어 있다.
문헌(Cani 등, British Journal of Nutrition, 2004, 92: 521-526;
Cani 등, Obesity, 2005, 13: 1000-1007;
Cani 등, Journal of Endocrinology, 2005, 185: 457-465;
Cani 등, Diabetes, 2006, 55: 1484-1490; WO2005/36990).
또한, 일본 특허 공개 (평)6-65080에는 L-아라비노오스, D-크실로오스 등을 포함하는 비만 방지용 보건식이 개시되어 있고, L-아라비노오스의 투여에 의해 마우스의 체중 증가가 억제된 것이 개시되어 있다.
또한, 일본 특허 공개 (평)10-290681에는 크실로올리고당을 유효 성분으로 하는 항비만 및/또는 체지방 감소제 등이 개시되어 있다.
그러나, 항비만을 위해 DPP 4 저해 화합물과 함께, 당류 등의 감미료를 이용하는 것에 대해서는 알려져 있지 않다.
[Augustyns 등, Expert Opin. Ther. Patents, 2003, 13:499-510]
[Campbell, Ann. Pharmacother., 2007, 41:51-60]
[Zander 등, Lancet, 2002, 359:824-830]
[Iltz JL 등, Clin Ther., 2006, 28(5):652-65]
[Mack 등, Int. J. Obes., 2006, 30(9):1332-40]
[DeFronzo 등, Diabetes Care. 2005, 28(5):1092-100]
[Shima 등, Acta Endocrinologica, 1990, 123:464-470]
[Tokunaga 등, J. Nutri. Sci. Vitaminol., 1986, 32:111-121]
[Cani 등, British Journal of Nutrition, 2004, 92:521-526]
[Cani 등, Obesity, 2005, 13:1000-1007]
[Cani 등, Journal of Endocrinology, 2005, 185:457-465]
[Cani 등, Diabetes, 2006, 55:1484-1490]
본 발명은 우수한 항비만 효과〔체중 감소(감량) 효과 및/또는 체지방 감소 효과〕를 발휘하는 신규한 치료 또는 예방 방법, 의약 조성물, 및 이들의 사용을 제공한다.
또한, 본 발명은 상기한 바와 같은 우수한 효과와 동시에, 당뇨병에 대한 치료 또는 예방 효과(혈당 강하 작용 등)를 발휘하는 방법, 의약 조성물, 및 이들의 사용을 제공한다.
본 발명자들은 예의 연구한 결과, 내재성 GLP-1의 분비를 촉진하는 작용을 갖는 감미료를 DPP 4 저해 화합물과 함께 이용함으로써, 우수한 항비만 효과〔체중 감소(감량) 효과 및/또는 체지방 감소 효과〕가 얻어지는 것을 발견하여, 본 발명을 완성하였다.
즉, 본 발명은 디펩티딜 펩티다아제 4 저해 화합물과 GLP-1 분비 촉진 작용을 갖는 감미료를 조합하여 포함하는 의약 조성물이다.
본 발명은 또한, 디펩티딜 펩티다아제 4 저해 화합물을 함유하고, GLP-1 분비 촉진 작용을 갖는 감미료와 병용되는 것을 특징으로 하는 의약 조성물이다.
또한, 본 발명은 비만의 증상을 갖는 환자에게 (a) 디펩티딜 펩티다아제 4 저해 화합물 및 (b) GLP-1 분비 촉진 작용을 갖는 감미료를 유효량 투여하는 것을 특징으로 하는 비만의 치료 또는 예방 방법이다. 본 발명의 일실시 형태로서 (a)의 투여는 (b)의 투여와 동시, 또는 (b)의 투여 전, 또는 (b)의 투여 후 중 어느 하나에 행할 수 있다.
또한, 본 발명은 의약의 제조에 있어서의 디펩티딜 펩티다아제 4 저해 화합물과 GLP-1 분비 촉진 작용을 갖는 감미료와의 배합물의 사용을 포함한다.
또한, 본 발명은 유효 성분으로서의 디펩티딜 펩티다아제 4 저해 화합물과 GLP-1 분비 촉진 작용을 갖는 감미료를 비만의 치료 또는 예방을 위해, 동시, 따로따로 또는 연속적으로 사용하기 위한 지시서와 함께 포함하는 상품 포장물을 포함한다.
본 발명의 의약 조성물, 치료 또는 예방 방법, 또는 사용에 따르면, 비만의 증상을 갖는 환자에 있어서 우수한 항비만 효과(체중 감소 효과 및/또는 체지방 감소 효과)가 얻어진다.
또한, 본 발명에 따르면, 상기한 바와 같은 우수한 효과와 동시에, 당뇨병에 대한 치료 또는 예방 효과(혈당 강하 작용 등)를 동시에 얻을 수 있다. 따라서, 본 발명의 의약 조성물, 치료 또는 예방 방법, 또는 사용은 비만의 증상과 함께 당뇨병(특히 2형 당뇨병)의 증상을 갖는 환자를 위해, 특히 유용하다.
[도 1] 도 1에는 DPP 4 결손 래트(F344/DuCrlCrlj)에 프락토올리고당을 투여한 경우의 혈장중 활성형 GLP-1 레벨 상승 작용을 시험한 결과를 나타내었다. -▲-는 프락토올리고당 6 g/kg 경구 투여군, -●-는 대조로서 정제수를 투여한 군(모두 n=6)의 각 군에 있어서의 혈장중 활성형 GLP-1 농도(평균치±표준 오차(SEM))의 경시 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트(Dunnett) 다중 비교법에 기초하는 유의차를 나타냄)
[도 2] 도 2에는 C57BL/6J 마우스에게 DPP 4 저해 화합물(화합물 A) 및 프락토올리고당을 투여한 경우의 혈장중 활성형 GLP-1 레벨 상승 작용을 시험한 결과를 나타내었다. -○-는 대조로서 정제수만을 투여한 군, -●-는 DPP 4 저해 화합물(화합물 A) 10 mg/kg만을 경구 투여한 군, -△-는 프락토올리고당 6 g/kg만을 경구 투여한 군, -▲-는 DPP 4 저해 화합물(화합물 A) 10 mg/kg 및 프락토올리고당 6 g/kg을 경구 투여한 군(모두 n=5)의 각 군에 있어서의 혈장중 활성형 GLP-1 농도(평균치±표준 오차(SEM))의 경시 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
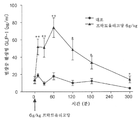
[도 3] 도 3에는 고지방식 부하한 C57BL/6J 마우스에게 DPP 4 저해 화합물(화합물 A) 및 프락토올리고당을 혼이(混餌) 투여한 경우에 있어서의 체중 감소 작용을 시험한 결과를 나타내었다. -○-는 고지방식 부하하지 않은 정상 마우스의 군, -●-는 대조로서 고지방식만을 부하한 군, -△-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A) 10 mg/100 g만을 혼이 투여한 군, -▽-는 고지방식 부하 마우스에게 프락토올리고당 10 w/w%만을 경구 투여한 군, -▼-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A) 10 mg/100 g 및 프락토올리고당 10 w/w%의 양자를 혼이 투여한 군(모두 n=9 내지 10)의 각 군에 있어서의 체중(평균치±표준 오차(SEM))의 경일 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 4a] 도 4a에는 C57BL/6J 마우스에게 D-만니톨 및 DPP 4 저해 화합물(화합물 A', 시타글립틴(Sitagliptin) 또는 알로글립틴(Alogliptin))을 투여한 경우의 혈장중 활성형 GLP-1 레벨 상승 작용을 시험한 결과를 나타내었다. -○-는 D-만니톨 3 g/kg만을 경구 투여한 군, -●-는 D-만니톨 3 g/kg 및 DPP 4 저해 화합물(화합물 A') 10 mg/kg을 경구 투여한 군, -▲-는 D-만니톨 3 g/kg 및 DPP 4 저해 화합물(시타글립틴) 10 mg/kg을 경구 투여한 군, -▼-는 D-만니톨 3 g/kg 및 DPP 4 저해 화합물(알로글립틴) 10 mg/kg을 경구 투여한 군(모두 n=5)의 각 군에 있어서의 혈장중 활성형 GLP-1 농도(평균치±표준 오차(SEM))의 경시 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 4b] 도 4b에는 C57BL/6J 마우스에게 메리비오스 및 DPP 4 저해 화합물(화합물 A', 시타글립틴 또는 알로글립틴)을 투여한 경우의 혈장중 활성형 GLP-1 레벨 상승 작용을 시험한 결과를 나타내었다. -○-는 메리비오스 6 g/kg만을 경구 투여한 군, -●-는 메리비오스 6 g/kg 및 DPP 4 저해 화합물(화합물 A') 10 mg/kg을 경구 투여한 군, -▲-는 메리비오스 6 g/kg 및 DPP 4 저해 화합물(시타글립틴) 10 mg/kg을 경구 투여한 군, -▼-는 메리비오스 6 g/kg 및 DPP 4 저해 화합물(알로글립틴) 10 mg/kg을 경구 투여한 군(모두 n=5)의 각 군에 있어서의 혈장중 활성형 GLP-1 농도(평균치±표준 오차(SEM))의 경시 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 4c] 도 4c에는 C57BL/6J 마우스에게 아세술팜 K 및 DPP 4 저해 화합물(화합물 A', 시타글립틴, 빌다글립틴(Vildagliptin), 삭사글립틴(Saxagliptin) 또는 화합물 B)을 투여한 경우의 혈장중 활성형 GLP-1 레벨 상승 작용을 시험한 결과를 나타내었다. -○-는 아세술팜 K 3 g/kg만을 경구 투여한 군, -●-는 아세술팜 K 3 g/kg 및 DPP 4 저해 화합물(화합물 A') 10 mg/kg을 경구 투여한 군, -■-는 아세술팜 K 3 g/kg 및 DPP 4 저해 화합물(시타글립틴) 10 mg/kg을 경구 투여한 군, -▼-는 아세술팜 K 3 g/kg 및 DPP 4 저해 화합물(빌다글립틴) 10 mg/kg을 경구 투여한 군, -▽-는 아세술팜 K 3 g/kg 및 DPP 4 저해 화합물(삭사글립틴) 10 mg/kg을 경구 투여한 군, -▲-는 아세술팜 K 3 g/kg 및 DPP 4 저해 화합물(화합물 B) 10 mg/kg을 경구 투여한 군, (모두 n=5)의 각 군에 있어서의 혈장중 활성형 GLP-1 농도(평균치±표준 오차(SEM))의 경시 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 5a] 도 5a에는 고지방식 부하한 C57BL/6J 마우스에게 DPP 4 저해 화합물(화합물 A') 및 D-만니톨을 혼이 투여한 경우에 있어서의 체중 감소 작용을 시험한 결과를 나타내었다. -●-는 대조로서 고지방식만을 부하한 군, -○-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g만을 혼이 투여한 군, -◇-는 고지방식 부하 마우스에게 D-만니톨 5 w/w%만을 경구 투여한 군, -◆-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g 및 D-만니톨 5 w/w%의 양자를 혼이 투여한 군(모두 n=9)의 각 군에 있어서의 체중(평균치±표준 오차(SEM))의 경일 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 5b] 도 5b에는 고지방식 부하한 C57BL/6J 마우스에게 DPP 4 저해 화합물(화합물 A') 및 메리비오스를 혼이 투여한 경우에 있어서의 체중 감소 작용을 시험한 결과를 나타내었다. -●-는 대조로서 고지방식만을 부하한 군, -○-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g만을 혼이 투여한 군, -△-는 고지방식 부하 마우스에게 메리비오스 5 w/w%만을 경구 투여한 군, -▲-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g 및 메리비오스 5 w/w%의 양자를 혼이 투여한 군(모두 n=9)의 각 군에 있어서의 체중(평균치±표준 오차(SEM))의 경일 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 5c] 도 5c에는 고지방식 부하한 C57BL/6J 마우스에게 DPP 4 저해 화합물(화합물 A') 및 아세술팜 K를 혼이 투여한 경우에 있어서의 체중 감소 작용을 시험한 결과를 나타내었다. -●-는 대조로서 고지방식만을 부하한 군, -○-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g만을 혼이 투여한 군, -▽-는 고지방식 부하 마우스에게 아세술팜 K 5 w/w%만을 경구 투여한 군, -▼-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g 및 아세술팜 K 5 w/w%의 양자를 혼이 투여한 군(모두 n=9)의 각 군에 있어서의 체중(평균치±표준 오차(SEM))의 경일 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 2] 도 2에는 C57BL/6J 마우스에게 DPP 4 저해 화합물(화합물 A) 및 프락토올리고당을 투여한 경우의 혈장중 활성형 GLP-1 레벨 상승 작용을 시험한 결과를 나타내었다. -○-는 대조로서 정제수만을 투여한 군, -●-는 DPP 4 저해 화합물(화합물 A) 10 mg/kg만을 경구 투여한 군, -△-는 프락토올리고당 6 g/kg만을 경구 투여한 군, -▲-는 DPP 4 저해 화합물(화합물 A) 10 mg/kg 및 프락토올리고당 6 g/kg을 경구 투여한 군(모두 n=5)의 각 군에 있어서의 혈장중 활성형 GLP-1 농도(평균치±표준 오차(SEM))의 경시 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 3] 도 3에는 고지방식 부하한 C57BL/6J 마우스에게 DPP 4 저해 화합물(화합물 A) 및 프락토올리고당을 혼이(混餌) 투여한 경우에 있어서의 체중 감소 작용을 시험한 결과를 나타내었다. -○-는 고지방식 부하하지 않은 정상 마우스의 군, -●-는 대조로서 고지방식만을 부하한 군, -△-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A) 10 mg/100 g만을 혼이 투여한 군, -▽-는 고지방식 부하 마우스에게 프락토올리고당 10 w/w%만을 경구 투여한 군, -▼-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A) 10 mg/100 g 및 프락토올리고당 10 w/w%의 양자를 혼이 투여한 군(모두 n=9 내지 10)의 각 군에 있어서의 체중(평균치±표준 오차(SEM))의 경일 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 4a] 도 4a에는 C57BL/6J 마우스에게 D-만니톨 및 DPP 4 저해 화합물(화합물 A', 시타글립틴(Sitagliptin) 또는 알로글립틴(Alogliptin))을 투여한 경우의 혈장중 활성형 GLP-1 레벨 상승 작용을 시험한 결과를 나타내었다. -○-는 D-만니톨 3 g/kg만을 경구 투여한 군, -●-는 D-만니톨 3 g/kg 및 DPP 4 저해 화합물(화합물 A') 10 mg/kg을 경구 투여한 군, -▲-는 D-만니톨 3 g/kg 및 DPP 4 저해 화합물(시타글립틴) 10 mg/kg을 경구 투여한 군, -▼-는 D-만니톨 3 g/kg 및 DPP 4 저해 화합물(알로글립틴) 10 mg/kg을 경구 투여한 군(모두 n=5)의 각 군에 있어서의 혈장중 활성형 GLP-1 농도(평균치±표준 오차(SEM))의 경시 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 4b] 도 4b에는 C57BL/6J 마우스에게 메리비오스 및 DPP 4 저해 화합물(화합물 A', 시타글립틴 또는 알로글립틴)을 투여한 경우의 혈장중 활성형 GLP-1 레벨 상승 작용을 시험한 결과를 나타내었다. -○-는 메리비오스 6 g/kg만을 경구 투여한 군, -●-는 메리비오스 6 g/kg 및 DPP 4 저해 화합물(화합물 A') 10 mg/kg을 경구 투여한 군, -▲-는 메리비오스 6 g/kg 및 DPP 4 저해 화합물(시타글립틴) 10 mg/kg을 경구 투여한 군, -▼-는 메리비오스 6 g/kg 및 DPP 4 저해 화합물(알로글립틴) 10 mg/kg을 경구 투여한 군(모두 n=5)의 각 군에 있어서의 혈장중 활성형 GLP-1 농도(평균치±표준 오차(SEM))의 경시 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 4c] 도 4c에는 C57BL/6J 마우스에게 아세술팜 K 및 DPP 4 저해 화합물(화합물 A', 시타글립틴, 빌다글립틴(Vildagliptin), 삭사글립틴(Saxagliptin) 또는 화합물 B)을 투여한 경우의 혈장중 활성형 GLP-1 레벨 상승 작용을 시험한 결과를 나타내었다. -○-는 아세술팜 K 3 g/kg만을 경구 투여한 군, -●-는 아세술팜 K 3 g/kg 및 DPP 4 저해 화합물(화합물 A') 10 mg/kg을 경구 투여한 군, -■-는 아세술팜 K 3 g/kg 및 DPP 4 저해 화합물(시타글립틴) 10 mg/kg을 경구 투여한 군, -▼-는 아세술팜 K 3 g/kg 및 DPP 4 저해 화합물(빌다글립틴) 10 mg/kg을 경구 투여한 군, -▽-는 아세술팜 K 3 g/kg 및 DPP 4 저해 화합물(삭사글립틴) 10 mg/kg을 경구 투여한 군, -▲-는 아세술팜 K 3 g/kg 및 DPP 4 저해 화합물(화합물 B) 10 mg/kg을 경구 투여한 군, (모두 n=5)의 각 군에 있어서의 혈장중 활성형 GLP-1 농도(평균치±표준 오차(SEM))의 경시 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 5a] 도 5a에는 고지방식 부하한 C57BL/6J 마우스에게 DPP 4 저해 화합물(화합물 A') 및 D-만니톨을 혼이 투여한 경우에 있어서의 체중 감소 작용을 시험한 결과를 나타내었다. -●-는 대조로서 고지방식만을 부하한 군, -○-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g만을 혼이 투여한 군, -◇-는 고지방식 부하 마우스에게 D-만니톨 5 w/w%만을 경구 투여한 군, -◆-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g 및 D-만니톨 5 w/w%의 양자를 혼이 투여한 군(모두 n=9)의 각 군에 있어서의 체중(평균치±표준 오차(SEM))의 경일 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 5b] 도 5b에는 고지방식 부하한 C57BL/6J 마우스에게 DPP 4 저해 화합물(화합물 A') 및 메리비오스를 혼이 투여한 경우에 있어서의 체중 감소 작용을 시험한 결과를 나타내었다. -●-는 대조로서 고지방식만을 부하한 군, -○-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g만을 혼이 투여한 군, -△-는 고지방식 부하 마우스에게 메리비오스 5 w/w%만을 경구 투여한 군, -▲-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g 및 메리비오스 5 w/w%의 양자를 혼이 투여한 군(모두 n=9)의 각 군에 있어서의 체중(평균치±표준 오차(SEM))의 경일 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
[도 5c] 도 5c에는 고지방식 부하한 C57BL/6J 마우스에게 DPP 4 저해 화합물(화합물 A') 및 아세술팜 K를 혼이 투여한 경우에 있어서의 체중 감소 작용을 시험한 결과를 나타내었다. -●-는 대조로서 고지방식만을 부하한 군, -○-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g만을 혼이 투여한 군, -▽-는 고지방식 부하 마우스에게 아세술팜 K 5 w/w%만을 경구 투여한 군, -▼-는 고지방식 부하 마우스에게 DPP 4 저해 화합물(화합물 A') 10 mg/100 g 및 아세술팜 K 5 w/w%의 양자를 혼이 투여한 군(모두 n=9)의 각 군에 있어서의 체중(평균치±표준 오차(SEM))의 경일 변화를 나타낸다.(*: p<0.05, **: p<0.01 대조군에 대한 다넷트 다중 비교법에 기초하는 유의차를 나타냄)
<발명을 실시하기 위한 최선의 형태>
본 발명에 있어서, 디펩티딜 펩티다아제 4 저해 화합물로서는 통상, 디펩티딜 펩티다아제 4에 직접 작용하여 그의 효소 활성을 저해하는 능력을 갖는 화합물이 이용된다. 상기 화합물은 펩티드성 또는 비펩티드성의 어느 것일 수도 있지만, 비펩티드성의 것이 바람직하다. 저해 형식으로서는, 예를 들면 길항형, 비길항형, 불길항형, 혼합형의 저해를 들 수 있다.
디펩티딜 펩티다아제 4 저해 화합물은 널리 알려져 있으며, 예를 들면 이하의 공보에 다양한 화합물이 개시되어 있다. 본 발명에서 이용하는 디펩티딜 펩티다아제 4 저해 화합물로서는 이들에 개시된 화합물을 적절하게 사용할 수 있지만, 이들로 한정되지 않는다.
특허 문헌 [타나베 세이야꾸 WO2002/30891 및 이것에 대응하는 미국 특허 US6849622];
[타나베 세이야꾸 WO2002/30890 및 이것에 대응하는 미국 특허 US7138397];
[Ferring WO1995/15309, WO2001/40180, WO2001/81304, WO2001/81337, WO2003/00250, WO2003/35057];
[Probiodrug AG WO1997/40832, EP1082314, WO1999/61431, WO2003/015775];
[Novartis WO1998/19998, WO2000/34241, WO2001/96295, US6107317, US6110949, US6172081];
[GSK WO2003/002531, WO2003/002530, WO2003/002553];
[BMS WO2001/68603, WO2002/83128, WO2005/012249];
[Merck WO2002/76450, WO2003/004498];
[Syrrx WO2005/026148, WO2005/030751, WO2005/095381, WO2004/087053, WO2004/103993];
[미쯔비시 웰팜 WO2002/14271, US7060722, US7074794, WO2003/24942, 일본 특허 공개 제2002-265439호, 일본 특허 공개 제2005-170792호, WO2006/88129];
[다이쇼 세이야꾸 WO2004/020407];
[야마노우찌 세이야꾸 WO2004/009544];
[교와 핫꼬 WO2002/051836];
[교린 세이야꾸 WO2005/075421, WO2005/077900, WO2005/082847];
[Alantos WO2006/116157];
[Glenmark WO2006/090244, WO2005/075426];
[산와 가가꾸 겐큐쇼 WO2004/067509];
[LG 생명과학 WO2005/037828, WO2006/104356].
바람직한 디펩티딜 펩티다아제 4 저해 화합물로서는, 예를 들면 미국 특허 US6,849,622에 개시된 화학식 Ia로 표시되는 화합물 또는 그의 약리적으로 허용되는 염을 들 수 있다.
[화학식 Ia]
〔식 중, A는 -CH2- 또는 -S-를 나타내고,
R1은 수소 원자, 저급 알킬, 히드록시 저급 알킬 또는 저급 알콕시 저급 알킬을 나타내고,
R2는 (1) 치환될 수 있는 환식기로서 상기 환식기 부분이 (i) 단환, 이환 또는 삼환식 탄화수소기 또는 (ii) 단환, 이환 또는 삼환식 복소환기인 환식기, 또는 (2) 치환될 수 있는 아미노기를 나타냄〕
이들 중에서, 보다 구체적으로는, 예를 들면
(2S)-2-시아노-1-[트랜스-4-(디메틸아미노카르보닐)시클로헥실아미노]아세틸피롤리딘;
(2S)-2-시아노-1-[트랜스-4-(모르폴리노카르보닐)시클로헥실아미노]아세틸피롤리딘; 및
(2S)-2-시아노-1-[트랜스-4-(4-아세틸피페라진-1-일카르보닐)시클로헥실아미노]아세틸피롤리딘; 등
및 이들의 약리적으로 허용되는 염을 들 수 있다.
또한, 바람직한 디펩티딜 펩티다아제 4 저해 화합물로서, 미국 특허 US7,138,397에 개시된 화학식 Ib로 표시되는 화합물 또는 그의 약리적으로 허용되는 염을 들 수 있다.
[화학식 Ib]
〔식 중,
A는 -CH2-를 나타내고,
R1은 H, 저급 알킬, 히드록시 저급 알킬, 또는 저급 알콕시 저급 알킬을 나타내고,
R2는 치환될 수 있는 피페라지닐기를 나타냄〕
이들 중에서, 보다 구체적으로는, 예를 들면
(2S)-2-시아노-1-[t-4-(4-아세틸-1-피페라지닐)-1-메틸-r-1-시클로헥실아미노]아세틸피롤리딘; 및
(2S)-2-시아노-1-[t-4-(4-프로피오닐-1-피페라지닐)-1-메틸-r-1-시클로헥실아미노]아세틸피롤리딘; 등
및 이들의 약리적으로 허용되는 염을 들 수 있다.
또한, 바람직한 디펩티딜 펩티다아제 4 저해 화합물로서, 미국 특허 US7,074,794에 개시된 하기 화학식으로 표시되는 L-프롤린 유도체 또는 그의 약리적으로 허용되는 염을 들 수 있다.
〔식 중,
X는: -NR1R2
(R1, R2는 동일하거나 상이할 수 있고, 각각 독립적으로 시클로알킬알킬, 아릴알킬, 헤테로아릴 또는 헤테로아릴알킬을 나타내거나, 또는 서로 결합하여 1 내지 2개의 질소 원자 또는 산소 원자를 각각 포함하고 있을 수 있는 헤테로사이클을 형성할 수도 있고, 또한 이 헤테로사이클에 치환기를 가질 수 있는 방향환이 축합하고 있을 수 있고, 또한 이 헤테로사이클은 스피로환일 수 있음);
-NR3COR4
(R3, R4는 동일하거나 상이할 수 있고, 각각 독립적으로 수소 원자, 알킬, 시클로알킬, 시클로알킬알킬, 아릴, 아릴알킬, 아릴알케닐, 헤테로아릴 또는 헤테로아릴알킬을 나타냄);
-NR5CONR6R7 또는 -NR5CH2CH2NR6R7
(R5, R6, R7은 동일하거나 상이할 수 있고, 각각 독립적으로 수소 원자, 알킬, 아실, 시클로알킬, 시클로알킬알킬, 아릴, 아릴알킬, 헤테로아릴 또는 헤테로아릴알킬을 나타내거나, 또는 R6, R7은 서로 결합하여 1 내지 2개의 질소 원자 또는 산소 원자를 각각 포함하고 있을 수 있는 헤테로사이클을 형성할 수 있고, 또한 이 헤테로사이클에 치환기를 가질 수 있는 방향환이 축합하고 있을 수 있음);
-NR8SO2R9
(R8, R9는 동일하거나 상이할 수 있고, 각각 독립적으로 수소 원자, 알킬, 시클로알킬, 시클로알킬알킬, 아릴, 아릴알킬, 헤테로아릴 또는 헤테로아릴알킬을 나타냄); 또는
-OR10 또는 -OCOR11
(R10, R11은 각각 수소 원자, 알킬, 시클로알킬, 시클로알킬알킬, 아릴, 아릴알킬, 헤테로아릴 또는 헤테로아릴알킬을 나타냄)
을 나타내고,
Y는: CH2, CH-OH, S,S=O 또는 SO2를 나타내고,
Z는: 수소 원자 또는 시아노를 나타내며,
또한, 상기 기 중, 알킬, 아릴, 아릴알킬, 아릴알케닐, 헤테로아릴, 헤테로아릴알킬, 시클로알킬, 시클로알킬알킬 및 헤테로사이클은 각각 치환기를 가질 수 있음〕
이들 중에서, 보다 구체적으로는, 예를 들면 3-{(2S,4S)-4-[4-(3-메틸-1-페닐-5-피라졸릴)-1-피페라지닐]-2-피롤리디닐카르보닐}-1,3-티아졸리딘 등, 및 이들의 약리적으로 허용할 수 있는 염을 들 수 있고, 보다 바람직하게는 WO2006/88129에 개시된 3-{(2S,4S)-4-[4-(3-메틸-1-페닐-1H-피라졸-5-일)피페라진-1-일]피롤리딘-2-일카르보닐}티아졸리딘 및 이의 약리적으로 허용할 수 있는 염을 들 수 있다.
미국 특허 US6,849,622, 미국 특허 US7,138,397, 미국 특허 US7,074,794 및 WO2006/88129는 참고로서 본원 발명에 포함된다.
상기 또는 이하에 있어서, 저급 알킬기(또는 알킬기), 저급 알킬티오기(또는 알킬티오기), 저급 알킬술포닐기(또는 알킬술포닐기), 저급 알콕시기(또는 알콕시기), 저급 알킬아미노기(또는 알킬아미노기)로서는 탄소수 1 내지 6의 직쇄상 또는 분지쇄상의 것을 들 수 있고, 특히 탄소수 1 내지 4의 것을 들 수 있다. 또한, 저급 알카노일기(또는 알카노일기), 저급 알카노일아미노기(또는 알카노일아미노기)로서는 탄소수 2 내지 7, 특히 탄소수 2 내지 5의 직쇄상 또는 분지쇄상의 것을 들 수 있다. 또한, 할로겐 원자로서는 불소, 염소, 브롬 또는 요오드를 들 수 있다.
상기 또는 이하에 있어서, 약리적으로 허용할 수 있는 염으로서는, 예를 들면 염산염, 황산염, 질산염, 인산염 또는 브롬화수소산염과 같은 무기산염, 또는 아세트산염, 푸마르산염, 옥살산염, 시트르산염, 메탄술폰산염, 벤젠술폰산염, p-톨루엔술폰산염 또는 말레산염과 같은 유기산염 등을 들 수 있다. 또한, 디펩티딜 펩티다아제 4 저해 화합물이 카르복실기 등의 치환기를 갖는 경우에는 염기와의 염(예를 들면 나트륨염, 칼륨염 등의 알칼리 금속염 또는 칼슘염과 같은 알칼리 토금속염)을 들 수 있다.
그 밖의 바람직한 디펩티딜 펩티다아제 4 저해 화합물로서, 예를 들면 이하와 같은 화합물을 들 수 있다.
ㆍ시타글립틴(Sitagliptin, 개발 코드 MK-0431, 판매명 자누비아(Januvia)) 또는 그의 등가물, 즉,
(3R)-3-아미노-1-[9-(트리플루오로메틸)-1,4,7,8-테트라아자비시클로[4.3.0]노나-6,8-디엔-4-일]-4-(2,4,5-트리플루오로페닐)부탄-1-온
〔영문명: (3R)-3-amino-1-[9-(trifluoromethyl)-1,4,7,8-tetrazabicyclo[4.3.0]nona-6,8-dien-4-yl]-4-(2,4,5-trifluorophenylbutan-1-one〕
또는 그의 약리적으로 허용할 수 있는 염(인산염 등).
ㆍ빌다글립틴(Vildagliptin, 개발 코드 LAF237, 판매명 가브스(Galvus)) 또는 그의 등가물, 즉,
(2S)-1-[2-[(3-히드록시-1-아다만틸)아미노]아세틸]피롤리딘-2-카르보니트릴
〔영문명: (2S)-1-[2-[(3-hydroxy-1-adamantyl)amino]acetyl]pyrrolidine-2-carbonitrile〕
또는 그의 약리적으로 허용할 수 있는 염.
ㆍ삭사글립틴(Saxagliptin, 개발 코드 BMS-477118) 또는 그의 등가물, 즉,
(1S,3S,5S)-2-[(2S)-2-아미노-2-(3-히드록시-1-아다만틸)아세틸]-2-아자비시클로[3.1.0]헥산-3-카르보니트릴
〔영문명: (1S,3S,5S)-2-[(2S)-2-amino-2-(3-hydroxy-1-adamantyl)acetyl]-2-azabicyclo[3.1.0] hexane-3-carbonitrile〕
또는 그의 약리적으로 허용할 수 있는 염.
ㆍ알로글립틴(Alogliptin, 개발 코드 SYR-322) 또는 그의 등가물, 즉,
6-[(3R)-3-아미노피페리딘-1-일]-1-(2-시아노벤질)-3-메틸피리미딘-2,4(1H,3H)-디온
〔영문명: 6-[(3R)-3-aminopiperidin-1-yl]-1-(2-cyanobenzyl)-3-methylpyrimidin-2,4(1H,3H)-dione〕
또는 그의 약리적으로 허용할 수 있는 염(벤조에이트 등).
ㆍL-트레오-이소로이실피롤리디드, L-알로-이소로이실티아졸리디드, L-알로-이소로이실피롤리디드 및 이들의 약리적으로 허용할 수 있는 염.
본 발명에 있어서 DPP 4 저해 화합물과 조합하여 이용하는 감미료는 GLP-1 분비 촉진 작용을 갖는 감미료이다.
본원 명세서에 있어서 「GLP-1 분비 촉진 작용」이란, 혈중 활성형 GLP-1 레벨을 상승시키는 작용을 의미하고, 예를 들면 인간 또는 비인간 포유류의 생체내에 경소화관에서 (경구 또는 경장적으로)투여한 경우에, 투여하지 않은 경우와 비교하여, 혈중(혈장중 등)의 활성형 GLP-1을 보다 높은 레벨까지 상승시키는 작용을 의미한다.
감미료는 당류 및 비당질계 감미료(합성 감미료 등)의 어느 것일 수도 있다.
GLP-1 분비 촉진 작용을 갖는 감미료는 인간 또는 비인간 포유류의 생체내에 경소화관으로(경구 또는 경장적으로) 투여한 경우에 있어서, 실질적으로 혈당치의 상승을 발생하지 않는 것이 바람직하다. 글루코오스는 그의 투여에 의해 현저한 혈당치의 상승이 생기기 때문에 바람직하지 않다.
이러한 관점에서, GLP-1 분비 촉진 작용을 갖는 감미료로서, 당류를 이용하는 경우에는 비대사성 및/또는 난소화흡수성의 성질을 갖는 당류를 이용하는 것이 바람직하다.
비대사성 및/또는 난소화흡수성의 당류로서는, 예를 들면 인간 또는 비인간 포유류의 생체가 이용능을 갖지 않는 단위당으로 구성되는 당류가 포함된다. 또는, 인간 또는 비인간 포유류의 생체 그 자체가 갖는 소화 효소군〔소장 상피 점막층에 존재하는 소화 효소군 등(예를 들면, 수크라아제, 글루코아미라제, 이소말타아제, 락타아제 등의 이당류 수해 효소 효소 등)〕에 의해서 분해되기 어려운 구조를 갖는 당류(예를 들면, α-1,4 결합 및 β-1,4 결합 이외의 형의 결합을 포함하는 당류, 소장의 이당류 수분해 효소에 의해 분해되기 어려운 단위당을 갖는 당류 등)가 포함된다.
합성 감미료 등의 비당질계 감미료는 저칼로리인 것이 많고, 통상, 혈당치를 상승시키지 않는다.
GLP-1의 분비를 촉진하는 작용을 갖는 감미료(당류)로서, 보다 구체적으로는, 예를 들면 프락토올리고당(fructooligosaccaride)〔즉, 1개의 α-D-글루코피라노실에 2 내지 8개의 프락토프라노실이 연결된 구조를 포함하는 당(케스토오스, 니스토오스, 프락토프라노실니스토오스 등)을 포함하는 혼합물〕을 바람직하게 사용할 수 있다.
또한, 프락토올리고당의 구성 성분인 케스토오스(kestose)〔glucose-1,2-fructose-1,2-fructose〕, 니스토오스(nistose)〔glucose-1,2-fructose-1,2-fructose-1,2-fructose〕, 및 프락토프라노실니스토오스〔glucose-1,2-fructose-1,2-fructose-1,2-fructose-1,2-fructose〕 등을 각각 혼합물의 형태가 아닌 단체로서, 실질적으로 순수한 형태의 것을 사용할 수 있다.
이들은 모두 비대사성 및/또는 난소화흡수성의 성질을 갖는 당류이다.
또한 또는, GLP-1의 분비를 촉진하는 작용을 갖는 감미료(당류)로서, 크실로오스(xylose)(특히 그의 D-체)를 바람직하게 사용할 수 있다.
본 명세서에 있어서, 올리고당류란, 단당의 구성이 복수개(통상 2 내지 9개, 바람직하게는 2 내지 6개) 결합한 구조를 갖는 당류 또는 이들의 혼합물을 의미한다.
GLP-1 분비 촉진 작용을 갖는 감미료(당류)로서는 상기한 것 이외에, 이하와 같은 당류〔올리고당류(2 내지 6 당류, 올리고당 혼합물 등) 및 당 알코올류〕를 들 수 있다.
ㆍ이당류: 예를 들면,
메리비오스〔α-D-galactopyranosyl-(1→6)-D-glucose〕,
이소말토오스〔α-D-glucopyranosyl-(1→6)-D-glucose〕,
겐티오비오스(gentiobiose)〔β-D-글루코피라노실-(1→6)-D-글루코오스〕,
트레할로오스(Trehalose)〔α-D-glucopyranosyl α-D-glucopyranoside〕,
이소트레할로오스(Isotrehalose)〔β-D-glucopyranosyl β-D-glucopyranoside〕,
네오트레할로오스(Neotrehalose)〔β-D-glucopyranosyl α-D-glucopyranoside〕,
니게로스(Nigerose)〔α-D-glucopyranosyl-(1→3)-D-glucose〕,
말툴로스(Maltulose)〔α-D-glucopyranosyl-(1→4)-D-fructose〕,
이소말툴로스(Isomaltulose)〔α-D-glucopyranosyl-(1→6)-D-fructose〕,
락툴로스(Lactulose)〔β-D-galactopyranosyl-(1→4)-D-fructose〕,
코지비오스(Kojibiose)〔α-D-glucopyranosyl-(1→2)-D-glucose〕,
소포로스(Sophorose)〔β-D-glucopyranosyl-(1→2)-D-glucose〕,
라미나라비오스(Laminarabiose)〔β-D-glucopyranosyl-(1→3)-D-glucose〕,
셀로비오스(Cellobiose)〔β-D-glucopyranosyl-(1→4)-D-glucose〕,
셀로비온산(Cellobionic acid)〔β-D-glucopyranosyl-(1→4)-D-gluconic acid〕,
갈락토수크로오스(Galactosucrose)〔β-D-fructofuranosyl α-D-galactopyranoside; Fruf(β2-1α)Gal〕,
락토사민(LacN)(Lactosamine)〔β-D-galactopyranosyl-(1→4)-D-glucosamine〕,
락토오스디아민(Lactosediamine)〔2-amino-2-deoxy-β-D-galactopyranosyl-(1→4)-D-glucosamine〕,
락토비온산(Lactobionic acid)〔β-D-galactopyranosyl-(1→4)-D-gluconic acid〕,
네오락토오스(Neolactose)〔β-D-galactopyranosyl-(1→4)-D-altrose〕,
프리메베로스(Primeverose)〔β-D-xylopyranosyl-(1→6)-D-glucose〕,
루티노오스(Rutinose)〔α-L-rhamnopyranosyl-(1→6)-D-glucose〕,
실라비오스(Scillabiose)〔β-D-glucopyranosyl-(1→4)-L-rhamnose〕,
튜라노스(Turanose)〔α-D-glucopyranosyl-(1→3)-D-fructose〕,
비시아노스(Vicianose)〔α-L-arabinopyranosyl-(1→6)-D-glucose〕,
크실로비오스(크실로오스 2분자가 β-1,4 결합한 이당류) 등.
ㆍ삼당류: 예를 들면,
라피노오스(Raffinose)〔galactose-1,6-glucose-1,2-fructose;
β-D-fructofuranosyl α-D-galactopyranosyl-(1→6)-α-D-glucopyranoside〕,
셀로트리오스(Cellotriose)
〔β-D-glucopyranosyl-(1→4)-β-D-glucopyranosyl-(1→4)-D-glucose〕,
카코트리오스(Chacotriose)
〔α-L-rhamnopyranosyl-(1→2)-[α-L-rhamnopyranosyl-(1→4)]-D-glucose〕,
겐티아노스(Gentianose)
〔β-D-fructofuranosyl β-D-glucopyranosyl-(1→6)-α-D-glucopyranoside〕,
이소말토트리오스(Isomaltotriose)
〔α-D-glucopyranosyl-(1→6)-α-D-glucopyranosyl-(1→6)-D-glucose〕,
이소파노오스(Isopanose)
〔α-D-glucopyranosyl-(1→4)-[α-D-glucopyranosyl-(1→6)]-D-glucose〕,
말토트리오스(Maltotriose)
〔α-D-glucopyranosyl-(1→4)-α-D-glucopyranosyl-(1→4)-D-glucose〕,
만니노트리오스(Manninotriose)
〔α-D-galactopyranosyl-(1→6)-α-D-galactopyranosyl-(1→6)-D-glucose〕,
멜레지토오스(Melezitose)
〔α-D-glucopyranosyl-(1→3)-β-D-fructofuranosyl α-D-glucopyranoside〕,
파노오스(Panose)
〔α-D-glucopyranosyl-(1→6)-α-D-glucopyranosyl-(1→4)-D-glucose〕,
플란테오스(Planteose)
〔α-D-galactopyranosyl-(1→6)-β-D-fructofuranosyl α-D-glucopyranoside〕,
솔라트리오스(Solatriose)
〔α-L-rhamnopyranosyl-(1→2)-[β-D-glucopyranosyl-(1→3)]-D-galactose〕,
움벨리페로오스(Umbelliferose)
〔β-D-fructofuranosyl α-D-galactopyranosyl-(1→2)-α-D-galactopyranoside〕 등.
ㆍ사당류:
스타키오스(Stachyose)
〔β-D-fructofuranosyl α-D-galactopyranosyl-(1→6)-α-D-galactopyranosyl-(1→6)-α-D-glucopyranoside〕,
리코테트라오스(Lycotetraose)
〔β-D-glucopyranosyl-(1→2)-[β-D-xylopyranosyl-(1→3)]-β-D-glucopyranosyl-(1→4)-β-D-galactose〕,
말토테트라오스(Maltotetraose)
〔α-D-glucopyranosyl-(1→4)-α-D-glucopyranosyl-(1→4)-α-D-glucopyranosyl-(1→4)-D-glucose〕 등.
ㆍ오당류: 예를 들면,
말토펜타오스(Maltopentaose)
〔α-D-glucopyranosyl-(1→4)-α-D-glucopyranosyl-(1→4)-α-D-glucopyranosyl-(1→4)-α-D-glucopyranosyl-(1→4)-D-glucose〕,
베르바스코스(Verbascose)
〔β-D-fructofuranosyl α-D-galactopyranosyl-(1→6)-α-D-galactopyranosyl-(1→6)-α-D-galactopyranosyl-(1→6)-α-D-glucopyranoside〕, 등.
ㆍ육당류: 예를 들면,
말토헥사오스(Maltohexaose)
〔α-D-glucopyranosyl-(1→4)-α-D-glucopyranosyl-(1→4)-α-D-glucopyranosyl-(1→4)-α-D-glucopyranosyl-(1→4)-α-D-glucopyranosyl-(1→4)-D-glucose〕, 등.
ㆍ올리고당 혼합물: 예를 들면,
올리고토오스〔말토오스, 말토트리오스 등의 혼합물〕,
말토올리고당,
이소말토올리고당,
글루코올리고당,
비트올리고당(사탕무 추출물, 라피노오스를 함유),
갈락토올리고당,
겐티오올리고당,
니게로올리고당,
이눌로올리고당,
유과 올리고당(락토수크로오스를 주성분으로 하는 혼합물),
대두 올리고당,
크실로올리고당 등.
ㆍ당 알코올류: 예를 들면,
트레이톨(특히 그의 D체),
에리트리톨,
자일리톨,
아라비니톨(특히 그의 D체),
리비톨,
소르비톨(sorbitol)〔별명: 소르비트(sorbit) 또는 글루시톨(glucitol)〕,
만니톨(특히 그의 D체),
아리톨,
갈락티톨(Galactitol)〔별명: 둘시톨(Dulcitol)〕,
이지톨(특히 그의 D체),
타리톨(알트리톨)(특히 그의 D체),
락티톨(Lactitol)〔β-D-가락토피라노실(1→4)-D-글루시톨〕,
팔라티니트(Palatinit),
말티톨(Maltitol)〔α-D-글루코피라노실(1→4)-D-글루시톨〕, 등.
GLP-1 분비 촉진 작용을 갖는 올리고당류(비대사성 및/또는 난소화흡수성의 것)로서는, 예를 들면 이하의 「단위당군」으로부터 선택되는 동일하거나 또는 상이한 복수개(통상 2 내지 9개, 바람직하게는 2 내지 6개)의 단위당이 결합한 구조를 갖는 당류(단, 단위당의 전체가 D-글루코피라노오스인 경우에는 제외함) 또는 이들의 혼합물을 들 수 있다. 이러한 당류에 있어서 바람직하게는 α-1,4글리코시드 결합 및 β-1,4글리코시드 결합 이외의 형의 결합을 포함하는 당류를 들 수 있다.
단위당군:
D-글루코피라노오스(글루코오스);
D-프락토프라노오스(프락토오스);
크실로피라노오스(크실로오스); 및
D-갈락토피라노오스(갈락토오스).
GLP-1 분비 촉진 작용을 갖는 당 알코올류(비대사성 및/또는 난소화흡수성의 것)로서는, 예를 들면 탄소수 4 내지 6의 알도스〔D-글루코오스, D-만노오스, D-에리트로오스, D-갈락토오스, D-트레오스, L-트레오스, D-리보오스, D-아라비노오스, D-크실로오스, D-알로오스, D-이도오스, D-탈로오스 등을 들 수 있고, 이들 중에서, D-체가 바람직함〕의 환원체인 당 알코올, 또는 탄소수 4 내지 6의 알도스를 단위당으로 하는 2 내지 3 당류의 환원체인 당 알코올을 들 수 있다.
GLP-1 분비 촉진 작용을 갖는 비당질계의 감미료로서는
아세술팜 K〔Acesulfame K(Acesulfame potassium)〕,
스쿠랄로스(Sucralose),
아스파탐(페닐알라닌의 메틸에스테르와, 아스파라긴산이 아미드 결합한 구조를 갖는 합성 감미료),
스테비아(스테비오시드, 스테비아 원엽의 추출ㆍ정제물) 등
을 사용할 수 있다.
본 발명에 있어서 이용되는 GLP-1 분비 촉진 작용을 갖는 감미료로서는, 바람직한 것으로서 이하의 (1), (2), (3), (4) 및 (5)를 들 수 있다.
(1) 프락토올리고당, 케스토오스, 니스토오스 또는 프락토프라노실니스토오스;
(2) 크실로오스(특히 D-크실로오스);
(3) 메리비오스, 라피노오스, 이소말토오스, 크실로비오스, 크실로올리고당 등의 올리고당류;
(4) 만니톨, 소르비톨, 에리트리톨, 말티톨, 자일리톨 등의 당 알코올류; 및
(5) 아세술팜 K, 스쿠랄로스 등의 비당질계 감미료.
또한, 이들 중에서, 보다 바람직한 것으로서는 메리비오스, 만니톨, 소르비톨, 에리트리톨 등의 당류 및 아세술팜 K 등의 비당질계 감미료 등을 들 수 있다.
또한, 이들 중에서, 더욱 바람직한 것으로서는 당류로서 메리비오스 및 만니톨을 들 수 있고, 비당질계 감미료로서 아세술팜 K를 들 수 있다.
감미료(당류 및 비당질계 감미료)는 액상, 분말상의 어느 쪽의 형태로 이용할 수도 있다.
GLP-1 분비 촉진 작용을 갖는 감미료는, 예를 들면 후술하는 실험예 1 또는 2에 기재된 방법에 의해, 그의 GLP-1 분비 촉진 작용을 확인할 수 있다.
DPP 4 저해 화합물의 투여 조건하에 있어서, 각 감미료의 GLP-1 분비 촉진 작용을 시험할 수도 있지만, 후술하는 실험예 1에 기재된 것과 같이, DPP 4 결손 동물을 이용함으로써, 보다 간편히 GLP-1 분비 촉진 작용을 확인할 수 있다.
닛본 찰스리버사의 F344 래트(F344/DuCrlCrlj)는 DPP 4 결손인 것이 알려져 있고, 이러한 시험을 위해 바람직하다.
DPP 4 저해 화합물과 GLP-1 분비 촉진 작용을 갖는 감미료의 병용의 형태는 특별히 한정되지 않는다.
예를 들면, DPP 4 저해 화합물 및 GLP-1 분비 촉진 작용을 갖는 감미료의 양자를 동일한 제제 중에 배합하는 배합제의 형태일 수도 있다.
또는, DPP 4 저해 화합물 및 GLP-1 분비 촉진 작용을 갖는 감미료의 각각을 별도의 제제로 하여, 이들 제제를 동시에 투여하는 형태일 수도 있다.
또는 또한, DPP 4 저해 화합물 및 GLP-1 분비 촉진 작용을 갖는 감미료를 별도의 제제로 하고, 이들 제제를 (상기 순서, 또는 역의 순으로) 순차, 또는 연속적으로 투여하는 형태일 수도 있다.
본 발명에 있어서, DPP 4 저해 화합물 및 GLP-1 분비 촉진 작용을 갖는 감미료는 각각, 투여 방법에 따른 불활성인 담체와 동시에 이용하고, 관용의 의약 제제로서 제제화하여 사용할 수 있다. 이러한 담체로서는, 예를 들면 일반적인 의약에 있어서 허용되는 결합제(아라비아 고무, 젤라틴, 소르비트, 폴리비닐피롤리돈 등), 부형제(젖당, 당, 옥수수 전분 등), 활택제(스테아르산마그네슘, 탈크, 폴리에틸렌글리콜 등), 붕해제(감자 전분 등) 등을 들 수 있다. 주사제나 점적제로 하는 경우에는 주사용 증류수, 생리적 식염수, 포도당 수용액 등을 이용하여 제제화할 수 있다.
제제의 제형은 특별히 한정되지 않으며, 예를 들면 정제, 과립제, 캡슐제, 산제, 용액, 현탁액, 유액, 주사제, 점적제 등의 관용의 제형을 적용할 수 있다.
또한, 드라이 시럽, 시럽, 츄어블정, 발포정 등으로서 제제화할 수도 있다. 이들 제형 중, 과립제, 산제, 드라이 시럽, 시럽, 츄어블정, 발포정이 바람직하다.
본 발명의 치료 또는 예방 방법, 의약 조성물, 및 이들의 사용은 비만의 치료 또는 예방을 위해 적용할 수 있다. 본 발명의 치료 또는 예방 방법, 의약 조성물, 및 이들의 사용은 또한 체중 감소 또는 체지방 감소를 위해 적용할 수 있다. 본 발명의 치료 또는 예방 방법, 의약 조성물, 및 이들의 사용은 또한 비만의 증상을 갖는 환자에 있어서의 체중 감소 또는 체지방 감소를 위해 적용할 수 있다. 본 발명의 치료 또는 예방 방법, 의약 조성물, 및 이들의 사용은 또한 2형 당뇨병 및 비만의 증상이 발병한 환자에게 적용할 수 있다. 본 발명의 치료 또는 예방 방법, 의약 조성물, 및 이들의 사용은 또한 2형 당뇨병 및 비만의 증상을 갖는 환자에 있어서의 체중 감소 또는 체지방 감소를 위해 적용할 수 있다.
본 발명의 의약 조성물은 디펩티딜 펩티다아제 4 저해 화합물 및 GLP-1 분비 촉진 작용을 갖는 감미료 이외에, 1종 이상의 의약적으로 허용되는 담체 또는 부형제를 포함할 수 있다. 또한, 본 발명의 의약 조성물은 동시, 따로따로, 순차 또는 연속적으로 사용하기 위한 조합 제제로 할 수 있다.
본 발명의 의약 조성물 및 치료 또는 예방 방법을 의약 용도에 적용하는 경우의 투여 방법은 특별히 한정되지 않으며, 일반적인 경구 또는 비경구적인 방법(정맥내, 근육내, 피하, 경피, 경비, 기타 경점막, 경장 등)을 적용할 수 있다.
DPP 4 저해 화합물의 투여량은 유효 성분으로 하는 화합물의 효력(potency)이나 특성에 따라, 약효를 발현하는 데 충분한 유효량의 범위에서, 적절하게 설정할 수 있다.
DPP 4 저해 화합물의 투여량은 투여 방법, 투여 대상(환자 등)의 연령, 체중, 상태에 따라서도 다르지만, 일반적인 투여량으로 설정되고, 예를 들면 1일당, 통상 0.001 내지 300 mg/kg 체중의 범위에서 적절한 양으로 설정된다.
DPP 4 저해 화합물의 투여량은 투여된 생체 내에서의 디펩티딜 펩티다아제 4의 효소 활성을 통상, 투여 후 24시간에서 30% 이상, 바람직하게는 60% 이상, 보다 바람직하게는 90% 이상 저해하기 위해서 필요한 양을 설정할 수 있다.
GLP-1 분비 촉진 작용을 갖는 감미료의 투여량은 이용하는 당의 효력이나 특성에 따라, DPP 4 저해 화합물과 조합한 경우에 약효를 발현하는 데 충분한 유효량의 범위에서, 적절하게 설정할 수 있다.
GLP-1 분비 촉진 작용을 갖는 감미료의 투여량은 투여 방법, 투여 대상(환자 등)의 연령, 체중, 상태에 따라서도 다르지만, 예를 들면 1일당, 통상 0.001 내지 5.0 g/kg 체중의 범위에서 적절한 양으로 설정된다.
GLP-1 분비 촉진 작용을 갖는 감미료(특히, 비대사성 및/또는 난소화흡수성의 당류)는 대량으로 투여한 경우, 설사 등의 소화관 증상을 나타내기 쉽다.
따라서, 감미료의 투여량은 가능한 한 소량으로 하고, DPP 4 저해 화합물과의 조합에 의해 약효를 발현하는 데 필요한 양만을 투여하는 것이 바람직하다.
비대사성 및/또는 난소화흡수성의 당류는 소화관 증상의 회피 측면에서는 통상 3 g/kg 체중 이하, 바람직하게는 1 g/kg 체중 이하, 보다 바람직하게는 0.3 g/kg 체중 이하의 범위로 설정된다.
또한, 한편 약효 발현을 위한 필요성 측면에서, 감미료(예를 들면 만니톨, 소르비톨 등)는 바람직하게는 0.01 g/kg 체중 이상, 보다 바람직하게는 0.03 g/kg 체중 이상의 범위로 설정된다.
또한, 만니톨, 소르비톨 등의 당류는 불활성 담체로서 제제화에 이용되는 경우가 있지만, 그와 같이 당류를 불활성 담체로서, DPP 4 저해 화합물과 동시에 이용하는 것은 본건 발명에는 포함되지 않는다.
본 발명에 있어서, DPP 4로서는 인간 또는 비인간 포유류의 DPP 4를 들 수 있다.
본 발명에 있어서, 의약, 의약 조성물, 및 치료 또는 예방 방법의 적용 대상으로서는 인간 또는 비인간 포유류(특히 적합하게는 인간)를 들 수 있다.
항비만 작용(체중 감소 작용 및/또는 지방 감소 작용)은 공지된 동물 모델을 이용한 생체내 시험에 의해 확인할 수 있다.
이러한 시험 방법으로서는 예를 들면, 고지방식 부하에 의해 제조한 DIO(diet-induced obesity) 마우스, 정상 래트(SD 래트), 고지방식 부하에 의해 제조한 DIO(diet-induced obesity) 래트 등을 이용하는 방법(Int. J. Obes., 2006, 30: 1332-1340, Obesity Res., 2005, 13, 1000-1007 등)을 들 수 있고, 또는 이들과 동등한 방법을 들 수 있다.
보다 상세하게는, 예를 들면 후술 실시예 3에 기재된 방법과 동일하게 하여 시험을 실시할 수 있다.
[실시예]
이하, 본 발명을 실시예를 이용하여 설명하지만, 본 발명은 이들 실시예로 한정되는 것은 아니다.
<실시예 1> DPP 4 결손 래트(F344DucrlCrlj)에 있어서의 감미료의 GLP-1 분비 촉진 작용(혈중 활성형 GLP-1 레벨 상승 작용):
(1) 시험 방법:
시험 동물로는 웅성 F344 DucrlCrlj 래트(닛본 찰스리버)(사용시 7 내지 10주령)를 이용하였다. F344 DucrlCrlj 래트는 자연 발생적으로 DPP 4 유전자 결손을 갖는 계통의 래트인 것이 알려져 있다(Watanabe 등, Experientia, 1987, 43:400-401).
이들 시험 동물은 전일 밤부터 절식 후, 체중을 지표로 그룹을 나누어서 이용하였다. 이들 동물에게 피검 감미료의 용액(또는 대조로서 정제수)을 경구 투여(10 mL/kg)하여, 0, 30, 60, 180, 360분 후에 꼬리 부분 선단으로부터 혈액 샘플을 채취하였다. 이들 샘플에 대해서, 혈장중 활성형 GLP-1 농도를 측정하였다.
혈장중 활성형 GLP-1 농도의 측정은 이하와 같이 행하였다. 채취한 혈액을 원심 처리(4 ℃, 3000 rpm, 10분간)하여 혈장을 채취하였다. 혈장중 GLP-1 농도는 바이오플렉스 서스펜션 어레이 시스템(Bio-Plex suspension Array System, Rat Endocrine LINCOplex kit; LINCO Research사 제조), 또는 글루카곤 유사 펩티드 1(활성) 엘라이자 키트(Glucagon-Like Peptide-1(Active) ELISA KIT(상품명); LINCO Research사 제조, 활성형 GLP-1 측정 키트)를 이용하여 측정하였다.
측정 결과에 대해서는 감미료 부하군과 대조군과의 비교를 다넷트형 다중 비교(양측 검정)로 실시하여, 군 사이의 유의차를 검정하였다. 또한, 유의 수준은 5%로 하고, 해석에는 통계 해석 소프트웨어(생물 실험 데이터 통계 해석 시스템: EXSAS, 가부시끼가이샤 암시스텍스)를 이용하였다.
(2) 시험 결과:
감미료를 투여한 경우 및 대조에 대하여, 상기 (1)의 방법으로 혈중 활성형 GLP-1 레벨 상승 작용을 시험하였다.
피검 감미료로서 프락토올리고당(메이지 세이까(주) 제조)을 이용하여, 6 g/kg/10 mL를 경구 투여하였다. 대조로서는 정제수를 투여하였다. 그 결과, 프락토올리고당 6 g/kg을 투여한 군에서는 투여 후 30, 60, 180, 360분 후의 어느 것에 있어서도 대조군과 비교하여 혈장중 활성형 GLP-1의 레벨이 유의하게 높은 값을 나타내었다.
결과를 도 1에 나타내었다.
또한, 피검 감미료로서, 크실로오스 및 자일리톨을 이용하고, 이들 각 3 내지 6 g/kg/10 mL를 경구 투여하여 동일하게 시험하였다. 그 결과, 이들 당류를 투여한 군에서는 대조군과 비교하여 혈장중 활성형 GLP-1의 레벨이 현저하게 높은 값을 나타내었다.
<실시예 2> DPP 4 저해 화합물과 감미료와의 병용에 의한 GLP-1 분비 촉진 작용(혈중 활성형 GLP-1 레벨 상승 작용) (1):
(1) 시험 방법:
시험에는 웅성 SD(CD)/Crj 래트(닛본 찰스리버)(사용시 6주령) 또는 웅성 C57BL/6J 마우스(니혼 구레아)(사용시 9주령)를 이용하였다.
이들 시험 동물은 미리 체중을 지표로 그룹을 나누어 이용하였다. 이들 동물에게 피검 DPP 4 저해 화합물(또는 대조로서 정제수)을 경구 투여(10 mL/kg)하였다. 투여 30분 후에 피검 감미료 용액(또는 대조로서 정제수)을 경구 투여(10 mL/kg)하고, 0, 30, 60, 180, 300분 후에 혈액 샘플을 채취하였다. 이들 샘플에 대해서, 혈장중 활성형 GLP-1 농도를 측정하였다.
혈장중 활성형 GLP-1 농도의 측정은 상기 실시예 1의 (1)과 동일하게 행하였다.
측정 결과에 대해서는 감미료 부하군과 대조군과의 비교를 다넷트형 다중 비교(양측 검정)로 실시하여, 군 사이의 유의차를 검정하였다. 또한, 유의 수준은 5%로 하고, 해석에는 통계 해석 소프트웨어(생물 실험 데이터 통계 해석 시스템: EXSAS, 가부시끼가이샤 암시스텍스)를 이용하였다.
(2) 시험 결과:
DPP 4 저해 화합물 및 감미료를 병용한 경우와, 각각 단독으로 투여한 경우에 대해서, 상기 (1)의 방법으로, 혈중 활성형 GLP-1 레벨 상승 작용을 시험하였다.
시험 동물로서, C57BL/6J 마우스를 이용하였다.
DPP 4 저해 화합물로서, (2S)-2-시아노-1-[트랜스-4-(디메틸아미노카르보닐)시클로헥실아미노]아세틸피롤리딘 염산염(이하, 화합물 A라고 칭함) 10 mg/kg을 경구 투여(10 mL/kg)하였다. 대조로서는 정제수를 경구 투여(10 mL/kg)하였다.
또한 감미료로서, 프락토올리고당(메이지 세이까(주) 제조) 6 g/kg을 경구 투여(10 mL/kg)하였다. 대조로서는 정제수를 경구 투여(10 mL/kg)하였다.
그 결과, 화합물 A(10 mg/kg) 및 프락토올리고당(6 g/kg)의 양자를 투여한 군에서는 투여 후 30, 60, 180, 300분 후 모두 대조군과 비교하여 혈장중 활성형 GLP-1이 유의하게 높은 값을 나타내고, 활성형 GLP-1 레벨이 지속적으로 높은 레벨로 유지되는 것을 알 수 있었다. 한편, 화합물 A(10 mg/kg)만 또는 프락토올리고당(6 g/kg)만을 투여한 군에서는 혈장중 활성형 GLP-1의 레벨의 상승은 나타나지 않았다. 결과를 도 2에 나타내었다.
또한, 피검 감미료로서, 크실로오스를 이용하고, 크실로오스 6 g/kg을 화합물 A(10 mg/kg)와 동시에 경구 투여하여 동일하게 시험하였다. 그 결과, 크실로오스를 화합물 A와 동시에 투여한 군에서는 대조군과 비교하여 혈장중 활성형 GLP-1의 레벨의 현저한 상승이 보였다.
<실시예 3> DPP 4 저해 화합물과 감미료와의 병용에 의한 체중 감소 작용 (1):
(1) 시험 방법
〔DIO(diet-induced obesity) 마우스를 이용한 체중 감소 작용 시험〕:
시험에는 고지방식 부하한 웅성 C57BL/6J 마우스(DIO 마우스)를 이용하였다.
고지방식의 부하는 3주령의 웅성 C57BL/6J 마우스(니혼 구레아)에 사료로서, 지방 함량 37.2 w/w%, 5.578 kcal/g의 고지방식(오리엔탈 핫꼬사 제조)을 자유 섭취시켜 실시하였다. 정상식 대조 마우스에게는 CRF-1(지방 함량 5.7 w/w%, 3.59 kcal/g, 오리엔탈 핫꼬사 제조)을 자유 섭취시켰다.
이와 같이 고지방식 부하하여 39주령까지 사육한 마우스를 시험에 이용하였다.
시험 동물은 미리 체중 및 혈당치를 지표로 군을 나누어 행하였다.
이들 동물에게 피검 DPP 4 저해 화합물 및 피검 감미료를 경구 투여 또는 혼이 투여하였다.
경구 투여의 경우에는 피검 물질〔피검 DPP 4 저해 화합물(또는 대조로서 정제수) 및 피검 감미료의 용액(또는 대조로서 정제수)〕 10 mL/kg을 1일 2회 경구 투여하고, 최장 2주간 반복 투여하였다.
혼이 투여의 경우, 피검 물질(피검 DPP 4 저해 화합물 및 피검 감미료)은 마노 유발을 이용하여 세분화하여 사료(고지방식, 오리엔탈 핫꼬사 제조)에 첨가하고, 최장 2주간 혼이 투여하였다.
피검 물질의 투여 개시 후, 경시적으로 체중 및 섭이량을 측정하였다.
또한, 체중 감소 작용이 나타난 경우, 펜토바르비탈 마취하(70 mg/kg, i.p.)에서, 실험 마우스 전용 X선 체지방률 측정 장치(PIXImus2, GE Medical System사)를 이용하여, 신체 조성을 측정하였다.
측정 결과에 대해서는 감미료 부하군과 대조군과의 비교를 다넷트형 다중 비교(양측 검정)로 실시하여, 군 사이의 유의차를 검정하였다. 또한, 유의 수준은 5%로 하고, 해석에는 통계 해석 소프트웨어(생물 실험 데이터 통계 해석 시스템: EXSAS, 가부시끼가이샤 암시스텍스)를 이용하였다.
(2) 시험 결과:
DPP 4 저해 화합물 및 감미료를 병용한 경우와, 각각 단독으로 투여한 경우에 대해서, 상기 (1)의 방법으로, 체중 감소 작용을 시험하였다.
DPP 4 저해 화합물로서, (2S)-2-시아노-1-[트랜스-4-(디메틸아미노카르보닐)시클로헥실아미노]아세틸피롤리딘 염산염(이하, 화합물 A라고 칭함) 10 mg/100 g을 혼이 투여하였다.
또한 감미료로서, 프락토올리고당(메이지 세이까(주) 제조) 10 w/w%를 혼이 투여하였다.
그 결과, 화합물 A(10 mg/100 g) 및 프락토올리고당(10 w/w%)의 양자를 투여한 군에서는 투여 후 2일 내지 14일 후 모두 대조군과 비교하여 체중이 유의하게 저하되어, 체중 감소 작용이 나타났다. 한편, 화합물 A(10 mg/100 g)만으로는 대조군과 비교하여 체중이 변하지 않았다. 또한, 프락토올리고당(10 w/w%)만을 투여한 군에서는 약간 체중이 저하되는 경향은 보였지만 대조군과 비교하여 유의한 차는 없었다. 결과를 도 3에 나타내었다.
또한, 투여 15일 후에 신체 조성을 측정한 결과, 화합물 A(10 mg/100 g) 및 프락토올리고당(10 w/w%)의 양자를 투여한 군에서는 제지방 중량(lean mass)(g)은 대조군과 비교하여 변화가 없고, 지방 중량(fat mass)(g)만 대조군과 비교하여 유의하게 감소하고 있었다. 이 점에서, 화합물 A 및 프락토올리고당의 양자의 투여에 의해, 체지방 감소 작용이 얻어졌다고 생각되었다.
<실시예 4> DPP 4 저해 화합물과 감미료와의 병용에 의한 GLP-1 분비 촉진 작용(혈중 활성형 GLP-1 레벨 상승 작용) (2):
(1) 시험 방법:
시험에는 웅성 C57BL/6J 마우스(니혼 구레아)(사용시 7주령)를 이용하였다.
시험 동물은 전일 밤부터 절식 후, 체중을 지표로 그룹을 나누어 이용하였다. 이들 동물에게 피검 DPP 4 저해 화합물(또는 대조로서 정제수)을 경구 투여(10 mL/kg)하였다. 투여 30분 후에 피검 감미료 용액(또는 대조로서 정제수)을 경구 투여(10 mL/kg)하여, 0, 30, 60, 180, 300분 후에 혈액 샘플을 채취하였다. 이들 샘플에 대해서, 혈장중 활성형 GLP-1 농도를 측정하였다.
혈장중 활성형 GLP-1 농도의 측정 및 측정 결과의 분석ㆍ검정은 상기 실시예 1의 (1)과 동일하게 행하였다.
(2) 시험 결과:
감미료로서, 프락토올리고당(메이지 세이까(주) 제조), 케스토오스(메이지 세이까(주) 제조, GF2), 라피노오스(와코 쥰야꾸(주) 제조), 메리비오스(와코 쥰야꾸(주) 제조), 크실로올리고당(산토리(주) 제조), 크실로오스(와코 쥰야꾸(주) 제조), 자일리톨(와코 쥰야꾸(주) 제조), 소르비톨(와코 쥰야꾸(주) 제조), D-만니톨(와코 쥰야꾸(주) 제조), 에리트리톨(와코 쥰야꾸(주) 제조), 말티톨((주)하야시바라 세이부쯔 가가꾸 겐큐쇼 제조), 스쿠랄로스(산에이겐 FFI(주) 제조) 또는 아세술팜 K(와코 쥰야꾸(주) 제조)를 이용하여, 6 g/kg, 3 g/kg 또는 1 g/kg을 경구 투여(10 mL/kg)하였다.
또한, DPP 4 저해 화합물로서, (2S)-2-시아노-1-[트랜스-4-(디메틸아미노카르보닐)시클로헥실아미노]아세틸피롤리딘 벤젠술폰산염(이하, 화합물 A'라고 칭함) 10 mg/kg(대조로서는 정제수)를 이용하고, 이것을 경구 투여(10 mL/kg)하였다.
이들 다양한 감미료와 DPP 4 저해 화합물을 병용한 경우에 대해서, 상기 (1)의 방법으로, 혈중 활성형 GLP-1 레벨 상승 작용을 시험하였다(각 군 n=4 내지 5).
결과를 표 1에 나타내었다. 각종 감미료(6 g/kg, 3 g/kg 또는 1 g/kg)와 화합물 A'(10 mg/kg)의 양자를 투여한 군에 있어서의 혈중 활성형 GLP-1 농도(투여 후 1시간)는 프락토올리고당(6 g/kg)과 화합물 A'를 투여한 군에 있어서의 혈중 활성형 GLP-1 농도(투여 후 1시간)에 대한 상대치로 나타내었다.
표 1의 각종 감미료(6 g/kg, 3 g/kg 또는 1 g/kg)와 화합물 A'를 투여한 각 군에 있어서, 활성형 GLP-1 레벨의 상승이 나타났고, 게다가 상승은 프락토올리고당(6 g/kg)과 화합물 A'(10 mg/kg)를 투여한 군에 있어서의 것과 동일한 정도보다 큰 상승이 얻어졌다.
[표 1]
*: 화합물 A'와 프락토올리고당(6 g/kg)과의 투여에 의해 얻어지는 혈장중 활성형 GLP-1 농도(투여 후 1시간)를 100으로 했을 때의 상대치
<실시예 5> DPP 4 저해 화합물과 감미료와의 병용에 의한 GLP-1 분비 촉진 작용(혈중 활성형 GLP-1 레벨 상승 작용) (3):
(1) 시험 방법:
상기 실시예 4의 (1)과 동일하게 하여 시험을 행하였다.
혈장중 활성형 GLP-1 농도의 측정 및 측정 결과의 분석ㆍ검정은 상기 실시예 1의 (1)과 동일하게 행하였다.
(2) 시험 결과:
DPP 4 저해 화합물로서, 시타글립틴(MK-0413) 10 mg/kg, 알로글립틴(SYR-322) 1 mg/kg, 빌다글립틴(LAF237) 10 mg/kg, 삭사글립틴(BMS-477118) 3 mg/kg, 화합물 A' 10 mg/kg, 또는 화합물 B〔(2S)-2-시아노-1-[t-4-(4-프로피오닐-1-피페라지닐)-1-메틸-r-1-시클로헥실아미노]아세틸피롤리딘〕 10 mg/kg을 이용하여, 이들을 경구 투여(10 mL/kg)하였다. 대조로서는 정제수를 경구 투여(10 mL/kg)하였다.
또한 감미료로서, D-만니톨(와코 쥰야꾸(주) 제조) 3 g/kg, 메리비오스(와코 쥰야꾸(주) 제조) 6 g/kg, 또는 아세술팜 K(와코 쥰야꾸(주)제조) 3 g/kg을 이용하여, 이들을 경구 투여(10 mL/kg)하였다. 대조로서는 정제수를 경구 투여(10 mL/kg)하였다.
이들 다양한 DPP 4 저해 화합물 및 다양한 감미료를 병용한 경우에 대해서, 상기 (1)의 방법으로, 혈중 활성형 GLP-1 레벨 상승 작용을 시험하였다(각 군 n=5).
결과를 도 4a, 도 4b, 도 4c 및 표 2에 나타내었다.
도 4a, 도 4b, 도 4c에 나타낸 대로, 각종 감미료와 다양한 DPP 4 저해 화합물을 투여한 군에 있어서의 혈장중 활성형 GLP-1의 레벨은 투여 후 30, 60, 180, 360분 후의 어느 것에 있어서도 대조군(각종 감미료만을 투여한 군)과 비교하여 높은 값을 나타내었다.
또한, 표 2에 나타난 바와 같이, 각종 감미료와 DPP 4 저해 화합물을 투여한 군에 있어서의 혈장중 활성형 GLP-1 레벨의 상승(AUC 증가량)은 대조군(각종 감미료만 또는 DPP 4 저해 화합물만을 투여한 군)과 비교하여 유의하게 높은 값을 나타내었다.
[표 2]
a) 평균값±표준 오차(SEM), n=5, *:p<0.05, **:p<0.01(대조군에 대한 다넷트 다중 비교법에 기초한 유의차)
<실시예 6> DPP 4 저해 화합물과 감미료와의 병용에 의한 체중 감소 작용 (2):
(1) 시험 방법
〔DIO(diet-induced obesity) 마우스를 이용한 체중 감소 작용 시험〕:
상기 실시예 3의 (1)과 동일하게 하여 시험을 행하였다. 시험에는 고지방식 부하하여 14 내지 22주령까지 사육한 웅성 C57BL/6J 마우스를 이용하였다.
시험 동물은 미리 체중 및 혈당치를 지표로 군을 나누어 행하였다.
이들 동물에게 피검 DPP 4 저해 화합물 및 피검 감미료를 최장 15일간, 혼이 투여하였다.
피검 물질의 투여 개시 후, 경시적으로 체중 및 섭이량을 측정하였다. 측정 결과의 검정 및 해석을 상기 실시예 3의 (1)과 동일하게 하여 행하였다.
또한, 체중 감소 작용이 나타난 경우, 상기 실시예 3의 (1)과 동일하게 하여, 신체 조성을 측정하였다.
(2) 시험 결과:
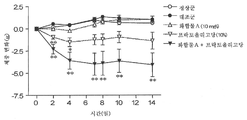
감미료로서, D-만니톨(와코 쥰야꾸(주) 제조), 메리비오스(와코 쥰야꾸(주) 제조) 또는 아세술팜 K(와코 쥰야꾸(주) 제조)를 이용하여, 각각 5 w/w%를 혼이 투여하였다. 또한, DPP 4 저해 화합물로서는 화합물 A'를 10 mg/100 g 혼이 투여하였다.
이들 다양한 감미료와 DPP 4 저해 화합물을 병용한 경우에 대해서, 상기 (1)의 방법으로, 체중 감소 작용을 시험하였다(각 군 n=9).
결과를 도 5a, 도 5b, 도 5c, 표 3a, 표 3b, 및 표 3c에 나타내었다.
도 5a, 도 5b 및 도 5c에 나타낸 대로, 각종 감미료(D-만니톨, 메리비오스 또는 아세술팜 K)와 DPP 4 저해 화합물의 양자를 투여한 군에서는 투여 후 2일부터 13일 후(또는 12일 후) 중 어디에 있어서도 대조군과 비교하여 체중이 유의하게 저하되어, 체중 감소 작용이 나타났다.
한편, 화합물 A'만에서는 대조군과 비교하여 체중이 변하지 않았다.
또한, 각종 감미료(D-만니톨, 메리비오스 또는 아세술팜 K)만을 투여한 군에서는 대조군과 비교하여 유의한 차가 없었다.
투여후 13일 후(또는 12일 후)의 데이터는 표 3(a), 표 3(b), 및 표 3(c)에 나타낸 바와 같다.
이들 결과로부터, 각종 감미료(D-만니톨, 메리비오스 또는 아세술팜 K)와 DPP 4 저해 화합물에 의해, 체중 감소의 상승적인 효과가 얻어진다고 생각되었다.
[표 3a]
a) 평균치±표준 오차(SEM), n=9, *:p<0.05, **:p<0.01(대조군에 대한 다넷트 다중 비교법에 기초한 유의차)
[표 3b]
a) 평균치±표준 오차(SEM), n=9, *:p<0.05, **:p<0.01(대조군에 대한 다넷트 다중 비교법에 기초한 유의차)
[표 3c]
a) 평균치±표준 오차(SEM), n=9, *:p<0.05, **:p<0.01(대조군에 대한 다넷트 다중 비교법에 기초한 유의차)
또한, 감미료로서 D-만니톨 및 아세술팜 K를 이용한 군에 있어서, 투여 15일 후에 신체 조성을 측정한 결과, 화합물 A'와 D-만니톨 또는 아세술팜 K의 양자를 투여한 군에서는 제지방 중량(lean mass)(g)은 대조군과 비교하여 변화가 없고, 지방 중량(fat mass)(g)만 대조군과 비교하여 유의하게 감소하였다.
<실시예 7> DPP 4 저해 화합물과 감미료와의 병용에 의한 체중 감소 작용 (3):
(1) 시험 방법
〔DIO(diet-induced obesity) 마우스를 이용한 체중 감소 작용 시험〕:
상기 실시예 3의 (1)과 동일하게 하여 시험을 행하였다. 시험에는 고지방식 부하하여 16주령까지 사육한 웅성 C57BL/6J 마우스를 이용하였다.
시험 동물은 미리 체중을 지표로 군을 나누어 행하였다.
이들 동물에게 피검 DPP 4 저해 화합물 및 피검 감미료를 최장 15일 후까지, 혼이 투여하였다. 피검 물질의 투여 개시 후, 경시적으로 체중 및 섭이량을 측정하였다.
(2) 시험 결과:
감미료로서, 소르비톨(와코 쥰야꾸(주) 제조) 또는 에리트리톨(와코 쥰야꾸(주) 제조)를 이용하여, 각각 5 w/w%를 혼이 투여하였다. 또한, DPP 4 저해 화합물로서는 화합물 A'를 10 mg/100 g 혼이 투여하였다. 이들 다양한 감미료와 DPP 4 저해 화합물을 병용한 경우에 대해서, 상기 (1)의 방법으로, 체중 감소 작용을 시험하였다(각 군 n=7).
결과를 표 4에 나타내었다.
표 4에 나타낸 대로, 각종 감미료(소르비톨 또는 에리트리톨)와 DPP 4 저해 화합물의 양자를 투여한 군에서는 대조군과 비교하여 체중의 저하가 나타났다.
또한, 별도로 행한 시험에서, 각종 감미료(소르비톨 또는 에리트리톨)만을 투여한 경우에, 대조군과 비교하여 체중의 저하는 나타나지 않았다.
[표 4]
a) 평균치±표준 오차(SEM), n=7, *:p<0.05, **:p<0.01(대조군에 대한 다넷트 다중 비교법에 기초한 유의차)
[산업상 이용가능성]
본 발명의 의약 조성물, 치료 또는 예방 방법, 또는 사용은 비만의 증상을 갖는 환자에 있어서의 체중 감소 및/또는 체지방 감소를 위해 유용하고, 비만의 치료 또는 예방에 있어서 유용하다.
Claims (29)
- 디펩티딜 펩티다아제 4 저해 화합물과 GLP-1 분비 촉진 작용을 갖는 감미료를 조합하여 포함하는 의약 조성물.
- 디펩티딜 펩티다아제 4 저해 화합물을 함유하고, GLP-1 분비 촉진 작용을 갖는 감미료와 병용되는 것을 특징으로 하는 의약 조성물.
- 제1항 또는 제2항에 있어서, GLP-1 분비 촉진 작용을 갖는 감미료가 비대사성 및/또는 난소화흡수성의 당류인 의약 조성물.
- 제1항 또는 제2항에 있어서, GLP-1 분비 촉진 작용을 갖는 감미료가 비당질계 감미료인 의약 조성물.
- 제1항 또는 제2항에 있어서, GLP-1 분비 촉진 작용을 갖는 감미료가 이하의 (1), (2), (3), (4) 및 (5)로부터 선택되는 감미료인 의약 조성물:
(1) 프락토올리고당, 니스토오스, 케스토오스 및 프락토프라노실니스토오스로부터 선택되는 당류;
(2) 크실로오스;
(3) 메리비오스, 라피노오스, 이소말토오스, 크실로비오스 및 크실로올리고당으로부터 선택되는 올리고당류;
(4) 만니톨, 소르비톨, 에리트리톨, 말티톨 및 자일리톨로부터 선택되는 당 알코올류; 및
(5) 아세술팜 K 및 스쿠랄로스로부터 선택되는 비당질계 감미료. - 제1항 또는 제2항에 있어서, GLP-1 분비 촉진 작용을 갖는 감미료가 프락토올리고당, 니스토오스, 케스토오스 및 프락토프라노실니스토오스로부터 선택되는 당류인 의약 조성물.
- 제1항 또는 제2항에 있어서, GLP-1 분비 촉진 작용을 갖는 감미료가 메리비오스, 라피노오스, 이소말토오스, 크실로비오스 및 크실로올리고당으로부터 선택되는 올리고당류인 의약 조성물.
- 제1항 또는 제2항에 있어서, GLP-1 분비 촉진 작용을 갖는 감미료가 만니톨, 소르비톨, 에리트리톨, 말티톨 및 자일리톨로부터 선택되는 당 알코올류인 의약 조성물.
- 제1항 또는 제2항에 있어서, GLP-1 분비 촉진 작용을 갖는 감미료가 아세술팜 K 및 스쿠랄로스로부터 선택되는 비당질계 감미료인 의약 조성물.
- 제1항 또는 제2항에 있어서, GLP-1 분비 촉진 작용을 갖는 감미료가 메리비오스, 만니톨, 소르비톨, 에리트리톨 및 아세술팜 K로부터 선택되는 감미료인 의약 조성물.
- 제1항 또는 제2항에 있어서, GLP-1 분비 촉진 작용을 갖는 감미료가 메리비오스, 만니톨 및 아세술팜 K로부터 선택되는 감미료인 의약 조성물.
- 제1항 또는 제2항에 있어서, GLP-1 분비 촉진 작용을 갖는 감미료가 메리비오스 또는 만니톨인 의약 조성물.
- 제1항 또는 제2항에 있어서, GLP-1 분비 촉진 작용을 갖는 감미료가 아세술팜 K인 의약 조성물.
- 제1항 내지 제13항 중 어느 한 항에 있어서, 비만의 치료 또는 예방을 위해 사용되는 것인 의약 조성물.
- 제1항 내지 제13항 중 어느 한 항에 있어서, 체중 감소 또는 체지방 감소를 위해 사용되는 것인 의약 조성물.
- 제1항 내지 제13항 중 어느 한 항에 있어서, 비만의 증상을 갖는 환자에 있어서의 체중 감소 또는 체지방 감소를 위해 사용되는 것인 의약 조성물.
- 제1항 내지 제13항 중 어느 한 항에 있어서, 2형 당뇨병 및 비만의 증상을 갖는 환자에 있어서의 체중 감소 또는 체지방 감소를 위해 사용되는 것인 의약 조성물.
- 제1항 내지 제17항 중 어느 한 항에 있어서, 디펩티딜 펩티다아제 4 저해 화합물과 GLP-1 분비 촉진 작용을 갖는 감미료 이외에, 1종 이상의 의약적으로 허용되는 담체 또는 부형제를 포함하는 의약 조성물.
- 제1항 내지 제18항 중 어느 한 항에 있어서, 동시, 따로따로, 순차 또는 연속적으로 사용하기 위한 조합 제제인 의약 조성물.
- 비만의 증상을 갖는 환자에게, (a) 디펩티딜 펩티다아제 4 저해 화합물 및 (b) GLP-1 분비 촉진 작용을 갖는 감미료를 유효량 투여하는 것을 특징으로 하는 비만의 치료 또는 예방 방법.
- 제20항 또는 제21항에 있어서, 해당 환자의 체중 감소 또는 체지방 감소를 위한 치료 또는 예방 방법.
- 제20항 또는 제21항에 있어서, 비만의 증상을 갖는 환자가 2형 당뇨병이 발병한 환자인 치료 또는 예방 방법.
- 제20항 내지 제22항 중 어느 한 항에 있어서, (a)의 투여가 (b)의 투여와 동시, 또는 (b)의 투여 전, 또는 (b)의 투여 후 중 어느 하나에 행해지는 것인 치료 또는 예방 방법.
- 의약의 제조에 있어서의, 디펩티딜 펩티다아제 4 저해 화합물과 GLP-1 분비 촉진 작용을 갖는 감미료와의 배합물의 사용.
- 제24항에 있어서, 해당 의약이 비만의 치료 또는 예방을 위한 의약인 사용.
- 제24항에 있어서, 해당 의약이 체중 감소 또는 체지방 감소를 위한 의약인 사용.
- 제24항에 있어서, 해당 의약이 비만의 증상을 갖는 환자에 있어서의 체중 감소 또는 체지방 감소를 위한 의약인 사용.
- 제24항에 있어서, 해당 의약이 2형 당뇨병 및 비만의 증상을 갖는 환자에 있어서의 체중 감소 또는 체지방 감소를 위한 의약인 사용.
- 유효 성분으로서의 디펩티딜 펩티다아제 4 저해 화합물과 GLP-1 분비 촉진 작용을 갖는 감미료를 비만의 치료 또는 예방을 위해, 동시, 따로따로 또는 연속적으로 사용하기 위한 지시서와 함께 포함하는 상품 포장물.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US90747107P | 2007-04-03 | 2007-04-03 | |
| JPJP-P-2007-097079 | 2007-04-03 | ||
| JP2007097079 | 2007-04-03 | ||
| US60/907,471 | 2007-04-03 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020097022913A Division KR101361427B1 (ko) | 2007-04-03 | 2008-04-03 | 디펩티딜 펩티다아제 4 저해 화합물과 감미료와의 병용 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20120030570A true KR20120030570A (ko) | 2012-03-28 |
Family
ID=39808393
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020127002221A KR20120030570A (ko) | 2007-04-03 | 2008-04-03 | 디펩티딜 펩티다아제 4 저해 화합물과 감미료와의 병용 |
| KR1020097022913A KR101361427B1 (ko) | 2007-04-03 | 2008-04-03 | 디펩티딜 펩티다아제 4 저해 화합물과 감미료와의 병용 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020097022913A KR101361427B1 (ko) | 2007-04-03 | 2008-04-03 | 디펩티딜 펩티다아제 4 저해 화합물과 감미료와의 병용 |
Country Status (9)
| Country | Link |
|---|---|
| US (1) | US8927504B2 (ko) |
| EP (1) | EP2143443B1 (ko) |
| JP (2) | JP5616630B2 (ko) |
| KR (2) | KR20120030570A (ko) |
| CN (2) | CN101652147B (ko) |
| AU (1) | AU2008233548B2 (ko) |
| CA (1) | CA2682736C (ko) |
| ES (1) | ES2529149T3 (ko) |
| WO (1) | WO2008120813A1 (ko) |
Families Citing this family (47)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7407955B2 (en) | 2002-08-21 | 2008-08-05 | Boehringer Ingelheim Pharma Gmbh & Co., Kg | 8-[3-amino-piperidin-1-yl]-xanthines, the preparation thereof and their use as pharmaceutical compositions |
| US7501426B2 (en) | 2004-02-18 | 2009-03-10 | Boehringer Ingelheim International Gmbh | 8-[3-amino-piperidin-1-yl]-xanthines, their preparation and their use as pharmaceutical compositions |
| DE102004054054A1 (de) | 2004-11-05 | 2006-05-11 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | Verfahren zur Herstellung chiraler 8-(3-Amino-piperidin-1-yl)-xanthine |
| DE102005035891A1 (de) | 2005-07-30 | 2007-02-08 | Boehringer Ingelheim Pharma Gmbh & Co. Kg | 8-(3-Amino-piperidin-1-yl)-xanthine, deren Herstellung und deren Verwendung als Arzneimittel |
| CA2810839A1 (en) | 2006-05-04 | 2007-11-15 | Boehringer Ingelheim International Gmbh | A polymorphic form of 1-[(4-methyl-quinazolin-2-yl)methyl]-3-methyl-7-(2-butyn-1-yl)-8-(3-(r)-amino-piperidin-1-yl)-xanthine |
| EP1852108A1 (en) | 2006-05-04 | 2007-11-07 | Boehringer Ingelheim Pharma GmbH & Co.KG | DPP IV inhibitor formulations |
| PE20110235A1 (es) | 2006-05-04 | 2011-04-14 | Boehringer Ingelheim Int | Combinaciones farmaceuticas que comprenden linagliptina y metmorfina |
| KR20120030570A (ko) * | 2007-04-03 | 2012-03-28 | 미쓰비시 타나베 파마 코퍼레이션 | 디펩티딜 펩티다아제 4 저해 화합물과 감미료와의 병용 |
| CL2008002427A1 (es) | 2007-08-16 | 2009-09-11 | Boehringer Ingelheim Int | Composicion farmaceutica que comprende 1-cloro-4-(b-d-glucopiranos-1-il)-2-[4-((s)-tetrahidrofurano-3-iloxi)bencil]-benceno combinado con 1-[(4-metilquinazolin-2-il)metil]-3-metil-7-(2-butin-1-il)-8-(3-(r)-aminopiperidin-1-il)xantina; y su uso para tratar diabetes mellitus tipo 2. |
| PE20140960A1 (es) | 2008-04-03 | 2014-08-15 | Boehringer Ingelheim Int | Formulaciones que comprenden un inhibidor de dpp4 |
| UY32030A (es) | 2008-08-06 | 2010-03-26 | Boehringer Ingelheim Int | "tratamiento para diabetes en pacientes inapropiados para terapia con metformina" |
| KR20200118243A (ko) | 2008-08-06 | 2020-10-14 | 베링거 인겔하임 인터내셔날 게엠베하 | 메트포르민 요법이 부적합한 환자에서의 당뇨병 치료 |
| US8513264B2 (en) | 2008-09-10 | 2013-08-20 | Boehringer Ingelheim International Gmbh | Combination therapy for the treatment of diabetes and related conditions |
| WO2010039124A1 (en) * | 2008-09-30 | 2010-04-08 | Mitsubishi Tanabe Pharma Corporation | Benzenesulfonic acid salt compounds |
| US20200155558A1 (en) | 2018-11-20 | 2020-05-21 | Boehringer Ingelheim International Gmbh | Treatment for diabetes in patients with insufficient glycemic control despite therapy with an oral antidiabetic drug |
| MX2011006713A (es) | 2008-12-23 | 2011-07-13 | Boehringer Ingelheim Int | Formas salinas de compuesto organico. |
| TW201036975A (en) | 2009-01-07 | 2010-10-16 | Boehringer Ingelheim Int | Treatment for diabetes in patients with inadequate glycemic control despite metformin therapy |
| GEP20135962B (en) | 2009-02-13 | 2013-11-11 | Boehringer Ingelheim Int | Pharmaceutical composition comprising sglt2 inhibitor, dpp-iv inhibitor, and optionally further antidiabetic agent; and usage thereof |
| KR20120107080A (ko) | 2009-11-27 | 2012-09-28 | 베링거 인겔하임 인터내셔날 게엠베하 | 리나글립틴과 같은 dpp-iv 억제제를 사용한 유전자형 검사된 당뇨병 환자의 치료 |
| JP5721232B2 (ja) * | 2009-12-04 | 2015-05-20 | 株式会社東洋新薬 | グルカゴン様ペプチド−1分泌促進剤 |
| JP5570244B2 (ja) * | 2010-02-23 | 2014-08-13 | 株式会社ヤクルト本社 | 腸間膜脂肪低減剤 |
| WO2011107494A1 (de) | 2010-03-03 | 2011-09-09 | Sanofi | Neue aromatische glykosidderivate, diese verbindungen enthaltende arzneimittel und deren verwendung |
| JP5561639B2 (ja) * | 2010-03-30 | 2014-07-30 | 静岡県公立大学法人 | Gpr43陽性・腸内分泌細胞増加促進剤 |
| JP6034781B2 (ja) * | 2010-05-05 | 2016-11-30 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 併用療法 |
| US8933024B2 (en) | 2010-06-18 | 2015-01-13 | Sanofi | Azolopyridin-3-one derivatives as inhibitors of lipases and phospholipases |
| US8530413B2 (en) | 2010-06-21 | 2013-09-10 | Sanofi | Heterocyclically substituted methoxyphenyl derivatives with an oxo group, processes for preparation thereof and use thereof as medicaments |
| AU2011268940B2 (en) | 2010-06-24 | 2015-05-21 | Boehringer Ingelheim International Gmbh | Diabetes therapy |
| TW201215388A (en) | 2010-07-05 | 2012-04-16 | Sanofi Sa | (2-aryloxyacetylamino)phenylpropionic acid derivatives, processes for preparation thereof and use thereof as medicaments |
| TW201221505A (en) | 2010-07-05 | 2012-06-01 | Sanofi Sa | Aryloxyalkylene-substituted hydroxyphenylhexynoic acids, process for preparation thereof and use thereof as a medicament |
| TW201215387A (en) | 2010-07-05 | 2012-04-16 | Sanofi Aventis | Spirocyclically substituted 1,3-propane dioxide derivatives, processes for preparation thereof and use thereof as a medicament |
| CN104220875A (zh) | 2010-10-19 | 2014-12-17 | 埃尔舍利克斯治疗公司 | 基于化学感应受体配体的治疗 |
| US9034883B2 (en) | 2010-11-15 | 2015-05-19 | Boehringer Ingelheim International Gmbh | Vasoprotective and cardioprotective antidiabetic therapy |
| UY33937A (es) | 2011-03-07 | 2012-09-28 | Boehringer Ingelheim Int | Composiciones farmacéuticas que contienen inhibidores de dpp-4 y/o sglt-2 y metformina |
| NZ618698A (en) | 2011-07-15 | 2015-08-28 | Boehringer Ingelheim Int | Substituted quinazolines, the preparation thereof and the use thereof in pharmaceutical compositions |
| WO2013037390A1 (en) | 2011-09-12 | 2013-03-21 | Sanofi | 6-(4-hydroxy-phenyl)-3-styryl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| EP2760862B1 (en) | 2011-09-27 | 2015-10-21 | Sanofi | 6-(4-hydroxy-phenyl)-3-alkyl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| US9555001B2 (en) | 2012-03-07 | 2017-01-31 | Boehringer Ingelheim International Gmbh | Pharmaceutical composition and uses thereof |
| WO2013171167A1 (en) | 2012-05-14 | 2013-11-21 | Boehringer Ingelheim International Gmbh | A xanthine derivative as dpp -4 inhibitor for use in the treatment of podocytes related disorders and/or nephrotic syndrome |
| WO2013174767A1 (en) | 2012-05-24 | 2013-11-28 | Boehringer Ingelheim International Gmbh | A xanthine derivative as dpp -4 inhibitor for use in modifying food intake and regulating food preference |
| EP2911655A1 (en) | 2012-10-24 | 2015-09-02 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Tpl2 kinase inhibitors for preventing or treating diabetes and for promoting -cell survival |
| US9526728B2 (en) | 2014-02-28 | 2016-12-27 | Boehringer Ingelheim International Gmbh | Medical use of a DPP-4 inhibitor |
| WO2016044756A1 (en) * | 2014-09-18 | 2016-03-24 | The Trustees Of Columbia University In The City Of New York | A neural substrate for sugar preference |
| US10426818B2 (en) | 2015-03-24 | 2019-10-01 | Inserm (Institut National De La Sante Et De La Recherche Medicale) | Method and pharmaceutical composition for use in the treatment of diabetes |
| MX2018015089A (es) | 2016-06-10 | 2019-05-13 | Boehringer Ingelheim Int | Combinacion de linagliptina y metformina. |
| JP6842072B2 (ja) * | 2019-03-07 | 2021-03-17 | 物産フードサイエンス株式会社 | エガセラ属細菌の菌数抑制剤 |
| JP6765090B2 (ja) * | 2019-05-14 | 2020-10-07 | 株式会社東洋新薬 | 黒生姜含有組成物 |
| JPWO2021153718A1 (ko) * | 2020-01-31 | 2021-08-05 |
Family Cites Families (56)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5982313A (ja) | 1982-11-04 | 1984-05-12 | Meiji Seika Kaisha Ltd | 体内脂質減少剤 |
| JPH0665080A (ja) | 1992-03-10 | 1994-03-08 | Godo Shiyusei Kk | α−グルコシダ−ゼ阻害剤を含有する、過血糖付随疾患の予防・治療剤、および保健食 |
| IL111785A0 (en) | 1993-12-03 | 1995-01-24 | Ferring Bv | Dp-iv inhibitors and pharmaceutical compositions containing them |
| US20020006899A1 (en) | 1998-10-06 | 2002-01-17 | Pospisilik Andrew J. | Use of dipeptidyl peptidase IV effectors for lowering blood pressure in mammals |
| DE19616486C5 (de) | 1996-04-25 | 2016-06-30 | Royalty Pharma Collection Trust | Verfahren zur Senkung des Blutglukosespiegels in Säugern |
| TW492957B (en) | 1996-11-07 | 2002-07-01 | Novartis Ag | N-substituted 2-cyanopyrrolidnes |
| JPH10290681A (ja) | 1997-04-18 | 1998-11-04 | Suntory Ltd | 抗肥満作用を有する飲食品 |
| DE19823831A1 (de) | 1998-05-28 | 1999-12-02 | Probiodrug Ges Fuer Arzneim | Neue pharmazeutische Verwendung von Isoleucyl Thiazolidid und seinen Salzen |
| CO5150173A1 (es) | 1998-12-10 | 2002-04-29 | Novartis Ag | Compuestos n-(glicilo sustituido)-2-cianopirrolidinas inhibidores de peptidasa de dipeptidilo-iv (dpp-iv) los cuales son efectivos en el tratamiento de condiciones mediadas por la inhibicion de dpp-iv |
| US6110949A (en) | 1999-06-24 | 2000-08-29 | Novartis Ag | N-(substituted glycyl)-4-cyanothiazolidines, pharmaceutical compositions containing them and their use in inhibiting dipeptidyl peptidase-IV |
| US6107317A (en) | 1999-06-24 | 2000-08-22 | Novartis Ag | N-(substituted glycyl)-thiazolidines, pharmaceutical compositions containing them and their use in inhibiting dipeptidyl peptidase-IV |
| US6172081B1 (en) | 1999-06-24 | 2001-01-09 | Novartis Ag | Tetrahydroisoquinoline 3-carboxamide derivatives |
| GB9928330D0 (en) | 1999-11-30 | 2000-01-26 | Ferring Bv | Novel antidiabetic agents |
| US6395767B2 (en) | 2000-03-10 | 2002-05-28 | Bristol-Myers Squibb Company | Cyclopropyl-fused pyrrolidine-based inhibitors of dipeptidyl peptidase IV and method |
| GB0010188D0 (en) | 2000-04-26 | 2000-06-14 | Ferring Bv | Inhibitors of dipeptidyl peptidase IV |
| GB0010183D0 (en) | 2000-04-26 | 2000-06-14 | Ferring Bv | Inhibitors of dipeptidyl peptidase IV |
| TW583185B (en) | 2000-06-13 | 2004-04-11 | Novartis Ag | N-(substituted glycyl)-2-cyanopyrrolidines and pharmaceutical composition for inhibiting dipeptidyl peptidase-IV (DPP-IV) or for the prevention or treatment of diseases or conditions associated with elevated levels of DPP-IV comprising the same |
| AU7775401A (en) | 2000-08-10 | 2002-02-25 | Welfide Corp | Proline derivatives and use thereof as drugs |
| WO2002030891A1 (fr) | 2000-10-06 | 2002-04-18 | Tanabe Seiyaku Co., Ltd. | Composes aliphatiques azotes a noyau a cinq elements |
| CA2433090A1 (en) | 2000-12-27 | 2002-07-04 | Kyowa Hakko Kogyo Co., Ltd. | Dipeptidyl peptidase iv inhibitor |
| JP2002265439A (ja) | 2001-03-08 | 2002-09-18 | Mitsubishi Pharma Corp | シアノピロリジン誘導体およびその医薬用途 |
| DE60226723D1 (de) | 2001-03-27 | 2008-07-03 | Merck & Co Inc | Dipeptidylpeptidase-hemmer für die behandlung oder prävention von diabetes |
| US20030031772A1 (en) * | 2001-03-28 | 2003-02-13 | Zehner Lee R. | Mixtures of fructose and lactose as a low-calorie bulk sweetener with reduced glyemic index |
| US6573287B2 (en) | 2001-04-12 | 2003-06-03 | Bristo-Myers Squibb Company | 2,1-oxazoline and 1,2-pyrazoline-based inhibitors of dipeptidyl peptidase IV and method |
| GB0115517D0 (en) | 2001-06-25 | 2001-08-15 | Ferring Bv | Novel antidiabetic agents |
| DE60221983T2 (de) | 2001-06-27 | 2008-05-15 | Smithkline Beecham Corp. | Fluorpyrrolidine als dipeptidyl-peptidase inhibitoren |
| DE60222667T2 (de) | 2001-06-27 | 2008-07-17 | Smithkline Beecham Corp. | Fluorpyrrolidine als dipeptidylpeptidaseinhibitoren |
| EP1399420B1 (en) | 2001-06-27 | 2007-12-05 | SmithKline Beecham Corporation | Pyrrolidines as dipeptidyl peptidase inhibitors |
| UA74912C2 (en) | 2001-07-06 | 2006-02-15 | Merck & Co Inc | Beta-aminotetrahydroimidazo-(1,2-a)-pyrazines and tetratriazolo-(4,3-a)-pyrazines as inhibitors of dipeptylpeptidase for the treatment or prevention of diabetes |
| US20040259883A1 (en) | 2001-09-14 | 2004-12-23 | Hiroshi Sakashita | Thiazolidine derivative and medicinal use thereof |
| GB0125445D0 (en) | 2001-10-23 | 2001-12-12 | Ferring Bv | Protease Inhibitors |
| US6710040B1 (en) * | 2002-06-04 | 2004-03-23 | Pfizer Inc. | Fluorinated cyclic amides as dipeptidyl peptidase IV inhibitors |
| TW200401635A (en) | 2002-07-23 | 2004-02-01 | Yamanouchi Pharma Co Ltd | 2-Cyano-4-fluoropyrrolidine derivative or salt thereof |
| EA007613B1 (ru) | 2002-08-29 | 2006-12-29 | Тайсо Фармасьютикал Ко., Лтд. | Бензолсульфонатная соль (2s,4s)-1-циано-4-фтор-1-[(2-гидрокси-1,1-диметил)этиламино]ацетилпирролидина |
| US20040087514A1 (en) | 2002-09-06 | 2004-05-06 | Hughes Thomas E | Nutritional compositions |
| JP2005170792A (ja) | 2002-11-22 | 2005-06-30 | Mitsubishi Pharma Corp | L−プロリン誘導体およびその医薬としての用途。 |
| EP1595866B1 (en) | 2003-01-31 | 2016-06-08 | Sanwa Kagaku Kenkyusho Co., Ltd. | Cyanopyrrolidines useful for the treatment of inter alia metabolic syndrome |
| US7550590B2 (en) | 2003-03-25 | 2009-06-23 | Takeda Pharmaceutical Company Limited | Dipeptidyl peptidase inhibitors |
| JP2007511467A (ja) | 2003-05-14 | 2007-05-10 | タケダ サン ディエゴ インコーポレイテッド | ジペプチジルペプチダーゼインヒビター |
| US6995183B2 (en) | 2003-08-01 | 2006-02-07 | Bristol Myers Squibb Company | Adamantylglycine-based inhibitors of dipeptidyl peptidase IV and methods |
| JP2007504230A (ja) * | 2003-09-02 | 2007-03-01 | メルク エンド カムパニー インコーポレーテッド | ジペプチジルペプチダーゼ−iv阻害剤のリン酸塩の新規結晶性形態 |
| EP1699777B1 (en) * | 2003-09-08 | 2012-12-12 | Takeda Pharmaceutical Company Limited | Dipeptidyl peptidase inhibitors |
| JP2007513058A (ja) | 2003-09-08 | 2007-05-24 | 武田薬品工業株式会社 | ジペプチジルぺプチダーゼ阻害剤 |
| EP1520486A1 (en) * | 2003-09-30 | 2005-04-06 | Tiense Suikerraffinaderij N.V. | Composition for suppressing ghrelin and method for same |
| TW200519105A (en) | 2003-10-20 | 2005-06-16 | Lg Life Science Ltd | Novel inhibitors of DPP-IV, methods of preparing the same, and pharmaceutical compositions containing the same as an active agent |
| WO2005075426A1 (en) | 2004-02-03 | 2005-08-18 | Glenmark Pharmaceuticals Ltd. | Novel dipeptidyl peptidase iv inhibitors; processes for their preparation and compositions thereof |
| KR101130433B1 (ko) | 2004-02-05 | 2012-03-27 | 교린 세이야꾸 가부시키 가이샤 | 비시클로에스테르 유도체 |
| US7560569B2 (en) | 2004-02-18 | 2009-07-14 | Kyorin Pharmaceutical Co., Ltd | Bicycloamide derivative |
| US7514571B2 (en) | 2004-02-27 | 2009-04-07 | Kyorin Pharmaceutical Co., Ltd. | Bicyclo derivative |
| NZ549716A (en) | 2004-03-15 | 2010-04-30 | Takeda Pharmaceutical | Pyrimidin-dione derivatives as dipeptidyl peptidase inhibitors |
| CN102372705A (zh) | 2005-02-18 | 2012-03-14 | 田边三菱制药株式会社 | 脯氨酸衍生物的盐,其溶剂合物,及其生产方法 |
| WO2006090244A1 (en) | 2005-02-22 | 2006-08-31 | Glenmark Pharmaceuticals S.A. | New adamantane derivatives as dipeptidyl, peptidase iv inhibitors, processes for their preparation, and pharmaceutical compositions containing them |
| TWI357902B (en) | 2005-04-01 | 2012-02-11 | Lg Life Science Ltd | Dipeptidyl peptidase-iv inhibiting compounds, meth |
| US7553861B2 (en) | 2005-04-22 | 2009-06-30 | Alantos Pharmaceuticals Holding, Inc. | Dipeptidyl peptidase-IV inhibitors |
| JP2007001946A (ja) * | 2005-06-24 | 2007-01-11 | Ono Pharmaceut Co Ltd | ピロリジン誘導体 |
| KR20120030570A (ko) * | 2007-04-03 | 2012-03-28 | 미쓰비시 타나베 파마 코퍼레이션 | 디펩티딜 펩티다아제 4 저해 화합물과 감미료와의 병용 |
-
2008
- 2008-04-03 KR KR1020127002221A patent/KR20120030570A/ko not_active Application Discontinuation
- 2008-04-03 WO PCT/JP2008/056678 patent/WO2008120813A1/ja active Application Filing
- 2008-04-03 ES ES08739785.7T patent/ES2529149T3/es active Active
- 2008-04-03 US US12/594,568 patent/US8927504B2/en not_active Expired - Fee Related
- 2008-04-03 KR KR1020097022913A patent/KR101361427B1/ko active IP Right Grant
- 2008-04-03 CN CN2008800111647A patent/CN101652147B/zh not_active Expired - Fee Related
- 2008-04-03 EP EP08739785.7A patent/EP2143443B1/en not_active Not-in-force
- 2008-04-03 CA CA2682736A patent/CA2682736C/en not_active Expired - Fee Related
- 2008-04-03 CN CN2013102037612A patent/CN103330939A/zh active Pending
- 2008-04-03 AU AU2008233548A patent/AU2008233548B2/en not_active Ceased
- 2008-04-03 JP JP2009507560A patent/JP5616630B2/ja not_active Expired - Fee Related
-
2012
- 2012-08-07 JP JP2012174860A patent/JP2012236849A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| WO2008120813A1 (ja) | 2008-10-09 |
| EP2143443A1 (en) | 2010-01-13 |
| EP2143443B1 (en) | 2014-11-19 |
| CN103330939A (zh) | 2013-10-02 |
| EP2143443A4 (en) | 2012-04-18 |
| AU2008233548B2 (en) | 2011-12-01 |
| US20100113382A1 (en) | 2010-05-06 |
| JPWO2008120813A1 (ja) | 2010-07-15 |
| CN101652147B (zh) | 2013-07-24 |
| CA2682736C (en) | 2013-07-09 |
| KR101361427B1 (ko) | 2014-02-10 |
| US8927504B2 (en) | 2015-01-06 |
| CA2682736A1 (en) | 2008-10-09 |
| JP2012236849A (ja) | 2012-12-06 |
| KR20090127946A (ko) | 2009-12-14 |
| JP5616630B2 (ja) | 2014-10-29 |
| CN101652147A (zh) | 2010-02-17 |
| AU2008233548A1 (en) | 2008-10-09 |
| ES2529149T3 (es) | 2015-02-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101361427B1 (ko) | 디펩티딜 펩티다아제 4 저해 화합물과 감미료와의 병용 | |
| Scheen et al. | Metabolic effects of SGLT-2 inhibitors beyond increased glucosuria: a review of the clinical evidence | |
| US20170305952A1 (en) | Pharmaceutical composition, methods for treating and uses thereof | |
| Fujita et al. | Renal sodium glucose cotransporter 2 inhibitors as a novel therapeutic approach to treatment of type 2 diabetes: clinical data and mechanism of action | |
| KR101463724B1 (ko) | Sglt-2 억제제를 사용한 병용 치료법 및 이의 약제학적 조성물 | |
| CN101601679B (zh) | 一种烟酰胺单核苷酸的应用 | |
| JP5595914B2 (ja) | グルコピラノシル置換ベンゼン誘導体を含有する医薬組成物 | |
| TW200911275A (en) | Pharmaceutical composition comprising a pyrazole-O-glucoside derivative | |
| WO2009022009A1 (en) | Pharmaceutical composition comprising a pyrazole-o-glucoside derivative | |
| TW200838548A (en) | Pharmaceutical composition comprising a pyrazole-O-glucoside derivative | |
| Lee et al. | Distinct action of the α-glucosidase inhibitor miglitol on SGLT3, enteroendocrine cells, and GLP1 secretion | |
| KR20120016051A (ko) | 제약 조성물 | |
| TW201202238A (en) | 1-[(3-cyano-pyridin-2-yl)methyl]-3-methyl-7-(2-butyn-1-yl)-8-[3-(R)-amino-piperidin-1-yl]-xanthine for the treatment of a metabolic disorder of a predominantly carnivorous non-human animal | |
| WO2012041898A1 (en) | Combination of sglt2 inhibitor and a sugar compound for the treatment of diabetes | |
| WO2015173584A1 (en) | Method for suppressing glucagon secretion of an sglt2 inhibitor | |
| KR20070086137A (ko) | FBPase 저해제를 함유하는 의약 조성물 | |
| KR20190141007A (ko) | 3-(4-(벤질옥시)페닐)헥스-4-이노익산 유도체의 신규 용도 | |
| AU2012201217B2 (en) | Combined use of dipeptidyl peptidase 4 inhibitor and sweetener | |
| KR100720055B1 (ko) | 육탄당 모노인산을 포함하는 혈당강하용 조성물 | |
| KR20240035374A (ko) | 이나보글리플로진의 대사체를 포함하는 약학적 조성물 및 이의 용도 | |
| WO2011126948A1 (en) | Pancreatic beta-cell melatonin receptor activation as a treatment for preservation of beta-cell mass and function in type 2 diabetes |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A107 | Divisional application of patent | ||
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application |