KR20100067099A - 눈물 임플랜트 검출 - Google Patents
눈물 임플랜트 검출 Download PDFInfo
- Publication number
- KR20100067099A KR20100067099A KR1020107007093A KR20107007093A KR20100067099A KR 20100067099 A KR20100067099 A KR 20100067099A KR 1020107007093 A KR1020107007093 A KR 1020107007093A KR 20107007093 A KR20107007093 A KR 20107007093A KR 20100067099 A KR20100067099 A KR 20100067099A
- Authority
- KR
- South Korea
- Prior art keywords
- implant
- tear
- detection device
- core
- detection
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F9/00—Methods or devices for treatment of the eyes; Devices for putting-in contact lenses; Devices to correct squinting; Apparatus to guide the blind; Protective devices for the eyes, carried on the body or in the hand
- A61F9/0008—Introducing ophthalmic products into the ocular cavity or retaining products therein
- A61F9/0017—Introducing ophthalmic products into the ocular cavity or retaining products therein implantable in, or in contact with, the eye, e.g. ocular inserts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/06—Devices, other than using radiation, for detecting or locating foreign bodies ; determining position of probes within or on the body of the patient
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/41—Detecting, measuring or recording for evaluating the immune or lymphatic systems
- A61B5/411—Detecting or monitoring allergy or intolerance reactions to an allergenic agent or substance
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F9/00—Methods or devices for treatment of the eyes; Devices for putting-in contact lenses; Devices to correct squinting; Apparatus to guide the blind; Protective devices for the eyes, carried on the body or in the hand
- A61F9/007—Methods or devices for eye surgery
- A61F9/00772—Apparatus for restoration of tear ducts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/04—Macromolecular materials
- A61L31/043—Proteins; Polypeptides; Degradation products thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/04—Macromolecular materials
- A61L31/043—Proteins; Polypeptides; Degradation products thereof
- A61L31/044—Collagen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/04—Macromolecular materials
- A61L31/06—Macromolecular materials obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L31/145—Hydrogels or hydrocolloids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L31/00—Materials for other surgical articles, e.g. stents, stent-grafts, shunts, surgical drapes, guide wires, materials for adhesion prevention, occluding devices, surgical gloves, tissue fixation devices
- A61L31/14—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L31/16—Biologically active materials, e.g. therapeutic substances
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01R—MEASURING ELECTRIC VARIABLES; MEASURING MAGNETIC VARIABLES
- G01R33/00—Arrangements or instruments for measuring magnetic variables
- G01R33/02—Measuring direction or magnitude of magnetic fields or magnetic flux
- G01R33/0213—Measuring direction or magnitude of magnetic fields or magnetic flux using deviation of charged particles by the magnetic field
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01R—MEASURING ELECTRIC VARIABLES; MEASURING MAGNETIC VARIABLES
- G01R33/00—Arrangements or instruments for measuring magnetic variables
- G01R33/02—Measuring direction or magnitude of magnetic fields or magnetic flux
- G01R33/06—Measuring direction or magnitude of magnetic fields or magnetic flux using galvano-magnetic devices
- G01R33/07—Hall effect devices
- G01R33/072—Constructional adaptation of the sensor to specific applications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B2562/00—Details of sensors; Constructional details of sensor housings or probes; Accessories for sensors
- A61B2562/08—Sensors provided with means for identification, e.g. barcodes or memory chips
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B5/00—Measuring for diagnostic purposes; Identification of persons
- A61B5/0002—Remote monitoring of patients using telemetry, e.g. transmission of vital signals via a communication network
- A61B5/0031—Implanted circuitry
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61B—DIAGNOSIS; SURGERY; IDENTIFICATION
- A61B8/00—Diagnosis using ultrasonic, sonic or infrasonic waves
- A61B8/08—Detecting organic movements or changes, e.g. tumours, cysts, swellings
- A61B8/0833—Detecting organic movements or changes, e.g. tumours, cysts, swellings involving detecting or locating foreign bodies or organic structures
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2250/00—Special features of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof
- A61F2250/0058—Additional features; Implant or prostheses properties not otherwise provided for
- A61F2250/0067—Means for introducing or releasing pharmaceutical products into the body
- A61F2250/0068—Means for introducing or releasing pharmaceutical products into the body the pharmaceutical product being in a reservoir
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F2250/00—Special features of prostheses classified in groups A61F2/00 - A61F2/26 or A61F2/82 or A61F9/00 or A61F11/00 or subgroups thereof
- A61F2250/0058—Additional features; Implant or prostheses properties not otherwise provided for
- A61F2250/0096—Markers and sensors for detecting a position or changes of a position of an implant, e.g. RF sensors, ultrasound markers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/404—Biocides, antimicrobial agents, antiseptic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/43—Hormones, e.g. dexamethasone
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Heart & Thoracic Surgery (AREA)
- Physics & Mathematics (AREA)
- Vascular Medicine (AREA)
- Surgery (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Ophthalmology & Optometry (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Medical Informatics (AREA)
- Pathology (AREA)
- General Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Chemical & Material Sciences (AREA)
- Human Computer Interaction (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Plastic & Reconstructive Surgery (AREA)
- Immunology (AREA)
- Medicinal Chemistry (AREA)
- Dispersion Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Prostheses (AREA)
Abstract
본 문헌은, 무엇보다, 적어도 부분적으로 눈물점 내에 삽입 가능한 눈물 임플랜트를 포함하는 장치를 논의한다. 상기 눈물 임플랜트는, 임플랜트 코어, 및 임플랜트 본체를 포함한다. 상기 임플랜트 본체는, 상기 임플랜트 코어를 수용하는 사이즈 및 형상을 가진 임플랜트 공동을 포함한다. 상기 임플랜트 코어와 상기 임플랜트 공동 중 하나 이상은, 별도의 검출기 디바이스를 사용하여 상기 눈물 임플랜트의 자동 검출을 가능하게 하도록 구성된 검출 디바이스를 포함한다.
Description
본 발명은, 일반적으로 인체 및/또는 동물에 사용하기 위한 임플랜트(implant)에 관한 것으로서, 더욱 구체적으로는 코눈물 배수 장치에서 또는 그 근처에서 임플랜트의 검출에 관한 것이며, 그러한 임플랜트는 자주 눈물 임플랜트(lacrimal implant)라고 지칭된다.
본 출원은, U.S.C.§119(e)하에서, 2007년 9월 7일자 출원된 미국 가특허출원 번호 60/970,807 및 2008년 5월 6일자 출원된 미국 가특허출원 번호 61/050,901를 우선권으로 주장한다.
눈 치료 분야에서 환자 및 의사는 다양한 어려움에 당면한다. 몇몇 예에서, 안구 질환 예를 들면 안구 건조증을 해결하기 위해 하나 이상의 눈물점 관(puctal duct)을 임플랜트로 플러깅하는 것이 바람직할 수 있다. 몇몇 예에서, 또한 장기간 환자를 치료할 수 있는 치료 약제(theraputic agent)를 임플랜트에 포함시키는 것이 바람직할 수 있다.
눈물점에 관련된 눈물 임플랜트의 몇 가지 문제점은, 눈물 임플랜트가 매우 작고 투명(clear)하거나 표피색의 실리콘 재료로 이루어져 보거나 검출하기 어렵다는 것이다. 눈물 임플랜트는 또한 환자가 눈을 비빔으로써 쉽게 제거되며, 환자는 삽입체를 잃어버린 것조차 알 수 없을 수도 있어, 임플랜트가 제공할 수 있는 임의의 치료 효과를 잃을 수 있다. 치료 임플랜트와 관련된 다른 문제점은, 환자가 치료 약제의 공급이 완료된 시점을 모른다는 것이다.
약제를 가진 임플랜트는 또한 눈 외의 것을 치료하기 위해서도 사용될 수 있다. 예를 들면, 약제 임플랜트는 암, HIV, 당뇨병의 체계적 치료, 또는 관절 및 종양의 특정 위치 치료에 사용될 수 있다. 일단 이식되면, 임플랜트가 임플랜트 사이트로부터 이동되었는지를 알기 어려워, 특정 치료 위치에 대한 문제점이 된다. 또한, 임플랜트에 어떤 약제 또는 요법이 사용되었는지를 판정하기 어렵다. 예를 들면, 임플랜트를 가진 환자는, 다른 약제과 상호작용할 수 있는 어떤 약제가 임플랜트 내에 있는지 잊을 수 있다.
상기 사항에 비추어, 상술한 단점중 적어도 몇가지를 극복하는 임플랜트의 향상된 검출을 제공하는 것이 바람직할 것이다.
본 발명은, 일반적으로 검출 디바이스를 포함하는 임플랜트를 사용하여 조직, 더욱 구체적으로는 눈을 치료하는 것에 관한 것이다. 또한, 임플랜트는 또한 눈을 치료하기 위해 치료 약제를 릴리스하는 치료 임플랜트일 수 있다.
1. 장치는, 적어도 부분적으로 눈물점 내에 삽입 가능한 눈물 임플랜트를 포함한다. 상기 눈물 임플랜트는 임플랜트 코어, 및 임플랜트 본체를 포함한다. 상기 임플랜트 본체는, 상기 임플랜트 코어를 수용하는 사이즈 및 형상을 가진 임플랜트 공동을 포함하며, 상기 임플랜트 코어와 상기 임플랜트 공동 중 하나 이상은, 별도의 검출기 디바이스를 사용하여 상기 눈물 임플랜트의 자동 검출을 가능하게 하도록 구성된 검출 디바이스를 포함한다.
2. 상기 검출 디바이스는 선택적으로, 상기 검출기 디바이스로 검출 신호를 통신하도록 구성된 무선 주파수 식별기(RFID) 칩을 포함하는, 면모(aspect) 1에 따른 장치.
3. 상기 검출 디바이스는 선택적으로, 상기 검출기 디바이스로 빛을 반사하도록 구성된 발광 재료를 포함하는, 면모 1 또는 면모 2에 따른 장치.
4. 상기 발광 재료는 선택적으로 양자 돗트(quantum dot)를 포함하는, 면모 1 내지 면모 3 중 어느 하나에 따른 장치.
5. 상기 검출 디바이스는 선택적으로, 상기 검출기 디바이스로 초음파 에너지를 반사하도록 구성된 초음파 반사 재료를 포함하는, 면모 1 내지 면모 4 중 어느 하나에 따른 장치.
6. 제1 실시예 내지 제6 실시예의 상기 검출 디바이스는 선택적으로, 상기 검출기 디바이스에 의해 검출될 수 있는 자계를 유지하기 위한 자기 재료를 포함하는, 면모 1 내지 면모 5 중 어느 하나에 따른 장치. 상기 자기 재료는, 마그네타이트, 금속 분말, 금속 링, 및 탄소 분말 중 하나 이상을 포함한다.
7. 제1 실시예 내지 제6 실시예의 상기 검출 디바이스는 선택적으로, 상기 검출기 디바이스에 의해 검출될 수 있는 자계를 유지하기 위한 자기 재료를 포함하는, 면모 1 내지 면모 6 중 어느 하나에 따른 장치.
8. 상기 검출 디바이스는 선택적으로, 감지 회로에 대한 상기 눈물 임플랜트의 근접도로 인해 상기 검출기 디바이스의 상기 감지 회로의 특성 임피던스를 변경시키도록 구성된 전기 전도성 재료를 포함하는, 면모 1 내지 면모 7 중 어느 하나에 따른 장치.
9. 상기 검출 디바이스는 선택적으로, 상기 임플랜트 코어와 상기 임플랜트 공동 중 하나 이상에, 눈의 영역으로부터 상기 눈물 임플랜트를 광학적으로 구별하도록 구성된 광학 대조 재료와 칼라 재료 중 하나 이상을 포함하는, 면모 1 내지 면모 8 중 어느 하나에 따른 장치.
10. 상기 검출 디바이스는 선택적으로, 자외선 소스에 의해 조명될 때 볼 수 있는 재료를 포함하는, 면모 1 내지 면모 9 중 어느 하나에 따른 장치.
11. 상기 임플랜트 코어는 선택적으로 지속적 릴리스 안구 제제(ocular agent)를 포함하는, 면모 1 내지 면모 10 중 어느 하나에 따른 장치.
12. 상기 임플랜트 코어는 선택적으로 상기 제제를 수용하기 위한 시드(sheath)를 포함하는, 면모 1 내지 면모 11 중 어느 하나에 따른 장치. 상기 검출 디바이스는 상기 시드 내에 배치되어 있다.
13. 상기 임플랜트 본체의 생체 적합성 재료는 선택적으로, 눈에 대한 지속적 릴리스를 위한 제제를 포함하는, 면모 1 내지 면모 12 중 어느 하나에 따른 장치.
14. 상기 눈물 임플랜트는 선택적으로 상기 임플랜트 본체의 외면에 중합체 코팅을 포함하고, 상기 중합체 코팅은 상기 제제를 포함하는, 면모 1 내지 면모 13 중 어느 하나에 따른 장치.
15. 방법은, 생체 적합성 재료의 눈물 임플랜트를 형성하는 단계, 상기 눈물 임플랜트의 본체 내에 임플랜트 공동을 형성하는 단계, 상기 공동 내에 임플랜트 코어를 제공하는 단계, 및 상기 임플랜트 코어와 상기 임플랜트 공동 중 하나 이상 내에 검출 디바이스를 제공하는 단계를 포함하며, 상기 임플랜트 코어는, 눈에 제제를 지속적으로 릴리스하도록 하는 사이즈로 구성되고, 상기 검출 디바이스는, 별도의 검출기 디바이스를 사용하여 상기 눈물 임플랜트의 자동 검출을 가능하게 하도록 구성된다.
16. 상기 검출 디바이스를 제공하는 상기 단계는 선택적으로, 상기 검출기 디바이스로 검출 신호를 통신하도록 구성되는 RFID 칩, 상기 검출기 디바이스로 빛을 반사하도록 구성되는 발광 재료, 상기 검출기 디바이스로 초음파 에너지를 반사하도록 구성되는 초음파 반사 재료, 외부 자계의 인가 및 제거 후에 상기 검출기 디바이스에 의해 검출 가능한 강자성 성질을 유지할 수 있는 강자성 재료, 상기 검출기 디바이스의 감지 회로의 특성 임피던스를 변경시키도록 구성되는 전기 전도성 재료, 눈의 영역으로부터 눈물점 러그(punctum lug)를 광학적으로 구별하도록 구성된 광학 대조 재료, 눈의 영역으로부터 상기 눈물 임플랜트를 광학적으로 구별하기 위한 칼라 재료, 및 자외선 소스로 조명될 때 볼 수 있는 재료 중 하나 이상을 제공하는 단계를 포함하는, 면모 15에 따른 방법.
17. 상기 검출 디바이스를 제공하는 상기 단계는 선택적으로 상기 발광 재료를 제공하는 단계를 포함하며, 상기 발광 재료는 선택적으로 양자 돗트를 포함하는, 면모 15 또는 면모 16에 따른 방법.
18. 제15 실시예 내지 제17 실시예 중 어느 하나의 상기 검출 디바이스를 제공하는 상기 단계는 선택적으로, 상기 강자성 재료를 제공하는 단계를 포함하는, 면모 15 내지 면모 17 중 어느 하나에 따른 방법. 상기 강자성 재료는, 마그네타이트, 금속 분말, 금속 링, 및 탄소 분말 중 하나 이상을 포함한다.
19. 상기 검출 디바이스를 제공하는 단계는 선택적으로, 상기 검출기 디바이스로 빛을 반사하도록 구성된 상기 발광 재료를 제공하는 단계를 포함하는, 면모 15 내지 면모 18 중 어느 하나에 따른 방법. 상기 방법은 선택적으로, 발광 소스를 사용하여 제1 파장 범위의 입사광에 상기 눈물 임플랜트를 노출시키는 단계, 상기 검출 디바이스에서 제2 파장 범위의 빛을 검출하는 단계, 및 충분한 반사광이 검출되었을 때 상기 눈물 임플랜트의 근접도를 표시하기 위한 표시를 제공하는 단계를 포함하고, 수광되는 빛은 상기 눈물 임플랜트로부터 반사된다.
20. 제19 실시예의 상기 제1 파장 범위는 선택적으로 청색 스펙트럼을 포함하며, 상기 제2 파장 범위는 녹색 스펙트럼을 포함하는, 면모 19에 따른 방법.
21. 상기 입사광에 상기 눈물 임플랜트를 노출시키는 상기 단계는 선택적으로, 적외선 스펙트럼의 제1 파장 범위의 빛에 상기 눈물 임플랜트를 노출시키는 단계를 포함하고, 상기 빛을 검출하는 상기 단계는, 적외선 스펙트럼의 제2 파장 범위의 빛을 검출하는 단계를 포함하는, 면모 19 또는 면모 20에 따른 방법.
22. 제19 실시예 내지 제21 실시예 중 어느 하나에 따른 상기 표시를 제공하는 상기 단계는 선택적으로, 가청 표시를 제공하는 단계를 포함하는, 면모 19 내지 면모 21 중 어느 하나에 따른 방법.
23. 상기 표시를 제공하는 상기 단계는 선택적으로, 가시성 표시를 제공하는 단계를 포함하는, 면모 19 내지 면모 22 중 어느 하나에 따른 방법.
24. 눈 질환을 치료하는 방법은, 눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계, 및 별도의 검출기 디바이스를 사용하여 상기 눈물 임플랜트의 상기 검출 디바이스를 검출하는 단계를 포함한다. 상기 눈물 임플랜트는, 생체 적합성 재료의 임플랜트 본체, 눈으로 제제를 지속적으로 릴리스하는 사이즈로 구성되는 임플랜트 코어, 및 상기 임플랜트 코어 내에 배치되는 상기 제제의 서플라이(supply)를 포함하며, 상기 임플랜트 본체는, 상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되는 공동을 포함하고, 상기 임플랜트 코어는 상기 임플랜트 본체의 상기 공동 내에 지지되며, 상기 임플랜트 코어와 상기 임플랜트 공동 중 하나 이상은, 상기 별도의 검출기 디바이스를 사용하여 상기 눈물 임플랜트의 자동 검출을 가능하게 하도록 구성되는 검출 디바이스를 포함하고, 상기 서플라이는, 상기 제제를 지속적으로 릴리스하도록 구성된다.
25. 상기 제제는 선택적으로 녹내장 질병을 치료하는 제제를 포함하는, 면모 24에 따른 눈 질환을 치료하는 방법.
26. 상기 제제는 선택적으로, 안구 고혈압증(ocular hypertension) 또는 1차 개방각 녹내장(primary open angle glaucoma) 중 하나 이상을 치료하는 제제를 포함하는, 면모 24 또는 면모 25 중 어느 하나에 따른 눈 질환을 치료하는 방법.
27. 장치는, 적어도 부분적으로 눈물점 내로 삽입 가능한 눈물 임플랜트를 포함한다. 상기 눈물 임플랜트는 생체 적합성 재료의 임플랜트 본체를 포함한다. 상기 임플랜트 본체는, 상기 눈물 임플랜트의 검출을 가능하게 하고, 상기 눈물 임플랜트의 하나 이상의 속성을 식별하도록 구성된 검출 디바이스를 포함한다.
28. 상기 검출 디바이스는 선택적으로, 별도의 검출기 디바이스로 속성 정보를 통신하도록 구성된 무선 주파수 식별기(RFID) 칩을 포함하는, 면모 27에 따른 장치.
29. 상기 검출 디바이스는 선택적으로 상기 눈물 임플랜트 내에 칼라를 포함하는, 면모 27 또는 면모 28에 따른 장치. 상기 칼라는 상기 눈물 임플랜트의 상기 속성을 식별한다.
30. 상기 검출 디바이스는 발광 재료를 선택적으로 포함하며, 상기 발광 재료는 상기 칼라를 반사시키는, 면모 27 내지 면모 29 중 어느 하나에 따른 장치.
31. 제27 실시예 내지 제30 실시예 중 어느 하나에 따른 상기 발광 재료는 선택적으로 양자 돗트를 포함하는, 면모 27 내지 면모 30 중 어느 하나에 따른 장치.
32. 상기 검출 디바이스는 선택적으로, 자외선 소스로 볼 수 있는 재료를 포함하며, 상기 검출 디바이스는, 자외선 소스로 조명될 때 상기 속성을 식별하는, 면모 27 내지 면모 31 중 어느 하나에 따른 장치.
33. 상기 검출 디바이스는 선택적으로, 상기 눈물 임플랜트에 의해 추출될 수 있는(elutable) 재료, 및 생-부식성 표면을 포함하는, 면모 27 내지 면모 32 중 어느 하나에 따른 장치. 상기 생-부식성 표면은, 상기 속성을 식별하기 위한 재료를 추출한다.
34. 상기 눈물 임플랜트는 선택적으로 지속적 릴리스 안구 제제를 포함하며, 상기 눈물 임플랜트의 상기 속성은, 상기 안구 제제의 유형, 상기 안구 제제의 선량(dose), 및 상기 안구 제제의 릴리스가 완료되는 때의 표시 중 하나 이상을 포함하는, 면모 27 내지 면모 33 중 어느 하나에 따른 장치.
35. 식별 가능한 상기 속성은, 상기 눈물 임플랜트의 제조자, 상기 눈물 임플랜트의 제조자의 제조 번호, 상기 눈물 임플랜트가 이식된 날자, 상기 임플랜트의 유효일자, 상기 눈물 임플랜트가 이식된 위치의 표시, 의사를 식별하기 위한 표시, 및 환자를 식별하기 위한 표시 중 하나 이상을 포함하는, 면모 27 내지 면모 34 중 어느 하나에 따른 장치.
36. 방법은, 생체 적합성 재료의 눈물 임플랜트를 형성하는 단계, 및 임플랜트 본체 내에 검출 디바이스를 배치하는 단계를 포함하며, 눈물점 마개는 상기 임플랜트 본체를 포함하고, 상기 검출 디바이스는, 상기 눈물 임플랜트의 검출을 가능하게 하고, 상기 눈물 임플랜트의 하나 이상의 속성을 식별하도록 구성된다.
37, 제36 실시예에 따른 상기 검출 디바이스는 선택적으로, 별도의 검출기 디바이스로 속성 정보를 통신하도록 구성되는 RFID 칩, 상기 눈물 임플랜트 내의 칼라, 발광 재료, 자외선 소스로 볼 수 있는 재료, 및 상기 눈물 임플랜트에 의해 추출 가능한 재료중 하나 이상을 포함하며, 상기 칼라는 상기 눈물 임플랜트의 상기 속성을 식별하고, 상기 발광 재료에 의해 반사된 상기 칼라는 상기 속성을 식별하며, 상기 검출 디바이스는, 상기 자외선 소스로 조명될 때 상기 속성을 식별하고, 상기 추출 가능한 재료는 상기 속성을 식별하는, 면모 36에 따른 방법.
38. 선택적으로 상기 눈물 임플랜트 내에 지속적 릴리스 안구 제제를 제공하는 단계를 더 포함하며, 상기 검출 디바이스는, 상기 안구 제제의 유형, 상기 안구 제제의 선량, 및 상기 안구 제제의 릴리스가 완료되는 때의 표시 중 하나 이상의 식별을 가능하게 하도록 구성되는, 면모 36 또는 면모 37에 따른 방법.
39. 상기 검출 디바이스는 선택적으로, 상기 눈물 임플랜트의 제조자, 상기 눈물 임플랜트의 제조자의 제조 번호, 상기 눈물 임플랜트가 이식된 날자, 상기 임플랜트의 유효일자, 상기 눈물 임플랜트가 이식된 위치의 표시, 의사를 식별하기 위한 표시, 및 환자를 식별하기 위한 표시 중 하나 이상의 식별을 가능하게 하도록 구성되는, 면모 36 내지 면모 38 중 어느 하나에 따른 방법.
40. 눈의 질환을 치료하는 방법은, 눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계, 상기 눈물 임플랜트 내에 포함된 검출 디바이스를 검출하는 단계, 및 상기 검출 디바이스를 통해 상기 눈물 임플랜트의 하나 이상의 속성을 식별하는 단계를 포함한다.
41. 상기 검출 디바이스를 검출하는 상기 단계는 선택적으로, 상기 눈물 임플랜트 내에 포함된 RFID 칩과 통신하는 단계를 포함하며, 상기 속성을 식별하는 상기 단계는, 상기 RFID 칩과 별도의 검출기 디바이스 사이에서 속성 정보를 통신하는 단계를 포함하는, 면모 40에 따른 눈의 질환을 치료하는 방법.
42. 상기 검출 디바이스를 검출하는 상기 단계는 선택적으로, 상기 눈물 임플랜트 내의 칼라를 검출하는 단계를 포함하며, 상기 속성을 식별하는 상기 단계는, 상기 칼라를 사용하여 상기 속성을 식별하는 단계를 포함하는, 면모 40 또는 면모 41에 따른 눈의 질환을 치료하는 방법.
43. 상기 눈물 임플랜트 내의 상기 칼라를 검출하는 상기 단계는 선택적으로, 상기 눈물 임플랜트 내에 포함된 발광 재료에 의해 반사되는 칼라를 검출하는 단계를 포함하는, 면모 40 내지 면모 42 중 어느 하나에 따른 눈의 질환을 치료하는 방법.
44. 상기 눈물 임플랜트 내의 상기 칼라를 검출하는 상기 단계는 선택적으로, 상기 눈물 임플랜트 내에 포함된 양자 돗트에 의해 반사되는 칼라를 검출하는 단계를 포함하는, 면모 40 내지 면모 43 중 어느 하나에 따른 눈의 질환을 치료하는 방법.
45. 상기 검출 디바이스를 검출하는 상기 단계는 선택적으로, 자외선 소스를 사용하여 볼 수 있는 상기 눈물 임플랜트 내의 상기 재료를 검출하는 단계를 포함하며, 상기 속성을 식별하는 상기 단계는, 상기 재료가 상기 자외선 소스를 사용하여 조명될 때 상기 속성을 식별하는 단계를 포함하는, 면모 40 내지 면모 45 중 어느 하나에 따른 눈의 질환을 치료하는 방법.
46. 상기 검출 디바이스를 검출하는 상기 단계는 선택적으로, 상기 눈물 임플랜트에 의해 추출 가능한 재료를 검출하는 단계를 포함하며, 상기 눈물 임플랜트의 상기 속성을 식별하는 상기 단계는, 상기 추출 가능 한 재료로부터 상기 속성을 식별하는 단계를 포함하는, 면모 40 내지 면모 45 중 어느 하나에 따른 눈의 질환을 치료하는 방법.
47. 상기 방법에 사용되는 상기 눈물 임플랜트는 선택적으로 지속적 릴리스 안구 제제를 포함하며, 상기 눈물 임플랜트의 상기 속성은, 상기 안구 제제의 유형, 상기 안구 제제의 선량, 및 상기 안구 제제의 릴리스가 완료되는 때의 표시 중 하나 이상을 포함하는, 면모 40 내지 면모 46 중 어느 하나에 따른 눈의 질환을 치료하는 방법.
48. 상기 속성을 식별하는 상기 단계는 선택적으로, 상기 눈물 임플랜트의 제조자, 상기 눈물 임플랜트의 제조자의 제조 번호, 상기 눈물 임플랜트가 이식된 날자, 상기 임플랜트의 유효일자, 상기 눈물 임플랜트가 이식된 위치의 표시, 의사를 식별하기 위한 표시, 및 환자를 식별하기 위한 표시 중 하나 이상을 식별하는 단계를 포함하는, 면모 40 내지 면모 47 중 어느 하나에 따른 눈의 질환을 치료하는 방법.
49. 장치는, 적어도 부분적으로 눈물점 내로 삽입 가능한 눈물 임플랜트를 포함한다. 상기 눈물 임플랜트는 임플랜트 본체를 포함한다. 상기 임플랜트 본체는 검출 디바이스를 포함한다. 상기 검출 디바이스는, 외부 자계의 인가 및 제거 후에 강자성 성질을 유지할 수 있는 강자성 재료, 별도의 초음파 검출기 디바이스로 상기 눈물 임플랜트의 자동 검출을 가능하게 하도록 구성된 초음파 반사 재료, 및 상기 임플랜트 본체 내에 포함되어 있고, 눈물 임플랜트 검출기 디바이스와 통신하도록 구성된 무선 주파수 식별기(RFID) 중 하나 이상을 포함한다.
50. 제49 실시예에 따른 상기 검출 디바이스는 선택적으로 강자성 재료를 포함하며, 상기 강자성 재료는, 마그네타이트, 금속 분말, 금속 링, 및 탄소 분말 중 하나 이상을 포함하는, 면모 49에 따른 장치.
51. 상기 검출 디바이스는 선택적으로 초음파 반사 재료를 포함하는, 면모 49 또는 면모 50에 따른 장치. 상기 초음파 반사 재료는 상기 임플랜트 본체의 생체 적합성 재료 내에 배치되어 있고, 상기 초음파 반사 재료는, 상기 눈물 임플랜트에 초음파 에너지를 인가할 때 상기 임플랜트 본체의 형상을 변경시키도록 구성되어 있다.
52. 상기 초음파 반사 재료는 선택적으로 압전 재료를 포함하는, 면모 49 내지 면모 51 중 어느 하나에 따른 장치.
53. 눈에 대한 지속적 릴리스를 위한 제제는 선택적으로 상기 임플랜트 본체 내에 배치되어 있는, 면모 49 내지 면모 52 중 어느 하나에 따른 장치.
54. 눈의 질환을 치료하는 방법은, 눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계, 및 별도의 초음파 검출기 디바이스로 검출 디바이스를 검출함으로써 상기 눈물 임플랜트를 검출하는 단계를 포함한다. 상기 눈물 임플랜트는 임플랜트 본체를 포함하고, 상기 임플랜트 본체는 상기 검출 디바이스를 포함하며, 상기 검출 디바이스는, 외부 자계의 인가 및 제거 후에 강자성 성질을 유지할 수 있는 강자성 재료, 상기 별도의 초음파 검출기 디바이스로 상기 눈물 임플랜트의 자동 검출을 가능하게 하도록 구성되는 초음파 반사 재료, 상기 임플랜트 본체 내에 포함되고, 눈물 임플랜트 검출기 디바이스와 통신하도록 구성되는 무선 주파수 식별기(RFID), 및 임플랜트 코어 내에 배치되는 제제의 서플라이 중 하나 이상을 포함하며, 상기 서플라이는 상기 제제를 지속적으로 릴리스하도록 구성된다.
55. 상기 제제는 선택적으로 녹내장 질병을 치료하는 제제를 포함하는, 면모 54에 따른 눈의 질환을 치료하는 방법.
56. 상기 제제는 선택적으로, 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 이상을 치료하는 제제를 포함하는, 눈의 질환을 치료하는 방법.
57. 검출 장치는, 눈물 임플랜트에 입사광을 제공하기 위한 발광원, 상기 눈물 임플랜트의 발광 재료로부터 반사되는 특정 파장 범위의 빛을 통과시키도록 구성된 광학 필터, 상기 필터에 의해 통과되는 빛을 수광하고, 충분한 빛이 수광되었을 때 상기 눈물 임플랜트의 근접도를 표시하기 위해 응답 전기 신호를 발생시키도록 구성된 광검출 디바이스, 및 상기 광검출 디바이스에 통신 가능하게 결합되어 있고, 상기 전기 신호를 수신하였을 때 사용자에게 마개 검출의 표시를 제공하기 위한 표시기를 포함한다.
58. 상기 발광원은 선택적으로, 제1 파장 범위를 가진 입사광을 제공하고, 상기 발광 재료는 제2 파장 범위의 입사광을 반사시키는, 면모 57에 따른 검출 장치.
59. 상기 발광원은 선택적으로 청색 스펙트럼의 입사광을 제공하고, 상기 발광 재료는 녹색 스펙트럼의 입사광을 반사시키는, 면모 57 또는 면모 58에 따른 검출 장치.
60. 상기 발광원은 선택적으로, 적외선 스펙트럼 내의 제1 파장 범위를 가진 입사광을 제공하고, 상기 발광 재료는 적외선 스펙트럼 내의 다른 제2 파장 범위의 입사광을 반사시키는, 면모 57 내지 면모 59 중 어느 하나에 따른 검출 장치.
61. 상기 표시기는 선택적으로 마개 검출의 시각적 표시를 제공하는, 면모 57 내지 면모 60 중 어느 하나에 따른 검출 장치.
62. 상기 표시기는 선택적으로 마개 검출의 가청 표시를 제공하는, 면모 57 내지 면모 61 중 어느 하나에 따른 검출 장치.
63. 검출 장치는, 적어도 부분적으로 눈물점 내로 삽입 가능한 눈물 임플랜트, 및 눈물 임플랜트 검출기 디바이스를 포함한다. 상기 눈물 임플랜트는 생체 적합성 재료의 임플랜트 본체를 포함한다. 상기 임플랜트 본체는, 외부 자계의 인가 및 제거 후에 강자성 성질을 유지할 수 있는 강자성 재료를 포함한다. 상기 눈물 임플랜트 검출기 디바이스는, 자계 검출 회로, 및 상기 자계 검출 회로에 통신 가능하게 결합되어 있고, 상기 눈물 임플랜트의 자계를 검출하였을 때 표시하도록 구성되어 있는 표시 디바이스를 포함한다.
64. 상기 자계 검출 회로는 선택적으로홀 효과 센서를 포함하는, 면모 63에 따른 검출 장치.
65. 상기 자계 검출 회로는 선택적으로, 상기 자계 검출 회로에 통신 가능하게 결합되어 있고, 상기 홀 효과 센서의 출력에서의 전압이 제1 임계치를 초과할 때 상기 표시 디바이스에 전기 신호를 제공하기 위한 비교 회로를 포함하는, 면모 63 또는 면모 64에 따른 검출 장치.
66. 상기 비교 회로는 선택적으로, 상기 홀 효과 센서의 출력에서의 전압이 제1 임계치를 초과하고 제2 임계치보다 작을 때 상기 표시 디바이스에 전기 신호를 제공하는, 면모 63 내지 면모 65 중 어느 하나에 따른 검출 장치.
67. 상기 표시 디바이스는 선택적으로 가청 표시를 제공하는, 면모 63 내지 면모 66 중 어느 하나에 따른 검출 장치.
68. 상기 표시 디바이스는 선택적으로 시각적 표시를 제공하는, 면모 63 내지 면모 67 중 어느 하나에 따른 검출 장치.
69. 상기 눈물 임플랜트 검출기 디바이스는 선택적으로, 인접 단부와 말단 단부를 포함하는 기다란 하우징을 포함하며, 상기 자계 검출 회로는, 상기 인접 단부에 또는 그 근처에 배치된 자계 센서를 포함하는, 면모 63 내지 면모 68 중 어느 하나에 따른 검출 장치.
70. 상기 표시 디바이스는 선택적으로 시각적 표시를 제공하고, 상기 자계 센서로부터 말단 방향으로 있는 지점에 있는, 면모 69에 따른 검출 장치.
71. 상기 눈물 임플랜트 검출 디바이스는, 선택적으로 대상물의 눈 위에 맞는 형상을 가진 하우징을 포함하는, 면모 63 내지 면모 70 중 어느 하나에 따른 검출 장치.
72. 방법은, 생체 적합성 재료의 눈물 임플랜트를 형성하는 단계, 상기 눈물 임플랜트 내에 강자성 재료를 제공하는 단계, 및 상기 눈물 임플랜트가 더 이상 자계에 노출되지 않을 때 강자성 성질을 보이도록, 상기 눈물 임플랜트를 상기 자계에 노출시키는 단계를 포함한다.
73. 상기 눈물 임플랜트를 형성하는 상기 단계는 선택적으로, 생체 적합성 재료의 임플랜트 본체를 형성하는 단계를 포함하고, 상기 눈물 임플랜트 내에 강자성 재료를 제공하는 상기 단계는, 상기 강자성 재료를 상기 임플랜트 본체의 상기 생체 적합성 재료 내에 배치하는 단계를 포함하는, 면모 72에 따른 방법.
74. 상기 눈물 임플랜트를 형성하는 상기 단계는 선택적으로, 상기 눈물 임플랜트의 본체 내에 공동을 형성하는 단계, 및 상기 공동 내에 임플랜트 코어를 제공하는 단계를 포함하며, 상기 임플랜트 코어는, 눈에 대한 지속적 릴리스를 위한 충분한 양의 제제를 제공하기 위한 사이즈 및 형상을 가지고, 상기 눈물 임플랜트 내에 강자성 재료를 제공하는 상기 단계는, 상기 눈물 임플랜트의 상기 임플랜트 코어 내에 강자성 재료를 제공하는 단계를 포함하는, 면모 72 또는 면모 73 중 어느 하나에 따른 방법.
75. 선택적으로 상기 제제를 수용하기 위해 상기 임플랜트 코어에 시드를 형성하는 단계를 더 포함하며, 상기 임플랜트 코어 내에 강자성 재료를 제공하는 상기 단계는, 상기 강자성 재료를 상기 시드 내에 배치하는 단계를 포함하는, 면모 72 내지 면모 74 중 어느 하나에 따른 방법.
76. 상기 눈물 임플랜트 내에 강자성 재료를 제공하는 상기 단계는 선택적으로, 상기 눈물 임플랜트 내에 마그네타이트를 제공하는 단계를 포함하는, 면모 72 내지 면모 75 중 어느 하나에 따른 방법.
77. 눈의 질환을 치료하는 방법은, 눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계, 및 눈물 임플랜트 검출 디바이스로로 상기 눈물 임플랜트의 강자성 성질을 검출하는 단계를 포함한다. 상기 눈물 임플랜트는, 생체 적합성 재료의 임플랜트 본체, 및 상기 임플랜트 코어 내에 배치되는 제제의 서플라이를 포함한다. 상기 서플라이는 상기 제제를 지속적으로 릴리스한다. 상기 임플랜트 본체는, 외부 자계의 인가 및 제거 후에 강자성 성질을 유지할 수 있는 강자성 재료, 상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되는 상기 임플랜트 본체 내에 있는 공동, 및 상기 공동 내에 있는 임플랜트 코어를 포함하며, 상기 임플랜트 코어는, 눈에 대한 지속적 릴리스를 위한 충분한 양의 제제를 제공하기 위한 사이즈 및 형상을 가진다.
78. 상기 제제는 선택적으로 녹내장 질병을 치료하는 제제를 포함하는, 면모 77에 따른 눈의 질환을 치료하는 방법.
79. 상기 제제는 선택적으로, 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 이상을 치료하는 제제를 포함하는, 면모 77 또는 78에 따른 눈의 질환을 치료하는 방법.
80. 검출 장치는, 눈물점 내로 삽입 가능한 눈물 임플랜트, 및 눈물 임플랜트 검출기 디바이스를 포함한다. 상기 눈물 임플랜트는, 생체 적합성 재료의 임플랜트 본체, 및 상기 임플랜트 본체 내에 있는 전기 전도성 재료를 포함한다. 상기 눈물 임플랜트 검출기 디바이스는, 특성 임피던스를 가진 감지 회로, 상기 감지 회로에 대한 상기 눈물 임플랜트의 근접으로 인한 상기 특성 임피던스의 변화를 검출하도록 구성된 검출 회로, 및 상기 검출 회로에 통신 가능하게 결합되어 있고, 상기 특성 임피던스의 변화를 검출하였을 때 표시하도록 구성된 표시기 디바이스를 포함한다.
81. 제80 실시예의 상기 전기 전도성 재료는 선택적으로, 상기 임플랜트 본체의 상기 생체 적합성 재료 내에 배치된 전기 전도성 입자를 포함하는, 면모 80에 따른 검출 장치.
82. 제80 실시예 및 제81 실시예의 상기 눈물 임플랜트는 선택적으로, 지속적 릴리스 안구 제제를 포함하는 임플랜트 코어를 포함하는, 면모 80 또는 면모 81에 따른 검출 장치. 상기 임플랜트 본체는, 상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되어 있는 공동을 포함한다. 상기 공동은 상기 임플랜트 코어를 수용하도록 하는 사이즈 및 형상을 가지고 있다.
83. 상기 임플랜트 코어는 선택적으로 상기 제제를 수용하기 위해 시드를 포함하며, 상기 전기 전도성 재료는 상기 시드 내에 배치되어 있는, 면모 80 내지 면모 82 중 어느 하나에 따른 검출 장치.
84. 상기 전기 전도성 재료는 선택적으로, 강철, 은, 금, 및 알루미늄 중 하나 이상을 포함하는, 면모 80 내지 면모 83 중 어느 하나에 따른 검출 장치.
85. 상기 감지 회로는, 상기 특성 임피던스에 기초하여 고유 응답 주파수를 포함하며, 상기 검출 회로는, 고유 응답 주파수의 이동으로부터 상기 특성 임피던스의 변화를 검출하는, 면모 80 내지 면모 84 중 어느 하나에 따른 검출 장치.
86. 상기 특성 임피던스는 선택적으로 특성 인덕턴스를 포함하며, 상기 검출 회로는, 상기 감지 회로에 대한 상기 눈물 임플랜트의 근접으로 인한 상기 특성 인덕턴스의 변화를 검출하도록 구성되어 있는, 면모 80 내지 면모 85 중 어느 하나에 따른 검출 장치.
87. 상기 특성 임피던스는 선택적으로 특성 커패시턴스를 포함하며, 상기 검출 회로는, 상기 감지 회로에 대한 상기 눈물 임플랜트의 근접으로 인한 상기 특성 커패시턴스의 변화를 검출하도록 구성되어 있는, 면모 80 내지 면모 86 중 어느 하나에 따른 검출 장치.
88. 눈에 대한 지속적 릴리스를 위한 상기 제제는 선택적으로 상기 임플랜트 본체 내에 배치되어 있는, 면모 80 내지 면모 87 중 어느 하나에 따른 검출 장치.
89. 방법은, 눈물 임플랜트를 제공하는 단계, 상기 눈물 임플랜트의 근접으로 인한 감지 회로의 특성 임피던스의 변화를 검출함으로써, 상기 눈물 임플랜트에 접촉하지 않고, 상기 눈물 임플랜트를 검출하는 단계, 및 상기 눈물 임플랜트가 검출되었는지에 관한 정보를 사용자에게 또는 자동화 프로세서에 제공하는 단계를 포함한다.
90. 상기 특성 임피던스의 변화를 검출하는 상기 단계는 선택적으로, 상기 감지 회로의 고유 응답 주파수의 이동을 검출하는 단계를 포함하는, 면모 89에 따른 방법.
91. 상기 눈물 임플랜트를 제공하는 상기 단계는 선택적으로, 생체 적합성 재료, 및 상기 생체 적합성 재료 내에 배치되는 전기 전도성 재료를 포함하는 상기 눈물 임플랜트를 제공하는 단계를 포함하는, 면모 89 또는 면모 90 중 어느 하나에 따른 방법.
92. 상기 눈물 임플랜트를 제공하는 상기 단계는 선택적으로, 상기 눈물 임플랜트의 본체 내에 있는 공동, 및 상기 공동 내에 있는 임플랜트 코어를 포함하는 눈물 임플랜트를 제공하는 단계를 포함하며, 상기 공동은, 상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되고, 상기 임플랜트 코어는, 제제를 지속적으로 릴리스하도록 하는 사이즈로 구성되며, 상기 임플랜트 코어는 전기 전도성 재료를 포함하는, 면모 89 내지 면모 91 중 어느 하나에 따른 방법.
93. 선택적으로 상기 제제를 수용하기 위해 상기 임플랜트 코어에 시드를 제공하는 단계, 및 상기 전기 전도성 재료를 상기 시드 내에 제공하는 단계를 포함하는, 면모 89 내지 면모 92 중 어느 하나에 따른 방법.
94. 눈의 질환을 치료하는 방법은, 눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계, 및 감지 회로에 대한 상기 눈물 임플랜트의 근접으로 인한 상기 감지 회로의 특성 임피던스의 변화를 검출함으로써, 상기 눈물 임플랜트를 검출하는 단계를 포함한다. 상기 눈물 임플랜트는, 생체 적합성 재료의 임플랜트 본체, 눈에 제제를 지속적으로 릴리스하도록 하는 사이즈로 구성되는 임플랜트 코어, 상기 임플랜트 코어 내에 배치되는 상기 제제의 서플라이, 및 상기 임플랜트 본체 내에 있는 전기 전도성 재료를 포함하고, 상기 임플랜트 본체는, 상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되는 공동을 포함하며, 상기 임플랜트 코어는 상기 임플랜트 코어의 상기 공동 내에 지지되고, 상기 서플라이는 상기 제제를 지속적으로 릴리스하도록 구성된다.
95. 상기 제제는 선택적으로 녹내장 질병을 치료하는 제제를 포함하는, 면모 94에 따른 눈의 질환을 치료하는 방법.
96. 상기 제제는 선택적으로, 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 이상을 치료하는 제제를 포함하는, 면모 94 또는 면모 95에 따른 눈의 질환을 치료하는 방법.
97. 검출 장치는, 이미지 센서, 및 이미지 분석기 회로를 포함한다. 상기 이미지 분석기 회로는, 이미지의 다른 영역에서의 이미지 대조(contrast)를 초과하는 이미지 대조를 가진 이미지 부분의 위치를 검출하여, 눈물 임플랜트의 일부의 이미지가 상기 이미지 내에 있는지에 대한 표시를 제공한다.
98. 상기 이미지 센서는, 카메라 내에 포함되어 있는 디지털 이미지 센서인, 면모 97에 따른 검출 장치.
99. 상기 검출 장치는 선택적으로 적외선 발광기를 더 포함하며, 상기 이미지 센서는 적외선 이미지 센서를 포함하는, 면모 97 또는 면모 98에 따른 검출 장치.
100. 눈의 질환을 치료하는 방법은, 눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계, 대상물의 상기 눈물점의 영역의 이미지를 얻는 단계, 및 상기 이미지의 다른 영역에서의 이미지 대조를 초과하는 이미지 대조를 가진 상기 이미지 부분의 위치를 검출함으로써, 상기 눈물 임플랜트를 검출하는 단계를 포함한다. 상기 눈물 임플랜트는, 생체 적합성 재료의 임플랜트 본체, 눈에 제제를 지속적으로 릴리스하도록 하는 사이즈로 구성되는 임플랜트 코어, 및 상기 임플랜트 코어 내에 배치되는 상기 제제의 서플라이를 포함하고, 상기 임플랜트 본체는, 상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되는 공동을 포함하며, 상기 임플랜트 본체의 상기 공동은 상기 임플랜트 코어를 수용하도록 하는 사이즈 및 형상을 가지고, 상기 임플랜트 코어는, 눈의 영역으로부터 상기 눈물 임플랜트를 구별하도록 구성되는 광학 대조 재료를 포함하며, 상기 서플라이는 상기 제제를 지속적으로 릴리스한다.
101. 상기 제제는 선택적으로 녹내장 질병을 치료하는 제제를 포함하는, 면모 100에 따른 눈의 질환을 치료하는 방법.
102. 상기 제제는 선택적으로, 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 이상을 치료하는 제제를 포함하는, 면모 100 또는 면모 101 중 어느 하나에 따른 눈의 질환을 치료하는 방법.
본 섹션은 본 특허출원의 주제에 대한 개략을 제공하기 위한 것이다. 본 섹션은 본 발명의 배타적이거나 소모적 설명을 제공하고자 하는 것이 아니다. 상세한 설명은 본 특허출원에 관한 추가적 정보를 제공하고자 포함된다.
도 1a 및 도 1b는, 본 발명의 실시예에 따른 여러 가지 임플랜트에 사용하기에 적합한 눈의 해부학적 조직 구조를 도시한다.
도 2a는, 본 발명의 실시예에 따른, 검출제(detection agent) 및 눈을 치료하기 위한 치료 약제를 가진 코어를 가진 임플랜트의 단면도이다.
도 2b는, 도 2a의 임플랜트의 측단면도이다.
도 3a는, 눈에 사용하기 위한 눈물점 마개의 형상을 가진 임플랜트의 개략도이다.
도 3b는, 도 3a의 임플랜트의 측단면도이다.
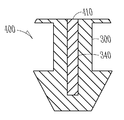
도 4는, 눈물점 마개 및 눈물점 마개 내의 검출 디바이스를 가진 임플랜트의 측단면도이다.
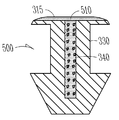
도 5는, 눈물점 마개 및 눈물점 마개 내의 검출제를 가진 임플랜트의 측단면도이다.
도 6은, 디바이스 검출 가능 눈물 임플랜트를 제조하는 방법의 실시예의 흐름도이다.
도 7a 및 도 7b는, 본 발명의 실시예에 따른, 실리콘 본체, 코어 및 유지 구조를 포함하는 임플랜트를 도시한다.
도 8a 및 도 8b는, 검출 디바이스를 내부에 가진 눈물점 마개를 포함하는 눈을 치료하기 위한 임플랜트의 다른 실시예를 도시한다.
도 9는, 디바이스 검출 가능 눈물 임플랜트를 제조하는 방법의 다른 실시예의 흐름도이다.
도 10은, 눈에 적용된 상태의 검출 디바이스를 포함하는 임플랜트를 도시한다.
도 11a 및 도 11b는, 강자성 입자 내에서 정렬하도록 자기 도메인을 유도하는 것을 설명하는 도면이다.
도 12는, 자화에 노출되었을 때 강자성 재료의 거동(behavior)을 설명하기 위해 사용되는 B-H 곡선이다.
도 13은, 임플랜트 검출 디바이스의 블럭도이다.
도 14는, 홀효과 센서로부터의 신호 출력의 실시예를 증폭하여 나타낸다.
도 15는, 임플랜트 검출 디바이스의 하우징의 실시예의 도면이다.
도 16은, 임플랜트 검출 디바이스의 하우징의 다른 실시예의 도면이다.
도 17은, 디바이스 검출 가능 눈물 임플랜트를 제조하는 방법의 또 다른 실시예의 흐름도이다.
도 18은, 임플랜트를 검출하기 위한 디바이스의 다른 실시예의 블럭도이다.
도 19는, 검출 디바이스를 사용하여 임플랜트를 검출하는 방법의 흐름도이다.
도 20은, 눈물 임플랜트의 다른 실시예를 도시한다.
도 21은, 눈물 임플랜트 코어의 시드(sheath)의 도면이다.
도 22는, 디바이스 검출 가능 눈물 임플랜트를 제조하는 방법의 또 다른 실시예의 흐름도이다.
도 23은 임플랜트 검출 디바이스의 다른 실시예의 블럭도이다.
도 24는, 눈물 임플랜트를 검출하는 방법의 다른 실시예의 흐름도이다.
도 25는, 눈물 임플랜트의 다른 실시예의 도면이다.
도 26은, 임플랜트 검출 디바이스의 다른 실시예의 블럭도이다.
도 27은, 검출 가능 임플랜트를 제조하는 방법의 또 다른 실시예의 흐름도이다.
도 28 및 도 28a는, 임플랜트 데이터를 상관짓는 임플랜트 장치, 및 무선 주파수 식별(FRID) 또는 다른 검출 구조를 사용하여 임플랜트 용도를 트랙킹하는 것을 개략적으로 도시한다.
도 29는, 본 발명의 실시예에 따른, 플루오레신(fluorescein)의 추출(elution) 및 플루오레신 추출에 대한 계면활성제(surfactant)의 효과를 도시한다.
도 30은, 본 발명의 실시예에 따른, 치료 약제 및 검출 디바이스를 가진 코어를 가진 임플랜트의 단면도이다.
도 31은, 검출 디바이스를 가지며 신체의 상태를 치료하기 위한 치료 임플랜트의 실시예를 도시한다.
도 2a는, 본 발명의 실시예에 따른, 검출제(detection agent) 및 눈을 치료하기 위한 치료 약제를 가진 코어를 가진 임플랜트의 단면도이다.
도 2b는, 도 2a의 임플랜트의 측단면도이다.
도 3a는, 눈에 사용하기 위한 눈물점 마개의 형상을 가진 임플랜트의 개략도이다.
도 3b는, 도 3a의 임플랜트의 측단면도이다.
도 4는, 눈물점 마개 및 눈물점 마개 내의 검출 디바이스를 가진 임플랜트의 측단면도이다.
도 5는, 눈물점 마개 및 눈물점 마개 내의 검출제를 가진 임플랜트의 측단면도이다.
도 6은, 디바이스 검출 가능 눈물 임플랜트를 제조하는 방법의 실시예의 흐름도이다.
도 7a 및 도 7b는, 본 발명의 실시예에 따른, 실리콘 본체, 코어 및 유지 구조를 포함하는 임플랜트를 도시한다.
도 8a 및 도 8b는, 검출 디바이스를 내부에 가진 눈물점 마개를 포함하는 눈을 치료하기 위한 임플랜트의 다른 실시예를 도시한다.
도 9는, 디바이스 검출 가능 눈물 임플랜트를 제조하는 방법의 다른 실시예의 흐름도이다.
도 10은, 눈에 적용된 상태의 검출 디바이스를 포함하는 임플랜트를 도시한다.
도 11a 및 도 11b는, 강자성 입자 내에서 정렬하도록 자기 도메인을 유도하는 것을 설명하는 도면이다.
도 12는, 자화에 노출되었을 때 강자성 재료의 거동(behavior)을 설명하기 위해 사용되는 B-H 곡선이다.
도 13은, 임플랜트 검출 디바이스의 블럭도이다.
도 14는, 홀효과 센서로부터의 신호 출력의 실시예를 증폭하여 나타낸다.
도 15는, 임플랜트 검출 디바이스의 하우징의 실시예의 도면이다.
도 16은, 임플랜트 검출 디바이스의 하우징의 다른 실시예의 도면이다.
도 17은, 디바이스 검출 가능 눈물 임플랜트를 제조하는 방법의 또 다른 실시예의 흐름도이다.
도 18은, 임플랜트를 검출하기 위한 디바이스의 다른 실시예의 블럭도이다.
도 19는, 검출 디바이스를 사용하여 임플랜트를 검출하는 방법의 흐름도이다.
도 20은, 눈물 임플랜트의 다른 실시예를 도시한다.
도 21은, 눈물 임플랜트 코어의 시드(sheath)의 도면이다.
도 22는, 디바이스 검출 가능 눈물 임플랜트를 제조하는 방법의 또 다른 실시예의 흐름도이다.
도 23은 임플랜트 검출 디바이스의 다른 실시예의 블럭도이다.
도 24는, 눈물 임플랜트를 검출하는 방법의 다른 실시예의 흐름도이다.
도 25는, 눈물 임플랜트의 다른 실시예의 도면이다.
도 26은, 임플랜트 검출 디바이스의 다른 실시예의 블럭도이다.
도 27은, 검출 가능 임플랜트를 제조하는 방법의 또 다른 실시예의 흐름도이다.
도 28 및 도 28a는, 임플랜트 데이터를 상관짓는 임플랜트 장치, 및 무선 주파수 식별(FRID) 또는 다른 검출 구조를 사용하여 임플랜트 용도를 트랙킹하는 것을 개략적으로 도시한다.
도 29는, 본 발명의 실시예에 따른, 플루오레신(fluorescein)의 추출(elution) 및 플루오레신 추출에 대한 계면활성제(surfactant)의 효과를 도시한다.
도 30은, 본 발명의 실시예에 따른, 치료 약제 및 검출 디바이스를 가진 코어를 가진 임플랜트의 단면도이다.
도 31은, 검출 디바이스를 가지며 신체의 상태를 치료하기 위한 치료 임플랜트의 실시예를 도시한다.
도 1a 및 도 1b는, 본 발명의 실시예에 따른 임플랜트에 의해 치료하기에 적합한 눈(2)의 해부학적 조직 구조를 도시한다. 눈(2)은 각막(4)과 홍채(6)를 포함한다. 공막(8)은 각막(4)과 홍채(6)를 둘러싸며 백색을 띤다. 결막층(9)은 실질적으로 투명하고 공막(8) 위에 배치된다. 결정 렌즈(5)는 눈 안에 위치된다. 망막(7)은 눈(2)의 후방 부근에 위치되고 일반적으로 빛에 민감하다. 망막(7)은, 높은 시력(visual acuity)과 색조 감각을 제공하는 와(fovea)(7F)를 포함한다. 각막(4)과 렌즈(5)는 빛을 반사하여 와(7F)와 망막(7)에 이미지를 형성한다. 각막(4)과 렌즈(5)의 광학 파워(optical power)는 와(7F)와 망막(7)에 이미지를 형성하는 데에 기여한다. 각막(4), 렌즈(5), 및 와(7F)의 상대적 위치는 또한 이미지 품질에 중요하다. 예를 들면, 각막(4)으로부터 망막(7F)까지의 눈(2)의 축방향 길이가 길면, 눈(2)은 근시일 수 있다. 또한, 조절 작용 동안에, 렌즈(5)는, 눈에 인접한 물체의 양호한 근거리 시력을 제공하도록 각막(4)을 향해 이동된다.
도 1a에 도시된 해부학적 조직 구조는 또한 눈물 장치를 포함하며, 눈물 장치는 상부 소관(canaliculus)(10), 하부 소관(12), 및 비루관 또는 주머니(naso-lacrimal duct or sac)(14)를 포함하고, 상부 소관(10)과 하부 소관(12)은 집합적으로 소관(canaliculae)이라 한다. 상부 및 하부 소관은 눈물점 애퍼처라고도 지칭되는 상부 눈물점(11) 및 하부 눈물점(13)으로 종료된다. 눈물점 애퍼처는, 중간 안각(17) 근처의 모양체의(ciliary) 및 눈물의 부분들의 접합점에서 눈꺼풀 가장자리의 중간 단부에서 약간 떨어져 위치된다. 눈물점 애퍼처는, 조직의 연결 링에 의해 둘러싸인 둥글거나 약간 계란형의 개구이다. 각각의 눈물점 개구(11, 13)는, 눈물 주머니(14)의 입구에 있는 소관과 결합되기 위해 수평으로 회전되기 전에, 각각의 소관의 수직부(10a, 12a)에 이르른다. 소관은 관형이며, 소관이 팽창될 수 있게 하는 탄성 조직에 의해 둘러싸인 층 모양의 비늘 모양의 상피에 의해 피복된다.
상술한 실시예에서, 임플랜트는 검출 디바이스 또는 검출 가능 디바이스를 가지거나 포함하는 것으로 설명된다. 검출 디바이스는 물리적 디바이스, 신호 전달 표면 또는 재료, 임플랜트에 첨가되는 컴포넌트, 검출제(detection agent)일 수 있거나, 제조 동안에 임플랜트에 특정 검출 가능 성질을 주기도록 임플랜트에 첨가되는 물질 또는 화학약제일 수 있다. 예를 들면, 검출 디바이스는, 임플랜트의 표면으로부터 추출(elution)되는 검출제일 수 있다. 다른 예에서, 검출 디바이스는 검출 신호 전달 표면 또는 재료를 포함할 수 있다. 몇몇 실시예에서, 전달 표면 또는 재료는 또한, 빛을 반사할 수 있는 거울 부분을 포함할 수 있다. 몇몇 실시예에서, 임플랜트의 형상은 검출을 보조할 수 있는데, 예를 들면 임플랜트는 공동의 형상을 변경할 수 있고, 임플랜트의 위치를 판정하기 위해 형상을 보도록 초음파가 사용될 수 있다.
검출 디바이스는 단지 임플랜트의 존재 여부를 검출하는 데에만 사용될 수 있는 것이 아니고, 검출 디바이스는 또한 임플랜트의 특성, 면모 또는 속성을 검출 또는 식별할 수 있는 식별 디바이스일 수 있다는 것을 이해하여야 한다. 임플랜트의 식별에는, 임플랜트의 형태에 대한 정보, 치료 약제의 포함여부, 치료 약제의 형태 등이 포함된다. 몇몇 실시예에서, 임플랜트는, 검출 및/또는 식별 리더에 의해 판독 및/또는 기록될 수 있으며 정보가 기록된 메모리 디바이스 또는 칩을 포함할 수 있다. 정보는, 선택적으로 임플랜트를 삽입하기 위해 사용되는 툴의 데이터 기록 구조를 사용하여, 임플랜트 제조 동안에 또는 이식될 때 기록될 수 있다. 그러한 정보에, 임플랜트 제조자, 임플랜트 제조자의 제조 번호, 임플랜트 내의 약제 또는 안구(ocular) 제제(agent) 형태, 약제의 양 또는 선량(dose), 유효 일자, 이식 일자, 약제의 릴리스가 완료된 때에 관한 표시, 이식 의사, 임플랜트가 이식된 장소의 표시, 환자 성명, 또는 환자를 식별하기 위한 다른 표시, 또는 임플랜트의 검출 또는 식별을 보조하는 다른 정보가 포함될 수 있다. 예시적 장치는, 적어도 임플랜트 제조 번호, 임플랜트 내에 포함된 활성(active) 약제, 및 임플랜트의 전체 약제의 양의 판정을 편리하게 할 것이다. 임플랜트는 또한 식별을 위한 재료를 추출하거나, 임플랜트에 관한 정보를 제공하기 위해 칼라를 변경시키고 및/또는 칼라를 소실시킬 수 있는 생물 부식성(bio-erodable) 표면을 포함할 수 있다. 다른 실시예에서, 전달 표면 또는 재료는, 임플랜트가 제거 또는 변경되어야 할 때와 같은 임플랜트에 대한 정보를 제공하기 위해, 팝-업(pop-up) 부분를 가진 것과 같이 형상을 변경할 수 있다.
도 2a는, 본 발명의 실시예에 따른, 검출 디바이스를 가진 눈을 치료하기 위한 임플랜트(200)의 평면 단면도이다. 임플랜트(200)는, 인접 단부(212)와 말단 단부(214)를 가지며 내부에 검출제를 가진 코어(210)를 포함한다. 도시된 실시예에서, 코어(210)는 또한 하나 이상의 치료 약제를 포함한다. 코어(210)는, 검출제의 제1 봉입체(260) 및 치료 약제의 제2 봉입체(265)를 포함하는 매트릭스(270)를 포함한다. 제1 봉입체(260)와 제2 봉입체(265)는 농축된 형태의 제제(agent), 예를 들면 액상 또는 고상 제제를 포함할 수 있고, 제제는 시간이 지나면 코어(210)의 매트릭스(270) 내로 용해될 수 있다. 매트릭스(270)는 실리콘 매트릭스 등을 포함할 수 있고, 매트릭스(270) 내의 검출제와 치료 약제의 혼합물은 비균질할 수 있다. 많은 실시예에서, 비균질 혼합물은 다상 비균질 혼합물을 포함하도록, 검출제와 치료 약제로 포화되는 실리콘 매트릭스부, 및 검출제와 치료 약제의 봉입체를 포함하는 봉입부를 포함한다. 몇몇 실시예에서, 매트릭스(270)는 제1 봉입체(260)와 제2 봉입체(265)를 봉입하고, 제1 봉입체(260)와 제2 봉입체(265)는 약 1 μm 내지 약 100 μm의 크기를 가지는 미세입자를 포함할 수 있다. 검출제와 치료 약제가 코어로부터 릴리스되는 동안에, 매트릭스(270)가 검출제와 치료 약제로 실질적으로 포화되도록, 봉입된 봉입체는, 둘러싸는 고체 매트릭스, 예를 들면 미세입자를 봉입하는 실리콘으로 용해된다.
코어(210)는 그 외경과 말단 단부(214)에서 시드 본체(220)의 채널 내에 들어맞는다. 시드 본체(220)는 검출제와 치료 약제에 대해 실질적으로 비투과성이어서, 검출제와 치료 약제는, 시드 본체(220)로 덮이지 않는 코어(210)의 인접 단부(212) 상의 노출된 표면으로부터 릴리스된다.
임플랜트(200)에, 이식을 위한 다른 부재 또는 구조물이 합체될 수 있다(임플랜트가 눈물점 마개와 결합된 도 5를 참조). 도 2a에 도시된 실시예에서, 유지 부재(230)는, 상술한 바와 같이, 중공 조직 구조 예를 들면 소관의 눈물점 내에 임플랜트(200)를 유지하도록 코어(210)와 시드 본체(220)에 연결될 수 있다.
폐쇄 부재(240)는 유지 부재(230) 상에 또는 그 주위에 배치될 수 있다. 폐쇄 부재(240)는 눈물 흐름에 대해 비투과성이고, 중공 조직 구조를 폐쇄시키며, 또한 더욱 유연한(benign) 조직 결합 표면을 제공함으로써 조직 구조의 조직을 유지 부재(230)로부터 보호하는 작용을 할 수 있다. 시드 본체(220)는, 시드 본체(220)와 코어(210)를 유지하기 위해 유지 부재(230)에 연결되는 시드 본체부(250)를 포함한다. 시드 본체부(250)는, 시드 본체(220)와 코어(210)의 이동을 제한하기 위해 멈춤부를 포함할 수 있다. 시드 본체부(250)는 또한 용이한 삽입을 위한 형상(250B)을 가질 수 있다.
도 2b는 도 2a의 임플랜트(200)의 측단면도이다. 임플랜트(200)는 원통형이며, 중심에 코어(210)를 가진 원형 단면으로 도시되었다. 시드 본체(220)는, 코어(210) 상에 배치되는 환형부를 포함한다. 도시된 실시예에서, 유지 부재(230)는, 유지 부재의 단부 근처에서 함께 연결되는 여러 개의 길이방향 스트럿(strut)을 포함한다. 길이방향 스트럿이 도시되었지만, 원주 방향 스트럿도 사용될 수 있다. 폐쇄 부재(240)는 유지 부재(230)의 길이방향 스트럿에 의해 지지되며 길이방향 스트럿 위에 배치되고, 반경 방향으로 팽창 가능한 막 등을 포함할 수 있다. 스트럿은 또한 임플랜트를 위한 검출 디바이스로서 사용될 수 있다.
유지 부재(230)는, 임플랜트가 필요한 조직 위치 예를 들면 눈물점 또는 소관 내에 용이하게 위치될 수 있도록 하는 사이즈 및 형상을 가진 적절한 재료를 포함한다. 유지 부재는 기계식으로 배치될 수 있고, 예를 들면 유지 부재가 NitinolTM과 같은 초탄성 형상 기억 합금을 포함함으로써, 유지 부재는 통상적으로 바람직한 단면 형상으로 팽창된다. 필요한 팽창을 제공하기 위해, NitinolTM 외의 다른 재료, 예를 들면 탄성 금속 또는 중합체, 소성 변형성 금속 또는 중합체, 형상 기억 중합체 등, 예를 들면 스프링 스테인레스 스틸, Eligloy®, 탄탈, 티탄, 코발트 크롬이 사용될 수 있다. 유지 부재는, 필요한 치료 시간, 및 환자가 의사의 접촉(follow-up)을 필요로 하는가에 따라 생물 분해성 또는 비 생물 분해성일 수 있다. 이러한 팽창 능력은, 임플랜트가 여러 가지 사이즈의 중공 조직 구조, 예를 들면 0.3mm 내지 1.2mm의 소관에 맞게 한다(즉, 하나의 사이즈로 모든 것에 맞음). 단일 유지 부재가 0.3mm 내지 1.2mm의 소관에 맞도록 만들어질 수 있더라도, 복수의 교대로 선택될 수 있는 유지 부재가 필요시에 이러한 범위에 맞도록 사용될 수 있는데, 예를 들면 제1 유지 부재는 0.3 내지 0.9mm의 소관을 위한 것이고, 제2 유지 부재는 0.9 내지 1.2m의 소관을 위한 것이다. 유지 부재는, 소관의 눈물점 근처에 위치되는 유지 부재에 대해서는 유지 부재가 약 3mm의 길이만큼 부착되는 해부학적 구조에 적합한 길이를 가진다.
시드 본체(220) 및 코어(210)가 상술한 바와 같이 유지 부재(230)의 일단부에 부착되더라도, 많은 실시예에서, 유지 부재의 다른 단부는 코어 및 시드 본체에 부착되지 않아, 유지 부재는 패창하는 동안에 시드 본체 및 코어 위에서 미끄러질 수 있다. 유지 부재가 필요한 단면 폭을 갖도록 폭 방향으로 팽창될 때 유지 부재는 길이가 통상적으로 수축될 것이기 때문에, 일단부 상에서의 이러한 미끄러지는 능력이 바람직하다. 또한, 상기 디바이스의 코어는, 정위치에 유지되는 시드 본체로 대치될 수 있다. 또는, 시드 본체는 상기 디바이스에 치료 약제를 보충하기 위해 코어를 교환하도록 유지 부재 내에 재위치될 수 있다.
폐쇄 부재(240)는, 임플랜트가 적어도 중공 조직 구조를 통한 유체의 흐름 예를 들면 소관을 통한 눈물 유체의 흐름을 방지 내지는 막을 수 있도록 하는 사이즈 및 형상을 가진 적절한 재료를 포함한다. 도시된 폐쇄 부재는, 유지 부재에 의해 팽창 및 수축될 수 있는 생체 적합성 재료 예를 들면 실리콘의 얇은 벽 막이다. 폐쇄 부재는, 유지 부재의 단부 위에서 미끄러지고 상술한 바와 같이 유지 부재의 일단부에 고정되는 재료의 별도의 얇은 튜브로서 형성된다. 또는, 폐쇄 부재는, 생체 적합성 중합체 예를 들면 실리콘 중합체 내에 유지 부재를 침지(dip) 코팅함으로써 형성될 수 있다. 폐쇄 부재의 두께는 약 0.03mm 내지 약 0.15mm, 자주 약 0.05mm 내지 약 0.1mm의 범위에 있을 수 있다.
상기 실시예가 검출제와 함께 치료 약제를 사용하는 것으로 설명되었지만, 임플랜트(200)는 치료 약제 없이 사용될 수 있거나, 2개 이상의 검출제가 조합으로 사용될 수도 있다고 생각된다.
상술한 임플랜트 코어는, 검출제 및 치료 약제를 지속적으로 릴리스하기 위해 검출 및 치료 제제와 재료를 포함한다. 검출제 및 치료 약제는 코어로부터 목표 조직 예를 들면 눈의 조직으로 이동된다. 몇몇 실시예에서, 치료 약제는, 눈의 조직을 관통할 수 있는 소수성 화합물 예를 들면 라타노프로스트(latanoprost)를 포함할 수 있고, 검출제는, 수용성 화합물, 예를 들면 안구 조직을 제한적으로 관통하면서 검출하기 위해 코어로부터 눈의 앞면으로 추출될 수 있는 플루오레신(fluorescein)을 포함할 수 있다. 검출제 및 치료 약제는 선택적으로 매트릭스 내에서 약간만 용해될 수 있어, 릴리스 레이트(release rate)는, 매트릭스 내에 분해되어 코어의 노출 표면으로부터 릴리스하기 위해 이용될 수 있을 때, 검출제 및 치료 약제의 릴리스의 수명 동안 "영(zero order)"으로 유지된다. 검출제 및 치료 약제가 코어의 노출 표면으로부터 눈물 또는 눈물 필름으로 확산될 때, 코어로부터 눈물 또는 눈물 필름으로의 이동의 레이트는, 매트릭스 내에 분해되는 검출제 및 치료 약제의 농도에 관련된다. 몇몇 실시예에서, 코어 내에 분해되는 검출제 및 치료 약제는 바람직한 레이트로 릴리스되도록 제어될 수 있다. 몇몇 실시예에서, 검출제의 릴리스의 바람직한 레이트는 치료 약제의 릴리스의 바람직한 레이트와 동일할 수 있다. 몇몇 실시예에서, 검출제의 릴리스의 바람직한 레이트는 치료 약제의 릴리스의 바람직한 레이트와 다를 수 있다. 코어 내에 포함되는 검출제 및 치료 약제는, 액상, 고상, 고체 겔, 고체 결정, 고체 무정형, 고체 입자 및/또는 분해된 형태의 검출제 및 치료 약제를 포함할 수 있다. 몇몇 실시예에서, 코어는, 검출제 및 치료 약제를 포함하는 실리콘 매트릭스를 포함한다.
코어는, 검출제 및 치료 약제를 지속적으로 릴리스할 수 있는 임의의 생체 적합성 재료로부터 이루어질 수 있다. 분해되는 제제의 입자가 내부에 위치되는 실질적으로 비-생물 분해성 실리콘 매트릭스를 가진 매트릭스를 포함하는 실시예에 대해 코어가 상술되었지만, 코어는, 검출제 및 치료 약제 예를 들면 생물 분해성 매트릭스, 다공성 코어, 액체 코어, 및 고체 코어를 지속적으로 릴리스하는 임의의 구조를 포함할 수 있다. 상기 구조가 눈에 삽입된 후에, 상기 구조는 약 1개월로부터 약 12개월까지의 기간에 걸쳐 검출제 및 치료 약제를 치료량으로 릴리스할 수 있다. 몇몇 실시예에서, 검출제 및 치료 약제의 릴리스 레이트는 동일하거나 유사할 수 있다. 다른 실시예에서, 검출제 및 치료 약제의 릴리스 레이트는 다를 수 있고, 치료 약제는 검출제보다 높거나 낮은 레이트로 릴리스된다. 몇몇 실시예에서, 검출제는 치료 약제가 완료되었을 때에만 릴리스된다.
몇몇 실시예에서, 검출제 및 치료 약제는 별개의 코어를 가질 수 있고, 제1 코어는 다 없어질 때까지 치료 약제를 릴리스할 수 있고, 임플랜트가 교체될 필요가 있다는 것을 환자가 알 수 있게 하기 위해, 다음에 제2 코어가 검출제를 릴리스한다. 특정한 실시예에서, 제2 코어는, 제1 코어가 교체될 필요가 있을 때 염료(dye)를 벗기고 릴리스하기 위해 부식성 재료가 부식되도록, 제2 코어는 생물 분해성 재료를 염료 위에 포함할 수 있다. 릴리스된 염료는 이식 후에 필요한 간격으로 환자에게 보여질 수 있다. 특정한 실시예에서, 예를 들면 염료 위의 부식성 재료의 의도된 부식 시간에 의해 결정되는, 임플랜트의 이식후 약 3개월 뒤에, 환자는 슬픈 눈으로 깨어나, 코어가 교체될 필요가 있음을 알고, 치료 의사를 접촉할 수 있다.
도 3a 및 도 3b는, 눈물점 마개(300)와 관련되는 검출 디바이스를 포함하는 임플랜트에 사용하기 위한 눈물점 마개(300) 모양의 눈물 삽입체의 일실시예를 개략 도시하고 있다. 검출 디바이스는, 마개(300)의 속성을 식별하기 위해 사용되는 임의의 디바이스를 포함한다. 몇몇 실시예에서, 속성은 마개의 사이즈, 형상 또는 조성과 같은 마개의 물리적 특성을 포함할 수 있다. 다른 실시예에서, 속성은, 마개가 이식되었을 때 일련 번호를 추적하는 타입과 같은 마개에 관한 정보, 및 마개에 관련되는 다른 정보를 포함할 수 있다.
눈물점 마개의 몇몇 실시예는 마개를 구별하기 위해 여러 가지 칼라를 사용한다. 눈물점 마개는, 눈물점 마개에 적용되는 칼라 코팅과 같은 칼라 재료로 형성될 수 있거나 칼라가 첨가될 수 있다. 다른 실시예에서, 색을 띤 코어가 마개의 채널 내에 삽입될 수 있고, 색을 띤 코어는 눈물점 마개와 다른 색을 가지거나, 눈물점 마개(300)의 물리적 특성, 면모 또는 속성을 식별하는 여러 가지 칼라를 가진다. 눈물점 마개 및/또는 코어의 여러 가지 칼라는 또한, 눈물점 마개가 아래에서 논의되는 약제 공급 임플랜트를 위해 사용될 때, 눈물점 마개와 관련되는 여러 가지 치료 약제를 식별하기 위해 사용될 수 있다. 칼라는 또한, 치료 약제의 여러 가지 화합물, 선량 또는 릴리스 레이트를 식별할 수 있다. 특정 실시예에서, 적색 마개는 녹내장 치료에 대응하고, 녹색 마개는 항생물질 치료에 대응하며, 청색 마개는 알레르기 치료에 대응한다. 필요한 칼라를 제공하기 위해 많은 염료가 사용될 수 있지만, 여러 가지 방출 파장을 자극하기 위해 단일 여기(excitation) 파장이 사용될 수 있고, 예를 들면 적색, 오렌지색, 황색 및 적색 방출을 자극하기 위해 청색이 사용될 수 있도록, 몇몇 실시예는, 양자 돗트(quantum dots)를 사용하는 스펙트럼 엔코딩을 사용할 수 있다. 몇몇 실시예에서, 검출 디바이스는 추출 가능 재료이다. 눈물점 마개의 속성은 재료가 눈 안으로 추출될 때 식별된다.
몇몇 실시예에서, 검출 디바이스는, 밴드 또는 링 또는 눈물점 마개 내의 금속 또는 탄소 분말과 같은, 눈물점 마개에 부착되는 금속편을 포함할 수 있다. 또한, 검출 디바이스는 눈물점 마개의 채널 내에 삽입되거나 눈물점 마개 내에 형성될 수 있다.
눈물점 마개(300)는, 눈물점(11, 13)(도 1a 참조)의 외부에 놓이는 인접 단부에 있는 칼라렛(collarette)(310), 소관(10, 12)(조 1a 참조) 내로 막기 위해 돌출하는 말단 단부에 있는 팁(335)에서 종료되는 테이퍼부(325)를 가진 벌브(320), 및 칼라렛(310)과 벌브(320)를 연결하는 본체부(330)를 포함한다. 눈물점 마개(300)는 길이가 약 2.0mm이다. 벌브(320)는, 눈물점 마개(300)가 소관(10, 12)으로부터 용이하게 분리되는 것을 방지하도록 디자인되고, 눈물점(11, 13) 내로의 용이한 삽입을 위해 테이퍼질 수 있다. 칼라렛(310)은, 눈물점 마개(300)가 소관(10, 12) 내로 완전히 들어가는 것을 방지하는 직경을 갖도록 디자인되며, 바람직하게 눈(2)의 성가심을 최소화하도록 매끄럽다. 눈물점 마개(300)의 마개 본체부(330)는 기본적으로, 칼라렛(310)과 벌브(320) 부분 사이의 비-기능적 연결부이다. 칼라렛(310)은, 검출 디바이스가 위치되는 본체부(330) 내로 연장되는 공동(340) 또는 채널을 포함한다. 공동(340)의 사이즈 및 형상은 디바이스를 정위치에 유지하도록 선택된다. 다른 실시예에서, 디바이스는 눈물점 마개 내에 개방되는 통상적 공동에 맞는 사이즈를 가진다. 몇몇 실시예에서, 검출 디바이스는 본체 내에 성형된다. 예시적 검출 디바이스는, 무선 주파수 식별자(RFID) 디바이스, 자성 또는 강자성 디바이스, 초음파 디바이스, 자외선 디바이스, 적외선 디바이스, 검출제, 형광 재료, 전기 전도성 재료, 및 식별제를 포함한다. 몇몇 실시예에서, 검출 디바이스는 가시성이다. 몇몇 실시예에서, 검출 디바이스는 별도의 검출 디바이스로 검출될 수 있다.
몇몇 실시예에서, 눈물점 마개(300)의 팁(335)은 폐쇄되고, 다른 실시예에서는, 말단 단부에 있는 팁(335) 내의 개구(350)는 공동(340) 내로의 액세스를 가능하게 하여, 눈물점 마개(300)를 통한 유체 흐름을 가능하게 한다(예를 들면, 도 7b 참조). 본체(310)는 생체 적합성인 실리콘과 같은 가요성 재료로부터 성형되거나 다르게 형성될 수 있다. 선택된 재료는 또한 공동(340) 내에 위치되는 검출제에 대해 투과성 또는 비투과성일 수 있다.
몇몇 실시예에서, 선택적 헤드 구조(315)(도 5 참조)는 공동(340)을 둘러싸도록 칼라렛(310) 위에 구비된다. 몇몇 실시예에서, 헤드 구조(315)는 본체와 동일한 재료로 이루어진다. 몇몇 실시예에서, 헤드 구조는, 공동(340) 내에 위치될 수 있는 임의의 검출제에 대해 투과성인 생체 적합성 재료, 바람직하게 부드러운 가요성 재료로 이루어진다. 몇몇 실시예에서, 눈물점 마개(300)가 정위치에 있을 때, 검출제는, 검출제가 눈물과 혼합되어 제제의 검출을 가능하게 하는 눈물못의 눈물 내로 공동(340)으로부터 헤드 구조를 통해 전개될 수 있다.
도 4는, 눈물점 마개(300)를 가지는 눈물 임플랜트(400)의 일실시예를 개략 도시하고 있다. 눈물점 마개(300)는 눈물점 내로 적어도 부분적으로 삽입될 수 있다. 눈물점 마개는, 마개 코어를 수용하는 사이즈 및 형상을 가진 공동(340)을 가진 마개 본체를 포함한다. 몇몇 실시예에서, 마개 코어는 검출 디바이스(410)를 포함한다. 몇몇 실시예에서, 마개 코어는 검출 디바이스(410) 및 지속적 릴리스 치료 약제를 포함한다. 도시된 실시예에서, 검출 디바이스(410)는 눈물점 마개(300)의 공동(340) 내에 위치된다. 검출 디바이스(410)는, 눈물점 애퍼처 내에 위치되었을 때 별도의 검출 디바이스에 의해 임플랜트(400)의 자동 검출 및/또는 식별을 보조하는 임의의 디바이스일 수 있다. 몇몇 실시예에서, 검출 디바이스(410)는, 검출 신호 전달 표면 또는 재료일 수 있고, 전달 표면 또는 재료로부터 오는 신호는, 전달 표면 또는 재료가 눈물점 내에서 희미할 때 임플랜트 본체의 검출을 가능하게 한다. 몇몇 실시예에서, 검출 디바이스(410)는 임플랜트의 복수의 다른 속성으로부터 임플랜트의 한 가지 속성을 식별한다. 일실시예에서, 전달 표면 또는 재료는, RFID 검출기에 의해 검출할 수 있는 RFID 칩의 무선 신호 전달 표면을 포함하며, 신호는 무선 신호 식별 신호를 포함한다. 다른 실시예에서, 신호 전달 표면 또는 재료는, 자기 검출기에 의해 검출할 수 있는 자기 신호 전달 표면 또는 재료, 또는 초음파 검출기에 의해 검출할 수 있는 초음파 반사 재료의 반향 표면을 포함한다.
RFID는 매우 작은 사이즈로 만들어질 수 있다. 예를 들면, 히타치는 0.4mm × 0.4mm인 "μ-칩"을 개발했고, 현재는 0.05mm × 0.05mm만큼 작은 RFID 칩을 개발하고 있다. 도 4에 도시된 실시예에서, RFID는 눈물점 마개의 채널 내로 삽입될 수 있다. 채널의 사이즈 및 형상은, 선택된 RFID 칩을 예를 들면 접착제 또는 마찰 끼워 맞춤에 의해 정위치에 유지는 사이즈를 가져야 한다. 다른 실시예에서, RFID는 마개 제조 동안에 눈물점 마개 내에 합체될 수 있고, 예를 들면, RFID 칩은 마개 내에 성형될 수 있다(예를 들면 도 7a를 참조). RFID 눈물점이 정위치에 있으면, RFID 눈물점 마개의 존재를 판정하기 위해, 가청 신호를 전달할 수 있는 RFID 검출 장치가 사용될 수 있거나, RFID 눈물점을 나타내기 위해 빛이 비추어질 수 있다. 다른 실시예에서, RFID 디바이스는 또한 임플랜트의 다른 특성을 전달할 수 있다. 환자가 검출 장치를 사용하고 있으면, 환자는 신호를 셀폰 또는 인터넷 연결을 통해 의사에게 전달할 수 있다.
강자성 재료가 또한 눈물 임플랜트 내의 검출 디바이스(410)로서 사용될 수 있다. 강자성 재료는, 자기 검출 장치에 의해 검출할 수 있는 임의의 재료를 포함한다. 몇몇 실시예에서, 강자성 재료는 검출 디바이스에 의해 검출할 수 있는 강자성 성질(예를 들면, 자계)을 유지한다. 검출 디바이스는, 성질이 검출되었을 때 빛 또는 소리를 발생할 수 있다. 강자성 재료의 예는, 마그네타이트, 금속 분말, 금속 링, 탄소 분말을 포함한다.
초음파 재료가 또한 눈물 임플랜트 내의 검출 디바이스(410)로서 사용될 수 있다. 초음파 재료는, 초음파 검출 장치에 의해 검출할 수 있는 임의의 초음파 반사 재료를 포함한다. 초음파 재료는, 검출 디바이스에 결합되었을 때(예를 들면, 결합 매체를 사용하여 마개 상에 위치됨) 신호(가시성 또는 가청)를 사용자에게 전달할 마개 내에 매립되는 압전 재료일 수 있다. 몇몇 실시예에서, 초음파 재료는 검출 디바이스에 의한 검출을 위해 입사 초음파 에너지를 반사할 수 있다. 몇몇 실시예에서, 초음파 반사 재료는 눈물 임플랜트에 초음파 에너지를 적용할 때 마개 본체가 형상을 변경하게 한다.
발광 재료는 검출 디바이스(410)로서 사용될 수 있다. 눈물점 마개(300)의 발광(예를 들면 양자 돗트)은 광원에 의해 자극된다. 발광은, 고파워/저파장 형태의 빛을 흡수하고, 입사광을 방출되거나 반사되는 저파워/고파장 형태의 빛으로 변환시킨다. 눈물 임플랜트(300)는, 예상되는 고파장 형태의 빛이 검출 디바이스에의해 검출될 때 검출된다.
전기 전도성 재료는 검출 디바이스(410)로서 사용될 수 있다. 몇몇 실시예에서, 검출 디바이스는 감지 회로를 포함한다. 눈물 임플랜트(300)를 검출하기 위해, 검출기는 눈물점 근처에 위치된다. 검출 디바이스(410)의 전기 전도성 재료는, 눈물점 마개가 감지 회로에 인접함으로 인해 감지 회로의 특성 임피던스를 변경시킨다.
도 5는, 눈물점 마개(500) 및 검출제를 가진 코어와 같은 검출 디바이스(510)를 가진 눈물 임플랜트의 일실시예를 개략 도시하고 있다. 도시된 실시예에서, 검출 디바이스(510)는 눈물점 마개(500)의 채널(340) 내에 위치된다. 검출 디바이스(510)는 눈물점 애퍼처(punctal apperture) 내에 위치될 때 임플랜트(500)의 검출 및/또는 식별을 보조하는 임의의 디바이스 또는 재료일 수 있다. 적절한 검출 디바이스의 예에, 자외선(UV) 광원으로 볼 수 있는 재료, 적외선 광원으로 볼 수 있는 재료, 가시광원으로 볼 수 있는 재료, 또는 다른 광원으로 볼 수 있는 다른 재료와 같은 검출 신호 전달 표면 또는 재료가 포함된다. 일실시예에서, 검출 신호 전달 표면 또는 재료는 플루오레신을 임플랜트로부터 추출하거나 치료 약제와 함께 공동 추출한다. 다른 실시예에서, 검출 신호 전달 표면 또는 재료는, 적외선 또는 자외선 광원을 사용하여 가시화될 수 있는 미세 돗트 또는 양자 돗트를 포함한다.
도 5에 도시된 눈물 임플랜트(500)의 실시예는, 검출제에 대해 투과성인 선택적 헤드(315)를 더 포함한다. 일실시예에서, 검출 디바이스는, 검출제와 치료 약제를 가진 코어(510)이다. 임플랜트(500)가 정위치에 있을 때, 제제들은 코어(510)의 인접 단부(212)로부터 투과성 헤드(315)를 통해 눈물못의 눈물로 전개되며, 눈물못에서 제제들은 아이 드롭(eye drops)처럼 눈물과 혼합되어 눈으로 이동되어, 눈에서 검출될 수 있다.
설명된 검출제 및/또는 치료 약제는 또한, 발명의 명칭이 "코눈물 장치를 위한 약제 공급 방법, 구조 및 조성"인 미국 출원 번호 11/695,537, 발명의 명칭이 "약제 치료를 위한 코눈물 배수 장치 임플랜트"인 미국 출원 번호 11/695,545, 발명의 명칭이 "광학적 결함을 방지하기 위한 약제 공급 임플랜트"인 미국 출원 번호 60/871,867, 발명의 명칭이 "약제 공급을 위한 임플랜트를 가진 코눈물 배수 장치"인 미국 출원 번호 60/970,709, 및 발명의 명칭이 "다중 약제 공급 장치, 및 눈물점 임플랜트와 약제의 조합"인 미국 출원 번호 60/970,820에 기술된 것과 같은 치료 약제의 공급과 조합될 수 있다.
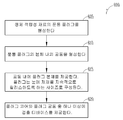
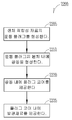
도 6은, 디바이스 검출 가능 눈물 임플랜트를 제조하는 방법(600)의 일실시예의 흐름도이다. 블럭(605)에서, 눈물점 마개 형상의 눈물 임플랜트는 생체 적합성 재료로 형성된다. 블럭(610)에서, 공동이 눈물점 마개의 본체 내에 형성된다. 블럭(615)에서, 마개 코어는 공동 내에 구비된다. 몇몇 실시예에서, 마개 코어는 환자 또는 대상물의 눈으로 제제를 지속적으로 릴리스하는 사이즈 및 형상을 가진다. 블럭(620)에서, 검출 디바이스는 마개 공동과 마개 코어 중 하나 이상에 구비된다. 검출 디바이스는 별도의 검출 디바이스를 사용하여 눈물점 마개의 자동 검출을 가능하게 한다.
디바이스 검출 가능 눈물 임플랜트는 눈 질환을 치료하는 방법에 사용될 수 있다. 눈물점 마개와 같은 눈물 임플랜트는 대상물의 하나 이상의 눈물점 내로 삽입된다. 눈물점 마개 본체는, 마개 본체의 단부로부터 마개 본체 내로 내향 연장되는 공동을 포함한다. 마개 코어는 마개 본체 내에 지지된다. 마개 코어는 제제의 서플라이(supply)를 포함하고, 코어는 제제를 눈으로 지속적으로 릴리스한다. 검출 디바이스는 별도의 검출 디바이스를 사용하여 눈물 임플랜트의 자동 검출을 가능하게 한다. 별도의 검출 디바이스를 사용하여 검출 디바이스를 검출하면, 눈물 임플랜트가 검출된다. 몇몇 실시예에서, 제제는 녹내장 질병을 치료한다. 녹내장 질병은 안구 고혈압증(ocular hypertension) 또는 1차 개방각 녹내장(primary open angle glaucoma) 중 하나 이상일 수 있다.
이제 도 7a 및 도 7b를 참조하면, 본 발명의 실시예에 따른, 눈물 임플랜트 예를 들면 눈물점 마개(700)가 도시되어 있는데, 눈물 임플랜트는, 실리콘 본체(710), 검출 디바이스(720) 및 유지 구조(730)를 포함한다. 본체(710)는, 검출 디바이스(720)를 수요하는 사이즈를 가진 인접 채널(714)을 포함한다. 본체(710)는 말단 채널(718)을 포함한다. 말단 채널(718)은 하이드로겔 막대(732)를 수용하는 사이즈를 가질 수 있다. 분리부(719)는 인접 채널을 말단 채널로부터 분리할 수 있다. 필라멘트(734)는 본체(710) 내에 매립되고, 하이드로겔 막대(732)를 본체(710)에 부착시키기 위해 하이드로겔 막대(732) 주의에 감길 수 있다. 몇몇 실시예에서, RFID "μ-칩" 또는 집적 회로가 실리콘 본체(710) 내에 위치되고, 예를 들면 분리부(719) 내에 성형될 수 있다. 몇몇 실시예에서, "μ-칩"은, 약제 코어 또는 하이드로겔 막대 중 적절한 것을 삽입하기 전에 임플랜트의 제조 동안에 채널들 중 하나에 위치될 수 있다.
일실시예에서, 검출 디바이스(720)는 코어 예를 들면 상술한 코어(210)를 포함한다. 코어 삽입체 및 코어 삽입체의 제조에 대한 설명은 미국 출원 번호 11/695,537 및 11/695,545에 기술되어 있다. 코어 삽입체가 도시되었지만, 몇몇 실시예는, 코한 명의의 미국 특허 번호 6,196,993, 프레스콧 명의의 미국 출원 번호 10/899,416, 프레스콧 명의의 미국 출원 번호 10/899,417, 애시톤 명의의 미국 출원 번호 10/762,421, 애시톤 명의의 미국 출원 번호 10/762,439, 라자르 명의의 미국 출원 번호 11/571,147, 및 오드리치 명의의 미국 출원 번호 10/825,047에 기술된 것과 같은 약제 용기, 반투과성 막, 약제 코팅 등을 포함할 수 있다.
유지 구조(730)는 하이드로겔 막대(732), 하이드로겔 코팅(736), 돌출부(712) 및 돌출부(716)를 포함할 수 있다. 하이드로겔 막대(732)는 좁은 프로파일 구성에서 눈물점을 통해 소관 루멘(lumen) 내로 삽입될 수 있다. 루멘 내로 하이드로겔 막대(732)를 삽입한 후에, 하이드로겔 코팅(736)은 넓은 프로파일 구성으로 가수화 팽창될 수 있다. 돌출부(712) 및 돌출부(716)는, 예를 들면 하이드로겔 코팅과 막대가 팽창되는 동안에 임플랜트(700)를 루멘 내에 유지할 수 있다.
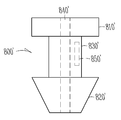
도 8a 및 도 8b는, 본 발명의 일실시예에 따른, 검출 디바이스를 합체하는 눈물점 마개를 포함하는 눈물 임플랜트(800, 800')를 도시하고 있다. 눈으로부터 눈물 유체 및/또는 약이 배수되는 것을 방지하거나 감소시키는 것이 필요한 눈의 고민(ophthalmic ailments)의 치료에서, 상부 및 하부 눈꺼풀 중 하나 또는 둘에 있는 눈물점 애퍼처는 임플랜트에 의해 막혀야 하며, 임플랜트의 2개의 각각의 실시예가 도 8a 및 도 8b에 도시되어 있다. 먼저 도 8a의 실시예를 참조하면, 임플랜트(800)는, 말단 단부에 있는 뭉툭한 팁 또는 미늘 부분(barb portion)(820), 팁보다 약간 작은 직경의 중간 목 또는 허리 부분(830), 및 인접 단부에 있으며 비교적 큰 직경의 유연한 디스크형 헤드 부분(810)을 가진다. 헤드 부분(810)에, 아래에서 설명되듯이, 삽입을 위해 조정될 때 치료 임플랜트에 릴리스 가능 그립(grip)을 제공하기 위해 삽입체 툴의 돌출 팁을 수용할 수 있는 중앙 보어 개구(840)가 구비된다. 상술한 검출 디바이스 중 어떤 것일 수 있는 검출 디바이스(850)가 마개 본체 내에 있다. 검출 디바이스(850)는 눈물점 마개의 검출을 가능하게 하고, 눈물점 마개의 속성을 식별한다.
도 8b는, 먼저 설명된 실시예와 대체로 유사한 크기를 가진 중공 눈물 임플랜트(800')를 도시하고 있는데, 눈물 임플랜트(800')는, 뭉툭한 팁 또는 미늘 부분(820'), 팁보다 약간 작은 직경의 중간 목 또는 허리 부분(830'), 비교적 큰 직경의 유연한 디스크형 헤드 부분(810'), 및 상술한 검출 디바이스 중 어떤 것일 수 있는 검출 디바이스(850')와 마개를 통해 연장되는 중앙 보어(840')를 가진다. 중앙 보어(840')는 임플랜트(800')의 인접 단부로부터 말단 단부로의 유체 흐름을 가능하게 한다.
본 발명의 몇몇 실시예에서, 여기에 설명된 검출 디바이스는, 미국 출원 공개 번호 2005/0197614에 설명된 눈물점 마개에 합체된다. 치료 임플랜트(800, 800')을 형성하기 위해 겔이 사용될 수 있고, 겔은 제1 직경으로부터 제2 직경으로 팽창될 수 있으며, 제2 직경은 제2 직경보다 약 50% 크다. 검출 디바이스를 합체시키는 것과 함께, 예를 들면 미세 다공성 구조에 치료 약제를 가두기 위해 겔이 사용될 수 있으며, 미세 다공성 구조에서, 치료 약제는 규일하게 분산되고, 겔은 치료 약제를 환자에게 서서히 추출할 수 있다. 여러 가지 치료 약제가, 발명의 명칭이 "눈물점 마개, 재료, 및 디바이스"인 미국 가출원 번호 60/550,132에 설명되어 있고, 여기에 설명된 겔 및 디바이스와 결합될 수 있다.
도 9는, 디바이스 검출 가능 눈물 임플랜트를 제조하는 방법(900)의 다른 실시예의 흐름도이다. 블럭(905)에서, 마개 본체를 가진 눈물점 마개 형상의 눈물 임플랜트는 생체 적합성 재료로 형성된다. 블럭(910)에서, 검출 디바이스는 마개 본체 내에 배치된다. 검출 디바이스는 눈물점 마개의 검출을 가능하게 하고, 눈물점 마개의 하나 이상의 속성을 식별한다. 검출 디바이스는 여기에 설명된 임의의 검출 디바이스일 수 있다.
디바이스 검출 가능 눈물 임플랜트가 눈 질병을 치료하는 방법에 사용될 수 있다. 그러한 방법에서, 눈물점 마개는 대상물의 하나 이상의 눈물점 내로 삽입된다. 눈물점 마개 내에 포함된 검출 디바이스가 검출되고, 검출 디바이스는 검출 디바이스를 통해 눈물점 마개의 하나 이상의 속성을 식별하기 위해 사용된다.
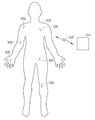
도 10은 눈에 적용된 상태의 검출 디바이스를 가진 눈물 임플랜트를 도시하고 있다. 도시된 실시예에서, 임플랜트(1000)는 눈(2)의 하부 눈물점 애퍼처(13) 내로, 애퍼처와 연통하는 소관(12)을 따라 삽입되도록 디자인된다. 임플랜트(1000)는 눈물점 마개를 포함하며, 눈물점 마개는, 인접 단부에 있는 칼라렛(1010), 말단 단부에 있는 플레어부(flared portion)(1020), 목 부분(1030), 및 검출 디바이스(1040)를 가진다. 칼라렛(1010)은 애퍼처(13)에 기대어 놓이도록 디자인된다. 검출 디바이스(1040)는, 상술한 바와 같이, 임플랜트가 바람직한 위치에 있는지, 및/또는 임플랜트가 치료 약제를 지속적으로 추출하는지를 판정할 수 있다. RFID 칩, 자성 재료, 초음파 재료, 미세돗트, 추출 검출제, 플루로레신,및 본 기술분야에 공지되어 있는 다른 것들과 같은 여려 가지 다른 검출 디바이스가 고려된다. 임플랜트(1000)는, 요구사항에 따라, 유체 흐름을 막기 위해 사용될 수 있거나, 유체 흐름을 가능하게 하는 중공 부분(예를 들면, 도 8b 참조)을 가질 수 있다.
도 10은 또한, 소관(10)으로의 눈물의 흐름을 막기 위해, 상부 툰툼 애퍼처(11) 내로 삽입된 형상이 실질적으로 원통형이며, 여기에 기술된 임플랜트(200)와 같은, 치료 약제를 가진 검출 디바이스를 포함하는 눈물 임플랜트(1000')를 도시하고 있다. 눈물 임플랜트(1000')는 또한, 여기에 설명된 임플랜트(800)와 같이, 내부에 검출 디바이스를 가진 어떤 불활성 생체 적합성 재료의 폐쇄 마개일 수 있다.
임플랜트(1000) 및 치료 임플랜트(1000')는 임의의 바람직한 조합으로, 별개도 또는 조합(도 10에 도시됨)으로 사용될 수 있다. 예를 들면, 임플랜트(1000')는 하부 소관에 위치되고, 임플랜트(1000)는 상부 소관에 위치될 수 있다. 또는, 2개의 동일한 임플랜트(1000 또는 1000')가 2개의 소관에 위치될 수 있다.
검출 디바이스는 많은 다른 방식으로 검출될 수 있다. 예를 들면, 몇몇 실시예에서, 상기 디바이스는 눈(1055)에 의해 검출되거나 볼 수 있다. 다른 실시예에서, 상기 디바이스는, 이식된 디바이스에 따라, 여러 가지 다른 검출 장치(1065)과 통신(1060)할 수 있다. 예를 들면, 검출 장치(1065)은, RFID 칩을 검출하기 위한 RFID 검출 장치, 자성 재료를 검출하기 위한 자기 검출기 장치, 초음파 반사 재료를 검출하기 위한 초음파 검출기 장치를 포함할 수 있다. 또 다른 실시예에서, 검출 디바이스는, 자외선 광원 또는 적외선 광원과 같은 다른 광원(1075)으로 검출(1070)될 수 있는 재료를 포함할 수 있다.
검출 디바이스를 포함하는 눈물 임플랜트는 눈의 질병을 치료하는 방법에 사용될 수 있다. 그러한 방법에서, 눈물점 마개와 같은 눈물 임플랜트는 대상물의 하나 이상의 눈물점 내로 삽입된다. 눈물점 마개의 본체는 여기에 설명된 검출 디바이스 중 어떤 것도 포함할 수 있다. 안구 제제의 서플라이는 눈물점 마개의 코어 내에 배치된다. 서플라이는 제제를 지속적으로 릴리스한다. 눈물 임플랜트는, 별도 검출기 디바이스를 사용하여 검출 디바이스를 검출함으로써 검출된다. 몇몇 실시예에서, 제제는 녹내장 질병을 치료하도록 구성된다. 예를 들면, 녹내장 질병은 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 이상일 수 있다.
자성 재료를 검출하기 위해, 몇몇 실시예에서, 검출 디바이스는, 눈물 임플랜트의 본체 내에 배치되는 강자성 재료를 포함한다. 강자성 재료는, 외부적으로 인가되는 자계의 제거 후에 강자성 성질을 유지한다. 어떤 실시예에서, 강자성 재료는 마그네타이트(Fe3O4)를 포함한다.
몇몇 실시예에서, 강자성 재료는 임플랜트 본체의 생체 적합성 재료 내에 배치된다. 자기 도메인은 강자성 재료의 공통한 물리적 특성이다. 임플랜트의 생체 적합성 재료 내에 성형되었을 때 강자성 재료의 자기 도메인이 정렬되도록 유도함으로써, 마개의 자계는 유도 자계의 자계에 접근한다. 그러면 눈물 임플랜트는 자계 센서에 의해 검출될 수 있다.
도 11a 및 도 11b는, 자기 도메인이 강자성 입자 내에 정렬되도록 유도하는 것을 설명하는 도면이다. 그러한 도면은 Ulaby, Fawwaz T., 엔지니어를 위한 전자기학, 146(2004)에서 발견할 수 있다. 도 11a는 자화 전의 강자성 입자(1105)를 나타낸다. 자기 도메인은 무작위로 되었다. 도 11b는, 외부 자계에 노출시킴으로써 자화한 후의 입자의 정렬된 자기 도메인을 나타낸다. 이러한 정렬은 각각의 구성 자기 도메인의 쌍극 모우멘트들 사이의 결합력으로 인한 것이다.
자화에 노출되었을 때의 강자성 재료의 거동(behavior)은 또한 도 12의 B-H 곡선을 사용하여 설명될 수 있다. 외부 인가 자계의 진폭(H)은 재료 내의 전체 자속 밀도(B)를 결정한다. 비자화 상태는 원점에서 O으로 표시된다. 곡선은, 유도 자계는 점(A1)에서 도메인의 자화가 최대 포화 Hmax 및 Bmax로 되게 하는 것을 보여준다. 외부 인가 자계의 진폭(H)이 제로로 복귀될 때, 입자의 자속 밀도의 값은 제로로 복귀하지 않고, 점(A2)에서 약간의 히스테리시스 에러(Br)에 의해 옵셋된다. 이러한 옵셋은 자주 잔여 자속 밀도라고 지칭된다. 강자성 재료, 따라서 눈물점 마개는 이제, 정렬된 상태로 유지되는 여러 개의 도메인으로 인해 영구자석과 유사하다.
도 10의 눈물 임플랜트(1000)가 눈물점 마개가고 눈물점 마개 본체 내에 약제를 포함하면, 강자성 입자 및 약제는 마개 본체 내에 배치될 수 있다. 상술한 바와 같이, 임플랜트는 외면에 시드를 포함할 수 있다. 시드의 다공성은, 약제는 마개로부터 걸러져 나오게 하고, 강자성 입자는 유지한다.
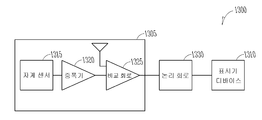
도 13은 눈물 임플랜트 검출기 디바이스(1300)의 블럭도이다. 검출기 디바이스(1300)는 이식된 눈물점 마개 또는 다른 안구 임플랜트를 검출한다. 검출기 디바이스(1300)는 자계 검출기 회로(1305)와 표시기 디바이스(1310)를 포함한다. 표시기 디바이스(1310)는 눈물 임플랜트의 자계의 검출 시에 사용자에게 또는 자동화 프로세스에 대해 표시한다. 자계 검출기 회로(1305)는 자계 센서(1315)를 포함한다. 어떤 실시예에서, 자계 센서(1315)는 홀 효과 센서이다. 어떤 실시예에서, 자계 검출기 회로(1305)는, 자계 검출기 회로(1305)로부터 출력되는 전압을 증폭하기 위한 증폭기 회로(1320)를 포함한다.
몇몇 실시예에서, 자계 검출기 회로(1305)는, 자계 검출기 회로에 통신 가능하게 결합되는 비교 회로(1325)를 포함한다. 통신 가능한 결합은, 중재 회로(예를 들면, 증폭기 회로(1320))가 있을 수 있지만 자계 센서(1315)가 비교 회로(1325)와 전기 신호를 통신할 수 있게 한다. 비교 회로(1325)는, 자계 센서(1315)의 출력에서의 전압이 제1 임계치를 초과할 때, 표시기 디바이스(1310)에 전기 신호를 공급한다. 자계 검출기 회로(1305)는, 눈물점 마개의 자계의 존재를 나타내는 비교 회로로부터의 출력에 변화를 포착하기 위해 논리 회로(예를 들면, 플립-플롭 회로 또는 래치)를 포함할 수 있다.
몇몇 실시예에서, 비교 회로(1325)는, 자계 센서(1315)의 출력에서의 전압이 제1 임계치를 초과하고 제2 임계치보다 작을 때, 표시기 디바이스(1310)에 전기 신호를 공급한다.
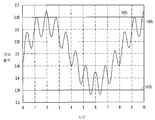
도 14는, 증폭 후의 홀 효과 센서로부터 출력되는 신호(1405)의 일예를 도시하고 있다. 비교 회로(1325)는, 신호가 제1 임계치(1410)(예에서 2.35V)를 초과하고 제2 임계치(1415)(2.65V)보다 작을 때, 표시기 디바이스(1310)에 전기 신호를 공급한다. 도 13으로 돌아가면, 검출기 디바이스(1300)는 논리 회로(1330)(예를 들면, 플립-플롭 회로 또는 래치)를 포함할 수 있다. 논리 회로(1330)는, 비교 회로(1325)로부터의 전기 신호의 상태(하이 또는 로우)를 저장한다.
몇몇 실시예에서, 표시기 디바이스(1310)는 스피커 또는 변환기를 포함한다. 표시기 디바이스(1310)는, 자계 검출기 회로(1305)가 눈물점 마개의 자계의 존재를 나타낼 때 가청 표시를 제공한다. 몇몇 실시예에서, 표시기 디바이스(1310)는, 광방출 다이오드(LED) 또는 디스플레이를 포함하며, 자계의 검출 시에 시각적 표시를 제공한다.
도 5에 도시되었듯이, 임플랜트 본체(300)는, 마개 본체(300)의 단부로부터 마개 본체 내로 내향 연장되는 공동(340)을 포함할 수 있다. 공동(340)은 임플랜트 코어(510) 또는 임플랜트 코어의 적어도 일부를 수용하는 형상 및 사이즈 를 가진다. 임플랜트 코어(510)는, 예를 들면 치료제를 눈에 공급하기 위해 지소적 릴리스 안구 제제를 포함한다. 몇몇 실시예에서, 안구 제제는 약제를 포함한다. 마개 코어(510) 내의 제제의 양은 장시간에 걸쳐 눈에 지속적으로 릴리스하기에 충분하다.
강자성 재료는 임플랜트 코어(510) 내에 배치될 수 있다. 임플랜트 코어(510)의 강자성 재료는, 외부적으로 인가되는 자계의 제거 후에 강자성 성질을 유지한다. 몇몇 실시예에서, 강자성 재료는 더 강한 자계를 제공하기 위해 임플랜트 본체와 임플랜트 코어(510) 내에 배치된다. 눈물 임플랜트(500)를 검출하는 것은, 치료제가 여전히 존재하고 임플랜트(500)에 의해 공급되고 있는지 판정하는 데에 보조할 수 있다.
몇몇 실시예에서, 자계는 임플랜트 본체(500) 내에 삽입되기 전에 임플랜트 코어(510) 내에 유도되고, 몇몇 실시예에서, 자계는 임플랜트 코어(510)가 임플랜트 본체(500) 내에 있은 후에 유도된다. 몇몇 실시예에서, 임플랜트 코어(510)의 외부 부분은 제제를 수용하기 위한 시드를 포함한다. 강자성 재료는 시드 내에 배치된다.
도 15는, 눈물 임플랜트 검출기 디바이스(1500)의 하우징(1505)의 일실시예를 도시하고 있다. 하우징(1505)은 컵의 형상이며, 대상물의 눈 위에 맞는 사이즈를 가진다. 자계 센서는, 검출기 디바이스(1500)가 눈 위에 위치될 때 눈물 임플랜트의 자계를 검출하도록 하우징(1505) 내에 배치된다. 검출기 디바이스(1500)는 2개의 LED(1510, 1512)를 포함할 수 있다. 제1 LED(1510)는, 눈물 임플랜트의 자계가 검출될 때 조명된다. 제2 LED는 자계가 검출되지 않을 때 조명된다. LED는 여러 가지 칼라일 수 있다. 예를 들면, 제1 LED(1510)는 녹색 LED일 수 있고, 제2 LED(1515)는 적색 LED일 수 있다.
도 16은, 눈물 임플랜트 검출기 디바이스(1600)의 하우징(1605)의 다른 실시예를 도시하고 있다. 이러한 하우징(1605)은 기다라며, 인접 단부(1625) 근처에 배치된다. 이것은 눈물 임플랜트 검출기 디바이스(1600)가 손 안에 유지되고 원드(wand)로서 사용될 수 있게 한다. LED(1610, 1612)는, 원드가 눈 근처에 유지되는 동안에 눈물 임플랜트가 검출되었는지를 나타내는 시각적 표시를 사용자가 볼 수 있게 하기 위해, 자계 센서(1615)로부터 말단 방향에 있는 지점에 위치된다.
도 17은, 디바이스 검출 가능 눈물 임플랜트의 제조 방법(1700)의 흐름도이다. 블럭(1705)에서, 눈물점 마개와 같은 눈물 임플랜트는 생체 적합성 재료로 형성된다. 블럭(1710)에서, 강자성 재료는 눈물점 마개 내에 구비된다. 어떤 실시예에서, 강자성 재료는 생체 적합성 재료 내에 배치된다. 어떤 실시예에서, 강자성 재료는 눈물점 마개의 본체 내에 형성되는 공동 내의 임플랜트 코어 내에 구비된다. 어떤 실시예에서, 임플랜트 코어는 안구 제제를 수용하기 위한 시드를 포함하고, 강자성 재료는 시드 내에 포함된다. 어떤 실시예에서, 강자성 재료는 마개 본체의 생체 적합성 재료 및 마개 코어 내에 구비된다. 블럭(1715)에서, 눈물점 마개는, 눈물 임플랜트가 더 이상 자계에 노출되지 않을 때 강자성 성질을 보이도록, 자계에 노출된다.
디바이스 검출 가능 눈물 임플랜트는 눈의 질병을 치료하는 방법에 사용될 수 있다. 그러한 방법에서, 강자성 재료를 가진 눈물 임플랜트가 대상물의 하나 이상의 눈물점 내에 삽입된다. 치료 약제의 서플라이는 제제를 지속적으로 릴리스하기 위해 임플랜트 코어 내에 배치된다. 어떤 실시예에서, 제제는, 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 또는 둘과 같은 녹내장을 치료하기 위해 사용된다. 삽입되는 눈물 임플랜트의 강자성 성질은 눈물 임플랜트 검출기 디바이스에 의해 검출된다.
검출기 디바이스가 전기 전도성 재료를 포함하면, 눈물 임플랜트 검출을 위해 임피던스 센싱이 사용될 수 있다. 전기 전도성 재료의 예에는, 무엇보다도, 강철, 은, 알루미늄 및 금이 포함된다. 전기 전도성 재료는 생체 적합성 재료 내의 입자로서 구비될 수 있다.
눈물 임플랜트가 눈물점 마개 본체 내에 제제를 포함하면, 전기 전도성 재료의 입자와 제제가 마개 본체 내에 배치될 수 있다. 눈물 임플랜트는 눈물 임플랜트의 외면에 시드를 포함할 수 있는데, 그것은 제제가 임플랜트로부터 걸러져 나오게 하지만 전기 전도성 입자를 유지한다.
몇몇 실시예에서, 눈물 임플랜트는 도 5에 도시된 바와 같이 임플랜트 코어를 포함하고, 전기 전도성 재료는 임플랜트 코어 내에 포함된다. 전기 전도성 재료는, 예를 들면 치료 약제를 수용하기 위해 사용되는 시드 내에 전기 전도성 재료를 포함함으로써, 임플랜트 코어 내에 또는 임플랜트 코어의 표면에 구비될 수 있다.
도 18은, 눈물 임플랜트를 검출하기 위한 디바이스(1800)의 다른 실시예의 블럭도이다. 눈물 임플랜트 검출기 디바이스(1800)는, 감지 회로(1805), 검출기 회로(1825), 및 표시기 디바이스(1810)을 포함한다. 감지 회로(1805)는, 감지 회로(1805)에 특성 임피던스를 주는 인덕턴스 및/또는 커패시턴스를 포함한다. 임피던스는 감지 회로에 감지 회로가 작동하는 고유 응답 주파수를 준다. 예를 들면, 감지 회로는 이러한 주파수로 진동하는 탱크 회로일 수 있다. 감지 회로(1805)가 눈물 임플랜트에 있거나 눈물 임플랜트 근처에 있을 때, 전기 전도성 재료는 감지 회로(1805)의 특성 임피던스를 변경시켜, 고유 주파수를 이동시킨다.
감지 회로(1805)의 특성 임피던스가 하나 이상의 인덕터에 의해 형성되면, 전기 전도성 재료는 감지 회로(1805)의 특성 인덕턴스를 교란시켜 주파수를 이동시킨다. 감지 회로(1805)가 하나 이상의 커패시터에 의해 형성되면, 눈물 임플랜트의 근접도(proximity)는 커패시턴스의 유전성을 변경시켜 주파수가 이동시킨다. 이것은, 재료(예를 들면, 알루미늄)의 유전성으로 인할 수 있거나, 생체 적합성 ㅣ재료 내에 포함되는 물로부터 오는 것일 수 있다.
검출 회로(1825)는 특성 임피던스의 변화를 검출한다(예를 들면, 고유 주파수의 이동을 검출함으로써). 변화가 검출되면, 검출 회로(1825)는 표시기 디바이스(1810)에 변화의 표시를 제공한다. 표시기 디바이스(1810)는, 눈물 임플랜트의 전기 전도성으로 인한 특성 임피던스의 변화를 검출할 때 가청 표시 또는 시각적 표시 중 하나 이상을 제공한다.
도 19는, 검출기 디바이스에 의해 눈물 임플랜트를 검출하는 방법(1200)의 흐름도이다. 블럭(1905)에서, 눈물점 마개와 같은 눈물 임플랜트가 제공된다. 블럭(1910)에서, 눈물점 마개는, 눈물점 마개의 근접성으로 인한 감지 회로의 특성 임피던스의 변화를 검출함으로써, 검출된다. 몇몇 실시예에서, 특성 임피던스의 검출된 변화는, 감지 회로의 고유 응답 주파수의 검출된 이동이다. 따라서, 디바이스는 눈물점 마개와 접촉하지 않고 눈물 임플랜트를 검출할 수 있다. 감지 회로에서 보이는 임피던스의 변화는 눈물 임플랜트와 상호작용하는 발생된 전계로 인한 것이다.
어떤 실시예에서, 디바이스 검출 가능 눈물 임플랜트는, 눈물 임플랜트의 생체 적합성 재료 내에 배치되는 전기 전도성 재료를 포함한다. 어떤 실시예에서, 공동이 눈물 임플랜트의 본체 내에 구비된다. 임플랜트 코어는, 제제를 지속적으로 릴리스하는 형상을 가지며 구성된다. 전기 전도성 재료는 임플랜트 코어 내에 구비될 수 있다. 어떤 실시예에서, 임플랜트 코어는 제제를 수용할 시드를 포함하고, 전기 전도성 재료는 시드 내에 포함된다. 어떤 실시예에서, 전기 전도성 재료는 임플랜트 본체의 생체 적합성 재료 및 임플랜트 코어 내에 구비된다.
블럭(1915)에서, 눈물 임플랜트가 검출되었는지에 대한 정보가 사용자 또는 자동화 프로세스에 제공된다. 어떤 실시예에서, 시각적 또는 가청 표시 중 하나 이상이 사용자에게 제공된다. 몇몇 실시예에서, 표시는 제2 디바이스의 자동화 프로세스에 전달된다.
디바이스 검출 가능 눈물 임플랜트는 눈의 질환을 치료하는 방법에 사용될 수 있다. 그러한 방법에서, 디바이스 검출 가능 눈물 임플랜트가 대상물의 하나 이상의 눈물점 내에 삽입된다. 눈물 임플랜트는, 제제를 지속적으로 릴리스하기 위해 임플랜트 코어 내에 제제의 서플라이를 포함한다. 어떤 실시예에서, 제제는, 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 또는 둘과 같은 녹내장 질병을 치료한다. 눈물 임플랜트는, 감지 회로애 대한 눈물 임플랜트의 근접으로 인한 감지 회로의 특성 임피던스의 변화를 검출함으로써 검출된다.
검출기 디바이스는, 눈물 임플랜트가 검출기 디바이스에 의해 광학적으로 검출되게 하는 성질을 가질 수 있다. 도 20은, 눈물점 마개와 같은 눈물 임플랜트(2000)의 다른 실시예를 도시한다. 눈물 임플랜트(2000)는 생체 적합성 재료의 임플랜트 본체(2005)를 포함한다. 임플랜트 본체(2005)는, 임플랜트 본체의 단부로부터 임플랜트 본체(2005) 내로 내향 연장되는 공동(2010)을 포함한다. 눈물 임플랜트(2000)는, 눈에 제제를 지속적으로 릴리스하는 사이즈로 구성된다. 임플랜트 코어(2015)는 임플랜트 본체의 공동(2010) 내에 지지되고, 발광 재료(2020)를 포함한다. 몇몇 실시예에서, 제제는 임플랜트 본체의 생체 적합성 재료 내에 배치되며, 발광 재료는 임플랜트 코어 내에 포함된다.
어떤 실시예에서, 발광 재료(2020)는 양자 돗트를 포함한다. 양자 돗트는, 제1 파장 범위(예를 들면, 제1 칼라)의 빛을 수광하고 다른 파장 범위(예를 들면, 제2 칼라)의 빛을 방출하는 반도체 디바이스이다. 일반적으로, 더 큰 양자 돗트는 저주파수 스펙트럼에서 작용한다. 예를 들면, 더 큰 양자 돗트는 적색(저주파수) 스펙트럼을 더 향하여 에너지를 방출하고, 더 작은 양자 돗트는 청색(고주파수) 스펙트럼을 더 향하여 에너지를 방출한다.
몇몇 실시예에서, 임플랜트 코어(2015)는 제제를 수용하기 위해 시드를 포함한다. 도 21은 임플랜트 코어의 시드(2100)를 도시한다. 시드(2100)는 발광 재료를 포함할 수 있다. 도 21은, 시드(2100)의 바닥에 포함되는 양자 돗트(2120)를 도시한다. 제제는 시드(2100)의 상부에 있는 개구를 통해 릴리스된다. 양자 돗트는 상승된 온도에서 불안정할 수 있기 때문에, 양자 돗트를 임플랜트 코어 내에 위치시키면 양자 돗트의 안정성을 향상시킬 수 있다.
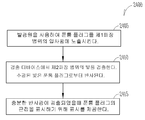
도 22는, 눈물점 마개와 같은 디바이스 검출 가능 눈물 임플랜트(2000)를 제조하는 방법(2200)의 다른 실시예의 흐름도이다. 블럭(2205)에서, 눈물점 마개는 생체 적합성 재료로 형성된다. 블럭(2210)에서, 공동은 눈물점 마개의 본체 내에 형성된다. 블럭(2215)에서, 마개 코어는 공동 내에 구비된다. 마개 코어는 눈에 제제를 지속적으로 릴리스하는 사이즈로 구성된다. 블럭(2220)에서, 발광 재료는 마개 코어 내에 구비된다.
그러면, 눈물 임플랜트 검출기 디바이스는 도 20의 눈물 임플랜트의 발광 재료(2020)를 검출한다. 검출기 디바이스 및 눈물 임플랜트(2000)는, 눈에 삽입될 수 있는 의료 디바이스를 통해 장시간에 걸쳐 치료 약제를 지속적으로 공급하고, 의료 디바이스가 계속 존재하는지 검증하고 제제를 공급함으로써 치료제를 모니터링하는 장치를 형성한다.
눈물 임플랜트(2000)의 발광체(예를 들면, 양자 돗트)는 광원에 의해 자극된다. 발광체는 고파워/저파장 형태의 빛을 흡수하고, 입사광을 방출되는 저파워/고파장 형태의 빛으로 변환한다. 눈물 임플랜트(2000)는, 예상된 고파장 형태의 빛이 검출될 때 검출된다.
도 23은, 눈물 임플랜트 검출기 디바이스(2300)의 다른 실시예의 블럭도이다. 검출기 디바이스(2300)는, 입사광을 근처의 눈물 임플랜트(2305)에 제공하기 위한 발광 소스(2335), 광학 필터(2325), 및 광 검출기 디바이스(2340)를 포함한다. 몇몇 실시예에서, 발광 소스(2335)는 발광 다이오드(LED)를 포함한다. 광학 필터(2325)는, 눈물 임플랜트(2305)의 발광 재료로부터 반사되는 특정 파장 범위의 빛을 통과시키도록 구성된다. 광 검출 디바이스(2340)는, 광학 필터(2325)에 의해 통과되는 빛을 수광하고, 충분한 빛이 수광되었을 때 눈물 임플랜트(2305)의 근접도를 표시하기 위해 응답 전기 신호를 발생하도록 구성된다. 몇몇 실시예에서, 광검출 디바이스(2340)는, 광학 필터(2325)에 의해 통과되는 에너지를 전기 신호로 변환하기 위한 광다이오드를 포함한다.
발광 소스(2335)는, 제1 파장 범위를 가지는 입사광을 제공하고, 발광 재료는 제2 파장 범위의 입사광을 반사시킨다. 몇몇 실시예에서, 제1 파장 범위는 제1 칼라의 빛에 대응하고, 제2 파장 범위는 제2 칼라의 빛에 대응한다. 예를 들면, 발광 재료가 양자 돗트를 포함하면, 발광 소스(2335)는 청색 스펙트럼(예를 들면, 청색 LED)의 입사광을 제공할 수 있고, 발광 재료는, 광학 필터(2325)에 의해 통과되고 광검출 디바이스(2340)에 의해 검출되는 녹색 스펙트럼의 입사광을 반사시킨다. 양자 돗트의 광여기(photoexcitation) 거동은, 광 에너지의 흡수와 방출 사이의 불연속(dicrete) 시간 간격을 보인다. 이러한 시간 간격은 20 나노초(ns) 정도이다.
몇몇 실시예에서, 입사광과 방출광은 모두 적외선 또는 근자외선 스펙트럼에 있다. 발광 소스(2335)는, 적외선 스펙트럼에 있는 제1 파장 범위의 입사광을 제공하고, 발광 재료는 적외선 스펙트럼의 다른 제2 파장 범위의 입사광을 반사시킨다. 입사광과 방출광 사이의 에너지의 이동은 가시성 스펙트럼의 빛에 대한 것보다 적외선 스펙트럼에 대해 더 크다. 입사광과 방출광 사이의 파장의 이러한 더 큰 분리는 필터링 및 검출 프로세스를 더 쉽게 만들 수 있다. 또한, 적외선광은 보조 장치를 사용하지 않고는 눈으로 볼 수 없다. 이것은, 밝은 가시성광이 환자의 눈에는 빛나지 않기 때문에, 검출 프로세스를 환자에게 더 안락하게 할 것이다.
검출기 디바이스(2300)는, 광검출 디바이스(2340)로부터 전기 신호를 수신할 때 임플랜트 검출의 표시를 사용자에게 제공하기 위한 표시기(2310)를 포함한다. 몇몇 실시예에서, 표시기(2310)는 시각적 표시 및/또는 가청 표시를 제공한다.
도 24는, 눈물점 마개와 같은 눈물 임플랜트를 검출하는 방법(2400) 다른 실시예의 흐름도이다. 블럭(2405)에서, 눈물점 마개는 발광 소스를 사용하여 제1 파장 범위의 입사광에 노출도니다. 몇몇 실시예에서, 입사광은 제1 범위에 있는 파장에 대응하는 칼라를 가진 가시광 스펙트럼 LED로부터 온다.
블럭(2410)에서, 제2 파장 범위의 빛은 검출 디바이스를 사용하여 검출되고, 수광된 빛은 눈물점 마개로부터 반사된다. 더 넓은 스펙트럼의 백색광이 광검출을 어렵게 할 수 있다. 몇몇 실시예에서, 입사광의 스펙트럼 범위는 녹색광 스펙트럼에 있고, 반사광의 스펙트럼 범위는 청색 스펙트럼에 있다. 해당 스펙트럼 범위 밖으로부터 오는 필요하지 않은 빛을 막기 위해 차단 챔버가 유용할 수 있다. 몇몇 실시예에서, 입사광은 적외선 스펙트럼의 제1 파장 범위를 가지며, 반사광은 적외선 스펙트럼의 제2 파장 범위를 가진다.
블럭(2415)에서, 눈물점 마개의 인접도를 나타내기에 충분한 반사광이 검출될 때 표시가 제공된다. 몇몇 실시예에서, 시각적 및/또는 가청 표시가 사용자에게 제공된다. 몇몇 실시예에서, 표시 신호는 제2 디바이스의 자동화 프로세스로 통신된다. 그러한 디바이스 검출 가능 눈물 임플랜트는 눈의 질환을 치료하기 위해 사용될 수 있다. 눈물 임플랜트는, 제제를 지속적으로 릴리스하기 위해 임플랜트 코어 내에 제제의 서플라이를 포함할 수 있다. 어떤 실시예에서, 제제는 녹내장 질병을 치료한다.
도 25는, 눈물 임플랜트(2500)의 다른 실시예를 도시하고 있다. 공동(2520) 내의 임플랜트 코어(2525)는, 눈의 영역으로부터 눈물 임플랜트를 광학적으로 구별하도록 구성되는 광학적 대비(contrast) 재료(2540)를 포함한다. 광학적 대비 재료는 안료 또는 염료를 포함할 수 있다. 몇몇 실시예에서, 광학적 대비 재료는 임플랜트 코어(2525)의 표면 상에 배치된다. 몇몇 실시예에서, 임플랜트 코어는, 지속적 릴리스를 위한 제제를 수용하기 위한 시드(2530)를 포함하고, 광학적 대비 재료는, 제제를 수용하는 시드(2530) 상에 배치된다.
눈물 임플랜트를 검출하기 위해, 예를 들면 디지털 카메라를 사용하여 눈의 눈물점 영역의 이미지가 얻어진다. 다음에는 이미지에서 대조가 더 심한 영역을 찾기 위해 이미지 프로세싱 알고리즘이 사용된다. 이미지 센서의 깊이 초점이 자동적으로 정확하게 세팅되지 않을 수 있기 때문에, 표면 아래에 있고 잠재적으로 눈물 소관 내에 잠기는 영역의 이미지를 얻는 것이 어려울 수 있다. 이미지를 얻는 한 가지 방법은 600 내지 1300 나노미터(nm)의 스펙트럼 대역 주위의 빛을 필터링하는 것이다. 이것은 이미지 센서와 눈물 임플랜트 사이의 끼어 있는 형태의 조직을 필터링하여 제거할 수 있다.
도 26은, 눈물 임플랜트 검출기 디바이스(2600)의 다른 실시예의 블럭도이다. 검출기 디바이스(2600)는, 눈의 적어도 일부(예를 들면, 눈물점 영역)의 이미지를 얻기 위한 이미지 센서(2615)를 포함한다. 눈물 임플랜트 검출기 디바이스(2600)는 또한 이미지 분석기 회로(2650)를 포함한다. 이미지 분석기 회로(2650)는, 이미지의 다른 영역의 이미지 대조를 초과하는 이미지 대조를 가진 이미지 부분의 위치를 검출하도록 구성된다. 따라서, 눈물 임플랜트가 존재하면, 눈물 임플랜트의 광학적 대조는 이미지의 다른 곳의 대조를 임계 이미지 대조값만큼 초과할 것이다. 이미지 분석기 회로(2650)는 광학적 대조를 검출하고, 눈물 임플랜트의 일부의 이미지가 이미지 내에 있는지에 대한 표시를 사용자 또는 자동 프로세스에 제공할 것이다.
몇몇 실시예에서, 이미지 분석기 회로(2650)는, 이미지 프로세싱 알고리즘을 실현할 명령을 수행하는 프로세서(예를 들면, 마이크로프로세서)를 포함한다.
몇몇 실시예에서, 이미지 센서(2615)는 카메라에 포함되는 디지털 이미지 센서이고, 검출기 디바이스(2600)는, 이미지 분석기 회로(2650)에 의해 프로세싱할 이미지를 저장하기 위한 메모리를 포함할 수 있다. 몇몇 실시예에서, 이미지 분석기 회로(2650)는 제2 디바이스에 포함된다.
중간에 있는 조직으로 인해 관심 있는 영역의 이미지를 얻는 것이 어려울 수 있다. 몇몇 실시예에서, 검출기 디바이스(2600)는 적외선 광 방출기(2655)를 포함하고, 이미지 센서(2615)는 적외선 이미지 센서를 포함한다.
도 27은, 디바이스 검출 가능 눈물 임플랜트를 제조하는 방법(2700)의 다른 실시예의 흐름도이다. 블럭(2705)에서, 눈물점 마개와 같은 눈물 임플랜트는 생체 적합성 재료로 형성된다. 블럭(2710)에서, 공동은 눈물점 마개의 본체 내에 형성된다. 블럭(2715)에서, 마개 코어는 공동 내에 구비된다. 마개 코어는 눈에 지속적으로 제제를 릴리스하는 사이즈로 구성된다. 블럭(2720)에서, 광학적 대조 재료는, 눈물점 마개를 눈의 눈물 영역으로부터 광학적으로 구별하기 위해 마개 코어 내에 구비된다. 몇몇 실시예에서, 광학적 대조 재료를 마개 코어 내에 구비하는 것은, 광학적 대조 재료를 마개 코어의 표면에 구비하는 것을 포함한다. 몇몇 실시예에서, 마개 코어를 구비하는 것은, 제제를 수용하기 위해 시드를 마개 코어 내에 구비하는 것을 포함한다. 마개 코어 내의 광학적 대조 재료는 시드 내에 포함된다.
검출 가능 눈물 임플랜트는 눈의 질환을 치료하기 위한 방법에 사용될 수 있다. 그러한 방법에서, 검출 가능 눈물 임플랜트는 대상물의 하나 이상의 눈물점 내에 삽입된다. 눈물 임플랜트는, 마개 코어 내에 배치되는 지속적 릴리스 제제의 서플라이를 가진다. 어떤 실시예에서, 제제는 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 또는 둘과 같은 녹내장 질병을 치료하기 위해 사용된다. 눈물 임플랜트를 검출하기 위해, 대상물의 눈물점 영역의 이미지가 얻어진다. 임플랜트는, 이미지의 다른 영역의 이미지 대조를 초과하는 이미지 대조를 가진 이미지 부분의 위치가 검출될 때 검출된다.
여기에서 기술된 임플랜트가 치료 약제 또는 약제 서플라이를 포함하면, 치료 약제 또는 약제 서플라이는, 상술한 임플랜트가 조직 내에 또는 눈 근처에 이식될 때 바람직한 치료 반응을 제공하도록 릴리스된다.
(치료 약제의 예)
상술한 여러 가지 예들은, 치료 약제(또는 간단하게 "제제")를 지속적으로 릴리스하는 마개 코어를 설명한다. 제제는 그외에도 하기 물질 또는 이의 등가체, 유도체 또는 유사체들 중 하나 또는 임의 조합으로 제조된 약제, 예컨대 항-녹내장 약제(예, 아드레날린 작용제, 아드레날린 길항제(베타 차단제), 탄산탈수효소 저해제(CAI: carbonic anhydrase inhibitor)(전신적 및 국소적), 부교감신경흥분제, 프로스타글란딘 및 저혈압성 지질(hypotensive lipid) 및 이들의 조합), 항미생물제(예, 항생제, 항바이러스제, 항기생충제, 항진균제 등), 코르티코스테로이드 또는 그외 항염증제(예, NSAID 또는 그외 진통성 및 통증 제어 약제), 충혈 완화제(예, 혈관 수축제), 알레르기 반응 예방 또는 완화제(예, 항히스타민, 사이토카인 저해제, 루코트리엔 저해제, IgE 저해제, 면역조절제), 비만 세포 안정화제, 안근 마비제(cycloplegic), 산동제(mydriatic) 등을 포함할 수 있다.
이용가능한 예시적인 제제로는, 트롬빈 저해제; 항혈전 약제(antithrombogenic agents); 혈전 용해제(thrombolytic agents); 섬유소 용해제(fibrinolytic agents); 혈관경련 저해제(vasospasm inhibitors); 혈관 확장제(vasodilators); 항고혈압 약제(antihypertensive agents); 항미생물 약제, 예를 들어 항생제(예, 테트라사이클린, 클로르테트라사이클린, 박시트라신, 네오마이신, 폴리믹신, 그라미시딘, 세팔렉신, 옥시테트라사이클린, 클로람페니콜, 리팜피신, 시프로플록사신, 토브라마이신, 젠타마이신, 에리트로마이신, 페니실린, 설폰아미드, 설파디아진, 설파세타미드, 설파메티졸, 설피속사졸, 니트로푸라존, 소듐 프로피오네이트), 항진균제(예, 암포테리신 B 및 미코나졸), 및 항진균제(예, 이독수리딘 트리플루오로티미딘, 아시클로비어, 갱시클로비어, 인터페론); 표면 당단백질 수용체의 저해제(surface glycoprotein receptor); 항혈전제; 유사분열 저해제; 미세소관 저해제(microtubule inhibitor); 분비억제제(anti-secretory agent); 활성 저해제(active inhibitor); 재구성 저해제(remodeling inhibitor); 안티센스 뉴클레오티드(antisense nucleotide); 항-대사 물질(anti-metabolite); 항증식제(예, 혈관신생 억제제); 항암 화학요법 약제; 항-염증제(예, 하이드로코르티손, 하이드로코르티손 아세테이트, 덱사메타손 21-포스페이트, 플루오시놀론, 메드리손, 메틸프레드니솔론, 프레드니솔론 21-포스페이트, 프레드니솔론 아세테이트, 플루오로메탈론, 베타메타손, 트리암시놀론, 트리암시놀론 아세토니드); 비-스테로이드성 항-염증제(NSAID: non steroidal anti-inflammatories) (예, 살리실레이트, 인도메타신, 이부프로펜, 디클로페낙, 플루비프로펜, 피록시캄 인도메타신, 이부프로펜, 낙소프렌(naxopren), 피록시캄 및 나부메톤)를 포함하나, 이들로 한정되지 않는다. 본 발명의 눈물점 마개에 사용이 고려되는 이러한 항염증 스테로이드의 예로는, 트리암시놀론 아세토니드(일반명) 및 코르티코스테로이드, 예를 들어 트리암시놀론, 덱사메타손, 플루오시놀론, 코르티손, 프레드니솔론, 플루메톨론, 및 그의 유도체; 항알러지제(예, 소듐 크로모글리케이트(sodium chromoglycate), 안타졸린, 메타피릴린, 클로르페니라민, 세트리진, 피릴아민, 프로펜피리다민); 항증식 약제(예, 1,3-시스 레티노산, 5-플루오로우라실, 탁솔, 라파마이신, 마이토마이신 C, 및 시스플라틴); 소염제(예, 페닐에프린, 나파졸린, 테트라하이드라졸린); 동공 축소제(miotic) 및 항-콜린에스테라제(예, 필로카르핀, 살리실레이트, 카바콜, 아세틸콜린 클로라이드, 파이소스티그민, 에세린, 디이소프로필 플루오로포스페이트, 포스폴린 아이오딘, 데메카리움 브로마이드); 항종양제(예, 카르무스틴, 시스플라틴, 플루오로우라실3); 면역제(예, 백신 및 면역 자극제); 호르몬제(예, 에스트로겐, -에스트라디올, 프로게스타오널(progestational), 프로게스테론, 인슐린, 칼시토닌, 파라티로이드 호르몬, 펩티드, 및 바소프레신 시상하부 분비 인자(vasopressin hypothalamus releasing factor)); 면역억제제, 성장 호르몬 길항제, 성장 인자(예, 상피세포 성장 인자, 섬유모세포 성장 인자, 혈소판 유래 성장 인자, 형질전환 성장 인자 베타, 소마토트랩핀, 피브로넥틴); 혈관신생 저해제(예, 안지오스타틴, 아네코르타브 아세테이트, 트롬보스폰딘, 항-VEGF 항체); 도파민 작용제; 방사선 요법 약제; 펩티드; 단백질; 효소; 세포외부기질(extracellular matrix); 컴포넌트(component); ACE 저해제; 유리 라디칼 제거제(free radical scavengers); 킬레이트제(chelator); 항산화제: 항 폴리머라제(anti polymerase); 광역학 요법 약제(photodynamic therapy agent); 유전자 요법 약제; 및 다른 치료 약제, 예를 들어 프로스타글란딘, 항프로스타글란딘, 프로스타글란딘 전구체, 예를 들어 항녹내장 약제, 예를 들어 베타-차단제, 예를 들어 티몰롤, 베탁솔롤, 레보부놀롤, 아테놀롤, 및 프로스타글란딘 유사체, 예를 들어 비마토프로스트, 트라보프로스트, 라타노프로스트 등; 탄산탈수효소 저해제, 예를 들어 아세타졸아미드, 도르졸아미드, 브린졸아미드, 메타졸아미드, 디클로르펜아미드, 디아목스; 및 신경 보호제(neuroprotectant), 예를 들어 루베졸, 니모디핀 및 관련 화합물; 및 부교감신경 흥분제, 예를 들어 필로카르핀, 카바콜, 파이소스티그민 등을 포함한다.
본 발명에 따른 눈물점 마개와 함께 사용할 수 있는 추가적인 제제로는, 미국 연방 식품, 의약제 및 화장품 법률 505조에 의거하여 승인받았거나, 또는 공중 보건 서비스 법률에 의거하여 승인받은 약제를 포함하나, 이들로 한정되지 않으며, 일부는 미국 식의약청(FDA) 웹사이트 http://www.accessdata.fda.gov/scripts/cder/drugsatfda/index에서 확인할 수 있다. 또한, 본 발명의 눈물점 마개는, 본 특허 문헌의 출원일 보다 일찍 또는 늦은 동일 일자가 찍혀있거나 기록되어 있는, FDA 오렌지서 웹사이트(http://www.fda.gov/cder/ob/)에서 확인할 수 있는, 전자 형태나 종이 형태의 오렌지서에 열거된 약제과 함께 사용할 수 있다. 예로, 이들 약제들은, 특히 도르졸아미드(dorzolamide), 올로파타딘(olopatadine), 트라보프로스트(travoprost), 비마토프로스트(bimatoprost), 사이클로스포린(cyclosporin), 브리모니딘(brimonidine), 목시플록삭신(moxifloxacin), 토브라마이신(tobramycin), 브린졸아미드(brinzolamide), 아시클로비르 티몰롤 말레이트(aciclovir timolol maleate), 케토롤락 트로메타민(ketorolac tromethamine), 프레드니솔론 아세테이트(prednisolone acetate), 소듐 히알루로네이트(sodium hyaluronate), 네파페낙(nepafenac), 브롬페낙(bromfenac), 디클로페낙(diclofenac), 플루르비프로펜(flurbiprofen), 수프로페낙(suprofenac), 비녹산(binoxan), 파타놀(patanol), 덱사메타손/토브라마이신 조합물(dexamethasone/tobramycin combination), 목시플록삭신(moxifloxacin) 또는 어사이클로비르(acyclovir)를 포함할 수 있다.
전술한 제제들로 치료할 수 있는 질환 또는 장애의 예는, 녹내장, 수술 전후 눈 치료, 안구 건조증, 항-눈 알레르기, 항-감염, 수술 후 염증 또는 통증, 호흡-관련 장애, 예컨대 알레르기, 내이 장애, 예컨대 현기증 또는 편두통을 포함하지만, 이들로 한정되는 것은 아니다. 일부 구체예에서, 치료 약제는 윤활제 또는 계면활성제, 예를 들어 안구 건조증 치료를 위한 윤활제일 수 있다. 일부 예들에서, 치료 약제는 눈으로부터 눈물을 흡수할 수 있는 흡수제를 포함할 수 있다.
(약제 서플라이의 예)
약제 서플라이는 1종 이상의 제제를 포함할 수 있으며, 일부 구현예에서는, 제제의 느린 방출을 제공하기 위한 한가지 이상의 매트릭스 물질을 포함할 수 있다. 상기 1종 이상의 제제는, 적어도 일정 부분 이상 매트릭스에서의 제제의 가용성을 토대로 하여, 약제 서플라이의 노출면으로부터 표적 조직(눈의 모양체근)으로 이동할 수 있다. 노출면으로부터의 제제의 이동 속도는 매트릭스에 용해된 제제의 농도와 관련있을 수 있다. 일부 예로, 약제 서플라이에 용해된 제제의 농도는 약제가나 제제의 바람직한 방출 속도를 제공하도록 조절할 수 있다. 그외에도, 또는 이와 더불어, 노출면으로부터의 제제의 이동 속도는 실리콘 매트릭스 제형의 특성 등의 제제가 용해되는 매트릭스의 한가지 이상의 특성과 관련있을 수 있다. 일부 예에서, 상기 약제 서플라이에 포함되는 제제는, 액체, 고체, 고체 겔, 고체 결정, 고체 비정질, 고체 미립자 또는 용해된 형태일 수 있다. 이러한 예로, 액체 Latanoprost 점적제 또는 고체 Bimatoprost 미립자가 실리콘에 분산된다.
약제 서플라이는 하나 이상의 제제의 느린 방출을 제공할 수 있는 하나 이상의 생체친화성 물질을 포함할 수 있다. 약제 서플라이는 매트릭스 내에 위치하여 용해가능한 제제 봉입을 가진 실질적으로 비-생분해성인 실리콘 매트릭스 등의 매트릭스를 포함하는 구체예를 들어 상기와 같이 기술되어 있지만, 약제 서플라이는 약제가나 제제의 느린 방출을 제공하는 다른 구조물, 예컨대 생분해성 매트릭스, 유공성 약제 서플라이, 액체 약제 서플라이 또는 고체 약제 서플라이를 포함할 수 있다. 제제를 포함하는 매트릭스는, 생분해성 또는 비-생분해성 폴리머로부터 제조할 수 있다. 일부 예로, 비-생분해성 약제 서플라이는 실리콘, 아크릴레이트, 폴리에틸렌, 폴리우레탄, 폴리우레탄, 하이드로겔, 폴리에스테르(예, DACRON.RTM., E. I. Du Pont de Nemours and Company, Wilmington, Del.), 폴리프로필렌, 폴리테트라플루오로에틸렌(PTFE), 팽창(expanded) PTFE (ePTFE), 폴리에테르 에테르 케톤(PEEK), 나일론, 압출 콜라겐, 폴리머 폼(polymer foam), 실리콘 고무, 폴리에틸렌 테레프탈레이트, 초고분자량 폴리에틸렌, 폴리카보네이트 우레탄, 폴리우레탄, 폴리이미드, 스테인레스 스틸, 니켈-티타늄 합금(예, 니티놀), 티타늄, 스테인레스 스틸, 코발트-크롬 합금(예, ELGILOY.RTM., Elgin Specialty Metals, Elgin, Ill.; CONICHROME.RTM., Carpenter Metals Corp., Wyomissing, Pa.)을 포함할 수 있다. 일부 예로, 생분해성 약제 서플라이는 하나 이상의 생분해성 폴리머, 예를 들어 단백질, 하이드로겔, 폴리글리콜산(PGA), 폴리락트산(PLA), 폴리(L-락트산)(PLLA), 폴리(L-글리콜산)(PLGA), 폴리글리콜리드, 폴리-L-락티드, 폴리-D-락티드, 폴리(아미노산), 폴리디옥사논, 폴리카프로락톤, 폴리글루코네이트, 폴리락트산-폴리에틸렌 옥사이드 공중합체, 개질된 셀룰로스, 콜라겐, 폴리오르토에스테르, 폴리하이드록시부티레이트, 폴리안하이드라이드, 폴리포스포에스테르, 폴리(알파-하이드록시산) 및 그들의 조합을 포함할 수 있다. 일부 예에서, 약제 서플라이는 하이드로겔 폴리머를 포함할 수 있다.
다른 차수(order) 예를 들면 1차의 반응 카이네틱스에 대응하는 레이트로 치료 약제가 릴리스될 수 있지만, 치료 약제 또는 약제 서플라이는 바람직하게 균일한 레이트 예를 들면 영차카이네틱스(zero-order kinetics)에 대응하는 레이트로 릴리스된다. 많은 실시예에서, 반응의 카이네틱 차수는, 치료 약제가 릴리스될 때, 0차로부터 1차까지 변화할 것이다. 따라서, 치료 약제는, 대략 0으로부터 대략 1까지 변화하는 카이네틱 차수의 범위에 대응하는 프로파일로 릴리스된다. 이상적으로는, 치료 약제를 균일하게 공급하도록, 치료 약제가 릴리스되는 레이트가 심각하게 변화하기 전에 임플랜트가 제거된다. 균일한 레이트의 공급이 필요하기 때문에, 반응 카이네틱스가 완전히 1차로 전이되기 전에 임플랜트를 제거 및/또는 교체하는 것이 바람직할 수 있다. 다른 실시예에서는, 치료 약제 릴리스 프로파일이 안전하고 효율적인 범위에 유지되는 한, 일부 또는 전체 치료 동안에 1차 또는 고차 릴리스 카이네틱스가 바람직할 수 있다. 몇몇 실시예에서, 코어는 1주 내지 5년의 기간 동안 더 구체적으로는 3개월 내지 24개월의 범위에서 효율적인 레이트로 치료 약제를 릴리스할 수 있다. 위에서 지적한 바와 같이, 몇몇 실시예에서, 검출제와 치료 약제가 유사한 릴리스 레이트를 가지는 것이 바람직할 수 있으며, 예를 들면 검출제는 치료 약제의 지속적 릴리스를 표시할 것이다. 다른 실시예에서, 검출제와 치료 약제가 상이한 릴리스 레이트를 가지는 것이 바람직할 수 있으며, 예를 들면 검출제는, 치료 약제가 릴리스되고 있을 때 환자에게 알려주고 임플랜트를 제거 또는 변경하기 위해 릴리스된다.
본 발명은, 코눈물 장치의 눈꺼풀 소관 눈물점 내로 이식되는 모든 임플랜트 또는 디바이스를 구현하고자 하는 것이다. 임플랜트 또는 디바이스는, 임플랜트 또는 디바이스가 정위치에 있는지, 몇몇 실시예에서는, 임플랜트 또는 디바이스가 여전히 올바르게 작용하고 있는지, 예를 들면 치료 약제 또는 약제를 여전히 공급하고 있는지를, 환자에게 알려주기 위한 검출 디바이스를 포함한다.
필요한 치료에 따라, 몇몇 임플랜트는 약제를 눈물못 따라서 눈에, 또는 코눈물 장치 따라서 신체의 체계적 순환에 공급하기 위해 눈물점 관 안으로 향할 수 있다. 도면들은 본 발명의 임플랜트의 단지 몇 가지 실시예를 도시할 뿐이다.
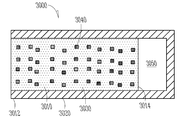
이제 도 28을 참조하면, 임플랜트 데이터 및 추적 장치(2800)은 일반적으로 임플랜트 데이터, 임플랜트의 추적 등의 상관을 편리하게 한다. 상기 장치는 통상적으로, 하나 이상의 상술한 임플랜트 구조를 포함할 수 있는 복수의 임플랜트(2810)를 포함한다. 이들 임플랜트는 통상적으로 안과 용도에 적합할 것이지만, 다른 약제 공급 임플랜트 등에 의한 다른 의료 지침 및 치료에 대해 다른 장치 실시예가 사용될 수 있다.
장치(2800)과 관련되는 각각의 임플랜트는, 판독기(2820)에 의해 식별될 수 있는 신호를 전송할 수 있다. 예를 들면, 신호는, 특정 클래스 또는 유형의 임플랜트의 일원(member), 특정 클래스 또는 유형의 임플랜트의 특정 집단, 및/또는 특정 유일한 임플랜트로서 임플랜트를 식별할 수 있게 하는 RFID 신호일 수 있다. 다른 장치는, 광-베이스 신호(임플랜트로부터 릴리스되는 꽃 신호 택(florescent signal tags)을 사용하여 발생되는 신호를 포함함), 자기 신호 등을 사용할 수 있다. 판독기는 자주 선반재고 판독기(시판되는 RFID 판독기, 시판되는 스펙트럼 코드 판독기 등과 같음)를 포함할 것이지만, 또는 특허(proprietary) 임플랜트 판독기를 포함할 수 있다. 판독기는 신호를 프로세서(2830)에 전달하여(통상적으로 전기로), 프로세서가 조사 또는 판독되고 있는 특정 임플랜트(2810)의 속성을 판정할 수 있게 한다.
프로세서(2830)는 시판되는 컴퓨터 장치의 일부 또는 모든 컴포넌트를 포함할 수 있다. 프로세서(2830)는, 예를 들면, 통상적으로 버스 서브장치를 통해 복수의 주변장치와 통신할 수 있는 하나 이상의 프로세서 회로(2830A)를 포함할 것이다. 이들 주변장치는 메모리 장치(2830B)을 포함할 수 있다. 메모리는 통상적으로, 방법(여기에 설명된 것들을 포함함)을 수행하기 위한 기계 판독 가능 명령을 구현하는 유형 저장 매체 및/또는 데이터를 포함할 것이다. 메모리(2830B)는 랜덤 액세스 메모리(RAM), 판독 전용 메모리(ROM), 하드 디스크 드라이브와 같은 영구(비휘발성) 저장장치, 관련 제거 가능 매체를 가진 플로피 디스크 드라이브, 컴팩트 디지털 판독 전용 메모리(CD-ROM) 드라이브, 광학 드라이브, DVD, CD-R, CD-RW, 고상 제거 가능 메모리, 및/또는 플래시 RAM을 포함하여 다른 제거 가능 매체 카트리지 또는 디스크를 포함할 수 있다.
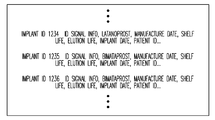
메모리(2830B 또는 2840)의 몇몇 예시적 내용은 도 28a에 개략적으로 도시되어 있다. 일반적으로, 메모리는, 개별적 임플랜트, 임플랜트 클래스/유형, 및/또는 임플랜트의 집단의 목록을 포함할 수 있다. 임플랜트의 목록은, 각각의 목록에 대해, 판독기(2820)에 의해 판독되는 신호로부터 임플랜트, 임플랜트 클래스, 및/또는 임플랜트 집단을 프로세서가 식별할 수 있게 하기 위해 ID 신호 정보를 포함할 수 있다. 선택적으로, 메모리는 또한, 임플랜트의 약제 또는 제제, 제조일자, 유효기간, 임플랜트를 위한 계획 약제 공급 기간(span), 임플랜트의 사이즈 등에 관한 정보를 포함(또는 정보에 대한 액세스를 허용)할 수 있다. 특히, 프로세서가 의사의 오피스와 같은 임플랜트 위치에서 사용되거나 임플랜트 위치에 결합되어 있는 경우에는, 메모리는 또한, 환자 ID, 이식일자에 관한 정보, 및 외래 방문시에 임플랜트의 존재 여부, 과거 및/또는 추후의 환자의 건강 데이터에 관한 정보(임플랜트의 효능의 표시를 포함) 등을 포함할 수 있다. 이러한 정보에 액세스함으로써, 장치(2800)은, 다양한 환자 집단에 이식되는 많은 재고의 임플랜트의 사용을 관리 및/또는 추적하기 위해 사용될 수 있다.
간단한 장치는, 일체식 컴퓨터 프로그램을 수행하고 소형 손잡이식 유닛 내에 판독기 및 출력과 함께 팩킹되는 단일 프로세서 칩 또는 집적 회로를 사용할 수 있다. 또는, 다양한 중앙집중 또는 분산 데이터 처리 하드웨어 및 소프트웨어 구조가 사용될 수 있다. 예를 들면, 중앙 처리기(2840)는 임플랜트 제조자 또는 분배인 또는 정부 당국(미국의 음식 및 약제 관리국과 같은)에 위치될 수 있다(또는 제어 하에 있을 수 있다). 중앙 처리기는, 인터넷(2850) 등과 같은 네트웍을 통해 복수의 국부 의료 프로세서의 각각에 링크될 수 있다. 이러한 분산된 프로세서 장치는, 의사의 오피스에서의 임플랜트의 사용 및 재고의 관리를 편리하게 하고, 또한 한 범위의 여러 가지 의료 세팅을 통해 효능, 역효과 등을 추적할 수 있게 할 수 있다. 따라서, 여기에 설명된 기능은, 여러 가지 데이터 프로세싱 구조 및 위치에 분산된 다양한 소프트웨어 및/또는 하드웨어 모듈에서 실시될 수 있다. 예를 들면, 각각 임플랜트의 속성(임플랜트에 의해 공급되는 약제, 임플랜트가 이식된 시기, 약제 공급이 종료되는 시기 등)을 판정할 수 있는 판독기(자주 프로세서와 관련됨)를 복수의 여러 의사의 오피스에 제공하는 것이 자주 바람직할 것이다. 이것은, 환자가 임플랜트에 관한 완전한 정보를 가지지 않은 때에도, 임플랜트를 가진 환자가 적절한 장비를 가진 임의의 의료 세팅에서 충고 또는 치료(임플랜트의 교체와 같은)를 받을 수 있게 할 수 있다. 임플랜트 데이터 장치는 또한 한 범위의 다른 전자 기록 장치에 합체될 수 있어, 임플랜트 데이터가 판독되고 및/또는 임플랜트가 이식 또는 제거될 때, 자동화된 메시지가 지멘스 SMS 의료 해결 장치 등을 사용하여 환자의 파일 또는 의사에게 보내어질 수 있게 한다.
(예 1, 플루오레신의 추출 및 플루오레신 추출에 대한 계면활성제의 효과)
도 29는, 본 발명의 실시예들에 따른, 플루오레신의 추출 및 플루오레신 추출에 대한 계면활성제의 효과를 도시하고 있다. 플루오레신에 대한 추출 데이터는, 수용성 및 비수용성 치료 약제 및 비교적 낮은 분자 중량 및 높은 분자 중량 치료 약제를 포함하여 많은 치료 약제의 지속적인 릴리스에 대한 상기 약제 코어 및 제조 프로세스의 신축성을 도시하고 있다. 몇몇 실시예에서, 검출제는 상술한 바와 같이 치료 약제로 추출되는 플루오레신을 포함할 수 있다. 플루오레신은 332.32g/mol의 분자 질량을 가지며, 수용성이고, 눈으로부터 릴리스되는 수용성 치료 약제를 위한 모델로서 작용할 수 있다. 본 발명의 실시와 관련된 작업은, 분자 중량 및 수용도는 각각 고체 약제 코어 매트릭스로부터의 약제의 릴리스 레이트에 영향을 줄 수 있다는 것을 나타낸다. 예를 들면, 낮은 분자 중량은 고체 매트릭스 재료를 통한 즉 실리콘을 통한 확산을 증가실 수 있어, 낮은 분자 중량 화합물이 더욱 신속히 릴리스될 수 있다. 또한, 수용도 역시 약제의 릴리스 레이트에 영향을 줄 수 있고, 어떤 경우에는, 약제의 증가된 수용도는, 예를 들면 고체 매트릭스 재료로부터 눈물 액체와 같은 신체 액체로의 운반을 통해, 고체 약제 코어 매트릭스로부터의 릴리스의 레이트를 증가시킬 수 있다. 이러한 실시예에 따라, 플루오레신보다 높은 분자 중량과 플루오레신보다 낮은 수용도를 가진 치료 약제, 예를 들면 위에 보여진 사이클로스포린 및 프로스타글란딘은 낮은 레이트로 고체 코어로부터 릴리스될 수 있다. 계면활성제 역시 약제 코어로부터 둘러싸는 신체 조직 및/또는 유체 예를 들면 눈물 막 유체로의 치료 약제의 릴리스의 레이트에 영향을 줄 수 있다.
실험된 각각의 약제 코어는 MED 4011 실리콘을 포함하였다. 일실시예에서, 약제 코어 제형(2910)은 9% 계면활성제와 0.09% 플루오레신을 포함하였다. 약제 코어 제형 (2910)의 추출 레이트에 대한 지수적 핏트(fit)(2912)가 도시되어 있다. 다른 실시예에서, 약제 코어 제형(2920)은 16.5% 계면활성제와 0.17% 플루오레신을 포함하였다. 약제 코어 제형 (2920)의 추출 레이트에 대한 지수적 핏트(fit)(2922)가 도시되어 있다. 또 다른 실시예에서, 약제 코어 제형(2930)은 22.85% 계면활성제와 0.23% 플루오레신을 포함하였다. 약제 코어 제형 (2930)의 추출 레이트에 대한 지수적 핏트(fit)(2932)가 도시되어 있다. 계면활성제가 없는 실시예에서, 약제 코어 제형(2940)은 0% 계면활성제와 0.3% 플루오레신을 포함하였다. 약제 코어 제형 (2940)의 추출 레이트에 대한 지수적 핏트(fit)(2942)가 도시되어 있다.
약제 코어는, 키(key) 제형들로 제조되었는데, 키 제형들에는, 실리콘 계면활성제 "190 유체"(다우 코닝); 계면활성제 혼합물:"190 유체" + 플루오레신; 실리콘(Nusil): MED 4011 파트 A, MED 4011 파트 B; 원심 튜브; 3mL 주사기; 20 ga. 바늘; 0.031 인치 내결 테플론 튜브; 및 버퍼가 포함된다.
키 변수들에는, 2.5g의 실리콘 계면활성제 및 0.025g의 플루오레신의 혼합물의 준비; 3.5g 파트 A 및 0.37g 파트 B(10:1 비)를 포함하는 Nusil MED 4011의 실리콘 조성의 준비; 각각 0.5g의 실리콘 및 여러 가지 계면활성제 혼합물 중량을 가진 4개의 원심 튜브의 준비{여러 가지 계면활성제 혼합물 중량은, A. 0.05g 계면활성제 혼합물: 9% 계면활성제, 0.09% 플루오레신; B. 0.1g 계면활성제 혼합물: 16.5% 계면활성제, 0.17% 플루오레신; C. 0.15g 계면활성제 혼합물: 22.85% 계면활성제, 0.23% 플루오레신; D. 0.0015g 계면활성제 혼합물: 0% 계면활성제, 0.3% 플루오레신이다}; 4개의 제형 각각을 주사기 및 바늘을 사용하여 각각의 테플론 튜브에 주입하기; 주입된 튜브를 오븐에서 45분간 140℃에서 경화시키기; 각ㄱ각의 튜브를 4mm 길이의 3개의 피스(pieces)로 절단하기; 및 절단된 각각의 피스를 0.3mL의 버퍼를 포함하는 원심 튜브 내에 잠그기가 포함된다.
데이터 수집에는: 24, 48, 72, 192, 및 312 시간의 시점에서 샘플을 수집하기; 각각의 샘플을 UV 스펙트럼 분석하기; 테플론 튜브의 크기(4mm 길이, 0.031 인치 내경)를 사용하여 각각의 추출 레이트를 μg/mL/hr로부터 μg/cm2/hr로 변환하기; 각각의 계면활성제의 레이트를 비교하기 위해 시간 대 추출 레이트를 위한 데이터를 플롯팅(plot)하기가 포함된다.
분석은, 표 1에 보여진 바와 같이, 각각의 추출 레이트의 추세를 지수 곡선에 맞추기 작업을 포함하였다.
| 샘플 # | % 계면활성제 | % 플루오레신 | R2 | 추세 방정식 |
| A | 9.0 | 0.09 | 0.9497 | 636.66×-1.1161 |
| B | 16.5 | 0.17 | 0.8785 | 4289.6×-1.3706 |
| C | 22.85 | 0.23 | 0.9554 | 1762.0×-1.0711 |
| D | 0 | 0.30 | 0.9478 | 1142.1×-1.2305 |
표 1의 추세 방정식은 다음의 사항을 보여준다. 데이터는, R2의 값이 0.8785 내지 09554일 때 지수 곡선에 양호하게 맞는다. 추세 방정식은 -1.0711 내지 -1.3706의 지수 계수를 보인다. 추출 레이트는 계면활성제의 레벨의 증가에 따라 증가되었다. 비교적 유사한 양의 플루오레신에도 불구하고, 샘플 C와 샘플 D 사이에는 추출 레이트의 극적인 증가가 있으며, 이것은, 실리콘 매트릭스에 대한 계면활성제의 첨가는 수용성 화합물의 추출 레이트에 극적으로 영향을 미친다는 것을 입증한다. 샘플 A는 단지 1/3의 양의 플루오레신만 포함함에도 불구하고, 샘플 A의 추출 레이트는 샘플 D의 추출 레이트에 필적한다. 이것 역시, 추출 레이트가 실리콘 매트릭스에 대한 계면활성제의 첨가에 의해 영향을 받을 수 있다는 것을 입증한다.
-1.0711 내지 -1.3706의 추세 방정식 지수 계수가 1차(first order) 릴리스와 일치하지만, 데이터는, 코어로부터의 플루오레신의 큰 덩어리의 릴리스가 관찰되는 초기 48 시간의 기간을 포함한다. 치료 레벨에서 지속된 릴리스의 기간이 뒤따르는, 높은 레벨의 치료 약제가 공급되는 2 내지 3일의 그러한 초기 세척(washout) 기간은, 몇몇 실시예에서, 예를 들면, 짧은 시간 기간 동안의 상승된 레벨이 참을 수 있고 눈에 가속된 효과를 줄 수 있는 경우에, 도움이 될 수 있다. 본 발명의 실시와 관련된 작업은, 48 시간 뒤에, 추출 데이터는 0차에 더 가까울 수 있으며, 예를 들면 약 0차로부터 약 1차의 범위에 있을 수 있다.
도 30은, 본 발명의 실시예들에 따른, 치료 약제와 검출 디바이스(3050)를 가진 약제 공급 임플랜트(3000)의 단면도이다. 임플랜트(3000)는, 인접 단부(3012)와 말단 단부(3014)를 가지며 내부에 검출제를 가진 코어(3010)를 포함한다. 도시된 실시예에서, 코어(3010)는 또한 치료 약제를 포함한다. 코어(3010)는, 치료 약제의 봉입체(3040)를 포함하는 매트릭스(3030)를 포함한다. 봉입체(3040)는, 농축된 형태의 치료 약제 예를 들면 액체 또는 고체 형태의 치료 약제를 포함할 수 있고, 치료 약제는 시간에 걸쳐 코어(3010)의 매트릭스(3030)로 분해될 수 있다. 매트릭스(3030)는 실리콘 매트릭스 등을 포함할 수 있고, 매트릭스(3030) 내의 검출제와 치료 약제의 혼합물은 비균질할 수 있다. 코어(3010), 매트릭스(3030), 봉입체(3040), 및 치료 약제는 본 출원에 설명된 임의의 코어, 매트릭스, 봉입체, 및 치료 약제를 포함할 수 있다. 많은 실시예에서, 비균질 혼합물은, 검출제와 치료 약제로 포화되는 실리콘 매트릭스 부분, 및 검출제와 치료 약제의 봉입체를 포함하는 봉입 부분을 포함할 수 있어, 비균질 혼합물은 다상 비균질 혼합물을 포함한다. 몇몇 실시예에서, 매트릭스(3030)는 봉입체(3040)를 봉입하며, 봉입체(3040)는, 약 1μm 내지 약 100μm의 크기를 가진 미세입자를 포함할 수 있다. 봉입된 봉입체는, 검출제와 치료 약제가 코어로부터 릴리스되는 동안에, 매트릭스(3030)가 검출제와 치료 약제로 실질적으로 포화되도록, 미세입자를 봉입하는 둘러싸는 고체 매트릭스, 예를 들면 실리콘 내로 분해된다. 치료 약제는, 임플랜트(3000)가 신체에 이식될 때 바람직한 반응을 제공하기 위해 치료 레벨로 릴리스된다. 약제 코어는 1주 내지 5년, 더 구체적으로는 3 내지 24개월의 범위에서, 효율적인 레이트로 치료 약제를 릴리스할 수 있다. 몇몇 실시예에서, 치료 레벨은 선량(dose) 관리된 양보다 작거나, 선량 관리된 양의 5 내지 10%이며, 통상적으로는 장기간 매일 선량 관리된 양의 10%보다 작고, 자주 5%보다 작다. 선량 관리된 양은 복용(oral) 선량이거나 주입 가능 선량일 수 있다.
코어(3010)의 말단 단부(3014)에 검출 디바이스(3050)가 있다. 검출 디바이스(3050)는, 신체 내에 위치되었을 때 임플랜트(3000)의 검출 및/또는 식별을 보조하는 임의의 디바이스일 수 있다. 일실시예에서, 검출 디바이스(3080)는, 임플랜트의 검출 및/또는 임플랜트들의 복수의 다른 속성 중에서 임플랜트의 속성의 식별을 가능하게 하는 검출 신호를 포함할 수 있다. 일실시예에서, 전달 신호는, RFID 검출기에 의해 검출할 수 있는 RFID 칩의 무선 신호를 포함하고, 신호는 무선 신호 식별 신호를 포함한다. 다른 실시예에서, 신호는, 자기 검출기로 검출할 수 있는 재료, 또는 초음파 검출기로 검출할 수 있는 초음파 반사 재료로부터의 자기 신호를 포함한다.
코어(3010)와 검출기(3050)는 시드 본체(3020)의 채널 내에 장착된다. 시드 본체(3020)는 치료 약제에 대해 실질적으로 투과성이어서, 치료 약제는, 시드 본체(3020)에 의해 덮이지 않은 코어(3010)의 인접 단부(3012) 상의 표면으로부터 릴리스된다. 검출기(3050)는 또한 시드 본체(3020) 내로 성형될 수 있다.
임플랜트(3000)에 사용되는 치료 약제는 여러 가지 치료 및 상태에 사용될 수 있고, 발명의 명칭이 "코눈물 장치를 위한 약제 공급 방법, 구조 및 조성"인 미국 출원 번호 11/695,537, 발명의 명칭이 "약제 치료를 위한 코눈물 배수 장치 임플랜트"인 미국 출원 번호 11/695,545, 발명의 명칭이 "광학적 검출의 금지를 위한 약제 공급 임플랜트"인 미국 출원 번호 60/871,867, 발명의 명칭이 "약제 공급을 위한 임플랜트를 가진 코눈물 배수 장치"인 미국 출원 번호 60/970,709, 및 발명의 명칭이 "다중 약제 공급 장치, 및 약제과 눈물점 임플랜트의 조합"인 미국 출원 번호 60/970,820에 기술된 치료 약제를 포함할 수 있다.
도 31은, 신체 상태를 치료하기 위해 신체(3100) 내에 있는 약제 공급 치료 임플랜트(3000)를 도시하고 있다. 치료 임플랜트(3000)는, 치료 약제를 포함하는 약제 코어 및 상술한 검출기를 가진 지속적 릴리스 임플랜트이다. 치료 임플랜트는 공지된 수단에 의해 이식될 수 있다.
사용시에, 치료 임플랜트(3000)는 신체(3100)에 이식되며, 신체의 유체는 약제 코어의 노출된 표면과 접촉되어, 치료 약제를 릴리스한다. 임플랜트 위치에 따라, 혈액과 같이 치료 임플랜트에 인접한 임의의 유체는 노출된 표면과 접촉되어, 치료 약제를 릴리스할 수 있다. 치료 임플랜트 위치는, 어깨, 무릎, 손목, 손가락 등에 인접한 관절에 국부적 약제 공급을 위한 신체 위치, 또는 외상 위치, 또는 종양 위치, 일반적 약제 공급을 위한 복부와 같은 다른 위치를 포함할 수 있다. 치료 임플랜트(3000)는, 상기 열거된 신체 위치와 같은 신체 위치 근처에 치료 임플랜트(3000)를 유지하기 위해 본 기술분야에서 공지되어 있는 하나 이상의 유지 부재를 포함할 수 있다.
치료 임플랜트(3000) 내에 있는 검출 디바이스(3050)는 여러 가지 방식으로 검출 및/또는 식별될 수 있다. 예를 들면, 몇몇 실시예에서, 검출 디바이스(3050)는, 임플랜트(3000)를 검출 및/또는 식별할 수 있는 검출 장치(3110)과 통신(3105)할 수 있다. 검출 장치(3110)은, 위에서 검출 장치(1065) 및 장치(2800)과 관련하여 논의된 임의의 면모 또는 모든 면모를 포함할 수 있다. 예를 들면, 검출 장치(3110)은, RFID 칩을 검출하기 위한 RFID 검출 장치, 자기 재료를 검출하기 위한 자기 검출기 장치, 초음파 반사 재료를 검출하기 위한 초음파 검출 장치 또는 여기에 기술된 임의의 다른 검출 장치를 포함할 수 있다.
일실시예에서, 치료 임플랜트(3000)는 종양학에 사용되는데, 국부 치료 임플랜트 약제 공급은, 수술 후에 종양 사이트를 치료하는 추가적 이점을 가능하게 하여, 신체의 나머지에 대한 부수적 손상을 최소화한다. 한 가지 예는, 가슴 종양을 위한 덩어리절제술 또는 전립선 암의 수술 치료일 것이며, 치료 임플랜트는 암 사이트 근처에 이식될 것이다. 실제로, 임의의 고체 종양이 타겟일 것이며, 치료 임플랜트는 종양 근처에 이식된다.
관절에서, 비-스테로이드 비-염증 약제(NSAID)이, 골관절염 및 류마티스양관절염과 같은 것의 치료를 위해 사용될 수 있다. NSAID를 국부적으로 공급하면, 위 궤양 또는 출혈, 및 가능하게는 위 또는 내장의 벽에 있는 가능하게는 생명을 위협하는 천공(립(rips) 또는 구멍)을 포함할 수 있는 위장관 문제(위 또는 내장에서의 문제)와 같이 전신성 콕스 II 억제제(systemic cox II inhibitors)와 관련되는 위험을 감소시킬 것이다. 이러한 실시예에서, 치료 임플랜트는 NSAID를 국부적으로 공급하기 위해 관절 근처에 위치된다.
또 다른 실시예에서, 치료 임플랜트는, 진통약 또는 항감염약을 공급하는 것과 같이, 외상 사이트에 대한 복수의 약제의 국부적 공급을 위해 사용될 수 있다.
본 발명의 원리의 응용을 설명하기 위해 본 발명의 특정 실시예가 상세히 도시되고 설명되었지만, 본 발명은 그러한 원리를 이탈하지 않고 다르게 구현될 수 있다는 것을 이해할 것이다. 예를 들면, 단수한 기계식 표시기는 임플랜트의 상태에 관한 정보(예를 들면, 임플랜트가 의도된 치료 시간 등을 위해 이식되었다는 것)를 제공하기 위해 사용될 수 있다. 예를 들면, 막(film)의 시간에 따른 부식은 표면의 칼라 또는 반사도를 변경시켜 임플랜트를 변경시킬 수 있어, 색이 있는 재료 또는 형광 재료의 릴리스를 가능하게 하며, 재료 등의 팽창을 가능하게 할 수 있다. 임플랜트의 단순한 화학적 또는 기계적 시계(clock)는 임플랜트가 이식되었을 때 작동되기 시작하고 및/또는 작동을 멈출 수 있어, 임플랜트 및/또는 필요한 제거 일자의 판정을 가능하게 한다.
요약서는, 독자가 기술적 내용의 성질을 신속히 알 수 있게 하기 위해 37 C.F.R. §1.72(b)에 따라 제공된다. 요약서는 청구범위의 범위 또는 의미를 해석하거나 제한하기 위해 사용되지 않는다는 이해를 하면서 제공된다. 또한, 상기 상세 설명에서, 본 명세서의 내용을 능률적으로 만들기 위해 여러 가지 면모들이 함께 그룹핑될 수 있다. 이것은, 설명은 되었지만 청구되지는 않은 면모가 임의의 청구항에 필수적이라고 의도하는 것으로 해석해서는 않 된다. 오히려, 본 발명의 주제는 특정하게 기술된 실시예의 모든 면모보다 작을 수 있다. 따라서, 다음의 청구범위는 상세한 설명에 합체되며, 각각의 청구항은 그 자체로서 별개의 실시예를 나타낸다. 본 발명의 범위는, 첨부된 청구범위가 권리를 가지는 균등물의 전체 범위와 함께, 청구범위를 참조하여 판정되어야 한다.
본 문헌에서 참조하는 모든 발행물, 특허 및 특허 문헌은 인용에 의해 본 명세서에 개별적으로 합체되었다 하더라도, 그 전체가 인용에 의해 본 명세서에 합체된다. 본 문헌과 인용에 의해 상기와 같이 합체된 이들 문헌들 사이의 용도(usage)가 불일치되는 경우에는, 합체된 참조 문헌들의 용도는 본 문헌의 용도를 보충하는 것으로 간주되어야 하며, 대립되는 불일치의 경우에는, 본 문헌의 용도가 우선한다.
본 문헌에서, 특허 문헌에서 일반적이듯이, "하나"라는 용어(terms)는, 임의의 다른 어떤 경우 또는 "적어도 하나" 또는 "하나 이상"이라는 용어를 사용한 것과 상관 없이, 하나 또는 하나 이상을 포함하기 위해 사용되었다. 본 문헌에서, "또는"이라는 용어는 배타적이 아니며, 다시 말해서, 다르게 표시되지 않는 한, "A 또는 B"는 "B가 아니고 A", "A가 아니고 B", 및 "A 및 B"를 포함한다. 첨부된 청구범위에서, "포함하는(including)" 및 "여기에서(in which)"라는 용어는 "포함하는(comprising)" 및 "여기에서(wherein)"라는 각각의 용어의 통상적 영어(English)의 동등어로서 사용된다. 또한, 다음의 청구범위에서, "포함하는(including)" 및 "포함하는(comprising)"이라는 용어는 열린 상태로 종료되며, 즉, 청구항에서 그러한 용어 뒤에 열거된 것에 더하여 추가로 부재를 포함하는 장치, 조립체, 디바이스, 물품 또는 프로세스는 여전히 그 청구항의 범위 내에 있는 것으로 간주된다. 또한, 다음의 청구범위에서, "제1", "제2", "제3" 등의 용어는 단순히 라벨(label)로서 사용되었으며, 그 대상물에 수치적 요구사항을 부과하는 것은 아니다.
여기에 설명된 방법의 실시예 중의 몇몇은 적어도 부분적으로 기계 또는 컴퓨터에 의해 실시될 수 있다. 몇몇 실시예는, 상기 예에서 설명된 방법을 수행하기 위해 전자 디바이스를 구성하도록 작동될 수 있는 명령으로 인코딩된 컴퓨터 판독 가능 매체 또는 기계 판독 가능 매체를 포함할 수 있다. 그러한 방법의 실시에, 마이크로코드, 어셈블리 언어 코드, 고수준 언어 코드 등과 같은 코드를 포함할 수 있다. 그러한 코드는, 여러 가지 방법을 수행하기 위한 컴퓨터 판독 가능 명령을 포함할 수 있다. 코드는 컴퓨터 프로그램 제품의 일부를 형성할 수 있다. 또한, 코드는, 실행시 또는 다른 시간에 하나 이상의 휘발성 또는 비휘발성 컴퓨터 판독 가능 매체에 유형적으로 저장될 수 있다. 이들 컴퓨터 판독 가능 매체에는, 하드 디스크, 제거 가능 자기 디스크, 제거 가능 광학 디스크(예를 들면, 컴팩트 디스크 및 디지털 비디오 디스크), 자기 카세트, 메모리 카드 또는 스틱(sticks), 랜덤 액세스 메모리(RAM), 읽기 전용 메모리(ROM) 등이 포함될 수 있지만, 이들에 제한되지 않는다.
2: 눈
10: 상부 소관
12: 하부 소관
200: 임플랜트
210: 코어
260: 제1 봉입체
300: 눈물점 마개
410: 검출 디바이스
1305: 자계 검출기 회로
10: 상부 소관
12: 하부 소관
200: 임플랜트
210: 코어
260: 제1 봉입체
300: 눈물점 마개
410: 검출 디바이스
1305: 자계 검출기 회로
Claims (102)
- 적어도 부분적으로 눈물점 내에 삽입 가능한 눈물 임플랜트를 포함하며,
상기 눈물 임플랜트는,
임플랜트 코어, 및
임플랜트 본체
를 포함하고,
상기 임플랜트 본체는, 상기 임플랜트 코어를 수용하는 사이즈 및 형상을 가진 임플랜트 공동을 포함하며,
상기 임플랜트 코어와 상기 임플랜트 공동 중 하나 이상은, 별도의 검출기 디바이스를 사용하여 상기 눈물 임플랜트의 자동 검출을 가능하게 하도록 구성된 검출 디바이스를 포함하는,
장치. - 제1항에 있어서,
상기 검출 디바이스는, 상기 검출기 디바이스로 검출 신호를 통신하도록 구성된 무선 주파수 식별기(RFID) 칩을 포함하는, 장치. - 제1항에 있어서,
상기 검출 디바이스는, 상기 검출기 디바이스로 빛을 반사하도록 구성된 발광 재료를 포함하는, 장치. - 제3항에 있어서,
상기 발광 재료는 양자 돗트(quantum dot)를 포함하는, 장치. - 제1항에 있어서,
상기 검출 디바이스는, 상기 검출기 디바이스로 초음파 에너지를 반사하도록 구성된 초음파 반사 재료를 포함하는, 장치. - 제1항에 있어서,
상기 검출 디바이스는, 외부 자계의 인가 및 제거 후에 강자성 성질을 유지할 수 있는 강자성 재료를 포함하며,
유지된 강자성 성질은 상기 검출기 디바이스에 의해 검출될 수 있는,
장치. - 제1항에 있어서,
상기 검출 디바이스는, 상기 검출기 디바이스에 의해 검출될 수 있는 자계를 유지하기 위한 자기 재료를 포함하며,
상기 자기 재료는, 마그네타이트, 금속 분말, 금속 링, 및 탄소 분말 중 하나 이상을 포함하는,
장치. - 제1항에 있어서,
상기 검출 디바이스는, 감지 회로에 대한 상기 눈물 임플랜트의 근접도로 인해 상기 검출기 디바이스의 상기 감지 회로의 특성 임피던스를 변경시키도록 구성된 전기 전도성 재료를 포함하는, 장치. - 제1항에 있어서,
상기 검출 디바이스는, 상기 임플랜트 코어와 상기 임플랜트 공동 중 하나 이상에, 눈의 영역으로부터 상기 눈물 임플랜트를 광학적으로 구별하도록 구성된 광학 대조 재료와 칼라 재료 중 하나 이상을 포함하는, 장치. - 제1항에 있어서,
상기 검출 디바이스는, 자외선 소스에 의해 조명될 때 볼 수 있는 재료를 포함하는, 장치. - 제1항에 있어서,
상기 임플랜트 코어는 지속적 릴리스 안구 제제(ocular agent)를 포함하는, 장치. - 제11항에 있어서,
상기 임플랜트 코어는 상기 제제를 수용하기 위한 시드(sheath)를 포함하며,
상기 검출 디바이스는 상기 시드 내에 배치되어 있는,
장치. - 제1항에 있어서,
상기 임플랜트 본체의 생체 적합성 재료는, 눈에 대한 지속적 릴리스를 위한 제제를 포함하는, 장치. - 제13항에 있어서,
상기 눈물 임플랜트는 상기 임플랜트 본체의 외면에 중합체 코팅을 포함하고,
상기 중합체 코팅은 상기 제제를 포함하는,
장치. - 생체 적합성 재료의 눈물 임플랜트를 형성하는 단계,
상기 눈물 임플랜트의 본체 내에 임플랜트 공동을 형성하는 단계,
상기 공동 내에 임플랜트 코어를 제공하는 단계, 및
상기 임플랜트 코어와 상기 임플랜트 공동 중 하나 이상 내에 검출 디바이스를 제공하는 단계
를 포함하며,
상기 임플랜트 코어는, 눈에 제제를 지속적으로 릴리스하도록 하는 사이즈로 구성되고,
상기 검출 디바이스는, 별도의 검출기 디바이스를 사용하여 상기 눈물 임플랜트의 자동 검출을 가능하게 하도록 구성되는,
방법. - 제15항에 있어서,
상기 검출 디바이스를 제공하는 상기 단계는,
상기 검출기 디바이스로 검출 신호를 통신하도록 구성되는 RFID 칩,
상기 검출기 디바이스로 빛을 반사하도록 구성되는 발광 재료,
상기 검출기 디바이스로 초음파 에너지를 반사하도록 구성되는 초음파 반사 재료,
외부 자계의 인가 및 제거 후에 상기 검출기 디바이스에 의해 검출 가능한 강자성 성질을 유지할 수 있는 강자성 재료,
상기 검출기 디바이스의 감지 회로의 특성 임피던스를 변경시키도록 구성되는 전기 전도성 재료,
눈의 영역으로부터 눈물점 러그(punctum lug)를 광학적으로 구별하도록 구성된 광학 대조 재료,
눈의 영역으로부터 상기 눈물 임플랜트를 광학적으로 구별하기 위한 칼라 재료, 및
자외선 소스로 조명될 때 볼 수 있는 재료
중 하나 이상을 제공하는 단계를 포함하는,
방법. - 제16항에 있어서,
상기 검출 디바이스를 제공하는 상기 단계는 상기 발광 재료를 제공하는 단계를 포함하며,
상기 발광 재료는 양자 돗트를 포함하는,
방법. - 제16항에 있어서,
상기 검출 디바이스를 제공하는 상기 단계는, 상기 강자성 재료를 제공하는 단계를 포함하며,
상기 강자성 재료는, 마그네타이트, 금속 분말, 금속 링, 및 탄소 분말 중 하나 이상을 포함하는,
방법. - 제15항에 있어서,
상기 검출 디바이스를 제공하는 단계는, 상기 검출기 디바이스로 빛을 반사하도록 구성된 상기 발광 재료를 제공하는 단계를 포함하며,
상기 방법은,
발광 소스를 사용하여 제1 파장 범위의 입사광에 상기 눈물 임플랜트를 노출시키는 단계,
상기 검출 디바이스에서 제2 파장 범위의 빛을 검출하는 단계, 및
충분한 반사광이 검출되었을 때 상기 눈물 임플랜트의 근접도를 표시하기 위한 표시를 제공하는 단계
를 포함하고,
수광되는 빛은 상기 눈물 임플랜트로부터 반사되는,
방법. - 제19항에 있어서,
상기 제1 파장 범위는 청색 스펙트럼을 포함하며,
상기 제2 파장 범위는 녹색 스펙트럼을 포함하는,
방법. - 제19항에 있어서,
상기 입사광에 상기 눈물 임플랜트를 노출시키는 상기 단계는, 적외선 스펙트럼의 제1 파장 범위의 빛에 상기 눈물 임플랜트를 노출시키는 단계를 포함하고,
상기 빛을 검출하는 상기 단계는, 적외선 스펙트럼의 제2 파장 범위의 빛을 검출하는 단계를 포함하는,
방법. - 제19항에 있어서,
상기 표시를 제공하는 상기 단계는, 가청 표시를 제공하는 단계를 포함하는, 방법. - 제19항에 있어서,
상기 표시를 제공하는 상기 단계는, 가시성 표시를 제공하는 단계를 포함하는, 방법. - 눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계, 및
별도의 검출기 디바이스를 사용하여 상기 눈물 임플랜트의 상기 검출 디바이스를 검출하는 단계
를 포함하며,
상기 눈물 임플랜트는,
생체 적합성 재료의 임플랜트 본체,
눈으로 제제를 지속적으로 릴리스하는 사이즈로 구성되는 임플랜트 코어, 및
상기 임플랜트 코어 내에 배치되는 상기 제제의 서플라이(supply)
를 포함하며,
상기 임플랜트 본체는, 상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되는 공동을 포함하고,
상기 임플랜트 코어는 상기 임플랜트 본체의 상기 공동 내에 지지되며,
상기 임플랜트 코어와 상기 임플랜트 공동 중 하나 이상은, 상기 별도의 검출기 디바이스를 사용하여 상기 눈물 임플랜트의 자동 검출을 가능하게 하도록 구성되는 검출 디바이스를 포함하고,
상기 서플라이는, 상기 제제를 지속적으로 릴리스하도록 구성되는,
눈 질환을 치료하는 방법. - 제24항에 있어서,
상기 제제는 녹내장 질병을 치료하도록 구성되어 있는, 눈 질환을 치료하는 방법. - 제25항에 있어서,
상기 녹내장 질병은, 안구 고혈압증(ocular hypertension) 또는 1차 개방각 녹내장(primary open angle glaucoma) 중 하나 이상을 포함하는, 눈 질환을 치료하는 방법. - 적어도 부분적으로 눈물점 내로 삽입 가능한 눈물 임플랜트를 포함하며,
상기 눈물 임플랜트는 생체 적합성 재료의 임플랜트 본체를 포함하고,
상기 임플랜트 본체는, 상기 눈물 임플랜트의 검출을 가능하게 하고, 상기 눈물 임플랜트의 하나 이상의 속성을 식별하도록 구성된 검출 디바이스를 포함하는,
장치. - 제27항에 있어서,
상기 검출 디바이스는, 별도의 검출기 디바이스로 속성 정보를 통신하도록 구성된 무선 주파수 식별기(RFID) 칩을 포함하는, 장치. - 제27항에 있어서,
상기 검출 디바이스는 상기 눈물 임플랜트 내에 칼라를 포함하며,
상기 칼라는 상기 눈물 임플랜트의 상기 속성을 식별하는,
장치. - 제29항에 있어서,
상기 검출 디바이스는 발광 재료를 포함하며,
상기 발광 재료는 상기 칼라를 반사시키는,
장치. - 제30항에 있어서,
상기 발광 재료는 양자 돗트를 포함하는, 장치. - 제27항에 있어서,
상기 검출 디바이스는, 자외선 소스로 볼 수 있는 재료를 포함하며,
상기 검출 디바이스는, 자외선 소스로 조명될 때 상기 속성을 식별하는,
장치. - 제27항에 있어서,
상기 검출 디바이스는,
상기 눈물 임플랜트에 의해 추출될 수 있는(elutable) 재료, 및
생-부식성 표면
을 포함하며,
상기 생-부식성 표면은, 상기 속성을 식별하기 위한 재료를 추출하는,
장치. - 제27항에 있어서,
상기 눈물 임플랜트는 지속적 릴리스 안구 제제를 포함하며,
상기 눈물 임플랜트의 상기 속성은, 상기 안구 제제의 유형, 상기 안구 제제의 선량(dose), 및 상기 안구 제제의 릴리스가 완료되는 때의 표시 중 하나 이상을 포함하는,
장치. - 제27항에 있어서,
상기 속성은, 상기 눈물 임플랜트의 제조자, 상기 눈물 임플랜트의 제조자의 제조 번호, 상기 눈물 임플랜트가 이식된 날자, 상기 임플랜트의 유효일자, 상기 눈물 임플랜트가 이식된 위치의 표시, 의사를 식별하기 위한 표시, 및 환자를 식별하기 위한 표시 중 하나 이상을 포함하는, 장치. - 생체 적합성 재료의 눈물 임플랜트를 형성하는 단계, 및
임플랜트 본체 내에 검출 디바이스를 배치하는 단계
를 포함하며,
눈물점 마개는 상기 임플랜트 본체를 포함하고,
상기 검출 디바이스는, 상기 눈물 임플랜트의 검출을 가능하게 하고, 상기 눈물 임플랜트의 하나 이상의 속성을 식별하도록 구성되는,
방법. - 제36항에 있어서,
상기 검출 디바이스는,
별도의 검출기 디바이스로 속성 정보를 통신하도록 구성되는 RFID 칩,
상기 눈물 임플랜트 내의 칼라,
발광 재료,
자외선 소스로 볼 수 있는 재료, 및
상기 눈물 임플랜트에 의해 추출 가능한 재료
중 하나 이상을 포함하며,
상기 칼라는 상기 눈물 임플랜트의 상기 속성을 식별하고,
상기 발광 재료에 의해 반사된 상기 칼라는 상기 속성을 식별하며,
상기 검출 디바이스는, 상기 자외선 소스로 조명될 때 상기 속성을 식별하고,
상기 추출 가능한 재료는 상기 속성을 식별하는,
방법. - 제36항에 있어서,
상기 눈물 임플랜트 내에 지속적 릴리스 안구 제제를 제공하는 단계를 더 포함하며,
상기 검출 디바이스는, 상기 안구 제제의 유형, 상기 안구 제제의 선량, 및 상기 안구 제제의 릴리스가 완료되는 때의 표시 중 하나 이상의 식별을 가능하게 하도록 구성되는,
방법. - 제36항에 있어서,
상기 검출 디바이스는, 상기 눈물 임플랜트의 제조자, 상기 눈물 임플랜트의 제조자의 제조 번호, 상기 눈물 임플랜트가 이식된 날자, 상기 임플랜트의 유효일자, 상기 눈물 임플랜트가 이식된 위치의 표시, 의사를 식별하기 위한 표시, 및 환자를 식별하기 위한 표시 중 하나 이상의 식별을 가능하게 하도록 구성되는, 방법. - 눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계,
상기 눈물 임플랜트 내에 포함된 검출 디바이스를 검출하는 단계, 및
상기 검출 디바이스를 통해 상기 눈물 임플랜트의 하나 이상의 속성을 식별하는 단계
를 포함하는, 눈의 질환을 치료하는 방법. - 제40항에 있어서,
상기 검출 디바이스를 검출하는 상기 단계는, 상기 눈물 임플랜트 내에 포함된 RFID 칩과 통신하는 단계를 포함하며,
상기 속성을 식별하는 상기 단계는, 상기 RFID 칩과 별도의 검출기 디바이스 사이에서 속성 정보를 통신하는 단계를 포함하는,
눈의 질환을 치료하는 방법. - 제40항에 있어서,
상기 검출 디바이스를 검출하는 상기 단계는, 상기 눈물 임플랜트 내의 칼라를 검출하는 단계를 포함하며,
상기 속성을 식별하는 상기 단계는, 상기 칼라를 사용하여 상기 속성을 식별하는 단계를 포함하는,
눈의 질환을 치료하는 방법. - 제42항에 있어서,
상기 눈물 임플랜트 내의 상기 칼라를 검출하는 상기 단계는, 상기 눈물 임플랜트 내에 포함된 발광 재료에 의해 반사되는 칼라를 검출하는 단계를 포함하는, 눈의 질환을 치료하는 방법. - 제42항에 있어서,
상기 눈물 임플랜트 내의 상기 칼라를 검출하는 상기 단계는, 상기 눈물 임플랜트 내에 포함된 양자 돗트에 의해 반사되는 칼라를 검출하는 단계를 포함하는, 눈의 질환을 치료하는 방법. - 제40항에 있어서,
상기 검출 디바이스를 검출하는 상기 단계는, 자외선 소스를 사용하여 볼 수 있는 상기 눈물 임플랜트 내의 상기 재료를 검출하는 단계를 포함하며,
상기 속성을 식별하는 상기 단계는, 상기 재료가 상기 자외선 소스를 사용하여 조명될 때 상기 속성을 식별하는 단계를 포함하는,
눈의 질환을 치료하는 방법. - 제40항에 있어서,
상기 검출 디바이스를 검출하는 상기 단계는, 상기 눈물 임플랜트에 의해 추출 가능한 재료를 검출하는 단계를 포함하며,
상기 눈물 임플랜트의 상기 속성을 식별하는 상기 단계는, 상기 추출 가능 한 재료로부터 상기 속성을 식별하는 단계를 포함하는,
눈의 질환을 치료하는 방법. - 제46항에 있어서,
상기 눈물 임플랜트는 지속적 릴리스 안구 제제를 포함하며,
상기 눈물 임플랜트의 상기 속성은, 상기 안구 제제의 유형, 상기 안구 제제의 선량, 및 상기 안구 제제의 릴리스가 완료되는 때의 표시 중 하나 이상을 포함하는,
눈의 질환을 치료하는 방법. - 제40항에 있어서,
상기 속성을 식별하는 상기 단계는, 상기 눈물 임플랜트의 제조자, 상기 눈물 임플랜트의 제조자의 제조 번호, 상기 눈물 임플랜트가 이식된 날자, 상기 임플랜트의 유효일자, 상기 눈물 임플랜트가 이식된 위치의 표시, 의사를 식별하기 위한 표시, 및 환자를 식별하기 위한 표시 중 하나 이상을 식별하는 단계를 포함하는, 눈의 질환을 치료하는 방법. - 적어도 부분적으로 눈물점 내로 삽입 가능한 눈물 임플랜트를 포함하며,
상기 눈물 임플랜트는 임플랜트 본체를 포함하고,
상기 임플랜트 본체는 검출 디바이스를 포함하며,
상기 검출 디바이스는,
외부 자계의 인가 및 제거 후에 강자성 성질을 유지할 수 있는 강자성 재료,
별도의 초음파 검출기 디바이스로 상기 눈물 임플랜트의 자동 검출을 가능하게 하도록 구성된 초음파 반사 재료, 및
상기 임플랜트 본체 내에 포함되어 있고, 눈물 임플랜트 검출기 디바이스와 통신하도록 구성된 무선 주파수 식별기(RFID)
중 하나 이상을 포함하는,
장치. - 제49항에 있어서,
상기 검출 디바이스는 강자성 재료를 포함하며,
상기 강자성 재료는, 마그네타이트, 금속 분말, 금속 링, 및 탄소 분말 중 하나 이상을 포함하는,
장치. - 제49항에 있어서,
상기 검출 디바이스는 초음파 반사 재료를 포함하며,
상기 초음파 반사 재료는 상기 임플랜트 본체의 생체 적합성 재료 내에 배치되어 있고,
상기 초음파 반사 재료는, 상기 눈물 임플랜트에 초음파 에너지를 인가할 때 상기 임플랜트 본체의 형상을 변경시키도록 구성되어 있는,
장치. - 제51항에 있어서,
상기 초음파 반사 재료는 압전 재료를 포함하는, 장치. - 제49항에 있어서,
눈에 대한 지속적 릴리스를 위한 제제는 상기 임플랜트 본체 내에 배치되어 있는, 장치. - 눈의 질환을 치료하는 방법에 있어서,
눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계, 및
별도의 초음파 검출기 디바이스로 검출 디바이스를 검출함으로써 상기 눈물 임플랜트를 검출하는 단계
를 포함하며,
상기 눈물 임플랜트는 임플랜트 본체를 포함하고,
상기 임플랜트 본체는 상기 검출 디바이스를 포함하며,
상기 검출 디바이스는,
외부 자계의 인가 및 제거 후에 강자성 성질을 유지할 수 있는 강자성 재료,
상기 별도의 초음파 검출기 디바이스로 상기 눈물 임플랜트의 자동 검출을 가능하게 하도록 구성되는 초음파 반사 재료,
상기 임플랜트 본체 내에 포함되고, 눈물 임플랜트 검출기 디바이스와 통신하도록 구성되는 무선 주파수 식별기(RFID), 및
임플랜트 코어 내에 배치되는 제제의 서플라이
중 하나 이상을 포함하며,
상기 서플라이는 상기 제제를 지속적으로 릴리스하도록 구성되는,
눈의 질환을 치료하는 방법. - 제54항에 있어서,
상기 제제는 녹내장 질병을 치료하도록 구성되는, 눈의 질환을 치료하는 방법. - 제54항에 있어서,
상기 녹내장 질병은, 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 이상을 포함하는, 눈의 질환을 치료하는 방법. - 눈물 임플랜트에 입사광을 제공하기 위한 발광원,
상기 눈물 임플랜트의 발광 재료로부터 반사되는 특정 파장 범위의 빛을 통과시키도록 구성된 광학 필터,
상기 필터에 의해 통과되는 빛을 수광하고, 충분한 빛이 수광되었을 때 상기 눈물 임플랜트의 근접도를 표시하기 위해 응답 전기 신호를 발생시키도록 구성된 광검출 디바이스, 및
상기 광검출 디바이스에 통신 가능하게 결합되어 있고, 상기 전기 신호를 수신하였을 때 사용자에게 마개 검출의 표시를 제공하기 위한 표시기
를 포함하는, 검출 장치. - 제57항에 있어서,
상기 발광원은, 제1 파장 범위를 가진 입사광을 제공하고,
상기 발광 재료는 제2 파장 범위의 입사광을 반사시키는,
검출 장치. - 제57항에 있어서,
상기 발광원은 청색 스펙트럼의 입사광을 제공하고,
상기 발광 재료는 녹색 스펙트럼의 입사광을 반사시키는,
검출 장치. - 제57항에 있어서,
상기 발광원은, 적외선 스펙트럼 내의 제1 파장 범위를 가진 입사광을 제공하고,
상기 발광 재료는 적외선 스펙트럼 내의 다른 제2 파장 범위의 입사광을 반사시키는,
검출 장치. - 제57항에 있어서,
상기 표시기는 마개 검출의 시각적 표시를 제공하는, 검출 장치. - 제57항에 있어서,
상기 표시기는 마개 검출의 가청 표시를 제공하는, 검출 장치. - 적어도 부분적으로 눈물점 내로 삽입 가능한 눈물 임플랜트, 및
눈물 임플랜트 검출기 디바이스
를 포함하며,
상기 눈물 임플랜트는 생체 적합성 재료의 임플랜트 본체를 포함하고,
상기 임플랜트 본체는, 외부 자계의 인가 및 제거 후에 강자성 성질을 유지할 수 있는 강자성 재료를 포함하며,
상기 눈물 임플랜트 검출기 디바이스는,
자계 검출 회로, 및
상기 자계 검출 회로에 통신 가능하게 결합되어 있고, 상기 눈물 임플랜트의 자계를 검출하였을 때 표시하도록 구성되어 있는 표시 디바이스
를 포함하는,
검출 장치. - 제63항에 있어서,
상기 자계 검출 회로는 홀 효과 센서를 포함하는, 검출 장치. - 제64항에 있어서,
상기 자계 검출 회로는, 상기 자계 검출 회로에 통신 가능하게 결합되어 있고, 상기 홀 효과 센서의 출력에서의 전압이 제1 임계치를 초과할 때 상기 표시 디바이스에 전기 신호를 제공하기 위한 비교 회로를 포함하는, 검출 장치. - 제65항에 있어서,
상기 비교 회로는, 상기 홀 효과 센서의 출력에서의 전압이 제1 임계치를 초과하고 제2 임계치보다 작을 때 상기 표시 디바이스에 전기 신호를 제공하는, 검출 장치. - 제63항에 있어서,
상기 표시 디바이스는 가청 표시를 제공하는, 검출 장치. - 제63항에 있어서,
상기 표시 디바이스는 시각적 표시를 제공하는, 검출 장치. - 제63항에 있어서,
상기 눈물 임플랜트 검출기 디바이스는, 인접 단부와 말단 단부를 포함하는 기다란 하우징을 포함하며,
상기 자계 검출 회로는, 상기 인접 단부에 또는 그 근처에 배치된 자계 센서를 포함하는,
검출 장치. - 제69항에 있어서,
상기 표시 디바이스는 시각적 표시를 제공하고, 상기 자계 센서로부터 말단 방향으로 있는 지점에 있는, 검출 장치. - 제63항에 있어서,
상기 눈물 임플랜트 검출 디바이스는, 대상물의 눈 위에 맞는 형상을 가진 하우징을 포함하는, 검출 장치. - 생체 적합성 재료의 눈물 임플랜트를 형성하는 단계,
상기 눈물 임플랜트 내에 강자성 재료를 제공하는 단계, 및
상기 눈물 임플랜트가 더 이상 자계에 노출되지 않을 때 강자성 성질을 보이도록, 상기 눈물 임플랜트를 상기 자계에 노출시키는 단계
를 포함하는 방법. - 제72항에 있어서,
상기 눈물 임플랜트를 형성하는 상기 단계는, 생체 적합성 재료의 임플랜트 본체를 형성하는 단계를 포함하고,
상기 눈물 임플랜트 내에 강자성 재료를 제공하는 상기 단계는, 상기 강자성 재료를 상기 임플랜트 본체의 상기 생체 적합성 재료 내에 배치하는 단계를 포함하는,
방법. - 제72항에 있어서,
상기 눈물 임플랜트를 형성하는 상기 단계는,
상기 눈물 임플랜트의 본체 내에 공동을 형성하는 단계, 및
상기 공동 내에 임플랜트 코어를 제공하는 단계
를 포함하며,
상기 임플랜트 코어는, 눈에 대한 지속적 릴리스를 위한 충분한 양의 제제를 제공하기 위한 사이즈 및 형상을 가지고,
상기 눈물 임플랜트 내에 강자성 재료를 제공하는 상기 단계는, 상기 눈물 임플랜트의 상기 임플랜트 코어 내에 강자성 재료를 제공하는 단계를 포함하는,
방법. - 제74항에 있어서,
상기 제제를 수용하기 위해 상기 임플랜트 코어에 시드를 형성하는 단계를 더 포함하며,
상기 임플랜트 코어 내에 강자성 재료를 제공하는 상기 단계는, 상기 강자성 재료를 상기 시드 내에 배치하는 단계를 포함하는,
방법. - 제72항에 있어서,
상기 눈물 임플랜트 내에 강자성 재료를 제공하는 상기 단계는, 상기 눈물 임플랜트 내에 마그네타이트를 제공하는 단계를 포함하는, 방법. - 눈의 질환을 치료하는 방법에 있어서,
눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계, 및
눈물 임플랜트 검출 디바이스로로 상기 눈물 임플랜트의 강자성 성질을 검출하는 단계
를 포함하며,
상기 눈물 임플랜트는,
생체 적합성 재료의 임플랜트 본체,
상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되는 상기 임플랜트 본체 내에 있는 공동,
상기 공동 내에 있는 임플랜트 코어, 및
상기 임플랜트 코어 내에 배치되는 제제의 서플라이
를 포함하고,
상기 임플랜트 본체는, 외부 자계의 인가 및 제거 후에 강자성 성질을 유지할 수 있는 강자성 재료를 포함하며,
상기 임플랜트 코어는, 눈에 대한 지속적 릴리스를 위한 충분한 양의 제제를 제공하기 위한 사이즈 및 형상을 가지고,
상기 서플라이는 상기 제제를 지속적으로 릴리스하도록 구성되는,
눈의 질환을 치료하는 방법. - 제77항에 있어서,
상기 제제는 녹내장 질병을 치료하도록 구성되는, 눈의 질환을 치료하는 방법. - 제78항에 있어서,
상기 녹내장 질병은, 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 이상을 포함하는, 눈의 질환을 치료하는 방법. - 눈물점 내로 삽입 가능한 눈물 임플랜트, 및
눈물 임플랜트 검출기 디바이스
를 포함하며,
상기 눈물 임플랜트는,
생체 적합성 재료의 임플랜트 본체, 및
상기 임플랜트 본체 내에 있는 전기 전도성 재료
를 포함하고,
상기 눈물 임플랜트 검출기 디바이스는,
특성 임피던스를 가진 감지 회로,
상기 감지 회로에 대한 상기 눈물 임플랜트의 근접으로 인한 상기 특성 임피던스의 변화를 검출하도록 구성된 검출 회로, 및
상기 검출 회로에 통신 가능하게 결합되어 있고, 상기 특성 임피던스의 변화를 검출하였을 때 표시하도록 구성된 표시기 디바이스
를 포함하는,
검출 장치. - 제80항에 있어서.
상기 전기 전도성 재료는, 상기 임플랜트 본체의 상기 생체 적합성 재료 내에 배치된 전기 전도성 입자를 포함하는, 검출 장치. - 제80항에 있어서.
상기 눈물 임플랜트는, 지속적 릴리스 안구 제제를 포함하는 임플랜트 코어를 포함하며,
상기 임플랜트 본체는, 상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되어 있는 공동을 포함하고,
상기 공동은 상기 임플랜트 코어를 수용하도록 하는 사이즈 및 형상을 가지고 있는,
검출 장치. - 제82항에 있어서.
상기 임플랜트 코어는 상기 제제를 수용하기 위해 시드를 포함하며,
상기 전기 전도성 재료는 상기 시드 내에 배치되어 있는,
검출 장치. - 제80항에 있어서.
상기 전기 전도성 재료는, 강철, 은, 금, 및 알루미늄 중 하나 이상을 포함하는, 검출 장치. - 제80항에 있어서.
상기 감지 회로는, 상기 특성 임피던스에 기초하여 고유 응답 주파수를 포함하며,
상기 검출 회로는, 고유 응답 주파수의 이동으로부터 상기 특성 임피던스의 변화를 검출하는,
검출 장치. - 제80항에 있어서.
상기 특성 임피던스는 특성 인덕턴스를 포함하며,
상기 검출 회로는, 상기 감지 회로에 대한 상기 눈물 임플랜트의 근접으로 인한 상기 특성 인덕턴스의 변화를 검출하도록 구성되어 있는,
검출 장치. - 제80항에 있어서.
상기 특성 임피던스는 특성 커패시턴스를 포함하며,
상기 검출 회로는, 상기 감지 회로에 대한 상기 눈물 임플랜트의 근접으로 인한 상기 특성 커패시턴스의 변화를 검출하도록 구성되어 있는,
검출 장치. - 제80항에 있어서.
눈에 대한 지속적 릴리스를 위한 상기 제제는 상기 임플랜트 본체 내에 배치되어 있는, 검출 장치. - 눈물 임플랜트를 제공하는 단계,
상기 눈물 임플랜트의 근접으로 인한 감지 회로의 특성 임피던스의 변화를 검출함으로써, 상기 눈물 임플랜트에 접촉하지 않고, 상기 눈물 임플랜트를 검출하는 단계, 및
상기 눈물 임플랜트가 검출되었는지에 관한 정보를 사용자에게 또는 자동화 프로세서에 제공하는 단계
를 포함하는, 방법. - 제89항에 있어서,
상기 특성 임피던스의 변화를 검출하는 상기 단계는, 상기 감지 회로의 고유 응답 주파수의 이동을 검출하는 단계를 포함하는, 방법. - 제89항에 있어서,
상기 눈물 임플랜트를 제공하는 상기 단계는, 생체 적합성 재료, 및 상기 생체 적합성 재료 내에 배치되는 전기 전도성 재료를 포함하는 상기 눈물 임플랜트를 제공하는 단계를 포함하는, 방법. - 제89항에 있어서,
상기 눈물 임플랜트를 제공하는 상기 단계는,
상기 눈물 임플랜트의 본체 내에 있는 공동, 및
상기 공동 내에 있는 임플랜트 코어
를 포함하는 눈물 임플랜트를 제공하는 단계를 포함하며,
상기 공동은, 상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되고,
상기 임플랜트 코어는, 제제를 지속적으로 릴리스하도록 하는 사이즈로 구성되며,
상기 임플랜트 코어는 전기 전도성 재료를 포함하는,
방법. - 제92항에 있어서,
상기 제제를 수용하기 위해 상기 임플랜트 코어에 시드를 제공하는 단계, 및
상기 전기 전도성 재료를 상기 시드 내에 제공하는 단계
를 더 포함하는,
방법. - 눈의 질환을 치료하는 방법에 있어서,
눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계, 및
감지 회로에 대한 상기 눈물 임플랜트의 근접으로 인한 상기 감지 회로의 특성 임피던스의 변화를 검출함으로써, 상기 눈물 임플랜트를 검출하는 단계
를 포함하며,
상기 눈물 임플랜트는,
생체 적합성 재료의 임플랜트 본체,
눈에 제제를 지속적으로 릴리스하도록 하는 사이즈로 구성되는 임플랜트 코어,
상기 임플랜트 코어 내에 배치되는 상기 제제의 서플라이, 및
상기 임플랜트 본체 내에 있는 전기 전도성 재료
를 포함하고,
상기 임플랜트 본체는, 상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되는 공동을 포함하며,
상기 임플랜트 코어는 상기 임플랜트 코어의 상기 공동 내에 지지되고,
상기 서플라이는 상기 제제를 지속적으로 릴리스하도록 구성되는,
눈의 질환을 치료하는 방법. - 제94항에 있어서,
상기 제제는 녹내장 질병을 치료하도록 구성되는, 눈의 질환을 치료하는 방법. - 제95항에 있어서,
상기 녹내장 질병은, 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 이상을 포함하는, 눈의 질환을 치료하는 방법. - 이미지 센서, 및
이미지 분석기 회로를 포함하며,
상기 이미지 분석기 회로는, 이미지의 다른 영역에서의 이미지 대조(contrast)를 초과하는 이미지 대조를 가진 이미지 부분의 위치를 검출하여, 눈물 임플랜트의 일부의 이미지가 상기 이미지 내에 있는지에 대한 표시를 제공하도록 구성되어 있는,
검출 장치. - 제97항에 있어서,
상기 이미지 센서는, 카메라 내에 포함되어 있는 디지털 이미지 센서인, 검출 장치. - 제97항에 있어서,
적외선 발광기를 더 포함하며,
상기 이미지 센서는 적외선 이미지 센서를 포함하는,
검출 장치. - 눈의 질환을 치료하는 방법에 있어서,
눈물 임플랜트를 대상물의 하나 이상의 눈물점 내로 삽입하는 단계,
대상물의 상기 눈물점의 영역의 이미지를 얻는 단계, 및
상기 이미지의 다른 영역에서의 이미지 대조를 초과하는 이미지 대조를 가진 상기 이미지 부분의 위치를 검출함으로써, 상기 눈물 임플랜트를 검출하는 단계
를 포함하며,
상기 눈물 임플랜트는,
생체 적합성 재료의 임플랜트 본체,
눈에 제제를 지속적으로 릴리스하도록 하는 사이즈로 구성되는 임플랜트 코어, 및
상기 임플랜트 코어 내에 배치되는 상기 제제의 서플라이
를 포함하고,
상기 임플랜트 본체는, 상기 임플랜트 본체의 단부로부터 상기 임플랜트 본체 내로 내향 연장되는 공동을 포함하며,
상기 임플랜트 본체의 상기 공동은 상기 임플랜트 코어를 수용하도록 하는 사이즈 및 형상을 가지고,
상기 임플랜트 코어는, 눈의 영역으로부터 상기 눈물 임플랜트를 구별하도록 구성되는 광학 대조 재료를 포함하며,
상기 서플라이는 상기 제제를 지속적으로 릴리스하도록 구성되는,
눈의 질환을 치료하는 방법. - 제100항에 있어서,
상기 제제는 녹내장 질병을 치료하도록 구성되는, 눈의 질환을 치료하는 방법. - 제101항에 있어서,
상기 녹내장 질병은, 안구 고혈압증 또는 1차 개방각 녹내장 중 하나 이상을 포함하는, 눈의 질환을 치료하는 방법.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US97080707P | 2007-09-07 | 2007-09-07 | |
| US60/970,807 | 2007-09-07 | ||
| US5090108P | 2008-05-06 | 2008-05-06 | |
| US61/050,901 | 2008-05-06 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20100067099A true KR20100067099A (ko) | 2010-06-18 |
Family
ID=40054163
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020107007093A KR20100067099A (ko) | 2007-09-07 | 2008-09-05 | 눈물 임플랜트 검출 |
Country Status (15)
| Country | Link |
|---|---|
| US (3) | US9011361B2 (ko) |
| EP (2) | EP2205193A2 (ko) |
| JP (4) | JP5411140B2 (ko) |
| KR (1) | KR20100067099A (ko) |
| CN (1) | CN101861135A (ko) |
| AU (1) | AU2008300022A1 (ko) |
| BR (1) | BRPI0817074A2 (ko) |
| CA (1) | CA2698580C (ko) |
| MX (1) | MX2010002619A (ko) |
| NZ (1) | NZ583858A (ko) |
| RU (1) | RU2010112417A (ko) |
| SG (1) | SG184728A1 (ko) |
| TW (1) | TW201006451A (ko) |
| WO (1) | WO2009035571A2 (ko) |
| ZA (1) | ZA201001739B (ko) |
Families Citing this family (95)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7431710B2 (en) | 2002-04-08 | 2008-10-07 | Glaukos Corporation | Ocular implants with anchors and methods thereof |
| EP3470108A1 (en) | 2004-07-02 | 2019-04-17 | Mati Therapeutics Inc. | Treatment medium delivery device for delivery of treatment media to the eye |
| CN103393483B (zh) | 2006-03-31 | 2016-08-24 | 玛提治疗有限公司 | 用于鼻泪系统的药物释放方法、结构及组合物 |
| CN101861135A (zh) * | 2007-09-07 | 2010-10-13 | Qlt栓塞输送公司 | 泪道植入物检测 |
| RU2010136822A (ru) * | 2008-02-18 | 2012-03-10 | Клт Плаг Диливери, Инк. (Us) | Лакримальные имплантаты и связанные с ними способы |
| CN102341144B (zh) * | 2009-01-23 | 2014-10-29 | Qlt股份有限公司 | 一种或多种药剂的持续释放递送 |
| CN104887389B (zh) | 2009-01-29 | 2017-06-23 | 弗赛特影像4股份有限公司 | 后段给药 |
| US8623395B2 (en) | 2010-01-29 | 2014-01-07 | Forsight Vision4, Inc. | Implantable therapeutic device |
| WO2012071476A2 (en) | 2010-11-24 | 2012-05-31 | David Haffner | Drug eluting ocular implant |
| AU2010249683B2 (en) * | 2009-05-18 | 2015-06-25 | Dose Medical Corporation | Drug eluting ocular implant |
| US10206813B2 (en) | 2009-05-18 | 2019-02-19 | Dose Medical Corporation | Implants with controlled drug delivery features and methods of using same |
| EP2503969A1 (en) * | 2009-11-27 | 2012-10-03 | QLT Inc. | Lacrimal implants including split and insertable drug core |
| US10166142B2 (en) | 2010-01-29 | 2019-01-01 | Forsight Vision4, Inc. | Small molecule delivery with implantable therapeutic device |
| AU2011285548B2 (en) | 2010-08-05 | 2014-02-06 | Forsight Vision4, Inc. | Combined drug delivery methods and apparatus |
| HUE057267T2 (hu) | 2010-08-05 | 2022-05-28 | Forsight Vision4 Inc | Berendezés szem kezelésére |
| SI2600930T1 (sl) | 2010-08-05 | 2021-08-31 | Forsight Vision4, Inc. | Injekcijska naprava za dajanje zdravila |
| US9022967B2 (en) | 2010-10-08 | 2015-05-05 | Sinopsys Surgical, Inc. | Implant device, tool, and methods relating to treatment of paranasal sinuses |
| US9821159B2 (en) | 2010-11-16 | 2017-11-21 | The Board Of Trustees Of The Leland Stanford Junior University | Stimulation devices and methods |
| CN103313754B (zh) * | 2010-11-16 | 2015-09-30 | 小利兰·斯坦福大学理事会 | 用于治疗干眼的系统和方法 |
| WO2012068549A2 (en) | 2010-11-19 | 2012-05-24 | Forsight Vision4, Inc. | Therapeutic agent formulations for implanted devices |
| US20120238994A1 (en) * | 2010-12-22 | 2012-09-20 | Martin Nazzaro | Two-piece injectable drug delivery device with heat-cured seal |
| ES2528350T3 (es) * | 2011-01-14 | 2015-02-09 | Ecole Polytechnique Federale De Lausanne (Epfl) | Aparato y método para el tratamiento del fluido intraocular en exceso |
| US10603214B2 (en) | 2011-01-14 | 2020-03-31 | Ecole Polytechnique Federale De Lausanne (Epfl) | Apparatus and methods for treating excess intraocular fluid |
| EP2726016B1 (en) | 2011-06-28 | 2023-07-19 | ForSight Vision4, Inc. | An apparatus for collecting a sample of fluid from a reservoir chamber of a therapeutic device for the eye |
| US9974685B2 (en) | 2011-08-29 | 2018-05-22 | Mati Therapeutics | Drug delivery system and methods of treating open angle glaucoma and ocular hypertension |
| JP6100782B2 (ja) | 2011-08-29 | 2017-03-22 | キューエルティー インコーポレイテッド | 緑内障および高眼圧症を治療するための活性剤の徐放送達 |
| US9883968B2 (en) | 2011-09-16 | 2018-02-06 | Forsight Vision4, Inc. | Fluid exchange apparatus and methods |
| US8859996B2 (en) * | 2011-10-18 | 2014-10-14 | Luminex Corporation | Methods and systems for image data processing |
| US8765210B2 (en) | 2011-12-08 | 2014-07-01 | Aquesys, Inc. | Systems and methods for making gelatin shunts |
| US8808256B2 (en) | 2012-01-16 | 2014-08-19 | Johnson & Johnson Vision Care, Inc. | Eye drug delivery system |
| WO2013116061A1 (en) | 2012-02-03 | 2013-08-08 | Forsight Vision4, Inc. | Insertion and removal methods and apparatus for therapeutic devices |
| US20130220346A1 (en) * | 2012-02-28 | 2013-08-29 | Victor Lust | Balloon punctal plug |
| TWI635855B (zh) * | 2012-02-29 | 2018-09-21 | 壯生和壯生視覺關懷公司 | 具有激能圍阻陣列之淚管塞 |
| US9980810B2 (en) * | 2012-04-03 | 2018-05-29 | Johnson & Johnson Vision Care, Inc. | System controller for variable-optic electronic ophthalmic lens |
| WO2013154843A1 (en) | 2012-04-11 | 2013-10-17 | Sinopsys Surgical, Inc. | Implantation tools, tool assemblies, kits and methods |
| CN105473130A (zh) | 2012-05-03 | 2016-04-06 | 麦提疗法有限公司 | 治疗开角型青光眼和高眼压症的药物递送系统和方法 |
| AU2014209177C1 (en) | 2013-01-25 | 2019-01-24 | Sinopsys Surgical, Inc. | Paranasal sinus access implant devices and related tools, methods and kits |
| US9125723B2 (en) | 2013-02-19 | 2015-09-08 | Aquesys, Inc. | Adjustable glaucoma implant |
| US10159600B2 (en) | 2013-02-19 | 2018-12-25 | Aquesys, Inc. | Adjustable intraocular flow regulation |
| WO2014138709A1 (en) | 2013-03-08 | 2014-09-12 | Oculeve, Inc. | Devices and methods for treating dry eye in animals |
| WO2014165124A1 (en) | 2013-03-12 | 2014-10-09 | Oculeve, Inc. | Implant delivery devices, systems, and methods |
| WO2014152959A1 (en) | 2013-03-14 | 2014-09-25 | Forsight Vision4, Inc. | Systems for sustained intraocular delivery of low solubility compounds from a port delivery system implant |
| US10517759B2 (en) | 2013-03-15 | 2019-12-31 | Glaukos Corporation | Glaucoma stent and methods thereof for glaucoma treatment |
| EP4302736A3 (en) | 2013-03-28 | 2024-04-03 | ForSight Vision4, Inc. | Ophthalmic implant for delivering therapeutic substances |
| NZ704579A (en) | 2013-04-19 | 2018-10-26 | Oculeve Inc | Nasal stimulation devices and methods |
| US9700459B2 (en) | 2013-10-16 | 2017-07-11 | Sinopsys Surgical, Inc. | Apparatuses, tools and kits relating to fluid manipulation treatments of paranasal sinuses |
| MX2016006297A (es) | 2013-11-14 | 2016-07-26 | Aquesys Inc | Insertador de derivacion intraocular. |
| WO2015111553A1 (ja) * | 2014-01-22 | 2015-07-30 | 株式会社カネカ | 涙道チューブ |
| EP3689338A1 (en) | 2014-02-25 | 2020-08-05 | Oculeve, Inc. | Polymer formulations for nasolacrimal stimulation |
| WO2015184173A1 (en) | 2014-05-29 | 2015-12-03 | Dose Medical Corporation | Implants with controlled drug delivery features and methods of using same |
| KR102416726B1 (ko) | 2014-07-15 | 2022-07-05 | 포사이트 비젼4, 인크. | 안구 이식물 전달 디바이스 및 방법 |
| EP3179968B1 (en) | 2014-07-24 | 2019-09-11 | Sinopsys Surgical, Inc. | Paranasal sinus access implant devices and related products and methods |
| AU2015292278B2 (en) | 2014-07-25 | 2020-04-09 | Oculeve, Inc. | Stimulation patterns for treating dry eye |
| WO2016022750A1 (en) | 2014-08-08 | 2016-02-11 | Forsight Vision4, Inc. | Stable and soluble formulations of receptor tyrosine kinase inhibitors, and methods of preparation thereof |
| CA2965363A1 (en) | 2014-10-22 | 2016-04-28 | Oculeve, Inc. | Implantable nasal stimulator systems and methods |
| WO2016065215A1 (en) | 2014-10-22 | 2016-04-28 | Oculeve, Inc. | Stimulation devices and methods for treating dry eye |
| WO2016065211A1 (en) | 2014-10-22 | 2016-04-28 | Oculeve, Inc. | Contact lens for increasing tear production |
| US10500091B2 (en) | 2014-11-10 | 2019-12-10 | Forsight Vision4, Inc. | Expandable drug delivery devices and methods of use |
| CA2989814A1 (en) | 2015-06-16 | 2016-12-22 | The Regents Of The University Of Colorado, A Body Corporate | Nasolacrimal implants and related methods for tear stimulation |
| US11291847B2 (en) | 2015-06-16 | 2022-04-05 | The Regents Of The University Of Colorado, A Body Corporate | Systems and methods for preventing, diagnosing, and/or treating one or more medical conditions via neuromodulation |
| JP2018525078A (ja) | 2015-07-22 | 2018-09-06 | インセプト・リミテッド・ライアビリティ・カンパニーIncept,Llc | 被覆された涙点プラグ |
| US11925578B2 (en) | 2015-09-02 | 2024-03-12 | Glaukos Corporation | Drug delivery implants with bi-directional delivery capacity |
| US11564833B2 (en) | 2015-09-25 | 2023-01-31 | Glaukos Corporation | Punctal implants with controlled drug delivery features and methods of using same |
| AU2016355345A1 (en) | 2015-11-20 | 2018-05-31 | Forsight Vision4, Inc. | Porous structures for extended release drug delivery devices |
| US10426958B2 (en) | 2015-12-04 | 2019-10-01 | Oculeve, Inc. | Intranasal stimulation for enhanced release of ocular mucins and other tear proteins |
| US9460328B1 (en) | 2016-01-15 | 2016-10-04 | International Business Machines Corporation | Extracting information from surface coatings |
| US10252048B2 (en) | 2016-02-19 | 2019-04-09 | Oculeve, Inc. | Nasal stimulation for rhinitis, nasal congestion, and ocular allergies |
| CN109195556B (zh) | 2016-04-05 | 2021-03-26 | 弗赛特影像4股份有限公司 | 可植入眼睛药物递送装置 |
| CN109937025B (zh) | 2016-04-20 | 2022-07-29 | 多斯医学公司 | 生物可吸收眼部药物的递送装置 |
| US10918864B2 (en) | 2016-05-02 | 2021-02-16 | Oculeve, Inc. | Intranasal stimulation for treatment of meibomian gland disease and blepharitis |
| US10596035B2 (en) | 2016-06-06 | 2020-03-24 | Ecole Polytechnique Federale De Lausanne (Epfl) | Apparatus for treating excess intraocular fluid |
| TWI601549B (zh) * | 2016-07-25 | 2017-10-11 | 國防醫學院 | 注射記憶筆針及其使用方法 |
| US9983418B2 (en) | 2016-08-04 | 2018-05-29 | Verily Life Sciences Llc | Tactile interface for eye-mountable device |
| EP3532866A1 (en) | 2016-10-28 | 2019-09-04 | PPG Industries Ohio, Inc. | Coatings for increasing near-infrared detection distances |
| RU2019118600A (ru) | 2016-12-02 | 2021-01-11 | Окулив, Инк. | Аппарат и способ составления прогноза синдрома сухого глаза и рекомендаций по лечению |
| CN110536654A (zh) * | 2017-04-06 | 2019-12-03 | 提尔迪克斯有限公司 | 眼部装置及其运用方法 |
| US11589807B2 (en) | 2017-05-11 | 2023-02-28 | The Regents Of The University Of California | Biosensor for monitoring eyedrop usage compliance |
| EP3634545A1 (en) * | 2017-06-09 | 2020-04-15 | Sanofi | Electronics for dosage sensing |
| CN110913809B (zh) * | 2017-06-13 | 2023-10-03 | 英福卡斯公司 | 用于治疗青光眼的系统、方法和装置 |
| EP3675780A4 (en) | 2017-09-20 | 2021-10-06 | Sinopsys Surgical, Inc. | IMPLANTATION TOOLS, ARRANGEMENTS, KITS, AND PROCEDURES FOR ACCESSING PERIODIC FLUIDS |
| WO2019103906A1 (en) | 2017-11-21 | 2019-05-31 | Forsight Vision4, Inc. | Fluid exchange apparatus for expandable port delivery system and methods of use |
| JP6501096B1 (ja) * | 2018-03-30 | 2019-04-17 | 真一 芦田 | 薬剤供給眼用器具 |
| JP6501097B1 (ja) * | 2018-03-30 | 2019-04-17 | 真一 芦田 | 薬剤供給眼用器具 |
| CN112689488B (zh) | 2018-09-06 | 2024-04-12 | 洛桑联邦理工学院 | 具有弹性膜的用于治疗过量眼内流体的设备 |
| RU2697308C1 (ru) * | 2018-09-27 | 2019-08-13 | федеральное государственное автономное учреждение "Национальный медицинский исследовательский центр "Межотраслевой научно-технический комплекс "Микрохирургия глаза" имени академика С.Н. Федорова" Министерства здравоохранения Российской Федерации | Способ определения эффективности использования лакримального обтуратора |
| EP3881236A1 (en) | 2018-11-13 | 2021-09-22 | PPG Industries Ohio Inc. | Method of detecting a concealed pattern |
| US11561329B2 (en) | 2019-01-07 | 2023-01-24 | Ppg Industries Ohio, Inc. | Near infrared control coating, articles formed therefrom, and methods of making the same |
| US11446495B2 (en) | 2019-05-14 | 2022-09-20 | Twenty Twenty Therapeutics Llc | Therapeutic devices for placement underneath the eyelid and associated systems, devices, and methods for dry eye treatment |
| US11779489B2 (en) | 2020-03-06 | 2023-10-10 | Ecole Polytechnique Federale De Lausanne (Epfl) | Apparatus for treating excess intraocular fluid having an elastic membrane |
| WO2022182740A1 (en) | 2021-02-24 | 2022-09-01 | Ocular Therapeutix, Inc. | Intracanalicular depot inserter device |
| CN113391365B (zh) * | 2021-05-12 | 2023-10-13 | Tcl王牌电器(惠州)有限公司 | 去膜检测方法及装置 |
| USD1033637S1 (en) | 2022-01-24 | 2024-07-02 | Forsight Vision4, Inc. | Fluid exchange device |
| IL291216A (en) * | 2022-03-08 | 2023-10-01 | Iop Medical Ltd | Method and implantable device for measuring pressure inside an organ in the patient's body |
| WO2024020505A2 (en) * | 2022-07-22 | 2024-01-25 | SpyGlass Pharma, Inc. | Intraocular drug delivery systems and methods of use |
| US20240024092A1 (en) * | 2022-07-22 | 2024-01-25 | SpyGlass Pharma, Inc. | Intraocular drug delivery systems and methods of use |
Family Cites Families (221)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3865108A (en) | 1971-05-17 | 1975-02-11 | Ortho Pharma Corp | Expandable drug delivery device |
| US3828777A (en) | 1971-11-08 | 1974-08-13 | Alza Corp | Microporous ocular device |
| US3949750A (en) | 1974-10-07 | 1976-04-13 | Freeman Jerre M | Punctum plug and method for treating keratoconjunctivitis sicca (dry eye) and other ophthalmic aliments using same |
| US4014335A (en) | 1975-04-21 | 1977-03-29 | Alza Corporation | Ocular drug delivery device |
| US4281654A (en) | 1980-04-07 | 1981-08-04 | Alza Corporation | Drug delivery system for controlled ocular therapy |
| US4304765A (en) | 1980-10-14 | 1981-12-08 | Alza Corporation | Ocular insert housing steroid in two different therapeutic forms |
| NZ200429A (en) | 1981-04-30 | 1984-10-19 | Smith & Nephew Ass | Applicator for placing pharmaceutically active agent in contact with moist surface,e.g.,eye |
| NO149454C (no) | 1982-01-13 | 1984-04-25 | Gunnar Mindor Mikalsen | Proteinkonsentrat for tilsetning til dyrefor, fremstilling av konsentratet fra gress og andre plantevekster og anvendelse av konsentratet i dyrefor |
| US4660546A (en) | 1984-11-07 | 1987-04-28 | Robert S. Herrick | Method for treating for deficiency of tears |
| US5049142A (en) | 1984-11-07 | 1991-09-17 | Herrick Robert S | Intracanalicular implant for horizontal canalicular blockade treatment of the eye |
| US5053030A (en) | 1984-11-07 | 1991-10-01 | Herrick Robert S | Intracanalicular implant for horizontal canalicular blockade treatment of the eye |
| US5229128A (en) | 1986-06-11 | 1993-07-20 | Haddad Heskel M | Drug delivery ophthalmic insert and method of preparing same |
| US5322691A (en) | 1986-10-02 | 1994-06-21 | Sohrab Darougar | Ocular insert with anchoring protrusions |
| US4747404A (en) | 1986-11-10 | 1988-05-31 | Kresge Eye Institute Of Wayne State University | Foldable intraocular lens inserter |
| US4886488A (en) | 1987-08-06 | 1989-12-12 | White Thomas C | Glaucoma drainage the lacrimal system and method |
| GB8806367D0 (en) | 1988-03-17 | 1988-04-13 | Erba Carlo Spa | Siloxane matrices with internal non-uniform drug distribution |
| US4915684A (en) | 1988-06-21 | 1990-04-10 | Mackeen Donald L | Method and apparatus for modulating the flow of lacrimal fluid through a punctum and associated canaliculus |
| US4938763B1 (en) * | 1988-10-03 | 1995-07-04 | Atrix Lab Inc | Biodegradable in-situ forming implants and method of producing the same |
| US5133159A (en) | 1989-01-13 | 1992-07-28 | Nestle S.A. | Method for polishing silicone products |
| US4959048A (en) | 1989-01-17 | 1990-09-25 | Helix Medical, Inc. | Lacrimal duct occluder |
| US5098443A (en) | 1989-03-23 | 1992-03-24 | University Of Miami | Method of implanting intraocular and intraorbital implantable devices for the controlled release of pharmacological agents |
| US5128058A (en) | 1989-05-31 | 1992-07-07 | Hoya Corporation | Contact lens cleaner containing a microcapsular polishing agent |
| US4923468A (en) * | 1989-06-13 | 1990-05-08 | Wild Victor F | Intraocular lens with fluorescing support loops |
| IE910450A1 (en) | 1990-02-15 | 1991-08-28 | Bausch & Lomb | Soft contact lens processing aid |
| US5163959A (en) | 1990-03-29 | 1992-11-17 | Herrick Robert S | Method for treating an eye with a canalicular implant having a collapsible flared section |
| US5171270A (en) | 1990-03-29 | 1992-12-15 | Herrick Robert S | Canalicular implant having a collapsible flared section and method |
| US5041081A (en) | 1990-05-18 | 1991-08-20 | Odrich Ronald B | Ocular implant for controlling glaucoma |
| US5116371A (en) | 1990-07-06 | 1992-05-26 | Christensen James M | Prosthesis with improved biocompatibility |
| US5143724A (en) | 1990-07-09 | 1992-09-01 | Biomatrix, Inc. | Biocompatible viscoelastic gel slurries, their preparation and use |
| JPH0592015A (ja) * | 1991-10-01 | 1993-04-16 | Asahi Chem Ind Co Ltd | 涙液流出防止用ロツド |
| JPH069648U (ja) * | 1991-12-05 | 1994-02-08 | スーガン株式会社 | 複数個の注射器の組 |
| WO1993012765A1 (en) | 1991-12-27 | 1993-07-08 | Merck & Co., Inc. | A controlled release drug dispersion delivery device |
| US5283063A (en) * | 1992-01-31 | 1994-02-01 | Eagle Vision | Punctum plug method and apparatus |
| US5334137A (en) | 1992-02-21 | 1994-08-02 | Eagle Vision, Inc. | Lacrimal fluid control device |
| US5178635A (en) | 1992-05-04 | 1993-01-12 | Allergan, Inc. | Method for determining amount of medication in an implantable device |
| US5366739A (en) | 1992-08-06 | 1994-11-22 | Deo Corporation | Method of ophthalmic drug delivery |
| US5514379A (en) | 1992-08-07 | 1996-05-07 | The General Hospital Corporation | Hydrogel compositions and methods of use |
| US5469867A (en) | 1992-09-02 | 1995-11-28 | Landec Corporation | Cast-in place thermoplastic channel occluder |
| US5318513A (en) | 1992-09-24 | 1994-06-07 | Leib Martin L | Canalicular balloon fixation stent |
| FR2700265B1 (fr) | 1993-01-08 | 1995-03-31 | France Chirurgie Instr | Bouchon méatique pour pathologie lacrymale. |
| US5707643A (en) | 1993-02-26 | 1998-01-13 | Santen Pharmaceutical Co., Ltd. | Biodegradable scleral plug |
| US5824048A (en) | 1993-04-26 | 1998-10-20 | Medtronic, Inc. | Method for delivering a therapeutic substance to a body lumen |
| US5417651A (en) | 1993-07-01 | 1995-05-23 | Guena; Nicolas | Punctum plug and monocanalicular probe for lacrimal pathology |
| WO1995003807A1 (en) | 1993-07-27 | 1995-02-09 | The University Of Sydney | Treatment of age-related macular degeneration |
| US5423777A (en) | 1993-10-27 | 1995-06-13 | Tajiri; Akira | Punctum plug |
| US5443505A (en) | 1993-11-15 | 1995-08-22 | Oculex Pharmaceuticals, Inc. | Biocompatible ocular implants |
| US5466233A (en) * | 1994-04-25 | 1995-11-14 | Escalon Ophthalmics, Inc. | Tack for intraocular drug delivery and method for inserting and removing same |
| JP3486758B2 (ja) | 1994-06-24 | 2004-01-13 | 株式会社高研 | 注入可能な涙小管閉鎖剤 |
| US5532925A (en) | 1994-08-12 | 1996-07-02 | Fisher Controls International, Inc. | Current-to-pressure transducer with selectable, adjustable input filter |
| EP0957949B1 (en) | 1995-05-14 | 2004-08-04 | Optonol Ltd. | Intraocular implant, delivery device, and method of implantation |
| US6149684A (en) | 1995-06-07 | 2000-11-21 | Herrick; Robert S. | Punctum plug having a thin elongated lip and a distal starting tip and method of using |
| US5723005A (en) | 1995-06-07 | 1998-03-03 | Herrick Family Limited Partnership | Punctum plug having a collapsible flared section and method |
| US5766243A (en) | 1995-08-21 | 1998-06-16 | Oasis Medical, Inc. | Abrasive polished canalicular implant |
| US5773019A (en) * | 1995-09-27 | 1998-06-30 | The University Of Kentucky Research Foundation | Implantable controlled release device to deliver drugs directly to an internal portion of the body |
| US5741292A (en) | 1995-10-26 | 1998-04-21 | Eagle Vision | Punctum dilating and plug inserting instrument with push-button plug release |
| US6441047B2 (en) | 1995-11-17 | 2002-08-27 | Alcon Manufacturing Ltd.. | Combination therapy for treating glaucoma |
| US5824073A (en) | 1996-03-18 | 1998-10-20 | Peyman; Gholam A. | Macular indentor for use in the treatment of subretinal neovascular membranes |
| JPH1033584A (ja) | 1996-07-26 | 1998-02-10 | M L C:Kk | 涙道挿管器具 |
| US5993407A (en) | 1996-10-25 | 1999-11-30 | Moazed; Kambiz Thomas | Transnasal lacrimal insert |
| CA2269029C (en) | 1996-11-01 | 2003-12-23 | Alcon Laboratories, Inc. | Cryogenic polishing method for soft acrylic articles |
| EP0944371A1 (fr) | 1997-02-04 | 1999-09-29 | Alain Fouere | Tampon meatique vissable pour canal lacrymal |
| JP4157168B2 (ja) * | 1997-03-27 | 2008-09-24 | アルフレッド イー マン ファウンデーション フォア サイエンティフィック リサーチ | 身体のパラメータを監視及び又はそれに作用するための植込型装置のシステム |
| US6082362A (en) | 1997-03-27 | 2000-07-04 | Eagle Vision, Inc. | Punctum plug |
| US6016806A (en) | 1997-03-27 | 2000-01-25 | Eaglevision, Inc | Punctum plug |
| US6027470A (en) | 1998-06-10 | 2000-02-22 | Eagle Vision, Inc. | Punctum plug and method for inserting the same into the punctual opening |
| US6041785A (en) | 1997-03-27 | 2000-03-28 | Eaglevision, Inc. | Punctum plug |
| US5961370A (en) | 1997-05-08 | 1999-10-05 | Chiron Vision Corporation | Intraocular lens tumbling process using coated beads |
| MY125870A (en) | 1997-07-25 | 2006-08-30 | Alza Corp | Osmotic delivery system flow modulator apparatus and method |
| US6306426B1 (en) | 1997-08-11 | 2001-10-23 | Allergan Sales, Inc. | Implant device with a retinoid for improved biocompatibility |
| US5830171A (en) | 1997-08-12 | 1998-11-03 | Odyssey Medical, Inc. | Punctal occluder |
| US6060439A (en) | 1997-09-29 | 2000-05-09 | Kyzen Corporation | Cleaning compositions and methods for cleaning resin and polymeric materials used in manufacture |
| US6335335B2 (en) | 1997-11-05 | 2002-01-01 | Senju Pharmaceutical Co., Ltd. | Prolonged-action eye drop |
| US6203513B1 (en) * | 1997-11-20 | 2001-03-20 | Optonol Ltd. | Flow regulating implant, method of manufacture, and delivery device |
| US5947974A (en) | 1997-12-09 | 1999-09-07 | Allergan | Folding device and method for an intraocular lens |
| US6646001B2 (en) | 1997-12-19 | 2003-11-11 | Alcon Manufacturing, Ltd. | Use of non-steroidal anti-inflammatory agents in combination with prostaglandin FP receptor agonists to treat glaucoma and ocular hypertension |
| NL1008090C2 (nl) | 1998-01-22 | 1999-07-26 | Lubberman Bernardus H M | Plug voor het afsluiten van een traanbuis. |
| US6290684B1 (en) | 1998-03-02 | 2001-09-18 | Herrick Family Limited Partnership | Punctum plug having a collapsible expanded section and distal tip extending substantially perpendicular thereto and method of inserting same |
| WO1999044553A1 (en) | 1998-03-02 | 1999-09-10 | Herrick Family Limited Partnership | A punctum plug having a collapsible flared section and method |
| US6512747B1 (en) | 1998-03-05 | 2003-01-28 | Nippon Telegraph And Telephone Corporation | ATM transmission system |
| US6196993B1 (en) * | 1998-04-20 | 2001-03-06 | Eyelab Group, Llc | Ophthalmic insert and method for sustained release of medication to the eye |
| US6224630B1 (en) | 1998-05-29 | 2001-05-01 | Advanced Bio Surfaces, Inc. | Implantable tissue repair device |
| US6306114B1 (en) | 1998-06-16 | 2001-10-23 | Eagle Vision, Inc. | Valved canalicular plug for lacrimal duct occlusion |
| US6117441A (en) | 1998-07-02 | 2000-09-12 | The Population Council, Inc. | Silicone core long term androgen delivery implant |
| DK1037627T3 (da) | 1998-07-14 | 2001-10-01 | Alcon Lab Inc | Anvendelse af 11-(3-dimethylamino-propyliden)-6, 11-dihydrodibenz[b,e]oxepin-2-eddikesyre og af farmaceutisk acceptable salte deraf til fremstillingen af et lægemiddel til behandlingen af non-allergiske... |
| JP2000070296A (ja) | 1998-08-27 | 2000-03-07 | M L C:Kk | 涙道内挿管器具 |
| US6095901A (en) | 1998-12-09 | 2000-08-01 | Alcon Laboratories, Inc. | Polishing method for soft acrylic articles |
| US6217895B1 (en) * | 1999-03-22 | 2001-04-17 | Control Delivery Systems | Method for treating and/or preventing retinal diseases with sustained release corticosteroids |
| US20040121014A1 (en) | 1999-03-22 | 2004-06-24 | Control Delivery Systems, Inc. | Method for treating and/or preventing retinal diseases with sustained release corticosteroids |
| US6234175B1 (en) | 1999-03-23 | 2001-05-22 | Medennium, Inc. | Smart ocular plug design and method of insertion for punctal and intracanalicular implants |
| US6383192B1 (en) | 1999-04-28 | 2002-05-07 | Mlc Limited Company | Apparatus for intubation of lacrimal duct |
| US6428502B1 (en) | 1999-06-25 | 2002-08-06 | Alcon Manufacturing, Ltd. | Punctal cannula |
| US6706275B1 (en) | 1999-09-08 | 2004-03-16 | Matthew W. Camp | Scleral plug system |
| US6331313B1 (en) * | 1999-10-22 | 2001-12-18 | Oculex Pharmaceticals, Inc. | Controlled-release biocompatible ocular drug delivery implant devices and methods |
| US6264971B1 (en) | 1999-11-04 | 2001-07-24 | Btg International Limited | Ocular insert |
| US6566345B2 (en) | 2000-04-28 | 2003-05-20 | Fziomed, Inc. | Polyacid/polyalkylene oxide foams and gels and methods for their delivery |
| US6344047B1 (en) * | 2000-02-02 | 2002-02-05 | Eagle Vision | Instrument for inserting a punctum plug and method for manufacturing the instrument |
| US6638239B1 (en) | 2000-04-14 | 2003-10-28 | Glaukos Corporation | Apparatus and method for treating glaucoma |
| US7867186B2 (en) | 2002-04-08 | 2011-01-11 | Glaukos Corporation | Devices and methods for treatment of ocular disorders |
| US7708711B2 (en) | 2000-04-14 | 2010-05-04 | Glaukos Corporation | Ocular implant with therapeutic agents and methods thereof |
| US20040175410A1 (en) * | 2000-04-26 | 2004-09-09 | Control Delivery Systems, Inc. | Sustained release device and method for ocular delivery of carbonic anhydrase inhibitors |
| US20040208910A1 (en) | 2000-04-26 | 2004-10-21 | Control Delivery Systems, Inc. | Sustained release device and method for ocular delivery of adrenergic agents |
| US6375972B1 (en) | 2000-04-26 | 2002-04-23 | Control Delivery Systems, Inc. | Sustained release drug delivery devices, methods of use, and methods of manufacturing thereof |
| GB0010958D0 (en) | 2000-05-05 | 2000-06-28 | Novartis Ag | Organic compounds |
| WO2001096822A1 (en) | 2000-06-12 | 2001-12-20 | Addest Technovation Pte. Ltd. | Arrangement and method for measuring the speed of sound |
| US6371122B1 (en) | 2000-06-20 | 2002-04-16 | Robert M. Mandelkorn | Gauge/dilator apparatus |
| US6629533B1 (en) | 2000-06-30 | 2003-10-07 | Eagle Vision, Inc. | Punctum plug with at least one anchoring arm |
| ES2231306T3 (es) | 2000-08-04 | 2005-05-16 | Medennium, Inc. | Tapon ocular para implantar en el punto lagrimal y el canaliculo. |
| US6534693B2 (en) | 2000-11-06 | 2003-03-18 | Afmedica, Inc. | Surgically implanted devices having reduced scar tissue formation |
| US7041868B2 (en) | 2000-12-29 | 2006-05-09 | Kimberly-Clark Worldwide, Inc. | Bioabsorbable wound dressing |
| WO2002056863A2 (en) | 2000-12-29 | 2002-07-25 | Bausch & Lomb Incorporated | Sustained release drug delivery devices |
| CA2432225C (en) | 2001-01-03 | 2008-01-15 | Michael J. Brubaker | Sustained release drug delivery devices with prefabricated permeable plugs |
| US6991808B2 (en) | 2001-01-26 | 2006-01-31 | Bausch & Lomb Inc. | Process for the production of sustained release drug delivery devices |
| US20020193441A1 (en) | 2001-02-21 | 2002-12-19 | Robertson Stella M. | Prostanoid therapies for the treatment of glaucoma |
| US6981958B1 (en) * | 2001-05-02 | 2006-01-03 | Glaukos Corporation | Implant with pressure sensor for glaucoma treatment |
| AU2002258754B2 (en) | 2001-04-07 | 2006-08-17 | Glaukos Corporation | Glaucoma stent and methods thereof for glaucoma treatment |
| US7431710B2 (en) | 2002-04-08 | 2008-10-07 | Glaukos Corporation | Ocular implants with anchors and methods thereof |
| US6605108B2 (en) | 2001-04-13 | 2003-08-12 | Eagle Vision, Inc. | Monocanalicular stent |
| US7916013B2 (en) * | 2005-03-21 | 2011-03-29 | Greatbatch Ltd. | RFID detection and identification system for implantable medical devices |
| US6982090B2 (en) * | 2001-05-10 | 2006-01-03 | Gillespie Donald E | More easily visualized punctum plug configurations |
| US7404825B2 (en) | 2001-06-11 | 2008-07-29 | Herrick Ii Robert S | Implant capable of forming a differential image in an eye |
| FR2829019B3 (fr) | 2001-08-31 | 2003-10-31 | Alain Fouere | Bouchons lacrymaux et methodes de mise en place de ces dispositifs |
| CA2452194A1 (en) | 2001-09-11 | 2003-03-20 | Smart Drug Systems Inc | Sustained release pharmaceutical compositions comprising a silicone support material |
| US20040142902A1 (en) * | 2001-11-08 | 2004-07-22 | Struijker- Boudier Harry A.J. | Implant dosage form and use thereof for the delivery of a cholosterol lowering agent |
| US6996063B2 (en) | 2001-11-16 | 2006-02-07 | Asustek Computer Inc. | Applicable PDU range test and calculation for window-based polling |
| US7001615B1 (en) | 2001-12-07 | 2006-02-21 | Alcon, Inc. | Sustained release ophthalmic, otic and nasal suspension |
| US6729939B2 (en) | 2001-12-17 | 2004-05-04 | Bausch & Lomb Incorporated | Polishing method for intraocular lens |
| FR2834446B1 (fr) | 2002-01-08 | 2004-02-13 | Ioltechnologie Production | Clou meatique a expansion |
| EP1466969A4 (en) | 2002-01-18 | 2006-02-01 | Takara Bio Inc | SULFATED FUCAN |
| US20030139673A1 (en) * | 2002-01-18 | 2003-07-24 | Vivenzio Robert L. | Illumination system |
| TW200305424A (en) | 2002-01-29 | 2003-11-01 | Santen Pharmaceutical Co Ltd | Glaucoma-treating agent comprising bunazosin and prostaglandin |
| US7204995B2 (en) | 2002-01-31 | 2007-04-17 | El-Sherif Dalia M | Treatment and control of dry eye by use of biodegradable polymer capsules |
| US9301875B2 (en) * | 2002-04-08 | 2016-04-05 | Glaukos Corporation | Ocular disorder treatment implants with multiple opening |
| US20040147870A1 (en) | 2002-04-08 | 2004-07-29 | Burns Thomas W. | Glaucoma treatment kit |
| US8871241B2 (en) | 2002-05-07 | 2014-10-28 | Psivida Us, Inc. | Injectable sustained release delivery devices |
| WO2003094888A1 (en) | 2002-05-07 | 2003-11-20 | Control Delivery Systems, Inc. | Processes for forming a drug delivery device |
| JP2004016333A (ja) * | 2002-06-13 | 2004-01-22 | Unique Medical Co Ltd | 硬膜外麻酔用カテーテルおよび該硬膜外麻酔用カテーテルを用いる電気刺激装置 |
| US20040043067A1 (en) | 2002-06-19 | 2004-03-04 | Salamone Joseph C. | Fluorosiloxane matrix controlled diffusion drug delivery systems |
| US6866563B2 (en) | 2002-06-27 | 2005-03-15 | Bausch & Lomb Incorporated | Apparatus and method for target polishing intraocular lenses |
| FR2841770B1 (fr) | 2002-07-05 | 2004-10-01 | Ioltechnologie Production | Clou meatique d'obturation d'un meat lacrymal |
| FR2844182B1 (fr) | 2002-09-11 | 2004-12-03 | Humanoptics Ag | Bouchon d'obturation d'un canalicule lacrymal |
| US7169163B2 (en) | 2002-09-30 | 2007-01-30 | Bruce Becker | Transnasal method and catheter for lacrimal system |
| US7785578B2 (en) | 2002-10-11 | 2010-08-31 | Aciont, Inc. | Non-invasive ocular drug delivery |
| ATE369717T1 (de) | 2002-10-16 | 2007-08-15 | Alcatel Lucent | Paketvermittlung für paketdatenübertragungssysteme in einer multikanalfunkanordnung |
| US7354574B2 (en) | 2002-11-07 | 2008-04-08 | Advanced Ocular Systems Limited | Treatment of ocular disease |
| US7580394B2 (en) | 2002-11-27 | 2009-08-25 | Nokia Corporation | System and method for collision-free transmission scheduling in a network |
| CA2511217A1 (en) | 2002-12-20 | 2004-07-15 | Chakshu Research, Inc. | Ophthalmic formulation for the prevention and treatment of ocular conditions |
| US20040144392A1 (en) | 2003-01-23 | 2004-07-29 | Mueller Richard L. | Breast nipple duct protective device |
| US8149707B2 (en) | 2003-02-12 | 2012-04-03 | Rockstar Bidco, LP | Minimization of radio resource usage in multi-hop networks with multiple routings |
| EP1603485A4 (en) | 2003-02-26 | 2011-03-30 | Medivas Llc | BIOACTIVE STENTS AND METHOD OF USE THEREOF |
| CN1942588B (zh) * | 2003-03-05 | 2013-06-12 | 海洋酶公司 | 可溶性透明质酸酶糖蛋白(sHASEGP)、制备它们的方法、它们的用途和包含它们的药物组合物 |
| US20050283109A1 (en) | 2003-03-07 | 2005-12-22 | Peyman Gholam A | Method and apparatus for lacrimal canal obstruction |
| US7065376B2 (en) | 2003-03-20 | 2006-06-20 | Microsoft Corporation | Multi-radio unification protocol |
| JP4824549B2 (ja) | 2003-05-02 | 2011-11-30 | サーモディクス,インコーポレイティド | 制御放出型の生体活性物質デリバリー・デバイス |
| US7204253B2 (en) | 2003-05-22 | 2007-04-17 | Clarity Corporation | Punctum plug |
| US7017580B2 (en) | 2003-05-22 | 2006-03-28 | Clarity Corporation | Punctum plug system including a punctum plug and passive insertion tool therefor |
| US20040236343A1 (en) | 2003-05-23 | 2004-11-25 | Taylor Jon B. | Insertion tool for ocular implant and method for using same |
| JP4104137B2 (ja) | 2003-05-30 | 2008-06-18 | 有限会社エム・エル・シー | 涙点プラグ |
| US7662864B2 (en) | 2003-06-04 | 2010-02-16 | Rutgers, The State University Of New Jersey | Solution polymerization processes to prepare a polymer that degrades to release a physiologically active agent |
| JP4339635B2 (ja) | 2003-06-12 | 2009-10-07 | 有限会社エム・エル・シー | 涙点プラグ |
| US6994684B2 (en) | 2003-06-16 | 2006-02-07 | Alphamed Inc. | Punctum plugs having fluid collecting recesses and methods of punctal occlusion |
| US20040265356A1 (en) | 2003-06-30 | 2004-12-30 | Bausch & Lomb Incorporated | Drug delivery device |
| JP4280128B2 (ja) | 2003-08-19 | 2009-06-17 | 有限会社エム・エル・シー | 涙点プラグ |
| JP2005110765A (ja) | 2003-10-03 | 2005-04-28 | M L C:Kk | 涙点プラグセット |
| JP2005110930A (ja) | 2003-10-07 | 2005-04-28 | M L C:Kk | 涙点プラグセット |
| US20050129731A1 (en) | 2003-11-03 | 2005-06-16 | Roland Horres | Biocompatible, biostable coating of medical surfaces |
| US20050095269A1 (en) | 2003-11-04 | 2005-05-05 | Ainpour Parviz R. | Gel plug for blockage of the canaliculus |
| DK1696822T3 (da) | 2003-11-13 | 2010-05-17 | Psivida Inc | Injicerbart vedvarende frigørelsesimplantat, som har en bioeroderbar matrixkerne og en bioeroderbar hus |
| US7291125B2 (en) | 2003-11-14 | 2007-11-06 | Transcend Medical, Inc. | Ocular pressure regulation |
| ES2347648T3 (es) | 2003-12-17 | 2010-11-03 | Telefonaktiebolaget Lm Ericsson (Publ) | Un metodo, un sistema, un terminal y un producto de progrma de ordenador para seleccionar un sistema de acceso de radio en un sistema de acceso multiple. |
| JP4537410B2 (ja) | 2003-12-29 | 2010-09-01 | エレクトロニクス アンド テレコミュニケーションズ リサーチ インスチチュート | 移動通信システムにおける自動再送要求のためのフィードバックメッセージ生成方法 |
| US20050220882A1 (en) | 2004-03-04 | 2005-10-06 | Wilson Pritchard | Materials for medical implants and occlusive devices |
| US20050197614A1 (en) | 2004-03-04 | 2005-09-08 | Wilson Pritchard | Occlusive biomedical devices, punctum plugs, and methods of use thereof |
| US20050232972A1 (en) | 2004-04-15 | 2005-10-20 | Steven Odrich | Drug delivery via punctal plug |
| JP2004202276A (ja) | 2004-04-16 | 2004-07-22 | M L C:Kk | 涙道再建用挿管器具 |
| JP2005312835A (ja) | 2004-04-30 | 2005-11-10 | M L C:Kk | 糸で補強した涙道ステント |
| US20050244469A1 (en) | 2004-04-30 | 2005-11-03 | Allergan, Inc. | Extended therapeutic effect ocular implant treatments |
| JP4644438B2 (ja) | 2004-05-11 | 2011-03-02 | 有限会社エム・エル・シー | ツバつき涙道ステント |
| JP4510511B2 (ja) | 2004-05-18 | 2010-07-28 | 有限会社エム・エル・シー | ツバを円盤で補強した涙道ステント及び涙道プラグ |
| EP3470108A1 (en) * | 2004-07-02 | 2019-04-17 | Mati Therapeutics Inc. | Treatment medium delivery device for delivery of treatment media to the eye |
| US7117870B2 (en) | 2004-07-26 | 2006-10-10 | Clarity Corporation | Lacrimal insert having reservoir with controlled release of medication and method of manufacturing the same |
| US20060020253A1 (en) | 2004-07-26 | 2006-01-26 | Prescott Anthony D | Implantable device having reservoir with controlled release of medication and method of manufacturing the same |
| AU2005269599A1 (en) | 2004-07-26 | 2006-02-09 | Clarity Corporation | Implantable device having reservoir with controlled release of medication and method of manufacturing the same |
| WO2006031658A2 (en) * | 2004-09-10 | 2006-03-23 | Allergan, Inc. | Therapeutic lacrimal canalicular inserts and related methods |
| US20060074370A1 (en) | 2004-09-24 | 2006-04-06 | Medennium, Inc. | Ocular occluder and method of insertion |
| CA2588449A1 (en) | 2004-11-24 | 2006-06-01 | Therakine Corporation | An implant for intraocular drug delivery |
| EP1833440B1 (en) * | 2004-12-16 | 2012-08-22 | Iscience Interventional Corporation | Ophthalmic implant for treatment of glaucoma |
| CN1790976A (zh) | 2004-12-17 | 2006-06-21 | 松下电器产业株式会社 | 用于多天线传输中的重传方法 |
| US7986633B2 (en) | 2004-12-27 | 2011-07-26 | Lg Electronics Inc. | Method of controlling data transmission for multimedia and broadcasting services in a broadband wireless access system |
| EP1699249B1 (en) | 2005-03-04 | 2007-06-20 | Matsushita Electric Industrial Co., Ltd. | Method and apparatus for the synchronisation of the physical layers in heterogeneous mobile communications networks |
| US20060233858A1 (en) | 2005-03-08 | 2006-10-19 | Allergan, Inc. | Systems and methods providing targeted intraocular drug delivery |
| US7708401B2 (en) * | 2005-04-19 | 2010-05-04 | Anton Sabeta | Ophthalmic lens characterization |
| WO2006122414A1 (en) | 2005-05-17 | 2006-11-23 | Matregen Corp. | Depot for sustained and controlled delivery of methotrexate |
| WO2007009061A2 (en) | 2005-07-13 | 2007-01-18 | Anthrogenesis Corporation | Ocular plug formed from placenta derived collagen biofabric |
| US7862532B2 (en) | 2005-10-07 | 2011-01-04 | Delta Life Sciences, Inc. | Punctum plugs having insertion guides and strengthening beams |
| US20070088444A1 (en) | 2005-10-13 | 2007-04-19 | Robert A Hodorek | Method for repairing a bone defect using a formable implant which hardens in vivo |
| US20070132125A1 (en) | 2005-12-08 | 2007-06-14 | Bausch & Lomb Incorporated | Use of a super-cooled fluid in lens processing |
| JP4078371B2 (ja) | 2006-01-27 | 2008-04-23 | 章弘 小栗 | 涙点プラグ |
| CN103393483B (zh) | 2006-03-31 | 2016-08-24 | 玛提治疗有限公司 | 用于鼻泪系统的药物释放方法、结构及组合物 |
| WO2007124128A2 (en) * | 2006-04-20 | 2007-11-01 | Liquidia Technologies, Inc. | Biological vessel flow control devices and methods |
| EP2019649A4 (en) * | 2006-04-27 | 2012-09-19 | Narmada R Shenoy | COMPOSITIONS AND METHODS FOR TREATING OR PREVENTING BODILUM DISORDER DISORDERS |
| US20080045911A1 (en) * | 2006-06-21 | 2008-02-21 | Borgia Maureen J | Punctal plugs for the delivery of active agents |
| US9173773B2 (en) | 2006-06-21 | 2015-11-03 | Johnson & Johnson Vision Care, Inc. | Punctal plugs for the delivery of active agents |
| US9474645B2 (en) | 2006-06-21 | 2016-10-25 | Johnson & Johnson Vision Care, Inc. | Punctal plugs for the delivery of active agents |
| US20080097442A1 (en) * | 2006-06-29 | 2008-04-24 | Dixon Robert A | Method and device for improving the function of taper locks used for spinal stabilization |
| FR2908042B1 (fr) | 2006-11-08 | 2009-06-05 | Bruno Fayet | Ensemble d'intubation monocanaliculonasal et/ou monocanaliculaire,notamment pour l'imperforation lacrymonasale. |
| UY30883A1 (es) | 2007-01-31 | 2008-05-31 | Alcon Res | Tapones punctales y metodos de liberacion de agentes terapeuticos |
| US20080299176A1 (en) | 2007-05-30 | 2008-12-04 | Yu-Chin Lai | Drug delivery device comprising crosslinked polyurethane-siloxane-containing copolymers |
| CN101861135A (zh) * | 2007-09-07 | 2010-10-13 | Qlt栓塞输送公司 | 泪道植入物检测 |
| JP2010537776A (ja) | 2007-09-07 | 2010-12-09 | キューエルティー プラグ デリバリー,インク. | 涙管インプラント用の挿入および抜き取り工具 |
| US20090104243A1 (en) * | 2007-09-07 | 2009-04-23 | Qlt Plug Delivery, Inc. - Qpdi | Drug cores for sustained release of therapeutic agents |
| WO2009035565A1 (en) | 2007-09-07 | 2009-03-19 | Qlt Plug Delivery, Inc | Prostaglandin analogues for implant devices and methods |
| JP5524841B2 (ja) | 2007-09-07 | 2014-06-18 | キュー エル ティー インク. | 涙管インプラント及び関連する方法 |
| RU2010136822A (ru) | 2008-02-18 | 2012-03-10 | Клт Плаг Диливери, Инк. (Us) | Лакримальные имплантаты и связанные с ними способы |
| US9132088B2 (en) | 2008-04-30 | 2015-09-15 | Mati Therapeutics Inc. | Composite lacrimal insert and related methods |
| CN102123713A (zh) | 2008-05-09 | 2011-07-13 | Qlt栓塞输送公司 | 治疗青光眼和眼高血压的活性剂的持续释放递送 |
| WO2009145755A1 (en) | 2008-05-30 | 2009-12-03 | Qlt Plug Delivery, Inc | Surface treated implantable articles and related methods |
| CA2728623A1 (en) | 2008-06-24 | 2010-01-21 | Qlt Plug Delivery, Inc. | Combination treatment of glaucoma |
| CA2730101A1 (en) | 2008-07-08 | 2010-01-14 | Qlt Plug Delivery, Inc. | Lacrimal implant body including comforting agent |
| EP2376019A1 (en) | 2008-12-19 | 2011-10-19 | QLT, Inc. | Substance delivering punctum implants and methods |
| CN102341144B (zh) | 2009-01-23 | 2014-10-29 | Qlt股份有限公司 | 一种或多种药剂的持续释放递送 |
| MX2011008875A (es) | 2009-02-23 | 2011-09-26 | Quadra Logic Tech Inc | Implantes lagrimales y metodos relacionados. |
-
2008
- 2008-09-05 CN CN200880113681A patent/CN101861135A/zh active Pending
- 2008-09-05 RU RU2010112417/14A patent/RU2010112417A/ru not_active Application Discontinuation
- 2008-09-05 JP JP2010524053A patent/JP5411140B2/ja active Active
- 2008-09-05 BR BRPI0817074 patent/BRPI0817074A2/pt not_active IP Right Cessation
- 2008-09-05 SG SG2012066213A patent/SG184728A1/en unknown
- 2008-09-05 NZ NZ583858A patent/NZ583858A/xx not_active IP Right Cessation
- 2008-09-05 CA CA2698580A patent/CA2698580C/en active Active
- 2008-09-05 AU AU2008300022A patent/AU2008300022A1/en not_active Abandoned
- 2008-09-05 MX MX2010002619A patent/MX2010002619A/es not_active Application Discontinuation
- 2008-09-05 EP EP08830574A patent/EP2205193A2/en not_active Ceased
- 2008-09-05 EP EP18151269.0A patent/EP3372205A1/en not_active Withdrawn
- 2008-09-05 WO PCT/US2008/010502 patent/WO2009035571A2/en active Application Filing
- 2008-09-05 KR KR1020107007093A patent/KR20100067099A/ko not_active Application Discontinuation
- 2008-09-05 US US12/231,987 patent/US9011361B2/en active Active
- 2008-09-08 TW TW097134436A patent/TW201006451A/zh unknown
-
2010
- 2010-03-11 ZA ZA2010/01739A patent/ZA201001739B/en unknown
-
2013
- 2013-11-07 JP JP2013230810A patent/JP2014113469A/ja active Pending
-
2015
- 2015-04-20 US US14/690,874 patent/US11141312B2/en active Active
-
2016
- 2016-10-19 JP JP2016204977A patent/JP6503328B2/ja active Active
-
2018
- 2018-03-23 JP JP2018056808A patent/JP6672362B2/ja active Active
-
2021
- 2021-10-12 US US17/499,656 patent/US20220031507A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP2010537777A (ja) | 2010-12-09 |
| JP2018140181A (ja) | 2018-09-13 |
| EP2205193A2 (en) | 2010-07-14 |
| WO2009035571A3 (en) | 2009-04-30 |
| US20150374541A1 (en) | 2015-12-31 |
| JP2014113469A (ja) | 2014-06-26 |
| TW201006451A (en) | 2010-02-16 |
| CA2698580A1 (en) | 2009-03-19 |
| JP5411140B2 (ja) | 2014-02-12 |
| RU2010112417A (ru) | 2011-10-10 |
| CN101861135A (zh) | 2010-10-13 |
| US11141312B2 (en) | 2021-10-12 |
| SG184728A1 (en) | 2012-10-30 |
| US20220031507A1 (en) | 2022-02-03 |
| JP6503328B2 (ja) | 2019-04-17 |
| BRPI0817074A2 (pt) | 2015-03-24 |
| WO2009035571A2 (en) | 2009-03-19 |
| AU2008300022A1 (en) | 2009-03-19 |
| US9011361B2 (en) | 2015-04-21 |
| US20090099626A1 (en) | 2009-04-16 |
| NZ583858A (en) | 2012-08-31 |
| JP6672362B2 (ja) | 2020-03-25 |
| JP2017029794A (ja) | 2017-02-09 |
| MX2010002619A (es) | 2010-06-01 |
| CA2698580C (en) | 2016-10-11 |
| ZA201001739B (en) | 2011-12-28 |
| EP3372205A1 (en) | 2018-09-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20220031507A1 (en) | Lacrimal implant detection | |
| KR101571434B1 (ko) | 치료 약제의 서방성 약물 코어 | |
| JP6885919B2 (ja) | 涙器系薬剤送達装置 | |
| EP3380040B1 (en) | Lacrimal system for drug delivery | |
| Menapace | Effect of anterior capsule polishing on capsule opacification and YAG laser capsulotomy |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| N231 | Notification of change of applicant | ||
| N231 | Notification of change of applicant | ||
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |