KR20060111731A - 사람 유두종 바이러스 항원과 스트레스 단백질을 포함하는융합 단백질을 포함하는 조성물에 의해 유도된 사람 유두종바이러스 항원에 대한 면역 반응 - Google Patents
사람 유두종 바이러스 항원과 스트레스 단백질을 포함하는융합 단백질을 포함하는 조성물에 의해 유도된 사람 유두종바이러스 항원에 대한 면역 반응 Download PDFInfo
- Publication number
- KR20060111731A KR20060111731A KR1020067019653A KR20067019653A KR20060111731A KR 20060111731 A KR20060111731 A KR 20060111731A KR 1020067019653 A KR1020067019653 A KR 1020067019653A KR 20067019653 A KR20067019653 A KR 20067019653A KR 20060111731 A KR20060111731 A KR 20060111731A
- Authority
- KR
- South Korea
- Prior art keywords
- protein
- hpv
- stress
- antigen
- cells
- Prior art date
Links
- 241000701806 Human papillomavirus Species 0.000 title claims abstract description 163
- 102000002812 Heat-Shock Proteins Human genes 0.000 title claims abstract description 108
- 108010004889 Heat-Shock Proteins Proteins 0.000 title claims abstract description 108
- 108091007433 antigens Proteins 0.000 title claims abstract description 107
- 102000036639 antigens Human genes 0.000 title claims abstract description 107
- 108020001507 fusion proteins Proteins 0.000 title claims abstract description 96
- 102000037865 fusion proteins Human genes 0.000 title claims abstract description 95
- 239000000203 mixture Substances 0.000 title claims abstract description 73
- 230000028993 immune response Effects 0.000 title claims abstract description 38
- 239000000427 antigen Substances 0.000 title claims abstract description 28
- 239000013604 expression vector Substances 0.000 claims abstract description 20
- 230000001939 inductive effect Effects 0.000 claims abstract description 5
- 238000000034 method Methods 0.000 claims description 31
- 102100038222 60 kDa heat shock protein, mitochondrial Human genes 0.000 claims description 24
- 101710154868 60 kDa heat shock protein, mitochondrial Proteins 0.000 claims description 18
- 150000007523 nucleic acids Chemical class 0.000 claims description 18
- 101100507655 Canis lupus familiaris HSPA1 gene Proteins 0.000 claims description 13
- 108020004707 nucleic acids Proteins 0.000 claims description 13
- 102000039446 nucleic acids Human genes 0.000 claims description 13
- 102100034051 Heat shock protein HSP 90-alpha Human genes 0.000 claims description 10
- 101001016865 Homo sapiens Heat shock protein HSP 90-alpha Proteins 0.000 claims description 10
- 102100024341 10 kDa heat shock protein, mitochondrial Human genes 0.000 claims description 8
- 101710122378 10 kDa heat shock protein, mitochondrial Proteins 0.000 claims description 7
- 108010042283 HSP40 Heat-Shock Proteins Proteins 0.000 claims description 7
- 239000002671 adjuvant Substances 0.000 claims description 7
- 230000024932 T cell mediated immunity Effects 0.000 claims description 4
- 108090000565 Capsid Proteins Proteins 0.000 claims description 3
- 102100023321 Ceruloplasmin Human genes 0.000 claims description 3
- 102000004447 HSP40 Heat-Shock Proteins Human genes 0.000 claims description 3
- 108010027179 Tacrolimus Binding Proteins Proteins 0.000 claims description 3
- 102000018679 Tacrolimus Binding Proteins Human genes 0.000 claims description 3
- 108090000848 Ubiquitin Proteins 0.000 claims description 3
- 102000044159 Ubiquitin Human genes 0.000 claims description 3
- 230000003612 virological effect Effects 0.000 claims description 3
- 102100021868 Calnexin Human genes 0.000 claims description 2
- 108010056891 Calnexin Proteins 0.000 claims description 2
- 102000006010 Protein Disulfide-Isomerase Human genes 0.000 claims description 2
- 239000003085 diluting agent Substances 0.000 claims description 2
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 2
- 108020003519 protein disulfide isomerase Proteins 0.000 claims description 2
- 239000004094 surface-active agent Substances 0.000 claims description 2
- 230000028996 humoral immune response Effects 0.000 claims 1
- 108090000623 proteins and genes Proteins 0.000 abstract description 181
- 102000004169 proteins and genes Human genes 0.000 abstract description 128
- 206010028980 Neoplasm Diseases 0.000 abstract description 71
- 230000014509 gene expression Effects 0.000 abstract description 44
- 230000004927 fusion Effects 0.000 abstract description 9
- 230000001404 mediated effect Effects 0.000 abstract description 9
- 230000012743 protein tagging Effects 0.000 abstract description 9
- 230000001461 cytolytic effect Effects 0.000 abstract description 8
- 230000021615 conjugation Effects 0.000 abstract description 6
- 239000000126 substance Substances 0.000 abstract description 6
- 230000001413 cellular effect Effects 0.000 abstract description 5
- 125000005647 linker group Chemical group 0.000 abstract 1
- 235000018102 proteins Nutrition 0.000 description 123
- 210000004027 cell Anatomy 0.000 description 115
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 74
- 108090000765 processed proteins & peptides Proteins 0.000 description 45
- 239000011780 sodium chloride Substances 0.000 description 45
- 239000000872 buffer Substances 0.000 description 38
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 33
- 241000588724 Escherichia coli Species 0.000 description 30
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 30
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 30
- 241001465754 Metazoa Species 0.000 description 27
- 108020004414 DNA Proteins 0.000 description 23
- 239000013612 plasmid Substances 0.000 description 23
- 241000699670 Mus sp. Species 0.000 description 22
- 102000004196 processed proteins & peptides Human genes 0.000 description 22
- 239000013598 vector Substances 0.000 description 22
- 230000035882 stress Effects 0.000 description 21
- 241000894006 Bacteria Species 0.000 description 19
- 238000005119 centrifugation Methods 0.000 description 18
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 17
- 210000004881 tumor cell Anatomy 0.000 description 16
- 102000011931 Nucleoproteins Human genes 0.000 description 15
- 108010061100 Nucleoproteins Proteins 0.000 description 15
- 201000011510 cancer Diseases 0.000 description 15
- 238000010369 molecular cloning Methods 0.000 description 15
- 238000011282 treatment Methods 0.000 description 15
- 229920004890 Triton X-100 Polymers 0.000 description 14
- 230000003053 immunization Effects 0.000 description 14
- 238000002649 immunization Methods 0.000 description 14
- 238000002474 experimental method Methods 0.000 description 13
- 238000003556 assay Methods 0.000 description 12
- 230000000694 effects Effects 0.000 description 12
- 239000002773 nucleotide Substances 0.000 description 12
- 125000003729 nucleotide group Chemical group 0.000 description 12
- 238000003752 polymerase chain reaction Methods 0.000 description 12
- 230000004044 response Effects 0.000 description 12
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 12
- 229920002684 Sepharose Polymers 0.000 description 11
- 210000001151 cytotoxic T lymphocyte Anatomy 0.000 description 11
- PJJJBBJSCAKJQF-UHFFFAOYSA-N guanidinium chloride Chemical compound [Cl-].NC(N)=[NH2+] PJJJBBJSCAKJQF-UHFFFAOYSA-N 0.000 description 11
- 239000012139 lysis buffer Substances 0.000 description 11
- 239000008188 pellet Substances 0.000 description 11
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 11
- 238000012360 testing method Methods 0.000 description 11
- 239000006285 cell suspension Substances 0.000 description 10
- 101150086609 groEL2 gene Proteins 0.000 description 10
- YBYRMVIVWMBXKQ-UHFFFAOYSA-N phenylmethanesulfonyl fluoride Chemical compound FS(=O)(=O)CC1=CC=CC=C1 YBYRMVIVWMBXKQ-UHFFFAOYSA-N 0.000 description 10
- 102100025064 Cellular tumor antigen p53 Human genes 0.000 description 9
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 9
- 101000721661 Homo sapiens Cellular tumor antigen p53 Proteins 0.000 description 9
- 210000001744 T-lymphocyte Anatomy 0.000 description 9
- 229940071106 ethylenediaminetetraacetate Drugs 0.000 description 9
- 238000011534 incubation Methods 0.000 description 9
- 239000000463 material Substances 0.000 description 9
- 229920001184 polypeptide Polymers 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 8
- 241000341655 Human papillomavirus type 16 Species 0.000 description 8
- 108091028043 Nucleic acid sequence Proteins 0.000 description 8
- 241000700605 Viruses Species 0.000 description 8
- 239000002609 medium Substances 0.000 description 8
- 238000002360 preparation method Methods 0.000 description 8
- 229920005989 resin Polymers 0.000 description 8
- 239000011347 resin Substances 0.000 description 8
- 230000009466 transformation Effects 0.000 description 8
- 108010039627 Aprotinin Proteins 0.000 description 7
- 206010008342 Cervix carcinoma Diseases 0.000 description 7
- 208000006105 Uterine Cervical Neoplasms Diseases 0.000 description 7
- 238000007792 addition Methods 0.000 description 7
- 150000001413 amino acids Chemical class 0.000 description 7
- 229960004405 aprotinin Drugs 0.000 description 7
- 230000001580 bacterial effect Effects 0.000 description 7
- 230000027455 binding Effects 0.000 description 7
- 201000010881 cervical cancer Diseases 0.000 description 7
- 230000001965 increasing effect Effects 0.000 description 7
- ZPNFWUPYTFPOJU-LPYSRVMUSA-N iniprol Chemical compound C([C@H]1C(=O)NCC(=O)NCC(=O)N[C@H]2CSSC[C@H]3C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@H](C(N[C@H](C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC=4C=CC=CC=4)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CC=4C=CC=CC=4)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC2=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H]2N(CCC2)C(=O)[C@@H](N)CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N2[C@@H](CCC2)C(=O)N2[C@@H](CCC2)C(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N2[C@@H](CCC2)C(=O)N3)C(=O)NCC(=O)NCC(=O)N[C@@H](C)C(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@H](C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@H](C(=O)N1)C(C)C)[C@@H](C)O)[C@@H](C)CC)=O)[C@@H](C)CC)C1=CC=C(O)C=C1 ZPNFWUPYTFPOJU-LPYSRVMUSA-N 0.000 description 7
- 239000002198 insoluble material Substances 0.000 description 7
- 229950000964 pepstatin Drugs 0.000 description 7
- 108010091212 pepstatin Proteins 0.000 description 7
- FAXGPCHRFPCXOO-LXTPJMTPSA-N pepstatin A Chemical compound OC(=O)C[C@H](O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)C[C@H](O)[C@H](CC(C)C)NC(=O)[C@H](C(C)C)NC(=O)[C@H](C(C)C)NC(=O)CC(C)C FAXGPCHRFPCXOO-LXTPJMTPSA-N 0.000 description 7
- 239000012460 protein solution Substances 0.000 description 7
- 108010058432 Chaperonin 60 Proteins 0.000 description 6
- 108020004705 Codon Proteins 0.000 description 6
- 101000767631 Human papillomavirus type 16 Protein E7 Proteins 0.000 description 6
- 102000016943 Muramidase Human genes 0.000 description 6
- 108010014251 Muramidase Proteins 0.000 description 6
- 108010062010 N-Acetylmuramoyl-L-alanine Amidase Proteins 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 239000013504 Triton X-100 Substances 0.000 description 6
- 230000000875 corresponding effect Effects 0.000 description 6
- 239000012636 effector Substances 0.000 description 6
- 238000009472 formulation Methods 0.000 description 6
- 238000011081 inoculation Methods 0.000 description 6
- 229960000274 lysozyme Drugs 0.000 description 6
- 239000004325 lysozyme Substances 0.000 description 6
- 235000010335 lysozyme Nutrition 0.000 description 6
- 230000002441 reversible effect Effects 0.000 description 6
- 239000011734 sodium Substances 0.000 description 6
- 238000011537 Coomassie blue staining Methods 0.000 description 5
- 102100029721 DnaJ homolog subfamily B member 1 Human genes 0.000 description 5
- 239000012591 Dulbecco’s Phosphate Buffered Saline Substances 0.000 description 5
- 241000672609 Escherichia coli BL21 Species 0.000 description 5
- 241000282414 Homo sapiens Species 0.000 description 5
- 241001467552 Mycobacterium bovis BCG Species 0.000 description 5
- -1 TF55 Proteins 0.000 description 5
- 229960000723 ampicillin Drugs 0.000 description 5
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 5
- 230000015572 biosynthetic process Effects 0.000 description 5
- 230000009089 cytolysis Effects 0.000 description 5
- 239000002158 endotoxin Substances 0.000 description 5
- 239000007924 injection Substances 0.000 description 5
- 238000002347 injection Methods 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 230000007246 mechanism Effects 0.000 description 5
- 239000002245 particle Substances 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 230000012846 protein folding Effects 0.000 description 5
- 238000000746 purification Methods 0.000 description 5
- 230000002829 reductive effect Effects 0.000 description 5
- 108091008146 restriction endonucleases Proteins 0.000 description 5
- 230000035939 shock Effects 0.000 description 5
- 238000000527 sonication Methods 0.000 description 5
- 238000010561 standard procedure Methods 0.000 description 5
- 230000004936 stimulating effect Effects 0.000 description 5
- 239000010414 supernatant solution Substances 0.000 description 5
- 229920001817 Agar Polymers 0.000 description 4
- 102000014914 Carrier Proteins Human genes 0.000 description 4
- 108010078791 Carrier Proteins Proteins 0.000 description 4
- 101150013359 E7 gene Proteins 0.000 description 4
- GDBQQVLCIARPGH-UHFFFAOYSA-N Leupeptin Natural products CC(C)CC(NC(C)=O)C(=O)NC(CC(C)C)C(=O)NC(C=O)CCCN=C(N)N GDBQQVLCIARPGH-UHFFFAOYSA-N 0.000 description 4
- 108010085220 Multiprotein Complexes Proteins 0.000 description 4
- 102000007474 Multiprotein Complexes Human genes 0.000 description 4
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 4
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 4
- 101710172711 Structural protein Proteins 0.000 description 4
- 239000007984 Tris EDTA buffer Substances 0.000 description 4
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 4
- 239000008272 agar Substances 0.000 description 4
- 235000001014 amino acid Nutrition 0.000 description 4
- 229960000190 bacillus calmette–guérin vaccine Drugs 0.000 description 4
- 229940041514 candida albicans extract Drugs 0.000 description 4
- 230000015556 catabolic process Effects 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 238000006731 degradation reaction Methods 0.000 description 4
- 230000029087 digestion Effects 0.000 description 4
- 239000000499 gel Substances 0.000 description 4
- 230000014726 immortalization of host cell Effects 0.000 description 4
- 238000000338 in vitro Methods 0.000 description 4
- 230000006698 induction Effects 0.000 description 4
- 208000015181 infectious disease Diseases 0.000 description 4
- 229930027917 kanamycin Natural products 0.000 description 4
- 229960000318 kanamycin Drugs 0.000 description 4
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 4
- 229930182823 kanamycin A Natural products 0.000 description 4
- GDBQQVLCIARPGH-ULQDDVLXSA-N leupeptin Chemical compound CC(C)C[C@H](NC(C)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C=O)CCCN=C(N)N GDBQQVLCIARPGH-ULQDDVLXSA-N 0.000 description 4
- 108010052968 leupeptin Proteins 0.000 description 4
- 210000001165 lymph node Anatomy 0.000 description 4
- 230000003287 optical effect Effects 0.000 description 4
- 238000010188 recombinant method Methods 0.000 description 4
- 238000000926 separation method Methods 0.000 description 4
- 238000012163 sequencing technique Methods 0.000 description 4
- 238000010186 staining Methods 0.000 description 4
- 238000010254 subcutaneous injection Methods 0.000 description 4
- 239000007929 subcutaneous injection Substances 0.000 description 4
- 210000001519 tissue Anatomy 0.000 description 4
- 230000009261 transgenic effect Effects 0.000 description 4
- 201000008827 tuberculosis Diseases 0.000 description 4
- 230000029812 viral genome replication Effects 0.000 description 4
- 239000012138 yeast extract Substances 0.000 description 4
- AZQWKYJCGOJGHM-UHFFFAOYSA-N 1,4-benzoquinone Chemical compound O=C1C=CC(=O)C=C1 AZQWKYJCGOJGHM-UHFFFAOYSA-N 0.000 description 3
- IDOQDZANRZQBTP-UHFFFAOYSA-N 2-[2-(2,4,4-trimethylpentan-2-yl)phenoxy]ethanol Chemical compound CC(C)(C)CC(C)(C)C1=CC=CC=C1OCCO IDOQDZANRZQBTP-UHFFFAOYSA-N 0.000 description 3
- QFVHZQCOUORWEI-UHFFFAOYSA-N 4-[(4-anilino-5-sulfonaphthalen-1-yl)diazenyl]-5-hydroxynaphthalene-2,7-disulfonic acid Chemical compound C=12C(O)=CC(S(O)(=O)=O)=CC2=CC(S(O)(=O)=O)=CC=1N=NC(C1=CC=CC(=C11)S(O)(=O)=O)=CC=C1NC1=CC=CC=C1 QFVHZQCOUORWEI-UHFFFAOYSA-N 0.000 description 3
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 3
- 230000004544 DNA amplification Effects 0.000 description 3
- 102000016928 DNA-directed DNA polymerase Human genes 0.000 description 3
- 108010014303 DNA-directed DNA polymerase Proteins 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 102100023737 GrpE protein homolog 1, mitochondrial Human genes 0.000 description 3
- 101710121996 Hexon protein p72 Proteins 0.000 description 3
- 101000829489 Homo sapiens GrpE protein homolog 1, mitochondrial Proteins 0.000 description 3
- 101100540311 Human papillomavirus type 16 E6 gene Proteins 0.000 description 3
- 101710125418 Major capsid protein Proteins 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- 108091034117 Oligonucleotide Proteins 0.000 description 3
- 108700026244 Open Reading Frames Proteins 0.000 description 3
- 208000009608 Papillomavirus Infections Diseases 0.000 description 3
- 108091005804 Peptidases Proteins 0.000 description 3
- 108091081024 Start codon Proteins 0.000 description 3
- 229920004929 Triton X-114 Polymers 0.000 description 3
- 239000011543 agarose gel Substances 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 230000037396 body weight Effects 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 210000003763 chloroplast Anatomy 0.000 description 3
- 101150036359 clpB gene Proteins 0.000 description 3
- 238000012217 deletion Methods 0.000 description 3
- 230000037430 deletion Effects 0.000 description 3
- 230000001747 exhibiting effect Effects 0.000 description 3
- 239000012634 fragment Substances 0.000 description 3
- 210000004392 genitalia Anatomy 0.000 description 3
- 230000012010 growth Effects 0.000 description 3
- HNDVDQJCIGZPNO-UHFFFAOYSA-N histidine Natural products OC(=O)C(N)CC1=CN=CN1 HNDVDQJCIGZPNO-UHFFFAOYSA-N 0.000 description 3
- 210000002865 immune cell Anatomy 0.000 description 3
- 230000001900 immune effect Effects 0.000 description 3
- 230000036039 immunity Effects 0.000 description 3
- 210000003000 inclusion body Anatomy 0.000 description 3
- 239000003112 inhibitor Substances 0.000 description 3
- 230000003834 intracellular effect Effects 0.000 description 3
- 238000013507 mapping Methods 0.000 description 3
- 230000002265 prevention Effects 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 230000001737 promoting effect Effects 0.000 description 3
- 230000001681 protective effect Effects 0.000 description 3
- 238000001742 protein purification Methods 0.000 description 3
- 239000011541 reaction mixture Substances 0.000 description 3
- 230000001105 regulatory effect Effects 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000002195 soluble material Substances 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 238000003786 synthesis reaction Methods 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 239000012137 tryptone Substances 0.000 description 3
- 238000005406 washing Methods 0.000 description 3
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical group N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 2
- BPHPUYQFMNQIOC-MBOVONDJSA-N (2r,3r,4s,5r)-2-(hydroxymethyl)-6-propan-2-ylsulfanyloxane-3,4,5-triol Chemical compound CC(C)SC1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O BPHPUYQFMNQIOC-MBOVONDJSA-N 0.000 description 2
- 208000023275 Autoimmune disease Diseases 0.000 description 2
- 108091026890 Coding region Proteins 0.000 description 2
- 229930105110 Cyclosporin A Natural products 0.000 description 2
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 description 2
- 108010036949 Cyclosporine Proteins 0.000 description 2
- 238000001712 DNA sequencing Methods 0.000 description 2
- 241000702421 Dependoparvovirus Species 0.000 description 2
- 102000016607 Diphtheria Toxin Human genes 0.000 description 2
- 108010053187 Diphtheria Toxin Proteins 0.000 description 2
- 108010093502 E2F Transcription Factors Proteins 0.000 description 2
- 102000001388 E2F Transcription Factors Human genes 0.000 description 2
- 101150071673 E6 gene Proteins 0.000 description 2
- 241001198387 Escherichia coli BL21(DE3) Species 0.000 description 2
- 241000206602 Eukaryota Species 0.000 description 2
- JRZJKWGQFNTSRN-UHFFFAOYSA-N Geldanamycin Natural products C1C(C)CC(OC)C(O)C(C)C=C(C)C(OC(N)=O)C(OC)CCC=C(C)C(=O)NC2=CC(=O)C(OC)=C1C2=O JRZJKWGQFNTSRN-UHFFFAOYSA-N 0.000 description 2
- 101001003102 Homo sapiens Hypoxia up-regulated protein 1 Proteins 0.000 description 2
- 102100020755 Hypoxia up-regulated protein 1 Human genes 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- 241000239218 Limulus Species 0.000 description 2
- 241000187479 Mycobacterium tuberculosis Species 0.000 description 2
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 2
- 102000035195 Peptidases Human genes 0.000 description 2
- 108010020062 Peptidylprolyl Isomerase Proteins 0.000 description 2
- 102000009658 Peptidylprolyl Isomerase Human genes 0.000 description 2
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 2
- RJKFOVLPORLFTN-LEKSSAKUSA-N Progesterone Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H](C(=O)C)[C@@]1(C)CC2 RJKFOVLPORLFTN-LEKSSAKUSA-N 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 2
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 2
- 230000018199 S phase Effects 0.000 description 2
- 238000012300 Sequence Analysis Methods 0.000 description 2
- 102100035254 Sodium- and chloride-dependent GABA transporter 3 Human genes 0.000 description 2
- 101710104417 Sodium- and chloride-dependent GABA transporter 3 Proteins 0.000 description 2
- IQFYYKKMVGJFEH-XLPZGREQSA-N Thymidine Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O)C1 IQFYYKKMVGJFEH-XLPZGREQSA-N 0.000 description 2
- 108091023040 Transcription factor Proteins 0.000 description 2
- 102000040945 Transcription factor Human genes 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 108010040002 Tumor Suppressor Proteins Proteins 0.000 description 2
- 102000001742 Tumor Suppressor Proteins Human genes 0.000 description 2
- ALEGHOASKPPZCO-UHFFFAOYSA-N [Cl-].[Na].Cl.NC(=[NH2+])N Chemical compound [Cl-].[Na].Cl.NC(=[NH2+])N ALEGHOASKPPZCO-UHFFFAOYSA-N 0.000 description 2
- 238000005273 aeration Methods 0.000 description 2
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 2
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 2
- 235000011130 ammonium sulphate Nutrition 0.000 description 2
- 230000003321 amplification Effects 0.000 description 2
- 210000000436 anus Anatomy 0.000 description 2
- 230000003416 augmentation Effects 0.000 description 2
- 244000052616 bacterial pathogen Species 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 239000012267 brine Substances 0.000 description 2
- 239000007853 buffer solution Substances 0.000 description 2
- 210000004899 c-terminal region Anatomy 0.000 description 2
- 210000000234 capsid Anatomy 0.000 description 2
- 239000004202 carbamide Substances 0.000 description 2
- 229910002091 carbon monoxide Inorganic materials 0.000 description 2
- 230000007969 cellular immunity Effects 0.000 description 2
- 229920001429 chelating resin Polymers 0.000 description 2
- 229960001265 ciclosporin Drugs 0.000 description 2
- 210000000805 cytoplasm Anatomy 0.000 description 2
- 230000007123 defense Effects 0.000 description 2
- 238000000502 dialysis Methods 0.000 description 2
- 239000000385 dialysis solution Substances 0.000 description 2
- 238000004090 dissolution Methods 0.000 description 2
- 239000012153 distilled water Substances 0.000 description 2
- 101150052825 dnaK gene Proteins 0.000 description 2
- 230000002708 enhancing effect Effects 0.000 description 2
- 230000009841 epithelial lesion Effects 0.000 description 2
- 210000003527 eukaryotic cell Anatomy 0.000 description 2
- 239000012894 fetal calf serum Substances 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- QTQAWLPCGQOSGP-GBTDJJJQSA-N geldanamycin Chemical compound N1C(=O)\C(C)=C/C=C\[C@@H](OC)[C@H](OC(N)=O)\C(C)=C/[C@@H](C)[C@@H](O)[C@H](OC)C[C@@H](C)CC2=C(OC)C(=O)C=C1C2=O QTQAWLPCGQOSGP-GBTDJJJQSA-N 0.000 description 2
- BRZYSWJRSDMWLG-CAXSIQPQSA-N geneticin Chemical compound O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](C(C)O)O2)N)[C@@H](N)C[C@H]1N BRZYSWJRSDMWLG-CAXSIQPQSA-N 0.000 description 2
- 239000001963 growth medium Substances 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 210000002443 helper t lymphocyte Anatomy 0.000 description 2
- 210000000987 immune system Anatomy 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- BPHPUYQFMNQIOC-NXRLNHOXSA-N isopropyl beta-D-thiogalactopyranoside Chemical compound CC(C)S[C@@H]1O[C@H](CO)[C@H](O)[C@H](O)[C@H]1O BPHPUYQFMNQIOC-NXRLNHOXSA-N 0.000 description 2
- 210000000265 leukocyte Anatomy 0.000 description 2
- 210000005265 lung cell Anatomy 0.000 description 2
- 208000020816 lung neoplasm Diseases 0.000 description 2
- 210000004962 mammalian cell Anatomy 0.000 description 2
- 230000035800 maturation Effects 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 210000003470 mitochondria Anatomy 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 230000035772 mutation Effects 0.000 description 2
- 239000013642 negative control Substances 0.000 description 2
- 229910052759 nickel Inorganic materials 0.000 description 2
- 238000003199 nucleic acid amplification method Methods 0.000 description 2
- 231100000590 oncogenic Toxicity 0.000 description 2
- 230000002246 oncogenic effect Effects 0.000 description 2
- 238000002559 palpation Methods 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- 230000002688 persistence Effects 0.000 description 2
- 239000013641 positive control Substances 0.000 description 2
- 230000003389 potentiating effect Effects 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 230000035755 proliferation Effects 0.000 description 2
- 230000009696 proliferative response Effects 0.000 description 2
- 230000000069 prophylactic effect Effects 0.000 description 2
- 108700042226 ras Genes Proteins 0.000 description 2
- 230000006798 recombination Effects 0.000 description 2
- 238000005215 recombination Methods 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- ATEBXHFBFRCZMA-VXTBVIBXSA-N rifabutin Chemical compound O([C@](C1=O)(C)O/C=C/[C@@H]([C@H]([C@@H](OC(C)=O)[C@H](C)[C@H](O)[C@H](C)[C@@H](O)[C@@H](C)\C=C\C=C(C)/C(=O)NC(=C2N3)C(=O)C=4C(O)=C5C)C)OC)C5=C1C=4C2=NC13CCN(CC(C)C)CC1 ATEBXHFBFRCZMA-VXTBVIBXSA-N 0.000 description 2
- 229960000885 rifabutin Drugs 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 239000001488 sodium phosphate Substances 0.000 description 2
- 229910000162 sodium phosphate Inorganic materials 0.000 description 2
- DAEPDZWVDSPTHF-UHFFFAOYSA-M sodium pyruvate Chemical compound [Na+].CC(=O)C([O-])=O DAEPDZWVDSPTHF-UHFFFAOYSA-M 0.000 description 2
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 2
- 230000003381 solubilizing effect Effects 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 210000000952 spleen Anatomy 0.000 description 2
- 210000004989 spleen cell Anatomy 0.000 description 2
- 239000012134 supernatant fraction Substances 0.000 description 2
- 238000013518 transcription Methods 0.000 description 2
- 230000035897 transcription Effects 0.000 description 2
- 230000014616 translation Effects 0.000 description 2
- 230000032258 transport Effects 0.000 description 2
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 2
- 230000000381 tumorigenic effect Effects 0.000 description 2
- 238000000108 ultra-filtration Methods 0.000 description 2
- 241000701161 unidentified adenovirus Species 0.000 description 2
- 241000712461 unidentified influenza virus Species 0.000 description 2
- 229960005486 vaccine Drugs 0.000 description 2
- 239000013603 viral vector Substances 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- 230000004572 zinc-binding Effects 0.000 description 2
- RDEIXVOBVLKYNT-VQBXQJRRSA-N (2r,3r,4r,5r)-2-[(1s,2s,3r,4s,6r)-4,6-diamino-3-[(2r,3r,6s)-3-amino-6-(1-aminoethyl)oxan-2-yl]oxy-2-hydroxycyclohexyl]oxy-5-methyl-4-(methylamino)oxane-3,5-diol;(2r,3r,4r,5r)-2-[(1s,2s,3r,4s,6r)-4,6-diamino-3-[(2r,3r,6s)-3-amino-6-(aminomethyl)oxan-2-yl]o Chemical compound OS(O)(=O)=O.O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H](CC[C@@H](CN)O2)N)[C@@H](N)C[C@H]1N.O1C[C@@](O)(C)[C@H](NC)[C@@H](O)[C@H]1O[C@@H]1[C@@H](O)[C@H](O[C@@H]2[C@@H](CC[C@H](O2)C(C)N)N)[C@@H](N)C[C@H]1N.O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N RDEIXVOBVLKYNT-VQBXQJRRSA-N 0.000 description 1
- DHBXNPKRAUYBTH-UHFFFAOYSA-N 1,1-ethanedithiol Chemical compound CC(S)S DHBXNPKRAUYBTH-UHFFFAOYSA-N 0.000 description 1
- IQFYYKKMVGJFEH-OFKYTIFKSA-N 1-[(2r,4s,5r)-4-hydroxy-5-(tritiooxymethyl)oxolan-2-yl]-5-methylpyrimidine-2,4-dione Chemical compound C1[C@H](O)[C@@H](CO[3H])O[C@H]1N1C(=O)NC(=O)C(C)=C1 IQFYYKKMVGJFEH-OFKYTIFKSA-N 0.000 description 1
- 101710149439 20 kDa chaperonin, chloroplastic Proteins 0.000 description 1
- SLXKOJJOQWFEFD-UHFFFAOYSA-N 6-aminohexanoic acid Chemical compound NCCCCCC(O)=O SLXKOJJOQWFEFD-UHFFFAOYSA-N 0.000 description 1
- 108091006112 ATPases Proteins 0.000 description 1
- 102000007469 Actins Human genes 0.000 description 1
- 108010085238 Actins Proteins 0.000 description 1
- 102000057290 Adenosine Triphosphatases Human genes 0.000 description 1
- 229920000936 Agarose Polymers 0.000 description 1
- 206010059313 Anogenital warts Diseases 0.000 description 1
- 241000203069 Archaea Species 0.000 description 1
- 241000271566 Aves Species 0.000 description 1
- DWRXFEITVBNRMK-UHFFFAOYSA-N Beta-D-1-Arabinofuranosylthymine Natural products O=C1NC(=O)C(C)=CN1C1C(O)C(O)C(CO)O1 DWRXFEITVBNRMK-UHFFFAOYSA-N 0.000 description 1
- 102000004631 Calcineurin Human genes 0.000 description 1
- 108010042955 Calcineurin Proteins 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- 108010059013 Chaperonin 10 Proteins 0.000 description 1
- 108020004638 Circular DNA Proteins 0.000 description 1
- 101710177832 Co-chaperonin GroES Proteins 0.000 description 1
- 208000000907 Condylomata Acuminata Diseases 0.000 description 1
- 101100117177 Coxiella burnetii (strain RSA 493 / Nine Mile phase I) dnaK gene Proteins 0.000 description 1
- 102000003903 Cyclin-dependent kinases Human genes 0.000 description 1
- 108090000266 Cyclin-dependent kinases Proteins 0.000 description 1
- 108010072220 Cyclophilin A Proteins 0.000 description 1
- 108010072210 Cyclophilin C Proteins 0.000 description 1
- 229920002271 DEAE-Sepharose Polymers 0.000 description 1
- 102000004594 DNA Polymerase I Human genes 0.000 description 1
- 108010017826 DNA Polymerase I Proteins 0.000 description 1
- 230000004543 DNA replication Effects 0.000 description 1
- 101100016370 Danio rerio hsp90a.1 gene Proteins 0.000 description 1
- 101100285708 Dictyostelium discoideum hspD gene Proteins 0.000 description 1
- 101100125027 Dictyostelium discoideum mhsp70 gene Proteins 0.000 description 1
- 102100029714 DnaJ homolog subfamily B member 2 Human genes 0.000 description 1
- 241000255581 Drosophila <fruit fly, genus> Species 0.000 description 1
- 108090000860 Endopeptidase Clp Proteins 0.000 description 1
- 241000305071 Enterobacterales Species 0.000 description 1
- 241000620209 Escherichia coli DH5[alpha] Species 0.000 description 1
- 108010069271 FKBP-13 Proteins 0.000 description 1
- 241000287828 Gallus gallus Species 0.000 description 1
- 208000022555 Genital disease Diseases 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 101150031823 HSP70 gene Proteins 0.000 description 1
- 101150051208 HSPH1 gene Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000883686 Homo sapiens 60 kDa heat shock protein, mitochondrial Proteins 0.000 description 1
- 101100387776 Homo sapiens DNAJB1 gene Proteins 0.000 description 1
- 101000866020 Homo sapiens DnaJ homolog subfamily B member 2 Proteins 0.000 description 1
- 101000827313 Homo sapiens Peptidyl-prolyl cis-trans isomerase FKBP3 Proteins 0.000 description 1
- 101000891649 Homo sapiens Transcription elongation factor A protein-like 1 Proteins 0.000 description 1
- 101150028525 Hsp83 gene Proteins 0.000 description 1
- 101150065069 Hsp90b1 gene Proteins 0.000 description 1
- 241000883306 Huso huso Species 0.000 description 1
- GRRNUXAQVGOGFE-UHFFFAOYSA-N Hygromycin-B Natural products OC1C(NC)CC(N)C(O)C1OC1C2OC3(C(C(O)C(O)C(C(N)CO)O3)O)OC2C(O)C(CO)O1 GRRNUXAQVGOGFE-UHFFFAOYSA-N 0.000 description 1
- 206010021143 Hypoxia Diseases 0.000 description 1
- 108060003951 Immunoglobulin Proteins 0.000 description 1
- 101710125507 Integrase/recombinase Proteins 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 101150043276 Lon gene Proteins 0.000 description 1
- 206010058467 Lung neoplasm malignant Diseases 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 108010058682 Mitochondrial Proteins Proteins 0.000 description 1
- 102000006404 Mitochondrial Proteins Human genes 0.000 description 1
- 108010006519 Molecular Chaperones Proteins 0.000 description 1
- 102000005431 Molecular Chaperones Human genes 0.000 description 1
- 101100451677 Mus musculus Hspa4 gene Proteins 0.000 description 1
- 101100400378 Mus musculus Marveld2 gene Proteins 0.000 description 1
- 102100038895 Myc proto-oncogene protein Human genes 0.000 description 1
- 101710135898 Myc proto-oncogene protein Proteins 0.000 description 1
- 206010062207 Mycobacterial infection Diseases 0.000 description 1
- 241000186366 Mycobacterium bovis Species 0.000 description 1
- 241000186362 Mycobacterium leprae Species 0.000 description 1
- 241000187480 Mycobacterium smegmatis Species 0.000 description 1
- 241000187644 Mycobacterium vaccae Species 0.000 description 1
- 108700020796 Oncogene Proteins 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 241001631646 Papillomaviridae Species 0.000 description 1
- 102100034539 Peptidyl-prolyl cis-trans isomerase A Human genes 0.000 description 1
- 102100040283 Peptidyl-prolyl cis-trans isomerase B Human genes 0.000 description 1
- 102100024968 Peptidyl-prolyl cis-trans isomerase C Human genes 0.000 description 1
- 102100027913 Peptidyl-prolyl cis-trans isomerase FKBP1A Human genes 0.000 description 1
- 102100026408 Peptidyl-prolyl cis-trans isomerase FKBP2 Human genes 0.000 description 1
- 102100023846 Peptidyl-prolyl cis-trans isomerase FKBP3 Human genes 0.000 description 1
- 102100020739 Peptidyl-prolyl cis-trans isomerase FKBP4 Human genes 0.000 description 1
- 208000009565 Pharyngeal Neoplasms Diseases 0.000 description 1
- 102000045595 Phosphoprotein Phosphatases Human genes 0.000 description 1
- 108700019535 Phosphoprotein Phosphatases Proteins 0.000 description 1
- 108010089430 Phosphoproteins Proteins 0.000 description 1
- 102000007982 Phosphoproteins Human genes 0.000 description 1
- 108010093965 Polymyxin B Proteins 0.000 description 1
- 241001505332 Polyomavirus sp. Species 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 101710132596 Protein E4 Proteins 0.000 description 1
- 102000001253 Protein Kinase Human genes 0.000 description 1
- 101710132701 Protein L1 Proteins 0.000 description 1
- LCTONWCANYUPML-UHFFFAOYSA-M Pyruvate Chemical compound CC(=O)C([O-])=O LCTONWCANYUPML-UHFFFAOYSA-M 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 101100235786 Rattus norvegicus Lonp1 gene Proteins 0.000 description 1
- 241001068295 Replication defective viruses Species 0.000 description 1
- 108700025701 Retinoblastoma Genes Proteins 0.000 description 1
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 1
- 101100071627 Schizosaccharomyces pombe (strain 972 / ATCC 24843) swo1 gene Proteins 0.000 description 1
- 239000012506 Sephacryl® Substances 0.000 description 1
- 241000700584 Simplexvirus Species 0.000 description 1
- 108010006877 Tacrolimus Binding Protein 1A Proteins 0.000 description 1
- 108010010427 Thermosomes Proteins 0.000 description 1
- 108010022394 Threonine synthase Proteins 0.000 description 1
- 102000006601 Thymidine Kinase Human genes 0.000 description 1
- 108020004440 Thymidine kinase Proteins 0.000 description 1
- 101710150448 Transcriptional regulator Myc Proteins 0.000 description 1
- 208000007097 Urinary Bladder Neoplasms Diseases 0.000 description 1
- 241000700618 Vaccinia virus Species 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- 108700005077 Viral Genes Proteins 0.000 description 1
- 108010067390 Viral Proteins Proteins 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- GFFGJBXGBJISGV-UHFFFAOYSA-N adenyl group Chemical class N1=CN=C2N=CNC2=C1N GFFGJBXGBJISGV-UHFFFAOYSA-N 0.000 description 1
- 238000001042 affinity chromatography Methods 0.000 description 1
- 108010007908 alpha-Crystallins Proteins 0.000 description 1
- 102000007362 alpha-Crystallins Human genes 0.000 description 1
- 229940037003 alum Drugs 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000000539 amino acid group Chemical group 0.000 description 1
- 229960002684 aminocaproic acid Drugs 0.000 description 1
- 102000001307 androgen receptors Human genes 0.000 description 1
- 108010080146 androgen receptors Proteins 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- FFBHFFJDDLITSX-UHFFFAOYSA-N benzyl N-[2-hydroxy-4-(3-oxomorpholin-4-yl)phenyl]carbamate Chemical compound OC1=C(NC(=O)OCC2=CC=CC=C2)C=CC(=C1)N1CCOCC1=O FFBHFFJDDLITSX-UHFFFAOYSA-N 0.000 description 1
- IQFYYKKMVGJFEH-UHFFFAOYSA-N beta-L-thymidine Natural products O=C1NC(=O)C(C)=CN1C1OC(CO)C(O)C1 IQFYYKKMVGJFEH-UHFFFAOYSA-N 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 235000020958 biotin Nutrition 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 229910021538 borax Inorganic materials 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000022131 cell cycle Effects 0.000 description 1
- 230000025084 cell cycle arrest Effects 0.000 description 1
- 230000006369 cell cycle progression Effects 0.000 description 1
- 230000010261 cell growth Effects 0.000 description 1
- 230000006037 cell lysis Effects 0.000 description 1
- 230000010307 cell transformation Effects 0.000 description 1
- 230000036755 cellular response Effects 0.000 description 1
- 208000019065 cervical carcinoma Diseases 0.000 description 1
- 210000003679 cervix uteri Anatomy 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- 210000000038 chest Anatomy 0.000 description 1
- 239000012459 cleaning agent Substances 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 101150096566 clpX gene Proteins 0.000 description 1
- 238000003501 co-culture Methods 0.000 description 1
- 230000001332 colony forming effect Effects 0.000 description 1
- 238000010835 comparative analysis Methods 0.000 description 1
- 230000009918 complex formation Effects 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 108010048032 cyclophilin B Proteins 0.000 description 1
- 125000000151 cysteine group Chemical group N[C@@H](CS)C(=O)* 0.000 description 1
- 210000004292 cytoskeleton Anatomy 0.000 description 1
- 230000001086 cytosolic effect Effects 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000007850 degeneration Effects 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 239000003398 denaturant Substances 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000012691 depolymerization reaction Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 102000004419 dihydrofolate reductase Human genes 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 238000002635 electroconvulsive therapy Methods 0.000 description 1
- 238000010828 elution Methods 0.000 description 1
- 210000002472 endoplasmic reticulum Anatomy 0.000 description 1
- 238000011013 endotoxin removal Methods 0.000 description 1
- 230000037149 energy metabolism Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000008508 epithelial proliferation Effects 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- 210000003617 erythrocyte membrane Anatomy 0.000 description 1
- 239000003797 essential amino acid Substances 0.000 description 1
- 235000020776 essential amino acid Nutrition 0.000 description 1
- 229940011871 estrogen Drugs 0.000 description 1
- 239000000262 estrogen Substances 0.000 description 1
- DNJIEGIFACGWOD-UHFFFAOYSA-N ethyl mercaptane Natural products CCS DNJIEGIFACGWOD-UHFFFAOYSA-N 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 210000003608 fece Anatomy 0.000 description 1
- 239000012091 fetal bovine serum Substances 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 239000013020 final formulation Substances 0.000 description 1
- 238000005194 fractionation Methods 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 102000011778 gamma-delta T-Cell Antigen Receptors Human genes 0.000 description 1
- 108010062214 gamma-delta T-Cell Antigen Receptors Proteins 0.000 description 1
- 238000002523 gelfiltration Methods 0.000 description 1
- 238000001476 gene delivery Methods 0.000 description 1
- 238000001415 gene therapy Methods 0.000 description 1
- 230000002068 genetic effect Effects 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- 239000003862 glucocorticoid Substances 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 108010017007 glucose-regulated proteins Proteins 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 229960002743 glutamine Drugs 0.000 description 1
- 125000005456 glyceride group Chemical group 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 229910001385 heavy metal Inorganic materials 0.000 description 1
- 102000046432 human HSPD1 Human genes 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 230000008348 humoral response Effects 0.000 description 1
- 229910052588 hydroxylapatite Inorganic materials 0.000 description 1
- GRRNUXAQVGOGFE-NZSRVPFOSA-N hygromycin B Chemical compound O[C@@H]1[C@@H](NC)C[C@@H](N)[C@H](O)[C@H]1O[C@H]1[C@H]2O[C@@]3([C@@H]([C@@H](O)[C@@H](O)[C@@H](C(N)CO)O3)O)O[C@H]2[C@@H](O)[C@@H](CO)O1 GRRNUXAQVGOGFE-NZSRVPFOSA-N 0.000 description 1
- 229940097277 hygromycin b Drugs 0.000 description 1
- 230000007954 hypoxia Effects 0.000 description 1
- 230000002519 immonomodulatory effect Effects 0.000 description 1
- 230000037451 immune surveillance Effects 0.000 description 1
- 238000003119 immunoblot Methods 0.000 description 1
- 230000002163 immunogen Effects 0.000 description 1
- 102000018358 immunoglobulin Human genes 0.000 description 1
- 230000001759 immunoprophylactic effect Effects 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 230000001506 immunosuppresive effect Effects 0.000 description 1
- 239000003018 immunosuppressive agent Substances 0.000 description 1
- 229940125721 immunosuppressive agent Drugs 0.000 description 1
- 230000001024 immunotherapeutic effect Effects 0.000 description 1
- 238000009169 immunotherapy Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 230000015788 innate immune response Effects 0.000 description 1
- 239000002054 inoculum Substances 0.000 description 1
- 230000010354 integration Effects 0.000 description 1
- 230000006525 intracellular process Effects 0.000 description 1
- 230000010189 intracellular transport Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000007912 intraperitoneal administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 206010023841 laryngeal neoplasm Diseases 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 231100000518 lethal Toxicity 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 238000001638 lipofection Methods 0.000 description 1
- 229920006008 lipopolysaccharide Polymers 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 229940124590 live attenuated vaccine Drugs 0.000 description 1
- 229940023012 live-attenuated vaccine Drugs 0.000 description 1
- 201000005202 lung cancer Diseases 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 239000003226 mitogen Substances 0.000 description 1
- 229960004857 mitomycin Drugs 0.000 description 1
- 229940126619 mouse monoclonal antibody Drugs 0.000 description 1
- 208000027531 mycobacterial infectious disease Diseases 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 238000007899 nucleic acid hybridization Methods 0.000 description 1
- 229920002113 octoxynol Polymers 0.000 description 1
- 108091008819 oncoproteins Proteins 0.000 description 1
- 102000027450 oncoproteins Human genes 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- GHEHNICLPWTXJC-UHFFFAOYSA-N p-Aminobenzamidine dihydrochloride Chemical compound [Cl-].[Cl-].NC(=[NH2+])C1=CC=C([NH3+])C=C1 GHEHNICLPWTXJC-UHFFFAOYSA-N 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 210000003899 penis Anatomy 0.000 description 1
- XYJRXVWERLGGKC-UHFFFAOYSA-D pentacalcium;hydroxide;triphosphate Chemical compound [OH-].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O XYJRXVWERLGGKC-UHFFFAOYSA-D 0.000 description 1
- 108010044156 peptidyl-prolyl cis-trans isomerase b Proteins 0.000 description 1
- 230000010412 perfusion Effects 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 239000002953 phosphate buffered saline Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 229920000024 polymyxin B Polymers 0.000 description 1
- 229960005266 polymyxin b Drugs 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 239000000186 progesterone Substances 0.000 description 1
- 229960003387 progesterone Drugs 0.000 description 1
- 102000003998 progesterone receptors Human genes 0.000 description 1
- 108090000468 progesterone receptors Proteins 0.000 description 1
- 235000019833 protease Nutrition 0.000 description 1
- 235000019419 proteases Nutrition 0.000 description 1
- 108060006633 protein kinase Proteins 0.000 description 1
- 238000001243 protein synthesis Methods 0.000 description 1
- 230000002797 proteolythic effect Effects 0.000 description 1
- 230000000722 protumoral effect Effects 0.000 description 1
- 229940076788 pyruvate Drugs 0.000 description 1
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 230000010837 receptor-mediated endocytosis Effects 0.000 description 1
- 230000022983 regulation of cell cycle Effects 0.000 description 1
- 230000008439 repair process Effects 0.000 description 1
- 230000010076 replication Effects 0.000 description 1
- 210000005000 reproductive tract Anatomy 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000028617 response to DNA damage stimulus Effects 0.000 description 1
- 230000004043 responsiveness Effects 0.000 description 1
- 230000000284 resting effect Effects 0.000 description 1
- 230000001177 retroviral effect Effects 0.000 description 1
- 238000003345 scintillation counting Methods 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 230000009758 senescence Effects 0.000 description 1
- 230000001568 sexual effect Effects 0.000 description 1
- 238000004904 shortening Methods 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 229960002930 sirolimus Drugs 0.000 description 1
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 1
- 229940054269 sodium pyruvate Drugs 0.000 description 1
- 235000010339 sodium tetraborate Nutrition 0.000 description 1
- LKUULGDICDGFIQ-UHFFFAOYSA-M sodium;1-[3-(2,5-dioxopyrrol-1-yl)benzoyl]oxy-2,5-dioxopyrrolidine-3-sulfonate Chemical compound [Na+].O=C1C(S(=O)(=O)[O-])CC(=O)N1OC(=O)C1=CC=CC(N2C(C=CC2=O)=O)=C1 LKUULGDICDGFIQ-UHFFFAOYSA-M 0.000 description 1
- 210000004988 splenocyte Anatomy 0.000 description 1
- 206010041823 squamous cell carcinoma Diseases 0.000 description 1
- 238000010972 statistical evaluation Methods 0.000 description 1
- 108020003113 steroid hormone receptors Proteins 0.000 description 1
- 102000005969 steroid hormone receptors Human genes 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 208000024891 symptom Diseases 0.000 description 1
- 229940037128 systemic glucocorticoids Drugs 0.000 description 1
- 108010067247 tacrolimus binding protein 4 Proteins 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- HNKJADCVZUBCPG-UHFFFAOYSA-N thioanisole Chemical compound CSC1=CC=CC=C1 HNKJADCVZUBCPG-UHFFFAOYSA-N 0.000 description 1
- 229940104230 thymidine Drugs 0.000 description 1
- 230000002103 transcriptional effect Effects 0.000 description 1
- 230000002463 transducing effect Effects 0.000 description 1
- 238000010361 transduction Methods 0.000 description 1
- 230000026683 transduction Effects 0.000 description 1
- 238000001890 transfection Methods 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- BSVBQGMMJUBVOD-UHFFFAOYSA-N trisodium borate Chemical compound [Na+].[Na+].[Na+].[O-]B([O-])[O-] BSVBQGMMJUBVOD-UHFFFAOYSA-N 0.000 description 1
- 239000000225 tumor suppressor protein Substances 0.000 description 1
- 238000011144 upstream manufacturing Methods 0.000 description 1
- 238000002255 vaccination Methods 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 210000002845 virion Anatomy 0.000 description 1
- 230000005727 virus proliferation Effects 0.000 description 1
- 230000000007 visual effect Effects 0.000 description 1
- 238000011179 visual inspection Methods 0.000 description 1
- 210000003905 vulva Anatomy 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/005—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/385—Haptens or antigens, bound to carriers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/62—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being a protein, peptide or polyamino acid
- A61K47/64—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent
- A61K47/646—Drug-peptide, drug-protein or drug-polyamino acid conjugates, i.e. the modifying agent being a peptide, protein or polyamino acid which is covalently bonded or complexed to a therapeutically active agent the entire peptide or protein drug conjugate elicits an immune response, e.g. conjugate vaccines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/35—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Mycobacteriaceae (F)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/515—Animal cells
- A61K2039/5156—Animal cells expressing foreign proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/525—Virus
- A61K2039/5256—Virus expressing foreign proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55516—Proteins; Peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/57—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/58—Medicinal preparations containing antigens or antibodies raising an immune response against a target which is not the antigen used for immunisation
- A61K2039/585—Medicinal preparations containing antigens or antibodies raising an immune response against a target which is not the antigen used for immunisation wherein the target is cancer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/60—Medicinal preparations containing antigens or antibodies characteristics by the carrier linked to the antigen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/60—Medicinal preparations containing antigens or antibodies characteristics by the carrier linked to the antigen
- A61K2039/6031—Proteins
- A61K2039/6043—Heat shock proteins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/20011—Papillomaviridae
- C12N2710/20022—New viral proteins or individual genes, new structural or functional aspects of known viral proteins or genes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2710/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA dsDNA viruses
- C12N2710/00011—Details
- C12N2710/20011—Papillomaviridae
- C12N2710/20034—Use of virus or viral component as vaccine, e.g. live-attenuated or inactivated virus, VLP, viral protein
Abstract
본 발명은 사람 유두종 바이러스(HPV)에 의해 제공되거나, 자궁경부 및 기타 종양으로부터의 세포를 포함한 감염된 세포에 의해 나타나는 HPV 단백질 항원에 대한 면역 반응, 바람직하게는 세포상, 특히 세포-매개된 세포용해성 면역 반응을 유도하기 위한 조성물에 관한 것이다. 한 양태에 있어서, 상기 조성물은 스트레스 단백질(또는 열 쇽 단백질(Hsp))에 결합된 HPV 단백질 항원을 포함한다. 상기 HPV 단백질 항원은 화학적 접합에 의해 또는 연결 잔기를 이용하여 비공유적으로 스트레스 단백질에 결합시킬 수 있거나, HPV 단백질 항원 및 스트레스 단백질을 HPV 단백질 항원과 스트레스 단백질 서열 모두를 함유하는 융합 단백질에 결합시킬 수 있다. 또 다른 양태에서는, 조성물이 HPV 단백질 항원을 암호화하는 서열과 스트레스 단백질을 암호화하는 서열을 포함하는, 발현가능한 형태의 발현 벡터를 포함한다. 이 발현 벡터는 피검체의 세포내로 도입하거나, 이를 사용하여 생체외에서 피검체의 세포를 형질도입할 수 있기 때문에, 이로써 HPV 단백질 항원에 대한 피검체의 면역 반응을 자극하게 될 HPV 단백질 항원-스트레스 단백질 융합 단백질이 발현된다. 본 발명은 또한, HPV 단백질 항원에 결합된 스트레스 단백질과 또 다른 약리학적으로 허용되는 성분을 포함하는 조성물; 스트레스 단백질-HPV 단백질 항원 융합물 및 접합체; 및 스트레스 단백질 및 HPV 단백질 항원 서열을 포함하는 융합 단백질을 암호화하고 피검체의 세포에서 발현을 지시할 수 있는 발현 벡터에 관한 것이다. 본 발명은 또한 HPV, 및 HPV-관련 종양을 포함한 HPV 단백질 항원-제시 세포에 대한 면역 반응을 유도하기 위한 이들 조성물의 용도에 관한 것이다.
스트레스 단백질, 사람 유두종 바이러스(HPV) 단백질 항원, 세포성 면역 반응, 미코박테리아성 스트레스 단백질, 접합체, 융합 단백질, 발현 벡터
Description
도 1은 작제물 pET65H의 도식도이다.
도 2는 작제물 pET65HE6의 도식도이다.
도 3은 작제물 pET65HE7의 도식도이다.
도 4는 TC-1 종양 챌린지 후의 시간에 대한 종양 발생률을 나타내는 그래프이며, 이는 상기 종양에 대하여 Hsp65-E6 및 -E7 융합 단백질로 마우스를 성공적으로 면역시켰음을 입증한다.
도 5는 효과기 세포(effector cell) 대 표적 세포의 비에 대한 TC-1 종양 세포의 특이적 세포 용해율을 나타내는 그래프이고, 이는 면역된 마우스에서 HPV 항원(E7)-발현 표적 종양 세포에 대한 세포-매개된 세포용해 반응을 입증한다.
도 6은 효과기 세포 대 표적 세포의 비에 대한 상이한 표적 세포의 용해율을 나타내는 그래프이고, 이는 면역된 마우스에서 HPV E7-발현 표적 종양 세포에 대한 세포-매개된 세포용해성 면역 반응의 특이성을 입증한다.
도 7은 1.3 x 105개 TC-1 종양 세포가 투여되고 연속적으로 염수, 염수 중의 Hsp65-E7 융합 단백질 또는 염수/IFA 중의 E7 펩타이드가 주사된 마우스에서의 종양 세포 투여 후의 일수에 대한 종양 발생률을 나타내는 그래프이다.
도 8은 2 x 105개 TC-1 종양 세포가 투여되고 연속적으로 염수, 염수 중의 Hsp65-E7 융합 단백질 또는 염수/IFA 중의 E7 펩타이드가 주사된 마우스에서의 종양 세포 투여 후의 일수에 대한 종양 발생률을 나타내는 그래프이다.
도 9는 작제물 pET/E7(H)의 도식도이다.
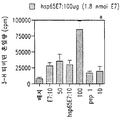
도 10은 Hsp65-E7 융합 단백질 또는 E7 단백질로 면역시킨 마우스로부터 수득된 배양된 림프절 세포에 의한 티미딘 혼입량을 나타내는 그래프를 수집한 것이다.
도 11은 TC-1 종양 세포를 갖는 마우스에서 종양 크기에 대한 Hsp-E7 융합 단백질 또는 E7로의 처리 효과를 나타내는 그래프이다.
도 12는 작제물 pET65C의 도식도이다.
도 13은 작제물 pET65C/E7-1N의 도식도이다.
사람 유두종 바이러스(HPV) 감염은 흔히 있는 일이며, 이러한 바이러스는 성 행위를 매개로 전염될 수 있다. 성행위를 하는 성인의 20 내지 80%가 감염된 것으로 추정된다. 대다수의 감염자가 무증후성이긴 하지만, 이러한 감염이 생식기 우췌(genital wart) 및 항문생식관 암으로 발전할 수 있다. 성인 중 1 내지 5%가 생식기 우췌 증상을 나타낸다. 전세계 여성의 약 1%가 50세 이하 여성의 가장 높은 사망 원인 중의 하나인 자궁 경부암에 걸린다. 자궁 경부암은 HPV와 상당한 연관이 있다[참조: Frazer, Genitourin Med 72:398-403(1996)].
현재에는, HPV에 대한 어떠한 효과적인 치료 조성물이나 예방용 조성물, 즉, 백신도 입수가능하지 않기 때문에, 유효한 조성물을 개발할 필요가 있다. 통상적인 사멸된 또는 살아 있는 약독화 백신에 대한 기대는 어려운 것으로 보인다. 상기 프라저(Frazer)의 문헌에 따르면, HPV는 지금까지 세포 배양물에서 증식된 바가 없으며, HPV 감염의 종양-촉진 효과 뿐만 아니라 HPV의 전체 종 특이성도 쉽게 극복될 수 없는 또 다른 어려움을 나타낸다[참조: Frazer, Genitourin Med 72:398-403(1996)]. 주요 캡시드 단백질이 진핵 세포에서 발현될 때 아주반트 없이 면역원성인 바이러스-유사 입자를 형성시킨다는 관찰 결과가 백신 개발에 대한 기본 원리를 제공할 수 있다는 것이 제안되었다[참조: Christensen et al., J Gen Virol 75:2271-6(1994); 및 PCT/EP95/03974 및 PCT/US95/12914].
HPV는 SV40 및 폴리오마바이러스를 포함하기도 하는 파포바비리대(papovaviridae)의 A 속에 속한다. 구조적으로는 상당히 연관되어 있지만 DNA 서열 수준에서 50% 미만이 동일한 68가지 이상의 상이한 유형의 HPV에 대한 성상이 확인되었다. 공지된 모든 유형은 특정 유형의 상피를 감염시키고 빈번히 상피 증 식을 일으키는 상피친화성(epitheliotropic) 바이러스이다. 몇 가지 유형은 통상의 우췌에서 확인된다. 23가지 유형이 여성과 남성의 항문생식관을 감염시키는 것으로 공지되어 있다. 이들 유형의 HPV에 의해 야기된 항문생식기 질환의 범주에는 첨형 습우에서부터 침습성 편평 세포 암종까지가 언급된다. HPV DNA는 생검-확인된 편평 상피내 병변이나 자궁 경부 상피내 종양을 지닌 여성의 80% 이상에서 확인될 수 있다. HPV 16, 18 및 31을 포함한 몇몇 특정 유형은 매우 심각한 편평 상피내 병변과 자궁경부, 음문, 음경 및 항문의 침습성 암과 상당한 연관이 있다[참조: Lorincz et al., Obstet Gynecol 79:328-37(1992)]. 상기 프라저의 문헌에 따르면, 자궁경부암의 90 내지 95%가 HPV와 연관이 있다[참조: Frazer, Genitourin Med 72:398-403(1996)]. HPV는 항문생식계 암과 연관이 있을 뿐만 아니라, 인두암, 후두암 및 방광암에도 존재한다[참조: Brachman et al., Cancer Res 52:4832-6(1992); Rotola et al., Int J Cancer 52:359-65(1992)]. 최근의 연구 보고서에 HPV DNA가 또한 시험된 폐암종의 30%에 존재하는 것으로 보고되었다. 동정된 유형에는 HPV 6, 11, 16, 18, 31 및 33이 포함된다[참조: Soini et al., Thorax 51:887-893(1996)]. 따라서, 암과 가장 종종 연관이 있는 것으로 밝혀진 HPV 유형은 6, 11, 16, 18, 31 및 33이며, 이 중에서 자궁경부 암종의 90% 이상에서 검출되는 HPV 16 및 18[참조: van Driel et al., Ann Med 28:471-477(1996)]이 가장 철저하게 연구되어 왔다.
유두종 바이러스는 7800 내지 7900 염기쌍의 이본쇄의 환상 DNA 게놈, 외피가 없는 비리온, 및 72개 캡소머로 이루어진 이십면체 캡시드를 갖는 DNA 바이러스 이다. 상기 게놈은 3가지 주요 영역, 즉, 후기 유전자를 암호화하는 영역, 초기 유전자를 암호화하는 영역 및 비암호화 영역을 함유한다[참조: Park et al., Cancer 76:1902-1913(1995)]. 상기 비암호화 영역은 또한 상부 조절 영역으로서 지칭된다. 이 영역은 약 400 염기쌍의 길이이고 초기 및 후기 유전자의 발현을 조절하는 각종 전사 인자에 대한 결합 부위의 배열을 함유한다. 상기 후기 유전자 영역은 바이러스성 캡시드 단백질 L1 및 L2를 암호화하는 2개의 별개의 개방 판독 프레임을 갖는다. 단백질 L1은 상이한 HPV 종에서 고도로 보존되는 주요 캡시드 단백질이다. 초기 유전자 영역은 E1, E2, E4, E5, E6 및 E7로 명명된 6개의 개방 판독 프레임을 포함한다. 단백질 E6 및 E7은 바이러스 복제 뿐만 아니라 숙주 세포 불멸화 및 형질전환에 결정적인 종양단백질(oncoprotein)이다. 단백질 E1, E2 및 E4는 또한 바이러스 복제에 중요한 역할을 한다. 또한, E4는 상기 바이러스의 성숙에 관여한다. E5의 역할은 비교적 덜 공지되어 있다.
악성 종양으로부터의 세포는 두 가지 중요한 성장 특징을 공유하고 있다. 이들은 불멸화되는데, 즉, 이들은 노쇠하지 않고 비부착증식(anchorage-independent growth)할 수 있다. HPV 16 또는 HPV 18 DNA를 불멸화된 설치류 세포내에 도입하면 이들이 형질전환되는데, 즉, 이들이 기체(substratum)에 부착되지 않고서도 성장할 수 있는 능력과 마우스에게 주입될 때 종양을 형성할 수 있는 능력을 획득하게 된다[참조: Crook et al., Proc. Natl. Acad. Sci. USA 85:8820-24(1988)]. HPV DNA를 초기 계대접종, 비-불멸화 세포에 도입하는 경우에 상이한 결과가 수득되는데; 즉, 상기 세포는 불멸화되지만 형질전환되지는 않는다[참조: Woodworth et al., Cancer Res. 18:4620-28(1988)]. 따라서, 종양이 진행되는 한가지 경로는 세포의 불멸화를 초래하는 변화에 이어서 이들을 형질전환시켜 주는 HPV 유전자의 발현과 관련이 있다. 시험관내에서 세포의 형질전환과 관련된 HPV 유전자는 E6 및/또는 E7을 암호화하는 유전자이다[참조: Bedell et al., J Virol 61:3635-40(1987)]. E6 및 E7 단백질이 세포내 형질전환을 야기시킬 수 있는 기전이 제안되었다[참조: Park et al., Cancer 76:1902-1913(1995) 및 이에 인용된 참조문헌].
E6은 Zn-결합성 도메인을 함유하는 소형(대략 15,000MW) 폴리펩타이드이다. 이의 형질전환 기능에 대한 단서는 상기 단백질이 p53에 결합된다는 관찰 결과에 의해 제공된다. 이러한 p53 단백질은 세포 주기 진행을 음성적으로 조절해 주므로 세포 성장과 분해도 음성적으로 조절하는 널리 공지된 종양 억제인자 단백질이다. E6이 p53에 결합되면, 후자 단백질이 우비퀸화(ubiquination)되고 결국 분해되는데, 이러한 과정은 "E6-관련 단백질"로 칭해지는 또 다른 세포내 단백질과 관련이 있다. 결과적으로, E6을 발현시키는 세포는 p53의 기본 수준을 감소시킬 것이다. p53 수준은 DNA 손상에 반응하여 상승된다. 이러한 증가된 수준으로 인해, 세포 주기 정지를 매개하는 단백질인 사이클린-의존성 키나제의 억제인자인 p21의 발현이 증진된다. 이러한 기전은 세포가 이의 복제에 앞서 손상된 DNA를 복구할 수 있는 시간 윈도우를 세포에게 제공하므로, 손상/돌연변이의 이론을 확립할 수 있을 것이다. p53의 E6-매개된 대사전환 증진은 이러한 기전이 작동되지 못하게 할 수 있다. 최근에는, E6이 p53의 분해를 촉진시킴으로써 세포 주기 조절에 영향을 줄 뿐만 아니라 더욱 최근에는, p53이 DNA와 상호작용하는 것을 차단시킴으로써 세포 주기 조절에 영향을 주는 것으로 밝혀졌다[참조: Thomas et al., Oncogene 10:261-8(1995)].
E7 단백질은 망막아종 유전자 생성물 Rb와 결합할 수 있는 소형(대략 10,000MW) Zn-결합성 인단백질이다. Rb는 전사 인자 E2F와 결합되어 이를 불활성화시키는 종양 억제인자이다. 후자 인자는 티미딘 키나제, c-myc, 디하이드로폴레이트 리덕타제 및 DNA 폴리머라제 알파를 암호화하는 것을 포함한 수많은 성장-관련 유전자의 전사를 조절한다. Rb-E2F 복합체 형성은 후자 유전자가 G0 및 G1 상에서 발현되는 것을 방지하며, 이들의 발현을 상기 Rb-E2F 복합체가 해리되도록 예정된 S 상에 제한시키고, 활성 전사 인자 E2F를 방출시킨다. Rb-E7 복합체의 형성은 Rb-E2F 복합체의 형성을 방지시키고, 프리-S 상이 단축되는 결과, 즉, 세포 주기를 통한 진행을 촉진시키는 결과를 수반한다. 이들 기전의 중요성과 상관있는 증거는, 고도의 종양원성 HPV 유형(예를 들면, HPV 16 & 18)으로부터의 E6 단백질이 비-종양원성 유형으로부터의 상응하는 단백질보다 p53에 대한 친화성이 더 높다는 관찰 결과와 고도의 종양원성 유형으로부터의 E7 단백질이 비-종양원성 유형으로부터의 상응하는 단백질보다 Rb에 대한 친화성이 더 높다는 관찰 결과에 의해 제공된다.
대다수의 자궁경부암과 전구체 병변에서는, HPV DNA가 숙주 세포 게놈내로 통합된다[참조: Cullen et al., J. Virol 65:606-12(1991)]. 대부분의 경우에서는, 통합이 E6/E7 영역은 본래대로 남겨 두면서 HPV 게놈성 DNA를 E1/E2 영역에서 파쇄시키는 것으로 여겨진다. E1/E2 영역에서의 파쇄 결과로 인해, 두 가지 상이한 E2 단백질(이 중 보다 소형인 단백질은 초기 유전자 발현의 전사 억제인자로서 작용한다)을 암호화하는 개방 판독 프레임이 끊어진다. 이로써 E6 및 E7 발현이 상향 조절된다.
본 발명은 일반적으로 사람 유두종 바이러스(human papillomavirus) 단백질 항원에 대한 면역 반응을 유도하기 위한, 결합된 스트레스 단백질과 사람 유두종 바이러스 단백질을 포함하는 조성물 및 방법에 관한 것이다.
본 발명은 투여할 피검체에서 HPV 단백질 항원에 대한 면역 반응을 유도하기 위한 조성물에 관한 것이다. 이러한 면역 반응은 HPV 단백질 항원에 대한 체액성 또는 세포성 반응, 특히 세포 매개된 세포용해성 반응일 수 있다. 당해 조성물은 예방적 또는 치료적으로 사용될 수 있다. 예방적 적용에서는, 면역 반응의 유도가 고유 면역의 매우 낮은 배경 수준 이상의 면역 반응을 유발시키는 것을 지칭한다. 치료적 적용에서는, 피검체에서의 면역 반응의 유도는, 상기 바이러스에 의해 또는 피검체의 감염되거나 형질전환된 세포에 의해 나타난 HPV 단백질 항원과 접촉시킴으로써 미리 유발된 반응을 양적으로나 질적으로 초월하는 반응을 일으키는 것을 지칭한다. 특정 양태에서는, 당해 조성물을 사용하여 HPV 단백질 항원을 발현시키 고 나타내는 종양 세포에 대한 면역 반응을 발생시킨다. 이들 양태에 있어서, 당해 조성물에 의해 표적화된 바람직한 HPV 단백질 항원은 HPV-관련 종양에서 일관되게 발현되는 것으로 공지된 E6 및 E7 초기 바이러스성 단백질이다. 한 양태에 있어서, 당해 조성물은 스트레스 단백질(또는 열 쇽 단백질(Hsp))에 결합된 HPV 단백질 항원을 포함한다. 이러한 HPV 단백질 항원은 화학적 접합에 의해 상기 스트레스 단백질에 결합될 수 있거나, 또는 항원과 스트레스 단백질이 이러한 항원 및 스트레스 단백질 서열 모두를 함유하는 융합 단백질의 발현 및 분리를 허용하는 뉴클레오티드 수준으로 결합될 수 있다. 당해 조성물을 피검체에 도입하거나 생체외에서 사용하여 HPV를 표적화하거나 이의 표적화를 매개하는 피검체의 면역 세포의 증대 또는 HPV 단백질 항원을 나타내는 종양 세포를 포함한 세포의 증대를 자극하고/하거나 야기시킬 수 있다. 당해 조성물은 아주반트의 부재하에서 비-미립형(예를 들면, 바이러스 또는 바이러스-유사 입자의 일부분으로서가 아님) 단백질 함유 용액으로서 투여될 때 면역 반응을 자극하는데 효과적이다.
또 다른 양태에 있어서, 당해 조성물은 HPV 단백질 항원과 스트레스 단백질을 암호화하는 핵산 서열을 포함한 발현 벡터를 포함한다. 이러한 발현 벡터는 상기 암호화 서열의 전사 및 해독을 지시하는 서열 요소를 추가로 포함하고, 또한 피검체의 세포에서 핵산으로의 운반과 이의 영속성이나 증폭을 촉진시켜 주는 요소를 포함할 수 있다. 이러한 발현 벡터를 피검체의 세포내로 도입할 수 있거나, 또는 이를 사용하여 피검체의 세포를 생체외에서 형질도입하여, HPV 단백질 항원에 대한 면역 반응을 유도할 HPV 단백질 항원-스트레스 단백질 융합 단백질을 발현시킬 수 있다.
본 발명은 또한 또 다른 약리학적으로 허용되는 성분과 함께, 스트레스 단백질에 결합된 HPV 단백질 항원을 포함하는 조성물에 관한 것이다. 한 양태에 있어서, 상기 조성물은 HPV 단백질 항원과 함께 결합된 스트레스 단백질을 포함하는 접합체를 포함한다. 또 다른 양태에 있어서, 당해 조성물은 스트레스 단백질이 HPV 단백질 항원에 융합된 융합 단백질(예를 들면, pET65HE6과 pET65HE7로부터 발현된 단백질)을 포함한다. 이들 조성물의 접합체 및 융합 단백질은 또한 피검체의 세포에서 스트레스 단백질 및 HPV 단백질 항원 서열을 포함하는 융합 단백질을 암호화하고 이의 발현을 지시할 수 있는 발현 벡터로서 청구된다.
본 발명은 또한 HPV 단백질 항원에 대한 면역 반응 및 특정 양태에서는, HPV 단백질 항원을 나타내는 종양에 대한 면역 반응을 증진시키기 위한 당해 조성물의 용도에 관한 것이다. 본원에서 인용된 과학 문헌 및 특허 공보로부터의 논문, 특히 본 발명의 조성물의 제조 방법과 용도에 관한 논문은 전문이 본원에 참조문헌으로 삽입된다.
본 발명은 HPV 단백질 항원을 나타내는 피검체 세포의 사람 유두종 바이러스에 대한 면역 반응을 피검체에서 유도하는 조성물에 관한 것이다. 한 양태에 있어서, 당해 조성물은 HPV 단백질 항원 및 스트레스 단백질을 포함한다. 또 다른 양태에 있어서, 당해 조성물은 HPV 단백질 항원-스트레스 단백질 융합 단백질의 발현을 지시할 수 있는 발현 벡터를 포함한다.
본 발명의 조성물은 예방적으로 사용되어 HPV 단백질 항원에 대한 면역성을 부여할 수 있으며, HPV의 정착 및 증식, 또는 HPV 단백질 항원을 발현시키고 나타내거나, 이의 일부분을 제시하는 피검체 세포의 정착과 증식을 억제한다. 당해 조성물은 또한 미리 HPV로 감염된 피검체에서 치료적으로 사용되어, 추가의 바이러스성 증식을 억제하거나, HPV 항원을 발현시키고 나타내거나, 이러한 항원의 일부분을 제시하는 종양을 포함한, HPV 감염 결과로서 증식되는 피검체의 세포를 제거할 수 있다. 본 발명의 조성물에 의해 유도된 면역 반응의 표적으로서 HPV 단백질 항원이 본원에서 언급되는 경우, 이러한 HPV 단백질 항원은 HPV의 표면 상에 나타나거나 피검체의 감염 세포 상에 나타난 완전한 HPV 단백질 또는 이러한 HPV 단백질의 폴리펩타이드(분자량 10kDa 초과) 부분 뿐만 아니라 예를 들면, 전형적인 MHC 계열 I 또는 II 경로를 통한 HPV 단백질의 프로세싱 및 제시의 결과로서 감염된 세포에 의해 발현된 펩타이드를 포함하는 것으로 이해해야 한다.
많은 상이한 유형의 HPV의 게놈 서열을 클로닝하고 DNA 서열 분석으로 성상을 확인한다. 완전한 또는 부분적 HPV 게놈을 함유하는 세균성 벡터는, 예를 들면, 아메리칸 타입 컬쳐 컬렉션(ATCC)을 포함한 각종 공급원으로부터 입수가능하다. 본 발명의 실시에 유용한 또 다른 유형의 HPV를, 이를 위하여 앞서 확립된 바 있고 당해 분야에 널리 공지되어 있는 방법으로 분리하고 유형을 결정할 수 있다.
HPV는 6개 또는 7개의 비-구조 단백질 및 2개의 구조 단백질을 발현시키며, 이들 단백질 각각은 원칙상, HPV 또는 감염된 세포 제거를 목표로 하는 면역예방적 접근법이나 면역치료적 접근법을 위한 표적으로서 작용할 수 있다. 바이러스성 캡시드 단백질 L1 및 L2는 후기 유전자에 의해 암호화되는 HPV의 구조 단백질이다. L1은 상이한 HPV 종 중에서 고도로 보존되는 주요 캡시드 단백질이다. 상기 7개의 비-구조 단백질은 초기 바이러스성 유전자의 생성물이다. 단백질 E1, E2 및 E4는 바이러스 복제에 중요한 역할을 한다. 단백질 E4는 바이러스의 성숙에 부가적으로 작용한다. E5의 역할은 비교적 덜 공지되어 있다. 단백질 E6 및 E7은 바이러스 복제 뿐만 아니라 숙주 세포 불멸화 및 형질전환에 결정적인 종양단백질이다. 본 발명의 조성물에 혼입될 수 있는 이들 단백질이 HPV 단백질 항원으로서 지칭된다.
HPV-관련된 암의 예방 및 치료에 본 발명을 적용시키는데 있어서 특히 중요한 것은 HPV E6 및 E7 단백질이 자궁경부암에서 일관되게 발현된다는 관찰 결과이다[참조: Zur Hausen, Appl. Pathol. 5:19-24(1987); Pater 및 Pater, Virology 145:313-8(1985)]. 문헌[참조: Kinoshita et al., Br. J. Cancer 71:344-9(1995)]에서는 E6 및 E7 유전자가 또한 폐암에서도 발현된다는 것을 입증하고 있다. 더우기, E7에 대한 몇몇 천연 면역(체액성) 반응이 자궁경부암 환자에게서 인지되었다[참조: Jochmus-Kudielka et al., J. Nat'l Cancer Inst. 81:1698-704(1989)]. 최종적으로, 모델 연구 결과, 변형된 E7 단백질로 면역시키면, 활성화된 c-Ha-ras 유전자 및 HPV E6/E7 유전자로 형질전환된 폐 세포로의 챌린지로부터 마우스가 보호되는 것으로 나타났다[참조: Lin et al., Cancer Res. 56:21-26(1996)]. 이들 단백질이 HPV 감염 결과로서 야기되는 암에서 전형적으로 발현된다는 사실, 동일한 단백질이 또한 상기 암의 진행과 유지에 중요한 역할을 할 것으로 가장 예상되는 종양원이라는 사실, 및 면역 반응이 이들 단백질에 대해 지시될 수 있다는 사실로 미루어 볼때, E6 및 E7이 면역조정 또는 예방에 바람직한 표적이고, 따라서 HPV-관 련된 암을 예방하거나 치료하는데 사용될 본 발명의 조성물의 바람직한 HPV 단백질 항원이다.
몇몇 동물 모델에서는, 세포독성 T 세포(CTL) 펩타이드가 특정 바이러스에 대한 보호 면역성을 유도할 수 있는 것으로 나타났다[참조: Kast 및 Melief, Immunol. Lett. 30:229(1991)]. 면역적격 개개인에서 보다 면역억제된 개개인에게서 훨씬 더 자주 자궁경부암이 발병되는 것으로 관찰되었다[참조: Schneider et al., Acta Cytologica 27:220-4(1983)]. 이는 면역계, 특히 T 세포계의 세포성 암(arm)이 HPV-관련된 악성종양에 대한 면역학적 방어에 매우 중요하다는 것을 강력히 제시하고 있다. E6- 및 E7-형질전환된 세포에 대한 보호 면역성을 생성시키는데 있어서의 CTL 반응의 중요성을 뒷받침해 주는 증거는, HPV 16 E7의 관련된 CTL 에피토프로 예방접종한 마우스가 이식가능한 HPV 16-유도된 종양에 대해 보호되었다는 실험으로부터 얻은 것이다[참조: Feltkamp et al., Eur. J. Immunol. 23:2242(1993)]. 본 발명은 스트레스 단백질을 HPV 단백질 항원에 결합시키면, 이와 같이 결합된 HPV 단백질 항원에 대한 세포성, 특히 세포-매개된 세포용해성 반응(이러한 반응은 HPV 항원을 나타내는 세포를 사멸시킬 수 있음)을 강력하게 자극하는 조성물이 생성된다는 본 발명자들의 관찰 결과를 근거로 한 것이다.
본 발명의 HPV 단백질 항원은 임의의 HPV-암호화된 폴리펩타이드일 수 있다. 또한, 이는 상기 HPV 단백질의 특정 부분일 수 있는데, 단, 이러한 부분은 스트레스 단백질과 결합될 때, 감염된 세포에 의해 나타나거나 HPV에 의해 제공된 HPV 단백질 항원에 대한 면역 반응을 유도하는 능력을 보유해야 한다. 완전한 HPV 단백 질 항원보다는 오히려 HPV 항원의 각종 부분을 포함하는 본 발명의 조성물은 이후 본원에 기재되거나 다음 분자 생물학 및 생화학 문헌에 기재된 방법과 같은 통상적인 방법으로 제조할 수 있다[참조: Sambrook et al., Molecular Cloning: A Laboratory Manual, 2d Ed., Cold Spring Harbor Laboratory Press(1989); Deutscher, M., Guide to Protein Purification Methods Enzymology, vol. 182. Academic Press. Inc., San Diego, CA(1990)]. HPV 단백질 항원의 특정한 부분을 갖는 각 조성물을 대상으로 하여, 다음에 기재된 실시예에 언급된 바와 같은 실험에서 이러한 HPV 단백질 항원에 대한 면역 반응 정도와 질을 알아보기 위해 시험한다. 최소한, 본 발명의 조성물 중의 HPV 단백질 항원은 HPV 단백질의 하나 이상의 B 또는 T 세포 에피토프(예를 들면, CTL 또는 T 헬퍼 세포 에피토프)를 함유할 것이다. 본 발명의 조성물을 언급하는 경우, 용어 "HPV 단백질 항원"은 HPV 단백질 항원의 부분들을 포함하는데, 단, 이러한 부분들은 감염된 세포에 의해 나타나거나 HPV에 의해 제공된 HPV 단백질 항원에 대한 면역 반응을 유도하는 능력을 보유해야 한다.
E6 및 특히 E7은 형질전환성 단백질이다. HPV 단백질 항원으로서 완전한 HPV E6 또는 E7 단백질 서열을 포함하거나 형질전환 능력을 보유하기에 충분히 완전한 부분을 포함하는 조성물에서는, 이러한 항원의 형질전환 특성이 HPV 항원을 제조하는 방법에 따라서 상당한 위험을 나타내거나 나타내지 않을 수 있다. 예를 들면, HPV 단백질 항원 또는 이러한 항원을 포함하는 조성물을 DNA 오염 위험을 수반하는 재조합 기술에 의해 제조하는 경우에는, 상기 항원의 형질전환 능력을 제거 하는 단계를 취하는 것이 유익할 수 있다. 완전한 HPV E6 또는 E7 단백질 서열을 포함하거나 형질전환 능력을 보유하기에 충분히 완전한 부분을 포함한 융합 단백질의 발현을 피검체에서 지시하는 발현 벡터를 포함한 조성물을 이용하는 경우에는, 단백질 생성물에 형질전환성을 부여하는 서열을 제거하는 것이 필요할 수 있다. E6 및 E7의 비-형질전환성 변이체는 E6 서열과 E7 서열을 융합시킴으로써 수득한다(PCT/AU95/00868). 따라서, E6 또는 E7 서열과 스트레스 단백질 서열을 포함한 특정의 융합 단백질이 이미 비-형질전환성일 수 있다. 또 다른 한편, 당해 분야에 널리 공지되어 있고 또한 PCT/AU95/00868에 기재되어 있는 기술을 사용하여 서열을 E6 또는 E7로부터 선택적으로 결실시킬 수 있다. 이러한 결실은 E6 또는 E7 서열만을 발현시키는 발현 벡터 또는 E6- 또는 E7-스트레스 단백질 융합 단백질을 발현시키는 벡터에서 이루어질 수 있다. 이러한 조작의 결과는 결실 단백질의 형질전환 능력을 형질감염 실험에서 시험함으로써 평가될 수 있다. 예를 들면, NIH3T3 세포를 결실 단백질에 대한 유전자를 포함한 발현 벡터로 형질감염시킬 수 있으며, 형질전환 능력은 연질 한천에서의 콜로니-형성 검정으로 평가할 수 있다. 이러한 특정한 시험은 또한 PCT/AU95/00868에 기재되어 있다.
본 발명의 한 양태에 있어서, 조성물은 2개의 잔기, 즉, 스트레스 단백질 및 세포성 면역 반응이 요망되는 HPV의 단백질 항원을 포함한다. 이러한 두 잔기를 결합시켜 단일 단위를 형성시킨다. 이러한 두 잔기를 접합시켜, 즉, 스트레스 단백질과 HPV 단백질 항원간의 공유 결합을 통하여 연결시킬 수 있다[참조: Hermanson, G.T., Bioconjugate Techniques, Academic Press, Inc., San Diego, CA(1996); Lussow, A.R. et al., Eur. J. Immun. 21:2297-2302(1991); Barrios, C. et al., Eur. J. Immun. 22:1365-1372(1992)]. 또 다른 한편, 재조합 기술을 사용하여 두 잔기를 연결시켜 발현시킬 수 있으며, 그 결과 단일 분자내에 스트레스 단백질 및 HPV 단백질 항원을 포함하는 재조합 융합 단백질이 생성된다. 이로써, 단일 재조합 분자를 생산 공정에서 제조하고 정제하는 것이 가능해진다. 상기 두 잔기는 또한 비공유적으로 결합시킬 수 있다. 공지된 몇몇 고-친화성 상호작용을 변형시켜 두 잔기를 비공유적으로 결합시킬 수 있다. 예를 들면, 바이오틴 그룹을 HPV 단백질 항원에 가할 수 있으며, 결합시킬 스트레스 단백질을 아비딘-스트레스 단백질 융합 단백질로서 발현시킬 수 있다. 이러한 아비딘-스트레스 단백질 융합 단백질은 바이오티닐화 HPV 단백질 항원에 강력하게 결합될 것이다. 유사하게, HPV 단백질 항원의 특정 부분을 완전한 스트레스 단백질에 결합시키거나 이러한 스트레스 단백질의 특정 부분에 결합시킬 수 있으며, 스트레스 단백질의 특정 부분을 완전한 HPV 단백질 항원 또는 이러한 HPV 단백질 항원의 특정 부분에 결합시킬 수 있는데, 단, 각각의 부분들은 투여될 피검체에서 HPV 단백질 항원에 대한 면역 반응을 유도하기에 충분해야 한다. 또 다른 양태에서는, 조성물이 HPV 단백질 항원-스트레스 단백질 융합 단백질의 발현을 지시할 수 있는 발현 벡터를 포함한다.
모든 적합한 스트레스 단백질(열 쇽 단백질(hsp))을 본 발명의 조성물에 사용할 수 있다. 예를 들면, 본 실시예에 기재된 바와 같이, Hsp60 및/또는 Hsp70을 사용할 수 있다. 스트레스 단백질을 일반적으로 논의해 보면, 세포는 스트레스 유전자 또는 열 쇽 유전자로서 통상 지칭되는 유전자 그룹의 발현을 증가시킴으로써 스트레스 인자(전형적으로 열 쇽 처리)에 반응한다. 열 쇽 처리는 세포 또는 유기체를 세포가 적응되는 온도보다 1℃ 내지 수 ℃ 높은 온도에 노출시키는 것을 포함한다. 이러한 유전자의 도입에 부합하여, 상응하는 스트레스 단백질의 수준이 스트레스 받은 세포에서 증가된다. 본원에서 사용된 바와 같이, "열 쇽 단백질" 또는 "Hsp"로서 공지되기도 한 "스트레스 단백질"은 스트레스 유전자에 의해 암호화되는 단백질이므로, 전형적으로 유기체에 스트레스 인자를 노출시키거나 이와 접촉시킬 때 상당히 많은 양이 생성된다. "열 쇽 유전자"로서 공지되기도 한 "스트레스 유전자"는 본원에서, 유기체(상기 유전자를 함유함)를 스트레스 인자, 예를 들면, 열 쇽, 저산소증, 글루코즈 결손, 중금속 염, 에너지 대사 및 전자 수송의 억제인자 및 단백질 변성제에 노출 또는 접촉시키거나 특정의 벤조퀴논 안사마이신에 노출 또는 접촉시킴으로 인해 활성화되거나 탐지가능한 수준으로 상향 조절되는 유전자로서 사용된다[참조: Nover, L., Heat Shock Response, CRC Press, Inc., Boca Raton, FL(1991)]. "스트레스 유전자"는 또한 공지된 스트레스 유전자 계열내의 동종 유전자, 예를 들면, Hsp70 및 Hsp90 스트레스 유전자 계열내의 특정한 유전자를 포함하지만, 이러한 동종 유전자가 스트레스 인자에 의해 자체적으로 유도되지는 않는다. 본 명세서에서 사용된 바와 같은 용어 스트레스 유전자 및 스트레스 단백질 각각은 본원에서 달리 언급되지 않는 한 서로를 포함할 수 있다.
특정한 양태, 예를 들면, 스트레스 단백질과 HPV 단백질 항원간의 화학적 접합체를 포함하는 경우에는, 본 발명에서 사용된 스트레스 단백질은 분리된 스트레스 단백질인데, 이는 상기 스트레스 단백질을, 이들을 생산하는 숙주 세포로부터 선별하여 분리하였음을 의미한다. 이러한 분리는 본원에 기재된 바와 같이 수행하고 당해 분야에 공지된 통상의 단백질 분리 방법을 사용하여 수행할 수 있다[참조: Maniatis et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y.(1982); Sambrook et al., Molecular Cloning: A Laboratory Manual, 2d Ed., Cold Spring Harbor Laboratory Press(1989); Deutscher, M., Guide to Protein Purification Methods Enzymology, vol. 182. Academic Press. Inc., San Diego, CA(1990)].
세균에서는, 우세한 스트레스 단백질이 분자 크기가 각각 약 70 및 60kDa인 단백질이며, 이는 통상 Hsp70 및 Hsp60으로 각각 지칭된다. 이들 및 기타 특이적 스트레스 단백질 및 이들을 암호화하는 유전자가 다음에 추가로 논의된다. 세균에서는, Hsp70 및 Hsp60이 전형적으로, 나트륨 도데실 설페이트 폴리아크릴아미드 겔 전기영동 및 염색물 쿠마시 블루(Coomassie blue)를 이용하는 염색 패턴을 기초로 하여 세포 단백질의 약 1 내지 3%을 나타내지만, 스트레스가 많은 조건하에서는 25% 정도로 높은 수준으로 축적된다. 스트레스 단백질은 단백질 합성, 세포내 트래픽킹(trafficking) 및 단백질 복합체의 조립 및 해체와 같은 중요한 세포내 과정에 관여하는 것으로 보인다. 스트레스 동안에 합성된 스트레스 단백질의 증가된 양은 주로, 유도된 단백질 비-폴딩의 결과를 최소화하는데 제공된다. 실제로, 스트레스 단백질의 합성을 유도하는 약한 수준의 스트레스가 가해지는 조건에 세포를 미리 노출시키면, 세포를 후속적인 보다 심각한 스트레스의 유해한 영향으로부터 보호할 수 있다.
주요 스트레스 단백질은 지금까지 조사된 모든 유기체와 조직 유형에서 발현되는 것으로 여겨진다. 또한, 이러한 스트레스 단백질은 지금까지 동정된 단백질의 가장 고도로 보존된 그룹을 나타낸다. 예를 들면, 광범위하게 다양한 유기체 중에서의 스트레스 단백질을 비교할 경우, Hsp90 및 Hsp70은 아미노산 수준에서 50% 이상의 동일성을 나타내며, 동일하지 않은 위치에서 많은 유사성을 공유하고 있다. 종내에서의 특정한 스트레스 단백질 계열의 상이한 구성원간에는 유사하거나 보다 높은 수준의 상동성이 존재한다는 것을 인지해야 한다.
스트레스 단백질을 암호화하는 유전자가 세포 또는 유기체의 게놈내에 단일 복사물로 존재하거나 동일하지 않은 다중 복사물로 존재할 수 있다. 예를 들면, 사람 게놈은 hsp100 유전자 1개 이상의 복사물, 2개 이상의 상이한 hsp90 유전자, 10개 이하의 hsp70 유전자(이 중 적어도 몇개는 동일하지 않은 복사물이다), 수 개의 T 복합체 유전자(Tcp 유전자) 및 관련 미토콘드리아 단백질 Hsp60을 암호화하는 1개 이상의 유전자를 함유할 뿐만 아니라 분자 크기가 20 내지 30kDa 범위인 Hsp를 암호화하는 소형 hsp 유전자의 3개 이상의 복사물을 함유하는 것으로 밝혀졌다. 대부분 계열의 스트레스 단백질에서는, 발현 수준이 비교적 높고, 전적으로 구성적(constitutive)이거나 단지 약하게 열 쇽-유도성인 유전자가 1개 이상 존재한다. 또한, 여러 계열의 스트레스 유전자는 열에 의해 상향 조절되지 않으나, 증가된 칼슘 수준 등과 같은 다른 자극에 의해 상향 조절되는 구성원을 포함한다.
스트레스 단백질, 특히 Hsp70, Hsp60, Hsp20 내지 30 및 Hsp10은, 미코박테륨 튜베르쿨로시스(Mycobacterium tuberculosis) 및 미코박테륨 레프 래(Mycobacterium leprae)에 의한 감염에 대한 면역 반응에서 숙주 면역계에 의해 인식된 주요 결정기들이다[참조: Young, R.A., 및 Elliott, T.J., Stress Proteins, Infection, And Immune Surveillance, Cell 50:5-8(1989)]. 추가로, 몇몇 래트 관절염원성(arthritogenic) T 세포가 Hsp60 에피토프를 인식한다[참조: Van Eden, W. et al., Nature 331:171-173(1988)]. 그러나, 미코박테리아성 감염이나 자가면역 질환 병력이 없는 건강한 개개인을 포함한 개개인이 또한 세균성 Hsp60 에피토프와 사람 Hsp60 에피토프 모두를 인식하는 T 세포를 수반하며; 감마-델타 T 세포 수용체의 발현을 특징으로 하는 건강한 개개인에게서 T 세포의 상당 부분이 자체 스트레스 단백질과 외래 스트레스 단백질 모두를 인식한다[참조: O'Brien, R. et al., Cell 57:664-674(1989)]. 따라서, 개개인, 심지어 건강한 개개인도 외래 스트레스 단백질과 자체 스트레스 단백질 에피토프 모두를 인식하는 T-세포 집단을 보유하고 있다.
스트레스 단백질 에피토프를 인식하는 이러한 시스템은 아마도 침입하는 유기체에 대한 "초기 방어 시스템"을 구성하고 있다[참조: Murray, P.J. 및 Young, R.A., J. Bacteriol 174:4193-6(1992)]. 이 시스템은 세균과 바이러스의 빈번한 자극에 의해 유지될 수 있다. 앞서 논의된 바와 같이, 건강한 개개인은 자체 스트레스 단백질을 인식하는 T 세포 집단을 갖는다. 따라서, 자가 반응성 T 세포의 존재가 정상적인 건강인에게 적합하며 자가면역 질환을 유발시키지 않는데, 이는 개개인내에서의 스트레스 단백질의 안전성을 입증한다. 스트레스 단백질의 안전성은, 미코박테륨 튜베르쿨로시스에 대해 보호성이기도 한 스트레스 단백질에 대한 면역 반응을 유도하는 BCG(Bacille Calmerte Guerin; Mycobacterium bovis의 한 균주임) 예방접종의 성공과 상대적인 안전성에 의해 추가로 입증된다.
본 발명에서 사용하기 위한 스트레스 유전자 및 단백질의 계열은 당해 분야에 널리 공지되어 있고, 예를 들면, Hsp100-200, Hsp100, Hsp90, Lon, Hsp70, Hsp60, TF55, Hsp40, FKBP, 사이클로필린, Hsp20-30, ClpP, GrpE, Hsp10, 우비퀴틴, 칼넥신 및 단백질 디설파이드 이소머라제가 있다[참조: Macario, A.J.L., Cold Spring Harbor Laboratory Res. 25:59-70, 1995; Parsell, D.A. & Lindquist, S. Ann. Rev. Genet. 27:437-496(1993); 미국 특허 제5,232,833호(Sanders et al.)]. 스트레스 단백질의 특정한 그룹으로는 Hsp90, Hsp70, Hsp60, Hsp20-30이 있고, 추가로 바람직하게는 Hsp70 및 Hsp60이 있다.
Hsp100-200의 예로는 Grp170(글루코즈-조절된 단백질용)이 있다. Grp170은 프리-골지 구획에서 ER의 루멘에 내재하며 면역글로불린 폴딩과 조립에서 일정 역할을 할 수 있다.
Hsp100의 예로는 포유동물 Hsp110, 효모 Hsp104, ClpA, ClpB, ClpC, ClpX 및 Clpy가 있다. 효모 Hsp104 및 이. 콜라이 ClpA는 6량체 입자를 형성하고 이. 콜라이 ClpB는 4량체 입자를 형성하며 이의 조립은 아데닌 뉴클레오티드 결합을 요구하는 것으로 보인다. Clp 프로테아제는 ClpP(단백질 분해성 아단위)와 ClpA로 구성된 750kDa 헤테로올리고머를 제공한다. ClpB-Y는 ClpA와 구조적으로 관련이 있지만, ClpA와 달리, 이는 ClpB와 복합체를 형성하는 것으로 여겨지진 않는다.
Hsp90의 예로는 이. 콜라이에서의 HtpG, Hsp83 및 Hsc83 효모, 및 사람에 있 어서의 Hsp90알파, Hsp90베타 및 Grp94가 있다. Hsp90은 단백질 그룹과 결합되며, 이러한 단백질은 전형적으로, 스테로이드 호르몬 수용체(예: 글루코코르티코이드, 에스트로겐, 프로게스테론 및 테스토스테론 수용체), 전사 인자, 및 시그날 전달 기전에서 중요한 역할을 하는 단백질 키나제와 같은 세포성 조절 분자이다. Hsp90 단백질은 또한 기타 스트레스 단백질을 포함하는 크고 풍부한 단백질 복합체의 형성에 참여한다.
Lon은 이. 콜라이에서 비-천연 단백질을 분해하는 ATP-의존성 프로테아제로서 작용하는 4량체 단백질이다.
Hsp70의 예로는 포유동물 세포로부터의 Hsp72 및 Hsc73; 세균, 특히 미코박테륨 레프래(Mycobacterium leprae), 미코박테륨 튜베르쿨로시스 및 미코박테륨 보비스(Mycobacterium bovis)(예를 들면, Bacille-Calmette Guerin; Hsp71로 지칭됨) 등의 미코박테리아로부터의 Dnak; 에스케리키아 콜라이(Escherichia coli), 효모 및 기타 원핵생물로부터의 Dnak; 및 BiP 및 Grp78이 있다. Hsp70은 ATP 뿐만 아니라 비-폴딩된 폴리펩타이드 및 펩타이드와 특이적으로 결합될 수 있기 때문에, 단백질 폴딩과 비-폴딩에 관여할 뿐만 아니라 단백질 복합체의 조립과 해체에 관여할 수 있다.
Hsp60의 예로는 미코박테리아로부터의 Hsp65가 있다. 세균성 Hsp60은 또한 이. 콜라이로부터의 GroEL과 같은 GroEL로서 통상 공지되어 있다. Hsp60은 대형 호모올리고머성 복합체를 형성하며, 단백질 폴딩에 중요한 역할을 하는 것으로 여겨진다. Hsp60 동족체가 진핵생물의 미토콘드리아 및 엽록체에 존재한다.
TF55의 예로는 Tepl, TRiC 및 테르모솜(thermosome)이 있다. 이러한 단백질은 전형적으로 진핵생물 및 몇몇 원시세균(archaebacteria)의 세포질에서 발생되고 단백질 폴딩을 증진시키는 다중-원 환을 형성한다. 이는 또한 Hsp60과 약간의 상동성을 나타낸다.
Hsp40의 예로는 이. 콜라이 및 미코박테리아 등의 원핵생물로부터의 DnaJ; 및 HSJ1, HDJ1 및 Hsp40이 있다. Hsp40은 여러 세포내 활성 중에서, 단백질 폴딩, 내열성 및 DNA 복제에서 분자 샤프롱(chaperone)으로서의 역할을 한다.
FKBP의 예로는 FKBP12, FKBP13, FKBP25 및 FKBP59, Fpri 및 Nepl이 있다. 이 단백질은 전형적으로, 펩티딜-프롤릴 이소머라제 활성을 지니고 있으며 FK506 및 라파마이신 등의 면역억제제와 상호작용한다. 이 단백질은 전형적으로, 세포질과 소포체에서 발견된다.
사이클로필린의 예로는 사이클로필린 A, B 및 C가 있다. 이 단백질은 펩티딜-프롤릴 이소머라제 활성을 지니고 있으며 면역억제제 사이클로스포린 A와 상호작용된다. 이러한 단백질 사이클로스포린 A는 칼시뉴린(calcineurin)(단백질 포스파타제)에 결합된다.
Hsp20-30은 소형 Hsp로서 지칭되기도 한다. Hsp20-30은 전형적으로, 대형 호모올리고머성 복합체에서 발견되거나, 또는 가능하게는, 유기체 또는 세포 유형이 몇몇 상이한 유형의 소형 Hsp를 발현시키는 헤테로올리고머성 복합체에서 발견된다. Hsp20-30은 세포골격의 구조와 상호작용하며, 액틴의 중합/탈중합 반응에서 조절 역할을 할 수 있다. Hsp20-30은 휴지기 세포가 성장 인자에 노출되거나 스트 레스를 받을 때 신속하게 포스포릴화된다. Hsp20-30 동족체로는 알파-크리스탈린이 있다.
ClpP는 비정상적인 단백질의 분해와 연관된 이. 콜라이 프로테아제이다. ClpP의 동족체가 엽록체에서 발견된다. ClpP는 ClpA와 헤테로올리고머성 복합체를 형성한다.
GrpE는 스트레스-손상된 단백질의 보호 뿐만 아니라 손상된 단백질의 분해 모두에 관련되는 약 20kDa의 이. 콜라이 단백질이다. GrpE는 이. 콜라이에서 스트레스 유전자 발현의 조절에 관여한다.
Hsp10의 예로는 GroES 및 Cpn10이 있다. Hsp10은 전형적으로 이. 콜라이에서 발견되고 진핵 세포의 미토콘드리아와 엽록체에서 발견된다. Hsp10은 Hsp60 올리고머와 연합되는 7-원 환을 형성한다. Hsp10은 또한 단백질 폴딩에 관여한다.
우비퀴틴은 ATP-의존성 사이토졸 프로테아제에 의한 단백질은 단백질 분해적 제거에 협조하여 이러한 단백질과 결합하는 것으로 밝혀졌다.
특정한 양태에서는, 본 발명의 스트레스 단백질은 엔테로박테리아, 미코박테리아(특히 엠. 레프래, 엠. 투베르쿨로시스, 엠. 바케(M. vaccae), 엠. 스메그마티스(M. smegmatis) 및 엠. 보비스), 이. 콜라이, 효모, 드로소필라(Drosophila), 척추동물, 조류, 치킨, 포유동물, 랫트, 마우스, 영장류 또는 사람으로부터 수득된다.
스트레스 단백질은 산성 또는 염기성 형태일 수 있거나 중성 형태일 수 있다. 또한, 개개의 아미노산 잔기를 산화 또는 환원시켜 변형시킬 수 있다. 더우 기, 아미노산 또는 핵산 서열에 대해 각종 치환, 결실 또는 부가가 이루어질 수 있으며, 이의 최종적인 효과는 스트레스 단백질의 증가된 생물학적 활성을 보존시키거나 추가로 증진시키는 것이다. 암호 축퇴성(degeneracy)으로 인해, 예를 들면, 동일한 아미노산 서열을 암호화하는 뉴클레오티드 서열에 상당한 차이가 있을 수 있다. 본 발명은 또한 스트레스 단백질의 부분이나 스트레스 단백질로부터 수득된 펩타이드를 이용하여 사용하기에 적합한데, 단, 이러한 부분이나 펩타이드는 선택된 HPV 단백질 항원에 대한 면역 반응을 증진시키는 것과 관련된 에피토프를 포함해야 한다. 스트레스 단백질의 부분들은 프로테이나제를 사용하여 분해함으로써 수득하거나, 또는 스트레스 단백질-암호화 뉴클레오티드 서열(단독이거나 또 다른 단백질-암호화 핵산 서열과 융합됨)의 일부만을 발현시키는 것과 같은 재조합 방법으로 수득할 수 있다. 펩타이드도 또한 이러한 방법으로 생성시키거나 화학적 합성에 의해 생성시킬 수 있다. 이러한 스트레스 단백질은 공지된 각종 기술에 의해 특정 부위에 도입된 돌연변이를 포함할 수 있다[참조: Sambrook et al., Molecular Cloning: A Laboratory Manual, 2d Ed., Cold Spring Harbor Laboratory Press(1989); Drinkwater and Klinedinst Proc. Natl. Acad. Sci. USA 83:3402-3406(1986); Liao 및 Wisc, Gene 88:107-111(1990); Horwitz et al., Genome 3:112-117(1989)]. 본원에서 사용된 바와 같은 용어 스트레스 단백질은 스트레스 단백질의 상기와 같은 부분과 펩타이드를 포함하는 것으로 간주된다.
스트레스 유전자 또는 단백질로서 고려중인 유전자 또는 단백질을 동정하는 방법은 당해 분야에 널리 공지되어 있다. 예를 들면, 특정한 스트레스 단백질 계 열의 유전자 및 단백질의 보존은, 예를 들면, 핵산 하이브리드화 또는 핵산 또는 아미노산 서열화에 이은 컴퓨터 비교 분석에 의해, 고려중인 유전자/단백질의 뉴클레오티드 또는 아미노산 서열을 Dnak, GroEL 또는 DnaJ 등의 널리 공지된 스트레스 유전자와 비교할 수 있게 해준다[참조: Voellmy, R. et al., Proc. Nat'l Acad. Sci. USA 82:4949-4953(1985)]. 또 다른 한편, 검정을 이용하여 선택된 스트레스 단백질의 필수 구조적 특징 및/또는 기능성을 확인하고/하거나 이들을 구별할 수 있다. 예를 들면, 항-Hsp 항체를 사용하여 발현 라이브러리를 스크리닝할 수 있다. Hsp90은 벤조퀴논 안사마이신 겔다나마이신과 고친화성으로 결합되는 것으로 널리 공지되어 있다. 따라서, 겔다나마이신을 사용하여 발현 라이브러리를 스크리닝하여 벤조퀴논 안사마이신과 결합하는 단백질로서 Hsp90의 추정상의 동족체를 밝혀낼 수 있다. 분리된 핵산에 의해 암호화된 단백질의 성질은 항체를 이용한 검정을 포함한 기타 검정에 의해 추가로 확인할 수 있다[참조: Antibodies: A Laboratory Manual. Harlow 및 Lane(eds.), Cold Spring Harbor Laboratory Press(1988)]. 또한, 소정의 스트레스 단백질의 생물학적 활성을 활용할 수 있다[참조: Guidon, P.T. 및 Hightower, L.E., Biochem. 25:3231-3239(1986)]. 예를 들면, Hsp70은 ATP와 특이적으로 결합할 수 있을 뿐만 아니라 단백질 복합체의 조립에서 비-폴딩된 폴리펩타이드 및 펩타이드와 특이적으로 결합할 수 있다. 따라서, 고려중인 특정 단백질을 적당한 폴리펩타이드, 펩타이드 또는 ATP를 포함하는 샘플과 혼합한 다음, 단백질-단백질 또는 단백질-뉴클레오티드 복합체 생성의 존재 또는 부재 여부를 결정하는 것은 Hsp70 단백질 또는 유전자의 식별가능한 존재 또 는 부재 여부를 나타내는데, 이러한 존재 또는 부재 여부는 항체 이용 검정과 같은 기타 검정을 이용하여 확인할 수 있다.
당해 조성물에 존재하는, 스트레스 단백질, 스트레스 단백질 부분, 스트레스 단백질 동족체, 및 스트레스 단백질이 접합되거나 비공유적으로 결합되는 HPV의 단백질 항원은 공지된 기술을 사용하여 생성시키거나 수득할 수 있다. 예를 들면, 상기 스트레스 단백질 및/또는 항원은 이를 발생시키는 것으로 공지된 공급원으로부터 수득(분리)할 수 있거나, 세포 배양물로부터 생성 및 수거할 수 있거나, 항원의 경우에는, 감염된 세포로부터 수득할 수 있거나, 경우에 따라 클로닝한 다음 목적하는 스트레스 단백질 또는 항원을 암호화하는 유전자를 발현시킴으로써 생성시킬 수 있거나, 또는 화학적으로 합성할 수 있다. 더우기, 목적하는 스트레스 단백질 또는 항원을 암호화하는 핵산 서열을 화학적으로 합성할 수 있다. 스트레스 단백질과 HPV 단백질 항원을 포함하는 융합 단백질을 재조합 방법에 의해 생성시킬 수 있다. 예를 들면, 스트레스 단백질을 암호화하는 핵산을 HPV 단백질 항원을 암호화하는 핵산 서열의 어느 한 말단에 결합시켜, 두 단백질-암호화 서열이 공통의 해독 판독 프레임을 공유하고 HPV 단백질-항원 및 스트레스 단백질을 포함하는 융합 단백질로서 발현시킬 수 있다. 이와 같이 조합된 서열을 목적하는 발현 양상과 숙주 세포의 특성에 의거하여 선택된 적합한 벡터내로 삽입한다. 후술되는 본 실시예에서는, 이러한 핵산 서열을 세균 이. 콜라이에서의 단백질 발현용으로 적합한 벡터에서 조립시킨다. 선택된 숙주 세포에서 발현시킨 후, 통상적인 생화학 분리 기술에 의하거나 상기 융합 단백질의 한 부분 또는 다른 부분에 대한 항체를 사용 하는 면역친화 방법에 의해 정제할 수 있다. 또 다른 방법으로는, 이와 같이 선택된 벡터는 상기 융합 단백질 서열에 태그, 예를 들면, 후술되는 실시예에 기재된 바와 같은 올리고히스티딘 태그를 가함으로써, 항체 또는 이러한 태그에 대하여 적당히 높은 친화성을 갖는 기타 물질을 이용하는 친화 방법에 의해 정제될 수 있는 태그 부착된 융합 단백질을 발현시킬 수 있다[참조: Sambrook et al., Molecular Cloning: A Laboratory Manual, 2d Ed., Cold Spring Harbor Laboratory Press(1989); Deutscher, M., Guide to Protein Purification Methods Enzymology, vol. 182. Academic Press. Inc., San Diego, CA(1990)]. 포유동물 세포에서의 발현에 적합한 벡터, 예를 들면, 아래에 논의된 벡터 중의 하나를 사용하는 경우에는, 융합 단백질을 포유동물 세포로부터 발현 및 정제할 수 있다. 또 다른 방법으로는, 포유동물 발현 벡터(융합 단백질-암호화 서열을 포함함)를 피검체에게 투여하여 이러한 피검체의 세포에서 상기 융합 단백질의 발현을 지시할 수 있다. 스트레스 단백질 및 HPV 단백질 항원을 포함하는 융합 단백질을 암호화하는 핵산을 화학적으로 생성시킨 다음, 이를 융합 단백질 생성과 정제에 적합한 벡터내로 삽입하거나 피검체에 투여할 수 있다. 최종적으로, 융합 단백질을 화학적으로 제조할 수도 있다.
본원에 기재된 스트레스 단백질 및 HPV 항원을 포함하는 조성물을 사용하여 HPV, 또는 HPV 항원을 발현시키는 HPV-감염된 세포나 형질전환된 세포에 대한 면역 반응, 특히 세포 매개된 세포용해 반응을 증진시킬 수 있다. 바람직하게는, 조성물이 특정한 HPV 유형(이의 단백질에 대해 면역 반응이 유발된다)으로부터의 단백 질 항원 서열을 함유할 것이다.
본원에 기재된 스트레스 단백질 및 HPV 항원을 포함하는 조성물을 각종 방법으로 피검체에 투여할 수 있다. 투여 경로로는 피내, 경피(예를 들면, 서방출 중합체), 근육내, 복강내, 정맥내, 피하, 경구, 경막외 및 비내 투여가 있다. 기타 통상적인 모든 투여 경로, 예를 들면, 주입 또는 일시 주사, 또는 상피 또는 점막피부 내층을 통한 흡수를 이용할 수 있다. 또한, 본원에 기재된 조성물은 기타 약리학적으로 허용되는 성분, 예를 들면, 생물학적 활성제(예: 알룸 등의 아주반트), 계면활성제(예: 글리세라이드), 부형제(예: 락토즈), 담체, 희석제 및 비히클을 함유하고 이와 함께 투여할 수 있다. 추가로, 당해 조성물을, 피검체로부터 수득된 백혈구 세포를 자극하기 위한 수단으로서 생체외에서 사용하여 시험관내에서 HPV 단백질 항원-특이적 면역 세포를 유발시키고, 증대시키고 증식시킨 다음, 연속적으로 이를 피검체에 재도입할 수 있다.
추가로, 스트레스 단백질-HPV 단백질 항원 융합 단백질은 이러한 단백질 서열을 암호화하는 핵산을 생체내 발현시킴으로써 사람 피검체내로 투여할 수 있다. 이러한 핵산의 발현을 피검체로부터 수득된 백혈구 세포를 자극하기 위한 수단으로서 생체외에서 달성하여, 시험관내에서 HPV 항원-특이적 면역 세포를 유발시키고, 증대시키고 증식시킨 다음, 연속적으로 이를 피검체내로 재도입할 수 있다. HPV 단백질 항원-스트레스 단백질 융합물의 발현을 지시하는데 적합한 발현 벡터는 현재 본 분야에서 사용되고 있는 각종 벡터 중에서 선택할 수 있다. 고수준으로 발현시킬 수 있을 뿐만 아니라 관심있는 유전자를 형질도입시키는데 유효한 벡터가 바람직할 것이다. 예를 들면, 재조합 아데노바이러스 벡터 pJM17[참조: All et al., Gene Therapy 1:367-84(1994); Berkner K.L., Biotechniques 6:616-24, 1988], 제2 세대 아데노바이러스 벡터 DE1/DE4[참조: Wang 및 Finer, Nature Medicine 2:714-6(1996)] 또는 아데노-관련 바이러스 벡터 AAV/Neo[참조: Muro-Cacho et al., J. Immunotherapy 11:231-7(1992)]를 사용할 수 있다. 추가로, 재조합 레트로바이러스 벡터 MFG[참조: Jaffee et al., Cancer Res. 53:2221-6(1993)] 또는 LN, LNSX, LNCX, LXSN[참조: Miller 및 Rosman, Biotechniques 7:980-9(1989)]을 사용할 수 있다. pHSV1와 같은 단순 포진 바이러스계 벡터[참조: Geller et al., Proc. Nat'l Acad. Sci 87:8950-4(1990)] 또는 MVA와 같은 백시니아 바이러스 벡터[참조: Sutter 및 Moss, Proc. Nat'l Acad. Sci, 89:10847-51(1992)]를 대안으로서 사용할 수 있다.
프로모터와 3' 서열을 포함한, 자주 사용되는 특정 발현 단위는 플라스미드 CDNA3(Invitrogen), 플라스미드 AH5, pRC/CMV(Invitrogen), pCMU II(Paabo et al., EMBO J. 5:1921-1927(1986)), pZip-Neo SV[참조: Cepko et al., Cell 37:1053-1062(1984)] 및 pSRa(DNAX, Palo Alto, CA)에서 발견된 것이다. 유전자를 발현 단위 및/또는 벡터내로 도입하는 것은 분자 생물학에 있어서 분자 클로닝 및 통용되는 프로토콜과 같은 매뉴얼[참조: Sambrook, J., et al., Molecular Cloning, Cold Spring Harbor Press(1989); Ausubel, F.M. et al., Current Protocols in Molecular Biology, Greene Publishing Associates and Willey-Interscience(1989)]에 기재된 바와 같은 유전공학 기술을 이용하여 달성할 수 있 다. 생성된 발현가능한 핵산은, 이러한 핵산을 발현가능한 형태, 예를 들면, 상기된 바와 같은 바이러스 벡터의 일부분으로서, 나출된(naked) 플라스미드 또는 기타 DNA로서, 또는 표적화된 리포좀이나 적혈구 고스트의 캡시드내에 봉입된 형태로 세포내에 놓을 수 있는 모든 방법에 의해서 사람 피검체의 세포내로 도입할 수 있다[참조: Friedman, T., Science, 244:1275-1281(1989); Rabinovich, N.R. et al., Science, 265:1401-1404(1994)]. 형질도입 방법에는 조직 및 종양내로의 직접적인 주사, 리포좀성 형질감염[참조: Fraley et al., Nature 370:111-117(1980)], 수용체-매개된 세포내이입[참조: Zatloukal et al., Ann. N.Y. Acad. Sci. 660:136-153(1992)] 및 입자 폭격(bombardment)-매개된 유전자 전달[참조: Eisenbraun et al., DNA & Cell. Biol. 12:791-797(1993)]이 포함된다.
본 발명의 조성물 중의 스트레스 단백질과 HPV 단백질 항원(앞서 논의된 바와 같이 융합되거나, 접합되거나 비공유적으로 결합됨)의 양은 피검체에서 유효한 면역자극 반응을 유발시키는 양이다. 유효량은 투여시 면역 반응을 유도하는 양이다. 또한, 피검체에 투여된 스트레스 단백질과 HPV 단백질 항원의 양은 이용된 HPV 단백질 항원 및 스트레스 단백질, 피검체의 체격, 연령, 체중, 전반적인 건강 상태, 성별 및 음식을 포함한 각종 요인 뿐만 아니라 이의 일반적인 면역학적 반응성에 따라서 다양할 것이다. 정립된 투여량 범위의 조정 및 조작은 당해 분야의 숙련인의 능력내이다. 예를 들면, 스트레스 단백질과 항원의 양은 약 1 마이크로그램 내지 약 1 그램, 바람직하게는 약 100 마이크로그램 내지 약 1 그램 및 약 1 밀리그램 내지 약 1 그램일 수 있다. 발현 벡터를 포함하는 조성물의 유효량은 투 여시, 이를 암호화하는 HPV 단백질 항원에 대한 면역 반응을 유도하는 양이다. 추가로, 피검체에게 투여된 발현 벡터의 양은 발현된 HPV 단백질 항원 및 스트레스 단백질, 피검체의 체격, 연령, 체중, 전반적인 건강 상태, 성별 및 음식을 포함한 각종 요인 뿐만 아니라 이의 일반적인 면역학적 반응성에 따라서 다양할 것이다. 고려해야만 하는 부가의 요인은 투여 경로 및 사용된 벡터의 유형이다. 예를 들면, HPV 단백질 항원-스트레스 단백질 융합 단백질을 암호화하는 핵산을 함유하는 바이러스 벡터를 사용하여 예방 또는 치료를 수행하는 경우, 유효량은 헬퍼-비함유, 복제-결함있는 바이러스 104 내지 1012개/체중 kg, 바람직하게는 105 내지 1011개/체중 kg, 가장 바람직하게는 106 내지 1010개/체중 kg의 범위일 것이다.
본 발명은 다음 실시예에 의해 예시되며, 이로써 본 발명의 범위가 제한되지는 않는다.
실시예 1
재조합 스트레스 단백질의 분리
재조합
미코박테리아성
Hsp71
플라스미드 Y3111은 발현 조절 서열들 사이에 작용 가능하게 삽입된 엠. 튜베르쿨로시스 hsp71 유전자를 함유한다[참조: Mehlert, A. 및 Young, D.B., Mol. Microbiol. 3:125-130(1989)]. 절두된(truncated) dnaK 유전자를 함유하는 이. 콜라이 균주 CG2027(C. Georgopoulos, University of Geneva, Switzerland로부터 구 입함)을 표준 과정에 의해 플라스미드 Y3111로 형질전환시킨다[참조: Maniatis et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y.(1982)].
플라스미드 Y3111을 함유하는 세균을 교반(250rpm)하에 37℃에서 100㎍/ml 앰피실린을 함유하는 2xYT 배지(20g 트립톤, 10g 효모 추출물, 10g NaCl/ℓ)에서 밤새 성장시킨다. 상기 배양물로부터 10% 글리세롤 스톡을 제조하고 -70℃에서 저장한다. 이와 같이 동결된 글리세롤 스톡으로부터의 수 차례 깎은 부스러기를 사용하여 다량의 배양물에 접종하고 이를 앞서와 같이 약 48시간 동안 항온처리한다. 590nm에서의 광학밀도가 2.5 내지 3.5에 도달하게 되면, 세포를 원심분리하여 수집한다.
다음 단계를 4℃에서 수행한다. 세포 펠렛을 펠렛화된 세포 1g당 용해 완충액 3ml에 재현탁시킨다. 용해 완충액의 조성은 10mM 트리스-HCl, 2mM 에틸렌디아민 테트라아세테이트(EDTA), 5mM 베타-머캅토에탄올, 10㎍/ml 아프로티닌, 10㎍/ml 류펩틴 및 1㎍/ml 펩스타틴이다. 라이소자임을 상기 세포 현탁액에 가하여 최종 농도가 0.14mg/ml가 되도록 한다. 이어서, 이 현탁액을 -70℃에서 동결시킨다.
상기 세포 현탁액을 해동시키고, 세포를 초음파처리하여 파쇄시킨다. 초음파처리물을 17,000rpm으로 30분 동안 원심분리한다(JA-17 회전기, Beckmann). 상기 용액이 (NH4)2SO4로 65% 포화될 때까지 고형의 (NH4)2SO4를 상기 상등액 용액에 가한다. 30분 동안 항온처리한 후, 상기 혼합물을 앞서와 같이 원심분리한다. 이 펠렛을 Q SEPHAROSE 완충액 A에 용해시킨다. 이 용액에 10㎍/ml 아프로티닌, 10㎍ /ml 류펩틴 및 1㎍/ml 펩스타틴을 가하고, 이 용액을 65용적의 Q SEPHAROSE 완충액 A에 대하여 밤새 투석시킨다. Q SEPHAROSE 완충액 A는 30mM 트리스-HCl(pH 7.5), 1mM EDTA, 5mM 베타-머캅토에탄올을 함유한다. 이와 같이 투석된 용액을 앞서 기재된 바와 같이 원심분리하여 정화시킨다.
투석시킨 용액을 Q SEPHAROSE 완충액 A에서 평형화시킨 Q SEPHAROSE 칼럼(Pharmacia)에 적용시킨다. 이 칼럼을 동일한 완충액 2용적으로 세척한다. 0 내지 600mM NaCl 구배를 이용하여 용출시킨다. 주요 71kDa 폴리펩타이드(즉, 재조합 엠. 튜베르쿨로시스 Hsp71 단백질)의 존재 여부를 알아보기 위하여, 분획을 SDS-PAGE로 시험하고 쿠마시 블루로 염색한다. 이러한 폴리펩타이드를 함유하는 분획을 수집하고, 이러한 수집물에 고형의 (NH4)2SO4를 가하여 65% 포화에 이르도록 한다. 이 혼합물을 앞서 기재된 바와 같이 원심분리하고, 펠렛을 ATP 출발 완충액(50mM 트리스-HCl(pH 8.0), 20mM NaCl, 5mM MgCl2, 15mM 베타-머캅토에탄올, 0.1mM EDTA)에 용해시키고, 생성된 단백질 용액을 65용적의 동일한 완충액에 대해 밤새 투석시킨 다음, 원심분리하여 정화시킨다.
이어서, 이와 같이 투석된 단백질 용액을 ATP 출발 완충액에서 평형화시킨 ATP-아가로즈 칼럼(Fluka)에 적용시킨다. 이 칼럼을 1M NaCl을 함유하는 1칼럼 용적의 ATP 출발 완충액으로 세척한다. 10mM ATP가 보충된 ATP 출발 완충액을 이용하여 용출시킨다. (NH4)2SO4를 이용하여 상기 용출액이 65% 포화에 이르도록 하고, 침전된 단백질을 앞서 기재된 바와 같이 수집한다. 원심분리 펠렛을 200용적의 Blue SEPHAROSE 완충액(30mM 트리스-HCl(pH 7.5), 5mM MgCl2, 5mM 베타-머캅토에탄올)에 용해시키고 이에 대해 투석시킨다.
마지막 단계로부터 투석된 단백질 용액을 Blue SEPHAROSE 완충액으로 평형화시킨 Blue SEPHAROSE 칼럼(Pharmacia)에 적용시킨다. 이 칼럼을 동일한 완충액 1.5칼럼 용적으로 세척한다. 관류(flow-through) 분획과 세척 분획(Hsp71을 함유함)을 단일 수집물로서 수집한다. 최종 제제의 순도를 SDS-PAGE 및 쿠마시 블루 염색법, 미코박테리아 Hsp71 및 이. 콜라이 Dnak 각각에 대해 특이적인 마우스 모노클로날 항체를 이용하는 웨스턴 블롯 분석법[참조: Maniatis et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y.(1982); Sambrook et al., Molecular Cloning: A Laboratory Manual, 2d Ed., Cold Spring Harbor Laboratory Press(1989)], 및 ATPase 활성 검정법에 의해 평가한다. 제제는 전형적으로, 쿠마시 블루-염색된 겔에서 상기 제제의 염색 패턴을 기준으로 하여 90% 이상, 바람직하게는 95% 이상 순수하며, 이. 콜라이 GroEL을 1% 미만 함유하고 이. 콜라이 DnaK는 전혀 검출되지 않았다.
재조합
미코박테리아
Hsp65
플라스미드 RIB 1300은 발현 조절 서열들 사이에 작용가능하게 삽입된 엠. 보비스 BCG hsp65 유전자를 함유한다[참조: Thole, J.E.R. et al., J. Exp. Med. 178:343-8(1993)]. 이. 콜라이 균주 M1546을 표준 과정에 의해 플라스미드 RIB 1300으로 형질전환시킨다[참조: Maniatis et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory, Cold Spring Harbor, N.Y.(1982)].
플라스미드 RIB 1300을 함유하는 세균의 접종물을 교반(250rpm)하에 28℃에서 앰피실린 200㎍/ml를 함유하는 NCZYM 배지(10g N-Z 아민 A, 5g 박토 효모 추출물, 1g 카사미노산, 5g NaCl, 2g (NH4)2SO4·7H2O/ℓ)에서 포화되도록 성장시킨다. 이 배양물을 사용하여, 배양물의 590nm에서의 광학밀도가 0.3 내지 0.6이 될 때까지 접종 배양물과 동일한 조건하에서 성장시킨 보다 다량의 배양물에 접종시킨다. 온수 욕에서 항온처리하여 배양물의 온도를 42℃로 신속하게 상승시킴으로써 재조합 단백질의 제조를 개시한다. 상기 배양물을 교반하에 3시간 동안 상기 온도로 유지시킨다. 이어서, 상기 세균을 원심분리하여 수집하고, 용해 완충액의 세균성 펠렛 중량당 6용적에 재현탁시킨다. 용해 완충액은 10mM 트리스-HCl(pH 8.0), 10mM 에틸렌디아민 테트라아세테이트(EDTA), 0.1mM PMSF 및 0.1% RIVM BA(0.104g 4-아미노-벤즈아미딘-2HCl, 0.066g 엡실론-아미노 카프로산/50ml)를 함유한다. 라이소자임을 0.1mg/ml의 농도로 가하고, 상기 현탁액을 -70℃에서 동결시킨다.
상기 세균성 현탁액을 해동시키고 4℃에 둔다. 하기 작업을 상기 온도에서 수행한다. 초음파처리함으로써 세균을 완전히 용해시킨다. 초음파처리물을 JA-17 회전기(Beckmann)에서 17,000rpm으로 30분 동안 원심분리한다. 20% 포화도가 달성될 때까지 포화 (NH4)2SO4를 상기 상등액 용액에 가한다. 침전물을 원심분리(상기 참조)에 의해 제거하고 폐기한다. 상기 상등액 용액을, 포화 (NH4)2SO4를 가함으로 써 55% 포화도에 이르도록 한다. 후속 원심분리로부터 생성된 펠렛을 TE 완충액(10mM 트리스-HCl(pH 8.0), 15mM 베타-머캅토에탄올, 1mM EDTA)에 용해시킨다. 이어서, TE 중의 단백질 용액을 50용적의 TE 완충액에 대하여 투석시킨다.
원심분리(상기와 같음)에 의해 침전된 물질을 제거한 후, 투석된 단백질 용액을 DEAE SEPHAROSE(Pharmacia) 칼럼에 적용시킨다. TE 완충액으로 세척한 후, 단백질을 TE 완충액 중의 0 내지 300mM NaCl 구배로 용출시킨다. 엠. 보비스 BCG Hsp65를 함유하는 분획을 SDS-PAGE 및 쿠마시 블루 염색에 의해 확인한 다음 수집한다. 10㎍/ml 아프로티닌, 10㎍/ml 류펩틴 및 1㎍/ml 펩스타틴을 상기 수집물에 가한 다음, YM30 막을 사용하여 아미콘(Amicon) 세포에 농축시킨다.
이와 같이 농축된 수집물을 S200 완충액(10mM Na2HPO4(pH 6.8), 150mM NaCl 및 15mM 베타-머캅토에탄올)로 평형화시킨 S-200 SEPHACRYL(Pharmacia) 칼럼에 적용시킨다. 동일한 완충액을 사용하여 용출시킨다. 상기와 같이 미코박테리아 Hsp65의 존재 여부를 알아보기 위해 분획을 시험하고, 고도로 정제된 단백질을 함유하는 양성 분획을 수집한 다음, HAP 완충액(10mM Na2HPO4(pH 6.8), 15mM 베타-머캅토에탄올)에 대해 밤새 투석시킨다.
이와 같이 투석된 수집물을 HAP 완충액에 평형화시킨 하이드록시아파타이트(Bio-Rad; Bio-Gel HTP Gel) 칼럼에 적용시킨다. 이 칼럼을 3칼럼 용적의 1mM MgCl2 및 15mM 베타-머캅토에탄올로 세척한 다음, 1mM Na2HPO4(pH 6.8) 및 15mM 베타-머캅토에탄올로 세척한다. 단백질을 10 내지 60mM 인산염 구배로 용출시킨다. 분획을 앞서와 같이 시험하고, 양성 분획을 수집하고, 농축시킨 다음, PD10(Pharmacia)을 통한 겔 여과에 의해 0.85% NaCl로 교환시킨다. 미코박테리아 Hsp65의 순도를 SDS-PAGE 및 쿠마시 블루 염색법, 및 이. 콜라이 Dnak 및 GroEL에 대해 특이적인 항체를 이용하는 웨스턴 블롯 분석법에 의해 평가한다. 제제는 전형적으로 90% 이상 순수하고, 0.5% 이하의 이. 콜라이 GroEL 및 0.1 내지 0.2%의 이. 콜라이 DnaK를 각각 함유하였다.
Hsp 제제를, 폴리마익신 B를 가하여 DetoxiGel 수지(Pierce) 상에서 친화 크로마토그래피하거나, 또는 트리톤 X-114 또는 X-100 등의 세정제를 이용하여 추출함으로써 발열물질을 제거할 수 있다. 리물러스(limulus) 변형세포(amoebocyte) 검정(LAL; Biowhittaker, QCL 1000)에 의해 지질다당류의 함량 감소가 수반될 수 있다. Hsp 제제를 -70℃에서 완충액내에 저장할 수 있거나, 동결건조 후의 건조된 펠렛으로서 바람직하게는 -70℃에서 방치할 수 있다.
실시예 2
단백질 항원-스트레스 단백질 접합체의 제조
본 실시예는 스트레스 단백질과 단백질 항원(본 실시예에서는 인플루엔자바이러스 핵단백질(NP)로부터 유래된 펩타이드)간의 접합체를 제조하기 위해 이용할 수 있는 기술을 예시하고자 제공된 것이다.
스트레스 단백질(
Hsp71
)과 항원(
NP
.B)의 합성
엠. 튜베르쿨로시스 Hsp71을 실시예 1에서와 같이 제조한다. 완전한 NP 중 의 잔기 363 내지 374에 상응하고 공지된 CTL 에피토프(H-2b-제한됨)를 함유하는, 아미노산 서열 [C]VQLASNENMETM(서열 1; 이 펩타이드는 엑스트라 아미노-말단 시스테인 잔기를 함유한다)을 갖는 NP 펩타이드(본원에서 NP.B로서 지칭됨; Motal, U.M.A. et al., Eur. J. Immunol. 25:11214(1995))를, 알파-아미노 보호 그룹으로서 Fmoc(9-플루오레닐메틸옥시-카보닐)을 사용하고 고체 지지체로서 HMP(Wang) 수지를 사용하여 어플라이드 바이오시스템즈(Applied Biosystems) 모델 431A 펩타이드 합성기에서 합성하여 제조한다(0.25mM 스케일). 모든 아미노산 및 합성용 화학물질은 어플라이드 바이오시스템즈로부터 구입한다. NP.B를 지지체로부터 절단하고, 10ml 트리플루오로아세트산, 0.5ml 물, 0.75g 결정성 페놀, 0.25ml 에탄디티올 및 0.5ml 티오아니솔을 합함으로써 제조된 혼합물 2ml 중에서 NP.B-수지를 3시간 동안 지속적인 교반하에 항온처리함으로써 측쇄-보호 그룹을 제거한다. 이러한 절단 혼합물을 빙냉 디에틸 에테르 40ml내로 여과시킨다. 불용성 물질을 5000xg에서 8분 동안 원심분리함으로써 수집한다. 에테르를 경사제거하고, 펠렛을 냉 디에틸 에테르에 재현탁시킨 다음 원심분리함으로써 3회 세척한다. 마지막 세척 후, 상기 펠렛을 공기 건조시키고, 증류수에 용해시킨 다음, 동결건조시킨다.
Hsp71
및 디프테리아 독소에 대한
NP
.B
펩타이드의
화학적 접합
Hsp71, 및 CTL 활성의 특정 자극 효능을 비교하기 위한 표준물을 제공하기 위해, 통상적으로 사용된 운반 단백질 디프테리아 독소(DT로 약칭; DT는 Wako Chemical로부터 구입함) 모두를 사용하여 접합을 수행한다.
활성화된 운반 단백질 용액: 9mg의 Hsp71을 4.5ml의 0.1M 붕산나트륨(pH 8.0)에 용해시킨다. 설포-MBS(m-말레이미도벤조일-N-하이드록시-설포석신이미드 에스테르)(100㎕ 디메틸 설폭사민 중의 2.3mg)을 상기 단백질에 가하고, 반응 혼합물을 실온에서 1시간 동안 배양한다. 이어서, pH를 6.0으로 조정하고, 이 반응 혼합물을 1ℓ의 20mM 인산나트륨 및 150mM NaCl(pH 5.6)에 대하여 4℃에서 밤새 투석시킨다. DT를 유사하게 처리한다.
환원된 펩타이드 용액: 각각의 접합 반응에 대해서, 펩타이드 3mg을 100㎕의 0.1M 베타-머캅토에탄올에 용해시킨다. 1시간 동안 항온처리하여 펩타이드를 환원시킨 후, 이 반응 혼합물을 SpeedVac 원심분리기에서 건조시킴으로써 환원제를 제거한다. 펩타이드를 증류수 0.5ml에 재용해시키고, 펩타이드가 완전히 용해될 때까지 이에 5㎕ 분액의 1N NaOH를 가한다. DT를 사용한 접합 실험의 경우에는, 펩타이드 6mg을 환원시킨 다음, 물 1ml에 재용해시킨다.
활성화된 운반 단백질 용액의 pH를 0.1N NaOH를 사용하여 6.8로 조정한다. 활성화된 운반 단백질 3mg을 함유하는 용액을 실온에서 3시간 동안 지속적으로 혼합하면서 환원된 펩타이드 용액 0.5ml(또는 DT와의 접합체를 제조하는 경우에는 환원된 펩타이드 용액 1ml)와 반응시킨다. 반응되지 않은 펩타이드를 제거하기 위해, 이와 같이 생성된 접합체-함유 용액을 1ℓ의 20mM 인산나트륨 및 150mM NaCl(pH 7)에 대하여 4℃에서 밤새 투석시킨다. 단백질 농도를 BCA 검정에 의해 측정한다. 이러한 과정에 의해 달성된 접합 효율은 방사선 표지된 NP.B 펩타이드를 이용하는 종래의 선행 실험에서 측정되었다. 펩타이드:단백질 비는 NP.B-Hsp71 접합체(71.NP)에 대해서는 17.5이고 NP.B-DT(DT.NP)에 대해서는 10.1인 것으로 밝혀졌다.
실시예 3
Hsp-E6 및 Hsp-E7 융합 유전자의 제조
세균성 발현 벡터
pET65H
의 제조
플라스미드 RIB 1300은 미코박테륨 보비스 BCG hsp65 유전자를 함유한다[참조: Thole, J.E.R. et al., J. Exp. Med. 178:343-8(1993)]. 이러한 hsp65 유전자 증폭용 프라이머 쌍을 자동화된 올리고뉴클레오티드 합성기에서 합성하고 통상적인 과정을 이용하여 정제한다. 정방향 프라이머는 NdeI 제한 부위를 포함하고 뉴클레오티드 서열 5' AAT CAC TTC CAT ATG GCC AAG ACA ATT를 갖는다. 역방향 프라이머는 정지 코돈을 플랭킹하는 EcoRI 및 NheI 부위를 포함하고 뉴클레오티드 서열 5' CGC TCG GAC GAA TTC TCA GCT AGC GAA ATC CAT GCC를 갖는다.
상기 프라이머 쌍을 이용하고 DNA 주형으로서 pRIB 1300을 사용하여 폴리머라제 연쇄 반응(PCR)을 수행한다. PCR 단편을 제한 엔도뉴클레아제 NdeI 및 EcoRI로 이중 분해하고, 통상적인 서브클로닝 과정을 사용하여 NdeI/EcoRI-이중 분해된 pET28a(Invitrogen)에 결합시킨다[참조: Maniatis et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Lab., Cold Spring Harbor, N.Y.(1989)]. 이. 콜라이 균주 DH5알파의 형질전환-적격(competent) 세포를 상기 결합 혼합물로 형질전환시키고, 100㎍/ml 앰피실린을 함유하는 한천 상에 플레이팅시킨다. 형질 전환된 세포의 콜로니를 분리하고, 플라스미드 DNA를 제조하며 이를 대상으로 하여, 제한 지도작성 및 뉴클레오티드 서열분석에 의해 hsp65 유전자와 벡터 서열의 존재 여부에 대해 분석한다. 미코박테리아 hsp65 유전자를 포함하는 정확한 작제물(pET65H로 명명)을 동정하고, 이를 hsp65 유전자의 발현 분석을 위해 이. 콜라이 균주 BL21(DE3; Novagen)내로 형질전환시킨다. 작제물 pET65H의 도식적인 지도가 도 1에 제시되어 있다. Hsp65의 발현에 대해 시험하기 위하여, 균주 BL21의 형질전환된 세균을 제조업자(Novagen)의 지시 사항에 따라서 성장시키고, 유도한 다음 수거한다. 세균을 용해시키고, 가용성 물질 뿐만 아니라 구아니디늄 하이드로클로라이드에 의해 봉입체로부터 가용화된 물질[참조: Maniatis et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Lab., Cold Spring Harbor, N.Y.(1989)]을 SDS-PAGE 상에 전기영동시키며, 이를 대상으로 하여, 미코박테리아 스트레스 단백질에 특이적인 모노클로날 항체를 사용하여 항-Hsp65 면역블롯을 수행한다.
세균에서
Hsp65
-
HPV16
E6
융합 단백질 발현용
작제물의
제조
완전한 HPV16 E6-암호화 영역을 pET65H 중의 hsp65 유전자의 카복시-말단부에 삽입한다.
플라스미드 pHPV16은 Bluescript 벡터 SK_(ATCC 45113)에 완전한 HPV16 게놈을 함유하고 있다. HPV16 게놈의 뉴클레오티드 서열에 대해서는 문헌[Seedorf et al., Virology 145:181-5(1985)]을 참조할 수 있다. 이러한 E6 유전자 증폭용 프 라이머 쌍을 자동화된 올리고뉴클레오티드 합성기에서 합성하고 통상적인 과정을 이용하여 정제한다. 정방향 프라이머는 NheI 제한 부위를 포함하고 뉴클레오티드 서열 5' AAA AGC AGA GCT AGC ATG CAC CAA AAG를 갖는다. 역방향 프라이머는 EcoRI 및 정지 코돈을 포함하고 뉴클레오티드 서열 5' CTC CAT GAA TTC TTA CAG CTG GGT를 갖는다.
상기 프라이머 쌍을 이용하고 DNA 주형으로서 pHPV16을 사용하여 폴리머라제 연쇄 반응(PCR)을 수행한다. PCR 단편을 제한 엔도뉴클레아제 NheI 및 EcoRI로 이중 분해하고, 통상적인 서브클로닝 과정을 사용하여 NheI/EcoRI-이중 분해된 pET65H에 결합시킨다[참조: Maniatis et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Lab., Cold Spring Harbor, N.Y.(1989)]. 이. 콜라이 균주 DH5알파의 형질전환-적격 세포를 상기 결합 혼합물로 형질전환시키고, 100㎍/ml 앰피실린을 함유하는 한천 상에 플레이팅시킨다. 형질전환된 세포의 콜로니를 분리하고, 플라스미드 DNA를 제조하며 이를 대상으로 하여, 제한 지도작성 및 뉴클레오티드 서열분석에 의해 hsp65-E6 융합 유전자와 벡터 서열의 존재 여부에 대해 분석한다. hsp65-E6 융합 유전자를 포함하는 정확한 작제물(pET65HE6으로 명명)을 동정하고, 이를 상기 융합 유전자의 발현 분석을 위해 이. 콜라이 균주 BL21(DE3; Novagen)내로 형질전환시킨다. 작제물 pET65HE6의 도식적인 지도가 도 2에 제시되어 있다. Hsp65-E6의 발현에 대해 시험하기 위하여, pET65HE6으로 형질전환된 균주 BL21의 세균을 제조업자(Novagen)의 지시 사항에 따라서 성장시키고, 유도한 다음 수거한다. 세균을 용해시키고, 가용성 물질 뿐만 아니라 구아니디늄 하이드로 클로라이드에 의해 봉입체로부터 가용화된 물질[참조: Maniatis et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Lab., Cold Spring Harbor, N.Y.(1989)]을 SDS-PAGE 상에서 전기영동시킨다. 표준물로서, 정제된 Hsp65를 나란히 전개시킨다. 상응하는 형질전환되지 않은 세균에 존재하지 않는 pET65HE6-형질전환된 세균으로부터의 샘플에서 본래의 Hsp65(겉보기 MW 약 56kDa)보다 약간 느리게 이동하는 강력한 쿠마시 블루-염색 밴드(겉보기 분자량(MOO) 약 73kDa)가 보이는 것으로써 Hsp65-E6 발현을 평가한다.
세균에서
Hsp65
-
HPV16
E7
융합 단백질 발현용
작제물의
제조
완전한 HPV16 E7-암호화 영역을 pET65H 중의 hsp65 유전자의 카복시-말단부에 삽입한다.
E7 유전자 증폭용 프라이머 쌍을 자동화된 올리고뉴클레오티드 합성기에서 합성하고 통상적인 과정을 이용하여 정제한다. 정방향 프라이머는 NheI 제한 부위를 포함하고 뉴클레오티드 서열 5' AAC CCA CCT GCT AGC ATG CAT GGA GAT를 갖는다. 역방향 프라이머는 EcoRI 및 정지 코돈을 포함하고 뉴클레오티드 서열 5' AGC CAT GAA TTC TTA TGG TTT CTG를 갖는다.
상기 프라이머 쌍을 이용하고 DNA 주형으로서 pHPV16을 사용하여 폴리머라제 연쇄 반응(PCR)을 수행한다. PCR 단편을 제한 엔도뉴클레아제 NheI 및 EcoRI로 이중 분해하고, 통상적인 서브클로닝 과정을 사용하여 NheI/EcoRI-이중 분해된 pET65H에 결합시킨다 이. 콜라이 균주 DH5알파의 형질전환-적격 세포를 상기 결합 혼합물로 형질전환시키고, 100㎍/ml 앰피실린을 함유하는 한천 상에 플레이팅시킨다. 형질전환된 세포의 콜로니를 분리하고, 플라스미드 DNA를 제조하며 이를 대상으로 하여, 제한 지도작성 및 뉴클레오티드 서열분석에 의해 hsp65-E7 융합 유전자와 벡터 서열의 존재 여부에 대해 분석한다. hsp65-E7 융합 유전자를 포함하는 정확한 작제물(pET65HE7로 명명)을 동정하고, 이를 상기 융합 유전자의 발현 분석을 위해 이. 콜라이 균주 BL21(DE3; Novagen)내로 형질전환시킨다. 작제물 pET65HE7의 도식적인 지도가 도 3에 제시되어 있다. Hsp65-E7의 발현에 대해 시험하기 위하여, pET65HE7로 형질전환된 균주 BL21의 세균을 통상적인 과정을 이용하여 성장시키고, 유도한 다음 수거한다. 세균을 용해시키고, 가용성 물질 뿐만 아니라 구아니디늄 하이드로클로라이드에 의해 봉입체로부터 가용화된 물질을 SDS-PAGE 상에서 전기영동시키고, 이를 대상으로 하여, HPV16 E7에 특이적인 모노클로날 항체를 사용하여 항-E7 블롯을 수행한다[참조: Zymed Laboratory Inc., 카탈로그 번호 28-0006].
실시예 4
융합 단백질의 발현 및 정제
Hsp65
-
E6
융합 단백질의 발현 및 정제: 과정 1
작제물 pET65HE6을 이. 콜라이 균주 BL21(DE3; Novagen)내로 형질전환시키고, 형질전환된 세포를 30℃에서 카나마이신 30㎍/ml를 함유하는 6ℓ 배양액의 2xYT 배지(20g 트립톤, 10g 효모 추출물, 10g NaCl/ℓ)에서 성장시킨다. 각 배양 의 경우, 밀도가 0.5(OD590)에 도달하게 되면, 0.5mM 이소프로필-티오-갈락토피라노사이드에 의해 융합 단백질의 발현을 유도하고, 상기 배양물을 37℃에서 추가로 3시간 동안 항온처리한다. 세포를 원심분리하여 수거하고, 라이소자임 200㎍/ml을 함유하는 용해 완충액(10mM 트리스-HCl, 0.5mM 베타-머캅토에탄올, pH 7.5) 90ml에 현탁시킨 다음, -70℃에서 동결시킨다. 1일 후, 동결된 세포 현탁액을 37℃-수욕에서 해동시키고, 2㎍/ml 아프로티닌, 2㎍/ml 류펩틴, 2㎍/ml 펩스타틴 및 2mM PMSF로 보충시킨다. 모든 후속 단계를 0 내지 4℃에서 수행한다. 초음파처리하여 세포를 용해시키고, 17,000rpm으로 15분 동안 원심분리(JA-17 회전기, Beckmann)하여 불용성 물질을 수집한다. 펠렛화 물질을 용해 완충액으로 2회 세척한 다음, 가용화시키고, 90ml의 완충액 A(50mM 트리스-HCl, pH 7.5, 6M 구아니디늄 하이드로클로라이드)에서 초음파처리함으로써 촉진시킨다. 불용성 물질을 앞서와 같이 원심분리하여 제거한다. 이어서, 가용화 물질을 완충액 A로 평형화시킨 니켈-충전된 금속-킬레이트화 수지(Chelating Sepharose Fast Flow; Pharmacia) 50ml를 함유하는 칼럼에 적용시킨다. 결합된 융합 단백질을 0 내지 1M NaCl 구배로 상기 수지에서 서서히 재폴딩시킨다. 이 수지를 완충액 B(1M NaCl) 5용적으로 세척하여 잔류하는 구아니디늄 하이드로클로라이드를 제거하고, 완충액 C(50mM 이미다졸, pH 7.5, 0.5mM 베타-머캅토에탄올, 150mM NaCl) 5용적으로 세척하여 오염성 단백질을 제거한다. 융합 단백질을 완충액 C에서 50 내지 500mM 선형 이미다졸 구배 6용적으로 용출시킨다. 풀링시킨 용출된 단백질을 약 40용적의 둘벡코(Dulbeco) 인산염 완충 염수(2.7mM KH2PO4, 4.3mM Na2HPO4, 2.7mM KCl, 0.137M NaCl)에 대해 밤새 투석시키고, 한외여과(Amicon, 30kDa MW 컷오프)에 의해 농축시킨 다음, 내독소 제거를 위해 둘벡코 인산염 완충 염수에서 평형화시킨 DetoxiGel 수지내로 통과시킨다.
Hsp65
-
E6
융합 단백질의 발현 및 정제: 과정 2
작제물 pET65HE6을 이. 콜라이 균주 BL21(DE3; Novagen)내로 형질전환시키고, 형질전환된 세포를 30℃에서 카나마이신 30㎍/ml를 함유하는 12ℓ 배양액의 2xYT 배지(20g 트립톤, 10g 효모 추출물, 10g NaCl/ℓ)에서 성장시킨다. 각 배양의 경우, 밀도가 0.5(OD590)에 도달하게 되면, 0.5mM 이소프로필-티오-갈락토피라노사이드에 의해 융합 단백질의 발현을 유도하고, 상기 배양물을 37℃에서 추가로 3시간 동안 항온처리한다. 세포를 원심분리하여 수거하고, 라이소자임 200㎍/ml을 함유하는 용해 완충액(10mM 트리스-HCl, 0.5mM 베타-머캅토에탄올, pH 7.5) 180ml에 현탁시킨 다음, -70℃에서 동결시킨다. 1일 후, 동결된 세포 현탁액을 37℃-수욕에서 해동시키고, 2㎍/ml 아프로티닌, 2㎍/ml 류펩틴, 2㎍/ml 펩스타틴 및 2mM PMSF로 보충시킨다. 모든 후속 단계를 0 내지 4℃에서 수행한다. 초음파처리하여 세포를 용해시키고, 17,000rpm으로 15분 동안 원심분리(JA-17 회전기, Beckmann)하여 불용성 물질을 수집한다. 펠렛화 물질을 용해 완충액으로 2회 세척한 다음, 가용화시키고, 180ml의 완충액 A(50mM 트리스-HCl, pH 7.5, 6M 구아니디늄 하이드로클로라이드)에서 초음파처리함으로써 촉진시킨다. 불용성 물질을 앞서와 같이 원 심분리하여 제거한다. 이어서, 가용화 물질을 완충액 A로 평형화시킨 니켈-충전된 금속-킬레이트화 수지(Chelating Sepharose Fast Flow; Pharmacia) 50ml를 함유하는 칼럼에 적용시킨다. 결합된 단백질을 완충액 D(5% 트리톤 X100을 갖는 완충액 A)로 세척한 다음, 0 내지 1M NaCl 구배로 상기 수지에서 서서히 재폴딩시킨다. 이 수지를 완충액 E(1M NaCl, 1% 트리톤 X100) 5용적 및 완충액 B(1M NaCl) 5용적으로 세척하여 잔류하는 구아니디늄 하이드로클로라이드를 제거하고, 완충액 F(50mM 이미다졸, pH 7.5, 0.5mM 베타-머캅토에탄올, 0.5M NaCl, 15% 글리세롤) 5용적으로 세척하여 오염성 단백질을 제거한다. 융합 단백질을 완충액 F에서 50 내지 500mM 선형 이미다졸 구배 6용적으로 용출시킨다. 수집한 용출된 단백질을 40용적의 완충액 G(30mM 트리스-HCl, pH 6.5, 2mM EDTA, 5mM 베타-머캅토에탄올, 15% 글리세롤)에 대해 밤새 투석시키고, 동일한 완충액에서 평형화시킨 50ml SP-세파로즈 칼럼에 적용시킨다. 융합 단백질(분획화되지 않은 추출물에 존재하는 총 융합 단백질의 약 50%를 나타내는 약 42mg)을 관류 분획으로 회수하고, 약 40용적의 둘벡코 인산염 완충 염수(2.7mM KH2PO4, 4.3mM Na2HPO4, 2.7mM KCl, 0.137M NaCl)에 대해 밤새 투석시키고, 한외여과(Amicon, 30kDa MW 컷오프)에 의해 농축시킨다.
Hsp65-E7 융합 단백질을 동일한 과정으로 발현 및 정제시킨다. 융합 단백질의 순도는 SDS-PAGE 및 겔의 쿠마시 블루 염색에 의해 평가한다. 상기 단백질은 전형적으로 과정 1 후에는 순도가 70 내지 90%이고, 바람직한 과정 2 후에는 약 95%이다. 과정 2를 이용하여 정제한 후의 내독소 수준은 20EU/mg 단백질 이하이다.
실시예 5
Hsp65-E6 및 Hsp65-E7을 사용한 면역화
6주 내지 8주생 암컷 C57/BL/6 마우스를 공급업자[Charles River Laboratory; St. Constant, Quebec, Canada]로부터 구입한다. 1그룹당 6 내지 8마리인 마우스 그룹에게, 실시예 4에 기재된 바와 같이 정제된 둘벡코 인산염 완충 염수 중의 동일량의 Hsp65-E6과 Hsp65-E7 융합 단백질을 상기 동물의 목덜미로 피하 주사하여 면역시킨다. 투여된 총 융합 단백질의 용량은 각각 20㎍ 또는 200㎍이다. 염수 중의 프로인트 불완전 아주반트(IFA)를 사용하여 음성 대조군 면역화를 수행하고, IFA 및 염수 중의 잔기 44 내지 62개를 포함하는 합성 HPV16 E7 펩타이드 100㎍을 사용하여 양성 대조군 면역화를 수행한다. 적용된 융합 단백질의 투여량에 비해, 투여된 E7 펩타이드의 양은 각각 20 또는 200배 과량으로 나타났다. 14일 후에 면역화를 반복 수행한다. 두 번째 면역시킨지 12일 후에, 세포주 TC-1의 1.3 x 103개 E7-발현 종양 세포를 마우스의 면도된 등 부위에 피하 주사함으로써 마우스를 챌린지한다. 50일 동안 2일마다 육안 관찰 및 촉진에 의거하여 종양의 존재 또는 부재로서 종양 발생률을 기록한다. HPV16 E7 단백질을 발현시키는 TC-1 종양 세포주는, 문헌[참조: Lin et al., Cancer Res. 56:21-26(1996)]에 기재된 바와 같이 HPV16 E6 및 E7 유전자와 활성화된 사람 c-Ha-ras 유전자로 면역 및 형질전환시킴으로써 C57/BI/6 마우스의 1차 폐 세포로부터 유도한다. 종양 접종을 위해, 공급업자[Dr. T.-C. Wu(The Johns Hopkins Medical Institutions, Baltimore, MD)]에 의해 공급된 TC-1 세포를, 10% 태내 송아지 혈청(Hyclone, Logan, UT), 비필수 아미노산, 글루타민, 피루베이트, 겐타마이신, 베타-머캅토에탄올, 0.4mg/ml 제네티신R(Life Technologies, Grand Island, N.Y.) 및 0.2mg/ml 하이그로마이신 B가 보충된 RPMI1640 배지에서 60 내지 70% 컨플루언스(confluence)에 이르도록 37℃에서 성장시킨다. 세포를 트립신 처리하여 수거하고 한크(Hank) 완충 용액에서 6.5 x 105개 세포/ml로 재현탁시킨다.
당해 실험 결과가 도 4에 제시되어 있다. 챌린지 직후, 모든 처리 그룹에서 종양 발생률이 증가하였다(챌린지 후 5 내지 15일). IFA 그룹의 경우에는 발생률이 높게 유지되는 반면, 융합 단백질 혼합물 200㎍으로 처리되거나 IFA 중의 E7 펩타이드로 처리된 그룹의 경우에는 발생률이 0%로 현격하게 저하되었다. 융합 단백질 20㎍으로 처리된 그룹의 경우에 중간 정도의 결과가 획득되었다. 따라서, 어떠한 아주반트의 부재하에서도 Hsp65-E6 및 Hsp65-E7 융합 단백질 혼합물로 면역시킬 경우, E7-발현 종양 세포를 사용한 치명적인 챌린지로부터 마우스를 효과적으로 보호할 수 있다. 당해 결과에 관한 요약이 표 1에 제시되어 있다.
| 면역화 그룹 | 종양 발생률* | |
| 첫 번째 챌린지 후(54일째) | 두 번째 챌린지 후(79일째) | |
| IFA 또는 없음** | 83(5/6) | 100(4/4) |
| 마이크로그램 융합 단백질 | 25(2/8) | 25(1/4) |
| 마이크로그램 융합 단백질 | 0(0/8) | 0(0/4) |
| IFA 중의 E7 펩타이드 | 0(0/8) | 0(0/4) |
| * 괄호안에는, 종양을 나타낸 동물의 수/그룹당 동물의 총 수가 제시된다. 우측 칼럼에는, (두 번째 챌린지 후) 추가 25일 동안 종양의 존재 여부에 대해 알아보기 위해 동물을 모니터링한 것이다. ** 두 번째 종양 챌린지에 대한 대조군으로서, 면역시키지 않은 동물 그룹이 비교용으로 포함된다. | ||
실시예 6
면역시킨 동물의 종양 세포로의 두 번째 챌린지에의 노출
HPV 항원에 대한 면역 반응의 존속을 평가하기 위해, 앞선 실험으로부터(54일째) 즉, 융합 단백질-처리된 그룹과 E7 펩타이드/IFA 그룹 모두로부터의 생존한 4마리의 동물 그룹들을 동물당 1.3 x 105개의 살아 있는 TC-1 종양 세포로 두 번째 챌린지한다. 대조군으로서, 실험 투약된 바는 없고 동일한 종양 챌린지에만 노출된 마우스 그룹이 포함된다. 25일 후에 종양 발생률을 평가한다.
결과가 표 1에 제시되어 있다. 융합 단백질로 미리 면역되거나 E7 펩타이드/IFA로 미리 면역된 동물은 두 번째 챌린지로부터 완전하게 또는 거의 완전하게 보호된 반면, 면역되지 않은 동물은 100% 종양 발생률을 나타내었다.
실시예 7
*면역된 동물과 면역되지 않은 동물로부터의 비장 세포의 세포용해 활성
융합 단백질 면역되거나, 펩타이드 면역되거나 면역되지 않은 2마리 마우스 동물 그룹을 경부 탈구시킴으로써 안락사시키고 이들의 비장을 꺼낸다. 수집된 비장의 단일 세포 현탁액을 제조하고 5% 태내 송아지 혈청이 보충된 한크 완충 용액에서 1회 세척한다. 20 x 106개 생존 세포를, 37℃ 및 5% CO2하에서 10% 태내 소 혈청, 2mM L-글루타민, 1mM 피루브산나트륨, 50μM 2-머캅토에탄올 및 50㎍/ml 겐타마이신 설페이트가 보충된 RPMI-1640 배지에서 5일 동안 2 x 106개 미토마이신 C-처리된 TC-1 세포와 함께 배양함으로써, 임파양 세포를 재자극한다. 이어서, 상기 비장 세포(효과기 세포)를 수거하고 이를 다음에 기재된 CTL 활성 검정에 사용한다.
E7 에피토프를 발현시키지 않는, TC-1 및 HLA 유형-일치된 세포주 EL4 및 MC57G를 표적 세포로서 사용한다. 세포를 150μCi Na2 51CrO4와 함께 90분 동안 항온처리하고, EL4 세포의 경우에는 106개 세포당 10㎍의 인플루엔자 바이러스 핵단백질 펩타이드3 66 -374와 함께 항온처리한다. 집중적으로 세척하여 과량의 방사성 표지를 제거한 후, 5 x 103개 표지된 표적 세포를 다양한 효과기 세포:표적 세포 비로 재자극된 효과기 세포와 함께 공동-배양한다. 항온처리한지 4 내지 5시간 후, 배양 플레이트를 200xg으로 5분 동안 원심분리하고, 세포로부터 방출된 방사성 표지를 함유하는 상등 용액 100㎕ 분액을 벡크만 레디 캡스(Beckman Ready Caps)에 수집한다. 액체 신틸레이션 계수로 방사능을 측정한다. 자발적으로 방출된 방사능 및 총 방출가능한 방사능을 측정하기 위하여, 표적 세포만을 함유하는 배양액으로부터 또는 트리톤 X100의 첨가에 의해 용해된 표적 세포로부터의 상등 용액을 수집하고, 방사능을 앞서와 같이 측정한다. 결과는 다음 식을 기준으로 하여 산정된, 보정된 용해율(%)로서 표현된다:
보정된 용해율(%) = 100 x (cpmtest - cpmspont)/(cpmtotal - cpmspont)
상기식에서, cpmtest는 특정한 공동-배양물로부터 방출된 방사능이고, cpmspont는 표적 세포 배양물의 자발적으로 방출된 방사능이며, cpmtotal은 표적 세포의 트리톤 X100 용해에 의해 방출된 방사능이다. CTL 검정을 3회 수행하고 이의 평균값을 제공한다.
표적 세포로서 TC-1 세포를 사용하는 실험 결과가 도 5에 제시되어 있다. TC-1 세포의 40% 및 25% 용해율은 융합 단백질 200㎍ 및 20㎍으로 각각 면역된 동물로부터 수득된 효과기 세포(표적 세포에 비해 100배 과량으로 사용)에 의해 매개된다.
두 번째 실험에서는, 융합 단백질 20㎍으로 면역시킨 동물로부터의 비장 세포를 사용하여 CTL 활성의 특이성을 시험한다. 도 6에 제시된 결과는 HPV16 E6/E7-형질전환된 TC-1 세포의 효과적인 용해를 입증한다. HPV 항원을 발현시키지 않는 2가지 상이한 세포 유형(EL4 및 MC57G)의 용해는 훨씬 저하된 효율로 이루어지는데, 이는 Hsp65-E6 및 -E7 융합 단백질로의 면역에 의해 유도된 CTL 반응의 특이성을 입증한다.
실시예 8
Hsp65-E7 융합 단백질로의 처리 후 마우스 중에서의 TC-1 종양의 퇴행
8마리 C57/BL/6 마우스의 3그룹을 본 실험에 사용한다. 각 동물의 면도된 등 부위에 1.3 x 105개 TC-1 세포를 피하 접종한다. 2일 후, 제1 그룹에게 염수를 투여하고(음성 대조군), 제2 그룹에게는 염수 중의 Hsp65-E7 융합 단백질 100㎍/동물을 투여하며, 제3 그룹에게는 염수 및 IFA 중의 E7 펩타이드 100㎍/동물을 투여한다(양성 대조군). 모든 주사액(0.2ml)은 목덜미에 피하 투여한다. 14일 후(종양 접종한지 16일 후), 주사를 반복한다. 종양 접종한지 1일 후부터 시작하여 그 후 2일마다, 마우스를 대상으로 하여 육안 검사 및 촉진에 의해 종양의 존재 여부를 검사한다.
도 7은 종양 접종한지 9일 후에 처리 그룹 모두가 85 내지 100% 범위의 최대 종양 발생률(종양을 나타내는 동물의 비율로서 표현됨)을 나타냈음을 보여준다. 그러나, 17일째, Hsp65-E7 융합 단백질로 처리된 그룹 뿐만 아니라 IFA 중의 E7 펩타이드로 처리된 그룹에서의 종양 발생률이 약 15% 수준으로 상당히 감소된 것으로 나타났다. 이와는 달리, 염수 처리된 그룹은 나머지 관찰 기간 내내 거의 100%의 종양 발생률을 계속해서 나타내었다. 이들 결과는 아주반트의 부재하에서 투여된 Hsp65-E7 융합 단백질이 HPV-유도된 종양의 현격한 퇴행을 유도한다는 것을 입증한다.
유사한 실험으로부터의 결과가 도 8에 제시되어 있다. 이 실험에서는, 동물에게 앞의 실험에서보다 높은 종양 용량(2 x 105개/동물)을 접종하였다. 수득된 결과는 앞의 실험 결과와 매우 유사하다.
실시예 9
세포성 면역 반응을 유도하는 E7 단백질과 Hsp65-E7 융합 단백질의 능력 비교
Hsp65-E7 융합 단백질을 제조하고 이를 실시예 4에 기재된 바와 같이 정제한다. 다음 과정에 의해 완전한 길이의 HPV E7 단백질을 수득한다.
AmpliTaq DNA 폴리머라제(Perkin Elmer)를 사용하여 HPV16 게놈 DNA(아메리칸 티슈 컬쳐 컬렉션(American Tissue Culture Collection)으로부터 구입된 pSK/HPV16)로부터 E7 유전자를 증폭시킨다. 정방향 프라이머(5'-AAC CCA GCT GCT AGC ATG CAT GGA GAT-3')는 ATG 개시 코돈의 바로 상류에 NheI 부위를 함유하는 반면, 역방향 프라이머(5'-AGC CAT GAA TTC TTA TGG TTT CTG-3')는 E7-암호화 서열의 TAA 정지 코돈 바로 하류에 EcoRI 부위를 함유한다. PCR 생성물을 NheI 및 EcoRI으로 분해하고, 아가로즈 겔로부터 정제하여, 동일한 제한 효소로 분해한 pET28a에 결합시킨다. 세균의 형질전환, 재조합체 함유 콜로니의 분리 및 증대된 콜로니로부터의 플라스미드 DNA의 제조를 표준 과정에 의해 수행한다[참조: Ausubel et al.(eds.), Short Protocols in Molecular Biology, 3rd Edition(John Wiley & Sons, Inc. 1995)]. 생성된 플라스미드 작제물 pET/E7(H)의 동정은 진단적 제한 분해 및 DNA 서열 분석으로 확인한다. pET/E7(H)의 도식적인 지도가 도 9에 제시되어 있다.
30㎍/ml 카나마이신을 함유하는 2xYT 배지 12ℓ를, pET/E7(H)를 함유하는 이. 콜라이 BL21(DE3)의 배양물에 접종하고 이를 통기시키면서 30℃에서 밤새 항온처리한다. 광학밀도가 0.5에 도달하게 되면, 배양을 0.5mM IPTG로 3시간 동안 유도한다. 이어서, 세포를 원심분리하여 수거하고, 라이소자임 200㎍/ml이 보충된 용해 완충액(10mM 트리스-HCl, pH 7.5, 0.5mM 2-머캅토에탄올) 180ml에 재현탁시킨 다음, -70℃에서 밤새 동결시킨다. 세포 현탁액을 2㎍/ml 아프로티닌, 2㎍/ml 류펩틴 및 2㎍/ml 펩스타틴의 존재하에 37℃ 수욕에서 해동시킨다. 2mM PMSF를 가한 후, 세포 현탁액을 격렬하게 초음파처리하고, 원심분리하여 불용성 물질을 수집한다. 단백질 펠렛을 용해 완충액에 2회 재현탁시키고, 재초음파처리한 다음 원심분리하여 재수집한다. 이어서, 단백질 펠렛을 완충액 A(50mM 트리스-HCl, pH 7.5, 6M 구아니디늄 하이드로클로라이드, 1mM 2-머캅토에탄올)에서 초음파처리함으로써 가용화시키고, 불용성 물질을 원심분리하여 제거한다. 이어서, 가용화 단백질을 완충액 A로 예비평형화시킨 Ni-킬레이트화 칼럼(2.6cm x 12cm; Pharmacia) 50ml에 적용시킨다. 결합된 단백질을 완충액 E(2% 트리톤 X100을 함유하는 완충액 A) 5충전 용적(bed volume)으로 세척한 다음, 1% 트리톤 X-100의 존재하에서 구아니디늄 하이드로클로라이드-염화나트륨 구배(0.1M NaCl/6.0M 구아니디늄 하이드로클로라이드; 5충전 용적)로 재폴딩시킨다. 이와 같이 재폴딩된 단백질을 완충액 F(30mM 트리스-HCl, pH 7.5, 1M NaCl, 15% 글리세롤, 2% 트리톤 X100, 1mM 2-머캅토에탄올) 5충전 용적으로 세척한 다음, 완충액 G(트리톤 X-100을 함유하지 않는 완충액 F) 5충전 용적으로 세척하여 트리톤 X-100을 제거한다. 이 칼럼을 완충액 H(50mM 이미다졸, pH 7.5, 0.5M NaCl, 15% 글리세롤, 1mM 2-머캅토에탄올) 5충전 용적으로 추가로 세척하여 약하게 결합된 단백질을 제거한다. E7 단백질을 선형 이미다졸 구배(완충액 H 중의 50mM 내지 1M 이미다졸)로 용출시킨다. E7 단백질을 농축시키고, 25% 글리세롤이 보충된 둘벡코 인산염 완충 염수에 대해 투석시킨다. 가용성 단백질을 -70℃에서 저장한다. 상기 E7 제제는 SDS-PAGE 및 단백질 염색에 의해 본질적으로 동종인 것으로 밝혀졌다.
상기 단백질 제제의 내독소 농도는 리물러스 변형세포 검정으로 평가한 결과, 단백질 1mg당 50 이하의 내독소 단위가 존재하는 것으로 밝혀졌다.
5마리 C57/BL/6 마우스 그룹을, 이의 꼬리 하부에 염수를 주사하거나, 염수 중의 E7 단백질 또는 Hsp65-E7 융합 단백질 0.055, 0.55 또는 1.8나노몰을 주사함으로써 면역시킨다. 주사 용량은 0.2ml이다. 10일 후, 서혜부 림프절(LN)을 각 동물로부터 무균적으로 꺼내고, 한 그룹의 5마리 동물 각각으로부터의 LN을 수집한다. 세포 현탁액을 표준 과정으로 제조한다. LN 세포의 각 수집물(2 x 106개 세포/ml)에 대해, 평저 96-웰 플레이트에 4 x 105개 세포/웰을 씨딩(seeding)한다. 배지, 10 또는 50㎍/ml E7 단백질, 10 또는 100㎍/ml Hsp65-E7 융합 단백질, 또는 1 또는 10㎍/ml E7 펩타이드("pep": 잔기 44-57개)의 첨가에 대한 증식 반응을 알아보기 위하여 세포를 3회 시험한다. 부가 후, 세포를 37℃ 및 5% CO2에서 4일 동안 항온처리한다. 3중 수소화 티미딘(1μCi)을 각 배양물에 가한다. 추가로 항온처리한지 15시간 후에, 세포를 수거하고 신틸레이션 계수용으로 준비한다. 데이타는 혼입된 방사능의 평균 cpm ±표준 편차로서 도 10에 제시되어 있다.
상이한 패널은 상기 인용된 Hsp65-E7 융합 단백질 또는 E7 단백질의 상이한 양으로 면역된 동물로부터의 LN 세포를 사용한 검정을 제시한다. 그 결과는 Hsp65-E7 융합 단백질을 사용한 면역화가 이러한 융합 단백질 자체에 대한 세포 면역성(상단 및 중간 좌측) 뿐만 아니라 E7 단백질에 대한 세포 면역성(중간 좌측)을 유도한다는 것을 나타낸다. E7 단백질의 인식은 E7 펩타이드에 의한 관찰된 증식 유도로써 추가로 입증되며, 상기 펩타이드는 T 헬퍼 세포 에피토프를 나타내는 것으로 공지되어 있다(중간 좌측). 이와는 달리, 상이한 양의 E7 단백질로 면역시키거나(중간 우측 및 하단) 염수로 의사-면역시킨 동물로부터의 LN 세포를 사용한 경우에는 증식 반응이 전혀 관찰되지 않았다. E7 단백질-면역된 동물로부터 제조된 세포는 T 세포 미토겐 ConA에 대한 반응에서 증식하는 이들의 능력으로 입증된 바와 같이 생존가능하다. 요약하면, E7 단백질을 사용한 면역과 비교할 경우, Hsp65-E7 융합 단백질을 사용한 면역은 면역된 동물로부터의 LN 세포의 증식으로 평가된 바와 같이 E7에 비해 탁월한 세포 면역 반응을 유도한다.
실시예 10
Hsp65-E7 융합 단백질로의 처리는 상당한 크기로 확립된 종양의 퇴행을 유발한다
종양 치료에서의 Hsp65-E7 융합 단백질의 효능을 시험하기 위하여, C57/BL/6 마우스의 면도된 등 부위에 피하 주사로 1.3 x 105개 TC-1 종양 세포를 접종한다. 7일 후에, 모든 동물에게서 촉진가능하고/측정가능한 종양이 발생된 경우, 동물을 임의로 3가지 처리 그룹에 할당한다. 각 그룹은 12 내지 14마리 동물을 포함한다. 모든 처리는 목덜미에 0.2ml 용량을 피하 주사하는 것이다. 제1 그룹에게는 100㎍ Hsp65-E7 융합 단백질을 주사하고, 제2 그룹에게는 20㎍ E7 단백질(100㎍ 융합 단백질과 유사한 몰량에 상응함)을 주사하며, 제3 그룹에게는 염수를 주사한다. 종양 접종한지 1일 후부터 시작하여, 마우스를 대상으로 하여 종양의 존재 여부를 알아보기 위해 육안으로 검사하고 촉진한다. 두 직각 방향으로 캘리퍼스를 이용하여 종양 용적을 측정한다. 문헌[참조: Naito et al., Cancer Research 46:4109(1986)]에 기재된 환산식을 이용하여 이들 측정치로부터 용적을 수득한다. 결과는 각 그룹에서의 평균 종양 용적 ± 표준 오차로서 도 11에 제시되어 있다.
이 결과는, Hsp65-E7 융합 단백질로 처리할 경우, 상당한 크기로 확립된 종양이 완전히 퇴행됨을 입증한다. 이러한 효과는 처리된 각각의 동물에서 명백히 나타난다. 이와는 달리, 의사-처리 뿐만 아니라 E7 단백질을 사용한 처리는 어느 것도 종양의 일시적인 퇴행 이상은 유발하지 못하였다. 본 실험에서 3회 시점 말기에 수행된 통계적인 평가가 표 2에 제시되어 있다. 산정된 p값으로부터 명백한 바와 같이, Hsp65-E7 융합 단백질을 사용한 처리가 종양 크기에 미치는 효과는 다른 처리의 효과와 통계적으로 상이하다.
| 비교 | 측정일 | p값 |
| 염수 대 Hsp65-E7 | 30 | 0.048 |
| 33 | 0.079 | |
| 35 | 0.046 | |
| 염수 대 E7 | 30 | 0.853 |
| 33 | 1 | |
| 35 | 0.86 |
앞의 실시예에서는, Hsp65-E7 단백질이 히스티딘-태그 부착된 단백질로서 생성되었다는 것을 인지해야 한다. 관찰된 치료학적 효과가 어떠한 방식으로든 융합 단백질내에 올리고-히스티딘 서열이 존재하는 것과 관련이 없다는 것을 명백히 입증하기 위해, 히스티딘 태그가 결여된 Hsp65-E7 융합 단백질을 제조하고 이를 본 실시예에 사용한다. 다음 과정을 이용하여 상기 융합 단백질을 수득한다.
플라스미드 ET65C(도 12)를 작제하기 위하여, AmpliTaq DNA 폴리머라제(Perkin Elmer)를 사용하여 플라스미드 RIB 1300(Van Eden et al., Nature 331:171, 1988)으로부터 BCG(Bacillus Calmette Guerin) hsp65 유전자를 증폭시킨다. 사용된 정방향 프라이머(5'-TTC GCC ATG GCC AAG ACA ATT GCG-3')는 hsp65 유전자의 ATG 개시 코돈을 포함하는 NdeI 부위를 함유하고, 역방향 프라이머(5'-CGC TCG GAC GCT AGC TCA CAT ATG GAA ATC CAT GCC-3')는 Hsp65-암호화 서열의 TGA 정지 코돈으로부터의 바로 하류에 NdeI 부위를 함유하고 바로 하류에 NheI 부위를 함유한다. PCR 생성물을 NcoI 및 NheI로 분해하고, 아가로즈 겔로부터 정제하여, 유사하게 분해한 pET28a에 결합시킨다. 상기 결합 혼합물을 이. 콜라이 DH5α내로 형질전환시키고, 항생제-내성 콜로니를 분리하여, 플라스미드 DNA의 제조를 위해 증폭시킨다. 진단적 제한 분해 및 DNA 서열 분석으로 플라스미드 ET65C를 동정한다.
태그가 부착되지 않은 Hsp65-E7 융합 단백질 유전자를 함유하는 플라스미드 ET65C/E7-1N을 제조하기 위하여, AmpliTaq DNA 폴리머라제(Perkin Elmer)를 사용하여 HPV16 게놈 DNA(아메리칸 티슈 컬쳐 컬렉션으로부터 수득된 pSK/HPV16)로부터 E7 유전자를 증폭시킨다. 정방향 프라이머(5'-CCA GCT GTA CAT ATG CAT GGA GAT-3')는 ATG 개시 코돈을 포함하는 NdeI 부위를 함유하는 반면, 역방향 프라이머(5'-AGC CAT GAA TTC TTA TGG TTT CTG-3')는 E7-암호화 서열의 TAA 정지 코돈 바로 하류에 EcoRI 부위를 함유한다. PCR 생성물을 NdeI 및 EcoRI로 분해하고, 아가로즈 겔로부터 정제하여, 동일한 제한 효소로 분해한 pET65C에 결합시킨다. 세균의 형질전환, 재조합체 함유 콜로니의 분리 및 증대된 콜로니로부터의 플라스미드 DNA의 제조를 표준 과정에 의해 수행한다[참조: Ausubel et al.(eds.), Short Protocols in Molecular Biology, 3rd Edition(John Wiley & Sons, Inc. 1995)]. 생성된 플라스미드 작제물 pET65C/E7-1N의 동정은 진단적 제한 분해 및 DNA 서열 분석으로 확인한다. pET65C/E7-1N의 도식적인 지도가 도 13에 제시되어 있다.
30㎍/ml 카나마이신을 함유하는 2xYT 배지 12ℓ를 pET65C/E7-1N를 함유하는 이. 콜라이 BL21(DE3)의 배양물에 접종하고 이를 통기시키면서 30℃에서 밤새 항온처리한다. 광학밀도가 0.5에 도달하게 되면, 배양을 0.5mM IPTG로 3시간 동안 유도한다. 이어서, 세포를 원심분리하여 수거하고, 라이소자임 200㎍/ml이 보충된 용해 완충액(10mM 트리스-HCl, pH 7.5, 0.5mM 2-머캅토에탄올) 180ml에 재현탁시킨 다음, -70℃에서 밤새 동결시킨다. 세포 현탁액을 2㎍/ml 아프로티닌, 2㎍/ml 류펩틴 및 2㎍/ml 펩스타틴의 존재하에 37℃ 수욕에서 해동시킨다. 2mM PMSF를 가한 후, 세포 현탁액을 격렬하게 초음파처리하고, 원심분리하여 불용성 물질을 제거한다. 태그가 부착되지 않은 Hsp65-E7 단백질의 대부분이 가용성 단백질 분획내에서 발견되었다. 내독소를 제거하기 위해, 1% 트리톤 X-114를 가용성 단백질 분획에 가하고, 이 혼합물을 얼음 상에서 냉각(5분 이상 동안)시킨 다음, 철저하게 혼합한다. 이어서, 상기 혼합물을 30℃ 수욕에서 10분 동안 가온시킨 다음, 24℃에서 원심분리한다. 청정한 상등액 분획(상부 층)을 깨끗한 튜브에 옮긴다. 원심분리를 3 내지 6회 반복하여 잔류하는 트리톤 X-114를 제거한다. 이어서, 상기 상등액 분획을 황산암모늄 분획화에 적용시킨다. 융합 단백질을 0 내지 15% 황산암모늄(w/v) 분획으로 회수한다. 침전된 단백질을 완충액 B(30mM 트리스-HCl, pH 7.5, 3M 우레아, 1mM EDTA, 1mM 2-머캅토에탄올)에 용해시키고, 완충액 B로 예비평형화시킨 170ml Source Q 칼럼(3.5cm x 20cm; Pharmacia)에 적용시킨다. 이 칼럼을 3충전 용적의 완충액 C(우레아를 제거한 완충액 B)로 세척한 다음, 3충전 용적의 완충액 D(250mM NaCl이 보충된 완충액 C)로 세척한다. 융합 단백질을 선형 염 구배(완충액 C에서 250mM-1M NaCl)로 용출시킨 다음(수집물 A), 6M 구아니디늄 하이드로클로라이드(완충액 A)로 용출시킨다(수집물 B). 수집물 B를 완충액 A로 예비평형화시킨 Ni-킬레이트화 칼럼(2.6cm x 12cm; Pharmacia) 50ml에 적용시킨다. 결합된 단백질을 완충액 E(2% 트리톤-X100을 함유하는 완충액 A) 5충전 용적으로 세척한 다음, 1% 트리톤 X-100의 존재하에서 구아니디늄 하이드로클로라이드-염화나트륨 구배(0.1M NaCl/6.0M 구아니디늄 하이드로클로라이드; 5충전 용적)로 재폴딩시킨다. 이와 같이 재폴딩된 단백질을 완충액 F(30mM 트리스-HCl, pH 7.5, 1M NaCl, 15% 글리세롤, 2% 트리톤 X-100, 1mM 2-머캅토에탄올) 5충전 용적으로 세척한 다음, 완충액 G(트리톤 X-100을 함유하지 않는 완충액 F) 5충전 용적으로 세척하여 트리톤 X-100을 제거한다. 상기 칼럼을 완충액 H(50mM 이미다졸, pH 7.5, 0.5M NaCl, 15% 글리세롤, 1mM 2-머캅토에탄올) 5충전 용적으로 추가로 세척하여 약하게 결합된 단백질을 제거한다. 융합 단백질을 선형 이미다졸 구배(완충액 H에서 50mM 내지 1M 이미다졸)로 용출시킨다. 태그가 부착되지 않은 Hsp65-E7 단백질을 농축시키고, 25% 글리세롤이 보충된 둘벡코 인산염 완충 염수에 대해 투석시킨다. 가용성 단백질을 -70℃에서 저장한다. SDS-PAGE 및 단백질 염색에 의한 분석 결과, 상기 제제의 순도가 약 90%인 것으로 나타났다.
히스티딘 태그가 중요하지 않음을 추가로 입증하기 위하여, 히스티딘 태그가 부착된 Hsp65-E7과 태그가 부착되지 않은 Hsp65-E7의 효능을 상기된 바와 상당히 동일한 실험으로 직접적으로 비교한다. 두 융합 단백질이 유사한 효능으로 종양을 퇴행시키는 것으로 밝혀졌다.
등가물
당해 분야의 숙련인은 단지 통상적인 실험 수준을 이용하여 본원에 기재된 본 발명의 구체적인 양태에 등가 수준인 많은 양태를 인지하고 있거나 이를 확인할 수 있을 것이다. 이들 및 기타 모든 등가물은 다음 청구의 범위에 의해 포괄되는 것으로 간주된다.
스트레스 단백질과 HPV 단백질 항원의 융합 단백질이 제공되어 이는 피검체에 투여하는 경우 강력한 세포용해성 면역반응을 유도할 수 있다.
Claims (15)
- 사람 유두종 바이러스(HPV) 단백질 항원 또는 이의 일부, 및 이에 펩타이드 결합을 통해 공유적으로 결합된 포유동물의 스트레스 단백질 또는 이의 일부를 포함하는 융합 단백질로서, 이것이 투여된 피험체내에서 HPV 단백질 항원 또는 이의 일부에 대한 면역 반응을 유도하고, 상기 스트레스 단백질의 부분이 HPV 단백질 항원 또는 이의 일부에 대한 면역 반응을 유도하거나 증강시키는, 융합 단백질.
- 제1항에 있어서, 당해 스트레스 단백질 또는 이의 일부가 Hsp10, Hsp60, Hsp70, Hsp90, 또는 소분자량 계열의 스트레스 단백질내에 존재하는 융합 단백질.
- 제1항에 있어서, 당해 스트레스 단백질 또는 이의 일부가 다음 계열의 스트레스 단백질: Hsp100-200, Hsp100, Hsp40, FKBP, 사이클로필린, Hsp20-30, 우비퀴틴, 칼넥신, 또는 단백질 디설피드 이소머라제 계열중의 하나내에 존재하는 융합 단백질.
- 제1항에 있어서, HPV 단백질 항원 또는 이의 일부가 L1, L2, E1, E2, E4, E5, E6, E7, 또는 바이러스 캡시드 단백질 항원 또는 이의 일부인 융합 단백질.
- 제1항에 있어서, HPV 단백질 항원 또는 이의 일부가 E6 또는 E7 단백질 항원 또는 이의 일부이고, 당해 스트레스 단백질 또는 이의 일부가 Hsp60 또는 Hsp 70 스트레스 단백질 또는 이의 일부인 융합 단백질.
- 제1항에 있어서, HPV 단백질 항원이 전체 길이의 HPV 단백질 항원인 융합 단백질.
- 제1항에 있어서, 당해 스트레스 단백질이 전체 길이의 스트레스 단백질인 융합 단백질.
- 제1항 내지 제7항 중의 어느 한 항에 따른 융합 단백질을 암호화하는 핵산 분자.
- 제1항 내지 제7항 중의 어느 한 항에 따른 융합 단백질을 포함하는, HPV 단백질 항원에 대해 면역 반응을 유도하기 위한 조성물.
- 제8항에 있어서, 발현 벡터를 추가로 포함하는 핵산 분자.
- 제10항에 있어서, 발현 벡터가 pET65HE6인 핵산 분자.
- 제10항에 있어서, 발현 벡터가 pET65HE7인 핵산 분자.
- 제9항에 있어서, 면역 반응이 세포성 면역 반응인 조성물.
- 제9항에 있어서, 면역 반응이 체액성 면역 반응인 조성물.
- 제9항에 있어서, 아주반트, 계면활성제, 부형제, 담체 또는 희석제를 추가로 포함하는 조성물.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US5483597P | 1997-08-05 | 1997-08-05 | |
| US60/054,835 | 1997-08-05 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020007001231A Division KR100843109B1 (ko) | 1997-08-05 | 1998-03-20 | 사람 유두종 바이러스 항원과 스트레스 단백질을 포함하는 융합 단백질을 포함하는 조성물에 의해 유도된 사람 유두종 바이러스 항원에 대한 면역 반응 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20060111731A true KR20060111731A (ko) | 2006-10-27 |
Family
ID=21993829
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020007001231A KR100843109B1 (ko) | 1997-08-05 | 1998-03-20 | 사람 유두종 바이러스 항원과 스트레스 단백질을 포함하는 융합 단백질을 포함하는 조성물에 의해 유도된 사람 유두종 바이러스 항원에 대한 면역 반응 |
| KR1020067019653A KR20060111731A (ko) | 1997-08-05 | 1998-03-20 | 사람 유두종 바이러스 항원과 스트레스 단백질을 포함하는융합 단백질을 포함하는 조성물에 의해 유도된 사람 유두종바이러스 항원에 대한 면역 반응 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020007001231A KR100843109B1 (ko) | 1997-08-05 | 1998-03-20 | 사람 유두종 바이러스 항원과 스트레스 단백질을 포함하는 융합 단백질을 포함하는 조성물에 의해 유도된 사람 유두종 바이러스 항원에 대한 면역 반응 |
Country Status (19)
| Country | Link |
|---|---|
| US (4) | US6524825B1 (ko) |
| EP (1) | EP1002110B2 (ko) |
| JP (2) | JP4198315B2 (ko) |
| KR (2) | KR100843109B1 (ko) |
| CN (3) | CN1680451A (ko) |
| AT (2) | ATE231917T1 (ko) |
| AU (1) | AU6492498A (ko) |
| BR (1) | BR9812272A (ko) |
| CA (1) | CA2298840A1 (ko) |
| DE (2) | DE69811087T2 (ko) |
| DK (1) | DK1002110T3 (ko) |
| ES (2) | ES2191929T3 (ko) |
| HK (2) | HK1028981A1 (ko) |
| HU (1) | HUP0003601A3 (ko) |
| IL (1) | IL134341A0 (ko) |
| NZ (3) | NZ502568A (ko) |
| PL (1) | PL196805B1 (ko) |
| PT (2) | PT1002110E (ko) |
| WO (1) | WO1999007860A1 (ko) |
Families Citing this family (75)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE212378T1 (de) | 1993-06-04 | 2002-02-15 | Whitehead Biomedical Inst | Stressproteine und ihre verwendung |
| US7157089B1 (en) | 1996-11-26 | 2007-01-02 | Stressgen Biotechnologies Corporation | Immune responses using compositions containing stress proteins |
| ES2191929T3 (es) * | 1997-08-05 | 2003-09-16 | Stressgen Biotechnologies Corp | Respuestas inmunologicas contra los antigenos pvh estimuladas por composiciones que comprenden un antigeno pvh y una proteina de estres o un vector de expresion capaz de expresar dichas proteinas. |
| US6495347B1 (en) | 1999-07-08 | 2002-12-17 | Stressgen Biotechnologies Corporation | Induction of a Th1-like response in vitro |
| US20050244434A1 (en) * | 1999-08-12 | 2005-11-03 | Cohen David I | Tat-based tolerogen compositions and methods of making and using same |
| US20050226890A1 (en) * | 1999-08-12 | 2005-10-13 | Cohen David I | Tat-based vaccine compositions and methods of making and using same |
| AUPQ233799A0 (en) | 1999-08-19 | 1999-09-09 | Minister For Agriculture, Minister For Land And Water Conservation For And On Behalf Of The State Of New South Wales | Recombinant sub-unit vaccine |
| US20050100928A1 (en) * | 1999-09-16 | 2005-05-12 | Zycos Inc., A Delaware Corporation | Nucleic acids encoding polyepitope polypeptides |
| US7378096B2 (en) | 1999-09-30 | 2008-05-27 | Health Research, Inc. | Stress protein compositions and methods for prevention and treatment of cancer and infectious disease |
| US6984384B1 (en) | 1999-09-30 | 2006-01-10 | Health Research, Inc. | Stress protein compositions and methods for prevention and treatment of cancer and infectious disease |
| AU784605B2 (en) * | 1999-10-20 | 2006-05-11 | Johns Hopkins University School Of Medicine, The | Chimeric immunogenic compositions and nucleic acids encoding them |
| US8128922B2 (en) | 1999-10-20 | 2012-03-06 | Johns Hopkins University | Superior molecular vaccine linking the translocation domain of a bacterial toxin to an antigen |
| DE60042704D1 (de) | 2000-01-14 | 2009-09-17 | Whitehead Biomedical Inst | Induktion zytotoxischer lymphozyten durch hitzeschockprotein-fusionsproteine hängt von der atp-bindungsdomäne in hsp ab und is cd4+ unabhängig |
| US20040214158A1 (en) * | 2000-05-12 | 2004-10-28 | Neerja Sethi | Treatment of human papillomavirus (hpv)-infected cells |
| IL153474A0 (en) * | 2000-06-26 | 2003-07-06 | Stressgen Biotechnologies Corp | Human papilloma virus treatment |
| AU2001278117A1 (en) | 2000-08-03 | 2002-02-18 | Johns Hopkins University | Molecular vaccine linking an endoplasmic reticulum chaperone polypeptide to an antigen |
| WO2006033665A1 (en) * | 2004-03-16 | 2006-03-30 | Inist Inc. | Tat-based vaccine compositions and methods of making and using same |
| CN100400099C (zh) * | 2001-01-04 | 2008-07-09 | 北京迪威华宇生物技术有限公司 | 预防和治疗人前列腺癌的重组蛋白疫苗 |
| WO2002061113A2 (en) * | 2001-02-01 | 2002-08-08 | The Johns Hopkins University | Nucleic acid derived vaccine that encodes an antigen linked to a polypeptide that promotes antigen presentation |
| WO2002062959A2 (en) * | 2001-02-05 | 2002-08-15 | Stressgen Biotechnologies Corp. | Hepatitis b virus treatment |
| AUPR446801A0 (en) | 2001-04-18 | 2001-05-17 | University Of Queensland, The | Novel compositions and uses therefor |
| KR100785397B1 (ko) * | 2001-06-28 | 2007-12-13 | 아피메즈 주식회사 | 인체 파필로마 바이러스 유사 입자를 생산하는 재조합아데노바이러스 벡터 및 자궁경부암 생백신 |
| KR100474114B1 (ko) * | 2001-12-24 | 2005-03-08 | 대한민국 | 소 타일레리아병에 대한 면역원성이 증진된 융합단백질, 및 그의 제조방법 및 용도 |
| US7763259B2 (en) * | 2003-01-10 | 2010-07-27 | The Regents Of The University Of Colorado | Therapeutic and prophylactic vaccine for the treatment and prevention of papillomavirus infection |
| US7211257B2 (en) * | 2003-02-10 | 2007-05-01 | Rosalind Franklin University Of Medicine And Science | Methods for inducing apoptosis in ovarian carcinoma cells using an anti-regeneration and tolerance factor antibody |
| EP1644048B1 (en) | 2003-05-05 | 2015-04-29 | Johns Hopkins University | Anti-cancer dna vaccine employing plasmids encoding signal sequence, mutant oncoprotein antigen, and heat shock protein |
| WO2005026375A2 (en) | 2003-05-22 | 2005-03-24 | Fraunhofer Usa, Inc. | Recombinant carrier molecule for expression, delivery and purification of target polypeptides |
| US8541002B2 (en) | 2003-09-12 | 2013-09-24 | Agenus Inc. | Vaccine for treatment and prevention of herpes simplex virus infection |
| US7304139B2 (en) * | 2003-10-28 | 2007-12-04 | University Of Florida Research Foundation, Inc. | Polynucleotides and polypeptides of Anaplasma phagocytophilum and methods of using the same |
| FR2868781B1 (fr) * | 2004-04-13 | 2008-02-22 | Immutep | Composition de vaccin comprenant un ligand cmh de classe ii couple a un antigene, procede de preparation et utilisations |
| CN1727362B (zh) * | 2004-07-30 | 2010-12-01 | 中国人民解放军第二军医大学 | 癌胚抗原阳性肿瘤治疗性疫苗的制备及应用 |
| CN1769298B (zh) * | 2004-11-05 | 2010-04-07 | 中国人民解放军军事医学科学院生物工程研究所 | 一种具有抗肿瘤作用的融合蛋白及其编码基因与应用 |
| CA2594040A1 (en) | 2005-01-06 | 2006-07-13 | The Johns Hopkins University | Rna interference that blocks expression of pro-apoptotic proteins potentiates immunity induced by dna and transfected dendritic cell vaccines |
| CN1299769C (zh) * | 2005-01-31 | 2007-02-14 | 中国医学科学院肿瘤医院肿瘤研究所 | 人乳头瘤病毒和热休克蛋白重组蛋白疫苗及其用途 |
| ES2363247T3 (es) * | 2005-04-27 | 2011-07-28 | Leiden University Medical Center | Tratamiento para neoplasias intraepiteliales anogenitales inducidas por vph. |
| WO2007117264A2 (en) | 2005-08-03 | 2007-10-18 | Fraunhofer Usa, Inc. | Compositions and methods for production of immunoglobulins |
| US7951384B2 (en) * | 2005-08-05 | 2011-05-31 | University Of Massachusetts | Virus-like particles as vaccines for paramyxovirus |
| US9216212B2 (en) * | 2005-08-05 | 2015-12-22 | University Of Massachusetts | Virus-like particles as vaccines for paramyxovirus |
| US7622121B2 (en) * | 2005-09-21 | 2009-11-24 | New York University | Heat shock proteins from Mycobacterium leprae and uses thereof |
| US7972776B2 (en) * | 2005-11-15 | 2011-07-05 | Oncohealth Corporation | Protein chips for HPV detection |
| US7732166B2 (en) * | 2005-11-15 | 2010-06-08 | Oncohealth Corporation | Detection method for human pappilomavirus (HPV) and its application in cervical cancer |
| US8124103B2 (en) | 2006-02-13 | 2012-02-28 | Fraunhofer Usa, Inc | Influenza antigens, vaccine compositions, and related methods |
| WO2008048344A2 (en) * | 2006-02-13 | 2008-04-24 | Fraunhofer Usa, Inc. | Bacillus anthracis antigens, vaccine compositions, and related methods |
| WO2007095320A2 (en) * | 2006-02-13 | 2007-08-23 | Fraunhofer Usa, Inc. | Hpv antigens, vaccine compositions, and related methods |
| JP2009538836A (ja) * | 2006-05-31 | 2009-11-12 | ヌベンタ バイオファーマシューティカルズ コーポレイション | 生物活性の精製HspE7組成物 |
| CN100410382C (zh) * | 2006-08-18 | 2008-08-13 | 上海交通大学医学院 | 一种可诱生细胞免疫应答的共表达载体和真核表达载体 |
| US20100003704A1 (en) * | 2008-06-13 | 2010-01-07 | Shuling Cheng | IN SITU detection of early stages and late stages HPV infection |
| US8916342B2 (en) | 2006-11-13 | 2014-12-23 | Oncohealth Corp. | Identification of high grade or ≧ CIN2 for early stages and late stages detection, screening, and diagnosis of human papillomavirus (HPV) and HPV-associated cancers |
| US8968995B2 (en) * | 2008-11-12 | 2015-03-03 | Oncohealth Corp. | Detection, screening, and diagnosis of HPV-associated cancers |
| EP2099916A2 (en) * | 2006-12-22 | 2009-09-16 | Dow AgroSciences LLC | Plant-made west nile virus (wnv) vaccines, vectors and plant codon optimized sequences |
| US9085638B2 (en) | 2007-03-07 | 2015-07-21 | The Johns Hopkins University | DNA vaccine enhancement with MHC class II activators |
| WO2008124483A1 (en) * | 2007-04-04 | 2008-10-16 | Specigen, Inc. | Protein cage immunotherapeutics |
| WO2008134643A2 (en) * | 2007-04-28 | 2008-11-06 | Fraunhofer Usa, Inc. | Trypanosoma antigens, vaccine compositions, and related methods |
| CN101952320B (zh) * | 2007-06-18 | 2013-08-14 | 上海泽润安珂生物制药有限公司 | 具有免疫原性的物质 |
| US8088392B2 (en) * | 2007-06-18 | 2012-01-03 | Yunxu Cao | Capsid proteins and uses therefore |
| CA2692933C (en) | 2007-07-11 | 2016-10-18 | Fraunhofer Usa, Inc. | Yersinia pestis antigens, vaccine compositions, and related methods |
| CU23674A1 (es) | 2007-07-31 | 2011-05-27 | Ct Ingenieria Genetica Biotech | Péptidos penetradores a células fusionados a una biomolécula con acción terapéutica |
| CN101820903A (zh) * | 2007-08-20 | 2010-09-01 | 美国弗劳恩霍夫股份有限公司 | 预防性和治疗性流感疫苗、抗原、组合物和方法 |
| WO2009127988A1 (en) * | 2008-04-16 | 2009-10-22 | Universite De Lausanne | Method and vaccine for optimizing the specific immune responses |
| US9527906B2 (en) * | 2008-04-18 | 2016-12-27 | The General Hospital Corporation | Immunotherapies employing self-assembling vaccines |
| US8734803B2 (en) | 2008-09-28 | 2014-05-27 | Ibio Inc. | Humanized neuraminidase antibody and methods of use thereof |
| US8580270B2 (en) | 2008-09-30 | 2013-11-12 | University Of Massachusetts | Respiratory synctial virus (RSV) sequences for protein expression and vaccines |
| ES2432863T3 (es) | 2009-03-23 | 2013-12-05 | Pin Pharma, Inc. | Tratamiento del cáncer con polipéptidos inmunoestimuladores derivados de Tat del VIH |
| WO2011041391A1 (en) | 2009-09-29 | 2011-04-07 | Fraunhofer Usa, Inc. | Influenza hemagglutinin antibodies, compositions, and related methods |
| US9128094B2 (en) | 2010-01-08 | 2015-09-08 | Oncohealth Corp. | High throughput cell-based HPV immunoassays for diagnosis and screening of HPV-associated cancers |
| WO2011115688A2 (en) | 2010-03-19 | 2011-09-22 | H. Lee Moffitt Cancer Center & Research Institute | Integrin interaction inhibitors for the treatment of cancer |
| US20140155469A1 (en) | 2011-04-19 | 2014-06-05 | The Research Foundation Of State University Of New York | Adeno-associated-virus rep sequences, vectors and viruses |
| US20140255449A1 (en) * | 2011-07-21 | 2014-09-11 | Biotech Tools S.A. | Dosage of dnak |
| US9993534B2 (en) * | 2013-03-12 | 2018-06-12 | Wisconsin Alumni Research Foundation | Method of treating fungal infection |
| RU2537233C2 (ru) * | 2013-03-26 | 2014-12-27 | Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования "Кабардино-Балкарский государственный университет им. Х.М. Бербекова" (КБГУ) | Применение комплекса антиоксидантных витаминов и аминокислот в качестве дополнения к стандартным методам терапии и способ лечения папилломавирус-ассоциированных предраковых заболеваний шейки матки и профилактики канцерогенеза при папилломавирусной инфекции |
| CA2926221A1 (en) | 2013-10-04 | 2015-04-09 | Pin Pharma, Inc. | Immunostimulatory hiv tat derivative polypeptides for use in cancer treatment |
| FR3011850B1 (fr) * | 2013-10-15 | 2018-04-06 | Cfl Biotech | Vaccin therapeutique contre le cancer a base de proteines de stress rendues immunogenes |
| EP3270958A4 (en) * | 2015-03-18 | 2018-11-14 | Omnicyte | Fusion proteins comprising modified alpha virus surface glycoproteins and tumor associated antigen and methods thereof |
| US10561723B2 (en) | 2015-07-21 | 2020-02-18 | Theodore C. Marbley | Treatment and prevention of anal conditions |
| CN108484776B (zh) * | 2018-03-19 | 2019-11-05 | 首都医科大学附属北京朝阳医院 | 一种融合蛋白、制备方法及其应用 |
Family Cites Families (50)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US550405A (en) * | 1895-11-26 | Island | ||
| GB8404280D0 (en) | 1984-02-17 | 1984-03-21 | Stanford J L | Biological preparations |
| IL71683A0 (en) | 1984-04-27 | 1984-09-30 | Yeda Res & Dev | Pharmaceutical compositions for treating arthritis type diseases comprising fractions obtained from mycobacteria |
| US4906742A (en) | 1986-07-31 | 1990-03-06 | Whitehead Institute For Biomedical Research | Encoding antigens of M. Leprae |
| US6007806A (en) | 1986-08-13 | 1999-12-28 | Transgene S.A. | Expression of a tumor-specific antigen by a recombinant vector virus and use thereof in preventive or curative treatment of the corresponding tumor |
| NL8701163A (nl) | 1986-09-09 | 1988-04-05 | Nederlanden Staat | Gebruik van een peptide voor de bereiding van preparaten voor het verlichten, het behandelen en de diagnose van autoimmuunziekten, in het bijzonder arthritische toestanden, verbindingen die met dit peptide verwant zijn, alsmede farmaceutische en diagnostische preparaten en testkits. |
| WO1988005823A2 (en) | 1987-02-02 | 1988-08-11 | Whitehead Institute For Biomedical Research | Mycobacterium tuberculosis genes encoding protein antigens |
| US4952395A (en) | 1987-02-26 | 1990-08-28 | Scripps Clinic And Research Foundation | Mycobacterial recombinants and peptides |
| US5504005A (en) | 1987-03-02 | 1996-04-02 | Albert Einstein College Of Medicine Of Yeshiva University | Recombinant mycobacterial vaccine |
| US4918166A (en) | 1987-04-10 | 1990-04-17 | Oxford Gene Systems Limited | Particulate hybrid HIV antigens |
| NL8703107A (nl) | 1987-12-22 | 1989-07-17 | Nederlanden Staat | Polypeptiden en derivaten daarvan, alsmede de toepassing daarvan in farmaceutische en diagnostische preparaten. |
| CA1338778C (en) | 1988-06-15 | 1996-12-10 | Richard A. Young | Stress proteins and uses therefor |
| US5114844A (en) | 1989-03-14 | 1992-05-19 | Yeda Research And Development Co., Ltd. | Diagnosis and treatment of insulin dependent diabetes mellitus |
| CA2063414A1 (en) | 1989-06-19 | 1990-12-20 | Richard A. Young | Vector-mediated genomic insertion and expression of dna in bcg |
| GB8919321D0 (en) | 1989-08-25 | 1989-10-11 | Univ London | Treatment of chronic inflammatory conditions |
| GB9007194D0 (en) | 1990-03-30 | 1990-05-30 | Wellcome Found | Live vaccines |
| US5348945A (en) | 1990-04-06 | 1994-09-20 | Wake Forest University | Method of treatment with hsp70 |
| GB9024320D0 (en) | 1990-11-08 | 1990-12-19 | Univ London | Treatment of uveitis |
| DK0556248T3 (da) | 1990-11-08 | 1997-10-27 | Univ London | Mycobacterium som adjuvans til antigener |
| GB2251186A (en) | 1990-12-04 | 1992-07-01 | Randall Neal Gatz | Polypeptide for use in treatment of autoimmune disease |
| IT1262896B (it) | 1992-03-06 | 1996-07-22 | Composti coniugati formati da proteine heat shock (hsp) e oligo-poli- saccaridi, loro uso per la produzione di vaccini. | |
| US5580563A (en) | 1992-05-01 | 1996-12-03 | Tam; James P. | Multiple antigen peptide system having adjuvant properties, vaccines prepared therefrom and methods of use thereof |
| GB9211736D0 (en) | 1992-06-03 | 1992-07-15 | Univ Cardiff | Allergic treatment |
| IL102687A (en) | 1992-07-30 | 1997-06-10 | Yeda Res & Dev | Conjugates of poorly immunogenic antigens and synthetic pepide carriers and vaccines comprising them |
| US5736146A (en) | 1992-07-30 | 1998-04-07 | Yeda Research And Development Co. Ltd. | Conjugates of poorly immunogenic antigens and synthetic peptide carriers and vaccines comprising them |
| JP2541081B2 (ja) * | 1992-08-28 | 1996-10-09 | 日本電気株式会社 | バイオセンサ及びバイオセンサの製造・使用方法 |
| ATE212378T1 (de) | 1993-06-04 | 2002-02-15 | Whitehead Biomedical Inst | Stressproteine und ihre verwendung |
| US5762939A (en) | 1993-09-13 | 1998-06-09 | Mg-Pmc, Llc | Method for producing influenza hemagglutinin multivalent vaccines using baculovirus |
| US5750119A (en) | 1994-01-13 | 1998-05-12 | Mount Sinai School Of Medicine Of The City University Of New York | Immunotherapeutic stress protein-peptide complexes against cancer |
| US5997873A (en) | 1994-01-13 | 1999-12-07 | Mount Sinai School Of Medicine Of The City University Of New York | Method of preparation of heat shock protein 70-peptide complexes |
| US5961979A (en) | 1994-03-16 | 1999-10-05 | Mount Sinai School Of Medicine Of The City University Of New York | Stress protein-peptide complexes as prophylactic and therapeutic vaccines against intracellular pathogens |
| IL109790A0 (en) * | 1994-05-25 | 1994-08-26 | Yeda Res & Dev | Peptides used as carriers in immunogenic constructs suitable for development of synthetic vaccines |
| GB9419979D0 (en) | 1994-10-04 | 1994-11-16 | Medeva Holdings Bv | Vaccine compositions |
| AUPN015794A0 (en) * | 1994-12-20 | 1995-01-19 | Csl Limited | Variants of human papilloma virus antigens |
| JP3958360B2 (ja) * | 1995-02-24 | 2007-08-15 | キャンタブ ファーマシューティカルズ リサーチ リミティド | 免疫治療剤として役立つポリペプチド及びポリペプチド調製の方法 |
| HUP9802819A2 (hu) * | 1995-08-18 | 1999-03-29 | Sloan-Kettering Institute For Cancer Research | Hősokkfehérje-alapú oltóanyagok és immunterápiák |
| US5935576A (en) | 1995-09-13 | 1999-08-10 | Fordham University | Compositions and methods for the treatment and prevention of neoplastic diseases using heat shock proteins complexed with exogenous antigens |
| US5837251A (en) | 1995-09-13 | 1998-11-17 | Fordham University | Compositions and methods using complexes of heat shock proteins and antigenic molecules for the treatment and prevention of neoplastic diseases |
| US5985270A (en) | 1995-09-13 | 1999-11-16 | Fordham University | Adoptive immunotherapy using macrophages sensitized with heat shock protein-epitope complexes |
| JPH11513369A (ja) | 1995-09-13 | 1999-11-16 | フォーダム ユニバーシティー | 熱ショックタンパク質を用いる治療及び予防方法 |
| WO1997026910A2 (de) | 1996-01-27 | 1997-07-31 | Max-Delbrück-Centrum für Molekulare Medizin | Tumorimpfstoff für die immuntherapie von malignen tumoren |
| US6130087A (en) | 1996-10-07 | 2000-10-10 | Fordham University | Methods for generating cytotoxic T cells in vitro |
| EP0941315B1 (en) | 1996-11-26 | 2006-03-01 | Stressgen Biotechnologies Corporation | Fusion proteins containing stress proteins for inducing immune responses |
| US6017540A (en) | 1997-02-07 | 2000-01-25 | Fordham University | Prevention and treatment of primary and metastatic neoplastic diseases and infectious diseases with heat shock/stress protein-peptide complexes |
| US5830464A (en) | 1997-02-07 | 1998-11-03 | Fordham University | Compositions and methods for the treatment and growth inhibition of cancer using heat shock/stress protein-peptide complexes in combination with adoptive immunotherapy |
| EP1047451A1 (en) | 1997-02-18 | 2000-11-02 | Whitehead Institute For Biomedical Research | Use of heat shock proteins to deliver moieties into cells |
| ES2191929T3 (es) * | 1997-08-05 | 2003-09-16 | Stressgen Biotechnologies Corp | Respuestas inmunologicas contra los antigenos pvh estimuladas por composiciones que comprenden un antigeno pvh y una proteina de estres o un vector de expresion capaz de expresar dichas proteinas. |
| US6007821A (en) | 1997-10-16 | 1999-12-28 | Fordham University | Method and compositions for the treatment of autoimmune disease using heat shock proteins |
| US5948646A (en) | 1997-12-11 | 1999-09-07 | Fordham University | Methods for preparation of vaccines against cancer comprising heat shock protein-peptide complexes |
| US6495347B1 (en) * | 1999-07-08 | 2002-12-17 | Stressgen Biotechnologies Corporation | Induction of a Th1-like response in vitro |
-
1998
- 1998-03-20 ES ES98910557T patent/ES2191929T3/es not_active Expired - Lifetime
- 1998-03-20 KR KR1020007001231A patent/KR100843109B1/ko not_active IP Right Cessation
- 1998-03-20 NZ NZ50256898A patent/NZ502568A/xx unknown
- 1998-03-20 CA CA 2298840 patent/CA2298840A1/en not_active Abandoned
- 1998-03-20 PL PL338478A patent/PL196805B1/pl not_active IP Right Cessation
- 1998-03-20 KR KR1020067019653A patent/KR20060111731A/ko not_active Application Discontinuation
- 1998-03-20 DK DK98910557T patent/DK1002110T3/da active
- 1998-03-20 ES ES03001726T patent/ES2266652T3/es not_active Expired - Lifetime
- 1998-03-20 IL IL13434198A patent/IL134341A0/xx unknown
- 1998-03-20 BR BR9812272A patent/BR9812272A/pt not_active Application Discontinuation
- 1998-03-20 PT PT98910557T patent/PT1002110E/pt unknown
- 1998-03-20 AU AU64924/98A patent/AU6492498A/en not_active Abandoned
- 1998-03-20 HU HU0003601A patent/HUP0003601A3/hu unknown
- 1998-03-20 AT AT98910557T patent/ATE231917T1/de not_active IP Right Cessation
- 1998-03-20 DE DE1998611087 patent/DE69811087T2/de not_active Expired - Lifetime
- 1998-03-20 PT PT03001726T patent/PT1336621E/pt unknown
- 1998-03-20 WO PCT/CA1998/000246 patent/WO1999007860A1/en not_active Application Discontinuation
- 1998-03-20 AT AT03001726T patent/ATE327259T1/de not_active IP Right Cessation
- 1998-03-20 JP JP2000506343A patent/JP4198315B2/ja not_active Expired - Fee Related
- 1998-03-20 NZ NZ538399A patent/NZ538399A/en unknown
- 1998-03-20 CN CNA2005100624792A patent/CN1680451A/zh active Pending
- 1998-03-20 EP EP19980910557 patent/EP1002110B2/en not_active Expired - Lifetime
- 1998-03-20 CN CNB988091216A patent/CN100489105C/zh not_active Expired - Fee Related
- 1998-03-20 DE DE1998634671 patent/DE69834671T2/de not_active Expired - Lifetime
- 1998-03-20 NZ NZ522653A patent/NZ522653A/en unknown
- 1998-03-20 CN CNA2006101055473A patent/CN1915425A/zh active Pending
-
2000
- 2000-02-04 US US09/498,918 patent/US6524825B1/en not_active Expired - Fee Related
- 2000-11-24 HK HK00107543A patent/HK1028981A1/xx not_active IP Right Cessation
-
2002
- 2002-11-07 US US10/289,760 patent/US6900035B2/en not_active Expired - Fee Related
-
2004
- 2004-02-16 HK HK04101103A patent/HK1058367A1/xx not_active IP Right Cessation
- 2004-09-10 US US10/938,695 patent/US7262014B2/en not_active Expired - Fee Related
-
2005
- 2005-07-21 JP JP2005211965A patent/JP2006001939A/ja not_active Withdrawn
-
2007
- 2007-07-26 US US11/828,900 patent/US20080050399A1/en not_active Abandoned
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR100843109B1 (ko) | 사람 유두종 바이러스 항원과 스트레스 단백질을 포함하는 융합 단백질을 포함하는 조성물에 의해 유도된 사람 유두종 바이러스 항원에 대한 면역 반응 | |
| US6797491B2 (en) | Human papilloma virus treatment | |
| AU2001271449A1 (en) | Human papilloma virus treatment | |
| EP1336621B1 (en) | Immune responses against HPV antigens elicited by compositions comprising an HPV antigen and a stress protein or an expression vector capable of expression of these proteins | |
| AU779770B2 (en) | Immune responses against HPV antigens elicited by compositions comprising an HPV antigen and a stress protein or an expression vector capable of expression of these proteins | |
| AU2005201826B2 (en) | Immune responses against HPV antigens elicited by compositions comprising an HPV antigen and a stress protein or an expression vector capable of expression of these proteins | |
| CZ2000422A3 (cs) | Imunitní odpověď proti HPV antigenům vyvolaná prostředky obsahujícími HPV antigen a stresový protein nebo expresní vektor schopný exprese těchto proteinů | |
| MXPA00001299A (en) | Immune responses against hpv antigens elicited by compositions comprising an hpv antigen and a stress protein or an expression vector capable of expression of these proteins |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A107 | Divisional application of patent | ||
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E902 | Notification of reason for refusal | ||
| E601 | Decision to refuse application |