JP7633397B2 - 眼の疾患の処置のための二重特異性抗VEGF及び抗TrkB結合分子 - Google Patents
眼の疾患の処置のための二重特異性抗VEGF及び抗TrkB結合分子 Download PDFInfo
- Publication number
- JP7633397B2 JP7633397B2 JP2023524323A JP2023524323A JP7633397B2 JP 7633397 B2 JP7633397 B2 JP 7633397B2 JP 2023524323 A JP2023524323 A JP 2023524323A JP 2023524323 A JP2023524323 A JP 2023524323A JP 7633397 B2 JP7633397 B2 JP 7633397B2
- Authority
- JP
- Japan
- Prior art keywords
- seq
- amino acid
- acid sequence
- heavy chain
- tpp
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/22—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against growth factors ; against growth regulators
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2863—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for growth factors, growth regulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/10—Immunoglobulins specific features characterized by their source of isolation or production
- C07K2317/14—Specific host cells or culture conditions, e.g. components, pH or temperature
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/35—Valency
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
- C07K2317/53—Hinge
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/54—F(ab')2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/62—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising only variable region components
- C07K2317/622—Single chain antibody (scFv)
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/60—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments
- C07K2317/64—Immunoglobulins specific features characterized by non-natural combinations of immunoglobulin fragments comprising a combination of variable region and constant region components
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/75—Agonist effect on antigen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Biochemistry (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Animal Behavior & Ethology (AREA)
- Ophthalmology & Optometry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Peptides Or Proteins (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Description
本発明は、血管内皮増殖因子(VEGF)及びトロポミオシンレセプターキナーゼB(TrkB)に結合する結合分子並びに医薬におけるその使用、それを含む医薬組成物並びに眼の疾患の治療及び/又は予防のための薬剤としてそれを使用する方法に関する。
黄斑変性症、特に、加齢黄斑変性症(AMD)は、先進諸国における失明の主な原因である。その進行期は、滲出性新生血管AMDと萎縮型地図状萎縮(GA)とに分けられる。wAMDは、眼の新生血管形成及び血管漏出の増加並びに進行性神経変性及び光レセプター喪失を特徴とする。抗VEGF処置は、この疾患のための現在の標準治療である。治療は、典型的には、VEGFをターゲットとする薬剤(Avastin、Lucentis、Eylea及び近年は、Beovu)からなり、これらは、眼の後部に注射により投与される。
本発明は、単一の結合分子内で、血管内皮増殖因子(VEGF)に特異的に結合する抗原結合部位と、トロポミオシンレセプターキナーゼB(TrkB)に特異的に結合する抗原結合部位とを組み合わせるという概念に基づいている。
a)配列番号:201(CDR1)、配列番号:202(CDR2)及び配列番号:203(CDR3)のアミノ酸配列を含む軽鎖CDRを含む抗原結合部位並びに
配列番号:204(CDR1)、配列番号:205(CDR2)及び配列番号:206(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:207(CDR1)、配列番号:208(CDR2)及び配列番号:209(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:210(CDR1)、配列番号:211(CDR2)及び配列番号:212(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位
から選択される。
a)配列番号:213又は215のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む軽鎖可変ドメインと、配列番号:214又は216のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む重鎖可変ドメインとを含む抗原結合部位
から選択される。
a)配列番号:145(CDR1)、配列番号:146(CDR2)及び配列番号:147(CDR3)のアミノ酸配列を含む軽鎖CDRを含む抗原結合部位並びに
配列番号:148(CDR1)、配列番号:149(CDR2)及び配列番号:150(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:151(CDR1)、配列番号:152(CDR2)及び配列番号:153(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:154(CDR1)、配列番号:155(CDR2)及び配列番号:156(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位;
b)配列番号:157(CDR1)、配列番号:158(CDR2)及び配列番号:159(CDR3)のアミノ酸配列を含む軽鎖CDRを含む抗原結合部位並びに
配列番号:160(CDR1)、配列番号:161(CDR2)及び配列番号:162(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:163(CDR1)、配列番号:164(CDR2)及び配列番号:165(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:166(CDR1)、配列番号:167(CDR2)及び配列番号:168(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位;
c)配列番号:169(CDR1)、配列番号:170(CDR2)及び配列番号:171(CDR3)のアミノ酸配列を含む軽鎖CDRを含む抗原結合部位並びに
配列番号:172(CDR1)、配列番号:173(CDR2)及び配列番号:174(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:175(CDR1)、配列番号:176(CDR2)及び配列番号:177(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:178(CDR1)、配列番号:179(CDR2)及び配列番号:180(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位
からなる群より選択される。
a)配列番号:181のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む軽鎖可変ドメインと、配列番号:182のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む重鎖可変ドメインとを含む抗原結合部位;
b)配列番号:183のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む軽鎖可変ドメインと、配列番号:184のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む重鎖可変ドメインとを含む抗原結合部位;
c)配列番号:189のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む軽鎖可変ドメインと、配列番号:190、191、192又は194のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む重鎖可変ドメインとを含む抗原結合部位;
d)配列番号:193のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む軽鎖可変ドメインと、配列番号:190、191、192又は194のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む重鎖可変ドメインとを含む抗原結合部位
からなる群より選択される。
a)配列番号:185のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む軽鎖と、配列番号:186のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む重鎖とを含む抗原結合部位;
b)配列番号:187のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む軽鎖と、配列番号:188のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む重鎖とを含む抗原結合部位;
c)配列番号:195のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む軽鎖と、配列番号:196、197、198又は200のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む重鎖とを含む抗原結合部位;
d)配列番号:199のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む軽鎖と、配列番号:196、197、198又は200のアミノ酸配列と少なくとも80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%又は少なくとも99%同一のアミノ酸配列を含む重鎖とを含む抗原結合部位
からなる群より選択される。
を含む、結合分子に関する。
(i)配列番号:189のアミノ酸配列を含む軽鎖可変ドメイン及び
配列番号:191のアミノ酸配列を含む重鎖可変ドメイン又は
配列番号:192のアミノ酸配列を含む重鎖可変ドメイン又は
配列番号:194のアミノ酸配列を含む重鎖可変ドメイン
(ii)配列番号:190のアミノ酸配列を含む重鎖可変ドメイン及び
配列番号:192のアミノ酸配列を含む軽鎖可変ドメイン又は
配列番号:193のアミノ酸配列を含む軽鎖可変ドメイン
を含む、VEGFに特異的に結合する抗体分子に関する。
(a)以下の分子の発現を可能にする条件下で、第13の態様の宿主細胞を培養することと、
(b)該分子を回収することと、場合により、
(c)該分子をさらに精製しかつ/又は修飾しかつ/又は製剤化することとを含む、
前述の態様及び実施態様のいずれかの結合分子、TrkB結合分子、scFv又は抗体分子を製造する方法に関する。
本発明は、単一の結合分子内で、血管内皮増殖因子(VEGF)に特異的に結合する抗原結合部位と、トロポミオシンレセプターキナーゼB(TrkB)に特異的に結合する抗原結合部位とを組み合わせるという概念に基づいている。
本明細書で具体的に定義されていない用語は、本開示及び文脈に照らして、当業者によりそれらに与えられるであろう意味を与えられるべきである。ただし、本明細書で使用する場合、特に断りない限り、下記用語は、示された意味を有し、下記慣例に従う。
トロポミオシンレセプターキナーゼB(TrkB)は、チロシンレセプターキナーゼB又はBDNF/NT-3増殖因子レセプター又は神経栄養チロシンキナーゼレセプター2型としても公知であり、ヒトにおいてNTRK2遺伝子(Genbank ID:4915)によりコードされるタンパク質である。TrkBは脳由来神経栄養因子(BDNF)についてのレセプターである。
配列番号:201(CDR1)、配列番号:202(CDR2)及び配列番号:203(CDR3)のアミノ酸配列を含む軽鎖CDR並びに
配列番号:204(CDR1)、配列番号:205(CDR2)及び配列番号:206(CDR3)のアミノ酸配列を含む重鎖CDR又は
配列番号:207(CDR1)、配列番号:208(CDR2)及び配列番号:209(CDR3)のアミノ酸配列を含む重鎖CDR又は
配列番号:210(CDR1)、配列番号:211(CDR2)及び配列番号:212(CDR3)のアミノ酸配列を含む重鎖CDR
から選択される軽鎖CDRと重鎖CDRとの組み合わせを有する。
血管内皮増殖因子(VEGF)は、VEGF-A又は血管透過性因子(VPF)とも呼ばれる最も重要な血管新生促進因子の1つである。VEGFは、胎盤増殖因子(PlGF)、VEGF-B、VEGF-C、VEGF-D、VEGF-E及びVEGF-Fを含む遺伝子ファミリーに属する。ヒトVEGFの単一遺伝子のmRNAの選択的スプライシングにより、少なくとも6つのアイソフォーム(VEGF121、VEGF145、VEGF165、VEGF183、VEGF189及びVEGF206)がもたらされ、VEGF165が、最も豊富なアイソフォームである。
本発明は、少なくとも2つの異なるターゲットに対する結合特異性を有する結合分子に関する。本発明に関して、結合分子は、抗体に由来する。結合分子を調製するための技術は、異なる特異性を有する2つの免疫グロブリン重鎖-軽鎖対のリコンビナント共発現(Milstein and Cuello, Nature 305: 537 (1983)、WO第93/08829号及びTraunecker et al., EMBO J. 10: 3655 (1991)を参照のこと)及び「ノブ-イン-ホール」操作(例えば、US第5,731,168号を参照のこと)を含むが、これらに限定されない。また、本発明の結合分子を、抗体Fc-ヘテロ二量体分子を調製するための静電的ステアリング効果を操作すること(WO第2009/089004号);2つ以上の抗体又はフラグメントを架橋すること(例えば、US第4,676,980号及びBrennan et al., Science, 229: 81 (1985)を参照のこと);ロイシンジッパーを使用して、二重特異性抗体を産生すること(例えば、Kostelny et al., Immunol., 148(5): 1547-1553 (1992)を参照のこと);二重特異性抗体フラグメントを調製するための「ダイアボディ」技術を使用すること(例えば、Hollinger et al., Proc. Natl. Acad. Sci. USA, 90:6444- 6448 (1993)を参照のこと)及び一本鎖Fv(sFv)二量体を使用すること(例えば、Gruber et al., /. Immunol., 152:5368 (1994)を参照のこと)及び例えば、Tutt et al. /. Immunol. 147: 60 (1991)に記載されているような三重特異性抗体を調製することによっても調製することができる。
(i)それぞれがN末端からC末端に向かって、
-VEGFに特異的な重鎖可変ドメイン(例えば、マウス、ヒト化又はヒトVHドメイン)
-IgG(例えば、ヒトIgG1又はIgG4)の定常ドメイン
-ペプチドリンカー(例えば、GSミニリンカー)及び
-TrkBに特異的なscFv(例えば、N末端からC末端へのVHドメイン(例えば、マウス、ヒト化又はヒトVHドメイン)を含むscFv)、リンカー及びVLドメイン(例えば、マウス、ヒト化又はヒトVLドメイン)又はその逆に、VLドメイン、リンカー及びVHドメイン)
含む2つの重鎖と、
(ii)それぞれがN末端からC末端に向かって
VEGFに特異的な軽鎖可変ドメイン(例えば、マウス、ヒト化又はヒトVLドメイン)、
軽鎖定常ドメイン(例えば、ヒトカッパ鎖)
を含む2つの軽鎖と
を有する、結合分子(本明細書において、多重特異性結合タンパク質又は修飾Ig分子とも呼ばれる)を提供する。
(a)以下の分子の発現を可能にする条件下で、本発明の宿主細胞を培養することと、
(b)該分子を回収することと、場合により、
を含む、本明細書に記載された結合分子又は抗体分子の製造方法を提供する。
本発明の結合分子におけるTrkB結合部位(2つのscFv)の設計が、TrkB結合及び活性化の最適な立体形成を明らかに支持するという驚くべき知見(これは、更なる抗原結合部位、例えば、VEGF結合部位又はVEGF誘発クラスター形成メカニズムとは無関係である場合がある)に基づいて、さらに、本発明は、2つのscFvを含むか又はそれからなり、ここで、各scFvがTrkBに特異的に結合し、両方ともTrkBアゴニストとして作用する、TrkB結合分子に関する。
(i)それぞれがN末端からC末端に向かって、
-(場合により)重鎖可変ドメイン(例えば、マウス、ヒト化又はヒトVHドメイン)
-好ましくは、IgG(例えば、ヒトIgG1又はIgG4)の定常ドメイン
-(場合により)ペプチドリンカー(例えば、GSミニリンカー)及び
-TrkBに特異的なscFv(例えば、N末端からC末端へのVHドメイン(例えば、マウス、ヒト化又はヒトVHドメイン)を含むscFv)、リンカー及びVLドメイン(例えば、マウス、ヒト化又はヒトVLドメイン)又はその逆に、VLドメイン、リンカー及びVHドメイン
含む2つの重鎖と、
(ii)それぞれがN末端からC末端に向かって
(場合により)軽鎖可変ドメイン(例えば、マウス、ヒト化又はヒトVLドメイン)、
好ましくは、IgGの軽鎖定常ドメイン(例えば、ヒトカッパ鎖)
を含む2つの軽鎖と
を含むか又はそれらからなる。
方法
Trkレセプターを発現するCHO細胞の培養
ヒトTrkBレセプターを発現するCHO細胞(ThermoFisher Scientific, #K1491)及びヒトTrkA又はTrkCレセプターを発現するカスタマイズされたCHO細胞を、10% ウシ胎児血清、glutamax、非必須アミノ酸、20mM HEPES、5μg/mL ブラストサイジン及び200μg/mL ゼオシンを補充したDMEM(Lonza, #BE12-604F)中で培養した。カニクイザル、ウサギ又はラットTrkBレセプターを発現するカスタマイズされたCHO細胞を、Hams F12(Lonza #BE12-615F)と、5% ウシ胎仔血清、8mM グルタミン、0.5mg/mL G418を含むDMEM(Lonza #BE12-604F)との1:1混合物中で培養した。マウスTrkBレセプターを発現するカスタマイズされたCHO細胞を、10% ウシ胎仔血清、glutamax、10mM HEPES及び0.8mg/mL G418を補充したDMEM(Lonza #BE12-604F)で培養した。
各Trkレセプターを発現する5000個のCHO細胞を、384ウェル透明組織培養プレート(BD Falcon, #353963)の各キャビティに播種し、37℃及び5% CO2での加湿インキュベーター中でインキュベーションした。播種の24時間後、細胞の上清を室温飢餓培地(0.1% BSA(Sigma, #A-3059)を含むが、他に補充しないDMEM)で置き換えた。15分後、上昇する濃度のヒトBDNF(R&D #248-BD又はBachem #H-5594)、ヒトNGF(Biovision #4303R-20)、ヒトNT-3(Sigma #N1905)、アゴニスト性抗体又はアイソタイプ対照を含む飢餓培地を室温において45分間トリプリケートで加えて、TrkB及びERK1/2リン酸化を刺激した。飢餓培地単独を対照とした。
ヒトTrkBを安定に発現するCHO細胞を上昇する濃度のTrkB-ECD(R&D Systems #1494-TB)を伴う、上昇する濃度の天然のリガンドであるBDNF又は10nM BDNFと共にインキュベーションした。TrkB活性化を、上記概説されたY706/707でのTrkBリン酸化を測定することにより評価した。データは、平均+/-SEMを表わす。
刺激の24時間前に、25000個のヒトTrkBレセプターを発現するCHO細胞を、96ウェル黒色透明底部組織培養プレート(PerkinElmer, #6055300)の各キャビティに播種し、37℃及び5% CO2の加湿インキュベーター中でインキュベーションした。CHO/hTrkB細胞の上清を飢餓培地(0.1% BSA(Sigma, #A-3059)及び20mM Hepes(Lonza, # BE17-737F)を含むDMEM)で置き換え、細胞を37℃で30分間インキュベーションした。ついで、細胞を、上昇する濃度のBDNF(R&D #248-BD又はBachem #H-5594)又はアゴニスト性TrkB抗体単独又は1nM BDNFと飢餓培地中の上昇する濃度のアゴニスト性抗体との組み合わせで、37℃において50分間刺激した。細胞を4% パラホルムアルデヒド中で20分間固定し、洗浄し、PBS中の5% 正常ロバ血清中において1時間ブロッキングし、1μg/mL ヤギ抗TrkB抗体(R&D Systems, #AF-397)と共に、室温で一晩インキュベーションし、続けて、徹底的に洗浄し、2μg/mL AlexaFluor 647ロバ抗ヤギ抗体(ThermoFisher Scientific, #A21447)及び1μg/mL Hoechst #H3570中において、室温で2時間インキュベーションした。徹底的な洗浄後、細胞をPBS/0.05% Tween-20中の2μg/mL HCS-Cellmask green(ThermoFisher Scientific, #H32714)で1時間染色した。細胞表面レセプターを、20×水対物レンズを備えたPerkinElmer Opera Phenix High Content Screening Systemで撮像し、PerkinElmer Harmony High-Content Imaging and Analysisソフトウェアで分析した。データを、蛍光閾値を上回る細胞の割合の高低をそれぞれ表わすヒートマップの暗視野及び明視野を有するヒートマップとして又は閾値を上回る表面TrkB染色強度を有する細胞の割合を表わす図としてのいずれかで提示する。後者の場合、生データ(平均±SEM)及び非線形回帰(log(アゴニスト)対応答(3つのパラメータ))を含むデータをGraphPad Prism(バージョン8)による提示のために作成した。
ヒト網膜微小血管内皮細胞(HRMEC;Cell Systems #ACBRI181)を、サプリメント(Promocell #C-39210)及び10U/mL ペニシリン/ストレプトマイシンそれぞれを含む内皮細胞基礎培地(Promocell #C-22210)中においてゼラチン(Millipore #ES-006B)被覆プレート上で培養した。VEGF捕捉の分析のために、12000個の細胞を、通常の増殖培地を使用して、96ウェル透明組織培養プレートの各キャビティに播種し、37℃及び5% CO2での加湿インキュベーター中でインキュベーションした。24時間後、培地を飢餓培地(0.1% BSA(Sigma, #A-3059)及び10U/mL ペニシリン/ストレプトマイシンを補充したPromocell #C-22210)で置き換え、細胞を37℃及び5% CO2での加湿インキュベーター中で20時間飢餓状態にした。VEGFR2シグナル伝達の刺激前に、50ng/mL ヒトVEGF(R&D Systems #293-VE-050)を、アンタゴニスト性抗体又はEyleaの有無で、室温において飢餓培地中で30~60分間プレインキュベーションし、ついで、37℃に15分間予め温めた。細胞刺激を、予め形成されたVEGF-抗体/Eylea複合体又はVEGF単独を細胞に加えることにより、37℃に温めたプレート上において5分間で達成した。飢餓培地単独を対照とした。細胞を溶解バッファー(Perkin Elmer #ALSU-PVGFR-A500)中において、室温で10分間溶解し、ついで、氷上でさらに10分間インキュベーションした。製造業者の説明書に従い、市販のアッセイを使用して、Y1175でのVEGFR2リン酸化(Perkin Elmer #ALSU-A500又は#ALSU-PVGFR-A10K)、Y951でのVEGFR2リン酸化(Perkin Elmer #ALSU-PVGFR-B500)、T202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化(Perkin Elmer #TGRES10K又はALSU-PERK-A10K)、Y419でのSrcリン酸化(Perkin Elmer #ALSU-PSRC-A10K)、Thr180/Tyr182でのp38-MAPKリン酸化(Perkin Elmer #ALSU-PP38-B500)を定量した。上記言及されたリン酸化事象を反映するアクセプタービーズの発光をPerking Elmer EnVisionマイクロプレートリーダーにおいて、570nmで記録し、生データ(平均±SEM)及び非線形回帰(log(アゴニスト)対応答(3つのパラメータ))を含むデータをGraphPad Prism(バージョン8)による提示のために作成した。
3000個のHRMECを、サプリメント(Promocell #C-39210)及び10U/mL ペニシリン/ストレプトマイシンを含む内皮細胞基礎培地(Promocell #C-22210)を使用して、透明平底96ウェルプレートの各キャビティに播種し、37℃及び5% CO2の加湿インキュベーター中でインキュベーションした。16時間後、増殖培地を飢餓培地(2% ウシ胎児血清を補充した内皮細胞基礎培地(Promocell #C-22210))で置き換え、細胞を37℃、5% CO2での加湿インキュベーター中において、8時間飢餓状態にした。刺激前に、ヒトVEGF(R&D Systems #293-VE-050)を、アンタゴニスト性抗体又はEyleaの有無で、室温において飢餓培地中で60分間プレインキュベーションした。細胞刺激を、予め形成されたVEGF-抗体/Eylea複合体又はVEGF単独を細胞に加えることにより行った。飢餓培地単独を対照とした(ベース増殖)。細胞増殖を総HRMEC核面積の自動位相コントラスト画像ベース定量化により評価した(Essen Bioscience, IncuCyte S3)。総HRMEC核面積は、HRMEC数に比例すると考えられた。ウェル当たりに4つの画像を4時間毎に、10×対物レンズを使用して、合計96時間記録した。データは、時間の関数としての相対細胞数(時点tでの細胞数/t=0での細胞数)を表わし、t=0での細胞数を1に設定した。一部の実験では、各増殖曲線とベース成長曲線(飢餓培地中での増殖)との間の面積を、各化合物濃度の10を底とする対数に対してプロットした。必要に応じて、生データ(平均±SEM)及び非線形回帰(log(アゴニスト)対応答(3つのパラメータ))を含むデータをGraphPad Prism(バージョン8)による提示のために作成した。
VEGF誘発発芽の阻害を、HRMECに基づくスフェロイドアッセイにおいて評価した。HRMECを、20% Methocoel(内皮基礎培地中の1.2% メチルセルロース及び10% ウシ胎児血清)を含有する通常の増殖培地に再懸濁させ、500個のHRMECを含有する滴 25μlを正方形ペトリ皿に適用した。プレートを上下逆さまにして、細胞を吊り下げた滴中で培養した。これにより、スフェロイドの自発的な形成が可能となった。24時間後、スフェロイドを収集し、48ウェルプレートにおいて、Methocoel-コラーゲン混合物(M199培地中の3mg/mL ラットテールコラーゲンI(Corning #354236)と混合した、80% Methocoel及び20% FCS 1:1)に包埋し、37℃及び5% CO2での加湿インキュベーター中で30分間インキュベーションして、コラーゲン重合を達成した。刺激前に、ヒトVEGF(R&D Systems #293-VE-050)を、2% ウシ胎児血清を補充した基礎内皮増殖培地中において、アンタゴニスト性抗体又はEyleaの有無で、室温において60分間プレインキュベーションした。発芽の刺激を、予め形成されたVEGF-抗体/Eylea複合体又はVEGF単独をスフェロイドに24時間加えることにより行った。2% ウシ胎児血清を補充し、VEGFを含まない基礎内皮増殖培地を対照とした。4% パラホルムアルデヒド中に固定した後、細胞を徹底的に洗浄し、0.2% Triton X-100を含有するPBS中の2μg/mL HCS-Cellmask green(ThermoFisher Scientific, #H32714)で一晩染色した。スフェロイドをZEISS LSM 780共焦点顕微鏡で分析した。HRMECの三次元発芽をZスタックの最大投影画像から、手作業で定量化し、スフェロイド当たりの累積発芽長(mm)として表わすか又はZeiss ZEN撮像ソフトウェアで半自動化し、スフェロイド外周長(ピクセル)として表わすかのいずれかをした。データをGraphPad Prism(バージョン8)による提示のために作成し、平均+/-SEMを表わす。
一般的な手法
網膜電図(ERG)は、種々の網膜ニューロンの光誘発電気的活動を評価するための非侵襲的電気生理学的技術であり、これにより、網膜機能の種々の態様、例えば、薄暗い光又は色覚を定量することが可能となる。ERGは、Espion E3 ERG記録システム(Diagnosys LLC)を使用して、角膜と参照電極との間の電位変化として測定した。ERG記録前に、動物を少なくとも2時間暗順応させ、ケタミン(Ketanest、約100mg/kg)及びキシラジン(Rompun、約7mg/kg)のi.p.注射により麻酔した。動物を、体温を37℃で一定に保つため、加熱したステージに置いた。瞳孔を局所トロピカミド及び10% フェニレフリンで拡張させた。角膜に2% Methocel溶液(OmniVision)の滴を載せて、記録中に角膜眼が乾燥しないようにした。記録を、金ループ電極を使用して、両眼で同時に行った。参照電極をMethocelで湿らせ、動物の頬に取り付けた、歯のないワニ口クリップとした。電気的接地のために、クリップを動物の尾部に取り付けた。ERGシグナルを1kHzでサンプリングし、0.15Hzの低周波数及び500Hzの高周波カットオフを使用して記録した。光刺激は、発光ダイオードのセット又はキセノン電球(1cd・s/m2以上のフラッシュの場合)により発せられる全視野フラッシュ(持続時間約4ms)からなった。全てのフラッシュを暗所又はバックグラウンド光のいずれかにおいて、Ganzfeld刺激装置(ColorDome; Diagnosys)により発生させた。
まず、ERG応答を暗順応動物(桿体駆動応答を単離するため)から記録し、続けて、赤色バックグラウンド光(50cd/m2、紫外線錐体駆動ERG応答を単離するため)に順応させた動物から記録し、最後に、緑色-青色バックグラウンド光(25.5cd/m2、M錐体駆動ERG応答を単離するため)に順応させた。
オスのBrown Norwayラット(BNラット)をCharles River(Germany)から入手した。高血糖をSTZのi.p.注射(65mg/kg 体重)により誘発した。試験には、応答しない動物又は応答が不十分な動物、すなわち、STZ適用後7日目の血糖濃度が20mM未満の動物を含めなかった。体重及び血糖値を定期的にモニターした。STZを硝子体内投与の約3週間前に投与した。
ivt注射のために、ラットを2.5~3% イソフルラン(Forene; Abbvie)で麻酔した。局所麻酔のために、4mg/mL オキシブプロカイン塩酸塩(Novesine; Omnivision)の滴を投与した。5μLを、(10μlのHamiltonガラスシリンジに取り付けた)34ゲージ針により、各眼の角膜縁のすぐ後ろの硝子体内に注射した。
ERGを、Espion E3 ERG記録システム(Diagnosys LLC)を使用して、角膜と参照電極との間の電位変化として測定した。
ヒトVEGF及びヒトTrkBを認識する結合分子の全体的な設計
図1
本発明者らは、VEGF及びTrkBに結合し、それぞれVEGFアンタゴニスト及びTrkBアゴニストとして作用する、結合分子を開発した。使用された分子設計は、重鎖のC末端に結合された異なる特異性のscFvを有する、1つのターゲット抗原に対する特異性を有するIgG抗体(「マスター抗体」と呼ばれる)を有する。図1に、設計模式図を示す。好ましくは、結合分子は、二重特異性かつ四価である。
VEGF及びTrkBを認識する結合ドメインの調製
図1
理解することができるように、ヒトVEGF及びTrkBに結合する二重特異性分子を調製するために、それらの個々のターゲット抗原に結合する可変ドメインを得る必要がある。
シリーズ1において、二重特異性結合分子中にTrkB結合部分として抗原結合フラグメント(Fab)を有する結合分子を生成した。VEGF結合部分をscFv(2)としてフォーマットし、種々のVEGFバインダー、例えば、B20、G6又はRanibizumabを評価した。さらに、種々のVL-VH又はVH-VL配向を試験し、複数のリンカー、例えば、20L3、20L1、15L1、10L1、6GSを結合分子の設計に使用した。
シリーズ2において、二重特異性結合分子中にVEGF結合部分として抗原結合フラグメント(Fab)を有する結合分子を生成し、再度、種々のVEGFバインダーを評価した。今回、TrkB結合部分をscFv(2)としてフォーマットし、種々のVL-VH又はVH-VL配向を試験した。
シリーズ3において、結合分子を二重特異性結合分子中の抗原結合フラグメント(Fab)及びVEGF結合部分としてのRanibizumabに基づいて生成した。再度、TrkB結合部分をscFv(2)としてかつC2 TrkBバインダーに基づいてフォーマットした。VL-VH又はVH-VL配向における並べ替え及び種々のリンカーを試験した。
最後のシリーズ4において、種々の突然変異、例えば、VHE1Q、VHE6Q及び/又はVLD70GをRanibizumabの結合部分に導入し、CC架橋の安定化効果をTrkB結合scFv部分において分析した。
C2、BDNF並びに第1シリーズの4種類のDoppelmab TPP-11735、736、737及び738によるヒトTrkB活性化の比較
図2A~図2B
ヒトTrkBを安定に発現するCHO細胞を、上昇する濃度の天然のTrkBリガンドであるBDNF、C2抗体、IgG1アイソタイプ対照又は4つのDoppelmab TPP-11735、TPP-11736、TPP-11737、TPP-11738と共にインキュベーションした。TrkB活性化を、(A)Y706/707でのTrkBリン酸化又はTrkBの下流である(B)T202/Y204(ERK1)及びT185/Y187(ERK2)それぞれでのERK1/2リン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とする。
DMabによるTrkB活性化は、親C2分子と実質的に同一であった。また、DMabは、親C2分子と同じ性質も示し、BDNFの約40~50%でTrkB活性化の有効性を有する部分的TrkBアゴニスト(pTrkB)として作用した。しかし、DMabは、配列又は配向/レイアウトを変化させることなく、親C2抗体の(Fab)2部分全体を組み込んだが、これは、非常に有望な結果であった。この特異的なフォーマットへのフォーマット化が、TrkBバインダーのTrkB及びTrkB下流シグナル伝達を活性化する能力に負の影響を及ぼさないことを示したためである。予想どおり、アイソタイプ対照はTrkBを活性化しなかった。
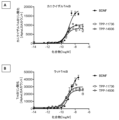
C2、BDNF及び第1シリーズのDoppelmab TPP-11735/736によるカニクイザル/ウサギ/ラット/マウスTrkB活性化の比較
図3A~図3D
(A)カニクイザルTrkB、(B)ウサギTrkB、(C)ラットTrkB又は(D)マウスTrkBを安定に発現するCHO細胞を上昇する濃度の天然のTrkBリガンドであるBDNF、C2抗体又はDoppelmab TPP-11735もしくはTPP-11736と共にインキュベーションした。TrkB活性化をY706/707でのTrkBリン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とする。データは、平均+/-SEMを表わす。
再度、DMabによるTrkB活性化は、親C2分子と実質的に同一であり、活性化は、ヒトTrkBレセプターの活性化と同等であった。このアッセイにおいても、DMabは、親C2分子と同じ特性を示し、BDNFの約40~50%でTrkB活性化の有効性を有する部分的TrkBアゴニスト(pTrkB)として作用した。
TPP-11735/736/737/738媒介性TrkB活性化の選択性
図4A~図4C
(A)ヒトTrkA、(B)ヒトTrkB又は(C)ヒトTrkCを安定に発現するCHO細胞を上昇する濃度のC2抗体又は4つのDoppelmab TPP-11735、TPP-11736、TPP-11737、TPP-11738と共にインキュベーションした。Trkレセプターの活性化を、Y706/707でのレセプターリン酸化を測定することにより評価した。上昇する濃度のTrkA(NGF)、TrkB(BDNF)及びTrkC(NT-3)についての天然のリガンドとのインキュベーションを対照として使用した。最低化合物濃度を溶媒単独とする。データは、平均+/-SEMを表わす。
試験されたDoppelmabはいずれも、TrkA又はTrkCを活性化しなかった。全てのDoppelmabは、TrkBに対して非常に特異的/選択的であった。
ヒトTrkBレセプターのC2、TPP-11736及び/又はBDNF誘発内部移行の比較
図5A~図5B
(A)ヒトTrkBを安定に発現するCHO細胞を上昇する濃度の天然のTrkBリガンドであるBDNF又は上昇する濃度のC2抗体もしくはDoppelmab TPP-11736を伴う1nM BDNFと共にインキュベーションした。(B)TrkB内部移行を、細胞の透過化を伴わない表面TrkBレセプターの免疫蛍光染色、続けて、共焦点顕微鏡分析により評価した。ヒートマップの暗視野及び明視野はそれぞれ、蛍光閾値を上回る細胞の割合の高低を表わす。
BDNFは、TrkBレセプター内部移行を誘発した(レーン1+2;ヒートマップフィールドは、上から下に暗くなっている)。
ヒトVEGFの存在下又は非存在下でのC2及びTPP-11736(第1のシリーズ)によるヒトTrkB活性化の比較
図6
ヒトTrkBを安定に発現するCHO細胞を200ng/mL ヒトVEGF-A(hVEGF)とのプレインキュベーションの有無で、上昇する濃度のC2ツール抗体又はDoppelmab TPP-11736と共にインキュベーションした。TrkB活性化を、TrkBの下流であるT202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化を測定することにより評価した。抗体を伴わない、上昇する濃度のヒトVEGF-Aとのインキュベーションを対照とした。最低化合物濃度を溶媒単独とした。データは、平均を表わす。明確にするために、エラーバーを省略する。
ヒトVEGF単独とのインキュベーションにより、ERK1/2リン酸化は変化しなかった。
STZ誘発糖尿病ラットにおけるDMab 11736及びC2の神経保護の有効性
図7
アゴニスト性TrkBツール抗体(C2)及びDoppelmab TPP-11736のIVT注射を使用した糖尿病誘発網膜神経変性のラットモデルにおけるTrkB活性化の神経保護機能。動物をSTZで処置して、高血糖を誘発した。網膜機能を処置の前後に、網膜電図(ERG)により評価した。糖尿病誘発により、STZ処置後3週間以内に暗示時間の遅延がもたらされた。この時点で、動物に、アイソタイプ対照抗体(抗TNP)もしくはC2(それぞれ19μg/5μL)又は等モル量のTPP-11736(25μg/5μL)を硝子体内投与した。処置の2週間後、ERG記録を繰り返し、分析した。抗体の硝子体内適用の直前及び同適用後2週間での桿体駆動B波暗示置換遅延を図7に示す。平均+/-SEM;n.s.p>0.05、有意差なし;**p<0.01;***p<0.001;テューキーの多重比較検定を使用した一元配置分散分析。
投与の2週間後、抗TNP抗体処置では、抗TNP処置前の時点と比較して、糖尿病誘発桿体駆動b波暗示時間は短縮しなかった(t=2週間で15.4ms対t=0で13.3ms;p>0.05、有意差なし)。
Eylea並びに第1のシリーズの4つのDoppelmab TPP-11735、736、737及び738によるヒトVEGF-Aの捕捉の比較-VEGF誘発VEGFR2リン酸化の阻害
図8A~図8B
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度の示された結合分子又はEyleaとのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。
TPP-11737対TPP-11738:これらの分子は両方とも、scFvとしてG6抗VEGF分子を有した。737は、VH-VL配向で連結されており、一方、738は、VL-VH配向を有する。VL-VH配向は、G6抗VEGF抗体に基づいて、はるかに良好に作用したことが判明した。
Eylea並びに第1のシリーズの4つのDoppelmab TPP-11735、736、737及び738によるヒトVEGF-Aの捕捉の比較-VEGF誘発ERK1/2リン酸化の阻害
図9A~図9B
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度の示された抗体又はEyleaとのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。
TPP-11737対TPP-11738:これらの分子は両方とも、scFvとしてG6抗VEGF分子を有した。737は、VH-VL配向で連結されており、一方、738は、VL-VH配向を有する。VL-VH配向は、G6抗VEGF抗体に基づいて、はるかに良好に作用したことが判明した。
Eylea及び第1のシリーズの4つのDoppelmab TPP-11736によるヒトVEGF-Aの捕捉の比較-VEGF誘発p38 MAPKリン酸化の阻害
図10
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度のTPP-11736又はEyleaとのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-Aの捕捉を、T180/Y182でのp38 MAPKリン酸化を測定することにより評価した。非刺激細胞(ベース)及び抗体処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。
Eylea(IC50=約0.74nM)は、TPP-11736(約7.4nM)より約10倍強力であった
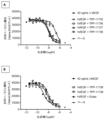
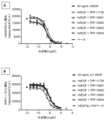
第1のシリーズの4つのDoppelmab TPP-11735、736、737及び738並びにEyleaによるヒトVEGF-Aの捕捉の比較-VEGF誘発性HRMEC増殖の阻害
図11A~図11E
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度の示された結合分子又はEyleaとのプレインキュベーションの有無で、10ng/mL ヒトVEGFと共にインキュベーションした。分子濃度をmol/Lで示す。VEGF-Aの捕捉を、HRMEC細胞数の自動化された画像ベースの定量化により評価した(IncuCyte)。画像を合計96時間にわたって4時間毎に記録した。相対細胞数を示す。t=0での細胞数を1に設定した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。
TPP-11737対TPP-11738:これらの分子は両方とも、scFvとしてG6抗VEGF分子を有した。TPP-11737は、VH-VL配向で連結されており、一方、TPP-11738は、VL-VH配向を有する。明らかに、VL-VH配向は、G6の場合に非常に良好に機能した。TPP-11737の効果は実質的に無かった。
TrkB活性化
DMabによるTrkB活性化は、親C2分子と実質的に同一であった。これは、予想されなかったことである。C2 TrkBバインダーの(Fab)2部全体が、配列又は配向/レイアウトを変化させることなく、DMabに組み込まれたためである。また、全てのDoppelmab(及びC2)は、部分的TrkBアゴニストに過ぎなかった。
明らかに、VL-VH配向は、VEGFバインダーとしてG6及びB20に対してより良好に作用し、B20(VL-VH)は、G6(VL-VH)より有効であった。また、両方のDoppelmab(B20及びG6)は、in vitroにおいてEyleaより劣っていた。
C2、BDNF並びに第1のシリーズの4つのDoppelmab TPP-16061、16062、16063及び16064によるヒトTrkB活性化の比較;TrkBリン酸化
図12
DMab TPP-16061~16064によるTrkB活性化は、親C2分子及びTPP-11736と実質的に同一であった。TrkB活性化は、タンパク質のFcとscFv(抗VEGF)部分との間のリンカーの差異とはほぼ無関係なようであった。これは、予想されたことであった。リンカーが、タンパク質のFcとscFv(抗VEGF)部との間のTrkB(Fab)2フラグメントから離れて位置していたためである。それにもかかわらず、結合分子の活性に影響を及ぼすことなく、種々のリンカーを利用することができるという良好な確証であった。最後に、全ての提示された結合分子は、部分的TrkBアゴニスト活性のみを示した。
BDNF、TPP-11736並びに第1のシリーズの2つのDoppelmab TPP-16061及び16062によるヒトTrkB活性化の比較;ERK1/2リン酸化
図13
ヒトTrkBを安定に発現するCHO細胞を上昇する濃度の天然のTrkBリガンドであるBDNF、TPP-11736(B20、scFv、20L3、VL-VH)又は種々のリンカーを有する2つのDoppelmab TPP-16061(B20、scFv、20L1、VL-VH)及びTPP-16062(B20、scFv、15L1、VL-VH)と共にインキュベーションした。TrkB活性化を、T202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
DMab TPP-16061及び16062によるTrkB活性化は、TPP-11736と実質的に同一であった。また、ここで、TrkB活性化は、リンカーの差異とはほぼ無関係なようであり、提示された結合分子は、部分的TrkBアゴニスト活性のみを示した。
第1のシリーズの4つのDoppelmab TPP-16061、062、063及び064とTPP-11736とによるヒトVEGF-A捕捉の比較-(A)VEGF誘発VEGFR2リン酸化の阻害、(B)ERK1/2リン酸化
図14A~図14B
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度の示された抗体;TPP-11736(B20、scFv、20L3、VL-VH)又は種々のリンカーを有する4つのDoppelmab TPP-16061(B20、scFv、20L1、VL-VH)、TPP-16062(B20、scFv、15L1、VL-VH)、TPP-16063(B20、scFv、10L1、VL-VH)、TPP-16064(B20、scFv、6GS、VL-VH)とのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-Aの捕捉を、(A)Y1175でのVEGFレセプター2(VEGFR2)リン酸化又は(B)T202/Y204(ERK1)及びT185/Y187(ERK2)それぞれでのERK1/2リン酸化を測定することにより評価した。非刺激細胞(ベース)及び抗体処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。
リンカーの差異は、VEGF捕捉の効力又は有効性に実質的に影響を及ぼさなかった。これは、リンカーがVEGF結合部位に近接して位置していたことを考えると、やや予想外であったが、種々のリンカーを結合分子の活性に影響を及ぼすことなく、利用することができることをさらに確認された。
第1のシリーズの4つのDoppelmab TPP-16061、062、063及び064によるヒトVEGF-Aの捕捉の比較-VEGF誘発HRMEC増殖の阻害
図15
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、0.5nM Doppelmab又は1nM Eyleaとのプレインキュベーションの有無で、10ng/mL ヒトVEGFと共にインキュベーションした。VEGF-Aの捕捉を、HRMEC細胞数の自動化された画像ベースの定量化により評価した(IncuCyte)。画像を合計96時間にわたって4時間毎に記録した。相対細胞数を示す。t=0での細胞数を1に設定した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。
実施例15に示されたリン酸化アッセイと同様に、リンカーの差異は、親分子であるTPP-11736と比較して、より良好に(又はより悪く)は機能しなかった。Eyleaを1nMで使用した。Eyleaは一価の分子であると考えられ、一方、Doppelmabは二価であるためである。これらの条件下で、Eyleaは、HRMECのVEGF誘発増殖の阻害においてより良好に機能した。
Eylea、TPP-11736並びに第1のシリーズの4つのDoppelmab TPP-16061、062、063及び064によるヒトVEGF-Aの捕捉の比較-VEGF誘発HRMEC発芽の阻害
図16
ヒト網膜微小血管内皮細胞(HRMEC)のスフェロイドをコラーゲンマトリックス中に包埋した。内皮の発芽を2.5nM 示されたDoppelmab又は5nM Eyleaとの24時間のプレインキュベーションの有無で、50ng/mL ヒトVEGFとのインキュベーションにより24時間誘発した。内皮の発芽を共焦点顕微鏡により評価し、Zスタックの最大投影から得られたスフェロイド外周を示した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。n.s. p>0.05 有意差なし対50ng/mL hVEGF+2.5nM TPP-11736。
実施例15に示されたリン酸化アッセイと同様に、リンカーの差異は、親分子であるTPP-11736と比較して、より良好に(又はより悪く)は機能しなかった。Eyleaを1nMで使用した。Eyleaは一価の分子であると考えられ、一方、Doppelmabは二価であるためである。これらの条件下で、Eyleaは、HRMECのVEGF誘発増殖の阻害においてより良好に機能した。
TrkB活性化:親分子であるTPP-11736と比較して差異/改善は観察されなかった。
TPP-11736及びTPP-13788(B20 IgG)によるヒトVEGF-Aの捕捉の比較-VEGFR2、ERK1/2及びp38 MAPKのVEGF誘発リン酸化の阻害
図17A~図17C
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度のDoppelmab TPP-11736(scFvとしてB20抗VEGF)又はTPP-13788(B20 IgG)とのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-Aの捕捉を、(A)Y1175でのVEGFレセプター2(VEGFR2)リン酸化、(B)T202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化又は(C)T180/Y182でのp38 MAPKリン酸化を測定することにより評価した。分子処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。以下の表4に、対応するベストフィットIC50(非線形回帰;log(アゴニスト)対応答(3つのパラメータ))を報告する。
試験されたB20 IgGであるTPP-13788は、TPP-11736に対して約3倍向上したVEGF-A捕捉能を示す。
TPP-11736及びTPP-13788(B20 IgG)によるヒトVEGF-Aの捕捉の比較-VEGF誘発HRMEC発芽の阻害
図18
ヒト網膜微小血管内皮細胞(HRMEC)のスフェロイドをコラーゲンマトリックスに包埋した。内皮の発芽を2.5nM Doppelmab TPP-11736又は2.5nM TPP-13788(B20 IgG)とのプレインキュベーションの有無で、50ng/mL ヒトVEGFとのインキュベーションにより24時間誘発した。内皮の発芽を共焦点顕微鏡により評価し、Zスタックの最大投影から得られたスフェロイド外周を示した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。n.s. p>0.05 有意差なし対50ng/mL hVEGF+2.5nM TPP-11736。
VEGFR2、ERK1/2及びp38 MAPKリン酸化アッセイにおけるVEGF捕捉の改善にもかかわらず、VEGF誘発発芽のTPP-13788(B20 IgG)媒介性阻害は、TPP-11736の阻害より良好ではなかった。
BDNF、TPP-11736並びに第1のシリーズの2つのDoppelmab TPP-14936及びTPP-14937によるヒトTrkB活性化の比較;TrkB及びERK1/2のリン酸化
図19A~図19C
ヒトTrkBを安定に発現するCHO細胞を、上昇する濃度の天然のTrkBリガンドであるBDNF、TPP-11736(B20、scFv、20L3、VL-VH)又は2つのDoppelmab TPP-13936(Ranibizumab、scFv、20L3、VH-VL)又はTPP-14937(Ranibizumab、scFv、20L3、VL-VH)と共にインキュベーションした。TrkB活性化を、(A)Y706/707でのTrkBリン酸化、(B及びC)T202/Y204(ERK1)及びT185/Y187(ERK2)それぞれでのERK1/2リン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
DMab TPP-14936及びTPP-14937によるTrkB活性化は、TPP-11736と実質的に同一であった。これは、予想されたことであった。結合分子のTrkB結合成分が、常に、FabフラグメントとしてのC2であったためである。
BDNF、TPP-11736及びDoppelmab TPP-14936によるカニクイザルとラットのTrkB活性化の比較;TrkBリン酸化
図20A~図20B
(A)カニクイザルTrkB又は(B)ラットTrkBを安定に発現するCHO細胞を、上昇する濃度の天然のTrkBリガンドであるBDNF、TPP-11736(B20、scFv、20L3、VL-VH)又はTPP-14936(Ranibizumab、scFv、20L3、VH-VL)と共にインキュベーションした。TrkB活性化を、Y706/707でのTrkBリン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
DMab TPP-14936によるTrkB活性化は、TPP-11736と実質的に同一であった。再度、これは、予想されたことであった。2つの分子のTrkB結合成分が、両方の場合において、FabフラグメントとしてのC2であるためである。
TPP-11736、TPP-14936又はTPP-14937によるヒトVEGF-A捕捉の比較-VEGFR2、ERK1/2及びSrcのVEGF誘発リン酸化の阻害
図21A~図21C
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度のDoppelmab TPP-11736(B20、scFv、20L3、VL-VH)、TPP-14936(Ranibizumab、scFv、20L3、VH-VL)又はTPP-14937(Ranibizumab、scFv、20L3、VL-VH)とのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-A捕捉を、(A)Y1175でのVEGFレセプター2(VEGFR2)リン酸化、(B)T202/Y204及びT185/Y187でのERK1/2リン酸化又は(C)Y419でのSrcリン酸化を測定することにより評価した。抗体処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。以下の表5に、対応するベストフィットIC50値及び絶対有効性値(底部のプラトー)をそれぞれ報告する(非線形回帰;log(アゴニスト)対応答(3つのパラメータ))。
VEGF捕捉の効力(IC50)は、TPP-11736とTPP-14936/TPP-14937との間で同様である。
TPP-11736及びDoppelmab TPP-14936及びTPP-14937によるヒトVEGF-A捕捉の比較-VEGF誘発HRMEC発芽の阻害
図22
ヒト網膜微小血管内皮細胞(HRMEC)のスフェロイドをコラーゲンマトリックス中に包埋した。内皮の発芽を2.5nM Doppelmab TPP-11736(B20、scFv、20L3、VL-VH)、TPP-14936(Ranibizumab、scFv、20L3、VH-VL)又はTPP-14937(Ranibizumab、scFv、20L3、VL-VH)とのプレインキュベーションの有無で、50ng/mL ヒトVEGFとのインキュベーションにより24時間誘発した。内皮の発芽を共焦点顕微鏡により評価し、Zスタックの最大投影から得られたスフェロイド外周を示した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。n.s. p>0.05 有意差なし、****p<0.0001。
TPP-14936及びTPP-14937によるVEGF捕捉は、VEGFR2/ERK1_2/Srcリン酸化アッセイにおいて同様であったが、VEGF誘発発芽の阻害には、劇的な差があった。TPP-11736とTPP-14937との間に有意差はなかったが、TPP-14936によるVEGF誘発HRMEC発芽の阻害は、TPP-14937又はTPP-11736よりはるかに有効であった。
Doppelmab TPP-11736、TPP-14936及びTPP-14937並びにEyleaによるヒトVEGF-A捕捉の比較-VEGF誘発HRMEC増殖の阻害
図23A~図23D
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度の示された結合分子又はEyleaとのプレインキュベーションの有無で、10ng/mL ヒトVEGFと共にインキュベーションした。結合分子/Eylea濃度をmol/Lで示す。VEGF-Aの捕捉を、HRMEC細胞数の自動化された画像ベースの定量化により評価した(IncuCyte)。画像を合計84時間にわたって4時間毎に記録した。相対細胞数を示す。t=0での細胞数を1に設定した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。
TPP-14936及びTPP-14937は、TPP-11736と比較して、より良好な効力、特に、VEGF誘発HRMEC増殖の阻害の有効性を示した。TPP-14936は、TPP-14937より強力であった。
TrkB活性化:TPP-11736と比較して、差異/改善は観察されなかった。両方の結合分子が、FabフラグメントとしてC2バインダーを有していたため、この種のことは、予想されたことであった。
リン酸化アッセイ:VEGF捕捉の効力(IC50)は、TPP-11736とTPP-14936/TPP-14937との間で同様であった。TPP-14936及びTPP-14937によるVEGF捕捉は、TPP-11736より有効であった(底部の値)。
BDNF、TPP-11736並びに第2のシリーズの4つのDoppelmab TPP-14938、TPP-14939、TPP-14940及びTPP-14941によるヒトTrkB活性化の比較;TrkB及びERK1/2のリン酸化
図24A~図24B及び図25
ヒトTrkBを安定に発現するCHO細胞を、上昇する濃度の天然のTrkBリガンドであるBDNF、TPP-11736(FabとしてのC2)又は第2のシリーズの4つのDoppelmab TPP-14938(scFvとしてのC2、20L3、VH-VL)、TPP-14939(scFvとしてのC2、20L3、VL-VH)、TPP-14940(scFvとしてのC2、20L3、VH-VL)及びTPP-14941(scFvとしてのC2、20L3、VL-VH)と共にインキュベーションした。TrkB活性化を、(A)Y706/707でのTrkBリン酸化を測定することにより又は(B)T202/Y204(ERK1)及びT185/Y187(ERK2)それぞれでのERK1/2リン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
TPP-11736は、FabとしてC2 CDRを含有した。4つのDoppelmab TPP-14938、TPP-14939、TPP-14940及びTPP-14941は、scFvとしてC2を含有した。
BDNF、TPP-11736並びに第2のシリーズの4つのDoppelmab TPP-14938、TPP-14939、TPP-14940及びTPP-14941によるカニクイザル/ラットTrkB活性化の比較;TrkB及びERK1/2リン酸化
図26A~図26B
(A)カニクイザルTrkB又は(B)ラットTrkBを安定に発現するCHO細胞を、上昇する濃度の天然のTrkBリガンドであるBDNF、TPP-11736(FabとしてのC2)又は第2のシリーズの2つのDoppelmab TPP-14940(scFvとしてのC2、20L3、VH-VL)及びTPP-14941(scFvとしてのC2、20L3、VL-VH)と共にインキュベーションした。TrkB活性化を、Y706/707でのTrkBリン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
ヒトTrkBについての実施例25の結果をカニクイザル及びラットのモデルにおいて再現することができた。また、ここでは、TPP-11736とは非常に対照的に、新規なDoppelmabは、完全なTrkBレセプターアゴニストであった。これらのDoppelmabによるTrkB活性化は、天然のリガンドであるBDNFと同様に有効であった。
ヒトVEGFの存在下又は非存在下における、C2、TPP-14940及びTPP-14941(第2のシリーズ)によるヒトTrkB活性化(TrkBリン酸化)の比較-相乗効果
図27A~図27C
ヒトTrkBを安定に発現するCHO細胞を200ng/mL ヒトVEGF-A(hVEGF)とのプレインキュベーションの有無で、上昇する濃度のDoppelmab(A)TPP-14940、(B)TPP-14941又は(C)C2と共にインキュベーションした。TrkB活性化を、Y706/707でのTrkBリン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
驚くべきことに、ヒトVEGFとのプレインキュベーションにより、TPP-14941(scFvとしてのC2、20L3、VL-VH)によるTrkBリン酸化(TrkB活性化)の効力が劇的に改善された。
ヒトVEGFの存在下又は非存在下における、C2、TPP-14940及びTPP-14941(第2のシリーズ)によるヒトTrkB活性化(ERK1/2リン酸)の比較-相乗効果
図28A~図28C
ヒトTrkBを安定に発現するCHO細胞を200ng/mL ヒトVEGF-A(hVEGF)とのプレインキュベーションの有無で、上昇する濃度のDoppelmab(A)TPP-14940、(B)TPP-14941又は(C)C2と共にインキュベーションした。TrkB活性化を、TrkBの下流であるT202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とする。データは、平均+/-SEMを表わす。
ここでも、驚くべきことに、ヒトVEGFとのプレインキュベーションにより、TPP-14941(scFvとしてのC2、20L3、VL-VH)によるERK1/2リン酸化(TrkB活性化)の効力が劇的に改善された。
VEGF単独及びBDNFとの組み合わせによるヒトTrkB活性化(TrkB/ERKリン酸化)の比較-相乗効果についての対照実験
図29A~図29B
ヒトTrkBを安定に発現するCHO細胞を、固定濃度の200ng/mL hVEGFを伴って又は伴わずに、上昇する濃度のヒトVEGF-A(hVEGF)単独又は上昇する濃度のBDNFと共にインキュベーションした。TrkBの活性化を、(A)Y706/707でのTrkBリン酸化又は(B)TrkBの下流であるT202/Y204(ERK1)及びT185/Y187(ERK2)それぞれでのERK1/2リン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
hVEGF単独では、TrkB又はERK1/2のリン酸化が誘発されなかった。
ヒトVEGFの存在下又は非存在下における、C2、TPP-14940及びTPP-14941(第2のシリーズ)によるカニクイザルTrkB活性化(TrkBリン酸)の比較-相乗効果
図30A~図30C
カニクイザルTrkBを安定に発現するCHO細胞を200ng/mL ヒトVEGF-A(hVEGF)とのプレインキュベーションの有無で、上昇する濃度のDoppelmab(A)TPP-14940、(B)TPP-14941又は(C)C2と共にインキュベーションした。TrkB活性化を、Y706/707でのTrkBリン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
また、このモデルでも、ヒトVEGFとのプレインキュベーションにより、TPP-14941(scFvとしてのC2、20L3、VL-VH)によるTrkBリン酸化(TrkB活性化)の効力が劇的に改善された。TPP-14940(scFvとしてのC2、20L3、HL)によるTrkBリン酸化(TrkB活性化)の効力に対するVEGFの影響はより小さかった。
ヒトVEGFの存在下又は非存在下における、C2、TPP-14940及びTPP-14941(第2のシリーズ)によるカニクイザルTrkB活性化(ERK1/2リン酸化)の比較-相乗効果
図31A~図31C
カニクイザルTrkBを安定に発現するCHO細胞を200ng/mL ヒトVEGF-A(hVEGF)とのプレインキュベーションの有無で、上昇する濃度のDoppelmab(A)TPP-14940、(B)TPP-14941又は(C)C2と共にインキュベーションした。TrkB活性化を、TrkBの下流であるT202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
また、このモデルでも、ヒトVEGFとのプレインキュベーションにより、TPP-14941(scFvとしてのC2、20L3、VL-VH)によるERK1/2リン酸化(TrkB活性化)の効力が劇的に改善された。TPP-14940(scFvとしてのC2、20L3、HL)によるERK1/2リン酸化(TrkB活性化)の効力に対するVEGFの影響はより小さかった。
TPP-11736(scFvとしてB20)、TPP-14938(FabとしてB20)又はTPP-14939(FabとしてB20)によるヒトVEGF-A捕捉の比較-VEGFR2、ERK1/2及びSrcのVEGF誘発リン酸化の阻害
図32A~図32C
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度のDoppelmab TPP-11736(scFvとしてのB20)、TPP-14938(FabとしてのB20)又はTPP-14939(FabとしてのB20)とのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-A捕捉を、(A)Y1175でのVEGFレセプター2(VEGFR2)リン酸化、(B)T202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化又は(C)Y419でのSrcリン酸化を測定することにより評価した。抗体処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。以下の表6に、対応するベストフィットIC50値及び絶対有効性値(底部のプラトー)をそれぞれ報告する(非線形回帰;log(アゴニスト)対応答(3つのパラメータ))。
TPP-14938/39によるVEGF捕捉の効力(IC50)は、TPP-11736より幾らか良好であった。
TPP-11736(B20 scFv)、TPP-14938(B20 Fab)又はTPP-14939(B20 Fab)によるヒトVEGF-A捕捉の比較-HRMECのVEGF誘発増殖の阻害
図33A~図33C
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度の示された結合分子とのプレインキュベーションの有無で、10ng/mL ヒトVEGFと共にインキュベーションした。分子濃度をmol/Lで示す。VEGF-A捕捉を、HRMEC細胞数の自動化された画像ベースの定量化により評価した(IncuCyte)。画像を合計84時間にわたって4時間毎に記録した。相対細胞数を示す。t=0での細胞数を1に設定した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。
B20 scFv(TPP-11736)をB20 Fab(TPP-14938及びTPP-14939)に再フォーマット化することによっては、増殖アッセイにおいて、VEGF-A捕捉の効力も有効性も改善されなかった。実際、B20 Fabベースの抗体は、TPP-11736より効力/有効性が幾らか低いと考えられた。
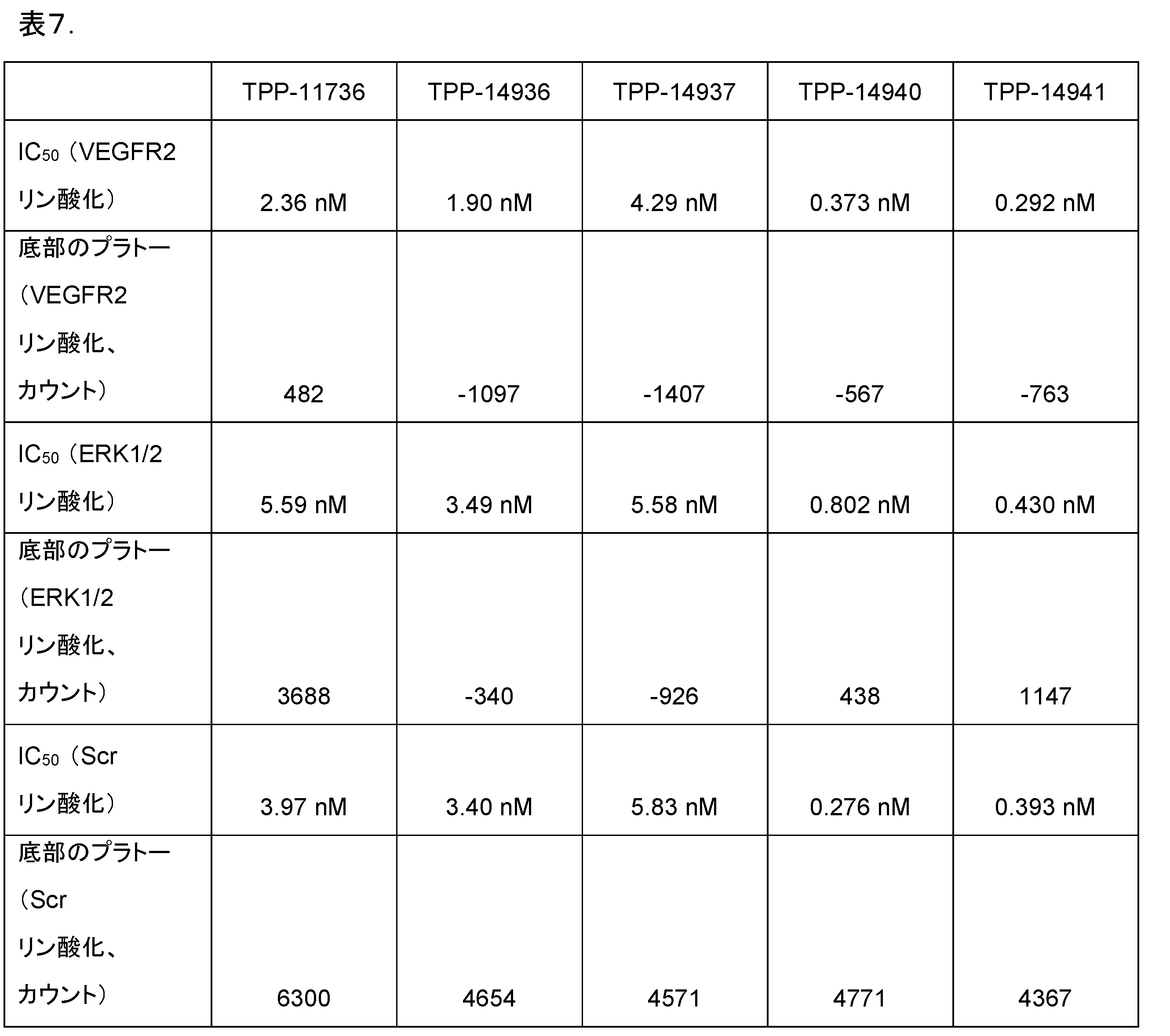
TPP-14936(Ranibizumab、scFv、HL)又はTPP-14937(Ranibizumab、scFv、LH)とTPP-14940及びTPP-14941(Ranibizumab Fab)とによるヒトVEGF-A捕捉の比較-VEGFR2、ERK1/2及びSrcのVEGF誘発リン酸化の阻害
図34A~図34C
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度のDoppelmab TPP-11736(scFvとしてのB20)、TPP-14936(scFvとしてのRanibizumab VH-VL)、TPP-14937(scFvとしてのRanibizumab、VL-VH)、TPP-14940(FabとしてのRanibizumab)又はTPP-14941(FabとしてのRanibizumab)とのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-A捕捉を、(A)Y1175でのVEGFレセプター2(VEGFR2)リン酸化、(B)T202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化又は(C)Y419でのSrcリン酸化を測定することにより評価した。抗体処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。以下の表7に、対応するベストフィットIC50値及び絶対有効性値(底部のプラトー)をそれぞれ報告する(非線形回帰;log(アゴニスト)対応答(3つのパラメータ))。
scFvからFabにRanibizumabに再フォーマット化することにより、3つ全てのアッセイにおいて、VEGF捕捉の効力が劇的に改善された(Ranibizumab scFv又は参照である分子TPP-11736より10倍良好なIC50)。
TPP-14936(scFvとしてのRanibizumab、VH-VL)又はTPP-14937(scFvとしてのRanibizumab、VL-VH)とTPP-14940及びTPP-14941(Ranibizumab Fab)とによるヒトVEGF-A捕捉の比較-HRMECのVEGF誘発増殖の阻害
図35A~図35D
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度の示された結合分子のプレインキュベーションの有無で、10ng/mL ヒトVEGFと共にインキュベーションした。分子濃度をmol/Lで示す。VEGF-A捕捉を、HRMEC細胞数の自動化された画像ベースの定量化により評価した(IncuCyte)。画像を合計84時間にわたって4時間毎に記録した。相対細胞数を示す。t=0での細胞数を1に設定した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。
scFvとしてのRanibizumab(TPP-11736/TPP-14937)をRanibizumab Fab(TPP-14940及びTPP-14941)に再フォーマット化することにより、増殖アッセイにおいて、VEGF-A捕捉の効力が顕著に改善された。
TPP-14938又はTPP-14939(B20 Fab)とTPP-14940及びTPP-14941(Ranibizumab Fab)とによるヒトVEGF-A捕捉の比較-VEGFR2、ERK1/2及びSrcのVEGF誘発リン酸化の阻害
図36A~図36C
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度のDoppelmab TPP-11736(scFvとしてのB20)、TPP-13938(FabとしてのB20)又はTPP-13939(FabとしてのB20)、TPP-14940(FabとしてのRanibizumab)又はTPP-14941(FabとしてのRanibizumab)とのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-A捕捉を、(A)Y1175でのVEGFレセプター2(VEGFR2)リン酸化、(B)T202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化又は(C)Y419でのSrcリン酸化を測定することにより評価した。分子処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。以下の表8に、対応するベストフィットIC50値及び絶対有効性値(底部のプラトー)をそれぞれ報告する(非線形回帰;log(アゴニスト)対応答(3つのパラメータ))。
Ranibizumab Fabを有するDoppelmabは、3つのアッセイ全てにおいて、B20 Fabに基づくDoppelmabよりVEGF捕捉の効力が明らかに良好であることを示した。
TPP-14938又はTPP-14939(FabとしてのB20)とTPP-14940及びTPP-14941(FabとしてのRanibizumab)とによるヒトVEGF-A捕捉の比較-HRMECのVEGF誘発増殖の阻害
図37A~図37D
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度の示された結合分子とのプレインキュベーションの有無で、10ng/mL ヒトVEGFと共にインキュベーションした。分子濃度をmol/Lで示す。VEGF-A捕捉を、HRMEC細胞数の自動化された画像ベースの定量化により評価した(IncuCyte)。画像を合計84時間にわたって4時間毎に記録した。相対細胞数を示す。t=0での細胞数を1に設定した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。
RanibizumabFabベースの分子であるTPP-14940及びTPP-14941によるVEGF誘発増殖の阻害の効力及び有効性は、B20 Fabベースの分子であるTPP-14938及びTPP-14939と比較して明らかに優れていた。
Doppelmab TPP-11736(scFvとしてのB20)、TPP-14936(scFvとしてのRanibizumab、VH-VL)、TPP-14937(scFvとしてのRanibizumab、VL-VH)、TPP-14938(FabとしてのB20)もしくはTPP-14939(B20 Fab)、TPP-14940(FabとしてのRanibizumab)、TPP-14941(FabとしてのRanibizumab)又はEyleaによるヒトVEGF-A捕捉の比較-VEGF誘発HRMEC発芽の阻害
図38
ヒト網膜微小血管内皮細胞(HRMEC)のスフェロイドをコラーゲンマトリックス中に包埋した。内皮の発芽を2.5nM Doppelmab TPP-11736(B20 scFv)、TPP-14936(Ranibizumab scFv、VH-VL)、TPP-14937(Ranibizumab scFv、VL-VH)、TPP-14938(B20 Fab)、TPP-14939(B20 Fab)、TPP-14940(Ranibizumab Fab)、TPP-14941(Ranibizumab Fab)又は5nM Eyleaとのプレインキュベーションの有無で、50ng/mL ヒトVEGFとのインキュベーションにより24時間誘発した。内皮の発芽を共焦点顕微鏡により評価し、Zスタックの最大投影から得られたスフェロイド外周を示した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。n.s. p>0.05 有意差なし;50ng/mL hVEGFと比較して、§p<0.0001;50ng/mL hVEGFと比較して、#p>0.05 有意差なし。***p<0.001;テューキーの多重比較検定を使用した一元配置分散分析。
Ranibizumab FabベースのDoppelmab TPP-14940及びTPP-14941は、明らかに、このアッセイにおいて、最良のVEGF捕捉剤であった。Eyleaとは対照的に、TPP-14940及びTPP-14941は、VEGF誘発発芽を完全に阻害した。VEGFの非存在下(ベース)での内皮発芽と2.5nM TPP-14940又はTPP-14941と共にプレインキュベーションされた50ng/mL hVEGFとの間に統計的有意差は見られなかった。
Doppelmab TPP-11940及びEyleaによるヒトVEGF-A捕捉の比較-Brown NorwayラットにおけるヒトVEGF-A誘発網膜透過性亢進の阻害
図39A~図39B
TPP-14940(Eyleaではない)は、ラット網膜におけるヒトVEGF-A誘発透過性亢進を予防した。(A)実験手法を示す時間プロトコール。抗VEGF化合物(13又は26pmol/眼 Eylea又はTPP-14940)又は対照(26pmol TPP-11737)の硝子体内(ivt)投与の15分後、13pmol ヒトVEGF-A/眼をivt注射により投与した。PBS注射を対照とした。24時間後、1mL/kg エバンスブルー(EB)溶液(0.9% 生理食塩水中の45mg/mL)を静脈内(iv)注射により30分間投与し、その後、眼を単離し、固定した。同じ時点で、血漿サンプルを収集し、全身EB曝露量が等しいことを確認した。(B)Brown Norwayラットの網膜におけるVEGF-A誘発透過性亢進の定量を、共焦点顕微鏡により網膜フラットマウントにおけるEB血管外漏出を測定することにより行った。眼を鋸状縁に沿って切断し、水晶体及び硝子体を除去し、眼杯をパラホルムアルデヒド(4%)中において、4℃で1時間固定し、ついで、4℃で一晩PBSに移した。網膜を外側セグメント(強膜及び脈絡膜)から分離し、スライドガラスに移し、4回切断して、平坦なクローバー葉様構造を達成した。組織をマウンティング媒体(DNA染色DAPIを含有するVectashield H-1200)で覆い、カバースリップを上に置き、網膜フラットマウントを得た。サンプルを639nmの波長で励起し、669nmでのエバンスブルーの発光をLSM 700共焦点レーザー走査顕微鏡(Carl Zeiss, Jena;ゲイン800、レーザー強度2%、5スタック 60μm)で記録し、最大強度投影を有する網膜フラットマウントの画像を得た。蛍光強度の合計の分析を30の閾値でプログラムImageJ中において画像を開いた後に行った。***p<0.001;*p<0.05;n.s. p>0.05;#p>0.05 TPP-11737+PBSに対して有意差なし。テューキーの多重比較検定を使用した一元配置分散分析。n=9~17。
対照条件下で、硝子体内VEGF-A注射により、血管透過性が約60%向上した。TPP-14940と同じ分子フォーマット(Doppelmab)を有するため、TPP-11737を対照抗体として使用したが、初期のin vitroアッセイでは、この化合物はVEGFを捕捉しなかった。
TrkB活性化
TPP-11736とは非常に対照的に、4つの新規な「Doppelmabは全て、完全なTrkBレセプターアゴニストであった。これらのDoppelmabによるTrkB活性化は、天然のリガンドであるBDNFと同様に有効であった。
B20 scFv(TPP-11736)をB20 Fab(TPP-14938及びTPP-14939)に再フォーマット化することによっては、増殖アッセイにおいて、VEGF-A捕捉の効力も有効性も改善されなかった。
BDNF、TPP-14940[C2、scFv、20L3、VH-VL]又はそのリンカー変形形態であるTPP-19986[C2、scFv、10L1、VH-VL]もしくはTPP-19987[C2、scFv、20L1、VH-VL]又はTPP-14941[C2、scFv、20L3、VL-VH]及びそのリンカー変形形態であるTPP-19988[C2、scFv、10L1、VL-VH]もしくはTPP-19989[C2、scFv、20L1、VL-VH]によるヒトTrkB活性化の比較;TrkB及びERK1/2のリン酸化-シリーズ3
図40A~図40D
ヒトTrkBを安定に発現するヒトCHO細胞を上昇する濃度の天然のTrkBリガンドであるBDNF、TPP-14940[C2、scFv、20L3、VH-VL]又はそのリンカー変形形態であるTPP-19986[C2、scFv、10L1、VH-VL]もしくはTPP-19987[C2、scFv、20L1、VH-VL]又はTPP-14941[C2、scFv、20L3、V-VH]及びそのリンカー変形形態であるTPP-19988[C2、scFv、10L1、VL-VH]もしくはTPP-19989[C2、scFv、20L1、VL-VH]と共にインキュベーションした。TrkB活性化を、(A及びB)Y706/707でのTrkBリン酸化を測定することにより又は(C及びD)T202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化をそれぞれ測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。以下の表9及び表10に、TrkB及びERK1/2リン酸化の対応するベストフィットIC50値及び絶対有効性値(底部のプラトー)をそれぞれ報告する(非線形回帰;log(アゴニスト)対応答(3つのパラメータ))。
親分子と各リンカー変形形態との間に有意差は無かった。TrkB及びERK1/2のリン酸化の効力及び有効性は、実質的に同一であった。これは、注目に値する。リンカーが、TrkB結合部位の近くに位置していたが、結合分子の生体活性には影響を及ぼさなかったためである。
BDNF、TPP-14940[C2、scFv、20L3、VH-VL]又はTPP-14941[C2、scFv、20L3、VL-VH]及びリンカー変形形態であるTPP-19988[C2、scFv、10L1、VL-VH]もしくはTPP-19989[C2、scFv、20L1、VL-VH]によるヒトTrkB内部移行の比較-シリーズ3
図41A~図41B
カニクイザルTrkBを安定に発現するCHO細胞を、上昇する濃度の天然のTrkBリガンドであるBDNF又は上昇する濃度の第1のシリーズのDoppelmab TPP-14940[C2、scFv、20L3、VH-VL]もしくはTPP-14941[C2、scFv、20L3、VL-VH]及びリンカー変形形態であるTPP-19988[C2、scFv、10L1、VL-VH]もしくはTPP-19989[C2、scFv、20L1、VL-VH]を伴う1nM BDNFと共にインキュベーションした。TrkB内部移行を細胞の透過化を伴わない表面TrkBレセプターの免疫蛍光染色、続けて、共焦点顕微鏡分析により評価した。ヒートマップの暗視野及び明視野はそれぞれ、蛍光閾値を上回る細胞の割合の高低を表わす。
BDNFにより、TrkBレセプター内部移行が誘発された。TPP-14940、TPP-14941、TPP-19988及びTPP-19989は、完全なTrkBレセプターアゴニストであったが、Doppelmabのいずれによっても、BDNF誘発レセプター内部移行を増加せず、むしろ、TrkBレセプターのBDNF誘発内部移行が減少した(注:ヒートマップフィールドは、下から上へ暗くなっている)。
TPP-14940並びにそのリンカー変形形態であるTPP-19986及びTPP-14941並びにそのリンカー変形形態であるTPP-19988によるヒトVEGF-A捕捉の比較-VEGFR2のVEGF誘発リン酸化の阻害-シリーズ3
図42
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度のDoppelmab TPP-14940並びにそのリンカー変形形態であるTPP-19986及びTPP-14941並びにそのリンカー変形形態であるTPP-19988とのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-A捕捉を、Y1175でのVEGFレセプター2(VEGFR2)リン酸化を測定することにより評価した。分子処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。以下の表11に、VEGFR2リン酸化の阻害の対応するベストフィットIC50値(非線形回帰;log(アゴニスト)対応答(3つのパラメータ))を報告する。
親分子であるTPP-14940/TPP-14941と各リンカー変形形態との間に有意差は無かった。VEGF誘発VEGFR2リン酸化の阻害の効力及び有効性は、実質的に同一であった。
Doppelmab TPP-14940[C2、scFv、20L3、VH-VL]又はそのリンカー変形形態であるTPP-19986[C2、scFv、10L1、VH-VL]もしくはTPP-19987[C2、scFv、20L1、VH-VL]又はTPP-14941[C2、scFv、20L3、VL-VH]及びそのリンカー変形形態であるTPP-19988[C2、scFv、10L1、VL-VH]もしくはTPP-19989[C2、scFv、20L1、VL-VH]によるヒトVEGF-A捕捉の比較-VEGF誘発HRMEC発芽の阻害-シリーズ3
図43
ヒト網膜微小血管内皮細胞(HRMEC)のスフェロイドをコラーゲンマトリックスに包埋した。内皮の発芽を2.5nM Doppelmab TPP-11736(B20 scFv)、TPP-14940[C2、scFv、20L3、VH-VL]又はそのリンカー変形形態であるTPP-19986[C2、scFv、10L1、VH-VL]もしくはTPP-19987[C2、scFv、20L1、VH-VL]又はTPP-14941[C2、scFv、20L3、VL-VH]及びそのリンカー変形形態であるTPP-19988[C2、scFv、20L1、VL-VH]もしくはTPP-19989[C2、scFv、20L1、VL-VH]とのプレインキュベーションの有無で、50ng/mL ヒトVEGFとのインキュベーションにより24時間誘発した。内皮の発芽を共焦点顕微鏡により評価し、Zスタックの最大投影から得られたスフェロイド外周を示した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。n.s. p>0.05 有意差なし;50ng/mL hVEGFと比較して、§p<0.0001;50ng/mL hVEGFと比較して、#p>0.05 有意差なし。***p<0.001;テューキーの多重比較検定を使用した一元配置分散分析。
親分子であるTPP-14940/TPP-14941と各リンカー変形形態との間に、有意差は観察されなかった。全ての分子が、HRMECのVEGF誘発発芽を完全に阻害した。
TrkB活性化
親分子(TPP-14940/14941)と各リンカー変形形態との間に、有意差は観察されなかった。
親分子(TPP-14940/14941)とそれぞれのリンカー変形形態との間に、有意差は観察されなかった。
リンカー10L1及び20L1リンカーの使用により、リンカークリッピングは、もはや観察されなかった(データを示さず)。
TrkB scFv部分におけるジスルフィド架橋(CC)の有無でのDoppelmabによるヒトTrkB活性化の比較;TrkBリン酸化-シリーズ4
図44A~図44D
ヒトTrkBを安定に発現するCHO細胞を抗TrkB scFv部分におけるCC架橋の有無で、上昇する濃度の示されたDoppelmabと共にインキュベーションした。(A)TPP-22180対TPP-22204;(B)TPP-22192対TPP-22216;(C)TPP-22190対TPP-22214;(D)TPP-22191対TPP-22215。TrkB活性化を、Y706/707でのTrkBリン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。以下の表12に、TrkB活性化の対応するベストフィットIC50値及び絶対又は相対有効性値(上部のプラトー)をそれぞれ報告する(非線形回帰;log(アゴニスト)対応答(3つのパラメータ))。
ジスルフィド架橋を主に、結合分子のCMC特性を改善するのに導入した。驚くべきことに、scFv抗TrkB部分にジスルフィド架橋を含ませることにより、TrkB活性化の効力及び有効性の両方がさらに改善された。VL-VH配向を有する結合分子において、より大きな影響が観察された。
TrkB scFv部分におけるジスルフィド架橋(CC)の有無でのDoppelmabによるラットTrkB活性化の比較;TrkBリン酸化-シリーズ4
図45A~図45B
ラットTrkBを安定に発現するCHO細胞を抗TrkB scFv部分におけるCC架橋の有無で、上昇する濃度の示されたDoppelmabと共にインキュベーションした。(A)TPP-22180対TPP-22204;(B)TPP-22192対TPP-22216。TrkB活性化を、Y706/707でのTrkBリン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。以下の表13に、TrkB活性化の対応するベストフィットIC50値及び絶対又は相対有効性値(上部のプラトー)をそれぞれ報告する(非線形回帰;log(アゴニスト)対応答(3つのパラメータ))。
scFv抗TrkB部品にジスルフィド架橋を含ませることにより、TrkB活性化の効力及び有効性の両方が改善された。再度、VL-VH配向の結合分子に対する影響は、より大きいようであった。全体として、データは、ヒトTrkBについて得られたデータと良好に一致した。
TPP-22204/22214媒介性TrkB活性化の選択性
図46
(A)ヒトTrkA、(B)ヒトTrkB又は(C)ヒトTrkCを安定に発現するCHO細胞を上昇する濃度のC2抗体又はDoppelmab TPP-22204もしくはTPP-22214と共にインキュベーションした。Trkレセプターの活性化を、Y706/707でのレセプターリン酸化を測定することにより評価した。上昇する濃度のTrkA(NGF)、TrkB(BDNF)及びTrkC(NT-3)についての天然のリガンドとのインキュベーションを対照として使用した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
両方のDoppelmabとも、TrkBに非常に特異的/選択的であった-それらは、TrkA又はTrkCのいずれも活性化しなかった。
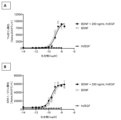
BDNF誘発TrkB活性化に対するTPP-22214の影響
図47A~図47B
ヒトTrkBレセプターを安定に発現するCHO細胞を、一定濃度の0.3nM、1nM又は3nM BDNFの有無で、上昇する濃度の(A)C2抗体又は(B)Doppelmab TPP-22214と共にインキュベーションした。TrkBの活性化を、Y706/707でのレセプターリン酸化を測定することにより評価した。データは、平均+/-SEMを表わす。
C2とは非常に対照的に、TPP-22214は、BDNF誘発TrkB活性化を制限しなかった。
ヒトVEGFの存在下又は非存在下におけるTPP-22214によるヒトTrkB活性化(TrkBリン酸化)の比較
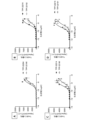
図48A~図48D
ヒトTrkBを安定に発現するCHO細胞を、(A)200ng/mL ヒトVEGF-A(hVEGF)、(B)50ng/mL hVEGF、(C)10ng/mL hVEGF、又は(D)2ng/mL hVEGFとのプレインキュベーションの有無で、上昇する濃度のDoppelmab TPP-22214と共にインキュベーションした。TrkB活性化を、Y706/707でのTrkBリン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
先に示されたように、200ng/mL ヒトVEGFとのプレインキュベーションにより、TPP-22214によるTrkBリン酸化(TrkB活性化)の効力が改善された。より重要なことには、この相乗効果が、50、10、さらには2ng/mL hVEGFでほぼ保持された。また、同様の効果が、他の種、例えば、カニクイザルでも得られた(データを示さず)。
ヒトVEGFの存在下又は非存在下におけるTPP-22214によるヒトTrkB活性化(ERKリン酸化)の比較
図49A~図49D
ヒトTrkBを安定に発現するCHO細胞を(A)200ng/mL ヒトVEGF-A(hVEGF)、(B)50ng/mL hVEGF、(C)10ng/mL hVEGF又は(D)2ng/mL hVEGFとのプレインキュベーションの有無で、上昇する濃度のDoppelmab TPP-22214と共にインキュベーションした。TrkBの活性化を、TrkBの下流であるT202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
同様に、200ng/mL ヒトVEGFとのプレインキュベーションにより、TPP-22214によるTrkB活性化の下流のERKリン酸化の効力も改善された。また、このアッセイにおいて、相乗効果は、2ng/mL hVEGFという低い濃度でほぼ保持された。同様の効果が、他の種、例えば、カニクイザルでも得られた(データを示さず)。
VEGF結合によりTrkB活性化が増強される-提案されたメカニズムの研究
図50
TPP-22214とhVEGFとの複合体を1×ダルベッコPBS中において、記載されたモル比(1:1、4:1又は20:1)でサンプル同士を混合することにより調製した。サンプルを室温で1時間インキュベーションし、その後、分析した。Agilent 1200をmini DAWN TREOS及びOptilab REXと繋げて使用した。サンプルを、移動相としての1×ダルベッコPBS中において、0.6ml/分の流量で流した。複合体又はTPP-22214単独 100μlをSuperose 6 Increaseカラム(30cm×10mm)に注入し、そこで、分子を流体力学的体積による分離に供した。ついで、データを、Astra 6.1.1.17を使用して分析した。
TPP-22214は、VEGF-Aの存在下で複合体を形成する。最大の複合体は、1:1のモル比で形成される。これらの複合体は、DoppelmabとVEGFとの1:1の比を超える複合体形成を示唆している。これらのより大きな複合体は、細胞表面上のTrkBレセプターのクラスター形成をもたらす場合がある。実験データは、提案されたメカニズムを支持している。
上昇する濃度のBDNF又はTPP-22214及び1nM BDNFの存在下での上昇する濃度のTPP-22214によるヒトTrkB内部移行の比較
図51A~図51C
ヒトTrkBを安定に発現するCHO細胞を(A)上昇する濃度の天然のTrkBリガンドであるBDNF、(B)上昇する濃度のTPP-22214又は(C)上昇する濃度のTPP-22214を伴う1nM BDNFと共にインキュベーションした。TrkB内部移行を、細胞の透過化を伴わない表面TrkBレセプターの免疫蛍光染色、続けて、共焦点顕微鏡分析により評価した。データは、閾値を上回る表面TrkB染色強度を有する細胞の割合を表わす;平均+/-SEM。
(A)BDNFとのインキュベーションにより、TrkBレセプター内部移行が誘発された。
STZ誘発糖尿病ラットにおけるTPP-22214及びC2の神経保護効果
図52
アゴニスト性TrkB抗体(C2)及びDoppelmab TPP-22214のIVT注射を使用した糖尿病誘発網膜神経変性のラットモデルにおけるTrkB活性化の神経保護機能。動物をSTZで処置して、高血糖を誘発した。網膜機能を処置の前後に、網膜電図(ERG)により評価した。糖尿病誘発により、STZ処置後3週間以内に暗示時間の遅延がもたらされた。この時点で、動物に、アイソタイプ対照抗体(抗TNP)もしくはC2(それぞれ19μg/5μL)又は等モル量のTPP-22214(25μg/5μL)を硝子体内投与した。桿体駆動B波暗示時間は、分子の硝子体内適用の直前及び2週間後に遅延することが示された;平均+/-SEM;n.s. p>0.05;有意差なし(n.s.)、****p<0.0001;テューキーの多重比較検定を使用した一元配置分散分析。
投与の2週間後、抗TNP抗体処置では、抗TNP処置前の時点と比較して、糖尿病誘発桿体駆動b波暗示時間は短縮しなかった。実際、暗示遅延時間は、抗TNP抗体適用前の時点と比較して、有意に延長さえした(t=2週間で17.1ms対t=0週間で11.2ms;****p<0.0001)。これは、STZ誘発網膜損傷がt=0週で完全には確立されなかったこと及び抗TNP処置が暗示時間遅延の更なる増加を止めることができなかったことを示す。
ジスルフィド架橋(CC)の有無でのDoppelmab及び親分子であるTPP-14940/TPP-14941によるヒトVEGF-A捕捉の比較-VEGFR2のVEGF誘発リン酸化の阻害
図53A~図53B
VEGF-A捕捉を、Y1175でのVEGFレセプター2(VEGFR2)リン酸化を測定することにより評価した。分子処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。以下の表14に、対応するベストフィットIC50値を報告する(非線形回帰;log(アゴニスト)対応答(3つのパラメータ))。
親分子であるTPP-14940/TPP-14941とジスルフィド架橋の有無での各Doppelmab変形形態との間に、有意差は無かった。VEGF誘発VEGFR2リン酸化の阻害の効力及び有効性は、実質的に同一であった。
TPP-22214又はEyleaによるヒトVEGF-A捕捉の比較-Y1175でのVEGFR2及びERK1/2のVEGF誘発リン酸化(両方ともEC増殖に関連する)の阻害
図54A~図54B
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度のTPP-22214又はEyleaとのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-A捕捉を、(A)Y1175でのVEGFレセプター2(VEGFR2)リン酸化又は(B)T202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化を測定することにより評価した。分子処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。以下の表15に、対応するベストフィット値を報告する(非線形回帰(log(アゴニスト)対応答(3つのパラメータ))。EyleaとTPP-22214との間で有意に異なるベストフィット値(P<0.05)を太字で示す。P値も、表15に報告する。
Eyleaと比較して、TPP-22214は、Y1175でのVEGFR2及びERK1/2のVEGF誘発リン酸化を完全に阻害した。また、TPP-22214のVEGF捕捉における改善された有効性も、底部のプラトーの値の大きな有意差に見ることができる(表15を参照のこと)。最後に、TPP-22214は、EyleaよりVEGF捕捉において有意により強力であった。
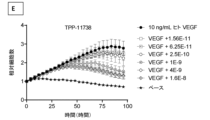
TPP-22204、TPP-22214又はTPP-22216とEyleaとによるヒトVEGF-A捕捉の比較-HRMECのVEGF誘発増殖の阻害
図55A~図55E
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度の示された結合分子:(A)TPPP-22204、(B)TPP-22214、(C)TPP-22216又は(D)Eyleaとのプレインキュベーションの有無で、10ng/mL ヒトVEGFと共にインキュベーションした。VEGF-A捕捉を、HRMEC細胞数の自動化された画像ベースの定量化により評価した(IncuCyte)。画像を合計84時間にわたって4時間毎に記録した。相対細胞数を示す。t=0での細胞数を1に設定した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。(E)Eylea又はTPP-22214の濃度に対する増殖曲線下面積とベース曲線下面積との差のプロット。以下の表16に、対応するベストフィット値を報告する(非線形回帰(log(アゴニスト)対応答(3つのパラメータ))。EyleaとTPP-22214との間で有意に異なるベストフィット値(P<0.05)を太字で示す。P値も、表16に報告する。
DoppelmabによるVEGF誘発増殖の阻害の効力及び有効性は、Eyleaより明らかに優れていた(TPP-22214とEyleaとの間のLogIC50及び底部のプラトーの数値における大きな有意差)。
TPP-22214又はEyleaによるヒトVEGF-A捕捉の比較-Y1214でのVEGFR2及びp38-MAPKのVEGF誘発リン酸化の阻害
図56A~図56B
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度のTPP-22214又はEyleaとのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-A捕捉を、(A)Y1214でのVEGFレセプター2(VEGFR2)リン酸化又は(B)T180/Y182でのp38-MAPKリン酸化を測定することにより評価した。分子処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。以下の表17に、対応するベストフィットIC50値(非線形回帰;(log(アゴニスト)対応答(3つのパラメータ))を報告する。EyleaとTPP-22214との間で有意に異なるベストフィット値(P<0.05)を太字で示す。P値も、表17に報告する。
Eyleaとは非常に対照的に、TPP-22214は、Y1214でのVEGFR2及びp38-MAPKのVEGF誘発リン酸化を完全に阻害した。TPP-22214のより有効なVEGF捕捉は、表17における底部のプラトーの値の大きな有意差に見ることができる。さらに、TPP-22214によるVEGF捕捉の効力がEyleaの効力より良好であるという傾向が観察された。
TPP-22204、TPP-22214、TPP-22215又はTPP-22216とEyleaとによるヒトVEGF-A捕捉の比較-VEGF誘発HRMEC発芽の阻害
図57A~図57B
ヒト網膜微小血管内皮細胞(HRMEC)のスフェロイドをコラーゲンマトリックス中に包埋した。内皮の発芽を2.5nM TPP-22204、TPP-22214、TPP-22215もしくはTPP-22216又は5nM Eyleaとのプレインキュベーションの有無で、50ng/mL ヒトVEGFとのインキュベーションにより24時間誘発した。(A)内皮の発芽を共焦点顕微鏡により評価し、Zスタックの最大投影から得られたスフェロイド外周を示した。非刺激細胞を対照(ベース)とした。データは、平均+/-SEMを表わす。n.s. p>0.05 有意差なし、****p<0.0001。(B)ベース条件下又は2.5nM TPP-22214もしくは5nM Eyleaとのプレインキュベーションの有無での50ng/mL ヒトVEGFにより刺激後の24時間の発芽後のスフェロイドからの代表的な最大投影画像を示す。バー=100μm。
Y1214 VEGFR2リン酸化アッセイと同様に、Doppelmabは、VEGF誘発HRMEC発芽の阻害において、常に有効であった。さらに、Doppelmabは、VEGF誘発内皮細胞発芽を完全に阻害することが可能であった。注目すべきことに、EyleaをDoppelmabと比較して2倍の分子濃度で使用したが、依然として、細胞発芽を完全には阻害することができなかった。
TPP-22214又はEyleaによるヒトVEGF-A捕捉の比較-Y951でのVEGFR2及びSrcのVEGF誘発リン酸化の阻害
図58A~図58B
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度のTPP-22214又はEyleaとのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-A捕捉を、(A)Y951でのVEGFレセプター2(VEGFR2)リン酸化又は(B)Y419でのSrcリン酸化を測定することにより評価した。抗体処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。以下の表18に、対応するベストフィット値を報告する(非線形回帰;(log(アゴニスト)対応答(3つのパラメータ))。EyleaとTPP-22214との間で有意に異なるベストフィット値(P<0.05)を太字で示す。P値も、表18に報告する。
Eyleaとは非常に対照的に、TPP-22214は、Y951でのVEGFR2及びY419でのSrcのVEGF誘発リン酸化を完全に阻害した。TPP-22214のより有効なVEGF-捕捉は、底部のプラトーの値の大きな有意差に見ることができる(表18)。
Doppelmab TPP-22214及びEyleaによるヒトVEGF-A捕捉の比較-Brown NorwayラットにおけるヒトVEGF-A誘発網膜透過性亢進の阻害
図59A~図59B
TPP-22214により、ラット網膜におけるヒトVEGF-A誘発透過性亢進が防止された。(A)実験手法を示す時間プロトコール。抗VEGF化合物(13又は26pmol/眼 Eylea又はTPP-14940)又は対照(26pmol TPP-11737)の硝子体内(ivt)投与の15分後、13pmol/眼 ヒトVEGF-Aをivt注射により投与した。PBS注射を対照とした。24時間後、1mL/kg エバンスブルー(EB)溶液(0.9% 生理食塩水中の45mg/mL)を静脈内(iv)注射により30分間投与し、その後、眼を単離し、固定した。同じ時点で、血漿サンプルを収集し、全身EB曝露量が等しいことを確認した。(B)Brown Norwayラットの網膜におけるVEGF-A誘発透過性亢進の定量を、共焦点顕微鏡により網膜フラットマウントにおけるEB血管外漏出を測定することにより行った。眼を鋸状縁に沿って切断し、水晶体及び硝子体を除去し、眼杯をパラホルムアルデヒド(4%)中において、4℃で1時間固定し、ついで、4℃で一晩PBSに移した。網膜を外側セグメント(強膜及び脈絡膜)から分離し、スライドガラスに移し、4回切断して、平坦なクローバー葉様構造を達成した。組織をマウンティング媒体(DNA染色DAPIを含有するVectashield H-1200)で覆い、カバースリップを上に置き、網膜フラットマウントを得た。サンプルを639nmの波長で励起し、669nmでのエバンスブルーの発光をLSM 700共焦点レーザー走査顕微鏡(Carl Zeiss, Jena;ゲイン800、レーザー強度2%、5スタック 60μm)で記録し、最大強度投影を有する網膜フラットマウントの画像を得た。蛍光強度の合計の分析を30の閾値でプログラムImageJ中において画像を開いた後に行った。***p<0.001;*p<0.05;n.s. p>0.05。テューキーの多重比較検定を使用した一元配置分散分析。n=9~17。67:1のモル比のEyleaと共にインキュベーション。VEGFを比較のために示す。
対象条件下において、硝子体内VEGF-A注射により、血管透過性が約60%向上した。注:TPP-11737を対照分子として使用した。TPP-22214と同じ分子フォーマット(Doppelmab)を有したが、初期のin vitroアッセイにおいて、VEGFを捕捉しなかったためである(上記を参照のこと)。
TPP-22214によるVEGF捕捉に対するTrkB結合の影響-TrkB細胞外ドメインの存在下又は非存在下でのTPP-22214によるヒトVEGF-A捕捉の比較
図60A~図60B
(A)TkrB細胞外ドメイン(TrkB-ECD)の機能的特徴。ヒトTrkBを安定に発現するCHO細胞を上昇する濃度の天然のリガンドであるBDNF又は上昇する濃度のTrkB-ECDを伴う10nM BDNFと共にインキュベーションした。TrkB活性化を、Y706/707でのTrkBリン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とする。データは、平均+/-SEMを表わす。
図(A):BDNFを上昇する濃度のTrkB-ECDと共にプレインキュベーションすると、TrkBレセプターの活性化が劇的に低下した。これは、BDNFに結合し、これを捕捉することが可能であることを示した。これは、機能的TrkB-ECDから期待されたことである。
CMC特性を改善するための操作の取り組み
シリーズ3~シリーズ4
シリーズ3及びシリーズ4からの分子の生物物理学的特性を評価した。分子の製造中、プロテインAがモノマーの割合により測定された後の品質を、分析用サイズ排除クロマトグラフィーを使用して試験した。さらに、各分子の熱安定性及び凝集開始を10mM ヒスチジンpH6.0中で評価した。熱安定性を、Sypro-orange色素を使用して温度によるタンパク質のアンフォールディングを測定する熱シフトアッセイを使用して測定した。各Tmを温度にわたる蛍光シグナルの一次導関数のピーク最大値として計算した。凝集開始を、動的光散乱を使用して測定し、流体力学的半径を温度の関数として測定した。最後に、種々のDoppelmabの保存安定性を、40℃又は5℃のいずれかで、2週間後の凝集を測定することにより試験した。凝集を、分析用サイズ排除クロマトグラフィーを使用して測定した。
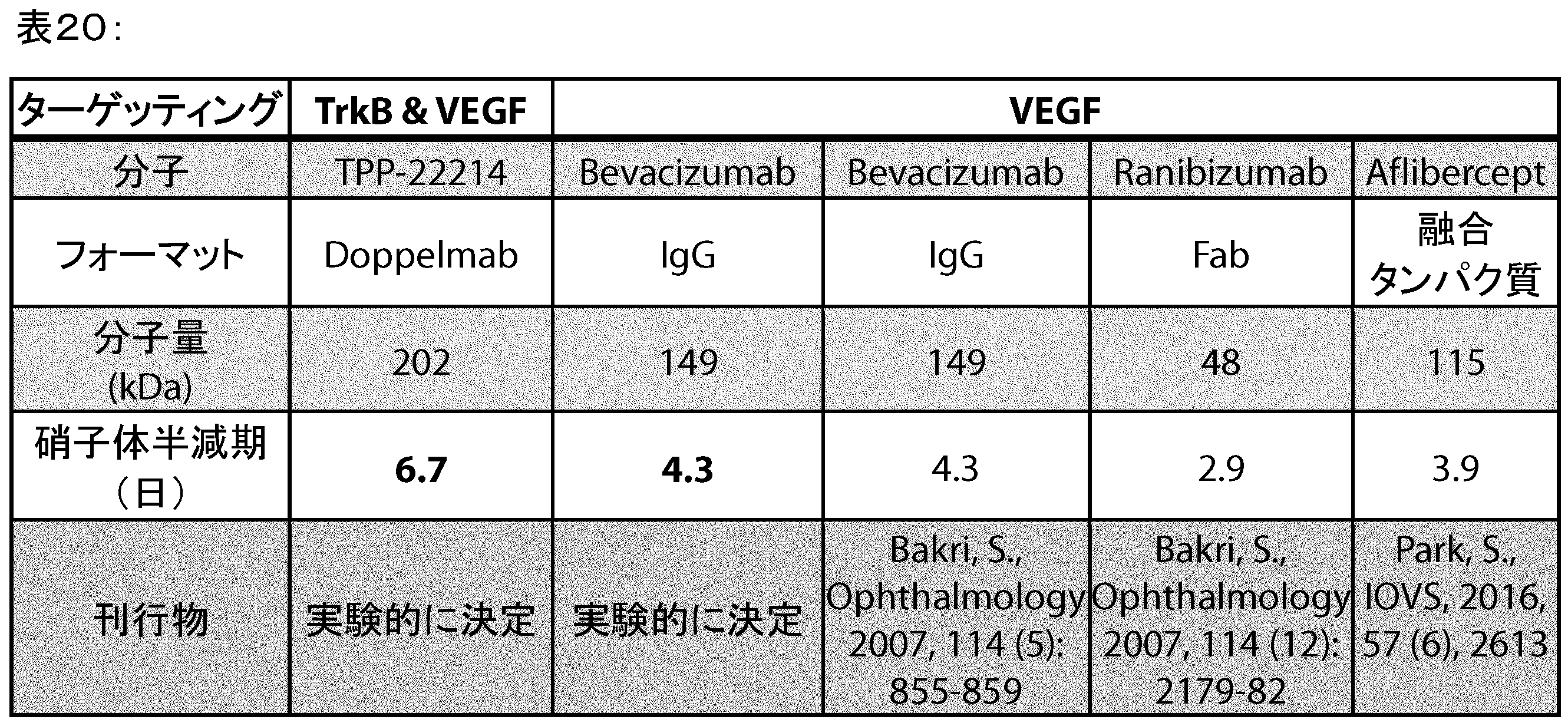
TPP-22214の硝子体半減期の測定
ニュージーランド白色メスのウサギに、TPP-22214又はBevacizumabの両側硝子体内投与を受けさせた。硝子体サンプルを種々の時点で収集し、TPP-22214又はBevacizumabについての濃度をELISAにより測定した。動物に、硝子体内投与前及び硝子体内投与後一定期間ごとに眼の検査を受けさせた。
BDNF、TPP-6830並びに2つのDoppelmab TPP-23457及びTPP-23459によるヒトTrkB活性化の比較
図61A~図61B
ヒトTrkBを安定に発現するCHO細胞を上昇する濃度の天然のTrkBリガンドであるBDNF、TPP-6830(更なるモノクローナルTrkB抗体)又は2つのDoppelmab TPP-23457(scFvとしてのTPP-6380、10L1、VH-VL;FabとしてのRanibizumab)及びTPP-23459(scFvとしてのTPP6380、10L1、VL-VH;FabとしてのRanibizumab)と共にインキュベーションした。
再度、TPP-6830(元のTrkB抗体は、部分的TrkBレセプターアゴニストである)とは非常に対照的に、2つの新規なDoppelmab TPP-23457及びTPP-23459 Doppelmabは、ここでは、完全なTrkBレセプターアゴニスト活性を示した。これらのDoppelmabによるTrkB活性化は、天然のリガンドであるBDNFと少なくとも同じ効果があった。
ヒトVEGFの存在下又は非存在下でのTPP-6830(TrkBモノクローナル抗体)並びに2つのDoppelmab TPP-23457及びTPP-23459によるヒトTrkB活性化(TrkBリン酸化)の比較
図62A~図62C
ヒトTrkBを安定に発現するCHO細胞を200ng/mL ヒトVEGF-A(hVEGF)とのプレインキュベーションの有無で、上昇する濃度のDoppelmab(A)TPP-23457、(B)TPP-23459又は(C)TPP-6830と共にインキュベーションした。TrkB活性化を、Y706/707でのTrkBリン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
再度、ヒトVEGFとのプレインキュベーションにより、TPP-23457(scFvとしてのTPP-6830、10L1、VH-VL;FabとしてのRanibizumab)及びTPP-23459(scFvとしてのTPP-6380、10L1、VL-VH;FabとしてのRanibizumab)によるTrkBリン酸化(TrkB活性化)の効力が、劇的に改善された。
ヒトVEGFの存在下又は非存在下でのTPP-6830(TrkBモノクローナル抗体)並びに2つのDoppelmab TPP-23457及びTPP-23459によるヒトTrkB活性化(ERKリン酸化)の比較
図63A~図63C
ヒトTrkBを安定に発現するCHO細胞を200ng/mL ヒトVEGF-A(hVEGF)とのプレインキュベーションの有無で、上昇する濃度のDoppelmab(A)TPP-23457、(B)TPP-23459又は(C)TPP-6830と共にインキュベーションした。TrkB活性化を、TrkBの下流であるT202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化を測定することにより評価した。最低化合物濃度を溶媒単独とした。データは、平均+/-SEMを表わす。
ここでも、ヒトVEGFとのプレインキュベーションにより、TPP-23457(scFvとしてのTPP-6830、10L1、VH-VL;FabとしてのRanibizumab)及びTPP-23459(scFvとしてのTPP-6380、10L1、VL-VH;FabとしてのRanibizumab)によるERK1/2リン酸化(TrkB活性化)の効力が、劇的に改善された。
BDNF誘発TrkB活性化(TrkBリン酸化)に対するTPP-23457の影響
図64A~図64B
ヒトTrkBレセプターを安定に発現するCHO細胞を一定濃度の0.3nM、1nM又は3nM BDNFの有無で、上昇する濃度の(A)C2抗体又は(B)Doppelmab TPP-23457と共にインキュベーションした。TrkBの活性化を、Y706/707でのレセプターリン酸化を測定することにより評価した。データは、平均+/-SEMを表わす。
C2とは非常に対照的に、TPP-23457は、BDNF誘導TrkB活性化を制限しなかった。
BDNF誘発TrkB活性化(Erkリン酸化)に対するTPP-23457の影響
図65A~図65B
ヒトTrkBレセプターを安定に発現するCHO細胞を一定濃度の0.3nM、1nM又は3nM BDNFの有無で、上昇する濃度の(A)C2抗体又は(B)Doppelmab TPP-23457と共にインキュベーションした。TrkBの活性化を、TrkBの下流であるT202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化を測定することにより評価した。データは、平均+/-SEMを表わす。
C2とは非常に対照的に、TPP-23457は、TrkBの下流であるBDNF誘発Erkリン酸化を制限しなかった。
Y1175でのVEGFR2及びERK1/2のVEGF誘発リン酸化(両方ともEC増殖に関連する)のTPP-22214、TPP-23457又はTPP-23459の阻害によるヒトVEGF-A捕捉の比較
図66A~図66B
ヒト網膜微小血管内皮細胞(HRMEC)を飢餓状態にし、ついで、上昇する濃度のTPP-22214、TPP-23457又はTPP23459とのプレインキュベーションの有無で、50ng/mL ヒトVEGFと共にインキュベーションした。VEGF-A捕捉を、(A)Y1175でのVEGFレセプター2(VEGFR2)リン酸化又は(B)T202/Y204(ERK1)及びT185/Y187(ERK2)でのERK1/2リン酸化を測定することにより評価した。分子処理を伴わない50ng/ml ヒトVEGFを対照とした。データは、平均+/-SEMを表わす。
Doppelmab TPP-23457及びTPP-23459のVEGF捕捉は、TPP-22215と実質的に同一であった。
Claims (17)
- 血管内皮増殖因子(VEGF)に特異的に結合する少なくとも1つの抗原結合部位と、トロポミオシンレセプターキナーゼB(TrkB)に特異的に結合する少なくとも1つの抗原結合部位とを含む、二重特異性かつ四価の結合分子であり、
VEGFに特異的に結合する抗原結合部位が、抗原結合部位a)~c):
a)配列番号:145(CDR1)、配列番号:146(CDR2)及び配列番号:147(CDR3)のアミノ酸配列を含む軽鎖CDRを含む抗原結合部位並びに
配列番号:148(CDR1)、配列番号:149(CDR2)及び配列番号:150(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:151(CDR1)、配列番号:152(CDR2)及び配列番号:153(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:154(CDR1)、配列番号:155(CDR2)及び配列番号:156(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位;
b)配列番号:157(CDR1)、配列番号:158(CDR2)及び配列番号:159(CDR3)のアミノ酸配列を含む軽鎖CDRを含む抗原結合部位並びに
配列番号:160(CDR1)、配列番号:161(CDR2)及び配列番号:162(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:163(CDR1)、配列番号:164(CDR2)及び配列番号:165(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:166(CDR1)、配列番号:167(CDR2)及び配列番号:168(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位;
c)配列番号:169(CDR1)、配列番号:170(CDR2)及び配列番号:171(CDR3)のアミノ酸配列を含む軽鎖CDRを含む抗原結合部位並びに
配列番号:172(CDR1)、配列番号:173(CDR2)及び配列番号:174(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:175(CDR1)、配列番号:176(CDR2)及び配列番号:177(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:178(CDR1)、配列番号:179(CDR2)及び配列番号:180(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位
からなる群より選択され、
TrkBに特異的に結合する抗原結合部位が、
a)配列番号:201(CDR1)、配列番号:202(CDR2)及び配列番号:203(CDR3)のアミノ酸配列を含む軽鎖CDRを含む抗原結合部位並びに
配列番号:204(CDR1)、配列番号:205(CDR2)及び配列番号:206(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:207(CDR1)、配列番号:208(CDR2)及び配列番号:209(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位又は
配列番号:210(CDR1)、配列番号:211(CDR2)及び配列番号:212(CDR3)のアミノ酸配列を含む重鎖CDRを含む抗原結合部位
から選択され、
前記結合分子が、配列番号:1、3、5、7、9、11、13、15、17、19、21、23、25、27、29、31、33、35、37、39、41、43、45、47、49、51、53、55、57、59、61、63、65、67、69、71、73、75、77、79、81、83、85、87、89、91、93、95、97、99、101、103、105、107、109、111、113、115、117、119、121、123、125、127、129、131、133、135、137、139、141又は143のアミノ酸配列と少なくとも90%同一のアミノ酸配列を含む軽鎖と、配列番号:2、4、6、8、10、12、14、16、18、20、22、24、26、28、30、32、34、36、38、40、42、44、46、48、50、52、54、56、58、60、62、64、66、68、70、72、74、76、78、80、82、84、86、88、90、92、94、96、98、100、102,104、106、108、110、112、114、116、118、120、122、124、126、128、130、132、134、136、138、140、142又は144のアミノ酸配列と少なくとも90%同一のアミノ酸配列を含む重鎖とを含む、
結合分子。 - 血管内皮増殖因子(VEGF)に特異的に結合する少なくとも1つの抗原結合部位と、トロポミオシンレセプターキナーゼB(TrkB)に特異的に結合する少なくとも1つの抗原結合部位とを含む、二重特異性かつ四価の結合分子であり、
(i)配列番号:41のアミノ酸配列を含む軽鎖及び配列番号:42のアミノ酸配列を含む重鎖又は(ii)配列番号:43のアミノ酸配列を含む軽鎖及び配列番号:44のアミノ酸配列を含む重鎖又は(iii)配列番号:45のアミノ酸配列を含む軽鎖及び配列番号:46のアミノ酸配列を含む重鎖又は(iv)配列番号:47のアミノ酸配列を含む軽鎖及び配列番号:48のアミノ酸配列を含む重鎖又は(v)配列番号:49のアミノ酸配列を含む軽鎖及び配列番号:50のアミノ酸配列を含む重鎖又は(vi)配列番号:51のアミノ酸配列を含む軽鎖及び配列番号:52のアミノ酸配列を含む重鎖又は(vii)配列番号:53のアミノ酸配列を含む軽鎖及び配列番号:54のアミノ酸配列を含む重鎖又は(viii)配列番号:55のアミノ酸配列を含む軽鎖及び配列番号:56のアミノ酸配列を含む重鎖又は(ix)配列番号:57のアミノ酸配列を含む軽鎖及び配列番号:58のアミノ酸配列を含む重鎖又は(x)配列番号:59のアミノ酸配列を含む軽鎖及び配列番号:60のアミノ酸配列を含む重鎖又は(xi)配列番号:61のアミノ酸配列を含む軽鎖及び配列番号:62のアミノ酸配列を含む重鎖又は(xii)配列番号:63のアミノ酸配列を含む軽鎖及び配列番号:64のアミノ酸配列を含む重鎖又は(xiii)配列番号:65のアミノ酸配列を含む軽鎖及び配列番号:66のアミノ酸配列を含む重鎖又は(xiv)配列番号:67のアミノ酸配列を含む軽鎖及び配列番号:68のアミノ酸配列を含む重鎖又は(xv)配列番号:69のアミノ酸配列を含む軽鎖及び配列番号:70のアミノ酸配列を含む重鎖又は(xvi)配列番号:71のアミノ酸配列を含む軽鎖及び配列番号:72のアミノ酸配列を含む重鎖又は(xvii)配列番号:73のアミノ酸配列を含む軽鎖及び配列番号:74のアミノ酸配列を含む重鎖又は(xviii)配列番号:75のアミノ酸配列を含む軽鎖及び配列番号:76のアミノ酸配列を含む重鎖又は(xix)配列番号:77のアミノ酸配列を含む軽鎖及び配列番号:78のアミノ酸配列を含む重鎖又は(xx)配列番号:79のアミノ酸配列を含む軽鎖及び配列番号:80のアミノ酸配列を含む重鎖又は(xxi)配列番号:81のアミノ酸配列を含む軽鎖及び配列番号:82のアミノ酸配列を含む重鎖又は(xxii)配列番号:83のアミノ酸配列を含む軽鎖及び配列番号:84のアミノ酸配列を含む重鎖又は(xxiii)配列番号:85のアミノ酸配列を含む軽鎖及び配列番号:86のアミノ酸配列を含む重鎖又は(xxiv)配列番号:87のアミノ酸配列を含む軽鎖及び配列番号:88のアミノ酸配列を含む重鎖又は(xxv)配列番号:89のアミノ酸配列を含む軽鎖及び配列番号:90のアミノ酸配列を含む重鎖又は(xxvi)配列番号:91のアミノ酸配列を含む軽鎖及び配列番号:92のアミノ酸配列を含む重鎖又は(xxvii)配列番号:93のアミノ酸配列を含む軽鎖及び配列番号:94のアミノ酸配列を含む重鎖又は(xxviii)配列番号:95のアミノ酸配列を含む軽鎖及び配列番号:96のアミノ酸配列を含む重鎖又は(xxix)配列番号:97のアミノ酸配列を含む軽鎖及び配列番号:98のアミノ酸配列を含む重鎖又は(xxx)配列番号:99のアミノ酸配列を含む軽鎖及び配列番号:100のアミノ酸配列を含む重鎖又は(xxxi)配列番号:101のアミノ酸配列を含む軽鎖及び配列番号:102のアミノ酸配列を含む重鎖又は(xxxii)配列番号:103のアミノ酸配列を含む軽鎖及び配列番号:104のアミノ酸配列を含む重鎖又は(xxxiii)配列番号:105のアミノ酸配列を含む軽鎖及び配列番号:106のアミノ酸配列を含む重鎖又は(xxxiv)配列番号:107のアミノ酸配列を含む軽鎖及び配列番号:108のアミノ酸配列を含む重鎖又は(xxxv)配列番号:109のアミノ酸配列を含む軽鎖及び配列番号:110のアミノ酸配列を含む重鎖又は(xxxvi)配列番号:111のアミノ酸配列を含む軽鎖及び配列番号:112のアミノ酸配列を含む重鎖又は(xxxvii)配列番号:113のアミノ酸配列を含む軽鎖及び配列番号:114のアミノ酸配列を含む重鎖又は(xxxviii)配列番号:115のアミノ酸配列を含む軽鎖及び配列番号:116のアミノ酸配列を含む重鎖又は(xxxix)配列番号:117のアミノ酸配列を含む軽鎖及び配列番号:118のアミノ酸配列を含む重鎖又は(xl)配列番号:119のアミノ酸配列を含む軽鎖及び配列番号:120のアミノ酸配列を含む重鎖又は(xli)配列番号:121のアミノ酸配列を含む軽鎖及び配列番号:122のアミノ酸配列を含む重鎖又は(xlii)配列番号:123のアミノ酸配列を含む軽鎖及び配列番号:124のアミノ酸配列を含む重鎖又は(xliii)配列番号:125のアミノ酸配列を含む軽鎖及び配列番号:126のアミノ酸配列を含む重鎖又は(xliv)配列番号:127のアミノ酸配列を含む軽鎖及び配列番号:128のアミノ酸配列を含む重鎖又は(xlv)配列番号:129のアミノ酸配列を含む軽鎖及び配列番号:130のアミノ酸配列を含む重鎖又は(xlvi)配列番号:131のアミノ酸配列を含む軽鎖及び配列番号:132のアミノ酸配列を含む重鎖又は(xlvii)配列番号:133のアミノ酸配列を含む軽鎖及び配列番号:134のアミノ酸配列を含む重鎖又は(xlviii)配列番号:135のアミノ酸配列を含む軽鎖及び配列番号:136のアミノ酸配列を含む重鎖又は(xlix)配列番号:137のアミノ酸配列を含む軽鎖及び配列番号:138のアミノ酸配列を含む重鎖又は(l)配列番号:139のアミノ酸配列を含む軽鎖及び配列番号:140のアミノ酸配列を含む重鎖又は(li)配列番号:141のアミノ酸配列を含む軽鎖及び配列番号:142のアミノ酸配列を含む重鎖又は(lii)配列番号:143のアミノ酸配列を含む軽鎖及び配列番号:144のアミノ酸配列を含む重鎖
を含む、
結合分子。 - 請求項1又は2記載の結合分子の(i)重鎖もしくは重鎖可変ドメイン及び/又は(ii)軽鎖もしくは軽鎖可変ドメインをコードする、
単離された核酸分子。 - 請求項3記載の単離された核酸分子を含む、
ウイルスベクター。 - 請求項3記載の核酸分子を含む、
発現ベクター。 - 請求項5記載の発現ベクターでトランスフェクションされた、
宿主細胞。 - (a)以下の分子の発現を可能にする条件下で、請求項6記載の宿主細胞を培養することと、
(b)該分子を回収することとを含む、
請求項1又は2記載の結合分子を製造する方法。 - 医薬に使用するための、請求項1又は2記載の結合分子。
- 該使用が、眼もしくは網膜の疾患又は神経変性疾患の処置である、請求項8記載の使用のための結合分子。
- 該使用が、神経/神経眼又は網膜の疾患の処置のためのものである、請求項9記載の使用のための結合分子。
- 該使用が、黄斑変性症、加齢黄斑変性症、糖尿病性網膜症、糖尿病性黄斑浮腫、網膜色素変性症、遺伝性網膜ジストロフィー、遺伝性黄斑ジストロフィー、近視性変性症、地図状萎縮症、網膜動脈閉塞症、眼内炎、ブドウ膜炎、嚢胞様黄斑浮腫、任意の網膜疾患に続発する脈絡膜新生血管膜、視神経症、緑内障、網膜剥離、中毒性網膜症、放射線網膜症並びに外傷性網膜症、前駆型及び軽度から中等度のアルツハイマー病、アルツハイマー病を有する患者の疾患進行の遅延、ハンチントン病、パーキンソン病、大うつ病性障害、統合失調症、統合失調症に関連する認知障害の処置、減弱精神病症候群を有する個体における初発精神病の予防、統合失調症を有する患者における再発の予防、処置抵抗性うつ病、過食症、肥満又はメタボリックシンドロームの処置のためのものである、請求項9記載の使用のための結合分子。
- 該使用が、滲出性加齢黄斑変性症(wAMD)の処置のためのものである、請求項9記載の使用のための結合分子。
- 該使用が、網膜静脈閉塞症(RVO)の処置のためのものである、請求項9記載の使用のための結合分子。
- 該使用が、地図状萎縮の治療及び/又は予防のためのものである、請求項9記載の使用のための結合分子。
- 薬学的に許容し得る担体と、請求項1又は2記載の結合分子とを含む、
医薬組成物。 - 眼もしくは網膜の疾患又は神経変性疾患を治療し又は予防するための医薬組成物を製造するための、請求項1又は2記載の結合分子の使用。
- 眼もしくは網膜の疾患又は神経変性疾患を治療し又は予防する方法に使用するための、請求項1又は2記載の結合分子。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP20203030.0 | 2020-10-21 | ||
| EP20203030 | 2020-10-21 | ||
| PCT/EP2021/079010 WO2022084354A1 (en) | 2020-10-21 | 2021-10-20 | Bispecific anti-vegf and anti-trkb binding molecules for the treatment of eye diseases |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023546228A JP2023546228A (ja) | 2023-11-01 |
| JP7633397B2 true JP7633397B2 (ja) | 2025-02-19 |
Family
ID=73005392
Family Applications (3)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023524323A Active JP7633397B2 (ja) | 2020-10-21 | 2021-10-20 | 眼の疾患の処置のための二重特異性抗VEGF及び抗TrkB結合分子 |
| JP2023524324A Pending JP2023546229A (ja) | 2020-10-21 | 2021-10-20 | 眼の疾患の処置のためのアゴニスト性TrkB結合分子 |
| JP2024179996A Pending JP2025011251A (ja) | 2020-10-21 | 2024-10-15 | 眼の疾患の処置のためのアゴニスト性TrkB結合分子 |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2023524324A Pending JP2023546229A (ja) | 2020-10-21 | 2021-10-20 | 眼の疾患の処置のためのアゴニスト性TrkB結合分子 |
| JP2024179996A Pending JP2025011251A (ja) | 2020-10-21 | 2024-10-15 | 眼の疾患の処置のためのアゴニスト性TrkB結合分子 |
Country Status (7)
| Country | Link |
|---|---|
| US (3) | US12110335B2 (ja) |
| EP (2) | EP4232476A2 (ja) |
| JP (3) | JP7633397B2 (ja) |
| CN (2) | CN116829586A (ja) |
| AR (1) | AR123862A1 (ja) |
| TW (1) | TW202233668A (ja) |
| WO (2) | WO2022084354A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7633397B2 (ja) | 2020-10-21 | 2025-02-19 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 眼の疾患の処置のための二重特異性抗VEGF及び抗TrkB結合分子 |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010086828A2 (en) | 2009-02-02 | 2010-08-05 | Rinat Neuroscience Corporation | Agonist anti-trkb monoclonal antibodies |
| WO2012061558A2 (en) | 2010-11-04 | 2012-05-10 | Abbott Laboratories | Dual variable domain immunoglobulins and uses thereof |
| JP2014193864A (ja) | 2013-03-28 | 2014-10-09 | Samsung Electronics Co Ltd | c−Met抗体およびVEGF結合断片が連結された融合タンパク質 |
| JP2018531005A (ja) | 2015-09-23 | 2018-10-25 | ジェネンテック, インコーポレイテッド | 抗vegf抗体の最適化変異体 |
| JP2019531762A (ja) | 2016-09-07 | 2019-11-07 | サクシン ライフサイエンシス ピーヴィーティー エルティディーSaksin Lifesciences Pvt Ltd | Vegfに対する合成の抗体およびそれらの使用 |
| JP2020514376A (ja) | 2017-03-22 | 2020-05-21 | ジェネンテック, インコーポレイテッド | 眼障害の治療のために最適化された抗体組成物 |
| JP2020513806A (ja) | 2017-03-15 | 2020-05-21 | チンファ ユニバーシティTsinghua University | 新規の抗TrkB抗体 |
| JP2020522270A (ja) | 2017-06-09 | 2020-07-30 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 抗trkb抗体 |
| WO2020187202A1 (zh) | 2019-03-18 | 2020-09-24 | 江苏恒瑞医药股份有限公司 | 特异性结合vegf和ang2的双特异性抗体 |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5731A (en) | 1848-08-22 | Elisha k | ||
| US168A (en) | 1837-04-17 | Improvement in fire-arms | ||
| US4676980A (en) | 1985-09-23 | 1987-06-30 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Target specific cross-linked heteroantibodies |
| ATE87659T1 (de) | 1986-09-02 | 1993-04-15 | Enzon Lab Inc | Bindungsmolekuele mit einzelpolypeptidkette. |
| WO1988007089A1 (en) | 1987-03-18 | 1988-09-22 | Medical Research Council | Altered antibodies |
| EP0368684B2 (en) | 1988-11-11 | 2004-09-29 | Medical Research Council | Cloning immunoglobulin variable domain sequences. |
| US5427908A (en) | 1990-05-01 | 1995-06-27 | Affymax Technologies N.V. | Recombinant library screening methods |
| WO1993008829A1 (en) | 1991-11-04 | 1993-05-13 | The Regents Of The University Of California | Compositions that mediate killing of hiv-infected cells |
| AU701578B2 (en) | 1992-08-21 | 1999-02-04 | Vrije Universiteit Brussel | Immunoglobulins devoid of light chains |
| ATE199392T1 (de) | 1992-12-04 | 2001-03-15 | Medical Res Council | Multivalente und multispezifische bindungsproteine, deren herstellung und verwendung |
| AU6852594A (en) | 1993-06-03 | 1995-01-03 | Therapeutic Antibodies Inc. | Production of antibody fragments |
| US5731168A (en) | 1995-03-01 | 1998-03-24 | Genentech, Inc. | Method for making heteromultimeric polypeptides |
| GB9625640D0 (en) | 1996-12-10 | 1997-01-29 | Celltech Therapeutics Ltd | Biological products |
| EP0981548A4 (en) | 1997-04-30 | 2005-11-23 | Enzon Inc | GLYCOSYLATABLE SINGLE CHAIN ANTIGEN-BINDING PROTEINS, MANUFACTURE AND USE THEREOF |
| EP2206720A1 (en) | 2000-04-12 | 2010-07-14 | Human Genome Sciences, Inc. | Albumin fusion proteins |
| AU2002241922B2 (en) | 2001-01-17 | 2007-10-25 | Aptevo Research And Development Llc | Binding domain-immunoglobulin fusion proteins |
| EP1456410A2 (en) | 2001-12-11 | 2004-09-15 | AlgoNomics N.V. | Method for displaying loops from immunoglobulin domains in different contexts |
| ES2263984T3 (es) | 2002-06-28 | 2006-12-16 | Domantis Limited | Ligandos doble-especificos con una vida media serica aumentada. |
| CA2505316C (en) | 2002-11-08 | 2014-08-05 | Ablynx N.V. | Single domain antibodies directed against tumour necrosis factor-alpha and uses therefor |
| CN1845938B (zh) | 2003-06-30 | 2010-05-26 | 杜门蒂斯有限公司 | 多肽 |
| EP2860192B1 (en) | 2005-10-12 | 2017-09-27 | MorphoSys AG | Generation and profiling of fully human HuCAL GOLD-derived therapeutic antibodies specific for human CD38 |
| KR101516823B1 (ko) * | 2006-03-17 | 2015-05-07 | 바이오겐 아이덱 엠에이 인코포레이티드 | 안정화된 폴리펩티드 조성물 |
| WO2008058127A2 (en) | 2006-11-09 | 2008-05-15 | Irm Llc | Agonist trkb antibodies and uses thereof |
| ES2563027T3 (es) | 2008-01-07 | 2016-03-10 | Amgen Inc. | Método para fabricación de moléculas heterodímeras Fc de anticuerpos utilizando efectos de conducción electrostática |
| US8268314B2 (en) * | 2008-10-08 | 2012-09-18 | Hoffmann-La Roche Inc. | Bispecific anti-VEGF/anti-ANG-2 antibodies |
| JP2019517787A (ja) * | 2016-05-03 | 2019-06-27 | ザ スクリプス リサーチ インスティテュート | 神経変性障害の処置のためのTrkBアゴニスト抗体 |
| JP2020187202A (ja) | 2019-05-13 | 2020-11-19 | キヤノン株式会社 | 画像形成装置 |
| JP7633397B2 (ja) * | 2020-10-21 | 2025-02-19 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 眼の疾患の処置のための二重特異性抗VEGF及び抗TrkB結合分子 |
-
2021
- 2021-10-20 JP JP2023524323A patent/JP7633397B2/ja active Active
- 2021-10-20 AR ARP210102899A patent/AR123862A1/es not_active Application Discontinuation
- 2021-10-20 CN CN202180070390.8A patent/CN116829586A/zh active Pending
- 2021-10-20 US US17/505,672 patent/US12110335B2/en active Active
- 2021-10-20 EP EP21798613.2A patent/EP4232476A2/en active Pending
- 2021-10-20 CN CN202180078806.0A patent/CN117043186A/zh active Pending
- 2021-10-20 EP EP21798332.9A patent/EP4232474A1/en active Pending
- 2021-10-20 US US17/505,763 patent/US20220119536A1/en not_active Abandoned
- 2021-10-20 WO PCT/EP2021/079010 patent/WO2022084354A1/en not_active Ceased
- 2021-10-20 TW TW110138827A patent/TW202233668A/zh unknown
- 2021-10-20 JP JP2023524324A patent/JP2023546229A/ja active Pending
- 2021-10-20 WO PCT/EP2021/079011 patent/WO2022084355A2/en not_active Ceased
-
2024
- 2024-08-19 US US18/808,311 patent/US20250051460A1/en active Pending
- 2024-10-15 JP JP2024179996A patent/JP2025011251A/ja active Pending
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010086828A2 (en) | 2009-02-02 | 2010-08-05 | Rinat Neuroscience Corporation | Agonist anti-trkb monoclonal antibodies |
| WO2012061558A2 (en) | 2010-11-04 | 2012-05-10 | Abbott Laboratories | Dual variable domain immunoglobulins and uses thereof |
| JP2014193864A (ja) | 2013-03-28 | 2014-10-09 | Samsung Electronics Co Ltd | c−Met抗体およびVEGF結合断片が連結された融合タンパク質 |
| JP2018531005A (ja) | 2015-09-23 | 2018-10-25 | ジェネンテック, インコーポレイテッド | 抗vegf抗体の最適化変異体 |
| JP2019531762A (ja) | 2016-09-07 | 2019-11-07 | サクシン ライフサイエンシス ピーヴィーティー エルティディーSaksin Lifesciences Pvt Ltd | Vegfに対する合成の抗体およびそれらの使用 |
| JP2020513806A (ja) | 2017-03-15 | 2020-05-21 | チンファ ユニバーシティTsinghua University | 新規の抗TrkB抗体 |
| JP2020514376A (ja) | 2017-03-22 | 2020-05-21 | ジェネンテック, インコーポレイテッド | 眼障害の治療のために最適化された抗体組成物 |
| JP2020522270A (ja) | 2017-06-09 | 2020-07-30 | ベーリンガー インゲルハイム インターナショナル ゲゼルシャフト ミット ベシュレンクテル ハフツング | 抗trkb抗体 |
| WO2020187202A1 (zh) | 2019-03-18 | 2020-09-24 | 江苏恒瑞医药股份有限公司 | 特异性结合vegf和ang2的双特异性抗体 |
Non-Patent Citations (2)
| Title |
|---|
| Biochemical and Biophysical Research Communications,2018年,Vol.504,p.19-24 |
| MABS,2017年,Vol.9, No.2,p.182-212 |
Also Published As
| Publication number | Publication date |
|---|---|
| TW202233668A (zh) | 2022-09-01 |
| EP4232474A1 (en) | 2023-08-30 |
| US20220119536A1 (en) | 2022-04-21 |
| US12110335B2 (en) | 2024-10-08 |
| JP2025011251A (ja) | 2025-01-23 |
| JP2023546228A (ja) | 2023-11-01 |
| WO2022084355A3 (en) | 2022-06-02 |
| EP4232476A2 (en) | 2023-08-30 |
| CN117043186A (zh) | 2023-11-10 |
| US20250051460A1 (en) | 2025-02-13 |
| WO2022084354A1 (en) | 2022-04-28 |
| WO2022084355A2 (en) | 2022-04-28 |
| US20220119535A1 (en) | 2022-04-21 |
| JP2023546229A (ja) | 2023-11-01 |
| CN116829586A (zh) | 2023-09-29 |
| AR123862A1 (es) | 2023-01-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6796184B2 (ja) | 二重特異性抗vegf/抗ang−2抗体及び眼血管疾患の処置におけるそれらの使用 | |
| US12398204B2 (en) | Method of treating an ocular condition by administering multispecific antibodies that activates TIE2 and binds a receptor tyrosine kinase agonist | |
| JP7107914B2 (ja) | VE-PTP(HPTP-β)を標的化するヒト化モノクローナル抗体 | |
| RU2702553C2 (ru) | Новое антитело против tie-2 человека | |
| KR20150095684A (ko) | 히알루로난에 결합하는 펩티드 태그를 이용하는 조성물 및 방법 | |
| CA2700481A1 (en) | Antigen binding proteins | |
| JP7826279B2 (ja) | 抗ベータセルリン抗体、その断片、及び多重特異性結合分子 | |
| JP2025011251A (ja) | 眼の疾患の処置のためのアゴニスト性TrkB結合分子 | |
| US20260049149A1 (en) | Bispecific agonistic antibodies to activin a receptor like type 1 (alk1) | |
| WO2023238845A1 (ja) | 加齢疾患の治療又は予防のための抗インテグリンα11抗体を含む医薬組成物 | |
| JP2026067859A (ja) | 抗ベータセルリン抗体、その断片、及び多重特異性結合分子 | |
| HK40099403A (zh) | 抗igf-1r igg4抗体及其在治疗甲状腺相关眼病中的用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230620 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240521 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240807 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20241021 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241031 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250121 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250206 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7633397 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |