JP7299647B2 - 高分子化合物、高分子化合物の製造方法、接着剤組成物、硬化物、接着剤組成物の製造方法および接着力の調整方法 - Google Patents
高分子化合物、高分子化合物の製造方法、接着剤組成物、硬化物、接着剤組成物の製造方法および接着力の調整方法 Download PDFInfo
- Publication number
- JP7299647B2 JP7299647B2 JP2021575867A JP2021575867A JP7299647B2 JP 7299647 B2 JP7299647 B2 JP 7299647B2 JP 2021575867 A JP2021575867 A JP 2021575867A JP 2021575867 A JP2021575867 A JP 2021575867A JP 7299647 B2 JP7299647 B2 JP 7299647B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- formula
- polymer compound
- adhesive composition
- represented
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J133/00—Adhesives based on homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by only one carboxyl radical, or of salts, anhydrides, esters, amides, imides, or nitriles thereof; Adhesives based on derivatives of such polymers
- C09J133/04—Homopolymers or copolymers of esters
- C09J133/06—Homopolymers or copolymers of esters of esters containing only carbon, hydrogen and oxygen, the oxygen atom being present only as part of the carboxyl radical
- C09J133/10—Homopolymers or copolymers of methacrylic acid esters
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J133/00—Adhesives based on homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by only one carboxyl radical, or of salts, anhydrides, esters, amides, imides, or nitriles thereof; Adhesives based on derivatives of such polymers
- C09J133/04—Homopolymers or copolymers of esters
- C09J133/14—Homopolymers or copolymers of esters of esters containing halogen, nitrogen, sulfur or oxygen atoms in addition to the carboxy oxygen
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/12—Esters of monohydric alcohols or phenols
- C08F220/14—Methyl esters, e.g. methyl (meth)acrylate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/12—Esters of monohydric alcohols or phenols
- C08F220/16—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms
- C08F220/18—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms with acrylic or methacrylic acids
- C08F220/1802—C2-(meth)acrylate, e.g. ethyl (meth)acrylate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/12—Esters of monohydric alcohols or phenols
- C08F220/16—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms
- C08F220/18—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms with acrylic or methacrylic acids
- C08F220/1803—C3-(meth)acrylate, e.g. (iso)propyl (meth)acrylate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/12—Esters of monohydric alcohols or phenols
- C08F220/16—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms
- C08F220/18—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms with acrylic or methacrylic acids
- C08F220/1804—C4-(meth)acrylate, e.g. butyl (meth)acrylate, isobutyl (meth)acrylate or tert-butyl (meth)acrylate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/12—Esters of monohydric alcohols or phenols
- C08F220/16—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms
- C08F220/18—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms with acrylic or methacrylic acids
- C08F220/1805—C5-(meth)acrylate, e.g. pentyl (meth)acrylate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/12—Esters of monohydric alcohols or phenols
- C08F220/16—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms
- C08F220/18—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms with acrylic or methacrylic acids
- C08F220/1806—C6-(meth)acrylate, e.g. (cyclo)hexyl (meth)acrylate or phenyl (meth)acrylate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/12—Esters of monohydric alcohols or phenols
- C08F220/16—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms
- C08F220/18—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms with acrylic or methacrylic acids
- C08F220/1808—C8-(meth)acrylate, e.g. isooctyl (meth)acrylate or 2-ethylhexyl (meth)acrylate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/12—Esters of monohydric alcohols or phenols
- C08F220/16—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms
- C08F220/18—Esters of monohydric alcohols or phenols of phenols or of alcohols containing two or more carbon atoms with acrylic or methacrylic acids
- C08F220/1811—C10or C11-(Meth)acrylate, e.g. isodecyl (meth)acrylate, isobornyl (meth)acrylate or 2-naphthyl (meth)acrylate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/26—Esters containing oxygen in addition to the carboxy oxygen
- C08F220/30—Esters containing oxygen in addition to the carboxy oxygen containing aromatic rings in the alcohol moiety
- C08F220/302—Esters containing oxygen in addition to the carboxy oxygen containing aromatic rings in the alcohol moiety and two or more oxygen atoms in the alcohol moiety
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F220/00—Copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and only one being terminated by only one carboxyl radical or a salt, anhydride ester, amide, imide or nitrile thereof
- C08F220/02—Monocarboxylic acids having less than ten carbon atoms; Derivatives thereof
- C08F220/10—Esters
- C08F220/26—Esters containing oxygen in addition to the carboxy oxygen
- C08F220/30—Esters containing oxygen in addition to the carboxy oxygen containing aromatic rings in the alcohol moiety
- C08F220/303—Esters containing oxygen in addition to the carboxy oxygen containing aromatic rings in the alcohol moiety and one or more carboxylic moieties in the chain
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J133/00—Adhesives based on homopolymers or copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by only one carboxyl radical, or of salts, anhydrides, esters, amides, imides, or nitriles thereof; Adhesives based on derivatives of such polymers
- C09J133/04—Homopolymers or copolymers of esters
- C09J133/06—Homopolymers or copolymers of esters of esters containing only carbon, hydrogen and oxygen, the oxygen atom being present only as part of the carboxyl radical
- C09J133/10—Homopolymers or copolymers of methacrylic acid esters
- C09J133/12—Homopolymers or copolymers of methyl methacrylate
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J4/00—Adhesives based on organic non-macromolecular compounds having at least one polymerisable carbon-to-carbon unsaturated bond ; adhesives, based on monomers of macromolecular compounds of groups C09J183/00 - C09J183/16
- C09J4/06—Organic non-macromolecular compounds having at least one polymerisable carbon-to-carbon unsaturated bond in combination with a macromolecular compound other than an unsaturated polymer of groups C09J159/00 - C09J187/00
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J2301/00—Additional features of adhesives in the form of films or foils
- C09J2301/40—Additional features of adhesives in the form of films or foils characterized by the presence of essential components
- C09J2301/416—Additional features of adhesives in the form of films or foils characterized by the presence of essential components use of irradiation
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J2433/00—Presence of (meth)acrylic polymer
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
Description
[2] 後述する式1Bで表される基が、後述する式1B′で表される基である、[1]に記載の高分子化合物。
[3] 後述する式1A中のL1が、炭素数1~20個の、直鎖状、又は、分岐鎖状のアルキレン基である、[1]又は[2]に記載の高分子化合物。
[4] 後述する式1A中のL1が炭素数1~6個の直鎖状のアルキレン基である、[1]~[3]のいずれかに記載の高分子化合物。
[5] 後述する式1A中のnが1である、[1]~[4]のいずれかに記載の高分子化合物。
[6] 後述する式1A中のZ1が水素原子である、[1]~[5]のいずれかに記載の高分子化合物。
[7] 後述する式1Bで表される基が、*を結合位置としたとき、後述する式2a~2gからなる群より選択される少なくとも1つの基である、[1]~[6]のいずれかに記載の高分子化合物。
[8] 更に、後述する式2で表される繰り返し単位を有する[1]~[7]のいずれかに記載の高分子化合物。
[9] 後述する式2中のZ2がメチル基である、[8]に記載の高分子化合物。
[10] 後述する式2中のR4が炭素数1~10個の直鎖状、又は、分岐鎖状のアルキル基である、[8]又は[9]に記載の高分子化合物。
[11] 後述する式1Aで表される繰り返し単位の含有量が、全繰り返し単位を100モル%としたとき、30モル%以下である、[1]~[10]のいずれかに記載の高分子化合物。
[12] [1]~[11]のいずれかに記載の高分子化合物を製造するための高分子化合物の製造方法であって、後述する式3で表される化合物と、後述する式4で表されるヒドロキシ基含有(メタ)アクリレート化合物とのエステル化反応により、後述する式5で表される単量体Aを合成することと、上記単量体Aを重合させ、上記高分子化合物を得ることと、を含む高分子化合物の製造方法。
[13] 後述する式3で表される化合物が、クマル酸、コーヒー酸、2,5-ジヒドロケイ皮酸、3,5-ジヒドロケイ皮酸、シナピン酸、フェルラ酸、2,3-ジヒドロケイ皮酸、及び、これらの誘導体からなる群より選択される少なくとも1種の化合物である、[12]に記載の高分子化合物の製造方法。
[14] [2]に記載の高分子化合物を製造するための高分子化合物の製造方法であって、後述する式3′で表される化合物と、後述する式4′で表されるヒドロキシ基含有(メタ)アクリレート化合物とのエステル化反応により、後述する式5′で表される単量体Bを合成することと、上記単量体Bのヒドロキシ基と保護化剤とを反応させ、保護されたヒドロキシ基を有する後述する式6′で表される単量体Cを合成することと、上記単量体Cを重合させて、後述する式7′で表される高分子化合物前駆体を合成することと、上記高分子化合物前駆体の上記保護されたヒドロキシ基を脱保護して、上記高分子化合物を得ることと、を含む、高分子化合物の製造方法。
[15] 後述する式3′で表される化合物が、クマル酸、コーヒー酸、2,5-ジヒドロケイ皮酸、3,5-ジヒドロケイ皮酸、シナピン酸、フェルラ酸、2,3-ジヒドロケイ皮酸、及び、これらの誘導体からなる群より選択される少なくとも1種の化合物である、[14]に記載の高分子化合物の製造方法。
[16] 上記保護基が、エーテル系保護基、シリルエーテル系保護基、エステル系保護基、カーボネート系保護基、カルバメート系保護基、ホスフィナート系保護基、及び、スルホナート系保護基からなる群より選択される少なくとも1種である、[14]又は[15]に記載の高分子化合物の製造方法。
[17] 上記保護基が、上記カーボネート系保護基である[14]~[16]のいずれかに記載の高分子化合物の製造方法。
[18] 上記保護化剤が、ピロ炭酸ジ-tert-ブチルである、[14]に記載の高分子化合物の製造方法。
[19] [1]~[11]のいずれかに記載の高分子化合物を2つ含む二量体であって、
2つの前記高分子化合物は、前記式1A中のR1に隣接する二重結合が開裂して互いに結合している、二量体。
[20] [1]~[11]のいずれかに記載の高分子化合物を含有する接着剤組成物。
[21] [1]~[11]のいずれかに記載の高分子化合物からなる単量体と、[19]に記載の二量体とを含有する、接着剤組成物。
[22] 架橋密度が10000~20000mol/cm3である、[21]に記載の接着剤組成物。
[23] 300~700nmの紫外線を照射した場合に架橋密度が増加し、前記照射の後、200~300nmの紫外線を照射した場合に、架橋密度が減少する、[20]に記載の接着剤組成物。
[24] 300~700nmの紫外線を照射した場合の架橋密度に対し、200~300nmの紫外線を照射した場合の架橋密度が30%以下である、[23]に記載の接着剤組成物。
[25] 300~700nmの紫外線を照射した場合の架橋密度が10000~20000mol/cm3であり、200~300nmの紫外線を照射した場合の架橋密度が3000~6000mol/cm3である、[23]に記載の接着剤組成物。
[26] [20]~[25]のいずれか1項に記載の接着剤組成物を硬化させて得られた硬化物。
[27] [21]に記載の接着剤組成物の製造方法であって、[20]に記載の接着剤組成物に紫外線を照射する工程を含む、接着剤組成物の製造方法。
[28] [20]に記載の接着剤組成物に、紫外線を1回以上照射する工程を含む、接着力の調整方法。
本発明の二量体によれば、接着剤組成物に適用した際、より優れた接着性を有する接着剤組成物、その硬化物が得られる。
さらに、本発明の接着剤組成物は、紫外線を照射することで、接着強度を調整することができる。
また、本発明の接着力の調整方法によれば、紫外線を1回以上照射する工程を含むことで、可逆的に接着強度を調整することができる。
以下に記載する構成要件の説明は、本発明の代表的な実施形態に基づいてなされることがあるが、本発明はそのような実施形態に制限されるものではない。
なお、本明細書において、「~」を用いて表される数値範囲は、「~」の前後に記載される数値を下限値及び上限値として含む範囲を意味する。
また、本明細書において、「(メタ)アクリレート」はアクリレート及びメタクリレートの双方、又は、いずれかを表し、「(メタ)アクリル」はアクリル及びメタクリルの双方、又は、いずれかを表す。また、「(メタ)アクリロイル」はアクリロイル及びメタクロイルの双方、又は、いずれかを表す。
本発明の実施形態に係る高分子化合物(以下、「本高分子化合物」ともいう。)は下記式1Aで表される繰り返し単位(以下、「単位1A」ともいう。)を有する。
なかでも、Z1とはしては、水素原子、又は、炭素数1~5個のアルキル基が好ましく、水素原子、メチル基、又は、エチル基がより好ましく、水素原子が更に好ましい。
なかでも、L2は単結合が好ましい。
R3としては、特に制限されないが、例えば、アルキル基(好ましくは炭素数1~10個のアルキル基)等が挙げられる。なお、R3としては、後述するZ3と同様の基も使用できる。
なかでも、R2のうち2つ以上がヒドロキシ基である場合、更に優れた接着性と、更に優れた親水性とを有する接着剤組成物が得られる。
R2がヒドロキシ基である場合、式1Bで表される基が有するヒドロキシ基の数としては特に制限されないが、1~3個が好ましく、2~3個がより好ましい。
また、R5は水素原子、又は、*-OR31で表される基を表し、*は結合位置を表し、R31はヘテロ原子を有してもよい炭化水素基を表す。R5の*-OR31で表される基としては、すでに説明した式1B中の*-OR3(R2で表される基の一形態である)で表される基と同様の基が挙げられ、好適形態も同様である。
なお、複数あるR31は互いに結合して環を形成してもよく、複数あるR5はそれぞれ同一でも異なってもよい。
単位1Aの含有量が上記範囲内であると、より優れた本発明の効果を有する高分子化合物が得られる。
なお、高分子化合物中の単位1Aの含有量は、1H-NMRを用いて求められる値を意味する。
なお、本明細書において、重量平均分子量とは、ゲル浸透クロマトグラフィー(Gel Permeation Chromatography:GPC)により測定されるポリスチレン換算の重量平均分子量を意味する。
本高分子化合物は、単位1Aを含有していれば、本発明の効果を奏する範囲内において、他の単位を含有していてもよい。他の単位としては特に制限されないが、例えば、式2で表される繰り返し単位(以下、「単位2」ともいう。)が挙げられる。なお、本明細書において、単位2は単位1Aとは異なる繰り返し単位を意味する。
Z2の1価の基としては特に制限されないが、Z1の1価の基と同様の基が挙げられ、なかでも、水素原子、メチル基、又は、エチル基が好ましく、水素原子、又は、メチル基がより好ましい。
また、R4が直鎖状のアルキル基である場合、炭素数が9個以下であると、高分子化合物はより優れた剛性を有し、結果として接着剤組成物に適用した際に、より優れた接着性を有する。
本高分子化合物は優れた成膜性、及び、優れた親水性を有するため、本高分子化合物と、溶媒とを含有する組成物は、接着剤組成物、特に、親水性表面にも適用可能な接着剤組成物として使用できる。
上記接着剤組成物は支持体上に接着剤組成物層を形成した後、必要に応じて溶媒を除去して被膜(接着剤層)を形成すれば、支持体と接着剤層とが積層された接着テープ等として使用できる。
本高分子化合物の製造方法としては特に制限されず、公知の製造方法が適用できる。なかでも、より効率的に本高分子化合物を製造できる点で、以下の高分子化合物の製造方法が好ましい。
本発明に係る高分子化合物の製造方法の第1の実施形態は、後述する式3で表されるケイ皮酸誘導体と、後述する式4で表されるヒドロキシ基含有(メタ)アクリレート化合物とのエステル化反応により、後述する式5で表される単量体Aを合成すること(単量体A合成工程)と、得られた単量体Aを重合させ、高分子化合物を得ること(重合工程)と、を含む高分子化合物の製造方法である。以下では、本製造方法の各工程について詳述する。
本工程は、以下の式3で表される化合物と、以下の式4で表されるヒドロキシ基含有(メタ)アクリレート化合物とのエステル化反応(エステル化する反応)させて、単量体Aを合成する工程である。
R24の*-OR34で表される基としては、式1B中の*-OR3(R2で表される基の一形態)で表される基と同様の基が挙げられ、好適形態も同様である。
より原料の入手が容易で、より簡便に本高分子化合物が得られやすい点で、式3で表される化合物としては、下記式3Aで表されるケイ皮酸誘導体であることが好ましい。
ケイ皮酸誘導体としては、入手がより容易で、より簡便に高分子化合物が得られやすい点で、クマル酸(p-クマル酸が好ましい)、コーヒー酸、2,5-ジヒドロケイ皮酸、3,5-ジヒドロケイ皮酸、シナピン酸、フェルラ酸、2,3-ジヒドロケイ皮酸、及び、これらの誘導体からなる群より選択される少なくとも一つであることが好ましく、クマル酸(p-クマル酸が好ましい)、コーヒー酸、2,5-ジヒドロケイ皮酸、3,5-ジヒドロケイ皮酸、シナピン酸、フェルラ酸、及び、2,3-ジヒドロケイ皮酸からなる群より選択される少なくとも1種の化合物がより好ましい。
式4中のZ14の1価の基としては特に制限されないが、式1A中のZ1の1価の基として説明した基が挙げられ、好適形態も同様である。
また、L14の2価の基としては特に制限されないが、式1A中のL1の2価の基として説明した基が挙げられ、好適形態も同様である。
n1の上限は特に制限されないが、50以下が好ましく、20以下がより好ましく、10以下が更に好ましい。なかでも、n1は1が特に好ましい。
なお、式5における各記号は、式3、及び、4における対応する各記号と同義であり、好適形態も同様である。
また、酸触媒の存在下に反応を行うとき、反応により生成する水(以下、生成水ともいう。)を反応系外へ除去することが好ましい。生成水の除去方法としては、例えば、減圧下で反応を行う方法、共沸溶媒を用いて反応を行う方法、乾燥剤の存在下で反応を行う方法等が挙げられる。これらの方法は、いずれか1つの方法を用いてもよく、2つ以上の方法を併用しても良い。
方法1の反応温度は、特に制限されないが、一般に、0~150℃が好ましい。
添加剤の使用量としては、特に制限されないが、ケイ皮酸誘導体の1モルに対して、0.01倍モル以上(0.01当量以上)が好ましく、1.5倍モル以下が好ましい。
本工程は、単量体Aを重合させ、上記高分子化合物を得る工程である。単量体Aを重合させる方法としては特に制限されず、公知の方法が使用できる。
単量体Aを重合させる方法(重合方法)としては、例えば、塊状重合法、溶液重合法、及び、水系分散重合法(懸濁重合法、乳化重合法等)等が挙げられ、なかでも、より簡便に高分子化合物が得られる点で、溶液重合法、又は、水系分散重合法が好ましい。
溶媒は、1種を単独で用いてもよく、2種以上を組み合わせて用いてもよい。
重合開始剤としては、例えば、有機過酸化物、及び、アゾ化合物等が使用できる。有機過酸化物として、例えば、1,1-ビス(t-ヘキシルパーオキシ)-3,3,5-トリメチルシクロヘキサン、t-ヘキシルパーオキシピバレート、t-ブチルパーオキシピバレート、2,5-ジメチル-2,5-ビス(2-エチルヘキサノイルパーオキシ)ヘキサン、t-ヘキシルパーオキシ-2-エチルヘキサノエート、t-ブチルパーオキシ-2-エチルヘキサノエート、t-ブチルパーオキシイソブチレート、t-ブチルパーオキシ-3,5,5-トリメチルヘキサノエート、及び、t-ブチルパーオキシラウレート等が挙げられる。
また、アゾ化合物として、例えば、アゾビスイソブチロニトリル(AIBN)、及び、アゾビスシクロヘキサンカルボニトリル等が挙げられる。
これらの重合開始剤は単独で用いてもよく、2種以上を併用してもよい。
本発明に係る高分子化合物の製造方法の第2の実施形態は、後述する式3′で表されるケイ皮酸誘導体と、後述する式4′で表されるヒドロキシ基含有(メタ)アクリレート化合物とのエステル化反応により、後述する式5′で表される単量体Bを合成すること(単量体B合成工程)と、単量体Bのヒドロキシ基と保護化剤とを反応させ、保護されたヒドロキシ基を有する後述する式6′で表される単量体Cを合成すること(単量体C合成工程)と、単量体Cを重合させて、後述する式7′で表される高分子化合物前駆体を合成すること(高分子化合物前駆体合成工程)と、高分子化合物前駆体の保護されたヒドロキシ基を脱保護して、高分子化合物を得ること(脱保護工程)と、を含む、高分子化合物の製造方法である。
そこで、本発明者らは上記着想に基づき、単量体を重合させて高分子化合物を得る前に、単量体が有するヒドロキシ基を保護化剤で保護したところ、非常に高い収率を得ることができ、本製造方法に係る発明が完成した。
以下では、本製造方法の各工程について詳述する。
単量体B合成工程は、以下の式3′で表される化合物と、以下の式4′で表されるヒドロキシ基含有(メタ)アクリレート化合物とのエステル化反応により、以下の式5′で表される単量体Bを合成する工程である。
なお、式3中におけるR55の*-OR35で表される基としては特に制限されないが、式1B中におけるR2で表される基の一形態としてすでに説明した*-OR3で表される基と同様の基が挙げられ、好適形態も同様である。
また、式4′中、n2の上限は特に制限されないが、50以下が好ましく、20以下がより好ましく、10以下が更に好ましい。なかでも、n2は1が特に好ましい。
なお、式5′中のZ15、及び、L15で表される基は、式4′中の対応する基と同義であり、好適形態も同様である。また、式5′中のL25、R55、及び、t2で表される基は、式3′中の対応する基と同義であり、好適形態も同様である。また、式5′中、n2は、式4′中のn2と同義であり、好適形態も同様である。
本工程は、単量体Bのヒドロキシ基と保護化剤とを反応させ、保護されたヒドロキシ基を有する式6′で表される単量体Cを合成する工程である。
式6中、Z15、L15、L25、R55、n2、及び、t2は、それぞれ、式3′、及び、式4′中の対応する各記号と同義であり、好適形態も同様である。
カルバメート系保護基としては、*-C(O)NHR等が挙げられる。
また、式6Bには、式6′中のtが2である形態のみ示されているが、繰り返し単位当たりの*-OZ35の数、及び、配置は例であり、下記に制限されるものではない。
本工程は、単量体Cを重合させて式7′で表される高分子化合物前駆体を得る工程である。
また、高分子化合物前駆体を重合する方法としては特に制限されず、公知の合成方法が使用できる。公知の合成方法としては、例えば、第1の実施形態において単量体Aの重合方法として説明した方法が使用でき、好適形態も同様であるため、説明を省略する。
本工程は、高分子化合物前駆体の保護されたヒドロキシ基を脱保護して、高分子化合物を得る工程である。
保護されたヒドロキシ基(*-OZ3)の脱保護の方法としては特に制限されず、保護基の種類に応じて公知の方法を使用すればよい。また、その反応条件も保護基の種類に応じて適宜調整すればよい。保護基の種類、及び、反応条件としては、例えば、プロテクティブ・グループス・イン・オルガニック・シンセシス第4版(ジョン・ウィリー・アンド・サンズ出版)p.367-430(PROTECTIVE GROUPS in ORGANIC SYNTHESIS 4thEd.(JOHN WILEY & SONS)p.367-430)に保護基の種類ごとに記載されており、参照可能である。
二量体は、上述した本発明の高分子化合物(化学式1)を2つ含む。したがって、上述した高分子化合物について説明した内容については、説明を省略する。
上述した本発明の高分子化合物(化学式1)は、前記化学式1の式1A中のR1に隣接する二重結合部位が光感受性を有している。このため、この二重結合部位が紫外線(UV)の照射によって開裂し、2つの高分子化合物同士が互いに結合して二量体を形成する。
下記Scheme1によりAEDPA(構造は、下記Scheme1を参照)を合成した。まず、DHCA(3,4-dihydroxycinnamic acid、DHCA、0.36g、1当量)を、100mLの2口フラスコに入れ、DMF(N,N-ジメチルホルムアミド)に溶解させ、溶液を得た。次に、上記溶液に、N,N′-ジシクロヘキシルカルボジイミド(DCC)(0.49g、1.2当量)と、N,N-ジメチル-4-アミノピリジン(DMAP、28mg、0.1当量)のDMF溶液(1mL)を氷浴中で滴下し、更に、ヒドロキシエチルアクリレート(AHE、0.28g、1.2当量)のDMF溶液(1mL)を氷浴中で滴下し、混合液を得た。
反応終了後、混合液のDMFが約半分の体積となるまで濃縮し、希塩酸に加え、酢酸エチルで抽出した。有機相を集め、飽和食塩水で洗浄し、Na2SO4で脱水し、濃縮し、粗生成物を得た。
その後、酢酸エチルとヘキサンと(30-40%酢酸エチル)を含有する移動相を用いて、粗生成物をカラム精製し、最終生成物(AEDPA)を得た。収率は約40%だった。
次に、下記Scheme2によりAEDPA-Boc(構造は、下記Scheme2を参照)を合成した。まず、AEDPA(500mg、1当量)を20mLのアセトンに溶解させ、溶液を得た。次に、上記溶液にK2CO3(5当量)を加え、混合液を得た。次に、アセトン3mLにピロ炭酸ジ-tert-ブチル(「Boc2O」、2.2当量)を溶解させて得たBoc2O溶液を、上記混合液に滴下して、反応液を得た。次に、反応液を室温で2時間攪拌し、反応させた。なお、反応の進捗は、ヘキサン/酢酸エチル=2/1の薄層クロマトグラフィで確認した。反応後の反応液を濾過し、固体残渣をアセトンで3回洗浄した。次に、回収したろ液を濃縮し、カラム精製し、無色の油状の生成物を得た。収率は90%超だった。
(AEDPA-Boc/メタクリレート共重合体の合成)
次に、Scheme3により、AEDPA-Boc/メタクリレート共重合体(下記Scheme3中では、「Poly(AEDPA-Boc-co-MMA)」と表記した。)を合成した。まず、開始剤として、AIBN(アゾビスイソブチロニトリル、AEDPA-BocとMMAとのモル基準の合計量に対して2モル%)をフラスコにいれ、Arガスで置換した。次に、AEDPA-Boc(500mg、1当量)をイソプロパノール30mLに溶解した溶液を加え、混合液を得た。次に、メチルメタクリレート(418mg、4当量)をイソプロパノール5mLに溶解した溶液を上記混合液に加え、反応液を得た。次に、反応液を80℃に加熱し、10時間攪拌して反応させた。反応後の反応液を、エタノール水溶液に滴下し、粗生成物(ポリマー)を析出させた。得られた粗生成物は60℃の減圧オーブンで乾燥させ、白色の粉状の生成物を得た。収率は約70%だった。
次に、Scheme 4よりにAEDPA/メタクリレート共重合体(Scheme4中ではPoly(AEDPA-co-MMA)と表記した。)を合成した。まず、AEDPA-Boc/メタクリレート共重合体をTFA(トリフルオロ酢酸)/THF(テトラヒドロフラン)の1:1溶液に溶解させ、室温で4時間攪拌して混合液を得た。次に、混合液を水に滴下して、粗生成物を析出させた。粗生成物をろ別して、60℃の減圧オーブンで乾燥させ、灰色の粉状の生成物を得た。収率は90%だった。
AEDPA(500mg、1当量)、HMA(n-ヘキシルメタクリレート、1224mg、4当量)、及び、AEDPAとHMAとのモル基準の合計量に対して2モル%のAIBNを50mLフラスコに入れ、10mLのIPAを加え、Arガスで20分間バブリングした。重合は、400rpmで攪拌しながら75℃で行った。3時間後、更にAEDPAとHMAとのモル基準の合計量に対して1モル%のAIBNを添加した。その後、重合を10時間続けた。最終混合物を100mLの水に沈殿させ、濾過し、乾燥させて、1.59gの高分子化合物11を得た(92%)。
HMAに代えて、2-エチルヘキシルメタクリレート(EHMA)を用いたことを除いては、合成例2と同様の方法で、表1に記載した条件で高分子化合物1~6を合成した。なお、表1中、「仕込み比」とあるのは、AEDPAとメタクリレートモノマー(「MA」と記載した)の仕込み比(モル%)を示しており、Mw、及び、Mnは得られた高分子化合物の重量平均分子量、及び、数平均分子量を示しており、「組成」とあるのは、得られた高分子化合物中における、AEDPA単位の含有量(モル%)、及び、メタクリレート単位の含有量(モル%)を意味している。
また、表1中、高分子化合物の重量平均分子量、及び、数平均分子量は、ゲル浸透クロマトグラフィー(GPC)を用いて以下の条件で計測された。
HMA(表中「6C」と記載した。)に代えて、エチルメタクリレート(表中、「2C」と記載した。)、n-プロピルメタクリレート(表中、「3C」と記載した。)、n-ブチルメタクリレート(表中「4C」と記載した。)、ペンチルメタクリレート(表中「5C」と記載した。)、及び、n-デシルメタクリレート(表中「10C」と記載した。)を用いたこと除いては、合成例2と同様にして、高分子化合物7~10、12を合成した。得られた各高分子化合物の組成を表1に示した。
AEDPA-Bocを用いなかったことを除いては、実施例1と同様にして、比較例化合物を合成した。比較例化合物の組成を表1にまとめて示した。
接着性は、重ね合わせ接着継ぎ手を用いたせん断強度試験(lap shear test)により評価した。
ASTM D2651標準プロトコルに従って、Al(アルミニウム)基板を処理した後、完全に乾燥させ、すぐに接着性試験に使用した。
Al基板の大きさは、100mm×25mm×2mmで、(株)スタンダードテストピース製の市販品を購入して用いた。
200mgの各高分子化合物を、1.2mLのアセトンに溶解させ、接着剤組成物を得た。次に、100μLの接着剤組成物を上記Al基板の表面に均一にコーティングし、70℃で30分間乾燥させた。次に、2枚の基板を接触させ、1atmの圧力で80℃で1時間硬化させた後、真空下で60℃で1時間硬化させて完全に乾燥させた。
一方、AEPDA単位を有しない、比較例1の高分子化合物は、所望の接着硬度を有していなかった。
また、AEDPA単位の含有量が、5~15モル%である高分子化合物3は、高分子化合物2、及び、高分子化合物5と比較して、更に優れた接着強度を有していた。
また、式2中のR4で表されるアルキル基の炭素数が3~10個である、高分子化合物11は、高分子化合物7と比較して、より優れた接着強度を有していた。
また、式2中のR4で表されるアルキル基の炭素数が4~10個である、高分子化合物11は、高分子化合物8と比較して、更に優れた接着強度を有していた。
また、式2中のR4で表されるアルキル基の炭素数が5~10個である、高分子化合物11は、高分子化合物9と比較して、特に優れた接着強度を有していた。
PTFE(ポリテトラフルオロエチレン)基板は、60mm×20mm×2mmであり、使用前にサンドペーパー(METSAPRP080240)で研磨し、水及びアセトンで洗浄してから用いた。
高分子化合物4の200mgをアセトン1.2mLに溶解させ、接着剤組成物を調製した。次に、この接着剤組成物の約100μLをPTFE基板上に塗布し、70℃で3分間乾燥した。さらに、この接着剤組成物を塗布したPTFE基板2枚の塗布面を向かい合わせ、クリップで固定した後、80℃でさらに一時間加熱した。その後、約30分間室温にて徐冷した後、引っ張りせん断試験を行った。PTFE基板の間に塗布された接着剤組成物層の厚みは、0.08±0.01mmであった。
図2に示したとおり、高分子化合物4を含有する接着剤組成物を用いることで、ポリテトラフルオロエチレン同士を接着することができた。
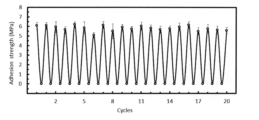
上記の高分子化合物における光感受性部位の存在を考慮して、接着特性に対する紫外線(UV)の影響を検討した(図3、図4)。接着力の測定、評価については、上述した実施例の評価を踏まえて行った。
実用的なアプリケーションでは、例えば雨の日には湿度が高いなど、接着された基材は湿潤状態に曝される。そのため、湿潤状態/水中および乾燥状態のいずれの条件でも使用できる接着剤が必要とされている。
P(AEDPA-co-EHMA)接着剤の可逆性を、紫外線照射の物理的刺激を切り替えることで検討した。
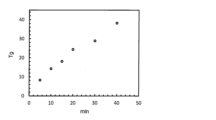
ドライ/ウェット条件での光可変接着の作用機構を明らかにするために、次に、UVトリガーに応答した接着剤の熱力学的特性と機械的特性の特徴を検討した。
UV-H照射20分後のTgは18℃から27℃まで上昇しており、UVが接着剤の硬度を高めていることが明らかになった。Tgの増加は、直鎖ポリマーの一部が、光架橋効果により光感受性部位(式1A中のR1に隣接する二重結合部位)で結合して二量体を形成し、部分的に網目構造が形成されることで、分子鎖セグメントの動きを阻害することで弾性率が増加していると考えられた。
(i)基材とカテコールポリマー鎖の界面に強いH-結合が存在することで接着性が向上している。(ii)カテコールポリマー鎖の分子間にH-結合が存在していることで凝集力が大きく向上している。これらのH-結合の相互作用は、最初のネットワーク状の構造を形成し、より高いTgとより大きなモジュールを引き起こす。(iii)紫外線下での環化による共有結合形成は、二重ネットワーク様構造を形成し、直鎖状ポリマーのものよりも高い強度になる。
Claims (11)
- 前記式1Aで表される繰り返し単位の含有量が、前記高分子化合物の全繰り返し単位を100モル%としたとき、30モル%以下である、請求項1に記載の接着剤組成物。
- 前記高分子化合物からなる単量体と、
前記高分子化合物を2つ含む二量体と
を含有し、
前記二量体における2つの前記高分子化合物は、前記式1A中のR1に隣接する二重結合が開裂して互いに結合している、請求項1に記載の接着剤組成物。 - 請求項1~6のいずれか1項に記載の接着剤組成物を硬化させて得られた硬化物。
- 請求項1~6のいずれか1項に記載の接着剤組成物の製造方法であって、
下記式3で表される化合物と、下記式4で表されるヒドロキシ基含有(メタ)アクリレート化合物とのエステル化反応により、下記式5で表される単量体Aを合成することと、
前記単量体Aを重合させ、前記高分子化合物を得ることと、
を含む接着剤組成物の製造方法。
(式3~5中、R24はヒドロキシ基、及び、*-OR34で表される基からなる群より選択される基を表し、R34はヘテロ原子を有してもよい炭化水素基を表し、*は結合位置を表し、複数あるR34は互いに結合して環を形成してもよく、Z14は水素原子、又は、1価の基を表し、L14は2価の基を表し、L24は単結合、又は、2価の基を表し、m1は1~5の整数を表し、n1は1以上の整数を表し、複数あるR24、及び、L14はそれぞれ同一でも異なってもよい。) - 請求項1~6のいずれか1項に記載の接着剤組成物の製造方法であって、
下記式3′で表される化合物と、下記式4′で表されるヒドロキシ基含有(メタ)アクリレート化合物とのエステル化反応により、下記式5′で表される単量体Bを合成することと、
前記単量体Bのヒドロキシ基と保護化剤とを反応させ、保護されたヒドロキシ基を有する式6′で表される単量体Cを合成することと、
前記単量体Cを重合させて、式7′で表される高分子化合物前駆体を合成することと、
前記高分子化合物前駆体の前記保護されたヒドロキシ基を脱保護して、前記高分子化合物を得ることと、
を含む、接着剤組成物の製造方法。
(式3′、4′、5′、6′、及び、7′中、R55は水素原子、又は、*-OR35で表される基を表し、R35はヘテロ原子を有していてもよい炭化水素基を表し、*は結合位置を表し、複数あるR35は互いに結合して環を形成してもよく、Z15は水素原子、又は、1価の基を表し、L15は2価の基を表し、L25は単結合、又は、2価の基を表し、Z3は前記ヒドロキシ基の保護基であり、複数あるZ3は互いに結合して環を形成してもよく、n2は1以上の整数であり、t2は1~5の整数であり、複数あるR55、L15、及び、Z3はそれぞれ同一でも異なってもよい。) - 請求項6に記載の接着剤組成物の製造方法であって、請求項1に記載の接着剤組成物に紫外線を照射する工程を含む、接着剤組成物の製造方法。
- 請求項1-6のいずれか1項に記載の接着剤組成物に、紫外線を1回以上照射する工程を含む、接着力の調整方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020019311 | 2020-02-07 | ||
| JP2020019311 | 2020-02-07 | ||
| PCT/JP2021/004170 WO2021157668A1 (ja) | 2020-02-07 | 2021-02-04 | 高分子化合物、高分子化合物の製造方法、接着剤組成物、硬化物、接着剤組成物の製造方法および接着力の調整方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JPWO2021157668A1 JPWO2021157668A1 (ja) | 2021-08-12 |
| JPWO2021157668A5 JPWO2021157668A5 (ja) | 2022-09-02 |
| JP7299647B2 true JP7299647B2 (ja) | 2023-06-28 |
Family
ID=77199952
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021575867A Active JP7299647B2 (ja) | 2020-02-07 | 2021-02-04 | 高分子化合物、高分子化合物の製造方法、接着剤組成物、硬化物、接着剤組成物の製造方法および接着力の調整方法 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US20230101138A1 (ja) |
| EP (1) | EP4101870A4 (ja) |
| JP (1) | JP7299647B2 (ja) |
| WO (1) | WO2021157668A1 (ja) |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3231984B2 (ja) | 1995-12-14 | 2001-11-26 | 京セラ株式会社 | 半導体素子収納用パッケージ及びその製造方法 |
| CN101812182A (zh) | 2010-02-02 | 2010-08-25 | 江南大学 | 一种光敏性荷电纳米粒子的制备方法 |
| JP2012107198A (ja) | 2010-10-28 | 2012-06-07 | Jnc Corp | 光配向法に適した化合物および該化合物からなる感光性ポリマー |
| JP6509889B2 (ja) | 2013-11-04 | 2019-05-08 | エシコン エルエルシー | 医療装置用の多構成要素パッケージ |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH03231984A (ja) * | 1990-01-31 | 1991-10-15 | Minnesota Mining & Mfg Co <3M> | 光架橋性粘着剤組成物及びそれを使用して一時的貼着後剥離する方法 |
| JPH06509889A (ja) * | 1992-06-19 | 1994-11-02 | エフ・ホフマン−ラ ロシュ アーゲー | 光学的非線形ポリマー |
| CN103370387B (zh) | 2011-02-18 | 2018-01-19 | 3M创新有限公司 | 光学透明的粘合剂、使用方法和由其制得的制品 |
| JP6485263B2 (ja) * | 2015-07-16 | 2019-03-20 | 日油株式会社 | 光修復剤および用途 |
| KR20180061217A (ko) * | 2015-09-28 | 2018-06-07 | 쓰리엠 이노베이티브 프로퍼티즈 캄파니 | 절단가능한 가교결합제를 포함하는 패턴화된 필름 물품 및 방법 |
| JPWO2018173727A1 (ja) * | 2017-03-24 | 2019-11-07 | 富士フイルム株式会社 | 光配向性共重合体、光配向膜および光学積層体 |
-
2021
- 2021-02-04 JP JP2021575867A patent/JP7299647B2/ja active Active
- 2021-02-04 US US17/796,757 patent/US20230101138A1/en active Pending
- 2021-02-04 WO PCT/JP2021/004170 patent/WO2021157668A1/ja unknown
- 2021-02-04 EP EP21750933.0A patent/EP4101870A4/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP3231984B2 (ja) | 1995-12-14 | 2001-11-26 | 京セラ株式会社 | 半導体素子収納用パッケージ及びその製造方法 |
| CN101812182A (zh) | 2010-02-02 | 2010-08-25 | 江南大学 | 一种光敏性荷电纳米粒子的制备方法 |
| JP2012107198A (ja) | 2010-10-28 | 2012-06-07 | Jnc Corp | 光配向法に適した化合物および該化合物からなる感光性ポリマー |
| JP6509889B2 (ja) | 2013-11-04 | 2019-05-08 | エシコン エルエルシー | 医療装置用の多構成要素パッケージ |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2021157668A1 (ja) | 2021-08-12 |
| EP4101870A4 (en) | 2024-03-20 |
| EP4101870A1 (en) | 2022-12-14 |
| US20230101138A1 (en) | 2023-03-30 |
| WO2021157668A1 (ja) | 2021-08-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US6784256B1 (en) | End-functionalized polymers by controlled free-radical polymerization process and polymers made therefrom | |
| EP1709089B1 (en) | Water-and oil-repellent fluoroacrylates | |
| ZA200207477B (en) | Crosslinkable or polymerizable propolymers. | |
| US20220041782A1 (en) | Practical synthesis of multiphase self-healing polymers from commodity monomers | |
| US20090270559A1 (en) | Acid functionalized gradient block copolymers | |
| JP2008525620A (ja) | フルオロアクリレート−メルカプト官能性コポリマー | |
| JP2008525619A (ja) | フルオロアクリレート多官能性アクリレートコポリマー組成物 | |
| US6228945B1 (en) | Three arm star compositions of matter having diblock arms based on polyisobutylene and methods of preparation | |
| US7067586B2 (en) | Methods of making ABA-type block copolymers having a random block of hydrophobic and hydrophilic monomers | |
| EP3344705A1 (en) | Copolymers containing polysiloxane macromonomer units, process of their preparation and their use in coating compositions and polymeric moulding compounds | |
| Verjans et al. | Supramolecular polymer materials based on ureidopyrimidinone quadruple hydrogen bonding units | |
| JP7299647B2 (ja) | 高分子化合物、高分子化合物の製造方法、接着剤組成物、硬化物、接着剤組成物の製造方法および接着力の調整方法 | |
| CN108473630B (zh) | 可固化的聚合物材料及其使用方法 | |
| AU2011258284A1 (en) | Fluoropolymer additive for coatings | |
| JP4878411B2 (ja) | 分子末端に重合性不飽和基を有するアクリル系重合体 | |
| US20220332859A1 (en) | Polymer material and method for producing same, and polymer compatibilizing agent | |
| Mahkam et al. | Synthesis and characterization of crosslinked polyacrylates containing cubane and silyl groups | |
| JPS6263560A (ja) | (メタ)アクリル酸フルオロアルキルオリゴマ−及びその誘導体 | |
| JPH01254719A (ja) | ポリシロキサン基含有重合体 | |
| KR102495336B1 (ko) | 아지리딘기를 함유하는 고분자 브러시를 포함하는 가교제, 이의 제조방법 및 이의 용도 | |
| WO2023190605A1 (ja) | 複合材料及びその製造方法並びに架橋剤 | |
| JPS6030715B2 (ja) | 被覆組成物 | |
| WO2023111723A1 (en) | Degradable crosslinkers for (meth)acrylic resins and methods thereof | |
| JP2019147857A (ja) | ガロール基様側鎖を有する共重合体を含む接着剤組成物 | |
| JP2021138876A (ja) | グリセロールデンドロン共重合体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220706 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220706 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230418 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230525 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230606 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230609 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7299647 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |