JP7235733B2 - Pd-1に特異的に結合する抗体、及び使用方法 - Google Patents
Pd-1に特異的に結合する抗体、及び使用方法 Download PDFInfo
- Publication number
- JP7235733B2 JP7235733B2 JP2020516792A JP2020516792A JP7235733B2 JP 7235733 B2 JP7235733 B2 JP 7235733B2 JP 2020516792 A JP2020516792 A JP 2020516792A JP 2020516792 A JP2020516792 A JP 2020516792A JP 7235733 B2 JP7235733 B2 JP 7235733B2
- Authority
- JP
- Japan
- Prior art keywords
- seq
- antibody
- antigen
- antibodies
- cells
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/40—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/06—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies from serum
- C07K16/065—Purification, fragmentation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2818—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against CD28 or CD152
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/57—Medicinal preparations containing antigens or antibodies characterised by the type of response, e.g. Th1, Th2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/33—Crossreactivity, e.g. for species or epitope, or lack of said crossreactivity
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
- C07K2317/732—Antibody-dependent cellular cytotoxicity [ADCC]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/75—Agonist effect on antigen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
Description
本出願は、ASCIIフォーマットで電子的に提出済みであり、その全体が参照により本明細書に組み込まれている配列表を含む。2018年5月30日に作成された上記ASCIIコピーは、「JBI5131WOPCT_ST25.txt」というファイル名で、サイズは220キロバイトである。
本発明は、PD-1に特異的に結合する抗体、抗体をコードするポリヌクレオチド又は抗原結合断片、並びに、前述の作製方法及び使用方法に関する。
PD-1に特異的に結合する抗体、又はその抗原結合断片、本明細書において提供する抗体をコードするポリヌクレオチド、ベクター、宿主細胞、並びに抗体の作製方法及び使用方法を本明細書で提供する。抗体又はその抗原結合断片はアゴニスト抗体であってよい。
TPH細胞は、以下のように識別することができる:生、CD19-CD56-/CD4+CD45RO+/HLADR+/CXCR5-/ICOS+PD1+;TFH/TPHの組み合わせは、以下のように識別することができる:生、CD19-CD56-/CD4+CD45RO+/HLADR+/ICOS+PD1+。メモリーT細胞は、CD4+ CD45RO+、又はCD8+ CD45RO+として識別することができる。
mAb PD1B505、PD1B742、PD1B743、PD1B878、PD1B1085、PD1B1086、PD1B1087、PD1B1088、PD1B1089、PD1B1090、PD1B1091、PD1B1092、PD1B1093、PD1B1094、又はPD1B1095は、PD1B505 mAbリネージの例示的な抗体である。これらのmAbは、いくつかの抗体が、HCDR2に1つのアミノ酸の違いを有し、LCDR1に1つ又は2つのアミノ酸の違いを有することを除いて、同一のCDR領域を有する。VH領域の同一性は82~100%であり、VL領域の同一性は78~100%である。PD1B505リネージmAbは、リガンドを遮断しない。
WINIETGXPT;
[式中、XはE、Y、H、又はWである。]
TASSSX1X2SSYLH;
[式中、
X1はV又はFであり、
X2はS又はPである。]
PD-L1の、PD-1への結合を遮断することであって、遮断の欠如は、実施例1に記載した、PD-L1を発現する細胞及びPD-1を発現する細胞のクラスター化を、抗体が阻害できないことにより測定される、遮断することと、
約5×10-8M以下の平衡解離定数(KD)でPD-1に結合することであって、KDが、+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、
約3×104 1/Ms以上の結合速度定数(ka)でPD-1に結合することであって、kaは+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、
約3×10-3 1/s以下の解離定数(kd)でPD-1に結合することであって、kdは、+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、抗原特異的T細胞の増殖を阻害することであって、
増殖はCMV-PBMCアッセイで評価される、阻害することと、
のうちの、1つ、2つ、3つ、4つ、又は5つを有する。
QVQLVQSGSELKKPGASVKVSCKASGYTFTSYAMNWVRQAPGQGLEWMGWINTNTGNPTYAQGFTGRFVFSLDTSVSTAYLQICSLKAEDTAVYYCAR
EIVLTQSPATLSLSPGERATLSCGASQSVSSSYLAWYQQKPGLAPRLLIYDASSRATGIPDRFSGSGSGTDFTLTISRLEPEDFAVYYCQQYGSSP
X1VQLX2X3SGX4ELKKPGX5X6VKX7SCKASGYTFTDYSMHWVX8QAPGX9GLX10WMGWINIETGX11PTYAX12X13FX14GRFX15FSLX16TSX17STAYLQIX18X19LKX20EDTAX21YFCARDYYGTYFYAMDYWGQGTX22X23TVSS;[式中、
X1はD若しくはQであり、
X2はQ若しくはVであり、
X3はE若しくはQであり、
X4はP若しくはSであり、
X5はE若しくはAであり、
X6はT若しくはSであり、
X7はI若しくはVであり、
X8はK若しくはRであり、
X9はK若しくはQであり、
X10はK若しくはEであり、
X11はE、Y、H、若しくはWであり、
X12はD若しくはQであり、
X13はD若しくはGであり、
X14はK若しくはTであり、
X15はA若しくはVであり、
X16はE若しくはDであり、
X17はA若しくはVであり、
X18はN、C、若しくはSであり、
X19はN若しくはSであり、
X20はN若しくはAであり、
X21はT若しくはVであり、
X22はT若しくはLであり、若しくは
X23はL若しくはVである。]
X1IVLTQSPAX2X3SX4SX5GERX6TX7X8CTASSSX9X10SSYLHWYQQKPGX11X12PX13LX14IYSTSNLASGX15PX16RFSGSGSGTX17X18X19LTISX20X21EX22EDX23AX24YYCH_QYHRSPLTFGX25GTKLEX26K;[式中、
X1はQ又はEであり、
X2はI又はTであり、
X3はM又はLであり、
X4はA又はLであり、
X5はL又はPであり、
X6はV又はAであり、
X7はM又はLであり、
X8はT又はSであり、
X9はV又はFであり、
X10はS又はPであり、
X11はS又はLであり、
X12はS又はAであり、
X13はK又はRであり、
X14はW又はLであり、
X15はV又はIであり、
X16はA又はDであり、
X17はS又はDであり、
X18はY又はFであり、
X19はS又はTであり、
X20はS又はRであり、
X21はM又はLであり、
X22はA又はPであり、
X23はA又はFであり、
X24はT又はVであり、
X25はA又はQであり、かつ
X26はL又はIである。]
配列番号8のVH及び配列番号14のVL、
配列番号9のVH及び配列番号15のVL、
配列番号9のVH及び配列番号16のVL、
配列番号10のVH及び配列番号16のVL、
配列番号140のVH及び配列番号16のVL、
配列番号141のVH及び配列番号16のVL、
配列番号142のVH及び配列番号16のVL、
配列番号10のVH及び配列番号143のVL、
配列番号10のVH及び配列番号144のVL、
配列番号140のVH及び配列番号143のVL、
配列番号141のVH及び配列番号143のVL、
配列番号142のVH及び配列番号143のVL、
配列番号140のVH及び配列番号144のVL、
配列番号141のVH及び配列番号144のVL、若しくは
配列番号142のVH及び配列番号144のVL、
を含む抗体又は抗原結合断片との結合に競合する、単離抗体又はその抗原結合断片も提供する。
配列番号8のVH及び配列番号14のVL、
配列番号9のVH及び配列番号15のVL、
配列番号9のVH及び配列番号16のVL、
配列番号10のVH及び配列番号16のVL、
配列番号140のVH及び配列番号16のVL、
配列番号141のVH及び配列番号16のVL、
配列番号142のVH及び配列番号16のVL、
配列番号10のVH及び配列番号143のVL、
配列番号10のVH及び配列番号144のVL、
配列番号140のVH及び配列番号143のVL、
配列番号141のVH及び配列番号143のVL、
配列番号142のVH及び配列番号143のVL、
配列番号140のVH及び配列番号144のVL、
配列番号141のVH及び配列番号144のVL、若しくは
配列番号142のVH及び配列番号144のVL、
を含む抗体により結合される同一のエピトープに結合する、単離抗体又はその抗原結合断片も提供する。
配列番号11及び17、
配列番号12及び18、
配列番号12及び19、
配列番号13及び19、
配列番号23及び29、
配列番号24及び30、
配列番号24及び31、
配列番号25及び31、
配列番号132及び133、若しくは
配列番号134及び135、
配列番号155及び19、
配列番号156及び19、
配列番号157及び19、
配列番号13及び158、
配列番号13及び159、
配列番号155及び158、
配列番号156及び158、
配列番号157及び158、
配列番号155及び159、
配列番号156及び159、
配列番号157及び159、
配列番号160及び31、
配列番号161及び31、
配列番号162及び31、
配列番号25及び163、
配列番号25及び164、
配列番号160及び163、
配列番号161及び163、
配列番号162及び163、
配列番号160及び164、
配列番号161及び164、若しくは
配列番号162及び164、
のポリヌクレオチド配列を含むポリヌクレオチドによりコードされる。
mAb PD1B506、PD1B750、PD1B751、PD1B845、PD1B846、PD1B847、PD1B848、PD1B849、及びPD1B850は、PD1B506 mAbリネージの例示的な抗体である。これらのmAbは、同一のHCDR1、HCDR3、LCDR1、LCDR2、及びLCDR3、並びに多様体HCDR2を有する。VH領域の同一性は80~100%であり、VL領域の同一性は約98%である。PD1B506リネージmAbは、リガンドを遮断する。リネージは、配列番号32、124、40、41、42、及び43のHCDR1、HCDR2、HCDR3、LCDR1、LCDR2、及びLCDR3、並びに、配列番号120のVH属配列、並びに、配列番号121のVL属配列を特徴とする。
EINPNX1X2GIN;[式中、
X1はN、D、Q、K、又はEであり、
X2はG、A、又はIである。]
PD-L1の、PD-1への結合を遮断することであって、遮断は、実施例1に記載した、PD-L1を発現する細胞及びPD-1を発現する細胞のクラスター化を、抗体が阻害する能力により測定される、遮断することと、
約5×10-8M以下の平衡解離定数(KD)でPD-1に結合することであって、KDが、+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、
約4×105 1/Ms以上の結合速度定数(ka)でPD-1に結合することであって、kaは、+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、
約1×10-2 1/s以下の解離定数(kd)でPD-1に結合することであって、kdは、+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、抗原特異的T細胞の増殖を阻害することであって、
増殖は、実施例1に記載されているCMV-PBMCアッセイにおいて評価される、阻害することと、
のうちの、1つ、2つ、3つ、4つ、又は5つを有する。
QVQLVQSGAEVKKPGASVKVSCKASGYTFTGYYMHWVRQAPGQGLEWMGWINPNSGGTNYAQKFQGRVTMTRDTSISTAYMELSRLRSDDTAVYYCAR
DIQMTQSPSSLSASVGDRVTITCRASQGISSWLAWYQQKPEKAPKSLIYAASSLQSGVPSRFSGSGSGTDFTLTISSLQPEDFATYYCQQYNSYP
QVQLX1QX2GAEX3X4KPGASVKX5SCKASGYTFTTYWMHWVX6QX7PGQGLEWX8GEINPNX9X10GINY X11X12KFX13X14X15X16TLTVDKSX17STAYMX18LSX19LX20SX21D X22AVYYCTIDYYDYGGYWGQGTX23X24TVSS;[式中、
X1はQ又はVであり、
X2はS又はPであり、
X3はL又はVであり、
X4はV又はKであり、
X5はL又はVであり、
X6はK又はRであり、
X7はR又はAであり、
X8はI又はMであり、
X9はN、D、Q、K、又はEであり、
X10はG、A、又はIであり、
X11はN又はAであり、
X12はE又はQであり、
X13はK又はQであり、
X14はK又はGであり、
X15はK又はRであり、
X16はA又はVであり、
X17はS又はIであり、
X18はQ又はEであり、
X19はS又はRであり、
X20はT又はRであり、
X21はE又はDであり、
X22はS又はTであり、
X23はT又はLであり、かつ
X24はL又はVである。]
DIX1MTQSX2X3X4X5SX6SVX7DRVX8X9TCKASQNVGTNVAWYQQKPX10X11X12PKX13LIYSASYRYSGVPX14RFX15GSGSGTDFTLTIX16X17X18QX19EDX20AX21YX22CQQYNIYPYTFGX23GTKLEX24K;[式中、
X1はV又はQであり、
X2はQ又はPであり、
X3はK又はSであり、
X4はF又はSであり、
X5はM又はLであり、
X6はT又はAであり、
X7はR又はGであり、
X8はS又はTであり、
X9はV又はIであり、
X10はG又はEであり、
X11はQ又はKであり、
X12はS又はAであり、
X13はA又はSであり、
X14はD又はSであり、
X15はT又はSであり、
X16はT又はSであり、
X17はN又はSであり、
X18はV又はLであり、
X19はS又はPであり、
X20はL又はFであり、
X21はE又はTであり、
X22はF又はYであり、
X23はS又はQであり、かつ
X24はM又はIである。]
配列番号44のVH及び配列番号60のVL、
配列番号45のVH及び配列番号61のVL、
配列番号45のVH及び配列番号62のVL、
配列番号46のVH及び配列番号61のVL、
配列番号47のVH及び配列番号61のVL、
配列番号48のVH及び配列番号61のVL、
配列番号49のVH及び配列番号61のVL、
配列番号50のVH及び配列番号61のVL、若しくは
配列番号51のVH及び配列番号61のVL、
を含む抗体又は抗原結合断片との結合に競合する、単離抗体又はその抗原結合断片も提供する。
配列番号44のVH及び配列番号60のVL、
配列番号45のVH及び配列番号61のVL、
配列番号45のVH及び配列番号62のVL、
配列番号46のVH及び配列番号61のVL、
配列番号47のVH及び配列番号61のVL、
配列番号48のVH及び配列番号61のVL、
配列番号49のVH及び配列番号61のVL、
配列番号50のVH及び配列番号61のVL、若しくは
配列番号51のVH及び配列番号61のVL、
を含む抗体により結合される同一のエピトープに結合する、単離抗体又はその抗原結合断片も提供する。
配列番号52及び63、
配列番号53及び64、
配列番号53及び65、
配列番号54及び64、
配列番号55及び64、
配列番号56及び64、
配列番号57及び64、
配列番号58及び64、
配列番号59及び64、
配列番号74及び85、
配列番号75及び86、
配列番号75及び87、
配列番号76及び86、
配列番号77及び86、
配列番号78及び86、
配列番号79及び86、
配列番号80及び86、
配列番号81及び86、
配列番号136及び137、若しくは
配列番号138及び139、
のポリヌクレオチド配列を含むポリヌクレオチドによりコードされる。
mAb PD1B505、PD1B756、及びPD1B757は、PD1B512 mAbリネージの例示的な抗体である。これらのmAbは、約84%のVH領域同一性、及び90~99%のVL領域同一性を有する、同一のCDR領域を有する。PD1B512リネージmAbは、リガンドを遮断しない。リネージは、配列番号88、89、90、91、92、及び93のHCDR1、HCDR2、HCDR3、LCDR1、LCDR2、及びLCDR3、並びに、配列番号122のVH属配列、並びに、配列番号123のVL属配列を特徴とする。
QITLKESGPTLVKPTQTLTLTCTFSGFSLSTSGVGVGWIRQPPGKALEWLALIYWNDDKRYSPSLKSRLTITKDTSKNQVVLTMTNMDPVDTGTYYCV
DIVMTQSPLSLPVTPGEPASISCRSSQSLLHSNGYNYLDWYLQKPGQSPQLLIYLGSNRASGVPDRFSGSGSGTDFTLKISRVEAEDVGVYYCMQALQTP
QX1TLKESGPX2LX3X4PX5QTLX6LTCX7FSGFSLSTSGMGVSWIRQPX8GKX9LEWLAHIYWDDDKRYX10PSLKSRLTIX11KDTSX12NQVX13LX14X15TX16X17DX18X19DTGTYYCVRKGYYDYGYVMDYWGQGTX20VTVSS[式中、
X1はV又はIであり、
X2はG又はTであり、
X3はL又はVであり、
X4はQ又はKであり、
X5はS又はTであり、
X6はS又はTであり、
X7はS又はTであり、
X8はS又はPであり、
X9はG又はAであり、
X10はN又はSであり、
X11はS又はTであり、
X12はS又はKであり、
X13はF又はVであり、
X14はK又はTであり、
X15はI又はMであり、
X16はS又はNであり、
X17はV又はMであり、
X18はT又はPであり、
X19はA又はVであり、かつ
X20はT又はLである。]
DIVMTQX1X2LSX3PVTX4GX5X6ASISCRSSKSLLHSNGITYLNWYLQKPGQSPQLLIYQMSNLASGVPDRFSX7SGSGTDFTLX8ISRVEAEDVGVYYCAQNLELPLTFGX9GTKX10EX11K[式中、
X1はA又はSであり、
X2はA又はPであり、
X3はN又はLであり、
X4はL又はPであり、
X5はT又はEであり、
X6はS又はPであり、
X7はS又はGであり、
X8はR又はKであり、
X9はS又はGであり、
X10はL又はVであり、かつ
X11はM又はIである。]
配列番号94のVH及び配列番号98のVL、
配列番号95のVH及び配列番号99のVL、若しくは
配列番号95のVH及び配列番号100のVL、
を含む抗体又は抗原結合断片との結合に競合する、単離抗体又はその抗原結合断片も提供する。
配列番号94のVH及び配列番号98のVL、
配列番号95のVH及び配列番号99のVL、若しくは
配列番号95のVH及び配列番号100のVL、
を含む抗体により結合される同一のエピトープに結合する、単離抗体又はその抗原結合断片も提供する。
配列番号96及び101、
配列番号97及び102、
配列番号97及び103、
配列番号106及び111、
配列番号107及び112、若しくは
配列番号107及び113、
のポリヌクレオチド配列を含むポリヌクレオチドによりコードされる。
本明細書において提供する、PD-1に特異的に結合する抗体の多様体又はその抗原結合断片は、本発明の範囲内である。例えば、多様体は、その多様体抗体が、親抗体と比較したときに改善された機能的性質を保持する、又は有する限り、VH及び/又はVLに、1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、又は29個のアミノ酸置換を含んでよい。いくつかの実施形態では、配列同一性は、本発明のVH及び/又はVLアミノ酸配列に対して、約80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、又は99%であってよい。いくつかの実施形態では、変化はフレームワーク領域に存在する。いくつかの実施形態では、多様体は保存的置換により生成される。
配列番号8のVH及び配列番号14のVL、
配列番号9のVH及び配列番号15のVL、
配列番号9のVH及び配列番号16のVL、
配列番号10のVH及び配列番号16のVL、
配列番号140のVH及び配列番号16のVL、
配列番号141のVH及び配列番号16のVL、
配列番号142のVH及び配列番号16のVL、
配列番号10のVH及び配列番号143のVL、
配列番号10のVH及び配列番号144のVL、
配列番号140のVH及び配列番号143のVL、
配列番号141のVH及び配列番号143のVL、
配列番号142のVH及び配列番号143のVL、
配列番号140のVH及び配列番号144のVL、
配列番号141のVH及び配列番号144のVL、
配列番号142のVH及び配列番号144のVL、
配列番号44のVH及び配列番号60のVL、
配列番号45のVH及び配列番号61のVL、
配列番号45のVH及び配列番号62のVL、
配列番号46のVH及び配列番号61のVL、
配列番号47のVH及び配列番号61のVL、
配列番号48のVH及び配列番号61のVL、
配列番号49のVH及び配列番号61のVL、
配列番号50のVH及び配列番号61のVL、
配列番号51のVH及び配列番号61のVL、
配列番号94のVH及び配列番号98のVL、
配列番号95のVH及び配列番号99のVL、若しくは
配列番号95のVH及び配列番号100のVL、
に少なくとも80%同一であるVH及びVLを含む、PD-1に特異的に結合する抗体、又はその抗原結合断片もまた提供する。
本明細書において提供する、PD-1に特異的に結合する抗体、又はその抗原結合断片を更に改変して、親抗体と比較したときに、同様の、又は変化した性質を有する改変抗体を生成することができる。本発明の抗体では、VH、VL、VH及びVL、定常領域、重鎖フレームワーク、軽鎖フレームワーク、又は6つのCDRのうちのいずれか又は全てが改変されていてもよい。
本明細書において提供する、PD-1に特異的に結合する抗体、又はその抗原結合断片は、野生型又は改変Fcを有する、任意の既知のアイソタイプ又はアロタイプのものであることができる。
ADCCを誘導するモノクローナル抗体の能力は、そのオリゴ糖成分を操作することにより増強され得る。ヒトIgG1又はIgG3は、Asn297においてN-グリコシル化される。ここで、グリカンの大部分は、公知の二分岐G0、G0F、G1、G1F、G2、又はG2Fの形態である。遺伝子操作されていないCHO細胞により生成される抗体は、典型的には、少なくとも約85%のグリカンフコース含量を有する。Fc領域に付加された二分岐の複合体型オリゴ糖からのコアフコースの除去は、抗原結合又はCDC活性を変更することなく、FcγRIIIa結合の改善によって抗体のADCCを増強する。このようなmAbは、二分岐の複雑なタイプのFcオリゴ糖を有する、比較的高い脱フコシル化抗体の成功した発現をもたらすことが報告された種々の方法、例えば、培養物浸透圧の制御(Konno et al.,Cytotechnology 64(:249-65,2012)、多様体CHO株Lec13を宿主細胞株として適用すること(Shields et al.,J Biol Chem 277:26733-26740,2002)、多様体CHO株EB66を宿主細胞株として適用すること(Olivier et al.,MAbs;2(4):405-415,2010;PMID:20562582)、ラットハイブリドーマ細胞YB2/0を宿主細胞株として適用すること(Shinkawa et al.,J Biol Chem 278:3466-3473,2003)、低分子干渉RNAを、1,6-フコシルトランスフェラーゼ(FUT8)遺伝子に対して特異的に導入すること(Mori et al.,Biotechnol Bioeng 88:901-908,2004)、又は、β-1,4-N-アセチルグルコサミン転移酵素III、及びゴルジα-マンノシダーゼII又は潜在的なα-マンノシダーゼI阻害剤であるキフネンシン(Ferrara et al.,J Biol Chem 281:5032-5036,2006,Ferrara et al.,Biotechnol Bioeng 93:851-861,2006;Xhou et al.,Biotechnol Bioeng 99:652-65,2008)を使用して達成することができる。
抗イディオタイプ抗体とは、本明細書にて開示したPD-1に特異的に結合する抗体に特異的に結合する、抗体である。
配列番号8のVH及び配列番号14のVL、
配列番号9のVH及び配列番号15のVL、
配列番号9のVH及び配列番号16のVL、
配列番号10のVH及び配列番号16のVL、
配列番号140のVH及び配列番号16のVL、
配列番号141のVH及び配列番号16のVL、
配列番号142のVH及び配列番号16のVL、
配列番号10のVH及び配列番号143のVL、
配列番号10のVH及び配列番号144のVL、
配列番号140のVH及び配列番号143のVL、
配列番号141のVH及び配列番号143のVL、
配列番号142のVH及び配列番号143のVL、
配列番号140のVH及び配列番号144のVL、
配列番号141のVH及び配列番号144のVL、
配列番号142のVH及び配列番号144のVL、
配列番号44のVH及び配列番号60のVL、
配列番号45のVH及び配列番号61のVL、
配列番号45のVH及び配列番号62のVL、
配列番号46のVH及び配列番号61のVL、
配列番号47のVH及び配列番号61のVL、
配列番号48のVH及び配列番号61のVL、
配列番号49のVH及び配列番号61のVL、
配列番号50のVH及び配列番号61のVL、
配列番号51のVH及び配列番号61のVL、
配列番号94のVH及び配列番号98のVL、
配列番号95のVH及び配列番号99のVL、若しくは
配列番号95のVH及び配列番号100のVL、
を含む抗体に特異的に結合する、抗イディオタイプ抗体も提供する。
本発明はまた、異種分子と複合体化した、PD-1に特異的に結合する単離抗体又はその抗原結合断片を含む、免疫複合体も提供する。
本発明はまた、本明細書にて開示した、PD-1に特異的に結合する抗体、又はその抗原結合断片を含むキットも提供する。
配列番号8のVH及び配列番号14のVL、
配列番号9のVH及び配列番号15のVL、
配列番号9のVH及び配列番号16のVL、
配列番号10のVH及び配列番号16のVL、
配列番号140のVH及び配列番号16のVL、
配列番号141のVH及び配列番号16のVL、
配列番号142のVH及び配列番号16のVL、
配列番号10のVH及び配列番号143のVL、
配列番号10のVH及び配列番号144のVL、
配列番号140のVH及び配列番号143のVL、
配列番号141のVH及び配列番号143のVL、
配列番号142のVH及び配列番号143のVL、
配列番号140のVH及び配列番号144のVL、
配列番号141のVH及び配列番号144のVL、
配列番号142のVH及び配列番号144のVL、
配列番号44のVH及び配列番号60のVL、
配列番号45のVH及び配列番号61のVL、
配列番号45のVH及び配列番号62のVL、
配列番号46のVH及び配列番号61のVL、
配列番号47のVH及び配列番号61のVL、
配列番号48のVH及び配列番号61のVL、
配列番号49のVH及び配列番号61のVL、
配列番号50のVH及び配列番号61のVL、
配列番号51のVH及び配列番号61のVL、
配列番号94のVH及び配列番号98のVL、
配列番号95のVH及び配列番号99のVL、若しくは
配列番号95のVH及び配列番号100のVL、
を含む、PD-1に特異的に結合する抗体、又はその抗原結合断片を含む。
本発明はまた、サンプルにおける、PD-1を検出する方法であって、当該サンプルを入手することと、当該サンプルを、本明細書において提供する、PD-1に特異的に結合する抗体、又はその抗原結合断片と接触させることと、当該サンプルにおいてPD-1に結合した抗体を検出することと、を含む、方法も提供する。
本明細書において提供する、PD-1に特異的に結合する抗体、又はその抗原結合断片は、様々な技術を用いて生成することができる。例えば、Kohler及びMilsteinのハイブリドーマ法を使用して、モノクローナル抗体を生成することができる。ハイブリドーマ法において、マウス又は他の宿主動物(例えばハムスター、ラット、若しくはニワトリ)を、PD-1の細胞外領域などのヒト及び/又はカニクイザルPD-1抗原で免疫付与し、続いて、標準的な方法を用いて、骨髄腫細胞で免疫付与した動物の脾臓細胞を融合させて、ハイブリドーマ細胞を形成する。1つの不死化ハイブリドーマ細胞から生じるコロニーを、所望の特性(例えば、結合の特異性、交差反応性又はその欠如、抗原への親和性、及びアゴニスト活性などの機能性)を有する抗体の産生のためにスクリーニングしてよい。
アゴニスト抗体
本明細書において提供するアゴニスト抗体により誘発される、典型的な生物活性は、抗原特異的CD4+又はCD8+ T細胞の阻害(例えば抑制)である。様々な読み取りを使用して、本明細書において提供する抗体のアゴニズム、例えば抗原特異的CD4+又はCD8+ T細胞による、インターフェロン-γ(IFN-γ)、IL-17、IL-2、IL-6、IL-22、IL-23、又はGM-CSFの、増殖の減少又は産生の減少を評価することができる。例示的なアッセイにおいて、破傷風トキソイド又はCMVなどの、同種異系樹状細胞又は特異的抗原により刺激される通常のドナーのT細胞における、抗体の効果を使用する。この設定において、抗体治療を用いたT細胞機能の変化は、T細胞の活性化の上清サイトカインレベル又はマーカーを測定することにより、検出可能である。例示的なアッセイにおいて、CMV抗原に対して反応性であると測定されたPBMCを、抗原特異的CD4+又はCD8+ T細胞の源として使用する。1.5×106cells/mL、又は2×106cells/mLのCMV反応性PBMCを培養皿に配置し、0.1~0.2μg/mLのCMVペプチドを、培養液に添加する。CMVペプチドは例えば、JPT Technologiesから購入することができる。試験抗体を、10μg/mLの一回用量で添加し、6日間プレートをインキュベートし、6時間、1μCi/ウェルのメチル-3H-チミジン(PerkinElmer)を添加して細胞増殖を評価し、各サンプルの放射能を測定する。あるいは、細胞によるサイトカイン産生を、ELISA又は既知の多重アッセイを用いて測定する。
本明細書において提供する本発明の抗体(例えば、PD-1に特異的に結合するアゴニスト抗体)は、リガンドを遮断する、又は遮断しないものであってよい。本明細書において提供するアゴニスト抗体の能力を、リガンド、例えばPD-L1若しくはPD-L2、又は両方を遮断する能力について、細胞クラスター化アッセイなどの競合アッセイを用いて評価することができる。
ヒト、又はカニクイザルPD-1などの非ヒトに対する、抗体の親和性を、任意の好適な方法を使用して実験により測定することができる。このような方法では、ProteOn XPR36、Biacore3000、若しくはKinExA装置、ELISA、又は当業者に公知の競合的結合アッセイを利用することができる。特定の抗体/PD-1相互作用について測定される親和性は、異なる条件下(例えば、浸透圧、pH)で測定した場合には異なり得る。したがって、親和性及びその他の結合パラメータ(例えば、KD、Kon、Koff)の測定は、典型的には、標準的な条件及び実施例1に記載される緩衝液などの標準化緩衝液を用いて行われる。例えばBiacore 3000又はProteOnを用いた親和性測定での内部誤差(標準偏差(SD)として測定されるもの)は通常、典型的な検出範囲内で測定した場合、5~33%の範囲内であり得ることが当業者には分かるであろう。したがって、KDとの関係における用語「約」は、アッセイにおける一般的な標準偏差を反映する。例えば、KDが1×10-9Mの場合の典型的なSDは、±0.33×10-9M以下である。
特定のVH及びVL配列を含む、本発明の抗体(例えば、リファレンス抗体)との、PD-1への結合の競合を、Octet Red384プラットフォーム(Forte Bio)にてインビトロでアッセイすることができる。ヒスチジンタグを付けたPD1をHISセンサーに装入し、センサーを20μg/mLのリファレンス抗-PD1抗体に暴露し、続いて等濃度の試験抗-PD1抗体に暴露する。飽和後の試験抗体のリファレンス抗体との更なる結合は、2つの抗体がPD-1に同時に結合することを示しており、このことは、リファレンス及び試験抗体が、PD-1への結合に関して競合しないことを示している。あるいは、試験抗体の更なる結合が存在しないことは、2つの抗体が、PD-1への結合に関して競合することを示す。
本発明の抗体が結合するPD-1エピトープは、例えば、水素/重水素交換(H/D交換)を使用するか、又はPD-1と複合対化した抗体の結晶構造を分析することによって解明され得る。H/D交換により、変性度合いが少なくとも5%の差である抗体により保護されたPD-1アミノ酸残基の、約70%又はそれ以上が2つの抗体間で同一であるとき、あるいは、抗体とPD-1の複合体の結晶構造において、抗体に結合していると判定されたPD-1表面露出アミノ酸残基の、70%又はそれ以上が、2つの抗体間で同一であるとき、2つのPD-1抗体が「PD-1の同一のエピトープに結合する」。抗体及びPD-1の複合体の結晶構造において、エピトープ残基は、抗体CDR残基のうちのいずれかから4Å以下の距離内に位置するPD-1残基である。
本発明はまた、本発明の抗体のいずれかをコードする単離ポリヌクレオチドも提供する。
当該抗体のVHをコードしている第1のポリヌクレオチド及び当該抗体のVLをコードしている第2のポリヌクレオチドを発現ベクターに組み込むことと、
宿主細胞を当該発現ベクターで形質転換することと、
当該VL及び当該VHが発現し、抗体を形成する条件下で、培養培地中で当該宿主細胞を培養することと、
当該宿主細胞又は当該培養培地から抗体を回収することと、
を含む、方法もまた提供する。
本発明はまた、本発明の抗体又はその抗原結合断片、及び医薬的に許容される担体を含む、医薬組成物も提供する。治療用途では、本発明の抗体は、医薬的に許容される担体中に活性成分として有効量の抗体を含有する医薬組成物として調製することができる。「担体」は、本発明の抗体と一緒に投与される希釈剤、補助剤、賦形剤、又はビヒクルを指す。このようなビヒクルは、水、及び石油、動物、植物、又は合成物由来のものを含む油、例えば、落花生油、大豆油、鉱油、ゴマ油などの液体であってよい。例えば、0.4%生理食塩水及び0.3%グリシンを用いてよい。これらの溶液は滅菌され、一般には粒子状物質を含まない。これらは、通常の周知の滅菌技術(例えば、濾過)によって滅菌することができる。組成物は、生理学的条件に近づけるために必要とされる医薬的に許容される補助物質、例えば、pH調整剤及び緩衝剤、安定化剤、増粘剤、潤滑剤及び着色剤などを含有し得る。このような医薬製剤中の本発明の抗体又はその抗原結合断片の濃度は、約0.5重量%未満から、通常は少なくとも約1重量%まで、最大で15又は20重量%まで変動し得、また、選択される具体的な投与方法に従って、必要とされる用量、流体体積、粘度などに主に基づいて選択され得る。好適なビヒクル、及び他のヒトタンパク質、例えばヒト血清アルブミンを含む製剤は、例えば、Remington:The Science and Practice of Pharmacy,21st Edition,Troy,D.B.ed.,Lipincott Williams and Wilkins,Philadelphia,PA 2006,Part 5,Pharmaceutical Manufacturing pp691-1092に記載され、特にpp.958-989を参照されたい。
本発明の抗体又はその抗原結合断片は、インビトロ及びインビボで、診断上、並びに治療及び予防上の有用性を有する。例えば、本発明の抗体又はその抗原結合断片を、インビトロ若しくはエクスビボで培養液中の細胞に、又は対象に投与して、免疫不全、又はPD-1を発現するT細胞の活性の減衰、及び/又は免疫応答の下方制御が所望される任意の状態といった、様々な病気を治療、予防、及び/又は診断することができる。
本明細書において提供する抗体は、第2の治療薬と組み合わせて投与することができる。
表面プラズモン共鳴(SPR)を用いる親和性測定
親和性測定は、ProteOn XPR36システム(BioRad)を用いて実施した。アミンカップリング化学反応についての製造元の使用説明書を使用し、抗ヒトIgG Fc(Jacksonカタログ番号109-005-098)を、GLCチップ(BioRad,カタログ番号176-5011)の加工アルギン酸ポリマー層にカップリングさせて、バイオセンサー表面を調製した。約5000RU(応答単位)のmAbを固定化した。ランニング緩衝液(DPBS+0.01% P20+100μg/mL BSA)中にて25℃で速度実験を実施した。速度実験を行うために、200RUのmAbを捕捉した後、1.563nM~400nMの範囲の濃度(4倍連続希釈)にて、検体(ヒト及びカニクイザルPD-1)を注入した。50μL/分で3分間会合段階をモニタした後、10又は15分間、緩衝液を流した(解離段階)。100μL/分で100mM H3PO4(Sigma、カタログ番号7961)を18秒間ずつ2回流してチップ表面を再生した。
CMV特異的リコール応答を利用するアッセイを用いて、CMV反応性ドナーのPBMCをCMVペプチド混合物(JPT Technologies)で処理する際の、細胞増殖の阻害により測定される、生成抗体がT細胞の活性化を阻害する能力を評価した。
PD-1(PD-1-HEK細胞)、又はPD-1のリガンドであるPD-L1(PD-L1-HEK細胞)、若しくはPD-L2(PD-L2-HEK細胞)のいずれかを過剰発現する、ヒト胎児腎臓(HEK)細胞の1:1混合物を利用するアッセイを用いて、フローサイトメトリーにより定量化される細胞クラスター化の阻害により測定される、生成抗体が細胞ベースの文脈における、受容体:リガンドの相互作用を評価した。
バイオ層干渉法に基づくOctet Red384プラットフォーム(Forte Bio)上で、競合結合アッセイによる抗体のエピトープビニングを実施した。本技術では、時間と共にバイオセンサチップの光学密度が増加する、結合した抗体による波長シフトとして、初期抗体のPD-1被覆バイオセンサーへの結合を測定する。簡潔に述べると、ヒスチジンタグを付けたPD-1抗原をHISセンサーにロードした。次に、センサーを20μg/mLの一次抗PD-1抗体に暴露し、続いて、等濃度の二次抗PD-1抗体に暴露した。ForteBio Data Analysis Softwareを用いてデータを処理した。一次抗体による飽和後の、二次抗体による追加の結合は、必然的に固有の非重複エピトープを有する、2つの抗体の同時結合を示す。あるいは、追加の結合が存在しないことは、2つの抗体が、PD-1抗原への結合を競合することを示す。
ヒトメモリーT細胞(標的細胞)の活性化:
ヒトメモリーT細胞(AllCells LLC)の凍結アリコートを、37℃の湯浴中で解凍し、40mLの培地(RPMI+10% FBS又は5%HuSAB+50μMβME(1:1000)+1% GlutaMax+10mM Hepes)に再懸濁した。細胞を室温で15分間、250gで遠心分離した。遠心分離後、上清を捨て、細胞を10mLの培地に再懸濁して、10分間250gにて遠心沈殿させた。遠心分離後、細胞を10mLのアッセイ培地に再懸濁し、計数した。細胞濃度を1.0×106cells/mLに調節し、10mLの細胞懸濁液を、抗CD3抗体で予め被覆した組織培養皿に移した(eBioscience、PBS中に5μg/mL、37℃にて1時間)。培地を、2μg/mLの抗CD28 Ab(eBioscience)、並びにIL-2、IL-15、及びIL-7サイトカインのカクテル(R&D Systems及びPeprotech)で、100ng/mLの濃度にて補充した。予備実験では、PD-1の発現が活性化後5日目にピークを迎えたことが示されたため、この時点をアッセイのために選択した。低量のPD-1を発現するため、改めて単離した残りのメモリーT細胞(CD3/CD28刺激により活性化されていない)を、対照として分析に含めた。
NK-92細胞を、直立して保管した組織培養フラスコ内で増殖させ、40mLの培地(Myelocult H5100(StemCell Technologies)、1×ピルビン酸ナトリウム/非必須アミノ酸/Pen Strep(Invitrogen)、4μMハイドロコルチゾン(StemCell Technologies)、100ng/mL rhIL-2(R&D Systems)に、0.5~1.0×106cells/mLの密度で保持した。凍結PBMC細胞(Hemacare)を実験の前日に解凍し、XVIVO-10培地(Lonza)、10% HI FBS(Invitrogen)、及び100ng/mL IL2(R&D Systems)に再懸濁した。細胞を室温で15分間、250gで遠心分離した。遠心分離後、上清を捨て、細胞を10mLの培地に再懸濁して、10分間250gにて遠心沈殿させた。遠心分離後、細胞を10mLの培地に再懸濁させて計数した。細胞濃度を1.0×106cells/mLに調節し、必要な細胞数をTCディッシュにプレーティングした。
ヒト汎T細胞(Biological Specialty、LSII 49301C)の凍結アリコートを37℃湯浴で解凍し、40mLの、予熱したRPMI 1640+Glutamax+25mM HEPES(Life Technologies、Cat# 72400-047)+10% FBS(Gibco、160000-36)に再懸濁した。細胞を250gにて5分間、室温で遠心分離した。遠心分離後、上清を捨て、細胞を10mL~20mLの培地に再懸濁して計数した。CDCアッセイの5~6日前に、ヒトT活性化因子CD3/CD28 Dynabeads(商標)(Life Technologies、Cat# 11132D)を用いて、ヒト汎T細胞(Biological Specialty、LSII 49301C)を活性化した。簡潔に述べると、75μLの予洗浄したダイナビーズを、6.0×106cells/フラスコのT細胞と混合し、10~20mLの培地内のT175に添加し、37℃/5% CO2のインキュベーター内で6日間インキュベートした。6日後、EasySep(商標)マグネット(STEMCELL Technologies、18000)を用いて、混合物からビーズを除去した。
(実験値-低対照)/(高対照-低対照)×100
高対照は、Triton-X細胞溶解対照ウェルの平均であり、低対照は、「培地のみ」のバックグラウンド対照ウェルの平均である。4パラメータロジスティック曲線適合モデル[log(アゴニスト)vs応答-可変勾配(4つのパラメータ)をGraphPad Prismにおいて、計算した細胞傷害性(%)に対するAb濃度のlog10に適用した。サンプルを二重に実行し、アッセイを2回実施した。
3匹のBalb/c、及び3匹のC3Hマウスを、Fc(huPD-1-Fc)、及び標準的な手順を用いて生成したハイブリドーマと複合体化した、ヒトPD-1(配列番号1)の細胞外ドメイン(ECD)で免疫付与した。組み換えPD-1(ECD)への結合に関して、ELISAによりハイブリドーマをスクリーニングした。陰性対照の平均の5倍を超えるELISA信号を与えるサンプルを、「当たり」として定義した。無関係なFc融合タンパク質に対して、及び、マウスPD-1への結合に関して、陽性クローンを交差スクリーニングした。単一細胞からクローニングしたハイブリドーマの上清を、ヒト及びカニクイザルPD-1タンパク質への結合について試験した。陰性対照の平均+3標準偏差を超える信号を、「当たり」として定義した。
PGWFLDSPDRPWNPPTFSPALLVVTEGDNATFTCSFSNTSESFVLNWYRMSPSNQTDKLAAFPEDRSQPGQDCRFRVTQLPNGRDFHMSVVRARRNDSGTYLCGAISLAPKAQIKESLRAELRVTERRAEVPTAHPSPSPRPAGQFQTLV
PGWFLDSPDRPWNPPTFSPALLVVTEGDNATFTCSFSNTSESFVLNWYRMSPSNQTDKLAAFPEDRSQPGQDCRFRVTQLPNGRDFHMSVVRARRNDSGTYLCGAISLAPKAQIKESLRAELRVTERRAEVPTAHPSPSPRPAGQFQTLVVGVVGGLLGSLVLLVWVLAVICSRAARGTIGARRTGQPLKEDPSAVPVFSVDYGELDFQWREKTPEPPVPCVPEQTEYATIVFPSGMGTSSPARRGSADGPRSAQPLRPEDGHCSWPL
PD1B505、PD1B506、及びPD1B512を含むいくつかの親抗体をヒト化した。ヒト化VH及びVLの最善の組み合わせを発見するために、1つ以上のヒト生殖細胞系重鎖及び軽鎖V領域の配列を、抗体のそれぞれについて選択した。ヒトJセグメント配列に対して、親Jセグメント配列を比較することにより、各親抗体のVL及びVHに対するヒトJセグメントを選択し、配列同一性を最大化した。各抗体の、全てのVH/VLヒト化対を作製し、抗原結合及びタンパク質発現に関して、粗上清としてマトリクス中で試験した。これらのデータに基づき、親マウス抗体に匹敵する、又はそれより改善されたPD-1結合を示す抗体を精製し、それらの有効性についてCMV-PBMCアッセイで試験した。
CAAGTGCAGCTGGTGCAGTCTGGCAGCGAGCTGAAAAAACCTGGCGCCTCCGTGAAGGTGTCCTGCAAGGCTAGCGGCTACACCTTTACCGACTACAGCATGCACTGGGTCCGACAGGCTCCAGGACAAGGCTTGGAATGGATGGGCTGGATCAACATCGAGACAGGCGAGCCCACATACGCCCAGGGCTTTACCGGCAGATTCGTGTTCAGCCTGGACACCTCTGTGTCCACCGCCTACCTGCAGATCAGCTCTCTGAAGGCCGAGGATACCGCCGTGTACTTCTGCGCCAGAGACTACTACGGCACCTACTTCTACGCCATGGATTACTGGGGCCAGGGCACCCTGGTTACCGTTTCTTCT
GAGATCGTGCTGACACAGTCTCCCGCCACACTGTCACTGTCTCCAGGCGAAAGAGCCACACTGAGCTGTACCGCCAGCAGCTCTGTGTCCAGCAGCTACCTGCACTGGTATCAGCAGAAGCCTGGACTGGCCCCTCGGCTGCTGATCTACAGCACAAGCAATCTGGCCAGCGGCATCCCCGATAGATTTTCCGGCTCTGGAAGCGGCACCGACTACACCCTGACAATCAGCAGACTGGAACCCGAGGACTTCGCCGTGTACTACTGCCACCAGTACCACAGAAGCCCTCTGACCTTTGGCCAGGGCACCAAGCTGGAAATCAAG
CAAGTGCAGCTGGTGCAGTCTGGCAGCGAGCTGAAAAAACCTGGCGCCTCCGTGAAGGTGTCCTGCAAGGCTAGCGGCTACACCTTTACCGACTACAGCATGCACTGGGTCCGACAGGCTCCAGGACAAGGCTTGGAATGGATGGGCTGGATCAACATCGAGACAGGCGAGCCCACATACGCCCAGGGCTTTACCGGCAGATTCGTGTTCAGCCTGGACACCTCTGTGTCCACCGCCTACCTGCAGATCAGCTCTCTGAAGGCCGAGGATACCGCCGTGTACTTCTGCGCCAGAGACTACTACGGCACCTACTTCTACGCCATGGATTACTGGGGCCAGGGCACCCTGGTTACCGTTTCTTCTGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACTACTTCCCCGAACCGGTGACGGTGTCGTGGAACTCAGGCGCCCTGACCAGCGGCGTGCACACCTTCCCGGCTGTCCTACAGTCCTCAGGACTCTACTCCCTCAGCAGCGTGGTGACCGTGCCCTCCAGCAGCTTGGGCACCCAGACCTACATCTGCAACGTGAATCACAAGCCCAGCAACACCAAGGTGGACAAGAAAGTTGAGCCCAAATCTTGTGACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTGGGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTCATGATCTCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAAGACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCATAATGCCAAGACAAAGCCGCGGGAGGAGCAGTACAACAGCACGTACCGTGTGGTCAGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTACAAGTGCAAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCCAAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGGGAGGAGATGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTCTCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAGAGCCTCTCCCTGTCTCCGGGTAAA
GAGATCGTGCTGACACAGTCTCCCGCCACACTGTCACTGTCTCCAGGCGAAAGAGCCACACTGAGCTGTACCGCCAGCAGCTCTGTGTCCAGCAGCTACCTGCACTGGTATCAGCAGAAGCCTGGACTGGCCCCTCGGCTGCTGATCTACAGCACAAGCAATCTGGCCAGCGGCATCCCCGATAGATTTTCCGGCTCTGGAAGCGGCACCGACTACACCCTGACAATCAGCAGACTGGAACCCGAGGACTTCGCCGTGTACTACTGCCACCAGTACCACAGAAGCCCTCTGACCTTTGGCCAGGGCACCAAGCTGGAAATCAAGCGTACGGTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGCAAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAAGCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGCTCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGT
CAAGTGCAGCTGGTGCAATCTGGCGCCGAAGTGAAAAAGCCTGGCGCCTCTGTGAAGGTGTCCTGCAAGGCCAGCGGCTACACCTTTACCACCTACTGGATGCACTGGGTCCGACAGGCTCCAGGACAAGGCTTGGAGTGGATGGGCGAGATCAACCCCAATGAAGGCGGCATCAACTACGCCCAGAAATTCCAGGGCAGAGTGACCCTGACCGTGGACAAGAGCATCAGCACCGCCTACATGGAACTGAGCCGGCTGAGATCCGATGACACCGCCGTGTACTACTGCACCATCGACTACTACGACTACGGCGGCTATTGGGGCCAGGGCACACTGGTTACAGTGTCCTCT
GACATCCAGATGACACAGAGCCCTAGCAGCCTGTCTGCCTCTGTGGGCGATAGAGTGACCATCACATGCAAGGCCAGCCAGAACGTGGGCACCAATGTGGCCTGGTATCAGCAGAAGCCTGAGAAGGCCCCTAAGAGCCTGATCTACAGCGCCAGCTACAGATACAGCGGCGTGCCAAGCAGATTTTCTGGAAGCGGCAGCGGCACCGACTTCACCCTGACAATTAGTAGCCTGCAGCCTGAGGACTTCGCCACCTACTACTGCCAGCAGTACAACATCTACCCCTACACCTTCGGCCAGGGCACCAAGCTGGAAATCAAG
CAAGTGCAGCTGGTGCAATCTGGCGCCGAAGTGAAAAAGCCTGGCGCCTCTGTGAAGGTGTCCTGCAAGGCCAGCGGCTACACCTTTACCACCTACTGGATGCACTGGGTCCGACAGGCTCCAGGACAAGGCTTGGAGTGGATGGGCGAGATCAACCCCAATGAAGGCGGCATCAACTACGCCCAGAAATTCCAGGGCAGAGTGACCCTGACCGTGGACAAGAGCATCAGCACCGCCTACATGGAACTGAGCCGGCTGAGATCCGATGACACCGCCGTGTACTACTGCACCATCGACTACTACGACTACGGCGGCTATTGGGGCCAGGGCACACTGGTTACAGTGTCCTCTGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACTACTTCCCCGAACCGGTGACGGTGTCGTGGAACTCAGGCGCCCTGACCAGCGGCGTGCACACCTTCCCGGCTGTCCTACAGTCCTCAGGACTCTACTCCCTCAGCAGCGTGGTGACCGTGCCCTCCAGCAGCTTGGGCACCCAGACCTACATCTGCAACGTGAATCACAAGCCCAGCAACACCAAGGTGGACAAGAAAGTTGAGCCCAAATCTTGTGACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTGGGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTCATGATCTCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAAGACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCATAATGCCAAGACAAAGCCGCGGGAGGAGCAGTACAACAGCACGTACCGTGTGGTCAGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTACAAGTGCAAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCCAAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGGGAGGAGATGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTCTCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAGAGCCTCTCCCTGTCTCCGGGTAAA
GACATCCAGATGACACAGAGCCCTAGCAGCCTGTCTGCCTCTGTGGGCGATAGAGTGACCATCACATGCAAGGCCAGCCAGAACGTGGGCACCAATGTGGCCTGGTATCAGCAGAAGCCTGAGAAGGCCCCTAAGAGCCTGATCTACAGCGCCAGCTACAGATACAGCGGCGTGCCAAGCAGATTTTCTGGAAGCGGCAGCGGCACCGACTTCACCCTGACAATTAGTAGCCTGCAGCCTGAGGACTTCGCCACCTACTACTGCCAGCAGTACAACATCTACCCCTACACCTTCGGCCAGGGCACCAAGCTGGAAATCAAGCGTACGGTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGCAAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAAGCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGCTCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGT
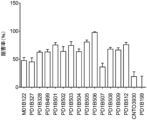
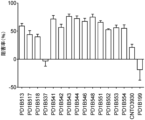
選択ヒト化抗体を、CMV特異的リコールアッセイ(実施例1に記載したCMV-PBMCアッセイ)において、活性化T細胞を阻害する能力について特性決定した。親抗体PD1B505及びPD1B506は、表16に示すいくつかの個別実験において、3つの異なるドナーにまたがり評価された、活性化T細胞の頑健な阻害を示し、これらの結果は、10μg/mLのmAbにおける、T細胞増殖の阻害率(%)として示される。図5Aは、アイソタイプコントロール(ヒトIgG1)(-9.5%±28.8%)と比較したときの、PD1B505(57.8%±9.5)、及びPD1B506(77.0%±7.8)に対する、平均阻害率及びSTDEVを示す。ヒト化抗体PD1B743、PD1B750、及びPD1B756ヒト化抗体もまた、10μg/mLにて、阻害率として表17に示すに示すように、T細胞の活性化を阻害した。図5Bは、アイソタイプコントロール(ヒトIgG1)(3.5%±25.6%)と比較したときの、PD1B743(58.0%±11.3%)、PD1B750(65.9%±13.2%)、PD1B756(36.7%±15.5%)に対する、平均阻害率及びSTDEVを示す。25%を超えるSTDEVを示すアッセイを、分析から除外した。表18に示すに示すように、改変抗体PD1B878及びPD1B849も同様に、活性化T細胞を阻害した。図5Cは、アイソタイプコントロール(ヒトIgG1)(4.1%±28.7%)と比較したときの、PD1B878(78.3%±18.1%)、及びPD1B849(69.0%±4.0%)に対する、平均阻害率及びSTDEVを示す。
親及びヒト化抗体の、PD-1への親和性を、実施例1に記載したSPRを用いて測定した。
実施例1に記載した手順を用いて、PD-1又はPD-1リガンド(PD-L1若しくはPD-L2)のいずれかを過剰発現する細胞のクラスター化における、抗体の効果を評価することにより、リガンド遮断を評価した。記録したダブルポジティブイベントの低い割合(%)は、試験mAbが、PD-1の試験リガンドへの結合を遮断したことを示す。
実施例1に記載する手順に従い、キメラ抗体を用いる初期マトリクスアッセイで、5つの異なるエピトープビンを識別した。ビン4及び5は、あらゆる他のビンと交差競合しなかった。ビン1、2、及び3は、部分的に重複した。ビン1はビン2及び3と競合し、ビン2及び3はビン1と競合した。ビン1、2、3、及び4は、PD-L1のPD-1への結合を遮断しなかったが、ビン5はPD-L1/PD-1相互作用を遮断した。図7は、異なるエピトープビン、及び各ビン内にある抗体を示す。
QVQLQQSGAELVKPGASVKLSCKASGYTFTSYDINWVRQRPEQGLEWIGWIFPGDGSTKYNEKFKGKATLTTDKSSSTAYMQFSRLTSEDSAVYFCARGGMRQLGRFVYWGQGTTLTVSS
DIVLTQSPSSLSASLGERVSLTCRASQEISGYLSWLQQKPDGTIKRLIYAASTLDSGVPKRFSGSRSGSDYSLTISSLESEDFADYYCLQYASNPYTFGGGTKLEIK
EVQLQQSGAELVKPGASVKLSCTASGFNVKDTYFHWVKQRPDQGLEWIGRIVSANGDTKYAPKLQDKATITTDTSSNTAYLQLSRLTSEDTAVYYCVLIYYGFEEGDFWGQGTTLTVSS
DIVMTQSPSSLSASLGDTITITCHASQNINVWLSWYQQKPGNVPKLLIYKASNLHTGVPSRFSGSGSGTGFTLNISSLQPEDIATYYCQQGQSFPLTFGAGTKLELK
PD1B878の結合親和性を改善するために、CDRスキャンを、重鎖及び軽鎖の両方で行った。6つのCDR(HCDR1、HCDR2、HCDR3、LCDR1、LCDR2、及びLCDR3)全ての各位置を多様化するために、非コンビナトリアルライブラリを設計した。簡潔に述べると、制限酵素部位に軽微な修正を加えた以外、国際公開第2009/085462号、Shi et al.,J Mol Biol 397:385-396(2010)、及びTornetta et al.J Immunol Methods 360:39-46(2010)に記載のとおり、FabライブラリをpIXファージFabディスプレイシステムにおいて構築した。国際公開第2009/085462号、及びShi et al,J Mol Biol 397:385-396(2010)に記載されているような、当該技術分野において公知のパニングスキームに従い、これらのライブラリを、ビオチン化ヒトPD-1/PDCD1(Acro Biosystems.Cat# PD1-H82E4)に対してパニングした。ヘルパーファージ感染によってファージを作製した。ビーズ/抗原/ファージ複合体を形成するためにビーズを添加することによって、結合剤を回収した。最終洗浄の後、指数関数的に成長しているTG-1大腸菌細胞の感染により、ファージをレスキューした。
QVQLVQSGSELKKPGASVKVSCKASGYTFTDYSMHWVRQAPGQGLEWMGWINIETGYPTYAQGFTGRFVFSLDTSVSTAYLQISSLKAEDTAVYFCARDYYGTYFYAMDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
QVQLVQSGSELKKPGASVKVSCKASGYTFTDYSMHWVRQAPGQGLEWMGWINIETGHPTYAQGFTGRFVFSLDTSVSTAYLQISSLKAEDTAVYFCARDYYGTYFYAMDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
QVQLVQSGSELKKPGASVKVSCKASGYTFTDYSMHWVRQAPGQGLEWMGWINIETGWPTYAQGFTGRFVFSLDTSVSTAYLQISSLKAEDTAVYFCARDYYGTYFYAMDYWGQGTLVTVSSASTKGPSVFPLAPSSKSTSGGTAALGCLVKDYFPEPVTVSWNSGALTSGVHTFPAVLQSSGLYSLSSVVTVPSSSLGTQTYICNVNHKPSNTKVDKKVEPKSCDKTHTCPPCPAPELLGGPSVFLFPPKPKDTLMISRTPEVTCVVVDVSHEDPEVKFNWYVDGVEVHNAKTKPREEQYNSTYRVVSVLTVLHQDWLNGKEYKCKVSNKALPAPIEKTISKAKGQPREPQVYTLPPSREEMTKNQVSLTCLVKGFYPSDIAVEWESNGQPENNYKTTPPVLDSDGSFFLYSKLTVDKSRWQQGNVFSCSVMHEALHNHYTQKSLSLSPGK
EIVLTQSPATLSLSPGERATLSCTASSSFSSSYLHWYQQKPGLAPRLLIYSTSNLASGIPDRFSGSGSGTDYTLTISRLEPEDFAVYYCHQYHRSPLTFGQGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
EIVLTQSPATLSLSPGERATLSCTASSSVPSSYLHWYQQKPGLAPRLLIYSTSNLASGIPDRFSGSGSGTDYTLTISRLEPEDFAVYYCHQYHRSPLTFGQGTKLEIKRTVAAPSVFIFPPSDEQLKSGTASVVCLLNNFYPREAKVQWKVDNALQSGNSQESVTEQDSKDSTYSLSSTLTLSKADYEKHKVYACEVTHQGLSSPVTKSFNRGEC
CAGGTGCAGCTGGTGCAGTCTGGAAGCGAACTGAAGAAACCTGGAGCCTCTGTGAAAGTGTCTTGTAAGGCCAGCGGCTACACCTTCACCGACTACAGCATGCACTGGGTGCGGCAGGCCCCTGGACAGGGCCTGGAATGGATGGGCTGGATCAACATCGAGACCGGCTATCCCACCTACGCCCAGGGCTTTACCGGACGGTTCGTGTTCAGCCTGGATACATCTGTGTCTACAGCCTATCTGCAGATCAGCTCTCTGAAGGCCGAAGATACAGCCGTGTACTTCTGCGCCCGGGACTACTACGGCACCTACTTCTACGCCATGGACTACTGGGGCCAGGGAACACTGGTGACAGTGTCTTCT
CAGGTGCAGCTGGTGCAGTCTGGAAGCGAACTGAAGAAACCTGGAGCCTCTGTGAAAGTGTCTTGTAAGGCCAGCGGCTACACCTTCACCGACTACAGCATGCACTGGGTGCGGCAGGCCCCTGGACAGGGCCTGGAATGGATGGGCTGGATCAACATCGAGACCGGCCATCCCACCTACGCCCAGGGCTTTACCGGACGGTTCGTGTTCAGCCTGGATACATCTGTGTCTACAGCCTATCTGCAGATCAGCTCTCTGAAGGCCGAAGATACAGCCGTGTACTTCTGCGCCCGGGACTACTACGGCACCTACTTCTACGCCATGGACTACTGGGGCCAGGGAACACTGGTGACAGTGTCTTCT
CAGGTGCAGCTGGTGCAGTCTGGAAGCGAACTGAAGAAACCTGGAGCCTCTGTGAAAGTGTCTTGTAAGGCCAGCGGCTACACCTTCACCGACTACAGCATGCACTGGGTGCGGCAGGCCCCTGGACAGGGCCTGGAATGGATGGGCTGGATCAACATCGAGACCGGCTGGCCCACCTACGCCCAGGGCTTTACCGGACGGTTCGTGTTCAGCCTGGATACATCTGTGTCTACAGCCTATCTGCAGATCAGCTCTCTGAAGGCCGAAGATACAGCCGTGTACTTCTGCGCCCGGGACTACTACGGCACCTACTTCTACGCCATGGACTACTGGGGCCAGGGAACACTGGTGACAGTGTCTTCT
GAGATCGTGCTGACACAGTCTCCTGCCACACTGTCTCTGTCTCCTGGAGAACGGGCCACACTGAGCTGCACCGCCAGCAGCAGCTTCAGCAGCAGCTACCTGCACTGGTACCAGCAGAAACCTGGACTGGCCCCTCGGCTGCTGATCTACAGCACCAGCAACCTGGCCAGCGGCATCCCTGATCGGTTTTCTGGCAGCGGATCTGGCACAGATTACACACTGACCATCAGCCGGCTGGAACCTGAGGATTTTGCCGTGTACTACTGCCACCAGTACCACCGGAGCCCCCTGACCTTCGGCCAGGGAACAAAGCTGGAAATCAAG
GAGATCGTGCTGACACAGTCTCCTGCCACACTGTCTCTGTCTCCTGGAGAACGGGCCACACTGAGCTGCACCGCCAGCAGCAGCGTGCCAAGCAGCTACCTGCACTGGTACCAGCAGAAACCTGGACTGGCCCCTCGGCTGCTGATCTACAGCACCAGCAACCTGGCCAGCGGCATCCCTGATCGGTTTTCTGGCAGCGGATCTGGCACAGATTACACACTGACCATCAGCCGGCTGGAACCTGAGGATTTTGCCGTGTACTACTGCCACCAGTACCACCGGAGCCCCCTGACCTTCGGCCAGGGAACAAAGCTGGAAATCAAG
TCTGATAAGAGTCAGAGGTAACTCCCGTTGCGGTGCTGTTAACGGTGGAGGGCAGTGTAGTCTGAGCAGTACTCGTTGCTGCCGCGCGCGCCACCAGACATAATAGCTGACAGACTAACAGACTGTTCCTTTCCATGGGTCTTTTCTGCAGTCACCGTCCTTAGATCCACTAGTCCAGTGTGGTGAAGCTTGCCGCCACCATGGCTTGGGTGTGGACCTTGCTATTCCTGATGGCAGCTGCCCAAAGTATACAGGCCCAGGTGCAGCTGGTGCAGTCTGGAAGCGAACTGAAGAAACCTGGAGCCTCTGTGAAAGTGTCTTGTAAGGCCAGCGGCTACACCTTCACCGACTACAGCATGCACTGGGTGCGGCAGGCCCCTGGACAGGGCCTGGAATGGATGGGCTGGATCAACATCGAGACCGGCTATCCCACCTACGCCCAGGGCTTTACCGGACGGTTCGTGTTCAGCCTGGATACATCTGTGTCTACAGCCTATCTGCAGATCAGCTCTCTGAAGGCCGAAGATACAGCCGTGTACTTCTGCGCCCGGGACTACTACGGCACCTACTTCTACGCCATGGACTACTGGGGCCAGGGAACACTGGTGACAGTGTCTTCTGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACTACTTCCCCGAACCGGTGACGGTGTCGTGGAACTCAGGCGCCCTGACCAGCGGCGTGCACACCTTCCCGGCTGTCCTACAGTCCTCAGGACTCTACTCCCTCAGCAGCGTGGTGACCGTGCCCTCCAGCAGCTTGGGCACCCAGACCTACATCTGCAACGTGAATCACAAGCCCAGCAACACCAAGGTGGACAAGAAAGTTGAGCCCAAATCTTGTGACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTGGGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTCATGATCTCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAAGACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCATAATGCCAAGACAAAGCCGCGGGAGGAGCAGTACAACAGCACGTACCGTGTGGTCAGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTACAAGTGCAAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCCAAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGGGAGGAGATGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTCTCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAGAGCCTCTCCCTGTCTCCGGGTAAATGATAGTTCGAATTCCTAGAAGACATGATAAGATACATTGATGAGTTTGGACAAACCACAACTAGAATGCAGTGAAAAAAATGCTTTATTTGTGAAATTTGTGATGCTATTGCTTTATTTGTAACCATTATAAGCTGCAATAAACAAGTTAACAACAACAATTGCATTCATTTTATGTTTCAGGTTCAGGGGGAGGTGTGGGA
TCTGATAAGAGTCAGAGGTAACTCCCGTTGCGGTGCTGTTAACGGTGGAGGGCAGTGTAGTCTGAGCAGTACTCGTTGCTGCCGCGCGCGCCACCAGACATAATAGCTGACAGACTAACAGACTGTTCCTTTCCATGGGTCTTTTCTGCAGTCACCGTCCTTAGATCCACTAGTCCAGTGTGGTGAAGCTTGCCGCCACCATGGCTTGGGTGTGGACCTTGCTATTCCTGATGGCAGCTGCCCAAAGTATACAGGCCCAGGTGCAGCTGGTGCAGTCTGGAAGCGAACTGAAGAAACCTGGAGCCTCTGTGAAAGTGTCTTGTAAGGCCAGCGGCTACACCTTCACCGACTACAGCATGCACTGGGTGCGGCAGGCCCCTGGACAGGGCCTGGAATGGATGGGCTGGATCAACATCGAGACCGGCCATCCCACCTACGCCCAGGGCTTTACCGGACGGTTCGTGTTCAGCCTGGATACATCTGTGTCTACAGCCTATCTGCAGATCAGCTCTCTGAAGGCCGAAGATACAGCCGTGTACTTCTGCGCCCGGGACTACTACGGCACCTACTTCTACGCCATGGACTACTGGGGCCAGGGAACACTGGTGACAGTGTCTTCTGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACTACTTCCCCGAACCGGTGACGGTGTCGTGGAACTCAGGCGCCCTGACCAGCGGCGTGCACACCTTCCCGGCTGTCCTACAGTCCTCAGGACTCTACTCCCTCAGCAGCGTGGTGACCGTGCCCTCCAGCAGCTTGGGCACCCAGACCTACATCTGCAACGTGAATCACAAGCCCAGCAACACCAAGGTGGACAAGAAAGTTGAGCCCAAATCTTGTGACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTGGGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTCATGATCTCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAAGACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCATAATGCCAAGACAAAGCCGCGGGAGGAGCAGTACAACAGCACGTACCGTGTGGTCAGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTACAAGTGCAAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCCAAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGGGAGGAGATGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTCTCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAGAGCCTCTCCCTGTCTCCGGGTAAATGATAGTTCGAATTCCTAGAAGACATGATAAGATACATTGATGAGTTTGGACAAACCACAACTAGAATGCAGTGAAAAAAATGCTTTATTTGTGAAATTTGTGATGCTATTGCTTTATTTGTAACCATTATAAGCTGCAATAAACAAGTTAACAACAACAATTGCATTCATTTTATGTTTCAGGTTCAGGGGGAGGTGTGGGA
TCTGATAAGAGTCAGAGGTAACTCCCGTTGCGGTGCTGTTAACGGTGGAGGGCAGTGTAGTCTGAGCAGTACTCGTTGCTGCCGCGCGCGCCACCAGACATAATAGCTGACAGACTAACAGACTGTTCCTTTCCATGGGTCTTTTCTGCAGTCACCGTCCTTAGATCCACTAGTCCAGTGTGGTGAAGCTTGCCGCCACCATGGCTTGGGTGTGGACCTTGCTATTCCTGATGGCAGCTGCCCAAAGTATACAGGCCCAGGTGCAGCTGGTGCAGTCTGGAAGCGAACTGAAGAAACCTGGAGCCTCTGTGAAAGTGTCTTGTAAGGCCAGCGGCTACACCTTCACCGACTACAGCATGCACTGGGTGCGGCAGGCCCCTGGACAGGGCCTGGAATGGATGGGCTGGATCAACATCGAGACCGGCTGGCCCACCTACGCCCAGGGCTTTACCGGACGGTTCGTGTTCAGCCTGGATACATCTGTGTCTACAGCCTATCTGCAGATCAGCTCTCTGAAGGCCGAAGATACAGCCGTGTACTTCTGCGCCCGGGACTACTACGGCACCTACTTCTACGCCATGGACTACTGGGGCCAGGGAACACTGGTGACAGTGTCTTCTGCCTCCACCAAGGGCCCATCGGTCTTCCCCCTGGCACCCTCCTCCAAGAGCACCTCTGGGGGCACAGCGGCCCTGGGCTGCCTGGTCAAGGACTACTTCCCCGAACCGGTGACGGTGTCGTGGAACTCAGGCGCCCTGACCAGCGGCGTGCACACCTTCCCGGCTGTCCTACAGTCCTCAGGACTCTACTCCCTCAGCAGCGTGGTGACCGTGCCCTCCAGCAGCTTGGGCACCCAGACCTACATCTGCAACGTGAATCACAAGCCCAGCAACACCAAGGTGGACAAGAAAGTTGAGCCCAAATCTTGTGACAAAACTCACACATGCCCACCGTGCCCAGCACCTGAACTCCTGGGGGGACCGTCAGTCTTCCTCTTCCCCCCAAAACCCAAGGACACCCTCATGATCTCCCGGACCCCTGAGGTCACATGCGTGGTGGTGGACGTGAGCCACGAAGACCCTGAGGTCAAGTTCAACTGGTACGTGGACGGCGTGGAGGTGCATAATGCCAAGACAAAGCCGCGGGAGGAGCAGTACAACAGCACGTACCGTGTGGTCAGCGTCCTCACCGTCCTGCACCAGGACTGGCTGAATGGCAAGGAGTACAAGTGCAAGGTCTCCAACAAAGCCCTCCCAGCCCCCATCGAGAAAACCATCTCCAAAGCCAAAGGGCAGCCCCGAGAACCACAGGTGTACACCCTGCCCCCATCCCGGGAGGAGATGACCAAGAACCAGGTCAGCCTGACCTGCCTGGTCAAAGGCTTCTATCCCAGCGACATCGCCGTGGAGTGGGAGAGCAATGGGCAGCCGGAGAACAACTACAAGACCACGCCTCCCGTGCTGGACTCCGACGGCTCCTTCTTCCTCTACAGCAAGCTCACCGTGGACAAGAGCAGGTGGCAGCAGGGGAACGTCTTCTCATGCTCCGTGATGCATGAGGCTCTGCACAACCACTACACGCAGAAGAGCCTCTCCCTGTCTCCGGGTAAATGATAGTTCGAATTCCTAGAAGACATGATAAGATACATTGATGAGTTTGGACAAACCACAACTAGAATGCAGTGAAAAAAATGCTTTATTTGTGAAATTTGTGATGCTATTGCTTTATTTGTAACCATTATAAGCTGCAATAAACAAGTTAACAACAACAATTGCATTCATTTTATGTTTCAGGTTCAGGGGGAGGTGTGGGA
TCTGATAAGAGTCAGAGGTAACTCCCGTTGCGGTGCTGTTAACGGTGGAGGGCAGTGTAGTCTGAGCAGTACTCGTTGCTGCCGCGCGCGCCACCAGACATAATAGCTGACAGACTAACAGACTGTTCCTTTCCATGGGTCTTTTCTGCAGTCACCGTCCTTAGATCCACTAGTCCAGTGTGGTGAAGCTTGCCGCCACCATGGCTTGGGTGTGGACCTTGCTATTCCTGATGGCGGCCGCCCAAAGTATACAGGCCGAGATCGTGCTGACACAGTCTCCTGCCACACTGTCTCTGTCTCCTGGAGAACGGGCCACACTGAGCTGCACCGCCAGCAGCAGCTTCAGCAGCAGCTACCTGCACTGGTACCAGCAGAAACCTGGACTGGCCCCTCGGCTGCTGATCTACAGCACCAGCAACCTGGCCAGCGGCATCCCTGATCGGTTTTCTGGCAGCGGATCTGGCACAGATTACACACTGACCATCAGCCGGCTGGAACCTGAGGATTTTGCCGTGTACTACTGCCACCAGTACCACCGGAGCCCCCTGACCTTCGGCCAGGGAACAAAGCTGGAAATCAAGCGTACGGTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGCAAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAAGCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGCTCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGTTAGTGATTCGAATTCCTAGAAGACATGATAAGATACATTGATGAGTTTGGACAAACCACAACTAGAATGCAGTGAAAAAAATGCTTTATTTGTGAAATTTGTGATGCTATTGCTTTATTTGTAACCATTATAAGCTGCAATAAACAAGTTAACAACAACAATTGCATTCATTTTATGTTTCAGGTTCAGGGGGAGGTGTGGGA
TCTGATAAGAGTCAGAGGTAACTCCCGTTGCGGTGCTGTTAACGGTGGAGGGCAGTGTAGTCTGAGCAGTACTCGTTGCTGCCGCGCGCGCCACCAGACATAATAGCTGACAGACTAACAGACTGTTCCTTTCCATGGGTCTTTTCTGCAGTCACCGTCCTTAGATCCACTAGTCCAGTGTGGTGAAGCTTGCCGCCACCATGGCTTGGGTGTGGACCTTGCTATTCCTGATGGCGGCCGCCCAAAGTATACAGGCCGAGATCGTGCTGACACAGTCTCCTGCCACACTGTCTCTGTCTCCTGGAGAACGGGCCACACTGAGCTGCACCGCCAGCAGCAGCGTGCCAAGCAGCTACCTGCACTGGTACCAGCAGAAACCTGGACTGGCCCCTCGGCTGCTGATCTACAGCACCAGCAACCTGGCCAGCGGCATCCCTGATCGGTTTTCTGGCAGCGGATCTGGCACAGATTACACACTGACCATCAGCCGGCTGGAACCTGAGGATTTTGCCGTGTACTACTGCCACCAGTACCACCGGAGCCCCCTGACCTTCGGCCAGGGAACAAAGCTGGAAATCAAGCGTACGGTGGCTGCACCATCTGTCTTCATCTTCCCGCCATCTGATGAGCAGTTGAAATCTGGAACTGCCTCTGTTGTGTGCCTGCTGAATAACTTCTATCCCAGAGAGGCCAAAGTACAGTGGAAGGTGGATAACGCCCTCCAATCGGGTAACTCCCAGGAGAGTGTCACAGAGCAGGACAGCAAGGACAGCACCTACAGCCTCAGCAGCACCCTGACGCTGAGCAAAGCAGACTACGAGAAACACAAAGTCTACGCCTGCGAAGTCACCCATCAGGGCCTGAGCTCGCCCGTCACAAAGAGCTTCAACAGGGGAGAGTGTTAGTGATTCGAATTCCTAGAAGACATGATAAGATACATTGATGAGTTTGGACAAACCACAACTAGAATGCAGTGAAAAAAATGCTTTATTTGTGAAATTTGTGATGCTATTGCTTTATTTGTAACCATTATAAGCTGCAATAAACAAGTTAACAACAACAATTGCATTCATTTTATGTTTCAGGTTCAGGGGGAGGTGTGGGA
PD-1は、メモリーT細胞(CD45RO+細胞)で主に発現し、ナイーブT細胞では発現しないことが判明し、発現は、T細胞の活性化時に上方制御されることが判明した。PD-1の発現は、CMVペプチドで刺激されたメモリーT細胞にて増加した(図8A)。
NK細胞又はPBMCをエフェクター細胞として使用し、PD1B849及びPD1B878の、活性化メモリーT細胞又は休止メメモリーT細胞のADCCを媒介する能力について試験した。活性化メモリーT細胞は、休止メモリーT細胞と比較したとき、より高いPD-1の発現を有すると識別された。実施例1に記載する手順に従い、実験を行った。PD1B849及びPD1B878を、2つの個別のCHO細胞株で発現させた。1つは、通常のCHO抗体グリコシル化プロファイルを有する抗体を産生し、他方は、炭水化物フコシル含量が低下した抗体(例えば、低フコース(LF)細胞株)を産生した。低フコース細胞株で発現した抗体は、約1~15%のフコシル含量を有した。
追加したウサギ補体を用いて、PD1B849及びPD1B878の、活性化汎T細胞のCDCを媒介する能力について試験した。活性化T細胞は、休止T細胞と比較したとき、より高いPD-1の発現を有した。実施例1に記載する手順に従い、実験を行った。試験した濃度にて、PD1B849及びPD1B878は、活性化T細胞のCDCを誘発しなかった(図11)。陽性対照OKT3は、補体の不存在下ではなく、存在下において、活性化T細胞に対するCDC活性を示した。
選択抗体が、デキストラマー化(dextramerized)PD-L1-Fcの、PD-1を発現するJurkat細胞への結合を遮断する能力について試験した。実験は、後述の手順に従い実施した。PD1B878、PD1B1090、及びPD1B1094は、試験濃度にてPD-L1の結合を遮断しなかった(図12)。陽性対照の既知のアンタゴニスト抗体は、用量に依存して、PD-1への結合に関してPD-L1と競合することが示された。
インビボでの、病原性T細胞におけるPD-1アゴニストmAbの効果を調査するために、ヒト末梢血単核球細胞(PBMC)を、免疫無防備化NODスキッドIL-2Rγnull(NSG)マウスに、適合的に移植することにより、異種移植片対宿主病(異種GVHD)モデルを開発した。メスNSGマウス(週齢7~9)をJackson Labsから入手した。使用前に一週間、マウスを動物施設にて隔離した。注入前に、凍結細胞を湯浴中、37℃にて速やかに解凍し、500gで5分間、室温にて遠心分離することにより、滅菌リン酸緩衝生理食塩水(PBS)を用いて3回洗浄した。細胞を冷却PBSに懸濁させ、50×106/mLの細胞の終濃度を得た。
ヒトPBMCを、液体窒素冷却貯蔵庫から取り出し、ちょうど解凍されるまで37℃の湯浴中で速やかに解凍した。バイアル瓶の内容物を、滅菌した50mLの円錐形の管に移し(各ドナーに対して、個別の管を用いた)、完成したRPMI培地(10% FBS、1倍ペニシリン/ストレプトマイシン、1倍ピルビン酸ナトリウム)を各管に、総体積が15mLとなるように滴加した。細胞を250×gで10分間、室温で遠心分離し、次いで上清を捨て、細胞を完成した5~10mLの培地に再懸濁し、トリパンブルー排除を用いて計数した。細胞を2.5×106cells/mLで再懸濁し、96ウェル滅菌U底ポリスチレンプレート内で、3とおりで2.5×105cells/ウェル(=100μL/ウェル)でプレーティングした。PD-1 mAb、又はヒトIgG1アイソタイプコントロールを4倍終濃度に希釈し、50μL/ウェルを適切なウェルに添加した。抗体の添加後、通常のヒト血清を添加して5%の終濃度にした。各ウェルの総体積は200μLであり、細胞を96時間37℃、5% CO2にてインキュベートした。サンプルに加え、いくつかのウェルの余分な細胞をプレーティングし、5%ヒト血清を受けて、フローサイトメトリー染色対照として使用される処理済みサンプルと共に、インキュベートした。
T濾胞性ヘルパー(Tfh):生、CD19-CD56-/CD4+CD45RO+/HLADR+/CXCR5+/ICOS+PD1+;
T末梢性ヘルパー(Tph):生、CD19-CD56-/CD4+CD45RO+/HLADR+/CXCR5-/ICOS+PD1+;
Tfh/Tph母集団の組み合わせ:生、CD19-CD56-/CD4+CD45RO+/HLADR+/ICOS+PD1+。
以下に、本願の当初の特許請求の範囲に記載の発明を列挙する。
[発明1]
配列番号2、165、4、166、6及び7の重鎖相補性決定領域1(HCDR1)、HCDR2、HCDR3、軽鎖相補性決定領域1(LCDR1)、LCDR2、及びLCDR3をそれぞれ含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明2]
前記抗体又は前記その抗原結合断片が、以下の性質:
a)PD-L1の、PD-1への結合を遮断しないことであって、
遮断の欠如は、前記抗体が、実施例1に記載したPD-L1を発現する細胞、及びPD-1を発現する細胞のクラスター化を阻害できないことにより測定される、遮断しないことと、
b)約5×10- 8 M以下の平衡解離定数(K D )でPD-1に結合することであって、前記K D は、+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、
c)約3×10 4 1/Ms以上の結合定数(ka)でPD-1に結合することであって、前記kaは+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、
d)約3×10 -3 1/s以下の解離定数(kd)でPD-1に結合することであって、前記kdは、+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、
e)抗原特異的T細胞の増殖を阻害することであって、
前記増殖は、実施例1に記載されているCMV-PBMCアッセイにおいて評価される、阻害すること、
のうちの、1つ、2つ、3つ、4つ、又は5つを有する、発明1に記載の抗体又はその抗原結合断片。
[発明3]
a)IGHV7-4-1 * 1(配列番号125)に由来する重鎖可変領域(VH)フレームワーク、
b)IGKV3D-20 * 1(配列番号126)に由来する軽鎖可変領域(VL)フレームワーク、又は、
c)IGHV7-4-1 * 1(配列番号125)に由来する前記VHフレームワーク、及びIGKV3D-20 * 1(配列番号126)に由来する前記VLフレームワーク
を含む、発明1又は2に記載の抗体又はその抗原結合断片。
[発明4]
配列番号3、145、146、若しくは147の前記HCDR2、及び/又は、配列番号5、148、若しくは149の前記LCDR1を含む、発明1~3のいずれか一つに記載の抗体又はその抗原結合断片。
[発明5]
a)配列番号2、3、4、5、6、及び7、
b)配列番号2、145、4、5、6、及び7、
c)配列番号2、146、4、5、6、及び7、
d)配列番号2、147、4、5、6、及び7、
e)配列番号2、3、4、148、6、及び7、
f)配列番号2、3、4、149、6、及び7、
g)配列番号2、145、4、148、6、及び7、
h)配列番号2、146、4、148、6、及び7、
i)配列番号2、147、4、148、6、及び7、
j)配列番号2、145、4、149、6、及び7、
k)配列番号2、146、4、149、6、及び7、又は
l)配列番号2、147、4、149、6、及び7
の、前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3を含む、発明1~4のいずれか一つに記載の抗体又はその抗原結合断片。
[発明6]
a)配列番号118の重鎖可変領域(VH)、
b)配列番号119の軽鎖可変領域(VL)、又は
c)配列番号118及び119の前記VH及び前記VL
を含む、発明1~5のいずれか一つに記載の抗体又はその抗原結合断片。
[発明7]
a)配列番号8、9、10、140、141、若しくは142の前記VH、
b)配列番号14、15、16、143、又は144の前記VL、
c)配列番号8の前記VH及び配列番号14の前記VL、
d)配列番号9の前記VH及び配列番号15の前記VL、
e)配列番号9の前記VH及び配列番号16の前記VL、
f)配列番号10の前記VH及び配列番号16の前記VL、
g)配列番号140の前記VH及び配列番号16の前記VL、
h)配列番号141の前記VH及び配列番号16の前記VL、
i)配列番号142の前記VH及び配列番号16の前記VL、
j)配列番号10の前記VH及び配列番号143の前記VL、
k)配列番号10の前記VH及び配列番号144の前記VL、
l)配列番号140の前記VH及び配列番号143の前記VL、
m)配列番号141の前記VH及び配列番号143の前記VL、
n)配列番号142の前記VH及び配列番号143の前記VL、
o)配列番号140の前記VH及び配列番号144の前記VL、
p)配列番号141の前記VH及び配列番号144の前記VL、又は
q)配列番号142の前記VH及び配列番号144の前記VL
を含む、発明1~6のいずれか一つに記載の抗体又はその抗原結合断片。
[発明8]
PD-1に特異的に結合する単離抗体、又はその抗原結合断片であって、前記抗体又は前記その抗原結合断片が、PD-1の、発明7に記載の抗体又はその抗原結合断片との結合を競合する、単離抗体、又はその抗原結合断片。
[発明9]
a)配列番号2、3、4、5、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号8、9、若しくは10の前記VH、及び配列番号14、15、若しくは16の前記VL、並びに/又は、
c)配列番号20、21、若しくは22の重鎖(HC)、及び配列番号26、27、若しくは28の軽鎖(LC)
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明10]
a)配列番号2、145、4、5、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号140の前記VH及び配列番号16の前記VL、並びに/又は、
c)配列番号150の前記HC及び配列番号28の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明11]
a)配列番号2、146、4、5、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号141の前記VH及び配列番号16の前記VL、並びに/又は、
c)配列番号151の前記HC及び配列番号28の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明12]
a)配列番号2、147、4、5、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号142の前記VH及び配列番号16の前記VL、並びに/又は、
c)配列番号152の前記HC及び配列番号28の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明13]
a)配列番号2、3、4、148、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号10の前記VH及び配列番号143の前記VL、並びに/又は、
c)配列番号22の前記HC及び配列番号153の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明14]
a)配列番号2、3、4、149、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号10の前記VH及び配列番号144の前記VL、並びに/又は、
c)配列番号22の前記HC及び配列番号154の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明15]
a)配列番号2、145、4、148、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号140の前記VH及び配列番号143の前記VL、並びに/又は、
c)配列番号150の前記HC及び配列番号153の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明16]
a)配列番号2、146、4、148、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号141の前記VH及び配列番号143の前記VL、並びに/又は、
c)配列番号151の前記HC及び配列番号153の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明17]
a)配列番号2、147、4、148、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号142の前記VH及び配列番号143の前記VL、並びに/又は、
c)配列番号152の前記HC及び配列番号153の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明18]
a)配列番号2、145、4、149、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号140の前記VH及び配列番号144の前記VL、並びに/又は、
c)配列番号150の前記HC及び配列番号154の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明19]
a)配列番号2、146、4、149、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号141の前記VH及び配列番号144の前記VL、並びに/又は、
c)配列番号151の前記HC及び配列番号154の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明20]
a)配列番号2、147、4、149、6、及び7の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号142の前記VH及び配列番号144の前記VL、並びに/又は、
c)配列番号152の前記HC及び配列番号154の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明21]
前記抗体又はその抗原結合断片が、PD-1のアゴニストである、若しくはPD-1を発現する細胞の抗体依存性細胞傷害(ADCC)を媒介する、又はこれらの両方である、発明1~20のいずれか一つに記載の抗体又はその抗原結合断片。
[発明22]
前記PD-1を発現する細胞が、活性化メモリーT細胞、T濾胞性ヘルパー細胞(T FH )、若しくはT末梢性ヘルパー細胞(T PH )、又はこれらの任意の組み合わせである、発明21に記載の抗体又はその抗原結合断片。
[発明23]
前記抗体又は前記その抗原結合断片が、IgG1、IgG2、及びIgG3、又はIgG4アイソタイプである、発明1~22のいずれか一つに記載の抗体又はその抗原結合断片。
[発明24]
前記抗体又は前記その抗原結合断片が、前記抗体の、Fc受容体(FcR)への結合を媒介する抗体Fcにおいて、少なくとも1つの変異を含む、発明1~23のいずれか一つに記載の抗体又はその抗原結合断片。
[発明25]
前記少なくとも1つの変異が、
a)S267E変異、
b)S267D変異、
c)S267E/I332E変異、
d)S267E/L328F変異、
e)G236D/S267E変異、
f)P238D変異、又は
g)P238D/E233D/G237D/H268D/P271G/A330R変異
である、発明24に記載の抗体又はその抗原結合断片。
[発明26]
前記抗体が、
a)配列番号20、21、22、150、151、若しくは152の重鎖(HC)、
b)配列番号26、27、28、153、又は154の軽鎖(LC)、
c)配列番号20、21、22、150、151、若しくは152の前記HC、及び配列番号26、27、28、153、又は154の前記LC、
d)配列番号20の前記HC、及び配列番号26の前記LC、
e)配列番号21の前記HC、及び配列番号27の前記LC、
f)配列番号21の前記HC、及び配列番号28の前記LC、
g)配列番号22の前記HC、及び配列番号28の前記LC、
h)配列番号150の前記HC、及び配列番号28の前記LC、
i)配列番号151の前記HC、及び配列番号28の前記LC、
i)配列番号152の前記HC、及び配列番号28の前記LC、
k)配列番号22の前記HC、及び配列番号153の前記LC、
l)配列番号22の前記HC、及び配列番号154の前記LC、
m)配列番号150の前記HC、及び配列番号153の前記LC、
n)配列番号151の前記HC、及び配列番号153の前記LC、
o)配列番号152の前記HC、及び配列番号153の前記LC、
p)配列番号150の前記HC、及び配列番号154の前記LC、
q)配列番号151の前記HC、及び配列番号154の前記LC、又は
r)配列番号152の前記HC、及び配列番号154の前記LC
を含む、発明1~8のいずれか一つに記載の抗体又はその抗原結合断片。
[発明27]
前記抗体VH及び前記抗体VL、又は前記抗体HC及び前記抗体LCが、
a)配列番号11及び17、
b)配列番号12及び18、
c)配列番号12及び19、
d)配列番号13及び19、
e)配列番号23及び29、
f)配列番号24及び30、
g)配列番号24及び31、
h)配列番号25及び31、
i)配列番号132及び133、
j)配列番号134及び135、
k)配列番号155及び19、
l)配列番号156及び19、
m)配列番号157及び19、
n)配列番号13及び158、
o)配列番号13及び159、
p)配列番号155及び158、
q)配列番号156及び158、
r)配列番号157及び158、
s)配列番号155及び159、
t)配列番号156及び159、
u)配列番号157及び159、
v)配列番号160及び31、
w)配列番号161及び31、
x)配列番号162及び31、
y)配列番号25及び163、
z)配列番号25及び164、
aa)配列番号160及び163、
bb)配列番号161及び163、
cc)配列番号162及び163、
dd)配列番号160及び164、
ee)配列番号161及び164、又は
ff)配列番号162及び164
のポリヌクレオチド配列を含むポリヌクレオチドによりコードされる、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明28]
前記抗体又は前記その抗原結合断片が、フコース含量が約1%~約15%である二分岐グリカン構造を有する、発明1~27のいずれか一つに記載の抗体又はその抗原結合断片。
[発明29]
a)配列番号118、8、9、10、140、141、若しくは142の前記VHをコードする、
b)配列番号119、14、15、16、143、若しくは144の前記VLをコードする、
c)配列番号118、8、9、10、140、141、若しくは142の前記VH、及び配列番号119、14、15、16、143、若しくは144の前記VLをコードする、
d)配列番号20、21、22、150、151、若しくは152の前記HCをコードする、
e)配列番号26、27、28、153、若しくは154の前記LCをコードする、
f)配列番号20、21、22、150、151、若しくは152の前記HC、及び配列番号26、27、28、153、若しくは154の前記LCをコードする、又は
g)配列番号11、12、13、17、18、19、23、24、25、29、30、31、132、133、134、135、155、156、157、158、159、160、161、162、163、若しくは164のポリヌクレオチド配列を含む、
ポリヌクレオチド。
[発明30]
発明29に記載のポリヌクレオチドを含むベクター。
[発明31]
発明30に記載のベクターを含む宿主細胞。
[発明32]
真核細胞、原核細胞、CHO細胞、HEK293細胞、又はハイブリドーマである、発明31に記載の宿主細胞。
[発明33]
前記抗体又は前記その抗原結合断片が発現する条件で、発明31に記載の宿主細胞を培養することと、前記抗体又は前記その抗原結合断片を単離することとを含む、発明1~28のいずれか一つに記載の抗体又はその抗原結合断片の作製方法。
[発明34]
発明1~28のいずれか一つに記載の抗体又はその抗原結合断片を含む、医薬組成物。
[発明35]
発明1~28のいずれか一つに記載の抗体又はその抗原結合断片を含むキット。
[発明36]
対象における、PD-1を発現するT細胞の活性化を抑制する方法であって、前記PD-1を発現するT細胞の活性化を抑制するのに十分な時間、発明1~28のいずれか一つに記載の単離抗体又はその抗原結合断片を、対象に投与することを含む、前記方法。
[発明37]
前記PD-1を発現するT細胞が、抗原特異的CD4 + T細胞、及び/又は抗原特異的CD8 + T細胞である、発明36に記載の方法。
[発明38]
免疫応答を下方制御する方法であって、免疫応答の下方制御を必要とする対象に、治療に有効な量の、発明1~28のいずれか一つに記載の抗体又はその抗原結合断片を投与して、前記免疫応答を下方制御することを含む、前記方法。
[発明39]
免疫不全の治療方法であって、免疫不全の治療を必要とする対象に、治療に有効な量の、発明1~28のいずれか一つに記載の抗体又はその抗原結合断片を投与して、前記免疫不全を治療することを含む、前記方法。
[発明40]
前記免疫不全が、狼瘡、全身性エリテマトーデス、シェーグレン症候群、関節炎、関節リウマチ、ぜんそく、COPD、骨盤内炎症性疾患、アルツハイマー病、炎症性腸疾患、クローン病、潰瘍性大腸炎、ペロニー病、セリアック病、胆嚢疾患、毛巣洞、腹膜炎、乾癬、乾癬性関節炎、脈管炎、手術による癒着、脳卒中、I型糖尿病、ライム病、髄膜脳炎、自己免疫性ぶどう膜炎、多発性硬化症、ギラン・バレー症候群、アトピー性皮膚炎、自己免疫性肝炎、線維化性肺胞炎、グレーブス病、IgA腎症、特発性血小板減少性紫斑病、メニエール病、天疱瘡、原発性胆汁性肝硬変、サルコイドーシス、強皮症、ヴェゲナー肉芽腫症、その他の自己免疫疾患、膵炎、外傷(外科)、移植片対宿主病、移植拒絶反応、筋梗塞並びにアテローム性動脈硬化症などの虚血性疾患を含む心臓疾患、血管内凝固、骨吸収、骨粗鬆症、変形性関節症、歯周炎及び低酸症、胎児-母体耐性の欠如に関連する不妊症、シェーグレン症候群、白斑、重症筋無力症、又は全身性硬化症である、発明39に記載の方法。
[発明41]
前記抗体又は前記その抗原結合断片が、第2の治療薬と共に投与される、発明36~40のいずれか一つに記載の方法。
[発明42]
発明7に記載の抗体又は抗原結合断片に特異的に結合する、抗イディオタイプ抗体。
[発明43]
異種分子と複合体化した、発明1~28のいずれか一つに記載の抗体又は抗原結合断片を含む、免疫複合体。
[発明44]
配列番号32、124、40、41、42、及び43の、重鎖相補性決定領域1(HCDR1)、HCDR2、HCDR3、軽鎖相補性決定領域1(LCDR1)、LCDR2、及びLCDR3を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明45]
前記抗体又は前記その抗原結合断片が、以下の性質:
a)PD-L1の、PD-1への結合を遮断することであって、遮断の欠如は、実施例1に記載した、PD-L1を発現する細胞及びPD-1を発現する細胞のクラスター化を、前記抗体が阻害できないことにより測定される、遮断することと、
b)約5×10 -8 M以下の平衡解離定数(K D )でPD-1に結合することであって、前記K D は、+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、
c)約4×10 5 1/Ms以上の結合定数(ka)でPD-1に結合することであって、前記kaは、+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、
d)約1×10 -2 1/s以下の解離定数(kd)でPD-1に結合することであって、前記kdは、+25℃にて、ProteOn XPR36システムを用いて測定される、結合することと、
e)抗原特異的T細胞の増殖を阻害することであって、
前記増殖は、実施例1に記載されているCMV-PBMCアッセイにおいて評価される、阻害することと
のうちの、1つ、2つ、3つ、4つ、又は5つを有する、発明44に記載の抗体又はその抗原結合断片。
[発明46]
a)IGHV1-2 * 02(配列番号127)に由来する重鎖可変領域(VH)フレームワーク、
b)IGKV1D-16 * 1(配列番号128)に由来する軽鎖可変領域(VL)フレームワーク、
c)IGHV1-2 * 02(配列番号127)に由来する前記VHフレームワーク、及びIGKV1D-16 * 1(配列番号128)に由来する前記VLフレームワーク
を含む、発明44又は45に記載の抗体又はその抗原結合断片。
[発明47]
配列番号33、34、35、36、37、38、又は39の前記HCDR2を含む、発明44~46のいずれか一つに記載の抗体又はその抗原結合断片。
[発明48]
a)配列番号32、33、40、41、42、及び43、
b)配列番号32、34、40、41、42、及び43、
c)配列番号32、35、40、41、42、及び43、
d)配列番号32、36、40、41、42、及び43、
e)配列番号32、37、40、41、42、及び43、
f)配列番号32、38、40、41、42、及び43、又は
g)配列番号32、39、40、41、42、及び43
の、前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3を含む、発明44~47のいずれか一つに記載の抗体又はその抗原結合断片。
[発明49]
a)配列番号120の重鎖可変領域(VH)、
b)配列番号121の軽鎖可変領域(VL)、又は
c)配列番号120及び121の前記VH及び前記VL
を含む、発明44~48のいずれか一つに記載の抗体又はその抗原結合断片。
[発明50]
a)配列番号44、45、46、47、48、49、50、若しくは51の前記VH、
b)配列番号60、61、若しくは62の前記VL、
c)配列番号44、45、46、47、48、49、50、若しくは51の前記VH、及び配列番号60、61、若しくは62の前記VL、
d)配列番号44の前記VH及び配列番号60の前記VL、
e)配列番号45のVH及び配列番号61の前記VL、
f)配列番号45の前記VH及び配列番号62の前記VL、
g)配列番号46の前記VH及び配列番号61の前記VL、
h)配列番号47の前記VH及び配列番号61の前記VL、
i)配列番号48の前記VH及び配列番号61の前記VL、
j)配列番号49の前記VH及び配列番号61の前記VL、
k)配列番号50の前記VH及び配列番号61の前記VL、又は
l)配列番号51の前記VH及び配列番号61の前記VL
を含む、発明44~49のいずれか一つに記載の抗体又はその抗原結合断片。
[発明51]
PD-1に特異的に結合する単離抗体、又はその抗原結合断片でであって、前記抗体又は前記その抗原結合断片が、PD-1との結合を、発明50に記載の抗体又はその抗原結合断片と競合する、単離抗体、又はその抗原結合断片。
[発明52]
a)配列番号:配列番号32、33、40、41、42、及び43の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号44若しくは45の前記VH、及び配列番号60、61、若しくは62の前記VL、並びに/又は、
c)配列番号66若しくは67の前記HC、及び配列番号82、83、若しくは84の前記LC、
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明53]
a)配列番号32、34、40、41、42、及び43の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号46の前記VH及び配列番号61の前記VL、並びに/又は、
c)配列番号68の前記HC及び配列番号83の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明54]
a)配列番号32、35、40、41、42、及び43の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号47の前記VH及び配列番号61の前記VL、並びに/又は、
c)配列番号69の前記HC及び配列番号83の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明55]
a)配列番号32、36、40、41、42、及び43の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号48の前記VH及び配列番号61の前記VL、並びに/又は、
c)配列番号70の前記HC及び配列番号83の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明56]
a)配列番号32、37、40、41、42、及び43の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号49の前記VH及び配列番号61の前記VL、並びに/又は、
c)配列番号71の前記HC及び配列番号83の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明57]
a)配列番号32、38、40、41、42、及び43の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号50の前記VH及び配列番号61の前記VL、並びに/又は、
c)配列番号72の前記HC及び配列番号83の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明58]
a)配列番号32、39、40、41、42、及び43の前記HCDR1、前記HCDR2、前記HCDR3、前記LCDR1、前記LCDR2、及び前記LCDR3、
b)配列番号51の前記VH及び配列番号61の前記VL、並びに/又は、
c)配列番号73の前記HC及び配列番号83の前記LC
を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明59]
前記抗体又はその抗原結合断片が、PD-1のアゴニストである、若しくはPD-1を発現する細胞の抗体依存性細胞傷害(ADCC)を媒介する、又はこれらの両方である、発明44~58のいずれか一つに記載の抗体又はその抗原結合断片。
[発明60]
前記PD-1を発現する細胞が、活性化メモリーT細胞、T濾胞性ヘルパー細胞(T FH )、若しくはT末梢性ヘルパー細胞(T PH )、又はこれらの任意の組み合わせである、発明59に記載の抗体又はその抗原結合断片。
[発明61]
前記抗体又は前記その抗原結合断片が、IgG1、IgG2、及びIgG3、又はIgG4アイソタイプである、発明44~60のいずれか一つに記載の抗体又はその抗原結合断片。
[発明62]
前記抗体又は前記その抗原結合断片が、前記抗体の、Fc受容体(FcR)への結合を媒介する抗体Fcにおいて、少なくとも1つの変異を含む、発明44~61のいずれか一つに記載の抗体又はその抗原結合断片。
[発明63]
前記少なくとも1つの変異が、
a)S267E変異、
b)S267D変異、
c)S267E/I332E変異、
d)S267E/L328F変異、
e)G236D/S267E変異、
f)P238D変異、又は
g)P238D/E233D/G237D/H268D/P271G/A330R変異
である、発明62に記載の抗体又はその抗原結合断片。
[発明64]
前記抗体が、
a)配列番号66、67、68、69、70、71、72、若しくは73の重鎖(HC)、
b)配列番号82、83、若しくは84の軽鎖(LC)、
c)配列番号66、67、68、69、70、71、72、若しくは73の前記HC、及び配列番号82、83、若しくは84の前記LC、
d)配列番号66の前記HC、及び配列番号82の前記LC、
i)配列番号67の前記HC、及び配列番号83の前記LC、
e)配列番号67の前記HC、及び配列番号84の前記LC、
f)配列番号68の前記HC、及び配列番号83の前記LC、
g)配列番号69の前記HC、及び配列番号83の前記LC、
h)配列番号70の前記HC、及び配列番号83の前記LC、
i)配列番号71の前記HC、及び配列番号83の前記LC、
j)配列番号72の前記HC、及び配列番号83の前記LC、又は
k)配列番号73の前記HC、及び配列番号83の前記LC
を含む、発明44~50のいずれか一つに記載の抗体又はその抗原結合断片。
[発明65]
前記抗体VH及び前記抗体VL、又は前記抗体HC及び前記抗体LCが、
a)配列番号52及び63、
b)配列番号53及び64、
c)配列番号53及び65、
d)配列番号54及び64、
e)配列番号55及び64、
f)配列番号56及び64、
g)配列番号57及び64、
h)配列番号58及び64、
i)配列番号59及び64、
j)配列番号74及び85、
k)配列番号75及び86、
l)配列番号75及び87、
m)配列番号76及び86、
n)配列番号77及び86、
o)配列番号78及び86、
p)配列番号79及び86、
q)配列番号80及び86、
r)配列番号81及び86、
s)配列番号136及び137、又は
t)配列番号138及び139
のポリヌクレオチド配列を含むポリヌクレオチドによりコードされる、PD-1に特異的に結合する単離抗体、又はPD-1に特異的に結合するその抗原結合断片。
[発明66]
前記抗体又は前記その抗原結合断片が、フコース含量が約1%~約15%である二分岐グリカン構造を有する、発明44~65のいずれか一つに記載の抗体又はその抗原結合断片。
[発明67]
a)配列番号120、44、45、46、47、48、49、50、若しくは51の前記VHをコードする、
b)配列番号121、60、61、若しくは62の前記VLをコードする、
c)配列番号120、44、45、46、47、48、49、50、若しくは51の前記VH、及び配列番号121、60、61、若しくは62の前記VLをコードする、
d)配列番号66、67、68、69、70、71、72、若しくは73の前記HCをコードする、
e)配列番号82、83、若しくは84の前記LCをコードする、
f)配列番号66、67、68、69、70、71、72、若しくは73の前記HC、及び配列番号82、83、若しくは84の前記LCをコードする、又は
g)配列番号52、53、54、55、56、57、58、59、63、64、65、74、75、76、77、78、79、80、81、85、86、87、136、137、138、若しくは139のポリヌクレオチド配列を含む、
ポリヌクレオチド。
[発明68]
発明67に記載の少なくとも1つのポリヌクレオチドを含むベクター。
[発明69]
発明68に記載のベクターを含む宿主細胞。
[発明70]
真核細胞、原核細胞、CHO細胞、HEK293細胞、又はハイブリドーマである、発明69に記載の宿主細胞。
[発明71]
前記抗体又は前記その抗原結合断片が発現する条件で、発明69に記載の宿主細胞を培養することと、前記抗体又は前記その抗原結合断片を単離することと、を含む、発明44に記載の抗体又はその抗原結合断片の作製方法。
[発明72]
発明44~66のいずれか一つに記載の抗体又はその抗原結合断片を含む、医薬組成物。
[発明73]
発明44~66のいずれか一つに記載の抗体又はその抗原結合断片を含むキット。
[発明74]
対象における、PD-1を発現するT細胞の活性化を抑制する方法であって、前記PD-1を発現するT細胞の活性化を抑制するのに十分な時間、発明44~66のいずれか一つに記載の単離抗体又はその抗原結合断片を前記対象に投与することを含む、方法。
[発明75]
前記PD-1を発現するT細胞が、抗原特異的CD4 + T細胞、及び/又は抗原特異的CD8 + T細胞である、発明74に記載の方法。
[発明76]
免疫応答を下方制御する方法であって、免疫応答の下方制御を必要とする対象に、治療に有効な量の、発明44~66のいずれか一つに記載の抗体又はその抗原結合断片を投与して、前記免疫応答を下方制御することを含む、方法。
[発明77]
免疫不全の治療方法であって、免疫不全の治療を必要とする対象に、治療に有効な量の、発明44~66のいずれか一つに記載の抗体又はその抗原結合断片を投与して、前記免疫不全を治療することを含む、方法。
[発明78]
前記免疫不全が、狼瘡、全身性エリテマトーデス、シェーグレン症候群、関節炎、関節リウマチ、ぜんそく、COPD、骨盤内炎症性疾患、アルツハイマー病、炎症性腸疾患、クローン病、潰瘍性大腸炎、ペロニー病、セリアック病、胆嚢疾患、毛巣洞、腹膜炎、乾癬、乾癬性関節炎、脈管炎、手術による癒着、脳卒中、I型糖尿病、ライム病、髄膜脳炎、自己免疫性ぶどう膜炎、多発性硬化症、ギラン・バレー症候群、アトピー性皮膚炎、自己免疫性肝炎、線維化性肺胞炎、グレーブス病、IgA腎症、特発性血小板減少性紫斑病、メニエール病、天疱瘡、原発性胆汁性肝硬変、サルコイドーシス、強皮症、ヴェゲナー肉芽腫症、その他の自己免疫疾患、膵炎、外傷(外科)、移植片対宿主病、移植拒絶反応、心臓筋梗塞並びにアテローム性動脈硬化症などの虚血性疾患を含む心臓疾患、血管内凝固、骨吸収、骨粗鬆症、変形性関節症、歯周炎及び低酸症、胎児-母体耐性の欠如に関連する不妊症、シェーグレン症候群、白斑、重症筋無力症、又は全身性硬化症である、発明77に記載の方法。
[発明79]
前記抗体又は前記その抗原結合断片が、第2の治療薬と共に投与される、発明74~78のいずれか一つに記載の方法。
[発明80]
発明52~58のいずれか一つに記載の抗体又は抗原結合断片に特異的に結合する、抗イディオタイプ抗体。
[発明81]
造影剤又は細胞毒性剤と複合体化した、発明44~66のいずれか一つに記載の抗体又はその抗原結合断片を含む、免疫複合体。
[発明82]
配列番号88、89、90、91、92、及び93の、重鎖相補性決定領域1(HCDR1)、HCDR2、HCDR3、軽鎖相補性決定領域1(LCDR1)、LCDR2、及びLCDR3を含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明83]
前記抗体又は前記その抗原結合断片が、PD-L1のPD-1への結合を遮断せず、遮断の欠如は、前記抗体が、実施例1に記載したPD-L1を発現する細胞、及びPD-1を発現する細胞のクラスター化を阻害できないことにより測定される、発明82に記載の抗体又はその抗原結合断片。
[発明84]
a)IGHV2-5 * 04(配列番号129)に由来する重鎖可変領域(VH)フレームワーク、
b)IGKV2-28 * 01(配列番号130)に由来する軽鎖可変領域(VL)フレームワーク、又は
c)IGHV2-5 * 04(配列番号129)に由来する前記VHフレームワーク、及びIGKV2-28 * 01(配列番号130)に由来する前記VLフレームワーク
を含む、発明82又は83に記載の抗体又はその抗原結合断片。
[発明85]
a)配列番号122の重鎖可変領域(VH)、
b)配列番号123の軽鎖可変領域(VL)、又は
c)配列番号122及び123の前記VH及び前記VL
を含む、発明82~84のいずれか一つに記載の抗体又はその抗原結合断片。
[発明86]
a)配列番号94若しくは95の前記VH、
b)配列番号98、99、若しくは100の前記VL、
c)配列番号94若しくは95の前記VH、及び配列番号98、99、若しくは100の前記VL、
d)配列番号94の前記VH及び配列番号98の前記VL、
e)配列番号95のVH及び配列番号99の前記VL、又は
f)配列番号95の前記VH及び配列番号100の前記VL
を含む、発明82~85のいずれか一つに記載の抗体又はその抗原結合断片。
[発明87]
PD-1に特異的に結合する単離抗体、又はその抗原結合断片であって、前記抗体は、PD-1への結合を、発明86に記載の抗体又はその抗原結合断片と競合する、単離抗体、又はその抗原結合断片。
[発明88]
前記抗体が、アンタゴニスト抗体である、若しくはPD-1を発現する細胞の抗体依存性細胞傷害(ADCC)を媒介する、又はこれらの両方である、発明82~87のいずれか一つに記載の抗体又はその抗原結合断片。
[発明89]
前記PD-1を発現する細胞は、活性化メモリーT細胞、T濾胞性ヘルパー細胞(T FH )、若しくはT末梢性ヘルパー細胞(T PH )、又はこれらの任意の組み合わせである、発明88に記載の抗体又はその抗原結合断片。
[発明90]
前記抗体又は前記その抗原結合断片は、IgG1、IgG2、及びIgG3、又はIgG4アイソタイプである、発明82~89のいずれか一つに記載の抗体又はその抗原結合断片。
[発明91]
前記抗体又は前記その抗原結合断片が、前記抗体の、Fc受容体への結合を媒介する抗体Fcにおいて、少なくとも1つの変異を含む、発明82~90のいずれか一つに記載の抗体又はその抗原結合断片。
[発明92]
前記少なくとも1つの変異が、
a)S267E変異、
b)S267D変異、
c)S267E/I332E変異、
d)S267E/L328F変異、
e)G236D/S267E変異、
f)P238D変異、又は
g)P238D/E233D/G237D/H268D/P271G/A330R変異
である、発明91に記載の抗体又はその抗原結合断片。
[発明93]
a)配列番号104若しくは105の重鎖(HC)、
b)配列番号108、109、若しくは110の軽鎖(LC)、
c)配列番号104若しくは105の前記HC、及び配列番号108、109、若しくは110の前記LC、
d)配列番号104の前記HC、及び配列番号108の前記LC、
e)配列番号105の前記HC、及び配列番号109の前記LC、又は
f)配列番号105の前記HC、及び配列番号110の前記LC
を含む、発明82~92のいずれか一つに記載の抗体又はその抗原結合断片。
[発明94]
前記抗体VH及び前記抗体VL、又は前記抗体HC及び前記抗体LCが、
a)配列番号96及び101、
b)配列番号97及び102、
c)配列番号97及び103、
d)配列番号106及び111、
e)配列番号107及び112、又は
f)配列番号107及び113
のポリヌクレオチド配列を含むポリヌクレオチドによりコードされる、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
[発明95]
前記抗体又は前記その抗原結合断片が、フコース含量が約1%~約15%である二分岐グリカン構造を有する、発明82~94のいずれか一つに記載の抗体又はその抗原結合断片。
[発明96]
a)配列番号122、94、若しくは95の前記VHをコードする、
b)配列番号123、98、99、若しくは100の前記VLをコードする、
c)配列番号122、94、若しくは95の前記VH、及び配列番号123、98、99、若しくは100の前記VLをコードする、
d)配列番号104若しくは105の前記HCをコードする、
e)配列番号108、109、若しくは110の前記LCをコードする、
f)配列番号104若しくは105の前記HC、及び配列番号108、109、若しくは110の前記LCをコードする、又は
g)配列番号96、97、101、102、103、106、107、111、112、若しくは113のポリヌクレオチド配列を含む、
ポリヌクレオチド。
[発明97]
発明96に記載の少なくとも1つのポリヌクレオチドを含むベクター。
[発明98]
発明97に記載のベクターを含む宿主細胞。
[発明99]
真核細胞、原核細胞、CHO細胞、HEK293細胞、又はハイブリドーマである、発明98に記載の宿主細胞。
[発明100]
前記抗体又は前記その抗原結合断片が発現する条件で、発明98に記載の宿主細胞を培養することと、前記抗体又は前記その抗原結合断片を単離することとを含む、発明82~95のいずれか一つに記載の抗体又はその抗原結合断片の作製方法。
[発明101]
発明82~95のいずれか一つに記載の抗体又はその抗原結合断片を含む、医薬組成物。
[発明102]
発明82~95のいずれか一つに記載の抗体又はその抗原結合断片を含むキット。
[発明103]
対象における、PD-1を発現するT細胞の活性化を抑制する方法であって、前記PD-1を発現するT細胞の活性化を抑制するのに十分な時間、発明82~95のいずれか一つに記載の単離抗体又はその抗原結合断片を前記対象に投与することを含む、前記方法。
[発明104]
前記PD-1を発現するT細胞が、抗原特異的CD4 + T細胞、及び/又は抗原特異的CD8 + T細胞である、発明103に記載の方法。
[発明105]
免疫応答を下方制御する方法であって、免疫応答の下方制御を必要とする対象に、治療に有効な量の、発明82~95のいずれか一つに記載の単離抗体又はその抗原結合断片を投与して、前記免疫応答を下方制御することを含む、前記方法。
[発明106]
免疫不全の治療方法であって、免疫不全の治療を必要とする対象に、治療に有効な量の、発明82~95のいずれか一つに記載の抗体又はその抗原結合断片を投与して、前記免疫不全を治療することを含む、前記方法。
[発明107]
前記免疫不全が、狼瘡、全身性エリテマトーデス、シェーグレン症候群、関節炎、関節リウマチ、ぜんそく、COPD、骨盤内炎症性疾患、アルツハイマー病、炎症性腸疾患、クローン病、潰瘍性大腸炎、ペロニー病、セリアック病、胆嚢疾患、毛巣洞、腹膜炎、乾癬、乾癬性関節炎、脈管炎、手術による癒着、脳卒中、I型糖尿病、ライム病、髄膜脳炎、自己免疫性ぶどう膜炎、多発性硬化症、ギラン・バレー症候群、アトピー性皮膚炎、自己免疫性肝炎、線維化性肺胞炎、グレーブス病、IgA腎症、特発性血小板減少性紫斑病、メニエール病、天疱瘡、原発性胆汁性肝硬変、サルコイドーシス、強皮症、ヴェゲナー肉芽腫症、その他の自己免疫疾患、膵炎、外傷(外科)、移植片対宿主病、移植拒絶反応、心筋梗塞並びにアテローム性動脈硬化症などの虚血性疾患を含む心臓疾患、血管内凝固、骨吸収、骨粗鬆症、変形性関節症、歯周炎及び低酸症、胎児-母体耐性の欠如に関連する不妊症、シェーグレン症候群、白斑、重症筋無力症、又は全身性硬化症である、発明106に記載の方法。
[発明108]
前記抗体又は前記その抗原結合断片が、第2の治療薬と共に投与される、発明103~107のいずれか一つに記載の方法。
[発明109]
発明64に記載の抗体又は抗原結合断片に特異的に結合する、抗イディオタイプ抗体。
[発明110]
造影剤又は細胞毒性剤と複合体化した、発明82~96のいずれか一つに記載の抗体又はその抗原結合断片を含む、免疫複合体。
Claims (23)
- 配列番号2、3、4、5、6及び7の重鎖相補性決定領域1(HCDR1)、HCDR2、HCDR3、軽鎖相補性決定領域1(LCDR1)、LCDR2、及びLCDR3をそれぞれ含む、PD-1に特異的に結合する単離抗体、又はその抗原結合断片。
- a)IGHV7-4-1*1(配列番号125)に由来する重鎖可変領域(VH)フレームワーク、
b)IGKV3D-20*1(配列番号126)に由来する軽鎖可変領域(VL)フレームワーク、又は、
c)IGHV7-4-1*1(配列番号125)に由来する前記VHフレームワーク、及びIGKV3D-20*1(配列番号126)に由来する前記VLフレームワーク
を含む、請求項1に記載の抗体又はその抗原結合断片。 - a)配列番号10の重鎖可変領域(VH)、
b)配列番号16の軽鎖可変領域(VL)、又は
c)配列番号10の前記VH及び配列番号16の前記VL
を含む、請求項1又は2に記載の抗体又はその抗原結合断片。 - 前記抗体又はその抗原結合断片が、PD-1のアゴニストである、若しくはPD-1を発現する細胞の抗体依存性細胞傷害(ADCC)を媒介する、又はこれらの両方である、請求項1~3のいずれか一項に記載の抗体又はその抗原結合断片。
- 前記PD-1を発現する細胞が、活性化メモリーT細胞、T濾胞性ヘルパー細胞(TFH)、若しくはT末梢性ヘルパー細胞(TPH)、又はこれらの任意の組み合わせである、請求項4に記載の抗体又はその抗原結合断片。
- 前記抗体又は前記その抗原結合断片が、IgG1、IgG2、及びIgG3、又はIgG4アイソタイプである、請求項1~5のいずれか一項に記載の抗体又はその抗原結合断片。
- 前記抗体又は前記その抗原結合断片が、前記抗体の、Fc受容体(FcR)への結合を媒介する抗体Fcにおいて、少なくとも1つの変異を含む、請求項1~6のいずれか一項に記載の抗体又はその抗原結合断片。
- 前記少なくとも1つの変異が、
a)S267E変異、
b)S267D変異、
c)S267E/I332E変異、
d)S267E/L328F変異、
e)G236D/S267E変異、
f)P238D変異、又は
g)P238D/E233D/G237D/H268D/P271G/A330R変異
である、請求項7に記載の抗体又はその抗原結合断片。 - 前記抗体が、
a)配列番号22の重鎖(HC)、
b)配列番号28の軽鎖(LC)、又は
c)配列番号22の前記HC、及び配列番号28の前記LC
を含む、請求項1~8のいずれか一項に記載の抗体又はその抗原結合断片。 - 前記抗体又は前記その抗原結合断片が、フコース含量が1%~15%である二分岐グリカン構造を有する、請求項1~9のいずれか一項に記載の抗体又はその抗原結合断片。
- 請求項1~10のいずれか一項に記載の抗体又はその抗原結合断片をコードする核酸配列を含む、ポリヌクレオチド。
- 請求項11に記載のポリヌクレオチドを含むベクター。
- 請求項12に記載のベクターを含む宿主細胞。
- 真核細胞、原核細胞、CHO細胞、HEK293細胞、又はハイブリドーマである、請求項13に記載の宿主細胞。
- 前記抗体又は前記その抗原結合断片が発現する条件で、請求項13に記載の宿主細胞を培養することと、前記抗体又は前記その抗原結合断片を単離することとを含む、請求項1~10のいずれか一項に記載の抗体又はその抗原結合断片の作製方法。
- 請求項1~10のいずれか一項に記載の抗体又はその抗原結合断片を含む、医薬組成物。
- 請求項1~10のいずれか一項に記載の抗体又はその抗原結合断片を含むキット。
- 対象における、PD-1を発現するT細胞の活性化を抑制するために用いられる、請求項16に記載の医薬組成物。
- 前記PD-1を発現するT細胞が、抗原特異的CD4+ T細胞、及び/又は抗原特異的CD8+ T細胞である、請求項18に記載の医薬組成物。
- 対象における免疫応答を下方制御するために用いられる、請求項16に記載の医薬組成物。
- 対象における免疫不全を治療するために用いられる、請求項16に記載の医薬組成物。
- 前記抗体又は前記その抗原結合断片が、第2の治療薬と共に投与されるものである、請求項18~21のいずれか一項に記載の医薬組成物。
- 異種分子と複合体化した、請求項1~10のいずれか一項に記載の抗体又は抗原結合断片を含む、免疫複合体。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762515188P | 2017-06-05 | 2017-06-05 | |
| US62/515,188 | 2017-06-05 | ||
| US201862648114P | 2018-03-26 | 2018-03-26 | |
| US62/648,114 | 2018-03-26 | ||
| US201862673185P | 2018-05-18 | 2018-05-18 | |
| US62/673,185 | 2018-05-18 | ||
| PCT/US2018/035843 WO2018226580A2 (en) | 2017-06-05 | 2018-06-04 | Antibodies that specifically bind pd-1 and methods of use |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2020522278A JP2020522278A (ja) | 2020-07-30 |
| JP2020522278A5 JP2020522278A5 (ja) | 2021-07-26 |
| JP7235733B2 true JP7235733B2 (ja) | 2023-03-08 |
Family
ID=64562613
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020516792A Active JP7235733B2 (ja) | 2017-06-05 | 2018-06-04 | Pd-1に特異的に結合する抗体、及び使用方法 |
Country Status (23)
| Country | Link |
|---|---|
| US (3) | US10995149B2 (ja) |
| EP (1) | EP3634995A4 (ja) |
| JP (1) | JP7235733B2 (ja) |
| KR (1) | KR20200014414A (ja) |
| CN (1) | CN110997712B (ja) |
| AU (1) | AU2018282094A1 (ja) |
| BR (1) | BR112019025574A2 (ja) |
| CA (1) | CA3065516A1 (ja) |
| CL (1) | CL2019003520A1 (ja) |
| CO (1) | CO2019013935A2 (ja) |
| CR (1) | CR20190550A (ja) |
| EC (1) | ECSP19086810A (ja) |
| IL (1) | IL271009A (ja) |
| MA (1) | MA52459A (ja) |
| MX (1) | MX2019014577A (ja) |
| NI (1) | NI201900123A (ja) |
| PE (1) | PE20200294A1 (ja) |
| PH (1) | PH12019502755A1 (ja) |
| TW (1) | TWI806873B (ja) |
| UA (1) | UA128035C2 (ja) |
| UY (1) | UY37761A (ja) |
| WO (1) | WO2018226580A2 (ja) |
| ZA (1) | ZA202000051B (ja) |
Families Citing this family (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA3065125A1 (en) * | 2017-06-02 | 2018-12-06 | Bayer Aktiengesellschaft | Combination of regorafenib and pd-1/pd-l1(2) inhibitors for treating cancer |
| AR114127A1 (es) | 2018-03-02 | 2020-07-22 | Lilly Co Eli | Anticuerpos agonistas contra pd-1 y usos de estos |
| US20220298211A1 (en) * | 2019-06-04 | 2022-09-22 | Qiang Chen | PLANT-PRODUCED mABs AGAINST CHIKUNGUNYA VIRUS WITH ENHANCED EFFECTOR FUNCTION AND EFFICACY |
| KR20220030956A (ko) | 2019-07-05 | 2022-03-11 | 오노 야꾸힝 고교 가부시키가이샤 | Pd-1/cd3 이중 특이성 단백질에 의한 혈액암 치료 |
| JP6856183B1 (ja) * | 2019-07-30 | 2021-04-07 | 小野薬品工業株式会社 | 二重特異性抗体 |
| WO2021025140A1 (ja) | 2019-08-08 | 2021-02-11 | 小野薬品工業株式会社 | 二重特異性タンパク質 |
| CN115956087A (zh) | 2020-05-26 | 2023-04-11 | 勃林格殷格翰国际有限公司 | 抗-pd-1抗体 |
| WO2022156773A1 (en) * | 2021-01-21 | 2022-07-28 | Biocytogen Pharmaceuticals (Beijing) Co., Ltd | Protein complexes targeting il12 pathway |
| AU2022272835A1 (en) | 2021-05-13 | 2023-11-02 | Foundation For Biomedical Research And Innovation At Kobe | Anti-human pd-1 agonist antibody and pharmaceutical composition comprising the antibody for treating or preventing inflammatory diseases |
| AU2022294106A1 (en) * | 2021-06-18 | 2024-01-25 | Therini Bio, Inc. | ANTIBODIES WHICH BIND HUMAN FIBRIN OR FIBRINOGEN γC DOMAIN AND METHODS OF USE |
| WO2023089377A2 (en) | 2021-11-19 | 2023-05-25 | Mirobio Limited | Engineered pd-1 antibodies and uses thereof |
| WO2024010861A2 (en) * | 2022-07-06 | 2024-01-11 | Santa Ana Bio, Inc. | Methods and compositions for treating autoimmune, allergic and inflammatory diseases |
| CN116854820B (zh) * | 2023-06-26 | 2024-02-06 | 华中科技大学同济医学院附属协和医院 | Pd-1非阻断性清除抗体及其用途 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013521769A (ja) | 2010-03-11 | 2013-06-13 | ユセベ ファルマ ソシエテ アノニム | 生物学的製剤:ヒト化アゴニスト抗pd−1抗体 |
| WO2015058573A1 (zh) | 2013-10-25 | 2015-04-30 | 苏州思坦维生物技术有限责任公司 | 拮抗抑制程序性死亡受体pd-1与其配体结合的单克隆抗体及其编码序列与用途 |
Family Cites Families (62)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4683195A (en) | 1986-01-30 | 1987-07-28 | Cetus Corporation | Process for amplifying, detecting, and/or-cloning nucleic acid sequences |
| US5225539A (en) | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| EP0281604B1 (en) | 1986-09-02 | 1993-03-31 | Enzon Labs Inc. | Single polypeptide chain binding molecules |
| GB8823869D0 (en) | 1988-10-12 | 1988-11-16 | Medical Res Council | Production of antibodies |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| IL162181A (en) | 1988-12-28 | 2006-04-10 | Pdl Biopharma Inc | A method of producing humanized immunoglubulin, and polynucleotides encoding the same |
| US6150584A (en) | 1990-01-12 | 2000-11-21 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| US6255458B1 (en) | 1990-08-29 | 2001-07-03 | Genpharm International | High affinity human antibodies and human antibodies against digoxin |
| ES2206447T3 (es) | 1991-06-14 | 2004-05-16 | Genentech, Inc. | Anticuerpo humanizado para heregulina. |
| US5635483A (en) | 1992-12-03 | 1997-06-03 | Arizona Board Of Regents Acting On Behalf Of Arizona State University | Tumor inhibiting tetrapeptide bearing modified phenethyl amides |
| JP3720353B2 (ja) | 1992-12-04 | 2005-11-24 | メディカル リサーチ カウンシル | 多価および多重特異性の結合タンパク質、それらの製造および使用 |
| US5780588A (en) | 1993-01-26 | 1998-07-14 | Arizona Board Of Regents | Elucidation and synthesis of selected pentapeptides |
| AUPO591797A0 (en) | 1997-03-27 | 1997-04-24 | Commonwealth Scientific And Industrial Research Organisation | High avidity polyvalent and polyspecific reagents |
| EP1724282B1 (en) | 1997-05-21 | 2013-05-15 | Merck Patent GmbH | Method for the production of non-immunogenic proteins |
| US6818749B1 (en) | 1998-10-31 | 2004-11-16 | The United States Of America As Represented By The Department Of Health And Human Services | Variants of humanized anti carcinoma monoclonal antibody cc49 |
| US6596541B2 (en) | 2000-10-31 | 2003-07-22 | Regeneron Pharmaceuticals, Inc. | Methods of modifying eukaryotic cells |
| JP3523245B1 (ja) | 2000-11-30 | 2004-04-26 | メダレックス,インコーポレーテッド | ヒト抗体作製用トランスジェニック染色体導入齧歯動物 |
| AR036993A1 (es) | 2001-04-02 | 2004-10-20 | Wyeth Corp | Uso de agentes que modulan la interaccion entre pd-1 y sus ligandos en la submodulacion de respuestas inmunologicas |
| US6884869B2 (en) | 2001-04-30 | 2005-04-26 | Seattle Genetics, Inc. | Pentapeptide compounds and uses related thereto |
| WO2004006955A1 (en) | 2001-07-12 | 2004-01-22 | Jefferson Foote | Super humanized antibodies |
| US10011858B2 (en) | 2005-03-31 | 2018-07-03 | Chugai Seiyaku Kabushiki Kaisha | Methods for producing polypeptides by regulating polypeptide association |
| DE102005028778A1 (de) | 2005-06-22 | 2006-12-28 | SUNJÜT Deutschland GmbH | Mehrlagige Folie mit einer Barriere- und einer antistatischen Lage |
| JP2009541275A (ja) | 2006-06-22 | 2009-11-26 | ノボ・ノルデイスク・エー/エス | 二重特異性抗体の生産 |
| US20080226635A1 (en) | 2006-12-22 | 2008-09-18 | Hans Koll | Antibodies against insulin-like growth factor I receptor and uses thereof |
| JP2010535032A (ja) | 2007-07-31 | 2010-11-18 | メディミューン,エルエルシー | 多重特異性エピトープ結合性タンパク質およびその用途 |
| US8748356B2 (en) | 2007-10-19 | 2014-06-10 | Janssen Biotech, Inc. | Methods for use in human-adapting monoclonal antibodies |
| CN101970730A (zh) | 2007-12-19 | 2011-02-09 | 森托科尔奥索生物科技公司 | 通过融合到pⅨ或pⅦ来设计和生成人从头pⅨ噬菌体展示文库,载体、抗体及方法 |
| US20090162359A1 (en) | 2007-12-21 | 2009-06-25 | Christian Klein | Bivalent, bispecific antibodies |
| US8227577B2 (en) | 2007-12-21 | 2012-07-24 | Hoffman-La Roche Inc. | Bivalent, bispecific antibodies |
| US8242247B2 (en) | 2007-12-21 | 2012-08-14 | Hoffmann-La Roche Inc. | Bivalent, bispecific antibodies |
| US9266967B2 (en) | 2007-12-21 | 2016-02-23 | Hoffmann-La Roche, Inc. | Bivalent, bispecific antibodies |
| WO2010029434A1 (en) | 2008-09-12 | 2010-03-18 | Isis Innovation Limited | Pd-1 specific antibodies and uses thereof |
| AU2009290544B2 (en) | 2008-09-12 | 2015-07-16 | Oxford University Innovation Limited | PD-1 specific antibodies and uses thereof |
| EP2347038A4 (en) | 2008-10-14 | 2013-06-12 | Janssen Biotech Inc | METHOD FOR HUMANIZATION AND AFFINITY TREATMENT OF ANTIBODIES |
| CN102459346B (zh) | 2009-04-27 | 2016-10-26 | 昂考梅德药品有限公司 | 制造异源多聚体分子的方法 |
| JP5920929B2 (ja) | 2010-03-11 | 2016-05-18 | ユセベ ファルマ ソシエテ アノニム | Pd−1抗体 |
| US9150663B2 (en) | 2010-04-20 | 2015-10-06 | Genmab A/S | Heterodimeric antibody Fc-containing proteins and methods for production thereof |
| AU2011325833C1 (en) | 2010-11-05 | 2017-07-13 | Zymeworks Bc Inc. | Stable heterodimeric antibody design with mutations in the Fc domain |
| EP2643351A1 (en) | 2010-11-24 | 2013-10-02 | Glaxo Group Limited | Multispecific antigen binding proteins targeting hgf |
| WO2013063702A1 (en) | 2011-11-04 | 2013-05-10 | Zymeworks Inc. | Stable heterodimeric antibody design with mutations in the fc domain |
| LT2970980T (lt) | 2013-03-15 | 2018-10-25 | Janssen Biotech, Inc. | Gamybos būdas kontroliuoti c galinio lizino, galaktozės ir sialo rūgšties kiekį rekombinantiniuose baltymuose |
| RS59480B1 (sr) | 2013-12-12 | 2019-12-31 | Shanghai hengrui pharmaceutical co ltd | Pd-1 antitelo, njegov fragment koji se vezuje na antigen, i njegova medicinska primena |
| CA2932476A1 (en) | 2013-12-12 | 2015-06-18 | Stemcentrx, Inc. | Novel anti-dpep3 antibodies and methods of use |
| TWI681969B (zh) | 2014-01-23 | 2020-01-11 | 美商再生元醫藥公司 | 針對pd-1的人類抗體 |
| JOP20200094A1 (ar) | 2014-01-24 | 2017-06-16 | Dana Farber Cancer Inst Inc | جزيئات جسم مضاد لـ pd-1 واستخداماتها |
| CN106232626B (zh) * | 2014-03-27 | 2022-05-03 | 鸟石生物公司 | 结合人大麻素1(cb1)受体的抗体 |
| PT3177644T (pt) * | 2014-08-05 | 2021-01-13 | MabQuest SA | Reagentes imunológicos que se ligam a pd-1 |
| TWI595006B (zh) * | 2014-12-09 | 2017-08-11 | 禮納特神經系統科學公司 | 抗pd-1抗體類和使用彼等之方法 |
| US10239942B2 (en) | 2014-12-22 | 2019-03-26 | Pd-1 Acquisition Group, Llc | Anti-PD-1 antibodies |
| TW201710286A (zh) | 2015-06-15 | 2017-03-16 | 艾伯維有限公司 | 抗vegf、pdgf及/或其受體之結合蛋白 |
| KR20180034588A (ko) | 2015-07-30 | 2018-04-04 | 마크로제닉스, 인크. | Pd-1-결합 분자 및 그것의 사용 방법 |
| CA2993276A1 (en) | 2015-08-11 | 2017-02-16 | Yong Zheng | Novel anti-pd-1 antibodies |
| EA201890630A1 (ru) | 2015-09-01 | 2018-10-31 | Эйдженус Инк. | Антитела против pd-1 и способы их применения |
| EA201890790A1 (ru) * | 2015-09-29 | 2018-10-31 | Селджин Корпорейшн | Связывающие pd-1 белки и способы их применения |
| BR112018008904A2 (pt) | 2015-11-03 | 2018-11-27 | Janssen Biotech Inc | anticorpos que se ligam especificamente a tim-3 e seus usos |
| RU2656181C1 (ru) | 2016-07-13 | 2018-05-31 | Закрытое Акционерное Общество "Биокад" | Анти-pd-1-антитела, способ их получения и способ применения |
| HUE051700T2 (hu) | 2016-09-14 | 2021-03-29 | Abbvie Biotherapeutics Inc | Anti-PD-1 antitestek |
| WO2018053405A1 (en) | 2016-09-19 | 2018-03-22 | Celgene Corporation | Methods of treating immune disorders using pd-1 binding proteins |
| US11225523B2 (en) | 2017-06-01 | 2022-01-18 | Compugen Ltd. | Triple combination antibody therapies |
| EP3679070A1 (en) | 2017-09-07 | 2020-07-15 | Augusta University Research Institute, Inc. | Antibodies to programmed cell death protein 1 |
| AR114127A1 (es) | 2018-03-02 | 2020-07-22 | Lilly Co Eli | Anticuerpos agonistas contra pd-1 y usos de estos |
-
2018
- 2018-06-04 EP EP18813493.6A patent/EP3634995A4/en active Pending
- 2018-06-04 JP JP2020516792A patent/JP7235733B2/ja active Active
- 2018-06-04 CR CR20190550A patent/CR20190550A/es unknown
- 2018-06-04 US US15/997,148 patent/US10995149B2/en active Active
- 2018-06-04 CN CN201880050979.XA patent/CN110997712B/zh active Active
- 2018-06-04 UA UAA201912296A patent/UA128035C2/uk unknown
- 2018-06-04 AU AU2018282094A patent/AU2018282094A1/en active Pending
- 2018-06-04 WO PCT/US2018/035843 patent/WO2018226580A2/en active Application Filing
- 2018-06-04 KR KR1020207000242A patent/KR20200014414A/ko not_active Application Discontinuation
- 2018-06-04 CA CA3065516A patent/CA3065516A1/en active Pending
- 2018-06-04 PE PE2019002510A patent/PE20200294A1/es unknown
- 2018-06-04 BR BR112019025574-5A patent/BR112019025574A2/pt unknown
- 2018-06-04 MX MX2019014577A patent/MX2019014577A/es unknown
- 2018-06-04 MA MA052459A patent/MA52459A/fr unknown
- 2018-06-05 UY UY0001037761A patent/UY37761A/es unknown
- 2018-06-05 TW TW107119358A patent/TWI806873B/zh active
-
2019
- 2019-11-28 IL IL271009A patent/IL271009A/en unknown
- 2019-12-02 CL CL2019003520A patent/CL2019003520A1/es unknown
- 2019-12-04 NI NI201900123A patent/NI201900123A/es unknown
- 2019-12-05 PH PH12019502755A patent/PH12019502755A1/en unknown
- 2019-12-05 EC ECSENADI201986810A patent/ECSP19086810A/es unknown
- 2019-12-11 CO CONC2019/0013935A patent/CO2019013935A2/es unknown
-
2020
- 2020-01-03 ZA ZA2020/00051A patent/ZA202000051B/en unknown
- 2020-12-17 US US17/125,263 patent/US11746161B2/en active Active
-
2023
- 2023-06-08 US US18/331,280 patent/US20230340155A1/en active Pending
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013521769A (ja) | 2010-03-11 | 2013-06-13 | ユセベ ファルマ ソシエテ アノニム | 生物学的製剤:ヒト化アゴニスト抗pd−1抗体 |
| WO2015058573A1 (zh) | 2013-10-25 | 2015-04-30 | 苏州思坦维生物技术有限责任公司 | 拮抗抑制程序性死亡受体pd-1与其配体结合的单克隆抗体及其编码序列与用途 |
Non-Patent Citations (2)
| Title |
|---|
| Hideaki Fujiwara et al.,Programmed Death-1 Pathway in Host Tissues Ameliorates Th17/Th1-Mediated Experimental Chronic Graft-versus-Host Disease,Journal of Immunology,2014年,Vol.193、No.5,p. 2565-2573 |
| ProteOn XPR36 分子間相互作用アレイシステム,2020年,https://www.bio-rad.com/ja-jp/product/proteon-xpr36-protein-interaction-array-system?ID=ea380548-08ca-4b4e-896b-87e5580ac411,[令和4年9月27日検索] |
Also Published As
| Publication number | Publication date |
|---|---|
| US10995149B2 (en) | 2021-05-04 |
| CN110997712B (zh) | 2024-03-19 |
| CO2019013935A2 (es) | 2020-01-17 |
| EP3634995A4 (en) | 2021-06-09 |
| EP3634995A2 (en) | 2020-04-15 |
| KR20200014414A (ko) | 2020-02-10 |
| ECSP19086810A (es) | 2020-02-28 |
| MA52459A (fr) | 2021-03-10 |
| CR20190550A (es) | 2020-04-05 |
| US20230340155A1 (en) | 2023-10-26 |
| TWI806873B (zh) | 2023-07-01 |
| WO2018226580A3 (en) | 2019-01-31 |
| PH12019502755A1 (en) | 2020-06-08 |
| CL2019003520A1 (es) | 2020-05-08 |
| WO2018226580A2 (en) | 2018-12-13 |
| PE20200294A1 (es) | 2020-02-05 |
| MX2019014577A (es) | 2020-07-29 |
| UY37761A (es) | 2019-01-02 |
| JP2020522278A (ja) | 2020-07-30 |
| ZA202000051B (en) | 2021-07-28 |
| TW201906863A (zh) | 2019-02-16 |
| US20180355061A1 (en) | 2018-12-13 |
| UA128035C2 (uk) | 2024-03-20 |
| BR112019025574A2 (pt) | 2020-06-23 |
| IL271009A (en) | 2020-01-30 |
| US11746161B2 (en) | 2023-09-05 |
| US20210102000A1 (en) | 2021-04-08 |
| NI201900123A (es) | 2020-12-01 |
| AU2018282094A1 (en) | 2019-12-12 |
| CA3065516A1 (en) | 2018-12-13 |
| CN110997712A (zh) | 2020-04-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7235733B2 (ja) | Pd-1に特異的に結合する抗体、及び使用方法 | |
| US20190048089A1 (en) | Antagonistic Antibodies Specifically Binding Human CD40 and Methods of Use | |
| US20180355043A1 (en) | Antibodies Specifically Binding HLA-DR and Their Uses | |
| US20240124583A1 (en) | Proteins Comprising Kallikrein Related Paptidase 2 Antigen Binding Domains And Their Uses | |
| TW202304987A (zh) | 包含cd3抗原結合域之蛋白質及其用途 | |
| US20240025992A1 (en) | Proteins comprising delta-like ligand 3 (dll3) antigen binding domains and their uses | |
| US20220411504A1 (en) | Proteins comprising cd3 antigen binding domains and uses thereof | |
| EA043064B1 (ru) | Антитела, специфически связывающиеся с pd-1, и способы их применения | |
| WO2020089769A1 (en) | Antibodies specifically binding hla-dr/colii_259 complex and their uses | |
| JP2024510200A (ja) | 自己免疫治療用途のためのcd79b抗体の使用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210601 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210601 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20220318 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220405 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20220704 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220905 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20221011 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230111 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230207 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230224 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7235733 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |