JP7110979B2 - 化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 - Google Patents
化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 Download PDFInfo
- Publication number
- JP7110979B2 JP7110979B2 JP2018528904A JP2018528904A JP7110979B2 JP 7110979 B2 JP7110979 B2 JP 7110979B2 JP 2018528904 A JP2018528904 A JP 2018528904A JP 2018528904 A JP2018528904 A JP 2018528904A JP 7110979 B2 JP7110979 B2 JP 7110979B2
- Authority
- JP
- Japan
- Prior art keywords
- group
- formula
- carbon atoms
- compound
- acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/78—Ring systems having three or more relevant rings
- C07D311/80—Dibenzopyrans; Hydrogenated dibenzopyrans
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C39/00—Compounds having at least one hydroxy or O-metal group bound to a carbon atom of a six-membered aromatic ring
- C07C39/12—Compounds having at least one hydroxy or O-metal group bound to a carbon atom of a six-membered aromatic ring polycyclic with no unsaturation outside the aromatic rings
- C07C39/15—Compounds having at least one hydroxy or O-metal group bound to a carbon atom of a six-membered aromatic ring polycyclic with no unsaturation outside the aromatic rings with all hydroxy groups on non-condensed rings, e.g. phenylphenol
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C43/00—Ethers; Compounds having groups, groups or groups
- C07C43/02—Ethers
- C07C43/20—Ethers having an ether-oxygen atom bound to a carbon atom of a six-membered aromatic ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C43/00—Ethers; Compounds having groups, groups or groups
- C07C43/02—Ethers
- C07C43/20—Ethers having an ether-oxygen atom bound to a carbon atom of a six-membered aromatic ring
- C07C43/205—Ethers having an ether-oxygen atom bound to a carbon atom of a six-membered aromatic ring the aromatic ring being a non-condensed ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C43/00—Ethers; Compounds having groups, groups or groups
- C07C43/02—Ethers
- C07C43/20—Ethers having an ether-oxygen atom bound to a carbon atom of a six-membered aromatic ring
- C07C43/205—Ethers having an ether-oxygen atom bound to a carbon atom of a six-membered aromatic ring the aromatic ring being a non-condensed ring
- C07C43/2055—Ethers having an ether-oxygen atom bound to a carbon atom of a six-membered aromatic ring the aromatic ring being a non-condensed ring containing more than one ether bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C43/00—Ethers; Compounds having groups, groups or groups
- C07C43/02—Ethers
- C07C43/20—Ethers having an ether-oxygen atom bound to a carbon atom of a six-membered aromatic ring
- C07C43/215—Ethers having an ether-oxygen atom bound to a carbon atom of a six-membered aromatic ring having unsaturation outside the six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/78—Ring systems having three or more relevant rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D311/00—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings
- C07D311/02—Heterocyclic compounds containing six-membered rings having one oxygen atom as the only hetero atom, condensed with other rings ortho- or peri-condensed with carbocyclic rings or ring systems
- C07D311/78—Ring systems having three or more relevant rings
- C07D311/80—Dibenzopyrans; Hydrogenated dibenzopyrans
- C07D311/82—Xanthenes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F12/00—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, each having only one carbon-to-carbon double bond, and at least one being terminated by an aromatic carbocyclic ring
- C08F12/02—Monomers containing only one unsaturated aliphatic radical
- C08F12/04—Monomers containing only one unsaturated aliphatic radical containing one ring
- C08F12/14—Monomers containing only one unsaturated aliphatic radical containing one ring substituted by hetero atoms or groups containing heteroatoms
- C08F12/22—Oxygen
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G8/00—Condensation polymers of aldehydes or ketones with phenols only
- C08G8/04—Condensation polymers of aldehydes or ketones with phenols only of aldehydes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G8/00—Condensation polymers of aldehydes or ketones with phenols only
- C08G8/04—Condensation polymers of aldehydes or ketones with phenols only of aldehydes
- C08G8/08—Condensation polymers of aldehydes or ketones with phenols only of aldehydes of formaldehyde, e.g. of formaldehyde formed in situ
- C08G8/10—Condensation polymers of aldehydes or ketones with phenols only of aldehydes of formaldehyde, e.g. of formaldehyde formed in situ with phenol
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G8/00—Condensation polymers of aldehydes or ketones with phenols only
- C08G8/04—Condensation polymers of aldehydes or ketones with phenols only of aldehydes
- C08G8/08—Condensation polymers of aldehydes or ketones with phenols only of aldehydes of formaldehyde, e.g. of formaldehyde formed in situ
- C08G8/20—Condensation polymers of aldehydes or ketones with phenols only of aldehydes of formaldehyde, e.g. of formaldehyde formed in situ with polyhydric phenols
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G8/00—Condensation polymers of aldehydes or ketones with phenols only
- C08G8/28—Chemically modified polycondensates
- C08G8/36—Chemically modified polycondensates by etherifying
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/0008—Organic ingredients according to more than one of the "one dot" groups of C08K5/01 - C08K5/59
- C08K5/0025—Crosslinking or vulcanising agents; including accelerators
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/027—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds
- G03F7/028—Non-macromolecular photopolymerisable compounds having carbon-to-carbon double bonds, e.g. ethylenic compounds with photosensitivity-increasing substances, e.g. photoinitiators
- G03F7/031—Organic compounds not covered by group G03F7/029
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/09—Photosensitive materials characterised by structural details, e.g. supports, auxiliary layers
- G03F7/11—Photosensitive materials characterised by structural details, e.g. supports, auxiliary layers having cover layers or intermediate layers, e.g. subbing layers
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/20—Exposure; Apparatus therefor
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/26—Processing photosensitive materials; Apparatus therefor
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L21/00—Processes or apparatus adapted for the manufacture or treatment of semiconductor or solid state devices or of parts thereof
- H01L21/02—Manufacture or treatment of semiconductor devices or of parts thereof
- H01L21/027—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34
- H01L21/0271—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34 comprising organic layers
- H01L21/0273—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34 comprising organic layers characterised by the treatment of photoresist layers
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L21/00—Processes or apparatus adapted for the manufacture or treatment of semiconductor or solid state devices or of parts thereof
- H01L21/02—Manufacture or treatment of semiconductor devices or of parts thereof
- H01L21/04—Manufacture or treatment of semiconductor devices or of parts thereof the devices having at least one potential-jump barrier or surface barrier, e.g. PN junction, depletion layer or carrier concentration layer
- H01L21/18—Manufacture or treatment of semiconductor devices or of parts thereof the devices having at least one potential-jump barrier or surface barrier, e.g. PN junction, depletion layer or carrier concentration layer the devices having semiconductor bodies comprising elements of Group IV of the Periodic System or AIIIBV compounds with or without impurities, e.g. doping materials
- H01L21/30—Treatment of semiconductor bodies using processes or apparatus not provided for in groups H01L21/20 - H01L21/26
Description
そこで、これまでに、より解像性の高いレジストパターンを与えるために、種々の低分子量レジスト材料が提案されている。低分子量レジスト材料は分子サイズが小さいことから、解像性が高く、ラフネスが小さいレジストパターンを与えることが期待される。
さらに光学部品形成組成物として、様々なものが提案されている。例えば、アクリル系樹脂が挙げられる(例えば、下記特許文献13~14参照)。
また、従来数多くの光学部材向け組成物が提案されているが、耐熱性、透明性及び屈折率を高い次元で両立させたものはなく、新たな材料の開発が求められている。
すなわち、本発明は、次のとおりである。
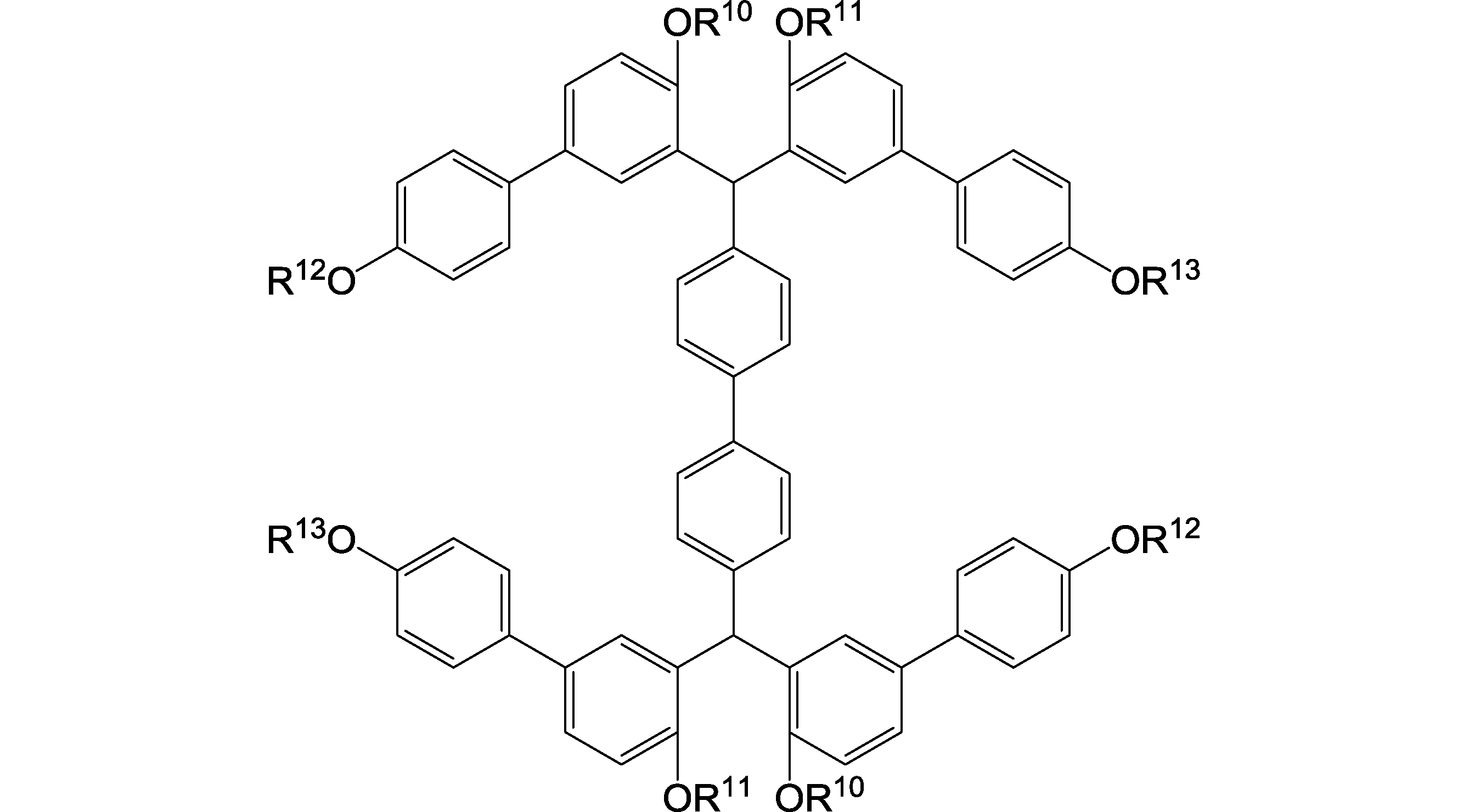
<1> 下記式(0)で表される、化合物。
(式(0)中、RYは、水素原子、炭素数1~30のアルキル基又は炭素数6~30のアリール基であり、
RZは、炭素数1~60のN価の基又は単結合であり、
RTは、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、置換基を有していてもよい炭素数1~30のアルコキシ基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基、水酸基又は水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、前記アルキル基、前記アリール基、前記アルケニル基、前記アルコキシ基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、ここで、RTの少なくとも1つは、水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、
Xは、酸素原子、硫黄原子又は無架橋であることを表し、
Mは、各々独立して0~9の整数であり、ここで、mの少なくとも1つは1~9の整数であり、
Nは、1~4の整数であり、Nが2以上の整数の場合、N個の[ ]内の構造式は同一であっても異なっていてもよく、
Rは、各々独立して0~2の整数である。)
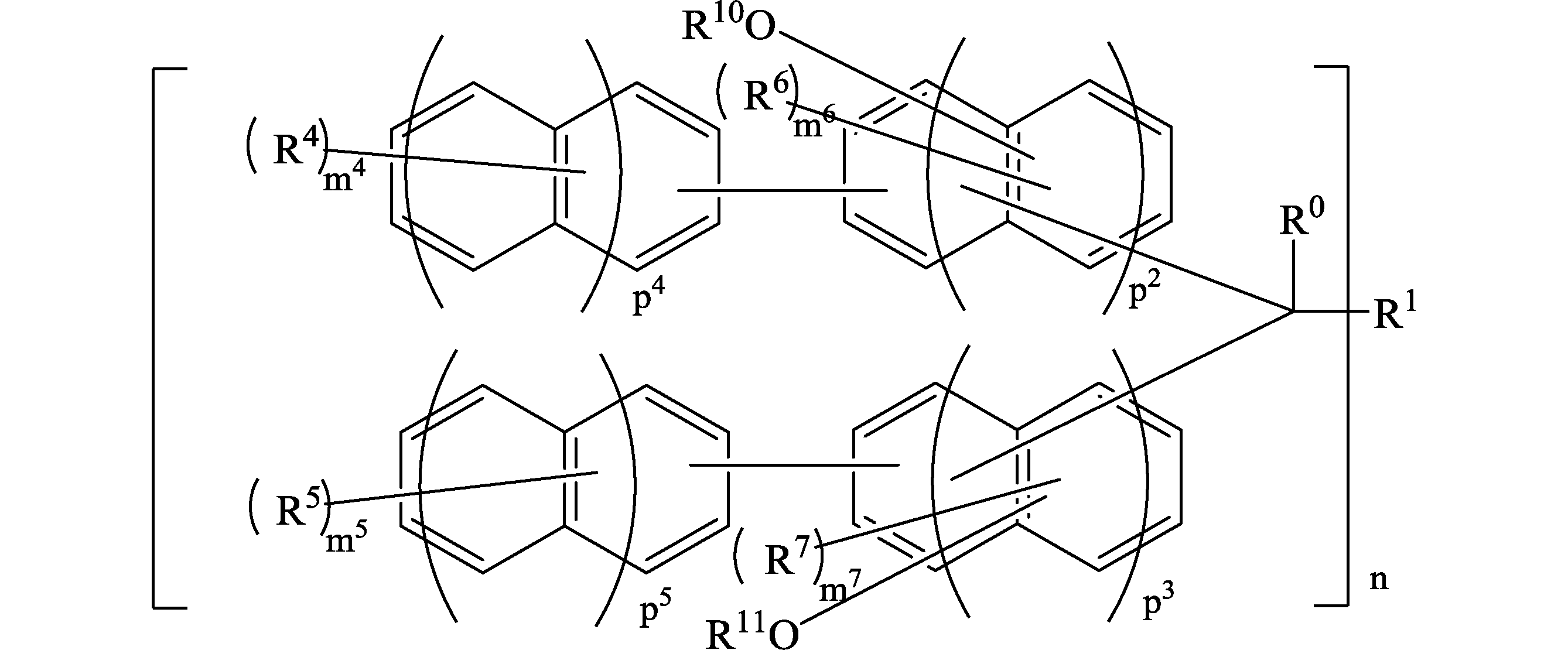
<2> 前記式(0)で表される化合物が下記式(1)で表される化合物である、前記<1>に記載の化合物。
(式(1)中、R0は、前記RYと同義であり、
R1は、炭素数1~60のn価の基又は単結合であり、
R2~R5は、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、置換基を有していてもよい炭素数1~30のアルコキシ基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基、水酸基又は水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、前記アルキル基、前記アリール基、前記アルケニル基、前記アルコキシ基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、ここで、R2~R5の少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、
M2及びm3は、各々独立して、0~8の整数であり、
M4及びm5は、各々独立して、0~9の整数であり、
但し、m2、m3、m4及びm5は同時に0となることはなく、
Nは前記Nと同義であり、ここで、nが2以上の整数の場合、n個の[ ]内の構造式は同一であっても異なっていてもよく、
P2~p5は、前記rと同義である。)
<3> 前記式(0)で表される化合物が下記式(2)で表される化合物である、前記<1>に記載の化合物。
(式(2)中、R0Aは、前記RYと同義であり、
R1Aは、炭素数1~60のna価の基又は単結合であり、
R2Aは、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、置換基を有していてもよい炭素数1~30のアルコキシ基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基、水酸基又は水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、前記アルキル基、前記アリール基、前記アルケニル基、前記アルコキシ基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、ここで、R2Aの少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、
Naは、前記Nと同義であり、ここで、naが2以上の整数の場合、na個の[ ]内の構造式は同一であっても異なっていてもよく、
XAは、前記Xと同義あり、
M2aは、各々独立して、0~7の整数であり、但し、少なくとも1つのm2aは1~7の整数であり、
Qaは、各々独立して、0又は1である。)
<4> 前記式(1)で表される化合物が下記式(1-1)で表される化合物である、前記<2>に記載の化合物。
(式(1-1)中、R0、R1、R4、R5、n、p2~p5、m4及びm5は、前記と同義であり、
R6~R7は、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基であり、
R10~R11は、各々独立して、水素原子又は含ビニルフェニルメチル基であり、
ここで、R10~R11の少なくとも1つは含ビニルフェニルメチル基であり、
M6及びm7は、各々独立して、0~7の整数であり、
但し、m4、m5、m6及びm7は同時に0となることはない。)
<5> 前記式(1-1)で表される化合物が下記式(1-2)で表される化合物である、前記<4>に記載の化合物。
(式(1-2)中、R0、R1、R6、R7、R10、R11、n、p2~p5、m6及びm7は、前記と同義であり、
R8~R9は、前記R6~R7と同義であり、
R12~R13は、前記R10~R11と同義であり、
M8及びm9は、各々独立して、0~8の整数であり、
但し、m6、m7、m8及びm9は同時に0となることはない。)
<6> 前記式(2)で表される化合物が下記式(2-1)で表される化合物である、前記<3>に記載の化合物。
(式(2-1)中、R0A、R1A、na、qa及びXA、は、前記式(2)で説明したものと同義である。
R3Aは、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基であり、
R4Aは、各々独立して、水素原子又は含ビニルフェニルメチル基であり、
ここで、R4Aの少なくとも1つは含ビニルフェニルメチル基であり、
M6aは、各々独立して、0~5の整数である。)
<7> 前記<1>に記載の化合物をモノマーとして得られる、樹脂。
<8> 下記式(3)で表される構造を有する、前記<7>に記載の樹脂。
(式(3)中、Lは、置換基を有していてもよい炭素数1~30のアルキレン基、置換基を有していてもよい炭素数6~30のアリーレン基、置換基を有していてもよい炭素数1~30のアルコキシレン基又は単結合であり、前記アルキレン基、前記アリーレン基、前記アルコキシレン基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、
R0は、前記RYと同義であり、
R1は、炭素数1~60のn価の基又は単結合であり、
R2~R5は、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、置換基を有していてもよい炭素数1~30のアルコキシ基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基、水酸基又は水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、前記アルキル基、前記アリール基、前記アルケニル基、前記アルコキシ基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、
M2及びm3は、各々独立して、0~8の整数であり、
M4及びm5は、各々独立して、0~9の整数であり、
但し、m2、m3、m4及びm5は同時に0となることはなく、R2~R5の少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基である。
Nは前記Nと同義であり、ここで、nが2以上の整数の場合、n個の[ ]内の構造式は同一であっても異なっていてもよく、
P2~p5は、前記rと同義である。)
<9> 下記式(4)で表される構造を有する、前記<7>に記載の樹脂。
(式(4)中、Lは、置換基を有していてもよい炭素数1~30のアルキレン基、置換基を有していてもよい炭素数6~30のアリーレン基、置換基を有していてもよい炭素数1~30のアルコキシレン基又は単結合であり、前記アルキレン基、前記アリーレン基、前記アルコキシレン基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、
R0Aは、前記RYと同義であり、
R1Aは、炭素数1~30のna価の基又は単結合であり、
R2Aは、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、置換基を有していてもよい炭素数1~30のアルコキシ基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基、水酸基又は水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、前記アルキル基、前記アリール基、前記アルケニル基、前記アルコキシ基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、ここで、R2Aの少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、
Naは、前記Nと同義であり、ここで、naが2以上の整数の場合、na個の[ ]内の構造式は同一であっても異なっていてもよく、
XAは、前記Xと同義あり、
M2aは、各々独立して、0~7の整数であり、但し、少なくとも1つのm2aは1~6の整数であり、
Qaは、各々独立して、0又は1である。)
<10> 前記<1>~<6>のいずれか一つに記載の化合物及び前記<7>~<9>のいずれか一つに記載の樹脂からなる群より選ばれる1種以上を含有する、組成物。
<11> 溶媒をさらに含有する、前記<10>に記載の組成物。
<12> 酸発生剤をさらに含有する、前記<10>又は前記<11>に記載の組成物。
<13> 架橋剤をさらに含有する、前記<10>~<12>のいずれか一つに記載の組成物。
<14> 前記架橋剤が、フェノール化合物、エポキシ化合物、シアネート化合物、アミノ化合物、ベンゾオキサジン化合物、メラミン化合物、グアナミン化合物、グリコールウリル化合物、ウレア化合物、イソシアネート化合物及びアジド化合物からなる群より選ばれる少なくとも1種である、前記<13>に記載の組成物。
<15> 前記架橋剤が、少なくとも1つのアリル基を有する、前記<13>又は<14>に記載の組成物。
<16> 前記架橋剤の含有量が、前記<1>~<6>のいずれか一つに記載の化合物及び前記<7>~<9>のいずれか一つに記載の樹脂からなる群より選ばれる1種以上を含有する組成物の合計質量100質量部に対し、0.1~100質量部である、前記<13>~<15>のいずれか一つに記載の組成物。
<17> 架橋促進剤をさらに含有する、前記<13>~<16>のいずれか一つに記載の組成物。
<18> 前記架橋促進剤が、アミン類、イミダゾール類、有機ホスフィン類、及びルイス酸からなる群より選ばれる少なくとも1種である、前記<17>に記載の組成物。
<19> 前記架橋促進剤の含有量が、前記<1>~<6>のいずれか一つに記載の化合物及び前記<7>~<9>のいずれか一つに記載の樹脂からなる群より選ばれる1種以上を含有する組成物の合計質量100質量部に対し、0.1~5質量部である、前記<17>又は<18>に記載の組成物。
<20> ラジカル重合開始剤をさらに含有する、前記<10>~<19>のいずれか一つに記載の組成物。
<21> 前記ラジカル重合開始剤が、ケトン系光重合開始剤、有機過酸化物系重合開始剤及びアゾ系重合開始剤からなる群より選ばれる少なくとも1種である、前記<10>~<20>のいずれか一つに記載の組成物。
<22> 前記ラジカル重合開始剤の含有量が、前記<1>~<6>のいずれか一つに記載の化合物及び前記<7>~<9>のいずれか一つに記載の樹脂からなる群より選ばれる1種以上を含有する組成物の合計質量100質量部に対し、0.05~25質量部である、前記<10>~<21>のいずれか一つに記載の組成物。
<23> リソグラフィー用膜形成に用いられる、前記<10>~<22>のいずれか一つに記載の組成物。
<24> レジスト永久膜形成に用いられる、前記<10>~<22>のいずれか一つに記載の組成物。
<25> 光学部品形成に用いられる、前記<10>~<22>のいずれか一つに記載の組成物。
<26> 基板上に、前記<23>に記載の組成物を用いてフォトレジスト層を形成した後、前記フォトレジスト層の所定の領域に放射線を照射し、現像を行う工程を含む、レジストパターン形成方法。
<27> 基板上に、前記<23>に記載の組成物を用いて下層膜を形成し、前記下層膜上に、少なくとも1層のフォトレジスト層を形成した後、前記フォトレジスト層の所定の領域に放射線を照射し、現像を行う工程を含む、レジストパターン形成方法。
<28> 基板上に、前記<23>に記載の組成物を用いて下層膜を形成し、前記下層膜上に、レジスト中間層膜材料を用いて中間層膜を形成し、前記中間層膜上に、少なくとも1層のフォトレジスト層を形成した後、前記フォトレジスト層の所定の領域に放射線を照射し、現像してレジストパターンを形成し、その後、前記レジストパターンをマスクとして前記中間層膜をエッチングし、得られた中間層膜パターンをエッチングマスクとして前記下層膜をエッチングし、得られた下層膜パターンをエッチングマスクとして基板をエッチングすることにより基板にパターンを形成する工程を含む、回路パターン形成方法。
<29>
下記式(5)で表される化合物。
(式(5)中、R5Aは、炭素数1~60のN価の基又は単結合であり、
M10は、各々独立して1~3の整数であり
NBは、1~4の整数であり、NBが2以上の整数の場合、N個の[ ]内の構造式は同一であっても異なっていてもよい。)
上述の組成物は、耐熱性が高く、溶媒溶解性も高い、特定構造を有する化合物又は樹脂を用いているため、高温ベーク時の膜の劣化が抑制され、酸素プラズマエッチング等に対するエッチング耐性にも優れたレジスト及び下層膜を形成することができる。加えて、下層膜を形成した場合、レジスト層との密着性にも優れるので、優れたレジストパターンを形成することができる。
さらに、上述の組成物は、屈折率が高く、また低温から高温までの広範囲の熱処理によって着色が抑制されることから、各種光学形成組成物としても有用である。
本実施形態の化合物は、下記式(0)で表される。
(式(0)中、RYは、水素原子、炭素数1~30のアルキル基又は炭素数6~30のアリール基であり、
RZは、炭素数1~60のN価の基又は単結合であり、
RTは、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、置換基を有していてもよい炭素数1~30のアルコキシ基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基、水酸基又は水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、前記アルキル基、前記アリール基、前記アルケニル基、前記アルコキシ基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、ここで、RTの少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、
Xは、酸素原子、硫黄原子又は無架橋であることを表し、
Mは、各々独立して0~9の整数であり、ここで、mの少なくとも1つは1~9の整数であり、
Nは、1~4の整数であり、Nが2以上の整数の場合、N個の[ ]内の構造式は同一であっても異なっていてもよく、
Rは、各々独立して0~2の整数である。)
またRYが、炭素数1~30の直鎖状、分岐状若しくは環状のアルキル基又は炭素数6~30のアリール基であると、更に、本化合物の酸化分解を抑制し着色を抑え、耐熱性が高く、溶媒溶解性を向上させる観点から好ましい。
ここで、「含ビニルフェニルメチル基」とは、ビニルフェニルメチル基を有する基であり、例えば、ビニルフェニルメチル基の他、ビニルフェニルメチルメチル基、ビニルフェニルメチルフェニル基等、酸素原子、アルキレン基、フェニレン基、オキシアルキレン基等にビニルフェニルメチル基が置換した基が挙げられる。
式(0)中、ナフタレン構造で示される部位は、r=0の場合には単環構造であり、r=1の場合には二環構造であり、r=2の場合には三環構造となる。Rは、各々独立して0~2の整数である。上述のmは、rで決定される環構造に応じてその数値範囲が決定される。
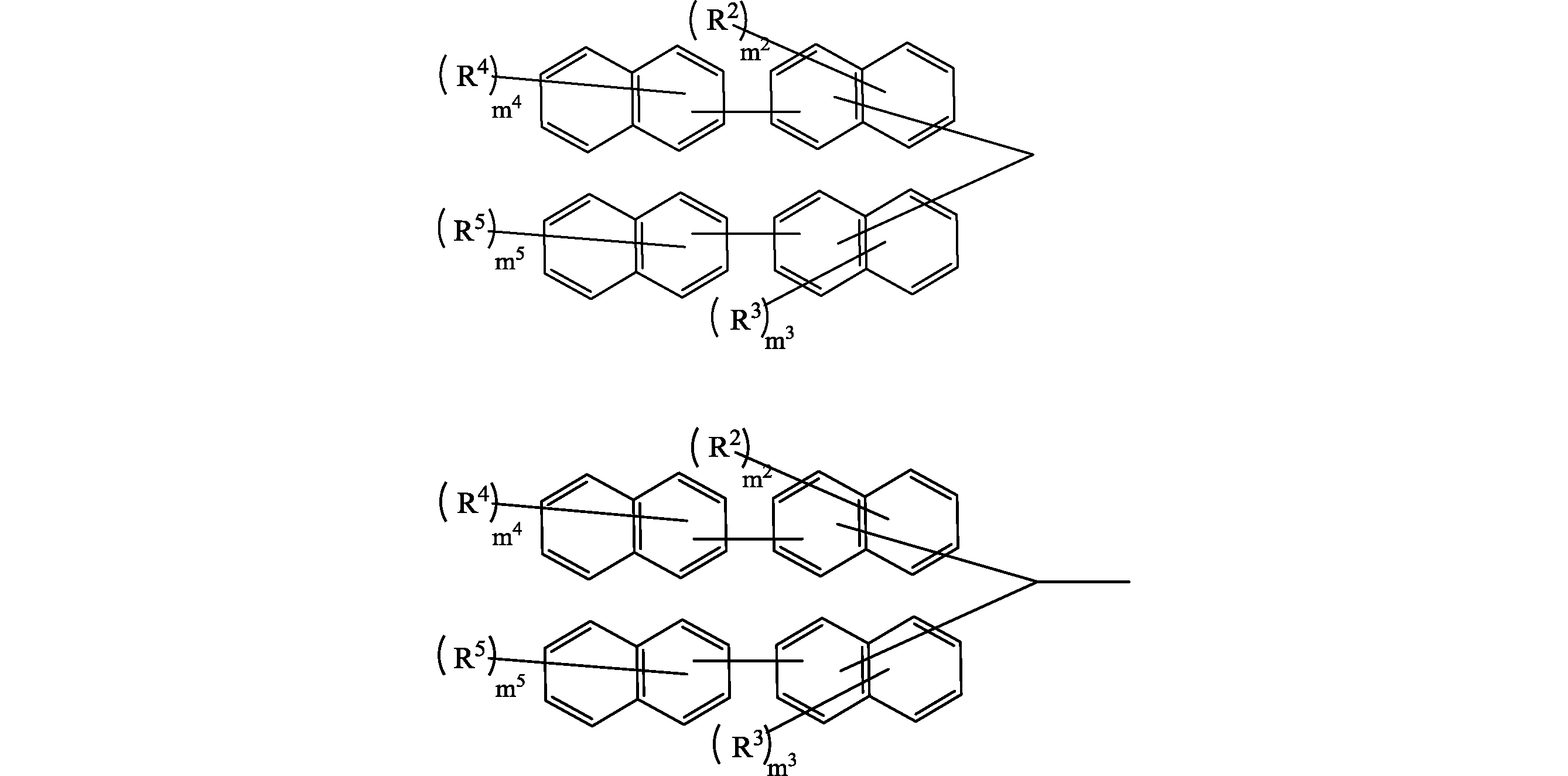
本実施形態の化合物は、下記式(1)で表されることが好ましい。式(1)で表される化合物は下記のように構成されているため、耐熱性が高く、溶媒溶解性も高い。
(式(1)中、R0は、前記RYと同義であり、
R1は、炭素数1~60のn価の基又は単結合であり、
R2~R5は、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、置換基を有していてもよい炭素数1~30のアルコキシ基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基、水酸基又は水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、前記アルキル基、前記アリール基、前記アルケニル基、前記アルコキシ基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、ここで、R2~R5の少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、m2及びm3は、各々独立して、0~8の整数であり、
M4及びm5は、各々独立して、0~9の整数であり、
但し、m2、m3、m4及びm5は同時に0となることはなく、
Nは前記Nと同義であり、ここで、nが2以上の整数の場合、n個の[ ]内の構造式は同一であっても異なっていてもよく、
P2~p5は、前記rと同義である。)
R1は炭素数1~60のn価の基又は単結合であり、このR1を介して各々の芳香環が結合している。Nは前記Nと同義であり、nが2以上の整数の場合、n個の[ ]内の構造式は同一であっても異なっていてもよい。なお、前記n価の基とは、n=1のときには、炭素数1~60のアルキル基、n=2のときには、炭素数1~60のアルキレン基、n=3のときには、炭素数2~60のアルカンプロパイル基、n=4のときには、炭素数3~60のアルカンテトライル基のことを示す。前記n価の基としては、例えば、直鎖状炭化水素基、分岐状炭化水素基又は脂環式炭化水素基を有するもの等が挙げられる。ここで、前記脂環式炭化水素基については、有橋脂環式炭化水素基も含まれる。また、前記n価の炭化水素基は、脂環式炭化水素基、二重結合、ヘテロ原子もしくは炭素数6~60の芳香族基を有していてもよい。
ここで、R10~R11の少なくとも1つは含ビニルフェニルメチル基であり、m6及びm7は、各々独立して0~7の整数である。但し、m4、m5、m6及びm7は同時に0となることはない。
但し、R2、R3、R4、R5から選ばれる少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基である。m2、m3、m4、m5が同時に0となることはない。
但し、R2、R3、R4、R5から選ばれる少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基である。m2、m3、m4、m5が同時に0となることはない。
但し、R2、R3、R4、R5から選ばれる少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、m2、m3、m4、m5が同時に0となることはない。
但し、R2、R3、R4、R5から選ばれる少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、m2、m3、m4、m5が同時に0となることはない。
R0は、例えば、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、ノニル基、デシル基、ウンデシル基、ドデシル基、トリアコンチル基、フェニル基、ナフチル基、アントラセン基、ピレニル基、ビフェニル基、ヘプタセン基が挙げられる。
R4'及びR5'は、例えば、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、ノニル基、デシル基、ウンデシル基、ドデシル基、トリアコンチル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、シクロオクチル基、シクロノニル基、シクロデシル基、シクロウンデシル基、シクロドデシル基、シクロトリアコンチル基、ノルボルニル基、アダマンチル基、フェニル基、ナフチル基、アントラセン基、ピレニル基、ビフェニル基、ヘプタセン基、ビニル基、アリル基、トリアコンテニル基、メトキシ基、エトキシ基、トリアコンチキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子、チオール基が挙げられる。
前記R0、R4'、R5'の各例示は、異性体を含む。例えば、ブチル基には、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が含まれる。
R16は、例えば、メチレン基、エチレン基、プロペン基、ブテン基、ペンテン基、ヘキセン基、ヘプテン基、オクテン基、ノネン基、デセン基、ウンデセン基、ドデセン基、トリアコンテン基、シクロプロペン基、シクロブテン基、シクロペンテン基、シクロヘキセン基、シクロヘプテン基、シクロオクテン基、シクロノネン基、シクロデセン基、シクロウンデセン基、シクロドデセン基、シクロトリアコンテン基、2価のノルボルニル基、2価のアダマンチル基、2価のフェニル基、2価のナフチル基、2価のアントラセン基、2価のピレン基、2価のビフェニル基、2価のヘプタセン基、2価のビニル基、2価のアリル基、2価のトリアコンテニル基が挙げられる。
前記R16の各例示は、異性体を含む。例えば、ブチル基には、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が含まれる。
R14は、例えば、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、ノニル基、デシル基、ウンデシル基、ドデシル基、トリアコンチル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、シクロオクチル基、シクロノニル基、シクロデシル基、シクロウンデシル基、シクロドデシル基、シクロトリアコンチル基、ノルボルニル基、アダマンチル基、フェニル基、ナフチル基、アントラセン基、ピレニル基、ビフェニル基、ヘプタセン基、ビニル基、アリル基、トリアコンテニル基、メトキシ基、エトキシ基、トリアコンチキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子、チオール基が挙げられる。
前記R14の各例示は、異性体を含む。例えば、ブチル基には、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が含まれる。
R14は、例えば、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、ノニル基、デシル基、ウンデシル基、ドデシル基、トリアコンチル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、シクロオクチル基、シクロノニル基、シクロデシル基、シクロウンデシル基、シクロドデシル基、シクロトリアコンチル基、ノルボルニル基、アダマンチル基、フェニル基、ナフチル基、アントラセン基、ピレニル基、ビフェニル基、ヘプタセン基、ビニル基、アリル基、トリアコンテニル基、メトキシ基、エトキシ基、トリアコンチキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子、チオール基が挙げられる。
前記R14の各例示は、異性体を含む。例えば、ブチル基には、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が含まれる。
R15は、例えば、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、ノニル基、デシル基、ウンデシル基、ドデシル基、トリアコンチル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、シクロオクチル基、シクロノニル基、シクロデシル基、シクロウンデシル基、シクロドデシル基、シクロトリアコンチル基、ノルボルニル基、アダマンチル基、フェニル基、ナフチル基、アントラセン基、ピレニル基、ビフェニル基、ヘプタセン基、ビニル基、アリル基、トリアコンテニル基、メトキシ基、エトキシ基、トリアコンチキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子、チオール基が挙げられる。
前記R15の各例示は、異性体を含む。例えば、ブチル基には、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が含まれる。
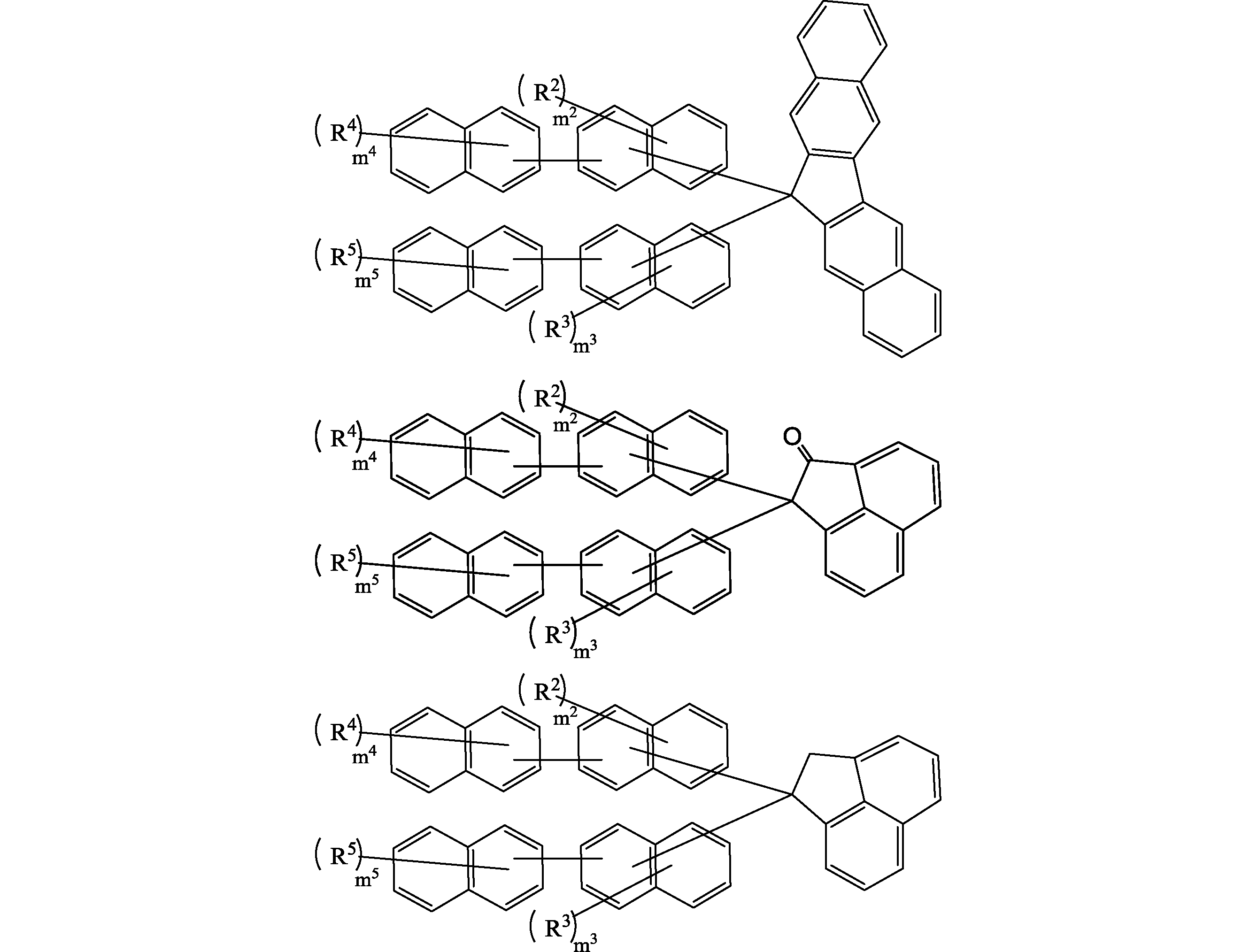
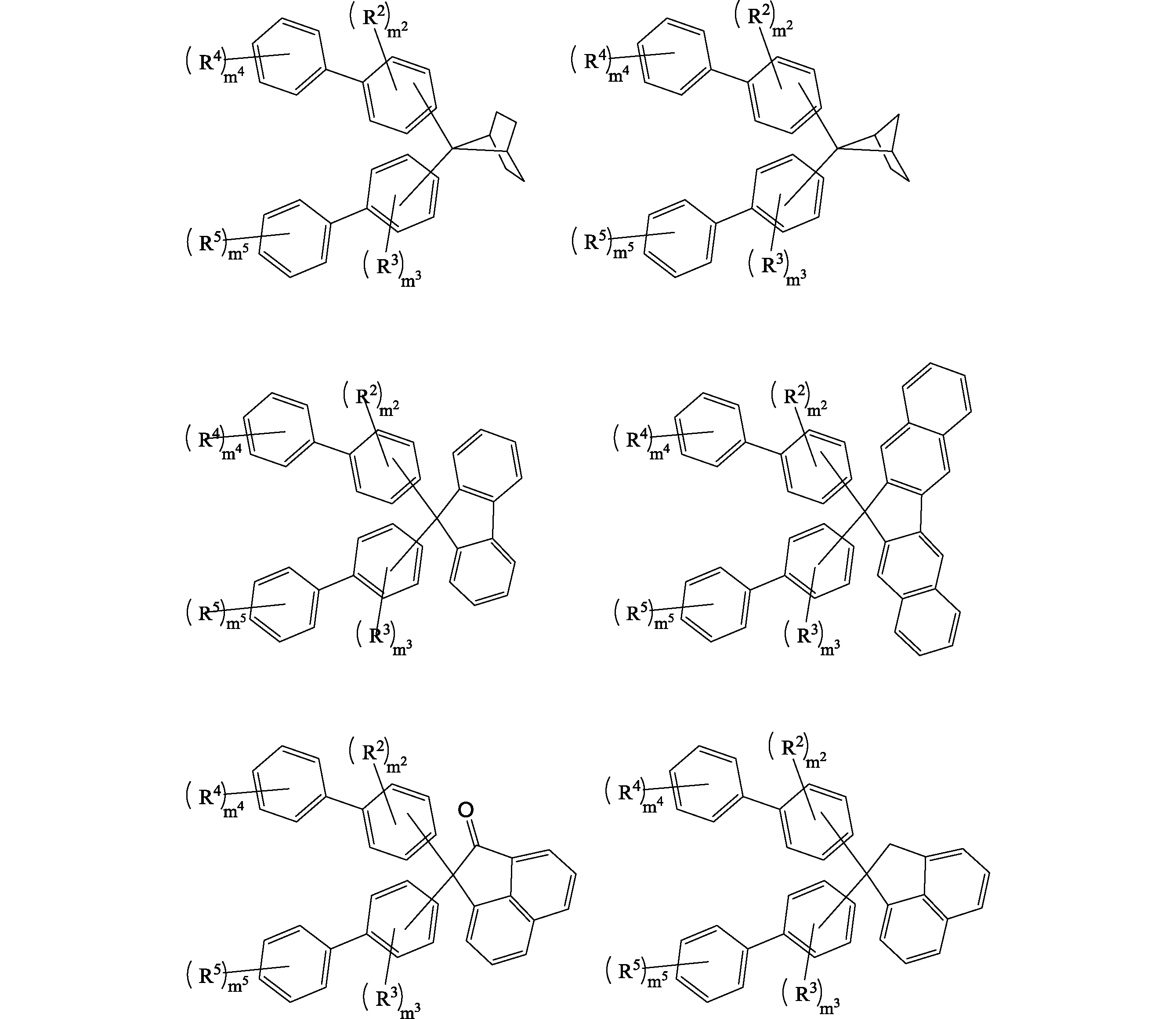
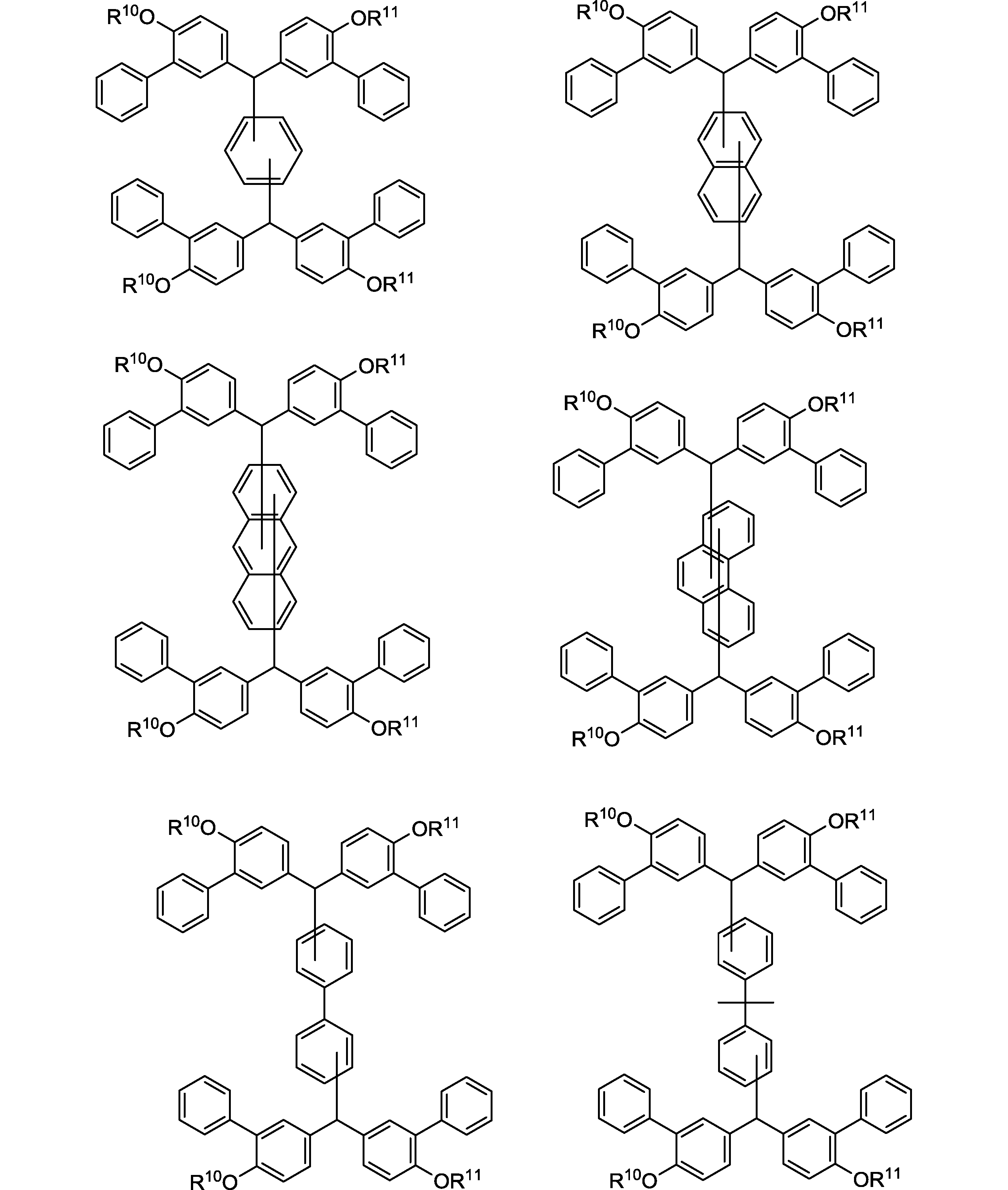
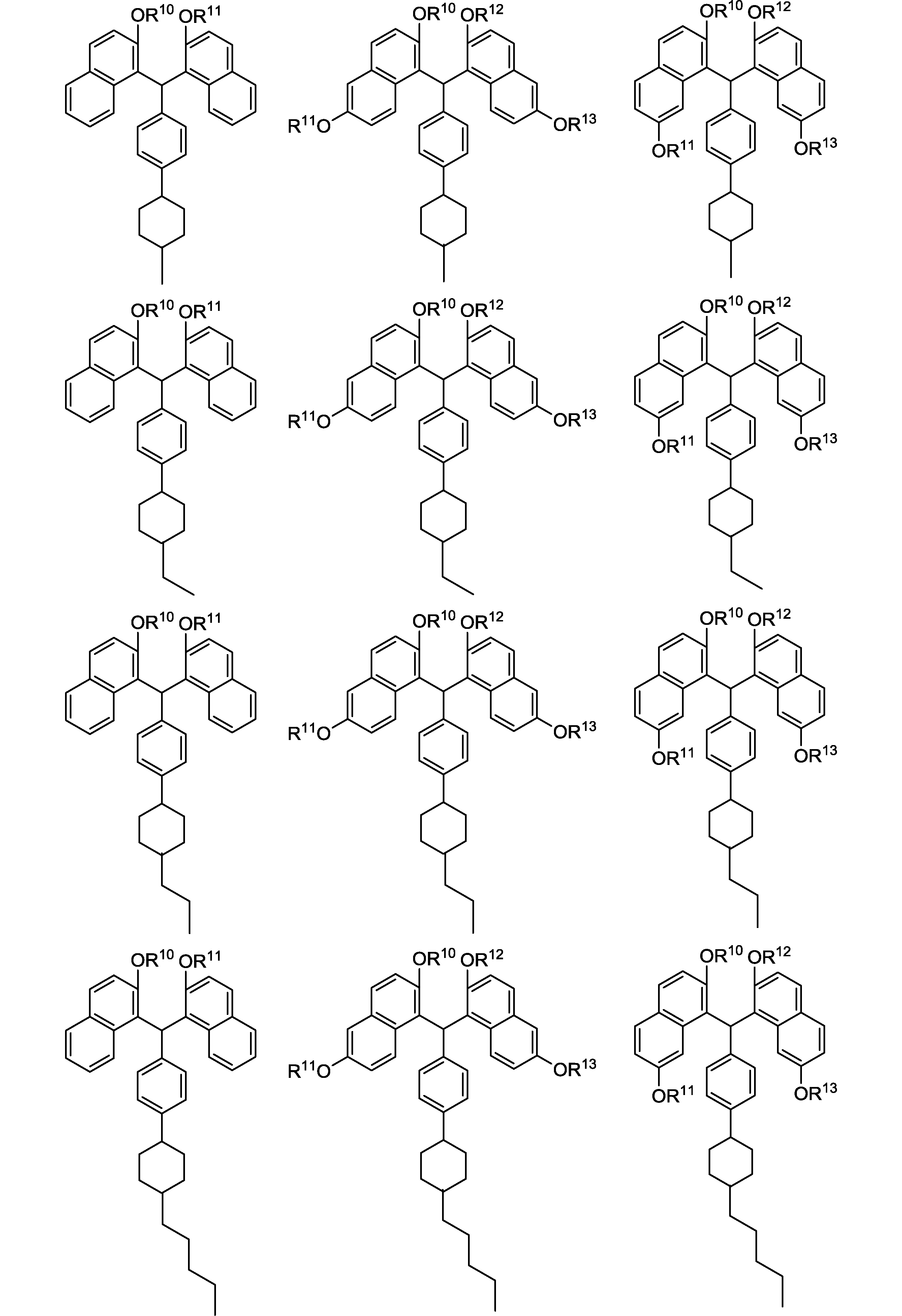
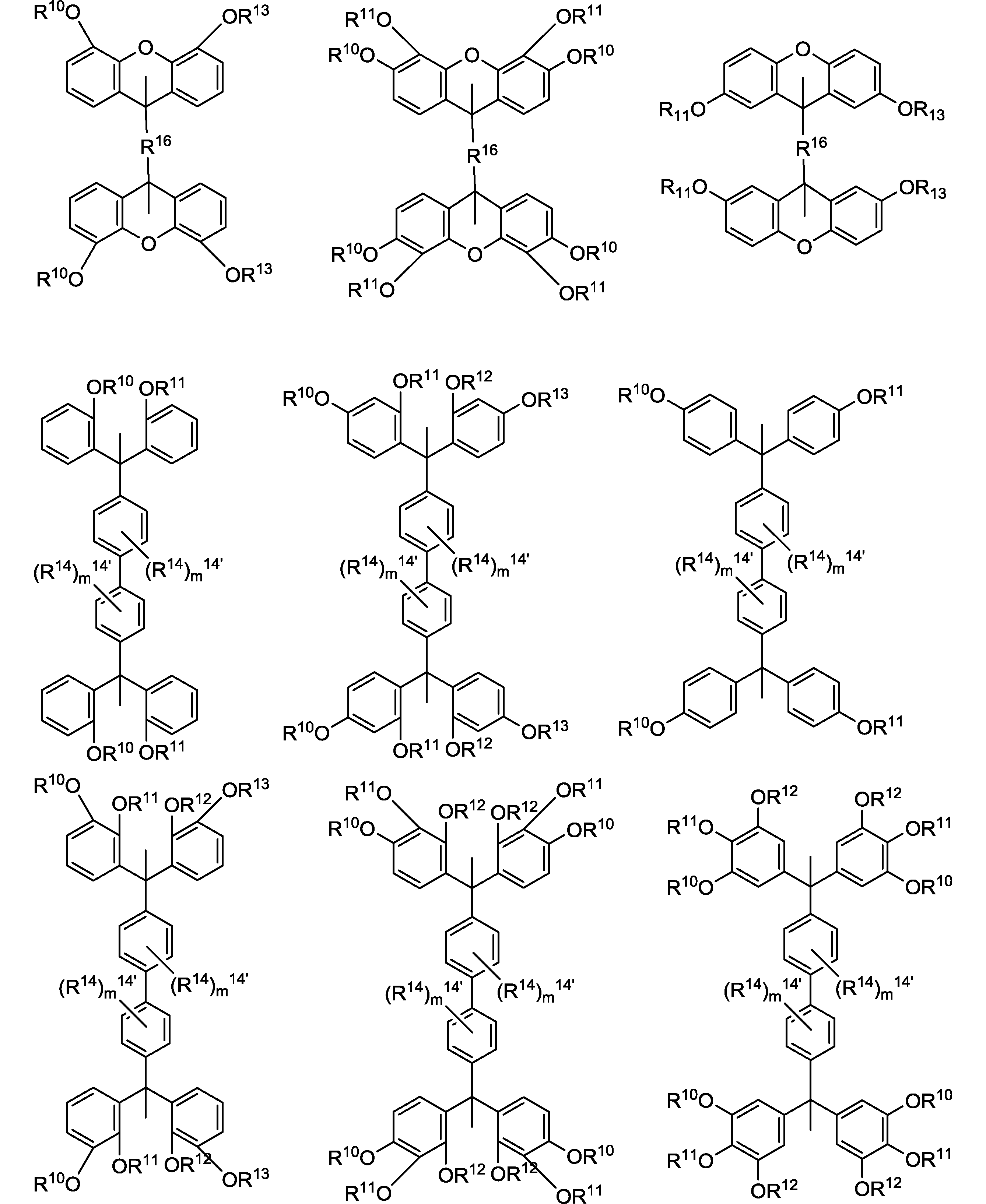
さらに前記式(0)で表される化合物は、式は、エッチング耐性の観点から以下の構造が好ましい。
R14は、例えば、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、ノニル基、デシル基、ウンデシル基、ドデシル基、トリアコンチル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、シクロオクチル基、シクロノニル基、シクロデシル基、シクロウンデシル基、シクロドデシル基、シクロトリアコンチル基、ノルボニル基、アダマンチル基、フェニル基、ナフチル基、アントラセン基、ヘプタセン基、ビニル基、アリル基、トリアコンテニル基、メトキシ基、エトキシ基、トリアコンチキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子、チオール基が挙げられる。
前記R14の各例示は、異性体を含む。例えば、ブチル基には、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が含まれる。
R15は、例えば、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、ノニル基、デシル基、ウンデシル基、ドデシル基、トリアコンチル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、シクロオクチル基、シクロノニル基、シクロデシル基、シクロウンデシル基、シクロドデシル基、シクロトリアコンチル基、ノルボニル基、アダマンチル基、フェニル基、ナフチル基、アントラセン基、ヘプタセン基、ビニル基、アリル基、トリアコンテニル基、メトキシ基、エトキシ基、トリアコンチキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子、チオール基が挙げられる。
前記R15の各例示は、異性体を含む。例えば、ブチル基には、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が含まれる。
R16は、例えば、メチレン基、エチレン基、プロペン基、ブテン基、ペンテン基、ヘキセン基、ヘプテン基、オクテン基、ノネン基、デセン基、ウンデセン基、ドデセン基、トリアコンテン基、シクロプロペン基、シクロブテン基、シクロペンテン基、シクロヘキセン基、シクロヘプテン基、シクロオクテン基、シクロノネン基、シクロデセン基、シクロウンデセン基、シクロドデセン基、シクロトリアコンテン基、2価のノルボニル基、2価のアダマンチル基、2価のフェニル基、2価のナフチル基、2価のアントラセン基、2価のヘプタセン基、2価のビニル基、2価のアリル基、2価のトリアコンテニル基が挙げられる。
前記R16の各例示は、異性体を含む。例えば、ブチル基には、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が含まれる。
R14は、例えば、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、ノニル基、デシル基、ウンデシル基、ドデシル基、トリアコンチル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、シクロオクチル基、シクロノニル基、シクロデシル基、シクロウンデシル基、シクロドデシル基、シクロトリアコンチル基、ノルボニル基、アダマンチル基、フェニル基、ナフチル基、アントラセン基、ヘプタセン基、ビニル基、アリル基、トリアコンテニル基、メトキシ基、エトキシ基、トリアコンチキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子、チオール基が挙げられる。
前記R14の各例示は、異性体を含む。例えば、ブチル基には、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が含まれる。
R14は、例えば、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、ノニル基、デシル基、ウンデシル基、ドデシル基、トリアコンチル基、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基、シクロヘプチル基、シクロオクチル基、シクロノニル基、シクロデシル基、シクロウンデシル基、シクロドデシル基、シクロトリアコンチル基、ノルボニル基、アダマンチル基、フェニル基、ナフチル基、アントラセン基、ヘプタセン基、ビニル基、アリル基、トリアコンテニル基、メトキシ基、エトキシ基、トリアコンチキシ基、フッ素原子、塩素原子、臭素原子、ヨウ素原子、チオール基が挙げられる。
前記R14の各例示は、異性体を含む。例えば、ブチル基には、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基が含まれる。
前記化合物は、耐熱性の観点から、ジベンゾキサンテン骨格を有することが好ましい。
前記式(0)で表される化合物の原料としては、例えば、ポリフェノール原料を用いることができ、例えば、下記式(5)で表される化合物を用いることができる。
(式(5)中、R5Aは、炭素数1~60のN価の基又は単結合であり、
M10は、各々独立して1~3の整数であり
NBは、1~4の整数であり、NBが2以上の整数の場合、N個の[ ]内の構造式は同一であっても異なっていてもよい。)
本実施形態で使用される式(0)で表される化合物は、公知の手法を応用して適宜合成することができ、その合成手法は特に限定されない。例えば、式(1)で表される化合物を例にとると、式(0)で表される化合物は以下のように合成することができる。
例えば、式(1)で表される化合物は、常圧下、ビフェノール類、ビナフトール類又はビアントラセンオール類と、対応するアルデヒド類又はケトン類とを酸触媒下にて重縮合反応させることによって、前記式(1)で表される化合物を得ることができる。また、その化合物の少なくとも1つのフェノール性水酸基に公知の方法により含ビニルフェニルメチル基を導入できる。また、必要に応じて、加圧下で行うこともできる。
例えば、以下のようにして、前記化合物の少なくとも1つのフェノール性水酸基にヒドロキシアルキル基を導入して、そのヒドロキシ基にビニルフェニルメチル基を導入することができる。
ヒドロキシアルキル基を導入するための化合物は、公知の方法で合成もしくは容易に入手でき、例えば、クロロエタノール、ブロモエタノール、酢酸-2-クロロエチル、酢酸-2-ブロモエチル、酢酸-2-ヨードエチル、エチレンオキサイド、プロピレンオキサイド、ブチレンオキサイド、エチレンカーボネート、プロピレンカーボネート、ブチレンカーボネートが挙げられるが特に限定はされない。
また、例えば、エチレンカーボネート、プロピレンカーボネート、ブチレンカーボネートを使用する場合、アルキレンカーボネートを付加させ、脱炭酸反応が生じることにより、ヒドロキシアルキル基が導入される。
その後、アセトン、テトラヒドロフラン(THF)、プロピレングリコールモノメチルエーテルアセテート等の非プロトン性溶媒に前記化合物と含ビニルフェニルメチル基を導入するための化合物とを溶解又は懸濁させる。続いて、水酸化ナトリウム、水酸化カリウム、ナトリウムメトキサイド、ナトリウムエトキサイド等の塩基触媒の存在下、常圧で、20~150℃、6~72時間反応させる。反応液を酸で中和し、蒸留水に加え白色固体を析出させた後、分離した固体を蒸留水で洗浄し、または溶媒を蒸発乾固させて、必要に応じて蒸留水で洗浄し、乾燥することにより、ヒドロキシ基の水素原子が含ビニルフェニルメチル基で置換された化合物を得ることができる。
前記式(0)で表される化合物は、リソグラフィー用膜形成組成物として、そのまま使用することができる。また、前記式(0)で表される化合物をモノマーとして得られる樹脂としても使用することができる。換言すると、本実施形態の樹脂は前記一般式(0)に由来する単位構造を有する樹脂である。例えば、前記式(0)で表される化合物と架橋反応性のある化合物とを反応させて得られる樹脂としても使用することができる。
前記式(0)で表される化合物をモノマーとして得られる樹脂としては、例えば、以下の式(3)に表される構造を有するものが挙げられる。すなわち、本実施形態の組成物は、下記式(3)に表される構造を有する樹脂を含有するものであってもよい。
(式(3)中、Lは、置換基を有していてもよい炭素数1~30のアルキレン基、置換基を有していてもよい炭素数6~30のアリーレン基、置換基を有していてもよい炭素数1~30のアルコキシレン基又は単結合であり、前記アルキレン基、前記アリーレン基、前記アルコキシレン基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、
R0は、前記RYと同義であり、
R1は、炭素数1~60のn価の基又は単結合であり、
R2~R5は、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、置換基を有していてもよい炭素数1~30のアルコキシ基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基、水酸基又は水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、前記アルキル基、前記アリール基、前記アルケニル基、前記アルコキシ基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、
M2及びm3は、各々独立して、0~8の整数であり、
M4及びm5は、各々独立して、0~9の整数であり、
但し、m2、m3、m4及びm5は同時に0となることはなく、R2~R5の少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基である。
Nは前記Nと同義であり、ここで、nが2以上の整数の場合、n個の[ ]内の構造式は同一であっても異なっていてもよく、
P2~p5は、前記rと同義である。)
本実施形態の樹脂は、前記式(0)で表される化合物を架橋反応性のある化合物と反応させることにより得られる。架橋反応性のある化合物としては、前記式(0)で表される化合物をオリゴマー化又はポリマー化し得るものである限り、公知のものを特に制限なく使用することができる。その具体例としては、例えば、アルデヒド、ケトン、カルボン酸、カルボン酸ハライド、ハロゲン含有化合物、アミノ化合物、イミノ化合物、イソシアネート、不飽和炭化水素基含有化合物等が挙げられるが、これらに特に限定されない。
本実施形態の化合物は、下記式(2)で表されることも好ましい。式(2)で表される化合物は以下のように構成されているため、耐熱性が高く、溶媒溶解性も高い。
(式(2)中、R0Aは、前記RYと同義であり、
R1Aは、炭素数1~30のna価の基又は単結合であり、
R2Aは、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、置換基を有していてもよい炭素数1~30のアルコキシ基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基、水酸基又は水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、前記アルキル基、前記アリール基、前記アルケニル基、前記アルコキシ基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、ここで、R2Aの少なくとも1つは水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、
Naは、前記Nと同義であり、ここで、naが2以上の整数の場合、na個の[ ]内の構造式は同一であっても異なっていてもよく、
XAは、前記Xと同義あり、
M2aは、各々独立して、0~7の整数であり、但し、少なくとも1つのm2aは1~7の整数であり、
Qaは、各々独立して、0又は1である。)
R1Aは、炭素数1~60のna価の基又は単結合である。Naは前記Nと同義であり、1~4の整数である。式(2)中、naが2以上の整数の場合、na個の[ ]内の構造式は同一であっても異なっていてもよい。
なお、前記na価の基とは、na=1のときには、炭素数1~60のアルキル基、na=2のときには、炭素数1~30のアルキレン基、na=3のときには、炭素数2~60のアルカンプロパイル基、na=4のときには、炭素数3~60のアルカンテトライル基のことを示す。前記n価の基としては、例えば、直鎖状炭化水素基、分岐状炭化水素基又は脂環式炭化水素基を有するもの等が挙げられる。ここで、前記脂環式炭化水素基については、有橋脂環式炭化水素基も含まれる。また、前記n価の炭化水素基は、脂環式炭化水素基、二重結合、ヘテロ原子もしくは炭素数6~60の芳香族基を有していてもよい。
R4Aは、各々独立して、水素原子又は含ビニルフェニルメチル基であり、ここで、R4Aの少なくとも1つは含ビニルフェニルメチル基であり、m6aは、各々独立して、0~5の整数である。
本実施形態で使用される式(2)で表される化合物は、公知の手法を応用して適宜合成することができ、その合成手法は特に限定されない。
例えば、常圧下、フェノール類、ナフトール類と、対応するケトン類又はアルデヒド類とを酸触媒下にて重縮合反応させることによりポリフェノール化合物を得て、続いて、ポリフェノール化合物の少なくとも1つのフェノール性水酸基に、含ビニルフェニルメチル基を導入することにより得られる。
また、前記合成は必要に応じて、加圧下で行うこともできる。
ケトン類として、芳香環を有するケトンを用いることが、高い耐熱性及び高いエッチング耐性を兼備し好ましい。
前記ポリフェノール化合物を製造する際、反応温度は、特に限定されず、反応原料の反応性に応じて適宜選択することができるが、10~200℃の範囲であることが好ましい。本実施形態の式(2)で表される化合物を選択性よく合成するには、温度が低い方が、効果が高く10~60℃の範囲がより好ましい。
前記式(2)で表される化合物の製造方法は、特に限定されないが、例えば、ナフトール類等、アルデヒド類又はケトン類、触媒を一括で仕込む方法や、触媒存在下ナフトール類やケトン類を滴下していく方法がある。重縮合反応終了後、系内に存在する未反応原料、触媒等を除去するために、反応釜の温度を130~230℃ にまで上昇させ、1~50mmhg程度で揮発分を除去することもできる。
ヒドロキシアルキル基は、オキシアルキル基を介してフェノール性水酸基に導入されることもある。例えば、ヒドロキシアルキルオキシアルキル基やヒドロキシアルキルオキシアルキルオキシアルキル基が導入される。例えば、以下のようにして、前記化合物の少なくとも1つのフェノール性水酸基にヒドロキシアルキル基を導入して、そのヒドロキシ基にビニルフェニルメチル基で置換された基を導入することができる。
例えば、以下のようにして、前記化合物の少なくとも1つのフェノール性水酸基にヒドロキシアルキル基を導入して、そのヒドロキシ基にビニルフェニルメチル基を導入することができる。
ヒドロキシアルキル基を導入するための化合物は、公知の方法で合成もしくは容易に入手でき、例えば、クロロエタノール、ブロモエタノール、酢酸-2-クロロエチル、酢酸-2-ブロモエチル、酢酸-2-ヨードエチル、エチレンオキサイド、プロピレンオキサイド、ブチレンオキサイド、エチレンカーボネート、プロピレンカーボネート、ブチレンカーボネートが挙げられるが特に限定はされない。
例えば、酢酸-2-クロロエチル、酢酸-2-ブロモエチル、酢酸-2-ヨードエチルを使用する場合、アセトキシエチル基が導入されたのち、脱アシル反応を生じることにより、ヒドロキシエチル基が導入される。
また、例えば、エチレンカーボネート、プロピレンカーボネート、ブチレンカーボネートを使用する場合、アルキレンカーボネートを付加させ、脱炭酸反応が生じることにより、ヒドロキシアルキル基が導入される。
その後、アセトン、テトラヒドロフラン(THF)、プロピレングリコールモノメチルエーテルアセテート等の非プロトン性溶媒に前記化合物と含ビニルフェニルメチル基を導入するための化合物とを溶解又は懸濁させる。続いて、水酸化ナトリウム、水酸化カリウム、ナトリウムメトキサイド、ナトリウムエトキサイド等の塩基触媒の存在下、常圧で、20~150℃、6~72時間反応させる。反応液を酸で中和し、蒸留水に加え白色固体を析出させた後、分離した固体を蒸留水で洗浄し、または溶媒を蒸発乾固させて、必要に応じて蒸留水で洗浄し、乾燥することにより、ヒドロキシ基の水素原子が含ビニルフェニルメチル基で置換された化合物を得ることができる。
前記式(2)で表される化合物は、リソグラフィー用膜形成組成物として、そのまま使用することができる。また、前記式(2)で表される化合物をモノマーとして得られる樹脂としても使用することができる。例えば、前記式(2)で表される化合物と架橋反応性のある化合物とを反応させて得られる樹脂としても使用することができる。
前記式(2)で表される化合物をモノマーとして得られる樹脂としては、例えば、以下の式(4)に表される構造を有するものが挙げられる。すなわち、本実施形態の組成物は、下記式(4)に表される構造を有する樹脂を含有するものであってもよい。
R0A、R1A、R2A、m2a、na、qa及びXAは前記式(2)におけるものと同義であり、
Naが2以上の整数の場合、na個の[ ]内の構造式は同一であっても異なっていてもよい。
但し、R2Aの少なくとも1つは水酸基の水素原子が、水素原子が含ビニルフェニルメチル基で置換された基を含む。
前記式(0)で表される化合物及びこれをモノマーとして得られる樹脂は以下の精製方法によって精製ことができる。即ち、本実施形態の化合物及び/又は樹脂の精製方法は、前記式(0)で表される化合物及びこれをモノマーとして得られる樹脂(例えば、前記式(1)で表される化合物、前記式(1)で表される化合物をモノマーとして得られる樹脂、前記式(2)で表される化合物及び前記式(2)で表される化合物をモノマーとして得られる樹脂から選ばれる1種以上)を、溶媒に溶解させて溶液(S)を得る工程と、得られた溶液(S)と酸性の水溶液とを接触させて、前記化合物及び/又は前記樹脂中の不純物を抽出する工程(第一抽出工程)とを含み、前記溶液(S)を得る工程で用いる溶媒が、水と任意に混和しない有機溶媒を含む。
当該第一抽出工程において、前記樹脂は、例えば、前記式(1)で表される化合物及び/又は式(2)で表される化合物と架橋反応性のある化合物との反応によって得られる樹脂であることが好ましい。前記精製方法によれば、上述した特定の構造を有する化合物又は樹脂に不純物として含まれうる種々の金属の含有量を低減することができる。
より詳細には、前記精製方法においては、前記化合物及び/又は前記樹脂を、水と任意に混和しない有機溶媒に溶解させて溶液(S)を得て、さらにその溶液(S)を酸性水溶液と接触させて抽出処理を行うことができる。これにより、前記溶液(S)に含まれる金属分を水相に移行させたのち、有機相と水相とを分離して金属含有量の低減された化合物及び/又は樹脂を得ることができる。
また、ここで用いる水は、本実施の形態の目的に沿って、金属含有量の少ない水、例えば、イオン交換水等であることが好ましい。抽出処理は1回だけでもかまわないが、混合、静置、分離という操作を複数回繰り返して行うのも有効である。また、抽出処理における両者の使用割合や、温度、時間等の条件は特に限定されないが、先の酸性の水溶液との接触処理の場合と同様で構わない。
本実施形態の組成物は、上述の本実施形態の化合物及び樹脂からなる群より選ばれる1種以上を含有する。本実施形態の組成物は、溶媒、酸発生剤、架橋剤、架橋促進剤、ラジカル重合開始剤等を更に含有することができる。本実施形態の組成物は、リソグラフィー用膜形成用途(即ち、リソグラフィー用膜形成組成物)や光学部品形成用途に用いることができる。
本実施形態の組成物は、上述の本実施形態の化合物及び樹脂からなる群より選ばれる1種以上(例えば、前記式(1)で表される化合物、前記式(1)で表される化合物をモノマーとして得られる樹脂、前記式(2)で表される化合物及び前記式(2)で表される化合物をモノマーとして得られる樹脂からなる群より選ばれる1種以上)をレジスト基材として含有することができる。
本実施形態の組成物は化学増幅型レジスト用途向けリソグラフィー用膜形成組成物(以下、レジスト組成物とも称す)として用いることができる。レジスト組成物は、例えば、本実施形態の化合物及び樹脂からなる群より選ばれる1種以上を含有する。
前記レジスト組成物において、レジスト基材として用いる上述の本実施形態の化合物及び樹脂の含有量は、特に限定されないが、固形成分の全質量(レジスト基材、酸発生剤(C)、酸架橋剤(G)、酸拡散制御剤(E)及びその他の成分(F)などの任意に使用される成分を含む固形成分の総和、以下同様。)の50~99.4質量%であることが好ましく、より好ましくは55~90質量%、さらに好ましくは60~80質量%、特に好ましくは60~70質量%である。前記含有量の場合、解像度が一層向上し、ラインエッジラフネス(LER)が一層小さくなる。
なお、レジスト基材として化合物と樹脂の両方を含有する場合、前記含有量は、両成分の合計量である。
前記レジスト組成物には、本発明の目的を阻害しない範囲で、必要に応じて、レジスト基材、酸発生剤(C)、酸架橋剤(G)および酸拡散制御剤(E)以外の成分として、溶解促進剤、溶解制御剤、増感剤、界面活性剤、有機カルボン酸又はリンのオキソ酸若しくはその誘導体、熱および/または光硬化触媒、重合禁止剤、難燃剤、充填剤、カップリング剤、熱硬化性樹脂、光硬化性樹脂、染料、顔料、増粘剤、滑剤、消泡剤、レベリング剤、紫外線吸収剤、界面活性剤、着色剤、ノニオン系界面活性剤等の各種添加剤を1種又は2種以上添加することができる。なお、本明細書において、その他の成分(F)を任意成分(F)ということがある。
好ましくは50~99.4/0.001~49/0.5~49/0.001~49/0~49、
より好ましくは55~90/1~40/0.5~40/0.01~10/0~5、
さらに好ましくは60~80/3~30/1~30/0.01~5/0~1、
特に好ましくは60~70/10~25/2~20/0.01~3/0、である。
各成分の配合割合は、その総和が100質量%になるように各範囲から選ばれる。前記配合にすると、感度、解像度、現像性等の性能に優れる。
前記レジスト組成物は、スピンコートによりアモルファス膜を形成することができる。また、一般的な半導体製造プロセスに適用することができる。上述の本実施形態の化合物及び樹脂の種類及び/又は用いる現像液の種類によって、ポジ型レジストパターン及びネガ型レジストパターンのいずれかを作り分けることができる。
ネガ型レジストパターンの場合、前記レジスト組成物をスピンコートして形成したアモルファス膜の23℃における現像液に対する溶解速度は、10Å/sec以上であることが好ましい。当該溶解速度が10Å/sec以上であると現像液に易溶で、レジストに一層向いている。また、10Å/sec以上の溶解速度を有すると、解像性が向上する場合もある。これは、上述の本実施形態の化合物及び樹脂のミクロの表面部位が溶解し、LERを低減するからと推測される。またディフェクトの低減効果がある。
前記溶解速度は、23℃にて、アモルファス膜を所定時間現像液に浸漬させ、その浸漬前後の膜厚を、目視、エリプソメーターまたはQCM法等の公知の方法によって測定し決定できる。
ネガ型レジストパターンの場合、前記レジスト組成物をスピンコートして形成したアモルファス膜のkrfエキシマレーザー、極端紫外線、電子線又はX線等の放射線により露光した部分の23℃における現像液に対する溶解速度は、5Å/sec以下が好ましく、0.05~5Å/secがより好ましく、0.0005~5Å/secがさらに好ましい。当該溶解速度が5Å/sec以下であると現像液に不溶で、レジストとすることができる。また、0.0005Å/sec以上の溶解速度を有すると、解像性が向上する場合もある。これは、上述の本実施形態の化合物及び樹脂を構成成分として含む樹脂の露光前後の溶解性の変化により、現像液に溶解する未露光部と、現像液に溶解しない露光部との界面のコントラストが大きくなるからと推測される。またLERの低減、ディフェクトの低減効果がある。
本実施形態の組成物は非化学増幅型レジスト用途向けリソグラフィー用膜形成組成物(以下、感放射線性組成物とも称す)として用いることができる。前記感放射線性組成物に含有させる成分(A)(上述の本実施形態の化合物及び樹脂)は、後述するジアゾナフトキノン光活性化合物(B)と併用し、g線、h線、i線、krfエキシマレーザー、arfエキシマレーザー、極端紫外線、電子線又はX線を照射することにより、現像液に易溶な化合物となるポジ型レジスト用基材として有用である。G線、h線、i線、krfエキシマレーザー、arfエキシマレーザー、極端紫外線、電子線又はX線により、成分(A)の性質は大きくは変化しないが、現像液に難溶なジアゾナフトキノン光活性化合物(B)が易溶な化合物に変化することで、現像工程によってレジストパターンを作り得る。
前記感放射線性組成物に含有させる成分(A)は、比較的低分子量の化合物であることから、得られたレジストパターンのラフネスは非常に小さい。また、前記式(1)中、R0~R5からなる群より選択される少なくとも1つがヨウ素原子を含む基であることが好ましく、前記式(2)中、R0A、R1A及びR2Aからなる群より選択される少なくとも1つがヨウ素原子を含む基であることが好ましい。前記レジスト組成物は、このような好ましい態様であるヨウ素原子を含む基を有する成分(A)を適用した場合は、電子線、極端紫外線(EUV)、X線などの放射線に対する吸収能を増加させ、その結果、感度を高めることが可能となり好ましい。
前記感放射線性組成物に含有させるジアゾナフトキノン光活性化合物(B)は、ポリマー性及び非ポリマー性ジアゾナフトキノン光活性化合物を含む、ジアゾナフトキノン物質であり、一般にポジ型レジスト組成物において、感光性成分(感光剤)として用いられているものであれば特に制限なく、1種又は2種以上任意に選択して用いることができる。
また、ナフトキノンジアジドスルホン酸クロライドやベンゾキノンジアジドスルホン酸クロライドなどの酸クロライドとしては、例えば、1、2-ナフトキノンジアジド-5-スルフォニルクロライド、1、2-ナフトキノンジアジド-4-スルフォニルクロライドなどが好ましいものとして挙げられる。
前記感放射線性組成物は、スピンコートによりアモルファス膜を形成することができる。また、一般的な半導体製造プロセスに適用することができる。用いる現像液の種類によって、ポジ型レジストパターン及びネガ型レジストパターンのいずれかを作り分けることができる。
ポジ型レジストパターンの場合、前記感放射線性組成物をスピンコートして形成したアモルファス膜の23℃における現像液に対する溶解速度は、5Å/sec以下が好ましく、0.05~5Å/secがより好ましく、0.0005~5Å/secがさらに好ましい。当該溶解速度が5Å/sec以下であると現像液に不溶で、レジストとすることができる。また、0.0005Å/sec以上の溶解速度を有すると、解像性が向上する場合もある。これは、上述の本実施形態の化合物及び樹脂を構成成分として含む樹脂の露光前後の溶解性の変化により、現像液に溶解する露光部と、現像液に溶解しない未露光部との界面のコントラストが大きくなるからと推測される。またLERの低減、ディフェクトの低減効果がある。
ネガ型レジストパターンの場合、前記感放射線性組成物をスピンコートして形成したアモルファス膜の23℃における現像液に対する溶解速度は、10Å/sec以上であることが好ましい。当該溶解速度が10Å/sec以上であると現像液に易溶で、レジストに一層向いている。また、10Å/sec以上の溶解速度を有すると、解像性が向上する場合もある。これは、上述の本実施形態の化合物及び樹脂を構成成分として含む樹脂のミクロの表面部位が溶解し、LERを低減するからと推測される。またディフェクトの低減効果がある。
前記溶解速度は、23℃にて、アモルファス膜を所定時間現像液に浸漬させ、その浸漬前後の膜厚を、目視、エリプソメーターまたはQCM法等の公知の方法によって測定し決定できる。
ネガ型レジストパターンの場合、前記感放射線性組成物をスピンコートして形成したアモルファス膜のkrfエキシマレーザー、極端紫外線、電子線又はX線等の放射線により照射した後、又は、20~500℃で加熱した後の露光した部分の、23℃における現像液に対する溶解速度は、5Å/sec以下が好ましく、0.05~5Å/secがより好ましく、0.0005~5Å/secがさらに好ましい。当該溶解速度が5Å/sec以下であると現像液に不溶で、レジストとすることができる。また、0.0005Å/sec以上の溶解速度を有すると、解像性が向上する場合もある。これは、上述の本実施形態の化合物及び樹脂の露光前後の溶解性の変化により、現像液に溶解する未露光部と、現像液に溶解しない露光部との界面のコントラストが大きくなるからと推測される。またLERの低減、ディフェクトの低減効果がある。
前記感放射線性組成物において、成分(A)の含有量は、固形成分全重量(成分(A)、ジアゾナフトキノン光活性化合物(B)及びその他の成分(D)などの任意に使用される固形成分の総和、以下同様。)に対して、好ましくは1~99質量%であり、より好ましくは5~95質量%、さらに好ましくは10~90質量%、特に好ましくは25~75質量%である。前記感放射線性組成物は、成分(A)の含有量が前記範囲内であると、高感度でラフネスの小さなパターンを得ることができる。
前記感放射線性組成物には、本発明の目的を阻害しない範囲で、必要に応じて、成分(A)及びジアゾナフトキノン光活性化合物(B)以外の成分として、酸発生剤、酸架橋剤、酸拡散制御剤、溶解促進剤、溶解制御剤、増感剤、界面活性剤、有機カルボン酸又はリンのオキソ酸若しくはその誘導体、熱および/または光硬化触媒、重合禁止剤、難燃剤、充填剤、カップリング剤、熱硬化性樹脂、光硬化性樹脂、染料、顔料、増粘剤、滑剤、消泡剤、レベリング剤、紫外線吸収剤、界面活性剤、着色剤、ノニオン系界面活性剤等の各種添加剤を1種又は2種以上添加することができる。なお、本明細書において、その他の成分(D)を任意成分(D)ということがある。
好ましくは1~99/99~1/0~98、
より好ましくは5~95/95~5/0~49、
さらに好ましくは10~90/90~10/0~10、
特に好ましくは20~80/80~20/0~5、
最も好ましくは25~75/75~25/0、である。
各成分の配合割合は、その総和が100質量%になるように各範囲から選ばれる。前記感放射線性組成物は、各成分の配合割合を前記範囲にすると、ラフネスに加え、感度、解像度等の性能に優れる。
本実施形態によるレジストパターンの形成方法は、上述した本実施形態の組成物(前記レジスト組成物又は感放射線性組成物)を用いてフォトレジスト層を形成した後、前記フォトレジスト層の所定の領域に放射線を照射し、現像を行う工程を含む。具体的には、本実施形態によるレジストパターンの形成方法は、基板上にレジスト膜を形成する工程と、形成されたレジスト膜を露光する工程と、前記レジスト膜を現像してレジストパターンを形成する工程とを備える。本実施形態におけるレジストパターンは多層プロセスにおける上層レジストとして形成することもできる。
界面活性剤としては特に限定されないが、例えば、イオン性や非イオン性のフッ素系及び/又はシリコン系界面活性剤等を用いることができる。これらのフッ素及び/又はシリコン系界面活性剤として、例えば、特開昭62-36663号公報、特開昭61-226746号公報、特開昭61-226745号公報、特開昭62-170950号公報、特開昭63-34540号公報、特開平7-230165号公報、特開平8-62834号公報、特開平9-54432号公報、特開平9-5988号公報、米国特許第5405720号明細書、同5360692号明細書、同5529881号明細書、同5296330号明細書、同5436098号明細書、同5576143号明細書、同5294511号明細書、同5824451号明細書記載の界面活性剤を挙げることができ、好ましくは、非イオン性の界面活性剤である。非イオン性の界面活性剤としては特に限定されないが、フッ素系界面活性剤又はシリコン系界面活性剤を用いることがさらに好ましい。
本実施形態の組成物は、下層膜用途向けリソグラフィー用膜形成組成物(以下、下層膜形成材料とも称す。)として用いることもできる。下層膜形成材料は、上述の本実施形態の化合物及び樹脂からなる群より選ばれる少なくとも1種の物質を含有する。本実施形態において前記物質は塗布性及び品質安定性の点から、下層膜形成材料中、1~100質量%であることが好ましく、10~100質量%であることがより好ましく、50~100質量%であることがさらに好ましく、100質量%であることが特に好ましい。
前記下層膜形成材料は、溶媒を含有してもよい。前記下層膜形成材料に用いられる溶媒としては、上述した物質が少なくとも溶解するものであれば、公知のものを適宜用いることができる。
前記下層膜形成材料は、インターミキシングを抑制する等の観点から、必要に応じて架橋剤を含有していてもよい。本実施形態で使用可能な架橋剤は特に限定されないが、例えば、国際公開第2013/024779号に記載の酸架橋剤をを用いることができる。
本実施形態の下層膜膜形成材料には、必要に応じて架橋、硬化反応を促進させるための架橋促進剤を用いることができる。
本実施形態の下層膜形成材料には、必要に応じてラジカル重合開始剤を配合することができる。ラジカル重合開始剤としては、光によりラジカル重合を開始させる光重合開始剤であってもよいし、熱によりラジカル重合を開始させる熱重合開始剤であってもよい。ラジカル重合開始剤としては、例えば、ケトン系光重合開始剤、有機過酸化物系重合開始剤及びアゾ系重合開始剤からなる群より選ばれる少なくとも1種とすることができる。
前記下層膜形成材料は、熱による架橋反応をさらに促進させるなどの観点から、必要に応じて酸発生剤を含有していてもよい。酸発生剤としては、熱分解によって酸を発生するもの、光照射によって酸を発生するものなどが知られているが、いずれのものも使用することができる。例えば、国際公開第2013/024779号に記載のものを用いることができる。
さらに、前記下層膜形成材料は、保存安定性を向上させる等の観点から、塩基性化合物を含有していてもよい。
また、本実施形態における下層膜形成材料は、熱や光による硬化性の付与や吸光度をコントロールする目的で、他の樹脂及び/又は化合物を含有していてもよい。このような他の樹脂及び/又は化合物としては、ナフトール樹脂、キシレン樹脂ナフトール変性樹脂、ナフタレン樹脂のフェノール変性樹脂、ポリヒドロキシスチレン、ジシクロペンタジエン樹脂、(メタ)アクリレート、ジメタクリレート、トリメタクリレート、テトラメタクリレート、ビニルナフタレン、ポリアセナフチレンなどのナフタレン環、フェナントレンキノン、フルオレンなどのビフェニル環、チオフェン、インデンなどのヘテロ原子を有する複素環を含む樹脂や芳香族環を含まない樹脂;ロジン系樹脂、シクロデキストリン、アダマンタン(ポリ)オール、トリシクロデカン(ポリ)オール及びそれらの誘導体等の脂環構造を含む樹脂又は化合物等が挙げられるが、これらに特に限定されない。さらに、本実施形態における下層膜形成材料は、公知の添加剤を含有していてもよい。前記公知の添加剤としては、以下に限定されないが、例えば、熱および/または光硬化触媒、重合禁止剤、難燃剤、充填剤、カップリング剤、熱硬化性樹脂、光硬化性樹脂、染料、顔料、増粘剤、滑剤、消泡剤、レベリング剤、紫外線吸収剤、界面活性剤、着色剤、ノニオン系界面活性剤等が挙げられる。
前記下層膜形成材料を用いて、リソグラフィー用下層膜を形成することができる。
なお、前記組成物を用いてレジスト永久膜を作製することもできる、本実施形態の組成物を塗布してなるレジスト永久膜は、必要に応じてレジストパターンを形成した後、最終製品にも残存する永久膜として好適である。永久膜の具体例としては、半導体デバイス関係では、ソルダーレジスト、パッケージ材、アンダーフィル材、回路素子等のパッケージ接着層や集積回路素子と回路基板の接着層、薄型ディスプレー関連では、薄膜トランジスタ保護膜、液晶カラーフィルター保護膜、ブラックマトリクス、スペーサーなどが挙げられる。特に、本実施形態の組成物からなる永久膜は、耐熱性や耐湿性に優れている上に昇華成分による汚染性が少ないという非常に優れた利点も有する。特に表示材料において、重要な汚染による画質劣化の少ない高感度、高耐熱、吸湿信頼性を兼ね備えた材料となる。
化合物の分子量は、Water社製Acquity UPLC/MALDI-Synapt HDMSを用いて、LC-MS分析により測定した。
また、以下の条件でゲル浸透クロマトグラフィー(GPC)分析を行い、ポリスチレン換算の重量平均分子量(Mw)、数平均分子量(Mn)、及び分散度(Mw/Mn)を求めた。
装置:Shodex GPC-101型(昭和電工(株)製)
カラム:KF-80M×3
溶離液:THF 1ml/min
温度:40℃
23℃にて、化合物をプロピレングリコールモノメチルエーテル(PGME)、シクロヘキサノン(CHN)、乳酸エチル(EL)、メチルアミルケトン(MAK)またはテトラメチルウレア(TMU)に対して3質量%溶液になるよう攪拌して溶解させた後、1週間経過させた。以下の基準に従って化合物の溶解性を評価した。
評価A:目視にていずれかの溶媒で析出物が生成していないことを確認した。
評価C:目視にていずれかの溶媒で析出物が生成されていることを確認した。
化合物の構造は、Bruker社製「Advance600II spectrometer」を用いて、以下の条件で、1H-NMR測定を行い、確認した。
周波数:400mhz
溶媒:d6-DMSO
内部標準:TMS
測定温度:23℃
攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に2,6-ナフタレンジオール(シグマ-アルドリッチ社製試薬)3.20g(20mmol)と4-ビフェニルカルボキシアルデヒド(三菱瓦斯化学社製)1.82g(10mmol)とを30mlメチルイソブチルケトンに仕込み、95%の硫酸5mlを加えて、反応液を100℃で6時間撹拌して反応を行った。次に反応液を濃縮し、純水50gを加えて反応生成物を析出させ、室温まで冷却した後、濾過を行って分離した。得られた固形物を濾過し、乾燥させた後、カラムクロマトによる分離精製を行い、下記式(XBisN-1)で示される目的化合物が3.05g得られた。400mhz-1H-NMRにより下記式(XBisN-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
Δ(ppm)9.7(2H,O-H)、7.2~8.5(19H,Ph-H)、6.6(1H,C-H)
尚、2,6-ナフタレンジオールの置換位置が1位であることは、3位と4位のプロトンのシグナルがダブレットであることから確認した。
攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に上述の式(XBisN-1)で示される化合物10g(21mmol)と炭酸カリウム14.8g(107mmol)とを50mlジメチルホルムアミドに仕込み、酢酸-2-クロロエチル6.56g(54mmol)を加えて、反応液を90℃で12時間撹拌して反応を行った。次に反応液を氷浴で冷却し結晶を析出させ、濾過を行って分離した。続いて攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に前記結晶40g、メタノール40g、THF100g及び24%水酸化ナトリウム水溶液を仕込み、反応液を還流下で4時間撹拌して反応を行った。その後、氷浴で冷却し、反応液を濃縮し析出した固形物を濾過し、乾燥させた後、カラムクロマトによる分離精製を行い、下記式(E-XBisN-1)で示される目的化合物が5.9g得られた。400mhz-1H-NMRにより下記式(E-XBisN-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
Δ(ppm)8.6(2H,O-H)、7.2~7.8(19H,Ph-H)、6.7(1H,C-H)、4.0(4H,-O-CH2-)、3.8(4H,-CH2-OH)
攪拌機、冷却管及びビュレットを備えた内容積200mlの容器を準備した。この容器に、4,4-ビフェノール(東京化成社製試薬)30g(161mmol)と、4-ビフェニルアルデヒド(三菱瓦斯化学社製)15g(82mmol)と、酢酸ブチル100mlとを仕込み、p-トルエンスルホン酸(関東化学社製試薬)3.9g(21mmol)を加えて、反応液を調製した。この反応液を90℃で3時間撹拌して反応を行った。次に、反応液を濃縮し、ヘプタン50gを加えて反応生成物を析出させ、室温まで冷却した後、濾過を行って分離した。濾過により得られた固形物を乾燥させた後、カラムクロマトによる分離精製を行うことにより、下記式で表される目的化合物(BisF-1)5.8gを得た。
なお、400mhz-1H-NMRにより以下のピークが見出され、下記式(BisF-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
Δ(ppm)9.4(4H,O-H)、6.8~7.8(22H,Ph-H)、6.2(1H,C-H)
得られた化合物について、前記方法により分子量を測定した結果、536であった。
攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に前記式(BisF-1)で表される化合物11.2g(21mmol)と炭酸カリウム14.8g(107mmol)とを50mlジメチルホルムアミドに仕込み、酢酸-2-クロロエチル6.56g(54mmol)を加えて、反応液を90℃で12時間撹拌して反応を行った。次に反応液を氷浴で冷却し結晶を析出させ、濾過を行って分離した。続いて攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に前記結晶40g、メタノール40g、THF100g及び24%水酸化ナトリウム水溶液を仕込み、反応液を還流下で4時間撹拌して反応を行った。その後、氷浴で冷却し、反応液を濃縮し析出した固形物を濾過し、乾燥させた後、カラムクロマトによる分離精製を行い、下記式(E-BisF-1)で表される目的化合物が5.9g得られた。
1H-NMR:(d-DMSO、内部標準TMS)
Δ(ppm)8.6(4H,O-H)、6.8~7.8(22H,Ph-H)、6.2(1H,C-H)、4.0(8H,-O-CH2-)、3.8(8H,-CH2-OH)
得られた化合物について、前記方法により分子量を測定した結果、712であった。
攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に前記式(XBisN-1)で表される化合物10.0g(21mmol)とビニルベンジルクロライド(商品名CMS-P;セイミケミカル(株)製)6.4gとを50mlジメチルホルムアミドに仕込み、50℃に加温して撹拌した状態で、28質量%ナトリウムメトキシド(メタノール溶液)8.0gを滴下ロートより20分かけて加えて、反応液を50℃で1時間撹拌して反応を行った。次に28質量%ナトリウムメトキシド(メタノール溶液)1.6gを加え、反応液を60℃加温して3時間撹拌し、さらに85質量%燐酸1.2gを加え、10分間撹拌した後、40℃まで冷却し、反応液を純水中に滴下して析出した固形物を濾過し、乾燥させた後、カラムクロマトによる分離精製を行い、下記式(SXBisN-1)で表される目的化合物が4.0g得られた。
400mhz-1H-NMRにより、下記式(SXBisN-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
Δ(ppm)7.2~8.5(27H,Ph-H)、5.2~6.7(11H,-CH2-、-CH=CH2、C-H)
熱分解温度は400℃、ガラス転移点は115℃、融点は225℃であり、高耐熱性が確認できた。
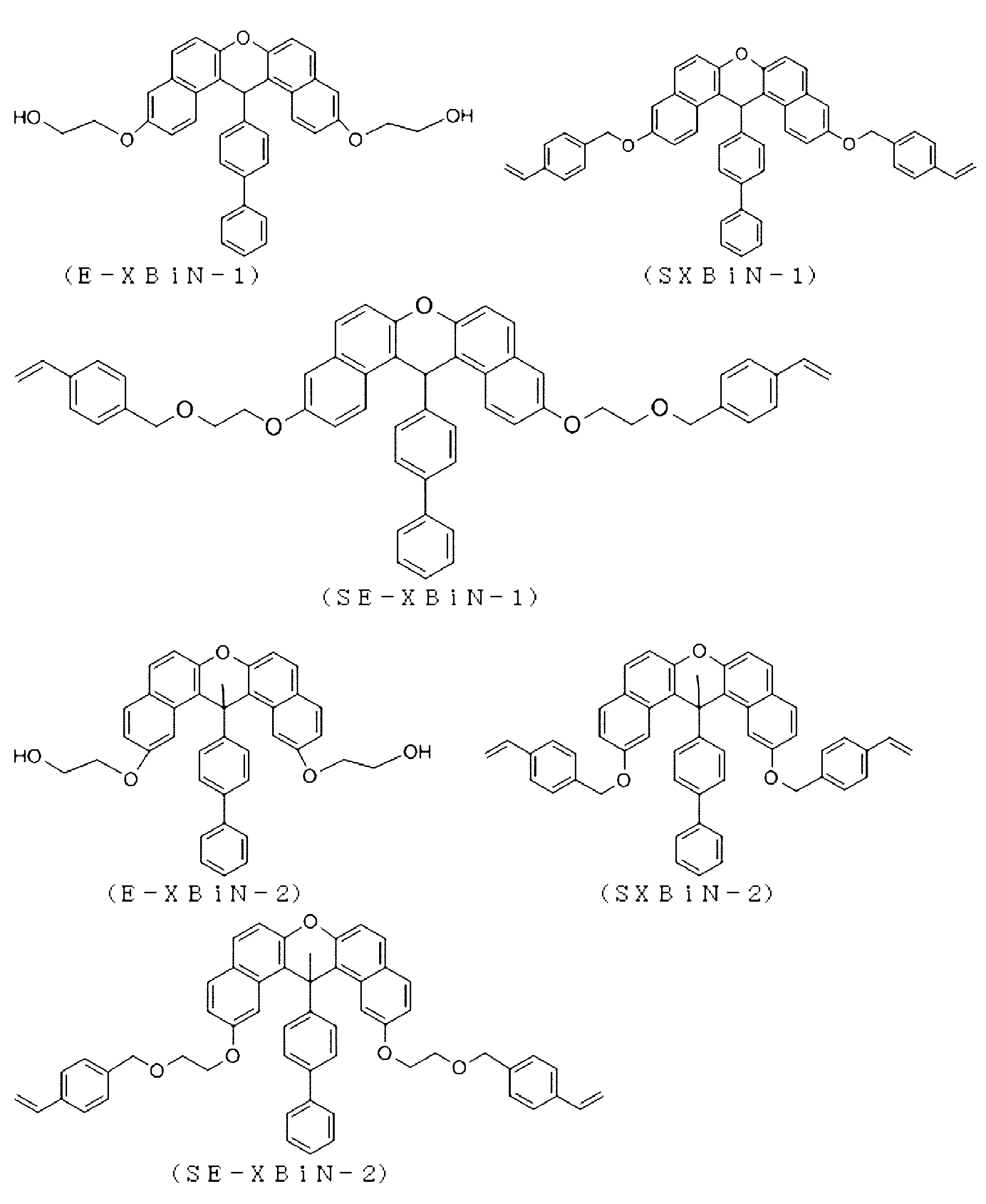
前記式(XBisN-1)で表される化合物の代わりに、前記式(E-XBisN-1)で表される化合物を用いた以外、合成実施例1-1と同様に反応させ、下記式(SE-XBisN-1)で表される目的化合物が4.0g得られた。
400mhz-1H-NMRにより、下記式(SE-XBisN-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
Δ(ppm)7.2~7.8(19H,Ph-H)、6.7(19H,-CH2-CH2-、-CH2-、-CH=CH2、C-H)
熱分解温度は380℃、ガラス転移点は100℃、融点は205℃であり、高耐熱性が確認できた。
前記式(XBisN-1)で表される化合物の代わりに、前記式(BisF-1)で表される化合物を用いた以外、合成実施例1-1と同様に反応させ、下記式(SBisF-1)で表される目的化合物が3.2g得られた。
400mhz-1H-NMRにより、下記式(sbisf-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
Δ(ppm)6.8~7.8(38H,Ph-H)、6.2(21H,-CH2-、-CH=CH2、C-H)
熱分解温度は400℃、ガラス転移点は90℃、融点は225℃であり、高耐熱性が確認できた。
前記式(BisF-1)で表される化合物の代わりに、前記式(E-BisF-1)で表される化合物を用いた以外、合成実施例2-1と同様に反応させ、下記式(SE-BisF-1)で表される目的化合物が3.3g得られた。
400mhz-1H-NMRにより、下記式(SE-BisF-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
Δ(ppm)6.8~7.8(22H,Ph-H)、6.2(37H,-CH2-CH2-、-CH2-、-CH=CH2、C-H)
熱分解温度は380℃、ガラス転移点は70℃、融点は200℃であり、高耐熱性が確認できた。
熱分解温度は375℃、ガラス転移点は65℃、融点は190℃であり、高耐熱性が確認できた。
<合成例3> BiN-1の合成
攪拌機、冷却管及びビュレットを備えた内容積300mLの容器において、2-ナフトール(シグマ-アルドリッチ社製試薬)10g(69.0mmol)を120℃で溶融後、硫酸0.27gを仕込み、4-アセチルビフェニル(シグマ-アルドリッチ社製試薬)2.7g(13.8mmol)を加えて、内容物を120℃で6時間撹拌して反応を行って反応液を得た。次に反応液にN-メチル-2-ピロリドン(関東化学株式会社製)100mL、純水50mLを加えたあと、酢酸エチルにより抽出した。次に純水を加えて中性になるまで分液後、濃縮を行って溶液を得た。
得られた溶液を、カラムクロマトによる分離後、下記式(BiN-1)で表される目的化合物(BiN-1)が1.0g得られた。
得られた化合物(BiN-1)について、上述の方法により分子量を測定した結果、466であった。
得られた化合物(BiN-1)について、上述の測定条件で、NMR測定を行ったところ、以下のピークが見出され、下記式(BiN-1)の化学構造を有することを確認した。
δ(ppm)9.69(2H,O-H)、7.01~7.67(21H,Ph-H)、2.28(3H,C-H)
攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に前記式で示される化合物(BiN-1)10.5g(21mmol)と炭酸カリウム14.8g(107mmol)とを50mlジメチルホルムアミドに仕込み、酢酸-2-クロロエチル6.56g(54mmol)を加えて、反応液を90℃で12時間撹拌して反応を行った。次に反応液を氷浴で冷却し結晶を析出させ、濾過を行って分離した。続いて攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に前記結晶40g、メタノール40g、THF100g及び24%水酸化ナトリウム水溶液を仕込み、反応液を還流下で5時間撹拌して反応を行った。その後、氷浴で冷却し、反応液を濃縮し析出した固形物を濾過し、乾燥させた後、カラムクロマトグラフによる分離精製を行い、下記式で示される目的化合物を4.6g得た。400MHz-1H-NMRにより下記式の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)8.6(2H,O-H)、7.2~7.8(19H,Ph-H)、6.7(1H,C-H)、4.0(4H,-O-CH2-)、3.8(4H,-CH2-OH)
攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に前記式(BiN-1)で表される化合物10.0g(21mmol)とビニルベンジルクロライド(商品名CMS-P;セイミケミカル(株)製)6.4gとを50mlジメチルホルムアミドに仕込み、50℃に加温して撹拌した状態で、28質量%ナトリウムメトキシド(メタノール溶液)8.0gを滴下ロートより20分かけて加えて、反応液を50℃で1時間撹拌して反応を行った。次に28質量%ナトリウムメトキシド(メタノール溶液)1.6gを加え、反応液を60℃加温して3時間撹拌し、さらに85質量%燐酸1.2gを加え、10分間撹拌した後、40℃まで冷却し、反応液を純水中に滴下して析出した固形物を濾過し、乾燥させた後、カラムクロマトグラフによる分離精製を行い、下記式(SBiN-1)で表される目的化合物4.0gを得た。
400MHz-1H-NMRにより、下記式(SBiN-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)7.2~7.8(19H,Ph-H)、5.2~6.7(10H,-CH2-、-CH=CH2、C-H)、2.3(3H,-CH3)
熱分解温度は375℃、ガラス転移点は105℃、融点は212℃であり、高耐熱性を有することが確認できた。
前記式(BiN-1)で表される化合物の代わりに、前記式(E-BiN-1)で表される化合物を用いた以外、合成実施例3-1と同様に反応させ、下記式(SE-BiN-1)で表される目的化合物が3.6g得られた。
400MHz-1H-NMRにより、下記式(SE-BiN-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)7.2~7.8(19H,Ph-H)、6.7(18H,-CH2-CH2-、-CH2-、-CH=CH2、C-H)、2.3(3H,-CH3)
熱分解温度は361℃、ガラス転移点は112℃、融点は212℃であり、高耐熱性を有することが確認できた。
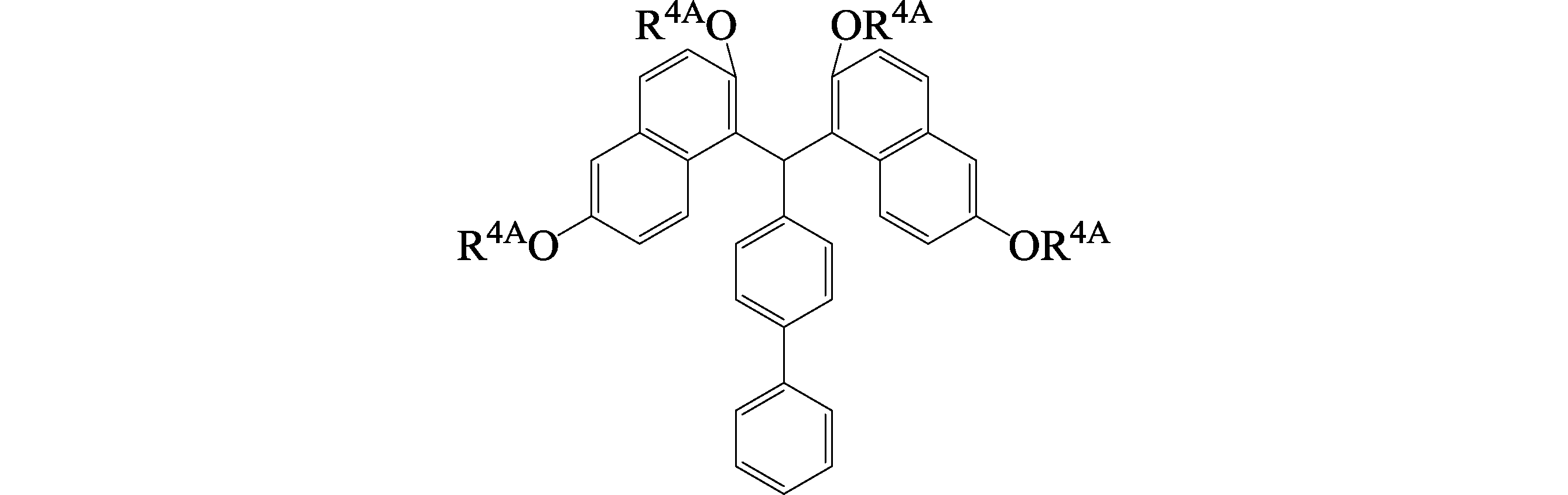
2-ナフトールの代わりに、o-フェニルフェノールを使用する以外は合成例1と同様に反応させ、下記式(BiP-1)で表される目的化合物が1.0g得られた。
得られた化合物(BiP-1)について、上述の方法により分子量を測定した結果、466であった。
得られた化合物(BiP-1)について、上述の測定条件で、NMR測定を行ったところ、以下のピークが見出され、下記式(BiP-1)の化学構造を有することを確認した。
δ(ppm)9.67(2H,O-H)、6.98~7.60(25H,Ph-H)、2.25(3H,C-H)
攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に前記式(BiP-1)で表される化合物11.2g(21mmol)と炭酸カリウム14.8g(107mmol)とを50mlジメチルホルムアミドに仕込み、酢酸-2-クロロエチル6.56g(54mmol)を加えて、反応液を90℃で12時間撹拌して反応を行った。次に反応液を氷浴で冷却し結晶を析出させ、濾過を行って分離した。続いて攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に前記結晶40g、メタノール40g、THF100g及び24%水酸化ナトリウム水溶液を仕込み、反応液を還流下で4時間撹拌して反応を行った。その後、氷浴で冷却し、反応液を濃縮し析出した固形物を濾過し、乾燥させた後、カラムクロマトグラフによる分離精製を行い、下記式(E-BisP-1)で表される目的化合物5.9gを得た。
400MHz-1H-NMRにより、下記式(E-BiP-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)8.6(4H,O-H)、6.8~7.6(25H,Ph-H)、4.0(4H,-O-CH2-)、3.8(4H,-CH2-OH)、2.2(3H,C-H)
得られた化合物について、前記方法により分子量を測定した結果、606であった。
前記式(XBisN-1)で表される化合物の代わりに、前記式(BiP-1)で表される化合物を用いたこと以外は合成実施例1-1と同様に反応させ、下記式(SBiP-1)で表される目的化合物3.0gを得た。
400MHz-1H-NMRにより、下記式(SBiP-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)6.8~7.8(25H,Ph-H)、5.2~6.7(10H,-CH2-、-CH=CH2、C-H)、2.3(3H,-CH3)
熱分解温度は390℃、ガラス転移点は74℃、融点は202℃であり、高耐熱性を有することが確認できた。
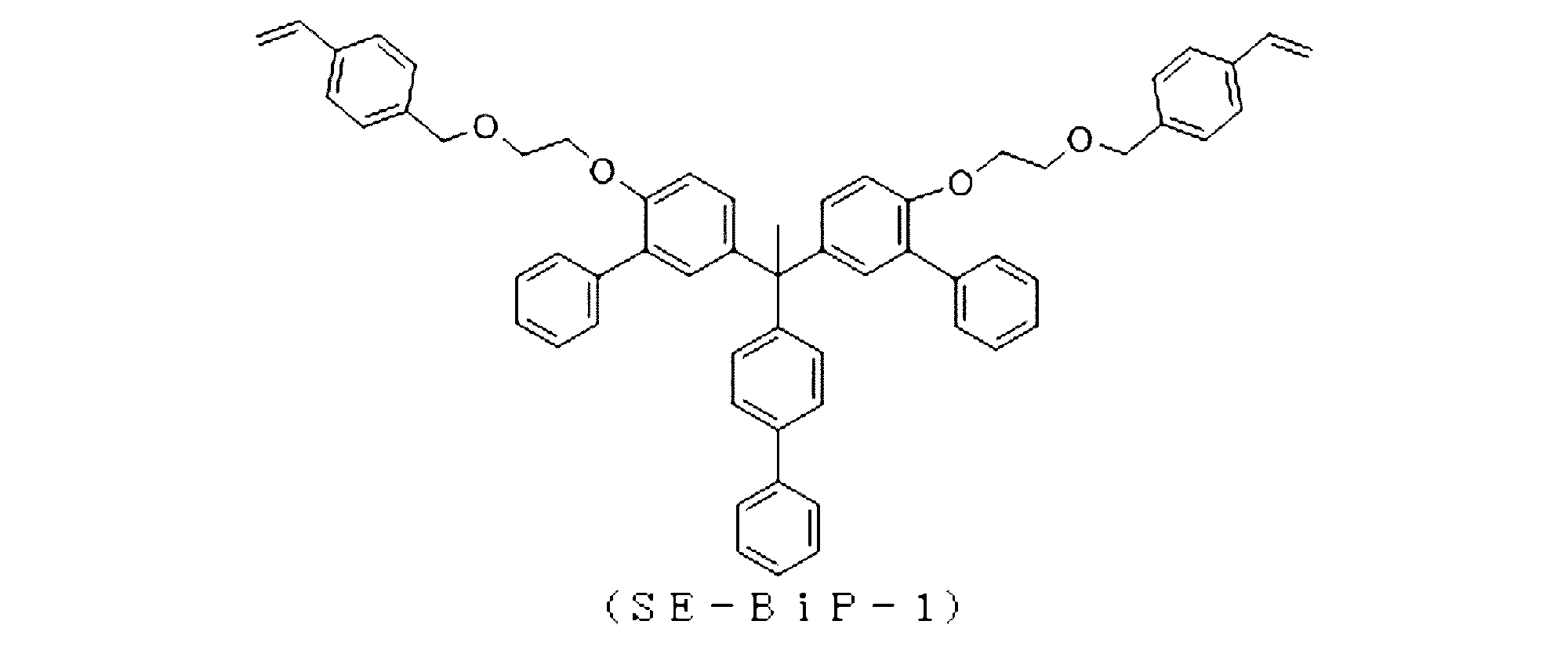
前記式(BiP-1)で表される化合物の代わりに、前記式(E-BiP-1)で表される化合物を用いた以外、合成実施例4-1と同様に反応させ、下記式(SE-BiP-1)で表される目的化合物が2.9g得られた。
400MHz-1H-NMRにより、下記式(SE-BiP-1)の化学構造を有することを確認した。
1H-NMR:(d-DMSO、内部標準TMS)
δ(ppm)6.8~7.8(25H,Ph-H)、6.7(18H,-CH2-CH2-、-CH2-、-CH=CH2、C-H)、2.3(3H,-CH3)
熱分解温度は365℃、ガラス転移点は82℃、融点は220℃であり、高耐熱性を有することが確認できた。
合成例3の原料である2-ナフトール(原料1)及び4-アセチルビフェニル(原料2)を表1のように変更し、その他は合成例3と同様に行い、各目的物を得た。
それぞれ、1H-NMRで同定した。
合成例1の原料である4-ビフェニルカルボキシアルデヒドを表3のように変更し、その他は合成実施例1と同様に行い、各目的物を得た。
それぞれ、1H-NMRで同定した。
合成例3の原料である2-ナフトール(原料1)及び4-アセチルビフェニル(原料2)を表5のように変更し、水1.5mL、ドデシルメルカプタン73mg(0.35mmol)、37%塩酸2.3g(22mmol)を加え、反応温度を55℃に変更し、その他は合成例31と同様に行い、各目的物を得た。
それぞれ、1H-NMRで同定した。
合成例3Aの原料である前記式(BiN-1)で表される化合物を表7のように変更し、その他は合成例3Aと同様の条件にて合成を行い、それぞれ、目的物を得た。各化合物の構造は400MHz-1H-NMR(d-DMSO、内部標準TMS)およびLC-MSで分子量を確認することにより、同定した。
合成実施例3-1の原料である前記式(BiN-1)で表される化合物を表7のように変更し、その他は合成実施例3-1と同様の条件にて合成を行い、それぞれ、目的物を得た。各化合物の構造は400MHz-1H-NMR(d-DMSO、内部標準TMS)およびLC-MSで分子量を確認することにより、同定した。
合成実施例3-2の原料である前記式(E-BiN-1)で表される化合物を表7のように変更し、その他は合成実施例3-2と同様の条件にて合成を行い、それぞれ、目的物を得た。各化合物の構造は400MHz-1H-NMR(d-DMSO、内部標準TMS)およびLC-MSで分子量を確認することにより、同定した。
ジムロート冷却管、温度計及び攪拌翼を備えた、底抜きが可能な内容積1Lの四つ口フラスコを準備した。この四つ口フラスコに、窒素気流中、合成例1で得られた化合物(XBisN-1)を32.6g(70mmol、三菱ガス化学(株)製)、40質量%ホルマリン水溶液21.0g(ホルムアルデヒドとして280mmol、三菱ガス化学(株)製)及び98質量%硫酸(関東化学(株)製)0.97mLを仕込み、常圧下、100℃で還流させながら7時間反応させた。その後、希釈溶媒としてオルソキシレン(和光純薬工業(株)製試薬特級)180.0gを反応液に加え、静置後、下相の水相を除去した。さらに、中和及び水洗を行い、オルソキシレンを減圧下で留去することにより、褐色固体の樹脂(R1-XBisN-1)34.1gを得た。
ジムロート冷却管、温度計及び攪拌翼を備えた、底抜きが可能な内容積1Lの四つ口フラスコを準備した。この四つ口フラスコに、窒素気流中、合成例1で得られた化合物(XBisN-1)を32.6g(70mmol、三菱ガス化学(株)製)、4-ビフェニルアルデヒド50.9g(280mmol、三菱ガス化学(株)製)、アニソール(関東化学(株)製)100mL及びシュウ酸二水和物(関東化学(株)製)10mLを仕込み、常圧下、100℃で還流させながら7時間反応させた。その後、希釈溶媒としてオルソキシレン(和光純薬工業(株)製試薬特級)180.0gを反応液に加え、静置後、下相の水相を除去した。さらに、中和及び水洗を行い、有機相の溶媒および未反応の4-ビフェニルアルデヒドを減圧下で留去することにより、褐色固体の樹脂(R2-XBisN-1)34.7gを得た。
攪拌機、冷却管及びビュレットを備えた内容積500mlの容器に上術の式で示される樹脂(R1-XBisN-1)30gと炭酸カリウム29.6g(214mmol)とを100mlジメチルホルムアミドに仕込み、酢酸-2-クロロエチル13.12g(108mmol)を加えて、反応液を90℃で12時間撹拌して反応を行った。次に反応液を氷浴で冷却し結晶を析出させ、濾過を行って分離した。続いて攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に前記結晶40g、メタノール80g、THF100g及び24%水酸化ナトリウム水溶液を仕込み、反応液を還流下で4時間撹拌して反応を行った。その後、氷浴で冷却し、反応液を濃縮し析出した固形物を濾過し、乾燥させることにより、褐色固体の樹脂(E-R1-XBisN-1)26.5gを得た。
攪拌機、冷却管及びビュレットを備えた内容積500mlの容器に前記式(R1-XBisN-1)で表される樹脂20.0gとビニルベンジルクロライド(商品名CMS-P;セイミケミカル(株)製)12.8gとを200mlジメチルホルムアミドに仕込み、50℃に加温して撹拌した状態で、28質量%ナトリウムメトキシド(メタノール溶液)16.0gを滴下ロートより20分かけて加えて、反応液を50℃で1時間撹拌して反応を行った。次に28質量%ナトリウムメトキシド(メタノール溶液)3.2gを加え、反応液を60℃加温して5時間撹拌し、さらに85質量%燐酸2.4gを加え、10分間撹拌した後、40℃まで冷却し、反応液を純水中に滴下して析出した固形物を濾過し、乾燥させた後、 50℃まで冷却し、反応液を純水中に滴下して析出した固形物を濾過し、乾燥させた後、灰色固体の(SR1-XBisN-1)で表される樹脂27.2gを得た。
合成例23で得られた前記式(R1-XBisN-1)で表される樹脂の代わりに、合成例23Aで得られた前記式(E-R1-XBisN-1)を用いたこと以外は合成実施例23-1と同様に反応させ、褐色固体の(SE-R1-XBisN-1)で表される樹脂31.3gを得た。
攪拌機、冷却管及びビュレットを備えた内容積500mlの容器に上述の樹脂(R2-XBisN-1)30gと炭酸カリウム29.6g(214mmol)とを100mlジメチルホルムアミドに仕込み、酢酸-2-クロロエチル13.12g(108mmol)を加えて、反応液を90℃で12時間撹拌して反応を行った。次に反応液を氷浴で冷却し結晶を析出させ、濾過を行って分離した。続いて攪拌機、冷却管及びビュレットを備えた内容積100mlの容器に前記結晶40g、メタノール80g、THF100g及び24%水酸化ナトリウム水溶液を仕込み、反応液を還流下で4時間撹拌して反応を行った。その後、氷浴で冷却し、反応液を濃縮し析出した固形物を濾過し、乾燥させることにより、褐色固体の樹脂(E-R2-XBisN-1)22.3gを得た。
合成例23で得られた上記式(R1-XBisN-1)の代わりに、合成例24で得られた上記式(R2-XBisN-1)で表される化合物30.5gを使用した以外は合成実施例23-1と同様に反応させ、薄灰色固体の(SR2-XBisN-1)で表される樹脂35.1gを得た。
合成例23で得られた上記式(R1-XBisN-1)で表される樹脂の代わりに、合成例24Aで得られた上記式(E-R2-XBisN-1)を用いたこと以外は合成実施例23-1と同様に反応させ、褐色固体の(SE-R2-XBisN-1)で表される樹脂28.4gを得た。
ジムロート冷却管、温度計及び攪拌翼を備えた、底抜きが可能な内容積10Lの四つ口フラスコを準備した。この四つ口フラスコに、窒素気流中、1,5-ジメチルナフタレン1.09kg(7mol、三菱ガス化学(株)製)、40質量%ホルマリン水溶液2.1kg(ホルムアルデヒドとして28mol、三菱ガス化学(株)製)及び98質量%硫酸(関東化学(株)製)0.97mlを仕込み、常圧下、100℃で還流させながら7時間反応させた。その後、希釈溶媒としてエチルベンゼン(和光純薬工業(株)製試薬特級)1.8kgを反応液に加え、静置後、下相の水相を除去した。さらに、中和及び水洗を行い、エチルベンゼン及び未反応の1,5-ジメチルナフタレンを減圧下で留去することにより、淡褐色固体のジメチルナフタレンホルムアルデヒド樹脂1.25kgを得た。
得られたジメチルナフタレンホルムアルデヒドの分子量は、Mn:562、であった。
得られた樹脂(CR-1)は、Mn:885、Mw:2220、Mw/Mn:4.17であった。
前記合成実施例1-1~24-2に記載の化合物あるいは樹脂、合成比較例1に記載のCR-1を用いて溶解度試験を行った。結果を表8に示す。
また、下記表8に示す組成のリソグラフィー用下層膜形成材料を各々調製した。次に、これらのリソグラフィー用下層膜形成材料をシリコン基板上に回転塗布し、その後、240℃で60秒間、さらに400℃で120秒間ベークして、膜厚200nmの下層膜を各々作製した。酸発生剤、架橋剤及び有機溶媒については次のものを用いた。
・酸発生剤:みどり化学社製 ジターシャリーブチルジフェニルヨードニウムノナフルオロメタンスルホナート(DTDPI)
・架橋剤:三和ケミカル社製 ニカラックMX270(ニカラック)
有機溶媒:プロピレングリコールモノメチルエーテルアセテートアセテート(PGMEA)
・ノボラック:群栄化学社製 PSM4357
・架橋剤:
三菱ガス化学製 ジアリルビスフェノールA型シアネート(DABPA-CN)
小西化学工業製 ジアリルビスフェノールA(BPA-CA)
小西化学工業製 ベンゾオキサジン(BF-BXZ)
日本化薬製 ビフェニルアラルキル型エポキシ樹脂(NC-3000-L)
・有機溶媒:
プロピレングリコールモノメチルエーテルアセテートアセテート(PGMEA)
以下に示す条件でエッチング試験を行い、エッチング耐性を評価した。評価結果を表8および表9に示す。
エッチング装置:サムコインターナショナル社製「RIE-10NR」
出力:50W
圧力:20Pa
時間:2min
エッチングガス
Arガス流量:CF4ガス流量:O2ガス流量=50:5:5(sccm)
まず、実施例1-1において用いる化合物(SXBisN-1)に代えてノボラック(群栄化学社製「PSM4357」)を用いること以外は、実施例1と同様の条件で、ノボラックの下層膜を作製した。そして、このノボラックの下層膜を対象として、上述のエッチング試験を行い、そのときのエッチングレートを測定した。
そして、ノボラックの下層膜のエッチングレートを基準として、以下の評価基準でエッチング耐性を評価した。
A:ノボラックの下層膜に比べてエッチングレートが、-10%未満
B:ノボラックの下層膜に比べてエッチングレートが、-10%~+5%
C:ノボラックの下層膜に比べてエッチングレートが、+5%超
また、上述のように実施例の化合物は耐熱性に優れていた。
次に、次に、SXBisN-1、SE-XBisN-1、SBisF-1又はSE-BisF-1を含むリソグラフィー用下層膜形成材料の各溶液を膜厚300nmのsio2基板上に塗布して、240℃で60秒間、さらに400℃で120秒間ベークすることにより、膜厚70nmの下層膜を形成した。この下層膜上に、arf用レジスト溶液を塗布し、130℃で60秒間ベークすることにより、膜厚140nmのフォトレジスト層を形成した。なお、arfレジスト溶液としては、下記式(11)の化合物:5質量部、トリフェニルスルホニウムノナフルオロメタンスルホナート:1質量部、トリブチルアミン:2質量部、及びPGMEA:92質量部を配合して調製したものを用いた。
下層膜の形成を行わないこと以外は、実施例45と同様にして、フォトレジスト層をsio2基板上に直接形成し、ポジ型のレジストパターンを得た。結果を表10に示す。
現像後のレジストパターン形状の相違から、実施例45~48において用いたリソグラフィー用下層膜形成材料は、レジスト材料との密着性がよいことが示された。
実施例1-1~2-2のリソグラフィー用下層膜形成材料の溶液を膜厚300nmのsio2基板上に塗布して、240℃で60秒間、さらに400℃で120秒間ベークすることにより、膜厚80nmの下層膜を形成した。この下層膜上に、珪素含有中間層材料を塗布し、200℃で60秒間ベークすることにより、膜厚35nmの中間層膜を形成した。さらに、この中間層膜上に、前記arf用レジスト溶液を塗布し、130℃で60秒間ベークすることにより、膜厚150nmのフォトレジスト層を形成した。なお、珪素含有中間層材料としては、特開2007-226170号公報<合成例1>に記載の珪素原子含有ポリマーを用いた。
その後、サムコインターナショナル社製 RIE-10NRを用いて、得られたレジストパターンをマスクにして珪素含有中間層膜(SOG)のドライエッチング加工を行い、続いて、得られた珪素含有中間層膜パターンをマスクにした下層膜のドライエッチング加工と、得られた下層膜パターンをマスクにしたsio2膜のドライエッチング加工とを順次行った。
(レジストパターンのレジスト中間層膜へのエッチング条件)
出力:50W
圧力:20Pa
時間:1min
エッチングガス
Arガス流量:CF4ガス流量:O2ガス流量=50:8:2(sccm)
出力:50W
圧力:20Pa
時間:2min
エッチングガス
Arガス流量:CF4ガス流量:O2ガス流量=50:5:5(sccm)
出力:50W
圧力:20Pa
時間:2min
エッチングガス
Arガス流量:C5F12ガス流量:C2F6ガス流量:O2ガス流量=50:4:3:1(sccm)
上述のようにして得られたパターン断面(エッチング後のsio2膜の形状)を、(株)日立製作所製電子顕微鏡(S-4800)を用いて観察したところ、本実施形態の下層膜を用いた実施例は、多層レジスト加工におけるエッチング後のsio2膜の形状は矩形であり、欠陥も認められず良好であることが確認された。
前記合成実施例で合成した各化合物を用いて、下記表11に示す配合で光学部品形成組成物を調製した。なお、表11中の光学部品形成組成物の各成分のうち、酸発生剤、架橋剤、酸拡散抑制剤、及び溶媒については、以下のものを用いた。
・酸発生剤:みどり化学社製 ジターシャリーブチルジフェニルヨードニウムノナフルオロメタンスルホナート(DTDPI)
・架橋剤:三和ケミカル社製 ニカラックMX270(ニカラック)
有機溶媒:プロピレングリコールモノメチルエーテルアセテートアセテート(PGMEA)
均一状態の光学部品形成組成物を清浄なシリコンウェハー上に回転塗布した後、110℃のオーブン中でプレベーク(prebake:PB)して、厚さ1μmの光学部品形成膜を形成した。調製した光学部品形成組成物について、膜形成が良好な場合には「A」、形成した膜に欠陥がある場合には「C」と評価した。
前記合成例、及び合成実施例で合成した各化合物を用いて、下記表12に示す配合でレジスト組成物を調製した。なお、表12中のレジスト組成物の各成分のうち、ラジカル発生剤、ラジカル拡散抑制剤、及び溶媒については、以下のものを用いた。
・ラジカル重合開始剤:BASF社製 IRGACURE184
・ラジカル拡散制御剤:BASF社製 IRGACURE1010
有機溶媒:プロピレングリコールモノメチルエーテルアセテートアセテート(PGMEA)
(1)レジスト組成物の保存安定性及び薄膜形成
レジスト組成物の保存安定性は、レジスト組成物を作成後、23℃、50%RHにて3日間静置し、析出の有無を目視にて観察することにより評価した。3日間静置後のレジスト組成物において、均一溶液であり析出がない場合にはA、析出がある場合はCと評価した。また、均一状態のレジスト組成物を清浄なシリコンウェハー上に回転塗布した後、110℃のオーブン中で露光前ベーク(PB)して、厚さ40nmのレジスト膜を形成した。作成したレジスト組成物について、薄膜形成が良好な場合にはA、形成した膜に欠陥がある場合にはCと評価した。
均一なレジスト組成物を清浄なシリコンウェハー上に回転塗布した後、110℃のオーブン中で露光前ベーク(PB)して、厚さ60nmのレジスト膜を形成した。得られたレジスト膜に対して、電子線描画装置(ELS-7500、(株)エリオニクス社製)を用いて、50nm、40nm及び30nm間隔の1:1のラインアンドスペース設定の電子線を照射した。当該照射後に、レジスト膜を、それぞれ所定の温度で、90秒間加熱し、PGMEに60秒間浸漬して現像を行った。その後、レジスト膜を、超純水で30秒間洗浄、乾燥して、ネガ型のレジストパターンを形成した。形成されたレジストパターンについて、ラインアンドスペースを走査型電子顕微鏡((株)日立ハイテクノロジー製S-4800)により観察し、レジスト組成物の電子線照射による反応性を評価した。
感度は、パターンを得るために必要な単位面積当たりの最小のエネルギー量で示し、以下に従って評価した。
A:50μC/cm2未満でパターンが得られた場合
C:50μC/cm2以上でパターンが得られた場合
パターン形成は、得られたパターン形状をSEM(走査型電子顕微鏡:Scanning Electron Microscope)にて観察し、以下に従って評価した。
A:矩形なパターンが得られた場合
B:ほぼ矩形なパターンが得られた場合
C:矩形でないパターンが得られた場合
また、湿式プロセスが適用可能であり、耐熱性及びエッチング耐性に優れるフォトレジスト下層膜を形成するために有用な化合物、樹脂及びリソグラフィー用膜形成組成物を実現することができる。そして、このリソグラフィー用膜形成組成物は、耐熱性が高く、溶媒溶解性も高い、特定構造を有する化合物又は樹脂を用いているため、高温ベーク時の膜の劣化が抑制され、酸素プラズマエッチング等に対するエッチング耐性にも優れたレジスト及び下層膜を形成することができる。さらには、下層膜を形成した場合、レジスト層との密着性にも優れるので、優れたレジストパターンを形成することができる。
さらには屈折率が高く、また低温~高温処理によって着色が抑制されることから、各種光学部品形成組成物としても有用である。
特に、本発明はリソグラフィー用レジスト、リソグラフィー用下層膜及び多層レジスト用下層膜及び光学部品の分野において、特に有効に利用可能である。
また、明細書に記載された全ての文献、特許出願、及び技術規格は、個々の文献、特許出願、及び技術規格が参照により取り込まれることが具体的かつ個々に記された場合と同程度に、本明細書中に参照により取り込まれる。
Claims (25)
- 下記式(1)で表される化合物。
(式(1)中、R0は、水素原子、炭素数1~30のアルキル基又は炭素数6~30のアリール基であり、
R1は、炭素数1~60のn価の基又は単結合であり、
R2~R5は、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、置換基を有していてもよい炭素数1~30のアルコキシ基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基、水酸基又は水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、前記アルキル基、前記アリール基、前記アルケニル基、前記アルコキシ基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、ここで、R2~R5の少なくとも1つは水酸基の水素原子がビニルフェニルメチル基又はビニルフェニルメチルオキシアルキル基で置換された基であり、
m2及びm3は、各々独立して、0~8の整数であり、
m4及びm5は、各々独立して、0~9の整数であり、
但し、m2、m3、m4及びm5は同時に0となることはなく、
nは1~4の整数であり、ここで、nが2以上の整数の場合、n個の[ ]内の構造式は同一であっても異なっていてもよく、
p2~p5は、各々独立して0~2の整数である。) - 前記式(1)で表される化合物が下記式(1-1)で表される化合物である、請求項1に記載の化合物。
(式(1-1)中、R0、R1、R4、R5、n、p2~p5、m4及びm5は、前記と同義であり、
R6~R7は、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基であり、
R10~R11は、各々独立して、水素原子又は含ビニルフェニルメチル基であり、
ここで、R10~R11の少なくとも1つはビニルフェニルメチル基又はビニルフェニルメチルオキシアルキル基であり、
m6及びm7は、各々独立して、0~7の整数である。) - 請求項4に記載の化合物をモノマーとして得られる、樹脂。
- 下記式(3)で表される構造を有する、樹脂。
(式(3)中、Lは、置換基を有していてもよい炭素数1~30のアルキレン基、置換基を有していてもよい炭素数6~30のアリーレン基、置換基を有していてもよい炭素数1~30のアルコキシレン基又は単結合であり、前記アルキレン基、前記アリーレン基、前記アルコキシレン基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、
R0は、水素原子、炭素数1~30のアルキル基又は炭素数6~30のアリール基であり、
R1は、炭素数1~60のn価の基又は単結合であり、
R2~R5は、各々独立して、置換基を有していてもよい炭素数1~30のアルキル基、置換基を有していてもよい炭素数6~30のアリール基、置換基を有していてもよい炭素数2~30のアルケニル基、置換基を有していてもよい炭素数1~30のアルコキシ基、ハロゲン原子、ニトロ基、アミノ基、カルボン酸基、チオール基、水酸基又は水酸基の水素原子が含ビニルフェニルメチル基で置換された基であり、前記アルキル基、前記アリール基、前記アルケニル基、前記アルコキシ基は、エーテル結合、ケトン結合またはエステル結合を含んでいてもよく、
m2及びm3は、各々独立して、0~8の整数であり、
m4及びm5は、各々独立して、0~9の整数であり、
但し、m2、m3、m4及びm5は同時に0となることはなく、R2~R5の少なくとも1つは水酸基の水素原子がビニルフェニルメチル基又はビニルフェニルメチルオキシアルキル基で置換された基である。
nは1~4の整数であり、ここで、nが2以上の整数の場合、n個の[ ]内の構造式は同一であっても異なっていてもよく、
p2~p5は、各々独立して0~2の整数である。) - 請求項1~4のいずれか一項に記載の化合物及び請求項5又は請求項6に記載の樹脂からなる群より選ばれる1種以上を含有する、組成物。
- 溶媒をさらに含有する、請求項7に記載の組成物。
- 酸発生剤をさらに含有する、請求項7又は請求項8に記載の組成物。
- 架橋剤をさらに含有する、請求項7~請求項9のいずれか一項に記載の組成物。
- 前記架橋剤が、フェノール化合物、エポキシ化合物、シアネート化合物、アミノ化合物、ベンゾオキサジン化合物、メラミン化合物、グアナミン化合物、グリコールウリル化合物、ウレア化合物、イソシアネート化合物及びアジド化合物からなる群より選ばれる少なくとも1種である、請求項10に記載の組成物。
- 前記架橋剤が、少なくとも1つのアリル基を有する、請求項10又は請求項11に記載の組成物。
- 前記架橋剤の含有量が、請求項1~4のいずれか一項に記載の化合物及び請求項5又は請求項6に記載の樹脂からなる群より選ばれる1種以上を含有する組成物の合計質量100質量部に対し、0.1~100質量部である、請求項10~請求項12のいずれか一項に記載の組成物。
- 架橋促進剤をさらに含有する、請求項10~13のいずれか一項に記載の組成物。
- 前記架橋促進剤が、アミン類、イミダゾール類、有機ホスフィン類、及びルイス酸からなる群より選ばれる少なくとも1種である、請求項14に記載の組成物。
- 前記架橋促進剤の含有量が、請求項1~4のいずれか一項に記載の化合物及び請求項5又は請求項6に記載の樹脂からなる群より選ばれる1種以上を含有する組成物の合計質量100質量部に対し、0.1~5質量部である、請求項14又は請求項15に記載の組成物。
- ラジカル重合開始剤をさらに含有する、請求項7~16のいずれか一項に記載の組成物。
- 前記ラジカル重合開始剤が、ケトン系光重合開始剤、有機過酸化物系重合開始剤及びアゾ系重合開始剤からなる群より選ばれる少なくとも1種である、請求項17に記載の組成物。
- 前記ラジカル重合開始剤の含有量が、請求項1~4のいずれか一項に記載の化合物及び請求項5又は請求項6に記載の樹脂からなる群より選ばれる1種以上を含有する組成物の合計質量100質量部に対し、0.05~25質量部である、請求項17又は請求項18に記載の組成物。
- リソグラフィー用膜形成に用いられる、請求項7~請求項19のいずれか一項に記載の組成物。
- レジスト永久膜形成に用いられる、請求項7~請求項19のいずれか一項に記載の組成物。
- 光学部品形成に用いられる、請求項7~請求項19のいずれか一項に記載の組成物。
- 基板上に、請求項20に記載の組成物を用いてフォトレジスト層を形成した後、前記フォトレジスト層の所定の領域に放射線を照射し、現像を行う工程を含む、レジストパターン形成方法。
- 基板上に、請求項20に記載の組成物を用いて下層膜を形成し、前記下層膜上に、少なくとも1層のフォトレジスト層を形成した後、前記フォトレジスト層の所定の領域に放射線を照射し、現像を行う工程を含む、レジストパターン形成方法。
- 基板上に、請求項20に記載の組成物を用いて下層膜を形成し、前記下層膜上に、レジスト中間層膜材料を用いて中間層膜を形成し、前記中間層膜上に、少なくとも1層のフォトレジスト層を形成した後、前記フォトレジスト層の所定の領域に放射線を照射し、現像してレジストパターンを形成し、その後、前記レジストパターンをマスクとして前記中間層膜をエッチングし、得られた中間層膜パターンをエッチングマスクとして前記下層膜をエッチングし、得られた下層膜パターンをエッチングマスクとして基板をエッチングすることにより基板にパターンを形成する工程を含む、回路パターン形成方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2021178444A JP7283515B2 (ja) | 2016-07-21 | 2021-11-01 | 化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2016143622 | 2016-07-21 | ||
| JP2016143622 | 2016-07-21 | ||
| PCT/JP2017/026530 WO2018016640A1 (ja) | 2016-07-21 | 2017-07-21 | 化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021178444A Division JP7283515B2 (ja) | 2016-07-21 | 2021-11-01 | 化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JPWO2018016640A1 JPWO2018016640A1 (ja) | 2019-05-09 |
| JP7110979B2 true JP7110979B2 (ja) | 2022-08-02 |
Family
ID=60993033
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018528904A Active JP7110979B2 (ja) | 2016-07-21 | 2017-07-21 | 化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 |
| JP2021178444A Active JP7283515B2 (ja) | 2016-07-21 | 2021-11-01 | 化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021178444A Active JP7283515B2 (ja) | 2016-07-21 | 2021-11-01 | 化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 |
Country Status (5)
| Country | Link |
|---|---|
| JP (2) | JP7110979B2 (ja) |
| KR (1) | KR20190033537A (ja) |
| CN (1) | CN109476575A (ja) |
| TW (1) | TW201815738A (ja) |
| WO (1) | WO2018016640A1 (ja) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7194355B2 (ja) * | 2016-07-21 | 2022-12-22 | 三菱瓦斯化学株式会社 | 化合物、樹脂、組成物及びパターン形成方法 |
| WO2018016634A1 (ja) * | 2016-07-21 | 2018-01-25 | 三菱瓦斯化学株式会社 | 化合物、樹脂及び組成物、並びにレジストパターン形成方法及び回路パターン形成方法 |
| WO2018101463A1 (ja) * | 2016-12-02 | 2018-06-07 | 三菱瓦斯化学株式会社 | 化合物、樹脂、組成物、パターン形成方法及び精製方法 |
| WO2019151403A1 (ja) * | 2018-01-31 | 2019-08-08 | 三菱瓦斯化学株式会社 | 組成物、並びに、レジストパターンの形成方法及び絶縁膜の形成方法 |
| JP7139622B2 (ja) * | 2018-02-28 | 2022-09-21 | 三菱瓦斯化学株式会社 | 化合物、樹脂、組成物及びパターン形成方法 |
| EP3760611A4 (en) * | 2018-02-28 | 2021-04-21 | Mitsubishi Gas Chemical Company, Inc. | COMPOUND, RESIN, COMPOSITION AND FILM FORMING MATERIAL FOR LITHOGRAPHY USING IT |
| JP2019200244A (ja) * | 2018-05-14 | 2019-11-21 | 三菱瓦斯化学株式会社 | リソグラフィー用膜形成材料、リソグラフィー用膜形成用組成物、リソグラフィー用下層膜及びパターン形成方法 |
| TW202019864A (zh) * | 2018-07-31 | 2020-06-01 | 日商三菱瓦斯化學股份有限公司 | 光學零件形成用組成物及光學零件,以及化合物及樹脂 |
| TWI812716B (zh) * | 2018-09-27 | 2023-08-21 | 日商Jsr股份有限公司 | 固體攝像元件、電子機器、感放射線性組成物及固體攝像元件的製造方法 |
| US11971659B2 (en) * | 2018-10-08 | 2024-04-30 | Taiwan Semiconductor Manufacturing Co., Ltd. | Photoresist composition and method of forming photoresist pattern |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003043687A (ja) | 2001-07-27 | 2003-02-13 | Mitsubishi Paper Mills Ltd | 感光性組成物および感光性平版印刷版材料 |
| JP2005274625A (ja) | 2004-03-22 | 2005-10-06 | Fuji Photo Film Co Ltd | 重合性組成物、及びそれを用いた画像記録材料 |
| JP2005300650A (ja) | 2004-04-07 | 2005-10-27 | Fuji Photo Film Co Ltd | 重合性組成物 |
| JP2007025275A (ja) | 2005-07-15 | 2007-02-01 | Fujifilm Holdings Corp | 感光性組成物及び感光性フィルム、並びに、永久パターン及びその形成方法 |
| JP2010072389A (ja) | 2008-09-19 | 2010-04-02 | Fujifilm Corp | 平版印刷版原版及び平版印刷版の製造方法 |
| JP2014174180A (ja) | 2013-03-05 | 2014-09-22 | Fuji Xerox Co Ltd | 電子写真感光体、プロセスカートリッジ、及び画像形成装置 |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS505084B1 (ja) * | 1970-09-16 | 1975-02-28 | ||
| FR2149433B1 (ja) * | 1971-08-19 | 1974-10-25 | Dow Chemical Co | |
| IT1161223B (it) * | 1983-04-22 | 1987-03-18 | Anic Spa | Procedimento per la preparazione di composti 2,3-diidrobenzofurano sostituito |
| JPH01503238A (ja) * | 1986-12-29 | 1989-11-02 | アライド・コーポレーション | スチレン末端基付きテトラキスフェノールの熱硬化ポリマー |
| JPS6442447A (en) * | 1987-08-10 | 1989-02-14 | Tokuyama Soda Kk | Vinylphenyl compound and production thereof |
| JPH0710902B2 (ja) * | 1987-09-04 | 1995-02-08 | 昭和高分子株式会社 | 硬化性樹脂組成物 |
| JP2868844B2 (ja) * | 1989-08-29 | 1999-03-10 | 株式会社トクヤマ | ビニルフェニル化合物及びその製造方法 |
| JPH087435B2 (ja) * | 1989-12-28 | 1996-01-29 | 日本ゼオン株式会社 | ポジ型レジスト組成物 |
| JPH03239260A (ja) * | 1990-02-16 | 1991-10-24 | Fuji Photo Film Co Ltd | 感光性平版印刷版 |
| JP2817441B2 (ja) * | 1991-03-29 | 1998-10-30 | 日本ゼオン株式会社 | ポジ型レジスト組成物 |
| JP2817442B2 (ja) * | 1991-03-29 | 1998-10-30 | 日本ゼオン株式会社 | ポジ型レジスト組成物 |
| JPH0519466A (ja) * | 1991-07-16 | 1993-01-29 | Fuji Photo Film Co Ltd | ポジ型フオトレジスト組成物 |
| JP4365494B2 (ja) * | 1999-10-27 | 2009-11-18 | 日本ペイント株式会社 | 体積ホログラム記録用感光組成物およびこれから得られるホログラム |
| US20070208087A1 (en) * | 2001-11-02 | 2007-09-06 | Sanders Virginia J | Compounds, compositions and methods for the treatment of inflammatory diseases |
| JP3774668B2 (ja) | 2001-02-07 | 2006-05-17 | 東京エレクトロン株式会社 | シリコン窒化膜形成装置の洗浄前処理方法 |
| JP3914493B2 (ja) | 2002-11-27 | 2007-05-16 | 東京応化工業株式会社 | 多層レジストプロセス用下層膜形成材料およびこれを用いた配線形成方法 |
| JP4382750B2 (ja) | 2003-01-24 | 2009-12-16 | 東京エレクトロン株式会社 | 被処理基板上にシリコン窒化膜を形成するcvd方法 |
| JP3981030B2 (ja) | 2003-03-07 | 2007-09-26 | 信越化学工業株式会社 | レジスト下層膜材料ならびにパターン形成方法 |
| JP4388429B2 (ja) | 2004-02-04 | 2009-12-24 | 信越化学工業株式会社 | レジスト下層膜材料ならびにパターン形成方法 |
| EP1739485B1 (en) | 2004-04-15 | 2016-08-31 | Mitsubishi Gas Chemical Company, Inc. | Resist composition |
| JP4781280B2 (ja) | 2006-01-25 | 2011-09-28 | 信越化学工業株式会社 | 反射防止膜材料、基板、及びパターン形成方法 |
| JP4638380B2 (ja) | 2006-01-27 | 2011-02-23 | 信越化学工業株式会社 | 反射防止膜材料、反射防止膜を有する基板及びパターン形成方法 |
| JP4858136B2 (ja) | 2006-12-06 | 2012-01-18 | 三菱瓦斯化学株式会社 | 感放射線性レジスト組成物 |
| JP5446118B2 (ja) | 2007-04-23 | 2014-03-19 | 三菱瓦斯化学株式会社 | 感放射線性組成物 |
| JP2010138393A (ja) | 2008-11-13 | 2010-06-24 | Nippon Kayaku Co Ltd | 光学レンズシート用エネルギー線硬化型樹脂組成物及びその硬化物 |
| JP6168474B2 (ja) | 2011-08-12 | 2017-07-26 | 三菱瓦斯化学株式会社 | レジスト組成物、レジストパターン形成方法、それに用いるポリフェノール化合物及びそれから誘導され得るアルコール化合物 |
| CN103733136B (zh) | 2011-08-12 | 2017-06-23 | 三菱瓦斯化学株式会社 | 光刻用下层膜形成材料、光刻用下层膜及图案形成方法 |
| JP2015174877A (ja) | 2014-03-13 | 2015-10-05 | 日産化学工業株式会社 | 特定の硬化促進触媒を含む樹脂組成物 |
-
2017
- 2017-07-21 TW TW106124670A patent/TW201815738A/zh unknown
- 2017-07-21 KR KR1020197002666A patent/KR20190033537A/ko not_active Application Discontinuation
- 2017-07-21 CN CN201780045244.3A patent/CN109476575A/zh not_active Withdrawn
- 2017-07-21 WO PCT/JP2017/026530 patent/WO2018016640A1/ja active Application Filing
- 2017-07-21 JP JP2018528904A patent/JP7110979B2/ja active Active
-
2021
- 2021-11-01 JP JP2021178444A patent/JP7283515B2/ja active Active
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2003043687A (ja) | 2001-07-27 | 2003-02-13 | Mitsubishi Paper Mills Ltd | 感光性組成物および感光性平版印刷版材料 |
| JP2005274625A (ja) | 2004-03-22 | 2005-10-06 | Fuji Photo Film Co Ltd | 重合性組成物、及びそれを用いた画像記録材料 |
| JP2005300650A (ja) | 2004-04-07 | 2005-10-27 | Fuji Photo Film Co Ltd | 重合性組成物 |
| JP2007025275A (ja) | 2005-07-15 | 2007-02-01 | Fujifilm Holdings Corp | 感光性組成物及び感光性フィルム、並びに、永久パターン及びその形成方法 |
| JP2010072389A (ja) | 2008-09-19 | 2010-04-02 | Fujifilm Corp | 平版印刷版原版及び平版印刷版の製造方法 |
| JP2014174180A (ja) | 2013-03-05 | 2014-09-22 | Fuji Xerox Co Ltd | 電子写真感光体、プロセスカートリッジ、及び画像形成装置 |
Non-Patent Citations (1)
| Title |
|---|
| Biomacromolecules,2011年,Vol.12,P.4386-4391,Scheme 1 中間体化合物4 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP7283515B2 (ja) | 2023-05-30 |
| TW201815738A (zh) | 2018-05-01 |
| KR20190033537A (ko) | 2019-03-29 |
| WO2018016640A1 (ja) | 2018-01-25 |
| CN109476575A (zh) | 2019-03-15 |
| JPWO2018016640A1 (ja) | 2019-05-09 |
| JP2022033731A (ja) | 2022-03-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7283515B2 (ja) | 化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 | |
| JP7194355B2 (ja) | 化合物、樹脂、組成物及びパターン形成方法 | |
| JP7069529B2 (ja) | 化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 | |
| JP7069530B2 (ja) | 化合物、樹脂、組成物及びパターン形成方法 | |
| JP7194356B2 (ja) | 化合物、樹脂及び組成物、並びにレジストパターン形成方法及び回路パターン形成方法 | |
| JP7290114B2 (ja) | 化合物、樹脂、組成物及びパターン形成方法 | |
| JP7205716B2 (ja) | 化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 | |
| JP7452947B2 (ja) | 化合物、樹脂、組成物、並びにレジストパターン形成方法及び回路パターン形成方法 | |
| JP7205715B2 (ja) | 化合物、樹脂、組成物並びにレジストパターン形成方法及び回路パターン形成方法 | |
| JP7061271B2 (ja) | 化合物、樹脂、組成物、並びにレジストパターン形成方法及び回路パターン形成方法 | |
| WO2018135498A1 (ja) | 化合物、樹脂、組成物及びパターン形成方法 | |
| JPWO2018056279A1 (ja) | 化合物、樹脂、組成物、並びにレジストパターン形成方法及びパターン形成方法 | |
| JP7385827B2 (ja) | 化合物、樹脂、組成物、レジストパターン形成方法、回路パターン形成方法及び樹脂の精製方法 | |
| JP7445382B2 (ja) | 化合物、樹脂、組成物及びパターン形成方法 | |
| JP7139622B2 (ja) | 化合物、樹脂、組成物及びパターン形成方法 | |
| JP7145415B2 (ja) | 化合物、樹脂、組成物、パターン形成方法及び精製方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181126 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200608 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210423 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210622 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20210831 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20211101 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220126 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220311 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220621 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220704 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 7110979 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |