JP6915417B2 - 光学成型材用硬化性樹脂組成物、及びその硬化物、並びに光学成型材、レンズ、カメラモジュール - Google Patents
光学成型材用硬化性樹脂組成物、及びその硬化物、並びに光学成型材、レンズ、カメラモジュール Download PDFInfo
- Publication number
- JP6915417B2 JP6915417B2 JP2017136496A JP2017136496A JP6915417B2 JP 6915417 B2 JP6915417 B2 JP 6915417B2 JP 2017136496 A JP2017136496 A JP 2017136496A JP 2017136496 A JP2017136496 A JP 2017136496A JP 6915417 B2 JP6915417 B2 JP 6915417B2
- Authority
- JP
- Japan
- Prior art keywords
- meth
- acrylate
- cured product
- resin composition
- curable resin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000011342 resin composition Substances 0.000 title claims description 81
- 230000003287 optical effect Effects 0.000 title claims description 31
- 239000012778 molding material Substances 0.000 title claims description 24
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 claims description 113
- -1 alkyl methacrylate Chemical compound 0.000 claims description 73
- 239000000178 monomer Substances 0.000 claims description 44
- 230000009477 glass transition Effects 0.000 claims description 29
- 125000004432 carbon atom Chemical group C* 0.000 claims description 25
- 125000000217 alkyl group Chemical group 0.000 claims description 21
- 229920000642 polymer Polymers 0.000 claims description 18
- 125000005395 methacrylic acid group Chemical group 0.000 claims description 12
- RUMACXVDVNRZJZ-UHFFFAOYSA-N 2-methylpropyl 2-methylprop-2-enoate Chemical compound CC(C)COC(=O)C(C)=C RUMACXVDVNRZJZ-UHFFFAOYSA-N 0.000 claims description 11
- 125000003118 aryl group Chemical group 0.000 claims description 8
- SJMYWORNLPSJQO-UHFFFAOYSA-N tert-butyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OC(C)(C)C SJMYWORNLPSJQO-UHFFFAOYSA-N 0.000 claims description 6
- 239000007870 radical polymerization initiator Substances 0.000 claims description 5
- 239000000047 product Substances 0.000 description 107
- 238000000034 method Methods 0.000 description 46
- 150000001875 compounds Chemical class 0.000 description 38
- 229920005601 base polymer Polymers 0.000 description 35
- 238000006243 chemical reaction Methods 0.000 description 19
- 229920005989 resin Polymers 0.000 description 19
- 239000011347 resin Substances 0.000 description 19
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 17
- 239000002253 acid Substances 0.000 description 17
- 238000004519 manufacturing process Methods 0.000 description 16
- 238000002156 mixing Methods 0.000 description 15
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 14
- 239000003505 polymerization initiator Substances 0.000 description 14
- 239000000126 substance Substances 0.000 description 14
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 14
- SOGAXMICEFXMKE-UHFFFAOYSA-N Butylmethacrylate Chemical compound CCCCOC(=O)C(C)=C SOGAXMICEFXMKE-UHFFFAOYSA-N 0.000 description 13
- 238000006116 polymerization reaction Methods 0.000 description 12
- 239000000203 mixture Substances 0.000 description 11
- 239000003963 antioxidant agent Substances 0.000 description 10
- 125000003055 glycidyl group Chemical group C(C1CO1)* 0.000 description 10
- 238000000465 moulding Methods 0.000 description 10
- 150000002978 peroxides Chemical class 0.000 description 10
- 125000003647 acryloyl group Chemical group O=C([*])C([H])=C([H])[H] 0.000 description 9
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 9
- 239000007809 chemical reaction catalyst Substances 0.000 description 9
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 9
- 238000012719 thermal polymerization Methods 0.000 description 9
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 8
- 239000007788 liquid Substances 0.000 description 8
- 239000000463 material Substances 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 7
- 238000004040 coloring Methods 0.000 description 7
- 125000000524 functional group Chemical group 0.000 description 7
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 7
- 239000003999 initiator Substances 0.000 description 7
- IQPQWNKOIGAROB-UHFFFAOYSA-N isocyanate group Chemical group [N-]=C=O IQPQWNKOIGAROB-UHFFFAOYSA-N 0.000 description 7
- 229920001296 polysiloxane Polymers 0.000 description 7
- 239000006097 ultraviolet radiation absorber Substances 0.000 description 7
- AVTLBBWTUPQRAY-UHFFFAOYSA-N 2-(2-cyanobutan-2-yldiazenyl)-2-methylbutanenitrile Chemical compound CCC(C)(C#N)N=NC(C)(CC)C#N AVTLBBWTUPQRAY-UHFFFAOYSA-N 0.000 description 6
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 6
- 230000003078 antioxidant effect Effects 0.000 description 6
- 238000007385 chemical modification Methods 0.000 description 6
- 239000003638 chemical reducing agent Substances 0.000 description 6
- VOZRXNHHFUQHIL-UHFFFAOYSA-N glycidyl methacrylate Chemical compound CC(=C)C(=O)OCC1CO1 VOZRXNHHFUQHIL-UHFFFAOYSA-N 0.000 description 6
- 230000035484 reaction time Effects 0.000 description 6
- VFHVQBAGLAREND-UHFFFAOYSA-N diphenylphosphoryl-(2,4,6-trimethylphenyl)methanone Chemical compound CC1=CC(C)=CC(C)=C1C(=O)P(=O)(C=1C=CC=CC=1)C1=CC=CC=C1 VFHVQBAGLAREND-UHFFFAOYSA-N 0.000 description 5
- 239000011521 glass Substances 0.000 description 5
- 238000005259 measurement Methods 0.000 description 5
- 150000001451 organic peroxides Chemical class 0.000 description 5
- 238000007717 redox polymerization reaction Methods 0.000 description 5
- 238000003756 stirring Methods 0.000 description 5
- JRMUNVKIHCOMHV-UHFFFAOYSA-M tetrabutylammonium bromide Chemical compound [Br-].CCCC[N+](CCCC)(CCCC)CCCC JRMUNVKIHCOMHV-UHFFFAOYSA-M 0.000 description 5
- DPGYCJUCJYUHTM-UHFFFAOYSA-N 2,4,4-trimethylpentan-2-yloxy 2-ethylhexaneperoxoate Chemical compound CCCCC(CC)C(=O)OOOC(C)(C)CC(C)(C)C DPGYCJUCJYUHTM-UHFFFAOYSA-N 0.000 description 4
- BAPJBEWLBFYGME-UHFFFAOYSA-N Methyl acrylate Chemical compound COC(=O)C=C BAPJBEWLBFYGME-UHFFFAOYSA-N 0.000 description 4
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 4
- IAXXETNIOYFMLW-GYSYKLTISA-N [(1r,3r,4r)-4,7,7-trimethyl-3-bicyclo[2.2.1]heptanyl] 2-methylprop-2-enoate Chemical compound C1C[C@@]2(C)[C@H](OC(=O)C(=C)C)C[C@@H]1C2(C)C IAXXETNIOYFMLW-GYSYKLTISA-N 0.000 description 4
- 238000005266 casting Methods 0.000 description 4
- SUPCQIBBMFXVTL-UHFFFAOYSA-N ethyl 2-methylprop-2-enoate Chemical compound CCOC(=O)C(C)=C SUPCQIBBMFXVTL-UHFFFAOYSA-N 0.000 description 4
- 239000003112 inhibitor Substances 0.000 description 4
- SLCVBVWXLSEKPL-UHFFFAOYSA-N neopentyl glycol Chemical compound OCC(C)(C)CO SLCVBVWXLSEKPL-UHFFFAOYSA-N 0.000 description 4
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 4
- FVQMJJQUGGVLEP-UHFFFAOYSA-N (2-methylpropan-2-yl)oxy 2-ethylhexaneperoxoate Chemical compound CCCCC(CC)C(=O)OOOC(C)(C)C FVQMJJQUGGVLEP-UHFFFAOYSA-N 0.000 description 3
- 239000012956 1-hydroxycyclohexylphenyl-ketone Substances 0.000 description 3
- TXBCBTDQIULDIA-UHFFFAOYSA-N 2-[[3-hydroxy-2,2-bis(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propane-1,3-diol Chemical compound OCC(CO)(CO)COCC(CO)(CO)CO TXBCBTDQIULDIA-UHFFFAOYSA-N 0.000 description 3
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 3
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 3
- 102100040409 Ameloblastin Human genes 0.000 description 3
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 3
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 3
- 101000891247 Homo sapiens Ameloblastin Proteins 0.000 description 3
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- OKKRPWIIYQTPQF-UHFFFAOYSA-N Trimethylolpropane trimethacrylate Chemical compound CC(=C)C(=O)OCC(CC)(COC(=O)C(C)=C)COC(=O)C(C)=C OKKRPWIIYQTPQF-UHFFFAOYSA-N 0.000 description 3
- MPIAGWXWVAHQBB-UHFFFAOYSA-N [3-prop-2-enoyloxy-2-[[3-prop-2-enoyloxy-2,2-bis(prop-2-enoyloxymethyl)propoxy]methyl]-2-(prop-2-enoyloxymethyl)propyl] prop-2-enoate Chemical compound C=CC(=O)OCC(COC(=O)C=C)(COC(=O)C=C)COCC(COC(=O)C=C)(COC(=O)C=C)COC(=O)C=C MPIAGWXWVAHQBB-UHFFFAOYSA-N 0.000 description 3
- 235000019400 benzoyl peroxide Nutrition 0.000 description 3
- AOJOEFVRHOZDFN-UHFFFAOYSA-N benzyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCC1=CC=CC=C1 AOJOEFVRHOZDFN-UHFFFAOYSA-N 0.000 description 3
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 3
- MQDJYUACMFCOFT-UHFFFAOYSA-N bis[2-(1-hydroxycyclohexyl)phenyl]methanone Chemical compound C=1C=CC=C(C(=O)C=2C(=CC=CC=2)C2(O)CCCCC2)C=1C1(O)CCCCC1 MQDJYUACMFCOFT-UHFFFAOYSA-N 0.000 description 3
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical class C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- 238000000576 coating method Methods 0.000 description 3
- 230000000052 comparative effect Effects 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 239000005357 flat glass Substances 0.000 description 3
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 3
- 229910052753 mercury Inorganic materials 0.000 description 3
- OTLDLKLSNZMTTA-UHFFFAOYSA-N octahydro-1h-4,7-methanoindene-1,5-diyldimethanol Chemical compound C1C2C3C(CO)CCC3C1C(CO)C2 OTLDLKLSNZMTTA-UHFFFAOYSA-N 0.000 description 3
- 238000010526 radical polymerization reaction Methods 0.000 description 3
- DTGKSKDOIYIVQL-WEDXCCLWSA-N (+)-borneol Chemical group C1C[C@@]2(C)[C@@H](O)C[C@@H]1C2(C)C DTGKSKDOIYIVQL-WEDXCCLWSA-N 0.000 description 2
- QNODIIQQMGDSEF-UHFFFAOYSA-N (1-hydroxycyclohexyl)-phenylmethanone Chemical compound C=1C=CC=CC=1C(=O)C1(O)CCCCC1 QNODIIQQMGDSEF-UHFFFAOYSA-N 0.000 description 2
- NOBYOEQUFMGXBP-UHFFFAOYSA-N (4-tert-butylcyclohexyl) (4-tert-butylcyclohexyl)oxycarbonyloxy carbonate Chemical compound C1CC(C(C)(C)C)CCC1OC(=O)OOC(=O)OC1CCC(C(C)(C)C)CC1 NOBYOEQUFMGXBP-UHFFFAOYSA-N 0.000 description 2
- ROZDMUUELHCVQC-ARJAWSKDSA-N (z)-4-oxo-4-(2-prop-2-enoyloxyethoxy)but-2-enoic acid Chemical compound OC(=O)\C=C/C(=O)OCCOC(=O)C=C ROZDMUUELHCVQC-ARJAWSKDSA-N 0.000 description 2
- AZQWKYJCGOJGHM-UHFFFAOYSA-N 1,4-benzoquinone Chemical compound O=C1C=CC(=O)C=C1 AZQWKYJCGOJGHM-UHFFFAOYSA-N 0.000 description 2
- XLPJNCYCZORXHG-UHFFFAOYSA-N 1-morpholin-4-ylprop-2-en-1-one Chemical compound C=CC(=O)N1CCOCC1 XLPJNCYCZORXHG-UHFFFAOYSA-N 0.000 description 2
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 2
- HLIQLHSBZXDKLV-UHFFFAOYSA-N 2-(2-hydroxyethoxy)-1-phenoxyethanol Chemical compound OCCOCC(O)OC1=CC=CC=C1 HLIQLHSBZXDKLV-UHFFFAOYSA-N 0.000 description 2
- UECGJSXCVLTIMQ-UHFFFAOYSA-N 2-(2-prop-2-enoyloxyethoxycarbonyl)cyclohexane-1-carboxylic acid Chemical compound OC(=O)C1CCCCC1C(=O)OCCOC(=O)C=C UECGJSXCVLTIMQ-UHFFFAOYSA-N 0.000 description 2
- WDQMWEYDKDCEHT-UHFFFAOYSA-N 2-ethylhexyl 2-methylprop-2-enoate Chemical compound CCCCC(CC)COC(=O)C(C)=C WDQMWEYDKDCEHT-UHFFFAOYSA-N 0.000 description 2
- XMLYCEVDHLAQEL-UHFFFAOYSA-N 2-hydroxy-2-methyl-1-phenylpropan-1-one Chemical compound CC(C)(O)C(=O)C1=CC=CC=C1 XMLYCEVDHLAQEL-UHFFFAOYSA-N 0.000 description 2
- DPNXHTDWGGVXID-UHFFFAOYSA-N 2-isocyanatoethyl prop-2-enoate Chemical compound C=CC(=O)OCCN=C=O DPNXHTDWGGVXID-UHFFFAOYSA-N 0.000 description 2
- XDQWJFXZTAWJST-UHFFFAOYSA-N 3-triethoxysilylpropyl prop-2-enoate Chemical compound CCO[Si](OCC)(OCC)CCCOC(=O)C=C XDQWJFXZTAWJST-UHFFFAOYSA-N 0.000 description 2
- KBQVDAIIQCXKPI-UHFFFAOYSA-N 3-trimethoxysilylpropyl prop-2-enoate Chemical compound CO[Si](OC)(OC)CCCOC(=O)C=C KBQVDAIIQCXKPI-UHFFFAOYSA-N 0.000 description 2
- SXIFAEWFOJETOA-UHFFFAOYSA-N 4-hydroxy-butyl Chemical group [CH2]CCCO SXIFAEWFOJETOA-UHFFFAOYSA-N 0.000 description 2
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- JIGUQPWFLRLWPJ-UHFFFAOYSA-N Ethyl acrylate Chemical compound CCOC(=O)C=C JIGUQPWFLRLWPJ-UHFFFAOYSA-N 0.000 description 2
- QIGBRXMKCJKVMJ-UHFFFAOYSA-N Hydroquinone Chemical compound OC1=CC=C(O)C=C1 QIGBRXMKCJKVMJ-UHFFFAOYSA-N 0.000 description 2
- JLTDJTHDQAWBAV-UHFFFAOYSA-N N,N-dimethylaniline Chemical compound CN(C)C1=CC=CC=C1 JLTDJTHDQAWBAV-UHFFFAOYSA-N 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- 239000004372 Polyvinyl alcohol Substances 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 2
- MCMNRKCIXSYSNV-UHFFFAOYSA-N Zirconium dioxide Chemical compound O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 description 2
- RMKZLFMHXZAGTM-UHFFFAOYSA-N [dimethoxy(propyl)silyl]oxymethyl prop-2-enoate Chemical compound CCC[Si](OC)(OC)OCOC(=O)C=C RMKZLFMHXZAGTM-UHFFFAOYSA-N 0.000 description 2
- 239000006096 absorbing agent Substances 0.000 description 2
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 2
- 239000000853 adhesive Substances 0.000 description 2
- 230000001070 adhesive effect Effects 0.000 description 2
- 125000002723 alicyclic group Chemical group 0.000 description 2
- XYLMUPLGERFSHI-UHFFFAOYSA-N alpha-Methylstyrene Chemical compound CC(=C)C1=CC=CC=C1 XYLMUPLGERFSHI-UHFFFAOYSA-N 0.000 description 2
- 230000001588 bifunctional effect Effects 0.000 description 2
- 125000000319 biphenyl-4-yl group Chemical group [H]C1=C([H])C([H])=C([H])C([H])=C1C1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 2
- 125000006226 butoxyethyl group Chemical group 0.000 description 2
- CQEYYJKEWSMYFG-UHFFFAOYSA-N butyl acrylate Chemical compound CCCCOC(=O)C=C CQEYYJKEWSMYFG-UHFFFAOYSA-N 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 239000008367 deionised water Substances 0.000 description 2
- 229910021641 deionized water Inorganic materials 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 150000002009 diols Chemical class 0.000 description 2
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- 125000005448 ethoxyethyl group Chemical group [H]C([H])([H])C([H])([H])OC([H])([H])C([H])([H])* 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- MDNFYIAABKQDML-UHFFFAOYSA-N heptyl 2-methylprop-2-enoate Chemical compound CCCCCCCOC(=O)C(C)=C MDNFYIAABKQDML-UHFFFAOYSA-N 0.000 description 2
- SCFQUKBBGYTJNC-UHFFFAOYSA-N heptyl prop-2-enoate Chemical compound CCCCCCCOC(=O)C=C SCFQUKBBGYTJNC-UHFFFAOYSA-N 0.000 description 2
- 125000000623 heterocyclic group Chemical group 0.000 description 2
- LNCPIMCVTKXXOY-UHFFFAOYSA-N hexyl 2-methylprop-2-enoate Chemical compound CCCCCCOC(=O)C(C)=C LNCPIMCVTKXXOY-UHFFFAOYSA-N 0.000 description 2
- LNMQRPPRQDGUDR-UHFFFAOYSA-N hexyl prop-2-enoate Chemical compound CCCCCCOC(=O)C=C LNMQRPPRQDGUDR-UHFFFAOYSA-N 0.000 description 2
- NWVVVBRKAWDGAB-UHFFFAOYSA-N hydroquinone methyl ether Natural products COC1=CC=C(O)C=C1 NWVVVBRKAWDGAB-UHFFFAOYSA-N 0.000 description 2
- 229910001507 metal halide Inorganic materials 0.000 description 2
- 150000005309 metal halides Chemical class 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 125000001624 naphthyl group Chemical group 0.000 description 2
- NZIDBRBFGPQCRY-UHFFFAOYSA-N octyl 2-methylprop-2-enoate Chemical compound CCCCCCCCOC(=O)C(C)=C NZIDBRBFGPQCRY-UHFFFAOYSA-N 0.000 description 2
- ANISOHQJBAQUQP-UHFFFAOYSA-N octyl prop-2-enoate Chemical compound CCCCCCCCOC(=O)C=C ANISOHQJBAQUQP-UHFFFAOYSA-N 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- GYDSPAVLTMAXHT-UHFFFAOYSA-N pentyl 2-methylprop-2-enoate Chemical compound CCCCCOC(=O)C(C)=C GYDSPAVLTMAXHT-UHFFFAOYSA-N 0.000 description 2
- ULDDEWDFUNBUCM-UHFFFAOYSA-N pentyl prop-2-enoate Chemical compound CCCCCOC(=O)C=C ULDDEWDFUNBUCM-UHFFFAOYSA-N 0.000 description 2
- PNJWIWWMYCMZRO-UHFFFAOYSA-N pent‐4‐en‐2‐one Natural products CC(=O)CC=C PNJWIWWMYCMZRO-UHFFFAOYSA-N 0.000 description 2
- 125000006187 phenyl benzyl group Chemical group 0.000 description 2
- ZQBAKBUEJOMQEX-UHFFFAOYSA-N phenyl salicylate Chemical compound OC1=CC=CC=C1C(=O)OC1=CC=CC=C1 ZQBAKBUEJOMQEX-UHFFFAOYSA-N 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- 150000003003 phosphines Chemical class 0.000 description 2
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 2
- 229920000058 polyacrylate Polymers 0.000 description 2
- 229920002451 polyvinyl alcohol Polymers 0.000 description 2
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 2
- 125000004079 stearyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- 238000010558 suspension polymerization method Methods 0.000 description 2
- ISXSCDLOGDJUNJ-UHFFFAOYSA-N tert-butyl prop-2-enoate Chemical compound CC(C)(C)OC(=O)C=C ISXSCDLOGDJUNJ-UHFFFAOYSA-N 0.000 description 2
- 150000003606 tin compounds Chemical class 0.000 description 2
- CNHDIAIOKMXOLK-UHFFFAOYSA-N toluquinol Chemical compound CC1=CC(O)=CC=C1O CNHDIAIOKMXOLK-UHFFFAOYSA-N 0.000 description 2
- 238000001721 transfer moulding Methods 0.000 description 2
- 125000002889 tridecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- HVLLSGMXQDNUAL-UHFFFAOYSA-N triphenyl phosphite Chemical compound C=1C=CC=CC=1OP(OC=1C=CC=CC=1)OC1=CC=CC=C1 HVLLSGMXQDNUAL-UHFFFAOYSA-N 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- QQBLOZGVRHAYGT-UHFFFAOYSA-N tris-decyl phosphite Chemical compound CCCCCCCCCCOP(OCCCCCCCCCC)OCCCCCCCCCC QQBLOZGVRHAYGT-UHFFFAOYSA-N 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 1
- BDACRXKSBPLSJG-UHFFFAOYSA-N (2-hydroxy-4-methoxyphenyl)-(4-methoxyphenyl)methanone Chemical compound C1=CC(OC)=CC=C1C(=O)C1=CC=C(OC)C=C1O BDACRXKSBPLSJG-UHFFFAOYSA-N 0.000 description 1
- HJIAMFHSAAEUKR-UHFFFAOYSA-N (2-hydroxyphenyl)-phenylmethanone Chemical class OC1=CC=CC=C1C(=O)C1=CC=CC=C1 HJIAMFHSAAEUKR-UHFFFAOYSA-N 0.000 description 1
- QEQBMZQFDDDTPN-UHFFFAOYSA-N (2-methylpropan-2-yl)oxy benzenecarboperoxoate Chemical compound CC(C)(C)OOOC(=O)C1=CC=CC=C1 QEQBMZQFDDDTPN-UHFFFAOYSA-N 0.000 description 1
- OGXYNNJLNXMMHM-UHFFFAOYSA-N (4-butoxy-2-hydroxyphenyl)-(4-butoxyphenyl)methanone Chemical compound C1=CC(OCCCC)=CC=C1C(=O)C1=CC=C(OCCCC)C=C1O OGXYNNJLNXMMHM-UHFFFAOYSA-N 0.000 description 1
- JQSSXIRDGUMPNP-UHFFFAOYSA-N (4-decoxy-2-hydroxyphenyl)-phenylmethanone Chemical compound OC1=CC(OCCCCCCCCCC)=CC=C1C(=O)C1=CC=CC=C1 JQSSXIRDGUMPNP-UHFFFAOYSA-N 0.000 description 1
- WXPWZZHELZEVPO-UHFFFAOYSA-N (4-methylphenyl)-phenylmethanone Chemical compound C1=CC(C)=CC=C1C(=O)C1=CC=CC=C1 WXPWZZHELZEVPO-UHFFFAOYSA-N 0.000 description 1
- MJYFYGVCLHNRKB-UHFFFAOYSA-N 1,1,2-trifluoroethyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OC(F)(F)CF MJYFYGVCLHNRKB-UHFFFAOYSA-N 0.000 description 1
- FYRCDEARNUVZRG-UHFFFAOYSA-N 1,1,5-trimethyl-3,3-bis(2-methylpentan-2-ylperoxy)cyclohexane Chemical compound CCCC(C)(C)OOC1(OOC(C)(C)CCC)CC(C)CC(C)(C)C1 FYRCDEARNUVZRG-UHFFFAOYSA-N 0.000 description 1
- HSLFISVKRDQEBY-UHFFFAOYSA-N 1,1-bis(tert-butylperoxy)cyclohexane Chemical compound CC(C)(C)OOC1(OOC(C)(C)C)CCCCC1 HSLFISVKRDQEBY-UHFFFAOYSA-N 0.000 description 1
- GJZFGDYLJLCGHT-UHFFFAOYSA-N 1,2-diethylthioxanthen-9-one Chemical compound C1=CC=C2C(=O)C3=C(CC)C(CC)=CC=C3SC2=C1 GJZFGDYLJLCGHT-UHFFFAOYSA-N 0.000 description 1
- JFZVSHAMRZPOPA-UHFFFAOYSA-N 1-[n-(2-hydroxypropyl)-4-methylanilino]propan-2-ol Chemical compound CC(O)CN(CC(C)O)C1=CC=C(C)C=C1 JFZVSHAMRZPOPA-UHFFFAOYSA-N 0.000 description 1
- DLKQHBOKULLWDQ-UHFFFAOYSA-N 1-bromonaphthalene Chemical compound C1=CC=C2C(Br)=CC=CC2=C1 DLKQHBOKULLWDQ-UHFFFAOYSA-N 0.000 description 1
- RMSGQZDGSZOJMU-UHFFFAOYSA-N 1-butyl-2-phenylbenzene Chemical group CCCCC1=CC=CC=C1C1=CC=CC=C1 RMSGQZDGSZOJMU-UHFFFAOYSA-N 0.000 description 1
- LHNRHYOMDUJLLM-UHFFFAOYSA-N 1-hexylsulfanylhexane Chemical compound CCCCCCSCCCCCC LHNRHYOMDUJLLM-UHFFFAOYSA-N 0.000 description 1
- PHRABVHYUHIYGY-UHFFFAOYSA-N 1-methylnaphthalene Chemical group C1=CC=C2C([CH2])=CC=CC2=C1 PHRABVHYUHIYGY-UHFFFAOYSA-N 0.000 description 1
- YIKSHDNOAYSSPX-UHFFFAOYSA-N 1-propan-2-ylthioxanthen-9-one Chemical compound S1C2=CC=CC=C2C(=O)C2=C1C=CC=C2C(C)C YIKSHDNOAYSSPX-UHFFFAOYSA-N 0.000 description 1
- PITQFWWNUHMYIC-UHFFFAOYSA-N 1-tert-butyl-4-(4-tert-butylcyclohexyl)peroxycyclohexane Chemical group C1CC(C(C)(C)C)CCC1OOC1CCC(C(C)(C)C)CC1 PITQFWWNUHMYIC-UHFFFAOYSA-N 0.000 description 1
- BGJQNPIOBWKQAW-UHFFFAOYSA-N 1-tert-butylanthracene-9,10-dione Chemical compound O=C1C2=CC=CC=C2C(=O)C2=C1C=CC=C2C(C)(C)C BGJQNPIOBWKQAW-UHFFFAOYSA-N 0.000 description 1
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 1
- JZODKRWQWUWGCD-UHFFFAOYSA-N 2,5-di-tert-butylbenzene-1,4-diol Chemical compound CC(C)(C)C1=CC(O)=C(C(C)(C)C)C=C1O JZODKRWQWUWGCD-UHFFFAOYSA-N 0.000 description 1
- DKCPKDPYUFEZCP-UHFFFAOYSA-N 2,6-di-tert-butylphenol Chemical compound CC(C)(C)C1=CC=CC(C(C)(C)C)=C1O DKCPKDPYUFEZCP-UHFFFAOYSA-N 0.000 description 1
- IEMBFTKNPXENSE-UHFFFAOYSA-N 2-(2-methylpentan-2-ylperoxy)propan-2-yl hydrogen carbonate Chemical compound CCCC(C)(C)OOC(C)(C)OC(O)=O IEMBFTKNPXENSE-UHFFFAOYSA-N 0.000 description 1
- XMNIXWIUMCBBBL-UHFFFAOYSA-N 2-(2-phenylpropan-2-ylperoxy)propan-2-ylbenzene Chemical compound C=1C=CC=CC=1C(C)(C)OOC(C)(C)C1=CC=CC=C1 XMNIXWIUMCBBBL-UHFFFAOYSA-N 0.000 description 1
- RKYJPYDJNQXILT-UHFFFAOYSA-N 2-(2-prop-2-enoyloxyethoxycarbonyl)benzoic acid Chemical compound OC(=O)C1=CC=CC=C1C(=O)OCCOC(=O)C=C RKYJPYDJNQXILT-UHFFFAOYSA-N 0.000 description 1
- GOXQRTZXKQZDDN-UHFFFAOYSA-N 2-Ethylhexyl acrylate Chemical class CCCCC(CC)COC(=O)C=C GOXQRTZXKQZDDN-UHFFFAOYSA-N 0.000 description 1
- WYGWHHGCAGTUCH-UHFFFAOYSA-N 2-[(2-cyano-4-methylpentan-2-yl)diazenyl]-2,4-dimethylpentanenitrile Chemical compound CC(C)CC(C)(C#N)N=NC(C)(C#N)CC(C)C WYGWHHGCAGTUCH-UHFFFAOYSA-N 0.000 description 1
- FDSUVTROAWLVJA-UHFFFAOYSA-N 2-[[3-hydroxy-2,2-bis(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propane-1,3-diol;prop-2-enoic acid Chemical compound OC(=O)C=C.OC(=O)C=C.OC(=O)C=C.OC(=O)C=C.OC(=O)C=C.OCC(CO)(CO)COCC(CO)(CO)CO FDSUVTROAWLVJA-UHFFFAOYSA-N 0.000 description 1
- UHFFVFAKEGKNAQ-UHFFFAOYSA-N 2-benzyl-2-(dimethylamino)-1-(4-morpholin-4-ylphenyl)butan-1-one Chemical compound C=1C=C(N2CCOCC2)C=CC=1C(=O)C(CC)(N(C)C)CC1=CC=CC=C1 UHFFVFAKEGKNAQ-UHFFFAOYSA-N 0.000 description 1
- ZACVGCNKGYYQHA-UHFFFAOYSA-N 2-ethylhexoxycarbonyloxy 2-ethylhexyl carbonate Chemical compound CCCCC(CC)COC(=O)OOC(=O)OCC(CC)CCCC ZACVGCNKGYYQHA-UHFFFAOYSA-N 0.000 description 1
- MIRQGKQPLPBZQM-UHFFFAOYSA-N 2-hydroperoxy-2,4,4-trimethylpentane Chemical compound CC(C)(C)CC(C)(C)OO MIRQGKQPLPBZQM-UHFFFAOYSA-N 0.000 description 1
- WFUGQJXVXHBTEM-UHFFFAOYSA-N 2-hydroperoxy-2-(2-hydroperoxybutan-2-ylperoxy)butane Chemical compound CCC(C)(OO)OOC(C)(CC)OO WFUGQJXVXHBTEM-UHFFFAOYSA-N 0.000 description 1
- VHSHLMUCYSAUQU-UHFFFAOYSA-N 2-hydroxypropyl methacrylate Chemical compound CC(O)COC(=O)C(C)=C VHSHLMUCYSAUQU-UHFFFAOYSA-N 0.000 description 1
- BQZJOQXSCSZQPS-UHFFFAOYSA-N 2-methoxy-1,2-diphenylethanone Chemical compound C=1C=CC=CC=1C(OC)C(=O)C1=CC=CC=C1 BQZJOQXSCSZQPS-UHFFFAOYSA-N 0.000 description 1
- LWRBVKNFOYUCNP-UHFFFAOYSA-N 2-methyl-1-(4-methylsulfanylphenyl)-2-morpholin-4-ylpropan-1-one Chemical compound C1=CC(SC)=CC=C1C(=O)C(C)(C)N1CCOCC1 LWRBVKNFOYUCNP-UHFFFAOYSA-N 0.000 description 1
- CFVWNXQPGQOHRJ-UHFFFAOYSA-N 2-methylpropyl prop-2-enoate Chemical compound CC(C)COC(=O)C=C CFVWNXQPGQOHRJ-UHFFFAOYSA-N 0.000 description 1
- FRIBMENBGGCKPD-UHFFFAOYSA-N 3-(2,3-dimethoxyphenyl)prop-2-enal Chemical compound COC1=CC=CC(C=CC=O)=C1OC FRIBMENBGGCKPD-UHFFFAOYSA-N 0.000 description 1
- XMZDUMRSGBAPGP-UHFFFAOYSA-N 3-butyl-2-phenoxybenzoic acid Chemical compound CCCCC1=CC=CC(C(O)=O)=C1OC1=CC=CC=C1 XMZDUMRSGBAPGP-UHFFFAOYSA-N 0.000 description 1
- JIGUICYYOYEXFS-UHFFFAOYSA-N 3-tert-butylbenzene-1,2-diol Chemical compound CC(C)(C)C1=CC=CC(O)=C1O JIGUICYYOYEXFS-UHFFFAOYSA-N 0.000 description 1
- VFXXTYGQYWRHJP-UHFFFAOYSA-N 4,4'-azobis(4-cyanopentanoic acid) Chemical compound OC(=O)CCC(C)(C#N)N=NC(C)(CCC(O)=O)C#N VFXXTYGQYWRHJP-UHFFFAOYSA-N 0.000 description 1
- UZDMJPAQQFSMMV-UHFFFAOYSA-N 4-oxo-4-(2-prop-2-enoyloxyethoxy)butanoic acid Chemical compound OC(=O)CCC(=O)OCCOC(=O)C=C UZDMJPAQQFSMMV-UHFFFAOYSA-N 0.000 description 1
- VMRIVYANZGSGRV-UHFFFAOYSA-N 4-phenyl-2h-triazin-5-one Chemical compound OC1=CN=NN=C1C1=CC=CC=C1 VMRIVYANZGSGRV-UHFFFAOYSA-N 0.000 description 1
- ZVVFVKJZNVSANF-UHFFFAOYSA-N 6-[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyloxy]hexyl 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoate Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)OCCCCCCOC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 ZVVFVKJZNVSANF-UHFFFAOYSA-N 0.000 description 1
- SREFFVHKIFTAKJ-UHFFFAOYSA-N CC(C)C1CCC(C)CC1.OO.OO Chemical class CC(C)C1CCC(C)CC1.OO.OO SREFFVHKIFTAKJ-UHFFFAOYSA-N 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- GHKOFFNLGXMVNJ-UHFFFAOYSA-N Didodecyl thiobispropanoate Chemical compound CCCCCCCCCCCCOC(=O)CCSCCC(=O)OCCCCCCCCCCCC GHKOFFNLGXMVNJ-UHFFFAOYSA-N 0.000 description 1
- JOYRKODLDBILNP-UHFFFAOYSA-N Ethyl urethane Chemical compound CCOC(N)=O JOYRKODLDBILNP-UHFFFAOYSA-N 0.000 description 1
- YIVJZNGAASQVEM-UHFFFAOYSA-N Lauroyl peroxide Chemical compound CCCCCCCCCCCC(=O)OOC(=O)CCCCCCCCCCC YIVJZNGAASQVEM-UHFFFAOYSA-N 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical compound CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 description 1
- NQSMEZJWJJVYOI-UHFFFAOYSA-N Methyl 2-benzoylbenzoate Chemical compound COC(=O)C1=CC=CC=C1C(=O)C1=CC=CC=C1 NQSMEZJWJJVYOI-UHFFFAOYSA-N 0.000 description 1
- 239000004677 Nylon Substances 0.000 description 1
- JKIJEFPNVSHHEI-UHFFFAOYSA-N Phenol, 2,4-bis(1,1-dimethylethyl)-, phosphite (3:1) Chemical compound CC(C)(C)C1=CC(C(C)(C)C)=CC=C1OP(OC=1C(=CC(=CC=1)C(C)(C)C)C(C)(C)C)OC1=CC=C(C(C)(C)C)C=C1C(C)(C)C JKIJEFPNVSHHEI-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- BGNXCDMCOKJUMV-UHFFFAOYSA-N Tert-Butylhydroquinone Chemical compound CC(C)(C)C1=CC(O)=CC=C1O BGNXCDMCOKJUMV-UHFFFAOYSA-N 0.000 description 1
- ZJCCRDAZUWHFQH-UHFFFAOYSA-N Trimethylolpropane Chemical compound CCC(CO)(CO)CO ZJCCRDAZUWHFQH-UHFFFAOYSA-N 0.000 description 1
- 235000010724 Wisteria floribunda Nutrition 0.000 description 1
- ULQMPOIOSDXIGC-UHFFFAOYSA-N [2,2-dimethyl-3-(2-methylprop-2-enoyloxy)propyl] 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCC(C)(C)COC(=O)C(C)=C ULQMPOIOSDXIGC-UHFFFAOYSA-N 0.000 description 1
- PZIVNMZOHNTMKE-UHFFFAOYSA-N [2-(2-hydroxyoctoxy)phenyl]-phenylmethanone Chemical compound CCCCCCC(O)COC1=CC=CC=C1C(=O)C1=CC=CC=C1 PZIVNMZOHNTMKE-UHFFFAOYSA-N 0.000 description 1
- NOZAQBYNLKNDRT-UHFFFAOYSA-N [diacetyloxy(ethenyl)silyl] acetate Chemical compound CC(=O)O[Si](OC(C)=O)(OC(C)=O)C=C NOZAQBYNLKNDRT-UHFFFAOYSA-N 0.000 description 1
- UKLDJPRMSDWDSL-UHFFFAOYSA-L [dibutyl(dodecanoyloxy)stannyl] dodecanoate Chemical compound CCCCCCCCCCCC(=O)O[Sn](CCCC)(CCCC)OC(=O)CCCCCCCCCCC UKLDJPRMSDWDSL-UHFFFAOYSA-L 0.000 description 1
- KYIKRXIYLAGAKQ-UHFFFAOYSA-N abcn Chemical compound C1CCCCC1(C#N)N=NC1(C#N)CCCCC1 KYIKRXIYLAGAKQ-UHFFFAOYSA-N 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- PYKYMHQGRFAEBM-UHFFFAOYSA-N anthraquinone Natural products CCC(=O)c1c(O)c2C(=O)C3C(C=CC=C3O)C(=O)c2cc1CC(=O)OC PYKYMHQGRFAEBM-UHFFFAOYSA-N 0.000 description 1
- 150000004056 anthraquinones Chemical class 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- RWCCWEUUXYIKHB-UHFFFAOYSA-N benzophenone Chemical compound C=1C=CC=CC=1C(=O)C1=CC=CC=C1 RWCCWEUUXYIKHB-UHFFFAOYSA-N 0.000 description 1
- 239000012965 benzophenone Substances 0.000 description 1
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical compound C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 1
- 239000012964 benzotriazole Substances 0.000 description 1
- 239000012986 chain transfer agent Substances 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 238000006482 condensation reaction Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 229940120693 copper naphthenate Drugs 0.000 description 1
- SEVNKWFHTNVOLD-UHFFFAOYSA-L copper;3-(4-ethylcyclohexyl)propanoate;3-(3-ethylcyclopentyl)propanoate Chemical compound [Cu+2].CCC1CCC(CCC([O-])=O)C1.CCC1CCC(CCC([O-])=O)CC1 SEVNKWFHTNVOLD-UHFFFAOYSA-L 0.000 description 1
- 238000005520 cutting process Methods 0.000 description 1
- 150000001925 cycloalkenes Chemical class 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- FOTKYAAJKYLFFN-UHFFFAOYSA-N decane-1,10-diol Chemical compound OCCCCCCCCCCO FOTKYAAJKYLFFN-UHFFFAOYSA-N 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- LSXWFXONGKSEMY-UHFFFAOYSA-N di-tert-butyl peroxide Chemical compound CC(C)(C)OOC(C)(C)C LSXWFXONGKSEMY-UHFFFAOYSA-N 0.000 description 1
- 239000012933 diacyl peroxide Substances 0.000 description 1
- 239000012975 dibutyltin dilaurate Substances 0.000 description 1
- ZFTFAPZRGNKQPU-UHFFFAOYSA-N dicarbonic acid Chemical compound OC(=O)OC(O)=O ZFTFAPZRGNKQPU-UHFFFAOYSA-N 0.000 description 1
- 239000006185 dispersion Substances 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- WNAHIZMDSQCWRP-UHFFFAOYSA-N dodecane-1-thiol Chemical compound CCCCCCCCCCCCS WNAHIZMDSQCWRP-UHFFFAOYSA-N 0.000 description 1
- MCPKSFINULVDNX-UHFFFAOYSA-N drometrizole Chemical compound CC1=CC=C(O)C(N2N=C3C=CC=CC3=N2)=C1 MCPKSFINULVDNX-UHFFFAOYSA-N 0.000 description 1
- 230000000694 effects Effects 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 238000005401 electroluminescence Methods 0.000 description 1
- 238000010556 emulsion polymerization method Methods 0.000 description 1
- 239000008393 encapsulating agent Substances 0.000 description 1
- NKSJNEHGWDZZQF-UHFFFAOYSA-N ethenyl(trimethoxy)silane Chemical compound CO[Si](OC)(OC)C=C NKSJNEHGWDZZQF-UHFFFAOYSA-N 0.000 description 1
- MABAWBWRUSBLKQ-UHFFFAOYSA-N ethenyl-tri(propan-2-yloxy)silane Chemical compound CC(C)O[Si](OC(C)C)(OC(C)C)C=C MABAWBWRUSBLKQ-UHFFFAOYSA-N 0.000 description 1
- JHYNXXDQQHTCHJ-UHFFFAOYSA-M ethyl(triphenyl)phosphanium;bromide Chemical compound [Br-].C=1C=CC=CC=1[P+](C=1C=CC=CC=1)(CC)C1=CC=CC=C1 JHYNXXDQQHTCHJ-UHFFFAOYSA-M 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 239000011152 fibreglass Substances 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- RMBPEFMHABBEKP-UHFFFAOYSA-N fluorene Chemical compound C1=CC=C2C3=C[CH]C=CC3=CC2=C1 RMBPEFMHABBEKP-UHFFFAOYSA-N 0.000 description 1
- 238000010528 free radical solution polymerization reaction Methods 0.000 description 1
- 238000005227 gel permeation chromatography Methods 0.000 description 1
- 238000001879 gelation Methods 0.000 description 1
- 150000004820 halides Chemical class 0.000 description 1
- XXMIOPMDWAUFGU-UHFFFAOYSA-N hexane-1,6-diol Chemical compound OCCCCCCO XXMIOPMDWAUFGU-UHFFFAOYSA-N 0.000 description 1
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 238000001746 injection moulding Methods 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002513 isocyanates Chemical class 0.000 description 1
- ZFSLODLOARCGLH-UHFFFAOYSA-N isocyanuric acid Chemical compound OC1=NC(O)=NC(O)=N1 ZFSLODLOARCGLH-UHFFFAOYSA-N 0.000 description 1
- 239000002075 main ingredient Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- ZQMHJBXHRFJKOT-UHFFFAOYSA-N methyl 2-[(1-methoxy-2-methyl-1-oxopropan-2-yl)diazenyl]-2-methylpropanoate Chemical compound COC(=O)C(C)(C)N=NC(C)(C)C(=O)OC ZQMHJBXHRFJKOT-UHFFFAOYSA-N 0.000 description 1
- 150000004702 methyl esters Chemical class 0.000 description 1
- 239000012046 mixed solvent Substances 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 239000006082 mold release agent Substances 0.000 description 1
- GYVGXEWAOAAJEU-UHFFFAOYSA-N n,n,4-trimethylaniline Chemical compound CN(C)C1=CC=C(C)C=C1 GYVGXEWAOAAJEU-UHFFFAOYSA-N 0.000 description 1
- GEMHFKXPOCTAIP-UHFFFAOYSA-N n,n-dimethyl-n'-phenylcarbamimidoyl chloride Chemical compound CN(C)C(Cl)=NC1=CC=CC=C1 GEMHFKXPOCTAIP-UHFFFAOYSA-N 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- IJGRMHOSHXDMSA-UHFFFAOYSA-N nitrogen Substances N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 1
- QJGQUHMNIGDVPM-UHFFFAOYSA-N nitrogen group Chemical group [N] QJGQUHMNIGDVPM-UHFFFAOYSA-N 0.000 description 1
- FVXBCDWMKCEPCL-UHFFFAOYSA-N nonane-1,1-diol Chemical compound CCCCCCCCC(O)O FVXBCDWMKCEPCL-UHFFFAOYSA-N 0.000 description 1
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- XKIVKIIBCJIWNU-UHFFFAOYSA-N o-[3-pentadecanethioyloxy-2,2-bis(pentadecanethioyloxymethyl)propyl] pentadecanethioate Chemical compound CCCCCCCCCCCCCCC(=S)OCC(COC(=S)CCCCCCCCCCCCCC)(COC(=S)CCCCCCCCCCCCCC)COC(=S)CCCCCCCCCCCCCC XKIVKIIBCJIWNU-UHFFFAOYSA-N 0.000 description 1
- NIHNNTQXNPWCJQ-UHFFFAOYSA-N o-biphenylenemethane Natural products C1=CC=C2CC3=CC=CC=C3C2=C1 NIHNNTQXNPWCJQ-UHFFFAOYSA-N 0.000 description 1
- 229940065472 octyl acrylate Drugs 0.000 description 1
- 150000002902 organometallic compounds Chemical class 0.000 description 1
- DXGLGDHPHMLXJC-UHFFFAOYSA-N oxybenzone Chemical compound OC1=CC(OC)=CC=C1C(=O)C1=CC=CC=C1 DXGLGDHPHMLXJC-UHFFFAOYSA-N 0.000 description 1
- 125000000864 peroxy group Chemical group O(O*)* 0.000 description 1
- 125000005634 peroxydicarbonate group Chemical group 0.000 description 1
- 239000002530 phenolic antioxidant Substances 0.000 description 1
- 229950000688 phenothiazine Drugs 0.000 description 1
- 229960000969 phenyl salicylate Drugs 0.000 description 1
- HPAFOABSQZMTHE-UHFFFAOYSA-N phenyl-(2,4,6-trimethylphenyl)methanone Chemical compound CC1=CC(C)=CC(C)=C1C(=O)C1=CC=CC=C1 HPAFOABSQZMTHE-UHFFFAOYSA-N 0.000 description 1
- LYXOWKPVTCPORE-UHFFFAOYSA-N phenyl-(4-phenylphenyl)methanone Chemical compound C=1C=C(C=2C=CC=CC=2)C=CC=1C(=O)C1=CC=CC=C1 LYXOWKPVTCPORE-UHFFFAOYSA-N 0.000 description 1
- 150000004714 phosphonium salts Chemical group 0.000 description 1
- OJMIONKXNSYLSR-UHFFFAOYSA-N phosphorous acid Chemical compound OP(O)O OJMIONKXNSYLSR-UHFFFAOYSA-N 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- DOIRQSBPFJWKBE-UHFFFAOYSA-N phthalic acid di-n-butyl ester Natural products CCCCOC(=O)C1=CC=CC=C1C(=O)OCCCC DOIRQSBPFJWKBE-UHFFFAOYSA-N 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229920001748 polybutylene Polymers 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 230000000379 polymerizing effect Effects 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 238000004382 potting Methods 0.000 description 1
- 239000005060 rubber Substances 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 238000007127 saponification reaction Methods 0.000 description 1
- 239000004065 semiconductor Substances 0.000 description 1
- 229910000077 silane Inorganic materials 0.000 description 1
- 239000000344 soap Substances 0.000 description 1
- WSFQLUVWDKCYSW-UHFFFAOYSA-M sodium;2-hydroxy-3-morpholin-4-ylpropane-1-sulfonate Chemical compound [Na+].[O-]S(=O)(=O)CC(O)CN1CCOCC1 WSFQLUVWDKCYSW-UHFFFAOYSA-M 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000001384 succinic acid Substances 0.000 description 1
- 229910052717 sulfur Inorganic materials 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- LVEOKSIILWWVEO-UHFFFAOYSA-N tetradecyl 3-(3-oxo-3-tetradecoxypropyl)sulfanylpropanoate Chemical compound CCCCCCCCCCCCCCOC(=O)CCSCCC(=O)OCCCCCCCCCCCCCC LVEOKSIILWWVEO-UHFFFAOYSA-N 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 229920005992 thermoplastic resin Polymers 0.000 description 1
- 229920001187 thermosetting polymer Polymers 0.000 description 1
- 150000003585 thioureas Chemical class 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- TUQOTMZNTHZOKS-UHFFFAOYSA-N tributylphosphine Chemical compound CCCCP(CCCC)CCCC TUQOTMZNTHZOKS-UHFFFAOYSA-N 0.000 description 1
- MZHULIWXRDLGRR-UHFFFAOYSA-N tridecyl 3-(3-oxo-3-tridecoxypropyl)sulfanylpropanoate Chemical compound CCCCCCCCCCCCCOC(=O)CCSCCC(=O)OCCCCCCCCCCCCC MZHULIWXRDLGRR-UHFFFAOYSA-N 0.000 description 1
- QQQSFSZALRVCSZ-UHFFFAOYSA-N triethoxysilane Chemical compound CCO[SiH](OCC)OCC QQQSFSZALRVCSZ-UHFFFAOYSA-N 0.000 description 1
- BDZBKCUKTQZUTL-UHFFFAOYSA-N triethyl phosphite Chemical compound CCOP(OCC)OCC BDZBKCUKTQZUTL-UHFFFAOYSA-N 0.000 description 1
- ZIBGPFATKBEMQZ-UHFFFAOYSA-N triethylene glycol Chemical compound OCCOCCOCCO ZIBGPFATKBEMQZ-UHFFFAOYSA-N 0.000 description 1
- 125000004205 trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- ILLOBGFGKYTZRO-UHFFFAOYSA-N tris(2-ethylhexyl) phosphite Chemical compound CCCCC(CC)COP(OCC(CC)CCCC)OCC(CC)CCCC ILLOBGFGKYTZRO-UHFFFAOYSA-N 0.000 description 1
- 229920001567 vinyl ester resin Polymers 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
Images
Landscapes
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Macromonomer-Based Addition Polymer (AREA)
Description
一方で、ガラス転移点が高く、より熱安定性に優れる樹脂が得られる「硬化性樹脂組成物」をレンズ材料に適用する検討が進められている。例えば、特許文献1には、側鎖に重合性二重結合を有する(メタ)アクリル系重合体、芳香環構造を有する単官能の(メタ)アクリル系重合性単量体及びラジカル重合開始剤を含有する硬化性樹脂組成物の硬化物が、透明性、耐熱性に優れ、カメラレンズ等の光学部材に好適であることが開示されている。また、特許文献2には、多官能共重合体、ポリオルガノシロキサン、分子内に1〜6個の(メタ)アクリロイル基を有する(メタ)アクリレート及び開始剤を含有する硬化性樹脂組成物の硬化物が、光学特性、耐熱性に優れ、カメラレンズ等の光学材料に好適であることが開示されている。
本発明は、アッベ数及びガラス転移点が共に高い硬化物が容易に得られる光学成型材用硬化性樹脂組成物、及びその硬化物、並びに光学成型材、レンズ、カメラモジュールを提供することを目的とする。
上記態様においては、前記メタクリル系重合体(A)の主鎖が、アルキル基の炭素数2〜8のアルキルメタクリレートモノマー単位を5〜99質量%含有することが好ましい。
本発明の一態様は、上記光学成型材用硬化性樹脂組成物が硬化した硬化物である。
本発明の一態様は、上記硬化物からなる光学成型材である。
本発明の一態様は、上記硬化物を含むレンズである。
本発明の一態様は、上記レンズを含むカメラモジュールである。
本発明の硬化物、光学成型材、レンズは、アッベ数及びガラス転移点が共に高い。
本発明のカメラモジュールは、熱安定性に優れ、レンズ組み合わせの設計の自由度が高い。
また、「単官能」とは、ラジカル重合性二重結合を1つ有することを意味する。「多官能」とは、ラジカル重合性二重結合を2つ以上有することを意味し、例えば「2官能」とは、ラジカル重合性二重結合を2つ有することを意味する。
また、「モノマー単位」とは、重合体を構成する繰り返し単位を意味する。
本発明の一態様の光学成型材用硬化性樹脂組成物(以下、「硬化性樹脂組成物」ともいう。)は、以下に説明する(A)成分、(B)成分、(C)成分及び(D)成分を含有する。本態様の硬化性樹脂組成物は、その他の成分を含有してもよい。
(A)成分は、主鎖の組成中にアルキル基の炭素数が1〜8のアルキルメタクリレートモノマー単位を50〜99.9質量%含有し、側鎖にラジカル重合性二重結合を有するメタクリル系重合体である。すなわち、(A)成分は、アルキル基の炭素数1〜8のアルキルメタクリレートモノマー単位を50〜99.9質量%含有するメタクリル系重合体(以下、「ベースポリマー」という。)の主鎖に、側鎖としてのラジカル重合性二重結合を有する官能基が置換された化学構造を有する。
ここで、アルキルメタクリレートのアルキル基とは、アルキルメタクリレート:CH2=C(CH3)−C(=O)−OR2におけるR2のことである。
(A)成分は(B)成分及び(C)成分に溶解していることが好ましい。(A)成分が(B)成分及び(C)成分に溶解していれば、硬化性樹脂組成物を成型する際の作業性が高くなる。
ベースポリマーは、(A)成分の主鎖となるポリマーであって、アルキル基の炭素数1〜8のアルキルメタクリレートモノマー単位を含有するメタクリル系重合体である。
該メタクリル系重合体は、アルキル基の炭素数1〜8のアルキルメタクリレートモノマー単位以外のモノマー単位を含有してもよい。アルキル基の炭素数1〜8のアルキルメタクリレートモノマー単位以外のモノマー単位としては、アルキル基の炭素数1〜8のアルキルメタクリレート以外の単官能の(メタ)アクリル系モノマー単位及び単官能のビニル基含有モノマー単位が挙げられる。
ベースポリマー(すなわち(A)成分の主鎖)は、(A)成分の(B)成分及び(C)成分に対する溶解性が高くなることから、アルキル基の炭素数1〜8のアルキルメタクリレートモノマー単位は50〜99.9質量%であり、80〜99質量%であることが好ましい。アルキル基の炭素数1〜8のアルキルメタクリレートモノマー単位が50質量%未満であると、硬化性樹脂組成物を成型する際の作業性が低下して光学成型材用として適さないものになるおそれがある。アルキル基の炭素数1〜8のアルキルメタクリレートモノマー単位が99.9質量%を超えると、(A)成分のラジカル重合性二重結合を有する側鎖が少なくなるので、該硬化性樹脂組成物が硬化した硬化物の強度及び透明性が不充分になることがある。
また、ベースポリマーは、アルキル基の炭素数2〜8のアルキルメタクリレートモノマー単位を5〜99質量%含有することが好ましく、10〜80質量%含有することがより好ましい。アルキル基の炭素数2〜8のアルキルメタクリレートモノマー単位が前記下限値以上であれば、硬化性樹脂組成物の粘度がより低位となり、作業性がより良好となり、前記上限値以下であれば、ガラス転移点をより容易に高くできる。
硬化物のガラス転移点がより容易に高くなることから、アルキルメタクリレートとしては、メチルメタクリレート、エチルメタクリレート、n−ブチルメタクリレート、i−ブチルメタクリレート、t−ブチルメタクリレートが特に好ましい。
単官能ビニル基含有モノマーの具体例としては、スチレン、α−メチルスチレン等の芳香族ビニル単量体、アクリロニトリル等のシアン化ビニル単量体及び酢酸ビニル等のビニルエステル単量体が挙げられる。これらモノマーは1種を単独で使用してもよいし、2種以上を併用してもよい。
ラジカル重合性二重結合とは、ラジカル重合ができる二重結合のことを意味する。
側鎖に含まれるラジカル重合性二重結合を有する官能基としては、例えば、(メタ)アクリロイル基、ビニル基が挙げられる。(B)成分や(C)成分との重合性の点から、ラジカル重合性二重結合を有する官能基は(メタ)アクリロイル基が好ましい。
(A)成分の製造方法としては、モノマーを重合してベースポリマーを合成し、次いで、化学修飾法によりベースポリマーにラジカル重合性二重結合を有する官能基を導入する製造する方法が好ましい。
化学修飾法として、カルボキシ基とグリシジル基の反応を利用する場合、例えば、下記(a),(b)の方法が挙げられる。
(a)メタクリル酸のようなカルボキシ基を有する(メタ)アクリル酸モノマー単位を含有したベースポリマーを製造し、得られたベースポリマーのカルボキシ基に、例えば、グリシジルメタクリレートなどのグリシジル基とラジカル重合性二重結合を有する修飾用化合物のグリシジル基を反応させる方法。
(b)グリシジル基を有する(メタ)アクリレートモノマー単位を含有したベースポリマーを製造し、得られたベースポリマーのグリシジル基に、例えば、(メタ)アクリル酸などのカルボキシ基とラジカル重合性二重結合を有する修飾用化合物のカルボキシ基を反応させる方法。
カルボキシ基とグリシジル基の反応には、反応時間の短縮のため反応触媒を用いることが好ましい。反応触媒としては、例えば、テトラブチルアンモニウムブロマイド等の第四級アンモニウム塩、エチルトリフェニルホスホニウムブロマイド等の第四級ホスホニウム塩、トリフェニルホスフィン等のホスフィン系化合物等が挙げられる。硬化物の着色が小さくなる点から、第四級アンモニウム塩が特に好ましい。
この反応触媒の量としては、修飾用化合物100質量部に対して、0.05〜20質量部が好ましく、0.1〜10質量部がより好ましい。反応触媒の量を上記範囲内とすることで、反応時間を短縮でき、かつ、硬化物の着色を小さくできる。
化学修飾法として、ヒドロキシ基とイソシアネート基の反応を利用する場合、例えば、下記(c),(d)の方法が挙げられる。
(c)2−ヒドロキシプロピルメタクリレートのようなヒドロキシ基を有する(メタ)アクリレートモノマー単位を含有したベースポリマーを製造し、得られたベースポリマーのヒドロキシ基に、例えば、2−(メタ)アクリロイルオキシエチルイソシアネートなどのイソシアネート基とラジカル重合性二重結合を有する修飾用化合物のイソシアネート基を反応させる方法。
(d)イソシアネート基を有する(メタ)アクリレートモノマー単位を含有したベースポリマーを製造し、得られたベースポリマーのイソシアネート基に、例えば、2−ヒドロキシエチル(メタ)アクリレートなどのヒドロキシ基とラジカル重合性二重結合を有する修飾用化合物のヒドロキシ基を反応させる方法。
この反応触媒の量としては、修飾用化合物100質量部に対して、0.05〜20質量部が好ましく、0.1〜10質量部がより好ましい。反応触媒の量を上記範囲内とすることで、反応時間を短縮でき、かつ、硬化物の着色を小さくできる。
(B)成分は、アルキル基の炭素数2〜8のアルキルメタクリレートである。
(B)の具体例としては、エチルメタクリレート、n−ブチルメタクリレート、i−ブチルメタクリレート、t−ブチルメタクリレート、ペンチルメタクリレート、ヘキシルメタクリレート、ヘプチルメタクリレート、n−オクチルメタクリレート、i−オクチルメタクリレート、2−エチルヘキシルメタクリレート等が挙げられる。
硬化物のガラス転移点がより容易に高くなることから、(B)成分は、エチルメタクリレート、n−ブチルメタクリレート、i−ブチルメタクリレート、t−ブチルメタクリレートが好ましく、アッベ数がより高くなることから、i−ブチルメタクリレートがより好ましい。
これら(B)成分は、1種単独で用いてもよいし、2種以上を併用してもよい。
(C)成分は、多官能の(メタ)アクリレートである。
(C)成分の具体例としては、エチレングリコールジ(メタ)アクリレート、プロピレングリコールジ(メタ)アクリレート、ブチレングリコールジ(メタ)アクリレート、1,6−ヘキサンジオールジ(メタ)アクリレート、1,9−ノナンジオールジ(メタ)アクリレート、1,10−デカンジオールジ(メタ)アクリレート、ポリエチレングリコールジ(メタ)アクリレート、ポリプロピレングリコールジ(メタ)アクリレート、ポリブチレングリコールジ(メタ)アクリレート、ネオペンチルグリコールジ(メタ)アクリレート、トリシクロデカンジメタノールジ(メタ)アクリレート、ポリカーボネートジオールジ(メタ)アクリレート、ポリエステルジオールジ(メタ)アクリレート、エトキシ化ビスフェノールAジ(メタ)アクリレート、プロポキシ化ビスフェノールAジ(メタ)アクリレート、9,9−ビス(4−(メタ)アクリロイルオキシエトキシフェニル)フルオレン、ウレタンジ(メタ)アクリレート等の2官能の(メタ)アクリレート;トリメチロールプロパントリ(メタ)アクリレート、エトキシ化イソシアヌル酸トリ(メタ)アクリレート、ε−カプロラクトン変性トリス((メタ)アクロキシエチル)イソシアヌレート等の3官能の(メタ)アクリレート;ジトリメチロールプロパンテトラ(メタ)アクリレート等の4官能の(メタ)アクリレート;ジペンタエリスリトールペンタ(メタ)アクリレート等の5官能の(メタ)アクリレート;ジペンタエリスリトールヘキサ(メタ)アクリレート等の6官能の(メタ)アクリレート等が挙げられる。
ラジカル重合性基を有するラジカル重合性基を有するオルガノポリシロキサン化合物としては市販品を用いることができる。市販品としては、例えば、東亞合成株式会社製の「商品名:AC−SQTA−100」、「商品名:AC−SQ SI−20」、「商品名:MAC−SQ TM−100」、「商品名:MAC−SQ SI−20」などのラジカル重合性基を有するシルセスキオキサン化合物が挙げられる。
これら(C)成分は、1種単独で用いてもよいし、2種以上を併用してもよい。
(D)成分は、重合開始剤であり、例えば、光重合開始剤、熱重合開始剤、レドックス重合に用いられる過酸化物などが挙げられる。(D)成分の種類は重合方法に応じて適宜選択することができる。
これらの中でも、硬化物の着色を抑制できる点で、アルキルフェノン型化合物が好ましく、2−ヒドロキシ−2−メチル−1−フェニルプロパン−1−オン、1−ヒドロキシシクロヘキシルフェニルケトンがより好ましい。また、硬化物の内部まで十分に硬化されやすくなる点で、アシルフォスフィンオキサイド型化合物が好ましく、硬化物の着色を抑制できる点で、2,4,6−トリメチルベンゾイルジフェニルホスフィンオキサイドがより好ましい。これらの光重合開始剤は、1種単独で用いてもよく、2種以上を併用してもよい。
有機過酸化物の具体例としては、メチルエチルケトンパーオキサイド等のケトンパーオキサイド;1,1−ジ(t−ヘキシルパーオキシ)−3,3,5−トリメチルシクロヘキサン、1,1−ジ(t−ヘキシルパーオキシ)シクロヘキサン、1,1−ジ(t−ブチルパーオキシ)シクロヘキサン等のパーオキシケタール;1,1,3,3−テトラメチルブチルハイドロパーオキサイド、クメンハイドロパーオキサイド、p−メンタンハイドロパーオキサイド等のハイドロパーオキサイド;ジクミルパーオキサイド、ジ−t−ブチルパーオキサイド等のジアルキルパーオキサイド;ジラウロイルパーオキサイド、ジベンゾイルパーオキサイド等のジアシルパーオキサイド;ジ(4−t−ブチルシクロヘキシル)パーオキシジカーボネート、ジ(2−エチルヘキシル)パーオキシジカーボネート等のパーオキシジカーボネート;t−ブチルパーオキシ−2−エチルヘキサノエート、t−ヘキシルパーオキシイソプロピルモノカーボネート、t−ブチルパーオキシベンゾエート、1,1,3,3−テトラメチルブチルパーオキシ−2−エチルヘキサノエート等のパーオキシエステルなどが挙げられる。
アゾ化合物の具体例としては、2,2’−アゾビスイソブチロニトリル、2,2’−アゾビス(2−メチルブチロニトリル)、2,2’−アゾビス(2,4−ジメチルバレロニトリル)、1,1’−アゾビス−1−シクロヘキサンカルボニトリル、ジメチル−2,2’−アゾビスイソブチレート、4,4’−アゾビス−4−シアノバレリック酸、2,2’−アゾビス−(2−アミジノプロパン)ジハイドロクロライドなどが挙げられる。
これらの熱重合開始剤は、1種単独で用いてもよく、2種以上を併用してもよい。
熱重合開始剤としては、硬化物に気泡が生じにくい点で、有機過酸化物が好ましい。硬化性樹脂組成物の硬化時間とポットライフとのバランスを考慮すると、有機過酸化物の10時間半減期温度は35〜80℃が好ましく、より好ましくは40〜75℃であり、さらに好ましくは45〜70℃である。10時間半減期温度が35℃以上であれば、常温で硬化性樹脂組成物がゲル化しにくくなり、ポットライフが良好となる。一方、10時間半減期温度が80℃以下であれば、硬化性樹脂組成物の硬化時間を短縮できる。このような半減期温度の有機過酸化物としては、例えば、1,1,3,3−テトラメチルブチルパーオキシ−2−エチルヘキサノエート、t−ブチルパーオキシ−2−エチルヘキサノエート、ジ(4−t−ブチルシクロヘキシル)パーオキシジカーボネートなどが挙げられる。1,1,3,3−テトラメチルブチルパーオキシ−2−エチルヘキサノエートの市販品としては、例えばパーオクタO(商品名、日油株式会社製、10時間半減期温度:65.3℃)等が挙げられる。t−ブチルパーオキシ−2−エチルヘキサノエートの市販品としては、例えばパーブチルO(商品名、日油株式会社製、10時間半減期温度:72.1℃)等が挙げられる。ジ(4−t−ブチルシクロヘキシル)パーオキシジカーボネートの市販品としては、例えばパーロイルTCP(商品名、日油株式会社製、10時間半減期温度:40.8℃)等が挙げられる。
なお、レドックス重合には、通常、レドックス系重合開始剤が用いられる。レドックス系重合開始剤は、過酸化物と還元剤とを併用した重合開始剤である。上述した過酸化物をレドックス系重合開始剤として使用する場合、還元剤との組み合わせの一例は以下の通りである。
(1)ジベンゾイルパーオキサイド(過酸化物)と、N,N−ジメチルアニリン、N,N−ジメチル−p−トルイジン、N,N−ビス(2−ヒドロキシプロピル)−p−トルイジン等の芳香族3級アミン類(還元剤)との組み合わせ。
(2)ハイドロパーオキサイド(過酸化物)と金属石鹸類(還元剤)との組み合わせ。
(3)ハイドロパーオキサイド(過酸化物)とチオ尿素類(還元剤)との組み合わせ。
これら(D)成分は、1種単独で用いてもよいし、2種以上を併用してもよい。
本態様の硬化性樹脂組成物は、本発明の効果を損なわない範囲内であれば、前記(A)〜(D)成分以外のその他の成分を含有してもよい。その他の成分としては、例えば、(B)成分以外の単官能のビニル基含有化合物、酸化防止剤、紫外線吸収剤、ゴム、シリカ粒子、ジルコニア、可塑剤、消泡剤、揺変剤、離型剤、充填剤、蛍光体、顔料等が挙げられる。その他の成分は1種単独で用いてもよく、2種以上を併用してもよい。
(B)成分以外の単官能のビニル基含有化合物の具体例としては、(メタ)アクリル酸、コハク酸2−(メタ)アクリロイルオキシエチル、マレイン酸2−(メタ)アクリロイルオキシエチル、フタル酸2−(メタ)アクリロイルオキシエチル、ヘキサヒドロフタル酸2−(メタ)アクリロイルオキシエチル等のカルボキシ基を有する(メタ)アクリレート;2−ヒドロキシエチル(メタ)アクリレート、2−ヒドロキシプロピル(メタ)アクリレート、2−ヒドロキシブチル(メタ)アクリレート、4−ヒドロキシブチル(メタ)アクリレート、6−ヒドロキシヘキシル(メタ)アクリレート等のヒドロキシ基を有する(メタ)アクリレート;メチルアクリレート、エチルアクリレート、n−ブチルアクリレート、i−ブチルアクリレート、t−ブチルアクリレート、ペンチルアクリレート、ヘキシルアクリレート、ヘプチルアクリレート、n−オクチルアクリレート、i−オクチルアクリレート、2−エチルヘキシルアクリレート等の炭素数1〜8のアルキルアクリレート;n−ノニル(メタ)アクリレート、i−ノニル(メタ)アクリレート、デシル(メタ)アクリレート、ラウリル(メタ)アクリレート、トリデシル(メタ)アクリレート、ステアリル(メタ)アクリレート等の炭素数9以上のアルキル(メタ)アクリレート;シクロヘキシル(メタ)アクリレート、ジシクロペンテニル(メタ)アクリレート、2−ジシクロペンテノキシエチル(メタ)アクリレート、イソボルニル(メタ)アクリレート、ジシクロペンタニル(メタ)アクリレート、アダマンチル(メタ)アクリレート等の脂環式構造を有する(メタ)アクリレート;フェニル(メタ)アクリレート、ベンジル(メタ)アクリレート、フェノキシエチル(メタ)アクリレート、フェノキシジエチレングリコール(メタ)アクリレート、フェノキシポリエチレングリコール(メタ)アクリレート、ノニルフェノキシポリエチレングリコール(メタ)アクリレート、フェノキシポリプロピレングリコール(メタ)アクリレート、フェニルフェニル(メタ)アクリレート、フェニルフェノキシエチル(メタ)アクリレート、フェノキシベンジル(メタ)アクリレート、フェニルベンジル(メタ)アクリレート、ナフチル(メタ)アクリレート、(1−ナフチル)メチル(メタ)アクリレート等の芳香環構造を有する(メタ)アクリレート;テトラヒドロフルフリル(メタ)アクリレート、グリシジル(メタ)アクリレート、(メタ)アクリロイルモルフォリン等のヘテロ環構造を有する(メタ)アクリレート;メトキシエチル(メタ)アクリレート、エトキシエチル(メタ)アクリレート、ブトキシエチル(メタ)アクリレート等のアルコキシ(メタ)アクリレート;3−(メタ)アクリロキシプロピルトリメトキシシラン、3−(メタ)アクリロキシプロピルトリエトキシシラン、2−(メタ)アクリロイロキシエチルアシッドホスフェート、トリフルオロエチル(メタ)アクリレート、ヘプタデカフルオロデシル(メタ)アクリレート及び2−(メタ)アクリロイルオキシエチルイソシアネート、スチレン、α−メチルスチレン、アクリロニトリル、酢酸ビニル等が挙げられる。
(B)成分以外の単官能のビニル基含有化合物は1種単独で用いてもよく、2種以上を併用してもよい。
ただし、硬化物のアッベ数を高くするという点では、(B)成分以外の単官能のビニル基含有化合物としては、芳香環を有さない化合物が好ましい。また、(B)成分以外の単官能のビニル基含有化合物として、芳香環を有する化合物を含まないことが好ましい。
酸化防止剤の具体例としては、2,6−ジ−t−ブチルフェノール、2,6−ジ−t−ブチル−p−クレゾール、n−オクタデシル−3−(3’,5’−ジ−t−ブチル−4’−ヒドロキシフェニル)プロピオネート、テトラキス−[メチレン−3−(3’,5’−ジ−t−ブチル−4’−ヒドロキシフェニル)プロピオネート]メタン、トリエチレングリコールビス[3−(3−t−ブチル−5−メチル−4−ヒドロキシフェニル)プロピオネート]、1,6−ヘキサンジオールビス[3−(3,5−ジ−t−ブチル−4−ヒドロキシフェニル)プロピオネート]等のフェノール系酸化防止剤;トリエチルホスファイト、トリ(2−エチルヘキシル)ホスファイト、トリデシルホスファイト、トリフェニルホスファイト、トリスイソデシルホスファイト、トリストリデシルホスファイト、トリス(2,4−ジ−t−ブチルフェニル)ホスファイト等のリン系酸化防止剤;ジヘキシルスルフィド、ジラウリル−3,3’−チオジプロピオネート、ジトリデシル−3,3’−チオジプロピオネート、ジミリスチル−3,3’−チオジプロピオネート、ジステリアル−3,3’−チオジプロピオネート、ペンタエリスリトールテトラキス(β−ラウリルチオプロピオネート)等の硫黄系酸化防止剤などが挙げられる。
酸化防止剤は1種単独で用いてもよく、2種以上を併用してもよい。
紫外線吸収剤の具体例としては、2−ヒドロキシ−4−メトキシベンゾフェノン、2−ヒドロキシ−オクチルオキシベンゾフェノン、2−ヒドロキシ−4−デシルオキシベンゾフェノン、2−ヒドロキシ−4,4’−ジメトキシベンゾフェノン、2−ヒドロキシ−4,4’−ジブトキシベンゾフェノンなどの2―ヒドロキシベンゾフェノンの誘導体;2−(2’−ヒドロキシ−5’−メチルフェニル)ベンゾトリアゾール、2−(2’−ヒドロキシ−3’,5’−ジターシャリイブチルフェニル)ベンゾトリアゾール或いはこれらのハロゲン化物;フェニルサリシレート、p−ターシャリイブチルフェニルサリシレート、ヒドロキシフェニルトリアジン系紫外線吸収剤等が挙げられる。
紫外線吸収剤は1種単独で用いてもよく、2種以上を併用してもよい。
硬化性樹脂組成物中の(A)成分の配合量は、(A)〜(C)成分の合計量100質量%に対し、1〜50質量%が好ましく、より好ましくは3〜40質量%、さらに好ましくは5〜35質量%である。硬化性樹脂組成物中の(A)成分の配合量を上記範囲とすることで、硬化性樹脂組成物を作業性が良好な粘度にできる。また、硬化性樹脂組成物中の(A)成分の配合量を上記範囲とすることで、硬化収縮率を抑制することができ、硬化物の白濁を防止することができる。
硬化性樹脂組成物中の(B)成分の配合量は、(A)〜(C)成分の合計量100質量%に対し、30〜80質量%が好ましく、より好ましくは35〜75質量%、さらに好ましくは40〜70質量%である。硬化性樹脂組成物中の(B)成分の配合量を上記範囲とすることで、硬化性樹脂組成物を作業性が良好な粘度にできる。また、(B)成分の配合量を80質量%以下とすることで(A)成分と(C)成分の配合量を増加することができるため、硬化物のガラス転移点をより容易に高くすることができる。
硬化性樹脂組成物中の(C)成分の配合量は、(A)〜(C)成分の合計量100質量%に対し、1〜50質量%が好ましく、より好ましくは3〜40質量%、さらに好ましくは5〜30質量%である。硬化性樹脂組成物中の(C)成分の配合量を1質量%以上とすることで硬化物のガラス転移点を良好にできる。また、(C)成分の配合量を50質量%以下とすることで、硬化物のアッベ数を良好にできる。
硬化性樹脂組成物中の(D)成分の配合量は、(A)〜(C)成分の合計量100質量部に対し、0.05〜10質量部が好ましく、0.3〜7.0質量部がより好ましく、0.5〜5.0質量部がさらに好ましい。硬化性樹脂組成物中の(D)成分の配合量を0.05質量部以上とすることで硬化性樹脂組成物の硬化性を良好なものとできる。また、10質量部以下とすることで、硬化物の透明性を良好なものとできる。
硬化性樹脂組成物が酸化防止剤を含有する場合、酸化防止剤の含有量は、(A)〜(C)成分の総量100質量部に対して、0.05〜5質量部であることが好ましく、0.1〜3質量部であることがより好ましく、0.2〜2質量部であることがさらに好ましい。酸化防止剤の含有量が0.05質量部以上であることにより、硬化物の酸化による着色を抑制できる。また、酸化防止剤の含有量が5質量部以下であることにより、硬化物の透明性が良好となる。
硬化性樹脂組成物が紫外線吸収剤を含有する場合、紫外線吸収剤の含有量は、(A)〜(C)成分の総量100質量部に対して、0.05〜5質量部であることが好ましく、0.1〜3質量部であることがより好ましく、0.2〜2質量部であることがさらに好ましい。紫外線吸収剤の含有量が0.05質量部以上であることにより、硬化物の耐候性を向上できる。また、紫外線吸収剤の含有量が5質量部以下であることにより、硬化物の透明性が良好となる。
硬化性樹脂組成物の製造方法としては、例えば、(B)成分に修飾用化合物及びベースポリマーを溶解して、前述した二重結合導入反応を行うことで(A)成分を合成し、更に、(C)成分、(D)成分及びその他の成分を適宜加え、攪拌混合することで、硬化性樹脂組成物を得る方法等が挙げられる。
硬化性樹脂組成物の粘度は、23℃においてB型粘度計を用いた測定値が50〜30,000mPa・sであることが好ましく、より好ましくは100〜20,000mPa・sであり、さらに好ましくは300〜15,000mPa・sである。硬化性樹脂組成物の粘度が上記範囲内であれば、型への流し込みや、コーティングの作業性が良好となる。
硬化性樹脂組成物の粘度は、各成分の配合量によって調整することができる。例えば、(A)成分の含有量が増える程、粘度は高くなる。また、(B)成分の含有量が増える程、粘度は低くなる。
本態様の硬化物は、上述の硬化性樹脂組成物を硬化して得ることができる。
硬化物を得る方法としては、例えば、本態様に係る硬化性樹脂組成物を目的の形状に賦形し、その状態で硬化させて目的の形状を有する硬化物を得る方法が挙げられる。このようにして目的の形状を有する硬化物を得る方式としては、例えば、硬化性樹脂組成物を型に流し込むキャスティング成形方式、液体樹脂射出成形方式(LIM方式)、トランスファー成形方式などや、硬化性樹脂組成物を塗工するコーティング方式やプリンティング成形方式、ポッティング成形方式などが挙げられる。
また、硬化性樹脂組成物を硬化する方法としては、硬化性樹脂組成物に含まれる重合開始剤((D)成分)の種類に応じて、光重合、熱重合及びレドックス重合のいずれかの方法を採用できる。いずれの場合にも、硬化の際には、(A)成分、(B)成分及び(C)成分がラジカル重合する。
熱重合により硬化性樹脂組成物を硬化して光学部材用樹脂を得る場合、硬化条件は特に限定されないが、着色が抑制された光学部材用樹脂が得られやすい点から、硬化温度は40〜150℃が好ましく、60〜130℃がより好ましい。LIM方式やトランスファー成形方式などのように、予め加熱された型に硬化性樹脂組成物を注入して成形する場合の硬化時間(加熱時間)は、硬化温度によっても異なるが、例えば硬化温度が100℃の場合、1〜180秒が好ましく、1〜120秒がより好ましく、1〜60秒がさらに好ましい。一方、キャスティング成形方式のように常温の型に硬化性樹脂組成物を注入後、加熱する場合の硬化時間は、硬化温度によっても異なるが、例えば硬化温度が70℃の場合、5分〜5時間が好ましく、10分〜3時間がより好ましい。
硬化性樹脂組成物を熱重合した後には、アフターキュアーをさらに行うことが好ましい。これにより、硬化物中に残存する未反応の(メタ)アクリロイル基の量を減少させることができ、硬化物の強度をより高めることができる。アフターキュアーの条件としては、50〜200℃で0.1〜10時間が好ましく、70〜150℃で0.2〜5時間がより好ましい。
レドックス重合により硬化性樹脂組成物を硬化して硬化物を得る場合、レドックス系重合開始剤を用いることで、5〜40℃の常温で硬化することができる。得られる硬化物に残存する未反応の(メタ)アクリロイル基の量を減少させることができ、硬化物の強度をより高めることができる点から、硬化温度は15〜40℃が好ましい。また、硬化性樹脂組成物がゲル化しにくく、安定的に取り扱える点から、予め還元剤を硬化性樹脂組成物に溶解させておき、これに過酸化物を追加する手順で硬化を実施する方法が好ましい。
硬化物のアッベ数は、54.5以上であることが好ましく、55.0以上であることがより好ましく、55.5以上であることはさらに好ましい。硬化物のアッベ数が54.5以上であれば、レンズ等の光学成型材に適用した場合に多様な光学設計が可能となる。なお、アッベ数は、後述する方法により測定される値である。
硬化物のガラス転移点は、110℃以上であることが好ましく、115℃以上であることがより好ましく、120℃以上であることがさらに好ましい。硬化物のガラス転移点が110℃以上であれば、85℃、85%RHの標準的な高温高湿試験環境においても硬化物の形状が安定する(すなわち、変形しにくい)ため、光学成型材に適用した場合に高い信頼性を得られる。なお、本発明において、「硬化物のガラス転移点」とは、動的粘弾性測定装置にて測定した損失正接(tanδ)が最大値を示す温度である。具体的には、硬化物のガラス転移点は、後述する方法により測定される値である。
本態様の光学成型材は、上述の硬化物からなる成型物である。該成型は、硬化性樹脂組成物を硬化した後に行ってもよく、硬化と同時に行ってもよい。
光学成型材の用途としては、例えば、レンズ、フィルム、シート、光導波路、封止材、接着剤、反射材、波長変換材、硝子繊維強化プラスチック等などが挙げられる。本態様に係る光学成型材は、高いアッベ数及び高いガラス転移点を有するため、カメラレンズ等のレンズとして特に有用である。
本態様のレンズは、本態様の硬化物を含む。該レンズは、例えば、携帯電話、スマートフォン、タブレット端末、ウェアラブル端末、パーソナルコンピュータ、デジタルカメラ等の電子機器、発光ダイオードモジュール、フォトトランジスタ等の半導体素子、有機エレクトロルミネッセンス(有機EL)デバイス、フラットパネルディスプレイ、タッチパネル、電子ペーパー、プロジェクター等の画像表示装置、自動車のバックカメラ、ドライブレコーダー、運転支援センサー等に備え付けられるカメラモジュール、太陽電池などに用いることができる。
本態様のレンズは、本態様の硬化物のみで構成されてもよいし、平面ガラス、曲面ガラスまたはガラスウエハー等の透明基材と、該透明基材の片面または両面上に形成された本態様の硬化物とからなるハイブリッドレンズであってもよい。
レンズの成形方法としては、上下型で硬化性樹脂組成物を挟み込んだ後、加熱または光照射により樹脂を硬化することでレンズを得るキャスティング方式などが挙げられる。キャスティング方式としては、レンズ個片を1点ずつ成形する方法や、複数のレンズ形状が転写されたウエハーを成形した後、レンズ個片を切り出すウエハーレベル方式などが挙げられる。
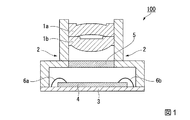
本態様に係るカメラモジュールは、本態様のレンズを含む。図1に、本態様に係るカメラモジュールの一例の断面図を示す。図1に示すカメラモジュール100は、本態様のレンズである2枚のカメラレンズ1a,1b及び赤外線カットフィルター5を備えるレンズホルダー2と、撮像素子であるセンサーチップ4及びセンサーチップ4に電気的に接続されたボンディングワイヤ6a,6bが取り付けられた基板3とを具備する。レンズホルダー2は基板3上に積層されている。
なお、図1に示すカメラモジュール100が備えるカメラレンズは2枚であるが、カメラレンズは1枚であってもよいし、3枚以上であってもよい。複数枚のレンズを備える場合、本態様のレンズ以外の樹脂製レンズや、ガラス製のカメラレンズが混在していてもよい。
また、その他の態様のカメラモジュールとしては、ウエハー上に形成された、レンズとイメージセンサーウエハーとの接着積層体をダイシングするウエハーレベル方式によって形成されるカメラモジュールが挙げられる。
本態様のカメラモジュールは、ガラス転移点が高い本態様のレンズを備えるため、熱安定性に優れる。また、本態様のカメラモジュールは、アッベ数が高い本態様のレンズを使用するため、レンズ組み合わせの設計の自由度が高い。
<評価方法>
実施例及び比較例における重量平均分子量、酸価、二重結合当量、粘度、アッベ数、ガラス転移点についての評価は以下の方法で実施した。
[重量平均分子量]
製造した下記ベースポリマー1〜4をそれぞれ溶剤(テトラヒドロフラン)に溶解し、ゲルパーミュエーションクロマトグラフィーを用いて分子量を測定した。測定した分子量は、ポリスチレンの標準物質を用いて求めた重量平均分子量である。
[酸価]
製造した下記ベースポリマー1〜4、及び下記樹脂液1〜6をそれぞれトルエンとエタノールの混合溶媒に溶解し、ベースポリマー1gまたは樹脂液1〜6中の(A)成分1gを中和する水酸化カリウムのmg数を測定し、酸価とした。ベースポリマー1〜4の酸価を「初期酸価」、樹脂液1〜6中の(A)成分の酸価を「反応後酸価」とした。
[二重結合当量]
以下の式(1),(2)を用いて、合成した(A)成分の二重結合当量を評価した。
(A)成分1g当たりの二重結合量(mol)={(初期酸価−反応後酸価)/(水酸化カリウムの分子量)}/1000・・・式(1)
(A)成分の二重結合当量(g/mol)=1/((A)成分1g当たりの二重結合量)・・・式(2)
[粘度]
得られた硬化性樹脂組成物の液温を23℃とし、B型粘度計を用いて粘度を測定した。
[アッベ数]
約6mm×35mm×厚さ1mmの硬化物の25℃の屈折率(nD:D線(589nm)、nF:F線(486nm)、nC:C線(656nm))を多波長アッベ屈折計(商品名:DR−M2、株式会社アタゴ製)により測定した。なお、測定中間液として、1−ブロモナフタレンを用いた。得られた屈折率から、式(3)を用いてアッベ数を算出した。
アッベ数=(nD−1)/(nF−nC) ・・式(3)
[ガラス転移点の測定]
約6mm×35mm×厚さ1mmの硬化物の損失正接(tanδ)を測定し、損失正接が最大値を示す温度を、該硬化物のガラス転移点とした。測定には、動的粘弾性測定装置(商品名:RSA−II、レオメトリクス社製)を用いた。測定条件は引っ張りモードとした。測定周波数は10Hzとした。
[製造例1:ベースポリマー1の製造]
撹拌機、冷却管、温度計を備えた重合装置中に、分散媒として脱イオン水145部、分散安定剤としてポリビニルアルコール(ケン化度:80%、重合度:1,700)0.5部を加えて撹拌した。ポリビニルアルコールが完全に溶解した後、撹拌を停止し、メチルメタクリレート60部、n−ブチルメタクリレート36部、メタクリル酸4部、重合開始剤として、2,2’−アゾビス(2−メチルブチロニトリル)(大塚化学株式会社製、商品名:AMBN)0.23部、連鎖移動剤として、n−ドデシルメルカプタン0.93部を加えて、再度撹拌した。
撹拌下で窒素置換を行い、80℃に昇温して重合を行った。重合発熱のピークを検出後、95℃に昇温して、さらに0.5時間反応を行い、30℃に冷却した。得られた水性懸濁液を目開き45μmのナイロン製濾過布で濾過し、濾過物を脱イオン水で洗浄した。脱水後、40℃で24時間乾燥して、粒状の(メタ)アクリル系重合体(これを「ベースポリマー1」と称する。表1で示した他のベースポリマーについても同様に番号を付して称する。)を得た。
得られたベースポリマー1の重量平均分子量(Mw)は42,000であった。また、酸価は、26mgKOH/gであった。
表1に示した内容に変更した以外は、製造例1と同様の方法で、ベースポリマー2〜4を製造し、重量平均分子量及び酸価の測定を行った。
ベースポリマー1〜4の製造で使用した成分の使用量と評価結果を表1に示す。なお、使用量は、モノマーの合計量を100部としたときの割合を示す。
冷却器を備えた反応容器に、(B)成分としてi−ブチルメタクリレート60部、重合禁止剤として、2−6−ジ−t−ブチル−4−メチルフェノール0.04部、グリシジル基とラジカル重合性二重結合を有する化合物として、グリシジルメタクリレート3.2部、反応触媒としてテトラブチルアンモニウムブロマイド0.12部を加えた。反応容器内の液を攪拌しながら、ベースポリマー1を40部加え、反応容器内を95℃に昇温した。温度を維持したまま10時間攪拌することで、ベースポリマー1への二重結合導入反応行い、(A)成分を得た。10時間後、常温まで冷却し、樹脂液(これを「樹脂液1」と称する。また、表2〜4で示した他の樹脂液についても同様に番号を付して称する。)を得た。樹脂液1中の(A)成分の酸価は、0.5mgKOH/gであった。酸価から算出した(A)成分の二重結合当量は、2290g/mol、生成量は42.6部であった。
表2に示した内容に変更した以外は、製造例1と同様の方法で、樹脂液2〜6を製造し、重量平均分子量及び酸価の測定、二重結合当量の算出を行った。主要成分の使用量と評価結果を表2に示した。なお、使用量は、ベースポリマー、及び(B)成分の合計量を100部とした場合の割合を示す。
冷却器を備えた反応容器に、樹脂液1を72部(内容物として、(A)成分29.7部、i−ブチルメタクリレート41.9部、グリシジルメタクリレート0.4部を含む。)加え、更に(B)成分として、i−ブチルメタクリレートを8.4部、(C)成分として、メタクリロイル基を有するシルセスキオキサン化合物(東亞合成株式会社製、商品名:MAC−SQ TM−100)を20部、(D)成分として光重合開始剤(BASF社製、商品名:IRGACURE184)を1部加え、50℃で1時間攪拌混合した。1時間後常温まで冷却し、硬化性樹脂組成物を得た。
得られた硬化性樹脂組成物を、約6mm×35mmの長方形状の切り抜きを形成した厚さ1mmのシリコーンシートをガスケットとして用いて、2枚のガラス板で挟み込み、高圧水銀灯で積算光量3,000mJ/cm2の紫外線を照射した後、100℃で30分間加熱した。冷却後、シリコーンシート及び板ガラスを除去し、約6mm×35mm×厚さ1mmの硬化物を得た。
得られた硬化物を用い、アッベ数及びガラス転移点を測定した。
冷却器を備えた反応容器に、樹脂液1を72部加え、更に(B)成分として、i−ブチルメタクリレートを8.4部、(C)成分として、メタクリロイル基を有するシルセスキオキサン化合物(東亞合成株式会社製、商品名:MAC−SQTM−100)20部を1部加え、50℃で1時間攪拌混合した。1時間後常温まで冷却し、(D)成分としてパーオクタO(熱重合開始剤)を加え、攪拌混合して硬化性樹脂組成物を得た。
得られた硬化性樹脂組成物を、約6mm×35mmの長方形状の切り抜きを形成した厚さ1mmのシリコーンシートをガスケットとして用いて、2枚のガラス板で挟み込み、80℃で2時間加熱した後、さらに120℃で1時間加熱した。冷却後、シリコーンシート及び板ガラスを除去し、約6mm×35mm×厚さ1mmの硬化物を得た。
得られた硬化物を用い、アッベ数及びガラス転移点を測定した。
用いた成分を表3,4に記載の内容に変更した以外は、実施例1と同様に硬化性樹脂組成物及び硬化物を作製し、アッベ数及びガラス転移点を測定した。
一方、比較例1の硬化物は(B)成分の代わりに、芳香環構造を有するメタクリレート化合物(ベンジルメタクリレート)を用いたため、アッベ数が低い結果となった。
MMA:メチルメタクリレート(三菱ケミカル株式会社製、製品名「アクリエステルM」)。
n−BMA:n−ブチルメタクリレート(三菱ケミカル株式会社製、製品名「アクリエステルB」)。
i−BMA:i−ブチルメタクリレート(三菱ケミカル株式会社製、製品名「アクリエステルIB」)。
MAA:メタクリル酸(三菱ケミカル株式会社製、製品名「メタクリル酸」)。
AMBN:2,2’−アゾビス(2−メチルブチロニトリル)(大塚化学株式会社製、製品名:AMBN)。
TBAB:テトラブチルアンモニウムブロマイド(富士純薬株式会社製、製品名「TBAB」)。
GMA:グリシジルメタクリレート(三菱ケミカル株式会社製、製品名「アクリエステルG」)。
BZMA:ベンジルメタクリレート(三菱ケミカル株式会社、製品名「アクリエステルBZ」)。
BHT:2−6−ジ−t−ブチル−4−メチルフェノール(本州化学株式会社製、製品名「H−BHT」)。
t−BMA:t−ブチルメタクリレート(三菱ケミカル株式会社製、製品名「アクリエステルTB」)。
MAC−SQ TM−100:メタクリロイル基を有するシルセスキオキサン化合物(東亞合成株式会社製、商品名「MAC−SQ TM−100」)。
TMPTMA:トリメチロールプロパントリメタクリレート(三菱ケミカル株式会社製、製品名「アクリエステルTMP」)。
DPHA:ジペンタエリスリトールペンタアクリレートとジペンタエリスリトールヘキサアクリレートの混合物(日本化薬株式会社製、製品名「KAYARAD DPHA」)。
NKエステルNPG:ネオペンチルグリコールジメタクリレート(新中村化学工業株式会社製、製品名「NKエステルNPG」)。
NKエステルDCP:トリシクロデカンジメタノールジメタクリレート(新中村化学工業株式会社製、製品名「NKエステルDCP」)。
IRGACURE184:1−ヒドロキシシクロヘキシルフェニルケトン(BASF社製、製品名「IRAGACURE184」)。
IRGACURE TPO:2,4,6−トリメチルベンゾイルジフェニルホスフィンオキサイド(BASF社製、製品名「IRGACURE TPO」)。
パーオクタO:1,1,3,3−テトラメチルブチルパーオキシ−2−エチルヘキサノエート(日油株式会社製、製品名「パーオクタO」)。
Claims (8)
- メタクリル系重合体(A)(ただし、芳香族環構造を有するメタクリル系重合体及びウレタン結合を有するメタクリル系重合体を除く。)、アルキル基の炭素数が2〜8のアルキルメタクリレート(B)、多官能の(メタ)アクリレート(C)及びラジカル重合開始剤(D)を含有し、
前記メタクリル系重合体(A)は、該重合体の主鎖が、アルキル基の炭素数が1〜8のアルキルメタクリレートモノマー単位を50〜99.9質量%含有し、側鎖にラジカル重合性二重結合を有し、
硬化物のアッベ数が54.5以上となる、光学成型材用硬化性樹脂組成物。 - 前記メタクリル系重合体(A)の主鎖は、アルキル基の炭素数2〜8のアルキルメタクリレートモノマー単位を5〜99質量%含有する、請求項1に記載の光学成型材用硬化性樹脂組成物。
- 前記アルキルメタクリレート(B)が、i−ブチルメタクリレート及びt−ブチルメタクリレートからなる群から選ばれる少なくとも1種以上である、請求項1または2に記載の光学成型材用硬化性樹脂組成物。
- 請求項1〜3のいずれか一項に記載の光学成型材用硬化性樹脂組成物が硬化した硬化物。
- ガラス転移点が、110℃以上である、請求項4に記載の硬化物。
- 請求項4または5に記載の硬化物からなる光学成型材。
- 請求項4または5に記載の硬化物を含むレンズ。
- 請求項7に記載のレンズを含むカメラモジュール。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017136496A JP6915417B2 (ja) | 2017-07-12 | 2017-07-12 | 光学成型材用硬化性樹脂組成物、及びその硬化物、並びに光学成型材、レンズ、カメラモジュール |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017136496A JP6915417B2 (ja) | 2017-07-12 | 2017-07-12 | 光学成型材用硬化性樹脂組成物、及びその硬化物、並びに光学成型材、レンズ、カメラモジュール |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2019019171A JP2019019171A (ja) | 2019-02-07 |
| JP6915417B2 true JP6915417B2 (ja) | 2021-08-04 |
Family
ID=65355088
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017136496A Active JP6915417B2 (ja) | 2017-07-12 | 2017-07-12 | 光学成型材用硬化性樹脂組成物、及びその硬化物、並びに光学成型材、レンズ、カメラモジュール |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP6915417B2 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP7149892B2 (ja) * | 2019-03-29 | 2022-10-07 | ホヤ レンズ タイランド リミテッド | 光学物品用コーティング組成物、眼鏡レンズ、眼鏡および眼鏡レンズの製造方法、ならびに光学物品および光学物品の製造方法 |
| WO2025164477A1 (ja) * | 2024-01-31 | 2025-08-07 | 三井化学株式会社 | 光硬化性樹脂組成物、光学成型体、光学デバイス、および光学成型体の製造方法 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS62513A (ja) * | 1985-06-26 | 1987-01-06 | Showa Highpolymer Co Ltd | 光硬化性樹脂組成物 |
| TW200904841A (en) * | 2007-03-29 | 2009-02-01 | Dainippon Ink & Chemicals | Active energy ray curing type resin composition for casting and hardening object |
| JP2010072428A (ja) * | 2008-09-19 | 2010-04-02 | Dic Corp | 光学物品用活性エネルギー線硬化型樹脂組成物及び硬化物 |
| KR101779531B1 (ko) * | 2010-02-26 | 2017-09-18 | 신닛테츠 수미킨 가가쿠 가부시키가이샤 | 경화성 수지 조성물, 그 경화물 및 광학 재료 |
| JP6582413B2 (ja) * | 2014-01-16 | 2019-10-02 | 三菱ケミカル株式会社 | 硬化性樹脂組成物、硬化物、光学部材及び光学デバイス |
-
2017
- 2017-07-12 JP JP2017136496A patent/JP6915417B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| JP2019019171A (ja) | 2019-02-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN101675083B (zh) | 光学用树脂组合物以及使用它的光学用树脂材料 | |
| TWI545166B (zh) | 影像顯示裝置用黏著片、影像顯示裝置及其製造方法、及黏著性樹脂組成物 | |
| CN101687953B (zh) | 光学部件用树脂、光学部件用树脂中使用的原料组合物和光学部件 | |
| TW200831547A (en) | Resin composition for optical use, resin material for optical use using the same, optical filter for image display device, and image display device | |
| KR101441851B1 (ko) | 적층체 및 그 용도 | |
| JP6500399B2 (ja) | 硬化性樹脂組成物、硬化物、光学部材、レンズ及びカメラモジュール | |
| JP6439277B2 (ja) | 硬化性樹脂組成物、その硬化物、光学部材及びコーティング物 | |
| JP5239169B2 (ja) | 光学部材 | |
| JP6848213B2 (ja) | 光学部材用硬化性樹脂組成物、光学部材用樹脂、光学部材、レンズ及びカメラモジュール | |
| JP4743493B2 (ja) | 液晶ディスプレイ向け衝撃吸収用樹脂組成物及びそれを用いた液晶ディスプレイ用衝撃吸収材並びにこれらを用いた液晶ディスプレイ用光学フィルタ及び液晶ディスプレイ | |
| JP2013076097A (ja) | 硬化性樹脂組成物及び光学部材 | |
| JP6915417B2 (ja) | 光学成型材用硬化性樹脂組成物、及びその硬化物、並びに光学成型材、レンズ、カメラモジュール | |
| JP4803331B2 (ja) | (メタ)アクリレート樹脂、その製造方法、硬化性樹脂組成物、その硬化物、及びプラスチックレンズ | |
| JP6020895B2 (ja) | 硬化性樹脂組成物、硬化物及び光学部材 | |
| JP6631092B2 (ja) | 透明光学部材用硬化性樹脂組成物、硬化物、透明光学部材、レンズ及びカメラモジュール | |
| CN107001548B (zh) | 固化性组合物及膜 | |
| JP2018090801A (ja) | 粘着剤用樹脂組成物及び粘着シート | |
| JP6597060B2 (ja) | 硬化性樹脂組成物、硬化物、光学部材、レンズ及びカメラモジュール | |
| JP2014205785A (ja) | 硬化性樹脂組成物、硬化物及び光学部材 | |
| JP7115015B2 (ja) | 硬化性樹脂組成物、及びその硬化物、並びに光学成型材、レンズ、カメラモジュール | |
| JP6582413B2 (ja) | 硬化性樹脂組成物、硬化物、光学部材及び光学デバイス | |
| JP6911422B2 (ja) | メタクリル酸エステル及びその製造方法、並びにその(共)重合体 | |
| JP2020158591A (ja) | 硬化性樹脂組成物、硬化物および光学部材 | |
| JP7091683B2 (ja) | オルガノポリシロキサン | |
| JP2015172117A (ja) | ブロックポリマー及び硬化性樹脂組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20200210 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20201111 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201124 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210119 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20210224 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210511 |
|
| C60 | Trial request (containing other claim documents, opposition documents) |
Free format text: JAPANESE INTERMEDIATE CODE: C60 Effective date: 20210511 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20210518 |
|
| C21 | Notice of transfer of a case for reconsideration by examiners before appeal proceedings |
Free format text: JAPANESE INTERMEDIATE CODE: C21 Effective date: 20210525 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210615 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210628 |
|
| R151 | Written notification of patent or utility model registration |
Ref document number: 6915417 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R151 |