JP6869947B2 - 置換キナゾリン化合物ならびにそのg12c変異kras、hrasおよび/またはnrasタンパク質の阻害剤としての使用 - Google Patents
置換キナゾリン化合物ならびにそのg12c変異kras、hrasおよび/またはnrasタンパク質の阻害剤としての使用 Download PDFInfo
- Publication number
- JP6869947B2 JP6869947B2 JP2018502355A JP2018502355A JP6869947B2 JP 6869947 B2 JP6869947 B2 JP 6869947B2 JP 2018502355 A JP2018502355 A JP 2018502355A JP 2018502355 A JP2018502355 A JP 2018502355A JP 6869947 B2 JP6869947 B2 JP 6869947B2
- Authority
- JP
- Japan
- Prior art keywords
- alkyl
- compound according
- aminyl
- compound
- cancer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
- 0 C*c1c(cc(*)c(I)c2*)c2nc(*)c1C Chemical compound C*c1c(cc(*)c(I)c2*)c2nc(*)c1C 0.000 description 9
- ISVGXBXADBBDME-UHFFFAOYSA-N CC[N](C)(C)CC Chemical compound CC[N](C)(C)CC ISVGXBXADBBDME-UHFFFAOYSA-N 0.000 description 1
- LITDFTWBOGEZHM-UHFFFAOYSA-N Cc(c([nH]nc1)c1cc1)c1[FH+] Chemical compound Cc(c([nH]nc1)c1cc1)c1[FH+] LITDFTWBOGEZHM-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D215/00—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems
- C07D215/02—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom
- C07D215/16—Heterocyclic compounds containing quinoline or hydrogenated quinoline ring systems having no bond between the ring nitrogen atom and a non-ring member or having only hydrogen atoms or carbon atoms directly attached to the ring nitrogen atom with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D215/38—Nitrogen atoms
- C07D215/42—Nitrogen atoms attached in position 4
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/70—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings condensed with carbocyclic rings or ring systems
- C07D239/72—Quinazolines; Hydrogenated quinazolines
- C07D239/86—Quinazolines; Hydrogenated quinazolines with hetero atoms directly attached in position 4
- C07D239/88—Oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing three or more hetero rings
Landscapes
- Organic Chemistry (AREA)
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Oncology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Quinoline Compounds (AREA)
Description
技術分野
本発明は、一般に、例えば、がんの処置のための新規の化合物ならびに治療薬または予防薬としてのその調製方法および使用方法に関する。
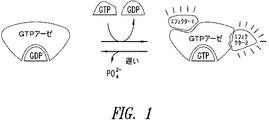
RASは、原形質膜と会合し、GDPまたはGTPのいずれかと結合する、189個のアミノ酸(分子質量21kDa)の密接に関連した単量体球状タンパク質群を表す。RASは分子スイッチとして作用する。RASが結合したGDPを有する場合は、休止状態またはオフ側にあり、「不活性」である。一定の成長促進刺激に対する細胞の曝露に応答して、RASは、結合したGDPをGTPと交換するように誘導される。GTP結合により、RASは「スイッチオン」し、他のタンパク質(その「下流標的」)と相互作用し、活性化することができる。RASタンパク質自体はGTPを加水分解してGDPに戻し、それによってRAS自体をオフ状態にする内因性の能力は非常に低い。RASのスイッチオフには、RASと相互作用してGTPのGDPへの変換を非常に促進するGTPアーゼ活性化タンパク質(GAP)と呼ばれる外因性タンパク質が必要である。GAPと相互作用するかGTPを変換してGDPに戻す能力に影響をおよぼすRASの任意の変異により、そのタンパク質の活性化が延長され、その結果細胞に成長および分裂を継続するように指示するシグナルが延長される。これらのシグナルによって細胞が成長および分裂するので、過度に活動的なRASシグナル伝達は、最終的にがんを引き起こし得る。
簡潔に述べれば、本発明は、G12C変異体KRAS、HRAS、および/またはNRASタンパク質を調整することができる化合物(その立体異性体、薬学的に許容され得る塩、互変異性体、およびプロドラッグが含まれる)を提供する。いくつかの例では、本化合物は、KRAS、HRAS、またはNRAS G12C変異体タンパク質の12位でシステイン残基と共有結合を形成することができる求電子剤として作用する。がんなどの種々の疾患または状態の処置のためのかかる化合物の使用方法も提供する。
被験体がKRAS、HRAS、またはNRASのG12C変異を有するかどうかを決定する工程;および
被験体がKRAS、HRAS、またはNRASのG12C変異を有すると決定された場合、被験体に治療有効量の1つまたはそれよりも多くの構造(I)の化合物を含む薬学的組成物を投与する工程を含む、方法に関する。
以下の説明では、本発明の種々の実施形態の完全な理解を得るために特定の具体的な細目が示される。しかし、当業者は、本発明をこれらの細目を用いることなく実施することができると理解するであろう。
1つの態様では、本発明は、G12C変異体KRAS、HRAS、またはNRASタンパク質に選択的に結合し、そして/またはこれらを調整することができる化合物を提供する。化合物は、アミノ酸との反応によってG12C変異体KRAS、HRAS、またはNRASタンパク質を調整することができる。理論に拘束されることを望まないが、本出願者らは、いくつかの実施形態では、G12C変異体KRAS、HRAS、またはNRASタンパク質の12位のシステインとの共有結合の形成によって本発明の化合物がG12C変異体KRAS、HRAS、またはNRASタンパク質と選択的に反応すると考える。シスチン12への結合により、本発明の化合物は、G12C変異体KRAS、HRAS、またはNRASのスイッチIIを不活性段階に閉じ込めることができる。この不活性段階は、GTPおよびGDPに結合したKRAS、HRAS、またはNRASで認められるものと異なり得る。いくつかの本発明の化合物はまた、スイッチIの高次構造を乱すことができる。いくつかの本発明の化合物は、GTPよりもむしろGDPに結合したKRAS、HRAS、またはNRASへの結合を優先し、したがって、KRAS、HRAS、またはNRASを不活性なKRAS、HRAS、またはNRASのGDP結合状態に隔離し得る。KRAS、HRAS、またはNRASへのエフェクター結合がスイッチIおよびIIの高次構造に高度に影響を受けやすいので、これらの化合物の不可逆的結合がKRAS、HRAS、またはNRASの下流シグナル伝達を破壊し得る。
Aは、NまたはCであり;
Bは、オキソ、シアノ、アルキル、アルケニル、アルキニル、シクロアルキル、ヘテロシクリル、ヘテロアリール、シクロアルキルアルキル、ヘテロシクロアルキル、ヘテロアリールアルキル、アミノ、アルキルアミノ、アリールアミノ、−CO2H、−CONH2、アミニルカルボニル、アミニルカルボニルアルキル、ヘテロアリールアミノ、ハロ、ハロアルキル、アルコキシ、ハロアルコキシ、アリール、または−X−L2−Raであり;
Xは、−NRb−または−O−であり;
L1は、アルキレン、シクロアルキレン、ヘテロシクリレンであるか、または存在せず;
L2は、アルキレンであるか、または存在せず;
Rは、H、シアノ、アミノ、ハロ、ハロアルキル、ヒドロキシル、シクロアルキル、ヘテロシクリル、ヘテロシクロアルキル、アリール、ヘテロアリール、−CO2H、−CONH2、アミニルカルボニル、C1〜C6アルキル、C1〜C6アルキルアミニル、またはC1〜C6アルコキシであり;
Raは、シクロアルキル、ヘテロシクリル、ヘテロアリール、−(C=O)OH、−(C=O)NH2、または−(C=O)NHOHであり;
Rbは、各出現において独立して、HまたはC1〜C6アルキルであり;
R1は、アリールまたはヘテロアリールであり;
R2a、R2bおよびR2cは、それぞれ独立して、H、アミノ、シアノ、ハロ、ヒドロキシル、C1〜C6アルキル、C1〜C6アルキルアミニル、−NRb(C=O)Rb、C1〜C6ハロアルキル、C1〜C6アルコキシ、C3〜C8シクロアルキル、ヘテロシクリルアルキル、C2〜C6アルキニル、C2〜C6アルケニル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、アミニルカルボニル、ヘテロアリール、またはアリールであり;
Eは、KRAS、HRAS、またはNRAS G12C変異体タンパク質の12位のシステイン残基と共有結合を形成することができる求電子部分である)
またはその薬学的に許容され得る塩、立体異性体、もしくはプロドラッグを有する。
Aは、NまたはCであり;
Bは、オキソ、アルキル、シクロアルキル、ヘテロシクリル、ヘテロアリール、シクロアルキルアルキル、ヘテロシクロアルキル、ヘテロアリールアルキル、アミノ、アルキルアミノ、アリールアミノ、−CO2H、−CONH2、アミニルカルボニル、アミニルカルボニルアルキル、ヘテロアリールアミノ、ハロ、ハロアルキル、アルコキシ、ハロアルコキシ、アリール、または−X−L2−Raであり;
Xは、−NRb−または−O−であり;
L1は、アルキレン、シクロアルキレン、ヘテロシクリレンであるか、または存在せず;
L2は、アルキレンであるか、または存在せず;
Rは、H、シアノ、アミノ、ハロ、ハロアルキル、ヒドロキシル、シクロアルキル、ヘテロシクリル、ヘテロシクロアルキル、アリール、ヘテロアリール、−CO2H、−CONH2、アミニルカルボニル、C1〜C6アルキル、C1〜C6アルキルアミニル、またはC1〜C6アルコキシであり;
Raは、シクロアルキル、ヘテロシクリル、ヘテロアリール、−(C=O)OH、−(C=O)NH2、または−(C=O)NHOHであり;
Rbは、各出現において独立して、HまたはC1〜C6アルキルであり;
R1は、アリールまたはヘテロアリールであり;
R2a、R2b、およびR2cは、それぞれ独立して、H、アミノ、ハロ、ヒドロキシル、C1〜C6アルキル、C1〜C6アルキルアミニル、−NRb(C=O)Rb、C1〜C6ハロアルキル、C1〜C6アルコキシ、C3〜C8シクロアルキル、ヘテロシクリルアルキル、C2〜C6アルキニル、C2〜C6アルケニル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、アミニルカルボニル、ヘテロアリール、またはアリールであり;
Eは、KRAS、HRAS、またはNRAS G12C変異体タンパク質の12位のシステイン残基と共有結合を形成することができる求電子部分である。
Aは、NまたはCであり;
Bは、オキソ、アルキル、シクロアルキル、ヘテロシクリル、ヘテロアリール、シクロアルキルアルキル、ヘテロシクロアルキル、ヘテロアリールアルキル、または−X−L2−Raであり;
Xは、−NRb−または−O−であり;
L1は、アルキレン、シクロアルキレン、ヘテロシクリレンであるか、または存在せず;
L2は、アルキレンであるか、または存在せず;
Rは、H、シアノ、アミノ、C1〜C6アルキル、C1〜C6アルキルアミニル、またはC1〜C6アルコキシであり;
Raは、シクロアルキル、ヘテロシクリル、ヘテロアリール、−(C=O)OH、−(C=O)NH2、または−(C=O)NHOHであり;
Rbは、HまたはC1〜C6アルキルであり;
R1は、アリールまたはヘテロアリールであり;
R2a、R2b、およびR2cは、それぞれ独立して、H、アミノ、ハロ、ヒドロキシル、C1〜C6アルキル、C1〜C6アルキルアミニル、−NRb(C=O)Rb、C1〜C6ハロアルキル、C1〜C6アルコキシ、C3〜C8シクロアルキル、ヘテロアリール、またはアリールであり;
Eは、KRAS、HRAS、またはNRAS G12C変異体タンパク質の12位のシステイン残基と共有結合を形成することができる求電子部分である。
G1は、NまたはCHであり;
G2は、NRcまたはCHRcであり;
Rcは、H、アルキル、アルキルカルボニル、アミノカルボニル、アルキルカルボニルアミニル、アミノカルボニルアミニル、またはヘテロアリールカルボニルであり;
R3aおよびR3bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR3aとR3bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR3aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R3bは、R4bと一緒になって、炭素環式環または複素環式環を形成し;
R4aおよびR4bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR4aとR4bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR4aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R4bは、R3bと一緒になって、炭素環式環または複素環式環を形成し;
m1およびm2は、それぞれ独立して、1、2、または3であり;
nは、0〜5の整数である)
を有する。
R3aおよびR3bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル(hydroxylalkly)、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR3aとR3bとが一緒になって、炭素環式環または複素環式環を形成するか;あるいはR3aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R3bは、R4bと一緒になって、炭素環式環または複素環式環を形成し;
R4aおよびR4bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR4aとR4bとが一緒になって、炭素環式環または複素環式環を形成するか;あるいはR4aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R4bは、R3bと一緒になって、炭素環式環または複素環式環を形成する。
Hは、R3a、R3b、R4a、およびR4bの1つまたはそれよりも多くで任意選択的に置換される5または6員のヘテロアリール環を示し;
G1は、NまたはCHであり;
G2は、NRcまたはCHRcであり;
Rcは、H、アルキル、アルキルカルボニル、アミノカルボニル、アルキルカルボニルアミニル、アミノカルボニルアミニル、またはヘテロアリールカルボニルであり;
R3aおよびR3bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR3aとR3bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR3aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R3bは、R4bと一緒になって、炭素環式環または複素環式環を形成し;
R4aおよびR4bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR4aとR4bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR4aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R4bは、R3bと一緒になって、炭素環式環または複素環式環を形成し;
m1およびm2は、それぞれ独立して、1、2、または3であり;
nは、0〜5の整数である)
のうちの1つを有する。
R3aおよびR3bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR3aとR3bとが一緒になって、炭素環式環または複素環式環を形成するか;あるいはR3aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R3bは、R4bと一緒になって、炭素環式環または複素環式環を形成し;
R4aおよびR4bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR4aとR4bとが一緒になって、炭素環式環または複素環式環を形成するか;あるいはR4aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R4bは、R3bと一緒になって、炭素環式環または複素環式環を形成する。
G1は、CHであり;
G2は、NまたはCHであり;
R3aおよびR3bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR3aとR3bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR3aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R3bは、R4bと一緒になって、炭素環式環または複素環式環を形成し;
R4aおよびR4bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR4aとR4bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR4aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R4bは、R3bと一緒になって、炭素環式環または複素環式環を形成し;
m1およびm2は、それぞれ独立して、1、2、または3である)
を有する。
R3aおよびR3bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR3aとR3bとが一緒になって、炭素環式環または複素環式環を形成するか;あるいはR3aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R3bは、R4bと一緒になって、炭素環式環または複素環式環を形成し;
R4aおよびR4bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR4aとR4bとが一緒になって、炭素環式環または複素環式環を形成するか;あるいはR4aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R4bは、R3bと一緒になって、炭素環式環または複素環式環を形成する。
Qは、−C(=O)−、−C(=NR8’)−、−NR8C(=O)−、−S(=O)2−、または−NR8S(=O)2−であり;
R8は、H、C1〜C6アルキル、またはヒドロキシルアルキルであり;
R8’は、H、−OH、−CN、またはC1〜C6アルキルであり;
R9およびR10は、それぞれ独立して、H、ハロ、シアノ、カルボキシル、C1〜C6アルキル、アルコキシカルボニル、アミニルアルキル、アルキルアミニルアルキル、アリール、ヘテロシクリル、ヘテロシクリルアルキル、ヘテロアリール、またはヒドロキシルアルキルであるか、あるいはR9とR10とが一緒になって、炭素環式環、複素環式環、またはヘテロアリール環を形成する)
を有する。
Qは、−C(=O)−、−NR8C(=O)−、−S(=O)2−、または−NR8S(=O)2−であり;
R8は、H、C1〜C6アルキル、またはヒドロキシルアルキルであり;
R10は、H、C1〜C6アルキル、アミニルアルキル、アルキルアミニルアルキル、またはヒドロキシルアルキルである)
を有する。
R8は、HまたはC1〜C6アルキルであり;
R9は、H、シアノ、またはC1〜C6アルキルであるか、あるいはR9は、R10と一緒になって、炭素環を形成し;
R10は、HまたはC1〜C6アルキルであるか、あるいはR10は、R9と一緒になって、炭素環を形成し、
R10aは、HまたはC1〜C6アルキルである)
のうちの1つを有する。
他の実施形態は、薬学的組成物に関する。薬学的組成物は、前述の化合物のうちのいずれか1つ(または複数)および薬学的に許容され得るキャリアを含む。いくつかの実施形態では、薬学的組成物は経口投与のために製剤化されている。他の実施形態では、薬学的組成物は注射のために製剤化されている。なおさらなる実施形態では、薬学的組成物は、本明細書中に開示の化合物およびさらなる治療薬(例えば、抗がん剤)を含む。かかる治療薬の非限定的な例を、本明細書中の以下に記載する。
本明細書中に記載の治療適用で用いるために、キットおよび製品も提供する。いくつかの実施形態では、かかるキットは、キャリア、パッケージ、または容器を含み、該容器は、バイアルおよびチューブなどの1つまたはそれよりも多くの容器(各容器は本明細書中に記載の方法で使用すべき個別の要素のうちの1つを含む)を入れるために区画化されている。適切な容器には、例えば、ボトル、バイアル、シリンジ、および試験管が含まれる。容器は、ガラスまたはプラスチックなどの種々の材料から形成されている。
本発明の実施形態は、RAS媒介細胞のシグナル伝達を阻害する方法であって、細胞を有効量の1つまたはそれよりも多くの本明細書中に開示の化合物と接触させる工程を含む方法を提供する。RAS媒介シグナル伝達の阻害を、当該分野で公知の広範な種々の方法によって評価および実証することができる。非限定的な例には、以下を示すことが含まれる:(a)RASのGTPアーゼ活性の減少;(b)GTP結合親和性の減少またはGDP結合親和性の増加;(c)GTPのK offの増加またはGDPのK offの減少;(d)RAS経路の下流のシグナル伝達分子レベルの減少(pMEKレベルの減少など);および/または(e)下流シグナル伝達分子(Rafが含まれるが、これらに限定されない)へのRAS複合体の結合の減少。キットおよび市販のアッセイを、1つまたは複数の上記の決定のために利用することができる。
2−アミノ−4−ブロモ−3−フルオロ安息香酸(10g、43mmol)の1,4−ジオキサン(400mL)およびH2O(100mL)中の撹拌溶液に、2−フルオロ−6−メトキシフェニルボロン酸(36g、213mmol)、テトラキス(トリフェニルホスフィン)パラジウム(2.5g、2.15mmol)およびNa2CO3(27g、258mmol)を添加した。この混合物を数回脱気し、N2で充填し直し、100℃で一晩撹拌した。この混合物を水(500mL)と分割し、酢酸エチルで抽出した(200mL×2)。有機層を廃棄し、水相に1M HCl溶液を添加してpHを<3に調整した。水相を酢酸エチルで抽出し(200mL×2)、ブラインで洗浄し、Na2SO4で乾燥させ、濃縮して、所望の生成物(11g、収率92%)を白色固体として得た。ESI−MS m/z:280.1[M+H]+。
RTの3−アミノ−2,2’−ジフルオロ−6’−メトキシ−[1,1’−ビフェニル]−4−カルボン酸(11g、39.6mmol)のN,N−ジメチルホルムアミド(100mL)中の溶液に、N−クロロスクシンイミド(chlorosuccinimde)(5.27g、39.6mmol)を添加した。得られた混合物を100℃で1時間撹拌した。この混合物をRTに冷却し、この反応混合物を水(300mL)にゆっくり添加し、混合物を濾過し、ケークを乾燥させて、所望の生成物(11.5g、収率93.1%)を茶色固体として得た。
3−アミノ−6−クロロ−2,2’−ジフルオロ−6’−メトキシ−[1,1’−ビフェニル]−4−カルボン酸(8.1g、25.8mmol)のEtOH(150mL)中の混合物に、ホルムイミドアミドアセタート(35g、336.4mmol)を添加した。この混合物を100℃で一晩撹拌した。この反応混合物を濃縮し、水を添加した。この混合物を濾過し、ケークを乾燥させて、所望の生成物(7.5g、収率90.3%)を淡黄色固体として得た。
6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)キナゾリン−4(3H)−オン(1.0g、3.1mmol)のMeCN(20mL)中の溶液に、HATU(4.7g、12.4mmol)、DBU(1.9g、12.4mmol)およびtert−ブチル3−アミノピペリジン−1−カルボキシラート(2.3g、12.4mmol)を添加し、得られた混合物をRTで48時間撹拌した。この混合物を酢酸エチルと水とに分割した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(酢酸エチル/石油エーテル=1:5〜1:3)によって精製して、生成物を得た(670mg、収率42.7%)。ESI−MS m/z:506.2[M+H]+。
tert−ブチル3−(6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)−4−オキソキナゾリン−3(4H)−イル)ピペリジン−1−カルボキシラート(230mg、0.57mmol)のジクロロメタン(10mL)中の溶液に、TFA(4mL)を添加し、得られた混合物をRTで1時間撹拌した。この混合物を真空中で濃縮した。残渣を水と酢酸エチルとに分割した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣(230mg)をDCM(10mL)に溶解し、BBr3(1.4g、5.7mmol)を−78℃において添加し、この混合物をRTで3時間撹拌した。この混合物を飽和NaHCO3溶液でクエンチし、酢酸エチルで抽出した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(MeOH/DCM=1:30)によって精製して、生成物を得た(150mg、収率67%)。ESI−MS m/z:392.1[M+H]+。
0℃の6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)−3−(ピペリジン−3−イル)キナゾリン−4(3H)−オン(150mg、0.38mmol)およびトリエチルアミン(0.3mL、1.9mmol)のDCM(10mL)中の溶液に、塩化アクリロイル(70mg、0.77mmol)を添加し、得られた混合物を20分間撹拌した。この混合物を飽和NaHCO3溶液でクエンチし、水とジクロロメタンとに分割した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をTHF(7mL)およびH2O(7mL)に溶解した。水酸化リチウム水和物(70mg、1.67mmol)を添加し、この混合物をRTで40分間撹拌した。混合物のpHを7に調整し、酢酸エチルで抽出した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をPre−TLCプレート(MeOH/DCM=1:20)によって精製して、生成物を得た(42mg、収率22.6%)。ESI−MS m/z: 446.3 [M+H]+. 1H−NMR (400 MHz, DMSO−d6) δ: 10.36 (s, 1H), 8.59 (s, 1H), 8.10 (s, 1H), 7.41−7.35 (m, 1H), 6.90−6.75 (m, 3H), 6.16 (d, J = 16.7 Hz, 1H), 5.73 (dd, J = 2.1, 10.6 Hz, 1H), 4.61−4.48 (m, 2H), 4.19 (dd, J = 12.2, 71.5 Hz, 1H), 3.54−2.65 (m, 1H), 3.20−3.09 (m, 1H), 2.28−2.16 (m, 1H), 2.04−1.88 (m, 2H), 1.59−1.53 (m, 1H).
6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)キナゾリン−4(3H)−オン(0.6g、1.86mmol)のMeCN(30mL)中の溶液に、HATU(1.4g、3.72mmol)、DBU(1.7g、11.16mmol)およびtert−ブチル3−アミノシクロブチルカルバマート(0.415g、2.23mmol)を添加し、得られた混合物をRTで48時間撹拌した。この混合物を酢酸エチルと水とに分割した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(酢酸エチル/石油エーテル=1:3)によって精製して、生成物を得た(200mg、収率22%)。ESI−MS m/z:491.1[M+H]+。
tert−ブチル3−(6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)−4−オキソキナゾリン−3(4H)−イル)シクロブチルカルバマート(200mg、0.40mmol)のDCM(5mL)中の溶液に、TFA(2mL)を添加し、得られた混合物をRTで1時間撹拌した。この混合物を真空中で濃縮した。残渣をDCM(3mL)に溶解し、BBr3(1mL、10.79mmol)を−78℃において添加し、この混合物をRTで2時間撹拌した。この混合物を−78℃にてMeOHおよび飽和NaHCO3溶液でクエンチし、次いで、混合溶媒(DCM:MeOH=10:1)で抽出した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をDCM(2mL)に溶解し、Et3N(162mg、1.6mmol)および塩化アクリロイル(55mg、0.6mmol)を0℃において添加し、得られた混合物を20分間撹拌した。この混合物を飽和NaHCO3溶液でクエンチし、水とDCMとに分割した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をTHF(3mL)およびH2O(2mL)に溶解した。水酸化リチウム水和物(42mg、1.2mmol)を添加し、この混合物をRTで40分間撹拌した。混合物のpHを6に調整し、酢酸エチルで抽出した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をPre−TLCプレート(MeOH/ジクロロメタン=1:20)によって精製して、生成物を得た(4工程で31mg、収率18%)。ESI−MS m/z: 431.1 [M+H]+. 1H NMR (400 MHz, DMSO−d6) δ:10.35 (s, 1H), 8.75 (d, J = 6.7 Hz, 1H), 8.61 (s, 1H), 8.07 (d, J = 1.4 Hz, 1H), 7.40−7.34 (m, 1H), 6.87−6.79 (m, 2H), 6.30−6.23 (m, 1H), 6.15−6.10 (m, 1H), 5.63 (dd, J = 2.1, 9.9Hz, 1H), 5.30−5.22 (m, 1H), 4.39−4.33 (m, 1H), 2.91−2.84 (m, 2H), 2.48−2.44 (m, 2H).
RTの1−ブロモ−2−フルオロ−3−ニトロベンゼン(13.75g、62.76mmol)のHOAc(26.36g、439mmol)、EtOH(150mL)およびH2O(60mL)中の混合物に、鉄粉(9.14g、163mmol)を小分けにして添加した。得られた混合物をRTで16時間撹拌し、次いで、NaOH(5N)溶液で中和した。この混合物を酢酸エチルで抽出した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(石油エーテル/酢酸エチル=10:1)によって精製して、所望の生成物(7.77g、収率65%)を茶色オイルとして得た。
RTの3−ブロモ−2−フルオロベンゼンアミン(1.9g、10mmol)のDMF(10mL)中の溶液に、NCS(1.4g、10.5mmol)を添加し、得られた混合物をRTで16時間撹拌した。この混合物を氷水に注ぎ、酢酸エチルで抽出した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルでのカラムクロマトグラフィ(石油エーテル/酢酸エチル=30:1)によって精製して、所望の生成物を得た(1.15g、収率51%)。ESI−MSm/z:225.9[M+H]+。
3−ブロモ−4−クロロ−2−フルオロベンゼンアミン(2.3g、10.2mmol)およびジエチル2−(エトキシメチレン)マロナート(2.42g、11.22mmol)の混合物を120℃で3時間撹拌した。この混合物をRTに冷却した。石油を添加し、RTで1時間撹拌した。沈殿物を濾過し、乾燥させて、所望の生成物を得た(2.76g、収率68.7%)。ESI−MS m/z:395.9[M+H]+。
ジエチル2−((3−ブロモ−4−クロロ−2−フルオロフェニルアミノ)メチレン)マロナート(2.76g、6.99mmol)をPh2O(20mL)に懸濁した。この混合物を250℃で2時間撹拌した。この混合物をRTに冷却し、次いで、100mLの石油エーテルを添加した。白色固体を濾過によって回収し、石油エーテル(100mL)でリンスして、所望の生成物を得た(1.85g、収率76%)。ESI−MS m/z:349.9[M+H]+。
エチル7−ブロモ−6−クロロ−8−フルオロ−4−ヒドロキシキノリン−3−カルボキシラート(1.85g、5.31mmol)およびPOCl3(10mL)の混合物を4時間還流しながら撹拌した。この混合物をRTに冷却し、真空中で濃縮して、粗生成物(1.41g)を得て、これを次の工程で直接使用した。
エチル7−ブロモ−4,6−ジクロロ−8−フルオロキノリン−3−カルボキシラート(1.41g、3.84mmol)、tert−ブチルピペラジン−1−カルボキシラート(1.43g、7.68mmol)、Et3N(1.55g、15.36mmol)のDMSO(20mL)中の混合物をアルゴン下、80℃で2時間撹拌した。この混合物をRTに冷却し、氷水に注ぎ、酢酸エチルで抽出した。合わせた有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルでのカラムクロマトグラフィ(石油エーテル/酢酸エチル=3:1)によって精製して、所望の生成物を得た(1.96g、収率98%)。ESI−MS m/z:518.1[M+H]+。
エチル4−(4−(tert−ブトキシカルボニル)ピペラジン−1−イル)−7−ブロモ−6−クロロ−8−フルオロキノリン−3−カルボキシラート(1.13g、2.19mmol)および(2−フルオロ−6−メトキシフェニル)ボロン酸(1.86g、10.93mmol)のNa2CO3水溶液(3.64mL、1.5M)およびジオキサン(80mL)中の混合物に、Pd(PPh)4をAr下で添加した。この混合物を90℃で16時間撹拌した。溶媒を除去し、残渣をシリカゲルでのカラムクロマトグラフィ(石油エーテル/酢酸エチル=6:1)によって精製して、所望の生成物を得た(851mg、収率69%)。ESI−MS m/z:562.2[M+H]+。
RTのエチル4−(4−(tert−ブトキシカルボニル)ピペラジン−1−イル)−6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)キノリン−3−カルボキシラート(851mg、1.52mmol)のDCM(20mL)中の混合物に、TFA(4mL)を添加し、得られた混合物を2時間撹拌した。この混合物を2M NaOH(40mL)および酢酸エチル(40mL)の撹拌混合物に添加した。次いで、この反応物に塩化アセチル(4mL)をゆっくり添加した。この混合物を酢酸エチルで抽出した。残渣をシリカゲルでのカラムクロマトグラフィ(石油エーテル/酢酸エチル=1:1)によって精製して、所望の生成物を得た(575mg、収率75%)。ESI−MS m/z:504.3[M+H]+。
エチル4−(4−アセチルピペラジン−1−イル)−6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)キノリン−3−カルボキシラート(267mg、053mmol)のTHF(20mL)および水(20mL)中の混合物に、水酸化リチウム(111mg、2.651mmol)を添加し、得られた混合物をRTで16時間撹拌した。この混合物を2M NaOH(30mL)で希釈し、50%酢酸エチル/石油エーテルで抽出した。水層を1M HClによって酸性化し、酢酸エチルで抽出した。溶媒を除去して、生成物を得た(277mg、粗)。ESI−MS m/z:476.2[M+H]+。
4−(4−アセチルピペラジン−1−イル)−6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)キノリン−3−カルボン酸(277mg、0.58mmol)およびEt3N(235mg、2.33mmol)のDMF(20mL)およびt−BuOH(3mL)中の混合物に、DPPA(401mg、1.456mmol)を添加し、得られた混合物を120℃で2.5時間撹拌した。この混合物をRTに冷却し、水(50mL)でクエンチした。この混合物を酢酸エチルで抽出し、真空中で濃縮した。残渣をDCM(10mL)およびTFA(3mL)の混合物に溶解し、次いで、1時間撹拌した。この混合物を2M NaOH(30mL)に添加し、酢酸エチルで抽出した。合わせた有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルでのカラムクロマトグラフィ(DCM/MeOH=30:1)によって精製して、所望の生成物を得た(120mg、収率46%)。ESI−MS m/z:447.2[M+H]+。
−78℃の1−(4−(3−アミノ−6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)キノリン−4−イル)ピペラジン−1−イル)エタノン(120mg、0.27mmol)のDCM(10mL)中の混合物に、BBr3(674mg、2.69mmol)を添加し、得られた混合物をRTで2時間撹拌した。この混合物を氷水に注ぎ、酢酸エチルとNaHCO3溶液とに分割した。有機層をNa2SO4で乾燥させ、真空中で濃縮して、所望の生成物を得た(194mg、粗)。ESI−MS m/z:433.2[M+H]+。
1−(4−(3−アミノ−6−クロロ−8−フルオロ−7−(2−フルオロ−6−ヒドロキシフェニル)キノリン−4−イル)ピペラジン−1−イル)エタノン(194mg、0.45mmol)およびEt3N(181mg、1.80mmol)のDCM(20mL)およびTHF(20mL)中の混合物に、塩化アクリロイル(162mg、1.796mmol)を添加し、得られた混合物を0℃で30分間撹拌した。この混合物をDCMとNaHCO3溶液とに分割した。有機層をNa2SO4で乾燥させ、真空中で濃縮した。残渣をTHF(10mL)および水(10mL)に溶解し、水酸化リチウム(75mg、1.794mmol)を添加した。この混合物をRTで1時間撹拌した。この混合物を1N HClおよびNaHCO3溶液でpH8に調整し、次いで、酢酸エチルで抽出した。有機層をNa2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルのフラッシュクロマトグラフィ(DCM/MeOH=30:1)によって精製して、所望の生成物を得た(2工程で32mg、収率24%)。ESI−MS m/z: 487.3 [M+H]+. 1H−NMR (400 MHz, DMSO−d6) δ: 10.26 (s, 1H), 10.06 (s, 1H), 8.70 (s, 1H), 8.04 (s, 1H), 7.39 (t, J1 = 7.6 Hz, J2 = 15.2 Hz, 1H), 6.88 (m, 2H), 6.61 (m, 1H), 6.36 (m, 1H), 5.88 (m, 1H), 3.69 (m, 4H), 3.29 (m, 4H), 2.07 (s, 3H).
6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)キナゾリン−4(3H)−オン(1g、3.1mmol)のMeCN(20mL)中の溶液に、HATU(3.53g、9.32mmol)、DBU(4.73g、31.06mmol)およびtert−ブチル3−アミノアゼチジン−1−カルボキシラート(2.14g、12.42mmol)を添加し、得られた混合物をRTで16時間撹拌した。この混合物を酢酸エチルと水とに分割した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(酢酸エチル/石油エーテル=1:10〜1:2)によって精製して、生成物を得た(500mg、収率34%)。ESI−MS m/z:478.2[M+H]+。
tert−ブチル3−(6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)−4−オキソキナゾリン−3(4H)−イル)アゼチジン−1−カルボキシラート(400mg、0.84mmol)のDCM(10mL)中の溶液に、TFA(4mL)を添加し、得られた混合物をRTで1時間撹拌した。この混合物を真空中で濃縮した。残渣を水と酢酸エチルとに分割した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣(220mg)をDCM(20mL)に溶解し、BBr3(0.2mL、2.16mmol)を−78℃において添加し、得られた混合物をRTで1.5時間撹拌した。この混合物を飽和NaHCO3溶液でクエンチし、酢酸エチルで抽出した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をシリカゲルのPre−TLCプレート(MeOH/DCM=1:10)によって精製して、生成物を得た(2工程で42mg、収率39%)。ESI−MS m/z:364.1[M+H]+。
−78℃の3−(アゼチジン−3−イル)−6−クロロ−8−フルオロ−7−(2−フルオロ−6−メトキシフェニル)キナゾリン−4(3H)−オン(130mg、0.36mmol)およびトリエチルアミン(217mg、2.15mmol)のDCM(10mL)中の溶液に、塩化アクリロイル(65mg、0.72mmol)を添加し、この混合物を−60℃で20分間撹拌した。この混合物を飽和NaHCO3溶液でクエンチし、水とDCMとに分割した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をTHF(7mL)およびH2O(7mL)に溶解した。水酸化リチウム水和物(360mg、8.6mmol)を添加し、得られた混合物をRTで40分間撹拌した。混合物のpHを6に調整し、次いで、酢酸エチルで抽出した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をPre−TLCプレート(MeOH/DCM=1:15)によって精製して、生成物を得た(42mg、収率29%)。ESI−MS m/z: 418.1 [M+H]+. 1HNMR (400MHz, DMSO−d6) δ:10.36 (s, 1H), 8.53 (s, 1H), 8.09 (s, 1H),7.40−7.34 (m ,1H), 6.87−6.80 (m ,2H), 6.40−6.33 (m, 1H), 6.18−6.13 (m,1H), 5.76−5.71(m, 1H), 5.34−5.30 (m, 1H), 4.68−4.64 (m, 2H), 4.47−4.44 (m,1H), 4.43−4.31(m,1H).
1−ブロモ−2−フルオロ−3−ニトロベンゼン(20.0g、91.37mmol)およびNH3のCH3OH溶液(7M、60mL)の混合物を密封チューブ内にて100℃で16時間撹拌した。溶媒を除去し、残渣をH2Oに溶解し、酢酸エチルで抽出した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣を、(酢酸エチル/石油エーテル=1:100)で溶出するカラムクロマトグラフィによって精製して、所望の生成物を黄色固体として得た(16.0g、収率81.2%)。
2−ブロモ−6−ニトロアニリン(16.0g、74.10mmol)、亜硝酸tert−ブチル(11.40g 111.15mmol)およびCuCl2(12.0g、88.90mmol)のCH3CN(160mL)中の混合物をアルゴン下、60℃で1時間撹拌した。この混合物をRTに冷却し、H2Oでクエンチし、酢酸エチルで抽出した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカのカラムクロマトグラフィ(酢酸エチル/石油エーテル=1:100)によって精製して、生成物を得た(15.0g、収率86.2%)。
RTの1−ブロモ−2−クロロ−3−ニトロベンゼン(15.0g、63.60mmol)、HOAc(20mL)、EtOH(120mL)およびH2O(40mL)の混合物に、鉄粉(10.7g、190.70mmol)を小分けにして添加した。得られた混合物をRTで16時間撹拌し、次いで、NaOH(5N)溶液で中和した。この混合物を酢酸エチルで抽出した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(石油エーテル/酢酸エチル=10:1)によって精製して、所望の生成物を得た(14.0g、収率100%)。
2,2,2−トリクロロエタン−1,1−ジオール(13.5g、82.00mmol)およびNa2SO4(87.3g、614.70mmol)の水中の混合物を35℃に加温した。3−ブロモ−2−クロロベンゼンアミン(14.0g、68.30mmol)の水溶液を添加した後、35%HCl水溶液(30mL)および塩酸ヒドロキシルアミン(14.2g、204.90mmol)を添加した。得られた混合物を90℃で16時間撹拌したところ、黄色沈殿物が形成した。この混合物をRTに冷却した。固体を濾過し、水で洗浄し、風乾して、所望の生成物を得た(14.5g、収率76.3%)。
60℃の濃硫酸(120mL)に、(E)−N−(3−ブロモ−2−クロロフェニル)−2−(ヒドロキシイミノ)アセトアミド(14.5g、52.25mmol)を添加した。温度を90℃に上げ、3時間維持した。この反応混合物をRTに冷却し、氷に注いで、黄色沈殿物を得た。この沈殿物を濾過によって回収し、乾燥させて、所望の生成物を得た(7.4g、収率54.4%)。
0℃の6−ブロモ−7−クロロインドリン−2,3−ジオン(7.4g、28.57mmol)の2N NaOH(200mL)中の溶液に、H2O2(30%、20mL)を添加し、得られた混合物を0℃で30分間撹拌し、次いで、RTで16時間撹拌した。この混合物を氷水に注ぎ、この溶液を濃HClで酸性化した。沈殿物を濾過によって回収し、風乾して、所望の生成物を得た(2.5g、収率35.2%)。
RTの2−アミノ−4−ブロモ−3−クロロ安息香酸(2.5g、10.00mmol)の2−メトキシエタノール(50mL)中の溶液に、酢酸ホルムアミジン(6.2g、60.00mmol)を添加し、得られた混合物を16時間還流しながら撹拌した。この混合物を真空中で濃縮した。残渣を水と酢酸エチルとに分割した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルでのカラムクロマトグラフィ(DCM/メタノール=100:1〜50:1)によって精製して、所望の生成物を得た(1.8g、収率69.2%)。ESI−MSm/z:258.8[M+H]+。
RTの7−ブロモ−8−クロロキナゾリン−4(3H)−オン(1.8g、6.95mmol)のH2SO4(20mL)中の溶液に、KNO3(1.1g、10.42mmol)を添加し、この混合物を100℃で16時間撹拌した。この混合物を氷水に注いだ。沈殿物を濾過によって回収し、水で洗浄し、乾燥させて、所望の生成物を得た(1.5g、収率71.4%)。ESI−MS m/z:303.9[M+H]+。
7−ブロモ−8−クロロ−6−ニトロキナゾリン−4(3H)−オン(1.5g、4.93mmol)のMeCN(20mL)中の溶液に、HATU(3.75g、9.86mmol)、DBU(4.5g、29.58mmol)およびtert−ブチル3−アミノアゼチジン−1−カルボキシラート(1.3g、7.40mmol)を添加し、得られた混合物をRTで2時間撹拌した。この混合物を酢酸エチルと水とに分割した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(酢酸エチル/石油エーテル=1:5〜1:3)によって精製して、生成物を得た(1.0g、収率43.5%)。ESI−MS m/z:459.0[M+H]+。
RTのtert−ブチル3−(7−ブロモ−8−クロロ−6−ニトロ−4−オキソキナゾリン−3(4H)−イル)アゼチジン−1−カルボキシラート(300mg、0.66mmol)、HOAc(2mL)、EtOH(12mL)およびH2O(4mL)の混合物に、鉄粉(183.4mg、3.28mmol)を小分けにして添加し、得られた混合物をRTで16時間撹拌した。この混合物をNaOH(2N)溶液で中和し、次いで、酢酸エチルで抽出した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(石油エーテル/酢酸エチル=10:1)によって精製して、所望の生成物を得た(283mg、収率100%)。
tert−ブチル3−(6−アミノ−7−ブロモ−8−クロロ−4−オキソキナゾリン−3(4H)−イル)アゼチジン−1−カルボキシラート(283mg、0.66mmol)、3−ヒドロキシナフタレン−1−イル−1−ボロン酸(142.1mg、0.66mmol)、Pd(PPh3)4(76.2mg、0.1mmol)およびNa2CO3(209.9mg、1.98mmol)の1,4−ジオキサン/H2O(16mL/4mL)中の混合物をアルゴン下、100℃で16時間撹拌した。この混合物をRTに冷却し、真空中で濃縮した。残渣をシリカゲルでのカラムクロマトグラフィによって精製して、所望の生成物を白色固体として得た(150mg、収率46.2%)。
tert−ブチル3−(6−アミノ−8−クロロ−7−(2−ヒドロキシナフタレン−4−イル)−4−オキソキナゾリン−3(4H)−イル)アゼチジン−1−カルボキシラート(150mg、0.30mmol)のDCM(16mL)中の溶液に、TFA(4mL)を添加し、得られた混合物をRTで1時間撹拌した。この混合物を真空中で濃縮した。残渣を水と酢酸エチルとに分割した。有機層を無水Na2SO4で乾燥させ、濾過し、真空中で濃縮して、所望の生成物を得た(80mg)。
0℃の6−アミノ−3−(アゼチジン−3−イル)−8−クロロ−7−(2−ヒドロキシナフタレン−4−イル)キナゾリン−4(3H)−オン(80mg、0.20mmol)およびNaOH(5mL、2N)のTHF(20mL)中の混合物に、塩化アクリロイル(18mg、0.20mmol)を添加し、得られた混合物を0℃で30分間撹拌した。この混合物を酢酸エチルとNaHCO3溶液とに分割した。有機層をNa2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルのフラッシュクロマトグラフィ(DCM/MeOH=30:1)によって精製して、所望の生成物を得た(18mg、収率20.2%)。ESI−MS m/z: 447.1 [M+H]+. 1H NMR (400 MHz, DMSO−d6) δ: 8.31 (s, 1H), 8.02(d, J = 8.0 Hz, 1H), 7.78 (d, J = 8.0 Hz, 1H), 7.47−7.43 (m, 1H), 7.35−7.33 (m, 1H), 7.26−7.21 (m, 2H), 7.10 (d, J = 2.8 Hz, 1H), 6.44 (dd, J = 1.6, 17.2 Hz, 1H), 6.24 (dd, J = 10.4, 17.2 Hz, 1H), 5.79 (dd, J = 1.2, 10.4 Hz, 1H), 5.43−5.30 (m, 1H), 4.78−4.56 (m, 4H).
−20℃の4−メトキシ−2−ニトロベンゼンアミン(6.72g、40mmol)のDCM(70mL)中の溶液に、臭素(2.50mL、48mmol)を滴下した。この混合物を−20℃で30分間撹拌した。この混合物を氷水に注いだ。pHを飽和炭酸水素ナトリウム水溶液で8に調整し、次いで、DCMで抽出した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルでのカラムクロマトグラフィ(DCM/石油エーテル=1:2)によって精製して、生成物を得た(6.42g、収率65%)。ESI−MS m/z:247.0[M+H]+。
60℃の亜硝酸t−ブチル(3.75g、36.4mmol)およびCuCl2(3.92g、29.2mmol)のアセトニトリル(120mL)中の溶液に、2−ブロモ−4−メトキシ−6−ニトロベンゼンアミン(6.0g、24.3mmol)を添加し、得られた混合物を60℃で一晩撹拌した。この混合物を真空中で濃縮した。残渣をDCM(100mL)に溶解し、ブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルでのカラムクロマトグラフィ(DCM/石油エーテル=1:3)によって精製して、生成物を得た(5.01g、収率77%)。
RTの1−ブロモ−2−クロロ−5−メトキシ−3−ニトロベンゼン(5.01g、18.8mmol)およびHOAc(6mL)のEtOH(36mL)およびH2O(12mL)中の混合物に、鉄粉(3.14g、56.3mmol)を分割して添加した。得られた混合物をRTで16時間撹拌し、次いで、NaOH(5N)溶液で中和した。この混合物を酢酸エチルで抽出した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(DCM/石油エーテル=1:3)によって精製して、所望の生成物(3.90g、収率88%)を茶色オイルとして得た。ESI−MSm/z:237.9[M+H]+。
0℃の3−ブロモ−2−クロロ−5−メトキシベンゼンアミン(3.9g、16.5mmol)の1,2−ジクロロメタン(50mL)中の溶液に、塩化オキサリル(2.7g、21.4mmol)を添加し、得られた混合物をRTに加温し、RTで4時間撹拌した。この混合物を55℃で30分間撹拌し、0℃に冷却し直した。AlCl3(2.8g、21.4mmol)を小分けにして添加した。この混合物を55℃で一晩撹拌した。この混合物をDCM(50mL)で希釈し、ブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルでのカラムクロマトグラフィ(DCM/石油エーテル=1:3)によって精製して、生成物を得た(3.1g、収率65%)。ESI−MS m/z:291.9[M+H]+。
6−ブロモ−7−クロロ−4−メトキシインドリン−2,3−ジオン(3.1g、10.7mmol)の2N NaOH(80mL)中の溶液に、H2O2(30%、8mL)を0℃において添加し、この混合物を0℃で30分間撹拌した。室温で16時間撹拌した後、この混合物を氷水に注ぎ、この溶液を濃HClで酸性化し、沈殿物を濾過し、風乾して、所望の生成物を白色固体として得た(1.6g、収率53%)。ESI−MSm/z:278.9[M+H]+。
RTの2−アミノ−4−ブロモ−3−クロロ−6−メトキシ安息香酸(1.6g、5.7mmol)のエタノール(25mL)中の溶液に、酢酸ホルムアミジン(3.6g、34.3mmol)を添加し、得られた混合物を16時間還流しながら撹拌した。この混合物を真空中で濃縮し、残渣を水で希釈した。この水溶液を酢酸エチルで抽出した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、真空中で濃縮した。残渣をシリカゲルでのカラムクロマトグラフィ(DCM/メタノール=100:1〜50:1)によって精製して、所望の生成物を得た(700mg、収率42%)。
7−ブロモ−8−クロロ−5−メトキシキナゾリン−4(3H)−オン(630mg、2.18mmol)のMeCN(15mL)中の溶液に、HATU(1.66g、4.36mmol)、DBU(1.99g、13.08mmol)およびtert−ブチル3−アミノアゼチジン−1−カルボキシラート(562mg、3.27mmol)を添加し、得られた混合物を80℃で一晩撹拌した。この混合物を酢酸エチルと水とに分割した。有機層をブラインで洗浄し、Na2SO4で乾燥させ、濾過し、真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(酢酸エチル/石油エーテル=1:1)によって精製して、生成物を得た(360mg、収率37%)。ESI−MSm/z:446.0[M+H]+。
tert−ブチル3−(7−ブロモ−8−クロロ−5−メトキシ−4−オキソキナゾリン−3(4H)−イル)アゼチジン−1−カルボキシラート(300mg、0.67mmol)、3−ヒドロキシナフタレン−1−イル−1−ボロン酸(127mg、0.67mmol)、Pd(PPh3)4(81mg、0.07mmol)およびNa2CO3(142mg、1.34mmol)の1,4−ジオキサン/H2O(8mL/2mL)中の混合物をアルゴン下、100℃で一晩撹拌した。この混合物をRTに冷却し、真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(酢酸エチル/石油エーテル=1:2)によって精製して、生成物を得た(221mg、収率65%)。ESI−MS m/z:508.2[M+H]+。
tert−ブチル3−(8−クロロ−7−(2−ヒドロキシナフタレン−4−イル)−5−メトキシ−4−オキソキナゾリン−3(4H)−イル)アゼチジン−1−カルボキシラート(160mg、0.44mmol)のDCM(6mL)中の溶液に、TFA(2mL)を添加し、得られた混合物をRTで1時間撹拌した。この混合物を真空中で濃縮した。残渣をシリカゲルのフラッシュカラムクロマトグラフィ(DCM/MeOH/NH3H2O=5:1:0.2)によって精製して、生成物を得た(160mg、収率90%)。ESI−MS m/z:408.1[M+H]+。
−78℃の3−(アゼチジン−3−イル)−8−クロロ−7−(2−ヒドロキシナフタレン−4−イル)−5−メトキシキナゾリン−4(3H)−オン(160mg、0.39mmol)のDCM(5mL)中の混合物に、BBr3(490mg、1.96mmol)をゆっくり添加した。この混合物をRTで3時間撹拌し、氷水に注いだ。K2CO3を添加した。この混合物を真空中で濃縮した。残渣をシリカゲルのフラッシュクロマトグラフィ(DCM/MeOH/NH3H2O=5:1:0.2)によって精製して、所望の生成物を得た(92mg、収率60%)。ESI−MS m/z:394.1[M+H]+。
−78℃の3−(アゼチジン−3−イル)−8−クロロ−5−ヒドロキシ−7−(2−ヒドロキシナフタレン−4−イル)キナゾリン−4(3H)−オン(92mg、0.23mmol)およびDIPEA(59mg、0.46mmol)のDCM(5mL)中の混合物に、塩化アクリロイル(21mg、0.23mmol)のDCM(2mL)中の溶液を滴下した。この混合物を−78℃で10分間撹拌した。この混合物を真空中で濃縮し、残渣をprep−TLCプレート(DCM/MeOH=8:1)によって精製して、所望の生成物を得た(8mg、収率8%)。ESI−MS m/z: 448.1 [M+H]+. 1HNMR (400MHz, CDCl3) δ:11.36 (s, 1H), 8.28 (s, 1H), 7.75 (d, J = 8.0 Hz, 1H), 7.45−7.41 (m, 1H), 7.35−7.32 (m, 1H), 7.28 (d, J = 2.4 Hz, 1H), 7.24〜7.21 (m, 1H), 7.06 (d, J = 2.4 Hz, 1H), 7.03 (s, 1H), 6.44 (dd, J = 1.6, 17.2 Hz, 1H), 6.24 (dd, J = 10.4, 16.8 Hz, 1H), 5.80 (dd, J = 1.6, 10.8 Hz, 1H), 5.41−5.34 (m, 1H), 4.77−4.57 (m, 4H).
化合物の生化学アッセイ
試験化合物を、10mMのDMSO原液(Fisherカタログ番号BP−231−100)として調製した。KRAS G12C 1−169(hisタグ化タンパク質、GDP負荷)を、緩衝液(20mM Hepes、150mM NaCl、1mM MgCl2)で2μmに希釈した。化合物を、以下のように活性について試験した。
1.最終化合物濃度を100μMにするために、化合物を5000μM(5μlの10mM化合物原液+5μlのDMSO)に希釈し、ピペッティングによって十分に混合した。
2.最終化合物濃度を30μMにするために、化合物を1500μM(3μlの10mM化合物原液+17μlのDMSO)に希釈し、ピペッティングによって十分に混合した。
3.最終化合物濃度を10μMにするために、化合物を500μM(2μlの10mM化合物原液+38μlのDMSO)に希釈し、ピペッティングによって十分に混合した。
MS装置を、正極性、分解能2GHz、および低質量(1700)モードに設定し、30分間平衡化する。次いで、装置を較正し、収集モードに切り替え、適切な方法をロードする。
KRAS G12Cタンパク質種の質量およびピーク強度を、Q Exactive Plus質量分析計(Thermo Scientific)に接続されたDionex RSLCナノシステム(Thermo Scientific)を使用して測定した。
本発明の化合物がRAS媒介細胞成長を阻害する能力を、以下のように評価し、実証する。野生型RASまたは変異体RASを発現する細胞を、白色透明底96ウェルプレート中に5,000細胞/ウェルの密度でプレートする。細胞を、プレート後約2時間付着させ、本明細書中に開示の化合物を添加する。一定時間後(例えば、24時間、48時間、または72時間の細胞成長後)、細胞増殖を、製造者の指示にしたがってCell Titer Glo試薬(Promega)を使用して総ATP含有量を測定することによって決定する。増殖EC50を、100μMからハーフログ間隔で減少する8点の化合物用量応答の分析によって決定する。
本明細書中に開示の化合物がRAS媒介シグナル伝達を阻害する能力を、以下のように評価し、実証する。野生型RASまたは変異体RAS(G12C、G12V、もしくはG12Aなど)を発現する細胞を、本発明の化合物を用いるか、用いずに(コントロール細胞)処置する。1つまたはそれよりも多くの本発明の化合物によるRASシグナル伝達の阻害を、コントロール細胞と比較した場合の1つまたはそれよりも多くの本発明の化合物で処置した細胞におけるリン酸化MEK、リン酸化ERK、リン酸化RSKの定常状態レベルおよび/またはRaf結合の減少によって実証する。
+は、5%までの結合活性を示す。
++は、5%から50%までの結合活性を示す。
+++は、50%またはそれよりも多くの結合活性を示す。
†は、4時間後に測定した結合活性を示す。
‡は、6時間後に測定した結合活性を示す。
TBD=未測定
特定の実施形態では、例えば以下の項目が提供される。
(項目1)
以下の構造(I):
(式中、
Aは、NまたはCであり;
Bは、オキソ、シアノ、アルキル、アルケニル、アルキニル、シクロアルキル、ヘテロシクリル、ヘテロアリール、シクロアルキルアルキル、ヘテロシクロアルキル、ヘテロアリールアルキル、アミノ、アルキルアミノ、アリールアミノ、−CO 2 H、−CONH 2 、アミニルカルボニル、アミニルカルボニルアルキル、ヘテロアリールアミノ、ハロ、ハロアルキル、アルコキシ、ハロアルコキシ、アリール、または−X−L 2 −R a であり;
Xは、−NR b −または−O−であり;
L 1 は、アルキレン、シクロアルキレン、ヘテロシクリレンであるか、または存在せず;
L 2 は、アルキレンであるか、または存在せず;
Rは、H、シアノ、アミノ、ハロ、ハロアルキル、ヒドロキシル、シクロアルキル、ヘテロシクリル、ヘテロシクロアルキル、アリール、ヘテロアリール、−CO 2 H、−CONH 2 、アミニルカルボニル、C 1 〜C 6 アルキル、C 1 〜C 6 アルキルアミニル、またはC 1 〜C 6 アルコキシであり;
R a は、シクロアルキル、ヘテロシクリル、ヘテロアリール、−(C=O)OH、−(C=O)NH 2 、または−(C=O)NHOHであり;
R b は、各出現において独立して、HまたはC 1 〜C 6 アルキルであり;
R 1 は、アリールまたはヘテロアリールであり;
R 2a 、R 2b およびR 2c は、それぞれ独立して、H、アミノ、シアノ、ハロ、ヒドロキシル、C 1 〜C 6 アルキル、C 1 〜C 6 アルキルアミニル、−NR b (C=O)R b 、C 1 〜C 6 ハロアルキル、C 1 〜C 6 アルコキシ、C 3 〜C 8 シクロアルキル、ヘテロシクリルアルキル、C 2 〜C 6 アルキニル、C 2 〜C 6 アルケニル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、アミニルカルボニル、ヘテロアリール、またはアリールであり;
は、全ての原子価を充足するような単結合または二重結合であり;
Eは、KRAS、HRAS、またはNRAS G12C変異体タンパク質の12位のシステイン残基と共有結合を形成することができる求電子部分である)
を有する化合物またはその薬学的に許容され得る塩、立体異性体、もしくはプロドラッグ。
(項目2)
Bが、シクロアルキル、ヘテロシクリル、またはヘテロアリールである、項目1に記載の化合物。
(項目3)
L 1 が、アルキレンであるか、または存在しない、項目1または2のいずれか1項に記載の化合物。
(項目4)
前記化合物が、以下の構造(IA):
(式中、
G 1 は、NまたはCHであり;
G 2 は、NR c またはCHR c であり;
R c は、H、アルキル、アルキルカルボニル、アミノカルボニル、アルキルカルボニルアミニル、アミノカルボニルアミニル、またはヘテロアリールカルボニルであり;
R 3a およびR 3b は、各出現において独立して、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR 3a とR 3b とが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR 3a は、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R 3b は、R 4b と一緒になって、炭素環式環または複素環式環を形成し;
R 4a およびR 4b は、各出現において独立して、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR 4a とR 4b とが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR 4a は、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R 4b は、R 3b と一緒になって、炭素環式環または複素環式環を形成し;
m 1 およびm 2 は、それぞれ独立して、1、2、または3であり;
nは、0〜5の整数である)
を有する、項目1〜3のいずれか1項に記載の化合物。
(項目5)
前記化合物が、以下の構造(IAa)または(IAb):
(式中、p 1 は、0〜3の整数である)を有する、項目4に記載の化合物。
(項目6)
前記化合物が、以下の構造(IAc)、(IAd)、または(IAe):
のうちの1つを有する、項目4または5のいずれか1項に記載の化合物。
(項目7)
R c が、アルキルカルボニル、アミノカルボニル、アルキルカルボニルアミニル、アミノカルボニルアミニル、またはヘテロアリールカルボニルである、項目4〜6のいずれか1項に記載の化合物。
(項目8)
アルキルカルボニルが、アミノカルボニル、ヒドロキシルアミノカルボニル、ヒドロキシル、またはアミノで置換される、項目7に記載の化合物。
(項目9)
R c が、以下の構造:
(式中、p 2 は、1〜3の整数である)
のうちの1つを有する、項目4〜8のいずれか1項に記載の化合物。
(項目10)
Bが、アルキル、シクロアルキルアルキル、ヘテロシクロアルキル、ヘテロアリールアルキル、または−X−L 2 −R a である、項目1に記載の化合物。
(項目11)
Bが、−X−L 2 −R a である、項目10に記載の化合物。
(項目12)
R a が、ヘテロシクリルまたはヘテロアリールである、項目11に記載の化合物。
(項目13)
L 1 が、アルキレンであるか、または存在しない、項目10〜12のいずれか1項に記載の化合物。
(項目14)
前記化合物が、以下の構造(IB)または(IC):
(式中、
Hは、R 3a 、R 3b 、R 4a 、およびR 4b の1つまたはそれよりも多くで任意選択的に置換される5または6員のヘテロアリール環を示し;
G 1 は、NまたはCHであり;
G 2 は、NR c またはCHR c であり;
R c は、H、アルキル、アルキルカルボニル、アミノカルボニル、アルキルカルボニルアミニル、アミノカルボニルアミニル、またはヘテロアリールカルボニルであり;
R 3a およびR 3b は、各出現において独立して、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR 3a とR 3b とが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR 3a は、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R 3b は、R 4b と一緒になって、炭素環式環または複素環式環を形成し;
R 4a およびR 4b は、各出現において独立して、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR 4a とR 4b とが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR 4a は、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R 4b は、R 3b と一緒になって、炭素環式環または複素環式環を形成し;
m 1 およびm 2 は、それぞれ独立して、1、2、または3であり;
nは、0〜5の整数である)
のうちの1つを有する、項目10〜13のいずれか1項に記載の化合物。
(項目15)
Hが、ピロリジニルまたはピリジニルである、項目14に記載の化合物。
(項目16)
前記化合物が、以下の構造(IBa)または(IBb):
(式中、R d は、各出現において独立して、H、ハロ、またはヒドロキシルであり、p 3 は、0〜3の整数である)
のうちの1つを有する、項目14に記載の化合物。
(項目17)
前記化合物が、以下の構造(IBc)、(IBd)、(IBe)、または(IBf):
のうちの1つを有する、項目14〜16のいずれか1項に記載の化合物。
(項目18)
Xが、NHである、項目11〜17のいずれか1項に記載の化合物。
(項目19)
L 2 が、存在しない、項目11〜18のいずれか1項に記載の化合物。
(項目20)
L 2 が、アルキレンである、項目11〜18のいずれか1項に記載の化合物。
(項目21)
Bが、以下の構造:
のうちの1つを有する、項目11〜20のいずれか1項に記載の化合物。
(項目22)
前記化合物が、以下の構造(ID):
(式中、p 3 は、0〜3の整数である)
を有する、項目11に記載の化合物。
(項目23)
R a が、−(C=O)OH、−(C=O)NH 2 、または−(C=O)NHOHである、項目22に記載の化合物。
(項目24)
前記化合物が、以下の構造(IDa):
を有する、項目22または23のいずれか1項に記載の化合物。
(項目25)
Xが、NHである、項目22〜24のいずれか1項に記載の化合物。
(項目26)
Bが、アルキルである、項目10に記載の化合物。
(項目27)
アルキルが、−(C=O)OH、−(C=O)NH 2 、または−(C=O)NHOHで置換される、項目26に記載の化合物。
(項目28)
Bが、ヘテロアリールアルキルである、項目10に記載の化合物。
(項目29)
前記ヘテロアリールアルキルが、ピロリジニルアルキルまたはピリジニルアルキルである、項目28に記載の化合物。
(項目30)
Bが、オキソである、項目1に記載の化合物。
(項目31)
前記化合物が、以下の構造(IE):
(式中、
G 1 は、CHであり;
G 2 は、NまたはCHであり;
R 3a およびR 3b は、各出現において独立して、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR 3a とR 3b とが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR 3a は、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R 3b は、R 4b と一緒になって、炭素環式環または複素環式環を形成し;
R 4a およびR 4b は、各出現において独立して、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR 4a とR 4b とが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR 4a は、H、−OH、−NH 2 、−CO 2 H、ハロ、シアノ、C 1 〜C 6 アルキル、C 1 〜C 6 ハロアルキル、C 1 〜C 6 ハロアルコキシ、C 2 〜C 6 アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R 4b は、R 3b と一緒になって、炭素環式環または複素環式環を形成し;
m 1 およびm 2 は、それぞれ独立して、1、2、または3である)
を有する、項目30に記載の化合物。
(項目32)
前記化合物が、以下の構造(IEa)、(IEb)、(IEc)、または(IEd):
のうちの1つを有する、項目31に記載の化合物。
(項目33)
前記化合物が、以下の構造(IEe)、(IEf)、(IEg)、(IEh)、(IEi)、(IEj)、(IEk)、または(IEl):
のうちの1つを有する、項目31または32のいずれか1項に記載の化合物。
(項目34)
R 1 が、アリールである、項目1〜33のいずれか1項に記載の化合物。
(項目35)
R 1 が、フェニルである、項目34に記載の化合物。
(項目36)
R 1 が、ナフチルである、項目34に記載の化合物。
(項目37)
R 1 が、1つまたはそれよりも多くの置換基で置換される、項目34〜36のいずれか1項に記載の化合物。
(項目38)
R 1 が、ハロ、アミノ、ヒドロキシル、C 1 〜C 6 アルキル、C 2 〜C 6 アルケニル、C 2 〜C 6 アルキニル、シアノ、C 1 〜C 6 ハロアルキル、C 1 〜C 6 アルコキシ、アルキルアミニル、シクロアルキル、ヘテロシクリルアルキル、ヘテロシクリルアルコキシ、ヘテロシクリルアミニル、シクロアルキルアミニル、アリール、ヘテロアリール、ホスフェート、ホスホアルコキシ、ボロン酸、ボロン酸エステル、−OC(=O)R、もしくはC 1 〜C 6 アルキルカルボニルオキシ、またはそれらの組み合わせで置換され、ここで、Rは、C 1 〜C 6 アルキルである、項目37に記載の化合物。
(項目39)
R 1 が、フルオロ、クロロ、シクロプロピル、シクロブチル、ヒドロキシル、アミノ、メチル、エチル、イソプロピル、トリフルオロメチル、もしくはメトキシ、またはそれらの組み合わせで置換される、項目38に記載の化合物。
(項目40)
R 1 が、以下の構造:
のうちの1つを有する、項目34〜39のいずれか1項に記載の化合物。
(項目41)
R 1 が、ヘテロアリールである、項目1〜33のいずれか1項に記載の化合物。
(項目42)
R 1 が、以下の構造:
のうちの1つを有する、項目41に記載の化合物。
(項目43)
R 2c が、Hである、項目1〜42のいずれか1項に記載の化合物。
(項目44)
R 2a およびR 2b が、それぞれ独立して、ハロ、ハロアルキル、アルキル、アミノ、ヒドロキシル、またはアルコキシである、項目1〜43のいずれか1項に記載の化合物。
(項目45)
R 2a が、フルオロ、クロロ、またはメトキシである、項目1〜44のいずれか1項に記載の化合物。
(項目46)
R 2b が、クロロ、フルオロ、アミノ、ヒドロキシル、またはCF 3 である、項目1〜45のいずれか1項に記載の化合物。
(項目47)
Rが、Hである、項目1〜46のいずれか1項に記載の化合物。
(項目48)
Eが、以下の構造:
(式中、
は、二重結合または三重結合を示し;
Qは、−C(=O)−、−C(=NR 8’ )−、−NR 8 C(=O)−、−S(=O) 2 −、または−NR 8 S(=O) 2 −であり;
R 8 は、H、C 1 〜C 6 アルキル、ヒドロキシルアルキル、アミノアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、C 3 〜C 8 シクロアルキル、またはヘテロシクロアルキルであり;
R 8’ は、H、−OH、−CN、またはC 1 〜C 6 アルキルであり;
が、二重結合である場合、R 9 およびR 10 は、それぞれ独立して、H、ハロ、シアノ、カルボキシル、C 1 〜C 6 アルキル、アルコキシカルボニル、アミニルアルキル、アルキルアミニルアルキル、アリール、ヘテロシクリル、ヘテロシクリルアルキル、ヘテロアリール、またはヒドロキシルアルキルであるか、あるいはR 9 とR 10 とが一緒になって、炭素環式環、複素環式環、またはヘテロアリール環を形成し;
が、三重結合である場合、R 9 は、存在せず、且つR 10 は、H、C 1 〜C 6 アルキル、アミニルアルキル、アルキルアミニルアルキル、またはヒドロキシルアルキルである)
を有する、項目1〜47のいずれか1項に記載の化合物。
(項目49)
Qが、−C(=O)−である、項目48に記載の化合物。
(項目50)
Qが、−S(=O) 2 −である、項目48に記載の化合物。
(項目51)
Qが、−NR 8 C(=O)−である、項目48に記載の化合物。
(項目52)
Qが、−NR 8 S(=O) 2 −である、項目48に記載の化合物。
(項目53)
R 9 およびR 10 の各々が、Hである、項目48〜52のいずれか1項に記載の化合物。
(項目54)
Eが、以下の構造:
のうちの1つを有する、項目1〜53のいずれか1項に記載の化合物。
(項目55)
前記化合物が、表1における化合物から選択される、項目1に記載の化合物。
(項目56)
項目1〜55のいずれか1項に記載の化合物の実質的に精製されたアトロプ異性体。
(項目57)
項目1〜56のいずれか1項に記載の化合物および薬学的に許容され得るキャリアを含む薬学的組成物。
(項目58)
前記薬学的組成物が経口投与のために製剤化されている、項目57に記載の薬学的組成物。
(項目59)
前記薬学的組成物が注射のために製剤化されている、項目57に記載の薬学的組成物。
(項目60)
がんの処置方法であって、有効量の項目57に記載の薬学的組成物を該処置を必要とする被験体に投与することを含む、方法。
(項目61)
前記がんが、KRAS G12C変異、HRAS G12C変異、またはNRAS G12C変異によって媒介される、項目60に記載の方法。
(項目62)
前記がんが、血液がん、膵臓がん、MYH関連ポリポーシス、結腸直腸がん、または肺がんである、項目60に記載の方法。
(項目63)
KRAS、HRAS、またはNRAS G12C変異体タンパク質の活性を調節する方法であって、該KRAS G12C変異体タンパク質を項目1〜56のいずれか1項に記載の化合物と反応させることを含む、方法。
(項目64)
細胞集団の増殖を阻害する方法であって、該細胞集団を項目1〜56のいずれか1項に記載の化合物と接触させることを含む、方法。
(項目65)
増殖の阻害が、前記細胞集団の細胞生存度の減少として測定される、項目64に記載の方法。
(項目66)
KRAS G12C変異、HRAS G12C変異、またはNRAS G12C変異によって媒介される障害の処置を必要とする被験体における、該障害の該処置方法であって、
該被験体がKRAS、HRAS、またはNRASのG12C変異を有するかどうかを決定すること;および
該被験体が該KRAS、HRAS、またはNRASのG12C変異を有すると決定された場合、該被験体に治療有効量の項目57に記載の薬学的組成物を投与すること
を含む、方法。
(項目67)
前記障害が、がんである、項目66に記載の方法。
(項目68)
前記がんが、血液がん、膵臓がん、MYH関連ポリポーシス、結腸直腸がん、または肺がんである、項目67に記載の方法。
(項目69)
標識されたKRAS、HRAS、またはNRAS G12C変異体タンパク質を調製する方法であって、該KRAS、HRAS、またはNRAS G12C変異体を項目1〜56のいずれか1項に記載の化合物と反応させて該標識されたKRAS、HRAS、またはNRAS G12Cタンパク質を得ることを含む、方法。
(項目70)
腫瘍転移を阻害する方法であって、有効量の項目57に記載の薬学的組成物を該阻害を必要とする被験体に投与することを含む、方法。
Claims (67)
- 以下の構造(I):
Aは、NまたはCであり;
Bは、オキソ、シアノ、アルキル、アルケニル、アルキニル、シクロアルキル、ヘテロシクリル、ヘテロアリール、シクロアルキルアルキル、ヘテロシクロアルキル、ヘテロアリールアルキル、アミノ、アルキルアミノ、アリールアミノ、−CO2H、−CONH2、アミニルカルボニル、アミニルカルボニルアルキル、ヘテロアリールアミノ、ハロ、ハロアルキル、アルコキシ、ハロアルコキシ、アリール、または−X−L2−Raであり;
Xは、−NRb−または−O−であり;
L1は、アルキレン、シクロアルキレン、ヘテロシクリレンであるか、または存在せず;
L2は、アルキレンであるか、または存在せず;
Rは、H、シアノ、アミノ、ハロ、ハロアルキル、ヒドロキシル、シクロアルキル、ヘテロシクリル、ヘテロシクロアルキル、アリール、ヘテロアリール、−CO2H、−CONH2、アミニルカルボニル、C1〜C6アルキル、C1〜C6アルキルアミニル、またはC1〜C6アルコキシであり;
Raは、シクロアルキル、ヘテロシクリル、ヘテロアリール、−(C=O)OH、−(C=O)NH2、または−(C=O)NHOHであり;
Rbは、各出現において独立して、HまたはC1〜C6アルキルであり;
R1は、アリールまたはヘテロアリールであり;
R2a、R2bおよびR2cは、それぞれ独立して、H、アミノ、シアノ、ハロ、ヒドロキシル、C1〜C6アルキル、C1〜C6アルキルアミニル、−NRb(C=O)Rb、C1〜C6ハロアルキル、C1〜C6アルコキシ、C3〜C8シクロアルキル、ヘテロシクリルアルキル、C2〜C6アルキニル、C2〜C6アルケニル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、アミニルカルボニル、ヘテロアリール、またはアリールであり;
Eは、以下の構造:
Qは、−C(=O)−、−C(=NR8’)−、−NR8C(=O)−、−S(=O)2−または−NR8S(=O)2−であり;
R8は、H、C1〜C6アルキル、ヒドロキシルアルキル、アミノアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、C3〜C8シクロアルキルまたはヘテロシクロアルキルであり;
R8’は、H、−OH、−CN、またはC1〜C6アルキルであり;そして
R9およびR10は、両方ともHである)
を有する化合物またはその薬学的に許容され得る塩、もしくは立体異性体。 - Bが、シクロアルキル、ヘテロシクリル、またはヘテロアリールである、請求項1に記載の化合物。
- L1が、アルキレンであるか、または存在しない、請求項1または2のいずれか1項に記載の化合物。
- 前記化合物が、以下の構造(IA):
G1は、NまたはCHであり;
G2は、NRcまたはCHRcであり;
Rcは、H、アルキル、アルキルカルボニル、アミノカルボニル、アルキルカルボニルアミニル、アミノカルボニルアミニル、またはヘテロアリールカルボニルであり;
R3aおよびR3bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR3aとR3bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR3aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R3bは、R4bと一緒になって、炭素環式環または複素環式環を形成し;
R4aおよびR4bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR4aとR4bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR4aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R4bは、R3bと一緒になって、炭素環式環または複素環式環を形成し;
m1およびm2は、それぞれ独立して、1、2、または3であり;
nは、0〜5の整数である)
を有する、請求項1〜3のいずれか1項に記載の化合物。 - Rcが、アルキルカルボニル、アミノカルボニル、アルキルカルボニルアミニル、アミノカルボニルアミニル、またはヘテロアリールカルボニルである、請求項4〜6のいずれか1項に記載の化合物。
- アルキルカルボニルが、アミノカルボニル、ヒドロキシルアミノカルボニル、ヒドロキシル、またはアミノで置換される、請求項7に記載の化合物。
- Bが、アルキル、シクロアルキルアルキル、ヘテロシクロアルキル、ヘテロアリールアルキル、または−X−L2−Raである、請求項1に記載の化合物。
- Bが、−X−L2−Raである、請求項10に記載の化合物。
- Raが、ヘテロシクリルまたはヘテロアリールである、請求項11に記載の化合物。
- L1が、アルキレンであるか、または存在しない、請求項10〜12のいずれか1項に記載の化合物。
- 前記化合物が、以下の構造(IB)または(IC):
Hは、R3a、R3b、R4a、およびR4bの1つまたはそれよりも多くで任意選択的に置換される5または6員のヘテロアリール環を示し;
G1は、NまたはCHであり;
G2は、NRcまたはCHRcであり;
Rcは、H、アルキル、アルキルカルボニル、アミノカルボニル、アルキルカルボニルアミニル、アミノカルボニルアミニル、またはヘテロアリールカルボニルであり;
R3aおよびR3bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR3aとR3bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR3aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R3bは、R4bと一緒になって、炭素環式環または複素環式環を形成し;
R4aおよびR4bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR4aとR4bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR4aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R4bは、R3bと一緒になって、炭素環式環または複素環式環を形成し;
m1およびm2は、それぞれ独立して、1、2、または3であり;
nは、0〜5の整数である)
のうちの1つを有する、請求項10〜13のいずれか1項に記載の化合物。 - Hが、ピロリジニルまたはピリジニルである、請求項14に記載の化合物。
- Xが、NHである、請求項11〜17のいずれか1項に記載の化合物。
- L2が、存在しない、請求項11〜18のいずれか1項に記載の化合物。
- L2が、アルキレンである、請求項11〜18のいずれか1項に記載の化合物。
- Raが、−(C=O)OH、−(C=O)NH2、または−(C=O)NHOHである、請求項22に記載の化合物。
- Xが、NHである、請求項22〜24のいずれか1項に記載の化合物。
- Bが、アルキルである、請求項10に記載の化合物。
- アルキルが、−(C=O)OH、−(C=O)NH2、または−(C=O)NHOHで置換される、請求項26に記載の化合物。
- Bが、ヘテロアリールアルキルである、請求項10に記載の化合物。
- 前記ヘテロアリールアルキルが、ピロリジニルアルキルまたはピリジニルアルキルである、請求項28に記載の化合物。
- Bが、オキソである、請求項1に記載の化合物。
- 前記化合物が、以下の構造(IE):
G1は、CHであり;
G2は、NまたはCHであり;
R3aおよびR3bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR3aとR3bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR3aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R3bは、R4bと一緒になって、炭素環式環または複素環式環を形成し;
R4aおよびR4bは、各出現において独立して、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであるか;あるいはR4aとR4bとが一緒になって、オキソ、炭素環式環、または複素環式環を形成するか;あるいはR4aは、H、−OH、−NH2、−CO2H、ハロ、シアノ、C1〜C6アルキル、C1〜C6ハロアルキル、C1〜C6ハロアルコキシ、C2〜C6アルキニル、ヒドロキシルアルキル、アルコキシアルキル、アミニルアルキル、アルキルアミニルアルキル、シアノアルキル、カルボキシアルキル、アミニルカルボニルアルキル、またはアミニルカルボニルであり、R4bは、R3bと一緒になって、炭素環式環または複素環式環を形成し;
m1およびm2は、それぞれ独立して、1、2、または3である)
を有する、請求項30に記載の化合物。 - R1が、アリールである、請求項1〜33のいずれか1項に記載の化合物。
- R1が、フェニルである、請求項34に記載の化合物。
- R1が、ナフチルである、請求項34に記載の化合物。
- R1が、1つまたはそれよりも多くの置換基で置換される、請求項34〜36のいずれか1項に記載の化合物。
- R1が、ハロ、アミノ、ヒドロキシル、C1〜C6アルキル、C2〜C6アルケニル、C2〜C6アルキニル、シアノ、C1〜C6ハロアルキル、C1〜C6アルコキシ、アルキルアミニル、シクロアルキル、ヘテロシクリルアルキル、ヘテロシクリルアルコキシ、ヘテロシクリルアミニル、シクロアルキルアミニル、アリール、ヘテロアリール、ホスフェート、ホスホアルコキシ、ボロン酸、ボロン酸エステル、−OC(=O)R、もしくはC1〜C6アルキルカルボニルオキシ、またはそれらの組み合わせで置換され、ここで、Rは、C1〜C6アルキルである、請求項37に記載の化合物。
- R1が、フルオロ、クロロ、シクロプロピル、シクロブチル、ヒドロキシル、アミノ、メチル、エチル、イソプロピル、トリフルオロメチル、もしくはメトキシ、またはそれらの組み合わせで置換される、請求項38に記載の化合物。
- R1が、ヘテロアリールである、請求項1〜33のいずれか1項に記載の化合物。
- R2cが、Hである、請求項1〜42のいずれか1項に記載の化合物。
- R2aおよびR2bが、それぞれ独立して、ハロ、ハロアルキル、アルキル、アミノ、ヒドロキシル、またはアルコキシである、請求項1〜43のいずれか1項に記載の化合物。
- R2aが、フルオロ、クロロ、またはメトキシである、請求項1〜44のいずれか1項に記載の化合物。
- R2bが、クロロ、フルオロ、アミノ、ヒドロキシル、またはCF3である、請求項1〜45のいずれか1項に記載の化合物。
- Rが、Hである、請求項1〜46のいずれか1項に記載の化合物。
- Qが、−C(=O)−である、請求項1〜47のいずれか1項に記載の化合物。
- Qが、−S(=O)2−である、請求項1〜47のいずれか1項に記載の化合物。
- Qが、−NR8C(=O)−である、請求項1〜47のいずれか1項に記載の化合物。
- Qが、−NR8S(=O)2−である、請求項1〜47のいずれか1項に記載の化合物。
- 請求項1〜53のいずれか1項に記載の化合物および薬学的に許容され得るキャリアを含む薬学的組成物。
- 前記薬学的組成物が経口投与のために製剤化されている、請求項54に記載の薬学的組成物。
- 前記薬学的組成物が注射のために製剤化されている、請求項54に記載の薬学的組成物。
- がんの処置のための請求項54に記載の薬学的組成物。
- 前記がんが、KRAS G12C変異、HRAS G12C変異、またはNRAS G12C変異によって媒介される、請求項57に記載の薬学的組成物。
- 前記がんが、血液がん、膵臓がん、MYH関連ポリポーシス、結腸直腸がん、または肺がんである、請求項57に記載の薬学的組成物。
- KRAS、HRAS、またはNRAS G12C変異体タンパク質の活性を調節する方法において使用するための、請求項1〜53のいずれか1項に記載の化合物を含む組成物であって、該方法は、該KRAS G12C変異体タンパク質を請求項1〜53のいずれか1項に記載の化合物と反応させることを含む、組成物。
- 細胞集団の増殖を阻害するための、請求項1〜53のいずれか1項に記載の化合物を含む組成物であって、該細胞集団が、該組成物と接触されることを特徴とする、組成物。
- 増殖の阻害が、前記細胞集団の細胞生存度の減少として測定される、請求項61に記載の組成物。
- KRAS G12C変異、HRAS G12C変異、またはNRAS G12C変異によって媒介される障害の処置を必要とする被験体において、該障害を処置する方法において使用するための、請求項54に記載の薬学的組成物であって、該方法は、
該被験体がKRAS、HRAS、またはNRASのG12C変異を有するかどうかを決定すること;および
該被験体が該KRAS、HRAS、またはNRASのG12C変異を有すると決定された場合、該被験体に該薬学的組成物を投与すること
を含む、薬学的組成物。 - 前記障害が、がんである、請求項63に記載の薬学的組成物。
- 前記がんが、血液がん、膵臓がん、MYH関連ポリポーシス、結腸直腸がん、または肺がんである、請求項64に記載の薬学的組成物。
- 標識されたKRAS、HRAS、またはNRAS G12C変異体タンパク質を調製する方法に使用するための、請求項1〜53のいずれか1項に記載の化合物を含む組成物であって、ここで、該方法は、該KRAS、HRAS、またはNRAS G12C変異体を請求項1〜53のいずれか1項に記載の化合物と反応させて該標識されたKRAS、HRAS、またはNRAS G12Cタンパク質を得ることを含む、組成物。
- 腫瘍転移を阻害するための請求項54に記載の薬学的組成物。
Applications Claiming Priority (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562195636P | 2015-07-22 | 2015-07-22 | |
| US62/195,636 | 2015-07-22 | ||
| US201662342078P | 2016-05-26 | 2016-05-26 | |
| US62/342,078 | 2016-05-26 | ||
| JO150/2016 | 2016-07-21 | ||
| GC201631750 | 2016-07-21 | ||
| GCGC-2016-31750 | 2016-07-21 | ||
| JOP/2016/0150A JOP20160150B1 (ar) | 2015-07-22 | 2016-07-21 | مركبات كينازولين مستبدلة وطرق استعمالها |
| PCT/US2016/043568 WO2017015562A1 (en) | 2015-07-22 | 2016-07-22 | Substituted quinazoline compounds and their use as inhibitors of g12c mutant kras, hras and/or nras proteins |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2018520195A JP2018520195A (ja) | 2018-07-26 |
| JP2018520195A5 JP2018520195A5 (ja) | 2019-08-15 |
| JP6869947B2 true JP6869947B2 (ja) | 2021-05-12 |
Family
ID=57821530
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2018502355A Expired - Fee Related JP6869947B2 (ja) | 2015-07-22 | 2016-07-22 | 置換キナゾリン化合物ならびにそのg12c変異kras、hrasおよび/またはnrasタンパク質の阻害剤としての使用 |
Country Status (5)
| Country | Link |
|---|---|
| EP (1) | EP3325447A1 (ja) |
| JP (1) | JP6869947B2 (ja) |
| CA (1) | CA2993013A1 (ja) |
| MX (1) | MX388781B (ja) |
| WO (1) | WO2017015562A1 (ja) |
Families Citing this family (115)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9227978B2 (en) | 2013-03-15 | 2016-01-05 | Araxes Pharma Llc | Covalent inhibitors of Kras G12C |
| JO3805B1 (ar) | 2013-10-10 | 2021-01-31 | Araxes Pharma Llc | مثبطات كراس جي12سي |
| JO3556B1 (ar) | 2014-09-18 | 2020-07-05 | Araxes Pharma Llc | علاجات مدمجة لمعالجة السرطان |
| JP2017528498A (ja) | 2014-09-25 | 2017-09-28 | アラクセス ファーマ エルエルシー | Kras g12c変異体タンパク質のインヒビター |
| WO2016049568A1 (en) | 2014-09-25 | 2016-03-31 | Araxes Pharma Llc | Methods and compositions for inhibition of ras |
| ES2898765T3 (es) | 2015-04-10 | 2022-03-08 | Araxes Pharma Llc | Compuestos de quinazolina sustituidos y métodos de uso de los mismos |
| ES2856880T3 (es) | 2015-04-15 | 2021-09-28 | Araxes Pharma Llc | Inhibidores tricíclicos condensados de KRAS y métodos de uso de los mismos |
| US10144724B2 (en) | 2015-07-22 | 2018-12-04 | Araxes Pharma Llc | Substituted quinazoline compounds and methods of use thereof |
| WO2017058792A1 (en) | 2015-09-28 | 2017-04-06 | Araxes Pharma Llc | Inhibitors of kras g12c mutant proteins |
| US10975071B2 (en) | 2015-09-28 | 2021-04-13 | Araxes Pharma Llc | Inhibitors of KRAS G12C mutant proteins |
| US10689356B2 (en) | 2015-09-28 | 2020-06-23 | Araxes Pharma Llc | Inhibitors of KRAS G12C mutant proteins |
| EP3356353A1 (en) | 2015-09-28 | 2018-08-08 | Araxes Pharma LLC | Inhibitors of kras g12c mutant proteins |
| EP3356347A1 (en) | 2015-09-28 | 2018-08-08 | Araxes Pharma LLC | Inhibitors of kras g12c mutant proteins |
| US10730867B2 (en) | 2015-09-28 | 2020-08-04 | Araxes Pharma Llc | Inhibitors of KRAS G12C mutant proteins |
| US10647703B2 (en) | 2015-09-28 | 2020-05-12 | Araxes Pharma Llc | Inhibitors of KRAS G12C mutant proteins |
| WO2017070256A2 (en) | 2015-10-19 | 2017-04-27 | Araxes Pharma Llc | Method for screening inhibitors of ras |
| US10414757B2 (en) | 2015-11-16 | 2019-09-17 | Araxes Pharma Llc | 2-substituted quinazoline compounds comprising a substituted heterocyclic group and methods of use thereof |
| US9988357B2 (en) | 2015-12-09 | 2018-06-05 | Araxes Pharma Llc | Methods for preparation of quinazoline derivatives |
| EP3394056B1 (en) | 2015-12-22 | 2021-04-14 | Shy Therapeutics LLC | Compounds for the treatment of cancer and inflammatory disease |
| WO2017172979A1 (en) | 2016-03-30 | 2017-10-05 | Araxes Pharma Llc | Substituted quinazoline compounds and methods of use |
| US10646488B2 (en) | 2016-07-13 | 2020-05-12 | Araxes Pharma Llc | Conjugates of cereblon binding compounds and G12C mutant KRAS, HRAS or NRAS protein modulating compounds and methods of use thereof |
| WO2018064510A1 (en) | 2016-09-29 | 2018-04-05 | Araxes Pharma Llc | Inhibitors of kras g12c mutant proteins |
| US10377743B2 (en) | 2016-10-07 | 2019-08-13 | Araxes Pharma Llc | Inhibitors of RAS and methods of use thereof |
| NZ754994A (en) | 2016-12-22 | 2022-12-23 | Amgen Inc | Benzisothiazole, isothiazolo[3,4-b]pyridine, quinazoline, phthalazine, pyrido[2,3-d]pyridazine and pyrido[2,3-d]pyrimidine derivatives as kras g12c inhibitors for treating lung, pancreatic or colorectal cancer |
| JOP20190272A1 (ar) | 2017-05-22 | 2019-11-21 | Amgen Inc | مثبطات kras g12c وطرق لاستخدامها |
| KR20200010306A (ko) | 2017-05-25 | 2020-01-30 | 아락세스 파마 엘엘씨 | Kras의 공유적 억제제 |
| CN110869357A (zh) * | 2017-05-25 | 2020-03-06 | 亚瑞克西斯制药公司 | 化合物及其用于治疗癌症的使用方法 |
| CA3066939A1 (en) | 2017-06-21 | 2018-12-27 | SHY Therapeutics LLC | Compounds that interact with the ras superfamily for the treatment of cancers, inflammatory diseases, rasopathies, and fibrotic disease |
| ES2928576T3 (es) | 2017-09-08 | 2022-11-21 | Amgen Inc | Inhibidores de KRAS G12C y métodos de uso de los mismos |
| EA202090652A1 (ru) * | 2017-09-20 | 2020-08-21 | Дзе Юнайтед Стейтс Оф Америка, Эз Репрезентед Бай Дзе Секретари, Департмент Оф Хелс Энд Хьюман Сёрвисез | T-клеточные рецепторы, рестриктированные по антигену лейкоцитов человека класса ii, против мутантного ras |
| WO2019110751A1 (en) * | 2017-12-08 | 2019-06-13 | Astrazeneca Ab | Tetracyclic compounds as inhibitors of g12c mutant ras protein, for use as anti-cancer agents |
| TW201942115A (zh) * | 2018-02-01 | 2019-11-01 | 美商輝瑞股份有限公司 | 作為抗癌藥之經取代的喹唑啉和吡啶並嘧啶衍生物 |
| MA52501A (fr) | 2018-05-04 | 2021-03-10 | Amgen Inc | Inhibiteurs de kras g12c et leurs procédés d'utilisation |
| CA3099118A1 (en) | 2018-05-04 | 2019-11-07 | Amgen Inc. | Kras g12c inhibitors and methods of using the same |
| WO2019217307A1 (en) | 2018-05-07 | 2019-11-14 | Mirati Therapeutics, Inc. | Kras g12c inhibitors |
| TW202012415A (zh) | 2018-05-08 | 2020-04-01 | 瑞典商阿斯特捷利康公司 | 化學化合物 |
| EP3790886B1 (en) | 2018-05-10 | 2024-06-26 | Amgen Inc. | Kras g12c inhibitors for the treatment of cancer |
| EP3802535B1 (en) | 2018-06-01 | 2022-12-14 | Amgen, Inc | Kras g12c inhibitors and methods of using the same |
| MA51848A (fr) | 2018-06-12 | 2021-04-21 | Amgen Inc | Inhibiteurs de kras g12c et leurs procédés d'utilisation |
| CA3105174A1 (en) * | 2018-06-27 | 2020-01-02 | Reborna Biosciences, Inc. | Prophylactic or therapeutic agent for spinal muscular atrophy |
| CN112996795B (zh) | 2018-09-18 | 2024-11-12 | 尼坎治疗公司 | 作为src同源-2磷酸酶抑制剂的稠合的三环衍生物 |
| JP7451419B2 (ja) | 2018-10-26 | 2024-03-18 | 大鵬薬品工業株式会社 | 新規なインダゾール化合物又はその塩 |
| JP7516029B2 (ja) | 2018-11-16 | 2024-07-16 | アムジエン・インコーポレーテツド | Kras g12c阻害剤化合物の重要な中間体の改良合成法 |
| US11053226B2 (en) | 2018-11-19 | 2021-07-06 | Amgen Inc. | KRAS G12C inhibitors and methods of using the same |
| JP7377679B2 (ja) | 2018-11-19 | 2023-11-10 | アムジエン・インコーポレーテツド | がん治療のためのkrasg12c阻害剤及び1種以上の薬学的に活性な追加の薬剤を含む併用療法 |
| US12391705B2 (en) | 2018-12-19 | 2025-08-19 | Shy Therapeutics, Llc | Compounds that interact with the Ras superfamily for the treatment of cancers, inflammatory diseases, rasopathies, and fibrotic disease |
| WO2020165732A1 (en) | 2019-02-12 | 2020-08-20 | Novartis Ag | Pharmaceutical combination comprising tno155 and a krasg12c inhibitor |
| EP3931188B1 (en) | 2019-02-26 | 2023-08-30 | Boehringer Ingelheim International GmbH | New isoindolinone substituted indoles and derivatives as ras inhibitors |
| CR20210504A (es) | 2019-03-05 | 2022-02-08 | Astrazeneca Ab | Compuestos tricíclicos condensados útiles como agentes anticancerígenos |
| EP3738593A1 (en) | 2019-05-14 | 2020-11-18 | Amgen, Inc | Dosing of kras inhibitor for treatment of cancers |
| WO2020234103A1 (en) | 2019-05-21 | 2020-11-26 | Bayer Aktiengesellschaft | Identification and use of kras inhibitors |
| EP3972973A1 (en) | 2019-05-21 | 2022-03-30 | Amgen Inc. | Solid state forms |
| CR20220230A (es) | 2019-10-28 | 2022-06-15 | Merck Sharp & Dohme | Inhibidores de pequeñas moléculas de mutante g12c de kras |
| KR20220109407A (ko) | 2019-11-04 | 2022-08-04 | 레볼루션 메디슨즈, 인크. | Ras 억제제 |
| JP7823816B2 (ja) | 2019-11-04 | 2026-03-04 | レヴォリューション・メディスンズ,インコーポレイテッド | Ras阻害剤 |
| EP4054719B1 (en) | 2019-11-04 | 2026-02-11 | Revolution Medicines, Inc. | Ras inhibitors |
| WO2021108683A1 (en) | 2019-11-27 | 2021-06-03 | Revolution Medicines, Inc. | Covalent ras inhibitors and uses thereof |
| EP4067343A4 (en) | 2019-11-29 | 2024-01-03 | Taiho Pharmaceutical Co., Ltd. | NEW PHENOLIC COMPOUND OR SALT THEREOF |
| GB202001344D0 (en) | 2020-01-31 | 2020-03-18 | Redx Pharma Plc | Ras Inhibitors |
| TW202210633A (zh) | 2020-06-05 | 2022-03-16 | 法商昂席歐公司 | 用於治療癌症之dbait分子與kras抑制劑的組合 |
| CA3183032A1 (en) | 2020-06-18 | 2021-12-23 | Mallika Singh | Methods for delaying, preventing, and treating acquired resistance to ras inhibitors |
| MX2023002248A (es) | 2020-09-03 | 2023-05-16 | Revolution Medicines Inc | Uso de inhibidores de sos1 para tratar neoplasias malignas con mutaciones de shp2. |
| CR20230165A (es) | 2020-09-15 | 2023-06-02 | Revolution Medicines Inc | Derivados indólicos como inhibidores de ras en el tratamiento del cáncer |
| US12162893B2 (en) | 2020-09-23 | 2024-12-10 | Erasca, Inc. | Tricyclic pyridones and pyrimidones |
| WO2022133345A1 (en) | 2020-12-18 | 2022-06-23 | Erasca, Inc. | Tricyclic pyridones and pyrimidones |
| US20240100172A1 (en) | 2020-12-21 | 2024-03-28 | Hangzhou Jijing Pharmaceutical Technology Limited | Methods and compounds for targeted autophagy |
| WO2022140472A1 (en) | 2020-12-22 | 2022-06-30 | Nikang Therapeutics, Inc. | Compounds for degrading cyclin-dependent kinase 2 via ubiquitin proteosome pathway |
| CR20230558A (es) | 2021-05-05 | 2024-01-24 | Revolution Medicines Inc | Inhibidores de ras para el tratamiento del cáncer |
| IL308193A (en) | 2021-05-05 | 2024-01-01 | Revolution Medicines Inc | RAS inhibitors |
| WO2022266206A1 (en) | 2021-06-16 | 2022-12-22 | Erasca, Inc. | Kras inhibitor conjugates |
| TW202317100A (zh) | 2021-06-23 | 2023-05-01 | 瑞士商諾華公司 | 包含kras g12c抑制劑的藥物組合及其用於治療癌症之用途 |
| WO2023284730A1 (en) | 2021-07-14 | 2023-01-19 | Nikang Therapeutics, Inc. | Alkylidene derivatives as kras inhibitors |
| TW202327569A (zh) | 2021-09-01 | 2023-07-16 | 瑞士商諾華公司 | 包含tead抑制劑的藥物組合及其用於癌症治療之用途 |
| AR127308A1 (es) | 2021-10-08 | 2024-01-10 | Revolution Medicines Inc | Inhibidores ras |
| JP2025500878A (ja) | 2021-12-17 | 2025-01-15 | ジェンザイム・コーポレーション | Shp2阻害剤としてのピラゾロピラジン化合物 |
| CN118696046A (zh) | 2022-02-10 | 2024-09-24 | 拜耳公司 | 作为kras抑制剂的稠合嘧啶 |
| EP4227307A1 (en) | 2022-02-11 | 2023-08-16 | Genzyme Corporation | Pyrazolopyrazine compounds as shp2 inhibitors |
| CN119136806A (zh) | 2022-03-08 | 2024-12-13 | 锐新医药公司 | 用于治疗免疫难治性肺癌的方法 |
| IL315603A (en) | 2022-03-28 | 2024-11-01 | Nikang Therapeutics Inc | Sulfonamido derivatives as cycle-dependent KINASE 2 inhibitors |
| WO2023199180A1 (en) | 2022-04-11 | 2023-10-19 | Novartis Ag | Therapeutic uses of a krasg12c inhibitor |
| EP4536363A1 (en) | 2022-06-08 | 2025-04-16 | Nikang Therapeutics, Inc. | Sulfamide derivatives as cyclin-dependent kinase 2 inhibitors |
| WO2023240263A1 (en) | 2022-06-10 | 2023-12-14 | Revolution Medicines, Inc. | Macrocyclic ras inhibitors |
| GB202212641D0 (en) | 2022-08-31 | 2022-10-12 | Jazz Pharmaceuticals Ireland Ltd | Novel compounds |
| AU2023377064A1 (en) | 2022-11-09 | 2025-05-22 | Revolution Medicines, Inc. | Compounds, complexes, and methods for their preparation and of their use |
| TW202434563A (zh) | 2022-11-11 | 2024-09-01 | 美商尼坎醫療公司 | 用於經由泛素蛋白酶體途徑降解週期蛋白依賴性激酶2的含有2,5-取代的嘧啶衍生物之雙功能化合物 |
| AU2024241633A1 (en) | 2023-03-30 | 2025-11-06 | Revolution Medicines, Inc. | Compositions for inducing ras gtp hydrolysis and uses thereof |
| PE20260039A1 (es) | 2023-04-07 | 2026-01-09 | Revolution Medicines Inc | Inhibidores macrociclicos de ras |
| WO2024211663A1 (en) | 2023-04-07 | 2024-10-10 | Revolution Medicines, Inc. | Condensed macrocyclic compounds as ras inhibitors |
| CN121100123A (zh) | 2023-04-14 | 2025-12-09 | 锐新医药公司 | Ras抑制剂的结晶形式 |
| TW202448897A (zh) | 2023-04-14 | 2024-12-16 | 美商銳新醫藥公司 | Ras抑制劑之結晶形式、含有其之組合物及其使用方法 |
| WO2024229406A1 (en) | 2023-05-04 | 2024-11-07 | Revolution Medicines, Inc. | Combination therapy for a ras related disease or disorder |
| KR20260020406A (ko) | 2023-06-02 | 2026-02-11 | 다이이찌 산쿄 가부시키가이샤 | 항 her3 항체-약물 콘주게이트와 rasg12c 저해제의 조합 |
| WO2025016899A1 (en) | 2023-07-19 | 2025-01-23 | Bayer Aktiengesellschaft | Spirocyclic compounds for the treatment of cancer |
| WO2025026903A1 (en) | 2023-07-31 | 2025-02-06 | Bayer Aktiengesellschaft | Imidazo pyrimidine compounds for the treatment of cancer |
| US20250049810A1 (en) | 2023-08-07 | 2025-02-13 | Revolution Medicines, Inc. | Methods of treating a ras protein-related disease or disorder |
| WO2025072462A1 (en) | 2023-09-27 | 2025-04-03 | Nikang Therapeutics, Inc. | Sulfonamide derivatives as cyclin-dependent kinase 2 inhibitors |
| TW202530228A (zh) | 2023-10-12 | 2025-08-01 | 美商銳新醫藥公司 | Ras抑制劑 |
| TW202535891A (zh) | 2023-10-20 | 2025-09-16 | 美商默沙東有限責任公司 | Kras蛋白之小分子抑制劑 |
| WO2025117616A1 (en) | 2023-11-27 | 2025-06-05 | Nikang Therapeutics, Inc. | Bifunctional compounds containing 2,5-substituted pyrimidine derivatives for degrading cyclin-dependent kinase 2 and cyclin-dependent kinase 4 via ubiquitin proteasome pathway |
| WO2025117881A1 (en) * | 2023-12-01 | 2025-06-05 | Casma Therapeutics, Inc. | Compounds and methods for inhibiting autophagy |
| WO2025117981A1 (en) | 2023-12-02 | 2025-06-05 | Nikang Therapeutics, Inc. | Bifunctional compounds containing 2,5-substituted pyrimidine derivatives for degrading cyclin-dependent kinase 2 via ubiquitin proteasome pathway |
| WO2025171296A1 (en) | 2024-02-09 | 2025-08-14 | Revolution Medicines, Inc. | Ras inhibitors |
| WO2025212828A1 (en) | 2024-04-03 | 2025-10-09 | Nikang Therapeutics, Inc. | Bifunctional compounds containing 2,5-substituted pyrimidine derivatives for degrading cyclin-dependent kinase 2 and cyclin-dependent kinase 4 via ubiquitin proteasome pathway |
| WO2025240536A1 (en) | 2024-05-15 | 2025-11-20 | Nikang Therapeutics, Inc. | Bifunctional compounds containing 2,5-substituted pyrimidine derivatives for degrading cyclin-dependent kinase 2 and/or cyclin-dependent kinase 4 via ubiquitin proteasome pathway |
| TW202547461A (zh) | 2024-05-17 | 2025-12-16 | 美商銳新醫藥公司 | Ras抑制劑 |
| WO2025255438A1 (en) | 2024-06-07 | 2025-12-11 | Revolution Medicines, Inc. | Methods of treating a ras protein-related disease or disorder |
| WO2025265060A1 (en) | 2024-06-21 | 2025-12-26 | Revolution Medicines, Inc. | Therapeutic compositions and methods for managing treatment-related effects |
| WO2026006747A1 (en) | 2024-06-28 | 2026-01-02 | Revolution Medicines, Inc. | Ras inhibitors |
| WO2026015796A1 (en) | 2024-07-12 | 2026-01-15 | Revolution Medicines, Inc. | Methods of treating a ras related disease or disorder |
| WO2026015825A1 (en) | 2024-07-12 | 2026-01-15 | Revolution Medicines, Inc. | Use of ras inhibitor for treating pancreatic cancer |
| WO2026015790A1 (en) | 2024-07-12 | 2026-01-15 | Revolution Medicines, Inc. | Methods of treating a ras related disease or disorder |
| WO2026015801A1 (en) | 2024-07-12 | 2026-01-15 | Revolution Medicines, Inc. | Methods of treating a ras related disease or disorder |
| WO2026035947A1 (en) | 2024-08-07 | 2026-02-12 | Tesseract Medicines Us, Llc | Kras-targeting covalent-induced drug conjugates comprising a topoisomerase payload |
| WO2026035945A1 (en) | 2024-08-07 | 2026-02-12 | Tesseract Medicines Us, Llc | Covalent-induced drug conjugates targeting kras and comprising a topoisomerase payload |
| WO2026050446A1 (en) | 2024-08-29 | 2026-03-05 | Revolution Medicines, Inc. | Ras inhibitors |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI271406B (en) * | 1999-12-13 | 2007-01-21 | Eisai Co Ltd | Tricyclic condensed heterocyclic compounds, preparation method of the same and pharmaceuticals comprising the same |
| JP2002371078A (ja) * | 2001-06-12 | 2002-12-26 | Sankyo Co Ltd | キノリン誘導体及びキノロン誘導体 |
| AU2002352444A1 (en) * | 2001-12-20 | 2003-07-09 | Celltech R And D Limited | Quinazolinedione derivatives |
| WO2005092894A1 (en) * | 2004-03-01 | 2005-10-06 | Eli Lilly And Company | Fused pyrazole derivatives as tgf-beta signal transduction inhibitors for the treatment of fibrosis and neoplasms |
| TW200643015A (en) * | 2005-03-11 | 2006-12-16 | Akzo Nobel Nv | 2-(4-oxo-4H-quinazolin-3-yl)acetamide derivatives |
| SG187633A1 (en) * | 2010-07-30 | 2013-03-28 | Oncotherapy Science Inc | Quinoline derivatives and melk inhibitors containing the same |
| CN105407894A (zh) * | 2013-03-14 | 2016-03-16 | 康威基内有限公司 | 用于抑制含布罗莫结构域的蛋白质的方法和组合物 |
| EP3636639A1 (en) * | 2013-10-10 | 2020-04-15 | Araxes Pharma LLC | Inhibitors of kras g12c |
| JP6377245B2 (ja) * | 2014-03-24 | 2018-08-22 | グアンドン ジョンシェン ファーマシューティカル カンパニー リミテッド | Smo阻害剤としてのキノリン誘導体 |
-
2016
- 2016-07-22 CA CA2993013A patent/CA2993013A1/en not_active Abandoned
- 2016-07-22 MX MX2018000777A patent/MX388781B/es unknown
- 2016-07-22 WO PCT/US2016/043568 patent/WO2017015562A1/en not_active Ceased
- 2016-07-22 EP EP16747678.7A patent/EP3325447A1/en not_active Withdrawn
- 2016-07-22 JP JP2018502355A patent/JP6869947B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| EP3325447A1 (en) | 2018-05-30 |
| MX388781B (es) | 2025-03-20 |
| WO2017015562A1 (en) | 2017-01-26 |
| JP2018520195A (ja) | 2018-07-26 |
| MX2018000777A (es) | 2018-03-23 |
| CA2993013A1 (en) | 2017-01-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6869947B2 (ja) | 置換キナゾリン化合物ならびにそのg12c変異kras、hrasおよび/またはnrasタンパク質の阻害剤としての使用 | |
| JP7628305B2 (ja) | 腫瘍転移を阻害するためのg12c変異体krasタンパク質の阻害剤としての2-(2-アクリロイル-2,6-ジアザスピロ[3.4]オクタン-6-イル)-6-(1h-インダゾール-4-イル)-ベンゾニトリル誘導体および関連化合物 | |
| JP6789239B2 (ja) | Krasの縮合三環系インヒビターおよびその使用の方法 | |
| JP7015059B2 (ja) | 置換複素環式基を含む2-置換キナゾリン化合物およびその使用方法 | |
| JP2022509830A (ja) | がんを処置するための化合物およびその使用方法 | |
| JP6849711B2 (ja) | Kras g12cの共有結合性阻害剤 | |
| JP6559123B2 (ja) | Krasg12cの阻害剤 | |
| JP2021098721A (ja) | 置換キナゾリン化合物およびその使用方法 | |
| JP7327802B2 (ja) | 縮合ヘテロ-ヘテロ二環式化合物およびその使用方法 | |
| JP2021532157A (ja) | がんを処置するための複素環式スピロ化合物およびその使用方法 | |
| JP2023041763A (ja) | 縮合n-複素環式化合物およびその使用方法 | |
| JP2020521741A (ja) | がんの処置のための化合物およびその使用の方法 | |
| JP2020521742A (ja) | Krasの共有結合性阻害剤 | |
| JP2019534260A (ja) | Rasの阻害剤としての複素環式化合物およびその使用方法 | |
| JP2020521740A (ja) | 変異体kras、hrasまたはnrasの調節因子としてのキナゾリン誘導体 | |
| JP2019529484A (ja) | Kras g12c変異体タンパク質の阻害剤 | |
| JP2017528498A (ja) | Kras g12c変異体タンパク質のインヒビター | |
| JP2017528488A (ja) | がんの処置のための併用療法 | |
| CN108026046B (zh) | 取代的喹唑啉化合物及其作为g12c突变体kras、hras和/或nras蛋白质的抑制剂的用途 | |
| HK40025458A (en) | Covalent inhibitors of kras | |
| HK40025457A (en) | Compounds and methods of use thereof for treatment of cancer |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190703 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20190703 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200728 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20200722 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20201028 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20201125 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210225 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20210401 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20210414 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6869947 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| LAPS | Cancellation because of no payment of annual fees |