JP6480457B2 - 変性ポリエチレングリコール溶液でガス中のSOxを除去する方法 - Google Patents
変性ポリエチレングリコール溶液でガス中のSOxを除去する方法 Download PDFInfo
- Publication number
- JP6480457B2 JP6480457B2 JP2016541787A JP2016541787A JP6480457B2 JP 6480457 B2 JP6480457 B2 JP 6480457B2 JP 2016541787 A JP2016541787 A JP 2016541787A JP 2016541787 A JP2016541787 A JP 2016541787A JP 6480457 B2 JP6480457 B2 JP 6480457B2
- Authority
- JP
- Japan
- Prior art keywords
- polyethylene glycol
- gas
- modified polyethylene
- desulfurization
- solution
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000034 method Methods 0.000 title claims description 205
- 229920001223 polyethylene glycol Polymers 0.000 title claims description 92
- 239000002202 Polyethylene glycol Substances 0.000 title claims description 91
- 238000006477 desulfuration reaction Methods 0.000 claims description 143
- 230000023556 desulfurization Effects 0.000 claims description 143
- 239000000243 solution Substances 0.000 claims description 104
- RAHZWNYVWXNFOC-UHFFFAOYSA-N Sulphur dioxide Chemical compound O=S=O RAHZWNYVWXNFOC-UHFFFAOYSA-N 0.000 claims description 92
- 239000007789 gas Substances 0.000 claims description 90
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 claims description 67
- 238000011069 regeneration method Methods 0.000 claims description 57
- 230000008569 process Effects 0.000 claims description 48
- 238000010521 absorption reaction Methods 0.000 claims description 47
- 229910052815 sulfur oxide Inorganic materials 0.000 claims description 46
- AKEJUJNQAAGONA-UHFFFAOYSA-N sulfur trioxide Chemical compound O=S(=O)=O AKEJUJNQAAGONA-UHFFFAOYSA-N 0.000 claims description 45
- 230000008929 regeneration Effects 0.000 claims description 42
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 31
- -1 sodium alkoxide Chemical class 0.000 claims description 27
- 238000010438 heat treatment Methods 0.000 claims description 24
- 230000005855 radiation Effects 0.000 claims description 23
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 claims description 22
- 239000003546 flue gas Substances 0.000 claims description 22
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 claims description 16
- ZUHZGEOKBKGPSW-UHFFFAOYSA-N tetraglyme Chemical compound COCCOCCOCCOCCOC ZUHZGEOKBKGPSW-UHFFFAOYSA-N 0.000 claims description 14
- 239000002912 waste gas Substances 0.000 claims description 14
- 230000000694 effects Effects 0.000 claims description 13
- 239000002994 raw material Substances 0.000 claims description 11
- SBASXUCJHJRPEV-UHFFFAOYSA-N 2-(2-methoxyethoxy)ethanol Chemical compound COCCOCCO SBASXUCJHJRPEV-UHFFFAOYSA-N 0.000 claims description 9
- SBZXBUIDTXKZTM-UHFFFAOYSA-N diglyme Chemical compound COCCOCCOC SBZXBUIDTXKZTM-UHFFFAOYSA-N 0.000 claims description 8
- XNWFRZJHXBZDAG-UHFFFAOYSA-N 2-METHOXYETHANOL Chemical compound COCCO XNWFRZJHXBZDAG-UHFFFAOYSA-N 0.000 claims description 7
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 claims description 7
- YFNKIDBQEZZDLK-UHFFFAOYSA-N triglyme Chemical compound COCCOCCOCCOC YFNKIDBQEZZDLK-UHFFFAOYSA-N 0.000 claims description 7
- 239000000654 additive Substances 0.000 claims description 5
- 230000000996 additive effect Effects 0.000 claims description 5
- 150000001412 amines Chemical class 0.000 claims description 5
- 239000007864 aqueous solution Substances 0.000 claims description 5
- 239000000203 mixture Substances 0.000 claims description 5
- 239000011259 mixed solution Substances 0.000 claims description 4
- 150000003457 sulfones Chemical class 0.000 claims description 4
- 150000001408 amides Chemical class 0.000 claims description 3
- 150000007942 carboxylates Chemical class 0.000 claims description 3
- 229910052751 metal Inorganic materials 0.000 claims description 3
- 239000002184 metal Substances 0.000 claims description 3
- 150000002902 organometallic compounds Chemical class 0.000 claims description 3
- 229910052700 potassium Inorganic materials 0.000 claims description 3
- 239000011591 potassium Substances 0.000 claims description 3
- 239000011734 sodium Substances 0.000 claims description 3
- 229910052708 sodium Inorganic materials 0.000 claims description 3
- 150000003462 sulfoxides Chemical class 0.000 claims description 3
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 claims 1
- 239000007788 liquid Substances 0.000 description 90
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 38
- 239000011593 sulfur Substances 0.000 description 38
- 229910052717 sulfur Inorganic materials 0.000 description 38
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 34
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 27
- 238000010586 diagram Methods 0.000 description 20
- QGJOPFRUJISHPQ-UHFFFAOYSA-N Carbon disulfide Chemical compound S=C=S QGJOPFRUJISHPQ-UHFFFAOYSA-N 0.000 description 18
- 229910052757 nitrogen Inorganic materials 0.000 description 17
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 12
- RWSOTUBLDIXVET-UHFFFAOYSA-N Dihydrogen sulfide Chemical compound S RWSOTUBLDIXVET-UHFFFAOYSA-N 0.000 description 12
- JJWKPURADFRFRB-UHFFFAOYSA-N carbonyl sulfide Chemical compound O=C=S JJWKPURADFRFRB-UHFFFAOYSA-N 0.000 description 12
- 238000005516 engineering process Methods 0.000 description 12
- 229910000037 hydrogen sulfide Inorganic materials 0.000 description 12
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 10
- 239000000126 substance Substances 0.000 description 10
- 239000006227 byproduct Substances 0.000 description 8
- AXCZMVOFGPJBDE-UHFFFAOYSA-L calcium dihydroxide Chemical compound [OH-].[OH-].[Ca+2] AXCZMVOFGPJBDE-UHFFFAOYSA-L 0.000 description 8
- 125000003342 alkenyl group Chemical group 0.000 description 7
- 125000000217 alkyl group Chemical group 0.000 description 7
- 125000000304 alkynyl group Chemical group 0.000 description 7
- 235000019738 Limestone Nutrition 0.000 description 6
- 229910021529 ammonia Inorganic materials 0.000 description 6
- 239000000428 dust Substances 0.000 description 6
- 239000006260 foam Substances 0.000 description 6
- XEEYBQQBJWHFJM-UHFFFAOYSA-N iron Substances [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 6
- 239000006028 limestone Substances 0.000 description 6
- 239000003513 alkali Substances 0.000 description 5
- 239000001569 carbon dioxide Substances 0.000 description 5
- 229910002092 carbon dioxide Inorganic materials 0.000 description 5
- 239000011261 inert gas Substances 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 5
- 238000006116 polymerization reaction Methods 0.000 description 5
- 238000005406 washing Methods 0.000 description 5
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 4
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- UQSXHKLRYXJYBZ-UHFFFAOYSA-N Iron oxide Chemical compound [Fe]=O UQSXHKLRYXJYBZ-UHFFFAOYSA-N 0.000 description 4
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 4
- 229910052783 alkali metal Inorganic materials 0.000 description 4
- 150000001340 alkali metals Chemical class 0.000 description 4
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 230000007423 decrease Effects 0.000 description 4
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 4
- AMWRITDGCCNYAT-UHFFFAOYSA-L hydroxy(oxo)manganese;manganese Chemical compound [Mn].O[Mn]=O.O[Mn]=O AMWRITDGCCNYAT-UHFFFAOYSA-L 0.000 description 4
- 238000003672 processing method Methods 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- 238000000926 separation method Methods 0.000 description 4
- 150000003453 sulfinic acid esters Chemical class 0.000 description 4
- 150000003459 sulfonic acid esters Chemical class 0.000 description 4
- FZTLLUYFWAOGGB-UHFFFAOYSA-N 1,4-dioxane dioxane Chemical compound C1COCCO1.C1COCCO1 FZTLLUYFWAOGGB-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 3
- 238000006266 etherification reaction Methods 0.000 description 3
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 3
- 229910052742 iron Inorganic materials 0.000 description 3
- 125000001741 organic sulfur group Chemical group 0.000 description 3
- 238000001556 precipitation Methods 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 238000007086 side reaction Methods 0.000 description 3
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 2
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- 239000004215 Carbon black (E152) Substances 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 description 2
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 2
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 2
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 2
- WGLPBDUCMAPZCE-UHFFFAOYSA-N Trioxochromium Chemical compound O=[Cr](=O)=O WGLPBDUCMAPZCE-UHFFFAOYSA-N 0.000 description 2
- 239000006096 absorbing agent Substances 0.000 description 2
- 125000002252 acyl group Chemical group 0.000 description 2
- 239000012670 alkaline solution Substances 0.000 description 2
- 150000003863 ammonium salts Chemical class 0.000 description 2
- 229910052786 argon Inorganic materials 0.000 description 2
- 125000003118 aryl group Chemical group 0.000 description 2
- 230000027455 binding Effects 0.000 description 2
- 230000015572 biosynthetic process Effects 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- HQABUPZFAYXKJW-UHFFFAOYSA-N butan-1-amine Chemical compound CCCCN HQABUPZFAYXKJW-UHFFFAOYSA-N 0.000 description 2
- 239000000920 calcium hydroxide Substances 0.000 description 2
- 229910001861 calcium hydroxide Inorganic materials 0.000 description 2
- 239000000292 calcium oxide Substances 0.000 description 2
- ODINCKMPIJJUCX-UHFFFAOYSA-N calcium oxide Inorganic materials [Ca]=O ODINCKMPIJJUCX-UHFFFAOYSA-N 0.000 description 2
- 159000000007 calcium salts Chemical class 0.000 description 2
- GBAOBIBJACZTNA-UHFFFAOYSA-L calcium sulfite Chemical compound [Ca+2].[O-]S([O-])=O GBAOBIBJACZTNA-UHFFFAOYSA-L 0.000 description 2
- 235000010261 calcium sulphite Nutrition 0.000 description 2
- 229910000423 chromium oxide Inorganic materials 0.000 description 2
- 229910000428 cobalt oxide Inorganic materials 0.000 description 2
- IVMYJDGYRUAWML-UHFFFAOYSA-N cobalt(ii) oxide Chemical compound [Co]=O IVMYJDGYRUAWML-UHFFFAOYSA-N 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000007797 corrosion Effects 0.000 description 2
- 238000005260 corrosion Methods 0.000 description 2
- 230000018044 dehydration Effects 0.000 description 2
- 238000006297 dehydration reaction Methods 0.000 description 2
- 238000005265 energy consumption Methods 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 2
- NCNCGGDMXMBVIA-UHFFFAOYSA-L iron(ii) hydroxide Chemical compound [OH-].[OH-].[Fe+2] NCNCGGDMXMBVIA-UHFFFAOYSA-L 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- 229940087646 methanolamine Drugs 0.000 description 2
- 229910000476 molybdenum oxide Inorganic materials 0.000 description 2
- PQQKPALAQIIWST-UHFFFAOYSA-N oxomolybdenum Chemical compound [Mo]=O PQQKPALAQIIWST-UHFFFAOYSA-N 0.000 description 2
- 239000002244 precipitate Substances 0.000 description 2
- WGYKZJWCGVVSQN-UHFFFAOYSA-N propylamine Chemical compound CCCN WGYKZJWCGVVSQN-UHFFFAOYSA-N 0.000 description 2
- 230000001172 regenerating effect Effects 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- HHVIBTZHLRERCL-UHFFFAOYSA-N sulfonyldimethane Chemical compound CS(C)(=O)=O HHVIBTZHLRERCL-UHFFFAOYSA-N 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 229910052723 transition metal Inorganic materials 0.000 description 2
- 238000013519 translation Methods 0.000 description 2
- 239000002351 wastewater Substances 0.000 description 2
- 239000011787 zinc oxide Substances 0.000 description 2
- OTJFQRMIRKXXRS-UHFFFAOYSA-N (hydroxymethylamino)methanol Chemical compound OCNCO OTJFQRMIRKXXRS-UHFFFAOYSA-N 0.000 description 1
- GEYOCULIXLDCMW-UHFFFAOYSA-N 1,2-phenylenediamine Chemical compound NC1=CC=CC=C1N GEYOCULIXLDCMW-UHFFFAOYSA-N 0.000 description 1
- PVXVWWANJIWJOO-UHFFFAOYSA-N 1-(1,3-benzodioxol-5-yl)-N-ethylpropan-2-amine Chemical compound CCNC(C)CC1=CC=C2OCOC2=C1 PVXVWWANJIWJOO-UHFFFAOYSA-N 0.000 description 1
- KQIXMZWXFFHRAQ-UHFFFAOYSA-N 1-(2-hydroxybutylamino)butan-2-ol Chemical compound CCC(O)CNCC(O)CC KQIXMZWXFFHRAQ-UHFFFAOYSA-N 0.000 description 1
- BFIAIMMAHAIVFT-UHFFFAOYSA-N 1-[bis(2-hydroxybutyl)amino]butan-2-ol Chemical compound CCC(O)CN(CC(O)CC)CC(O)CC BFIAIMMAHAIVFT-UHFFFAOYSA-N 0.000 description 1
- LOWMYOWHQMKBTM-UHFFFAOYSA-N 1-butylsulfinylbutane Chemical compound CCCCS(=O)CCCC LOWMYOWHQMKBTM-UHFFFAOYSA-N 0.000 description 1
- AIDFJGKWTOULTC-UHFFFAOYSA-N 1-butylsulfonylbutane Chemical compound CCCCS(=O)(=O)CCCC AIDFJGKWTOULTC-UHFFFAOYSA-N 0.000 description 1
- MBDUIEKYVPVZJH-UHFFFAOYSA-N 1-ethylsulfonylethane Chemical compound CCS(=O)(=O)CC MBDUIEKYVPVZJH-UHFFFAOYSA-N 0.000 description 1
- BQCCJWMQESHLIT-UHFFFAOYSA-N 1-propylsulfinylpropane Chemical compound CCCS(=O)CCC BQCCJWMQESHLIT-UHFFFAOYSA-N 0.000 description 1
- JEXYCADTAFPULN-UHFFFAOYSA-N 1-propylsulfonylpropane Chemical compound CCCS(=O)(=O)CCC JEXYCADTAFPULN-UHFFFAOYSA-N 0.000 description 1
- VVDBZDRIMIXITI-UHFFFAOYSA-N 2-[bis(carboxymethyl)amino]acetic acid;iron Chemical compound [Fe].OC(=O)CN(CC(O)=O)CC(O)=O VVDBZDRIMIXITI-UHFFFAOYSA-N 0.000 description 1
- BLFRQYKZFKYQLO-UHFFFAOYSA-N 4-aminobutan-1-ol Chemical compound NCCCCO BLFRQYKZFKYQLO-UHFFFAOYSA-N 0.000 description 1
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- GSNUFIFRDBKVIE-UHFFFAOYSA-N DMF Natural products CC1=CC=C(C)O1 GSNUFIFRDBKVIE-UHFFFAOYSA-N 0.000 description 1
- PQUCIEFHOVEZAU-UHFFFAOYSA-N Diammonium sulfite Chemical compound [NH4+].[NH4+].[O-]S([O-])=O PQUCIEFHOVEZAU-UHFFFAOYSA-N 0.000 description 1
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 1
- MBMLMWLHJBBADN-UHFFFAOYSA-N Ferrous sulfide Chemical compound [Fe]=S MBMLMWLHJBBADN-UHFFFAOYSA-N 0.000 description 1
- QMMZSJPSPRTHGB-UHFFFAOYSA-N MDEA Natural products CC(C)CCCCC=CCC=CC(O)=O QMMZSJPSPRTHGB-UHFFFAOYSA-N 0.000 description 1
- WUGQZFFCHPXWKQ-UHFFFAOYSA-N Propanolamine Chemical compound NCCCO WUGQZFFCHPXWKQ-UHFFFAOYSA-N 0.000 description 1
- 208000018569 Respiratory Tract disease Diseases 0.000 description 1
- CZKMHJRUUDUFNH-UHFFFAOYSA-N S.C(COCCOCCO)O Chemical compound S.C(COCCOCCO)O CZKMHJRUUDUFNH-UHFFFAOYSA-N 0.000 description 1
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- BNIAKAQSIZOVSN-UHFFFAOYSA-N [Na].CC(O)CO Chemical compound [Na].CC(O)CO BNIAKAQSIZOVSN-UHFFFAOYSA-N 0.000 description 1
- ITBPIKUGMIZTJR-UHFFFAOYSA-N [bis(hydroxymethyl)amino]methanol Chemical compound OCN(CO)CO ITBPIKUGMIZTJR-UHFFFAOYSA-N 0.000 description 1
- IKHGUXGNUITLKF-XPULMUKRSA-N acetaldehyde Chemical compound [14CH]([14CH3])=O IKHGUXGNUITLKF-XPULMUKRSA-N 0.000 description 1
- 125000002777 acetyl group Chemical group [H]C([H])([H])C(*)=O 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 238000003916 acid precipitation Methods 0.000 description 1
- 125000003647 acryloyl group Chemical group O=C([*])C([H])=C([H])[H] 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 150000003973 alkyl amines Chemical class 0.000 description 1
- 230000004075 alteration Effects 0.000 description 1
- BFNBIHQBYMNNAN-UHFFFAOYSA-N ammonium sulfate Chemical compound N.N.OS(O)(=O)=O BFNBIHQBYMNNAN-UHFFFAOYSA-N 0.000 description 1
- 229910052921 ammonium sulfate Inorganic materials 0.000 description 1
- 235000011130 ammonium sulphate Nutrition 0.000 description 1
- 150000004982 aromatic amines Chemical class 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- BRPQOXSCLDDYGP-UHFFFAOYSA-N calcium oxide Chemical compound [O-2].[Ca+2] BRPQOXSCLDDYGP-UHFFFAOYSA-N 0.000 description 1
- 235000011132 calcium sulphate Nutrition 0.000 description 1
- 239000003054 catalyst Substances 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 239000003245 coal Substances 0.000 description 1
- 239000000571 coke Substances 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 238000005262 decarbonization Methods 0.000 description 1
- 230000006837 decompression Effects 0.000 description 1
- 230000006866 deterioration Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- CCAFPWNGIUBUSD-UHFFFAOYSA-N diethyl sulfoxide Chemical compound CCS(=O)CC CCAFPWNGIUBUSD-UHFFFAOYSA-N 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 229910001882 dioxygen Inorganic materials 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 238000003912 environmental pollution Methods 0.000 description 1
- ZSXFZANQMJQBTQ-UHFFFAOYSA-N ethane-1,2-diol;potassium Chemical compound [K].OCCO ZSXFZANQMJQBTQ-UHFFFAOYSA-N 0.000 description 1
- NWJKPSLXLQLUTC-UHFFFAOYSA-N ethane-1,2-diol;sodium Chemical compound [Na].OCCO NWJKPSLXLQLUTC-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 235000010299 hexamethylene tetramine Nutrition 0.000 description 1
- VKYKSIONXSXAKP-UHFFFAOYSA-N hexamethylenetetramine Chemical compound C1N(C2)CN3CN1CN2C3 VKYKSIONXSXAKP-UHFFFAOYSA-N 0.000 description 1
- 150000002430 hydrocarbons Chemical class 0.000 description 1
- 125000001183 hydrocarbyl group Chemical group 0.000 description 1
- DOUHZFSGSXMPIE-UHFFFAOYSA-N hydroxidooxidosulfur(.) Chemical compound [O]SO DOUHZFSGSXMPIE-UHFFFAOYSA-N 0.000 description 1
- 238000009776 industrial production Methods 0.000 description 1
- 239000011630 iodine Substances 0.000 description 1
- 229910052740 iodine Inorganic materials 0.000 description 1
- 235000014413 iron hydroxide Nutrition 0.000 description 1
- 229910021506 iron(II) hydroxide Inorganic materials 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- XMYQHJDBLRZMLW-UHFFFAOYSA-N methanolamine Chemical compound NCO XMYQHJDBLRZMLW-UHFFFAOYSA-N 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 244000005700 microbiome Species 0.000 description 1
- 238000002715 modification method Methods 0.000 description 1
- 239000003345 natural gas Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 239000012071 phase Substances 0.000 description 1
- YQYYPDBLQPFRIL-UHFFFAOYSA-N potassium;propane-1,2,3-triol Chemical compound [K].OCC(O)CO YQYYPDBLQPFRIL-UHFFFAOYSA-N 0.000 description 1
- ZVDJKPHNSCMPGU-UHFFFAOYSA-N potassium;propane-1,2-diol Chemical compound [K].CC(O)CO ZVDJKPHNSCMPGU-UHFFFAOYSA-N 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- SQGMBDQWNFMOIU-UHFFFAOYSA-N propane-1,1,1-triol;propane-1,2,3-triol Chemical compound CCC(O)(O)O.OCC(O)CO SQGMBDQWNFMOIU-UHFFFAOYSA-N 0.000 description 1
- AMCPECLBZPXAPB-UHFFFAOYSA-N propane-1,2,3-triol;sodium Chemical compound [Na].OCC(O)CO AMCPECLBZPXAPB-UHFFFAOYSA-N 0.000 description 1
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 1
- 125000001501 propionyl group Chemical group O=C([*])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 238000007670 refining Methods 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 238000010850 salt effect Methods 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- 229910000029 sodium carbonate Inorganic materials 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000002910 solid waste Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000009628 steelmaking Methods 0.000 description 1
- 125000001424 substituent group Chemical group 0.000 description 1
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- XTQHKBHJIVJGKJ-UHFFFAOYSA-N sulfur monoxide Chemical class S=O XTQHKBHJIVJGKJ-UHFFFAOYSA-N 0.000 description 1
- 239000001648 tannin Substances 0.000 description 1
- 235000018553 tannin Nutrition 0.000 description 1
- 229920001864 tannin Polymers 0.000 description 1
- 238000004448 titration Methods 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- 150000003624 transition metals Chemical class 0.000 description 1
- JLGLQAWTXXGVEM-UHFFFAOYSA-N triethylene glycol monomethyl ether Chemical compound COCCOCCOCCO JLGLQAWTXXGVEM-UHFFFAOYSA-N 0.000 description 1
- 238000002604 ultrasonography Methods 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D53/00—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols
- B01D53/14—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols by absorption
- B01D53/1425—Regeneration of liquid absorbents
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D53/00—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols
- B01D53/14—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols by absorption
- B01D53/1456—Removing acid components
- B01D53/1481—Removing sulfur dioxide or sulfur trioxide
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D53/00—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols
- B01D53/14—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols by absorption
- B01D53/1493—Selection of liquid materials for use as absorbents
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D53/00—Separation of gases or vapours; Recovering vapours of volatile solvents from gases; Chemical or biological purification of waste gases, e.g. engine exhaust gases, smoke, fumes, flue gases, aerosols
- B01D53/34—Chemical or biological purification of waste gases
- B01D53/46—Removing components of defined structure
- B01D53/48—Sulfur compounds
- B01D53/50—Sulfur oxides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2252/00—Absorbents, i.e. solvents and liquid materials for gas absorption
- B01D2252/20—Organic absorbents
- B01D2252/202—Alcohols or their derivatives
- B01D2252/2023—Glycols, diols or their derivatives
- B01D2252/2026—Polyethylene glycol, ethers or esters thereof, e.g. Selexol
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2257/00—Components to be removed
- B01D2257/30—Sulfur compounds
- B01D2257/302—Sulfur oxides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2258/00—Sources of waste gases
- B01D2258/02—Other waste gases
- B01D2258/0283—Flue gases
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B17/00—Sulfur; Compounds thereof
- C01B17/48—Sulfur dioxide; Sulfurous acid
- C01B17/50—Preparation of sulfur dioxide
- C01B17/60—Isolation of sulfur dioxide from gases
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/20—Air quality improvement or preservation, e.g. vehicle emission control or emission reduction by using catalytic converters
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Analytical Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Organic Chemistry (AREA)
- Biomedical Technology (AREA)
- Health & Medical Sciences (AREA)
- Environmental & Geological Engineering (AREA)
- Inorganic Chemistry (AREA)
- Treating Waste Gases (AREA)
- Gas Separation By Absorption (AREA)
Description
本発明は、煙道ガス、硫黄含有廃ガス及び/又は工業用原料ガスの浄化方法に関し、具体的に、煙道ガス、SOx含有廃ガス及び/又は工業用原料ガス中のSOx (x=2および/または3)を除去する方法に関する。
[背景技術]
工業の迅速な発展によって、煙道ガス、硫黄含有工業用原料ガスおよびその他の廃ガスの消耗や排出量が日々増えつつけている。硫黄含有廃ガスの排出に、深刻な環境汚染、例えば、酸性雨の形成、建築物の酸腐食、呼吸道疾患および皮膚病などを引き起こし、人々の健康に直接害を及ぼしている。数年来、世界中の科学者は、煙道ガス、硫黄含有工業用原料ガスおよびその他の廃ガスの脱硫技術に対して多くの研究を行い、たくさんの研究資料を蓄積してくる。環境意識の高まりに一方、煙道ガス、硫黄含有工業用原料ガスおよびその他の廃ガスの脱硫問題が重視されつつある。しかしながら、今まで、煙道ガス、硫黄含有工業用原料ガスおよびその他の廃ガスの脱硫技術は、まだ飛躍的な進歩を遂げていない。煙道ガス、硫黄含有工業用原料ガスおよびその他の廃ガスの脱硫問題は、ずっとチャレンジングな課題である。
[参考文献]
[1]Benson, H.E. Parrish,R.W.(1974) HiPure Process Removes CO2/H2S. Hydrocarbon Processing, April.81-82.
[2]Jenett,E.(1962),Giammarco-VetrocokeProcess.The Oil and Gas Journal. April 30,72-79.
[3] F.C.Riesenfeld,A.L.Kohl,沈余生訳、<ガス浄化>、北京、中国建築出版社、1982(F.C.Riesenfeld,A.L.Kohl,沈余生訳,《气体浄化》,北京,中国建筑出版社,1982).
[4] 戴文斌,唐宏青,<コンピュータと応用科学>,1994,11(1),P44-51(戴文斌,唐宏青,《計算机与応用化学》,1994,11(1),P44-51).
[5] 馬斌,<石炭化学工業>,1994,総68期,P35-38(馬斌,《煤化工》,1994,総68期,P35-38).
[6]Zh.Prikl.Khim.(S.-Peterburg),66(10),2383-2385(Russian),1993.
[7] 魏雄輝,戴乾圜,陳忠明,邵可声,張晨鼎,(1998) 塩基性鉄塩緩衝水溶液で硫黄を除去する原理,化学工業学報,49(1),48-58(魏雄輝,戴乾圜,陳忠明,邵可声,張晨鼎,(1998) ▲ジェン▼性鉄▲イェン▼緩衝水溶液脱硫法原理, 化工学報,49(1),48-58).
[8] 魏雄輝,(1994) 半水性ガスで脱硫脱酸素新方法,中国特許CN1087110(魏雄輝,(1994)半水煤气脱硫脱▲ヤン▼新方法,中国専利CN1087110).
[9] 魏雄輝,(1996)加圧鉄-アルカリ溶液で炭素・硫黄を除去する,中国特許CN1133817(魏雄輝,(1996)加圧鉄-▲ジェン▼溶液脱▲タン▼脱硫,中国専利CN1133817).
[10] 魏雄輝,鄒美花,魏鳳輝,(1999) 鉄-アルカリ溶液触媒法でガス中の炭素・硫黄・シアンを除去する方法,中国発明特許,特許番号ZL99100596.1(魏雄鄒,鄒美花,魏鳳輝,(1999) 鉄-▲ジェン▼溶液催化法气体脱▲タン▼脱硫脱▲チン▼方法,中国発明専利,専利号ZL99100596.1).
[11] 魏雄輝,(2002)生化学鉄-アルカリ溶液触媒法でガス中の硫黄を除去する方法,中国発明特許,特許番号ZL02130605.2(魏雄輝,(2002)生化鉄-▲ジェン▼溶液催化法气体脱硫方法,中国発明専利,専利号 ZL02130605.2).
[12]Galeeva R.G.,Kamalov Kh.S.,Aminov M.Kh.,Gafiatullin R.R.,Mitina A.P.,Bakhshijan D. Ts.,Safin G.R.,Levanov V.V.,Installation for Complete purification of Petroleum and Nattural Gases,RU2070423C1.
[13]Biedermann,Jean-Michel,Process for Eliminating Hydrogen Sulphide Contained in Gas Mixture,PCT/FR83/00174.
[14]Biedermann,Jean-Michel,etc.,Process for Eliminating Hydrogen Sulphide Contained in Gas Mixture,FR2532190-A1.
[15] 村岡、▲ひろ▼允,エチレングリコールで脱水方法、JP62-95118A(村岡,▲ひろ▼允,用乙二醇脱水方法,JP62-95118A).
[16] ドイツ特許、エチレングリコールで脱水方法,DT2333708A1(▲徳▼国専利,用乙二醇脱水方法,DT2333708A1).
[17] 旧ソ連特許,SU655410A(前蘇聯専利,SU1611411A1).
[18] 小室、武勇,JP6-228573A(小室,武勇,JP6-228573A).
[19] 旧ソ連特許,SU655410A(前蘇聯専利,SU655410A).
[20]WYSCHOFSKY Michael,HOBERG Dirk,Method for the Separation of Gaseous Components from Technical Gases by Means of Ethylene Glycol Dimethyl Ethersat Low Temperatures, WO03011432A1(PCT/EP02/07915).
[21] 旧ソ連特許,SU927282B(前蘇聯専利,SU927282B).
[22]DILLON Edward Thomas,Composition and Method for Sweetening Hydrocarbons, WO9007467A1(PCT/US89/05742).
Zaida Diaz,Process for the Removal of H2S and CO2from Gaseous Streams,US4368178.
[発明の概要]
本発明の目的は、変性ポリエチレングリコールを溶液にして(以下、「変性ポリエチレングリコール溶液」と略す)ガス中のSOx(x=2及び/又は3)を吸収する方法(以下、「変性ポリエチレングリコール脱硫法」と略す)を提供することであり、我々のこの前の特許「ポリエチレングリコールでガス中のSOxを除去する方法(中国特許番号ZL200910009058.1)」及び「エチレングリコールで煙道ガス中のSOxを除去する方法(中国特許番号ZL200710110446.X」における上記不足を解決し、スルフィン酸エステルおよびスルホン酸エステル系物質の生成を避けることである。
R1-O-C2H4-O-R2 エーテル化後のエチレングリコール;
R1-O-C2H4-O-C2H4-O-R2 重合度が2であるエーテル化ポリエチレングリコール;
R1-O-C2H4-O-C2H4-O-C2H4-O-R2 重合度が3であるエーテル化ポリエチレングリコール;
R1-O-C2H4-O-C2H4-O-C2H4-O-C2H4-O-R2 重合度が3であるエーテル化ポリエチレングリコール;
…… 前記に基づいて類推する。
即ち、R1-(O-C2H4)n-O-R2、nが正の整数である。
以上の分子式中の置換基であるR1、R2が同一でも異なっても良く、それぞれ独立にアルキル、アルニケル、アルキニル、アシル又はアリール基である。
再生後の変性ポリエチレングリコール溶液( 以下、単に「脱硫液」と略す) を循環利用する。
[図面の簡単な説明]
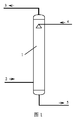
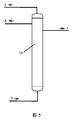
[図l]図lは、脱硫吸収プロセスの概略図である。
[具体的な実施形態]
以下、具体的な実施形態により、本発明の変性ポリエチレングリコール脱硫法を説明する。本実施形態は、本発明をよりよく説明するためのものであり、本発明の特許請求の範囲を制限するものと解してはならない。
Claims (8)
- 変性ポリエチレングリコール溶液でガス中のSOxを吸収させる、ガス中のSOxを除去する方法であって、前記変性ポリエチレングリコール溶液は、エチレングリコールジメチルエーテル、ジエチレングリコールジメチルエーテル、トリエチレングリコールジメチルエーテル、テトラエチレングリコールジメチルエーテル、ジオキサン、エチレングリコールモノメチルエーテル、ジエチレングリコールモノメチルエーテルであり、前記変性ポリエチレングリコール溶液とSOx含有ガスとを接触させ、ガス中のSOx(x=2及び/又は3を表す)を吸収させ、
SOxを吸収した変性ポリエチレングリコール溶液を、加熱法、或いは、加熱法と、真空法、ストリッピング法、超音波法、マイクロ波法および放射法から選ばれる1種又は複数種との組合せ方法で再生し、再生温度が0〜300℃であり、再生過程で二酸化硫黄および/又は三酸化硫黄を放出し、再生後の前記変性ポリエチレングリコール溶液を循環利用することを特徴とする、ガス中のSOxを除去する方法。 - 前記変性ポリエチレングリコール溶液が、含有量が質量で80%以上である変性ポリエチレングリコールの水溶液であることを特徴とする、請求項1に記載のガス中のSOxを除去する方法。
- 前記変性ポリエチレングリコール溶液が、単一分子量の変性ポリエチレングリコールの溶液、もしくは複数種の異なる分子量の変性ポリエチレングリコールの混合溶液であることを特徴とする、請求項1に記載のガス中のSOxを除去する方法。
- 前記変性ポリエチレングリコール溶液が、前記変性ポリエチレングリコール溶液における含有量が質量で20%未満であるエチレングリコール、又はポリエチレングリコール、又はエチレングリコールとポリエチレングリコールとの混合液を一定量含有することを特徴とする、請求項1に記載のガス中のSOxを除去する方法。
- 前記変性ポリエチレングリコール溶液が、前記変性ポリエチレングリコール溶液における含有量が質量で20%未満であり、有機アミン類、ヒドロキシアミン類、アミド類、スルホン類、スルホキシド類、ナトリウムアルコキシド類、カリウムアルコキシド類、金属カルボキシレート類及び/又は金属有機化合物類である添加剤を一定量含有することを特徴とする、請求項1に記載のガス中のSOxを除去する方法。
- 前記変性ポリエチレングリコール溶液が、常圧又は加圧の条件下でガス中のSOxを吸収し、吸収温度が−20〜80℃であることを特徴とする、請求項1に記載のガス中のSOxを除去する方法。
- 再生後の変性ポリエチレングリコール溶液中の水の含有量が質量で20%を超えて脱硫効果に影響を及ぼす場合、変性ポリエチレングリコール溶液中の水を除去してから循環利用することを特徴とする、請求項1に記載のガス中のSOxを除去する方法。
- 煙道ガス、SOx含有廃ガス及び/又は工業用原料ガス中のSOxを前記方法で除去することを特徴とする、請求項1に記載のガス中のSOxを除去する方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201310409296.8A CN103432890B (zh) | 2013-09-10 | 2013-09-10 | 改性聚乙二醇脱除气体中SOx的方法 |
| CN201310409296.8 | 2013-09-10 | ||
| PCT/CN2014/085924 WO2015035878A1 (zh) | 2013-09-10 | 2014-09-04 | 改性聚乙二醇脱除气体中SOx的方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2016533893A JP2016533893A (ja) | 2016-11-04 |
| JP6480457B2 true JP6480457B2 (ja) | 2019-03-13 |
Family
ID=49686661
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2016541787A Active JP6480457B2 (ja) | 2013-09-10 | 2014-09-04 | 変性ポリエチレングリコール溶液でガス中のSOxを除去する方法 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US9795917B2 (ja) |
| EP (1) | EP3045219B1 (ja) |
| JP (1) | JP6480457B2 (ja) |
| KR (1) | KR20160055207A (ja) |
| CN (1) | CN103432890B (ja) |
| AU (1) | AU2014320953B2 (ja) |
| CA (1) | CA2923777C (ja) |
| EA (1) | EA201690562A1 (ja) |
| ES (1) | ES2966852T3 (ja) |
| MX (1) | MX367409B (ja) |
| WO (1) | WO2015035878A1 (ja) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103432890B (zh) | 2013-09-10 | 2015-12-09 | 北京博源恒升高科技有限公司 | 改性聚乙二醇脱除气体中SOx的方法 |
| CN103611391B (zh) * | 2013-12-12 | 2016-01-20 | 北京博源恒升高科技有限公司 | 乙二醇类复合溶液脱除气体中SOx的方法 |
| CN103623689B (zh) * | 2013-12-12 | 2016-06-29 | 北京博源恒升高科技有限公司 | 多元醇复合溶液脱除气体中SOx的方法 |
| CN105214457B (zh) | 2014-06-05 | 2018-04-17 | 魏雄辉 | 一种烟道气脱硫脱硝工艺及设备 |
| CN106031844B (zh) * | 2015-03-20 | 2020-01-07 | 江西永丰博源实业有限公司 | 一种脱硫脱硝剂 |
| CN105797783A (zh) * | 2016-04-06 | 2016-07-27 | 山东成泰化工有限公司 | 一种低温原油催化剂及其制备方法 |
| CN109621640B (zh) * | 2018-12-28 | 2021-02-26 | 河北科技大学 | 一种用于吸收so2的负载型离子液体变色材料及其制备方法和应用 |
| CN110408423A (zh) * | 2019-08-09 | 2019-11-05 | 磁悬浮润滑油(苏州)有限公司 | 一种利用改性聚乙二醇脱除燃料油中硫化物的方法 |
Family Cites Families (40)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2139375A (en) | 1937-06-14 | 1938-12-06 | Shell Dev | Removal of so from gases |
| US3737392A (en) * | 1969-06-11 | 1973-06-05 | Allied Chem | Solvent composition useful in acid gas removal from gas mixtures |
| FR2213793B2 (ja) * | 1972-09-22 | 1975-08-22 | Inst Francais Du Petrole | |
| DE2333708B2 (de) | 1973-07-03 | 1977-09-15 | Dsd Dillinger Stahlbau Gmbh, 6630 Saarlouis | Verfahren zum selektiven entfernen von schwefelwasserstoff aus kohlenwasserstoffhaltigen gasen |
| SU655410A1 (ru) | 1977-10-28 | 1979-04-05 | Всесоюзный научно-исследовательский институт природных газов | Абсорбент дл сушки и очистки углеводородных газов |
| SU927282A1 (ru) | 1979-04-25 | 1982-05-15 | Всесоюзный Научно-Исследовательский И Проектный Институт По Подготовке @К Транспортировке И Переработке Природного Газа | Абсорбент дл очистки газов от кислых компонентов |
| US4368178A (en) | 1981-05-26 | 1983-01-11 | Shell Oil Company | Process for the removal of H2 S and CO2 from gaseous streams |
| FR2532190A1 (fr) | 1982-08-25 | 1984-03-02 | Raffinage Cie Francaise | Dispositif pour l'elimination a froid de l'hydrogene sulfure contenu dans un melange gazeux, par reaction sur de l'anhydride sulfureux, et pour la separation du soufre solide ainsi produit |
| FR2532189A1 (fr) | 1982-08-25 | 1984-03-02 | Raffinage Cie Francaise | Procede d'elimination de l'hydrogene sulfure contenu dans un melange gazeux |
| DE3237387A1 (de) | 1982-10-08 | 1984-04-12 | Linde Ag, 6200 Wiesbaden | Verfahren zur entfernung unerwuenschter gasfoermiger bestandteile aus heissen rauchgasen |
| DE3239603A1 (de) * | 1982-10-26 | 1984-04-26 | Linde Ag, 6200 Wiesbaden | Verfahren zum gleichzeitigen entfernen von h(pfeil abwaerts)2(pfeil abwaerts)s, so(pfeil abwaerts)2(pfeil abwaerts) und elementarem schwefel aus gasgemischen |
| DE3428548A1 (de) * | 1984-08-02 | 1986-02-13 | Linde Ag, 6200 Wiesbaden | Verfahren zur erzeugung von elementarem schwefel |
| DE3501118A1 (de) | 1985-01-15 | 1986-07-17 | Linde Ag, 6200 Wiesbaden | Verfahren zur entfernung von so(pfeil abwaerts)2(pfeil abwaerts) und no(pfeil abwaerts)x(pfeil abwaerts) aus gasen |
| JPS6227021A (ja) | 1985-07-25 | 1987-02-05 | Nippon Shokubai Kagaku Kogyo Co Ltd | 酸性ガス吸収剤 |
| DD249856A5 (de) | 1985-09-27 | 1987-09-23 | Linde Ag,De | Verfahren zum auswaschen von no und/oder so tief 2 aus gasgemischen |
| DE3612123A1 (de) | 1985-09-27 | 1987-04-09 | Linde Ag | Verfahren zum auswaschen von no und/oder so(pfeil abwaerts)2(pfeil abwaerts) aus gasgemischen |
| JPS6295118A (ja) | 1985-10-21 | 1987-05-01 | Mitsubishi Heavy Ind Ltd | グリコ−ルを用いる脱水方法 |
| DE3624768A1 (de) * | 1986-07-22 | 1988-01-28 | Linde Ag | Verfahren zur verhinderung der korrosion von apparateteilen |
| US4741890A (en) * | 1986-07-24 | 1988-05-03 | Betz Laboratories, Inc. | Gas scrubbing method |
| US5273679A (en) * | 1986-10-30 | 1993-12-28 | Toho Kagaku Kogyo Co., Ltd. | Stabilizers for compositions for acid gas absorbent |
| SU1611411A1 (ru) | 1988-06-21 | 1990-12-07 | Всесоюзный Научно-Исследовательский И Проектный Институт По Переработке Газа | Способ очистки углеводородного газа от кислых компонентов |
| AU619375B2 (en) | 1988-12-23 | 1992-01-23 | Baker Hughes Incorporated | Composition and method for sweetening hydrocarbons |
| JPH03238022A (ja) * | 1990-02-16 | 1991-10-23 | Nkk Corp | コークス炉ガスの脱硫方法 |
| CN1087110A (zh) | 1992-11-16 | 1994-05-25 | 魏雄辉 | 半水煤气脱硫脱氧新方法 |
| JPH06228573A (ja) | 1993-02-08 | 1994-08-16 | Hitachi Ltd | 石炭ガス化プラントのテールガス処理法 |
| JPH06279007A (ja) | 1993-03-25 | 1994-10-04 | Sumitomo Seika Chem Co Ltd | 亜硫酸ガスの回収方法 |
| RU2070423C1 (ru) | 1993-09-14 | 1996-12-20 | Акционерное общество Миннибаевский газоперерабатывающий завод | Установка для комплексной очистки нефтяного и природного газов |
| CN1133817A (zh) | 1996-02-17 | 1996-10-23 | 魏雄辉 | 加压铁-碱溶液脱碳脱硫 |
| CN1092994C (zh) | 1999-02-05 | 2002-10-23 | 魏雄辉 | 铁-碱溶液催化法气体脱碳脱硫脱氰方法 |
| US6203599B1 (en) * | 1999-07-28 | 2001-03-20 | Union Carbide Chemicals & Plastics Technology Corporation | Process for the removal of gas contaminants from a product gas using polyethylene glycols |
| DE10136484A1 (de) | 2001-07-27 | 2003-02-13 | Uhde Gmbh | Verfahren zur Entfernung von Gasbestandteilen aus technischen Gasen mittels Ethylenglykoldimethylethern bei tieferen Temperaturen |
| CN1162203C (zh) | 2001-09-26 | 2004-08-18 | 南化集团研究院 | 一种物理溶剂脱硫脱碳新技术 |
| CN1158133C (zh) | 2002-09-09 | 2004-07-21 | 魏雄辉 | 生化铁—碱溶液催化法气体脱硫方法 |
| CN100384510C (zh) * | 2003-12-09 | 2008-04-30 | 南化集团研究院 | 一种高压脱除硫化物和二氧化碳的方法 |
| CN101053746B (zh) * | 2007-06-06 | 2010-06-09 | 北京大学 | 乙二醇脱除烟道气中sox的方法 |
| CN101502741B (zh) * | 2009-02-16 | 2011-01-05 | 北京博源恒升高科技有限公司 | 聚乙二醇脱除气体中SOx的方法 |
| US8905742B2 (en) | 2010-09-17 | 2014-12-09 | Synerdyne Corporation | Compact rotary platen 3D printer |
| EP2696970A4 (en) * | 2011-04-11 | 2014-09-03 | Electrosep Technologies Inc | METHOD FOR PURIFYING ABSORBENTS COMPRISING DIMETHYL ETHERS OF POLYETHYLENE GLYCOL |
| CN103432890B (zh) | 2013-09-10 | 2015-12-09 | 北京博源恒升高科技有限公司 | 改性聚乙二醇脱除气体中SOx的方法 |
| CN103623689B (zh) * | 2013-12-12 | 2016-06-29 | 北京博源恒升高科技有限公司 | 多元醇复合溶液脱除气体中SOx的方法 |
-
2013
- 2013-09-10 CN CN201310409296.8A patent/CN103432890B/zh active Active
-
2014
- 2014-09-04 ES ES14843772T patent/ES2966852T3/es active Active
- 2014-09-04 US US15/021,152 patent/US9795917B2/en active Active
- 2014-09-04 EP EP14843772.6A patent/EP3045219B1/en active Active
- 2014-09-04 MX MX2016003062A patent/MX367409B/es active IP Right Grant
- 2014-09-04 KR KR1020167009265A patent/KR20160055207A/ko not_active Application Discontinuation
- 2014-09-04 CA CA2923777A patent/CA2923777C/en active Active
- 2014-09-04 JP JP2016541787A patent/JP6480457B2/ja active Active
- 2014-09-04 WO PCT/CN2014/085924 patent/WO2015035878A1/zh active Application Filing
- 2014-09-04 EA EA201690562A patent/EA201690562A1/ru unknown
- 2014-09-04 AU AU2014320953A patent/AU2014320953B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| AU2014320953A1 (en) | 2016-04-28 |
| JP2016533893A (ja) | 2016-11-04 |
| CN103432890A (zh) | 2013-12-11 |
| EP3045219A4 (en) | 2017-05-17 |
| EA201690562A1 (ru) | 2016-10-31 |
| MX2016003062A (es) | 2016-12-08 |
| CN103432890B (zh) | 2015-12-09 |
| KR20160055207A (ko) | 2016-05-17 |
| EP3045219A1 (en) | 2016-07-20 |
| CA2923777A1 (en) | 2015-03-19 |
| EP3045219B1 (en) | 2023-10-04 |
| WO2015035878A1 (zh) | 2015-03-19 |
| MX367409B (es) | 2019-08-20 |
| CA2923777C (en) | 2018-03-20 |
| US9795917B2 (en) | 2017-10-24 |
| US20160220946A1 (en) | 2016-08-04 |
| ES2966852T3 (es) | 2024-04-24 |
| AU2014320953B2 (en) | 2017-03-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6480457B2 (ja) | 変性ポリエチレングリコール溶液でガス中のSOxを除去する方法 | |
| JP6473446B2 (ja) | 複合アルコールアミン類溶液でガス中のSOxを除去する方法 | |
| JP6188952B2 (ja) | エチレングリコール類複合溶液でガス中のSOxを除去する方法 | |
| JP5694957B2 (ja) | ポリエチレングリコールでガス中のSOxを除去する方法 | |
| JP6526677B2 (ja) | ポリオール複合溶液でガス中のSOxを除去する方法 | |
| BR112016013016B1 (pt) | Método para remover sox de gás com o uso de solução compósita de poliol |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20170214 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20170419 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20170613 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20181003 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20181026 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20190207 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6480457 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |
|
| R250 | Receipt of annual fees |
Free format text: JAPANESE INTERMEDIATE CODE: R250 |